Текст описания приведен в факсимильном виде.









































| название | год | авторы | номер документа |
|---|---|---|---|
| ЧЕЛОВЕЧЕСКИЕ АНТИ-CD38-АНТИТЕЛА И ИХ ПРИМЕНЕНИЕ | 2005 |
|
RU2402568C2 |
| АНТИТЕЛА ПРОТИВ MST1R И ИХ ПРИМЕНЕНИЕ | 2010 |
|
RU2534890C2 |
| АНТИ-GM-CSF АНТИТЕЛА И ИХ ПРИМЕНЕНИЕ | 2006 |
|
RU2447085C2 |
| ЧЕЛОВЕЧЕСКИЕ АНТИТЕЛА К ОНКОСТАТИНУ М И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2011 |
|
RU2600444C2 |
| АНТИТЕЛА, СВЯЗЫВАЮЩИЕСЯ ПРЕИМУЩЕСТВЕННО С ВНЕКЛЕТОЧНЫМ ДОМЕНОМ 4 ЧЕЛОВЕЧЕСКОГО CSF-1R, И ИХ ПРИМЕНЕНИЕ | 2010 |
|
RU2565541C2 |
| АНТИТЕЛА К ЧЕЛОВЕЧЕСКОМУ МСР-1 | 2001 |
|
RU2314316C2 |
| АНТИТЕЛА К ЧЕЛОВЕЧЕСКОМУ IL-1БЕТА | 2001 |
|
RU2286351C2 |
| АНТИТЕЛА ПРОТИВ ИНТЕРЛЕЙКИНА-13 ЧЕЛОВЕКА И ИХ ПРИМЕНЕНИЕ | 2005 |
|
RU2427589C2 |
| АНТИТЕЛА РЕЦЕПТОРА 1 ИНТЕРФЕРОНА АЛЬФА И ИХ ПРИМЕНЕНИЕ | 2005 |
|
RU2600884C2 |
| НОВЫЕ ПОЛНОСТЬЮ ЧЕЛОВЕЧЕСКИЕ МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА ПРОТИВ VAP-1 | 2008 |
|
RU2459832C2 |




























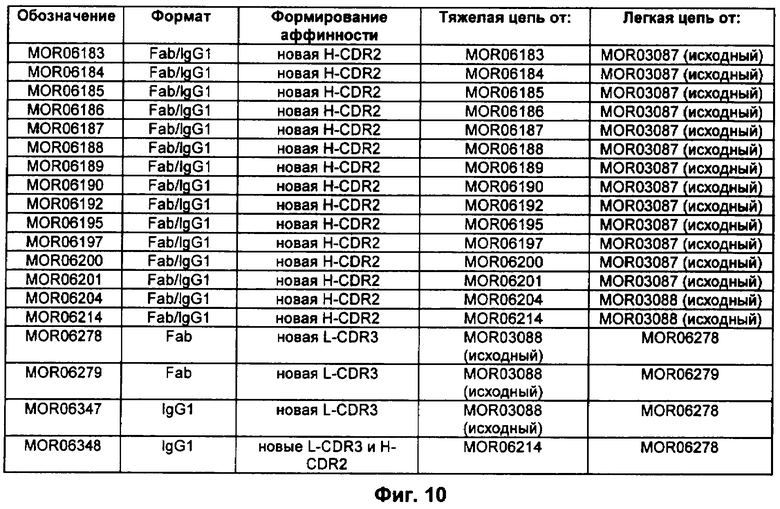

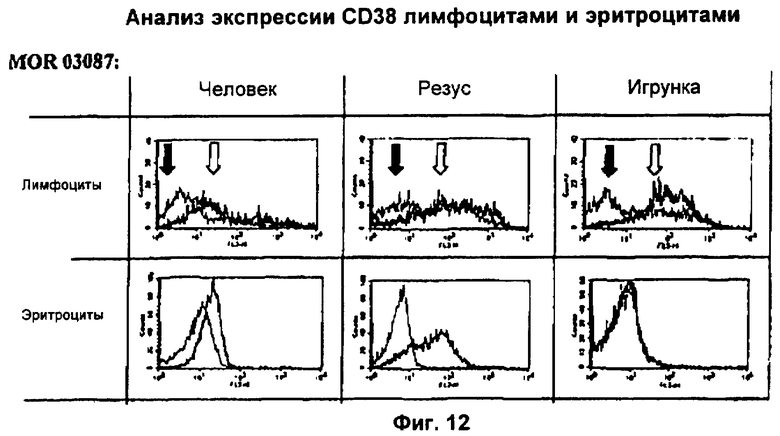
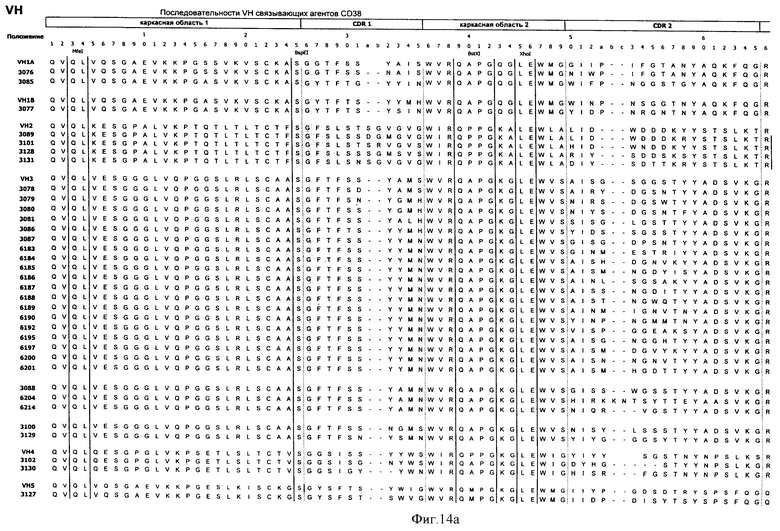



Настоящее изобретение относится к иммунологии и биотехнологии. Предложены варианты антител и их функциональных фрагментов, специфичных к CD38. Каждый вариант характеризуется тем, что содержит три CDRs легкой и три CDRs тяжелой цепи. Описаны: кодирующий полинуклеотид, а также вектор экспрессии и клетка-хозяин, включающие кодирующий полинуклеотид. Раскрыты: фармацевтическая и диагностическая композиции, способ лечения, способ выявления CD38 в эритроците, способ индукции специфичного цитолиза опухолевых клеток, экспрессирующих CD38 с использованием антитела. Предложенные новые антитела обладают неожиданными свойствами: связывать CD38 минипига и вызывать посредством перекрестного сшивания специфичный цитолиз клеток, экспрессирующих CD38. Использование изобретения может найти дальнейшее применение в терапии расстройств, опосредованных CD38, например, для лечения злокачественных заболеваний крови, таких как множественная миелома. 9 н. и 78 з.п. ф-лы, 37 ил., 4 табл.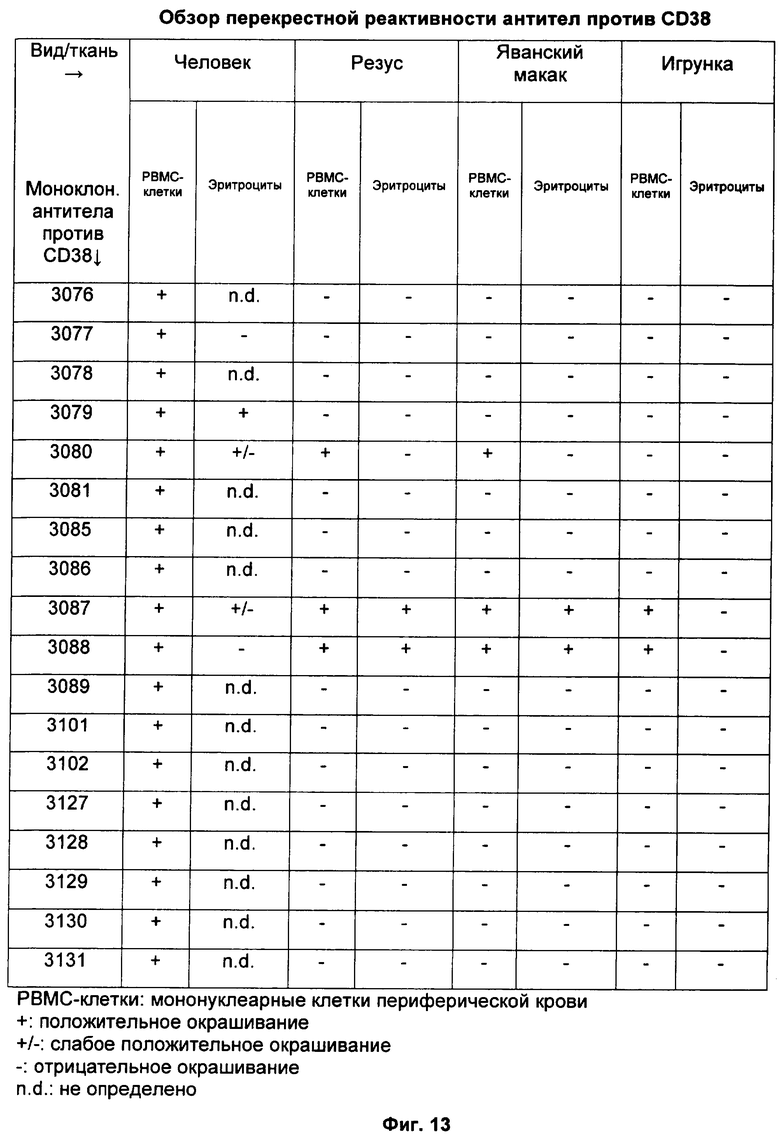
1. Выделенное антитело или его функциональный фрагмент, которые специфичны к CD38, содержащие (1) H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO: 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105 или 106, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO: 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 109 или 110, или (2) H-CDR1, H-CDR2 и Н-CDR3 области, по меньшей мере на шестьдесят процентов идентичные Н-CDR1, H-CDR2 и H-CDR3 областям, представленным в SEQ ID NO: 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105 или 106, и L-CDR1, L-CDR2 и L-CDR3 области, по меньшей мере на шестьдесят процентов идентичные L-CDR1, L-CDR2 и L-CDR3 областям, представленным в SEQ ID NO: 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59,60, 109 или 110.
2. Выделенное антитело по п.1, представляющее собой IgG (иммуноглобулин G).
3. Выделенное антитело по п.2, представляющее собой IgG1.
4. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:16, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:46.
5. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:16, и вариабельную легкую цепь, представленную в SEQ ID NO:46.
6. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:17, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:47.
7. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:17, и вариабельную легкую цепь, представленную в SEQ ID NO:47.
8. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:18, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:48.
9. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:18, и вариабельную легкую цепь, представленную в SEQ ID NO:48.
10. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:19, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:49.
11. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:19, и вариабельную легкую цепь, представленную в SEQ ID NO:49.
12. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:20, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:50.
13. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:20, и вариабельную легкую цепь, представленную в SEQ ID NO:50.
14. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, по меньшей мере на шестьдесят процентов идентичные H-CDR1, H-CDR2 и H-CDR3 областям, представленным в SEQ ID NO:21, и L-CDR1, L-CDR2 и L-CDR3 области, по меньшей мере на шестьдесят процентов идентичные L-CDR1, L-CDR2 и L-CDR3 областям, представленным в SEQ ID NO:51.
15. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, по меньшей мере на восемьдесят процентов идентичные H-CDR1, H-CDR2 и H-CDR3 областям, представленным в SEQ ID NO:21, и L-CDR1, L-CDR2 и L-CDR3 области, по меньшей мере на восемьдесят процентов идентичные L-CDR1, L-CDR2 и L-CDR3 областям, представленным в SEQ ID NO:51.
16. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, по меньшей мере на девяносто процентов идентичные H-CDR1, H-CDR2 и H-CDR3 областям, представленным в SEQ ID NO:21, и L-CDR1, L-CDR2 и L-CDR3 области, по меньшей мере на девяносто процентов идентичные L-CDR1, L-CDR2 и L-CDR3 областям, представленным в SEQ ID NO:51.
17. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:21, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:51.
18. Выделенное антитело или его функциональный фрагмент по п.17, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:21.
19. Выделенное антитело или его функциональный фрагмент по п.17, содержащие вариабельную легкую цепь, представленную в SEQ ID NO:51.
20. Выделенное антитело или его функциональный фрагмент по п.17, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:21, и вариабельную легкую цепь, представленную в SEQ ID NO:51.
21. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:22, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:52.
22. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:22, и вариабельную легкую цепь, представленную в SEQ ID NO:52.
23. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:23, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:53.
24. Выделенное антитело или его функциональный фрагмент по п 1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:23, и вариабельную легкую цепь, представленную в SEQ ID NO:53.
25. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:24, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:54.
26. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:24, и вариабельную легкую цепь, представленную в SEQ ID NO:54.
27. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:25, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:55.
28. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:25, и вариабельную легкую цепь, представленную в SEQ ID NO:55.
29. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:26, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:56.
30. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:26, и вариабельную легкую цепь, представленную в SEQ ID NO:56.
31. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:27, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:57.
32. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:27, и вариабельную легкую цепь, представленную в SEQ ID NO:57.
33. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:28, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:58.
34. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:28, и вариабельную легкую цепь, представленную в SEQ ID NO:58.
35. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:29, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:59.
36. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO: 29, и вариабельную легкую цепь, представленную в SEQ ID NO: 59.
37. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:30, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:60.
38. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:30, и вариабельную легкую цепь, представленную в SEQ ID NO:60.
39. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:92, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:51.
40. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:92, и вариабельную легкую цепь, представленную в SEQ ID NO:51.
41. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:93, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:51.
42. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:93, и вариабельную легкую цепь, представленную в SEQ ID NO:51.
43. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:94, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:51.
44. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:94, и вариабельную легкую цепь, представленную в SEQ ID NO:51.
45. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:95, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:51.
46. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:95, и вариабельную легкую цепь, представленную в SEQ ID NO:51.
47. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:96, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:51.
48. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:96, и вариабельную легкую цепь, представленную в SEQ ID NO:51.
49. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:97, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:51.
50. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:97, и вариабельную легкую цепь, представленную в SEQ ID NO:51.
51. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:98, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:51.
52. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:98, и вариабельную легкую цепь, представленную в SEQ ID NO:51.
53. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:99, и L-CDR1, L -CDR2 и L-CDR3 области, представленные в SEQ ID NO:51.
54. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:99, и вариабельную легкую цепь, представленную в SEQ ID NO:51.
55. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:100, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:51.
56. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:100, и вариабельную легкую цепь, представленную в SEQ ID NO:51.
57. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:101, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:51.
58. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:101, и вариабельную легкую цепь, представленную в SEQ ID NO:51.
59. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:102, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:51.
60. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:102, и вариабельную легкую цепь, представленную в SEQ ID NO:51.
61. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:103, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:51.
62. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:103, и вариабельную легкую цепь, представленную в SEQ ID NO:51.
63. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:104, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:51.
64. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:104, и вариабельную легкую цепь, представленную в SEQ ID NO:51.
65. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:105, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:52.
66. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:105, и вариабельную легкую цепь, представленную в SEQ ID NO:52.
67. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:106, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:52.
68. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:106, и вариабельную легкую цепь, представленную в SEQ ID NO:52.
69. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:22, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:109.
70. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:22, и вариабельную легкую цепь, представленную в SEQ ID NO:109.
71. Выделенное антитело или его функциональный фрагмент по п.1, содержащие H-CDR1, H-CDR2 и H-CDR3 области, представленные в SEQ ID NO:22, и L-CDR1, L-CDR2 и L-CDR3 области, представленные в SEQ ID NO:110.
72. Выделенное антитело или его функциональный фрагмент по п.1, содержащие вариабельную тяжелую цепь, представленную в SEQ ID NO:22, и вариабельную легкую цепь, представленную в SEQ ID NO:110.
73. Выделенная последовательность нуклеиновой кислоты, кодирующая антитело или его функциональный фрагмент по любому из пп.1-3.
74. Вектор экспрессии, содержащий последовательность нуклеиновой кислоты по п.73.
75. Выделенная клетка, содержащая вектор по п.74, которая продуцирует антитело или его функциональный фрагмент, которые специфичны к CD38.
76. Выделенная клетка по п.75, где указанная клетка является бактериальной.
77. Выделенная клетка по п.75, где указанная клетка представляет собой клетку млекопитающего.
78. Фармацевтическая композиция, обладающая свойствами специфичного связывания с антигеном CD38, содержащая антитело или его функциональный фрагмент по любому из пп.1-3 в терапевтически эффективном количестве и фармацевтически приемлемый носитель или эксципиент для них.
79. Способ лечения расстройства или состояния, связанного с нежелательным присутствием CD38+ клеток, включающий введение субъекту, нуждающемуся в этом, эффективного количества фармацевтической композиции по п.78.
80. Способ по п.79, где указанное расстройство или состояние представляет собой гематологическое заболевание.
81. Способ по п.80, где указанное гематологическое заболевание выбрано из перечня: множественной миеломы, хронического лимфолейкоза, хронического миелоидного лейкоза, острого миелоидного лейкоза и острого лимфолейкоза.
82. Способ по п.79, где указанное расстройство или состояние представляет собой воспалительное заболевание.
83. Способ по п.82, где указанное воспалительное заболевание выбрано из перечня: ревматоидного артрита и системной красной волчанки.
84. Способ индукции специфичного цитолиза опухолевых клеток, экспрессирующих CD38, где указанный специфичный цитолиз происходит посредством перекрестного сшивания CD38, включающий стадию инкубации указанных клеток в присутствии достаточного количества выделенного человеческого или гуманизированного антитела против CD38 или его функционального фрагмента, как определено в любом из пп.1-3.
85. Способ выявления CD38 в эритроците, экспрессирующем CD38, включающий стадии:
(1) предоставления возможности человеческому или гуманизированному антителу против CD38 или его функциональному фрагменту по любому из пп.1-3 вступить в контакт с указанным эритроцитом, экспрессирующим CD38, и
(2) выявления специфичного связывания указанного человеческого или гуманизированного антитела против CD38 или его функционального фрагмента с указанными эритроцитами, экпрессирующими CD38, где указанное антитело или его функциональный фрагмент также способны специфично связывать человеческий CD38 из клетки или ткани, отличных от эритроцитов человека.
86. Способ по п.85, где указанное антитело или его функциональный фрагмент также способны специфично связывать человеческий CD38 из клетки, представляющей собой лимфоцит человека.
87. Диагностическая композиция, содержащая антитело или его функциональный фрагмент, которые специфичны к CD38, по любому из пп.1-3.
| US 20020164788 А1, 07.11.2002 | |||
| Способ модификации синтетического латекса | 1984 |
|
SU1174440A1 |
| US 2004105862 А, 03.06.2004 | |||
| Штамм гибридных культивируемых клеток животных MUS мUSсULUS L, используемый для получения моноклональных антител к антигену СД38 кортикальных тимоцитов | 1988 |
|
SU1595902A1 |
Авторы
Даты
2011-08-10—Публикация
2006-10-12—Подача