Изобретение относится к новому химическому соединению, конкретно к сложному оксиду молибдена состава (VO)0.09V0.18Mo0.82O3·0.54H2O, который может быть использован в качестве электродного материала для определения концентрации V4+ в растворе в присутствии V5+, а также к способу его получения.
В настоящее время для количественного определения ионов V4+ в аналитической химии используют титриметрический способ анализа (Антонович В.П., Чивирева Н.А., Пресняк И.С. "Методы определения форм ванадия в разных степенях окисления при совместном присутствии", Журнал аналитической химии,. 1997, т.52, №6, с.566-571). Определение V+4 проводят по следующей схеме: навеску исследуемого вещества растворяют в серной кислоте, а затем титруют ванадий (IV) раствором KMnO4 до появления бледно-розовой окраски, не исчезающей в течение 2 минут. Содержание ванадия (IV) (вес.%) определяют по формуле
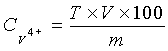 ,
,
где T - предварительно установленный по стандартному образцу титр раствора KMnO4;
V - количество KMnO4, пошедшее на титрование, мл;
m - навеска исследуемого вещества, г.
Недостатком известного способа является необходимость соблюдения кислотности раствора, так как процесс окисления ванадия (IV) происходит с заметной скоростью только в слабокислой среде (~ 0,1 М H2SO4), при меньшей кислотности (pH 2) ванадий (IV) начинает окисляться кислородом воздуха, а не KMnO4. Кроме того, перед каждым определением ванадия (IV) необходимо проверять титр раствора перманганата калия. Наличие в определяемом растворе любых восстановителей и вольфрама также мешают титрованию.
Известен также способ комплексометрического определения ванадия (IV) с раствором комплексона (Музгин В.Н., Хамзина Л.Б., Золотавин В.Л., Безруков И.Я. "Аналитическая химия ванадия". М.: Наука, 1981, с.216). В известном способе к раствору, содержащему ванадий (IV), добавляют по каплям индикатор N-бензоил-N-фенилгидроксиламин в 95%-ном этаноле. Титруют раствором комплексона III до перехода красной окраски раствора в голубую.
Недостатком известного способа является необходимость поддержания кислотности раствора в интервале значений pH 3-3,5; так как только в этом интервале значений происходит взаимодействие ванадия (IV) с комплексоном III в присутствии индикатора N-бензоил-N-фенилгидроксиламина. Кроме того, комплексометрия используется только в том случае, если другие компоненты анализируемого раствора также определяют комплексометрически. В обоих известных способах определения ванадия (IV) существует индикаторная ошибка, связанная с установлением точки эквивалентности.
Таким образом, перед авторами стояла задача разработать электродный материал, обладающий ионоселективными свойствами в отношении ванадия (IV), который бы позволил просто и надежно определять концентрацию ванадия (IV) в растворе. Причем предлагаемый материал должен быть селективен в отношении ванадия (IV) в присутствии ионов ванадия (V).
Поставленная задача решена путем применения нового химического соединения сложного оксида молибдена состава (VO)0.09V0.18Mo0.82O3·0.54H2O в качестве электродного материала для селективного определения концентрации ванадия (IV) в растворах, содержащих пятивалентный ванадий.
Поставленная задача также решена в способе получения сложного оксида молибдена состава (VO)0.09V0.18Mo0.82O3·0.54H2O, включающем приготовление раствора порошка металлического молибдена в водном растворе пероксида водорода, добавление к полученному раствору ванадила сульфата гидрата при мольном соотношении Мо:V=1:0.5, с последующей гидротермальной обработкой смеси при температуре 140-170°С в течение 4-6 дней, фильтрацию, промывание и сушку.
В настоящее время в патентной и научно-технической литературе не описано новое химическое соединение предлагаемого состава, структуры и морфологии, а также способ его получения.
Новое соединение состава (VO)0.09V0.18Mo0.82O3·0.54H2O может быть получено следующим образом. Порошок металлического молибдена растворяют в водном растворе пероксида водорода в течение 5-8 часов, к полученному раствору добавляют сульфат ванадила гидрат VO·SO4·3H2O при мольном соотношении Mo6+:V4+=1:0,5. Полученную смесь помещают в автоклав и выдерживают при температуре 140-170°С в течение 4-6 дней. Полученный продукт фильтруют, промывают водой и сушат при комнатной температуре на воздухе. Контроль фазовой однородности и морфологии полученного продукта проводят соответственно методами рентгенофазового анализа (РФА) и сканирующей электронной микроскопии (СЭМ). По данным РФА и химического анализов продукт является сложным оксидом состава (VO)0.09V0.18Mo0.82O3·0.54H2O гексагональной сингонии. Согласно электронно-микроскопическим исследованиям частицы сложного оксида имеют форму стержней с гексагональным поперечным сечением диаметром 1-2 мкм и длиной до 45 мкм. Исследование ионселективной функции электродноактивного материала в интервале концентраций 3<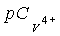 <5 и кислотности среды 4<рН<6 проводили путем измерения ЭДС гальванического элемента типа
<5 и кислотности среды 4<рН<6 проводили путем измерения ЭДС гальванического элемента типа
электрод | исследуемый раствор || KCl нас., AgCl |Ag
с использованием иономера И-130.2М.
Исследования, проведенные авторами, позволили сделать вывод, что новое химическое соединение состава (VO)0.09V0.18Mo0.82O3·0.54H2O, обладающее свойством, которое позволяет использовать его в качестве электродного материала для селективного определения концентрации ванадия (IV) в растворах, содержащих пятивалентный ванадий, может быть получено только при условии соблюдения параметров процесса синтеза, заявляемых в предлагаемом способе. Так, использование раствора пероксокомплекса молибдена, полученного растворением порошка металлического молибдена в H2O2, позволяет получить конечный продукт без посторонних примесей. Экспериментальным путем было установлено мольное соотношение Мо6+ и ванадия V4+. Так, при несоблюдении заявленного интервала мольного соотношения, а также при снижении температуры гидротермальной обработки менее 140°С или при повышении ее выше 170°С и при выходе за заявленные значения временного интервала, в конечном продукте появляются примесные фазы оксидов молибдена и ванадия. При этом четырехвалентный ванадий окисляется до пятивалентного ванадия, стержневая морфология продукта не сохраняется.
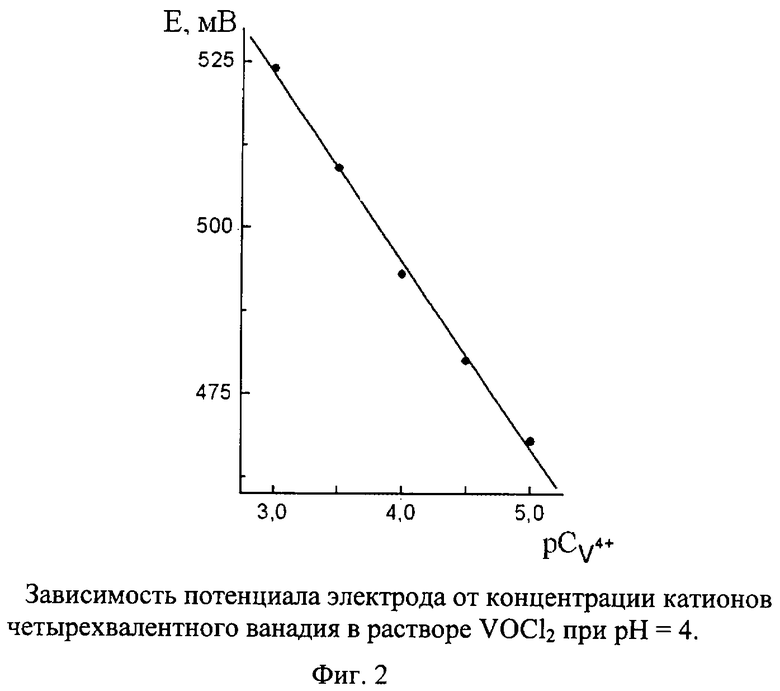
Пример 1. Берут 0.5 г порошка металлического молибдена и растворяют его в 10 мл водного раствора 15%-ного H2O2. К полученному раствору добавляют 0.56 г VSO4·3H2O с содержанием ванадия 19.9 мас.% (мольное соотношение Мо6+:V4+=1:0.5). Затем перемешивают до полного растворения сульфат ванадила. Полученную смесь помещают в автоклав, нагревают до 140°С и при этой температуре выдерживают 6 дней. После этого автоклав охлаждают до комнатной температуры, полученный продукт фильтруют, промывают водой и сушат на воздухе при комнатной температуре. По данным химического, рентгенофазового и электронно-микроскопического анализов полученный продукт имеет состав (VO)0.09V0.18Mo0.82O3·0.54H2O гексагональной сингонии с параметрами кристаллической решетки а=10.586 Å, с=3.698 Å, V=358.87 Å3 и состоит из микростержней диаметром 1-2 мкм, длиной до 45 мкм. На рис.1 приведено изображение микростержней, полученное на сканирующем электронном микроскопе высокого разрешения. На рис.2 представлена зависимость потенциала электрода от концентрации катионов четырехвалентного ванадия в растворе VOCl2 при рН=4. При рН 4 в интервале концентраций 3<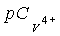 <5 угловой коэффициент электродной функции близок к теоретическому значению и равен 28±2 мВ/
<5 угловой коэффициент электродной функции близок к теоретическому значению и равен 28±2 мВ/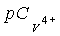 . Потенциал электрода не реагирует на изменение концентрации ионов пятивалентного ванадия. Следовательно, сложный оксид молибдена является электродным материалом для селективного определения ионов четырехвалентного ванадия в присутствии пятивалентного ванадия.
. Потенциал электрода не реагирует на изменение концентрации ионов пятивалентного ванадия. Следовательно, сложный оксид молибдена является электродным материалом для селективного определения ионов четырехвалентного ванадия в присутствии пятивалентного ванадия.
Пример 2. Берут 0.5 г порошка металлического молибдена и растворяют его в 10 мл водного раствора 15%-ного H2O2. К полученному раствору добавляют 0.56 г VOSO4·3H2O с содержанием ванадия 19.9 мас.% (мольное соотношение Мо6+:V4+=1:0.5). Затем перемешивают до полного растворения сульфат ванадила. Полученную смесь помещают в автоклав, нагревают до 170°С и при этой температуре выдерживают 4 дней. После этого автоклав охлаждают до комнатной температуры, полученный продукт фильтруют, промывают водой и сушат на воздухе при комнатной температуре. По данным химического, рентгенофазового и электронно-микроскопического анализов полученный продукт имеет состав (VO)0.09V0.18Mo0.82O3·0.54H2O гексагональной сингонии с параметрами кристаллической решетки а=10.586 Å, с=3.698 Å, V=358.87 Å3 и состоит из микростержней диаметром 1-2 мкм, длиной до 45 мкм. При рН 5 в интервале концентраций 3<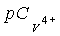 <5 угловой коэффициент электродной функции близок к теоретическому значению и равен 27±2 мВ/
<5 угловой коэффициент электродной функции близок к теоретическому значению и равен 27±2 мВ/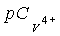 . Потенциал электрода не реагирует на изменение концентрации ионов пятивалентного ванадия. Следовательно, сложный оксид молибдена является электродным материалом для селективного определения ионов четырехвалентного ванадия в присутствии пятивалентного ванадия.
. Потенциал электрода не реагирует на изменение концентрации ионов пятивалентного ванадия. Следовательно, сложный оксид молибдена является электродным материалом для селективного определения ионов четырехвалентного ванадия в присутствии пятивалентного ванадия.
Пример 3. Берут 0.5 г порошка металлического молибдена и растворяют его в 10 мл водного раствора 15%-ного H2O2. К полученному раствору добавляют 0.56 г VOSO4·3H2O с содержанием ванадия 19.9 мас.% (мольное соотношение Мо6+:V4+=1:0.5). Затем перемешивают до полного растворения сульфат ванадила. Полученную смесь помещают в автоклав, нагревают до 160°С и при этой температуре выдерживают 5 дней. После этого автоклав охлаждают до комнатной температуры, полученный продукт фильтруют, промывают водой и сушат на воздухе при комнатной температуре. По данным химического, рентгенофазового и электронно-микроскопического анализов полученный продукт имеет состав (VO)0.09V0.18Mo0.82O3·0.54H2O гексагональной сингонии с параметрами кристаллической решетки а=10.586 Å, с=3.698 Å, V=358.87 Å3 и состоит из микростержней диаметром 1-2 мкм, длиной до 45 мкм. При рН 6 в интервале концентраций 3<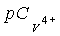 <5 угловой коэффициент электродной функции близок к теоретическому значению и равен 26±2 мВ/
<5 угловой коэффициент электродной функции близок к теоретическому значению и равен 26±2 мВ/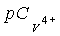 . Потенциал электрода не реагирует на изменение концентрации ионов пятивалентного ванадия. Следовательно, сложный оксид молибдена является исонселективным материалом для селективного определения ионов четырехвалентного ванадия в присутствии ионов пятивалентного ванадия.
. Потенциал электрода не реагирует на изменение концентрации ионов пятивалентного ванадия. Следовательно, сложный оксид молибдена является исонселективным материалом для селективного определения ионов четырехвалентного ванадия в присутствии ионов пятивалентного ванадия.
Таким образом, авторами получен новый смешанный оксид состава (VO)0.09V0.18Mo0.82O3·0.54H2O гексагональной сингонии в виде микростержней, обладающий ионселективными свойствами, который может быть использован в качестве электродного материала для селективного определения ионов четырехвалентного ванадия в присутствии ионов пятивалентного ванадия.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИОНОСЕЛЕКТИВНЫЙ МАТЕРИАЛ ДЛЯ ОПРЕДЕЛЕНИЯ ИОНОВ АММОНИЯ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2542260C2 |
| Способ получения триоксида молибдена h-MoO | 2023 |
|
RU2814773C1 |
| Способ получения триоксида молибдена h-MoO | 2023 |
|
RU2799648C1 |
| Оксидные ванадиевые бронзы редкоземельных элементов в качестве электродноактивного материала и способ их получения | 1983 |
|
SU1110751A1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИОННОГО ЭЛЕКТРОДНОГО МАТЕРИАЛА НА ОСНОВЕ КОБАЛЬТ ВАНАДИЕВОГО ОКСИДА И ОКСИДНЫХ СОЕДИНЕНИЙ МОЛИБДЕНА | 2014 |
|
RU2570070C1 |
| Способ получения катодного материала состава LiV(PO) | 2023 |
|
RU2801381C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОИГЛ ОКСИДНОЙ ВАНАДИЕВОЙ БРОНЗЫ НАТРИЯ | 2013 |
|
RU2549421C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭПСИЛОН-КАПРОЛАКТАМА | 2002 |
|
RU2275358C2 |
| СПОСОБ ОЧИСТКИ УГЛЕВОДОРОДНОГО СЫРЬЯ ОТ СЕРАОРГАНИЧЕСКИХ СОЕДИНЕНИЙ | 1998 |
|
RU2125080C1 |
| Способ получения наночастиц диоксида молибдена | 2021 |
|
RU2767917C1 |

Изобретение относится к сложному оксиду молибдена состава (VO)0.09V0.18Mo0.82O3·0.54Н2O, а также к способу его получения. Сложный оксид молибдена состава (VO)0.09V0.18Mo0.82O3·0.54Н2O в качестве электродного материала для селективного определения концентрации ванадия (IV) в растворах, содержащих ванадий (V). Способ получения сложного оксида молибдена состава (VO)0.09V0.18Mo0.82O3·0.54Н2O включает приготовление раствора порошка металлического молибдена в водном растворе пероксида водорода, добавление к полученному раствору ванадила сульфата гидрата при мольном соотношении Мо6+:V4+=1:0.5, с последующей гидротермальной обработкой смеси при температуре 140-170°С в течение 4-6 дней, фильтрацию, промывание и сушку. Заявленный смешанный оксид состава (VO)0.09V0.18Mo0.82O3·0.54H2O гексагональной сингонии в виде микростержней, обладающий ионоселективными свойствами, может быть использован в качестве электродного материала для селективного определения ионов четырехвалентного ванадия в присутствии ионов пятивалентного ванадия. 2 н.п. ф-лы, 2 ил.
1. Сложный оксид молибдена состава (VO)0,09V0,18Mo0,82O3·0,54H2O в качестве электродного материала для селективного определения концентрации ванадия (IV) в растворах, содержащих ванадий (V).
2. Способ получения сложного оксида молибдена состава (VO)0,09V0,18Mo0,82O3·0,54H2O, включающий приготовление раствора порошка металлического молибдена в водном растворе пероксида водорода, добавление к полученному раствору ванадила сульфата гидрата при мольном соотношении Mo6+:V4+=1:0,5, с последующей гидротермальной обработкой смеси при температуре 140-170°С в течение 4-6 дней, фильтрацию, промывание и сушку.
| МУРЗИН В.Н | |||
| и др | |||
| Аналитическая химия ванадия | |||
| - М.: Наука, 1981, с.38 | |||
| ГИЛЛЕБРАНД В.Ф | |||
| и др | |||
| Практическое руководство по неорганическому анализу | |||
| - М.: Химия, 1966, с.515-519 | |||
| ГОДОВИКОВ А.А | |||
| Минералогия | |||
| - М.: Недра, 1983, с.193, 212, 214 | |||
| DE 10321398 A1, 27.05.2004. |
Авторы
Даты
2012-03-27—Публикация
2010-06-11—Подача