Изобретение относится к способу получения наночастиц, в частности, диоксида молибдена MoO2, который может быть использован в качестве селективного катализатора окисления олефинов (Bento A., Sanches A., Medina E. et al. MoO2 nanoparticles as highly efficient olefin epoxidation catalysts // Appl. Catal. A: Gen. 2015 V. 504. P. 399-407), ион-электронного преобразователя твердофазных ионоселективных электродов для определения ионов калия в растворе (Zeng X., Qin W. A solid-contact potassium-selective electrode with MoO2 microspheres as ion-to-electron transducer // Anal. Chim. Acta 2017. V. 982. P. 72-77), эффективного анодного материала литиевых источников тока (Zhang X., Hou Z., Li X. et al. MoO2 nanoparticles as high capacity intercalation anode material for long-cycle lithium ion battery // Electrochim. Acta 2016. V. 213. P. 416-422), в качестве анодных материалов суперконденсаторов на основе водных электролитов (Li X., Shao J., Li J. et al. Ordered mesoporous MoO2 as a high-performance anode material for aqueous supercapacitors // J. Power Sources 2013. V. 237. P. 80-83), материала для фототермической терапии онкологических заболеваний (Liu W., Li X., Li W. et al. Highly stable molybdenum dioxide nanoparticles with strong plasmon resonance are promising in photothermal cancer therapy // Biomaterials 2018. V. 163. P. 43-54), газосенсорного материала для определения концентрации паров этанола и ацетона (Yunusi T., Yang C., Cai W. et al. Synthesis of MoO3 submicron belts and MoO2 submicron spheres via polyethylene glycol-assisted hydrothermal method and their gas sensing properties // Ceramics Internat. 2013. V. 39. P. 3435-3439).
Известен способ получения диоксида молибдена MoO2, включающий добавление к водной суспензии ацетилацетоната молибдена концентрацией 0.1-0.5 мМ лимонной кислоты в молярном соотношении (5÷15):1. Затем реакционную смесь помещают в автоклав и осуществляют гидротермальную обработку при температуре 150-180°С в течение 8-12 ч с последующим отделением осадка центрифугированием. По данным рентгенофазового анализа (РФА) полученный продукт индексируется как диоксид молибдена моноклинной модификации. Согласно сканирующей электронной микроскопии (СЭМ), полученный продукт образован частицами диаметром 100-200 нм. Величина удельной поверхности полученного порошка MoO2 составляет 98.4 м2/г. (Патент CN 110182847, МПК B01Y 23/28, B82Y 40/00, C01G 39/02, 2019 год).
Недостатком известного способа является использование в качестве источника молибдена нерастворимого в воде ацетилацетоната молибдена, что может привести к формированию в продуктах реакции в качестве примесной фазы оксида молибдена общей формулы MoO3-x (0 < x < 1). Кроме того, использование лимонной кислоты в качестве хелатообразующего агента не позволяет получать MoO2 с высокой удельной поверхностью.
Известен способ получения пленок диоксида молибдена MoO2, включающий растворение в водно-спиртовом растворе при объемном соотношении вода : этанол = 30:(0.1÷0.3) при перемешивании молибдата аммония с добавлением 30 %-ного раствора пероксида водорода Н2О2. Затем реакционную смесь помещают в автоклав, на дно которого помещают молибденовую сеточку с размерами пор 2-4 см, и осуществляют гидротермальную обработку при температуре 150-230°С в течение 6-15 ч. После чего продукт промывают водой и сушат при 60°С в течение 1 ч. Согласно СЭМ полученный порошок MoO2 образован частицами диаметром 10-50 нм и длиной 100-200 нм. (Патент CN 110359061, МПК B82Y 30/00, B82Y 40/00, C25B 1/04, C25B 11/06, 2019 год).
Недостатком известного способа является использование в качестве компонента реакционной смеси остро токсичного молибдата аммония, который при попадании в органы дыхания и пищеварения откладывается в костях, печени, почках. Кроме того, молибдат аммония является пожаровзрывоопасным веществом третьего класса опасности. Известный способ предполагает получение массива тонких пленок с морфологией нанопроволок или нанопластин, что ограничивает применение получаемого материала только в производстве электрокатализаторов.
Известен способ получения диоксида молибдена MoO2, включающий добавление к раствору парамолибдата аммония (NH4)6Mo7O24⋅4H2O при перемешивании в течение 1-8 ч лимонной кислоты C6H8O7⋅H2O. Затем реакционную смесь помещают в автоклав и осуществляют гидротермальную обработку при температуре 160-200°С в течение 40-60 ч. После чего продукт отделяют центрифугированием, промывают водой, этанолом и сушат. Согласно СЭМ полученный порошок MoO2 образован частицами с морфологией нанотрубок диаметром 1-8 нм и длиной 2-7 мкм. (Патент CN 108585046, МПК C01G 39/06, 2018 год).
Недостатком известного способа является использование в качестве компонента реакционной смеси остро токсичного и пожаровзрывоопасного молибдата аммония, который при попадании в организм человека накапливается в костях, печени, почках. Кроме того, недостатком известного способа является длительность процесса (до 68 ч).
Известен способ получения диоксида молибдена MoO2 путем восстановления триоксида молибдена MoO3 в инертной атмосфере при повышенной температуре. В известном способе в воде растворяют 0.01-1 М порошка одного из источника молибдена (молибденовой кислоты H2MoO4, молибдата аммония (NH4)6Mo7O24⋅4H2O, молибдата натрия Na2MoO4) с последующим добавлением к полученному раствору одной из карбоновых кислот или ее производной (цитрата натрия Na3C6H5O7, лимонной кислоты C6H8O7⋅H2O, аскорбиновой кислоты C6H8O6, бензойной кислоты C7H6O2) при молярном соотношении карбоновая кислота или ее производная : источник молибдена = (0.5÷2) : 1, установлением рН раствора равного 0-6 путем добавления при перемешивании раствора концентрированной соляной кислоты HCl, а затем добавлением одного из предложенного растворителя (хлороформа CHCl3, толуола C7H8, ксилола C8H10, олеиновой кислоты C18H34O2) в молярном соотношении растворитель : источник молибдена = (1÷3) : 1. Полученную реакционную смесь загружают в автоклав, выдерживают при температуре 150-200°С в течение 3-48 ч, перемешивая со скоростью 300-600 мин-1, а затем осадок центрифугируют, промывают, сушат при 70°С. В результате образуется триоксид молибдена MoO3. Затем продукт подвергают отжигу в инертной атмосфере (в токе аргона, или азота, или смеси водорода и аргона, или смеси моно- и диоксида углерода) при температуре 200-800°С в течение 0.5-6 ч. По данным РФА состав полученного продукта индексируется как MoO2 моноклинной сингонии (JCPDS 65-5787). Согласно СЭМ размер частиц MoO2 составляет 10-25 нм. Величина удельной поверхности полученного порошка MoO2 составляет 245-364 м2/г. (Патент CN 106711432, МПК B82Y 30/00, B82Y 40/00, H01M 10/0525, H01M 4/48, 2017 год).
Недостатками известного способа являются многостадийность, а также длительность процесса (до 54 ч). Кроме того, известный способ не позволят получить чистую фазу диоксида молибдена MoO2. На представленной рентгенограмме порошка конечного продукта, полученного по известному способу, фиксируются дифракционный пики, принадлежащие основной фазе MoO2, а также триоксиду молибдена MoO3. Следующие дополнительный дифракционные пики, представленные на рентгенограмме порошка конечного продукта, полученного по известному способу, следует отнести к орторомбической модификации триоксида молибдена MoO3 12.7°, 23.3°, 27.4°, 33.7°, 38.6° и 46.3° индексируемые как плоскости (020), (110), (021), (111), (131) и (210), соответственно. Таким образом, известный способ не позволят получить чистую фазу диоксида молибдена MoO2, являющегося уникальным материалом, обладающим высокой химической стабильностью в кислых средах, плотностью (6.47 г/см3) и металлической проводимостью (электросопротивление объемного MoO2 равно 8.8⋅10-5 Ом). Наличие примеси MoO3 не позволяет использовать MoO2 в качестве эффективного анодного материала литиевых источников тока и суперконденсаторов с высокими электрохимическими параметрами.
Известен способ получения диоксида молибдена MoO2, включающий растворение в воде порошка одного из источника молибдена (молибдата натрия, молибдата аммония, молибдата калия) с использованием ультразвука в течение 10-60 мин с последующим добавлением к полученному раствору одной из кислот (соляной кислоты, серной кислоты, азотной кислоты, хлорной кислоты, муравьиной кислоты, уксусной кислоты, пропионовой кислоты, масляной кислоты, валериановой кислоты, капроновой кислоты, энантовой кислоты, каприловой кислоты), взятой в молярном соотношении источник молибдена : кислота = (5÷20) : 1. К образующейся молибденовой кислоте добавляют 20 М раствор одной из перечисленных выше кислот, взятой в молярном соотношении кислота : молибденовая кислота = 1:(2÷10) с последующим добавлением (9-8) мМ раствора одной из карбоновых кислот (молочной кислоты, щавелевой кислоты, лимонной кислоты), взятых при молярном соотношении карбоновая кислота : молибденовая кислота = 1:(1÷15), после чего реакционную смесь подвергают ультразвуковой обработке в течение 10-60 мин. Затем полученную суспензию помещают в автоклав и выдерживают при температуре 120-300°С в течение 8-48 ч. Конечный продукт промывают этанолом, водой и сушат на воздухе. Согласно СЭМ частицы MoO2 имеют морфологию подобную сферам диаметром 150-300 нм. (Патент CN 111825118, МПК B01J 23/28, B01J 35/00, B01J 35/02, B01J 35/10, C01G 39/02, 2020 год).
Недостатком известного способа является сложность процесса за счет использования 2-х стадийной ультразвуковой обработки, не обеспечивающей, в частности полную гомогенизацию реакционной массы вследствие неравномерного воздействия ультразвуковых колебаний на обрабатываемую смесь. Кроме того, в способе используется большое количество реагентов, что также усложняет процесс.
Наиболее близким к предлагаемому способу является способ получения диоксида молибдена MoO2, в котором порошок молибдата аммония (NH4)6Mo7O24⋅4H2O и винную кислоту C4H6O6 растворяют в воде, добавляют 3 М раствор соляной кислоты HCl до установления рН раствора 0-1.5, после чего реакционную массу подвергают ультразвуковой обработке в течение 10-30 мин. Образующуюся суспензию загружают в автоклав и выдерживают в гидротермальных условиях при температуре 180°С в течение 12-48 ч. Полученный осадок фильтруют, промывают водой, этанолом и сушат при 60°С. Согласно СЭМ полученный порошок MoO2 образован частицами диаметром менее 10 нм (Патент CN 101780981, МПК C01G 39/02, 2010 год). (прототип).
Недостатком известного способа является его сложность, во-первых, за счет использования ультразвуковой обработки, во-вторых, за счет использования в качестве компонента реакционной смеси остро токсичного и пожаровзрывоопасного молибдата аммония, который при попадании в организм человека накапливается в костях, печени, почках. Кроме того, при использовании известного способа порошок MoO2 формируется однородными частицами размером менее 10 нм, для которых не характерно наличие мезопористой структуры, которая обусловливает высокую удельную поверхность.
Таким образом, перед авторами стояла задача разработать более простой и технологичный способ получения диоксида молибдена MoO2, позволяющий исключить использование токсичных соединений, наряду с достаточно высокими значениями удельной поверхности за счет получения мезопористой структуры.
Поставленная задача решена в предлагаемом способе получения наночастиц диоксида молибдена MoO2, включающем гидротермальную обработку исходного раствора, содержащего источник молибдена и винную кислоту, с последующим промыванием и сушкой, в котором исходный раствор получают добавлением порошка металлического молибдена к 30 %-ому раствору пероксида водорода в соотношении, равном т : ж = 1:(30÷40), с последующим добавлением винной кислоты при молярном соотношении молибден : винная кислота = 1:(1÷2).
В настоящее время из патентной и научно-технической литературы не известен способ получения диоксида молибдена MoO2 с использованием в качестве исходного раствора раствор, полученный добавлением порошка металлического молибдена к 30 %-ому раствору пероксида водорода в соотношении, равном т : ж = 1:(30÷40), с последующим добавлением винной кислоты при молярном соотношении молибден : винная кислота = 1:(1÷2).
Исследования, проведенные авторами, позволили сделать вывод, что диоксид молибдена MoO2 может быть получен простым и технологичным способом при условии взаимодействия металлического молибдена и пероксида водорода с получением пероксомолибденовой кислоты H2MoO5, в присутствии винной кислоты C4H6O6, являющейся мягким восстановительным агентом. Это объясняется синергическим эффектом, достигаемым в результате использования водного раствора пероксида водорода, молибдена и винной кислоты. Пероксид водорода, проявляющий свойства окислителя в растворах с 30% -ной концентрацией основного вещества, легко окисляет металлический молибден Mo до Mo6+ с образованием пероксомолибденовой кислоты состава H2MoO5. Винная кислота, относящаяся к оксикарбоновым кислотам и отличающаяся наличием двух карбоксильных групп (О=С-ОН) и двух гидроксильных группы (С-ОН), проявляет свойства, характерные для спиртов, участвуя в окислительно-восстановительных реакциях. При этом, как показали, экспериментальные исследования, использование винной кислоты позволяет проводить мягкое восстановление ионов Mo6+ до Mo4+. Кроме того, использование в качестве источника молибдена пероксомолиденовой кислоты и винной кислоты, как мягкого восстановителя, позволяет получать диоксид молибдена MoO2 без примесей для использования конечного продукта как материала. Дополнительно, проведение синтеза в условиях жидкофазного гомогенного взаимодействия химических ингредиентов обеспечивает формирование диоксида молибдена MoO2 с мезопористой структурой, обеспечивающей достаточно высокую удельную поверхность.
Такой подход к осуществлению процесса получения диоксида молибдена MoO2 обеспечивает простоту и технологичность его выполнения, а также гарантирует отсутствие возможных посторонних примесей в конечном продукте, что в конечном итоге повышает эффективность использования диоксида молибдена как материала.
Авторами экспериментальным путем было установлено, что существенным фактором, определяющим состав и структуру конечного продукта является соблюдения соотношения порошка металлического молибдена к 30 %-ому раствору пероксида водорода в соотношении, равном т : ж = 1:(30÷40), при уменьшении соотношения менее, чем 1 : 30, дополнительно с основной фазой MoO2 наблюдается образование оксидов молибдена с переменной валентностью, так называемых фаз Магнели, общей формулы MonO2n-1, при увеличении соотношения более, чем 1:40, наблюдается образование в качестве примеси триоксида молибдена MoO3. Так же существенным фактором является молярное соотношение молибден : винная кислота = 1:(1÷2). При уменьшении молярного соотношения исходных компонентов реакционной массы (содержание винной кислоты по отношению к молибдену меньше, чем 1) в продуктах реакции наблюдаются в качестве примеси Mo4O11 и MoO3. При увеличении молярного соотношения исходных компонентов реакционной массы (содержание винной кислоты по отношению к молибдену больше, чем 2) дополнительно с основной фазой MoO2 образуются оксиды молибдена с переменной валентностью (фазы Магнели) общей формулы MonO2n-1.
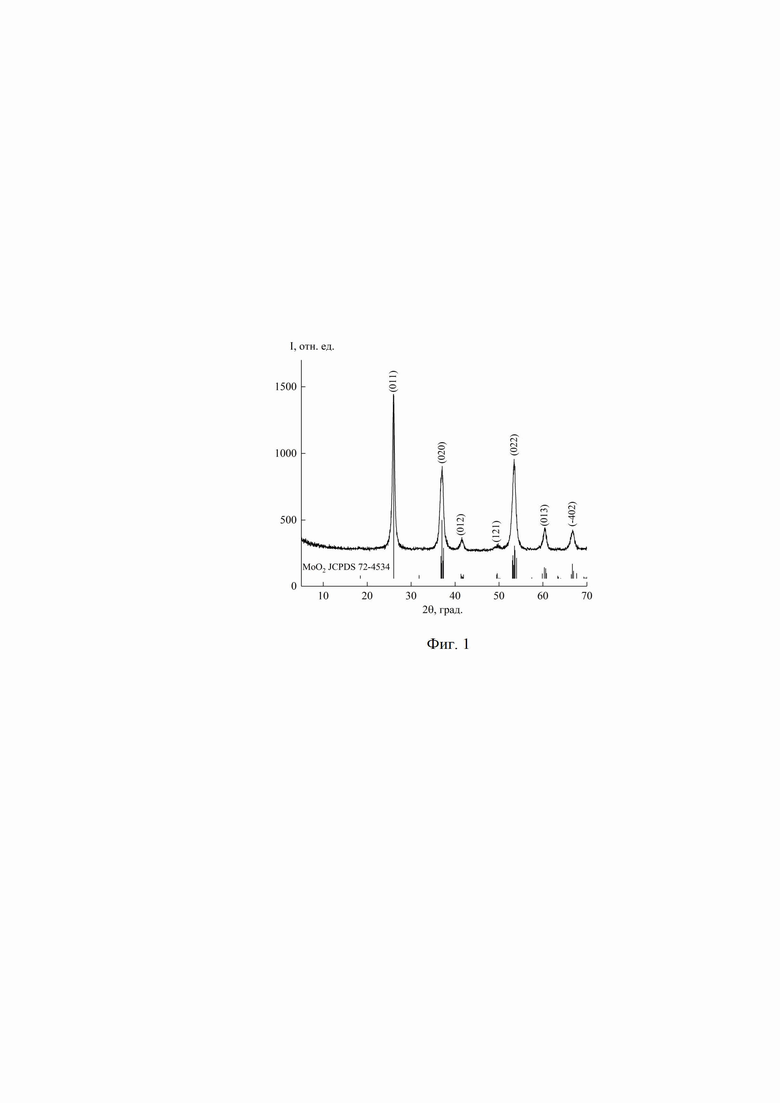
Предлагаемый способ может быть осуществлен следующим образом. Берут порошок молибдена Mo и растворяют его в 30%-ном пероксиде водорода H2O2 до получения прозрачного раствора желтого цвета при соблюдении соотношения т : ж = 1:(30÷40). К полученному раствору при перемешивании добавляют порошок винной кислоты C4H6O6, взятой в молярном соотношении молибден : винная кислота = 1:(1÷2). Перемешивание ведут до полного растворения винной кислоты. Полученный раствор подвергают гидротермальной обработке при температуре 160-200°С и избыточном давлении 617-1554 кПа в течение 12-24 ч. Полученный продукт фильтруют, промывают водой и сушат на воздухе при 50°С. Аттестацию полученного продукта проводят с помощью РФА и СЭМ. Текстурные характеристики (удельную поверхность, пористость) продукта определяли методом низкотемпературной адсорбции азота. По данным РФА полученный порошок является диоксидом молибдена MoO2 моноклинной сингонии с параметрами элементарной ячейки a = 5.598 Å, b = 4.833 Å, c = 5,645 Å и β = 131.96° (фиг. 1). Средний размер кристаллитов МоО2, рассчитанный с использованием уравнения Шеррера, составляет ~ 11 нм. Согласно СЭМ частицы MoO2 имеют морфологию в виде сфер диаметром 50 нм (фиг. 2). Величина удельной поверхности диоксида молибдена МоО2 составляет 110 м2/г. Для диоксида молибдена МоО2 характерно мономодальное распределение пор с преобладанием мезопор размером 8 нм (фиг. 3).
На фиг. 1 представлена экспериментальная рентгенограмма диоксида молибдена MoO2 и позиции брегговских пиков MoO2 по данным JCPDS 72-4534.
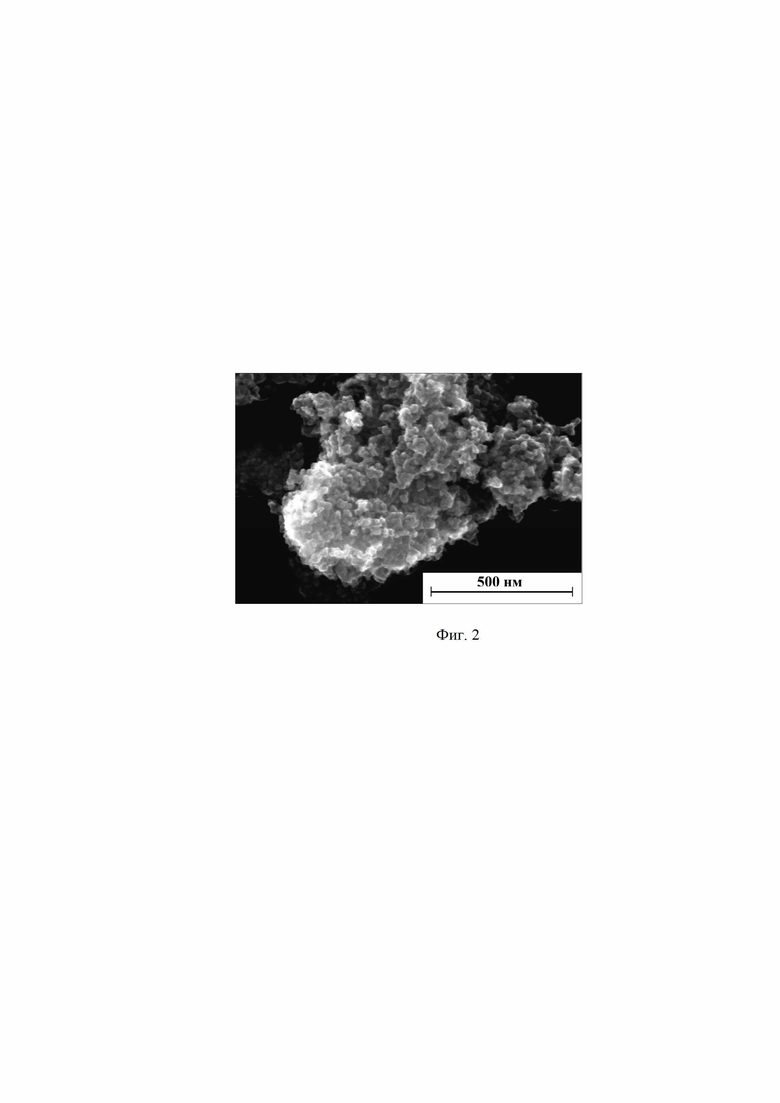
На фиг. 2 приведено изображение диоксида молибдена MoO2 со сферической морфологией частиц, полученное на СЭМ высокого разрешения.
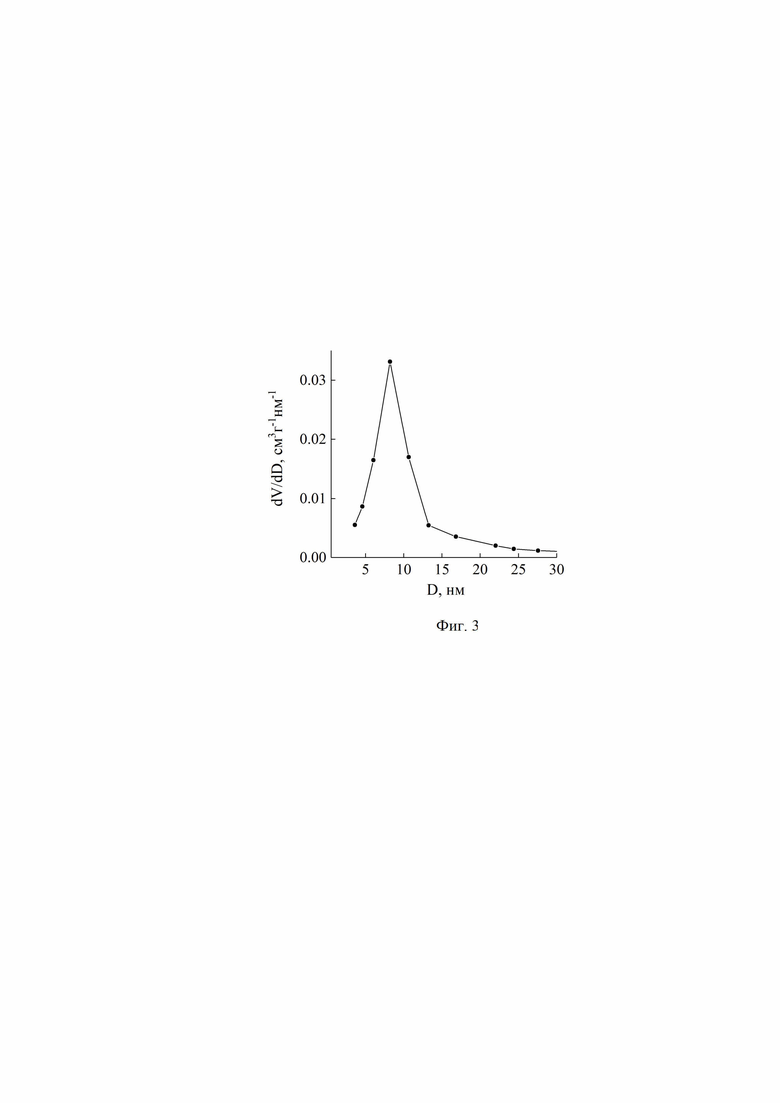
На фиг. 3 представлена экспериментальная кривая распределения пор по размерам диоксида молибдена MoO2.
Предлагаемый способ иллюстрируется следующими примерами.
Пример 1. Берут 1.0 г порошка молибдена Mo и растворяют его в 30 мл 30 %-ного раствора пероксида водорода H2O2, что соответствует соотношению т : ж = 1:30. К полученному раствору добавляют 1.564 г винной кислоты C4H6O6 (молярное соотношение молибден : винная кислота = 1:1). Полученный раствор подвергают гидротермальной обработке в автоклаве при температуре 160°С и избыточном давлении 617 кПа в течение 24 ч. Полученный продукт фильтруют, промывают водой и сушат на воздухе при 50°С. По данным РФА, СЭМ и низкотемпературной адсорбции азота полученный продукт является диоксидом молибдена MoO2 моноклинной сингонии со средним размером кристаллитов равным ~ 11 нм, состоящим из частиц с морфологией в виде сфер диаметром 50 нм и удельной поверхностью равной 110 м2/г с преобладанием мезопор размером 8 нм..
Пример 2. Берут 1.0 г порошка молибдена Mo и растворяют его в 35 мл 30 %-ного раствора пероксида водорода H2O2, что соответствует соотношению т : ж = 1:35. К полученному раствору добавляют 2.346 г винной кислоты C4H6O6 (молярное соотношение молибден : винная кислота = 1:1.5). Полученный раствор подвергают гидротермальной обработке в автоклаве при температуре 180°С и избыточном давлении 1000 кПа в течение 20 ч. Полученный продукт фильтруют, промывают водой и сушат на воздухе при 50°С. Полученный продукт фильтруют, промывают водой и сушат на воздухе при 50°С. По данным РФА, СЭМ и низкотемпературной адсорбции азота полученный продукт является диоксидом молибдена MoO2 моноклинной сингонии со средним размером кристаллитов равным ~ 11 нм, состоящим из частиц с морфологией в виде сфер диаметром 50 нм и удельной поверхностью равной 110 м2/г с преобладанием мезопор размером 8 нм.
Пример 3. Берут 1.0 г порошка молибдена Mo и растворяют его в 40 мл 30 %-ного раствора пероксида водорода H2O2, что соответствует соотношению т : ж = 1:40. К полученному раствору добавляют 3.127 г винной кислоты C4H6O6 (молярное соотношение молибден : винная кислота = 1:2). Полученный раствор подвергают гидротермальной обработке в автоклаве при температуре 200°С и избыточном давлении 1554 кПа в течение 12 ч. Полученный продукт фильтруют, промывают водой и сушат на воздухе при 50°С. По данным РФА, СЭМ и низкотемпературной адсорбции азота полученный продукт является диоксидом молибдена MoO2 моноклинной сингонии со средним размером кристаллитов равным ~ 11 нм, состоящим из частиц с морфологией в виде сфер диаметром 50 нм и удельной поверхностью равной 110 м2/г с преобладанием мезопор размером 8 нм.
Таким образом, авторами предлагается простой и технологичный способ получения диоксида молибдена MoO2, обеспечивающий получение высоких значений удельной поверхности за счет наличия мезопористой структуры.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения композита диоксид молибдена/углерод | 2017 |
|
RU2656466C1 |
| Ионоселективный материал для определения ионов калия | 2020 |
|
RU2732249C1 |
| Способ получения нанопорошка оксида марганца Mn3O4 | 2023 |
|
RU2813907C1 |
| Способ получения композита триоксид молибдена/углерод | 2016 |
|
RU2630140C1 |
| Способ получения триоксида молибдена h-MoO | 2023 |
|
RU2814773C1 |
| Способ получения триоксида молибдена h-MoO | 2023 |
|
RU2799648C1 |
| Способ получения композита монооксид марганца/углерод | 2022 |
|
RU2790818C1 |
| Способ получения композита триоксид молибдена/углерод | 2023 |
|
RU2804364C1 |
| Способ получения композита триоксид ванадия/углерод | 2020 |
|
RU2747772C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОЧАСТИЦ ДИОКСИДА ВАНАДИЯ | 2015 |
|
RU2602896C1 |
Изобретение относится к технологии производства наночастиц диоксида молибдена MoO2, который может быть использован в качестве селективного катализатора окисления олефинов, ион-электронного преобразователя твердофазных ионоселективных электродов для определения ионов калия в растворе, эффективного анодного материала литиевых источников тока, в качестве анодных материалов суперконденсаторов на основе водных электролитов, материала для фототермической терапии онкологических заболеваний, газосенсорного материала для определения концентрации паров этанола и ацетона. Способ получения наночастиц диоксида молибдена МoО2 включает гидротермальную обработку исходного раствора, содержащего источник молибдена и винную кислоту, с последующим промыванием и сушкой, при этом исходный раствор получают добавлением порошка металлического молибдена к 30%-ному раствору пероксида водорода в соотношении, равном т : ж = 1 : (30÷40), с последующим добавлением винной кислоты при молярном соотношении молибден : винная кислота = 1 : (1÷2). Простой и технологичный способ получения диоксида молибдена MoO2 обеспечивает получение высоких значений удельной поверхности сферических наночастиц за счет наличия мезопористой структуры. 3 ил., 3 пр.
Способ получения наночастиц диоксида молибдена МoО2, включающий гидротермальную обработку исходного раствора, содержащего источник молибдена и винную кислоту, с последующим промыванием и сушкой, отличающийся тем, что исходный раствор получают добавлением порошка металлического молибдена к 30%-ному раствору пероксида водорода в соотношении, равном т : ж = 1 : (30÷40), с последующим добавлением винной кислоты при молярном соотношении молибден : винная кислота = 1 : (1÷2).
| CN 0101780981 A, 21.07.2010 | |||
| Способ получения нанодисперсного порошка диоксида молибдена для изготовления анода твердооксидного топливного элемента | 2019 |
|
RU2729049C1 |
| CN 111825118 А, 27.10.2020 | |||
| CN 106711432 A, 24.05.2017 | |||
| CN 110182847 A, 30.08.2019. | |||
Авторы
Даты
2022-03-22—Публикация
2021-10-19—Подача