Изобретение относится к получению библиотеки соединений, обогащенной агонистами и антагонистами представителей класса G-белок сопряженных рецепторов.
Представители класса мембранных белков G-белок сопряженных рецепторов (G-protein coupled receptors, GCPR) (также известные как рецепторы, содержащие семь трансмембранных доменов (7ТМ) или «змеевидные» (serpentine) рецепторы) опосредуют предачу сигналов в клетку (клеточный сигналинг) в ответ на чрезвычайно широкий спектр внеклеточных сигналов, включая гормоны, нейротрансмиттеры, цитокины и даже вещества из внешней среды, например, ответственные за запах и вкус. В ответ на взаимодействие лиганда с внеклеточной частью рецептора (обычно N-концевой «хвост» рецепторного белка), рецептор временно переходит в активированное состояние (это преобразование обычно обозначают как R+L→R*L, где R - неактивный рецептор, R* - активированный рецептор и L - лиганд).
Рецептор в активированной конформации (или R*) затем способен взаимодействовать с представителями семейства G-белков. G-белки представляют собой большое семейство внутриклеточных тримерных белков, связывающих нуклеотиды гуанина. После взаимодействия с активированным рецептором (вероятно, по механизму, называемому «ударное сопряжение» (collisional coupling)) G-белок обменивает связанный гуанозиндифосфат (ГДФ) на гуанозинтрифосфат (ГТФ). При этом тример G-белка в ГТФ-связанной форме диссоциирует, высвобождая субъединицу Gα и димер βγ. И Gα и βγ субъединицы затем могут участвовать в дальнейших сигнальных каскадах. Например, субъединица Gα может активировать фермент аденилатциклазу (АЦ), вырабатывающий циклический аденозинмонофосфат (цАМФ) из аденозинтрифосфата. Субъединица βγ может активировать представителей семейства PI-3-киназ. В конечном счете эти сигналы могут привести к модулированию практически всех аспектов поведения клетки, от сокращения до подвижности, от изменения метаболизма до дальнейшей передачи сигналов.
После активации сигнал затем постепенно затухает под действием различных механизмов. ГТФ, связанный с субъединицей Gα, гидролизуется обратно в ГДФ, что приводит к реассоциации Gα и βγ субъединиц с формированием неактивного тримерного G-белка, связанного с ГДФ. Сам рецептор, сопряженный с G-белком, подвергается фосфорилированию в С-концевой внутриклеточной области, что предотвращает дальнейшее взаимодействие с G-белками. Наконец, связанный лиганд также может диссоциировать.
Этот общий сигнальный путь является настолько основополагающим и распространенным в физиологии млекопитающих, что до 40% лицензированных фармацевтических препаратов имеют среди своих молекулярных мишеней G-белок сопряженный рецептор. Аналогично бактерии эволюционировали таким образом, чтобы воздействовать на опосредованную G-белками передачу сигналов с целью нарушения физиологии и иммунитета хозяина: Vibrio cholerae (возбудитель холеры), например, производит белок, известный как холерный токсин, который необратимо ингибирует субъединицу Gα широко распространенных G-белков, называемых Gs. Аналогично Bordetella pertussis (возбудитель коклюша) производит белок, известный как токсин коклюша, который оказывает аналогичный эффект на другой G-белок, Gi.
Один из подходов для идентификации фармацевтических препаратов, воздействующих на передачу сигналов G-белок сопряженными рецептора, заключался в проведении скрининга библиотек большого числа произвольных соединений на способность препятствовать связыванию лиганда с препаратами мембран, содержащими рекомбинантные или очищенные G-белок сопряженные рецепторы. Для облегчения обнаружения связывания при проведении такого рода скринингов с высокой пропускной способностью были разработаны различные способы. Например, при анализе с помощью проксимальной сцинтилляции связывание меченного радиоактивным изотопом лиганда с рецептором приводит к сближению радионуклида с молекулой сцинтиллятора, связанной с рецептором, когда радионуклид распадается, испускается излучение, которое можно детектировать и количественно анализировать. Альтернативно лиганд может быть помечен флуоресцентной меткой, и связывание выявляют по поляризации флуоресценции (зависящей от уменьшения вращательных степеней свободы флуоресцентной метки в результате иммобилизации лиганда при связывании с рецептором).
Хотя применение этих способов в некоторых случаях имело успех, и были выявлены соединения, на основе которых впоследствии были разработаны фармацевтические препараты для человека (например, антагонист рецептора 5НТ3 Ondansetron, применяемый для лечения мигрени), остается множество G-белок сопряженных рецепторов, для которых, несмотря на интенсивный скрининг в фармацевтической индустрии, было идентифицировано лишь несколько (или вообще не было идентифицировано) подходящих непептидных агонистов или соединений-антагонистов. Например, для семейства хемокиновых рецепторов, сопряженных с G-белком, выявлено незначительное количество специфических непептидных антагонистов и не выявлено агонистов. Поскольку хемокины играют центральную роль в иммунной регуляции, такие молекулы, как ожидают, должны быть чрезвычайно ценными фармацевтическими препаратами с иммуномодулирующими свойствами, полезными при лечении широкого спектра заболеваний, включающих воспалительную составляющую.
Возможный успех программ по проведению скрининга произвольных соединений лимитируют два фактора: во-первых, существует огромное количество соединений, которые требуется проверить, и даже с применением технологии с наибольшей пропускной способностью и наилучших подходов комбинаторной химии для создания разнообразных библиотек, может быть исследована лишь малая доля всех возможных молекулярных структур; во-вторых, даже если наилучшие образцы были успешно идентифицированы, коровые фармакофоры часто не пригодны для применения in vivo, поскольку выявленные соединения и их аналоги могут быть просто слишком токсичными.
Другая основная проблема при подходах «негативного скрининга» (где выявляют способность исследуемой библиотеки блокировать связывание меченого лиганда) заключается в том, что большинство из выявленных образцов являются антагонистами рецептора. Лишь немногие из образцов имеют какую-либо агонистическую активность (как предполагается, агонистическая активность требует способности связываться с рецептором и затем приводить его в активированное состояние, тогда как для антагониста требуется только способность связываться с рецептором или лигандом таким образом, чтобы предотвратить их взаимодействие), а создание аналогов исходных образцов антагонистов с преобразованием их в агонисты является бессистемным подходом с очень низкой степенью успеха.
Один из способов разрешения данной проблемы мог бы заключаться в замене библиотеки произвольных соединений на библиотеку молекулярных структур, которая имеет высокое содержание соединений, связывающихся с G-белок сопряженным рецептором как результат их предварительного отбора. Такая библиотека в идеальном случае должна содержать как антагонисты, так и агонисты в равном соотношении так, чтобы и те и другие можно было бы легко выявить. Также было бы идеально, если основные молекулярные структуры, представленные в указанной библиотеке, являлись нетоксичными.
Могут ли быть созданы такие реальные библиотеки, приближенные к таким идеальным, или нет, не ясно. Если да, то необходимо существование предполагаемого «идеального» субстрата для G-белок сопряженного рецептора, который бы взаимодействовал с различными G-белок сопряженными рецепторами вне зависимости от их природного сродства к определенным лигандам. Получая такой идеализированный субстрат с различными заместителями, его можно было бы делать более селективным по отношению к одному рецептору в классе по сравнению со всеми остальными.
В данной заявке мы описываем «идеальный» субстрат для G-белок сопряженного рецептора, который можно применять в качестве трехмерного каркаса, который может быть различным образом замещен с получением агонистов и/или антагонистов ряда различных G-белок сопряженных рецепторов. Изобретение также предусматривает создание библиотеки вышеуказанных замещенных соединений для применения в ходе скрининга с целью получения лигандов для G-белок сопряженных рецепторов с любым заданным набором характеристик. Таким образом, становится возможным «конструировать» лиганд для G-белок сопряженного рецептора с известным набором свойств (например, лиганд, который имеет агонистическую активность по отношению к рецепторам допамина D2 и в то же самое время антагонистичекую активность по отношению к 5HT1a (рецепторам) серотонина). В противоположность этому, выявление таких смешанных лигандов из произвольных библиотек является редкой счастливой случайностью.
Изобретение предлагает соединения и их соли общей формулы (I)

где y представляет собой любое целое число от 1 до 8;
z представляет собой любое целое число от 0 до 8 при условии, что у и z не могут одновременно быть равными 1;
Х представляет собой -CO(Y)k-(R1)n или SO2(Y)k-(R1)n;
k представляет собой 0 или 1;
Y представляет собой циклоалкил или полициклоалкил (такой как адамантил, адамантанметил, бициклооктил, циклогексил, циклопропил)
или Y представляет собой циклоалкенил или полициклоалкенил;
каждый R1 независимо выбран из водорода или алкила, галоалкила, алкокси, галоалкокси, алкенила, алкинила, алкиламино, алкиламиноалкила, алкиламинодиалкила, имеющего заряд алкиламинотриалкила или имеющего заряд алкилкарбоксилата, содержащего от 1 до 20 атомов углерода,
или каждый R1 независимо выбран из фтора, хлора, брома, йода, гидрокси, оксиалкила, амино, аминоалкила, аминодиалкила, имеющего заряд аминотриалкила, или карбоксилатрадикала и
n - любое целое число от 1 до m, где m - максимальное количество заместителей, возможных в циклической группе Y.
Кроме того, R1 может быть выбран из пептидного радикала, например, содержащего от 1 до 4 пептидных звеньев, соединенных пептидной связью (например, пептидный радикал, содержащий от 1 до 4 аминокислотных остатков).
Этот класс соединений описан как α-аминоциклолактамы. Ключевой структурной особенностью данных молекул являются наличие лактамамида в системе циклоалкильного кольца с аминогруппой, присоединенной к атому углерода, следующего за лактамкарбонильной группой (обозначается как α-углерод).
Термины «α-аминоциклолактам» и «система циклоалкильного кольца», используемые в данном описании, охватывают как моноциклические, так и бициклические кольца.
Если в формуле (I) z=0, то соединения представляют собой α-аминоциклолактамы;
если в формуле (I) z=1-8, то соединения представляют собой α-аминобициклолактамы.
α-Углерод α-аминоциклолактамов может быть асимметричным (если y<>z в общей формуле (I)) и, следовательно, некоторые из соединений согласно настоящему изобретению имеют две возможные энантиомерные формы, то есть R и S конфигурации. Настоящее изобретение охватывает две энантиомерные формы и все комбинации этих форм, включая рацемические RS смеси. Для упрощения, если в структурных формулах не показана конкретная конфигурация, то следует понимать, что представлены две энантиомерные формы и их смеси.
Соединения общей формулы (I) представляют собой N-замещенные α-аминоциклолактамы или их фармацевтически приемлемые соли. N-Заместитель представляет собой либо карбонамид, либо сульфаниламид. Геометрия атома углерода, следующего за карбонильной группой карбонамида или сульфонильной группой сульфаниламида («ключевой» углерод) может быть важна для биологической активности молекулы. Природа N-заместителей может быть таковой, что кольцо или кольца Y ограничивают углы валентных связей при «ключевом» углероде, делая их, по существу, тетраэдрическими (т.е. sp3 гибридные связи). Любой заместитель R1 может быть заместителем в любом допустимом положении кольца или колец циклической группы Y. В частности, следует отметить, что изобретение включает соединения, у которых «ключевой углерод» входит в состав циклической группы и при этом сам является замещенным. Определение (R1)n охватывает соединения согласно изобретению без заместителей (т.е. R1 = водород), соединения согласно изобретению однозамещенные (т.е. R1 не является водородом и n=1), а также с несколькими замещениями (т.е., по меньшей мере, две R1 группы не являются водородом и n=2 или более).
Изобретение также предусматривает фармацевтические составы, содержащие в качестве активного компонента соединение общей формулы (I) или его фармацевтически приемлемую соль и по меньшей мере один фармацевтически приемлемый наполнитель и/или носитель:

где у представляет собой любое целое число от 1 до 8;
z представляет собой любое целое число от 0 до 8 при условии, что у и z не могут одновременно быть равными 1;
Х представляет собой -CO(Y)k-(R1)n или SO2(Y)k-(R1)n;
k представляет собой 0 или 1;
Y представляет собой циклоалкил или полициклоалкил (например, адамантил, адамантанметил, бициклооктил, циклогексил, циклопропил)
или Y представляет собой циклоалкенил или полициклоалкенил;
каждый R1 независимо выбран из водорода или алкила, галоалкила, алкокси, галоалкокси, алкенила, алкинила, алкиламино, алкиламиноалкила, алкиламинодиалкила, имеющего заряд алкиламинотриалкила или имеющего заряд алкилкарбоксилата, содержащего от 1 до 20 атомов углерода,
или каждый R1 независимо выбирают из фтора, хлора, брома, йода, гидрокси, оксиалкила, амино, аминоалкила, аминодиалкила, имеющего заряд аминотриалкила, или карбоксилатрадикала и
n - любое целое число от 1 до m, где m - максимальное количество заместителей, возможных в циклической группе Y.
Кроме того, R1 может быть выбран из пептидного радикала, например, содержащего от 1 до 4 пептидных звеньев, соединенных пептидными связями (например, пептидный радикал, содержащий от 1 до 4 аминокислотных остатков).
Под фармацевтически приемлемой солью понимают, в частности, аддитивные соли неорганических кислот, такие как гидрохлорид, гидробромид, гидройодид, сульфат, фосфат, бифосфат и нитрат или соли органических кислот, такие как ацетат, малеат, фумарат, тартрат, сукцинат, цитрат, лактат, метансульфонат, п-толуолсульфонат, пальмитат и стеарат. Также в область охвата настоящего изобретения, в случаях, когда их можно применять, включены соли, образованные из оснований, например, из гидроокиси натрия или калия. Другие примеры фармацевтически приемлемых солей см. в работе "Salt selection for basic drugs", Int. J. Pharm. (1986), 33, 201-217.
Фармацевтический состав может быть в твердой форме, например в виде порошков, гранул, таблеток, желатиновых капсул, липосом или суппозиториев. Подходящей твердой основой может служить, например, фосфат кальция, стеарат магния, тальк, сахара, лактоза, декстрин, крахмал, желатин, целлюлоза, метилцеллюлоза, натрийкарбоксиметилцеллюлоза, поливинилпирролидин и воск. Другие подходящие фармацевтически приемлемые наполнители и/или носители известны специалистам в данной области техники
Фармацевтические составы согласно изобретению также могут быть представлены в жидкой форме, например в виде растворов, эмульсий, суспензий или сиропов. Подходящей жидкой основой может быть, например, вода, органические растворители, такие как глицерол или гликоли, а также их водные смеси в различных пропорциях.
Изобретение также предусматривает применение соединения общей формулы (I) или его фармацевтически приемлемой соли для получения лекарственных препаратов, предназначенных для модулирования активности одного или более представителей класса G-белок сопряженных рецепторов:

где y представляет собой любое целое число от 1 до 8;
z представляет собой любое целое число от 0 до 8 при условии, что у и z не могут одновременно быть равными 1;
Х представляет собой -CO(Y)k-(R1)n или SO2(Y)k-(R1)n;
k представляет собой 0 или 1;
Y представляет собой циклоалкил или полициклоалкил (например, адамантил, адамантанметил, бициклооктил, циклогексил, циклопропил)
или Y представляет собой циклоалкенил или полициклоалкенил;
каждый R1 независимо выбран из водорода или алкила, галоалкила, алкокси, галоалкокси, алкенила, алкинила, алкиламино, алкиламиноалкила, алкиламинодиалкила, имеющего заряд алкиламинотриалкила или имеющего заряд алкилкарбоксилата, содержащего от 1 до 20 атомов углерода,
или каждый R1 независимо выбран из фтора, хлора, брома, йода, гидрокси, оксиалкила, амино, аминоалкила, аминодиалкила, имеющего заряд аминотриалкила, или карбоксилатрадикала и
n - любое целое число от 1 до m, где m - максимальное количество заместителей, возможных в циклической группе Y.
Кроме того, R1 может быть выбран из пептидного радикала, например, содержащего от 1 до 4 пептидных звеньев, соединенных пептидными связями (например, пептидный радикал, содержащий от 1 до 4 аминокислотных остатков).
Изобретение предлагает соединения, составы и способы применения соединений общей формулы (I) или их фармацевтически приемлемых солей, у которых радикал R1 содержит «ключевой» углерод, замещенный двумя одинаковыми или разными группами, выбранными из алкил, галоалкил, алкокси, галоалкокси, алкенил, алкинил или алкиламинорадикалов.
Изобретение предлагает соединения, составы и способы применения, в которых «ключевой» углерод является хиральным.
Изобретение предлагает соединения, составы и способы применения, в которых «ключевой» углерод образует sp3 гибридные связи.
Изобретение предлагает соединения, составы и способы применения, в которых «ключевой» углерод имеет, по существу, тетраэдрические углы валентных связей.
Соединения общей формулы (I) при применении в изобретении или их соли могут быть таковыми, что кольцо или кольца Y ограничивают углы валентных связей при «ключевом» углероде, делая их по существу тетраэдрическими (т.е. sp3 гибридные связи).
В альтернативном варианте реализации изобретения общую формулу (I) модифицируют так, что вместо С3-С7-алкильного мостика -(СН2)у- присутствует группа, независимо выбранная из группы, включающей алкенил, галоалкил, алкиламино, алкиламиноалкил, алкиламинодиалкил, заряженный алкиламинотриалкил, заряженный алкилкарбоксилат и алкилгидроксигруппы, имеющие углеродную цепочку, содержащую от 1 до 8 атомов.
Изобретение предусматривает применение, состав или соединение, где у и z представляют собой одинаковые целые числа от 1 до 8, в результате чего кольцо бициклолактама не является хиральным.
Изобретение предусматривает применение, состав или соединение, в котором у и z представляют собой не одинаковые целые числа от 1 до 8, в результате чего кольцо бициклолактама является хиральным.
Изобретение предусматривает применение, состав или соединение, в котором z представляет собой 3 и у представляет собой 1, 2 или 4-8, в результате чего соединение содержит лактамное кольцо, которое является семичленным.
Изобретение предусматривает применение, состав или соединение, в котором z представляет собой 2 и у представляет собой 1 или 3-8, в результате чего соединение содержит лактамное кольцо, которое является шестичленным.
Примерами соединений общей формулы (I) и их солей в соответствии с настоящим изобретением являются:
4-(адамантан-1-карбониламино)-3-оксо-2-азабицикло[2.2.2]октан,
5-(адамантан-1-карбониламино)-10-оксо-9-азабицикло[3.3.2]декан,
4-(2',2'-диметилдодеканоиламино)-3-оксо-2-азабицикло[2.2.2]октан,
5-(2',2'-диметилдодеканоиламино)-10-оксо-9-азабицикло[3.3.2]декан и их соли.
Изобретение также предлагает сульфаниламидные аналоги приведенных в качестве примеров соединений, т.е. сульфонил-α-аминоциклолактамные эквиваленты соединений формулы (I).
Изобретение охватывает указанные соединения, составы и применение при этом соединения находятся в гидратированной или сольватированной форме.
Амидные и сульфонамидные производные α-аминоциклолактамов, описанных в данной заявке, являются функциональными агонистами G-белок сопряженных рецепторов. Они стабильны в сыворотке крови человека и, следовательно, имеют превосходные фармакокинетические свойства; биодоступны при пероральном приеме; являются сильнодействующими агонистами G-белок сопряженных рецепторов; их введение не сопровождается какой-либо значительной острой токсичностью при дозах, необходимых для достижения максимального терапевтического эффекта. В целом эти свойства указывают на то, что амидные и сульфонамидные производные α-аминоциклолактамов представляют собой совокупность соединений с улучшенными свойствами агонистов и антагонистов G-белок сопряженных рецепторов.
Центральная часть, состоящая из «ключевого» углерода, карбонильной или сульфонильной группы, α-аминогруппы и системы циклолактама (в частности, ограниченная система бициклолактамного кольца), представляет собой пример «идеального» лиганда для G-белок сопряженного рецептора. Меняя заместители данной центральной части, можно получать агонисты и антагонисты G-белок сопряженных рецепторов с широким спектром желаемых свойств намного более легким способом, чем с помощью скрининга библиотек произвольных соединений.
В результате изобретение также предлагает библиотеку, состоящую из двух или более представителей класса соединений, определяемых общей формулой (I), такую, что можно проводить скрининг указанной библиотеки для идентификации молекулы с некоторым желательным набором свойств в отношении модулирования процесса передачи сигналов от одного (или более) G-белок сопряженных рецепторов. Затем можно провести скрининг вышеупомянутой библиотеки на антагонистическую или агонистическую активность по отношению к вышеупомянутому G-белок сопряженному рецептору (рецепторам) с применением способов, хорошо известных в данной области техники. Например, можно скринировать библиотеки на способность отдельных ее элементов блокировать связывание меченного радиоактивным изотопом лиганда G-белок сопряженного рецептора с препаратами мембраны, содержащими рекомбинантный или очищенный G-белок сопряженный рецептор. Кроме того, можно проводить скрининг библиотеки на способность отдельных ее элементов стимулировать образование цАМФ в клетках, экспрессирующих рекомбинантный G-белок сопряженный рецептор.
Изобретение также обеспечивает способы лечения, облегчения или профилактики симптомов болезни или состояния, выбранного из группы, включающей гипертонию, атеросклероз, астму, ожирение, нейродегенеративные заболевания, аутоиммунные заболевания или психопатические заболевания путем введения пациенту эффективного количества соединения, состава или лекарственного препарата согласно изобретению, предназначенного для модулирования активности G-белок сопряженного рецептора.
ОПРЕДЕЛЕНИЯ
Термин «приблизительно» относится к интервалу, который включает рассматриваемое значение. При использовании в данной заявке на патент «приблизительно X» означает интервал от значения Х минус 10% от значения Х до значения Х плюс 10% от значения X, предпочтительно интервал от значения Х минус 5% от значения Х до значения Х плюс 5% от значения X.
Использование числового диапазона в данном описании предназначено для того, чтобы однозначно включить в область охвата изобретения каждое конкретное целое значение данного диапазона и все комбинации значений верхнего и нижнего пределов расширенной области данного диапазона. Таким образом, например, диапазон от 1 до 20 атомов углерода, указанный (в числе прочего) в отношении формулы I, охватывает все целые числа от 1 до 20 и все подобласти каждой комбинации верхних и нижних значений, приведенных или не приведенных в качестве примеров в явной форме.
Термины «включающий» и «содержащий», используемые в данном описании, следует понимать и как «включающий» (имеющий в составе) и как «состоящий из». Таким образом, если указано, что изобретение относится к «фармацевтическому составу, включающему/содержащему в качестве активного компонента» соединение, то данные термины относятся и к составам, в которые могут входить другие активные компоненты, и к составам, состоящим только из одного активного компонента, как определено.
Термин «пептидные звенья», используемый в настоящей заявке, обозначает следующие 20 природных аминокислотных остатков:
Модифицированные и редко используемые аминокислотные остатки, как и пептидомиметики, также входят в объем понятия «пептидные звенья».
Если не определено иначе, все технические и научные термины, используемые в настоящей заявке, имеют значение, которое обычно понимается средним специалистом в области техники, к которой принадлежит данной изобретение. Аналогично содержание всех публикаций, заявок на патент, всех патентов и других источников, упоминаемых в настоящем описании, включено в настоящее описание посредством ссылки (если это юридически допустимо).
Следующие примеры иллюстрируют, но никоим образом не ограничивают область изобретения.
ПРИМЕРЫ
Общий способ синтеза исходных соединений
Гидрохлориды (R) и (S)-3-аминокапролактама и гидропирролидин-5-карбоксилаты (R,R) и (S,S)-3-аминокапролактама синтезировали согласно способам, описанным в литературе (ср. Boyle et al., J. Am. Chem. Soc. (1979), 44, 4841-4847; Rezler et al., J. Med. Chem. (1997), 40, 3508-3515).
ПРИМЕР 1
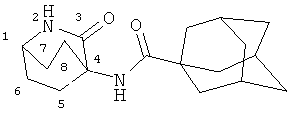
4-(Адамантан-1-карбониламино)-3-оксо-2-азабицикло[2.2.2]октан
ПРИМЕР 2
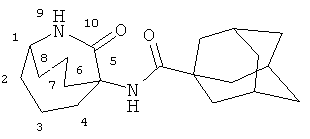
5-(Адамантан-1-карбониламино)-10-оксо-9-азабицикло[3.3.2]декан
ПРИМЕР 3

4-(2',2'-Диметилдодеканоиламино)-3-оксо-2-азабицикло[2.2.2]октан
ПРИМЕР 4
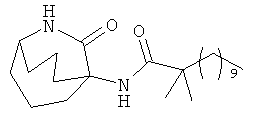
5-(2',2'-диметилдодеканоиламино)-10-оксо-9-азабицикло[3.3.2]декан
Фармакологическое исследование продуктов согласно изобретению
Принципы исследования
А. Антагонисты G-белок сопряженных рецепторов
Как правило, соединения согласно изобретению можно исследовать на антагонистическую активность по отношению к конкретному G-белок сопряженному рецептору, воздействуя на рецептор меченным радиоизотопом лигандом в подходящих для связывания условиях при отсутствии и в присутствии различных концентраций исследуемого соединения. Далее оценивают количество метки, связавшейся с рецептором. В случае, если исследуемое соединение способно конкурировать с меченным лигандом за связывание, количество метки, связавшейся с рецептором, уменьшается с увеличением концентрации исследуемого соединения. По графику зависимости количества связавшегося лиганда от концентрации исследуемого соединения можно оценить сродство исследуемого соединения к связыванию с рецептором.
Таким образом, такой способ анализа требует:
(1) Источник представляющего интерес G-белок сопряженного рецептора. Последовательность каждого члена суперсемейства G-белок сопряженных рецепторов человека на настоящий момент доступна в результате секвенирования генома человека. Такие последовательности можно клонировать в соответствующем векторе и экспрессировать в клетках соответствующего типа (например, Т-клетки Jurkat, которые, как известно, фактически не экспрессируют эндогенные G-белок сопряженные рецепторы, за исключением хемокинового рецептора CXCR4). После селекции с применением антибиотика, соответствующего используемому вектору, можно получить стабильные клеточные линии с высоким уровнем экспрессии выбранного G-белок сопряженного рецептора.
Мембранные фракции клеточных линий, экспрессирующих выбранный G-белок сопряженный рецептор, можно получить с применением ряда способов, хорошо известных в данной области техники. Например, согласно Куо с соавторами (Kuo et al., Proc. Natl. Acad. Sci. USA (1980) 77:7039), клетки можно ресуспендировать в буфере 25 мМ HEPES - (N-2-гидроксиэтилпиперзин-N'-2-этансульфоновая кислота), рН 7,5, содержащем 0,25 М сахарозу, 2,5 мМ MgCl2, 2,5 мМ EGTA и 50 мМ β-меркаптоэтанол, а также ингибиторы протеаз, такие как PMSF и леупептин, и разрушить с высвобождением компонент с применением гомогенизатора Даунса. Затем суспензию центрифуговали при 120×g для получения осадка из неразрушенных клеток и больших фрагментов клеток и отбирали надосадочную жидкость, содержащую небольшие фрагменты мембраны и компоненты цитозоля. Затем полученную надосадочную жидкость ультрацентрифугировали при 100000×g, получая осадок из фрагментов мембраны с высоким содержанием выбранного G-белок сопряженного рецептора. Осадок ресуспендируют в подходящем для связывания буфере и определяют общую концентрацию белка с применением, например, коммерчески доступных наборов для белкового анализа, таких как Coomassie Plus (Pierce). Препарат мембраны можно довести до нужного объема для получения стандартизированной общей концентрации белка, например 1 мг/мл. Препарат можно хранить при - 85°С в аликвотах до необходимости применения.
(2) Меченый лиганд с высоким сродством к выбранному G-белок сопряженному рецептору. Соответствующие лиганды большинства G-белок сопряженных рецепторов хорошо известны в литературе. Такие лиганды могут представлять собой природные лиганды рецептора (например, допамин) или представлять собой фармакологическое средство (как, например, домперидон). Список пригодных лигандов щирокого спектра изученных G-белок сопряженных рецепторов приведен в таблице, но, как очевидно для специалиста в данной области техники, для многих из этих рецепторов существуют другие подходящие лиганды. Лиганды, наиболее пригодные для данных целей, должны иметь константу сродства для связывания с выбранным рецептором, по крайней мере, 1 мкМ, предпочтительно менее чем 100 нМ и более предпочтительно менее чем 10 нМ.
После выбора лиганда, возможно, его будет необходимо пометить, чтобы впоследствии можно было определить количество лиганда, связавшегося с выбранным G-белок сопряженным рецептором (хотя можно провести анализ и без мечения лиганда, при условии доступности чувствительного и точного способа определения количества несвязанного лиганда, например, можно применять твердофазный ИФА (ELISA) для измерения не связавшегося лиганда, таким способом, определяя количество связавшегося лиганда). Подходящие способы мечения лиганда меняют в зависимости от природы лиганда: небольшие молекулы можно легко пометить радионуклидами, такими как 3H, 14С или 35S; пептиды можно легко пометить ко-синтетическим биотином (и впоследствии меченым стрептавидином), флуоресцентными метками (например, флуоресцеинизотиоцианатом) или радионуклидами (например, 125I-йодирование остатков тирозина в пептиде); белки можно легко пометить флуоресцентными метками (такими как флуоресцеинизотиоцианат) или радионуклидами (например, с помощью 125I-йодирования остатков тирозина в белке).
Степень мечения (то есть доля молекул в образце, которые несут метку) должна быть достаточна для того, чтобы количество лиганда, связывающегося с рецептором, можно было достоверно определить количественно.
С указанными двумя компонентами затем возможно проверить, модулируют ли соединения согласно изобретению связывание лиганда с каким-либо определенным G-белок сопряженным рецептором, применяя способы, хорошо известные в данной области техники. Например, в серии пробирок препарат мембраны смешивают с радиоактивно меченым лигандом в концентрации, близкой по величине к константе сродства связывания лиганда с выбранным G-белок сопряженным рецептором. В некоторые пробирки также добавляют соединения согласно изобретению в различных концентрациях. В другие пробирки добавляют в качестве положительного контроля ингибитор (который может быть тем же лигандом в значительном избытке, что и радиоактивно меченый лиганд, но без радиоактивной метки). Обычно для каждого набора условий готовят по 3 пробирки. Пробирки затем инкубируют, обычно при 4-37°С, предпочтительнее при комнатной температуре, в течение периода времени, необходимого для достижения равновесия между свободной и связанной формами радиоактивно меченого лиганда. Обычно это может занять от 20 минут до 4 часов, период времени, необходимый для каждого конкретного набора условий реакции можно определить способами, хорошо известными в данной области техники (например, проведением экспериментов в динамике). Как только равновесие достигнуто, необходимо определить количество связавшегося радиоактивно меченого лиганда. Например, мембраносвязанный рецептор (плюс любой связанный радиоактивно меченый лиганд) можно отделить от свободного радиоактивно меченого лиганда в растворе путем фильтрации через фильтры (такие как GF/C фильтры, обработанные 1%-ным полиэтиленимином). Фильтры можно затем высушить на воздухе и подвергнуть сцинтилляционному подсчету для определения фракции добавленного радиоактивно меченого лиганда, которая связалась с рецептором.
Альтернативно соединения согласно изобретению можно подвергать скринингу с применением коммерчески доступных процедур скрининга рецепторов (например, услуги, предлагаемые Cerep, 128 Rue Danton, Париж, Франция). С помощью подобных служб можно легко идентифицировать члены библиотеки, такой как библиотека согласно настоящему изобретению, которые модулируют связывание лиганда с одним или более G-белок сопряженных рецепторов.
Соединения, идентифицированные как модулирующие связывание лиганда с одним или более G-белок сопряженным рецептором, с применением способов, упомянутых выше, обычно представляют собой полные антагонисты. Однако, для того чтобы подтвердить свойства соединения в качестве антагониста, необходимо выполнить функциональный анализ. Например, в зависимости от используемого G-белок сопряженного рецептора и/или лиганда, при передаче сигнала о присутствии лиганда стимулируются (или ингибируются) определенные вторичные посредники. В ответ на появление лиганда в клетках может наблюдаться и увеличение (или уменьшение) внутриклеточной концентрации циклического аденозинмонофосфата (цАМФ), различных фосфорилированных содержащих инозитол соединений (включая инозитолтрифосфаты I(1,4,5)Р3 и I(1,3,5)Р3), ионов кальция, полиаденозина или других внутриклеточных посредников, известных в данной области. Полные антагонисты нивелируют изменение содержания внутриклеточных посредников, вызванное природным лигандом(ами), и не оказывают эффекта в отсутствие природного лиганда. В отличие от этого полные агонисты не оказывают эффекта при добавлении природного лиганда(ов), но имитируют изменения внутриклеточных посредников, вызванные природным лигандом(ами), в отсутствие природного лиганда. Некоторые соединения, включая соединения согласно настоящему изобретению, могут быть частичными антагонистами, частичными агонистами или смешанными агонист-антагонистами в зависимости от характера действия на внутриклеточные посредники. Несмотря на комплексные фармакологические характеристики таких соединений, они могут иметь полезные терапевтические свойства в лечении определенных заболеваний, и известно, что ряд хорошо зарекомендовавших себя медицинских препаратов представялют собой частичные агонисты, частичные антагонисты или смешанные агонист-антагонисты одного или более G-белок сопряженного рецептора.
Б. Агонисты G-белок сопряженных рецепторов
По существу значительно более трудно исследовать активность агониста, чем антагониста, особенно при использовании способов скрининга с высокой пропускной способностью. Соединения согласно изобретению, таким образом, вероятно будут особенно полезны для поиска агонистов, чем общие библиотеки для обнаружения соединений-кандидатов из-за большего количества агонистов G-белок сопряженного рецептора среди элементов библиотеки.
Исследование агонистов G-белок сопряженного рецептора, в принципе, требует культуры клеток или органа, которая реагирует на природный лиганд выбранного G-белок сопряженного рецептора (рецепторов), продуцируя желаемый биохимический или физиологический ответ. Примеры таких ответов без ограничения включают изменения, связанные с внутриклеточными посредниками (такими как цАМФ, I(1,4,5)Р3, ионы кальция или полиаденозина), изменения ферментативной активности (такие как активация протеинкиназ, фосфатаз, ферментов метаболизма или транспортных белков), изменения характера экспрессии генов, изменения фагоцитоза, изменения в секреции белков, изменения скорости пролиферации, уменьшение мышечных клеток/ткани, нейротрансмиссию и т.п. Поскольку ответы, такие как эти, являются по существу более сложными для измерения, чем связывание природного лиганда(ов) с выбранным G-белок сопряженным рецептором, то способы анализа агонистов G-белок сопряженных рецепторов связаны с большими трудностями, чем для антагонистов.
Общий способ, необходимый для проверки того, представляет ли собой соединение согласно изобретению агонист одного или более выбранного G-белок сопряженного рецептора, хорошо разработан в данной области техники. Клетки выдерживают при различных концентрациях исследуемого соединения, например, при добавлении соединения в соответствующем растворителе (таком как ДМСО, этанол или метанол) в различных концентрациях (например, от примерно 0,1 нМ до примерно 10 мМ) в среду для культивирования клеток на определенный период времени (например, от 1 минуты до 48 часов в зависимости от времени протекания измеряемого ответа), обычно при 37°С. Параллельно на клетки также воздействуют природным лигандом и оставляют без воздействия какого-либо дополнительного соединения(ий) (в качестве контроля). В конце периода инкубации измеряют ответ, который, как известно в данной области, имеет место как следствие связывания природного лиганда с выбранным G-белок сопряженным рецептором. Если соединение согласно изобретению является агонистом выбранных G-белок сопряженных рецепторов, то ответ на исследуемое соединение (в определенных концентрациях) будет количественно сходен с ответом на природный лиганд.
Примеры подходящих систем анализа для выявления агонистов к определенному G-белок сопряженному рецептору
Соматостатин представляет собой агонист рецепторов sstr2 и sstr5, ингибирующий секрецию гормонов роста в изолированных клетках гипофиза. Для того чтобы определить, является ли соединение согласно изобретению агонистом sstr2 и/или sstr5, клетки гипофиза крысы выделяют и переводят в культуру. Затем клетки ингибируют в отсутствие или в присутствии соматостатина в концентрации 33 нМ или в присутствии исследуемого соединения (соединений) в различных концентрациях от 0,1 нМ до приблизительно 10 мМ при 37°С в течение 24 часов. В конце эксперимента культуральную среду удаляют, очищают центрифугированием и проводят анализ на гормон роста (ГР), например, с использованием коммерчески доступного твердофазного ИФА (ELISA) или радиоиммуноанализа. Клетки под воздействием соматостатина производят на 30%-90% меньше ГР, по сравнению с клетками, инкубируемыми без воздействия данного агониста. Если соединение согласно изобретению представляют собой агонист соматостатина для указанных рецепторов, то уровень ГР будет более низок в среде от клеток, подвергнутых воздействию исследуемого соединения (по крайней мере, в определенной концентрации), по сравнению со средой от клеток, инкубируемых без воздействия агониста. Обычно среду анализируют для трех отдельных лунок, в которых инкубируемые в ней клетки обрабатывают идентично при каждом из условий эксперимента, так чтобы можно было применить подходящий статистический анализ (такой как дисперсионный анализ или непарный 1-тест Стьюдента), для того, чтобы показать, что исследуемое соединение вызывает статистически значимое уменьшение секреции ГР и, следовательно, вероятно, обладает агонистической активностью по отношению к выбранным рецепторам sstr2 и/или sstr5.
Эндотелин-1 представляет собой пептид, который запускает сигнальный каскад через рецепторы ЕТ-А и/или ЕТ-В, вызывая вазоконстрикцию. Для того чтобы определить, являются ли соединения согласно изобретению агонистами ЕТ-А и/или ЕТ-В, кольца аорты человека (полученные от сердца донора трансплантанта) можно поместить в условия культуры органов. Затем кольца подвергают или воздействию Эндотелина-1 с увеличением концентрации (от 0,01 нМ до 100 нМ), или исследуемого соединения (соединений) с увеличением концентрации (приблизительно 0.1 нМ - 10 мМ) при 37°С, увеличивая концентрацию соответствующего агента приблизительно каждые 5 минут. В ходе эксперимента измеряют сжатие кольца аорты с применением тензиометрического датчика, разработанного и коммерчески доступного для таких целей. Кольца, на которые воздействуют Эндотелином-1, сокращаются при повышении концентрации Эндотелина-1 так, что к моменту достижения верхнего значения концентрации, сила, действующая на тензиометрический датчик, будет значительно выше, чем до добавления Эндотелина-1. Если соединение согласно изобретению является агонистом рецепторов Эндотелина, то сила, действующая на тензиометрический датчик, также будет выше (по крайней мере, при определенной концентрации), чем до добавления исследуемого соединения. Обычно три или более отдельных кольца аорты подвергают воздействию возрастающей концентрации одного и того же агента при идентичных условиях эксперимента для возможности применения подходящего статистического анализа (такого, как дисперсионный анализ или непарный t-тест Стьюдента) для того, чтобы показать, что исследуемое соединение вызывает статистически значимое увеличение сжатия аорты и, следовательно, вероятно, обладает агонистической активностью по отношению к выбранным рецепторам ЕТ-А и/или ЕТ-В.
Хемокин SDF-1a является пептидом, запускающим сигнальный каскад через рецептор CXCR4, вызывая миграцию лейкоцитов. Для того чтобы определить, является ли соединение согласно изобретению агонистом CXCR4, культивируемые иммортализованные Т-клетки человека (например, Т-клетки Jurkat) помещают в верхнюю лунку специализированного коммерчески доступного прибора для анализа миграции из лунки в лунку. Лунки затем погружают в нижние камеры, содержащие только культуральную среду, или в нижние камеры, содержащие SDF-1a в концентрации 75 нМ, или в нижние камеры, содержащие исследуемое соединение (соединения) в различных концентрациях (приблизительно 0,1 нМ - 10 мМ), и инкубируют в течение определенного промежутка времени (обычно от 30 минут до 3 часов) при 37°С. В конце инкубации число клеток в нижней камере является мерой величины произошедшей миграции. Число клеток в нижней камере можно подсчитать прямым визуальным наблюдением или различными известными способами, например с помощью инкубации с красителем МТТ, который преобразуется в нерастворимый синий формазан пропорционально количеству присутствующих клеток. В лунках, помещенных в нижнюю камеру, содержащую SDF-1a, число клеток в нижней камере будет в 2-10 раз выше, чем число клеток в нижней камере, содержащей только культуральную среду. Если соединение согласно изобретению представляет собой агонист CXCR4, то число клеток в нижних камерах, содержащих исследуемое соединение (соединения), также будет выше (по крайней мере, при определенной концентрации), чем в нижних камерах, содержащих только среду. Обычно анализ проводят в трех повторностях при идентичных условиях каждого эксперимента для возможности применения подходящего статистического анализа (например, дисперсионного анализа или непарного t-теста Стьюдента), чтобы показать, что соединение согласно изобретению вызывает статистически значимое увеличение миграции лейкоцитов и, следовательно, вероятно, обладает агонистической активностью по отношению к выбранным рецепторам ЕТ- и/или ЕТ-В.
Биологически активный амин адреналин увеличивает внутриклеточную концентрацию цАМФ в сосудистых гладкомышечных клетках. Для определения того, являются ли соединения согласно изобретению агонистами (β-адренорецепторов, сосудистые гладкомышечные клетки изолируют из грудной аорты крыс и помещают в культуру. Затем клетки инкубируют в отсутствие или в присутствии агониста адреналина сальбутамола при 33 нМ, или в присутствии исследуемого соединения (соединений) в различной концентрации от 0,1 нМ до 10 мМ при 37°С в течение 15 минут. В конце эксперимента культуральную среду клеток удаляют, промывают клетки 3 раза в ледяном буфере и затем лизируют в соответствующем буфере для лизиса до измерения концентрации внутриклеточного цАМФ, например, с применением коммерчески доступных наборов для твердофазного ИФА (ELISA) или радиоиммуноанализа. Клетки, на которых воздействовали сальбутамолом, имеют концентрацию внутриклеточного цАМФ выше на 15%-150%, по сравнению с клетками без воздействия агониста. Если соединение согласно изобретению представляет собой агонист β-адренорецептора, тогда концентрация внутриклеточного цАМФ будет более высокой в клетках, на которые воздействовали исследуемым соединением (по крайней мере, в определенной концентрации), чем в клетках, инкубируемых только в среде.
Обычно клеточный лизат готовят в трех повторностях из клеток, обработанных при идентичных условиях каждого эксперимента для возможности применения подходящих статистических анализов (таких, как дисперсионный анализ или непарный t-тест Стьюдента) для того, чтобы показать, что исследуемое соединение вызывает статистически значимое увеличение концентрации внутриклеточного цАМФ и, следовательно, вероятно, обладает агонистической активностью по отношению к выбранным β-адренорецепторам.
Очевидно, что способы анализа, такие как приведены выше в качестве примеров, выявляют агонистов выбранных G-белок сопряженных рецепторов и разделяют соединения согласно изобретению на неактивные соединения и соединения с антагонистической или частичной антагонистической активностью по отношению к выбранному G-белок сопряженному рецептору, но не обязательно однозначно идентифицируют выбранный G-белок сопряженный рецептор как молекулярную мишень соединения согласно изобретению. Например, соединение согласно изобретению, для которого было показано, что оно увеличивает уровень цАМФ в сосудистых гладкомышечных клетках в той же степени, что и агонист β-адренорецептора сальбутамол, может быть агонистом β-адренорецептора (G-белок сопряженного рецептора) или может быть агонистом другого G-белок сопряженного рецептора, который также увеличивает уровень цАМФ (такого, как рецептор допамина D2). Кроме того, соединение согласно изобретению, стимулирующее миграцию лейкоцитов в той же степени, что и SDF-1a, может быть агонистом CXCR4 или может являться агонистом другого G-белок сопряженного рецептора, стимулирующего миграцию лейкоцитов (такого как рецептор С5а). Подтверждение того, что G-белок сопряженный рецептор является молекулярной мишенью, на которую соединения согласно изобретению действуют как агонисты, требует проведения дополнительных экспериментов с применением специфических антагонистов, уже идентифицированных для выбранного G-белок сопряженного рецептора, или применения рекомбинантных клеточных линий, которые экспрессируют только выбранный G-белок сопряженный рецептор. Например, если миграция лейкоцитов, индуцированная соединением согласно изобретению, ингибируется добавлением СХСР4-специфичного антагониста AMD3100 в соответствующей концентрации, тогда логично заключить, что CXCR4 является молекулярной мишенью соединения согласно изобретению. Аналогично, если миграция лейкоцитов, индуцированная соединением согласно изобретению, наблюдалась при применении клеточной линии, экспрессирующей CXCR4, но отсутствовала в той же клеточной линии, не экспрессирующей CXCR4, тогда логично заключить, что CXCR4 является молекулярной мишенью соединения согласно изобретению.
Изобретение относится к соединению общей формулы (I), его солям и сольватам в качестве лигандов для G-белок сопряженных рецепторов

а также к библиотеке, состоящей из элементов, которые представляют собой соединения формулы (I). В общей формуле (I) у равно 1 или 2; z равно 0; X представляет собой -CO-(Y)k-(R1)n или SO2-(Y)k-(R1)n; k равно 0; каждый R1 независимо выбран из водорода или алкила, галоалкила, алкокси, галоалкокси, алкенила, алкинила, алкиламино, алкиламиноалкила, алкиламинодиалкила, имеющего заряд алкиламинотриалкила или имеющего заряд алкилкарбоксилата из 1-20 атомов углерода; или каждый R1 независимо выбран из фтора, хлора, брома, йода, гидрокси, оксиалкила, амино, аминоалкила, аминодиалкила, имеющего заряд аминотриалкила или карбоксилат радикала; n является целым числом от 1 до m, где m представляет собой максимальное число допустимых заместителей; R1 содержит атом углерода, следующий за карбонильной группой карбонамида или сульфонильной группой сульфаниламида, который является двузамещенным либо идентичными, либо разными группами, выбранными из алкила, галоалкила, алкокси, галоалкокси, алкенила, алкинила и алкиламинорадикала; и атом углерода, следующий за карбонильной группой карбонамида или сульфонильной группой сульфаниламида в составе R1 образует по существу тетраэдральные углы валентных связей. 2 н. и 2 з.п. ф-лы, 1 табл., 4 пр.
1. Соединение общей формулы (I),

где у равно 1 или 2;
z равно 0;
Х представляет собой -CO-(Y)k-(R1)n или SO2-(Y)k-(R1)n;
k равно 0;
каждый R1 независимо выбран из водорода или алкила, галоалкила, алкокси, галоалкокси, алкенила, алкинила, алкиламино, алкиламиноалкила, алкиламинодиалкила, имеющего заряд алкиламинотриалкила или имеющего заряд алкилкарбоксилата из 1-20 атомов углерода;
или каждый R1 независимо выбран из фтора, хлора, брома, йода, гидрокси, оксиалкила, амино, аминоалкила, аминодиалкила, имеющего заряд аминотриалкила или карбоксилат радикала;
n является целым числом от 1 до m, где m представляет собой максимальное число допустимых заместителей;
R1 содержит атом углерода, следующий за карбонильной группой карбонамида или сульфонильной группой сульфаниламида, который является двузамещенным либо идентичными, либо разными группами, выбранными из: алкила, галоалкила, алкокси, галоалкокси, алкенила, алкинила и алкиламино радикала; и
атом углерода, следующий за карбонильной группой карбонамида или сульфонильной группой сульфаниламида в составе R1 образует, по существу, тетраэдральные углы валентных связей;
или соль или сольват указанного соединения.
2. Соединение по п.1, отличающееся тем, что атом углерода, следующий за карбонильной группой карбонамида или сульфонильной группой сульфаниламида, является хиральным.
3. Соединение п.1, отличающееся тем, что атом углерода, следующий за карбонильной группой карбонамида или сульфонильной группой сульфаниламида, образует sp3 гибридные связи.
4. Библиотека, состоящая из элементов, которые представляют собой соединения по любому из пп.1-3.
| FOX D J et al, J | |||
| Mtd | |||
| Chem | |||
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
| DAVIDSON В S et al., Tetrahedron, 1993, 49(30), 6569-6574 | |||
| ЗАМЕЩЕННЫЕ 3,7-ДИАЗОБИЦИКЛО[3.3.1]НОНАНЫ, ФОКУСИРОВАННАЯ БИБЛИОТЕКА И КОМБИНАТОРНАЯ БИБЛИОТЕКА | 2003 |
|
RU2228934C1 |
| ПРОИЗВОДНЫЕ 2-(2,6-ДИОКСОПИПЕРИДИН-3-ИЛ)ИЗОИНДОЛИНА, ИХ ПОЛУЧЕНИЕ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ВОСПАЛИТЕЛЬНЫХ ЦИТОКИНОВ | 1999 |
|
RU2200159C2 |
Авторы
Даты
2012-06-27—Публикация
2005-08-10—Подача