Изобретение относится к технологии извлечения тетрафторида кремния из газов производств фтороводорода и фосфорной кислоты.
Изобретение направлено на получение синтетического флюорита, обладающего высокими сорбционными свойствами по отношению к тетрафториду кремния.
Основной проблемой извлечения тетрафторида кремния из разбавленных технологических газов является его концентрирование.
Известно извлечение SiF4 из технологических газов хемосорбцией на фторидах металлов щелочной и щелочноземельной групп. Из-за низкой скорости взаимодействия SiF4 с фторидами щелочноземельных металлов, таких как Ва, Sr, Ca, предпочтение отдано NaF [Галкин Н.П. и др. Улавливание и переработка фторсодержащих газов. - М.: Атомиздат, 1975, сс.77-80]. Однако использование NaF с целью извлечения SiF4 также осложнено недостаточно высокой сорбционной емкостью, выражаемой соотношением масс SiF4/NaF - 0,24/1,0, высокой температурой десорбции SiF4 при термическом разложении образовавшегося Na2SiF6, приводящей к плавлению сорбента, что отмечено в работе [Современные неорганические фториды. Труды третьего международного сибирского семинара. Российская академия наук, институт химии дальневосточного отделения Российской академии наук. - 2008, сс.77-84]. Кроме того, отработанный сорбент NaF не находит применение в производстве фтороводорода из плавикового шпата. Наиболее приемлемым в производстве фтороводорода в качестве сорбента SiF мог бы быть CaF2 при наличии удовлетворительной сорбционной способности. Проведенные нами исследования сорбционной способности плавикового шпата по отношению к SiF при их взаимодействии в кипящем слое в течение 70 часов показали образование CaSiF6 всего 18,7%. Возникла необходимость исследовать сорбционную способность флюорита, полученного искусственным путем.
Однако известно, что синтетический флюорит, независимо от способов его получения с использованием кальцийсодержащих соединений СаО, Са(ОН)2, СаСО3, CaSO4, обладает общим существенным недостатком, а именно: плохой фильтруемостью, высокой влажностью и низким содержанием основного вещества, в частности, при его получении из раствора кремнефтористоводородной кислоты [Зайцев В.А. Производство фтористых соединений при переработке фосфатного сырья. - М.: Химия, 1982, cc.128-130; Позин М.Е. Технология минеральных солей. - Л.: Госхимиздат, 1961, с.757]:

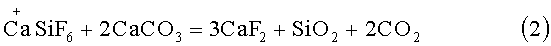
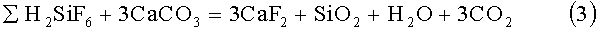
Известен способ получения CaF2 осаждением гексафторосиликата кальция из раствора кремнефтористоводородной кислоты оксидом кальция с последующим разложением полученной соли при 380-400°С [Зайцев В.А. и др. Производство фтористых соединений при переработке фосфатного сырья. - М.: Химия, 1982, 128-130 с., прототип]:
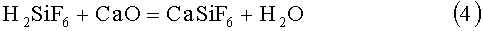
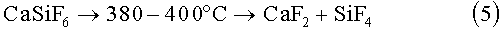
Существенными недостатками данного способа являются очень плохая фильтруемость осадка CaSiF6, необходимость дополнительного извлечения растворенного CaSiF6 из маточного раствора, недостаточно высокое качество получаемого CaF2.
Технической задачей, решаемой изобретением, является получение легко фильтруемого гексафторосиликата кальция для последующего термического разложения до синтетического флюорита с высокими сорбционными свойствами по отношению к тетрафториду кремния.
Решение поставленной задачи достигается тем, что в способе получения синтетического флюорита путем взаимодействия раствора кремнефтористоводородной кислоты и кальцийсодержащего соединения, отделения осадка от маточного раствора, сушки и прокалки при 380-400°С порошок карбоната кальция и 3,5-6,5 молярный раствор кремнефтористоводородной кислоты добавляют в нагретый до 60-80°С, насыщенный гексафторосиликатом кальция, содержащий не менее 3,5 моля кремнефтористоводородной кислоты раствор или в оборотный маточный раствор. Объем добавляемого в зону реакции раствора кремнефтористоводородной кислоты поддерживают равным убыли возвращаемого в зону реакции оборотного маточного раствора после отделения осадка гексафторосиликата кальция. Соотношение фтора и кремния 6:1 поддерживают в растворе кремнефтористоводородной кислоты добавлением фтороводорода при недостатке фтора и диоксида или тетрафторида кремния при избытке фтора.
В отличие от прототипа, при осуществлении которого использовалась несбалансированная по фтору и кремнию кремнефтористоводородная кислота, которая подвергалась практически полной нейтрализации добавлением оксида кальция без нагрева реакционной массы и учета содержания растворенного CaSiF6 в растворе H2SiF6 определенной концентрации, что неизбежно приводило к получению практически не фильтруемого геля CaSiF6 и снижению качества CaF2, получаемого при термическом разложении CaSiF6, нами было установлено, что очень хорошо фильтруемый осадок CaSiF6 образуется при добавлении 3,5-6,5 молярного раствора H2SiF6 и порошка карбоната кальция в нагретый до 60-80°С насыщенный солью CaSiF6 раствор кремнефтористоводородной кислоты концентрации не менее 3,5 моля.
В дальнейшем вместо насыщенного солью CaSiF6 раствора H2SiF6, используют оборотный маточный раствор после отделения осадка, благодаря чему отпадает необходимость дополнительного извлечения растворенного CaSiF6 из маточного раствора и утилизации маточного раствора. При этом объем добавляемого в зону реакции раствора кремнефтористоводородной кислоты поддерживают равным убыли, происходящей за счет потерь с влагой осадка и испарения возвращаемого в зону реакции оборотного маточного раствора. Практически при использовании 5-6 молярной кремнефтористоводородной кислоты соотношение их объемов варьируют в пределах 1:2.
Для обеспечения высокого качества CaSiF6 и получаемого из него CaF2 в раствор кремнефтористоводородной кислоты, получаемой водной абсорбцией SiF4 из технологических газов и, как правило, не сбалансированной по фтору или кремнию в соотношении 6:1 [см. Зайцев В.А. и др. Производство фтористых соединений при переработке фосфатного сырья. - М.: Химия, 1982, сс.29-31], соответствующем гексафторокремниевой кислоте, добавляют фтороводород при недостатке фтора или диоксид или тетрафторид кремния при избытке фтора. Это позволяет исключить на стадии получения CaSiF6 образование примеси CaF2 или SiO2, существенно ухудшающих фильтрационные свойства, да и качество CaSiF6, а после его термического разложения и качество CaF2.
Примеры
Серия 1. В концентрированный до 6,5 молей и в основном сбалансированный по фтору и кремнию раствор состава H2SiF6 при перемешивании добавляли равномерно в течение 1 часа порошок СаСО3 марки «ХЧ» в количестве, не превышающем 50% от стехиометрически необходимого по реакции (1), т.к. при большем количестве введенного СаСО3 образуется нефильтруемый гель (таблица 1, опыт 3). Маточный раствор был использован в качестве буферного раствора в очередном опыте и т.д. В опытах 4-6 без нагрева маточного раствора фильтруемость осадка хотя и лучше, но еще недостаточная. При проведении осаждения в нагретом до 60°С, насыщенном солью CaSiF6 маточном растворе достигается очень хорошая фильтруемость осадка CaSiF6 (опыт 7-9).
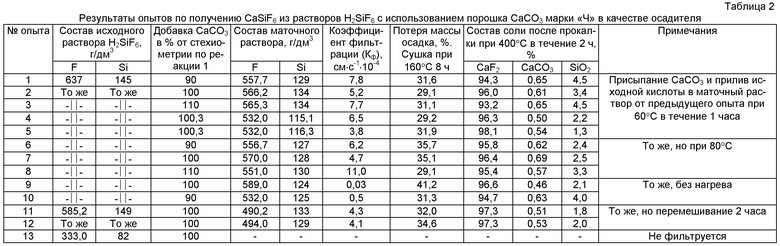
Серия 2. В данной серии опытов изучено влияние температуры, концентрации H2SiF6, времени взаимодействия реагирующих веществ при их соотношении, близком стехиометрическому по реакции (1), при равномерном и пропорциональном их введении в маточный раствор от предыдущего опыта. Результаты таблицы 2 свидетельствуют, что существенное влияние на фильтруемость осадка CaSiF6 оказывают температура буферной среды и концентрация исходной кислоты H2SiF6. Незначительное снижение содержания CaF2 и увеличение содержания SiO2 в продукте после прокалки CaSiF6 обусловлено использованием менее активного CaCO3 марки «ч» вместо «хч».
Серия 3. В данной серии опытов, результаты которых представлены в таблице 3, изучена зависимость растворимости CaSiF6 от концентрации H2SiF6 и влияние растворенного CaSiF6 на фильтруемость осадка при проведении осаждения CaSiF6 в насыщенном солью CaSiF6 растворе H2SiF6, чем, по сути, и является маточный раствор.
Результаты опытов 5-7 из таблицы 3 свидетельствуют, что очень хорошая фильтруемость осадков достигается при использовании ≥3,5 молярной кислоты H2SiF6, насыщенной растворенным CaSiF6, в качестве буферного раствора, в роли которого может использоваться маточник от предыдущего опыта. Причем при достижении в опыте 5 концентрации фтора в исходном растворе, обеспечивающей баланс исходного и конечного содержания фтора (ΔF-=0), достигается самое высокое содержание CaSiF6 и CaF2, даже при использовании менее активного CaCO3 марки «Ч» в сравнении с «ХЧ». Масс-спектрометрический анализ газовой фазы после термического разложения CaSiF6 при 400°С показал содержание SiF4 99,0%.
Серия 4. В данной серии опытов изучена сорбционная активность полученного синтетического флюорита по отношению к тетрафториду кремния в сравнении с плавиковым шпатом марки ФФ-95. Результаты опытов приведены в таблице 4.
Примеры
Вариант 1. В качестве сорбента SiF4 был использован плавиковый шпат с содержанием: CaF2 - 97,6%; CaCO3 - 0,25%; SiO2 - 1,64%. Технологический газ, содержащий SiF4 - 15-20%, HF - 8-10% и воздух, контактировали в кипящем слое с порошком CaF2 приведенного состава.
Вариант 2. Условия проведения опыта аналогичные, только в качестве сорбента SiF4 был использован синтетический флюорит состава: CaF2 - 99,1%; CaCO3 - 0,37%; SiO2 - 0,6%, полученный прокалкой при 380-400°С гексафторосиликата кальция, осажденного из раствора кремнефтористоводородной кислоты карбонатом кальция.
Вариант 2*. Условия опыта аналогичные, только в качестве сорбента был использован CaF2, полученный в результате термического разложения при температуре 380-400°С продукта со стадии улавливания SiF4, при проведении опытов по варианту 2.
Из результатов опытов таблицы 4 видно, что сорбционная емкость синтетического флюорита в 5 раз больше в сравнении с плавиковым шпатом при одинаковом времени контакта с газом до момента насыщения. При повторном цикле сорбции SiF4 на синтетическом CaF2 (вариант 2) динамика и степень насыщения (образования) CaSiF6 практически сохранились.


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ МОНОСИЛАНА | 2011 |
|
RU2466089C1 |
| СПОСОБ ПОЛУЧЕНИЯ СИНТЕТИЧЕСКОГО ФЛЮОРИТА | 2011 |
|
RU2472705C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФТОРИДА НАТРИЯ ИЗ КРЕМНЕФТОРИСТЫХ СОЕДИНЕНИЙ | 2000 |
|
RU2175639C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ФТОРА ИЗ ФТОРИДСОДЕРЖАЩИХ СОЕДИНЕНИЙ | 1998 |
|
RU2155709C2 |
| СПОСОБ ПОЛУЧЕНИЯ КРЕМНЕФТОРИДА НАТРИЯ | 2002 |
|
RU2226502C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТЕТРАФТОРИДА КРЕМНИЯ | 1991 |
|
RU2046095C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИСКУССТВЕННОГО ПЛАВИКОВОГО ШПАТА (CaF) ИЗ ОТХОДА ПРОИЗВОДСТВА ФОСФОРНОЙ КИСЛОТЫ (ФОСФОГИПСА) ДЛЯ ПРИМЕНЕНИЯ В ТЕХНОЛОГИИ ПРОИЗВОДСТВА ЦЕМЕНТА | 2015 |
|
RU2604693C1 |
| СПОСОБ ПОЛУЧЕНИЯ КРЕМНЕФТОРИСТОВОДОРОДНОЙ КИСЛОТЫ | 2006 |
|
RU2324649C2 |
| Способ инактивации примесей в сорбенте фторид лития | 2016 |
|
RU2627427C1 |
| СПОСОБ ПОЛУЧЕНИЯ КРЕМНЕФТОРСОДЕРЖАЩЕГО РАСТВОРА ДЛЯ ПРОИЗВОДСТВА ФТОРИДА АЛЮМИНИЯ | 1997 |
|
RU2116966C1 |
Изобретение относится к получению синтетического флюорита, обладающего высокими сорбционными свойствами по отношению к тетрафториду кремния. Порошок карбоната кальция и 3,5-6,5 молярный раствор кремнефтористоводородной кислоты добавляют в нагретый до 60-80°С, насыщенный гексафторосиликатом кальция, содержащий не менее 3,5 моля кремнефтористоводородной кислоты раствор, или в оборотный маточный раствор. Объем добавляемого в зону реакции раствора кремнефтористоводородной кислоты поддерживают равным убыли возвращаемого в зону реакции оборотного маточного раствора после отделения осадка гексафторосиликата кальция. Соотношение фтора и кремния 6:1 поддерживают в растворе кремнефтористоводородной кислоты добавлением фтороводорода при недостатке фтора и диоксида или тетрафторида кремния при избытке фтора. Изобретение обеспечивает получение высококачественного синтетического флюорита, используемого в качестве сорбента тетрафторида кремния, а также в качестве сырья в производстве фтороводорода и тетрафторида кремния, используемого в электронной, световолоконной и других областях техники. 3 з.п. ф-лы, 4 табл.
1. Способ получения синтетического флюорита путем взаимодействия раствора кремнефтористоводородной кислоты и кальцийсодержащего соединения, отделения осадка от маточного раствора, сушки и прокалки при 380-400°С, отличающийся тем, что порошок карбоната кальция и 3,5-6,5 молярный раствор кремнефтористоводородной кислоты добавляют в нагретый до 60-80°С, насыщенный гексафторосиликатом кальция, содержащий не менее 3,5 моля кремнефтористоводородной кислоты раствор.
2. Способ по п.1, отличающийся тем, что в качестве насыщенного раствора используют оборотный маточный раствор.
3. Способ по п.1, отличающийся тем, что объем добавляемого в зону реакции раствора кремнефтористоводородной кислоты поддерживают равным убыли возвращаемого в зону реакции оборотного маточного раствора после отделения осадка гексафторосиликата кальция.
4. Способ по п.1, отличающийся тем, что соотношение фтора и кремния 6:1 поддерживают в растворе кремнефтористоводородной кислоты добавлением фтороводорода при недостатке фтора и диоксида или тетрафторида кремния при избытке фтора.
| Способ получения фтористого кальция | 1983 |
|
SU1142446A1 |
| Способ получения фтористого кальция | 1975 |
|
SU585807A3 |
| СПОСОБ ПОЛУЧЕНИЯ ФТОРИДА КАЛЬЦИЯ | 1996 |
|
RU2072324C1 |
| Способ получения фторида кальция | 1985 |
|
SU1286520A1 |
| ДИНАМИЧЕСКИЕ ЖИДКОСТНЫЕ ЗОНЫ В КОНТАКТНЫХ ЛИНЗАХ | 2013 |
|
RU2535658C2 |
| СПОСОБ И ФРЕЗЕРНОЕ УСТРОЙСТВО ДЛЯ ВОЗВЕДЕНИЯ В ГРУНТЕ ИЗОЛЯЦИОННЫХ СТЕН | 2005 |
|
RU2307897C2 |
Авторы
Даты
2012-10-27—Публикация
2011-02-25—Подача