Область техники
Настоящее изобретение относится к процессу производства метанола, диметилового эфира и низкоуглеродистых олефинов из синтез-газа.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Синтез метанола является важным процессом в химической технологии. В настоящее время катализатор Cu-Zn-Al является главным компонентом широко используемого промышленного катализатора для синтеза метанола при низком давлении. В основном он приготавливается способом соосаждения, и полученный катализатор представляет собой смесь меди, цинка и окислов алюминия. Например, патент США 4436833 раскрывает способ соосаждения, включающий смешивание раствора меди, цинка и нитратов алюминия с углекислым натрием как агента осаждения, чтобы сформировать углеродистый осадок, затем смывая ионы натрия дистиллированной водой, высушивая и прокаливая осадок, чтобы получить смесь меди, цинка и окислов алюминия для каталитического синтеза метанола. Однако этот катализатор имеет недостаток, заключающийся в том, что трудно смывать ионы натрия и управлять температурой во время процесса восстановления, приводящего к значительному уменьшению активности катализатора.
Патент США 4366260 раскрывает способ производства метанола или смеси метанола и диметилового эфира. Катализатор, используемый в этом способе, является медным катализатором Ренея, который получен из сплава, содержащего от 35 до 60% по весу алюминия, от 0,1 до 25% по весу цинка и остаток в основном в виде меди. Специалистам в данной области известно, что сплав медный катализатор Ренея - кристаллический сплав. Выход метанола под воздействием катализатора в условиях реакции, подходящих для производства метанола из синтез-газа, является относительно низким (только 10,9%).
Диметиловый эфир (ДМЭ) является широкоприменяемым, безвредным для окружающей среды, сверхчистым продуктом - заменителем автомобильного и бытового топлива. Имеются в основном два способа производства диметилового эфира: одноступенчатый и двухступенчатый. Двухступенчатый способ состоит в синтезе метанола из синтез-газа с последующей дегидратацией с получением диметилового эфира. Одноступенчатый способ включает синтез диметилового эфира из исходного сырья - синтез-газа за одну стадию и содержит три ступени реакции, которые зависят друг от друга и идут последовательно:




Хотя все три реакции обратимы, весь процесс реакции может продолжаться в состоянии, которое отклоняется от термодинамического равновесия, поскольку продукты от каждой стадии реакции расходуются в следующей реакции. Следовательно, по сравнению с единственной реакцией синтеза метанола условия для процесса реакции синтеза диметилового эфира непосредственно из синтез-газ являются намного более умеренными, и однопроходное преобразование СО намного эффективнее. По сравнению с двухступенчатым способом одноступенчатый способ синтеза диметилового эфира выполняется без промежуточной процедуры синтеза метанола, и он имеет преимущество более простого процесса, меньшего количества устройств и требует меньших производственных и эксплуатационных расходов. Таким образом, одноступенчатый способ синтеза диметилового эфира очень интересен для исследований и коммерческих разработок во многих странах. Система катализаторов для одноступенчатого синтеза диметилового эфира в основном представляет собой физическую смесь катализатора для синтеза метанола и катализатора дегидратации метанола. Промышленный катализатор для синтеза метанола в основном содержит один или несколько атомов Сu, Zn, А1 и Сr, и специалистам в данной области известно, что катализатор представляет собой кристаллический сплав, тогда как катализатор дегидратации метанола в основном выбран из твердых кислых материалов.
Патент США 5389689 раскрывает способ приготовления катализатора для получения диметилового эфира в одной стадии, включающей распыление смеси, содержащей окись цинка, окись меди или окись хрома и окись алюминия с величиной частиц примерно от 0,1 до 20 µm, сжатие под давлением 100-500 кг/см, чтобы спрессовать окислы в единую массу, взвешивание в растворителе с повторным распылением жидкого осадка, чтобы получить из него катализатор. Условия реакции включают мольное отношение Н2/СО, равное единице, температуру реакции 280°С и давление реакции 3 МПа; при этом степень преобразования СО составляет 60,1%, выход диметилового эфира составляет 42,8% и выход СO2 составляет 14,4%. Катализатор для получения диметилового эфира имеет низкую активность, желательная температура является относительно высокой и преобразование СО является относительно низким. Кроме того, приблизительно одна треть СО преобразуется в бесполезный СО2 из-за низкой активности катализатора при дегидратации. Во время процесса реакции происходят другие побочные реакции, приводящие к наличию углерода для реакции в основном меньше 60%. Процесс реакции менее рентабелен.
Легкие олефины, которые в основном относятся к этилену и пропилену, являются очень важным сырьем для химического производства. В настоящее время более 90% легких олефинов производятся крекингом легкой нефти. Однако предложение легких олефинов не удовлетворяет потребности рынка. Ввиду непрерывного экономического развития и увеличивающейся нехватки нефти абсолютно необходимо найти замену источника легких олефинов. Методика непосредственного производства олефинов из синтез-газа вытекает из традиционного синтеза F-T. Поскольку углеродное число продукта, полученного из синтеза F-T катализатором, следует за законом распределения S-T, селективность низших углеродных олефинов является низкой. Приготовление катализаторов, имеющих высокую активность и селективность, представляет большой интерес для современных исследователей.
Патент CN1065026A раскрывает катализатор для производства этилена из синтез-газа. Катализатор содержит один окисел элемента, выбранного из Cu, Al, Ti, Nb и Hf, одного или двух окислов элемента, выбранного из Nb, Y, Ga, Ge, В и Т1, одного или нескольких окислов элемента, выбранного из Sn, Pb, Sc, La, Рr, Се и Nd, и приготавливается способом, включающим пропитку, соосаждение, механическое смешивание, перемешивание суспензии, сочетания пропитки и соосаждения или механического смешивания и пропитки. Хотя селективность этилена может составить до 94%, когда катализатор используется для производства этилена из синтез-газа, преобразование СО составляет только 15%.
Патент CN1537674А раскрывает углеродный катализатор для производства этилена, пропилена и бутилена из синтез-газа. Катализатор содержит α-Fe, FexCf, (Fe, Mn) О, CuO, ZnO и K2O, и его удельная поверхность составляет 350-400 м2/г. Катализатор для приготовления низших углеродных олефинов из синтез-газа приготавливается, загружая Fe на активный углерод способом вакуумной пропитки, распределяя Fe и другие вещества на активный углерод и прокаливая результирующий продукт при температуре 500-800°С. Используя катализатор, преобразование СО при 300°С составляет 97,3%, и С--С- селективность в органических продуктах составляет 43%. Однако содержание метана и этана в продуктах является относительно высоким (15% и 12%, соответственно, на основе всех органических продуктов). Следовательно, доступность углерода является низкой.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение имеет целью преодолевать недостатки низкого преобразования СО, селективности целевого продукта и доступности углерода предыдущих процессов приготовления метанола, диметилового эфира и/или низших углеродных олефинов из синтез-газа, и обеспечивать процесс производства метанола, диметилового эфира и/или низших углеродных олефинов из синтез-газа с высоким преобразованием СО, хорошей селективностью целевого продукта и доступностью углерода.
Настоящее изобретение обеспечивает процесс производства метанола, диметилового эфира и легких олефинов из синтез-газа, при этом указанный процесс содержит стадию контакта синтез-газа с катализатором в условиях, обеспечивающих преобразование синтез-газа в метанол, диметиловый эфир и низкоуглеродистый олефин, отличающийся тем, что катализатор содержит аморфный сплав, состоящий из первого компонента А1 и второго компонента, исключающего элемент А1, и указанный второй компонент содержит один или несколько элементов или их окислов, выбранных из группы IA, IIIА, IVA, VA, IB, ПВ, IVB, VB, VIB, VIIB и VIII, и ряд лантанидов Периодической таблицы элементов.
В изобретательском процессе производства метанола, диметилового эфира и низкоуглеродистого олефина из синтез-газа используется катализатор, содержащий аморфный сплав, состоящий из первого компонента А1 и второго компонента, причем указанный второй компонент является одним или несколькими элементами или их окислами, выбранными из группы IA, IIIА, IVA, VA, IB, IIВ, IVB, VB, VIB, VIIB и VIII, и ряда лантанидов периодической таблицы элементов, результатом которого является очень высокое преобразование СО, селективность целевого продукта и доступность углерода.
ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фигуры 1-3 являются XRD спектром сплавов, приготовленных по примерам и сравнительным примерам изобретения.
МЕТОДЫ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Термин "синтез-газ" означает смесь газов исходного сырья, содержащую СО и Н2 в качестве главных компонентов. Синтез-газ в основном извлекается из твердого сырья (уголь, кокс), жидкого сырья (легкая нефть, сырая нефть) и газообразного сырья (природный газ, попутный газ). Например, синтез-газ может быть одним или несколькими газами, выбранными из коксовых газов, сжиженных газов, водяных газов, полуводяных газов, природных газов и попутных газов нефтяных месторождений.
Настоящее изобретение обеспечивает процесс производства метанола, диметилового эфира и низкоуглеродистого олефина из синтез-газа, в котором технологический процесс содержит стадию контакта синтез-газа с катализатором в условиях, обеспечивающих преобразование синтез-газа в метанол, диметиловый эфир и низкоуглеродистый олефин, отличающийся тем, что катализатор содержит аморфный сплав, состоящий из первого компонента А1 и второго компонента, при этом указанный второй компонент, является одним или несколькими элементами или их окислами, выбранными из группы IA, IIIА, IVA, VA, IB, IIВ, IVB, VB, VIB, VIIB и VIII, и ряда лантанидов периодической таблицы элементов, при этом указанный второй компонент отличается от первого компонента А1.
Согласно процессу по настоящему изобретению, предпочтительно количество А1 составляет 0,5-60% от общего веса аморфного сплава, предпочтительно 20-55% по весу, и количество второго компонента - 40-99,5% по весу, предпочтительно 45-80% по весу. С другой стороны, если способ приготовления аморфного сплава содержит щелочную промывку А1, количество А1 - предпочтительно 0,5-20% по весу, более предпочтительно 5-15% по весу, и количество второго компонента - предпочтительно 80-99,5% по весу, более предпочтительно 85-95% по весу.
Согласно процессу по настоящему изобретению, предпочтительно, чтобы указанный второй компонент представлял собой один или несколько элементов или их окислов, выбранных из ряда лантанидов и третьего, четвертого и пятого рядов группы IA, IIIА, IVA, VA, IB, IIВ, IVB, VB, VIB, VIIB и VIII из периодической таблицы элементов, более предпочтительно из одного или несколько элементов или их окислов, выбранных из Сu, Zn, V, Сr, Mn, Fe, Со, Ni, К, Zr, Mo, Sn, С, Сu, La и Р. В некоторых примерах воплощения, указанный второй компонент содержит медь или ее окись. В некоторых других примерах воплощения, указанный второй компонент содержит или состоит из Сu и Zn или их окислов. В некоторых других примерах воплощения, в которых аморфный сплав содержит медь, количество элементов группы VIII или их окислов меньше чем 30% по весу, предпочтительно меньше чем 20% по весу от общего веса аморфного сплава. В некоторых других примерах воплощения, в которых аморфный сплав содержит медь, сплав может не содержать элементов группы VIII или их окислов.
Согласно процессу по настоящему изобретению, компоненты в указанном аморфном сплаве могут присутствовать в чисто аморфном виде или в виде смеси аморфных сплавов и микрокристаллических и/или кристаллических сплавов (то есть часть сплава находится в аморфном состоянии), в котором микрокристаллические и кристаллические сплавы присутствуют в общем объеме предпочтительно меньше чем 30% по весу. Присутствие аморфного сплава может быть обнаружено с помощью дифракционного рентгеновского анализа (XRD). Широкий пик дифракции в спектре XRD означает, что сплав находится в виде аморфного сплава. Предпочтительно, аморфный сплав-порошок имеет размер частиц меньше чем или равный 500 меш.
В процессе по настоящему изобретению, указанный катализатор дополнительно содержит матрицу, в которой распределен аморфный сплав. Предпочтительно количество аморфного сплава составляет 20-90% от общего веса катализатора, более предпочтительно 20-60% по весу, и количество матрицы - 10-80% по весу, более предпочтительно 40-80% по весу.
Для процесса по настоящему изобретению матрица может быть выбрана из тех, которые часто используются в катализаторах в данной технологии, например один или несколько неокислительных пористых неорганических окислов, молекулярные сита, активный углерод, глины, фосфаты (например, ортофосфат алюминия), сульфаты (например, сульфат магния) и металлические галоидные соединения (например, FeCl, SnCu, ZnCl2).
Неокислительные пористые неорганические окиси известны специалисты в данной области, и могут быть выбраны как один или несколько из оксида алюминия, кремнезема, кремнезема оксида алюминия, двуокиси циркония, двуокиси титана, окиси цинка, окиси галлия, окиси бора и окиси щелочно-земельного металла. Неокислительные пористые неорганические окиси доступны на рынке, или могут быть приготовлены способом соосаждения, который известен специалистам в данной области.
Указанные молекулярные сита известны специалистам, например кремниево-алюминиевые молекулярные сита, гетероатомные молекулярные сита.
Указанные глины известны специалистам в данной области, например каолин, галлуазит, монтмориллонит, кизельгур, сапонит, гекторит, сепиолит, аттапульгит, гидроталькит, бентонит; из них наиболее предпочтительны каолин и монтмориллонит.
Как известно к специалистам в данной области, например, в матрицу может быть загружена гетерополикислота, фосфорно-вольфрамовая кислота и/или фосфорно-молибденовая кислота.
В соответствии с процессом по настоящему изобретению, предпочтительно указанная матрица содержит присадку, которая загружена на или в матрицу и выбрана из одного или нескольких элементов или ее окислов группы IA, IIА, IIIА, IVA, VA, IB, IIВ, IVB и VIII, и ряда лантанидов периодической таблицы элементов. Более предпочтительно, указанная присадка - один или несколько элементов или их окислов, выбранных из ряда лантанидов и третьего, четвертого и пятого рядов группы IA, IIIА, IVA, VA, IB, IIВ, IVB, VB, VIB, VIIB и VIII периодической таблицы элементов, более предпочтительно из одного или нескольких элементов или окислов, выбранных из К, Са, Mr, Ga, Sn, Р, Сu, Zn, Zr, Fe, и La. Загрузка присадки в матрицу может повысить активность и селективность реакции.
В соответствии с процессом по настоящему изобретению, предпочтительно количество присадки составляет 0,5-40% от общего веса матрицы.
Катализатор, состоящий из аморфного сплава и матрицы, имеет высокую активность катализатора, селективность целевого продукта, стойкость к отравлению и повторяемость свойств катализатора. Вместе с тем стабильность катализатора также является высокой. Период регенерации катализатора может быть равен 3 месяцам или более. Кроме того, катализатор удобно используется в реакции. Регенерация и активация катализатора, которые в другом случае должны быть выполнены до реакции в известном уровне техники и часто является комплексным соединением, трудным и отнимающим много времени, в настоящем процессе могут быть пропущены. Изобретательский способ приготовления катализатора является простым, легко выполнимым и легко расширен до промышленных масштабов.
Предпочтительно, катализатор может быть приготовлен следующим образом:
(1) Приготовление аморфного сплава
Способ приготовления аморфного сплава содержит стадии легирования смеси первого компонента А1 и второго компонента в вышеупомянутых количествах под вакуумом при температуре выше температуры их плавления, и быстрое охлаждение сплавленной смеси под вакуумом, в котором условия для быстрого охлаждения включают линейную скорость медного валка 20-40 м/с, давление инжекции 0,05-0,1 МПа и температуру инжекции 1100-2000°С. Затем полученный сплав распыляется до размера частиц меньше чем или равного 500 меш (то есть больше чем или равного 25 нм), чтобы получить порошок сплава.
(2) Приготовление матрицы
Вышеупомянутая присадка в количестве 0,5-40% по весу загружается во всю матрицу или в ее часть способом ионного обмена, способом пропитки или способом осаждения, известным специалистам в данной области.
Например, в способе ионного обмена матрица прилипает с Н+ и/или Na+ к поверхности, и водный раствор, содержащий ионы элемента присадки, может быть однородным, смешанным, нагретым до 80°С и размешиваться в течение 1 часа; смесь затем фильтруется, и продукт фильтрации несколько раз промывается дистиллированной водой и сушится при температуре 110°С.
По способу пропитки матрица может быть пропитана в водном растворе, содержащем ионы элемента присадки, при 60°С в течение 8 часов, высушивается при 110°С и затем прокаливается при 550°С в течение 2 часов.
В способе осаждения, например, матрица и водный раствор, содержащий ионы элемента присадка, могут быть смешаны в однородную массу, затем добавляется осаждающий агент, например, углекислый натрий, чтобы получить осадок, и полученный осадок фильтруется, несколько раз промывается дистиллированной водой, сушится при 110°С и затем прокаливается при 550°С в течение 2 часов.
(3) Приготовление аморфного сплава и матрицы
Как известно специалистам, аморфный сплав и матрица могут быть приготовлены способом механического смешивания без любого другого компонента, или с добавлением клея перед механическим смешиванием. Указанный клей может быть силикатный золем, алюминиевым золем или их смесью.
Способ приготовления катализатора может содержать стадию промывки аморфного сплава или катализатора щелочным раствором, чтобы извлечь часть А1 в аморфном сплаве. Например, стадия промывки щелочью может быть выполнена, контактируя щелочной раствор, например гидроокись натрия с концентрацией 10-25% по весу с порошком аморфного сплава или с катализатором, полученным из аморфного сплава и матрицы, чтобы извлечь часть А1 в аморфном сплаве. Условия для щелочной промывки, например время, температура, концентрация щелочи, могут зависеть от состава аморфного сплава или катализатора и процесса реакции, в котором используется катализатор. Предпочтительно, количество алюминия в сплаве после стадии щелочной промывки должно быть не меньше чем 0,5% по весу, более предпочтительно не меньше чем 5% по весу, но не больше 60% по весу, более предпочтительно не больше 55% по весу, и наиболее предпочтительно не больше 20% по весу, или даже не больше 15% по весу от общего веса сплава. Температура контакта от 0 до 50°С и время контакта от 0,5 до 5 часов. Что касается стехиометрии А1 в сплаве, то щелочь, например углекислый натрий, используется в избытке от 10 до 30% по весу. Предпочтительная стадия извлечения А1 щелочью может увеличить скорость диффузии реагентов и, таким образом, увеличить активность катализатора.
Состав катализатора определяется рентгенофлуоресцентным спектрометром (XRFS). Экспериментальный прибор, используемый в рентгенофлуоресцентном спектрометре типа 3271, поставляется корпорацией Rigaku Industrial Corporation. Напряжения возбуждения родиевой цели - 50 кВ, и в эксперименте используется ток возбуждения 50 мА; интенсивность линии спектра каждого элемента обнаруживается сцинтилляционным счетчиком, и с помощью пропорционального счетчика выполняют количественный или полуколичественный анализ.
В соответствии с процессом по настоящему изобретению предпочтительные условия для преобразования синтез-газа в метанол, диметиловый эфир и низкоуглеродистый олефин включают температуру реакции 200-400°С, давление реакции 0,5-6 МПа, объемную скорость синтез-газа как исходного сырья 1000-1000 мл/г·час и мольное отношение между Н2 and СО в синтез-газе от 1 до 3.
Когда настоящий процесс используется для получения метанола и диметилового эфира как целевых продуктов и низкоуглеродных олефинов как побочных продуктов, температура реакции - предпочтительно 200-270°С и давление реакции - предпочтительно 1-6 МПа. Когда в результате настоящего процесса стремятся получить низкоуглеродные олефины в качестве целевых продуктов, и метанол и диметиловый эфир в качестве побочных продуктов, температура реакции предпочтительно 270-400°С и давление реакции предпочтительно 0,5-2 МПа.
Реактор может быть реактором с псевдоожиженным слоем или реактором с неподвижным слоем, и сам процесс может быть выполнен в периодическом или непрерывном режиме.
Процесс согласно настоящему изобретению предпочтительно содержит стадию восстановления катализатора до контакта катализатора с синтез-газом. Стадия восстановления содержит загрузку в реактор катализатора в количестве от 1 до 5 граммов, и до реакции очистку реактора, содержащего катализатор, восстановительным газом при температуре очистки 130-600°С в течение 0,5-1 часа до активного катализатора. Восстановительный газ может быть смесью водорода в количестве 1-10% по весу с инертным газом, который может быть выбран из азота, гелия и аргона.
После стадии восстановления синтез-газ подается в реактор как исходное сырье с объемной скоростью 1000-1000 мл/г·час при температуре реакции 200-400°С и рабочем давлении 0,5-6 МПа. Синтез-газ может быть одним или несколькими газами, которые содержат Н2 и СО в мольном отношении от 1 до 3, например, один или несколько газов могут быть выбраны из коксовых газов, сжиженных газов, водяных газов, полуводяных газов, природных газов и попутных газов нефтяных месторождений.
Следующие примеры описывают и демонстрируют примерные варианты воплощения в рамках настоящего изобретения. Примеры даны исключительно для иллюстрации и не должны рассматриваться как ограничения настоящего изобретения, поскольку возможны многочисленные изменения, не выходя из духа и объема этого изобретения. Для специалистов в данной области различные модификации изобретения в дополнение к показанным и описанным здесь являются очевидными и входят в объем приложенной формулы изобретения.
Пример 1
1. Приготовление аморфного сплава
20 г порошкового алюминия (промышленной чистоты, ниже то же самое), 60 г медного порошка (промышленной чистоты, ниже то же самое) и 20 г ZnO (промышленной чистоты, ниже то же самое) смешивались и затем и нагревались в вакуумной печи с донной загрузкой под вакуумом порядка 10-2 Па и при температуре 1200°С смесь плавилась в течение 10 минут, затем в печь подавался газообразный аргон до тех пор, пока давление в печи не уравнивалось с атмосферным, получая, таким образом, жидкий расплав смеси Сu, А1 и ZnO.
Расплав Сu, А1 и ZnO был подвергнут быстрому охлаждению под вакуумом, чтобы получить сплав Al-Cu-ZnO. Условия быстрого охлаждения включали линейную скорость медного валка 30 м/с, давление инжекции 0,08 МПа и температуру инжекции 1300°С.
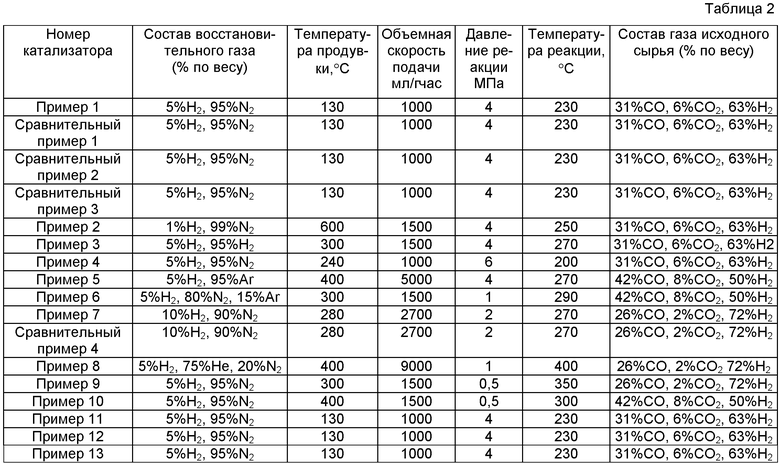
Полученный сплав распылялся в вентилируемой среде на частицы с максимальным размером 300 меш (то есть менее чем или равным 48 µм). Для дифракционного рентгеновского анализа полученного порошка использовался рентгеновский дифрактометр (типа D/MAX-2500 Сu Кα ray компании Rigaku Cooperation) с током 100 мА, ниже то же самое). Полученный спектр XRD показал, что присутствовал только широкой диффузионный пик при 29=42° (фигура 1(1)), который является типичной характеристикой аморфного сплава. Следовательно, полученный сплав Al-Cu-ZnO был сплавом в аморфном состоянии.
2. Приготовление матрицы смешанных окислов
112 г ZnO и 200 г дистиллированной воды смешивались с раствором, содержащим 100 г водного раствора 63,32% по весу ZrOCl2 (чистый для анализа, поставки Songhe Chemical Reagent Factory, ниже то же самое), 50 г водного раствора 15% по весу СаС12 (промышленной чистоты) и 50 г водного раствора 1% по весу НС1 (чистый для анализа, Beijing Chemical Works)), были добавлены по каплям с интенсивным перемешиванием, затем по каплям добавлялся водный раствор 5% по весу углекислого натрия (чистый для анализа, Beijing Chemical Works, ниже то же самое) до тех пор, пока рН фактор смешанной жидкости не стал равен 9. Полученная смесь дополнительно размешивалась в течение 1 часа после завершения добавления ингредиентов. Полученный осадок фильтровался, неоднократно промывался дистиллированной водой до полного удаления С1, высушивался при 110°С и прокаливался при 550°С в течение 2 часов, чтобы получить 160 г матрицы, содержащей 27,5% по весу ZrC2, 70% по весу ZnO и 2,5% по весу присадки СаО.
3. Приготовление катализатора
Вышеупомянутый аморфный сплав и матрица механически смешивались в весовом соотношении 2:3, таблетировались, распылялись и просеивались на частицы, имеющие размер от 20 до 40 меш. Состав полученного катализатора показан в таблице 1.
Пример 2
1. Приготовление аморфного сплава
Способ приготовления аморфного сплава был подобен описанному в примере 1. 55 г алюминиевого порошка и 45 г медного порошка смешивались, затем нагревались в вакуумной печи под вакуумом порядка 10-2 Па, и при температуре 1200°С смесь выдерживалась в расплавленном состоянии в течение 10 минут, затем в печь подавался газообразный аргон до тех пор, пока давление в печи не уравнивалось с атмосферным, получая, таким образом, расплав Сu и А1.
Расплав Сu и А1 быстро охлаждался под вакуумом, чтобы получить сплав Al-Cu. Условия быстрого охлаждения включали линейную скорость медного валка 30 м/с, давление инжекции 0,08 МПа и температуру инжекции 1300°С.
Полученный сплав распылялся в вентилируемой среде на частицы с максимальным размером 300 меш (то есть менее чем или равным 48 µм). Для дифракционного рентгеновского анализа (XRD) использовался рентгеновский дифрактометр. Полученный спектр XRD был аналогичен спектру, показанному на фигуре 1(1), который является типичной характеристикой аморфного сплава. Следовательно, полученный сплав Al-Cu был сплавом в аморфном состоянии.
2. Приготовление матрицы, содержащей активный углерод и хлориды металла
5 г FeCl3 (чистый для анализа, Jiangyin Hengye Chemical Engineering Co. Ltd., Китай, ниже то же самое), 5 г SnCl4 (чистый для анализа, Liaoyang Dingxin Chemical Engineering Co. Ltd., Китай), 30 г ZnCl2 (промышленной чистоты) и 60 г активного угольного порошка (Xinsen Tanye Co. Ltd., город Шаову, область Фуцзяни, Китай) размешивались, чтобы получить 100 г матрицы, содержащей 5% по весу FeCl3, 5% по весу SnCl4, 30% по весу ZnCl2, и 60% по весу активного углерода.
3. Приготовление катализатора
33 г аморфного сплава, 100 г матрицы, 12,5 г золя кремниевой кислоты (40% по весу, Sinopec Catalyst Company Qilu) и 25 г золя глинозема (20% по весу, Sinopec Catalyst Company Qilu) смешивались до однородного состава, извлекались с помощью экструдера, распылялись и просеивались на частицы, имеющие размер от 20 до 40 меш, высушивались под вакуумом порядка 10-1 Па и при температуре 120°С в течение 4 часов, чтобы получить катализатор, который содержал 23% по весу аморфного сплава, и его состав показан в таблице 1.
Пример 3
1. Приготовление аморфного сплава
10 г Р (промышленной чистоты), 5 г L2O3 (чистый для анализа, Zibo Rongruida Micro Materials Plant, ниже то же самое) и 10 г ZnO смешивались до однородного состава в тигле и затем прессовались, 45 г расплавленного медного порошка были добавлены в тигель, содержащий Р, Lа2О3 и ZnO, и охлаждались, затем в тигель было добавлено 30 г алюминиевого порошка при активном перемешивании. Полученная смесь была помещена в вакуумную печь с донной загрузкой с вакуумом порядка 10-2 Па, и при температуре 1200°С смесь выдерживалась в расплавленном состоянии в течение 10 минут, затем в печь подавался газообразный аргон до тех пор, пока давление в печи не уравнивалось с атмосферным, получая, таким образом, жидкий расплав смеси.
Расплав был быстро охлажден под вакуумом, чтобы получить сплав А1-Сu-Р-Lа2О3-ZnO. Условия быстрого охлаждения включали линейную скорость медного валка 30 м/с, давление инжекции 0,08 МПа и температуру инжекции 1300°С.
Полученный сплав распылялся в вентилируемой среде на частицы с максимальным размером 300 меш. Для дифракционного рентгеновского анализа (XRD) использовался рентгеновский дифрактометр. Конечный спектр XRD показал, что имеется только широкий диффузионный пик при 20-42° (полученный спектр XRD был аналогичен спектру на фигуре 1(1)), который является типичной характеристикой аморфного сплава. Следовательно, конечный продукт Cu-Al-P-La2O3-ZnO был сплавом в аморфном состоянии.
2. Приготовление матрицы молекулярного сита ZSM-5
233 г молекулярного сита ZSM-5 (экспериментальный образец от компании Sinopec Catalyst Company Jianchang, со структурой MFI: Nа2О<0,2% по весу, отношение Si/Al=40) и 3000 г 0,1 моль/л КОН (чистый для анализа, Beijing Chemical Works, ниже то же самое) смешивались, нагревались до 80°С и перемешивались в течение 1 часа; полученный осадок фильтровался и неоднократно промывался дистиллированной водой до нейтрального состояния, высушивался при 110°С и затем прокаливался при 550°С в течение 2 часов, чтобы получить 234 г матрицы, содержащей молекулярное сито ZSM-5 в количестве 99,5% по весу и 0,5% по весу присадки К2О.
3. Приготовление катализатора
Вышеупомянутый аморфный сплав и матрица механически смешивались в весовом соотношении 3:7, таблетировались, распылялись и просеивались на частицы, имеющие размер от 20 до 40 меш. Состав полученного катализатора показан в таблице 1.
Пример 4
1. Приготовление аморфного сплава
40 г алюминиевого порошка, 10 г Gа2О3 и 50 г медного порошка смешивались и затем помещались в вакуумную печь с донной загрузкой с вакуумом порядка 10-2 Па, и при температуре 1200°С смесь выдерживалась в расплавленном состоянии в течение 10 минут, затем в печь подавался газообразный аргон до тех пор, пока давление в печи не уравнивалось с атмосферным, получая, таким образом, жидкий расплав смеси.
Расплав был быстро охлажден под вакуумом, чтобы получить продукт Al-Cu-Gа2О3. Условия быстрого охлаждения включали линейную скорость медного валка 30 м/с, давление инжекции 0,08 МПа и температуру инжекции 1300°С.
Полученный сплав распылялся в вентилируемой среде на частицы с максимальным размером 300 меш. Для дифракционного рентгеновского анализа (XRD) использовался рентгеновский дифрактометр. Полученный спектр XRD показал, что присутствует только широкий диффузионный пик при 20=42° (полученный спектр XRD был аналогичен спектру на фигуре 1(1)), который является типичной характеристикой аморфного сплава. Следовательно, полученный сплав Al-Cu-Ga2O3 был сплавом в аморфном состоянии.
2. Приготовление матрицы гамма-Аl2О3 с присадкой
86 г гамма-Аl2О3 (образец от компании Sinopec Catalyst Company Jianchang, то же самое ниже) и 40 г водного раствора 52,5% по весу Zn(NO3)2 (чистый для анализа, Beijing Chemical Works, ниже то же самое) смешивались, чтобы пропитать Zn(NO3)2 на гамма-А12O3, смесь нагревалась до 60°С в течение 8 часов для старения, высушивалась при 110°С и затем прокаливалась при 550°С в течение 2 часов, чтобы получить гамма-Аl2О3, загруженный окисью ZnO.
5 г Lа(NО3)3 были загружены в раствор 23 г 22% по весу и пропитывались на гамма-Аl2О3 с ZnO; смесь нагревалась до 60°С в течение 8 часов для старения, высушивалась при 110°С и затем прокаливалась при 550°С в течение 2 часов, чтобы получить матрицу гамма-Аl2О3 с присадкой. Матрица содержала 86% по весу гамма-AL2O3, 9% по весу присадки ZnO и 5% по весу присадки Lа2О3.
3. Приготовление катализатора
Вышеупомянутый аморфный сплав и матрица механически смешивались в весовом соотношении 1:1, таблетировались, распылялись и просеивались на частицы, имеющие размер от 20 до 40 меш. Состав полученного катализатора показан в таблице 1.
Пример 5
1. Приготовление аморфного сплава
30 г алюминиевого порошка, 10 г ZnO, 10 г ванадия (промышленной чистоты), 5 г Сr (промышленной чистоты) и 45 г Сu смешивались и помещались в вакуумную печь с донной загрузкой с вакуумом порядка
10-2 Па и при температуре 1900°С плавились в течение 10 минут и затем в печь подавался газообразный аргон, пока давление в печи не уравнивалось с атмосферным, получая, таким образом, жидкий расплав смеси.
Расплав быстро охлаждался под вакуумом, чтобы получить сплав Al-Cu-V-Cr-ZnO. Условия быстрого охлаждения включали линейную скорость медного валка 30 м/с, давление инжекции 0,08 МПа и температуру инжекции 1500°С.
Полученный сплав распылялся в вентилируемой среде на частицы с максимальным размером 300 меш. Для дифракционного рентгеновского анализа (XRD) полученного порошка был использован рентгеновский дифрактометр.
Полученный спектр XRD показал, что присутствует только широкий диффузионный пик при 28=42° (полученный спектр XRD был аналогичен спектру на фигуре 1(1)), который является типичной характеристикой аморфного сплава. Следовательно, полученный сплав Al-Cu-V-Cr-ZnO был сплавом в аморфном состоянии.
2. Приготовление матрицы, содержащей сульфат магния и кремнезем
40 г сульфата магния (чистый для анализа, Beijing Wuzhou Shiji Hongxing Chemical Works), 10 г FeCl3, 11,8 г 85% по весу фосфорной кислоты (чистой для анализа, Beijing Chemical Works) и 40 г кремнезема (Wuxi Jindinglonghua Chemical Co., LTD, ниже то же самое) было смешано, и высушено под вакуумом при 120°С в течение 4 часов, чтобы получить 100 г матрицы.
3. Приготовление катализатора
Вышеупомянутый аморфный сплав и матрица механически смешивались в весовом соотношении 3:2, таблетировались, распылялись и просеивались на частицы, имеющие размер от 20 до 40 меш. Состав полученного катализатора показан в таблице 1.
Пример 6
1. Приготовление аморфного сплава
13 г активного угольного порошка, 15 г МnО2 (промышленной чистоты) и 2 г SiO2 смешивались до однородной массы, затем в эту смесь было быстро добавлено 5 г калия (промышленной чистоты), 20 г алюминия и 45 г Сu. После быстрого смешивания смесь была помещена в вакуумную печь с донной загрузкой с вакуумом порядка 10-2 Па и при температуре 1200°С смесь выдерживалась в расплавленном состоянии в течение 10 минут, затем в печь подавался газообразный аргон до тех пор, пока давление в печи не уравнивалось с атмосферным, получая, таким образом, жидкий расплав смеси.
Расплав быстро охлаждался под вакуумом, чтобы получить сплав Al-Cu-K-C-MnO2-SiO2. Условия быстрого охлаждения включали линейную скорость медного валка 30 м/с, давление инжекции 0,08 МПа и температуру инжекции 1200°С.
Полученный сплав распылялся в вентилируемой среде на частицы с максимальным размером 300 меш. Для дифракционного рентгеновского анализа (XRD) использовался рентгеновский дифрактометр. Полученный спектр XRD показал, что присутствует только широкий диффузионный пик при 29=42° (полученный спектр XRD был аналогичен спектру на фигуре 1(1)), который является типичной характеристикой аморфного сплава.
Следовательно, полученный продукта в виде сплава Al-Cu-K-C-MnO2-SiO2 был сплавом в аморфном состоянии.
2. Приготовление катализатора
Аморфный сплав и молекулярное сито SAPO-34 (экспериментальный образец от Sinopec Catalyst Company Jianchang filiale, со структурой СНА: Nа2О<0,2% по весу, отношение Si/Al=13) и матрица были смешаны механически в весовом соотношении 7:3; смесь таблетировалась, распылялась и просеивалась на частицы, имеющие размер от 20 до 40 меш; состав полученного катализатора показан в таблице 1.
Пример 7
1. Приготовление аморфного сплава
Способ приготовления был аналогичен способу примера 6. Полученный спектр XRD подобен спектру на фигуре 1(1).
2. Приготовление составного катализатора
Аморфный сплав и активный угольный порошок механически смешивались в весовом соотношении 9:1, таблетировались, распылялись и просеивались на частицы, имеющие размер от 20 до 40 меш. Состав полученного катализатора показан в таблице 1.
Пример 8
1. Приготовление аморфного сплава
20 г МnO2 и 5 г ZrO2 смешивались до однородного состава в тигле и затем прессовались, 5 г расплавленного Ni (промышленной чистоты) было добавлено в тигель и охлаждено, затем 50 г Fe (промышленной чистоты, ниже то же самое) и 20 г А1 были добавлены в тигель и смешаны. Полученная смесь была помещена в вакуумную печь с донной загрузкой с вакуумом порядка 10-2 Па и при температуре 1200°С смесь выдерживалась в расплавленном состоянии в течение 10 минут, затем в печь подавался газообразный аргон до тех пор, пока давление в печи не уравнивалось с атмосферным, получая, таким образом, жидкий расплав смеси.
Расплав быстро охлаждался под вакуумом, чтобы получить сплав Al-Ni-Fe-МnО2-ZrO2. Условия быстрого охлаждения включали линейную скорость медного валка 30 м/с, давление инжекции 0,08 МПа и температуру инжекции 1300°С.
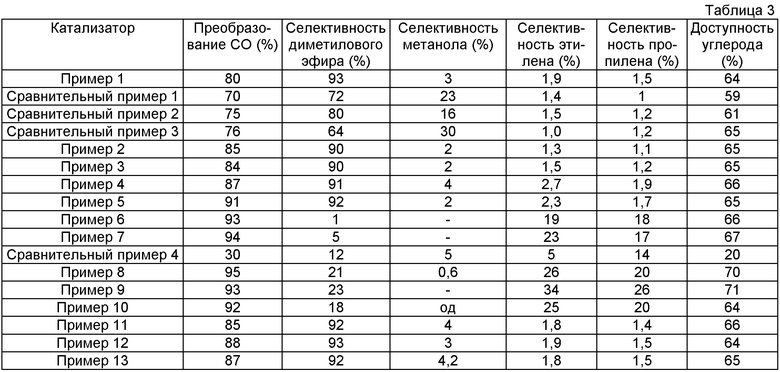
Полученный сплав распылялся в вентилируемой среде на частицы с максимальным размером 300 меш. Для дифракционного рентгеновского анализа (XRD) использовался рентгеновский дифрактометр. Полученный спектр XRD показал, что присутствует только широкий диффузионный пик (фигура 2(1)), который является типичной характеристикой аморфного сплава. Следовательно, полученный сплав Ni-Fe-Al-MnО2-ZrО2 был сплавом в аморфном состоянии.
2. Приготовление катализатора
Вышеупомянутый аморфный сплав и глина (Jiangsu Xuyi Yushi Clay Plant) механически смешивались в весовом соотношении 1:1, таблетировались, распылялись и просеивались на частицы, имеющие размер от 20 до 40 меш. Состав полученного катализатора показан в таблице 1.
Пример 9
1. Приготовление аморфного сплава
20 г ZrO2 было помещено в тигель, и затем 40 г молибдена (промышленной чистоты) и 40 г А1 были добавлены в тигель и смешивались. Полученная смесь была помещена в вакуумную печь с донной загрузкой с вакуумом порядка 10-2 Па, и при температуре 1200°С смесь выдерживалась в расплавленном состоянии в течение 10 минут, затем в печь подавался газообразный аргон до тех пор, пока давление в печи не уравнивалось с атмосферным, получая, таким образом, жидкий расплав смеси.
Расплав быстро охлаждался под вакуумом, чтобы получить сплав Al-Mo-ZrO2. Условия быстрого охлаждения включали линейную скорость медного валка 30 м/с, давление инжекции 0,08 МПа и температуру инжекции 1300°С.
Полученный сплав распылялся в вентилируемой среде на частицы с максимальным размером 300 меш. Для дифракционного рентгеновского анализа (XRD) использовался рентгеновский дифрактометр. Полученный спектр XRD показал, что присутствует только широкий диффузионный пик (фигура 2 (2)), который является типичной характеристикой аморфного сплава. Следовательно, конечный сплав Mo-AlZrO2 был сплавом в аморфном состоянии.
2. Приготовление матрицы загруженной гетерополикислотой
70 г SiO2 были пропитаны 40 г водного раствора, содержащего 62,5% по весу Сu(NО3)2 (чистый для анализа, Zibo Rongruida Micro Materials Plant), смесь высушивалась при 80°С в течение 6 часов, 120°С в течение 4 часов, и затем прокаливалась при 550°С в течение 2 часов, чтобы получить комплексное соединение CuO-SiO2.
Комплексное соединение CuO-SiO2 было пропитано 40 граммами водного раствора 12,5% по весу Gа(NО3)3 (чистый для анализа, Hunan Huaihua Yinhuan Smelt Co., Ltd.), затем высушивалось при 80°C в течение 6 часов, при 120°С в течение 4 часов, и затем прокаливалось при 550°С в течение 2 часов, чтобы получить комплексное соединение Ga2O3-CuO-SiO2.
На заключительной стадии комплексное соединение Ga2O3-CuO-SiO2 было пропитано 32 г 50% по весу фосфорно-вольфрамовой кислотой (HPW) (чистой для анализа, Kunshan Xingbang W&M Technology Co., Ltd.) как гетерополикислотой, высушивалось при 80°С в течение 6 часов, дополнительно при 120°С в течение 4 часов, и затем прокаливалось при 550°С в течение 2 часов, чтобы получить матрицу, загруженную гетерополикислотой, и присадку, в которой количество фосфорно-вольфрамовой кислоты как гетерополикислоты было 15,8% по весу, количество присадки Qа2О3 составляло 3,7% по весу и количество присадки СuО составляло 10,5% по весу.
3. Приготовление катализатора
Вышеупомянутый аморфный сплав и матрица механически смешивались в весовом соотношении 3:2, таблетировались, распылялись и просеивались на частицы, имеющие размер от 20 до 40 меш. Состав полученного катализатора показан в таблице 1.
1. Приготовление аморфного сплава
5 г ZnO, 15 г СоО (промышленной чистоты) и 16 г медного порошка были смешаны в гомогенный состав, и затем были добавлены 20 г А1 и 30 г Fe. После быстрого смешивания смесь была помещена в вакуумную печь с донной загрузкой под вакуумом порядка 10-2 Па и при температуре 1200°С смесь плавилась в течение 10 минут, затем в печь подавался газообразный аргон до тех пор, пока давление в печи не стало равным атмосферному, получая, таким образом, расплав смеси.
Расплав быстро охлаждался под вакуумом, чтобы получить сплав Al-Fe-ZnO-CoO-Cu. Условия быстрого охлаждения включали линейную скорость медного валка 30 м/с, давление инжекции 0,08 МПа и температуру инжекции 1300°С.
Полученный сплав распылялся в вентилируемой среде на частицы с максимальным размером 300 меш. Для дифракционного рентгеновского анализа (XRD) полученного порошка был использован рентгеновский дифрактометр.
Полученный спектр XRD показал, что присутствует только широкий диффузионный пик (полученный спектр XRD был аналогичен спектру на фигуре 1(1)), который является типичной характеристикой аморфного сплава. Следовательно, полученный сплав Al-Fe-ZnO-CoO-Cu был сплавом в аморфном состоянии.
2. Подготовка матрицы фосфата алюминия
10% А1(No)3 и 10% по весу раствора фосфата было смешано в мольном отношении А1/Р 3:1, затем аммиачная вода 4N (чистая для анализа, Beijing Chemical Works) медленно добавлялась в раствор смеси до тех пор, пока коэффициент рН не стал равным 9, полученная смесь была отфильтрована и троекратно промыта этиловым спиртом, высушивалась под вакуумом при 120°С в течение 4 часов, и затем прокаливалась при 650°С в течение 3 часов, чтобы получить 100 г матрицу фосфата алюминия.
3. Приготовление катализатора
Вышеупомянутый аморфный сплав и матрица механически смешивались в весовом соотношении 2:3, таблетировались, распылялись и просеивались на частицы, имеющие размер от 20 до 40 меш. Состав полученного катализатора показан в таблице 1.
Пример 11
1. Приготовление катализатора, содержащего аморфный сплав и оксидную матрицу Способ приготовления был аналогичен способу примера 1.
2. Стадия промывки щелочью для аморфного сплава
100 г частиц вышеупомянутого катализатора, содержащих аморфный сплав и оксидную матрицу и имеющих размер 20-40 меш, были введены в 400 г раствора 10% по весу гидроокиси натрия, чтобы выполнить стадию щелочной промывки и извлечь часть алюминия в аморфном сплаве. Температура при контакте была равна 5°С и время ввода в контакт составляло 0,5 часа. После окончания реакции катализатор был отфильтрован и промывался дистиллированной водой до тех пор, пока рН фактор промывочной воды не стал равен 7. Результаты XRFS показали, что отношение А1:Сu по весу в катализаторе было 0,23. Из этого отношения было вычислено количество А1 в аморфном сплаве после стадии щелочной промывки, которое оказалось равным 15% по весу от общего веса сплава. Катализатор был помещен в безводный этиловый спирт для дальнейшего использования.
Пример 12
1. Приготовление катализатора, содержащего аморфный сплав и оксидную матрицу.
Способ приготовления был аналогичен способу примера 1.
2. Стадия щелочной промывки аморфного сплава
100 г вышеупомянутых частиц катализатора, содержащих аморфный сплав и оксидную матрицу и имеющих размер 20-40 меш, вводятся в контакт с 230 г раствора 20% по весу гидроокиси натрия, чтобы выполнить стадию щелочной промывки и извлечь часть А1 в аморфном сплаве. Температура раствора была равна 20°С и время ввода в контакт составляло 1,0 час. После окончания реакции катализатор фильтровался и промывался дистиллированной водой до тех пор, пока рН фактор промывочной воды не стал равен 7.
Результаты XRFS показали что отношение А1:Сu по весу в катализаторе было 0,07. Из отношения количества А1 в аморфном сплаве после щелочной стадии мытья было вычислено, что он составляет 5% по весу от общего веса сплава. Катализатор был помещен в безводный этиловый спирт для последующего использования.
Пример 13
1. Приготовление катализатора, содержащего аморфный сплав и оксидную матрицу
Способ приготовления был аналогичен способу примера 1.
2. Стадия щелочной промывки аморфного сплава
100 г вышеупомянутых частиц катализатора, содержащих аморфный сплав и оксидную матрицу и имеющих размер 20-40 меш, вводятся в 300 г раствора 15% по весу гидроокиси натрия, чтобы выполнить стадию щелочной промывки и извлечь часть А1 в аморфном сплаве. Температура раствора была 50°С и время ввода в контакт время составляло 5 часов. После окончания реакции катализатор фильтровался и промывался дистиллированной водой до тех пор, пока рН фактор промывочной воды не стал равен 7. Результаты XRFS показали что отношение А1:Сu по весу в катализаторе было 0,0067. Отношение количества А1 в аморфном сплаве после стадии щелочной промывки было вычислено и найдено равным 0,5% по весу от общего веса сплава. Катализатор был помещен в безводный этиловый спирт для последующего использования.

Сравнительный пример 1
40 г гамма-Аl2О3 отжигалось при 550°С в течение 4 часов и затем использовалось как компонент для реакции дегидратации метанола, и 20 г коммерческого катализатора синтеза метанола QC308 (Nanjing Qingshan Chemical Engineering Co., Ltd.), в котором кристаллический сплав А1 был удален промывкой щелочью и содержал Сu и Zn, и его спектр XRD показан на фигуре 1 (2), который использовался как компонент для реакции синтеза метанола, был механически смешан, таблетирован, распылен и просеян на частицы, имеющие размер 20-40 меш. Был получен сравнительный катализатор, в котором весовое соотношение между компонентом реакции дегидратации метанола и компонентом для реакции синтеза метанола составляло 2:1.
Сравнительный пример 2
1. Приготовление кристаллического сплава
20 г алюминиевого порошка (промышленной чистоты, ниже то же самое), 60 г медного порошка (промышленной чистоты, ниже то же самое) и 20 г ZnO (промышленной чистоты, ниже то же самое) смешивались и нагревались в вакуумной печи с донной загрузкой с вакуумом порядка 10-2 Па, и при температуре 1200°С смесь плавилась в течение 10 минут, затем в печь подавался газообразный аргон до тех пор, пока давление в печи не уравнивалось с атмосферным, получая, таким образом, жидкий расплав смеси Сu, А1 и ZnO.
Расплав Сu, А1 и ZnO был подвергнут быстрому охлаждению под вакуумом, чтобы получить сплав Al-Cu-ZnO. Условия быстрого охлаждения включали линейную скорость медного валка 10 м/с, давление инжекции 0,08 МПа и температуру инжекции 1100°С, полученный сплав Al-Cu-ZnO прокаливался под защитной атмосферой N2 при 600°С в течение 4 часов, чтобы получить порошкообразный кристаллический сплав.
Рентгеновский дифрактометр (дифрактометр типа D/MAX-2500, поставляемый компанией Rigaku Cooperation, Сu Кα ray, ток 100 мА, ниже то же самое) был использован для XRD-анализа полученного порошка. Анализ XRD показал, что имеется острый пик 29=42° (фигура 1 (3)). Следовательно, полученный сплав Al-Cu-ZnO был сплавом в кристаллической форме.
2. Приготовление матрицы смешанных окислов
112 г ZnO и 200 г дистиллированной воды смешивались, в 100 г водного раствора 63,32% по весу ZrOCl2 (чистый для анализа, Xinghua Songhe Химическое Chemical reagent Factory, ниже то же самое), 50 г водного раствора 15% по весу СаСl2 (промышленной частоты) и 50 г водного раствора 1% по весу НС1 (чистой для анализа, Beijing Chemical Works) были добавлены по каплям с интенсивным перемешиванием, затем водный раствор 5% по весу углекислого натрия (чистый для анализа, Beijing Chemical Works, ниже то же самое) добавлялся до тех пор, пока рН фактор смешанной жидкости не стал равен 9. Полученная смесь дополнительно размешивалась в течение 1 часа после завершения добавления ингредиентов. Полученный осадок фильтровался, неоднократно промывался дистиллированной водой до полного удаления С1, высушивался при 110°С и прокаливался при 550°С в течение 2 часов, чтобы получить 160 г матрицы, содержащей 27,5% по весу ZrO2, 70% по весу ZnO и 2,5% по весу присадка СаО.
3. Приготовление катализатора
Вышеупомянутый кристаллический сплав и матрица механически смешивались в весовом соотношении 2:3, таблетировались, распылялись и просеивались на частицы, имеющие размер от 20 до 40 меш.
Сравнительный пример 3
1. Приготовление аморфного сплава
73,3 г медного порошка (промышленной чистоты, ниже то же самое) и 26,7 г ZnO (промышленной чистоты, ниже то же самое) смешивались и нагревались в вакуумной печи с донной загрузкой с вакуумом порядка 10-2 Па, и при температуре 1200°С смесь выдерживалась в расплавленном состоянии в течение 10 минут, затем в печь подавался газообразный аргон до тех пор, пока давление в печи не уравнивалось с атмосферным, получая, таким образом, жидкий расплав смеси Сu и ZnO.
Расплавленная смесь Сu и ZnO быстро охлаждалась под вакуумом, чтобы получить сплав Cu-ZnO. Условия быстрого охлаждения включали линейную скорость медного валка 30 м/с, давление инжекции 0,08 МПа и температуру инжекции 1300°С.
Полученный сплав распылялся в вентилируемой среде на частицы с максимальным размером 300 меш (то есть менее чем или равным 48 им). Дифрактометр для анализа порошка (рентгеновский дифрактометр типа D/MAX-2500, поставляемый компанией Rigaku Cooperation, Cu Кα ray, ток 100 мА, ниже то же самое) использовался для XRD-анализа полученного порошка. Полученный спектр XRD был аналогичен спектру, показанному на фигуре 1(1), который является типичной характеристикой аморфного сплава. Следовательно, полученный сплав Cu-ZnO был сплавом в аморфном состоянии.
2. Приготовление матрицы смешанных окислов
112 г ZnO и 200 г дистиллированной воды смешивались, в 100 г водного раствора 63,32% по весу ZrOCl2 (чистый для анализа, Xinghua Songhe Chemical Reagent Company, ниже то же самое), 50 г водного раствора 15% по весу СаСl2 (промышленной частоты) и 50 г водного раствора 1% по весу НС1 (чистый для анализа, Beijing Chemical Works) были добавлены по каплям с интенсивным перемешиванием, затем водный раствор 5% по весу углекислый натрия (чистый для анализа, Beijing Chemical Works, ниже то же самое) добавлялся до тех пор, пока рН фактор смешанной жидкости не стал равным 9. После завершения добавления ингредиентов полученная смесь дополнительно размешивалась в течение 1 часа. Полученный осадок фильтровался, неоднократно промывался дистиллированной водой до полного удаления О, высушивался при 110°С и прокаливался при 550°С в течение 2 часов, чтобы получить 160g матрицы, содержащей 27,5% по весу ZrO2, 70% по весу ZnO и 2,5% по весу присадка СаО.
3. Приготовление катализатора
Вышеупомянутый аморфный сплав и матрица механически смешивались в весовом соотношении 2:3, таблетировались, распылялись и просеивались на частицы, имеющие размер от 20 до 40 меш.
Сравнительный пример 4
Сравнительный катализатор приготавливается следующим способом:
70 г SiO2 были помещены в 40 г водного раствора 62,5% по весу Сu(NО3) (чистый для анализа, Zibo Rongruida Micro Materials Plant), затем высушивались при 80°С в течение 6 часов, 120°С в течение 4 часов, затем прокаливались при 550°С в течение 2 часов, чтобы получить комплексное соединение CuO-SiO2.
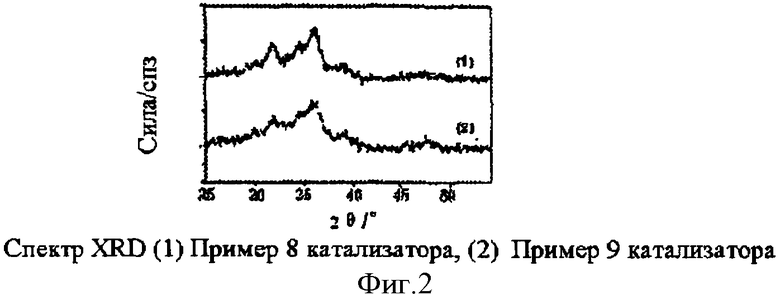
Полученное комплексное соединение CuO-SiO2 было дополнительно пропитано 40 г водного раствора 12.5% по весу Gа(NСО3)3 (чистый для анализа, Hunan Huaihua Yinhuan Smelt Co., Ltd.), затем высушивалось при 80°C в течение 6 часов, 120°С в течение 4 часов и затем прокаливалось при 550°С в течение 2 часов, чтобы получить комплексные соединения Ga2O3-CuO-SiO2 (фигура 3).
На заключительной стадии комплексное соединение Ga2O3-CuO-SiO2 было пропитано 32 г 50% по весу фосфорно-вольфрамовой кислотой (HPW) (чистой для анализа, Hunan Xingbang W&M Technology Co., Ltd.) как гетерополикислотой, которая высушивалась при 80°С в течение 6 часов, 120°С в течение дополнительных 4 часов, и затем прокаливалась при 550°С в течение 2 часов, чтобы получить матрицу, содержащую загруженную в нее гетерополикислоту и присадку, в которой количество фосфорно-вольфрамовой кислоты как гетерополикислоты составляло 15,8% по весу, количество присадка Ga2O3 составляло 3,7% по весу и количество присадка СuО составляло 10,5% по весу.
Пример 14
Процесс производства метанола, диметилового эфира и низкоуглеродистого олефина из синтез-газа выполнялся с помощью каждого катализатора, приготовленного по примерам 1-13 и сравнительным примерам 1-4.
Реакция газовой фазы осуществлялась путем реакции под давлением в герметичном экспериментальном реакторе непрерывного действия с неподвижным слоем.
В реактор было загружено 1,5 г катализатора. Перед реакцией реактор, содержащий катализатор, продувался восстановительным газом в течение 0,5 часа. Затем температура реакции была отрегулирована, и в реактор был подан синтез-газ с нужной объемной скоростью. Состав восстановительного газа, температура продувки, рабочие условия и состав исходного сырья - синтез-газа приведены в таблице 2. Проба для анализа была взята после проведения реакции в течение 3 часов, Окись углерода была проанализирована газовым хроматографом HP 6890, и продукты метанола, диметилового эфира и низших углеродных олефинов были проанализированы хроматографической колонкой PORAPAK-N.
Чтобы сравнить пример 1 со сравнительными примерами 1-3, и пример 7 со сравнительным примером 4, пример 1 и сравнительные примеры 1-3 были использованы в основном те же самые рабочие условия и состав исходного сырья синтез-газа, и также было с примером 7 и сравнительным примером 4.
Преобразование СО, селективность каждого продукта типа метанола, диметилового эфира, этилена и пропилена, так же как доступность углерода во время процесса производства метанола, диметилового эфира и низкоуглеродистого олефина из синтез-газа, были вычислены по следующим уравнениям, и результаты показаны в таблице 3.
Преобразование СО(%)=моли СО, потребляемые реакцией/моли СО, поданные в реакцию.
Селективность диметилового эфира (%)=моли диметилового эфира, произведенного реакцией/моли СО, потребляемые реакцией
Селективность метанола (%)=моли метанола, произведенные реакцией/моли СО, потребляемого реакцией.
Селективность этилена (%)=(моли этилена, произведенные реакцией х 2)/моли СО, потребляемые реакцией.
Селективность пропилена (%)=(моли пропилена, произведенные реакцией х 3)/моли СО, потребляемые реакцией.
Доступность углерода (%)=(моли СО, потребляемые реакцией - моли СО, произведенные реакцией)/моли СО, поданные в реакцию.
Как можно видеть из таблицы 3, в процессе производства метанола, диметилового эфира и низкоуглеродистого олефина из синтез-газа катализаторы по настоящему изобретению могут обеспечить высокую степень преобразования СО, высокую селективность целевого продукта и высокую доступность углерода.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОИЗВОДСТВА МЕТАНОЛА, ДИМЕТИЛОВОГО ЭФИРА И НИЗКОУГЛЕРОДИСТЫХ ОЛЕФИНОВ ИЗ СИНТЕЗ-ГАЗА | 2009 |
|
RU2520218C2 |
| МОЛЕКУЛЯРНОЕ СИТО SCM-34, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2838325C1 |
| КАТАЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ ДИМЕТИЛОВОГО ЭФИРА ИЗ МЕТАНОЛА | 2008 |
|
RU2459799C2 |
| МАСЛЯНАЯ СРЕДА, ИСПОЛЬЗУЕМАЯ В РЕАКЦИИ СИНТЕЗА В РЕАКТОРЕ, СПОСОБ ПОЛУЧЕНИЯ ДИМЕТИЛОВОГО ЭФИРА, СПОСОБ ПОЛУЧЕНИЯ СМЕСИ ДИМЕТИЛОВОГО ЭФИРА И МЕТАНОЛА | 2004 |
|
RU2456261C2 |
| СПОСОБ ПОЛУЧЕНИЯ МОТОРНЫХ ТОПЛИВ ИЗ УГЛЕРОДСОДЕРЖАЩЕГО СЫРЬЯ | 1998 |
|
RU2143417C1 |
| КАТАЛИЗАТОР КОНВЕРСИИ УГЛЕВОДОРОДОВ | 2006 |
|
RU2409422C2 |
| КАТАЛИЗАТОР И СПОСОБ ПОЛУЧЕНИЯ ВЫСОКООКТАНОВЫХ БЕНЗИНОВ С НИЗКИМ СОДЕРЖАНИЕМ БЕНЗОЛА И ДУРОЛА | 2010 |
|
RU2440189C1 |
| СТРУКТУРИРОВАННЫЙ КАТАЛИЗАТОР НА ОСНОВЕ ЖЕЛЕЗА ДЛЯ ПРОИЗВОДСТВА α-ОЛЕФИНА ИЗ СИНТЕЗ-ГАЗА И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ И ПРИМЕНЕНИЕ | 2015 |
|
RU2659067C2 |
| Катализатор для селективного гидрирования диоксида углерода с получением метанола | 2023 |
|
RU2804195C1 |
| СПОСОБ КАТАЛИТИЧЕСКОЙ КОНВЕРСИИ УГЛЕВОДОРОДОВ | 2006 |
|
RU2418842C2 |

Настоящее изобретение обеспечивает процесс производства метанола, диметилового эфира как основных продуктов и низкоуглеродистого олефина как побочного продукта из синтез-газа, в котором указанный процесс содержит стадию контакта синтез-газа с катализатором. Катализатор содержит аморфный сплав, состоящий из первого компонента А1 и второго компонента, при этом указанный второй компонент является одним или несколькими элементами или их окислами, выбранными из группы IA, IIIА, IVA, VA, IB, IIВ, IVB, VB, VIB, VIIB, VIII и ряда лантанидов периодической таблицы элементов, при этом указанный второй компонент отличается от первого компонента А1. Условия для преобразования имеют температуру реакции 200-270°C, давление реакции 1-6 МПа, объемную скорость подачи синтез-газа 1000-10000 мл/г·час и мольное отношение между Н2 и CO в синтез-газе от 1 до 3. Согласно настоящему процессу синтез-газ может быть преобразован в метанол, диметиловый эфир и низкоуглеродистый олефин с высокой степенью преобразования СО, высокой селективностью целевого продукта и высокой доступностью углерода. 18 з.п. ф-лы, 3 ил., 3 табл., 14 пр.
1. Способ производства метанола, диметилового эфира и низкоуглеродистого олефина из синтез-газа, включающий стадию контакта синтез-газа с катализатором в условиях, обеспечивающих преобразование синтез-газа в метанол, диметиловый эфир и низкоуглеродистый олефин, катализатор содержит аморфный сплав, состоящий из первого компонента Al и второго компонента, при этом указанный второй компонент, является одним или несколькими элементами или их окислами, выбранными из группы IA, IIIA, IVA, VA, IB, IIВ, IVB, VB, VIB, VIIB и VIII и ряда лантанидов периодической таблицы элементов, и указанный второй компонент отличается от первого компонента Al, в котором условия для преобразования синтез-газа в метанол, диметиловый эфир, и низкоуглеродистые олефины имеют температуру реакции 200-270°C, давление реакции 1-6 МПа, объемную скорость подачи синтез-газа 1000-10000 мл/г·час и мольное отношение между Н2 и CO в синтез-газе от 1 до 3, в котором метанол и диметиловый эфир производятся как основные продукты, а низкоуглеродистые олефины производятся как побочные продукты.
2. Способ по п.1, в котором на основе общего веса аморфного сплава количество Al составляет 0,5-60% по весу и количество второго компонента составляет 40-99,5% по весу.
3. Способ по п.1, в котором на основе общего веса аморфного сплава количество Al составляет 20-55% по весу и количество второго компонента составляет 45-80% по весу.
4. Способ по п.1, в котором на основе общего веса аморфного сплава количество Al составляет 0,5-20% по весу и количество второго компонента - 80-99,5% по весу.
5. Способ по п.1, в котором указанный второй компонент - один или несколько элементов или их окислов, выбранных из ряда лантанидов и третьего, четвертого и пятого рядов группы IA, IIIA, IVA, VA, IB, IIB, IVB, VB, VIB, VIIB и VIII периодической таблицы элементов.
6. Способ по п.1, в котором указанный второй компонент - один или несколько элементов или их окислов, выбранных из Cu, Zn, V, Cr, Mn, Fe, Co, Ni, К, Zr, Mo, Sn, С, Cu, La и Р.
7. Способ по п.1, в котором указанный второй компонент содержит Cu или ее окись.
8. Способ по п.1, в котором указанный второй компонент содержит Cu и Zn или их окислы.
9. Способ по п.1, в котором указанный второй компонент состоит из Cu и Zn или их окислов.
10. Способ по п.7, в котором количество элементов или окислов элементов группы VIII, если они присутствуют, меньше чем 30% по весу от общего веса аморфного сплава.
11. Способ по п.1, в котором указанный катализатор дополнительно содержит матрицу, в которой распределен аморфный сплав, и на основе общего веса катализатора количество аморфного сплава составляет 20-90% по весу и количество матрицы составляет 10-80% по весу.
12. Способ по п.11, в котором указанная матрица - одно или несколько веществ, выбранных из неокислительных пористых неорганических окислов, молекулярных сит, активного углерода, глин, фосфатов, сульфатов и металлических галоидных соединений.
13. Способ по п.11, в котором указанная матрица содержит присадку, которая загружена на/в матрицу и выбрана из одного или нескольких элементов или их окислов группы IA, IIA, IIIA, IVA, VA, IB, IIB, IVB и VIII и ряда лантанидов периодической таблицы элементов.
14. Способ по п.13, в котором указанная присадка - один или нескольких элементов или их окислов, выбранных из ряда лантанидов и третьего, четвертого и пятого рядов группы IA, IIIA, IVA, VA, IB, IIB, IVB, VB, VIB, VIIB и VIII периодической таблицы элементов.
15. Способ по п.13, в котором указанная присадка - один или нескольких элементов или окислов, выбранных из К, Са, Mr Ga, Sn, Р, Cu, Zn, Zr, Fe и La.
16. Способ по п.13, в котором количество присадки составляет 0,5-40% по весу от общего веса матрицы.
17. Способ по п.1, в котором аморфный сплав приготавливается способом, включающим следующие стадии: легирование смеси первого компонента Аl и второго компонента под вакуумом и при температуре выше их температуры плавления, быстрое охлаждение расплава смеси под вакуумом и распыление полученного сплава.
18. Способ по п.1, в котором катализатор приготавливается способом, включающим стадию щелочной промывки аморфного сплава или катализатора щелочным раствором, чтобы извлечь часть Al в аморфном сплаве.
19. Способ по п.1, в котором аморфный сплав - порошок, частицы которого имеют размер менее чем или равный 500 меш.
| CN 101164692 А, 23.04.2008 | |||
| US 4349464 A, 14.09.1982 | |||
| Аппаратура частотного электромагнитного зондирования | 1982 |
|
SU1073726A1 |
| JP 58159847 A, 22.09.1983 | |||
| ТШГНО- ЧПi It'!\ЦI 1У-.г-.'^-гиЛИ '"i'"•^'"" _.„ 1I^HEJlSQ-Ttii^ { | 0 |
|
SU266727A1 |
| Гирлянда иззоляторов | 1986 |
|
SU1683076A1 |
| КАТАЛИЗАТОР И СПОСОБ ПОЛУЧЕНИЯ УГЛЕВОДОРОДОВ И ИХ КИСЛОРОДСОДЕРЖАЩИХ ПРОИЗВОДНЫХ ИЗ СИНТЕЗ-ГАЗА | 2001 |
|
RU2210432C1 |
| Способ получения каталитически действующих затвердевших в стеклообразном состоянии металлов | 1985 |
|
SU1402246A3 |
Авторы
Даты
2014-05-20—Публикация
2009-11-26—Подача