Изобретение относится к области органической химии и может найти применение в аналитической химии и биологических исследованиях.
При изучении физиологически активных соединений необходимы их меченые аналоги.
Известно, что замена атомов соединений на их меченые аналоги не приводит к изменению каких-либо свойств исходного соединения (Evans E.A. - Tritium and its compounds London Butterworths, 1974, p.48) [1].
Известен 4-иодо-N-[4-метокси-3-(4-метил-1-пиперазинил)фенил]бензенсульфонамид формулы:

Данное соединение проявляет ноотропные, антидепрессантные и анксиолитические свойства (Stean Т.О., Hirst W.D., Thomas D.R., Price G.W., Rogers D., Riley G., Bromidge S.M., Serafmowska H.T., Smith D.R., Bartlett S., Deeks N., Duxon M., Upton N. // Pharmacology, Biochemistry, and Behavior. 2002. V.71. N 4. P.645-654 [2]; Loiseau F., Dekeyne A., Millan M.J. // Psychopharmacology. 2008. V.196. N 1. P.93-104 [3]; Wesolowska A., Nikifbruk A., Stachowicz K. // Behavioural Pharmacology. 2007. V.18. N 5-6. P.439-446 [4]). Также 4-иодо-N-[4-метокси-3-(4-метил-1-пиперазинил)фенил]бензенсульфонамид является сильнейшим антагонистом 5-НТ6 рецепторов (Hirst W.D., Minton J.A., Bromidge S.M., Moss S.F., Latter A.J., Riley G., Routledge C., Middlemiss D.N., Price G.W. // British Journal of Pharmacology. 2000. V.130. N 7. P.1597-1605 [5]) и перспективным препаратом, который может быть использован при таких когнитивных расстройствах, как шизофрения и болезнь Альцгеймера.
Однако его равномерномеченный тритием аналог не описан.
Техническим результатом, достигаемым настоящим изобретением, является расширение ассортимента меченых аналогов физиологически активных соединений.
Достигается указанный технический результат получением равномерномеченного тритием 4-иодо-N-[4-метокси-3-(4-метил-1-пиперазинил)фенил]бензенсульфонамида формулы:
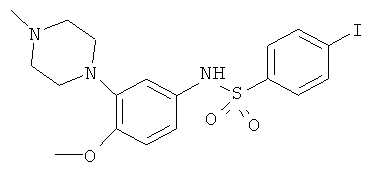
Ниже приведен пример реализации изобретения.
Пример I.
Раствор 1.5 мг 4-иодо-N-[4-метокси-3-(4-метил-1-пиперазинил)фенил]бензенсульфонамида в 75 мкл метанола смешали с 37.5 мг окиси алюминия. При пониженном давлении растворитель упарили и остаток лиофилизировали.
Высушенный остаток и 15 мг катализатора Линдлара на основе 5% Pd/BaSO4 помещали в ампулу и механически перемешивали. Ампулу вакуумировали и заполняли газообразным тритием до давления 400 гПа. Реакцию вели при 240°C в течение 5 мин. Ампулу снова вакуумировали, катализатор наносили на фильтр, вещество экстрагировали метанолом (5×0.5 мл). Экстракты упаривали, остаток растворяли в метаноле (3×1 мл) и вновь упаривали для удаления лабильного трития.
Анализ проводили на хроматографе Милихром А-02, колонка ProntoSIL-120-5-C18 AQ DB-2003, 2.0×75 мм, 5 мкм, 0.2 мл/мин, 35°C, детекция - 210 нм, А - 0.2 М LiClO4+0.005М HClO4 буфер, Б - метанол, градиент Б→0-100 за 12.5 мин: время удерживания 4-иодо-N-[4-метокси-3-(4-метил-1-пиперазинил)фенил]бензенсульфонамида - 8.89 мин. Равномерномеченый 4-иодо-N-[4-метокси-3-(4-метил-1-пиперазинил)фенил]бензенсульфонамид очищали препаративной высокоэффективной жидкостной хроматографией. Хроматографию проводили на колонке Kromasil 100C18, 8×150 мм, 7 мкм, система: А - метанол - 25 мМ фосфатный буфер (30:70), Б - метанол, градиент Б→(0-100) за 30 мин, скорость потока - 2 мл/мин, время удерживания - 27.7 мин.
Радиохимическая чистота равномерномеченного 4-иодо-N-[4-метокси-3-(4-метил-1-пиперазинил)фенил]бензенсульфонамида после хроматографии - не менее 98%, выход - 20-25%, молярная радиоактивность - 15 Ки/ммоль.
Таким образом, получен равномерномеченный тритием 4-иодо-N-[4-метокси-3-(4-метил-1-пиперазинил)фенил]бензенсульфонамид.
| название | год | авторы | номер документа |
|---|---|---|---|
| РАВНОМЕРНО МЕЧЕННЫЙ ТРИТИЕМ (R)-(+)-[5-МЕТИЛ-3-(4-МОРФОЛИНИЛМЕТИЛ)-2,3-ДИГИДРО-[1,4]ОКСАЗИНО [2,3,4-hi]-6-ИНДОЛИЛ]-1-НАФТАЛИНИЛМЕТАНОН АЦЕТАТ | 2009 |
|
RU2404185C1 |
| РАВНОМЕРНО МЕЧЕННЫЙ ДЕЙТЕРИЕМ ИЛИ ТРИТИЕМ 4-(2-АМИНОЭТИЛ)ПИРОКАТЕХОЛ С ИСПОЛЬЗОВАНИЕМ НАНОАЛМАЗНОГО ПОРОШКА | 2010 |
|
RU2422436C1 |
| Меченный тритием 6,7-диметокси-4,4-диметил-1-(4-фенокси-фенил)-3Н-изохинолин | 2019 |
|
RU2695074C1 |
| РАВНОМЕРНОМЕЧЕННЫЙ ТРИТИЕМ ПИРО-Glu-His-Pro-NH | 2013 |
|
RU2513852C1 |
| Синтез меченного тритием 6,7-диметокси-4,4-диметил-1-[4-(4-трифторметилфенокси)фенил]-3Н-изохинолина | 2019 |
|
RU2711646C1 |
| РАВНОМЕРНО МЕЧЕННЫЙ ТРИТИЕМ 2-АМИНО-4-[БЕТА-ГИДРОКСИЭТИЛАМИНО]АНИЗОЛ | 2005 |
|
RU2291142C1 |
| Равномерномеченный дейтерием и тритием 3-(1-метилпирролидин-2-ил)пиридин | 2014 |
|
RU2620190C2 |
| РАВНОМЕРНОМЕЧЕННЫЙ ТРИТИЕМ [Н]АМФОТЕРИЦИН В | 2006 |
|
RU2323224C1 |
| РАВНОМЕРНОМЕЧЕННЫЙ ТРИТИЕМ (3aS,5S,6R,7aR,7bS,9aS,10R,12aS,12bS)-10-[(2S,3R,4R,5S)-3,4-ДИГИДРОКСИ-5,6-ДИМЕТИЛ-2-ГЕПТАНИЛ]-5,6-ДИГИДРОКСИ-7а,9а-ДИМЕТИЛГЕКСАДЕКАНГИДРО-3Н-БЕНЗО[c]ИНДЕНО[5,4-е]ОКСЕПИН-3-ОН | 2012 |
|
RU2499786C1 |
| ВЫСОКОМЕЧЕННЫЙ ТРИТИЕМ 2-МЕТИЛ-4-(4-МЕТИЛ-1-ПИПЕРАЗИНИЛ)-10Н-ТИЕНО[2,3-b][1,5]БЕНЗОДИАЗЕПИН | 2001 |
|
RU2185383C1 |
Изобретение относится к области органической химии, а именно к равномерномеченному тритием 4-иодо-N-[4-метокси-3-(4-метил-1-пиперазинил)фенил]бензенсульфонамиду формулы:
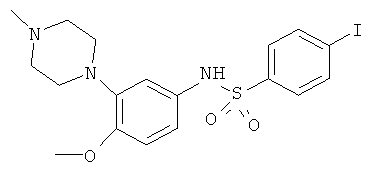 .
.
Технический результат: получен равномерномеченный тритием аналог 4-иодо-N-[4-метокси-3-(4-метил-1-пиперазинил)фенил]бензенсульфонамида, который может найти применение в аналитической химии, биологических исследованиях и в медицине для лечения шизофрении и болезни Альцгеймера. 1 пр.
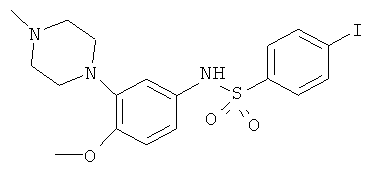
Равномерномеченный тритием 4-иодо-N-[4-метокси-3-(4-метил-1-пиперазинил)фенил]бензенсульфонамид формулы:
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| РАВНОМЕРНО МЕЧЕННЫЙ ТРИТИЕМ 4,4-ДИФТОР-N-{(1S)-3-[3-(3-ИЗОПРОПИЛ-5-МЕТИЛ-4Н-1,2,4-ТРИАЗОЛ-4-ИЛ)-8-АЗАБИЦИКЛО[3.2.1]ОКТ-8-ИЛ]-1-ФЕНИЛПРОПИЛ}ЦИКЛОГЕКСАН КАРБОДИИМИД | 2008 |
|
RU2368613C1 |
Авторы
Даты
2013-08-27—Публикация
2012-07-05—Подача