Изобретение относится к новому способу получения соединений с общей структурной формулой 1-4:
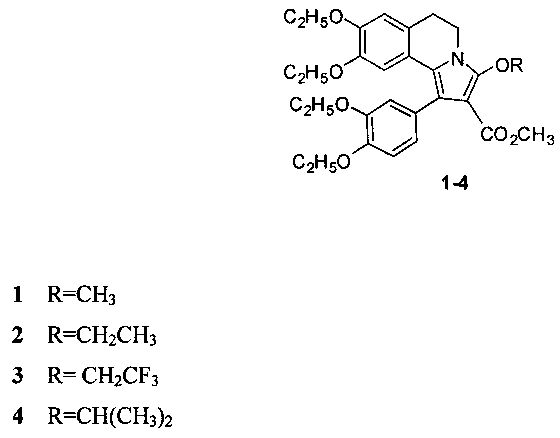
Синтез близких по строению соединений описан в следующих работах: N.N. Poligalova, A.G. Mikhailovskii, E.V. Vikhareva, M.I. Vakhrin. Enamines of the 1,2,3,4-tetrahydroisoquinolines series in the Chichibabin synthesis of pyrrolo[2,1-a]isoquinolines and in reaction with oxalil chloride. Chemistry of Heterocyclic Compounds, 2007, Vol. 43, №7, 900-905:
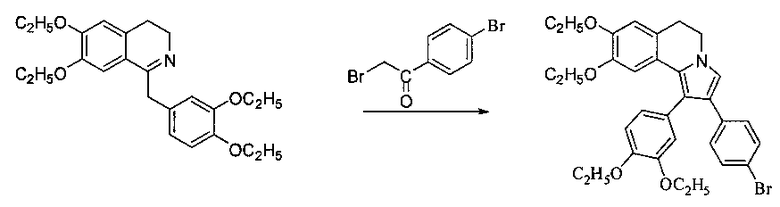
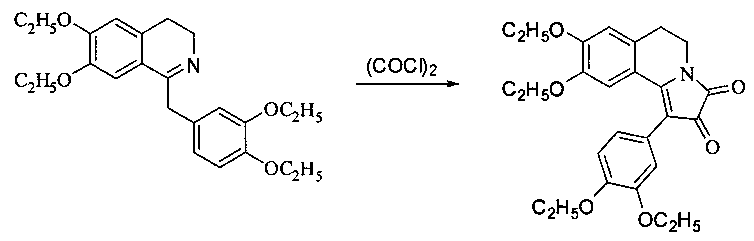
а также в работе: (Shun Su, John A. Porco и др. Synthesis of Pyrroloisoquinolines Related to the Lamellaris Using Silver-Catalyzed Cycloisomerisation/Dipolar Cycloaddition. Journal of American Chemical Societe, 2007, Vol. 129, №25, 7744-7745:
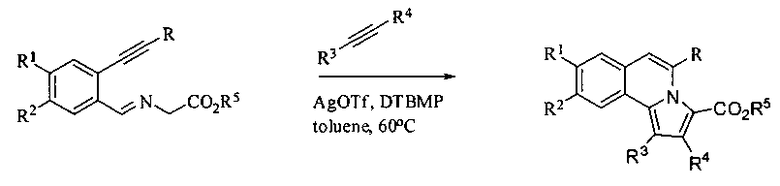
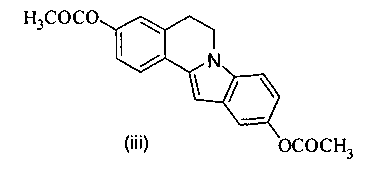
Фрагмент 5,6-дигидропирроло[2,1-a]изохинолина входит в состав таких алкалоидов, как cryptaustoline (i) и cryptovoline (ii), которые проявляют различную биологическую активность, в частности антилейкемическую, противоопухолевую, а также являются ингибиторами полимеризации тубулина. Синтетический аналог - диацетоксизамещенный 5,6-дигидропирроло[2,1-a]изохинолин (iii) - обладает сродством к эстрогеновым рецепторам:
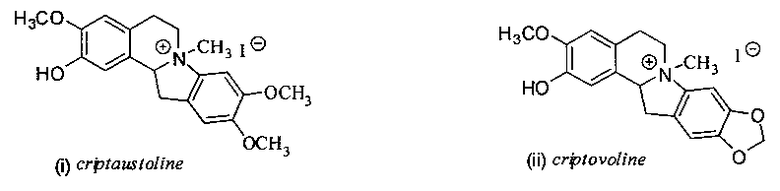
Техническим результатом, на решение которого направлено изобретение, является разработка нового способа синтеза производных 5,6-дигидропирроло[2,1-a]изохинолинов с помощью трехкомпонентной реакции. Технический результат достигается тем, что способ получения производных 5,6-дигидропирроло[2,1-a]изохинолинов с общей структурной формулой:
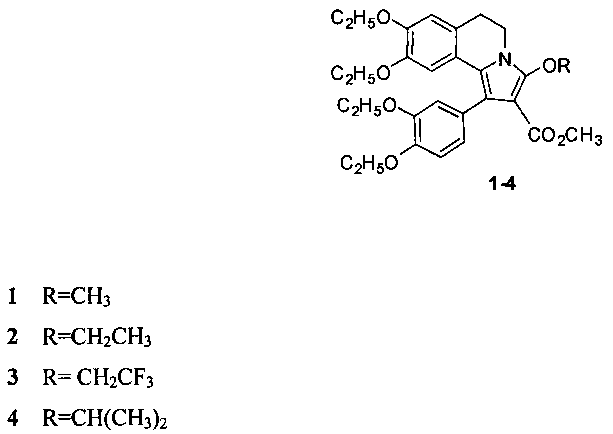
заключается в том, что 6,7-диэтокси-3,4-дигидро-1-(3,4-диэтоксибензоил)изохинолин смешивают с метилпропиолатом и метанолом или этанолом, или 2,2,2-трифторэтанолом, или изопропанолом и перемешивают при температуре +50°C, остаток, полученный после окончания реакции и удаления реагентов, кристаллизуют в эфире.
Таким образом, предложенный способ позволяет с помощью трехкомпонентной реакции действием избытка метилпропиолата и метанола или этанола, или 2,2,2-трифторэтанола, или изопропанола на 6,7-диэтокси-3,4-дигидро-1-(3,4-диэтоксибензоил)изохинолин получать производные 5,6-дигидропирроло[2,1-a]изохинолинов 1-4.
Способ осуществляется следующим образом. Смешивают 6,7-диэтокси-3,4-дигидро-1-(3,4-диэтоксибензоил)изохинолин (1 моль), метилпропиолат (3 моль) и метанол или этанол, или 2,2,2-трифторэтанол, или изопропанол (11 моль), далее перемешивают при температуре +50°C. Ход реакции контролируют с помощью тонкослойной хроматографии на сорбфиле. Время реакции составляет от 2 до 9 дней в зависимости от природы спирта. После окончания реакции растворитель упаривают досуха, полученный остаток растирают в эфире до кристаллизации соединений 1-4. Таким образом, производные 5,6-дигидропирроло[2,1-a]изохинолинов 1-4 получают из 6,7-диэтокси-3,4-дигидро-1-(3,4-диэтоксибензоил)изохинолина при взаимодействии с метилпропиолатом и различными спиртами при температуре +50°C:
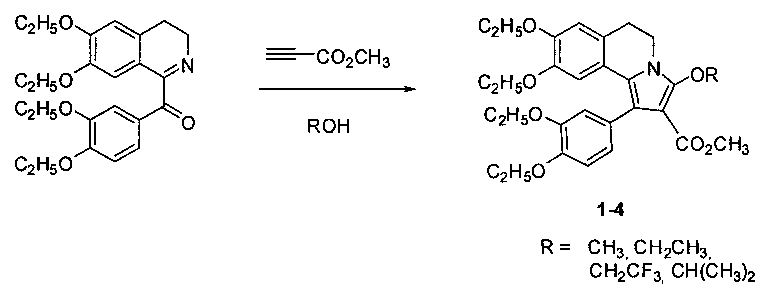
Выходы соединений 1-4 колеблются от 22 до 92% и зависят от природы спирта.
Строение полученных соединений подтверждено методами масс-спектрометрии, ИК спектроскопии и спектроскопии ПМР. Строение соединения 1 подтверждено также методом РСА.
Пример 1
Смешивают 0,41 г (0,001 моль) 6,7-диэтокси-3,4-дигидро-1-(3,4-диэтоксибензоил)изохинолина, 0,25 г (0,003 моль) метилпропиолата и 5 мл (0,11 моль) метанола. Реакцию проводят при перемешивании при +50°C. Ход реакции контролируют с помощью ТСХ (sorbfil, этилацетат-гексан, 1:2). Реакция проходит за 9 дней. Растворитель упаривают, полученную реакционную массу кристаллизуют в эфире. Получают 0,11 г соединения 1 в виде кристаллов белого цвета.
Метил 1-(3,4-диэтоксифенил)-3-метокси-5,6-дигидропирроло[2,1-а]изохинолин-2-карбоксилат (1): выход 22%, белые кристаллы с т.пл. 137-139°C, Rf 0,65 (sorbfil, этилацетат-гексан, 1:1). ИК спектр (в KBr), υ/см-1: 1700 (CO2CH3). Спектр 1H ЯМР (CDCl3, 400 МГц): δ=1.15 (т, 3H, J=6.9 Гц, O-CH2 CH 3), 1.40 (т, 6H, J=6.9 Гц, O-CH2 CH 3), 1.45 (т, 3H, J=6.9 Гц, O-CH2 CH 3), 2.93 (т, 2H, J=6.2 Гц, 6-CH2), 3.54 (кв, 2H, J=6.9 Гц, O-CH 2CH3), 3.60 (с, 3H, 3-OCH3), 3.97 (т, 2H,.J=6.2 Гц, 5-CH2), 4.05 (с, 3H, CO2CH3), 4.00-4.08 (м, 4H, O-CH 2CH3), 4.12 (кв, 2H, J=6.9 Гц, O-CH 2CH3), 6.45 (с, 1H, 7-H), 6.64 (с, 1H, 10-H), 6.84-6.92 (м, 3H, CH-Ar). Найдено: C 68.35%, H 6.92%, N 2.75%. Масс-спектр, m/z: 509 (M+). C29H35NO7. M 509. Вычислено: C 68.32%, H 6.93%, N 2.76%. M 509.
Пример 2
Смешивают 0,41 г (0,001 моль) 6,7-диэтокси-3,4-дигидро-1-(3,4-диэтоксибензоил)изохинолина, 0,25 г (0,003 моль) метилпропиолата и 4 мл (0,11 моль) этанола. Реакцию проводят при перемешивании при +50°C. Ход реакции контролируют с помощью ТСХ, (sorbfil, этилацетат-гексан, 1:2). Реакция проходит за 6 дней. Растворитель упаривают, полученную реакционную массу кристаллизуют в эфире. Получают 0,25 г соединения 2 в виде кристаллов белого цвета.
Метил 1-(3,4-диэтоксифенил)-3-этокси-5,6-дигидропирроло[2,1-а]изохинолин-2-карбоксилат (2): выход 63%, белые кристаллы с т.пл. 121-123°C, Rf 0,53 (sorbfil, этилацетат-гексан, 1:1). ИК спектр, υ/см-1: 1702 (CO2CH3). Спектр 1H ЯМР (CDCl3, 400 МГц): δ=1.15 (т, 3H, J=6.9 Гц, О-CH2-CH 3), 1.37-1.43 (м, 6H, O-CH2-CH 3), 1.42-1.47 (м, 6H, O-CH2-CH 3), 2.92 (т, 2H, J=6.2 Гц, 6-CH2), 3.54 (кв, 2H, J=6.9 Гц, O-CH 2-CH3), 3.59 (с, 3H, CO2CH3), 3.97 (т, 2H, J=6.2 Гц, 5-CH2), 4.03 (кв, 4H, J=6.9 Гц, О-CH 2-CH3), 4.11 (кв, 2H, J=6.9 Гц, O-CH 2-CH3), 4.30 (кв, 2H, J=6.9 Гц, 3-O-CH 2-CH3), 6.45 (с, 1H, 7-H), 6.63 (с, 1H, 10-H), 6.81-6.91 (м, 3H, CH-Ar). Найдено: C 68.78%, H 7.35%, N 2.96%. Масс-спектр, m/z: 523 (M+). C30H37NO7. M 523. Вычислено: C 68.83%, H 7.07%, N 2.68%.
Пример 3
Смешивают 0,41 г (0,001 моль) 6,7-диэтокси-3,4-дигидро-1-(3,4-диэтоксибензоил)изохинолина, 0,25 г (0,003 моль) метилпропиолата и 15 мл (0,11 моль) 2,2,2-трифторэтанола. Реакцию проводят при перемешивании при +50°C. Ход реакции контролируют с помощью ТСХ (sorbfil, этилацетат-гексан, 1:2). Реакция проходит за 2 дня. Растворитель упаривают, полученную реакционную массу кристаллизуют в эфире. Получают 0,38 г соединения 3 в виде кристаллов белого цвета.
Метил 1-(3,4-диэтоксифенил)-3-(2,2,2-трифторэтокси)-5,6-дигидропирроло[2,1-а]изохинолин-2-карбоксилат (3): выход 92%, белые кристаллы с т.пл. 157-159°C, Rf 0,58 (sorbfil, этилацетат-гексан, 1:1). ИК спектр, υ/см-1: 1685 (CO2CH3). Спектр 1H ЯМР (CDCl3, 400 МГц): δ=1.15 (т, 3H, J=6.9 Гц, О-CH2-CH 3), 1.36-1.43 (м, 6Н, O-CH2-CH 3), 1.46 (т, 3H, J=6.9 Гц, O-CH2-CH 3), 2.93 (т, 2H, J=6.2 Гц, 6-CH2), 3.53 (кв, 2H, J=6.9 Гц, О-CH 2-CH3), 3.57 (с, 3H, CO2CH3), 3.96-4.08 (м, 6H, О-CH 2-CH3, 5-CH2), 4.12 (кв, 2H, J=6.9 Гц, О-CH 2-CH3), 4.70 (кв, 2H, J=8.2 Гц, 3-O-CH 2CF3), 6.44 (с, 1H, 7-H), 6.64 (с, 1H, 10-H), 6.81-6.87 (м, 2H, CH-Ar), 6.89 (д, 1H, J=8.3 Гц, CH-Ar). Найдено: C 62.28%, H 5.90 N 2.38%. Масс-спектр, m/z: 577 (M+). C30H34F3NO7. M 577. Вычислено: C 62.38%, H 5.93 N 2.43%.
Пример 4
Смешивают 0,41 г (0,001 моль) 6,7-диэтокси-3,4-дигидро-1-(3,4-диэтоксибензоил)изохинолина, 0,25 г (0,003 моль) метилпропиолата и 5 мл (0,11 моль) изопропанола. Реакцию проводят при перемешивании при 50°C. Ход реакции контролируют с помощью ТСХ (sorbfil, этилацетат-гексан, 1:2). Реакция проходит за 5 дней. Растворитель упаривают, полученную реакционную массу кристаллизуют в эфире. Получают 0,14 г соединения 4 в виде кристаллов белого цвета.
Метил 1-(3,4)-диэтоксифенил-3-изопропилокси-5,6-дигидропирроло[2,1-а]изохинолин-2-карбоксилат (4): выход 27%, белые кристаллы с т.пл. 138-140°C, Rf 0,56 (sorbfil, этилацетат-гексан, 1:1). ИК спектр, υ/см-1: 1700 (CO2CH3). Спектр 1H ЯМР (CDCl3, 400 МГц): δ=1.15 (т, 3H,.J=6.9 Гц, СН(CH 3)2), 1.34-1.43 (м, 12H, O-CH2-CH 3), 1.45 (д, 3H,J=6.9 Гц, СН(CH 3)2), 2.90 (т, 2H, J=6.2 Гц, 6-CH2), 3.54 (кв, 2H, J=6.9 Гц, O-CH 2-CH3), 3.57 (с, 3H, CO2CH3), 3.96 (т, 2H, J=6.2 Гц, 5-CH2), 3.99-4.08 (м, 4H, O-CH 2-CH3), 4.76 (септ, 2H, J=6.9 Гц, 3-СН(CH3)2), 6.46 (с, 1H, 7-H), 6.63 (с, 1H, 10-H), 6.83-6.91 (м, 3H, CH-Ar). Найдено: C 69.05%, H 7.21 N 2.34%. Масс-спектр, m/z: 537 (M+). C31H39NO7. M 537. Вычислено: C 69.25%, H 7.31 N 2.61%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 5,6-ДИГИДРОПИРРОЛО[2,1-a]ИЗОХИНОЛИНОВ, СОДЕРЖАЩИХ В ПОЛОЖЕНИИ 2 ФУНКЦИОНАЛЬНУЮ ГРУППУ | 2015 |
|
RU2575174C1 |
| Способ получения производных пирроло[2,1-a]изохинолинов | 2017 |
|
RU2656225C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ БЕНЗО[7,8]АЗОНИНО[5,4-b]ИНДОЛОВ, 7,9-ЭТЕНОАЗЕЦИНО[5,4-b]ИНДОЛОВ И 7,9-ЭТАНОАЗЕЦИНО[5,4-b]ИНДОЛОВ | 2009 |
|
RU2397984C1 |
| СПИРОЦИКЛИЧЕСКИЕ ПИРРОЛОПИРАЗИН(ПИПЕРИДИН)АМИДЫ В КАЧЕСТВЕ МОДУЛЯТОРОВ ИОННЫХ КАНАЛОВ | 2012 |
|
RU2634900C2 |
| ПРОИЗВОДНЫЕ ПИРИДОКСИНА С НЕЛИНЕЙНЫМИ ОПТИЧЕСКИМИ СВОЙСТВАМИ | 2012 |
|
RU2501801C1 |
| ПРОИЗВОДНЫЕ СПИРО[ИЗОХИНОЛИН-4(1Н),3-ПИРРОЛИДИН]-1,2',3,5'[2Н]ТЕТРОНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРЕДОТВРАЩЕНИЯ ИЛИ ЛЕЧЕНИЯ ОСЛОЖНЕНИЙ, СВЯЗАННЫХ С САХАРНЫМ ДИАБЕТОМ | 1991 |
|
RU2110518C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ БЕНЗГИДРИЛОКСИЭТИЛПИПЕРАЗИНА | 1987 |
|
RU2032680C1 |
| ПРОМЕЖУТОЧНОЕ ПРОИЗВОДНОЕ ЦЕФАЛОСПОРИНА И СПОСОБ ПОЛУЧЕНИЯ ЦЕФАЛОСПОРИНА | 1995 |
|
RU2150471C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 3',4',5,6-ТЕТРАГИДРО-1Н-СПИРО[ПИРИДИН-4,5'-ТИЕНО[2,3-d]ПИРИМИДИНОВ] | 2011 |
|
RU2455306C1 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ИНДЕНО[ [1,2-с] ИЗОХИНОЛИНА, КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ НА ИХ ОСНОВЕ | 2002 |
|
RU2300523C2 |
Изобретение относится к области органической химии, а именно к способу получения производных 5,6-дигидропирроло[2,1-a]изохинолинов 1-4 с общей структурной формулой: 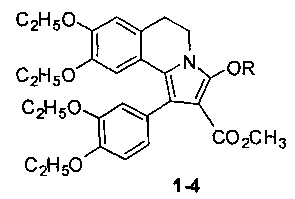
где 1 - R=CH3, 2 - R=CH2CH3, 3 - R=CH2CF3, 4 - R=CH(CH3)2, отличающийся тем, что 6,7-диэтокси-3,4-дигидро-1-(3,4-диэтоксибензоил)изохинолин смешивают с метилпропиолатом и метанолом, или этанолом, или 2,2,2-трифторэтанолом, или изопропанолом и перемешивают при температуре +50°C, остаток, полученный после окончания реакции и удаления реагентов, кристаллизуют в эфире. Технический результат: разработан способ получения производных 5,6-дигидропирроло[2,1-a]изохинолинов, которые могут найти применение в качестве промежуточных соединений в процессе получения биологически активных соединений. 4 пр.
Способ получения производных 5,6-дигидропирроло[2,1-a]изохинолинов 1-4 с общей структурной формулой:

1- R=CH3
2- R=CH2CH3
3- R=CH2CF3
4- R=CH(CH3)2
отличающийся тем, что 6,7-диэтокси-3,4-дигидро-1-(3,4-диэтоксибензоил)изохинолин смешивают с метилпропиолатом и метанолом, или этанолом, или 2,2,2-трифторэтанолом, или изопропанолом и перемешивают при температуре +50°C, остаток, полученный после окончания реакции и удаления реагентов, кристаллизуют в эфире.
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| (ДИГИДРО)ПИРРОЛО[2,1-А]ИЗОХИНОЛИНЫ | 2009 |
|
RU2495037C2 |
| Машина для прядения искусственного шелка | 1929 |
|
SU12110A1 |
Авторы
Даты
2015-05-10—Публикация
2014-05-22—Подача