Изобретение относится к области химии и может быть использовано в медицине в качестве маркера при исследовании метаболизма печени и миокарда.
Известен способ получения линолевой кислоты, при котором 7-хлорундекадиин-2,5 подвергают конденсации с метиловым эфиром 7-хлоргептановой кислоты и полученный метиловый эфир октадиин-9,12-овой-1 кислоты гидрируют с дальнейшим омылением последнего в цис-октадекадиен-9,12-овую-1 кислоту (линолевую кислоту).
(Авторское свидетельство СССР №144170, МПК С12Р 7/64, опубл. БИ №2, 1962 г.).
Недостатками данного способа является то, что процесс занимает много времени и имеет низкий выход целевого продукта, около 26%, кроме того процесс длится больше 40 часов.
Задачей изобретения является создание эффективного способа получения линолевой кислоты, позволяющего сократить время длительности процесса и увеличить выход целевого продукта.
Технический результат изобретения заключается в сокращении времени процесса и увеличении выхода целевого продукта.
Это достигается тем, что в заявляемом способе получения линолевой кислоты, включающем получение метилового эфира 7-хлоргептановой кислоты или метилового эфира 7-йодгептановой кислоты, конденсацию 1-хлорундекаина-2,5 с метиловым эфиром 7-хлоргептановой кислоты или с метиловым эфиром 7-йодгептановой кислоты и гидрирование полученного метилового эфира октадиин-9,12-овой-1 кислоты с дальнейшим омылением полученного метилового эфира октадиен-9,12-овой-1 кислоты до октадекадиен-9,12-овой-1 кислоты (линолевой кислоты), причем стадии реакции получения метиловых эфиров, реакции конденсации в присутствии магния и реакции гидрирования в присутствии палладиевого катализатора проводят в поле ультразвукового излучения мощностью 300 Вт и частотой 22 кГц. Способ осуществляется следующим образом.
Стадии с 1 по 4 проводят в поле ультразвукового излучения мощностью 300 Вт и частотой 22 кГц. Для этого химический реактор (колбу) погружают в ультразвуковую ванну.
1-я стадия. Получение метилового эфира 7-хлоргептановой кислоты.
Смесь 50,0 г 7-хлоргептановой-1 кислоты, 29,8 г метилового спирта и 5 мл H2SO4 (уд.в. 1.84) в 100 мл сухого бензола нагревают при кипении в течение 3 часов. Охлаждают и отделяют верхний органический слой. Водный слой обрабатывают бензолом (2 раза по 20 мл), соединенные экстракты промывают 10 мл насыщенного водного раствора бикарбоната натрия и сушат хлористым кальцием. Растворитель удаляют, а остаток перегоняют. Выход ClCH2(СН2)5СООСН3 (I) составляет 90%.
2-я стадия. Получение метилового эфира 7-йодгептановой кислоты (II).
35,0 г (I) и 53,5 г йодистого натрия нагревают при кипении в течение 3 часов в 200 мл ацетона. Массу охлаждают, отделяют осадок от маточного раствора, отгоняют ацетон. Из остатка бензолом (5 раз по 20 мл) извлекают продукт. Экстракты соединяют, промывают 10 мл насыщенного водного раствора бисульфита натрия и сушат хлористым кальцием. Растворитель отгоняют, а остаток перегоняют, выход ICH2(CH2)5COOCH3 (II) составляет 89%.
3-я стадия. Получение метилового эфира октадекадиин-9,12-овой-1 кислоты (III).
Раствор 20,2 г 1-хлорундекаиина-2,5 CH3(CH2)4C≡CCH2C≡CCH2C (IV) и 20,0 г (II) в 60 мл безводной смеси эфира и бензола(1:1) приливают в течение 5 минут к 2,5 г магния в 30 мл эфира. Прибавляют кристаллик йода и 20 мг сулемы и 2 часа кипятят в токе азота. Затем прибавляют 20 мг сулемы и продолжают греть еще 3 часа. Массу охлаждают до 5-10°C и обрабатывают соляной кислотой (уд.в. 1,02). Верхний слой отделяют, а водный - обрабатывают эфиром (2 раза по 20 мл), соединенные экстракты промывают 10 мл насыщенного водного раствора метабисульфита натрия, нейтрализуют водной суспензией бикарбоната натрия и сушат над сернокислым натрием. Растворитель удаляют, а остаток перегоняют. Выход СН3(СН2)4С≡ССН2С≡С(СН2)7СООСН3 (III) составляет 82%.
4-я стадия. Получение метилового эфира октадекадиен-9,12-1 кислоты (IV).
Раствор 1,26 г (III) в 20 мл безводного метанола гидрируют при 18-19°C и перемешивании в присутствии 0,25 г палладиевого катализатора в течение 4,5 часа. При этом поглощается 188 мл водорода. Катализатор отделяют и промывают 10 мл метанола. Растворитель удаляют а остаток перегоняют. Выход СН3(СН2)4СН=СНСН2СН=СН(СН2)7СООСН3 (IV) составляет 87%.
5-я стадия. Получение конечного продукта октадекадиен-9,12-овой-1 (линолевой) кислоты (V).
Смесь 0,96 г (IV), 0,18 г едкого калия и 45 мл сухого метанола выдерживают 6 часов в токе азота при 18-20°C. От реакционной массы отгоняют метанол в вакууме (16-17 мм), приливают 20 мл воды и неомыленные соединения экстрагируют эфиром (2 раза по 25 мл), водный слой подкисляют серной кислотой (уд.в. 1,10) до рН=6 и вещество извлекают эфиром (3 раза по 15 мл), объединенные экстракты сушат над сернокислым натрием. Растворитель удаляют, а остаток перегоняют. Выход СН3(СН2)4СН=СНСН2СН=СН(СН2)7СООН (V) составляет 89%.
В таблице приведены сравнительные данные по отдельным стадиям и итоговые показатели.
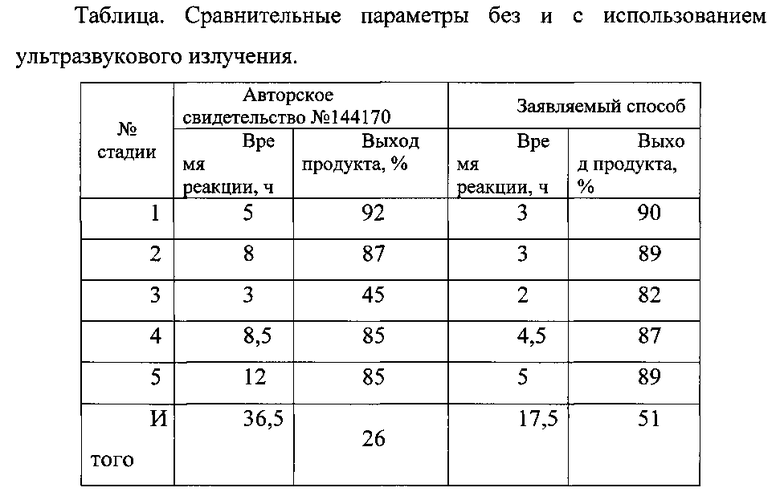
Как видно из таблицы, при интенсификации химических реакций ультразвуковым излучением в два раза сокращается время проведения химических реакций и почти в два раза повышается выход целевого продукта.
Таким образом, заявляемый способ получения линолевой кислоты является эффективным, и кроме того, поскольку исходные продукты имеют высокую стоимость, то увеличение выхода целевого продукта заметным образом повлияет на стоимость линолевой кислоты.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения линолевой кислоты | 1961 |
|
SU144170A1 |
| Способ синтеза линолевой и линоленовой кислот, меченных изотопами углерода С и С | 2016 |
|
RU2630691C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИС-, ЦИС-, ДЯС-ОКТАДЕКАТРИЕН-Э, 11, 13-ОВОй КИСЛОТЫ | 1964 |
|
SU164272A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДЕКАДИЕН-4,8-овой КИСЛОТЫBCiiCi; | 1966 |
|
SU182143A1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ 8-(5-ГЕКСИЛТИОФАН-2-ИЛ) КАПРИЛОВОЙ КИСЛОТЫ И 8-(5-ГЕКСИЛ-3,4-ДЕГИДРОТИОФАН-2-ИЛ) КАПРИЛОВОЙ КИСЛОТЫ | 2007 |
|
RU2368605C2 |
| СПОСОБ ПОЛУЧЕНИЯ (R) - (Z) - 7 (2-АМИНО-2-КАРБОКСИЭТИЛ) ТИО-2- (2,2-ДИМЕТИЛЦИКЛОПРОПИЛКАРБОНИЛ)АМИНО-2-ГЕПТЕНОВОЙ КИСЛОТЫ | 1993 |
|
RU2046792C1 |
| СПОСОБ ПОЛУЧЕНИЯ р-МЕТИЛЗАМЕЩЕННЫХ со-ОКСИКАРБОНОВЫХ КИСЛОТ | 1973 |
|
SU384814A1 |
| СПОСОБ ПОЛУЧЕНИЯ МОНОНАТРИЕВОЙ СОЛИ ИЗОГЛУТАМИЛ-ТРИПТОФАНА | 2019 |
|
RU2703991C1 |
| ОЖЙТНО-ИХКЙЧЕСИБИБЛИОТЕКА | 1971 |
|
SU309933A1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛОВЫХ ЭФИРОВ НЕНАСЫЩЕННЫХ КИСЛОТ | 1967 |
|
SU192690A1 |
Изобретение относится к усовершенствованному способу получения линолевой кислоты. Изобретение относится к области химии и может быть использовано в медицине в качестве маркера при исследовании метаболизма печени и миокарда. Способ получения линолевой кислоты включает получение метилового эфира 7-хлоргептановой кислоты или метилового эфира 7-йодгептановой кислоты, конденсацию 1-хлорундекаина-2,5 с метиловым эфиром 7-хлоргептановой кислоты или с метиловым эфиром 7-йодгептановой кислоты, и гидрирование полученного метилового эфира октадиин-9,12-овой-1 кислоты с дальнейшим омылением полученного метилового эфира октадиен-9,12-овой-1 кислоты до октадекадиен-9,12-овой-1 кислоты (линолевой кислоты), причем стадии реакции получения метиловых эфиров, реакции конденсации в присутствии магния и реакции гидрирования в присутствии палладиевого катализатора проводят в поле ультразвукового излучения мощностью 300 Вт и частотой 22 кГц. Технический результат изобретения заключается в сокращении времени процесса и увеличении выхода целевого продукта. 1 табл.
Способ получения линолевой кислоты, включающий получение метилового эфира 7-хлоргептановой кислоты или метилового эфира 7-йодгептановой кислоты, конденсацию 1-хлорундекаина-2,5 с метиловым эфиром 7-хлоргептановой кислоты или с метиловым эфиром 7-йодгептановой кислоты, и гидрирование полученного метилового эфира октадиин-9,12-овой-1 кислоты с дальнейшим омылением полученного метилового эфира октадиен-9,12-овой-1 кислоты до октадекадиен-9,12-овой-1 кислоты (линолевой кислоты), причем стадии реакции получения метиловых эфиров, реакции конденсации в присутствии магния и реакции гидрирования в присутствии палладиевого катализатора проводят в поле ультразвукового излучения мощностью 300 Вт и частотой 22 кГц.
| Способ получения линолевой кислоты | 1961 |
|
SU144170A1 |
Авторы
Даты
2016-01-20—Публикация
2015-02-17—Подача