Изобретение относится к области нефтехимии и может быть использовано в нефтеперерабатывающей промышленности.
В связи с возросшими требованиями к качеству окружающей среды и рациональному использованию природных ресурсов резко возрос интерес к процессу переработки попутного нефтяного газа. Зачинными продуктами процесса являются олефины, а основной компонент - пропан. Разработка технологии, пригодной для внедрения в промышленность, в первую очередь, зависит от создания каталитической системы, проявляющей высокую активность, селективность в получении целевых продуктов и стабильность. В настоящее время для процесса крекинга пропана в промышленном масштабе в качестве катализаторов используются оксидные смеси, цеолитные катализаторы на основе оксида алюминия и нанесенные на оксидную подложку редкоземельные и драгоценные металлы. Однако их применение вызывает ряд проблем, связанных с дороговизной получения, неустойчивостью к зауглероживанию и невысокой селективностью к непредельным углеводородам. В качестве альтернативных в последнее время стали появляться катализаторы аэрогельного типа. Наиболее перспективными считаются катализаторы, имеющие в своем составе активную подложку, в которую для увеличения активности и селективности вводят различные модификаторы.
Известен способ приготовления катализатора на основе оксида алюминия [DE patent 2529316 А1 22.01.1976], который получают осаждением из водного раствора соли никеля, содержащей примеси соединения алюминия и циркония, затем подвергают сушке и прокаливанию при 573-773 K до получения соответствующих оксидов, после чего проводят формование и прокаливание при 1023-1373 K, при этом по меньшей мере часть оксида никеля восстанавливается до металлического никеля. Данный катализатор представляет собой 15-40% вес. NiO на носителе, содержащем на 1 в.ч. оксид алюминия, от 0.05 до 2 в.ч. диоксида циркония. Но данный катализатор имеет значительные потери сырья в результате коксования.
Известен катализатор и способ его приготовления с использованием основных оксидов: алюминия, титана, кремния [SU patent 367635 А, 30.08.86]. Синтез катализатора заключается в приготовлении шихты, включающей глинозем, титансодержащее соединение, в качестве которого используют металлургический шлак ферротитана, добавлении связующего - азотной кислоты, формовании методом экструзии, провяливании на воздухе, сушки, прокаливании полученного носителя с последующей пропиткой его раствором азотнокислых солей никеля и алюминия, сушке и прокаливании катализаторной массы при 673-773 K. Недостаток катализатора заключается в больших потерях сырья, вызванных нежелательным образованием кокса и легких углеводородов, чувствительности к соединениям серы и невозможности использования сырья, содержащего алкены. Состав катализатора: масс. %: оксид никеля - 10.0, оксид титана - 13.0, оксид кальция - 10.0, оксид магния - 2.4, оксид железа - 1.5, оксид кремния - 0.1, оксид алюминия - 63.0.
Наиболее совершенным, в этой области, считается катализатор, представляющий смесь: глинозем, оксид титана, борная кислота, оксид марганца, оксид лантана, оксид цезия в масс. %: 84,68-92,97:0,06-2,28:0,25-5,79:0,01-3,97:0,11-7,09:0,01-2,59 [RU патент 2446879, 07.10.2010]. Способ получения катализатора включает приготовление шихты, включающей глинозем, оксид титана, борную кислоту, оксид марганца, оксид лантана, оксид цезия, добавления связующего, включающего парафин, воск и олеиновую кислоту, формование носителя в виде гранул методом шликерного литья при избыточном давлении 0,4-2 МПа при температуре 340-350 K, провяливание на воздухе и прокаливание полученного носителя в две стадии: прокаливание в керамических формах при температуре 1373-1473 K в течение 4-8 часов, затем подъем температуры в течение часа до температуры 1623-1693 K и прокаливание при данной температуре в течение 2-4 часов, после прокаливания и пропитывания носителя раствором азотнокислых солей никеля, алюминия и/или лантана и цезия, сушки и прокаливания катализаторной массы при 673-773 K. Для приготовления шихты берут гранулы носителя, формуют в виде шаров диаметром 10-25 мм с цилиндрическими каналами диаметром 1-5 мм в количестве от 1 до 10. Данный катализатор имеет ряд значительных недостатков: высокая температура прокаливания носителя, что промышленно не выгодно, и недостаточная активность.
Аналогами по составу являются катализаторы для крекинга углеводородов с применением ультрастабильного цеолита и способ его получения, в котором ультрастабилизации подвергают цеолит в катион-декатионированной форме при температуре 500-550°С и парциальном давлении паров воды ниже 0,8 атмосфер [РФ патент №2127632, 1999]. Недостатком указанного способа является низкий решеточный модуль получаемого цеолита и, соответственно, его невысокие термостабильные и каталитические свойства. Микросферический катализатор для крекинга нефтяных фракций содержит ультрастабильный цеолит Y в катион-декатионированной форме с решеточным модулем 5,2-6,0, содержащий 1,0-1,5 мас. % оксида натрия, 10-14 мас. % оксидов редкоземельных элементов и/или ультрастабильный цеолит с решеточным модулем 6,0-10,0, содержащий 0,5-1,0 мас. % оксида натрия, 7-10 мас. % оксидов редкоземельных элементов и матрицу, в качестве компонентов которой используют аморфный алюмосиликат, гидроксид алюминия и бентонитовую глину, при следующем соотношении компонентов, мас. %: цеолит Y или смесь цеолитов Y 15-30, аморфный алюмосиликат 20-45, гидроксид алюминия 10-40, бентонитовая глина 10-40 [РФ патент №2473385, 2011]. Существенный недостаток в том, что данный катализатор больше подходит для первичного крекинга тяжелой части нефтяного сырья и не активен для газовой фазы. Также данный катализатор плохо поддается регенерации.
В качестве прототипа были выбраны нановолокнистые аэрогельные оксидные катализаторы типа Al2O3 [Патент на изобретение RU 2150429 05.11.1998; Vignes J.-L. Frappart С. Di Costanzo Т. Rouchaud J.-С. Mazerolles L. Michel D. Ultraporous monoliths of alumina prepared at room temperature by aluminium oxidation. J. Mater. Sci. V. 43. 2008, 1234-1240 р.]. Катализаторы нановолокнистых аэрогелей оксида алюминия в крекинге пропана проявляют не высокую каталитическую активность [Маркова Е.Б., Красильникова О.К., Серов Ю.М., Копылов В.В. Исследование нановолокнистых катализаторов на основе оксидов алюминия и титана в реакции крекинга пропана. Бутлеровские сообщения. Т. 34. №4. 2013, 69-74 с.].
Техническим результатом изобретения является получение высокоактивного катализатора, обеспечивающего высокий выход олефинов.
Технический результат достигается тем, что нанокристаллический катализатор для крекинга пропана с целью получения олефинов представляет собой нанокристаллическую форму аэрогеля оксида алюминия.
Технический результат достигается также тем, что способ получения нанокристаллического катализатора для крекинга пропана с целью получения олефинов включает амальгамное окисление с дальнейшей кристаллизацией нановолокнистого оксида алюминия в токе водорода при температуре начиная с 600 K и каждый час поднимая температуру на 50° и достигая температуры в 1200 K, при которой выдерживают в течение 10 часов или в атмосфере водорода в течение 5 часов.
Приготовление нанокристаллического катализатора включает следующие этапы. На первом этапе получают нановолокнистый аэрогель оксида алюминия методом амальгамного окисления пластины алюминия влажным воздухом при комнатной температуре. В качестве исходного материала были взяты алюминиевые пластины прямоугольной формы чистоты 99.999%, размером 100×100×1 мм марки A5N, на поверхности которых нет трещин, деформаций и инородных включений. С одной стороны алюминиевой пластины пассивирующий слой из оксида удаляется химическим путем. Для этого пластина обрабатывается спиртом и помещается на 7 минут в раствор гидрооксида натрия с концентрацией 2 моль/л. Для нанесения слоя ртути на поверхность алюминиевой пластинки, с последующим образованием амальгамы, пластинку выдерживают в растворе соли Hg2+, который содержит ионы серебра Ag+ [Vignes J.-L. Frappart С. Di Costanzo Т. Rouchaud J.-C. Mazerolles L. Michel D. Ultraporous monoliths of alumina prepared at room temperature by aluminium oxidation. J. Mater. Sci. V. 43. 2008, 1234-1240 p.].
Затем получают нанокристаллический аэрогель оксида алюминия методом пошаговой температурной обработки в атмосфере или токе водорода. Для этого в случае обработки током водорода начиная с температуры 600 K каждый час поднимается температура на 50° и достигая температуры в 1200 K выдерживают 10 часов. Альтернативным методом получения является выдерживание в атмосфере водорода при температуре 1200 K в течение 5 часов.
В результате получен высокоактивный и селективный нанокристаллический катализатор с параметрами, приведенными в таблице 1.

SБЭТ - удельная поверхность, рассчитанная по уравнению БЭТ в интервале 0,05<P/Ps<0,35;
объем Wo и условная поверхность микропор SМик в образцах рассчитаны t-plot сравнительным методом
WBJH - объем мезопор по BJH.
Размер пор (две полуширины для щелевой модели 2х) оценен по 4V/a в области БЭТ и в области капиллярной конденсации по десорбционной ветви с использованием модели Баррета-Джойнера-Холенды BJH.
2хo BJH - средний размер пор в области капиллярной конденсации, определенный по методу Баррета-Джойнера-Холенды;
2хo max - размер пор, соответствующий максимум на кривой распределения пор по размерам, рассчитанной по методу Баррета-Джойнера-Холенды;
SМЕ - поверхность мезопор, рассчитанная из линейных участков сравнительных графиков в области полимолекулярной адсорбции;
SМР - суммарная поверхность пор, определяемая из сравнительных графиков, исходящих из начала координат.
Анализ представленных материалов позволяет сделать вывод о том, что предлагаемое техническое решение дает возможность получать нанокристаллический катализатор по достаточно простой технологии.
Степень конверсии пропана определяли при достижении стационарного состояния по количеству вступившего в реакцию пропану:

где nисх - количество пропана, вступившего в реакции (мкмоль),
nост - количество непрореагировавшего пропана (мкмоль).
Исходя из того, что определенные для всех катализаторов поверхности отличаются на 15-20%, а загрузка реактора катализатором была одинаковой, для расчета скорости конверсии пропана использовали выражение:
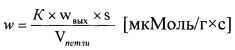
где К - поправочный коэффициент;
wвых - скорость выхода реакционной смеси;
s - площадь пика;
Vпетли - объем петли.
Селективность по каждому компоненту рассчитывается по формуле:
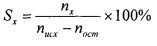
Sx - селективность по компоненту;
nх - количество вещества компонента (мкмоль);
nисх - количество поступающего пропана (мкмоль);
nx - количество непрореагировавшего пропана (мкмоль).
Нанокристаллический катализатор Al2O3/H2-1150 к в области температур 773-1123 K имеет высокую селективность по этилену порядка 63% при температуре 773 K, при этом его выход составляет 50%. Несмотря на то, что промышленные катализаторы содержат весьма активный компонент в виде различных металлов, выход этилена, начиная с температуры 873 K в присутствии катализаторов аэрогельного типа, активированных водородом, значительно больше, чем для промышленных катализаторов. Кроме того, степень превращения в 66% в случае применения катализатора Al2O3/Н2-1150 К достигается при температуре 923 K, что на 200 K меньше, чем при термокрекинге, и на 70 K меньше, чем при использовании промышленного катализатора Pt/Al2O3, что позволяет избежать осмоления при высоких степенях превращения и значительно уменьшить энергоемкость процесса.
Установлено, что стабильность работы катализатора нанокристаллического аэрогеля оксида алюминия достаточно высокая. Для этого катализатора при каталитическом крекинге пропана в области температур до 873 K время работы без изменения активности составило 400 ч, а в температурном интервале 873-1023 K срок эксплуатации составил 150 ч. Однако увеличение температуры выше 1123 K привело к тому, что в течение пяти часов катализаторы практически полностью дезактивировались.
Удаление образовавшегося углерода в течение 10 ч при 923 K током воздуха приводит к полному восстановлении каталитической активности в случае, если катализатор работал при температуре до 873 K в течение 400 часов. Для катализатора, потерявшего каталитическую активность при 1000 K в течение 150 часов, активность восстанавливается наполовину. Катализаторы, потерявшие каталитическую активность при температуре выше 1123 K, регенерировать не удалось, хотя образовавшийся при крекинге углерод частично выгорает. Проведение регенерации более продолжительное время не имеет смысла, так как при данной температуре по прошествии этого времени выделения CO2 не происходит (таблица 2).
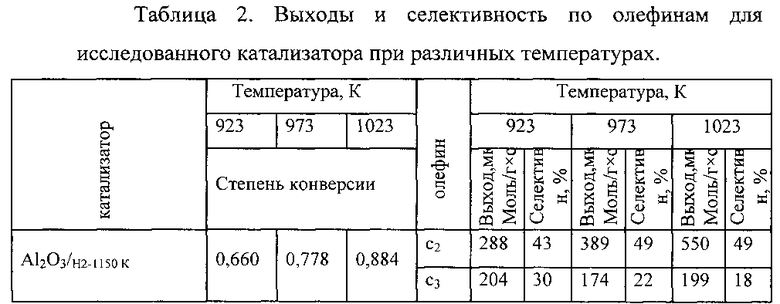
Катализатор отвечает требованиям, предъявленным к катализаторам для крекинга пропана:
1) избирательно отщепляет водород без разрыва всех С-С связей;
2) обладает способностью легко регенерироваться;
3) срок службы измеряется сотнями часов;
4) производство не энергоемкое.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИТНЫЙ НАНОКРИСТАЛЛИЧЕСКИЙ КАТАЛИЗАТОР ДЛЯ КРЕКИНГА ПРОПАНА С ЦЕЛЬЮ ПОЛУЧЕНИЯ ОЛЕФИНОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2015 |
|
RU2604884C1 |
| КАТАЛИЗАТОР И СПОСОБ | 2010 |
|
RU2565757C2 |
| Способ каталитической переработки пропана тетрахлорферрата калия | 2022 |
|
RU2800445C1 |
| ВЫСОКОАКТИВНЫЙ КАТАЛИЗАТОР ДЕГИДРИРОВАНИЯ АЛКАНОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2019 |
|
RU2724902C1 |
| СПОСОБ ПОЛУЧЕНИЯ "ЛЕГКИХ" ОЛЕФИНОВ | 2023 |
|
RU2819849C1 |
| КАТАЛИТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРЕВРАЩЕНИЯ АЛКАНОВ В АЛКЕНЫ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2019 |
|
RU2705574C1 |
| КАТАЛИЗАТОР ДЕГИДРИРОВАНИЯ СЖИЖЕННЫХ УГЛЕВОДОРОДНЫХ ГАЗОВ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2016 |
|
RU2638171C1 |
| ГЕТЕРОГЕННЫЙ КАТАЛИЗАТОР ДЛЯ ВЫСОКОТЕМПЕРАТУРНОГО ДЕГИДРИРОВАНИЯ ПРОПАНА И СПОСОБ ПОЛУЧЕНИЯ ПРОПИЛЕНА С ЕГО ИСПОЛЬЗОВАНИЕМ | 2022 |
|
RU2806558C1 |
| КАТАЛИТИЧЕСКИ НЕАКТИВНЫЙ ТЕПЛОВОЙ ГЕНЕРАТОР И УСОВЕРШЕНСТВОВАННЫЙ ПРОЦЕСС ДЕГИДРИРОВАНИЯ | 2006 |
|
RU2428250C2 |
| СПОСОБ ПОЛУЧЕНИЯ ОЛЕФИНОВ | 2008 |
|
RU2422420C1 |
Изобретение относится к области нефтехимии. Нанокристаллический катализатор для крекинга пропана с целью получения олефинов представляет собой нанокристаллическую форму аэрогеля оксида алюминия. Способ получения нанокристаллического катализатора для крекинга пропана с целью получения олефинов включает амальгамное окисление с дальнейшей кристаллизацией нановолокнистого оксида алюминия в токе водорода при температуре начиная с 600 K и каждый час поднимая температуру на 50° и достигая температуры в 1200 K, при которой выдерживают в течение 10 часов или в атмосфере водорода в течение 5 часов. Применение катализатора обеспечивает высокий выход олефинов. 2 н.п. ф-лы, 2 табл.
1. Способ получения нанокристаллического катализатора для крекинга пропана с целью получения олефинов, путем конверсии углеводородных газов, включающий амальгамное окисление с дальнейшей кристаллизацией нановолокнистого оксида алюминия в атмосфере водорода при температуре 1200 К в течение 5 ч или в токе водорода при температуре начиная с 600 К с повышением каждый час температуры с шагом 50°/ч до достижения температуры в 1200 К и выдерживание в течение 10 ч.
2. Нанокристаллический катализатор, полученный способом по п. 1, представляющий собой нанокристаллическую форму аэрогеля оксида алюминия.
| ВЛИЯНИЕ ПРОЦЕССА АКТИВАЦИИ ТОКОМ ВОДОРОДА НА СТРУКТУРУ НОСИТЕЛЯ КАТАЛИЗАТОРА КРЕКИНГА ПРОПАНА Маркова Е.Б., Серов Ю.М | |||
| В сборнике: ВЫСОКИЕ ТЕХНОЛОГИИ В СОВРЕМЕННОЙ НАУКЕ И ТЕХНИКЕ Сборник научных трудов III Международной научно-технической конференции молодых ученых, аспирантов и студентов ";Высокие технологии в современной науке и технике"; ВТСНТ |
Авторы
Даты
2016-12-20—Публикация
2015-08-14—Подача