ССЫЛКИ НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка заявляет приоритет предварительной заявки на патент США №61/500518, поданной 23 июня 2011, и заявки №61/583325, поданной 5 января 2012 года, содержание которых полностью включено в данную заявку посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к производству ароматических молекул в эукариотических и прокариотических клетках-хозяевах, таких как Е. coli, дрожжи, мицелиальные грибы, водоросли, микроскопические водоросли и другие растительные клетки.
УРОВЕНЬ ТЕХНИКИ
На данный момент существует неудовлетворенная потребность в производстве многих специальных химикатов и жидких видов топлива из возобновляемых ресурсов. Несмотря на значительное отрицательное влияние на окружающую среду, атмосферу и водные запасы земли, большинство химических соединений и транспортных видов топлива все еще получаются из горючих ископаемых, таких как сырая нефть, каменноугольная смола, горючие сланцы и так далее. Особого внимания заслуживают простые фенольные соединения, такие как крезолы, которые извлекаются из каменноугольной смолы в процессе, который имеет такое отрицательное влияние на окружающую среду, что заводы США, специализировавшиеся в производстве крезола, были закрыты в последние годы. Однако это не является общим решением, поскольку проблема может быть просто перенесена в другое географическое расположение. Синтетическая биология предлагает возможные решения проблемы производства некоторых специальных химических веществ, таких как приведены выше.
Поликетиды обычно синтезируются путем конденсации соединений, содержащих два атома углерода, аналогично синтезу жирной кислоты. В общем, синтез подразумевает наличие начального соединения и разбавителя; эти соединения, «содержащие два атома углерода», получаются, например, из ацилтиоэфиров, обычно ацетил, пронионил или метилмалонил кофермент А. Существует четыре класса поликетидсинтазов (ПКС), которые отличаются таким «образом», в котором используются каталитические участки (Watanabe и Ebizuka, 2004). Модульные ПКС типа I являются одиночными белками с многочисленными «модулями», которые содержат каталитические участки, которые используются только в случае линейной организации «конвейерной линии». Итерационные ПКС типа I являются одиночными белками с участками, которые многократно используются для получения окончательного продукта поликетидов. Настоящее изобретение может использовать последовательности кодировки каждого из классов, но в предпочтительных вариантах реализации, используемые ПКС, будут получены в основном из этого класса ПКС, например, синтазы ароматических 6-метилсалициловых кислот или синтазы орселлиновой кислоты или модифицированные версии этих ферментов. Для микробиологического производства поликетидов в разнородных микроорганизмах, таких как грибы и Е. coli, были использованы кодирующие гены полипептидные компоненты ПКС типа I. См., например, патенты США 6033883, 6258566 и 7078233.
ПКС типа II содержат различные белки, каждый из которых имеет один монофункциональный активный участок. Активные участки могут использоваться только один раз или неоднократно. Наконец, ПКС типа III являются одиночными белками с различными модулями, в которых неоднократно используются активные участки.
ПКС действуют аналогично синтазам жирных кислот (СЖК). Жирные кислоты обычно состоят из гидрофобных компонентов и могут также использоваться в качестве источников энергии, таких как биотопливо. Многие эукариоты синтезируют жирные кислоты с использованием обычных или подобных метаболических путей. Жирные кислоты как часть триглицеридов хранятся в семени в качестве источника энергии для дальнейшего проращения. Путь СЖК расположен в пластиде. Ацетил-АПБ (ацил-переносящий белок) образован с помощью конденсирующего фермента, β-кетоацил-АПБ синтаза (КАС) III. Удлинение ацетил-АЦП до более длинных цепочек жирных кислот требует циклического действия конденсации соединений, содержащих 2 атома углерода, из малонил-АПБ для образования более длинного β-кетоацил-АПБ β-кетоацил-АПБ синтаза), уменьшение функции кето-вещества до спирта (β-кетоацил-АПБ редуктаза), дегидратация для образования еноил-АПБ (β-гидроксиацил-АПБ дегидраза), и наконец, уменьшение еноил-АПБ для образования удлиненного насыщенного ацил-АПБ (еноил-АПБ редуктаза). β-кетоацил-АПБ синтаза I (КАС I), главным образом отвечает за удлинение до пальмитоил-АПБ (С 16:0), причем β-кетоацил-АПБ синтаза II (КАС II) главным образом отвечает за окончательное удлинение до стеароил АПБ (С 18:0).
Аналогично, итерационные ароматические ПКС используют конденсацию соединения, содержащего 2 атома углерода, из малонил-АПБ для образования продуктов, таких как 6-метилсалициловая кислота (6-МСК), известная также как 2-гидрокси-6-метилбензойная кислота (ГМБК), и орселлиновая кислота (ССК) по биосинтетическим путям, иллюстрируемых Фигурами 1 и 2. Гибкость этих путей подчеркивается тем фактом, что бактериальные 6-СМСК могут быть предназначены для синтеза ССК простым «выбиванием» каталитической активности из области кеторедуктазы (КР) (Ding et al., Chemistry & Biology 17, 495-503, 2010).
Настоящее изобретение представляет системы для производства молекул и молекул предшественников различного применения в областях бактерицидного, фармацевтического и возобновляемого жидкого топлива. В некоторых вариантах реализации добавление механических устройств для образования пантотеновой кислоты ацил-переносящего белка (т.е. с использованием целой АПБ синтазы, известного также как ППБаза) позволяет производство указанных молекул в широком диапазоне клеток-хозяев, которые не обязательно производят такие молекулы естественным образом.
Ароматические молекулы, прямо или неявно полученные из клеток-хозяев микроорганизмов, таких как крезолы, орсины, гидроксиметилбензойные кислоты и их родственные эфиры, эстеры и лактоны, дают однородные или неоднородные соединения, которые учитываются или могут учитываться для получения соответствия используемых соединений. К таким соединениям относятся бактерициды, фармкомпозиции, витамины, ароматизаторы или возобновляемые источники энергии, такие как топливо, топливные добавки, например, обогащенные кислородом продукты, топливные вспомогательные средства, т.е. высокооктановые агенты смешивания бензинов и т.д.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фигура 1 иллюстрирует путь биосинтеза 6-МСК (Beck et al., Eur J Biochem 192:487-498 (1990)).
Фигура 2 иллюстрирует путь биосинтеза 6-МСК и ССК (Ding et al., Chemistry and Biology 17:495-503 (2010)).
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к производству ароматических молекул в прокариотических и эукариотических клетках-хозяевах, таких как Е. coli, дрожжи, нитчатые грибы, водоросли, микроводоросли, другие растительные клетки и так далее. В одном варианте реализации молекулы получены с использованием функциональных ароматических поликетидсинтазов (ПКС) и окончательное разнообразие молекул превращается в организме для производства специальных химикатов для бактерицидного или фармацевтического использования. Кроме того, настоящее изобретение рассматривает производство предшественников соединений для бактерицидного или фармацевтического использования. В одном варианте реализации предшественники обрабатываются дополнительно для получения высокооктановых ароматических или циклогексановых и циклогексаноловых молекул, которые могут быть предшественниками для дополнительных специальных химикатов и полимеров. Обрабатываемые предшественники могут быть совместимыми с реактивными топливами и топливами на основе бензина и поэтому могут использоваться в качестве возобновляемого источника энергии.
Настоящее изобретение рассматривает рекомбинантные материалы для производства и получения производных поликетидов в разнообразии хозяев и окончательных поликетидов и их производных. Для создания хозяев для производства соединений могут использоваться одиночные или множественные векторы, что известно в области техники. Одиночные векторы позволяют минимальную обработку клеток-хозяев, множественные векторы способствуют дополнительным превращениям в организме и дают большую гибкость при разработке различных новых синтетических путей.
В одном варианте реализации настоящее изобретение рассматривает модифицированную рекомбинантную клетку-хозяина для производства фенольного соединения, которое содержит i) первую систему экспрессии, по меньшей мере, с одной нуклеотидной последовательностью, кодирующей ароматическую поликетидсинтазу (ПКС) для 6-метилсалициловой кислоты (6-СМСК), которая может быть экспрессирована. В другом варианте изобретения клетка-хозяин дополнительно содержит ii) вторую систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую голо-ацил-переносящий белок (АПБ) синтазу, где АПБ пантотенат синтаза содержит указанную ПКС. В дополнительном варианте изобретения клетка-хозяин дополнительно содержит iii) третью систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую декарбоксилазу. В другом варианте изобретения продукт, изолированный от указанной клетки является фенольным соединением. В другом варианте изобретения ароматическая ПКС является синтазой для 6-метилсалициловой кислоты из прокариота. В другом варианте изобретения система экспрессии 6-СМСК из прокариота содержит функциональную декарбоксилазу на одном и том же векторе или на различных векторах. В другом варианте изобретения ароматическая ПКС кодируется с помощью гена ChlB1 из S. antibioticus в форме дикого типа. В дополнительном варианте изобретения фенольное соединение, которое может быть произведено клеткой и может быть изолировано из клетки, является метакрезолом.
В одном варианте изобретения ароматическая ПКС содержит неактивированную область кеторедуктазы (КР). В другом варианте изобретения ароматическая ПКС является синтазой для 6-метилсалициловой кислоты из грибка. В дополнительном варианте изобретения ароматическая ПКС является синтазой орселлиновой кислоты (СОК), закодированной геном AviM из Streptomyces viridochromogenes. В другом варианте изобретения фенольное соединение, которое может быть произведено клеткой и может быть изолировано, является орсином.
В другом варианте изобретения нуклеотидная последовательность, кодирующая декарбоксилазу, выбирается из группы, которая содержит ген декарбоксилазы 6-МСК из P. patulum, ген PatG из Aspergillus clavatus, ген декарбоксилазы ССК из Gliocladium roseum, гены декарбоксилазы 2,3-дигидроксибензойной кислоты из видов леечных грибов аспаргиллов и ген декарбоксилазы 5-карбоксиванильной кислоты из Sphingomonas paucimobilis SYK-6.
В другом варианте изобретения система экспрессии указанной ПКС и система экспрессии указанной голо синтазы АПБ находятся на одном векторе. В других вариантах осуществления система экспрессии указанной ПКС и указанная система экспрессии голо синтазы АПБ находятся на разных векторах. В другом варианте изобретения ПКС и указанная голо синтаза АПБ экспрессированы из дицистронной РНК.
В другом варианте изобретения модифицированная клетка содержит систему экспрессии функциональной декарбоксилазы, которая находится на одном векторе либо с системой экспрессии указанной минимальной ПКС, либо указанной системы экспрессии голо синтазы АПБ или на отдельном векторе. В другом варианте изобретения система экспрессии указанной минимальной ПКС и указанной системы экспрессии голо синтазы АПБ, и указанная система экспрессии функциональной декарбоксилазы находятся на одном векторе. В одном варианте изобретения одна, две или все три из указанных систем экспрессии интегрированы в хромосому клетки-хозяина или экспрессированы из искусственных хромосом дрожжей (ИХД). В других вариантах изобретения, по меньшей мере, две из экспрессированных ПКС, голо синтаза АПБ и декарбоксилаза получены, как производные из мультицистронной РНК. В другом варианте изобретения организм хозяина выбирается из группы, которая содержит виды Pichia pastoris и Aspergillus. В одном варианте изобретения организмом хозяина является Aspergillus niger. В другом варианте изобретения Aspergillus niger не содержит разнородную систему экспрессии голо синтазы АПБ.
В другом варианте настоящее изобретение представляет способ производства фенольного соединения. В одном варианте изобретения способ включает операцию а) представления модифицированной рекомбинантной клетки-хозяина, которая содержит i) первую систему экспрессии, по меньшей мере, с одной нуклеотидной цепочкой, кодирующей ароматическую поликетидсинтазу (ПКС) для 6-метилсалициловой кислоты (6-СМСК), которая может быть экспрессирована; ii) вторую систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую голо синтазу ацил-переносящего белка (АПБ), причем АПБ пантотенат синтаза содержит указанную ПКС; и iii) третью систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую декарбоксилазу. В другом варианте изобретения способ дополнительно включает b) производство промежуточного фенольного соединения в рекомбинантной клетке-хозяине. В другом варианте изобретения способ дополнительно включает с) синтезирование фенольного соединения из промежуточного фенольного соединения, в котором рекомбинантная декарбоксилаза катализирует декарбоксилирование промежуточного фенольного соединения для образования фенольного соединения. В одном варианте изобретения промежуточное фенольное соединение является 6-МСК. В другом варианте изобретения фенольное соединение является метакрезолом.
В одном варианте изобретения ароматическая ПКС содержит неактивированную область кеторедуктазы (КР). В другом варианте изобретения ароматическая ПКС представляет собой синтазу орселлиновой кислоты (СОК), закодированную геном AviM из Streptomyces viridochromogenes. В некоторых вариантах осуществления промежуточное фенольное соединение является орселлиновой кислотой (ОК). В других вариантах изобретения фенольное соединение является орсином.
В другом варианте настоящее изобретение представляет способ производства фенольного соединения. В одном варианте осуществления способ включает а) обеспечение модифицированной рекомбинантной клетки-хозяина, которая включает i) первую систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую ароматическую поликетидсинатазу (ПКС) для 6-метилсалициловой кислоты (6-СМСК), которая может быть экспрессирована; и ii) вторую систему, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую голо синтазу ацил переносящего белка (АПБ), причем синтаза АПБ содержит пантотеновую кислоту указанной ПКС. В одном варианте изобретения способ дополнительно включает b) изолирование промежуточного фенольного соединения, произведенного в рекомбинантной клетке-хозяине. В одном варианте изобретения способ дополнительно включает с) декарбоксилирующее промежуточное фенольное соединение в операции b) образования фенольного соединения путем нагрева металлическим катализатором (или другим типом катализатора) с последующим растворением. В дополнительном варианте изобретния промежуточное фенольное соединение является 6-МСК. В другом варианте изобретения промежуточное фенольное соединение является метакрезолом. В одном варианте изобретения металлический катализатор представлен в порошкообразной форме. В другом варианте изобретения металлический катализатор является цинковым катализатором.
В другом варианте настоящее изобретение представляет модифицированную рекомбинантную клетку-хозяина для производства алкилированного фенольного соединения. В одном варианте изобретения клетка содержит i) первую систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую ароматическую поликетидсинтазу (ПКС) для 6-метилсалициловой кислоты (6-СМСК), которая может быть экспрессирована, и ii) вторую систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую голо синтазу ацил переносящего белка (АПБ), причем синтаза АПБ содержит пантотеновую кислоту указанной ПКС, iii) третью систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую декарбоксилазу, и (iv) четвертую систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую О-метилтрансферазу (ООМТ). В одном варианте изобретения продукт, который может быть произведен клеткой и изолирован от указанной клетки, является алкалированным фенольным соединением. В одном варианте изобретения алкалированное фенольное соединение является 3-метиланизол.
В одном варианте изобретения ароматическая ПКС содержит неактивированную область кеторедуктазы (КР). В другом варианте изобретения ароматическая ПКС является синтазой орселлиновой кислоты (СОК), закодированной геном AviM из Streptomyces viridochromogenes. В одном дополнительном изобретении алкалированное фенольное соединение является 3,5-диметокситолуолом.
В дополнительном варианте изобретения ООМТ закодирована геном Rosa chinensis, выбранным из группы, которая содержит ООМТ1, ООМТ2, ООМТ3, ООМТ4, СОМТ1.
В другом варианте настоящее изобретение представляет способ производства алкалированного фенольного соединения. В одном варианте изобретения способ включает а) обеспечение модифицированной рекомбинантной клетки-хозяина, которая содержит, i) по меньшей мере, одну нуклеотидную последовательность, кодирующую ароматическую поликеидсинтазу (ПКС) для 6-метилсалициловой кислоты (6-СМСК), которая может быть экспрессирована; ii) вторую систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую голо синтазу ацил переносящего белка (АПБ), причем синтаза АПБ содержит пантотеновую кислоту указанной ПКС; и iii) третью систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую декарбоксилазу. В другом варианте изобретения способ дополнительно включает b) изолирование промежуточного фенольного соединения, произведенного в рекомбинантных клетках-хозяевах. В одном варианте изобретения способ дополнительно включает с) алкилирование промежуточного фенольного соединения в операции b) образования алкилированного фенольного соединения путем обработки алкилирующим агентом. В другом варианте изобретения алкилирующим агентом является метанол.
В одном варианте изобретения алкилированное промежуточное фенольное соединение является m-крезолом. В другом варианте изобретения алкилированное фенольное соединение является 3-метиланизолом.
В другом варианте изобретения ароматическая ПКС содержит неактивированную область кеторедуктазы (КР). В одном варианте изобретения ароматическая ПКС является синтазой орселлиновой кислоты (СОК), закодированной геном AviM из Streptomyces viridochromogenes. В одном варианте изобретения промежуточным алкилированным фенольным соединением является орсин. В другом варианте изобретения алкилированное фенольное соединение является 3,5-диметокситолуолом.
В другом варианте настоящее изобретения представляет способ производства фталевого ангидридного соединения, который включает а) обеспечение модифицированной рекомбинантной клетки-хозяина, которая содержит i) первую систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую ароматическую поликетидсинтазу (ПКС) для 6-метилсалициловой килсоты (6-СМСК), которая может быть экспрессирована; ii) вторую систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую голо синтазу ацил-переносящего белка (АПБ), причем синтаза АПБ содержит пантетеновую кислоту указанной ПКС. В другом варианте изобретения способ дополнительно включает b) изолирование промежуточного фталевого ангидридного соединения, произведенного в рекомбинантной клетке-хозяине. В другом варианте изобретения способ дополнительно включает с) окисление промежуточного фталевого ангидридного соединения в операции b) образования фталевого ангидридного соединения посредством обработки окисляющим агентом. В одном варианте изобретения промежуточное фталевое ангидридное соединение является 6-МСК. В другом варианте изобретения фталевый ангидрид является 3-гидроксифталевым ангидридом.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Если не указано обратное, то все термины из области техники, обозначения и другая используемая здесь научная терминология имеют общепонятное значение для специалистов в области техники, к которой относится это изобретение. В некоторых случаях приводится пояснение используемых здесь терминов с общепонятным значением для внесения ясности и/или для справки, и внесение таких определений не обязательно должно объясняться существующей значительной разницей с обычным пониманием в области техники. Технологии и процедуры, описанные или приведенные здесь в виде ссылки, обычно понимаются и широко используются специалистами в области техники в традиционной методологии, например, широко используемая методология молекулярного клонирования, которая была описана Sambrook et al., Molecular Cloning: A Laboratory Manual 2nd edition (1989) Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N. Y. Соответственно, процедуры, в которых используются коммерчески доступные наборы и реагенты, обычно осуществляются в соответствии с протоколами и/или параметрами производителя, если не указано обратное. До приведения настоящих способов описываются наборы и применение, которое стоит понимать так, что это изобретение не ограничено определенной методологией, протоколами, клеточными линиями, видами или родами животных, и описанные здесь компоненты и реагенты естественно могут изменяться. Также стоит понимать, что используемая здесь терминология имеет целью только описание отдельных вариантов изобретения и не предназначена для ограничения области действия настоящего изобретения, которое будет ограничено только в прилагаемой формуле изобретения.
Стоит заметить, что используемые здесь и в формуле изобретения формы единственного числа предполагают соответствующее множественное число, если из контекста не явствует обратное.
В настоящем описании изобретения и формуле изобретения слово «содержит» или его однокоренные слова стоит понимать как включение заявленного целого или группы целых, а не исключение любого другого целого или группы целых.
ПКС означает поликетидсинтазу (например, 6-СМСК или ССК).
АПБ означает ацил-переносящий блок.
САПБ означает синтазу ацил-переносящего белка {например, голо синтазу АПБ).
ДК означает декарбоксилазу.
ПКС* означает модифицированную поликетидсинтазу или вариант ПКС (например, ПКС с неактивной областью кеторедуктазы).
6-СМСК означает синтазу 6-метилсалициловой кислоты.
СОК означает синтазу орселлиновой кислоты.
ООМТ означает орсин O-метилтрансферазы.
6-МСК означает 6-метилсалициловую кислоту.
ОК означает орселлиновую кислоту.
ГМБК означает 2-гидрокси-6-метилбензойную кислоту.
Все патенты, патентные заявки, ссылки на литературу, которые использованы в настоящем описании изобретения, полностью включены посредством ссылки.
Настоящее изобретение представляет способы и материалы для производства интересующих органических соединений быстрым, недорогим и эффективным образом. Так, настоящее изобретение удовлетворяет большое число коммерческих и промышленных нужд. Термин «органическая молекула» означает, например, любую молекулу, которая состоит преимущественно из углерода и водорода, например, ароматические соединения. Органические соединения, которые представляют интерес, содержат, но не ограничиваются фенольными смолами или соединениями, такими как 6-МСК/ГМБК, ОСК, метакрезол, орсин; 3-метиланизол; 3,5-диметокситолуол; и фталаты, такие как фталевый ангидрид (например, 3-гидроксифталевый ангидрид).
В частности производство интересующих микроорганизмов (например, метакрезол, орсин, метиланизол) и их производных из возобновляемых ресурсов рассмотрено в настоящем изобретении. Ароматические соединения получены с помощью функциональных ароматических поликетидсинтаз (ПКС), и окончательное многообразие молекул преобразуется в организме для образования специальных химических веществ микробицидного или фармацевтического применения; или обрабатываются дополнительно для получения высокооктановых ароматических или циклогексановых и циклогексанольных молекул, которые могут служить предшественниками для других специальных химических веществ и полимером, или совместимы с реактивными топливами и топливами на основе бензина и поэтому могут быть использованы в качестве возобновляемого источника энергии.
В одном случае настоящее изобретение относится к синтезу фенольных смол, фенольных соединений и промежуточных фенольных соединений. Используемые здесь термины «фенольная смола» или «фенольное соединение» означает органическое соединение, которое содержит фенильную группу (-C6H5), связанную с гидроксильной группой (-ОН).
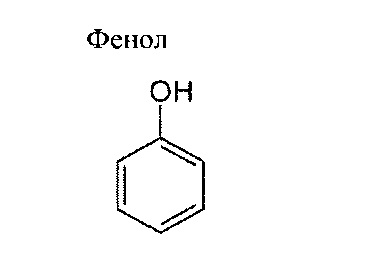
В предпочтительном варианте изобретения фенольная смола или фенольное соединение является m-крезолом (также называемым 3-метилфенол) или орсин (также называемым 5-метилбензен-1,3-диол).
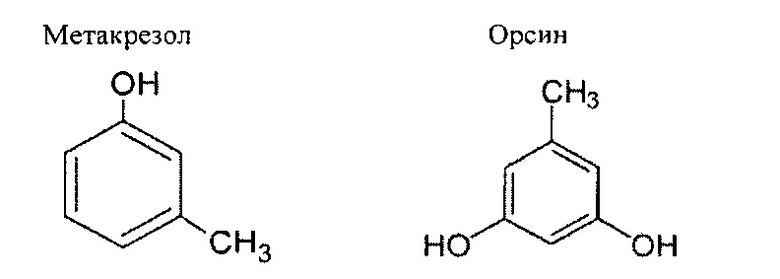
Настоящее изобретение также рассматривает синтез промежуточных фенольных соединений. В одном варианте изобретения промежуточное фенольное соединение является соединением, произведенным в одной из операций описанного здесь метаболического пути (например, Фиг.1 и Фиг.2). Термин «метаболический путь» означает последовательность из двух или более ферментных реакций, в который продукт одной ферментной реакции становится субстратом для следующей ферментной реакции. В каждой операции метаболического пути промежуточные соединения формируются и используются в качестве субстратов для последующей операции. В одном варианте изобретения каждая операция метаболического пути происходит в модифицированной рекомбинантной клетке, которая описана здесь. В другом варианте изобретения, по меньшей мере, одна операция метаболического пути происходит в описанной здесь модифицированной рекомбинантной клетке, и, по меньшей мере, одна операция метаболического пути происходит вне описанной здесь модифицированной рекомбинантной клетки. Соединения, полученные в каждой операции метаболического пути, называются «промежуточными», «промежуточными соединениями» или «промежуточными смесями».
В одном варианте изобретения метаболический путь содержит ферментную реакцию, катализатором которой выступает одно из следующих веществ: 6-СМСК; СОК; голо синтаза АПБ; декарбоксилаза, O-метилтрансфераза; и любая их комбинация. Такие метаболические пути могут производить интересующие соединения, а также промежуточные описанные здесь соединения.
В другом варианте изобретения метаболический путь содержит ферментную реакцию, катализатором которой является i) 6-СМСК или СОК и ii) голо синтаза АПБ.
В одном варианте изобретения метаболический путь содержит использование пантетена 6-СМСК посредством голо синтазы АПБ. В одном варианте изобретения соединение, произведенное в метаболическом пути, является 6-МСК или СОК. В одном варианте изобретения 6-МСК или ОСК является промежуточным фенольным соединением. В другом варианте осуществления 6-МСК является промежуточным фталевым ангидридным соединением.
В одном варианте изобретения промежуточное фенольное соединение выбирается из группы, содержащей 6-метилсалициловую кислоту (6-МСК) (известную также как 2-гидрокси-6-метилбензойная кислота (ГМБК)) и орселлиновую кислоту (ОК). В другом варианте изобретения описанные здесь рекомбинантные клетки и способы представляют синтез интересующего фенольного соединения из промежуточного фенольного соединения. В другом варианте изобретения, m-крезол синтезируется из 6-МСК или орсин синтезируется из промежуточного вещества ОСК.
В другом варианте изобретения 6-МСК является промежуточным фталевым ангидридным соединением. В другом варианте изобретения описанные здесь рекомбинантные клетки и способы представляют синтез фталевого ангидридного соединения из промежуточного фенольного соединения.
В другом варианте изобретения метаболический путь содержит ферментную реакцию, катализатором которой является i) ПКС (например, 6-МСК, модифицированная 6-СМСК или СОК); ii) голо синтаза АПБ и iii) декарбоксилаза. В другом варианте изобретения соединение, произведенное в метаболическом пути, является m-крезолом или орсином.
В другом варианте изобретения метаболический путь содержит ферментную реакцию, катализатором которой является i) ПКС (например, 6-СМСК, модифицированная 6-СМСК или СОК); ii) голо синтаза АПБ и iii) декарбоксилаза. В другом варианте изобретения соединение, произведенное в метаболическом пути, является промежуточное метилированное фенольное соединение. В другом варианте изобретения промежуточное метилированное фенольное соединение является m-крезолом или орсином. В одном варианте изобретения m-крезол является промежуточным веществом для 3-метиланизола, орсин является промежуточным веществом для 3,5-диметокситолуол.
В другом варианте изобретения метаболический путь содержит ферментную реакцию, катализатором которой является i) ПКС (например, 6-СМСК, модифицированная 6-СМСК или ОСК); ii) голо синтаза АПБ; iii) декарбоксилаза и iv) O-метилтрансфераза. В другом варианте изобретения соединение, полученное в метаболическом пути, является метилированным фенольным соединением. В одном варианте изобретения катализатором реакции является 6-СМСК, голо синтаза АПБ, декарбоксилаза и ООМТ для получения 3-метиланизола. В одном варианте изобретения катализатором является модифицированная 6-МСК (или СОК), голо синтаза АПБ, декарбоксилаза и ООМТ для получения 3,5-диметокситолуола.
В другом варианте настоящее изобретение относится к производству интересующего органического соединения в микроорганизме и представляет способы производства таких соединений из источника углеводородов микроорганизма.
Способ включает микроорганизмы, способные производить одно из следующих интересующих органических соединений, например, 6-метилсалициловой кислоты (6-МСК) (также известную, как 2-гидрокси-6-метилбензойная кислота (ГМБК)), m-крезол, орсин, 3-метиланизол; 3,5-диметилтолуол, толуол и эфиры фталевой кислоты. Настоящее изобретение представляет инженерные метаболические пути, изолированные нуклеиновые кислоты или синтетические нуклеиновые кислоты, полипептиды или синтетические полипептиды, клетки-хозяева или генетически синтезированные клетки-хозяева, способы и материалы производства интересующих инженерных соединений.
В другом варианте настоящее изобретение относится к синтетическим полипептидам и полинуклеотидам, кодирующим ферменты, которые обладают активностью или повышенной активностью по отношению к естественным или неестественным субстратам или которые могут быть применены к различным специальным субстратам. Термин «полипептид» и термины «белок» и «пептид», которые здесь являются взаимозаменяемыми, означают аминокислотные полимеры, например, генные продукты, белки естественного происхождения, гомологи, ортологи, паралоги, фрагменты и другие эквиваленты, варианты и аналоги вышеуказанных веществ. Термин «полипептид с ферментной активностью» означает любой полипептид, который катализирует химическую реакцию других веществ, при этом не разрушаясь или не изменяясь по завершении реакции. Обычно полипептид с ферментной активностью является катализатором образования одного или нескольких продуктов из одного или нескольких субстратов. В некоторых вариантах изобретения существующие ферменты модифицируются для использования в органическом биосинтезе. В некоторых предпочтительных вариантах изобретения ферменты, участвующие в производстве интересующих органических соединений, содержит, но не ограничиваются 6-метилсалициловой кислотой (6-СМСК); синтазой орселлиновой кислоты (СОК); голо синтазой ацил-переносящего белка (АПБ); декарбоксилазой и O-метилтрансферазой (ООМТ). В одном варианте изобретения ферментом является 6-СМСК, содержащая неактивированную область кеторедуктазы (КР). В другом варианте изобретения 6-СМСК содержит неактивированную область КР, которая способствует производству орселлиновой кислоты в модифицированных рекомбинантных клетках и описанные здесь способы.
Настоящее изобретение в различных его вариантах использует различные компоненты ароматической системы ПКС или их модифицированные формы или часть более, чем одной из них, вместе с дополнительными модифицированными ферментами, поступающими в необходимый продукт.
Итерационные или «ароматические» системы ПКС, применяемые в настоящем изобретении, характеризуются итерационным использованием каталитических участков произведенных ферментов. Таким образом, в этих ароматических системах ПКС производится только один фермент определенного типа, который является катализатором соответствующей активность системы при синтезе поликетидов.
В некоторых вариантах изобретения механизм реакции фермента может быть изменен для ускорения новых реакций, изменения, расширения или улучшения специфичности субстрата. Стоит отметить, что если ферментная структура (например, структура кристалла) известна, свойства ферментов могут быть модифицированы соответствующим изменением конструкции (см. заявки на патенты США US 20060160138, US 20080064610 и US 20080287320, полное содержание которых приведено посредством ссылки). Модификации или улучшение свойств фермента могут возникать из-за введения модификаций в цепочку полипептидов, которая может изменять структуру и функции фермента и/или взаимодействие с другой молекулой (например, субстрат и неестественный субстрат). В области техники хорошо известно, что некоторые участки полипептидов могут быть критичны для активности фермента. Например, небольшое изменение состава аминокислот, участвующих в катализе и/или в связывающих областях субстрата, будет иметь значительное влияние на функции фермента. Некоторые остатки аминокислот могут иметь существенное значение в поддержании вторичной или третичной структуры фермента, и могут производить значительные изменения в свойствах фермента при модификации. В некоторых вариантах изобретения возможные компоненты пути являются вариантами любых из вышеуказанных веществ. Такие варианты могут быть произведены путем неспецифического мутагенеза или путем рационального устройства для производства ферментной активности, например, с измененной специфичностью субстрата, увеличенной ферментной активностью, большей устойчивостью и т.д. Таким образом, в некоторых вариантах изобретения число модификаций относительно исходного фермента, который производит фермент, обладающий необходимыми свойствами, может содержать одну или более аминокислот, 2 или более аминокислот, 5 или более аминокислот, 10 или более аминокислот, 20 или более аминокислот, до 10% от общего числа аминокислот, до 20% от общего числа аминокислот, до 30% от общего числа аминокислот, до 40% от общего числа аминокислот, составляющих исходный фермент, или до 50% общего числа аминокислот, составляющих исходный фермент. В одном варианте изобретения исходный или контрольный фермент является 6-СМСК, измененная для удаления области кеторедуктазы (КР). В другом варианте изобретения модифицированная 6-СМСК, которой недостает в области КР, может производить орселлиновую кислоту в клетке или с помощью описанного здесь способа.
Специалисты в области техники понимают, что искусственные пути, являющиеся здесь примером, описаны относительно специальных видов генов и охватывают гомологи или ортологи последовательности нуклеиновой кислоты или аминокислоты, но не ограничиваются ими. Гомологические и ортологические последовательности обладают относительно высокой степенью сходства/идентичности последовательности при настройке с помощью способов, известных в области техники.
Варианты изобретения рассматривают новые микроорганизмы или «генетически модифицированные» микроорганизмы или клетки-хозяева, которые были синтезированы с присущими новыми метаболическими свойствами или новыми метаболическими путями. Используемый здесь термин «генетически модифицированные» микроорганизмы означает микроорганизмы, по меньшей мере, с одним генетическим изменением от нормально встречающегося в диком штамме исходных видов. В некоторых вариантах изобретения генетически модифицированные микроорганизмы синтезированы для экспрессирования или сверхэкспрессирования, по меньшей мере, одного фермента в критических точках метаболического пути, и/или блокировать синтез других ферментов для преодоления или обхождения узких мест метаболизма.
Варианты изобретения представляют способы разработки и производства синтезированных метаболических путей. В некоторых вариантах изобретения альтернативные пути производства интересующего продукта из одного или нескольких доступных жизнеспособных субстратов могут быть представлены одной или несколькими клетками-хозяевами или интересующими микроорганизмами. Стоит оценить, что синтезированный путь производства интересующих соединений может предполагать использование различных ферментов, и поэтому поток в пути может быть неоптимальным для производства интересующего продукта. Следовательно, в некоторых вариантах изобретения поток оптимально сбалансирован путем модуляции уровня активности ферментов относительно друг друга. Примеры такой модуляции приведены в тексте настоящей патентной заявки.
В одном варианте настоящее изобретение представляет генетически модифицированные клетки-хозяева или способы их использования для производства интересующих органических соединений. Используемая здесь клетка-хозяин означает эукариотическую клетку в организме или в лабораторных условиях, прокариотическую клетку многоклеточного организма (например, клеточная линия), культивированную, как одноклеточный организм. Клетка-хозяин может быть прокариотической (например, бактериальной, такой как Е. coli или В. subtilis) или эукариотической (например, дрожжи, клетки насекомых или млекопитающих).
Например, клетками-хозяевами могут быть бактериальные клетки (такие как, Е coli, Bacillus subtilis, Mycobacterium spp., M. tuberculosis или другие соответствующие бактериальные клетки), археи (например, Methanococcus Jannaschii или Methanococcus Maripaludis или другие соответствующие клетки архей), клетки дрожжей (например, виды сахаромицетов, такие как S. cerevisiae, S. pombe, Picchia species, вида кандиды, такие как С. albicans или другие соответствующие виды дрожжей).
Стоит заметить, что в некоторых рекомбинантных хозяевах может также быть необходимо активировать поликетиды, произведенные путем постсинтетических модификаций, при которых поликетиды имеют необходимую антибиотическую активность. В случае определенного хозяина, клетка-хозяин будет модифицирована, например, путем трансформации, и будет содержать ферменты, необходимые для эффективных модификаций. К таким ферментам относятся, например, гликолизирующие ферменты.
Таким образом, для производства, например, поликетидов в настоящем изобретении, соответствующие клетки-хозяева модифицируются так, чтобы они содержали векторы, обычно плазмиды, с системой экспрессии для производства белков с одной или несколькими связанными с ПКС активностями. Помещение различных активностей на различные векторы экспрессии может дать высокую степень вариации.
Может использоваться широкое разнообразие клеток, например, естественно встречающиеся клетки, генетически модифицированные клетки, такие как трансгенные клетки, синтетические клетки и так далее; любые соответствующие клетки-хозяева, для которых могут быть разработаны маркеры выделения, которые доказывают содержание различных векторов в готовом виде. Предпочтительными клетками-хозяевами являются дрожжи, Е. coli и другие бактерии, такие как ацентоены и виды Streptomyces, грибы, такие как виды Neurospora and Aspergillus, актиномицеты, виды Clostridium, такие как, С. acetobutylicum, который производит n-бутанол, Methanosaeta thermophila, Micrococcus luteus, который производит длинные цепочки алкенов, Vibrio furnissii, такие как штамм M1, который производит n-алканы, и растительные клетки, несмотря на отсутствие теоретического обоснования того, почему клетки млекопитающих, насекомых или другие соответствующие рекомбинантные клетки не могут быть использованы. Среди штаммов дрожжей предпочтительными являются Saccharomyces cerevisiae и Pichia pastoris. Предпочтительными клетками растений являются клетки водорослей, таких как одноклеточные виды водорослей, диатомовые водоросли и так далее. Однако другие типы и штаммы могут быть использованы со свойственными ферментами ПКС, что можно видеть, например, в WO 98/55625. То есть патент США №7256023 рассматривает поликетидсинтазу полиненасыщенных жирных кислот для производства, например, ДГК и ЕПК, омега-3 масла, которые предположительно имеют преимущества для здоровья. Предпочтительными клетками-хозяевами для переноса этой синтазы, являются, например, Schizochytrium, который является морским микроорганизмом Thraustochytrid, накапливающим большое количество богатых триглицеридом кислот ДГК и докозапентаеновой кислоты.
Растительные клетки, и в некоторых вариантах изобретения одноклеточные растительные клетки, могут использоваться в настоящем изобретении. Например, следующие виды могут использоваться в качестве хозяев интересующих систем векторов: Neochloris oleoabundans, микроводоросль, которая относится к классу Chlorophyceae; Scenedesmus dimorphus, одноклеточная водоросль класса Chlorophyceae, предпочтительно сохранять при постоянном перемешивании; Euglena gracilis; Phaeodactylum tricornutum, диатомовая водоросль; Pleurochrysis carterae, одноклеточные кокколитофориды водорослей, способные кальцинировать внутри клетки, относится к классу Haptophyta (Prymnesiophyceae); Prymnesium parvum; Tetraselmis chui, морская одноклеточная водоросль; Tetraselmis suecica; Isochrysis galbana, микроводоросль; Nannochloropsis salina, называемая также Nannochloris oculata, находится в одной группе с Nannochloris atomus Butcher, Nannochloris maculata Butcher, Nannochloropsis gaditana Lubian и Nannochloropsis oculata (Droop); Botryococcus braunii, зеленая водоросль; Dunaliella tertiolecta, быстрорастущий штамм с высокой скоростью секвестрации СО2 и так далее.
Выбор клеток-хозяев, естественно, определяет выбор контрольных последовательностей, связанных с системой экспрессии, а также с селектируемыми маркерами. Соответствующие системы промотирования, например, для использования в Е. coli, содержат промотор триптофана (трп), промотор лактозы (лак), промотор Т7 и λ-произведенный промотор PL и N-ген участка связывающего рибосомы. Для дрожжей соответствующие управляющие последовательности содержат промоторы для синтеза гликолитических ферментов, таких как глицеральдегид-3-фосфат дегидрогеназы (ГАФДГ), 3-фосфоглицераткиназа (ФГК). Другие промоторы содержат алкогольдегидрогеназы (АДГ-1 и АДГ-2), изоцитохром-С, кислая фосфатаза, деструктивные ферменты, связанные с метаболизмом азота и ферментами, ответственными за утилизацию мальтозы и галактозы. Также известно, что последовательности-терминаторы желательны в конце 3' кодирующих последовательностей.
Способы ферментации могут быть применены к определенному штамму грибов из-за разности в пути использования углерода или режима контроля экспрессии. Например, ферментация дрожжей Saccharomyces может потребовать отдельной подачи глюкозы, источника сложного азота (например, казеин гидролизат), и различных витаминных добавок. Это отличается от метилотрофных дрожжей Pichia pastoris, для которых может требоваться глицерин, метанол и подача микроэлементов, но только простых солей аммиака (азота), для оптимального роста и экспрессии. См., например, Elliott et al. J. Protein Chem. (1990) 9:95 104, патент США № 5324639 и Fieschko et al. Biotechnol. Bioeng. (1987) 29:1113 1121.
Существует большое число генов, реагирующих на метанол, в метилотрофных дрожжах, экспрессия каждого регулируется участками, реагирующими на метанол (называемыми также промоторами). Любой из таких реагирующих на метанол промоторов подходит для использования в настоящем изобретении. Примеры специальных регулирующих участков содержат промоторы для начального гена алкогольоксидазы из клеток дрожжей Pichia pastoris АОХ1, промотор для вторичного гена алкогольоксидазы из P. pastoris АОХ2, промотор для дегидроксиацетонсинтазы гена из P. pastoris (ДАС), промотор гена Р40 из P. pastoris, промотор для гана каталазы из P. pastoris, и так далее. Соответствующие средства для использования с Pichia описаны в патентах США №5231178 и 5324639.
Иллюстрирующие примеры соответствующих клеток-хозяев содержат любые клетки архей, бактерий или эукариотов. Примеры клеток архей содержат, но не ограничиваются принадлежностью к следующим видам: Aeropyrum, Archaeglobus, Halobacterium, Methanococcus, Methanobacterium, Pyrococcus, Sulfolobus и Thermoplasma. Иллюстрирующие примеры видов archae содержат, но не ограничиваются: Aeropyrum pernix, Archaeoglobus fulgidus, Methanococcus jannaschii, Methanobacterium thermoautotrophicum, Pyrococcus abyssi, Pyrococcus horikoshii, Thermoplasma acidophilum, Thermoplasma volcanium.
Примеры клеток бактерий содержат, но не ограничиваются принадлежностью к следующим видам: Agrobacterium, Alicyclobacillus, Anabaena, Anacystis, Arthrobacter, Azobacter, Bacillus, Brevibacterium, Chromatium, Clostridium, Corynebacterium, Enterobacter, Erwinia, Escherichia, Lactobacillus, Lactococcus, Mesorhizobium, Methylobacterium, Microbacterium, Phormidium, Pseudomonas, Rhodobacter, Rhodopseudomonas, Rhodospirillum, Rhodococcus, Salmonella, Scenedesmun, Serratia, Shigella, Staphlococcus, Strepromyces, Synnecoccus и Zymomonas.
Иллюстрирующие примеры видов бактерий содержат, но не ограничиваются: Bacillus subtilis, Bacillus amyloliquefacines, Brevibacterium ammoniagenes, Brevibacterium immariophilum, Clostridium beigerinckii, Enterobacter sakazakii, Escherichia coli, Lactococcus lactis, Mesorhizobium loti, Pseudomonas aeruginosa, Pseudomonas mevalonii, Pseudomonas pudica, Rhodobacter capsulatus, Rhodobacter sphaeroides, Rhodospirillum rubrum, Salmonella enterica, Salmonella typhi, Salmonella typhimurium, Shigella dysenteriae, Shigella flexneri, Shigella sonnei, Staphylococcus aureus и им подобными.
Анаэробные бактерии могут относиться к одному штамму бактерий или смешанной культуре, содержащей две или более ацетогенных бактерий, к которым относятся: Acetobacterium kivui, A. woodii, Butyribacterium methylotrophicum, Clostridium aceticum, C. acetobutylicum, C. formoaceticum, C. kluyveri, C. thermoaceticum, C. thermocellum, C. thermohydrosulfuricum, C. thermosaccharolyticum, Eubacterium limosum, Lactobacillus casei, Peptostreptococcus productus, C. Ljungdahlii и их смеси, но не ограничиваются ими.
В некоторых вариантах изобретения анаэробные организмы бактерий являются метаболически синтезированными. Используемый здесь анаэробный организм являются любым организмом, не требующим кислорода для роста (т.е. анаэробные условия). Преимущественно клетками бактерий могут быть клетки Е. coli, С. glutanicum, В. flavum или В. lactofermentum; эти штаммы промышленно используются на сегодняшний день для создания амино соединений с помощью процессов ферментации бактерий. Например, С. glutanicum широко использовался для производства аминокислот (например, L-глутамата, L-лизина, см. Eggleging L et al., 2005, Handbook for Corynebacterium glutanicum. Boca Raton, USA: CRC Press).
В общем, если используется бактериальная клетка-хозяин, тогда предпочтительным является непатогенный штамм. Иллюстрирующими примерами видов непаталогических штаммов являются: Bacillus subtilis, Escherichia coli, Lactibacillus acidophilus, Lactobacillus helveticus, Pseudomonas aeruginosa, Pseudomonas mevalonii, Pseudomonas pudita, Rhodobacter sphaeroides, Rodobacter capsulatus, Rhodospirillum rubrum и им подобные, но не ограничиваются этими примерами.
Примеры эукариотических клеток содержат, но не ограничиваются клетками грибов. Примерными клетками грибов являются следующие виды грибов: Aspergillus, Candida, Chrysosporium, Cryotococcus, Fusarium, Kluyveromyces, Neotyphodium, Neurospora, Penicillium, Pichia, Saccharomyces, Trichoderma и Xanthophyllomyces (ранее Phajfia), но не ограничиваются ими.
Иллюстрирующие примеры видов эукариотов содержат, но не ограничиваются: Aspergillus nidulans, Aspergillus niger, Aspergillus oryzae, Candida albicans, Chrysosporium lucknowense, Fusarium graminearum, Fusarium venenatum, Kluyveromyces lactis, Neurospora crassa, Pichia angusta, Pichia finlandica, Pichia kodamae, Pichia membranaefaciens, Pichia methanolica, Pichia opuntiae, Pichia pastoris, Pichia pijperi, Pichia quercuum, Pichia salictaria, Pichia thermotolerans, Pichia trehalophila, Pichia stipitis, Streptomyces ambofaciens, Streptomyces aureofaciens, Streptomyces aureus, Saccaromyces bayanus, Saccaromyces boulardi, Saccharomyces cerevisiae, Streptomyces fungicidicus, Streptomyces griseochromogenes, Streptomyces griseus, Streptomyces lividans, Streptomyces olivogriseus, Streptomyces rameus, Streptomyces tanashiensis, Streptomyces vinaceus, Trichoderma reesei и Xanthophyllomyces dendrorhous (ранее Phajfia rhodozyma).
В общем, если используется эукариотическая клетка, тогда предпочтительным является непатогенный штамм. Иллюстрирующие примеры видов непатогенных штаммов содержат, но не ограничиваются следующими видами: Fusarium graminearum, Fusarium venenatum, Pichia pastoris, Saccaromyces boulardi и Saccaromyces cerevisiae.
В некоторых вариантах изобретения присутствуют те селектированные организмы из группы золотистых водорослей (таких как микроорганизмы царства Stramenopiles), зеленые водоросли, диатомовые водоросли, динофлагелляты (такие как микроорганизмы порядка Dinophyceae, в том числе относящиеся к роду Crypthecodinium, например Crypthecodinium cohnii), дрожжи и грибы вида Mucor и Mortierella, которые содержат, но не ограничиваются Mortierella alpina и Mortierella sect. schmuckeri. Клетки группы микроорганизмов Stramenopiles содержат микроводоросли и водорослеобразные микроорганизмы, в том числе следующие группы микроорганизмов: Hamatores, Proteromonads, Opalines, Develpayella, Diplophrys, Labrinthulids, Thraustochytrids, Biosecids, Oomycetes, Hypochytridiomycetes, Commotion, Reticulosphaera, Pelagomonas, Pelagococcus, Ollicola, Aureococcus, Parmales, Diatoms, Xanthophytes, Phaeophytes (brown algae), Eustigmatophytes, Raphidophytes, Synurids, Axodines (в том числе Rhizochromulinaales, Pedinellales, Dictyochales), Chrysomeridales, Sarcinochrysidales, Hydrurales, Hibberdiales и Chromulinales. Thraustochytrids содержит вид Schizochytrium (к виду относятся aggregatum, limnaceum, mangrovei, minutum, octosporum), Thraustochytrium (к виду относятся arudimentale, aureum, benthicola, globosum, kinnei, motivurn, multirudimentale, pachydermum, proliferum, roseum, striatum), Ulkenia (к виду относятся amoeboidea, kerguelensis, minuta, profunda, radiate, sailens, sarkariana, schizochytrops, visurgensis, yorkensis), Aplanochytrium (к виду относятся haliotidis, kerguelensis, profunda, stocchinoi), Japonochytrium (к виду относятся marinum), Althornia (к виду относятся crouchii) и Elina (к виду относятся marisalba, sinorifica). Labrinthulids содержит вид Labyrinthula (к виду относятся algeriensis, coenocystis, chattonii, macrocystis, macrocystis atlantica, macrocystis macrocystis, marina, minuta, roscoffensis, valkanovii, vitellina, vitellina pacifica, vitellina vitellina, zopfi), Labyrinthomyxa (к виду относятся морские растения), Labyrinthuloides (к виду относятся haliotidis, yorkensis), Diplophrys (к виду относятся archeri), Pyrrhosorus* (к виду относятся marinus), Sorodiplophrys* (к виду относятся stercorea), Chlamydomyxa* (к виду относятся labyrinthuloides, montana).
Соответствующие организмы могут быть получены из большого числа доступных источников, которые могут быть получены в естественной среде. Например, Американская коллекция типовых культур приводит много общедоступынх штаммов вышеуказанных микроорганизмов. Используемый здесь любой организм или любой специальный тип организма содержит дикие штаммы, мутанты или рекомбинантные типы. Известные в области техники условия роста, в которых происходит культивирование или рост этих организмов, и соответствующие условия роста описаны, по меньшей мере, для некоторых их этих организмов, например, в патентах США №5130242, 5407957, 5397591, 5492938, 5711983 и 6607900, полное содержание которых приведено здесь посредством ссылки. Предпочтительно эффективная среда также промотирует быстрый рост микроорганизмов. Микроорганизмы могут культивироваться в традиционных режимах ферментации, к которым относится периодическая ферментация, периодическая ферментация с добавлением субстрата и непрерывная ферментация.
В дополнительном варианте изобретения трансгенные растения выбираются из группы, к которой относятся зерновые культуры, соя, рапсовое семя (в том числе масло рапсового семени, особенно канола и зимнее масло рапсового семени), хлопчатый тростник и картофель, особенно кукуруза, соя, рапсовое семя (в том числе масло рапсового семени, особенно канола и зимнее масло рапсового семени), хлопок, пшеница и рис.
В другом варианте изобретения трансгенное растение является голосеменным растением, особенно ель, сосна или пихта.
В предпочтительном варианте изобретения клетка-хозяин выбирается из семейств Aceraceae, Anacardiaceae, Apiaceae, Asteraceae, Brassicaceae, Cactaceae, Cucurbitaceae, Euphorbiaceae, Fabaceae, Malvaceae, Nymphaeaceae, Papaveraceae, Rosaceae, Salicaceae, Solanaceae, Arecaceae, Bromeliaceae, Cyperaceae, Iridaceae, Liliaceae, Orchidaceae, Gentianaceae, Labiaceae, Magnoliaceae, Ranunculaceae, Carifolaceae, Rubiaceae, Scrophulariaceae, Caryophyllaceae, Ericaceae, Polygonaceae, Violaceae, Juncaceae или Poaceae и предпочтительно из растения группы семейств Apiaceae, Asteraceae, Brassicaceae, Cucurbitaceae, Fabaceae, Papaveraceae, Rosaceae, Solanaceae, Liliaceae или Poaceae. Предпочтительными являются зерновые культуры, особенно некоторые из указанных здесь растений-хозяев, относящихся к вышеуказанным семействам и видам, например Anacardium occidentals Calendula officinalis, Carthamus tinctorius, Cichorium intybus, Cynara scolymus, Helianthus annus, Tagetes lucida, Tagetes erecta, Tagetes tenuifolia; Daucus carota; Corylus avellana, Corylus colurna, Borago officinalis; Brassica napus, Brassica rapa ssp., Sinapis arvensis Brassica juncea, Brassica juncea var. juncea, Brassica juncea var. crispifolia, Brassica juncea var. foliosa, Brassica nigra, Brassica sinapioides, Melanosinapis communis, Brassica oleracea, Arabidopsis thaliana, Anana comosus, Ananas ananas, Bromelia comosa, Carica papaya, Cannabis sative, Ipomoea batatus, Ipomoea pandurata, Convolvulus batatas, Convolvulus tiliaceus, Ipomoea fastigiata, Ipomoea tiliacea, Ipomoea triloba, Convolvulus panduratus, Beta vulgaris, Beta vulgaris var. altissima, Beta vulgaris var. vulgaris, Beta maritima, Beta vulgaris var. perennis, Beta vulgaris var. conditiva, Beta vulgaris var. esculenta, Cucurbita maxima, Cucurbita mixta, Cucurbita pepo, Cucurbita moschata, Olea europaea, Manihot utilissima, Janipha manihot., Jatropha manihot., Manihot aipil, Manihot dulcis, Manihot manihot, Manihot melanobasis, Manihot esculenta, Ricinus communis, Pisum sativum, Pisum arvense, Pisum humile, Medicago sativa, Medicago falcata, Medicago varia, Glycine max Dolichos soja, Glycine gracilis, Glycine hispida, Phaseolus max, Soja hispida, Soja max, Cocos nucifera, Pelargonium grossularioides, Oleum cocoas, Laurus nobilis, Persea americana, Arachis hypogaea, Linum usitatissimum, Linum humile, Linum austriacum, Linum bienne, Linum angustifolium, Linum catharticum, Linum flavum, Linum grandiflorum, Adenolinum grandiflorum, Linum lewisii, Linum narbonense, Linum perenne, Linum perenne var. lewisii, Linum pratense, Linum trigynum, Punica granatum, Gossypium hirsutum, Gossypium arboreum, Gossypium barbadense, Gossypium herbaceum, Gossypium thurberi, Musa nana, Musa acuminata, Musa paradisiaca, Musa spp., Elaeis guineensis, Papaver orientate, Papaver rhoeas, Papaver dubium, Sesamum indicum, Piper aduncum, Piper amalago, Piper angustifolium, Piper auritum, Piper betel, Piper cubeba, Piper longum, Piper nigrum, Piper retrofractum, Artanthe adunca, Artanthe elongata, Peperomia elongata, Piper elongatum, Steffensia elongata, Hordeum vulgare, Hordeum jubatum, Hordeum murinum, Hordeum secalinum, Hordeum distichon Hordeum aegiceras, Hordeum hexastichon., Hordeum hexastichum, Hordeum irregulare, Hordeum sativum, Hordeum secalinum, Avena sativa, Avena fatua, Avena byzanlina, Avena fatua var. sativa, Avena hybrida, Sorghum bicolor, Sorghum halepense, Sorghum saccharatum, Sorghum vulgare, Andropogon drummondii, Holcus bicolor, Holcus sorghum, Sorghum aethiopicum. Sorghum arundinaceum, Sorghum caffrorum, Sorghum cernuum, Sorghum dochna, Sorghum drummondii, Sorghum durra, Sorghum guineense, Sorghum lanceolatum, Sorghum nervosum, Sorghum saccharatum, Sorghum subglabrescens, Sorghum verticilliflorum, Sorghum vulgare, Holcus halepensis, Sorghum miliaceum millet, Panicum militaceum, Zea mays, Triticum aestivum, Triticum durum, Triticum turgidum, Triticum hybernum, Triticum macha, Triticum sativum или Triticum vulgare, Cofea spp., Coffea arabica, Coffea canephora, Coffea liberica, Capsicum annuum, Capsicum annuum var. glabriusculum, Capsicum frutescens, Capsicum annuum, Nicotiana tabacum, Solanum tuberosum, Solanum melongena, Lycopersicon esculentum, Lycopersicon lycopersicum, Lycopersicon pyriforme, Solanum integrifolium, Solanum lycopersicum Theobroma cacao или Camellia sinensis.
Anacardiaceae, например виды Pistacia, Mangifera, Anacardium, виды Pistacia vera [pistachios, Pistazie], Mangifer indica [Mango] или Anacardium occidentale [анакард]; Asteraceae, например виды Calendula, Carthamus, Centaurea, Cichorium, Cynara, Helianthus, Lactuca, Locusta, Tagetes, Valeriana, виды Calendula officinalis [календула], Carthamus tinctorius [сафлор], Centaurea cyanus [золототысячник обыкновенный], Cichorium intybus [цикорий обыкновенный], Cynara scolymus [артишок], Helianthus annus [подсолнечник], Lactuca sativa, Lactuca crispa, Lactuca esculenta, Lactuca scariola L. ssp.sativa, Lactuca scariola L. var. integrata, Lactuca scariola L. var. integrifolia, Lactuca sativa subsp.romana, Locusta communis, Valeriana locusta [латук], Tagetes lucida, Tagetes erecta или Tagetes tenuifolia [календула]; Apiaceae, например, Daucus, виды Daucus carota [морковь]; Betulaceae, например, Corylus, виды Corylus avellana или Corylus colurna [лесной орех]; Boraginaceae, виды Borago, например Borago officinalis [огуречник]; Brassicaceae, например виды, Brassica, Melanosinapis, Sinapis, Arabadopsis, виды Brassica napus, Brassica rapa ssp.[канола, рапсовое масло, репа масличная], Sinapis arvensis Brassica juncea, Brassica juncea var. juncea, Brassica juncea var. crispifolia, Brassica juncea var. foliosa, Brassica nigra, Brassica sinapioides, Melanosinapis communis [горчица], Brassica oleracea [свекла кормовая] или Arabidopsis thaliana; Bromeliaceae, например виды Anana, Bromelia, виды Anana comosus, Ananas ananas или Bromelia comosa [ананас]; Caricaceae, например вид Carica, вид Carica papaya [папайя]; Cannabaceae, например вид Cannabis, вид Cannabis sative [конопля], Convolvulaceae, например вид Ipomea, Convolvulus, виды Ipomoea batatus, Ipomoea pandurata, Convolvulus batatas, Convolvulus tiliaceus, Ipomoea fastigiata, Ipomoea tiliacea, Ipomoea triloba или Convolvulus panduratus [сладкий картофель, вьюнок скрипковидный, дикий картофель], Chenopodiaceae, например вид Beta, т.е. виды Beta vulgaris, Beta vulgaris var. altissima, Beta vulgaris var. Vulgaris, Beta maritima, Beta vulgaris var. perennis, Beta vulgaris var. conditiva или Beta vulgaris var. esculenta [сахарная свекла]; Cucurbitaceae, например вид Cucubita виды Cucurbita maxima, Cucurbita mixta, Cucurbita реро или Cucurbita moschata [тыква, тыква крупноплодная]; Elaeagnaceae, например вид Elaeagnus, вид Olea europaea [olive]; Ericaceae, например вид Kalmia, виды Kalmia latifolia, Kalmia angustifolia, Kalmia microphylla, Kalmia polifolia, Kalmia occidentalis, Cistus chamaerhodendros или Kalmia lucida [кальмия, кальмия широколистная, кальмия самшитолистная, spoon wood, кальмия узколистная, кальмия альпийская, кальмия дубровниколистная, кальмия многолистная]; Euphorbiaceae, например виды Manihot, Janipha, Jatropha, Ricinus, виды Manihot utilissima, Janipha manihot, Jatropha manihot, Manihot aipil, Manihot dulcis, Manihot manihot, Manihot melanobasis, Manihot esculenta [маниока, маранта, макиок съедобный, кассия] или Ricinus communis [касторовое семя, касторовое масло, касторовый боб, клещевина, клещевина обыкновенная]; Fabaceae, например виды Pisum, Albizia, Cathormion, Feuillea, Inga, Pithecolobium, Acacia, Mimosa, Medicajo, Glycine, Dolichos, Phaseolus, Soja, например виды Pisum sativum, Pisum arvense, Pisum humile [горох], Albizia berteriana, Albizia julibrissin, Albizia lebbeck, Acacia berteriana, Acacia littoralis, Albizia berteriana, Albizzia berteriana, Cathormion berteriana, Feuillea berteriana, Inga fragrans, Pithecellobium berterianum, Pithecellobium fragrans, Pithecolobium berterianum, Pseudalbizzia berteriana, Acacia julibrissin, Acacia nemu, Albizia nemu, Feuilleea julibrissin, Mimosa julibrissin, Mimosa speciosa, Sericanrda julibrissin, Acacia lebbeck, Acacia macrophylla, Albizia lebbek, Feuilleea lebbeck, Mimosa lebbeck, Mimosa speciosa [кампешевое дерево, шелковая акация, альбиция Лебекка], Medicago sativa, Medicago falcata, Medicago varia [люцерна] Glycine max Dolichos soja, Glycine gracilis, Glycine hispida, Phaseolus max, Soja hispida или Soja max [соевые бобы]; Geraniaceae, например виды Pelargonium, Cocos, Oleum, например виды Cocos nucifera, Pelargonium grossularioides или Oleum cocois [кокосовая пальма]; Gramineae, например вид Saccharum, например вид Saccharum officinarum; Juglandaceae, например виды Juglans, Wallia, например виды Juglans regia, Juglans ailanthifolia, Juglans sieboldiana, Juglans cinerea, Wallia cinerea, Juglans bixbyi, Juglans californica, Juglans hindsii, Juglans intermedia, Juglans jamaicensis, Juglans major, Juglans microcarpa, Juglans nigra или Wallia nigra [грецкий орех, орех черный, орех обыкновенный, орех серый, орех серый калифорнийский, черный орех]; Lauraceae, например виды Persea, Laurus, например виды laurel Laurus nobilis [лавр, лавр благородный, магнолия виргинская], Persea americana Persea americana, Persea gratissima или Persea persea [авокадо]; Leguminosae, например вид Arachis, например виды Arachis hypogaea [арахис]; Linaceae, например виды Linum, Adenolinum, например виды Linum usitatissimum, Linum humile, Linum austriacum, Linum bienne, Linum angustifolium, Linum catharticum, Linum flavum, Linum grandiflorum, Adenolinum grandiflorum, Linum lewisii, Linum narbonense, Linum perenne, Linum perenne var. lewisii, Linum pratense или Linum trigynum [лен, льняное семя]; Lythrarieae, например виды Punica, например виды Punica granatum [гранат]; Malvaceae, например виды Gossypium, например виды Gossypium hirsutum, Gossypium arboreum, Gossypium barbadense, Gossypium herbaceum или Gossypium thurberi [хлопок]; Musaceae, например вид Musa, например виды Musa nana, Musa acuminata, Musa paradisiaca, Musa spp. [банан]; Onagraceae, например виды Camissonia, Oenothera, например виды Oenothera biennis или Camissonia brevipes [первоцвет, энотера]; Palmae, например вид Elacis, например виды Elaeis guineensis [масличная пальма]; Papaveraceae, например вид Papaver, например виды Papaver orientale, Papaver rhoeas, Papaver dubium [мак, мак восточный, мак-самосейка, дикий мак, мак садовый, мачок, мак декоративный]; Pedaliaceae, например вид Sesamum, например вид Sesamum indicum [кунжут]; Piperaceae, например виды Piper, Artanthe, Peperomia, Steffensia, например вид Piper aduncum, Piper amalago, Piper angustifolium, Piper auritum, Piper betel, Piper cubeba, Piper longum, Piper nigrum, Piper retrofractum, Artanthe adunca, Artanthe elongata, Peperomia elongata, Piper elongatum, Steffensia elongata. [перец кайенский, перец дикий]; Poaceae, например виды Hordeum, Secale, Avena, Sorghum, Andropogon, Holcus, Panicum, Oryza, Zea, Triticum, например виды Hordeum vulgare, Hordeum jubatum, Hordeum murinum, Hordeum secalinum, Hordeum distichon Hordeum aegiceras, Hordeum hexastichon, Hordeum hexastichum, Hordeum irregulare, Hordeum sativum, Hordeum secalinum [ячмень, перловая крупа, ячмень гривастый, ячмень заячий, ячмень луговой], Secale cereale [рожь], Avena sativa, Avena fatua, Avena byzantina, Avena fatua var. sativa, Avena hybrida [овес], Sorghum bicolor, Sorghum halepense, Sorghum saccharatum, Sorghum vulgare, Andropogon drummondii, Holcus bicolor, Holcus sorghum, Sorghum aethiopicum, Sorghum arundinaceum, Sorghum caffrorum, Sorghum cernuum, Sorghum dochna, Sorghum drummondii, Sorghum durra, Sorghum guineense, Sorghum lanceolatum. Sorghum nervosum, Sorghum saccharatum, Sorghum subglabrescens, Sorghum verticilliflorum, Sorghum vulgare, Holcus halepensis, Sorghum miliaceum millet, Panicum militaceum [сорго, просо], Oryza sativa, Oryza latifolia [рис], Zea mays [кукуруза, маис] Triticum aestivum, Triticum durum, Triticum turgidum, Triticum hybernum, Triticum macha, Triticum sativum или Triticum vulgare [пшеница, пшеница хлебная, пшеница обыкновенная], Proteaceae, например вид Macadamia, например вид Macadamia intergrifolia [макадамия]; Rubiaceae, например вид Coffea, например виды Coffea spp., Coffea arabica, Coffea canephora или Coffea liberica [кофе]; Scrophulariaceae, например вид Verbascum, например вид Verbascum blattaria, Verbascum chaixii, Verbascum densiflorum, Verbascum lagurus, Verbascum longifolium, Verbascum lychnitis, Verbascum nigrum, Verbascum olympicum, Verbascum phlomoides, Verbascum phoenicum, Verbascum pulverulentum или Verbascum thapsus [коровяк, коровяк крапиволистный, коровяк скипетровидный, коровяк серебристый, коровяк длиннолистный, коровяк белый, коровяк черный, коровяк греческий, коровяк оранжевый, коровяк пурпурный, коровяк серый, коровяк большой]; Solanaceae, например виды Capsicum, Nicotiana, Solanum, Lycopersicon, например виды Capsicum annuum, Capsicum annuum var. glabriusculum, Capsicum frutescens [перец], Capsicum annuum [перец], Nicotiana tabacum, Nicotiana alata, Nicotiana attenuata, Nicotiana glauca, Nicotiana langsdorffii, Nicotiana obtusifolia, Nicotiana quadrivalvis, Nicotiana re panda, Nicotiana rustica, Nicotiana sylvestris [табак], Solanum tuberosum [картофель], Solanum melongena [баклажан] (Lycopersicon esculentum, Lycopersicon lycopersicum., Lycopersicon pyriforme, Solanum integrifolium or Solanum lycopersicum [томат]; Sterculiaceae, например вид Theobroma, например вид Theobroma cacao [какао]; Theaceae, например виды Camellia, например вид Camellia sinensis) [чай].
Эукариотические и прокариотические клетки-хозяева могут быть или были генетически модифицированными (называемые также «рекомбинантные клетки-хозяева», «метаболические синтезированные клетки» или «генетически модифицированные клетки»), и используются в качестве реципиентов нуклеотидной последовательности, кодирующей одну или несколько бинсинтетических или синтезированных продуктов пути гена. Эукариотические и прокариотические клетки-хозяева также обозначают потомство исходной клетки, которая была генетически синтезирована с помощью нуклеиновой кислоты. В некоторых вариантах изобретения клетка-хозяин может выбираться из-за ее метаболических свойств. Например, если выбор или экран связан с конкретным метаболическим путем, то может быть полезным использовать клетку-хозяина, имеющую связанный путь. Такая клетка-хозяин может иметь определенный физиологические потребности, которые делают возможной обработку или импорт, или экспорт одного или нескольких промежуточных или окончательных продуктов пути. Однако в других вариантах изобретения клетка-хозяин, которая не экспрессирует ферменты, связанные с конкретным интересующим путем, может быть выбрана для определения всех компонентов, необходимых для этого пути, с помощью соответствующих наборов генных элементов, и не зависит от отсутствия одной или нескольких операций клетки-хозяина.
Метаболически синтезированная клетка в этом изобретении получена путем трансформации клетки-хозяина, по меньшей мере, с одной нуклеотидной последовательностью, кодирующей ферменты, которые участвуют в синтезированных метаболических путях. Используемые здесь термины «нуклеотидная последовательность», «последовательность нуклеиновой кислоты», «генетический конструкт» используются взаимозаменяемо и означают полимер РНК или ДНК, одно-или двухспиральную, содержащую в разных вариантах синтетическую, ненатуральную или измененную нуклеотидную базу. Нуклеотидная последовательность может содержать один или несколько участков кДНК, геномной ДНК, синтетической ДНК или РНК. В предпочтительном варианте изобретения нуклеотидная последовательность является триплет-оптимизированной для отображения типичного применения триплета клетки-хозяина без изменений полипептида, закодированного нуклеотидной последовательностью. В некоторых вариантах изобретения термин «оптимизация триплета» или «триплет-оптимизация» означает модифицироваание содержимого триплета последовательности нуклеиновой кислоты без модифицирования последовательности полипептида, закодированной нуклеиновой кислотой для усиления экспрессии конкретной клетки-хозяина. В некоторых вариантах изобретения термин используется для обозначения модификации содержимого триплета последовательности нуклеиновой кислоты как средства регулирования уровня экспрессии полипептида (например, либо рост, либо уменьшение уровня экспрессии). Соответственно, варианты изобретения содержат нуклеиновые последовательности, кодирующие ферменты, которые участвуют в синтезированных метаболических путях. В некоторых вариантах изобретения метаболически синтезированная клетка может экспрессировать один или несколько полипептидов с ферментной активностью, необходимых для выполнения описанных ниже операций. В одном варианте изобретения нуклеотидная последовтельность является триплет-оптимизированной для экспрессии в дрожжах.
Например, определенная клетка может содержать одну, две, три, четыре, пять или более пяти последовательностей нуклеиновой кислоты, каждая из которых кодирует полипептид(ы), необходимый для производства фенольного соединения или описанного здесь промежуточного фенольного соединения. В другом варианте одна молекула нуклеиновой кислоты может кодировать один или более одного полипептида. Например, одна молекула нуклеиновой кислоты может содержат последовательности нуклеиновой кислоты, кодирующие два, три, четыре или даже пять разных полипептидов. Последовательности нуклеиновой кислоты, используемые в настоящем изобретении, могут быть получены из различных источников, таких как усиление последовательностей кДНК, библиотеки ДНК, новообразование, вырезание сегмента генома. Последовательности, полученные из таких источников, могут затем быть модифицированы с помощью стандартной молекулярной биологии и/или технологии рекомбинантной ДНК для производства нуклеиновых последовтельностей с необходимыми модификациями. Примерные способы модификации последовательности нуклеиновой кислоты содержат, например, направленный мутагенез, мутагенез ПЦР, делеция, вставка, замещение, обмен частей последовательности с помощью ограничивающих ферментов, в некоторых вариантах совместно с лигированием, гомологической рекомбинацией, направленной рекомбинацией или их различными комбинациями. В других вариантах изобретения последовательности нуклеиновой кислоты могут быть последовательностью синтетической нуклеиновой кислоты. Последовательности синтетических полинуклеотидов могут быть произведены с помощью различных способов, описанных патентом США №7323320, в одновременной заявке Сер. №11/804996 и в публикациях патента США №1006/0160138 и 2007/0269870, полное содержание которых указано здесь посредством ссылки.
Способы трансформации клеток бактерий, растений и животных хорошо известны в области техники. Обычные способы трансформации микроорганизмов содержат электропорацию и химическую модификацию.
В некоторых вариантах изобретения генетически модифицированная клетка-хозяин является генетически модифицированной, так что при культивировании в лабораторных условиях в соответствующей среде она производит интересующий продукт или промежуточное вещество на уровне, по меньшей мере, около 0,1 г/л, по меньшей мере, около 0,5 г/л, по меньшей мере, около 0,75 г/л, по меньшей мере, около 1 г/л L, по меньшей мере, около 1,5 г/л, по меньшей мере, около 2 г/л, по меньшей мере, около 2,5 г/л, по меньшей мере, около 3 г/л, по меньшей мере, около 3,5 г/л, по меньшей мере, около 4 г/л, по меньшей мере, около 4,5 г/л, по меньшей мере, около 5 г/л, по меньшей мере, около 5,5 г/л, по меньшей мере, около 6 г/л, по меньшей мере, около 7 г/л, по меньшей мере, около 8 г/л, по меньшей мере, около 9 г/л, или, по меньшей мере, около 10 г/л.
Следует отметить, что уровень интересующего продукта или его метаболических промежуточных веществ, произведенных генетически модифицированной клеткой-хозяином, может быть контролируема различными способами. В некоторых вариантах изобретения уровень экспрессии контролируется числом образцов последовательностей нуклеиновой кислоты, кодирующих один или несколько ферментов, которые участвуют в синтезированном пути (например, высокая экспрессия вектора или средняя, или низкая экспрессия векторов). Предпочтительно, последовательности нуклеиновой кислоты вводятся в клетку с помощью вектора. Низкая экспрессия образцов векторов обычно дает менее 20 образцов векторов на клетку (например, от 1 до 5, от 5 до 10, от 10 до 15, от 15 до 20 образцов вектора экспрессии на клетку. Соответствующие образцы векторов низкой экспрессии прокариотических клеток (например, Е. Coli) содержат, но не ограничиваются pAYC184, pBeloBac11, pBR332, pBAD33, pBBR1MCS и их производные, pSC101, SuperCos (космида) и pWE15 (космида). Среднее число экспрессии образцов векторов обычно представляет от 20 до около 50 экспрессированных образцов векторов на клетку или от 20 до около 80 экспрессированных образцов векторов на клетку). Соответствующие векторы средней экспрессии образцов прокариотических клеток (например, кишечная палочка) содержат, но не ограничиваются pTrc99A, pBAD24 и векторами, содержащими точку начала репликации ColE1 и его производных. Высокое число векторов экспрессии образцов обычно представляет от 80 до около 200 или более образцов векторов экспрессии на клетку. Соответствующие векторы с высокой экспрессией образцов прокариотических клеток (например, кишечная палочка) содержат, но не ораничиваются векторами pUC, PCV1, pBluescript, pGEM и pTZ.
В другом варианте настоящее изобретение представляет кассеты экспрессии, которые содержат нуклеиновую кислоту или ее последовательность, кодирующую полипептид, участвующий в синтезированном пути. В некоторых вариантах изобретения кассета экспрессии может содержать нуклеиновую кислоту, которая связана рабочими условиями с транскрипционного элемента (например, промотора) и терминатором. Используемый здесь термин «кассета» означает нуклеотидную последовательность, способную к экспрессии конкретного гена, если указанный ген введен с целью связать рабочими условиями с одной или несколькими регулирующими последовательностями, присутствующими в нуклеотидной последовательности. Таким образом, например, кассеты экспрессии могут содержать необходимый гетерологичный ген, который может быть экспрессирован в клетке-хозяине. В некоторых вариантах изобретения одна или несколько кассет экспрессии может быть введена в вектор известными рекомбинантными технологиями. Промотор является последовательностью нуклеотидов, которые начинают и регулируют транскрипцию необходимой последовательности нуклеиновой кислоты с помощью фермента полимеразы РНК. В некоторых вариантах промоторы могут быть индуцируемыми. В некоторых вариантах изобретения промоторы могут быть конститутивными. Неограничивающие промоторы подходящих промоторов для использования в прокариотических клетках-хозяевах содержат бактериофаг Т7 промотора полимеразы РНК, промотор trp, а промотор lac operon и им подобные. Неограничивающий пример подходящего сильного промотора для использования в прокариотических клетках содержат промотор lacUV5, Т5, Т7, Trc, Тас и им подобные. Неограничивающие примеры подходящих промоторов для использования в эукариотических клетках содержат ранний мгновенный промотор CMV, ранний или поздний промотор SV40, промотор тимидинкиназы HSV и им подобные. Участки регулирования терминирования могут быть производиться из различных генов, родственных для предпочтительных хозяев.
Также настоящее изобретение в дополнительном варианте участок промотора, связанный с кодирующим участком в нитчатых грибах, таких как A. niger, A. nidulans или связанные виды грибов, такие как N. Crassa, идентифицирован и изолирован, связанный соответствующим образом в функциональной связи со вторым отличным кодирующим участком вне клетки, и затем повторно вводится в нитчатый гриб-хозяин с использованием соответствующего вектора. Затем клетки-хозяева экспрессируют белок из второго кодирующего участка под контролем введенного участка промотора. Второй кодирующий участок может быть одним из инородных видов хозяев, таких как ПКС, в случае которого хозяин будет экспрессировать белок, не экспрессируемый данным хозяином. В другом варианте второй кодирующий участок может быть родственным для хозяина, что свяазано с участком промотора, отличным от того участка, с которым данный хозяин связан естественным образом, чтобы придать модифицированную или усиленную экспрессию и работу белка.
Настоящее изобретение также представляет способность вводить инородные кодирующие участки в грибы вместе с промоторами для устройства гриба-хозяина, экспрессирующего различные белки. Это изобретение также представляет способность регулировать транскрипцию отдельных генов, которые там естественно случаются или введенные туда инородные гены, посредством участка промотора, который был введен в клетку-хозяин вместе с геном. Например, участок промотора, связанный естественным образом с геном алкогольдегидрогеназы I. (alcA) и геном альдегидегидрогеназы (aldA) A. Nidulans, которые регулируются с помощью этанола, треонини или других индуцирующих веществ в межклеточной среде. Этот эффект зависит от целостности гена, известного как alcR. Когда участок промотора alcA или aldA связан с другим структурным геном в Aspergillus или им подобных в соответствии с настоящим изобретении, подобное регулирование экспрессии различных генов может быть достигнуто с помощью этанола и других индуцирующих элементов.
В качестве дополнительного примера участок промотора естественным образом связан геном глюкоамилазы в Aspergillus niger и используется в вариантах настоящего изобретения положительно индуцирован крахмалом и другими сахарами.
В общем, любая подходящая клетка-хозяин микроорганизма может быть генетически модифицирована для производства соединений, которые являются предметом этого изобретения.
Соответствующие промоторы для использования в клетках млекопитающих, актиномицетах, клетках растений, клетках насекомых и им подобных хорошо известны специалистам в области техники. Таким образом, например, в контексте отдельных клеток растений, таких как водоросли или культуры клеток растений, в некоторых вариантах изобретения интересующий трансгенный элемент может быть помещен в векторе с соответствующими регулирующими и другими функциональными элементами для обеспечения стабильности конструкции, репликации конструкции. Элементы конструкции связаны рабочими условиями для обеспечения функциональности. Словосочетание «связан рабочими условиями» означает, что элементы конструкции связаны для обеспечения функционирования, например, экспрессии трансгенного вещества. Конструкция может быть составлена из различных компонентов, полученных с помощью известных техник в области техники, таких как были описаны в Sambrook et al. (1989, Molecular Cloning, A Laboratory Manual, Nolan, ed., New York: Cold Spring Harbor Laboratory Press).
Как известно в области техники преимуществнным может быть включение элементов, оптимизируемых для использования в интересующих хозяевах, таких как те, которые известны работающими в клетках растений, например, в клетках водорослей. Например, может использоваться соответствующий растительный промотор. Многие из таких растительных промоторов известны и содержат конститутивные, тканевые и временные специфичные промоторы. Примеры конститутивных промоторов содержат, но не ограничиваются октопинсинтазой (Ellis et al., 1987, EMBO J. 6, 11-16, нопалинсинтазой (Bevan et al., NAR 1983 25, 11(2):369-85), маннопинсинтазой (Langridge et al, PNAS, 1989, 86, 3219-3223), производимыми из Т-ДНК Agrobacterium tumefaciens; CaMV35S (Odell et al, Nature. 1985, 313(6005):810-2) и CaMV19S (Lawton et al. Plant Mol. Biol. 9:315-324, 1987); актин риса (McElroy et al. Plant Cell, 2:163-171, 1990), убиквитин кукурузы (Christensen et al, 1992, Plant Mol Biol 18:675-689), убиквитин подсолнечника (Binet et al., 1991, Plant Science, 79, pp 87-94) и промоторы растительного гистона (Brignon et al., Plant J. 1993, 4(3):445-457). Примеры тканеспецифических промоторов содержат семяспецифические промоторы, которые содержат, но не ограничиваются промотором фазеолином (Sengupta-Gopalan et al., 1985, Proc Natl Acad Sci USA 85:3320-3324), промотором конглицинином (Beachy et al., 1985, EMBO J. 4:3407-3053), промотором конклинином (Truksa et al, 2003, Plant Phys and Biochem 41:141-147), промотором олеозином (Plant et al., 1994, Plant Mol Biol 25(2):193-205) и промотором глиатилином (Nunberg et al, 1984, Plant Cell 6:473-486). Другими интересующими промоторами являются Brassica napus промотор напин (European Pat No 0255278), который является семяспецифическим промотором элонгазы жирной кислоты (WO 2/052024), промоторы растительных генов АПБ (патент США №5420034), промоторы генов десатуразы (Thompson et al. (Proc. Nat. Acad. Sci. (1991) 88:2578-2582)), ген Bce-4 (патент США №5530194) или 5' регулирующий участок, связанный со структурным геном синтазы растений.
Также могут использоваться участки терменирования транскрипции, которые определяются сразу 3' по току структурного гена синтазы растений. Так же, как с другими описанными здесь эукариотическими организмами, интроны, места склейки и другие элементы, известные в области техники, могут использоваться для способствования необходимых свойств.
Интересующий ген может быть введен в интересующую клетку с помощью различных средств. Например, трансген per se может вводиться непосредственно, как при использовании частиц, покрытых интересующим трансгеном. Могут использоваться бактериальные векторы клонирования. В другом варианте может использоваться система на основе Agrobacterium, см., например, ЕР-В-0116718 или ЕР-В-0120516. Также, трансформация протопласта с использованием кальция, полиэтиленгликоля или электропорации, микроинжектирования с помощью карбидокремниевых тканей и подобных веществ, известных в области техники.
Селектируемые маркеры, подходящие для использования бактерий, таких как Е. coli и актиномицетов, которые обычно придают устойчивость к антибиотикам; те, которые используются в дрожжах, часто дополняют питательные требования. Селектируемые маркеры для использования в дрожжах содержат, но не ограничиваются URA3, LEU2, LEU2-d, TRP1, LYS2, HIS1, HIS3. Селектируемые маркеры для использования в актиномицетах содержат, но не ограничиваются тиострепто-, апрамицин-, гидромицин- и эритромицин-устойчивостью.
Способы и материалы конструкции векторов, трансформация клеток-хозяев и продукты успешной трансформации хорошо известны в области техники.
Таким образом, в соответствии с одним вариантом изобретением одна клетка-хозяин будет модифицирована и будет содержать один или множество векторов, каждый из которых дает часть синтеза окончательного продукта. При создании различных векторов для производства ароматических соединений отдельные границы значений могут быть связаны с отдельными векторами или, при правильной конструкции, части границ значений могут быть распределены среди более, чем одного вектора, каждый из которых имеет соответствующие последовательности для регулирования экспрессии или в других вариантах которые могут быть интегрированы с хромосомами, которые дают вклад в синтез окончательного продукта. Действительно, все гены, кодирующие все ферменты определенного продукта (т.е. оперон), могут содержаться в геноме промышленного организма. Более того, оперон может быть сконструирован «портативным», таким что ДНК, кодирующая оперон, может быть быстро протестирована в дополнительных штаммах и организмы для оптимального производства необходимого продукта в промышленном масштабе.
В другом варианте два или более ферментов могут быть выражены из одной или нескольких плазмид или хромосомно-интегрированной ДНК с помощью ди- и/или мультрицистронных частей конструкции. В таких конструкциях открытые границы значений могут быть участками внутренней посадки рибосомы (УВПР), что позволяет эффективную трансляцию всех открытых границ значений элементов РНК. Были описаны полезные последовательности дрожжей УВПР S. cerevisiae, и они также эффективно функционировали в метилотрофным дрожжах P. pastoris (http://gra103.aca.ntu.edu.tw/gdoc/98/D92B47403a.pdf).
В другом варинте настоящее изобретение представляет системы экспрессии, которые содержат, по меньшей мере, одну УВПР. В одном варианте изобретения открытые границы значений двух или более из следующих вариантов отделены одной или несколькими УВПР: i) по меньшей мере, одна нуклеотдиная последовательность, кодирующая ароматическую поликетидсинтазу (ПКС) для 6-метилсалициловой кислоты (6-СМСК) или синтазы орселлиновой кислоты (СОК); ii) по меньшей мере, одна нуклеотидная последовательность, кодирующая голо синтазу ацил-переносящего белка (АПБ); и iii) по меньшей мере, одна нуклеотидная последовательность, кодирующая декарбоксилазу.
В соответствии с настоящим изобретением один или несколько из вышеуказанных систем экспрессии, введеных в хозяина, могут быть интегрированы в хромосому или экспрессированы из искусственной хромосомы дрожжей (ИХЖ).
Интегрирование может испытывать влияние, например, использования гомологической рекомбинации. Если используется гомологическая рекомбинация интегрирование может также удалять активность эндогенной ПКС, которая обычно находистя в хромосоме, что описано в вышеуказанной патентной заявке WO 95/08548. В этих вариантах изобретения селектируемый маркер, такой как устойчивость гигромицина или тиострептона будет содержаться в векторе, влияющем на интегрирование.
Как было описано выше, дополнительные ферменты, которые вияют на посттрансляционную модификацию систем ферментов ПКС могут быть необходимы для введения в хозяина через подходящие системы рекомбинантной экспрессии. Кроме того, могут быть необходимы ферменты, которые преобразуют сами поликетиды, например, с помощью декарбоксилирования, метилирования или гликолизации. Может также быть необходимо модифицировать каталитические области для изменения специфичности их субстратов или для замены областей с соответствующей специфичностью и каталитической активностью. Например, уровни малонила СоА в дрожжах могут быть усилены включением в клетку-хозяина систем экспрессии для усиленного синтеза малонила-СоА, такого как сверхэкспрессированный ген синтазы малонила СоА, или карбоксилазы ацетила СоА, как описано в Wattanachaisaereekul et al., Metab Eng 10, 246-54, 2008.
В других вариантах изобретения нормальные процессы метаболизма клеток могут быть усилены или удалены для максимального производства крезола, орсина или продуктов крезол-орсин-эфира. Например, для изменения потока углерода от производства эткнола к производству необходимого продукта экспрессия одного или нескольких ферментов в пути производства этанола активность может быть удалена или уменьшена с помощью генетических изменений. В одном варианте изобретения активность пируватдекарбоксилазы может быть удалена полностью или уменьшена путем делеции или разрушения гена. Кроме того, ген ADH1 может быть модифицирован подобным образом.
Таким образом, настоящее изобретение представляет возможность для усиления молекул, произведенных из поликетидов в хозяевах с основными средствами для создания поликетидов, но для дополнительного направления производства молекул, которые могут быть использованы непосредственно в качестве предшественников специальных химических веществ как источников энергии, или могут быть модифицированы для преобразования в источник энергии. Настоящее изобретение также представляет более эффективные средства для обеспечения разнообразия продуктов предоставлением элементов вводимых ПКС вместе с активностью модифицировнный ферментов, создающих даже более желаемые продукты в реальных условиях.
В предпочтительном варианте изобретения ген ПКС встраивается в один или несколько генов модифицированных ферментов. Например, синтезированный белок с удаленной 6-СМСК или КР 6-СМСК/декарбоксилазой, причем оба фермента активно используются для преобразования сахаров в m-крезол или орсин непосредственно с помощью гликолитического пути. Комплекс трифункционального фермента, выработанный из вышеуказанного, который содержит синтезированную O-метилтрансферазу с закодированным геном, может быть экспрессирован с прямым учетом сахара с помощью пирувата в метиланизол или диметилтолуол.
Топлива на основе бензина, такие как бензин, авиационный бензин, керосин, реактивное топливо и так далее являются смесями соединений, подходящих для использования в сгораемой среде. В общем, такая классификация относится к соединениям, получаемым частичной дистилляцией сырой нефти на основе диапазонов температур. Таким образом, бензин обычно содержит углеводороды (НС) от С5 до С12, получаемые в диапазоне около 150°, керосин, который содержит реактивные топлива с углеводородами от С12 до С15, получаемые в диапазоне около 200° и так далее. Дизельное топливо имеет плотность около 0,85 кг/л, приблизительно на 15% больше, чем у бензина. Дизельное топливо обычно содержит около 75% парафиновых соединений, линейных и циклических, и около 25% ароматических соединений. Обычно молекулы содержат от 10 до 15 молекул углерода. Биодизельное топливо содержит метилэстеры вместо алканов и ароматических углеводородов, многие из которых получены частичной деградацией триглицеридов, которые содержатся в жирных кислотах и эфирах жирных кислот. Ароматические соединения и производные циклогексана из настоящего изобретения могут использоваться прямо в качестве смешивающих агентов вышеуказанных топлив или в некоторых вариантах может быть исходными материалами для эстерификации и этерификации с алкильными группами соответствующей длины для необходимых характеристик топлива.
В некоторых вариантах изобретения первый фермент синтезированного метаболического пути может быть под управлением первого промотора, второй фермент синтезированного пути может быть под управлением второго промотора, причем первый и второй промоторы имеют различную силу. Например, первый промотор может быть сильнее, чем второй промотор, или второй промотор может быть сильнее, чем первый промотор. Следовательно, уровень первого фермента может быть повышен относительно уровня второго фермента синтезированного пути путем увеличения числа образцов первого фермента и/или путем увеличения силы промотора, к которому первый фермент связан рабочими условиями относительно силы промотора, с которой связан второй фермент. В некоторых вариантах изобретения множество ферментов синтезированного пути может быть под управлением одного промотора.
В одном варианте настоящее изобретения представляет модифицированные клетки-хозяева и способы производства метилированного фенольного соединения, в котором промотор используется для контроля экспресси одного ферментного компонента внутри клетки. Во время процесса создания метилированного фенольного соединения скорость биосинтеза фенольного соединнения обычно превышает скорость метилирования фенольного соединения. Например, скорость биосинтеза m-крезола или орсина из клеток и описанные здесь способы превышают скорость метилирования m-крезола или орсина с помощью О-метилтрансферазы. В результате перепроизводство m-крезола или орсина може вызвать проблемы токсичности клеток. В одном варианте настоящее изобретение представляет модифицированную рекомбинантную клетку-хозяина, которая содержит систему экспрессии для декарбоксилазы, причем экспрессия декарбоксилазы регулируется промотором, который уменьшает экспрессию декарбоксилазы. В одном варианте изобретения промотор является промотором Leu2d. Leu2d известен как частично дефектный. В другом варианте изобретения клетка-хозяин с промотором для уменьшенной экспрессии декарбоксилазы, способной производить метилированное фенольное соединение, такое как 3-метиланизол или 3,5-димеокситолуол. В другом варианте изобретения декарбоксилаза с уменьшенной экспрессией из-за промотора представлена декарбоксилазой 6-СМК, экспрессированной из гена PatG Aspergillus clavatus.
В других вариантах изобретения изменение относительного перемещения участков рибосомной связи и экспрессии различных ферментов в пути. Измененние участков рибосомной связи может использоваться только для контроля относительной экспрессии ферментов в пути, или может использоваться совместно с вышеупомянутыми модификациями промоторов и триплетной оптимизацией, которая также влияет на уровень экспрессии гена.
В примерном варианте изобретения экспрессия возможного пути ферментов может зависеть от присутствия субстрата, на который будет действовать путь фермента в реакционной смеси. Например, экспрессия фермента, катализирующего преобразование из А в В, может быть вызвана присутствием А в среде. Экспрессия такого пути ферментов может быть вызвана либо добавлением соединения, вызывающего индуцирование, либо естественным встраиванием соединения во время процессса биосинтетического пути (например, индуктор может быть промежуточным веществом, произвденным для получения желаемого продукта).
В некоторых вариантах изобретения технологии компьютерного дизайна могут использоваться для создания альтернативных путей создания интересующей органической молекулы. В некоторых вариантах изобретения базы данных содержат информацию о геноме, и их связь может использоваться для создания новых метаболических путей. Примерами баз данных являются MetaCyc (база данных метаболических путей и ферментов, база данных биокатализа/биодеградации Университета Миннесоты (база данных каталитических реакций микроорганизмов и путей биодеградации органических химических соединений), LGAND (сводная база данных, предоставляющая информацию о метаболитах и других химических соединениях, связях субстрата с продуктом, представляющих метаболические и другие реакции и информацию о молекулах фермента). База данных компонентов пути также содержит компоненты предвидимых, предполагаемых или неизвестных функций. Она может также содержать мнимые компоненты определенной функции возможной неопределенной композиции. В некоторых вариантах изобретения программа может разрабатывать комбинации регулирующих и/или функциональных элементов, находящихся в общей области (например, которые не охватываются патентными правами и/или с них не взымается лицензионный сбор). Базы данных свободно доступных генетических элементов могут создаваться и/или использоваться в качестве источника последовательностей нуклеиновой кислоты, которая может быть соединена для создания альтернативных путей. Альтернативные пути, которые содержат различные сочетания известных функциональных и/или регулирующих элементов (например, различных видов), могут быть разработаны, составлены и/или протестированы. Библиотеки, содержащие различные участки ферментов, могут использоваться для подтверждения относительного влияния различных типов ферментов или различных вариантов одного фермента. Библиотеки, содержащие вариации различных участков ферментов могут использоваться для подтверждения оптимального уровня экспрессии или регулироваания среди набора генов.
Могут быть составлены нуклеиновые кислоты, кодирующие различные пути. В некоторых вариантах изобретения функциональные свойства различных синтезированных путей могут быть протестированы в организме путем трансформирования клеток-хозяев или организмов с соответствующими составленными нуклеиновыми кислотами и созданием свойств синтезированных организмов. В некоторых вариантах изобретения функциональные свойства различных синтезированных путей могут быть протестированы в лабораторных условиях путем изолирования компонентов, экспрессированных из составленных нуклеиновых кислот, и тестирования соответствующего сочетания компонентов системы в лабораторных условиях.
В некоторых вариантах настоящего изобретения могут использоваться штаммы гаплоидных дрожжей. В других вариантах предпочтительными являются диплоидные штаммы. Это могут быть модифицированные лабораторные штаммы или модифицированные промышленные штаммы. Возобновляемые исходные материалы для роста дрожжей могут быть произведены из очищенных или частично очищенных сахаров, выработанных из кукурузы, пшеницы, сахарного тростника, сахарной свеклы и так далее, или из целлюлозных источников, таких как дерево, просо, бамбук, ятрофа и так далее. Они могут также быть произведены из микроводорослей, цианобактерий и подобных организмов, которые могут производить сахара из диоксида углерода и солнечного света.
Производство соединений
В таблице 1 ниже приведены примеры модифицированных рекомбинантных клеток-хозяев и описанных здесь способов, которое позволяет производство и изоляцию многочисленных интересующих соединений.
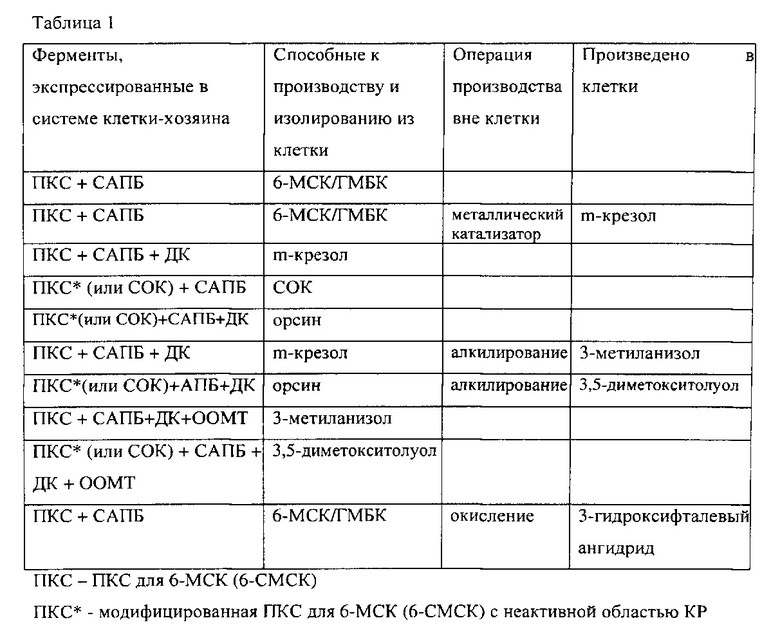
1. 6-МСК или OK
В одном варианте настоящее изобретение представляет рекомбинантные клетки и способы производства 6-метилсалициловой кислоты (6-МСК) или орселлиновой кислоты (ОК). В одном варианте изобретения модифицированная рекомбинантная клетка содержит первую систему экспрессии, по меньшей мере, одной нуклеотидной последовательности, кодирующей ароматическую поликетидсинтазу (ПКС) для 6-метилсалициловой кислоты (6-СМСК) или синтазы орселлиновой кислоты (СОК), которая может быть экспрессирована. В другом варианте изобретения клетка-хозяин дополнительно содержит вторую систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую голо синтазу ацил-переносящего белка (АПБ). В другом варианте изобретения синтаза АПБ содержит пантетеновую кислоту указанной ПКС. В другом случае клетка-хозяин экспрессирует ароматическую ПКС для 6-МСК (6-СМСК). В одном варианте изобретения ароматическая ПКС является синтазой 6-МСК (6-СМСК) гриба. В другом варианте изобретения ароматическая ПКС является синтазой 6-МСК (6-СМСК) прокариота. В другом варианте изобретения синтаза прокариотической 6-СМСК кодируется геном ChlB1 S. antibioticus в дикой форме. В некоторых вариантах изобретения ароматическая ПКС является синтазой СОК. В одном варианте изобретения СОК кодируется геном AviM Streptomyces viridochromogenes.
В другом варианте изобретения синтаза прокариотической 6-СМСК содержит неактивированную область кеторедуктазы (КР), при этом орселлиновая кислота (ОК) производится клеткой. В предпочтительных вариантых изобретения 6-МСК и ОК являются промежуточными соединениями, например описанными здесь промежуточными соединениями фенольного или фталевого ангидрида.
В одном варианте настоящее изобретение рассматривает использование бактериальной интерационной ПКС. В одном варианте изобретения бактериальная итерационная ПКС выбирается из группы, к которой относятся Streptomyces antibioticus DQ116941 ChLB1; Streptomyces pactum AB 303063 pctS; Actinomadura madurae AY271660 6-MCK); Frankia sp. NC 009921; Salinispora arenicola NC 009953 a; Micromonospora echinospora AF 505622 CalO5; Streptomyces viridochromogenes AF333038 AviM; Salinispora arenicola NC 009953 b; Streptomyces carcinostaticus AY117439 NcsB; Saccharopolyspora erythraea NC 009142; и Mycobacterium tuberculosis NC 000962 ppsA.
Гены 6-СМСК могут быть получены из любого естественного источника, такого как грибы, бактерии или растения, или могут быть синтетическими, гибридными или производными модифицированных веществ, которые дают оптимизированные биосинтетические характеристики экспрессированной 6-СМСК ПКС. В одном варианте изобретения ген 6-СМСК, используемый для получения производных растений, таких как узколистный клейкий эриодиктион (Eriodyction pavonina), Khaden S. and Maries, RJ. Molecules 15; 7985-8005 (2010). Модификация и оптимизация активности ферментов хорошо известна специалистам в области техники.
В другом варианте одна или несколько систем экспрессии определенной части системы ПКС интегрированы в хромосому хозяина, и, по меньшей мере, дополнительная система экспрессии остается на реплицируемом векторе. Таким образом, в случае 6-СМСК или СОК система экспрессии одной из открытых границ значений может сначала быть интегрирована в хромосоме, и системы экспрессии других открытых границ значений могут находиться на векторах. Интегрирование таких систем экспрессии в хромосоме может происходить либо с помощью известных способов и средств.
В одном варианте настоящее изобретение представляет модифицированную рекомбинантную клетку-хозяина, которая содержит первую систему экспрессии 6-СМСК (или СОК) и/или вторую систему экспрессии голо синтазы АПБ, интегрированной в хромосому хозяина. В другом варианте изобретения модифицированная клетка-хозяин содержит первую систему экспрессии 6-СМСК (или СОК), которая присутствует в клетке на реплицируемом векторе и вторую систему экспрессии голо синтазы АПБ, интегрированной в хромосому хозяина. В одном варианте изобретения модифицированная клетка-хозяин содержит первую систему экспрессии 6-СМСК (или СОК) присутствует в клетке на реплицируемом векторе, и вторая система экспрессии голо синтазы АПБ интегрирована в хромосому хозяина.
В другом варианте 6-МСК и СОК могут быть произведены и/или изолированы с помощью модифицированных клеток-хозяев и описанных здесь способов. 6-МСК и сок, произведенные и изолированные из клеток, могут служить промежуточными соединениями для производства интересующих соединений (например, m-крезол; 3-метиланизол; 3,5-диметокситолуол; фталевый ангидрид и т.д.).
2. m-крезол или орсин
В другом варианте настоящее изобретение педставляет модифицированные рекомбинантные клетки и способы производства m-крезола или орсина. В одном варианте изобретения модифицированная рекомбинантная клетка-хозяин содержит первую и вторую системы экспрессии, что описано в вышеуказанном разделе. В другом варианте изобретения клетка дополнительно содержит третью систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую декарбоксилазу.
В одном варианте настоящее изобретение рассматривает модифицированную рекомбинантную клетку-хозяина, которая содержит первую систему экспрессии 6-СМСК (или СОК) и/или вторую систему экспрессии голо синтазы АПБ, интегрированную в хромосому. В другом варианте изобретения модифицированная клетка-хозяин дополнительно содержит третью систему экспрессии декарбоксилазы, которая присутствует в клетке на реплицируемом векторе. В одном варианте изобретения модифицированная клетка-хозяин дополнительно содержит третью систему экспрессии декарбоксилазы, интегрированную в хромосому хозяина. В одном варианте изобретения клетка-хозяин содержит, по меньшей мере, одну систему экспрессии 6-СМСК (или СОК), голо синтазы АПБ и декарбоксилазы, интегрированной в хромосому хозяина; и, по меньшей мере, одна из этих систем экспрессии присутствует на реплицируемом векторе. В другом варианте изобретения клетка-хозяин содержит все системы экспрессии 6-СМСК (или СОК), голо синтазы АПБ и декарбоксилазы, интегрированных в хромосому хозяина; или все одинаковые системы экспрессии представлены на реплицируемом векторе.
В одном варианте изобретения нуклеотидная последовательность декарбоксилазы выбирается из группы, которая содержит ген декарбоксилазы 6-МСК P. patulum, ген PatG Aspergillus clavatus или ген декарбоксилазы СОК Gliocladium roseum, гены декарбоксилазы 2,3-дигидробензойной кислоты леечных грибов аспаргиллов и ген декарбоксилазы 5-карбоксиванильной кислоты Sphingomonas paucimobilis SYK-6. В другом варианте изобретения продукт, который может быть произведен и изолирован от клетки-хозяина, является m-крезолом или орсином.
В другом варианте настоящее изобретение рассматривает модифицированную клетку для произодства m-крезола или орсина посредством декарбоксилирования в организме или вне организма. В предыдущей клеточной линии специфическая декарбоксилаза 6-МСК (ГМБК) или орселлиновой кислоты экспрессируется из естественного или модифицированного гена декарбоксилазы в пределах той же клетки. Естественные гены декарбоксилазы содержат ген декарбоксилазы 6-МСК P. patulum, ген PatG Aspergillus clavatus и ген декарбоксилазы орселлиновой кислоты Gliocladium roseum (Pettersson et ah, 1965; Acta Chem. Scand. 19:2013-2021). Стоит также понимать, что другие гены декарбоксилазы, кодирующие произведенные ферменты со специфичностью субстратов для непосредственно или косвенно связанных ароматических карбоксильных кислот, могут быть модифицированы путем мутации или селективного выращивания для производства эффективных декарбоксилирующих ферментов.
В другом варианте изобретения используются два различных типа модифицированных рекомбинантных клеток-хозяев для производства интересующего соединения. В одном варианте настоящее изобретение представляет первую клетку, которая содержит первую систему экспрессии ПКС (6-СМСК или СОК) и вторую систему экспрессии голо синтазы АПБ, а также вторую клетку, которая содержит третью систему экспрессии декарбоксилазы. В другом варианте изобретения первая система экспрессии ПКС и/или система экспрессии второй голо синтазы АПБ интегрирована в хромосому первой клетки, или же присутствует в первой клетке на реплицируемом векторе. В одном варианте изобретения третья система экспрессии декарбоксилазы интегрирована в хромосому второй клетки или присутствует во второй клетке на реплицируемом векторе.
В одном варианте настоящее изобретение представляет смесь модифицированных рекомбинантных клеток-хозяев для производства интересующего соединения. В одном варианте изобретения эта смесь содержит первую модифицированную рекомбинантную клетку-хозяина, в которой есть i) первая система экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующу. ароматическую поликетидсинтазу (ПКС) 6-метилсалициловой кислоты (6-СМСК), которая может быть экспрессирована, и ii) вторая система экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую голо синтазу ацил-переносящего белка (АПБ), причем синтаза АПБ содержит пантетеновую кислоту указанной ПКС; и вторую модифицированную рекомбинантную клетку-хозяина, в которой есть iii) третья система экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую декарбоксилазу. В другом варианте изобретения смесь является совместно культивируемой смесью первой и второй модифицированных рекомбинантных клеток-хозяев. В другом варианте изобретения первая модифицированная рекомбинантная клетка-хозяин представлена клеткой дрожжей. В другом варианте изобретения клетка дрожжей является клеткой S. cerevisiae. В другом варианте изобретения вторая модифицированная рекомбинантная клетка-хозяин является клеткой водорослей. В другом варианте изобретения клетка водорослей представлена A. clavatus. В дополнительном варианте настоящее изобретение представляет способ совместного культивирования первой модифицированной рекомбинантной клетки-хозяина и второй модифицированной рекомбинантной клетки-хозяина, которое позволяет производство фенольного соединения. В одном варианте изобретения фенольное соединение является m-крезолом. Этот способ рассматривается в Примере 6.
3. 3-метиланизол и 3,5-диметокситолуол
В другом варианте настоящее изобретение представляет рекомбинантные клетки и способы производства метилированных фенольных соединений. В одном варианте изобретения кроме описанных здесь первой (например, ПКС), второй (например, голо синтаза АПБ) и третьей (например, декарбоксилазы) систем экспрессии способы и клетки содержат четвертую или дополнительную систему экспрессии гетерогенной O-метилтрансферазы (ООМТ). Такие модифицированные рекомбинантные клетки и способы утилизации системы экспрессии ООМТ обеспечивают производство 3-метиланизола или 3,5-диметокситолуола.
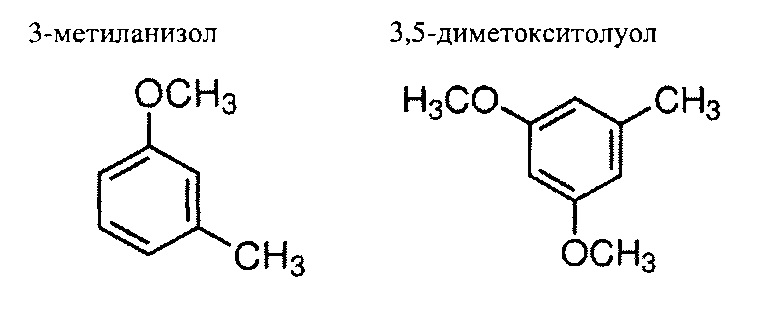
В другом варианте изобретения в векторы, хромосомы или ИХД содержат дополнительную систему экспрессии дополнительная система экспрессии, такую, что изолированными продуктами являются 3-метиланизол или 3,5-диметокситолуол. В другом варианте изобретения O-метилтрансфераза выбирается из генов ООМТ1, ООМТ2, ООМТ3, ООМТ4, СОМТ1 сорта Rosa chinensis и гибридных штаммов розы.
В одном варианте настоящее изобретение представляет модифицированные рекомбинантные клетки и способы производства метилированных фенольных соединений, таких как 3-метиланизол или 3,5-диметокситолуол. В одном варианте изобретения модифицированная рекомбинантная клетка содержит первую систему экспрессии, по меньшей мере, одной нуклеотидной последовательности, кодирующей ароматическую поликетидсинтазу (ПКС) 6-метилсалициловой кислоты (6-СМСК) или синтазы орселлиновой кислоты (СОК), которая может быть экспрессирована. В другом варианте изобретения клетка-хозяин дополнительно содержит вторую систему экспрессии, по меньшей мере, с одной нуклеотидной последовательностью, кодирующей голо синтазу ацил-переносящего белка (АПБ). В другом варианте изобретения синтаза АПБ содержит пантетеновую кислоту указанной ПКС. В другом варианте изобретения клетка дополнительно содержит третью систему экспрессии, по меньшей мере, с одной нуклеотидной последовательностью, кодирующей декарбоксилазу.
В другом варианте изобретения клетка-хозяин экспрессирует ароматическую ПКС для 6-МСК (6-СМСК). В одном вариантез изобретения ароматическая ПКС является синтазой для 6-МСК (6-СМСК) гриба. В другом варианте изобретения ароматическая ПКС является синтазой для 6-МСК (6-СМСК) прокариота. В другом варианте изобретения синтаза прокариотической 6-СМСК кодируется геном ChlB1 S. antibioticus в дикой форме. В некоторых случаях ароматическая ПКС является синтазой СОК. В одном варианте изобретения СОК кодируется геном AviM Streptomyces viridochromogenes. В другом варианте изобретения синтаза прокариотической 6-СМСК содержит неактивированную область кеторедуктазы (КР), так что орселлиновая кислота (ОК) производится в клетке.
В предпочтительных вариантах изобретения клетки-хозяева и описанные здесь способы обеспечивают производство m-крезола в качестве промежуточного фенольного соединения для 3-метиланизола; или орсина в качестве промежуточного фенольного соединения для 3,5-диметокситолуола. В другом варианте изобретения способ включает изолирование m-крезола или орсина из клеток-хозяев и обработку метилирующим агентом для образования 3-метиланизола или 3,5-диметокситолуола соответственно.
В другом варианте настоящее изобретение представляет модифицированные рекомбинантные клетки-хозяева и способы производства метилированных фенольных соединений прямо из клеток-хозяев. В одном варианте настоящее изобретение представляет клетку, которая содержит первую систему экспрессии ПКС, вторую систему экспрессии голо синтазы АПБ и третью систему экспрессии декарбоксилазы, которая содержит дополнительную систему экспрессии метилтрансферазы. В дополнительном варианте изобретения дополнительная система экспрессии содержит нуклеотидную последовательность, кодирующую, по меньшей мере, один ген O-метилтрансферазы, связанный рабочими условиями с промотором в указанной клетке, который обеспечивает производство и изоляцию эфиров метила продуктов ароматических поликетидов. Гены O-метилтрансферазы и их элементы потомства, модифицированные для усиленной ферментной активности или большей специфичности субстратов, могут быть получены из различных источников. Например, в предпочтительном варианте изобретения для трансформации используется орсин O-метилтрансферазы ООМТ1 лепестков розы. Последовательности ДНК O-метилтрансферазы могут быть получены из следующих источников, которые не имеют ограничивающего характера: Rosa Chinensis, R. rugosa, R. majalis, R. beggeriana, R. odorata, R. canina, R. gallica, r. woodsii, R. marettii, R. roxburghii, Vitis vinifera, Humulus lupulus, Prunus dulcis и Prunus armeniaca.
В одном варианте настоящее изобретение представляет модифицированную рекомбинантную клетку-хозяина и первую систему экспрессии 6-СМСК или СОК, которая может быть экспрессирована, и/или вторую систему экспрессии голо синтазы АПБ, интегрированной в хромосому хозяина. В другом варианте изобретения модифицированная клетка-хозяин дополнительно содержит третью систему экспрессии декарбоксилазы и/или ООМТ, которая присутствует в клетке на реплицируемом векторе. В другом варианте изобретения модифицированная клетка-хозяин дополнительно содержит третью систему экспрессии декарбоксилазы и/или ООМТ, которые интегрированы в хромосому хозяина. В одном варианте изобретения клетка-хозяин содержит, по меньшей мере, одну из систем экспрессии для 6-СМСК (или СОК), голо синтазы АПБ, декарбоксилазы и ООМТ, которые интегрированы в хромосому хозяина; и, по меньшей мере, одна из этих систем представлена на реплицируемом векторе. В другом варианте изобретения клетка-хозяин содержит все системы экспрессии 6-СМСК (или СОК), голо синтазы АПБ, декарбоксилаы и ООМТ, которые интегрированы в хромосому хозяина; или все эти системы экспрессии представлены на реплицируемом векторе.
В дополнительном варианте изобретения сверхэкспрессия генов, кодирующая различные метилентетрагидрофолевые редуктазы (МТГФР) или белки слияния МТГФР могут использоваться для поддержания доступной повышенной подачи S-аденозилметионин в качестве субстрата реакции O-метилтрансферазы, как описано Roje et al., J. Biol Chem 277; 4056-4061 (2002). В одном варианте изобретения модифицированные рекомбинантные клетки-хозяева и способы их использования могут включать пятую систему экспрессии, в которой, по меньшей мере, одна нуклеотидная последовательность кодирует МТГФР так, что в клетке производится S-аденозилметионин. В другом варианте изобретения модифицированная рекомбинантная клетка-хозяин содержит первую систему экспрессии ПКС, вторую систему экспрессии АПБ, третью систему экспрессии декарбоксилазы, четвертую систему экспрессии ООМТ, которая содержит дополнительную систему экспрессии метилентетрагидрофолевой редуктазы.
В другом варианте настоящее изобретение представляет способ производства и изолирования промежуточного фенольного соединения в клетке-хозяине. В одном варианте изобретения способ включает обеспечение модифицированной рекомбинантной клетки-хозяина, которая содержит i) первую систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую ароматические поликетидсинтазы (ПКС) для 6-метилсалициловой кислоты (6-СМСК), которая может быть экспрессирована; ii) вторую систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую голо синтазу ацил-переносящего белка (АПБ), причем синтаза АПБ содержит пантетеновую кислоту указанной ПКС; и iii) третью систему экспрессии, которая содержит, по меньшей мере, одну нуклотидную последовательность, кодирующую декарбоксилазы. В другом варианте изобретения способ дополнительно включает операцию изолирования промежуточного фенольного соединения, произведенного в рекомбинантной клетке-хозяине. В другом варианте изобретения способ дополнительно включает алкилирование промежуточного фенольного соединения путем обработки алкилирующим агентом. К алкилирующим агентам относятся любые агенты, которые могут быть добавить алкильную группу к субстрату, в том числе агенты, способствующие замещению атома водорода алкилирующим агентом. В некоторых вариантах изобретения алкилирующий агент выбирается из группы, к которой относится этанол, метанол, изопропанол, бутанол и им подобные. В другом варианте изобретения способ включает обработку промежуточного соединения, изолироованного из клетки алкилирующим агентом одной из следующих алкильных групп: этил, метил, изопропил, третичный бутил, бутил и им подобных в промежуточное соединение.
В одном варианте изобретения фенольное промежуточное соединение является m-крезолом, который обрабатывается алкилирующим агентом для производства алкилированного фенольного соединения. В одном варианте изобретения алкилирующим агентом является этанол для производства 3-этиланизола; метанол для производства 3-метиланизола; изопропанол для производства 3-изопропиланизола; или третичный бутанол для производства 3-бутиланизола. В одном вариантез изобретения алкилирующий агент является метилирующим агентом, выбираемым из вариантов метанола, метилийодида, диметилкарбоната. В другом варианте изобретения метилирование представляет собой О-метилирование.
В одном варианте изобретения промежуточным фенольным соединением является орсин, который затем обрабатывается алкилирующим агентом для производства алкилированного фенольного соединения. В одном варианте изобретения алкилирующим агентом является этанол для производства 3,5-диэтокситолуола; метанол для производства 3,5-диметокситолуола; изопропанол для производства 3,5-диизопрокситолуола; или третичный бутанол для производства 3,5-дибутокситолуола. В одном варианте изобретения алкилирующим агентом является метилирующий агент, выбранный из метанола и диметилкарбоната. В другом варианте изобретения метилирование является О-метилированием.
4. Фталевый ангидрид
В одном варианте настоящее изобретение представляет модифицированные рекомбинантные клетки и способы производства соединений фталевого ангидрида. В одном варианте изобретениия соединение является 3-гидроксифталевым ангидридом.
В одном варианте изобретения модифицированная рекомбинантная клетка содержит первую систему экспрессии, по меньшей мере, одной нуклеотидной последовательности, кодирующей ароматическую поликетидсинтазу (ПКС) 6-метилсалициловой кислоты (6-СМСК), которая может быть экспрессирована. В другом варианте изобретения хозяин дополнительно содержит вторую систему экспрессии, в которой, по меньшей мере, одна нуклеотидная последовательность кодирует голо синтазу ацил-переносящего белка (АПБ). В другом варианте изобретения синтаза АПБ содержит пантетеновую кислоту указанной ПКС. Компоненты ПКС и АПБ могут отличаться от описанных здесь вариантов.
В другом варианте настоящее изобретение представляет способ производства соединения фталевого ангидрида. В одном варианте изобретения способ включает обеспечение модифицированной рекомбинантной клетки-хозяина, которая содержит i) первую систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую ароматическую поликетидсинтазу (ПКС) 6-метилсалициловой кислоты (6-СМСК), которая может быть выражена; и ii) вторую систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую голо синтазу ацил-переносящего белка (АПБ), причем синтаза АПБ содержит пантетеновую кислоту указанной ПКС. В другом варианте изобретения способ дополнительно включает операцию изолирования промежуточного соединения фталевого ангидрида, произведенного в рекомбинантной клетке-хозяине. В другом варианте изобретения способ дополнительно включает окисление промежуточного соединения фталевого ангидрида, полученного в операции изолирования для образования соединения фталевого ангидрида путем обработки окисляющим агентом. К окисляющим агентам относятся любые агенты, которые могут способствовать удалению. В некоторых вариантах изобретения окисляющим агентом является воздух, в том числе атмосферный воздух. Специалистам в области техники известны другие окисляющие агенты, подходящие для использования в настоящем изобретении. В одном варианте изобретения промежуточным соединением фталевого ангидрида является 6-МСК.
4. Системы экспрессии
Настоящее изобретение использует системы экспрессии для каталитической активности системы ароматической ПКС для производства специфических химических соединений крезола, анизола, толуола, циклогексана, циклогексанола и других семейств шестикомпонентных колец. Это молекулы, совместимые с топливом на основе бензина, такие как 3-метиланизол (см., например, патент США №4407661) или 3-этокситолуол, 3-изопропокситолуол или m-крезол, этерифицированный глицерином, и соответствующие диалкилированные производные орсина. Произведенные белки могут содержать родственные последовательности аминокислот и таким образом может использоваться специфичность субстратов и активность родственных или измененных форм этих белков пока поддерживается необходимая каталитическая активность. Специфичность и эффективность этой активности может, однако, отличаться от активности родственных форм. Определенная активность присутствует в родственной системе, однако, они могут быть непреднамеренно удалены или инактивированы, например, инактивированием области кеторедуктазы (КР) гена 6-СМСК для создания фермента с активностью СОК (см., например, Ding et al, Chem Biol 17:495-503, 2010). Дополнительно компоненты различных ароматических систем могут быть смешаны и сравнены, как и компоненты различных модулей модульной системы модульных систем. Патентная заявка WO 95/08548, приведенная здесь посредством ссылки, описывает конструкцию систем гибридной ароматической ПКС, где открытые границы значений актинорходина содержатся в векторах экспрессии с открытыми границами значений альтернативных ароматических систем.
Системы экспрессии белков ПКС не достаточно самой по себе для действительного производства поликетидов, если рекомбинантные клетки-хозяева не имеют активности голо синтазы АПБ, которая влияет на содержание пантетеновой кислоты в ацил-переносящем белке. Эта операция активирования необходима для способности АПБ «подбирать» 2-углеродные соединения, которые являются исходным элементом или растущей поликетидной цепочкой конденсаций Клайзена, которые дают окончательный поликетид. Для хозяев с недостатком фермента фосфопантетеновой кислоты, который ведет себя, как голо синтаза АПБ, изобретение представляет средства придания этой активности с помощью соответствующих систем экспрессии этого фермента. Система экспрессии голо синтазы АПБ может предоставляться на векторе отдельно от того вектора, который несет элемент ПКС или могут предоставляться на том же векторе, или могут быть интегрированы в хромосому хозяина, или могут предоставляться в виде системы экспрессии рекомбинантного белка со всей или частью поликетидсинтазы. В общем, голо синтазы АПБ, связанные с синтезом жирных кислот, не применимы; в связи с этим применяются синтазы, специфически связанные с синтезом поликетидов или с синтезом нерибосомных белков. Определенные голо синтазы АПБ, связанные с синтезом жирных кислот, например белок npgA Aspergillus nidulans, были рассморены по функционированию в биосинтезе поликетидов в гетерогенных хозяевах, таких как дрожжи (Wattanachaisaereekul et al., Biotech Bioeng 97: 893-900, 2007).
Особенно модульные системы ПКС не активируются фосфопантетеновой кислотой, полученной из фосфопантетеновых ферментов внутри определенных клеток-хозяева, таких как Е. coli; однако, ферменты, произведенные из Bacillus, в частности грамицидин голо синтазы АПБ Bacillus brevis, поверхностно связанной голо синтазы АПБ из Bacillus subtilis, и связанный с винтезом жирной кислоты белок npgA ППБазы из Aspergillus nidulans могут использовать модульные области ПКС АПБ в качестве субстратов. Аналогично, было показано, что npgA также способен активировать итерационные ароматические ПКС 6-СМСК. Поскольку использование системы экспрессии для соответствующей голо синтазы АПБ не требуется только для экспрессии генов, кодирующих модульную ПКС, дрожжей или других эукариотов, введение таких систем экспрессии может потребоваться, если поликетиды и их производные должны производиться экспрессированными ферментами.
В другом варианте изобретения системы экспрессии в клетках-хозяевах могут быть представлены на одном или нескольких векторах. В одном варианте изобретения первая система экспрессии ПКС и вторая система экспрессии голо синтазы АПБ могут присутствовать на одном векторе, на различных векторах или могут быть экспрессированы из дицистронной РНК. В другом варианте изобретения третья система экспрессии функциональной декарбоксилазы присутствует на одном векторе с ПКС и/или голо синтазой АПБ, или присутствует на отдельном векторе. В одном варианте изобретения первая система экспрессии ПКС и вторая система экспрессии голо синтазы АПБ, и третья система экспрессии функциональной декарбоксилазы присутствуют на одном векторе. В некоторых вариантах изобретения одна или несколько (или все) первая, вторая и третья системы экспрессии интегрированы в хромосому клетки-хозяина или экспрессированы из искусственных хромосом дрожжей (ИХД). В другом варианте изобретения, в котором, по меньшей мере, два (или все три) экспрессированных ПКС, голо синтазы АПБ и декарбоксилазы производятся из мультицистронной РНК.
Таким образом, в одном варианте настоящее изобретение относится к рекомбинантным клеткам-хозяевам, причем клетка-хозяин модифицирована так, что содержит, по меньшей мере, два вектора; при этом первый вектор содержит первый селективный маркер и первую систему экспрессии, и второй вектор содержит второй селективный маркер и в некоторых вариантах дополнительные векторы с дополнительными селективными маркерами и системами экспрессии, причем системы экспрессии, находящиеся на векторах, закодированы и способны производить, по меньшей мере, минимальную систему ПКС. Если минимальная система ПКС является ароматической системой, то такая минимальная система содержит каталитический участок кетосинтазы/ацил трансферазы (КС/AT), каталитический участок и активность ацил-переносящего белка (АПБ). В одном варианте изобретения клетка-хозяин выбирается из группы, к которой относятся клетки-хозяева бактерий, дрожжей, нитчатых грибов, растений, водорослей и микроводорослей.
В одном особом варианте настоящего изобретения рекомбинантная клетка-хозяин модифицирована так, что она содержит: (а) первый вектор с первым селектируемым маркером и систему экспрессии, которая содержит нуклеотидную последовательность, кодирующую ген синтазы 6-метилсалициловой кислоты (6-СМСК) или ген синтазы орселлиновой кислоты (СОК) и; (b) второй вектор со вторым селектируемым маркером и системой экспрессии, которая содержит нуклеотидную последовательность, кодирующую голо синтазу АПБ; и (с) третий вектор с третьим селектируемым маркером и систему экспрессии, которая содержит нуклеотидную последовательность, кодирующую активность декарбоксилазы, связанную рабочим образом с промотором указанной клетки. В других вариантах, по меньшей мере, два вектора могут быть скомбинированы так, что клетка-хозяин будет содержать только два вектора, или даже один вектор; вектор, содержащий две системы экспрессии может поддерживать их в виде отдельных систем экспрессии или одним промотором может регулироваться две или три открытые границы диапазонов, при этом либо ди-, либо трицистронные участки транскрибируются для трансляции в разработанном ферментном пути. В других вариантах изобретения системы экспрессии всех и каждой частей разработанного ферментного пути могут быть интегрированы в хромосомы клетки-хозяина. Например, ген голо синтазы АПБ npgA Aspergillus nidulans эффективно функционирует при интегрировании в геном S. cerevisiae (Ma et al., Science 326: 589-592 (2009).
В другом варианте изобретения модифицированная рекомбинантная клетка-хозяин содержит, по меньшей мере, одну систему экспрессии, которая содержит по меньшей мере, один из следующих вариантов: i) по меньшей мере, одну нуклеотидную последовательность, кодирующую поликетидсинтазу (ПКС) 6-метилсалициловой кислоты (6-СМСК) или синтазу орселлиновой кислоты (СОК); ii) по меньшей мере, одну нуклеотидную последовательность, кодирующую голо синтазу ацил-переносящего белка (АПБ); и iii) по меньшей мере, одну нуклеотидную последовательность, кодирующую декарбоксилазу.
В одном варианте изобретения клетка-хозяин содержит первую систему экспрессии, содержащую, по меньшей мере, одну нуклеотидную последовательность, кодирующую ароматическую поликетидсинтазу (ПКС) 6-метилсалициловой кислоты (6-СМСК) или синтазу орселлиновой кислоты (СОК); и, по меньшей мере, одну нуклеотидную последовательность, кодирующую голо синтазу ацил-переносящего белка (АПБ). В другом варианте изобретения клетка-хозяин содержит вторую систему экспрессии, содержащую, по меньшей мере, одну нуклеотидную последовательность, кодирующую декарбоксилазу.
В другом варианте настоящее изобретение представляет клетки-хозяева, экспрессирующие рекомбинирующие белки ароматической поликетидсинтазы (ПКС) 6-метилсалициловой кислоты (6-СМСК) или синтазы орселлиновой кислоты (СОК); синтазы голо ацил-переносящего белка (АПБ); и декарбоксилазы. Такие «белки тройной рекомбинации» могут быть экспрессированы с помощью описанных здесь способов.
5. Клетки-хозяева
В одном варианте настоящее изобретение представляет модифицированные рекомбинантные клетки-хозяева для производства поликетидов, которые имеют преимущество в уровне техники. Патент США №6033833 описывает рекомбинантные клетки-хозяева, использующие нуклеотидную последовательность, кодирующую белок слияния ПКС (модульной или грибной) и синтазу голо АПБ. Патент США №6258566 описывает модифицированные рекомбинантные клетки-хозяева, использующие модульные или грибные ПКС. Патент США №7078233 описывает рекомбинантные модифицированные клетки-хозяева, использующие модульные или грибные ПКС и синтазы АПБ, не связанные с синтезом жирных кислот. В одном варианте настоящее изобретение представляет рекомбинантные клетки-хозяева, которые не содержат нуклеотидных последовательностей, кодирующих рекомбинантный белок ПКС и голо синтазу АПБ. В другом варианте изобретения ПКС не является ПКС грибов или модульной ПКС. В другом варианте изобретения ПКС является ароматической ПКС. В другом варианте изобретения синтаза АПБ связана с синтезом жирных кислот.
В другом варианте изобретения клетка-хозяин выбирается из группы, к которой относятся клетки бактерий, дрожжей, нитчатых грибов, растений, водорослей или микроводорослей. В одном варианте настоящее изобретение представляет множество клеток-хозяев или организмов, которые могут быть модифицированы для производства продуктов, описываемых настоящим изобретением. В одном варианте клетка-хозяин или организм является Pichia pastoris.
В другом варианте изобретения клетка-хозяин или организм представлены видом Aspergillus и Aspergillus niger. Специалистам в области техники известны дополнительные виды грибов, подходящие для использования в настоящем изобретении. В одном варианте изобретения модифицированная клетка-хозяин не содержит гетерогенную систему экспрессирования голо синтазы АПБ.
6. Способы производства
В одном варианте настоящее изобретения представляет способ производства m-крезола или орсина в гетерогенном микроорганизме. В одном варианте изобретения способ содержит использование субстрата потока углерода. В другом варианте изобретения субстрат потока углерода выбирается из группы, к которой относится: очищенная или частично очищенная глюкоза или декстроза, кукурузный сахар, сахарный тростник, целлюлозные сахары, например, из дерева, бамбука, проса или ятрофы. Специалистам в области техники известны дополнительные источники углерода, подходящие для использования в настоящем изобретении. В другом варианте изобретения микроорганизм является Pichia pastoris.
В другом варианте настоящее изобретение рассматривает способы синтеза супрафизиологических уровней ароматических соединений в хозяинах. Обеспечение системы экспрессии совместимой голо синтазы АПБ либо на отдельном векторе, на одном из векторов в различных системах векторов (или на одном векторе для экспрессии ПКС), или в качестве рекомбинантного белка с ПКС или ее частью; клетки-хозяева, такие как, Е. coli, дрожжи, нитчатые грибы, водоросли и другие системы микроорганизмов могут обрабатываться для получения главным образом увеличения числа образцов релевантных генов или других средств дупликации генов в хозяине или путем положительного регулирования, например, с помощью индуцирования промоторов, усилителей, и так далее, полученной усиленной транскрипции и/или трансляции, и так далее; повышенные уровни поликетидов, крезолов, орсинов и их эфиров метилов могут быть произведены в соответствующих хозяевах, доступных для выбора и масштабов производства.
В одном варианте настоящее изобретение представляет модифицированные рекомбинантные клетки и способы получения высоких интересующих окончательных результатов, которые содержат интересующие описанные здесь промежуточные соединения. В одном варианте изобретения способ включает обеспечение модифицированной рекомбинантной клетки дрожжей, которая содержит i) первую систему экспрессии, содержащую, по меньшей мере, одну нуклеотидную последовательность, кодирующую ароматическую поликетидсинтазу (ПКС) 6-метилсалициловой кислоты (6-СМСК), которая может быть экспрессирована, и ii) вторую систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую голо синтазу ацил-переносящего белка (АПБ), причем синтаза АПБ содержит пантетеновую кислоту указанной ПКС. В другом варианте изобретения способ дополнительно содержит производство промежуточного фенольного соединения в рекомбинантной модифицированной клетке дрожжей. В одном варианте изобретения промежуточным фенольным соединением является 6-МСК.
Производство соединений из клеток-хозяев микроорганизмов с использованием ПКС, например 6-СМСК, привело к ограничению производства и ограничению эффективности преобразования глюкозы. Например, Kealey et al. сообщал о получении 1,7 г/л 6-МСК с помощью клетки-хозяина дрожжей, экспрессирующей 6-СМСК (PNAS USA, Vol.95, pp.505-509, January 1998), в то время как Xie et al. сообщал о преобразовании глюкозы на уровне 6% в клетке-хозяине дрожжей, экспрессирующей 6-CMCK (Biotechnology and Bioengineering, Vol. 93, No. 4, March 5, 2006). В предпочтительном варианте изобретения операция производства дает на выходе более, чем 3 г/л 6-МСК из клетки-хозяина, экспрессирующей ПКС (см. Пример 1). В другом варианте изобретения операция производства более, чем 3 г/л 6-МСК заключает использование 40 г/л глюкозы для роста клеток. В другом варианте изобретения описанные здесь способы представляют изолирование 6-МСК с более чем 60%-ным преобразованием глюкозы в молярное основание (см. Пример 1). В одном варианте изобретения операция производства с более чем 60% преобразованием означает использование 5 г/л глюкозы для роста клеток.
В соответствии с описанными здесь способами, реагирующие смеси для разработки путей могут работать в любом сосуде, позволяющем рост и/или размножение клеток. Например, реагирующая смесь может представлять собой биореактор, колбу или пластину с клеточной культурой, перфорированную пластину (например, перфорированные пластины микротитратора с 96, 384, 1056 отверстиями и т.д.), колбу для культивирования, ферментатор или другой сосуд для роста или размножения клеток.
Экранирование может осуществляться путем обнаружения селектируемого маркера, который в определенных генетических условиях позволяет клеткам экспрессировать маркер, чтобы выжить в то вермя как другие клетки погибнут (или наоборот). Эффективные технологии экранирования необходимы для обеспечения эффективного развития новых путей с помощью описанных здесь способов. Предпочтительно соответствующие технологии экранирования соединений, произведенных ферментными путями, обеспечивают быстрое и чувствительное экранирование интересующих свойств. Визуальные (калориметрические) исследования являются оптимальными в этой связи и являются легко применимыми для соединений с соответствующими свойствами легкого абсорбирования. К более сложным технологиям экранирования относится, например, анализ высокой производительности HPLC-MS, SPME (Микроэкстрагирование в твердой фазе) и GC-MS (Газовая хроматография-масс спектрометрия) (см. Handbook of analytical derivatization reaction, D. R. Knapp; John Wiley & Sons, 1979). В некоторых случаях экранирующие роботы присоединены к системам HPLC-MS для автоматического инжектирования и быстрого анализа образца. Эти технологии позволяют обнаружение высокой производительности и количественное определение практически любых желаемых соединений.
Интересующие биологические продукты могут быть изолированы от среды ферментации или экстракта клетки с помощью способов известных в области техники. Например, твердые тела или клеточный детрит могут быть удалены путем центрифугирования или фильтрации. Интересующие биопродукты могут быть изолированы путем дистиллирования, жидкость-жидкостного экстрагирования, испарения мембраны, адсорпции или с помощью любых способов, известных в области техники.
В некоторых вариантах изобретения определение интересующего продукта может осуществляться с помощью HPLC. Например, стандартные образцы подготавливаются в известных количествах органического вещества в среде (например, 6-МСК, ОК, m-крезол или орсин). Время удержания соединения или произведенного промежуточного соединения может затем быть сравнено с исходным стандартом. В некоторых вариантах изобретения определение интересующего продукта может осуществляться с помощью GC-MS. Разрешенные образцы затем анализируются с помощью масс-селективного детектора и сравниваются со спектром предыдущих масс и времени удержания исходных стандартов.
Применение настоящих способов предполагает традиционные технологии клеточной биологии, молекулярной биологии, трансгенной биологии, микробиологии, рекомбинантной ДНК, иммунологии, техники, роботехники, оптики, программного обеспечения и компьютерного интегрирования. Технологии и процедуры обычно осуществляются в соответствии со стандартными способами в области техники и различных общих ссылок, которые относятся к этой области техники. Такие технологии подробно объяснены в литературе. См., например, Molecular Cloning A Laboratory Manual, 2.sup.nd Ed., ed. by Sambrook, Fritsch and Maniatis (Cold Spring Harbor Laboratory Press: 1989); DNA Cloning, Volumes I and II (D.N. Glover ed., 1985); Oligonucleotide Synthesis (M. J. Gait ed., 1984); Mullis et al. патент США №4683195; Nucleic Acid Hybridization (B.D. Hames & S.J. Higgins eds. 1984); Transcription And Translation (B.D. Hames & S.J. Higgins eds. 1984); Culture Of Animal Cells (R.I. Freshney, Alan R. Liss, Inc., 1987); Immobilized Cells And Enzymes (IRL Press, 1986); B. Perbal, A Practical Guide To Molecular Cloning (1984); the treatise, Methods In Enzymology (Academic Press, Inc., N.Y.); Gene Transfer Vectors For Mammalian Cells (J.H. Miller and M.P. Calos eds., 1987, Cold Spring Harbor Laboratory); Methods In Enzymology, Vols. 154 and 155 (Wu et al. eds.), Immunochemical Methods In Cell And Molecular Biology (Mayer and Walker, eds., Academic Press, London, 1987); Handbook Of Experimental Immunology, Volumes I-IV (D.M. Weir and С.C. Blackwell, eds., 1986); Manipulating the Mouse Embryo, (Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y., 1986); Lakowicz, J.R. Principles of Fluorescence Spectroscopy, New York: Plenum Press (1983), and Lakowicz, J.R. Emerging Applications of Fluorescence Spectroscopy to Cellular Imaging: Lifetime Imaging, Metal-ligand Probes, Multi-photon Excitation and Light Quenching, Scanning Microsc. Suppl Vol. 10 (1996) pages 213-24 для знакомства с флуоресцирующими технологиями, Optics Guide 5 Melles Griot. TM. Irvine Calif, для знакомства с общими оптическими способами, Optical Waveguide Theory, Snyder & Love, опубликованную Chapman & Hall, и Fiber Optics Devices and Systems by Peter Cheo, опубликованную Prentice-Hall, для знакомства с теорией и материалами оптического волокна.
Настоящее изобретение иллюстративно описывает может также использоваться при отсутствии каких-либо элементов, ограничения или ограничений, который отдельно здесь не указаны. Таким образом, например, в каждом случае здесь любое из понятий «содержит», «главным образом состоит из» и «которая содержит» может быть заменено любым из двух других. Так, в варианте изобретения, в котором используется одно из этих понятий, это изобретение также содержит другие варианты изобретения, в которых одно из этих понятий заменено другим из списка. В каждом варианте изобретения понятия имеют свое установленное значение. Так, например, один вариант изобретения может рассматривать клетку-хозяина, «которая содержит» некое количество компонентов, другой вариант изобретения может рассматривать клетку-хозяина, «которая главным образом состоит из» одинаковых компонентов, и третий вариант изобретения может рассматривать клетку-хозяина, которая «содержит» одинаковые компоненты. Используемые здесь понятия и выражения применены здесь с целью описания, а не ограничения, и использование этих понятий и выражений не предполагает никакого исключающего значения каких-либо эквивалентов описанных свойств или их частей; в пределах области действия заявленного изобретения возможны различные модификации. Так, следует понимать, что, несмотря на то, что в настоящем изобретении приводится описание предпочтительных вариантов изобретения и других свойств, модификации и изменения описанных здесь понятий могут быть пересортированы специалистами в области техники; а также, что такие модификации и изменения считаются в области действия настоящего изобретения в соответствии с прилагаемой формулой изобретения.
Предыдущее письменное описание считается достаточным, чтобы специалист в области техники мог использовть изобретение. Следующие Примеры приведены только с целью иллюстрирования, и не предназначены для ограничения области действия настоящего изобретения каким-либо образом. В действительности, различные модификации настоящего изобретения кроме описанных и показанных модификаций будут понятны специалисту в области техники из вышеследующего описания и находятся в пределах области распространения приложенной формулы изобретения.
ПРИМЕРЫ
ПРИМЕР 1 - Экспрессирование 6-СМСК и СОК в Saccharomvces cerevisiae
Преобразование продуктов поликетидов в m-крезол и орсин. Промотор ADH2 S. cerevisiae является химически синтезированным и рекомбинированным в синтетических генов гена ChlB Streptomyces antibioticus или СОК, AviM Streptomyces viridochromogenes 6-СМСК. Терминирующая последовательность 5. cerevisiae также встраивается в последовательность гена непосредственно после остановки триплета(ов) каждого соответствующего гена ПКС. Кассета экспрессии была клонирована в вектор экспрессии дрожжей, который содержит селиктируемый маркер URA3. Аналогично, белок A. nidulans npgA, который кодирует ген, клонирован в вектор экспрессии дрожжей, содержащий селектируемый маркер для роста в среде с недостатком триптофана.
Соответствующий Saccharomyces cerevisiae InvScl (МАТа his3D1 leu2 trp1-289 ura3-52) (Инвитроген) последовательно трансформируется с векторами экспрессии и затем размещается на небольших пластинах агара (1,7 г/л азотного основания дрожжей без аминокислот или сульфата аммония (DIFCO), 5 г/л (NH4)2SO4, 20 г/л глюкозы, 20 г/л агар-содержащих аминокислот для выбора на основе прототрофии траптофана или урацила. Трансформируемые вещества подхватываются и выращиваются в течение 24 часов в среде с недостатком урацила и триптофана. Плазмида ДНК изолирована от других трансформируемых веществ и анализируется путем ограничения анализа ферментации для подтверждения идентичности.
Успешно трансформированное вещество используется для введения 2 мл среды с недостатком урацила и выращивается в течение ночи при 30°C в круговой качалке. 500 мкл аликвоты этой культуры используется для введения 50 мл среды YEPD (Wobbe in Current Protocols in Molecular Biology, Supplement 34:13.0.1-13.13.9 (Wiley, 1996)) (10 г/л экстракта дрожжей, 20 г/л пептона, 20 г/л глюкозы glucose), и культура выращивается при 30°C в качалке. В раздельном эксперименте, идентичном вышеуказанному, кроме использования 40 г/л глюкозы 6-МСК была изолирована на уровне >3 граммов/литр. В другом раздельном эксперименте, идентичном вышеуказанному, кроме использования 5 г/л глюкозы 6-MSA была изолирована с >60% преобразованием глюкозы в молярное основание.
Клетки собираются путем центрифугирования аликвоты 500 мкл культуры, взятой через 24, 48 и 72 часа после начала роста и растворяются с кипячением 50 мкл гелевый заполняющий буферный раствор 2×SDS в течение около 2 минут. Растворы клеток анализируются путем нагрузки 12% SDS-PAGE гелей. Ленты, соответствующие ожидаемому размеру 6-СМСК, можно наблюдать при ca. 190 кД и белка AviM СОК при са. 145 кД.
6-МСК и СОК изолируются из супернатантов дрожжей, как это было ранее описано (Kealey et al., Proc Natl Acad Sci USA 95:505-9, 1998), и определяются сравнением с известными стандартами пластин тонкопленочной хроматографии (TLC) и HPLC.
Очищенная 6-МСК и СОК затем декарбоксилируются с помощью известных химических способов для получения m-крезола или орсина, или, в некоторых вариантах, декарбоксилируется с помощью рекомбинантной или естественной декарбоксилазы 6-МСК, такой как фермент, полученный из P. patulum, декарбоксилаза PatG 6-МСК из A. clavatus, декарбоксилаза ОК, например, образованная из Gliocladium roseum, или декарбоксилаза 2,3-дигидроксибензойной кислоты, например, из A. niger, или декарбоксилаза 5-карбоксиванильной кислоты из Sphingomonas paucimobilis SYK-6. Продукты m-крезола и орсина идентифицируются с помощью методов TLC и HPLC по известным стандартам.
Затем гидроксильная группы m-крезола удаляется путем химического восстановления с использованием известных способов получения толуола, например, нагрев с последующим дистиллированием цинковой пылью. Толуол дополнительно восстанавливается для насыщения ароматического кольца с целью получения метилциклогексана, затем насыщается соответствующий источник энергии, кроме того, он является необходимым для использования в реактивном топливе. В некоторых вариантах m-крезол восстанавливается и отделяет свободный кислород для преобразования в метилциклогексан в соответствии со способами, описанными в патентной заявке WO /2006/086457 с помощью металлических катализаторов для управления гидрированием и отделением свободного кислорода, m-крезол также восстанавливается стандартными способами в метилциклогексанол, который может использоваться в реактивном топливе и может также присутствовать в бензине.
ПРИМЕР 2 - Производство m-крезола прямо в S. cerevisiae
Штамм дрожжей, в котором ген npgA A. nidulans встроен в геном штамма дрожжей BJ 2168 (полученный из АТСС) стандартными способами для получения штамма Rho 100-npgA. Плазмиды, содержащие системы экспрессии гена ChBl, зависят от выбора Ura3, экспрессия декарбоксилазы 6-МСК P. patulum или декарбоксилазы 6-МСК PatG из A. clavatus зависит от выбора Trpl которые последовательно преобразуются с Rho100-npgA.
Трансформированные клетки дрожжей выращены в качалках, содержащих среду YEPD с 2% глюкозы в течение 48 и 72 часов, и проанализированные супернатанты для производства m-крезола. Клетки удаляются центрифугированием, m-крезол экстрагируется из среды с помощью этилацетата для дополнительного анализа, определения количества и дистиллирования для получения высокой чистоты.
В дальнейшей серии экспериментов два гена, экспрессированных на одном векторе с помощью последовательностей УВПР S. Cerevisiae, разделяющих два гена, экспрессированных из одного промотора. Последовательности УВПР S. cerevisiae были сравнены по их способности производить m-крезол из соответственных системам экспрессии.
ПРИМЕР 3 - Производство орсина прямо в S. cerevisiae
Плазмиды, содержащие системы экспрессии гена СОК AviM из Streptomyces viridochromogenes при выборе Ura3, и экспрессия декарбоксилазы PatG из Aspergillus clavatus при селективном управлении Trp1 последовательно трансформируются в Rho100-npgA.
Трансформированные клетки дрожжей выращиваются в качалках, содержащих среду YEPD с 2% глюкозы в течение 48 и 72 часов, и супернатанты анализируются для производства орсина. Клетки удаляются с помощью центрифугирования, орсин экстрагируется из среды для дальнейшего анализа, определения количества и дистиллирования для получения высокой чистоты с помощью этилацетата.
В дополнительной серии экспериментов два гена экспрессируются на один вектор с помощью последовательностей УВПР, разделяющих два гена, экспрессированных из одного промотора. Последовательности УВПР сравниваются по их способности производить орсин из соответствующих систем экспрессии.
ПРИМЕР 4 - Преобразование 6-МСК и ОК в m-крезол и орсин соответственно в ферментационные супернатанты S. cerevisiae
Клетки дрожжей из ПРИМЕРОВ 2 и 3 выращиваются в подпитываемой среде с ферментаторе объемом 1 л (New Brunswick) с использованием различного исходного сырья, такого как кукурузный сахар, целлюлозные сахара и сахарный тростник. Среда подпитывается и удаляется с постоянной скоростью в непрерывном режиме потока, и среда подпитывается в растворах, содержащих рекомбинантные белки декарбоксилазы. Окончательные продукты m-крезола и орсина экстрагируются с помощью этилацетата для вышеуказанного анализа.
В дополнительной серии экспериментов супернатанты, содержащие m-крезол и орсин подпитываются прямо в колоннах, содержащих соответствующие неподвижные ферменты декарбоксилазы на соответствующих матрицах. Аналогично, m-крезол и орсин, произведенные соответственно из элюатов, экстрагируются с помощью атилацетата для анализа уровней производства, как было описано выше.
ПРИМЕР 5 - Производство 3-метиланизола и 3.5-диметокситолуола в S. cerevisiae
Третья система экспрессии включена в штаммы экспрессии из ПРИМЕРОВ 2,3 и 4. Синтетические гены О-метилтрансфераз лепестков роз (Scalliet et al., FEBS Letters 523:113-118 (2002) Rosa chinensis (сорта Lady Hillingdon и Old Blush) создаются и находятся под контролем промоторов генов гликолитических ферментов ADH-2 S. cerevisiae ADH-2 или S. cerevisiae.
Штаммы с полными системами экспрессии выращиваются и собираются в соответствии с тем, что описано здесь, супернатанты клетки анализируются для производства 3-метиланизола (1-метокси-3-метилбензена) и 3,5-диметокситолуола (1,3-диметокси-5-метилбензена) с дальнейшим экстрагированием с помощью этилацетата или диэтирэфира.
ПРИМЕР 6 - Совместное культивирование клеток дрожжей, производящих 6-МСК и клеток, производящих фермент декарбоксилазы
Клетки 5. cerevisiae, экспрессирующие ген ChlB1 Streptomyces antibioticus 6-СМСК, как это указано выше, и белок npgA A. nidulans выращиваются, как указано выше, в течение 48 часов. Равный объем среды, содержащей клетки, экспрессирующие декарбоксилазу PatG из A. clavatus, также выращивается в течение 48 часов и добавляется к культуре; совместная культура выращивается в течение 24 часов при 30°C. Клетки удаляются центрифугированием, m-крезол экстрагируется из среды с помощью этил ацетата для дополнительного анализа, определения количества и дистиллирования для получения высокой чистоты.
ПРИМЕР 7 - Декарбоксилирование 6-МСК с помощью нагрева с порошковыми металлическими катализаторами
Очищенная 6-MSA смешивается с различными порошковыми металлическими каталитическими веществами, и нагревается под давлением окружающей среды. m-крезол может испаряться и конденсироваться в сборочном сосуде. Анализ окончательного продукта показал процент чистоты >99%.
В особом примере порошковая 6-МСК (20 граммов) была смешана с цинковой пылью (2,5 грамма) и нагрета в реторте до превращения всех твердых веществ в жидкость. Нагрев был продолжен, и m-крезол мог испаряться и конденсироваться в емкости, охлажденной льдом, что в результате дало 11,35 граммов >99,9% чистого бесцветного m-крезола.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПОЛУЧЕНИЕ ДГК И ДРУГИХ ДЦ-ПНЖК В РАСТЕНИЯХ | 2012 |
|
RU2644241C2 |
| БИОЛОГИЧЕСКИЙ СИНТЕЗ ДИФУНКЦИОНАЛЬНЫХ АЛКАНОВ ИЗ АЛЬФА-КЕТОКИСЛОТ | 2009 |
|
RU2496880C2 |
| СПОСОБ ПРОИЗВОДСТВА L-АМИНОКИСЛОТ | 2007 |
|
RU2422530C2 |
| КОНСТРУКЦИИ НУКЛЕИНОВОЙ КИСЛОТЫ, СОДЕРЖАЩИЕ КЛАСТЕР ГЕНОВ БИОСИНТЕЗА ПИРИПИРОПЕНА И МАРКЕРНЫЙ ГЕН | 2011 |
|
RU2576001C2 |
| СПОСОБЫ И ВЕЩЕСТВА ДЛЯ ОСНОВАННОГО НА РЕКОМБИНАЦИИ ПОЛУЧЕНИЯ СОЕДИНЕНИЙ ШАФРАНА | 2012 |
|
RU2676730C2 |
| РЕКОМБИНАНТНЫЙ МИКРООРГАНИЗМ, ОБЛАДАЮЩИЙ ПОВЫШЕННОЙ СПОСОБНОСТЬЮ ПРОДУЦИРОВАТЬ ПУТРЕСЦИН, И СПОСОБ ПОЛУЧЕНИЯ ПУТРЕСЦИНА С ИСПОЛЬЗОВАНИЕМ ЭТОГО МИКРООРГАНИЗМА | 2013 |
|
RU2603089C2 |
| ВЫДЕЛЕННЫЙ ПОЛИНУКЛЕОТИД, КОДИРУЮЩИЙ ПОЛИПЕПТИД, ВОВЛЕЧЕННЫЙ В БИОСИНТЕЗ ПИРИПИРОПЕНА А, ВЕКТОР И КЛЕТКА-ХОЗЯИН СОДЕРЖАЩИЕ ТАКОЙ ПОЛИНУКЛЕОТИД И СПОСОБ ПОЛУЧЕНИЯ ПРЕДШЕСТВЕННИКА ПИРИПИРОПЕНА А (ВАРИАНТЫ) | 2009 |
|
RU2540017C2 |
| ВЕКТОРЫ ДЛЯ ПРОИЗВОДСТВА БЕЛКОВ | 2019 |
|
RU2820218C2 |
| ПОЛИНУКЛЕОТИД НА ОСНОВЕ ГЕНА MDH, ОБЛАДАЮЩИЙ ПРОМОТОРНОЙ АКТИВНОСТЬЮ, И ЕГО ПРИМЕНЕНИЕ | 2022 |
|
RU2825450C2 |
| СИНТАЗА КАННАБИХРОМЕНОВОЙ КИСЛОТЫ ИЗ КОНОПЛИ ПОСЕВНОЙ | 2015 |
|
RU2708144C2 |
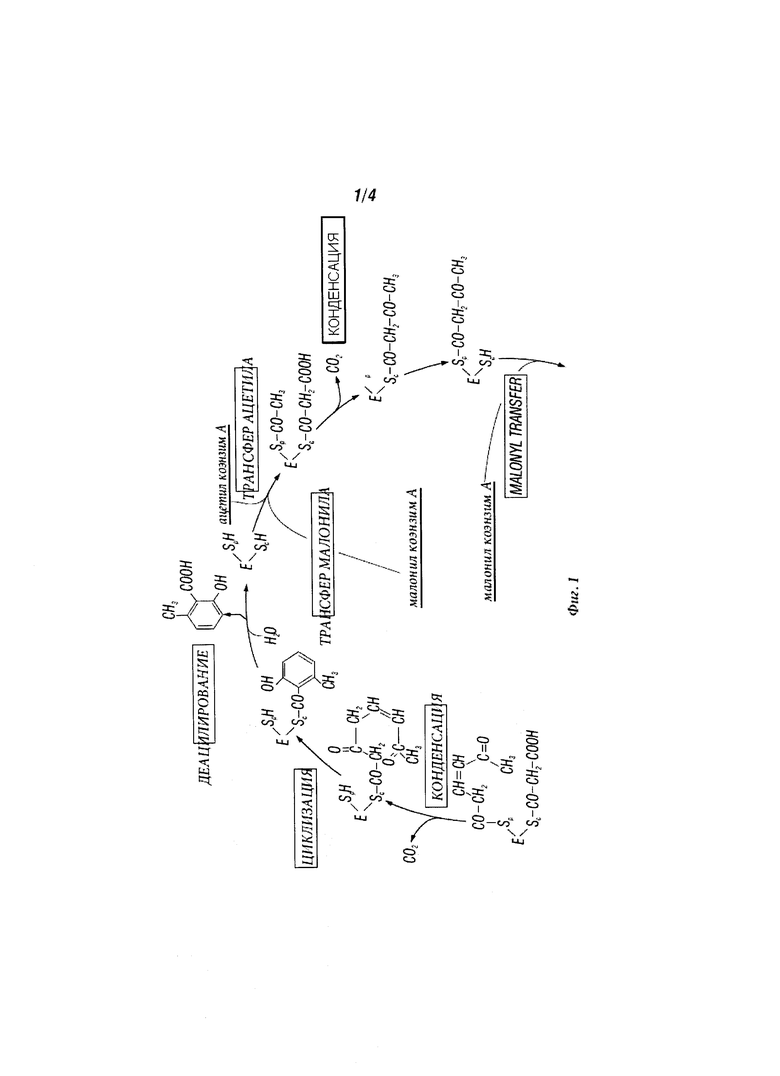
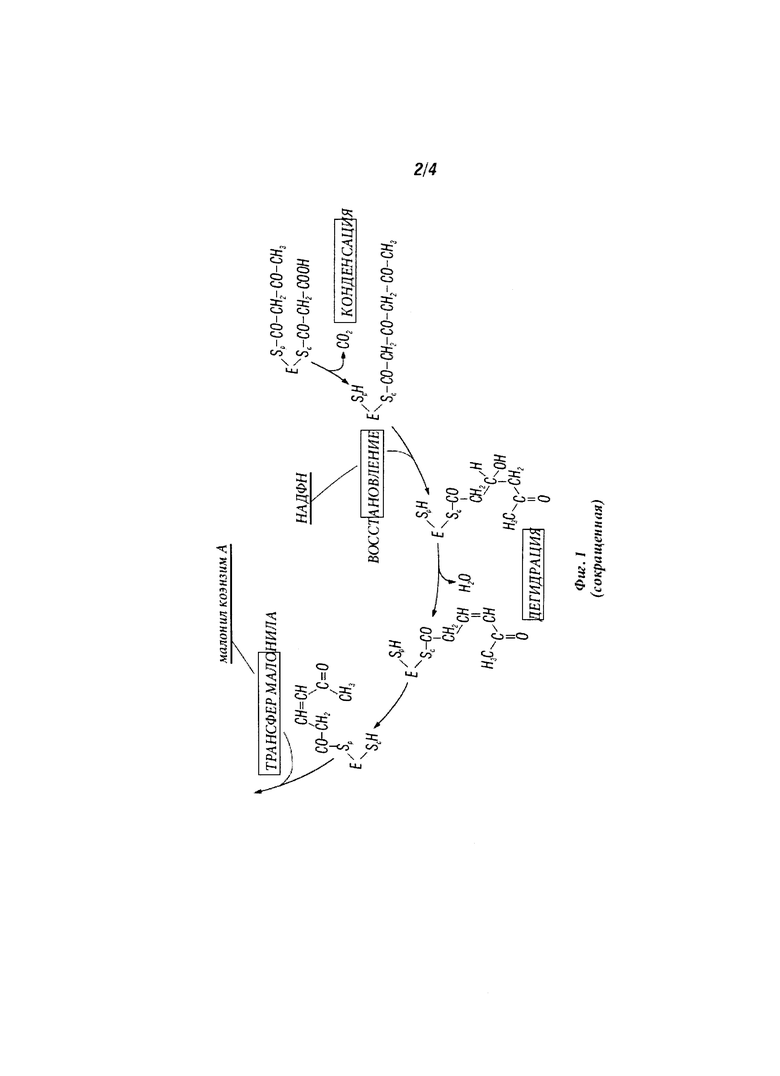
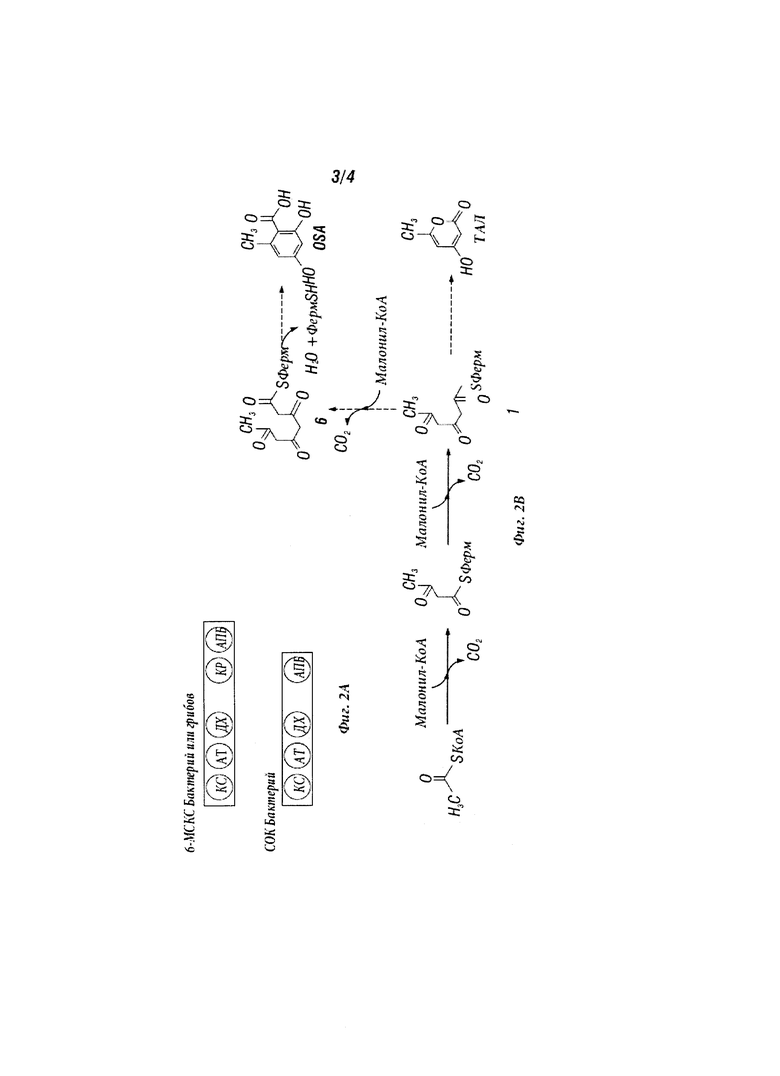
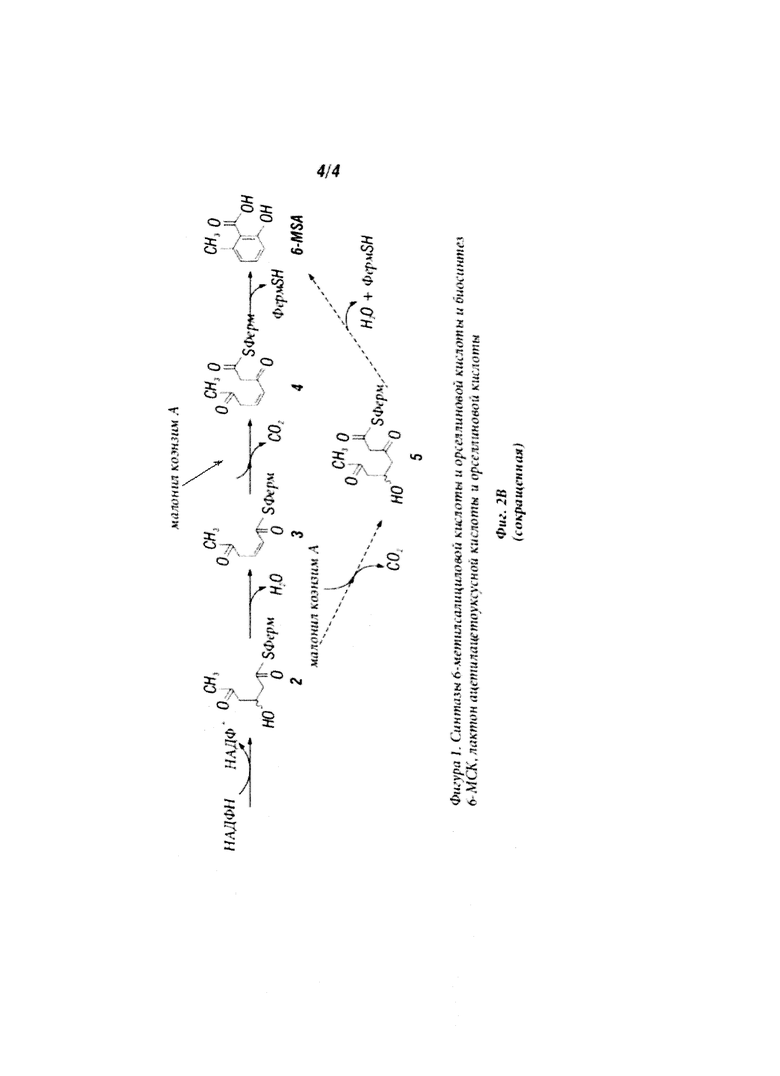
Предложены модифицированная рекомбинантная клетка-хозяин для производства фенольного соединения и способ производства фенольного соединения (варианты). Клетка-хозяин содержит три системы экспрессии. Первая система экспрессии содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую ароматическую поликетидсинтазу (ПКС), содержащую синтазу 6-метилсалициловой кислоты (6-СМСК) или синтазу орселлиновой кислоты (СОК), которая может быть экспрессирована. Вторая система экспрессии содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую голо синтазу ацил-переносящего белка (АПБ), причем синтаза АПБ содержит пантотеновую кислоту указанной ПКС. Третья система экспрессии содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую функциональную декарбоксилазу, которая катализирует декарбоксилирование для указанного получения фенольного соединения таким образом, что продукт, изолированный из указанной клетки, является фенольным соединением. При этом либо первая система экспрессии ПКС и вторая система экспрессии АПБ присутствуют на одном векторе или на раздельных векторах и третья система экспрессии функциональной декарбоксилазы либо присутствует на том же векторе, что и первая система экспрессии ПКС и/или вторая система экспрессии АПБ, либо присутствует на отдельном векторе, либо первая, вторая или третья система экспрессии интегрирована в хромосому клетки хозяина или экспрессируется из искусственных хромосом дрожжей (ИХД). Способ производства фенольного соединения предусматривает обеспечение рекомбинантной клетки-хозяина, содержащей три системы экспрессии, получение промежуточного фенольного соединения в рекомбинантной клетке-хозяине и синтезирование фенольного соединения из промежуточного фенольного соединения. Вариант способа производства фенольного соединения предусматривает обеспечение рекомбинантной клетки-хозяина, содержащей первую и вторую системы экспрессии, изолирование промежуточного фенольного соединения, произведенного в рекомбинантной клетке-хозяине, и декарбоксилирование промежуточного фенольного соединения для образования фенольного соединения путем нагрева с металлическим катализатором с последующим дистиллированием. Группа изобретений обеспечивает получение фенольного соединения с высокими чистотой и выходом. 3 н. и 14 з.п. ф-лы, 5 ил., 1 табл. 7 пр.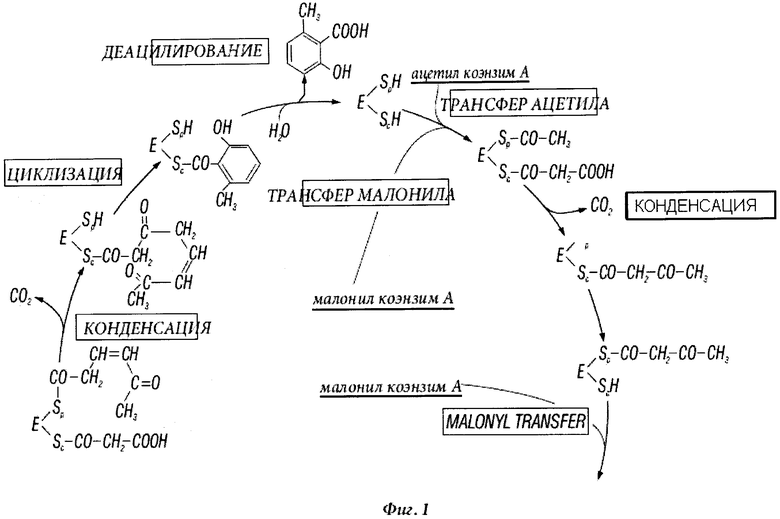
1. Модифицированная рекомбинантная клетка-хозяин для производства фенольного соединения, содержащая:
i) первую систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую ароматическую поликетидсинтазу (ПКС), содержащую синтазу 6-метилсалициловой кислоты (6-СМСК) или синтазу орселлиновой кислоты (СОК), которая может быть экспрессирована,
ii) вторую систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую голо синтазу ацил-переносящего белка (АПБ), причем синтаза АПБ содержит пантотеновую кислоту указанной ПКС, и
iii) третью систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую функциональную декарбоксилазу, которая катализирует декарбоксилирование для указанного получения фенольного соединения таким образом, что продукт, изолированный из указанной клетки, является фенольным соединением, где либо
первая система экспрессии ПКС и вторая система экспрессии АПБ присутствуют на одном векторе или на раздельных векторах и третья система экспрессии функциональной декарбоксилазы либо присутствует на том же векторе, что и первая система экспрессии ПКС и/или вторая система экспрессии АПБ, либо присутствует на отдельном векторе, либо
первая, вторая или третья система экспрессии интегрирована в хромосому клетки хозяина или экспрессируется из искусственных хромосом дрожжей (ИХД).
2. Клетка-хозяин по п. 1, отличающаяся тем, что фенольное соединение является мета-крезолом или орсином.
3. Модифицированная клетка по п. 1, отличающаяся тем, что ароматическая ПКС является синтазой 6-метилсалициловой кислоты гриба или прокариота.
4. Модифицированная клетка по пп. 1-3, отличающаяся тем, что нуклеотидная последовательность, кодирующая декарбоксилазу, выбирается из группы, состоящей
из гена декарбоксилазы P. patulum 6-МСК, гена PatG Aspergillus clavatus, гена декарбоксилазы СОК Gliocladium roseum, генов декарбоксилазы 2,3-дигидроксибензойной кислоты из видов аспергилл и гена декарбоксилазы 5-карбоксиванильной кислоты Sphingomonas paucimobilis SYK-6.
5. Модифицированная клетка по п. 1, отличающаяся тем, что указанная ПКС и голо синтаза АПБ экспрессируются из дицистронной части РНК.
6. Модифицированная клетка по п. 1, отличающаяся тем, что организм хозяина выбирается из группы, состоящей из Saccharomyces cerevisiae, Pichia pastoris и Aspergillus species.
7. Способ производств фенольного соединения, который включает:
a) обеспечение модифицированной рекомбинантной клетки-хозяина, которая содержит:
i) первую систему экспрессии, по меньшей мере, с одной нуклеотидной последовательностью, кодирующей ароматическую поликетидсинтазу (ПКС), содержащую синтазу 6-метилсалициловой кислоты (6-СМСК) или синтазу орселлиновой кислоты (СОК), которая может быть экспрессирована;
ii) вторую систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую голо синтазу ацил-переносящего белка (АПБ), причем синтаза АПБ содержит пантотеновую кислоту указанной ПКС; и
iii) третью систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую функциональную декарбоксилазу;
b) производство промежуточного фенольного соединения в рекомбинантной клетке-хозяине; и
c) синтезирование фенольного соединения из промежуточного фенольного соединения, в котором рекомбинантная декарбоксилаза является катализатором декарбоксилирования промежуточного фенольного соединения для образования фенольного соединения,
где либо
первая система экспрессии ПКС и вторая система экспрессии АПБ присутствуют на одном векторе или на раздельных векторах и третья система экспрессии функциональной декарбоксилазы либо присутствует на том же векторе, что и первая система экспрессии ПКС и/или вторая система экспрессии АПБ, либо присутствует на отдельном векторе, либо
первая, вторая или третья система экспрессии интегрирована в хромосому клетки хозяина или экспрессируется из искусственных хромосом дрожжей (ИХД).
8. Способ по п. 7, отличающийся тем, что промежуточным фенольным соединением является 6-МСК или орселлиновая кислота (ОК), где фенольным соединением является мета-крезол или орсин.
9. Способ производства фенольного соединения, который включает:
a) обеспечение модифицированной рекомбинантной клетки-хозяина, которая содержит:
i) первую систему экспрессии, которая содержит по меньшей мере одну нуклеотидную последовательность, кодирующую ароматическую поликетидсинтазу (ПКС), содержащую синтазу 6-метилсалициловой кислоты (6-СМСК) или синтазу орселлиновой кислоты (СОК), которая может быть экспрессирована; и
ii) вторую систему экспрессии, по меньшей мере, с одной нуклеотидной последовательностью, кодирующей голо синтазу ацил-переносящего белка (АПБ), причем синтаза АПБ содержит пантотеновую кислоту указанной ПКС;
b) изолирование промежуточного фенольного соединения, произведенного в рекомбинантной клетке-хозяине; и
c) декарбоксилирование промежуточного фенольного соединения согласно стадии b) для образования фенольного соединения путем нагрева с металлическим катализатором с последующим дистиллированием.
10. Способ по п. 9, отличающийся тем, что промежуточным фенольным соединением является 6-МСК, где фенольным соединением является мета-крезол.
11. Способ по п. 9 или 10, отличающийся тем, что металлический катализатор является цинковым катализатором.
12. Модифицированная клетка по п. 1, где фенольным соединением является алкилированное фенольное соединение, где модифицированная клетка дополнительно содержит:
(iv) четвертую систему экспрессии, которая содержит, по меньшей мере, одну нуклеотидную последовательность, кодирующую О-метилтрансферазу (ООМТ), так что продукт, изолированный из клетки, является алкилированным фенольным соединением.
13. Модифицированная клетка по п. 12, отличающаяся тем, что алкилированное фенольное соединение является 3-метиланизолом или 3,5-диметокситолуолом.
14. Модифицированная клетка по п. 12, отличающаяся тем, что ООМТ кодирована геном R. Chinensis, выбираемым из группы, состоящей из ООМТ1, ООМТ2, ООМТ3, ООМТ4, СОМТ1.
15. Способ по п. 7 для производства алкилированного фенольного соединения, который дополнительно включает:
d) изолирование промежуточного фенольного соединения, произведенного в рекомбинантной клетке-хозяине; и
e) алкилирование промежуточного фенольного соединения согласно стадии d) для образования алкилированного фенольного соединения путем обработки алкилирующим агентом.
16. Способ по п. 15, отличающийся тем, что промежуточным фенольным соединением является мета-крезол или орсин.
17. Способ по пп. 7, 8, 15 или 16, отличающийся тем, что нуклеотидная последовательность, кодирующая декарбоксилазу, выбирается из группы, состоящей из гена декарбоксилазы P. patulum 6-МСК, гена PatG Aspergillus clavatus, гена декарбоксилазы СОК Gliocladium roseum, генов декарбоксилазы 2,3-дигидроксибензойной кислоты из видов аспергилл и гена декарбоксилазы 5-карбоксиванильной кислоты Sphingomonas paucimobilis SYK-6.
Авторы
Даты
2017-08-14—Публикация
2012-06-22—Подача