Область изобретения
В настоящем изобретении раскрываются некоторые новые твердые формы (S)-4-амино-N-(1-(4-хлорфенил)-3-гидроксипропил)-1-(7H-пирроло[2,3-d]пиримидин-4-ил)пиперидин-4-карбоксамида, способы получения таких форм, фармацевтические композиции, содержащие их, и применение таких форм в лечении.
Предшествующий уровень техники
Для лекарственного вещества в составе композиций лекарственного средства важно находиться в форме, в которой с ним можно легко обращаться и обрабатывать его. Это является важным не только с точки зрения получения коммерчески жизнеспособного способа производства, но также с точки зрения последующего изготовления фармацевтических композиций (например, пероральных лекарственных форм, таких как таблетки), содержащих активное соединение.
Различные физические свойства кристаллических форм по отношению друг к другу и к некристаллическому состоянию могут заметно влиять на химическую и фармацевтическую обработку соединения, особенно, когда соединение получают или используют в промышленном масштабе.
Кроме того, в изготовлении пероральных композиций лекарственных средств важно обеспечивать достоверный и воспроизводимый профиль концентрации лекарственного средства в плазме крови после введения пациенту. Вариабельность в профилях абсорбции лекарственного средства в желудке, кишечнике или кровотоке у разных пациентов может влиять на безопасность и эффективность лекарственного средства.
Химическая стабильность, стабильность в твердом состоянии и «срок годности» активных ингредиентов также являются очень важными факторами. Лекарственное вещество и композиции, содержащие его, должны быть способны эффективно храниться в течение длительных периодов времени без проявления значимых изменений физико-химических свойств активного компонента (например, его химического состава, плотности, гигроскопичности и растворимости).
Кроме того, также является важной возможность обеспечить лекарственное средство в форме, которая является химически чистой настолько, насколько это возможно.
Аморфные вещества могут представлять собой проблемы в этом отношении. Например, с такими веществами обычно трудно обращаться и изготавливать их в виде фармацевтического средства, подразумевая их ненадежную растворимость, и часто обнаруживается их нестабильность и наличие химических примесей.
Специалисту будет очевидно, что, если лекарственное средство можно легко получать в кристаллической форме, которая также является стабильной, может быть решена одна из многих указанных выше проблем.
Таким образом, в изготовлении коммерчески жизнеспособных и фармацевтически приемлемых лекарственных композиций, важно, когда это возможно, получать лекарственное средство в кристаллической и стабильной форме.
Однако следует заметить, что эта цель не всегда достижима. В действительности, обычно невозможно прогнозировать только по молекулярной структуре, каким будет характер кристаллизации соединения (либо в чистом виде, либо в форме соли). Это можно определить только эмпирически.
В WO 2009/047563 раскрыта новая группа бициклических гетероциклов, которые могут быть полезными в лечении или предотвращении заболевания или медицинского состояния, опосредованного протеинкиназой В (РКВ, известной также как АКТ).
В WO 2009/047563 также раскрыт конкретный бициклический гетероцикл, идентифицированный в ней как (S)-4-амино-N-(1-(4-хлорфенил)-3-гидроксипропил)-1-(7Н-пирроло[2,3-d]пиримидин-4-ил)пиперидин-4-карбоксамид (пример 9). Это соединение обозначается в данном описании изобретения как «соединение (I)» и альтернативно известно как «AZD5363».
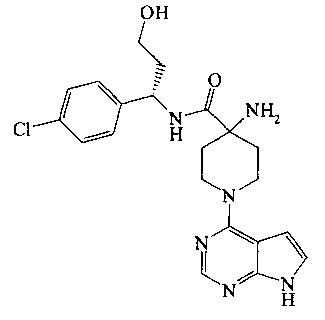
Соединение (I)
Было показано, что соединение (I) проявляет сильную активность против всех 3 изоморф фермента АКТ млекопитающих - с IC50 (концентрация полумаксимального ингибирования) 3 нМ против АКТ1, IC50 7 нМ против АКТ2 и IC50 7 нМ против АКТ3. В настоящее время соединение (I) разрабатывается в качестве потенциального нового лекарственного средства для лечения нескольких различных форм рака, либо в качестве монотерапии, либо в качестве части комбинированной терапии.
В WO 2009/047563 также раскрыты три способа получения соединения (I) - сам пример 9 и альтернативные способы синтеза 1 и 2 для примера 9. «Пример 9, альтернативный способ синтеза 1» включает получение суспензии соединения (I) в этилацетате, а согласно двум другим способам соединение (I) выделяют в виде твердого вещества путем упаривания фракций, элюированных из колонки. Авторы настоящего изобретения анализировали (посредством XRD (диффракции рентгеновских лучей)) три архивных образца соединения (I) из коллекции соединений авторов изобретения, которые синтезировали, используя способ, идентичный, или по существу подобный, одному из этих трех способов, и идентифицировали все три как находящиеся в полукристаллической форме, обозначенной как «форма А».
Раскрытие изобретения
В настоящее время авторы изобретения обнаружили, что соединение (I) можно получать в нескольких твердых формах. Две из этих новых твердых форм называют далее «формой В» и «формой С». Форма В является кристаллической, а форма С является полукристаллической по природе. Анализом посредством XRD (дифракция рентгеновских лучей на порошке) определили, что эти формы представляют собой новые формы, и что форма А вообще не содержит вещество в форме В или С.
Таким образом, в первом аспекте изобретения предложено соединение (I) в кристаллической форме.
В альтернативном аспекте изобретения соединение (I) в кристаллической форме находится в виде формы В.
Под «кристаллическим» авторы изобретения понимают кристаллический более чем на 80%, предпочтительно более чем на 90%, и более предпочтительно более чем на 95%. Наиболее предпочтительно «кристаллический» более чем на 98%. В «полукристаллический» авторы изобретения включают кристаллический более чем на 5%, но менее чем на 80%. Степень кристалличности (%) может быть определена специалистом при использовании дифракции рентгеновских лучей на порошке (XRPD). Можно также использовать другие методы, такие как ЯМР твердого тела, преобразование Фурье - инфракрасная спектроскопия (FT-IR), рамановская спектроскопия, дифференциальная сканирующая калориметрия (ДСК) и микрокалориметрия.
Кристаллическая форма по изобретению может иметь улучшенные свойства, например, стабильность, например по сравнению с соединением (I), полученным как описано в WO 2009/047563.
Таким образом, согласно еще одному аспекту изобретения предлагается стабильная кристаллическая форма соединения (I). В частности, эта стабильная кристаллическая форма соединения (I) представляет собой форму В. Авторы настоящего изобретения обнаружили, что суспендирование формы А в подходящем органическом растворителе, например ацетонитриле, при перемешивании в течение периода времени соответствующей продолжительности, например в течение 3 суток, приводит к получению формы В. Форму В можно также получать посредством перемешивания суспензии формы С в подходящем органическом растворителе, таком как ацетон или изопропиловый спирт (IPA) в течение соответствующего периода времени. В свете этих превращений с течением времени других форм в форму В, авторы настоящего изобретения пришли к выводу, что форма В наиболее вероятно является наиболее термодинамически стабильной формой. По этой причине прогнозировали, что форма В имеет выгодные свойства в сравнении с другими формами соединения (I), например, с точки зрения стабильности и предрасположенности превращаться или частично превращаться в другие менее желательные твердые формы. Все это делает форму В потенциально предпочтительной для обеспечения более продолжительного срока годности продукта и минимизации любой вариабельности в абсорбции между разными пациента и индивидуальной вариабельности в абсорбции соединения (I).
Термин «стабильность», при определении в данном описании изобретения, включает химическую стабильность и/или стабильность твердого состояния.
Под «химической стабильностью» авторы изобретения понимают, что соответствующие соединения могут храниться в выделенной форме, или в форме композиции, в которой предлагается смешивать его с фармацевтически приемлемыми носителями, разбавителями или вспомогательными веществами (например, в пероральной лекарственной форме, такой как таблетка, капсула и так далее), при нормальных условиях хранения с ограниченной степенью химической деградации или разложения.
Под «стабильностью твердого состояния» авторы изобретения понимают, что соответствующие соединения могут храниться в выделенной твердой форме или в форме твердой композиции, в которой его предлагается смешивать с фармацевтически приемлемыми носителями, разбавителями или вспомогательными веществами (например, в пероральной лекарственной форме, такой как таблетка, капсула и так далее), при нормальных условиях хранения, с незначительной степенью трансформации твердого состояния (например кристаллизации, рекристаллизации, фазового перехода в твердых телах, гидратации, дегидратации, сольватации или десольватации).
Примеры «нормальных хранения условий» включают температуры от минус 80°С до плюс 50°С (предпочтительно от 0°С до 40°С и более предпочтительно комнатные температуры, такие как от 15°С до 30°С), давление от 0,1 до 2 бар (от 1×104 Па до 2×105 Па) (предпочтительно при атмосферном давлении), относительную влажность от 5 до 95% (предпочтительно от 10 до 75%) и/или подвергание воздействию 460 люкс УФ (ультрафиолетового)/видимого света, в течение продолжительных периодов (то есть больше или равных шести месяцам). В таких условиях кристаллические формы по изобретению могут быть обнаружены менее чем на 15%, предпочтительно менее чем на 10%, и более предпочтительно менее чем на 5% химически деградированными/разложившимися, или с трансформированным твердым состоянием, в зависимости от обстоятельств. Специалисту будет очевидно, что вышеупомянутые верхние и нижние пределы для температуры, давления и относительной влажности представляют собой экстремумы нормальных условий хранения, и что некоторые комбинации этих экстремумов не будут испытываться во время нормального хранения (например температура 50°С и давление 0,1 бар (1×104 Па)).
Согласно еще одному аспекту изобретения предлагается процесс получения соединения (I) в кристаллической форме в виде формы В, включающий перемешивание суспензии соединения (I), предпочтительно соединения (I) в виде формы А или формы С, более предпочтительно формы А, в подходящем растворителе, таком как ацетон или ацетонитрил, предпочтительно в ацетонитриле, с последующей фильтрацией и сушкой. В таком способе важно оставлять суспензию перемешиваться в течение достаточного периода времени с целью достижения оптимального превращения в форму В. Продолжительность периода времени может также зависеть от температуры суспензии. Если суспензия находится при 50°С, то приемлемых выходов превращения можно добиться, если реакционную смесь перемешивать по меньшей мере в течение 3 суток.
Согласно еще одному аспекту предлагается способ получения соединения (I) в виде формы С, включающий перемешивание суспензии соединения (I), предпочтительно соединения (I) в виде формы А, в метаноле с последующей фильтрацией и сушкой. В таком способе важно оставлять суспензию перемешиваться в течение достаточного периода времени с целью достижения полного превращения в форму С. Продолжительность периода времени может зависеть от температуры суспензии. Если суспензия находится при комнатной температуре, то приемлемых выходов превращения можно добиться, если реакционную смесь перемешивать по меньшей мере в течение 3 суток.
В альтернативном аспекте изобретения Соединение (I) в кристаллической форме находится в виде формы В и по существу не содержит других форм.
В альтернативном аспекте изобретения соединение (I) в кристаллической форме находится в виде формы В и по существу не содержит формы А.
В альтернативном аспекте изобретения соединение (I) в кристаллической форме находится в виде формы В и по существу не содержит формы С.
В альтернативном аспекте изобретения соединение (I) в кристаллической форме находится в виде формы В и по существу не содержит формы А и формы С.
В альтернативном аспекте соединение (I) находится в виде формы С и по существу не содержит других форм.
В альтернативном аспекте соединение (I) находится в виде формы С и по существу не содержит формы А.
В альтернативном аспекте соединение (I) находится в виде формы С и по существу не содержит формы В.
В альтернативном аспекте Соединение (I) находится в виде формы С и по существу не содержит формы А и формы В.
Термин «по существу не содержит» относится к содержанию другой формы или форм менее 10%, предпочтительно менее 5%.
Дополнительная информация о способах по изобретению и продуктах, получаемых в них, описана в примерах в данном описании изобретения.
Кристаллические формы по изобретению можно выделять, используя методы, которые хорошо известны специалисту в данной области техники, например декантирование, фильтрацию или центрифугирование.
Кристаллические формы по изобретению можно сушить, используя стандартные методы. Специалисту будет очевидно, что температура сушки и время сушки могут влиять на свойства твердого состояния соединений, которые находятся в форме сольватов (например, при некоторых температурах и/или пониженном давлении может иметь место десольватация).
Кристаллические формы по изобретению можно легко характеризовать, используя методы дифракции рентгеновских лучей на порошке (XRPD), например как описано ниже. Можно также использовать стандартные способы ДСК и TGA. («TGA» = термогравиметрический анализ).
Формы А, В и С соединения (I) можно различать посредством указания их температур начала плавления, картин дифракции рентгеновских лучей на порошке и/или данных рентгеновского анализа монокристалла. В формуле изобретения, во всех аспектах и воплощениях, изложенных в данном описании изобретения, пики картин дифракции рентгеновских лучей измеряют, используя излучение CuKα (то есть рентгеновское излучение с длиной волны  ).
).
Форма А соединения (I) характеризуется полученной картиной дифракции рентгеновских лучей на порошке, по существу такой, как показано на Фиг. 1. Десять пиков картины дифракции рентгеновских лучей на порошке (полученных при использовании рентгеновского излучения с длиной волны  , то есть излучение CuKα) показаны в Таблице А:
, то есть излучение CuKα) показаны в Таблице А:

Таким образом, форма А соединения (I) имеет картину дифракции рентгеновских лучей на порошке по существу такую же самую, как картина дифракции рентгеновских лучей на порошке, показанная на Фиг. 1.
Форма А соединения (I) дает картины дифракции рентгеновских лучей на порошке по существу такие, как картины дифракции рентгеновских лучей на порошке, показанные на Фиг. 1, и имеет десять пиков [значения угла 2-тета (2θ)], показанных в таблице А. Следует понимать, что значения 2-тета картины дифракции рентгеновских лучей на порошке могут незначительно варьировать от одного устройства к другому или от одного образца к другому, и поэтому приведенные значения не должны считаться абсолютными.
ДСК-анализ формы А соединения (I) демонстрирует эндотерму плавления с началом при 155,2°С (Фиг. 2).
Форма В соединения (I)
Если форму В соединения (I) получали способом, описанным ниже в примере 1, и анализировали с использованием рентгеновского порошкового дифрактометра Bruker D8, то получали картину дифракции рентгеновских лучей на порошке, показанную на Фиг. 3.1 (использовалось рентгеновское излучение с длиной волны  , то есть излучение CuKα).
, то есть излучение CuKα).
Таким образом, форму В соединения (I) можно охарактеризовать по меньшей мере одним из следующих значений 2θ, измеренных с применением излучения CuKα: 15,0 и 19,2. Форму В можно охарактеризовать получением картины дифракции рентгеновских лучей на порошке, по существу такой, как показано на Фиг. 3.1. На основании картины дифракции рентгеновских лучей на порошке, показанной на Фиг. 3.1, десять пиков картины дифракции рентгеновских лучей на порошке (использовалось рентгеновское излучение с длиной волны  , то есть излучение CuKα), относящихся к форме В, показаны в Таблице В-1:
, то есть излучение CuKα), относящихся к форме В, показаны в Таблице В-1:

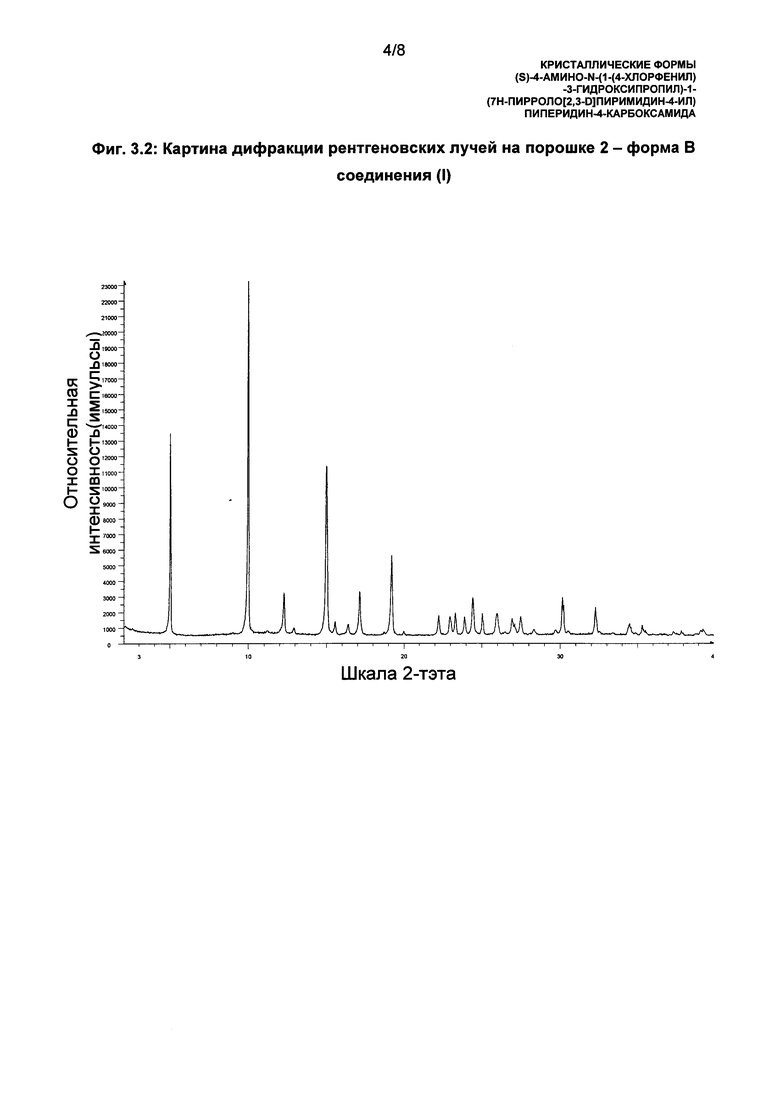
Когда форму В соединения (I) получали способом, описанным ниже в примере 3, и анализировали с использованием рентгеновского порошкового дифрактометра PANalytical CUBIX PRO, а также достигали улучшенного отношения сигнала к шуму, то получали картину дифракции рентгеновских лучей на порошке, указанную на Фиг. 3.2 (использовалось рентгеновское излучение с длиной волны  , то есть излучение CuKα).
, то есть излучение CuKα).
Таким образом, форму В можно характеризовать получением картины дифракции рентгеновских лучей на порошке, которая, по существу такая, как показано на Фиг. 3.2. На основании картины дифракции рентгеновских лучей на порошке, показанной на Фиг. 3.2, десять пиков картины дифракции рентгеновских лучей на порошке (использовалось рентгеновское излучение с длиной волны  , то есть излучение CuKα), относящихся к форме В, показаны в Таблице В-2:
, то есть излучение CuKα), относящихся к форме В, показаны в Таблице В-2:

В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с одним характерным пиком при 2-тета равном примерно 15,0°.
В настоящем изобретении предложена кристаллической форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с одним характерным пиком при 2-тета равном примерно 19,2°.
В настоящем изобретении предложена кристаллической форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с одним характерным пиком при 2-тета равном примерно 12,3°.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с двумя характерными пиками при 2-тета равном примерно 15,0° и 19,2°.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с тремя характерными пиками при 2-тета равном примерно 12,3°, 15,0° и 19,2°.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке с характерными пиками при 2-тета равном примерно 10,0, 12,3, 15,0, 17,1, 19,2 и 24,4°.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке с характерными пиками при 2-тета равном примерно 15,0, 19,2, 12,3, 10,0, 17,1, 24,4, 16,4, 26,0, 15,5 и 23,9°.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке с характерными пиками при 2-тета равном примерно 10,0, 5,0, 15,0, 19,2, 17,1, 12,3, 24,4, 30,2, 32,2 и 23,3°.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке, по существу такую, как картина дифракции рентгеновских лучей на порошке, показанная на Фиг. 3.1.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке, по существу такую, как картина дифракции рентгеновских лучей на порошке, показанная на Фиг. 3.2.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с одним характерным пиком при 2-тета равном 15,0° плюс или минус 0,2°.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с одним характерным пиком при 2-тета равном 19,2° плюс или минус 0,2°.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с одним характерным пиком при 2-тета равном 12,3° плюс или минус 0,2° 2-тета.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с двумя характерными пиками при 2-тета равном 15,0° и 19,2°, где указанные значения 2-тета могут отличаться на плюс или минус 0,2°.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с тремя характерными пиками при 2-тета равном 12,3°, 15,0° и 19,2°, где указанные значения 2-тета могут отличаться на плюс или минус 0,2°.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке с характерными пиками при 2-тета равном 10,0, 12,3, 15,0, 17,1, 19,2 и 24,4°, где указанные значения 2-тета могут отличаться на плюс или минус 0,2°.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке с характерными пиками при 2-тета равном 15,0, 19,2, 12,3, 10,0, 17,1, 24,4, 16,4, 26,0, 15,5 и 23,9°, где указанные значения 2-тета могут отличаться на плюс или минус 0,2°.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке с характерными пиками при 2-тета равном 10,0, 5,0, 15,0, 19,2, 17,1, 12,3, 24,4, 30,2, 32,2 и 23,3° где указанные значения 2-тета могут равняться плюс или минус 0,2°.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с одним характерным пиком при 2-тета равном 15,0°.
В настоящем изобретении предложена кристаллическая форма, форме В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с одним характерным пиком при 2-тета равном 19,2°.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с одним характерным пиком при 2-тета равном 12,3°.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с двумя характерными пиками при 2-тета равном 15,0° и 19,2°.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с тремя характерными пики при 2-тета равном 12,3°, 15,0° и 19,2°.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке с характерными пиками при 2-тета равном 10,0, 12,3, 15,0, 17,1, 19,2 и 24,4°.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке с характерными пиками при 2-тета равном 15,0, 19,2, 12,3, 10,0, 17,1, 24,4, 16,4, 26,0, 15,5 и 23,9°.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке с характерными пиками при 2-тета равном 10,0, 5,0, 15,0, 19,2, 17,1, 12,3, 24,4, 30,2, 32,2 и 23,3°.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке, которая показана на Фиг. 3.1.
В настоящем изобретении предложена кристаллическая форма, а именно форма В соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке, которая показана на Фиг. 3.2.
ДСК-анализ формы В соединения (I) [полученной способом по примеру 1, см. ниже] демонстрирует эндотерму плавления с началом 162,3°С и пиком при 167,1°С (Фиг. 4).
ДСК-анализ формы В соединения (I) [полученной способом по примеру 3, см. ниже] показывает эндотерму плавления с началом 168,5°С и пиком при 171,0°С (Фиг. 7).
Таким образом, форма В, полученная способом по примеру 1, имеет немного более низкую точку плавления по сравнению с формой В, полученной по примеру 3. Полагают, что это небольшое различие точек плавления возникает, потому что форма В, полученная способ Примера 3, является более высококристаллической, чем форма В, полученная способом по примеру 1.
Таким образом, ДСК-анализ показывает, что форма В соединения (I) может представлять собой высокоплавкое твердое вещество с началом плавления при примерно 162,3°С и пиком при примерно 167,1°С.
Равным образом, ДСК-анализ показывает, что форма В соединения (I) может представлять собой высокоплавкое твердое вещество с началом плавления при 168,5°С и пиком при 171,0°С.
Таким образом, в любом воплощении или аспекте данного описания изобретения, или в любом пункте формулы изобретения форма В соединения (I) имеет пик в точке плавления (который измерен посредством ДСК) в диапазоне от 165°С до 173°С.
Форма В соединения (I) предусматривает картины дифракции рентгеновских лучей на порошке, по существу такие, как картины дифракции рентгеновских лучей на порошке, показанные на Фиг. 3.1 и 3.2, которые имеют десять пиков (значений угла 2-тета), показанных в Таблицах В-1 и В-2. Понятно, что значения 2-тета картин дифракции рентгеновских лучей на порошке могут незначительно варьировать от одного прибора к другому или от одного образца к другому, и поэтому приведенные значения не должны считаться абсолютными. В действительности, такая вариация является очевидной на Фиг. 3.1 и 3.2, и в соответствующих Таблицах В-1 и В-2.
Форму С соединения (I) характеризуют по меньшей мере одним из следующих значений 20, измеренных с использованием излучения CuKα: 23,2 и 16,2. Форма С соединения (I) характеризуется картиной дифракции рентгеновских лучей на порошке, по существу такой, как показанная на Фиг. 5. Десять пиков картины дифракции рентгеновских лучей на порошке (использовалось рентгеновское излучение с длиной волны  , то есть излучение CuKα) показаны в Таблице С:
, то есть излучение CuKα) показаны в Таблице С:

Таким образом, предложена форма С соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с одним характерным пиком при 2-тета равном примерно 23,2°.
Таким образом, предложена форма С соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с одним характерным пиком при 2-тета равном примерно 16,2°.
Таким образом, предложена форма С соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с двумя характерными пиками при 2-тета равном примерно 23,2° и 16,2°.
Таким образом, предложена форма С соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке с характерными пиками при 2-тета равном примерно 23,2, 16,2, 15,2, 11,6, 24,1, 19,3, 17,5, 21,7, 20,5 и 25,0°.
Таким образом, предложена форма С соединения (I) которая имеет картину дифракции рентгеновских лучей на порошке, по существу такую, как картина дифракции рентгеновских лучей на порошке, показанная на Фиг. 5.
Таким образом, предложена форма С соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с одним характерным пиком при 2-тета равном 23,2° плюс или минус 0,2°.
Таким образом, предложена форма С соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с одним характерным пиком при 2-тета равном 16,2° плюс или минус 0,2°.
Таким образом, предложена форма С соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с двумя характерными пиками при 2-тета равном 23,2° и 16,2°, где указанные значения 2-тета могут отличаться на плюс или минус 0,2°.
Таким образом, предложена форма С соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке с характерными пиками при 2-тета равном 23,2, 16,2, 15,2, 11,6, 24,1, 19,3, 17,5, 21,7, 20,5 и 25,0°, где указанные значения 2-тета могут отличаться на плюс или минус 0,2°.
Таким образом, предложена форма С соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с одним характерным пиком при 2-тета равном 23,2°.
Таким образом, предложена форма С соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с одним характерным пиком при 2-тета равном 16,2°.
Таким образом, предложена форма С соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с двумя характерными пиками при 2-тета равном 15,0° и 19,2°.
Таким образом, предложена форма С соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке с характерными пиками при 2-тета равном 23,2, 16,2, 15,2, 11,6, 24,1, 19,3, 17,5, 21,7, 20,5 и 25,0°.
Таким образом, предложена форма С соединения (I), которая имеет картину дифракции рентгеновских лучей на порошке, которая показана на Фиг. 5.
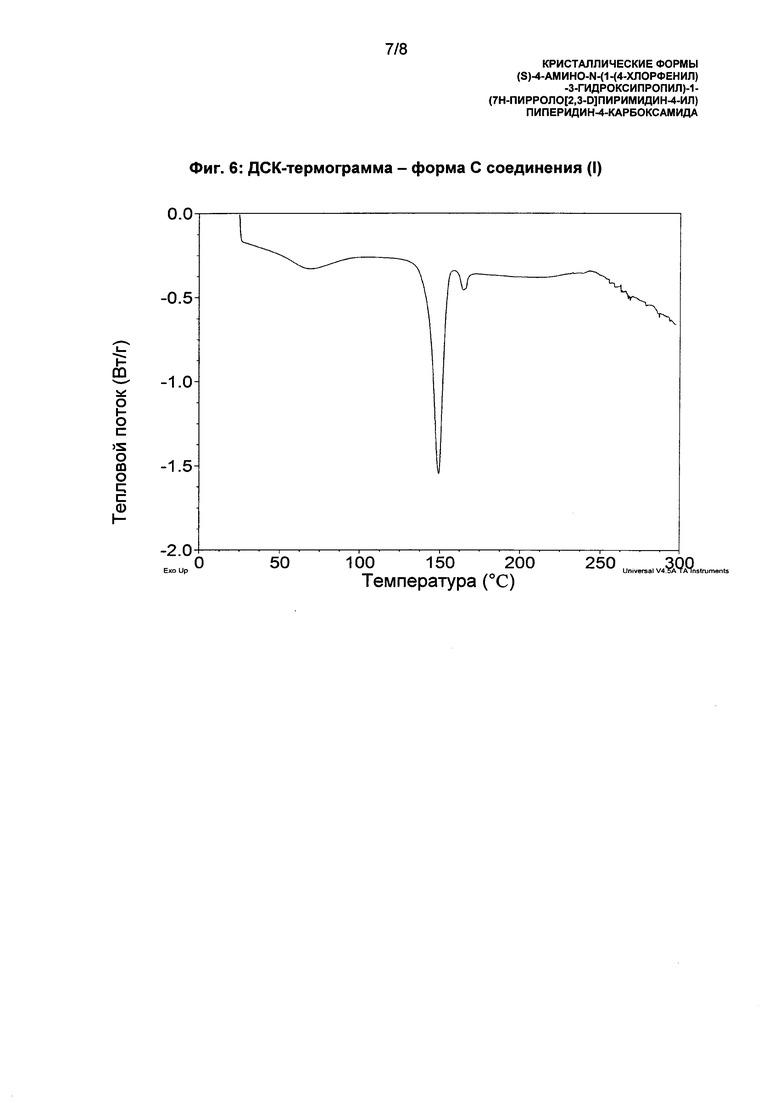
ДСК-анализ формы С соединения (I) демонстрирует широкую эндотерму с началом при 41,7°С и пиком при 67,2°С, последующей острой эндотермой с началом при 142,7°С и пиком при 149,2°С и последующий небольшой эндотермой с началом 161,6°С и пиком при 164,5°С (Фиг. 6).
Форма С соединения (I) предусматривает картины дифракции рентгеновских лучей на порошке, по существу такие, как картины дифракции рентгеновских лучей на порошке, показанные на Фиг. 5, и имеет десять пиков (значения угла 2-тета), показанных в Таблице С. Понятно, что значения 2-тета картины дифракции рентгеновских лучей на порошке могут незначительно варьировать от одного устройства к другому или от одного образца к другому, и поэтому приведенные значения не должны считаться абсолютными.
Известно, что картина дифракции рентгеновских лучей на порошке, которая может быть получена, имеет одну или более ошибок измерения, в зависимости от условий измерений (таких как используемое оборудование или устройство). В частности, общеизвестно, что интенсивности на картине дифракции рентгеновских лучей на порошке могут изменяться в зависимости от условий измерения. По этой причине следует понимать, что формы по настоящему изобретению не ограничиваются кристаллами, которые дают картины дифракции рентгеновских лучей на порошке, идентичные картинам дифракции рентгеновских лучей на порошке, показанным на Фиг., и любые кристаллы, дающие картины дифракции рентгеновских лучей на порошке, по существу такие, как показаны на Фиг., попадают в область настоящего изобретения. Специалист в области дифракции рентгеновских лучей на порошке способен оценить практическую идентичность картин дифракции рентгеновских лучей на порошке.
Специалист в области дифракции рентгеновских лучей на порошке, поймет, что на относительную интенсивность пиков могут влиять, например, зерна с размером более 30 мкм и соотношения неунитарных аспектов, которые могут влиять на анализ образцов. Специалист также поймет, что на положение отражений может влиять точная высота, на которой образец установлен в дифрактометре и калибровка нуля дифрактометра. Планарность образца может также иметь небольшой эффект. Следовательно, представленные дифракционной картины не принимают в качестве абсолютных (Jenkins, R & Snyder, R.L. «Introduction to X-Ray Powder Diffractometry» John Wiley & Sons 1996; Bunn, C.W. (1948), Chemical Crystallography, Clarendon Press, London; Klug, H.P. & Alexander, L.E. (1974), X-Ray Diffraction Procedures).
Как правило, ошибка измерения угла дифракции 2-тета на картине дифракции рентгеновских лучей на порошке составляет приблизительно плюс или минус 0,2°, и такой уровень ошибки измерения следует принимать во внимание при рассматривании картины дифракции рентгеновских лучей на порошке на Фиг. и при чтении таблиц. Кроме того, следует понимать, что интенсивности могут колебаться в зависимости от экспериментальных условий и получения образца (предпочтительная ориентация).
Согласно еще одному аспекту изобретения предлагается фармацевтическая композиция, содержащая соединение (I) в кристаллической форме, которая определена выше, вместе с фармацевтически приемлемым разбавителем или носителем.
Композиции по изобретению могут находиться в форме, подходящей для перорального применения (например, в виде таблеток, пастилок, твердых или мягких капсул, водных или масляных суспензий, эмульсий, диспергируемых порошков или гранул, сиропов или эликсиров), для местного применения (например в виде кремов, мазей, гелей, или водных или масляных растворов или суспензий), для введения путем ингаляции (например в виде мелкодисперсного порошкового или жидкостного аэрозоля), для введения путем инсуффляции (например, в виде мелкодисперсного порошка), или для парентерального введения (например, в виде стерильного водного или масляного раствора для внутривенного, подкожного, внутримышечного или внутримышечного введения доз или в виде суппозитория для ректального введения доз).
Композиции по изобретению можно получать посредством общепринятых способов, используя общепринятые фармацевтические эксципиенты, хорошо известные в данной области техники. Таким образом, композиции, предназначенные для перорального применения, могут содержать, например, один или более красящих, подслащивающих, ароматизирующих и/или консервирующих агентов.
Подходящая композиция соединения (I) в кристаллической форме такая, где соединением заполняют белую твердую капсулу из гипромеллозы (НРМС) без других эксципиентов. Дозировка лекарственного продукта может меняться от 5 до 165 мг.
Композиция этой капсулы следующая:

Примечание А: Количество лекарственного вещества соединения (I), помещенного в капсулу, корректируют с учетом активности применяемой партии.
Примечание В: Эти оболочки для капсул на основе НРМС содержат гипромеллозу, каррагинан, хлорид калия, диоксид титана и карнаубский воск. Каждый из этих ингредиентов соответствует стандартам Фармакопеи США/Национальному формуляру США, Европейской Фармакопеи и Фармакопеи Японии или Стандартам вспомогательных веществ согласно Фармакопеи Японии.
Альтернативная подходящая композиция соединения (I) в кристаллической форме (в частности в форме В) представляет собой таблеточную композицию, в частности композицию в виде таблетки, покрытой пленочной оболочкой.
Пример подходящей композиции покрытой пленочной оболочкой таблетки, содержащей соединение (I), описан ниже:

Примечание С: Как описано более подробно ниже, 0,5% масс. стеарата магния используют в интрагранулярной среде, а оставшийся 1,0% масс. используют в экстрагранулярной среде.
Различные размеры таблеток можно изготовлять из гранул (описано ниже), используя обычные процессы смешивания, сухого гранулирования, прессования и покрытия пленочной оболочкой, согласно стандартам Надлежащей Производственной Практики (Good Manufacturing Practice). Например, таблетки, содержащие от 50 мг до 500 мг соединения (I), можно изготовить, используя вышеупомянутую композицию, применяя способы, описанные в данном описании изобретения.
Получение гранул: форму В соединения (I), микрокристаллическую целлюлозу, маннит, кроскармеллозу натрия и интрагранулярный стеарат магния смешивали в блендере со скоростью 16 оборотов в минуту в течение 5 минут для достижения однородного распределения соединения (I) в смеси. Затем эту смесь пропускали через роликовый компактор для получения ленты, которую измельчали и пропускали через сито 1 мм для получения гранул с однородным размером частиц.
Получение ядра таблетки: Оставшийся экстрагранулярный стеарат магния добавляли к гранулам и смесь перемешивали со скоростью 30 оборотов в минуту в течение 1 минуты. Затем эту смесь прессовали в таблеточные ядра, используя обычное таблеточное оборудование, применяя стандартные вогнутые пуансоны, для достижения желательных размеров таблеток.
Пленочное покрытие ядра таблетки: Прессованные ядра таблеток покрывали оболочкой при помощи водной (очищенная вода) суспензии, содержащей компоненты пленочного покрытия Opadry™ II, используя установку для нанесения пленочных покрытий с перфорированным барабаном. Материал пленочного покрытия Opadry™ II имеется в продаже от Colorcon™, ее вебсайт www.colorcon.com.
В одном воплощении изобретения предложена фармацевтическая композиция, содержащая соединение (I) в кристаллической форме, которая описана в данном описании изобретения (в частности в виде формы В), вместе с микрокристаллической целлюлозой, маннитом, кроскармеллозой натрия и стеаратом магния.
В одном воплощении предложена фармацевтическая таблетка (то есть подходящая для перорального введения пациенту-человеку), содержащая от 50 до 500 мг соединения (I) в кристаллической форме (в частности в виде формы В), которая описана в данном описании изобретения, вместе с одним или более чем одним фармацевтически приемлемым эксципиентом.
В одном воплощении предложена фармацевтическая таблетка (то есть подходящая для перорального введения пациенту-человеку), содержащая от 0,5 до 2% масс. стеарата магния, от 2 до 5% масс. кроскармеллозы натрия, от 15 до 60% масс. соединения (I) в кристаллической форме (в частности в виде формы В), которая описана в данном описании изобретения, микрокристаллическую целлюлозу и маннит, где относительные массы микрокристаллической целлюлозы и маннита в составе фармацевтической таблетки находятся в соотношении от 3:1 до 1:1.
В одном воплощении предложена фармацевтическая таблетка (то есть подходящая для перорального введения пациенту-человеку), содержащая от 0,5 до 2% масс. стеарата магния, от 2 до 5% масс. кроскармеллозы натрия, от 15 до 60% масс. соединения (I) в кристаллической форме (в частности в виде формы В), которая описана в данном описании изобретения, микрокристаллическую целлюлозу и маннит, где относительные массы микрокристаллической целлюлозы и маннита в таблетке находятся в соотношении от 3:1 до 1:1, и где количество соединения (I) в кристаллической форме в таблетке составляет от 50 до 500 мг.
В любом аспекте и воплощении в этом описании изобретения или пункте формулы изобретения, относящимся к таблетке, количество Соединения (I) в кристаллической форме в таблетке может составлять от 50 до 500 мг.
В одном воплощении предложена фармацевтическая таблетка (то есть подходящая для перорального введения пациенту-человеку), содержащая более 55% масс. соединения (I) в кристаллической форме, которая описана в данном описании изобретения (в частности в виде формы В).
В одном воплощении предложена фармацевтическая таблетка (то есть подходящая для перорального введения пациенту-человеку), содержащая 50-70% масс. соединения (I) в кристаллической форме, которая описана в данном описании изобретения (в частности в виде формы В).
Такая таблетка может содержать микрокристаллическую целлюлозу (в частности от 20 до 30% от массы целой таблетки).
Такая таблетка может содержать маннит (в частности от 5 до 12% от массы целой таблетки).
Такая таблетка может содержать кроскармеллозу натрия (в частности от 2 до 5% от массы целой таблетки).
Такая таблетка может содержать стеарат магния (в частности от 0,5 до 2% от массы целой таблетки).
Такая таблетка может включать пленочное покрытие вокруг ядра таблетки (в частности когда пленочное покрытие составляет от 1 до 5% от массы целой таблетки).
Соединение (I) в кристаллической форме обычно вводят теплокровному животному в стандартной дозе в диапазоне 5-5000 мг/м2 площади тела животного, то есть приблизительно 0,1-100 мг/кг, и это обычно обеспечивает терапевтически эффективную дозу. Стандартная лекарственная форма, такая как таблетка или капсула, обычно содержит, например 1-500 мг активного ингредиента. В частности, суточные дозы могут составлять 400 мг дважды в сутки для монотерапии и 320 мг дважды в сутки (непрерывной) или 360 мг дважды в сутки (интермиттирующей терапии) для комбинации с другой химиотерапией. Однако суточную дозу необходимо будет варьировать в зависимости от организма, подвергаемого лечению, конкретного пути введения и степени тяжести заболевания, подлежащего лечению. Таким образом, практикующий врач, который лечит любого конкретного пациента, может определять оптимальную дозировку.
В контексте настоящего описания изобретения, термин «терапия» также включает «профилактику», если отсутствуют конкретные указания на обратное. Термины «терапевтический» и «терапевтически» следует истолковывать соответствующим образом.
При использовании в данном описании изобретения, подразумевают, что термин «лечение» имеет свое обычное значение, касающееся заболевания, для того чтобы полностью или частично облегчить один, несколько или все его симптомы, или корректировать или купировать лежащую в основе патологию.
При использовании в данном описании изобретения подразумевают, что термин «профилактика» имеет свое обычное значение и включает первичную профилактику для предупреждения развития заболевания и вторичную профилактику, в соответствии с которой заболевание уже развивается и пациент временно или постоянно защищается от обострения или ухудшения заболевания или развития новых симптомов, ассоциированных с заболеванием.
В результате своей ингибирующей активности в отношении РКВ, ожидается, что соединение (I) в кристаллической форме является полезным в лечении заболеваний или медицинских состояний, опосредованных только или частично активностью РКВ, например рака. Типы рака, которые могут быть поддающимися лечению с применением соединения (I) в кристаллической форме по настоящему изобретению, включают, но не ограничиваются этим, рак яичника, рак шейки матки, колоректальный рак, рак молочной железы, рак поджелудочной железы, глиому, глиобластому, меланому, рак предстательной железы, лейкемию, лимфому, неходжкинскую лимфому, рак желудка, рак легкого, печеночно-клеточный рак, рак желудка, гастроинтенстинальную стромальную опухоль (GIST), глиому, рак щитовидной железы, рак желчного протока, эндометриальный рак, рак почки, анапластическую крупноклеточную лимфому, острый миелоидный лейкоз (AML), множественную миелому, меланому и мезотелиому. Рак молочной железы и, более конкретно, люминальный рак молочной железы, может быть особенно поддающимся лечению с применением соединений по настоящему изобретению. В частности, соединение (I) в кристаллической форме может быть полезным в лечении рака молочной железы, включая эстроген-рецептор позитивный рак молочной железы, рака предстательной железы, включая устойчивый к кастрации рак предстательной железы и метастатический устойчивый к кастрации рак предстательной железы, и рака желудка.
В одном аспекте изобретения соединение (I) в кристаллической форме может быть полезным в лечения рака молочной железы, особенно эстроген-рецептор позитивного рака молочной железы. В другом аспекте изобретения соединение (I) в кристаллической форме может быть полезным в лечении рака предстательной железы, в частности устойчивого к кастрации рака предстательной железы. В еще одном аспекте изобретения соединение (I) в кристаллической форме может быть полезным в лечении рака предстательной железы, в частности метастатического устойчивого к кастрации рака предстательной железы. В другом аспекте изобретения соединение (I) в кристаллической форме может быть полезным в лечении рака желудка.
Для способов лечения рака, указанного в данном описании изобретения, предполагается, что соединение (I) в кристаллической форме будут вводить млекопитающему, более конкретно представляющему собой человека. Схожим образом, при применении соединения (I) в кристаллической форме для лечения рака, указанного в данном описании изобретения, предполагается, что соединение (I) в кристаллической форме будут вводить млекопитающему, более предпочтительно представляющему собой человека.
Согласно другому аспекту изобретения, предложено соединение (I) в кристаллической форме, которая определена выше, для применения в качестве лекарственного средства.
Согласно еще одному аспекту изобретения предложено соединение (I) в кристаллической форме, которая определена выше, для применения в лечении заболевания, опосредованного РКВ. Согласно еще одному аспекту изобретения предложено соединение (I) в кристаллической форме, которая определена выше, для применения в лечении рака. Согласно еще одному аспекту изобретения предлагается соединение (I) в кристаллической форме, которая определена выше, для применения в лечении рака молочной железы, включая эстроген-рецептор позитивный рак молочной железы, рака предстательной железы, включая устойчивый к кастрации рак предстательной железы и метастатический устойчивый к кастрации рак предстательной железы, и рака желудка.
Согласно еще одному аспекту изобретения предложено применение соединения (I) в кристаллической форме, которая определена выше, для изготовления лекарственного средства для лечения заболевания, опосредованного РКВ. Согласно еще одному аспекту изобретения предлагается применение соединения (I) в кристаллической форме, которая определена выше, для изготовления лекарственного средства для лечения рака. Согласно еще одному аспекту изобретения предлагается применение соединения (I) в кристаллической форме, которая определена выше, для изготовления лекарственного средства для лечения рака молочной железы, включая эстроген-рецептор позитивный рак молочной железы, рака предстательной железы, включая устойчивый к кастрации рак предстательной железы и метастатический устойчивый к кастрации рак предстательной железы, и рака желудка.
Согласно еще одному аспекту изобретения предлагается способ лечения человека, страдающего от заболевания, при котором является полезным ингибирование РКВ, включающий стадию введения человеку, нуждающемуся в этом, терапевтически эффективного количества соединения (I) в кристаллической форме, которая определена выше. В одном воплощении изобретения предлагается способ лечения рака, включающий стадию введения человеку, нуждающемуся в этом, терапевтически эффективного количества соединения (I) в кристаллической форме, которая определена выше. В одном воплощении изобретения предлагается способ лечения рака молочной железы, включая эстроген-рецептор позитивный рак молочной железы, рака предстательной железы, включая устойчивый к кастрации рак предстательной железы и метастатический устойчивый к кастрации рак предстательной железы, и рака желудка, включающий стадию введения человеку, нуждающемуся в этом, терапевтически эффективного количества соединения (I) в кристаллической форме, которая определена выше.
В любом воплощении, аспекте или пункте формулы изобретения, где указано «рак», рак может представлять собой рак молочной железы.
В любом воплощении, аспекте или пункте формулы изобретения, где указано «рак», рак может представлять собой эстроген-рецептор позитивный рак молочной железы.
В любом воплощении, аспекте или пункте формулы изобретения, где указано «рак», рак может представлять собой рак предстательной железы.
В любом воплощении, аспекте или пункте формулы изобретения, где указано «рак», рак может представлять собой устойчивый к кастрации рак предстательной железы.
В любом воплощении, аспекте или пункте формулы изобретения, где указано «рак», рак может представлять собой метастатический устойчивый к кастрации рак предстательной железы.
В любом воплощении, аспекте или пункте формулы изобретения, где указано «рак», рак может представлять собой рак желудка.
Лечение рака, определенного выше, можно осуществлять в виде монотерапии или можно задействовать, в дополнение к соединению по изобретению, общепринятые хирургическое вмешательство или радиотерапию или химиотерапию. Такая химиотерапия может включать комбинацию, содержащую соединение (I) в кристаллической форме с модулятором сигнала андрогенных рецепторов, выбранным из:
- MDV-3100 (4-{3-[4-циано-3-(трифторметил)-фенил]-5,5-диметил-4-оксо-2-тиоксоимидазолидин-1-ил}-2-фтор-N-метилбензамида);
- AZD3514 (1-{4-[2-(4-{1-[3-(трифторметил)-7,8-дигидро[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперидин-4-ил}фенокси)этил]пиперазин-1-ил}этанона);
- абиратерона, или его пролекарства в виде сложного эфира ((3β)-17-(пиридин-3-ил)андроста-5,16-диен-3-ола «абиратерона», или «абиратерона ацетата»); и
- бикалутамида (N-[4-циано-3-(трифторметил)-фенил]-3-[(4-фторфенил)-сульфонил]-2-гидрокси-2-метилпропанамида);
или их фармацевтически приемлемых солей.
MDV-3100 также известен как «энзалутамид».
Такая химиотерапия может также включать комбинацию, содержащую соединение (I) в кристаллической форме и таксан, в частности таксан, выбранный из доцетаксела и паклитаксела.
В данном описании изобретения, когда используют термин «комбинация» понимают, что он относится к одновременному, раздельному или последовательному введению. В одном аспекте изобретения «комбинация» относится к одновременному введению. В другом аспекте изобретения «комбинация» относится к раздельному введению. В еще одном аспекте изобретения «комбинация» относится к последовательному введению. Когда введение является последовательным или раздельным, задержка введения второго компонента не должна быть такой, чтобы терялся целебный и/или синергический эффект комбинации.
В одном воплощении изобретения предлагается способ лечения рака предстательной железы, включая устойчивый к кастрации рак предстательной железы и метастатический устойчивый к кастрации рак предстательной железы, включающий стадию введения субъекту, нуждающемуся в этом, терапевтически эффективного количества соединения (I) в кристаллической форме, которая определена выше, в комбинации с модулятором сигнала андрогенных рецепторов, выбранным из:
- MDV-3100 (4-{3-[4-циано-3-(трифторметил)-фенил]-5,5-диметил-4-охо-2-тиоксоимидазолидин-1-ил}-2-фтор-N-метилбензамида);
- AZD3514 (1-{4-[2-(4-{1-[3-(трифторметил)-7,8-дигидро[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперидин-4-ил}фенокси)этил]пиперазин-1-ил}этанона);
- абиратерона, или его пролекарства в виде сложного эфира ((3β)-17-(пиридин-3-ил)андроста-5,16-диен-3-ола «абиратерона», или «абиратерона ацетата»); и
- бикалутамида (N-[4-циано-3-(трифторметил)-фенил]-3-[(4-фторфенил)-сульфонил]-2-гидрокси-2-метилпропанамида);
или их фармацевтически приемлемых солей.
Согласно еще одному аспекту изобретения предлагается применение соединения (I) в кристаллической форме, которая определена выше, в комбинации с модулятором сигнала андрогенных рецепторов, выбранным из:
- MDV-3100 (4-{3-[4-циано-3-(трифторметил)-фенил]-5,5-диметил-4-охо-2-тиоксоимидазолидин-1-ил}-2-фтор-N-метилбензамида);
- AZD3514 (1-{4-[2-(4-{1-[3-(трифторметил)-7,8-дигидро[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперидин-4-ил}фенокси)этил]пиперазин-1-ил}этанона);
- абиратерона, или его пролекарства в виде сложного эфира ((3β)-17-(пиридин-3-ил)андроста-5,16-диен-3-ола «абиратерона», или «абиратерона ацетата»); и
- бикалутамида (N-[4-циано-3-(трифторметил)-фенил]-3-[(4-фторфенил)-сульфонил]-2-гидрокси-2-метилпропанамида);
или их фармацевтически приемлемых солей;
для изготовления лекарственного средства для лечения рака предстательной железы, включая устойчивый к кастрации рак предстательной железы и метастатический устойчивый к кастрации рак предстательной железы.
Согласно еще одному аспекту изобретения предлагается соединение (I) в кристаллической форме, которая определена выше, в комбинации с модулятором сигнала андрогенных рецепторов, выбанным из:
- MDV-3100 (4-{3-[4-циано-3-(трифторметил)-фенил]-5,5-диметил-4-оксо-2-тиоксоимидазолидин-1-ил}-2-фтор-N-метилбензамида);
- AZD3514 (1-{4-[2-(4-{1-[3-(трифторметил)-7,8-дигидро[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперидин-4-ил}фенокси)этил]пиперазин-1-ил}этанона);
- абиратерона, или его пролекарства в виде сложного эфира ((3β)-17-(пиридин-3-ил)андроста-5,16-диен-3-ола «абиратерона», или «абиратерона ацетата»); и
- бикалутамида (N-[4-циано-3-(трифторметил)-фенил]-3-[(4-фторфенил)-сульфонил]-2-гидрокси-2-метилпропанамида);
или их фармацевтически приемлемых солей;
для применения в лечении рака предстательной железы, включая устойчивый к кастрации рак предстательной железы и метастатический устойчивый к кастрации рак предстательной железы.
В еще одном воплощении изобретения предлагается способ лечения рака молочной железы, включая эстроген-рецептор позитивный рак молочной железы, включающий стадию введения субъекту, нуждающемуся в этом, терапевтически эффективного количества соединения (I) в кристаллической форме, которая определена выше, в комбинации с таксаном, в частности с таксаном, выбранным из доцетаксела и паклитаксела.
Согласно еще одному аспекту изобретения предлагается применение соединения (I) в кристаллической форме, которая определена выше, в комбинации с таксаном, в частности с таксаном, выбранным из доцетаксела и паклитаксела для изготовления лекарственного средства для лечения рака молочной железы, включая эстроген-рецептор позитивный рак молочной железы.
Согласно еще одному аспекту изобретения предлагается соединение (I) в кристаллической форме, которая определена выше, в комбинации с таксаном, в частности с таксаном, выбранным из доцетаксела и паклитаксела, для применения в лечении рака молочной железы, включая эстроген-рецептор позитивный рак молочной железы. В одном воплощении таксан представляет собой доцетаксел. В другом воплощении таксан представляет собой паклитаксел.
Перечень графических материалов
Фиг. 1: Картина диффракции рентгеновских лучей на порошке - форма А соединения (I).
Фиг. 2: ДСК-термограмма - форма А соединения (I).
Фиг. 3.1: Картина диффракции рентгеновских лучей на порошке №1 - форма В соединения (I).
Фиг. 3.2: Картина диффракции рентгеновских лучей на порошке №2 - форма В соединения (I).
Фиг. 4: ДСК термограмма №1 - форма В соединения (I).
Фиг. 5: Картина диффракции рентгеновских лучей на порошке - форма С соединения (I).
Фиг. 6: ДСК-термограмма - форма С соединения (I).
Фиг. 7: ДСК-термограмма №2 - форма В соединения (I).
Подробности использованных методов.
Рентгеновский порошковый дифрактометр Siemens D5000 использовали для получения данных рентгеновской дифракции для формы А соединения (I). Спектры дифракции рентгеновских лучей на порошке определяли посредством установки образца кристаллического вещества на держатель из монокристаллического кремния (SSC) фирмы Siemens и распределения образца тонким слоем при помощи предметного стекла. Образец вращали со скоростью 30 оборотов в минуту (для улучшения статистики измерений) и облучали при помощи рентгеновских лучей, генерированных посредством медной длиннофокусной трубки, работающей при 40 кВ и 40 мА с длиной волны  (то есть излучение CuKα). Коллимированные рентгеновские лучи от источника пропускали через автоматическую переменную щель расходимости, установленную на V20, и отраженное излучение направляли через 2 мм антирассеивающую щель и 0,2 мм щель детектора. Образец подвергали воздействию в течение 1 секунды на каждые 0,02 градуса угла 2-тета (режим непрерывного сканирования) в диапазоне от 2 градусов до 40 градусов 2-тета в режиме тэта-тэта. Время воздействия составляло 31 минуту и 41 секунду. Прибор оснащали сцинтилляционным счетчиком, являющегося детектором. Контроль и сбор данных выполняли посредством Dell Optiplex 686 NT 4.0 Workstation, работающим с программным обеспечением Diffract+.
(то есть излучение CuKα). Коллимированные рентгеновские лучи от источника пропускали через автоматическую переменную щель расходимости, установленную на V20, и отраженное излучение направляли через 2 мм антирассеивающую щель и 0,2 мм щель детектора. Образец подвергали воздействию в течение 1 секунды на каждые 0,02 градуса угла 2-тета (режим непрерывного сканирования) в диапазоне от 2 градусов до 40 градусов 2-тета в режиме тэта-тэта. Время воздействия составляло 31 минуту и 41 секунду. Прибор оснащали сцинтилляционным счетчиком, являющегося детектором. Контроль и сбор данных выполняли посредством Dell Optiplex 686 NT 4.0 Workstation, работающим с программным обеспечением Diffract+.
Рентгеновский порошковый дифрактометр Bruker D8 использовали для получения данных о рентгеновской дифракции для Форм В и С соединения (I). Дифракционную рентгенограмму, показанную на Фиг. 3.1 (но не на Фиг. 3.2), для формы В получали, используя этот дифрактометр, посредством установки образца кристаллической вещества на держатель из монокристаллического кремния (SSC) фирмы Bruker и распределения образца тонким слоем при помощи предметного стекла. Образец вращали со скоростью 30 оборотов в минуту (для улучшения статистики измерений) и облучали при помощи рентгеновских лучей, генерированных посредством медной длиннофокусной трубки, работающей при 40 кВ и 40 мА с длиной волны  (то есть излучение CuKα). Коллимированные рентгеновские лучи от источника пропускали через фиксированную щель расходимости. Образец подвергали воздействию в течение 0,2 секунды на каждые 0,014° угла 2-тета (режим непрерывного сканирования) в диапазоне от 2 градусов до 40 градусов 2-тета в режиме тэта-тэта. Время воздействия составляло приблизительно 9 минут и 3 секунды. Прибор оснащали позиционно-чувствительным детектором. Контроль и сбор данных выполняли посредством Dell Optiplex 686 NT 4.0 Workstation, работающим с программным обеспечением Diffrac+.
(то есть излучение CuKα). Коллимированные рентгеновские лучи от источника пропускали через фиксированную щель расходимости. Образец подвергали воздействию в течение 0,2 секунды на каждые 0,014° угла 2-тета (режим непрерывного сканирования) в диапазоне от 2 градусов до 40 градусов 2-тета в режиме тэта-тэта. Время воздействия составляло приблизительно 9 минут и 3 секунды. Прибор оснащали позиционно-чувствительным детектором. Контроль и сбор данных выполняли посредством Dell Optiplex 686 NT 4.0 Workstation, работающим с программным обеспечением Diffrac+.
Рентгеновский порошковый дифрактометр PANalytical CUBIX PRO использовали для анализа формы В соединения (I). Дифракционную рентгенограмму, показанную на Фиг. 3.2 (но не на Фиг. 3.1), для формы В получали, используя этот дифрактометр, посредством установки образца кристаллического вещества на держатель из монокристаллического кремния (SSC) и распределения образца тонким слоем. Образец вращали со скоростью 30 оборотов в минуту (для улучшения статистики измерений) и облучали при помощи рентгеновских лучей, генерированных посредством медной длиннофокусной трубки, работающей при 45 кВ и 40 мА с длиной волны  (то есть излучение CuKα). Образец подвергали воздействию в течение 25 секунд на каждые 0,025° 2-тета (режим непрерывного сканирования) в диапазоне от 2 градусов до 40 градусов 2-тета в режиме тэта-тэта, применяя детектор XCelerator (длина активной области 2,55° 2θ).
(то есть излучение CuKα). Образец подвергали воздействию в течение 25 секунд на каждые 0,025° 2-тета (режим непрерывного сканирования) в диапазоне от 2 градусов до 40 градусов 2-тета в режиме тэта-тэта, применяя детектор XCelerator (длина активной области 2,55° 2θ).
Дифференциальный сканирующий калориметр «ТА Instruments Q1000» использовали для анализа форм А, В и С соединения (I). Обычно менее 5 мг вещества (содержащегося в стандартном алюминиевом тигле с крышкой) нагревали от 25 до 300°С с постоянной скоростью нагревания 10°С/минута. Применяли продувочный газ азот - скорость потока 50 мл в минуту.
Любая кристаллическая форма, которая дает дифрактограмму XRPD, рамановский/IR (инфракрасный) спектр, твердофазный ЯМР (ядерный магнитный резонанс) спектр или ДСК-термограмму, по существу идентичную формам, раскрытым в данном описании изобретения, попадает в объем настоящего описания изобретения. Специалист в данной области техники будет иметь возможность определить фактические идентичности дифрактограмм, спектров и термограмм.
Примеры
Ссылочный пример 1: Получение Формы А
В WO 2009/047563 раскрыты три способа получения соединения (I) - пример 9 и альтернативные способы синтеза 1 и 2. «Пример 9, альтернативный способ синтеза 1» включает суспензию соединения (I) в этилацетате, другие два процесса выделяют соединение (I) в виде твердого вещества путем упаривания фракций из колонки. Три архивных образца соединения (I) из коллекции соединений авторов изобретения, синтезированные с применением способа, идентичного, или по существу подобного, одному из этих трех способов, анализировали посредством XRD и все три идентифицированы как имеющие полукристаллическую форму, обозначенную как форма А, которая имела точку плавления 155,2°С (начало плавления).
Пример 1: Получение Формы В
Приблизительно 20 мг формы А соединения (I) помещали во флакон с якорем магнитной мешалки и добавляли приблизительно 2 мл ацетонитрила. Затем флакон плотно укупоривали при помощи крышки и оставляли перемешиваться на плите магнитной мешалки. Через 3 суток образец снимали с плиты, снимали крышку и суспензию оставляли сушиться в условиях окружающей среды до ее анализа посредством XRPD и ДСК. Эту форму (форму В) определяли как кристаллическую посредством XRPD. Это вещество имело точку плавления 162,3°С (начало). Картина дифракции рентгеновских лучей на порошке формы В, полученная посредством этого способа, показана на Фиг. 3.1.
Пример 2: Получение формы С
Приблизительно 20 мг формы А соединения (I) помещали во флакон с магнитным стержнем и добавляли приблизительно 2 мл метанола, затем флакон плотно укупоривали при помощи крышки и оставляли перемешиваться на плите магнитной мешалки. Через 3 суток образец снимали с плиты, снимали крышку и суспензию оставляли сушиться в условиях окружающей среды до ее анализа посредством XRPD и ДСК. Эту форму (форму С) определяли как полукристаллическую посредством XRPD. Это вещество имело точку плавления 142,7°С (начало) и пик примерно при 149,2°С с последующей дополнительной эндотермой плавления с началом 161,6°С и пиком при 164,5°С.
Пример 3: Альтернативное получение формы В
Полученную вначале форму А соединения (I) можно превращать в форму В, следующим способом: Соединение (I) смешивают с 7-8 относительными объемами абсолютного этанола и затем смесь нагревают с обратным холодильником до 70-75°С. Затем смесь фильтруют для удаления нерастворенных частиц твердого вещества и фильтрат охлаждают до 60-65°С. Небольшое количество предварительно полученных зерен (например 0,5% масс, формы В соединения (I)) добавляют затем в смесь. Затем текучую среду, окружающую реакционный сосуд, охлаждают до -10°С при скорости охлаждения 0,3°С/минуту и затем смесь перемешивают в течение дополнительных 8-12 часов до выделения путем фильтрации полученного твердого вещества. Это влажное твердое вещество затем сушат в вакууме при температуре 60-65°С с получением формы В соединения (I). Картина дифракции рентгеновских лучей на порошке формы В, полученная посредством этого способа, показана на Фиг. 3.2. ДСК-анализ формы В соединения (I), которая была получена посредством этого способа, демонстрирует эндотерму плавления с началом 168,5°С и пиком при 171,0°С (Фиг. 7). Во избежание разночтений, один «относительный объем» означает, что используют 1 мл жидкости на 1 г соединения.






Изобретение относится к новой кристаллической форме В (S)-4-амино-N-(1-(4-хлорфенил)-3-гидроксипропил)-1-(7Н-пирроло[2,3-d]-пиримидин-4-ил)пиперидин-4-карбоксамида (соединение (I), проявляющей ингибирующую активность в отношении PKB (протеинкиназы В). Соединение может быть использовано для лечения рака или для приготовления лекарственного средства для лечения, опосредованного активностью PKB, в частности рака молочной железы, рака предстательной железы или рака желудка. Изобретение также относится к фармацевтической композиция, пригодной для лечения рака, опосредованного активностью PKB, содержащей соединение (I) в кристаллической форме В в терапевтически эффективном количестве, возможно вместе с микрокристаллической целлюлозой, маннитом, кроскармеллозой натрия и стеаратом магния. Кристаллическая форма В имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с тремя характерными пиками при 2-тета примерно равном 12,3, 15,0 и 19,2°, в частности картину дифракции рентгеновских лучей на порошке с характерными пиками при 2-тета примерно равном 10,0, 12,3, 15,0, 17,1, 19,2 и 24,4°. Кристаллическая форма В термодинамически является более стабильной, чем другие кристаллические формы, и более предпочтительной с точки зрения продолжительности срока годности продукта и минимизации вариабельности в абсорбции. 4 н. и 5 з.п. ф-лы, 8 ил., 6 табл., 3 пр.
1. (S)-4-Амино-N-(1-(4-хлорфенил)-3-гидроксипропил)-1-(7Н-пирроло[2,3-d]-пиримидин-4-ил)пиперидин-4-карбоксамид (соединение (I)) в кристаллической форме В, где указанная форма В имеет картину дифракции рентгеновских лучей на порошке по меньшей мере с тремя характерными пиками при 2-тета примерно равном 12,3°, 15,0° и 19,2°.
2. Соединение (I) в кристаллической форме по п. 1, где указанная форма В имеет картину дифракции рентгеновских лучей на порошке с характерными пиками при 2-тета примерно равном 10,0, 12,3, 15,0, 17,1, 19,2 и 24,4°.
3. Соединение (I) в кристаллической форме по п. 1, где указанная форма В имеет картину дифракции рентгеновских лучей на порошке по существу такую, как показано на Фиг. 3.1.
4. Соединение (I) в кристаллической форме по п. 1, где указанная форма В имеет картину дифракции рентгеновских лучей на порошке по существу такую, как показано на Фиг. 3.2.
5. Фармацевтическая композиция, проявляющая ингибирующую активность в отношении PKB (протеинкиназы В) и содержащая соединение (I) в кристаллической форме по любому из пп. 1-4 в терапевтически эффективном количестве вместе с фармацевтически приемлемым разбавителем или носителем.
6. Соединение (I) в кристаллической форме по любому из пп. 1-4 для применения в качестве лекарственного средства для лечения рака, опосредованного активностью PKB.
7. Применение соединения (I) в кристаллической форме по любому из пп. 1-4 для изготовления лекарственного средства для лечения рака, опосредованного активностью PKB.
8. Соединение (I) в кристаллической форме по любому из пп. 1-4 для использования в терапевтически эффективном количестве для лечения рака молочной железы, рака предстательной железы или рака желудка.
9. Фармацевтическая композиция, пригодная для лечения рака, опосредованного активностью PKB, содержащая соединение (I) в кристаллической форме по любому из пп. 1-4 в терапевтически эффективном количестве вместе с микрокристаллической целлюлозой, маннитом, кроскармеллозой натрия и стеаратом магния.
| WO 2009047563 A1, 16.04.2009 & EA 018512 B1, 30.08.2013 | |||
| Устройство для получения смеси пара и продуктов горения | 1928 |
|
SU14187A1 |
| Джагдиш Баласубраманиам и др., Влияние дезинтегрантов быстрого действия на скорость растворения твердых лекарственных форм перорального применения,Фармацевтическая отрасль, 2010, (21), 4, 92-99. | |||
Авторы
Даты
2018-04-26—Публикация
2013-04-16—Подача