ПЕРЕКРЕСТНЫЕ ССЫЛКИ НА РОДСТВЕННЫЕ ЗАЯВКИ
По данной заявке испрашивается приоритет на основании предварительной патентной заявки США № 61/779509, поданной 13 марта 2013 г., предварительной патентной заявки США № 61/707733, поданной 28 сентября 2012 г., и предварительной патентной заявки США № 61/703890, поданной 21 сентября 2012 г., полное содержание каждой из которых включено в настоящий документ посредством ссылки.
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
1. Область техники
Настоящее изобретение относится к новым способам лечения рака. Способы включают лечение карциномы или саркомы с применением стратегии совместного введения, которая предполагает совместную локальную доставку терапевтического средства и средства, усиливающего внутриклеточное проникновение, необязательно в сочетании с по меньшей мере одним дополнительным терапевтическим средством (например, локальным или системным введением иммунотерапевтического средства). Способы по изобретению приводят к замедлению роста, уменьшению и/или ликвидации опухоли-мишени, а также тех злокачественных клеток, которые метастазировали в другие части тела.
2. Уровень техники
В настоящее время считается, что раковые клетки регулярно возникают в организме, но постоянно уничтожаются здоровой иммунной системой. Считается, что злокачественные опухоли образуются, когда иммунная система не в состоянии уничтожить эти регулярно образующиеся пораженные клетки. Термин «рак» используют для обозначения целого ряда заболеваний, при которых имеет место неконтролируемое деление аномальных клеток. Рак может первоначально возникать практически в любой ткани или органе в организме и развивается в результате сложного взаимодействия как врожденных генетических факторов, так и факторов окружающей среды, например, диеты или воздействия радиации, токсинов и тому подобного. Несмотря на успехи в медицине и понимание молекулярных основ рака, точные причины того или иного вида рака в значительной степени остаются неизвестными, особенно у конкретного индивидуума. Учитывая этот недостаток знаний, не удивительно, что по-прежнему очень трудно найти эффективные методы лечения рака.
Поиск эффективных методов лечения также является сложной задачей, поскольку рак часто вырабатывает устойчивость к различным терапевтическим методам. Кроме того, создание эффективных средств лечения рака становится еще более сложной задачей ввиду способности некоторых видов рака распространяться из своего первичного источника. Этот процесс, называемый метастазированием, позволяет раковым клеткам распространяться в другие жизненно важные части тела через кровеносную и лимфатическую системы. Некоторые эксперты считают, что только одна клетка на миллион способна выживать достаточно долго для того, чтобы могла образоваться метастатическая опухоль. Эти шансы, как считают, обусловлены теми сложностями, которые возникают для метастатических клеток в ткани, в которую они в конечном итоге проникают, включая размещение в этой ткани, преодоление местной иммунной защиты и приобретение собственного кровоснабжения и снабжения питательными веществами в результате ангиогенеза. Тем не менее, метастазирование остается основной причиной трудностей в разработке эффективных методов лечения рака.
Существующие на сегодняшний день методы лечения рака включают множество различных методов абляции, таких как хирургические процедуры, криогенные или термические методы воздействия на ткани, воздействие ультразвуком, радиочастотное воздействие и радиационная терапия, химические методы, например, с использованием фармацевтических препаратов, цитотоксических средств, моноклональных антител, или трансартериальная химиоэмболизация (TACE), а также их сочетания в соответствии с конкретными режимами лечения, основанными на конкретном виде и стадии рака, который подвергают лечению. Однако эти методы лечения связаны с довольно высокими затратами. Кроме того, современные методы лечения чрезвычайно инвазивны, связаны со значительной токсичностью и в конечном итоге приводят к низкому качеству жизни пациентов.
Стандартное лечение рака, как правило, сочетает хирургическое удаление пораженной ткани с химиотерапией или радиационной терапией. Стандартные подходы к введению химиотерапевтических средств включают введение в кровь, например, системную доставку, которую осуществляют различными путями введения, например, внутривенным введением и/или доставкой через желудочно-кишечный тракт. Однако токсичность является существенным недостатком, связанным с системной доставкой химиотерапевтических лекарственных средств. Стандартные хирургические методы лечения также создают проблемы, включая попадание раковых клеток в кровеносную и/или лимфатическую системы, что дает возможность раковым клеткам метастазировать в другие участки тела и вызывать образование дополнительных опухолей.
Когда хирургическая операция невозможна, для лечения рака принято использовать радиационную или химиотерапию. Однако коэффициент выживаемости в случае неоперабельного рака очень низок по сравнению с коэффициентом выживаемости в случае раковых опухолей, которые были хирургически удалены перед проведением химиотерапии или радиационной терапии.
Региональная химиотерапия является последним достижением в области химиотерапевтического лечения рака. Этот подход включает доставку химиотерапевтического средства непосредственно в опухоль, например, близко к опухоли, рядом с ней или в саму опухоль, в отличие от введения токсического средства в кровоток. Одной из целей региональной химиотерапии является сведение к минимуму токсических побочных эффектов, как правило, связанных с системным введением химиотерапевтического средства.
Однако региональные химиотерапевтические подходы, как правило, не приводили к удовлетворительным результатам. Основная проблема при использовании химиотерапии - включая региональную химиотерапию - заключается в том, что раковые клетки обладают высокой устойчивостью к проникновению химиотерапевтических средств. Например, некоторые соединения платины в основном поступают в раковые клетки в процессе активного транспорта с вовлечением CTR1 пути (см. Holzer et al., Molecular Pharmacology 70: 1390-1394 (2006)). Кроме того, поскольку химиотерапевтические средства, как правило, доставляются кровью, они должны растворяться в крови, что делает их по сути водорастворимыми. Водорастворимые материалы, такие как химиотерапевтические средства, не могут эффективно проходить через липидные клеточные мембраны пассивным образом, и таким образом, не могут легко доставляться во внутриклеточное пространство раковых клеток, особенно при низких концентрациях. Кроме того, даже если они проникли внутрь, клетки опухолей имеют механизмы и различные процессы, предназначенные для выведения химиотерапевтических средств. Например, клетки опухолей могут избавляться от химических средств за счет образования комплексов с глутатионом и/или металлотионеином и имеют характерные механизмы репарации ДНК для преодоления действия химиотерапевтических средств.
Некоторые злокачественные опухоли имеют сходство с тканями организма, и таким образом, иммунной системе сложнее распознавать и уничтожать их. Некоторые технологии борьбы с раком (например, противораковые вакцины) направлены на стимуляцию иммунной системы в отношении злокачественных клеток. Хотя один такой продукт в настоящее время одобрен для применения (провендж® от компании Dendreon Corporation, который используют против рака предстательной железы), успех противораковых вакцин был ограниченным. Поскольку клетки опухолей получают от индивидуума, больного раком, клетки опухолей очень сходны с собственными клетками человека. Способности иммунной системы атаковать опухолевые клетки препятствует то, что клетка опухоли экспонирует мало, или совсем не экспонирует антигены, являющиеся чужеродными для индивидуума. Кроме того, в опухоли могут находиться клетки самых разных типов. Клетки каждого типа имеют разные антигены клеточной поверхности, что опять-таки мешает атаке со стороны иммунной системы. Более того, опухоли могут секретировать цитокины, которые непосредственно ингибируют иммунную активность. И наконец, в зависимости от стадии заболевания опухоль может быть слишком запущенной (например, большого объема), чтобы вакцина оказалась эффективной. Эти, а также и другие факторы являются причиной того, почему у опухолей может быть недостаточное количество антигенов (или мишеней), чтобы в достаточной степени стимулировать иммунную систему.
Тем не менее, обычно бывает так, что в случае раннего обнаружения рака стандартные методы противоракового лечения могут быть очень эффективными. Однако, даже при достижении наилучших результатов, такое лечение является инвазивным, токсичным, наносящим вред организму и тяжелым в психологическом смысле для пациента. Если рак обнаружен на поздней стадии, лишь немногие методы лечения оставляют пациенту надежду на долгосрочное выживание.
Таким образом, в данной области по-прежнему сохраняется потребность выявления и развития новых стратегий борьбы с раком, которые более эффективны для лечения заболевания и которые, как правило, являются менее дорогостоящими для людей и для общества.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В настоящем документе раскрыт способ лечения рака. В аспектах изобретения предложены способы эффективного лечения солидной опухоли путем локального совместного введения (например, вблизи, локально, непосредственно в, и тому подобное) сочетания терапевтического средства (например, малой молекулы, фармацевтического лекарственного средства, антитела и тому подобного) и средства, усиливающего внутриклеточное проникновение. Терапевтическое средство и средство, усиливающее внутриклеточное проникновение, вводят в количествах и/или в режиме, которые приводят к существенному уменьшению и/или уничтожению опухоли. Конкретный режим введения может варьироваться, включая то, что средства могут доставляться в одно и то же время или одновременно друг с другом (например, одной и той же инъекцией), или в разные моменты времени и в любом порядке. Кроме того, режим введения может включать несколько повторений или раундов введения, при этом средства доставляются одним и тем же или разными способами несколько раз в один день или в разные дни. Введение повторных доз в течение определенного периода времени часто называют лекарственным циклом. Описанные способы могут также включать несколько лекарственных циклов. Способы могут также варьироваться в зависимости от типа опухоли. Способ по изобретению также включает усиление лечебного действия терапевтического средства и средства, усиливающего внутриклеточное проникновение, путем сочетания их локального введения с введением иммуностимулирующего средства, такого как противораковая вакцина или агонист T-клеток, которое может быть доставлено до, одновременно или почти одновременно, или вслед за терапевтическим средством и средством, усиливающим внутриклеточное проникновение. В вариантах осуществления терапевтическое средство может представлять собой сочетание двух или более средств, выбранных из группы, состоящей из химиотерапевтического средства, антитела и молекулы нуклеиновой кислоты.
В одном варианте осуществления способ по изобретению можно также рассматривать как двухэтапный терапевтический подход. На первом этапе субъекту локально вводят совместно терапевтическое средство и средство, усиливающее внутриклеточное проникновение, в соответствии с эффективным режимом дозирования. Например, средства могут доставляться одновременно или почти одновременно в участок тела, который находится в той же области, что и опухоль-мишень, или который находится по периметру опухоли-мишени, или который находится внутри (интратуморально) самой опухоли. Средство, усиливающее внутриклеточное проникновение, неожиданно приводит к значительному увеличению способности терапевтического средства проникать в клетки опухолей. На втором этапе, который может совпадать, предшествовать или следовать за первым этапом, субъекту локально вводят иммуностимулирующее средство, такое как противораковая вакцина, средство, стимулирующее CD4 или NKT клетки, или сочетание средств. Однако неожиданно было обнаружено, что средство для внутриклеточного проникновения в сочетании с некоторыми цитотоксическими лекарственными средствами вызывает иммунный ответ при введении интратуморально, даже в отсутствие дополнительных иммуностимулирующих средств. Изобретение также относится к составам для использования в лечении рака способами по изобретению. В составах скомбинированы, отдельно или вместе, терапевтическое средство и средство, усиливающее внутриклеточное проникновение. Такие составы можно вводить локально или регионально, или интратуморально в опухоль субъекта. В некоторых вариантах осуществления изобретение относится к составам, в которых дополнительно скомбинированы, отдельно или вместе, терапевтическое средство, средство, усиливающее внутриклеточное проникновение, и иммунотерапевтическое средство, например, противораковая вакцина. Такие составы можно вводить локально или регионально, или интратуморально в опухоль субъекта.
Соответственно, в аспектах изобретения предложены способы лечения субъекта, который нуждается в этом (например, субъекта с одной или более опухолями), эффективным количеством терапевтического средства и средства, усиливающего внутриклеточное проникновение. В вариантах осуществления введение средства для внутриклеточного проникновения повышает вероятность эффективности терапевтического средства. В связанных вариантах осуществления введение средства для внутриклеточного проникновения повышает вероятность эффективности терапевтического средства по меньшей мере на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95%, 99% или более (или на любое промежуточное количество) по сравнению с лечением без средства для внутриклеточного проникновения.
В другом аспекте изобретение относится к способам уменьшения побочных эффектов терапевтического средства. В вариантах осуществления способы включают введение эффективного количества терапевтического средства и средства, усиливающего внутриклеточное проникновение, субъекту (например, субъекту с опухолью).
В другом аспекте изобретение относится к способам уничтожения злокачественных клеток в организме субъекта (например, субъекта с одной или более опухолями). В вариантах осуществления способы включают введение эффективного количества терапевтического средства и средства, усиливающего внутриклеточное проникновение.
В следующем аспекте изобретение относится к способам лечения опухоли у субъекта. В вариантах осуществления способы включают введение эффективного количества терапевтического средства и средства, усиливающего внутриклеточное проникновение.
В других аспектах изобретение относится к способам подавления роста опухоли у субъекта. В вариантах осуществления способы включают введение эффективного количества терапевтического средства и средства, усиливающего внутриклеточное проникновение.
В любом из вышеуказанных аспектов и вариантов осуществления терапевтическое средство можно вводить субъекту локально, регионально или системно.
В любом из вышеуказанных аспектов и вариантов осуществления средство, усиливающее внутриклеточное проникновение, можно вводить субъекту локально или регионально.
В вариантах осуществления способы включают локальное или региональное совместное введение субъекту терапевтического средства и средства, усиливающего внутриклеточное проникновение.
В вариантах осуществления опухоль представляет собой солидную опухоль. В некоторых вариантах осуществления опухоль образовывала метастазы.
В вариантах осуществления опухоль представляет собой карциному или саркому. В связанных вариантах осуществления опухоль представляет собой карциному или саркому кожи, кости, мышцы, молочной железы, ротовой полости, толстой кишки, органа, почки, печени, легких, желчного пузыря, поджелудочной железы, головного мозга, пищевода, мочевого пузыря, толстого кишечника, тонкого кишечника, селезенки, желудка, предстательной железы, яичек, яичников или матки. В некоторых вариантах осуществления опухоль представляет собой карциному поджелудочной железы, толстой кишки или печени.
В вариантах осуществления терапевтическое средство вводят интратуморально и/или средство, усиливающее внутриклеточное проникновение, вводят интратуморально. В некоторых вариантах осуществления терапевтическое средство вводят системно и средство, усиливающее внутриклеточное проникновение, вводят интратуморально.
В любом из вышеуказанных аспектов и вариантов осуществления способы могут приводить к замедлению роста одной или более опухолей, уменьшению одной или более опухолей или ликвидации одной или более опухолей. Например, масса опухоли не увеличивается. В некоторых вариантах осуществления опухоль уменьшается на 10%, 25%, 50%, 75%, 85%, 90%, 95% или 99% или более (или на любое промежуточное количество) по сравнению с ее исходной массой.
В любом из вышеуказанных аспектов и вариантов осуществления способы могут предотвращать метастазирование опухоли.
В любом из вышеуказанных аспектов и вариантов осуществления эффективное количество терапевтического средства можно выбирать, исходя из объема и типа опухоли.
В любом из вышеуказанных аспектов и вариантов осуществления эффективное количество средства, усиливающего внутриклеточное проникновение, и/или лекарственного средства можно выбирать, исходя из объема и типа опухоли.
В вариантах осуществления способы включают введение терапевтического средства в первый день и повторное введение в один или более последующих дней. В связанных вариантах осуществления первый день и один или более последующих дней разделены интервалом от 1 дня до примерно 3 недель.
В вариантах осуществления способы включают введение средства, усиливающего внутриклеточное проникновение, в первый день и повторное введение в один или более последующих дней. В связанных вариантах осуществления первый день и один или более последующих дней разделены интервалом от 1 дня до примерно 3 недель. В другом варианте осуществления средство, усиливающее внутриклеточное проникновение, можно вводить последовательно 3-5 дней или с одним днем отдыха в течение периода.
В некоторых вариантах осуществления способы включают совместное введение терапевтического средства и средства, усиливающего внутриклеточное проникновение, в первый день и повторное введение в один или более последующих дней. В связанных вариантах осуществления первый день и один или более последующих дней разделены интервалом от 1 дня до примерно 3 недель.
В некоторых вариантах осуществления терапевтическое средство и средство, усиливающее внутриклеточное проникновение, вводят совместно в соотношении примерно 1:2, 1:4, 1:10, 1:20, 1:25, 1:50, 1:100 или 1:200 (массовое отношение терапевтическое средство:средство, усиливающее внутриклеточное проникновение).
В некоторых вариантах осуществления средство, усиливающее внутриклеточное проникновение, вводят в концентрации от примерно 0,5 мг на мл до примерно 50 мг на мл. В других вариантах осуществления средство, усиливающее внутриклеточное проникновение, вводят в концентрации от примерно 10 мг на мл до примерно 30 мг на мл.
В некоторых вариантах осуществления терапевтическое средство и средство, усиливающее внутриклеточное проникновение, доставляют одновременно в одном составе или одновременно в отдельных составах. В других вариантах осуществления средство, усиливающее внутриклеточное проникновение, вводят перед терапевтическим средством.
В любом из вышеуказанных аспектов и вариантов осуществления терапевтическое средство может представлять собой противораковое средство.
В некоторых вариантах осуществления противораковое средство представляет собой химиотерапевтическое средство (например, абиратерона ацетат, афатиниб, альдеслейкин, алемтузумаб, алитретиноин, алтретамин, амифостин, аминоглутетимид, анагрелид, анастрозол, триоксид мышьяка, аспарагиназу, азацитидин, азатиоприн, бендамустин, бевацизумаб, бексаротин, бикалутамид, блеомицин, бортезомиб, бусульфан, капецитабин, карбоплатин, кармустин, цетуксимаб, хлорамбуцил, цисплатин, кладрибин, кризотиниб, циклофосфамид, цитарабин, дакарбазин, дактиномицин, дазатиниб, даунорубицин, денилейкина дифлитокс, децитабин, доцетаксел, дексаметазон, доксифлуридин, доксорубицин, эпирубицин, эпоэтин альфа, эпотилон, эрлотиниб, эстрамустин, энтиностат, этопозид, эверолимус, экземестан, филграстим, флоксуридин, флударабин, фторурацил, флуоксиместерон, флутамид, связанные с фолатом алкалоиды, гефитиниб, гемцитабин, гемтузумаб озогамицин, GM-CT-01, гозерелин, гексаметилмеламин, гидроксимочевины, ибритумомаб, идарубицин, ифосфамид, иматиниб, интерферон альфа, интерферон бета, иринотекан, иксабепилон, лапатиниб, лейковорин, леупролид, леналидомид, летрозол, ломустин, мехлорэтамин, мегестрол, мелфалан, меркаптопурин, метотрексат, митомицин, митоксантрон, неларабин, нилотиниб, нилутамид, октреотид, офатумумаб, опрелвекин, оксалиплатин, паклитаксел, панитумумаб, пеметрексед, пентостатин, полисахаридные ингибиторы галектина, прокарбазин, ралоксифен, ретиноевые кислоты, ритуксимаб, ромиплостим, сарграмостим, сорафениб, стрептозоцин, сунитиниб, тамоксифен, темсиролимус, темозоламид, тенипозид, талидомид, тиогуанин, тиотепу, тиогуанин, топотекан, торемифен, тозитумомаб, траметиниб, трастузумаб, третиноин, валрубицин, ингибиторы и уловители VEGF, винбластин, винкристин, виндезин, винорелбин, винтафолид (EC145), вориностат, их соль или любое сочетание вышеперечисленных.
В других вариантах осуществления терапевтическое средство представляет собой терапевтическое антитело или сочетание двух или более терапевтических антител (например, абаговомаб, алацизумаб пегол, алемтузумаб, алтумомаб пентетат (Hybri-ceaker), аматуксимаб, анатумомаб мафенатокс, анти-PD-1 антитела, аполизумаб, арцитумомаб (CEA-Scan), белимумаб, бевацизумаб, биватузумаб мертанзин, блинатумомаб, брентуксимаб ведотин, кантузумаб мертанзин, кантузумаб равтанзин, капромаб пендетид (Prostascint), катумаксомаб (Removab), цетуксимаб (Erbitux), цитатузумаб богатокс, циксутумумаб, кливатузумаб тетраксетан (hPAM4-Cide), конатумумаб, далотузумаб, деносумаб, дрозитумаб, эдреколомаб (Panorex), энаватузумаб, гемтузумаб, ибритумомаб тиуксетан, ипилимумаб (MDX-101), офатумумаб, панитумумаб, ритуксимаб, тозитумомаб, трастузумаб или любое их сочетание).
В другом варианте осуществления терапевтическое средство представляет собой молекулу нуклеиновой кислоты. Например, молекула нуклеиновой кислоты может представлять собой интерферирующую РНК (например, РНКи или кшРНК), генно-терапевтический экспрессионный вектор или выключающий ген вектор.
В некоторых вариантах осуществления терапевтическое средство представляет собой радиоизотоп.
В некоторых вариантах осуществления терапевтическое средство представляет собой ингибитор тимидилатсинтазы.
В некоторых вариантах осуществления терапевтическое средство представляет собой соединение платины.
В некоторых вариантах осуществления терапевтическое средство представляет собой алкалоид барвинка.
В любом из вышеуказанных аспектов и вариантов осуществления средство, усиливающее внутриклеточное проникновение, может представлять собой химическое соединение, которое усиливает пассивный транспорт терапевтического соединения в клетку.
В вариантах осуществления средство, усиливающее внутриклеточное проникновение, представляет собой функционализированную кетокислоту, 6-оксо-6-фенилгексановую кислоту, 8-оксо-8-фенилоктановую кислоту, 8-(2,5-дихлорфенил)-8-оксооктановую кислоту, функционализированный кетоэфир или альдегид, модифицированную аминокислоту, модифицированные аминокислоты, N-[8-(2-гидроксибензоил)аминооктановую кислоту, N-[8-(2-гидроксибензоил)аминодекановую кислоту, N-(5-хлорсалицилоил)-8-аминокаприловую кислоту, N-[4-(4-хлор-2-гидроксибензоил)аминобутановую кислоту, 2-этилгексил-2-гидроксибензоат, 5-циклогексил-5-оксовалериановую кислоту, 6-циклогексил-6-оксогексановую кислоту, 7-циклогексил-7-оксогептановую кислоту, 8-циклогексил-8-оксооктановую кислоту, 4-циклопентил-4-оксомасляную кислоту, 5-циклопентил-5-оксовалериановую кислоту, 6-циклопентил-6-оксогексановую кислоту, 7-циклопентил-7-оксогептановую кислоту, 8-циклопентил-8-оксооктановую кислоту, 4-циклобутил-4-оксомасляную кислоту, 5-циклобутил-5-оксовалериановую кислоту, 6-циклобутил-6-оксогексановую кислоту, 7-циклобутил-7-оксогептановую кислоту, 8-циклобутил-8-оксооктановую кислоту, 4-циклопропил-4-оксомасляную кислоту, 5-циклопропил-5-оксовалериановую кислоту, 6-циклопропил-6-оксогексановую кислоту, 7-циклопропил-7-оксогептановую кислоту, 8-циклопропил-8-оксооктановую кислоту, 8-[(3-метилциклогексил)окси]октановую кислоту, 7-[(3-метилциклогексил)окси]гептановую кислоту, 6-[(3-метилциклогексил)окси]гексановую кислоту, 5-[(3-метилциклогексил)окси]пентановую кислоту, 4-[(3-метилциклогексил)окси]бутановую кислоту, 3-[(3-метилциклогексил)окси]пропановую кислоту, октисалат, дикетопиперазины, сапонин, ацилкарнитин, алканоилхолин, тауродигидрофузидат, сульфоксид, оксазолидинон, пирролидон, спирт или алканол, бензойную кислоту, гликоль, поверхностно-активное вещество, терпен, функционально эффективную соль любого из вышеперечисленных, производное любого из вышеперечисленных или их сочетания.
В некоторых вариантах осуществления средство, усиливающее внутриклеточное проникновение, представляет собой 6-оксо-6-фенилгексановую кислоту, 8-циклогексил-8-оксооктановую кислоту, N-[8-(2-гидроксибензоил)аминооктановую кислоту, функционально эффективную соль любого из вышеперечисленных, производное любого из вышеперечисленных или любое их сочетание.
В некоторых вариантах осуществления терапевтическое средство представляет собой цисплатин или другое соединение платины (например, сатраплатин, пикоплатин, недаплатин, триплатин, карбоплатин или оксаплатин) и при этом средство, усиливающее внутриклеточное проникновение, представляет собой 6-оксо-6-фенилгексановую кислоту, N-[8-(2-гидроксибензоил)аминооктановую кислоту, соль или производное любого из вышеперечисленных или любое их сочетание.
В вариантах осуществления вышеуказанные способы дополнительно включают введение терапевтически эффективного количества иммунотерапевтического средства. В некоторых вариантах осуществления иммунотерапевтическое средство представляет собой противораковую вакцину, гормон, эпитоп, цитокин, опухолевый антиген, стимулятор CD4-клеток, агонист NKT клеток или адъювант. Например, иммунотерапевтическое средство может представлять собой интерферон, интерлейкин, фактор некроза опухолей, овальбумин, Neuvenge®, онкофаг, CimaVax-EGF, мобилан, α-Gal гликолипид, α-галактозилцерамид (α-GalCer), β-маннозилцерамид (β-ManCer), доставляемые аденовирусами вакцины, от компании Celldex CDX1307 и CDX1401, GRNVAC1, вакцины на основе вирусов, от компании Advaxis MVA-BN, PROSTVAC®, ADXS11-001, ADXS31-001, ADXS31-164, BiovaxID, фолат-связывающий белок (E39), гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF) с и без E75 (NeuVax) или OncoVEX, трастузумаб, Ae-37, IMA901, SC1B1, стимувакс, пептиды, способные вызывать ответ цитотоксических лимфоцитов, пептидные вакцины, включая вакцину на основе теломеразных пептидов (GV1001), пептидов сурвивина, пептидов MUC1, пептидов ras, пептидов с усиленным эпитопом TARP 29-37-9V, ДНК вектор pPRA-PSM с синтетическими пептидами E-PRA и E-PSM, вакцину Ad.p53 DC, плазмидную ДНК NY-ESO-1 (pPJV7611), генетически модифицированные аллогенные (человеческие) клетки опухолей для экспрессии IL-1, IL-7, GM-CSF, CD80 или CD154, вакцину против рака поджелудочной железы HyperAcute(R) (компоненты HAPa-1 и HAPa-2), Melaxin (аутологичная вакцина на основе дендритом) и BCG, GVAX (CG8123), модифицированные по CD40-лиганду и гену IL-2 аутологичные кожные фибробласты и клетки опухолей, ALVAC-hB7.1, от компании Vaximm Gmbh VXM01, от компании Immunovative Therapies AlloStim-7, ProstAtak™, TG4023 (MVA-FCU1), от компании Antigenic HSPPC-96, от компании Immunovaccine Technologies DPX-0907, которая состоит из специфических HLA-A2-рестрицированных пептидов, универсальный T-хелперный пептид, полинуклеотидный адъювант, липосомы и монтанид (ISA51 VG), GSK2302032A, от компании Memgen ISF35, от компании Avax OVax: вакцину на основе DNP-модифицированных аутологичных клеток яичников, Theratope®, Ad100-gp96Ig-HLA A1, от компании Bioven вакцину на основе рекомбинантного человеческого rEGF-P64K/монтанида, TARP 29-37 или от компании Dendreon DN24-02.
В некоторых вариантах осуществления иммунотерапевтическое средство представляет собой α-Gal гликолипид.
В некоторых вариантах осуществления иммунотерапевтическое средство представляет собой β-ManCer, содержащий фрагмент сфингозина и фрагмент жирной кислоты, содержащий линейную или разветвленную, насыщенную или ненасыщенную алифатическую углеводородную группу, имеющую от примерно 8 до примерно 49 атомов углерода. В связанных вариантах осуществления фрагмент жирной кислоты содержит линейную или разветвленную, насыщенную или ненасыщенную алифатическую углеводородную группу, имеющую от примерно 8 до примерно 15 атомов углерода. В других связанных вариантах осуществления фрагмент жирной кислоты содержит линейную или разветвленную, насыщенную или ненасыщенную алифатическую углеводородную группу, имеющую от примерно 18 до примерно 30 атомов углерода. β-ManCer имеет следующую структуру:
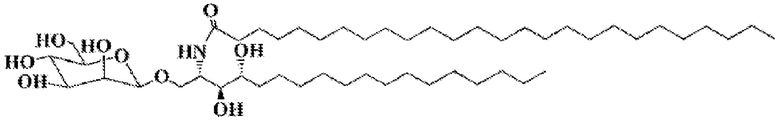 .
.
В вышеуказанных вариантах осуществления иммунотерапевтическое средство усиливает терапевтическое действие терапевтического средства. Например, иммунотерапевтическое средство дополнительно замедляет рост опухоли или дополнительно уменьшает опухоль.
В некоторых вариантах осуществления иммунотерапевтическое средство вводят после введения терапевтического средства и средства, усиливающего внутриклеточное проникновение. В других вариантах осуществления, иммунотерапевтическое средство вводят одновременно с первым введением терапевтического средства и средства, усиливающего внутриклеточное проникновение.
В вариантах осуществления иммунотерапевтическое средство вводят локально, регионально или системно. Например, иммунотерапевтическое средство можно вводить внутрибрюшинно. Иммунотерапевтическое средство можно также вводить интратуморально.
В любом из вышеуказанных аспектов и вариантов осуществления терапевтическое средство и средство, усиливающее внутриклеточное проникновение, могут быть связаны.
В аспектах изобретения вышеуказанные способы могут дополнительно включать получение субъектом стандартного лечения. В вариантах осуществления стандартное лечение представляет собой хирургическую операцию, радиационную терапию, радиочастотное воздействие, криогенное воздействие, ультразвуковую абляцию, системную химиотерапию или их сочетание.
В любом из вышеуказанных аспектов и вариантов осуществления введение терапевтического средства, средства, усиливающего внутриклеточное проникновение, или иммунотерапевтического средства можно осуществлять с помощью системы визуализации (например, рентгеновской компьютерной томографии (КТ), рентгеноскопии, магнитно-резонансной томографии (МРТ), ультразвукового исследования или позитронной эмиссионной томографии (ПЭТ)/компьютерной томографии (КТ)).
В других аспектах изобретение включает способы визуализации одной или более опухолей при помощи системы визуализации, выбранной из группы, состоящей из рентгеновской компьютерной томографии (КТ), рентгеноскопии, магнитно-резонансной томографии (МРТ), ультразвукового исследования или позитронной эмиссионной томографии (ПЭТ)/компьютерной томографии (КТ), определение объема одной или более опухолей и расчет на основании определенного объема опухолей терапевтически эффективного специфичного для опухоли количества доз терапевтического средства и средства, усиливающего внутриклеточное проникновение. В некоторых вариантах осуществления в каждую или в несколько из одной или более опухолей можно интратуморально вводить совместно терапевтически эффективную специфичную для опухоли дозу терапевтического средства и средства, усиливающего внутриклеточное проникновение, рассчитанную для данной опухоли.
В любом из вышеуказанных аспектов и вариантов осуществления субъект может быть млекопитающим (например, человеком, собакой, кошкой, лошадью, коровой, овцой, козой, свиньей, мышью, крысой, морской свинкой или обезьяной).
Изобретение также относится к способам лечения субъекта, который нуждается в этом (например, субъекта, имеющего опухоль), с помощью эффективного количества средства, усиливающего внутриклеточное проникновение.
В некоторых аспектах изобретение относится к способам уничтожения злокачественных клеток в организме субъекта (например, субъекта, имеющего опухоль). В вариантах осуществления способы включают введение эффективного количества средства, усиливающего внутриклеточное проникновение.
В некоторых аспектах изобретение относится к способам лечения опухоли у субъекта. В вариантах осуществления способы включают введение эффективного количества средства, усиливающего внутриклеточное проникновение.
В некоторых аспектах изобретение относится к способам подавления роста опухоли у субъекта. В вариантах осуществления способы включают введение эффективного количества средства, усиливающего внутриклеточное проникновение.
В любом из вышеуказанных аспектов и вариантов осуществления средство, усиливающее внутриклеточное проникновение, можно вводить субъекту локально или регионально.
В вариантах осуществления опухоль представляет собой солидную опухоль. В некоторых вариантах осуществления опухоль образовала метастазы.
В вариантах осуществления опухоль представляет собой карциному или саркому. В связанных вариантах осуществления опухоль представляет собой карциному или саркому кожи, кости, мышцы, молочной железы, ротовой полости, органа, почки, печени, легких, желчного пузыря, поджелудочной железы, головного мозга, пищевода, мочевого пузыря, толстого кишечника, тонкого кишечника, селезенки, желудка, предстательной железы, яичек, яичников или матки. В некоторых вариантах осуществления опухоль представляет собой карциному или саркому поджелудочной железы.
В вариантах осуществления средство, усиливающее внутриклеточное проникновение, вводят интратуморально.
В вышеуказанных аспектах и вариантах осуществления способы могут приводить к замедлению роста опухоли, уменьшению опухоли или ликвидации опухоли. Например, масса опухоли не увеличивается. В некоторых вариантах осуществления опухоль уменьшается на 10%, 25%, 50%, 75%, 85%, 90%, 95% или 99% или более (или на любое промежуточное количество) по сравнению с ее исходной массой.
В вышеуказанных аспектах и вариантах осуществления способы могут предотвращать метастазирование опухоли.
В любом из вышеуказанных аспектов и вариантов осуществления эффективное количество средства, усиливающего внутриклеточное проникновение, можно выбирать, исходя из объема и типа опухоли.
В вариантах осуществления способы включают введение средства, усиливающего внутриклеточное проникновение, в первый день и повторное введение в один или более последующих дней. В связанных вариантах осуществления первый день и один или более последующих дней разделены интервалом от 1 дня до примерно 3 недель.
В вышеуказанных аспектах и вариантах осуществления средство, усиливающее внутриклеточное проникновение, может представлять собой химическое соединение, которое усиливает пассивный транспорт терапевтического соединения в клетку.
В вариантах осуществления средство, усиливающее внутриклеточное проникновение, представляет собой функционализированную кетокислоту, 6-оксо-6-фенилгексановую кислоту, 8-оксо-8-фенилоктановую кислоту, 8-(2,5-дихлорфенил)-8-оксооктановую кислоту, функционализированный кетоэфир или альдегид, модифицированную аминокислоту, модифицированные аминокислоты, N-[8-(2-гидроксибензоил)аминооктановую кислоту, N-[8-(2-гидроксибензоил)аминодекановую кислоту, N-(5-хлорсалицилоил)-8-аминокаприловую кислоту, N-[4-(4-хлор-2-гидроксибензоил)аминобутановую кислоту, 2-этилгексил-2-гидроксибензоат, 5-циклогексил-5-оксовалериановую кислоту, 6-циклогексил-6-оксогексановую кислоту, 7-циклогексил-7-оксогептановую кислоту, 8-циклогексил-8-оксооктановую кислоту, 4-циклопентил-4-оксомасляную кислоту, 5-циклопентил-5-оксовалериановую кислоту, 6-циклопентил-6-оксогексановую кислоту, 7-циклопентил-7-оксогептановую кислоту, 8-циклопентил-8-оксооктановую кислоту, 4-циклобутил-4-оксомасляную кислоту, 5-циклобутил-5-оксовалериановую кислоту, 6-циклобутил-6-оксогексановую кислоту, 7-циклобутил-7-оксогептановую кислоту, 8-циклобутил-8-оксооктановую кислоту, 4-циклопропил-4-оксомасляную кислоту, 5-циклопропил-5-оксовалериановую кислоту, 6-циклопропил-6-оксогексановую кислоту, 7-циклопропил-7-оксогептановую кислоту, 8-циклопропил-8-оксооктановую кислоту, 8-[(3-метилциклогексил)окси]октановую кислоту, 7-[(3-метилциклогексил)окси]гептановую кислоту, 6-[(3-метилциклогексил)окси]гексановую кислоту, 5-[(3-метилциклогексил)окси]пентановую кислоту, 4-[(3-метилциклогексил)окси]бутановую кислоту, 3-[(3-метилциклогексил)окси]пропановую кислоту, октисалат, дикетопиперазины, сапонин, ацилкарнитин, алканоилхолин, тауродигидрофузидат, сульфоксид, оксазолидинон, пирролидон, спирт или алканол, бензойную кислоту, гликоль, поверхностно-активное вещество, терпен или их функционально эффективную соль, производное или сочетание.
В некоторых вариантах осуществления средство, усиливающее внутриклеточное проникновение, представляет собой 6-оксо-6-фенилгексановую кислоту, 8-циклогексил-8-оксооктановую кислоту, N-[8-(2-гидроксибензоил)аминооктановую кислоту или их функционально эффективную соль или производное.
В вышеуказанных аспектах и вариантах осуществления субъект может быть млекопитающим (например, человеком, собакой, кошкой, лошадью, коровой, овцой, козой, свиньей, мышью, крысой, морской свинкой или обезьяной).
Кроме того, изобретение относится к фармацевтическим композициям для использования в способах, описанных в настоящем документе. В вариантах осуществления композиция оптимизирована для интратуморального введения. В других вариантах осуществления средство, усиливающее внутриклеточное проникновение, и терапевтическое средство совместно вводят интратуморально.
Эти и другие варианты осуществления описаны или станут очевидными из следующего далее подробного описания.
Определения и использование терминов
Настоящее изобретение может стать более понятным из следующего далее подробного описания изобретения и включенных в него примеров. Перед тем, как будут раскрыты и описаны настоящие способы и методики, следует понимать, что данное изобретение не ограничено конкретными методами анализа или синтеза, поскольку они могут, безусловно, варьироваться. Также следует понимать, что терминология, используемая в настоящем документе, предназначена только для описания конкретных вариантов осуществления и не должна быть ограничивающей. Если не указано иное, все технические и научные термины, используемые в настоящем документе, имеют то же значение, которое им обычно придают специалисты в области, к которой относится изобретение.
«Средство» или «терапевтическое средство» означает любое низкомолекулярное химическое соединение, антитело, молекулу нуклеиновой кислоты или полипептид, или их фрагменты.
«Облегчать» означает уменьшать, подавлять, ослаблять, сокращать, останавливать или стабилизировать развитие или прогрессирование заболевания или его симптома.
«Аналог» означает молекулу, которая не является идентичной, но имеет аналогичные функциональные или структурные признаки. Например, аналог полипептида сохраняет биологическую активность соответствующего природного полипептида при том, что имеет некоторые биохимические модификации, которые усиливают функцию аналога по сравнению с природным полипептидом. Такие биохимические модификации могут повышать устойчивость аналога к протеазам, способность проникать через мембраны или время полужизни, не изменяя, например, связывание лиганда. Аналог может содержать искусственную аминокислоту.
Используемый в настоящем документе термин «интерферирующая РНК» относится к любой последовательности двухцепочечной или одноцепочечной РНК, способной либо непосредственно, либо косвенно (т.е., после преобразования) ингибировать или подавлять экспрессию гена, опосредуя РНК-интерференцию. Интерферирующая РНК включает, но не ограничивается ими, короткие интерферирующие РНК («киРНК») и короткие шпилечные РНК («кшРНК»). «РНК интерференция» означает избирательную деградацию совместимого с последовательностью транскрипта матричной РНК.
Используемый в настоящем документе термин «кшРНК» (короткая шпилечная РНК) означает молекулу РНК, содержащую антисмысловую область, петлевую часть и смысловую область, при этом смысловая область имеет комплементарные нуклеотиды, которые спариваются с антисмысловой областью, образуя дуплекс-стебель. После посттранскрипционного процессинга короткая шпилечная РНК превращается в короткую интерферирующую РНК в результате расщепления, опосредуемого ферментом Dicer, который является членом семейства РНКазы III.
Используемый в настоящем документе термин «РНКи» (РНК-интерференция) относится к механизму посттранскрипционного сайленсинга, инициируемого молекулами короткой двухцепочечной РНК, которые подавляют экспрессию генов с гомологией последовательностей.
Используемый в настоящем документе термин «противоопухолевая терапия» относится к любой терапии для замедления роста или метастазирования опухоли, включая хирургическую операцию, радиационную и/или химиотерапию.
Используемый в настоящем документе термин «измененный по сравнению с контролем» образец или субъект означает, что он имеет определяемый аналитический или диагностический, или терапевтический индикатор на уровне, который статистически достоверно отличается от уровня в нормальном, не подвергнутом воздействию или контрольном образце. Контрольный образец включает, например, клетки в культуре, одно или более лабораторных экспериментальных животных, или одного или более субъектов-людей. Способы выбора и тестирования контрольных образцов находятся в пределах квалификации специалистов в данной области. Аналитическое вещество может быть природным веществом, которое характерным образом экспрессируется или продуцируется клеткой или организмом (например, антитела, патогенные пептиды или частицы и тому подобное), или веществом, продуцируемым репортерным конструктом (например, β-галактозидазой или люциферазой). В зависимости от метода, используемого для обнаружения, количество и показатели изменения могут варьироваться. Определение статистической значимости находится в пределах компетенции специалистов в данной области.
Используемый в настоящем документе термин «со-введение» или «совместное введение», и тому подобное, относится к процессу введения двух или более средств (например, терапевтического средства с усиливающим проникновение средством), соединений, терапевтических препаратов, или тому подобного, одновременно или почти одновременно. Порядок или последовательность введения различных средств по изобретению, например, химиотерапевтических средств, усиливающих внутриклеточное проникновение средств или иммунотерапевтических средств, могут варьироваться и не ограничиваются какой-либо конкретной последовательностью. «Совместное введение» может также относиться к ситуации, когда два или более средств вводят в различные участки тела или различными способами доставки, например, когда первое средство вводят системно и второе средство вводят интратуморально или когда первое средство вводят интратуморально и второе средство вводят системно в кровь или близко к опухоли. «Совместное введение» может также относиться к ситуации, когда два или более средств вводят одним и тем же способом доставки, например, когда первое средство вводят интратуморально и второе средство вводят интратуморально.
Используемые в настоящем документе термины «содержит» «содержащий», «заключающий в себе» и «имеющий», и тому подобные, являются неограничивающими, как определено в патентном законе США, и могут означать «включает», «включающий» и тому подобное; аналогично, термин «состоящий в основном из» или «состоит в основном из» имеет значение, определенное в патентном законе США, и данный термин является неограничивающим, допуская присутствие кое-чего помимо того, что уже было перечислено, при условии, что основные или новые характеристики того, что было перечислено, не изменятся от присутствия кое-чего помимо того, что уже было перечислено, однако исключение составляют варианты осуществления предшествующего уровня техники.
«Создание контакта с клеткой» означает в данном документе доставку средства к клетке, например, клетке, на которую предстоит воздействовать в культуре, ex vivo или в организме животного, таким образом, что средство может взаимодействовать с клеткой (например, клеткой, на которую предстоит воздействовать), потенциально быть поглощенным клеткой и оказывать воздействие на клетку. Средство (например, адъювант) можно доставлять к клетке непосредственно (например, добавляя средство в среду для культивирования или вводя инъекцией в интересующую клетку, ткань или опухоль) или доставлять в организм топическим или парентеральным путем введения для доставки в клетку при помощи кровеносной, лимфатической систем или другими способами. Специалисту в данной области будет легко понять, что введение терапевтического средства субъекту включает создание контакта терапевтического средства с клеткой, опухолью, или тканью субъекта.
Используемый в настоящем документе термин «связанные» применительно к двум или более средствам, которые «связаны» вместе, относится к ковалентной или другой стабильной ассоциации между двумя или более средствами. Например, терапевтическое средство может быть связано со средством, усиливающим внутриклеточное проникновение, ковалентной связью, ковалентно связанным фрагментом линкера или нековалентно через ионные взаимодействия или водородные связи. Одно или более средств, связанных вместе, в значительной степени сохраняют свои независимые функции и характеристики. Например, терапевтическое средство, будучи связанным с другим средством, может сохранять свою активность в такой же степени, как если бы оно было независимым.
«Цикл» или «лекарственный цикл» означает повторяющееся введение доз в течение определенного периода времени, который может составлять от нескольких минут до нескольких часов, дней, недель, месяцев или даже лет.
«Цитокин» означает гормон, который действует локально и который модулирует иммунный ответ индивидуума.
Используемый в настоящем документе термин «цитотоксическое средство» относится к любому средству, способному разрушать клетки, предпочтительно делящиеся клетки, такие как раковые клетки.
Используемый в настоящем документе термин «обнаруживающий», «обнаружение» и тому подобное означает, что проводят анализ для определения одной или более характеристик образца, например, определения наличия, отсутствия или количества аналита, который должен быть обнаружен. Например, обнаружение может включать определение конкретного аналита в образце или активности средства в образце. Обнаружение может включать определение наличия нуклеиновой кислоты, белка (например, антитела, цитокина и тому подобного) методом ПЦР, иммуноанализа (например, ELISA), микроскопии, проверочным заражением патогенами и тому подобным. Количество аналита или активность, обнаруженная в образце, могут быть равны нулю или быть ниже предела обнаружения данного анализа или метода.
«Заболевание» означает любое состояние или нарушение, которое наносит вред или препятствует нормальному функционированию клетки, ткани или органа. Иллюстративным заболеванием является рак.
Используемые в настоящем документе термины «эффективное количество», «терапевтически эффективное количество» или «фармацевтически эффективное количество» относятся к количеству средства или соединения, которое достаточно для лечения заболевания, например, рака. В некоторых вариантах осуществления результатом является уменьшение и/или ослабление признаков, симптомов или причин заболевания, или любое другое желаемое изменение биологической системы. Например, «эффективное количество» для терапевтического применения представляет собой количество композиции, содержащей соединение, раскрытое в настоящем документе, необходимое для достижения клинически значимого ослабления заболевания. «Эффективное количество» или терапевтически эффективное количество средства или сочетания средств по изобретению может также представлять собой такое количество или дозу, которые эффективны для значительного уменьшения или уничтожения опухоли, или создания возможности ее хирургического удаления. Соответствующее «эффективное» количество в каждом отдельном случае определяют с использованием любого подходящего метода (например, исследования с увеличением дозы), и оно будет зависеть от решения лечащего врача. Однако подходящие диапазоны доз легко могут быть определены специалистом в данной области.
Для достижения эффективной дозы может потребоваться более одной дозы. Понятно, что эффективная доза в одной популяции может быть или не быть достаточной во всех популяциях. Таким образом, применительно к введению терапевтического средства, терапевтическое средство является «эффективным против» заболевания или состояния, когда введение клинически подходящим образом приводит к достижению у по меньшей мере статистически значимой фракции субъектов благотворного эффекта, такого как предотвращение начала заболевания, ослабление симптомов, излечение, уменьшение проявлений признаков или симптомов заболевания, увеличение продолжительности жизни, улучшение качества жизни, или другого эффекта, обычно признаваемого как положительный врачами, сведущими в лечении конкретного типа заболевания или состояния.
Термин «увеличивает» означает изменение в положительную сторону на по меньшей мере 10%, 25%, 50%, 75%, 100% или на любое промежуточное количество.
Используемый в настоящем документе термин «рост» относится к любой ткани или органу, который содержит клеточную массу, для которой, как считают, характерна аномальная пролиферация. Такой рост может быть канцерогенным, не канцерогенным, злокачественным или не злокачественным. Если термин «рост» используют в случае злокачественного заболевания, речь может идти об опухоли. Такие опухоли могут быть солидными или несолидными.
Используемый в настоящем документе термин «иммуноанализ» означает способ обнаружения, основанный на специфическом связывании по меньшей мере одного антитела с антигеном, например, ELISA, RIA, вестерн-блоттинг и тому подобное.
Используемые в настоящем документе термины «иммуноген», «иммуногенный», и тому подобное, относятся к веществам, которые способны стимулировать иммунный ответ, например, гуморальный или клеточный иммунный ответ, у по меньшей мере одного организма.
«Иммуногенная композиция» означает композицию, содержащую молекулу, способную индуцировать или модулировать иммунный ответ у субъекта. Такой иммунный ответ может быть профилактическим или терапевтическим иммунным ответом. В вариантах осуществления иммуногенная композиция представляет собой вакцину или агонист T-клеток.
Используемый в настоящем документе термин «иммунотерапевтическое средство» относится к любому средству, соединению или биологическому веществу, которое способно модулировать функции иммунной системы хозяина. Например, иммунотерапевтическое средство способно вызывать стимуляцию иммунной системы против клетки опухоли.
Используемый в настоящем документе термин «индукция иммунитета» относится к любому иммунному ответу, развивающемуся против антигена. В вариантах осуществления иммунитет опосредован вырабатываемыми позвоночными (например, человеком) антителами против инфекционного агента, которые предотвращают или ослабляют инфекцию или уменьшают проявление по меньшей мере одного ее симптома. Иммуногенные композиции по изобретению могут стимулировать выработку антител, которые, например, нейтрализуют инфекционные агенты, препятствуют проникновению инфекционных агентов в клетки, блокируют репликацию инфекционных агентов и/или защищают клетки-хозяева от инфекции и разрушения. Термин может также относиться к иммунному ответу, опосредуемому T-лимфоцитами и/или другими лейкоцитами, против инфекционного агента, который развивается у позвоночных (например, человека) и предотвращает или ослабляет инфекцию, или уменьшает проявление по меньшей мере одного ее симптома.
Используемый в настоящем документе термин «внутрь» относится к успешному проникновению молекулы через клеточную мембрану или в нее. Например, вирусный вектор можно вводить в клетку солидной опухоли в таких условиях, что клетка опухоли становится трансфицированной. В другом примере гликолипид можно вводить в клетку солидной опухоли в таких условиях, что гликолипид становится встроенным в фосфолипидную двухслойную мембрану клетки. В еще одном примере антиген или вектор, кодирующий антиген, можно вводить в клетку солидной опухоли в таких условиях, что гликолипид становится встроенным в фосфолипидную двухслойную мембрану клетки.
Используемый в настоящем документе термин «средство, усиливающее внутриклеточное проникновение» означает соединение, молекулу, вещество или тому подобное, которые увеличивают прохождение терапевтического средства через клеточную мембрану, например, клетки солидной опухоли, и таким образом, делают возможным воздействие терапевтического средства на компоненты (например, белки, ДНК, клеточный аппарат) внутриклеточной среды.
Используемый в настоящем документе термин «выделенная» относится к любой композиции, молекуле или смеси, к которой были применены лабораторные методы очистки, включая, но не ограничиваясь ими, экстрагирование, центрифугирование, хроматографическое разделение (т.е., например, тонкослойную хроматографию или высокоэффективную жидкостную хроматографию). Как правило, такой метод очистки приводит к получению композиции, молекулы или смеси, выделенной на основании физических, химических свойств или наличия электрического потенциала. В зависимости от выбора метода выделенная композиция, молекула или смесь может содержать другие композиции, соединения или смеси, имеющие аналогичные химические свойства. Например, выделенная композиция, молекула или смесь может содержать 1-20%, 1-10% или 1-5% композиций или смесей, имеющих аналогичные химические свойства. В одном варианте осуществления выделенная композиция или смесь содержит смесь гликолипидов, свободную от холестерина и фосфолипидов. В одном варианте осуществления выделенная композиция или смесь содержит гликолипиды, имеющие 5-15 гликозидных связей.
Используемый в настоящем документе термин «локальный» или «локально», как в случае локального введения или совместного ведения одного или более терапевтических препаратов, означает доставку терапевтического средства в участок тела, который находится близко или рядом с зоной опухоли, в прилегающей области или в непосредственной близости от зоны опухоли, по периметру или в контакте с опухолью, либо внутри или в глубине самой опухоли. Доставку терапевтического средства в опухоль можно также назвать «интратуморальным» введением. Локальное введение, как правило, исключает системные пути введения.
Используемый в настоящем документе термин «неоперабельная» относится к любой части органа или структуры организма, которую невозможно удалить хирургическим путем. Например, «неоперабельная опухоль» может представлять собой опухоль, физически недостижимую обычными хирургическими методами, или опухоль в случае, когда ее удаление не улучшит общее состояние пациента, больного раком.
Используемый в настоящем документе термин «нуклеиновая кислота», например, нуклеиновая кислота для доставки в клетку, имеет свое обычное значение, принятое в данной области, т.е., полинуклеотид или олигонуклеотид, что означает цепочку из по меньшей мере двух сочетаний основание-сахар-фосфат. Нуклеотиды являются мономерными единицами полимеров нуклеиновых кислот. Термин включает дезоксирибонуклеиновую кислоту (ДНК) и рибонуклеиновую кислоту (РНК) в форме олигонуклеотидной матричной РНК, антисмысловой, плазмидной ДНК, частей плазмидной ДНК, генетического материала вирусного происхождения и тому подобного. Полинуклеотиды включают нуклеиновые кислоты из по меньшей мере двух мономеров. Антисмысловые полинуклеотиды представляют собой нуклеиновые кислоты, которые препятствуют функции ДНК или РНК. киРНК или кшРНК представляет собой двухцепочечную РНК, которая ингибирует или нарушает активность или трансляцию, например, стимулирует деградацию или изменяет сплайсинг или процессинг клеточной нуклеиновой кислоты, например, мРНК, микроРНК и тому подобного, которые являются ее мишенью. При использовании в настоящем документе киРНК и кшРНК включают любую двухцепочечную молекулу РНК, которая может модулировать стабильность, трансляцию или сплайсинг РНК, с которой гибридизуется по меньшей мере одна цепь двухцепочечной нуклеиновой кислоты. РНК хорошо известны в данной области, см., например, патентные публикации WO 02/44321, WO/2003/099298, US 20050277610, US 20050244858 и патенты США 7297786, 7560438 и 7056704, содержание всех из которых включено в настоящий документ посредством ссылки. Следует понимать, что нуклеиновая кислота, описанная в настоящем документе, включает искусственные нуклеотиды (не существующие в природе), например: производные природных нуклеотидов, такие как фосфотионаты или пептидо-нуклеиновые кислоты (такие как те, которые описаны в патентах и патентных заявках, приведенных выше). Нуклеиновую кислоту можно доставлять в клетку для осуществления изменения в клетке, которое является терапевтическим. Доставку нуклеиновой кислоты или другого генетического материала для терапевтических целей называют генной терапией. Нуклеиновая кислота может экспрессировать белок или полипептид, например, белок, который отсутствует или является нефункциональным в клетке или в организме субъекта. Нуклеиновая кислота может быть одно- или двухцепочечной, может быть смысловой или антисмысловой и может быть доставлена в клетку в виде «голой» ДНК в сочетании со средствами, стимулирующими поступление нуклеиновой кислоты в клетку (например, реагентами для трансфекции), в контексте вирусного вектора и тому подобного. Нуклеиновая кислота может быть нацелена на нуклеиновую кислоту, которая является эндогенной для клетки (мРНК или микроРНК), или гетерологичную нуклеиновую кислоту (например, нуклеиновую кислоту патогена, такую как вирусный ген). Доставка нуклеиновой кислоты означает перенос нуклеиновой кислоты из внешней для субъекта среды через наружную клеточную мембрану в клетку субъекта.
«Получение» в настоящем документе означает производство, закупку, синтезирование, выделение, очистку или иной способ приобретения.
Используемый в настоящем документе термин «фармацевтически приемлемый» относится к материалу (например, носителю или разбавителю), который не нарушает биологическую активность или свойства соединений, описанных в настоящем документе, и является относительно нетоксичным (т.е., материал вводят индивидууму, не вызывая нежелательных биологических эффектов или взаимодействия неблагоприятным образом с любым из компонентов композиции, в которой он содержится).
Выражение «фармацевтически приемлемый носитель, эксципиент или разбавитель» является признанным в данной области и включает фармацевтически приемлемый материал, композицию или носитель, подходящие для введения соединений по настоящему изобретению млекопитающим. Используемый в настоящем документе термин «фармацевтически приемлемый» означает одобренный регулирующим органом федерального или государственного правительства или перечисленный в фармакопее США, европейской фармакопее или других общепризнанных фармакопеях для применения к млекопитающим, например, людям.
Используемый в настоящем документе термин «фармацевтически эффективный режим» означает систематический план введения одного или более терапевтических средств, который включает такие аспекты, как тип терапевтического средства, концентрации терапевтического средства, концентрации, количества или уровни интратуморального усилителя, основанные на типе, расположении или размере опухоли, расписание и повторение введения, а также любые изменения в нем, сделанные во время курса введения лекарственного средства, которое при введении является эффективным в лечении опухоли и/или ее метастазов. Такие соображения зависит от решения лечащего врача, и легко могут быть определены специалистом в данной области.
Используемый в настоящем документе термин «пролиферативное заболевание» означает заболевание, при котором рост какой-либо популяции клеток превышает и не согласуется с ростом окружающих клеток. В некоторых случаях пролиферативное заболевание приводит к образованию опухоли. В некоторых вариантах осуществления опухоль является доброкачественной, предзлокачественной или злокачественной. В некоторых вариантах осуществления пролиферативное заболевание представляет собой рак поджелудочной железы. В некоторых вариантах осуществления пролиферативное заболевание представляет собой предзлокачественный рост клеток поджелудочной железы.
Используемый в настоящем документе термин «полипептид» или «пептид» следует понимать как две или более независимо выбранные природные или искусственные аминокислоты, связанные ковалентной связью (например, пептидной связью). Пептид может содержать 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более природных или искусственных аминокислот, связанных пептидными связями. Описанные в настоящем документе полипептиды включают полноразмерные белки (например, полностью процессированные белки), а также более короткие аминокислотные последовательности (например, фрагменты природных белков или фрагменты синтетических полипептидов).
Диапазоны, приведенные в настоящем документе, следует понимать как сокращенное обозначение всех значений в диапазоне. Например, следует понимать, что диапазон от 1 до 50 включает любое число, сочетание чисел или поддиапазон из группы, состоящей из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49 или 50, а также все промежуточные десятичные значения между вышеуказанными целыми числами, такие как, например, 1,1, 1,2, 1,3, 1,4, 1,5, 1,6, 1,7, 1,8 и 1,9. Что касается поддиапазонов, специально предусмотрены «вложенные поддиапазоны», которые простираются от каждой конечной точки диапазона. Например, вложенный поддиапазон иллюстративного диапазона от 1 до 50 может включать от 1 до 10, от 1 до 20, от 1 до 30 и от 1 до 40 в одном направлении, или от 50 до 40, от 50 до 30, от 50 до 20 и от 50 до 10 в другом направлении.
Термин «уменьшает» означает изменение в отрицательную сторону на по меньшей мере 10%, 25%, 50%, 75%, 100% или на любое промежуточное количество.
«Референс» означает стандартное или контрольное состояние.
Используемый в настоящем документе термин «режим» относится к различным параметрам, которые характеризуют то, каким образом лекарственное средство или препарат вводят, включая уровень доз, расписание и итерации, а также соотношение между различными лекарственными средствами или препаратами. Термин «фармацевтически эффективный режим» означает конкретный режим, который обеспечивает желаемый терапевтический результат или эффект, включая значительное уменьшение и/или уничтожение опухоли или клеток, которые метастазировали от нее. Термин «итерации» относится к общей концепции повторяющихся циклов введения одного или более средств. Например, пациент может получать сочетание лекарственного средства X и лекарственного средства Y (совместно введенных одновременно или почти одновременно и в любом порядке) в первый день в дозе Z. Затем лекарственные средства X и Y могут быть введены (совместно введены одновременно или почти одновременно и в любом порядке) вновь в дозе Z или другой дозе во второй день. Промежуток времени между первым и вторым днями может составлять 1 день или до нескольких дней, или неделю, или несколько недель или месяцев. Итеративные введения могут также иметь место в тот же день, разнесенные во времени на определенное количество минут (например, 10 минут, 20 минут, 30 минут или более) или часов (например, 1 час, 2 часа, 4 часа, 6 часов, 12 часов). Эффективный режим дозирования могут определять специалисты в данной области, например, лечащие врачи, с помощью стандартных методов.
Используемый в настоящем документе термин «образец» означает биологический материал, который был выделен из своего окружения (например, кровь или ткань от животного, клетки или кондиционированная среда от тканевой культуры). В вариантах осуществления образец предположительно содержит или известно, что содержит аналит, такой как инфекционный агент или интересующий белок (например, антитело, цитокин и тому подобное). Образец может также представлять собой частично очищенную фракцию ткани или жидкости организма. Референсный образец может быть «нормальным» образцом от донора, не имеющего заболевания или состояния, или полученным из нормальной ткани субъекта, имеющего заболевание или состояние, или субъекта, не получавшего лечение (например, субъекта, не получавшего вакцину). Референсный образец также может быть получен в «нулевой момент времени» до применения к клетке или субъекту средства или терапевтического вмешательства, которое предстоит тестировать.
Используемый в настоящем документе термин «избирательно» означает тенденцию к более высокой частоте встречаемости в одной популяции, чем в другой популяции.
Используемый в настоящем документе термин «солидная опухоль» относится к аномальной массе ткани, которая обычно не содержит кист или жидких областей. Солидные опухоли могут быть доброкачественными (не раковыми) или злокачественными (раковыми). Как правило, солидная опухоль ассоциируется с раком тканей организма, за исключением крови, костного мозга или лимфатической системы.
Термин «специфически связывается» означает узнавание и связывание с мишенью (например, полипептидом, клеткой и тому подобным), но при этом отсутствует существенное узнавание и связывание с другими молекулами в образце, например, биологическом образце.
Используемый в настоящем документе термин «субъект» относится к любому организму, у которого может развиться солидная опухоль. Такие организмы включают, но не ограничиваются ими, человека, собаку, кошку, лошадь, корову, овцу, козу, мышь, крысу, морскую свинку, обезьяну, птицу, рептилию и так далее.
Используемый в настоящем документе термин «значительно уменьшает или уничтожает» относится к ситуации, когда произошло уменьшение размера и/или массы опухоли или она была полностью ликвидирована или убита. В случае уменьшения опухоли, опухоль может уменьшиться по меньшей мере на примерно 10% или примерно 25%, или примерно 50%, или примерно 75%, или примерно 85%, или примерно 90%, или на примерно 95%, или на 99%, или более, или на любое промежуточное количество. В вариантах осуществления уменьшение является таким, что неоперабельная опухоль становится операбельной, если в этом есть необходимость. Значительное уменьшение можно также называть «регрессией», что означает уменьшение роста новообразования, такого как опухоль. Такое уменьшение можно определять по уменьшению измеряемых параметров, таких как, но не ограничиваясь ими, диаметр, масса (т.е., вес) или объем. Это уменьшение ни в коем случае не указывает на то, что размер уменьшен полностью, а только на то, что измеряемый параметр стал меньше в количественном выражении, чем при предыдущем определении.
В случае «значительного уничтожения» опухоли, данный термин может означать либо значительную ликвидацию фактических клеток опухоли, либо он может означать значительное уничтожение клеток опухоли, но при этом клетки не удаляются или ликвидируются, но остаются в организме в виде мертвых клеток и/или ткани. В случае значительной ликвидации, понятие означает полное разрушение клеток новообразования, такого как, например, солидная опухоль. Такое разрушение может включать внутриклеточный апоптоз и/или фагоцитоз макрофагами так, что новообразование полностью переваривается и выводится из организма.
Субъект, «страдающий или предположительно страдающий» конкретным заболеванием, состоянием или синдромом, имеет достаточное количество факторов риска или у него проявляются в достаточном количестве или сочетании признаки или симптомы заболевания, состояния или синдрома, так что компетентный специалист может диагностировать или предположить, что субъект страдает заболеванием, состоянием или синдромом. Способы выявления субъектов, страдающих или предположительно страдающих раком, находятся в пределах компетенции специалистов в данной области. Субъекты, страдающие или предположительно страдающие конкретным заболеванием, состоянием или синдромом, не обязательно относятся к двум разным группам.
Используемый в настоящем документе термин «подверженный» или «расположенный к» или «предрасположенный к» конкретному заболеванию или состоянию и тому подобному, относится к индивидууму, у которого на основании генетических, экологических, относящихся к состоянию здоровья и/или других факторов риска с большей вероятностью разовьется заболевание или состояние, чем у популяции в целом. Увеличение вероятности развития заболевания может быть увеличением на примерно 10%, 20%, 50%, 100%, 150%, 200% или более.
Используемый в настоящем документе термин «направляющий фрагмент» означает фрагмент, который может повышать способность терапевтического средства или другого средства по изобретению (например, средства, усиливающего внутриклеточное проникновение, или иммунотерапевтического средства) быть направленным к, связываться с, или проникать в клетку-мишень по изобретению (например, клетку раковой опухоли). В некоторых вариантах осуществления направляющие фрагменты представляют собой полипептиды, углеводы или липиды. Необязательно, направляющие фрагменты представляют собой антитела, фрагменты антител или нанотела. Иллюстративные направляющие фрагменты включают направляющие на опухоль фрагменты, такие как соматостатин (sst2), бомбезин/GRP, рилизинг гормон лютеинизирующего гормона (LHRH), нейропептид Y (NPY/Y1), нейротензин (NT1), вазоактивный интестинальный полипептид (VIP/VPAC1) и холицистокинин (CCK/CCK2). В некоторых вариантах осуществления направляющий фрагмент нековалентно связан со средством по изобретению.
Используемые в настоящем документе термины «лечение», «лечить», и тому подобные, относятся к получению желаемого фармакологического и/или физиологического эффекта. Эффект может быть профилактическим в случае полного или частичного предотвращения заболевания или его симптома, и/или может быть терапевтическим в случае частичного или полного излечения заболевания и/или неблагоприятного эффекта, относящегося к заболеванию. «Лечить рак или опухоль» или «лечение рака или опухоли» у млекопитающего означает одно или более из: ослабления симптома, корректирования лежащего в основе молекулярного или физиологического нарушения или снижения частоты или степени тяжести патологических или вредных физиологических последствий рака или опухоли у субъекта. В качестве примера, но без ограничения, вредные физиологические последствия рака или опухоли могут включать неконтролируемую пролиферацию, метастазы и прорастание в другие ткани, а также подавление иммунного ответа. Таким образом, лечение опухоли включает, но не ограничивается ими, подавление роста опухоли, ингибирование пролиферации клеток опухоли, уменьшение объема опухоли или подавление распространения клеток опухолей в другие части тела (метастазирование).
Используемый в настоящем документе термин «эпитопы α-gal», означает любую молекулу или часть молекулы с концевой структурой, содержащей Galα 1-3Galβ 1-4GlcNAc-R, Galα 1-3Galβ 1-3GlcNAc-R, или любую углеводную цепь с концевым фрагментом Galα 1-3Gal на невосстанавливающем конце.
Используемый в настоящем документе термин «гликолипиды» означает любую молекулу с по меньшей мере одной углеводной цепью, связанной с церамидом, цепью жирной кислоты или любым другим липидом. Альтернативно, гликолипид можно называть гликосфинголипидом.
Используемый в настоящем документе термин «α-1,3-галактозилтрансфераза» относится к любому ферменту, способному синтезировать эпитопы α-gal.
Используемый в настоящем документе термин «анти-Gal связывающий эпитоп» означает любую молекулу или часть молекулы, которая способна связывать in vivo природное анти-Gal антитело.
Термин «β-ManCer» означает β-маннозилцерамид, содержащий фрагмент сфингозина и фрагмент жирной кислоты, содержащий линейную или разветвленную, насыщенную или ненасыщенную алифатическую углеводородную группу, имеющую от примерно 8 до примерно 49 атомов углерода, от примерно 18 до примерно 49 атомов углерода, от примерно 8 до примерно 15 атомов углерода или от примерно 18 до примерно 30 атомов углерода. В вариантах осуществления β-ManCer имеет следующую структуру:
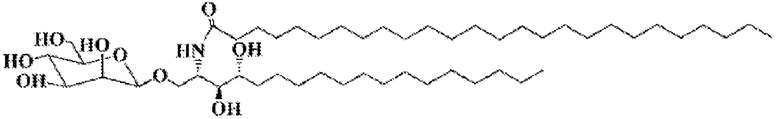 .
.
Используемый в настоящем документе термин «сфингозин» означает 2-амино-4-октадецен-1,3-диол, который представляет собой аминоспирт, имеющий 18 атомов углерода, с углеводородной цепью, которая образует основную часть молекулы церамида.
Используемый в настоящем документе термин «церамид» относится к одному из членов класса сфинголипидов, N-ацильных производных с длинными цепями насыщенных или ненасыщенных жирных кислот. Жирно-кислотный фрагмент церамидов может иметь длину углеводной цепи, начиная по меньшей мере примерно с восьми атомов углерода. В вариантах осуществления жирно-кислотный фрагмент β-ManCer может иметь где-то от по меньшей мере примерно восьми атомов углерода в длину. Например, он может иметь жирно-кислотный фрагмент от примерно 8 атомов углерода до примерно 49 атомов углерода в длину, или например, он может иметь жирно-кислотный фрагмент от примерно 8 атомов углерода до примерно 15 атомов углерода в длину. В других вариантах осуществления β-ManCer может иметь жирно-кислотный фрагмент от примерно 16 атомов углерода до примерно 30 атомов углерода в длину.
Используемое в настоящем документе и в прилагаемой формуле изобретения единственное число существительных включает соответствующее множественное число, если из контекста явно не следует иное. Таким образом, например, ссылка на «ген» является ссылкой на один или более генов и включает их эквиваленты, известные специалистам в данной области, и так далее.
Если специально не указано или не очевидно из контекста, используемый в настоящем документе термин «или» следует понимать как инклюзивный.
Если специально не указано или не очевидно из контекста, используемый в настоящем документе термин «примерно» следует понимать как отклонение в пределах допустимого в данной области диапазона, например, в пределах 2 стандартных отклонений от среднего значения. «Примерно» следует понимать как отклонение в пределах 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2%, 1%, 0,5%, 0,1%, 0,05% или 0,01% от указанного значения. Если иное не очевидно из контекста, ко всем числовым значениям, приведенным в настоящем документе, может быть применен термин «примерно».
В настоящем документе перечисление списка химических групп в любом определении переменной включает определения данной переменной как любой одной группы или сочетания перечисленных групп. В настоящем документе перечисление вариантов осуществления для переменной или аспекта включает данные варианты осуществления как любой один из вариантов осуществления или в сочетании с любыми другими вариантами осуществления или их частями.
Другие определения приводятся в контексте на протяжении всего данного описания.
Любые терапевтические средства, композиции или способы, приведенные в настоящем документе, можно комбинировать с одним или более из любых других терапевтических средств, композиций и способов, приведенных в настоящем документе.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Следующее подробное описание, приведенное в качестве примера, но не предназначенное для ограничения изобретения исключительно описанными конкретными вариантами осуществления, может быть понято лучше в сочетании с прилагаемыми чертежами.
На фигуре 1 приведены фотографии биолюминесцентных изображений мышей s.c.i.d. с обработанными люциферазой опухолями BxPc-3 поджелудочной железы.
На фигуре 2 приведена фотография ткани иссеченной опухоли BxPC, демонстрирующая проникновение 50 микролитров усилителя с красителем. 50 микролитров раствора усилителя с чернилами India были распределены в течение 2 минут с использованием программируемого шприца в опухоль BxPc объемом примерно 500 мм3 у мыши s.c.i.d.
На фигуре 3 приведена фотография ткани иссеченной опухоли BxPC, демонстрирующая проникновение 100 микролитров усилителя с красителем. 100 микролитров раствора усилителя с чернилами India были распределены в течение 2 минут с использованием программируемого шприцевого насоса в опухоль BxPc-3 объемом примерно 500 мм3 у мыши s.c.i.d.
На фигуре 4 приведен график, демонстрирующий показатели биолюминесценции (БЛВ) (BLI) для групп дозирования в примере 8 от исходного уровня до уровня через 72 часа.
На фигуре 5 приведен график, демонстрирующий относительное изменение биолюминесценции (БЛВ) от исходного уровня до уровня через 72 часа.
На фигуре 6 приведен график, демонстрирующий значения биолюминесценции (БЛВ) от исходного уровня до уровня в день 10 из примера 10.
На фигуре 7 приведен график, демонстрирующий относительные значения биолюминесценции (БЛВ) от исходного уровня до уровня в день 10 из примера 10.
На фигуре 8 приведен график, демонстрирующий изменения массы тела от исходного уровня до уровня в день 10 из примера 10.
На фигуре 9 приведен график, демонстрирующий прогрессирование объема опухоли для 120 животных, которые были подобраны по объему опухоли и распределены в 12 групп, при этом исходный средний объем опухоли перед дозированием в расчете на животное и на группу находился в диапазоне от 341 мм3 до 349 мм3. Линии, соответствующие каждой группе, указаны в подписи к фигуре.
На фигуре 10 приведен график Каплана-Мейера, демонстрирующий способность иллюстративных внутриклеточных составов по изобретению продлевать жизнь животных.
На фигурах 11A-11C приведены графики, демонстрирующие результаты иллюстративного исследования, в котором мышам, опухоли которых регрессировали до менее чем 18 мм3, были повторно инокулированы 1×106 клеток CT26 рака толстого кишечника мышей. На фигуре 11A показана динамика прогрессирования роста опухоли для отдельных ранее не подвергавшихся воздействию животных. На фигуре 11B показана динамика прогрессирования роста опухоли только для отдельных, с полным ответом и И/Т дозированных животных. На фигуре 11C показана средняя динамика роста опухоли для подобранного по возрасту контроля, животных с полным ответом, дозированных И/Т, и животных с полным ответом, дозированных И/Т, без разброса выборки.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новым региональным подходам к лечению рака.
Изобретение основано, по меньшей мере частично, на том открытии, что традиционные противораковые терапевтические средства на удивление являются более эффективными при локальном или региональном введении в сочетании со средством, усиливающим внутриклеточное проникновение. Изобретение также основано на открытии, что введение по меньшей мере одного иммунотерапевтического средства дополнительно увеличивает противораковые эффекты терапевтического средства и средства, усиливающего внутриклеточное проникновение (например, замедление роста опухоли и/или уменьшение размера опухоли).
Методы лечения
Хирургическая операция остается наиболее эффективным методом лечения рака; однако многие опухоли являются неоперабельными или имеют метастазы (например, только двадцать процентов раковых опухолей поджелудочной железы являются резектабельными). Кроме того, несмотря на абляцию (т.е., удаление всей окружающей здоровой ткани), после хирургической операции часто сохраняются остаточные клетки опухолей в той же зоне или клетки попадают в систему циркуляции. Эти свободные клетки часто приводят к образованию дополнительных опухолей либо вблизи, либо вдали от зоны исходной опухоли.
Дополнительные методы регионального лечения опухолей включают направленную доставку химиотерапевтических средств к области раковой опухоли, без оказания влияния на остальную часть тела. См. Collins, J.M., J. Clin. Oncol. 2: 498-504 (1984); Markman, M., Semin. Oncolo. 12: 38-42 (1985) и патентную публикацию США №2007/0196277, патент США №4619913, Oct 1986, Jia, Y: Int J Nanomedicine. 2012; 7: 1697-708, Kim J.I.: Biomaterials. 2012 Jun; 33(19): 4836-42; Hamstra, D.A.: J Neurooncol. 2005 Jul; 73(3): 225-38, McArdle Harwood Academic Publishers 2000 ISBN 90-5702-436-5). При этом обычные побочные эффекты химиотерапии, такие как тошнота, рвота, выпадение волос и инфекция, могут быть уменьшены. К сожалению, эти региональные подходы с использованием химиотерапевтического средства имели ограниченный успех, если вообще имели, с точки зрения улучшения результатов.
Как описано подробно в настоящем документе, было открыто новое региональное противораковое терапевтическое средство и метод дозирования, позволяющий преодолеть ограничения, связанные с современными методами лечения. Новые терапевтические методы включают локальное или региональное совместное введение терапевтического средства и средства, усиливающего внутриклеточное проникновение, субъекту, за счет чего достигаются высокие концентрации терапевтического средства в клетках опухолей. Способы доставки по настоящему изобретению сводят к минимуму воздействие на остальную часть тела цитотоксического терапевтического средства. Новые терапевтические методы также включают введение иммунотерапевтического средства. Иммунотерапевтическое средство, которое вводят до, во время или после доставки терапевтического средства и средства, усиливающего внутриклеточное проникновение, стимулирует иммунную систему и усиливает противораковые эффекты терапевтического средства и средства, усиливающего внутриклеточное проникновение.
В некоторых аспектах изобретение относится к способам индукции иммунного ответа у субъекта. Способы включают введение эффективного количества терапевтического средства и средства, усиливающего внутриклеточное проникновение. В вариантах осуществления субъект имеет опухоль. В вариантах осуществления терапевтическое средство и/или средство, усиливающее внутриклеточное проникновение, вводят субъекту локально или регионально.
В некоторых аспектах изобретение относится к способам модулирования иммунного ответа у субъекта. Способы включают введение эффективного количества терапевтического средства и средства, усиливающего внутриклеточное проникновение. В вариантах осуществления субъект имеет опухоль. В вариантах осуществления терапевтическое средство и/или средство, усиливающее внутриклеточное проникновение, вводят субъекту локально или регионально.
В некоторых аспектах изобретение относится к способам лечения опухоли у субъекта. Способы включают локальное или региональное совместное введение субъекту терапевтического средства и средства, усиливающего внутриклеточное проникновение.
В любом из вышеуказанных аспектов или вариантов осуществления опухоль может представлять собой солидную опухоль. В других вариантах осуществления опухоль образовывала метастазы. В вариантах осуществления опухоль представляет собой карциному или саркому. В связанных вариантах осуществления опухоль представляет собой карциному или саркому кожи, кости, мышцы, молочной железы, ротовой полости, органа, почки, печени, легких, желчного пузыря, поджелудочной железы, головного мозга, пищевода, мочевого пузыря, толстого кишечника, тонкого кишечника, селезенки, желудка, предстательной железы, яичек, яичников или матки. В некоторых вариантах осуществления опухоль представляет собой карциному поджелудочной железы или толстой кишки.
В любом из вышеуказанных аспектов или вариантов осуществления терапевтическое средство и/или средство, усиливающее внутриклеточное проникновение, можно вводить интратуморально.
В любом из вышеуказанных аспектов или вариантов осуществления способ может приводить к замедлению роста опухоли, уменьшению опухоли или ликвидации опухоли. В связанных вариантах осуществления опухоль уменьшается на 5%, 10%, 25%, 50%, 75%, 85%, 90%, 95% или 99% или более по сравнению с ее исходным размером.
В любом из вышеуказанных аспектов или вариантов осуществления способы могут включать введение терапевтического средства и/или средства, усиливающего внутриклеточное проникновение, в первый день и повторное введение в один или более последующих дней. В связанных вариантах осуществления терапевтическое средство и средство, усиливающее внутриклеточное проникновение, совместно вводят в первый день и повторно вводят в один или более последующих дней. В других связанных вариантах осуществления первый день и один или более последующих дней разделены интервалом от 1 дня до примерно 3 недель. В связанных вариантах осуществления терапевтическое средство и средство, усиливающее внутриклеточное проникновение, совместно вводят в соотношении примерно 1:2, 1:4, 1:10, 1:20, 1:25, 1:50, 1:100, 1:200 или в любом промежуточном соотношении (массовое отношение терапевтическое средство:средство, усиливающее внутриклеточное проникновение). Кроме того, в рамках данного изобретения предусмотрено, что терапевтическое средство и/или средство, усиливающее внутриклеточное проникновение, можно вводить в течение одного или более циклов.
В любом из вышеуказанных аспектов или вариантов осуществления терапевтическое средство и средство, усиливающее внутриклеточное проникновение, можно доставлять одновременно.
В любом из вышеуказанных аспектов или вариантов осуществления средство, усиливающее внутриклеточное проникновение, можно вводить до введения терапевтического средства.
В любом из вышеуказанных аспектов или вариантов осуществления терапевтическое средство представляет собой любое противораковое терапевтическое средство, хорошо известное в данной области. См., например, Anticancer Drugs: Design, Delivery and Pharmacology (Cancer Etiology, Diagnosis and Treatments) (eds. Spencer, P. & Holt, W.) (Nova Science Publishers, 2011); Clinical Guide to Antineoplastic Therapy: A Chemotherapy Handbook (ed. Gullatte) (Oncology Nursing Society, 2007); Chemotherapy and Biotherapy Guidelines and Recommendations for Practice (eds. Polovich, M. et al.) (Oncology Nursing Society, 2009); Physicians’ Cancer Chemotherapy Drug Manual 2012 (eds. Chu, E. & DeVita, Jr., V.T.) (Jones & Bartlett Learning, 2011); DeVita, Hellman, and Rosenberg's Cancer: Principles and Practice of Oncology (eds. DeVita, Jr., V.T. et al.) (Lippincott Williams & Wilkins, 2011); и Clinical Radiation Oncology (eds. Gunderson, L.L. & Tepper, J.E.) (Saunders) (2011), полное содержание которых включено в настоящий документ посредством ссылки.
В некоторых вариантах осуществления терапевтическое средство представляет собой противораковое средство. Противораковое средство может быть любым противораковым средством, хорошо известным в данной области, включая, но не ограничиваясь ими, химиотерапевтические средства, описанные в настоящем документе.
В других вариантах осуществления терапевтическое средство представляет собой терапевтическое антитело. Терапевтическое антитело может быть любым терапевтическим антителом, хорошо известным в данной области, включая, но не ограничиваясь ими, те, которые описаны в настоящем документе.
В вариантах осуществления терапевтическое средство представляет собой терапевтическую молекулу нуклеиновой кислоты. Терапевтическая молекула нуклеиновой кислоты может быть любой терапевтической молекулой нуклеиновой кислоты, хорошо известной в данной области.
В вариантах осуществления терапевтическое средство представляет собой радиоизотоп. Радиоизотоп может быть любым радиоизотопом, хорошо известным в данной области.
В вариантах осуществления терапевтическое средство представляет собой ингибитор тимидилатсинтазы.
В вариантах осуществления терапевтическое средство представляет собой соединение платины.
В вариантах осуществления терапевтическое средство представляет собой лекарственное средство из барвинка.
В других вариантах осуществления терапевтическое средство представляет собой сочетание двух или более лекарственных соединений.
В любом из вышеуказанных аспектов или вариантов осуществления способы включают введение терапевтически эффективного количества иммунотерапевтического средства. Иммунотерапевтическое средство может быть любым подходящим средством для вызывания дополнительного иммунного ответа, который направлен на разрушение клеток опухоли. Такая направленность иммунной системы может также позволить иммунной системе атаковать клетки опухолей, которые метастазировали в другие области тела.
В вариантах осуществления иммунотерапевтическое средство усиливает иммуномодулирующие эффекты терапевтического средства и/или средства, усиливающего внутриклеточное проникновение. В связанных вариантах осуществления иммунотерапевтическое средство дополнительно замедляет рост опухоли или дополнительно уменьшает опухоль.
Иммунотерапевтическое средство можно вводить до, во время или после введения терапевтического средства и средства, усиливающего внутриклеточное проникновение. В вариантах осуществления иммунотерапевтическое средство вводят перед первым введением терапевтического средства и средства, усиливающего внутриклеточное проникновение. В вариантах осуществления иммунотерапевтическое средство вводят одновременно с первым введением терапевтического средства и средства, усиливающего внутриклеточное проникновение.
В любом из вышеуказанных аспектов или вариантов осуществления терапевтическое средство и иммунотерапевтическое средство можно вводить в соотношении примерно 1:2, 1:4, 1:10, 1:25, 1:50, 1:100, 1:200 или в любом промежуточном соотношении (массовое отношение терапевтическое средство:иммунотерапевтическое средство).
В любом из вышеуказанных аспектов или вариантов осуществления средство, усиливающее внутриклеточное проникновение, и иммунотерапевтическое средство можно вводить в соотношении примерно 1:2, 1:4, 1:10, 1:20, 1:25, 1:50, 1:100, 1:100 или в любом промежуточном соотношении (массовое отношение средство, усиливающее внутриклеточное проникновение:иммунотерапевтическое средство).
В любом из вышеуказанных аспектов или вариантов осуществления иммунотерапевтическое средство можно вводить внутрибрюшинно, локально или регионально, системно (например, внутривенно) или интратуморально.
В любом из вышеуказанных аспектов или вариантов осуществления терапевтическое средство и средство, усиливающее внутриклеточное проникновение, могут быть связаны.
В любом из вышеуказанных аспектов или вариантов осуществления способ может включать дополнительное получение субъектом стандартного лечения. В вариантах осуществления стандартное лечение представляет собой хирургическую операцию, радиационную терапию, системную химиотерапию или их сочетание.
В любом из вышеуказанных аспектов или вариантов осуществления введение терапевтического средства, средства, усиливающего внутриклеточное проникновение, или иммунотерапевтического средства можно проводить с помощью системы визуализации. Например, систему визуализации можно использовать для расчета объема конкретной опухоли, так что на основе объема опухоли можно рассчитать дозу средств по изобретению. Кроме того, в рамках данного изобретения предусмотрено, что такую систему визуализации можно использовать для направления иглы в определенную зону инъекции внутри опухоли. Система визуализации может быть любой системой визуализации, хорошо известной в данной области (см., например, The MD Anderson Manual of Medical Oncology (eds. Kantarjian, H.M. et al.) (McGraw-Hill Professional, 2011), полное содержание которой включено в настоящий документ посредством ссылки), и методы использования системы визуализации для облегчения введения терапевтического средства, средства, усиливающего внутриклеточное проникновение, или иммунотерапевтического средства также хорошо известны в данной области (см., например, Majumder, S. et al., Expert Rev. Gastroenterol Hepatol. 6: 95-103 (2012); Liu, F. et al., J. Thorac. Oncol. 5: 879-84 (2010); Schmuecking, M. et al., Int. J. Radiat. Biol. 85: 814-24 (2009); Zhao, B. et al., Radiology 252: 263-72 (2009); Thrall, M.M. et al., Gynecol. Oncol. 105: 17-22 (2007); Bogoni. L. et al., Br. J. Radiol. 1: S57-62 (2005); Bluemke, D.A. et al., Radiographics 17: 303-13 (1997); Arimoto, T., Cancer 72: 2383-8 (1993); Feyerabend, T. et al., Strahlenther Onkol. 166: 405-10 (1990) и Lee, N., IEEE Reviews 2: 136-146 (2009), полное содержание которых включено в настоящий документ посредством ссылки). В вариантах осуществления система визуализации представляет собой рентгеновскую компьютерную томографию (КТ), рентгеноскопию, магнитно-резонансную томографию (МРТ), ультразвуковое исследование или позитронную эмиссионную томографию (ПЭТ)/компьютерную томографию (КТ).
Терапевтические средства
По настоящему изобретению предусмотрено любое терапевтическое средство, подходящее для использования в способах, описанных в настоящем документе (например, противораковое средство любого типа для лечения рака). Подходящие терапевтические средства включают, но не ограничиваются ими, фармацевтические лекарственные средства или соединения (т.е., низкомолекулярные лекарственные средства), терапевтические антитела, терапевтические белки или биологические препараты (например, гормональные терапевтические средства) и молекулы нуклеиновой кислоты (например, киРНК).
В вариантах осуществления терапевтическое средство представляет собой средство, которое, как было показано, обладает цитотоксическими свойствами против клеток опухолей. В связанных вариантах осуществления терапевтическое средство представляет собой существующее одобренное для коммерческого использования фармацевтическое лекарственное средство или другую одобренную для коммерческого использования композицию для лечения рака с использованием общепринятого подхода.
«Химиотерапевтическое средство» включает химические реагенты, которые ингибируют рост пролиферирующих клеток или тканей, когда рост таких клеток или тканей является нежелательным. Химиотерапевтические средства хорошо известны в данной области, и любое такое средство подходит для использования по настоящему изобретению. См., например, Anticancer Drugs: Design, Delivery and Pharmacology (Cancer Etiology, Diagnosis and Treatments) (eds. Spencer, P. & Holt, W.) (Nova Science Publishers, 2011); Clinical Guide to Antineoplastic Therapy: A Chemotherapy Handbook (ed. Gullatte) (Oncology Nursing Society, 2007); Chemotherapy and Biotherapy Guidelines and Recommendations for Practice (eds. Polovich, M. et al.) (Oncology Nursing Society, 2009); Physicians’ Cancer Chemotherapy Drug Manual 2012 (eds. Chu, E. & DeVita, Jr., V.T.) (Jones & Bartlett Learning, 2011); DeVita, Hellman, and Rosenberg's Cancer: Principles and Practice of Oncology (eds. DeVita, Jr., V.T. et al.) (Lippincott Williams & Wilkins, 2011); и Clinical Radiation Oncology (eds. Gunderson, L.L. & Tepper, J.E.) (Saunders) (2011), полное содержание которых включено в настоящий документ посредством ссылки.
В одном варианте осуществления фармацевтическое лекарственное средство может представлять собой алкилирующее средство. Алкилирующие средства непосредственно повреждают ДНК, предотвращая воспроизводство раковых клеток. Как класс лекарственных средств, эти средства не являются фаза-специфичными; иными словами, они действуют во всех фазах клеточного цикла. Алкилирующие средства используют для лечения различных видов рака, включая, но не ограничиваясь ими, лейкоз, лимфому, болезнь Ходжкина, множественную миелому, саркому, а также рак легких, молочной железы и яичников. Примеры алкилирующих средств включают, например, азотистые иприты (например, мехлорэтамин, хлорамбуцил, циклофосфамид (Cytoxan®), ифосфамид и мелфалан), алкилсульфонаты (например, бусульфан), триазины (например, дакарбазин (DTIC), темозоломид (Temodar®)), нитрозомочевины (в том числе, стрептозоцин, кармустин (BCNU) и ломустин) и этиленимины (например, тиотепу и алтретамин). Кроме того, лекарственные средства на основе платины (например, цисплатин, карбоплатин и оксалиплатин) часто считают алкилирующими средствами, поскольку они убивают раковые клетки аналогичным образом. По изобретению предусмотрены все эти лекарственные средства или их сочетания.
В другом варианте осуществления по изобретению предусмотрено любое антиметаболическое лекарственное средство. Антиметаболиты составляют класс лекарственных средств, которые препятствуют наращиванию ДНК и РНК, заменяя нормальные строительные блоки РНК и ДНК. Эти средства повреждают клетки во время фазы S. Как правило, их используют для лечения лейкозов, раковых опухолей молочной железы, яичников и желудочно-кишечного тракта, а также других видов рака. Примеры антиметаболитов, включают, например, 5-фторурацил (5-FU), 6-меркаптопурин (6-MP), капецитабин (Xeloda®), кладрибин, клофарабин, цитарабин (Ara-C®), флоксуридин, флударабин, гемцитабин (Gemzar®), гидроксимочевину, метотрексат, пеметрексед (Alimta®), пентостатин и тиогуанин.
По изобретению также предусмотрено использование противоопухолевых антибиотиков, таких как антрациклины. Антрациклины представляют собой противоопухолевые антибиотики, которые препятствуют действию ферментов, вовлеченных в репликацию ДНК. Эти лекарственные средства действуют во всех фазах клеточного цикла. Их широко используют для лечения различных видов рака. Главное, что нужно учитывать при приеме данных лекарственных средств, это то, что они наносят необратимый вред сердцу, если их принимать в высоких дозах. По этой причине данные лекарственные средства часто имеют ограничения по дозе, которую можно принимать в течение жизни. Примеры включают даунорубицин, доксорубицин (Adriamycin®), эпирубицин и идарубицин. Другие противоопухолевые антибиотики включают, например, актиномицин-D, блеомицин и митомицин-C.
Также предусмотрено использование ингибиторов топоизомеразы. Эти лекарственные средства препятствуют действию ферментов, называемых топоизомеразами, которые помогают разделять цепи ДНК для копирования. Их используют для лечения некоторых лейкозов, а также рака легких, яичников, желудочно-кишечного тракта и других видов рака. Примеры ингибиторов топоизомеразы I включают топотекан и иринотекан (CPT-11). Примеры ингибиторов топоизомеразы II включают этопозид (VP-16) и тенипозид. Митоксантрон также ингибирует топоизомеразу II. Лечение ингибиторами топоизомеразы II увеличивает риск возникновения второго рака - острого миелогенного лейкоза (AML). При использовании такого лекарственного средства вторичный лейкоз может развиться уже через 2-3 года после приема лекарственного средства.
По настоящему изобретению также предусмотрено использование терапевтических средств, известных как ингибиторы митоза. Ингибиторы митоза часто представляют собой растительные алкалоиды и другие соединения, полученные из природных продуктов. Они могут останавливать митоз или ингибировать ферменты, препятствуя образованию белков, необходимых для репродукции клеток. Эти лекарственные средства действуют в фазе M клеточного цикла, но могут повреждать клетки во всех фазах. Их используют для лечения различных видов рака, включая рак молочной железы, легких, миеломы, лимфомы и лейкозы. Эти лекарственные средства известны своей способностью вызывать повреждение периферических нервов, что может являться ограничивающим дозу побочным эффектом. Примеры ингибиторов митоза включают таксаны (например, паклитаксел (Taxol®) и доцетаксел (Taxotere®)), эпотилоны (например, иксабепилон (Ixempra®)), алкалоиды барвинка (например, винбластин (Velban®), винкристин (Oncovin®) и винорелбин (Navelbine®)) и эстрамустин (Emcyt®).
Противораковые средства также могут представлять собой кортикостероиды. Стероиды являются природными гормонами и гормоноподобными лекарственными средствами, которые полезны в лечении некоторых видов рака (лимфомы, лейкозов и множественной миеломы), а также других заболеваний. Когда эти лекарственные средства используют для уничтожения или замедления роста раковых клеток, их считают химиотерапевтическими лекарственными средствами. Кортикостероиды также широко используют в качестве противорвотных средств для предотвращения тошноты и рвоты, вызванных химиотерапией. Их также используют перед химиотерапией для предотвращения тяжелых аллергических реакций (реакций гиперчувствительности). Примеры включают преднизон, метилпреднизолон (например, Solumedrol®) и дексаметазон (например, Decadron®).
В некоторых вариантах осуществления фармацевтическое средство выбрано из группы, состоящей из: абиратерона ацетата, афатиниба, альдеслейкина, алемтузумаба, алитретиноина, алтретамина, амифостина, аминоглутетимида, анагрелида, анастрозола, триоксида мышьяка, аспарагиназы, азацитидина, азатиоприна, бендамустина, бевацизумаба, бексаротина, бикалутамида, блеомицина, бортезомиба, бусульфана, капецитабина, карбоплатина, кармустина, цетуксимаба, хлорамбуцила, цисплатина, кладрибина, кризотиниба, циклофосфамида, цитарабина, дакарбазина, дактиномицина, дазатиниба, даунорубицина, денилейкина дифлитокса, децитабина, доцетаксела, дексаметазона, доксифлуридина, доксорубицина, эпирубицина, эпоэтина альфа, эпотилона, эрлотиниба, эстрамустина, энтиностата, этопозида, эверолимуса, экземестана, филграстима, флоксуридина, флударабина, фторурацила, флуоксиместерона, флутамида, связанных с фолатом алкалоидов, гефитиниба, гемцитабина, гемтузумаб озогамицина, GM-CT-01, гозерелина, гексаметилмеламина, гидроксимочевин, ибритумомаба, идарубицина, ифосфамида, иматиниба, интерферона альфа, интерферона бета, иринотекана, иксабепилона, лапатиниба, лейковорина, леупролида, леналидомида, летрозола, ломустина, мехлорэтамина, мегестрола, мелфалана, меркаптопурина, метотрексата, митомицина, митоксантрона, неларабина, нилотиниба, нилутамида, октреотида, офатумумаба, опрелвекина, оксалиплатина, паклитаксела, панитумумаба, пеметрекседа, пентостатина, полисахаридных ингибиторов галектина, прокарбазина, ралоксифена, ретиноевых кислот, ритуксимаба, ромиплостима, сарграмостима, сорафениба, стрептозоцина, сунитиниба, тамоксифена, темсиролимуса, темозоламида, тенипозида, талидомида, тиогуанина, тиотепы, тиогуанина, топотекана, торемифена, тозитумомаба, траметиниба, трастузумаба, третиноина, валрубицина, ингибиторов и уловителей VEGF, винбластина, винкристина, виндезина, винорелбина, винтафолида (EC145), вориностата, а также их функционально эффективных производных, пегилированных форм, солей, полиморфных форм, хиральных форм и их сочетаний.
По изобретению также предусмотрены любые производные формы вышеуказанных фармацевтических средств и терапевтических средств. Общепринятые дериватизации могут включать, например, добавление химического фрагмента для повышения растворимости и/или стабильности, или направляющего фрагмента, который позволяет более специфически направлять молекулу к конкретной клетке или области тела. Фармацевтические средства также могут быть сформулированы в любых подходящих сочетаниях, при этом лекарственные средства либо могут быть смешаны в своей индивидуальной форме, либо связаны вместе таким образом, что сохраняется функциональность каждого лекарственного средства. Лекарственные средства также могут быть дериватизированы для включения радиоизотопа или другого уничтожающего клетку фрагмента, чтобы сделать молекулу еще более эффективной в уничтожении клеток. Кроме того, лекарственные средства или их части можно модифицировать флуоресцентным соединением или другими обнаруживаемыми метками, которые могут позволить отслеживать лекарственное средство или препарат в организме или внутри опухоли. Фармацевтическое лекарственное средство или любое из вышеуказанных терапевтических средств может быть предоставлено в форме предшественника, так что лекарственное средство приобретает свою активность или функцию только после того, как оно будет процессировано каким-либо образом, например, метаболизировано клеткой.
Терапевтические антитела, предусмотренные по настоящему изобретению, могут включать противораковое антитело любого изотипа (IgA, IgG, IgE, IgM или IgD) или его иммуноактивный фрагмент, или производное. Такие фрагменты могут включать, например, одноцепочечные фрагменты вариабельной области (scFv), антигенсвязывающий фрагмент (Fab), кристаллизуемый фрагмент (Fc), модифицированный для содержания области связывания антигена или эпитопа, и домен антитела. Дериватизированные варианты терапевтических антител могут включать, например, диатела, нанотела и практически любую производную от антитела структуру, которая содержит или модифицирована для содержания соответствующего и эффективного антигенсвязывающего сайта.
Примеры противораковых терапевтических средств на основе антител, которые могут быть использованы по изобретению, могут включать, например, абаговомаб, алацизумаб пегол, алемтузумаб, алтумомаб пентетат (Hybri-ceaker), аматуксимаб, анатумомаб мафенатокс, анти-PD-1 антитела, аполизумаб, арцитумомаб (CEA-Scan), белимумаб, бевацизумаб, биватузумаб мертанзин, блинатумомаб, брентуксимаб ведотин, кантузумаб мертанзин, кантузумаб равтанзин, капромаб пендетид (Prostascint), катумаксомаб (Removab), цетуксимаб (Erbitux), цитатузумаб богатокс, циксутумумаб, кливатузумаб тетраксетан (hPAM4-Cide), конатумумаб, далотузумаб, деносумаб, дрозитумаб, эдреколомаб (Panorex), энаватузумаб, гемтузумаб, ибритумомаб тиуксетан, ипилимумаб (MDX-101), офатумумаб, панитумумаб, ритуксимаб, тозитумомаб и трастузумаб.
По изобретению также предусмотрены любые подходящие биологические препараты, например, гормональные терапевтические средства, которые можно использовать для лечения рака. В одном неограничивающем примере подходящие биологические препараты, которые могут быть использованы, включают гормональные терапевтические средства. Лекарственные средства в этой категории могут представлять собой половые гормоны или гормоноподобные лекарственные средства, которые изменяют действие или продуцирование женских или мужских гормонов. Их можно использовать для замедления роста раковых опухолей молочной железы, предстательной железы и эндометрия (матки), которые обычно растут в ответ на природные гормоны в организме. Эти гормоны для лечения рака не действуют так, как стандартные химиотерапевтические лекарственные средства, а скорее предотвращают использование раковой клеткой гормонов, которые необходимы ей для роста, или предотвращают производство организмом гормонов, необходимых для роста раковой опухоли. Такие гормональные терапевтические средства могут включать, например, анти-эстрогены (например, фулвестрант (Faslodex®), тамоксифен и торемифен (Fareston®)), ингибиторы ароматазы (например, анастрозол (Arimidex®), экземестан (Aromasin®) и летрозол (Femara®)), прогестины (например, мегестрола ацетат (Megace®)), эстрогены, анти-андрогены (например, бикалутамид (Casodex®), флутамид (Eulexin®) и нилутамид (Nilandron®)), а также агонисты или аналоги гонадотропин-рилизинг гормона (GnRH) (иначе называемого рилизинг гормоном лютеинизирующего гормона (LHRH), например, леупролид (Lupron®) и гозерелин (Zoladex®)).
По изобретению также предусмотрено, что лечение рака можно осуществлять с использованием молекулы нуклеиновой кислоты, которая направлена на определенный «ген-мишень», играющий роль в развитии рака. Эффект молекулы нуклеиновой кислоты на ген-мишень может включать сайленсинг гена, разрушение мРНК или ингибирование транскрипции, или тому подобное, так что уровень экспрессии и/или преобразования гена-мишени в функциональный закодированный полипептид подвергается значительному воздействию (в сторону повышения или понижения), в результате чего рост раковой опухоли подавляется и/или она уничтожается данным средством. Термин «ген-мишень» означает нуклеотидные последовательности (например, геномные ДНК или мРНК), которые кодируют целевой белок, пептид или полипептид, или которые кодируют или сами являются регуляторными нуклеиновыми кислотами (например, «ген-мишень» для целей настоящего изобретения может также представлять собой микроРНК или кодирующую микроРНК генную последовательность), играющими роль в развитии рака. В некоторых вариантах осуществления термин «ген-мишень» также должен включать изоформы, мутанты, полиморфные формы и сплайс-варианты генов-мишеней.
Любое средство на основе нуклеиновой кислоты, хорошо известное в данной области, подходит для использования по изобретению. Иллюстративные типы средств на основе нуклеиновой кислоты включают, но не ограничиваются ими, средства на основе одноцепочечной рибонуклеиновой кислоты (например, микроРНК), средства на основе антисмыслового олигонуклеотида, средства на основе двухцепочечной рибонуклеиновой кислоты и тому подобное.
Способы конструирования терапевтических нуклеиновых кислот хорошо известны в данной области. Например, интерферирующая РНК может быть собрана из двух отдельных олигонуклеотидов, из которых одна цепь является смысловой цепью и другая является антисмысловой цепью, при этом антисмысловая и смысловая цепи являются самокомплементарными (т.е., каждая цепь содержит нуклеотидную последовательность, которая комплементарна нуклеотидной последовательности в другой цепи; таким образом, антисмысловая цепь и смысловая цепь образуют дуплекс или двухцепочечную структуру); антисмысловая цепь содержит нуклеотидную последовательность, которая комплементарна нуклеотидной последовательности в молекуле-мишени нуклеиновой кислоты или ее части и смысловая цепь содержит нуклеотидную последовательность, соответствующую последовательности-мишени нуклеиновой кислоты или ее части.
Альтернативно, интерферирующая РНК собрана из одного олигонуклеотида, в котором самокомплементарные смысловая и антисмысловая области связаны при помощи линкера(ов) на основе нуклеиновой кислоты или не нуклеиновой кислоты. Интерферирующая РНК может представлять собой полинуклеотид с дуплексной, асимметрично дуплексной, шпилечной или асимметрично шпилечной вторичной структурой, имеющий самокомплементарные смысловую и антисмысловую области, при этом антисмысловая область содержит нуклеотидную последовательность, которая комплементарна нуклеотидной последовательности в отдельной молекуле-мишени нуклеиновой кислоты или ее части и смысловая область содержит нуклеотидную последовательность, соответствующую последовательности-мишени нуклеиновой кислоты или ее части. Интерферирующая РНК может представлять собой кольцевой одноцепочечный полинуклеотид, имеющий две или более петлевых структур и стебель, содержащий самокомплементарные смысловую и антисмысловую области, при этом антисмысловая область содержит нуклеотидную последовательность, которая комплементарна нуклеотидной последовательности в молекуле-мишени нуклеиновой кислоты или ее части и смысловая область содержит нуклеотидную последовательность, соответствующую последовательности-мишени нуклеиновой кислоты или ее части, и при этом кольцевой полинуклеотид может процессироваться либо in vivo, либо in vitro, с образованием активной молекулы киРНК, способной опосредовать РНК-интерференцию.
Способы введения/доставки терапевтических нуклеиновых кислот хорошо известны в данной области. Например, молекулы терапевтической нуклеиновой кислоты могут быть доставлены в носителе для доставки, таком как липидные везикулы или другой полимерный материал носителя, известный в данной области. Неограничивающие примеры дополнительных систем носителей на основе липидов (которые могут быть получены с по меньшей мере одним модифицированным катионным липидом по изобретению), подходящих для использования по настоящему изобретению, включают липоплексы (см., например, патентную публикацию США №20030203865 и Zhang et al., J. Control Release, 100: 165-180 (2004)), pH-чувствительные липоплексы (см., например, патентную публикацию США №2002/0192275), обратимо маскированные липоплексы (см., например, патентную публикацию США №2003/0180950), композиции на основе катионных липидов (см., например, патент США № 6756054 и патентную публикацию США №2005/0234232), катионные липосомы (см., например, патентные публикации США №№2003/0229040, 2002/0160038 и 2002/0012998, патент США №5908635 и PCT публикацию № WO 01/72283), анионные липосомы (см., например, патентную публикацию США №2003/0026831), pH-чувствительные липосомы (см., например, патентную публикацию США №2002/0192274 и AU 2003/210303), покрытые антителами липосомы (см., например, патентную публикацию США №2003/0108597 и PCT публикацию № WO 00/50008), специфичные для типа клеток липосомы (см., например, патентную публикацию США №2003/0198664), липосомы, содержащие нуклеиновые кислоты и пептиды (см., например, патент США №6207456), липосомы, содержащие липиды, дериватизированные высвобождаемыми гидрофильными полимерами (см., например, патентную публикацию США №2003/0031704), заключенную в липиде нуклеиновую кислоту (см., например, PCT публикации №№ WO 03/057190 и WO 03/059322), инкапсулированную в липиде нуклеиновую кислоту (см., например, патентную публикацию США №2003/0129221 и патент США №5756122), другие липосомные композиции (см., например, патентные публикации США №№ 2003/0035829 и 2003/0072794 и патент США №6200599), стабилизированные смеси липосом и эмульсии (см., например, EP 1304160), эмульсионные композиции (см., например, патент США №6747014) и микроэмульсии нуклеиновых кислот (см., например, патентную публикацию США №2005/0037086).
Если это удобно, любые из средств по изобретению, включая фармацевтические лекарственные средства, биологические препараты и терапевтические антитела, можно также доставлять с использованием описанных выше систем носителей. Все системы носителей можно дополнительно модифицировать направляющим фрагментом или тому подобным для облегчения доставки композиции к интересующей опухоли-мишени.
В одном из вариантов осуществления настоящего изобретения используют соединения платины в качестве терапевтического средства. Содержащие платину соединения использовались в течение нескольких лет в качестве эффективного средства лечения некоторых видов рака. Соединения на основе платины (например, карбоплатин, цисплатин, оксалиплатин) являются анти-неопластическими средствами, которые врачи вводят внутривенно (в/в) для лечения различных видов рака. Как правило, используют внутривенное введение, поскольку при пероральном введении биодоступность только одного карбоплатина является низкой (примерно 4%) и крайне изменчивой. Препараты на основе платины потенциально уничтожают быстро делящиеся клетки. Однако введение карбоплатина внутривенной инфузией приводит к распределению терапевтического средства по всему телу и уничтожению здоровых быстро делящихся клеток, в том числе, и особенно, клеток костного мозга. Внутривенное введение карбоплатина приводит к уменьшению за счет разбавления в крови концентрации лекарственного средства, достигающего зоны опухоли. Кроме того, из-за разбавленной концентрации терапевтическое средство плохо проникает в клетки опухолей.
После проникновения в раковые клетки данные соединения повреждают ДНК и вызывают образование перекрестных сшивок цепей, тем самым, предотвращая дальнейшее производство ДНК, что в конечном итоге приводит к гибели раковой клетки. Данный эффект, судя по всему, является неспецифичным для клеточного цикла. При внутривенном введении платина может приводить к тяжелым заболеваниям крови (например, анемии, угнетению костного мозга), в результате чего развивается инфекция или кровотечение. Главным путем выведения двух основных соединений платины является почечная экскреция. Цисплатин и карбоплатин являются стандартными и широкодоступными химиотерапевтическими средствами на основе платины. Химическим названием карбоплатина является диамин[1,1-циклобутандикарбоксилат(2-)-0,0´]-(SP-4-2) платины. Карбоплатин представляет собой кристаллический порошок с молекулярной формулой C6H12N2O4Pt и молекулярной массой 371,25. Его растворимость в воде составляет примерно 14 мг/мл, и pH 1% раствора составляет 5-7, в то время как растворимость цисплатина составляет примерно 1-2 мг/мл. Данные соединения практически нерастворимы в этаноле, ацетоне и диметилацетамиде. В настоящее время их вводят только внутривенной инфузией.
В другом варианте осуществления настоящего изобретения используют ингибиторы синтеза тимидилата. Эти средства включают средство 5-FU (фторурацил), которое используют против рака уже около 40 лет. Соединение имеет несколько механизмов действия, но главным образом действует как ингибитор тимидилатсинтазы, прерывая действие фермента, являющегося ключевым фактором в синтезе пиримидина тимина, который важен для репликации ДНК. 5-FU не абсорбируется при пероральном введении. В настоящее время лучшим лечением для рака поджелудочной железы является курс лечения гемцитабином (Gemzar®).
Как аналоги пиримидина, данные соединения преобразуются в клетке в различные цитотоксические метаболиты, которые затем включаются в ДНК и РНК, в конечном счете вызывая остановку клеточного цикла и апоптоз за счет подавления способности клетки синтезировать ДНК. Данные соединения, как правило, являются специфичными для S-фазы лекарственными средствами и активными только в течение нескольких клеточных циклов. Помимо включения в ДНК и РНК эти лекарственные средства, как показано, ингибируют активность экзосомального комплекса, экзорибонуклеазная активность которого важна для выживания клеток.
Средства, усиливающие внутриклеточное проникновение
Настоящее изобретение частично основано на использовании средств для внутриклеточного проникновения, таких как связанные с бензоатом алифатические кислоты, функционализированные кетокислоты (например, оксо-6-фенилгексановая кислота), кетоэфиры, модифицированные ацилированные аминокислоты (например, N-[8-2-(2-гидроксибензоил)аминокаприлат натрия), для значительного усиления проникающей способности или проникновения лекарственных средств в раковые клетки, неожиданно приводящего к на удивление более эффективному уничтожению раковых клеток. Таким образом, в одном аспекте настоящее изобретение относится к способу лечения рака путем локального или регионального совместного введения сочетания терапевтического средства, такого как те, которые описаны выше, и средства, усиливающего внутриклеточное проникновение, в количествах и с использованием методов, которые приводят к значительному уменьшению и/или уничтожению опухоли.
По изобретению предусмотрено использование любого подходящего средства, усиливающего внутриклеточное проникновение, известного или которое в будущем будет открыто или разработано.
Целый ряд компаний в области разработки способов доставки лекарственных средств разработали такие соединения для усиления проникновения в клетку с целью доставки заряженных или макромолекулярных соединений в кровоток не инъекционными методами. Среди этих компаний Emisphere Technologies, Acrux Pharma Pty, Ltd., Oramed Pharmaceuticals, Apollo Life Sciences, Diabetology и Unigene. Как правило, такие платформы были разработаны для системной доставки терапевтических средств общепринятыми путями введения, такими как пероральный, трансбуккальный, легочный или кожный; однако ни в одной из них не предусмотрено настоящее применение таких усиливающих проникновение средств способом, описанным в связи с настоящим изобретением.
Следует иметь в виду, что общепринятые способы доставки активных средств часто сильно ограничены биологическими, химическими и физическими барьерами. Как правило, эти барьеры создаются средой окружения, через которую происходит доставка, средой, в которой находится мишень для доставки, или самой мишенью. Биологически или химически активные средства особенно уязвимы для таких барьеров. При доставке в организм животного биологически активных или химически активных фармакологических и терапевтических средств физические и химические барьеры создаются телом. Примерами физических барьеров являются кожа и мембраны различных органов, которые пересекаются перед тем, как мишень будет достигнута, и примеры химических барьеров включают, но не ограничиваются ими, различные уровни pH, липидные бислои и разрушающие ферменты. Клеточная мембрана также представляет собой важный барьер, оказывающий существенное влияние на эффективность доставки лекарственного средства.
Настоящее изобретение основано на сочетании доставки противоракового терапевтического средства и средства, усиливающего внутриклеточное проникновение, которое вводят локально, используя передовые методы визуализации для доставки дозы и направления введения, заранее, одновременно или почти одновременно с терапевтическим средством с целью значительного усиления проникновения через клеточную мембрану доставляемых локально противораковых средств.
Соответственно, в одном аспекте изобретения способ,описанный в настоящем документе, включает использование «усилителя проникновения» или носителя, который обеспечивает улучшенный перенос в клетку. Эти молекулы облегчают или делают возможным проникновение и/или транспорт терапевтических молекул через биологические мембраны в клетки. Данное конкретное применение соединений, облегчающих проникновение, таких как те, которые описаны в патенте США №5650386, выданном компании Emisphere Technologies (полное содержание которого включено в настоящий документ посредством ссылки), ранее не было предусмотрено. Иными словами, использование в сочетании усилителей проникновения, способных облегчать внутриклеточный транспорт локально доставляемых противораковых средств, ранее не рассматривалось, и не было предусмотрено в данной области.
В одном варианте осуществления настоящее изобретение включает использование 6-оксо-6-фенилгексановой кислоты в качестве соединения, усиливающего внутриклеточное проникновение, или ее соли или аналога,

в способе лечения рака, например, солидной опухоли, включающем локальное совместное введение указанного выше соединения и противоракового терапевтического средства в терапевтически эффективных количествах и в соответствии с режимом введения, которые эффективны для значительного уменьшения опухоли и/или уничтожения опухоли.
В других вариантах осуществления средство, усиливающее внутриклеточное проникновение, представляет собой модифицированные аминокислоты, N-[8-(2-гидроксибензоил)аминооктановую кислоту,
 ,
,
N-[8-(2-гидроксибензоил)аминодекановую кислоту, N-(5-хлорсалицилоил)-8-аминокаприловую кислоту, N-[4-(4-хлор-2-гидроксибензоил)аминобутановую кислоту, 8-(N-2-гидрокси-4-метоксибензоил)аминокаприловую кислоту (4-MOAC), 8-оксо-8-фенилоктановую кислоту, 8-(2,5-дихлорфенил)-8-оксооктановую кислоту, 2-этилгексил-2-гидроксибензоат, 5-циклогексил-5-оксовалериановую кислоту, 6-циклогексил-6-оксогексановую кислоту, 7-циклогексил-7-оксогептановую кислоту, 8-циклогексил-8-оксооктановую кислоту, 4-циклопентил-4-оксомасляную кислоту, 5-циклопентил-5-оксовалериановую кислоту, 6-циклопентил-6-оксогексановую кислоту, 7-циклопентил-7-оксогептановую кислоту, 8-циклопентил-8-оксооктановую кислоту, 4-циклобутил-4-оксомасляную кислоту, 5-циклобутил-5-оксовалериановую кислоту, 6-циклобутил-6-оксогексановую кислоту, 7-циклобутил-7-оксогептановую кислоту, 8-циклобутил-8-оксооктановую кислоту, 4-циклопропил-4-оксомасляную кислоту, 5-циклопропил-5-оксовалериановую кислоту, 6-циклопропил-6-оксогексановую кислоту, 7-циклопропил-7-оксогептановую кислоту, 8-циклопропил-8-оксооктановую кислоту, 8-[(3-метилциклогексил)окси]октановую кислоту, 7-[(3-метилциклогексил)окси]гептановую кислоту, 6-[(3-метилциклогексил)окси]гексановую кислоту, 5-[(3-метилциклогексил)окси]пентановую кислоту, 4-[(3-метилциклогексил)окси]бутановую кислоту, 3-[(3-метилциклогексил)окси]пропановую кислоту и другие их фармацевтически приемлемые соли, а также октилсалицилат или октисалат, дикетопиперазины, сапонин, ацилкарнитины, алканоилхолины, тауродигидрофузидат, сульфоксиды, оксазолидиноны, пирролидоны, спирты или алканолы, бензойную кислоту, гликоли, поверхностно-активное вещества, терпены или их функционально эффективные соли, производные или их сочетания.
В других вариантах осуществления соединение, усиливающее внутриклеточное проникновение, выбрано из любого из соединений, описанных в патентах США №№4764381, 4783450, 4885174, 4983396, 5045553, 5118845, 5219877, 5401516, 5451410, 5540939, 5443841, 5541155, 5578323, 5601839, 5601846, 5627270, 5629020, 5643957, 5650386, 5693338, 5693769, 5709861, 5714167, 5773647, 5766633, 5776888, 5792451, 5804688, 5863944, 5866536, 5876710, 5879681, 5820881, 5834010, 5840340, 5935601, 5939381, 5955503, 5990166, 5958457, 5965121, 5972387, 5976569, 5989539, 6001347, 6051258, 6051561, 6060513, 6071510, 6090958, 6099856, 6100298, 6180140, 6221367, 6242495, 6245359, 6313088, 6331318, 6333046, 6344213, 6358504, 6395774, 6413550, 6428780, 6461643, 6525020, 6610329, 6623731, 6627228, 6642411, 6646162, 6663887, 6663898, 6693208, 6699467, 6673574, 6818226, 6846844, 6906030, 6916489, 6916789, 6960355, 6972300, 6991798, 7005141, 7067119, 7071214, 7084279, 7115663, 7125910, 7129274, 7138546, 7151191, 7186414, 7208483, 7217703, 7268214, 7276534, 7279597, 7297794, 7351741, 7384982, 7387789, 7390834, 7485321, 7491796, 7495030, 7553872, 7638599, 7670626, 7700775, 7727558, 7744910, 7820722, 7893297, 7951971, 7977506, 8003697, 8017727, 8026392, 8088734 и RE 35862, каждый из которых включен в настоящий документ посредством ссылки.
Усилители внутриклеточного проникновения, как правило, сами имеют небольшую, или вовсе не имеют известную фармакологическую активность. Данные технологии, такие как те, которые описаны и приведены выше, делают возможным проникновение через мембраны для доставки терапевтического средства без изменения его химической формы или биологической целостности. Такие усилители проникновения, как показано, значительно увеличивают поглощение средств нескольких различных типов.
Иммунотерапевтические средства
В другом аспекте изобретение относится к использованию одного или более иммунотерапевтических средств для дополнительного усиления ингибирующих и/или разрушающих эффектов на клетки опухоли, оказываемых сочетанием противоракового терапевтического средства и средства, усиливающего внутриклеточное проникновение. Например, иммунотерапевтическое средство доставляется после того, как первые два средства оказали свое воздействие, однако изобретение не ограничено данной концепцией. По изобретению предусмотрен любой режим введения с использованием всех трех средств, при условии, что могут проявляться благоприятные терапевтические эффекты от каждого из средств. В рамках изобретения также предусмотрено, что введение одного или более иммунотерапевтических средств оказывает иммуностимулирующее действие, обеспечивающее профилактику против дальнейшего рецидива рака. Этот иммуностимулирующий эффект может быть достигнут, если средство вводят интратуморально или внутрибрюшинно либо с усилителем внутриклеточного проникновения, либо без него.
Специалисты в данной области понимают, что использование иммунотерапевтического средства является методом лечения, направленным на использование собственной иммунной системы индивидуума для борьбы с раком или другим заболеванием. Это может быть достигнуто путем стимуляции собственной иммунной системы индивидуума или путем обеспечения недостающих элементов, без которых иммунная система является дефектной или несовершенной.
Иммунотерапия является формой биологической терапии, которую можно использовать по настоящему изобретению для дополнения и/или усиления эффектов лечения терапевтическим средством/усиливающим проникновение средством. В целом, существуют две признанные формы иммунотерапии, которые называют активной иммунотерапией и пассивной иммунотерапией. При активной иммунотерапии стимулируют собственную иммунную систему организма для борьбы с заболеванием. При пассивной иммунотерапии используют компоненты иммунной системы, такие как антитела, полученные вне тела, для усиления уровня иммунного ответа организма. Иммунотерапевтические средства могут также действовать направленно на определенные типы клеток или антигены (специфические иммунотерапевтические средства) или они могут действовать путем более общей стимуляции иммунной системы (неспецифические иммунотерапевтические средства, иногда называемые адъювантами). Некоторые примеры иммунотерапевтических средств, предусмотренных по изобретению, включают терапевтические средства на основе моноклональных антител (такие как ритуксимаб и алемтузумаб), неспецифические иммунотерапевтические средства и адъюванты (вещества, которые стимулируют иммунный ответ, такие как интерлейкин-2 и интерферон-альфа), иммуномодулирующие лекарственные средства (такие как талидомид и леналидомид) и противораковые вакцины (например, агонисты NKT клеток, включая, но не ограничиваясь ими, α-GalCer, βMannCer или α-Gal гликолипиды).
Соответственно, иммунотерапевтические средства, которые можно также называть в некотором смысле «иммуномодуляторами», могут включать, например, интерлейкины (например, IL-2, IL-7, или IL-12), некоторые другие цитокины (например, интерфероны, колониестимулирующий фактор (G-CSF), имиквимод), хемокины, а также другие виды средств, которые могут включать антигены, эпитопы, антитела, моноклональные антитела или даже средство доставки для доставки одного или более из этих соединений и, кроме того, могут даже включать рекомбинантные клетки иммунной системы. Такие иммунотерапевтические средства могут включать рекомбинантные формы, синтетические формы и натуральные препараты (см. D'Alessandro, N. et al., Cancer Therapy: Differentiation, Immunomodulation and Angiogenesis, New York: Springer-Verlag, 1993).
В некоторых вариантах осуществления иммунотерапевтическое средство по изобретению представляет собой противораковую вакцину, которая может включать, например, овальбумин, Neuvenge®, онкофаг, CimaVax-EGF, мобилан, α-Gal гликолипиды, доставляемые аденовирусами вакцины, от компании Celldex CDX1307 и CDX1401, GRNVAC1, вакцины на основе вирусов, от компании Advaxis MVA-BN, PROSTVAC®, ADXS11-001, ADXS31-001, ADXS31-164, BiovaxID, фолат-связывающий белок (E39), гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF) с и без E75 (NeuVax) или OncoVEX, трастузумаб, Ae-37, IMA901, SC1B1, стимувакс, пептиды, способные вызывать ответ цитотоксических лимфоцитов, пептидные вакцины, включая вакцину на основе теломеразных пептидов (GV1001), пептидов сурвивина, пептидов MUC1, пептидов ras, пептидов с усиленным эпитопом TARP 29-37-9V, ДНК вектор pPRA-PSM с синтетическими пептидами E-PRA и E-PSM, вакцину Ad.p53 DC, плазмидную ДНК NY-ESO-1 (pPJV7611), генетически модифицированные аллогенные (человеческие) клетки опухолей для экспрессии IL-1, IL-7, GM-CSF, CD80 или CD154, вакцину против рака поджелудочной железы HyperAcute(R) (компоненты HAPa-1 и HAPa-2), Melaxin (аутологичная вакцина на основе дендритом) и BCG, GVAX (CG8123), модифицированные по CD40-лиганду и гену IL-2 аутологичные кожные фибробласты и клетки опухолей, ALVAC-hB7.1, от компании Vaximm Gmbh VXM01, от компании Immunovative Therapies AlloStim-7, ProstAtak™, TG4023 (MVA-FCU1), от компании Antigenic HSPPC-96, от компании Immunovaccine Technologies DPX-0907, которая состоит из специфических HLA-A2-рестрицированных пептидов, универсальный T-хелперный пептид, полинуклеотидный адъювант, липосомы и монтанид (ISA51 VG), GSK2302032A, от компании Memgen ISF35, от компании Avax OVax: вакцину на основе DNP-модифицированных аутологичных клеток яичников, Theratope®, Ad100-gp96Ig-HLA A1, от компании Bioven вакцину на основе рекомбинантного человеческого rEGF-P64K/монтанида, TARP 29-37 или от компании Dendreon DN24-02.
В другом варианте осуществления иммунотерапевтическое средство действует через врожденную иммунную систему и при введении оказывает действие, которое заключается в активировании врожденного иммунитета против нежелательной раковой опухоли. В одном конкретном варианте осуществления настоящего изобретения используют иммунотерапевтическое средство, которое эффективно превращает опухоль-мишень в вакцину in situ (например, с использованием противоопухолевого средства, стимулирующего NKT клетки).
Например, данный вариант осуществления может включать образование аутологичных опухолеассоциированных антигенов (ОАА) у получающих лечение пациентов. α-Gal гликолипиды несут углеводный эпитоп α-gal (Galα1-3β1-4GlcNac-R), который связывает наиболее распространенное природное антитело у человека - анти-Gal антитело. Анти-Gal антитело присутствует в высоких концентрациях из-за постоянного экспонирования эпитопа α-Gal, который присутствует в бактериях. Ткани человека не содержат природных эпитопов α-Gal, поскольку это бы вызвало атаку иммунной системы на эти ткани. Таким образом, опухоли не являются уязвимыми для природных анти-α-Gal антител. Основным патентоспособным аспектом является то, что α-Gal гликолипиды, инъецированные в виде мицелл, встраиваются в мембраны клеток опухолей, что приводит к экспрессии α-Gal эпитопа на клетках опухолей, и таким образом, связыванию природного анти-Gal антитела. Таким образом, опухоль сама становится вакциной in situ. Взаимодействие Ag-эпитоп/Gal Ат приводит к активации комплемента и образованию при расщеплении компонентов системы комплемента хемотаксических факторов, которые рекрутируют антигенпредставляющие клетки (АПК). АПК переносят интернализированные ОАА к региональным лимфатическим узлам, процессируют и представляют многочисленные пептиды ОАА для активации опухолеспецифичных T-клеток. T-клетки пролиферируют, покидают лимфатические узлы и циркулируют, находя и уничтожая опухоль и любые микрометастазы, на которых представлены аутологичные ОАА.
Данная технология продемонстрировала высокую эффективность in vivo. Показано, что интратуморальная инъекция эпитопов α-gal, связанных с липидами, в модели на «нокаутных» мышах (т.е., мышах, у которых отсутствует эпитоп α-gal) с образовавшимися опухолями аденокарциномы значительного размера вызывает регрессию опухолей и предотвращает образование дистальных метастазов. Кроме того, проводимое на людях клиническое исследование с диапазоном доз (внесенное в реестр ND), в котором полученные в соответствии с требованиями GMP α-Gal липиды вводили 11 пациентам с аденокарциномами на поздней стадии, продемонстрировало безопасность системы и увеличение ожидаемой продолжительности жизни для ряда пациентов, включая пациентов с аденокарциномой поджелудочной железы. Дополнительную информацию в пользу данного иммунотерапевтического средства можно найти в патенте США №7820628, полное содержание которого включено в настоящий документ посредством ссылки.
В другом варианте осуществления изобретение относится к использованию β-маннозилцерамида (β-ManCer) для лечения пациентов. β-ManCer представляет собой агонист NKT, стимулирующий иммунитет против опухолей и инфекционных агентов с помощью механизмов, зависимых от оксида азота и TNFα. β-ManCer можно также использовать с α-GalCer для синергического усиления эффекта α-GalCer. β-ManCer может содержать фрагмент сфингозина и фрагмент жирной кислоты, содержащий линейную или разветвленную, насыщенную или ненасыщенную алифатическую углеводородную группу, имеющую от примерно 8 до примерно 49 атомов углерода, от примерно 18 до примерно 49 атомов углерода, от примерно 8 до примерно 15 атомов углерода или от примерно 18 до примерно 30 атомов углерода. В связанных вариантах осуществления β-ManCer имеет следующую структуру:
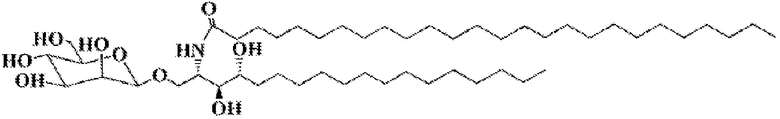 .
.
Дополнительную информацию в пользу данного иммунотерапевтического средства можно найти в международной патентной заявке № PCT/US2011/028024, полное содержание которой включено в настоящий документ посредством ссылки.
Соответственно, в одном аспекте настоящее изобретение относится к локальному совместному введению противоракового терапевтического средства и средства, усиливающего внутриклеточное проникновение, в терапевтически эффективных количествах и в соответствии с режимом введения, которые приводят к значительному уменьшению и/или уничтожению опухоли-мишени. Способ по изобретению дополнительно включает усиление действия терапевтического средства и средства, усиливающего внутриклеточное проникновение, путем введения иммунотерапевтического средства. Лечение приводит к значительному уменьшению и/или уничтожению клеток опухолей, любых микрометастазов или метастатических клеток, которые переместились в другие части тела. В одном из вариантов осуществления иммунотерапевтическое средство представляет собой противораковую вакцину, которая заставляет опухоль действовать как in situ вакцина, например, за счет включения эпитопов α-gal в опухоль.
Введение иммунотерапевтических средств по изобретению, например, противораковой вакцины (например, агонистов T-клеток), можно осуществлять с использованием любого подходящего подхода, в том числе локального или регионального введения средства в зону, поблизости или внутрь опухоли или микрометастазов. Средство также может быть доставлено, где это уместно, генно-терапевтическими методами. Например, в случае противораковой вакцины, которая основана на введении конкретного антитело-индуцирующего антигена в опухоль, антитело-индуцирующий антиген может быть введен путем инъекции или иным методом прямого введения генетического вектора или другой молекулы нуклеиновой кислоты, способной экспрессировать нужный антиген в опухоли. Сами антигены также могут быть непосредственно введены в ткань-мишень.
Виды раковых опухолей-мишеней
По настоящему изобретению предусмотрено лечение широкого спектра заболеваний, включая опухоли всех типов, местоположений, размеров и характеристик. Например, способ по изобретению подходит для лечения, например, рака поджелудочной железы и рака толстой кишки.
В других вариантах осуществления практически любой вид рака можно лечить способами по настоящему изобретению, включая следующие виды рака:
острый миелоидный лейкоз;
адренокортикальная карцинома;
Связанные со СПИДом виды рака;
связанная со СПИДом лимфома;
рак анального канала;
рак аппендикса;
астроцитома, детская, мозжечковая или церебральная;
базально-клеточная карцинома;
рак желчных протоков, внепеченочный;
рак мочевого пузыря;
рак кости, остеосаркома/злокачественная фиброзная гистиоцитома;
глиома ствола мозга;
опухоль мозга;
опухоль мозга, мозжечковая астроцитома;
опухоль мозга, церебральная астроцитома/злокачественная глиома;
опухоль мозга, эпендимома;
опухоль мозга, медуллобластома;
опухоль мозга, супратенториальные примитивные нейроэктодермальные опухоли;
опухоль мозга, глиома зрительного пути и гипоталамуса;
рак молочной железы;
бронхиальные аденомы/карциноиды;
лимфома Беркитта;
карциноидная опухоль, детская;
карциноидная опухоль, желудочно-кишечная;
карцинома с неизвестной первичной локализацией;
лимфома центральной нервной системы, первичная;
мозжечковая астроцитома, детская;
церебральная астроцитома/Злокачественная глиома, детская;
рак шейки матки;
детский рак;
хронический лимфоцитарный лейкоз;
хронический миелогенный лейкоз;
хронические миелопролиферативные заболевания;
рак толстой кишки;
Т-клеточная лимфома кожи;
десмопластическая мелкокруглоклеточная опухоль;
рак эндометрия;
эпендимома;
рак пищевода;
саркома Юинга в семействе опухолей Юинга;
экстракраниальная опухоль из зародышевых клеток, детская;
внегонадная герминогенная опухоль;
рак внепеченочных желчных протоков;
рак глаз, внутриглазная меланома;
рак глаз, ретинобластома;
рак желчного пузыря;
гастральный рак (желудка);
карциноидная опухоль желудочно-кишечного тракта;
стромальная опухоль желудочно-кишечного тракта (GIST);
герминома: экстракраниальная, внегонадная или яичников;
гестационная трофобластическая опухоль;
глиома ствола мозга;
глиома, детская церебральная астроцитома;
глиома зрительного пути и гипоталамуса, детская;
карциноид желудка;
волосатоклеточный лейкоз;
рак головы и шеи;
рак сердца;
печеночно-клеточный рак (печени);
лимфома Ходжкина;
гипофарингеальный рак;
глиома гипоталамуса и зрительного пути, детская;
внутриглазная меланома;
карцинома островковых клеток поджелудочной железы (эндокринная, поджелудочной железы);
саркома Капоши;
рак почки (почечно-клеточный рак);
рак гортани;
лейкозы;
лейкоз, острый лимфобластный (также называемый острым лимфоцитарным лейкозом);
лейкоз, острый миелоидный (также называемый острым миелогенным лейкозом);
лейкоз, хронический лимфоцитарный (также называемый хроническим лимфоцитарным лейкозом);
лейкоз, хронический миелогенный (также называемый хроническим миелоидным лейкозом);
лейкоз, волосатоклеточный;
рак губы и ротовой полости;
липосаркома;
рак печени (первичный);
рак легкого, немелкоклеточный;
рак легкого, мелкоклеточный;
лимфомы;
лимфома, связанная со СПИДом;
лимфома Беркитта;
лимфома, Т-клеточная кожная;
лимфома Ходжкина;
лимфомы, неходжкинские (старая классификация всех лимфом, кроме лимфомы Ходжкина);
лимфома, первичная, центральной нервной системы;
макроглобулинемия Вальденстрема;
злокачественная фиброзная гистиоцитома кости/остеосаркома;
медуллобластома, детская;
меланома;
меланома, Внутриглазная (глаза);
меркель-клеточная карцинома;
мезотелиома, взрослых, злокачественная;
мезотелиома, детская;
метастатический плоскоклеточный рак шеи с клинически неиндентифицированной первичной опухолью;
рак ротовой полости;
синдром множественной эндокринной неоплазии, детский;
множественная миелома/новообразование плазматических клеток;
фунгоидный микоз;
миелодиспластические синдромы;
миелодиспластические/миелопролиферативные заболевания;
миелогенный лейкоз, хронический;
миелоидный лейкоз, взрослых, острый;
миелоидный лейкоз, детский, острый;
миелома, множественная (рак костного мозга);
миелопролиферативные заболевания, хронические;
рак носовой полости и придаточных пазух;
назофарингеальная карцинома;
нейробластома;
неходжкинская лимфома;
немелкоклеточный рак легкого;
рак полости рта;
рак ротоглотки;
остеосаркома/злокачественная фиброзная гистиоцитома кости;
рак яичников;
эпителиальный рак яичников (поверхностная эпителиально-стромальная опухоль);
герминогенная опухоль яичников;
опухоль яичников с низким злокачественным потенциалом;
рак поджелудочной железы;
рак поджелудочной железы, островковых клеток;
рак придаточных пазух носа и носовой полости;
рак паращитовидной железы;
рак полового члена;
рак глотки;
феохромоцитома;
астроцитома шишковидной железы;
герминома шишковидной железы;
пинеобластома и супратенториальные примитивные нейроэктодермальные опухоли, детские;
аденома гипофиза;
неоплазия плазматических клеток/множественная миелома;
плевролегочная бластома;
первичная лимфома центральной нервной системы;
рак предстательной железы;
рак прямой кишки;
почечно-клеточная карцинома (рак почки);
рак почечной лоханки и мочеточника, переходно-клеточный;
ретинобластома;
рабдомиосаркома, детская;
рак слюнных желез;
саркома, семейство опухолей Юинга;
саркома Капоши;
саркома мягких тканей;
саркома матки;
синдром Сезари;
рак кожи (не меланома);
рак кожи (меланома);
карцинома кожи, Меркель-клеточная;
мелкоклеточный рак легкого;
рак тонкого кишечника;
саркома мягких тканей;
плоскоклеточная карцинома – см. рак кожи (не меланома);
плоскоклеточный рак шеи с клинически неиндентифицированной первичной опухолью, метастатический;
рак желудка;
супратенториальные примитивные нейроэктодермальные опухоли, детские;
T-клеточная лимфома, кожи – см. фунгоидный микоз и синдром Сезари;
рак яичка;
рак горла;
тимома, детская;
тимома и карцинома тимуса;
рак щитовидной железы;
рак щитовидной железы, детский;
переходно-клеточный рак почечной лоханки и мочеточника;
трофобластическая опухоль, гестационная;
карцинома, с клинически неиндентифицированной первичной опухолью, взрослых;
рак, с клинически неиндентифицированной первичной опухолью, детский;
переходно-клеточный рак мочеточника и почечной лоханки;
рак уретры;
рак тела матки, эндометрия;
саркома матки;
рак влагалища;
глиома зрительного пути и гипоталамуса, детская;
рак вульвы;
макроглобулинемия Вальденстрема;
опухоль Вильмса (рак почки), детская.
Специалистам в данной области понятно, как классифицируются раковые опухоли. Как правило, раковые опухоли классифицируются по типу клеток, которые опухолевые клетки напоминают, и, следовательно, которые предположительно дают начало опухоли. Эти типы включают следующее:
- карцинома: раковые опухоли развиваются из эпителиальных клеток. Эта группа включает многие из наиболее распространенных видов рака, особенно у пожилых людей, и включает почти все опухоли, образующиеся в молочной железе, предстательной железе, легких, поджелудочной железе и толстой кишке.
- Саркома: раковые опухоли развиваются из соединительной ткани (т.е., кости, хряща, жира, нервов), каждая из них развивается из клеток, происходящих из мезенхимальных клеток за пределами костного мозга.
- Лимфома и лейкоз: эти два класса раковых опухолей возникают из гемопоэтических (кроветворных) клеток, которые покидают костный мозг и, как правило, созревают в лимфатических узлах и крови, соответственно.
- Герминогенная опухоль: раковые опухоли развиваются из плюрипотентных клеток, наиболее часто возникают в яичках или яичниках (семинома и дисгерминома, соответственно).
- Бластома: раковые опухоли развиваются из незрелых клеток-«предшественников» или эмбриональной ткани. Они также наиболее часто встречаются у детей.
Кроме того, следует иметь в виду, что раковые опухоли, как правило, называют с использованием слов карцинома, саркома или бластома в качестве добавления к названию, основу которого составляет латинское или греческое название органа или ткани, из которых они происходят. Например, раковую опухоль паренхимы печени, возникающую из злокачественных эпителиальных клеток, называют гепатокарциномой, в то время как злокачественное новообразование, возникающее из примитивных клеток-предшественников печени, называют гепатобластомой, и раковую опухоль, возникающую из жировых клеток, называют липосаркомой. Для некоторых наиболее распространенных видов рака используют общепринятое название органа. Например, наиболее распространенный вид рака молочной железы называют карциномой протоков молочной железы. В настоящем описании слово «протоков» относится к микроскопическому изображению опухоли, из которого следует, что она образована в молочных протоках.
Доброкачественные опухоли (которые не являются раковыми) имеют названия, оканчивающиеся на «ома», при этом корнем слова является название органа. Например, доброкачественная опухоль гладкомышечных клеток называется лейомиома (общим названием этой часто встречающейся доброкачественной опухоли в матке является «фиброма»). По непонятной причине, в названиях некоторых видов рака также используется окончание «ома», например, меланома и семинома.
Некоторые виды раковых опухолей получили название на основании размера и формы клеток под микроскопом, например, гигантоклеточная карцинома, веретеноклеточная карцинома и мелкоклеточная карцинома.
Настоящее изобретение, в целом, направлено на лечение всех вышеперечисленных форм рака. Например, способ по изобретению предпочтительно можно использовать в лечении солидных опухолей, возникающих в любой ткани организма, включая, но не ограничиваясь ими, кожу, кость, мышцы, молочную железу, органы, почку, печень, легкое, желчный пузырь, поджелудочную железу, головной мозг, пищевод, мочевой пузырь, толстый кишечник, тонкий кишечник, селезенку, желудок, предстательную железу, яички, яичники или матку.
Настоящее изобретение, в целом, также направлено на лечение всех вышеперечисленных форм рака и при этом на любой его стадии. Специалистам понятно, что степень тяжести рака обозначают стадиями (I-IV), при этом прогноз выживаемости на стадиях III и IV часто бывает неблагоприятным при некоторых видах рака.
Настоящее изобретение также может быть эффективным в лечении опухолей, которые образуются из метастазов от другого источника или первичной опухоли. Участки метастазов могут быть видимыми опухолями, или могут также быть на уровне одиночных клеток, или микрометастазов.
В одном из вариантов осуществления настоящее изобретение относится к способу лечения опухоли поджелудочной железы или образовавшей метастазы опухоли поджелудочной железы.
В одном из иллюстративных вариантов осуществления настоящее изобретение относится к способу лечения опухоли толстой кишки или образовавшей метастазы опухоли толстой кишки.
Замедление роста опухоли означает поддающееся измерению замедление роста опухоли по меньшей мере примерно в 0,01 раза (например, 0,01, 0,1, 1, 3, 4, 5, 10, 100, 1000 раз или более) или замедление на по меньшей мере примерно 0,01% (например, 0,01, 0,1, 1, 3, 4, 5, 10, 20, 30, 40, 50, 60, 70, 80, 90, 95, 99 или 100%) по сравнению с ростом, измеренным в динамике до начала лечения, описанного в настоящем документе.
Полной ликвидации опухоли также можно достичь при помощи способов по изобретению. Ликвидация означает элиминацию опухоли. Опухоль считают элиминированной, когда ее становится невозможно обнаружить с использованием методов обнаружения, известных в данной области (например, визуализации).
Фармацевтические композиции
Изобретение относится к фармацевтическим композициям для использования в любом из способов, описанных в настоящем документе. Фармацевтические композиции содержат терапевтическое средство, средство, усиливающее внутриклеточное проникновение, и/или иммунотерапевтическое средство.
В вариантах осуществления фармацевтические композиции содержат фармацевтически приемлемый носитель. Термин «фармацевтически приемлемый» означает одобренный регулирующим органом федерального или государственного правительства или перечисленный в фармакопее США, европейской фармакопее или других общепризнанных фармакопеях для применения к животным, и более конкретно, к человеку. Термин «носитель» означает разбавитель, адъювант, эксципиент или среду, с которыми вводят терапевтическое средство. Такие фармацевтические носители могут представлять собой стерильные жидкости, такие как вода и масла, в том числе из нефти, животного, растительного или синтетического происхождения, например, арахисовое масло, соевое масло, минеральное масло, кунжутное масло, оливковое масло, гель (например, гидрогель) и тому подобное. Солевой раствор является предпочтительным носителем, если фармацевтическую композицию вводят внутривенно. Солевые растворы, а также водные растворы декстрозы и глицерина также можно использовать в качестве жидких носителей, особенно для инъекционных растворов.
Подходящие фармацевтические эксципиенты включают крахмал, глюкозу, лактозу, сахарозу, желатин, солод, рис, муку, мел, силикагель, стеарат натрия, моностеарат глицерина, тальк, хлорид натрия, сухое снятое молоко, глицерин, пропиленгликоль, воду, этанол и тому подобное. Композиция, при желании, может также содержать незначительные количества смачивающих или эмульгирующих веществ, или средства для поддержания pH. Эти композиции можно принимать в форме растворов, суспензий, эмульсий, таблеток, пилюль, капсул, порошков, составов с замедленным высвобождением и тому подобного. Пероральный состав может включать стандартные носители, такие как фармацевтической категории маннит, лактоза, крахмал, стеарат магния, сахаринат натрия, целлюлоза, карбонат магния и так далее. Примеры подходящих фармацевтических носителей приведены в книге «Remington's Pharmaceutical Sciences» автора E.W. Martin, полное содержание которой включено в настоящий документ посредством ссылки. Такие композиции, как правило, содержат терапевтически эффективное количество терапевтического средства, средства, усиливающего внутриклеточное проникновение, и/или иммунотерапевтического средства в очищенном виде вместе с подходящим количеством носителя для создания формы, подходящей для правильного введения пациенту. Состав должен соответствовать способу введения.
В вариантах осуществления терапевтическое средство, средство, усиливающее внутриклеточное проникновение, или их сочетание и/или иммунотерапевтическое средство вводят локально в виде композиции немедленного высвобождения или контролируемого высвобождения, например, за счет контролируемого растворения и/или диффузии активного вещества. Высвобождение, контролируемое растворением или диффузией, может быть достигнуто путем включения активного вещества в соответствующую матрицу. Матрица контролируемого высвобождения может содержать одно или более из шеллака, пчелиного воска, гликовакса, гидрированного касторового масла, карнаубского воска, стеарилового спирта, глицерилмоностеарата, глицерилдистеарата, глицеринпальмитостеарата, этилцеллюлозы, акриловых смол, dl-полимолочной кислоты, ацетобутирата целлюлозы, поливинилхлорида, поливинилацетата, винилпирролидона, полиэтилена, полиметакрилата, метилметакрилата, 2-гидроксиметакрилата, метакрилатных гидрогелей, 1,3-бутиленгликоля, этиленгликоль метакрилата и/или полиэтиленгликолей. В составе с матрицей контролируемого высвобождения материал матрицы может также включать, например, гидратированную метилцеллюлозу, карнаубский воск и стеариловый спирт, карбопол 934, силикон, глицерилтристеарат, сополимер метилакрилат-метилметакрилат, поливинилхлорид, полиэтилен и/или галогенированный фторуглерод.
В связанных вариантах осуществления матрица контролируемого высвобождения представляет собой гидрогель. Гидрогель представляет собой трехмерную, гидрофильную или амфифильную полимерную сеть, способную поглощать большое количество воды. Сети состоят из гомополимеров или сополимеров, которые нерастворимы из-за наличия ковалентных химических или физических (например, ионных, гидрофобных взаимодействий, переплетений) сшивок. Сшивки обеспечивают структуру и физическую целостность сети. Гидрогели обладают термодинамической совместимостью с водой, что позволяет им набухать в водной среде. Цепи сети соединены таким образом, что образуются поры, и значительная часть этих пор имеет размеры от 1 нм до 1000 нм.
Гидрогели можно получать путем сшивки гидрофильных биополимеров или синтетических полимеров. Примеры гидрогелей, образованных в результате физических или химических сшивок гидрофильных биополимеров, включают, но не ограничиваются ими, гиалуронаны, хитозаны, альгинаты, коллаген, декстран, пектин, каррагинан, полилизин, желатин, агарозу, (мет)акрилат-олиголактид-ПЭО-олиголактид-(мет)акрилат, поли(этиленгликоль) (ПЭО), поли(пропиленгликоль) (ППО), сополимеры ПЭО-ППО-ПЭО (плюроники), поли(фосфазен), поли(метакрилаты), поли(N-винилпирролидон), сополимеры ПМ(Г)К-ПЭО-ПМ(Г)К, поли(этиленимин) и тому подобное. См. Hennink and van Nostrum, Adv. Drug Del. Rev. 54: 13-36 (2002); Hoffman, Adv. Drug Del. Rev. 43: 3-12 (2002); Cadee et al., J Control. Release 78: 1-13 (2002); Surini et al., J. Control. Release 90: 291-301 (2003) и патент США №7968085, полное содержание каждого из которых включено в настоящий документ посредством ссылки. Эти материалы состоят из высокомолекулярных каркасных цепей, образованных линейными или разветвленными полисахаридами или полипептидами.
Количество фармацевтической композиции по изобретению, которое будет эффективным для лечения или предотвращения солидных опухолей, может зависеть от природы опухоли и может быть определено стандартными клиническими методами, в том числе методами визуализации. Кроме того, при желании можно использовать анализы in vitro для определения оптимальных диапазонов доз. Точная доза, используемая в составе, может также зависеть от пути введения и степени тяжести опухоли, и должна быть определена на основании решения лечащего врача и обстоятельств каждого пациента. Эффективные дозы можно экстраполировать из кривых «доза-ответ», полученных в тест-системах in vitro или на животных моделях.
Дозировки и режимы введения
Терапевтические средства, средства, усиливающие внутриклеточное проникновение, иммунотерапевтические средства или композиции, содержащие эти средства, вводят способом, совместимым с лекарственным составом, и в таком количестве, которое может быть терапевтически эффективным, обеспечивающим защиту и иммуногенным.
Средства и/или композиции можно вводить различными путями, включая, но не ограничиваясь ими, пероральный, парентеральный, трансбуккальный и подъязычный, ректальный, ингаляцию, назальный, внутримышечный, подкожный, внутрикожный и местный. Используемый в настоящем документе термин «парентеральный» включает, например, внутриглазную, подкожную, внутрибрюшинную, внутрикожную, внутривенную, внутримышечную, внутрисуставную, внутриартериальную, интрасиновиальную, интрастернальную, интратекальную, внутриочаговую и интракраниальную инъекцию или другие методы инфузии.
В вариантах осуществления введение терапевтических средств и/или средства, усиливающего внутриклеточное проникновение, осуществляют локально или регионально (например, интратуморально).
В вариантах осуществления средства и/или композиции, сформулированные в соответствии с настоящим изобретением, формулируют и доставляют таким образом, чтобы вызвать системный иммунный ответ. Таким образом, в вариантах осуществления составы получают однородным и тщательным смешиванием активного ингредиента с жидкими носителями. Составы, подходящие для введения, включают водные и неводные стерильные растворы, которые могут содержать антиокислители, буферы, бактериостатические средства и растворенные вещества, которые делают этот состав изотоническим с кровью реципиента, а также водные и неводные стерильные суспензии, которые могут содержать суспендирующие средства и загустители. Составы могут находиться в однодозовых или многодозовых контейнерах, например, запаянных ампулах и флаконах, и могут храниться в сублимированном (лиофилизированном) состоянии, требующем лишь добавления стерильного жидкого носителя, например воды, непосредственно перед использованием. Растворы и суспензии для немедленного использования можно получать из стерильных порошков, гранул и таблеток, обычно используемых специалистами в данной области.
Средства и/или композиции можно вводить в различных формах, включая, но не ограничиваясь ими, растворы, эмульсии и суспензии, микросферы, частицы, микрочастицы, наночастицы, липосомы и тому подобное.
Средства и/или композиции вводят способом, совместимым с лекарственным составом, и в таком количестве, которое может быть терапевтически эффективным, иммуногенным и обеспечивающим защиту. Вводимое количество зависит от субъекта, которого предстоит лечить, включая, например, размер конкретной опухоли, стадию заболевания и способность иммунной системы индивидуума синтезировать антитела и/или продуцировать клеточно-опосредованный иммунный ответ. Точные количества активных ингредиентов, необходимых для введения, зависят от решения лечащего врача. Однако подходящие диапазоны доз могут быть легко определены специалистом в данной области и могут составлять от нескольких микрограмм до нескольких миллиграмм активного ингредиента(ов) на дозу. Дозировка может также зависеть от пути введения и может варьироваться в зависимости от размеров хозяина.
Средства и/или композиции следует вводить субъекту в количестве, эффективном для стимуляции защитного иммунного ответа у субъекта. Конкретная дозировка и режимы лечения для каждого конкретного субъекта могут зависеть от различных факторов, включая активность конкретного используемого соединения, возраст, массу тела, общее состояние здоровья, пол, диету, время введения, скорость выведения, сочетание лекарственных средств, степень тяжести и протекание заболевания (в том числе размер опухоли), состояние или симптомы, предрасположенность субъекта к заболеванию, состояние или симптомы, способ введения и решение лечащего врача. Фактические дозировки может легко определять специалист в данной области.
Иллюстративные составы в стандартной лекарственной форме представляют собой составы, содержащие дозу или единицу вводимого ингредиента, или ее соответствующую часть. Следует понимать, что в дополнение к ингредиентам, упомянутым в настоящем документе, составы по настоящему изобретению могут содержать другие средства, обычно используемые специалистами в данной области.
Как правило, при использовании обычных системно вводимых терапевтических средств терапевтически эффективная доза должна создавать в сыворотке концентрацию соединения от примерно 0,1 нг/мл до примерно 50-100 мкг/мл. Фармацевтические композиции, как правило, используют в дозах от примерно 0,001 мг до примерно 2000 мг соединения на килограмм массы тела в сутки. Например, дозы для системного введения пациенту-человеку могут находиться в диапазоне 1-10 мкг/кг, 20-80 мкг/кг, 5-50 мкг/кг, 75-150 мкг/кг, 100-500 мкг/кг, 250-750 мкг/кг, 500-1000 мкг/кг, 1-10 мг/кг, 5-50 мг/кг, 25-75 мг/кг, 50-100 мг/кг, 100-250 мг/кг, 50-100 мг/кг, 250-500 мг/кг, 500-750 мг/кг, 750-1000 мг/кг, 1000-1500 мг/кг, 1500-2000 мг/кг, 5 мг/кг, 20 мг/кг, 50 мг/кг, 100 мг/кг, 500 мг/кг, 1000 мг/кг, 1500 мг/кг или 2000 мг/кг. Фармацевтические стандартные лекарственные формы готовят так, чтобы получать от примерно 1 мг до примерно 5000 мг, например, от примерно 100 до примерно 2500 мг, соединения или сочетания необходимых ингредиентов на стандартную лекарственную форму.
В целом, терапевтически эффективное количество настоящих соединений в лекарственной форме, как правило, находится в диапазоне от немного менее чем примерно 0,025 мг/кг/сутки до примерно 2,5 г/кг/сутки, предпочтительно от примерно 0,1 мг/кг/сутки до примерно 100 мг/кг/сутки для пациента или значительно более, в зависимости от используемого соединения, состояния или подвергаемой лечению инфекции, а также пути введения, хотя исключения из данного диапазона доз могут быть предусмотрены по настоящему изобретению. В иллюстративном варианте осуществления соединения, усиливающие внутриклеточное проникновение, по настоящему изобретению можно вводить интратуморально в диапазоне количеств от примерно 0,5 мг/мл до примерно 50 мг/мл дозируемого раствора. В другом иллюстративном варианте осуществления соединения, усиливающие внутриклеточное проникновение, по настоящему изобретению можно вводить интратуморально в диапазоне количеств от примерно 10 мг/мл до примерно 30 мг/мл. Доза соединения(ий), усиливающего внутриклеточное проникновение, может зависеть от вида рака, который подвергают лечению, конкретного используемого соединения, терапевтического средства и других клинических факторов, а также от состояния пациента и пути введения. Следует понимать, что настоящее изобретение может быть использовано как в медицине, так и в ветеринарии.
Средства и/или композиции вводят в одной или более дозах, по мере необходимости, для достижения желаемого эффекта. Таким образом, средства и/или композиции можно вводить в 1, 2, 3, 4, 5 или более дозах. Кроме того, дозы могут быть разделены любым периодом времени, например, несколько часов, дней, недель, месяцев и лет.
Средства и/или композиции можно формулировать в виде жидкостей или порошков, или в форме микросфер.
Средства и/или композиции можно хранить при температурах от примерно -100°C до примерно 25°C в зависимости от продолжительности хранения. Средства и/или композиции можно также хранить в лиофилизированном состоянии при различных температурах, включая комнатную температуру. Средства и/или композиции можно стерилизовать общепринятыми методами, известными специалистам в данной области. Такие методы включают, но не ограничиваются ими, фильтрование. Композицию можно также объединять с бактериостатическими средствами для ингибирования роста бактерий.
Количество активного ингредиента, который можно объединять с материалами носителя для получения стандартной лекарственной формы, может варьироваться в зависимости от получающего лечение хозяина и конкретного способа введения. В вариантах осуществления препарат может содержать от примерно 0,1% до примерно 95% активного соединения (по массе), от примерно 20% до примерно 80% активного соединения, или любой процент в этом диапазоне.
В вариантах осуществления pH состава можно доводить фармацевтически приемлемыми кислотами, основаниями или буферами для повышения стабильности сформулированного соединения или его формы для доставки.
В вариантах осуществления фармацевтические носители могут находиться в виде стерильного жидкого препарата, например, в виде стерильной водной или маслянистой суспензии.
В число приемлемых носителей и растворителей, которые можно использовать, входят маннит, вода, раствор Рингера и изотонический раствор хлорида натрия.
Кроме того, стерильные нелетучие масла обычно используют в качестве растворителя или суспензионной среды. Для этой цели можно использовать любое мягкое нелетучее масло, включая синтетические моно- или диглицериды. Жирные кислоты, такие как олеиновая кислота и ее глицеридные производные, полезны для получения инъекционных препаратов, так же, как и природные фармацевтически приемлемые масла, например, оливковое масло или касторовое масло, особенно в их полиоксиэтилированных вариантах. Такие масляные растворы или суспензии могут также содержать разбавитель из длинноцепного спирта или диспергатор, или карбоксиметилцеллюлозу или аналогичные диспергирующие средства, которые обычно используют в фармацевтически приемлемых лекарственных формах состава, таких как эмульсии и/или суспензии.
Другие обычно используемые поверхностно-активное вещества, такие как TWEEN® или SPAN®, и/или другие аналогичные эмульгаторы или усилители биодоступности, которые обычно используют в производстве фармацевтически приемлемых твердых, жидких или других лекарственных форм, также можно использовать для создания состава.
В вариантах осуществления средства и/или композиции можно доставлять при помощи экзосомальной системы доставки. Экзосомы представляют собой небольшие мембранные везикулы, которые попадают во внеклеточную среду в процессе слияния мультивезикулярных тел с плазматической мембраной. Экзосомы секретируются клетками различных типов, включая гемопоэтические клетки, нормальные эпителиальные клетки и даже некоторые клетки опухолей. Известно, что экзосомы несут молекулы MHC класса I, различные костимулирующие молекулы и некоторые тетраспанины. Недавние исследования показали потенциал использования природных экзосом в качестве иммунологических стимуляторов.
По изобретению также предусмотрена доставка средств и/или композиций с помощью наночастиц. Например, средства и/или композиции, предложенные в настоящем документе, могут содержать наночастицы с присоединенным к ним по меньшей мере одним или более средствами, например, связанными с поверхностью наночастиц. Композиция, как правило, содержит множество наночастиц, при этом каждая наночастица имеет по меньшей мере одно или более средств, связанных с ней. Наночастицы могут представлять собой коллоидные металлы. Коллоидный металл включает любую нерастворимую в воде металлическую частицу или металлическое соединение, диспергированное в жидкой воде. Как правило, коллоидный металл представляет собой суспензию металлических частиц в водном растворе. Можно использовать любой металл, который можно получать в коллоидной форме, включая золото, серебро, медь, никель, алюминий, цинк, кальций, платину, палладий и железо. В некоторых случаях используют наночастицы золота, например, полученные из HAuCl4. Наночастицы могут быть любой формы и иметь диапазон размеров от примерно 1 нм до примерно 10 нм, например, от примерно 2 нм до примерно 8 нм, от примерно 4 до примерно 6 нм или примерно 5 нм. Методы получения коллоидных металлических наночастиц, включая коллоидные наночастицы золота из HAuCl4, известны специалистам в данной области. Например, способы, описанные в настоящем документе, а также те, которые описаны в другой литературе (например, патентных публикациях США №№2001/005581, 2003/0118657 и 2003/0053983, которые включены в настоящий документ посредством ссылки), являются полезными руководствами для получения наночастиц.
В некоторых случаях наночастица может иметь два, три, четыре, пять, шесть или более активных средств, связанных с ее поверхностью. Как правило, многие молекулы активных средств связаны с поверхностью наночастицы во многих участках. Соответственно, если наночастицу описывают как имеющую, например, два активных средства, связанных с ней, наночастица имеет два активных средства, каждое из которых имеет собственную уникальную молекулярную структуру, связанную с ее поверхностью. В некоторых случаях одна молекула активного средства может быть связана с наночастицей на одном сайте связывания или на нескольких сайтах связывания.
Активное средство может быть связано непосредственно или опосредованно с поверхностью наночастицы. Например, активное средство может быть связано непосредственно с поверхностью наночастицы или опосредованно через промежуточный линкер.
Молекулу любого типа можно использовать в качестве линкера. Например, линкер может представлять собой алифатическую цепь, содержащую по меньшей мере два атома углерода (например, 3, 4, 5, 6, 7, 8, 9, 10 или более атомов углерода), и может быть замещен одной или более функциональными группами, включая кетоновую, эфирную, сложноэфирную, амидную, спиртовую, аминовую, мочевинную, тиомочевинную, сульфоксидную, сульфоновую, сульфонамидную и дисульфидную функциональные группы. В тех случаях, когда наночастица содержит золото, линкер может быть любой тиол-содержащей молекулой. Реакция тиоловой группы с золотом приводит к образованию ковалентной сульфидной (-S-) связи. Проектирование и синтез линкеров хорошо известны в данной области.
В вариантах осуществления наночастица связана с направляющим средством/фрагментом. Направляющая функциональная группа позволяет наночастицам накапливаться в мишени в более высоких концентрациях, чем в других тканях. Как правило, направляющая молекула может быть одним членом связывающейся пары, который проявляет аффинность и специфичность в отношении второго члена связывающейся пары. Например, терапевтическое средство на основе антитела или фрагмента антитела может направлять наночастицу к конкретной области или молекуле тела (например, области или молекуле, для которой данное антитело специфично), при этом также выполняя терапевтическую функцию. В некоторых случаях рецептор или фрагмент рецептора может направлять наночастицу в конкретную область тела, например, к местонахождению члена его связывающейся пары. Другие терапевтические средства, такие как малые молекулы, могут аналогично направлять наночастицу к рецептору, белку или другому сайту связывания, имеющему аффинность для терапевтического средства.
Если композиции по данному изобретению содержат одно или более дополнительных терапевтических или профилактических средств, терапевтическое/усиливающее/иммунотерапевтическое средство и дополнительное средство должны присутствовать в уровнях доз от примерно 0,1 до 100% или от примерно 5 до 95% дозы, обычно вводимой в режиме монотерапии. Дополнительные средства можно вводить отдельно, как часть режима многократных доз для средств по данному изобретению. Альтернативно, эти дополнительные средства могут быть частью одной лекарственной формы, смешанными со средствами по данному изобретению в одной композиции.
Введение средств и/или композиций по изобретению вызывает иммунный ответ против иммуногена, например, ракового антигена. Как правило, дозу можно корректировать в данном диапазоне, исходя, например, из возраста субъекта, состояния здоровья и физического состояния субъекта, способности иммунной системы субъекта продуцировать иммунный ответ, массы тела субъекта, пола субъекта, диеты, времени введения, желаемой степени защиты и других клинических факторов. Специалисты в данной области могут также рассматривать такие параметры, как биологический период полувыведения, биодоступность, путь введения и токсичность, при формулировании средств и/или композиций по изобретению.
Следующие примеры дополнительно демонстрируют некоторые варианты осуществления данного изобретения. При том, что примеры иллюстрируют изобретение, они не предназначены для его ограничения.
ПРИМЕРЫ
Структуры, материалы, композиции и способы, описанные в настоящем документе, предназначены быть репрезентативными примерами по изобретению, и следует понимать, что объем изобретения не ограничивается объемом примеров. Специалистам в данной области будет понятно, что изобретение можно осуществлять на практике с вариациями описанных структур, материалов, композиций и способов, и такие вариации считаются входящими в объем изобретения.
Пример 1
Получение раствора для дозирования 1: 167 мг NaOH растворяли в 20 мл деионизированной воды, получая 0,21 молярный раствор гидроксида натрия. Восемьдесят (80) мг 6-оксо-6-фенилгексановой кислоты (полученной от Rieke Metals, Lincoln Nebraska) взвешивали и растворяли в 2 мл 0,21 нормального раствора гидроксида натрия. В отдельном контейнере 6,2 мг цис-диаминодихлорплатины (полученной от Tocris Bioscience, Elisville MO) растворяли в 2,5 мл деионизированной воды. Каждый материал перемешивали на вихревой мешалке в течение 1 минуты и обрабатывали ультразвуком в течение 15 минут. 1,25 мл раствора 6-оксо-6-фенилгексановой кислоты смешивали с 2,5 мл раствора цис-диаминодихлорплатины и перемешивали на вихревой мешалке в течение 1 минуты. pH полученного прозрачного раствора измерили и определили, что он составляет примерно 5,5. Двадцать (20) микролитров 1 Н гидроксида натрия добавляли к объединенному раствору. pH измерили и определили, что он составляет примерно 6,8. Объем доводили до 5 мл путем добавления примерно 1,2 мл деионизированной воды.
Пример 2
Получение раствора для дозирования 2: Восемьдесят (80) мг 6-оксо-6-фенилгексановой кислоты (полученной от Rieke Metals, Lincoln Nebraska) взвешивали и растворяли в 2 мл 0,21 нормального раствора гидроксида натрия, как описано в примере 1. В отдельном контейнере 20 мг цис-диамин(1,1-циклобутандикарбоксилaт)платины (Sigma Aldrich C2538) растворяли в 2,5 мл деионизированной воды. Каждый материал перемешивали на вихревой мешалке в течение 1 минуты и обрабатывали ультразвуком в течение 15 минут. 1,25 мл раствора 6-оксо-6-фенилгексановой кислоты смешивали с 2,5 мл раствора цис-диамин(1,1-циклобутандикарбоксилaт)платины и перемешивали на вихревой мешалке в течение 1 минуты. pH полученного прозрачного объединенного раствора измерили и определили, что он составляет примерно 6,0. Десять (10) микролитров 1 Н гидроксида натрия добавляли к объединенному раствору. pH измерили и определили, что он составляет примерно 6,9. Объем доводили до 5 мл путем добавления примерно 1,2 мл деионизированной воды.
Пример 3
Получение раствора для дозирования 3: 137 мг NaOH растворяли в 20 мл деионизированной воды, получая 0,16 молярный раствор гидроксида натрия. Восемьдесят (80) микролитров 2-этилгексил-2-гидроксибензоата (полученного от ChemPacific, Baltimore Maryland) взвешивали и смешивали с 2 мл 0,16 нормального раствора гидроксида натрия. В отдельном контейнере 6,2 мг цис-диаминодихлорплатины (полученной от Tocris Bioscience, Elisville MO) растворяли в 2,5 мл деионизированной воды. Каждый материал перемешивали на вихревой мешалке в течение 1 минуты и обрабатывали ультразвуком в течение 15 минут. 1,25 мл раствора 2-этилгексил-2-гидроксибензоата смешивали с 2,5 мл раствора цис-диаминодихлорплатины и перемешивали на вихревой мешалке в течение 1 минуты. pH полученного прозрачного раствора измерили и определили, что он составляет примерно 11. Полученный объединенный раствор несколько раз титровали 50% раствором HCl и 2 Н раствором гидроксида натрия. После нескольких титрований pH измерили и определили, что он составляет примерно 6,8.
Пример 4
Получение раствора для дозирования 4: Восемьдесят (80) микролитров 2-этилгексил-2-гидроксибензоата (полученного от ChemPacific, Baltimore Maryland) взвешивали и смешивали с 2 мл 0,16 нормального раствора гидроксида натрия, как описано в примере 3. В отдельном контейнере 20 мг цис-диамин(1,1-циклобутандикарбоксилaт)платины (Sigma Aldrich C2538) растворяли в 2,5 мл деионизированной воды. Каждый материал перемешивали на вихревой мешалке в течение 1 минуты и обрабатывали ультразвуком в течение 15 минут. 1,25 мл раствора соли 2-этилгексил-2-гидроксибензоата смешивали с 2,5 мл раствора цис-диамин(1,1-циклобутандикарбоксилaт)платины и перемешивали на вихревой мешалке в течение 1 минуты. pH полученного прозрачного раствора измерили и определили, что он составляет примерно 11. Объединенный раствор несколько раз титровали 50% раствором HCl и 2 Н раствором гидроксида натрия. После нескольких титрований pH измерили и определили, что он составляет примерно 6,8.
Пример 5
30 мг 6-оксо-6-фенилгексановой кислоты добавляли к 1,5 мл 0,1 молярного гидроксида натрия, и pH доводили до примерно 7,0. Несколько капель черных чернил India добавляли к раствору усилителя проникновения и чернил с pH 7,0. 2×106 клеток BxPC-3-luc2 инокулировали в правый бок 9 самкам мышей C.B-17 scid. Рост опухоли контролировали раз или два раза в неделю путем измерения штангенциркулем до того момента, когда размеры опухоли достигали ~500 мм3. Биолюминесцентную визуализацию in vivo проводили в день введения химического раствора с чернилами, как показано на фигуре 1. 50 микролитров раствора усилителя вводили инъекцией в подкожные опухоли BxPC двух мышей с тяжелым комбинированным иммунодефицитом (scid), используя программируемый шприцевой насос с иглой-«бабочкой». Игла оставалась в опухолях еще в течение примерно 2 минут. После удаления иглы опухоли немедленно иссекали и исследовали; изучали эффективность полученного диспергирования чернил, результаты приведены на фигуре 2.
Пример 6
Двум мышам scid с подкожными опухолями BxPC вводили интратуморально 100 микролитров раствора усилителя с чернилами India, полученного в примере 5, в течение двух минут, используя программируемый шприцевой насос. Игла оставалась в опухолях еще в течение примерно 2 минут. После удаления иглы опухоли немедленно иссекали и исследовали; изучали эффективность полученного диспергирования чернил, результаты приведены на фигуре 3.
Пример 7
2×106 клеток BxPC-3-luc2 инокулировали в правый бок 32 самкам мышей C.B-17 scid. Рост опухоли контролировали раз или два раза в неделю путем измерения штангенциркулем до того момента, когда размеры опухоли достигали ~500 мм3. Двадцать четыре мыши с опухолями соответствующего размера выбрали для дозирования. Каждому выбранному животному на хвост был нанесен номер и такой же номер был на ушной метке. Информация об окончательных сформированных группах животных приведена в таблице 1.
Размер опухоли каждого животного измеряли штангенциркулем и животных делили на четыре группы таким образом, чтобы средние объемы опухолей (измеренных штангенциркулем) в каждой группе были схожими. Информация по группам приведена в таблице 2.
Затем животным вводили инъекцией люциферазу 3 для измерения опухоли при помощи биолюминесценции (БЛВ) на фотонном приборе Xenogen (компания Xenogen стала подразделением Caliper Life Sciences). Затем для четырех групп были определены режимы лечения. Животные первой группы получали интратуморально 100 микролитров усилителя 6-оксо-6-фенилгексановой кислоты, приготовленной в виде натриевой соли при pH примерно 7,0 и с концентрацией 13,3 мг/мл. Животные второй группы получали 100 микролитров цисплатина, введенного внутривенно в хвостовую артерию в буферном растворе в концентрации 1,2 мг/мл. Животные третьей группы получали интратуморально 100 микролитров цисплатина в буферном растворе в дозе примерно 0,45 мг/мл. Животным 4 группы вводили интратуморально 100 микролитров усилителя 6-оксо-6-фенилгексановой кислоты в форме натриевой соли с конечной концентрацией 13,3 мг/мл в сочетании с цисплатином в конечной концентрации 0,45 мг/мл.
Пример 8
Показания БЛВ для животных, которым вводили составы в примере 7, снимали через шесть часов после введения доз, 24 часа после введения доз и 72 часа после введения доз. Измерение опухолей штангенциркулем у животных во всех группах проводили перед дозированием и через 72 часа после введения доз. Результаты сравнения показателей БЛВ во временных точках исходного уровня, через 6 часов, 24 часа и 72 часа для животных приведены на фигуре 4.
Пример 9
Для животных, описанных в примере 7, проводили вторую серию инъекций после биолюминесцентного измерения их опухолей через 72 часа. Животные первой группы получали интратуморально 100 микролитров усилителя 6-оксо-6-фенилгексановой кислоты, приготовленной в виде натриевой соли при pH примерно 7,0 и с концентрацией 13,3 мг/мл. Животные второй группы получали 100 микролитров цисплатина, введенного внутривенно в хвостовую артерию в буферном растворе в концентрации 1,2 мг/мл. Животные третьей группы получали интратуморально 100 микролитров цисплатина в буферном растворе в дозе примерно 1,2 мг/мл. Животным 4 группы вводили интратуморально 100 микролитров усилителя 6-оксо-6-фенилгексановой кислоты в форме натриевой соли с конечной концентрацией 13,3 мг/мл в сочетании с цисплатином в конечной концентрации 1,2 мг/мл. Значения БЛВ для животных, получавших эти интратуморальные дозы цисплатина, оценивали через 3 дня исследования. Относительные значения БЛВ через 3 дня приведены на фигуре 5.
Пример 10
Для животных, описанных в примере 7, проводили третью серию инъекций после биолюминесцентного измерения их опухолей через 7 и 10 дней после начала эксперимента. Вводимые дозы в третьей серии процедур для каждой группы (1-4) были идентичны тем, которые вводили во второй серии процедур, описанной в примере 9. Значения БЛВ за весь период исследования приведены на фигуре 6. Относительные изменения значений БЛВ за весь период исследования приведены на фигуре 7. На фигуре 8 показаны изменения массы тела от начала исследования до дня 10.
Пример 11
Были подготовлены составы для введения. Примером является состав для группы 7, который готовили следующим образом: 11,8 мг гранул гидроксида натрия растворяли в 6,0 мл воды. Раствор обрабатывали ультразвуком в течение 2-3 минут. 80 мг 8-[(2-гидроксибензоил)амино]октановой кислоты добавляли к 6,0 мл раствора гидроксида натрия, полученного, как описано выше, и обрабатывали ультразвуком в течение 2 минут. 2,0 мл раствора Tween 80 из подготовленного маточного раствора (0,8 мг Tween 80/мл) добавляли к 6 мл раствора солевой формы усилителя. К 8,0 мл вышеуказанного раствора солевой формы усилителя добавляли 12,0 мг порошка цисплатина, полученного от Tocris Bioscience, и весь раствор при необходимости обрабатывали ультразвуком, чтобы обеспечить полное растворение всех компонентов. pH доводили до 6,8-7,2 с использованием слабой HCl или 1 Н раствора гидроксида натрия. После достижения нужного значения pH раствор фильтровали через 0,45-микронный фильтр. Этот материал был получен для дозирования, описанного в примере 12.
Пример 12
1×106 клеток CT26 опухоли толстой кишки инокулировали в бок более чем 120 самкам иммунокомпетентных мышей balb/c. Рост опухоли контролировали раз или два раза в неделю путем измерения штангенциркулем до того момента, когда размеры опухоли достигали ~500 мм3. Через шестнадцать дней 120 мышей с опухолями отбирали для включения в исследование. Каждому выбранному животному присваивали номер и прикрепляли метку с соответствующим номером. Затем животных подбирали по размерам опухолей и распределяли в 12 групп, при этом средний объем опухолей для животных в каждой группе находился в диапазоне от 341 мм3 до 349 мм3. Животные получали составы в соответствии с 1 из 12 различных режимов и были классифицированы как относящиеся к группам 1-12, соответственно, на основании идентификационных характеристик, приведенных в таблице 3.
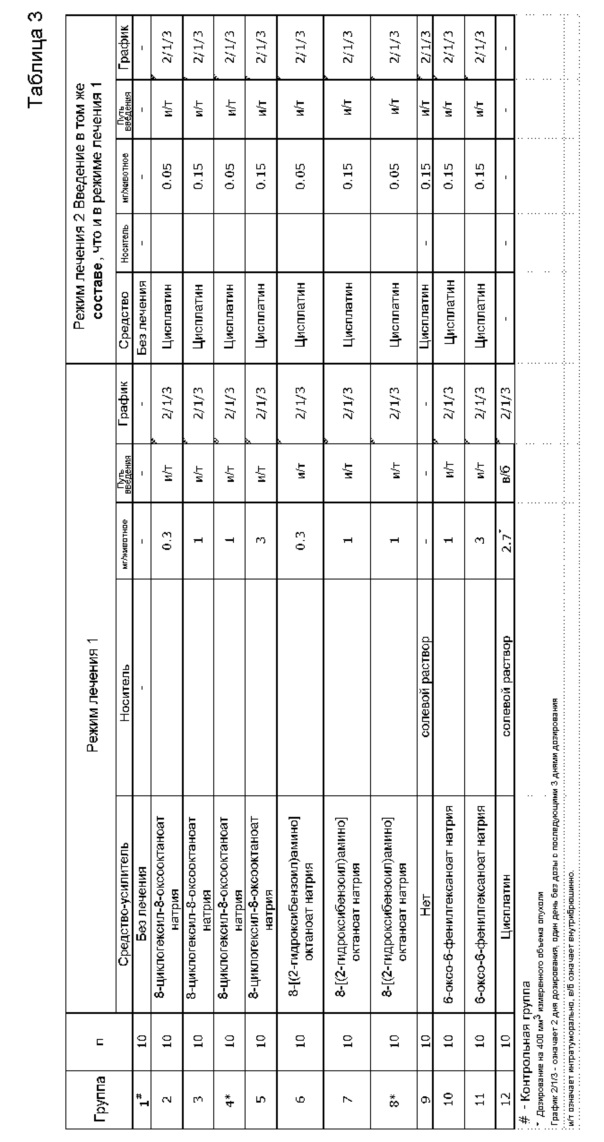
Результаты данного исследования приведены на фигуре 9, изображающей динамику объема опухолей для каждой из 12 групп, проанализированных в исследовании. Кроме того, как показано на фигуре 10, некоторые составы для усиления внутриклеточного проникновения были способны продемонстрировать значительное увеличение продолжительности жизни животных по сравнению с контрольными группами, а также благоприятные показатели общей выживаемости относительно животных, не получавших лечение, и относительно животных, получавших только лекарственное средство, вводимое системно. Иллюстративные составы в соответствии с иллюстративным вариантом осуществления приведены в таблице 4.
Пример 13
У десяти животных из исследования, описанного в примере 12, которые получали интратуморально вводимое лекарственное средство, опухоли регрессировали до размеров менее 18 мм3. Этих животных включили в новое исследование наряду с контрольной группой подобранных по возрасту не подвергавшихся воздействию животных. Затем животным обеих групп инокулировали в бок 1×106 клеток CT26 рака толстой кишки. Животные, которым ранее была проведена инокуляция, получали повторную инокуляцию в другой бок. Ни к одной группе не применяли лечение лекарственным средством. Рост опухолей был подавлен у тех животных, у которых ранее наблюдалась регрессия, тогда как у животных, ранее не участвовавших в экспериментах, наблюдался значительный рост опухолей. На фигурах 11A-C показано, что 90% животных, продемонстрировавших полный ответ, были полностью иммунизированы против рецидива рака. Верхняя фигура (a) соответствует 10 животным из контрольной группы. Вторая фигура (b) соответствует животным, продемонстрировавшим полный ответ в исследовании, описанном в примере 12. На нижней фигуре (c) показаны средние значения и стандартная ошибка среднего для двух групп.
Несмотря на подробно описанные предпочтительные варианты осуществления настоящего изобретения, следует понимать, что изобретение, описанное в приведенных выше параграфах, не ограничено конкретными деталями, изложенными в приведенном выше описании, поскольку возможны различные очевидные вариации без отклонения от сущности или объема настоящего изобретения.
Все документы, цитируемые или упоминаемые в настоящем документе, и все документы, цитируемые или упоминаемые в цитируемых в настоящем описании документах, наряду с любыми инструкциями производителей, описаниями, спецификациями составов и картами технологических процессов для любых составов, упомянутых в настоящем документе или в любом документе, включенном в настоящее описание посредством ссылки, включены в настоящий документ посредством ссылки и могут быть использованы при осуществлении на практике данного изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ДРОЖЖЕВАЯ ИММУНОТЕРАПИЯ ХОРДОМЫ | 2014 |
|
RU2679806C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, НАБОРЫ И СПОСОБЫ ЛЕЧЕНИЯ ОПУХОЛЕЙ | 2019 |
|
RU2810906C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ИНГИБИРОВАНИЯ ИСТОЩЕНИЯ Т-КЛЕТОК | 2018 |
|
RU2804282C2 |
| ПОЛУЧЕННЫЕ ИЗ БАКТЕРИЙ ИНТАКТНЫЕ МИНИ-КЛЕТКИ ДЛЯ ДОСТАВКИ ЛЕКАРСТВЕННЫХ СРЕДСТВ К ОПУХОЛЯМ МОЗГА | 2012 |
|
RU2664698C2 |
| СПОСОБ УМЕНЬШЕНИЯ МУЛЬТИЛЕКАРСТВЕННОЙ РЕЗИСТЕНТНОСТИ С ИСПОЛЬЗОВАНИЕМ ТРИПИРОФОСФАТА ИНОЗИТА | 2010 |
|
RU2563127C2 |
| МОДИФИЦИРОВАННЫЕ МОНОЦИТЫ/МАКРОФАГИ, ЭКСПРЕССИРУЮЩИЕ ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, И ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2766690C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ РАКА ПЕЧЕНИ | 2018 |
|
RU2802962C2 |
| ОНКОЛИТИЧЕСКИЕ ВИРУСЫ ПРОСТОГО ГЕРПЕСА 1 ТИПА ДЛЯ ЛЕЧЕНИЯ ОПУХОЛЕЙ ГОЛОВНОГО МОЗГА | 2021 |
|
RU2824514C1 |
| АДРЕСНОЕ ВОЗДЕЙСТВИЕ НА УСТОЙЧИВЫЙ К ТРАСТУЗУМАБУ HER2+ РАК МОЛОЧНОЙ ЖЕЛЕЗЫ ПОСРЕДСТВОМ HER3-НАЦЕЛЕННЫХ НАНОЧАСТИЦ | 2015 |
|
RU2692104C2 |
| СПОСОБЫ ЛЕЧЕНИЯ | 2020 |
|
RU2822394C1 |
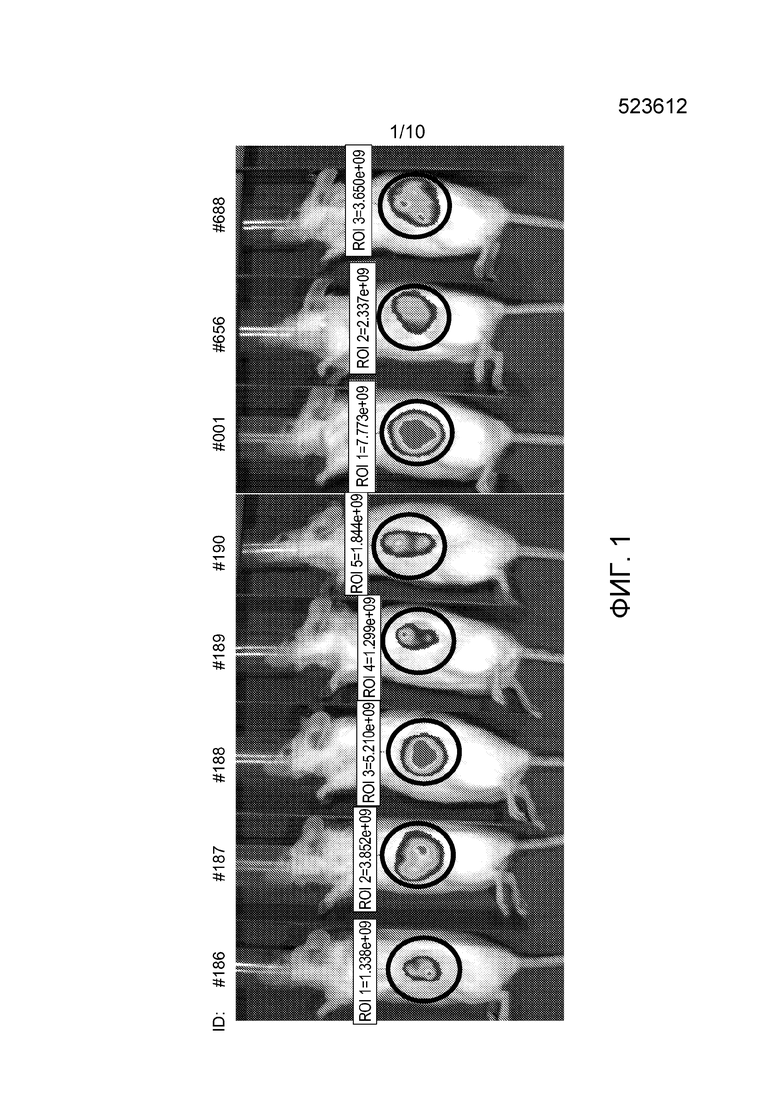
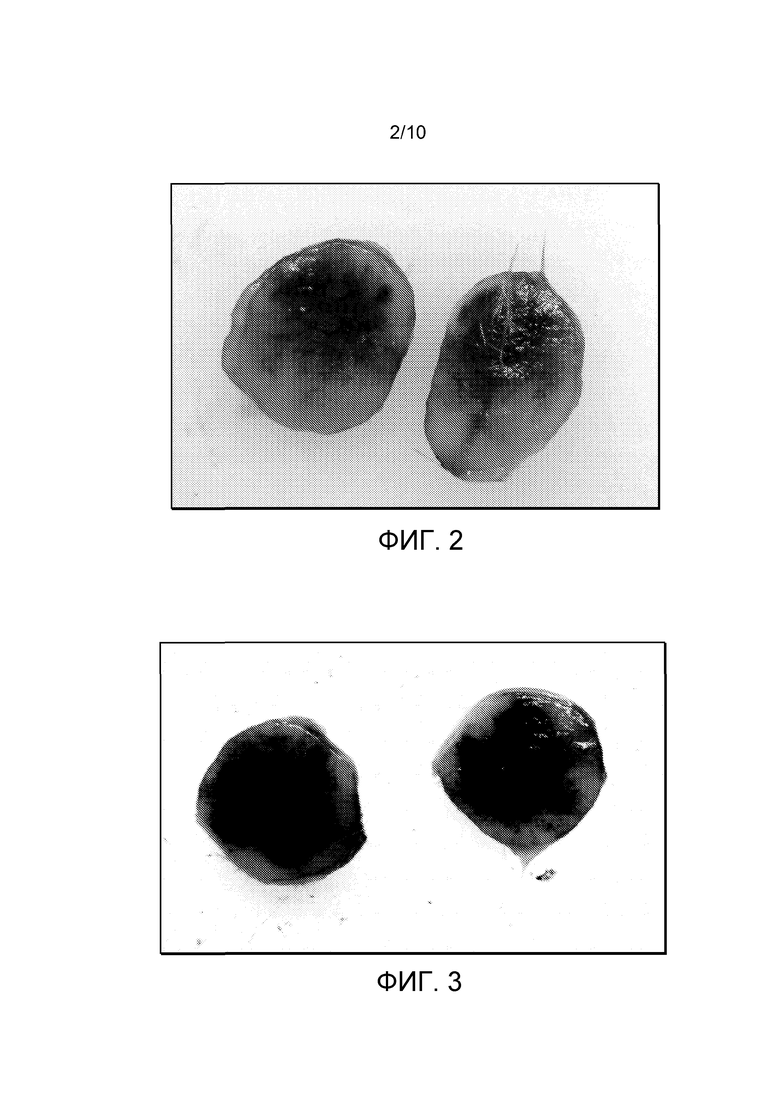
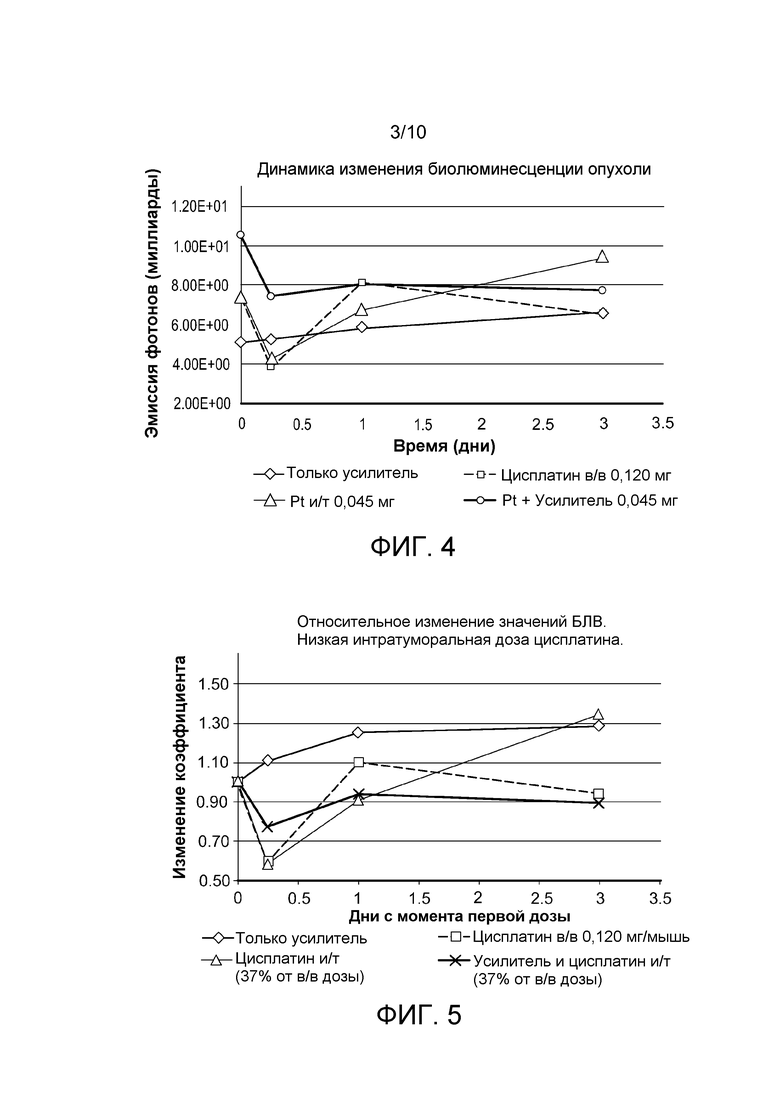
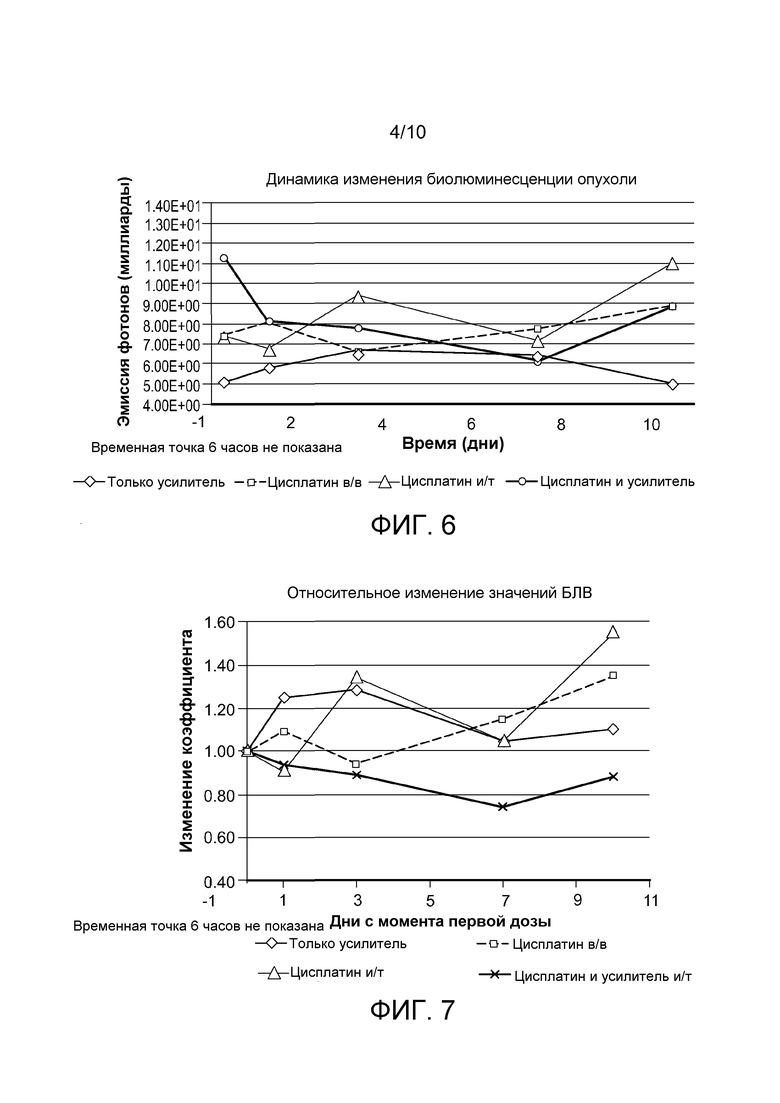
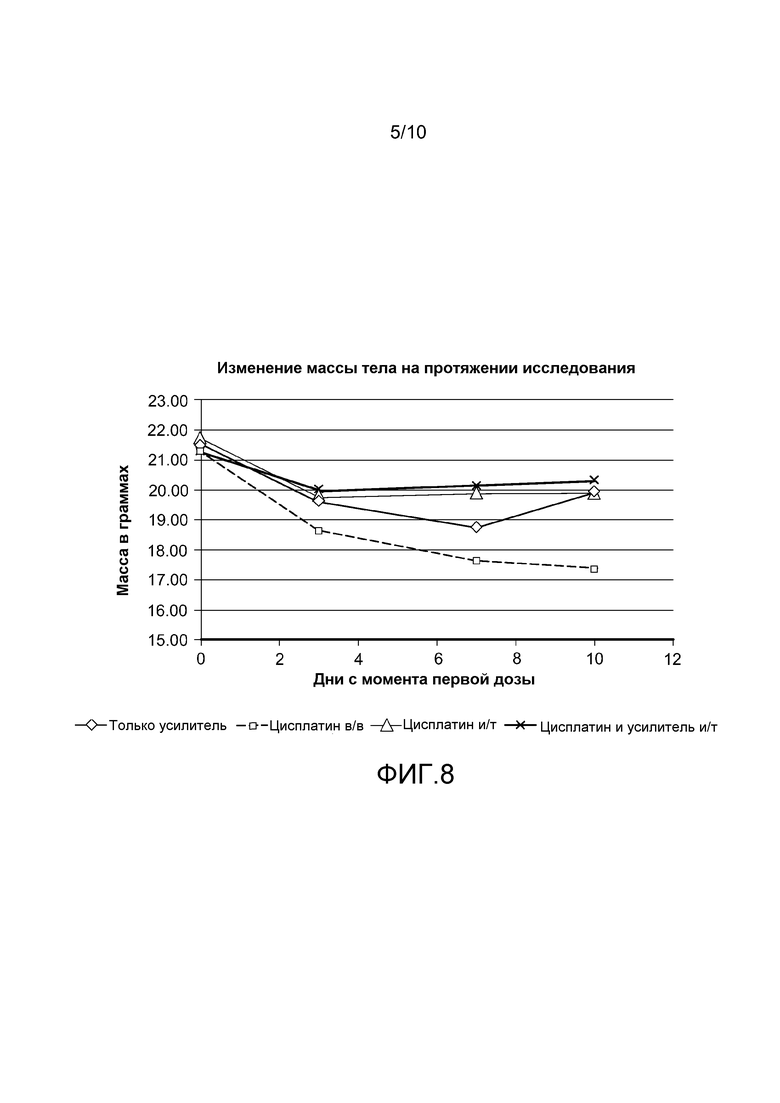
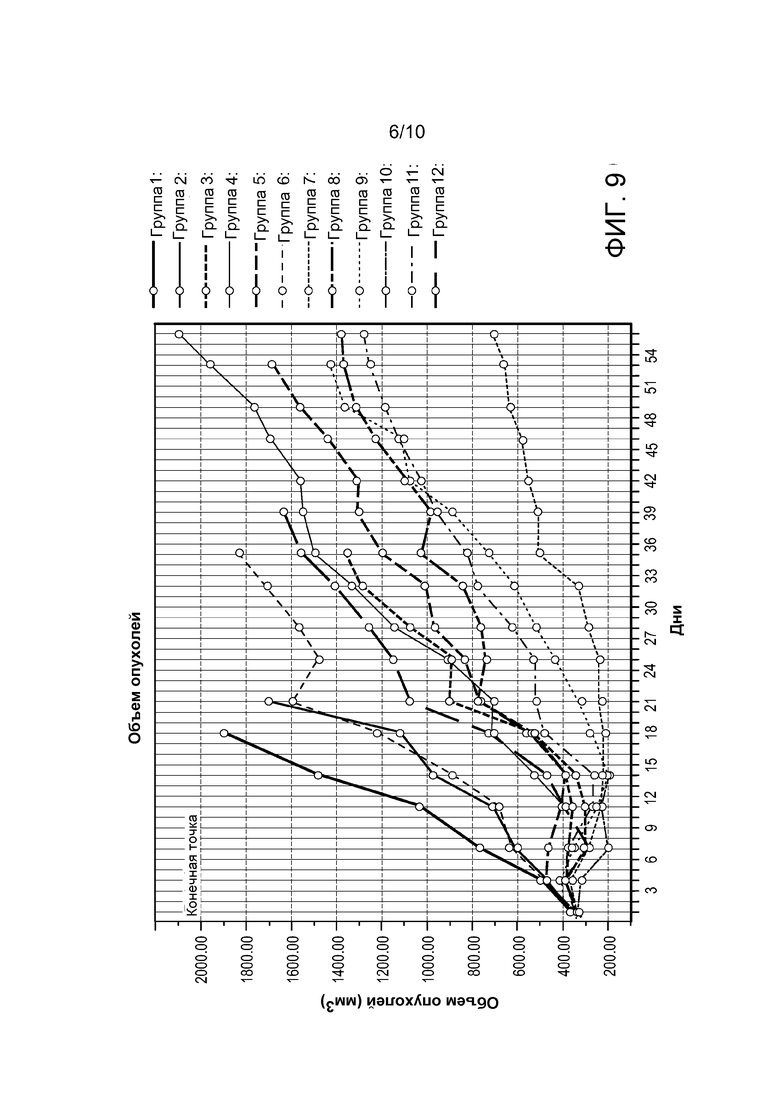
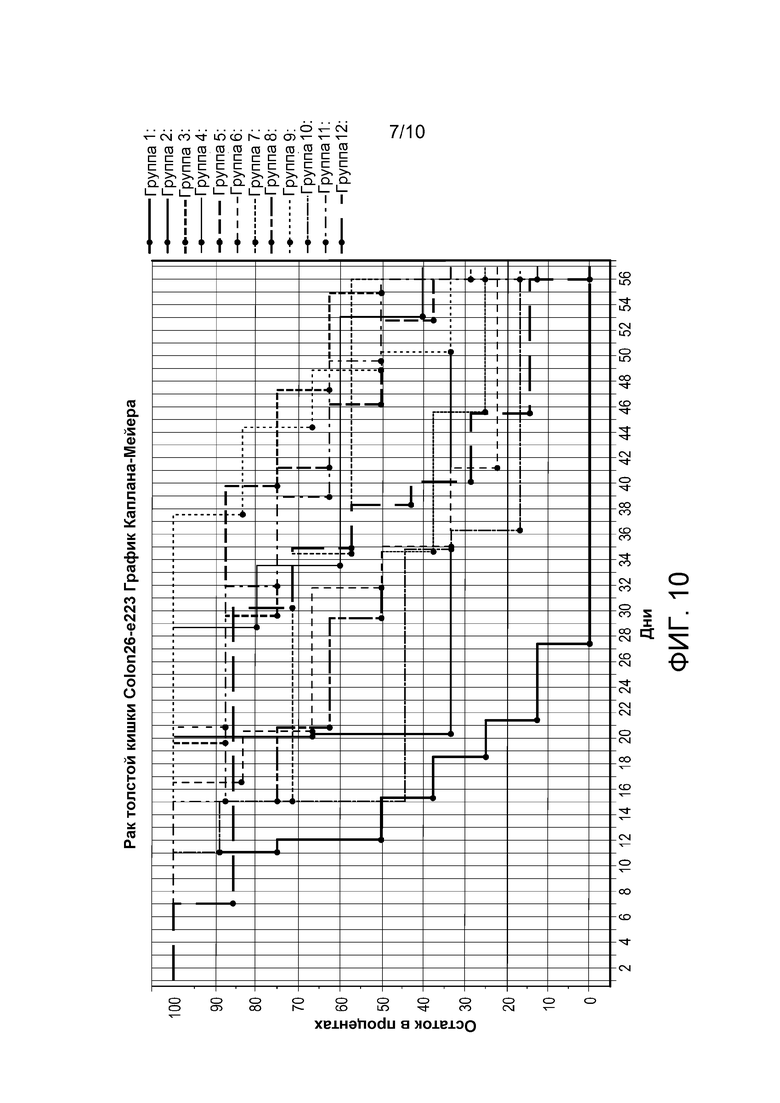
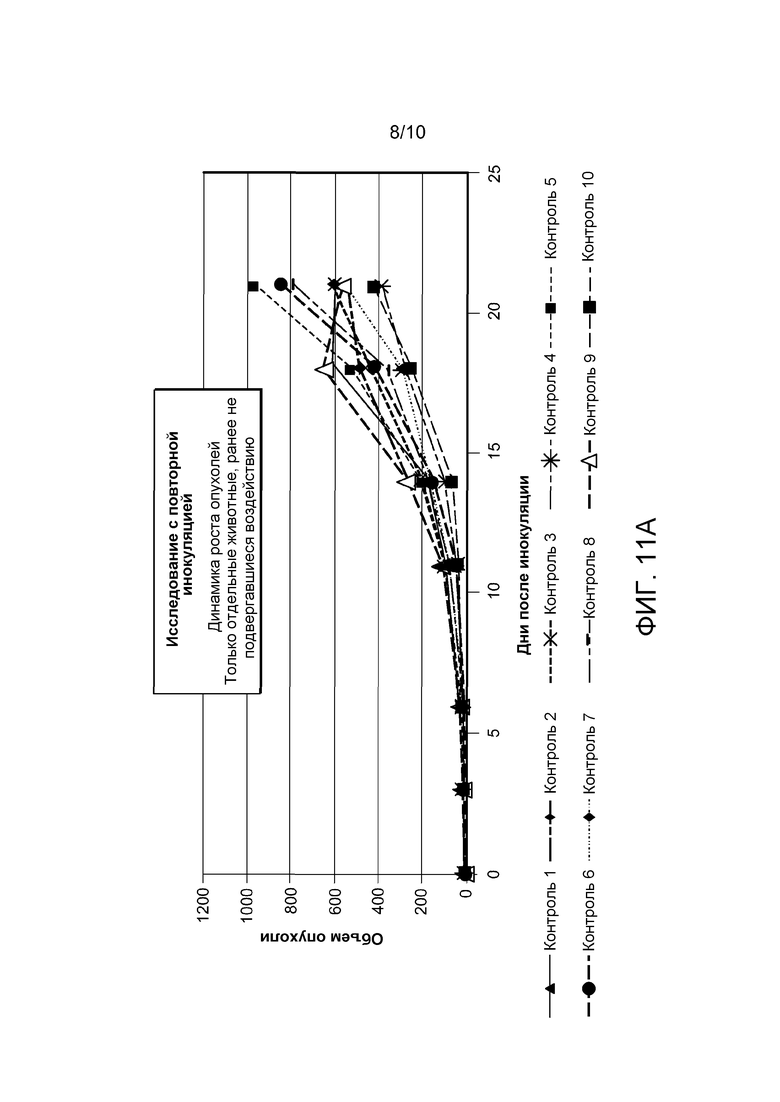
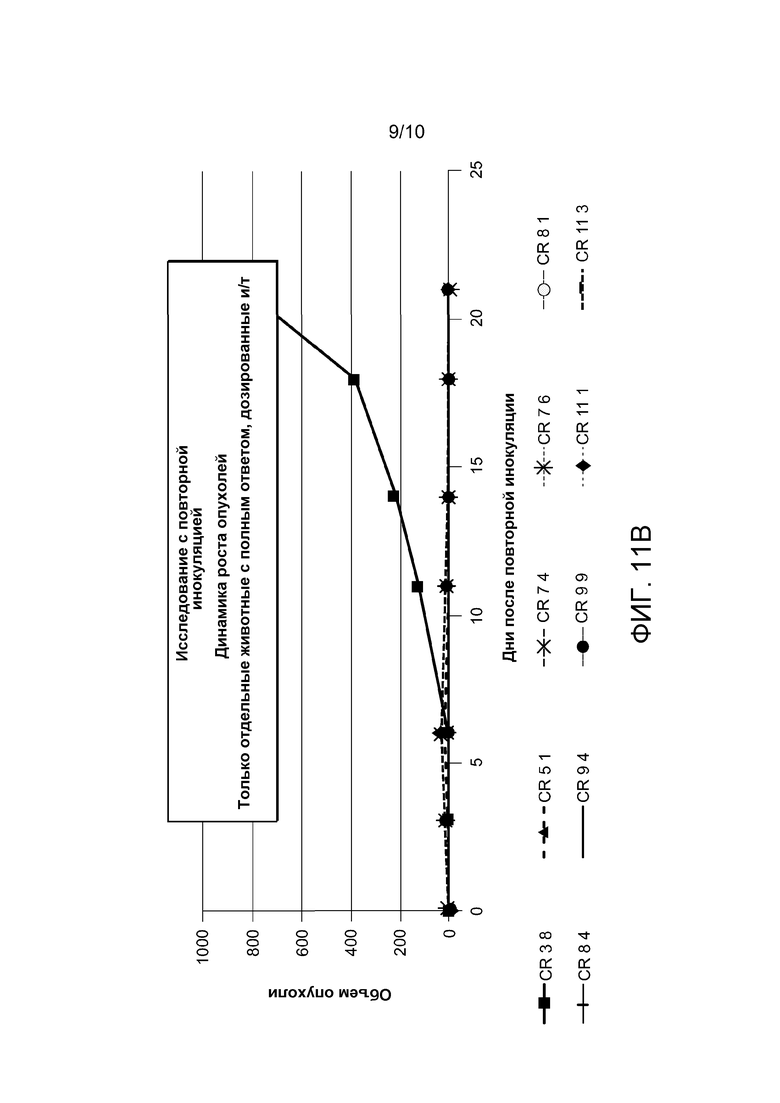
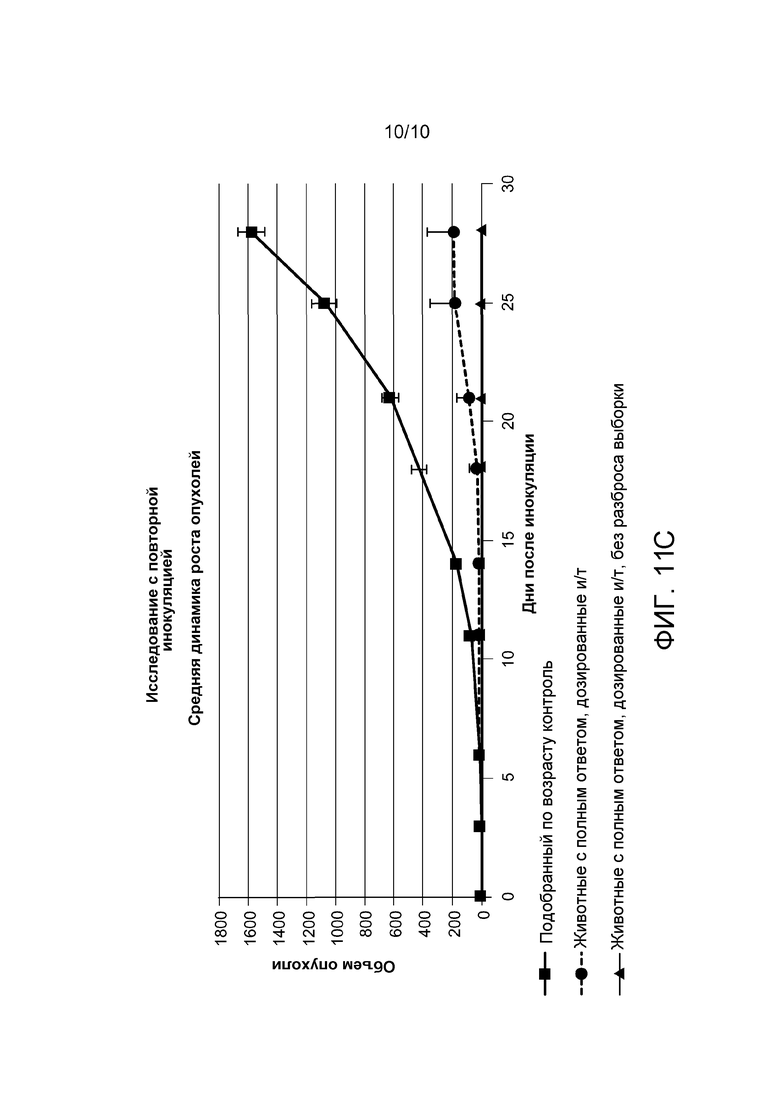
Группа изобретений относится к медицине, а именно к онкологии, и может быть использована для лечения рака у субъекта. Для этого субъекту осуществляют интратуморальное введение фармацевтической композиции, содержащей терапевтическое средство, при этом терапевтическое средство представляет собой соединение платины и/или алкалоид барвинка, и средство, усиливающее внутриклеточное проникновение. Причем средство, усиливающее внутриклеточное проникновение, не обладает терапевтической активностью и выбрано из 6-оксо-6-фенилгексановой кислоты, 8-циклогексил-8-оксооктановой кислоты, N-[8-(2-гидроксибензоил)амино]октановой кислоты или фармацевтически приемлемых солей любого из вышеперечисленных. Композиция представляет собой жидкий раствор и сформулирована для интратуморального введения. Также представлены способы лечения рака путем введения композиции, содержащей цисплатин и/или винбластин и средство, усиливающее внутриклеточное проникновение, выбранное из 6-оксо-6-фенилгексановой кислоты, 8-циклогексил-8-оксооктановой кислоты, N-[8-(2-гидроксибензоил)амино]октановой кислоты. Группа изобретений обеспечивает лечение рака и его метастазов у субъекта. 3 н. и 18 з.п. ф-лы, 4 табл., 13 ил., 13 пр.
1. Способ лечения рака у субъекта, который нуждается в лечении, включающий интратуморальное введение фармацевтической композиции, содержащей терапевтически эффективное количество терапевтического средства, где терапевтическое средство представляет собой соединение платины и/или алкалоид барвинка, и средства, усиливающего внутриклеточное проникновение, при этом указанное средство, усиливающее внутриклеточное проникновение, не обладает терапевтической активностью и выбрано из 6-оксо-6-фенилгексановой кислоты, 8-циклогексил-8-оксооктановой кислоты, N-[8-(2-гидроксибензоил)амино]октановой кислоты или фармацевтически приемлемых солей любого из вышеперечисленных, где композиция представляет собой жидкий раствор и сформулирована для интратуморального введения.
2. Способ по п.1, в котором введение средства для усиления внутриклеточного проникновения повышает терапевтическую эффективность терапевтического средства, и субъект является млекопитающим, выбранным из группы, состоящей из собаки, кошки, лошади, коровы, овцы, козы, свиньи, мыши, крысы, морской свинки, обезьяны или человека.
3. Способ по п.1, в котором рак представляет собой одну или более опухолей, выбранных из группы, состоящей из солидной опухоли, карциномы и саркомы.
4. Способ по п.3, в котором солидная опухоль, карцинома или саркома представляет собой опухоль кожи, кости, мышцы, молочной железы, ротовой полости, толстой кишки, органа, почки, печени, легкого, желчного пузыря, поджелудочной железы, головного мозга, пищевода, мочевого пузыря, толстого кишечника, тонкого кишечника, селезенки, желудка, предстательной железы, яичек, яичников, шейки матки, прямой кишки или матки.
5. Способ по п.3, в котором одна или более опухолей образовали метастазы.
6. Способ по п.3, приводящий к замедлению роста одной или более опухолей, уменьшению одной или более опухолей, ликвидации одной или более опухолей или предотвращению образования новых опухолей.
7. Способ по п.3, предотвращающий метастазирование опухоли.
8. Способ по п.1, в котором терапевтически эффективное количество терапевтического средства и/или средства, усиливающего внутриклеточное проникновение, выбирают исходя из объема и типа опухоли.
9. Способ по п.1, в котором терапевтическое средство и/или средство, усиливающее внутриклеточное проникновение, вводят в первый день и повторно вводят в один или более последующих дней.
10. Способ по п.9, в котором первый день и один или более последующих дней разделены интервалом от примерно 1 дня до примерно 3 недель.
11. Способ по п.9, в котором терапевтическое средство и средство, усиливающее внутриклеточное проникновение, совместно вводят в соотношении примерно 1:2, 1:4, 1:10, 1:20, 1:25, 1:50, 1:100 или 1:200 (массовое отношение терапевтическое средство:средство, усиливающее внутриклеточное проникновение).
12. Способ по п.9, в котором средство, усиливающее внутриклеточное проникновение, вводят в концентрации от примерно 0,5 до примерно 50 мг в мл раствора для дозирования.
13. Способ по п.9, в котором средство, усиливающее внутриклеточное проникновение, вводят в концентрации от примерно 10 до примерно 30 мг в мл раствора для дозирования.
14. Способ по п.1, в котором терапевтическое средство и средство, усиливающее внутриклеточное проникновение, доставляют одновременно в одном составе или одновременно в отдельных составах.
15. Способ по п.1, в котором средство, усиливающее внутриклеточное проникновение, вводят перед терапевтическим средством.
16. Способ по п.1, в котором терапевтическое средство представляет собой карбоплатин, цисплатин, винбластин или их соли.
17. Способ по п.1, в котором соединение платины представляет собой цисплатин, сатраплатин, пикоплатин, недаплатин, триплатин, карбоплатин или оксаплатин.
18. Способ лечения рака у субъекта, который нуждается в лечении, где способ включает интратуморальное введение фармацевтической композиции, содержащей терапевтическое средство, где терапевтическое средство представляет собой цисплатин и/или винбластин, и средство, усиливающее внутриклеточное проникновение, выбранное из 6-оксо-6-фенилгексановой кислоты, 8-циклогексил-8-оксооктановой кислоты, N-[8-(2-гидроксибензоил)амино]октановой кислоты, 2-этилгексил-2-гидроксибензоата или фармацевтически приемлемой соли любого из вышеперечисленных, где композиция представляет собой жидкий раствор и сформулирована для интратуморального введения.
19. Способ лечения рака у субъекта, который нуждается в лечении, включающий интратуморальное введение фармацевтической композиции, содержащей терапевтически эффективное количество по меньшей мере одного терапевтического средства и средства, усиливающего внутриклеточное проникновение, где композиция представляет собой жидкий раствор и сформулирована для интратуморального введения, и при этом композиция содержит цисплатин в качестве терапевтического средства с N-[8-(2-гидроксибензоил)амино]октановой кислотой в качестве средства, усиливающего внутриклеточное проникновение, или цисплатин и винбластин в качестве терапевтического средства с N-[8-(2-гидроксибензоил)амино]октановой кислотой в качестве средства, усиливающего внутриклеточное проникновение.
20. Способ по п.19, в котором композиция содержит 0,5 мг/мл цисплатина в качестве терапевтического средства и 10 мг/мл N-[8-(2-гидроксибензоил)амино]октановую кислоту в качестве средства, усиливающего внутриклеточное проникновение.
21. Способ по п.19, в котором состав содержит 0,5 мг/мл цисплатина и 1 мг/мл винбластина в качестве терапевтического средства и приблизительно 10 мг/мл N-[8-(2-гидроксибензоил)амино]октановую кислоту в качестве средства, усиливающего внутриклеточное проникновение.
| US 5866536 А, 02.02.1999 | |||
| WO 2004081196 A2, 23.09.2004 | |||
| SHEN Z et al, Intravesical treatments of bladder cancer: review, Рharmaceutical research, 2008, vol | |||
| Видоизменение пишущей машины для тюркско-арабского шрифта | 1923 |
|
SU25A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Устройство для уравновешивания одноцилиндровых двигателей и насосов | 1924 |
|
SU1500A1 |
| GUPTA VANDANA et al,Reduction in cisplatin genotoxicity (micronucleus formation) in non target cells of mice by protransfersome gel formulation used for management of cutaneous squamous cell carcinoma, 2011, Acta Pharm | |||
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
Авторы
Даты
2018-06-15—Публикация
2013-09-15—Подача