Область техники
[0001]
Перекрестная ссылка на родственную заявку
По настоящему изобретению испрашивается приоритет заявки на патент Японии 2013-129591, поданной 20 июня 2013, содержание которой полностью включено путем ссылки.
Область техники
Настоящее изобретение относится к способу предсказания терапевтической эффективности химиотерапии с использованием противоопухолевого средства, включающего ингибитор PI3K/AKT/mTOR, к противоопухолевому средству и к набору.
Уровень техники
[0002]
Сигнальный путь PI3K/AKT/mTOR регулирует различные важные функции клеток, такие как пролиферация клеток, устойчивость к апоптозу и метаболизм углеводов. Известно, что этот путь является гиперактивным в широком диапазоне злокачественных опухолей (Непатентная литература 1). Клинические испытания проводили на многих ингибиторах PI3K/AKT/mTOR, используемых в качестве противоопухолевых средств (например, ингибитор PI3K, ингибитор AKT, ингибитор mTOR или двойной ингибитор PI3K-mTOR). Однако, особенно в клинических испытаниях с использованием PI3K или AKT-нацеливаемого ингибитора в качестве единственного лекарственного средства, ни один из них пока не продемонстрировал удовлетворительные клинические результаты (Непатентная литература 2).
[0003]
Молекулярно нацеленные лекарственные средства, такие как ингибиторы PI3K/AKT/mTOR, могут обычно показывать высокий потенциал на опухолевых клетках, в которых молекулы-мишени высоко экспрессируются или являются гиперактивными. Таким образом, важно стратифицировать пациентов, используя терапевтически эффективный прогностический маркер для выбора группы пациентов, для которых ожидаются благоприятные воздействия (Непатентная Литература 3). Что касается ингибиторов PI3K/AKT/mTOR, мутация PIK3CA, делеция PTEN и т.п. были исследованы в качестве терапевтически эффективного прогностического маркера в клинической практике (Непатентная литература 4).
[0004]
Как отмечено выше, интенсивно разрабатывались различные ингибиторы PI3K/AKT/mTOR. Тем не менее, их терапевтическая эффективность в отношении всех пациентов, пациентов, страдающих раком, осталась неудовлетворительной, и не было обнаружено терапевтически эффективных прогностических маркеров, пригодных для стратификации пациентов для того, чтобы выбрать группу пациентов, которые, вероятно, в достаточной степени ответят на ингибиторы PI3K/AKT/mTOR.
Список литературы
Непатентная литература
[0005]
Непатентная литература 1: Nature Reviews Cancer 2, 489-501 (2002)
Непатентная литература 2: Nature Reviews Cancer 9, 550-562 (2009)
Непатентная литература 3: Nature Reviews Clinical Oncology 8, 587-596 (2011)
Непатентная литература 4: Lancet Oncology 12, 594-603 (2011)
Сущность изобретения
Техническая задача
[0006]
Цель настоящего изобретения состоит в разработке химиотерапии с использованием ингибитора PI3K/AKT/mTOR, которая произвела бы превосходный противоопухолевый эффект у пациента, страдающего раком.
Решение задачи
[0007]
Авторы настоящего изобретения проводили обширное исследование относительно отношения между экспрессией различных генов и терапевтической эффективностью ингибиторов PI3K/AKT/mTOR и обнаружили, что ингибиторы PI3K/AKT/mTOR (в частности, транс-3-амино-1-метил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[3,4-e][1,3]оксазин-2-ил)фенил)циклобутанол) имеют значительный высокий противоопухолевый эффект на пациентов, страдающих раком, демонстрирующих низкий уровень экспрессии PHLDA1 или высокий уровень экспрессии PIK3C2B. Таким образом, авторы осуществили настоящее изобретение.
[0008]
Не было никаких отчетов относительно отношения ингибиторов PI3K/AKT/mTOR к PHLDA1 либо к PIK3C2B.
[0009]
В частности, настоящее изобретение относится к следующим способу, противоопухолевому средству и набору.
Пункт 1.
Способ предсказания терапевтической эффективности химиотерапии с использованием противоопухолевого средства, включающего ингибитор PI3K/AKT/mTOR, у пациента, страдающего раком, на основании уровня экспрессии PHLDA1 и/или PIK3C2B в опухолевых клетках, выделенных от пациента, страдающего раком.
Пункт 2.
Способ согласно Пункту 1, включающий следующие стадии (1) и (2):
(1) измерение уровня экспрессии PHLDA1 и/или PIK3C2B в биологическом образце, содержащем опухолевые клетки, выделенном от пациента; и
(2) предсказание, что для пациента вероятен достаточный ответ на химиотерапию с использованием противоопухолевого средства, включающего ингибитор PI3K/AKT/mTOR, когда уровень экспрессии PHLDA1, измеренного на стадии (1), равен или ниже предопределенной пороговой точки, или когда уровень экспрессии PIK3C2B, измеренного на стадии (1), равен или выше предопределенной пороговой точки.
[0010]
Пункт 3.
Способ согласно Пункту 1 или 2, в котором ингибитор PI3K/AKT/mTOR представляет собой соединение имидазо-оксазина, представленное формулой (I), или его фармацевтически приемлемую соль
[0011]
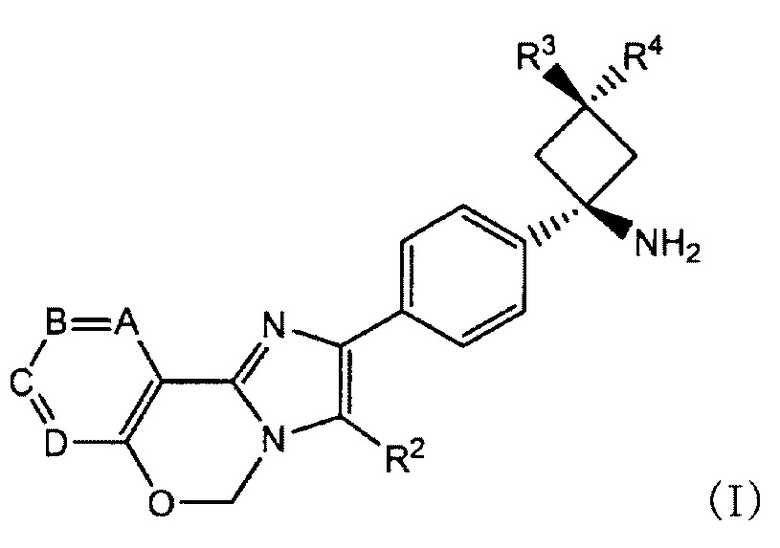
[0012]
в которой
A, B, C и D обозначают C-R1a, C-R1b, C-R1c и C-R1d, соответственно, или один или два из таким образом определенных A, B, C и D заменены азотом;
по меньшей мере два из R1a, R1b, R1c и R1d обозначают водород, и другой(другие) каждый обозначает(обозначают) галоген, циано, C1-6 алкил, необязательно замещенный одной или более гидроксильными группами, C1-6 алкокси, карбонил, имеющий гидроксил, амино, необязательно замещенный моно- или ди(C1-6 алкил)амино или моно- или ди(C1-6 алкокси)амино в качестве заместителя, или ненасыщенную гетероциклическую группу;
R2 обозначает фенил, пиридил или тиенил;
R3 обозначает водород, метил, этил или циклопропил; и
R4 обозначает водород или гидроксил;
или ингибитор PI3K/AKT/mTOR представляет собой AMG-319, AZD-6482, BYL-719, копанлисиб (BAY-80-6946), GDC-0032, GDC-0084, GSK-1059615, GSK-2126458, GSK-2636771, иделалисиб (CAL-101), IPI-145, MLN-1117 (INK-1117), PA-799 (CH-5132799), пиктилисиб (GDC-0941), пиларалисиб (XL-147), SF-1126, сонолисиб (PX-866), воксталисиб (SAR-245409, XL-765), афуресертиб гидрохлорид (GSK-2110183), ARQ-092, AZD5363, энзастаурин гидрохлорид, GDC-0068, GSK-2141795, GSK690693, LY-2780301, MK-2206, перифосин, трицирибин фосфат (VQD-002), AZD-2014, AZD-8055, CC-115, CC-223, DS-3078, эверолимус, темсиролимус, ME-344, MLN-0128 (INK-128), OSI-027, PWT-33597, ридафоролимус, сиролимус, дактолисиб (BEZ235), DS-7423, GDC-0980, NVP-BGT-226, PF-04691502, PF-05212384 (PKI-587) или PWT-33597.
Пункт 4.
Способ согласно Пункту 3, в котором соединение имидазо-оксазина, представленное формулой (I), представляет собой соединение, в котором A, B, C и D обозначают C-R1a, C-R1b, C-R1c и C-R1d, соответственно, или любой один или два из таким образом определенных A, B, C и D заменены азотом;
по меньшей мере два из R1a, R1b, R1c и R1d обозначают водород, и другой(другие) каждый обозначает(обозначают) хлор, фтор, циано, метил, гидроксиметил, метокси, этокси, карбоксил, карбамоил, метиламинокарбонил, этиламинокарбонил, гидроксиэтиламинокарбонил, этоксиаминокарбонил или пиразолил;
R2 обозначает фенил, пиридил или тиенил;
R3 обозначает водород, метил, этил или циклопропил; и
R4 обозначает водород или гидроксил.
[0013]
Пункт 5.
Способ согласно Пункту 3 или 4, в котором соединение имидазо-оксазин, представленное формулой (I), представляет собой любое из следующих соединений (a)-(t),
(a) транс-3-амино-1-циклопропил-3-(4-(10-фтор-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(b) транс-3-амино-1-циклопропил-3-(4-(10-фтор-3-(пиридин-4-ил)-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(c) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(d) транс-3-амино-1-циклопропил-3-(4-(10-метокси-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(e) транс-3-амино-1-циклопропил-3-(4-(9-метокси-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(f) транс-3-амино-1-циклопропил-3-(4-(8-метокси-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(g) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[2,3-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(h) транс-3-амино-1-метил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[2,3-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(i) транс-3-амино-1-этил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[2,3-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(j) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[3,4-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(k) транс-3-амино-1-метил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[3,4-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(l) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[4,3-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(m) транс-3-амино-1-метил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[4,3-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(n) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[3,2-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(o) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-имидазо[1,2-c] пиразино [2,3-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(p) транс-3-амино-3-(4-(9-(гидроксиметил)-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)-1-метилциклобутанол,
(q) 2-(4-(транс-1-амино-3-гидрокси-3-метилциклобутил)фенил)-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-9-карбонитрил,
(r) транс-3-амино-1-метил-3-(4-(3-фенил-9-(1H-пиразол-5-ил)-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(s) 2-(4-(транс-1-амино-3-гидрокси-3-метилциклобутил)фенил)-N-метил-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-8-карбоксамид, и
(t) 2-(4-(транс-1-амино-3-гидрокси-3-метилциклобутил)фенил)-N-этокси-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-8-карбоксамид.
Пункт 6.
Способ согласно любому из Пунктов 1-5, в котором ингибитор PI3K/AKT/mTOR представляет собой MK-2206, BEZ235, GDC-0941, сиролимус или транс-3-амино-1-метил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[3,4-e][1,3]оксазин-2-ил)фенил)циклобутанол.
Пункт 7.
Противоопухолевое средство для лечения пациента, страдающего раком, включающее ингибитор PI3K/AKT/mTOR, причем пациент, страдающий раком, имеет опухолевые клетки, в которых уровень экспрессии PHLDA1 равен или ниже предопределенной пороговой точки или уровень экспрессии PIK3C2B равен или выше предопределенной пороговой точки.
[0014]
Пункт 8.
Противоопухолевое средство, включающее ингибитор PI3K/AKT/mTOR, которое вводят пациенту, для которого предсказана вероятность достаточного ответа на химиотерапию с использованием противоопухолевого средства способом, включающим следующие стадии (1) и (2):
(1) измерение уровня экспрессии PHLDA1 и/или PIK3C2B в биологическом образце, содержащем опухолевые клетки, выделенном от пациента; и
(2) предсказание, что для пациента вероятен достаточный ответ на химиотерапию с использованием противоопухолевого средства, включающего ингибитор PI3K/AKT/mTOR, когда уровень экспрессии PHLDA1, измеренный на стадии (1), равен или ниже предопределенной пороговой точки, или когда уровень экспрессии PIK3C2B, измеренный на стадии (1), равен или выше предопределенной пороговой точки.
Пункт 9.
Набор, включающий реактив для измерения уровня экспрессии PHLDA1 и/или PIK3C2B, предназначенный для предсказания терапевтической эффективности химиотерапии с использованием противоопухолевого средства, включающего ингибитор PI3K/AKT/mTOR, у пациента, страдающего раком, способом, включающим следующие стадии (1) и (2):
(1) измерение уровня экспрессии PHLDA1 и/или PIK3C2B в биологическом образце, содержащем опухолевые клетки, выделенном от пациента; и
(2) предсказание, что для пациента вероятен достаточный ответ на химиотерапию с использованием противоопухолевого средства, включающего ингибитор PI3K/AKT/mTOR, когда уровень экспрессии PHLDA1, измеренный на стадии (1), равен или ниже предопределенной пороговой точки, или когда уровень экспрессии PIK3C2B, измеренный на стадии (1), равен или выше предопределенной пороговой точки.
Пункт 10.
Способ лечения пациента, страдающего раком, включающий введение противоопухолевого средства, включающего ингибитор PI3K/AKT/mTOR, пациенту, для которого способом согласно любому из Пунктов 1-6 предсказана вероятность достаточного ответа на химиотерапию с использованием противоопухолевого средства.
Пункт 11.
Противоопухолевое средство, включающее ингибитор PI3K/AKT/mTOR, для применения в лечении пациента, страдающего раком, для которого способом согласно любому из Пунктов 1-6 предсказана вероятность достаточного ответа на химиотерапию с использованием противоопухолевого средства.
[0015]
Настоящее изобретение дополнительно включает следующий объект.
Пункт 12.
Способ тестирования терапевтической эффективности химиотерапии с использованием противоопухолевого средства, включающего ингибитор PI3K/AKT/mTOR, на пациенте, страдающем раком, на основании уровня экспрессии PHLDA1 и/или PIK3C2B в опухолевых клетках пациента, страдающего раком.
[0016]
Пункт 13.
Способ согласно Пункту 12, включающий следующие стадии (1) и (2):
(1) измерение уровня экспрессии PHLDA1 и/или PIK3C2B в биологическом образце, содержащем опухолевые клетки, выделенном от пациента; и
(2) предсказание, что для пациента вероятен достаточный ответ на химиотерапию с использованием противоопухолевого средства, включающего ингибитор PI3K/AKT/mTOR, когда уровень экспрессии PHLDA1, измеренный на стадии (1), равен или ниже предопределенной пороговой точки, или когда уровень экспрессии PIK3C2B, измеренный на стадии (1), равен или выше предопределенной пороговой точки.
Полезные эффекты изобретения
[0017]
Настоящее изобретение относится к новому способу предсказания терапевтической эффективности ингибитора PI3K/AKT/mTORов у пациента, страдающего раком. В частности, способ согласно настоящему изобретению позволяет предсказать, на основании экспрессии PHLDA1 и/или PIK3C2B, показывает ли пациент, страдающий раком, чувствительность к ингибитору PI3K/AKT/mTORам. Это позволяет осуществить выбор подходящих лекарственных средств и избежать ненужного лечения при лечении рака, таким образом обеспечивая возможность планирования подходящего режима введения или изменения подходящего режима введения.
Краткое описание чертежей
[0018]
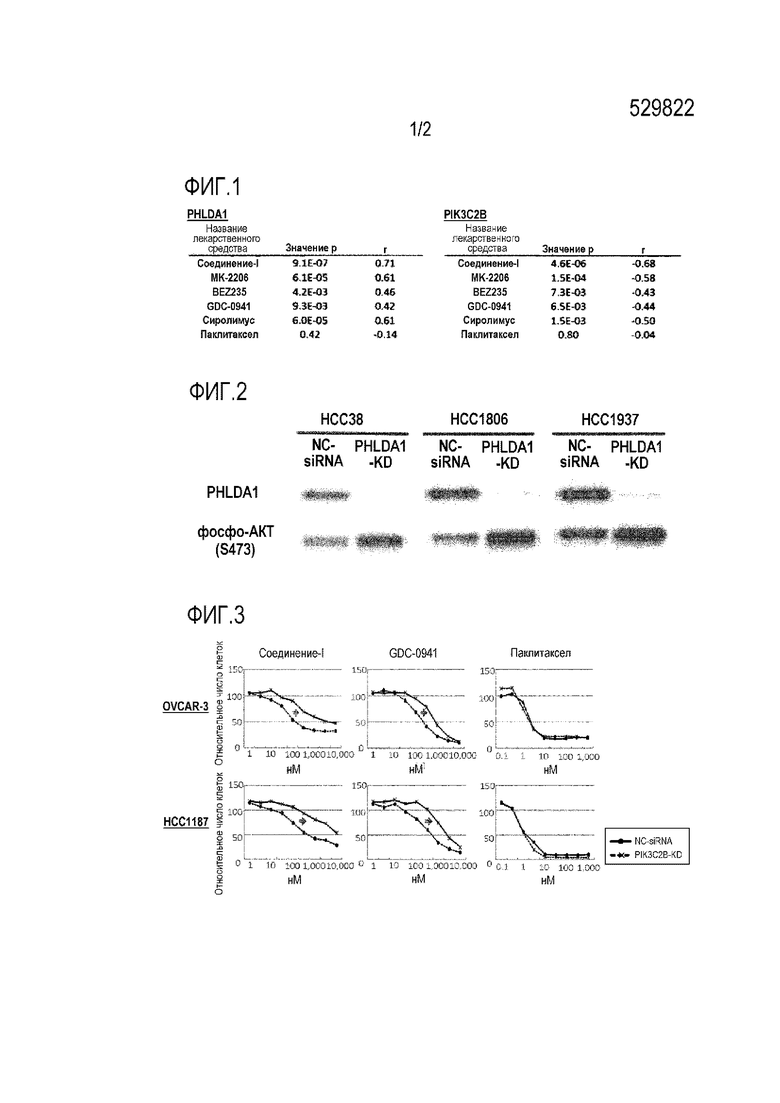
Фиг.1 показывает корреляцию между уровнем экспрессии PHLDA1 или PIK3C2B и чувствительностью к ингибиторам PI3K/AKT/mTOR.
Фиг.2 показывает результаты анализа нокдауна гена PHLDA1, уровня экспрессии белка и статуса фосфорилирования.
Фиг.3 показывает результаты анализа изменения чувствительности к ингибиторам PI3K/AKT/mTOR, вызванным нокдауном гена PIK3C2B.
Фиг.4 показывает сравнение измерения уровня экспрессии PHLDA1/PIK3C2B с измерением обычной мутации PIK3CA/делеции PTEN в предсказании терапевтической эффективности ингибитора PI3K/AKT/mTORе.
Описание вариантов осуществления
[0019]
Способ прогноза согласно настоящему изобретению предназначен для предсказания или тестирования терапевтической эффективности химиотерапии с использованием противоопухолевого средства, включающего ингибитор PI3K/AKT/mTOR, у пациента, страдающего раком, на основании уровня экспрессии PHLDA1 и/или PIK3C2B в биологическом образце, содержащем опухолевые клетки, выделенном от пациента, страдающего раком.
[0020]
Частные примеры рака, рассматриваемые в настоящем изобретении, включают рак головы и шеи, рак пищеварительного органа (рак пищевода, рак желудка, рак двенадцатиперстной кишки, рак печени, рак желчевыводящих путей (например, рак желчного пузыря и желчного протка), рак поджелудочной железы, рак тонкого кишечника, рак толстого кишечника (например, колоректальный рак, рак ободочной кишки и рак прямой кишки), рак легкого (например, немелкоклеточный рак легкого и мелкоклеточный рак легкого), рак молочной железы, рак яичника, рак матки (например, рак шейки матки и рак эндометрия), рак почек, рак мочевого пузыря и рак предстательной железы. "Рак" в рамках изобретения включает не только первичные опухоли, но также и опухоли, распространяющиеся в другие органы (например, печень). "Пациент, страдающий раком" в рамках изобретения включает не только пациентов, у которых в настоящее время имеются опухолевые клетки, но также и пациенты, у которых опухолевые клетки исчезли или перестали выявляться в результате лечения, такого как хирургическая операция и химиотерапия.
“Ингибитор PI3K/AKT/mTOR” согласно настоящему изобретению особенно не ограничен, при условии, что ингибитор представляет собой лекарственное средство, которое имеет ингибирующую активность в отношении сигнальной гиперактивности в сигнальном пути PI3K/AKT/mTOR. Примеры включают ингибиторы, которые имеют мишенью одну или две или более молекул, выбранные из группы, состоящей из PI3K, AKT и mTOR. Ингибиторами предпочтительно являются ингибитор PI3K, ингибитор AKT, ингибитор mTOR или двойной ингибитор PI3K-mTOR. Эти ингибиторы могут дополнительно иметь ингибирующую активность против молекул-мишеней, отличных от PI3K, AKT и mTOR. Термин "ингибитор" в рамках изобретения включает не только лекарственные средства для ингибирования активности молекул-мишеней, но также и лекарственные средства для ингибирования экспрессии молекул-мишеней. Вид ингибитора PI3K/AKT/mTOR особенно не ограничен, и примеры включают низкомолекулярные соединения, антитела, антисмысловые олигонуклеотиды, siРНК и аптамеры.
[0021]
В предпочтительном варианте осуществления настоящего изобретения, частные примеры ингибиторов PI3K/AKT/mTOR включают соединения имидазо-оксазина, представленные формулой (I), и их соли. Соединения имидазо-оксазина, представленные формулой (I), могут быть использованы в качестве ингибиторов фермента AKT.
[0022]
В формуле (I) A, B, C и D обозначают C-R1a, C-R1b, C-R1c и C-R1d, соответственно, или один или два из таким образом определенных A, B, C и D заменены азотом.
[0023]
Примеры галогенов, представленных R1a, R1b, R1c или R1d, включают хлор, бром, фтор и йод, и предпочтительно хлор и фтор.
[0024]
C1-6 алкил в “C1-6 алкиле, необязательно замещенном одной или более гидроксильными группами”, представленном R1a, R1b, R1c или R1d, представляет собой прямой или разветвленный алкил, имеющий от 1 до 6 атомов углерода, включая метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, пентил и гексил, предпочтительно C1-3 алкил, и более предпочтительно метил. Число гидроксильных групп (заместителей) составляет от 0 до 2, и предпочтительно 0 или 1.
[0025]
“C1-6 алкокси”, представленный R1a, R1b, R1c или R1d, представляет собой прямой или разветвленный алкокси, имеющий от 1 до 6 атомов углерода, включая метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси и трет-бутокси, предпочтительно C1-3 алкокси, и более предпочтительно метокси и этокси.
[0026]
“Карбонил, имеющий гидроксил, амино, необязательно замещенный моно- или ди(C1-6 алкил)амино или моно- или ди(C1-6 алкокси) амино в качестве заместителя”, представленный R1a, R1b, R1c или R1d, представляет собой карбонил, имеющий гидроксил в качестве заместителя (то есть, карбоксил), карбонил, имеющий амино в качестве заместителя (то есть, карбамоил), необязательно замещенный моно или ди(C1-6 алкил)аминокарбонил, или моно или ди(C1-6 алкокси)аминокарбонил.
[0027]
“Моно или ди(C1-6 алкил)аминокарбонил” в “необязательно замещенном моно или ди(C1-6 алкил)аминокарбониле” “карбонила, имеющего гидроксил, амино, необязательно замещенный моно- или ди(C1-6 алкил)амино или моно- или ди(C1-6 алкокси)амино в качестве заместителя”, представленного R1a, R1b, R1c или R1d, представляет собой аминокарбонил, имеющий одну или две C1-6 алкильные группы, описанные выше, предпочтительно моно или ди(C1-3 алкил)аминокарбонил, и более предпочтительно метиламинокарбонил, диметиламинокарбонил, или этиламинокарбонил. Заместитель предпочтительно представляет собой гидроксил. Количество заместителей, если они содержатся, предпочтительно равно одному.
[0028]
Моно или ди(C1-6 алкокси)аминокарбонил представляет собой аминокарбонил, имеющий одну или две C1-6 алкоксигруппы, описанные выше, предпочтительно моно или ди(C1-3 алкокси)аминокарбонил, и более предпочтительно этоксиаминокарбонил.
[0029]
“Карбонил, имеющий гидроксил, амино, необязательно замещенный моно- или ди(C1-6 алкил)амино или моно- или ди(C1-6 алкокси) амино в качестве заместителя”, представленный R1a, R1b, R1c или R1d, особенно предпочтительно представляет собой карбоксил, карбамоил, метиламинокарбонил, этиламинокарбонил, гидроксиэтиламинокарбонил или этоксиаминокарбонил.
[0030]
“Ненасыщенная гетероциклическая группа”, представленная R1a, R1b, R1c или R1d, представляет собой моноциклическую или бициклическую 5-10-членную ненасыщенную гетероциклическую группу, имеющую от одного до четырех гетероатомов из числа N, S и O. Примеры включают имидазолил, тиенил, фурил, пирролил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиразолил, триазолил, тетразолил, пиридил, пиразил, пиримидинил, пиридазинил, индолил, изоиндолил, индазолил, бензофуранил, бензоимидазолил, бензоксазолил, бензотиазолил, пуринил, хинолил, изохинолил, хиназолинил и хиноксалил, причем пиразолил является предпочтительным.
[0031]
Частные примеры предпочтительных соединений имидазо-оксазина, представленных формулой (I), включают следующие соединения (a)-(t).
[0032]
(a) транс-3-амино-1-циклопропил-3-(4-(10-фтор-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(b) транс-3-амино-1-циклопропил-3-(4-(10-фтор-3-(пиридин-4-ил)-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(c) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(d) транс-3-амино-1-циклопропил-3-(4-(10-метокси-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(e) транс-3-амино-1-циклопропил-3-(4-(9-метокси-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(f) транс-3-амино-1-циклопропил-3-(4-(8-метокси-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(g) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[2,3-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(h) транс-3-амино-1-метил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[2,3-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(i) транс-3-амино-1-этил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[2,3-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(j) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[3,4-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(k) транс-3-амино-1-метил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[3,4-e][1,3]оксазин-2-ил)фенил)циклобутанол (в дальнейшем называемый “Соединение I”),
(l) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[4,3-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(m) транс-3-амино-1-метил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[4,3-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(n) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[3,2-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(o) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-имидазо[1,2-c] pyrazino [2,3-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(p) транс-3-амино-3-(4-(9-(метил гидрокси)-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)-1-метилциклобутанол,
(q) 2-(4-(транс-1-амино-3-гидрокси-3-метилциклобутил)фенил)-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-9-карбонитрил,
(r) транс-3-амино-1-метил-3-(4-(3-фенил-9-(1H-пиразол-5-ил)-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(s) 2-(4-(транс-1-амино-3-гидрокси-3-метилциклобутил)фенил)-N-метил-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-8-карбоксамид, и
(t) 2-(4-(транс-1-амино-3-гидрокси-3-метилциклобутил)фенил)-N-этокси-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-8-карбоксамид
Примеры фармацевтически приемлемых солей соединений имидазо-оксазина, представленных формулой (I), включают соли присоединения с кислотой, образованные с неорганическими кислотами, такими как соляная кислота, бромистоводородная кислота, йодистоводородная кислота, серная кислота, азотная кислота и фосфорная кислота; присоединения с кислотой, образованные с органическими кислотами, такими как муравьиная кислота, уксусная кислота, пропионовая кислота, щавелевая кислота, малоновая кислота, янтарная кислота, фумаровая кислота, малеиновая кислота, молочная кислота, яблочная кислота, лимонная кислота, винная кислота, угольная кислота, пикриновая кислота, метансульфоновая кислота, паратолуолсульфоновая кислота и глутаминовая кислота; соли, образованные с неорганическими основаниями, такими как натрий, калий, магний, кальций и алюминий; соли, образованные с органическими основаниями, такие как метиламин, этиламин, меглумин и этаноламин; соли, образованные с основными аминокислотами, такими как лизин, аргинин и орнитин; и соли аммония. Соединения имидазо-оксазина, представленные формулой (I), включают энантиомеры и гидраты.
[0033]
Соединения имидазо-оксазина, представленные формулой (I), или их фармацевтически приемлемые соли могут быть получены в соответствии с процедурой, описанной в WO2012/137870.
[0034]
В другом предпочтительном варианте осуществления настоящего изобретения, частные примеры ингибиторов PI3K/AKT/mTOR являются следующими: частные примеры ингибиторов PI3K включают AMG-319, AZD-6482, BYL-719, копанлисиб (BAY-80-6946), GDC-0032, GDC-0084, GSK-1059615, GSK-2126458, GSK-2636771, иделалисиб (CAL-101), IPI-145, MLN-1117 (INK-1117), PA-799 (CH-5132799), пиктилисиб (GDC-0941), пиларалисиб (XL-147), SF-1126, сонолисиб (PX-866) и воксталисиб (SAR-245409, XL-765); частные примеры ингибиторов AKT включают афуресертиб гидрохлорид (GSK-2110183), ARQ-092, AZD5363, энзастаурин гидрохлорид, GDC-0068, GSK-2141795, GSK690693, LY-2780301, MK-2206, перифосин и трицирибин фосфат (VQD-002); частные примеры ингибиторов mTOR включают AZD-2014, AZD-8055, CC-115, CC-223, DS-3078, эверолимус, темсиролимус, ME-344, MLN-0128 (INK-128), OSI-027, PWT-33597, ридафоролимус и сиролимус; и частные примеры двойных ингибиторов PI3K-mTOR включают дактолисиб (BEZ235), DS-7423, GDC-0980, NVP-BGT-226, PF-04691502, PF-05212384 (PKI-587) и PWT-33597. Эти ингибиторы коммерчески доступны, и могут также быть получены в соответствии с обычными известными процедурами.
[0035]
Из перечисленных выше ингибиторов PI3K/AKT/mTOR, MK-2206, BEZ235, GDC-0941, сиролимус и транс-3-амино-1-метил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[3,4-e][1,3]оксазин-2-ил)фенил)циклобутанол являются более предпочтительными, и транс-3-амино-1-метил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[3,4-e][1,3]оксазин-2-ил)фенил)циклобутанол является особенно предпочтительным с точки зрения эффектов стратификиции PHLDA1 и/или PIK3C2B.
[0036]
Лекарственная форма противоопухолевого средства, включающего ингибитор PI3K/AKT/mTOR согласно настоящему изобретению, особенно не ограничена и может быть выбрана из обычно известных лекарственных форм в зависимости от типа ингибитора PI3K/AKT/mTOR. Частные примеры включают пероральные лекарственные средства (например, таблетки, таблетки, покрытые оболочкой, порошковые лекарственные средства, гранулированные лекарственные средства, капсулы и жидкие лекарственные средства), инъецируемые лекарственные средства, суппозитории, пластыри и мази. Противоопухолевое средство может быть получено в соответствии с обычными известными процедурами с использованием фармакологически приемлемого носителя в зависимости от лекарственной формы. Примеры носителей включают такие, которые широко используются в типичных лекарственных средствах, такие как эксципиенты, связующие, дезинтеграторы, лубриканты, разбавители, солюбилизирующие средства, суспендирующие агенты, средства для придания тоничности, регуляторы рН, буферы, стабилизаторы, красители, ароматизаторы и средства, маскирующие аромат.
[0037]
“Химиотерапия с использованием противоопухолевого средства, включающего ингибитор PI3K/AKT/mTOR” согласно настоящему изобретению относится к химиотерапии, в которой вводят по меньшей мере противоопухолевое средство, включающее ингибитор PI3K/AKT/mTOR согласно настоящему изобретению. Химиотерапия включает не только химиотерапию с отдельным использованием противоопухолевого средства, включающего ингибитор PI3K/AKT/mTOR, но также и химиотерапию с использованием противоопухолевого средства, включающего ингибитор PI3K/AKT/mTOR, в комбинации с одним или более другими противоопухолевого средствами.
Количество ингибитора PI3K/AKT/mTOR, содержащегося в противоопухолевом средстве, варьирует в зависимости от симптомов пациента, получающего лечение средством, лекарственной формы средства и т.п. Однако предпочтительное количество ингибитора PI3K/AKT/mTOR в стандартной лекарственной форме обычно составляет приблизительно от 0,05 до 1000 мг для перорального лекарственного средства, приблизительно от 0,01 до 500 мг для инъецируемого лекарственного средства, и приблизительно от 1 до 1000 мг для суппозитория. Суточная доза противоопухолевого средства в вышеописанных лекарственных формах варьирует в зависимости от симптомов, массы тела, возраста, пола и других факторов пациента, и таким образом не может быть определена безусловно. Однако суточная доза средства для взрослого (масса тела: 50 кг) может обычно составлять приблизительно от 0,05 до 5000 мг, и предпочтительно от 0,1 до 1000 мг, и средство в таком количестве предпочтительно вводят в единственной дозе или в двух или трех разделенных дозах в сутки.
[0038]
Схему введения для химиотерапии предпочтительно определяют в зависимости от таких условий, как тип ингибитора PI3K/AKT/mTOR, наличие или отсутствие совместно используемого лекарственного средства, история лечения, стадия заболевания, наличие или отсутствие метастазов и возраст и пол пациента.
[0039]
Химиотерапия не делает никакого различия относительно того, прибегают ли к хирургии для удаления опухоли в течение химиотерапии, или до или после химиотерапии. Химиотерапия может быть любой из следующего: химиотерапия, которая не включает удаление опухоли, предназначенная в значительной степени для эффекта продления жизни; предоперационная адъювантная химиотерапия, включающая удаление опухоли, уменьшившейся после химиотерапии, предназначенная в значительной степени для уменьшения опухоли; и послеоперационная адъювантная химиотерапия, осуществляемая в превентивных целях после удаления опухоли, предназначенная в значительной степени для подавления рецидива или метастазирования.
[0040]
“Терапевтическая эффективность” в настоящем изобретении может быть оценена на основании эффектов сокращения опухоли, подавления рецидива или метастазирования, эффектов продления жизни и других эффектов, как описано выше. Фраза “для пациента вероятен достаточный ответ на химиотерапию с использованием противоопухолевого средства, включающего ингибитор PI3K/AKT/mTOR”, указывает, что терапевтическая эффективность у пациента, демонстрирующего низкий уровень экспрессии PHLDA1 или высокий уровень экспрессии PIK3C2B, заметно превосходит терапевтическую эффективность у пациента, демонстрирующего высокий уровень экспрессии PHLDA1 или низкий уровень экспрессии PIK3C2B, причем превосходство демонстрируется статистически значимым различием между ними.
[0041]
Биологический образец в настоящем изобретении особенно не ограничен, при условии, что образец выделен от пациента, страдающего раком, и содержит опухолевые клетки. Примеры включают жидкости организма (например, кровь, мочу и волосы скальпа), ткани (например, образцы биопсии ткани и иссеченные органы), их экстракты и культуры. Способ выделения биологического образца может быть соответственно выбран в зависимости от типа биологического образца.
[0042]
PHLDA1 (Подобный гомологии плекстрина домен семейства А член 1), индикатор согласно настоящему изобретению, является одним типом нуклеопротеида, имеющего домен гомологии плекстрина, и как сообщают, связан с антиапоптотическим действием инсулиноподобных факторов роста. Ассоциация PHLDA1 с путем PI3K/AKT/mTOR была неизвестна.
[0043]
PIK3C2B (фосфатидилинозитол-4-фосфат 3-киназа, каталитической субъединицы типа 2 бета), индикатор согласно настоящему изобретению, включен в суперсемейство PI3K. Однако, в отличие от PIK3CA, об ассоциации которого с ингибиторами PI3K/AKT/mTOR сообщалось, PIK3C2B является членом семейства PI3K класса II и не имеет регуляторной субъединицы.
[0044]
В способе прогноза согласно настоящему изобретению нет никаких специфических ограничений того, что подвергают измерению для того, чтобы измерить уровень экспрессии, при условии, что уровень экспрессии может быть измерен количественно или полуколичественно. Примеры включают уровень экспрессии мРНК, количество копий ДНК и уровня экспрессии белка.
[0045]
Уровень экспрессии мРНК, когда его выбирают для измерения, может быть измерен с использованием зонда или праймера, который специфически гибридизуется к мРНК PHLDA1 или PIK3C2B в соответствии с традиционно используемой методикой для измерения уровня экспрессии мРНК, такой как Нозерн-блоттинг, RT-ПЦР, ПЦР в реальном времени, микроматрица ДНК и гибридизация in situ.
[0046]
Количество копий ДНК, когда его выбирают для измерения, может быть измерено с использованием зонда, которое специфично гибридизуется с ДНК PHLDA1 или PIK3C2B в соответствии с традиционно используемой методикой для измерения количества копий ДНК, такой как гибридизация in situ, матрица CGH, микроматрица ДНК и Саузерн-блоттинг.
[0047]
Уровень экспрессии белка, когда его выбирают для измерения, может быть измерен с использованием антитела, которое специфически распознает белок PHLDA1 или PIK3C2B в соответствии с традиционно используемым иммунологическим анализом, таким как ELISA, Вестерн-блоттинг и иммуногистохимическое окрашивание.
[0048]
Праймер и зонд в настоящем изобретении могут быть получены как полинуклеотид, который специфически гибридизуется с ДНК или мРНК человеческого PHLDA1 или человеческого PIK3C2B на основе известной информации о последовательностях ДНК или мРНК человеческого PHLDA1 или человеческого PIK3C2B (человеческая ДНК PHLDA1: GenBankID NC_000012.11, мРНК: GenBankID NM_007350; человеческая ДНК PIK3C2B: GenBankID NC_000001.10, мРНК: GenBankID NM_002646) в соответствии с обычной известной методикой. Длина праймера составляет от 10 до 50 оснований, предпочтительно от 15 до 50 оснований, и более предпочтительно от 18 до 35 оснований. Длина зонда составляет от 15 оснований до полной длины основания, предпочтительно от 20 оснований до полной длины основания, и более предпочтительно от 30 оснований до полной длине основания.
[0049]
Праймер и зонд не обязательно должны иметь полную комплементарность, при условии, что они могут специфически гибридизоваться с ДНК или мРНК PHLDA1 или PIK3C2B. Праймер и зонд представляют собой, каждый, полинуклеотид, который имеет по меньшей мере 70%, предпочтительно по меньшей мере 80%, более предпочтительно по меньшей мере 90%, еще более предпочтительно по меньшей мере 95%, и особенно более предпочтительно по меньшей мере 98%-ую идентичность соответствующей последовательности основания.
[0050]
Фраза “специфически гибридизуется” в настоящем изобретении означает, что в строгих условиях гибридизации, образуется специфический гибрид и не образуется неспецифический гибрид. Строгие условия гибридизации могут быть определены на основании температуры плавления (Tm) нуклеиновой кислоты, которая образует гибрид в соответствии с обычной известной процедурой. Частные примеры условий промывки, которые могут поддерживать гибридизованное состояние, обычно включают состояния по существу “1×SSC, 0,1% SDS, 37°C”, более строгие условия - по существу “0,5×SSC, 0,1% SDS, 42°C”, и еще более строгие условия - по существу “0,1×SSC, 0,1% SDS, 65°C.”
[0051]
Зонд или праймер могут быть мечены обычно используемым радиоактивным веществом, флюоресцентным веществом, хемилюминесцентным веществом или ферментом для легкой детекции.
[0052]
Антитело в настоящем изобретении особенно не ограничено, при условии, что антитело может специфически распознавать белок PHLDA1 или PIK3C2B. Антитело может быть моноклональным антителом или поликлональным антителом и может быть фрагментом антитела, таким как фрагмент Fab и фрагмент F(ab’)2. Антитело может быть получено в соответствии с обычной известной процедурой (например, Current Protocols in Molecular Biology edit. Ausubel et al. (1987), Publish. John Wiley and Sons. Section 11.12-11.13) на основе известной информации аминокислотной последовательности белка человеческого PHLDA1 или человеческого PIK3C2B (человеческий PHLDA1 GenBankID NP_031376; человеческий PIK3C2B GenBankID NP_002637). Альтернативно, могут также использоваться коммерчески доступные антитела. Примеры античеловеческих антител PHLDA1 для использования включают Abcam Cat. #ab67849 и Abnova Cat. #H00022822-B01P, и примеры античеловеческих антител PIK3C2B включают Abcam Cat. #ab55589 и Abgent Cat. #AP3309a.
[0053]
В способе прогноза согласно настоящему изобретению, когда низкий уровень экспрессии PHLDA1 и/или высокий уровень экспрессии PIK3C2B наблюдается в опухолевых клетках пациента, страдающего раком, для пациента, страдающего раком, делают предсказание вероятности достаточного ответа на химиотерапию с использованием противоопухолевого средства, включающего ингибитор PI3K/AKT/mTOR.
[0054]
“Низкий уровень экспрессии PHLDA1” в рамках изобретения указывает, что уровень экспрессии PHLDA1 у пациента относительно ниже среди всех пациентов, страдающих раком; более конкретно, уровень экспрессии PHLDA1 равен или ниже, чем предопределенная пороговая точка.
[0055]
Пороговая точка в рамках изобретения варьирует в зависимости от различных условий, таких как тип измеряемого объекта и тип способа измерения. Таким образом, настоящее изобретение охватывает широкий диапазон изобретений, в которых используют пороговую точку, которая может варьировать в зависимости от этих условий, и пороговая точка не ограничена специфическим значением. Конкретная пороговая точка может быть определена в соответствии с различными методиками статистического анализа с использованием предызмеренных уровней экспрессии PHLDA1 пациентов, страдающих раком. Примеры пороговых точек включают среднее или медианное значение уровней экспрессии PHLDA1 пациентов, страдающих раком; и пороговую точку, которая разделяет пациентов на группы низкой и высокой экспрессии PHLDA1 и представляет собой значение, по которому p-значение теста логарифмического рангового критерия, проводимого в отношении терапевтической эффективности (например, период выживания) групп низкой и высокой экспрессии PHLDA1 является минимальным или меньшим чем определенный уровень (например, значение, по которому p-значение составляет менее 0,1, или значение, по которому p-значение составляет менее 0,05). Из них, среднее или медианное значение уровней экспрессии PHLDA1 пациентов, страдающих раком, является предпочтительным, и среднее значение уровней экспрессии PHLDA1 пациентов, страдающих раком, является более предпочтительным.
[0056]
Фраза “высокий уровень экспрессии PIK3C2B” указывает, что уровень экспрессии PIK3C2B у пациента относительно более высок среди всех пациентов, страдающих раком; более конкретно, уровень экспрессии PIK3C2B равен или выше чем предопределенная пороговая точка. Пороговая точка может быть определена тем же самым образом, как в уровне экспрессии PHLDA1, описанном выше. Среднее или медианное значение уровней экспрессии PIK3C2B пациентов, страдающих раком, является предпочтительным, и среднее значение уровней экспрессии PIK3C2B пациентов, страдающих раком, является более предпочтительным.
[0057]
Настоящее изобретение также относится к противоопухолевому средству, включающему ингибитор PI3K/AKT/mTOR, для лечения пациента, страдающего раком, для которого способом прогноза согласно настоящему изобретению предсказана или определена вероятность достаточного ответа на химиотерапию с использованием противоопухолевого средства, включающего ингибитор PI3K/AKT/mTOR.
[0058]
Настоящее изобретение также относится к применению такого противоопухолевого средства по изобретению.
[0059]
Противоопухолевое средство согласно настоящему изобретению может также сопровождаться инструкцией, руководством и т.п., в которых описана процедура осуществления на практике способа предсказания согласно изобретению.
[0060]
Настоящее изобретение также относится к набору для предсказания или тестирования терапевтической эффективности химиотерапии с использованием противоопухолевого средства согласно настоящему изобретению у пациента, страдающего раком. Набор согласно настоящему изобретению предпочтительно используют, чтобы предсказать или протестировать, способом прогноза согласно настоящему изобретению, терапевтическую эффективность химиотерапии.
[0061]
Чтобы измерить уровень экспрессии PHLDA1 и/или PIK3C2B, определяя количественно ДНК или мРНК в биологическом образце, содержащем опухолевые клетки, выделенном от пациента, страдающего раком, набор согласно настоящему изобретению может включать праймер и/или зонд, который является полинуклеотидом, который специфически гибридизуется с ДНК или мРНК человеческого PHLDA1 или человеческого PIK3C2B.
[0062]
Чтобы измерить уровень экспрессии PHLDA1 и/или PIK3C2B, определяя количественно белок (фермент) в биологическом образце, содержащем опухолевые клетки, выделенном от пациента, страдающего раком, набор согласно настоящему изобретению может включать антитело (первичное антитело) к PHLDA1 и/или PIK3C2B (фермент) и вторичное антитело к первичному антителу, причем вторичное антитело предпочтительно мечено люциферазной меткой, радиоактивной меткой, флюоресцентной меткой или ферментной меткой.
[0063]
Набор согласно настоящему изобретению может дополнительно включать инструкцию или руководство с описанием процедуры осуществления на практике способа прогноза согласно настоящему изобретению.
Примеры
[0064]
Следующие Примеры описывают настоящее изобретение более подробно. Однако настоящее изобретение, само собой разумеется, не ограничено этими Примерами.
Пример 1
Корреляция Между Уровнем Экспрессии PHLDA1 или PIK3C2B и Чувствительностью к ингибитору PI3K/AKT/mTOR
Анализ цитотоксичности проводили как описано ниже с использованием 37 линий клеток от человеческого рака молочной железы (AU565, BT20, BT474, BT549, CAMA-1, DU4475, HCC1187, HCC1419, HCC1428, HCC1500, HCC1569, HCC1599, HCC1806, HCC1937, HCC1954, HCC202, HCC2218, HCC38, HCC70, MDA-MB-157, MDA-MB-175, MDA-MB-231, MDA-MB-361, MDA-MB-415, MDA-MB-436, MDA-MB-453, MDA-MB-468, UACC-812 и UACC-893 (все получены от American Type Culture Collection (ATCC); MCF-7, SK-BR-3, T47D, and ZR-75-1 (все получены от Sumitomo Dainippon Pharma Co., Ltd.); KPL-1, KPL-3C и KPL-4 (предоставлены Dr. Kurebayashi at Kawasaki Medical School)). Каждую линию клеток высевали в плоскодонный микропланшет с 96 лунками в количестве 150 мкл и культивировали в термостате, содержащем 5%-ый газ диоксида углерода, при 37°C в течение одного дня. Ингибиторы PI3K/AKT/mTOR (ингибитор AKT: Соединение-I, MK-2206, двойной ингибитор PI3K-mTOR: BEZ235, ингибитор PI3K: GDC-0941, ингибитор mTOR: сиролимус), разбавляли постадийно диметилсульфоксидом, паклитаксел разбавляли постадийно диметилсульфоксидом, и диметилсульфоксид индивидуально добавляли к соответствующей среде для линий клеток. 50 мкл каждой среды добавляли в лунки вышеупомянутого плоскодонного микропланшета с 96 лунками так, чтобы конечная концентрация каждого лекарственного средства составила 10000, 3000, 1000, 300, 100, 30, 3 и 1 нМ. Отдельно полученный плоскодонный микропланшет с 96 лунками, в котором каждую линию клеток культивировали в течение одного дня, оставляли стоять при комнатной температуре в течение 30 минут, и 50 мкл супернатанта удаляли из каждой лунки, оставляя 100 мкл раствора клеточной культуры. К каждой лунке, содержащей оставшиеся 100 мкл раствора клеточной культуры, добавляли то же самое количество Люминесцентного Теста Жизнеспособности Клеток CellTiter-Glo (Promega, Cat. #G7573), был добавлен. Микропланшет оставляли стоять в темном месте в течение 10 минут, и затем интенсивность люминесценции живых клеток каждой лунки, к которой было добавлено лекарственное средство, измеряли, используя считыватель микропланшетов (PerkinElmer, ARVOsx). Линии клеток, к которым добавляли лекарственное средство или только диметилсульфоксид, далее культивировали при 37°C в термостате, содержащем 5%-ый газ диоксида углерода, в течение 3 дней. После культивирования, линиям клеток давали стоять при комнатной температуре в течение 30 минут, и 100 мкл супернатанта удаляли из каждой лунки, оставляя 100 мкл раствора клеточной культуры. К оставшимся 100 мкл растворов клеточной культуры добавляли то же самое количество Люминесцентного Теста Жизнеспособности Клеток CellTiter-Glo. Микропланшет оставляли стоять в темном месте в течение 10 минут, и затем интенсивность люминесценции живых клеток каждой лунки измеряли, используя считыватель микропланшетов. Темп роста клеток 37 линий клеток человеческого рака молочной железы определяли в соответствии со следующими уравнениями, и определяли концентрацию, при которой темп роста клеток составляет 50%, то есть, концентрацию (GI50; (мкМ)) каждого лекарственного средства, при которой рост клетки оказывался подавлен на 50%.
[0065]
Когда T≥C0, Темп роста клеток (%) = (T-C0)/(C-C0)×100
Когда T<C0, Темп роста клеток (%) = (T-C0)/C0×100
C0: интенсивность люминесценции в лунке, содержащей среду с клетками перед добавлением лекарственного средства (индексов в секунду)
C: Интенсивность люминесценции в лунке, содержащей среду с клетками, к которым был добавлен только диметилсульфоксид (индексов в секунду)
T: Интенсивность люминесценции в лунке, содержащей среду с клетками, к которым было добавлено тестируемое лекарственное средство (индексов в секунду)
После этого измеряли уровень экспрессии PHLDA1 и PIK3C2B на 37 линиях клеток человеческого рака молочной железы. Каждую линию клеток культивировали в 10 см чашке для клеточной культуры, пока приблизительно 50-80% слияния не было достигнуто, и полную РНК экстрагировали, используя RNeasy Mini Kit (Qiagen, Cat. #74106) в соответствии с инструкцией. Концентрацию и чистоту экстрагированной полной РНК исследовали, используя спектрофотометр (NanoDrop 1000, Thermo Fisher Scientific). Разложение также исследовали, используя Agilent 2100 Bioanalyzer (Agilent Technologies). Экстрагированную полную РНК подвергали обратной транскрипции в кДНК, используя GeneChip 3' IVT Express Kit (Affymetrix), и затем транскрибировали в биотинилированную кРНК. Затем амплифицированную биотинилированную кРНК (20 мкг) фрагментировали. Каждое действие проводили в соответствии с процедурой согласно инструкции, включенной в набор. Полученную биотинилированную кРНК от каждой линии клеток как образец добавляли к GeneChip Human Genome U-133 Plus 2.0 Array (Affymetrix, PIK3C2B probe set ID:204484_at, PHLDA1 probe set ID:217997_at) и затем помещали в GeneChip Hybridization Oven 640 (Affymetrix), с последующей гибридизацией при 45°C при 60 об/мин в течение 16 часов. После гибридизации, каждый образец промывали и метили флюоресцентной меткой с использованием GeneChip Fluidics Station 450 (Affymetrix) и затем сканировали с использованиес GeneChip Scanner 3000 7G (Affymetrix), чтобы получить данные микроматрицы. Анализ данных микроматрицы осуществляли, используя MATLAB (MathWorks). Уровень экспрессии генов определяли с помощью методики RMA (Robust Multi-array Average).
[0066]
Фиг.1 показывает корреляцию Pearson между логарифмом полученной выше GI50 каждого лекарственного средства и логарифмом уровня экспрессии PHLDA1 и PIK3C2B.
[0067]
Результаты показывают, что все исследованные ингибиторы PI3K/AKT/mTOR имели статистически значимую положительную корреляцию с уровнем экспрессии PHLDA1 и также имели статистически значимую отрицательную корреляцию с уровнем экспрессии PIK3C2B. Паклитаксел, однако, не показал корреляцию с уровнем экспрессии PHLDA1 или PIK3C2B. В частности, результаты показывают, что уровень экспрессии PIK3C2B и PHLDA1 может быть предиктивным маркером чувствительности для широкого спектра ингибиторов PI3K/AKT/mTOR.
[0068]
Было также исследовано, имеет ли уровень экспрессии PHLDA1 или PIK3C2B корреляцию с чувствительностью к ингибиторам PI3K/AKT/mTOR в группе 240 линий клеток (OncoPanelTM, Ricerca Biosciences), составленной из различных видов рака, таких как рак легкого, рак почек, рак печени, рак поджелудочной железы, рак толстого кишечника, рак мочевого пузыря, рак молочной железы, рак головы и шеи, рак предстательной железы, рак кожи, рак крови и злокачественная лимфома. Результаты показывают, что, как в случае 37 линий клеток человеческого рака молочной железы, наблюдалась значительная корреляция между логарифмом GI50 различных ингибиторов PI3K/AKT/mTOR (Соединение-I, MK-2206, BEZ235, GDC-0941 и сиролимус) и логарифмом уровня экспрессии PHLDA1 и PIK3C2B в группе 240 линий клеток.
[0069]
Пример 2
Анализ нокдауна гена PHLDA1, уровня экспрессии белка и статуса фосфорилирования
Ген PHLDA1 подвергали нокдауну, чтобы исследовать статус фосфорилирования AKT, и анализировали отношения между PHLDA1 и сигнальным путем PI3K/AKT/mTOR.
[0070]
Три линии клеток рака молочной железы (HCC38, HCC1806, HCC1937; все были получены от American Type Culture Collection (ATCC)), которые показывали относительно высокую экспрессию PHLDA1, культивировали в среде RPMI (Life Technologies Corp., Cat. #A104910-01), содержащей 10% FBS.
[0071]
siРНК отрицательного контроля (ON-TARGET Plus control pool, Thermo Fisher Scientific, Cat. #D-001810-10-20) и PHLDA1-siРНК (ON-TARGET Plus siRNA Human PHLDA1, Thermo Fisher Scientific, Cat. #J-012389-08) получали для этих линий клеток в конечной концентрации 10 нМ. siРНК вводили в клетки, используя Lipofectamine RNAiMAX (Life Technologies, Cat. #13778-150) в соответствии с инструкцией для нокдауна гена. После 3-дневного нокдауна, линии клеток промывали холодным PBS (Life Technologies, Cat. #10010-023) дважды, и солюбилизированный буфер (PhosSTOP (Roche, Cat. #4906837), полный, и буфер Pierce RIPA (Thermo Fisher Scientific, Cat. #89901), не содержащий EDTA (Roche, Cat. #1873580), добавляли к промытым линиям клеток с последующим охлаждением льдом в течение 30 минут для солюбилизации. Солюбилизированные экстракты центрифугировали при 4°C и 15000 об/мин в течение 30 минут, чтобы собрать супернатанты, таким образом получая экстракты белка. В полученных экстрактах белка измеряли концентрацию белка, используя BCA Protein Assay Reagent (Thermo Fisher Scientific, Cat. #23225) в соответствии с инструкцией. Восстанавливающий буфер (ImmunoPure Lane Marker Reducing Sample Buffer (Thermo Fisher Scientific, Cat. #39000)) добавляли к экстрактам белка, и экстракты доводили до кипения и таким образом модифицировали. 20 мкг каждого экстракта восстановленного белка наносили на полоски Criterion TGX Precast Gels (Bio-Rad, Cat. #567-1084) и осуществляли SDS-PAGE.
[0072]
После завершения SDS-PAGE, белки переносили на соответствующие мембраны PVDF (Trans-Blot Turbo Midi PVDF Transfer Pack, Bio-Rad, Cat. #170-4157) с использованием прибора для блоттинга (Trans-Blot Turbo Transfer System, Bio-Rad). Перенесенные мембраны инкубировали при комнатной температуре в течение 1 часа, чтобы осуществить блокирование с Blocking One-P (Nacalai, Cat. #05999-84). Затем мембраны вводили в реакцию при 4°C в течение ночи с античеловеческим козьим антителом PHLDA1 (Santa Cruz, Cat. #sc-6142) и античеловеческим фосфорилированным антителом кролика AKT (S473) (Cell Signaling Technology, Cat. #4060), которые разбавляли заранее в 1000 раз и 2000 раз, соответственно, буфером TBS (“TBS-T”), содержащим 5% BSA и 0,05% Tween20. Мембраны PVDF промывали TBS-T три раза при комнатной температуре в течение 10 минут и затем вводили в реакцию при комнатной температуре в течение 1 часа со вторичными антителами (антикозье антитело (Santa Cruz, Cat. #sc-2020) и антикроличье антитело (GE Healthcare, Cat. #NA9340V), которые были мечены пероксидазой хрена (HRP)), разбавленными в 2000 раз 5% снятый латекс/TBS-T. Мембраны PVDF промывали TBS-T три раза при комнатной температуре в течение 10 минут, и затем хемилюминесценцию детектировали с помощью LAS-3000 (Fujifilm) с использованием ECL Prime Western Blotting Detection Reagent (GE Healthcare, Cat. #RPN2232). На Фиг.2 показаны результаты.
[0073]
Как показано на Фиг.2, на трех линиях клеток рака молочной железы, которые демонстрируют высокую экспрессию PHLDA1, нокдаун гена PHLDA1 приводил к увеличению фосфорилирования AKT (S473), а также активации сигнального пути PI3K/AKT/mTOR. Поскольку уровень фосфорилирования AKT (S473) коррелирует in vitro и in vivo с противоопухолевыми эффектами ингибиторов PI3K (Cancer Research 70, 4982-4994 (2010)), результаты, показывает, что уровень экспрессии PHLDA1 может быть связан с терапевтической эффективностью ингибиторов PI3K/AKT/mTOR.
[0074]
Пример 3
Анализ изменения чувствительности к ингибитору PI3K/AKT/mTOR, вызванного нокдауном гена PIK3C2B
Линию клеток рака яичника человека OVCAR-3 (полученную от ATCC) культивировали в среде RPMI (Life Technologies Corp., Cat. #A104910-01), содержащей 20% FBS и 0,01 мг/мл бычьего инсулина (Sigma-Aldrich, Cat. #I0516). Человеческую линию клеток рака молочной железы HCC1187 (полученную от ATCC) культивировали в среде RPMI (Life Technologies Corp., Cat. #A104910-01), содержащей 10% FBS.
[0075]
Цитотоксичность ингибиторов PI3K/AKT/mTOR (ингибитор AKT: Соединение-I, ингибитор PI3K: GDC-0941) и паклитаксела на линиях клеток тестировали в соответствии с Примером 1. На Фиг.3 показан относительный индекс клеток линий клеток, обработанных лекарственными средствами в различных концентрациях, причем индекс клеток контрольных клеток (добавлен диметилсульфоксид), культивированных в течение трех дней, принимают за 100, и отсутствие клеток - за 0.
[0076]
Как показано на Фиг.3, в линиях клетки OVCAR-3 и HCC1187, нокаут гена PIK3C2B приводил к уменьшению чувствительности к Соединению-I и GDC-0941, которые являются ингибиторами PI3K/AKT/mTOR. Однако почти никакого изменения не наблюдалось в чувствительности к паклитакселу, который не является ингибитором PI3K/AKT/mTOR. В частности, результаты показывают, что PIK3C2B является определяющим фактором, который один может регулировать чувствительность раковых клеток к ингибитору PI3K/AKT/mTOR.
[0077]
Пример 4
Сравнение измерения уровня экспрессии PHLDA1/PIK3C2B с измерением обычная PIK3CA мутация/PTEN делеция в предсказании терапевтической эффективности ингибитора PI3K/AKT/mTOR
Уровень экспрессии PHLDA1 или PIK3C2B сравнивали с мутацией PIK3CA или делецией PTEN, которые были исследованы в качестве предиктивного маркера терапевтической эффективности в клинической практике, в терминах корреляции с чувствительностью к ингибитору PI3K/AKT/mTOR.
[0078]
Из 37 линий клеток человеческого рака молочной железы, описанных в Примере 1, 36 линий клеток (KPL-3C исключена), как известно, имели мутацию PIK3CA или делецию PTEN. На Фиг.4 показана GI50 (мкМ) Соединения-I для 36 линий клеток с наличием или отсутствием мутации PIK3CA (E545K или H1047R) или делеции PTEN. Делеция PTEN (8 линий клеток) не показывала корреляции с чувствительностью к Соединению-I. Мутация PIK3CA (10 линий клеток) демонстрировала тенденцию к корреляции с высокой чувствительностью к Соединению-I, но корреляция не была значительной (P=0,051). Аналогично, исследования проводили в отношении ассоциации уровня экспрессии PHLDA1 или PIK3C2B с чувствительностью к Соединению-I на 37 линиях клеток человеческого рака молочной железы. На Фиг.4 показано, например, распределение GI50 (мкМ) Соединения-I в случае, где среднее значение уровней экспрессии PHLDA1 или PIK3C2B было определено как пороговая точка, и уровни экспрессии были разделены на две группы. Уровень экспрессии каждого PHLDA1 и PIK3C2B показал сильную корреляцию с чувствительностью к Соединению-I (P=0,00061 и 0,0060).
[0079]
Уровень экспрессии PHLDA1 или PIK3C2B имеет явно более высокую корреляцию с чувствительностью к Соединению-I, чем обычные методики, мутация PIK3CA и делеция PTEN, и может быть использован как прогностический маркер терапевтической эффективности в клинической практике.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВОЕ ИМИДАЗООКСАЗИНОВОЕ СОЕДИНЕНИЕ ИЛИ ЕГО СОЛЬ | 2012 |
|
RU2578608C2 |
| УСИЛИТЕЛЬ ПРОТИВООПУХОЛЕВОГО ЭФФЕКТА, СОДЕРЖАЩИЙ ИМИДАЗООКСАЗИНОВОЕ СОЕДИНЕНИЕ | 2013 |
|
RU2618423C2 |
| СПОСОБ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ | 2020 |
|
RU2816126C2 |
| ПРЕПАРАТ И КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ | 2017 |
|
RU2777595C2 |
| СОЕДИНЕНИЯ БЕНЗОКСАЗЕПИНОКСАЗОЛИДИНОНОВ И СПОСОБЫ ПРИМЕНЕНИЯ | 2016 |
|
RU2730529C2 |
| СИНЕРГИСТИЧЕСКИЕ КОМБИНАЦИИ АУРИСТАНА | 2015 |
|
RU2717570C2 |
| БИОМАРКЕРЫ ДЛЯ ПРОГНОЗИРОВАНИЯ ЧУВСТВИТЕЛЬНОСТИ К ПРОТИВООПУХОЛЕВОЙ ТЕРАПИИ | 2012 |
|
RU2635193C2 |
| КОМБИНАЦИЯ, СОДЕРЖАЩАЯ ПИРИМИДИНОВОЕ СОЕДИНЕНИЕ, ДЛЯ ПРИМЕНЕНИЯ В ЛЕЧЕНИИ ОПУХОЛЕЙ | 2021 |
|
RU2827100C1 |
| МОРФОЛИНО-ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ МОЧЕВИНЫ ИЛИ КАРБАМАТА В КАЧЕСТВЕ ИНГИБИТОРОВ MTOR | 2012 |
|
RU2616619C2 |
| КОМБИНАЦИИ СОЕДИНЕНИЙ-ИНГИБИТОРОВ АКТ И АБИРАТЕРОНА, И СПОСОБЫ ПРИМЕНЕНИЯ | 2012 |
|
RU2631240C2 |
Настоящее изобретение относится к области биотехнологии, конкретно к оценке терапевтической эффективности химиотерапии с использованием противоопухолевого средства, и может быть использовано в медицине. Изобретение позволяет предсказывать терапевтическую эффективность химиотерапии с использованием противоопухолевого средства, включающего ингибитор PI3K/AKT/mTORна основе имидазо-оксазина, у пациента, страдающего раком, на основании уровня экспрессии PHLDA1 и/или PIK3C2B в выделенном от пациента биологическом образце. 2 н. и 3 з.п. ф-лы, 4 ил., 3 пр.
1. Способ предсказания терапевтической эффективности химиотерапии с использованием противоопухолевого средства, включающего ингибитор PI3K/AKT/mTOR, у пациента, страдающего раком, на основании уровня экспрессии PHLDA1 и/или PIK3C2B в опухолевых клетках, выделенных от пациента, страдающего раком, включающий следующие стадии (1) и (2):
(1) измерение уровня экспрессии PHLDA1 и/или PIK3C2B в биологическом образце, содержащем опухолевые клетки, выделенном от пациента; и
(2) предсказание, что для пациента вероятен достаточный ответ на химиотерапию с использованием противоопухолевого средства, включающего ингибитор PI3K/AKT/mTOR, когда уровень экспрессии PHLDA1, измеренного на стадии (1), равен или ниже предопределенной пороговой точки или когда уровень экспрессии PIK3C2B, измеренного на стадии (1), равен или выше предопределенной пороговой точки,
в котором указанная предопределенная пороговая точка для уровня экспрессии PHLDA1 представляет собой среднее или медианное значение уровней экспрессии PHLDA1 пациентов, страдающих раком, или значение, по которому p-значение теста логарифмического рангового критерия, проводимого в отношении терапевтической эффективности, составляет менее 0,1, и в котором указанная предопределенная пороговая точка для уровня экспрессии PIK3C2B представляет собой среднее или медианное значение уровней экспрессии PIK3C2B пациентов, страдающих раком;
в котором ингибитор PI3K/AKT/mTOR представляет собой соединение имидазо-оксазина, представленное формулой (I), или его фармацевтически приемлемую соль
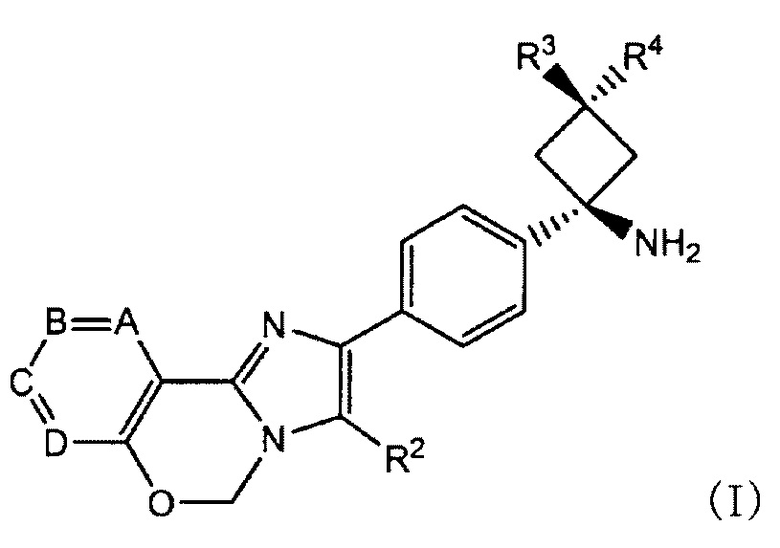
в которой
A, B, C и D обозначают C-R1a, C-R1b, C-R1c и C-R1d соответственно или один или два из таким образом определенных A, B, C и D заменены азотом;
по меньшей мере два из R1a, R1b, R1c и R1d обозначают водород, и другой (другие) каждый обозначает (обозначают) галоген, циано, C1-6 алкил, необязательно замещенный одной или более гидроксильными группами, C1-6 алкокси, карбонилом, имеющим гидроксил, амино, необязательно замещенный моно- или ди(C1-6 алкил)амино или моно- или ди(C1-6 алкокси)амино в качестве заместителя, или ненасыщенную гетероциклическую группу;
R2 обозначает фенил, пиридил или тиенил;
R3 обозначает водород, метил, этил или циклопропил; и
R4 обозначает водород или гидроксил;
или ингибитор PI3K/AKT/mTOR представляет собой AMG-319, AZD-6482, BYL-719, копанлисиб (BAY-80-6946), GDC-0032, GDC-0084, GSK-1059615, GSK-2126458, GSK-2636771, иделалисиб (CAL-101), IPI-145, MLN-1117 (INK-1117), PA-799 (CH-5132799), пиктилисиб (GDC-0941), пиларалисиб (XL-147), SF-1126, сонолисиб (PX-866), воксталисиб (SAR-245409, XL-765), афуресертиб гидрохлорид (GSK-2110183), ARQ-092, AZD5363, энзастаурин гидрохлорид, GDC-0068, GSK-2141795, GSK690693, LY-2780301, MK-2206, перифосин, трицирибин фосфат (VQD-002), AZD-2014, AZD-8055, CC-115, CC-223, DS-3078, эверолимус, темсиролимус, ME-344, MLN-0128 (INK-128), OSI-027, PWT-33597, ридафоролимус, сиролимус, дактолисиб (BEZ235), DS-7423, GDC-0980, NVP-BGT-226, PF-04691502, PF-05212384 (PKI-587) или PWT-33597.
2. Способ по п.1, в котором соединение имидазо-оксазина, представленное формулой (I), представляет собой соединение, в котором A, B, C и D обозначают C-R1a, C-R1b, C-R1c и C-R1d соответственно или любой один или два из таким образом определенных A, B, C и D заменены азотом;
по меньшей мере два из R1a, R1b, R1c и R1d обозначают водород, и другой (другие) каждый обозначает (обозначают) хлор, фтор, циано, метил, гидроксиметил, метокси, этокси, карбоксил, карбамоил, метиламинокарбонил, этиламинокарбонил, гидроксиэтиламинокарбонил, этоксиаминокарбонил или пиразолил;
R2 обозначает фенил, пиридил или тиенил;
R3 обозначает водород, метил, этил или циклопропил; и
R4 обозначает водород или гидроксил.
3. Способ по п.1, в котором соединение имидазо-оксазин, представленное формулой (I), представляет собой любое из следующих соединений (a)-(t),
(a) транс-3-амино-1-циклопропил-3-(4-(10-фтор-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(b) транс-3-амино-1-циклопропил-3-(4-(10-фтор-3-(пиридин-4-ил)-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(c) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(d) транс-3-амино-1-циклопропил-3-(4-(10-метокси-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(e) транс-3-амино-1-циклопропил-3-(4-(9-метокси-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(f) транс-3-амино-1-циклопропил-3-(4-(8-метокси-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(g) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[2,3-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(h) транс-3-амино-1-метил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[2,3-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(i) транс-3-амино-1-этил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[2,3-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(j) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[3,4-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(k) транс-3-амино-1-метил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[3,4-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(l) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[4,3-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(m) транс-3-амино-1-метил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[4,3-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(n) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[3,2-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(o) транс-3-амино-1-циклопропил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиразино[2,3-e][1,3]оксазин-2-ил)фенил)циклобутанол,
(p) транс-3-амино-3-(4-(9-(гидроксиметил)-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)-1-метилциклобутанол,
(q) 2-(4-(транс-1-амино-3-гидрокси-3-метилциклобутил)фенил)-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-9-карбонитрил,
(r) транс-3-амино-1-метил-3-(4-(3-фенил-9-(1H-пиразол-5-ил)-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-2-ил)фенил)циклобутанол,
(s) 2-(4-(транс-1-амино-3-гидрокси-3-метилциклобутил)фенил)-N-метил-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-8-карбоксамид, и
(t) 2-(4-(транс-1-амино-3-гидрокси-3-метилциклобутил)фенил)-N-этокси-3-фенил-5H-бензо[e]имидазо[1,2-c][1,3]оксазин-8-карбоксамид.
4. Способ по п.1, в котором ингибитор PI3K/AKT/mTOR представляет собой MK-2206, BEZ235, GDC-0941, сиролимус или транс-3-амино-1-метил-3-(4-(3-фенил-5H-имидазо[1,2-c]пиридо[3,4-e][1,3]оксазин-2-ил)фенил)циклобутанол.
5. Способ лечения пациента, страдающего раком, включающий введение противоопухолевого средства, включающего ингибитор PI3K/AKT/mTOR, пациенту, для которого способом по любому из пп.1-4 предсказана вероятность достаточного ответа на химиотерапию с использованием противоопухолевого средства, при этом ингибитор PI3K/AKT/mTOR представляет собой соединение имидазо-оксазина, представленное формулой (I), или его фармацевтически приемлемую соль

в которой
A, B, C и D обозначают C-R1a, C-R1b, C-R1c и C-R1d соответственно или один или два из таким образом определенных A, B, C и D заменены азотом;
по меньшей мере два из R1a, R1b, R1c и R1d обозначают водород, и другой (другие) каждый обозначает (обозначают) галоген, циано, C1-6 алкил, необязательно замещенный одной или более гидроксильными группами, C1-6 алкокси, карбонилом, имеющим гидроксил, амино, необязательно замещенный моно- или ди(C1-6 алкил)амино или моно- или ди(C1-6 алкокси)амино в качестве заместителя, или ненасыщенную гетероциклическую группу;
R2 обозначает фенил, пиридил или тиенил;
R3 обозначает водород, метил, этил или циклопропил; и
R4 обозначает водород или гидроксил;
или ингибитор PI3K/AKT/mTOR представляет собой AMG-319, AZD-6482, BYL-719, копанлисиб (BAY-80-6946), GDC-0032, GDC-0084, GSK-1059615, GSK-2126458, GSK-2636771, иделалисиб (CAL-101), IPI-145, MLN-1117 (INK-1117), PA-799 (CH-5132799), пиктилисиб (GDC-0941), пиларалисиб (XL-147), SF-1126, сонолисиб (PX-866), воксталисиб (SAR-245409, XL-765), афуресертиб гидрохлорид (GSK-2110183), ARQ-092, AZD5363, энзастаурин гидрохлорид, GDC-0068, GSK-2141795, GSK690693, LY-2780301, MK-2206, перифосин, трицирибин фосфат (VQD-002), AZD-2014, AZD-8055, CC-115, CC-223, DS-3078, эверолимус, темсиролимус, ME-344, MLN-0128 (INK-128), OSI-027, PWT-33597, ридафоролимус, сиролимус, дактолисиб (BEZ235), DS-7423, GDC-0980, NVP-BGT-226, PF-04691502, PF-05212384 (PKI-587) или PWT-33597.
| BOLLER D | |||
| et al., Targeting PI3KC2[beta] Impairs Proliferation and Survival in Acute Leukemia, Brain Tumors and Neuroendocrine Tumors, ANTICANCER RESEARCH, 2012, v | |||
| Способ образования коричневых окрасок на волокне из кашу кубической и подобных производных кашевого ряда | 1922 |
|
SU32A1 |
| КЛОЗЕТНЫЙ ПРОМЫВНОЙ БАК С ПРИСПОСОБЛЕНИЕМ ДЛЯ ПРИМЕШИВАНИЯ ДЕЗИНФЕКЦИОННОЙ ЖИДКОСТИ | 1925 |
|
SU3015A1 |
| WO 2010087497 A1, 05.08.2010 | |||
| LIU Z | |||
| et al., Phosphatidylinositol 3-kinase-C2[beta] inhibits cisplantin-mediated apoptosis via the Akt pathway in oesophageal squamous cell carcinoma, The J.I.Med.S., 2011, v | |||
| Машина для изготовления проволочных гвоздей | 1922 |
|
SU39A1 |
| Молокоотсос-шприц для парентерального введения стерильного молока | 1924 |
|
SU1319A1 |
| KNOBBE C | |||
| et al., Genetic alterations and aberrant expression of genes related to the phosphatidyl-inositol-2'-kinase/protein kinase B (Akt) signal transduction pathway in glioblasomas, BRAIN PATHOLOGY, 2003, v | |||
| Насос | 1917 |
|
SU13A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Способ получения олифы или массы для приготовления лаков | 1913 |
|
SU507A1 |
| WO 2012137870 A1, 11.10.2012 | |||
| SADEGHI N | |||
| et al., Targeting the PI3K pathway for cancer therapy, FUTURE MEDICINAL CHEMISTRY, 2012, v | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Трепально-чесальный станок | 1924 |
|
SU1153A1 |
| EA 201200101 A1, 30.08.2012. | |||
Авторы
Даты
2018-09-13—Публикация
2014-06-19—Подача