Область техники, к которой относится изобретение
Настоящее изобретение относится к созданию производного бактериального штамма авирулентной, непатогенной Clostridium ghonii, который способен подавлять рост одной или более солидных опухолей, вызывать регрессию одной или более солидных опухолей или же практически полное или полное разрушение одной или более солидных опухолей. Настоящее изобретение также относится к композиции, включающей производный бактериальный штамм для направленного лизиса солидных опухолей.
Уровень техники
Образование рака - многоступенчатый процесс, который вовлекает ряд молекулярных и структурных изменений. Солидные опухоли, такие как меланома, рак легкого, толстой кишки, головы/шеи, яичника, молочной железы, поджелудочной железы и предстательной железы, составляют 90% всех раковых опухолей. Признаками солидных опухолей последней стадии являются обширный ангиогенез, некроз и гипоксия, наряду с явным присутствием центральной (внутренней) области и периферической области. Центральная область солидной опухоли характеризуется высоким интерстициальным давлением, низким внеклеточным pH, гетерогенностью опухолевых клеток и анаэробным метаболизмом, включая гликолиз с высокой концентрацией глюкозы и уровнем лактата. Периферическая область, как правило, содержит быстро делящиеся раковые клетки, хотя эти клетки составляют лишь 25-50% от общего количества клеток, присутствующих в периферической области. Остальные клетки в периферической области обычно являются не раковыми клетками соединительной ткани.
Внутренние центральные области опухоли не поддаются современным методам химио- и лучевой терапии, поскольку недоступны для пассивно дифундирующих химиотерапевтических средств, вследствие плохой васкуляризации и высокого интерстициального давления. Кроме того, дефицит кислородных радикалов также способствует резистентности к химиотерапии и лучевой терапии, а также уменьшению повреждения ДНК в процессе лечения.
Если диагноз поставлен на ранней стадии, оперативное вмешательство является основным методом терапии для устранения рака, с последующей лучевой терапией и/или химиотерапией для предотвращения рецидива. Впрочем, из-за отсутствия определенных симптомов в клинических условиях, до 85% пациентов с солидными опухолями выявляются на поздней стадии, когда операция уже не эффективна. Химио/лучевая терапия или их комбинации часто использовались в качестве паллиативной терапии, которая не способна улучшить общий уровень выживаемости таких пациентов. Химические/лекарственные соединения в форме антител и ингибиторов передачи сигнала испытывали в доклинических исследованиях на животных с раковыми опухолями последней стадии для оценки противоопухолевой терапии, но такие соединения оказались не способны проникать в солидные опухоли, не могли накапливаться в высокой концентрации, эффективно достигать достаточного количества раковых клеток и покидать нераковые стромальные клетки, стволовые клетки, и при этом не затрагивалась структура опухолевой ткани. Кроме того, частое возникновение резистентности делает указанные методы молекулярной терапии в целом неэффективными.
Генную терапию для лечения рака считается более эффективным методом, чем указанные выше медикаментозные терапии. Виротерапия с применением живых вирусов, как предполагают, является лучшим подходом, в настоящее время уже используемым для лечения солидных опухолей поздних стадий, но имеет недостатки, такие как слабое распространение в опухоли (Shayakhmetov et al., 2002) и быстрый печеночный клиренс из кровотока после внутривенного введения. В совокупности, все доступные в настоящее время методы противоопухолевой терапии, направленные на устранение солидных опухолей, до сих пор не решили проблему эффективного лечения рака на поздних стадиях.
В случаях, когда внутреннее окружение опухоли, также известное как микроокружение, не позволяет эффективно применять химио, лучевую и виротерапию, такое окружение может обеспечивать уникальную возможность для применения терапии на основе бактерий, в которой используются анаэробные бактерии и присущие им онколитические свойства. Были изучены различные анаэробные бактерии, включая штаммы, относящиеся к роду Clostridium. В естественной среде, Clostridium имеют два состояния роста - вегетативная палочка и круглая спора. Последний тип представляет собой устойчивую защитную форму клостридий, которая помогает им выживать в сложных условиях. Спора имеет твердую оболочку, окружающую внешнюю поверхность ключевых жизненно важных частей внутри бактерий. Кроме того, на внутренней поверхности оболочек также присутствуют мембранные слои. В сочетании, твердая оболочка и мембранный слой позволяют клостридиям выживать в неблагоприятной среде, которая не подходит для вегетативной палочки. Когда становятся доступны такие условия роста, как анаэробная среда и большее количество питательных веществ, спора усиливает экспрессию генов и ускоряет рост вегетативных палочек.
Было показано, что облигатные анаэробные протеолитические спорообразующие клостридии, C. novyi (включают novyi-NT без удаленного основного токсина, но все еще несущий несколько других токсинов и токсичных факторов) и C. sordellii, обладают специфичной направленностью в уникальную гипоксическую/некротическую внутреннюю область опухоли (см. Фигуру 8), вызывая умеренный онколизис в некоторых раковых опухолях в сочетании с антиангиогенными средствами. Впрочем, указанные штаммы являются патогенными микроорганизмами и обычно вызывают различные болезни у человека, при этом основные проблемы вызывает их характерная токсичность для людей. Этими сложностями является то, что (1) уровни токсичности слишком высоки, чтобы они могли быть приемлемыми в качестве пригодных терапевтических моделей для лечения человека, и (2) условие биологической безопасности в случае применения патогенной бактерии для человека невозможно нарушить. Кроме того, штаммы дикого типа Clostridium novyi и C. sordellii показывали быстрое развитие токсических явлений, приводя к существенной гибели у экспериментальных мышей.
Настоящее изобретение основано на открытии и создании производных, облигатно анаэробных штаммов Clostridium ghonii, которые были адаптированы с целью того, чтобы вызывать более медленный, но уверенный онколизис, и, что важно и неожиданно, являются относительно не токсичными по сравнению с другими штаммами клостридий. Недавно обнаруженные штаммы являются производными авирулентного, непатогенного штамма Clostridium ghonii. Указанные производные штаммы Clostridium ghonii не только являются полезной альтернативой известным штаммам клостридий (например, C. sporogenes, C. novyi и C. sordeili), но проявляют меньше токсических побочных эффектов, нежели другие штаммы клостридий. Не будучи связанным никаким биологическим механизмом или процессом, новый способ адаптации, разработанный авторами изобретения и описанный в настоящей заявке, позволяет новым производным бактериальным штаммам приобретать дополнительную способность проникать через поврежденные сосуды в ангиогенные/гипоксические/некротические области солидной опухоли после внутривенной инъекции клостридиальных спор настоящего изобретения, чтобы прорастать в палочки, эффективно и неизбирательно лизировать/разжижать различные клетки, а также структурную основу (фибронектины и коллагены) в опухоли, вызывая, таким образом, существенное разрушение и изменение микроокружения опухоли. Такое разрушение микроокружения опухоли эффективно подавляет рост опухоли, возможно, сопровождается регрессом опухоли и, в некоторых случаях, в конечном счете, приводит к практически полному или совершенно полному разрушению всей опухоли. Настоящее изобретение дает возможность объединить подход применения инъекций спор с существующими методами, гарантируя полное устранение опухоли. В качестве неограничивающего примера, одной из таких возможностей является применение моноклонального антитела направленного действия, которое в иных случаях не будет эффективным в терапии солидной опухоли. Применение направленного моноклонального антитела в опухоли, микроокружение которой частично или полностью разрушено новыми бактериальными штаммами настоящего изобретения, становится намного более эффективным, вследствие недавнего изменения микроокружения опухоли. Применение спор настоящего изобретения, как описано и определено в настоящей заявке, несомненно, является вкладом в уровень техники как в форме противоопухолевой монотерапии, так и в комбинации с другой противоопухолевой терапией.
Сущность изобретения
Согласно первому аспекту, в настоящем изобретении предложен бактериальный штамм, который получен из авирулентного, непатогенного штамма Clostridium ghonii, где производный бактериальный штамм способен подавлять рост солидной опухоли. В настоящем изобретении также предложен бактериальный штамм, который получен из авирулентного, непатогенного штамма Clostridium ghonii, где производный бактериальный штамм способен вызывать регрессию или разрушение солидной опухоли. Штамм вызывает онколизис клеток, содержащихся в микроокружении опухоли. В настоящем изобретении также предложен онколизис тканевых структур, содержащихся в микроокружении, под действием одного или более ферментов, присутствующих в бактериальных клетках новых штаммов, таких как протеиназы, липазы и коллагеназы.
В одном варианте осуществления лизису подвергается от приблизительно 20% до приблизительно 90% или от приблизительно 20% до приблизительно 70%, или от приблизительно 20% до приблизительно 40%, или от приблизительно 20% до приблизительно 35%, или от приблизительно 25% до приблизительно 35% клеток в микроокружении опухоли. В другом варианте осуществления полученный бактериальный штамм вызывает меньшую токсичность по сравнению с референсным клостридиальным штаммом.
В другом варианте осуществления авирулентный, непатогенный штамм Clostridium ghonii может быть выбран из группы, состоящей из штаммов под регистрационными номерами ATCC 25757, BCRC 14548, CCUG 9282, DSM 15049, NCIMB 10636, PEV, Prevot PEV, VPI 4897 и VTT E-042451.
Бактериальный штамм настоящего изобретения может быть выбран из группы, состоящей из MW-DCG_LCv1, MW-DCG_LCv2, MW-DCG_LCv3, MW-DCG_LCv4, MW-DCG_LCv5, MW-DCG_LCv6, MW-DCG_LCv7, MW-DCG_LCv8, MW-DCG_LCv9, MW-DCG_LCv10, MW-DCG_LCv11, MW-DCG_LCv12, MW-DCG_LCv13, MW-DCG_LCv14, MW-DCG_LCv15, MW-DCG_LCv16, MW-DCG_LCv17, MW-DCG_LCv18, MW-DCG_LCv19, MW-DCG_LCv20, MW-DCG_LCv21, MW-DCG_LCv22, MW-DCG_LCv23, MW-DCG_LCv24, MW-DCG_LCv25, MW-DCG_LCv26, MW-DCG_CCv13, MW-DCG_CCv14, MW-DCG_CCv15, MW-DCG_CCv16, MW-DCG_CCv17, MW-DCG_HNCv13, MW-DCG_HNCv14, MW-DCG_HNCv15, MW-DCG_HNCv16, MW-DCG_HNCv17 и MW-DCG_HNCv18.
Штаммы бактерий MW-DCG_LCv1, MW-DCG_LCv2, MW-DCG_LCv3, MW-DCG_LCv4, MW-DCG_LCv5, MW-DCG_LCv6, MW-DCG_LCv7, MW-DCG_LCv8, MW-DCG_LCv9, MW-DCG_LCv10, MW-DCG_LCv11, MW-DCG_LCv12, DCG_HNCv13, MW-DCG_HNCv14, MW-DCG_HNCv15, MW-DCG_HNCv16, MW-DCG_HNCv17 и MW-DCG_HNCv18 обладают специфичностью в отношении и терапевтически эффективны против злокачественных солидных опухолей головы и шеи. Штамм MW-DCG_HNCv18 является предпочтительным штаммом и представлен регистрационным номером V12/001485.
Штаммы бактерий MW-DCG_LCv1, MW-DCG_LCv2, MW-DCG_LCv3, MW-DCG_LCv4, MW-DCG_LCv5, MW-DCG_LCv6, MW-DCG_LCv7, MW-DCG_LCv8, MW-DCG_LCv9, MW-DCG_LCv10, MW-DCG_LCv11, MW-DCG_LCv12, MW-DCG_CCv13, MW-DCG_CCv14, MW-DCG_CCv15, MW-DCG_CCv16 и MW-DCG_CCv17 обладают специфичностью в отношении и терапевтически эффективны против злокачественных солидных опухолей толстой кишки. Штамм MW-DCG_CCv17 является предпочтительным штаммом и представлен регистрационным номером V12/001487.
Штаммы бактерий MW-DCG_LCv1, MW-DCG_LCv2, MW-DCG_LCv3, MW-DCG_LCv4, MW-DCG_LCv5, MW-DCG_LCv6, MW-DCG_LCv7, MW-DCG_LCv8, MW-DCG_LCv9, MW-DCG_LCv10, MW-DCG_LCv11, MW-DCG_LCv12, MW-DCG_LCv13, MW-DCG_LCv14, MW-DCG_LCv15, MW-DCG_LCv16, MW-DCG_LCv17, MW-DCG_LCv18, MW-DCG_LCv19, MW-DCG_LCv20, MW-DCG_LCv21, MW-DCG_LCv22, MW-DCG_LCv23, MW-DCG_LCv24, MW-DCG_LCv25 и MW-DCG_LCv26 обладают специфичностью в отношении и терапевтически эффективны против злокачественных солидных опухолей легкого. Штамм MW-DCG_LCv26 является предпочтительным штаммом и представлен регистрационным номером V12/001486.
Согласно второму аспекту, в настоящем изобретении предложены клостридиальные споры одного или более бактериальных штаммов первого аспекта. В одном варианте осуществления клостридиальные споры второго аспекта могут быть объединены с физиологически приемлемым носителем и/или вспомогательным веществом.
Согласно третьему аспекту, в настоящем изобретении предложен способ подавления роста, регрессии или разрушения одной или более солидных злокачественных опухолей у субъекта, где способ включает введение терапевтически эффективного количества клостридиальных спор второго аспекта субъекту, нуждающемуся в этом.
Согласно четвертому аспекту, в настоящем изобретении предложено применение клостридиальных спор второго аспекта с целью вызвать подавление роста, регрессию или разрушение одной или более солидных опухолей у субъекта, где терапевтически эффективное количество клостридиальных спор второго аспекта вводят субъекту, нуждающемуся в этом.
Согласно пятому аспекту, в настоящем изобретении предложен способ лечения одной или более солидных злокачественных опухолей у субъекта, где подавление роста одной или более опухолей, регрессия опухоли или разрушение опухоли служит показателем лечения, где способ включает введение:
(1) терапевтически эффективного количества клостридиальных спор согласно второму аспекту и
(2) терапевтически эффективного количества противоопухолевого средства субъекту.
Согласно шестому аспекту, в настоящем изобретении предложено применение клостридиальных спор второго аспекта и противоопухолевого средства в комбинированной терапии для лечения одной или более солидных злокачественных опухолей у субъекта, где подавление роста одной или более опухолей, регрессия опухолей или разрушение опухолей является показателем лечения, где (1) терапевтически эффективное количество клостридиальных спор второго аспекта и (2) терапевтически эффективное количество противоопухолевого средства вводят субъекту, нуждающемуся в этом.
В варианте осуществления пятого и шестого аспектов, введение (1) и (2) субъекту происходит последовательно или одновременно. (1) и (2) можно вводить субъекту в виде одной фармацевтической композиции. Введение (1) и (2), в виде одной композиции или по отдельности, может быть повторено один или более раз, чтобы гарантировать регрессию опухоли. Например, (1) и (2) можно вводить субъекту в качестве первой дозы, с последующим введением одного (2) в качестве второй дозы. Можно вводить больше одного противоопухолевого средства в любом количестве доз.
В другом варианте осуществления (1) представляет собой клостридиальные споры MW-DCG_HNCv18, а (2) - химерное моноклональное антитело против EGFR. В другом варианте осуществления (2) представляет собой Цетуксимаб. В еще одном варианте осуществления клостридиальные споры MW-DCG_HNCv18 и Цетуксимаб одновременно вводят субъекту, с последующим вторым введением одного Цетуксимаба.
В одном варианте осуществления третьего, четвертого, пятого и шестого аспектов терапевтически эффективное количество клостридиальных спор второго аспекта составляет от приблизительно 106 колониеобразующих единиц (КОЕ) до приблизительно 1014 КОЕ/кг на дозу. В другом варианте осуществления терапевтически эффективное количество клостридиальных спор второго аспекта составляет приблизительно 108-1012 или приблизительно 109-1011 КОЕ/кг на дозу. В другом варианте осуществления терапевтически эффективное количество клостридиальных спор второго аспекта составляет приблизительно 1010-1011 КОЕ/кг на дозу. В еще одном варианте осуществления терапевтически эффективное количество клостридиальных спор второго аспекта составляет приблизительно 1010,5 КОЕ/кг на дозу. Введение терапевтически эффективного количества клостридиальных спор второго аспекта субъекту может быть выполнено внутривенно, люмбально, подкожно или внутримышечно. Например, введение может быть внутривенным.
Согласно седьмому аспекту, в настоящем изобретении предложена фармацевтическая композиция, включающая клостридиальные споры второго аспекта и физиологически приемлемый носитель и/или вспомогательное вещество. Композиция может дополнительно включать противоопухолевое средство. Противоопухолевое средство может быть средством, определенным согласно пятому и шестому аспектам.
Противоопухолевое средство является любым средством, которое может использоваться в химиотерапии, лучевой терапии или терапии на основе антител или их комбинациях. Средство может быть одним или более химическими соединениями, одной или более молекулами РНК, одним или более антителами или их любой комбинацией.
Например, одно или более химических соединений могут быть дихлорацетатом натрия, паклитакселом, доксилом, топотеканом, ДНК-модифицирующими лекарственными средствами, карбоплатином, антиметаболитами, гемцитабином, лекарственными средствами, которые блокируют деление клеток, винкристином, антиангиогенными средствами и пазопанибом.
Примером одной или большего количества молекул РНК является малая интерферирующая РНК (миРНК). миРНК может быть специфична к лактатдегидрогеназе (LDHA) или специфична к CD147.
Примером одного или большего количества антител является противоопухолевое моноклональное антитело. Противоопухолевое антитело может быть антителом против иммуностимуляции или моноклональным антителом против регуляторных T-клеток. Примером антитела против иммуностимуляции является моноклональное антитело против CD40. Моноклональным антителом против CD40 может быть FGK45. Примером моноклонального антитела против регуляторных T-клеток является моноклональное антитело против CD25. Моноклональным антителом против CD25 может быть PC61. В другом варианте осуществления средство направлено против рецептора эпидермального фактора роста (EGFR).
Противоопухолевое моноклональное антитело может быть конъюгированным или "голым". Голые антитела, например, действуют через комплемент-опосредованный цитолиз и антителозависимую клеточноопосредованную цитотоксичность. Конъюгированные антитела включают антитела, которые конъюгированы с радиоизотопом или ферментом, активирующим лекарственное соединение. Радиоизотопно конъюгированное антитело может использоваться в радиоиммунотерапии. Примерами радиоизотопно конъюгированного антитела или радиоизотопа является рений-188 или рений-186, фтордезоксиглюкоза (18F), также известная, как FDG, иттрий-90 (90Y)-конъюгированное антитело против CD20, Y90-ибритутомаб тиуксетан, и иод-131 (131I)-конъюгированное антитело против CD20, I131-тозитумомаб. Антитела, конъюгированные с активирующим лекарственное соединение ферментом, могут использоваться в антителонаправленной терапии с применением фермента и пролекарства (ADEPT). Противоопухолевое моноклональное антитело может быть конъюгировано с липосомой или наночастицей, которые могут заключать в себе различные лекарственные средства и терапевтические нуклеотиды, такие как молекулы миРНК.
Способ согласно пятому аспекту и применение согласно шестому аспекту может дополнительно включать гормональную терапию, гипертермию, хирургию, радиацию или их любую комбинацию, в качестве альтернативы или в дополнение к введению одного или более противоопухолевых средств. Радиация может быть ионизирующим излучением.
Согласно восьмому аспекту, в настоящем изобретении предложен способ получения бактериального штамма из авирулентного, непатогенного штамма Clostridium ghonii, где производный бактериальный штамм, полученный указанным способом, способен подавлять рост, вызывать регрессию или разрушение одной или более солидных опухолей в результате онколизиса клеток в микроокружении одной или большего количества опухолей, где производный бактериальный штамм, полученный указанным способом, вызывает меньшую токсичность, чем референсный клостридиальный штамм.
В одном варианте осуществления способ получения бактериального штамма из авирулентного, непатогенного штамма Clostridium ghonii включает:
(1) Получение инъекционной формы клостридиальных спор из авирулентного, непатогенного штамма Clostridium ghonii, включающее:
(a) инокуляцию вегетативных палочек бактериального штамма (1) в среду спорулирования,
(b) выдерживание в течение достаточного времени и в определенных условиях для спорулирования палочек, и
(c) очистку спор;
(2) Введение очищенных клостридиальных спор (1) животному, которое поддерживает рост солидной опухоли;
(3) Оценку параметров для определения скорости и степени онколизиса и токсичности;
(4) Сбор вегетативных палочек из опухоли (2) при извлечении опухоли;
(5) Посев палочек (4) на агаровую чашку;
(6) Отбор двух или более одиночных колоний с чашки (5) и инокуляцию питательной культуры с целью выращивания вегетативных палочек; и
(7) Повтор этапов (1)(a)-(6) от приблизительно 10 до приблизительно 35 раз.
В другом варианте осуществления две или более одиночных колоний (6) являются тремя одиночными колониями.
В другом варианте осуществления этапы (1)(a)-(6) повторяют от приблизительно 15 до приблизительно 30 раз или от приблизительно 17 до приблизительно 26 раз.
В другом варианте осуществления параметры (3) могут включать время колонизации спор, онколизис, образование и выход гноя, объем опухоли, системную токсичность, выживание животных, количество спор/палочек, выделенных из опухолей после внутривенного введения спор или любую комбинацию перечисленного.
В другом варианте осуществления бактериальный штамм вызывает лизис от приблизительно 20% до приблизительно 90% или от приблизительно 20% до приблизительно 70%, или от приблизительно 20% до приблизительно 40%, или от приблизительно 20% до приблизительно 35%, или от приблизительно 25% до приблизительно 35% клеток в микроокружении опухоли. В другом варианте осуществления авирулентный, непатогенный штамм Clostridium ghonii может быть выбран из группы, состоящей из штаммов с регистрационными номерами ATCC 25757, BCRC 14548, CCUG 9282, DSM 15049, NCIMB 10636, PEV, Prevot PEV, VPI 4897 и VTT E-042451.
Согласно девятому аспекту, в настоящем изобретении предложен набор для лечения одной или более солидных злокачественных опухолей, включающий бактериальный штамм согласно первому аспекту, клостридиальные споры согласно второму аспекту или фармацевтическую композицию согласно седьмому аспекту, дополнительно включающий противоопухолевое средство и инструкции по применению.
В варианте осуществления согласно одному или нескольким предыдущим аспектам, субъект может быть млекопитающим. Млекопитающее может быть человеком.
В варианте осуществления согласно одному или нескольким предыдущим аспектам, солидная злокачественная опухоль выбрана из группы, состоящей из карцином дыхательной системы, карцином желудочно-кишечной системы, карцином мочеполовой системы, карцином яичков, карцином молочной железы, карцином предстательной железы, карцином эндокринной системы, меланом, хориокарциномы и карцином шейки матки, легкого, головы и шеи, толстой кишки, яичника, головного мозга, мочевого пузыря, молочной железы, предстательной железы, опухолей костной, жировой и хрящевой ткани, болезни Ходжкина, нехождкинской лимфомы, B-клеточной лимфомы, эпителиотропной лимфомы, композитной лимфомы, анапластической крупноклеточной лимфомы, лимфомы лимфоидной ткани, ассоциированной с желудочной и нежелудочной слизистой, лимпфопролиферативной болезни, T-клеточной лимфомы, лимфомы Беркитта, мантийноклеточной лимфомы, диффузной крупноклеточной лимфомы, лимфоплазмацитоидной лимфомы и множественной миеломы.
Определения
В рамках настоящего описания, термин "включающий" означает "включает в основном, но не обязательно исключительно". Кроме того, вариации слова "включающий", такие как "включает", имеют соответственно измененные значения.
Термин "штамм" означает подмножество бактериальных видов, отличающееся от других бактерий тех же видов одним или несколькими незначительными, но определяемыми, различиями. Штамм представляет собой "популяцию организмов, которая происходит от одного организма или изолята чистой культуры. Штаммы в пределах вида могут несколько отличаться друг от друга различными способами" (стр. 392, Prescott et al., 1996). Штаммы часто создаются в лаборатории путем мутагенеза существующих штаммов или диких вариантов бактериальные видов.
При использовании в настоящем описании, термин "производный" является любым бактериальным штаммом, полученным из авирулентного, непатогенного Clostidium ghonii, такого как, без ограничения, штаммы под регистрационным номером ATCC 25757, BCRC 14548, CCUG 9282, DSM 15049, NCIMB 10636, PEV, Prevot PEV, VPI 4897 и VTT E-042451, с использованием которых было осуществлено получение производных штаммов путем последовательных этапов селекции, выделения и инокуляции с ксенографтной солидной опухолью у животного, в результате чего наблюдается онколизис опухоли, а токсичность для животного является незначительной.
При использовании в настоящем описании, термины "некротическая область", "гипоксическая область", "центральное окружение" и "микроокружение" являются взаимозаменяемыми и относятся к внутренней части солидной опухоли, которая имеет одно или несколько следующих особенностей: наличие высокого интерстициального давления, низкого внеклеточного pH, гетерогенности опухолевых клеток и анаэробного метаболизма, включая гликолиз с высокой концентрацией глюкозы и уровнем лактата.
При использовании в настоящем описании, термин "выделенный" или "выделение" означает, что бактериальные клетки были удалены или собраны с культуральных чашек или из их естественной окружающей среды или хозяина (например, опухоли).
При использовании в настоящем описании, фраза "меньшая токсичность, чем референсный клостридиальный штамм" и "вызывает меньшую токсичность, чем референсный клостридиальный штамм" означает, что рост производного клостридиального штамма в солидной опухоли субъекта и последующий онколизис дает меньшую токсичность для субъекта по сравнению с субъектом, которому ввели референсный клостридиальный штамм, где референсный штамм может быть, без ограничения, сахаролитической разновидностью, протеолитическим C. sporogenes, протеолитическим C. novyi-NT и C. sordellii, или даже C. ghonii, которые не были получены способом настоящего изобретения или только прошли процесс адаптации. Уровень токсичности определяют и оценивают с использованием полного оценочного листа, включающего следующие четыре уровня: Внешний вид; Клинические симптомы; Неспровоцированное поведение; и Поведенческие реакции на внешние стимулы.
Термин "рак" включает злокачественные новообразования, характеризующиеся нерегулируемым или неконтролируемым ростом клеток, такие как солидные злокачественные новообразования, которые могут формироваться в виде карциномы, саркомы или лимфомы. Термин "рак" включает первичные злокачественные опухоли, например, опухоли, клетки которых еще не мигрировали в другие участки в теле субъекта помимо участка локализации исходной опухоли, и вторичные злокачественные опухоли, например, опухоли, которые являются результатом метастазирования, миграции клеток опухоли во вторичные участки, отличные от участка локализации исходной опухоли.
При использовании в настоящем описании, термин "солидная опухоль" является аномальной массой ткани, которая обычно не содержит кисты или области с жидкостью. Солидные опухоли могут быть доброкачественными или злокачественными. Солидные опухоли, рассматриваемые в настоящей заявке, являются злокачественными опухолями. Саркомы, карциномы и лимфомы могут иметь отношение к солидным опухолям. Лейкозы обычно не формируют солидные опухоли.
При использовании в настоящем описании, термин "карцинома" означает любое злокачественное новообразование из эпителиальных или эндокринных тканей, включая карциномы дыхательной системы, карциномы желудочно-кишечной системы, карциномы мочеполовой системы, карциномы яичка, карциномы молочной железы, карциномы предстательной железы, карциномы эндокринной системы, меланомы, хориокарциному, а также карциномы шейки матки, легкого, головы и шеи, толстой кишки и яичника.
При использовании в настоящем описании, термин "саркома" означает любые злокачественные опухоли мезодермальной соединительной ткани, например, опухоли костной, жировой и хрящевой ткани.
При использовании в настоящем описании, термин "лимфома" означает любое злокачественное новообразование из гематопоэтических клеток костного мозга. Эти злокачественные новообразования обычно проявляются как солидные опухоли. Примеры лимфом включают болезнь Ходжкина, неходжкинскую лимфому, B-клеточную лимфому, эпителиотропную лимфому, комплексную лимфому, анапластическую крупноклеточную лимфому, лимфому лимфоидной ткани, ассоциированной с желудочной и нежелудочной слизистой, лимфопролиферативную болезнь, T-клеточную лимфому, лимфому Беркитта, мантийноклеточную лимфому, диффузную крупноклеточную лимфому, лимфоплазмацитоидную лимфому и множественную миелому.
При использовании в настоящем описании, термин "подавление" означает, что опухоль прекратила расти.
При использовании в настоящем описании, термин "регрессия опухоли" означает уменьшение солидных опухолей после введении клостридиальных спор настоящего изобретения, отдельно или в комбинации с противоопухолевым средством и/или дополнительной противоопухолевой терапией. Для определения регрессии опухоли, размер обработанной и необработанной (контрольной) опухоли измеряют в определенной точке времени и сравнивают друг с другом. Как "подавление", так и "регрессия" могут, в конечном счете, приводить или не приводить к разрушению опухоли.
При использовании в настоящем описании, термин "субъект" означает организмы, которые могут страдать от рака, особенно в форме солидных опухолей. Организмы могут быть млекопитающими и включают человека и различных, не относящихся к человеку, животных, таких как приматы, собаки и кошки. Предпочтительные животные, относящиеся к человеку, включают относящихся к человеку субъектов. Как рассматривается в настоящем описании, субъект может подвергаться большему риску возникновения солидных злокачественных опухолей, развивающихся в их теле, по сравнению со средним представителем популяции.
При использовании в настоящем описании, термин "лечение" и его вариации относится к любым возможным применениям, которые устраняют состояние болезни или симптомы, предотвращают развитие болезни, или иным образом предотвращают, препятствуют, задерживают или меняют вспять прогрессию болезни или других нежелательных симптомов каким бы то ни было образом. Как рассматривается в настоящем описании, лечение солидной опухоли означает подавление роста, регрессию или полное или практически полное разрушение опухоли.
При использовании в настоящем описании, термин "эффективное количество" включает, в рамках своего значения, нетоксичное, но достаточное количество компонента как такового, которое обеспечивает требуемый терапевтический или профилактический эффект. Точное требуемое количество будет изменяться от субъекта к субъекту в зависимости от таких факторов, как биологический вид, подвергаемый лечению, возраст и общее состояние субъекта, тяжесть состояния, подвергаемого лечению, конкретное вводимое вещество, способ введения и т.д. Таким образом, не возможно определить точное "эффективное количество". Однако, для любого данного случая, соответствующее "эффективное количество" может быть определено средним специалистом в данной области при использовании стандартных экспериментов. В частности, термины "эффективное количество" и "терапевтически эффективное количество" синонимично относятся к такому количеству композиции или единичной дозированной формы, которая в группе пациентов производит эффект (1) уменьшения размера опухоли; (2) ингибирования (то есть, замедления в некоторой степени, предпочтительно остановки) метастазирования опухоли; (3) ингибирования в некоторой степени (то есть, замедления в некоторой степени, предпочтительно подавления) роста опухоли; и/или; (4) ослабление в некоторой степени (или предпочтительно устранение) одного или нескольких симптомов, связанных с раком; (5) практически полное или полное разрушение опухоли; (6) увеличение времени прогрессии болезни; и/или (7) повышение общей выживаемости.
При использовании в настоящем описании, "фармацевтическая композиция" относится к клостридиальным спорам, в отдельности или в одной или более комбинациях, описанных в настоящей заявке. В одном варианте осуществления комбинация представляет собой клостридиальные споры производных бактериальных штаммов настоящего изобретения и одно или более противоопухолевых средств, которые могут быть известны в уровне техники. Другие химические компоненты, такие как физиологически приемлемые носители и вспомогательные вещества, также рассматриваются в настоящем описании.
При использовании в настоящем описании, термин "фармацевтически приемлемый" означает, что агент или вспомогательное вещество в целом считаются приемлемыми для применения в фармацевтической композиции.
При использовании в настоящем описании, "физиологически приемлемый носитель" относится к носителю или разбавителю, который не вызывает существенного раздражения организма и не нарушает биологической активности и свойств вводимой композиции. Примерные фармацевтически приемлемые носители включают твердые и жидкие разбавители. Примерами фармацевтически приемлемых жидких разбавителей являются вода, этанол, пропиленгликоль и глицерин; из них, в некоторых вариантах осуществления, предпочтительной является вода.
При использовании в настоящем описании, "вспомогательное вещество" относится к фармацевтически инертному веществу, добавляемому к фармацевтической композиции для дополнительного облегчения введения фармацевтической композиции настоящего изобретения. Неограничивающие примеры вспомогательных веществ включают карбонат кальция, фосфат кальция, различные сахара и типы крахмала, производные целлюлозы, желатин, растительные масла и полиэтиленгликоли. Группы вспомогательных веществ и активных фармацевтических компонентов в области фармацевтики считаются взаимоисключающими.
Краткое описание фигур
Фигура 1. Схематическое изображение образования спор. На схематическом изображении показано, что новую аликвоту суспензии клостридиальных спор сеют на чашку с усиленным клостридиальным агаром в анаэробных условиях на 24 часа. Затем отбирают до пяти колоний, инокулируют в 10 мл среды HI и анаэробно культивируют. Через двадцать четыре часа культуру переносят в 50 мл или 100 мл модифицированной среды для спорулирования и культивируют в анаэробных условиях. Если используется емкость с плотно закрытой крышкой, культуру можно инкубировать в обычном инкубаторе без анаэробных условий. Споры готовы для сбора через 7 дней, но могут быть собраны даже через 14 дней. Во время сбора колбу быстро встряхивают, затем оставляют на пару минут, верхний слой культуры отбирают пипеткой во флакон для центрифужных стаканов и центрифугируют при 5000g для промывки спор. Очищенные споры титруют, чтобы определить титр в колониеобразующих единицах (КОЕ). Эта работа занимает 2-4 дня. Процесс может быть масштабирован.
Фигура 2. Онколитическая активность полученных бактериальных штаммов. Мышей рандомизировано распределяли в 3 группы. В день 15, группу 1 оставляли без инъекции в качестве контроля (обозначили как 'нет' в подписи на фигуре), Группе 2 вводили фосфатно-солевой буфер (обозначили как 'PBS' в подписи на фигуре) и группе 3 вводили споры производного бактериального штамма (обозначили как 'DCG' в подписи на фигуре). Объем опухоли регистрировали все последующие дни. Группа DCG показала замедленный рост объема опухоли.
Фигура 3. Схематическое изображение доставки спор и повторной адаптации клостридиальных спор. Мышам (n=3), имеющим опухоли различных размеров (от поддающихся обнаружению до 0,45 см3), в/в вводили 108 КОЕ спор. Рост и объем опухоли у мышей оценивали через день, используя ультразвук и цифровые штангенциркули. Кроме того, оценивали промежуток времени до изменения цвета поверхности опухоли, образование некроза/жидкости/гноя в опухоли и выход жидкости/гноя/разрыв опухоли, время и количество спор в опухолях, рост/уменьшение/исчезновение опухоли, а также любые токсические проявления и изменения поведения у животных. Только те опухоли, которые показывают выход жидкости/гноя/разрыв опухоли или образование некроза/жидкости/гноя на уровне 80%, вырезали и гомогенизировали. Лизаты этих опухолей использовали для посева на чашки с агаром для последующего и повторного выделения клостридиальной культуры. Процесс адаптации повторяли в зависимости от типа опухолей.
Фигура 4. Онколитическая активность MW-DCG_LCv26 (указан на фигуре как DCGnv26) в модели рака легкого (НМРЛ) (A549). Мышей рандомизировано распределяли в 4 группы. В день 15, группу 1 оставляли без инъекции в качестве контроля, Группе 2 вводили PBS, 3 - DCG и 4 - споры MW-DCG_LCv26. Объем опухоли регистрировали все последующие дни.
Фигура 5. Онколитическая активность MW-DCG_CCv17 (указан на фигуре как DCGv17) в модели рака толстой кишки. Мышей рандомизировано распределяли в 4 группы. В день 15, группу 1 оставляли без инъекции в качестве контроля, Группе 2 вводили PBS, 3 - DCG и 4 - споры MW-DCG_CCv17. Объем опухоли регистрировали все последующие дни.
Фигура 6. Онколитическая активность MW-DCG_HNCv18 (указан на фигуре как DCGhv18) в модели рака головы и шеи. Мышей рандомизировано распределяли в 4 группы. В день 15, группу 1 оставляли без инъекции в качестве контроля, Группе 2 вводили PBS, 3 - DCG и 4 - споры MW-DCG_HNCv18. Объем опухоли регистрировали все последующие дни.
Фигура 7. (I). Противоопухолевые терапевтические эффекты. Мышей рандомизировано распределяли в группы. В день 16, группе 1 вводили PBS, Группе 2 и 3 - споры DCG. Группе 3 также вводили Цетуксимаб. Объем опухоли регистрировали все последующие дни. (II). Процент выживших животных. Представлены три группы.
Фигура 8. Схематическая диаграмма, на которой показано разжижение опухоли изнутри и гибель живых раковых клеткок снаружи (по периферии). Данный подход представляет собой концептуальное изменение в развитии противоопухолевой терапии.
Фигура 9. Специфичность колонизации опухоли штаммом MW-DCG_LCv26. Споры MW-DCG_LCv26 внутривено вводили мышам, имеющим подкожную НМРЛ, в дозе 108 КОЕ/кг на мышь. Ткань опухоли и нераковую ткани сердца, легкого, селезенки, почки и печени забирали после прорастания спор в течение 24 и 96 часов после инъекции. Половину забранной ткани гомогенизировали и подвергали анализу на присутствие спор, подсчитывая проросшие споры.
Фигура 10. Фотоизображения НМРЛ после доставки спор показывают специфичную колонизацию и онколизис опухоли. На снимке a показан НМРЛ из мыши, которая не получала инъекции, то есть, контроль без инъекции. На снимке b показан НМРЛ из мыши, которой вводили PBS - контроль PBS. На снимке c показан НМРЛ из мыши, которой внутривено вводили споры штамма MW-DCG_LCv26.
Фигура 11. Фотоизображения окрашенных грамположительных палочек MW-DCG_LCv26 в некротических/гипоксических областях НМРЛ, извлеченных у мыши, которой внутривено вводили споры MW-DCG_LCv26. Срезы НМРЛ приготавливали и фиксировали на покровных стеклах. Выполняли окрашивание по Граму. Окрашенные срезы исследовали визуально и получали изображения при увеличении 10×4. Стрелки обозначают присутствие палочек MW-DCG_LCv26.
Подробное описание
Описание ниже полностью подтверждает и описывает настоящее изобретение, которое относится к идентификации новых штаммов, полученных из Clostridium ghonii, которые вызывают эффективный, но умеренный онколизис. Эти штаммы настолько уникальны, что они решают проблему быстрого онколизиса других штаммов, которые приводят к существенной токсичности и невозможности их применения в клинических условиях. Новые производные штаммы Clostridium ghonii были обнаружены с помощью нового способа многократного адаптирования авирулентного штамма C. ghonii в экспериментальных солидных раковых опухолях ксенотрансплантатных (человеческие раковые образования) и сингенных раковых опухолях мыши, таких как, без ограничения, опухоли легкого, толстой кишки, головы и шеи, молочной железы и меланома, что демонстрирует онколитическую терапевтическую эффективность адаптированной C. ghonii в вышеуказанных раковых опухолях.
Наибольшая эффективность новых штаммов достигается при онколизисе микроокружения (центральной области) солидных злокачественных опухолей, при этом наблюдается низкая токсичность или вообще никакой. В рамках своей сферы применения, новые штаммы обладают онколитической способностью лизировать живые злокачественные клетки, а также лизировать тканевые структуры, содержащиеся в микроокружении. Лизис тканевых структур микроокружения обеспечивается ферментами в бактериальных клетках новых штаммов. Например, бактериальные протеиназы, липазы и коллагеназы новых штаммов эффективно расщепляют тканевые структуры, которые включают, помимо прочего, фибронектин и коллаген. Это - явное преимущество по сравнению с вирусным онколизисом, поскольку вирусы не обладают такими ферментами, которые позволяют расщеплять тканевые структуры и, таким образом, ограничены лишь онколизисом живых клеток.
Как рассматривается в настоящей заявке, солидные опухоли могут быть в форме карциномы, саркомы или лимфомы. Эти солидные опухоли могут быть первичными, как в случае массы клеток, которые не мигрировали в другие участки в теле субъекта помимо участка локализации исходной опухоли, или вторичными, то есть, массы клеток, которые являются результатом метастазирования, при котором миграция клеток опухоли во вторичные участки отличается от участка локализации исходной опухоли. Любая солидная опухоль, которая поражается клостридиальными спорами новых производных бактериальных штаммов настоящего изобретения в рамках онколизиса, разрушения микроокружения, подавления роста, регрессии опухоли и практически полного или полного разрушения опухоли, рассматривается в настоящей заявке. Солидные опухоли, как определено в настоящем описании, как предполагают, являются аномальной массой ткани, которая обычно не содержит кисты или области с жидкостью. Как рассматривается в настоящей заявке, солидная опухоль может быть в форме карцином дыхательной системы, карцином желудочно-кишечной системы, карцином мочеполовой системы, карцином яичка, карцином молочной железы, карцином предстательной железы, карцином эндокринной системы, меланом, хориокарциномы, карциномы шейки матки, легкого, головы и шеи, толстой кишки и яичника, опухолей костной, жировой и хрящевой ткани, болезни Ходжкина, неходжкинской лимфомы, B-клеточной лимфомы, эпителиотропной лимфомы, комплексной лимфомы, анапластической крупноклеточной лимфомы, желудочной и лимфомы лимфоидной ткани, ассоциированной с желудочной и нежелудочной слизистой, лимпфопролиферативной болезни, T-клеточной лимфомы, лимфомы Беркитта, мантийноклеточной лимфомы, диффузной крупноклеточной лимфомы, лимфоплазмацитоидной лимфомы и множественной миеломы.
Терапевтические способы и применения настоящего изобретения могут быть применены к злокачественным клеткам мезенхимального происхождения, таким как клетки, которые дают саркомы (например, фибросаркому, миксосаркому, лиосаркому, хондросаркому, остеогенную саркому или хордосаркому, ангиосаркому, эндотелиосаркому, лимфангиосаркому, синовиасаркому или мезотелиосаркому); лейкозы и лимфомы, такие как гранулоцитарный лейкоз, моноцитарный лейкоз, лимфоцитарный лейкоз, злокачественная лимфома, плазмоцитома, ретикулосаркома или болезнь Ходжкина; саркомы, такие как лейомиосаркома или рабдомиосаркома, опухоли эпителиального происхождения, такие как плоскоклеточная карцинома, базальноклеточная карцинома, карцинома потовых желез, карцинома сальных желез, аденокарцинома, папиллярная карцинома, папиллярная аденокарцинома, цистаденокарцинома, медуллярная карцинома, недифференцированная карцинома, бронхогенная карцинома, меланома, почечноклеточная карцинома, гепатома-печеночноклеточная карцинома, карцинома желчного протока, холангиокарцинома, папиллярная карцинома, переходно-клеточная карцинома, хориокарцинома, семинома или эмбриональная карцинома; и опухоли нервной системы, включая глиому, менингиому, медуллобластому, шванному или эпидиому. Дополнительные типы клеток, поддающиеся терапии согласно способам, описанным в настоящей заявке, включают клетки, которые дают карциномы молочной железы, карциномы желудочно-кишечного тракта, такие как карциномы толстой кишки, карциномы мочевого пузыря, карциномы предстательной железы и плоскоклеточные карциномы области шеи и головы. Примеры раковых опухолей, поддающихся терапии согласно способам, описанным в настоящей заявке, включают раковые опухоли влагалища, шейки матки, печени, почки и молочной железы, а также меланомы.
Эффективность новых производных бактериальных штаммов показана и подтверждена в экспериментальных данных, представленных в Примерах. Например, введение клостридиальных спор новых производных бактериальных штаммов настоящего изобретения мышам приводило к практически полному лизису у 30% мышей, имеющих раковые опухоли легкого, толстой кишки, головы и шеи, и меланомы поздних стадий. Лизис включает разрушение структуры опухоли и клеточной массы с превращением твердых масс в жидкость, которая после инфильтрации лейкоцитов становится похожа на гной. Эти опухоли типично исчезали. Остальные мыши показывали обширный центральный онколизис своих опухолей, кожа приобретала красный цвет, затем черный, и у некоторых мышей, в конечном счете, разрывались через кожу. Но лизис был неполным из-за наличия богатой кислородом внешней части опухоли, при этом оставался тонкий слой периферийной части, которая содержит жизнеспособные, как правило, быстро делящиеся раковые клетки. На основе этого результата авторы изобретения обнаружили, что подход комбинаторной терапии мог бы усиливать онколизис, и рассмотрели применение дополнительных терапий для повышения онколитической эффективности. Как рассматривается в настоящей заявке, комбинированная терапия включает введение клостридиальных спор настоящего изобретения и противоопухолевого средства субъекту, нуждающемуся в лечении солидной опухоли. Альтернативой или дополнением к введению противоопухолевого средства является гормонотерапия, гипертермия, хирургическая операция, лучевая терапия или их любая комбинация. Комбинационный подход, как описано и определено в настоящем описании, приводит к подавлению роста солидных злокачественных опухолей, таких как раковые опухоли легкого, толстой кишки и головы и шеи, регрессии опухолей и, в конечном счете, к разрушению опухолей.
Производные бактериальные штаммы
Как предусмотрено в настоящей заявке, в настоящем изобретении предложен бактериальный штамм, который получен из авирулентного, непатогенного штамма Clostridium ghonii, где бактериальный штамм способен подавлять рост солидной опухоли, вследствие онколизиса клеток, содержащихся в микроокружении опухоли. От приблизительно 20% до приблизительно 90% или от приблизительно 20% до приблизительно 70%, или от приблизительно 20% до приблизительно 40%, или от приблизительно 20% до приблизительно 35%, или от приблизительно 25% до приблизительно 35% клеток в микроокружении опухоли подвергаются лизису под воздействием бактериальных штаммов настоящего изобретения, которые вызывают меньше токсичности по сравнению с референсным клостридиальным штаммом. Авирулентный, непатогенный штамм Clostridium ghonii может быть любым штаммом, который обеспечивает осуществление изобретения, и рассматривается в рамках объема изобретения. Например, используемым авирулентным штаммом может быть штамм с регистрационным номером ATCC 25757, BCRC 14548, CCUG 9282, DSM 15049, NCIMB 10636, PEV, Prevot PEV, VPI 4897 или VTT E-042451.
Неограничивающими примерами бактериальных штаммов настоящего изобретения являются MW-DCG_LCv1, MW-DCG_LCv2, MW-DCG_LCv3, MW-DCG_LCv4, MW-DCG_LCv5, MW-DCG_LCv6, MW-DCG_LCv7, MW-DCG_LCv8, MW-DCG_LCv9, MW-DCG_LCv10, MW-DCG_LCv11, MW-DCG_LCv12, MW-DCG_LCv13, MW-DCG_LCv14, MW-DCG_LCv15, MW-DCG_LCv16, MW-DCG_LCv17, MW-DCG_LCv18, MW-DCG_LCv19, MW-DCG_LCv20, MW-DCG_LCv21, MW-DCG_LCv22, MW-DCG_LCv23, MW-DCG_LCv24, MW-DCG_LCv25, MW-DCG_LCv26, MW-DCG_CCv13, MW-DCG_CCv14, MW-DCG_CCv15, MW-DCG_CCv16, MW-DCG_CCv17, MW-DCG_HNCv13, MW-DCG_HNCv14, MW-DCG_HNCv15, MW-DCG_HNCv16, MW-DCG_HNCv17 и MW-DCG_HNCv18. Штаммы бактерий MW-DCG_LCv1, MW-DCG_LCv2, MW-DCG_LCv3, MW-DCG_LCv4, MW-DCG_LCv5, MW-DCG_LCv6, MW-DCG_LCv7, MW-DCG_LCv8, MW-DCG_LCv9, MW-DCG_LCv10, MW-DCG_LCv11, MW-DCG_LCv12, DCG_HNCv13, MW-DCG_HNCv14, MW-DCG_HNCv15, MW-DCG_HNCv16, MW-DCG_HNCv17 и MW-DCG_HNCv18 обладают специфичностью в отношении и терапевтически эффективны против злокачественных солидных опухолей головы и шеи. MW-DCG_HNCv18 является предпочтительным штаммом. MW-DCG_HNCv18 был депонирован в Национальном Институте Измерений (National Measurement Institute, 1/153 Bertie Street, Port Melbourne, Victoria, Australia 3207) в лице Международного депозитарного органа 18 апреля 2012 года под регистрационным номером V12/001485.
Штаммы бактерий MW-DCG_LCv1, MW-DCG_LCv2, MW-DCG_LCv3, MW-DCG_LCv4, MW-DCG_LCv5, MW-DCG_LCv6, MW-DCG_LCv7, MW-DCG_LCv8, MW-DCG_LCv9, MW-DCG_LCv10, MW-DCG_LCv11, MW-DCG_LCv12, MW-DCG_CCv13, MW-DCG_CCv14, MW-DCG_CCv15, MW-DCG_CCv16 и MW-DCG_CCv17 обладают специфичностью в отношении и терапевтически эффективны против злокачественных солидных опухолей толстой кишки. MW-DCG_CCv17 является предпочтительным штаммом. MW-DCG_CCv17 был депонирован в Национальном Институте Измерений (National Measurement Institute, 1/153 Bertie Street, Port Melbourne, Victoria, Australia 3207) в лице Международного депозитарного органа 18 апреля 2012 года под регистрационным номером V12/001487.
Штаммы бактерий MW-DCG_LCv1, MW-DCG_LCv2, MW-DCG_LCv3, MW-DCG_LCv4, MW-DCG_LCv5, MW-DCG_LCv6, MW-DCG_LCv7, MW-DCG_LCv8, MW-DCG_LCv9, MW-DCG_LCv10, MW-DCG_LCv11, MW-DCG_LCv12, MW-DCG_LCv13, MW-DCG_LCv14, MW-DCG_LCv15, MW-DCG_LCv16, MW-DCG_LCv17, MW-DCG_LCv18, MW-DCG_LCv19, MW-DCG_LCv20, MW-DCG_LCv21, MW-DCG_LCv22, MW-DCG_LCv23, MW-DCG_LCv24, MW-DCG_LCv25 и MW-DCG_LCv26 обладают специфичностью в отношении и терапевтически эффективны против злокачественных солидных опухолей легкого. MW-DCG_LCv26 является предпочтительным штаммом. MW-DCG_LCv26 был депонирован в Национальном Институте Измерений (National Measurement Institute, 1/153 Bertie Street, Port Melbourne, Victoria, Australia 3207) в лице Международного депозитарного органа 18 апреля 2012 года под регистрационным номером V12/001486.
Клостридиальные споры
Как предусмотрено в настоящей заявке, в настоящем изобретении предложены клостридиальные споры одного или более бактериальных штаммов, описанных по всему тексту настоящей заявки. Указанные клостридиальный споры могут быть объединены с физиологически приемлемым носителем и/или вспомогательным веществом. Любой известный носитель или вспомогательное вещество рассматриваются в настоящем описании.
Подавление роста опухоли, регрессия опухоли и разрушение опухоли
Как предусмотрено в настоящей заявке, в настоящем изобретении предложен способ подавления роста, регрессии или разрушения одной или более солидных злокачественных опухолей у субъекта, где способ включает введение терапевтически эффективного количества клостридиальных спор, как описано в настоящей заявке, субъекту, нуждающемуся в этом. Также рассматривается применение клостридиальных спор таким же или подобным способом.
Комбинаторная терапия
Рассматривается комбинаторная терапия для лечения одной или более солидных злокачественных опухолей у субъекта, где подавление роста, регрессия опухоли или разрушение опухоли являются показателем лечения, где способ включает введение (1) терапевтически эффективного количества клостридиальных спор согласно второму аспекту и (2) терапевтически эффективного количества противоопухолевого средства субъекту. Также рассматривается применение клостридиальных спор и противоопухолевого средства таким же или подобным способом. Введение (1) и (2) субъекту происходит последовательно или одновременно. (1) и (2) можно вводить субъекту в виде одной фармацевтической композиции. Введение (1) и (2), в виде одной композиции или по отдельности, может быть повторено один или более раз, чтобы гарантировать регрессию опухоли. Например, (1) и (2) можно вводить субъекту в качестве первой дозы, с последующим отдельным введением (2) в качестве второй дозы. Более одного противоопухолевого средства может быть введено в любом количестве доз. Например, (1) является клостридиальными спорами MW-DCG_HNCv18, а (2) является средством против EGFR. В одном примере, (2) является моноклональным антителом против EGFR или ингибитором EGFR тирозинкиназы. В другом примере, (2) является Цетуксимабом. В еще одном другом примере, согласно Примеру 3, предполагается, что клостридиальные споры MW-DCG_HNCv18 и Цетуксимаб одновременно вводят субъекту, с последующим вторым введением одного Цетуксимаба, впрочем, любая комбинация спор настоящего изобретения и противоопухолевого средства (средств) в любом количестве доз и лекарственных форм включена в объем и сущность изобретения. Также в рамки объема и сущности изобретения входит применение других противоопухолевых терапий, известных в уровне техники, в качестве части комбинаторной терапии, описанной в настоящей заявке, при этом такие терапии включают, без ограничения, гормотерапию, гипертермию, хирургическое вмешательство и лучевую терапию.
Способ получения производных бактериальных штаммов (адаптация)
Как предусмотрено в настоящей заявке, в настоящем изобретении предложен способ получения производного бактериального штамма из авирулентного, непатогенного штамма Clostridium ghonii, где производный бактериальный штамм, полученный указанным способом, способен подавлять рост, вызывать регрессию или разрушение солидной опухоли, вследствие онколизиса клеток в микроокружении опухоли, где производный бактериальный штамм, полученный указанным способом, вызывает меньшую токсичность по сравнении с референсным клостридиальным штаммом. Способ включает:
(1) Получение инъекционной формы клостридиальных спор из авирулентного, непатогенного штамма Clostridium ghonii, включающее:
(a) инокуляцию вегетативных палочек бактериального штамма (1) в среду для спорулирования,
(b) выдерживание в течение достаточного времени и при необходимых условиях для спорулирование палочек, и
(c) очистку спор;
(2) Введение очищенных клостридиальных спор путем инъекции (1) животному, которое поддерживает рост солидной опухоли;
(3) Оценку параметров для определения скорости и степени онколизиса и токсичности;
(4) Сбор вегетативных палочек из опухоли (2) при извлечении опухоли;
(5) Посев палочек (4) на чашку с агаром;
(6) Отбор двух или более одиночных колоний с чашки (5) и инокуляцию питательной культуры с целью выращивания вегетативных палочек; и
(7) Повтор этапов (1)(a)-(6) от приблизительно 10 до приблизительно 35 раз.
В примере, две или более одиночных колонии (6) являются тремя одиночными колониями. Кроме того, этапы (1)(a)-(6) повторяют от приблизительно 15 до приблизительно 30 раз или от приблизительно 17 до приблизительно 26 раз, и параметры (3) могут включать время колонизации спор, онколизис, образование гноя и разрыва, объем опухоли, системную токсичность, выживаемость животных, количество спор/палочек, выделенных из опухолей после внутривенного введения спор или любую комбинацию перечисленного.
Способ позволяет получать бактериальные штаммы, которые вызывают лизис от приблизительно 20% до приблизительно 90% или от приблизительно 20% до приблизительно 70%, или от приблизительно 20% до приблизительно 40%, или от приблизительно 20% до приблизительно 35%, или от приблизительно 25% до приблизительно 35% клеток в микроокружении опухоли.
Процесс культивирования и сбора клостридиальных спор, описанный в настоящей заявке, может быть масштабирован. Способы масштабирования известны в уровне техники и рассмотрены в настоящем описании.
Наборы
Как предусмотрено в настоящей заявке, в настоящем изобретении предложен набор для лечения одной или более солидных злокачественных опухолей, включающий бактериальный штамм, клостридиальные споры или фармацевтическую композицию, как описано и определено в настоящей заявке, и дополнительно включающий противоопухолевое средство. Инструкции по применению наборов также предоставлены.
Другие признаки изобретения
Настоящее изобретение применимо к любому субъекту, у которого потенциально могут возникнуть и/или присутствовать солидные опухоли. Субъект может быть млекопитающим, например, человеком, но при этом любое животное рассматривается в настоящей заявке и включено в объем изобретения.
Как предусмотрено в настоящей заявке, примерами солидных злокачественных опухолей, которые можно лечить в соответствии с настоящим изобретением, без ограничения являются карциномы дыхательной системы, карциномы желудочно-кишечной системы, карциномы мочеполовой системы, карциномы яичка, карциномы молочной железы, карциномы предстательной железы, карциномы эндокринной системы, меланомы, хориокарцинома и карциномы шейки матки, легкого, головы и шеи, толстой кишки, яичника, мозга, мочевого пузыря, молочной железы, предстательной железы, опухоли костной, жировой и хрящевой ткани, болезнь Ходжкина, неходжкинская лимфома, B-клеточная лимфома, эпителиотропная лимфома, комплексная лимфома, анапластическая крупноклеточная лимфома, лимфома лимфоидной ткани, ассоциированной с желудочной и нежелудочной слизистой, лимфопролиферативная болезнь, T-клеточная лимфома, лимфома Беркитта, мантийноклеточная лимфома, диффузная крупноклеточная лимфома, лимфоплазмацитоидная лимфома и множественная миелома.
Композиции, дозировки и пути введении
Производные бактериальные штаммы (и полученные из них споры) настоящего изобретения могут применяться в качестве терапевтических средств при лечении солидных раковых опухолей и рассматриваются в качестве монотерапии или как компонент в комбинированной терапии. Указанные бактериальные штаммы находят применение, например, в подавлении роста, в регрессии или разрушении одной или более солидных опухолей у субъекта при введении терапевтически эффективного количества спор бактериальных штаммов субъекту. Солидные опухоли могут быть обнаружены, например, в области головы и шеи, спине, толстой кишке и легких.
Споры производных бактериальных штаммов можно вводить стандартными путями, при этом специалист в данной области сумеет понять, что фактически на определенные типы рака можно направленно воздействовать, используя определенные способы введения. Как правило, производные бактериальные штаммы (и полученные из них споры) можно вводить парентерально, например, внутривенно, люмбально, подкожно или внутримышечно. Предпочтительно, споры вводят в тело животных. В случае введения спор в виде раствора или суспензии для инъекций, нетоксичные парентерально приемлемые разбавители или носители могут включать раствор Рингера, изотонический солевой раствор, фосфатно-солевой буфер, этанол и 1,2-пропиленгликоль.
Способы получения вводимых парентерально композиций, включающих споры согласно настоящему изобретению, очевидны специалистам в данной области и более подробно описаны, например, в справочнике Remington's Pharmaceutical Science, 15th ed., Mack Publishing Company, Easton, Pa., включенном в настоящее описание посредством ссылки.
Споры настоящего изобретения и другие противоопухолевые средства, такие как антитела, можно вводить субъектам в виде композиций/компонентов в комбинированной терапии. В случае терапевтического применения, композиции вводят субъекту, уже имеющему солидную раковую опухоль, в количестве, достаточном для разрушения или, по меньшей мере, подавления роста опухоли. Композиция должна обеспечивать такое количество спор и других противоопухолевых средств, таких как антитела, которое является достаточным, чтобы эффективно лечить субъекта.
Противоопухолевое средство (средства) является любым средством, которое может применяться в химиотерапии, лучевой терапии или терапиях на основе антител, или в их комбинациях. Средство может быть одним или несколькими химическими соединениями, одной или несколькими молекулами РНК, одним или несколькими антителами или их любой комбинацией.
Например, одно или несколько химических соединений могут быть дихлорацетатом натрия, паклитакселом, доксилом, топотеканом, ДНК-модифицирующими средствами, карбоплатином, антиметаболитами, гемцитабином, лекарственными средствами, которые блокируют деление клеток, винкристином, антиангиогенными средствами и пазопанибом.
Примером одной или нескольких молекул РНК является малая интерферирующая РНК (миРНК). миРНК может быть специфична к лактатдегидрогеназе (LDHA) или специфична к CD147.
Примером одного или нескольких антител является противоопухолевое моноклональное антитело, которое описано ниже.
Терапевтически эффективный уровень дозы для любого конкретного пациента или субъекта будет зависеть от ряда факторов, включающих: тип солидной опухоли; размер солидной опухоли; тип дополнительных средств, если таковые вообще имеются, которые используются в комбинированной терапии вместе с другими подобными факторами, известными в медицине.
Специалист, квалифицированный в данной области, сумеет путем стандартных экспериментов и с учетом настоящего описания определить эффективное, нетоксичное количество клостридиальных спор и других средств, которое потребуется для подавления роста опухоли, для регрессии или разрушения одной или большего количества солидных опухолей.
Как правило, терапевтически эффективное количество клостридиальных спор настоящего изобретения для лечения солидных опухолей, таких как солидные опухоли толстой кишки и легкого, у человека составляет от приблизительно 106 колониеобразующих единиц (КОЕ) до приблизительно 1014 КОЕ на дозу или приблизительно 108-1012 КОЕ на дозу или приблизительно 1010-1011 КОЕ на дозу или приблизительно 1010,5 КОЕ на дозу. В неограничивающем примере введение терапевтически эффективного количества клостридиальных спор производят внутривенно, люмбально, подкожно или внутримышечно. Например, предпочтительно введение является внутривенным.
Как правило, в терапевтических применениях, терапию ведут в течение всей продолжительности состояния болезни.
Также рассматривается лекарственное средство, включающее:
(1) терапевтически эффективное количество одной или более клостридиальных спор согласно пункту 16 и
(2) терапевтически эффективное количество противоопухолевого средства,
для его применения в лечении одной или более солидных злокачественных опухолей у субъекта, где регрессия опухоли является показателем лечения, где способ включает введение лекарственного средства указанному субъекту. Также рассматривается производство лекарственного средства.
Также среднему специалисту в данной области будет очевидно, что оптимальное количество и интервал между индивидуальными дозировками будут определяться природой и степенью формирования опухоли, а также типом опухоли. Кроме того, такие оптимальные условия могут быть определены с помощью стандартных методов.
В случае комбинированных терапий, каждый компонент комбинированной терапии можно вводить в одно и то же время или последовательно, в любом порядке, или в разное время, чтобы обеспечить требуемый эффект. В альтернативе компоненты могут быть включены вместе в состав одной единичной дозированной лекарственной формы в качестве комбинированного продукта. При отдельном введении, может быть предпочтительно, вводить компоненты одним и тем же путем введения, хотя это не является необходимым условием.
Антитела
В настоящем изобретении предложены антитела, которые вводят субъекту в комбинации с клостридиальными спорами новых производных бактериальных штаммов настоящего изобретения. Эффективная комбинаторная терапия лечения солидных опухолей, в результате которой регрессия опухоли является показателем лечения, как предусмотрено в настоящей заявке, может включать клостридиальные споры новых производных бактериальных штаммов настоящего изобретения и противоопухолевые моноклональные антитела, хотя любое подходящее антитело рассматривается в настоящей заявке и включает, без ограничения, поликлональное, моноклональное, химерное, гуманизированное, одноцепочечное, Fab-фрагменты и Fab-экспрессионную библиотеку. Фрагменты и аналоги антител также рассматриваются.
Противоопухолевое антитело, как предусмотрено в настоящей заявке, включает антитело против иммунной стимуляции или моноклональное антитело против регуляторных T-клеток. Примером антитела против иммунной стимуляции является моноклональное антитело против CD40. Моноклональным антителом против CD40 может быть FGK45. Примером моноклонального антитела против регуляторных T-клеток является моноклональное антитело против CD25. Моноклональным антителом против CD25 может быть PC61. В другом варианте осуществления, средство направленно против рецептора эпидермального фактора роста (EGFR). Средство может быть в форме моноклонального антитела против EGFR и, более конкретно, химерного (мышь/человек) моноклонального антитела против EGFR, такого как Цетуксимаб, для применения в лечении, например, раковых опухолей толстой и прямой кишки и головы и шеи. Другими моноклональными антителами против EGFR, рассматриваемые в настоящей заявке, являются Панитумумаб, Залутумумаб, Нимотузумаб и Матузумаб. Другими средствами, направленными против EGFR, являются низкомолекулярные ингибиторы EGFR тирозинкиназы, такие как Гефитиниб, Эрлотиниб и Лапатиниб. Они могут использоваться для лечения, например, раковых опухолей легкого (например, НМРЛ), раковых опухолей молочной железы и раковых опухолей поджелудочной железы. Природные ингибиторы EFGR рассматриваются в настоящей заявке и включают картофельный ингибитор карбоксипептидазы (PCI), который содержит малый цистеин-богатый модуль, называемый a T-узловой каркас, общий для нескольких различных семейств белков, включая семейство EGF. Гранидин является другим природным ингибитором EGFR. Это - эллагитаннин, обнаруженный в листьях дерева Melaleuca quinquenervia и в дубе. Он обладает способностью подавлять фосфорилирование рецептора эпидермального фактора роста в клетках карциномы толстой кишки человеке.
Противоопухолевое моноклональное антитело может быть конъюгированным или "голым". Голые антитела, например, действуют через комплемент-опосредованный цитолиз и антителозависимую клеточно-опосредованную цитотоксичность. Конъюгированные антитела включают антитела, которые конъюгированы с радиоизотопом или ферментом, активирующим лекарственное соединение. Радиоактивно конъюгированное антитело может использоваться в радиоиммунотерапии. Примерами радиоактивно конъюгированного антитела или радиоизотопа являются рений-188 или рений-186, фтордезоксиглюкоза (18F), также известная, как FDG, иттрий-90 (90Y) -конъюгированное антитело против CD20 Y90-ибритутомаб тиуксетан и иод-131 (131I) -конъюгированное антитело против CD20, I131-тозитумомаб. Антитела, конъюгированные с активизирующим лекарственное соединение ферментом, могут использоваться в антителонаправленной терапии с использованием пролекарства и фермента (ADEPT). Противоопухолевое моноклональное антитело может быть конъюгировано с липосомой или наночастицей, которые заключают различные лекарственные средства и терапевтические нуклеотиды, такие как молекулы миРНК.
Противоопухолевые моноклональные антитела могут быть направлены против злокачественных клеток несколькими механизмами. Как предусмотрено в настоящей заявке, такие механизмы включают (1) радиоиммунотерапию (RIT), которая включает применение радиоактивно конъюгированных мышиных антител против клеточных антигенов, (2) антителонаправленную терапию с использованием пролекарства и фермента (ADEPT), которая включает применение рак-ассоциированных моноклональных антител, которые связаны с активирующим лекарственное соединение ферментом, в результате чего, после системного введения, нетоксичное средство превращается в токсичное лекарственное соединение, оказывая цитостатическое действие, которое может быть направлено на злокачественные клетки, и (3) иммунолипосомы, которые являются антитело-конъюгированными липосомами, несущими лекарственные соединения или терапевтические нуклеотиды, и, при конъюгировании с моноклональными антителами, могут быть направлены против злокачественных клеток.
Способы получения подходящих антител будут известны специалистам в данной области. Например, моноклональное антитело может быть получено при использовании технологии гибридом, описанной в Antibodies-A Laboratory Manual, Harlow and Lane, eds., Cold Spring Harbor Laboratory, N.Y. (1988).
В сущности, при получении моноклональных антител, их фрагментов или аналогов, может использоваться любая методика, которая позволяет получать молекулы антител с использованием стабильных линий клеток в культуре. Они включают методику гибридом, первоначально разработанную Kohler et al., Nature, 256:495-497 (1975), а так же методику триом, методику гибридом B-клеток человека [Kozbor et al., Immunology Today, 4:72 (1983)] и методику EBV-гибридом для получения человеческих моноклональных антител [Cole et al., in Monoclonal Antibodies and Cancer Therapy, pp. 77-96, Alan R. Liss, Inc., (1985)]. Иммортализованные антитело-продуцирующие линии клеток могут быть созданы с помощью других методов помимо слияния, таких как прямая трансформация B-лимфоцитов онкогенной ДНК или трансфекция вирусом Эпштейна-Барр. См., например, M. Schreier et al., "Hybridoma Techniques" (1980); Hammerling et al., "Monoclonal Antibodies and T-cell Hybridomas" (1981); Kennett et al., "Monoclonal Antibodies" (1980).
В заключение, способ получения гибридомы, из которой получают моноклональное антитело, миелому или другую бессмертную клеточную линию сливают с лимфоцитами, полученными из селезенки млекопитающего, гипериммунизированного фрагментом белка, связывающего фактор распознавания, или фактором распознавания, или ДНК-связывающим фрагментом, специфичным к точке начала репликации. Гибридомы, продуцирующие моноклональное антитело, применимое при осуществлении настоящего изобретения, идентифицируют по их способности иммунно реагировать с существующим фактором распознавания и их способности ингибировать определенную транскрипционную активность в клетках-мишенях.
Моноклональное антитело, применимое при осуществлении настоящего изобретения, может быть получено путем инициации моноклональной гибридомной культуры, включающей питательную среду, содержащую гибридому, которая секретирует молекулы антитела требуемой антигенной специфичности. Культуру поддерживают при таких условиях и в течение такого периода времени, которые достаточны для секреции гибридомой молекул антитела в среду. Затем содержащую антитело среду собирают. Молекулы антитела могут быть затем выделены с помощью методов, известных в уровне техники.
Аналогично, существуют различные методики, известные в уровне техники, которые могут использоваться для получения поликлональных антител или их фрагментов или аналогов. Для получения поликлонального антитела, различные животные-хозяева могут быть иммунизированы при инъекции антигеном или его фрагментом или аналогом, включая, без ограничения, кроликов, мышей, крыс, овец, коз и т.д.
Скрининг на наличие требуемого антитела может быть также выполнен с помощью различных методов, известных в уровне техники. Анализы иммуноспецифичного связывания антител могут включить, без ограничения, радиоиммуноанализы, ELISA (твердофазный иммуноферментный анализ), сэндвич-иммуноанализы, иммунорадиометрические анализы, реакции диффузной преципитации в геле, иммунодиффузионные анализы, иммуноанализы in situ, Вестерн-блот анализы, реакции преципитации, анализы агглютинации, анализы связывания комплемента, иммунофлуоресцентные анализы, анализы с белком А и иммуноэлектрофоретические анализы, и т.п. (см., например, Ausubel et al., eds, 1994, Current Protocols in Molecular Biology, Vol. 1, John Wiley & Sons, Inc., New York). Из уровня техники известны различные методы обнаружения связывания в иммуноанализе, которые включены в объем настоящего изобретения.
Антитела или их фрагменты, используемые при осуществлении изобретения, обладают аффинностью связывания или авидностью более чем приблизительно 105 M-1, более предпочтительно более чем приблизительно 106 M-1, еще более предпочтительно более чем приблизительно 107 M-1 и наиболее предпочтительно более чем приблизительно 108 M-1.
Если требуется получать антитело, которое будет использоваться в комбинированной терапии с клостридиальными спорами новых производных бактериальных штаммов настоящего изобретения, можно производить антитело(а), используя периодическую ферментацию с бессывороточной средой. После ферментации антитело может быть очищено с помощью многостадийной методики, включающей стадии хроматографии и инактивации/удаления вирусов. Например, антитело может быть сначала выделено с помощью аффинной хроматографии с белком А, а затем обработано растворителем/детергентом для инактивации каких-либо вирусов с липидной оболочкой. Дополнительная очистка, обычно с помощью анионообменной и катионообменной хроматографии, может использоваться для удаления остаточных белков, растворителей/детергентов и нуклеиновых кислот. Очищенное антитело может быть дополнительно очищено и включено в 0,9% раствор хлорида натрия при использовании гель-фильтрационных колонок. Готовый нерасфасованный препарат может быть затем стерилизован, очищен от вирусов фильтрованием и расфасован.
Любая технология создания и деиммунизации антител, которая обеспечивает эффективность лечения и снижение токсичности солидных раковых опухолей, рассматривается в настоящей заявке. Конъюгирование радиоизотопов, низкомолекулярных цитостатических средств и белковых токсинов с направленными антителами и повышение эффекторной функции антителозависимой клеточной цитотоксичности с целью повышения эффективности противоопухолевых антител также рассматривается в настоящей заявке. Токсичность являлась главным препятствием при разработке терапевтических антител против рака и противоопухолевой терапии в целом. В случае антител, перекрестная реактивность с нормальными тканями может вызывать существенные побочные эффекты, включая затрудненное дыхание, вследствие легочных токсических эффектов, периодические осложнения центральной и периферической нервной системы, сниженную функцию печени, повреждение почек и, в редких случаях, неожиданные токсические эффекты, такие как повреждение мышц сердца, связанное, например, с применением трастузумаба. Кроме того, радиоиммунотерапия с применением изотопно-конъюгированных антител также может вызвать подавление функции костного мозга. Подход комбинаторной терапии с применением клостридиальных спор новых производных бактериальных штаммов с противоопухолевым средствами, такими как антитела, может позволить снизить дозировку антител, требуемую для достижения терапевтического эффекта, уменьшая, таким образом, токсическое действие.
Методики конъюгирования, в которых получают комплекс химических соединений, лекарственных веществ, токсинов и т.д. с антителом, рассматриваются в настоящей заявке. Конъюгаты с антителами включают радиоизотоп и активирующий лекарственное средство фермент, как рассматривается выше, но также включают полученные из грибков мощные токсины, гемтузумаб озогамицин и майтанзиноид (DM-1).
Дополнительные терапии
Лучевая терапия рассматривается в настоящей заявке как часть подхода комбинаторной терапии для регрессии солидных опухолей, включающей применение клостридиальных спор бактериальных штаммов настоящего изобретения. Как правило, ионизирующее излучение используется как компонент комбинаторной терапии рака для борьбы со злокачественными клетками. Существует два различных способа доставки радиации в подвергаемые терапии ткани:
- аппарат, называемый линейным ускорителем, который подает радиацию в тело извне;
- гранулы или зерна материала, который испускает радиоактивное излучение внутри тела.
Пример обрабатываемых тканей может включать область молочной железы, лимфатические узлы или другую часть тела, но при этом рассматривается любая солидная опухоль, на которую может воздействовать радиация. Необходимо включить пограничную область нормальной ткани вокруг опухоли, чтобы исключить неточности в ежедневной установке, и учесть внутреннее движение опухоли. Эти неточности могут быть вызваны внутренним движением (например, дыханием и заполнением мочевого пузыря) и движением внешних отметок на кожи относительно положения опухоли. Лучевая терапия наряду с инокуляцией клостридиальных спор настоящего изобретения может быть объединена с хирургией, химиотерапией, гормональной терапией, иммунотерапией или некоторой комбинацией этих четырех методов. Наиболее распространенные типы рака можно в некоторой степени лечить с применением лучевой терапии. Точная цель лечения (лечебная, вспомогательная, неоадъювантная, терапевтическая или паллиативная) обычно зависит от типа опухоли, ее местоположения и стадии, а также от общего состояния здоровья пациента. Тотальное облучение тела (TBI) представляет собой методику лучевой терапии, которую используют для подготовки организма к пересадке трансплантата костного мозга. Брахитерапия, при которой источник излучения помещают внутрь или рядом с областью, требующей обработки, является другой формой лучевой терапии, которая минимизирует облучение здоровой ткани в процессе процедур лечения раковых опухолей молочной железы, предстательной железы и других органов.
Гормональная терапия также рассматривается в настоящей заявке как возможный аспект комбинаторной терапии для лечения солидных злокачественных опухолей. Гормональная терапия включает манипуляцию эндокринной системой посредством введения извне определенных гормонов, в особенности стероидных гормонов, или лекарственных средств, которые ингибируют выработку или активность таких гормонов (антагонисты гормонов). Поскольку стероидные гормоны являются мощными регуляторами экспрессии генов в некоторых раковых клетках, изменение уровней или активности некоторых гормонов может вызвать прекращение роста некоторых раковых опухолей или даже гибель их клеток. Хирургическое удаление эндокринных органов, например, орхиэктомия и оофорэктомия также могут использоваться в качестве формы гормональной терапии.
Гормональная терапия используется в случае нескольких типов раковых опухолей, происходящих из гормонально чувствительных тканей, включающих, без ограничения, молочную железу, предстательную железу, эндометрий и кору надпочечников. Гормональная терапия также может применяться при лечении паранеопластических синдромов или для ослабления некоторых связанных с раком и химиотерапией симптомов, таких как анорексия. Возможно, самым знакомым примером гормональной терапии в онкологии является использование селективного модулятора ответа эстрогена, тамоксифена, для лечения рака молочной железы, хотя другой класс гормональных средств, ингибиторов ароматазы, приобретает все большую роль в этой болезни.
Настоящее изобретение далее описано в отношении определенных примеров, которые не следует рассматривать как какое-либо ограничение объема изобретения.
ПРИМЕРЫ
В Примерах ниже показаны такие преимущества новых производных клостридиальных штаммов в качестве онколитических средств по сравнению с другими клостридиальными штаммами, как превосходные профили специфичности, безопасности и эффективности. Из Примеров становится ясно, что другие клостридиальные штаммы, включая C. novyi и C. sordellii, обладают способностью вызывать онколизис, но они очень токсичны, поскольку их онколитическое действие является слишком быстрым, что вызывает существенные побочные/токсические действия, включая гибель животных, имеющих опухоли. Это ограничивает их применение в качестве клинического метода терапии.
Пример 1: Идентификация, выделение и колонизация новых производных клостридиальных штаммов
Авторы изобретения исследовали C. novyi-NT и C. sordellii, а также две сахаролитических разновидности, C. acetobutylicum и C. beijerinckii, и сравнили их с дополнительными доступными протеолитическими Clostridium spp (шесть клинических вариантов C. sodellii, два C. bifermentas, и ATCC 25757 (то есть, авирулентный протеолитический штамм C. ghonii, о котором ранее не сообщали, является эффективным противоопухолевым средством против солидных опухолей) в моделях меланомы, рака толстой кишки и рака легкого (0,45 см3) поздней стадии, таких как ксенотрансплантатные и сингенные модели немелкоклеточной карциномы легкого (НМРЛ) на мышах.
В начале авторы изобретения подготовили инеъкционные препараты клостридиальных спор для введения в моделях (см. Фигуру 1 - Схематическое изображение получения спор). Способ эффективного культивирования и сбора клостридиальных спор был открыт авторами изобретения и включает следующие этапы:
- Применение модифицированной среды спорулирования, включающей, например;
° Среда с сердечной вытяжкой и Усиленная клостридиальная среда производства OXOID.
° Среда спорулирования, pH 7,4, на 1 литр содержит:
° Na2HPO4 (Sigma) 5 г
° L-цистеин (Sigma) 0,5 г
° Мальтозы моногидрат (Chem-Supply) 10 г
° Протеозопептон (OXOID) 30 г
° Мясная среда (OXOID) 10%
- Использовать аликвоты по 50-100 мл, это лучше всего подходит для получения спор;
- Инокулировать бактериальные палочки в среду спорулирования, содержащуюся в пробирке, и инкубировать при 35°C для выращивания культуры;
- Спорулирование будет готово для сбора через 10 дней.
- Быстро встряхнуть пробирки, чтобы тяжелое высушенное мясо в среде осело на дно. Оставить культуры на несколько минут, затем пипеткой отобрать верхний слой культуры в пробирке и поместить во флакон для центрифужного стакана,
- Использовать скорость 5000g для центрифугирования флакона.
Во-вторых, в модели проводили инъекции клостридиальных спор и оценивали различные параметры, такие как время колонизации спор и онколизиса, образование гноя и разрыва, объем опухоли (то есть, рост, уменьшение или исчезновение), системную токсичность, выживаемость животных, а также количество спор/палочек, выделенных из опухолей после внутривенного введения спор.
Результаты показали, что хотя две сахаролитических разновидности и протеолитический C. sporogenes не показали существенную колонизацию и онколизис, протеолитические C. novyi-NT и C. sordellii оказались очень эффективными. У 50% животных, имеющих опухоли поздних стадий, через 12 часов после в/в инъекции начался онколизис, который закончился через 24 часа. Опухоль подверглась некрозу с изменениями цвета кожи от фиолетового до черного, что сопровождалось образованием гноя/жидкости и разрывом кожи на опухоли, при этом животное-хозяин выглядело сонным и больным, очевидное проявление токсичности в результате быстрого лизиса опухоли.
Напротив, ATCC 25757 медленнее осуществлял колонизацию и онколизис, но был более эффективным при онколизисе и в ксенотрансплантатной, и в сингенной моделях НМРЛ на мышах. Колонизация спор была заметна через 48 часов, а онколизис - через 72 часа, потом он длился более 10 дней после введения спор. Впрочем, онколитическая способность C. ghonii дикого типа является переменной, таким образом, в среднем она не сильно отличается от онколитической способности авирулентного штамма C. ghonii (ATCC 25757), но ясно, что авирулентный штамм имел задержку онколизиса и роста опухоли (см. Фигуру 2). Что важно и неожиданно, этот штамм не был связан с токсичностью в отличие от других клостридиальных штаммов.
Как и в случае штамма дикого типа, споры авирулентного штамма, которые были введены в модели на мышах, имели переменный онколитический эффект. Чтобы улучшать единообразие онколитического эффекта C. ghonii, авторы изобретения обнаружили способ повышения единообразия путем многократной адаптации, отбора и повторного выделения штамма в течение 26 циклов (см. Пример 2, ниже, и Фигуру 3 со схематической диаграммой способа). В конечном счете, авторы изобретения выделили новый производный штамм авирулентного штамма C. ghonii, который обладает превосходной способностью проникать, колонизировать и прорастать в меланоме, раковых опухолях толстой кишки и легкого по сравнению с другими известными клостридиальными штаммами, которые считаются полезными в лечении рака.
Пример 2: Адаптация для получения новых производных клостридиальных штаммов
Авирулентный штамм C. ghonii многократно адаптировали в трех моделях опухолей: (1) НМРЛ поздней стадии (A549), (2) модели рака толстой кишки (HCT116) и (3) рака головы и шеи (HN5). Опухоли, используемые для адаптации, в каждой группе (n=6) вызывали полный онколизис. Клостридиальные палочки собирали изнутри опухоли, инокулированной спорами авирулентного штамма C. ghonii, ATCC 25757, путем извлечения солидной опухоли и последующей гомогенизации опухолевой ткани, которую затем переносили на чашку с усиленной клостридиальной средой/агаром. Три одиночных колонии с чашки затем объединяли в 40 мл усиленной клостридиальной питательной среды и инкубировали в анаэробных условиях при 37°C в течение ночи. Для спорулирования 40 мл бактериальной культуры добавляли в 1 литр среды спорулирования (0,5% Na2HPO4, 3% пептона Thiotone E, 0,05% L-цистеина, 1% мальтозы, 5% гранул сушеного мяса, pH 7,4) и инкубировали в анаэробных условиях при 37°C в течение 2 недель. В этот момент времени, клостридии сформировали эндоспоры и были готовы к очистке. Для очистки спор, 200 мл суспензии спор сначала центрифугировали при 12000 об/мин в течение 15 мин при 4°C. Полученный осадок затем ресуспендировали и дважды промывали 200 мл холодного PBS с последующим центрифугированием. После промывки, осадок спор ресуспендировали в холодном PBS и обрабатывали ультразвуком в течение 5 минут на льду, чтобы высвободить эндоспоры и разрушить вегетативные клетки. После обработки ультразвуком, споры промывали еще 6-10 раз, используя холодный PBS, пока суспензия спор не была очищена от клеточного дебриса. Чистоту суспензии спор наконец подтверждали с помощью фазово-контрастной микроскопии, при этом суспензия спор содержала <1% материала вегетативных клеток и была обозначена как штамм MW-DCG_LCv12.
Ресуспендированные споры MW-DCG_LCv12 в соответствующих концентрациях, например, 5×107 - 1×108 КОЕ, вводили в хвостувую вену моделей для последующей повторной инокуляции новых опухолей НМРЛ (то есть, легкого), рака толстой кишки и головы и шеи с повторным выделением новых вариантов штаммов.
После 17-26 таких повторных циклов, авторы изобретения выделили несколько новых производных бактериальных штаммов, которые обладают превосходными свойствами по сравнению с неадаптированным, авирулентным C. ghonii, такими как уверенная способность проникновения, колонизации, прорастания и существенного онколизиса в НМРЛ, раковых опухолях толстой кишки и головы и шеи, без каких-либо заметных токсических эффектов. Онколизис сопровождался существенной задержкой роста опухоли согласно Фигурам 4-6, но без токсичности/признаков токсичности, что согласуется с предыдущими исследованиями, в которых использовали клостридии, такие как C. novyi-NT и C. sordellii. Это очень существенно, так как методику повторного выделения и адаптации никогда не применяли таким способом.
Указанные новые производные бактериальные штаммы вызывали практически полное разрушение опухоли в результате онколизиса (некроза) у 30% мышей, имеющих меланому и рак легкого поздних стадий. Этих мышей наблюдали в течение трех последующих месяцев и не обнаруживали никакого доказательства повторного появления опухоли. У остальных мышей также наблюдали различные степени онколизиса и задержки роста опухоли. Новые производные бактериальные штаммы, которые были бы наиболее эффективными в комбинаторной терапии для лечения солидных опухолей, могут быть специфичными к определенному типу солидных опухолей (например, раку толстой кишки), приводили более чем к 20% некроза раковых клеток, расположенных в опухоли и оказывали низкую или не оказывали никакой токсичности при измерении и сравнении с референсным клостридиальным штаммом. Штаммы, которые удовлетворяли этим критериям, которые являются специфичными и эффективными против солидных опухолей НМРЛ, толстой кишки и раковых опухолей головы и шеи, описаны ниже.
НМРЛ
В общей сложности 26 изолятов (штаммов) были специфично адаптированы к НМРЛ (рак легкого) и включают MW-DCG_LCv1, MW-DCG_LCv2, MW-DCG_LCv3, MW-DCG_LCv4, MW-DCG_LCv5, MW-DCG_LCv6, MW-DCG_LCv7, MW-DCG_LCv8, MW-DCG_LCv9, MW-DCG_LCv10, MW-DCG_LCv11, MW-DCG_LCv12, MW-DCG_LCv13, MW-DCG_LCv14, MW-DCG_LCv15, MW-DCG_LCv16, MW-DCG_LCv17, MW-DCG_LCv18, MW-DCG_LCv19, MW-DCG_LCv20, MW-DCG_LCv21, MW-DCG_LCv22, MW-DCG_LCv23, MW-DCG_LCv24, MW-DCG_LCv25 и MW-DCG_LCv26. Из этих 26 изолятов, данные для трех предпочтительных изолятов представлены в таблице ниже. Уровень токсичности определяли и оценивали при использовании полного оценочного листа, включавшего следующие четыре уровня: Внешний вид; Клинические симптомы; Неспровоцированное поведение; и Поведенческие реакции на внешние стимулы. MW-DCG_LCv26 является штаммом, который давал высокий процент некроза солидной опухоли НМРЛ в модели на мышах без какой-либо токсичности кроме синдрома лизиса опухоли (который является проявлением модели на мышах).
(кроме TLS)
Рак толстой кишки
В общей сложности 17 изолятов (штаммов) были специфично адаптированы к раку толстой кишки и включают MW-DCG_LCv1, MW-DCG_LCv2, MW-DCG_LCv3, MW-DCG_LCv4, MW-DCG_LCv5, MW-DCG_LCv6, MW-DCG_LCv7, MW-DCG_LCv8, MW-DCG_LCv9, MW-DCG_LCv10, MW-DCG_LCv11, MW-DCG_LCv12, MW-DCG_CCv13, MW-DCG_CCv14, MW-DCG_CCv15, MW-DCG_CCv16 и MW-DCG_CCv17. Из этих 17 изолятов, данные для четырех предпочтительных изолятов представлены в таблице ниже. Уровень токсичности определяли и оценивали с использованием полного оценочного листа, включавшего следующие четыре уровня: Внешний вид; Клинические симптомы; Неспровоцированное поведение; и Поведенческие реакции на внешние стимулы. MW-DCG_CCv17 является штаммом, который давал высокий процент некроза солидной раковой опухоли толстой кишки в модели на мышах без какой-либо токсичности кроме синдрома лизиса опухоли (который является проявлением модели на мышах).
(кроме TLS)
Рак головы и шеи
В общей сложности 18 изолятов (штаммов) были специфично адаптированы к раку головы и шеи и включают MW-DCG_LCv1, MW-DCG_LCv2, MW-DCG_LCv3, MW-DCG_LCv4, MW-DCG_LCv5, MW-DCG_LCv6, MW-DCG_LCv7, MW-DCG_LCv8, MW-DCG_LCv9, MW-DCG_LCv10, MW-DCG_LCv11, MW-DCG_LCv12, DCG_HNCv13, MW-DCG_HNCv14, MW-DCG_HNCv15, MW-DCG_HNCv16, MW-DCG_HNCv17 и MW-DCG_HNCv18. Из этих 18 изолятов, данные для трех предпочтительных изолятов представлены в таблице ниже. Уровень токсичности определяли и оценивали с использованием полного оценочного листа, включавшего следующие четыре уровня: Внешний вид; Клинические симптомы; Неспровоцированное поведение; и Поведенческие реакции на внешние стимулы. MW-DCG_HNCv18 является штаммом, который давал высокий процент некроза солидной раковой опухоли головы и шеи в модели на мышах без какой-либо токсичности кроме синдрома лизиса опухоли (который является проявлением модели на мышах).
(кроме TLS)
В заключение, штамм MW-DCG_HNCv18, который является специфичным и эффективным в отношении злокачественных солидных опухолей головы и шеи, штамм MW-DCG_CCv17, который является специфичным и эффективным в отношении злокачественных солидных опухолей толстой кишки, штамм MW-DCG_LCv26, который является специфичным и эффективным в отношении солидных опухолей НМРЛ, обладают превосходными свойствами по сравнеию с неадаптированным, авирулентным C. ghonii, такими как уверенная способность проникновения, колонизации, прорастания и существенного онколизиса в солидных опухолях НМРЛ, раковых опухолях толстой кишки и раковых опухолях головы и шеи, без каких-либо заметных токсических эффектов.
Специфичность
При дальнейшем подтверждении предыдущих данных, споры штамма MW-DCG_LCv26 внутривенно вводили мышам, имеющим подкожный НМРЛ в дозе 108 КОЕ/мышь. Ткань из опухоли НМРЛ и нераковую ткань сердца, легкого, селезенки, почки и печени забирали после прорастания спор в течение 24 и 96 часов после инъекции. Половину забранной ткани гомогенизировали и проверяли на присутствие спор. Как показано на Фигуре 9, проросшие споры присутствовали в опухоли через 24 часа после инъекции. Споры также проросли в нераковой ткани различных органов, таких как селезенка, почка и печень в тот же момент времени, но в меньшей степени, чем в опухоли. Однако, через 96 часов после инъекции никаких спор не было обнаружено ни в одной из проверенных образцов нераковой ткани. Напротив, MW-DCG_LCv26 показал прорастание спор в опухоли через 96 часов после инъекции на уровне, аналогичном величине прорастания в опухоли через 24 часа после инъекции.
Немаловажно, что C. ghonii вызывал очевидный онколизис без каких-либо признаков токсичности, обычно связанной с другими клостридиальными штаммами (C. novyi-NT, C. sporogenes и C. sordellii) в дозе 108 КОЕ/мышь. Фигура 10 содержит фотографии образцов НМРЛ, которые были удалены у мышей. В секции a показан НМРЛ мыши, которой не делали инъекции. В секции b показан НМРЛ мыши, которой вводили PBS. В секции c показан НМРЛ мыши, которой внутривено вводили споры штамма MW-DCG_LCv26. Участки НМРЛ в секции c заметно более темные, чем НМРЛ, показанные в секции a и b, и представляют собой области некроза, указывая, таким образом, на эффективный онколизис НМРЛ штаммом MW-DCG_LCv26. Согласно Фигуре 11, наблюдали прорастающие споры (то есть, палочки) MW-DCG_LCv26 (см. стрелки) внутри некротических/гипоксических областей НМРЛ, что показывает прямую корреляцию между прорастанием спор MW-DCG_LCv26 и индукцией онколизиса.
Пример 3: Комбинированная терапия
Авторы изобретения тестировали добавление Цетуксимаба в сочетании с введением одного из полученных производных клостридиальных штаммов в ксенотрансплантатной модели на мышах.
Цетуксимаб представляет собой химерное (мышиное/человеческое) моноклональное антитело (mAb против EGFR), которое ингибирует рецепторы эпидермального фактора роста (EGFR). Цетуксимаб обычно вводят пациенту путем внутривенной инфузии для терапии метастатического рака толстого кишечника и раковых опухолей головы и шеи.
MW-DCG_HNCv18 вводили с mAb против EGFR (Цетуксимаб - 3× в/б) в ксенотрансплантатной модели солидной раковой опухоли головы и шеи поздней стадии на мышах. Согласно Фигуре 7, указанный новый производный клостридиальный штамм проникал в солидную раковую опухоль головы и шеи поздней стадии модели. Эти споры прорастали и локализовались в гипоксических/некротических областях, где они воспроизводились до высокой плотности, вызывая онколизис двухстадийного типа во всех солидных опухолях. Первая стадия являлась полной остановкой роста опухоли сразу после инъекции спор и колонизации; затем медленный, но уверенный онколизис начинался в день 4 и оканчивался приблизительно в день 10. Практически полную регрессию опухоли наблюдали более чем у 40% животных. Этот онколизис и подавление роста опухоли могли продолжаться в течение существенного периода времени в НМРЛ поздней стадии у всех мышей (до 34 дополнительных дней по сравнению с мышами без терапии или с ложной терапией, которые могли гибнуть через 20 дней, Фиг. 7). Опухоли были почти полностью уничтожены после второй дозы терапии Цетуксимабом. Мышей подвергали комбинированной терапии, продлевая их выживаемость более чем на 80 дней, что почти в 4 раза большая продолжительность жизни.
Все композиции и способы, раскрытые и заявленные в настоящей заявке, могут быть сделаны и осуществлены без неуместного экспериментирования с учетом настоящего описания. Хотя композиции, способы и применения настоящего изобретения были описаны в рамках предпочтительных вариантов осуществления, специалистам в данной области техники будет очевидно, что изменения могут быть внесены в композиции и способы, а также в этапы или в последовательности этапов способов, описанных и определенных в настоящей заявке, без отступления от концепции, сущности и объема изобретения. Более конкретно, будет очевидно, что некоторыми средствами, которые являются химически и физиологически подобными, можно заменить средства, описанные в настоящей заявке, и при этом могут быть достигнуты те же или подобные результаты. Все подобные замены и модификации, очевидные специалистам в данной области, как полагают, включены в сущность, объем и концепцию изобретения, определенного в соответствии с прилагаемой формулой изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИСПОЛЬЗОВАНИЕ CLOSTRIDIUM GHONII В СОЧЕТАНИИ С ИНГИБИТОРОМ АНГИОГЕНЕЗА ОПУХОЛИ | 2022 |
|
RU2839044C2 |
| ИНГИБИТОР КОНТРОЛЬНЫХ ТОЧЕК И ЦЕЛЬНОКЛЕТОЧНАЯ МИКРОБАКТЕРИЯ ДЛЯ ИСПОЛЬЗОВАНИЯ ПРИ ЛЕЧЕНИИ ОНКОЛОГИЧЕСКОГО ЗАБОЛЕВАНИЯ | 2014 |
|
RU2719934C2 |
| СПОСОБ ЛЕЧЕНИЯ РАКА (ВАРИАНТЫ) | 2006 |
|
RU2447889C2 |
| Противоопухолевое средство на основе рекомбинантного штамма вируса осповакцины и способ его получения | 2019 |
|
RU2730657C1 |
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА ДЛЯ ЛЕЧЕНИЯ ОПУХОЛЕЙ | 2009 |
|
RU2531758C2 |
| СПОСОБЫ ЛЕЧЕНИЯ РАКА, ИМЕЮЩЕГО ГЕМИЗИГОТНУЮ ПОТЕРЮ ТР53 | 2016 |
|
RU2721953C2 |
| ИММУНОМОДИФИЦИРУЮЩИЕ ЧАСТИЦЫ ДЛЯ ЛЕЧЕНИЯ РАКА | 2019 |
|
RU2794261C2 |
| БИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА К CD25 И Fc ГАММА-РЕЦЕПТОРУ ДЛЯ ЭЛИМИНАЦИИ ОПУХОЛЕСПЕЦИФИЧЕСКИХ КЛЕТОК | 2017 |
|
RU2759970C2 |
| ДУОКАРМИЦИНОВЫЕ ADC, ДЕМОНСТРИРУЮЩИЕ УЛУЧШЕННУЮ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ IN VIVO | 2015 |
|
RU2689779C2 |
| ЛЕЧЕНИЕ РАКА С ПОМОЩЬЮ АНТИТЕЛА К СЕМАФОРИНУ 4D В КОМБИНАЦИИ С ЭПИГЕНЕТИЧЕСКИМ МОДУЛИРУЮЩИМ АГЕНТОМ | 2018 |
|
RU2783535C2 |





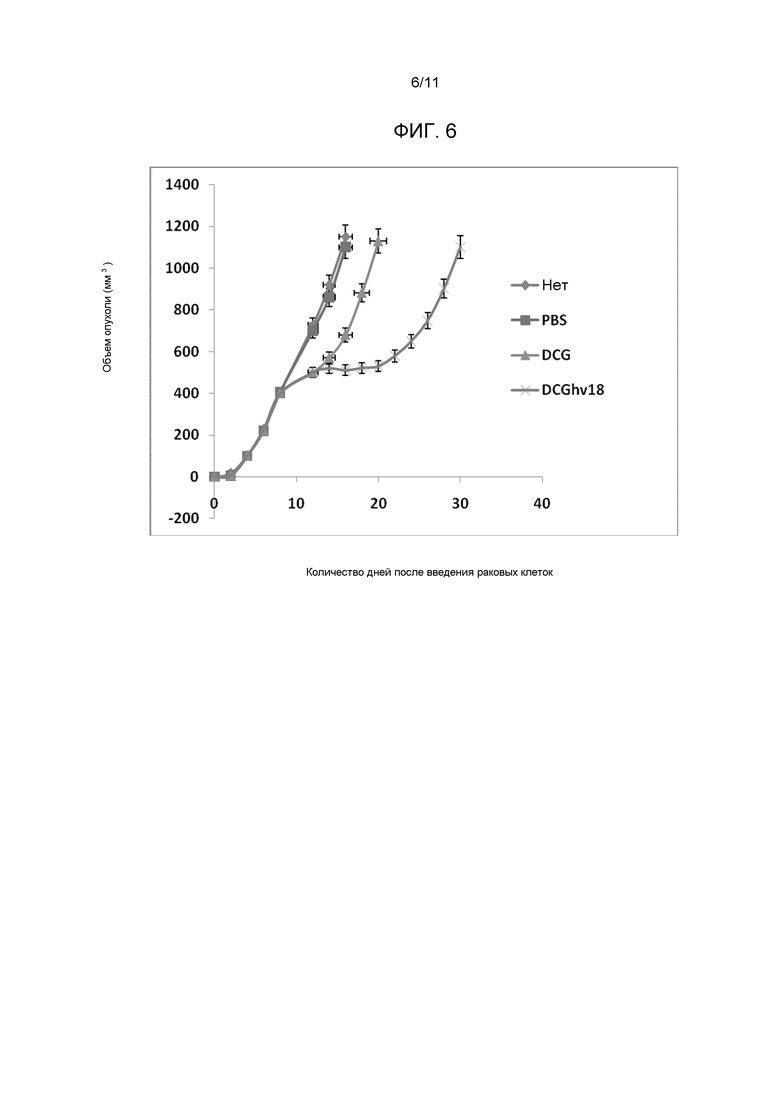

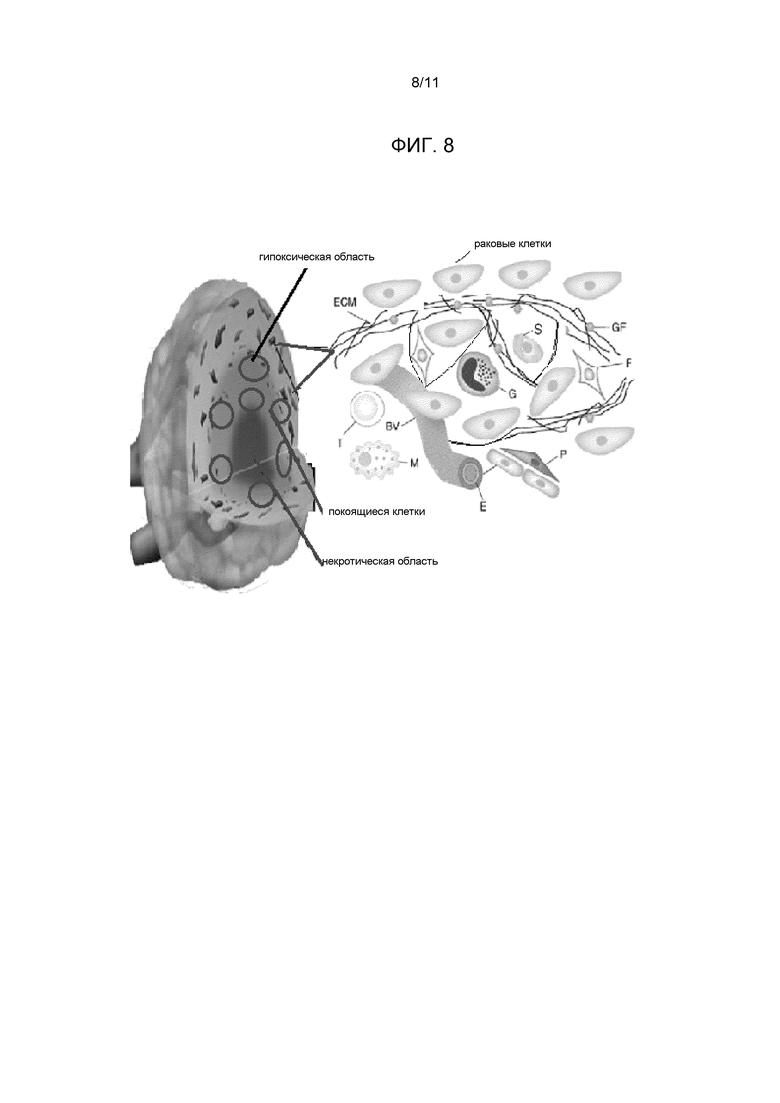



Группа изобретений относится к бактериальным штаммам Clostridium ghonii, способным подавлять рост солидной злокачественной опухоли, вызывать регрессию и разрушение солидной злокачественной опухоли, а также их применению. Предложены штаммы Clostridium ghonii MW-DCG_HNCv18, Clostridium ghonii MW-DCG_CCv17 и Clostridium ghonii MW-DCG_LCv26, депонированные в Национальном Институте Измерений (National Measurement Institute, 1/153 Bertie Street, Port Melbourne, Victoria, Australia 3207) под соответствующими регистрационными номерами V12/001485, V12/001487 и V12/001486. Предложенные штаммы используют для подавления роста солидной злокачественной опухоли, ее регрессии и разрушения у субъекта, для лечения такой опухоли у субъекта, для получения лекарственного средства для лечения солидной злокачественной опухоли. Предложенные штаммы также могут быть использованы для подавления или лечения солидной злокачественной опухоли в составе фармацевтической композиции или в составе набора. 10 н. и 37 з.п. ф-лы, 11 ил., 3 табл., 3 пр.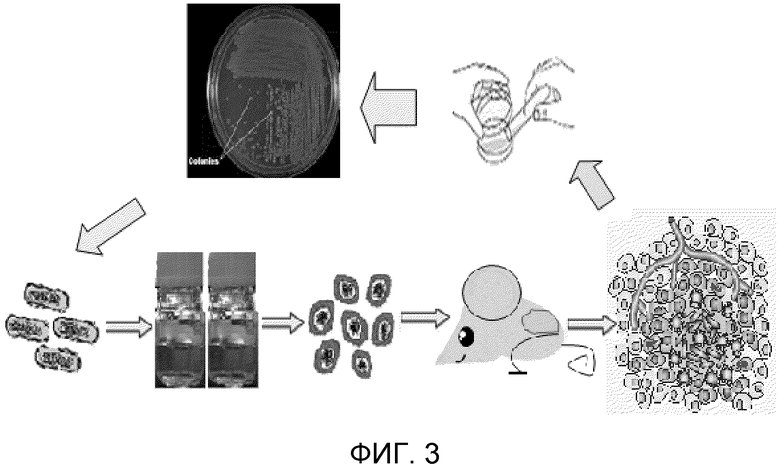
1. Бактериальный штамм Clostridium ghonii MW-DCG_HNCv18, депонированный в Национальном Институте Измерений (National Measurement Institute, 1/153 Bertie Street, Port Melbourne, Victoria, Australia 3207) под регистрационным номером V12/001485, способный подавлять рост солидной злокачественной опухоли, вызывать регрессию и разрушение солидной злокачественной опухоли.
2. Бактериальный штамм Clostridium ghonii MW-DCG_CCv17, депонированный в Национальном Институте Измерений (National Measurement Institute, 1/153 Bertie Street, Port Melbourne, Victoria, Australia 3207) под регистрационным номером V12/001487, способный подавлять рост солидной злокачественной опухоли, вызывать регрессию и разрушение солидной злокачественной опухоли.
3. Бактериальный штамм Clostridium ghonii MW-DCG_LCv26, депонированный в Национальном Институте Измерений (National Measurement Institute, 1/153 Bertie Street, Port Melbourne, Victoria, Australia 3207) под регистрационным номером V12/001486, способный подавлять рост солидной злокачественной опухоли, вызывать регрессию и разрушение солидной злокачественной опухоли.
4. Бактериальный штамм по любому из пп.1-3, отличающийся тем, что указанный штамм вызывает онколизис клеток, содержащихся в микроокружении опухоли.
5. Бактериальный штамм по любому из пп.1-3, отличающийся тем, что штамм вызывает лизис от приблизительно 20% до приблизительно 90% клеток в микроокружении опухоли.
6. Бактериальный штамм по любому из пп.1-3, отличающийся тем, что штамм вызывает лизис приблизительно 20% до приблизительно 70% клеток в микроокружении опухоли.
7. Бактериальный штамм по любому из пп.1-3, отличающийся тем, что штамм вызывает лизис от приблизительно 20% до приблизительно 40% клеток в микроокружении опухоли.
8. Бактериальный штамм по любому из пп.1-3, отличающийся тем, что штамм вызывает лизис от приблизительно 20% до приблизительно 35% клеток в микроокружении опухоли.
9. Бактериальный штамм по любому из пп.1-3, отличающийся тем, что штамм вызывает лизис от приблизительно 25% до приблизительно 35% клеток в микроокружении опухоли.
10. Бактериальный штамм по любому из пп.1-3, отличающийся тем, что штамм вызывает меньшую токсичность, чем референсный клостридиальный штамм.
11. Способ подавления роста солидной злокачественной опухоли, регрессии и разрушения солидной злокачественной опухоли у субъекта, где способ включает введение терапевтически эффективного количества одного или более бактериальных штаммов по любому из пп.1-10 указанному субъекту, нуждающемуся в этом.
12. Применение одного или более бактериальных штаммов по любому из пп.1-10 для подавления роста солидной злокачественной опухоли, регрессии и разрушения солидной злокачественной опухоли у субъекта.
13. Способ лечения солидной злокачественной опухоли у субъекта, включающий введение:
(1) терапевтически эффективного количества одного или более бактериальных штаммов по любому из пп.1-10 и
(2) терапевтически эффективного количества противоопухолевого средства указанному субъекту.
14. Применение одного или более бактериальных штаммов по любому из пп.1-10 и противоопухолевого средства в комбинированной терапии для лечения солидной злокачественной опухоли у субъекта, где подавление роста солидной злокачественной опухоли, регрессия и разрушение солидной злокачественной опухоли являются показателем лечения.
15. Способ по п.13, где введение (1) и (2) указанному субъекту происходит последовательно или одновременно.
16. Способ по п.13, где (1) и (2) вводят как одну фармацевтическую композицию указанному субъекту.
17. Способ по п.13, где введение (1) и (2) повторяют один или более раз, чтобы гарантировать регрессию опухоли.
18. Способ по п.13, где (1) и (2) вводят указанному субъекту в качестве первой дозы, с последующим введением (2) в качестве второй дозы.
19. Способ по п.13, где указанному субъекту вводят более одного противоопухолевого средства.
20. Способ по п.13, где терапевтически эффективное количество бактериального штамма составляет от приблизительно 106 колониеобразующих единиц (КОЕ) до приблизительно 1014 КОЕ/кг на дозу.
21. Способ по п.13, где введение терапевтически эффективного количества бактериальных штаммов указанному субъекту производят посредством внутривенного, люмбального, подкожного или внутримышечного введения.
22. Фармацевтическая композиция для подавления роста солидной злокачественной опухоли, вызова регрессии и разрушения солидной злокачественной опухоли, включающая эффективное количество одного или более бактериальных штаммов по любому из пп.1-10 и физиологически приемлемый носитель и/или вспомогательное вещество.
23. Композиция по п.22, дополнительно включающая одно или более противоопухолевых средств.
24. Композиция по п.23, где противоопухолевое средство выбрано из группы, состоящей из химических соединений, молекул РНК, антител или их любой комбинации.
25. Композиция по п.24, где химическое соединение выбрано из группы, состоящей из дихлорацетата натрия, паклитаксела, доксила, топотекана, ДНК-модифицирующих средств, карбоплатина, антиметаболитов, гемцитабина, лекарственных средств, которые блокируют деление клеток, винкристина, антиангиогенных средств и пазопаниба.
26. Композиция по п.24, где молекула РНК является малой интерферирующей РНК (миРНК).
27. Композиция по п.26, где миРНК специфична к лактатдегидрогеназе (LDHA) или специфична к CD147.
28. Композиция по п.24, где антитело является противоопухолевым моноклональным антителом.
29. Композиция по п.28, где противоопухолевое антитело является антителом против иммунной стимуляции или моноклональным антителом против регуляторных T-клеток.
30. Композиция по п.29, где антитело против иммунной стимуляции является моноклональным антителом против CD40.
31. Композиция по п.30, где моноклональным антителом против CD40 является FGK45.
32. Композиция по п.29, где моноклональное антитело против регуляторных T-клеток является моноклональным антителом против CD25.
33. Композиция по п.32, где моноклональным антителом против CD25 является PC61.
34. Композиция по п.28, где антитело направлено против рецептора эпидермального фактора роста (EGFR).
35. Композиция по п.28, где противоопухолевое моноклональное антитело конъюгировано.
36. Композиция по п.35, где антитело конъюгировано с радиоизотопом или активизирующим лекарственное средство ферментом.
37. Композиция по п.36, где антителом или радиоизотопом являются рений-188 или рений-186, фтордезоксиглюкоза (18F), иттрий-90 (90Y)-конъюгированное антитело против CD20 Y90-ибритутомаб тиуксетан, или иод-131 (131I)-конъюгированное антитело против CD20 I131-тозитумомаб.
38. Композиция по п.35, где антитело конъюгировано с липосомой или наночастицей.
39. Набор для лечения солидной злокачественной опухоли, включающий один или более бактериальных штаммов по любому из пп.1-10 или фармацевтическую композицию по п.22, дополнительно включающий противоопухолевое средство, и инструкции по применению.
40. Способ по п.13, где субъектом является млекопитающее.
41. Способ по п.40, где млекопитающим является человек.
42. Способ по п.13, где солидная злокачественная опухоль выбрана из группы, состоящей из карцином дыхательной системы, карцином желудочно-кишечной системы, карцином мочеполовой системы, карцином яичка, карцином молочной железы, карцином предстательной железы, карцином эндокринной системы, меланом, хориокарциномы и карцином шейки матки, легкого, головы и шеи, толстой кишки, яичника, мозга, мочевого пузыря, молочной железы, предстательной железы, опухолей костной, жировой и хрящевой ткани, болезни Ходжкина, неходжкинской лимфомы, B-клеточной лимфомы, эпителиотропной лимфомы, комплексной лимфомы, анапластической крупноклеточной лимфомы, лимфомы лимфоидной ткани, ассоциированной с желудочной и нежелудочной слизистой, лимфопролиферативной болезни, T-клеточной лимфомы, лимфомы Беркитта, мантийноклеточной лимфомы, диффузной крупноклеточной лимфомы, лимфоплазмацитоидной лимфомы и множественной миеломы.
43. Применение:
(1) терапевтически эффективного количества одного или более бактериальных штаммов по любому из пп.1-10 и
(2) терапевтически эффективного количества противоопухолевого средства,
в производстве лекарственного средства для лечения солидной злокачественной опухоли у субъекта, где подавление роста солидной злокачественной опухоли, регрессия и разрушение солидной злокачественной опухоли является показателем лечения.
44. Применение по п.43, дополнительно включающее два или более противоопухолевых средств.
45. Бактериальный штамм по п.4, где штамм дополнительно способен разрушать или подавлять рост солидной опухоли в результате онколизиса тканевых структур, содержащихся в микроокружении.
46. Штамм по п.45, где онколизис вызывает один или более ферментов в клетках нового штамма.
47. Штамм по п.46, где один или более ферментов выбраны из группы, состоящей из протеиназ, липаз и коллагеназ.
| VAN MELLAERT L | |||
| ET AL | |||
| Clostridium spores as anti-tumor agents // Trends in Microbiology, 2006, vol | |||
| Паровоз для отопления неспекающейся каменноугольной мелочью | 1916 |
|
SU14A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| MINTON N.P | |||
| Clostridia in cancer therapy // Nat | |||
| Rev | |||
| Microbiol | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ТОРЦОВБ1Х СЕРДЕЧНИКОВ ЭЛЕКТРИЧЕСКИХ МАШИН | 0 |
|
SU237243A1 |
| WEI M.Q | |||
| ET AL | |||
| Clostridial spores as live "Trojan horse" vectors for cancer gene therapy: comparison with viral delivery systems // Genetic Vaccines and Therapy, 2008, 6:8, pp | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| WO 2002007741 A1, 31.01.2002 | |||
| Прокладка для автомобильных шин | 1925 |
|
SU8824A1 |
Авторы
Даты
2018-09-19—Публикация
2013-04-29—Подача