Изобретение относится к области медицины, онкологии и может быть использовано для диагностики возникновения злокачественных новообразований в тканях.
В ткань вводят экзогенные молекулы - зонды. Такими зондами могут служить молекулы органических красителей, способные излучать замедленную флуоресценцию (ЗФ) и фосфоресценцию. Затем введенные в ткань молекулы возбуждают импульсами лазерного излучения в основной полосе поглощения S0→S1, где S0 - основное состояние молекулы, S1 - первое возбужденное синглетное состояние. В результате интеркомбинационной конверсии S1→Т1 из первого возбужденного синглетного состояния, появляются молекулы красителей в триплетном T1 состоянии (которые характеризуются большими значениями времени жизни 10-6 - 10-3 с). Триплетные состояния молекул эффективно тушатся молекулярным кислородом 3О2 с образованием синглетного кислорода 1О2.
В работе [«Журнал физической химии», 2013, том. 87, №9, с. 1602-1607] показано, что в биотканях в присутствии синглетного и молекулярного кислорода возможны следующие каналы релаксации триплетных состояний молекул:
- термоинициированная обратная T1→S1 интеркомбинационная конверсия с последующей замедленной флуоресценцией T1→S1→S0+hνЗФ (в дальнейшем будем называть этот тип замедленной флуоресценции - ТЗФ);
- синглет-триплетная аннигиляция T1+1O2, сопровождающаяся возникновением S1 состояний молекул с последующей замедленной флуоресценцией T1+1О2→3О2+S1→S0+hνЗФ (в дальнейшем будем называть этот тип замедленной флуоресценции - СТА ЗФ);
- фосфоресценция T1→S0+hνФОС.
Авторами настоящей заявки ["Вестник ОГУ", 2015, №13, С. 175-180; Journal of Photochemistry & Photobiology, В: Biology 163 (2016) 232-236] показано, что в злокачественных опухолях, в отличие от нормальных тканей, при импульсно-периодическом возбуждении, из-за разности скоростей расходования фотосенсибилизированного синглетного 1О2 кислорода внутри ткани и поступления 3О2 кислорода из внешней среды в ткань в промежутке между возбуждающими импульсами, наблюдается эффект тушения СТА ЗФ. В работе ["Вестник ОГУ", 2015, №13, С. 175-1802] этот эффект предложено использовать для диагностики возникновения опухолей на ранней стадии.
Интегральный измеряемый сигнал замедленной флуоресценции зондов в биотканях представляет собой суперпозицию двух типов свечения - ТЗФ и СТА ЗФ. Интенсивность замедленной флуоресценции IЗФ (площадь под кинетической кривой ЗФ) определяется выражением:
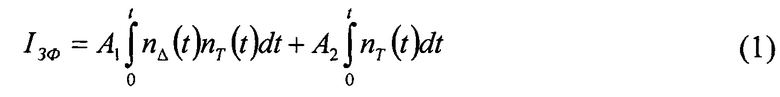
где А1 и А2 - постоянные коэффициенты;
nΔ(t) - концентрация синглетного кислорода;
nT(t) - концентрация зондов в триплетном состоянии.
Первое слагаемое в (1) представляет вклад СТА ЗФ в общий сигнал, второе - вклад ТЗФ.
Тушение СТА ЗФ в опухолях происходит потому, что при возбуждении в строб-режиме для каждого последующего импульса концентрация молекул кислорода в ткани оказывается меньшей, чем для предыдущего импульса. Уменьшение концентрации кислорода в ткани влечет за собой уменьшение
величины nΔ(t) в выражении (1) и, как следствие, уменьшение вклада первого слагаемого в общий сигнал ЗФ.
Другой причиной тушения ЗФ может быть фотохимическое обесчвечивание красителей в тканях при лазерном возбуждении, т.е. уменьшение величины nT(t) в выражении (1). Для учета возможной фотохимической деградации красителей предлагается при каждом отдельном измерении кинетики ЗФ зондов одновременно измерять кинетику их фосфоресценции.
Интенсивность фосфоресценции IФ0С равна:

где A3 - постоянный коэффициент.
Измерения фосфоресценции зондов позволяет контролировать изменение величины nT(t). Практически эта задача решается введением в установку дополнительного фотоприемника, регистрирующего свечение в спектральном диапазоне, соответсвующем фосфоресценции зондов. Величина разностного интегрального сигнала фосфоресценции, определяемого во временном интервале 0-15 мкс, добавляется к интегральному сигналу замедленной флуорисценции. Врезультате описаной процедцры получаем скорректированные данные о кинетике СТА ЗФ, что повышает достоверность процедуры диагностики паталогии биологических тканей.
Ближайшим по техническому решению к предлагаемому способу является способ определения патологий в биологических тканях на основе измерения тушения СТА ЗФ молекулярных зондов в тканях в режиме импульсно-периодического возбуждения [Journal of Photochemistry & Photobiology, В: Biology, 163, 2016, 232-236]. Недостатком способа является отсутствие контроля изменения концентрации триплетных состояний фотосенсибилизаторов (зондов) после каждого возбуждающего импульса, что вносит неточность в интерпретацию результатов измерений.
Техническим результатом изобретения является повышение точности и обеспечение корректности способа диагностики онкологических заболеваний основанного на тушении замедленной флуоресценции зондов при импульсно-периодическом возбуждении, путем создания возможности контроля изменения концентрации триплетных состояний молекул зондов непосредственно в процессе измерения кинетики затухания замедленной флуоресценции. Задача решается тем, что в экспериментальную установку вводится дополнительный канал регистрации свечения и одновременно с замедленной флуоресценцией измеряется кинетика фосфоресценции молекулярных зондов после каждого возбуждающего импульса. По изменениям, происходящим в кинетике фосфоресценции, контролируется концентрация триплетных состояний молекул зондов в ткани и производится (при необходимости) корректировка данных измерений кинетики замедленной флуоресценции.
Реализация способа оптической диагностики патологий в биологических тканях с одновременным контролем концентрации триплетных состояний молекул зондов непосредственно в процессе измерения кинетики затухания замедленной флуоресценции приведена в следующем примере.
Измерения проводились in vitro в тканях здоровых и больных раком молочной железы мышей линии BYRB и раком желудка крыс линии Wistar. Образцы тканей окрашивались ксантеновыми красителями (молекулярными зондами, фотосенсибилизаторами) - эритрозином, эозином или бенгальским розовым и подвергались облучению серией лазерных импульсов с плотностью мощности 0,5 МВт/см2 и длительностью импульса 15 нс. Импульсы следовали через равные промежутки времени в 200 мс. Обычно в серии было от 5 до 7 импульсов. После каждого импульса измерялись кинетические кривые замедленной флуоресценции (λmax=570 нм) и фосфоресценции (λmax=680 нм).
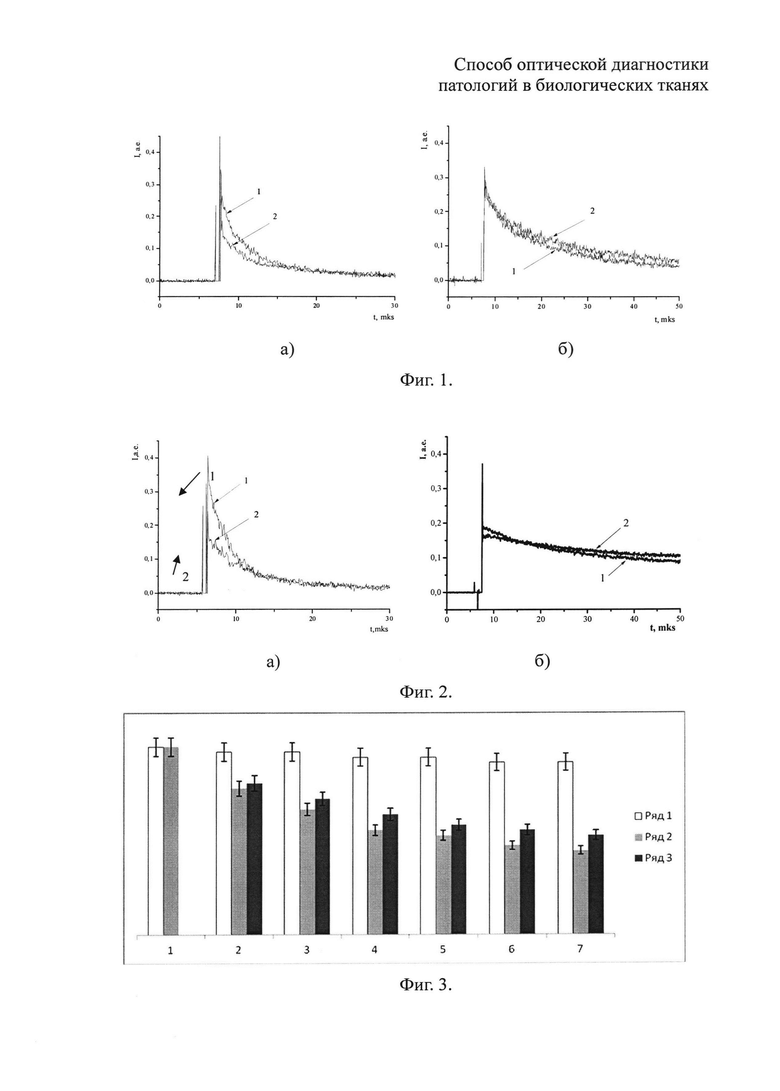
На фиг. 1а приведены кинетические кривые ЗФ, а на фиг. 1б кинетические кривые фосфоресценции эритрозина, измеренные после первого (линия 1) и седьмого (линия 2) импульсов возбуждения. Видно, что после седьмого импульса наблюдается заметное тушение СТА ЗФ, что свидетельствует о наличии патологии в исследуемом образце ткани.
Для контроля концентрации триплетных состояний молекулярных зондов осуществляли измерение кинетики фосфоресценции. На фиг. 1б видно, что интенсивность фосфоресценции фотосенсибилизатора (эритрозина) при выбранном режиме облучения во временном интервале 0-15 мкс не изменяется, что свидетельствует об отсутствии фотохимической деградации красителя.
На фиг. 2 представлены кинетические кривые замедленной флуоресценции и фосфоресценции красителя бенгальского розового в злокачественной опухоли ткани желудка крысы линии Wistar. На фиг. 2а видно, что имеет место сильное тушение ЗФ бенгальского розового. Это свидетельствует о возможном наличии в исследуемой ткани патологии.
Однако измерения кинетики фосфоресценции красителя показывают, что от импульса к импульсу происходит уменьшение интенсивности фосфоресценции. На фиг. 2б приведены кинетические кривые после 1-го и после 7-го импульсов. Этот результат указывает на то, что имеет место фотохимическая деградация фотосенсибилизатора, которая также приводит к уменьшению интенсивности ЗФ бенгальского розового.
В данном случае, для корректной диагностики наличия патологии в исследуемой ткани, следует скорректировать кинетическую кривую ЗФ путем учета фотохимических процессов. Результаты процедуры корректировки показаны на фиг. 3. Здесь приведена гистограмма сравнительных изменений интенсивности замедленной флуоресценции и фосфоресценции бенгальского розового, внедренного в ткани желудка больной и здоровой крысы линии Wistar при импульсно-периодическом возбуждении с частотой 5 Гц (гистограмма построена по площади под кинетическими кривыми, регистрируемыми после каждого импульса во временном интервале 0-15 мкс). По оси абсцисс отложен порядковый номер возбуждающего импульса.
Ряд 1 - интегральная интенсивность ЗФ бенгальского розового в ткани здоровой крысы (небольшое уменьшение интенсивности ЗФ обусловлено фотохимической деградацией красителя);
Ряд 2 - интегральная интенсивность ЗФ бенгальского розового в ткани больной крысы (без учета фотохимической деградации красителя);
Ряд 3 - интенсивность СТА ЗФ бенгальского розового в ткани больной крысы с учетом фотохимической деградации красителя.
Из фиг. 3 видно, что к седьмому импульсу интенсивность сигналов СТА ЗФ (Ряд 3) красителя, внедренного в испытуемую ткань желудка, уменьшается на 60%, что надежно и достоверно свидетельствует о наличии в ней патологии.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения концентрации кислорода в жидкостях и газах | 1989 |
|
SU1712839A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ КИСЛОРОДА В ГАЗАХ | 2007 |
|
RU2349902C1 |
| НАНОКОМПОЗИТНЫЙ ФОТОСЕНСИБИЛИЗАТОР ДЛЯ МЕТОДА ФОТОДИНАМИЧЕСКОГО ВОЗДЕЙСТВИЯ НА КЛЕТКИ | 2006 |
|
RU2329061C1 |
| СПОСОБ ИЗМЕРЕНИЯ КОНЦЕНТРАЦИИ КИСЛОРОДА В ГАЗОВЫХ СМЕСЯХ | 2012 |
|
RU2523756C1 |
| УСТРОЙСТВО ДЛЯ СПЕКТРАЛЬНО-ФЛУОРЕСЦЕНТНОГО КОНТРОЛЯ СОСТОЯНИЯ БИОЛОГИЧЕСКИХ ТКАНЕЙ В ПРОЦЕССЕ ФОТОДИНАМИЧЕСКОГО ВОЗДЕЙСТВИЯ С ПРИМЕНЕНИЕМ ФОТОСЕНСИБИЛИЗАТОРОВ НА ОСНОВЕ ХЛОРИНА E6 | 2022 |
|
RU2807133C1 |
| Фотосенсибилизатор на основе карбоцианинового красителя для фотодинамической терапии опухолей | 2016 |
|
RU2638131C1 |
| Способ фотодинамической терапии базально-клеточного рака кожи I стадии | 2022 |
|
RU2826594C2 |
| Способ обнаружения опухолевой ткани в операционном материале при раке молочной железы | 2024 |
|
RU2835219C1 |
| Способ определения внутримицеллярного кислорода в растворах катионных поверхностно-активных веществ | 1990 |
|
SU1760444A1 |
| БИОСОВМЕСТИМЫЙ НАНОМАТЕРИАЛ ДЛЯ ФОТОСЕНСИБИЛИЗАЦИИ СИНГЛЕТНОГО КИСЛОРОДА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2014 |
|
RU2607579C2 |
Изобретение относится к медицине, в частности к онкологии, и может быть использовано для диагностики возникновения злокачественных опухолей в тканях in vitro. Вводят в ткань фотосенсибилизатор. Воздействуют на ткань лазерным излучением серией импульсов с плотностью мощности 0,5 МВт/см2 и длительностью импульса 15 нс. Во временном интервале 1-15 мкс после каждого импульса облучения одновременно измеряют интенсивность замедленной флуоресценции и фосфоресценции фотосенсибилизатора. При снижении интенсивности фосфоресценции, свидетельствующем о снижении концентрации триплетных состояний фотосенсибилизатора, осуществляют корректировку показаний интенсивности замедленной флуоресценции после каждого возбуждающего импульса. Корректировку осуществляют путем добавления величины разностного интегрального сигнала фосфоресценции к интегральному сигналу замедленной флуоресценции. Наличие опухоли в ткани диагностируют при снижении скорректированного показателя интенсивности замедленной флуоресценции на 60% к седьмому лазерному импульсу. Способ обеспечивает повышение точности и достоверности диагностики онкологических патологий в биологических тканях за счет обнаружения тушения замедленной флуоресценции молекулярных зондов в тканях при их импульсно-периодическом возбуждении путем контроля изменения концентрации молекул зондов в триплетных состояниях непосредственно в процессе измерения кинетики затухания замедленной флуоресценции. 3 ил.
Способ оптической диагностики злокачественных опухолей в тканях in vitro, включающий введение в ткань фотосенсибилизатора и воздействие на ткань импульсно-периодическим лазерным излучением, отличающийся тем, что лазерное воздействие осуществляют серией импульсов с плотностью мощности 0,5 МВт/см2 и длительностью импульса 15 нс, затем во временном интервале 1-15 мкс после каждого импульса облучения одновременно измеряют интенсивность замедленной флуоресценции и фосфоресценции фотосенсибилизатора, и при снижении интенсивности фосфоресценции, свидетельствующем о снижении концентрации триплетных состояний фотосенсибилизатора, осуществляют корректировку показаний интенсивности замедленной флуоресценции после каждого возбуждающего импульса путем добавления величины разностного интегрального сигнала фосфоресценции к интегральному сигналу замедленной флуоресценции, наличие опухоли в ткани диагностируют при снижении скорректированного показателя интенсивности замедленной флуоресценции на 60% к седьмому лазерному импульсу.
| ЛЕТУТА С.Н | |||
| и др | |||
| Флуоресцентная дозиметрия в фотодинамической терапии | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| УСТРОЙСТВО ДЛЯ ФЛУОРЕСЦЕНТНОЙ ДИАГНОСТИКИ И МОНИТОРИНГА ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2015 |
|
RU2596869C1 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2014 |
|
RU2552032C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ КИСЛОРОДА | 2002 |
|
RU2231775C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ КИСЛОРОДА | 2002 |
|
RU2231775C2 |
| WO 2013109966 A1, 25.07.2013 | |||
| Kim MM et al | |||
| A Comparison of Singlet Oxygen Explicit Dosimetry (SOED) and Singlet Oxygen Luminescence Dosimetry (SOLD) for Photofrin-Mediated Photodynamic Therapy.Cancers (Basel) | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| Шкив для канатной передачи | 1920 |
|
SU109A1 |
Авторы
Даты
2018-11-15—Публикация
2017-08-03—Подача