Изобретение относится к медицине, конкретно к фармакологии, гематологии и онкологии.
Высокая частота встречаемости миелосупрессивных состояний, развивающихся в результате химиотерапии опухолевых заболеваний [1], является основанием необходимости применения гемостимулирующих (используются после химиотерапии) и гемопротекторных (используются перед химиотерапией) средств в медицинской практике.
Известны гемопротекторные средства [2-5].
Недостатком данных средств является зачастую их низкая эффективность [5, 6].
Задачей, решаемой настоящим изобретением, является расширение арсенала высокоэффективных гемопротекторных средств.
Поставленная задача достигается применением активатора протеинкиназы А (РКА) в качестве гемопротекторного средства.
Новым в предлагаемом изобретении является использование в качестве гемопротекторного средства активатора РКА.
Химиотерапия представляет собой одним из основных методов лечения в онкологии. Однако применение противоопухолевых средств зачастую приводит к развитию тяжелых побочных эффектов [1]. Мишенью цитостатических агентов, в первую очередь, являются митотически активные клеточные элементы. К данной категории, помимо опухолевых, относятся клетки здоровых тканей с высокой способностью к физиологическому клеточному обновлению, в том числе костный мозг [6].
Одним из путей повышения безопасности химиотерапии является профилактика повреждающего действия цитостатических препаратов на ткани и органы, не вовлеченные в опухолевый патологический процесс [3]. Для предупреждения развития миелосупрессивных состояний используют гемопротекторы, вводимые в организм (в отличие от гемостимуляторов) перед проведением химиотерапии либо в промежутках между ее курсами (например, дикарбамин [1]).
Согласно современным представлениям, функционирование клеток осуществляется, в том числе посредством системы внутриклеточной сигнальной трансдукции. В связи с этим перспективной выглядит возможность разработки гемопротекторов в рамках
«Стратегии фармакологической регуляции внутриклеточной сигнальной трансдукции в регенераторно-компетентных клетках» [7, 8], предполагающей использование в качестве мишеней воздействия отдельные звенья внутриклеточной сигнальной трансдукции, ответственные за функционирование прогениторных клеток и элементов микроокружения. В настоящее время известны лишь общие представления о том, что процессы пролиферации и дифференцировки кроветворных клеток регулируются сАМР-, NF-кВ-, PI3K- и МАР-опосредованными сигнальными путями [7, 8]. При этом считается, что повышение концентрации цАМФ в клетке, активирующего протеинкиназу А (РКА), способно приводить к торможению их митотической активности. Более того, существуют данные о выраженных антипролиферативных эффектах РКА в отношении опухолевых клеток [9]. В то же время известно, что поддержание необходимого уровня интенсивности кроветворения и развитие адекватных компенсаторно-приспособительных реакций со стороны системы крови, в том числе при введении цитостатических агентов, обеспечиваться, в первую очередь, напротив, за счет повышения пролиферативной активности гемопоэтических клеток-предшественников, отражением которого является увеличение их количества в костном мозге [10, 11].
Возможность влияния активаторов РКА на процессы кроветворения, в том числе ускорять восстановление гемопоэза в постцитостатическом периоде, не известна. Эксперимент показал непредсказуемые результаты.
Факт применения активатора РКА с достижением нового технического результата, заключающегося в гемопротекции, для специалиста является не очевидным.
Новые свойства не вытекают явным образом из уровня техники в данной области и не обнаружены в патентной и научно-технической литературе.
Предлагаемое изобретение может быть использовано в медицине.
Исходя из вышеизложенного, следует считать заявляемое техническое решение соответствующим критериям: «Новизна», «Изобретательский уровень», «Промышленная применимость».
Эксперименты были проведены на 60 мышах линии С57В 1/6. Животные получены из отдела экспериментальных биологических моделей НИИФиРМ им. Е.Д. Гольдберга Томского НИМЦ.
Исследования проводили в соответствии с правилами лабораторной практики (GLP), Приказом 199н от 15.08.2016 «Об утверждении Правил надлежащей лабораторной практики», ГОСТ 33044-2014 «Принципы надлежащей лабораторной практики» (2015), Федеральным Законом от 12 апреля 2010 г. №61-ФЗ «Об обращении лекарственных средств», «Методическими рекомендациями по изучению гемостимулирующей активности фармакологических веществ» Руководства по проведению доклинических исследований новых лекарственных средств (2013) [11].
Пример 1
Эффективность гемопротекции определялась на модели цитостатической миелосупрессии.
Цитостатическую миелосупрессию моделировали путем однократного внутрибрюшинно введения раствора циклофосфана (ЦФ) в максимально переносимой дозе (МПД) (250 мг/кг).
Мыши опытных групп однократно за 6 часов до введения цитостатика получали активатор РКА (8-Cl-сАМР, 8-Chloradenosine 3',5'-cyclic-monophosphat, «Sigma»), либо активатор РКА (8-Br-cAMP, 8-Bromoadenosine-3',5'-cyclic monophosphate sodium salt, «Abcam plc.») подкожно в дозе 20 мкг/кг. Животным группы сравнения в аналогичном режиме внутрижелудочно в дозе 0,5 мг/кг вводили Дикарбамин (ОАО «Валента Фарм»), Контрольные животные получали растворитель в эквивалентном объеме (0,2 мл). Указанные дозы дикарбамина и активаторов были определены на основании данных предварительных экспериментов.
На 5, 8 и 12 сутки после введения цитостатика животных умерщвляли путем ингаляции СО2. У опытных и контрольных мышей стандартными методами определяли показатели периферической крови и костномозгового кроветворения. С помощью культуральных методов оценивали содержание коммитированных клеток-предшественников эритро- (КОЕ-Э) и гранулоцитопоэза (КОЕ-ГМ) в костном мозге [11].
Статистическую обработку полученных данных проводили методом вариационной статистики с использованием t-критерия Стьюдента. В случаях отклонения распределения вариант в выборках от нормального для оценки достоверности различий применяли непараметрический критерий Уилкоксона-Манна-Уитни.
Введение ЦФ проводило к закономерному [11] развитию миелосупрессии. Отмечалось падение содержания незрелых нейтрофильных гранулоцитов (5 сутки), лимфоидных и эритроидных клеток (5 и 8 сутки) в гемопоэтической ткани (табл. 1).
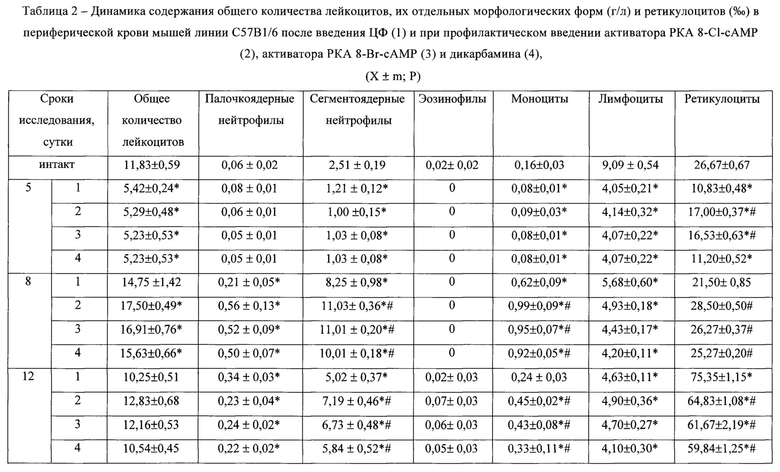
Отражением указанных изменений костномозгового кроветворения явилось падение числа сегментоядерных нейтрофилов, лимфоцитов, моноцитов и ретикулоцитов в периферической крови на 5 сутки и увеличение данных параметров на 8 (сегментоядерные нейтрофилы, лимфоциты, моноциты) и 12 сутки опыта (ретикулоциты) (табл. 2).
В основе развития миелосупрессии лежало повреждающее действие цитостатического агента на кроветворные предшественники костного мозга [6, 11]. При этом в дальнейшем отмечалась активация компенсаторной реакции [6] со стороны пула прекурсоров гемопоэза. Отмечалось увеличение числа КОЕ-ГМ на 5 сутки и восстановление числа КОЕ-Э к 12 суткам опыта (табл. 3).
Профилактическое введение активаторов РКА существенно корригировало изменения гемопоэза, вызываемые цитостатиком. Наблюдалось увеличение клеточности костного мозга. При этом число эритроидных клеток в костном мозге экспериментальных животных на 5 сутки составило 152,2% для активатора РКА 8-Cl-сАМР и 134,5% для активатора РКА 8-Br-сАМР от цитостатического контроля соответственно. В дальнейшем наблюдалось увеличение содержания в костном мозге зрелых нейтрофильных гранулоцитов до 145,4% и 141,1%, моноцитов до 406,8% и 393.1%, лимфоидных клеток до 145,4% и 141,1% на 8 сутки опыта, а также зрелых нейтрофильных гранулоцитов до 136,8% и 136,4% на 12 сутки от цитостатического контроля при применении активатора РКА 8-Cl-сАМР и активатора РКА 8-Br-сАМР соответственно (табл. 1). Дикарбамин вызывал аналогичные по динамике, но менее выраженные изменения (табл. 1).
В периферической крови содержание ретикулоцитов при профилактическом введении активаторов РКА 8-Cl-сАМР и 8-Br-сАМР уже на 5 сутки опыта составило 260,3% и 262,2% от группы с циклофосфаном соответственно. Имело место повышение числа сегментоядерных нейтрофилов (до 133,7% и 133,5% на 8 сутки, до 143.2% и 134,1% на 12 сутки) и моноцитов (до 159,7% и 153,2% на 8 сутки, до 187,5% и 179,2% на 12 сутки) от цитостатического контроля соответственно. Введение дикарбамина приводило к восстановлению числа ретикулоцитов на лишь на 8 сутки опыта (табл. 2).
Исследование механизмов гемопротекторного действия активаторов РКА выявило зависимость формирования картины крови и костного мозга от состояния пула костномозговых родоначальных клеток. Профилактическое введение растворов исследуемых фармакологических веществ увеличивала содержание КОЕ-Э и КОЕ-ГМ в гемопоэтической ткани, подвергшейся цитостатическому воздействию. Имело место значительное повышение количества КОЕ-Э и КОЕ-ГМ на 5, 8-е и 5, 8, 12-е сутки опыта соответственно как при использовании 8-Cl-сАМР, так и 8-Br-сАМР (табл. 3). Курсовое введение дикарбамина также способствовало более раннему восстановлению содержания кроветворных предшественников в кроветворной ткани, которое, однако, было менее выраженным по сравнению с таковым у животных, получавших активаторы РКА (табл. 3).
Полученные результаты свидетельствуют о выраженных гемопротекторных свойствах активаторов РКА [11]. При этом механизмом действия данных модификаторов внутриклеточной сигнальной трансдукции являлось их влияние на функционирование родоначальных гемопоэтических клеток.
Таким образом, проведенные исследования свидетельствуют о высокой эффективности применения активаторов РКА в качестве гемопротекторных средств при гипопластических состояниях кроветворения.
Цитируемая литература:
1) Assessment of erythroid and granulocytic hematopoietic lineages in patients with non-small-cell lung carcinoma / T.Y. Polyakova [et al.] // Bulletin of Experimental Biology and Medicine. 2017. T. 163. №4. C. 469-474.
2) Моисеенко, B.M. Волков O.H. Симптоматическая терапия больных распространенным раком ободочной кишки / В.М. Моисеенко, О.Н. Волков // Практическая онкология. 2000. №1. С.38-42.
3) Птушкин, В.В. Профилактика осложнений химиотерапии / В.В. Птушкин // Русский медицинский журнал. 2004. Том 12. №11.
4) Симптоматическое лечение осложнений современной химиотерапии и текущего опухолевого процесса. Краткий обзор работ, посвященных теме преодоления неспецифических расстройств // Научно-информационный медицинский журнал. Весна. 2004. №1.
5) Стенина, М.Б. Поддерживающая терапия при проведении современной химиотерапии (гемоцитокины и антиэметики) / М.Б. Стенина // Русский медицинский журнал. 1999. №10. С.455-457.
6) Механизмы протективного действия «дикарбамина» в отношении системы крови при цитостатическом воздействии / В.Е. Небольсин [и др.] // Бюллетень экспериментальной биологии и медицины. 2010. Т. 150. №9. С. 312-316.
7) Participation of Pi3k, Марк Erk1/2 and P38 in the realization of growth potential of mesenchymal precursor cells under in vitro conditions / G.N. Zyuzkov [et al.] // Bulletin Of Experimental Biology And Medicine. 2014. T. 156. №4. C. 556-559.
8) PI3K, MAPK EPK1/2 and Р38 are involved in the realization of growth potential of mesenchymal progenitor cells under the infl uence of basic fibroblast growth factor / G.N. Zyuzkov [et al.] // Bulletin of Experimental Biology and Medicine. 2014. T. 157. №4. C. 436-439.
9) Phase i study of the novel cyclic AMP (cAMP) Analogue 8-Chloro-cAMP in patients with cancer: toxicity, hormonal, and immunological effects / D.J. Propper [et al.] // Clin. Cancer Res. 1999. Vol. 5. P. 1682-1689.
10) Mechanisms of regulation of hemopoiesis during experimental cytostatic myelosuppression induced by carboplatin / A.M. Dygai [et al.] // Bulletin of Experimental Biology and Medicine. 2007. T. 143. №5. C. 581-584.
11) Методические рекомендации по изучению гемостимулирующей активности фармакологических веществ Руководство по проведению доклинических исследований новых лекарственных средств. Часть первая Под ред. А.Н. Миронова / A.M. Дыгай [и др.]. М.: Гриф и К, 2013. С. 759-766.
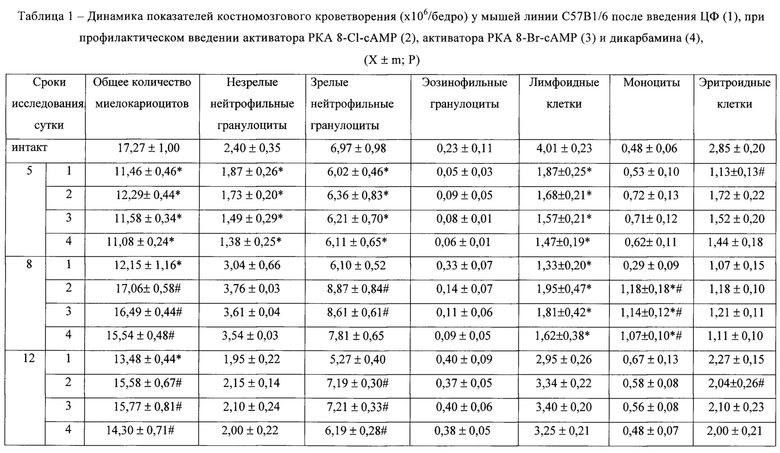
Примечание: в таблицах 1-3* - статистически значимые отличия от интактной группы; # - статистически значимые различия с группой 1 (Р<0,05)

| название | год | авторы | номер документа |
|---|---|---|---|
| Гемопротекторное средство | 2019 |
|
RU2725135C1 |
| Гемостимулирующее средство | 2017 |
|
RU2647833C1 |
| ГЕМОСТИМУЛИРУЮЩЕЕ СРЕДСТВО | 2013 |
|
RU2535021C1 |
| ГЕМОСТИМУЛИРУЮЩЕЕ СРЕДСТВО | 2013 |
|
RU2514648C1 |
| ГЕМОСТИМУЛИРУЮЩЕЕ СРЕДСТВО | 2012 |
|
RU2505308C1 |
| СПОСОБ СТИМУЛЯЦИИ МИЕЛОПОЭЗА | 2010 |
|
RU2442589C1 |
| СПОСОБ СТИМУЛЯЦИИ МИЕЛОПОЭЗА | 2007 |
|
RU2336899C1 |
| СПОСОБ СТИМУЛЯЦИИ МИЕЛОПОЭЗА | 2008 |
|
RU2366452C1 |
| СПОСОБ ПОЛУЧЕНИЯ КЛЕТОЧНОГО МАТЕРИАЛА ДЛЯ ТРАНСПЛАНТАЦИИ ПРИ МИЕЛОСУПРЕССИИ | 2008 |
|
RU2392947C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЭФФЕКТИВНОСТИ ГЕМОСТИМУЛЯТОРОВ ПРИ ЦИТОСТАТИЧЕСКОЙ МИЕЛОСУПРЕССИИ | 2009 |
|
RU2421720C2 |
Изобретение относится к медицине, конкретно к фармакологии, гематологии и онкологии. Предложено применение активатора протеинкиназы А (РКА) в качестве гемопротекторного средства, эффективного при введении in vivo в отношении эритро- и грануломоноцитопоэза. Технический результат состоит в реализации назначения активаторами РКА аналогами цАМФ 8-Cl-сАМР и 8-Br-сАМР, которые корректировали изменения числа эритроидных клеток и моноцитов у мышей с цитостатической миелосупрессией, вызванной циклофосфаном. 3 табл., 1 пр.
Применение активатора протеинкиназы А (РКА) в качестве гемопротекторного средства, эффективного при введении in vivo в отношении эритро- и грануломоноцитопоэза.
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| BREITINGR U | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Front Mol | |||
| Neurosci | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| LI Y | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Oncogene | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| ДМИТРИЕВА Н.В | |||
| и др | |||
| Фебрильная нейтропения у онкологических больных | |||
| Фарматека | |||
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
Авторы
Даты
2019-08-05—Публикация
2018-07-02—Подача