Изобретение относится к области каталитического синтеза бутенов из этилена с использованием гомогенных и нанесенных катализаторов на основе иминопиридиновых комплексов никеля(II) и алюминийорганических сокатализаторов, которые могут содержать алюминий, углерод, водород, кислород, хлор.
Линейные альфа-олефины (в основном 1-бутен и 1-гексен), получаемые путем димеризации и тримеризации этилена, используются в полимеризационной промышленности в качестве сырья для получения линейного полиэтилена низкой плотности. Данный материал представляет собой статистический сополимер этилена с 1-бутеном или 1-гексеном и широко применяется в качестве упаковочного материала (Shimizu A. Synth. Org. Chem. Japan 1981, v. 39, p. 554-560). Поэтому в патентной литературе и открытых источниках в основном описываются процессы селективной димеризации этилена в 1-бутен на металлокомплексных, гетерогенных, либо кислотно-основных катализаторах. Как правило, каталитические системы для процессов данного типа являются двухкомпонентными и включают в себя катализатор на основе комплекса переходного металла (титана, никеля, хрома, палладия, кобальта) и сокатализатор (активатор) на основе металлоорганических соединений (алюминийорганических или борорганических соединений).
Вместе с тем, в настоящее время актуальной задачей нефтехимической промышленности является вовлечение нефтезаводских (углеводородных) газов в процессы получения ценных химических продуктов. Повышение глубины переработки нефти может быть реализовано, в частности, за счет использования этан-этиленовой фракции нефтезаводских газов. Одной из ключевых стадий переработки этан-этиленовой фракции является димеризация этилена в 2-бутены (цис-2-бутен, транс-2-бутен), которые могут быть введены в реакцию метатезиса с этиленом (Popoff N., Mazoyer Е., Pelletier J., Gauvin R.M., Taoufik M. Chem. Soc. Rev. 2013, v. 42, p. 9035-9054) с образованием пропилена. Пропилен в дальнейшем подвергается гидратации для получения изопропанола, который может использоваться в качестве октаноповышающей добавки к моторным топливам. Помимо этого, 2-бутены могут использоваться в реакциях алкилирования при производстве моторных топлив.
Таким образом, в настоящее время востребованными являются катализаторы селективной димеризации этилена, демонстрирующие высокую каталитическую активность, высокую селективность по С4-фракции (1-бутен + цис-2-бутен + транс-2-бутен) и низкий выход фракций C6+, а также высокую селективность по 2-бутенам (цис-2-бутен + транс-2-бутен).
Однако, число каталитических систем, способных селективно вести димеризацию этилена в 2-бутены и имеющих перспективы практического применения, невелико. Известные способы суспензионной димеризации этилена в 2-бутены с использованием гомогенных катализаторов с числом компонентов от двух до четырех (US 2012095275 A1, С07С 2/08, 19.04.2012; US 5162595 A, С07С 2/30, 10.11.1992; JPH07165620, B01J 31/24, 27.06.1995; Yang Q., Kermagoret A., Agostinho M., Siri O., Braunstein P. Organometallics 2006, v. 25, p. 5518-5527; Xu C., Shen Q., Sun X., Tang Y. Chin. J. Chem. 2012, v. 30, p. 1105-1113; Song S., Xiao Т., Wang L., Redshaw C., Wang F., Sun W.-H. J. Organomet. Chem. 2012, v. 699, p. 18-25) позволяют получать смеси продуктов, содержащие 90-96% вес. фракции С4 и с селективностью фракции С4 по 2-бутенам 90-97%. Однако для данных способов характерен ряд недостатков: сложность проведения эксперимента из-за необходимости последовательного добавления двух-четырех компонентов в реактор, зачастую - невозможность иммобилизации используемых катализаторов на твердом носителе, в ряде случаев - недостаточно высокая активность катализатора либо его низкая стабильность, что делает нецелесообразным применение подобных каталитических систем на практике.
Примером газофазного каталитического процесса селективной димеризации этилена в 2-бутены является процесс с использованием катализатора на основе комплекса никеля(II), растворенного в ионной жидкости, нанесенной на силикагель (Scholz J., Hager V., Wang X.J., Kohler F.T.U., Sternberg M., Haumann M., Szesni N., Meyer K., Wasserscheid, P. ChemCatChem. 2014, v. 6, p. 162-169; Kohler F.T.U., 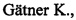 Hager V., Haumann M., Sternberg M., Wang X., Szesni N., Meyer K., Wasserscheid P. Catal. Sci. Technol. 2014, v. 4, p. 936-947). Процесс проводили в реакторе с неподвижным слоем катализатора, подавая в реактор этилен с постоянной скоростью потока. При температуре 40°С в течение первых нескольких часов конверсия этилена была близка к 100%, селективность образования фракции С4 составляла 94%, селективность фракции С4 по 2-бутенам - 95%. Основным недостатком данного процесса была быстрая дезактивация катализатора: при температуре выше 40°С из-за выделения большого количества теплоты в ходе димеризации этилена и локального перегрева отдельных частей реактора.
Hager V., Haumann M., Sternberg M., Wang X., Szesni N., Meyer K., Wasserscheid P. Catal. Sci. Technol. 2014, v. 4, p. 936-947). Процесс проводили в реакторе с неподвижным слоем катализатора, подавая в реактор этилен с постоянной скоростью потока. При температуре 40°С в течение первых нескольких часов конверсия этилена была близка к 100%, селективность образования фракции С4 составляла 94%, селективность фракции С4 по 2-бутенам - 95%. Основным недостатком данного процесса была быстрая дезактивация катализатора: при температуре выше 40°С из-за выделения большого количества теплоты в ходе димеризации этилена и локального перегрева отдельных частей реактора.
Таким образом, в патентной и открытой литературе в основном описаны процессы получения 2-бутенов путем каталитической димеризации этилена с использованием гомогенных многокомпонентных катализаторов. Примеров процессов селективной димеризации этилена в 2-бутены в присутствии нанесенных (гетерогенных) катализаторов практически не встречается.
В настоящем изобретении предлагается новый способ димеризации этилена в бутены с использованием в качестве катализаторов комплексов никеля(II) с бидентатными N,N-донорными лигандами иминопиридинового типа (LNiX2) - производными 2-[(фенилимино)метил]-6-метилпиридина, 2-[(фенилимино)метил]-6-бромпиридина либо 2-[(фенилимино)метил]-хинолина (Схема 1). При этом в фенильном кольце при иминном атоме азота содержится один или несколько электроноакцепторных заместителей (F, Cl, CF3). Процесс димеризации этилена может проводиться как в присутствии гомогенных катализаторов LNiX2, так и в присутствии гетерогенных катализаторов - комплексов LNiX2, нанесенный на силикагель, модифицированный алюминием (SiO2/Al). В качестве второго компонента каталитической системы (сокатализатора) используется алюминийорганический сокатализатор - МАО, Et2AlCl либо Et3Al2Cl3. Димеризация этилена проводится в среде органического растворителя, предпочтительно, толуола при постоянном давлении этилена.
Изобретение решает задачу разработки эффективного каталитического процесса селективной димеризации этилена в смесь 2-бутенов.
Технический результат - достигнуто увеличение каталитической активности катализатора до 9740 кг продуктов/(моль Ni час бар), повышена селективность образования фракции С4 - до 100%, повышена селективность С4 фракции по 2-бутенам - до 96%, достигнуто упрощение технического процесса за счет загрузки гетерогенного катализатора в форме порошка, сокатализатора - в виде раствора в толуоле, увеличена растворимость катализатора за счет использования в синтезе комплексов аддукта бромида никеля с диметоксиэтаном.
Задача решается проведением процесса селективной димеризации этилена в 2-бутены в присутствии гомогенных катализаторов - комплексных соединений никеля(II), содержащих в качестве лигандов производные 2-иминопиридинов, при получении которых в качестве основания используется анилин, содержащий один или несколько электроноакцепторных заместителей (F, Cl, CF3) в ароматическом кольце - в среде толуола, с использованием алюминийорганического сокатализатора.
Задача решается также проведением процесса селективной димеризации этилена в 2-бутены в присутствии гетерогенных катализаторов - вышеупомянутых комплексных соединений никеля(II), нанесенный на силикагель, модифицированный алюминием - в среде толуола, с использованием алюминийорганического сокатализатора.
Сущность изобретения иллюстрируется следующими примерами и таблицами.
Пример 1.
Общий метод приготовления иминопиридиновых лигандов с электроноакцепторными заместителями
Навеску 2-формил-6-метилпиридина, 2-формил-6-бромпиридина либо 2-формилхинолина (1.2 ммоль) и анилин с электроноакцепторными заместителями (1.2 ммоль) растворяют в 10 мл бензола, добавляют 20 мкл трифторуксусной кислоты. Кипятят раствор с обратным холодильником в течение 18 ч в присутствии молекулярных сит 4  (1 г), следят за протеканием реакции при помощи метода тонкослойной хроматографии (ТСХ). Затем дают колбе остыть до комнатной температуры, отфильтровывают молекулярные сита на стеклянном пористом фильтре (40) и промывают их хлористым метиленом. Объединяют органическую фазу, удаляют растворитель в вакууме. Полученное вещество перекристаллизовывают из гексана, выделяют продукт в виде кристаллов с выходом 75-88%. Строение лиганда подтверждают методом спектроскопии ЯМР и элементного анализа.
(1 г), следят за протеканием реакции при помощи метода тонкослойной хроматографии (ТСХ). Затем дают колбе остыть до комнатной температуры, отфильтровывают молекулярные сита на стеклянном пористом фильтре (40) и промывают их хлористым метиленом. Объединяют органическую фазу, удаляют растворитель в вакууме. Полученное вещество перекристаллизовывают из гексана, выделяют продукт в виде кристаллов с выходом 75-88%. Строение лиганда подтверждают методом спектроскопии ЯМР и элементного анализа.
Пример 2.
Общий метод приготовления иминопиридиновых лигандов с электроноакцепторными заместителями
Лиганд синтезируют в условиях примера 1, за исключением того, что процесс проводят в толуоле, в качестве катализатора используют моногидрат n-толуолсульфокислоты (5 мольн. %), реакционную смесь перемешивают при температуре 40-70°С в течение 24-72 ч. Получают продукт в виде кристаллов с выходом 60-91%.
Пример 3.
Метод приготовления иминопиридиновых комплексов никеля LNiCl2.
Иминопиридиновый лиганд (0.3 ммоль) и хлорид никеля(II) (0.3 ммоль) растворяют в CH3CN (4 мл) при быстром перемешивании. Реакционную смесь перемешивают при комнатной температуре в течение 5 ч. Затем добавляют диэтиловый эфир (3 мл), наблюдают выпадение осадка. Комплекс отфильтровывают на стеклянном пористом фильтре (16), промывают диэтиловым эфиром (3 мл), сушат в вакууме при комнатной температуре. Продукт выделяют в виде порошка, подтверждают его строение методом спектроскопии ЯМР и элементного анализа. Для выращивания монокристалла комплекс растворяют в N,N-диметилформамиде и при +4°С создают условия для медленной диффузии диэтилового эфира в раствор комплекса.
Пример 4.
Метод приготовления иминопиридиновых комплексов никеля LNiBr2.
Иминопиридиновый либо иминохинолиновый лиганд (0.6 ммоль) и аддукт бромида никеля(II) с диметоксиэтаном (0.6 ммоль) растворяют в CH2Cl2 либо ТГФ (6 мл) при быстром перемешивании. Реакционную смесь перемешивают при комнатной температуре в течение 18 ч. Затем упаривают раствор до объема 1 мл, добавляют диэтиловый эфир (3 мл), наблюдают выпадение осадка. Комплекс отфильтровывают на стеклянном пористом фильтре (16), промывают диэтиловым эфиром (3 мл), сушат в вакууме при комнатной температуре. Продукт выделяют в виде порошка, подтверждают его строение методом спектроскопии ЯМР и элементного анализа.
Пример 5.
Метод приготовления катализаторов LNiBr2, нанесенных на SiO2/Al.
Полученный комплекс LNiBr2 растворяют в хлористом метилене (0.0085-0.01 г в 20 мл CH2Cl2) при 40°С в течение 30 мин. Полученный раствор красно-коричневого цвета используют для обработки носителя SiO2/Al, полученного по методике [Panchenko V.N., Semikolenova N.V., Danilova I.G., Paukshtis E.A., Zakharov V.A., J. Mol. Catal A: Chem. 1999, v. 142, p. 27-37].
В заполненный аргоном реактор (0.1 л), снабженный магнитной мешалкой, помещают 0.3 г носителя SiO2/Al и прибавляют 20 мл раствора комплекса LNiBr2 в хлористом метилене. Полученную суспензию перемешивают 30 мин при комнатной температуре (25°С). Твердый осадок отстаивают, бесцветный раствор декантируют. Катализатор два раза промывают хлористым метиленом порциями по 5 мл и сушат в токе аргона. Содержание никеля в полученном катализаторе определяют методом атомно-эмиссионной спектроскопии с индуктивно-связанной плазмой (АЭС ИСП).
Пример 6.
Димеризация этилена с использованием системы Ni3a/MAO
Димеризацию этилена проводят в реакторе из нержавеющей стали объемом 0.3 л, снабженным устройством для перемешивания и термостатируемой рубашкой (эксп. 3, таблица 1). В вакуумированный при 80°С и продутый этиленом реактор вносят 50 мл толуола и 1 мл раствора МАО в толуоле (концентрация МАО 1.0 моль/л). Реактор нагревают до 35°С, подают этилен до давления 2 атм. Затем вводят 0.81 мг катализатора Ni3a (2 мкмоль). Реакцию проводят при 35°С в течение 15 мин при постоянном перемешивании реакционной массы. Получают 6.44 г олигомеров этилена с селективностью 54.0% по 2-бутенам. Активность катализатора 6040 кг продуктов/(моль Ni час атм С2Н4). После завершения эксперимента охлаждают реактор до температуры 20°С, снижают давление в реакторе до атмосферного, реакционную смесь переносят из реактора в герметичную емкость и анализируют методом газовой хроматографии. Условия разделения: капиллярная колонка Silica PLOT Capillary GC Column 30 m × 0.32 mm × 4 μm или аналогичная, газ-носитель - гелий, температура испарителя 250°С, температура пламенно-ионизационного детектора 250°С, метод расчета - внутренняя нормализация. Температурная программа: 50°С в течение 3 мин, затем повышение до 80°С со скоростью 5°С/мин, 80°С в течение 5 мин, затем повышение до 230°С со скоростью 10°С/мин, 230°С в течение 10 мин (сумм. 36 мин).
Времена удерживания: tR=2.733 мин (метан, площадь пика S=0.048), tR=3.145 мин (этан, S=0.004), tR=3.309 мин (этилен, S=0.249), tR=9.407 мин (1-бутен, S=20.623), tR=10.501 мин (транс-2-бутен, S=15.111), tR=11.079 мин (цис-2-бутен, S=10.210), tR=18.579 мин (цис-2-гексен, S=0.676); tR=19.040 мин (транс-2-гексен, S=1.142), tR=19.339 мин (2-этил-1-бутен, S=2.055), tR=24.176 мин (толуол, S=564.896).
Пример 7.
Димеризация этилена с использованием системы Ni3b/MAO
Димеризацию этилена проводят в условиях примера 6, за исключением того, что в качестве катализатора используют комплекс Ni3b (0.95 мг, 2 мкмоль), устанавливают в реакторе давление этилена 1 атм (эксп. 6, таблица 1). Получают 3.75 г олигомеров этилена с селективностью 58.8% по 2-бутенам. Активность катализатора 7400 кг продуктов/(моль Ni час атм С2Н4).
Времена удерживания: tR=2.744 мин (метан, площадь пика S=0.025), tR=3.160 мин (этан, S=0.003), tR=3.324 мин (этилен, S=0.327), tR=9.450 мин (1-бутен, S=17.055), tR=10.547 мин (транс-2-бутен, S=15.049), tR=11.124 мин (цис-2-бутен, S=10.165), tR=18.592 мин (цис-2-гексен, S=0.531); tR=19.057 мин (транс-2-гексен, S=0.962), tR=19.357 мин (2-этил-1-бутен, S=1.691), tR=24.169 мин (толуол, S=814.996).
Пример 8.
Димеризация этилена с использованием системы Ni8/MAO
Димеризацию этилена проводят в условиях примера 6, за исключением того, что в качестве катализатора используют комплекс Ni8 (0.95 мг, 2 мкмоль), устанавливают в реакторе давление этилена 1 атм (эксп. 12, таблица 1). Получают 3.15 г олигомеров этилена с селективностью 60.3% по 2-бутенам. Активность катализатора 5970 кг продуктов/(моль Ni час атм С2Н4).
Времена удерживания: tR=2.745 мин (метан, площадь пика S=0.086), tR=3.155 мин (этан, S=0.006), tR=3.325 мин (этилен, S=1.045), tR=9.475 мин (1-бутен, S=14.725), tR=10.605 мин (тиранс-2-бутен, S=12.896), tR=11.173 мин (цис-2-бутен, S=9.482), tR=18.625 мин (цис-2-гексен, S=0.499), tR=19.099 мин (транс-2-гексен, S=0.499), tR=19.392 мин (2-этил-1-бутен, S=0.349), tR=24.176 мин (толуол, S=1127.435).
Пример 9:
Димеризация этилена с использованием системы Ni8/Et2AlCl
Димеризацию этилена проводят в условиях примера 6, за исключением того, что в качестве катализатора используют комплекс Ni8 в количестве 1.80 мг (4 мкмоль), в качестве сокатализатора используют раствор Et2AlCl, устанавливают в реакторе давление этилена 1 атм (эксп. 5, табл. 2). Получают 2.16 г олигомеров этилена с селективностью 96.1% по 2-бутенам. Активность катализатора 2160 кг продуктов/(моль Ni час атм С2Н4).
Времена удерживания: tR=3.185 мин (этан, S=1.159), tR=3.325 мин (этилен, S=1.045), tR=9.638 мин (1-бутен, S=1.013), tR=10.609 мин (транс-2-бутен, S=15.633), tR=11.127 мин (цис-2-бутен, S=9.58), tR=19.097 мин (транс-2-гексен, S=0.019), tR=19.417 мин (2-этил-1-бутен, S=0.933), tR=24.093 мин (толуол, S=826.305).
Пример 10.
Димеризация этилена с использованием системы Ni3b/SiO2/Al/MAO
Димеризацию этилена проводят в условиях примера 6, за исключением того, что в качестве катализатора используют нанесенный катализатор Ni3b/SiO2/Al в количестве 32.0 мг (1.9 мкмоль Ni, 0.355 вес. % Ni в нанесенном катализаторе), устанавливают в реакторе давление этилена 1 атм (эксп. 6, таблица 3). Получают 4.73 г олигомеров этилена с селективностью 57.7% по 2-бутенам. Активность катализатора 9740 кг продуктов/(моль Ni час атм С2Н4).
Времена удерживания: tR=2.727 мин (метан, площадь пика S=0.08), tR=3.157 мин (этан, S=0.004), tR=3.31 мин (этилен, S=0.333), tR=9.45 мин (1-бутен, S=13.99), tR=10.524 мин (транс-2-бутен, S=11.283), tR=11.062 мин (цис-2-бутен, S=8.277), tR=18.709 мин (цис-2-гексен, S=0.41); tR=19.129 мин (транс-2-гексен, S=0.726), tR=19.405 мин (2-этил-1-бутен, S=1.425), tR=24.102 мин (толуол, S=657.054).
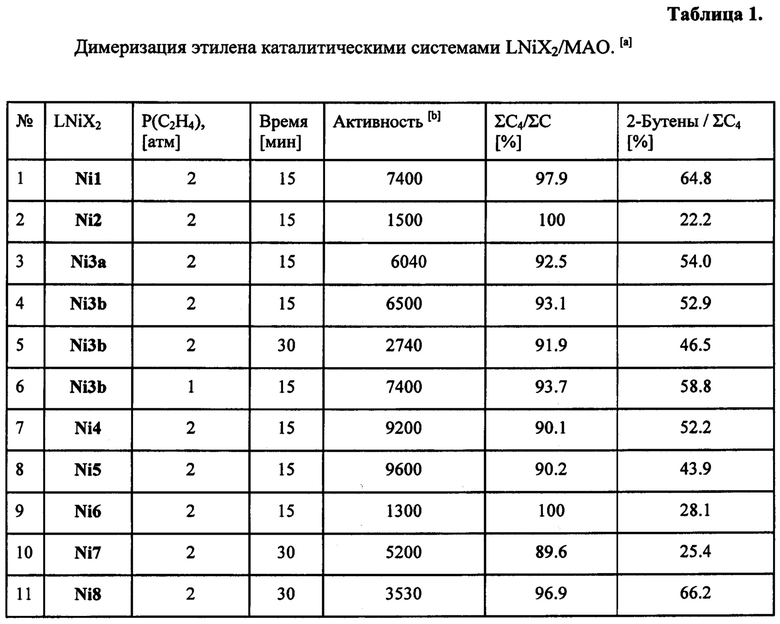
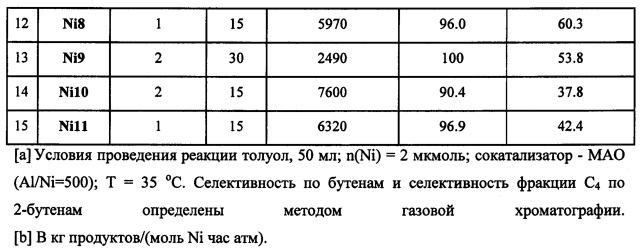
Иминопиридиновые комплексы никеля могут быть получены как из хлорида никеля(II), так и из аддукта бромида никеля(II) с диметоксиэтаном. На каталитические свойства (активность, селективность по фракции С4 и селективность фракции С4 по бутенам-2) природа галогена не оказывает заметного влияния (сравн. эксп. 3 и 4, табл. 1). Однако комплексы никеля с бромид-анионами демонстрировали более высокую растворимость в органических растворителях, что позволило нанести их на SiO2/Al из раствора в хлористом метилене.
Была установлена взаимосвязь между строением органического лиганда и каталитическими свойствами систем LNiX2/MAO. Так, введение трифторметильной группы в орто-положение ароматического кольца при иминном атоме азота приводит к увеличению каталитической активности комплексов в ди- и тримеризации этилена (сравн. эксп. 1 и 7, 2 и 8, 9 и 10 соответственно, таблица 1).
Селективность образования фракции С4 существенно зависит от размера заместителей в орто-положении ароматического кольца 2-иминопиридиновых лигандов при иминном атоме азота. Так, увеличение стерических затруднений в орто-положении приводит к образованию смеси изомеров бутена и гексена (эксп. 7, 8, 10, табл. 1), в то время как комплексы с атомами фтора в орто- и мета-положениях, а также с атомами хлора в мета-положениях позволяют получать преимущественно димеры этилена (Ni1, Ni2, Ni3a, Ni3b, Ni8, Ni9, Ni11).
Наибольшую селективность фракции C4 по 2-бутенам в присутствии сокатализатора МАО продемонстрировал катализатор на основе комплекса Ni8 (эксп. 11, таблица 1), содержащего удаленные от металлического центра атомы фтора (в мета-положениях ароматического кольца).
При замене метальной группы в шестом положении пиридинового кольца на атом брома наблюдалось снижение каталитической активности катализаторов (сравн. эксп. 2 и 9, 7 и 10, табл. 1), селективность образования фракции С4 не претерпевала заметных изменений, а селективность фракции С4 по бутенам-2 не изменялась либо снижалась. При сравнении каталитических свойств комплексов Ni4, Ni10 (с метальной группой в 6 положении пиридинового кольца) и Ni8, Ni11 (содержащих хинолиновый фрагмент) происходило заметное снижение селективности фракции С4 по 2-бутенам (сравн. эксп. 7 и 14, 12 и 15 соотв., таблица 1). По-видимому, дополнительные стерические затруднения вблизи металлического центра препятствуют повторной координации 1-бутена и его изомеризации в 2-бутен.
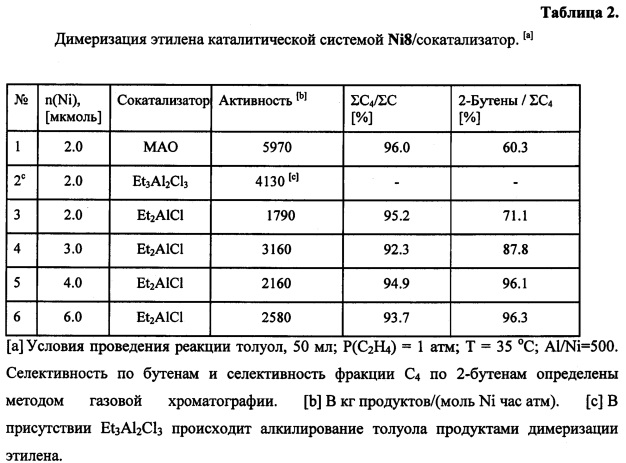
Замена сокатализатора МАО на Et2AlCl подит к снижению каталитической активности комплекса Ni8, однако при этом растет селективность фракции С4 по 2-бутенам (ср. эксп. 1 и 3, табл. 2). При испытаниях катализатора Ni8 с в присутствии сокатализатора Et2AlCl селективность фракции С4 по 2-бутенам зависит от количества помещенного в реактор никеля и достигает максимальных значений (96%) при загрузке катализатора n(Ni)=4-6 мкмоль (эксп. 5, 6, таблица 2).
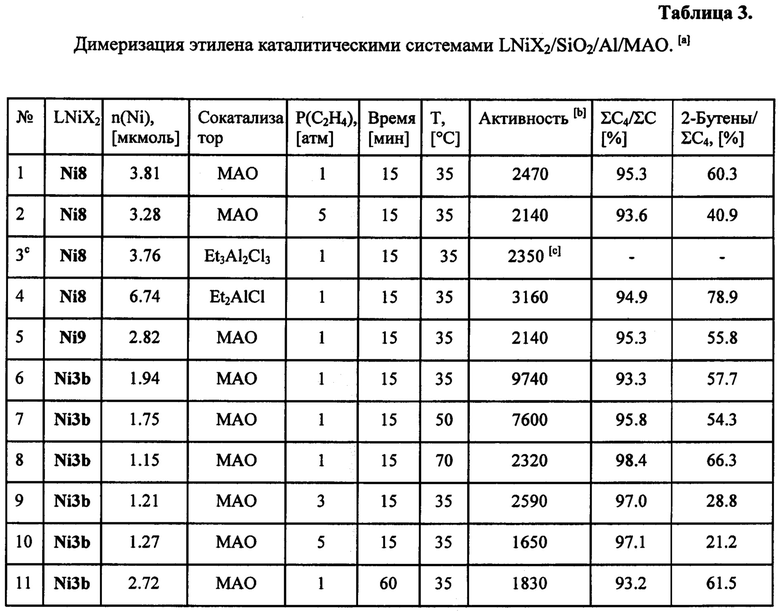
Комплексы никеля Ni3b, Ni8, Ni9, продемонстрировавшие наибольшую С4-селективность, селективность фракции С4 по 2-бутенам и высокую каталитическую активность, были нанесены на SiO2/Al, и полученные гетерогенные катализаторы были испытаны в реакции димеризации этилена (табл. 3). Для всех нанесенных катализаторов наблюдалось незначительное снижение каталитической активности с сохранением С4-селективности и селективности фракции С4 по 2-бутенам, характерных для гомогенных каталитических систем.
Было установлено, что при увеличении давления этилена (ср. эксп. 1 и 2; 8, 9 и 10, табл. 3) наблюдается незначительное уменьшение С4-селективности и значительное (на 20-40%) снижение селективности фракции С4 по 2-бутенам. Вероятно, повышение концентрации этилена в растворе может способствовать диссоциации первично образующегося продукта - 1-бутена - с каталитически активных центров за счет ускорения β-гидридного переноса, а также препятствует повторной координации 1-бутена к атому металла и его изомеризации в 2-бутен, что приводит к снижению селективности по 2-бутенам.
При повышении температуры реакции наблюдалось заметное снижение активности систем LNiX2/МАО (эксп. 6-8, табл. 3) из-за увеличения скорости дезактивации катализаторов. При этом селективность фракции С4 по 2-бутенам незначительно увеличилась (с 56 до 66%).

Таким образом, разработан новый способ димеризации этилена в бутены в присутствии гомогенных и гетерогенных каталитических систем на основе комплексов никеля(II) с 2-иминопиридиновыми лигандами, содержащими электроноакцепторные заместители в ароматическом кольце при иминном атоме азота. В сочетании с МАО, Et3Al2Cl3 и Et2AlCl данные катализаторы демонстрируют высокую активность (до 9740 кг продуктов/(моль Ni час атм)), селективность образования фракции С4 (до 100%), селективность С4 фракции по 2-бутенам (до 96%).
| название | год | авторы | номер документа |
|---|---|---|---|
| Катализатор димеризации этилена в бутены и способ его приготовления | 2018 |
|
RU2701511C1 |
| Способ получения бутенов | 1980 |
|
SU950706A1 |
| Способ получения н-бутенов | 1985 |
|
SU1356384A1 |
| Способ получения димеров олефинов С @ -С @ | 1989 |
|
SU1664779A1 |
| Катализатор для димеризации низших олефинов | 1989 |
|
SU1624763A1 |
| КАТАЛИТИЧЕСКАЯ СИСТЕМА ДЛЯ ДИМЕРИЗАЦИИ ЭТИЛЕНА И СПОСОБ ДИМЕРИЗАЦИИ ЭТИЛЕНА В 1-БУТЕН | 2005 |
|
RU2304147C2 |
| Никельорганический сигма-комплекс, каталитическая система для димеризации этилена и способ получения бутена-1 | 2021 |
|
RU2778506C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОЛЕФИНОВ С.—Cg | 1973 |
|
SU382598A1 |
| Катализатор для димеризации и олигомеризации этилена | 1988 |
|
SU1512650A1 |
| Способ получения бутена-1 | 1974 |
|
SU692822A1 |
Предложен способ получения бутенов в процессе селективной димеризации этилена с использованием высокоактивных двухкомпонентных катализаторов на основе комплексных соединений никеля(II). Процесс осуществляют в присутствии гомогенных катализаторов - комплексных соединений никеля(II), а именно используют соединения формул:

где: R1=Me; R2=F, Н, CF3; R3=F, H, Cl; R4=F, H; R5=F, H; R6=F, H, X=Cl, Br, или в присутствии гетерогенных катализаторов - вышеупомянутых комплексных соединений никеля(II), нанесенный на силикагель, модифицированный алюминием, процесс проводят в среде органического растворителя, такого как толуол, при постоянном давлении этилена и с использованием алюминийорганического сокатализатора, выбранного из МАО, Et2AlCl, Et3Al2Cl3. Технический результат - увеличение каталитической активности катализатора до 9740 кг продуктов/(моль Ni час бар), повышение селективности образования фракции С4 – до 100% повышение селективности С4 фракции по 2-бутенам – до 96% достижение упрощения технического процесса за счет загрузки гетерогенного катализатора в форме порошка, сокатализатора – в виде раствора в толуоле, увеличение растворимости катализатора за счет использования в синтезе комплексов аддукта бромида никеля с диметоксиэтаном. 3 табл., 10 пр.
Способ получения бутенов в процессе селективной димеризации этилена с использованием высокоактивных двухкомпонентных катализаторов на основе комплексных соединений никеля(II), отличающийся тем, что процесс осуществляют в присутствии гомогенных катализаторов - комплексных соединений никеля(II), а именно используют соединения формул:

где: R1=Me; R2=F, Н, CF3; R3=F, H, Cl; R4=F, H; R5=F, H; R6=F, H, X=Cl, Br, или в присутствии гетерогенных катализаторов - вышеупомянутых комплексных соединений никеля(II), нанесенный на силикагель, модифицированный алюминием, процесс проводят в среде органического растворителя, такого как толуол, при постоянном давлении этилена и с использованием алюминийорганического сокатализатора, выбранного из МАО, Et2AlCl, Et3Al2Cl3.
| Способ получения бутенов | 1980 |
|
SU950706A1 |
| Катализатор для димеризации и олигомеризации этилена | 1988 |
|
SU1512650A1 |
| Способ получения бутена-1 | 1989 |
|
SU1692976A1 |
| СПОСОБ ДИМЕРИЗАЦИИ ЭТИЛЕНА В БУТЕН-1 С ИСПОЛЬЗОВАНИЕМ КОМПОЗИЦИИ, СОДЕРЖАЩЕЙ КОМПЛЕКС ТИТАНА С АЛКОКСИ-ЛИГАНДОМ, ФУНКЦИОНАЛИЗИРОВАННЫМ ГЕТЕРОАТОМОМ | 2011 |
|
RU2570419C2 |
| CN 106673935 A, 17.05.2017 | |||
| US 20110213104 A1, 01.09.2011. | |||
Авторы
Даты
2019-11-26—Публикация
2019-04-29—Подача