ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
По настоящей заявке испрашивается приоритет на основании предварительной патентной заявки США с серийным № 62/088228, поданной 5 декабря 2014 г., полное содержание которой включено в настоящий документ посредством ссылки и по отношению к которой испрашивается приоритет.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к человеческим антителам, которые связываются с рецептором, связанным с G-белками (например, представителем D группы 5 семейства C рецепторов, связанных с G-белками (GPRC5D)), и способам их применения.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Рецепторы, связанные с G-белками, также известные как рецепторы с семью трансмембранными доменами, 7TM рецепторы, гептаспиральные рецепторы, серпантинные рецепторы и рецепторы, сопряженные с G-белками, составляют большое белковое семейство рецепторов, которые воспринимают молекулы за пределами клетки и активируют внутренние пути передачи сигнала и, в конечном итоге, клеточные ответы. Рецепторы GPCR можно разделить на шесть классов на основании гомологии последовательностей и функционального сходства: класс A (родопсин-подобные), класс B (семейство рецепторов секретина), класс C (метаботропные глутаматные рецепторы/рецепторы феромона), класс D (рецепторы феромона спаривания грибков), класс E (рецепторы циклической АМФ) и класс F (Frizzled/Smoothened).
Представитель D группы 5 семейства C рецепторов, связанных с G-белками (GPRC5D), представляет собой рецептор-сироту с неизвестными лигандами или функциями у человека. Он является членом семейства индуцируемых ретиноевой кислотой связанных с G-белками рецепторов. Он избыточно экспрессируется в клетках множественной миеломы (MM) и не экспрессируется, или экспрессируется на гораздо более низком уровне, в клетках любого другого типа, доброкачественных или злокачественных, как показано на фигуре 1. Несколько групп исследователей идентифицировали этот ген, как дифференциально экспрессируемый на высоком уровне, при профилировании экспрессии генов в клетках первичной MM по сравнению с нормальной тканью или другими злокачественными заболеваниями крови (Frigyesi, I., et al. Robust isolation of malignant plasma cells in multiple myeloma. Blood 123, 1336-1340 (2014); Cohen, Y., Gutwein, O., Garach-Jehoshua, O., Bar-Haim, A. & Kornberg, A. GPRC5D is a promising marker for monitoring the tumor load and to target multiple myeloma cells. Hematology (Amsterdam, Netherlands) 18, 348-351 (2013); Bam, R., et al. GPRC5D Is a Cell Surface Plasma Cell Marker Whose Expression Is High In Myeloma Cells and Reduced Following Coculture With Osteoclasts. Blood 122, 3099 (2013)). Показано, что более высокий уровень экспрессии мРНК коррелирует с более низкой общей выживаемостью (Atamaniuk, J., et al. Overexpression of G protein-coupled receptor 5D in the bone marrow is associated with poor prognosis in patients with multiple myeloma. European journal of clinical investigation 42, 953-960 (2012)). Поверхностное окрашивание пунктатов костного мозга от пациентов с MM показало окрашивание, специфичное для плазматических клеток (Bam, R., et al. GPRC5D Is a Cell Surface Plasma Cell Marker Whose Expression Is High In Myeloma Cells and Reduced Following Coculture With Osteoclasts. Blood 122, 3099 (2013)). Учитывая важную роль GPRC5D при множественной миеломе, существует потребность в антителах, узнающих GPRC5D, и способах применения таких средств.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к человеческим антителам, которые связываются с рецептором, связанным с G-белками (например, GPRC5D), и способам их применения.
В конкретных вариантах осуществления настоящее изобретение относится к выделенному антителу, или его антигенсвязывающему фрагменту, содержащему вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая по меньшей мере на примерно 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NOS: 1, 5, 9, 13, 17, 21, 25, 29, 33, 37, 41, 45, 49, 53, 57, 61, 65, 69, 73, 77, 81, 85, 89, 93, 274, 286, 298, 310, 322, 334, 346 и 358, при этом антитело, или его антигенсвязывающий фрагмент, специфически связывается с GPRC5D человека.
В конкретных вариантах осуществления настоящее изобретение относится к выделенному антителу, или его антигенсвязывающему фрагменту, содержащему вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая по меньшей мере на примерно 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NOS: 2, 6, 10, 14, 18, 22, 26, 30, 34, 38, 42, 46, 50, 54, 58, 62, 66, 70, 74, 78, 82, 86, 90, 94, 275, 287, 299, 311, 323, 335, 347 и 359, при этом антитело, или его антигенсвязывающий фрагмент, специфически связывается с GPRC5D человека.
В конкретных вариантах осуществления настоящее изобретение относится к выделенному антителу, или его антигенсвязывающему фрагменту, содержащему (a) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая по меньшей мере на примерно 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NOS: 1, 5, 9, 13, 17, 21, 25, 29, 33, 37, 41, 45, 49, 53, 57, 61, 65, 69, 73, 77, 81, 85, 89, 93, 274, 286, 298, 310, 322, 334, 346 и 358; и (b) вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая по меньшей мере на примерно 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NOS: 2, 6, 10, 14, 18, 22, 26, 30, 34, 38, 42, 46, 50, 54, 58, 62, 66, 70, 74, 78, 82, 86, 90, 94, 275, 287, 299, 311, 323, 335, 347 и 359, при этом антитело, или его антигенсвязывающий фрагмент, специфически связывается с GPRC5D человека.
В конкретных вариантах осуществления настоящее изобретение относится к выделенному антителу, или его антигенсвязывающему фрагменту, содержащему вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельную область тяжелой цепи и вариабельную область легкой цепи выбирают из группы, состоящей из: (i) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 1, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 2; (ii) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 5, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 6; (iii) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 9, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 10; (iv) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 13, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 14; (v) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 17, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 18; (vi) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 21, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 22; (vii) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 25, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 26; (viii) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 29, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 30; (ix) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 33, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 34; (x) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 37, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 38; (xi) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 41, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 42; (xii) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 45, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 46; (xiii) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 49, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 50; (xiv) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 53, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 54; (xv) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 57, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 58; (xvi) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 61, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 62; (xvii) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 65, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 66; (xviii) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 69, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 70; (xix) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 73, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 74; (xx) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 77, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 78; (xxi) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 81, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 82; (xxii) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 85, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 86; (xxiii) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 89, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 90; (xxiv) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 93, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 94; (xxv) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 274, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 275; (xxvi) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 286, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 287; (xxvii) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 298, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 299; (xxviii) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 310, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 311; (xxix) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 322, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 323; (xxx) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 334, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 335; (xxxi) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 346, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 347; или (xxxii) вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 358, и вариабельной области легкой цепи, содержащей аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична последовательности, приведенной в SEQ ID NO: 359, при этом антитело, или его антигенсвязывающий фрагмент, специфически связывается с GPRC5D человека.
В конкретных вариантах осуществления антитело или антигенсвязывающий фрагмент содержит: (i) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 1, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 2; (ii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 5, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 6; (iii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 9, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 10; (iv) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 13, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 14; (v) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 17, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 18; (vi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 21, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 22; (vii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 25, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 26; (viii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 29, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 30; (ix) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 33, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 34; (x) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 37, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 38; (xi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 41, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 42; (xii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 45, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 46; (xiii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 49, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 50; (xiv) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 53, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 54; (xv) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 57, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 58; (xvi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 61, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 62; (xvii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 65, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 66; (xviii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 69, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 70; (xix) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 73, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 74; (xx) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 77, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 78; (xxi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 81, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 82; (xxii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 85, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 86; (xxiii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 89, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 90; (xxiv) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 93, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 94; (xxv) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 274, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 275; (xxvi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 286, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 287; (xxvii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 298, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 299; (xxviii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 310, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 311; (xxix) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 322, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 323; (xxx) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 334, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 335; (xxxi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 346, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 347; или (xxxii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 358, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 359.
В конкретных вариантах осуществления настоящее изобретение относится к выделенному антителу, или его антигенсвязывающему фрагменту, содержащему вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 1, 5, 9, 13, 17, 21, 25, 29, 33, 37, 41, 45, 49, 53, 57, 61, 65, 69, 73, 77, 81, 85, 89, 93, 274, 286, 298, 310, 322, 334, 346 и 358, а также их консервативных модификаций, при этом антитело, или его антигенсвязывающий фрагмент, специфически связывается с GPRC5D человека.
В конкретных вариантах осуществления настоящее изобретение относится к выделенному антителу, или его антигенсвязывающему фрагменту, содержащему вариабельную область легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 2, 6, 10, 14, 18, 22, 26, 30, 34, 38, 42, 46, 50, 54, 58, 62, 66, 70, 74, 78, 82, 86, 90, 94, 275, 287, 299, 311, 323, 335, 347 и 359, а также их консервативных модификаций, при этом антитело, или его антигенсвязывающий фрагмент, специфически связывается с GPRC5D человека.
В конкретных вариантах осуществления настоящее изобретение относится к выделенному антителу, или его антигенсвязывающему фрагменту, содержащему: вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 1, 5, 9, 13, 17, 21, 25, 29, 33, 37, 41, 45, 49, 53, 57, 61, 65, 69, 73, 77, 81, 85, 89, 93, 274, 286, 298, 310, 322, 334, 346 и 358, а также их консервативных модификаций; и вариабельную область легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 2, 6, 10, 14, 18, 22, 26, 30, 34, 38, 42, 46, 50, 54, 58, 62, 66, 70, 74, 78, 82, 86, 90, 94, 275, 287, 299, 311, 323, 335, 347 и 359, а также их консервативных модификаций, при этом антитело, или его антигенсвязывающий фрагмент, специфически связывается с GPRC5D человека.
Настоящее изобретение также относится к выделенному антителу, или его антигенсвязывающему фрагменту, содержащему вариабельную область тяжелой цепи, которая содержит домены CDR1, CDR2 и CDR3; и вариабельную область легкой цепи, которая содержит домены CDR1, CDR2 и CDR3, при этом домены CDR3 вариабельной области тяжелой цепи и вариабельной области легкой цепи выбирают из группы, состоящей из:
(i) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 126, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 129, и ее консервативные модификации;
(ii) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 132, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 135, и ее консервативные модификации;
(iii) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 138, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 141, и ее консервативные модификации;
(iv) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 144, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 147, и ее консервативные модификации;
(v) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 150, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 153, и ее консервативные модификации;
(vi) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 156, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 159, и ее консервативные модификации;
(vii) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 162, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 165, и ее консервативные модификации;
(viii) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 168, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 171, и ее консервативные модификации;
(ix) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 174, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 177, и ее консервативные модификации;
(x) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 180, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 183, и ее консервативные модификации;
(xi) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 186, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 189, и ее консервативные модификации;
(xii) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 192, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 195, и ее консервативные модификации;
(xiii) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 198, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 201, и ее консервативные модификации;
(xiv) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 204, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 207, и ее консервативные модификации;
(xv) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 210, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 213, и ее консервативные модификации;
(xvi) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 216, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 219, и ее консервативные модификации;
(xvii) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 222, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 225, и ее консервативные модификации;
(xviii) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 228, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 231, и ее консервативные модификации;
(xix) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 234, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 237, и ее консервативные модификации;
(xx) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 240, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 243, и ее консервативные модификации;
(xxi) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 246, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 249, и ее консервативные модификации;
(xxii) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 252, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 255, и ее консервативные модификации;
(xxiii) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 258, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 261, и ее консервативные модификации;
(xxiv) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 264, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 267, и ее консервативные модификации;
(xxv) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 270, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 273, и ее консервативные модификации;
(xxvi) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 282, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 285, и ее консервативные модификации;
(xxvii) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 294, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 297, и ее консервативные модификации;
(xxviii) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 305, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 308, и ее консервативные модификации;
(xxix) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 318, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 321, и ее консервативные модификации;
(xxx) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 330, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 333, и ее консервативные модификации;
(xxxi) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 342, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 345, и ее консервативные модификации; и
(xxxii) CDR3 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 354, и ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 357, и ее консервативные модификации,
при этом антитело, или его антигенсвязывающий фрагмент, специфически связывается с GPRC5D.
В конкретных вариантах осуществления домены CDR2 вариабельной области тяжелой цепи и вариабельной области легкой цепи антитела, или его антигенсвязывающего фрагмента, выбирают из группы, состоящей из:
(i) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 125, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 128, и ее консервативные модификации;
(ii) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 131, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 134, и ее консервативные модификации;
(iii) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 137, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 140, и ее консервативные модификации;
(iv) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 143, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 146, и ее консервативные модификации;
(v) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 149, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 152, и ее консервативные модификации;
(vi) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 155, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 158, и ее консервативные модификации;
(vii) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 161, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 164, и ее консервативные модификации;
(viii) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 167, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 170, и ее консервативные модификации;
(ix) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 173, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 176, и ее консервативные модификации;
(x) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 179, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 182, и ее консервативные модификации;
(xi) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 185, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 188, и ее консервативные модификации;
(xii) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 191, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 194, и ее консервативные модификации;
(xiii) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 197, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 200, и ее консервативные модификации;
(xiv) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 203, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 206, и ее консервативные модификации;
(xv) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 209, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 212, и ее консервативные модификации;
(xvi) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 215, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 218, и ее консервативные модификации;
(xvii) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 221, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 224, и ее консервативные модификации;
(xviii) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 227, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 230, и ее консервативные модификации;
(xix) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 233, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 236, и ее консервативные модификации;
(xx) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 239, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 242, и ее консервативные модификации;
(xxi) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 245, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 248, и ее консервативные модификации;
(xxii) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 251, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 254, и ее консервативные модификации;
(xxiii) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 257, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 260, и ее консервативные модификации;
(xxiv) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 263, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 266, и ее консервативные модификации;
(xxv) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 269, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 272, и ее консервативные модификации;
(xxvi) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 281, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 284, и ее консервативные модификации;
(xxvii) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 293, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 296, и ее консервативные модификации;
(xxviii) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 304, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 307, и ее консервативные модификации;
(xxix) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 317, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 320, и ее консервативные модификации;
(xxx) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 329, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 332, и ее консервативные модификации;
(xxxi) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 341, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 344, и ее консервативные модификации; и
(xxxii) CDR2 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 353, и ее консервативные модификации; и CDR2 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 356, и ее консервативные модификации,
при этом антитело, или его антигенсвязывающий фрагмент, специфически связывается с GPRC5D.
В конкретных вариантах осуществления домены CDR1 вариабельной области тяжелой цепи и вариабельной области легкой цепи антитела, или его антигенсвязывающего фрагмента, выбирают из группы, состоящей из:
(i) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 124, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 127, и ее консервативные модификации;
(ii) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 130, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 133, и ее консервативные модификации;
(iii) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 136, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 139, и ее консервативные модификации;
(iv) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 142, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 145, и ее консервативные модификации;
(v) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 148, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 151, и ее консервативные модификации;
(vi) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 154, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 157, и ее консервативные модификации;
(vii) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 160, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 163, и ее консервативные модификации;
(viii) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 166, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 169, и ее консервативные модификации;
(ix) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 172, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 175, и ее консервативные модификации;
(x) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 178, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 181, и ее консервативные модификации;
(xi) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 184, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 187, и ее консервативные модификации;
(xii) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 190, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 193, и ее консервативные модификации;
(xiii) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 196, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 199, и ее консервативные модификации;
(xiv) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 202, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 205, и ее консервативные модификации;
(xv) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 208, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 211, и ее консервативные модификации;
(xvi) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 214, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 217, и ее консервативные модификации;
(xvii) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 220, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 223, и ее консервативные модификации;
(xviii) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 226, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 229, и ее консервативные модификации;
(xix) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 232, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 235, и ее консервативные модификации;
(xx) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 238, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 241, и ее консервативные модификации;
(xxi) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 244, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 247, и ее консервативные модификации;
(xxii) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 250, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 253, и ее консервативные модификации;
(xxiii) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 256, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 259, и ее консервативные модификации;
(xxiv) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 262, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 265, и ее консервативные модификации;
(xxv) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 268, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 271, и ее консервативные модификации;
(xxvi) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 280, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 283, и ее консервативные модификации;
(xxvii) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 292, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 295, и ее консервативные модификации;
(xxviii) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 303, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 306, и ее консервативные модификации;
(xxix) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 316, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 319, и ее консервативные модификации;
(xxx) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 328, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 331, и ее консервативные модификации;
(xxxi) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 340, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 343, и ее консервативные модификации; и
(xxxii) CDR1 вариабельной области тяжелой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 352, и ее консервативные модификации; и CDR1 вариабельной области легкой цепи, содержащего аминокислотную последовательность, приведенную в SEQ ID NO: 355, и ее консервативные модификации,
при этом антитело, или его антигенсвязывающий фрагмент, специфически связывается с GPRC5D.
Кроме того, настоящее изобретение относится к выделенному антителу, или его антигенсвязывающему фрагменту, содержащему:
(i) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 124; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 125; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 126;
(ii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 130; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 131; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 132;
(iii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 136; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 137; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 138;
(iv) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 142; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 143; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 144;
(v) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 148; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 149; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 150;
(vi) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 154; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 155; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 156;
(vii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 160; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 161; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 162;
(viii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 166; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 167; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 168;
(ix) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 172; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 173; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 174;
(x) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 178; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 179; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 180;
(xi) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 184; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 185; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 186;
(xii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 190; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 191; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 192;
(xiii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 196; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 197; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 198;
(xiv) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 202; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 203; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 204;
(xv) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 208; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 209; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 210;
(xvi) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 214; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 215; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 216;
(xvii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 220; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 221; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 222;
(xviii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 226; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 227; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 228;
(xix) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 232; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 233; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 234;
(xx) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 238; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 239; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 240;
(xxi) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 244; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 245; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 246;
(xxii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 250; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 251; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 252; и
(xxiii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 256; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 257; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 258;
(xxiv) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 262; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 263; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 264;
(xxv) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 268; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 269; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 270;
(xxvi) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 280; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 281; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 282;
(xxvii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 292; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 293; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 294;
(xxviii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 303; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 304; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 305;
(xxix) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 316; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 317; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 318;
(xxx) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 328; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 329; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 330;
(xxxi) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 340; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 341; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 342; или
(xxxii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 352; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 353; и CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 354;
при этом антитело, или его антигенсвязывающий фрагмент, специфически связывается с GPRC5D.
Кроме того, настоящее изобретение относится к выделенному антителу, или его антигенсвязывающему фрагменту, содержащему:
(i) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 127; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 129; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 130;
(ii) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 133; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 134; и CDR3 вариабельной области легкой цепи, содержащий SEQ ID NO: 135;
(iii) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 139; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 140; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 141;
(iv) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 145; CDR2 вариабельной области легкой цепи, содержащий SEQ ID NO: 146; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 147;
(v) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 151; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 152; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 153;
(vi) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 157; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 158; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 159;
(vii) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 163; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 164; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 165;
(viii) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 169; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 170; и CDR3 вариабельной области легкой цепи, содержащий SEQ ID NO: 171;
(ix) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 175; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 176; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 177;
(x) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 181; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 182; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 183;
(xi) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 187; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 188; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 189;
(xii) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 193; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 194; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 195;
(xiii) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 199; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 200; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 201;
(xiv) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 205; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 206; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 207;
(xv) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 211; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 212; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 213;
(xvi) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 217; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 218; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 219;
(xvii) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 223; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 224; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 225;
(xviii) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 229; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 230; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 231;
(xix) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 235; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 236; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 237;
(xx) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 241; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 242; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 243;
(xxi) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 247; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 248; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 249;
(xxii) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 253; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 254; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 255;
(xxiii) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 259; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 250; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 261; или
(xxiv) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 265; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 266; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 267;
(xxv) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 271; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 272; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 273;
(xxvi) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 283; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 284; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 285;
(xxvii) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 295; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 296; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 297;
(xxviii) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 306; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 307; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 308;
(xxix) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 319; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 320; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 321;
(xxx) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 331; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 332; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 333;
(xxxi) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 343; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 344; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 345; или
(xxxii) CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 355; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 356; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 357,
при этом антитело, или его антигенсвязывающий фрагмент, специфически связывается с GPRC5D.
Настоящее изобретение также относится к выделенному антителу, или его антигенсвязывающему фрагменту, содержащему:
(i) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 124; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 125; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 126; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 127; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 128; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 129;
(ii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 130; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 131; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 132; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 133; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 134; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 135;
(iii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 136; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 137; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 138; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 139; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 140; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 141;
(iv) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 142; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 143; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 144; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 145; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 146; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 147;
(v) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 148; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 149; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 150; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 151; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 152; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 153;
(vi) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 154; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 155; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 156; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 157; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 158; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 159;
(vii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 160; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 161; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 162; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 163; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 164; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 165;
(viii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 166; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 167; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 168; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 169; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 170; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 171;
(ix) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 172; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 173; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 174; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 175; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 176; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 177;
(x) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 178; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 179; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 180; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 181; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 182; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 183;
(xi) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 184; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 185; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 186; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 187; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 188; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 189;
(xii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 190; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 191; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 192; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 193; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 194; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 195;
(xiii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 196; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 197; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 198; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 199; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 200; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 201;
(xiv) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 202; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 203; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 204; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 205; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 206; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 207;
(xv) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 208; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 209; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 210; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 211; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 212; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 213;
(xvi) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 214; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 215; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 216; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 217; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 218; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 219;
(xvii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 220; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 221; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 222; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 223; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 224; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 225;
(xviii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 226; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 227; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 228; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 229; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 230; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 231;
(xix) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 232; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 233; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 234; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 235; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 236; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 237;
(xx) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 238; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 239; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 240; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 241; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 242; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 243;
(xxi) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 244; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 245; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 246; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 247; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 248; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 249;
(xxii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 250; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 251; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 252; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 253; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 254; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 255;
(xxiii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 256; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 257; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 258; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 259; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 260; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 261;
(xxiv) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 262; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 263; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 264; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 265; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 266; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 267;
(xxv) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 268; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 269; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 270; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 271; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 272; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 273;
(xxvi) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 280; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 281; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 282; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 283; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 284; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 285;
(xxvii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 292; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 293; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 294; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 295; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 296; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 297;
(xxviii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 303; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 304; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 305; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 306; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 307; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 308;
(xxix) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 316; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 317; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 318; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 319; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 320; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 321;
(xxx) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 328; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 329; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 330; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 331; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 332; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 333;
(xxxi) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 340; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 341; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 342; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 343; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 344; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 345; или
(xxxii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 352; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 353; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 354; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 355; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 356; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 357.
Кроме того, настоящее изобретение относится к выделенному антителу, или его антигенсвязывающему фрагменту, перекрестно конкурирующему за связывание с человеческим GPRC5D с любым из раскрытых антител. В конкретных вариантах осуществления настоящее изобретение относится к выделенному антителу, или его антигенсвязывающему фрагменту, связывающемуся с тем же эпитопом на человеческом GPRC5D, что и выделенное антитело, или его антигенсвязывающий фрагмент, из любых антител, раскрытых в настоящем документе.
В конкретных вариантах осуществления настоящее изобретение относится к выделенному антителу, или его антигенсвязывающему фрагменту, перекрестно конкурирующему за связывание с человеческим GPRC5D с эталонным антителом, или его эталонным антигенсвязывающим фрагментом, содержащим: (i) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 1, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 2; (ii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 5, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 6; (iii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 9, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 10; (iv) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 13, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 14; (v) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 17, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 18; (vi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 21, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 22; (vii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 25, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 26; (viii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 29, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 30; (ix) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 33, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 34; (x) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 37, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 38; (xi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 41, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 42; (xii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 45, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 46; (xiii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 49, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 50; (xiv) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 53, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 54; (xv) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 57, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 58; (xvi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 61, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 62; (xvii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 65, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 66; (xviii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 69, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 70; (xix) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 73, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 74; (xx) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 77, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 78; (xxi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 81, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 82; (xxii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 85, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 86; (xxiii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 89, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 90; (xxiv) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 93, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 94; (xxv) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 274, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 275; (xxvi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 286, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 287; (xxvii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 298, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 299; (xviii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 310, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 311; (xxi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 322, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 323; (xx) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 334, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 335; (xxi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 346, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 347; или (xxii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 358, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 359.
Кроме того, настоящее изобретение относится к выделенному антителу, или его антигенсвязывающему фрагменту, связывающемуся с тем же эпитопом на человеческом GPRC5D, что и эталонное антитело, или его эталонный антигенсвязывающий фрагмент, содержащее: (i) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 1, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 2; (ii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 5, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 6; (iii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 9, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 10; (iv) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 13, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 14; (v) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 17, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 18; (vi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 21, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 22; (vii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 25, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 26; (viii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 29, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 30; (ix) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 33, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 34; (x) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 37, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 38; (xi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 41, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 42; (xii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 45, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 46; (xiii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 49, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 50; (xiv) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 53, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 54; (xv) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 57, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 58; (xvi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 61, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 62; (xvii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 65, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 66; (xviii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 69, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 70; (xix) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 73, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 74; (xx) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 77, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 78; (xxi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 81, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 82; (xxii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 85, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 86; (xxiii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 89, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 90; (xxiv) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 93, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 94; (xxv) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 274, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 275; (xxvi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 286, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 287; (xxvii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 298, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 299; (xviii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 310, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 311; (xxi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 322, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 323; (xx) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 334, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 335; (xxi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 346, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 347; или (xxii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 358, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 359.
В конкретных вариантах осуществления антитела по настоящему изобретению связываются с GPRC5D, содержащим аминокислотную последовательность, приведенную в SEQ ID NO: 97. В конкретных вариантах осуществления антитела по настоящему изобретению связываются с GPRC5D человека с аффинностью связывания (Kd), составляющей от примерно 1×10-9 M до примерно 1×10-8 M.
В конкретных вариантах осуществления антитела по настоящему изобретению связываются с одной, двумя, тремя или четырьмя областями эпитопа, выбранными из группы, состоящей из области эпитопа в N-концевой области, содержащей аминокислоты 1-27 из SEQ ID NO: 97, области эпитопа в области ECL1, содержащей аминокислоты 85-93 из SEQ ID NO: 97, области эпитопа в области ECL2, содержащей аминокислоты 145-167 из SEQ ID NO: 97, и области эпитопа в области ECL3, содержащей аминокислоты 226-239 из SEQ ID NO: 97. В конкретных вариантах осуществления антитела по настоящему изобретению связываются с областью эпитопа, содержащей аминокислоты 16-23 из SEQ ID NO: 97. В конкретных вариантах осуществления антитела по настоящему изобретению связываются с областью эпитопа, содержащей аминокислоты 15-23 из SEQ ID NO: 97. В конкретных вариантах осуществления антитела по настоящему изобретению связываются с областью эпитопа, содержащей аминокислоты 16-25 из SEQ ID NO: 97. В конкретных вариантах осуществления антитела по настоящему изобретению связываются с областью эпитопа, содержащей аминокислоты 10-17 из SEQ ID NO: 97. В конкретных вариантах осуществления антитела по настоящему изобретению связываются с областью эпитопа, содержащей аминокислоты 5-17 из SEQ ID NO: 97. В конкретных вариантах осуществления антитела по настоящему изобретению связываются с областью эпитопа, содержащей аминокислоты 85-95 из SEQ ID NO: 97. В конкретных вариантах осуществления антитела по настоящему изобретению связываются с областью эпитопа, содержащей аминокислоты 157-164 из SEQ ID NO: 97. В конкретных вариантах осуществления антитела по настоящему изобретению связываются с областью эпитопа, содержащей аминокислоты 157-167 из SEQ ID NO: 97. В конкретных вариантах осуществления антитела по настоящему изобретению связываются с областью эпитопа, содержащей аминокислоты 230-237 из SEQ ID NO: 97. В конкретных вариантах осуществления антитела по настоящему изобретению связываются с областью эпитопа, содержащей аминокислоты 229-237 из SEQ ID NO: 97. В конкретных вариантах осуществления антитела по настоящему изобретению связываются с областью эпитопа, содержащей аминокислоты 230-243 из SEQ ID NO: 97. В конкретных вариантах осуществления антитела по настоящему изобретению связываются с областью эпитопа, содержащей аминокислоты 227-237 из SEQ ID NO: 97.
Настоящее изобретение также относится к выделенному антителу, или его антигенсвязывающему фрагменту, содержащему аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 100-123, 276, 288, 300, 312, 324, 336, 348 и 360.
В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит человеческую каркасную область вариабельной области антитела. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, представляет собой полностью человеческое антитело, или его антигенсвязывающий фрагмент. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, представляет собой химерное антитело, или его антигенсвязывающий фрагмент. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, представляет собой гуманизированное антитело, или его антигенсвязывающий фрагмент. В конкретных вариантах осуществления антигенсвязывающий фрагмент антитела представляет собой Fab, Fab', F(ab')2, Fv или одноцепочечный Fv (scFv) фрагмент.
Настоящее изобретение также относится к композиции, содержащей раскрытое в настоящем документе антитело, или его антигенсвязывающий фрагмент, и фармацевтически приемлемый носитель.
Кроме того, настоящее изобретение относится к иммуноконъюгату, содержащему раскрытое в настоящем документе антитело, или его антигенсвязывающий фрагмент, связанное с терапевтическим средством. В конкретных вариантах осуществления терапевтическое средство представляет собой лекарственное средство, цитотоксин или радиоактивный изотоп. Настоящее изобретение также относится к композиции, содержащей такой иммуноконъюгат и фармацевтически приемлемый носитель.
Кроме того, настоящее изобретение относится к биспецифичной молекуле, содержащей раскрытое в настоящем документе антитело, или его антигенсвязывающий фрагмент, связанное со вторым функциональным фрагментом. В конкретных вариантах осуществления второй функциональный фрагмент имеет иную специфичность связывания, чем антитело, или его антигенсвязывающий фрагмент. В конкретных вариантах осуществления второй функциональный фрагмент имеет специфичность связывания для иммунной клетки. В конкретных вариантах осуществления второй функциональный фрагмент имеет специфичность связывания для CD3.
Настоящее изобретение также относится к композиции, содержащей такую биспецифичную молекулу и фармацевтически приемлемый носитель.
Кроме того, настоящее изобретение относится к выделенной нуклеиновой кислоте, кодирующей раскрытое в настоящем документе антитело, или его антигенсвязывающий фрагмент, экспрессионному вектору, содержащему такую молекулу нуклеиновой кислоты, и клетке-хозяину, содержащей такой экспрессионный вектор.
Кроме того, настоящее изобретение относится к способу обнаружения GPRC5D в целой клетке или ткани. В конкретных вариантах осуществления способ включает: приведение в контакт клетки или ткани с раскрытым в настоящем документе антителом, или его антигенсвязывающим фрагментом, при этом указанное антитело, или его антигенсвязывающий фрагмент, содержит детектируемую метку; и определение количества меченого антитела, или его антигенсвязывающего фрагмента, связанного с указанной клеткой или тканью, путем измерения количества детектируемой метки, связанной с указанной клеткой или тканью, при этом количество связанного антитела, или его антигенсвязывающего фрагмента, является показателем количества GPRC5D в указанной клетке или ткани.
Кроме того, настоящее изобретение относится к способу лечения опухоли у субъекта. В конкретных вариантах осуществления способ включает: введение эффективного количества раскрытого в настоящем документе антитела, или его антигенсвязывающего фрагмента, субъекту, в результате чего индуцируется гибель опухолевых клеток у субъекта. В конкретных вариантах осуществления способ приводит к уменьшению количества опухолевых клеток. В конкретных вариантах осуществления способ приводит к уменьшению размера опухоли. В конкретных вариантах осуществления способ приводит к уничтожению опухоли у субъекта. В конкретных вариантах осуществления субъект является человеком.
Кроме того, настоящее изобретение относится к применению раскрытого в настоящем документе антитела, или его антигенсвязывающего фрагмента, для лечения опухоли, а также к раскрытому в настоящем документе антителу, или его антигенсвязывающему фрагменту, предназначенному для лечения опухоли у субъекта.
Кроме того, настоящее изобретение относится к набору для лечения опухоли, включающему раскрытое в настоящем документе антитело, или его антигенсвязывающий фрагмент. В конкретных вариантах осуществления набор дополнительно включает письменные инструкции по использованию антитела, или его антигенсвязывающего фрагмента, для лечения субъекта, имеющего опухоль.
В конкретных вариантах осуществления опухоль представляет собой множественную миелому или макроглобулинемию Вальденстрема. В конкретных вариантах осуществления опухоль представляет собой множественную миелому.
КРАТКОЕ ОПИСАНИЕ ФИГУР
Следующее далее подробное описание, приведенное в качестве примера, но не предназначенное для ограничения изобретения конкретными описанными вариантами осуществления, может быть понятным в сочетании с сопроводительными чертежами.
На фигуре 1 показана экспрессия GPRC5D человека в различных тканях.
На фигуре 2 проиллюстрирована технология CLIPS. Реакция CLIPS происходит между группами брома каркаса CLIPS и тиоловыми группами боковых цепей остатков цистеина. Реакция является быстрой и специфической в мягких условиях. С использованием этой элегантной химии, природные белковые последовательности превращаются в CLIPS-конструкты с целым диапазоном структур. Слева направо: две разные одиночные T2 петли, T3 двойная петля, конъюгированные T2+T3 петли, стабилизированный бета-слой и стабилизированная альфа-спираль (Timmerman et al., J. Mol. Recognit. 2007; 20: 283-29).
На фигуре 3 показан скрининг комбинаторной библиотеки CLIPS. Целевой белок (слева), содержащий прерывистый конформационный эпитоп, превращают в матричную библиотеку (центр). Комбинаторные пептиды синтезируют на запатентованной миникарте и химически преобразуют в CLIPS-конструкты с определенными пространственными структурами (справа).
На фигуре 4 представлен T3-петлевой конструкт CLIPSTM.
На фигурах 5A-5D показана технология тепловых карт. (i) Таблица комбинированных пептидов с двумя подпоследовательностями, обозначенными «Петля 1» и «Петля 2». (ii) Данные из (i) представлены в виде матрицы. (iii) Шкала цветовой индикации представленной тепловой карты. (iv) Изображение тепловой карты для данных из (i).
На фигуре 6 приведены профили интенсивности, полученные для ET150-2. Линии проведены от начального остатка до конечного остатка одного пептида на высоте, на которой был получен сигнал для этого пептида.
На фигуре 7 представлен анализ методом тепловых карт данных, полученных для ET150-5 в условиях высокой строгости.
На фигуре 8 приведены профили интенсивности, полученные для ET150-18.
На фигуре 9 приведены профили интенсивности, полученные для ET150-8.
На фигуре 10 представлено схематическое изображение GPCR, содержащего семь трансмембранных спиралей (TM) и 3 внеклеточные области (ECL). Цветными стрелками указаны сайты связывания для каждого антитела.
На фигуре 11 представлен анализ при помощи диаграммы рассеяния всех данных, полученных для каждого образца. По диагонали представлено распределение статистических данных.
На фигуре 12 представлены результаты FACS-анализа анти-GPRC5D антител.
На фигуре 13 представлены результаты FACS-анализа анти-GPRC5D антител.
На фигуре 14 представлены результаты FACS-анализа анти-GPRC5D/CD3 биспецифичных антител.
ПОДРОБНОЕ ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Все публикации, патенты и другие литературные источники, цитированные в настоящем документе, включены в настоящий документ посредством ссылки в полном объеме.
При осуществлении на практике настоящего изобретения используют множество общепринятых методов молекулярной биологии, микробиологии, клеточной биологии, биохимии и иммунологии, которые находятся в пределах компетенции специалиста в данной области. Такие методы подробно описаны в литературе, например, «Molecular Cloning: a Laboratory Manual» 3-е издание, J.F. Sambrook and D.W. Russell, ed. Cold Spring Harbor Laboratory Press 2001; «Recombinant Antibodies for Immunotherapy», Melvyn Little, ed. Cambridge University Press 2009; «Oligonucleotide Synthesis» (M. J. Gait, ed., 1984); «Animal Cell Culture» (R.I. Freshney, ed., 1987); «Methods in Enzymology» (Academic Press, Inc.); «Current Protocols in Molecular Biology» (F.M. Ausubel et al., eds., 1987, и периодические переиздания); «PCR: The Polymerase Chain Reaction», (Mullis et al., ed., 1994); «A Practical Guide to Molecular Cloning» (Perbal Bernard V., 1988); «Phage Display: A Laboratory Manual» (Barbas et al., 2001). Содержание этих и других литературных источников, содержащих стандартные протоколы, широко известные и применяемые специалистами в данной области, включая инструкции производителей, включены в настоящий документ посредством ссылки, как часть настоящего изобретения.
Определения
В приведенном ниже описании будут соблюдаться определенные соглашения в отношении использования терминологии. Как правило, термины, используемые в настоящем документе, должны быть интерпретированы в соответствии с тем значением этих терминов, которое известно специалистам в данной области.
«Антигенсвязывающий белок» представляет собой белок или полипептид, который содержит антигенсвязывающую область или антигенсвязывающую часть, то есть, обладает сильным сродством к другой молекуле, с которой он связывается. Антигенсвязывающие белки включают антитела, химерные антигенные рецепторы (CAR) и слитые белки.
Как известно в данной области, термины «антитело» и «антитела» относятся к антигенсвязывающим белкам иммунной системы. Используемый в настоящем документе термин «антитело» включает целые, полноразмерные антитела, имеющие антигенсвязывающую область, а также любой их фрагмент, в котором сохранена «антигенсвязывающая часть» или «антигенсвязывающая область», или их одиночные цепи, например, одноцепочечный вариабельный фрагмент (scFv). Природное «антитело» представляет собой гликопротеин, содержащий по меньшей мере две тяжелые (H) цепи и две легкие (L) цепи, связанные дисульфидными связями. Каждая тяжелая цепь состоит из вариабельной области тяжелой цепи (используемое в настоящем документе сокращение VH) и константной области (CH) тяжелой цепи. Константная область тяжелой цепи состоит из трех доменов, CH1, CH2 и CH3. Каждая легкая цепь состоит из вариабельной области легкой цепи (используемое в настоящем документе сокращение VL) и константной (CL) области легкой цепи. Константная область легкой цепи состоит из одного домена, CL. Области VH и VL могут быть дополнительно разделены на области гипервариабельности, называемые определяющими комплементарность областями (CDR), которые перемежаются с более консервативными, называемыми каркасными, областями (FR). Каждая VH и VL состоит из трех CDR и четырех FR, расположенных от амино-конца до карбоксильного конца в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. Вариабельные области тяжелой и легкой цепей содержат связывающий домен, который взаимодействует с антигеном. Константные области антитела могут опосредовать связывание иммуноглобулина с тканями или факторами хозяина, включая различные клетки иммунной системы (например, эффекторные клетки) и первый компонент (C1q) классической системы комплемента.
Используемый в настоящем документе термин «человеческое антитело» охватывает антитела, имеющие вариабельные области, в которых как каркасные, так и CDR, области происходят из последовательностей человеческих иммуноглобулинов зародышевой линии. Более того, если антитело содержит константную область, то константная область также происходит из последовательностей человеческих иммуноглобулинов зародышевой линии. Человеческие антитела по настоящему изобретению могут содержать аминокислотные остатки, не кодируемые последовательностями человеческих иммуноглобулинов зародышевой линии (например, мутации, внесенные путем случайного или сайт-специфического мутагенеза in vitro, или за счет соматической мутации in vivo).
Используемый в настоящем документе термин «моноклональное антитело» означает антитело, полученное из популяции по существу однородных антител, то есть, отдельные антитела, образующие популяцию, являются идентичными и/или связывают один и тот же эпитоп, за исключением возможных вариантов антител, например, содержащих природные мутации или возникающих в процессе производства препаратов моноклонального антитела; такие варианты, как правило, присутствуют в незначительных количествах. В отличие от препаратов поликлональных антител, которые, как правило, содержат разные антитела, направленные против разных детерминант (эпитопов), каждое моноклональное антитело в препарате моноклонального антитела направлено против одной детерминанты на антигене. Таким образом, определение «моноклональное» указывает на особенность этого антитела, как полученного из по существу однородной популяции антител, и его не следует воспринимать как указание на то, что антитело получено каким-либо конкретным методом. Например, моноклональные антитела, используемые в соответствии с настоящим изобретением, могут быть получены самыми разными методами, включая, но без ограничения, метод гибридом, метод рекомбинантной ДНК, методы фагового дисплея, а также методы с использованием трансгенных животных, в геноме которых присутствуют все или часть локусов человеческих иммуноглобулинов, такие методы и другие иллюстративные методы получения моноклональных антител, описаны в настоящем документе.
Используемый в настоящем документе термин «рекомбинантное человеческое антитело» охватывает все человеческие антитела, которые получены, экспрессированы, созданы или выделены рекомбинантными методами, например, (a) антитела, выделенные из организма животного (например, мыши), которое является трансгенным или трансхромосомным в отношении генов человеческих иммуноглобулинов, либо из гибридомы, полученной из его клеток (описано ниже), (b) антитела, выделенные из клетки-хозяина, трансформированной для экспрессии человеческого антитела, например, из трансфектомы, (c) антитела, выделенные из рекомбинантной комбинаторной библиотеки человеческих антител, и (d) антитела, полученные, экспрессированные, созданные или выделенные любыми другими методами, включающими сплайсинг последовательностей генов человеческих иммуноглобулинов с другими последовательностями ДНК. Такие рекомбинантные человеческие антитела имеют вариабельные области, в которых области каркаса и CDR происходят из последовательностей человеческих иммуноглобулинов зародышевой линии. Однако в конкретных вариантах осуществления такие рекомбинантные человеческие антитела могут быть подвергнуты мутагенезу in vitro (или, если используют животное, трансгенное в отношении последовательностей человеческих Ig, соматическому мутагенезу in vivo) и, следовательно, аминокислотные последовательности областей VH и VL рекомбинантных антител представляют собой последовательности, которые, хотя получены из, и родственны последовательностям человеческих VH и VL зародышевой линии, могут не существовать естественным образом в репертуаре человеческих антител зародышевой линии in vivo.
Термин «гуманизированное антитело» означает антитела, в которых последовательности CDR, полученные из антител зародышевой линии других видов млекопитающих, таких как мышь, были привиты на каркасные последовательности иммуноглобулинов человека. Внутри каркасных последовательностей иммуноглобулинов человека могут быть сделаны дополнительные модификации каркасной области.
Термин «химерное антитело» означает антитело, в котором последовательности вариабельной области происходят из иммуноглобулинов одного биологического вида, а последовательности константной области происходят из иммуноглобулинов другого биологического вида, например, антитело, в котором последовательности вариабельной области происходят из антитела мыши, а последовательности константной области происходят из человеческого антитела.
При использовании в настоящем документе, антитело, которое «специфически связывается с GPRC5D человека» означает антитело, которое связывается с GPRC5D человека с KD, составляющей 5×10-7 M или менее, 1×10-7 M или менее, 5×10-8 M или менее, 1×10-8 M или менее, 5×10-9 M или менее, 1×10-9 M или менее, 5×10-10 M или менее, или 1×10-10 M или менее.
Выражения «антитело, которое конкурирует за связывание» или «антитело, которое перекрестно конкурирует за связывание» с эталонным антителом при связывании с антигеном, например, GRPC5D, относятся к антителу, которое блокирует связывание эталонного антитела с антигеном (например, GRPC5D) в анализе конкурентного связывания на 50% или более, и наоборот, эталонное антитело блокирует связывание антитела с антигеном (например, GRPC5D) в анализе конкурентного связывания на 50% или более. Иллюстративный анализ конкурентного связывания описан в разделе «Antibodies», Harlow and Lane (Cold Spring Harbor Press, Cold Spring Harbor, NY).
Используемый в настоящем документе термин «изотип» означает класс антител (например, IgM или IgG1), который закодирован генами константной области тяжелой цепи.
Выражения «антитело, узнающее антиген» и «антитело, специфичное для антигена» в настоящем документе используют взаимозаменяемо с термином «антитело, которое специфически связывается с антигеном (например, полипептидом GPRC5D)».
Используемый в настоящем документе термин «антигенсвязывающая часть» или «антигенсвязывающая область» антитела означает область или часть антитела, которая связывается с антигеном, и которая придает антителу специфичность в отношении антигена; фрагменты антигенсвязывающих белков, например, антител, включают один или более фрагментов антитела, которые сохраняют способность специфически связываться с антигеном (например, полипептидом GPRC5D). Показано, что антигенсвязывающую функцию антитела могут выполнять фрагменты полноразмерного антитела. Примеры антигенсвязывающих фрагментов антитела, охваченных термином «фрагменты антитела», включают Fab-фрагмент, одновалентный фрагмент, состоящий из доменов VL, VH, CL и CH1; F(ab)2-фрагмент, двухвалентный фрагмент, содержащий два Fab-фрагмента, связанные дисульфидным мостом в шарнирной области; Fd-фрагмент, состоящий из доменов VH и CH1; Fv-фрагмент, состоящий из доменов VL и VH одного плеча антитела; dAb-фрагмент (Ward et al., 1989 Nature 341: 544-546), который состоит из домена VH; и выделенную определяющую комплементарность область (CDR).
Кроме того, хотя два домена Fv-фрагмента, VL и VH, закодированы разными генами, они могут быть соединены рекомбинантными методами с использованием синтетического линкера, который делает возможным их получение в виде одной белковой цепи, в которой области VL и VH спариваются, образуя одновалентные молекулы. Они известны как одноцепочечные Fv (scFv); смотри, например, Bird et al., 1988 Science 242: 423-426; и Huston et al., 1988 Proc. Natl. Acad. Sci. 85: 5879-5883. Такие фрагменты антитела получают с использованием общепринятых методов, известных специалистам в данной области, и эти фрагменты подвергают скринингу на наличие у них полезных свойств таким же образом, как и целые антитела.
«Выделенное антитело» или «выделенный антигенсвязывающий белок» представляет собой белок, который был идентифицирован и отделен и/или извлечен из компонентов его естественного окружения. «Синтетические антитела» или «рекомбинантные антитела», как правило, получают рекомбинантными методами или методами пептидного синтеза, известными специалистам в данной области.
Термины «GPRC5D» и «представитель D группы 5 семейства C рецепторов, связанных с G-белками» используются взаимозаменяемо и включают варианты, изоформы, гомологи у других биологических видов человеческого GPRC5D, а также аналоги, имеющие по меньшей мере один общий эпитоп с GPRC5D (например, GPRC5D человека). Иллюстративную последовательность GPRC5D человека можно найти в базе данных белков GenBank под регистрационным № NP_061124.1.
Используемый в настоящем документе термин «одноцепочечный вариабельный фрагмент» или «scFv» означает слитый белок из вариабельных областей тяжелой (VH) и легкой (VL) цепей иммуноглобулина (например, мыши или человека), ковалентно связанных, с образованием VH::VL гетеродимера. Вариабельные области тяжелой (VH) и легкой (VL) цепей либо связаны напрямую, либо связаны с помощью закодированного пептидного линкера (например, длиной 10, 15, 20, 25 аминокислот), который соединяет N-конец VH с C-концом VL или C-конец VH с N-концом VL. Как правило, линкер бывает богат остатками глицина для гибкости, а также остатками серина или треонина для растворимости. Линкер может связывать вариабельную область тяжелой цепи и вариабельную область легкой цепи антитела, или его антигенсвязывающего фрагмента. Неограничивающие примеры линкеров приведены в Shen et al., Anal. Chem. 80(6): 1910-1917 (2008) и WO 2014/087010, полное содержание которых включено в настоящий документ посредством ссылки. В конкретных вариантах осуществления линкер представляет собой линкер G4S.
В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 309, которая представлена ниже:
GGGGSGGGGSGGGGS [SEQ ID NO: 309].
В конкретных вариантах осуществления нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 309, приведена в SEQ ID NO: 364, которая представлена ниже:
GGTGGAGGTGGATCAGGTGGAGGTGGATCTGGTGGAGGTGGATCT [SEQ ID NO: 364].
В одном неограничивающем примере линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98, которая представлена ниже.
SRGGGGSGGGGSGGGGSLEMA [SEQ ID NO: 98].
В конкретных вариантах осуществления нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 98, приведена в SEQ ID NO: 99, которая представлена ниже:
tctagaggtggtggtggtagcggcggcggcggctctggtggtggtggatccctcgagatggcc [SEQ ID NO: 99].
В конкретных вариантах осуществления линкер содержит аминокислотную последовательность GGGGS [SEQ ID NO: 365].
В конкретных вариантах осуществления линкер содержит аминокислотную последовательность SGGSGGS [SEQ ID NO: 366].
В конкретных вариантах осуществления линкер содержит аминокислотную последовательность GGGGSGGGS [SEQ ID NO: 367].
В конкретных вариантах осуществления линкер содержит аминокислотную последовательность GGGGSGGGGS [SEQ ID NO: 368].
В конкретных вариантах осуществления линкер содержит аминокислотную последовательность GGGGSGGGGSGGGGGGGS [SEQ ID NO: 369].
В конкретных вариантах осуществления линкер содержит аминокислотную последовательность GGGGSGGGGSGGGGSGGGGS [SEQ ID NO: 370].
В конкретных вариантах осуществления линкер содержит аминокислотную последовательность GGGGSGGGGSGGGGSGGGGSGGGGS [SEQ ID NO: 371].
В конкретных вариантах осуществления линкер содержит аминокислотную последовательность GGGGSGGGGSGGGGSGGGGSGGGGSGGGGS [SEQ ID NO: 372].
В конкретных вариантах осуществления линкер содержит аминокислотную последовательность GGGGSGGGGSGGGGSGGGGSGGGGSGGGGSGGGGS [SEQ ID NO: 373].
В конкретных вариантах осуществления линкер содержит аминокислотную последовательность EPKSCDKTHTCPPCP [SEQ ID NO: 374].
В конкретных вариантах осуществления линкер содержит аминокислотную последовательность GGGGSGGGSEPKSCDKTHTCPPCP [SEQ ID NO: 375].
В конкретных вариантах осуществления линкер содержит аминокислотную последовательность ELKTPLGDTTHTCPRCPEPKSCDTPPPCPRCPEPKSCDTPPPCPRCPEPKSCDTPPPCPRCP [SEQ ID NO: 376].
В конкретных вариантах осуществления линкер содержит аминокислотную последовательность GSGSGS [SEQ ID NO: 377].
В конкретных вариантах осуществления линкер содержит аминокислотную последовательность AAA [SEQ ID NO: 378].
Несмотря на удаление константных областей и введение линкера, белки scFv сохраняют специфичность исходного иммуноглобулина. Антитела, представляющие собой одноцепочечный полипептид Fv, могут экспрессироваться с нуклеиновой кислоты, содержащей кодирующие VH и VL последовательности, как описано в Huston, et al. (Proc. Nat. Acad. Sci. USA, 85: 5879-5883, 1988). Смотри также патенты США №№ 5091513, 5132405 и 4956778; и публикации патентов США №№ 20050196754 и 20050196754. Описаны антагонистические scFv, обладающие ингибирующей активностью (смотри, например, Zhao et al., Hyrbidoma (Larchmt) 2008 27(6): 455-51; Peter et al., J Cachexia Sarcopenia Muscle 2012 August 12; Shieh et al., J Imunol 2009 183(4): 2277-85; Giomarelli et al., Thromb Haemost 2007 97(6): 955-63; Fife et al., J Clin Invst 2006 116(8): 2252-61; Brocks et al., Immunotechnology 1997 3(3): 173-84; Moosmayer et al., Ther Immunol 1995 2(10: 31-40). Описаны агонистические scFv, обладающие стимулирующей активностью (смотри, например, Peter et al., J Biol Chem 2003 25278(38): 36740-7; Xie et al., Nat Biotech 1997 15(8): 768-71; Ledbetter et al., Crit Rev Immunol1997 17(5-6): 427-55; Ho et al., BioChim Biophys Acta 2003 1638(3): 257-66).
Используемый в настоящем документе термин «F(ab)» означает фрагмент структуры антитела, который связывается с антигеном, но является одновалентным и не имеет Fc-части, например, при расщеплении антитела ферментом папаином образуются два F(ab)-фрагмента и Fc-фрагмент (например, константная область тяжелой (H) цепи; Fc-область, которая не связывается с антигеном).
Используемый в настоящем документе термин «F(ab')2» означает фрагменты антитела, получаемые при расщеплении пепсином целых IgG антител, при этом данный фрагмент имеет две антигенсвязывающие области (ab') (двухвалентные), причем каждая (ab') область содержит две отдельные аминокислотные цепи, часть H-цепи и легкая (L) цепь соединены S-S связью для связывания антигена и при этом оставшиеся части H-цепей связаны вместе. «F(ab')2»-фрагмент может быть разделен на два отдельных Fab'-фрагмента.
Используемый в настоящем документе термин «вектор» означает любой генетический элемент, такой как плазмида, фаг, транспозон, космида, хромосома, вирус, вирион и так далее, который способен к репликации, будучи связан с правильными контрольными элементами, и который может переносить последовательности генов в клетки. Таким образом, термин охватывает клонирующие и экспрессионные векторы, а также вирусные векторы и плазмидные векторы.
Используемый в настоящем документе термин «CDR» означает аминокислотные последовательности определяющей комплементарность области антитела, которые представляют собой гипервариабельные области тяжелых и легких цепей иммуноглобулинов. Смотри, например, Kabat et al., Sequences of Proteins of Immunological Interest, 4-е издание, U.S. Department of Health and Human Services, National Institutes of Health (1987). Используемый в настоящем документе термин «гипервариабельная область» или «HVR» означает каждую из областей вариабельного домена антитела, которая имеет гипервариабельную последовательность («определяющие комплементарность области» или «CDR») и/или образует петли с определенной структурой («гипервариабельные петли»), и/или содержит контактирующие с антигеном остатки («области контакта с антигеном»). Как правило, антитела содержат по три области CDR, или CDR, в вариабельных областях тяжелой цепи и легкой цепи. CDR предоставляют большинство контактирующих остатков для связывания антитела с антигеном или эпитопом.
«Выделенное антитело» представляет собой антитело, которое отделено от компонентов его естественного окружения. В конкретных вариантах осуществления антитело очищено до степени более чем 95% или 99% чистоты, что определяют, например, методом электрофореза (например, SDS-ПААГ, изоэлектрофокусирования (ИЭФ), капиллярного электрофореза) или хроматографии (например, ионообменной или обращенно-фазовой ВЭЖХ). Для получения информации о методах оценки чистоты антитела смотри, например, Flatman et al., J. Chromatogr. B 848: 79-87 (2007).
Термин «выделенная нуклеиновая кислота» относится к молекуле нуклеиновой кислоты, которая была отделена от компонентов ее естественного окружения. Выделенная нуклеиновая кислота включает молекулу нуклеиновой кислоты, содержащуюся в клетках, которые обычно содержат эту молекулу нуклеиновой кислоты, однако эта молекула нуклеиновой кислоты присутствует внехромосомно или в участке хромосомы, который отличается от участка ее естественной локализации в хромосоме.
«Выделенная нуклеиновая кислота, кодирующая антитело» (включая ссылку на конкретное антитело, например, анти-KLB антитело) означает одну или более молекул нуклеиновой кислоты, кодирующих тяжелую и легкую цепи антитела (или его фрагментов), включая такую молекулу(ы) нуклеиновой кислоты, которая находится в одном векторе, отдельных векторах, и такую молекулу(ы) нуклеиновой кислоты, которая присутствует в одном или более участках в клетке-хозяине.
Используемый в настоящем документе термин «вектор» означает молекулу нуклеиновой кислоты, способную к распространению другой нуклеиновой кислоты, с которой она связана. Термин включает вектор в виде структуры самореплицирующейся нуклеиновой кислоты, а также вектор, встроенный в геном клетки-хозяина, в которую он был введен. Некоторые векторы способны управлять экспрессией нуклеиновых кислот, с которыми они функционально связаны. В настоящем документе такие векторы называют «экспрессионными векторами».
«Иммуноконъюгат» представляет собой антитело, конъюгированное с одной или более гетерологичными молекулами, включая, но без ограничения, цитотоксическое средство.
«Эффективное количество» средства, например, анти-GPRC5D антитела, или его антигенсвязывающего фрагмента, фармацевтической композиции, содержащей его, означает количество, эффективное, в дозах и в течение периодов времени, которые необходимы, для достижения желательного терапевтического или профилактического результата, например, лечения опухоли (например, множественной миеломы).
«Индивидуум» или «субъект» является млекопитающим. Млекопитающие включают, но без ограничения, одомашненных животных (например, коров, овец, кошек, собак и лошадей), приматов (например, людей и отличных от людей приматов, таких как обезьяны), кроликов и грызунов (например, мышей и крыс). В конкретных вариантах осуществления индивидуум или субъект является человеком.
Используемый в настоящем документе термин «лечение» (и его грамматические вариации, такие как «лечить» или «лечащий») означает клиническое вмешательство в попытке изменить естественное течение заболевания у индивидуума, который получает лечение, и которое может производиться либо в профилактических целях, либо во время клинической патологии. Желательные эффекты лечения включают, но не ограничиваются ими, предотвращение возникновения или рецидива заболевания, ослабление симптомов, уменьшение любых прямых или косвенных патологических последствий заболевания, предотвращение метастазирования, снижение скорости прогрессирования заболевания, облегчение или ослабление болезненного состояния, а также достижение ремиссии или более благоприятного прогноза. В конкретных вариантах осуществления антитела по настоящему изобретению используют для отсрочки развития заболевания или для замедления прогрессирования заболевания, например, опухоли (множественной миеломы).
Используемый в настоящем документе термин «примерно» или «приблизительно» означает допустимый диапазон ошибки для конкретной величины, что может определять рядовой специалист в данной области; этот диапазон будет зависеть частично от того, каким образом величину определяют или измеряют, то есть, от ограничений системы измерения. Например, «примерно» может означать «в пределах 3 или более чем 3 стандартных отклонений», в соответствии с практикой в данной области. Альтернативно, «примерно» может означать «диапазон вплоть до 20%, предпочтительно до 10%, более предпочтительно до 5% и даже более предпочтительно до 1% от конкретной величины». Альтернативно, особенно в случае биологических систем или процессов, термин может означать «в пределах порядка величины», предпочтительно в пределах 5-кратного значения, и более предпочтительно, в пределах 2-двукратного значения величины.
При использовании в настоящем документе, любой диапазон концентраций, диапазон процентных значений, диапазон соотношений или диапазон целых чисел следует понимать, как включающий любое целое число в пределах указанного диапазона и, при необходимости, его части (например, одну десятую часть и одну сотую часть целого числа), если нет иных указаний.
Анти-GPRC5D антитела
Антитела по настоящему изобретению характеризуются конкретными функциональными особенностями или свойствами антител. Например, антитела специфически связываются с GPRC5D (например, связываются с GPRC5D человека и могут перекрестно реагировать с GPRC5D других биологических видов, таких как мышь). В конкретных вариантах осуществления антитело по настоящему изобретению связывается с GPRC5D с высокой аффинностью, например, с Kd, составляющей 1×10-7 M или менее, например, примерно 1×10-8 M или менее, примерно 1×10-9 M или менее, или примерно 1×10-10 M или менее. В конкретных вариантах осуществления раскрытое в настоящем документе анти-GPRC5D антитело связывается с GPRC5D (например, GPRC5D человека) с Kd, составляющей от примерно 1×10-10 M до примерно 1×10-7 M, например, от примерно 1×10-10 M до примерно 1×10-9 M, от примерно 1×10-9 M до примерно 1×10-8 M или от примерно 1×10-8 M до примерно 1×10-7 M. В конкретных вариантах осуществления раскрытое в настоящем документе анти-GPRC5D антитело связывается с GPRC5D (например, GPRC5D человека) с Kd, составляющей примерно 1×10-8 M или менее. В конкретных вариантах осуществления раскрытое в настоящем документе анти-GPRC5D антитело связывается с GPRC5D (например, GPRC5D человека) с Kd, составляющей от примерно 1×10-9 M до примерно 1×10-8 M. В конкретных вариантах осуществления раскрытое в настоящем документе анти-GPRC5D антитело связывается с GPRC5D (например, GPRC5D человека) с Kd, составляющей от примерно 1×10-9 M до примерно 1,5×10-9 M. В конкретных вариантах осуществления раскрытое в настоящем документе анти-GPRC5D антитело связывается с GPRC5D (например, GPRC5D человека) с Kd, составляющей примерно 1,2×10-9 M. В конкретных вариантах осуществления раскрытое в настоящем документе анти-GPRC5D антитело связывается с GPRC5D (например, GPRC5D человека) с Kd, составляющей от примерно 4×10-9 M до примерно 5×10-9 M. В конкретных вариантах осуществления раскрытое в настоящем документе анти-GPRC5D антитело связывается с GPRC5D (например, GPRC5D человека) с Kd, составляющей примерно 5×10-9 M. В конкретных вариантах осуществления раскрытое в настоящем документе анти-GPRC5D антитело связывается с GPRC5D (например, GPRC5D человека) с Kd, составляющей примерно 4,8×10-9 M. В конкретных вариантах осуществления раскрытое в настоящем документе анти-GPRC5D антитело связывается с GPRC5D (например, GPRC5D человека) с Kd, составляющей от примерно 8×10-9 M до примерно 9×10-9 M. В конкретных вариантах осуществления раскрытое в настоящем документе анти-GPRC5D антитело связывается с GPRC5D (например, GPRC5D человека) с Kd, составляющей примерно 8×10-9 M. В конкретных вариантах осуществления раскрытое в настоящем документе анти-GPRC5D антитело связывается с GPRC5D (например, GPRC5D человека) с Kd, составляющей примерно 8,1×10-9 M.
Тяжелая и легкая цепи антитела по настоящему изобретению могут быть полноразмерными (например, антитело может содержать по меньшей мере одну (например, одну или две) полную тяжелую цепь и по меньшей мере одну (например, одну или две) полную легкую цепь) или могут содержать антигенсвязывающую часть (Fab, F(ab')2, Fv или одноцепочечный Fv-фрагмент («scFv»)). В конкретных вариантах осуществления константную область тяжелой цепи антитела выбирают из, например, IgG1, IgG2, IgG3, IgG4, IgM, IgA1, IgA2, IgD и IgE, в частности, выбирают из, например, IgG1, IgG2, IgG3 и IgG4, более конкретно, IgG1 (например, IgG1 человека). В другом варианте осуществления константную область легкой цепи антитела выбирают из, например, каппа или лямбда, в частности, каппа.
1. Одноцепочечные вариабельные фрагменты (scFv)
В конкретных вариантах осуществления настоящее изобретение охватывает антитела, которые содержат последовательность scFv, слитую с одним или более константными доменами, с образованием антитела с Fc-областью человеческого иммуноглобулина, для получения двухвалентного белка, что повышает общую авидность и стабильность антитела. Кроме того, Fc-фрагмент делает возможной прямую конъюгацию других молекул, включая, но без ограничения, флуоресцентные красители, цитотоксины, радиоизотопы и так далее, с антителом, например, для использования в количественном определении антигена, иммобилизации антитела для определения аффинности, для направленной доставки терапевтического средства, для тестирования на Fc-опосредованную цитотоксичность с использованием иммунных эффекторных клеток и для многих других вариантов применения.
Представленные в настоящем документе результаты подчеркивают специфичность, чувствительность и полезность антител по изобретению при таргетировании полипептида GRPC5D.
Молекулы по изобретению получены в результате идентификации и выбора с использованием фагового дисплея одноцепочечных вариабельных фрагментов (scFv), аминокислотная последовательность которых придает молекулам специфичность в отношении интересующего полипептида GRPC5D и создает основу для всех антигенсвязывающих белков по изобретению. Таким образом, scFv можно использовать для конструирования множества различных молекул «антител», включая, например, полноразмерные антитела, их фрагменты, такие как Fab и F(ab')2, минитела, слитые белки, в том числе слитые белки scFv-Fc, мультивалентные антитела, то есть, антитела, которые имеют более одной специфичности для одного и того же антигена или разных антигенов, например, биспецифичные антитела, триотела и так далее (смотри Cuesta et al., Multivalent antibodies: when design surpasses evolution. Trends in Biotechnology 28: 355-362 2010).
В конкретных вариантах осуществления антигенсвязывающий белок представляет собой полноразмерное антитело, тяжелая и легкая цепи антитела по настоящему изобретению могут быть полноразмерными (например, антитело может содержать по меньшей мере одну, и предпочтительно две полные тяжелые цепи, и по меньшей мере одну, и предпочтительно две полные легкие цепи), или может содержать антигенсвязывающую часть (Fab, F(ab')2, Fv или одноцепочечный Fv-фрагмент («scFv»)). В конкретных вариантах осуществления константную область тяжелой цепи антитела выбирают из, например, IgG1, IgG2, IgG3, IgG4, IgM, IgA1, IgA2, IgD и IgE. В конкретных вариантах осуществления изотип иммуноглобулина выбирают из IgG1, IgG2, IgG3 и IgG4, более конкретно, IgG1 (например, IgG1 человека). Выбор изотипа антитела может зависеть от иммунной эффекторной функции, которую антитело предназначено выполнять.
Для конструирования рекомбинантного иммуноглобулина, соответствующие аминокислотные последовательности константных областей различных изотипов иммуноглобулина и способы получения широкого спектра антител известны специалистам в данной области.
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 100 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97, которая представлена ниже, или ее фрагменты).
MYKDCIESTGDYFLLCDAEGPWGIILESLAILGIVVTILLLLAFLFLMRKIQDCSQWNVLPTQLLFLLSVLGLFGLAFAFIIELNQQTAPVRYFLFGVLFALCFSCLLAHASNLVKLVRGCVSFSWTTILCIAIGCSLLQIIIATEYVTLIMTRGMMFVNMTPCQLNVDFVVLLVYVLFLMALTFFVSKATFCGPCENWKQHGRLIFITVLFSIIIWVVWISMLLRGNPQFQRQPQWDDPVVCIALVTNAWVFLLLYIVPELCILYRSCRQECPLQGNACPVTAYQHSFQVENQELSRARDSDGAEEDVALTSYGTPIQPQTVDPTQECFIPQAKLSPQQDAGGV [SEQ ID NO: 97]
N-концевая область GPRC5D человека содержит аминокислоты 1-27 из SEQ ID NO: 97. Область внеклеточной петли 1 (ECL1) GPRC5D человека содержит аминокислоты 85-93 из SEQ ID NO: 97. Область внеклеточной петли 2 (ECL2) GPRC5D человека содержит аминокислоты 145-167 из SEQ ID NO: 97. Область внеклеточной петли 3 (ECL3) GPRC5D человека содержит аминокислоты 226-239 из SEQ ID NO: 97.
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 100 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-153 scFv (другое название «ET150-3 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 1, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 2, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 1. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 1, смотри таблицу 1. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 2, смотри таблицу 1. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 1, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 2, смотри таблицу 1. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 124, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 125, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 126, или ее консервативные модификации, смотри таблицу 1. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 127, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 128, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 129, или ее консервативные модификации, смотри таблицу 1. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 124, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 125, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 126, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 127, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 128, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 129, или ее консервативные модификации, смотри таблицу 1. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 124, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 125, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 126, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 127, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 128, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 129.
Таблица 1
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 101 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-166 scFv (другое название «ET150-16 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 5, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 6, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 2. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 5, смотри таблицу 2. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 6, смотри таблицу 2. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 5, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 6, смотри таблицу 2. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 130, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 131, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 132, или ее консервативные модификации, смотри таблицу 2. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 133, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 134, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 135, или ее консервативные модификации, смотри таблицу 2. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 130, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 131, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 132, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 133, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 134, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 135, или ее консервативные модификации, смотри таблицу 2. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 130, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 131, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 132, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 133, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 134, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 135.
Таблица 2
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 102 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-170 scFv (другое название «ET150-20 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 9, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 10, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 3. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 9, смотри таблицу 3. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 10, смотри таблицу 3. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 9, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 10, смотри таблицу 3. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 136, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 137, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 138, или ее консервативные модификации, смотри таблицу 3. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 139, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 140, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 141, или ее консервативные модификации, смотри таблицу 3. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 136, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 137, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 138, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 139, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 140, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 141, или ее консервативные модификации, смотри таблицу 3. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 136, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 137, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 138, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 139, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 140, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 141.
Таблица 3
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 103 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-171 scFv (другое название «ET150-21 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 13, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 14, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 4. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 13, смотри таблицу 4. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 14, смотри таблицу 4. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 13, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 14, смотри таблицу 4. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 142, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 143, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 144, или ее консервативные модификации, смотри таблицу 4. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 145, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 146, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 147, или ее консервативные модификации, смотри таблицу 4. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 142, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 143, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 144, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 145, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 146, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 147, или ее консервативные модификации, смотри таблицу 4. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 142, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 143, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 144, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 145, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 146, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 147.
Таблица 4
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 104 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-175 scFv (другое название «ET150-25 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 17, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 18, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 5. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 17, смотри таблицу 5. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 18, смотри таблицу 5. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 17, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 18, смотри таблицу 5. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 148, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 149, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в0 SEQ ID NO: 150, или ее консервативные модификации, смотри таблицу 5. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 151, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 152, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 153, или ее консервативные модификации, смотри таблицу 5. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 148, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 149, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 150, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 151, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 152, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 153, или ее консервативные модификации, смотри таблицу 5. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 148, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 149, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 150, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 151, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 152, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 153.
Таблица 5
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 105 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-154 scFv (другое название «ET150-4 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 21, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 22, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 6. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 21, смотри таблицу 6. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 22, смотри таблицу 6. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 21, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 22, смотри таблицу 6. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 154, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 155, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 156, или ее консервативные модификации, смотри таблицу 6. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 157, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 158, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 159, или ее консервативные модификации, смотри таблицу 6. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 154, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 155, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 156 или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 157, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 158, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 159, или ее консервативные модификации, смотри таблицу 6. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 154, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 155, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 156, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 157, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 158, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 159.
Таблица 6
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 106 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-156 scFv (другое название «ET150-6 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 25, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 26, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 7. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 25, смотри таблицу 7. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 26, смотри таблицу 7. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 25, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 26, смотри таблицу 7. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 160, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 161, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 162, или ее консервативные модификации, смотри таблицу 7. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 163, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 164, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 165, или ее консервативные модификации, смотри таблицу 7. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 160, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 161, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 162, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 163, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 164, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 165, или ее консервативные модификации, смотри таблицу 7. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 160, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 161, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 162, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 163, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 164, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 165.
Таблица 7
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 107 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-157 scFv (другое название «ET150-7 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 29, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 30, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 8. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 29, смотри таблицу 8. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 30, смотри таблицу 8. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 29, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 30, смотри таблицу 8. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 166, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 167, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 168, или ее консервативные модификации, смотри таблицу 8. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 169, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 170, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 171, или ее консервативные модификации, смотри таблицу 8. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 166, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 167, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 168, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 169, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 170, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 171, или ее консервативные модификации, смотри таблицу 8. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 166, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 167, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 168, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 169, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 170, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 171.
Таблица 8
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 108 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-159 scFv (другое название «ET150-9 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 33, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 34, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 9. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 33, смотри таблицу 9. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 34, смотри таблицу 9. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 33, и VL содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 34, смотри таблицу 9. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 172, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 173, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 174, или ее консервативные модификации, смотри таблицу 9. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 175, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 176, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 177, или ее консервативные модификации, смотри таблицу 9. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 172, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 173, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 174, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 175, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 176, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 177, или ее консервативные модификации, смотри таблицу 9. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 172, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 173, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 174, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 175, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 176, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 177.
Таблица 9
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 109 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-160 scFv (другое название «ET150-10 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 37, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 38, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 10. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 37, смотри таблицу 10. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 38, смотри таблицу 10. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 37, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 38, смотри таблицу 10. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 178, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 179, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 180, или ее консервативные модификации, смотри таблицу 10. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 181, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 182, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 183, или ее консервативные модификации, смотри таблицу 10. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 178, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 179, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 180, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 181, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 182, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 183, или ее консервативные модификации, смотри таблицу 10. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 178, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 179, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 180, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 181, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 182, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 183.
Таблица 10
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 110 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-161 scFv (другое название «ET150-11 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 41, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 42, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 11. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 41, смотри таблицу 11. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 42, смотри таблицу 11. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 41, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 42, смотри таблицу 11. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 184, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 185, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 186, или ее консервативные модификации, смотри таблицу 11. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 187, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 188, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 189, или ее консервативные модификации, смотри таблицу 11. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 184, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 185, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 186, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 187, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 188, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 189 или ее консервативные модификации, смотри таблицу 11. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 184, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 185, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 186, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 187, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 188, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 189.
Таблица 11
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 111 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-162 scFv (другое название «ET150-12 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 45, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 46, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 12. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 45, смотри таблицу 12. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 46, смотри таблицу 12. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 45, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 46, смотри таблицу 12. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 190, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 191, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 192, или ее консервативные модификации, смотри таблицу 12. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 193, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 194, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 195, или ее консервативные модификации, смотри таблицу 12. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 190, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 191, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 192, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 193, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 194, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 195, или ее консервативные модификации, смотри таблицу 12. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 190, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 191, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 192, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 193, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 194, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 195.
Таблица 12
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 112 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-163 scFv (другое название «ET150-13 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 49, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 50, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 13. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 49, смотри таблицу 13. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 50, смотри таблицу 13. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 49, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 50, смотри таблицу 13. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 196, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 197, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 198, или ее консервативные модификации, смотри таблицу 13. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 199, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 200, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 201, или ее консервативные модификации, смотри таблицу 13. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 196, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 197, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 198, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 199, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 200, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 201, или ее консервативные модификации, смотри таблицу 13. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 196, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 197, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 198, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 199, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 200, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 201.
Таблица 13
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 113 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-151 scFv (другое название «ET150-1 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 53, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 54, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 14. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 53, смотри таблицу 14. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 54, смотри таблицу 14. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 53, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 54, смотри таблицу 14. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 202, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 203, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 204, или ее консервативные модификации, смотри таблицу 14. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 205, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 206, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 207, или ее консервативные модификации, смотри таблицу 14. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 202, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 203, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 204, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 205, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 206, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 207, или ее консервативные модификации, смотри таблицу 14. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 202, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 203, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 204, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 205, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 206, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 207.
Таблица 14
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 114 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-152 scFv (другое название «ET150-2 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 57, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 58, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 15. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 57, смотри таблицу 15. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 58, смотри таблицу 15. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 57, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 58, смотри таблицу 15. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 208, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 209, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 210, или ее консервативные модификации, смотри таблицу 15. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 211, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 212, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 213, или ее консервативные модификации, смотри таблицу 15. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 208, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 209, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 210, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 211, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 212, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 213, или ее консервативные модификации, смотри таблицу 15. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 208, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 209, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 210, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 211, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 212, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 213.
Таблица 15
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 115 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-155 scFv (другое название «ET150-5 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 61, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 62, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 16. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 61, смотри таблицу 16. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 62, смотри таблицу 16. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 61, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 62, смотри таблицу 16. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 214, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 215, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 216, или ее консервативные модификации, смотри таблицу 16. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 217, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 218, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 219, или ее консервативные модификации, смотри таблицу 16. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 214, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 215, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 216, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 217, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 218, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 219, или ее консервативные модификации, смотри таблицу 16. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 214, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 215, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 216, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 217, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 218, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 219.
Таблица 16
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 116 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-158 scFv (другое название «ET150-8 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 65, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 66, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 17. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 65, смотри таблицу 17. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 66, смотри таблицу 17. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 65, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 66, смотри таблицу 17. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 220, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 221, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 222, или ее консервативные модификации, смотри таблицу 17. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 223, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 224, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 225, или ее консервативные модификации, смотри таблицу 17. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 220, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 221, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 222, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 223, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 224, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 225, или ее консервативные модификации, смотри таблицу 17. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 220, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 221, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 222, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 223, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 224, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 225.
Таблица 17
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 117 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-168 scFv (другое название «ET150-18 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 69, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 70, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 18. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 69, смотри таблицу 18. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 70, смотри таблицу 18. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 69, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 70, смотри таблицу 18. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 226, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 227, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 228, или ее консервативные модификации, смотри таблицу 18. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 229, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 230, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 231, или ее консервативные модификации, смотри таблицу 18. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 226, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 227, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 228, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 229, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 230, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 231, или ее консервативные модификации, смотри таблицу 18. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 226, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 227, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 228, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 229, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 230, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 231.
Таблица 18
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 118 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-164 scFv (другое название «ET150-14 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 73, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 74, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 19. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 73, смотри таблицу 19. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 74, смотри таблицу 19. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 73, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 74, смотри таблицу 19. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 232, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 233, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 234, или ее консервативные модификации, смотри таблицу 19. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 235, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 236, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 237, или ее консервативные модификации, смотри таблицу 19. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 232, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 233, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 234, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 235, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 236, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 237, или ее консервативные модификации, смотри таблицу 19. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 232, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 233, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 234, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 235, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 236, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 237.
Таблица 19
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 119 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-165 scFv (другое название «ET150-15 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 77, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 78, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 20. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 77, смотри таблицу 20. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 78, смотри таблицу 20. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 77, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 78, смотри таблицу 20. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 238, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 239, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 240, или ее консервативные модификации, смотри таблицу 20. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 241, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 242, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 243, или ее консервативные модификации, смотри таблицу 20. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 238, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 239, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 240, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 241, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 242, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 243, или ее консервативные модификации, смотри таблицу 20. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 238, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 239, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 240, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 241, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 242, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 243.
Таблица 20
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 120 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-167 scFv (другое название «ET150-17 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 81, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 82, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 21. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 81, смотри таблицу 21. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 82, смотри таблицу 21. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 81, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 82, смотри таблицу 21. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 244, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 245, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 246, или ее консервативные модификации, смотри таблицу 21. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 247, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 248, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 249, или ее консервативные модификации, смотри таблицу 21. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 244, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 245, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 246, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 247, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 248, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 249, или ее консервативные модификации, смотри таблицу 21. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 244, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 245, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 246, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 247, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 248, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 249.
Таблица 21
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 121 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-169 scFv (другое название «ET150-19 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 85, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 86, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 22. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 85, смотри таблицу 22. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 86, смотри таблицу 22. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 85, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 86, смотри таблицу 22. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 250, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 251, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 252, или ее консервативные модификации, смотри таблицу 22. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 253, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 254, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 255, или ее консервативные модификации, смотри таблицу 22. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 250, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 251, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 252, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 253, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 254, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 255, или ее консервативные модификации, смотри таблицу 22. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 250, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 251, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 252, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 253, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 254, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 255.
Таблица 22
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 122 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-172 scFv (другое название «ET150-22 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 89, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 90, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 23. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 89, смотри таблицу 23. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 90, смотри таблицу 23. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 89, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 90, смотри таблицу 23. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 256, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 257, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 258, или ее консервативные модификации, смотри таблицу 23. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 259, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 260, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 261, или ее консервативные модификации, смотри таблицу 23. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 256, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 257, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 258, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 259, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 260, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 261, или ее консервативные модификации, смотри таблицу 23. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 256, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 257, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 258, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 259, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 260, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 261.
Таблица 23
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 123 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-173 scFv (другое название «ET150-23 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 93, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 94, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 24. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 93, смотри таблицу 24. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 94, смотри таблицу 24. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 93, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 94, смотри таблицу 24. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 262, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 263, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 264, или ее консервативные модификации, смотри таблицу 24. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 265, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 266, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 267, или ее консервативные модификации, смотри таблицу 24. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 262, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 263, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 264, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 265, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 266, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 267, или ее консервативные модификации, смотри таблицу 24. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 262, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 263, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 264, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 265, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 266, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 267.
Таблица 24
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 276 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-024 scFv (другое название «ET150-174 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 274, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 275, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 25. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 274, смотри таблицу 25. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 275, смотри таблицу 25. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 274, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 275, смотри таблицу 25. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 268, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 269, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 270, или ее консервативные модификации, смотри таблицу 25. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 271, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 272, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 273, или ее консервативные модификации, смотри таблицу 25. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 268, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 269, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 270, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 271, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 272, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 273, или ее консервативные модификации, смотри таблицу 25. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 268, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 269, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 270, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 271, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 272, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 273.
Таблица 25
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 288 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-026 scFv (другое название «ET150-176 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 286, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 287, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 26. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 286, смотри таблицу 26. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 287, смотри таблицу 26. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 286, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 287, смотри таблицу 26. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 280, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 281, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 282, или ее консервативные модификации, смотри таблицу 26. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 283, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 284, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 285, или ее консервативные модификации, смотри таблицу 26. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 280, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 281, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 282, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 283, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 284, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 285, или ее консервативные модификации, смотри таблицу 26. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 280, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 281, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 282, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 283, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 284, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 285.
Таблица 26
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 300 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-028 scFv (другое название «ET150-178 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 298, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 299, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 27. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 298, смотри таблицу 27. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 299, смотри таблицу 27. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 298, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 299, смотри таблицу 27. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 292, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 293, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 294, или ее консервативные модификации, смотри таблицу 27. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 295, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 296, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 297, или ее консервативные модификации, смотри таблицу 27. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 292, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 293, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 294, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 295, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 296, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 297, или ее консервативные модификации, смотри таблицу 27. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 292, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 293, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 294, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 295, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 296, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 297.
Таблица 27
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 312 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-029 scFv (другое название «ET150-179 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 310, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 311, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 28. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 310, смотри таблицу 28. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 311, смотри таблицу 28. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 310, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 311, смотри таблицу 28. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 303, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 304, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 305, или ее консервативные модификации, смотри таблицу 28. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 306, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 307, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 308, или ее консервативные модификации, смотри таблицу 28. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 303, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 304, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 305, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 306, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 307, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 308, или ее консервативные модификации, смотри таблицу 28. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 303, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 304, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 305, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 306, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 307, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 308.
Таблица 28
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 324 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-030 scFv (другое название «ET150-180 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 322, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 323, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 29. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 322, смотри таблицу 29. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 323, смотри таблицу 29. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 322, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 323, смотри таблицу 29. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 316, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 317, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 318, или ее консервативные модификации, смотри таблицу 29. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 319, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 320, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 321, или ее консервативные модификации, смотри таблицу 29. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 316, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 317, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 318, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 319, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 320, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 321, или ее консервативные модификации, смотри таблицу 29. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 316, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 317, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 318, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 319, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 320, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 321.
Таблица 29
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 336 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-031 scFv (другое название «ET150-181 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 334, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 335, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 30. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 334, смотри таблицу 30. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 335, смотри таблицу 30. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 334, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 335, смотри таблицу 30. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 328, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 329, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 330, или ее консервативные модификации, смотри таблицу 30. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 331, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 332, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 333, или ее консервативные модификации, смотри таблицу 30. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 328, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 329, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 330, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 331, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 332, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 333, или ее консервативные модификации, смотри таблицу 30. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 328, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 329, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 330, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 331, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 332, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 333.
Таблица 30
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 348 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-032 scFv (другое название «ET150-182 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 346, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 347, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 31. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 346, смотри таблицу 31. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 347, смотри таблицу 31. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 346, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 347, смотри таблицу 31. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 340, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 341, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 342, или ее консервативные модификации, смотри таблицу 31. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 343, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 344, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 345, или ее консервативные модификации, смотри таблицу 31. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 340, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 341, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 342, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 343, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 344, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 345, или ее консервативные модификации, смотри таблицу 31. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 340, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 341, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 342, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 343, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 344, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 345.
Таблица 31
В конкретных вариантах осуществления антитело или другой антигенсвязывающий белок представляет собой анти-GPRC5D scFv, или его антигенсвязывающий фрагмент, имеющий антигенсвязывающую область, которая содержит аминокислотную последовательность SEQ ID NO: 360 и специфически связывается с полипептидом GPRC5D (например, полипептидом GPRC5D, содержащим аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты), обозначенный ET150-033 scFv (другое название «ET150-183 scFv»).
В конкретных вариантах осуществления анти-GPRC5D scFv антитело содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 358, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 359, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления анти-GPRC5D scFv антитело представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 32. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 358, смотри таблицу 32. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 359, смотри таблицу 32. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 358, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 359, смотри таблицу 32. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 352, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 353, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 354, или ее консервативные модификации, смотри таблицу 32. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 355, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 356, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 357, или ее консервативные модификации, смотри таблицу 32. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 352, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 353, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 354, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 355, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 356, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 357, или ее консервативные модификации, смотри таблицу 32. В конкретных вариантах осуществления анти-GPRC5D scFv содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 352, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 353, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 354, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 355, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 356, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 357.
Таблица 32
Настоящее изобретение также относится к анти-GPRC5D scFv антителам, содержащим вариабельную область тяжелой цепи, вариабельную область легкой цепи, пептидный линкер между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи, а также His-метку и HA-метку. В конкретных вариантах осуществления аминокислотная последовательность His-метки и HA-метки содержит аминокислотную последовательность SEQ ID NO: 379, которая представлена ниже:
TSGQAGQHHHHHHGAYPYDVPDYAS [SEQ ID NO: 379]
Нуклеотидная последовательность, кодирующая SEQ ID NO: 379, соответствует SEQ ID NO: 380, которая представлена ниже:
ACTAGTGGCCAGGCCGGCCAGCACCATCACCATCACCATGGCGCATACCCGTACGACGTTCCGGACTACGCTTCT [SEQ ID NO: 380].
2. Моноклональные антитела
Настоящее изобретение относится к человеческим антителам (например, человеческим моноклональным антителам), которые специфически связываются с GPRC5D (например, GPRC5D человека), и которые выделены и структурно охарактеризованы, как описано в примере 2. Аминокислотные последовательности VH человеческих анти-GPRC5D антител ET150-153, ET150-166, ET150-170, ET150-171, ET150-175, ET150-154, ET150-156, ET150-157, ET150-159, ET150-160, ET150-161, ET150-162, ET150-163, ET150-151, ET150-152, ET150-155, ET150-158, ET150-168, ET150-165, ET150-167, ET150-169, ET150-172, ET150-173, ET150-024, ET150-026, ET150-028, ET150-029, ET150-030, ET150-031, ET150-032 и ET150-033 приведены в SEQ ID NOs: 1, 5, 9, 13, 17, 21, 25, 29, 33, 37, 41, 45, 49, 53, 57, 61, 65, 69, 73, 77, 81, 85, 89, 93, 274, 286, 298, 310, 322, 334, 346 и 358, соответственно. Аминокислотные последовательности VL из ET150-153, ET150-166, ET150-170, ET150-171, ET150-175, ET150-154, ET150-156, ET150-157, ET150-159, ET150-160, ET150-161, ET150-162, ET150-163, ET150-151, ET150-152, ET150-155, ET150-158, ET150-168, ET150-165, ET150-167, ET150-169, ET150-172, ET150-173, ET150-024, ET150-026, ET150-028, ET150-029, ET150-030, ET150-031, ET150-032 и ET150-033 приведены в SEQ ID NOs: 2, 6, 10, 14, 18, 22, 26, 30, 34, 38, 42, 46, 50, 54, 58, 62, 66, 70, 74, 78, 82, 86, 90, 94, 275, 287, 299, 311, 323, 335, 347 и 359, соответственно.
Учитывая, что каждое из антител ET150-153, ET150-166, ET150-170, ET150-171, ET150-175, ET150-154, ET150-156, ET150-157, ET150-159, ET150-160, ET150-161, ET150-162, ET150-163, ET150-151, ET150-152, ET150-155, ET150-158, ET150-168, ET150-165, ET150-167, ET150-169, ET150-172, ET150-173, ET150-024, ET150-026, ET150-028, ET150-029, ET150-030, ET150-031, ET150-032 и ET150-033 может связываться с GPRC5D, последовательности VH и VL можно «комбинировать» для создания других анти-GPRC5D связывающих молекул. Связывание GPRC5D с такими «комбинированными» антителами можно тестировать в анализах связывания, известных в данной области, включая, например, анализы ELISA, вестерн-блоттинг, RIA, Biacore. Предпочтительно, когда цепи VH и VL комбинируют, то последовательность VH из конкретной пары VH/VL заменяют структурно сходной последовательностью VH. Аналогично, последовательность VL из конкретной пары VH/VL заменяют структурно сходной последовательностью VL.
В конкретных вариантах осуществления настоящее изобретение относится к выделенному антителу, или его антигенсвязывающему фрагменту, содержащему: (i) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOs: 1, 5, 9, 13, 17, 21, 25, 29, 33, 37, 41, 45, 49, 53, 57, 61, 65, 69, 73, 77, 81, 85, 89, 93, 274, 286, 298, 310, 322, 334, 346 и 358; и (ii) вариабельную область легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOs: 2, 6, 10, 14, 18, 22, 26, 30, 34, 38, 42, 46, 50, 54, 58, 62, 66, 70, 74, 78, 82, 86, 90, 94, 275, 287, 299, 311, 323, 335, 347 и 359; при этом антитело специфически связывает GPRC5D, например, GPRC5D человека.
Предпочтительные комбинации тяжелой и легкой цепей включают:
(i) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 1, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 2; или
(ii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 5, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 6;
(iii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 9, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 10;
(iv) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 13, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 14;
(v) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 17, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 18;
(vi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 21, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 22;
(vii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 25, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 26;
(viii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 29, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 30;
(ix) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 33, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 34;
(x) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 37, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 38;
(xi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 41, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 42;
(xii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 45, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 46;
(xiii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 49, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 50;
(xiv) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 53, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 54;
(xv) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 57, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 58;
(xvi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 61, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 62;
(xvii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 65, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 66;
(xviii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 69, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 70;
(xix) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 73, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 74;
(xx) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 77, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 78;
(xxi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 81, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 82;
(xxii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 85, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 86;
(xxiii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 89, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 90;
(x) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 93, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 94.
(xvi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 274, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 275;
(xvii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 286, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 287;
(xviii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 298, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 299;
(xix) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 310, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 311;
(xx) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 322, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 323;
(xxi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 334, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 335;
(xxii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 346, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 347; или
(xxiii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 358, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 359.
В конкретных вариантах осуществления настоящее изобретение относится к антителам, которые содержат CDR1, CDR2 и CDR3 тяжелой цепи и легкой цепи из антител ET150-153, ET150-166, ET150-170, ET150-171, ET150-175, ET150-154, ET150-156, ET150-157, ET150-159, ET150-160, ET150-161, ET150-162, ET150-163, ET150-151, ET150-152, ET150-155, ET150-158, ET150-168, ET150-165, ET150-167, ET150-169, ET150-172, ET150-173, ET150-024, ET150-026, ET150-028, ET150-029, ET150-030, ET150-031, ET150-032 и ET150-033. Аминокислотные последовательности VH CDR1 из ET150-153, ET150-166, ET150-170, ET150-171, ET150-175, ET150-154, ET150-156, ET150-157, ET150-159, ET150-160, ET150-161, ET150-162, ET150-163, ET150-151, ET150-152, ET150-155, ET150-158, ET150-168, ET150-165, ET150-167, ET150-169, ET150-172, ET150-173, ET150-024, ET150-026, ET150-028, ET150-029, ET150-030, ET150-031, ET150-032 и ET150-033 приведены в SEQ ID NOs: 124, 130, 136, 142, 148, 154, 160, 166, 172, 178, 184, 190, 196, 202, 208, 214, 220, 226, 232, 238, 244, 250, 256, 262, 268, 280, 292, 303, 316, 328, 340 и 352, соответственно. Аминокислотные последовательности VH CDR2 из антител ET150-153, ET150-166, ET150-170, ET150-171, ET150-175, ET150-154, ET150-156, ET150-157, ET150-159, ET150-160, ET150-161, ET150-162, ET150-163, ET150-151, ET150-152, ET150-155, ET150-158, ET150-168, ET150-165, ET150-167, ET150-169, ET150-172, ET150-173, ET150-024, ET150-026, ET150-028, ET150-029, ET150-030, ET150-031, ET150-032 и ET150-033 приведены в SEQ ID NOs: 125, 131, 137, 143, 149, 155, 161, 167, 173, 179, 185, 191, 197, 203, 209, 215, 221, 227, 233, 239, 245, 251, 257, 263, 269, 281, 293, 304, 317, 329, 341 и 353, соответственно. Аминокислотные последовательности VH CDR3 из ET150-153, ET150-166, ET150-170, ET150-171, ET150-175, ET150-154, ET150-156, ET150-157, ET150-159, ET150-160, ET150-161, ET150-162, ET150-163, ET150-151, ET150-152, ET150-155, ET150-158, ET150-168, ET150-165, ET150-167, ET150-169, ET150-172, ET150-173, ET150-024, ET150-026, ET150-028, ET150-029, ET150-030, ET150-031, ET150-032 и ET150-033 приведены в SEQ ID NOs: 126, 132, 138, 144, 150, 156, 162, 168, 174, 180, 186, 192, 198, 204, 210, 216, 222, 228, 234, 240, 246, 252, 258, 264, 270, 282, 294, 305, 318, 330, 342 и 354, соответственно.
Аминокислотные последовательности VL CDR1 из ET150-153, ET150-166, ET150-170, ET150-171, ET150-175, ET150-154, ET150-156, ET150-157, ET150-159, ET150-160, ET150-161, ET150-162, ET150-163, ET150-151, ET150-152, ET150-155, ET150-158, ET150-168, ET150-165, ET150-167, ET150-169, ET150-172, ET150-173, ET150-024, ET150-026, ET150-028, ET150-029, ET150-030, ET150-031, ET150-032 и ET150-033 приведены в SEQ ID NOs: 127, 133, 139, 145, 151, 157, 163, 169, 175, 181, 187, 193, 199, 205, 211, 217, 223, 229, 235, 241, 247, 253, 259, 265, 271, 283, 295, 306, 319, 331, 343 и 355, соответственно. Аминокислотные последовательности VL CDR2 из ET150-153, ET150-166, ET150-170, ET150-171, ET150-175, ET150-154, ET150-156, ET150-157, ET150-159, ET150-160, ET150-161, ET150-162, ET150-163, ET150-151, ET150-152, ET150-155, ET150-158, ET150-168, ET150-165, ET150-167, ET150-169, ET150-172, ET150-173, ET150-024, ET150-026, ET150-028, ET150-029, ET150-030, ET150-031, ET150-032 и ET150-033 приведены в SEQ ID NOs: 128, 134, 140, 146, 152, 158, 164, 170, 176, 182, 188, 194, 200, 206, 212, 218, 224, 230, 236, 242, 248, 254, 260, 266, 272, 284, 296, 307, 320, 332, 344 и 356, соответственно. Аминокислотные последовательности VL CDR3 из ET150-153, ET150-166, ET150-170, ET150-171, ET150-175, ET150-154, ET150-156, ET150-157, ET150-159, ET150-160, ET150-161, ET150-162, ET150-163, ET150-151, ET150-152, ET150-155, ET150-158, ET150-168, ET150-165, ET150-167, ET150-169, ET150-172, ET150-173, ET150-024, ET150-026, ET150-028, ET150-029, ET150-030, ET150-031, ET150-032 и ET150-033 приведены в SEQ ID NOs: 129, 135, 141, 147, 153, 159, 165, 171, 177, 183, 189, 195, 201, 207, 213, 219, 225, 231, 237, 243, 249, 255, 261, 267, 273, 285, 297, 308, 321, 333, 345 и 357, соответственно. Границы областей CDR определены с использованием системы Kabat (Kabat, E. A., et al. (1991) Sequences of Proteins of Immunological Interest, пятое издание, U.S. Department of Health и Human Services, NIH Publication No. 91-3242).
Учитывая, что каждое из этих антител может связываться с GPRC5D, и что специфичность связывания антигена обеспечивается, главным образом, областями CDR1, CDR2 и CDR3, последовательности CDR1, CDR2 и CDR3 из VH и последовательности CDR1, CDR2 и CDR3 из VL можно «комбинировать» (то есть, CDR из разных антител можно комбинировать, хотя каждое антитело должно содержать CDR1, CDR2, и CDR3 в VH и CDR1, CDR2, и CDR3 в VL) для создания других анти-GPRC5D связывающих молекул. Связывание с GPRC5D таких «комбинированных» антител можно тестировать в анализах связывания, описанных выше. Когда последовательности VH CDR комбинируют, то последовательности CDR1, CDR2 и/или CDR3 из конкретной последовательности VH заменяют структурно сходными последовательностями CDR. Аналогично, когда последовательности VL CDR комбинируют, то последовательности CDR1, CDR2 и/или CDR3 из конкретной последовательности VL, предпочтительно, заменяют структурно сходными последовательностями CDR. Для специалиста в данной области будет очевидно, что можно создавать новые последовательности VH и VL путем замены последовательностей одной или более областей CDR из VH и/или VL структурно сходными последовательностями из последовательностей CDR раскрытых в настоящем документе антител ET150-153, ET150-166, ET150-170, ET150-171, ET150-175, ET150-154, ET150-156, ET150-157, ET150-159, ET150-160, ET150-161, ET150-162, ET150-163, ET150-151, ET150-152, ET150-155, ET150-158, ET150-168, ET150-165, ET150-167, ET150-169, ET150-172, ET150-173, ET150-024, ET150-026, ET150-028, ET150-029, ET150-030, ET150-031, ET150-032 и ET150-033.
В конкретных вариантах осуществления настоящее изобретение относится к выделенному антителу, или его антигенсвязывающему фрагменту, содержащему: (i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOs: 124, 130, 136, 142, 148, 154, 160, 166, 172, 178, 184, 190, 196, 202, 208, 214, 220, 226, 232, 238, 244, 250, 256, 262, 268, 280, 292, 303, 316, 328, 340 и 352; (ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOs: 125, 131, 137, 143, 149, 155, 161, 167, 173, 179, 185, 191, 197, 203, 209, 215, 221, 227, 233, 239, 245, 251, 257, 263, 269, 281, 293, 304, 317, 329, 341 и 353; (iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOs: 126, 132, 138, 144, 150, 156, 162, 168, 174, 180, 186, 192, 198, 204, 210, 216, 222, 228, 234, 240, 246, 252, 258, 264, 270, 282, 294, 305, 318, 330, 342 и 354; (iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOs: 127, 133, 139, 145, 151, 157, 163, 169, 175, 181, 187, 193, 199, 205, 211, 217, 223, 229, 235, 241, 247, 253, 259, 265, 271, 283, 295, 306, 319, 331, 343 и 355; (v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOs: 128, 134, 140, 146, 152, 158, 164, 170, 176, 182, 188, 194, 200, 206, 212, 218, 224, 230, 236, 242, 248, 254, 260, 266, 272, 284, 296, 307, 320, 332, 344 и 356; и (f) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOs: 129, 135, 141, 147, 153, 159, 165, 171, 177, 183, 189, 195, 201, 207, 213, 219, 225, 231, 237, 243, 249, 255, 261, 267, 273, 285, 297, 308, 321, 333, 345 и 357; при этом антитело специфически связывает GPRC5D, например, GPRC5D человека.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 124;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 125;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 126;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 127;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 128; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 129.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 130;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 131;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 132;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 133;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 134; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 135.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 136;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 137;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 138;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 139;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 140; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 141.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 142;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 143;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 144;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 145;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 146; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 147.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 148;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 149;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 150;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 151;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 152; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 153.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 154;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 155;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 156;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 157;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 158; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 159.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 160;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 161;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 162;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 163;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 164; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 165.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 166;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 167;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 168;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 169;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 170; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 171.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 172;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 173;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 174;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 175;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 176; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 177.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 178;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 179;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 180;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 181;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 182; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 183.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 184;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 185;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 186;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 187;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 188; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 189.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 190;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 191;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 192;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 193;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 194; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 195.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 196;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 197;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 198;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 199;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 200; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 201.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 202;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 203;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 204;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 205;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 206; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 207.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 208;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 209;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 210;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 211;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 212; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 213.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 214;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 215;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 216;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 217;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 218; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 219.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 220;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 221;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 222;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 223;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 224; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 225.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 226;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 227;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 228;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 229;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 230; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 231.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 232;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 233;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 234;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 235;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 236; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 237.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 238;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 239;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 240;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 241;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 242; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 243.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 244;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 245;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 246;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 247;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 248; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 249.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 250;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 251;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 252;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 253;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 254; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 255.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 256;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 257;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 258;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 259;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 260; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 261.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 262;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 263;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 264;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 265;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 266; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 267.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 268;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 269;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 270;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 271;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 272; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 273.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 280;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 281;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 282;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 283;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 284; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 285.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 292;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 293;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 294;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 295;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 296; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 297.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 303;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 304;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 305;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 306;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 307; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 308.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 316;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 317;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 318;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 319;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 320; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 321.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 328;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 329;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 330;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 331;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 332; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 333.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 340;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 341;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 342;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 343;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 344; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 345.
В конкретных вариантах осуществления антитело содержит:
(i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 352;
(ii) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 353;
(iii) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 354;
(iv) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 355;
(v) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 356; и
(vi) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 357.
Константная область/каркасная область анти-GPRC5D антител, раскрытых в настоящем документе, может быть изменена, например, за счет аминокислотной замены, с целью изменения свойств антитела (например, для увеличения, либо уменьшения одного или более из: аффинности связывания антигена, связывания Fc-рецептора, углевода антитела, например, за счет гликозилирования, фукозилирования и так далее, числа остатков цистеина, эффекторной клеточной функции, функции комплемента или для введения сайта конъюгации).
В конкретных вариантах осуществления раскрытое в настоящем документе анти-GPRC5D антитело представляет собой полностью человеческое антитело, например, любое из ET150-153, ET150-166, ET150-170, ET150-171, ET150-175, ET150-154, ET150-156, ET150-157, ET150-159, ET150-160, ET150-161, ET150-162, ET150-163, ET150-151, ET150-152, ET150-155, ET150-158, ET150-168, ET150-165, ET150-167, ET150-169, ET150-172, ET150-173, ET150-024, ET150-026, ET150-028, ET150-029, ET150-030, ET150-031, ET150-032 и ET150-033. Полностью человеческие мАт являются предпочтительными для терапевтического использования применительно к людям, поскольку мышиные антитела при введении людям вызывают иммунную реакцию, известную как HAMA-ответ (антитела человека против антител мыши) (Azinovic I., et al. Survival benefit associated with human anti-mouse antibody (HAMA) in patients with B-cell malignancies. Cancer Immunol Immunother 2006; 55(12): 1451-8; Tjandra J.J., et al. Development of human anti-murine antibody (HAMA) response in patients. Immunol Cell Biol 1990; 68(6): 367-76), приводя к серьезным побочным эффектам, включая анафилаксию и реакции гиперчувствительности. Эта иммунная реакция запускается иммунной системой человека, воспринимающей мышиные антитела как чужеродные из-за небольших отличий аминокислотных последовательностей от последовательностей природных человеческих антител. Можно использовать методы гуманизации, известные в данной области (Riechmann L, et al. Reshaping human antibodies for therapy. Nature 1988; 332 (6162): 332:323; Queen C, et al. A humanized antibody that binds to the interleukin 2 receptor. Proc Natl Acad Sci USA 1989; 86 (24): 10029-33), для уменьшения иммуногенности мышиных антител (Gerd R., et al. Serological Analysis of Human Anti-Human Antibody Responses in Colon Cancer Patients Treated with Repeated Doses of Humanized Monoclonal Antibody A33. Cancer Res 2001; 61, 6851-6859).
Использование библиотек фагового дисплея сделало возможным отбор в большом количестве репертуаров Ат на уникальные и редкие Ат против конкретных эпитопов (для более подробной информации о фаговом дисплее смотри McCafferty et al., Phage antibodies: filamentous phage displaying antibody variable domains. Nature, 348: 552-554). Вследствие этого, стала возможной быстрая идентификация человеческих Fab или одноцепочечных Fv (ScFv) фрагментов, высокоспецифичных для молекул комплексов пептид опухолевого антигена-MHC (19-22). Недавно было показано, что иммунотоксины, полученные путем слияния TCR-подобного Fab, специфичного для Аг меланомы MART-1 26-35/A2 или gp100 280-288/A2, с укороченной формой эндотоксина Pseudomonas, ингибируют рост меланомы человека как in vitro, так и in vivo (Klechevsky E., et al. Antitumor activity of immunotoxins with T-cell receptor-like specificity against human melanoma xenografts. Cancer Res 2008; 68 (15): 6360-6367). Кроме того, за счет конструирования полноразмерного мАт с использованием Fab-фрагментов можно напрямую создавать терапевтические человеческие мАт, не тратя месяцы трудоемкой работы, обычно необходимой для разработки терапевтических мАт. Настоящее изобретение включает разработку полностью человеческого мАт, которое узнает, например, полипептид GPRC5D человека (например, полипептид, имеющий аминокислотную последовательность, приведенную в SEQ ID NO: 97), для терапии рака.
3. Гомологичные антитела
В конкретных вариантах осуществления антитело по настоящему изобретению содержит вариабельные области тяжелой и легкой цепей, содержащие аминокислотные последовательности, которые гомологичны аминокислотным последовательностям антител, описанных в настоящем документе (например, антител ET150-153, ET150-166, ET150-170, ET150-171, ET150-175, ET150-154, ET150-156, ET150-157, ET150-159, ET150-160, ET150-161, ET150-162, ET150-163, ET150-151, ET150-152, ET150-155, ET150-158, ET150-168, ET150-165, ET150-167, ET150-169, ET150-172, ET150-173, ET150-024, ET150-026, ET150-028, ET150-029, ET150-030, ET150-031, ET150-032 и ET150-033), и при этом антитела сохраняют желательные функциональные свойства анти-PGPRC5D антител по настоящему изобретению.
Например, настоящее изобретение относится к выделенному антителу, или его антигенсвязывающему фрагменту, содержащему вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом:
(a) вариабельная область тяжелой цепи содержит аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NOs: 1, 5, 9, 13, 17, 21, 25, 29, 33, 37, 41, 45, 49, 53, 57, 61, 65, 69, 73, 77, 81, 85, 89, 93, 274, 286, 298, 310, 322, 334, 346 и 358; и
(b) вариабельная область легкой цепи содержит аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NOs: 2, 6, 10, 14, 18, 22, 26, 30, 34, 38, 42, 46, 50, 54, 58, 62, 66, 70, 74, 78, 82, 86, 90, 94, 275, 287, 299, 311, 323, 335, 347 и 359; и антитело связывается с GPRC5D человека с Kd, составляющей 1×10-7 M или менее.
В конкретных вариантах осуществления аминокислотные последовательности VH и/или VL могут быть по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологичны последовательностям, приведенным выше. Антитело, содержащее области VH и VL, имеющие высокую степень (то есть, 80% или более) гомологии с областями VH и VL, имеющими последовательности, приведенные выше, можно получать путем мутагенеза (например, сайт-направленного или ПЦР-опосредованного мутагенеза), с последующим тестированием закодированного измененного антитела на сохранение функции (то есть, аффинности связывания) с использованием анализов связывания, описанных в настоящем документе.
При использовании в настоящем документе, процент гомологии между двумя аминокислотными последовательностями эквивалентен проценту идентичности между двумя последовательностями. Процент идентичности между двумя последовательностями зависит от числа идентичных положений в этих последовательностях (то есть, % гомологии=число идентичных положений/общее число положений x 100), с учетом числа разрывов и длины каждого разрыва, который должен быть внесен для оптимального выравнивания двух последовательностей. Сравнение последовательностей и определение процента идентичности между двумя последовательностями можно выполнять с использованием математического алгоритма, как описано в неограничивающих примерах, приведенных ниже.
Процент гомологии между двумя аминокислотными последовательностями можно определять с использованием алгоритма E. Meyers и W. Miller (Comput. Appl. Biosci., 4: 11-17 (1988)), который включен в программу ALIGN (версия 2.0), с использованием таблицы «веса замен остатков» PAM120, штрафа за удлинение разрыва 12 и штрафа за внесение разрыва 4. Кроме того, процент гомологии между двумя аминокислотными последовательностями можно определять с помощью алгоритма Needleman и Wunsch (J. Mol. Biol. 48: 444-453 (1970)), который включен в программу GAP пакета программ GCG (доступна на сайте www.gcg.com), с использованием либо матрицы Blossum 62, либо матрицы PAM250, штрафа за внесение разрыва 16, 14, 12, 10, 8, 6, или 4 и штрафа за удлинение разрыва 1, 2, 3, 4, 5 или 6.
Дополнительно или альтернативно, белковые последовательности по настоящему изобретению также можно использовать в качестве «искомой последовательности» для проведения поиска в общедоступных базах данных с целью, например, выявления родственных последовательностей. Такой поиск можно выполнять с использованием программы XBLAST (версия 2.0), основанной на принципах, описанных в Altschul, et al. (1990) J. Mol. Biol. 215: 403-10. Можно выполнять BLAST-поиск белков с помощью программы XBLAST, оценка=50, длина слова=3, для получения аминокислотных последовательностей, гомологичных молекулам антител по изобретению. Для получения выравниваний с внесенными разрывами в целях сравнения можно использовать программу Gapped BLAST, как описано в Altschul et al., (1997) Nucleic Acids Res. 25(17): 3389-3402. При использовании программ BLAST и Gapped BLAST можно использовать параметры по умолчанию соответствующих программ (например, XBLAST и NBLAST). (Смотри www.ncbi.nlm.nih.gov).
4. Антитела с консервативными модификациями
В конкретных вариантах осуществления антитело по настоящему изобретению содержит вариабельную область тяжелой цепи, содержащую последовательности CDR1, CDR2 и CDR3, и вариабельную область легкой цепи, содержащую последовательности CDR1, CDR2 и CDR3, при этом одна или более из этих последовательностей CDR содержат конкретные аминокислотные последовательности предпочтительных антител, описанных в настоящем документе (например, антител ET150-153, ET150-166, ET150-170, ET150-171, ET150-175, ET150-154, ET150-156, ET150-157, ET150-159, ET150-160, ET150-161, ET150-162, ET150-163, ET150-151, ET150-152, ET150-155, ET150-158, ET150-168, ET150-165, ET150-167, ET150-169, ET150-172, ET150-173, ET150-024, ET150-026, ET150-028, ET150-029, ET150-030, ET150-031, ET150-032 и ET150-033), или их консервативные модификации, и при этом антитела сохраняют желательные функциональные свойства анти-GPRC5D антител по настоящему изобретению.
Настоящее изобретение относится к выделенному антителу, или его антигенсвязывающему фрагменту, содержащему вариабельную область тяжелой цепи, содержащую последовательности CDR1, CDR2, и CDR3, и вариабельную область легкой цепи, содержащую последовательности CDR1, CDR2, и CDR3, при этом:
(a) CDR3 вариабельной области тяжелой цепи содержит аминокислотную последовательность, выбранную из группы, состоящей из аминокислотных последовательностей SEQ ID NOs: 126, 132, 138, 144, 150, 156, 162, 168, 174, 180, 186, 192, 198, 204, 210, 216, 222, 228, 234, 240, 246, 252, 258, 264, 270, 282, 294, 305, 318, 330, 342 и 354, а также их консервативных модификаций;
(b) CDR3 вариабельной области легкой цепи содержит аминокислотную последовательность, выбранную из группы, состоящей из аминокислотных последовательностей SEQ ID NOs: 129, 135, 141, 147, 153, 159, 165, 171, 177, 183, 189, 195, 201, 207, 213, 219, 225, 231, 237, 243, 249, 255, 261, 267, 273, 285, 297, 308, 321, 333, 345 и 357 и 431, а также их консервативных модификаций; и антитело связывается с GPRC5D человека с Kd, составляющей 1×10-7 M или менее.
В конкретных вариантах осуществления последовательность CDR2 вариабельной области тяжелой цепи содержит аминокислотную последовательность, выбранную из группы, состоящей из аминокислотных последовательностей SEQ ID NOs: 125, 131, 137, 143, 149, 155, 161, 167, 173, 179, 185, 191, 197, 203, 209, 215, 221, 227, 233, 239, 245, 251, 257, 263, 269, 281, 293, 304, 317, 329, 341 и 353, а также их консервативных модификаций; и последовательность CDR2 вариабельной области легкой цепи содержит аминокислотную последовательность, выбранную из группы, состоящей из аминокислотных последовательностей SEQ ID NOs: 128, 134, 140, 146, 152, 158, 164, 170, 176, 182, 188, 194, 200, 206, 212, 218, 224, 230, 236, 242, 248, 254, 260, 266, 272, 284, 296, 307, 320, 332, 344 и 356, а также их консервативных модификаций.
В конкретных вариантах осуществления последовательность CDR1 вариабельной области тяжелой цепи содержит аминокислотную последовательность, выбранную из группы, состоящей из аминокислотных последовательностей SEQ ID NOs: 124, 130, 136, 142, 148, 154, 160, 166, 172, 178, 184, 190, 196, 202, 208, 214, 220, 226, 232, 238, 244, 250, 256, 262, 268, 280, 292, 303, 316, 328, 340 и 352, а также их консервативных модификаций; и последовательность CDR1 вариабельной области легкой цепи содержит аминокислотную последовательность, выбранную из группы, состоящей из аминокислотных последовательностей SEQ ID NOs: 127, 133, 139, 145, 151, 157, 163, 169, 175, 181, 187, 193, 199, 205, 211, 217, 223, 229, 235, 241, 247, 253, 259, 265, 271, 283, 295, 306, 319, 331, 343 и 355, а также их консервативных модификаций.
Используемый в настоящем документе термин «консервативные модификации последовательности» означает аминокислотные модификации, которые существенно не затрагивают или не изменяют характеристики связывания антитела, содержащего аминокислотную последовательность. Такие консервативные модификации включают аминокислотные замены, добавления и делеции. Модификации могут быть внесены в антитело по изобретению стандартными методами, известными в данной области, такими как сайт-направленный мутагенез и ПЦР-опосредованный мутагенез.
Консервативные аминокислотные замены являются такими заменами, при которых аминокислотный остаток заменен аминокислотным остатком, имеющим аналогичную боковую цепь. Семейства аминокислотных остатков, имеющих аналогичные боковые цепи, известны в данной области. Иллюстративные консервативные аминокислотные замены приведены в таблице 33. Аминокислотные замены можно вносить в интересующее антитело и проводить скрининг полученных продуктов на наличие желательной активности, например, сохраненного/улучшенного связывания антигена, сниженной иммуногенности, либо улучшенной ADCC или CDC. В конкретных вариантах осуществления последовательность, раскрытая в настоящем документе, например, последовательность CDR, последовательность VH или последовательность VL, может иметь до примерно одного, до примерно двух, до примерно трех, до примерно четырех, до примерно пяти, до примерно шести, до примерно семи, до примерно восьми, до примерно девяти или до примерно десяти аминокислотных остатков, которые модифицированы и/или заменены.
Таблица 33
Аминокислоты могут быть сгруппированы на основании общих свойств боковой цепи:
- гидрофобные: норлейцин, Met, Ala, Val, Leu, Ile;
- нейтральные гидрофильные: Cys, Ser, Thr, Asn, Gln;
- кислые: Asp, Glu;
- основные: His, Lys, Arg;
- остатки, которые влияют на ориентацию цепи: Gly, Pro;
- ароматические: Trp, Tyr, Phe.
Не консервативные замены являются заменой представителя одного класса на представителя другого класса.
5. Анти-GPRC5D антитела, которые перекрестно конкурируют за связывание с GPRC5D с анти-GPRC5D антителами по изобретению
Настоящее изобретение относится к антителам, которые перекрестно конкурируют с любым из раскрытых анти-GPRC5D антител за связывание с GPRC5D (например, GPRC5D человека). Например, и без ограничения, перекрестно конкурирующие антитела могут связываться с той же областью эпитопа, например, тем же эпитопом, соседним эпитопом или перекрывающимся эпитопом, что и любое из анти-GPRC5D антител по настоящему изобретению. В конкретных вариантах осуществления эталонное антитело для исследований перекрестного конкурирования может быть любым из анти-GPRC5D антител, раскрытых в настоящем документе, например, антител ET150-153, ET150-166, ET150-170, ET150-171, ET150-175, ET150-154, ET150-156, ET150-157, ET150-159, ET150-160, ET150-161, ET150-162, ET150-163, ET150-151, ET150-152, ET150-155, ET150-158, ET150-168, ET150-165, ET150-167, ET150-169, ET150-172, ET150-173, ET150-024, ET150-026, ET150-028, ET150-029, ET150-030, ET150-031, ET150-032 и ET150-033.
В конкретных вариантах осуществления перекрестно конкурирующее антитело связывается с областью эпитопа, содержащей аминокислоты 14-22 из SEQ ID NO: 97. В конкретных вариантах осуществления перекрестно конкурирующее антитело связывается с одной, двумя, тремя, четырьмя, пятью, шестью или семью областями эпитопа, выбранными из группы, состоящей из аминокислот 5-17, 10-17, 1-27, 15-23, 16-23, 16-25, 85-93, 85-95, 145-167, 157-164, 157-167, 226-239, 230-237, 229-237, 230-243 и 227-237 из SEQ ID NO: 97.
Такие перекрестно конкурирующие антитела можно идентифицировать на основании их способности перекрестно конкурировать с любым из раскрытых в настоящем документе анти-GPRC5D антител в стандартных анализах связывания GPRC5D. Например, можно использовать анализ Biacore, анализы ELISA или метод проточной цитометрии для демонстрации перекрестной конкуренции с антителами по настоящему изобретению. Способность тестируемого антитела ингибировать связывание, например, любого из раскрытых в настоящем документе антител к GPRC5D (например, антител ET150-153, ET150-166, ET150-170, ET150-171, ET150-175, ET150-154, ET150-156, ET150-157, ET150-159, ET150-160, ET150-161, ET150-162, ET150-163, ET150-151, ET150-152, ET150-155, ET150-158, ET150-168, ET150-165, ET150-167, ET150-169, ET150-172, ET150-173, ET150-024, ET150-026, ET150-028, ET150-029, ET150-030, ET150-031, ET150-032 и ET150-033) с GPRC5D человека показывает, что тестируемое антитело может конкурировать с любым из раскрытых в настоящем документе анти-GPRC5D антител за связывание с GPRC5D человека и, таким образом, связывается с той же областью эпитопа на GPRC5D человека, что и любое из раскрытых в настоящем документе анти-GPRC5D антител. В конкретных вариантах осуществления перекрестно конкурирующее антитело связывается с тем же эпитопом на GPRC5D человека, что и любое из раскрытых в настоящем документе анти-GPRC5D антител.
6. Характеризация связывания антитела с антигеном
Антитела по настоящему изобретению можно тестировать на связывание с GPRC5D, например, стандартным методом ELISA. Для определения того, связываются ли выбранные анти-GPRC5D антитела с уникальными эпитопами, каждое антитело можно биотинилировать с использованием коммерчески доступных реагентов (Pierce, Rockford, IL). Исследования конкурентного связывания с использованием немеченых моноклональных антител и биотинилированных моноклональных антител можно выполнять, используя покрытые GPRC5D планшеты для ELISA, как описано выше. Связывание биотинилированного мАт можно обнаруживать с помощью зонда стрептавидин-щелочная фосфатаза.
Для определения изотипа очищенных антител можно проводить изотипирование методом ELISA с использованием реагентов, специфичных для антител конкретного изотипа. Затем анти-GPRC5D человеческие IgG можно тестировать методом вестерн-блоттинга на способность реагировать с антигеном GPRC5D.
В конкретных вариантах осуществления Kd измеряют в анализе связывания радиоактивно меченого антигена (RIA). В конкретных вариантах осуществления RIA выполняют, используя Fab-вариант интересующего антитела и его антиген. Например, аффинность связывания Fab с антигеном в растворе измеряют путем уравновешивания Fab с минимальной концентрацией (125I)-меченого антигена в присутствии серийно титрованного немеченого антигена, с последующим удержанием связанного антигена на покрытом анти-Fab антителом планшете (смотри, например, Chen et al., J. Mol. Biol. 293: 865-881(1999)).
В конкретных вариантах осуществления Kd измеряют методом поверхностного плазмонного резонанса с использованием системы BIACORE®. Например, в анализе с использованием BIACORE®-2000 или BIACORE®-3000 (BIAcore, Inc., Piscataway, NJ).
Картирование эпитопов
В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, связывается с полипептидом GPRC5D человека, содержащим аминокислотную последовательность, приведенную в SEQ ID NO: 97. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, связывается с одной, двумя, тремя или четырьмя областями эпитопа из N-концевой области (аминокислоты 1-27 из SEQ ID NO: 97), области ECL1 (аминокислоты 85-93 из SEQ ID NO: 97), области ECL2 (аминокислоты 145-167 из SEQ ID NO: 97) и области ECL3 (аминокислоты 226-239 из SEQ ID NO: 97). В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, по настоящему изобретению связывается с областью эпитопа в N-концевой области, включая, но без ограничения, область эпитопа, содержащую аминокислоты 16-23 из SEQ ID NO: 97, и область эпитопа, содержащую аминокислоты 10-17 из SEQ ID NO: 97. В конкретных вариантах осуществления область эпитопа в N-концевой области содержит аминокислоты 15-23 из SEQ ID NO: 97. В конкретных вариантах осуществления область эпитопа в N-концевой области содержит аминокислоты 16-25 из SEQ ID NO: 97. В конкретных вариантах осуществления область эпитопа в N-концевой области содержит аминокислоты 10-17 из SEQ ID NO: 97. В конкретных вариантах осуществления область эпитопа в N-концевой области содержит аминокислоты 5-17 из SEQ ID NO: 97.
В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, по настоящему изобретению связывается с областью эпитопа в области ECL1, включая, но без ограничения, область эпитопа, содержащую аминокислоты 85-95 из SEQ ID NO: 97.
В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, по настоящему изобретению связывается с областью эпитопа в области ECL2, включая, но без ограничения, область эпитопа, содержащую аминокислоты 157-164 из SEQ ID NO: 97. В конкретных вариантах осуществления область эпитопа в области ECL2 содержит аминокислоты 157-164 из SEQ ID NO: 97. В конкретных вариантах осуществления область эпитопа в области ECL2 содержит аминокислоты 157-167 из SEQ ID NO: 97.
В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, по настоящему изобретению связывается с областью эпитопа в области ECL3, включая, но без ограничения, область эпитопа, содержащую аминокислоты 230-237 из SEQ ID NO: 97. В конкретных вариантах осуществления область эпитопа в области ECL3 содержит аминокислоты 229-237 из SEQ ID NO: 97. В конкретных вариантах осуществления область эпитопа в области ECL3 содержит аминокислоты 230-243 из SEQ ID NO: 97. В конкретных вариантах осуществления область эпитопа в области ECL3 содержит аминокислоты 227-237 из SEQ ID NO: 97.
В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, связывается с областью эпитопа, содержащей аминокислоты 16-25 из SEQ ID NO: 97, областью эпитопа, содержащей аминокислоты 157-164 из SEQ ID NO: 97, и областью эпитопа, содержащей аминокислоты 229-237 из SEQ ID NO: 97. Например, антитело, или его антигенсвязывающий фрагмент, содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 57, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 58, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, представляет собой scFv. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 15. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 57. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 57. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VL, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 58. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 58. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 57, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 58. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 208, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 209, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 210, или ее консервативные модификации. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 211, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 212, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 213, или ее консервативные модификации. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 208, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 209, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 210, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 211, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 212, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 213, или ее консервативные модификации. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 208, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 209, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 210, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 211, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 212, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 213. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, представляет собой ET150-2 scFv (или ET150-152 scFv).
В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, связывается с областью эпитопа, содержащей аминокислоты 5-17 из SEQ ID NO: 97, областью эпитопа, содержащей аминокислоты 85-95 из SEQ ID NO: 97, и областью эпитопа, содержащей аминокислоты 157-164 из SEQ ID NO: 97. Например, антитело, или его антигенсвязывающий фрагмент, содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 61, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 62, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, представляет собой scFv. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 16. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 61. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 61. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VL, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 62. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 62. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 61, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 62. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 214, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 215, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 216, или ее консервативные модификации. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 217, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 218, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 219, или ее консервативные модификации. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 214, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 215, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 216, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 217, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 218, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 219, или ее консервативные модификации. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 214, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 215, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 216, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 217, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 218, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 219. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, представляет собой ET150-155 scFv (или ET150-5 scFv).
В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, связывается с областью эпитопа, содержащей аминокислоты 15-23 из SEQ ID NO: 97, и областью эпитопа, содержащей аминокислоты 230-243 из SEQ ID NO: 97. Например, антитело, или его антигенсвязывающий фрагмент, содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 65, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 66, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, представляет собой scFv. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 17. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 65. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 65. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VL, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 66, смотри таблицу 17. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 66. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 65, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 66. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 220, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 221, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 222, или ее консервативные модификации. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 223, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 224, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 225, или ее консервативные модификации. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 220, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 221, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 222, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 223, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 224, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 225, или ее консервативные модификации. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 220, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 221, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 222, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 223, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 224, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 225. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, представляет собой ET150-8 scFv (или ET150-158 scFv).
В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, связывается с областью эпитопа, содержащей аминокислоты 10-17 из SEQ ID NO: 97, областью эпитопа, содержащей аминокислоты 157-167 из SEQ ID NO: 97, и областью эпитопа, содержащей аминокислоты 227-237 из SEQ ID NO: 97. Например, антитело, или его антигенсвязывающий фрагмент, содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 69, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 70, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, представляет собой scFv. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, представляет собой слитый белок scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 18. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 69. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 69. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VL, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 70. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 70. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 69, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 70. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 226, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 227, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 228, или ее консервативные модификации. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 229, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 230, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 231, или ее консервативные модификации. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 226, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 227, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 228, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 229, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 230, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 231, или ее консервативные модификации. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 226, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 227, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 228, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 229, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 230, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 231. В конкретных вариантах осуществления антитело, или его антигенсвязывающий фрагмент, представляет собой ET150-18 scFv (или ET150-168 scFv).
7. Иммуноконъюгаты
Настоящее изобретение относится к анти-GPRC5D антителу, или его фрагменту, конъюгированному с терапевтическим фрагментом, таким как цитотоксин, лекарственное средство (например, иммунодепрессант) или радиотоксин. Такие конъюгаты в настоящем документе называют «иммуноконъюгатами». Иммуноконъюгаты, которые содержат один или более цитотоксинов, называют «иммунотоксинами». Цитотоксин или цитотоксическое средство включает любое средство, которое наносит вред (например, уничтожает) клеткам. Примеры включают таксол (например, рицин, дифтерийный токсин, гелонин), цитохалазин B, грамицидин D, бромид этидия, эметин, митомицин, этопозид, тенопозид, винкристин, винбластин, колхицин, доксорубицин, даунорубицин, дигидроксиантрацин дион, митоксантрон, митрамицин, актиномицин D, 1-дегидротестостерон, глюкокортикоиды, прокаин, тетракаин, лидокаин, пропранолол и пуромицин, а также их аналоги или гомологи. Терапевтические средства также включают, например, калехеамицин, уреастатин, антиметаболиты (например, метотрексат, 6-меркаптопурин, 6-тиогуанин, цитарабин, 5-фторурацил декарбазин), алкилирующие средства (например, мехлорэтамин, тиотепа, хлорамбуцил, мелфалан, кармустин (BSNU) и ломустин (CCNU), циклофосфамид, бусульфан, дибромманнит, стрептозотоцин, митомицин C и цис-дихлордиамин платину (II) (DDP) цисплатин), антрациклины (например, даунорубицин (бывший дауномицин) и доксорубицин), антибиотики (например, дактиномицин (бывший актиномицин), блеомицин, митрамицин и антрамицин (AMC)), а также антимитотические средства (например, винкристин и винбластин).
Другие примеры терапевтических цитотоксинов, которые можно конъюгировать с анти-GPRC5D антителом, раскрытым в настоящем документе, включают дуокармицины, калихеамицины, майтанзины и ауристатины, а также их производные. Примером конъюгата калихеамицина с антителом является коммерчески доступный милотарг (Mylotarg™; Wyeth-Ayerst).
Цитотоксины можно конъюгировать с анти-GPRC5D антителом, раскрытым в настоящем документе, с использованием технологии линкеров, известной в данной области. Примеры типов линкеров, которые были использованы для конъюгации цитотоксина с антителом, включают, но не ограничиваются ими, гидразоновые, тиоэфирные, сложноэфирные, дисульфидные и пептид-содержащие линкеры. Можно выбирать линкер, который, например, подвержен расщеплению при низком значении pH в лизосомальном компартменте или подвержен расщеплению протеазами, такими как протеазы, предпочтительно экспрессируемые в опухолевой ткани, например, катепсины (например, катепсины B, C, D). Для дополнительной информации о типах цитотоксинов, линкерах и способах конъюгации терапевтических средств с антителами, смотри также Saito, G. et al. (2003) Adv. Drug Deliv. Rev. 55: 199-215; Trail, P.A. et al. (2003) Cancer Immunol. Immunother. 52: 328-337; Payne, G. (2003) Cancer Cell 3: 207-212; Allen, T.M. (2002) Nat. Rev. Cancer 2: 750-763; Pastan, I. and Kreitman, R.J. (2002) Curr. Opin. Investig. Drugs 3: 1089-1091; Senter, P.D. and Springer, C.J. (2001) Adv. Drug Deliv. Rev. 53: 247-264.
Анти-GPRC5D антитела по настоящему изобретению также можно конъюгировать с радиоактивным изотопом для создания цитотоксических радиофармацевтических средств, иначе называемых радиоиммуноконъюгатами. Примеры радиоактивных изотопов, которые можно конъюгировать с антителами для диагностического или терапевтического применения, включают, но не ограничиваются ими, 90Y, 131I, 225Ac, 213Bi, 223Ra и 227Th. Методы получения радиоиммуноконъюгатов известны в данной области. Иллюстративные радиоиммуноконъюгаты коммерчески доступны, в том числе зевалин™ (IDEC Pharmaceuticals) и бексар™ (Corixa Pharmaceuticals), и аналогичные методы можно использовать для получения радиоиммуноконъюгатов с антителами по изобретению.
Конъюгаты с антителами по настоящему изобретению можно использовать для изменения конкретного биологического ответа, и фрагмент лекарственного средства не следует воспринимать, как ограниченный классическими химическими терапевтическими средствами. Например, фрагмент лекарственного средства может представлять собой белок или полипептид, обладающий желаемой биологической активностью. Такие белки могут включать, например, ферментативно активный токсин, или его активный фрагмент, например, абрин, рицин A, экзотоксин Pseudomonas или дифтерийный токсин; такой белок, как фактор некроза опухоли (TNF) или интерферон-γ; или модификаторы биологического ответа, такие как, например, лимфокины, интерлейкин-1 («IL-1»), интерлейкин-2 («IL-2»), интерлейкин-6 («IL-6»), гранулоцитарно-макрофагальный колониестимулирующий фактор («GM-CSF»), гранулоцитарный колониестимулирующий фактор («G-CSF») или другие факторы роста.
Методы конъюгации такого терапевтического фрагмента с антителами хорошо известны, смотри, например, Arnon et al., «Monoclonal Antibodies For Immunotargeting Of Drugs In Cancer Therapy», в: Monoclonal Antibodies And Cancer Therapy, Reisfeld et al. (eds.), pp. 243-56 (Alan R. Liss, Inc. 1985); Hellstrom et al., «Antibodies For Drug Delivery», в: Controlled Drug Delivery (2-е издание), Robinson et al. (eds.), pp. 623-53 (Marcel Dekker, Inc. 1987); Thorpe, «Antibody Carriers Of Cytotoxic Agents In Cancer Therapy: A Review», в: Monoclonal Antibodies '84: Biological And Clinical Applications, Pinchera et al. (eds.), pp. 475-506 (1985); «Analysis, Results, And Future Prospective Of The Therapeutic Use Of Radiolabeled Antibody In Cancer Therapy», в: Monoclonal Antibodies For Cancer Detection And Therapy, Baldwin et al. (eds.), pp. 303-16 (Academic Press 1985), и Thorpe et al., «The Preparation And Cytotoxic Properties Of Antibody-Toxin Conjugates», Immunol. Rev., 62: 119-58 (1982).
8. Биспецифичные молекулы
Настоящее изобретение относится к биспецифичным молекулам, содержащим раскрытое в настоящем документе анти-GPRC5D антитело, или его фрагмент. Антитело по настоящему изобретению, или его антигенсвязывающие фрагменты, можно дериватизировать или связывать с другой функциональной молекулой, например, другим пептидом или белком (например, другим антителом или лигандом для рецептора), для создания биспецифичной молекулы, которая связывается с по меньшей мере двумя разными сайтами связывания или целевыми молекулами. Антитело по настоящему изобретению, фактически, можно дериватизировать или связывать с более, чем одной другой функциональной молекулой, для создания мультиспецифичных молекул, которые связываются с более, чем двумя разными сайтами связывания или целевыми молекулами; такие мультиспецифичные молекулы также должны быть охвачены используемым в настоящем документе термином «биспецифичная молекула». Для создания биспецифичной молекулы раскрытое в настоящем документе анти-GPRC5D антитело может быть функционально связано (например, путем химического связывания, генетического слияния, не ковалентной ассоциации или иным образом) с одной или более другими связывающими молекулами, такими как другое антитело, фрагмент антитела, пептид или связывающий миметик, в результате чего образуется биспецифичная молекула.
Настоящее изобретение относится к биспецифичным молекулам, имеющим по меньшей мере первую специфичность связывания для GRPC5D и вторую специфичность связывания для второго целевого эпитопа. Второй целевой эпитоп может представлять собой эпитоп GPRC5D, или эпитоп не GPRC5D, например, другого антигена. В конкретных вариантах осуществления биспецифичная молекула является мультиспецифичной, молекула может дополнительно иметь третью специфичность связывания. Если первая часть биспецифичного антитела связывается с антигеном на клетке опухоли, например, и вторая часть биспецифичного антитела узнает антиген на поверхности иммунной эффекторной клетки человека, то антитело способно к рекрутингу активности этой эффекторной клетки за счет специфического связывания с эффекторным антигеном на иммунной эффекторной клетке человека. Вследствие этого, в конкретных вариантах осуществления биспецифичные антитела способны создавать связь между эффекторными клетками, например, T-клетками, и клетками опухолей, тем самым вызывая усиление эффекторной функции. В конкретных вариантах осуществления биспецифичное антитело по настоящему изобретению содержит по меньшей мере первый сайт связывания с GPRC5D и по меньшей мере второй сайт связывания с иммунной клеткой. Например, и без ограничения, биспецифичное антитело по настоящему изобретению содержит по меньшей мере первый сайт связывания с GPRC5D и по меньшей мере второй сайт связывания с рецептором, находящемся на поверхности иммунной клетки, например, CD3.
Биспецифичные молекулы по настоящему изобретению можно получать путем конъюгации обладающих специфичностью связывания фрагментов с использованием методов, известных в данной области. Например, каждый обладающий специфичностью связывания фрагмент биспецифичной молекулы можно создавать отдельно, а затем конъюгировать их друг с другом. Если обладающие специфичностью связывания фрагменты представляют собой белки или пептиды, для ковалентной конъюгации можно использовать различные связывающие или сшивающие реагенты. Примеры сшивающих реагентов включают белок A, карбодиимид, N-сукцинимидил-S-ацетил-тиоацетат (SATA), 5,5'-дитиобис-(2-нитробензойную кислоту) (DTNB), o-фенилендималеимид (oPDM), N-сукцинимидил-3-(2-пиридилдитио)пропионат (SPDP) и сульфосукцинимидил-4-(N-малеимидометил)циклогексан-1-карбоксилат (сульфо-SMCC) (смотри, например, Karpovsky et al. (1984) J. Exp. Med. 160: 1686; Liu, M.A. et al. (1985) Proc. Natl. Acad. Sci. USA 82: 8648). Другие методы включают те, которые описаны в Paulus (1985) Behring Ins. Mitt. No. 78, 118-132; Brennan et al. (1985) Science 229: 81-83) и Glennie et al. (1987) J. Immunol. 139: 2367-2375). Предпочтительными конъюгирующими реагентами являются SATA и сульфо-SMCC, оба реагента производит компания Pierce Chemical Co. (Rockford, IL).
Если обладающие специфичностью связывания фрагменты представляют собой антитела, то их можно конъюгировать путем связывания сульфгидрильных групп C-концевых шарнирных областей двух тяжелых цепей. В конкретных вариантах осуществления шарнирная область модифицирована для содержания нечетного числа сульфгидрильных остатков, предпочтительно одного, до конъюгации.
Альтернативно, оба обладающих специфичностью связывания фрагмента могут быть закодированы в одном и том же векторе, с последующей экспрессией и сборкой в одной и той же клетке-хозяине. Такой способ является особенно полезным, если биспецифичная молекула представляет собой слитый белок мАт x мАт, мАт x Fab, Fab x F(ab')2 или лиганд x Fab.
Связывание биспецифичных молекул с их специфическими мишенями можно подтверждать, например, твердофазным иммуноферментным анализом (ELISA), радиоиммунным анализом (RIA), FACS-анализом, биоанализом (например, ингибированием роста) или вестерн-блоттингом. Каждый из этих анализов, как правило, позволяет обнаруживать наличие конкретных интересующих комплексов белок-антитело за счет использования меченого реагента (например, антитела), специфичного для интересующего комплекса. Альтернативно, комплексы можно обнаруживать с помощью различных других иммуноанализов. Например, антитело можно метить радиоактивным изотопом и использовать в радиоиммунном анализе (RIA) (смотри, например, публикацию Weintraub, B., Principles of Radioimmunoassays, Seventh Training Course on Radioligand Assay Techniques, The Endocrine Society, March, 1986, содержание которой включено в настоящий документ посредством ссылки). Радиоактивный изотоп можно обнаруживать, например, с помощью γ-счетчика или сцинтилляционного счетчика, или авторадиографии.
9. Выбор ScFv с высокой аффинностью в отношении полипептида GPRC5D
Следующим этапом является отбор фага, который связывается с целевым интересующим антигеном с высокой аффинностью, из фагов библиотеки фагового дисплея человеческих белков, которые либо не связываются, либо связываются с низкой аффинностью. Это осуществляют путем итерационного связывания фага с антигеном, который связан с твердой подложкой, например, гранулами или клетками млекопитающих, с последующим удалением не связавшегося фага и элюированием специфически связавшегося фага. В конкретных вариантах осуществления антигены сначала биотинилируют для иммобилизации, например, на Dynabeads M-280 с конъюгированным стрептавидином. Библиотеку фагов инкубируют с клетками, гранулами или другой твердой подложкой, и не связавшийся фаг удаляют промыванием. Связавшиеся клоны отбирают и тестируют.
После отбора положительные клоны scFv тестируют на их связывание с GPRC5D (GPRC5D человека) на поверхности живых клетках 3T3 методом проточной цитометрии. Вкратце, фаговые клоны инкубируют с клетками 3T3, избыточно экспрессирующими GPRC5D. Клетки промывают, а затем добавляют мышиное мАт против белка оболочки M13. Клетки вновь промывают и метят с помощью конъюгата с FITC антител козы против Ig мыши перед проведением проточной цитометрии.
В других вариантах осуществления анти-GPRC5D антитела могут иметь одну или более аминокислотных замен в каркасной области, внесенных для повышения стабильности белка, связывания антитела, уровней экспрессии или для введения сайта для конъюгации терапевтических средств. Затем эти scFv используют для получения рекомбинантных человеческих моноклональных Ig способами, известными специалистам в данной области.
10. Конструирование полноразмерного мАт с использованием выбранных ScFv-фрагментов
Технология фагового дисплея позволяет быстро отбирать и производить антигенспецифичные scFv и Fab-фрагменты, которые полезны сами по себе, или которые в дальнейшем могут быть использованы для получения полноразмерных антител, антигенсвязывающих белков или их антигенсвязывающих фрагментов. Полноразмерные мАт с Fc-доменами обладают рядом преимуществ перед scFv и Fab антителами. Во-первых, только полноразмерные Ат обладают такой иммунологической функцией, как CDC и DCC, которая опосредована Fc-доменом. Во-вторых, двухвалентные мАт имеют более сильную аффинность при связывании антигена, чем мономерные Fab Ат. В-третьих, время полужизни в плазме и почечный клиренс будет отличаться в случае Fab и двухвалентного мАт. Конкретные особенности и преимущества каждого из них можно соотносить с планируемой эффекторной стратегией. В-четвертых, двухвалентное мАт может быть интернализовано с иной скоростью, чем scFv и Fab, что изменяет иммунную функцию или функцию переносчика. Альфа-эмиттеры, например, не обязательно должны быть интернализованы, чтобы уничтожать мишени, однако эффективность многих лекарственных средств и токсинов повышается при интернализации иммунных комплексов. Таким образом, в конкретных вариантах осуществления после получения клонов scFv, специфичных для GRPC5D, из библиотек фагового дисплея были созданы полноразмерные IgG мАт с использованием полученных scFv фрагментов.
Для получения рекомбинантных человеческих моноклональных IgG в клетках яичника китайского хомячка (CHO) полноразмерное IgG мАт можно конструировать способом, известным специалистам в данной области (Tomomatsu et al., Production of human monoclonal antibodies against FceRIa by a method combining in vitro immunization with phage display. Biosci Biotechnol Biochem 73(7): 1465-1469 2009). Вкратце, вариабельные области антитела можно субклонировать в экспрессионные векторы млекопитающих с соответствующими константными последовательностями лямбда или каппа легких цепей и Fc подкласса IgG1 (например) (Lidija P., et al. An integrated vector system for the eukaryotic expression of antibodies or their fragments after selection from phage display libraries. Gene 1997; 187(1): 9-18; Lisa J.H., et al. Crystallographic structure of an intact lgG1 monoclonal antibody. Journal of Molecular Biology 1998; 275 (5): 861-872). Можно использовать анализ кинетики связывания (Yasmina N.A., et al. Probing the binding mechanism and affinity of tanezumab, a recombinant humanized anti-NGF monoclonal antibody, using a repertoire of biosensors. Protein Science 2008; 17(8): 1326-1335) для подтверждения специфичного связывания полноразмерного IgG с GRPC5D, с величиной KD в наномолярном диапазоне.
Фармацевтические композиции и способы лечения
Анти-GPRC5D антитела по настоящему изобретению можно вводить для терапевтического лечения пациенту, имеющему опухоль (например, множественную миелому), в количестве, достаточном для предотвращения, ингибирования или уменьшения прогрессирования опухоли. Прогрессирование включает, например, рост, инвазию, метастазирование и/или рецидив опухоли. Количества, эффективные для этой цели, будут зависеть от степени тяжести заболевания и от общего состояния собственной иммунной системы пациента. Режим дозирования также будет варьироваться в зависимости от степени тяжести заболевания и состояния здоровья пациента, и, как правило, будет включать диапазон от одной болюсной дозы или непрерывной инфузии до нескольких введений в сутки (например, каждые 4-6 часов), или в соответствии с предписанием лечащего врача и состоянием здоровья пациента.
Определение болезненных состояний, поддающихся лечению анти-GPRC5D антителами по настоящему изобретению, находится в пределах компетенции специалиста в данной области. Например, люди, либо страдающие множественной миеломой, либо имеющие риск развития множественной миеломы, подходят для введения им раскрытых в настоящем документе анти-GPRC5D антител. Квалифицированный клиницист может с легкостью определять, например, на основании клинических анализов, физического обследования и медицинской/семейной истории, является ли индивидуум кандидатом для подобного лечения.
В конкретных вариантах осуществления настоящее изобретение относится к способу лечения опухоли путем введения анти-GPRC5D антитела, раскрытого в настоящем документе, в сочетании с одним или более другими средствами. Например, настоящее изобретение относится к способу лечения опухоли путем введения анти-GPRC5D антитела, раскрытого в настоящем документе, совместно с антинеопластическим средством. Анти-GPRC5D антитело может быть химически или биосинтетически связано с одним или более антинеопластическими средствами.
Неограничивающие примеры соответствующих опухолей включают множественную миелому и макроглобулинемию Вальденстрема. В конкретных вариантах осуществления опухоль представляет собой множественную миелому.
Любой подходящий способ или путь введения можно использовать для введения анти-GPRC5D антитела, раскрытого в настоящем документе, и, необязательно, для совместного введения антинеопластических средств. Пути введения включают, например, пероральное, внутривенное, внутрибрюшинное, подкожное или внутримышечное введение. Следует подчеркнуть, однако, что настоящее изобретение не ограничено каким-либо конкретным способом или путем введения.
Следует отметить, что раскрытое в настоящем документе анти-GPRC5D антитело можно вводить в виде конъюгата, который специфически связывается с рецептором и доставляет токсическую, летальную нагрузку после интернализации комплекса лиганд-токсин.
Понятно, что анти-GPRC5D антитела по настоящему изобретению можно вводить в форме композиции, дополнительно содержащей фармацевтически приемлемый носитель. Подходящие фармацевтически приемлемые носители включают, например, одно или более из: воды, солевого раствора, фосфатно-солевого буфера, декстрозы, глицерина, этанола и тому подобного, а также их сочетания. Фармацевтически приемлемые носители могут дополнительно содержать незначительные количества вспомогательных веществ, таких как увлажняющие средства или эмульгаторы, консерванты или буферы, которые увеличивают срок хранения или эффективность связывающих белков. Инъекционные композиции, как хорошо известно в данной области, могут быть сформулированы так, чтобы обеспечивать быстрое, замедленное или отсроченное высвобождение активного ингредиента после введения млекопитающему.
Настоящее изобретение также относится к применению антител и нуклеиновых кислот, кодирующих их, для лечения опухоли (например, множественной миеломы), для диагностических и прогностических целей, а также в качестве исследовательских инструментов для обнаружения GPRC5D в клетках и тканях. Фармацевтические композиции, содержащие раскрытые антитела и нуклеиновые кислоты, входят в объем настоящего изобретения. Векторы, содержащие нуклеиновые кислоты по настоящему изобретению, для лечения антителами путем введения иммунотерапевтических векторов, также входят в объем настоящего изобретения. Векторы включают экспрессионные векторы, которые обеспечивают экспрессию и секрецию антител, а также векторы, которые направляют к клеточной поверхности экспрессию антигенсвязывающих белков, таких как химерные антигенные рецепторы.
Клетки, содержащие указанные нуклеиновые кислоты, например, клетки, которые были трансфицированы векторами по изобретению, также входят в объем настоящего изобретения.
Наборы
Настоящее изобретение относится к наборам для лечения или предотвращения опухоли (например, множественной миеломы). В конкретном варианте осуществления набор включает терапевтическую композицию, содержащую эффективное количество анти-GPRC5D антитела, в стандартной лекарственной форме. В конкретных вариантах осуществления набор включает стерильный контейнер, содержащий терапевтическую или профилактическую вакцину; такие контейнеры могут представлять собой коробки, ампулы, бутылки, флаконы, пробирки, мешки, пакеты, блистерные упаковки или другие подходящие формы контейнеров, известные в данной области. Такие контейнеры могут быть выполнены из пластика, стекла, ламинированной бумаги, металлической фольги или других материалов, подходящих для хранения лекарственных средств.
При необходимости, анти-GPRC5D антитело предоставляют совместно с инструкциями по введению антитела субъекту, имеющему, или имеющему риск развития опухоли (например, множественной миеломы). Инструкции, как правило, будут содержать информацию об использовании композиции для лечения или предотвращения опухоли (например, множественной миеломы). В других вариантах осуществления инструкции включают по меньшей мере одно из следующего: описание лекарственного средства; схему доз и режим введения для лечения или предотвращения неоплазии (например, множественной миеломы) или ее симптомов; меры предосторожности; предупреждения; показания; противопоказания; информацию о передозировке; побочные реакции; результаты фармакологических исследований на животных, клинических исследований и/или литературные источники. Инструкции могут быть напечатаны непосредственно на контейнере (при возможности), или представлять собой этикетку, прикрепленную к контейнеру, или представлять собой отдельный листок, брошюру, карточку или папку, которые предоставляют в контейнере или вместе с ним.
Методы
Анализ методом проточной цитометрии. Для окрашивания клеточной поверхности клетки можно инкубировать с соответствующими мАт в течение 30 минут на льду, промывать и инкубировать со вторичным реагентом-антителом, при необходимости. Данные проточной цитометрии можно получать на приборе FACS Calibur (Becton Dickinson) и анализировать с помощью программы FlowJo V8.7.1 и 9.4.8.
Отбор и характеризация scFv, специфичных для GPRC5D. Для отбора клонов мАт используют библиотеку фагового дисплея scFv антитела человека. Вкратце, биотинилированное антигены сначала можно смешивать с фаговой библиотекой человеческих scFv, затем комплексы антиген-scFv антитело можно извлекать с помощью конъюгированных со стрептавидином гранул Dynabeads M-280 при пропускании через магнитную решетку. Связавшиеся клоны затем можно элюировать и использовать для инфицирования E. coli XL1-Blue. Фаговые клоны scFv, экспрессированные в бактерии, можно очищать (Yasmina N.A., et al. Probing the binding mechanism and affinity of tanezumab, a recombinant humanized anti-NGF monoclonal antibody, using a repertoire of biosensors. Protein Science 2008; 17(8): 1326-1335; Roberts W.K., et al. Vaccination with CD20 peptides induces a biologically active, specific immune response in mice. Blood 2002: 99 (10): 3748-3755). Можно выполнять 3-4 цикла пэннинга для обогащения фаговых клонов scFv, специфически связывающихся с GPRC5D. Положительные клоны можно определять методом проточной цитометрии против биотинилированного одноцепочечного GPRC5D. Затем положительные клоны можно тестировать на их связывание с GPRC5D на поверхности живых клеток методом проточной цитометрии, используя GPRC5D+ линию клеток, 3T3. Клетки можно промывать и выполнять следующие этапы окрашивания.
Клетки можно окрашивать, сначала используя очищенные фаговые клоны scFv, с последующим добавлением мышиных анти-M13 мАт и, в завершение, антител козы против Ig мыши, конъюгированных с FITC. Каждый этап окрашивание можно выполнять в течение 30-60 минут на льду, и клетки промывать дважды между всеми этапами окрашивания.
Конструирование полноразмерного мАт с использованием выбранных ScFv фрагментов. Полноразмерный IgG человека из выбранных фаговых клонов можно получать в линии клеток HEK293 и клеток яичника китайского хомячка (CHO), как описано (Caron P.C., Class K., Laird W., Co M.S., Queen C., Scheinberg D.A. Engineered humanized dimeric forms of IgG are more effective antibodies. J Exp Med 176:1 191-1 195 (1992). Вкратце, вариабельные области антитела можно субклонировать в экспрессионные векторы млекопитающих с соответствующими человеческими последовательностями константной области лямбда или каппа легкой цепи и человеческими последовательностями константной области IgG. Молекулярную массу очищенного полноразмерного IgG антитела можно измерять методом электрофореза как в восстанавливающих, так и в не восстанавливающих условиях.
Характеризация полноразмерного IgG человека в отношении GPRC5D. Сначала можно определять специфичности полностью человеческих IgG мАт в отношении GPRC5D путем окрашивания клеток 3T3, трансдуцированных для избыточной экспрессии GPRC5D, с последующим использованием вторичного мАт козы против человеческих IgG, конъюгированного с PE или FITC. Интенсивность флуоресценции можно измерять методом проточной цитометрии. Тот же способ можно использовать для определения связывания мАт со свежими опухолевыми клетками и линиями клеток.
Антителозависимая клеточная цитотоксичность (ADCC). Клетками-мишенями, используемыми для изучения ADCC, могут быть клетки 3T3, избыточно экспрессирующие GPRC5D. Анти-GPRC5D антитело или контрольное для него человеческое IgG антитело в различных концентрациях можно инкубировать с клетками-мишенями и свежими МКПК в разных соотношениях эффектор:мишень (Э:М) в течение 16 часов. Супернатант можно собирать и цитотоксичность можно измерять в анализе высвобождения LDH с использованием набора Cytotox 96 (без радиоактивности) от компании Promega в соответствии с инструкциями производителя. Цитотоксичность также можно измерять в стандартном 4-часовом анализе высвобождения 51Cr.
ПРИМЕРЫ
Следующие примеры приведены, чтобы предоставить специалистам в данной области полное раскрытие и описание того, как получать и использовать антитела, биспецифичные антитела, содержащие их композиции, применять скрининг и методы лечения по настоящему изобретению, и не предназначены для ограничения объема того, что авторы заявки считают своим изобретением. Понятно, что различные другие варианты осуществления можно выполнять на практике, учитывая, что основное описание приведено выше.
Пример 1 - Экспрессия GPRC5D в различных тканях
Экспрессию GPRC5D человека оценивали в различных злокачественных и нормальных тканях путем изучения профилей экспрессии генов в базах данных, таких как энциклопедия линий раковых клеток и BioGPS. Как показано на фигуре 2, GPRC5D человека экспрессируется на высоком уровне в клетках множественной миеломы, но не в других злокачественных тканях. Нормальная экспрессия, судя по всему, ограничена плазматическими клетками. Потенциальное уничтожение нацеленными на GPRC5D CAR T-клетками нормальных клеток этого типа не может иметь существенные неблагоприятные последствия, о чем свидетельствует опыт с пациентом авторов изобретения при использовании нацеленных на CD19 CAR T-клеток. Любое отсутствие физиологического продуцирования антител может быть исправлено внутривенным введением иммуноглобулинов.
Пример 2 - Отбор ScFv, специфичных для GPRC5D, с использованием библиотеки фагового дисплея полностью человеческих белков.
Проводили 4 цикла пэннинга библиотеки фагового дисплея против GPRC5D для обогащения фаговых клонов scFv, специфически связывающихся с GPRC5D. Было проведено четыре независимых пэннинга с 12 разными фаговыми библиотеками против избыточно экспрессирующих GPRC5D клеток 3T3, что привело к идентификации 80 положительных клонов. Отдельные фаговые клоны scFv, положительные в отношении GPRC5D, определяли методом ELISA, и клоны, имеющие уникальные кодирующие последовательности ДНК, дополнительно характеризовали. Для проверки того, связываются ли ScFv с GPRC5D на живых клетках, положительные фаговые клоны тестировали на связывание с GPRC5D-положительной линией клеток, 3T3. При скрининге методом FACS были идентифицированы 72 положительных клона из 80 клонов; показатель выявления положительных клонов составил 90%. После секвенирования были обнаружены 32 уникальных и положительных по связыванию с GPRC5D-3T3 клонов из 72 секвенированных положительных клонов; показатель отбора уникальных клонов составил 45%.
Пример 3 - Картирование эпитопов анти-GPRC5D антител
Четыре анти-GPRC5D антитела: ET150-2, ET150-5, ET150-8 и ET150-18 mIgG1. «mIgG1» при использовании во всех примерах указывает на то, что вариабельная область является полностью человеческой, а Fc-часть происходит из IgG1 мыши. Смотри таблицу 34.
Таблица 34
Целевой белок представляет собой GPRC5D человека, имеющий аминокислотную последовательность, приведенную в SEQ ID NO: 97. N-концевая область GPRC5D человека содержит аминокислоты 1-27 из SEQ ID NO: 97. Область внеклеточной петли 1 (ECL1) GPRC5D человека содержит аминокислоты 85-93 из SEQ ID NO: 97. Область внеклеточной петли 2 (ECL2) GPRC5D человека содержит аминокислоты 145-167 из SEQ ID NO: 97. Область внеклеточной петли 3 (ECL3) GPRC5D человека содержит аминокислоты 226-239 из SEQ ID NO: 97.
Методы
Принципы технологии CLIPS. Технология CLIPS позволяет структурно фиксировать пептиды в определенные трехмерные структуры. Результатом этого является функциональная имитация даже самых сложных сайтов связывания. В настоящее время технологию CLIPS повсеместно используют для формирования пептидных библиотек в одно-, двух- или трех-петлевые структуры, а также в складчатые и спиралевидные структуры (фигура 2).
Подробности скрининга комбинаторной библиотеки CLIPS. Скрининг библиотеки CLIPS начинается с превращения целевого белка в библиотеку, включающую вплоть до 10000 перекрывающихся пептидных конструктов, с использованием дизайна комбинаторной матрицы. На твердом носителе синтезируют матрицу линейных пептидов, которые впоследствии преобразуются в CLIPS-конструкты с определенными пространственными структурами (фигура 3). Конструкты, представляющие обе части прерывистого эпитопа в правильной конформации, связывают антитело с высокой аффинностью, которую обнаруживают и количественно определяют. Конструкты, представляющие неполный эпитоп, связывают антитело с более низкой аффинностью, в то время как конструкты, не содержащие эпитоп, совсем не связывают антитело. Информацию об аффинности используют в итерационном скрининге для подробного определения последовательности и конформации эпитопов.
Анализ тепловых карт. Тепловая карта является графическим представлением данных, при котором значения, принимаемые переменной на двухмерной карте, представлены разными цветами. Для двухпетлевых пептидов CLIPS такая двухмерная карта может быть создана из независимых последовательностей первой и второй петель. Например, последовательности 16 CLIPS-пептидов, представленных на фигуре 5, являются эффективными пермутациями 4 уникальных подпоследовательностей в петле 1 (окрашено в синий цвет на фигуре 4) и 4 уникальных подпоследовательностей в петле 2 (окрашено в зеленый цвет на фигуре 4). Таким образом, полученные данные ELISA (окрашено в красный цвет на фигуре 5A) могут быть построены в виде матрицы 4×4, в которой каждая координата X соответствует последовательности первой петли, и каждая координата Y соответствует последовательности второй петли. Например, значение ELISA, наблюдаемое в случае CLIPS-пептида CLSSERERVEDLFEYECELLTSEPIFHCRQEDC (отмечено стрелкой на фигуре 4A) можно найти в третьем ряду, третьей колонки на фигуре 5B (отмечено стрелкой и красным квадратом). Для дальнейшего облегчения визуализации значения ELISA можно заменять цветами из непрерывного градиента. В этом случае чрезвычайно низкие значения окрашены зеленым цветом, чрезвычайно высокие значения окрашены красным цветом, и средние значения окрашены черным цветом (смотри фигуру 5C). Для вышеуказанного примера среднее значение составляет 0,71. Если эту цветовую карту применить к матрице данных, представленной на фигуре 5B, получается цветная тепловая карта (смотри фигуру 5D, оригинальные данные по-прежнему приведены для большей ясности).
Синтез пептидов. Для реконструирования эпитопов целевой молекулы синтезировали библиотеку пептидов. Функционализированную аминогруппами полипропиленовую подложку получали путем привитой сополимеризации с запатентованным препаратом гидрофильного полимера, за которой следовала реакция с t-бутилоксикарбонил-гексаметилендиамином (BocHMDA) с использованием дициклогексилкарбодиимида (DCC) с N-гидроксибензотриазолом (HOBt) и последующее расщепление Boc-групп трифторуксусной кислотой (TFA). Стандартный Fmoc-пептидный синтез использовали для синтеза пептидов на функционализированной аминогруппами твердой подложке с использованием специально модифицированных рабочих станций для дозирования JANUS (Perkin Elmer). Синтез структурных миметиков выполняли с использованием запатентованной технологии химического связывания пептидов на каркасах (CLIPS) компании Pepscan. Технология CLIPS позволяет структурировать пептиды в одиночные петли, двойные петли, тройные петли, складчатые, спиралевидные структуры, а также их сочетания. Матрицы CLIPS связываются с остатками цистеина. Боковые цепи нескольких остатков цистеина в пептидах связываются с одной или двумя матрицами CLIPS. Например, 0,5 мМ раствор P2 CLIPS (2,6-бис(бромметил)пиридина) растворяли в смеси бикарбоната аммония (20 мМ, pH 7,8)/ацетонитрила (1:3 (по объему)). Этот раствор добавляли на матрицы пептидов. Матрица CLIPS связывалась с боковыми цепями двух остатков цистеина, присутствующих в иммобилизованных на твердой фазе пептидах в матрице пептидов (455-луночные планшеты с 3-мкл лунками). Матрицы пептидов осторожно встряхивали в растворе в течение 30-60 минут, при этом они были полностью покрыты раствором. В завершение, матрицы пептидов интенсивно промывали избытком H2O и обрабатывали ультразвуком в деструктурирующем буфере, содержащем 1% SDS/0,1% бета-меркаптоэтанола в PBS (pH 7,2), при 70°C в течение 30 минут, с последующей обработкой ультразвуком в H2O в течение следующих 45 минут. T3 CLIPS несущие пептиды получали аналогичным образом, но в этот раз с тремя остатками цистеина.
Скрининг методом ELISA. Связывание антитела с каждым из синтезированных пептидов тестировали в анализе ELISA на основе технологии компании PEPSCAN. Матрицы пептидов инкубировали с раствором первичного антитела (в течение ночи при 4°C). После промывания матрицы пептидов инкубировали с разведенным 1/1000 конъюгатом соответствующего антитела с пероксидазой (SBA) в течение часа при 25°C. После промывания добавляли субстрат пероксидазы 2,2'-азино-ди-3-этилбензтиазолина сульфонат (ABTS) и 2 мкл/мл 3-процентного раствора H2O2. Через час измеряли развившуюся окраску. Развитие окраски количественно определяли с помощью прибора с зарядовой связью (CCD) - камеры и системы обработки изображений.
Обработка данных. Значения, полученные с помощью CCD камеры, находились в диапазоне от 0 до 3000 mAU, как и в случае стандартного ELISA-ридера для 96-луночных планшетов. Результаты количественно определяли и сохраняли в базу данных Peplab. Время от времени воздушный пузырь в лунке приводил к получению ложноположительных значений; карты вручную инспектировали и любые значения, вызванные воздушными пузырями, принимали за 0.
Контроль качестве синтеза - Для подтверждения качества синтезированных пептидов параллельно синтезировали отдельный набор пептидов в качестве положительного и отрицательного контроля. Проводили их скрининг с использованием антитела 57.9 (ссылка: Posthumus et al., J. Virology, 1990, 64: 3304-3309).
Результаты
Скрининг
Связывание антитела зависит от сочетания факторов, включая концентрацию антитела, а также количество и природу конкурирующих белков в буфере для ELISA. Кроме того, на связывание влияют условия предварительного нанесения (специфическая обработка матриц пептидов перед инкубацией с экспериментальным образцом). Относящиеся к этому данные приведены в таблице 35. Для буфера Pepscan и предварительной обработки (SQ) числа указывают относительное количество конкурирующего белка (сочетание лошадиного сывороточного альбумина и овальбумина).
Таблица 35. Условия скрининга
Антитело ET150-2. При тестировании в условиях умеренной строгости антитело ET150-2 авидно связывает пептиды из всех наборов (фигура 6). Кумулятивный анализ данных показывает, что антитело узнает прерывистый эпитоп, состоящий из пептидных фрагментов 16CDAEGPWGII25 (N-конец), 157MFVNMTPC164 (ECL2) и 229PQFQRQPQW237 (ECL3), при этом для связывания достаточно лишь пептидных фрагментов 16CDAEGPWGII25 и 229PQFQRQPQW237.
Антитело ET150-5. При тестировании в условиях высокой строгости антитело ET150-5 авидно связывает пептиды из всех наборов (фигура 7). Кумулятивный анализ данных показывает, что антитело узнает прерывистый эпитоп, состоящий из пептидных фрагментов 5CIESTGDYFLLCD17 (N-конец), 85NQQTAPVRYFL95 (ECL1) и 157MFVNMTPC164 (ECL2), при этом для связывания достаточно одного пептидного фрагмента 5CIESTGDYFLCD17.
Антитело ET150-18. При тестировании в условиях высокой строгости антитело ET150-18 связывает пептиды из набора 4 и набора 7, которые содержат пептиды с закрепленной структурой. Никакого существенного связывания не было отмечено для наборов, содержащих линейные пептиды (фигура 8). Кумулятивный анализ данных показывает, что антитело узнает прерывистый эпитоп, состоящий из фрагментов 10GDYFLLCD17 (N-конец), 157MFVNMTPCQLN167 (ECL2) и 227GNPQFQRQPQW237 (ECL3). Пептидные фрагменты 10GDYFLLCD17 и 227GNPQFQRQPQW237 представляют ядро эпитопа, поскольку оба пептидных фрагмента в отдельности достаточны для связывания.
Антитело ET150-8. При тестировании в условиях высокой строгости антитело ET150-8 связывает пептиды из всех наборов, за исключением набора 2 (фигура 9). Кумулятивный анализ данных показывает, что антитело узнает прерывистый эпитоп, состоящий из пептидных фрагментов 15LCDAEGPWG23 (N-конец) и 230QFQRQPQWDDPVVC243 (ECL3), при этом пептидный фрагмент 15LCDAEGPWG23 является доминантной частью эпитопа, поскольку его одного достаточно для связывания. Кроме того, сравнение результатов, полученных для набора 1 (линейные) и набора 4 (петля), показывает, что введение структурных ограничений для миметиков эпитопов приводит к усилению связывания пептидов, особенно в случае пептидов, содержащих последовательность 230QFQRQPQWDDPVVC243.
Выводы
Все изучаемые антитела узнавали прерывистые эпитопы, которые были картированы с использованием матриц Pepscan. Предварительные коровые эпитопы приведены в таблице 36. Все антитела обычно узнавали перекрывающиеся области на N-конце белка в сочетании с областями из одной или двух областей ECL. Два антитела ET150-18 и ET150-8 продемонстрировали потребность в структурных ограничениях для поддержания связывания антитела, это указывает на то, что данные два антитела узнают не только прерывистые, но также и конформационные эпитопы. Антитела ET150-2 и ET150-5 не обнаруживали заметных различий в связывании линейных и петлевых пептидов.
Таблица 36. Список эпитопов
*) доминантная часть
На фигуре 10 приведены результаты изучения общей организации GPCR. Поскольку N-конец является очень гибким и неструктурированным, вероятно, он временно взаимодействует с областями ECL, образуя прерывистые иммунодоминантные области.
Различия и сходство связывания пептидов могут быть проиллюстрированы с помощью анализа диаграммы рассеяния данных на фигуре 11. Точки данных в верхнем левом и нижнем правом углах указывают на различия в связывании. Несмотря на значительное перекрывание эпитопов, детальные особенности эпитопов отдельных антител различаются в большой степени.
Пример 4 - Данные скрининга для анти-GPRC5D антител
FACS-скрининг. На фигуре 12 представлены результаты FACS-анализа фаговых клонов GPRC5D-специфичных антител (ET150-1, ET150-2, ET150-5, ET150-8, ET150-18). Фаговые клоны инкубировали с клетками линии 3T3-GPRC5D, затем с анти-M13 антителом мыши. В завершение, APC-меченое 2-е антитело против IgG мыши добавляли в реакционную смесь после промывания. Связывание измеряли методом FACS и выражали в единицах средней интенсивности флуоресценции (СИФ). Клетки, инкубированные с M13 K07 хелперным фагом, и просто клетки использовали в качестве отрицательного контроля.
Пример 5 - Аффинность связывания анти-GPRC5D антител
На фигуре 13 представлены результаты FACS-анализа фаговых клонов GPRC5D-специфичных антител (ET150-2, ET150-5, ET150-8, ET150-18). Каждое антитело (ET150-2, ET150-5, ET150-8, ET150-18) в концентрации 10 или 1 мкг/мл инкубировали с клетками 3T3 или 3T3-GPRC5D, затем проводили инкубацию с анти-M13 антителом мыши. В завершение, в реакционную смесь добавляли PE-меченое 2-е антитело против IgG мыши. Связывание измеряли методом FACS и выражали в единицах средней интенсивности флуоресценции (СИФ) (фигура 13). Клетки, инкубированные только со 2-м антителом, с контролем по изотипу ET901 mIgG1, и просто клетки использовали в качестве отрицательных контролей.
Пример 6 - Биспецифичные антитела, специфичные для GPRC5D и CD3.
На фигуре 14 представлены результаты FACS-анализа анти-GPRC5D/анти-CD3 биспецифичных антител, полученных с использованием клонов ET150-2, ET150-5, ET150-8, ET150-18, описанных в настоящем документе. Каждое антитело в концентрации 10 мкг/мл инкубировали с клетками 3T3 или 3T3-GPRC5D, с последующей инкубацией с FITC-конъюгированным антителом против His-метки. Связывание измеряли методом FACS и выражали в единицах средней интенсивности флуоресценции (СИФ). Клетки, инкубированные только со 2-м антителом, биспецифичным контрольным антителом ET901, и просто клетки использовали в качестве отрицательных контролей. Как показано на фигуре 14, анти-GPRC5D/CD3 биспецифичные антитела, полученные с использованием описанных scFv, специфически связывались с клетками 3T3, экспрессирующими GPRC5D.
Хотя настоящее изобретение было описано в некоторых подробностях и проиллюстрировано примерами для ясности понимания, приведенное описание и примеры не должны быть истолкованы как ограничивающие объем настоящего изобретения. Содержание всех патентов и специальных литературных источников, цитированных в настоящем документе, специально включено в настоящий документ посредством ссылки.
| название | год | авторы | номер документа |
|---|---|---|---|
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, НАЦЕЛЕННЫЕ НА РЕЦЕПТОР, СВЯЗАННЫЙ С G-БЕЛКАМИ, И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2762359C2 |
| АНТИТЕЛА, НАЦЕЛЕННЫЕ НА АНТИГЕН СОЗРЕВАНИЯ В-КЛЕТОК, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2766094C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, НАЦЕЛЕННЫЕ НА АНТИГЕН СОЗРЕВАНИЯ В-КЛЕТОК, И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2761632C2 |
| АНТИ-C5 АНТИТЕЛА И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2774716C2 |
| ГУМАНИЗИРОВАННЫЕ АНТИ-C5 АНТИТЕЛА И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2792237C2 |
| АНТИТЕЛА ПРОТИВ ПРЕДСТАВИТЕЛЯ А5 СЕМЕЙСТВА 19 СО СХОДСТВОМ ПОСЛЕДОВАТЕЛЬНОСТЕЙ И СПОСОБ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2785436C2 |
| АНТИТЕЛА К ФАКТОРУ XI И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2739946C2 |
| АНТИ-VEGF-АНТИТЕЛО И СОДЕРЖАЩАЯ ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРЕДУПРЕЖДЕНИЯ, ДИАГНОСТИКИ ИЛИ ЛЕЧЕНИЯ РАКА ИЛИ СВЯЗАННОГО С АНГИОГЕНЕЗОМ ЗАБОЛЕВАНИЯ | 2014 |
|
RU2644245C2 |
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА ЧЕЛОВЕКА К БЕЛКУ ПРОГРАММИРУЕМОЙ СМЕРТИ 1 (PD-1) И СПОСОБЫ ЛЕЧЕНИЯ РАКА С ИСПОЛЬЗОВАНИЕМ АНТИ-PD-1-АНТИТЕЛ САМОСТОЯТЕЛЬНО ИЛИ В КОМБИНАЦИИ С ДРУГИМИ ИММУНОТЕРАПЕВТИЧЕСКИМИ СРЕДСТВАМИ | 2016 |
|
RU2732924C2 |
| АНТИТЕЛА ПРОТИВ АЛЬФА5-БЕТА 1 И ИХ ПРИМЕНЕНИЕ | 2009 |
|
RU2528736C2 |
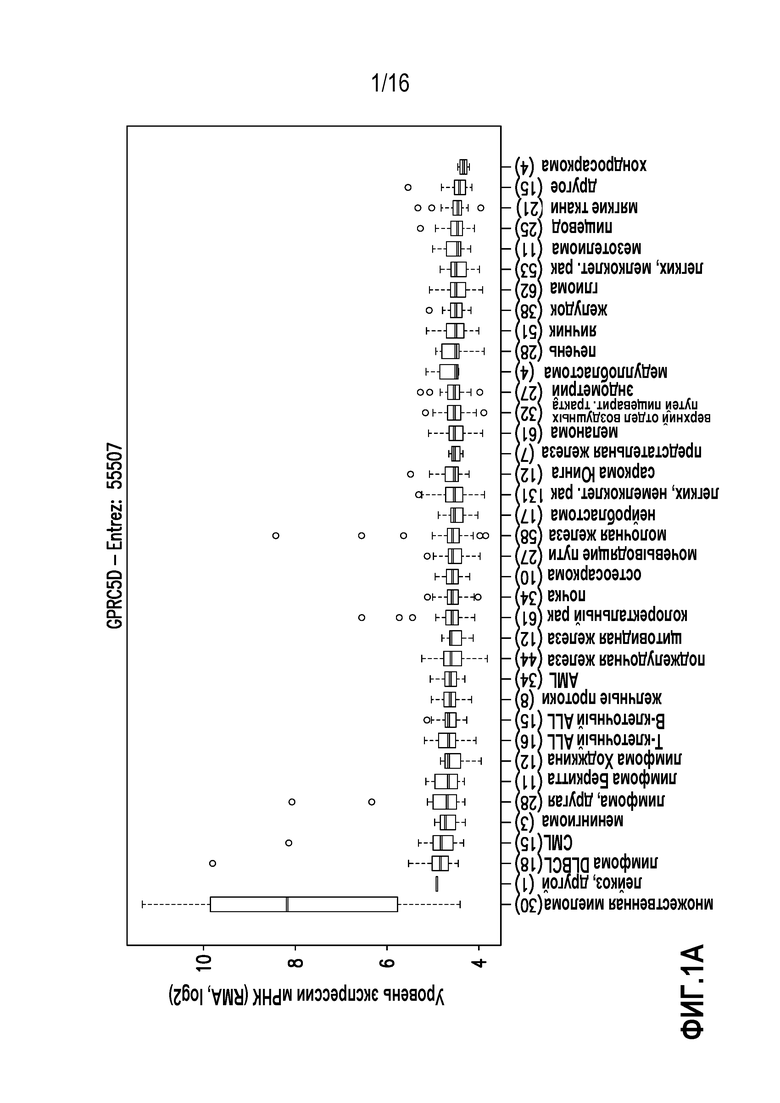
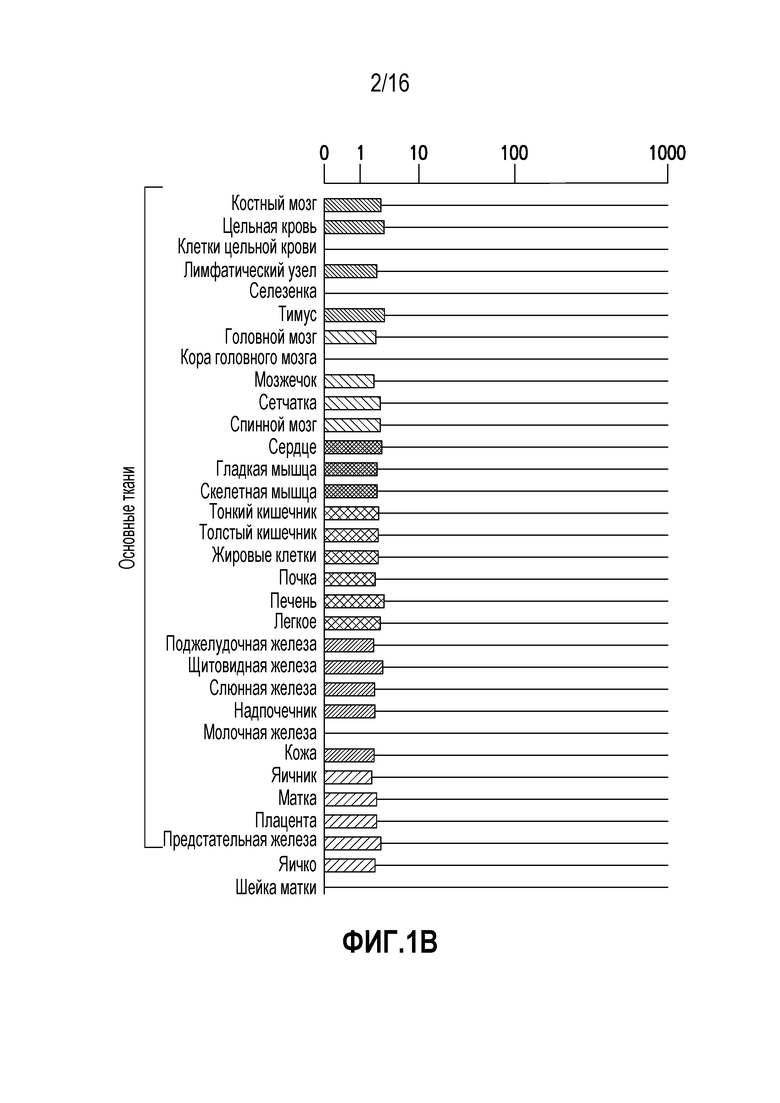
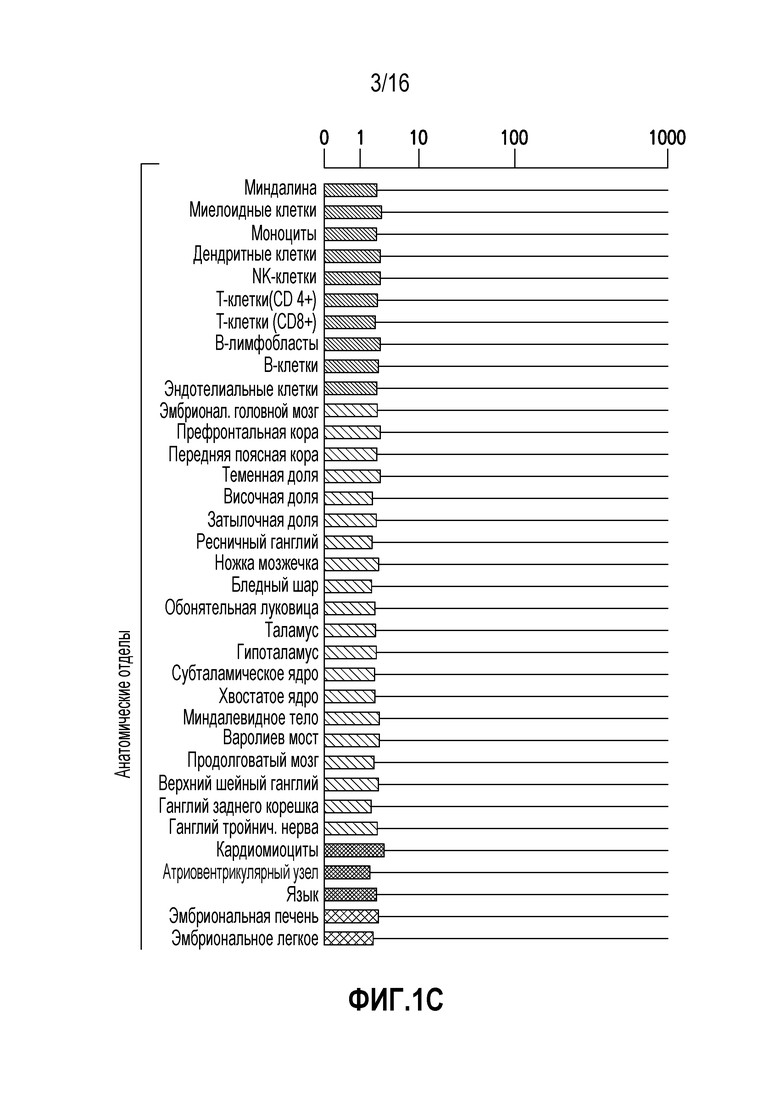

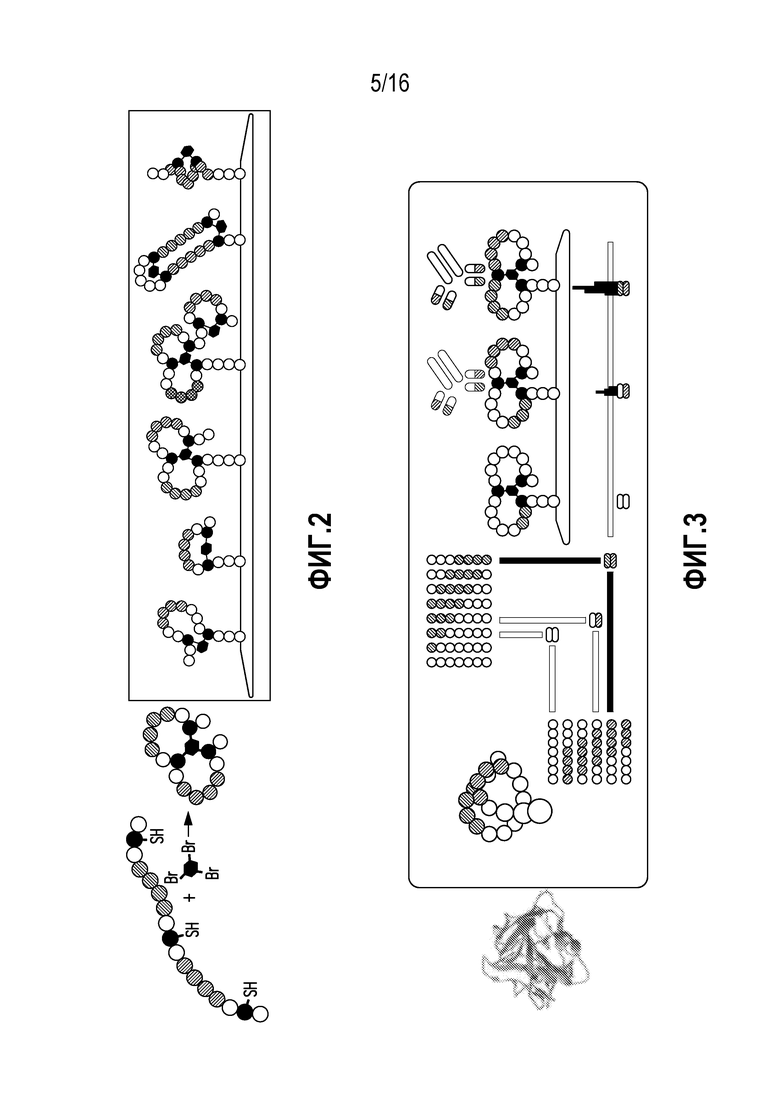
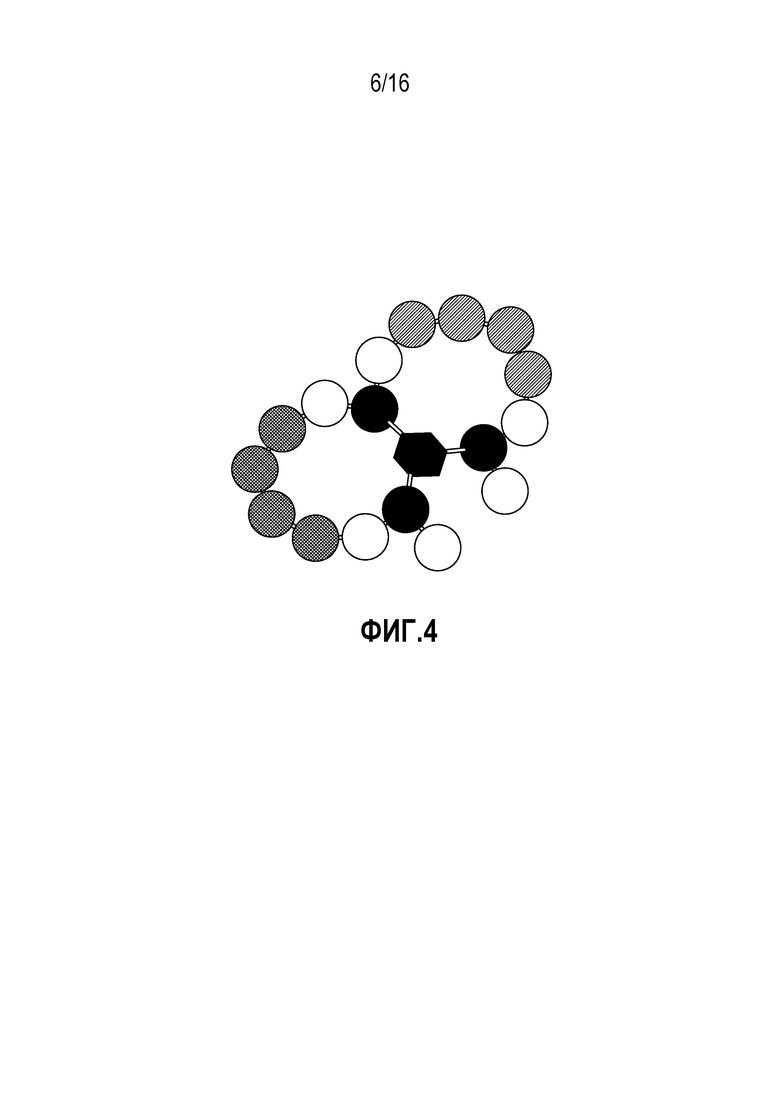
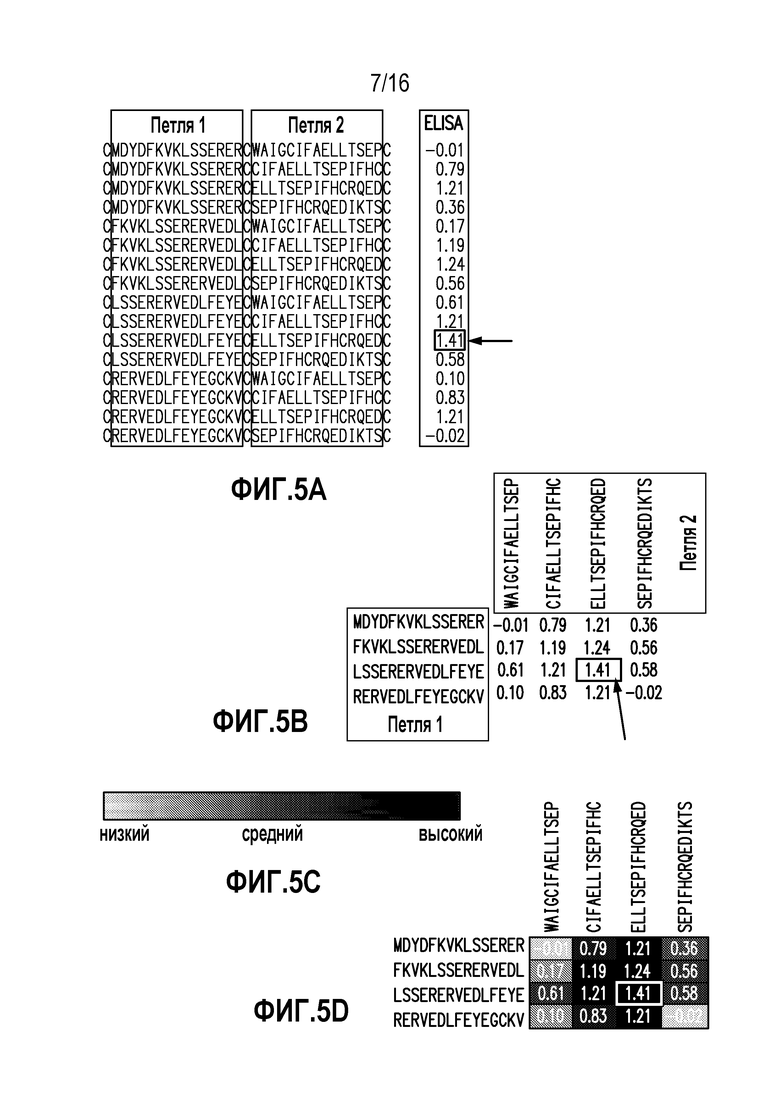
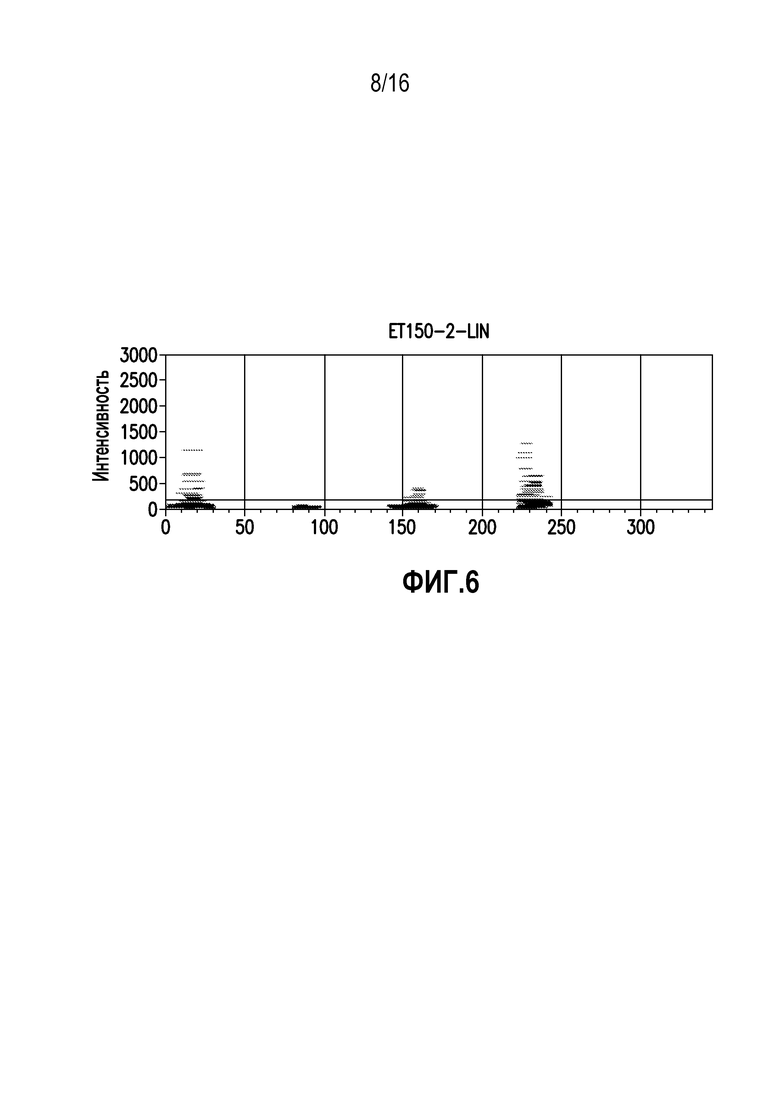

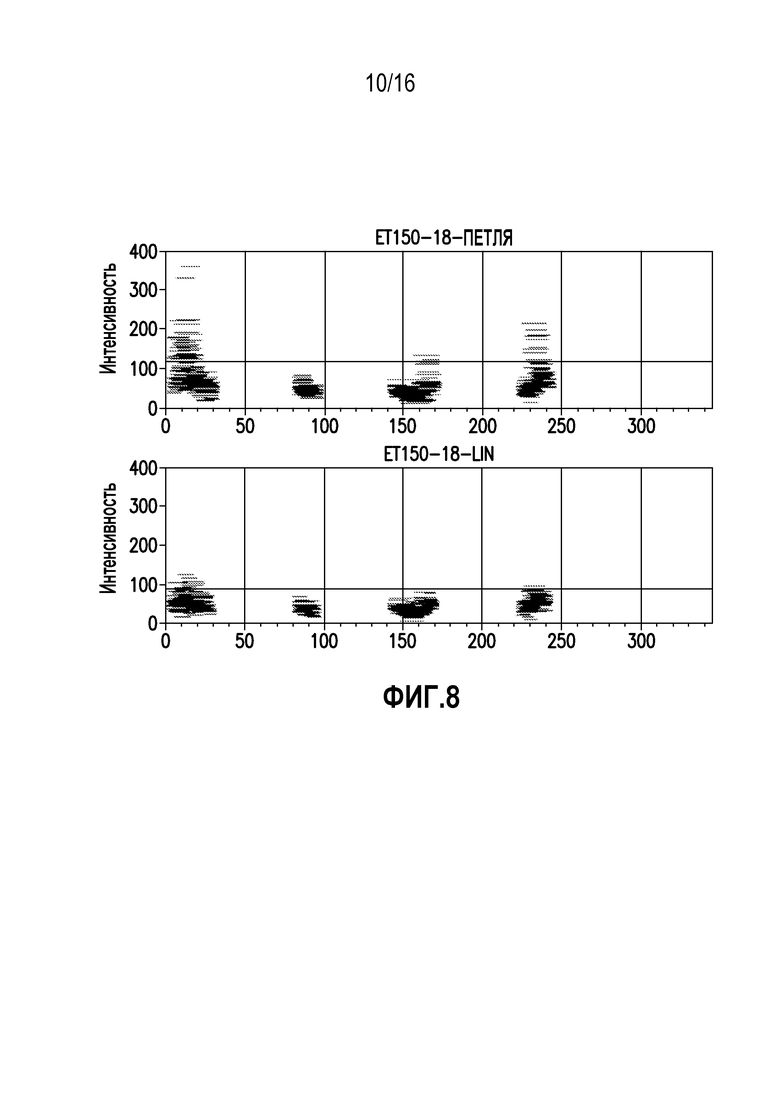
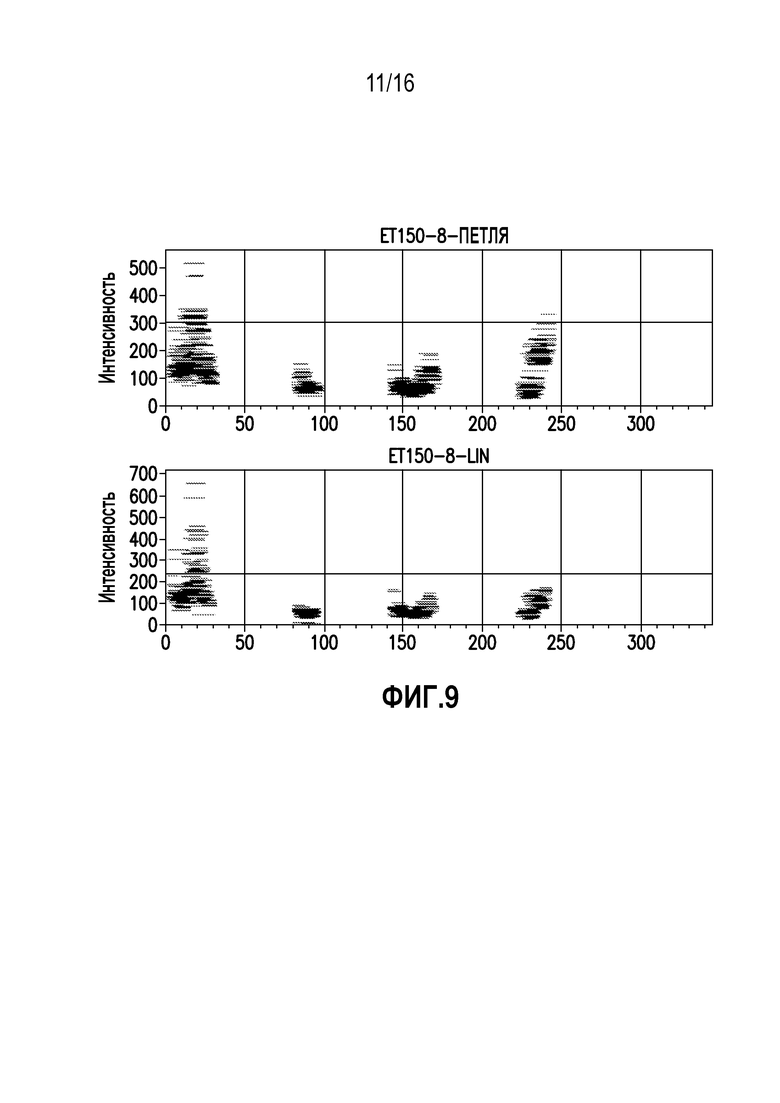
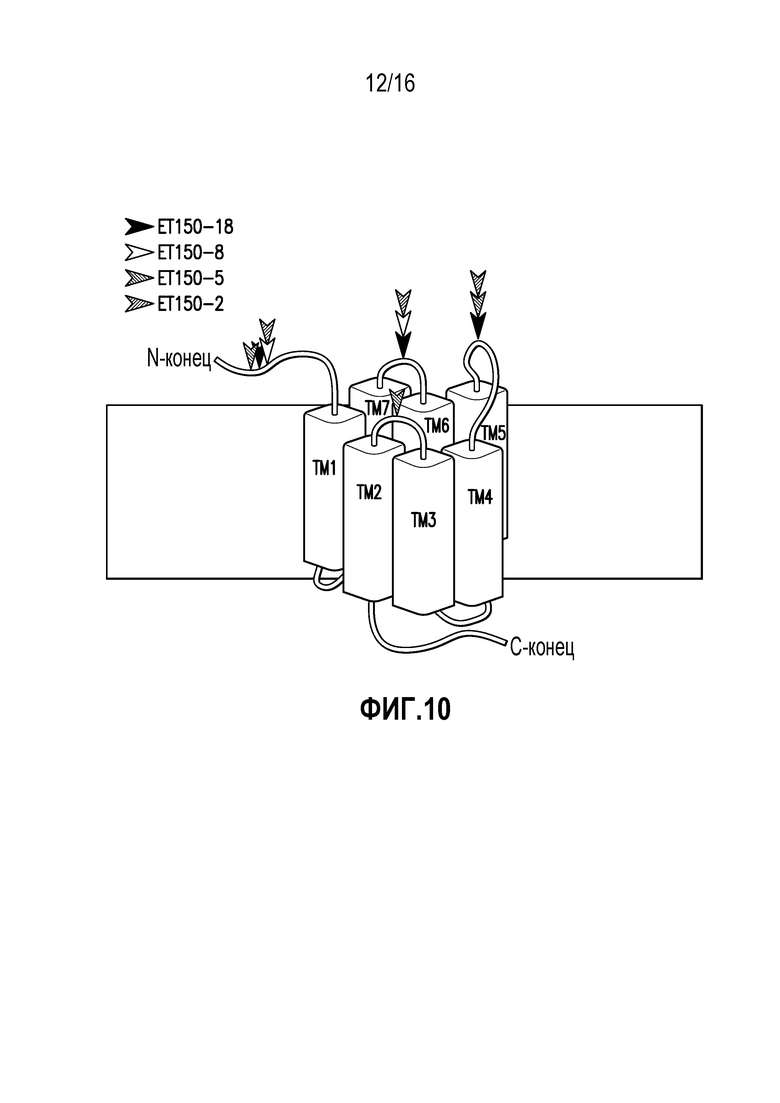
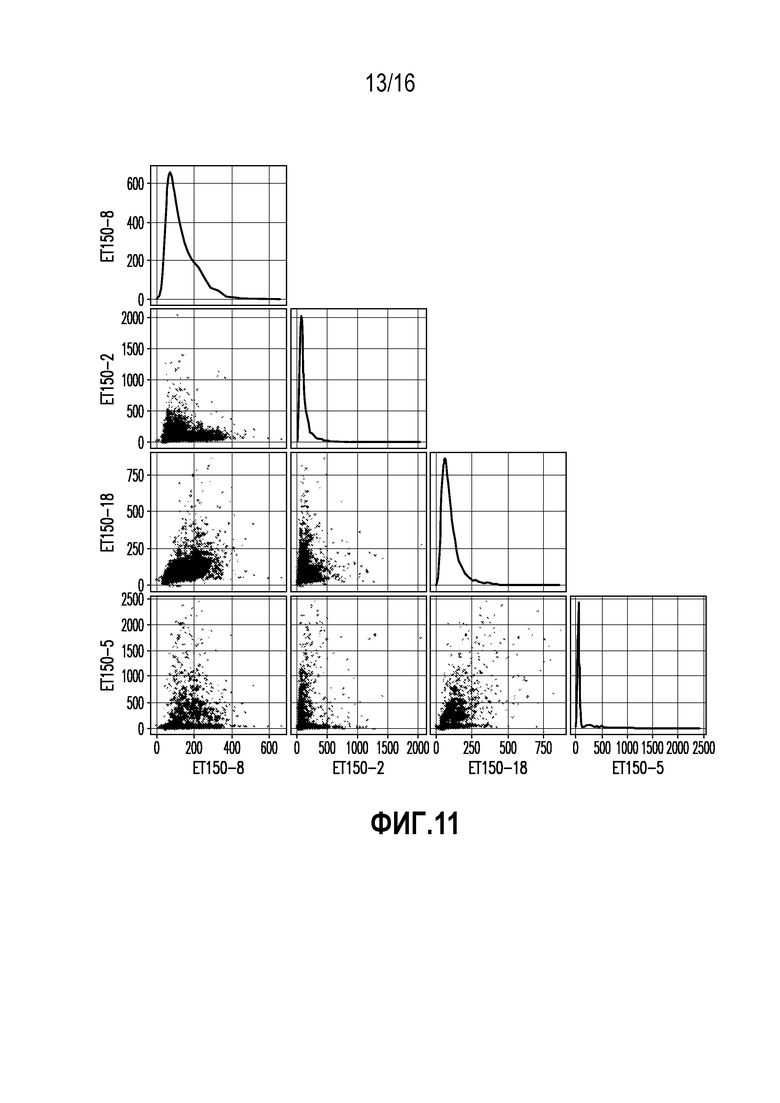
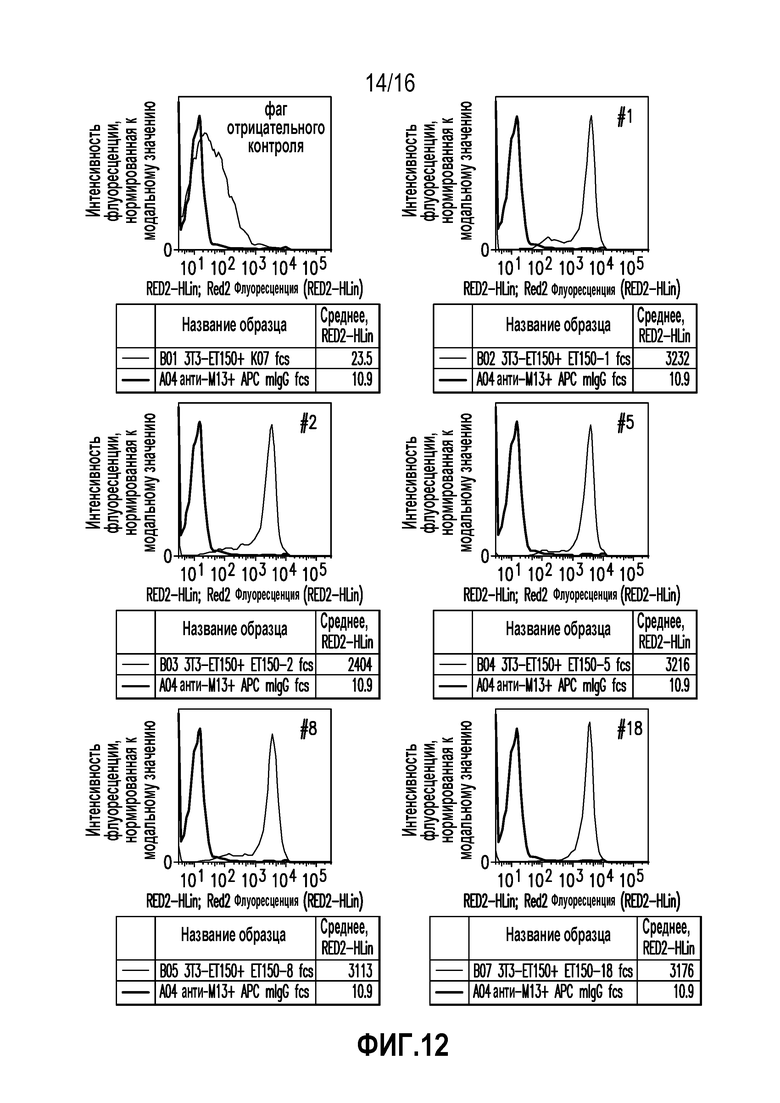
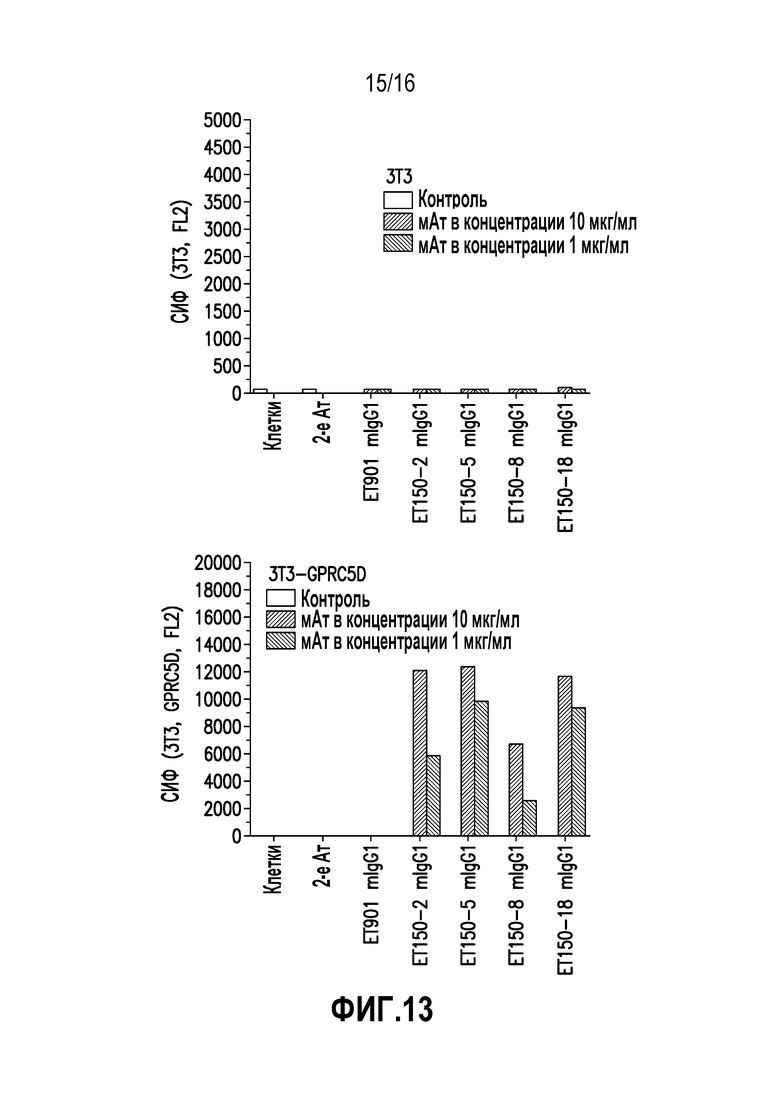

Изобретение относится к биотехнологии и медицине, в частности к антителам, которые связываются с GPRC5D, и способам их применения для лечения опухоли. Изобретение позволяет осуществлять эффективное лечение опухоли, опосредованной GPRC5D. 14 н. и 42 з.п. ф-лы, 14 ил., 36 табл., 6 пр.
1. Антитело, которое связывается с рецептором, связанным с G-белками, представителем D группы 5 семейства C рецепторов (GPRC5D), или его антигенсвязывающий фрагмент, содержащее(ий):
(i) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 130; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 131; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 132; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 133; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 134; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 135;
(ii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 142; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 143; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 144; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 145; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 146; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 147;
(iii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 154; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 155; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 156; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 157; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 158; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 159;
(iv) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 160; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 161; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 162; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 163; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 164; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 165;
(v) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 166; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 167; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 168; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 169; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 170; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 171;
(vi) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 172; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 173; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 174; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 175; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 176; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 177;
(vii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 178; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 179; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 180; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 181; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 182; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 183;
(viii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 184; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 185; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 186; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 187; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 188; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 189;
(ix) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 190; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 191; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 192; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 193; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 194; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 195;
(x) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 196; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 197; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 198; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 199; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 200; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 201;
(xi) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 202; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 203; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 204; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 205; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 206; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 207;
(xii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 208; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 209; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 210; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 211; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 212; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 213;
(xiii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 214; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 215; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 216; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 217; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 218; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 219;
(xiv) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 220; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 221; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 222; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 223; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 224; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 225;
(xv) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 226; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 227; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 228; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 229; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 230; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 231;
(xvi) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 232; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 233; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 234; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 235; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 236; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 237;
(xvii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 238; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 239; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 240; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 241; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 242; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 243;
(xviii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 244; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 245; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 246; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 247; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 248; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 249;
(xix) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 250; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 251; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 252; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 253; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 254; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 255;
(xx) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 256; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 257; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 258; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 259; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 260; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 261;
(xxi) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 262; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 263; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 264; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 265; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 266; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 267;
(xxii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 292; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 293; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 294; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 295; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 296; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 297;
(xxiii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 303; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 304; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 305; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 306; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 307; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 308;
(xxiv) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 316; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 317; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 318; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 319; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 320; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 321;
(xxv) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 328; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 329; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 330; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 331; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 332; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 333;
(xxvi) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 340; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 341; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 342; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 343; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 344; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 345; или
(xxvii) CDR1 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 352; CDR2 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 353; CDR3 вариабельной области тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 354; CDR1 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 355; CDR2 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 356; и CDR3 вариабельной области легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 357.
2. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент, содержащее(ий):
(i) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 5, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 6;
(ii) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 13, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 14;
(iii) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 21, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 22;
(iv) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 25, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 26;
(v) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 29, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 30;
(iv) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 33, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 34;
(vii) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 37, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 38;
(viii) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 41, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 42;
(ix) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 45, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 46;
(x) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 49, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 50;
(xi) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 53, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 54;
(xii) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 57, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 58;
(xiii) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 61, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 62;
(xiv) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 65, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 66;
(xv) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 69, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 70;
(xvi) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 73, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 74;
(xvii) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 77, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 78;
(xviii) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 81, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 82;
(xix) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 85, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 86;
(xx) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 89, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 90;
(xxi) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 93, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 94;
(xxii) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 298, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 299;
(xxiii) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 310, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 311;
(xxiv) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 322, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 323;
(xxv) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 334, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 335;
(xxvi) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 346, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 347;
(xxvii) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи SEQ ID NO: 358, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи SEQ ID NO: 359.
3. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по п. 1 или 2, в котором вариабельная область тяжелой цепи содержит аминокислотную последовательность, которая по меньшей мере на 90% идентична аминокислотной последовательности SEQ ID NO: 5, SEQ ID NO: 13, SEQ ID NO: 21, SEQ ID NO: 25, SEQ ID NO: 29, SEQ ID NO: 33, SEQ ID NO: 37, SEQ ID NO: 41, SEQ ID NO: 45, SEQ ID NO: 49, SEQ ID NO: 53, SEQ ID NO: 57, SEQ ID NO: 61, SEQ ID NO: 65, SEQ ID NO: 69, SEQ ID NO: 73, SEQ ID NO: 77, SEQ ID NO: 81, SEQ ID NO: 85, SEQ ID NO: 89, SEQ ID NO: 93, SEQ ID NO: 298, SEQ ID NO: 310, SEQ ID NO: 322, SEQ ID NO: 334, SEQ ID NO: 346 или SEQ ID NO: 358.
4. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, в котором вариабельная область легкой цепи содержит аминокислотную последовательность, которая по меньшей мере на 90% идентична аминокислотной последовательности SEQ ID NO: 6, SEQ ID NO: 14, SEQ ID NO: 22, SEQ ID NO: 26, SEQ ID NO: 30, SEQ ID NO: 34, SEQ ID NO: 38, SEQ ID NO: 42, SEQ ID NO: 46, SEQ ID NO: 50, SEQ ID NO: 54, SEQ ID NO: 58, SEQ ID NO: 62, SEQ ID NO: 66, SEQ ID NO: 70, SEQ ID NO: 74, SEQ ID NO: 78, SEQ ID NO: 82, SEQ ID NO: 86, SEQ ID NO: 90, SEQ ID NO: 94, SEQ ID NO: 299, SEQ ID NO: 311, SEQ ID NO: 323, SEQ ID NO: 335, SEQ ID NO: 347 или SEQ ID NO: 359.
5. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-4, в котором:
(i) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 5; и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 6;
(ii) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 13; и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 14;
(iii) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 21; и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 22;
(iv) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 25; и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 26;
(v) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 29; и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 30;
(vi) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 33; и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 34;
(vii) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 37; и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 38;
(viii) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 41; и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 42;
(ix) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 45; и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 46;
(x) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 49; и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 50;
(xi) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 53; и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 54;
(xii) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 57; и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 58;
(xiii) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 61; и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 62;
(xiv) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 65, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 66;
(xv) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 69, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 70;
(xvi) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 73, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 74;
(xvii) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 77, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 78;
(xviii) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 81, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 82;
(xix) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 85, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 86;
(xx) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 89, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 90;
(xxi) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 93, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 94;
(xxii) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 298, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 299;
(xxiii) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 310, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 311;
(xxiv) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 322, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 323;
(xxv) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 334, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 335;
(xxvi) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 346, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 347; или
(xxvii) вариабельная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO: 358, и вариабельная область легкой цепи содержит аминокислотную последовательность SEQ ID NO: 359.
6. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-5, где GPRC5D представляет собой GPRC5D человека.
7. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-6, где GPRC5D содержит аминокислотную последовательность SEQ ID NO: 97.
8. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-7, где анти-GPRC5D антитело или его антигенсвязывающий фрагмент связывается с одной, двумя, тремя или четырьмя эпитопными областями, выбранными из группы, состоящей из:
эпитопной области в N-концевой области, содержащей аминокислоты 1-27 последовательности SEQ ID NO: 97,
эпитопной области в области ECL1, содержащей аминокислоты 85-93 последовательности SEQ ID NO: 97,
эпитопной области в области ECL2, содержащей аминокислоты 145-167 последовательности SEQ ID NO: 97, и
эпитопной области в области ECL3, содержащей аминокислоты 226-239 последовательности SEQ ID NO: 97.
9. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-8, где анти-GPRC5D антитело или его антигенсвязывающий фрагмент связывается с эпитопной областью, содержащей аминокислоты 16-23 последовательности SEQ ID NO: 97.
10. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-9, где анти-GPRC5D антитело или его антигенсвязывающий фрагмент связывается с эпитопной областью, содержащей аминокислоты 15-23 последовательности SEQ ID NO: 97.
11. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-10, где анти-GPRC5D антитело или его антигенсвязывающий фрагмент связывается с эпитопной областью, содержащей аминокислоты 16-25 последовательности SEQ ID NO: 97.
12. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-11, где анти-GPRC5D антитело или его антигенсвязывающий фрагмент связывается с эпитопной областью, содержащей аминокислоты 10-17 последовательности SEQ ID NO: 97.
13. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-12, где анти-GPRC5D антитело или его антигенсвязывающий фрагмент связывается с эпитопной областью, содержащей аминокислоты 5-17 последовательности SEQ ID NO: 97.
14. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-13, где анти-GPRC5D антитело или его антигенсвязывающий фрагмент связывается с эпитопной областью, содержащей аминокислоты 85-95 последовательности SEQ ID NO: 97.
15. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-14, где анти-GPRC5D антитело или его антигенсвязывающий фрагмент связывается с эпитопной областью, содержащей аминокислоты 157-164 последовательности SEQ ID NO: 97.
16. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-15, где анти-GPRC5D антитело или его антигенсвязывающий фрагмент связывается с эпитопной областью, содержащей аминокислоты 157-167 последовательности SEQ ID NO: 97.
17. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-16, где анти-GPRC5D антитело или его антигенсвязывающий фрагмент связывается с эпитопной областью, содержащей аминокислоты 230-237 последовательности SEQ ID NO: 97.
18. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-17, где анти-GPRC5D антитело или его антигенсвязывающий фрагмент связывается с эпитопной областью, содержащей аминокислоты 229-237 последовательности SEQ ID NO: 97.
19. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-18, где анти-GPRC5D антитело или его антигенсвязывающий фрагмент связывается с эпитопной областью, содержащей аминокислоты 230-243 последовательности SEQ ID NO: 97.
20. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-19, где анти-GPRC5D антитело или его антигенсвязывающий фрагмент связывается с эпитопной областью, содержащей аминокислоты 227-237 последовательности SEQ ID NO: 97.
21. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-20, содержащее(ий) аминокислотную последовательность SEQ ID NO: 101, SEQ ID NO: 103, SEQ ID NO: 105, SEQ ID NO: 106, SEQ ID NO: 107, SEQ ID NO: 108, SEQ ID NO: 109, SEQ ID NO: 110 , SEQ ID NO: 111, SEQ ID NO: 112, SEQ ID NO: 113, SEQ ID NO: 114, SEQ ID NO: 115, SEQ ID NO: 116, SEQ ID NO: 117, SEQ ID NO: 118, SEQ ID NO: 119, SEQ ID NO: 120, SEQ ID NO: 121, SEQ ID NO: 122, SEQ ID NO: 123, SEQ ID NO: 300, SEQ ID NO: 312, SEQ ID NO: 324, SEQ ID NO: 336, SEQ ID NO: 348 или SEQ ID NO: 360.
22. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-21, где антитело или его антигенсвязывающий фрагмент связывается с GPRC5D человека с аффинностью связывания (Kd), равной от около 1×10-9M до около 1×10-8 M.
23. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-22, где антитело содержит каркасную область вариабельной области человека.
24. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-22, которое(ый) представляет собой полноразмерное антитело человека или его антигенсвязывающий фрагмент.
25. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-22, которое(ый) представляет собой химерное антитело или его антигенсвязывающий фрагмент.
26. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-22, которое(ый) представляет собой гуманизированное антитело или его антигенсвязывающий фрагмент.
27. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-26, где антигенсвязывающий фрагмент антитела представляет собой антигенсвязывающий фрагмент (Fab), Fab', F(ab')2, вариабельный фрагмент (Fv) или одноцепочечный Fv (scFv).
28. Композиция для лечения опухоли, содержащая анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-27 и фармацевтически приемлемый носитель.
29. Иммуноконъюгат для лечения опухоли, содержащий анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-27, связанный с терапевтическим средством, выбранным из группы, состоящей из лекарственного средства, цитотоксина или радиоактивного изотопа.
30. Иммуноконъюгат по п. 29, где опухоль представляет собой множественную миелому или макроглобулинемию Вальденстрема.
31. Композиция для лечения опухоли, содержащая иммуноконъюгат по п. 29 или 30 и фармацевтически приемлемый носитель.
32. Биспецифическая молекула для лечения опухоли, содержащая анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-27, связанная со второй функциональной группой, выбранной из группы, состоящей из антитела, фрагмента антитела, пептида или связывающего миметика.
33. Биспецифическая молекула по п. 32, где опухоль представляет собой множественную миелому или макроглобулинемию Вальденстрема.
34. Биспецифическая молекула по п. 32, в которой вторая функциональная группа имеет отличную специфичность связыванию от специфичности связывания анти-GPRC5D антитела или антигенсвязывающего фрагмента.
35. Биспецифическая молекула по п. 34, где вторая функциональная группа обладает специфичностью связывания с иммунной клеткой.
36. Биспецифическая молекула по п. 34, где вторая функциональная группа специфически связывается с CD3.
37. Композиция для лечения опухоли, содержащая биспецифическую молекулу по любому из пп. 32-36 и фармацевтически приемлемый носитель.
38. Композиция по любому из пп.28, 31 и 37, где опухоль представляет собой множественную миелому или макроглобулинемию Вальденстрема.
39. Молекула нуклеиновой кислоты, которая кодирует анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-27.
40. Вектор экспрессии, содержащий молекулу нуклеиновой кислоты по п. 39.
41. Клетка-хозяин для экспрессии анти-GPRC5D антитела или антигенсвязывающего фрагмента, содержащая вектор экспрессии по п. 40.
42. Способ детекции GPRC5D в цельной клетке или ткани, включающий:
приведение клетки или ткани в контакт с анти-GPRC5D антителом или с его антигенсвязывающим фрагментом по любому из пп. 1-27, где анти-GPRC5D антитело или его антигенсвязывающий фрагмент содержит метку для детекции; и
определение количества меченного анти-GPRC5D антитела или его антигенсвязывающего фрагмента, связанного с клеткой или тканью, путем измерения количества метки для детекции, связанной с клеткой или тканью, при этом количество связанного анти-GPRC5D антитела или его антигенсвязывающего фрагмента является показателем количества GPRC5D в клетке или ткани.
43. Способ лечения опухоли у пациента, включающий введение пациенту эффективного количества анти-GPRC5D антитела или его антигенсвязывающего фрагмента по любому из пп. 1-27, иммуноконъюгата по п. 29 или 30, биспецифической молекулы по любому из пп. 32-36 или композиции по любому из пп. 28, 31 и 37, где опухоль представляет собой множественную миелому или макроглобулинемию Вальденстрема.
44. Способ по п. 43, где способ уменьшает количество опухолевых клеток.
45. Способ по п. 43, где способ уменьшает размер опухоли.
46. Способ по п. 43, где способ уничтожает опухоль у пациента.
47. Способ по любому из пп. 43-46, где опухоль представляет собой множественную миелому.
48. Способ по любому из пп. 43-47, где пациент представляет собой человека.
49. Применение анти-GPRC5D антитела или его антигенсвязывающего фрагмента по любому из пп. 1-27, иммуноконъюгата по п. 29 или 30, биспецифической молекулы по любому из пп. 32-36 или композиции по любому из пп. 28, 31 и 37 для лечения опухоли, где опухоль представляет собой множественную миелому или макроглобулинемию Вальденстрема.
50. Применение по п. 49, где опухоль представляет собой множественную миелому.
51. Анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-27, иммуноконъюгат по п. 29 или 30, биспецифическая молекула по любому из пп. 32-36 или композиция по любому из пп. 28, 31 или 37 для лечения опухоли у пациента, где опухоль представляет собой множественную миелому или макроглобулинемию Вальденстрема.
52. Анти-GPRC5D или его антигенсвязывающий фрагмент по п. 51, где опухоль представляет собой множественную миелому.
53. Набор для лечения опухоли, содержащий анти-GPRC5D антитело или его антигенсвязывающий фрагмент по любому из пп. 1-27.
54. Набор по п. 53, где набор дополнительно содержит письменные инструкции по применению анти-GPRC5D антитела или его антигенсвязывающего фрагмента для лечения пациента с опухолью.
55. Набор по п. 53 или 54, где опухоль представляет собой множественную миелому или макроглобулинемию Вальденстрема.
56. Набор по любому из пп. 53-55, где опухоль представляет собой множественную миелому.
| US 20050019320 A1, 27.01.2005 | |||
| US 20030207288 A1, 06.11.2003 | |||
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА ДЛЯ ЛЕЧЕНИЯ ОПУХОЛЕЙ | 2009 |
|
RU2531758C2 |
Авторы
Даты
2020-07-06—Публикация
2015-12-04—Подача