Область техники
Настоящее изобретение относится к новой системе и способу удаления хлорида из промышленных сточных вод с производства удобрений и, в частности, сточных вод с производства нитрофосфатных удобрений или сточных вод с процессов производства других минеральных или органоминеральных удобрений.
Уровень техники
Промышленные сточные воды являются одним из важных источников загрязнения водной среды. В течение прошлого столетия огромное количество промышленных сточных вод было слито в реки, озера и прибрежные территории. Это привело к серьезным проблемам загрязнения в водной среде и оказало негативное влияние на экосистему.
Существует много типов промышленных сточных вод исходя из различных отраслей промышленности и примесей; каждая отрасль производит свою собственную комбинацию загрязняющих веществ. Подобно различным характеристикам промышленных сточных вод, обработку промышленных сточных вод необходимо разрабатывать специально для конкретного типа произведенного сброса.
Во многих промышленных системах целью является уменьшение количества сточных вод, сливаемых в окружающую среду, путем рециркуляции сброса сточных вод обратно в саму промышленную систему.
В промышленности по производству удобрений природа сточных вод может меняться в зависимости от типа производимого удобрения и задействованных процессов.
Минеральные удобрения содержат одно или более основных (главных) питательных веществ азот (N), фосфор (Р) или калий (K) в неорганической форме или в виде мочевины или цианамида. Основные питательные вещества N, Р и K необходимы растениям в больших или умеренных количествах. В зависимости от состава, минеральные удобрения также содержат другие питательные вещества, необходимые растениям в меньшей степени, такие как Са, Mg, и S. Микроэлементы, необходимые в малых количествах, представляют собой В, Cl, Cu, Fe, Mn, Mo, Zn. Удобрения классифицируют исходя из содержания их главных питательных веществ: простые удобрения содержат, как правило, только одно главное или основное питательное вещество (N, Р или K), в то время как комплексные удобрения содержат два или более главных питательных веществ (азотно-фосфорные (NP), фосфорно-калийные (РК) или азотно-фосфорно-калийные (NPK) и, в частности, NP или NPK удобрения).
Существует два общепринятых способа производства комплексных удобрений, а именно, способ с применением кислотной смеси и нитрофосфатный способ. В частности, в нитрофосфатном способе фосфорит на начальной стадии растворяют в избытке азотной кислоты и удаляют Ca(NO3)2*4H2O из раствора обработанного сырого фосфорита охлаждением и фильтрацией. Затем путем нейтрализации полученного фильтрата образуется раствор, содержащий в основном нитрат аммония и фосфаты аммония-кальция. Путем выпаривания раствора образуется шламовый расплав AN-MAP-DCP (нитрат аммония- фосфат моноаммония- дикальцийфосфат), к которому можно добавить соли хлорид калия/сульфат калия. Используя данные исходные компоненты, а также описанный способ, можно предложить широкий ассортимент удобрений по составу.
Главными компонентами сброса в азотно-фосфорных (NP) или азотно-фосфорно-калийных (NPK) сточных водах являются аммиак, нитрат, фторид и фосфат, и сточные воды могут также содержать тяжелые металлы из фосфоритов, такие как Cd, Hg и Zn.
В 2002 году австрийское федеральное агентство по охране окружающей среды выпустило доклад под заголовком "State of the Art for the Production of Fertilisers with Regard to the IPPC-Directive" (Текущее состояние техники в области производства удобрений относительно директивы комплексного предотвращения и контроля загрязнений) (англ аббревиатура IPPC - от Integrated Pollution Prevention and Control) Monographien Band 105, M-105 (см: http://www.umweltbundesamt.at/fileadmin/site/publikationen/M105.pdf) доступ к которому осуществлялся 05 октября 2015; см. также "Best Available Techniques for Pollution Prevention and Control in the European Fertilizer Industry" (Лучшие доступные технологии для предотвращения и контроля загрязнения в европейской индустрии производства удобрений), буклет №7 из 8: Production of NPK Fertilizers by the Nitrophosphate Route, European Fertilizer Manufacturers' Association, 2000. (Производство NPK удобрений нитрофосфатным путем, Ассоциация европейских производителей удобрений, 2000). В австрийском докладе представлено обсуждение конкретных способов сокращения выбросов сточных вод, и они включили 7 новейших рекомендаций для нитрофосфатного способа, в частности:
1. Недопущение антивспенивающих агентов при разложении фосфоритов.
2. Повторное использование скрубберной жидкости, возникшей в результате обработки газов, отходящих при разложении фосфоритов, в производственном процессе.
3. Переработка промывной воды для промывки от песка в производственном процессе;
4. Недопущение непосредственного охлаждения/закалки, например, соконденсации отработанных паров;
5. Переработка скрубберной жидкости от очистки отработанного газа от аммонизации в производственном процессе;
6. Очистка смешанных отработанных газов установок для нейтрализации/выпаривания и грануляции/сушки; и
7. Применение буферных резервуаров для компенсации колебаний объема и нагрузки сточных вод.
Существует множество рекомендаций, предназначенных для различных типов загрязняющих веществ. Однако, удаление хлоридов не является одной из них. Фактически, хлорид, как правило, не считается существенной примесью в сточных водах производства удобрений. Это может быть следствием относительно низких уровней хлоридов, наблюдаемых в сточных водах производства удобрений, которые могут составлять только порядка 1000 млн-1 (частей на миллион). Для сравнения, питьевая вода содержит максимальные уровни, равные 250 млн-1, в то время как морская вода содержит 35,000 млн-1, а рапа содержит свыше 50,000 млн-1. В связи с этим, уровни, наблюдаемые в сточных водах производства удобрений, как правило, не считаются экологической проблемой.
Сущность изобретения
В соответствии с первым аспектом настоящего изобретения, сточные воды с предприятия по производству удобрений направляют к электрохимической ячейке и удаляют хлорид путем электролиза. В частности, предприятие по производству удобрений представляет собой предприятие по производству нитрофосфатных удобрений, то есть предприятие использует нитрофосфатный способ для производства удобрений, таких как комплексные удобрения. В альтернативном варианте сточные воды могут происходить из процессов производства других минеральных или органоминеральных удобрений. В частности, предприятие по производству удобрений может производить композиции, содержащие нитрат аммония. В частности, предприятие по производству удобрений может производить композиции, содержащие нитрат аммония, посредством стадии гранулирования из расплава. В контексте настоящего документа, предприятие по производству удобрений представляет собой любое предприятие по производству композиций, которые можно использовать в качестве удобрений, такие как, в том числе, нитрат аммония. Как известно из уровня техники, нитрат аммония можно применять в качестве взрывчатого вещества наряду с его использованием в качестве удобрения. Соответственно любой предприятие, производящее нитрат аммония, считается предприятием по производству удобрений вне зависимости от конечного использования нитрата аммония.
Снижение концентрации хлорида позволяет обработанным сточным водам безопасно рециркулировать обратно на предприятие по производству удобрений. В соответствии с некоторыми вариантами воплощения изобретения, концентрацию хлорида можно снизить до уровней ниже чем 500 млн-1, в частности 350 млн-1 или даже, в частности, ниже чем 250 млн-1.
В соответствии с еще одним частным вариантом осуществления изобретения, массоперенос в электрохимической ячейке можно увеличить с целью повышения эффективности электрохимической ячейки. Существует много способов увеличения массопереноса, включающих: механическое перемешивание электролита, вибрирование электродов, вращение электродов, ультразвуковое воздействие на электрод или электролит, использование 3D электродов или инертных сетчатых усилителей турбулентности, или впрыскивание электролита. В соответствии с еще одним частным вариантом воплощения изобретения, массоперенос увеличивают путем впрыскивания электролита.
В соответствии с еще одним вариантом осуществления изобретения, предприятие по производству удобрений соединено по текучей среде с электрохимической ячейкой, имеющей анод и катод, таким образом, чтобы сточные воды с предприятия по производству удобрений можно было обрабатывать посредством электрохимической ячейки для удаления хлорида. В частности, предприятие по производству удобрений представляет собой предприятие по производству нитрофосфатных, других минеральных или органоминеральных удобрений. Кроме того, электрохимическая ячейка может быть соединена по текучей среде с предприятием по производству удобрений таким образом, чтобы позволить сточным водам рециркулировать обратно на предприятие по производству удобрений. Электрохимическая ячейка может дополнительно включать впрыскиватели электролита. Когда впрыскиватели электролита расположены на аноде, то указанные впрыскиватели могут повышать эффективность электролиза за счет увеличения массопереноса. Когда впрыскиватели дополнительно расположены на катоде, они также могут быть использованы с целью избежать высокого уровня локального рН и образования отложений на катоде.
В соответствии с еще одним вариантом воплощения изобретения, электролиз используют для удаления хлорида из промышленных сточных вод с предприятия по производству удобрений. В частности, предприятие по производству удобрений представляет собой предприятие по производству нитрофосфатных, других минеральных или органоминеральных удобрений.
Краткое описание чертежей
Варианты осуществления изобретения описаны далее со ссылкой на сопутствующие чертежи, в которых:
Фигура 1А представляет собой вид сбоку электрохимической ячейки; Фигура 1В представляет собой вид в поперечном разрезе одного варианта осуществления изобретения вдоль оси А фигуры 1А; а фигура 1С представляет собой вид в поперечном разрезе альтернативного варианта осуществления изобретения вдоль оси А фигуры 1А;
Фигура 2А представляет собой вид спереди электрохимической ячейки, изображенной на фигурах 1А и В; Фигура 2В представляет собой вид в поперечном разрезе вдоль оси В фигуры 2А; а фигура 2С представляет собой вид в поперечном разрезе вдоль оси С фигуры 2А.
Фигура 3 представляет собой диаграмму концентрации хлорида по времени при проведении электролиза образца сточных вод с предприятия по производству нитрофосфатных удобрений.
Фигура 4 представляет собой диаграмму концентрации хлорида по времени при проведении электролиза при трех различных плотностях тока и с применением впрыскивания электролита.
Фигура 5 представляет собой диаграмму концентрации хлорида по времени после того, как электролиз был завершен в системе с крышкой (квадрат) и в системе без крышки (треугольник).
Размеры, показанные на фигурах 1 и 2, всего лишь отражают размеры конкретной электрохимической ячейки, используемой в примере 2, и служат только для иллюстративных целей и не ограничивают каким-либо образом изобретение.
Подробное описание изобретения
Хлориды можно обнаружить в сточных водах производства удобрений, в частности, в сточных водах от нитрофосфатного, другого минерального или органоминерального процесса. Не ограничиваясь теорией, хлориды могли произойти из фосфоритов, в зависимости от источника фосфоритов. Данная примесь может присутствовать только в умеренных концентрациях порядка 1000 млн-1. Если сточные воды просто сливают в окружающую среду, то данный уровень присутствующих хлоридов может не представлять собой какую-либо экологическую или нормативную проблему. Однако, если сточные воды затем рециркулируют обратно на предприятие по производству удобрений, то хлориды, присутствуя даже в умеренных количествах, могут дестабилизировать нитрат аммония, который может стать взрывоопасным и представлять собой значительную угрозу безопасности. В частности, в процессе производства, например, NPK гранул, воду выпаривают и при этом локальная концентрация любого присутствующего хлорида может существенно повыситься. Поскольку нитрат аммония тоже будет присутствовать, соединение может стать взрывоопасным. Если сточные воды, содержащие хлорид, рециркулируют обратно на предприятие по производству композиций, содержащих нитрат аммония, любое повышение концентрации хлорида может представлять собой риск детонации. Термическую устойчивость нитрата аммония снижают даже незначительным присутствием хлоридов, подобных хлориду железа, хлориду кальция и хлориду аммония. В частности, это может быть главной проблемой при производстве гранул, содержащих нитрат аммония, путем гранулирования из расплава, включающего в себя выпаривание воды.
Хлорид был идентифицирован в других промышленных процессах как загрязняющее вещество, которое можно удалить, хотя его относительно высокие концентрации часто наблюдали до того, как его идентифицировали в качестве загрязняющего вещества. В этом случае хлорид признавали как добавленный к содержанию твердой фазы и повышающий корродирующие качества воды. В качестве альтернативы хлорид удаляют, когда конечным результатом является питьевая вода, требующая очень низких уровней присутствия хлорида, обычно менее 250 млн-1. Средствами обработки являются, как правило, деминерализация, обратный осмос, электродиализ и выпаривание (см. главу 1 "Water Sources, Impurities and Chemistry" (Источники воды, примеси, содержащиеся в воде и химический состав), руководство по обработке промышленных вод, GE Power & Water, www.gewater.com/handbook/index.jsp, по состоянию на 5 октября 2015).
Деминерализованная вода представляет собой воду, в которой удалены практически все ионы минералов, такие как катионы наподобие натрия, кальция, железа и меди и анионы, такие как хлорид, фторид, нитрат, карбонат и сульфат. Деминерализация представляет собой химический процесс, в котором используют специально изготовленные ионообменные смолы, которые обменивают ионы водорода и гидроксид-ионы на растворенные минералы и затем рекомбинируют для образования воды. Так как большинство примесей, содержащихся в воде не в виде частиц, представляет собой растворенные соли, то деминерализация дает воду высокой степени очистки, как правило похожую на дистиллированную воду, и данный процесс является быстрым и проходит без образования накипи.
Обратный осмос включает в себя продавливание воды через осмотическую мембрану, которая не пропускает соли и пропускает поток воды под давлением, превышающим осмотическое давление. На данный момент обратный осмос является самым широко практикуемым способом опреснения морской воды и производит опресненный пермеат, в котором отсутствуют ионные компоненты и который может быть слишком чистым для слива в окружающую среду. При выпаривании или термическом опреснении воду выпаривают и конденсируют, иногда многостадийно, для переработки скрытой теплоты конденсации.
Электрохимически, электродиализ обычно применяют для опреснения. В электродиализных системах ионы солей переносят через ионообменные мембраны в пакет под воздействием гальванического потенциала. Гальванический потенциал подают в виде напряжения, генерируемого на аноде и катоде. В отличие от обратного осмоса, концентрацию солей, получаемой в результате электролиза, воды можно регулировать путем регулировки тока, подаваемого в пакет. Ионы солей переводят из разбавителя или камеры продукта в концентрированную соленую воду в камере концентрата под воздействием электрического поля постоянного тока, приложенного к электродам. Практический коэффициент концентрации, равный 5-10, является общепринятым; то есть, перенос ионов из разбавленной соленой воды с концентрацией, равной 2000 млн-1, в концентрированную соленую воду с концентрацией между 10,000 млн-1 и 20,000 млн-1. Недавние патентные заявки, описывающие электродиализ для опреснения загрязненной соленой воды, включают патентную заявку №US 2015/0096891 и патентную заявку WO2014/197966.
В то время как вышеприведенные технологии являются самыми широко используемыми способами опреснения, поиск патентной литературы выявляет две других электрохимических технологии: электролиз и емкостная деионизация.
Электролиз является старинной технологией, относящейся к 19 веку и все еще применяемой в хлор-щелочной промышленности, где хлорид натрия подвергают электролизу для получения химических продуктов хлора и гидроксида натрия (каустическая сода). Однако данный процесс начинается с рапы, то есть с очень высоких концентраций хлорида натрия порядка 50,000 млн-1. Такие высокие концентрации позволяют проводить эффективный электролиз. В патентной заявке Великобритании GB 2499025 описан способ, в котором используют агрессивные дезактивирующие агенты, такие как HCl или NaCl, при выводе из эксплуатации ядерных установок. Далее в патентной заявке Великобритании сообщается об использовании электролиза для удаления хлоридов из радиоактивных сточных вод. Отсутствует рассмотрение того, почему хлорид упоминают в качестве загрязняющего вещества или рассмотрение каких-либо угроз, связанных с этим. Однако также указана конечная концентрация хлорида, равная всего лишь 5 млн-1, и это не является достоверным результатом простого электролиза. Как уже отмечалось, для эффективного электролиза хлор-щелочная промышленность требует концентраций хлорида в 50,000 млн-1. Для сравнения нормативы для питьевой воды требуют уровней исключительно менее 250 млн-1, и ни в одном из документов из уровня техники нет описания использования электролиза для удаления хлорида в питьевой воде. Кроме того, в GB 2499035 не упоминается о дополнительных технологиях, необходимых для снижения уровня хлорида до такого низкого уровня.
Для сравнения, в китайской патентной заявке CN 102001776 описан относительно новый способ, в котором используют емкостную деионизацию (технология электросорбции) для снижения концентрации солей, наблюдаемых в различных отраслях промышленности, а именно, в нефтяной, химической и фармацевтической промышленностях. Емкостная ионизация представляет собой новую технологию, с перспективой стать альтернативой обратному осмосу, и основана на электросорбции ионов (см. М.Е. Suss и др, Energy Environ Sci, 2015, 8, 2296).
Было обнаружено, что электролиз можно применять для обработки сточных вод с предприятий по производству удобрений. В частности, было обнаружено, что электролиз можно в действительности применять при умеренных начальных уровнях концентрации хлоридов около 1000 млн-1, что значительно меньше того, что наблюдают в хлор-щелочной промышленности, где концентрации хлоридов в 50,000 млн-1, необходимы для эффективного гидролиза хлорида. Кроме того, электролиз можно применять для снижения концентрации хлорида до уровней ниже чем 500 млн-1 и, в частности, ниже чем 350 млн-1 и даже, в частности, ниже чем 250 млн-1. Как уже отмечалось, это может иметь особые преимущества относительно процессов производства нитрофосфатных, других минеральных или органоминеральных удобрений даже, в частности, тогда, когда сточные воды рециркулируют обратно на предприятие по производству удобрений.
Электролиз представляет собой широко известную технологию, и последующее рассмотрение реакций на электродах, а также природы потенциальных электродов и электролитов не подразумевает ограничения универсальности способа для специалиста.
Обработка отходов с предприятия по производству нитрофосфатов, других минеральных или органоминеральных удобрений в электрохимической ячейке способствует удалению хлорида, который затем выделяется в виде газообразного хлора. Газообразный хлор можно затем обрабатывать в системе очистки отходящих газов перед выбросом любых оставшихся безвредных газов в атмосферу.
Подходящие газоочистительные системы, которые можно применять для очистки выделившегося хлора, могут, например, использовать NaOH в качестве очищающего средства. Это затем даст NaCl и NaClO, которые можно повторно использовать в качестве дезактивирующего агента. В соответствии с альтернативными вариантами осуществления изобретения, можно применять твердотельные газоочистители.
Как правило, катодная реакция включает в себя выделение водорода, в то время как кислород и хлор выделяются на аноде. В целом, полезно разделять анодные и катодные реакции посредством использования сепаратора или мембраны (пористой или ионоселективной). Это может иметь многочисленные преимущества, включая:
1. предотвращение снижения эффективности тока паразитными окислительно-восстановительными парами (например, Fe2+/Fe3+ и NO3-/NO2-);
2. Удерживание ионов металла вдали от катода в целях минимизирования риска электроосаждения; и
3. Разделение газовых потоков (то есть хлор/кислород, выделяющийся на аноде и водород на катоде) по соображениям безопасности и для возможной последующей обработки, так как смешивание газовых потоков может быть взрывоопасным.
В то время как типичная ячейка разделяет анолитный и католитный отсеки посредством микропористого сепаратора или мембраны, неразделенная ячейка может также быть использована в целях настоящего изобретения. Данный альтернативный подход дает преимущество более простой конструкции ячейки с только одним контуром текучей среды и, конечно, снимает необходимость в сепараторе. Однако, он не обладает теми преимуществами, которые обсуждались выше.
Анолит представляет собой сброс от процессов производства удобрений, в частности, от процессов производства нитрофосфатов, других минеральных или органоминеральных удобрений, обозначаемый выше как сточные воды производства удобрений. Католит может также представлять собой сброс сточных вод или концентрированный раствор соли, раствор кислоты, такой как азотная кислота, воде или другой подходящий раствор, выбранный специалистом в области техники. В соответствии в с другими частными вариантами осуществления изобретения, католит представляет собой сточные воды с предприятия по производству удобрений.
Материал анода ячейки должен проявлять стабильность в электролите. Кроме того, данный материал должен подходить как для выделения кислорода и хлора, так и демонстрировать низкие степени износа для обеих реакций, а также низкие перенапряжения для выделения хлора. Кроме того, желательно, чтобы материал анода проявлял более высокие уровни перенапряжения для других реакций, таких как выделение кислорода. Типичные материалы для использования в качестве материалов анода включают в себя алмаз с примесью бора, титан с покрытием (покрытый оксидами металлов, например, оксидом иридия, смесью из оксида иридия/рутения и оксидом олова) и сыпучую платину. В целом, можно применять электроды, известные из хлор-щелочной промышленности, такие как электроды типа DSA™ от Permascand.
Выбор материалов для материалов катода не настолько критичен, при этом главным требованием является стабильность в электролите. В этой связи нержавеющая сталь является особенно подходящим материалом, но это никак не ограничивает количество доступных материалов, и можно применять с этой целью широкий спектр других материалов, которые будут совершенно очевидными специалисту в данной области техники.
Типичные сепараторы/мембраны являются полимерными по природе и могут включать любую из числа коммерчески доступных альтернатив, которые будут очевидны специалисту. Типичные образцы включают, например, асбестовую диафрагму, катионную селективную мембрану Nation® (фторополимерный сополимер на основе сульфонированного тетрафторэтилена) или микропористый полиэтиленовый сепаратор. В частности, можно выгодно использовать сепараторы, применяемые в хлор-щелочной промышленности. Мембраны, применяемые в хлор-щелочной промышленности, обычно сделаны из перфорированных полимеров. Мембраны могут иметь от одного до трех слоев, но, как правило, состоят из двух слоев. Один из данных слоев состоит из перфорированного полимера с замещенными карбоксильными группами и прилегает к стороне катода. Другой слой состоит из перфорированного полимера с замещенными сульфоновыми группами и прилегает к стороне анода. Для придания мембране механической прочности ее, как правило, армируют волокнами из политетрафторэтилена (PTFE от англ. polytetrafluoroethylene). Без ограничения общего характера вышеприведенного, подходящим сепаратором может быть мембрана РМХ® от De Nora.
На аноде реакцию можно разбить на несколько дискретных стадий:
1. транспортировка хлорида посредством диффузии, миграции или конвекции из основной массы раствора на поверхность электрода (массоперенос);
2. десольвация сольватированного хлорида
3. окисление хлорид-ионов на поверхности анода (перенос заряда)
4. выделение газообразного хлора.
При электролизе хлорида из промышленного стока с предприятий по производству удобрений и, в частности, где используют нитрофосфатный, другой минеральный или органоминеральный процесс, первая стадия, а именно, массоперенос является лимитирующей стадией.
В электрохимии одним из главных способов увеличения массопереноса различных процессов является относительное движение электрод-электролит. Помимо возможности использования более высоких плотностей тока и, как следствие, повышения производительности и улучшения режима потока, оно также помогает удалить газообразный хлор.
Существует много различных способов увеличения массопереноса, известных в уровне техники, например, механическое перемешивание электролита, вибрирование электродов, вращение электродов, воздействие ультразвуком на электрод/электролит, применение 3D электродов, введение инертных сетчатых усилителей турбулентности.
Кроме того, было обнаружено, чтоб массоперенос можно также увеличить посредством использования впрыскивателей, используемых для форсирования конвекции вдоль анода. Струйное течение может происходить из сопла, такого как трубка или отверстие, или тому подобное, направленного под углом, часто перпендикулярно поверхности анода. Коэффициент массопереноса будет очень высоким в центре впрыскивателя (также известным как точка застоя) и он снизится с увеличением расстояния от точки застоя. Обзором литературы в данной области является Zuckerman and Lior, "Jet impingement heat transfer: physics, correlations, and numerical modelling" Advances in Heat Transfer, 39, 565-631 (2006) (Теплопередача ударной струи: физическая сторона, соотношения и численное моделирование, Достижения в теплообмене). Использование таких впрыскивателей можно обозначить как «электролитическое впрыскивание».
Впрыскиватели могут содержать стандартные насосы, которые направляют анолит через питающие трубы с отверстиями соответствующего диаметра. Ориентацию отверстий можно затем отрегулировать для направления потока анолита к аноду. В соответствии с некоторыми вариантами осуществления изобретения, впрыскиватели могут быть расположены в основании электрохимической ячейки, хотя специалист в данной области техники посредством обычного экспериментирования способен оптимизировать расположение впрыскивателей, количество впрыскивателей, размер отверстий и скорость результирующего потока анолита в зависимости от размеров и ориентации конкретной электрохимической ячейки.
Впрыскиватели можно без труда адаптировать для многих различных электрохимических ячеек, как в масштабах лабораторного тестирования, так и в промышленном применении. Это попросту включает в себя регулировку скорости потока, ориентацию и количество впрыскивателей, применимых для большого количества электрохимических ячеек разных размеров и ориентаций. Это может быть сделано без применения каких-либо изобретательских навыков и включает в себя лишь рутинную оптимизацию. В этом состоит отличие от многих других технологий, где необходимо использовать только конкретные размеры или ориентации подразумеваемой электрохимической ячейки для эффективного увеличения массопереноса. Например, в литературе часто упоминают ультразвук, где он вызывает имплозию пузырьков, приводящую к ударным волнам и турбулентности. Однако это требует относительно большой мощности источника, который расположен близко к электродам, что делает это осуществимым только для относительно маленьких ячеек.
Впрыскивание электролита можно также применять на катоде с целью избежать повышения уровня локального рН и образования отложений на катоде.
Использование впрыскивателей электролита дает возможность проводить намного более эффективный электролиз и позволяет снизить концентрацию хлорида до уровня ниже 500 млн-1, в частности ниже 350 млн-1, или ниже 250 млн-1. Компоненты ячейки, включая электролиты и контуры текучей среды, выполнены с возможностью управления выделением газа таким образом, чтобы выделяющиеся газы можно было отделить от потоков текучей среды и затем подвергнуть последующей обработке соответствующим образом. Тем не менее, газообразные хлор, в частности, растворим в водных растворах. Это может привести к тому, что газ останется в растворе и потенциально будет участвовать в обратных реакциях для восстановления хлорид-иона.
Не ограничиваясь теорией, растворенные ионы хлора в сточных водах могут вступать в реакцию для образования хлорноватистой кислоты (HOCl) согласно:

Ожидается, что ион аммония также будет находиться в сточных водах, особенно в том случае, когда сточные воды представляют собой сточные воды с предприятия по производству NPK удобрений. Затем хлорноватистая кислота может вступить в реакцию с ионом аммония следующим образом:
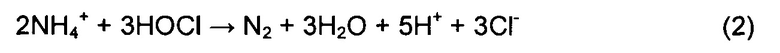
или в соответствии с

Следуя данным механизмам, с течением времени растворенный хлор сможет затем вступить в реакцию для восстановления хлорида в сточных водах. Использование впрыскивателей, как отмечалось выше, помогает не только увеличить массоперенос, но и выделить газообразный хлор из раствора и снизить вероятность случающихся обратных реакций. Тем не менее, ожидается, что некоторое количество растворенного хлора останется в растворе.
Желаемый уровень хлорида может составлять менее 500 млн-1 и, в частности, менее 350 млн-1. Использование впрыскивателей электролита позволяет снизить концентрацию хлорида до менее чем 250 млн-1, или менее чем 200 млн-1 или даже менее чем 150 млн-1 и на данном уровне, даже если имеет место некоторая обратная реакция из растворенного хлора в хлорид-ионы, результирующий уровень хлорид-ионов, присутствующих в растворе, будет все еще ниже требуемого уровня, равного 500 млн-1 или 350 млн-1.
По соображениям безопасности, при рециркуляции сточных вод обратно на предприятие по производству нитрофосфатных удобрений, более низкие предельные уровни полученного хлора или хлорида были бы наиболее благоприятны. Однако, для наиболее практичных целей, уровень ниже 500, в частности ниже 350 млн-1 считается обычно допустимым.
Не ограничиваясь частными случаями осуществления изобретения, фигуры 1 и 2 иллюстрируют типовые электрохимические ячейки. Фигура 1А представляет собой вид сбоку электрохимической ячейки 10 с вводом электролита 20 и выводом электролита 30. Фигура 1В представляет собой вид в поперечном разрезе вдоль оси А фигуры 1А с впрыскивателями электролита 45 и сепаратором 40. Впрыскиватели электролита 45 могут, например, представлять собой, отверстия в металлической трубке, проходящей от входа электролита 20.
Насос (не показан) можно затем использовать для проталкивания электролита через отверстия в впрыскивателях электролита 45 с конкретной скоростью и ориентацией. Точное количество отверстий, ориентацию, размер и результирующую скорость струйного потока можно без труда оптимизировать без каких-либо изобретательских навыков и это будет зависеть от размера и измерений конкретной электролитической ячейки 10. Электролит может затем рециркулировать из ввода электролита 20, через электролитическую ячейку 10 и выйти через вывод электролита 30 в насос и затем обратно через ввод электролита 20. Данная рециркуляция может продолжаться на протяжении всего электролиза. Когда впрыскиватели также используют совместно с катодом, то наличие второго насоса, используемого для рециркуляции католита отдельно, было бы предпочтительным с целью избежать какого-либо смешивания газов, выделяющихся из анода и катода.
В альтернативном варианте электролиз можно проводить беспрерывно. Однако когда электролиз проводят на взятой пробе сточных вод, продолжительность электролиза может составлять менее 24 часов, менее 5 часов, в частности, менее 4 часов, в частности, менее 3 часов или менее 2 часов. В соответствии с некоторыми вариантами осуществления изобретения, электролиз длится от всего лишь 5 минут, например, от 5 минут до 24 часов, от 5 минут до 5 часов, от 5 минут до 4 часов, 5 минут до 3 часов, от 5 минут до 2 часов, от 5 минут до 1 часа, от 30 минут до 5 часов, от 30 минут до 4 часов, от 30 минут до 3 часов, от 30 минут до 2 часов, 1-8 часов, 1-5 часов, 1-4 часов, 1-3 часов, или 1-2 часов. Не ограничиваясь теорией, требуемое время определяет соотношение между площадью электрода и объемной долей.
В качестве иллюстрации, фигура 1С представляет собой альтернативный вариант осуществления изобретения, где дополнительные металлические трубки 50 проходят перпендикулярно от впрыскивателей электролита 40, тем самым дополнительные отверстия в трубках 50 могут быть ориентированы для дополнительного увеличения массопереноса в электрохимической ячейке 10.
Для сравнения, в варианте осуществления 1 В, в соответствии с которым скорость текучей среды, составляющая приблизительно 2.2 м с-1 была создана нормальной скоростью потока, составляющей 50 л/час-1 с четырьмя отверстиями диаметром 2 мм в каждом впрыскивателе электролита 45. В варианте осуществления 1С есть были дополнительные трубки 50 с 22 отверстиями в каждой и общим числом струйных течений 44. Пары отверстий были равномерно распределены вдоль трубок 50, и угол между впрыскивателями в каждой паре составлял приблизительно 90°. В данном альтернативном варианте осуществления изобретения суммарная скорость потока составляла приблизительно 100 50 л/час-1, соответствуя потоку текучей среды из впрыскивателей электролита приблизительно 0.2 м с-1.
В целом, более высокие скорости потоков приведут к улучшенному массопереносу в электрохимической ячейке. Однако если скорость потока слишком высокая, то это может привести к сильному турбулентному потоку. Кроме того, существует баланс между потребностью в энергии, задействованной в создании скоростей потока в сравнении с выигрышем в эффективности от улучшения массопереноса. Это предполагает рутинную оптимизацию, которая будет варьироваться в зависимости от конкретных измерений и ориентации электрохимической ячейки.
Фигура 2А представляет собой вид спереди варианта осуществления изобретения на фигуре 1В и показывает электрохимическую ячейку 10 с входом электролита 20, выходом электролита 30, входом газа 80 и выходом газа 90. Фигура 2В представляет собой вид в поперечном разрезе фигуры 2А через ось В и показывает анод 60, сепаратор 40 и катод 70. Фигура 2С представляет собой вид в поперечном разрезе фигуры 2А через ось С и дополнительно показывает впрыскиватели электролита 45.
Размеры, показанные на фигурах 1 и 2, приведены только в ознакомительных целях и просто представляют собой размеры электролитических ячеек, используемых в примере 2.
Примеры
Пример 1
Была сконструирована электрохимическая ячейка с двумя неполярными анодами, соединенными параллельно и тремя неполярными катодами, также соединенными параллельно. Аноды были сделаны из DSA пластин (DSA от англ. dimensionally stable anode - износостойкий анод) толщиной 2,5 мм (Permascand, Sweden). Указанные три катода были сделаны из нержавеющей стали толщиной 3 мм (316L). Электролит представлял собой водный раствор, содержащий 3.6 вес. % растворенного NH4NO3 и 1000 млн-1 Cl- в форме растворенного NH4Cl. рН был отрегулирован до значения 1.4 путем добавления водного HNO3. Электролит подвергали циркуляции с помощью насоса. Сепаратор использовали в целях избежать контакта между выделяющимися газами O2, Cl2 и Н2. Сепаратор был сделан из политетрафторэтилена (PTFE от англ - polytetrafluoroethylene) и обработан Membratex (Svenska Textilfilter), а его толщина составляла 1.3 мм с плотностью 750 кгм-3. Водород, который выделялся на катоде, собирали в камеру, помещенную на верхушку катода, и газ рассеивали в вентиляционном шкафу около 2 м над ячейкой. Анодные газы, O2 и Cl2 рассеяли прямо в вентиляционной камере. Электрод, чувствительный к хлоридам (Radiometer Copenhagen) использовали для непрерывного измерения концентрации хлоридов. Условия эксплуатации поддерживали при температуре окружающей среды с рН равным 1-1.4 на аноде и ниже 3.5 на катоде.
Из фигуры 2 можно увидеть, что удаление хлорида было самым быстрым в начале, но замедлилось с течением времени. Кроме того, наблюдалось повышение коэффициента использования тока с понижением плотности тока. Это указывало на недостаточный массоперенос хлорид-ионов к аноду.
Пример 2
Электрохимическая ячейка была оснащена анодом, который представлял собой износостойкий анод от Permascand, а катод представлял собой нержавеющую сталь SS 316. Мембранный сепаратор представлял собой РМХ® мембрану от De Nora. Уровень рН как катодного, так и анодного электролитов беспрерывно отслеживали с помощью рН электродов. Электрод, чувствительный к хлоридам, использовали на стороне анода для беспрерывного измерения концентрации хлоридов.
Используемым электролитом являлись сточные воды из Yara International в Порсгрунне. Они представляли собой образец сточных вод нитрофосфатного способа производства комплексного удобрения. Плотность тока на аноде составляла 62 А м-2. Электрохимическая ячейка была дополнительно оснащена двумя насосами, один был предназначен для анолита, а другой - для католита. Насосы использовали с питающей трубкой у основания электрохимической ячейки для создания струй электролита, которые были направлены к соответствующим электродам. Схема электрохимической ячейки продемонстрирована на фигурах 1А и 1В.
Конструкционным материалом ячейки был поливинилхлорид (PVC - от англ "Polyvinyl chloride"). Главный отсек был изготовлен из блока ПВХ толщиной 60 мм. Винты сделаны из 316 за исключением винтов, фиксирующих анод, которые сделаны из ПВХ. Уплотнительные кольца сделаны из материала Viton.
Анолит и католит подавали через входы электролита 20, показанные на дне ячейки 10, и затем в впрыскиватели электролита 45, оснащенные впрыскивателями (см. фигуру 1В). Впрыскиватели представляли собой просто отверстия в металлической трубке диаметром 2 мм (4 отверстия в каждой подводящей трубе). Затем электролит пропустили через выход электролита 30 и в маленький резервуар с электродом, избирательным к Cl- и рН электродом (не показан). Затем электролит проводили в насос (не показан) и откачивали его обратно в электролитическую ячейку 10. Нормальная скорость потока составляла примерно 50 л ч-1, что эквивалентно скорости текучей среды из впрыскивателей, составляющей приблизительно 2.2 м с-1.
Сепаратор 40 поместили на террасу шириной 20 мм, изготовленную из ПВХ и закрепленную каркасом из ПВХ шириной 5 мм. Данный каркас отделяет газы от анода и катода. Оба электрода прикручены к внутренней стенке ячейки, и токосъемник проходит через стенку ячейки, оснащенную кольцевым уплотнением.
Дополнительные впрыскиватели, направленные к катодам, использовали с целью избежать высокого локального рН и снизить любое образование отложений на катоде.
Фигура 3 иллюстрирует 3 типичных эксперимента, где концентрация хлорида была измерена при разных токах. Отрезок А был при 5 А, отрезок В был при 10 А; и отрезок С был при 20 А. Сила тока, равная 10 А, эквивалентна 120 А/м-2.
Фигура 3 иллюстрирует значительное улучшение удаления хлорида по сравнению с ячейкой, представленной в примере 1. Данная фигура также показывает, что скорость удаления хлорида повысилась с увеличением силы тока и что данная скорость понизилась с концентрацией хлорида. Расчеты показали, что коэффициент использования по току Фарадея составлял около 9% для удаления хлорида для всех экспериментов, представленных на фигуре 2.
Пример 3
Анолит с отрезка В из примера 2 оставили в покое на несколько дней для наблюдения за изменением концентрации хлорида в течение данного периода времени, как с электролитом, накрытым крышкой (квадрат), так из без крышки (треугольник) как представлено на фигуре 5. Присутствие крышки не создало значительной разницы в обоих случаях, концентрация хлоридов повысилась до выравнивания на приблизительно 275 млн-1.
Это указывает на то, что газообразный хлор, оставшийся растворенным в электролите, следуя механизмам, описанным выше, реагировал в течение нескольких дней для преобразования хлорид-иона. Тем не менее, ввиду того что сам по себе электролиз был достаточно эффективным, концентрация хлоридов оставалась все время ниже 350 млн-1.
В описании и формуле изобретения настоящей заявки слова «включает» и «содержит» и их вариации значат «включая, но не ограничиваясь», и они не предназначены для исключения других фрагментов, добавок, компонентов, целых чисел или стадий. В описании и формуле настоящей заявки единственное число заключает в себе множественное, если иного не требует контекст. В частности, там, где используется неопределенный артикль, описание следует понимать как рассматриваемую множественность, а также как сингулярность, если иного не потребует контекст.
Признаки, целые числа, характеристики, соединения, химические фрагменты или группы, описанные в рамках конкретного аспекта, воплощения или примера изобретения нужно истолковывать как применимые в любом другом аспекте, воплощении или примере, описанном здесь, за исключением несовместимого с этим. Все признаки, описанные в данной заявке (включая любые сопроводительные пункты, реферат и чертежи), и/или все стадии любого способа или процесса, раскрытые таким образом, можно соединить в любую комбинацию, за исключением комбинаций, где по меньшей мере некоторые из таких признаков и/или стадий являются взаимоисключающими. Изобретение не ограничено деталями каких-либо вышеупомянутых воплощений. Изобретение распространяется на любое новое изобретение или любую новую комбинацию признаков, раскрытых в данной заявке (включая любые сопроводительные пункты, реферат и чертежи), или на любое новое изобретение, или любую новую комбинацию стадий любого способа или процесса, раскрытого таким образом.
Внимание читателя направлено на все бумаги и документы, поданные одновременно с или до настоящего описания, связанного с данной заявкой, и которые открыты для всеобщего ознакомления с данным описанием, и содержание всех таких бумаг и документов включено в данный текст посредством ссылки.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ ОБРАБОТКИ ПРОМЫШЛЕННЫХ СТОЧНЫХ ВОД ЭЛЕКТРОЛИЗОМ | 2016 |
|
RU2730328C1 |
| СПОСОБ УДАЛЕНИЯ ЗАГРЯЗНЯЮЩИХ ВЕЩЕСТВ ИЗ СТОЧНОЙ ВОДЫ ОТ ПРОМЫШЛЕННОГО ПРОИЗВОДСТВА И СИСТЕМА ДЛЯ ОСУЩЕСТВЛЕНИЯ ТАКОГО СПОСОБА | 2019 |
|
RU2793787C2 |
| ЭЛЕКТРОХИМИЧЕСКАЯ МОДУЛЬНАЯ ЯЧЕЙКА ДЛЯ ОБРАБОТКИ РАСТВОРОВ ЭЛЕКТРОЛИТОВ | 2007 |
|
RU2350692C1 |
| ЭЛЕКТРОХИМИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ АЗОТНЫХ УДОБРЕНИЙ | 2008 |
|
RU2479558C2 |
| СПОСОБ ОКИСЛИТЕЛЬНОГО ЖИДКОФАЗНОГО ОБЕЗВРЕЖИВАНИЯ ПЕСТИЦИДОВ ФОСФОРСОДЕРЖАЩЕГО РЯДА | 2009 |
|
RU2421261C1 |
| СПОСОБ УДАЛЕНИЯ НИТРИТ-ИОНОВ ИЗ ВОДНЫХ РАСТВОРОВ | 2011 |
|
RU2471718C1 |
| СПОСОБ ОЧИСТКИ ВОДЫ | 2000 |
|
RU2244687C2 |
| ЭЛЕКТРОХИМИЧЕСКАЯ ОБРАБОТКА РАСТВОРОВ, СОДЕРЖАЩИХ ШЕСТИВАЛЕНТНЫЙ ХРОМ | 2006 |
|
RU2422374C2 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРА И ХЛОРСОДЕРЖАЩИХ ОКИСЛИТЕЛЕЙ И УСТАНОВКА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2005 |
|
RU2315132C2 |
| Способ очистки природных и сточных вод от нитратов | 2020 |
|
RU2751891C1 |





Группа изобретений относится к способу удаления хлорида из сточных вод от предприятия по производству удобрений, предприятию по производству удобрений и применению электролиза для удаления хлорида. Способ включает направление содержащих хлорид сточных вод от предприятия по производству удобрений к электрохимической ячейке и удаление хлорида из сточных вод, выделившегося в виде газообразного хлора, посредством электролиза. Содержащие хлорид сточные воды, вырабатываемые предприятием, соединены по текучей среде с электрохимической ячейкой, имеющей анод и катод. Компоненты электрохимической ячейки выполнены с возможностью управления выделением газообразного хлора таким образом, чтобы он мог быть отделен от потоков текучей среды. Указанная электрохимическая ячейка соединена по текучей среде с предприятием по производству удобрений таким образом, чтобы рециркулировать сточные воды обратно на предприятие по производству удобрений. Технический результат заключается в снижение концентрации хлорида, что позволяет обработанным сточным водам безопасно рециркулировать обратно на предприятие по производству удобрений. 3 н. и 16 з.п. ф-лы, 9 ил.
1. Способ удаления хлорида из сточных вод от предприятия по производству удобрений, включающий:
a) направление содержащих хлорид сточных вод от предприятия по производству удобрений к электрохимической ячейке; и
b) удаление хлорида из сточных вод, выделившегося в виде газообразного хлора, посредством электролиза.
2. Способ по п. 1, отличающийся тем, что предприятие по производству удобрений представляет собой предприятие по производству нитрофосфатных или других минеральных или органоминеральных удобрений.
3. Способ по п. 1 или 2, отличающийся тем, что предприятие по производству удобрений производит композиции, содержащие нитрат аммония.
4. Способ по любому из пп. 1-3, отличающийся тем, что указанный способ дополнительно включает рециркуляцию обработанных сточных вод обратно на предприятие по производству удобрений.
5. Способ по любому из пп. 1-4, отличающийся тем, что стадия удаления дополнительно включает увеличение массопереноса в электрохимической ячейке.
6. Способ по п. 5, отличающийся тем, что массоперенос увеличивают механическим перемешиванием электролита, вибрированием электродов, вращением электродов, ультразвуковым воздействием на электрод или электролит, использованием 3D-электродов или инертных сетчатых усилителей турбулентности, или впрыскиванием электролита.
7. Способ по п. 5, отличающийся тем, что массоперенос увеличивают путем впрыскивания электролита.
8. Способ по любому из пп. 1-7, отличающийся тем, что концентрацию хлорида снижают до менее чем 500 млн-1.
9. Способ по любому из пп. 1-8, отличающийся тем, что концентрацию хлорида снижают до менее чем 350 млн-1.
10. Способ по любому из пп. 1-9, отличающийся тем, что концентрации хлорида снижают до менее чем 250 млн-1.
11. Способ по любому из пп. 1-10, отличающийся тем, что стадия удаления хлорида составляет от 5 минут до 24 часов.
12. Способ по любому из пп. 1-11, отличающийся тем, что стадия удаления хлорида составляет от 1 до 8 часов.
13. Предприятие по производству удобрений, в котором содержащие хлорид сточные воды, вырабатываемые предприятием, соединены по текучей среде с электрохимической ячейкой, имеющей анод и катод, при этом компоненты электрохимической ячейки выполнены с возможностью управления выделением газообразного хлора таким образом, чтобы он мог быть отделен от потоков текучей среды, причем указанная электрохимическая ячейка соединена по текучей среде с предприятием по производству удобрений таким образом, чтобы рециркулировать сточные воды обратно на предприятие по производству удобрений.
14. Предприятие по производству удобрений по п. 13, отличающееся тем, что указанное предприятие по производству удобрений представляет собой предприятие по производству нитрофосфатных, других минеральных или органоминеральных удобрений.
15. Предприятие по производству удобрений по п. 13 или 14, отличающееся тем, что указанное предприятие по производству удобрений производит композиции, содержащие нитрат аммония.
16. Предприятие по производству удобрений по любому из пп. 13-15, отличающееся тем, что электрохимическая ячейка дополнительно содержит впрыскиватели электролита для направления электролита к аноду.
17. Предприятие по производству удобрений по любому из пп. 13-16, отличающееся тем, что электрохимическая ячейка дополнительно содержит впрыскиватели электролита для направления электролита к катоду.
18. Применение электролиза для удаления хлорида, выделившегося в виде газообразного хлора, из промышленных сточных вод от предприятия по производству удобрений.
19. Применение по п. 18, отличающееся тем, что предприятие по производству удобрений представляет собой предприятие по производству нитрофосфатных, других минеральных или органоминеральных удобрений.
| US 6132627 A1, 17.10.2000 | |||
| СПОСОБ ЭЛЕКТРОХИМИЧЕСКОЙ ОБРАБОТКИ ВОДЫ И УСТРОЙСТВО | 2012 |
|
RU2500625C1 |
| РЕЦИРКУЛЯЦИЯ ВОДЫ В ПРОИЗВОДСТВЕННОМ ПРОЦЕССЕ ПОЛУЧЕНИЯ МЕЛАМИНА | 2010 |
|
RU2553982C2 |
| ЭЛЕКТРОХИМИЧЕСКАЯ МОДУЛЬНАЯ ЯЧЕЙКА ДЛЯ ОБРАБОТКИ РАСТВОРОВ ЭЛЕКТРОЛИТОВ | 2007 |
|
RU2350692C1 |
| СПОСОБ ЭЛЕКТРОХИМИЧЕСКОЙ ОБРАБОТКИ СТОЧНЫХ ВОД И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2010 |
|
RU2534125C2 |
| JP 51130070 A, 12.11.1976. | |||
Авторы
Даты
2020-09-02—Публикация
2016-12-16—Подача