ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Данная заявка испрашивает приоритет по предварительной заявке США №62/236429, поданной 2 октября 2015 г., которая тем самым включена в данный документ в полном объеме посредством ссылки.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Данная заявка содержит перечень последовательностей, который был подан в электронном виде в формате ASCII и включен в данный документ в полном объеме посредством ссылки. Указанная копия ASCII, созданная 30 сентября 2016 года, называется P32858-WO_SL.txt и имеет размер 56520 байт.
ОБЛАСТЬ ТЕХНИКИ
Изобретение относится в целом к антителам, конъюгированным с промежуточными соединениями пирролбензодиазепина для того, чтобы образовать конъюгаты антитело-лекарственное средство для терапевтического или диагностического применений. Антитела могут быть сконструированы со свободными аминокислотами цистеина, являющимися реакционноспособными для конъюгации с промежуточными соединениями пирролобензодиазепина. Изобретение также относится к способам применения соединений конъюгатов антитело-лекарственное средство для лечения гиперпролиферативных патологий, таких как рак, или для in vitro, in situ и in vivo диагностики таких патологий.
УРОВЕНЬ ТЕХНИКИ
Конъюгаты антитело-лекарственное средство (КАЛС (ADC)) являются целенаправленными химиотерапевтическими молекулами, объединяющими свойства как антител, так и цитотоксических препаратов, за счет нацеливания сильных цитотоксических лекарственных препаратов на антиген-экспрессирующие опухолевые клетки, поглощения клеткой и высвобождения лекарственного средства, тем самым усиливая их противоопухолевую активность (Carter, P. and Senter, P. (2008) The Cancer Jour. 14(3):154-169). Успешная разработка КАЛС (ADC) для данного антигена-мишени зависит от оптимизации выбора антитела, дизайна и стабильности линкера, активности цитотоксического лекарственного средства, и способа соединения лекарственного средства и линкера с антителом (Dosio et al (2011) Toxins, 3:848-883; Polakis, P. (2005) Current Opinion in Pharmacology 5:382-387).
Некоторые соединения пирролбензодиазепина (ПБД (PBD)) обладают способностью распознавать и связываться с конкретными последовательностями ДНК; предпочтительной последовательностью является PuGPu (Pu=пурин, такой как аденин A и гуанин G). Первый антибактериальный антибиотик ПБД (PBD), антрамицин, был обнаружен в 1965 году (Leimgruber, et al., J. Am. Chem. Soc., 87:5793-5795 (1965); Leimgruber, et al., J. Am. Chem. Soc., 87, 5791-5793 (1965)). С тех пор было обнаружено и описано ряд природных ПБД (PBD) и аналогов (Thurston, et al., Chem. Rev. 1994, 433-465 (1994); Antonow, D. and Thurston, D.E., (2011) Chem. Rev. 111 (4):2815-2864). Члены семейства включают аббеймицин (Hochlowski, et al., (1987) J. Antibiotics, 40:145-148), чикамицин (Konishi, et al., (1984) J. Antibiotics, 37:200-206), Thurston, et al., (1990) Chem. Brit., 26:767-772; Bose, et al., (1992) Tetrahedron, 48: 751-758), мазетарамицин (Kuminoto, et al., J. Antibiotics, 33, 665-667 (1980)), неотрамицины A и B (Takeuchi, et al., J. Antibiotics, 29, 93-96 (1976)), поротамицин (Tsunakawa, et al., (1988) J. Antibiotics, 41:1366-1373), протракрацин (Shimizu, et al., J. Antibiotics, (1982)) 29:2492-2503, Langley and Thurston, (1987) J. Org. Chem., 52:91-97), сибаномицин, DC-102 (Hara, et al., (1988) J. Antibiotics, 41:702 -704, Itoh, et al., J. Antibiotics, (1988) 41:1281-1284), сибиромицин (Leber, et al., (1988) J. Am. Chem. Soc., 110:2992-2993) и томамицин (Arima, et al., (1972) J. Antibiotics, 25:437-444).
Пирролобензодиазепины имеют общую структуру:
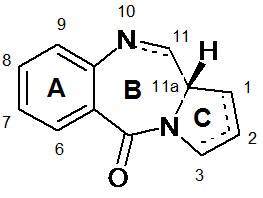
и отличаются по количеству, типу и положению заместителей как в ароматических кольцах А, так и в пирроло C-кольцах и по степени насыщения С-кольца. В B-кольце присутствует или имин (N =C), карбиноламин (NH-CH(OH)), или метиловый эфир карбиноламина (NH-CH(OMe)) в положении N10-C11, электрофильный центр ответственный за алкилирование ДНК. Все известные природные продукты имеют (S)-конфигурацию в хиральной позиции С11а, что придает им правостороннюю закрученость при просмотре от кольца С в направлении кольца А и определяет трехмерную структуру, изоспиральную малой бороздке B-формы ДНК, что приводит к плотному прилеганию в сайте связывания (Kohn, In Antibiotics III. Springer-Verlag, New York, pp. 3-11 (1975); Hurley and Needham-VanDevanter, (1986) Acc. Chem. Res., 19:230-237). Способность ПБД (PBD) образовывать аддукт в малой канавке позволяет им мешать процессингу ДНК, следовательно, делает возможным их применение в качестве противоопухолевых веществ. Димерные соединения пирролобензодиазепина, где две структуры пирролбензодиазепина ковалентно присоединены линкером через позицию С8 колец А, могут диалкилировать и перекрестно сшивать двухцепочечную ДНК (WO 2005/085251).
Соединения пирролобензодиазепина могут быть применены в качестве пролекарств, защищая их в позиции N10 защитной группой азота, такой как карбамат, который является отсоединяемым in vivo (WO 2000/12507, WO 2005/023814). Защитные группы являются отсоединяемыми от позиции N10 компонента ПБД (PBD) для того, чтобы оставить иминовую связь N10-C11. Описывается ряд защитных групп, включая группы, которые могут быть расщеплены действием ферментов.
Конъюгаты антитело-лекарственное средство, где димер пирролобензодиазепина (ПБД (PBD)) связан через позицию N10 с антителом, специфичным к ассоциированному с опухолью антигену, обладают эффективностью in vitro и in vivo против опухолевых клеток (WO 2011/130598). Были описаны конъюгаты антитело-лекарственное средство с димерными компонентами ПБД (PBD) в качестве лекарственного средства, имеющими линкерные группы для присоединения к связывающемуся с клеткой веществу, такому как антитело, через мостиковую связь («привязь»), соединяющую мономерные единицы димера ПБД (PBD) (WO 2007/085930). Были описаны конъюгаты антитело-лекарственное средство с димерными компонентами ПБД (PBD) в качестве лекарственного средства, имеющими амидные группы и аминогруппы в кольце В в позиции N10-C11 (WO 2014/096368; WO 2013/177481; WO 2012/112708). Были описаны конъюгаты антитело-лекарственное средство, содержащие диалкилирующие пирролбензодиазепиновые (ПБД (PBD)) димерные лекарственные компоненты, присоединенные в позиции N10 ПБД (PBD) дисульфидной связью к антителам (WO2013/055987; Gregson et al. (2001) J. Med. Chem. 44:1161-1174).
КРАТКОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Изобретение включает в себя промежуточное соединение линкер-лекарственное средство Формулы I:
 I
I
где X Y выбран из CH2-CH2, CH=CH, C(=O)-NH, или CH2-NH;
Y выбран из CH2-CH2, CH=CH, C(=O)-NH, или CH2-NH;
A представляет собой 5-членное или 6-членное гетероциклическое кольцо, необязательно замещенное группой, выбранной из F, C1-C6-алкила или =C(R)2, где R независимо выбран из H, F, C1-C6-алкила или C1-C6-фторалкила;
R1 и R2 независимо выбраны из H или C1-C6-алкила, или R1 и R2 образуют 3, 4, 5 или 6-членную циклоалкильную или гетероциклильную группу;
R3 независимо выбран из NO2, Cl, F, CN, CO2H или Br; и
m равно 0, 1 или 2.
Изобретение включает в себя моноалкилирующие пирролбензодиазепиновые лекарственные компоненты, ковалентно связанные с антителами дисульфидным линкером с образованием соединений конъюгата антитело-лекарственное средство (КАЛС (ADC)) для терапевтического или диагностического применений.
Другим аспектом изобретения является соединение конъюгата антитело-лекарственное средство Формулы II:
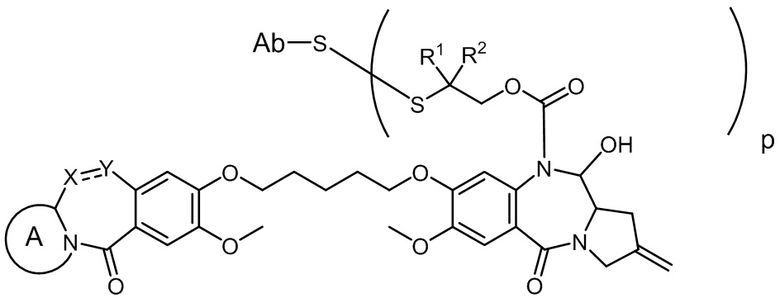 II
II
или его фармацевтически приемлемая соль, где:
X Y выбран из CH2-CH2, CH2-C(=O), CH=CH, или CH2-NH;
Y выбран из CH2-CH2, CH2-C(=O), CH=CH, или CH2-NH;
A представляет собой 5-членное или 6-членное гетероциклическое кольцо, необязательно замещенное группой, выбранной из F, C1-C6-алкила или =C(R)2, где R независимо выбран из H, F, C1-C6-алкила или C1-C6-фторалкила;
R1 и R2 независимо выбраны из H или C1-C6-алкила, или R1 и R2 образуют 3, 4, 5 или 6-членную циклоалкильную или гетероциклильную группу;
p равно целому числу от 1 до 8; и
Ab представляет собой антитело.
В иллюстративном варианте осуществления, антитело связывается с одним или больше ассоциированными с опухолью антигенами, или рецепторами клеточной поверхности, выбранными из 1)-53):
1) BMPR1B (рецептор типа IB костного морфогенетического белка);
2) E16 (LAT1, SLC7A5);
3) STEAP1 (шеститрансмембранный эпителиальный антиген простаты);
4) MUC16 (0772P, CA125);
5) MPF (MPF, MSLN, SMR, потенциирующий мегакариоциты фактор, мезотелин);
6) Napi2b (NAPI-3B, NPTIIb, SLC34A2, cемейство транспортеров растворенных веществ 34 (фосфат натрия), член 2, натрий-зависимый фосфатный транспортер 3b типа II);
7) Sema 5b (FLJ10372, KIAA1445, Mm.42015, SEMA5B, SEMAG, семафорин 5b Hlog, домен sema, семь тромбоспондиновых повторов (тип 1 и подобный типу 1), трансмембранный домен I и короткий цитоплазматический домен, (семафорин) 5B);
8) PSCA hlg (2700050C12Rik, C530008O16Rik, RIKEN кДНК 2700050C12, RIKEN кДНК 2700050C12 ген);
9) ETBR (рецептор эндотелина типа B);
10) MSG783 (RNF124, гипотетический белок FLJ20315);
11) STEAP2 (HGNC_8639, IPCA-1, PCANAP1, STAMP1, STEAP2, STMP, ассоциированный с раком простаты ген 1, ассоциированный с раком простаты белок 1, шеститрансмембранный эпителиальный антиген предстательной железы 2, шеститрансмембранный белок простаты);
12) TrpM4 (BR22450, FLJ20041, TRPM4, TRPM4B, катионный канал, действующий по механизму транзиторного рецепторного потенциала, подсемейство M, элемент 4);
13) CRIPTO (CR, CR1, CRGF, CRIPTO, TDGF1, фактор роста, полученный из тератокарциномы);
14) CD21 (CR2 (рецептор 2 комплемента) или C3DR (C3d/рецептор вируса Эпштейна-Барр) или Hs 73792);
15) CD79b (CD79B, CD79β, IGb (иммуноглобулин-ассоциированный бета), B29);
(16) FcRH2 (IFGP4, IRTA4, SPAP1A (якорный фосфатазный белок 1а, содержащий домен SH2), SPAP1B, SPAP1C);
17) HER2;
18) NCA;
19) MDP;
20) IL20Rα;
21) Brevican;
22) EphB2R;
23) ASLG659;
24) PSCA;
25) GEDA;
26) BAFF-R (рецептор фактора активации В-лимфоцитов, BLyS рецептор 3, BR3);
27) CD22 (изоформа CD22-В рецептора В-лимфоцитов);
28) CD79a (CD79A, CD79α, иммуноглобулин-ассоциированный альфа);
29) CXCR5 (рецептор 1 лимфомы Беркитта);
30) HLA-DOB (бета-субъединица молекулы ГКГС класса II (антиген Ia));
31) P2X5 (управляемый лигандом пуринергического рецептора P2X ионный канал 5);
32) CD72 (антиген CD72 дифференциации В-лимфоцитов, Lyb-2);
33) LY64 (антиген 64 (RP105) лимфоцитов, мембранный белок типа I семейства белков, богатых на лейциновые повторы (LRR - leucine rich repeat));
34) FcRH1 (Fc-рецептор-подобный белок 1);
35) FcRH5 (IRTA2, ассоциированный с транслокацией рецепторов суперсемейства иммуноглобулинов 2);
36) TENB2 (предполагаемый трансмембранный протеогликан);
37) PMEL17 (гомолог silver; SILV; D12S53E; PMEL17; SI; SIL);
38) TMEFF1 (трансмембранный белок 1 с EGF-подобным и двумя фолистатино-подобными доменами, Tomoregulin-1);
39) GDNF-Ra1 (рецептор альфа-1 семейства GDNF; GFRA1; GDNFR; GDNFRA; RETL1; TRNR1; RET1L; GDNFR-alpha1; GFR-ALPHA-1);
40) Ly6E (комплекс лимфоцитарного антигена 6, локус E; Ly67, RIG-E, SCA-2, TSA-1);
41) TMEM46 (гомолог shisa 2 (Xenopus laevis); SHISA2);
42) Ly6G6D (комплекс лимфоцитарного антигена 6, локус G6D; Ly6-D, MEGT1);
43) LGR5 (богатый на лейциновые повторы рецептор 5, сопряженный с G белком; GPR49, GPR67);
44) RET (протоонкоген ret; MEN2A; HSCR1; MEN2B; MTC1; PTC; CDHF12; Hs.168114; RET51; RET-ELE1);
45) LY6K (комплекс лимфоцитарного антигена 6, локус K; LY6K; HSJ001348; FLJ35226);
46) GPR19 (рецептор 19, сопряженный с G белком; Mm.4787);
47) GPR54 (рецептор KISS1; KISS1R; GPR54; HOT7T175; AXOR12);
48) ASPHD1 (содержащий домен аспартат-бета-гидроксилазы белок 1; LOC253982);
49) Тирозиназа (TYR; OCAIA; OCA1A; тирозиназа; SHEP3);
50) TMEM118 (белок 2, содержащий трансмембранный домен и домен «палец RING (Really Interesting New Gene)»; RNFT2; FLJ14627);
51) GPR172A (рецептор 172A, сопряженный с G белком; GPCR41; FLJ11856; D15Ertd747e);
52) CD33; или
53) CLL-1.
Другим аспектом изобретения является фармацевтическая композиция, содержащая конъюгат антитело-лекарственное средство Формулы II и фармацевтически приемлемый разбавитель, носитель или вспомогательное вещество.
Другим аспектом изобретения является применение конъюгата антитело-лекарственное средство Формулы II при изготовлении лекарства для лечения рака у млекопитающего.
Другим аспектом изобретения является способ лечения рака путем введения пациенту фармацевтической композиции, содержащей соединение конъюгата антитело-лекарственное средство Формулы II.
Другим аспектом изобретения является способ получения конъюгата антитело-лекарственное средство Формулы II.
Другим аспектом изобретения является изделие, содержащее фармацевтическую композицию, содержащую конъюгат антитело-лекарственное средство Формулы II, контейнер, и листок-вкладыш или этикетку, указывающие, что фармацевтическая композиция может применяться для лечения рака.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На Фиг. 1А изображен график жизнеспособности клеток in vitro для клеток BJAB, обработанных ADC-107, ADC-103 и контролем ADC-108, не нацеленным на мишень.
На Фиг. 1В изображен график жизнеспособности клеток in vitro для клеток WSU-DLCL2, обработанных ADC-107, ADC-103 и контролем ADC-108, не нацеленным на мишень.
На Фиг. 1C изображен график жизнеспособности клеток in vitro для клеток Jurkat, обработанных ADC-107, ADC-103 и контролем ADC-108, не нацеленным на мишень.
На Фиг. 1D изображен график жизнеспособности клеток in vitro для клеток BJAB, обработанных ADC-101, ADC-113, ADC-103, ADC-111 и ADC-112.
На Фиг. 1E изображен график жизнеспособности клеток in vitro для клеток WSU-DLCL2, обработанных ADC-101, ADC-113, ADC-103, ADC-111 и ADC-112.
На Фиг. 1F изображен график жизнеспособности клеток in vitro для клеток SK-BR-3, обработанных ADC-108, ADC-102, ADC-203, ADC-201 и ADC-107.
На Фиг. 1G изображен график жизнеспособности клеток in vitro для клеток KPL-4, обработанных ADC-108, ADC-102, ADC-203, ADC-201 и ADC-107.
На Фиг. 2 изображена эффективность конъюгатов антитело-лекарственное средство на графике изменения объема опухоли in vivo с течением времени в модели ксенотрансплантата WSU-DLCL2 у мышей CB-17 Fox Chase SCID, которым вводили внутривенно однократно дозу следующего:
1) Наполнитель (гистидиновый буфер № 8), 100 мкл
2) Тио Hu анти-CD22 10F4v3 LC K149C-(CLD-1), ADC-202, 0,5 мг/кг
3) Тио Hu анти-CD22 10F4v3 LC K149C-(CLD-1), ADC-202, 2 мг/кг
4) Тио Hu анти-CD22 10F4v3 LC K149C-(LD-51), моноамид, ADC-103, 2 мг/кг
5) Тио Hu анти-CD22 10F4v3 LC K149C-(LD-51), моноамид, ADC-103, 5 мг/кг
6) Тио Hu анти-CD22 10F4v3 LC K149C-(LD-51), моноамид, ADC-103, 10 мг/кг
7) Тио Hu анти-Her2 (hu7C2) LC K149C-(LD-51), моноамид, ADC-102, 10 мг/кг.
На Фиг. 3 изображена эффективность конъюгатов антитело-лекарственное средство на графике изменения объема опухоли in vivo с течением времени в модели ксенотрансплантата Bjab-luc у мышей CB-17 Fox Chase SCID, которым вводили внутривенно однократно дозу следующего:
1) Наполнитель (гистидиновый буфер № 8 HisAc 20 мМ, сахароза 240 мМ, TW-20 0,02%, pH 5,5), 100 мкл (микролитр)
2) Тио Hu анти-CD22 10F4v3 LC K149C-(CLD-1), ADC-202, 0,1 мг/кг
3) Тио Hu анти-CD22 10F4v3 LC K149C-(CLD-1), ADC-202, 0,2 мг/кг
4) Тио Hu анти-CD22 10F4v3 LC K149C-(C-LD1), ADC-202, 0,4 мг/кг
5) Тио Hu анти-CD22 10F4v3 LC K149C-(LD-51) моноамид ADC-105, 1 мг/кг
6) Тио Hu анти-CD22 10F4v3 LC K149C-(LD-51) моноамид ADC-105, 2 мг/кг
7) Тио Hu анти-CD22 10F4v3 LC K149C-(LD-51) моноамид ADC-105, 4 мг/кг
8) Тио Hu анти-CD22 10F4v3 LC K149C-(LD-51) моноамид ADC-105, 8 мг/кг
9) Тио Hu анти-Her2 hu7C2 LC K149C-(CLD-1) ADC-201, 0,4 мг/кг
10) Тио Hu анти-Her2 hu7C2 LC K149C-(LD-51) моноамид ADC-104, 8 мг/кг.
На Фиг. 4 изображена эффективность конъюгатов антитело-лекарственное средство на графике изменения объема опухоли in vivo с течением времени для клеточной линий человека WSU-DLCL2 в мышиной модели, которой вводили внутривенно однократно дозу следующего:
1) Наполнитель (гистидиновый буфер № 8), 100 мкл
2) Тио Hu анти-CD22 10F4v3 LC K149C-(LD-51) моноамид ADC-105, 5 мг/кг
3) Тио Hu анти-CD22 10F4v3 LC K149C-(LD-52) моноамин, ADC-107, 0,5 мг/кг
4) Тио Hu анти-CD22 10F4v3 LC K149C-(LD-52) моноамин, ADC-107, 2 мг/кг
5) Тио Hu анти-CD22 10F4v3 LC K149C--(LD-52) моноамин, ADC-107, 5 мг/кг
6) Тио Hu анти-CD22 10F4v3 LC K149C-(LD-52) моноамин, ADC-107, 10 мг/кг
7) Тио Hu анти-CD22 10F4v3 LC K149C-(CLD-4) моноамин, ADC-204, 0,5 мг/кг
8) Тио Hu анти-CD22 10F4v3 LC K149C-(CLD-4) моноамин, ADC-204, 2 мг/кг
9) Тио Hu анти-CD22 10F4v3 LC K149C-(CLD-4) моноамин, ADC-204, 5 мг/кг
10) Тио Hu анти-CD22 10F4v3 LC K149C-(CLD-4) моноамин, ADC-204, 10 мг/кг
11) Тио Hu анти-Her2 hu7C2 LC K149C-(LD-52) моноамин, ADC-108, 2 мг/кг
12) Тио Hu анти-Her2 hu7C2 LC K149C-(CLD-4) моноамин, ADC-205, 2 мг/кг.
На Фиг. 5A изображена эффективность конъюгатов антитело-лекарственное средство на графике изменения объема опухоли in vivo с течением времени в модели опухоли HER2 KPL4 у мышей scid beige, которым вводили внутривенно однократно дозу следующего:
1) Наполнитель
2) Тио-Her2 hu7C2 LC-K149C-(LD-51) моноамид, ADC-106, 1 мг/кг
3) Тио-Her2 hu7C2 LC-K149C-(LD-51) моноамид, ADC-106, 5 мг/кг
4) Тио-Her2 hu7C2 LC-K149C-(LD-52) моноамин, ADC-108, 0,5 мг/кг
5) Тио-Her2 hu7C2 LC-K149C-(LD-52) моноамин, ADC-108, 1 мг/кг
6) Тио-Her2 hu7C2 LC-K149C-(LD-52) моноамин, ADC-108, 2 мг/кг
7) Тио-Her2 hu7C2 LC-K149C-(LD-52) моноамин, ADC-108, 5 мг/кг
8) CD22 LC-K149C-(LD-52) моноамин, ADC-107, 1 мг/кг.
На Фиг. 5B изображена эффективность конъюгатов антитело-лекарственное средство на графике изменения объема опухоли in vivo с течением времени в модели опухоли HER2 KPL4 у мышей scid beige, которым вводили внутривенно однократно дозу следующего:
1) Наполнитель
2) Tmab-DM1, ADC-211, 1 мг/кг
3) Тио-Her2 hu7C2 LC-K149C-(LD-51) моноамид, ADC-106, 1 мг/кг
4) Тио-Her2 hu7C2 LC-K149C-(LD-51) моноамид, ADC-106, 5 мг/кг
5) Tmab-DM1, ADC-211, 1мг/кг+Тио-Her2 hu7C2 LC-K149C-(LD-51) моноамид, ADC-106, 1 мг/кг
6) Tmab-DM1, ADC-211, 1мг/кг+Тио-Her2 hu7C2 LC-K149C-(LD-51) моноамид, ADC-106, 5 мг/кг.
На Фиг. 6 изображена эффективность конъюгатов антитело-лекарственное средство на графике изменения объема опухоли in vivo с течением времени в модели HER2 Fo5 у мышей CRL nu/nu, которым вводили внутривенно однократно дозу следующего:
1) Наполнитель (гистидиновый буфер № 8), 100 мкл
2) Тио-Her2 hu7C2 LC-K149C-(CLD-1), ADC-201, 0,5 мг/кг
3) Тио-Her2 hu7C2 LC-K149C-(CLD-1), ADC-201, 1 мг/кг
4) Тио-Her2 hu7C2 LC-K149C-(LD-51), моноамид, ADC-104, 5 мг/кг
5) Тио-Her2 hu7C2 LC-K149C-(LD-51), моноамид, ADC-104, 10 мг/кг
6) Тио-Her2 hu7C2 LC-K149C-(LD-51), моноамид, ADC-104, 15 мг/кг
7) Тио-Her2 hu7C2 LC-K149C неконъюгированное антитело 15 мг/кг
8) Тио-CD22 LC-K149C-(CLD-1), ADC-202, 1 мг/кг
9) Тио-CD22 LC-K149C-(LD-51) моноамид ADC-105, 15 мг/кг.
На Фиг. 7 изображена эффективность конъюгатов антитело-лекарственное средство на графике изменения объема опухоли in vivo с течением времени в модели опухоли HER2 KPL4 у мышей SCID Beige, которым вводили внутривенно однократно дозу следующего:
1) Наполнитель
2) Тио-Her2 hu7C2 LC-K149C-(CLD-1), ADC-201, 1 мг/кг
3) Тио-Her2 hu7C2 LC-K149C-(CLD-1), ADC-201, 3 мг/кг
4) Тио-Her2 hu7C2 LC-K149C-(LD-51) моноамид ADC-104, 3 мг/кг
5) Тио-Her2 hu7C2 LC-K149C-(LD-51) моноамид ADC-104, 6 мг/кг
6) Тио-Her2 hu7C2 LC-K149C-(LD-51) моноамид ADC-104, 10 мг/кг
7) Тио-Her2 hu7C2 LC-K149C, неконъюгированное антитело, 3 мг/кг
8) Тио-Her2 hu7C2 LC-K149C, неконъюгированное антитело, 10 мг/кг
9) Тио-CD22 LC-K149C-(CLD-1), ADC-202, 3 мг/кг
10) Тио-CD22 LC-K149C-(LD-51) моноамид, ADC-105, 10 мг/кг.
На Фиг. 8 изображена эффективность конъюгатов антитело-лекарственное средство на графике изменения объема опухоли in vivo с течением времени в модели HER2 Fo5 у мышей CRL nu/nu, которым вводили внутривенно однократно дозу следующего:
1) Наполнитель
2) Тио-Her2 hu7C2 LC-K149C-(LD-51), моноамид, ADC-106, 5 мг/кг
3) Тио-Her2 hu7C2 LC-K149C-(LD-51), моноамид, ADC-106, 10 мг/кг
4) Тио-Her2 hu7C2 LC-K149C-(LD-52), моноамин, ADC-108, 0,5 мг/кг
5) Тио-Her2 hu7C2 LC-K149C-(LD-52), моноамин, ADC-108, 2 мг/кг
6) Тио-Her2 hu7C2 LC-K149C-(LD-52), моноамин, ADC-108, 5 мг/кг
7) Контроль CD22 LC-K149C-(LD-52), моноамин, ADC-107, 2 мг/кг.
На Фиг. 9 изображена эффективность конъюгатов антитело-лекарственное средство на графике изменения объема опухоли in vivo с течением времени в модели ксенотрансплантата WSU-DLCL2 у мышей CB-17 Fox Chase SCID, которым вводили внутривенно однократно дозу следующего:
1) Наполнитель (гистидиновый буфер № 8), 100 мкл
2) Тио Hu анти-CD22 LC-K149C-(LD-51), моноамид, ADC-104, 6 мг/кг
3) Тио Hu анти-CD22 LC-K149C-(LD-51), моноамид, ADC-104, 16,4 мг/кг
4) Тио Hu анти-CD22 LC-K149C-HC-L177C-(LD-51), моноамид, ADC-111, 3,3 мг/кг
5) Тио Hu анти-CD22 LC-K149C-HC-L177C-(LD-51), моноамид, ADC-111, 6 мг/кг
6) Тио Hu анти-CD22 LC-K149C-HC-L177C-(LD-51), моноамид, ADC-111, 9 мг/кг
7) Тио Hu анти-CD22 LC-K149C-HC-L177C-HC-Y376C-(LD-51), моноамид, ADC-112, 2,2 мг/кг
8) Тио Hu анти-CD22 LC-K149C-HC-L177C-HC-Y376C-(LD-51), моноамид, ADC-112, 6 мг/кг
9) Тио Hu анти-Her2 hu7C2 LC K149C-(LD-51), моноамид, ADC-106, 16,2 мг/кг
10) Тио Hu анти-Her2 4D5 LC K149C-HC L177C-(LD-51), моноамид, ADC-113, 8,3 мг/кг.
На Фиг. 10 изображена эффективность конъюгатов антитело-лекарственное средство на графике изменения объема опухоли in vivo с течением времени в модели ксенотрансплантата HCC1569X2 у мышей SCID Beige, которым вводили внутривенно однократно дозу следующего:
1) Наполнитель (гистидиновый буфер № 8), 100 мкл
2) Тио Hu анти-Ly6E LC K149C-(CLD-1), ADC-212, 1 мг/кг
3) Тио Hu анти-Ly6E LC K149C-(CLD-1), ADC-212, 3 мг/кг
4) Тио Hu анти-Ly6E LC K149C-(LD-51) моноамид, ADC-115, 3 мг/кг
5) Тио Hu анти-Ly6E LC K149C-(LD-51) моноамид, ADC-115, 6 мг/кг
6) Тио Hu анти-Ly6E LC K149C-(LD-51) моноамид, ADC-115, 12 мг/кг
7) Тио Hu анти-Ly6E LC K149C-(LD-51) моноамид, ADC-115, 18 мг/кг
8) Тио Hu анти-CD22 10F4v3 LC K149C-(LD-51) моноамид, ADC-110, 12 мг/кг
9) Тио Hu анти-Ly6E LC K149C-(CLD-4), моноамин, ADC-210, 1 мг/кг
10) Тио Hu анти-Ly6E LC K149C-(CLD-4), моноамин, ADC-210, 3 мг/кг
11) Тио Hu анти-Ly6E LC K149C-(CLD-4), моноамин, ADC-210, 6 мг/кг
12) Тио Hu анти-CD22 10F4v3 LC K149C-(CLD-4), моноамин, ADC-204, 3 мг/кг.
На Фиг. 11 изображены предполагаемые взаимодействия диалкилирующего пирролбензодиазепинового соединения (ПБД (PBD)) и двух моноалкилирующих пирролбензодиазепиновых соединений с ДНК.
На Фиг. 12 изображены сравнение эффективности для мыши и токсичности для яванского макака HER2 LC K149C LD-51 КАЛС (ADC) в сравнении с HER2 LC K149C CLD-1 КАЛС (ADC).
На Фиг. 13 изображены оценка терапевтического индекса на основе экспозиции HER2 LC K149C LD-51 КАЛС (ADC) по сравнению с HER2 LC K149C CLD-1 КАЛС (ADC).
На Фиг. 14 изображены данные по анализу жизнеспособности клеток с несколькими HER2 hu7C2 LC K149C КАЛС (ADC) с различными линкерами.
На Фиг. 15 изображен объем опухоли с течением временем для различных КАЛС (ADC) в мышиной модели аллотрансплантатной опухоли.
ПОДРОБНОЕ ОПИСАНИЕ ИЛЛЮСТРАТИВНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Здесь будет сделана ссылка на определенные варианты осуществления изобретения, примеры которых проиллюстрированы в прилагаемых структурах и формулах. Хотя изобретение будет описано совокупно с проиллюстрированными вариантами осуществления, следует понимать, что они не предназначены для ограничения изобретения этими вариантами осуществления. Напротив, изобретение предназначено для охвата всех альтернативных вариантов, модификаций и эквивалентов, которые могут быть включены в объем настоящего изобретения, как определено формулой изобретения.
Специалист в данной области техники распознает многие способы и материалы, подобные или эквивалентные описанным в данном документе, которые могут быть применены в практической реализации настоящего изобретения. Настоящее изобретение никоим образом не ограничивается описанными способами и материалами.
Если не указано иное, технические и научные термины, применяемые в данном документе, имеют то же значение, которое обычно понимается специалистом в данной области техники, к которой относится настоящее изобретение, и согласуются с: Singleton et al (1994) Dictionary of Microbiology and Molecular Biology, 2nd Ed., J. Wiley & Sons, New York, NY; and Janeway, C., Travers, P., Walport, M., Shlomchik (2001) Immunobiology, 5th Ed., Garland Publishing, New York.
ОПРЕДЕЛЕНИЯ
Если не указано иное, следующие термины и фразы, применяемые в данном документе, имеют следующие значения:
Когда в данном документе используются торговые наименования, заявители намерены самостоятельно включать рецептуру продукта торгового наименования, синоним оригинального препарата (эквивалентный лекарственный препарат без торгового наименования) и активный фармацевтический компонент(ы) продукта товарного наименования.
«Акцепторный каркас человека» в контексте данного документа представляет собой каркас, содержащий аминокислотную последовательность каркаса вариабельного домена легкой цепи (VL) или каркаса вариабельного домена тяжелой цепи (VH), полученного из каркаса иммуноглобулина человека или консенсусного каркаса человека, как определено ниже. Акцепторный каркас человека, «полученный из» каркаса иммуноглобулина человека или консенсусного каркаса человека, может содержать одну и ту же аминокислотную последовательность вышеупомянутого, или может содержать изменения в аминокислотной последовательности. В некоторых вариантах осуществления, количество аминокислотных изменений составляет 10 или менее, 9 или менее, 8 или менее, 7 или менее, 6 или менее, 5 или менее, 4 или менее, 3 или менее, или 2 или менее. В некоторых вариантах осуществления, акцепторный каркас VL человека идентичен по последовательности каркасу VL иммуноглобулина человека, или последовательности консенсусного каркаса человека.
«Аффинность» относится к силе совокупности нековалентных взаимодействий между одиночным сайтом связывания молекулы (например, антитело) и ее партнером по связыванию (например, антиген). Если не указано иное, так как используется в настоящем документе, «аффинность связывания» относится к внутренней аффинности связывания, которая отображает 1:1 взаимодействие между членами пары связывания (например, антитело и антиген). Аффинности молекулы X к ее партнеру Y в целом, как правило может быть представлена константой дисоциации (Кд). Аффинность может быть измерена с помощью общепринятых способов, которые известны в данной области техники, включая те, что описаны в данном документе. Конкретные иллюстративные и типичные варианты реализации изобретения, применяемые для измерения аффинности связывания, описаны в тексте, что следует ниже.
В некоторых вариантах осуществления, антитело, как описано в данном документе, имеет константу диссоциации (Кд) ≤1мкM, ≤100 нM, ≤10 нM, ≤5 нМ, ≤4 нM, ≤3 нM, ≤2 нM, ≤1 нM, ≤0,1 нM, ≤0,01 нM, или ≤0,001 нM (например, 10-8 M или меньше, например от 10-8 M до 10-13 M, например от 10-9 M до 10-13 M).
Антитело со «зрелой аффинностью» относится к антителу с одним или несколькими изменениями в одной или более гипервариабельной области (HVR), по сравнению с исходным антителом, которое не имеет таких изменений, например, таких изменений, результатом которых является улучшения аффинности антитела к антигену.
Термин «антитело» в настоящем документе используется в широком смысле и охватывает различные структуры антитела, которые включают, но не ограничиваются моноклональными антителами, поликлональными антителами, полиспецифическими антителами (например, биспецифические антитела), и фрагментами антитела при условии, что они проявляют желаемую антигенсвязывающую активность.
«Фрагмент антитела» относится к молекуле, отличной от интактного антитела, которая содержит часть интактного антитела и которая связывает антиген, с которым связывается интактное антитело. Примеры фрагментов антитела включают, но не ограничиваются Fv, Fab, Fab', Fab'-SH, F(ab')2; диателами; линейными антителами; одноцепочечными молекулами антителами (например, scFv); и полиспецифическими антителами, которые сформированы из фрагментов антитела.
Термины «рак» и «раковый» относятся к или описывают физиологическое состояние у млекопитающих, которое обычно характеризуется неконтролируемым ростом/делением клеток. «Опухоль» содержит одну или больше раковых клеток. Примеры рака включают, но не ограничиваются лишь этими: карциному, лимфому, бластому, саркому и лейкоз или лимфоидные злокачественные новообразования. Более конкретные примеры таких видов рака включают плоскоклеточный рак (например, эпителиальный плоскоклеточный рак), рак легкого, включая мелкоклеточный рак легкого, немелкоклеточный рак легкого («НМРЛ»), аденокарциному легкого и плоскоклеточную карциному легкого, рак брюшины, гепатоцеллюлярный рак, желудочный рак или рак желудка, включая рак желудочно-кишечного тракта, рак поджелудочной железы, глиобластому, рак шейки матки, рак яичников, рак печени, рак мочевого пузыря, гепатому, рак молочной железы, рак толстой кишки, рак прямой кишки, колоректальный рак, карциному эндометрия или матки, карциному слюнной железы, рака почек или почечный рак, рак предстательной железы, рак вульвы, рак щитовидной железы, карциному печени, анальную карциному, карциному полового члена, а также рак головы и шеи.
«HER2-положительный» рак содержит раковые клетки, которые имеют более высокие, по сравнению с нормальными, уровни HER2. Примеры HER2-положительного рака включают HER2-положительный рак молочной железы и HER2-положительный рак желудка. Необязательно HER2-положительный рак характеризуется иммуногистохимическим (ИГХ) баллом 2+ или 3+ и/или коэффициентом амплификации ≥2,0, определенном по гибридизации in situ (ISH - in situ hybridization).
Термин «рак молочной железы на ранней стадии (РРМЖ)» или «ранний рак молочной железы» используется в данном документе для обозначения рака молочной железы, который не распространился за пределы молочной железы или подмышечных лимфатических узлов. Термин включает протоковую карциному in situ и стадию I, стадию IIA, стадию IIB и стадию IIIA рака молочной железы
Отсылка к опухоли или раку как «Стадия 0», «Стадия I», «Стадия II», «Стадия III» или «Стадия IV», а также различные подстадии в рамках этой классификации, указывает на классификацию опухоли или рака с применением известных в данной области техники способов общей группировки по стадиям или стадирования с помощью римских цифр. Хотя фактическая стадия рака зависит от типа рака, как правило, 0 стадия рака представляет собой поражение in situ, I стадия рака представляет собой небольшую локализованную опухоль, II и III стадия рака представляет собой местно распространенную опухоль с вовлечением местных лимфатических узлов, и IV стадия рака представляет собой метастатический рак. Конкретные стадии для каждого типа опухоли известны квалифицированному клиницисту.
Термин «метастатический рак молочной железы» обозначает состояние рака молочной железы, когда раковые клетки переносятся из первоначального места в одно или более мест в других частях тела по кровеносным или лимфатическим сосудам, с образованием одной или более вторичных опухолей в одном или более органов, помимо молочной железы.
«Распространенный» рак представляет собой рак, который распространился за пределы места или органа происхождения либо путем местной инвазии, либо путем метастазирования. Соответственно, термин «распространенный» рак включает как местно-распространенное, так и метастатическое заболевание.
«Рецидивирующий» рак представляет собой рак, который повторно вырос либо на первоначальном месте, либо в удаленном от первоначального месте, после ответа на первоначальное лечение, такое как оперативное вмешательство.
«Местно-рецидивирующий» рак представляет собой рак, который рецидивирует после лечения в том же месте, что и ранее пролеченный рак.
«Операбельный» или «резектабельный» рак представляет собой рак, который ограничивается первичным органом и пригоден для хирургического вмешательства (удаления).
«Нерезектабельный» или «неоперабельный» рак не может быть удален (иссечен) хирургическим путем.
Термин «химерное» антитело относится к антителу, в котором часть тяжелой и/или легкой цепи получена из определенного источника или вида, а оставшаяся часть тяжелой и/или легкой цепи получена из различных источников или видов.
«Класс» антитела относится к типу константного домена или константной области, которые принадлежат его тяжелой цепи. Существует пять основных классов антител: IgA, IgD, IgE, IgG, и IgM, и некоторые из них могут быть дополнительно разделены на подклассы (изотипы), например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2. Константные домены тяжелой цепи, которые соответствуют различным классам иммуноглобулинов, называются α, δ, ε, γ и μ, соответственно.
Термин «цитотоксическое вещество», который используется в данном документе, относится к веществу, которое ингибирует клеточную функцию или препятствует ей, и/или вызывает клеточную смерть, или разрушение. Цитотоксические вещества включают, но не ограничиваются, радиоактивными изотопами (например, At211, I131, I125, Y90, Re186, Re188, Sm153, Bi212, P32, Pb212 и радиоактивный изотоп Lu); хемотерапевтическими веществами или лекарственными веществами (например, метотрексат, адриамицин, винка-алкалоиды (винкристин, винбластин, этопозид), доксорубицин, мелфалан, митомицин С, хлорамбуцил, даунорубицин или другие интеркалирующие вещества); веществами-ингибиторами роста; ферментами и их фрагментами, такими как нуклеолитические ферменты; антибиотиками; токсинами, такими как низкомолекулярные токсины или ферментативно активные токсины бактериального, грибкового, растительного или животного происхождения, включая их фрагменты и/или варианты; и различными противоопухолевыми или противораковыми веществами, которые раскрыты ниже.
«Эффекторные функции» относятся к тем биологическим активностям, которые приписывают Fc области антитела, и которые варьируют в зависимости от изотипа антитела. Примеры эффекторных функций антитела включают: связывание c C1q и комплемент-зависимую цитотоксичность (КЗЦ); связывания c рецептором Fc; антитело-зависимую клеточно-опосредованную цитотоксичность (АЗКЦ); фагоцитоз; подавление клеточных поверхностных рецепторов (например, рецептора B-лимфоцита); и активацию В-лимфоцитов.
«Эффективное количество» вещества, например, фармацевтической лекарственной формы, относится к количеству эффективных, в дозировках и в течение периодов времени, необходимых для достижения желаемого терапевтического или профилактического результата. Эффективное количество лекарственного средства может уменьшать количество раковых клеток; уменьшать размер опухоли; ингибировать (т.е. замедлять до некоторой степени и предпочтительно останавливать) инфильтрацию раковых клеток в периферические органы; ингибировать (т.е. замедлять до некоторой степени и предпочтительно останавливать) метастазирование опухоли; ингибировать до некоторой степени рост опухоли; и/или ослаблять до некоторой степени один или более симптомов, ассоциированных с раком. В той мере, насколько препарат может предотвратить рост и/или разрушать существующие раковые клетки, он может быть цитостатическим и/или цитотоксическим. Эффективное количество может продлить выживаемость без прогрессирования (например, которая измеряется с помощью Критериев оценки ответа для солидных опухолей (RECIST) или изменений CA-125) и проводить к объективному ответу (включая частичный ответ (ЧО (PR)) или полный ответ (ПО(CR))), продлению времени общей выживаемости и/или ослаблению одного или более симптомов рака (например, по оценке FOSI).
Термин «эпитоп» относится к конкретному сайту на молекуле антигена, с которым связывается антитело.
«Эпитоп 4D5» или «эпитоп 4D5» или «4D5» представляет собой область во внеклеточном домене HER2, с которой связывается антитело 4D5 (АТСС CRL 10463) и трастузумаб. Этот эпитоп примыкает к трансмембранному домену HER2 и находится в пределах домена IV HER2. Для скрининга антител, которые связываются с эпитопом 4D5, может быть выполнен перекресто-блокирующий анализ, как описано в Antibodies, A Laboratory Manual, Cold Spring Harbor Laboratory, Ed Harlow and David Lane (1988). В альтернативном варианте может быть осуществлено картирование эпитопов для оценки того, связывается ли антитело с эпитопом 4D5 HER2 (например, каким-либо одним или больше остатков в области от остатка около 550 до остатка около 610, включительно, HER2 (SEQ ID NO: 39)).
«Эпитоп 2С4» или «2С4 эпитоп» представляет собой область во внеклеточном домене HER2, с которой связывается антитело 2С4. С целью скрининга антител, которые связываются с эпитопом 2C4, может быть выполнен перекресто-блокирующий анализ, как описано в Antibodies, A Laboratory Manual, Cold Spring Harbor Laboratory, Ed Harlow and David Lane (1988). В альтернативном варианте может быть осуществлено картирование эпитопов для оценки того, связывается ли антитело с эпитопом 2C4 HER2. Эпитоп 2C4 содержит остатки из домена II во внеклеточном домене HER2. Антитело 2C4 и пертузумаб связываются с внеклеточным доменом HER2 на стыке доменов I, II и III (Franklin et al. Cancer Cell 5:317-328 (2004)).
Анти-HER2 мышиное антитело 7C2 связывается с эпитопом в домене I HER2. См., например, публикацию PCT № WO 98/17797. Данный эпитоп отличается от эпитопа, связываемого трастузумабом, который связывается с доменом IV HER2, и эпитопа, связываемого пертузумабом, который связывается с доменом II HER2. Трастузумаб, при связывании домена IV, разрушает лиганд-независимые комплексы HER2-HER3, тем самым ингибируя нисходящий сигналинг (например, PI3K/AKT). В противоположность этому, пертузумаб, связывающийся с доменом II, предотвращает лиганд-управляемое взаимодействие HER2 с другими членами семейства HER (например, HER3, HER1 или HER4), что также предотвращает нисходящую передачу сигнала. Связывание MAb 7C2 с доменом I не приводит к препятствованию связывания трастузумаба или пертузумаба с доменами IV и II соответственно, тем самым предполагает возможность объединения КАЛС (ADC) MAb 7C2 с трастузумабом, трастузумабом эмтанзином (Т-DM-1) и/или пертузумабом. Антитело 7C2, 7C2.B9 мыши описано в публикации PCT № WO 98/17797. Анти-HER2 7C2 гуманизированное антитело описано в WO2016/040723A1.
Термин «Fc область» в настоящем документе применяется для определения C-концевой области тяжелой цепи иммуноглобулина, которая содержит по меньшей мере часть константной области. Термин включает в себя нативные последовательности Fc областей и различные Fc области. В одном варианте осуществления, Fc область тяжелой цепи человеческого IgG продолжается от Cys226, или от Pro230, до карбоксильного конца тяжелой цепи. Однако, C-концевой лизин (Lys447) Fc области может присутствовать или отсутствовать. Если в настоящем документе не указано иное, нумерация аминокислотных остатков в Fс области или в константной области соответствует системе нумерации ЕС, также называемый индексом ЕС, как описано в Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD, 1991.
«Каркас» или «FR» относится к остаткам вариабельного домена, кроме остатков гипервариабельной области (HVR). FR вариабельного домена в целом, как правило состоит из четырех FR доменов: FR1, FR2, FR3, и FR4. Соответственно, HVR и FR последовательности в целом, как правило, появляются в следующей последовательности VH (или VL): FR1-H1(L1)-FR2-H2(L2)-FR3-H3(L3)-FR4.
Термины «полноразмерное антитело», «интактное антитело», и «целое антитело» используются в настоящем документе взаимозаменяемо для обозначения антитела, которое имеет структуру, что существенно похожа на нативные структуры антитела или имеет тяжелые цепи, которые содержат Fc область как определено в настоящем документе.
Термины «клетка-хозяин», «линия клетки-хозяина», и «культура клетки-хозяина» используются взаимозаменяемо, и относятся к клеткам в которые была введена экзогенная нуклеиновая кислота, включая потомство таких клеток. Клетки-хозяева включают «трансформанты» и «трансформированные клетки», которые включают первично трансформированные клетки и потомство, которое получено от них без учета количества пассажей. Потомство не может быть полностью идентичным по содержанию нуклеиновых кислот относительно материнской клетки, но может содержать мутации. В настоящий документ включено мутантное потомство, которое имеет одну и ту же функцию, или биологическую активность, что и первоначальная трансформированная клетка после скрининга и отбора.
«Человеческое антитело» представляет собой антитело, которое имеет аминокислотную последовательность, что соответствует таковой антитела, которое произведено человеком или человеческой клетка, или получено из нечеловеческого источника, который использует репертуар человеческих антител или другие человеческие антитело-кодирующие последовательности. Это определение человеческого антитела специфически исключает гуманизированные антитела, которые содержат нечеловеческие, антигенсвязывающие остатки.
«Человеческий консенсусный каркас» представляет собой каркас, который представляет наиболее часто встречающиеся аминокислотные остатки в наборе VL или VH каркасных иммуноглобулиновых последовательностей человека. В целом, как правило, набор иммуноглобулиновых VL или VH последовательностей человека представляет собой подгруппу последовательностей вариабельного домена. В целом, как правило, подгруппа последовательностей представляет собой подгруппу, как в Kabat et al., Sequences of Proteins of Immunological Interest, Fifth Edition, NIH Publication 91-3242, Bethesda MD (1991), vols. 1-3. В одном варианте осуществления, для VL, подгруппа представляет собой подгруппу каппа I, как в Kabat et al., выше. В одном варианте осуществления, для VH, подгруппа представляет собой подгруппу III как в Kabat et al., выше.
«Гуманизированное» антитело относится к химерному антителу, содержащему аминокислотные остатки из нечеловеческих HVR и аминокислотные остатки из FR человека. В некоторых вариантах осуществления, гуманизированное антитело будет содержать в основном все остатки хотя бы одного, и типично двух, вариабельных доменов, в которых все, или в основном все HVR (например, CDR), соответствуют таким же нечеловеческого антитела, и все, или в основном все FR, соответствуют таким же человеческого антитела. Гуманизированное антитело необязательно может содержать по меньшей мере часть константной области антитела, которая получена из человеческого антитела. «Гуманизированная форма» антитела, например, нечеловеческое антитело, относится к антителу которое подверглось гуманизации.
Термин «гипервариабельная область» или «HVR», используемый в настоящем документе, относится к каждой из областей вариабельного домена антитела, которые являются гипервариабельными по последовательности и/или которые формируют структурно определенные петли («гипервариабельные петли»). В целом, как правило, нативные четырецепочечные антитела содержат шесть HVR: три в VH (H1, H2, H3), и три в VL (L1, L2, L3). В целом, как правило, HVR содержат аминокислотные остатки из гипервариабельных петель и/или из «определяющих комплементарность областей» (CDR), последние характеризуются самой высокой вариабельностью последовательностей и/или вовлечены в распознавание антигена. Типичные гипервариабельные петли находятся в области аминокислотных остатков 26-32 (L1), 50-52 (L2), 91-96 (L3), 26-32 (H1), 53-55 (H2), и 96-101 (H3). (Chothia and Lesk, J. Mol. Biol. 196:901-917 (1987).) Типичные CDR (CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3) находятся в области аминокислотных остатков 24-34 L1, 50-56 L2, 89-97 L3, 31-35B H1, 50-65 H2 и 95-102 H3. (Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD (1991).) За исключением CDR1 в VH, CDR в целом, как правило, содержат аминокислотные остатки, образующие гипервариабельные петли. CDR также содержат «остатки, определяющие специфичность» или «SDR», которые представляют собой остатки, контактирующие с антигеном. SDR содержатся в областях CDR, называемых укороченными CDR или a-CDR. Типичные a-CDR (a-CDR-L1, a-CDR-L2, a-CDR-L3, a-CDR-H1, a-CDR-H2 и a-CDR-H3) находятся в области аминокислотных остатков 31-34 L1, 50-55 L2, 89-96 L3, 31-35B H1, 50-58 H2 и 95-102 H3. (See Almagro and Fransson, Front. Biosci. 13:1619-1633 (2008).) Если не указано иное, остатки HVR и другие остатки в вариабельном домене (например, FR-остатки) в настоящем документе пронумерованы в соответствии с Кабат et al., выше.
«Иммуноконъюгат» представляет собой антитело, конъюгированное с одной или больше гетерологичными молекулами, включая цитотоксическое вещество, но не ограничиваясь лишь им.
«Пациент», или «индивид», или «субъект» представляет собой млекопитающее. Млекопитающие включают, но не ограничиваются лишь этими: одомашненных животных (например, коров, овец, кошек, собак и лошадей), приматов (например, людей и низших приматов, таких как обезьяны), кроликов и грызунов (например, мышей и крыс). В некоторых вариантах осуществления, пациент, индивид или субъект является человеком. В некоторых вариантах осуществления, пациент может быть «пациентом с раком», т.е. таким, который страдает от или подвержен риску развития одного или более симптомов рака, в частности, рака желудка или рака молочной железы.
Термин «популяция пациентов» относится к группе пациентов с раком. Такие популяции могут быть использованы для демонстрации статистически значимой эффективности и/или безопасности лекарственного препарата.
Пациент «с рецидивом» - это тот, кто имеет признаки или симптомы рака после ремиссии. Необязательно, у пациента может быть рецидив после адъювантной или неоадъювантной терапии.
Рак или биологический образец, который «характеризуется экспрессией, амплификацией или активацией HER», является таким, который в диагностическом тесте экспрессирует (в том числе сверхэкспрессирует) рецептор HER, имеет амплифицированный ген HER, и/или иным образом демонстрирует активацию или фосфорилирование рецептора HER.
В настоящем документе термин «неоадъювантная терапия» или «предоперационная терапия» относится к терапии, назначаемой до оперативного вмешательства. Целью неоадъювантной терапии является обеспечение немедленного системного лечения с потенциальной эрадикацией микрометастазов, которые в противном случае начали бы пролиферировать, если бы осуществлялась стандартная последовательность выполнения оперативного вмешательства с последующим назначением системной терапии. Неоадъювантная терапия может также способствовать уменьшению размера опухоли, тем самым позволяя производить полную резекцию первоначально неоперабельных опухолей или сохранить часть органа и его функции. Кроме того, неоадъювантная терапия позволяет оценить in vivo эффективность лекарственного препарата, которая может определять выбор последующих способов лечения.
В настоящем документе термин «адъювантная терапия» относится к терапии, назначаемой после радикального оперативного вмешательства, для того чтобы уменьшить риск рецидива заболевания, при этом никаких признаков остаточной болезни не обнаруживается. Целью адъювантной терапии является предотвращение рецидива рака, и, следовательно, снижение вероятности смерти, связанной с раком. Адъювантная терапия в настоящем изобретении, в частности, исключает неоадъювантную терапию.
Термин «радикальное оперативное вмешательство» используется так, как он используется в медицинском сообществе. Радикальное оперативное вмешательство включает, например, хирургические или другие процедуры, в результате которых осуществляется удаление или резекция опухоли, в том числе те, в результате которых осуществляется удаление или резекция всей видимой невооруженным глазом опухоли. Радикальное оперативное вмешательство включает, например, полную или клинически радикальную резекцию, или резекцию опухоли в полном объеме. Радикальное оперативное вмешательство включает процедуры, которые происходят в один или более этапов, и включает, например, многоэтапные хирургические процедуры, причем одна или больше хирургических или других процедур выполняются до резекции опухоли. Радикальное оперативное вмешательство включает процедуры по удалению или резекции опухоли, включая вовлеченные органы, части органов и тканей, а также окружающие органы, такие как лимфатические узлы, части органов, или ткани. Удаление может быть неполным, вследствие чего опухолевые клетки могли оставаться, даже в том случае, если были незамеченными.
Термин «выживаемость» относится к пациенту, оставшемуся в живых, и включает выживаемость без признаков заболевания (ВБПЗ (DFS)), выживаемость без прогрессирования (ВБП (PFS)) и общую выживаемости (OВ (OS)). Показатели выживаемости могут быть оценены по методу Каплана-Мейера, а какие-либо их различия вычисляются с помощью стратифицированного логрангового критерия.
«Выживаемость без прогрессирования заболевания» (ВБП (PFS)) представляет собой время с первого дня лечения до задокументированного прогрессирования заболевания (включая изолированную прогрессию в ЦНС) или смерти от любой причины в период исследования, в зависимости от того, что произойдет раньше.
Термин «выживаемость без признаков заболевания (ВБПЗ (DFS))» относится к пациенту, оставшемуся в живых, без рецидива рака в течение определенного периода времени, например, около 1 года, около 2 лет, около 3 лет, около 4 лет, около 5 лет, около 10 лет и т.д. от начала лечения или от первой постановки диагноза. В одном из аспектов настоящего изобретения, ВБПЗ (DFS) анализируют согласно назначенному лечению, т.е. пациентов оценивают на основании назначенной им терапии. События, анализируемые в рамках ВБПЗ (DFS), могут включать местные, регионарные и отдаленные рецидивы рака, возникновение вторичного рака и смерти от любой причины у пациентов без предварительного события (например, рецидив рака молочной железы или второй первичный рак).
Термин «общая выживаемость» относится к пациенту, оставшемуся в живых в течение определенного периода времени, например, около 1 года, около 2 лет, около 3 лет, около 4 лет, около 5 лет, около 10 лет и т.д. от начала лечения или от первой постановки диагноза. В исследованиях, лежащих в основе изобретения, событием, которое учитывалось при анализе выживаемости, была смерть от любой причины.
Под термином «увеличение выживаемости» подразумевают увеличение ВБПЗ (DFS) и/или OВ (OS) в пролеченных пациентов по сравнению с пациентами, не получавшими лечения, или по сравнению с контрольным протоколом лечения. Выживание контролируется в течение по меньшей мере около шести месяцев, или по меньшей мере около 1 года, или по меньшей мере около 2 лет, или по меньшей мере около 3 лет, или по меньшей мере около 4 лет, или по меньшей мере около 5 лет, или по меньшей мере около 10 лет и т.д. от начала лечения или от первой постановки диагноза.
Под термином «монотерапия» подразумевается терапевтическая схема, которая включает только одно терапевтическое вещество для лечения рака или опухоли в течение периода лечения.
Под термином «поддерживающая терапия» подразумевается терапевтическая схема, которая назначается с целью снижения вероятности рецидива или прогрессирования заболевания. Поддерживающая терапия может назначаться в течение длительного времени, включая длительные периоды времени вплоть до периода продолжительности жизни субъекта. Поддерживающая терапия может быть назначена после первичной терапии или в сочетании с первичной или дополнительной терапией. Дозы, используемые для поддерживающей терапии, могут изменяться и включать сниженные дозы по сравнению с дозами, используемыми для других видов терапии.
«Выделенное антитело» представляет собой антитело, отделенное от компонента своего природного окружения. В некоторых вариантах осуществления, антитело является очищенным до более чем 95% или 99% чистоты, определяемой, например, посредством электрофореза (например, электрофореза в ДСН-ПААГ, изоэлектрического фокусирования (ИЭФ), капиллярного электрофореза) или хроматографии (например, ионообменной или обращенно-фазной ВЭЖХ). Обзор способов анализа чистоты антител, см., например, Flatman et al., J. Chromatogr. B 848:79-87 (2007).
Термин «выделенная нуклеиновая кислота» относится к молекуле нуклеиновой кислоты, отделенной от компонента своего природного окружения. Выделенная нуклеиновая кислота содержит молекулу нуклеиновой кислоты, содержавшуюся в клетках, обычно содержащих молекулу нуклеиновой кислоты, однако молекула нуклеиновой кислоты присутствует вне хромосомы или в области хромосомы, отличающейся от ее естественного местоположения в хромосоме.
«Выделенная нуклеиновая кислота, кодирующая антитело» относится к одной или больше молекулам нуклеиновых кислот, кодирующим тяжелые и легкие цепи антитела (или их фрагменты), включая молекулы нуклеиновых кислот в одном векторе или отдельных векторах, и молекулы нуклеиновых кислот, присутствующие в одной или более локациях в клетке-хозяине.
Термин «HER2», как применяется в данном документе, относится к нативному, созревшему HER2, который продуцируется при процессинге белкового предшественника HER2 в клетке. Термин включает HER2 из любого позвоночного животного, включая млекопитающих, таких как приматы (например, люди и яванские макаки) и грызуны (например, мыши и крысы), до тех пор, пока не указано иное. Термин также включает естественно встречающиеся варианты HER2, например сплайс-варианты или аллельные варианты. Аминокислотная последовательность типичного белка предшественника HER2 человека с сигнальной последовательностью (с сигнальной последовательностью, аминокислоты 1-22) показана в SEQ ID NO: 64. Аминокислотная последовательность иллюстративного зрелого белка HER2 человека представляет собой аминокислотные остатки 23-1255 SEQ ID NO: 64.
Термин «HER2-положительная клетка» относится к клетке, которая экспрессирует HER2 на ее поверхности.
Термин «моноклональное антитело», как используется в настоящем документе, относится к антителу, полученному из популяции практически гомогенных антител, т.е. отдельные антитела, составляющие популяцию, являются идентичными и/или связывают один и тот же эпитоп, за исключением возможных вариантов антител, например, содержащих встречающиеся в природе мутации или появляющиеся в процессе получения препарата моноклонального антитела, при этом такие варианты в целом, как правило, присутствуют в незначительных количествах. В отличие от препаратов поликлональных антител, которые обычно содержат различные антитела, направленные против различных детерминант (эпитопов), каждое моноклональное антитело препарата моноклонального антитела направлено против одной детерминанты на антигене. Таким образом, определение «моноклональный» указывает на характеристику антитела, полученного по существу из гомогенной популяции антител, и не должно быть истолковано как необходимость получения антитела каким-либо конкретным способом. Например, моноклональные антитела, которые предполагается применять в соответствии с настоящим изобретением, могут быть получены множеством методик, включая, но не ограничиваясь лишь этими: гибридомный способ, способы с использованием рекомбинантных ДНК, способы фагового дисплея и способы с применением трансгенных животных, содержащих все или часть локусов иммуноглобулинов человека, при этом такие способы, а также другие типичные способы получения моноклональных антител описаны в данном документе.
«Неконъюгированное антитело» обозначает антитело, которое не конъюгировано с гетерологичным компонентом (например, цитотоксическим компонентом) или радиометкой. Неконъюгированное антитело может присутствовать в фармацевтической композиции.
«Нативные антитела» относятся к встречающимся в природе молекулам иммуноглобулинов с различной структурой. Например, нативные антитела IgG обычно представляют собой гетеротетрамерные гликопротеины с молекулярной массой около 150000 дальтон, состоящие из двух идентичных легких цепей и двух идентичных тяжелых цепей, связанных дисульфидными связями. Каждая тяжелая цепь от N-конца к C-концу содержит вариабельную область (VH), также называемую вариабельным тяжелым доменом или вариабельным доменом тяжелой цепи, с последующими тремя константными доменами (CH1, CH2 и CH3). Аналогично, каждая легкая цепь от N-конца к C-концу содержит вариабельную область (VL), также называемую вариабельным легким доменом или вариабельным доменом легкой цепи, с последующим константным легким доменом (CL). Легкую цепь антитела на основании аминокислотной последовательности ее константного домена можно отнести к одному из двух типов, называемых каппа (κ) и лямбда (λ).
«Флакон» представляет собой контейнер, пригодный для наполнения жидким или лиофилизированным препаратом. В одном варианте осуществления, флакон представляет собой одноразовый флакон, например, одноразовый флакон 20 сс с пробкой.
Термин «листок-вкладыш» используется для обозначения инструкций, обычно помещаемых в коммерческие упаковки терапевтических средств, которые содержат информацию о показаниях, применении, дозах, введении, комбинированной терапии, противопоказаниях и/или предупреждениях, касающихся использования таких терапевтических средств.
«Процент (%) идентичности аминокислотной последовательности» по отношению к последовательности эталонного полипептида определяется как процент аминокислотных остатков в последовательности-кандидате, которые являются идентичными аминокислотным остаткам в последовательности эталонного полипептида после выравнивания последовательностей и, при необходимости, внесения пробелов, для достижения максимального процента идентичности последовательностей, без учета консервативных замен как части идентичности последовательностей. Выравнивание для целей определения процента идентичности аминокислотных последовательностей можно осуществить различными способами, известными специалистам в данной области техники, например, применяя общедоступное компьютерное программное обеспечение, например, программное обеспечение BLAST, BLAST-2, ALIGN или Megalign (DNASTAR). Специалисты в данной области техники могут определить походящие параметры для выравнивания последовательностей, включая любые алгоритмы, необходимые для достижения максимального выравнивания по всей длине последовательностей, подлежащих сравнению. Однако, в контексте данного документа значения % идентичности аминокислотной последовательности получают применяя компьютерную программу для сравнения последовательностей ALIGN-2. Компьютерная программа для сравнения последовательностей ALIGN-2 была разработана Genentech, Inc., и исходный код был подан с пользовательской документацией в Бюро регистрации авторских прав США (U.S. Copyright Office), Вашингтон, округ Колумбия, 20559, где она была зарегистрирована как объект авторского права США под регистрационным № TXU510087. Программа ALIGN-2 является общедоступной от Genentech, Inc., Южный Сан-Франциско, Калифорния, или может быть скомпилирована с исходной программы. Программа ALIGN-2 требует компиляции для применения в операционной системе UNIX, включая цифровую UNIX V4.0D. Все параметры сравнения последовательностей установлены программой ALIGN-2 и не изменяются.
Когда для сравнения аминокислотных последовательностей применяют ALIGN-2, % идентичности аминокислотных последовательностей заданной аминокислотной последовательности A по отношению к, с или против заданной аминокислотной последовательности B (что в альтернативном варианте можно перефразировать как заданная аминокислотная последовательность А, которая имеет или характеризуется % идентичности аминокислотных последовательностей по отношению к, с или против заданной аминокислотной последовательности B) рассчитывают следующим образом:
100 умножить на соотношение X/Y,
где X - это число аминокислотных остатков, соответствующих идентичным совпадениям согласно программе выравнивания последовательностей ALIGN-2 при выравнивании А и B, осуществленном этой программой, а Y - это общее количество аминокислотных остатков в B. Следует понимать, что если длина аминокислотной последовательности А не равна длине аминокислотной последовательности В, % идентичности аминокислотных последовательностей А к В не равен % идентичности аминокислотных последовательностей В к А. Если четко не указано иное, все значения % идентичности аминокислотных последовательностей, применяемые в данном документе, получены так, как описано в предыдущем параграфе при помощи компьютерной программы ALIGN-2.
Термин «фармацевтический состав» относится к препарату, который находится в такой форме, что позволяет биологической активности содержащегося в нем активного ингредиента быть эффективной, и который не содержит дополнительных компонентов, которые являются неприемлемо токсичными для субъекта, которому вводят состав.
«Фармацевтически приемлемый носитель» относится к ингредиенту в фармацевтическом составе, отличному от активного ингредиента, который является нетоксичным для субъекта. Фармацевтически приемлемые носители включают, но не ограничиваются лишь этими: буфер, вспомогательное вещество, стабилизатор или консервант.
Как применяется в данном документе, «лечение» (и его грамматические варианты, такие как «лечить» или «проводить лечение») относится к клиническому вмешательству при попытке изменить естественное развитие заболевание индивида, подвергаемого лечению, и может осуществляться либо для профилактики, либо в ходе развития клинической патологии. Желательные эффекты лечения включают, но не ограничиваются лишь этими: предупреждение возникновения или возврата заболевания, облегчение симптомов, уменьшение любых прямых или косвенных патологических последствий заболевания, предотвращение метастазов, уменьшение скорости прогрессирования болезни, улучшение или временное облегчение болезненного состояния и достижение ремиссии или улучшенного прогноза. В некоторых вариантах осуществления, антитела по данному изобретению применяются для задержки развития заболевания или замедления прогрессирования заболевания.
Под термином «совместное введение» подразумевают внутривенное введение двух (или больше) препаратов в процессе одного и того же введения, в отличие от последовательных инфузий двух или более препаратов. Как правило, это будет предусматривать комбинирование двух (или более) препаратов в одном и том же ВВ (IV) контейнере перед совместным введением.
Лекарственное средство, которое вводят «одновременно» с одним или больше другими лекарственными средствами, вводится в течение одного и того же цикла лечения, в одни и те же сутки лечения, что и одно или больше других лекарственных средств, и в некоторых случаях - в одно и то же время, что и одно или больше других лекарственных средств. Например, при противораковой терапии, применяемой каждые 3 недели, одновременно вводимые препараты являются теми, которые вводятся в 1 сутки 3-недельного цикла.
«Химиотерапевтическое вещество» представляет собой химическое соединение, применяемое в лечении рака. Примеры химиотерапевтических веществ включают: алкилирующие вещества, такие как тиотепа и циклофосфамид (CYTOXAN®); алкилсульфонаты, такие как бусульфан, импросульфан и пипосульфан; азиридины, такие как бензодопа, карбоквон, метуредопа и уредопа; этиленимины и метиламеламины, включая алтретамин, триэтиленмеламин, триэтиленфосфорамид, триэтилентиофосфорамид и триметилолмеламин; ацетогенины (особенно буллатацин и буллатацинон); дельта-9-тетрагидроканнабинол (дронабинол, MARINOL®); бета-лапакон; лапахол; колхицины; бетулиновая кислота; камптотецин (включая синтетический аналог топотекан (HYCAMTIN®), СРТ-11 (иринотекан, CAMPTOSAR®), ацетилкамптотецин, скополетин, и 9-аминокамптотецин); бриостатин; каллистатин; CC-1065 (включая его синтетические аналоги адозелезин, карзелезин и бизелезин); подофиллотоксин; подофиллиновая кислота; тенипозид; криптофицины (в частности, криптофицин 1 и криптофицин 8); доластатин; дуокармицин (включая синтетические аналоги, KW-2189 и CB1-TM1); элеутеробин; панкратистатин; саркодиктин; спонгистатин; азотистый иприт, такой как хлорамбуцил, хлорнафазин, хлорфосфамид, эстрамустин, ифосфамид, мехлорэтамин, гидрохлорид оксида мехлорэтамина, мелфалан, новембихин, фенэстерин, преднимустин, трофосфамид, урациловый иприт; производные нитрозомочевины, такие как кармустин, хлорозотоцин, фотемустин, ломустин, нимустин и ранимнустин; антибиотики, такие как энедииновые антибиотики (например, калихимицин, особенно калихимицин гамма1I и калихимицин омегаI1 (см., например, Nicolaou et al., Angew. Chem Intl. Ed. Engl., 33: 183-186 (1994)); CDP323, пероральный ингибитор интегрина альфа-4; динемицин, включая динемицин А; эсперамицин; а также хромофор неокарциностатина и родственные хромопротеиновые эндиеновые антибиотические хромофоры), аклациномизины, актиномицин, аутрамицин, азасерин, блеомицины, кактиномицин, карабицин, карминомицин, карцинофилин, хромомицины, дактиномицином, даунорубицин, деторубицин, 6-диазо-5-оксо-L-норлейцин, доксорубицин (включая ADRIAMYCIN®, морфолинодоксорубицин, цианоморфолинодоксорубицин, 2-пирролинодоксорубицин, инъекции липосом доксорубицин-HCl (DOXIL®), липосомальный доксорубицин TLC D-99 (MYOCET®), пегглизированный липосомальный доксорубицин (CAELYX®) и дезоксидоксорубицин; эпирубицин, эзорубицин, идарубицин, марцеломицин, митомицины, такие как митомицин C, микофеноловая кислота, ногаламицин, оливомицины, пепломицин, порфиромицин, пуромицин, квеламицин, родорубицин, стрептонигрин, стрептозоцин, туберцидин, убенимекс, зиностатин, зорубицин; антиметаболиты, такие как метотрексат, гемцитабин (GEMZAR®), тегафур (UFTORAL®), капецитабин (XELODA®), эпотилона и 5-фторурацил (5-FU); аналоги фолиевой кислоты, такие как деноптерин, метотрексат, птероптерин, триметрексат; пуриновые аналоги, такие как флударабин, 6-меркаптопурин, тиамиприн, тиогуанин; аналоги пиримидина, такие как анцитабин, азацитидин, 6-азауридин, кармофур, цитарабин, ди-деоксиуридин, доксифлуридин, эноцитабин, флоксуридин, андрогены, такие как каластоун, пропионат дромоностанола, эпитиостанол, мепитиостан, тестолактон; средства, угнетающие функции надпочечников, такие как аминоглютетимид, митотан, трилостан; компенсаторы фолиевой кислоты, такие как фолиновая кислота; ацеглатон; гликозид алдофосфамида; аминолевулиновая кислота; энилурацил; амсакрин; бестрабуцил; бизантрен; эдатраксат; дефофамин; демеколицин; диазиквон; эльфорнитин; эллиптиум ацетат; эпотилон; этоглюцид; нитрат галлия; гидроксимочевина; лентинан; лонидайнин; майтанзиноиды, такие как маитанзин и ансамитоцины; митогуазон; митоксантрон; мопиданмол; нитраэрин; пентостатин; фенамет; пирарубицин; лозоксантрон; 2-этилгидразид; прокарбазин; полисахаридный комплекс PSK® (JHS Natural Products, Eugene, OR); разоксан; ризоксин; сизофиран; спирогерманий; тенуазоновая кислота; триазиквон; 2,2',2'-трихлортриэтиламин; трихотецены (особенно токсин Т-2, верракурин А, роридин А и ангуидин); уретан; виндезин (ELDISINE®, FILDESIN®); дакарбазин; манномустин; митобронитол; митолактол; пипоброман; гацитозин; арабинозид («Ara-C»); тиотепа; таксоиды, например, паклитаксел (TAXOL®), препарат альбумин-спроектированных наночастиц паклитаксела (ABRAXANETM), и доцетаксел (TAXOTERE®); хлоранбуцил; 6-тиогуанин; меркаптопурин; метотрексат; аналоги платины, такие как цисплатин, оксалиплатин (например, ELOXATIN®), и карбоплатин; винкас, который предотвращает полимеризацию тубулина в микротрубочки, включая винбластин (VELBAN®); винкристин (ONCOVIN®); виндезин (ELDISINE®, FILDESIN®); винорелбин (NAVELBINE®); этопозид (VP-16); ифосфамид; митоксантрон; лейковорин; новантрон; эдатрексат; дауномицин; аминоптерин; ибандронат; ингибитор топоизомеразы RFS 2000; дифторметилорнитин (DMFO); ретиноиды, такие как ретиноевая кислота, включая бексаротен (TARGRETIN®); бифосфонаты, такие как клодронат (например, BONEFOS® или OSTAC®), этидронат (DIDROCAL®), NE-58095, золедроновую кислоту/золедронат (ZOMETA®), алендронат (FOSAMAX®), памидронат (AREDIA®), тилудронат (SKELID®) или ризедронат (ACTONEL®); троксацитабин (1,3-диокслолановый аналог нуклеозина цитозина); антисмысловые олигонуклеотиды, в частности те, которые ингибируют экспрессию генов сигнальных путей, вовлеченных в пролиферацию аберрантных клеток, таких как, например, PKC-альфа, Raf, H-Ras, и рецептор эпидермального фактора роста (EGF-R); вакцины, такие как вакцины THERATOPE®, и вакцины для генной терапии например, вакцина ALLOVECTIN®, вакцина LEUVECTIN® и вакцина VAXID®; ингибитор топоизомеразы 1(например, LURTOTECAN®); rmRH (например, ABARELIX®); BAY439006 (сорафениба; Bayer); SU-11248 (сунитиниб, SUTENT®, Pfizer); перифозин, ингибитор COX-2 (например, целекоксиб или эторикоксиб), ингибитор протеасом (например, PS341); бортезомиб (VELCADE®); CCI-779; типифарниб (R11577); орафениб, ABT510; ингибитор Bcl-2, такой как облимерсен натрий (GENASENSE®); пиксантрон; ингибиторы EGFR (см. определение ниже); ингибиторы тирозинкиназ; ингибиторы серин-треонин киназ, такой как рапамицин (сиролимус, RAPAMUNE®) ингибиторы фарнезилтрансфераз, такие как лонафарниб (SCH 6636, SARASARTM); и фармацевтически приемлемые соли, кислоты или производные любого из перечисленных выше веществ; а также комбинации из двух или более из перечисленных выше веществ, таких как CHOP, аббревиатура для комбинированной терапии циклофосфамида, доксорубицина, винкристина и преднизолона, и FOLFOX, аббревиатура для схемы лечения с оксалиплатином (ELOXATINTM), комбинированным с 5-ФУ и лейковорином.
Химиотерапевтические вещества, как определенно в настоящем документе, включают «антигормональные вещества» или «эндокринные терапевтические средства», действие которых состоит в регуляции, снижении, блокировании или ингибировании действий гормонов, которые могут стимулировать рост рака. Они могут быть гормонами сами по себе, включая, но не ограничиваясь лишь этими: антиэстрогены со смешанным профилем агонист/антагонист, включая тамоксифен (NOLVADEX®), 4-гидрокситамоксифен, торемифен (FARESTON®); идоксифен, дролоксифен, ралоксифен (EVISTA®), триоксифен, кеоксифен и селективные модуляторы рецепторов эстрогена (SERM) такие как SERM3; чистые антиэстрогены без агонистических свойств, такие как фулвестрант (FASLODEX®), и EM800 (такие вещества могут блокировать димеризацию рецептора эстрогена (ER), ингибировать связывание ДНК, увеличивать оборот ER и/или подавлять уровни ER); ингибиторы ароматазы, включая ингибиторы стероидных ароматаз, такие как форместан и экземестан (AROMASIN®), и нестероидные ингибиторы ароматаз, такие как анастразол (ARIMIDEX®), летрозол (FEMARA®) и аминоглютетимид, и другие ингибиторы ароматаз включают ворозол (RIVISOR®), мегестролацетат (MEGASE®), фадрозол, и 4(5)-имидазолы; агонисты гормонов, высвобождающих лютеинизирующий гормон, включая лейпролид (LUPRON® и ELIGARD®), госерелин, бусерелин и триптерилин; половые стероиды, включая прогестины, такие как мегестролацетат и ацетат медроксипрогестерона, эстрогены, такие как диэтилстильбэстрол и премарин, и андрогены/ретиноиды, такие как флуоксиместерон, полностью транс-ретиноевая кислота и фенретинид; онапристон; анти-прогестероны; супрессоры рецептора эстрогена (ERD); антиандрогены, такие как флутамид, нилутамид и бикалютамид; и фармацевтически приемлемые соли, кислоты или производные любого из вышеуказанных; а также комбинации двух или больше из указанных выше.
Термин «иммунодепрессант», как применяется в данном документе, для дополнительной терапии, относится к веществам, которые действуют путем подавления или маскирования иммунной системы млекопитающего, подлежащего лечению. Это будет включать вещества, которые подавляют продукцию цитокинов, понижают или подавляют экспрессию аутоантигенов или маскируют антигены ГКГС. Примеры таких веществ включают 2-амино-6-арил-5-замещенные пиримидины (см. патент США № 4665077); нестероидные противовоспалительные препараты (NSAID); ганцикловир, такролимус, глюкокортикоиды, такие как кортизол или альдостерон, противовоспалительные вещества, такие как ингибитор циклооксигеназы, ингибитор 5-липоксигеназы или антагонист лейкотриенового рецептора; пуриновые антагонисты, такие как азатиоприн или микофенолят мофетил (ММФ (MMF)); алкилирующие вещества, такие как циклофосфамид; бромокриптин; даназол; дапсон; глутаровый альдегид (который маскирует антигены ГКГС, как описано в патенте США № 4120649); анти-идиотипические антитела к антигенам ГКГС и фрагментам ГКГС; циклоспорин A; стероиды, такие как кортикостероиды или глюкокортикостероиды или аналоги глюкокортикоидов, например преднизон, метилпреднизолон, включая SOLU-MEDROL® метилпреднизолон натрия сукцинат, и дексаметазон; ингибиторы дигидрофолатредуктазы, такие как метотрексат (пероральные или подкожные); противомалярийные вещества, такие как хлорохин и гидроксихлорохин; сульфасалазин; лефлуномид; антитела к цитокинам или цитокиновым рецепторам, включая антитела к интерферону-альфа, -бета или -гама, антитела к фактору некроза опухоли альфа (ФНО) (инфликсимаб (REMICADE®) или адалимумаб), анти-ФНО-альфа иммуноадгезины (этанерцепт), антитела к ФНО-бета, антитела к интерелейкину 2 (ИЛ-2) и антитела к рецептору ИЛ-2, и антагонисты и антитела к рецептору интерлейкина 6 (ИЛ-6) (такое как ACTEMRATM (тоцилизумаб)); антитела к LFA-1, включая антитела к CD11a и CD18; антитела к L3T4; гетерологичный антилимфоцитарный глобулин; pan-T антитела, предпочтительно антитела к CD3 или к CD4/CD4a; растворимый пептид, содержащий домен, связывающий LFA-3 (WO 90/08187 опубликовано 7/26/90); стрептокиназу; трансформирующий ростовой фактор бета (ТРФ-бета(TGF-beta)); стрептодорназу; РНК или ДНК из хозяина; FK506; RS-61443; хлорамбуцил; дезоксиспергуалин; рапамицин; рецептор T-лимфоцитов (Cohen et al., патент США № 5114721); фрагменты рецептора Т-лимфоцитов (Offner et al., Science, 251: 430-432 (1991); WO 90/11294; Ianeway, Nature, 341: 482 (1989); и WO 91/01133); антагонисты BAFF, такие как антитела к BAFF и антитела к BR3 и антагонисты zTNF4 (для обзора см. Mackay and Mackay, Trends Immunol., 23:113-5 (2002) и см. также определение ниже); биологические вещества, которые препятствуют сигналам Т-хелперов, такой как анти-CD40 рецептор или анти-CD40 лиганд (CD154), включая блокирующие антитела к лиганду CD40-CD40 (например, Durie et al., Science, 261: 1328-30 (1993); Mohan et al., J. Immunol., 154: 1470-80 (1995)) и CTLA4-Ig (Finck et al., Science, 265: 1225-7 (1994)); и антитела к рецептору Т-лимфоцитов (EP 340,109), такое как T10B9. Некоторые предпочтительные иммунодепрессанты в данном документе включают циклофосфамид, хлорамбуцил, азатиоприн, лефлуномид, ММФ (MMF) или метотрексат.
Термин «антагонист, связывающийся с компонентом сигнального пути PD-1», представляет собой молекулу, которая ингибирует взаимодействие партнера по связыванию с компонентом сигнального пути PD-1 с любым одним или больше партнером по связыванию, для того чтобы устранить дисфункцию Т-клеток, возникающую из-за передачи сигналов на PD-1 сигнальный путь, что приводит к восстановлению или усилению функции Т-клеток (например, пролиферация, продукция цитокинов, уничтожение клеток-мишеней). Как применяется в данном документе, антагонист, связывающийся с компонентом сигнального пути PD-1, включает PD-1-связывающий антагонист, PD-L1-связывающий антагонист и PD-L2-связывающий антагонист.
Термин «PD-1-связывающий антагонист» относится к молекуле, которая снижает, блокирует, ингибирует, подавляет или препятствует передаче сигнала вследствие взаимодействия PD-1 с одним или более его партнерами по связыванию, такими как PD-L1, PD-L2. В некоторых вариантах осуществления, PD-1-связывающий антагонист является молекулой, которая ингибирует связывание PD-1 с одним или больше его партнерами по связыванию. В конкретном аспекте, PD-1-связывающий антагонист ингибирует связывание PD-1 с PD-L1 и/или PD-L2. Например, PD-1-связывающие антагонисты включают анти-PD-1 антитела, их антигенсвязывающие фрагменты, иммуноадгезины, гибридные белки, олигопептиды и другие молекулы, которые снижают, блокируют, ингибируют, подавляют или препятствуют передаче сигнала вследствие взаимодействия PD-1 с PD-L1 и/или PD-L2. В одном варианте осуществления, PD-1-связывающий антагонист снижает отрицательный костимулирующий сигнал, опосредуемый белками клеточной поверхности, экспрессируемыми на Т-лимфоцитах, которые опосредуют передачу сигнала через PD-1, чтобы сделать дисфункциональные Т-клетки менее дисфункциональными (например, повышая эффекторный ответ на распознавание антигена). В некоторых вариантах осуществления, PD-1-связывающий антагонист является анти-PD-1 антителом. В конкретном аспекте, PD-1-связывающий антагонист представляет собой MDX-1106 (ниволумаб), описанный в данном документе. В другом конкретном аспекте, PD-1-связывающий антагонист представляет собой MK-3475 (ламбролизумаб), описанный в данном документе. В другом конкретном аспекте, PD-1-связывающий антагонист представляет собой CT-011 (пидилизумаб), описанный в данном документе. В другом конкретном аспекте, PD-1-связывающий антагонист представляет собой AMP-224, описанный в данном документе.
Термин «PD-L1-связывающий антагонист» относится к молекуле, которая снижает, блокирует, ингибирует, подавляет или препятствует передаче сигнала вследствие взаимодействия PD-L1 с любым одним или более его партнерами по связыванию, такими как PD-1, B7-1. В некоторых вариантах осуществления, PD-L1-связывающий антагонист является молекулой, которая ингибирует связывание PD-L1 с его партнерами по связыванию. В конкретном аспекте, PD-L1-связывающий антагонист ингибирует связывание PD-L1 с PD-1 и/или B7-1. В некоторых вариантах осуществления, PD-L1-связывающие антагонисты включают анти-PD-L1 антитела, их антигенсвязывающие фрагменты, иммуноадгезины, гибридные белки, олигопептиды и другие молекулы, которые снижают, блокируют, ингибируют, подавляют или препятствуют передаче сигнала вследствие взаимодействия PD-L1 с его одним или больше партнерами по связыванию, такими как PD-1, B7-1. В одном варианте осуществления, PD-L1-связывающий антагонист снижает отрицательный костимулирующий сигнал, опосредуемый белками клеточной поверхности, экспрессируемыми на Т-лимфоцитах, которые опосредуют передачу сигнала через PD-L1, чтобы сделать дисфункциональные Т-клетки менее дисфункциональными (например, повышая эффекторный ответ на распознавание антигена). В некоторых вариантах осуществления, PD-L1-связывающий антагонист является антителом к PD-L1. В конкретном аспекте, антитело к PD-L1 представляет собой YW243.55.S70, описанное в данном документе. В другом конкретном аспекте, антитело к PD-L1 представляет собой MDX-1105, описанное в данном документе. В еще другом конкретном аспекте, антитело к PD-L1 представляет собой MPDL3280A, описанное в данном документе. В конкретном аспекте, антитело к PD-L1 представляет собой MEDI4736, описанное в данном документе.
Термин «PD-L2-связывающий антагонист» относится к молекуле, которая снижает, блокирует, ингибирует, подавляет или препятствует передаче сигнала вследствие взаимодействия PD-L2 с любым одним или больше его партнерами по связыванию, такими как PD-1. В некоторых вариантах осуществления, PD-L2-связывающий антагонист является молекулой, которая ингибирует связывание PD-L2 с одним или больше его партнерами по связыванию. В конкретном аспекте, PD-L2-связывающий антагонист ингибирует связывание PD-L2 с PD-1. В некоторых вариантах осуществления, PD-L2-связывающие антагонисты включают анти-PD-L2 антитела, их антигенсвязывающие фрагменты, иммуноадгезины, гибридные белки, олигопептиды и другие молекулы, которые снижают, блокируют, ингибируют, подавляют или препятствуют передаче сигнала вследствие взаимодействия PD-L2 с любым одним или более его партнерами по связыванию, такими как PD-1. В одном варианте осуществления, PD-L2-связывающий антагонист снижает отрицательный костимулирующий сигнал, опосредуемый белками клеточной поверхности, экспрессируемыми на Т-лимфоцитах, которые опосредуют передачу сигнала через PD-L2, чтобы сделать дисфункциональные Т-клетки менее дисфункциональными (например, повышая эффекторный ответ на распознавание антигена). В некоторых вариантах осуществления, PD-L2-связывающий антагонист является иммуноадгезином.
Термин «фиксированная» или «постоянная» доза терапевтического вещества относится к дозе, которая вводится человеку-пациенту, не обращая внимания на вес (массу тела) или площадь поверхности тела (ППТ) пациента. Следовательно, фиксированная или постоянная доза не предоставляется в виде дозы мг/кг или дозы мг/м2, а скорее, как абсолютное количество терапевтического вещества.
В данном документе «ударная» доза, в целом, как правило, содержит начальную дозу терапевтического вещества, которую вводят пациенту, и затем следует одна или более ее поддерживающей(их) дозы (доз). В целом, как правило, вводят разовую ударную дозу, но в данном документе предусматриваются многократные ударные дозы. Как правило, количество вводимой(ых) ударной(ых) дозы (доз) превышает количество вводимой(ых) поддерживающей(их) дозы (доз), и/или ударную(ые) дозу(ы) вводят чаще, чем поддерживающую(ие) дозу(ы), с тем, чтобы достичь желаемой неизменяющейся концентрации терапевтического вещества раньше, чем это может быть достигнуто с помощью поддерживающей(их) дозы (доз).
В данном документе термин «поддерживающая» доза относится к одной или больше дозам терапевтического вещества, которые вводят пациенту в течение периода лечения. Как правило, при лечении поддерживающие дозы вводят через определенные интервалы, например, примерно каждую неделю, примерно каждые 2 недели, примерно через каждые 3 недели или примерно через каждые 4 недели, предпочтительно каждые 3 недели.
«Инфузия» или «вливание» относится к внутривенному введению в организм в терапевтических целях раствора, содержащего лекарственное средство. В целом, как правило, это достигается с помощью внутривенного (ВВ (IV)) пакета.
«Внутривенный пакет» или «ВВ (IV) пакет» представляет собой пакет, который может содержать раствор, который может быть введен пациенту внутривенно. В одном варианте реализации изобретения раствор представляет собой солевой раствор (например, около 0,9% или около 0,45% NaCl). Необязательно, ВВ (IV) мешок изготовлен из полиолефина или поливинилхлорида.
Термин «вариабельная область» или «вариабельный домен» относится к домену тяжелой или легкой цепи антитела, который участвует в связывании антитела с антигеном. Вариабельные домены тяжелой цепи и легкой цепи (VH и VL, соответственно) природного антитела обычно имеют подобные структуры, причем каждый домен содержит четыре консервативные каркасные области (FR) и три гипервариабельных участка (HVR). (См. например, Kindt et al. Kuby Immunology, 6th ed., W.H. Freeman and Co., page 91 (2007).) Для обеспечения антигенсвязывающей специфичности может быть достаточно одного домена VH или VL. Кроме того, антитела, которые связываются с конкретным антигеном, можно выделить, используя домен VH или VL из антитела, которое связывается с антигеном, для скрининга библиотеки последовательностей, комплементарных доменам VL или VH, соответственно. См., например, Portolano et al., J. Immunol. 150:880-887 (1993); Clarkson et al., Nature 352:624-628 (1991).
Термин «вектор», как используется в данном документе, относится к молекуле нуклеиновой кислоты, способной переносить другую нуклеиновую кислоту, с которой она связана. Термин включает вектор в виде самореплицирующейся структуры нуклеиновой кислоты, а также вектор, встраиваемый в геном клетки-хозяина, в которую он введен. Некоторые векторы способны направлять экспрессию нуклеиновых кислот с которыми они функционально связаны. Такие векторы называют в данном документе «векторами экспрессии».
«Свободная аминокислота цистеина» относится к аминокислотному остатку цистеина, который был внесен в исходное антитело, имеет функциональную тиоловую группу (-SH) и не соединяется в внутримолекулярный или межмолекулярный дисульфидный мостик.
«Линкер», «линкерная единица» или «связующее звено» обозначает химический фрагмент, содержащий цепочку атомов, которая ковалентно присоединяет антитело к лекарственному фрагменту.
При указании количества заместителей термин «один или больше» относится к диапазону от одного заместителя до максимально возможного числа замещения, то есть замещения заместителями от одного водорода до замещения всех атомов водорода. Термин «заместитель» обозначает атом или группу атомов, заменяющих атом водорода в исходной молекуле. Термин «замещенный» обозначает, что указанная группа имеет один или несколько заместителей. Если любая группа может содержать множество заместителей и предлагается множество возможных заместителей, заместители выбираются независимо и не обязательно должны быть одинаковыми. Термин «незамещенный» обозначает, что указанная группа не имеет заместителей. Термин «необязательно замещенный» обозначает, что указанная группа является незамещенной или замещенной одним или несколькими заместителями, независимо выбранными из группы возможных заместителей. При указании количества заместителей термин «один или больше» обозначает от одного заместителя до максимально возможного числа замещения, то есть замещения заместителями от одного водорода, до замещения всех атомов водорода.
Термин «алкил», как используется в данном документе, относится к насыщенному линейному или с разветвленной цепью одновалентному углеводородному радикалу любой длины от одного до двенадцати атомов углерода (C1-C12), причем алкильный радикал может быть необязательно замещен независимо одним или несколькими заместителями, описанными ниже. В другом варианте осуществления, алкильный радикал представляет собой от одного до восьми атомов углерода (C1-C8), или от одного до шести атомов углерода (C1-C6). Примеры алкильных групп включают, но не ограничиваются лишь этими: метил (Me, -CH3), этил (Et, -CH2CH3), 1-пропил (n-Pr, n-пропил, -CH2CH2CH3), 2-пропил (i-Pr, i-пропил, -CH(CH3)2), 1-бутил (n-Bu, n-бутил, -CH2CH2CH2CH3), 2-метил-1-пропил (i-Bu, i-бутил, -CH2CH(CH3)2), 2-бутил (s-Bu, втор-бутил, -CH(CH3)CH2CH3), 2-метил-2-пропил (t-Bu, t-бутил, -C(CH3)3), 1-пентил н-пентил, -CH2CH2CH2CH2CH3), 2-пентил (-CH(CH3)CH2CH2CH3), 3-пентил (-CH(CH2CH3)2), 2-метил-2-бутил (-C(CH3)2CH2CH3), 3-метил-2-бутил (-CH(CH3)CH(CH3)2), 3-метил-1-бутил (-CH2CH2CH(CH3)2), 2-метил-1-бутил (-CH2CH(CH3)CH2CH3), 1-гексил (-CH2CH2CH2CH2CH2CH3), 2-гексил (-CH(CH3)CH2CH2CH2CH3), 3-гексил (-CH(CH2CH3)(CH2CH2CH3)), 2-метил-2-пентил (-C(CH3)2CH2CH2CH3), 3-метил-2-пентил (-CH(CH3)CH(CH3)CH2CH3), 4-метил-2-пентил (-CH(CH3)CH2CH(CH3)2), 3-метил-3-пентил (-C(CH3)(CH2CH3)2), 2-метил-3-пентил (-CH(CH2CH3)CH(CH3)2), 2,3-диметил-2-бутил (-C(CH3)2CH(CH3)2), 3,3-диметил-2-бутил (-CH(CH3)C(CH3)3, 1-гептил, 1-октил, и тому подобное.
Термин «алкилен», как используется в данном документе, относится к насыщенному линейному или с разветвленной цепью одновалентному углеводородному радикалу любой длины от одного до двенадцати атомов углерода (C1-C12), причем алкиленовый радикал может быть необязательно замещен независимо одним или большим количеством заместителей, описанных ниже. В другом варианте осуществления, алкиленовый радикал представляет собой от одного до восьми атомов углерода (C1-C8), или от одного до шести атомов углерода (C1-C6). Примеры алкиленовых груп включают, но не ограничиваются лишь этими: метилен (-CH2-), этилен (-CH2CH2-), пропилен (-CH2CH2CH2-), и тому подобное.
Термин «алкенил» относится к линейному или с разветвленной цепью одновалентному углеводородному радикалу любой длины от двух до восьми атомов углерода (C2-C8), с по меньшей мере одним сайтом ненасыщенности, т.е. углерод-углерод, sp2-двойной связью, причем алкенильный радикал может быть необязательно независимо замещен одним или больше заместителем, описанным в данном документе, и включает радикалы, имеющие ориентации «цис» и «транс», или в качестве альтернативы, ориентации «Е» и «Z». Примеры включают, без ограничений, этиленил или винил (-CH=CH2), аллил (-CH2CH=CH2), и т.п.
Термин «алкенилен» относится к линейному или с разветвленной цепью двухвалентному углеводородному радикалу любой длинны от двух до восьми атомов углерода (C2-C8), с по меньшей мере одним сайтом ненасыщенности, т.е. углерод-углерод, sp2-двойной связью, причем алкениленовый радикал может быть необязательно независимо замещен одним или больше заместителем, описанным в данном документе, и включает радикалы, имеющие ориентации «цис» и «транс», или в качестве альтернативы, ориентации «Е» и «Z». Примеры включают, но не ограничиваются лишь этими: этиленинлен или винилен (-CH=CH-), аллил (-CH2CH=CH-), и тому подобное.
Термин «алкинил» относится к линейному или разветвленному одновалентному углеводородному радикалу, любой длинны от двух до двенадцати атомов углерода (C2-C8), c по меньшей мере одной ненасыщенной связью, т.е. углерод-углерод, sp тройной связью, причем алкиниловый радикал может быть необязательно независимо замещен одним или больше заместителем, описанным в данном документе. Примеры включают, но не ограничиваются лишь этими: этинил (C≡CH), пропинил (пропаргил, CH2C≡CH), и тому подобное.
Термин «алкинилен» относится к линейному или разветвленному двухвалентному углеводородному радикалу, любой длинны от двух до восьми атомов углерода (C2-C8), c по меньшей мере одной ненасыщенной связью, т.е. углерод-углерод, sp тройной связью, причем алкиниленовый радикал может быть необязательно независимо замещен одним или больше заместителем, описанным в данном документе. Примеры включают, но не ограничиваются лишь этими: этинилен (-C≡C-), пропинилен (пропаргилен, -CH2C≡C-) и тому подобное.
Термины «карбоцикл», «карбоциклил», «карбоциклическое кольцо» и «циклоалкил» относится к одновалентному неароматическому, насыщенному или частично ненасыщенному циклу, содержащему от 3 до 12 атомов углерода (C3-C12) в виде моноциклического кольца, или от 7 до 12 атомов углерода в виде бициклического кольца. Бициклические карбоциклы, имеющие от 7 до 12 атомов могут быть расположены, например, как бицикло [4,5], [5,5], [5,6] или [6,6] система, а также бициклические карбоциклы, имеющие 9 или 10 кольцевых атомов могут быть организованы в виде бицикло [5,6] или [6,6] систем, или как мостиковые системы, такие, как [2,2,1]гептан, бицикло[2,2,2]октан и бицикло[3,2,2]нонан. Спиральные фрагменты также включены в объем данного определения. Примеры моноциклических карбоциклов включают, но не ограничиваются лишь этими: циклопропил, циклобутил, циклопентил, 1-циклопент-1-енил, 1-циклопент-2-енил, 1-циклопент-3-енил, циклогексил, 1-циклогексен-1-енил, 1-циклогексен-2-енил, 1-циклогексен-3-енил, циклогексадиенил, циклогептил, циклооктил, циклононил, циклодецил, циклоундецил, циклододецил, и тому подобное. Карбоциклильные группы необязательно замещены независимо одним или больше заместителями, описанными в данном документе.
«Арил» обозначает одновалентный ароматический углеводородный радикал, содержащий 6-20 атомов углерода (C6-C20), полученные удалением одного атома водорода от одного атома углерода исходной ароматической кольцевой системы. Некоторые арильные группы представлены в иллюстративных структурах как «Ar». Арил включает в себя бициклические радикалы, содержащие ароматическое кольцо, конденсированное с насыщенным, частично ненасыщенным кольцом или ароматическим карбоциклическим кольцом. Типичные арильные группы включают, но не ограничиваются лишь этими: радикалы, образованные из бензола (фенил), замещенные бензолы, нафталин, антрацен, бифенил, инденил, инданил, 1,2-дигидронафталин, 1,2,3,4-тетрагидронафтил и тому подобное. Арильные группы необязательно замещены независимо одним или больше заместителями, описанными в данном документе.
«Арилен» обозначает двухвалентный ароматический углеводородный радикал, содержащий 6-20 атомов карбона (C6-C20), полученный путем удаления двух атомов водорода из двух атомов углерода исходной ароматической кольцевой системы. Некоторые ариленовые группы представлены в иллюстративных структурах как «Ar». Арилен включает бициклические радикалы, содержащие ароматическое кольцо, слитое с насыщенным, частично ненасыщенным кольцом или ароматическим карбоциклическим кольцом. Типичные ариленовые группы включают, но не ограничиваются ими: радикалы, полученные из бензола (фенилена), замещенные бензолы, нафталин, антрацен, бифенилен, инденилен, инданилен, 1,2-дигидронафталин, 1,2,3,4-тетрагидронафтил и тому подобное. Ариленовые группы необязательно замещены одним или больше заместителями, описанными в данном документе.
Термины «гетероцикл», «гетероциклил» и «гетероциклическое кольцо» используются в данном документе взаимозаменяемо, и относятся к насыщенному или частично ненасыщенному (т.е. имеющему одну или больше двойных и/или тройных связей в кольце) карбоциклическому радикалу от 3 до около 20 кольцевых атомов в которых по меньшей мере один кольцевой атом представляет собой гетероатом, выбранный из азота, кислорода и серы, а остальные кольцевые атомы представляют собой С, где один или больше кольцевых атомов необязательно замещены независимо одним или больше заместителями, описанными ниже. Гетероцикл может быть моноциклом, содержащим от 3 до 7 членов кольца (от 2 до 6 атомов углерода и от 1 до 4 гетероатомов, выбранных из N, O, P и S) или бициклом, содержим от 7 до 10 кольцевых членов (от 4 до 9 атомов углерода, и от 1 до 6 гетероатомов, выбранных из N, О, Р и S), например: бицикло [4,5], [5,5], [5,6], или [6,6] система. Гетероциклы описаны в Paquette, Leo A.; ʺPrinciples of Modern Heterocyclic Chemistryʺ (W.A. Benjamin, New York, 1968), частично в главах 1, 3, 4, 6, 7, и 9; ʺThe Chemistry of Heterocyclic Compounds, A series of Monographsʺ (John Wiley & Sons, New York, с 1950 года по настоящее время), в частности томах 13, 14, 16, 19, и 28; и J. Am. Chem. Soc. (1960) 82:5566. «Гетероциклил» также включает радикалы, где гетероциклические радикалы конденсированы с насыщенным, частично ненасыщенным кольцом или ароматическим карбоциклическим, или гетероциклическим кольцом. Примеры гетероциклических колец включают, но не ограничиваются лишь этими: морфолин-4-ил, пиперидин-1-ил, пиперазинил, пиперазин-4-ил-2-он, пиперазин-4-ил-3-он, пирролидин-1-ил, тиоморфолин-4-ил, S-диоксотиоморфолин-4-ил, азокан-1-ил, азетидин-1-ил, октагидропиридо[1,2-a]пиразин-2-ил, [1,4]диазепан-1-ил, пирролидинил, тетрагидрофуранил, дигидрофуранил, тетрагидротиенил, тетрагидропиранил, дигидропиранил, тетрагидротиопиранил, пиперидино, морфолино, тиоморфолино, тиоксанил, пиперазинил, гомопиперазинил, азетидинил, оксетанил, тиетанил, гомопиперидинил, оксапанил, тиапанил, оксазепинил, диазепинил, тиазепинил, 2- пирролинил, 3-пирролинил, индолинил, 2Н-пиранил, 4Н-пиранил, диоксанил, 1,3-диоксоланил, пиразолинил, дитианил, дитиоланил, дигидропиранил, дигидротиенил, дигидрофуранил, пиразолидинимидазолинил, имидазолидинил, 3-азабицикло[3.1.0]гексанил, 3-азабицикло[4.1.0]гептанил, азабицикло[2.2.2]гексанил, 3H-индолилхинолизинил и N-пиридилмочевину. Спиральные фрагменты также включены в объем данного определения. Примеры гетероциклической группы, в которой 2 атома кольца замещены оксо (=О), представляют собой пиримидинонил и 1,1-диоксотиоморфолинил. Гетероциклические группы в данном документе необязательно замещены независимо друг от друга одним или больше заместителями, описанными в данном документе.
Термин «гетероарил» относится к одновалентному ароматическому радикалу, содержащему 5-, 6- или 7-членные кольца, и включает конденсированные кольцевые системы (по меньшей мере одна из которых является ароматической) из 5-20 атомов, содержащих один или больше гетероатомов, независимо выбранных из азота, кислорода и серы. Примеры гетероарильных групп представляют собой пиридинил (включая, например, 2-гидроксипиридинил), имидазолил, имидазопиридинил, 1-метил-1Н-бензо[d]имидазол, [1,2,4]триазоло[1,5-а]пиридинил, пиримидинил (включая, например, 4-гидроксипиримидинил), пиразолил, триазолил, пиразинил, тетразолил, фурил, тиенил, изоксазолил, тиазолил, оксадиазолил, оксазолил, изотиазолил, пирролил, хинолинил, изохинолинил, тетрагидроизохинолинил, индолил, бензимидазолил, бензофуранил, цинолинил, индазолил, индолизинил, фталазинил, пиридазинил, триазинил, изоиндолил, птеридинил, пуринил, оксадиазолил, тиадиазолил, тиадиазолил, фуразанил, бензофуразанил, бензотиофенил, бензотиазолил, бензоксазолил, хиназолинил, хиноксалинил, нафтиридинил и фуропиридинил. Гетероарильные группы необязательно замещены независимо одним или больше заместителями, описанными в данном документе.
Гетероциклические или гетероарильные группы могут быть присоединены, где такое возможно, через углерод (углерод-связанные) или азот (азот-связанные). В качестве примера, но не ограничения, присоединенные к углероду гетероциклы или гетероарилы являются присоединенными в положении 2, 3, 4, 5 или 6 пиридина, положение 3, 4, 5 или 6 пиридазина, положении 2, 4, 5 или 6 пиримидина, положении 2, 3, 5 или 6 пиразина, положении 2, 3, 4 или 5 фурана, тетрагидрофурана, тиофурана, тиофена, пиррола или тетрагидропиррола, положении 2, 4 или 5 оксазола, имидазола или тиазола, положении 3, 4 или 5 изоксазола, пиразола или изотиазола, положении 2 или 3 азиридина, положении 2, 3 или 4 азетидина, положении 2, 3, 4, 5, 6, 7 или 8 хинолина или положении 1, 3, 4, 5, 6, 7 или 8 изохинолина.
В качестве неограничивающего примера азотные гетероциклы или гетероарилы соединены в положении 1 азиридина, азетидина, пиррола, пирролидина, 2-пирролина, 3-пирролина, имидазола, имидазолидина, 2-имидазолина, 3-имидазолина, пиразола, пиразолина, 2-пиразолина, 3-пиразолина, пиперидина, пиперазина, индола, индолина, 1H-индазола, положении 2 изоиндола или изоиндолина, положении 4 морфолина и положении 9 карбазола, или β-карболина.
Термин «хиральный» относится к молекулам, которые обладают свойством несопоставимости при наложении их зеркально отображенного изображения, тогда как термин «ахиральний» относится к молекулам, которые совпадают со своим зеркально отображенного изображением при наложении.
Термин «стереоизомеры» относится к соединениям, которые имеют идентичное химическое строение, но отличаются по расположению атомов или групп в пространстве.
«Диастереомер» относится к стереоизомеру с двумя или более центрами хиральности и молекулы которого не являются зеркальными отображениями друг друга. Диастереомеры имеют разные физические свойства, например точки плавления, точки кипения, спектральные свойства и реакционную способность. Смеси диастереомеров могут быть разделены при аналитических процедурах высокого разрешения, таких как электрофорез и хроматография.
«Энантиомеры» относятся к двум стереоизомерам соединения, которые являются не накладываемыми зеркальными изображениями друг друга.
Стереохимические определения и условные обозначения, используемые в данном документе, в целом, как правило, соответствуют S. P. Parker, Ed., McGraw-Hill Dictionary of Chemical Terms (1984) McGraw-Hill Book Company, New York; and Eliel, E. and Wilen, S., Stereochemistry of Organic Compounds (1994) John Wiley & Sons, Inc., New York. Многие органические соединения существуют в оптически активных формах, т. е. они имеют возможность вращать плоскость плоского поляризованного света. При описании оптически активного соединения префиксы D и L, или R и S, применяются для обозначения абсолютного расположение молекулы вокруг ее хирального центра (центров). Префиксы d и l или (+) и (-) применяются для обозначения знака поворота плоского поляризованного света соединением с (-) или 1, обозначающим, что соединение является левовращающим. Соединение с префиксом (+) или d является правовращающим. Для данной химической структуры указанные стереоизомеры идентичны, за исключением того, что они являются зеркальными отображениями друг друга. Конкретный стереоизомер можно также назвать энантиомером, и смесь таких изомеров часто называют смесью энантиомеров. Смесь энантиомеров 50:50 упоминается как рацемическая смесь или рацемат, что может происходить там, где не было стереоселекции или стереоспецифичности в химической реакции или процессе. Термины «рацемическая смесь» и «рацемат» относятся к эквимолярной смеси двух энантиомерных частиц, лишенных оптической активности.
Как применяется в данном документе, фраза «фармацевтически приемлемая соль» относится к фармацевтически приемлемым органическим или неорганическим солям конъюгата антитело-лекарственное средство (КАЛС (ADC)). Иллюстративные соли включают, но не ограничиваются лишь этими: сульфатные, цитратные, ацетатные, оксалатные, хлоридные, бромидные, иодидные, нитратные, бисульфатные, фосфатные, кисло-фосфатные, изоникотинатные, лактатные, салицилатные, кисло-цитратные, тартратные, олеатные, таннатные, пантотенатные, битартратные, аскорбатные, сукцинатные, малеатные, гентизинатные, фумаратные, глюконатные, глюкуронатные, сахаратные, формиатные, бензоатные, глутаматные, метансульфонатные, этансульфонатные, бензолсульфонатные, р-толуолсульфонатные, памоатные (то есть, 1,1'-метилен-бис-(2-гидрокси-3-нафтоат)) соли. Фармацевтически приемлемая соль может включать включение другой молекулы, такой как иона ацетата, иона сукцината или другого противоиона. Противоионом может быть любой органический или неорганический компонент, который стабилизирует заряд на исходном соединении. Кроме того, фармацевтически приемлемая соль может иметь более одного заряженного атома в своей структуре. Случаи, когда несколько заряженных атомов являются частью фармацевтически приемлемой соли, могут иметь несколько противоионов. Следовательно, фармацевтически приемлемая соль может иметь один или больше заряженных атомов, и/или один или больше противоионов.
В данном документе применяются следующие аббревиатуры, имеющие указанные определения: БМЭ (BME) представляет собой бета-меркаптоэтанол, Boc представляет собой N- (трет-бутоксикарбонил), cit представляет собой цитруллин (2-амино-5-уреидо-пентановая кислота), ДЦК (DCC) представляет собой 1,3-дициклогексилкарбодиимид, ДХМ представляет собой дихлорметан, ДЭА (DEA) представляет собой диэтиламин, ДЭАД (DEAD) представляет собой диэтилазодикарбоксилат, ДЭФЦ (DEPC) представляет собой диэтилфосфорицианидат, ДИАД (DIAD) представляет собой диизопропилазодикарбоксилат, ДИЭА (DIEA) представляет собой N,N-диизопропилэтиламин, ДМА (DMA) представляет собой диметилацетамид, ДМАП (DMAP) представляет собой 4-диметиламинопиридин, ДМЭ (DME) представляет собой диметиловый эфир этиленгликоля (или 1,2-диметоксиэтан), ДМФА (DMF) представляет собой N,N-диметилформамид, ДМСО (DMSO) представляет собой диметилсульфоксид, ДТТ (DTT) представляет собой дитиотреитол, ЭДКИ (EDCI) представляет собой 1-этил-3-(3-диметиламинопропил)карбодиимид, ЭЭДХ (EEDQ) представляет собой 2-этокси-1-этоксикарбонил-1,2-дигидрохинолин, ES-MS представляет собой масс-спектрометрию с электрораспылением, EtOAc представляет собой этилацетат, Fmoc представляет собой N-(9-флуоренилметоксикарбонил), gly представляет собой глицин, HATU представляет собой O-(7-азабензотриазол-1-ил)-N,N,N',N' тетраметилуронум гексафторфосфатазу, HOBt представляет собой 1-гидроксибензотриазол, ВЭЖХ (HPLC) представляет собой высокоэффективную жидкостную хроматографию, ile представляет собой изолейцин, lys представляет собой лизин, MeCN (CH3CN) представляет собой ацетонитрил, MeOH представляет собой метанол, Mtr представляет собой 4-анизилдифенилметил (или 4-метокситритил), NHS представляет собой N-гидроксисукцинимид, ФСБ (PBS) представляет собой забуренный фосфатом солевой раствор (pH 7), ПЭГ (PEG) представляет собой полиэтиленгликоль или единицу этиленгликоля (-OCH2CH2-), Ph представляет собой фенил, Pnp представляет собой п-нитрофенил, MC представляет собой 6-малеимидокапроил, phe представляет собой L-фенилаланин, PyBrop представляет собой бромо tris-пирролидино фосфатную гексафторфозсфатазу, ЭХ (SEC) представляет собой эксклюзионная хроматография, Su представляет собой сукцинимид, ТФК (TFA) представляет собой трифтороцтовою кислоту, ТСХ (TLC) представляет собой тонкослойную хроматографию, UV- ультрафиолет, и val представляет собой валин.
ОПУХОЛЬ-АССОЦИИРОВАННЫЕ АНТИГЕНЫ
1) BMPR1B (рецептор костного морфогенетического белка типа IB, идентификационный номер ГенБанка NM_001203)
ten Dijke,P., et al Science 264 (5155):101-104 (1994), Oncogene 14 (11):1377-1382 (1997)); WO2004063362 (пункт формулы № 2); WO2003042661 (пункт формулы № 12); US2003134790-A1 (страницы 38-39); WO2002102235 (пункт формулы № 13; страница 296); WO2003055443 (страницы 91-92); WO200299122 (пример 2; страницы 528-530); WO2003029421 (пункт формулы № 6); WO2003024392 (пункт формулы № 2; фиг. 112); WO200298358 (пункт формулы № 1; страница 183); WO200254940 (страницы 100-101); WO200259377 (страницы 349-350); WO200230268 (пункт формулы № 27; страница 376); WO200148204 (пример; фиг. 4)
NP_001194 рецептор костного морфогенетического белка типа IB /pid=NP_001194.1 -
Перекрестные ссылки: MIM:603248; NP_001194.1; AY065994
2) E16 (LAT1, SLC7A5, идентификационный номер ГенБанка NM_003486)
Biochem. Biophys. Res. Commun. 255 (2), 283-288 (1999), Nature 395 (6699):288-291 (1998), Gaugitsch, H.W., et al (1992) J. Biol. Chem. 267 (16):11267-11273); WO2004048938 (пример 2); WO2004032842 (пример IV); WO2003042661 (пункт формулы № 12); WO2003016475 (пункт формулы № 1); WO200278524 (пример 2); WO200299074 (пункт формулы № 19; страницы 127-129); WO200286443 (пункт формулы № 27; страница 222, 393); WO2003003906 (пункт формулы № 10; страница 293); WO200264798 (пункт формулы № 33; страницы 93-95); WO200014228 (пункт формулы № 5; страницы 133-136); US2003224454 (фиг. 3); WO2003025138 (пункт формулы № 12; страница 150);
NP_003477 семейство 7 транспортеров растворенных веществ (катионный аминокислотный транспортер, y+
система), член 5 /pid=NP_003477.3 - Homo sapiens
Перекрестные ссылки: MIM:600182; NP_003477.3; NM_015923; NM_003486_1
3) STEAP1 (шеститрансмембранный эпителиальный антиген простаты, идентификационный номер ГенБанка NM_012449)
Cancer Res. 61 (15), 5857-5860 (2001), Hubert, R.S., et al (1999) Proc. Natl. Acad. Sci. U.S.A. 96 (25):14523-14528); WO2004065577 (пункт формулы № 6); WO2004027049 (фиг. 1L); EP1394274 (пример 11); WO2004016225 (пункт формулы № 2); WO2003042661 (пункт формулы № 12); US2003157089 (пример 5); US2003185830 (пример 5); US2003064397 (фиг. 2); WO200289747 (пример 5; страницы 618-619); WO2003022995 (пример 9; фиг. 13A, пример 53; страница 173, пример 2; фиг. 2A);
NP_036581 шеститрансмембранный эпителиальный антиген простаты
Перекрестные ссылки: MIM:604415; NP_036581.1; NM_012449_1
4) 0772P (CA125, MUC16, идентификационный номер ГенБанка AF361486)
J. Biol. Chem. 276 (29):27371-27375 (2001)); WO2004045553 (пункт формулы № 14); WO200292836 (пункт формулы № 6; фиг. 12); WO200283866 (пункт формулы № 15; страницы 116-121); US2003124140 (пример 16); US 798959. Перекрестные ссылки: GI:34501467; AAK74120.3; AF361486_1
5) MPF (MPF, MSLN, SMR, фактор активации мегакариоцитов, мезотелин, идентификационный номер ГенБанка NM_005823) Yamaguchi, N., et al Biol. Chem. 269 (2), 805-808 (1994), Proc. Natl. Acad. Sci. U.S.A. 96 (20):11531-11536 (1999), Proc. Natl. Acad. Sci. U.S.A. 93 (1):136-140 (1996), J. Biol. Chem. 270 (37):21984-21990 (1995)); WO2003101283 (пункт формулы № 14); (WO2002102235 (пункт формулы № 13; страницы 287-288); WO2002101075 (пункт формулы № 4; страницы 308-309); WO200271928 (страницы 320-321); WO9410312 (страницы 52-57); Перекрестные ссылки: MIM:601051; NP_005814.2; NM_005823_1
6) Napi2b (Napi3b, NAPI-3B, NPTIIb, SLC34A2, семейство переносчиков растворенных веществ 34 (фосфат натрия), представитель 2, натрий-зависимый переносчик фосфата 3b типа II, идентификационный номер ГенБанка NM_006424)
J. Biol. Chem. 277 (22):19665-19672 (2002), Genomics 62 (2):281-284 (1999), Feild, J.A., et al (1999) Biochem. Biophys. Res. Commun. 258 (3):578-582); WO2004022778 (пункт формулы № 2); EP1394274 (пример 11); WO2002102235 (пункт формулы № 13; страница 326); EP875569 (пункт формулы № 1; страницы 17-19); WO200157188 (пункт формулы № 20; страница 329); WO2004032842 (пример IV); WO200175177 (пункт формулы № 24; страницы 139-140);
Перекрестные ссылки: MIM:604217; NP_006415.1; NM_006424_1
7) Sema 5b (FLJ10372, KIAA1445, Mm.42015, SEMA5B, SEMAG, семафорин 5b Hlog, домен sema, семь тромбоспондиновых повторов (тип 1 и подобный типу 1), трансмембранный домен (TД) и короткий цитоплазматический домен, (семафорин) 5B, идентификационный номер ГенБанка AB040878)
Nagase T., et al (2000) DNA Res. 7 (2):143-150); WO2004000997 (пункт формулы № 1); WO2003003984 (пункт формулы № 1); WO200206339 (пункт формулы № 1; страница 50); WO200188133 (пункт формулы № 1; страницы 41-43, 48-58); WO2003054152 (пункт формулы № 20); WO2003101400 (пункт формулы № 11);
Идентификационный номер: Q9P283; EMBL; AB040878; BAA95969.1. Genew; HGNC:10737;
8) PSCA hlg (2700050C12Rik, C530008O16Rik, кДНК RIKEN 2700050C12, ген кДНК RIKEN 2700050C12, идентификационный номер ГенБанка AY358628); Ross et al (2002) Cancer Res. 62:2546-2553; US2003129192 (пункт формулы № 2); US2004044180 (пункт формулы № 12); US2004044179 (пункт формулы № 11); US2003096961 (пункт формулы № 11); US2003232056 (пример 5); WO2003105758 (пункт формулы № 12); US2003206918 (пример 5); EP1347046 (пункт формулы № 1); WO2003025148 (пункт формулы № 20);
Перекрестные ссылки: GI:37182378; AAQ88991.1; AY358628_1
9) ETBR (рецептор эндотелина типа В, идентификационный номер ГенБанка AY275463);
Nakamuta M., et al Biochem. Biophys. Res. Commun. 177, 34-39, 1991; Ogawa Y., et al Biochem. Biophys. Res. Commun. 178, 248-255, 1991; Arai H., et al Jpn. Circ. J. 56, 1303-1307, 1992; Arai H., et al J. Biol. Chem. 268, 3463-3470, 1993; Sakamoto A., Yanagisawa M., et al Biochem. Biophys. Res. Commun. 178, 656-663, 1991; Elshourbagy N.A., et al J. Biol. Chem. 268, 3873-3879, 1993; Haendler B., et al J. Cardiovasc. Pharmacol. 20, s1-S4, 1992; Tsutsumi M., et al Gene 228, 43-49, 1999; Strausberg R.L., et al Proc. Natl. Acad. Sci. U.S.A. 99, 16899-16903, 2002; Bourgeois C., et al J. Clin. Endocrinol. Metab. 82, 3116-3123, 1997; Okamoto Y., et al Biol. Chem. 272, 21589-21596, 1997; Verheij J.B., et al Am. J. Med. Genet. 108, 223-225, 2002; Hofstra R.M.W., et al Eur. J. Hum. Genet. 5, 180-185, 1997; Puffenberger E.G., et al Cell 79, 1257-1266, 1994; Attie T., et al, Hum. Mol. Genet. 4, 2407-2409, 1995; Auricchio A., et al Hum. Mol. Genet. 5:351-354, 1996; Amiel J., et al Hum. Mol. Genet. 5, 355-357, 1996; Hofstra R.M.W., et al Nat. Genet. 12, 445-447, 1996; Svensson P.J., et al Hum. Genet. 103, 145-148, 1998; Fuchs S., et al Mol. Med. 7, 115-124, 2001; Pingault V., et al (2002) Hum. Genet. 111, 198-206; WO2004045516 (пункт формулы № 1); WO2004048938 (пример 2); WO2004040000 (пункт формулы № 151); WO2003087768 (пункт формулы № 1); WO2003016475 (пункт формулы № 1); WO2003016475 (пункт формулы № 1); WO200261087 (фиг. 1); WO2003016494 (фиг. 6); WO2003025138 (пункт формулы № 12; страница 144); WO200198351 (пункт формулы № 1; страницы 124-125); EP522868 (пункт формулы № 8; фиг. 2); WO200177172 (пункт формулы № 1; страницы 297-299); US2003109676; US6518404 (фиг. 3); US5773223 (пункт формулы № 1a; Col 31-34); WO2004001004;
10) MSG783 (RNF124, гипотетический белок FLJ20315, идентификационный номер ГенБанка NM_017763);
WO2003104275 (пункт формулы № 1); WO2004046342 (пример 2); WO2003042661 (пункт формулы № 12); WO2003083074 (пункт формулы № 14; страница 61); WO2003018621 (пункт формулы № 1); WO2003024392 (пункт формулы № 2; фиг. 93); WO200166689 (пример 6);
Перекрестные ссылки: LocusID:54894; NP_060233.2; NM_017763_1
11) STEAP2 (HGNC_8639, IPCA-1, PCANAP1, STAMP1, STEAP2, STMP, ассоциированный с раком простаты ген 1, ассоциированный с раком простаты белок 1, шеститрансмембранный эпителиальный антиген предстательной железы 2, шеститрансмембранный белок простаты, идентификационный номер ГенБанка AF455138)
Lab. Invest. 82 (11):1573-1582 (2002)); WO2003087306; US2003064397 (пункт формулы № 1; фиг. 1); WO200272596 (пункт формулы № 13; страницы 54-55); WO200172962 (пункт формулы № 1; фиг. 4B); WO2003104270 (пункт формулы № 11); WO2003104270 (пункт формулы № 16); US2004005598 (пункт формулы № 22); WO2003042661 (пункт формулы № 12); US2003060612 (пункт формулы № 12; фиг. 10); WO200226822 (пункт формулы № 23; фиг. 2); WO200216429 (пункт формулы № 12; фиг. 10);
Перекрестные ссылки: GI:22655488; AAN04080.1; AF455138_1
12) TrpM4 (BR22450, FLJ20041, TRPM4, TRPM4B, катионный канал, действующий по механизму транзиторного рецепторного потенциала, подсемейство M, элемент 4, идентификационный номер ГенБанка NM_017636)
Xu, X.Z., et al Proc. Natl. Acad. Sci. U.S.A. 98 (19):10692-10697 (2001), Cell 109 (3):397-407 (2002), J. Biol. Chem. 278 (33):30813-30820 (2003)); US2003143557 (пункт формулы № 4); WO200040614 (пункт формулы № 14; страницы 100-103); WO200210382 (пункт формулы № 1; фиг. 9A); WO2003042661 (пункт формулы № 12); WO200230268 (пункт формулы № 27; страница 391); US2003219806 (пункт формулы № 4); WO200162794 (пункт формулы № 14; фиг. 1A-D);
Перекрестные ссылки: MIM:606936; NP_060106.2; NM_017636_1
13) CRIPTO (CR, CR1, CRGF, CRIPTO, TDGF1, фактор роста, полученный из тератокарциномы, идентификационный номер ГенБанка NP_003203 или NM_003212)
Ciccodicola, A., et al EMBO J. 8 (7):1987-1991 (1989), Am. J. Hum. Genet. 49 (3):555-565 (1991)); US2003224411 (пункт формулы № 1); WO2003083041 (пример 1); WO2003034984 (пункт формулы № 12); WO200288170 (пункт формулы № 2; страницы 52-53); WO2003024392 (пункт формулы № 2; фиг. 58); WO200216413 (пункт формулы № 1; страницы 94-95, 105); WO200222808 (пункт формулы № 2; фиг. 1); US5854399 (пример 2; Col 17-18); US5792616 (фиг. 2);
Перекрестные ссылки: MIM:187395; NP_003203.1; NM_003212_1
14) CD21 (CR2 (рецептор комплемента 2) или C3DR (C3d/рецептор вируса Эпштейна-Барр) или Hs.73792 идентификационный номер ГенБанка M26004)
Fujisaku et al (1989) J. Biol. Chem. 264 (4):2118-2125); Weis J.J., et al J. Exp. Med. 167, 1047-1066, 1988; Moore M., et al Proc. Natl. Acad. Sci. U.S.A. 84, 9194-9198, 1987; Barel M., et al Mol. Immunol. 35, 1025-1031, 1998; Weis J.J., et al Proc. Natl. Acad. Sci. U.S.A. 83, 5639-5643, 1986; Sinha S.K., et al (1993) J. Immunol. 150, 5311-5320; WO2004045520 (пример 4); US2004005538 (пример 1); WO2003062401 (пункт формулы № 9); WO2004045520 (пример 4); WO9102536 (фиг. 9.1-9.9); WO2004020595 (пункт формулы № 1);
Идентификационный номер: P20023; Q13866; Q14212; EMBL; M26004; AAA35786.1.
15) CD79b (CD79B, CD79β, IGb (иммуноглобулин-ассоциированный бета), B29, идентификационный номер ГенБанка NM_000626 or 11038674)
Proc. Natl. Acad. Sci. U.S.A. (2003) 100 (7):4126-4131, Blood (2002) 100 (9):3068-3076, Muller et al (1992) Eur. J. Immunol. 22 (6):1621-1625); WO2004016225 (пункт формулы № 2, фиг. 140); WO2003087768, US2004101874 (пункт формулы № 1, страница 102); WO2003062401 (пункт формулы № 9); WO200278524 (пример 2); US2002150573 (пункт формулы № 5, страница 15); US5644033; WO2003048202 (пункт формулы № 1, страницы 306 и 309); WO 99/558658, US6534482 (пункт формулы № 13, фиг. 17A/B); WO200055351 (пункт формулы № 11, страницы 1145-1146);
Перекрестные ссылки: MIM:147245; NP_000617.1; NM_000626_1
16) FcRH2 (IFGP4, IRTA4, SPAP1A (якорный фосфатазный белок 1а, содержащий домен SH2), SPAP1B, SPAP1C, идентификационный номер ГенБанка NM_030764, AY358130)
Genome Res. 13 (10):2265-2270 (2003), Immunogenetics 54 (2):87-95 (2002), Blood 99 (8):2662-2669 (2002), Proc. Natl. Acad. Sci. U.S.A. 98 (17):9772-9777 (2001), Xu, M.J., et al (2001) Biochem. Biophys. Res. Commun. 280 (3):768-775; WO2004016225 (пункт формулы № 2); WO2003077836; WO200138490 (пункт формулы № 5; фиг. 18D-1-18D-2); WO2003097803 (пункт формулы № 12); WO2003089624 (пункт формулы № 25);
Перекрестные ссылки: MIM:606509; NP_110391.2; NM_030764_1
17) HER2 (ErbB2, идентификационный номер ГенБанка M11730)
Coussens L., et al Science (1985) 230(4730):1132-1139); Yamamoto T., et al Nature 319, 230-234, 1986; Semba K., et al Proc. Natl. Acad. Sci. U.S.A. 82, 6497-6501, 1985; Swiercz J.M., et al J. Cell Biol. 165, 869-880, 2004; Kuhns J.J., et al J. Biol. Chem. 274, 36422-36427, 1999; Cho H.-S., et al Nature 421, 756-760, 2003; Ehsani A., et al (1993) Genomics 15, 426-429; WO2004048938 (пример 2); WO2004027049 (фиг. 1I); WO2004009622; WO2003081210; WO2003089904 (пункт формулы № 9); WO2003016475 (пункт формулы № 1); US2003118592; WO2003008537 (пункт формулы № 1); WO2003055439 (пункт формулы № 29; фиг. 1A-B); WO2003025228 (пункт формулы № 37; фиг. 5C); WO200222636 (пример 13; страницы 95-107); WO200212341 (пункт формулы № 68; фиг. 7); WO200213847 (страницы 71-74); WO200214503 (страницы 114-117); WO200153463 (пункт формулы № 2; страницы 41-46); WO200141787 (страница 15); WO200044899 (пункт формулы № 52; фиг. 7); WO200020579 (пункт формулы № 3; фиг. 2); US5869445 (пункт формулы № 3; Col 31-38); WO9630514 (пункт формулы № 2; страницы 56-61); EP1439393 (пункт формулы № 7); WO2004043361 (пункт формулы № 7); WO2004022709; WO200100244 (пример 3; фиг. 4);
Идентификационный номер: P04626; EMBL; M11767; AAA35808.1. EMBL; M11761; AAA35808.1.
18) NCA (CEACAM6, идентификационный номер ГенБанка M18728);
Barnett T., et al Genomics 3, 59-66, 1988; Tawaragi Y., et al Biochem. Biophys. Res. Commun. 150, 89-96, 1988; Strausberg R.L., et al Proc. Natl. Acad. Sci. U.S.A. 99:16899-16903, 2002; WO2004063709; EP1439393 (пункт формулы № 7); WO2004044178 (пример 4); WO2004031238; WO2003042661 (пункт формулы № 12); WO200278524 (пример 2); WO200286443 (пункт формулы № 27; страница 427); WO200260317 (пункт формулы № 2);
Идентификационный номер: P40199; Q14920; EMBL; M29541; AAA59915.1. EMBL; M18728;
19) MDP (DPEP1, идентификационный номер ГенБанка BC017023)
Proc. Natl. Acad. Sci. U.S.A. 99 (26):16899-16903 (2002)); WO2003016475 (пункт формулы № 1); WO200264798 (пункт формулы № 33; страницы 85-87); JP05003790 (фиг. 6-8); WO9946284 (фиг. 9);
Перекрестные ссылки: MIM:179780; AAH17023.1; BC017023_1
20) IL20Rα (IL20Ra, ZCYTOR7, идентификационный номер ГенБанка AF184971);
Clark H.F., et al Genome Res. 13, 2265-2270, 2003; Mungall A.J., et al Nature 425, 805-811, 2003; Blumberg H., et al Cell 104, 9-19, 2001; Dumoutier L., et al J. Immunol. 167, 3545-3549, 2001; Parrish-Novak J., et al J. Biol. Chem. 277, 47517-47523, 2002; Pletnev S., et al (2003) Biochemistry 42:12617-12624; Sheikh F., et al (2004) J. Immunol. 172, 2006-2010; EP1394274 (пример 11); US2004005320 (пример 5); WO2003029262 (страницы 74-75); WO2003002717 (пункт формулы № 2; страница 63); WO200222153 (страницы 45-47); US2002042366 (страницы 20-21); WO200146261 (страницы 57-59); WO200146232 (страницы 63-65); WO9837193 (пункт формулы № 1; страницы 55-59);
Идентификационный номер: Q9UHF4; Q6UWA9; Q96SH8; EMBL; AF184971; AAF01320.1.
21) Brevican (BCAN, BEHAB, идентификационный номер ГенБанка AF229053)
Gary S.C., et al Gene 256, 139-147, 2000; Clark H.F., et al Genome Res. 13, 2265-2270, 2003; Strausberg R.L., et al Proc. Natl. Acad. Sci. U.S.A. 99, 16899-16903, 2002; US2003186372 (пункт формулы № 11); US2003186373 (пункт формулы № 11); US2003119131 (пункт формулы № 1; фиг. 52); US2003119122 (пункт формулы № 1; фиг. 52); US2003119126 (пункт формулы № 1); US2003119121 (пункт формулы № 1; фиг. 52); US2003119129 (пункт формулы № 1); US2003119130 (пункт формулы № 1); US2003119128 (пункт формулы № 1; фиг. 52); US2003119125 (пункт формулы № 1); WO2003016475 (пункт формулы № 1); WO200202634 (пункт формулы № 1);
22) EphB2R (DRT, ERK, Hek5, EPHT3, Tyro5, идентификационный номер ГенБанка NM_004442)
Chan,J. and Watt, V.M., Oncogene 6 (6), 1057-1061 (1991) Oncogene 10 (5):897-905 (1995), Annu. Rev. Neurosci. 21:309-345 (1998), Int. Rev. Cytol. 196:177-244 (2000)); WO2003042661 (пункт формулы № 12); WO200053216 (пункт формулы № 1; страница 41); WO2004065576 (пункт формулы № 1); WO2004020583 (пункт формулы № 9); WO2003004529 (страницы 128-132); WO200053216 (пункт формулы № 1; страница 42);
Перекрестные ссылки: MIM:600997; NP_004433.2; NM_004442_1
23) ASLG659 (B7h, идентификационный номер ГенБанка AX092328)
US20040101899 (пункт формулы № 2); WO2003104399 (пункт формулы № 11); WO2004000221 (фиг. 3); US2003165504 (пункт формулы № 1); US2003124140 (пример 2); US2003065143 (фиг. 60); WO2002102235 (пункт формулы № 13; страница 299); US2003091580 (пример 2); WO200210187 (пункт формулы № 6; фиг. 10); WO200194641 (пункт формулы № 12; фиг. 7b); WO200202624 (пункт формулы № 13; фиг. 1A-1B); US2002034749 (пункт формулы № 54; страницы 45-46); WO200206317 (пример 2; страницы 320-321, пункт формулы № 34; страницы 321-322); WO200271928 (страницы 468-469); WO200202587 (пример 1; фиг. 1); WO200140269 (пример 3; страницы 190-192); WO200036107 (пример 2; страницы 205-207); WO2004053079 (пункт формулы № 12); WO2003004989 (пункт формулы № 1); WO200271928 (страницы 233-234, 452-453); WO 0116318;
24) PSCA (предшественник антигена стволовых клеток простаты, идентификационный номер ГенБанка AJ297436)
Reiter R.E., et al Proc. Natl. Acad. Sci. U.S.A. 95, 1735-1740, 1998; Gu Z., et al Oncogene 19, 1288-1296, 2000; Biochem. Biophys. Res. Commun. (2000) 275(3):783-788; WO2004022709; EP1394274 (пример 11); US2004018553 (пункт формулы № 17); WO2003008537 (пункт формулы № 1); WO200281646 (пункт формулы № 1; страница 164); WO2003003906 (пункт формулы № 10; страница 288); WO200140309 (пример 1; фиг. 17); US2001055751 (пример 1; фиг. 1b); WO200032752 (пункт формулы № 18; фиг. 1); WO9851805 (пункт формулы № 17; страница 97); WO9851824 (пункт формулы № 10; страница 94); WO9840403 (пункт формулы № 2; фиг. 1B);
Идентификационный номер: O43653; EMBL; AF043498; AAC39607.1.
25) GEDA (идентификационный номер ГенБанка AY260763);
AAP14954 белок подобный гибридному партнеру HMGIC липомы /pid=AAP14954.1 - Homo sapiens
Виды: Homo sapiens (human)
WO2003054152 (пункт формулы № 20); WO2003000842 (пункт формулы № 1); WO2003023013 (пример 3, пункт формулы № 20); US2003194704 (пункт формулы № 45);
Перекрестные ссылки: GI:30102449; AAP14954.1; AY260763_1
26) BAFF-R (рецептор фактора активации В-лимфоцитов, BlyS рецептор 3, BR3, идентификационный номер ГенБанка AF116456); рецептор BAFF /pid=NP_443177.1 - Homo sapiens
Thompson, J.S., et al Science 293 (5537), 2108-2111 (2001); WO2004058309; WO2004011611; WO2003045422 (пример; страницы 32-33); WO2003014294 (пункт формулы № 35; фиг. 6B); WO2003035846 (пункт формулы № 70; страницы 615-616); WO200294852 (Col 136-137); WO200238766 (пункт формулы № 3; страница 133); WO200224909 (пример 3; фиг. 3);
Перекрестные ссылки: MIM:606269; NP_443177.1; NM_052945_1; AF132600
27) CD22 (изоформа CD22-В рецептора В-лимфоцитов, BL-CAM, Lyb-8, Lyb8, SIGLEC-2, FLJ22814, идентификационный номер ГенБанка AK026467);
Wilson et al (1991) J. Exp. Med. 173:137-146; WO2003072036 (пункт формулы № 1; фиг. 1);
Перекрестные ссылки: MIM:107266; NP_001762.1; NM_001771_1
28) CD79a (CD79A, CD79α, иммуноглобулин-ассоциированный альфа, специфический к В-клеткам белок, который ковалентно взаимодействует с Ig бета (CD79B) и образует комплекс на поверхности с молекулами Ig M, передает сигнал, связанный с дифференцировкой В-клеток), pI: 4,84, MW: 25028 TM: 2 [P] хромосома гена: 19q13.2, идентификационный номер ГенБанка NP_001774.10)
WO2003088808, US20030228319; WO2003062401 (пункт формулы № 9); US2002150573 (пункт формулы № 4, страницы 13-14); WO9958658 (пункт формулы № 13, фиг. 16); WO9207574 (фиг. 1); US5644033; Ha et al (1992) J. Immunol. 148(5):1526-1531; Mueller et al (1992) Eur. J. Biochem. 22:1621-1625; Hashimoto et al (1994) Immunogenetics 40(4):287-295; Preud'homme et al (1992) Clin. Exp. Immunol. 90(1):141-146; Yu et al (1992) J. Immunol. 148(2) 633-637; Sakaguchi et al (1988) EMBO J. 7(11):3457-3464;
29) CXCR5 (рецептор лимфомы Беркитта 1, сопряженный с протеином G рецептор, который активируется хемокином CXCL13, принимает участие в миграции лимфоцитов и гуморальной защите, играет роль в инфицировании ВИЧ-2 и, возможно, развитии СПИДа, лимфомы, миеломы и лейкоза); 372 aa, pI: 8,54 MW: 41959 TM: 7 [P] хромосома гена: 11q23.3, идентификационный номер ГенБанка NP_001707.1)
WO2004040000; WO2004015426; US2003105292 (пример 2); US6555339 (пример 2); WO200261087 (фиг. 1); WO200157188 (пункт формулы № 20, страница 269); WO200172830 (страницы 12-13); WO200022129 (пример 1, страницы 152-153, пример 2, страницы 254-256); WO9928468 (пункт формулы № 1, страница 38); US5440021 (пример 2, col 49-52); WO9428931 (страницы 56-58); WO9217497 (пункт формулы № 7, фиг. 5); Dobner et al (1992) Eur. J. Immunol. 22:2795-2799; Barella et al (1995) Biochem. J. 309:773-779;
30) HLA-DOB (бета-субъединица молекулы ГКГС класса II (антиген Ia), которая связывает пептиды и представляет их CD4+ Т-лимфоцитам); 273 aa, pI: 6,56 MW: 30820 TM: 1 [P] хромосома гена: 6p21.3, идентификационный номер ГенБанка NP_002111.1)
Tonnelle et al (1985) EMBO J. 4(11):2839-2847; Jonsson et al (1989) Immunogenetics 29(6):411-413; Beck et al (1992) J. Mol. Biol. 228:433-441; Strausberg et al (2002) Proc. Natl. Acad. Sci USA 99:16899-16903; Servenius et al (1987) J. Biol. Chem. 262:8759-8766; Beck et al (1996) J. Mol. Biol. 255:1-13; Naruse et al (2002) Tissue Antigens 59:512-519; WO9958658 (пункт формулы № 13, фиг. 15); US6153408 (Col 35-38); US5976551 (col 168-170); US6011146 (col 145-146); Kasahara et al (1989) Immunogenetics 30(1):66-68; Larhammar et al (1985) J. Biol. Chem. 260(26):14111-14119;
31) P2X5 (управляемый лигандом пуринергического рецептора P2X ионный канал 5, ионный канал, управляемый внеклеточной АТФ, может быть вовлечен в синаптическую передачу и нейрогенез, его дефицит может влиять на патофизиологию идиопатической нестабильности детрузора); 422 aa), pI: 7,63, MW: 47206 TM: 1 [P] хромосома гена: 17p13.3, идентификационный номер ГенБанка NP_002552.2)
Le et al (1997) FEBS Lett. 418(1-2):195-199; WO2004047749; WO2003072035 (пункт формулы № 10); Touchman et al (2000) Genome Res. 10:165-173; WO200222660 (пункт формулы № 20); WO2003093444 (пункт формулы № 1); WO2003087768 (пункт формулы № 1); WO2003029277 (страница 82);
32) CD72 (антиген дифференцировки В-клеток CD72, Lyb-2) PROTEIN SEQUENCE Full maeaity...tafrfpd (1..359; 359 aa), pI: 8,66, MW: 40225 TM: 1 [P] хромосома гена: 9p13.3, идентификационный номер ГенБанка NP_001773.1)
WO2004042346 (пункт формулы № 65); WO2003026493 (страницы 51-52, 57-58); WO200075655 (страницы 105-106); Von Hoegen et al (1990) J. Immunol. 144(12):4870-4877; Strausberg et al (2002) Proc. Natl. Acad. Sci USA 99:16899-16903;
33) LY64 (лимфоцитарный антиген 64 (RP105), мембранный белок типа I из семейства богатых лейцином повторов (LRR), регулирует активацию В-клеток и апоптоз, потеря его функциональности связана с повышенной активностью заболевания у пациентов с системной красной волчанкой); 661 aa, pI: 6,20, MW: 74147 TM: 1 [P] хромосома гена: 5q12, идентификационный номер ГенБанка NP_005573.1)
US2002193567; WO9707198 (пункт формулы № 11, страницы 39-42); Miura et al (1996) Genomics 38(3):299-304; Miura et al (1998) Blood 92:2815-2822; WO2003083047; WO9744452 (пункт формулы № 8, страницы 57-61); WO200012130 (страницы 24-26);
34) FcRH1 (Fc-рецептор-подобный белок 1, предполагаемый рецептор для домена Fc иммуноглобулина, который содержит Ig-подобный и ITAM домены типа C2, может играть роль в дифференциации B-лимфоцитов); 429 aa, pI: 5,28, MW: 46925 TM: 1 [P] хромосома гена: 1q21-1q22, идентификационный номер ГенБанка NP_443170.1)
WO2003077836; WO200138490 (пункт формулы № 6, фиг. 18E-1-18-E-2); Davis et al (2001) Proc. Natl. Acad. Sci USA 98(17):9772-9777; WO2003089624 (пункт формулы № 8); EP1347046 (пункт формулы № 1); WO2003089624 (пункт формулы № 7);
35) IRTA2 (ассоциированный с транслокацией рецептор 2 суперсемейства иммуноглобулинов, предполагаемый иммунорецептор с возможным участием в развитии В-лимфоцитов и лимфомагенеза; дисрегуляция гена путем транслокации происходит в некоторых злокачественных новообразованиях В-лимфоцитов); 977 aa, pI: 6,88 MW: 106468 TM: 1 [P] хромосома гена: 1q21, идентификационный номер ГенБанка Human:AF343662, AF343663, AF343664, AF343665, AF369794, AF397453, AK090423, AK090475, AL834187, AY358085; Mouse:AK089756, AY158090, AY506558; NP_112571.1
WO2003024392 (пункт формулы № 2, фиг. 97); Nakayama et al (2000) Biochem. Biophys. Res. Commun. 277(1):124-127; WO2003077836; WO200138490 (пункт формулы № 3, фиг. 18B-1-18B-2);
(36) TENB2 (TMEFF2, томорегулин, TPEF, HPP1, TR, предполагаемый трансмембранный протеогликан, связанный с семейством факторов роста EGF/херегулина и фоллистатином); 374 aa, NCBI Идентификационный номер: AAD55776, AAF91397, AAG49451, NCBI RefSeq: NP_057276; NCBI Gene: 23671; OMIM: 605734; SwissProt Q9UIK5; идентификационный номер ГенБанка AF179274; AY358907, CAF85723, CQ782436
WO2004074320 (SEQ ID NO 810); JP2004113151 (SEQ ID NOS 2, 4, 8); WO2003042661 (SEQ ID NO 580); WO2003009814 (SEQ ID NO 411); EP1295944 (страницы 69-70); WO200230268 (страница 329); WO200190304 (SEQ ID NO 2706); US2004249130; US2004022727; WO2004063355; US2004197325; US2003232350; US2004005563; US2003124579; Horie et al (2000) Genomics 67:146-152; Uchida et al (1999) Biochem. Biophys. Res. Commun. 266:593-602; Liang et al (2000) Cancer Res. 60:4907-12; Glynne-Jones et al (2001) Int J Cancer. Oct 15;94(2):178-84;
37) PMEL17 (гомолог silver; SILV; D12S53E; PMEL17; SI; SIL); ME20; gp100) BC001414; BT007202; M32295; M77348; NM_006928; McGlinchey, R.P. et al (2009) Proc. Natl. Acad. Sci. U.S.A. 106 (33), 13731-13736; Kummer, M.P. et al (2009) J. Biol. Chem. 284 (4), 2296-2306;
(38) TMEFF1 (трансмембранный белок 1 с EGF-подобным и двумя фолистатино-подобными доменами; Tomoregulin-1); H7365; C9orf2; C9ORF2; U19878; X83961; NM_080655; NM_003692; Harms, P.W. (2003) Genes Dev. 17 (21), 2624-2629; Gery, S. et al (2003) Oncogene 22 (18):2723-2727;
39) GDNF-Ra1 (рецептор альфа-1 семейства GDNF; GFRA1; GDNFR; GDNFRA; RETL1; TRNR1; RET1L; GDNFR-alpha1; GFR-ALPHA-1); U95847; BC014962; NM_145793 NM_005264; Kim, M.H. et al (2009) Mol. Cell. Biol. 29 (8), 2264-2277; Treanor, J.J. et al (1996) Nature 382 (6586):80-83;
(40) Ly6E (комплекс лимфоцитарного антигена 6, локус E; Ly67,RIG-E,SCA-2,TSA-1); NP_002337.1; NM_002346.2; de Nooij-van Dalen, A.G. et al (2003) Int. J. Cancer 103 (6), 768-774; Zammit, D.J. et al (2002) Mol. Cell. Biol. 22 (3):946-952; WO 2013/17705;
(41) TMEM46 (гомолог 2 shisa (Xenopus laevis); SHISA2); NP_001007539.1; NM_001007538.1; Furushima, K. et al (2007) Dev. Biol. 306 (2), 480-492; Clark, H.F. et al (2003) Genome Res. 13 (10):2265-2270;
(42) Ly6G6D (комплекс лимфоцитарного антигена 6, локус G6D; Ly6-D, MEGT1); NP_067079.2; NM_021246.2; Mallya, M. et al (2002) Genomics 80 (1):113-123; Ribas, G. et al (1999) J. Immunol. 163 (1):278-287;
(43) LGR5 (богатый на лейциновые повторы рецептор 5, сопряженный с G белком; GPR49, GPR67); NP_003658.1; NM_003667.2; Salanti, G. et al (2009) Am. J. Epidemiol. 170 (5):537-545; Yamamoto, Y. et al (2003) Hepatology 37 (3):528-533;
(44) RET (протоонкоген ret; MEN2A; HSCR1; MEN2B; MTC1; PTC; CDHF12; Hs.168114; RET51; RET-ELE1); NP_066124.1; NM_020975.4; Tsukamoto, H. et al (2009) Cancer Sci. 100 (10):1895-1901; Narita, N. et al (2009) Oncogene 28 (34):3058-3068;
(45) LY6K (комплекс лимфоцитарного антигена 6, локус K; LY6K; HSJ001348; FLJ35226); NP_059997.3; NM_017527.3; Ishikawa, N. et al (2007) Cancer Res. 67 (24):11601-11611; de Nooij-van Dalen, A.G. et al (2003) Int. J. Cancer 103 (6):768-774;
(46) GPR19 (рецептор 19, сопряженный с G белком; Mm.4787); NP_006134.1; NM_006143.2; Montpetit, A. and Sinnett, D. (1999) Hum. Genet. 105 (1-2):162-164; O'Dowd, B.F. et al (1996) FEBS Lett. 394 (3):325-329;
(47) GPR54 (рецептор KISS1; KISS1R; GPR54; HOT7T175; AXOR12); NP_115940.2; NM_032551.4; Navenot, J.M. et al (2009) Mol. Pharmacol. 75 (6):1300-1306; Hata, K. et al (2009) Anticancer Res. 29 (2):617-623;
(48) ASPHD1 (содержащий домен аспартат-бета-гидроксилазы 1; LOC253982); NP_859069.2; NM_181718.3; Gerhard, D.S. et al (2004) Genome Res. 14 (10B):2121-2127;
(49) Тирозиназа (TYR; OCAIA; OCA1A; тирозина; SHEP3); NP_000363.1; NM_000372.4; Bishop, D.T. et al (2009) Nat. Genet. 41 (8):920-925; Nan, H. et al (2009) Int. J. Cancer 125 (4):909-917;
(50) TMEM118 (белок 2, содержащий трансмембранный домен и домен «палец RING (Really Interesting New Gene)»; RNFT2; FLJ14627); NP_001103373.1; NM_001109903.1; Clark, H.F. et al (2003) Genome Res. 13 (10):2265-2270; Scherer, S.E. et al (2006) Nature 440 (7082):346-351
51) GPR172A (рецептор 172A, сопряженный с G белком; GPCR41; FLJ11856; D15Ertd747e); NP_078807.1; NM_024531.3; Ericsson, T.A. et al (2003) Proc. Natl. Acad. Sci. U.S.A. 100 (11):6759-6764; Takeda, S. et al (2002) FEBS Lett. 520 (1-3):97-101.
52) CD33, член семейства иммуноглобулин-подобных лектинов, связывающих сиаловую кислоту, является 67-кДа гликозилированным трансмембранным белком. CD33 экспрессируется на большинстве миелоидных и моноцитарных лейкозных клеток в дополнение к коммитированным клеткам-предшественникам миеломоноцитов и эритроидов. Его не наблюдают на самых ранних плюрипотентных стволовых клетках, зрелых гранулоцитах, лимфоцитах или негематопоэтических клетках (Sabbath et al., (1985) J. Clin. Invest. 75:756-56; Andrews et al., (1986) Blood 68:1030-5). CD33 содержит два остатка тирозина на цитоплазматическом конце, после каждого из которых идут гидрофобные остатки, что подобно ингибирующему мотиву на основе тирозина иммунорецепторов на (ITIM), наблюдаемому во многих ингибиторных рецепторах.
53) CLL-1 (CLEC12A, MICL и DCAL2), кодирует члена суперсемейства лектинов С-типа/доменов, подобных лектинам С-типа (CTL/CTLD). Представители этого семейства характеризуются одинаковым типом сворачивания белка и имеют разнообразные функции, такие как клеточная адгезия, передача сигнала от клетки к клетке, обмен гликопротеинов, и играют роль в воспалительных и иммунных ответах. Белок, кодируемый этим геном является отрицательным регулятором функции гранулоцитов и моноцитов. Было описано несколько альтернативных сплайс-вариантов транскрипта этого гена, но полноразмерная природа некоторых из этих вариантов определена не была. Этот ген тесно связан с другими представителями суперсемейства CTL/CTLD в области комплекса генов естественных киллеров в хромосоме 12p13 (Drickamer K (1999) Curr. Opin. Struct. Biol. 9 (5):585-90; van Rhenen A, et al., (2007) Blood 110 (7):2659-66; Chen CH, et al. (2006) Blood 107 (4):1459-67; Marshall AS, et al. (2006) Eur. J. Immunol. 36 (8):2159-69; Bakker AB, et al (2005) Cancer Res. 64 (22):8443-50; Marshall AS, et al (2004) J. Biol. Chem. 279 (15):14792-802). Было показано, что CLL-1 является трансмембранным рецептором типа II, содержащим один домен, подобный лектинам С-типа (который предполагаемо не связывает кальций или сахар), стеблеобразную область, трансмембранный домен и короткий цитоплазматический хвост, содержащий мотив ITIM).
Антитела анти-CD22
В некоторых вариантах осуществления, антитела анти-CD22 КАЛС (ADC) в таблицах 3А и 3В содержат три гипервариабельные области легкой цепи (HVR-L1, HVR-L2 и HVR-L3) и три гипервариабельные области тяжелой цепи (HVR-H1, HVR-H2 и HVR-H3), согласно US 8226945:
HVR-L1 RSSQSIVHSVGNTFLE (SEQ ID NO:1)
HVR-L2 KVSNRFS (SEQ ID NO:2)
HVR-L3 FQGSQFPYT (SEQ ID NO:3)
HVR-H1 GYEFSRSWMN (SEQ ID NO:4)
HVR-H2 GRIYPGDGDTNYSGKFKG (SEQ ID NO:5)
HVR-H3 DGSSWDWYFDV (SEQ ID NO:6)
Антитела анти-Ly6E
В некоторых вариантах осуществления, КАЛС (ADC) таблиц 3А и 3В включают в себя антитела против Ly6E. Комплекс лимфоцитарного антигена 6, локус E (Ly6E), также известный как ген E (RIG-E), индуцированный ретиноевой кислотой, и антиген 2 стволовых клеток (SCA-2). Это связанный с GPI, длинной в 131 аминокислоту, около 8,4 кДа белок неизвестной функции без каких-либо известных партнеров по связыванию. Первоначально он был идентифицирован как транскрипт, экспрессированный в незрелых тимоцитах, тимусных медулярных эпителиальных клетках у мышей (Mao, et al. (1996) Proc. Natl. Acad. Sci. U.S.A. 93:5910-5914). В некоторых вариантах осуществления, в изобретении предложено иммуноконъюгат, содержащий антитело против Ly6E, описанное в публикации PCT № WO 2013/177055.
В некоторых вариантах осуществления, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело к Ly6E, содержащее по меньшей мере одну, две, три, четыре, пять или шесть HVR выбранных из: a) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 12; b) HVR-H2 содержащей аминокислотную последовательность SEQ ID NO: 13; c) HVR-H3 содержащей аминокислотную последовательность SEQ ID NO: 14; d) HVR-L1 содержащей аминокислотную последовательность SEQ ID NO: 9; e) HVR-L2 содержащей аминокислотную последовательность SEQ ID NO: 10; и f) HVR-L3 содержащей аминокислотную последовательность SEQ ID NO: 11.
В одном аспекте, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело, которое содержит по меньшей мере одну, две или все три последовательности HVR VH, выбранные из: a) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 12; b) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 13; и c) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 14. В дополнительном варианте осуществления, антитело содержит: a) HVR-H1, содержащую аминокислотную последовательность SEQ ID NO: 12; b) HVR-H2, содержащую аминокислотную последовательность SEQ ID NO: 13; и c) HVR-H3, содержащую аминокислотную последовательность SEQ ID NO: 14.
В другом аспекте, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело, которое содержит по меньшей мере одну, две или все три последовательности HVR VL, выбранные из: a) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 9; b) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 10; и c) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 11. В одном варианте осуществления, антитело содержит: a) HVR-L1, содержащую аминокислотную последовательность SEQ ID NO: 9; b) HVR-L2, содержащую аминокислотную последовательность SEQ ID NO: 10; и c) HVR-L3, содержащую аминокислотную последовательность SEQ ID NO: 11.
В другом аспекте, конъюгат антитело-лекарственное средство по изобретению содержит антитело, содержащее: a) домен VH, содержащий по меньшей мере одну, две, или все три последовательности HVR VH, выбранные из: (i) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 12, (ii) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 13, и (iii) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 14; и b) домен VL, содержащий по меньшей мере одну, две, или все три последовательности HVR VL, выбранные из: (i) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 9, (ii) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 10, и c) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 11.
В другом аспекте, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело, которое содержит: a) HVR-H1, содержащую аминокислотную последовательность SEQ ID NO: 12; b) HVR-H2, содержащую аминокислотную последовательность SEQ ID NO: 13; c) HVR-H3, содержащую аминокислотную последовательность SEQ ID NO: 14; d) HVR-L1, содержащую аминокислотную последовательность SEQ ID NO: 9; e) HVR-L2, содержащую аминокислотную последовательность SEQ ID NO: 10; и f) HVR-L3, содержащую аминокислотную последовательность SEQ ID NO: 11.
В любом из указанных выше вариантов осуществления изобретения, антитело к Ly6E конъюгата антитело-лекарственное средство является гуманизированным. В одном из вариантов осуществления, антитело к Ly6E содержит HVR, как в любом из указанных выше вариантов осуществления изобретения, и дополнительно содержит акцепторный человеческий каркас, например, каркас человеческого иммуноглобулина или человеческий консенсусный каркас.
В другом аспекте, антитело к Ly6E конъюгата антитело-лекарственное средство содержит последовательность вариабельного домена (VH) тяжелой цепи, имеющую по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, или 100% идентичности последовательности аминокислотной последовательности SEQ ID NO: 8. В некоторых вариантах осуществления, последовательность VH, имеющая по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичности аминокислотной последовательности SEQ ID NO:8 содержит замены (например, консервативные замены), вставки или делеции по сравнению с эталонной последовательностью, но антитело к Ly6E, содержащее эту последовательность, сохраняет способность связываться с Ly6E человека. В некоторых вариантах осуществления, в общей сложности от 1 до 10 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 8. В некоторых вариантах осуществления, в общей сложности от 1 до 5 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 8. В некоторых вариантах осуществления, замены, вставки или делеции происходят в областях вне HVR (то есть, в FR). Необязательно, антитело к Ly6E содержит последовательность VH SEQ ID NO: 8, включая пост-трансляционные модификации этой последовательности. В конкретном варианте осуществление, VH содержит одну, две или три HVR, выбранные из: а) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 12; b) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 13; c) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 14.
В другом аспекте, предлагается антитело к Ly6E конъюгата антитело-лекарственное средство, причем антитело содержит вариабельный домен легкой цепи (VL), имеющий по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, или 100% идентичности последовательности аминокислотной последовательности SEQ ID NO: 7. В некоторых вариантах осуществления, последовательность VL, имеющая по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичности аминокислотной последовательности SEQ ID NO:7 содержит замены (например, консервативные замены), вставки или делеции по сравнению с эталонной последовательностью, но антитело к Ly6E, содержащее эту последовательность, сохраняет способность связываться с Ly6E. В некоторых вариантах осуществления, в общей сложности от 1 до 10 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 7. В некоторых вариантах осуществления, в общей сложности от 1 до 5 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 7. В некоторых вариантах осуществления, замены, вставки или делеции происходят в областях вне HVR (то есть, в FR). Необязательно, антитело к Ly6E содержит последовательность VL SEQ ID NO: 7, включая пост-трансляционные модификации этой последовательности. В конкретном варианте осуществление, VL содержит одну, две или три HVR, выбранные из: а) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 9; b) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 10; c) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 11.
В другом аспекте, предлагается конъюгат антитело-лекарственное средство, содержащий антитело к Ly6E, причем антитело содержит VH как в любом из вариантов осуществления изобретения, приведенных выше, и VL как в любом из вариантов осуществления изобретения, приведенных выше.
В одном варианте осуществления, предлагается конъюгат антитело-лекарственное средство, причем антитело содержит последовательности VH и VL в SEQ ID NO: 8 и SEQ ID NO: 7, соответственно, включая пост-трансляционные модификации этих последовательностей.
В дополнительном аспекте, в данном документе предлагается конъюгат антитело-лекарственное средство, содержащий антитела, которые связываются с тем же самым эпитопом, что и антитело к Ly6E, предложенное в данном документе. Например, в некоторых вариантах осуществления предлагается иммуноконъюгат, содержащий антитело, которое связывается с тем же эпитопом, что и антитело против Ly6E, содержащее последовательность VH SEQ ID NO: 8 и последовательность VL SEQ ID NO: 7, соответственно.
В дополнительном аспекте изобретения, антитело против Ly6E конъюгата антитело-лекарственное средство в соответствии с любым из вышеуказанных вариантов осуществления представляет собой моноклональное антитело, включая человеческое антитело. В одном варианте осуществления, антитело против Ly6E конъюгата антитело-лекарственное средство представляет собой фрагмент антитела, например фрагмент Fv, Fab, Fab', scFv, диатело, или фрагмент F(ab')2. В другом варианте осуществления, антитело представляет собой, по существу, полноразмерное антитело, например антитело IgG1, антитело IgG2a или другой класс антител или изотип, как определено в данном документе. В некоторых вариантах осуществления, иммуноконъюгат (КАЛС (ADC)) содержит антитело против Ly6E, содержащее тяжелую цепь и легкую цепь, содержащие аминокислотные последовательности SEQ ID NO: 16 и 15 соответственно.
Таблица последовательностей антитела против Ly6E
GKTVKLLIYY TSNLHSGVPS RFSGSGSGTD YTLTISSLQP
EDFATYYCQQ YSELPWTFGQ GTKVEIK
GKTVKLLIYY TSNLHSGVPS RFSGSGSGTD YTLTISSLQP
EDFATYYCQQ YSELPWTFGQ GTKVEIK RTVAAPSVFIF
PPSDEQLKSG TASVVCLLNN FYPREAKVQW CVDNALQSGN
SQESVTEQDS KDSTYSLSST LTLSKADYEK HKVYACEVTH
QGLSSPVTKS FNRGEC
PGKALEWLGM IWGDGSTDYN SALKSRLTIS KDTSKNQVVL
TMTNMDPVDT ATYYCARDYY FNYASWFAYW GQGTLVTVSS
ASTKGPSVFP LAPSSKSTSG GTAALGCLVK DYFPEPVTVS
WNSGALTSGV HTFPAVLQSS GLYSLSSVVT VPSSSLGTQT
YICNVNHKPS NTKVDKKVEP KSCDKTHTCP PCPAPELLGG
PSVFLFPPKP KDTLMISRTP EVTCVVVDVS HEDPEVKFNW
YVDGVEVHNA KTKPREEQYN STYRVVSVLT VLHQDWLNGK
EYKCKVSNKA LPAPIEKTIS KAKGQPREPQ VYTLPPSREE
MTKNQVSLTC LVKGFYPSDI AVEWESNGQP ENNYKTTPPV
LDSDGSFFLY SKLTVDKSRW QQGNVFSCSV MHEALHNHYT
QKSLSLSPGK
Антитела к HER2
В некоторых вариантах осуществления, КАЛС (ADC) таблиц 3А и 3В включают в себя антитела против HER2. В одном варианте осуществления изобретения, антитело против HER2 КАЛС (ADC) по изобретению включает в себя гуманизированное антитело против HER2, например huMAb4D5-1, huMAb4D5-2, huMAb4D5-3, huMAb4D5-4, huMAb4D5-5, huMAb4D5- 6, huMAb4D5-7 и huMAb4D5-8, как описано в таблице 3 US 5821337, которая специально включена в посредством ссылки в данный документ. Данные антитела содержат каркасные области человека с определяющими комплементарность областями мышиного антитела (4D5), которое связывается с HER2. Гуманизированное антитело huMAb4D5-8 также упоминается как трастузумаб, коммерчески доступный под торговой маркой HERCEPTIN.® В другом варианте осуществления изобретения, антитело против HER2 КАЛС (ADC) по изобретению включает в себя гуманизированное антитело против HER2, например гуманизированное 2C4, как описано в US7862817. Примером гуманизированного антитела 2C4 является пертузумаб, коммерчески доступный под торговым наименованием PERJETA.®
В другом варианте осуществления изобретения, антитело против HER2 КАЛС (ADC) по изобретению включает в себя гуманизированное антитело 7C2 против HER2. Гуманизированное антитело 7C2 представляет собой антитело против HER2.
В некоторых вариантах осуществления, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело к HER2, содержащее по меньшей мере одну, две, три, четыре, пять или шесть HVR выбранных из: a) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 22; b) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 23, 27 или 28; c) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 24 или 29; d) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 19; e) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 20; и f) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 21. В некоторых вариантах осуществления, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело к HER2, содержащее по меньшей мере одну, две, три, четыре, пять или шесть HVR выбранных из: a) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 22; b) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 23 c) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 24; d) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 19; e) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 20; и f) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 21.
В одном аспекте, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело, которое содержит по меньшей мере одну, по меньшей мере две или все три последовательности HVR VH, выбранные из: a) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 22; b) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 23, 27 или 28; и c) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 24 или 29. В одном аспекте, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело, которое содержит по меньшей мере одну, по меньшей мере две или все три последовательности HVR VH, выбранные из: a) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 22; b) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 23; и c) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 24. В дополнительном варианте осуществления, антитело содержит: a) HVR-H1, содержащую аминокислотную последовательность SEQ ID NO: 22; b) HVR-H2, содержащую аминокислотную последовательность SEQ ID NO: 23, 27 или 28; и c) HVR-H3, содержащую аминокислотную последовательность SEQ ID NO: 24 или 29. В дополнительном варианте осуществления, антитело содержит: a) HVR-H1, содержащую аминокислотную последовательность SEQ ID NO: 22; b) HVR-H2, содержащую аминокислотную последовательность SEQ ID NO: 23; и c) HVR-H3, содержащую аминокислотную последовательность SEQ ID NO: 24.
В другом аспекте, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело, которое содержит по меньшей мере одну, по меньшей мере две или все три последовательности HVR VL, выбранные из: a) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 19; b) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 20; и c) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 21. В одном варианте осуществления, антитело содержит: a) HVR-L1, содержащую аминокислотную последовательность SEQ ID NO: 19; b) HVR-L2, содержащую аминокислотную последовательность SEQ ID NO: 20; и c) HVR-L3, содержащую аминокислотную последовательность SEQ ID NO: 21.
В другом аспекте, конъюгат антитело-лекарственное средство по изобретению содержит антитело, содержащее: a) домен VH, содержащий по меньшей мере одну, по меньшей мере две, или все три последовательности HVR VH, выбранные из: (i) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 22, (ii) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 23, 27 или 28, и (iii) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 24 или 29; и b) домен VL, содержащий по меньшей мере одну, по меньшей мере две, или все три последовательности HVR VL, выбранные из: (i) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 19, (ii) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 20, и c) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 21. В другом аспекте, конъюгат антитело-лекарственное средство по изобретению содержит антитело, содержащее: a) домен VH, содержащий по меньшей мере одну, по меньшей мере две, или все три последовательности HVR VH, выбранные из: (i) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 22, (ii) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 23, и (iii) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 24; и b) домен VL, содержащий по меньшей мере одну, по меньшей мере две, или все три последовательности HVR VL, выбранные из: (i) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 19, (ii) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 20, и c) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 21.
В другом аспекте, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело, которое содержит: a) HVR-H1, содержащую аминокислотную последовательность SEQ ID NO: 22; b) HVR-H2, содержащую аминокислотную последовательность SEQ ID NO: 23, 27 или 28; c) HVR-H3, содержащую аминокислотную последовательность SEQ ID NO: 24 или 29; d) HVR-L1, содержащую аминокислотную последовательность SEQ ID NO: 19; e) HVR-L2, содержащую аминокислотную последовательность SEQ ID NO: 20; и f) HVR-L3, содержащую аминокислотную последовательность SEQ ID NO: 21. В другом аспекте, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело, которое содержит: a) HVR-H1, содержащую аминокислотную последовательность SEQ ID NO: 22; b) HVR-H2, содержащую аминокислотную последовательность SEQ ID NO: 23; c) HVR-H3, содержащую аминокислотную последовательность SEQ ID NO: 24; d) HVR-L1, содержащую аминокислотную последовательность SEQ ID NO: 19; e) HVR-L2, содержащую аминокислотную последовательность SEQ ID NO: 20; и f) HVR-L3, содержащую аминокислотную последовательность SEQ ID NO: 21.
В любом из указанных выше вариантов осуществления изобретения, антитело к HER2 конъюгата антитело-лекарственное средство является гуманизированным. В одном варианте осуществления, антитело к HER2 содержит HVR, как в любом из указанных выше вариантов осуществления изобретения, и дополнительно содержит акцепторный человеческий каркас, например, каркас человеческого иммуноглобулина или человеческий консенсусный каркас.
В другом аспекте, антитело к HER2 конъюгата антитело-лекарственное средство содержит последовательность вариабельного домена (VH) тяжелой цепи, имеющую по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, или 100% идентичности последовательности c аминокислотной последовательностью SEQ ID NO: 18. В некоторых вариантах осуществления, последовательность VH, имеющая по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичности с аминокислотной последовательностью SEQ ID NO: 18 содержит замены (например, консервативные замены), вставки или делеции по сравнению с эталонной последовательностью, но антитело к HER2, содержащее эту последовательность, сохраняет способность связываться с HER2 человека. В некоторых вариантах осуществления, в общей сложности от 1 до 10 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 18. В некоторых вариантах осуществления, в общей сложности от 1 до 5 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 18. В некоторых вариантах осуществления, замены, вставки или делеции происходят в областях вне HVR (то есть, в FR). Необязательно, антитело к HER2 содержит последовательность VH SEQ ID NO: 18, включая пост-трансляционные модификации этой последовательности. В конкретном варианте осуществление, VH содержит одну, две или три HVR, выбранные из: а) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 22; b) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 23; c) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 24.
В другом аспекте, предлагается антитело к HER2 конъюгата антитело-лекарственное средство, причем антитело содержит вариабельный домен легкой цепи (VL), имеющий по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, или 100% идентичности последовательности с аминокислотной последовательностью SEQ ID NO: 17. В некоторых вариантах осуществления, последовательность VL, имеющая по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичности с аминокислотной последовательностью SEQ ID NO: 17 содержит замены (например, консервативные замены), вставки или деле по сравнению с эталонной последовательностью, но антитело к HER2, содержащее эту последовательность, сохраняет способность связываться с HER2. В некоторых вариантах осуществления, в общей сложности от 1 до 10 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 17. В некоторых вариантах осуществления, в общей сложности от 1 до 5 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 17. В некоторых вариантах осуществления, замены, вставки или делеции происходят в областях вне HVR (то есть, в FR). Необязательно, антитело к HER2 содержит последовательность VL SEQ ID NO: 17, включая пост-трансляционные модификации этой последовательности. В конкретном варианте осуществление, VL содержит одну, две или три HVR, выбранные из: а) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 19; b) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 20; c) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 21.
В другом аспекте, предлагается конъюгат антитело-лекарственное средство, содержащий антитело к HER2, причем антитело содержит VH как в любом из вариантов осуществления изобретения, приведенных выше, и VL как в любом из вариантов осуществления изобретения, приведенных выше.
В одном варианте осуществления, предлагается конъюгат антитело-лекарственное средство, содержащий антитело, причем антитело содержит последовательности VH и VL в SEQ ID NO: 18 и SEQ ID NO: 17, соответственно, включая пост-трансляционные модификации этих последовательностей.
В одном варианте осуществления, предлагается конъюгат антитело-лекарственное средство, содержащее антитело, причем антитело содержит гуманизированную последовательность легкой цепи каппа 7C2.v2.2.LA (hu7C2) K149C SEQ ID NO: 30
В одном варианте осуществления, предлагается конъюгат антитело-лекарственное средство, содержащее антитело, причем антитело содержит последовательность тяжелой цепи IgG1 Hu7C2 A118C SEQ ID NO: 31
В дополнительном аспекте, в данном документе предлагается конъюгат антитело-лекарственное средство, содержащий антитела, которые связываются с тем же самым эпитопом, что и антитело к HER2, предложенное в данном документе. Например, в некоторых вариантах осуществления предлагается иммуноконъюгат, содержащий антитело, которое связывается с тем же эпитопом, что и антитело против HER2, содержащее последовательность VH SEQ ID NO: 18 и последовательность VL SEQ ID NO: 17, соответственно.
В дополнительном аспекте изобретения, антитело к HER2 конъюгата антитело-лекарственное средство в соответствии с любым из вышеуказанных вариантов осуществления представляет собой моноклональное антитело, включая человеческое антитело. В одном варианте осуществления, антитело к HER2 иммуноконъюгата представляет собой фрагмент антитела, например фрагмент Fv, Fab, Fab', scFv, диатело или F(ab')2. В другом варианте осуществления, иммуноконъюгат содержит антитело, которое является, по существу, полноразмерным антителом, например антителом IgG1, антителом IgG2a или другим классом или изотипом антитела, как определено в данном документе.
Таблица гуманизированных последовательностей 7C2 анти-HER2 антитела
Антитела к MUC16
В некоторых вариантах осуществления, КАЛС (ADC) таблиц 3А и 3В содержат антитела к MUC16.
В некоторых вариантах осуществления, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело к MUC16, содержащее по меньшей мере одну, две, три, четыре, пять или шесть HVR выбранных из: a) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 35; b) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 36 c) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 37; d) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 32; e) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 33; и f) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 34.
В одном аспекте, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело, которое содержит по меньшей мере одну, по меньшей мере две или все три последовательности HVR VH, выбранные из: a) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 35; b) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 36; и c) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 37. В дополнительном варианте осуществления, антитело содержит: a) HVR-H1, содержащую аминокислотную последовательность SEQ ID NO: 35; b) HVR-H2, содержащую аминокислотную последовательность SEQ ID NO: 36; и c) HVR-H3, содержащую аминокислотную последовательность SEQ ID NO: 37.
В другом аспекте, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело, которое содержит по меньшей мере одну, по меньшей мере две или все три последовательности HVR VL, выбранные из: a) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 32; b) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 33; и c) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 34. В одном варианте осуществления, антитело содержит: a) HVR-L1, содержащую аминокислотную последовательность SEQ ID NO: 32; b) HVR-L2, содержащую аминокислотную последовательность SEQ ID NO: 33; и c) HVR-L3, содержащую аминокислотную последовательность SEQ ID NO: 34.
В другом аспекте, конъюгат антитело-лекарственное средство по изобретению содержит антитело, содержащее: a) домен VH, содержащий по меньшей мере одну, по меньшей мере две, или все три последовательности HVR VH, выбранные из: (i) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 35, (ii) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 36, и (iii) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 37; и b) домен VL, содержащий по меньшей мере одну, по меньшей мере две, или все три последовательности HVR VL, выбранные из: (i) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 32, (ii) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 33, и c) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 34.
В другом аспекте, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело, которое содержит: a) HVR-H1, содержащую аминокислотную последовательность SEQ ID NO: 35; b) HVR-H2, содержащую аминокислотную последовательность SEQ ID NO: 36; c) HVR-H3, содержащую аминокислотную последовательность SEQ ID NO: 37; d) HVR-L1, содержащую аминокислотную последовательность SEQ ID NO: 32; e) HVR-L2, содержащую аминокислотную последовательность SEQ ID NO: 33; и f) HVR-L3, содержащую аминокислотную последовательность SEQ ID NO: 34.
В любом из указанных выше вариантов осуществления изобретения, антитело к MUC16 конъюгата антитело-лекарственное средство является гуманизированным. В одном из вариантов осуществления, антитело к MUC16 содержит HVR, как в любом из указанных выше вариантов осуществления изобретения, и дополнительно содержит акцепторный человеческий каркас, например, каркас человеческого иммуноглобулина или человеческий консенсусный каркас.
В другом аспекте, антитело к MUC16 конъюгата антитело-лекарственное средство содержит последовательность вариабельного домена (VH) тяжелой цепи, имеющую по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, или 100% идентичности последовательности c аминокислотной последовательностью SEQ ID NO: 39. В некоторых вариантах осуществления, последовательность VH, имеющая по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичности с аминокислотной последовательностью SEQ ID NO: 39 содержит замены (например, консервативные замены), вставки или делеции по сравнению с эталонной последовательностью, но антитело к MUC16, содержащее эту последовательность, сохраняет способность связываться с MUC16 человека. В некоторых вариантах осуществления, в общей сложности от 1 до 10 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 39. В некоторых вариантах осуществления, в общей сложности от 1 до 5 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 39. В некоторых вариантах осуществления, замены, вставки или делеции происходят в областях вне HVR (то есть, в FR). Необязательно, антитело к MUC16 содержит последовательность VH SEQ ID NO: 39, включая пост-трансляционные модификации этой последовательности. В конкретном варианте осуществление, VH содержит одну, две или три HVR, выбранные из: а) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 35; b) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 36; c) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 37.
В другом аспекте, предлагается антитело к MUC16 конъюгата антитело-лекарственное средство, причем антитело содержит вариабельный домен легкой цепи (VL), имеющий по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, или 100% идентичности последовательности аминокислотной последовательностью SEQ ID NO: 38. В некоторых вариантах осуществления, последовательность VL, имеющая по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичности с аминокислотной последовательностью SEQ ID NO: 38 содержит замены (например, консервативные замены), вставки или делеции по сравнению с эталонной последовательностью, но антитело к MUC16, содержащее эту последовательность, сохраняет способность связываться с MUC16 человека. В некоторых вариантах осуществления, в общей сложности от 1 до 10 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 38. В некоторых вариантах осуществления, в общей сложности от 1 до 5 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 38. В некоторых вариантах осуществления, замены, вставки или делеции происходят в областях вне HVR (то есть, в FR). Необязательно, антитело к MUC16 содержит последовательность VL SEQ ID NO: 38, включая пост-трансляционные модификации этой последовательности. В конкретном варианте осуществление, VL содержит одну, две или три HVR, выбранные из: а) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 32; b) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 33; c) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 34.
В другом аспекте, предлагается конъюгат антитело-лекарственное средство, содержащий антитело к MUC16, причем антитело содержит VH как в любом из вариантов осуществления изобретения, приведенных выше, и VL как в любом из вариантов осуществления изобретения, приведенных выше.
В одном варианте осуществления, предлагается конъюгат антитело-лекарственное средство, причем антитело содержит последовательности VH и VL в SEQ ID NO: 39 и SEQ ID NO: 38, соответственно, включая пост-трансляционные модификации этих последовательностей.
В дополнительном аспекте, в данном документе предлагается конъюгат антитело-лекарственное средство, содержащий антитела, которые связываются с тем же самым эпитопом, что и антитело к MUC16, предложенное в данном документе. Например, в некоторых вариантах осуществления предлагается иммуноконъюгат, содержащий антитело, которое связывается с тем же эпитопом, что и антитело против MUC16, содержащее последовательность VH SEQ ID NO: 39 и последовательность VL SEQ ID NO: 38, соответственно.
В дополнительном аспекте изобретения, антитело к MUC16 конъюгата антитело-лекарственное средство в соответствии с любым из вышеуказанных вариантов осуществления представляет собой моноклональное антитело, включая человеческое антитело. В одном варианте осуществления, антитело против MUC16 конъюгата антитело-лекарственное средство представляет собой фрагмент антитела, например фрагмент Fv, Fab, Fab', scFv, диатело, или F(ab')2. В другом варианте осуществления, антитело представляет собой, по существу, полноразмерное антитело, например антитело IgG1, антитело IgG2a или другой класс антител или изотип, как определено в данном документе.
Таблица последовательностей антитела к MUC16
Антитела к STEAP-1
В некоторых вариантах осуществления, КАЛС (ADC) таблиц 3А и 3В содержат антитела к STEAP-1.
В некоторых вариантах осуществления, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело к STEAP-1, содержащее по меньшей мере одну, две, три, четыре, пять или шесть HVR выбранных из: a) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 40; b) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 41 c) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 42; d) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 43; e) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 44; и f) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 45.
В одном аспекте, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело, которое содержит по меньшей мере одну, по меньшей мере две или все три последовательности HVR VH, выбранные из: a) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 40; b) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 41; и c) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 42. В дополнительном варианте осуществления, антитело содержит: a) HVR-H1, содержащую аминокислотную последовательность SEQ ID NO: 40; b) HVR-H2, содержащую аминокислотную последовательность SEQ ID NO: 41; и c) HVR-H3, содержащую аминокислотную последовательность SEQ ID NO: 42.
В другом аспекте, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело, которое содержит по меньшей мере одну, по меньшей мере две или все три последовательности HVR VL, выбранные из: a) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 43; b) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 44; и c) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 45. В одном варианте осуществления, антитело содержит: a) HVR-L1, содержащую аминокислотную последовательность SEQ ID NO: 43; b) HVR-L2, содержащую аминокислотную последовательность SEQ ID NO: 44; и c) HVR-L3, содержащую аминокислотную последовательность SEQ ID NO: 45.
В другом аспекте, конъюгат антитело-лекарственное средство по изобретению содержит антитело, содержащее: a) домен VH, содержащий по меньшей мере одну, по меньшей мере две, или все три последовательности HVR VH, выбранные из: i) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 40, ii) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 41, и iii) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 42; и b) домен VL, содержащий по меньшей мере одну, по меньшей мере две, или все три последовательности HVR VL, выбранные из: i) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 43, (ii) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 44, и c) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 45.
В другом аспекте, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело, которое содержит: a) HVR-H1, содержащую аминокислотную последовательность SEQ ID NO: 40; b) HVR-H2, содержащую аминокислотную последовательность SEQ ID NO: 41; c) HVR-H3, содержащую аминокислотную последовательность SEQ ID NO: 42; d) HVR-L1, содержащую аминокислотную последовательность SEQ ID NO: 43; e) HVR-L2, содержащую аминокислотную последовательность SEQ ID NO: 44; и f) HVR-L3, содержащую аминокислотную последовательность SEQ ID NO: 45.
В любом из указанных выше вариантов осуществления изобретения, антитело к STEAP-1 конъюгата антитело-лекарственное средство является гуманизированным. В одном из вариантов осуществления, антитело к STEAP-1 содержит HVR, как в любом из указанных выше вариантов осуществления изобретения, и дополнительно содержит акцепторный человеческий каркас, например, каркас человеческого иммуноглобулина или человеческий консенсусный каркас.
В другом аспекте, антитело к STEAP-1 конъюгата антитело-лекарственное средство содержит последовательность вариабельного домена (VH) тяжелой цепи, имеющую по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, или 100% идентичности последовательности c аминокислотной последовательностью SEQ ID NO: 46. В некоторых вариантах осуществления, последовательность VH, имеющая по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичности с аминокислотной последовательностью SEQ ID NO: 46 содержит замены (например, консервативные замены), вставки или делеции по сравнению с эталонной последовательностью, но антитело к STEAP-1, содержащее эту последовательность, сохраняет способность связываться с STEAP-1 человека. В некоторых вариантах осуществления, в общей сложности от 1 до 10 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 46. В некоторых вариантах осуществления, в общей сложности от 1 до 5 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 46. В некоторых вариантах осуществления, замены, вставки или делеции происходят в областях вне HVR (то есть, в FR). Необязательно, антитело к STEAP-1 содержит последовательность VH SEQ ID NO: 46, включая пост-трансляционные модификации этой последовательности. В конкретном варианте осуществление, VH содержит одну, две или три HVR, выбранные из: а) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 40; b) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 41; c) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 42.
В другом аспекте, предлагается антитело к STEAP-1 конъюгата антитело-лекарственное средство, причем антитело содержит вариабельный домен легкой цепи (VL), имеющий по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, или 100% идентичности последовательности с аминокислотной последовательностью SEQ ID NO: 47. В некоторых вариантах осуществления, последовательность VL, имеющая по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичности с аминокислотной последовательностью SEQ ID NO: 47 содержит замены (например, консервативные замены), вставки или делеции по сравнению с эталонной последовательностью, но антитело к STEAP-1, содержащее эту последовательность, сохраняет способность связываться с STEAP-1 человека. В некоторых вариантах осуществления, в общей сложности от 1 до 10 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 47. В некоторых вариантах осуществления, в общей сложности от 1 до 5 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 47. В некоторых вариантах осуществления, замены, вставки или делеции происходят в областях вне HVR (то есть, в FR). Необязательно, антитело к STEAP-1 содержит последовательность VL SEQ ID NO: 47, включая пост-трансляционные модификации этой последовательности. В конкретном варианте осуществление, VL содержит одну, две или три HVR, выбранные из: а) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 43; b) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 44; c) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 45.
В другом аспекте, предлагается конъюгат антитело-лекарственное средство, содержащий антитело к STEAP-1, причем антитело содержит VH как в любом из вариантов осуществления изобретения, приведенных выше, и VL как в любом из вариантов осуществления изобретения, приведенных выше.
В одном варианте осуществления, предлагается конъюгат антитело-лекарственное средство, причем антитело содержит последовательности VH и VL в SEQ ID NO: 46 и SEQ ID NO: 47, соответственно, включая пост-трансляционные модификации этих последовательностей.
В дополнительном аспекте, в данном документе предлагается конъюгат антитело-лекарственное средство, содержащий антитела, которые связываются с тем же самым эпитопом, что и антитело к STEAP-1, предложенное в данном документе. Например, в некоторых вариантах осуществления предлагается иммуноконъюгат, содержащий антитело, которое связывается с тем же эпитопом, что и антитело против STEAP-1, содержащее последовательность VH SEQ ID NO: 46 и последовательность VL SEQ ID NO: 47, соответственно.
В дополнительном аспекте изобретения, антитело к STEAP-1 конъюгата антитело-лекарственное средство в соответствии с любым из вышеуказанных вариантов осуществления представляет собой моноклональное антитело, включая человеческое антитело. В одном варианте осуществления, антитело против STEAP-1 конъюгата антитело-лекарственное средство представляет собой фрагмент антитела, например фрагмент Fv, Fab, Fab', scFv, диатело, или F(ab')2. В другом варианте осуществления, антитело представляет собой, по существу, полноразмерное антитело, например антитело IgG1, антитело IgG2a или другой класс антител или изотип, как определено в данном документе.
Таблица последовательностей антитела к STEAP
Антитела к NaPi2b
В некоторых вариантах осуществления, КАЛС (ADC) таблиц 3А и 3В содержат антитела к NaPi2b.
В некоторых вариантах осуществления, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело к NaPi2b, содержащее по меньшей мере одну, две, три, четыре, пять или шесть HVR выбранных из: a) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 48; b) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 49 c) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 50; d) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 51; e) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 52; и f) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 53.
В одном аспекте, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело, которое содержит по меньшей мере одну, по меньшей мере две или все три последовательности HVR VH, выбранные из: a) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 48; b) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 49; и c) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 50. В дополнительном варианте осуществления, антитело содержит: a) HVR-H1, содержащую аминокислотную последовательность SEQ ID NO: 48; b) HVR-H2, содержащую аминокислотную последовательность SEQ ID NO: 49; и c) HVR-H3, содержащую аминокислотную последовательность SEQ ID NO: 50.
В другом аспекте, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело, которое содержит по меньшей мере одну, по меньшей мере две или все три последовательности HVR VL, выбранные из: a) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 51; b) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 52; и c) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 53. В одном варианте осуществления, антитело содержит: a) HVR-L1, содержащую аминокислотную последовательность SEQ ID NO: 51; b) HVR-L2, содержащую аминокислотную последовательность SEQ ID NO: 52; и c) HVR-L3, содержащую аминокислотную последовательность SEQ ID NO: 53.
В другом аспекте, конъюгат антитело-лекарственное средство по изобретению содержит антитело, содержащее: a) домен VH, содержащий по меньшей мере одну, по меньшей мере две, или все три последовательности HVR VH, выбранные из: (i) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 48, (ii) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 49, и (iii) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 50; и b) домен VL, содержащий по меньшей мере одну, по меньшей мере две, или все три последовательности HVR VL, выбранные из: (i) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 51, (ii) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 52, и c) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 53.
В другом аспекте, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело, которое содержит: a) HVR-H1, содержащую аминокислотную последовательность SEQ ID NO: 48; b) HVR-H2, содержащую аминокислотную последовательность SEQ ID NO: 49; c) HVR-H3, содержащую аминокислотную последовательность SEQ ID NO: 50; d) HVR-L1, содержащую аминокислотную последовательность SEQ ID NO: 51; e) HVR-L2, содержащую аминокислотную последовательность SEQ ID NO: 52; и f) HVR-L3, содержащую аминокислотную последовательность SEQ ID NO: 53.
В любом из указанных выше вариантов осуществления изобретения, антитело к NaPi2b конъюгата антитело-лекарственное средство является гуманизированным. В одном из вариантов осуществления, антитело к NaPi2b содержит HVR, как в любом из указанных выше вариантов осуществления изобретения, и дополнительно содержит акцепторный человеческий каркас, например, каркас человеческого иммуноглобулина или человеческий консенсусный каркас.
В другом аспекте, антитело к NaPi2b конъюгата антитело-лекарственное средство содержит последовательность вариабельного домена (VH) тяжелой цепи, имеющую по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, или 100% идентичности последовательности c аминокислотной последовательностью SEQ ID NO: 54. В некоторых вариантах осуществления, последовательность VH, имеющая по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичности с аминокислотной последовательностью SEQ ID NO: 54 содержит замены (например, консервативные замены), вставки или делеции по сравнению с эталонной последовательностью, но антитело к NaPi2b, содержащее эту последовательность, сохраняет способность связываться с NaPi2b человека. В некоторых вариантах осуществления, в общей сложности от 1 до 10 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 54. В некоторых вариантах осуществления, в общей сложности от 1 до 5 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 54. В некоторых вариантах осуществления, замены, вставки или делеции происходят в областях вне HVR (то есть, в FR). Необязательно, антитело к NaPi2b содержит последовательность VH SEQ ID NO: 54, включая пост-трансляционные модификации этой последовательности. В конкретном варианте осуществление, VH содержит одну, две или три HVR, выбранные из: а) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 48; b) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 49; c) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 50.
В другом аспекте, предлагается антитело к NaPi2b конъюгата антитело-лекарственное средство, причем антитело содержит вариабельный домен легкой цепи (VL), имеющий по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, или 100% идентичности последовательности с аминокислотной последовательностью SEQ ID NO: 55. В некоторых вариантах осуществления, последовательность VL, имеющая по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичности с аминокислотной последовательностью SEQ ID NO: 55 содержит замены (например, консервативные замены), вставки или делеции по сравнению с эталонной последовательностью, но антитело к NaPi2b, содержащее эту последовательность, сохраняет способность связываться с NaPi2b человека. В некоторых вариантах осуществления, в общей сложности от 1 до 10 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 55. В некоторых вариантах осуществления, в общей сложности от 1 до 5 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 55. В некоторых вариантах осуществления, замены, вставки или делеции происходят в областях вне HVR (то есть, в FR). Необязательно, антитело к NaPi2b содержит последовательность VL SEQ ID NO: 55, включая пост-трансляционные модификации этой последовательности. В конкретном варианте осуществление, VL содержит одну, две или три HVR, выбранные из: а) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 51; b) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 52; c) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 53.
В другом аспекте, предлагается конъюгат антитело-лекарственное средство, содержащий антитело к NaPi2b, причем антитело содержит VH как в любом из вариантов осуществления изобретения, приведенных выше, и VL как в любом из вариантов осуществления изобретения, приведенных выше.
В одном варианте осуществления, предлагается конъюгат антитело-лекарственное средство, причем антитело содержит последовательности VH и VL в SEQ ID NO: 54 и SEQ ID NO: 55, соответственно, включая пост-трансляционные модификации этих последовательностей.
В дополнительном аспекте, в данном документе предлагается конъюгат антитело-лекарственное средство, содержащий антитела, которые связываются с тем же самым эпитопом, что и антитело к NaPi2b, предложенное в данном документе. Например, в некоторых вариантах осуществления предлагается иммуноконъюгат, содержащий антитело, которое связывается с тем же эпитопом, что и антитело против NaPi2b, содержащее последовательность VH SEQ ID NO: 54 и последовательность VL SEQ ID NO: 55, соответственно.
В дополнительном аспекте изобретения, антитело к NaPi2b конъюгата антитело-лекарственное средство в соответствии с любым из вышеуказанных вариантов осуществления представляет собой моноклональное антитело, включая человеческое антитело. В одном варианте осуществления, антитело против NaPi2b конъюгата антитело-лекарственное средство представляет собой фрагмент антитела, например фрагмент Fv, Fab, Fab', scFv, диатело, или F(ab')2. В другом варианте осуществления, антитело представляет собой, по существу, полноразмерное антитело, например антитело IgG1, антитело IgG2a или другой класс антител или изотип, как определено в данном документе.
Таблица последовательностей антитела к NaPi2b
Антитела к CD79b
В некоторых вариантах осуществления, КАЛС (ADC) таблиц 3А и 3В содержат антитела к CD79b.
В некоторых вариантах осуществления, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело к CD79b, содержащее по меньшей мере одну, две, три, четыре, пять или шесть HVR выбранных из: a) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 58; b) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 59 c) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 60; d) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 61; e) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 62; и f) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 63.
В одном аспекте, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело, которое содержит по меньшей мере одну, две или все три последовательности HVR VH, выбранные из: a) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 58; b) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 59; и c) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 60. В дополнительном варианте осуществления, антитело содержит: a) HVR-H1, содержащую аминокислотную последовательность SEQ ID NO: 58; b) HVR-H2, содержащую аминокислотную последовательность SEQ ID NO: 59; и c) HVR-H3, содержащую аминокислотную последовательность SEQ ID NO: 60.
В другом аспекте, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело, которое содержит по меньшей мере одну, по меньшей мере две или все три последовательности HVR VL, выбранные из: a) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 61; b) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 62; и c) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 63. В одном варианте осуществления, антитело содержит: a) HVR-L1, содержащую аминокислотную последовательность SEQ ID NO: 61; b) HVR-L2, содержащую аминокислотную последовательность SEQ ID NO: 62; и c) HVR-L3, содержащую аминокислотную последовательность SEQ ID NO: 63.
В другом аспекте, конъюгат антитело-лекарственное средство по изобретению содержит антитело, содержащее: a) домен VH, содержащий по меньшей мере одну, по меньшей мере две, или все три последовательности HVR VH, выбранные из: (i) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 58, (ii) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 59, и (iii) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 60; и b) домен VL, содержащий по меньшей мере одну, по меньшей мере две, или все три последовательности HVR VL, выбранные из: (i) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 61, (ii) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 62, и c) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 63.
В другом аспекте, согласно настоящему изобретению предложено конъюгат антитело-лекарственное средство, содержащий антитело, которое содержит: a) HVR-H1, содержащую аминокислотную последовательность SEQ ID NO: 58; b) HVR-H2, содержащую аминокислотную последовательность SEQ ID NO: 59; c) HVR-H3, содержащую аминокислотную последовательность SEQ ID NO: 60; d) HVR-L1, содержащую аминокислотную последовательность SEQ ID NO: 61; e) HVR-L2, содержащую аминокислотную последовательность SEQ ID NO: 62; и f) HVR-L3, содержащую аминокислотную последовательность SEQ ID NO: 63.
В любом из указанных выше вариантов осуществления изобретения, антитело к CD79b конъюгата антитело-лекарственное средство является гуманизированным. В одном из вариантов осуществления, антитело к CD79b содержит HVR, как в любом из указанных выше вариантов осуществления изобретения, и дополнительно содержит акцепторный человеческий каркас, например, каркас человеческого иммуноглобулина или человеческий консенсусный каркас.
В другом аспекте, антитело к CD79b конъюгата антитело-лекарственное средство содержит последовательность вариабельного домена (VH) тяжелой цепи, имеющую по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, или 100% идентичности последовательности c аминокислотной последовательностью SEQ ID NO: 56. В некоторых вариантах осуществления, последовательность VH, имеющая по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичности с аминокислотной последовательностью SEQ ID NO: 56 содержит замены (например, консервативные замены), вставки или делеции по сравнению с эталонной последовательностью, но антитело к CD79b, содержащее эту последовательность, сохраняет способность связываться с CD79b человека. В некоторых вариантах осуществления, в общей сложности от 1 до 10 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 56. В некоторых вариантах осуществления, в общей сложности от 1 до 5 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 56. В некоторых вариантах осуществления, замены, вставки или делеции происходят в областях вне HVR (то есть, в FR). Необязательно, антитело к CD79b содержит последовательность VH SEQ ID NO: 8, включая пост-трансляционные модификации этой последовательности. В конкретном варианте осуществление, VH содержит одну, две или три HVR, выбранные из: а) HVR-H1, содержащей аминокислотную последовательность SEQ ID NO: 58; b) HVR-H2, содержащей аминокислотную последовательность SEQ ID NO: 59; c) HVR-H3, содержащей аминокислотную последовательность SEQ ID NO: 60.
В другом аспекте, предлагается антитело к CD79b конъюгата антитело-лекарственное средство, причем антитело содержит вариабельный домен легкой цепи (VL), имеющий по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, или 100% идентичности последовательности с аминокислотной последовательностью SEQ ID NO: 57. В некоторых вариантах осуществления, последовательность VL, имеющая по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичности с аминокислотной последовательностью SEQ ID NO: 57 содержит замены (например, консервативные замены), вставки или делеции по сравнению с эталонной последовательностью, но антитело к Ly6E, содержащее эту последовательность, сохраняет способность связываться с CD79b человека. В некоторых вариантах осуществления, в общей сложности от 1 до 10 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 57. В некоторых вариантах осуществления, в общей сложности от 1 до 5 аминокислот были замещены, вставлены и/или удалены в SEQ ID NO: 57. В некоторых вариантах осуществления, замены, вставки или делеции происходят в областях вне HVR (то есть, в FR). Необязательно, антитело к CD79b содержит последовательность VL SEQ ID NO: 57, включая пост-трансляционные модификации этой последовательности. В конкретном варианте осуществление, VL содержит одну, две или три HVR, выбранные из: а) HVR-L1, содержащей аминокислотную последовательность SEQ ID NO: 61; b) HVR-L2, содержащей аминокислотную последовательность SEQ ID NO: 62; c) HVR-L3, содержащей аминокислотную последовательность SEQ ID NO: 63.
В другом аспекте, предлагается конъюгат антитело-лекарственное средство, содержащий антитело к CD79b, причем антитело содержит VH как в любом из вариантов осуществления изобретения, приведенных выше, и VL как в любом из вариантов осуществления изобретения, приведенных выше.
В одном варианте осуществления, предлагается конъюгат антитело-лекарственное средство, причем антитело содержит последовательности VH и VL в SEQ ID NO: 56 и SEQ ID NO: 57, соответственно, включая пост-трансляционные модификации этих последовательностей.
В дополнительном аспекте, в данном документе предлагается конъюгат антитело-лекарственное средство, содержащий антитела, которые связываются с тем же самым эпитопом, что и антитело к CD79b, предложенное в данном документе. Например, в некоторых вариантах осуществления предлагается иммуноконъюгат, содержащий антитело, которое связывается с тем же эпитопом, что и антитело против CD79b, содержащее последовательность VH SEQ ID NO: 56 и последовательность VL SEQ ID NO: 57, соответственно.
В дополнительном аспекте изобретения, антитело к CD79b конъюгата антитело-лекарственное средство в соответствии с любым из вышеуказанных вариантов осуществления представляет собой моноклональное антитело, включая человеческое антитело. В одном варианте осуществления, антитело против CD79b конъюгата антитело-лекарственное средство представляет собой фрагмент антитела, например фрагмент Fv, Fab, Fab', scFv, диатело, или F(ab')2. В другом варианте осуществления, антитело представляет собой, по существу, полноразмерное антитело, например антитело IgG1, антитело IgG2a или другой класс антител или изотип, как определено в данном документе.
Таблица последовательностей антитела к CD79b
Аффинность антител
В определенных вариантах осуществления, предложенное в данном документе антитело характеризуется константой диссоциации, составляющей (Kд) ≤1 мкM, ≤100 нМ, ≤50 нМ, ≤10 нМ, ≤ 5 нМ, ≤1 нМ, ≤0,1 нМ, ≤0,01 нМ или ≤0,001 нМ и, необязательно, ≥10-13 M (например, 10-8 M или меньше, например, от 10-8 M до 10-13 M, например, от 10-9 M до 10-13 M).
В одном варианте осуществления, Kд измеряют методом анализа связывания радиоактивно меченого антигена (РИА), выполненного с Fab-версией представляющего интерес антитела и его антигеном, как описано в следующем анализе. Аффинность связывания Fab в растворе в отношении антигена измеряют, уравновешивая Fab минимальной концентрацией (125I)-меченого антигена в присутствии ряда титров немеченого антигена, затем иммобилизируя связанный антиген на покрытой анти-Fab антителом плашке (смотрите, например, Chen et al., J. Mol. Biol. 293:865-881(1999)). Чтобы установить условия для анализа, многолуночные плашки MICROTITER® (Thermo Scientific) покрывают на ночь 5 мкг/мл захватывающего анти-Fab антитела (Cappel Labs) в 50 мM карбонате натрия (pH 9,6), а после этого блокируют 2% (м/об) бычьим сывороточным альбумином в ФСБ (PBS) в течение от двух до пяти часов при комнатной температуре (около 23°C). В неадсорбирующей плашке (Nunc №269620) смешивают 100 пM или 26 пM [125I]-антигена с серийными разведениями представляющего интерес Fab (например, в соответствии с оценкой анти-VEGF антитела Fab-12 в Presta et al., Cancer Res. 57:4593-4599 (1997)). Затем представляющий интерес Fab инкубируют в течение ночи; при этом инкубация может длиться более долгий период (например, около 65 часов), чтобы гарантировать, что равновесие достигнуто. После этого смеси переносят на плашку для захвата для инкубации при комнатной температуре (например, в течение одного часа). Затем раствор удаляют, а плашку промывают восемь раз 0,1% полисорбатом 20 (TWEEN-20®) в ФСБ (PBS). Когда плашки высыхают, добавляют 150 мкл/лунка сцинтиллятора (MICROSCINT-20 TM; Packard), а плашки считывают на гамма-счетчике TOPCOUNT TM (Packard) в течение десяти минут. Концентрации каждого Fab, которые дают результаты, составляющие 20% или меньше от максимального связывания, отбирают для применения в конкурентном анализе связывания.
В соответствии с другим вариантом осуществления, Kд измеряют методом поверхностного плазмонного резонанса BIACORE®. Например, анализ с применением BIACORE®-2000 или BIACORE®-3000 (BIAcore, Inc., Piscataway, NJ) проводят при 25°C с иммобилизованными антигенными чипами CM5 при около 10 единицах ответа (ЕО). Кратко, биосенсорные чипы с карбоксиметилированным декстраном (CM5, BIACORE, Inc.) активируют N-этил-N'-(3-диметиламинопропил)-карбодиимид гидрохлоридом (ЭДК) и N-гидроксисукцинимидом (NHS) в соответствии с инструкциями поставщика. Антиген разводят 10 мM ацетатом натрия, pH 4,8, до 5 мкг/мл (около 0,2 мкM) перед внесением при скорости потока 5 мкл/минута для достижения около 10 единиц ответа (ЕО) сопряженного белка. После внесения антигена, вносят 1 М этаноламина, чтобы блокировать непрореагировавшие группы. Для кинетических измерений двукратные серийные разведения Fab (от 0,78 нM до 500 нM) вносят в ФСБ (PBS) с 0,05% сурфактантом полисорбатом 20 (TWEEN-20TM) (PBSТ) при 25°C при скорости потока приблизительно 25 мкл/мин. Скорости ассоциации (kасс) и скорости диссоциации (kдисс) рассчитывают, применяя простую взаимно однозначную модель связывания Лэнгмюра (программное обеспечение для оценки BIACORE® версия 3.2), путем одновременной подгонки сенсограмм ассоциации и диссоциации. Равновесную константу диссоциации (Kд) рассчитывают как соотношение kасс/kдисс. См., например, Chen et al., J. Mol. Biol. 293:865-881 (1999). Если скорость ассоциации превышает 106 M-1с-1 согласно данным вышеописанного поверхностного плазмонного резонанса, то скорость ассоциации можно определить при помощи метода гашения флуоресценции, в котором измеряют повышение или снижение интенсивности флуоресценции (возбуждение=295 нм; излучение=340 нм, 16 нм полоса пропускания) при 25°C для 20 нM антитела к антигену (Fab-формы) в ФСБ (PBS), pH 7,2, в присутствии увеличивающихся концентраций антигена, измеряемое при помощи спектрометра, такого как спектрофотометр с возможностью остановки потока (Aviv Instruments) или спектрофотометр серии 8000 SLM-AMINCO TM (ThermoSpectronic) с кюветой с перемешиванием.
Фрагменты антител
В определенных вариантах осуществления, предложенное в данном документе антитело представляет собой фрагмент антитела. Фрагменты антител включают, но не ограничиваются лишь этими: фрагменты Fab, Fab', Fab'-SH, F(ab')2, Fv и scFv, а также другие фрагменты, описанные ниже. Обзор некоторых фрагментов антител смотрите в Hudson et al. Nat. Med. 9:129-134 (2003). Обзор фрагментов scFv смотрите, например, в Pluckthün, в The Pharmacology of Monoclonal Antibodies, vol. 113, Rosenburg and Moore eds., (Springer-Verlag, New York), pp. 269-315 (1994); также смотрите WO 93/16185; и патенты США № 5571894 и 5587458. Обсуждение фрагментов Fab и F(ab')2, содержащих остатки эпитопа связывания рецептора реутилизации и имеющих увеличенное in vivo время полужизни, смотрите в патенте США № 5869046.
Диатела представляют собой фрагменты антител с двумя антигенсвязывающими участками, которые могут быть бивалентными или биспецифическими. Смотрите, например, EP 404,097; WO 1993/01161; Hudson et al., Nat. Med. 9:129-134 (2003); и Hollinger et al., Proc. Natl. Acad. Sci. USA 90: 6444-6448 (1993). Триатела и тетратела также описаны в Hudson et al., Nat. Med. 9:129-134 (2003).
Однодоменные антитела представляют собой фрагменты антител, содержащие весь или часть вариабельного домена тяжелой цепи, или весь или часть вариабельного домена легкой цепи антитела. В определенных вариантах осуществления, однодоменное антитело является человеческим однодоменным антителом (Domantis, Inc., Waltham, MA; смотрите, например, патент США № 6248516 B1).
Фрагменты антител можно получать различными методами, включая, но не ограничиваясь лишь этими: протеолитическое расщепление интактного антитела, а также получение рекомбинантных клеток-хозяев (например, E. coli или фага), как описано в данном документе.
Химерные и гуманизированные антитела
В определенных вариантах осуществления, предложенное в данном документе антитело представляет собой химерное антитело. Некоторые химерные антитела описаны, например, в патенте США № 4816567; и Morrison et al., Proc. Natl. Acad. Sci. USA, 81:6851-6855 (1984)). В одном примере, химерное антитело содержит нечеловеческую вариабельную область (например, вариабельную область, полученную от мыши, крысы, хомяка, кролика или низшего примата, такого как обезьяна) и человеческую константную область. В дополнительном примере, химерное антитело является антителом с «переключенным классом», у которого класс или подкласс был изменен по сравнению с исходным антителом. Химерные антитела включают их антигенсвязывающие фрагменты.
В определенных вариантах осуществления, химерное антитело является гуманизированным антителом. Как правило, нечеловеческое антитело гуманизируют для снижения иммуногенности для человека, сохраняя при этом специфичность и аффинность исходного нечеловеческого антитела. В целом, как правило, гуманизированное антитело содержит один или больше вариабельных доменов, в которых HVR, например, CDR (или их часть), получены из нечеловеческого антитела, а FR (или их часть) получены из последовательностей человеческого антитела. Необязательно, гуманизированное антитело содержит также по меньшей мере часть человеческой константной области. В некоторых вариантах осуществления, некоторые остатки FR в гуманизированном антителе замещены соответствующими остатками из нечеловеческого антитела (например, антитела, из которого получены остатки HVR), например, для восстановления или улучшения специфичности или аффинности антитела.
Гуманизированные антитела и способы их получения описаны, например, в Almagro and Fransson, Front. Biosci. 13:1619-1633 (2008), и дополнительно описаны, например, в Riechmann et al., Nature 332:323-329 (1988); Queen et al., Proc. Nat'l Acad. Sci. USA 86:10029-10033 (1989); патентах США № 5821337, 7527791, 6982321 и 7087409; Kashmiri et al., Methods 36:25-34 (2005) (описывается прививание определяющей специфичность области (SDR (a-CDR))); Padlan, Mol. Immunol. 28:489-498 (1991) (описывается «изменение поверхности»); Dall'Acqua et al., Methods 36:43-60 (2005) (описывается «перетасовка FR»); и Osbourn et al., Methods 36:61-68 (2005) и Klimka et al., Br. J. Cancer, 83:252-260 (2000) (описывается подход «управляемая селекция» для перетасовки FR).
Человеческие каркасные области, которые можно применять для гуманизации, включают, но не ограничиваются лишь этими: каркасные области, выбранные методом «наилучшего соответствия» (смотрите, например, Sims et al. J. Immunol. 151:2296 (1993)); каркасные области, полученные из консенсусной последовательности человеческих антител конкретной подгруппы вариабельных областей легкой или тяжелой цепей (смотрите, например, Carter et al. Proc. Natl. Acad. Sci. USA, 89:4285 (1992); и Presta et al. J. Immunol., 151:2623 (1993)); человеческие зрелые (соматически мутированные) каркасные области или каркасные области человеческой зародышевой линии (смотрите, например, Almagro and Fransson, Front. Biosci. 13:1619-1633 (2008)); и каркасные области, полученные путем скрининга библиотек FR (смотрите, например, Baca et al., J. Biol. Chem. 272:10678-10684 (1997) и Rosok et al., J. Biol. Chem. 271:22611-22618 (1996)).
Человеческие антитела
В определенных вариантах осуществления, предложенное в данном документе антитело представляет собой человеческое антитело. Человеческие антитела можно получать различными известными в данной области техники методами. Общее описание человеческих антител приведено в van Dijk and van de Winkel, Curr. Opin. Pharmacol. 5: 368-74 (2001) и Lonberg, Curr. Opin. Immunol. 20:450-459 (2008).
Человеческие антитела можно получать путем введения антигена трансгенному животному, которое было модифицировано для выработки интактных человеческих антител или интактных антител с человеческими вариабельными областями в ответ на стимуляцию антигеном. Такие животные, как правило, содержат все или часть локусов человеческого иммуноглобулина, которые замещают эндогенные локусы иммуноглобулина или которые находятся во внехромосомном пространстве или случайным образом интегрированы в хромосомы животного. У таких трансгенных мышей эндогенные локусы иммуноглобулина в целом, как правило, инактивированы. Обзор способов получения человеческих антител от трансгенных животных смотрите в Lonberg, Nat. Biotech. 23:1117-1125 (2005). Также смотрите, например, патенты США № 6075181 и 6150584, описывающие технологию XENOMOUSETM; патент США № 5770429, описывающий технологию HUMAB®; патент США № 7041870, описывающий технологию K-M MOUSE®, и заявку на патент США № US 2007/0061900, описывающую технологию VelociMouse®). Человеческие вариабельные области из интактных анитител, вырабатываемые такими животными, можно дополнительно модифицировать, например, комбинируя с разными человеческими константными областями.
Человеческие антитела также можно получать способами на основе гибридом. Были описаны клеточные линии человеческой миеломы и мышино-человеческой гетеромиеломы для получения человеческих моноклональных антител. (Смотрите, например, Kozbor J. Immunol., 133: 3001 (1984); Brodeur et al., Monoclonal Antibody Production Techniques and Applications, pp. 51-63 (Marcel Dekker, Inc., New York, 1987); и Boerner et al., J. Immunol., 147: 86 (1991).) Человеческие антитела, полученные с использованием технологии человеческой В-клеточной гибридомы, описаны в Li et al., Proc. Natl. Acad. Sci. USA, 103:3557-3562 (2006). Дополнительные способы включают описанные, например, в патенте США № 7189826 (описывающем получение моноклональных человеческих антител IgM из гибридомных клеточных линий) и Ni, Xiandai Mianyixue, 26(4):265-268 (2006) (описывающей человек-человеческие гибридомы). Технология человеческих гибридом (технология триом) также описана в Vollmers and Brandlein, Histology and Histopathology, 20(3):927-937 (2005) и Vollmers and Brandlein, Methods and Findings in Experimental and Clinical Pharmacology, 27(3):185-91 (2005).
Человеческие антитела также можно получать путем выделения последовательностей вариабельного домена Fv-клона из библиотек фагового дисплея человеческого происхождения. Затем такие последовательности вариабельного домена можно комбинировать с желаемым человеческим константным доменом. Методы отбора человеческих антител из библиотек антител описаны ниже.
Полученные из библиотек антитела
Антитела согласно изобретению можно выделять путем скрининга комбинаторных библиотек для антител с необходимой активностью или необходимыми активностями. Например, в данной области техники известно множество способов создания библиотек фагового дисплея и скрининга таких библиотек в отношении антител, обладающих необходимыми характеристиками связывания. Обзор таких способов приведен, например, в Hoogenboom et al. in Methods in Molecular Biology 178:1-37 (O'Brien et al., ed., Human Press, Totowa, NJ, 2001) и дополнительно описан, например, в McCafferty et al., Nature 348:552-554; Clackson et al., Nature 352: 624-628 (1991); Marks et al., J. Mol. Biol. 222: 581-597 (1992); Marks and Bradbury, in Methods in Molecular Biology 248:161-175 (Lo, ed., Human Press, Totowa, NJ, 2003); Sidhu et al., J. Mol. Biol. 338(2): 299-310 (2004); Lee et al., J. Mol. Biol. 340(5): 1073-1093 (2004); Fellouse, Proc. Natl. Acad. Sci. USA 101(34): 12467-12472 (2004); и Lee et al., J. Immunol. Methods 284(1-2): 119-132(2004).
В некоторых способах фагового дисплея наборы генов VH и VL отдельно клонируют при помощи полимеразной цепной реакции (ПЦР) и повторно комбинируют случайным образом в фаговых библиотеках, которые затем можно исследовать в отношении антигенсвязывающего фага, как описано в Winter et al., Ann. Rev. Immunol., 12: 433-455 (1994). Фаг, как правило, представляет фрагменты антител, как одноцепочечные фрагменты Fv (scFv), так и фрагменты Fab. Библиотеки из иммунизированных источников обеспечивают высокоаффинные антитела к иммуногену, не требуя конструирования гибридом. В альтернативном варианте, можно клонировать первичный набор (например, из человека), чтобы обеспечить единый источник антител к широкому диапазону чужих, а также своих антигенов без какой-либо иммунизации, как описано в Griffiths et al., EMBO J, 12: 725-734 (1993). И наконец, первичные библиотеки также можно создавать синтетически, клонируя неперестроенные V-генные сегменты из стволовых клеток и используя ПЦР-праймеры, содержащие случайную последовательность, для кодирования высоковариабельных областей CDR3 и для осуществления перестройки in vitro, как описано Hoogenboom and Winter, J. Mol. Biol., 227: 381-388 (1992). Патентные публикации, описывающие фаговые библиотеки человеческих антител, включают, например: патент США № 5750373 и публикации патентов США № 2005/0079574, 2005/0119455, 2005/0266000, 2007/0117126, 2007/0160598, 2007/0237764, 2007/0292936 и 2009/0002360.
Антитела или фрагменты антител, выделенные из библиотек человеческих антител, считаются в данном документе человеческими антителами или фрагментами человеческих антител.
Мультиспецифические антитела
В некоторых вариантах осуществления, антитело является мультиспецифическим антителом, например, биспецифическим антителом. Мультиспецифические антитела представляют собой моноклональные антитела, которые обладают специфичностью связывания в отношении по меньшей мере двух разных участков. В некоторых вариантах осуществления, биспецифические антитела могут связываться с двумя разными эпитопами одной и той же цели. Биспецифические антитела могут также быть применены для переноса цитотоксических средств к клеткам, который экспрессируют мишень. Биспецифические антитела могут быть приготовлены как полноразмерные антитела или фрагменты антитела.
Методы получения мультиспецифических антител включают, но не ограничиваются лишь этими: рекомбинантную коэкспрессию двух пар «тяжелой цепи-легкой цепи» иммуноглобулина, имеющих различные специфичности (см. Milstein and Cuello, Nature 305: 537 (1983)), WO 93/08829, and Traunecker et al., EMBO J. 10: 3655 (1991)), и принцип «выступ-во-впадину» (см., например, патент США № 5731168). Упоминаемый в данном документе термин технология «выступ-во-впадину» или «KnH» относится к технологии управления спариванием двух полипептидов in vitro или in vivo путем внесения выпуклости (выступа) в один полипептид и углубления (впадины) в другой полипептид на поверхности контакта, где происходит их взаимодействие. Например, KnH вносили в поверхность связывания Fc:Fc, поверхности контакта CL:CH1 или поверхности контакта VH/VL антител (например, US 2011/0287009, US2007/0178552, WO 96/027011, WO 98/050431, Zhu et al., 1997, Protein Science 6:781-788, and WO2012/106587). В некоторых вариантах осуществления, KnH управляет спариванием двух разных тяжелых цепей во время получения мультиспецифических антител. Например, мультиспецифические антитела, содержащие KnH в Fc-областях, могут дополнительно содержать одиночные вариабельные домены, связанные с каждой Fc-областью, или дополнительно содержать разные вариабельные домены тяжелой цепи, которые спариваются со сходными или разными вариабельными доменами легкой цепи. Технологию KnH также можно применять для спаривания внеклеточных доменов двух разных рецепторов или каких-либо других полипептидных последовательностей, которые содержат разные распознающие мишень последовательности (например, включая аффитела, пептитела и другие продукты гибридные Fc).
Как используется в данном документе, термин «мутация выступа» относится к мутации, которая вносит выпуклость (выступ) в полипептид в области взаимодействия, в которой полипептид взаимодействует с другим полипептидом. В некоторых вариантах осуществления, другой полипептид имеет мутацию с углублением.
Как используется в данном документе, термин «мутация впадины» относится к мутации, которая вносит углубление (впадину) в полипептид в области взаимодействия, в которой полипептид взаимодействует с другим полипептидом. В некоторых вариантах осуществления, другой полипептид имеет мутацию в выступе.
Ниже приводится краткое неограничивающее обсуждение.
«Выпуклостью» называется по меньшей мере одна аминокислотная боковая цепь, которая выступает с поверхности области взаимодействия первого полипептида и, следовательно, может размещаться в компенсирующем углублении смежной поверхности области взаимодействия (т.е. поверхности области взаимодействия второго полипептида) так, чтобы стабилизировать гетеромультимер и тем самым способствовать, например, образованию гетеромультимера но не образованию гомомультимера. Выпуклость может находиться на исходной поверхности области взаимодействия или может быть привнесена синтетически (например, путем изменения нуклеиновой кислоты, кодирующей поверхность области взаимодействия). В некоторых вариантах осуществления, чтобы кодировать выпуклость, изменяют нуклеиновую кислоту, кодирующую поверхность области взаимодействия первого полипептида. Для достижения этого нуклеиновую кислоту, кодирующую по меньшей мере один «исходный» аминокислотный остаток на поверхности области взаимодействия первого полипептида, заменяют нуклеиновой кислотой, кодирующей по меньшей мере один «вносимый» аминокислотный остаток, который имеет больший объем боковой цепи, чем исходный аминокислотный остаток. Понятно, что может быть больше одного исходного и соответствующего вносимого остатка. Объемы боковых цепей разных аминокислотных остатков показаны например в таблице 1 US2011/0287009. Мутация для внесения «выпуклости» может быть названа как «мутация выступа».
В некоторых вариантах осуществления, вносимыми остатками для образования выпуклости являются аминокислотные остатки природного происхождения, которые выбраны из аргинина (R), фенилаланина (F), тирозина (Y) и триптофана (W). В некоторых вариантах осуществления, вносимыми остатками являются триптофан и тирозин. В некоторых вариантах осуществления, исходный остаток для образования выпуклости имеет небольшой объем боковой цепи, например аланин, аспарагин, аспарагиновая кислота, глицин, серин, треонин или валин.
«Углубление» относится по меньшей мере к одной аминокислотной боковой цепи, которая утоплена в поверхность области взаимодействия второго полипептида и, следовательно, она является совместимой с выпуклостью на смежной поверхности области взаимодействия первого полипептида. Углубление может находиться на исходной поверхности области взаимодействия или может быть привнесено синтетически (например, путем изменения нуклеиновой кислоты, кодирующей поверхность области взаимодействия). В некоторых вариантах осуществления, чтобы кодировать углубление, изменяют нуклеиновую кислоту, кодирующую поверхность области взаимодействия второго полипептида. Для достижения этого нуклеиновую кислоту, кодирующую по меньшей мере один «исходный» аминокислотный остаток на поверхности области взаимодействия второго полипептида, заменяют ДНК, кодирующей по меньшей мере один «вносимый» аминокислотный остаток, который имеет меньший объем боковой цепи, чем исходный аминокислотный остаток. Понятно, что может быть больше одного исходного и соответствующего вносимого остатка. В некоторых вариантах осуществления, вносимыми остатками для образования углубления являются аминокислотные остатки природного происхождения, которые выбраны из аланина (А), серина (S), треонина (Т) и валина (V). В некоторых вариантах осуществления, вносимыми остатками являются серин, аланин или треонин. В некоторых вариантах осуществления, исходный остаток для образования углубления имеет большой объем боковой цепи, например тирозин, аргинин, фенилаланин или триптофан. Мутация для внесения «углубления» может быть названа как «мутация впадины».
Выпуклость является «размещаемой» в углублении обозначает то, что пространственное расположение выпуклости и углубления на поверхности области взаимодействия первого полипептида и второго полипептида, соответственно, совпадает, а размеры выпуклости и углубления являются такими, что выпуклость может расположиться в углублении без существенного нарушения нормальной связи на поверхности области взаимодействия первого и второго полипептидов. Так как выпуклости, такие как Tyr, Phe и Trp, как правило, не перпендикулярны оси поверхности области взаимодействия и имеют предпочтительные конформации, выравнивание выпуклости с соответствующим углублением основано на моделировании пары выпуклость/углубление на основании трехмерной структуры, которую получают методами рентгеновской кристаллографии или ядерного магнитного резонанса (ЯМР). Этого можно достичь, используя широко применяемые в данной области техники методы.
В некоторых вариантах осуществления, мутация выпуклости в константной области IgG1 представляет собой T366W (нумерация по ЕС). В некоторых вариантах осуществления, мутация углубления в константной области IgG1 включает одну или несколько мутаций, выбранных из T366S, L368A и Y407V (нумерация по ЕС). В некоторых вариантах осуществления, мутация углубления в константной области IgG1 представляет собой T366S, L368A и Y407V (нумерация по ЕС).
В некоторых вариантах осуществления, мутация выпуклости в константной области IgG4 представляет собой T366W (нумерация по ЕС). В некоторых вариантах осуществления, мутация углубления в константной области IgG4 включает одну или несколько мутаций, выбранных из T366S, L368A и Y407V (нумерация по ЕС). В некоторых вариантах осуществления, мутация углубления в константной области IgG4 представляет собой T366S, L368A и Y407V (нумерация по ЕС).
Мультиспецифические антитела могут быть также получены с помощью метода конструирования с использованием эффекта электростатического взаимодействия для получения Fc-гетеродимерных молекул антител (WO 2009/089004A1); с помощью сшивания двух или больше антител или их фрагментов (см., например, патент США № 4676980 и Brennan et al., Science, 229: 81 (1985)); с помощью лейциновых молний для продукции биспецифических антител (см., например, Kostelny et al., J. Immunol., 148(5):1547-1553 (1992)); с помощью технологии «диатела» для получения биспецифических фрагментов антител (см., например, Hollinger et al., Proc. Natl. Acad. Sci. USA, 90:6444-6448 (1993)); и с использованием одноцепочечных Fv (SFV)-димеров (см., например, Gruber et al., J. Immunol., 152:5368 (1994)); и путем приготовления триспецифичных антител, как описано, например, в Tutt et al. J. Immunol. 147: 60 (1991).
В данный документ также включены сконструированные антитела с тремя или больше функциональными сайтами связывания антигена, включая «антитела Octopus» (см., например, US 2006/0025576A1).
В данном документе антитела или фрагменты антител также могут включать «FAb двойного действия» или «DAF», содержащий антигенсвязывающий сайт, который связывается с мишенью, а также с другим, отличным антигеном (смотрите, например, US 2008/0069820).
Варианты антител
В некоторых вариантах осуществления, предложены варианты аминокислотной последовательности антител, которые предоставлены в настоящем документе. Например, это может быть желательным для улучшения аффинности связывания и/или других биологических свойств антитела. Варианты аминокислотной последовательности антитела могут быть подготовлены с помощью внесения подходящих модификаций в нуклеотидную последовательность, которая кодирует антитело, или с помощью пептидного синтеза. Такие модификации включают, например, делеции, и/или инсерции и/или замены остатков в аминокислотной последовательности антитела. Может быть сделано любое сочетание делеции, вставки и замены, чтобы достичь конечной конструкции, при условии, что конечная конструкция обладает нужными характеристиками, например, связыванием антигена.
Варианты замены, вставки и делеции
В некоторых вариантах осуществления, предлагаются варианты антитела, которые имеют одну или более аминокислотных замен. Сайты интереса для замещающего мутагенеза включают HVR и FR. Консервативные замены показаны в таблице 1 под заголовком «предпочитаемые замены». Больше существенных изменений предлагается в таблице 1 под заголовком «типичные замены», и как дополнительно описано ниже со ссылкой на классы аминокислотных боковых цепей. Аминокислотные замены могут быть внесены в антитело интереса, и продукты проскринированы на наличие желаемой активности, например, сохраненное/улучшенное связывания антигена, сниженная иммуногенность, или улучшенный АЗКЦ или КЗЦ.
Таблица 1
остаток
замены
замены
Аминокислоты могут быть сгруппированы в соответствии со свойствами общей боковой цепи:
1) гидрофобные: Norleucine, Met, Ala, Val, Leu, Ile;
2) нейтральные гидрофильные: Cys, Ser, Thr, Asn, Gln;
3) кислые: Asp, Glu;
4) основные: His, Lys, Arg;
5) остатки которые влияют на ориентацию цепи: Gly, Pro;
6) ароматические: Trp, Tyr, Phe.
Неконсервативные замены повлекут за собой замену члена одного из этих классов на другой класс.
Один тип варианта замещения предполагает замены одного или более остатков гипервариабельной области исходного антитела (например гуманизированное или человеческое антитело). В целом, как правило, полученный вариант(ы), выбранный(е) для дополнительного исследования, будет(ут) иметь модификации (например, улучшения) определенных биологических свойств (например, повышенное сродство, сниженная иммуногенность) относительно исходного антитела, и/или будет(ут) иметь существенно сохраненные определенные биологические свойства исходного антитела. Типичный вариант замещения представляет собой антитело с созревшей аффинностью, которое может быть произведено удобным способом, например, применяя технологии созревания аффинности основанные на фаг-дисплее, такие как те, что были описаны в настоящем документе. Кратко, один или более HVR остатков мутируют, а вариант антитела выставляют на фаге, и проводят скрининг для конкретной биологической активности (например, аффинность связывания).
Изменения (например, замены) могут быть сделаны в HVR, например, чтобы улучшить аффинность антитела. Такие изменения могут быть сделаны в «горячих точках» HVR, например, остатках, которые кодируются кодонами, что подвергаются мутации с высокой частотой во время процесса соматического созревания (см., например, Chowdhury, Methods Mol. Biol. 207:179-196 (2008)), и/или остатках, которые контактируют с антигеном (SDRs (a-CDRs)), с проведением тестирования аффинности связывания полученных вариантов VH или VL. Созревание аффинности, с помощью конструирования и повторного отбора из вторичных библиотек было описано, например, в Hoogenboom et al. in Methods in Molecular Biology 178:1-37 (O'Brien et al., ed., Human Press, Totowa, NJ, (2001).) В некоторых вариантах осуществления созревания аффинности, вносится разнообразие в вариабельные гены, которые выбраны для созревания с помощью любого из множества способов (например, вносящая ошибки ПЦР, перетасовывание цепей, или олигонуклеотид-направленный мутагенез). Затем создается вторичная библиотека. Затем проводят скрининг библиотеки чтобы идентифицировать варианты антитела с желаемой аффинностью. Другие способы внесения разнообразия предполагают HVR-направленные подходы, в которых несколько HVR остатков (например, 4-6 остатков за раз) подвергаются рандомизации. HVR остатки, которые вовлечены в антигенное связывание, могут быть специфически идентифицированы, например, используя сканирование с помощью аланинового мутагенеза, или моделирование. CDR-H3, и CDR-L3 в частности, часто становятся мишенями.
В некоторых вариантах осуществления, замены, инсерции, или делеции могут случатся в одном или более HVR до тех пор пока такие изменения существенно не снижают способность антитела связывать антиген. Например, могут быть произведены консервативные изменения в HVR (например, консервативные замены, как указано в настоящем документе), которые существенно не снижают аффинность связывания. Такие изменения могут быть вне HVR «горячих точек» или SDR. В некоторых вариантах осуществления вариантов последовательностей VH и VL, которые представлены выше, каждый HVR, или является неизменяемым, или содержит не больше чем одну, две или три аминокислотных замены.
Полезным способом для идентификации остатков, или областей антитела, которые могут быть целями для мутагенеза, называется «аланин-сканирующий мутагенез», как описано Cunningham and Wells (1989) Science, 244:1081-1085. В этом способе, остаток или группа целевых остатков (например, заряженные остатки такие как Аrg, Аsp, His, Lys, и Glu) определяется и заменяется на нейтральные или негативно заряженные аминокислоты (например, аланин или полиаланин), чтобы определить затрагивается ли взаимодействие антитела с антигеном. Дополнительные замены могут быть введены в аминокислотные местоположения, которые демонстрируют функциональную чувствительность к начальным заменам. В альтернативном варианте, или дополнительно, может быть определена кристаллическая структура комплекса антиген-антитело для идентификации точек контакта между антителом и антигеном. Такие контактные остатки и соседние остатки могут быть сделаны мишенями, или исключены в качестве кандидатов для замены. Могут быть проскринированы варианты, чтобы определить, содержат ли они нужные свойства.
Аминокислотная последовательность вставок включают амино- и/или карбоксильные-концевые объединения, колеблясь в длине от одного остатка до полипептидов, которые содержат сто или больше остатков, также как и инсерции одного или нескольких аминокислотных остатков внутри последовательности. Примеры концевых вставок включают антитело с N-концевым метионильным остатком. Другие инсерционные варианты молекулы антитела включают слияние N- или C-конца антитела с ферментом (например, для ADEPT) или полипептидом, который увеличивает сывороточный период полувыведения антитела.
Варианты гликозилирования
В некоторых вариантах осуществления, антитело, которое предлагается в настоящем документе изменяют, чтобы увеличить или уменьшить степень, до которой антитело гликозилировано. Добавление или удаление сайтов гликозилирования антитела может быть удобно сделано изменением аминокислотной последовательности, таким образом, что создается или удаляется один или больше сайтов гликозилирования.
Может быть изменен карбогидрат, который прикреплен к Fc-области, которую содержит антитело. Нативные антитела, которые произведены клетками млекопитающего, как правило, содержат разветвленный, двухантенный олигосахарид, который в целом, как правило прикреплен N-связью к Asn297 CH2 домена Fc области. См., например, Wright et al., TIBTECH 15:26-32 (1997). Олигосахарид может включать различные карбогидраты, например, маннозу, N-ацетил глюкозамин (GlcNAc), галактозу, и сиаловую кислоту, так же как и фукозу, которая прикреплена к GlcNAc в «стебель» двухантенной олигосахаридной структуры. В некоторых вариантах осуществления, модификации олигосахарида в антителе, согласно данному изобретению, могут быть сделаны для того, чтобы создать варианты антител с определенными улучшенными свойствами.
В одном варианте осуществления, предлагаемые варианты антитела имеют карбогидратную структуру, что не имеет фукозы, и эта структура прикреплена (прямо или непрямо) к Fc области. Например, количество фукозы в таком антителе может быть от 1% до 80%, од 1% до 65%, от 5% до 65% или от 20% до 40%. Количество фукозы определяется из расчета среднего количества фукозы в цепи сахара в Asn297, относительно суммы глюкоструктур, которые прикреплены к Asn 297 (например, комплексные, гибридные и высоко манозные структуры) как измерено с помощью MALDI-TOF масс-спектрометрии, как описано, например, в WO 2008/077546. Asn297 относится к аспарагиновому остатку, который размещен около в положении 297 в Fc области (ЕС нумерация остатков Fc области); однако, Asn297 может также быть расположен около ±3 аминокислоты выше или ниже позиции 297, например, между позициями 294 и 300, из-за незначительных вариаций последовательности в антителах. Такие варианты фукозилирования могут иметь улучшенную функцию АЗКЦ. См., например, публикации патентных заявок США № US 2003/0157108 (Presta, L.); US 2004/0093621 (Kyowa Hakko Kogyo Co., Ltd). Примеры публикаций, которые связаны с «дефукозилироваными» или «фукоз-лишенными» вариантами антитела включают: US 2003/0157108; WO 2000/61739; WO 2001/29246; US 2003/0115614; US 2002/0164328; US 2004/0093621; US 2004/0132140; US 2004/0110704; US 2004/0110282; US 2004/0109865; WO 2003/085119; WO 2003/084570; WO 2005/035586; WO 2005/035778; WO2005/053742; WO2002/031140; Okazaki et al. J. Mol. Biol. 336:1239-1249 (2004); Yamane-Ohnuki et al. Biotech. Bioeng. 87: 614 (2004). Примеры клеточных линий, способных продуцировать дефукозилированые антитела, включают Lec13 CHO клетки, которые лишены фуколизирования белков (Ripka et al. Arch. Biochem. Biophys. 249:533-545 (1986); US Pat Appl No US 2003/0157108 A1, Presta, L; и WO 2004/056312 A1, Adams et al., особенно в примере 11), и нокаутные клеточные лини, такие как альфа-1,6-фукозилтрансферазный ген, FUT8, нокаутные CHO клетки (см., например, Yamane-Ohnuki et al. Biotech. Bioeng. 87: 614 (2004); Kanda, Y. et al., Biotechnol. Bioeng., 94(4):680-688 (2006); и WO2003/085107).
Дополнительно предлагаются варианты антител с разделенными олигосахаридами, например, в которых двухантенный олигосахарид, который прикреплен к Fc области антитела, разделен GlcNAc. Такие варианты антитела могут уменьшить фукозилирование и/или улучшить АЗКЦ функцию. Примеры таких вариантов антитела описаны, например, в WO 2003/011878 (Jean-Mairet et al.); US Patent No. 6,602,684 (Umana et al.); и US 2005/0123546 (Umana et al.). Предлагаются также варианты антитела по меньшей мере с одним галактозным остатком в олигосахариде, который прикреплен к Fc области. Такие варианты антитела могут улучшить функции КЗЦ. Такие варианты антитела описаны, например, в WO 1997/30087 (Patel et al.); WO 1998/58964 (Raju, S.); и WO 1999/22764 (Raju, S.).
Варианты Fc области
В некоторых вариантах осуществления, может быть введена одна или более аминокислотных модификаций в Fc область антитела, которое предлагается в настоящем документе, тем самым порождая варианты Fc области. Вариант Fc области может содержать последовательность человеческой Fc области (например, человеческую IgG1, IgG2, IgG3 или IgG4 Fc область), которая содержит аминокислотные модификации (например, замены) в одной, или больше аминокислотных позициях.
В некоторых вариантах осуществления, изобретение предусматривает вариант антитела, которое обладает некоторыми, но не всеми эффекторными функциями, которые делают его желательным кандидатом для приложений, в которых важен период полувыведения антитела in vivo, тем не менее определенные эффекторные функции (такие как комплемент и АЗКЦ) являются ненужными или вредными. Может быть проведен анализ цитотоксичности in vitro и/или in vivo, чтобы подтвердить уменьшение/истощение КЗЦ и/или АЗКЦ активностей. Например, могут быть проведены анализы связывания Fc рецептора (FcR), чтобы гарантировать, что антитело утратило FcγR связывания (отсюда, скорее всего, не хватает активность АЗКЦ), но сохраняет способность связываться с FcRn. Первичные клетки для опосредования АЗКЦ, NK клетки, экспрессируют только FcγRIII, тогда как моноциты экспрессируют FcγRI, FcγRII и FcγRIII. FcR экспрессия на гематопоетических клетках резюмирована в таблице 3 на странице 464 Ravetch and Kinet, Annu. Rev. Immunol. 9:457-492 (1991). Неограничивающие примеры in vitro анализа для оценки АЗКЦ активности молекулы интереса описаны в патенте США № 5500362 (см., например, Hellstrom, I. et al. Proc. Nat'l Acad. Sci. USA 83:7059-7063 (1986)) and Hellstrom, I et al., Proc. Nat'l Acad. Sci. USA 82:1499-1502 (1985); 5,821,337 (смотрите Bruggemann, M. et al., J. Exp. Med. 166:1351-1361 (1987)). В альтернативном варианте, могут быть использованы нерадиоактивные способы анализа (см., например, ACTI™ нерадиоактивный анализ цитотоксичности для проточной цитометрии (CellTechnology, Inc. Маунтин Вью Калифорния; и CytoTox 96® нерадиоактивный анализ цитотоксичности (Promega, Мэдиссон, Висконсин). Полезные эффекторные клетки для таких анализов включают мононуклеарные клетки периферической крови (МКПК (PBMC)), и клетки естественные киллеры (NK). В альтернативном варианте, или дополнительно может быть оценена АЗКЦ активность молекулы интереса in vivo, например, в животной модели, так как раскрыто в Clynes et al. Proc. Nat'l Acad. Sci. USA 95:652-656 (1998). Анализы связывания C1q могут также проводиться для подтверждения того, что антитело не может связываться с C1q и, следовательно, лишено КЗЦ активности. См., например, C1q и C3c связывания ИФА в WO 2006/029879 и WO 2005/100402. Для оценки активации комплемента может быть выполнен анализ КЗЦ (см., например, Gazzano-Santoro et al., J. Immunol. Methods 202:163 (1996); Cragg, M.S. et al., Blood 101:1045-1052 (2003); и Cragg, M.S. and M.J. Glennie, Blood 103:2738-2743 (2004)). FcRn связывание и in vivo определение клиренса/полужизни также может быть произведено способами, которые известные в данной области техники (см., например, Petkova, S.B. et al., Int'l. Immunol. 18(12):1759-1769 (2006)).
В некоторых вариантах осуществления, одна или несколько модификаций аминокислот могут быть введены в Fc-часть антитела, представленного в данном документе, для увеличения связывания IgG с неонатальным Fc-рецептором. В некоторых вариантах осуществления, антитело содержит следующие три мутации в соответствии с нумерацией ЕС: M252Y, S254T и T256E («мутация YTE») (патент США № 8697650, см. также Dall'Acqua et al., Journal of Biological Chemistry 281(33):23514-23524 (2006). В некоторых вариантах осуществления, мутация YTE не влияет на способность антитела связываться с узнаваемым им антигеном. В некоторых вариантах осуществления, мутация YTE увеличивает период полувыведения антитела в сыворотке по сравнению с нативным (т.е. не-YTE-мутантом) антителом. В некоторых вариантах осуществления, мутация YTE увеличивает период полувыведения антитела в сыворотке в 3 раза по сравнению с нативным (т.е. не-YTE-мутантом) антителом. В некоторых вариантах осуществления, мутация YTE увеличивает период полувыведения антитела в сыворотке в 2 раза по сравнению с нативным (т.е. не-YTE-мутантом) антителом. В некоторых вариантах осуществления, мутация YTE увеличивает период полувыведения антитела в сыворотке в 4 раза по сравнению с нативным (т.е. не-YTE-мутантом) антителом. В некоторых вариантах осуществления, мутация YTE увеличивает период полувыведения антитела в сыворотке по меньшей мере в 5 раз по сравнению с нативным (т.е. не-YTE-мутантом) антителом. В некоторых вариантах осуществления, мутация YTE увеличивает период полувыведения антитела в сыворотке по меньшей мере в 10 раз по сравнению с нативным (т.е. не-YTE-мутантом) антителом. См., например, патент США № 8697650; см. также Dall'Acqua et al., Journal of Biological Chemistry 281(33):23514-23524 (2006).
В некоторых вариантах осуществления, мутант YTE обеспечивает средство для модуляции активности антитело-зависимой клеточно-опосредованной цитотоксичности (АЗКЦ) антитела. В некоторых вариантах осуществления, мутант YTEO обеспечивает средство для модуляции активности АЗКЦ гуманизированного IgG-антитела, направленного против человеческого антигена. См., например, патент США № 8697650; см. также Dall'Acqua et al., Journal of Biological Chemistry 281(33):23514-23524 (2006).
В некоторых вариантах осуществления, мутант YTE позволяет одновременно модулировать период полувыведения в сыворотке, распределение в тканях и активность антитела (например, активность АЗКЦ IgG-антитела). См., например, патент США № 8697650; см. также Dall'Acqua et al., Journal of Biological Chemistry 281(33):23514-23524 (2006).
Антитела с уменьшенной эффекторной функцией включают те, что имеют в области Fc замены остатков 238, 265, 269, 270, 297, 327 и 329 (патент США № 6737056). Такие Fc-мутанты включают Fc-мутанты с заменами двух или больше аминокислотных остатков в позициях 265, 269, 270, 297 и 327, включая так называемый «DANA» Fc-мутант с заменой аминокислотных остатков 265 и 297 на аланин (патент США № 7332581).
В некоторых вариантах осуществления, пролин в позиции 329 (нумерация ЕС) (P329) человеческой области Fc дикого типа замещен глицином или аргинином, или аминокислотным остатком, достаточно большим для разрушения пролинового стека в пределах области взаимодействия Fc/Fc гамма-рецептора, который образуется между P329 Fc и остатками триптофана W87 и W110 FcgRIII (Sondermann et al.: Nature 406, 267-273 (20 July 2000)). В дополнительном варианте осуществления, по меньшей мере одна дополнительная аминокислотная замена в варианте Fc представляет собой S228P, E233P, L234A, L235A, L235E, N297A, N297D или P331S, и еще в другом варианте осуществления упомянутая, по меньшей мере одна дополнительная аминокислотная замена представляет собой L234A и L235A области Fc IgG1 человека, или S228P и L235E области Fc IgG4 человека, все согласно нумерации ЕС (патент США № 8969526, который включен посредством ссылки в полном объеме).
В некоторых вариантах осуществления, полипептид содержит вариант Fc человеческой области Fc IgG дикого типа, причем полипептид имеет P329 в области Fc человеческого IgG, замещенный глицином, и при этом вариант Fc содержит по меньшей мере две дополнительные аминокислотные замены в L234A и L235A области Fc IgG1 человека, или S228P и L235E области Fc IgG4 человека, и при этом остатки нумеруются в соответствии с нумерацией ЕС (патент США № 8969526, который включен посредством ссылки в полном объеме). В некоторых вариантах осуществления, полипептид, содержащий замены P329G, L234A и L235A (нумерация по ЕС), имеет сниженную аффинность к FcγRIIIA и FcγRIIA человека для понижающей модуляции АЗКЦ до по меньшей мере 20% АЗКЦ, индуцированной полипептидом, содержащим Fc-область дикого типа IgG человека, и/или для понижающей модуляции ADCP (патент США № 8969526, который включен посредством ссылки в полном объеме).
В конкретном варианте осуществления, полипептид, содержащий Fc-вариант полипептида Fc дикого типа человека, содержит тройную мутацию: аминокислотную замену в позиции Pro329, L234A, и мутацию L235A в соответствии с нумерацией ЕС (P329/LALA) (патент США № 8969526 который включен посредством ссылки в полном объеме). В конкретных вариантах осуществления, полипептид содержит следующие аминокислотные замены: P329G, L234A и L235A в соответствии с нумерацией ЕС.
Описаны некоторые варианты антитела с улучшенным или уменьшенным связыванием с FcR. (См., например, патент США № 6737056, WO 2004/056312, и Shields et al., J. Biol. Chem. 9(2): 6591-6604 (2001).)
В некоторых вариантах осуществления, вариант антитела содержит область Fc с одной или больше аминокислотными заменами, которые улучшают АЗКЦ, например, заменами в позициях 298, 333 и/или 334 в области Fc (нумерация остатков по ЕС).
В некоторых вариантах осуществления, изменения сделаны в Fc области, которые приводят к измененному (т. е., либо улучшенному, либо уменьшенному) связыванию C1q и/или комплемент-зависимой цитотоксичности (КЗЦ), например, как описано в патенте США № 6194551, WO 99/51642, и Idusogie et al. J. Immunol. 164: 4178-4184 (2000).
Антитела с увеличенным временем полувыведения и улучшенным связыванием с неонатальным рецептором Fc (FcRn), который отвечает за перенос материнских IgG к плоду (Guyer et al., J. Immunol. 117:587 (1976) и Kim et al., J. Immunol. 24:249 (1994)), описаны в US2005/0014934A1 (Hinton et al.). Такие антитела содержат область Fc с одной или больше заменами в них, которые улучшают связывание области Fc с FcRn. Такие варианты Fc включают те, где есть замены по одному или больше остаткам в области Fc: 238, 256, 265, 272, 286, 303, 305, 307, 311, 312, 317, 340, 356, 360, 362, 376, 378, 380, 382, 413, 424 или 434, например, замена остатка 434 в области Fc (патент США № 7371826).
Относительно других примеров вариантов области Fc смотрите также Duncan & Winter, Nature 322:738-40 (1988); патент США № 5648260; патент США № 5624821; и WO 94/29351.
Варианты антител с внесенным цистеином
В некоторых вариантах осуществления, может быть желательно создать антитела с введенным цистеином, например, «THIOMAB™» или TDC, в которых один или больше остатков антитела замещены остатками цистеина. В конкретных вариантах реализации изобретения, замещенные остатки встречаются в сайтах антитела, которые доступны для соединения. Таким образом, в результате замены таких остатков на цистеин, реактивные тиольные группы располагаются в доступных местах антитела и могут быть применены для конъюгации антитела с другими компонентами, такими как лекарственные компоненты или линкер-лекарственные компоненты, для создания иммуноконъюгата, как дополнительно описано в данном документе. В некоторых вариантах осуществления, любой один или больше из следующих остатков могут быть замещены цистеином: K149 (нумерация Кабата) легкой цепи; V205 (нумерация Кабата) легкой цепи; A118 (нумерация ЕС) тяжелой цепи; A140 (нумерация ЕС) тяжелой цепи; L174 (нумерация ЕС) тяжелой цепи; Y373 (нумерация ЕС) тяжелой цепи; и S400 (нумерация ЕС) области Fc тяжелой цепи. В конкретных вариантах осуществления, описанные в данном документе антитела содержат замену на цистеин HC-A140C (ЕС). В конкретных вариантах осуществления, описанные в данном документе антитела содержат замену на цистеин LC-K149C (нумерация по Кабату). В конкретных вариантах осуществления, описанные в данном документе антитела содержат замену на цистеин HC-A118C (нумерация по ЕС). Цистеин-внесенные антитела могут быть получены, как описано, например, в патенте США № 7521541.
В некоторых вариантах осуществления, антитело содержит одну из следующих замен на цистеин в тяжелой цепи:
В некоторых вариантах осуществления, антитело содержит одну из следующих замен на цистеин легкой цепи:
Неограничивающая иллюстративная легкая цепь (LC) K149C hu7C2.v2.2.LA THIOMAB™ имеет аминокислотные последовательности тяжелой цепи и легкой цепи SEQ ID NO: 26 и 30, соответственно. Неограничивающая иллюстративная тяжелая цепь (HC) A118C hu7C2.v2.2.LA THIOMAB™ имеет аминокислотные последовательности тяжелой цепи и легкой цепи SEQ ID NO: 31 и 25, соответственно.
Производные антител
В некоторых вариантах осуществления, антитело, предложенное в данном документе, может быть дополнительно модифицировано для включения дополнительных непротеиногенных компонентов, которые известны в данной области техники и общедоступны. Компоненты, пригодные для получения производных антитела, включают, но не ограничиваются лишь этими: водорастворимые полимеры. Неограничивающие примеры водорастворимых полимеров включают, но не ограничиваются лишь этими: полиэтиленгликоль (ПЭГ (PEG)), сополимеры этиленгликоля/ пропиленгликоля, карбоксиметилцеллюлозу, декстран, поливиниловый спирт, поливинилпирролидон, поли-1,3-диоксолан, поли-1,3,6-триоксан, сополимер этилена с малеиновым ангидридом, полиаминокислоты (либо гомополимеры, либо статистические сополимеры) и декстран или поли(n-винилпирролидон)полиэтиленгликоль, гомополимеры пропиленгликоля, сополимеры полипропиленоксида с этиленоксидом, полиоксиэтилированные полиолы (например, глицерин), поливиниловый спирт и их комбинации. Полиэтиленгликоль пропиональдегид может иметь преимущества в производстве благодаря его стабильности в воде. Полимер может быть любой молекулярной массы и может быть разветвленным или неразветвленным. Количество полимеров, присоединенных к антителу может варьировать, и в случае присоединения больше чем одного полимера, молекулы могут быть одинаковыми или разными. В целом, как правило, количество и/или тип полимеров, которые применяются для получения производных, могут быть определены учитывая особенности, включающие, но не ограничивающихся лишь этими: улучшение конкретных свойств или функций антитела, возможное использование производного антитела в терапии при определенных условиях и т. д.
В другом варианте осуществления, предлагаются конъюгаты антитела и непротеиногенного компонента, который может селективно нагреваться путем воздействия радиации. В одном варианте осуществления, непротеиногенный компонент представляет собой углеродную нанотрубку (Kam et al., Proc. Natl. Acad. Sci. USA 102: 11600-11605 (2005)). Радиация может быть любой длины волны и включает в себя, но не ограничивается лишь этими: длины волн, которые не вредят обычным клеткам, но которые нагревают непротеиногенные компоненты до температуры, при которой клетки проксимальные по отношению к антитело-непротеиногенному компоненту погибают.
Рекомбинантные способы и композиции
Антитела могут быть получены с использованием рекомбинантных способов и композиций, например, как описано в патенте США № 4816567. В одном варианте осуществления, предлагается изолированная нуклеиновая кислота, кодирующая антитело, описанное в данном документе. Такая нуклеиновая кислота может кодировать аминокислотную последовательность, которая содержит VL, и/или аминокислотную последовательность, которая содержит VH антитела (например, легкие и/или тяжелые цепи антитела). В дополнительном варианте осуществления, предлагается один или больше векторов (например, экспрессионные векторы), которые содержат такую нуклеиновую кислоту. В дополнительном варианте осуществления, предлагается клетка-хозяин, которая содержит такую нуклеиновую кислоту. В одном таком варианте осуществления, клетка-хозяин содержит (например, трансформирована): 1) вектор, содержащий нуклеиновую кислоту, кодирующую аминокислотную последовательность, содержащую VL антитела, и аминокислотную последовательность, содержащую VH антитела; или 2) первый вектор, содержащий нуклеиновую кислоту, кодирующую аминокислотную последовательность, содержащую VL антитела, и второй вектор, содержащий нуклеиновую кислоту, кодирующую аминокислотную последовательность, содержащую VH антитела. В одном варианте осуществления, клетка-хозяин представляет собой эукариотическую клетку, например, клетку яичников китайского хомячка (CHO) или лимфоидную клетку (например, Y0, NS0, Sp20 клетку). В одном варианте осуществления, предложен способ получения антитела, в котором способ включает культивирование клетки-хозяина, содержащей нуклеиновую кислоту, кодирующую антитело, как предложено выше, в условиях, подходящих для экспрессии антитела, и при необходимости восстановления антитела из клетки-хозяина (или среды для культивирования клетки-хозяина).
Для рекомбинантного получения антитела, нуклеиновую кислоту, кодирующую антитело, например, как описано выше, выделяют и встраивают в один или больше векторов для дальнейшего клонирования и/или экспрессии в клетке-хозяине. Такая нуклеиновая кислота может быть легко выделена и секвенирована с использованием обычных процедур (например, с использованием олигонуклеотидных зондов, которые способны к специфическому связыванию с генами, кодирующими тяжелую и легкую цепи антитела).
Клетки-хозяева, подходящие для клонирования или экспрессии кодирующих антитела векторов, включают прокариотические или эукариотические клетки, описанные в данном документе. Например, антитела могут быть получены в бактериях, в частности, когда гликозилирование и эффекторная функция Fc не требуются. Для экспрессии фрагментов антител и полипептидов в бактериях см., например, патенты США № 5648237, 5789199, и 5840523. (См. также Charlton, Methods in Molecular Biology, Vol. 248 (B.K.C. Lo, ed., Humana Press, Totowa, NJ, 2003), pp. 245-254, описывающие экспрессию фрагментов антител в E. coli.). После экспрессии антитело может быть выделено из массы бактериальных клеток в растворимой фракции и может быть в дальнейшем очищено.
В дополнение к прокариотам, эукариотические микроорганизмы, такие как мицелиальные грибы или дрожжи, являются подходящими хозяевами для клонирования или экспрессии кодирующих антитела векторов, включая штаммы грибов и дрожжей, чьи пути гликозилирования были «гуманизированы», приводя к получению антитела с частично или полностью человеческим профилем гликозилирования. См. Gerngross, Nat. Biotech. 22:1409-1414 (2004), and Li et al., Nat. Biotech. 24:210-215 (2006).
Клетки-хозяева, подходящие для экспрессии гликозилированного антитела, также получены от многоклеточных организмов (беспозвоночных и позвоночных). Примеры клеток беспозвоночных включают клетки растений и насекомых. Были идентифицированы многочисленные штаммы бакуловирусов, которые могут применяться совместно с клетками насекомых, в частности, для трансфекции клеток Spodoptera frugiperda.
Культуры клеток растений могут также применяться в качестве хозяев. См., например, патенты США № 5959177, 6040498, 6420548, 7125978, и 6417429 (описывающие технологию PLANTIBODIESTM для получения антител в трансгенных растениях).
Клетки позвоночных могут также использоваться в качестве хозяев. Например, могут быть полезны линии клеток млекопитающих, которые адаптированы к росту в суспензии. Другими примерами используемых линий клеток-хозяев млекопитающих являются: линия CV1 почки обезьяны, трансформированная SV40 (COS-7); линия клеток эмбриональной почки человека (293 или 293 клетки, как описано, например, в Graham et al., J. Gen Virol. 36:59 (1977)); клетки почки детеныша хомячка (BHK); клетки Сертоли мыши (клетки TM4, описанные, например, в Mather, Biol. Reprod. 23:243-251 (1980); клетки почки обезьяны (CV1); клетки почки африканской зеленой мартышки (VERO-76); клетки карциномы шейки матки человека (HELA); клетки почки собаки (MDCK); клетки печени крысы линии buffalo (BRL 3A); клетки легкого человека (W138); клетки печени человека (Hep G2); опухоль молочной железы мыши (MMT 060562); клетки TRI, описанные, например, в Mather et al., Annals N.Y. Acad. Sci. 383:44-68 (1982); клетки MRC 5; и клетки FS4. Другие полезные линии клеток-хозяев млекопитающих включают клетки яичника китайского хомячка (CHO), включающие DHFR- CHO клетки (Urlaub et al., Proc. Natl. Acad. Sci. USA 77:4216 (1980)); и линии клеток миеломы, такие как Y0, NS0 и Sp2/0. Для обзора некоторых линий клеток-хозяев млекопитающих, подходящих для получения антител, см., например, Yazaki and Wu, Methods in Molecular Biology, Vol. 248 (B.K.C. Lo, ed., Humana Press, Totowa, NJ), pp. 255-268 (2003).
Моноалкилирующие пирролобензодиазепиновые лекарственные компоненты
Конъюгат антитело-лекарственное средство согласно настоящему изобретению содержит моноалкилирующий пирролбензодиазепиновый лекарственный компонент, дериватизированный по группе N10 дисульфидным линкером к антителу.
Были подготовлены иллюстративные моноалкилирующие пирролбензодиазепиновые (ПБД (PBD)) компоненты, представленные в таблице 1а.
Таблица 1а. Моноалкилирующие пирролбензодиазепиновые лекарственные компоненты
М+Н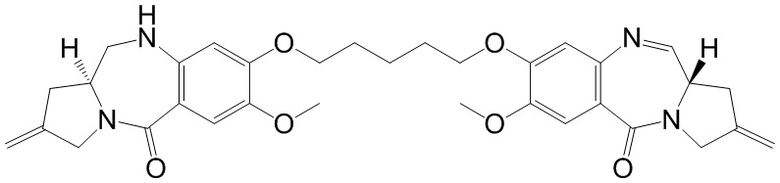
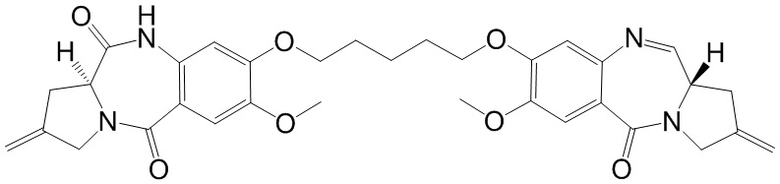
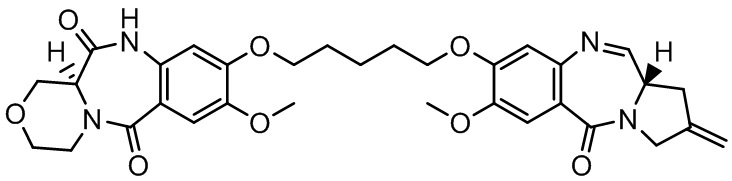

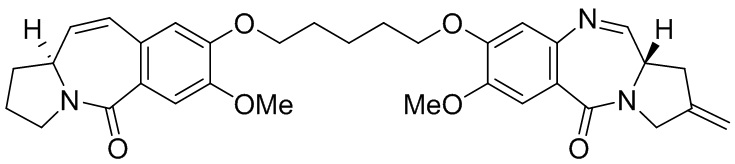
Таблица 1b. Компараторные лекарственные компоненты
Номер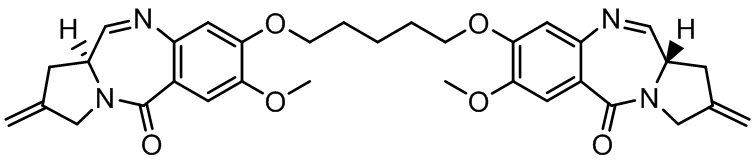
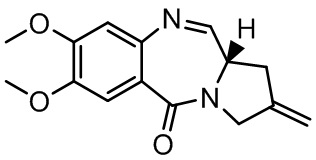

Моноалкилирующие пирролобензодиазепиновые линкер-лекарственные промежуточные соединения
Конъюгат антитело-лекарственное средство (КАЛС (ADC)) по изобретению может быть получен путем конъюгации моноалкилирующего пирролбензодиазепинового линкер-лекарственного промежуточного соединения с антителом. Тиопиридильную группу линкер-лекарственного промежуточного соединения вытесняют тиолом цистеина антитела с образованием дисульфид-связанного КАЛС (ADC).
Моноалкилирующее пирролобензодиазепиновое линкер-лекарственное промежуточное соединение имеет формулу I:
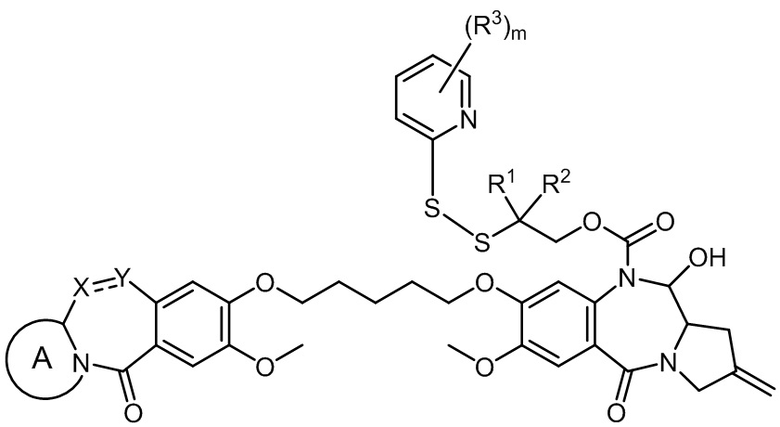 I
I
где X Y выбраны из CH2-CH2, CH=CH, C(=O)-NH, и CH2-NH;
Y выбраны из CH2-CH2, CH=CH, C(=O)-NH, и CH2-NH;
A представляет собой 5-членное или 6-членное гетероциклическое кольцо, необязательно замещенное группой, выбранной из F, C1-C6 алкила, и =C(R)2, где R независимо выбран из H, F, C1-C6 алкила, и C1-C6 фторалкила;
R1 и R2 независимо выбраны из H и C1-C6-алкила, или R1 и R2 образуют 3, 4, 5 или 6-членную циклоалкильную или гетероциклильную группу;
R3 независимо выбран из NO2, Cl, F, CN, CO2H и Br; и
m равно 0, 1 или 2.
В иллюстративном варианте осуществления, А представляет собой 5-членное кольцо.
В иллюстративном варианте осуществления, А представляет собой 5-членное кольцо с экзоциклической метиленовой группой, =CH2.
В иллюстративном варианте осуществления, А представляет собой 6-членное кольцо.
В иллюстративном варианте осуществления, А представляет собой морфолинильное кольцо.
В иллюстративном варианте осуществления, R1 представляет собой -CH3, и R2 представляет собой H.
В иллюстративном варианте осуществления, R1 и R2 образуют циклопропил или циклобутил.
В иллюстративном варианте осуществления, R3 представляет собой -NO2 и m равно 1.
В иллюстративном варианте осуществления, X Y представляет собой CH2-CH2 или CH=CH.
Y представляет собой CH2-CH2 или CH=CH.
В иллюстративном варианте осуществления, X Y представляет собой C(=O)-NH или CH2-NH.
Y представляет собой C(=O)-NH или CH2-NH.
Типичным вариантом реализации моноалкилирующего пирролобензодиазепинового линкер-лекарственного промежуточного соединения является формула Ia:
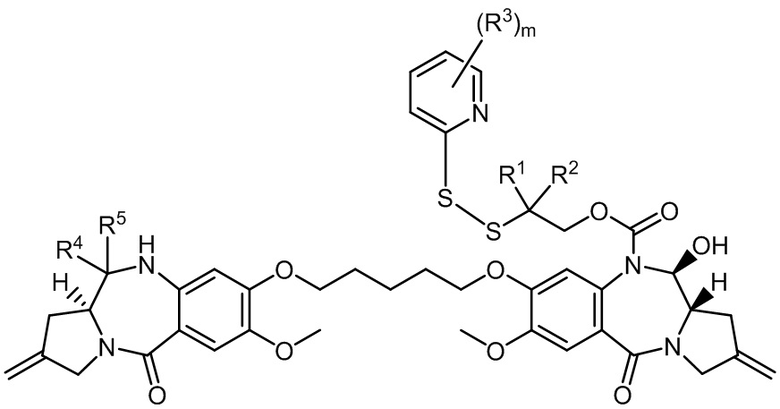 Ia
Ia
В иллюстративном варианте осуществления, R4 и R5 каждый представляют собой H.
В иллюстративном варианте осуществления, R4 и R5 представляют собой =O.
Типичным вариантом реализации моноалкилирующего пирролобензодиазепинового линкер-лекарственного промежуточного соединения является формула Ib:
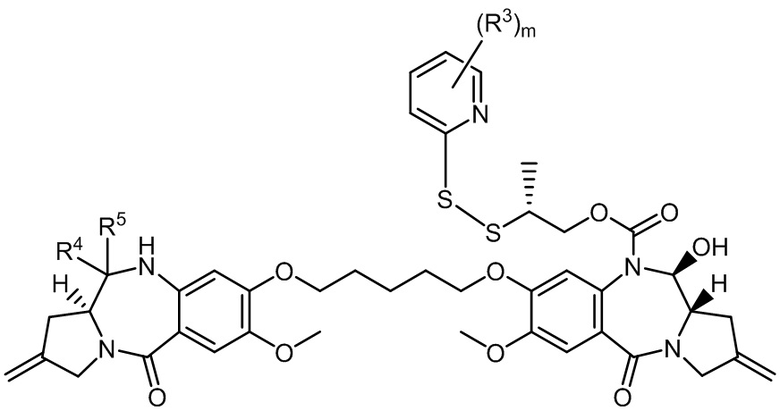 Ib.
Ib.
Типичным вариантом реализации моноалкилирующего пирролобензодиазепинового линкер-лекарственного промежуточного соединения является формула Ic:
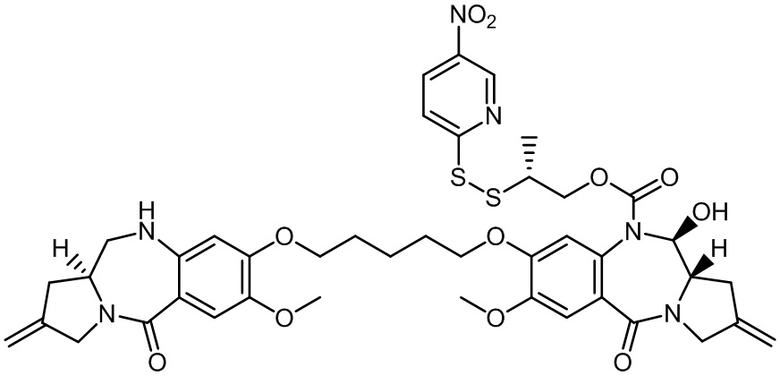 Ic.
Ic.
Типичным вариантом реализации моноалкилирующего пирролобензодиазепинового линкер-лекарственного промежуточного соединения является формула Id:
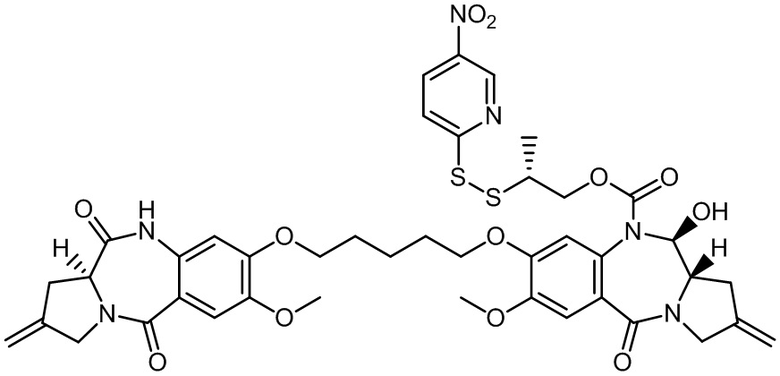 Id.
Id.
Не ограничиваясь конкретным механизмом или эффектом, присутствие электроноакцепторной группы R3, такой как NO2, Cl, F, CN, CO2H или Br на пиридильном кольце моноалкилирующего пирролобензодиазепинового линкерного промежуточного соединения ускоряет реакцию с цистеиновым тиолом антитела с внесенным цистеином. Когда цистеиновый тиол вносили в утрудняющий или менее реактивный сайт антитела, такое моноалкилирующее пирролобензодиазепиновое линкерное промежуточное соединение может давать более эффективную реакцию конъюгации с антителом относительно соответствующего незамещенного пиридилового аналога (R3=H).
Иллюстративные моноалкилирующие пирролобензодиазепиновые линкер-лекарственные промежуточные соединения показаны в таблице 2А. Компараторные (старый препарат из установленного класса, с которым сравнивается другое вещество) диалкилирующие пирролобензодиазепиновые линкер-лекарственные промежуточные соединения показаны в таблице 2В. Синтез линкер-лекарственных промежуточных соединений и компараторных лекарственных веществ описан в примерах.
Таблица 2А Моноалкилирующие пирролобензодиазепиновые линкер-лекарственные промежуточные соединения
Номер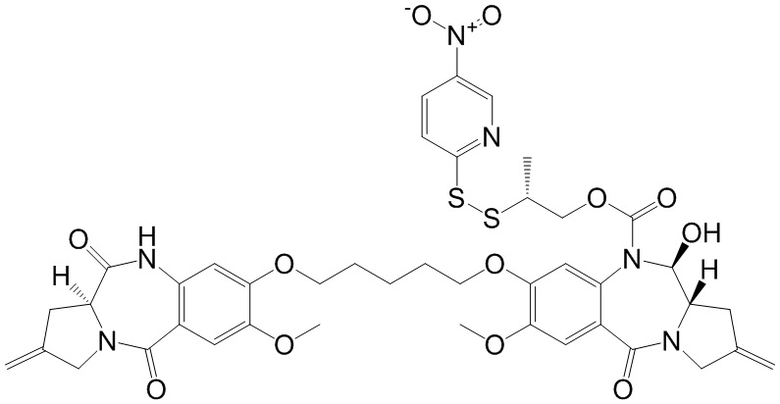
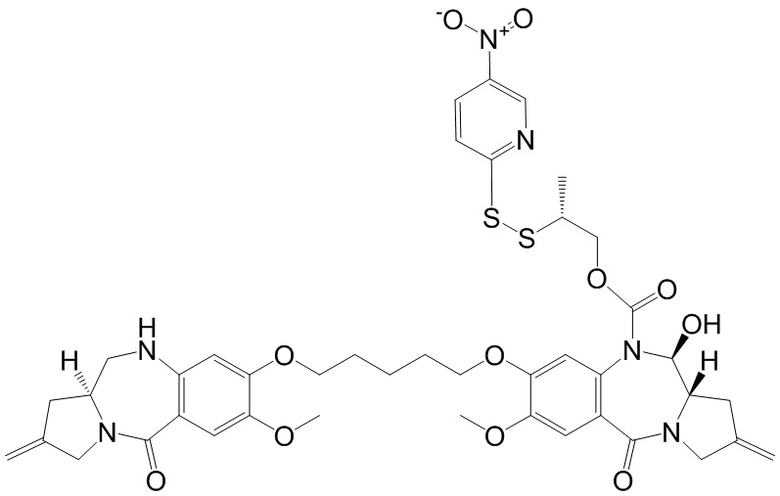
Таблица 2В. Компараторные пирролобензодиазепиновые линкер-лекарственные промежуточные соединения
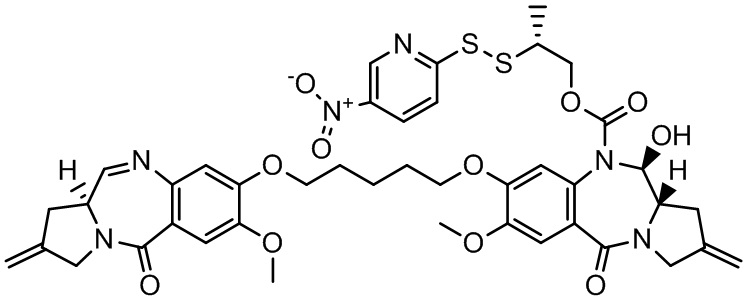
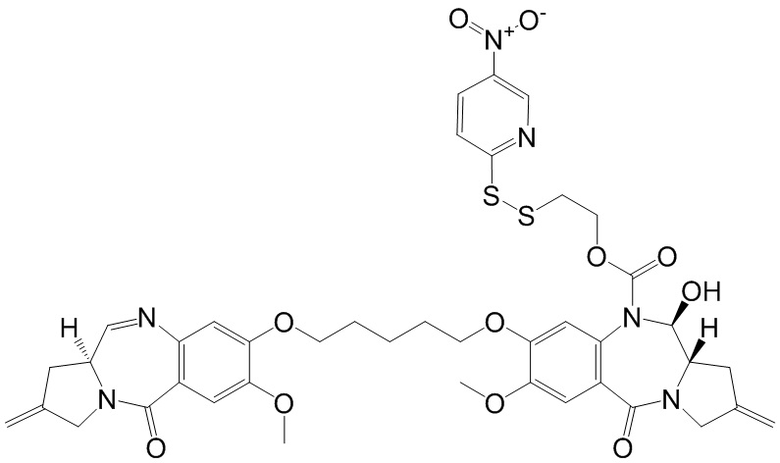
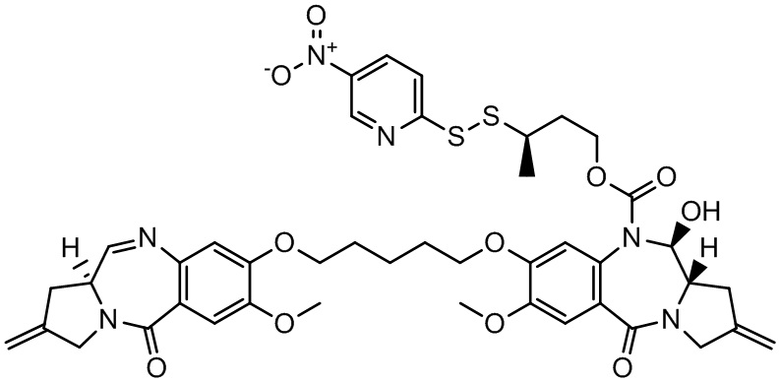
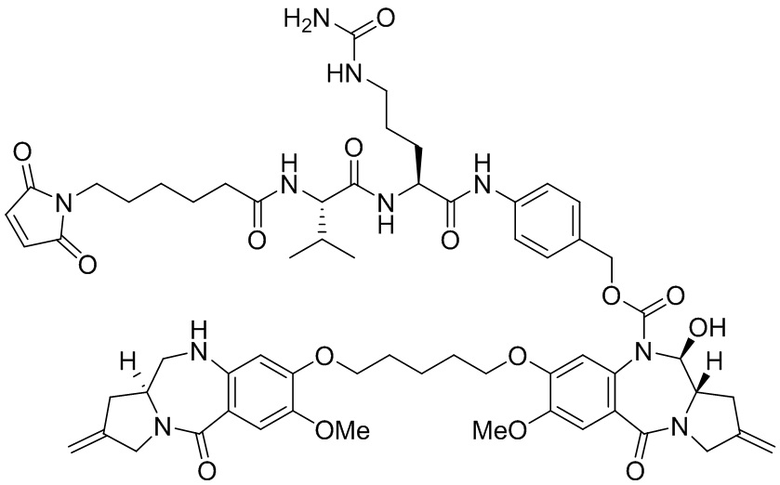
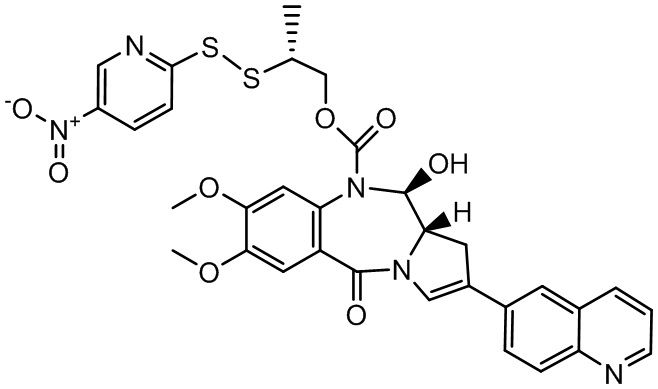
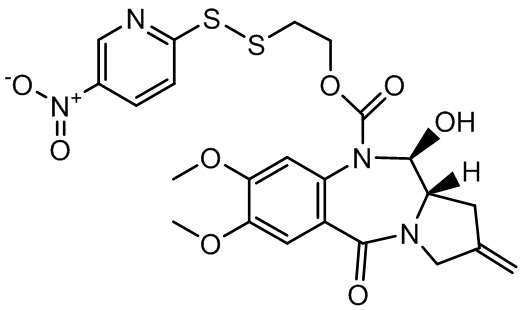
Конъюгаты антитело-лекарственное средство (КАЛС (ADC))
Соединения конъюгата антитело-лекарственное средство (КАЛС (ADC)) согласно настоящему изобретению включает антитело, специфичное к опухоль-ассоциированному антигену, ковалентно присоединенное к моноалкилирующему пирролбензодиазепиновому лекарственному компоненту, дериватизированному по группе N10 с помощью дисульфидного линкера, и включает те, что имеют биологическую активность. КАЛС (ADC) по изобретению может иметь терапевтическую активность и быть эффективным против ряда гиперпролиферативных патологий, включая рак. Биологическая активность моноалкилирующего пирролбензодиазепинового лекарственного компонента модулируется путем конъюгации с антителом. КАЛС (ADC) согласно изобретению выборочно доставляет эффективную дозу моноалкилирующего пирролбензодиазепинового лекарственного средства или токсина в опухолевую клетку или сайт, благодаря чему может быть достигнута большая селективность, т.е. более низкая эффективная доза, при увеличении терапевтического индекса («терапевтическое окно»). В иллюстративном варианте осуществления, соединения КАЛС (ADC) включают модифицированное цистеином антитело, конъюгированное, т.е. ковалентно присоединенное линкером, с моноалкилирующим пирролбензодиазепиновым лекарственным компонентом.
Следует понимать, что когда более чем одна нуклеофильная цистеиновая тиоловая группа антитела реагирует с линкер-лекарственным промежуточным соединением или линкерным веществом, то полученный продукт представляет собой смесь соединений КАЛС (ADC) с размещением одного или нескольких лекарственных компонентов, присоединенных к антителу. Среднее количество лекарственных средств на антитело (ОЛА (DAR)) может быть вычислено из смеси с помощью анализа ELISA c двумя антителами, который специфичен для антитела и специфичен для лекарственного средства. Отдельные молекулы КАЛС (ADC) можно идентифицировать в смеси с помощью масс-спектроскопии и разделить с помощью ВЭЖХ, например хроматографией гидрофобного взаимодействия (см., например, McDonagh et al (2006) Prot. Engr. Design & Selection 19(7):299-307; Hamblett et al (2004) Clin. Cancer Res. 10:7063-7070; Hamblett, K.J., et al. ʺEffect of drug loading on the pharmacology, pharmacokinetics, and toxicity of an anti-CD30 antibody-drug conjugate,ʺ Abstract No. 624, American Association for Cancer Research, 2004 Annual Meeting, March 27-31, 2004, Proceedings of the AACR, Volume 45, March 2004; Alley, S.C., et al. ʺControlling the location of drug attachment in antibody-drug conjugates,ʺ Abstract No. 627, American Association for Cancer Research, 2004 Annual Meeting, March 27-31, 2004, Proceedings of the AACR, Volume 45, March 2004). В некоторых вариантах осуществления, гомогенный КАЛС (ADC) с одним значением нагрузки может быть выделен из конъюгационной смеси электрофорезом или хроматографией.
Соединение конъюгата антитело-лекарственное средство по настоящему изобретению имеет структуру формулы II:
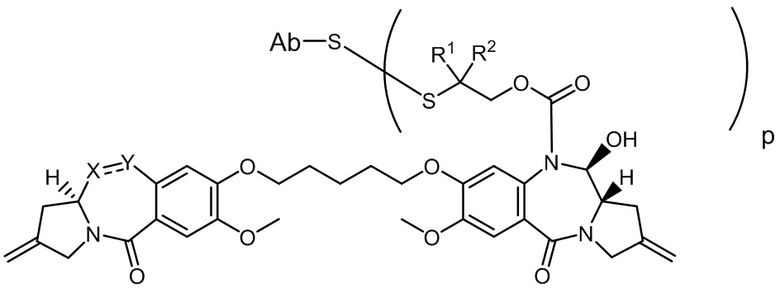 II
II
или его фармацевтически приемлемая соль, где:
где:
X Y выбран из CH2-CH2, CH2-C(=O), CH=CH или CH2-NH;
Y выбран из CH2-CH2, CH2-C(=O), CH=CH или CH2-NH;
R1 и R2 независимо выбраны из H или C1-C6-алкила, или R1 и R2 образуют 3, 4, 5 или 6-членную циклоалкильную или гетероциклильную группу;
p равно целому числу от 1 до 8; и
Ab представляет собой антитело.
В иллюстративном варианте осуществления, антитело связывается с одним или больше ассоциированными с опухолью антигенами, или рецепторами клеточной поверхности, выбранными из 1)-53):
1) BMPR1B (рецептор типа IB костного морфогенетического белка);
2) E16 (LAT1, SLC7A5);
3) STEAP1 (шеститрансмембранный эпителиальный антиген простаты);
4) MUC16 (0772P, CA125);
5) MPF (MPF, MSLN, SMR, потенциирующий мегакариоциты фактор, мезотелин);
6) Napi2b (NAPI-3B, NPTIIb, SLC34A2, cемейство транспортеров растворенных веществ 34 (фосфат натрия), член 2, натрий-зависимый фосфатный транспортер 3b типа II);
(7) Sema 5b (FLJ10372, KIAA1445, Mm.42015, SEMA5B, SEMAG, семафорин 5b Hlog, домен sema, семь тромбоспондиновых повторов (тип 1 и подобный типу 1), трансмембранный домен I (TД) и короткий цитоплазматический домен, (семафорин) 5B);
8) PSCA hlg (2700050C12Rik, C530008O16Rik, RIKEN кДНК 2700050C12, RIKEN кДНК 2700050C12 ген);
9) ETBR (рецептор эндотелина типа B);
10) MSG783 (RNF124, гипотетический белок FLJ20315);
11) STEAP2 (HGNC_8639, IPCA-1, PCANAP1, STAMP1, STEAP2, STMP, ассоциированный с раком простаты ген 1, ассоциированный с раком простаты белок 1, шеститрансмембранный эпителиальный антиген предстательной железы 2, шеститрансмембранный белок простаты);
12) TrpM4 (BR22450, FLJ20041, TRPM4, TRPM4B, катионный канал, действующий по механизму транзиторного рецепторного потенциала, подсемейство M, элемент 4);
13) CRIPTO (CR, CR1, CRGF, CRIPTO, TDGF1, фактор роста, полученный из тератокарциномы);
14) CD21 (CR2 (рецептор 2 комплемента) или C3DR (C3d/рецептор вируса Эпштейна-Барр) или Hs 73792);
15) CD79b (CD79B, CD79β, Igb (иммуноглобулин-ассоциированный бета), B29);
(16) FcRH2 (IFGP4, IRTA4, SPAP1A (якорный фосфатазный белок 1а, содержащий домен SH2), SPAP1B, SPAP1C);
17) HER2;
18) NCA;
19) MDP;
20) IL20Rα;
21) Brevican;
22) EphB2R;
23) ASLG659;
24) PSCA;
25) GEDA;
26) BAFF-R (рецептор фактора активации В-лимфоцитов, BlyS рецептор 3, BR3);
27) CD22 (изоформа CD22-В рецептора В-лимфоцитов);
28) CD79a (CD79A, CD79α, иммуноглобулин-ассоциированный альфа);
29) CXCR5 (рецептор 1 лимфомы Беркитта);
30) HLA-DOB (бета-субъединица молекулы ГКГС класса II (антиген Ia));
31) P2X5 (управляемый лигандом пуринергического рецептора P2X ионный канал 5);
32) CD72 (антиген CD72 дифференциации В-лимфоцитов, Lyb-2);
33) LY64 (антиген 64 (RP105) лимфоцитов, мембранный белок типа I семейства белков, богатых на лейциновые повторы (LRR - leucine rich repeat));
34) FcRH1 (Fc-рецептор-подобный белок 1);
35) FcRH5 (IRTA2, ассоциированный с транслокацией рецепторов суперсемейства иммуноглобулинов 2);
36) TENB2 (предполагаемый трансмембранный протеогликан);
37) PMEL17 (гомолог silver; SILV; D12S53E; PMEL17; SI; SIL);
38) TMEFF1 (трансмембранный белок 1 с EGF-подобным и двумя фолистатино-подобными доменами, Tomoregulin-1);
39) GDNF-Ra1 (рецептор альфа-1 семейства GDNF; GFRA1; GDNFR; GDNFRA; RETL1; TRNR1; RET1L; GDNFR-alpha1; GFR-ALPHA-1);
40) Ly6E (комплекс лимфоцитарного антигена 6, локус E; Ly67,RIG-E,SCA-2,TSA-1);
41) TMEM46 (гомолог shisa 2 (Xenopus laevis); SHISA2);
42) Ly6G6D (комплекс лимфоцитарного антигена 6, локус G6D; Ly6-D, MEGT1);
43) LGR5 (богатый на лейциновые повторы рецептор 5, сопряженный с G белком; GPR49, GPR67);
44) RET (протоонкоген ret; MEN2A; HSCR1; MEN2B; MTC1; PTC; CDHF12; Hs.168114; RET51; RET-ELE1);
45) LY6K (комплекс лимфоцитарного антигена 6, локус K; LY6K; HSJ001348; FLJ35226);
46) GPR19 (рецептор 19, сопряженный с G белком; Mm.4787);
47) GPR54 (рецептор KISS1; KISS1R; GPR54; HOT7T175; AXOR12);
48) ASPHD1 (содержащий домен аспартат-бета-гидроксилазы белок 1; LOC253982);
49) Тирозиназа (TYR; OCAIA; OCA1A; тирозиназа; SHEP3);
50) TMEM118 (белок 2, содержащий трансмембранный домен и домен «палец RING (Really Interesting New Gene)»; RNFT2; FLJ14627);
51) GPR172A (рецептор 172A, сопряженный с G белком; GPCR41; FLJ11856; D15Ertd747e);
52) CD33; или
53) CLL-1.
Иллюстративные соединения конъюгата антитело-лекарственное средство включают формулу IIa:
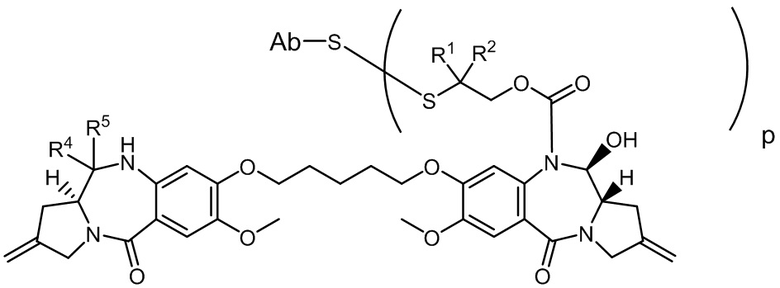 IIa
IIa
Иллюстративные соединения конъюгата антитело-лекарственное средство Формулы IIa включают причем R4 и R5 каждый представляет собой H, или R4 и R5 представляют собой =O.
Иллюстративные соединения конъюгата антитело-лекарственное средство включают формулу IIb:
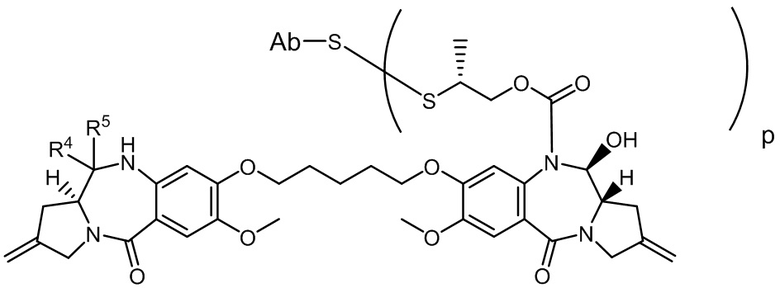 IIb.
IIb.
Конъюгаты антитело-лекарственное средство ADC-101-ADC-119 Таблицы 3А были получены путем конъюгирования моноалкилирующего пирролбензодиазепинового линкер-лекарственного промежуточного соединения LD-51 или LD-52 таблицы 2А с антителом, включая модифицированное цистеином антитело. Компараторные конъюгаты антитело-лекарственное средство ADC-201-ADC-211 таблицы 3В были получены путем конъюгирования компараторных пирролбензодиазепиновых линкер-лекарственных промежуточных соединений CLD-1-6 таблицы 2В с антителом, включая модифицированное цистеином антитело.
Таблица 3A Моноалкилирующие дисульфидные конъюгаты антитело-лекарственное средство (КАЛС (ADC))
Номер LD
(таблица 2А)
Таблица 3В Компараторные конъюгаты антитело-лекарственное средство (КАЛС (ADC))
(таблица 2В)
A118C (нумерация ЕС)=A121C (Последовательная нумерация)=A114C (нумерация Кабата)
K149C (нумерация Кабата) легкой цепи
Дикий тип («WT»), мутантное модифицированное цистеином антитело («тио»), легкая цепь («LC»), тяжелая цепь («HC»), 6-малеимидокапроил («MC»), малеимидопропаноил («MP»), валин-цитруллин («val-cit» или «vc»), аланин-фенилаланин («ala-phe»), p-аминобензил («PAB») и p-аминобензилоксикарбонил («PABC»)
Компараторное соединение ADC-211, трастузумаб эмманзин (KADCYLA®, трастузумаб-MCC-DM1 (T-DM1, Tmab-DM1), представляет собой конъюгат антитело-лекарственное средство (CAS Reg. No. 139504-50-0; Phillips G. et al. (2008) Cancer Res. 68:9280-90; US 8142784), и имеет следующую структуру:
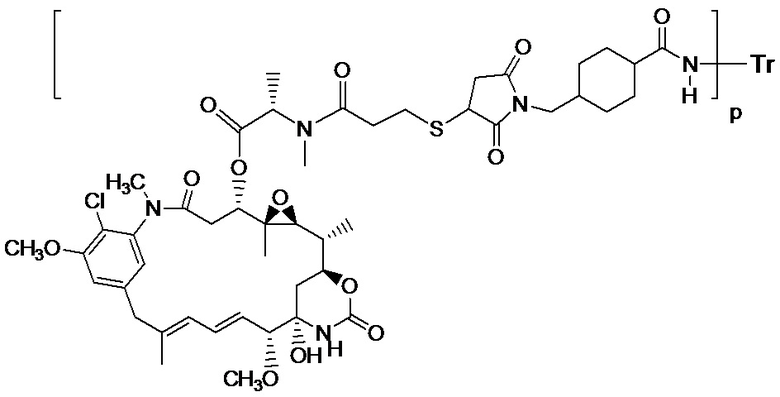
в котором Tr является анти-HER2-антителом трастузумаб.
АНАЛИЗЫ КЛЕТОЧНОЙ ПРОЛИФЕРАЦИИ IN VITRO
В целом, как правило, цитотоксическую или цитостатическую активность конъюгата антитело-лекарственное средство (КАЛС (ADC)) измеряют путем: экспонирования клеток млекопитающих имеющих рецепторные белки, например HER2, антителу КАЛС (ADC) в клеточной культуральной среде; культивирования клеток в течение периода от около 6 часов до около 5 дней; и измерения жизнеспособности клеток. Клеточные анализы in vitro применяли для измерения жизнеспособности (пролиферации), цитотоксичности и индукции апоптоза (активации каспазы) КАЛС (ADC) по изобретению.
Активность in vitro конъюгатов антитело-лекарственное средство (КАЛС (ADC)) измеряли с помощью анализа пролиферации клеток (пример 6). КАЛС (ADC) по изобретению продемонстрировали удивительную и неожиданную активность в ингибировании пролиферации опухолевых клеток. Активность КАЛС (ADC) коррелировала с экспрессией клетками антигена-мишени. Тестируемые конъюгаты способны связываться с определенным антигеном, экспрессируемым на поверхности клеток и вызывать гибель этих клеток in vitro.
Анализ жизнеспособности люминесцентных клеток CellTiter-Glo® является коммерчески доступным (Promega Corp., Мэдисон, Висконсин), это одношаговый способ анализа, основанный на рекомбинантной экспрессии люциферазы Coleoptera (US 5583024, US5674713, US5700670). Анализ пролиферации клеток определяет количество жизнеспособных клеток в культуре на основе количественного анализа присутствующего АТФ, который является индикатором метаболически активных клеток (Crouch et al (1993) J. Immunol. Meth. 160:81-88; US 6602677). Анализ CellTiter-Glo® можно выполнять в 96-луночном формате, что делает его доступным для автоматизированного высокопроизводительного скрининга (HTS) (Cree et al (1995) AntiCancer Drugs 6:398-404). Способ одношагового анализа включает добавление одного реагента (реагента CellTiter-Glo®) непосредственно к культивируемым клеткам в клеточную культуральную среду дополненную сывороткой. Промывание клеток, удаление среды и несколько этапов пипетирования не требуются. Система способна обнаруживать малые количества клеток - 15 клеток/лунка в 384-луночном формате через 10 минут после добавления реагента и смешивания. Клетки могут непрерывно обрабатываться КАЛС (ADC), или они могут обрабатываться и отделяться от КАЛС (ADC). В целом, как правило, клетки, обработанные кратковременно, т.е. 3 часа, проявляли те же самые эффекты активности, что и непрерывно обработанные клетки.
Одношаговый формат «измерение добавленной смеси» приводит к лизису клеток и появлению люминесцентного сигнала, пропорционального количеству присутствующего АТФ. Количество АТФ прямо пропорционально количеству клеток, присутствующих в культуре. Анализ CellTiter-Glo® производит люминесцентный сигнал по типу «накаливающегося свечения», вырабатываемый реакцией люциферазы, который имеет период полужизни, обычно более пяти часов, в зависимости от используемого типа клеток и среды. Жизнеспособные клетки отображаются в относительных единицах люминесценции (ОЕЛ(RLU)). Субстрат Beetle Luciferin окислительно декарбоксилируется рекомбинантной люциферазой светлячков с сопутствующим преобразованием АТФ в AMP и образованием фотонов.
Клеточные анализы in vitro применяются для измерения жизнеспособности (пролиферации), цитотоксичности и индукции апоптоза (активации каспазы) КАЛС (ADC) по изобретению. В целом, как правило, цитотоксическую или цитостатическую активность конъюгата антитело-лекарственное средство (КАЛС (ADC)) измеряют путем: экспонирования клеток млекопитающих, экспрессирующих антиген, такой как полипептид Her2 или MUC16, соединению КАЛС (ADC) в клеточной культуральной среде; культивирования клеток в течение периода от около 6 часов до около 5 дней; и измерения жизнеспособности клеток. Клетки млекопитающих, пригодные для анализа пролиферации клеток для анти-MUC16 КАЛС (ADC), включают: (1) экспрессирующую полипептид MUC16 клеточную линию OVCAR-3; 2) клеточную линию, полученную на основе PC3, сконструированную для стабильной экспрессии части полипептида MUC16 на клеточной поверхности (PC3/MUC16); 3) исходную клеточную линию PC3, которая не экспрессирует полипептид MUC16; и 4) клеточную линию PC3, которая не экспрессирует полипептид MUC16, но несет вектор, используемый для управления экзогенной экспрессией MUC16 (PC3/neo).
Фиг. 1А, 1В, 1С иллюстрируют, что моноамин Тио Hu анти-CD22 10F4v3 LC K149C-(LD-52) ADC-107 проявляет нМ активность в числовом выражении меньше 10, с примерно 4-кратной разницей по сравнению с не нацеленным на мишень контролем ADC-108, в BJAB (фиг. 1А), примерно 7-кратной разницей по сравнению с не нацеленным на мишень контролем в WSU-DLCL2 (фиг. 1B), примерно в 5 раз большей активностью по сравнению с не нацеленным на мишень контролем ADC-108, в Jurkat (фиг. 1C). Моноамин ADC-107 примерно в 10 раз более активный, чем моноамин ADC-103 Тио Hu анти-CD22 10F4v3 LC K149C-(LD-51), и примерно в 22 раза более активный чем не нацеленный на мишень контроль ADC-108 в BJAB и в WSU-DLCL2 (фиг. 1A-C).
Таблица 4 Анализ конъюгатов антитело-лекарственное средство по пролиферации клеток in vitro (фиг. 1F, 1G)
IC50 (нг/мл)
IC50 (нг/мл)
LD-52
Таблица 5 Активность in vitro (фиг. 1А, 1В, 1С)
ЭФФЕКТИВНОСТЬ IN VIVO
Эффективность in vivo конъюгатов антитело-лекарственное средство (КАЛС (ADC)) измеряли через ингибирование роста опухоли у мышей (пример 7). КАЛС (ADC) по изобретению продемонстрировали удивительную и неожиданную активность в ингибировании опухолевого роста. Эффективность КАЛС (ADC) коррелировала с экспрессией опухолевыми клетками антигена-мишени.
Эффективность конъюгатов антитело-лекарственное средство измеряли in vivo путем имплантации аллотрансплантатов или ксенотрансплантатов раковых клеток в грызунов и лечения опухолей с помощью КАЛС (ADC). Ожидаются разные результаты в зависимости от клеточной линии, специфичности связывания антитела КАЛС (ADC) с рецепторами, присутствующими на раковых клетках, режимов дозирования и других факторов. Эффективность КАЛС (ADC) in vivo измеряли с применением модели трансгенной эксплантной мыши, экспрессирующей от умеренного до высокого уровня ассоциированного с опухолью антигена, такого как Her2, CD22 и Ly6E. Субъектов обрабатывали один раз с помощью КАЛС (ADC) и наблюдали в течение 3-6 недель, чтобы измерить время увеличения вдвое опухоли, log гибель клеток и уменьшение опухоли. Проводились эксперименты после ответа на дозу и эксперименты с множественными дозами.
Например, эффективность in vivo анти-HER2 КАЛС (ADC) по изобретению может быть измерена с помощью высоко экспрессирующей HER2 эксплантационной трансгенной мышиной модели (Phillips et al (2008) Cancer Res. 68:9280-90). Аллотрансплантат получен от трансгенной мыши Fo5 mmtv, которая не реагирует, или плохо реагирует на терапию HERCEPTIN®. Субъектов лечили один раз КАЛС (ADC) при определенных уровнях дозы (мг/кг) и контрольного плацебо-буфера (наполнителя) и наблюдали в течение двух недель или больше для измерения времени увеличения вдвое опухоли, log гибель клеток и уменьшение опухоли.
Фиг. 2 иллюстрирует эффективность конъюгатов антитело-лекарственное средство, ADC-202, ADC-103 и ADC-102 на графике изменения объема опухоли in vivo с течением времени в модели ксенотрансплантата WSU-DLCL2 в модели CB-17 Fox Chase SCID мыши.
Фиг. 3 иллюстрирует эффективность конъюгатов антитело-лекарственное средство на графике изменения объема опухоли in vivo с течением времени в модели ксенотрансплантата Bjab-luc в модели CB-17 Fox Chase SCID мыши. Дозы 0,2 и 0,4 мг/кг компаратора ADC-202 приводят к регрессии опухоли, с дозой 0,1 мг/кг, что приводит к 62% ингибированию роста опухоли (ИРО(TGI)). Диапазон ИРО от 40-58% для доз 1, 2 и 4 мг/кг моноамида ADC-105 показывает, что эти уровни доз имеют аналогичный ответ, когда только самая высокая доза 8 мг/кг показывает значительную активность, 89% ИРО(TGI). Дополнительно, активность при дозе 8 мг/кг попадает между 0,1 и 0,2 мг/кг дозы компаратора диалкилирующего ADC-202, что дает в результате в примерно 50 раз меньшую активность. Не нацеленный на мишень контроль анти-Her2 hu7C2 ADC-104 -моноамид при 8 мг/кг показал в 2 раза меньшую активность чем не нацеленный на мишень контроль компаратор анти-Her2 hu7C2 ADC-201 при 0,4 мг/кг, 18 против 36% ИРО (TGI). При оценке безопасного веса тела все группы демонстрировали увеличение веса.
Фиг. 4 иллюстрирует эффективность конъюгатов антитело-лекарственное средство на графике изменения объема опухоли in vivo с течением времени в мышиной модели с клеточной линией WSU-DLCL2 человека. Эффективность для мишеней, анти-CD22 моноамина ADC-107 и ADC-204 с val-cit связью оценивали при дозах от 0,5 до 10 мг/кг. Для сравнения был включен моноамид ADC-105. Не нацеленные на мишень анти-Her2 моноамин ADC-108 и ADC-205 были применены в качестве контролей. Активность как для моноамина ADC-107, так и для ADC-204 оказалась аналогичной. Минимальная эффективная доза (МЭД) для обоих составляет от 0,5 до 2 мг/кг. При максимальной дозе 10 мг/кг оба препарата приводили к полному отклику у 5/5 животных, что не наблюдалось с моноамидным КАЛС (ADC). Дополнительно, моноаминовые КАЛС (ADC) имели больше чем 10-кратную активность по сравнению с моноамидными КАЛС (ADC) (сравните ответ на дозу 0,5 мг/кг моноамина и на дозу 5 мг/кг моноамида). Оба Her2 контроля с дозировкой 2 мг/кг имеют похожий ответ (около 30% ИРО(TGI)). Не наблюдалось никакой значительной потери веса для всех групп.
Фиг. 5A иллюстрирует эффективность конъюгатов антитело-лекарственное средство ADC-106, ADC-108 и ADC-107 на графике изменения объема опухоли in vivo с течением времени в модели опухоли HER2 KPL4 у мышей SCID Beige.
Фиг. 5B иллюстрирует эффективность конъюгатов антитело-лекарственное средство на графике изменения объема опухоли in vivo с течением времени в модели опухоли HER2 KPL4 у мышей SCID Beige. Измеряли эффективность моноамида Тио-Her2 hu7C2 LC-K149C-(LD-51), ADC-106 и ADC-106 в комбинации с Tmab-DM1.
Фиг. 6 иллюстрирует эффективность конъюгатов антитело-лекарственное средство ADC-201, ADC-104, ADC-202 и ADC-105 и неконъюгированного антитела hu7C2 на графике изменения объема опухоли in vivo с течением времени в HER2 Fo5 модели у CRL nu/nu мышей, дозированных один раз внутривенно (ВВ (IV)). Нацеленные на мишень ADC-201 и ADC-104 показывают ингибирование опухоли и дозозависимые эффекты. Не нацеленные на мишень ADC-202 и ADC-105, и неконъюгированное антитело hu7C2 не проявляют ингибирования опухоли.
Фиг. 7 иллюстрирует эффективность конъюгатов антитело-лекарственное средство ADC-201, ADC-104, ADC-202 и ADC-105, и неконъюгированного антитела hu7C2 на графике изменения объема опухоли in vivo с течением времени в HER2 KPL4 модели опухоли у мышей SCID Beige. Нацеленные на мишень ADC-201 и ADC-104 показывают ингибирование опухоли и дозозависимые эффекты. Не нацеленные на мишень ADC-202 и ADC-105, и неконъюгированное антитело hu7C2 проявляют слабое ингибирования опухоли или его отсутствие.
Фиг. 8 иллюстрирует эффективность конъюгатов антитело-лекарственное средство ADC-106, ADC-18 и ADC-17 на графике изменения объема опухоли in vivo с течением времени в HER2 Fo5 модели у CRL nu/nu мышей. Нацеленные на мишень ADC-106 и ADC-108 показывают ингибирование опухоли и дозозависимые эффекты. Не нацеленный на мишень ADC-107 проявляет слабое ингибирования опухоли или его отсутствие.
Фиг. 9 иллюстрирует эффективность конъюгатов антитело-лекарственное средство ADC-104, ADC-111, ADC-112, ADC-106 и ADC-113 на графике изменения объема опухоли in vivo с течением времени в CD22-экспрессирующей модели ксенотрансплантата WSU-DLCL2 у CB-17 Fox Chase SCID мыши. Нацеленные на мишень ADC-104, ADC-111 и ADC-112 показывают ингибирование опухоли и дозозависимые эффекты. Не нацеленные на мишень ADC-106 и ADC-133 показывают отсутствие ингибирования опухоли.
Фиг. 10 иллюстрирует эффективность конъюгатов антитело-лекарственное средство на графике изменения объема опухоли in vivo с течением времени в модели ксенотрансплантата HCC1569X2. Ly6E-SG3451-моноамид обладает дозозависимой активностью, наблюдается задержка роста при 6 и 12 мг/кг и остановка роста опухолей при дозировке 18 мг/кг. Наблюдается регрессия опухоли с Ly6E-SG3451, дозированном в количестве 1 и 3 мг/кг, и с Ly6E-SG3203-моноамином, дозированном в количестве 1, 3 и 6 мг/кг. Группы Ly6E SG3451 и SG3203-моноамин группируются вместе.
Анализ олигонуклеотидного связывания/алкилирования
Известно, что соединения пирролобензодиазепина (ПБД (PBD)) образуют зависимые от последовательности, внутрицепочечные ДНК поперечные связи и моноалкилированные аддукты в дополнение к межцепочечным перекрестным связям (Rahman KM, et al (2009) J Am Chem Soc 131:13756-13766). ПБД (PBD) имеют хиральную C11a(S)-позицию, которая обеспечивает им соответствующую форму, которая надежно закрепляется в малой канавке ДНК. Кроме того, электрофильный фрагмент N10-C11 (т.е. взаимопревращаемый имин, карбиноламин или карбиноламин-метиловый эфир) может образовывать ковалентную аминальную связь между их C11-положением и нуклеофильной группой C2-NH2 гуанинового нуклеотидного основания. Изучали взаимодействие соединений пирролбензодиазепина с дуплекс-образующими олигонуклеотидами различной длины и различных последовательностей с последовательностями Pu-GAATG-Py> Pu-GATC-Py>>Pu-GATG-Py или Pu-GAATC-Py для образования внутрицепочечных и межцепочечных связей, обнаруженных ранее (пример 8). Анализ олигонуклеотидного связывания и алкилирования представляет собой простую модель для оценки потенциала связывания лекарственных пирролбензодиазепиновых компонентов в КАЛС (ADC) с нуклеиновыми кислотами с помощью разделения ВЭЖХ и обнаружения МС (MS) (Narayanaswamy M. et al (2008) Anal. Biochem. 374:173-181). Таким образом, активность и эффективность КАЛС (ADC) могут быть сопоставлены и предсказаны. Моноалкилирующие пирролобензодиазепиновые лекарственные компоненты могут быть дифференцированы, например моноамид DM-3 от моноамина DM-1, и моноалкилирующие из таблицы 1а от компараторных диалкилирующих пирролбензодиазепиновых лекарственных компонентов в таблице 1b, например C-1 (пример 8).
Частота появления выбранных олигонуклеотидных последовательностей, которые могли бы связывать/алкилировать пирролбензодиазепиновые соединения, очень велика и не прямо пропорциональна размеру хромосом, в которой они встречаются. Соединения пирролбензодиазепина в настоящем исследовании включают моноалкилирующие пирролобензодиазепиновые лекарственные компоненты из таблицы 1а и компараторные лекарственные компоненты из таблицы 1b. В исследовании были показаны отличимые уровни лекарственных средств, алкилирующих двухцепочечных олигонуклеотиды, и активность алкилирования может быть точно оценена путем исчезновения начальных дуплексных олигонуклеотидов, Pu-GAAATC-Py и Pu-GAAATG-Py, где Pu представляет собой пуриновый нуклеотид A или G, и Py представляет собой пиримидиновый нуклеотид С или Т. Моноамид ПБД (PBD) DM-2 (таблица 1а) был примерно в 8 раз менее эффективен для связывания/алкилирования дуплексных олигонуклеотидов, чем моноамин ПБД (PBD) DM-1. Компараторное диалкилирующее соединение C-1 (таблица 1b) показывает в 2-3 раза большую эффективность для ковалентного алкилирования дуплексных олигонуклеотидов, чем моноамин DM-1. ПБД-мономер C-2 показывает большую чем в 50 раз меньшую эффективность ковалентного алкилирования дуплексных олигонуклеотидов, чем димер C-1. Восстановление иминновых связей С-1 для формирования С-3 полностью исключает связывание ДНК. Различные олиго-ПБД-аддукты были сформированы с различными алкилирующими соединениями, разделенными ВЭЖХ, и были охарактеризованы по массе с помощью анализа МС.
Фиг. 11 иллюстрирует предполагаемые аддукты после реакций диалкилирующего пирролбензодиазепинового (ПБД (PBD)) димерного соединения CLD-1 (сверху) и двух моноалкилирующих пирролбензодиазепиновых димерных соединений, моноамина DM-1 (средний) и моноамида DM-2 (снизу) с ДНК (Rahman KM, et al (2009) J Am Chem Soc 131:13756-13766). Димерные соединения диалкилирующего ПБД (PBD) могут образовывать два ковалентных соединения (сшивки) с группой C2-NH2 гуаниновой нуклеотидной основы на противоположных цепях ДНК-дуплекса. Моноалкилирующие димерные соединения ПБД (PBD) могут образовывать только одну ковалентную связь с гуаниновой нуклеотидной основой, что влияет на кинетику асс./диссоц. связывания и разрушение делящихся клеток.
Моноамид DM-2 демонстрирует в 8-10 раз меньшее связывание/алкилирование, чем моноамин DM-1, с дуплексными олигонуклеотидам, что коррелирует с активности и эффективностью их КАЛС (ADC) в линиях раковых клеток и моделях ксенотрансплантата опухоли in vivo. Более низкий уровень алкилирования ДНК для моноамида поддерживает эффективность с пониженной токсичностью и может демонстрировать лучший терапевтический индекс. В целом степень связывания/алкилирования ДНК коррелирует с эффективностью аналогов ПБД (PBD) и отличает ПБД (PBD) моноамид от моноамина, и от диалкилирующего ПБД (PBD). Оптимизированные терапевтические индексы (TИ) для ПБД-КАЛС (ADC) могут быть достигнуты путем модуляции активности связывания/алкилирования моноалкилирующих ДНК соединений, а способ олигосвязывания/алкилирования можно использовать для управления дизайном и оценки аналогов ПБД (PBD) с оптимальной противоопухолевой эффективностью с приемлемой безопасностью.
СВОЙСТВА БЕЗОПАСНОСТИ/ТОКСИЧНОСТИ
Конъюгаты антитело-лекарственное средство (КАЛС (ADC)) по изобретению и компараторные КАЛС (ADC) были изучены с учетом их свойств, связанных с безопасностью и токсичностью.
Анти-HER2 hu7C2 антитело ADC-108 с моноалкилирующим моноамином (LD-52) показало улучшенную толерантность у мышей CD-1 и улучшенный терапевтический индекс (ТИ) относительно соответствующего анти-HER2 hu7C2 антитела ADC-201 с диалкилирующим имином (C-1) при расчете по процентному изменению массы тела в течение 45 дней после дозирования (50, 75, 125 мкг (мкг) на кг в дни 0, 7, 14. Максимальная переносимая доза (МПД) для ADC-108 составляет 200 мкг/кг, тогда как МПД для ADC-201 составляет 75 мкг/кг. Сигналы токсичности у крыс (Sprague-Dawley) и яванских макак могут включать в себя кратковременное снижение количества ретикулоцитов, незначительные изменения цвета кожи и шелушение вблизи места инъекции, пропотевание жидкости из сосудов, повышенные количества печеночных ферментов, дегенерацию нервов, истощение костного мозга/лимфоидной ткани, показания почек, глаз и легких и клинические проявления.
Предварительные данные безопасности указывают на значительное преимущество КАЛС (ADC) по изобретению относительно компараторных КАЛС (ADC).
ФАРМАЦЕВТИЧЕСКИЕ СОСТАВЫ
Фармацевтические составы терапевтических конъюгатов антитело-лекарственное средство (КАЛС (ADC)) по изобретению обычно готовят для парентерального введения, то есть болюсной, внутривенной, внутриопухолевой инъекции с фармацевтически приемлемым парентеральным носителем и в стандартной дозе для инъекций. Конъюгат антитело-лекарственное средство (КАЛС (ADC)), имеющий желаемую степень чистоты, необязательно смешивают с фармацевтически приемлемыми разбавителями, носителями, вспомогательными веществами или стабилизаторами (Remington's Pharmaceutical Sciences (1980) 16th edition, Osol, A. Ed.), в форме лиофилизированного препарата или водного раствора.
СПОСОБЫ ЛЕЧЕНИЯ КОНЪЮГАТАМИ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО
Предполагается, что конъюгаты антитело-лекарственное средство (КАЛС (ADC)) по настоящему изобретению могут быть использованы для лечения различных заболеваний или патологий, например, характеризующихся сверхэкспрессией опухолевого антигена. Иллюстративные заболевания или гиперпролиферативные патологии включают доброкачественные или злокачественные солидные опухоли и гематологические патологии, такие как лейкемия и лимфоидные злокачественные опухоли. Другие включают в себя нейрональные, глиальные, астроцитальные, гипоталамичесике, железистые, макрофагальные, эпителиальные, стромальные, бластоцельные, воспалительные, ангиогенные и иммунологические, включая аутоиммунные, патологии.
Конъюгаты антитело-лекарственное средство (КАЛС (ADC)) по изобретению можно вводить любым способом, подходящим для состояния, подлежащего лечению. КАЛС (ADC) обычно вводят парентерально, то есть инфузией, подкожно, внутримышечно, внутривенно, внутрикожно, интратекально и эпидурально.
В целом, как правило, заболевание или патология, подлежащая лечению, представляет собой гиперпролиферативное заболевание, такое как рак. Примеры рака, подлежащего лечению, в данном документе включают, но не ограничиваются лишь этими: карциному, лимфому, бластому, саркому и лейкемию, или лимфоидные злокачественные опухоли. Более конкретные примеры таких видов рака включают плоскоклеточный рак (например, эпителиальный плоскоклеточный рак), рак легкого, включая мелкоклеточный рак легкого, немелкоклеточный рак легкого, аденокарциному легкого и плоскоклеточную карциному легкого, рак брюшины, гепатоцеллюлярный рак, рак желудка или желудочный рак, включая рак желудочно-кишечного тракта, рак поджелудочной железы, глиобластому, рак шейки матки, рак яичников, рак печени, рак мочевого пузыря, гепатому, рак молочной железы, рак толстой кишки, рак прямой кишки, колоректальный рак, карциному эндометрия или матки, карциному слюнной железы, рака почек или почечный рак, рак предстательной железы, рак вульвы, рак щитовидной железы, карциному печени, анальную карциному, карциному полового члена, а также рак головы и шеи.
Аутоиммунные заболевания, для которых соединения КАЛС (ADC) могут применяться в лечении, включают: ревматологические патологии (такие как, например, ревматоидный артрит, синдром Шегрена, склеродермия, волчанка, такая как системная красная волчанка (СКВ) и волчаночный нефрит, полимиозит/дерматомиозит, криоглобулинемия, синдромом с антифосфолипидными антителами и псориатический артрит), остеоартрит, аутоиммунные заболевания желудочно-кишечного тракта и печени (такие как, например, воспалительные заболевания кишечника (например, язвенный колит и болезнь Крона), аутоиммунный гастрит и пернициозная анемия, аутоиммунный гепатит, первичный билиарный цирроз, первичный склерозирующий холангит и глютеиновую болезнь), васкулит (например, ассоциированный с АНЦА васкулит, в том числе васкулит Чарга-Страуса, гранулематоз Вегенера и полиартериит), аутоиммунные неврологические расстройства (такие как, например, рассеянный склероз, опсо-миоклональный синдром, миастения гравис, болезнь Девика, болезнь Паркинсона, болезнь Альцгеймера и аутоиммунные полинейропатии), почечные расстройства (такие как, например, гломерулонефрит, синдром Гудпасчера, и болезнь Бергера), аутоиммунные дерматологические патологии (такие как, например, псориаз, крапивница, крапивница, обыкновенная пузырчатка, буллезный пемфигоид и кожная красная волчанка), гематологические патологии (такие как, например, тромбоцитопеническая пурпура, тромботическая тромбоцитопеническая пурпура, пост -трансфузионная пурпура и аутоиммунная гемолитическая анемия), атеросклероз, увеит, аутоиммунные заболевания слуха (такие как, например, заболевание внутреннего уха и потеря слуха), Болезнь Бехчета, синдром Рейно, трансплантацию органов и аутоиммунные эндокринные патологии (такие как, например, связанные с диабетом аутоиммунные заболевания, такие как инсулинзависимый сахарный диабет (ИЗСД), болезнь Аддисона и аутоиммунная болезнь щитовидной железы (например, болезнь Грейвса и тиреоидит)). Более предпочтительными такими заболеваниями являются, например, ревматоидный артрит, язвенный колит, ассоциированный с АНЦА васкулит, волчанка, рассеянный склероз, синдром Шегрена, болезнь Грейвса, инсулино-зависимый сахарный диабет, пернициозная анемия, тиреоидит и гломерулонефрит.
Для профилактики или лечения заболевания, соответствующая дозировка КАЛС (ADC) будет зависеть от типа заболевания, которое подлежит лечению, как определено выше, тяжести и течения заболевания, вводят ли молекулу в профилактических или лечебных целях, предыдущей терапии, клинической истории пациента и его реакции на антитело, и усмотрение лечащего врача. Молекулу соответствующим образом вводят пациенту за один раз, или в течение ряда процедур. В зависимости от типа и тяжести заболевания, от около 1 мкг/кг до 15 мг/кг (например, 0,1-20 мг/кг) молекулы составляет начальная потенциальная доза для введения пациенту, будь то, например, одно или нескольких отдельных введений, или непрерывная инфузия. Типичная суточная дозировка может находится в диапазоне от около 1 мкг/кг до 100 мг/кг или больше, в зависимости от вышеуказанных факторов. Типичная доза КАЛС (ADC) для введения пациенту находится в диапазоне от около 0,1 до около 10 мг/кг веса пациента.
В терапии антитела или иммуноконъюгаты по изобретению могут применятся как самостоятельно, так и в сочетании с другими веществами. Например, антитело или иммуноконъюгат по изобретению может быть введен совместно, по меньшей мере, с одним дополнительным терапевтическим веществом.
В некоторых вариантах осуществления, конъюгат hu7C2.v.2.2.LA антитело-лекарственное средство (hu7C2 КАЛС (ADC)) совместно вводят с дополнительным терапевтическим веществом, которое является другим антителом или иммуноконъюгатом, что связывается с HER2. В некоторых вариантах осуществления, дополнительным терапевтическим веществом является i) антитело или иммуноконъюгат, которое(ый) связывается с доменом II HER2, и/или ii) антитело или иммуноконъюгат, которое(ый) связывается с доменом IV или HER2. В некоторых вариантах осуществления, дополнительным терапевтическим веществом является i) антитело или иммуноконъюгат, которое(ый) связывается с эпитопом 2C4, и/или ii) антитело или иммуноконъюгат, которое(ый) связывается с эпитопом 4D5.
В некоторых вариантах осуществления, конъюгат hu7C2.v.2.2.LA антитело-лекарственное средство (hu7C2 КАЛС (ADC)) совместно вводят с одним или больше дополнительными терапевтическими веществами, выбранными из трастузумаба (Herceptin®), T-DM1 (Kadcyla®) и пертузумаба (Perjeta®). В некоторых вариантах осуществления, КАЛС (ADC) hu7C2 вводится совместно с трастузумабом. В некоторых вариантах осуществления, КАЛС (ADC) hu7C2 вводится совместно с T-DM1. В некоторых вариантах осуществления, КАЛС (ADC) hu7C2 вводится совместно с пертузумабом. В некоторых вариантах осуществления, КАЛС (ADC) hu7C2 вводится совместно с трастузумабом и пертузумабом. В некоторых вариантах осуществления, КАЛС (ADC) hu7C2 вводится совместно с T-DM1 и пертузумабом.
В некоторых вариантах осуществления, дополнительное терапевтическое вещество представляет собой антагонист, связывающийся с компонентом сигнального пути PD-1, такое как связывающийся с PD-L1 антагонист.
Такие комбинированные виды терапии, как отмеченные выше, охватывают комбинированное введение (когда два или больше терапевтических вещества включены в те же или отдельные составы), а также раздельное введение, в последнем случае введение антитела или иммуноконъюгата по настоящему изобретению может осуществляться до, одновременно и/или после введения дополнительного терапевтического вещества и/или адъюванта. Антитела или иммуноконъюгаты по настоящему изобретению также могут быть использованы в комбинации с лучевой терапией.
Антитело или иммуноконъюгат по изобретению (и любое дополнительное терапевтическое вещество) может быть введено любыми подходящими способами, включая парентеральное, внутрилегочное и интраназальное, и, при желании для местного лечения, внутривенное введение. Парентеральные инфузии включают внутримышечное, внутривенное, внутриартериальное, внутрибрюшинное или подкожное введение. Дозирование может быть выполнено любым подходящим путем, например, путем инъекций, таких как внутривенные или подкожные инъекции, в зависимости от того, является ли введение кратковременным или продолжительным. В настоящем документе рассматриваются различные графики дозирования, включая, но не ограничиваясь лишь этими: однократное или множественное введение в различные моменты времени, болюсное введение и прерывистую инфузию.
Антитела или иммуноконъюгаты по изобретению будут приготовлены в состав, дозированы и введены в соответствии с надлежащей медицинской практикой. Факторы, которые следует учитывать в данном контексте, включают конкретную патологию, подлежащую лечению, конкретное млекопитающее, подвергаемое лечению, клиническое состояние отдельно взятого пациента, причину патологии, место доставки вещества, способ введения, схему введения и другие факторы, известные практикующим врачам. Необязательно, но в некоторых случаях антитело или иммуноконъюгат могут быть приготовлены в виде состава с одним или больше веществами, используемыми в настоящее время для предотвращения или лечения рассматриваемой патологии. Эффективное количество таких других веществ зависит от количества антитела или иммуноконъюгата, присутствующего в составе, вида патологии или лечения и других факторов, описанных выше. Такие вещества, как правило, вводятся в тех же дозах и с помощью тех же путей, которые описаны в настоящем документе, или в дозе, составляющей от около 1 до 99% дозы, описанной в настоящем документе, или в любой дозе и с помощью любого пути, который эмпирически/клинически определен как пригодный.
Для профилактики или лечения заболевания соответствующая доза антитела или иммуноконъюгата по изобретению (при использовании отдельно или в комбинации с одним или больше другими дополнительными терапевтическими веществами), будет зависеть от типа заболевания, подлежащего лечению, типа антитела или иммуноконъюгата, тяжести и течения заболевания, от того, применяется антитело или иммуноконъюгат в профилактических либо в терапевтических целях, предшествующей терапии, истории болезни пациента и реакции на антитело или иммуноконъюгат, и усмотрения лечащего врача. Антитело или иммуноконъюгат соответствующим образом вводят пациенту однократно или в ходе курса лечения. В зависимости от типа и тяжести заболевания, первоначальная предполагаемая доза антитела или иммуноконъюгата для введения пациенту например, посредством одного или более раздельных введений или непрерывной инфузии, может составлять от около 1 мкг/кг до 15 мг/кг (например, 0,1 мг/кг - 10 мг/кг). Типичная ежедневная доза может находиться в диапазоне от около 1 мкг/кг до 100 мг/кг или больше в зависимости от вышеупомянутых факторов. При повторных введениях в течение нескольких дней или дольше, в зависимости от состояния, лечение, как правило, должно поддерживаться до тех пор, пока не произойдет желаемое подавление симптомов болезни. Одна типичная доза антитела или иммуноконъюгата находится в диапазоне от около 0,05 мг/кг до около 10 мг/кг. Так, пациенту может быть введена одна или больше доз, составляющих около 0,5 мг/кг, 2,0 мг/кг, 4,0 мг/кг или 10 мг/кг (или любые их комбинации). Такие дозы можно вводить с перерывами, например, каждую неделю или каждые три недели (например, таким образом, что пациент получает от около двух до около двадцати, или, например, около шести доз антитела). Можно вводить начальную повышенную нагрузочную дозу, за которой следует одна или больше пониженные дозы. Тем не менее, могут применяться и другие схемы приема. Эффективность данной терапии легко контролировать с помощью обычных методик и анализов.
ГОТОВЫЕ ИЗДЕЛИЯ
В другом аспекте осуществления настоящего изобретения, предлагается изделие, или «набор», содержащее(ий) материалы, пригодные для лечения патологий как описано выше. Готовое изделие содержит контейнер и этикетку или листок-вкладыш, которая(ый) находится на контейнере или идет вместе с ним. Подходящие контейнеры включают, например, бутылки, флаконы, шприцы, блистерные упаковки и т.д. Контейнеры могут быть изготовлены из различных материалов, таких как стекло или пластик. Контейнер содержит композицию конъюгата антитело-лекарственное средство (КАЛС (ADC)), которая является эффективной для лечения патологии и может иметь стерильный порт доступа (например, контейнер может представлять собой пакет с раствором или флакон с пробкой, прокалываемой иглой для подкожной инъекции). По меньшей мере одно активное вещество в композиции представляет собой КАЛС (ADC). Этикетка или листок-вкладыш указывает на то, что композиция применяется для лечения патологии по выбору, такой как рак. В альтернативном или дополнительном варианте изделие может дополнительно содержать второй (или третий) контейнер, содержащий фармацевтически приемлемый буфер, такой как бактериостатическая вода для инъекций (БВДИ (BWFI)), фосфатно-буферный солевой раствор, раствор Рингера или раствор декстрозы. Изделие может дополнительно включать в себя другие материалы, желательные с коммерческой и потребительской точки зрения, в том числе другие буферы, разбавители, фильтры, иглы и шприцы.
ПРИМЕРЫ
Пример 1. Получение моноалкилирующих пирролбензодиазепиновых лекарственных компонентов (таблица 1а)
Синтез (S)-7-метокси-8-((5-(((S)-7-метокси-2-метилен-5-оксо-2,3,5,10,11,11a-гексагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-8-ил)окси)пентил)окси)-2-метилен-2,3-дигидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-5(11aH)-она DM-1
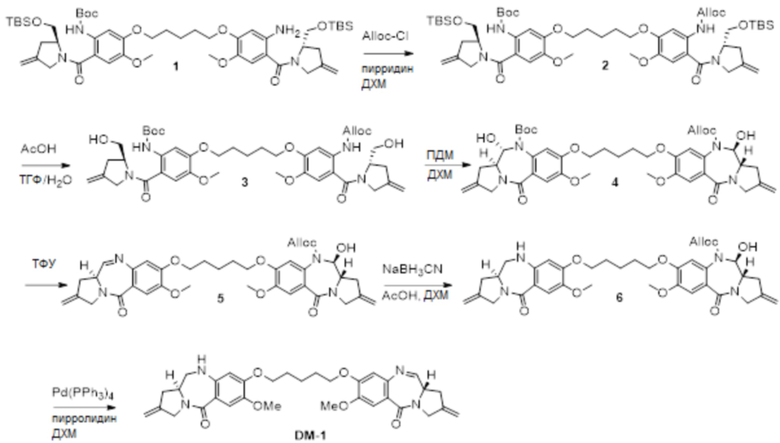
К раствору трет-бутил (5-((5-(5-амино-4-((S)-2-(((трет-бутилдиметилсилил)окси)метил)-4-метиленпирролидин-1-карбонил)-2-метоксифенокси)пентил)окси)-2-((S)-2-(((трет-бутилдиметилсилил)окси)метил)-4-метиленпирролидин-1-карбонил)-4-метоксифенил)карбамат 1 (0,50 г, 0,524 ммоль) в ДХМ (5,0 мл) добавляли пиридин (83 мг, 1,05 ммоль), с последующим добавлением аллилхлорформиата, Alloc-Cl (95 мг, 0,786 ммоль, Sigma Aldrich, номер ХРС(CAS - Chemical Abstracts Service) 2937-50-0) при 16 oC. Смесь перемешивали в течение 12 часов. Смесь разбавляли ДХМ (30 мл) и промывали водным HCl (1 н., 5,0 мл ×2), а затем водным NaHCO3 (5 мл ×2). Органический слой концентрировали с получением неочищенного продукта, который очищали колонкой для отгона легких фракции (20% EtOAc в петролейном эфире) с получением третбутил (5-((5-(5-(((аллилокси)карбонил)амино)-4-((S)-2-(((трет-бутилдиметилсилил)окси)метил)-4-метиленпирролидин-1-карбонил)-2-метоксифенокси)пентил)окси)-2-((S)-2-(((трет-бутилдиметилсилил)окси)метил)-4-метиленпирролидин-1-карбонил)-4-метоксифенил)карбамата 2 (500 мг, 92%) в виде бесцветного масла. ЖХМС: (ИЭР(ионизация электрораспылением, ESI - Electrospray ionization), 10-80, AB, 1,5 мин), ВУ (время удержания, ВУ - retention time)=1,200 мин, масса/заряд=1037 [M+1]+.
Раствор соединения 2 (500 мг, 0,48 ммоль) в HOAc/ТГФ(тетрагидрофуран,)/H2O (6 мл/3 мл/2 мл) перемешивали при комнатной температуре в течение 1 дня. Раствор разбавляли EtOAc (60 мл), промывали H2O (20 мл × 4), водным раствором NaHCO3 (20 мл × 2), и H2O (20 мл). Органический слой сушили над Na2SO4, фильтровали и концентрировали под вакуумом, чтобы получить трет-бутил (5-((5-(5-(((аллилокси)карбонил)амино)-4-((S)-2-(гидроксиметил)-4-метиленпирролидин-1-карбонил)-2-метоксифенокси)пентил)окси)-2-((S)-2-(гидроксиметил)-4-метиленпирролидин-1-карбонил)-4-метоксифенил)карбамат 3 (390 g, 100%) в виде масла.
К перемешиваемому раствору соединения 3 (200 мг, 0,247 ммоль) в безводном ДХМ (15 мл) добавляли перйодат Десса-Мартина (419 мг, 0,988 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 2 часов. Реакцию гасили (деактивация любых непрореагировавших реагентов) с помощью водного раствора Na2SO3 (30 мл) при 0°C и экстрагировали ДХМ (20 мл × 3). Объединенный органический слой промывали насыщенным водным раствором хлорида натрия (20 мл), сушили над Na2SO4, фильтровали и концентрировали. Остаток очищали с помощью предварительной ТСХ (ДХМ /MeOH=20:1) чтобы получить аллил (11S,11aS)-8-((5-(((11S,11aS)-10-(трет-бутоксикарбонил)-11-гидрокси-7-метокси-2-метилен-5-оксо-2,3,5,10,11,11a-гексагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-8-ил)окси)пентил)окси)-11-гидрокси-7-метокси-2-метилен-5-оксо-2,3,11,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-10(5H)-карбоксилат 4 (80 мг, 40,2%) в виде бесцветного твердого вещества. ЖХМС (ИЭР(ESI)): ВУ=0,709 мин, M-Boc-H2O+H+=687,1. Способ=5-95AB/1,5 мин.
Раствор соединения 4 (80 мг, 0,099 ммоль) в ТФК (2,0 мл) перемешивали при 0°C в течение 0,5 часа. Раствор добавляли по каплям в насыщенный раствор NaHCO3 (120 мл) при 0°C. Смесь экстрагировали ДХМ (20 мл ×3) и объединенный органический слой сушили над Na2SO4, фильтровали и концентрировали с получением неочищенного аллил (11S,11aS)-11-гидрокси-7-метокси-8-((5-(((S)-7-метокси-2-метилен-5-оксо-2,3,5,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-8-ил)окси)пентил)окси)-2-метилен-5-оксо-2,3,11,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-10(5H)-карбоксилата 5 (50 мг, 73,5%).
К перемешиваемому раствору соединения 5 (50 мг, 0,073 ммоль) в безводном ДХМ (4,0 мл) добавляли HOAc (13 мг, 0,219 ммоль), а затем NaBH3CN (23 мг, 0,365 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Затем смесь концентрировали под вакуумом и очищали предварительной ТСХ (ДХМ /MeOH=9:1), чтобы получить аллил-(11S,11aS)-11-гидрокси-7-метокси-8-((5-(((S)-7-метокси-2-метилен-5-оксо-2,3,5,10,11,11a-гексагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-8-ил)окси)пентил)окси)-2-метилен-5-оксо-2,3,11,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-10(5H)-карбоксилат 6 (40 мг, 80,0%) в виде бесцветного твердого вещества. ЖХМС (ИЭР (ESI)): ВУ=3,085 мин, M+H+=689,1. способ=10-80AB /7 мин.
К перемешиваемому раствору соединения 6 (40 мг, 0,058 ммоль) в безводном ДХМ (3,0 мл) добавляли пирролидин (21 мг, 0,29 ммоль), а затем Pd(PPh3)4 (7,0 мг, 0,006 ммоль). Реакционную смесь перемешивали при комнатной температуре в атмосфере N2 в течение 2 часов. Затем смесь концентрировали под вакуумом и очищали предварительной ТСХ (ДХМ /MeOH=1:1) с получением DM-1 (12 мг, 35,3%) в виде не совсем белого твердого вещества. ЖХМС (ИЭР (ESI)): ВУ=0,651 мин, M+H+=587,1. способ=5-95AB /1,5 мин 1H ЯМР (400 MГц, DCCl3) δ 7,67 (d, J=4,4 Гц, 1H), 7,57 (s, 1H), 7,49 (s, 1H), 6,79 (s, 1H), 6,04 (s, 1H), 5,18 (d, J=11,6 Гц, 2H), 5,04 (d, J=11,2 Гц, 2H), 4,41-4,37 (m, 1H), 4,28-4,25 (m, 3H), 4,13-4,00 (m, 3H), 3,98-3,95 (m, 2H), 3,93 (s, 3H), 3,89-3,85 (m, 1H), 3,82 (s, 3H), 3,54 (d, J=30 Гц, 1H), 3,34-3,28 (dd, J=12,4, 9,2 Гц, 1H), 3,15-3,08 (m, 1H), 2,96-2,86 (m, 2H), 2,44-2,39 (dd, J=15,2, 6,0 Гц, 1H), 1,95-1,90 (m, 4H), 1,67-1,62 (m, 2H).
Синтез (S)-7-метокси-8-((5-(((S)-7-метокси-2-метилен-5-оксо-2,3,5,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-8-ил)окси)пентил)окси)-2-метилен-2,3-дигидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-5,11(10H,11aH)-диона DM-2
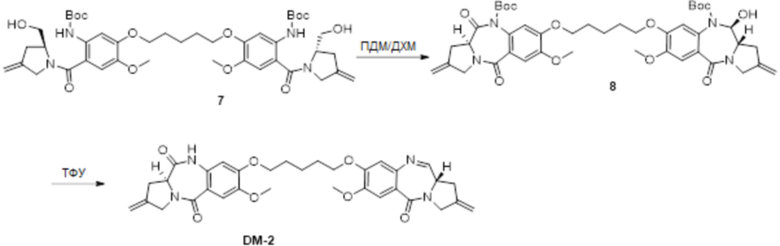
К перемешиваемому раствору ди-трет-бутил ((pentane-1,5-диилбис(окси))бис(6-((S)-2-(гидроксиметил)-4-метиленпирролидин-1-карбонил)-4-метокси-3,1-фенилен))дикарбамата 7 (200 мг, 0,24 ммоль) в безводном ДХМ (20 мл) был добавлен ДМП (перйодат Десса-Мартина, DMP) (610 мг, 1,44 ммоль) при 0°C. Реакционную смесь перемешивали при комнатной температуре в течение 3 часов. Смесь разбавляли EtOAc (100 мл) и гасили водным раствором Na2SO3 (30 мл) при 0°C. Органический слой промывали H2O (30 мл ×3), водным раствором NaHCO3 (30 мл), и H2O (30 мл), затем сушили над (Na2SO4), фильтровали и концентрировали. Остаток очищали с помощью предварительной ВЭЖХ, чтобы получить третбутил (S)-8-((5-(((11S,11aS)-10-(трет-бутоксикарбонил)-11-гидрокси-7-метокси-2-метилен-5-оксо-2,3,5,10,11,11a-гексагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-8-ил)окси)пентил)окси)-7-метокси-2-метилен-5,11-диоксо-2,3,11,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-10(5H)-карбоксилат 8 (58 мг, 30,0%) в виде белого твердого вещества. ЖХМС (ИЭР (ESI)): ВУ=0,748 мин, M+Na+=841,4. способ=5-95AB /1,5 мин.
Раствор соединения 8 (58 мг, 0,07 ммоль) в 95% ТФК/H2O (2,0 мл) перемешивали при 0°C в течение 2 часов. Затем раствор добавляли по каплям в насыщенный раствор NaHCO3 (120 мл) при 0°C. Смесь экстрагировали ДХМ (20 мл ×3). Объединенный органический слой сушили над Na2SO4, фильтровали, концентрировали и очищали подготавливающей ВЭЖХ с получением DM-2 (15,7 мг, 38%) в виде белого твердого вещества. 1H ЯМР (400 МГц, CDCl3) δ м.д. 1,65-1,73 (m, 2 H) 1,89-2,00 (m, 4 H) 2,77-2,89 (m, 1 H) 2,91-3,00 (m, 1 H) 3,08-3,19 (m, 1 H) 3,46 (d, J=16,6 Гц, 1 H) 3,91 (s, 3 H) 3,94 (s, 3 H) 4,02 (t, J=6,5 Гц, 2 H) 4,06-4,19 (m, 2 H) 4,20-4,26 (m, 2 H) 4,30 (s, 2 H) 4,43 (d, J=15,6 Гц, 1 H) 5,09-5,26 (m, 4 H) 6,41 (s, 1 H) 6,80 (s, 1 H) 7,43 (s, 1 H) 7,51 (s, 1 H) 7,71 (d, J=4,5 Гц, 1 H) 7,83 (s, 1 H).
Синтез (S)-8-метокси-9-((5-(((S)-7-метокси-2-метилен-5-оксо-2,3,5,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-8-ил)окси)пентил)окси)-1,3,4,12a-тетрагидро-6H-бензо[e][1,4]оксазино[4,3-a][1,4]диазепин-6,12(11H)-диона DM-3
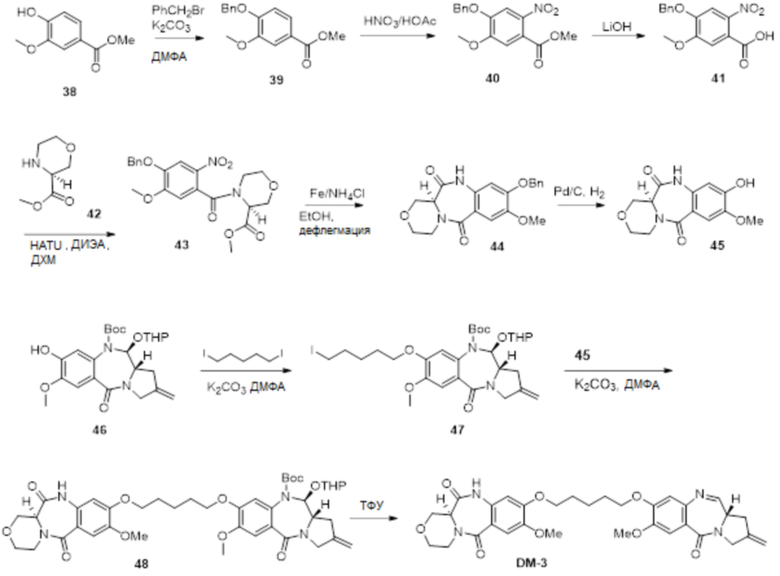
Раствор метил-4-гидрокси-3-метоксибензоата 38 (3,0 г, 16,5 ммоль) в ДМФА (DMF) (100 мл) добавляли бензилбромид (4,22 г, 24,7 ммоль) и K2CO3 (4,56 г, 32,9 ммоль). Реакционную смесь перемешивали при 100°C в течение 3 часов. Смесь концентрировали под вакуумом и растворяли в воде (50 мл), экстрагировали EtOAC (30 мл ×2), промывали NaCl (30 мл), сушили над Na2SO4. Ее концентрировали и очищали хроматографией на силикагеле (0-30% EtOAc в петролейном эфире) с получением метил 4-(бензилокси)-3-метоксибензоата 39 (3,8 г, 13,5 ммоль, выход 82,2%) в виде белого твердого вещества. ЖХМС (5-95AB/1,5 мин): КТ=0,787 мин, [M+H]+272,9.
Раствор 39 (2,0 г, 7,34 ммоль) в HOAc (5,0 мл) добавляли к смеси HOAc (5,0 мл) и HNO3 (20,6 мл, 441 ммоль) при 0 °C. Реакционную смесь перемешивали при 20 °С в течение 30 мин. Смесь выливали в ледяную воду (100 мл) и доводили рН до 5-6. Смесь фильтровали и фильтраты концентрировали с получением метил-4-(бензилокси)-5-метокси-2-нитробензоата 40 (2,3 г, 7,25 ммоль, выход 98,7%) в виде желтого твердого вещества.
Раствор 40 (2,3 г, 7,25 ммоль) в МеОН (20 мл) добавляли к раствору LiOH (2,25 мл, 36,24 ммоль) в воде (5 мл). Реакционную смесь перемешивали при 20°C в течение 2 часов. Смесь выливали в воду (50 мл) и промывали EtOAc (50 мл). pH водной фазы доводили до 3-4 с помощью 2 М HCl и экстрагировали EtOAc (50 мл ×3). Промывали NaCl (25 мл), сушили над Na2SO4 и концентрировали под вакуумом с получением неочищенной 4-(бензилокси)-5-метокси-2-нитробензойной кислоты 41 (2,0 г, 6,59 ммоль, выход 91%) в виде белого твердого вещества.
Смесь 41 (460,0 мг, 1,52 ммоль) и метил (S)-морфолин-3-карбоксилата 42, регистрационный ХРС(CAS) № 741288-31-3, Hicks, F. et al, (2013) Organic Process Research & Development, 17(5):829-837, (330 мг, 2,28 ммоль) и диизопропилэтиламина, ДИЭА (DIEA) (392 мг, 3,03 ммоль) в ДХМ (30 мл) добавляли HATU (865 мг, 2,28 ммоль). Реакционный раствор перемешивали при 20°C в течение 8 часов. Раствор концентрировали под вакуумом и очищали хроматографией на силикагеле (0-50% EtOAC в петролейном эфире) с получением метил(S)-4-(4-(бензилокси)-5-метокси-2-нитробензоил)морфолин-3-карбоксилата 43 (520 мг, 1,21 ммоль, выход 79,7%) в виде желтого масла. ЖХМС (5-95AB/1,5 мин): ВУ=0,731мин, [M+Na]+453,0.
Раствор NH4Cl (646 мг, 12,1 ммоль) в EtOH (20 мл) и воде (15 мл) добавляли 43 (520 мг, 1,21 ммоль) и железо (539 мг, 9,67 ммоль). После того как реакционную смесь перемешивали при 90°C в течение 12 часов, ее фильтровали и фильтраты экстрагировали EtOAc (50 мл ×3), промывали NaCl (20 мл), сушили над Na2SO4 и концентрировали под вакуумом. Реакционную смесь очищали хроматографией на силикагеле (0-30% EtOAc в петролейном эфире) с получением (S)-9-(бензилокси)-8-метокси-1,3,4,12a-тетрагидро-6H-бензо[e][1,4]оксазино[4,3-a][1,4]диазепин-6,12(11H)-диона 44 (320 мг, 0,84 ммоль, выход 69,7%) в виде белого твердого вещества. ЖХМС (5-95AB/1,5 мин): ВУ=0,638 мин, [M+H]+368,9.
Раствор 44 (260 мг, 0,71 ммоль) в ДХМ (10 мл) и МеОН (1,0 мл) добавляли 10% палладия на угле (26,0 мг, 0,020 ммоль). Реакционную смесь перемешивали при 18°C в течение 1 часа при H2 (15 фунтов на квадратный дюйм). Реакционную смесь фильтровали и концентрировали под вакуумом, получая (S)-9-гидрокси-8-метокси-1,3,4,12a-тетрагидро-6H-бензо[e][1,4]оксазино[4,3-a][1,4]диазепин-6,12(11H)-дион 45 (100 мг, 0,359 ммоль, 50,9%) в виде белого твердого вещества.
Раствор трет-бутил (11S,11aS)-8-гидрокси-7-метокси-2-метилен-5-оксо-11-((тетрагидро-2H-пиран-2-ил)окси)-2,3,11,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-10(5H)-карбоксилат 46 (200 мг, 0,43 ммоль) в ДМФА (DMF) (5,0 мл) добавляли K2CO3 (60 мг, 0,43 ммоль) и 1,5-дииодопентан (703 мг, 2,17 ммоль). Реакционную смесь перемешивали при 90°C в течение 12 часов. Реакционную смесь концентрировали и очищали с помощью хроматографии на силикагеле (0-50% EtOAc в петролейном эфире) с получением трет-бутил (11S,11aS)-8-((5-иодпентил)окси)-7-метокси-2-метилен-5-оксо-11-((тетрагидро-2H-пиран-2-ил)окси)-2,3,11,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-10(5H)-карбоксилата 47 (129 мг, 0,191 ммоль, 43,9%) в виде желтого масла. ЖХМС (5-95AB/1,5 мин): ВУ=0,907 мин, [M+H]+657,1.
Смесь 47 (100 мг, 0,150 ммоль), 45 (50,9 мг, 0,18 ммоль) и K2CO3 (31,6 мг, 0,23 ммоль) в ДМФА (DMF) (5,0 мл). Смесь перемешивали при 90°C в течение 3 часов. Смесь концентрировали под вакуумом и очищали хроматографией (0-5% MeOH в ДХМ Rf=0,4), получая трет-бутил (11S,11aS)-7-метокси-8-((5-(((S)-8-метокси-6,12-диоксо-3,4,6,11,12,12a-гексагидро-1H-бензо[e][1,4]оксазино[4,3-a][1,4]диазепин-9-ил)окси)пентил)окси)-2-метилен-5-оксо-11-((тетрагидро-2H-пиран-2-ил)окси)-2,3,11,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-10(5H)-карбоксилат 48 (75 мг, 0,093 ммоль, выход 61%) в виде бесцветного масла.
Соединение 48 (75,0 мг, 0,090 ммоль) добавляли ТФК (1,9 мл) и воду (0,10 мл) при 0°С. Смесь перемешивали при 17°C в течение 1 часа. Реакционную смесь выливали в насыщенный раствор NaHCO3 (200 мл) и экстрагировали ДХМ (100 мл × 3), промывали насыщенным раствором соли (50 мл), сушили и очищали с помощью подготавливающей ТСХ (4% метанола в ДХМ Rf=0,5), получая DM-3 (18,9 мг, 0,030 ммоль, выход 32,3%) в виде белого твердого вещества. ЖХМС (5-95AB/1,5 мин): ВУ=0,633 мин, [M+H]+ 605,2, 1H ЯМР (400 МГц, CDCl3) δ 8,16 (s, 1H), 7,64 (d, J=4,4 Гц, 1H), 7,43 (s, 1H), 7,22 (d, J=23,2 Гц, 1H), 6,73 (d, J=2,4 Гц, 1H), 6,35(d, J=2,8 Гц, 1H), 5,11 (d, J=10,8 Гц, 2H), 4,41 (s, 3H), 4,38 (s, 2H), 4,22 (s, 3H), 4,05 (s, 3H), 4,04 (s, 3H), 4,02 (s, 3H), 3,95-3,92 (m, 1H), 3,86 (s, 1H), 3,83-3,62 (m, 1H), 3,18 (s, 1H), 2,88 (d, J=30,8 Гц, 1H), 1,86 (s, 4H) 1,79-1,62 (m, 2H).
Синтез (S)-7-метокси-8-((5-(((S)-7-метокси-5-оксо-2,3,5,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a]азепин-8-ил)окси)пентил)окси)-2-метилен-1,2,3,11a-тетрагидро-5H-бензо[e]пирроло[1,2-a][1,4]диазепин-5-он DM-5
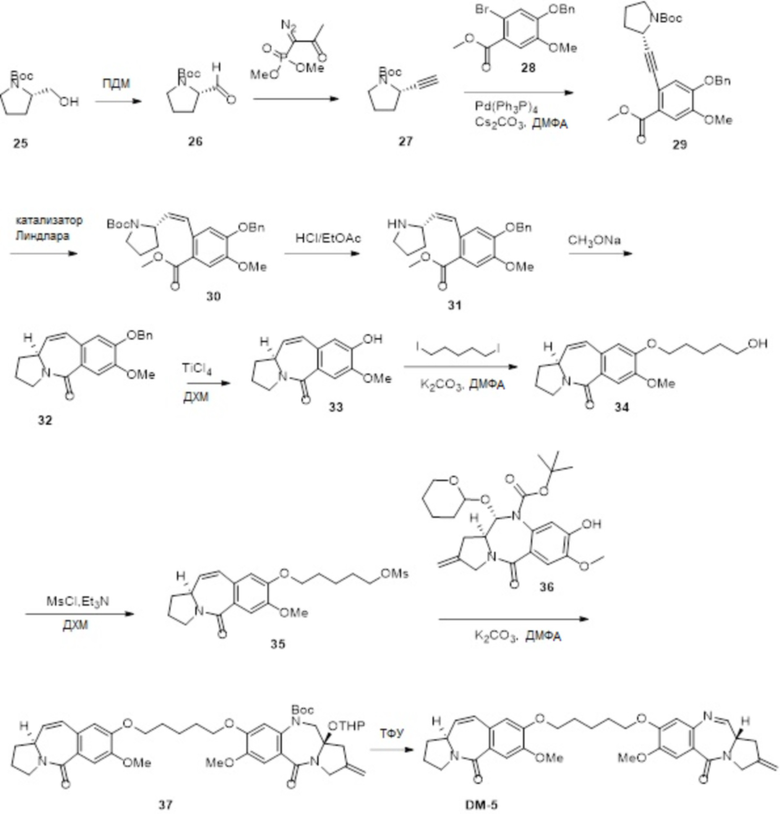
К раствору трет-бутил (S)-2-(гидроксиметил)пирролидин-1-карбоксилат 25 (3,0 г, 14,9 ммоль) в ДХМ (80 мл) добавляли перйодат Десса-Мартина, ПДМ (9,48 г, 22,4 ммоль). После перемешивания смеси при 0°C в течение 1 часа добавляли Na2S2O3 (50 мл)/NaHCO3 (50 мл) и МТБЭ (метил-трет-бутиловый эфир, MTBE) (130 мл). Органическую фазу промывали водой (60 мл × 3) и концентрировали с получением трет-бутил-(S)-2-формилпирролидин-1-карбоксилата 26 (2,9 г, 14,6 ммоль, выход 97,6%) в виде бесцветного масла.
К раствору соединения 26 (2,9 г, 14,6 ммоль) и диметил (1-диазо-2-оксопропил) фосфоната в MeOH (20 мл) добавляли K2CO3 (6,03 г, 43,7 ммоль). После того как реакционную смесь перемешивали при 20°C в течение 1 часа, ее концентрировали под вакуумом, остаток очищали колоночной хроматографией (10% EtOAc в РЕ) с получением трет-бутил (S)-2-этинилпирролидин-1-карбоксилата 27 (2,0 г, 10,24 ммоль, выход 70,4%) в виде бесцветного масла.
К раствору соединения 27 (2,0 г, 10,2 ммоль) и метил-4- (бензилокси)-2-бром-5-метоксибензоата 28 (5,4 г, 15,4 ммоль) в ДМФА (DMF) (50 мл) добавляли Cs2CO3 (3,97 г, 20,5 ммоль) и Pd(PPh3)4 (785 мг, 1,54 ммоль). Смесь перемешивали при 95°C в атмосфере азота в течение 1 часа. Смесь концентрировали и очищали колоночной флэш-хроматографией (20% EtOAc в РЕ) с получением трет-бутил (S)-2-((5-(бензилокси)-4-метокси-2-(метоксикарбонил)фенил) этинил)пирролидин-1-карбоксилата 29 (1,60 г, 2,44 ммоль, выход 23,8%) в виде бесцветного масла. ЖХМС (5-95AB/1,5 мин): ВУ=0,994 мин, [M+H-56]+410,0.
К раствору соединения 29 (2,0 г, 4,3 ммоль) в MeOH (10 мл) добавляли Pd/CaCO3 (200,0 мг, 21,5 ммоль). Смесь перемешивали при 30°C в течение 1 часа в атмосфере водорода (1 атм). Смесь фильтровали и фильтрат концентрировали с получением неочищенного продукта, который очищали колоночной флэш-хроматографией (10% EtOAc в РЕ), чтобы получить трет-бутил (S,Z)-2-(5-(бензилокси)-4-метокси-2-(метоксикарбонил)стирил)пирролидин-1-карбоксилат 30 (1,0 г, 2,14 ммоль, выход 49,8%) в виде белого твердого вещества. ЖХМС (5-95AB/1,5 мин): ВУ=0,983 мин, [M+Na]+490,1.
К раствору соединения 30 (0,9 г, 1,92 ммоль) в EtOAc (10 мл) добавляли HCl/EtOAc (6,0 мл). После перемешивания смеси при 25°C в течение 1 часа ее концентрировали, получая метил (S,Z)-4-(бензилокси)-5-метокси-2-(2-(пирролидин-2-ил)винил)бензоат 31 (0,77 г, 1,90 ммоль, выход 99%) в виде белого твердого вещества.
К раствору соединения 31 (0,77 г, 1,91 ммоль) в MeOH (30 мл) добавляли NaOMe (1,03 г, 19,06 ммоль). Смесь перемешивали при 30°C в течение 2 часов. Смесь концентрировали и очищали колоночной флэш-хроматографией (25-75% EtOAc в РЕ), получая (S)-8-(бензилокси)-7-метокси-1,2,3,11a-тетрагидро-5H-бензо[e]пирроло[1,2-a]азепин-5-он 32 (0,60 г, 1,79 ммоль, выход 93,8%) в виде желтого масла. 1H ЯМР (400 MГц, CDCl3)δ м.д. 1,89-2,11 (m, 3 H) 2,18-2,33 (m, 1 H) 3,59 (dt, J=12,0, 7,6 Гц, 1 H) 3,80 (dt, J=11,5, 5,8 Гц, 1 H) 3,90-3,96 (m, 1 H) 3,97 (s, 3 H) 5,19 (s, 2 H) 5,86 (dd, J=10,0, 4,8 Гц, 1 H) 6,53 (dd, J=10,0, 2,0 Гц, 1 H) 6,69 (s, 1 H) 7,29-7,35 (m, 1 H) 7,36-7,41 (m, 2 H) 7,42-7,48 (m, 2 H) 7,62 (s, 1 H).
К раствору соединения 32 (580 мг, 1,73 ммоль) в ДХМ (50 мл) добавляли TiCl4 (656 мг, 3,46 ммоль). Смесь перемешивали при 30°C в течение 12 часов. Смесь добавляли 1 М HCl (20 мл) и EtOAc (100 мл). Органический слой промывали водой (50 мл ×3) и концентрировали с получением (S)-8-гидрокси-7-метокси-1,2,3,11a-тетрагидро-5H-бензо[e]пирроло[1,2-a]азепин-5-он 33 (250 мг, 0,44 ммоль, выход 25,3%) в виде желтого твердого вещества.
Раствор соединения 33 (50,0 мг, 0,20 ммоль) в ДМФА (DMF) (5,0 мл) добавляли K2CO3 (42,26 мг, 0,31 ммоль) и 1,5-дииопентан (333 мг, 1,0 ммоль). Реакционную смесь перемешивали при 90°C в течение 3 часов. Реакционную смесь очищали хроматографией на силикагеле (0-50% EtOAC в петролейном эфире) с получением (S)-8-((5-гидроксипентил)окси)-7-метокси-1,2,3,11а-тетрагидро-5Н-бензо[е]пирроло[1,2-а]азепин-5-он 34 (60 мг, 0,178 ммоль, выход 87,6%) в виде масла. ЖХМС (5-95AB/1,5 мин): ВУ=0,765 мин, [M+H]+332,0.
К раствору соединения 34 (60,0 мг, 0,18 ммоль) в ДХМ (6,0 мл) добавляли триэтиламин (55 мг, 0,54 ммоль) и метансульфонилхлорид, MsCl (41 мг, 0,36 ммоль). После перемешивания смеси при 35°C в течение 1 часа EtOAc (80 мл) и промывали водой (50 мл × 3). Органический слой концентрировали, получая (S)-5-((7-метокси-5-оксо-2,3,5,11a-тетрагидро-1H-бензо[e]пи рроло[1,2-a]азепин-8-ил)окси)пентил метансульфонат 35 (70 мг) в виде бесцветного масла. ЖХМС (5-95AB/1,5 мин): ВУ=0,679 мин, [M+H]+410,0.
К раствору соединения 35 (70 мг, 0,17 ммоль) и трет-бутил (11S,11aS)-8-гидрокси-7-метокси-2-метилен-5-оксо-11-((тетрагидро-2H-пиран-2-ил)окси)-2,3,11,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-10(5H)-карбоксилата 36 (87 мг, 0,19 ммоль) в ДМФА (DMF) (5,0 мл) добавляли K2CO3 (47 мг, 0,34 ммоль) и KI (5,68 мг, 0,030 ммоль). Смесь перемешивали при 90°C в течение 3 часов и очищали подготавливающей ВЭЖХ (HCOOH), получая трет-бутил (11aR)-7-метокси-8-((5-(((S)-7-метокси-5-оксо-2,3,5,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a]азепин-8-ил)окси)пентил)окси)-2-метилен-5-оксо-11a-((тетрагидро-2H-пиран-2-ил)окси)-2,3,11,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-10(5H)-карбоксилат 37 (70 мг, 0,084 ммоль, выход 49,2%) в виде белого твердого вещества. ЖХМС (5-95AB/1,5 мин): ВУ=0,845 мин, [M+H]+774,4.
Раствор соединения 37 (50 мг, 0,060 ммоль) в ТФК (1,9 мл) и воде (0,10 мл) перемешивали при 35°C в течение 1 часа. Смесь распределяли между насыщенным NaHCO3 (30 мл) и EtOAc (50 мл). Органический слой промывали водой (30 мл ×2) и насыщенным раствором соли (30 мл) и сушили над Na2SO4. Его концентрировали и очищали подготавливающей ТСХ (5% МеОН в ДХМ, Rf=0,5) с получением DM-5 (20 мг, 0,034 ммоль, выход 53,1%) в виде белого твердого вещества. ЖХМС (5-95AB/1,5 мин): ВУ=0,825 мин, [M+H]+572,1. 1H ЯМР (400 МГц, CDCl3)δ м.д. 1,65-1,75 (m, 3 H) 1,88-2,10 (m, 8 H) 2,19-2,31 (m, 1 H) 2,82-3,29 (m, 2 H) 3,60 (dt, J=11,9, 7,5 Гц, 1 H) 3,81 (dt, J=11,6, 5,9 Гц, 1 H) 3,86-3,91 (m, 1 H) 3,94 (s, 6 H) 3,97 (br. s., 1 H) 4,01-4,18 (m, 4 H) 4,30 (s, 2 H) 5,19 (d, J=10,6 Гц, 2 H) 5,89 (dd, J=9,9, 5,1 Гц, 1 H) 6,53-6,63 (m, 1 H) 6,66 (s, 1 H) 6,81 (s, 1 H) 7,51 (s, 1 H) 7,59 (s, 1 H) 7,68 (d, J=4,4 Гц, 1 H).
Пример 2. Получение моноалкилирующих пирролбензодиазепиновых линкер-лекарственных промежуточных соединений (таблица 2А)
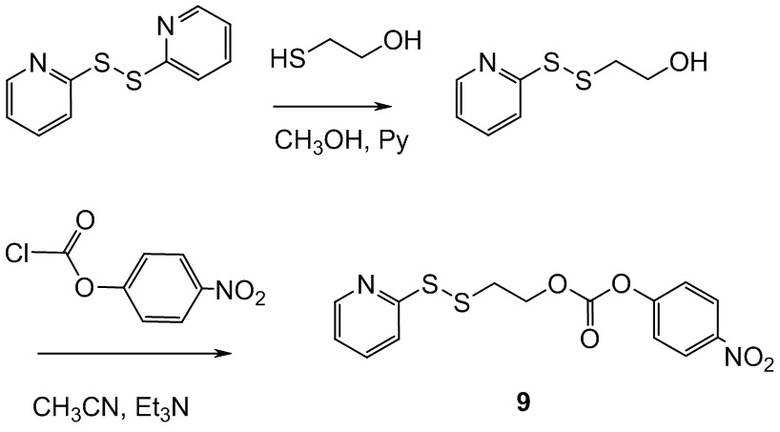
1,2-ди(пиридин-2-ил)дисульфан и 2-меркаптоэтанол приводили в контакт в пиридине и метаноле при комнатной температуре с получением 2-(пиридин-2-илдисульфанил)этанола. Ацилирование с 4-нитрофенилкарбонохлоридатом в триэтиламине и ацетонитриле давало 4-нитрофенил-2- (пиридин-2-илдисульфанил)этилкарбонат 9.
К смеси 1,2-бис(5-нитропиридин-2-ил)дисульфана 10 (1,0 г, 3,22 ммоль) в безводном ДМФА (DMF)/МеОН (25 мл/25 мл) добавляли HOAc (0,1 мл), а затем 2-аминоэтантиол гидрохлорид 11 (183 мг, 1,61 ммоль). После того, как реакционную смесь перемешивали при комнатной температуре в течение ночи, ее концентрировали под вакуумом для удаления растворителя и остаток промывали ДХМ (30 мл ×4) с получением 2-((5-нитропиридин-2-ил) дисульфанил)этанамин гидрохлорида 12 в виде бледно-желтого твердого вещества (300 мг, 69,6%). 1H ЯМР (400 МГц, ДМСО (DMSO)-d6) δ 9,28 (d, J=2,4 Гц, 1H), 8,56 (dd, J=8,8, 2,4 Гц, 1H), 8,24 (s, 4H), 8,03 (d, J=8,8 Гц, 1H), 3,15-3,13 (m, 2H), 3,08-3,06 (m, 2H).
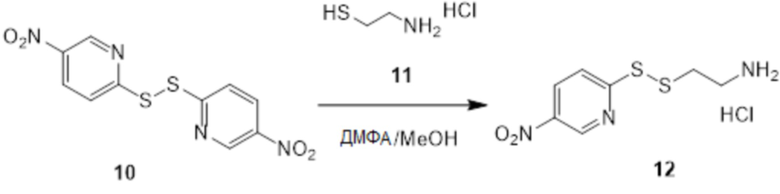
Раствор 1,2-бис(5-нитропиридин-2-ил)дисульфана 10 (9,6 г, 30,97 ммоль) и 2-меркаптоэтанола (1,21 г, 15,49 ммоль) в безводном ДХМ /CH3OH (250 мл/250 мл) перемешивали при комнатной температуре в атмосфере азота в течение 24 часов. После концентрирования смеси под вакуумом, остаток разбавляли ДХМ (300 мл). Добавляли MnO2 (10 г) и смесь перемешивали при комнатной температуре в течение еще 0,5 часа. Смесь очищали колоночной хроматографией на силикагеле (ДХМ /MeOH=100/1 до 100/1) с получением 2-((5-нитропиридин-2-ил)дисульфанил)этанола 13 (2,2 г, 61,1%) в виде коричневого масла. 1H ЯМР (400 МГц, CDCl3) δ 9,33 (d, J=2,8 Гц, 1H), 8,38-8,35 (dd, J=9,2, 2,8 Гц, 1H), 7,67 (d, J=9,2 Гц, 1H), 4,10 (t, J=7,2 Гц, 1H), 3,81-3,76 (q, 2H), 3,01 (t, J=5,2 Гц, 2H).
К раствору 13 (500 мг, 2,15 ммоль) в безводном ДМФА (DMF) (10 мл) добавляли ДИЭА (DIEA) (834 мг, 6,45 ммоль), после чего следовал PNP карбонат (бис(4-нитрофенил)карбонат, 1,31 г, 4,31 ммоль). Реакционный раствор перемешивали при комнатной температуре в течение 4 часов и смесь очищали подготовительной ВЭЖХ (FA) с получением 4-нитрофенил 2-((5-нитропиридин-2-ил)дисульфанил)этилкарбоната 14 (270 мг, 33,1%) в виде светло-коричневого масла. 1H ЯМР (400 МГц, CDCl3) δ 9,30 (d, J=2,4 Гц, 1H), 8,43-8,40 (dd, J=8,8, 2,4 Гц, 1H), 8,30-8,28 (m, 2H), 7,87 (d, J=8,8 Гц, 1H), 7,39-7,37 (m, 2H), 4,56 (t, J=6,4 Гц, 2H), 3,21 (t, J=6,4 Гц, 2H).
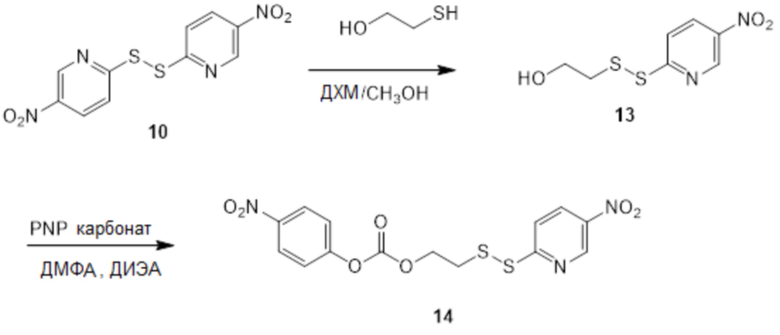
Синтез (11S,11aS)-(R)-2-((5-нитропиридин-2-ил)дисульфанил)пропил 11-гидрокси-7-метокси-8-((5-(((S)-7-метокси-2-метилен-5,11-диоксо-2,3,5,10,11,11a-гексагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-8-ил)окси)пентил)окси)-2-метилен-5-оксо-2,3,11,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-10(5H)-карбоксилата (LD-51)
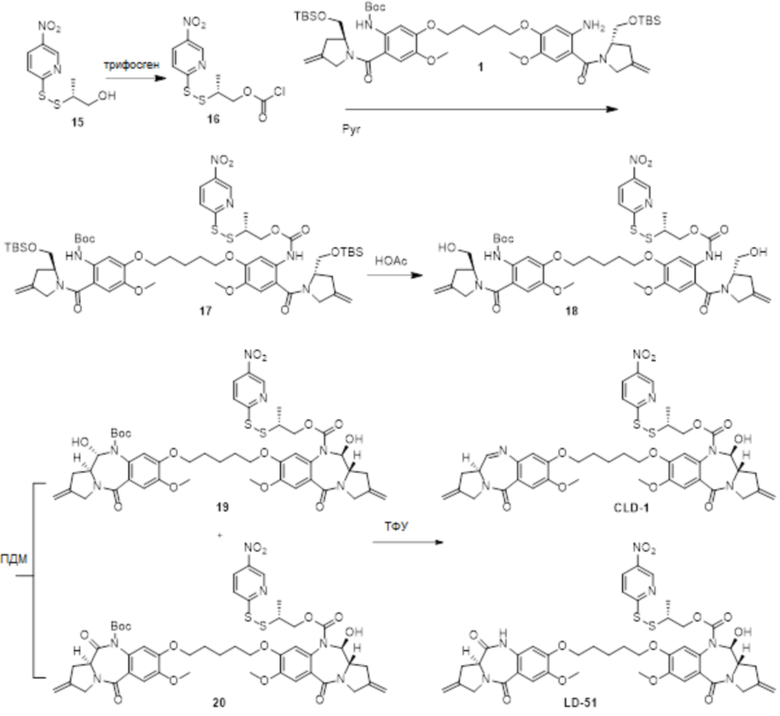
В перемешиваемую суспензию 5-нитропиридин-2-тиола (334 мг, 2,14 ммоль) в сухом ДХМ (7,5 мл) при 0°С (лед/ацетон) в атмосфере аргона добавляли по каплям сульфурилхлорид (2,35 мл 1,0 М раствора в ДХМ, 2,35 ммоль). Реакционную смесь превращали из желтой суспензии в желтый раствор и оставляли нагреваться до комнатной температуры, затем перемешивали в течение 2 часов, после чего растворитель удаляли выпариванием под вакуумом с получением желтого твердого вещества. Твердое вещество повторно растворяли в ДХМ (15 мл) и обрабатывали по каплям раствором (R)-2-меркаптопропан-1-ола (213 мг, 2,31 ммоль) в сухом ДХМ (7,5 мл) при 0°С в атмосфере аргона. Реакционной смеси давали нагреться до комнатной температуры и перемешивали в течение 20 часов, после чего анализ методом ЖХ/МС показал значительное образование продукта во время удерживания 1,41 мин (ES+) масса/заряд 247 ([M+ H]+, около 100% относительная интенсивность). Осадок удаляли фильтрованием и фильтрат выпаривали под вакуумом, получая оранжевое твердое вещество, которое обрабатывали H2O (20 мл) и подщелачивали раствором гидроксида аммония. Смесь экстрагировали ДХМ (3×25 мл) и объединенные экстракты промывали H2O (20 мл), насыщенным раствором соли (20 мл), сушили (MgSO4), фильтровали и выпаривали под вакуумом с получением неочищенного продукта. Очистка флеш-хроматографией (градиентное элюирование с шагом увеличения 1%: 100% ДХМ до 98:2 об./об. ДХМ /MeOH) давала (R)-2-((5-нитропиридин-2-ил)дисульфанил)пропан-1-ол 15 в виде масла (111 мг, выход 21%).
К раствору трифосгена Cl3COCOOCCl3, Sigma Aldrich, регистрационный ХРС(CAS) № 32315-10-9 (241 мг, 0,812 ммоль) в ДХМ (10 мл) добавляли раствор (R)-2 -((5-нитропиридин-2-ил)дисульфанил)пропан-1-ола 15 ( 500 мг, 2,03 ммоль) и пиридина (153 мг, 1,93 ммоль) в ДХМ (10 мл) по каплям при 20°C. После того, как реакционную смесь перемешивали при 20°C в течение 30 мин, ее концентрировали и (R)-2-((5-нитропиридин-2-ил)дисульфанил)пропилкарбонохлоридат 16 использовали непосредственно на следующей стадии без дополнительной очистки.
Раствор соединения 16 (626 мг, 2,03 ммоль) в ДХМ (10 мл) добавляли по каплям к раствору трет-бутил (5-((5-(5-амино-4-((S)-2-(((трет-бутилдиметилсилил)окси)метил)-4-метиленпирролидин-1-карбонил)-2-метоксифенокси)пентил)окси)-2-((S)-2-(((трет-бутилдиметилсилил)окси)метил)-4-метиленпирролидин-1-карбонил)-4-метоксифенил)карбамата 1 (1,50 г, 1,57 ммоль) и пиридина (161 мг, 2,05 ммоль) при 20 oC. Реакционную смесь перемешивали при 20°C в течение 3 часов. Растворитель удаляли и остаток очищали флэш-хроматографией на колонке (EtOAc в петролейном эфире 0~30%), получая трет-бутил (2-((S)-2-(((трет-бутилдиметилсилил)окси)метил)-4-метиленпирролидин-1-карбонил)-5-((5-(4-((S)-2-(((трет-бутилдиметилсилил)окси)метил)-4-метиленпирролидин-1-карбонил)-2-метокси-5-((((R)-2-((5-нитропиридин-2-ил)дисульфанил)проpокси)карбонил)амино)фенокси)пентил)окси)-4-метоксифенил)карбамат 17 (1,6 г, 83%) в виде желтой пены. ЖХМС (5-95AB/1,5 мин): ВУ=1,360 мин, [M+Na]+1247,4.
К раствору соединения 17 (900 мг, 0,734 ммоль) в ТГФ/Н2О (10 мл/10 мл) добавляли HOAc (15 мл) при 20°C. Реакционную смесь перемешивали при 20°C в течение 24 часов. Реакционную смесь разбавляли EtOAc (50 мл) и промывали водой (2×20 мл), насыщенным водным раствором NaHCO3 (30 мл) и насыщенным раствором соли (30 мл). Ее сушили и концентрировали с получением неочищенного продукта, который очищали флэш-хроматографией (ДХМ:MeOH=100:1~20:1), чтобы получить трет-бутил (2-((S)-2-(гидроксиметил)-4-метиленпирролидин-1-карбонил)-5-((5-(4-((S)-2-(гидроксиметил)-4-метиленпирролидин-1-карбонил)-2-метокси-5-((((R)-2-((5-нитропиридин-2-ил)дисульфанил)пропокси)карбонил)амино)фенокси)пентил)окси)-4-метоксифенил)карбамат 18 (700 мг, 95,6%) в виде желтой пены. ЖХМС (5-95AB/1,5 мин): ВУ=0,978 мин, [M+H]+997,6.
К раствору соединения 18 (700 мг, 0,702 ммоль) в ДХМ (40 мл) добавляли прейодат Десса-Мартина, ПДМ, 1,1,1-Трис (ацетилокси)-1,1-дигидро-1,2-бензиодоксол-3-(1H)-он, Sigma Aldrich, регистрационный ХРС(CAS) № 87413-09-0 (1,19 мг, 2,81 ммоль) при 20°C. Реакционную смесь перемешивали при 20°C в течение 1 часа. Реакцию гасили насыщенным раствором NaHCO3/Na2SO3 (20 мл/20 мл) и экстрагировали с помощью ДХМ (3×10 мл). Объединенный органический слой промывали NaHCO3/Na2SO3 (10 мл/10 мл), насыщенным раствором соли (20 мл), сушили и концентрировали, получая смесь трет-бутил (11S,11aS)-11-гидрокси-8-((5-(((11S,11aS)-11-гидрокси-7-метокси-2-метилен-10-(((R)-2-((5-нитропиридин-2-ил)дисульфанил)пропокси)карбонил)-5-оксо-2,3,5,10,11,11a-гексагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-8-ил)окси)пентил)окси)-7-метокси-2-метилен-5-оксо-2,3,11,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-10(5H)-карбоксилата 19 (ЖХМС (5-95AB/1,5 мин): ВУ =0,912 мин, [M+Na]+1015,3) и трет-бутил (S)-8-((5-(((11S,11aS)-11-гидрокси-7-метокси-2-метилен-10-(((R)-2-((5-нитропиридин-2-ил)дисульфанил)пропокси)карбонил)-5-оксо-2,3,5,10,11,11a-гексагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-8-ил)окси)пентил)окси)-7-метокси-2-метилен-5,11-диоксо-2,3,11,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-10(5H)-карбоксилата 20, которая была непосредственно использована в следующей стадии.
Холодную ТФК (8 мл) добавляли к неочищенной смеси 19 и 20 (600 мг, 0,604 ммоль) при 0°С. Реакционную смесь перемешивали при 0°С в течение 30 мин. Реакционную смесь добавляли по каплям к холодному насыщенному водному раствору NaHCO3 (150 мл) при 0°C и экстрагировали ДХМ (4×40 мл). Объединенный органический слой промывали насыщенным раствором соли (50 мл), сушили и концентрировали с получением неочищенного продукта, который очищали с помощью подготавливающей ТСХ (ДХМ:MeOH=15:1) для отделения чистого LD-51 (28 мг, 5,2%), в виде желтой пены. ЖХМС: (5-95, АВ, 1,5 мин), 0,739 мин, масса/заряд=891,2 (М +1). 1H ЯМР (400 МГц, CDCl3) δ 9,26 (s, 1H), 8,31 (d, J=6,8 H, 1Гц), 8,18 (s, 1H), 7,62 (d, J=8,4 Гц, 1H), 7,41 (s, 1H), 7,18 (s, 1H), 6,77 (s, 1H), 6,41 (s, 1H), 5,60 (d, J=10,0 Гц, 1H), 5,20-5,06 (m, 4H), 4,50-3,81 (m, 18H), 3,70-3,60 (m, 1H), 3,50-3,40 (m, 1H), 3,18 (br, 1H), 2,98-2,62 (m, 6H), 1,95-1,86 (m, 4H), 1,70-1,52 (m, 2H), 1,17 (d, J=6,4 Гц, 3H).
Синтез (11S,11aS)-(R)-2-((5-нитропиридин-2-ил)дисульфанил)пропил 11-гидрокси-7-метокси-8-((5-(((S)-7-метокси-2-метилен-5-оксо-2,3,5,10,11,11a-гексагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-8-ил)окси)пентил)окси)-2-метилен-5-оксо-2,3,11,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-10(5H)-карбоксилата (LD-52)
К раствору CLD-1 (45 мг, 0,050 ммоль) в ТГФ (3,0 мл) добавляли NaBH3CN (3 мг, 0,050 ммоль) и HOAc (0,05 мл) при 0 oC. Смесь перемешивали при 0°C в течение 2 мин. Реакционный раствор очищали подготавливающей ТСХ (7% метанол в ДХМ, Rf=0,5) с получением LD-52 (20 мг, 0,022 ммоль, выход 42,1%) в виде белого твердого вещества. ЖХМС (5-95AB/1,5 мин): ВУ=0,878 мин, [M+H]+877,2. 1H ЯМР (400 МГц, CDCl3) δ 9,19 (s, 1H), 8,27 (d, J=6,8 Гц, 1H), 7,58 (d, J=8,8 Гц, 1H), 7,53 (s, 1H), 7,24 (s, 1H), 6,69 (s, 1H), 6,02 (s, 1H), 5,56 (d, J=9,7 Гц, 1H), 5,12 (s, 2H), 5,05 (d, J=11,2 Гц, 2H), 4,54 (br.s, 1H), 4,42-4,38 (m, 1H), 4,29-4,22 (m, 4H), 4,13-4,09 (m, 1H), 4,02-3,39 (m, 8H), 3,79 (s, 3H), 3,63 (t, J=8,0 Гц, 1H), 3,53 (d, J=11,9 Гц, 1H), 3,37-3,31 (m, 1H), 3,16-3,14 (m, 1H), 2,94-2,88 (m, 2H), 2,74-2,71 (m, 1H), 2,44-2,39 (m, 1H), 1,93-1,85 (m, 4H), 1,66-1,56 (m, 2H), 1,24-1,14 (m, 3H).
Пример 3. Получение компараторных пирролбензодиазепиновых линкер-лекарственных промежуточных соединений (таблица 2В)
Синтез (R)-2-((5-нитропиридин-2-ил)дисульфанил)пропил (11S,11aS)-11-гидрокси-7-метокси-8-((5-(((S)-7-метокси-2-метилен-5-оксо-2,3,5,10,11,11a-гексагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-8-ил)окси)пентил)окси)-2-метилен-5-оксо-2,3,11,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-10(5H)-карбоксилата (CLD-1)
К раствору 18 (50 мг, 0,050 ммоль) в ДХМ (2,0 мл) добавляли ПДМ (149 мг, 0,35 ммоль) при 25°C. Реакционную смесь перемешивали при 25°C в течение 2 часов. Реакционную смесь разбавляли ДХМ (5 мл) и гасили насыщенным раствором NaHCO3/Na2SO3 (2 мл/2 мл) и экстрагировали ДХМ (2×5 мл). Объединенный органический слой промывали NaHCO3/Na2SO3 (2 мл/2 мл), насыщенным раствором соли (5 мл), сушили и концентрировали. Остаток очищали с помощью подготавливающей ТСХ ДХМ:MeOH=20:1), получая трет-бутил (11S,11aS)-11-гидрокси-8-((5-(((11S,11aS)-11-гидрокси-7-метокси-2-метилен-10-(((R)-2-((5-нитропиридин-2-ил)дисульфанил)пропокси)карбонил)-5-оксо-2,3,5,10,11,11a-гексагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-8-ил)окси)пентил)окси)-7-метокси-2-метилен-5-оксо-2,3,11,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-10(5H)-карбоксилат 19, который использовался непосредственно в следующем этапе. ЖХМС: (5-95, АВ, 1,5 мин), 0,830 мин, масса/заряд=1013,4 (М +23).
Холодную ТФК (1 мл) добавляли к 19 (20 мг, 0,020 ммоль) при 0 oC. Реакционную смесь перемешивали при 0°C в течение 20 мин. Реакционную смесь добавляли по каплям к холодному насыщенному водному раствору NaHCO3 (20 мл) при 0°C и экстрагировали ДХМ (3×15 мл). Объединенный органический слой промывали насыщенным раствором соли (15 мл), сушили и концентрировали с получением неочищенного продукта, который очищали с помощью подготавливающей ТСХ (ДХМ:MeOH=15:1) с получением CLD-1 (4 мг, 23%) в виде серого твердого вещества. ЖХМС: (5-95, АВ, 1,5 мин), 0,89 мин, масса/заряд=873,6 (М +1). 1H ЯМР (400 МГц, CDCl3) δ 9,22 (s, 1H), 8,38 (d, J=8,8 Гц, 1H), 7,78 (d, J=8,8 Гц, 1H), 7,68 (d, J=4,4 Гц, 1H), 7,49 (s, 1H), 7,33 (s, 1H), 6,82 (s, 1H), 6,77 (s, 1H), 5,20-5,13 (m, 4H), 4,36-4,26 (m, 5H), 4,20-3,95 (m, 7H), 4,89-3,70 (m, 8H), 3,50-2,70 (m, 5H), 2,05-1,82 (m, 4H), 1,40-1,15 (m, 3H).
Синтез 4-((S)-2-((S)-2-(6-(2,5-диоксо-2,5-дигидро-1H-пиррол-1-ил)гексанамидо)-3-метилбутанамидо)-5-уреидопентанамидо)бензил(11S,11aS)-11-гидрокси-7-метокси-8-((5-(((S)-7-метокси-2-метилен-5-оксо-2,3,5,10,11,11a-гексагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-8-ил)окси)пентил)окси)-2-метилен-5-оксо-2,3,11,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-10(5H)-карбоксилата CLD-4
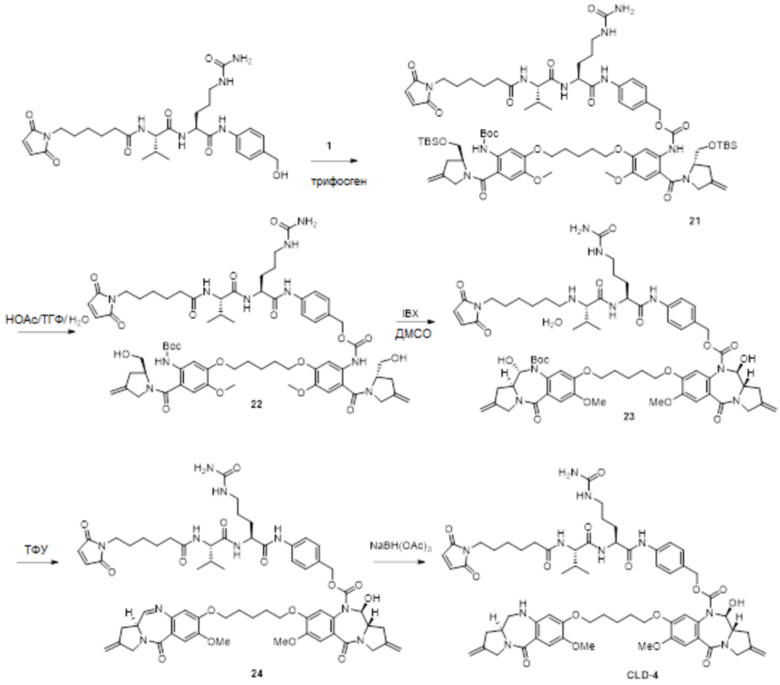
К раствору трифосгена (156 мг, 0,52 ммоль) в ДХМ (20 мл) добавляли раствор 1 (1,0 г, 1,05 ммоль) и Et3N (318 мг, 3,15 ммоль) в ДХМ (5,0 мл). Смесь перемешивали при 0°C в течение 1 часа и концентрировали с получением неочищенного промежуточного соединения, которое добавляли (0,88 г, 1,53 ммоль) в ДХМ (20 мл), добавляли к смеси триэтиламина (310 мг, 3,07 ммоль) и 6-(2,5-диоксо-2,5-дигидро-1H-пиррол-1-ил)-N-((S)-1-(((S)-1-((4-(гидроксиметил)фенил)амино)-1-оксо-5-уреидопентан-2-ил)амино)-3-метил-1-оксобутан-2-ил)гексанамида, MC-VC-PAB (1,0 г, 1,02 ммоль) в ДМФА (DMF) (10 мл) при 0°C. Смесь разбавляли ДХМ (40 мл), промывали водой (2×30 мл). Органический слой сушили над Na2SO4, концентрировали и очищали хроматографией на силикагеле (0-10% MeOH в ДХМ ) с получением трет-бутил (2-((S)-2-(((трет-бутилдиметилсилил)окси)метил)-4-метиленпирролидин-1-карбонил)-5-((5-(4-((S)-2-(((трет-бутилдиметилсилил)окси)метил)-4-метиленпирролидин-1-карбонил)-5-((((4-((S)-2-((S)-2-(6-(2,5-диоксо-2,5-дигидро-1H-пиррол-1-ил)гексанамидо)-3-метилбутанамидо)-5-уреидопентанамидо)бензил)окси)карбонил)амино)-2-метоксифенокси)пентил)окси)-4-метоксифенил)карбамата 21 (1,0 г, 0,64 ммоль, выход 62,4%) в виде желтого твердого вещества.
К раствору соединения 21 (1,0 г, 0,64 ммоль) в ТГФ (6,0 мл) добавляли воду (6,0 мл) и уксусную кислоту (9,0 мл). Смесь перемешивали при 20°C в течение 12 часов. В смесь добавляли EtOAc (100 мл), и органический слой промывали водой (50 мл ×3) и насыщенным раствором NaHCO3 (50 мл) и концентрировали, чтобы получить трет-бутил (5-((5-(5-((((4-((S)-2-((S)-2-(6-(2,5-диоксо-2,5-дигидро-1H-пиррол-1-ил)гексанамидо)-3-метилбутанамидо)-5-уреидопентанамидо)бензил)окси)карбонил)амино)-4-((S)-2-(гидроксиметил)-4-метиленпирролидин-1-карбонил)-2-метоксифенокси)пентил)окси)-2-((S)-2-(гидроксиметил)-4-метиленпирролидин-1-карбонил)-4-метоксифенил)карбамат 22 (700 мг, 0,53 ммоль, выход 82,1%) в виде белого твердого вещества.
К раствору 22 (597 мг, 0,45 ммоль) в ДМСО (DMSO) (5,0 мл) добавляли 2-иодоксибензойную кислоту, IBX (126 мг, 0,45 ммоль) при 18 oC. Реакционную смесь перемешивали при 37°C в течение 8 часов и очищали подготавливающей ВЭЖХ (ацетонитрил 40-70%/0,225% FA в воде) с получением трет-бутил (11S,11aS)-8-((5-(((11S,11aS)-10-(((4-((S)-2-((S)-2-((6-(2,5-диоксо-2,5-дигидро-1H-пиррол-1-ил)гексил)амино)-3-метилбутанамидо)-5-уреидопентанамидо)бензил)окси)карбонил)-11-гидрокси-7-метокси-2-метилен-5-оксо-2,3,5,10,11,11a-гексагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-8-ил)окси)пентил)окси)-11-гидрокси-7-метокси-2-метилен-5-оксо-2,3,11,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-10(5H)-карбоксилат гидрата 23 (120 мг, 0,089 ммоль, выход 19,8%) в виде белого твердого вещества.
Раствор 23 (100 мг, 0,080 ммоль) в ТФК (4,0 мл) перемешивали при 0°C в течение 30 минут, а затем добавляли к холодному насыщенному раствору NaHCO3 (40 мл). Его экстрагировали EtOAc (60 мл ×3). Объединенные органические слои концентрировали, получая 4-((S)-2-((S)-2-(6-(2,5-диоксо-2,5-дигидро-1H-пиррол-1-ил)гексанамидо)-3-метилбутанамидо)-5-уреидопентанамидо)бензил (11S,11aS)-11-гидрокси-7-метокси-8-((5-(((S)-7-метокси-2-метилен-5-оксо-2,3,5,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-8-ил)окси)пентил)окси)-2-метилен-5-оксо-2,3,11,11a-тетрагидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-10(5H)-карбоксилат 24 (90 мг) в виде желтого твердого вещества, которое непосредственно использовалось в следующей стадии.
К раствору соединения 24 (90 мг, 0,070 ммоль) в ДМФА (DMF) (4,0 мл) добавляли триацетоксиборгидрид натрия (9,42 мг, 0,1500 ммоль). Цианоборгидрид натрия также можно использовать в качестве восстановителя. Смесь перемешивали при 20°C в течение 30 мин. Полученный остаток очищали подготавливающей ВЭЖХ (ацетонитрил 0-40/0,1% HCl в воде) с получением CLD-4 (28 мг, 0,022 ммоль, выход 29,5%) в виде белого твердого вещества. ЖХМС: (5-95, АВ, 1,5 мин), 0,832 мин, масса/заряд=602,7, 1203,6 (M+1).
Пример 4. Получение антител с внесенным цистеином для конъюгации путем восстановления и повторного окисления
Аминокислоты легкой цепи нумеруют в соответствии с нумерацией Кабата (Kabat et al., Sequences of proteins of immunological interest, (1991) 5th Ed., US Dept of Health and Human Service, National Institutes of Health, Bethesda, MD). Аминокислоты тяжелой цепи нумеруют в соответствии с системой нумерации ЕС (Edelman et al (1969) Proc. Natl. Acad. of Sci. 63(1):78-85), за исключением случаев, когда отмечено что нумерация выполнена по Кабату. Используются однобуквенные аббревиатуры аминокислот.
Полноразмерные моноклональные антитела с внесенным цистеином (THIOMAB™), экпрессированные в клетках CHO, содержат цистеиновые аддукты (цистины) или являются глутатионилированными по внесенных цистеинах в связи с условиями культивирования клеток. Как есть, THIOMAB™ выделенные из клеток СНО нельзя конъюгировать с Cys-реакционноспособными линкер-лекарственными промежуточными соединениями. Антитела с внесенным цистеином могут быть сделаны реакционноспособными для конъюгации с линкер-лекарственными промежуточными соединениями, такими как в таблице 2А, путем обработки восстановителем, таким как ДТТ (DTT) (реактив Клеланда, дитиотреитол) или TCEP (трис(2-карбоксиэтил)фосфин гидрохлорид, Getz et al (1999) Anal. Biochem. Vol 273:73-80; Soltec Ventures, Беверли, Массачусетс) с последующим повторным формированием межцепочечных дисульфидных связей (повторное окисление) мягким окислителем, таким как дегидроаскорбиновая кислота. Полноразмерные моноклональные антитела с внесенным цистеином (THIOMAB™), экспрессированные в клетках CHO (Gomez et al (2010) Biotechnology and Bioeng. 105(4):748-760; Gomez et al (2010) Biotechnol. Prog. 26:1438-1445) были восстановлены, например, с помощью около 50-кратного избытка ДТТ (DTT) в течение ночи в 50 мМ Трис, pH 8,0 с 2 мМ ЭДТА при комнатной температуре, который удаляет Cys и глутатионовые аддукты, а также восстанавливает межцепочечные дисульфидные связи в антителе. Удаление аддуктов контролировалось обращенно-фазовой ЖХМС с использованием колонки PLRP-S. Восстановленный THIOMAB™ разбавляли и подкисляли добавлением по меньшей мере к четырем объемам 10 мМ сукцината натрия, буфер рН 5.
В альтернативном варианте, антитело разбавляли и подкисляли путем добавления по меньшей мере к четырем объемам 10 мМ сукцината, рН 5 и титровали 10% уксусной кислотой до тех пор, пока рН не составляло около пяти. Затем пониженный pH и разбавленный THIOMAB™ загружали в ионообменную колонку HiTrap S, промывали несколькими объемами колонки 10 мМ ацетата натрия, pH 5 и элюировали 50 мМ Tris, pH 8,0, 150 мМ хлорида натрия. Дисульфидные связи восстанавливались между остатками цистеина, присутствующими в исходном Mab, путем повторного окисления. Элюированный восстановленный THIOMABTM, описанный выше, обрабатывается 15X дегидроаскорбиновой кислотой (DHAA) в течение около 3 часов или, в альтернативном варианте, от 200 нМ до 2 мМ водным сульфатом меди (CuSO4) при комнатной температуре в течение ночи. Могут быть применены другие окислители, то есть окисляющие вещества и окислительные условия, которые известны в данной области техники. Также может быть эффективным окисление окружающим воздухом. Этот мягкий, частично повторно окисляющий этап с высокой точностью формирует внутрицепочечные дисульфидные связи. Повторное окисление контролировали обращенно-фазовой ЖХМС с применением колонки PLRP-S. Повторно окисленный THIOMAB™ разбавляли сукцинатным буфером, как описано выше, для достижения рН около 5, и очистку на колонке S проводили, как описано выше, за исключением того, что элюирование проводили с помощью градиента 10 мМ сукцинат, рН 5, 300 мМ натрий хлорид (буфер B) в 10 мМ сукцинате, рН 5 (буфер А). К элюированному THIOMAB™ добавляли EDTA до конечной концентрации 2 мМ и концентрировали, если необходимо, до конечной концентрации больше чем 5 мг/мл. Полученный THIOMAB™, готовый к конъюгации, хранили при -20°C в аликвотах. Жидкостную хроматографию/масс-спектрометрический анализ проводили на серии 6200 TOF или QTOF Agilent ЖХ/МС. Образцы хроматографировали на микрокапиллярной колонке PRLP-S®, 1000 A, (50 мм ×2,1 мм, Polymer Laboratories, Шропшир, Великобритания), нагретой до 80°C. Использовали линейный градиент от 30-40% B (растворитель A: 0,05% ТФК в воде, растворитель B: 0,04% ТФК в ацетонитриле), и элюент был непосредственно ионизирован с использованием источника электрораспыления. Данные были собраны и скорректированы c поправкой на помехи программным обеспечением MassHunter. Перед анализом ЖХ/МС антитела или лекарственные конъюгаты (50 мкг) обрабатывали PNGase F (2 единицы/мл, Prozyme, Сан-Леандро, Калифорния) в течение 2 часов при 37°C для удаления N-связанных углеводов.
В альтернативном варианте, антитела или лекарственные конъюгаты частично расщепляли LysC (0,25 мкг на 50 мкг (микрограмм) антитела или конъюгата) в течение 15 минут при 37°С с получением фрагмента Fab и Fc для анализа ЖХМС. Пики в скорректированных c поправкой на помехи спектрах ЖХМС были определены и количественно посчитаны. Отношение лекарственное средство-антитело (ОЛА, DAR - Drug-to-antibody ratios) рассчитывали путем вычисления отношения интенсивностей пика или пиков, соответствующих антителу, конъюгированному с лекарственным средством, по отношению ко всем наблюдаемым пикам.
Пример 5. Конъюгация линкер-лекарственных промежуточных соединений с антителами
После процедур восстановления и повторного окисления в примере 2, для антитела с внесенным цистеином (THIOMAB™), в 10 мМ сукцинате, pH 5, 150 мМ NaCl, 2 мМ ЭДТА, доводили pH до рН 7,5-8,5 с помощью 1 М Триса. Избыток, от около 3 до 20 эквивалентов линкер-лекарственного промежуточного соединения с тио-реакционноспособной пиридилдисульфидной группой, включая, но не ограничиваясь теми что в таблице 2А, растворяют в ДМФА (DMF) или ДМА (DMA) и добавляют к восстановленному, повторно окисленному антителу с доведенным рН. Реакцию инкубируют при комнатной температуре или 37°C и контролируют до завершения (от 1 до 24 часов), как определено ЖХ-МС-анализом реакционной смеси. Когда реакция завершена, конъюгат очищают одной или любой комбинацией нескольких способов, целью которой является удаление оставшегося непрореагировавшего линкер-лекарственного промежуточного соединения и агрегированного белка (если присутствует в значительных количествах). Например, конъюгат может быть разбавлен 10 мМ гистидин-ацетатом с рН 5,5 до конечного значения рН около 5,5 и очищен с помощью катионообменной хроматографии S с использованием либо колонок HiTrap S, соединенных с системой очистки Akta (GE Healthcare), либо спин-колонок S maxi (Pierce). В альтернативном варианте, конъюгат может быть очищен гель-фильтрационной хроматографией с использованием колонки S200, соединенной с системой очистки Akta, или спиновых колонок Zeba. В альтернативном варианте, может применятся диализ. Конъюгаты лекарственного средства THIOMAB были составлены в 20 мМ His/ацетат, pH 5, 240 мМ сахарозы, применяя или гель-фильтрацию, или диализ. Очищенный конъюгат концентрируют ультрафильтрацией центрифугированием и фильтруют через 0,2 мкм фильтр в стерильных условиях и замораживают для хранения. Конъюгаты антитело-лекарственное средство были охарактеризованы методом BCA для определения концентрации белка, аналитической ЭХ (SEC) для анализа агрегации, и ЖХ-МС после обработки эндопептидазой Lysine C (LysC) для расчета ОЛА (DAR).
Эксклюзионную хроматографию проводят на конъюгатах с применением колонки Shodex KW802.5 в 0,2 М фосфате калия pH 6,2 с 0,25 мМ хлоридом калия и 15% IPA при скорости потока 0,75 мл/мин. Состояние агрегации конъюгата определяли путем интегрирования площади элюированного пика поглощения при 280 нм.
Анализ ЖХ-МС может выполняться на КАЛС (ADC) с применением прибора Agilent QTOF 6520 ESI. В качестве примера конъюгат антитело-лекарственное средство обрабатывают 1:500 мас./об. эндопротеиназой Lys C (Promega) в Tris, pH 7,5, в течение 30 мин при 37°С. Полученные расщепленные фрагменты загружают в колонку 1000Å (Ангстрем), 8 мкм (микрон) PLRP-S (сильно перекрестно-сшитый полистирол), нагретую до 80°C, и элюируют с градиентом от 30% B до 40% B за 5 минут. Подвижная фаза А представляла собой H2O с 0,05% ТФК, а подвижная фаза В представляла собой ацетонитрил с 0,04% ТФК. Скорость потока составляла 0,5 мл/мин. Элюирование белков контролировали детектированием УФ-поглощения при 280 нм до электрораспылительной ионизации и МС-анализа. Обычно достигалось хроматографическое разделение неконъюгированного фрагмента Fc, остаточного неконъюгированного Fab и лекарственного Fab. Полученные спектры масса/заряд были скорректированы c поправкой на помехи с использованием программного обеспечения Mass Hunter™ (Agilent Technologies) для расчета массы фрагментов антител.
В соответствии с этими процедурами готовили конъюгаты лекарственное средство-модифицированное цистеином антитело из таблиц 3А и 3В.
Пример 6. Анализ пролиферации клеток in vitro
Эффективность КАЛС (ADC) измеряли с помощью анализа пролиферации клеток, применяя следующий протокол (Анализ жизнеспособности люминесцентных клеток CELLTITER GLO™, технический бюллетень TB288 Promega Corp., Mendoza et al (2002) Cancer Res. 62:5485-5488). Протокол является модификацией анализа клеток люминесцентных клеток CELLTITER GLO™:
1. Аликвоту 100 мкл клеточной культуры, содержащей около 104 клеток (SKBR-3, BT474, MCF7 или MDA-MB-468) в среде, осаждали в каждую лунку 96-луночной плашки с непрозрачными стенками.
2. Готовили контрольные лунки, содержащие среду и без клеток.
3. КАЛС (ADC) добавляли в экспериментальные лунки и инкубировали в течение 3-5 дней.
4. Плашки уравновешивали до комнатной температуры в течение около 30 минут.
5. Добавляли объем реактива CELLTITER GLO™, равный объему клеточной культуральной среды, присутствующей в каждой лунке.
6. Содержимое перемешивали в течение 2 минут на орбитальном шейкере для индукции клеточного лизиса.
7. Плашку инкубировали при комнатной температуре в течение 10 минут для стабилизации сигнала люминесценции.
8. Люминесценция регистрировалась и представлялась на графиках как ОЕЛ(RLU)=относительные единицы люминесценции.
Данные нанесены на график как среднее значение люминесценции для каждого набора реплик с планками погрешности среднего квадратического отклонения, как показано на фиг. 1A-E.
Среда: SK-BR-3 растет в 50/50/10%ФБС/глутамин/250 мкг/мл G-418 OVCAR-3 растет в RPMI/20%ФБС/глутамин.
Пример 7. Ингибирование роста опухоли, эффективность in vivo у мышей с ксенотрансплантатом
Опухоли были пересажены и им позволяли расти до объема 150-200 мм3 (как измерено с применением штангенциркулей) до однократного лечения в день 0. Объем опухоли измеряли с применением штангенциркулей по формуле: V (мм3)=0,5A X B2, где A и B - длинный и короткий диаметры соответственно. Мышей подвергали эвтаназии до того, как объем опухоли достигал 3000 мм3 или когда опухоли проявляли признаки надвигающегося изъязвления. Данные, собранные из каждой экспериментальной группы (10 мышей на группу), были выражены как среднее значение+среднеквадратическая ошибка.
Инокулируют n=150 мышей клетками KPL-4 HER2 в количестве 3 миллиона клеток/мышь, суспендированных в HBSS/матригеле, в торакальную молочную железу в объеме 0,2 мл. Когда опухоли достигали среднего объема опухоли 100-250 мм3, их группировали в 10 групп по 8-10 мышей каждая. Однократное лечение будет вводиться внутривенно через хвостовую вену в День 0. Объем не должен превышать 0,3 мл, размер иглы 28 или 29 калибр.
Линия клеток HCC1569 экспрессирует Ly6E и была получена из АКТП (Американская коллекция типовых культур, Манассас, Вирджиния), и сублиния HCC1569X2 была получена в Genlineech для оптимального роста у мышей. Каждую самку C.B-17 SCID-бежевых мышей (лаборатория Чарльз-Ривер) инокулировали в торакальную молочную железу пятью миллионами клеток HCC1569X2, суспендированными в HBSS/матригель (соотношение 1:1). Когда ксенотрансплантатные опухоли достигали среднего объема опухоли 100-300 мм3 (обозначено как День 0), животных рандомизировали в группы по 5 мышей каждая и они получали одну внутривенную инъекцию конъюгата антитело-лекарственное средство через хвостовую вену. Опухоли и массы тела мышей измеряли 1-2 раза в неделю на протяжении всего исследования. Мышей быстро подвергали эвтаназии, когда потеря массы тела составляла больше чем 20% от начального веса. Все животные были подвергнуты эвтаназии до того, как опухоли достигли 3000 мм3 или появлялись признаки надвигающегося изъязвления. Объем опухоли измеряли в двух измерениях (длина и ширина) с применением штангенциркулей, и объем опухоли рассчитывали по формуле: размер опухоли (мм3)=(более длинное измерение x более короткое измерение2) x 0,5 (WO 2013/177055).
Модель опухоли молочной железы мыши Fo5 использовали для оценки эффективности in vivo конъюгатов антитело-лекарственное средство по изобретению после однократных внутривенных инъекций и как описано ранее (Phillips GDL, Li GM, Dugger DL, et al. Targeting HER2-Positive Breast Cancer with Trastuzumab-DM1, an Antibody-Cytotoxic Drug Conjugate. (2008) Cancer Res. 68:9280-90), включено в данный документ посредством ссылки. Анти-Her2 КАЛС (ADC) тестировали с помощью модели Fo5, модели трансгенной мыши, в которой человеческий ген HER2 чрезмерно экспрессируется в эпителии молочной железы при транскрипционной регуляции промотора вируса опухоли молочной железы мыши (MMTV-HER2), как показано на фиг. 3 и 5. Чрезмерная экспрессия HER2 вызывает спонтанное развитие опухоли молочной железы. Опухоль молочной железы одного из этих животных-основателей (основатель № 5 [Fo5]) была распространена в последующих поколениях мышей FVB путем последовательной трансплантации опухолевых фрагментов (размером около 2×2 мм). Все исследования проводились в соответствии с Руководством по уходу и использованию лабораторных животных. Каждый конъюгат антитело-лекарственное средство (разовая доза) дозировался девяти животным внутривенно в начале исследования и через 14 дней после трансплантации. Первоначальный размер опухоли составлял около 200 мм3 объема. Измерения ингибирования роста опухоли со временем конъюгатами антитело-лекарственное средство по изобретению и контролями показаны на фиг. 2-8.
Другая модель эффективности трансплантации молочной железы может быть использована, как описано (Chen et al. (2007) Cancer Res 67:4924-4932), оценивая объем опухоли после однократной внутривенной дозы и используя опухоли, вырезанные из мыши с внутрибрюшинной опухолью, затем серийно пассируя в молочных железах реципиентных мышей.
Активности уничтожения клеток для анти-CD22 и анти-Napi-КАЛС (ADC) определяли в CD22 или Napi-экспрессирующих клеточных линиях после 5-дневной инкубаций и у мышей с ксенотрансплантатом.
Пример 8. Анализ связывания/алкилирования олигонуклеотидов
Изучали взаимодействие соединений пирролобензодиазепина с дуплекс-образующими олигонуклеотидами различной длины и последовательностей с последовательностями Pu-GAATG-Py>Pu-GATC-Py>>Pu-GATG-Py или Pu-GAATC-Py, где Pu представляет собой пуриновый нуклеотид A или G, и Py представляет собой пиримидиновый нуклеотид C или T для внутрицепочечного и межцепочечного перекрестного сшивания что было ранее идентифицированно (Rahman KM, et al (2009) J Am Chem Soc 131:13756-13766). Внутрицепочечный G дуплекс, 5'-TATAGAAATCTATA-3' и 3'-ATATCTTTAGATAT-5', и межцепочечный G дуплекс, 5'-TATAGAAATGTATA-3' и 3'-ATATCTTTACATAT-5', были изучены следующим образом:
Соединения в объеме 100 мкМ инкубировали с 50 мкМ двухцепочечных дезоксиолигонуклеотидов (ДНК) в течение 1 часа в 10 мМ Бис-Трис, рН 7,1 при 37°С. Образцы анализировали с помощью ЖХ/МС/УФ на Sciex TripleTOF 5600 на колонке Hypersil Gold C18 (100×2,1, 1,9 мкМ, Thermo Scientific). Колонку элюировали со скоростью 0,4 мл/мин с помощью градиента буфера A (50 мМ гексафторизопропанола и 15 мМ диэтиламина) к буферу B (50% А и 50% метанола:ацетонитрил 1:1), от 5% до 25% B через 8 мин, до 75% В через 5 мин, и до 95% В через 1 мин.
Пример 9. Исследование безопасности/токсичности на яванских макаках
Конъюгаты антитело-лекарственное средство по изобретению оценивали на предмет токсичности у яванских макак, включая легочные эффекты антигензависимой токсичности из-за экспрессии в легких.
План исследования:
Курс лечения: ВВ (IV) (внутривенное) дозирование дважды, в дни 1 и 22 для оценки токсичности в течение 2 полных циклов. 10 дней свинец (1M на группу), дозированный за 10 дней до 1М/2F для снижения риска развития острой заболеваемости/смертности.
Потенциальные клинические наблюдения могут включать покраснение кожи, черное обесцвечивание кожи, шелушение/отслаивание, язвы, отечность лица/отек, тело с низким процентом жировой ткани, отсутствие аппетита и общее предсмертное состояние.
Возможные клинические патологические изменения, связанные с дозировкой конъюгата антитело-лекарственное средство у яванских макак, могут включать увеличение азота мочевины и креатинина в сочетании с неадекватно сконцентрированной мочой, изменениями количеств натрия, хлора и калия, вероятно, связанными с нарушенной функцией трубочек почек, альвеолярную дегенерацию легких, и изменения в гематологических параметрах и воспаление в ответ на дозу.
Основные органы подверженные токсичности могут включать почки, глаза, кожу/подкожный слой/мышцы, костный мозг, легкие, лимфоидные органы (истощение селезенки и тимуса).
Дозозависимое увеличение тяжести результатов патологии может позволить сравнить характеристики безопасности/токсичности конъюгатов антитело-лекарственное средство и контрольных соединений.
Пример 10. Эффективность в мышах
Эффективность конъюгатов анти-Her2 антитело-лекарственное средство исследовали в модели аллотрансплантата мыши MMTV-HER2 Основатель № 5 (Founder #5) (опухоль молочной железы мыши) или мышиной модели ксенотрансплантата KPL4, HCC1569X2 (рак молочной железы человека).
Модель MMTV-HER2 Основатель № 5 (Fo5) (разработанная в Genentech) представляет собой модель трансгенной мыши, в которой ген HER2 человека под транскрипционной регуляцией промотора вируса опухоли молочной железы мыши (MMTV-HER2) сверхэкспрессируется в эпителии молочной железы. Сверхэкспрессия вызывает спонтанное развитие опухолей молочной железы, которые сверхэкспрессируют человеческий рецептор HER2. Опухоль молочной железы из одного из животных-основателей (основателя № 5, Fo5) была хирургически имплантирована в торакальную молочную железу мышиных самок nu/nu или FVB (Charles River Laboratories) в виде опухолевых фрагментов размером около 15-30 мм3.
Клеточная линия рака молочной железы KPL4 была получена в лаборатории доктора Дж. Куребайаши (Япония). Клеточная линия рака молочной железы HCC1569 была получена из АКТК (Американская коллекция типовых культур, Манассас, Вирджиния), и сублиния HCC1569X2 была получена в Genentech для оптимального роста в мышах. Обе клеточные линии экспрессируют HER2, как определено СКАФ (сортировка клеток с активированной флуоресценцией, FACS) и ИГХ (иммуногистохимия, IHC). Чтобы создать модель, каждой мышиной самке C.B-17 SCID-beige (Charles River Laboratories) инокулировали в торакальную молочную железу 3 миллиона клеток KPL4 или 5 миллионов клеток HCC1569X2, суспендированных в HBSS/матригель (соотношение 1:1).
Когда опухоли достигли среднего объема опухоли 100-300 мм3, животных рандомизировали в группы по 5-10 мышей каждая и они получали однократную внутривенную инъекцию КАЛС (ADC) (обозначено День 0). Опухоли и массы тела мышей измеряли 1-2 раза в неделю на протяжении всего исследования. Мышей быстро подвергали эвтаназии, когда потеря массы тела составляла больше чем 20% от начального веса. Все животные были подвергнуты эвтаназии до того, как опухоли достигли 3000 мм3 или появлялись признаки надвигающегося изъязвления. Объем опухоли измеряли в двух измерениях (длина и ширина) с применением штангенциркулей, и объем опухоли рассчитывали по формуле: размер опухоли (мм3)=0,5×(длинна × ширина × ширина). Данные этого теста показаны на фиг. 12 и 13.
Пример 11. Токсикология у яванских макак
Анти-HER2 hu7C2 LC:K149C-LD-51 исследование токсикологии яванских макак
Экспериментальное исследование токсичности повышения доз было проведено на яванских макаках. Животные получали две или четыре медленных болюсных дозы ВВ (IV) каждые три недели анти-HER2 hu7C2 LC:K149C-LD-51, начиная с дозы 1 мг/кг. Повышение дозы проводилось поэтапно к 2-3 недели. План исследования приведен в таблице 7 ниже.
Таблица 7: План исследования токсикологии анти-HER2-LD51 LC: K149C у яванских макак
Токсичность оценивали с помощью клинических и офтальмологических исследований и лабораторной клинической диагностики (гематология, химия сыворотки, коагуляция и анализ мочи, примерно еженедельно в течение всего исследования). Определение гистологических макро- и микропатологий проводили на тканях, собранных при вскрытии через три недели после последней дозы.
У животных, которым вводили четыре дозы 16 мг/кг анти-HER2 hu7C2 LC:K149C-LD-51 каждые три недели, гистологические патологии обычно были более тяжелыми, чем после двух доз 16 мг/кг. Наблюдалась дегенерация трубочек почек (легко-умеренная), лимфоидное истощение (тимус, селезенка, лимфатические узлы, легко- умеренное), пигментация кожи/гиперкератоз (легкий), дегенерация слизистой оболочки тонкой кишки (легкая) и легкая альвеолярная дегенерация/фиброплазия (легкая) легких.
Основными целевыми органами анти-HER2 hu7C2 LC:K149C-LD-51 у яванских макак являются почки, костный мозг, кожа, легкие, лимфоидные органы (селезенка, тимус, лимфатические узлы), тонкая кишка и глаз (роговица). Максимальная переносимая доза (МПД) в виде схемы приема лекарств 2X каждые три недели составляет 16 мг/кг, тогда как МПД в виде схемы приема лекарств 4X каждые три недели составляет 8 мг/кг.
Никаких исследований анти-HER2-CLD-1 не проводилось у обезьян. Тем не менее, 2X МПД доза CLD-1 каждые три недели при конъюгировании с другими антителами с внесенным цистеином определялась у яванских макак. МПД двух доз анти-NaPi2b-CLD-1 каждые три недели составляла 0,5 мг/кг, тогда как у не нацеленного на мишень конъюгата gD-CLD-1 она составляла 0,5 мг/кг. Наблюдаемые аналогичные эффекты для органов-мишеней свидетельствуют о том, что токсичность в значительной степени антиген-независима и связана к CLD-1 или LD-51. Увеличенная МПД конъюгатов LD-51 по сравнению с конъюгатами CLD-1 указывает на улучшение переносимости LD-51 по сравнению с CLD-1. Данные для этих испытаний показаны на фиг. 12 и 13.
Пример 12. Исследование токсичности C-1 и DM-2 на крысах
Проведено токсикологическое исследование экспериментальных одиночных доз на крысах, для сравнения свободных лекарственных средств C-1 (ПБД-бис-алкилирующее вещество) и DM-2 (ПБД-моноалкилирующее вещество). Животные получали ВВ (IV) единичную дозу C-1, DM-2 или наполнителя, и за ними наблюдали в течение семидневного периода восстановления. План исследования приведен в таблице 8 ниже.
Таблица 8: План исследования токсичности свободных лекарственных средств C-1 и DM-2 на крысах
Токсичность оценивали по клиническими наблюдениями и с помощью лабораторной клинической диагностики (гематология и клиническая химия в 72 и 168 час после дозы). В целом, как правило, результаты были одинаковыми для DM-2 при в десять раз большей дозе по сравнению с C-1. Для C-1 дозозависимое снижение количества ретикулоцитов наблюдалось при всех дозах через 72 часа, восстанавливаясь в группах 0,05 и 0,1 мг/кг к 168 часу после введения дозы. При дозе 0,2 мг/кг наблюдались клинико-патологические изменения, указывающие на токсичность для печени и почек. Дозы 0,05 и 0,1 мг/кг хорошо переносились без клинических проявлений.
Величины доз 0,5 и 1 мг/кг DM-2 хорошо переносились, что не приводило к появлению клинических проявлений или ранних эвтаназий. Животные, которым вводили 2 мг/кг, теряли около 14% от их массы тела с 2 по 4 день и подвергались эвтаназии в предсмертном состоянии в День 4. Дозозависимое снижение количества ретикулоцитов наблюдалось при всех дозах DM-2 через 72 часа после дозы, которое восстанавливалось в группах 0,5 и 1 мг/кг к 168 часу после введения дозы. При дозе 2 мг/кг наблюдались клинико-патологические изменения, указывающие на токсичность для печени и почек.
Таким образом, профиль токсичности, возникающий в результате однократной дозы С-1 или DM-2, был аналогичным, при этом С-1 примерно в десять раз превосходил DM-2. Основными органами-мишенями обоих тестируемых изделий были костный мозг, почки и печень. МПД С-1 и DM-2 составляли 0,1 и 1 мг/кг, соответственно, в виде одной ВВ (IV) дозы у крыс. Результаты этого исследования показывают улучшенную переносимость DM-2 по сравнению с C-1.
Пример 13. Активность in vitro в HER2 положительных клеточных линиях рака молочной железы SK-BR-3 и KPL-4
Клетки высевали в 96-луночные плашки и оставляли для прилипания в течение ночи при 37 °С в увлажненной атмосфере с 5% СО2. Затем среду удаляли и заменяли свежей культуральной средой, содержащей различные концентрации каждого лекарственного средства. Cell Titer-Glo (Promega Corp.) добавляли в лунки через 5 дней после введения лекарственного средства, а люминесцентный сигнал измеряли с применением EnVision Multilabel Plate Reader (PerkinElmer). Тестируемыми соединениями являлись анти-HER2 hu7C2 LC:K149C CLD-7; анти-HER2 hu7C2 LC:K149C CLD-8; анти-HER2 hu7C2 LC:K149C CLD-9; и анти-HER2 hu7C2 LC:K149C LD-51.
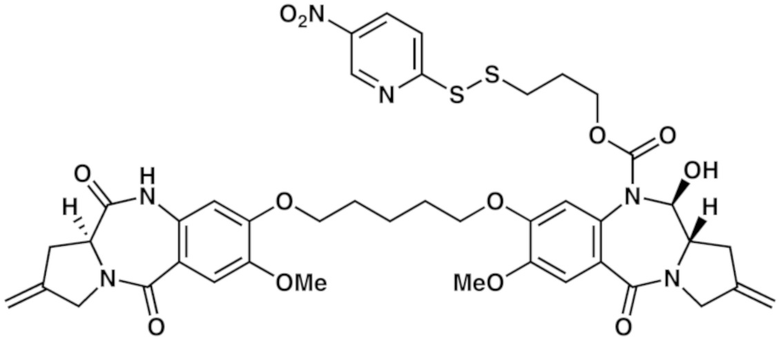
CLD-7
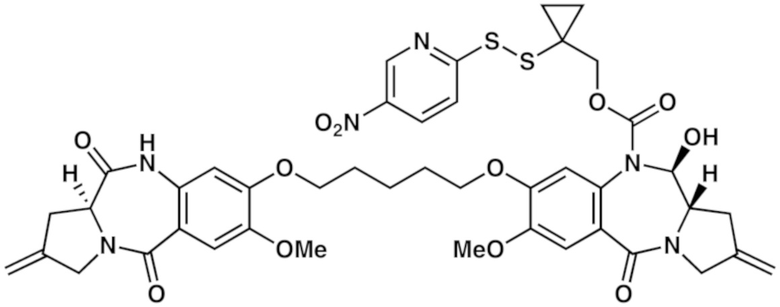
CLD-8
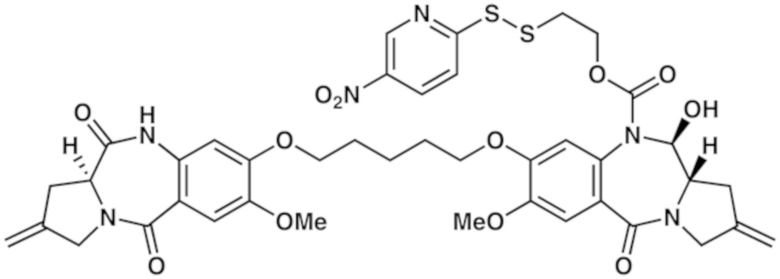
CLD-9
Данные этого теста показаны на фиг. 14 и в таблице 9 ниже.
Таблица 9
IC50
IC50
Пример 14. Эффективность in vivo для мышиного аллотрансплантата
Эффективность конъюгатов анти-Her2 антитело-лекарственное средство (КАЛС (ADC)) исследовали в модели аллотрансплантата мыши MMTV-HER2 Основатель № 5 (опухоль молочной железы мыши). Модель MMTV-HER2 Основатель № 5 (Fo5) (разработанная в Genentech) представляет собой модель трансгенной мыши, в которой ген HER2 человека под транскрипционной регуляцией промотора вируса опухоли молочной железы мыши (MMTV-HER2) сверхэкспрессируется в эпителии молочной железы. Сверхэкспрессия вызывает спонтанное развитие опухолей молочной железы, которые сверхэкспрессируют человеческий рецептор HER2. Опухоль молочной железы из одного из животных-основателей (основателя № 5, Fo5) была размножена у мышей FVB (Charles River Laboratories) путем последовательной трансплантации опухолевых фрагментов.
Для исследований эффективности трансгенную опухоль молочной железы Fo5 хирургически имплантировали в торакальную молочную железу мышиных самок nu/nu (Charles River Laboratories; Холлистер, Калифорния) в виде опухолевых фрагментов размером около 15-30 мм3. Когда опухоли аллотрансплантата достигали среднего объема опухоли 100-300 мм3 (обозначено День 0), животных рандомизировали в группы по 7 мышей каждая и они получали однократную внутривенную инъекцию КАЛС (ADC). Опухоли и массы тела мышей измеряли 1-2 раза в неделю на протяжении всего исследования. Мышей быстро подвергали эвтаназии, когда потеря массы тела составляла больше чем 20% от начального веса. Все животные были подвергнуты эвтаназии до того, как опухоли достигали 3000 мм3 или появлялись признаки надвигающегося изъязвления. Объем опухоли измеряли в двух измерениях (длина и ширина) с применением штангенциркулей, и объем опухоли рассчитывали по формуле: размер опухоли (мм3)=0,5×(длинна × ширина × ширина). Данные этого исследования показаны на фиг. 15. Среди четырех анти-Her2 КАЛС (ADC) только анти-Her2-LD-51 продемонстрировал явную противоопухолевую активность по сравнению с группой наполнителей (контролей). Эффективность анти-Her2-LD-51 была зависимой от мишени, поскольку соответствующий не нацеленный на мишень анти-CD22-LD-51 не влиял на рост опухоли.
Пример 15. Синтез DM-4, C-1, C-2, C-3, CLD-2, CLD, 3, CLD-5 и CLD-6
Метод синтеза для получения C-1, C-2, C-3 и CLD-2 может быть найден в следующих документах: C-1: Journal of Medicinal Chemistry (2004), 47(5), 1161-1174; C-2: Bioorganic & Medicinal Chemistry Letters (2000), 10(16), 1845-1847 or PCT Int. Appl. WO 2000012508; C-3: PCT Int. Appl. WO 2000012508; C-3: PCT Int. Appl. WO 2015155753; и CLD-2 US 20160074527.
Синтез CLD-7
Схема
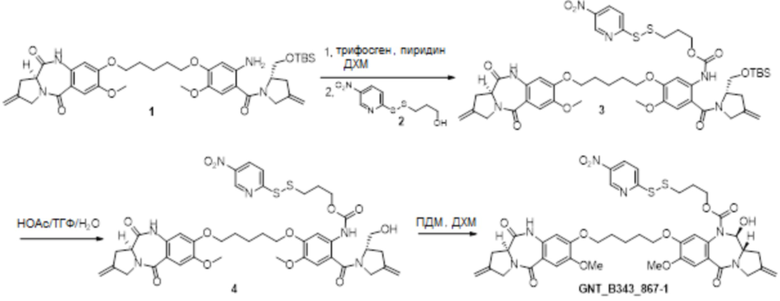
Экспериментальный
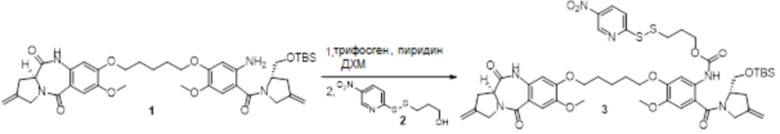
К раствору трифосгена (60,6 мг, 0,200 ммоль) в ДХМ (15 мл) добавляли раствор пиридина (129 мг, 1,63 ммоль) и 2 (55,3 мг, 0,220 ммоль) в ДХМ (15 мл). Смесь перемешивали при 0°С в течение 10 мин, ТСХ (25% EtOAc в петролейном эфире, Rf=0,5) показала, что исходный материал израсходован. Смесь концентрировали досуха и растворяли в ДХМ (10 мл) и добавляли к раствору соединения 1 (150,0 мг, 0,200 ммоль) и Et3N 103,3 мг, 1,02 ммоль в ДХМ (15 мл). Смесь перемешивали при 0°С в течение 1 часа. ТСХ (50% EtOAc в петролейном эфире) показала, что исходное вещество было израсходовано. Смесь концентрировали и неочищенный продукт очищали колоночной флэш-хроматографией на силикагеле (0-33% EtOAc в петролейном эфире). Его концентрировали, получая 3 (180,0 мг, 81%) в виде желтого твердого вещества. ЖХМС (5-95AB/1,5 мин): ВУ=1,014 мин, [M+H]+ 1007,1.
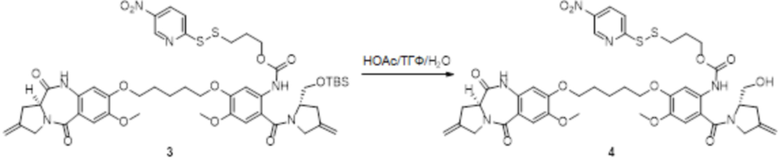
К раствору HOAc (5,0 мл, 87 ммоль) в смеси ТГФ (3,0 мл) и воды (3,0 мл) добавляли 3 (150,0 мг, 0,1500 ммоль). Реакционный раствор перемешивали при 40°С в течение 16 часов. Раствор концентрировали для удаления растворителя и остаток разбавляли EtOAc (100 мл), промывали H2O (30 мл ×4), сушили над Na2SO4, фильтровали и концентрировали. Остаток очищали подготавливающей ТСХ (5% МеОН в ДХМ, Rf=0,5), получая 4 (100 мг, 75%) в виде желтого твердого вещества. ЖХМС (5-95AB/1,5 мин): ВУ=0,776 мин, [M+H]+893,2.
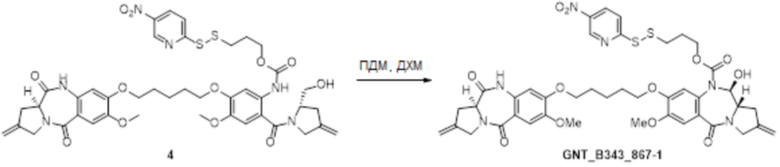
К раствору ПДМ (22,8 мг, 0,0500 ммоль) в безводном ДХМ (10,0 мл) добавляли соединение 4 (40,0 мг, 0,0400 ммоль). Реакционную смесь перемешивали при 18 °С в течение 1 часа. Смесь разбавляли ДХМ (50 мл), фильтровали. Фильтрат промывали Na2SO3 (30 мл ×3), сушили над Na2SO4, фильтровали и концентрировали под вакуумом. Остаток очищали подготавливающей ТСХ (5% MeOH в ДХМ, Rf=0,5) с получением CLD-7 (GNT_B343_867-1) (20 мг, 50%) в виде желтого твердого вещества. ЖХМС (5-95AB/1,5 мин): ВУ=0,761 мин, [M+H]+ 891,0 показали 96% целевого продукта. ВЭЖХ (10-80AB/15 мин): ВУ=8,40 мин, показала 94,9% желаемого продукта.
Синтез CLD-8
Схема
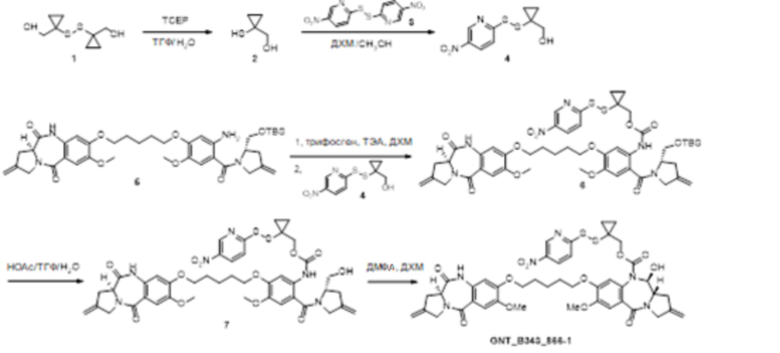
Экспериментальный
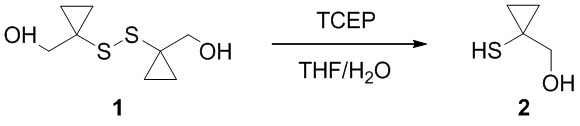
К раствору соединения 1 (40,0 мг, 0,190 ммоль) в ТГФ (5,0 мл)/вода (5,0 мл) добавляли ТКЭФ (TCEP) (277,9 мг, 0,970 ммоль). Реакционную смесь перемешивали при 16 °С в течение 48 часов. Раствор разбавляли H2O (10 мл), экстрагировали ДХМ (20 мл × 3). Объединенные органические слои сушили над Na2SO4, фильтровали и непосредственно использовали в следующем этапе.
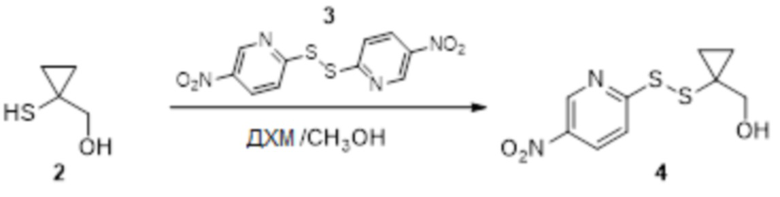
К раствору соединения 2 (40,0 мг, 0,380 ммоль) в смеси ДХМ (25 мл) и MeOH (25 мл) добавляли соединение 3 (238,3 мг, 0,770 ммоль). Реакционный раствор перемешивали при 16°C в течение 16 часов и добавляли MnO2 (500 мг) и смесь перемешивали в течение 0,5 часа. Смесь фильтровали и фильтрат концентрировали в вакууме. Остаток разбавляли MeOH (5 мл), снова фильтровали, чтобы удалить большую часть оставшегося соединения 3, фильтрат концентрировали и очищали подготавливающей ТСХ (33% EtOAc в петролейном эфире, Rf=0,5) с получением соединения 4 (50 мг, 0,157 ммоль, выход 40,8%) в виде бесцветного масла. ЖХМС (5-95AB/1,5 мин): ВУ=0,805 мин, [M+H]+ 258,9 показали 81% целевого продукта.
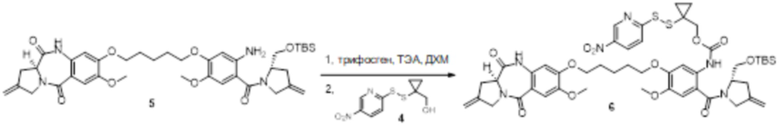
К перемешиваемой смеси трифосгена (64,6 мг, 0,220 ммоль) и 4Å MS (30 мг) в безводном ДХМ (8 мл) добавляли раствор соединения 5 (160,0 мг, 0,220 ммоль) и триэтиламина (110,1 мг, 1,09 ммоль ) в безводном ДХМ (8 мл) медленно. Реакционную смесь перемешивали при 16°С в течение 1 часа и смесь концентрировали под вакуумом для удаления растворителя. Его растворяли в безводном ДХМ (10,0 мл) и добавляли триэтиламин (65,8 мг, 0,650 ммоль) с последующим добавлением раствора 4 (50,0 мг, 0,190 ммоль) в безводном ДХМ (5,0 мл). Реакционную смесь перемешивали при 16°С в течение 16 часов. Смесь фильтровали, фильтрат концентрировали и очищали подготавливающей ТСХ (10% MeOH в ДХМ , Rf=0,8), получая соединение 6 (100 мг, 0,0814 ммоль, выход 37,6%) в виде желтого твердого вещества. ЖХМС (5-95AB/1,5 мин): ВУ=1,119 мин, [M+H]+ 1019,4 показали 83% целевого продукта.
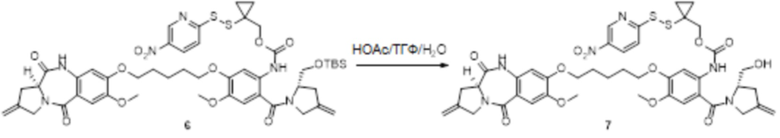
Раствор соединения 6 (100,0 мг, 0,1000 ммоль) в смеси уксусной кислоты (3,0 мл), ТГФ (2,0 мл) и воды (1,0 мл) перемешивали при 16°С в течение 48 часов. Раствор концентрировали под вакуумом и остаток разбавляли ДХМ (30 мл), промывали H2O (20 мл ×3), сушили, фильтровали и концентрировали. Остаток очищали подготавливающей ТСХ (10% MeOH в ДХМ, Rf=0,5) с получением соединения 7 (55 мг, 0,0602 ммоль, выход 61,3%) в виде желтого твердого вещества. ЖХМС (5-95AB/1,5 мин): ВУ=0,892 мин, [M+H]+ 905,2 показали 99% целевого продукта.
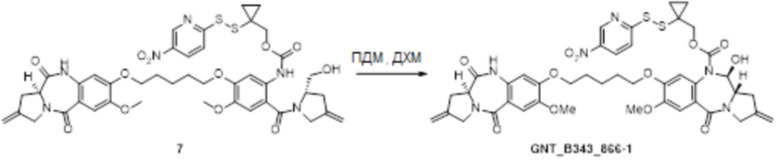
К смеси соединения 7 (55 мг, 0,060 ммоль) и 4Å MS (30 мг) в безводном ДХМ (6,0 мл) добавляли ПДМ (44,0 мг, 0,104 ммоль). Реакционную смесь перемешивали при 16°С в течение 1 часа. Смесь разбавляли EtOAc (30 мл), гасили насыщенным раствором Na2SO3 (30 мл) и экстрагировали EtOAc (30 мл ×3). Объединенные органические слои сушили над Na2SO4, фильтровали и концентрировали. Остаток очищали подготавливающей ТСХ (10% MeOH в ДХМ, Rf=0,5), получая CLD-8 (GNT_B343_866-1) (42 мг, выход 77%) в виде бледно-желтого твердого вещества. ЖХМС (5-95AB/1,5 мин): ВУ=0,868 мин, [M+H]+ 903,2 показали 98% целевого продукта.
Синтез CLD-9
Схема
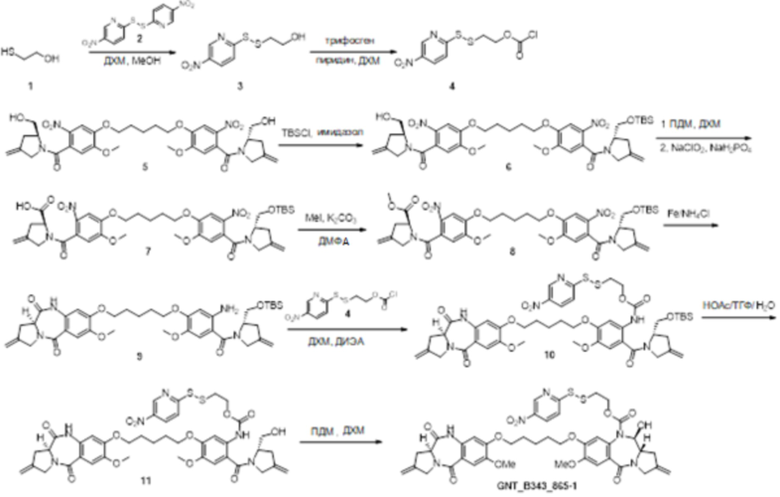
Экспериментальный
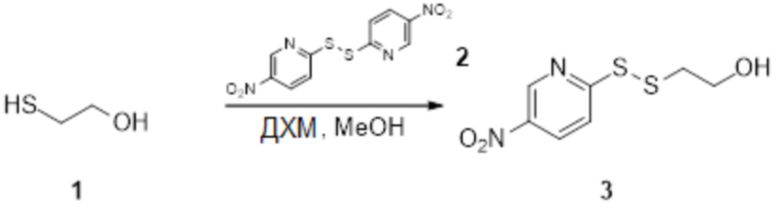
К раствору соединения 2 (2383 мг, 7,68 ммоль) в ДХМ (10 мл)/MeOH (10 мл) добавляли соединение 1 (300 мг, 3,84 ммоль). Раствор перемешивали при 16°С в течение 2 часов. MnO2 (5,0 г) добавляли в раствор, смесь перемешивали при 16°С в течение 30 мин. Смесь фильтровали и фильтрат концентрировали под вакуумом и остаток промывали MeOH (15 мл), фильтровали и концентрировали. Неочищенный продукт очищали колоночной флэш-хроматографией на силикагеле (ДХМ) с получением соединения 3 (800 мг, 3,25 ммоль, выход 84,8%) в виде масла. ЖХМС (5-95AB/1,5 мин): ВУ=0,608 мин, [M+H]+232,8.
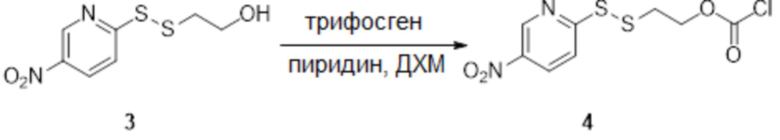
Соединение 3 (65,0 мг, 0,280 ммоль) и пиридин (88,5 мг, 1,12 ммоль) в безводном ДХМ (5,0 мл) добавляли по каплям в раствор трифосгена (41,5 мг, 0,140 ммоль) в безводном ДХМ (5,0 мл) при 0°С. Раствор перемешивали при 0°С в течение 10 мин и смесь концентрировали, получая неочищенное соединение 4 в виде белого твердого вещества, которое использовали в следующем этапе.
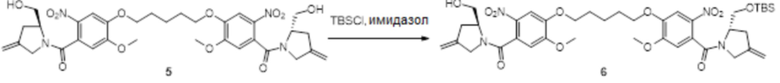
К раствору соединения 5 (4000 мг, 5,84 ммоль) в безводном ДХМ (80 мл) добавляли имидазол (2,38 г, 35,1 ммоль) с последующим добавлением TBSCl (1,761 г, 11,7 ммоль). Реакционную смесь перемешивали при 40°С в течение 3 часов. Смесь разбавляли ДХМ (100 мл), промывали H2O (50 мл ×3), сушили над Na2SO4, фильтровали и концентрировали. Остаток очищали колоночной флэш-хроматографией на силикагеле (0-3,3% MeOH в ДХМ) с получением соединения 6 (2,50 г, 3,13 ммоль, выход 53,6%) в виде бледно-желтого твердого вещества.
ЖХМС (5-95AB/1,5 мин): ВУ=0,945 мин, [M+H]+799,2.
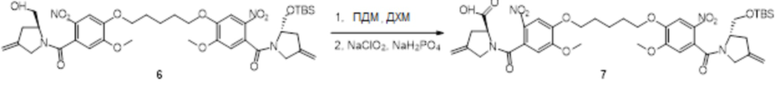
К раствору соединения 6 (2,30 г, 2,88 ммоль) в безводном ДХМ (100 мл) добавляли ПДМ (4,88 г, 11,52 ммоль). Реакционную смесь перемешивали при 10°С в течение 2 часов. Ее фильтровали, фильтрат разбавляли EtOAc (600 мл), гасили насыщенным раствором Na2SO3 (200 мл), насыщенным раствором Na2SO3/NaHCO3 (об./об.=1:1, 200 мл) и насыщенным раствором соли. Органический слой сушили над Na2SO4, фильтровали и концентрировали с получением неочищенного масла, которое растворяли в tBuOH (40 мл, 2,88 ммоль)/вода (20 мл) и затем обрабатывали 2-метил-2-бутеном (30 мл, 2,88 ммоль) и дигидрофосфатом натрия (1,382 мг, 11,5 ммоль) последовательно при 10°С. После перемешивания при 10°С в течение 0,5 часа реакционную смесь перемешивали с хлоритом натрия (1,56 г, 17,3 ммоль) при 10°С в течение 1 часа. Смесь разбавляли EtOAc (300 мл) и промывали водой (100 мл) и насыщенным раствором соли (100 мл). Органический слой сушили над Na2SO4, фильтровали и концентрировали под вакуумом с получением соединения 7 (2,0 г, 2,46 ммоль, выход 85,5%) в виде неочищенного продукта. ЖХМС (5-95AB/1,5 мин): ВУ=0,929 мин, [M+H]+813,2.
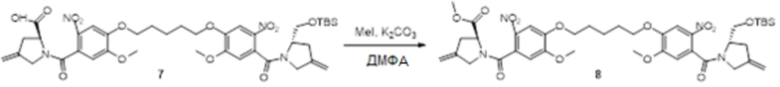
К раствору соединения 7 (2,0 г, 2,46 ммоль) в ДМФА (DMF) (20 мл) добавляли K2CO3 (680 мг, 4,92 ммоль) с последующим добавлением MeI (3,95 г, 27,8 ммоль). Реакционную смесь перемешивали при 10°С в течение 1 часа. Смесь разбавляли EtOAc (200 мл), промывали насыщенным раствором соли (40 мл ×5), затем сушили над Na2SO4, фильтровали и концентрировали под вакуумом с получением соединения 8 (2,0 г, 2,42 ммоль, выход 98,3%) в виде желтого масла. ЖХМС (5-95AB/1,5 мин): ВУ=0,975 мин, [M+H]+827,2.
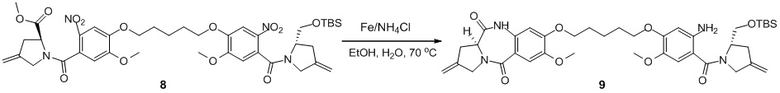
К смеси соединения 8 (2,0 г, 2,42 ммоль) и железа (1,35 г, 24,2 ммоль) в EtOH (20 мл)/вода (10 мл) добавляли NH4Cl (2,59 г, 48,7 ммоль). Реакционную смесь перемешивали при 70 °С в течение 2 часов. Смесь фильтровали, фильтрат концентрировали под вакуумом для удаления EtOH, и водную суспензию экстрагировали EtOAc (50 мл × 3). Объединенные EtOAc-слои сушили над Na2SO4, фильтровали, концентрировали и очищали колоночной флэш-хроматографией на силикагеле (3-5% MeOH в ДХМ, Rf=0,5), получая соединение 9 (1,5 г, 1,89 ммоль, выход 78,1%) в виде желтого твердого вещества. ЖХМС (5-95AB/1,5 мин): ВУ=0,845 мин, [M+H]+735,3.
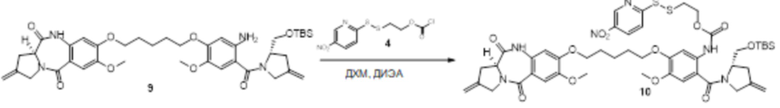
К раствору соединения 9 (100 мг, 0,140 ммоль) и ДИЭА (DIEA) (68,8 мг, 0,680 ммоль) в ДХМ (15 мл) добавляли соединение 4 (80,2 мг, 0,270 ммоль) и реакционную смесь перемешивали при 0 °С в течение 1 часа. Смесь концентрировали и остаток очищали колоночной флэш-хроматографией на силикагеле (0-5% MeOH в ДХМ, Rf=0,5), получая соединение 10 (130 мг, 0,117 ммоль, выход 85,8%) в виде желтого масла. ЖХМС (5-95AB/1,5 мин): ВУ=0,985 мин, [M+H]+993,4.
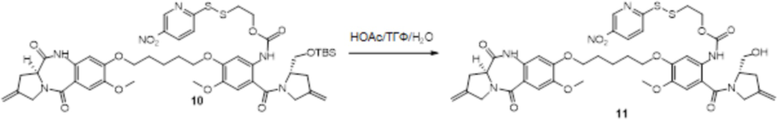
К раствору уксусной кислоты (6,0 мл, 105 ммоль) в ТГФ (6,0 мл)/вода (3,0 мл) добавляли соединение 10 (130 мг, 0,130 ммоль). Реакционный раствор перемешивали при 40°С в течение 24 часов. Раствор концентрировали под вакуумом для удаления растворителя, остаток разбавляли EtOAc (30 мл), промывали H2O (10 мл ×4), сушили над Na2SO4, фильтровали и концентрировали под вакуумом. Остаток очищали подготавливающей ТСХ (8% MeOH в ДХМ, Rf=0,5) с получением соединения 11 (60 мг, 0,0683 ммоль, выход 52,2%) в виде желтого масла. ЖХМС (5-95AB/1,5 мин): ВУ=0,763 мин, [M+H]+879,0.
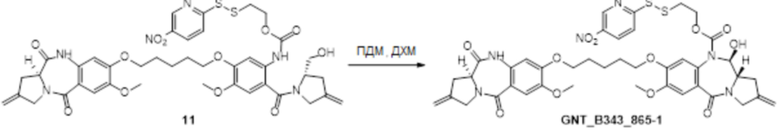
К раствору соединения 11 в безводном ДХМ (5 мл) добавляли ПДМ (17,4 мг, 0,0400 ммоль). Реакционную смесь перемешивали при 18°С в течение 1 часа. Смесь разбавляли ДХМ (50 мл), фильтровали. Фильтрат промывали Na2SO3 (30 мл ×3), сушили над Na2SO4, фильтровали и концентрировали под вакуумом. Неочищенный продукт очищали подготавливающей ТСХ (5% MeOH в ДХМ, Rf=0,5), получая CLD-9 (GNT_B343_865-1) (12,2 мг, 0,0136 ммоль, выход 39,9%) в виде бледно-желтого твердого вещества. ЖХМС (5-95AB/1,5 мин): ВУ=0,739 мин, [M+H]+877,2.
Синтез DM-4
Схема
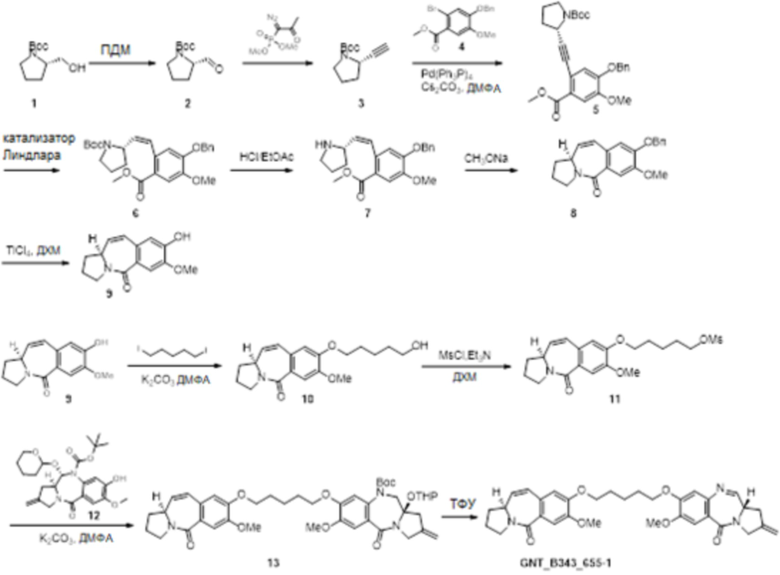
Экспериментальный

К раствору соединения 1 (3,0 г, 14,9 ммоль) в ДХМ (80 мл) добавляли ПДМ (9,48 г, 22,4 ммоль). После перемешивания смеси при 0°С в течение 1 часа ее разбавляли Na2S2O3 (50 мл)/NaHCO3 (50 мл) и MTBE (130 мл). Органическую фазу промывали водой (60 мл ×3) и концентрировали с получением соединения 2 (2,9 г, 14,6 ммоль, выход 97,6%) в виде бесцветного масла.
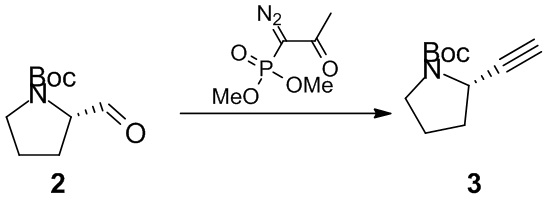
К раствору соединения 2 (2,9 г, 14,6 ммоль) и диметил (1-диазо-2-оксопропил) фосфоната в MeOH (20 мл) добавляли K2CO3 (6,03 г, 43,7 ммоль). После того как реакционную смесь перемешивали при 20°С в течение 1 часа, ее концентрировали под вакуумом и остаток очищали колоночной флэш-хроматографией на силикагеле (10% EtOAc в РЕ) с получением соединения 3 (2,0 г, 10,24 ммоль, выход 70,4%) в виде бесцветного масла.
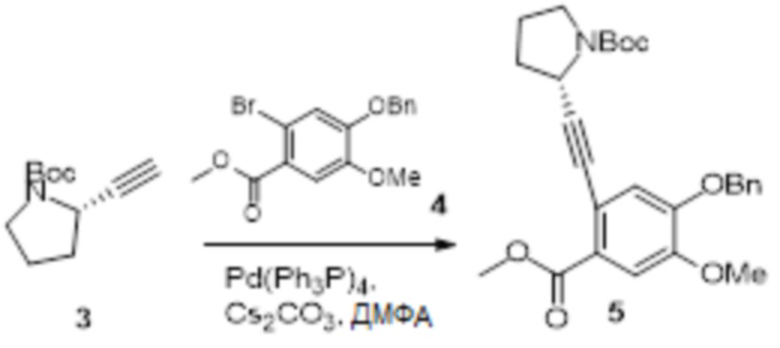
К раствору соединения 3 (2,0 г, 10,2 ммоль) и соединения 4 (5,4 г, 15,4 ммоль) в ДМФА (DMF) (50 мл) добавляли Cs2CO3 (3,97 г, 20,5 ммоль) и Pd(PPh3)4 (785 мг, 1,54 ммоль). Смесь перемешивали при 95 °С в атмосфере азота в течение 1 часа. Смесь концентрировали и очищали колоночной флэш-хроматографией на силикагеле (20% EtOAc в РЕ) с получением соединения 5 (1,60 г, 2,44 ммоль, 23,8% выход) в виде бесцветного масла.
ЖХМС (5-95AB/1,5 мин): ВУ=0,994 мин, [M+H-56]+410,0.
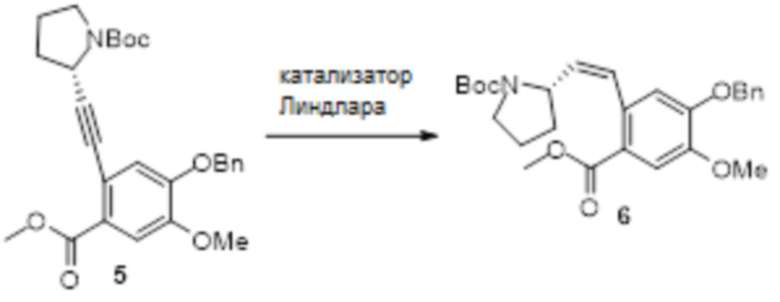
К раствору соединения 5 (2,0 г, 4,3 ммоль) в MeOH (10 мл) добавляли Pd/CaCO3 (200,0 мг, 21,5 ммоль). Смесь перемешивали при 30°С в течение 1 часа в атмосфере H2 (1 атм). Смесь фильтровали и фильтрат концентрировали с получением неочищенного продукта, который очищали колоночной флэш-хроматографией на силикагеле (10% EtOAc в РЕ) с получением продукта соединение 6 (1,0 г, 2,14 ммоль, выход 49,8%) в виде белого твердого вещества. ЖХМС (5-95AB/1,5 мин): ВУ=0,983 мин, [M+Na]+490,1.

К раствору соединения 6 (0,90 г, 1,92 ммоль) в EtOAc (10 мл) добавляли HCl/EtOAc (6,0 мл). После перемешивания смеси при 25°С в течение 1 часа ее концентрировали с получением неочищенного соединения 7 (0,77 г, 1,90 ммоль, выход 99%) в виде белого твердого вещества.
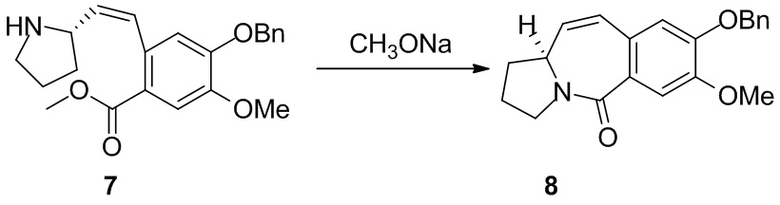
К раствору соединения 7 (0,77 г, 1,91 ммоль) в MeOH (30 мл) добавляли NaOMe (1,03 г, 19,06 ммоль). Смесь перемешивали при 30 °С в течение 2 часов. Смесь концентрировали и очищали колоночной флэш-хроматографией на силикагеле (25-75% EtOAc в РЕ) с получением соединения 8 (0,60 г, 1,79 ммоль, выход 93,8%) в виде желтого масла. 1H ЯМР (400 МГц, CDCl3)δ м.д. 1,89-2,11 (m, 3 H) 2,18-2,33 (m, 1 H) 3,59 (dt, J=12,0, 7,6 Гц, 1 H) 3,80 (dt, J=11,5, 5,8 Гц, 1 H) 3,90-3,96 (m, 1 H) 3,97 (s, 3 H) 5,19 (s, 2 H) 5,86 (dd, J=10,0, 4,8 Гц, 1 H) 6,53 (dd, J=10,0, 2,0 Гц, 1 H) 6,69 (s, 1 H) 7,29-7,35 (m, 1 H) 7,36-7,41 (m, 2 H) 7,42-7,48 (m, 2 H) 7,62 (s, 1 H).
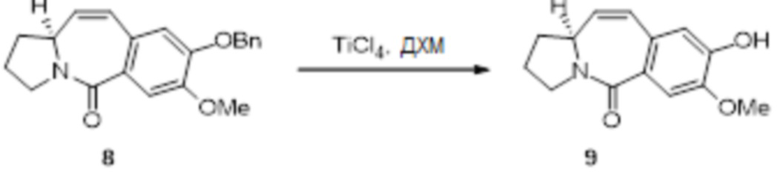
К раствору соединения 8 (580 мг, 1,73 ммоль) в ДХМ (50 мл) добавляли TiCl4 (656 мг, 3,46 ммоль). Смесь перемешивали при 30°С в течение 12 часов. В смесь добавляли HCl (1,0 М, 20 мл) и EtOAc (100 мл). Органический слой промывали водой (50 мл ×3) и концентрировали с получением неочищенного продукта соединения 9 (250 мг, 0,44 ммоль, выход 25,3%) в виде желтого твердого вещества.
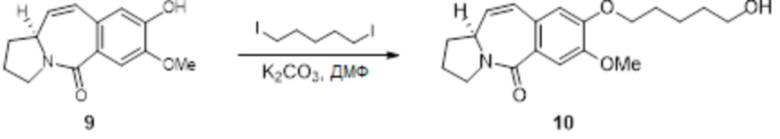
В раствор соединения 9 (50,0 мг, 0,20 ммоль) в ДМФА (DMF) (5,0 мл) добавляли K2CO3 (42,26 мг, 0,31 ммоль) и 1,5-дииодопентан (333 мг, 1,0 ммоль). Реакционную смесь перемешивали при 90°С в течение 3 часов. Реакционную смесь очищали хроматографией на колонке с силикагелем (0-50% EtOAC в петролейном эфире) с получением соединения 10 (60 мг, 0,178 ммоль, выход 87,6%) в виде масла. ЖХМС (5-95AB/1,5 мин): ВУ=0,765 мин, [M+H]+332,0.
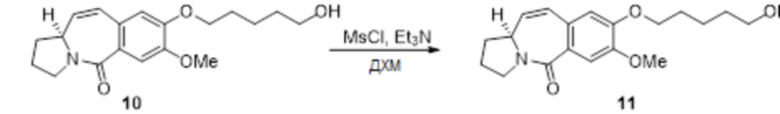
К раствору соединения 10 (60,0 мг, 0,18 ммоль) в ДХМ (6,0 мл) добавляли триэтиламин (55 мг, 0,54 ммоль) и MsCl (41 мг, 0,36 ммоль). После перемешивания смеси при 35°С в течение 1 часа ее разбавляли EtOAc (80 мл) и промывали водой (50 мл ×3). Органический слой концентрировали с получением неочищенного продукта (70 мг) в виде бесцветного масла. ЖХМС (5-95AB/1,5 мин): ВУ=0,679 мин, [M+H]+410,0.
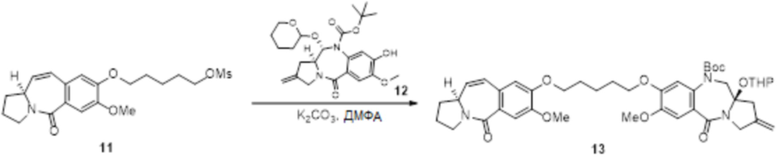
К раствору соединения 11 (70 мг, 0,17 ммоль) и соединения 12 (87 мг, 0,19 ммоль) в ДМФА (DMF) (5,0 мл) добавляли K2CO3 (47 мг, 0,34 ммоль) и KI (5,68 мг, 0,030 ммоль). Смесь перемешивали при 90°С в течение 3 часов и очищали подготавливающей ВЭЖХ (НСООН) с получением соединения 13 (70 мг, 0,084 ммоль, выход 49,2%) в виде белого твердого вещества. ЖХМС (5-95AB/1,5 мин): ВУ=0,845 мин, [M+H]+774,4.
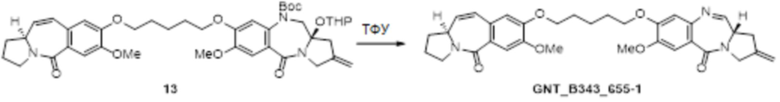
Раствор соединения 13 (50 мг, 0,060 ммоль) в смеси ТФК (1,9 мл) и воды (0,10 мл) перемешивали при 35°С в течение 1 часа. Смесь распределяли между насыщенным раствором NaHCO3 (30 мл) и EtOAc (50 мл). Органический слой промывали водой (30 мл ×2), насыщенным раствором соли (30 мл) и сушили над Na2SO4. Его концентрировали и очищали подготавливающей ТСХ (5% МеОН в ДХМ, Rf=0,5) с получением продукта DM-4 (GNT_B343_655-1) (20 мг, 0,034 ммоль, выход 53,1%) в виде белого твердого вещества. ЖХМС (5-95AB/1,5 мин): ВУ=0,825 мин, [M+H]+572,1. 1H ЯМР (400 МГц, CDCl3)δ м.д. 1,65-1,75 (m, 3H) 1,88-2,10 (m, 8H) 2,19-2,31 (m, 1H) 2,82-3,29 (m, 2H) 3,60 (dt, J=11,9, 7,5 Гц, 1H) 3,81 (dt, J=11,6, 5,9 Гц, 1H) 3,86-3,91 (m, 1H) 3,94 (s, 6H) 3,97 (br. s., 1H) 4,01-4,18 (m, 4H) 4,30 (s, 2H) 5,19 (d, J=10,6 Гц, 2H) 5,89 (dd, J=9,9, 5,1 Гц, 1H) 6,53-6,63 (m, 1H) 6,66 (s, 1H) 6,81 (s, 1H) 7,51 (s, 1H) 7,59 (s, 1H) 7,68 (d, J=4,4 Гц, 1H).
Синтез CLD-3
Схема
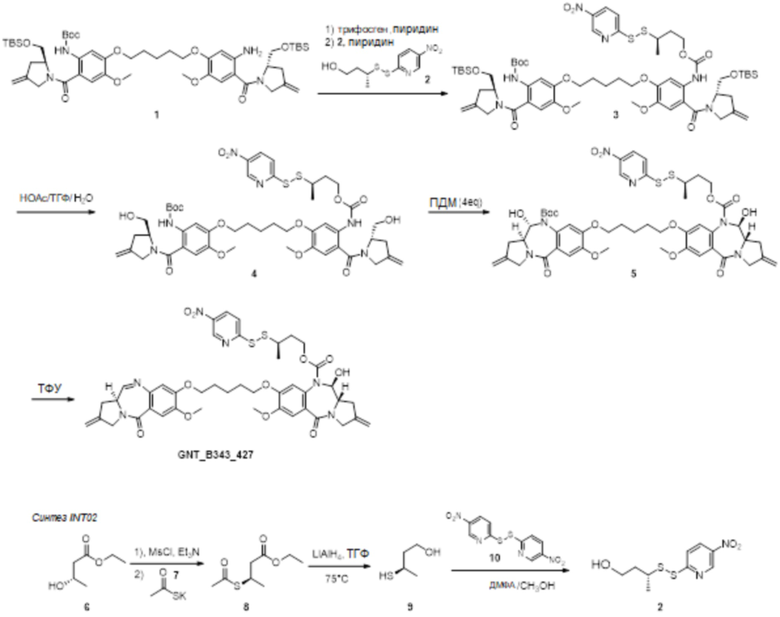
Экспериментальный
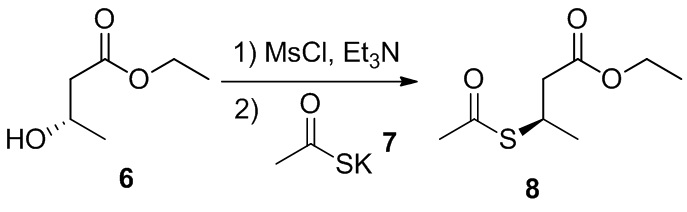
К раствору соединения 6 (5,00 г, 37,83 ммоль) и Et3N (11,49 г, 113,50 ммоль) в ДХМ (100 мл) добавляли по каплям MsCl (8,97 г, 78,32 ммоль) при 0°С. После перемешивания при 25°С в течение 2 часов в атмосфере N2 реакционную смесь выливали в ледяную воду (200 мл) и экстрагировали ДХМ (100 мл ×2). Органическую фазу промывали насыщенным раствором соли, сушили над Na2SO4 и концентрировали под вакуумом, получая неочищенный продукт (7,0 г, 95%) в виде желтого масла. Его смешивали с KSAc (6,59 г, 57,66 ммоль) в ацетоне/воде (50 мл/50 мл) и перемешивали при 25°C в течение 10 часов. Реакционную смесь концентрировали и очищали колоночной флэш-хроматографией на силикагеле (PE/EtOAc=100/1~40/1) с получением чистого соединения 8 (1,0 г, 14,6%) в виде желтого масла.
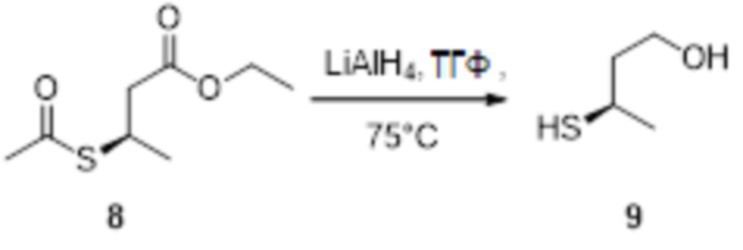
К суспензии LiAlH4 (692 мг, 18,23 ммоль) в ТГФ (20 мл) добавляли раствор соединения 8 (867 мг, 4,56 ммоль) в ТГФ (5 мл) при 0°С в атмосфере N2. Реакционную смесь перемешивали при 75 °С при нагревании с обратным холодильником в течение 2 часов. Реакционную смесь гасили EtOAc (3,0 мл) и раствором HCl (2,0 М, 5 мл) при 0°С. Реакционную смесь непосредственно использовали в следующем этапе.

К раствору соединения 10 (2,84 г, 9,12 ммоль) в ДХМ /МеОН (25 мл/25 мл) добавляли раствор соединения 9 (с вышеописанного этапа) при 25°С. Смесь перемешивали при 25°С в течение 10 часов. В реакционную смесь добавляли MnO2 (3,4 г, 39,6 ммоль) и фильтровали. Фильтрат концентрировали под вакуумом и очищали колоночной флэш-хроматографией на силикагеле (ДХМ) и SFC с получением соединения 2 (0,80 г, 67,4%) в виде желтого масла. ЖХМС (5-95 АВ, 1,5 мин): ВУ=1,020 мин, М+Н+=260,9.
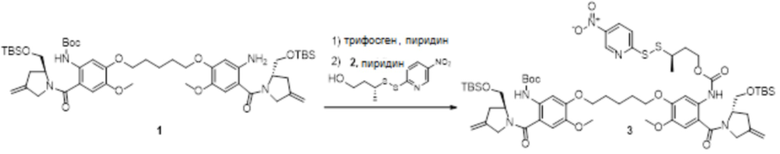
К раствору трифосгена (46 мг, 0,16 ммоль) в ДХМ (3,0 мл) добавляли по каплям раствор соединения 2 (100 мг, 0,38 ммоль) и пиридина (30 мг, 0,38 ммоль) в ДХМ (3 мл) при 0°С. Реакционную смесь перемешивали при 0°С в течение 15 мин и добавляли по каплям при 26°С к раствору соединения 1 (280 мг, 0,29 ммоль) и пиридина (30 мг, 0,38 ммоль) в ДХМ (4,0 мл). Реакционную смесь перемешивали при 26°С в течение 2 часов. Растворитель удаляли и остаток очищали подготавливающей ТСХ (растворитель: 30% EtOAc в петролейном эфире) с получением соединения 3 (300 мг, 82,4%) в виде желтой пены. ЖХМС (5-95AB/1,5 мин): ВУ=1,248 мин, [M+H]+1239,5.
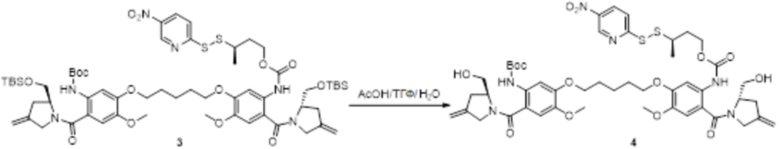
К раствору соединения 3 (312 мг, 0,24 ммоль) в ТГФ/Н2О (4 мл/4 мл) добавляли HOAc (6,0 мл) при 26°С. После того, как реакционную смесь перемешивали при 26°С в течение 24 часов, ее разбавляли EtOAc (20 мл) и промывали водой (2×10 мл), насыщенным. водн. NaHCO3 (15 мл) и насыщенным раствором соли (15 мл). Его сушили, концентрировали и очищали колоночной флэш-хроматографией на силикагеле (0-5% MeOH в ДХМ) с получением соединения 4 (240 мг, 97,1%) в виде желтой пены. ЖХМС (5-95AB/1,5 мин): ВУ=0,876 мин, [M+H]+ 1011,3.
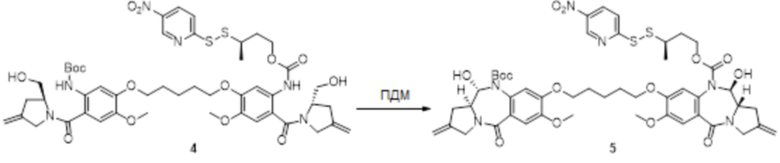
К раствору соединения 4 (101 мг, 0,10 ммоль) в ДХМ (5,0 мл) добавляли ПДМ (125 мг, 0,29 ммоль) при 0°C. Реакционную смесь перемешивали при 26°С в течение 2 часов. Реакцию гасили с помощью насыщенного раствора NaHCO3/Na2SO3 (2,0 мл/2,0 мл) и экстрагировали ДХМ (3×5 мл). Объединенный органический слой промывали NaHCO3/Na2SO3 (2 мл/2 мл), насыщенным раствором соли (5 мл), сушили и концентрировали. Остаток очищали подготавливающей ТСХ (ДХМ /MeOH=15:1) с получением соединения 5 (66 мг, 66,2%) в виде желтой пены. ЖХМС (5-95AB/1,5 мин): ВУ=0,815 мин, [(M-100)/2+Na]+ 476,1.
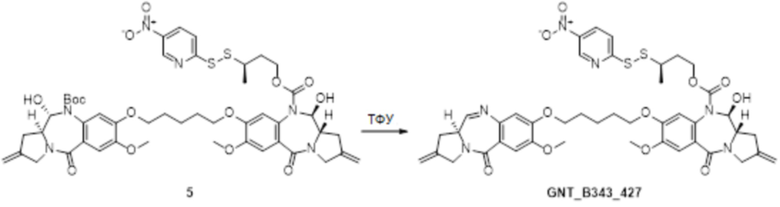
Холодную ТФК (95% в воде, 2,0 мл) добавляли к соединению 5 (66 мг, 0,06 ммоль) при 0°С. Реакционную смесь перемешивали при 0°С в течение 30 мин. Реакционную смесь добавляли по каплям к холоду. водн. раствору NaHCO3 (4,0 мл) при 0°С и экстрагировали ДХМ (4×8,0 мл). Объединенный органический слой промывали насыщенным раствором соли (20 мл), сушили и концентрировали с получением неочищенного продукта, который очищали с помощью подготавливающей ТСХ (6,25% MeOH в ДХМ, Rf=0,5) с получением CLD-3 (GNT_B343_427-1) (27,4 мг, 47,4%) в виде желтой пены. 1H ЯМР (400 МГц, CDCl3) δ 9,21 (s, 1H), 8,38-8,35 (m, 1H), 7,79 (d, J=8,8 Гц, 1H), 7,69 (d, J=4,4 Гц, 1H), 7,47 (s, 1H), 7,17 (s, 1H), 6,80 (s, 1H), 6,50 (s, 1H), 5,57 (d, J=9,2 Гц, 1H), 5,20-5,13 (m, 4H), 4,29-4,25 (m, 5H), 4,14-4,09 (m. 4H), 3,96-3,87 (m, 8H), 3,38 (d, J=8,0 Гц, 1H), 3,58 (d, J=8,0 Гц, 2H), 3,44 (s, 1H), 3,16-3,09 (m, 1H), 2,97-2,89 (m, 3H), 2,71-2,67 (m, 1H), 1,95-1,91 (m, 6H), 1,45-1,22 (m, 3H). ЖХМС (5-95AB/1,5 мин): ВУ=0,750 мин, [M+H]+ 889,8.
Синтез CLD-5
(R)-2-((4-нитрофенил)дисульфанил)пропил (11S,11aS)-11-гидрокси-7,8-диметокси-5-оксо-2-(хинолин-6-ил)-11,11a-дигидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-10(5H)-карбоксилат
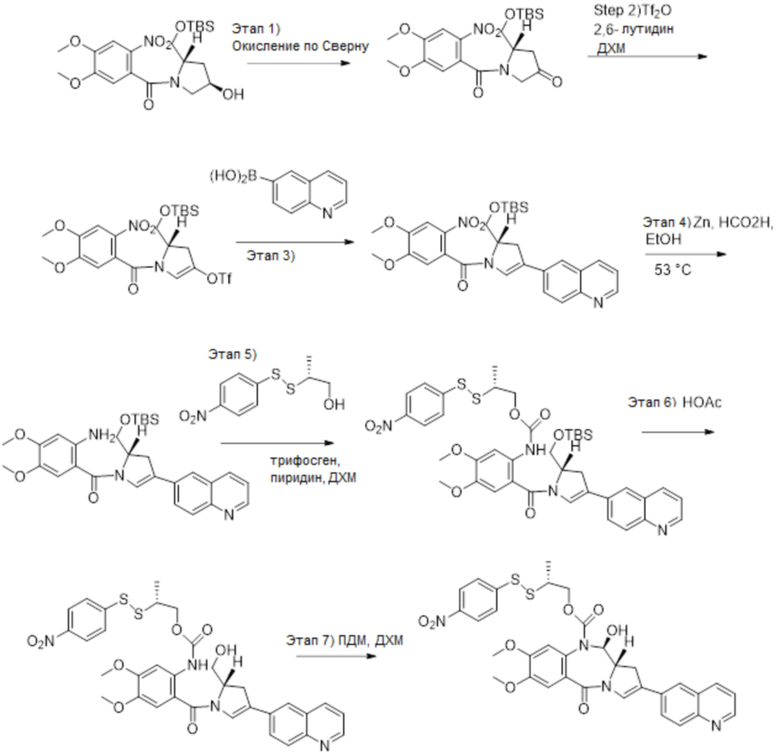
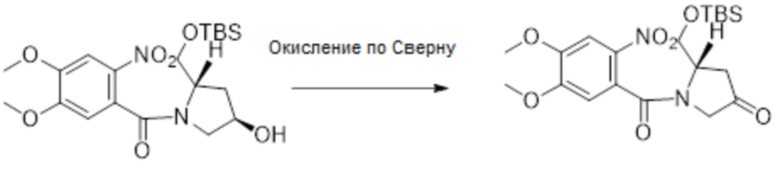
2М раствор оксалилхлорида (39 мл, 77,14 ммоль) и 60 мл дихлорметана смешивали в колбе на 500 мл, охлаждали до -78°С. ДМСО (DMSO) (5,77 мл, 77,14 ммоль) добавляли шприцом в течение около 2-3 мин. Смесь перемешивали в течение 20 мин при -78°C, затем добавляли шприцом исходное вещество (5S)-5-[[трет-бутил(диметил)силил]оксиметил]-1-(4,5-диметокси-2-нитро-бензоил)пирролидин-3-он (11,33 г, растворенное в 30 мл дихлорметана плюс 10 мл промывки, синтезированное в соответствии с Journal of Medicinal Chemistry, 2010, 53, 2927-2941 и Bioorganic & Medicinal Chemistry Letters, 2000, 10, 1845-1847). Через 30 мин при -78°С шприцом добавляли Et3N (22,6 мл, 154,3 ммоль) в течение 2 мин. Через около 4 мин смесь нагревали до 0°С и перемешивали в течение 1 часа. Смесь выливали в 100 мл воды. Дихлорметан отделяли. Водный слой экстрагировали EtOAc (2×75 мл). Объединенные органические экстракты промывали 1 н. HCl, затем насыщенным раствором бикарбонат натрия, сушили над Na2SO4 и концентрировали. Остаток очищали хроматографией на колонке с силикагелем (70%-90% EtOAc/гептан) с получением целевого продукта в виде слегка желтой пены (10,12 г).
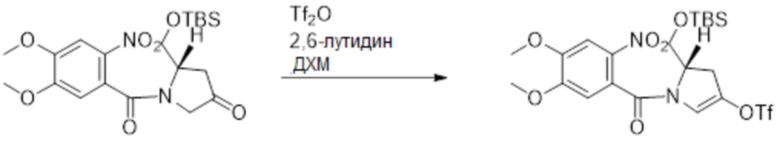
(5S)-5-[[трет-бутил(диметил)силил]оксиметил]-1-(4,5-диметокси-2-нитро-бензоил)пирролидин-3-он (1,20 г, 2,74 ммоль), 2,6 -лутидина (1,27 мл, 10,9 ммоль) смешивали в дихлорметане (45 мл) и затем охлаждали до -35°С. Затем медленно добавляли ангидрид трифторметансульфокислоты (0,87 мл, растворенный в около 5,2 мл ДХМ ) шприцом---смесь становилась ярко-желтой, а температура ванны увеличивалась до -33°С. Температура реакции не должна превышать -20°C. После в общем около 1 часа реакционную смесь пипетировали в смеси насыщенного водного раствора NaHCO3, льда и EtOAc, затем дважды экстрагировали этилацетатом (всего около 400 мл). Объединенный органический слой промывали 1н. вод. HCl, затем насыщенным раствором соли, а затем сушили над сульфатом натрия, концентрировали. Остаток очищали колоночной хроматографией на силикагеле (40%-100% EtOAc/гептан) с получением целевого продукта в виде желтого твердого вещества (957 мг).
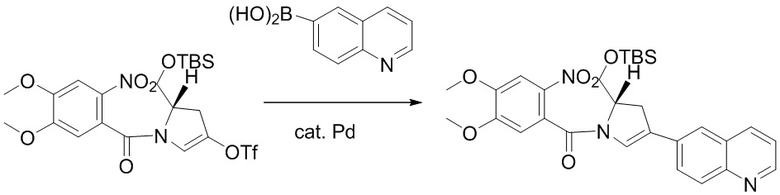
К винилтрифлату (957 мг, 1,68 ммоль) в колбе на 250 мл добавляли этанол (8,75 мл) и воду (2,5 мл), 6-хинолилбороновую кислоту (348 мг, 2,01 ммоль), фосфат калия (1,10 г, 5,03 ммоль), а затем добавляли [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладий(ii) (982 мг, 0,134 ммоль). Смесь продували азотом и затем перемешивали при комнатной температуре в атмосфере азота. После проведения реакции (около 10 мин) к реакционной смеси добавляли EtOAc (50 мл). Смесь фильтровали, чтобы удалить любое твердое вещество. К фильтрату добавляли воду (около 5 мл). Фильтрат экстрагировали EtOAc (2x). Объединенные органические слои сушили сульфатом натрия и концентрировали. Остаток очищали колоночной хроматографией на силикагеле (40%-100% EtOAc/гептан) с получением целевого продукта в виде желтого твердого вещества (928 мг).
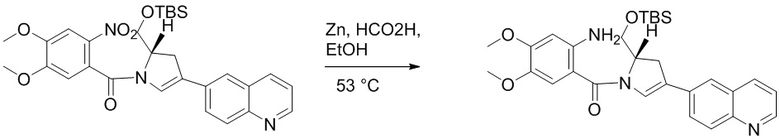
Нитро-исходный материал (322 мг, 0,586 ммоль) растворяли в 6 мл этанола и затем добавляли пыль цинка (383 мг, 5,86 ммоль) с последующим добавлением 1,5 мл 5% муравьиной кислоты в воде (75 мкл муравьиной кислоты в 1,5 мл воды). Затем смесь нагревали до 53°С и перемешивали до завершения реакции (около 3,5 часа). Смесь охлаждали до комнатной температуры, фильтровали. Фильтрат разбавляли EtOAc (около 10 мл) и затем добавляли 3 М аммиак (около 3 мл). Смесь экстрагировали EtOAc (3х). Объединенные органические слои сушили сульфатом натрия и концентрировали с получением неочищенного анилина, который использовали в следующем этапе без очистки.
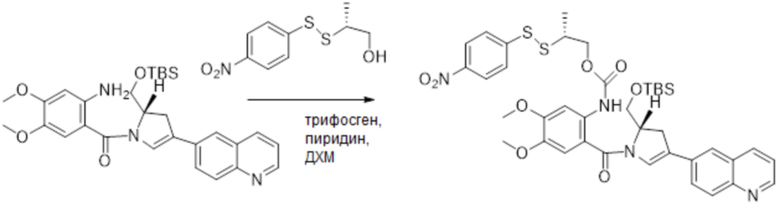
Трифосген (79,4 мг, 0,268 ммоль) растворяли в 1,5 мл дихлорметана, затем добавляли раствор (2R)-2-[(5-нитро-2-пиридил)дисульфанил]пропан-1-ола (196 мг, 0,797 ммоль) и пиридина (0,092 мл) в 2 мл дихлорметана. Через 30 мин вышеуказанный раствор добавляли к раствору исходного анилина и пиридина (0,092 мл) в 4,5 мл дихлорметана. После окончания реакции (около 1 часа) смесь разбавляли EtOAc, затем промывали 1 М раствором HCl и затем насыщенным раствором карбоната натрия. Органические слои сушили над сульфатом натрия и концентрировали. Остаток очищали колоночной хроматографией на силикагеле (30%-70% EtOAc/гептан) с получением целевого карбамата (182 мг).
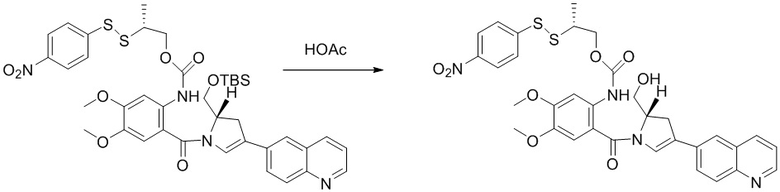
Спирт, защищенный TBS (182 мг, 0,230 ммоль), растворяли в 4 мл:1 мл ТГФ:вода и затем добавляли 4 мл уксусной кислоты. Смесь нагревали до 55°С. После завершения реакции (около двух суток) смесь охлаждали до комнатной температуры и затем разбавляли 50 мл этилацетата. Добавляли карбонат калия для нейтрализации уксусной кислоты до достижения рН около 10. Смесь дважды экстрагировали этилацетатом. Объединенные органические слои сушили сульфатом натрия и концентрировали. Остаток очищали колоночной хроматографией на силикагеле (0-10% MeOH/EtOAc) с получением целевого спирта (125 мг).
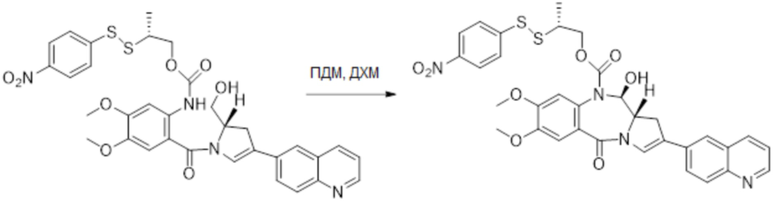
Спиртовое исходное вещество (116 мг, 0,171 ммоль) растворяли в 6 мл дихлорметана, а затем при комнатной температуре добавляли перйодат Десса-Мартина (89,8 мг, 0,205 ммоль). Через около 2,5 часов добавляли насыщенный раствор бикарбоната натрия (около 6 мл) и 1 М раствор тиосульфата натрия (около 4 мл). Смесь экстрагировали дихлорметаном один раз и дважды хлороформом. Объединенные органические слои (около 75 мл) сушили над сульфатом натрия, концентрировали, получая около 103 мг неочищенного продукта, который очищали с помощью обращенно-фазовой ВЭЖХ с получением желаемого продукта (29,5 мг).
1H ЯМР (400 МГц, ДМСО (DMSO)-d6) δ 9,24 (s, 1H), 8,83 (dd, J=1,6, 4,2 Гц, 1H), 8,47 (dd, J=2,6, 8,9 Гц, 1H), 8,32 (d, J=8,0 Гц, 1H), 8,12 (dd, J=1,9, 8,9 Гц, 1H), 7,92 (d, J=8,8 Гц, 1H), 7,87 (d, J=1,8 Гц, 1H), 7,80 (s, 1H), 7,75 (d, J=8,5 Гц, 1H), 7,51 (dd, J=4,2, 8,3 Гц, 1H), 7,20 (s, 1H), 7,07 (s, 1H), 6,95 (d, J=6,3 Гц, 1H), 5,78-5,62 (m, 1H), 4,30 (d, J=6,8 Гц, 1H), 4,00 (td, J=3,2, 10,0 Гц, 1H), 3,85 (s, 6H), 3,56-3,44 (m, 1H), 3,08 (d, J=14,6 Гц, 1H), 1,14 (d, J=6,3 Гц, 3H), 0,07 (s, 12H). МС масса/заряд=676 [M+1]+;
Синтез CLD-6
2-((4-нитрофенил)дисульфанил)этил(11S, 11aS)-11-гидрокси-7,8-диметокси-5-оксо-2-(хинолин-6-ил) -11,11а-дигидро-1Н-бензо[е]пирроло[1,2-а][1,4]диазепин-10 (5H)-карбоксилат
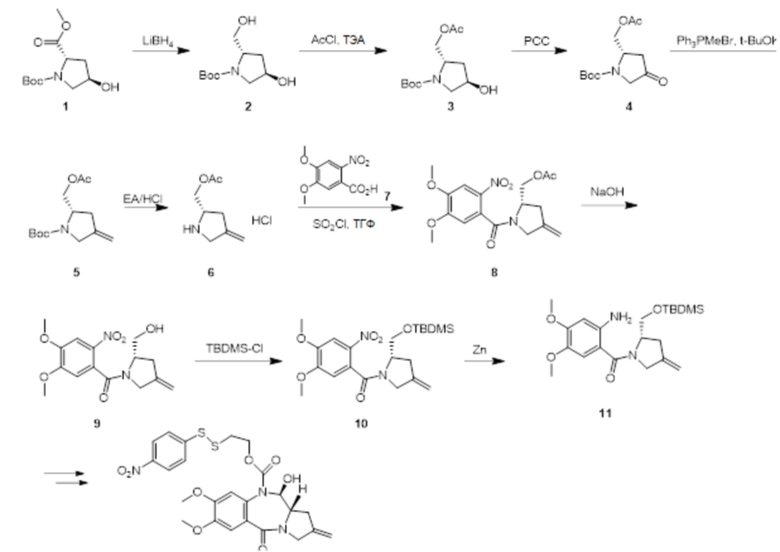
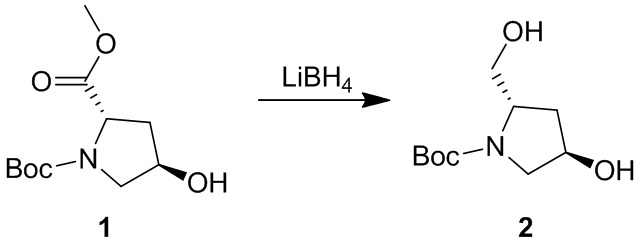
К раствору соединения 1 (1,13 кг, 4,59 моль, 1,00 экв.) в ТГФ (10 л) при 0°C добавляли LiBH4 (99,90 г, 4,59 моль, 1,00 экв.) двумя порциями (почти без температурного заряда при добавлении LiBH4). Суспензию перемешивали при 0°C в течение 1 часа, затем при 10-20°C в течение 18 часов. Смесь охлаждали до 0°С и добавляли водный NH4Cl (5 л). Слои разделяли и водный слой экстрагировали EA (5 л ×3). Объединенные органические слои промывали насыщенным раствором соли. Органические слои сушили над Na2SO4, фильтровали и концентрировали, получая соединение 2 в виде прозрачного масла (1600 г, 7,36 моль, выход 80,2%).
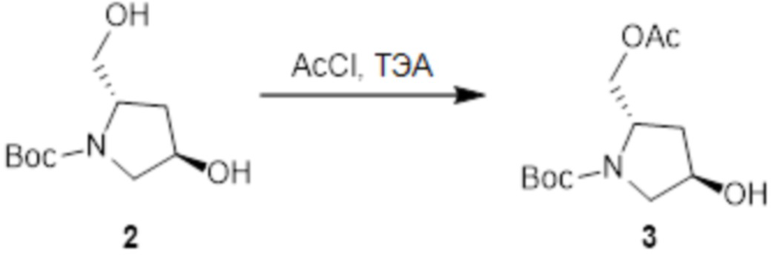
В 50-литровую колбу было загружено соединение 2 (1,60 кг, 7,36 моль, 1,00 экв.), ДХМ (20 л) с последующим добавлением по каплям по очереди TEA (1,12 кг, 11,05 моль, 1,50 экв.) и ацетилхлорида (635,54 г, 8,10 моль, 1,10 экв.) с перемешиванием при 0°C. После добавления полученный раствор перемешивали при 15-25°С в течение 18 часов, гасили добавлением 5 л воды и экстрагировали 3×2 л ДХМ. Объединенные органические слои сушили над безводным сульфатом натрия и концентрировали под вакуумом, получая соединение 3 в виде бесцветного масла (2,46 кг, 9,49 моль, выход 128,90%).
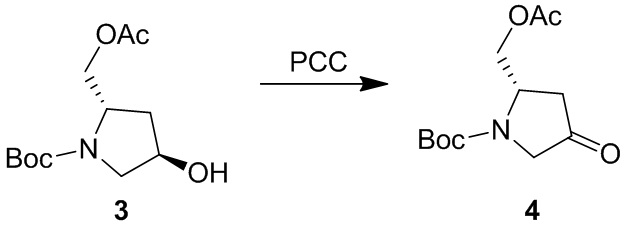
В 20-литровую трехгорлую круглодонную колбу загружали соединение 3 (1,23 кг, 4,75 моль, 1,00 экв.) в ДХМ (12 л) с последующим добавлением PCC (1,54 кг, 7,13 моль) несколькими партиями при 15°C. Полученный раствор перемешивали при 15-25°C в течение 18 часов. Твердые вещества отфильтровывали и фильтрат концентрировали под вакуумом. Остаток очищали на колонке с силикагелем, элюируя смесью этилацетат:петролейный эфир (1:5), получая соединение 4 в виде светло-желтой жидкости (1,13 кг, 4,38 моль, выход 46,15%).
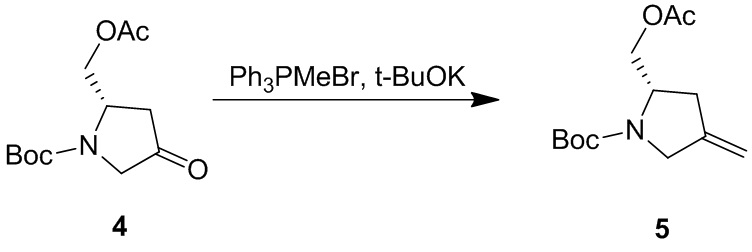
В 10-литровую трехгорлую круглодонную колбу загружали метил(трифенил)фосфонийбромид (958,03 г, 2,68 моль), ТГФ (2,5 л) с последующим добавлением трет-BuOK (300,94 г, 2,68 моль) порциями при 0°C в течение 2 часов. К этому добавляли по каплям раствор 4 (460,00 г, 1,79 моль) в ТГФ (2,5 л) с перемешиванием при 0°C. Полученный раствор перемешивали при -5~0°С в течение 20 мин, гасили добавлением 500 мл воды и экстрагировали 3×500 мл этилацетата. Объединенные органические слои сушили над безводным сульфатом натрия и концентрировали под вакуумом. Остаток очищали на колонке с силикагелем, элюируя смесью этилацетат:петролейный эфир (1:20), получая соединение 5 в виде светло-желтой жидкости (275,00 г, 1,08 моль, 30,09%).

Смесь соединения 5 (330,00 г, 1,29 моль) в HCl (газ)/EtOAc (3 л, 4 М/л) перемешивали при 0°C 20 мин. Затем смесь перемешивали при 10-30°С в течение 1 часа. Смесь концентрировали под вакуумом, получая соединение 6 в виде желтого твердого вещества (250,00 г, 1,30 моль, 101%), которое использовали в следующем этапе без очистки.
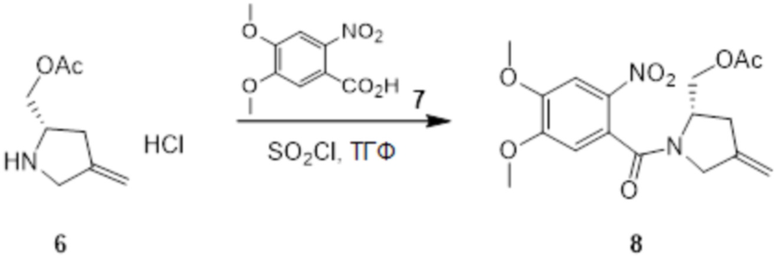
В 3000-мл трехгорлую круглодонную колбу, продутую и поддерживаемую инертной атмосферой азота, загружали раствор соединения 7 (354,42 г, 1,56 моль, 1,30 экв.) в ТГФ (1,5 л) с последующим добавлением SOCl2 (1,71 кг, 14,33 моль, 11,94 экв.) по каплям при перемешивании. Полученный раствор перемешивали при 20-30°C в течение 4 часов и затем концентрировали под вакуумом. В другую трехгорлую круглодонную колбу объемом 3000 мл, продутую и поддерживаемую инертной атмосферой азота, загружали раствор соединения 6 (230,00 г, 1,20 моль, 1,00 экв.) в ДХМ (2,5 л). К этому добавляли по каплям Et3N (485,75 г, 4,80 моль, 4,00 экв.) при перемешивании при -40°С, затем раствор в первой колбе при -40°С. Давали подняться температуре до 0°C естественным образом, гасили добавлением 3000 мл воды/льда и экстрагировали 3×1000 мл дихлорметана. Объединенные органические слои сушили над безводным сульфатом натрия и концентрировали под вакуумом. Остаток очищали на колонке с силикагелем, элюируя EtOAc:PE (1:3), получая соединение 8 в виде светло-коричневого масла (210,00 г), которое использовали на следующей стадии без очистки.
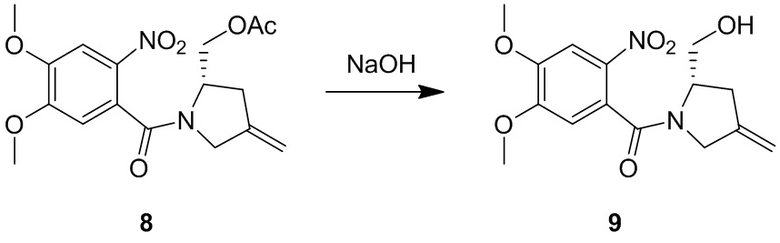
К смеси соединения 8 (90,00 г, 247,02 ммоль, 1,00 экв.) в ТГФ (400 мл), MeOH (100 мл), H2O (400 мл) добавляли NaOH (29,64 г, 741,05 ммоль, 3,00 экв.) в одной порции при 0 oC. Смесь перемешивали при 20-30°C в течение 18 часов. Водную фазу экстрагировали EtOAc (300 мл ×3). Объединенную органическую фазу промывали насыщенным раствором соли (100 мл), сушили безводным Na2SO4, фильтровали и концентрировали под вакуумом, чтобы получить соединение 9 в виде желтого твердого вещества (90,26 г, неочищенное), которое применяли в следующем этапе без дополнительной очистки.
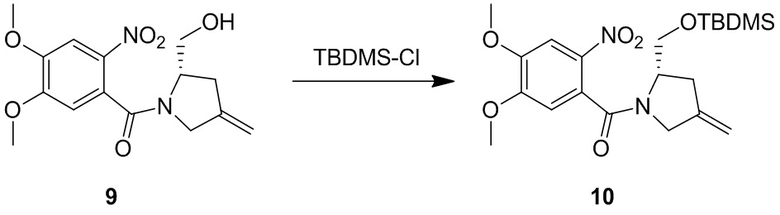
В 2000 мл трехгорлую круглодонную колбу, снабженную температурным зондом, магнитными мешалками и входом для азота, были добавлены TBDMSCl (126,62 г, 840,12 ммоль), имидазол (57,20 г, 840,12 ммоль, 3,00 экв.) в ДМФА (DMF) (1 л). Затем к смеси добавляли раствор соединения 9 (90,26 г, 280,04 ммоль, 1,00 экв.) в ДМФА (DMF) (1 л) при 0°C. Полученную реакционную смесь перемешивали в течение 2 часов при 25-30°C. Реакционную смесь выливали в ледяную воду (1 л) и затем экстрагировали ДХМ (200 мл ×3). Объединенные органические фазы промывали насыщенным раствором соли (100 мл), сушили над Na2SO4 и концентрировали под вакуумом с получением остатка, с получением соединения 10 в виде желтого масла (126,00 г), которое использовали в следующем этапе без дополнительной очистки.
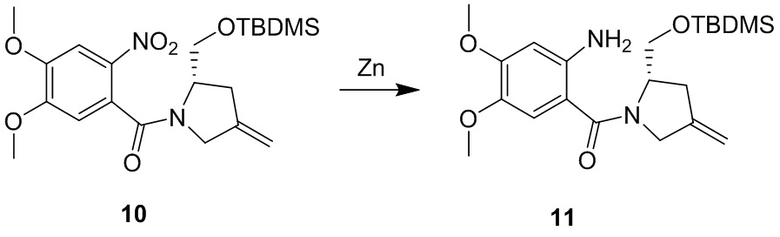
К смеси соединения 10 (126,00 г, 288,61 ммоль, 1,00 экв.) в AcOH (1 л) порциями добавляли Zn (188,72 г, 2,89 моль), поддерживая температуру ниже 30°C. Смесь перемешивали при 20-30°С в течение 30 мин. Остаток выливали в EtOAc (500 мл) и фильтровали. Фильтрат концентрировали под вакуумом. Остаток очищали хроматографией на силикагеле (PE/EtOAc=10/1, 1/1) с получением 11 в виде желтого масла (58,00 г, 142,64 ммоль, выход 49%).
1H ЯМР (400 МГц, хлороформ-d) δ м.д. 6,71 (s, 1 H) 6,22 (s, 1 H) 4,85-4,97 (m, 2 H) 4,52 (br. s., 1 H) 4,14-4,23 (m, 1 H) 3,99-4,13 (m, 1 H) 3,82 (s, 3 H) 3,77 (s, 3 H) 3,59 (d, J=5,73 Гц, 1 H) 2,63-2,72 (m, 2 H) 2,01-2,04 (m, 1 H) 1,23 (t, J=7,06 Гц, 1 H) 0,85 (s, 9 H) -0,06-0,06 (m, 5 H).
2-((4-нитрофенил)дисульфанил)этил(11S, 11aS)-11-гидрокси-7,8-диметокси-5-оксо-2-(хинолин-6-ил) -11,11а-дигидро-1Н-бензо[е]пирроло[1,2-а][1,4]диазепин-10 (5H)-карбоксилат
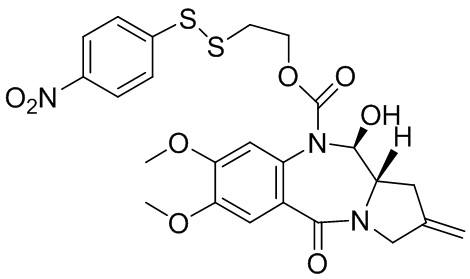
Указанное в заголовке соединение синтезировали следуя стадиям 5-7, как описано выше. 1H ЯМР (400 МГц, ДМСО -d6) δ 9,24 (d, J=2,3 Гц, 1H), 8,66-8,34 (m, 1H), 8,15-7,62 (m, 1H), 7,11 (s, 1H), 6,98 (s, 1H), 6,67 (d, J=5,8 Гц, 1H), 5,37 (dd, J=9,5, 6,3 Гц, 1H), 5,13 (d, J=6,2 Гц, 2H), 4,54-4,31 (m, 1H), 4,12 (d, J=15,6 Гц, 1H), 4,03-3,91 (m, 2H), 3,86-3,78 (m, 6H), 3,76 (d, J=3,4 Гц, 1H), 3,48 (t, J=8,8 Гц, 1H), 3,24-3,00 (m, 2H), 2,96-2,80 (m, 1H). МС масса/заряд=549 [M+1]+.
Хотя вышеприведенное изобретение было описано более подробно с помощью иллюстрации и примера для ясности понимания, описания и примеры не следует рассматривать как ограничивающие объем изобретения. Все патенты, заявки на патенты и ссылки, приведенные в описании, полностью включены посредством ссылки.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> GENENTECH, INC., ET AL.
<120> ПИРРОЛОБЕНЗОДИАЗЕПИНОВЫЕ КОНЪЮГАТЫ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО И
СПОСОБЫ ИХ ПРИМЕНЕНИЯ
<130> P32858-WO
<140>
<141>
<150> 62/236,429
<151> 2015-10-02
<160> 70
<170> PatentIn версия 3.5
<210> 1
<211> 16
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 1
Arg Ser Ser Gln Ser Ile Val His Ser Val Gly Asn Thr Phe Leu Glu
1 5 10 15
<210> 2
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 2
Lys Val Ser Asn Arg Phe Ser
1 5
<210> 3
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 3
Phe Gln Gly Ser Gln Phe Pro Tyr Thr
1 5
<210> 4
<211> 10
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 4
Gly Tyr Glu Phe Ser Arg Ser Trp Met Asn
1 5 10
<210> 5
<211> 18
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 5
Gly Arg Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Ser Gly Lys Phe
1 5 10 15
Lys Gly
<210> 6
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 6
Asp Gly Ser Ser Trp Asp Trp Tyr Phe Asp Val
1 5 10
<210> 7
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
полипептид"
<400> 7
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Ala Ser Gln Gly Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Thr Val Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Asn Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Ser Glu Leu Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 8
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
полипептид"
<400> 8
Glu Val Gln Leu Val Glu Ser Gly Pro Ala Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Gly Tyr
20 25 30
Ser Val Asn Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu Trp Leu
35 40 45
Gly Met Ile Trp Gly Asp Gly Ser Thr Asp Tyr Asn Ser Ala Leu Lys
50 55 60
Ser Arg Leu Thr Ile Ser Lys Asp Thr Ser Lys Asn Gln Val Val Leu
65 70 75 80
Thr Met Thr Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Asp Tyr Tyr Phe Asn Tyr Ala Ser Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 9
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 9
Ser Ala Ser Gln Gly Ile Ser Asn Tyr Leu Asn
1 5 10
<210> 10
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 10
Tyr Thr Ser Asn Leu His Ser
1 5
<210> 11
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 11
Gln Gln Tyr Ser Glu Leu Pro Trp Thr
1 5
<210> 12
<211> 10
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 12
Gly Phe Ser Leu Thr Gly Tyr Ser Val Asn
1 5 10
<210> 13
<211> 16
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 13
Met Ile Trp Gly Asp Gly Ser Thr Asp Tyr Asn Ser Ala Leu Lys Ser
1 5 10 15
<210> 14
<211> 12
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 14
Asp Tyr Tyr Val Asn Tyr Ala Ser Trp Phe Ala Tyr
1 5 10
<210> 15
<211> 214
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
полипептид"
<400> 15
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Ala Ser Gln Gly Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Thr Val Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Asn Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Ser Glu Leu Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Cys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 16
<211> 450
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
полипептид"
<400> 16
Glu Val Gln Leu Val Glu Ser Gly Pro Ala Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Gly Tyr
20 25 30
Ser Val Asn Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu Trp Leu
35 40 45
Gly Met Ile Trp Gly Asp Gly Ser Thr Asp Tyr Asn Ser Ala Leu Lys
50 55 60
Ser Arg Leu Thr Ile Ser Lys Asp Thr Ser Lys Asn Gln Val Val Leu
65 70 75 80
Thr Met Thr Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Asp Tyr Tyr Phe Asn Tyr Ala Ser Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 17
<211> 112
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
полипептид"
<400> 17
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Arg Ala Ser Gln Ser Val Ser Gly Ser
20 25 30
Arg Phe Thr Tyr Met His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Lys Tyr Ala Ser Ile Leu Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln His Ser Trp
85 90 95
Glu Ile Pro Pro Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 18
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
полипептид"
<400> 18
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Met Ile His Pro Leu Asp Ala Glu Ile Arg Ala Asn Gln Lys Phe
50 55 60
Arg Asp Arg Val Thr Ile Thr Val Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Leu Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Thr Tyr Asp Gly Gly Phe Glu Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 19
<211> 15
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 19
Arg Ala Ser Gln Ser Val Ser Gly Ser Arg Phe Thr Tyr Met His
1 5 10 15
<210> 20
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 20
Tyr Ala Ser Ile Leu Glu Ser
1 5
<210> 21
<211> 10
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 21
Gln His Ser Trp Glu Ile Pro Pro Trp Thr
1 5 10
<210> 22
<211> 5
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 22
Gly Tyr Trp Met Asn
1 5
<210> 23
<211> 17
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 23
Met Ile His Pro Leu Asp Ala Glu Ile Arg Ala Asn Gln Lys Phe Arg
1 5 10 15
Asp
<210> 24
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 24
Gly Thr Tyr Asp Gly Gly Phe Glu Tyr
1 5
<210> 25
<211> 219
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
полипептид"
<400> 25
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Arg Ala Ser Gln Ser Val Ser Gly Ser
20 25 30
Arg Phe Thr Tyr Met His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Lys Tyr Ala Ser Ile Leu Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln His Ser Trp
85 90 95
Glu Ile Pro Pro Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 26
<211> 448
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
полипептид"
<400> 26
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Met Ile His Pro Leu Asp Ala Glu Ile Arg Ala Asn Gln Lys Phe
50 55 60
Arg Asp Arg Val Thr Ile Thr Val Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Leu Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Thr Tyr Asp Gly Gly Phe Glu Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
260 265 270
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
405 410 415
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 27
<211> 17
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 27
Met Ile His Pro Met Asp Ser Glu Ile Arg Ala Asn Gln Lys Phe Arg
1 5 10 15
Asp
<210> 28
<211> 17
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 28
Met Ile His Pro Leu Asp Ser Glu Ile Arg Ala Asn Gln Lys Phe Arg
1 5 10 15
Asp
<210> 29
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 29
Gly Thr Tyr Asp Gly Gly Phe Lys Tyr
1 5
<210> 30
<211> 219
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
полипептид"
<400> 30
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Arg Ala Ser Gln Ser Val Ser Gly Ser
20 25 30
Arg Phe Thr Tyr Met His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Lys Tyr Ala Ser Ile Leu Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln His Ser Trp
85 90 95
Glu Ile Pro Pro Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Cys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 31
<211> 448
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
полипептид"
<400> 31
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Met Ile His Pro Leu Asp Ala Glu Ile Arg Ala Asn Gln Lys Phe
50 55 60
Arg Asp Arg Val Thr Ile Thr Val Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Leu Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Thr Tyr Asp Gly Gly Phe Glu Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Cys Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
260 265 270
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
405 410 415
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 32
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 32
Lys Ala Ser Asp Leu Ile His Asn Trp Leu Ala
1 5 10
<210> 33
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 33
Tyr Gly Ala Thr Ser Leu Glu Thr
1 5
<210> 34
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 34
Gln Gln Tyr Trp Thr Thr Pro Phe Thr
1 5
<210> 35
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 35
Gly Tyr Ser Ile Thr Asn Asp Tyr Ala Trp Asn
1 5 10
<210> 36
<211> 17
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 36
Gly Tyr Ile Ser Tyr Ser Gly Tyr Thr Thr Tyr Asn Pro Ser Leu Lys
1 5 10 15
Ser
<210> 37
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 37
Ala Arg Trp Ala Ser Gly Leu Asp Tyr
1 5
<210> 38
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
полипептид"
<400> 38
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Asp Leu Ile His Asn Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Thr Ser Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Trp Thr Thr Pro Phe
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 39
<211> 116
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
полипептид"
<400> 39
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Ser Ile Thr Asn Asp
20 25 30
Tyr Ala Trp Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
35 40 45
Val Gly Tyr Ile Ser Tyr Ser Gly Tyr Thr Thr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Phe Thr Ile Ser Arg Asp Thr Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Trp Ala Ser Gly Leu Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 40
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 40
Gly Tyr Ser Ile Thr Ser Asp Tyr Ala Trp Asn
1 5 10
<210> 41
<211> 17
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 41
Gly Tyr Ile Ser Asn Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
1 5 10 15
Ser
<210> 42
<211> 15
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 42
Glu Arg Asn Tyr Asp Tyr Asp Asp Tyr Tyr Tyr Ala Met Asp Tyr
1 5 10 15
<210> 43
<211> 17
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 43
Lys Ser Ser Gln Ser Leu Leu Tyr Arg Ser Asn Gln Lys Asn Tyr Leu
1 5 10 15
Ala
<210> 44
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 44
Trp Ala Ser Thr Arg Glu Ser
1 5
<210> 45
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 45
Gln Gln Tyr Tyr Asn Tyr Pro Arg Thr
1 5
<210> 46
<211> 124
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
полипептид"
<400> 46
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Tyr Ser Ile Thr Ser Asp
20 25 30
Tyr Ala Trp Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
35 40 45
Val Gly Tyr Ile Ser Asn Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Phe Thr Ile Ser Arg Asp Thr Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Arg Asn Tyr Asp Tyr Asp Asp Tyr Tyr Tyr Ala Met Asp
100 105 110
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 47
<211> 113
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
полипептид"
<400> 47
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ser Ser Gln Ser Leu Leu Tyr Arg
20 25 30
Ser Asn Gln Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys
35 40 45
Ala Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Asn Tyr Pro Arg Thr Phe Gly Gln Gly Thr Lys Val Glu Ile
100 105 110
Lys
<210> 48
<211> 10
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 48
Gly Phe Ser Phe Ser Asp Phe Ala Met Ser
1 5 10
<210> 49
<211> 18
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 49
Ala Thr Ile Gly Arg Val Ala Phe His Thr Tyr Tyr Pro Asp Ser Met
1 5 10 15
Lys Gly
<210> 50
<211> 13
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 50
Ala Arg His Arg Gly Phe Asp Val Gly His Phe Asp Phe
1 5 10
<210> 51
<211> 16
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 51
Arg Ser Ser Glu Thr Leu Val His Ser Ser Gly Asn Thr Tyr Leu Glu
1 5 10 15
<210> 52
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 52
Arg Val Ser Asn Arg Phe Ser
1 5
<210> 53
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 53
Phe Gln Gly Ser Phe Asn Pro Leu Thr
1 5
<210> 54
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
полипептид"
<400> 54
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Asp Phe
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Gly Arg Val Ala Phe His Thr Tyr Tyr Pro Asp Ser Met
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Arg Gly Phe Asp Val Gly His Phe Asp Phe Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 55
<211> 113
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
полипептид"
<400> 55
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ser Ser Glu Thr Leu Val His Ser
20 25 30
Ser Gly Asn Thr Tyr Leu Glu Trp Tyr Gln Gln Lys Pro Gly Lys Ala
35 40 45
Pro Lys Leu Leu Ile Tyr Arg Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Phe Gln Gly
85 90 95
Ser Phe Asn Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg
<210> 56
<211> 117
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
полипептид"
<400> 56
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Ser Ser Tyr
20 25 30
Trp Ile Glu Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Leu Pro Gly Gly Gly Asp Thr Asn Tyr Asn Glu Ile Phe
50 55 60
Lys Gly Arg Ala Thr Phe Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Arg Val Pro Ile Arg Leu Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 57
<211> 112
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
полипептид"
<400> 57
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Val Asp Tyr Glu
20 25 30
Gly Asp Ser Phe Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Asn Leu Glu Ser Gly Val Pro Ser
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asn
85 90 95
Glu Asp Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105 110
<210> 58
<211> 10
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 58
Gly Tyr Thr Phe Ser Ser Tyr Trp Ile Glu
1 5 10
<210> 59
<211> 18
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 59
Gly Glu Ile Leu Pro Gly Gly Gly Asp Thr Asn Tyr Asn Glu Ile Phe
1 5 10 15
Lys Gly
<210> 60
<211> 10
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 60
Thr Arg Arg Val Pro Ile Arg Leu Asp Tyr
1 5 10
<210> 61
<211> 15
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 61
Lys Ala Ser Gln Ser Val Asp Tyr Glu Gly Asp Ser Phe Leu Asn
1 5 10 15
<210> 62
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 62
Ala Ala Ser Asn Leu Glu Ser
1 5
<210> 63
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
пептид"
<400> 63
Gln Gln Ser Asn Glu Asp Pro Leu Thr
1 5
<210> 64
<211> 1255
<212> PRT
<213> Homo sapiens
<400> 64
Met Glu Leu Ala Ala Leu Cys Arg Trp Gly Leu Leu Leu Ala Leu Leu
1 5 10 15
Pro Pro Gly Ala Ala Ser Thr Gln Val Cys Thr Gly Thr Asp Met Lys
20 25 30
Leu Arg Leu Pro Ala Ser Pro Glu Thr His Leu Asp Met Leu Arg His
35 40 45
Leu Tyr Gln Gly Cys Gln Val Val Gln Gly Asn Leu Glu Leu Thr Tyr
50 55 60
Leu Pro Thr Asn Ala Ser Leu Ser Phe Leu Gln Asp Ile Gln Glu Val
65 70 75 80
Gln Gly Tyr Val Leu Ile Ala His Asn Gln Val Arg Gln Val Pro Leu
85 90 95
Gln Arg Leu Arg Ile Val Arg Gly Thr Gln Leu Phe Glu Asp Asn Tyr
100 105 110
Ala Leu Ala Val Leu Asp Asn Gly Asp Pro Leu Asn Asn Thr Thr Pro
115 120 125
Val Thr Gly Ala Ser Pro Gly Gly Leu Arg Glu Leu Gln Leu Arg Ser
130 135 140
Leu Thr Glu Ile Leu Lys Gly Gly Val Leu Ile Gln Arg Asn Pro Gln
145 150 155 160
Leu Cys Tyr Gln Asp Thr Ile Leu Trp Lys Asp Ile Phe His Lys Asn
165 170 175
Asn Gln Leu Ala Leu Thr Leu Ile Asp Thr Asn Arg Ser Arg Ala Cys
180 185 190
His Pro Cys Ser Pro Met Cys Lys Gly Ser Arg Cys Trp Gly Glu Ser
195 200 205
Ser Glu Asp Cys Gln Ser Leu Thr Arg Thr Val Cys Ala Gly Gly Cys
210 215 220
Ala Arg Cys Lys Gly Pro Leu Pro Thr Asp Cys Cys His Glu Gln Cys
225 230 235 240
Ala Ala Gly Cys Thr Gly Pro Lys His Ser Asp Cys Leu Ala Cys Leu
245 250 255
His Phe Asn His Ser Gly Ile Cys Glu Leu His Cys Pro Ala Leu Val
260 265 270
Thr Tyr Asn Thr Asp Thr Phe Glu Ser Met Pro Asn Pro Glu Gly Arg
275 280 285
Tyr Thr Phe Gly Ala Ser Cys Val Thr Ala Cys Pro Tyr Asn Tyr Leu
290 295 300
Ser Thr Asp Val Gly Ser Cys Thr Leu Val Cys Pro Leu His Asn Gln
305 310 315 320
Glu Val Thr Ala Glu Asp Gly Thr Gln Arg Cys Glu Lys Cys Ser Lys
325 330 335
Pro Cys Ala Arg Val Cys Tyr Gly Leu Gly Met Glu His Leu Arg Glu
340 345 350
Val Arg Ala Val Thr Ser Ala Asn Ile Gln Glu Phe Ala Gly Cys Lys
355 360 365
Lys Ile Phe Gly Ser Leu Ala Phe Leu Pro Glu Ser Phe Asp Gly Asp
370 375 380
Pro Ala Ser Asn Thr Ala Pro Leu Gln Pro Glu Gln Leu Gln Val Phe
385 390 395 400
Glu Thr Leu Glu Glu Ile Thr Gly Tyr Leu Tyr Ile Ser Ala Trp Pro
405 410 415
Asp Ser Leu Pro Asp Leu Ser Val Phe Gln Asn Leu Gln Val Ile Arg
420 425 430
Gly Arg Ile Leu His Asn Gly Ala Tyr Ser Leu Thr Leu Gln Gly Leu
435 440 445
Gly Ile Ser Trp Leu Gly Leu Arg Ser Leu Arg Glu Leu Gly Ser Gly
450 455 460
Leu Ala Leu Ile His His Asn Thr His Leu Cys Phe Val His Thr Val
465 470 475 480
Pro Trp Asp Gln Leu Phe Arg Asn Pro His Gln Ala Leu Leu His Thr
485 490 495
Ala Asn Arg Pro Glu Asp Glu Cys Val Gly Glu Gly Leu Ala Cys His
500 505 510
Gln Leu Cys Ala Arg Gly His Cys Trp Gly Pro Gly Pro Thr Gln Cys
515 520 525
Val Asn Cys Ser Gln Phe Leu Arg Gly Gln Glu Cys Val Glu Glu Cys
530 535 540
Arg Val Leu Gln Gly Leu Pro Arg Glu Tyr Val Asn Ala Arg His Cys
545 550 555 560
Leu Pro Cys His Pro Glu Cys Gln Pro Gln Asn Gly Ser Val Thr Cys
565 570 575
Phe Gly Pro Glu Ala Asp Gln Cys Val Ala Cys Ala His Tyr Lys Asp
580 585 590
Pro Pro Phe Cys Val Ala Arg Cys Pro Ser Gly Val Lys Pro Asp Leu
595 600 605
Ser Tyr Met Pro Ile Trp Lys Phe Pro Asp Glu Glu Gly Ala Cys Gln
610 615 620
Pro Cys Pro Ile Asn Cys Thr His Ser Cys Val Asp Leu Asp Asp Lys
625 630 635 640
Gly Cys Pro Ala Glu Gln Arg Ala Ser Pro Leu Thr Ser Ile Ile Ser
645 650 655
Ala Val Val Gly Ile Leu Leu Val Val Val Leu Gly Val Val Phe Gly
660 665 670
Ile Leu Ile Lys Arg Arg Gln Gln Lys Ile Arg Lys Tyr Thr Met Arg
675 680 685
Arg Leu Leu Gln Glu Thr Glu Leu Val Glu Pro Leu Thr Pro Ser Gly
690 695 700
Ala Met Pro Asn Gln Ala Gln Met Arg Ile Leu Lys Glu Thr Glu Leu
705 710 715 720
Arg Lys Val Lys Val Leu Gly Ser Gly Ala Phe Gly Thr Val Tyr Lys
725 730 735
Gly Ile Trp Ile Pro Asp Gly Glu Asn Val Lys Ile Pro Val Ala Ile
740 745 750
Lys Val Leu Arg Glu Asn Thr Ser Pro Lys Ala Asn Lys Glu Ile Leu
755 760 765
Asp Glu Ala Tyr Val Met Ala Gly Val Gly Ser Pro Tyr Val Ser Arg
770 775 780
Leu Leu Gly Ile Cys Leu Thr Ser Thr Val Gln Leu Val Thr Gln Leu
785 790 795 800
Met Pro Tyr Gly Cys Leu Leu Asp His Val Arg Glu Asn Arg Gly Arg
805 810 815
Leu Gly Ser Gln Asp Leu Leu Asn Trp Cys Met Gln Ile Ala Lys Gly
820 825 830
Met Ser Tyr Leu Glu Asp Val Arg Leu Val His Arg Asp Leu Ala Ala
835 840 845
Arg Asn Val Leu Val Lys Ser Pro Asn His Val Lys Ile Thr Asp Phe
850 855 860
Gly Leu Ala Arg Leu Leu Asp Ile Asp Glu Thr Glu Tyr His Ala Asp
865 870 875 880
Gly Gly Lys Val Pro Ile Lys Trp Met Ala Leu Glu Ser Ile Leu Arg
885 890 895
Arg Arg Phe Thr His Gln Ser Asp Val Trp Ser Tyr Gly Val Thr Val
900 905 910
Trp Glu Leu Met Thr Phe Gly Ala Lys Pro Tyr Asp Gly Ile Pro Ala
915 920 925
Arg Glu Ile Pro Asp Leu Leu Glu Lys Gly Glu Arg Leu Pro Gln Pro
930 935 940
Pro Ile Cys Thr Ile Asp Val Tyr Met Ile Met Val Lys Cys Trp Met
945 950 955 960
Ile Asp Ser Glu Cys Arg Pro Arg Phe Arg Glu Leu Val Ser Glu Phe
965 970 975
Ser Arg Met Ala Arg Asp Pro Gln Arg Phe Val Val Ile Gln Asn Glu
980 985 990
Asp Leu Gly Pro Ala Ser Pro Leu Asp Ser Thr Phe Tyr Arg Ser Leu
995 1000 1005
Leu Glu Asp Asp Asp Met Gly Asp Leu Val Asp Ala Glu Glu Tyr
1010 1015 1020
Leu Val Pro Gln Gln Gly Phe Phe Cys Pro Asp Pro Ala Pro Gly
1025 1030 1035
Ala Gly Gly Met Val His His Arg His Arg Ser Ser Ser Thr Arg
1040 1045 1050
Ser Gly Gly Gly Asp Leu Thr Leu Gly Leu Glu Pro Ser Glu Glu
1055 1060 1065
Glu Ala Pro Arg Ser Pro Leu Ala Pro Ser Glu Gly Ala Gly Ser
1070 1075 1080
Asp Val Phe Asp Gly Asp Leu Gly Met Gly Ala Ala Lys Gly Leu
1085 1090 1095
Gln Ser Leu Pro Thr His Asp Pro Ser Pro Leu Gln Arg Tyr Ser
1100 1105 1110
Glu Asp Pro Thr Val Pro Leu Pro Ser Glu Thr Asp Gly Tyr Val
1115 1120 1125
Ala Pro Leu Thr Cys Ser Pro Gln Pro Glu Tyr Val Asn Gln Pro
1130 1135 1140
Asp Val Arg Pro Gln Pro Pro Ser Pro Arg Glu Gly Pro Leu Pro
1145 1150 1155
Ala Ala Arg Pro Ala Gly Ala Thr Leu Glu Arg Pro Lys Thr Leu
1160 1165 1170
Ser Pro Gly Lys Asn Gly Val Val Lys Asp Val Phe Ala Phe Gly
1175 1180 1185
Gly Ala Val Glu Asn Pro Glu Tyr Leu Thr Pro Gln Gly Gly Ala
1190 1195 1200
Ala Pro Gln Pro His Pro Pro Pro Ala Phe Ser Pro Ala Phe Asp
1205 1210 1215
Asn Leu Tyr Tyr Trp Asp Gln Asp Pro Pro Glu Arg Gly Ala Pro
1220 1225 1230
Pro Ser Thr Phe Lys Gly Thr Pro Thr Ala Glu Asn Pro Glu Tyr
1235 1240 1245
Leu Gly Leu Asp Val Pro Val
1250 1255
<210> 65
<211> 14
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
олигонуклеотид"
<400> 65
tatagaaatc tata 14
<210> 66
<211> 14
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
олигонуклеотид"
<400> 66
tatagatttc tata 14
<210> 67
<211> 14
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
олигонуклеотид"
<400> 67
tatagaaatg tata 14
<210> 68
<211> 14
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетический
олигонуклеотид"
<400> 68
tatacatttc tata 14
<210> 69
<211> 7
<212> PRT
<213> Homo sapiens
<400> 69
Met Ala Glu Ala Ile Thr Tyr
1 5
<210> 70
<211> 7
<212> PRT
<213> Homo sapiens
<400> 70
Thr Ala Phe Arg Phe Pro Asp
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| КОНЪЮГАТ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО, ПРОМЕЖУТОЧНОЕ СОЕДИНЕНИЕ ДЛЯ ЕГО ПОЛУЧЕНИЯ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2800137C1 |
| САЙТ-СПЕЦИФИЧЕСКИЕ КОНЪЮГАТЫ АНТИТЕЛА К HER2 И ЛЕКАРСТВЕННОГО СРЕДСТВА | 2016 |
|
RU2745565C2 |
| АНТИТЕЛА ПРОТИВ CD79b, КОНЪЮГАТЫ С ЛЕКАРСТВЕННЫМ СРЕДСТВОМ И ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2805251C2 |
| КОНЪЮГАТЫ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ОСНОВЕ ЭРИБУЛИНА И СПОСОБЫ ПРИМЕНЕНИЯ | 2017 |
|
RU2754369C2 |
| АМАТОКСИНОВЫЕ КОНЪЮГАТЫ АНТИТЕЛА С ЛЕКАРСТВЕННЫМ СРЕДСТВОМ И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2826004C2 |
| АНТИТЕЛА И ФРАГМЕНТЫ АНТИТЕЛ ДЛЯ САЙТ-СПЕЦИФИЧЕСКОГО КОНЪЮГИРОВАНИЯ | 2016 |
|
RU2757815C2 |
| КОНЪЮГАТЫ СВЯЗУЮЩЕГО И АКТИВНОГО ВЕЩЕСТВА (ADC), ИМЕЮЩИЕ ФЕРМЕНТАТИВНО РАСЩЕПЛЯЕМЫЕ ГРУППЫ | 2017 |
|
RU2761390C2 |
| КОНЪЮГАТЫ АНТИТЕЛА И ЛЕКАРСТВЕННОГО СРЕДСТВА, СОДЕРЖАЩИЕ МОДУЛЯТОР СПЛАЙСИНГА НА ОСНОВЕ ГЕРБОКСИДИЕНА, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2820607C2 |
| БИСПЕЦИФИЧНЫЕ АНТИГЕНСВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2800779C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОНЪЮГАТА АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ОСНОВЕ ЭРИБУЛИНА | 2020 |
|
RU2840013C1 |
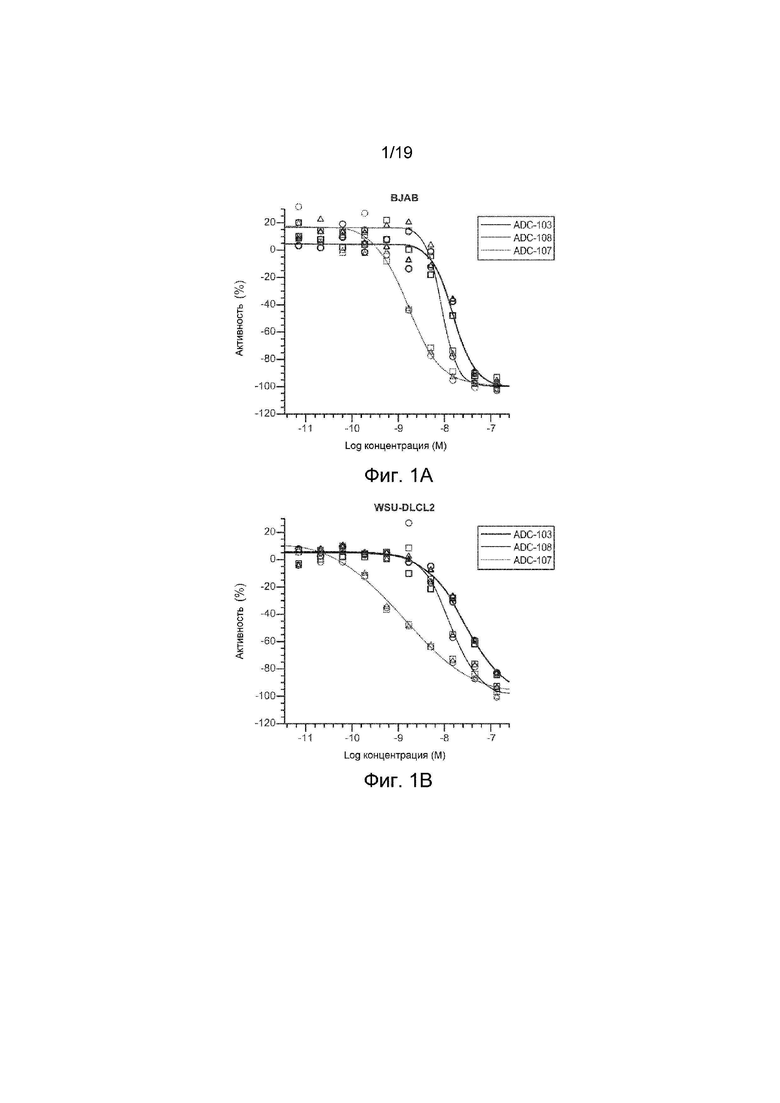
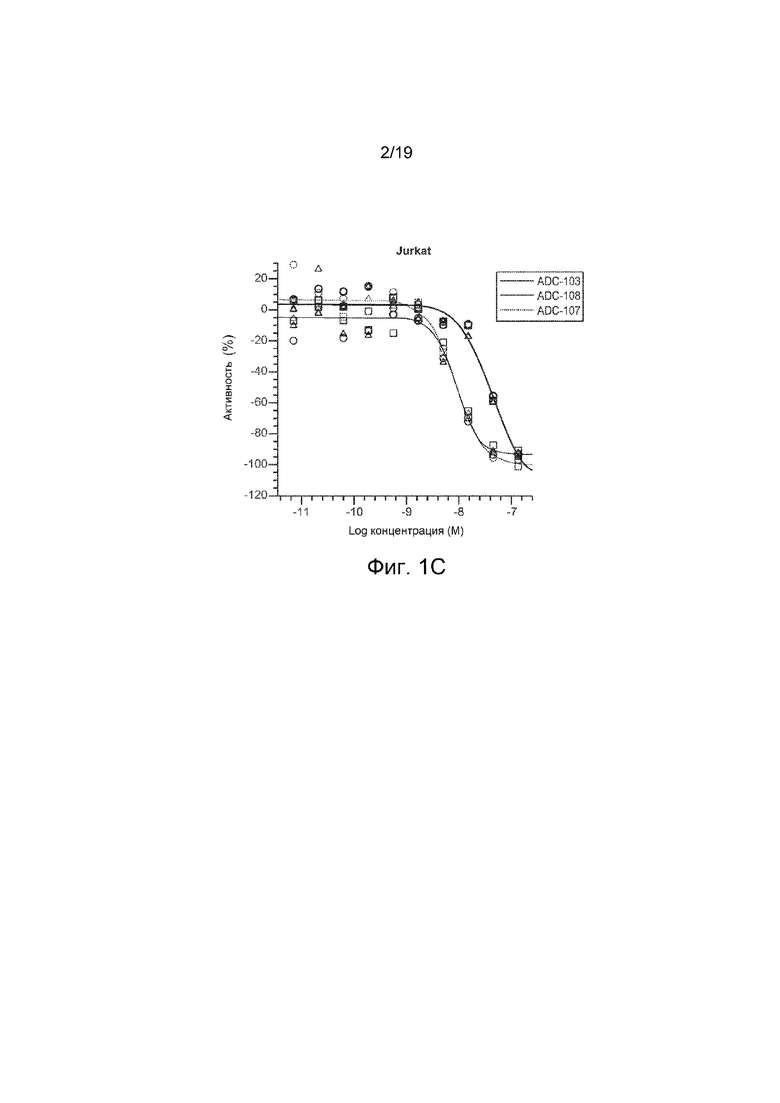
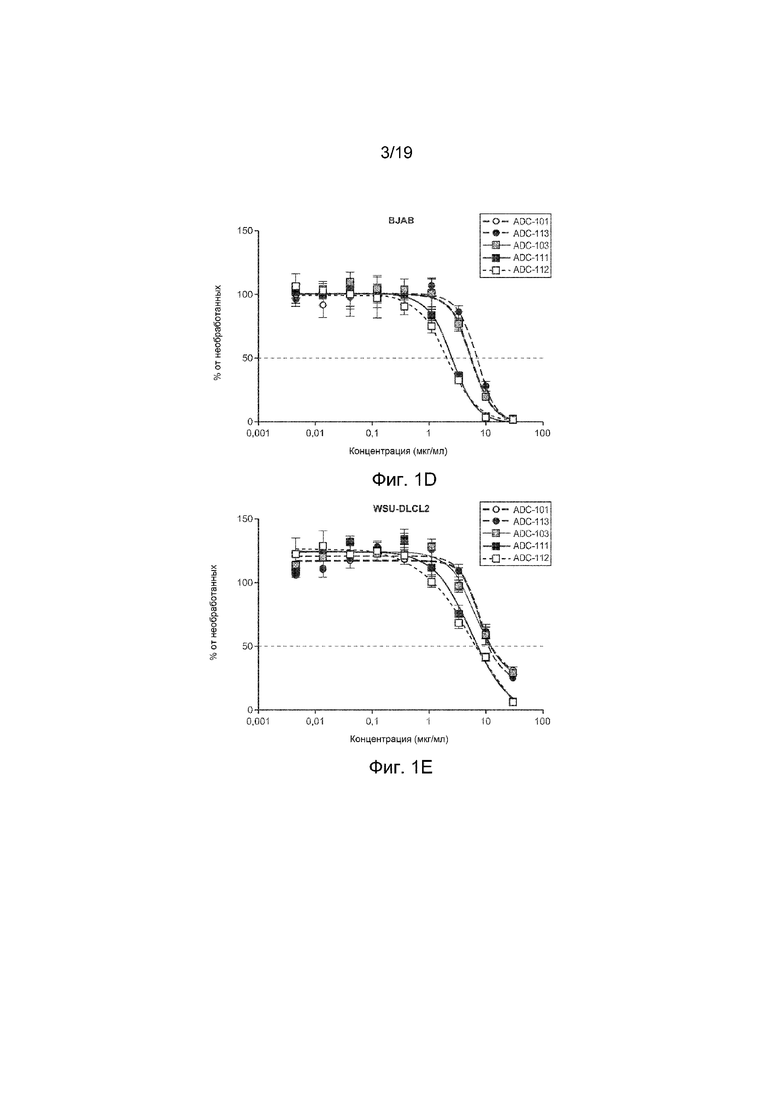
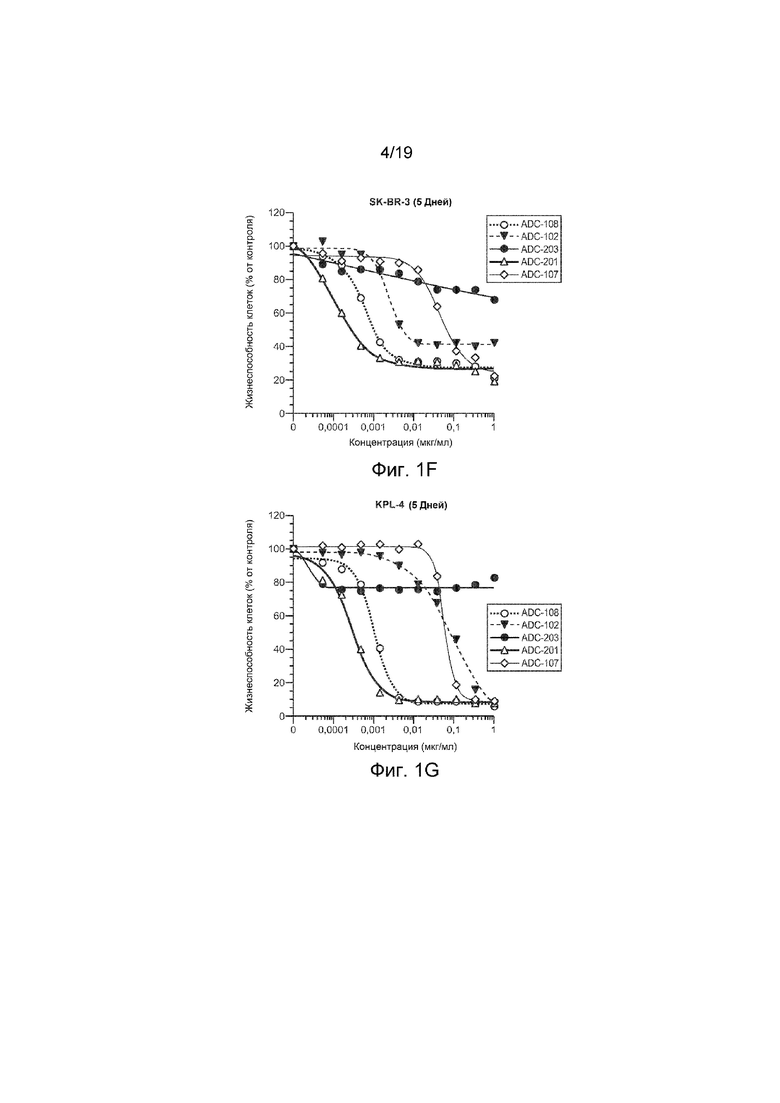
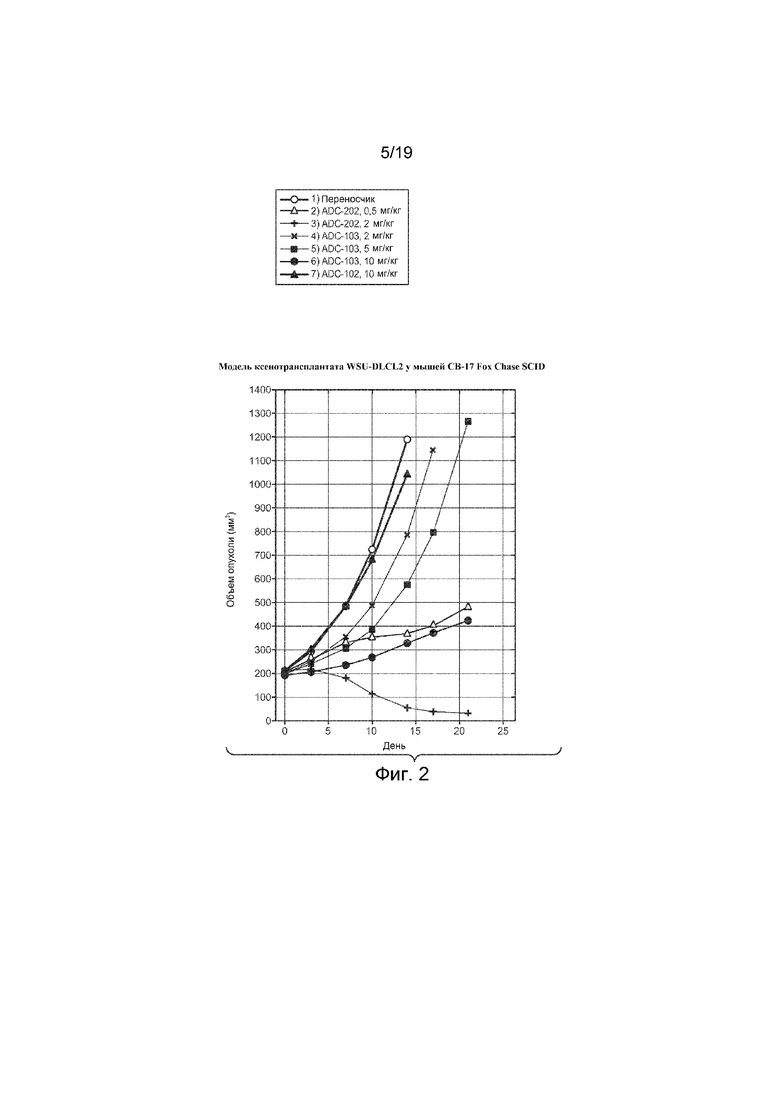
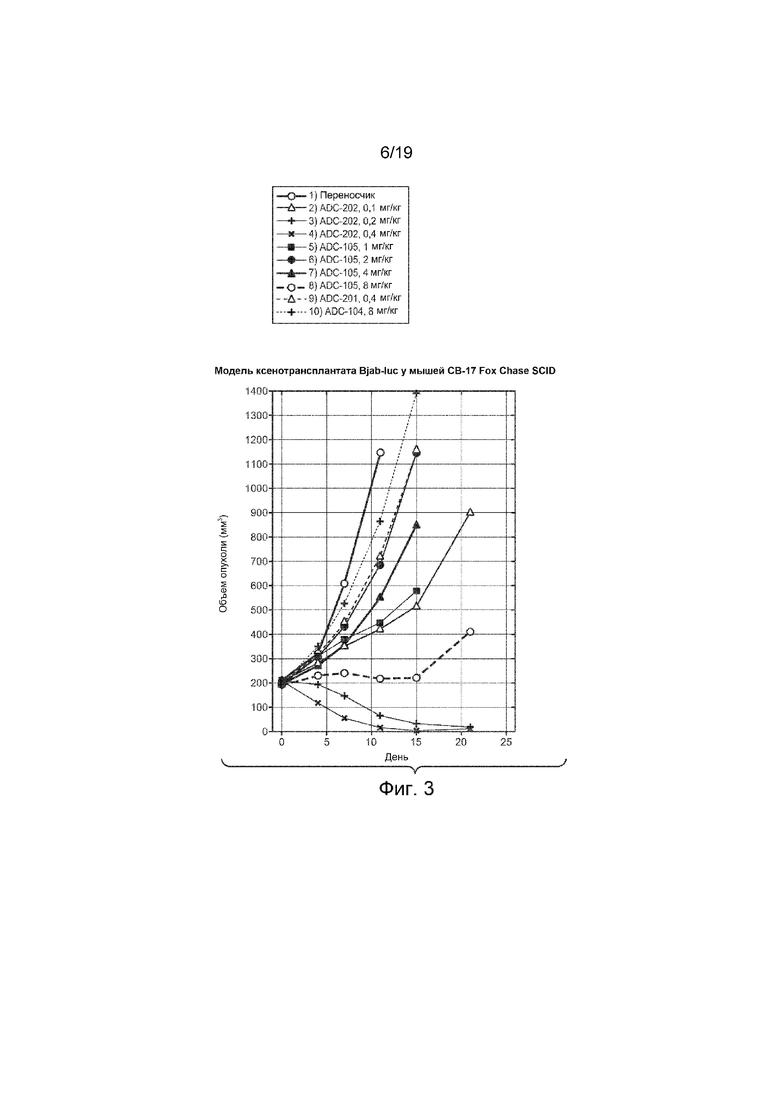

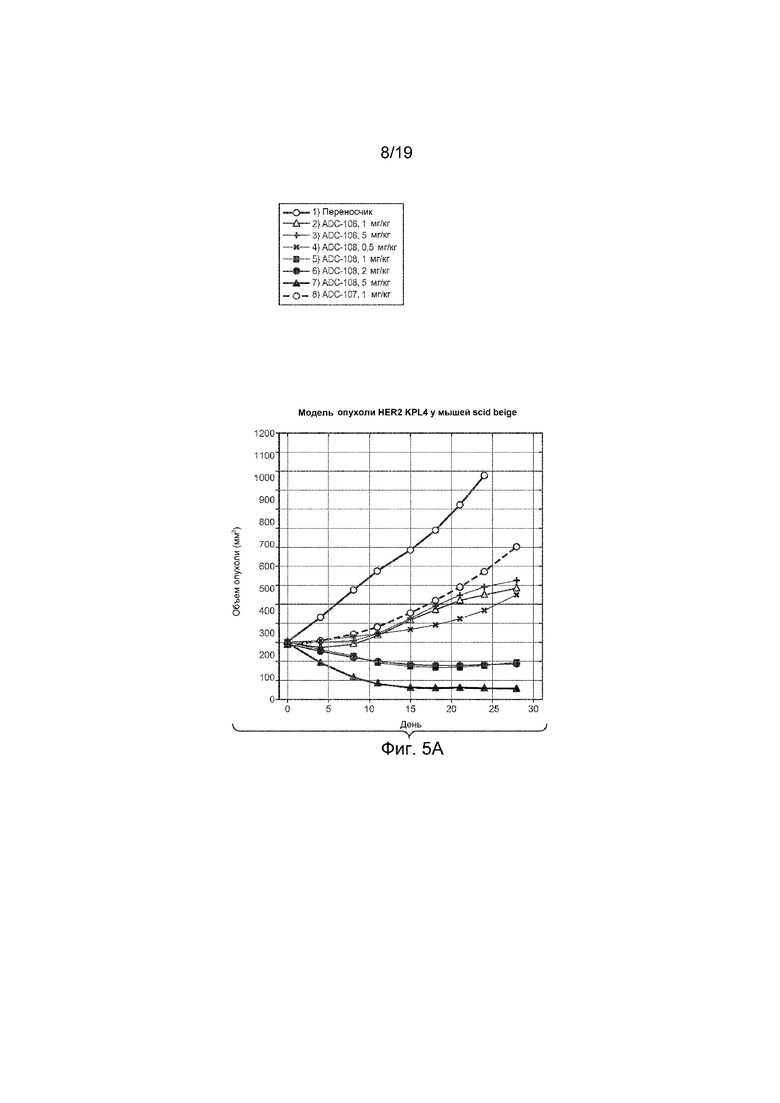
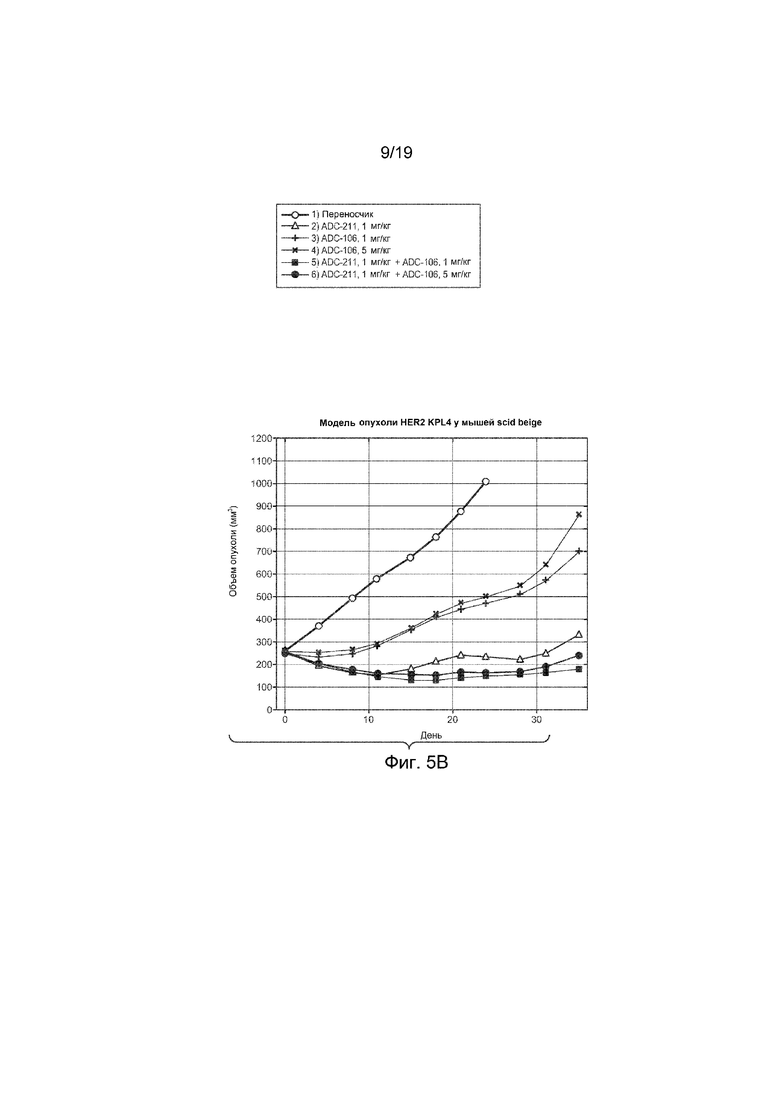
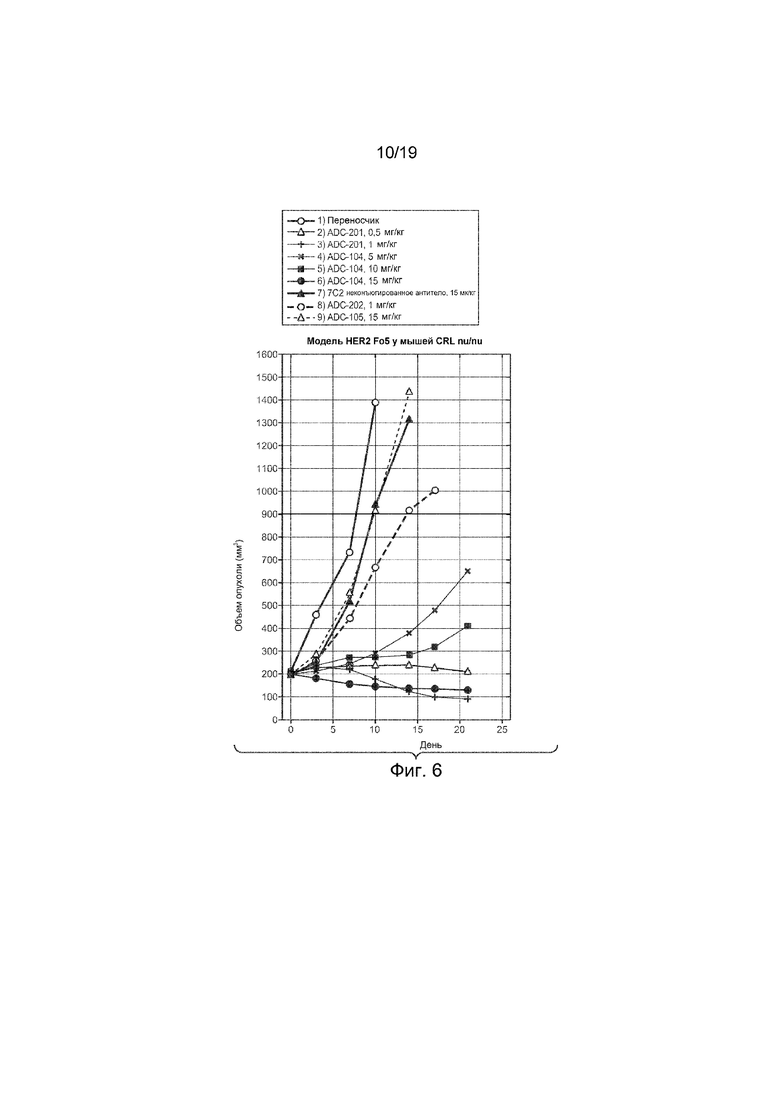
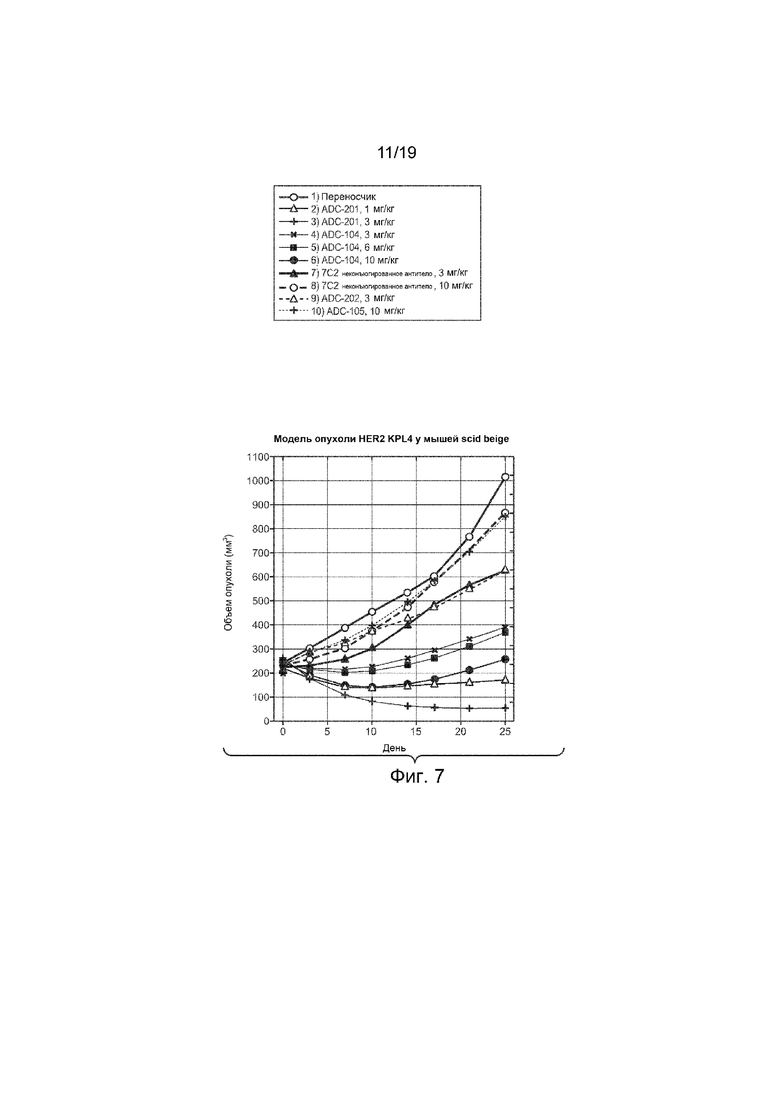
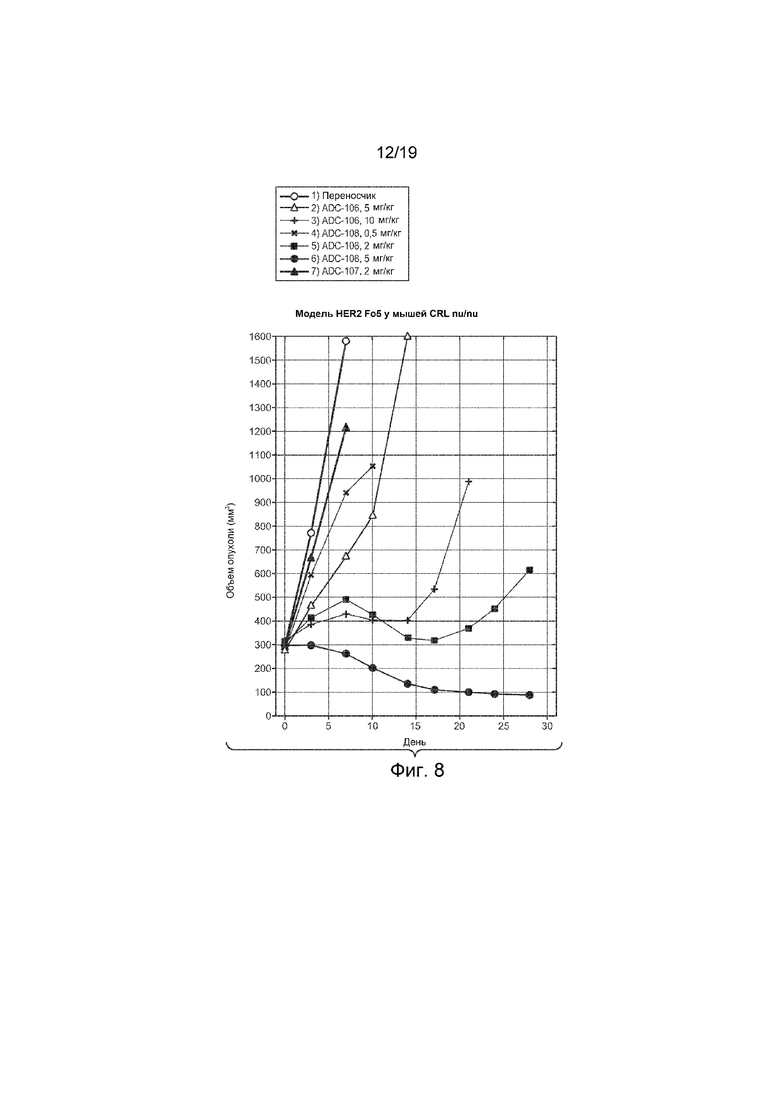
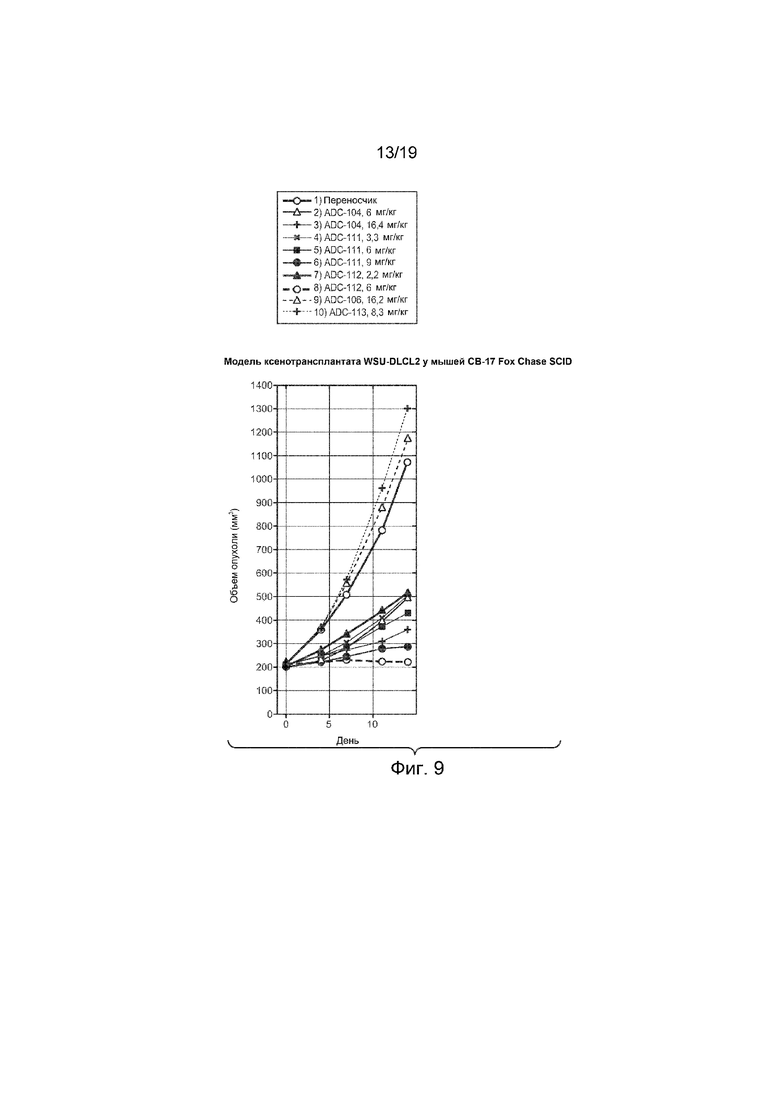
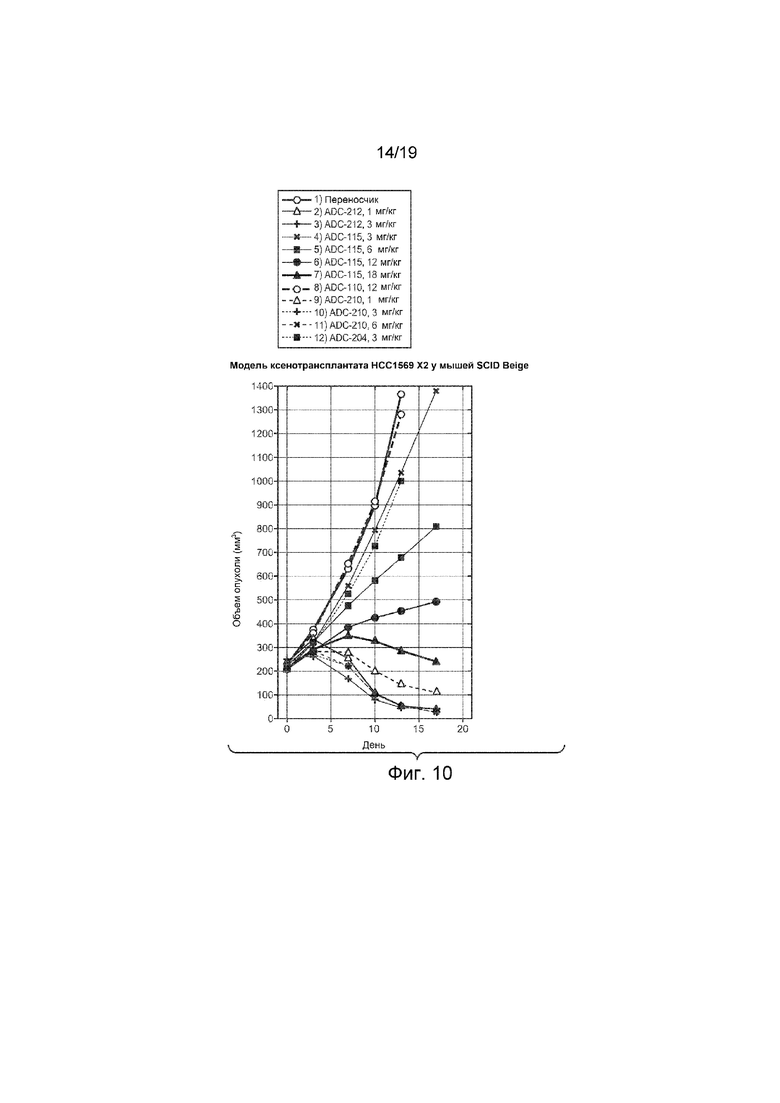
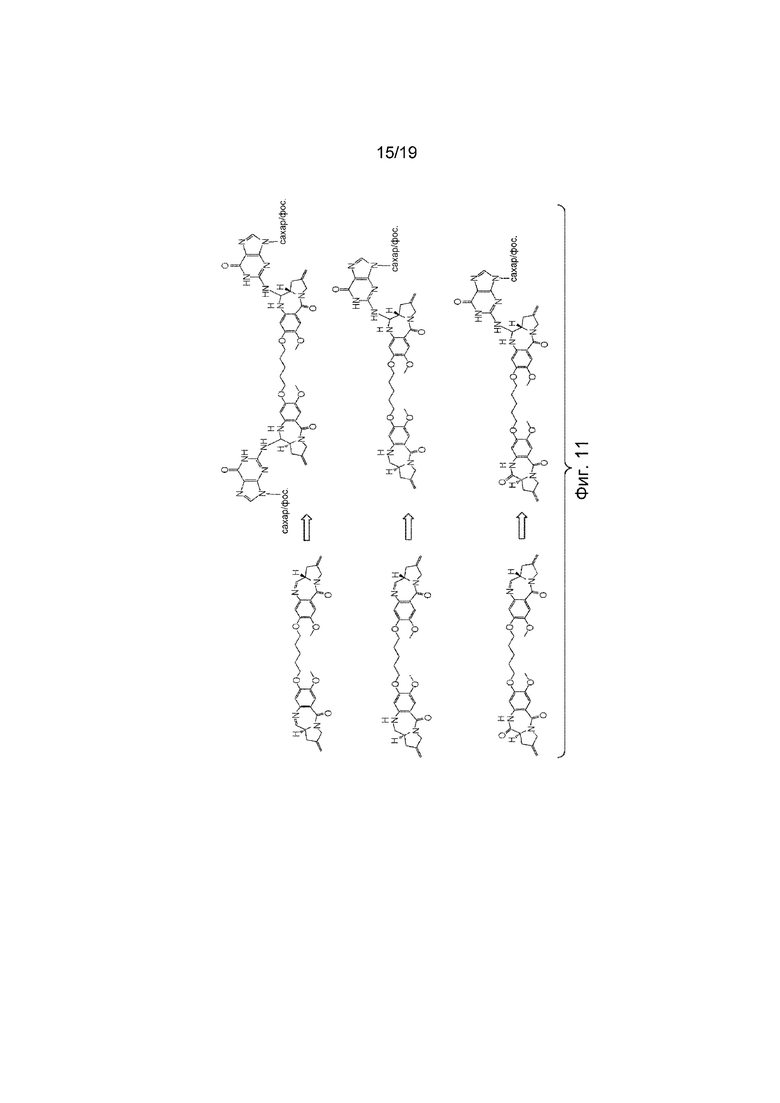
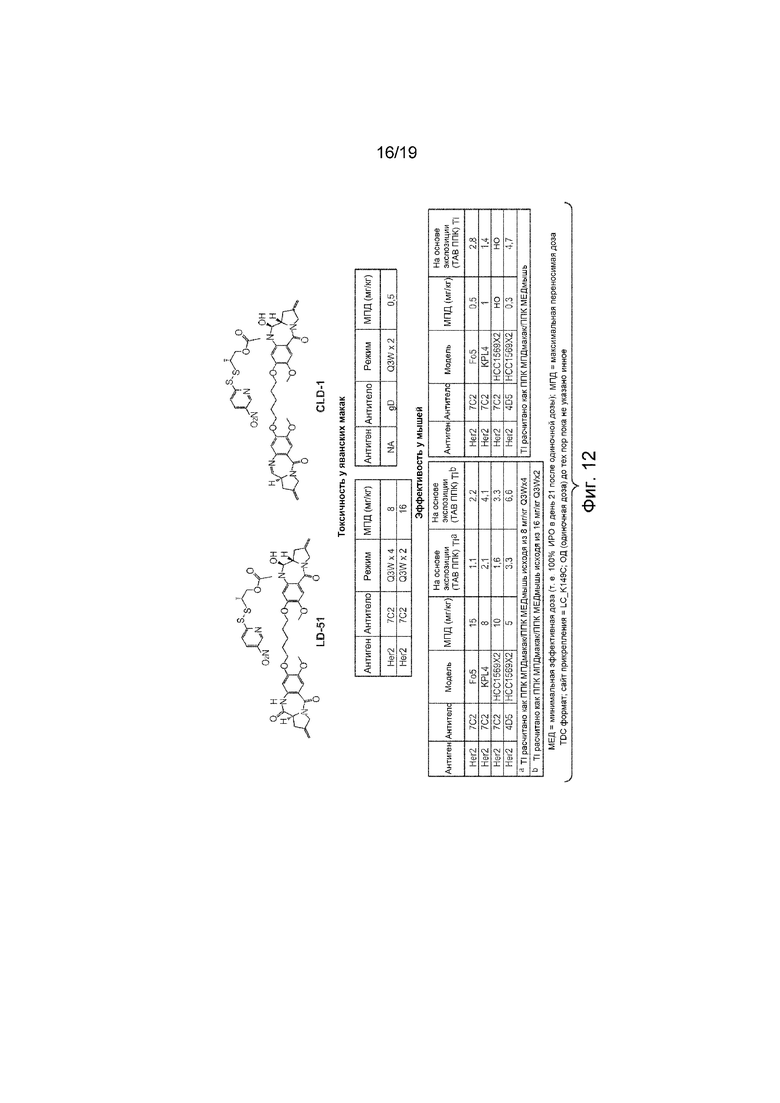
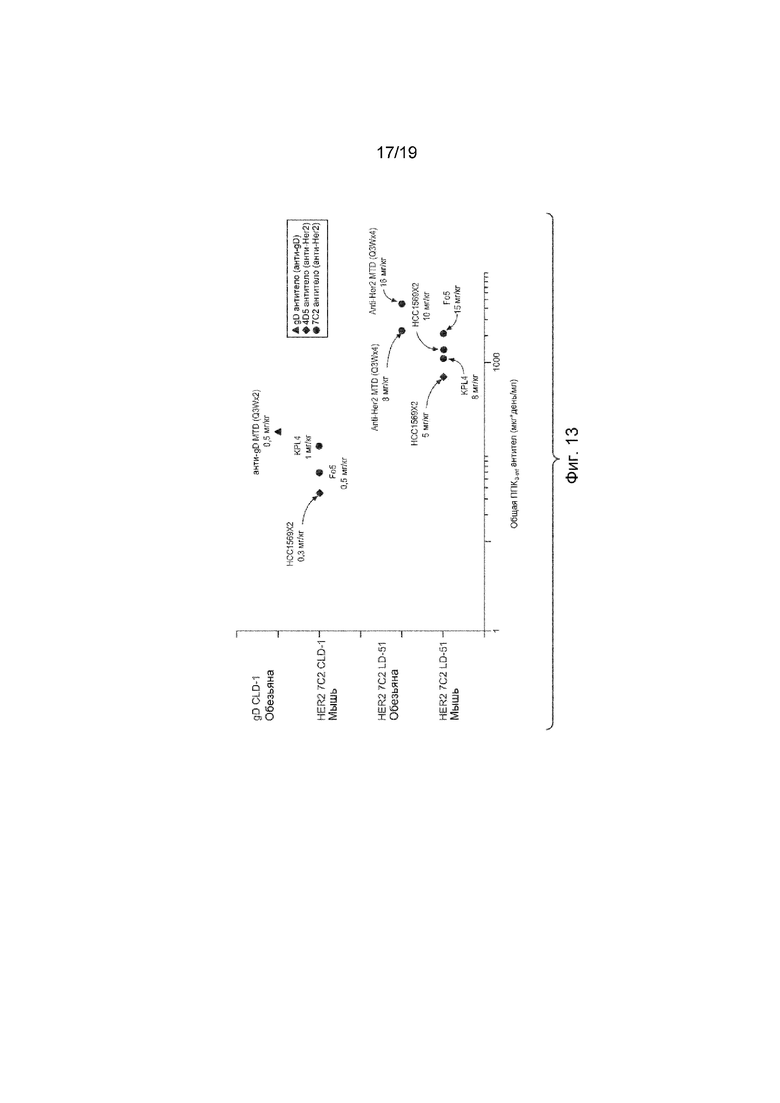
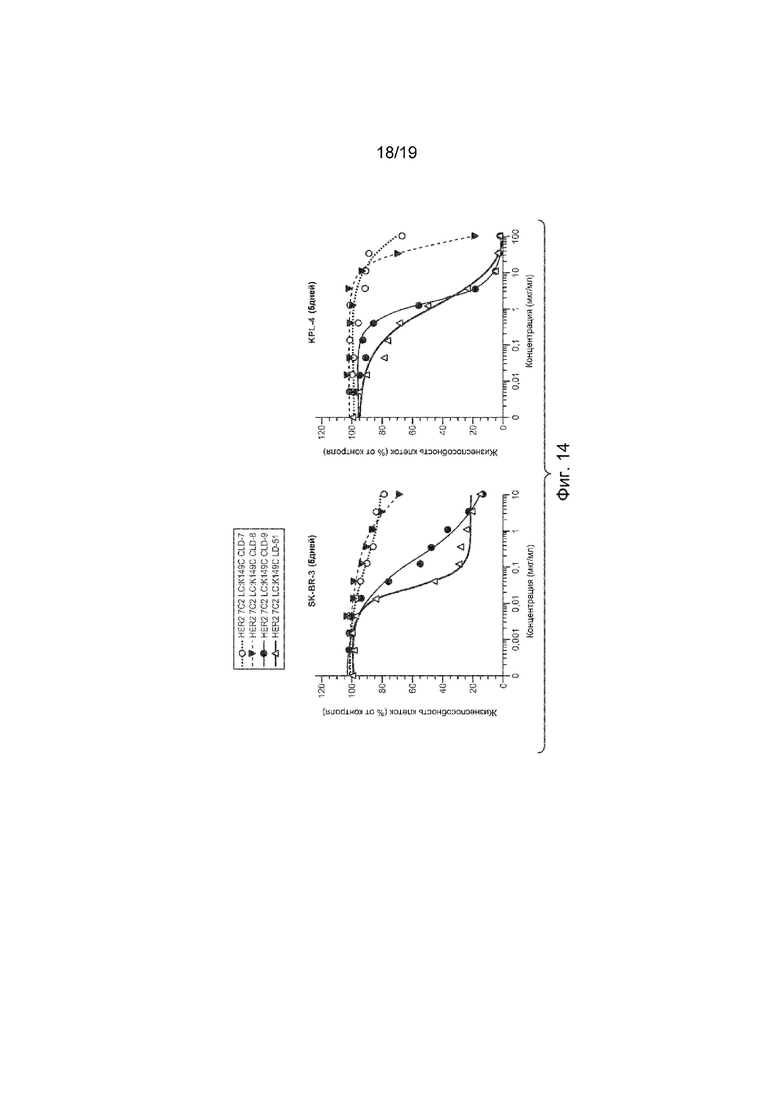

В изобретении предложены конъюгаты антитело-лекарственное средство, содеражащие антитело, конъюгированное с лекарственным пирролобензодиазепиновым компонентом через дисульфидный линкер,
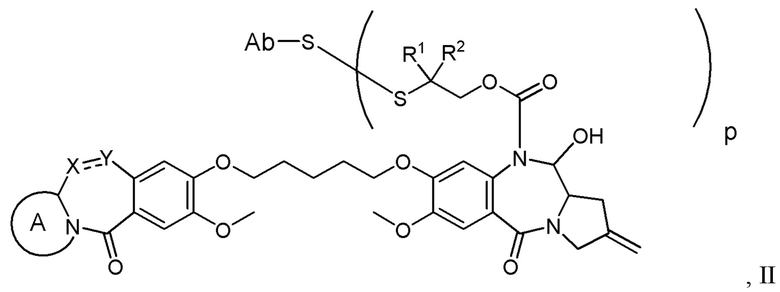
где X Y представляет собой C(=O)-NH или CH2-NH; A представляет собой пиррол, необязательно замещенный группой =C(R)2, в которой R независимо выбран из H и C1-C6-алкила; R1 и R2 независимо выбраны из H или C1-C6-алкила или R1 и R2 образуют циклопропил; p равно целому числу от 1 до 8; и Ab представляет собой антитело, которое выбрано из группы, состоящей из анти-HER2, анти-CD22, анти-CD33, анти-Napi2b и анти-CLL-1, а также пирролобензодиазепиновые промежуточные соединения линкера, фармацевтические композиции и способы применения конъюгатов антитело-лекарственное средство для лечения гиперпролиферативных заболеваний. 11 н. и 45 з.п. ф-лы, 15 ил., 9 табл., 15 пр.
Y представляет собой C(=O)-NH или CH2-NH; A представляет собой пиррол, необязательно замещенный группой =C(R)2, в которой R независимо выбран из H и C1-C6-алкила; R1 и R2 независимо выбраны из H или C1-C6-алкила или R1 и R2 образуют циклопропил; p равно целому числу от 1 до 8; и Ab представляет собой антитело, которое выбрано из группы, состоящей из анти-HER2, анти-CD22, анти-CD33, анти-Napi2b и анти-CLL-1, а также пирролобензодиазепиновые промежуточные соединения линкера, фармацевтические композиции и способы применения конъюгатов антитело-лекарственное средство для лечения гиперпролиферативных заболеваний. 11 н. и 45 з.п. ф-лы, 15 ил., 9 табл., 15 пр.
1. Промежуточное соединение линкер-лекарственное средство Формулы I
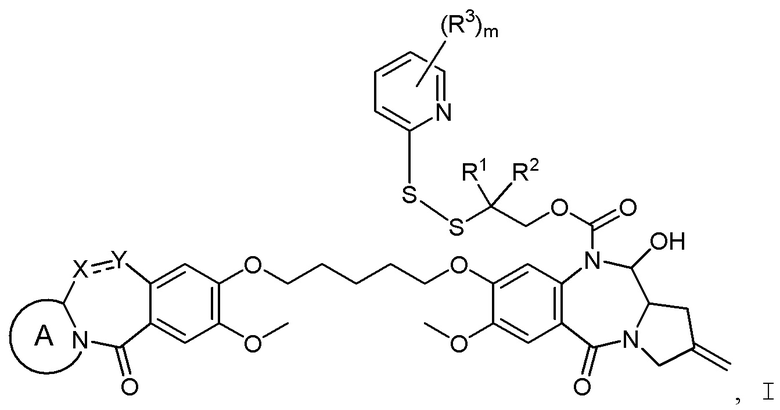
где X Y представляет собой C(=O)-NH или CH2-NH;
Y представляет собой C(=O)-NH или CH2-NH;
A представляет собой пиррол, необязательно замещенный группой =C(R)2, в которой R независимо выбран из H и C1-C6-алкила;
R1 и R2 независимо выбраны из H или C1-C6-алкила или R1 и R2 образуют циклопропил;
R3 представляет собой NO2; и
m равно 1 или 2.
2. Промежуточное соединение линкер-лекарственное средство по п.1 Формулы Ia
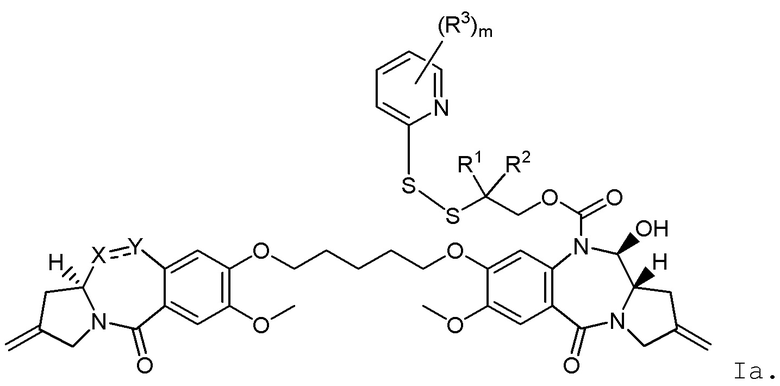
3. Промежуточное соединение линкер-лекарственное средство по п.1 Формулы Ic
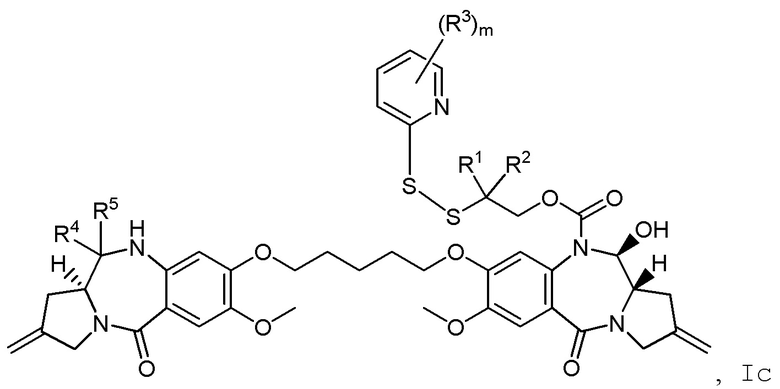
где каждый R4 и R5 представляет собой H или R4 и R5 представляют собой =O.
4. Промежуточное соединение линкер-лекарственное средство по п.1 Формулы Id
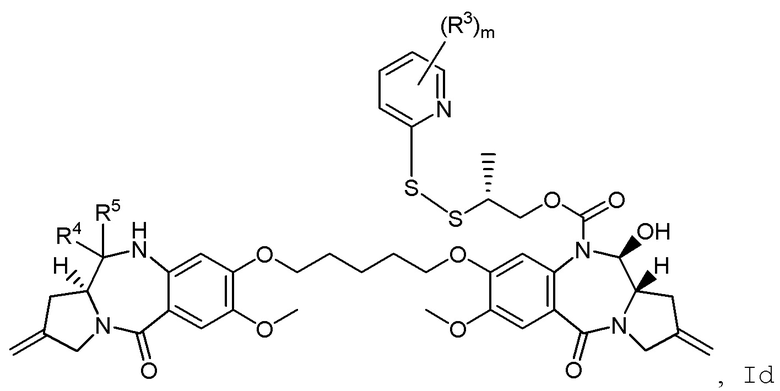
где каждый R4 и R5 представляет собой H или R4 и R5 представляют собой =O.
5. Промежуточное соединение линкер-лекарственное средство по п.4, где каждый R4 и R5 представляет собой H.
6. Промежуточное соединение линкер-лекарственное средство по п.1 Формулы Ie
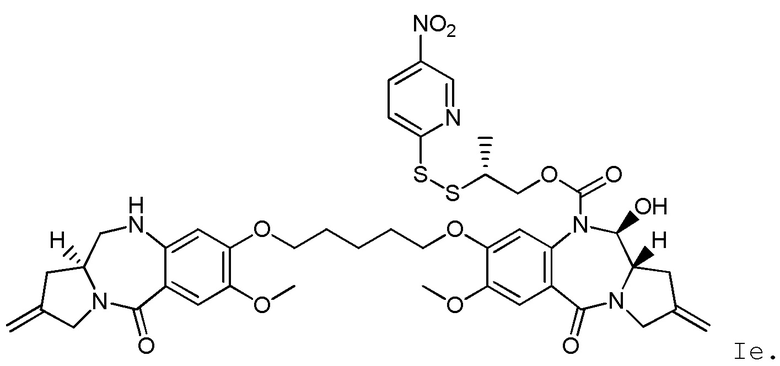
7. Промежуточное соединение линкер-лекарственное средство по п.3, где R4 и R5 представляют собой =O.
8. Промежуточное соединение линкер-лекарственное средство по п.1 Формулы If
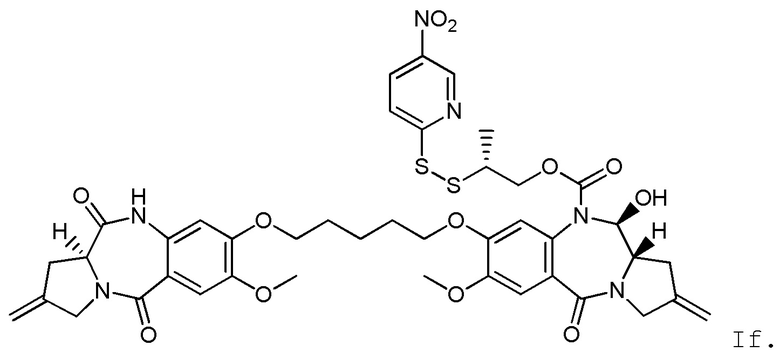
9. Промежуточное соединение линкер-лекарственное средство по п.1, где R1 и R2 вместе с атомом углерода, к которому они присоединены, образуют циклопропильное или циклобутильное кольцо.
10. Соединение конъюгата антитело-лекарственное средство Формулы II
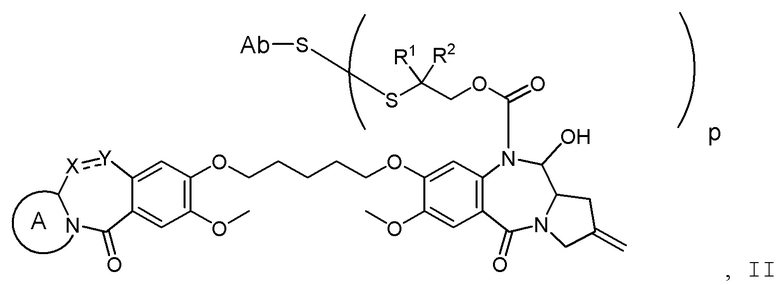
где X Y представляет собой C(=O)-NH или CH2-NH;
Y представляет собой C(=O)-NH или CH2-NH;
A представляет собой пиррол, необязательно замещенный группой =C(R)2, в которой R независимо выбран из H и C1-C6-алкила;
R1 и R2 независимо выбраны из H или C1-C6-алкила или R1 и R2 образуют циклопропил;
p равно целому числу от 1 до 8; и
Ab представляет собой антитело, которое выбрано из группы, состоящей из анти-HER2, анти-CD22, анти-CD33, анти-Napi2b и анти-CLL-1.
11. Соединение конъюгата антитело-лекарственное средство по п.10 Формулы IIa
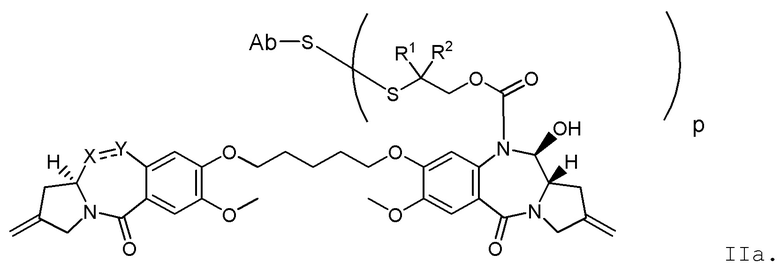
12. Соединение конъюгата антитело-лекарственное средство по п.10 Формулы IIc
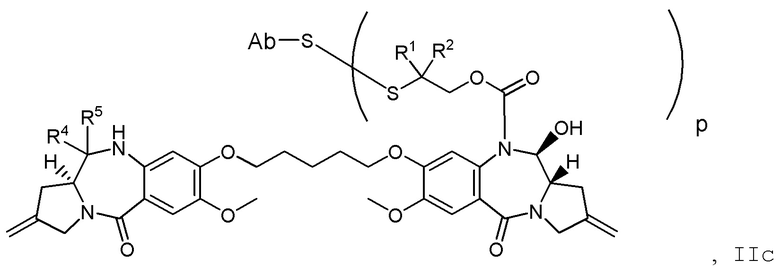
где каждый R4 и R5 представляет собой H или R4 и R5 представляют собой =O.
13. Соединение конъюгата антитело-лекарственное средство по п.12, где каждый R4 и R5 представляет собой H.
14. Соединение конъюгата антитело-лекарственное средство по п.12, где каждый R4 и R5 представляет собой =О.
15. Соединение конъюгата антитело-лекарственное средство по п.12 Формулы IId
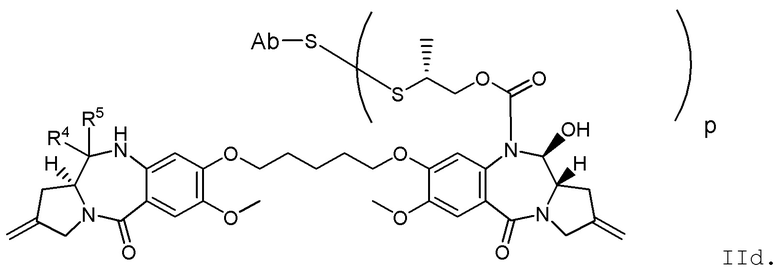
16. Соединение конъюгата антитело-лекарственное средство по п.12 Формулы IIe
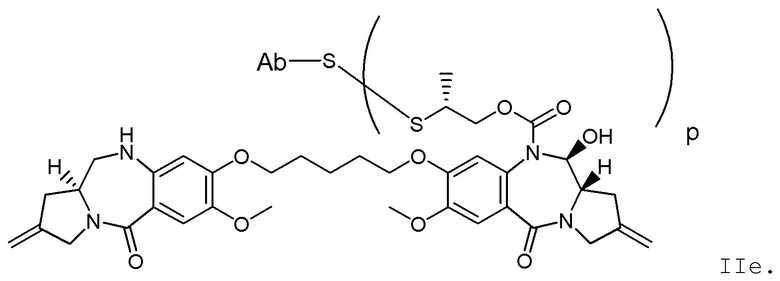
17. Соединение конъюгата антитело-лекарственное средство по п.12 Формулы IIf
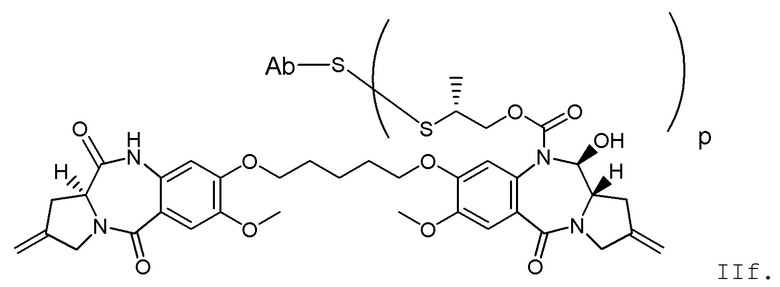
18. Соединение конъюгата антитело-лекарственное средство по п.10, в котором Ab представляет собой модифицированное цистеином антитело.
19. Соединение конъюгата антитело-лекарственное средство по п.18, в котором модифицированное цистеином антитело содержит K149C LC или A118C HC в качестве сайта конъюгации лекарственного средства.
20. Соединение конъюгата антитело-лекарственное средство по п.10, где p равно 1, 2, 3 или 4.
21. Соединение конъюгата антитело-лекарственное средство по п.10, включающее смесь соединений конъюгата антитело-лекарственное средство, причем среднее количество молекул лекарственного средства на антитело, р, в смеси соединений конъюгата антитело-лекарственное средство составляет от около 2 до около 5.
22. Фармацевтическая композиция, содержащая терапевтически эффективное количество соединения конъюгата антитело-лекарственное средство по п.10 и фармацевтически приемлемое вспомогательное вещество.
23. Способ лечения злокачественной опухоли позитивной по HER2, включающий введение пациенту терапевтически эффективного количества фармацевтической композиции по п.22.
24. Соединение конъюгата антитело-лекарственное средство Формулы II
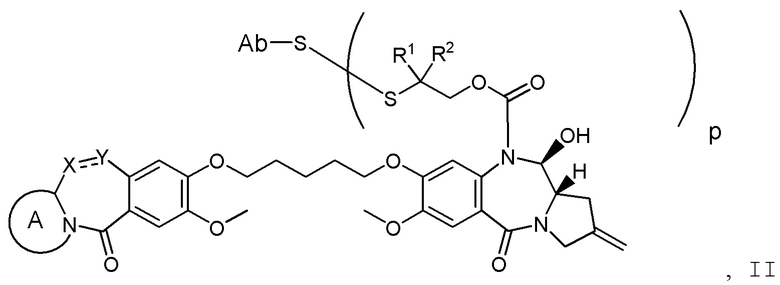
где X Y представляет собой C(=O)-NH или CH2-NH;
Y представляет собой C(=O)-NH или CH2-NH;
A представляет собой пиррол, необязательно замещенный группой =C(R)2, в которой R независимо выбран из H и C1-C6-алкила;
R1 и R2 независимо выбраны из H или C1-C6-алкила или R1 и R2 образуют циклопропил;
p равно целому числу от 1 до 8; и
Ab представляет собой анти-HER2 антитело, содержащее:
(a) HVR-H1, содержащую аминокислотную последовательность SEQ ID NO: 22;
(b) HVR-H2, содержащую аминокислотную последовательность SEQ ID NO: 23;
(c) HVR-H3, содержащую аминокислотную последовательность SEQ ID NO: 24;
(d) HVR-L1, содержащую аминокислотную последовательность SEQ ID NO: 19;
(e) HVR-L2, содержащую аминокислотную последовательность SEQ ID NO: 20; и
(f) HVR-L3, содержащую аминокислотную последовательность SEQ ID NO: 21.
25. Соединение конъюгата антитело-лекарственное средство по п.24, в котором антитело против HER2 содержит вариабельную область легкой цепи, содержащую последовательность SEQ ID NO: 17, и вариабельную область тяжелой цепи, содержащую последовательность SEQ ID NO: 18.
26. Соединение конъюгата антитело-лекарственное средство по п.25 Формулы IIa
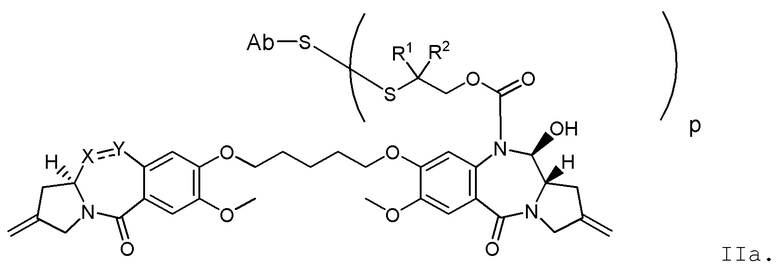
27. Соединение конъюгата антитело-лекарственное средство по п.25 Формулы IIc
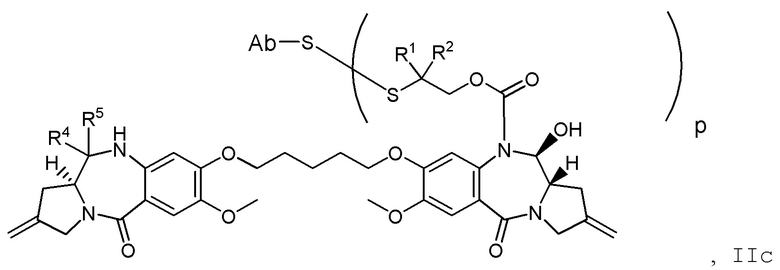
где каждый R4 и R5 представляет собой H или R4 и R5 представляют собой =O.
28. Соединение конъюгата антитело-лекарственное средство по п.27, где каждый R4 и R5 представляет собой H.
29. Соединение конъюгата антитело-лекарственное средство по п.27, где R4 и R5 представляют собой =О.
30. Соединение конъюгата антитело-лекарственное средство по п.27 Формулы IId
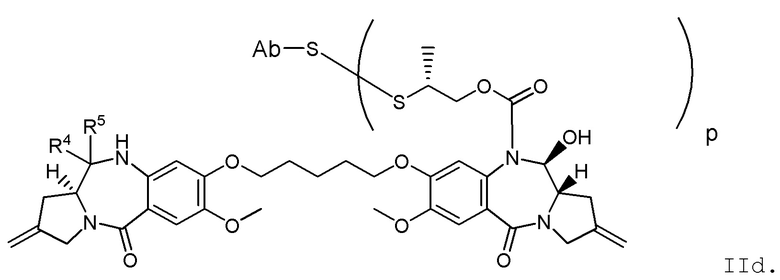
31. Соединение конъюгата антитело-лекарственное средство по п.27 Формулы IIe
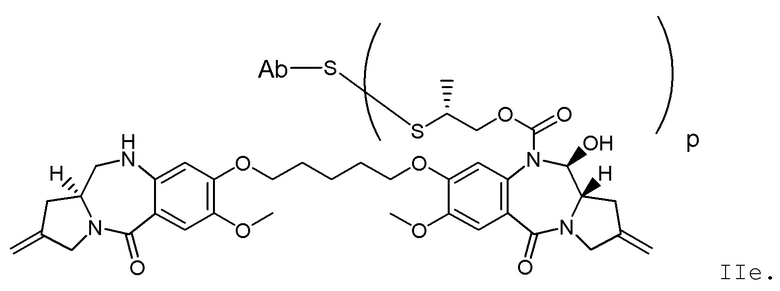
32. Соединение конъюгата антитело-лекарственное средство по п.27 Формулы IIf
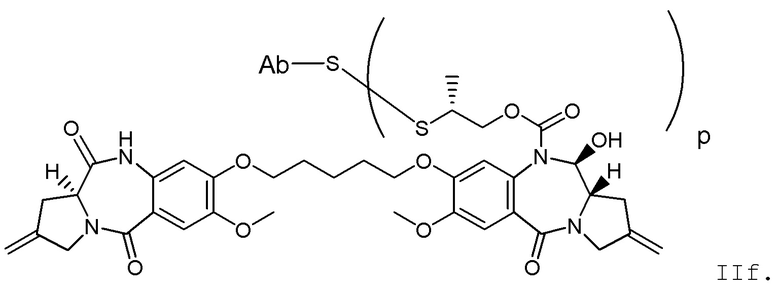
33. Соединение конъюгата антитело-лекарственное средство по п.24, в котором анти-HER2 антитело представляет собой модифицированное цистеином антитело.
34. Соединение конъюгата антитело-лекарственное средство по п.33, в котором модифицированное цистеином антитело, содержит K149C LC или A118C HC в качестве сайта конъюгации лекарственного средства.
35. Соединение конъюгата антитело-лекарственное средство по п.24, где p равно 1, 2, 3 или 4.
36. Соединение конъюгата антитело-лекарственное средство по п.24, включающее смесь соединений конъюгата антитело-лекарственное средство, причем среднее количество молекул лекарственного средства на антитело, р, в смеси соединений конъюгата антитело-лекарственное средство составляет от около 2 до около 5.
37. Фармацевтическая композиция для лечения гиперпролиферативного заболевания, содержащая терапевтически эффективное количество соединения конъюгата антитело-лекарственное средство по п.24, равное от 0,1 до 10 мг/кг от веса пациента, и фармацевтически приемлемое вспомогательное вещество.
38. Способ лечения злокачественной опухоли, включающий введение пациенту терапевтически эффективного количества соединения конъюгата антитело-лекарственное средство по п.24, где злокачественная опухоль представляет собой злокачественную опухоль позитивную по HER2.
39. Способ по п.38, где злокачественная опухоль позитивная по HER2 представляет собой рак молочной железы или рак желудка.
40. Способ по п.38, дополнительно включающий введение пациенту дополнительного терапевтического агента, выбранного из антитела или иммуноконъюгата, который связывается с HER2.
41. Способ по п.40, где дополнительным терапевтическим агентом является
(i) антитело или иммуноконъюгат, который связывается с доменом II HER2, и/или
(ii) антитело или иммуноконъюгат, который связывается с доменом IV HER2.
42. Способ по п.40, где дополнительным терапевтическим агентом является
(i) антитело или иммуноконъюгат, который связывается с эпитопом 2C4, и/или
(ii) антитело или иммуноконъюгат, который связывается с эпитопом 4D5.
43. Способ по п.40, где дополнительный терапевтический агент выбран из трастузумаба, трастузумаба-MCC-DM1 (T-DM1) или пертузумаба.
44. Способ по п.40, дополнительно включающий введение пациенту
(1) трастузумаба или Т-DM1 и
(2) пертузумаба.
45. Конъюгат антитело-лекарственное средство Формулы IIf
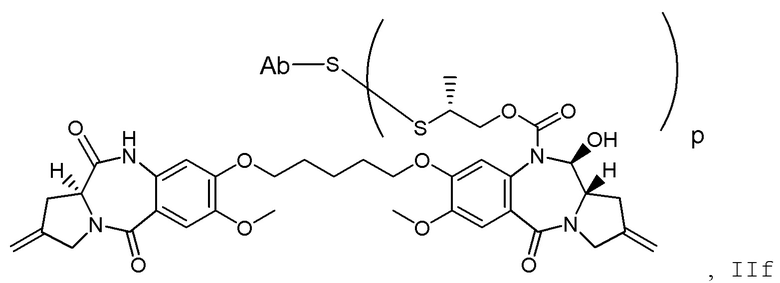
где Ab представляет собой модифицированное цистеином анти-HER2 антитело и p равно около 2 и
где Ab представляет собой анти-HER2 антитело, содержащее:
(a) HVR-H1, содержащую аминокислотную последовательность SEQ ID NO: 22;
(b) HVR-H2, содержащую аминокислотную последовательность SEQ ID NO: 23;
(c) HVR-H3, содержащую аминокислотную последовательность SEQ ID NO: 24;
(d) HVR-L1, содержащую аминокислотную последовательность SEQ ID NO: 19;
(e) HVR-L2, содержащую аминокислотную последовательность SEQ ID NO: 20; и
(f) HVR-L3, содержащую аминокислотную последовательность SEQ ID NO: 21.
46. Соединение конъюгата антитело-лекарственное средство по п.45, в котором анти-HER2 антитело содержит вариабельную область легкой цепи, содержащую последовательность SEQ ID NO: 17, и вариабельную область тяжелой цепи, содержащую последовательность SEQ ID NO: 18.
47. Фармацевтическая композиция для лечения гиперпролиферативного заболевания, содержащая терапевтически эффективное количество соединения конъюгата антитело-лекарственное средство по п.45, равное от 0,1 до 10 мг/кг от веса пациента, и фармацевтически приемлемое вспомогательное вещество.
48. Конъюгат антитело-лекарственное средство по п.45, где анти-HER2 антитело содержит:
(i) тяжелую цепь с последовательностью SEQ ID NO: 26 и легкую цепь с последовательностью SEQ ID NO: 30; или
(ii) тяжелую цепь с последовательностью SEQ ID NO: 31 и легкую цепь с последовательностью SEQ ID NO: 25.
49. Конъюгат антитело-лекарственное средство по п.45, где p равно примерно 2.
50. Конъюгат антитело-лекарственное средство по п.45, где модифицированное цистеином антитело содержит замену K149C в легкой цепи согласно нумерации Кабат или замену A118C в тяжелой цепи согласно нумерации EU в качестве места конъюгации лекарственного средства.
51. Конъюгат антитело-лекарственное средство Формулы IIe
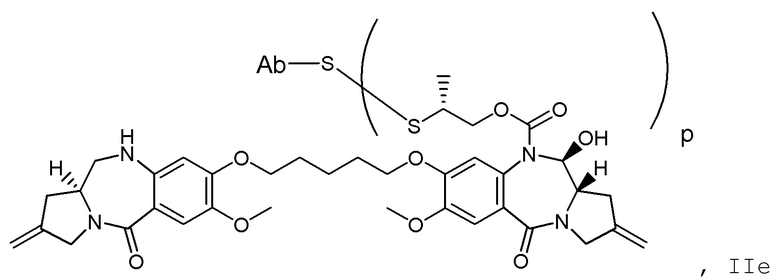
где Ab представляет собой модифицированное цистеином анти-HER2 антитело и р равно примерно 2 и
где Ab представляет собой анти-HER2 антитело, содержащее:
(а) HVR-H1, содержащую аминокислотную последовательность SEQ ID NO: 22;
(b) HRV-H2, содержащую аминокислотную последовательность SEQ ID NO: 23;
(c) HVR-H3, содержащую аминокислотную последовательность SEQ ID NO: 24;
(d) HVR-L1, содержащую аминокислотную последовательность SEQ ID NO: 19;
(e) HVR-L2, содержащую аминокислотную последовательность SEQ ID NO: 20; и
(f) HVR-L3, содержащую аминокислотную последовательность SEQ ID NO: 21.
52. Конъюгат антитело-лекарственное средство по п.51, где анти-HER2 антитело содержит вариабельную область легкой цепи, содержащую последовательность SEQ ID NO: 17, и вариабельную область тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 18.
53. Фармацевтическая композиция для лечения гиперпролиферативного заболевания, содержащая терапевтически эффективное количество конъюгата антитело-лекарственное средство по п.51, равное от 0,1 до 10 мг/кг от веса пациента, и фармацевтически приемлемое вспомогательное вещество.
54. Конъюгат антитело-лекарственное средство по п.51, где анти-HER2 антитело содержит:
(i) тяжелую цепь с последовательностью SEQ ID NO: 26 и легкую цепь с последовательностью SEQ ID NO: 30; или
(ii) тяжелую цепь с последовательностью SEQ ID NO: 31 и легкую цепь с последовательностью SEQ ID NO: 25.
55. Конъюгат антитело-лекарственное средство по п.51, где p равно примерно 2.
56. Конъюгат антитело-лекарственное средство по п.51, где модифицированное цистеином антитело содержит замену K149C в легкой цепи согласно нумерации Кабат или замену A118C в тяжелой цепи согласно нумерации EU в качестве места конъюгации лекарственного средства.
| WO 2014096368 A1, 26.06.2014 | |||
| WO 2014011518 A1, 16.01.2014 | |||
| Grimm, J., Liu, F., Stefanick, S., Sorgi, K | |||
| L., & Maryanoff, C | |||
| A | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Organic Process Research & Development, 7(6), | |||
Авторы
Даты
2020-11-19—Публикация
2016-09-30—Подача