Область техники, к которой относится изобретение
[0001] Настоящее изобретение относится к способу получения конъюгата антитело-лекарственное средство на основе эрибулина.
Уровень техники
[0002] Рак представляет собой одну из основных причин заболевания и смерти, и приблизительно 14000000 новых случаев рака и приблизительно 8200000 смертей от рака были зарегистрированы в 2012 г. Наиболее частыми причинами смерти от рака являются рак легкого (1590000 смертей); рак печени (745000 смертей); рак желудка (723000 смертей); колоректальный рак (694000 смертей); рак молочной железы (521000 смертей) и рак пищевода (400000 смертей). Ожидается, что число новых случаев рака вырастет на приблизительно 70% в течение следующих 20 лет, до приблизительно 22000000 новых случаев рака в год (непатентный литературный источник 1).
[0003] Микротрубочки представляют собой динамические нитевидные белки цитоскелета, связанные с различными клеточными функциями, включая внутриклеточную миграцию и транспорт, передачу клеточных сигналов и поддержание формы клетки. Микротрубочки также играют важную роль в митотическом делении клетки путем образования митотического веретена, которое необходимо для деления хромосомы в две дочерние клетки. Большая часть биологических функций микротрубочек во всех клетках регулируются их динамическими характеристиками полимеризации, которые обусловлены обратимым нековалентным присоединением димеров α- и β-тубулина к обоим концам микротрубочек. Данное динамическое поведение и обусловленный им контроль длины микротрубочек являются жизненно важными для надлежащего функционирования веретена. Даже незначительное изменение динамических характеристик микротрубочек может затрагивать контрольную точку веретена, останавливать прогрессирование клеточного цикла при митозе и затем приводить к гибели клетки (непатентный литературный источник 2). Из-за своей высокой скорости деления раковые клетки в целом являются более чувствительными к соединениям, которые связываются с тубулином и нарушают его нормальное функционирование, по сравнению с нормальными клетками. По этой причине ингибиторы тубулина и другие средства, целенаправленно воздействующие на микротрубочки, стали перспективным классом лекарственных средств для лечения рака (непатентный литературный источник 3).
[0004] Фолатный рецептор альфа (FRA) представляет собой гликофосфатидилинозитол (GPI)-связанный мембранный белок, который связывает фолат. Хотя роль FRA в биологии нормальных тканей и раковых тканей не понятна полностью, FRA сверхэкспрессируется в высокой степени в большом проценте случаев рака яичника эпителиального происхождения (непатентный литературный источник 4), а также в некотором проценте случаев немелкоклеточного рака легкого (непатентный литературный источник 5). FRA также характеризуется ограниченной экспрессией в нормальных тканях. Эти свойства делают FRA привлекательной мишенью для иммунотерапии рака.
[0005] Протоонкогенный рецептор-2 эпидермального фактора роста человека (HER2) кодирует трансмембранный тирозинкиназный рецептор, который принадлежит к семейству рецепторов эпидермального фактора роста человека (непатентный литературный источник 6). Сверхэкспрессия HER2 обеспечивает конститутивную активацию сигнальных путей фактора роста, таких как путь PI3K-AKT-mTOR, и тем самым выступает в качестве онкогенного фактора при нескольких типах рака, включая примерно 20% инвазивных видов рака молочной железы (непатентные литературные источники 7 и 8). Поскольку амплификация HER2 опосредует трансформированный фенотип, HER2 представляет собой другую потенциальную мишень для лечения рака.
Список цитируемой литературы
Патентные литературные источники
[0006]
[Патентный литературный источник 1] WO2017/151979
Непатентные литературные источники
[0007]
[Непатентный литературный источник 1] World Cancer Report 2014
[Непатентный литературный источник 2] Mukhtar et al. (2014) Mol. Cancer Ther. 13:275-84
[Непатентный литературный источник 3] Dumontet and Jordan (2010) Nat. Rev. Drug Discov. 9:790-803
[Непатентный литературный источник 4] O'Shannessy et al. (2013) Int. J. Gynecol. Pathol. 32(3):258-68
[Непатентный литературный источник 5] Christoph et al. (2014) Clin. Lung Cancer 15(5):320-30
[Непатентный литературный источник 6] King et al. (1985) Science 229:974-6
[Непатентный литературный источник 7] Slamon et al. (1989) Science 244:707-12
[Непатентный литературный источник 8] Gajria and Chandarlapaty (2011) Expert Rev. Anticancer Ther. 11:263-75
[Непатентный литературный источник 9] O'Shannessy et al., (2011) Oncotarget 2:1227-43
Сущность изобретения
Техническая задача
[0008] Целью настоящего изобретения является обеспечение способа получения конъюгата антитело-лекарственное средство с высоким выходом и синтетического промежуточного соединения, применимого для данного способа.
Решение задачи
[0009] В настоящем изобретении предусмотрено следующее [1] - [8].
[1] Способ получения конъюгата антитело-лекарственное средство, представленного Формулой (I),
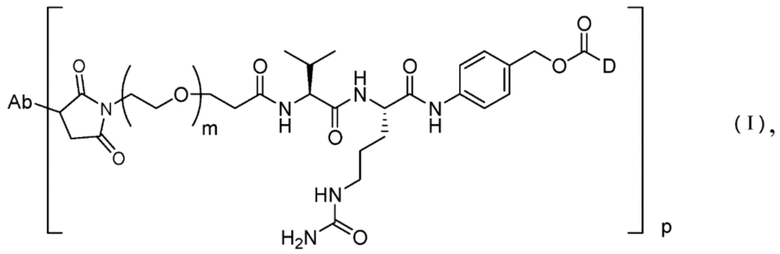
причем в Формуле: Ab представляет собой антитело или его антигенсвязывающий фрагмент, D представляет собой эрибулин, m представляет собой целое число от 1 до 10, и p представляет собой целое число от 1 до 8,
при этом способ включает:
стадию 1 получения соединения, представленного Формулой (B), путем осуществления реакции эрибулина или его соли с соединением, представленным Формулой (A),
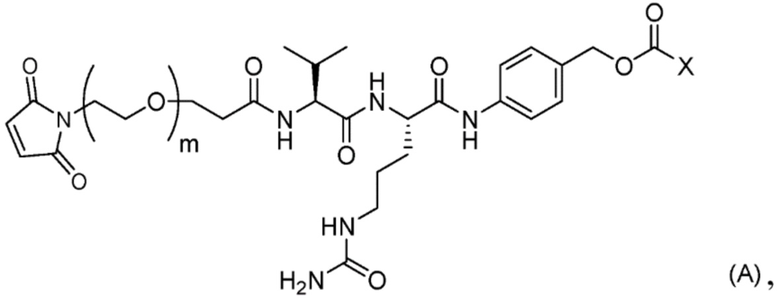
причем в Формуле: m представляет собой целое число от 1 до 10, и X представляет собой феноксигруппу или нитрофеноксигруппу, и
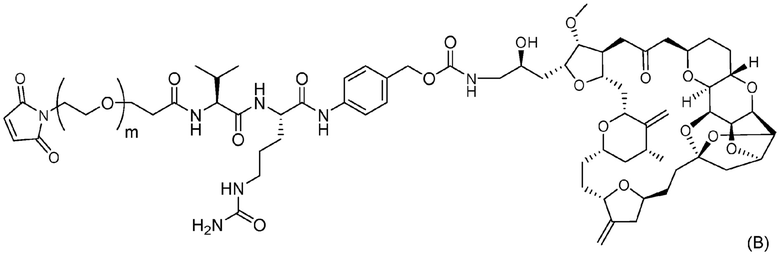
причем в Формуле: m представляет собой целое число от 1 до 10, и
стадию 2 получения конъюгата антитело-лекарственное средство, представленного Формулой (I), путем осуществления реакции соединения, представленного Формулой (B), с Ab.
[2] Способ в соответствии с [1], в котором Ab содержит (i) домен тяжелой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 1, и домен легкой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 6, (ii) вариабельный домен тяжелой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 23, и вариабельный домен легкой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 24, (iii) вариабельный домен тяжелой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 27, и вариабельный домен легкой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 28, или (iv) домен тяжелой цепи, содержащий аминокислотную последовательность представленную под SEQ ID NO: 347, и домен легкой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 308.
[3] Способ в соответствии с [1] или [2], в котором p равняется 3 или 4.
[4] Способ в соответствии с любым из [1] - [3], в котором эрибулин или его соль представляют собой эрибулина метансульфонат.
[5] Способ в соответствии с любым из [1] - [4], в котором стадию 1 осуществляют в присутствии основания.
[6] Способ получения соединения, представленного Формулой (B),
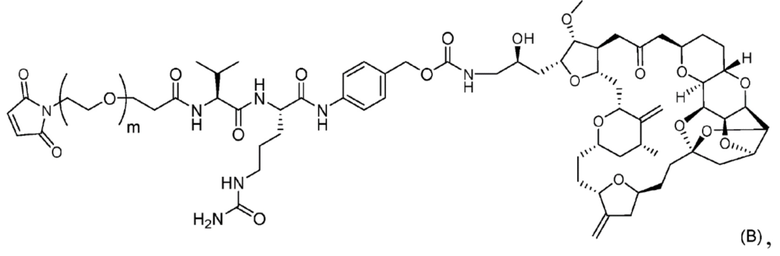
причем в Формуле: m представляет собой целое число от 1 до 10,
при этом способ включает:
стадию получения соединения, представленного Формулой (B), путем осуществления реакции эрибулина или его соли с соединением, представленным Формулой (A),
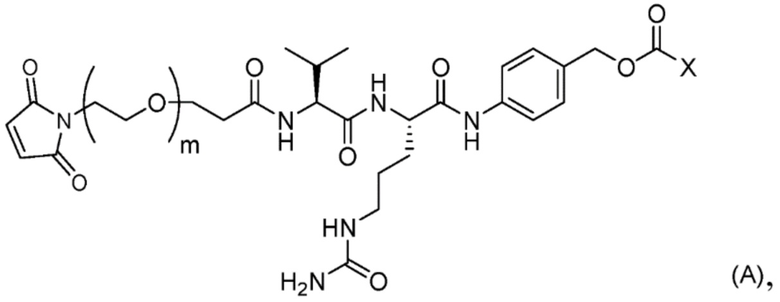
причем в Формуле: m представляет собой целое число от 1 до 10, и X представляет собой феноксигруппу или нитрофеноксигруппу.
[7] Способ в соответствии с [6], в котором стадию осуществляют в присутствии основания.
[8] Соединение, представленное Формулой (A), 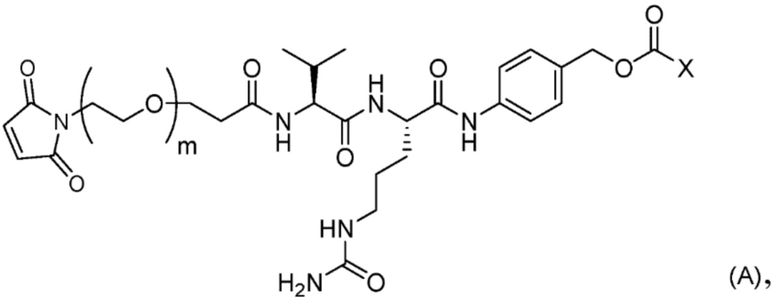
причем в Формуле: m представляет собой целое число от 1 до 10, и X представляет собой феноксигруппу или нитрофеноксигруппу.
Полезные эффекты настоящего изобретения
[0010] Настоящее изобретение может обеспечить способ получения конъюгата антитело-лекарственное средство с высоким выходом. Кроме того, настоящее изобретение может обеспечивать синтетическое промежуточное соединение, которое является применимым для получения конъюгата антитело-лекарственное средство с высоким выходом.
Описание вариантов осуществления
[0011] Вариант осуществления настоящего изобретения будет подробно описан ниже.
[0012] Вариант осуществления настоящего изобретения относится к способу получения конъюгата антитело-лекарственное средство, представленного Формулой (I).
[0013] Во-первых, будет описан ADC, представленный Формулой (I).
[0014] ADC может связываться с опухолевыми клетками, интернализоваться ними и уничтожать их (например, опухолевые клетки, экспрессирующие FRA). Кроме того, предпочтительным является то, что фрагмент, представляющий собой антитело (Ab), применяемый в ADC, представляет собой антитело или его антигенсвязывающий фрагмент и целенаправленно воздействует на опухолевые клетки. Антитело или антигенсвязывающий фрагмент содержит, например:
(a) три CDR тяжелой цепи и три CDR легкой цепи, которые определены согласно системе нумерации Kabat (Kabat, Sequences of Proteins of Immunological Interest (National Institutes of Health, Bethesda, Md. (1987 и 1991))), три CDR тяжелой цепи, содержащие аминокислотные последовательности определяющей комплементарность области 1 тяжелой цепи (CDR тяжелой цепи), представленной под SEQ ID NO: 2, CDR2 тяжелой цепи, представленную под SEQ ID NO: 3, и CDR3 тяжелой цепи, представленную под SEQ ID NO: 4, и три CDR легкой цепи, содержащие аминокислотные последовательности определяющей комплементарность области 1 легкой цепи (CDR легкой цепи), представленной под SEQ ID NO: 7, CDR2 легкой цепи, представленную под SEQ ID NO: 8, и CDR3 легкой цепи, представленную под SEQ ID NO: 9; или
(b) три CDR тяжелой цепи и три CDR легкой цепи, которые определены согласно системе нумерации IMGT (Международная иммуногенетическая информационная система (IMGT (зарегистрированное торговое наименование)), три CDR тяжелой цепи, содержащие аминокислотные последовательности CDR1 тяжелой цепи, представленной под SEQ ID NO: 13, CDR2 тяжелой цепи, представленную под SEQ ID NO: 14, и CDR3 тяжелой цепи, представленную под SEQ ID NO: 15, и три CDR легкой цепи, содержащие аминокислотные последовательности CDR1 легкой цепи, представленной под SEQ ID NO: 16, CDR2 легкой цепи, представленную под SEQ ID NO: 17, и CDR3 легкой цепи, представленную под SEQ ID NO: 18.
[0015] В настоящем описании термины "конъюгат антитело-лекарственное средство", "конъюгат на основе антитела", "конъюгат", "иммуноконъюгат" и "ADC" используются взаимозаменяемо и относятся к соединению или к его производному, которое соединено с антителом (например, антитело к FRA), и определено Формулой I [в Формуле: Ab представляет собой фрагмент, представляющий собой антитело (т. е. представляет собой антитело или его антигенсвязывающий фрагмент), L представляет собой линкерный фрагмент, D представляет собой эрибулин, и p представляет собой число фрагментов, представляющих собой эрибулин, на фрагмент, представляющий собой антитело].
[0016] Термин "антитело" используется в самом широком смысле для обозначения молекулы иммуноглобулина, которая распознает мишень и специфически связывается с ней, такой как белок, полипептид, углевод, полинуклеотид, липид или комбинация вышеуказанных, посредством по меньшей мере одного сайта распознавания антигена в пределах вариабельной области молекулы иммуноглобулина. Тяжелая цепь антитела состоит из вариабельного домена тяжелой цепи (VH) и константного домена тяжелой цепи (CH). Легкая цепь антитела состоит из вариабельного домена легкой цепи (VL) и константного домена легкой цепи (CL). Для целей настоящей заявки каждый зрелый вариабельный домен тяжелой цепи и легкой цепи содержит три определяющие комплементарность области (CDR1, CDR2 и CDR3) в пределах четырех каркасных областей (FR1, FR2, FR3 и FR4), расположенных от N-конца к C-концу: FR1, CDR1, FR2, CDR2, FR3, CDR3 и FR4. "Антитело" может быть встречающимся в природе или сконструированным человеком, таким как моноклональные антитела, полученные с помощью традиционной гибридомной технологии. Термин "антитело" включает в себя полноразмерные моноклональные антитела, полноразмерные поликлональные антитела и одноцепочечные антитела. Кроме того, примеры антигенсвязывающего фрагмента антитела включают в себя Fab, Fab', F(ab')2 и Fv. Антитело может принадлежать к любому из пяти основных классов иммуноглобулинов: IgA, IgD, IgE, IgG и IgM или к их подклассам (например, изотипам IgG1, IgG2, IgG3, IgG4). Данный термин дополнительно охватывает антитела человека, химерные антитела, гуманизированные антитела и любую модифицированную молекулу иммуноглобулина, содержащую сайт распознавания антигена, при условии, что они демонстрируют требуемые значения биологической активности.
[0017] Используемый в данном документе термин "моноклональное антитело" означает антитело, полученное из популяции практически однородных антител, что означает то, что отдельные антитела, входящие в состав популяции, являются идентичными, за исключением возможных встречающихся в природе мутаций, которые могут присутствовать в незначительных количествах. Моноклональные антитела являются высокоспецифичными, направленными против одного антигенного эпитопа. В отличие от этого, традиционные препараты (поликлональных) антител, как правило, включают большое разнообразие антител, направленных против (или специфических в отношении) разных эпитопов. Модификатор "моноклональный" указывает на характеристику антитела как полученного из практически однородной популяции антител и не должен рассматриваться как требующий получения антитела с помощью какого-либо конкретного способа. Например, моноклональные антитела, подлежащие применению в соответствии с настоящим изобретением, могут быть получены посредством гибридомного способа, впервые описанного в Kohler et al. (1975) Nature 256:495, или могут быть получены посредством способов рекомбинантной ДНК (см., например, патент США №4816567). Моноклональные антитела также могут быть выделены из фаговых библиотек антител с использованием способов, описанных в Clackson et al. (1991) Nature 352:624-8 и Marks et al. (1991) J. Mol. Biol. 222:581-97, к примеру.
[0018] Моноклональные антитела, описанные в данном документе, в частности, включают "химерные" антитела, в которых часть тяжелой и/или легкой цепей идентична или гомологична соответствующим последовательностям в антителах, полученных от конкретного вида или, принадлежащих к конкретному классу или подклассу антител, при этом остальная часть цепи(-ей) идентична или гомологична соответствующим последовательностям в антителах, полученных от другого вида или принадлежащих к другому классу или подклассу антител, а также фрагменты таких антител, при условии, что они специфически связывают антиген-мишень и/или проявляют требуемую биологическую активность.
[0019] Термин "гомолог" относится к молекуле, которая проявляет гомологию с другой молекулой, например, имеет последовательности химических остатков, которые являются идентичными или аналогичными в соответствующих положениях.
[0020] Используемый в данном документе термин "антитело человека" означает антитело, продуцируемое человеком, или антитело, имеющее аминокислотную последовательность антитела, продуцируемого человеком.
[0021] Используемый в данном документе термин "химерное антитело" означает антитела, в которых аминокислотная последовательность молекулы иммуноглобулина получена от двух или более видов. В некоторых случаях вариабельные домены как тяжелой, так и легкой цепей соответствуют вариабельным доменам антител, полученных от одного вида с требуемой специфичностью, аффинностью и активностью, при этом константные области гомологичны антителам, полученным от другого вида (например, человека), чтобы минимизировать иммунный ответ у последнего вида.
[0022] Используемый в данном документе термин "гуманизированное антитело" означает формы антител, которые содержат последовательности из антител, отличных от антител человека (например, мышиные), а также антитела человека. Такие антитела представляют собой химерные антитела, которые содержат минимальную последовательность, полученную из иммуноглобулина, отличного от иммуноглобулина человека. В целом гуманизированное антитело содержит практически весь из по меньшей мере одного и, как правило, двух вариабельных доменов, в которых все или практически все из гипервариабельных петель соответствуют петлям иммуноглобулина, отличного от иммуноглобулина человека, а все или практически все из каркасных областей (FR) представляют собой каркасные области из последовательности иммуноглобулина человека. Гуманизированное антитело необязательно также содержит по меньшей мере часть константной области (Fc) иммуноглобулина, как правило, часть константной области (Fc) иммуноглобулина человека. Гуманизированное антитело может быть дополнительно модифицировано посредством замены остатков в каркасной области Fv и/или в пределах замененных остатков, отличных от человеческих, для улучшения и оптимизации специфичности, аффинности и/или активности антитела.
[0023] Используемый в данном документе термин "антигенсвязывающий фрагмент" антитела относится к одному или нескольким фрагментам антитела, которые сохраняют способность специфично связываться с антигеном (например, FRA). Антигенсвязывающие фрагменты также преимущественно сохраняют способность к интернализации в клетку, экспрессирующую антиген. В некоторых вариантах осуществления антигенсвязывающие фрагменты также сохраняют иммунную эффекторную активность. Было показано, что фрагменты полноразмерного антитела способны выполнять антигенсвязывающую функцию полноразмерного антитела. Примеры связывающих фрагментов, охватываемых термином "антигенсвязывающий фрагмент" антитела, включают: (i) Fab-фрагмент, одновалентный фрагмент, состоящий из доменов VL, VH, CL и CH1; (ii) a F(ab')2-фрагмент, двухвалентный фрагмент, содержащий два Fab-фрагмента, связанных дисульфидным мостиком в шарнирной области; (iii) Fd-фрагмент, состоящий из доменов VH и CH1; (iv) Fv-фрагмент, состоящий из доменов VL и VH одного плеча антитела; (v) dAb-фрагмент, который содержит один вариабельный домен, например домен VH (см., например, Ward et al. (1989) Nature 341:544-6; и Winter et al. или WO 90/05144); и (vi) выделенную определяющую комплементарность область (CDR). Кроме того, хотя два домена Fv-фрагмента, VL и VH, кодируются отдельными генами, они могут быть соединены с применением рекомбинантных способов с помощью синтетического линкера, который позволяет получать их в виде одной белковой цепи, в которой домены VL и VH формируют пару с образованием одновалентных молекул (известных как одноцепочечный Fv (scFv)). См., например, Bird et al. (1988) Science 242:423-6 и Huston et al. (1988) Proc. Natl. Acad. Sci. USA 85:5879-83. Подразумевается, что такие одноцепочечные антитела также охватываются термином "антигенсвязывающий фрагмент" антитела, и они известны в уровне техники как иллюстративный тип связывающего фрагмента, который может подвергаться интернализации в клетки после связывания. См., например, Zhu et al. (2010) 9:2131-41; He et al. (2010) J. Nucl. Med. 51:427-32 и Fitting et al. (2015) MAbs 7:390-402. В определенных вариантах осуществления молекулы scFv могут быть включены в слитый белок. Также охватываются другие формы одноцепочечных антител, такие как диатела. Диатела представляют собой биспецифические диатела, в случае которых домены VH и VL экспрессируются в виде одной полипептидной цепи, но с применением линкера, который является слишком коротким, чтобы обеспечить формирование пары между двумя областями в одной цепи, что, таким образом, заставляет домены формировать пары с комплементарными областями другой цепи и создавать два антигенсвязывающих сайта (например, см. Holliger et al. (1993) Proc. Natl. Acad. Sci. USA 90:6444-8 и Poljak et al. (1994) Structure 2:1121-3). Антигенсвязывающие фрагменты получают с применением традиционных методик, известных специалистам в данной области техники, и антигенсвязывающие фрагменты подвергают скринингу в отношении применимости (например, аффинности связывания, интернализации) таким же образом, что и интактные антитела. Антигенсвязывающие фрагменты можно получать путем расщепления интактного белка, например с помощью протеазы или химического расщепления.
[0024] В настоящем описании антитело или его антигенсвязывающий фрагмент представляет собой интернализующееся антитело или его интернализующийся антигенсвязывающий фрагмент. "Интернализирование", как применяется в данном документе при ссылке на антитело или антигенсвязывающий фрагмент, относится к антителу или антигенсвязывающему фрагменту, которые могут поглощаться через липидную бислойную мембрану клетки во внутренний компартмент (что означает "подвергнуться интернализации") после связывания с клеткой, предпочтительно в компартмент в клетке, в котором происходит деградация, такой как лизосома. Например, интернализующееся антитело к FRA представляет собой антитело, которое может поглощаться в клетку после связывания с FRA на клеточной мембране.
[0025] Применяемый в данном документе термин "фолатный рецептор-альфа" или "FRA" относится к любой нативной форме FRA человека. Термин охватывает полноразмерный FRA (например, эталонную последовательность в NCBI: NP_000793; SEQ ID NO: 19), а также любую Форму FRA человека, которая возникает в результате процессинга в клетке. Этот термин также охватывает встречающиеся в природе варианты FRA, включая без ограничения варианты сплайсинга, аллельные варианты и изоформы. FRA можно выделять из клеток человека или можно получать рекомбинантным путем или с помощью способов синтеза.
[0026] Термин "антитело к FRA" или "антитело, которое специфически связывает FRA" означает любую Форму антитела или его антигенсвязывающего фрагмента, которые специфически связываются с FRA, и охватывает моноклональные антитела (включая полноразмерные моноклональные антитела), поликлональные антитела и биологически функциональные фрагменты антител, при условии, что они специфически связываются с FRA. Предпочтительно антитело к FRA, применяемое в ADC, раскрытое в данном документе, представляет собой антитело или его антигенсвязывающий фрагмент. MORAb-003 представляет собой иллюстративное антитело к FRA человека. Используемые в данном документе термины "специфический", "специфически связывает" относятся к селективному связыванию антитела с эпитопом антигена-мишени. Антитела можно тестировать в отношении специфичности связывания путем сравнения связывания с соответствующим антигеном со связыванием с нерелевантным антигеном или смесью антигенов при определенном наборе условий. Если антитело связывается с соответствующим антигеном с аффинностью, превышающей в по меньшей мере 2, 5, 7 и предпочтительно в 10 раз аффинность к нерелевантному антигену или к смеси антигенов, то считается, что оно является специфическим. В одном варианте осуществления специфическое антитело представляет собой антитело, которое связывается только с FRA-антигеном, но не связывается (или проявляет минимальное связывание) с другими антигенами.
[0027] Используемый в данном документе термин "рецептор 2 эпидермального фактора роста человека", "her2" или "her2/neu", относится к любой нативной форме her2 человека. Термин охватывает полноразмерную последовательность her2 (например, эталонную последовательность в NCBI: NP_004439.2; SEQ ID NO: 21), а также любую Форму her2 человека, которая может возникать в результате процессинга в клетке. Этот термин также охватывает встречающиеся в природе варианты her2, включая без ограничения варианты сплайсинга, аллельные варианты и изоформы. Her2 можно выделять из клеток человека или можно получать рекомбинантным путем или с помощью способов синтеза.
[0028] Термин "антитело к her2" или "антитело, которое специфически связывается с her2" означает любую Форму антитела или его антигенсвязывающего фрагмента, который специфически связывается с her2 и охватывает моноклональные антитела (включая полноразмерные моноклональные антитела), поликлональные антитела и биологически функциональные фрагменты антител, при условии, что они специфически связываются с her2. В патенте США №5821337 (включенном в данный документ посредством ссылки) представлены иллюстративные her2-связывающие последовательности, включая иллюстративные последовательности антител к her2. Предпочтительно антитело к her2, применяемое в ADC, раскрытых в данном документе, представляет собой антитело или его антигенсвязывающий фрагмент. Трастузумаб представляет собой иллюстративное антитело к her2 человека.
[0029] Термин "эпитоп" относится к части антигена, которую может распознавать антитело и специфически связываться с ней. Если антиген представляет собой полипептид, эпитопы образуются из смежных аминокислот или несмежных аминокислот, приводимых в соприкосновение за счет третичной укладки полипептида. Эпитоп, связываемый антителом, может быть идентифицирован путем применения любой методики картирования эпитопов, известной из уровня техники. Примеры методик картирования эпитопов включают в себя рентгеноструктурную кристаллографию для идентификации эпитопов, осуществляемую путем непосредственной визуализации комплекса антиген-антитело, отслеживание связывания антитела с фрагментами или мутированными вариантами антигена и отслеживание доступа растворителя к разным частям антитела и антигена. Иллюстративные стратегии, применяемые для картирования эпитопов, включают без ограничения олигопептидное сканирование, ограниченный протеолиз, сайт-направленный мутагенез, высокопроизводительное картирование на основе мутагенеза, водород-дейтериевый обмен и масс-спектрометрию (см., например, Gershoni et al. (2007) 21:145-56 и Hager-Braun and Tomer (2005) Expert Rev. Proteomics 2:745-56).
[0030] Для определения антител, совместно связывающих идентичные или перекрывающиеся эпитопы, также можно применять конкурентное связывание и эпитоп-специфическую сортировку. Конкурентное связывание может оцениваться с применением анализа перекрестного блокирования, такого как анализ, описанный в "Antibodies, A Laboratory Manual", Cold Spring Harbor Laboratory, Harlow and Lane (1st edition 1988, 2nd edition 2014). В некоторых вариантах осуществления конкурентное связывание тестируемого антитела или его антигенсвязывающего фрагмента оценивают, когда тестируемое антитело или его антигенсвязывающий фрагмент снижает степень связывания референсного антитела или его антигенсвязывающего фрагмента с антигеном-мишенью, таким как FRA или her2 (например, связывающего белка, содержащего CDR и/или вариабельные домены, выбранные из идентифицированных в таблицах 2, 4 и 6), на по меньшей мере приблизительно 50% в анализе перекрестного блокирования (например, на 50%, 60%, 70%, 80%, 90%, 95%, 99%, 99,5% или больше или на любое значение процента в диапазоне представленных значений) и/или наоборот. В некоторых вариантах осуществления конкурентное связывание может быть обусловлено идентичными или подобными (например, частично перекрывающимися) эпитопами или обусловлено стерическим несоответствием, при котором антитела или их антигенсвязывающие фрагменты связываются с близкорасположенными эпитопами. См., например, Tzartos, Methods in Molecular Biology (Morris, ed. (1998) vol. 66, pp. 55-66). В некоторых вариантах осуществления конкурентное связывание можно использовать для сортировки групп связывающих белков, которые имеют аналогичные эпитопы, например эпитопы, которые конкурируют за связывание, могут быть "отсортированы" как группа связывающих белков, которые имеют перекрывающиеся или близкорасположенные эпитопы, при этом белки, которые не конкурируют, могут быть помещены в отдельную группу связывающих белков, которые не имеют перекрывающихся или близкорасположенных эпитопов.
[0031] Термин "kon" или "ka" означает константу скорости ассоциации в случае ассоциации антитела с антигеном с образованием комплекса антитело/антиген. Скорость могут определять с применением стандартных анализов, таких как анализ Biacore или ELISA.
[0032] Термин "koff" или "kd" означает константу скорости диссоциации в случае диссоциации антитела из комплекса антитело-антиген. Скорость могут определять с применением стандартных анализов, таких как анализ Biacore или ELISA.
[0033] Термин "KD" означает равновесную константу диссоциации для конкретного взаимодействия антитело-антиген. KD рассчитывают как ka/kd. Скорость могут определять с применением стандартных анализов, таких как анализ Biacore или ELISA.
[0034] Термин "p" или "соотношение антитело:лекарственное средство" относится к числу структурных единиц, содержащих фрагменты, представляющие собой линкеры, и эрибулин, на фрагмент, представляющий собой антитело (Ab) (то есть содержание лекарственного вещества). В некоторых вариантах осуществления p представляет собой целое число от 1 до 10, от 1 до 9, от 1 до 8, от 1 до 7, от 1 до 6, от 1 до 5, от 1 до 4, от 1 до 3 или 1 или 2 и предпочтительно целое число 3 или 4. В композициях, содержащих множественные копии ADC, представленных Формулой I, "p" относится к среднему числу структурных единиц, включая в себя фрагменты, представляющие собой линкеры, и эрибулин на фрагмент, представляющий собой антитело (Ab) (также упоминается, как среднее содержание лекарственного вещества). В случаях, когда p представлено средним значением содержания лекарственного вещества, p может представлять собой число от 3 до 4, от 3,2 до 3,8, от 3,5 до 4,5, от 3,6 до 4,4 или 4.
[0035] В некоторых вариантах осуществления p представляет собой целое число от 1 до 6, от 2 до 5 или 3 или 4. В случаях, когда p представляет собой большее число, количество фрагментов, представляющих собой эрибулин на фрагмент, представляющий собой антитело, повышается. Следовательно, большее число эрибулина может доставляться к клеткам-мишеням с каждым антителом, и его фармакологический эффект может возрастать дополнительно.
[0036] В случаях, когда ADC представляют вне клетки, ADC остается интактным. В случаях, когда ADC подвергается интернализации в клетку (например, раковую клетку), линкерный фрагмент из ADC расщепляется, и эрибулин, находящийся в клетке, высвобождается. Линкерный фрагмент, как правило, является стабильным за пределами клетки Т. е. ADC распознает клетку (например, раковую клетку), которая экспрессирует антиген, специфичный к фрагменту, представляющему собой антитело (Ab), и попадает в клетку. Что касается ADC, который находится в клетке, линкерный фрагмент, который соединяет эрибулин и фрагмент, представляющий собой антитело (Ab), расщепляется так, что эрибулин высвобождается и проявляется фармакологический эффект.
[0037] 1. Фрагмент, представляющий собой антитело (Ab)
Фрагмент, представляющий собой антитело (Ab) в ADC представляет собой антитело или его антигенсвязывающий фрагмент, в частности антитело к фолатному рецептору альфа (FRA) или его антигенсвязывающий фрагмент, и может связываться с FRA-экспрессирующей опухолевой клеткой.
[0038] В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент связывается с фолатным рецептором альфа (FRA) и может целенаправленно воздействовать на FRA-экспрессирующую опухолевую клетку. Кроме того, в некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент содержит: (a) три CDR тяжелой цепи (CDR1 тяжелой цепи, представленную под SEQ ID NO: 2, CDR2 тяжелой цепи, представленную под SEQ ID NO: 3, и CDR3 тяжелой цепи, представленную под SEQ ID NO: 4) и три CDR легкой цепи (CDR1 легкой цепи, представленную под SEQ ID NO: 7, CDR2 легкой цепи, представленную под SEQ ID NO: 8, и CDR3 легкой цепи, представленную под SEQ ID NO: 9), которые определены согласно системе нумерации Kabat; или (b) три CDR тяжелой цепи (CDR1 тяжелой цепи, представленную под SEQ ID NO: 13, CDR2 тяжелой цепи, представленную под SEQ ID NO: 14, и CDR3 тяжелой цепи, представленную под SEQ ID NO: 15) и три CDR легкой цепи (CDR1 легкой цепи, представленную под SEQ ID NO: 16, CDR2 легкой цепи, представленную под SEQ ID NO: 17, и CDR3 легкой цепи, представленную под SEQ ID NO: 18), которые определены согласно системе нумерации IMGT. Кроме того, в некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент содержат каркасные последовательности человека. В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент содержит вариабельный домен тяжелой цепи, представленный под SEQ ID NO: 23, и вариабельный домен легкой цепи, представленный под SEQ ID NO: 24. В некоторых вариантах осуществления антитело или антигенсвязывающий фрагмент содержат константный домен тяжелой цепи IgG1 человека и константный домен легкой каппа-цепи Ig. В некоторых вариантах осуществления антитело или антигенсвязывающий фрагмент конкурируют за связывание и/или связывается с тем же эпитопом, что и антитело, которое содержит вариабельный домен тяжелой цепи, представленный под SEQ ID NO: 23, и вариабельный домен легкой цепи, представленный под SEQ ID NO: 24. В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент связываются с эпитопом, который содержит последовательность аланин-гистидин-лизин-аспарагиновая кислота (Ala-His-Lys-Asp, SEQ ID NO: 345) (непатентный литературный источник 9). В некоторых вариантах осуществления антитело или антигенсвязывающий фрагмент связывается с эпитопом, который содержит NTSQEAHKDVSYL (asn-Thr-Ser-Gln-Glu-Ala-His-Lys-Asp-Val-Ser-Tyr-Leu, SEQ ID NO: 346).
[0039] В других вариантах осуществления антитело или его антигенсвязывающий фрагмент связываются с рецептором-2 эпидермального фактора роста человека (her2) и могут целенаправленно воздействовать на her2-экспрессирующие опухолевые клетки. В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент содержит: (a) три CDR тяжелой цепи (CDR1 тяжелой цепи, представленную под SEQ ID NO: 71, CDR2 тяжелой цепи, представленную под SEQ ID NO: 72, и CDR3 тяжелой цепи, представленную под SEQ ID NO: 73) и три CDR легкой цепи (CDR1 легкой цепи, представленную под SEQ ID NO: 74, CDR2 легкой цепи, представленную под SEQ ID NO: 75, и CDR3 легкой цепи, представленную под SEQ ID NO: 76), которые определены согласно системе нумерации Kabat; или (b) три CDR тяжелой цепи (CDR1 тяжелой цепи, представленную под SEQ ID NO: 191, CDR2 тяжелой цепи, представленную под SEQ ID NO: 192, и CDR3 тяжелой цепи, представленную под SEQ ID NO: 193) и три CDR легкой цепи (CDR1 легкой цепи, представленную под SEQ ID NO: 194, CDR2 легкой цепи, представленную под SEQ ID NO: 195, и CDR3 легкой цепи, представленную под SEQ ID NO: 196), которые определены согласно системе нумерации IMGT. Кроме того, в некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент содержат каркасные последовательности человека. В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент содержит вариабельный домен тяжелой цепи, представленный под SEQ ID NO: 27, и вариабельный домен легкой цепи, представленный под SEQ ID NO: 28. В некоторых вариантах осуществления антитело или антигенсвязывающий фрагмент содержат константный домен тяжелой цепи IgG1 человека и константный домен легкой каппа-цепи Ig. В некоторых вариантах осуществления антитело или антигенсвязывающий фрагмент конкурируют за связывание и/или связывается с тем же эпитопом, что и антитело, которое содержит вариабельный домен тяжелой цепи, представленный под SEQ ID NO: 27, и вариабельный домен легкой цепи, представленный под SEQ ID NO: 28.
[0040] В других вариантах осуществления антитело или его антигенсвязывающий фрагмент связываются с мезотелином (MSLN) и могут целенаправленно воздействовать на MSLN-экспрессирующие опухолевые клетки. В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент содержит: (a) три CDR тяжелой цепи (CDR1 тяжелой цепи, представленную под SEQ ID NO: 65, CDR2 тяжелой цепи, представленную под SEQ ID NO: 66, и CDR3 тяжелой цепи, представленную под SEQ ID NO: 67) и три CDR легкой цепи (CDR1 легкой цепи, представленную под SEQ ID NO: 68, CDR2 легкой цепи, представленную под SEQ ID NO: 69, и CDR3 легкой цепи, представленную под SEQ ID NO: 70), которые определены согласно системе нумерации Kabat; или (b) три CDR тяжелой цепи (CDR1 тяжелой цепи, представленную под SEQ ID NO: 185, CDR2 тяжелой цепи, представленную под SEQ ID NO: 186, и CDR3 тяжелой цепи, представленную под SEQ ID NO: 187) и три CDR легкой цепи (CDR1 легкой цепи, представленную под SEQ ID NO: 188, CDR2 легкой цепи, представленную под SEQ ID NO: 189, и CDR3 легкой цепи, представленную под SEQ ID NO: 190), которые определены согласно системе нумерации IMGT. В некоторых вариантах осуществления антитело или антигенсвязывающий фрагмент содержит вариабельный домен тяжелой цепи, представленный под SEQ ID NO: 25, и вариабельный домен легкой цепи, представленный под SEQ ID NO: 26. В некоторых вариантах осуществления антитело или антигенсвязывающий фрагмент содержат константный домен тяжелой цепи IgG1 человека и константный домен легкой каппа-цепи Ig. В некоторых вариантах осуществления антитело или антигенсвязывающий фрагмент конкурируют за связывание и/или связываются с тем же эпитопом, что и антитело, которое содержит вариабельный домен тяжелой цепи, представленный под SEQ ID NO: 25, и вариабельный домен легкой цепи, представленный под SEQ ID NO: 26.
[0041] В настоящем варианте осуществления предпочтительный фрагмент, представляющий собой антитело (Ab), представляет собой антитело к фолатному рецептору альфа или его антигенсвязывающий фрагмент, содержащие: (a) три CDR тяжелой цепи, содержащие аминокислотные последовательности, представленные под SEQ ID NO: 2 (CDR1 тяжелой цепи), SEQ ID NO: 3 (CDR2 тяжелой цепи) и SEQ ID NO: 4 (CDR3 тяжелой цепи), или три CDR легкой цепи, содержащие аминокислотные последовательности, представленные под SEQ ID NO: 7 (CDR1 легкой цепи), SEQ ID NO: 8 (CDR2 легкой цепи) и SEQ ID NO: 9 (CDR3 легкой цепи), которые определены согласно системе нумерации Kabat; или (b) три CDR тяжелой цепи, содержащие аминокислотные последовательности, представленные под SEQ ID NO: 13 (CDR1 тяжелой цепи), SEQ ID NO: 14 (CDR2 тяжелой цепи) и SEQ ID NO: 15 (CDR3 тяжелой цепи) или три CDR легкой цепи, содержащие аминокислотные последовательности, представленные под SEQ ID NO: 16 (CDR1 легкой цепи), SEQ ID NO: 17 (CDR2 легкой цепи) и SEQ ID NO: 18 (CDR3 легкой цепи), которые определены согласно системе нумерации IMGT. Другой предпочтительный фрагмент, представляющий собой антитело (Ab), представляет собой антитело к рецептору 2 эпидермального фактора роста человека (her2) или его антигенсвязывающий фрагмент, содержащие: (c) три CDR тяжелой цепи, содержащие аминокислотные последовательности, представленные под SEQ ID NO: 71 (CDR1 тяжелой цепи), SEQ ID NO: 72 (CDR2 тяжелой цепи) и SEQ ID NO: 73 (CDR3 тяжелой цепи), или три CDR легкой цепи, содержащие аминокислотные последовательности, представленные под SEQ ID NO: 74 (CDR1 легкой цепи), SEQ ID NO: 75 (CDR2 легкой цепи) и SEQ ID NO: 76 (CDR3 легкой цепи), которые определены согласно системе нумерации Kabat; или (d) три CDR тяжелой цепи, содержащие аминокислотные последовательности, представленные под SEQ ID NO: 191 (CDR1 тяжелой цепи), SEQ ID NO: 192 (CDR2 тяжелой цепи) и SEQ ID NO: 193 (CDR3 тяжелой цепи) или три CDR легкой цепи, содержащие аминокислотные последовательности, представленные под SEQ ID NO: 194 (CDR1 легкой цепи), SEQ ID NO: 195 (CDR2 легкой цепи) и SEQ ID NO: 196 (CDR3 легкой цепи), которые определены согласно системе нумерации IMGT. Более предпочтительно, что фрагмент, представляющий собой антитело (Ab), представляет собой антитело к фолатному рецептору альфа или его антигенсвязывающий фрагмент.
[0042] Фрагмент, представляющий собой антитело (Ab), содержит любое антитело или антигенсвязывающий фрагмент, которые специфически связываются с антигеном-мишенью на раковой клетке. Антитело или антигенсвязывающий фрагмент может связываться с антигеном-мишенью с константой диссоциации (KD), составляющей ≤1 мМ, ≤100 нМ или ≤10 нМ или любое значение в пределах данных значений, измеренной, например, с помощью анализа BIAcore (зарегистрированное торговое наименование). В некоторых вариантах осуществления KD составляет от 1 пМ до 500 пМ. В некоторых вариантах осуществления KD составляет от 500 пМ до 1 мкМ, от 1 мкМ до 100 нМ или от 100 мМ до 10 нМ.
[0043] В некоторых вариантах осуществления фрагмент, представляющий собой антитело, представляет собой четырехцепочечное антитело (также называемое иммуноглобулином), содержащее две тяжелые цепи и две легкие цепи. В некоторых вариантах осуществления фрагмент, представляющий собой антитело, представляет собой двухцепочечное полуантитело (одна легкая цепь и одна тяжелая цепь) иммуноглобулина или его антигенсвязывающего фрагмента.
[0044] Аминокислотные последовательности и последовательности нуклеиновых кислот иллюстративных антител согласно настоящему изобретению представлены в таблицах от 1 до 9.
[0045] [Таблица 1]
Аббревиатуры: xi представляет собой химерное антитело, и zu представляет собой гуманизированное антитело.
[0046] Аминокислотные последовательности вариабельных доменов mAb
[Таблица 2]
[0047] Последовательности нуклеиновых кислот, кодирующие вариабельные домены mAb
[Таблица 3]
[0048] Аминокислотные последовательности CDR mAb по Kabat
[Таблица 4]
[Таблица 4 (продолжение)]
[0049] Последовательности нуклеиновых кислот, кодирующие CDR mAb по Kabat
[Таблица 5]
[Таблица 5 (продолжение)]
[0050] Аминокислотные последовательности CDR mAb по IMGT
[Таблица 6]
[Таблица 6 (продолжение)]
[0051] Последовательности нуклеиновых кислот, кодирующие CDR mAb по IMGT
[Таблица 7]
[Таблица 7 (продолжение)]
[0052] Аминокислотные последовательности цепей Ig, представляющих собой полноразмерное mAb
[Таблица 8]
[0053] Последовательности нуклеиновых кислот, кодирующие полноразмерные цепи Ig mAb
[Таблица 9]
Иллюстративные последовательности не содержат лидерные последовательности.
[0054] ADC может содержать любой набор вариабельных доменов тяжелой и легкой цепей, перечисленных в таблицах выше (например, вариабельные домены тяжелой и легкой цепей MORAb-003 или вариабельные домены тяжелой и легкой цепей трастузумаба), или набор из последовательностей шести CDR из набора тяжелой и легкой цепей. В некоторых вариантах осуществления ADC содержит константные области тяжелой и легкой цепей человека или их фрагменты. Например, ADC может содержать константный домен тяжелой цепи IgG человека (например, IgG1) и константный домен легких каппа- или лямбда-цепей человека. Фрагмент, представляющий собой антитело, содержит константную область тяжелой цепи иммуноглобулина G подтипа 1 (IgG1) человека и константную область легкой каппа-цепи Ig человека.
[0055] Раковый антиген-мишень ADC может представлять собой фолатный рецептор-альфа (FRA).
[0056] Антитело к FRA или его антигенсвязывающий фрагмент может содержать три CDR тяжелой цепи (CDR1 тяжелой цепи, представленную под SEQ ID NO: 2, CDR2 тяжелой цепи, представленную под SEQ ID NO: 3, и CDR3 тяжелой цепи, представленную под SEQ ID NO: 4) и три CDR легкой цепи (CDR1 легкой цепи, представленную под SEQ ID NO: 7, CDR2 легкой цепи, представленную под SEQ ID NO: 8, и CDR3 легкой цепи, представленную под SEQ ID NO: 9), которые определены согласно системе нумерации Kabat.
[0057] Кроме того, антитело к FRA или его антигенсвязывающий фрагмент может содержать три CDR тяжелой цепи (CDR1 тяжелой цепи, представленную под SEQ ID NO: 13, CDR2 тяжелой цепи, представленную под SEQ ID NO: 14, и CDR3 тяжелой цепи, представленную под SEQ ID NO: 15) и три CDR легкой цепи (CDR1 легкой цепи, представленную под SEQ ID NO: 16, CDR2 легкой цепи, представленную под SEQ ID NO: 17, и CDR3 легкой цепи, представленную под SEQ ID NO: 18), которые определены согласно системе нумерации IMGT.
[0058] В различных вариантах осуществления антитело к FRA или его антигенсвязывающий фрагмент содержат: вариабельный домен тяжелой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 23, и вариабельный домен легкой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 24; или вариабельный домен тяжелой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 1, и вариабельный домен легкой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 6. В некоторых вариантах осуществления антитело к FRA или его антигенсвязывающий фрагмент содержат вариабельный домен тяжелой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 23, и вариабельный домен легкой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 24, или содержат последовательности, которые на по меньшей мере 95% идентичны вышеописанным последовательностям. В некоторых вариантах осуществления антитело к FRA или его антигенсвязывающий фрагмент содержит аминокислотную последовательность вариабельного домена тяжелой цепи, которая на по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентична SEQ ID NO: 23, и аминокислотную последовательность вариабельного домена легкой цепи, которая на по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентична SEQ ID NO: 24.
[0059] Антитело к FRA может содержать константный домен тяжелой цепи IgG1 человека и константный домен легкой каппа-цепи Ig человека.
[0060] Антитело к FRA содержит аминокислотную последовательность тяжелой цепи, представленную под SEQ ID NO: 1, или последовательность, которая на по меньшей мере 95% идентична SEQ ID NO: 1, и аминокислотную последовательность легкой цепи, представленную под SEQ ID NO: 6, или последовательность, которая на по меньшей мере 95% идентична SEQ ID NO: 6. В определенных вариантах осуществления антитело содержит аминокислотную последовательность тяжелой цепи, представленную под SEQ ID NO: 1, и аминокислотную последовательность легкой цепи, представленную под SEQ ID NO: 6, или содержит последовательности, которые на по меньшей мере 95% идентичны вышеописанным последовательностям. В некоторых вариантах осуществления антитело к FRA содержит аминокислотную последовательность тяжелой цепи, которая на по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентична SEQ ID NO: 1 и/или аминокислотную последовательность легкой цепи, которая на по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентична SEQ ID NO: 6. В некоторых вариантах осуществления антитело к FRA содержит тяжелую цепь, кодируемую нуклеотидной последовательностью, представленной под SEQ ID NO: 11 (в том числе нуклеотиды, кодирующие лидерную последовательность) или под SEQ ID NO: 325 (не включая нуклеотиды, кодирующие лидерную последовательность), и легкую цепь, кодируемую нуклеотидом, представленным под SEQ ID NO: 12 (в том числе нуклеотиды, кодирующие лидерную последовательность) или под SEQ ID NO: 326 (не включая нуклеотиды, кодирующие лидерную последовательность). В некоторых вариантах осуществления у аминокислотной последовательности тяжелой цепи отсутствует C-концевой лизин. В различных вариантах осуществления антитело к FRA содержит аминокислотную последовательность антитела, продуцируемого клеточной линией, депонированной в соответствии с условиями Будапештского договора в Американской коллекции типовых культур (ATCC, 10801 Университетский Бульвар, Манассас, штат Вирджиния 20110-2209) 24 апреля 2006 г. под номером доступа PTA-7552, или такие последовательности тяжелой цепи, в которых отсутствует C-концевой лизин. В различных вариантах осуществления антитело к FRA представляет собой MORAb-003 (название согласно USAN: фарлетузумаб) (Ebel et al. (2007) Cancer Immunity 7:6) или его антигенсвязывающий фрагмент.
[0061] Раковый антиген-мишень ADC может представлять собой рецептор 2 эпидермального фактора роста человека (her2).
[0062] Кроме того, антитело к her2 или его антигенсвязывающий фрагмент могут содержать три CDR тяжелой цепи (CDR1 тяжелой цепи, представленную под SEQ ID NO: 71, CDR2 тяжелой цепи, представленную под SEQ ID NO: 72, и CDR3 тяжелой цепи, представленную под SEQ ID NO: 73) и три CDR легкой цепи (CDR1 легкой цепи, представленную под SEQ ID NO: 74, CDR2 легкой цепи, представленную под SEQ ID NO: 75, и CDR3 легкой цепи, представленную под SEQ ID NO: 76), которые определены согласно системе нумерации Kabat.
[0063] Кроме того, антитело к her2 или его антигенсвязывающий фрагмент могут содержать три CDR тяжелой цепи (CDR1 тяжелой цепи, представленную под SEQ ID NO: 191, CDR2 тяжелой цепи, представленную под SEQ ID NO: 192, и CDR3 тяжелой цепи, представленную под SEQ ID NO: 193) и три CDR легкой цепи (CDR1 легкой цепи, представленную под SEQ ID NO: 194, CDR2 легкой цепи, представленную под SEQ ID NO: 195, и CDR3 легкой цепи, представленную под SEQ ID NO: 196), которые определены согласно системе нумерации IMGT.
[0064] В различных вариантах осуществления антитело к her2 или его антигенсвязывающий фрагмент содержат: вариабельный домен тяжелой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 27, и вариабельный домен легкой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 28; или домен тяжелой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 347, и домен легкой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 308. В некоторых вариантах осуществления антитело к her2 или его антигенсвязывающий фрагмент содержат аминокислотную последовательность вариабельного домена тяжелой цепи, представленную под SEQ ID NO: 27, и аминокислотную последовательность вариабельного домена легкой цепи, представленную под SEQ ID NO: 28, или содержат последовательности, которые на по меньшей мере 95% идентичны вышеописанным последовательностям. В некоторых вариантах осуществления антитело к her2 или его антигенсвязывающий фрагмент содержат аминокислотную последовательность вариабельного домена тяжелой цепи, которая на по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентична SEQ ID NO: 27 и/или аминокислотную последовательность вариабельного домена легкой цепи, которая на по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентична SEQ ID NO: 28.
[0065] Антитело к her2 может содержать константный домен тяжелой цепи IgG1 человека и константный домен легкой каппа-цепи Ig человека.
[0066] В различных вариантах осуществления антитело к her2 содержит аминокислотную последовательность тяжелой цепи, представленную под SEQ ID NO: 307, или последовательность, которая на по меньшей мере 95% идентична SEQ ID NO: 307, и аминокислотную последовательность легкой цепи, представленную под SEQ ID NO: 308, или последовательность, которая на по меньшей мере 95% идентична SEQ ID NO: 308. В определенных вариантах осуществления антитело содержит аминокислотную последовательность тяжелой цепи, представленную под SEQ ID NO: 307, и аминокислотную последовательность легкой цепи, представленную под SEQ ID NO: 308, или содержит последовательности, которые на по меньшей мере 95% идентичны вышеописанным последовательностям. В некоторых вариантах осуществления антитело к her2 содержит аминокислотную последовательность тяжелой цепи, которая на по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентична SEQ ID NO: 307 и аминокислотную последовательность легкой цепи, которая на по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентична SEQ ID NO: 308. В различных вариантах осуществления антитело к her2 представляет собой трастузумаб или его антигенсвязывающий фрагмент.
[0067] В различных вариантах осуществления антитело к FRA или его антигенсвязывающий фрагмент содержат три CDR тяжелой цепи и три CDR легкой цепи MORAb-003 или содержат аминокислотные последовательности, полученные путем добавления, делеции или замены одной или меньше, двух или меньше, трех или меньше, четырех или меньше, пяти или меньше или шести или меньше аминокислот в CDR1 тяжелой цепи (SEQ ID NO: 2, определенной согласно системе Kabat или SEQ ID NO: 13, определенной согласно системе IMGT), CDR2 тяжелой цепи (SEQ ID NO: 3, определенной согласно системе Kabat или SEQ ID NO: 14, определенной согласно системе IMGT), CDR3 тяжелой цепи (SEQ ID NO: 4, определенной согласно системе Kabat или SEQ ID NO: 15, определенной согласно системе IMGT), CDR1 легкой цепи (SEQ ID NO: 7, определенной согласно системе Kabat или SEQ ID NO: 16, определенной согласно системе IMGT), CDR2 легкой цепи (SEQ ID NO: 8, определенной согласно системе Kabat или SEQ ID NO: 17, определенной согласно системе IMGT) и CDR3 легкой цепи (SEQ ID NO: 9, определенной согласно системе Kabat, или SEQ ID NO: 18, определенной согласно системе IMGT).
[0068] В других различных вариантах осуществления антитело к her2 или его антигенсвязывающий фрагмент содержат три CDR тяжелой цепи и три CDR легкой цепи трастузумаба или содержат аминокислотные последовательности, полученные путем добавления, делеции или замены одной или меньше, двух или меньше, трех или меньше, четырех или меньше, пяти или меньше или шести или меньше аминокислот в CDR1 тяжелой цепи (SEQ ID NO: 71, определенной согласно системе Kabat или SEQ ID NO: 191, определенной согласно системе IMGT), CDR2 тяжелой цепи (SEQ ID NO: 72, определенной согласно системе Kabat или SEQ ID NO: 192, определенной согласно системе IMGT), CDR3 тяжелой цепи (SEQ ID NO: 73, определенной согласно системе Kabat или SEQ ID NO: 193, определенной согласно системе IMGT), CDR1 легкой цепи (SEQ ID NO: 74, определенной согласно системе Kabat или SEQ ID NO: 194, определенной согласно системе IMGT), CDR2 легкой цепи (SEQ ID NO: 75, определенной согласно системе Kabat или SEQ ID NO: 195, определенной согласно системе IMGT), и CDR3 легкой цепи (SEQ ID NO: 76, определенной согласно системе Kabat или SEQ ID NO: 196, определенной согласно системе IMGT).
[0069] В различных вариантах осуществления замена аминокислоты представляет собой замену одного остатка. Вставка обычно представляет собой вставку от приблизительно 1 до приблизительно 20 аминокислотных остатков, хотя могут допускаться значительно более длинные вставки при условии, что сохраняется биологическая функция (например, связывание с FRA или her2). Делеция обычно представляет собой делецию в диапазоне от приблизительно 1 до приблизительно 20 аминокислотных остатков, хотя в некоторых случаях делеции могут быть намного более длинными. Замены, делеции, вставки или любые их комбинации могут применяться для достижения конечного производного или варианта. Обычно такие изменения выполняют для небольшого числа аминокислот, чтобы свести к минимуму изменение молекулы, в частности иммуногенности и специфичности антигенсвязывающего белка. Однако в некоторых обстоятельствах может допускаться более значительное изменение. Консервативная замена обычно выполняется в соответствии со следующей схемой, изображенной в таблице 10.
[0070] [Таблица 10]
[0071] Значительное изменение функции или иммунологической идентичности осуществляются путем выбора замены, которая является менее консервативной, чем показанные в таблице 10. Например, можно осуществлять замену, которая в более значительной степени воздействует на структуру полипептидного остова в области изменения, например, структуру α-спирали или β-спирали; заряд или гидрофобность молекулы в сайте-мишени или объем боковой цепи. Замены, которые, как правило, ожидаемо приводят к самым большим изменениям свойств полипептида, являются такими, при которых (a) - (d):
(a) гидрофильный аминокислотный остаток (например, Ser или Thr) заменен гидрофобным аминокислотным остатком (например, Leu, Ile, Phe, Val или Ala);
(b) Cys или Pro заменен любым другим остатком;
(c) аминокислотный остаток с электроположительной боковой цепью (например, Lys, Arg или His) заменен электроотрицательным аминокислотным остатком (например, Gln или Asn); и
(d) остаток с объемной боковой цепью (например, Phe) заменен аминокислотой, не имеющей боковой цепи (например, Gly).
[0072] В различных вариантах осуществления, где в ADC применяются варианты последовательностей антител, варианты, как правило, проявляют такую же качественную биологическую активность и вызывают такой же иммунный ответ, хотя при необходимости также могут быть выбраны варианты для модификации характеристик антигенсвязывающих белков. В качестве альтернативы вариант может быть сконструирован таким образом, чтобы биологическая активность антигенсвязывающего белка изменилась. Например, могут быть изменены или удалены сайты гликозилирования, как обсуждается в данном документе.
[0073] В ADC в соответствии с настоящим вариантом осуществления могут применяться различные антитела для целенаправленного воздействия на раковые клетки. Подходящие антигены, экспрессируемые на опухолевых клетках, но не на здоровых клетках, или экспрессируемые на опухолевых клетках с более высокой частотой, чем на здоровых клетках, известны из уровня техники, как и антитела, направленные против них. Такие антитела можно применять вместе с линкером и эрибулином, раскрытыми в данном документе.
[0074] Фрагмент, представляющий собой антитело, в ADC может представлять собой фрагмент, представляющий собой антитело к FRA, такой как MORAb-003. В некоторых вариантах осуществления линкер и эрибулин в соответствии с настоящим изобретением могут быть неожиданно эффективными в случае нескольких антител, целенаправленно воздействующих на разные опухоли. В случаях, когда фрагмент, представляющий собой антитело, в ADC может представлять собой фрагмент, представляющий собой антитело к FRA, такой как MORAb-003, ADC может обеспечить, в частности, улучшение соотношения лекарственное средство:антитело, целенаправленного воздействия на опухоль, неспецифического цитолиза и эффективности лечения и снижение нецелевого цитолиза. Улучшение эффективности лечения может быть измерено in vitro или in vivo и может предусматривать снижение скорости роста опухоли и/или уменьшение объема опухоли.
[0075] В случаях, когда фрагмент, представляющий собой антитело, в ADC представляет собой фрагмент, представляющий собой антитело к her2, такой как трастузумаб, наблюдаются некоторые или все из благоприятных функциональных свойств. Кроме того, фрагмент, представляющий собой антитело, в ADC может представлять собой фрагмент, представляющий собой антитело к her2, такой как трастузумаб. В случаях, когда фрагмент, представляющий собой антитело, в ADC представляет собой фрагмент, представляющий собой антитело к MSLN, такой как MORAb-009, наблюдаются некоторые или все из благоприятных функциональных свойств.
[0076] В некоторых вариантах осуществления свободные остатки цистеина вводятся в аминокислотную последовательность фрагмента, представляющего собой антитело. Например, можно получить антитела (цистеин-модифицированные антитела), в которых одна или несколько аминокислот в аминокислотной последовательности в исходном антителе заменены цистеином. Например, посредством введения цистеина в фрагмент исходного FAb-антитела может образовываться цистеин-модифицированное Fab-антитело (также называемое "ThioFab"). Подобным образом посредством введения цистеина в исходное моноклонального антитело может образовываться цистеин-модифицированное моноклональное антитело (также называемое "ThioMab"). Мутация в одном сайте приводит к образованию одного модифицированного остатка цистеина в ThioFab, при этом мутация в одном сайте приводит к образованию двух модифицированных остатков цистеина в ThioMab вследствие димерной природы антитела класса IgG. ДНК, кодирующая вариант аминокислотной последовательности исходного полипептида, может быть получена с помощью ряда способов, известных из уровня техники (см., например, способы, описанные в WO2006/034488). Эти способы включают без ограничения получение посредством сайт-направленного (или олигонуклеотид-опосредованного) мутагенеза, ПЦР-мутагенеза и кассетного мутагенеза ранее полученной ДНК, кодирующей полипептид. Варианты рекомбинантных антител также могут быть сконструированы также посредством манипуляции с фрагментами с применением рестрикции или посредством ПЦР с перекрывающимися праймерами с применением синтетических олигонуклеотидов. ADC, представленный Формулой I, содержит без ограничения антитела, которые содержат одну, две, три или четыре модификации цистеина (Lyon et al. (2012) Methods Enzymol. 502:123-38). В некоторых вариантах осуществления, когда один или несколько свободных остатков цистеина уже присутствуют во фрагменте антитела, существующие свободные остатки цистеина можно использовать для конъюгации фрагмента антитела с эрибулином без применения модифицирования.
[0077] 2. Линкерный фрагмент
Линкерный фрагмент в настоящем варианте осуществления имеет следующую химическую структуру и состоит из пяти звеньев, включая в себя малеимидное звено (Mal), оксиэтиленовое звено (PEG), звено в виде пропионовой кислоты (PA), аминокислотное звено (Val-Cit) и саморасщепляющееся звено (pAB: п-аминобензилоксикарбонил), начиная от стороны, смежной с фрагментом, представляющим собой антитело.
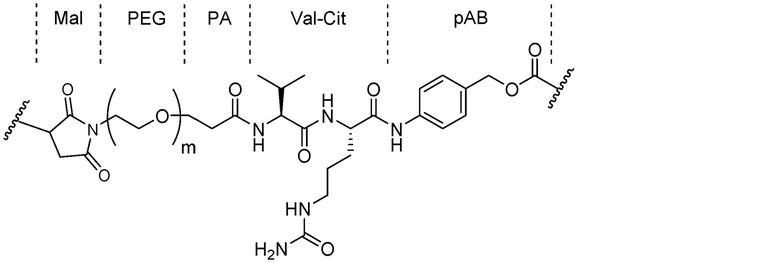
[0078] Линкерный фрагмент является стабильным вне клетки в достаточной степени, чтобы быть терапевтически эффективным. В некоторых вариантах осуществления линкерный фрагмент является стабильным вне клетки в достаточной степени, так что ADC остается интактным, когда он находится во внеклеточных условиях (например, до транспорта или доставки в клетку). Термин "интактный", применяемый в контексте ADC, означает, что фрагмент, представляющий собой антитело, остается присоединенным к эрибулину. Применяемый в данном документе термин "стабильный" в контексте ADC означает, что 20% или меньше, приблизительно 15% или меньше, приблизительно 10% или меньше, приблизительно 5% или меньше, приблизительно 3% или меньше или приблизительно 1% или меньше линкеров (или любой процент в пределах приведенных значений) в образце ADC является расщепленным (или, в случае всего ADC, не является интактным иным образом), если ADC находится во внеклеточных условиях.
[0079] Является ли линкерный фрагмент стабильным вне клетки, можно определить, например, путем помещения ADC в плазму крови на предварительно заданный период времени (например, 2, 4, 6, 8, 16 или 24 часа) и затем количественного определения количества свободного фрагмента лекарственного средства, присутствующего в плазме крови. Стабильность может обеспечивать для ADC время для локализации опухолевых клеток для целенаправленного воздействия и предотвращать преждевременное высвобождение лекарственного средства, что может снижать терапевтический индекс ADC при неизбирательном повреждении как нормальных, так и опухолевых тканей. Линкерный фрагмент, является стабильным за пределами клетки-мишени и обеспечивает высвобождение эрибулина из ADC внутри клетки таким образом, что эрибулин может связываться с его мишенью (например, с микротрубочками). Таким образом, линкерный фрагмент согласно настоящему варианту осуществления: (i) поддерживает свойства специфического связывания фрагмента, представляющего собой антитело; (ii) обеспечивает доставку, например внутриклеточную доставку, эрибулина за счет стабильного связывания с фрагментом, представляющим собой антитело; (iii) сохраняет стабильность и интактность до тех пор, пока ADC не будет транспортирован или доставлен к своему сайту-мишени; и (iv) обеспечивает терапевтический эффект, например цитотоксический эффект, эрибулина после расщепления.
[0080] Линкер может расщепляться во внутриклеточных условиях таким образом, что расщепление линкера достаточным образом высвобождает эрибулин из фрагмента, представляющего собой антитело, во внутриклеточной среде, чтобы активировать эрибулин и/или сделать лекарственное средство терапевтически эффективным. В некоторых вариантах осуществления эрибулин не отщепляется от фрагмента, представляющего собой антитело, до тех пор, пока ADC не попадет в клетку, которая экспрессирует антиген, специфический для фрагмента ADC, представляющего собой антитело, и эрибулин отщепляется от фрагмента, представляющего собой антитело, после попадания в клетку. В некоторых вариантах осуществления линкер содержит расщепляемый фрагмент, который расположен таким образом, что ни одна из частей линкера или фрагмента, представляющего собой антитело, не остается связанной с эрибулином после расщепления.
[0081] Линкерный фрагмент содержит аминокислотное звено валин-цитруллин (Val-Cit). Аминокислотное звено валин-цитруллин (Val-Cit) является расщепляемым под действием расщепляющего средства (например, внутриклеточного фермента пептидазы или протеазы), которое присутствует во внутриклеточной среде (например, в пределах лизосомы, или эндосомы, или кавеолы). Пептидаза, такая как катепсин (например, катепсин B, C, F, H, K, L, O, S, V, X или W), может расщеплять последовательность валин-цитруллин (Val-Cit) или последовательность аланин-аланин-аспарагин (Ala-Ala-Asn) (см., например, Dubowchik (2002) Bioconjugate Chem. 13: 855-69). Линкерный фрагмент расщепляется ферментом в клетке-мишени таким образом, что ADC разделяется на часть, представляющую собой антитело, и на часть, представляющую собой эрибулин. ADC, который содержит Val-Cit, обеспечивает повышенную стабильность, снижение нецелевого цитолиза, усиление целевого цитолиза, более низкие уровни агрегации и/или более высокое содержание лекарственного вещества по сравнению с ADC, который содержит альтернативное аминокислотное звено (например, Gly-Gly).
[0082] Цитруллин и эрибулин соединены с помощью п-аминобензилоксикарбонила (pAB). В частности, аминогруппа п-аминобензилоксикарбонила образует амидную связь с цитруллином, а карбонильная группа ковалентно связывается с первичным амином (C-35 амин) в составе эрибулина. П-аминобензилоксикарбонил является саморасщепляющимся. Не ограничиваясь теорией, считается, что саморасщепление pAB включает в себя самопроизвольную реакцию 1,6-элиминирования (Jain et al. (2015) Pharm. Res. 32:3526-40). В случаях, когда линкерный фрагмент (например, Val-Cit) в ADC расщепляется в клетке-мишени, из-за саморасщепления саморасщепляющегося звена (pAB) немодифицированный эрибулин может высвобождаться без избыточных функциональных групп остающихся в фрагменте, представляющем собой эрибулин.
[0083] Саморасщепляющиеся химические структуры известны из уровня техники и могут быть легко выбраны для ADC в соответствии с настоящим изобретением. В различных вариантах осуществления спейсерное звено, связывающее расщепляемый фрагмент в линкере к фрагменту, представляющему собой лекарственное средство (например, эрибулин), является саморасщепляющимся и подвергается саморасщеплению одновременно с или непосредственно до/после расщепления расщепляемого фрагмента во внутриклеточных условиях.
[0084] С другой стороны, малеимидное звено (Mal), оксиэтиленовое звено (PEG) и звено в виде пропионовой кислоты (PA) расположены между валином и антителом Ab. α,β-ненасыщенный карбонил в малеимиде является реакционноспособным в отношении остатка цистеина (в частности, сульфгидрильной группы (-SH)) в антителе и влияет на способность связываться линкерного фрагмента и эрибулина с антителом. Линкерный фрагмент содержит малеимидное звено и связан с антителом с помощью малеимидного звена. В результате: можно дополнительно улучшить содержание лекарственного вещества в антителе (p: количество фрагментов, представляющих собой эрибулин на фрагмент, представляющий собой антитело).
[0085] Оксиэтиленовое звено (PEG) представляет собой звено, состоящее из одной или нескольких оксиэтиленовых групп, и является в значительной степени гидрофильным. Эрибулин можно применять для снижения степени, с которой эрибулин может быть выведен из резистентных раковых клеток посредством белка множественной лекарственной устойчивости (MDR) или функционально сходных транспортеров. В некоторых вариантах осуществления линкерный фрагмент представляет собой более короткий PEG-линкер и обеспечивает улучшенную стабильность и пониженную агрегацию слишком длинных PEG-линкеров. В Формуле (I) количество оксиэтиленовых групп обозначено посредством m, и m представляет собой целое число от 1 до 10. Предпочтительно m равняется 2. В случаях, когда m представляет собой целое число менее 2, длина линкерного фрагмента снижена, и может демонстрироваться более низкий уровень агрегации и/или более высокое содержание лекарственного вещества по сравнению с ADC содержащим более длинный линкерный фрагмент (например, m равняется 8).
[0086] В некоторых вариантах осуществления ADC, содержащий расщепляемый пептидный фрагмент, демонстрирует более низкие уровни агрегации, улучшенное соотношение антитело:лекарственное средство, повышенный целевой цитолиз раковых клеток, пониженный нецелевой цитолиз нераковых клеток и/или более высокое содержание лекарственного вещества (p) по сравнению с ADC, который содержит альтернативный расщепляемый фрагмент. В некоторых вариантах осуществления добавление расщепляемого фрагмента повышает цитотоксичность и/или активность относительно нерасщепляемого линкера. В некоторых вариантах осуществления может наблюдаться повышенная активность и/или цитотоксичность при раке, при котором антиген экспрессируется на умеренных уровнях, на который целенаправленно воздействует фрагмент ADC, представляющий собой антитело (например, умеренная экспрессия FRA). В некоторых вариантах осуществления расщепляемый пептидный фрагмент может расщепляться ферментом, а линкер представляет собой расщепляемый ферментом линкер. В некоторых вариантах осуществления фрагмент представляет собой катепсин, а линкер представляет собой расщепляемый катепсином линкер. В определенных вариантах осуществления расщепляемый ферментом линкер (например, расщепляемый катепсином линкер) проявляет одно или несколько улучшенных свойств, упомянутых выше, по сравнению с альтернативным механизмом расщепления.
[0087] Кроме того, линкерный фрагмент может влиять на физико-химические свойства ADC. Поскольку многие цитотоксические средства являются гидрофобными по природе, связывание их с антителом с дополнительным гидрофобным фрагментом может приводить к агрегации. Агрегаты ADC являются нерастворимыми и зачастую ограничивают достижимое содержание лекарственного вещества на антителе, что может отрицательно воздействовать на активность ADC. Белковые агрегаты биологических веществ, в целом также связывались с повышенной иммуногенностью. Линкер в соответствии с настоящим вариантом осуществления обеспечивает получение ADC с низкими уровнями агрегации и требуемыми уровнями содержания лекарственного вещества.
[0088] В различных вариантах осуществления линкер предназначен для облегчения интернализации в клетку, расщепления после интернализации в клетку и неспецифического цитолиза (цитолиза соседних клеток) посредством и диффузии линкера-эрибулина и/или эрибулина отдельно в соседние клетки. В некоторых вариантах осуществления разработан линкер для минимизации расщепления во внеклеточной среде и, таким образом, снижения токсичности в отношении нецелевой ткани (например, ткани, не являющейся раковой), при этом он сохраняет способность к связыванию ADC с тканью-мишенью и к неспецифическому цитолизу раковой ткани, которая не экспрессирует антиген, на который целенаправленно воздействует фрагмент ADC, представляющий собой антитело, но которая окружает раковую ткань-мишень, экспрессирующую данный антиген. Линкерный фрагмент в соответствии с настоящим вариантом осуществления особенно эффективен в обеспечении этих функциональных свойств, например при соединении фрагмента, представляющего собой антитело к FRA, такого как MORAb-003, и фрагмента, представляющего собой лекарственное средство, такого как эрибулин. В некоторых вариантах осуществления могут также наблюдаться по меньшей мере некоторые из этих функциональных свойств без фрагмента, представляющего собой антитело к FRA, и/или без MORAb-003. Линкерный фрагмент в соответствии с настоящим вариантом осуществления эффективен в обеспечении некоторых или всех из этих функциональных свойств, например, при соединении фрагмента, представляющего собой антитело к her2, такого как трастузумаб, и фрагмента, представляющего собой лекарственное средство, такого как эрибулин.
[0089] Было обнаружено, что ADC демонстрирует конкретную комбинацию необходимых свойств, в частности при соединении к антителу к FRA, такому как MORAb-003, или его антигенсвязывающему фрагменту. Такие свойства включают без ограничения эффективные уровни содержания лекарственного вещества (p ≥ приблизительно 4), низкие уровни агрегации, стабильность при условиях хранения или при нахождении в кровотоке в организме (например, стабильность в сыворотке крови), сохранение аффинности в отношении клеток, экспрессирующих мишень, сравнимой с аффинностью неконъюгированного антитела, сильную цитотоксичность в отношении клеток, экспрессирующих мишень, низкие уровни нецелевого цитолиза, высокие уровни неспецифического цитолиза и/или эффективную противораковую активность in vivo, причем все из вышеперечисленных - по сравнению с ADC, в которых применяются другие фрагменты, представляющие собой линкер-эрибулин и/или антитело.
[0090] 3. Эрибулин
Термин "эрибулин", применяемый в данном документе, относится к синтетическому аналогу галихондрина В, макроциклическому соединению, которое первоначально было выделено из морской губки Halichondria okadais. Эрибулин является ингибитором динамики микротрубочек, который, как считается, связывает тубулин и вызывает остановку клеточного цикла в фазе G2/M путем ингибирования сборки митотического веретена. Термин "эрибулина мезилат" относится к мезилатной соли эрибулина, которая поступает в продажу под торговым названием Halaven (товарный знак). В ADC в соответствии с настоящим вариантом осуществления, эрибулин связывается с линкером ADC посредством первичной аминогруппы эрибулина.
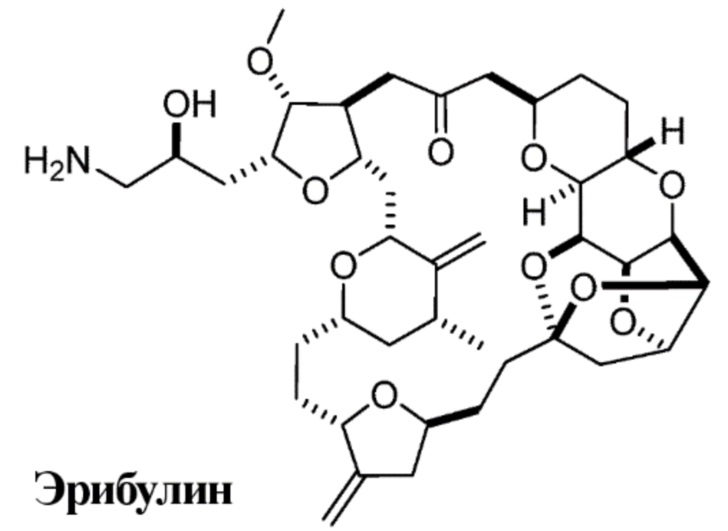
[0091] 4. Конъюгат антитело-лекарственное средство (ADC)
В ADC в соответствии с настоящим вариантом осуществления эрибулин связывается с фрагментом, представляющим собой антитело, с помощью вышеописанного линкерного фрагмента. Фрагмент, представляющий собой антитело, может представлять собой, например, антитело к FRA, антитело к мезотелину, антитело к her2, такое как трастузумаб.
[0092] ADC в соответствии с настоящим вариантом осуществления способен селективно доставлять эффективную дозу цитотоксического или цитостатического средства к раковым клеткам или к опухолевой ткани. Было обнаружено, что представленный ADC характеризуется сильной цитотоксической и/или цитостатической активностью в отношении клеток, экспрессирующих соответствующий антиген-мишень (например, FRA или her2). В некоторых вариантах осуществления цитотоксическая и/или цитостатическая активность ADC зависит от уровня экспрессии антигена-мишени в клетке. В некоторых вариантах осуществления ADC в соответствии с настоящим изобретением особенно эффективен в уничтожении раковых клеток, экспрессирующих антиген-мишень на умеренном уровне, по сравнению с раковыми клетками, экспрессирующими тот же антиген на низком уровне.
[0093] Термин "рак" относится к физиологическому состоянию у млекопитающих, при котором популяция клеток характеризуется нерегулируемым клеточным ростом. Примеры рака включают без ограничения карциному, лимфому, бластому, саркому и лейкоз. Более конкретные примеры таких видов рака включают плоскоклеточный рак, мелкоклеточный рак легкого, немелкоклеточный рак легкого, аденокарциному легкого, плоскоклеточную карциному легкого, рак брюшной полости, печеночноклеточный рак, рак желудочно-кишечного тракта, рак поджелудочной железы, глиобластому, рак шейки матки, рак яичника, рак печени, рак мочевого пузыря, гепатому, рак молочной железы (например, трижды негативный рак молочной железы), остеосаркому, меланому, рак толстой кишки, колоректальный рак, рак эндометрия (например, серозный) или рак матки, карциному слюнной железы, рак почки, рак печени, рак предстательной железы, рак вульвы, рак щитовидной железы, гепатокарциному и некоторые типы рака головы и шеи. Трижды негативный рак молочной железы относится к раку молочной железы с отсутствием экспрессии генов эстрогенового рецептора (ER), прогестеронового рецептора (PR) или Her2/neu.
[0094] Термин "опухоль" означает любую массу ткани, которая образуется в результате избыточного роста или пролиферации клеток, либо доброкачественной, либо злокачественной, включая предраковые поражения.
[0095] Термины "раковая клетка" и "опухолевая клетка" относятся к отдельным клеткам или к общей популяции клеток, происходящих из опухоли, включая как неканцерогенные клетки, так и раковые стволовые клетки. Применяемый в данном документе термин "опухолевая клетка" будет модифицирован с помощью термина "неканцерогенная", когда он относится исключительно к тем опухолевым клеткам, у которых отсутствует способность обновляться и дифференцироваться, чтобы отличать эти опухолевые клетки от раковых стволовых клеток.
[0096] Иллюстративные виды рака, при которых экспрессия FRA-происходит на высоком уровне, включают без ограничения рак яичника (например, серозный рак яичника, светлоклеточный рак яичника), карциноид легкого, трижды негативный рак молочной железы, рак эндометрия и немелкоклеточный рак легкого (например, аденокарциному). Иллюстративные виды рака, при которых экспрессия FRA-происходит на умеренном уровне, включают без ограничения рак желудка и колоректальный рак. Иллюстративные виды рака, при которых экспрессия FRA происходит на низком уровне, включают без ограничения меланому и лимфому. Иллюстративные виды рака, при которых экспрессия her2 происходит на высоком уровне, включают без ограничения рак молочной железы, рак желудка, рак пищевода, рак яичника и рак эндометрия. Иллюстративные виды рака, при которых экспрессия her2 происходит на умеренном уровне, включают без ограничения рак легкого и рак мочевого пузыря.
[0097] Используемый в данном документе термин "подавлять" или "подавление" означает уменьшение на измеряемое количество и может включать, но не обязательно, полное предотвращение или подавление.
[0098] "Эффективное количество" ADC, которое раскрыто в данном документе, представляет собой количество, достаточное для выполнения конкретно заявленной цели, например для получения терапевтического эффекта после введения, такого как снижение скорости роста опухоли или объема опухоли, уменьшение степени проявления симптома рака или некоторые другие показатели эффективности лечения. Эффективное количество можно определять традиционным образом с учетом поставленной цели. Термин "терапевтически эффективное количество" относится к количеству ADC, эффективному для лечения заболевания или нарушения у субъекта. В случае рака терапевтически эффективное количество ADC может снижать количество раковых клеток, уменьшать размер опухоли, подавлять (например, замедлять или останавливать) метастазирование опухоли, подавлять (например, замедлять или останавливать) рост опухоли и/или облегчать один или несколько симптомов. "Профилактически эффективное количество" означает количество, при необходимых дозах и в течение необходимых периодов времени эффективное в достижении требуемого профилактического результата. Как правило, поскольку профилактическую дозу используют у субъектов до проявления заболевания или на более ранней стадии заболевания, профилактически эффективное количество будет меньшим терапевтически эффективного количества.
[0099] Используемые в данном документе "лечить" или "терапевтический" и грамматически родственные термины означают любое улучшение любого последствия заболевания, такое как продление выживания, меньшая заболеваемость и/или уменьшение побочных эффектов, которые являются побочными продуктами альтернативного терапевтического способа воздействия. Из уровня техники легко понять, что полное устранение заболевания предпочтительно, хоть и не является требованием для лечебного действия. Применяемые в данном документе "лечение" или "лечить" относятся к введению описанного ADC субъекту, например пациенту. Лечение может представлять собой излечение, заживление, смягчение, ослабление, изменение, устранение, облегчение, временное ослабление, улучшение или воздействие на нарушение, симптомы нарушения или предрасположенность к нарушению, например раку.
[0100] В некоторых вариантах осуществления применяют меченый ADC. Подходящие "метки" включают радионуклиды, ферменты, субстраты, кофакторы, ингибиторы, флуоресцентные фрагменты, хемилюминесцентные фрагменты, магнитные частицы и т. п.
[0101] Под применяемым в данном документе "белком" подразумевают по меньшей мере две ковалентно связанные аминокислоты. Термин охватывает полипептиды, олигопептиды и пептиды. В некоторых вариантах осуществления две или более ковалентно связанные аминокислоты связаны посредством пептидной связи. Белок может быть составлен из встречающихся в природе аминокислот и пептидных связей, например, когда белок получают рекомбинантным образом с применением систем экспрессии и клеток-хозяев. В качестве альтернативы белок может содержать синтетические аминокислоты (например, гомофенилаланин, цитруллин, орнитин и норлейцин) или пептидомиметические структуры, т. е. "аналоги пептидов или белков", такие как пептоиды. Пептоиды представляют собой иллюстративный класс пептидомиметиков, боковые цепи которых прикреплены к атому азота пептидного остова, а не к α-атомам углерода (как они расположены в аминокислотах), и характеризуются иным расположением водородных связей и конформационными характеристиками по сравнению с пептидами (см., например, Simon et al. (1992) Proc. Natl. Acad. Sci. USA 89:9367). В связи с этим пептоиды могут быть устойчивыми к протеолизу или к другим физиологическим условиям или условиям хранения и быть эффективными при проникновении через клеточные мембраны. Такие синтетические аминокислоты можно включать, в частности, когда антитело синтезируется in vitro с помощью общепринятых способов, широко известных из уровня техники. Кроме того, может применяться любая комбинация пептидомиметических, синтетических и встречающихся в природе остатков/структур. "Аминокислота" также содержит иминокислотные остатки, такие как пролин и гидроксипролин. "R-группа" или "боковая цепь" аминокислоты могут находиться в одной из (L)- или (S)-конфигурации. В конкретном варианте осуществления аминокислоты находятся в (L)- или (S)-конфигурации.
[0102] "Рекомбинантный белок" представляет собой белок, полученный с применением рекомбинантных методик с применением любых методик и способов, известных из уровня техники, т. е. вследствие экспрессии рекомбинантной нуклеиновой кислоты. Способы и методики получения рекомбинантных белков широко известны из уровня техники.
[0103] "Выделенный" белок не сопровождается по меньшей мере некоторой частью материала, с которым он в норме ассоциирован в природном состоянии, например, составляет по меньшей мере приблизительно 5% или по меньшей мере приблизительно 50% по весу от общего белка в указанном образце. Известно, что выделенный белок может составлять от 5% до 99,9% по весу от общего содержания белка в зависимости от обстоятельств. Например, белок может продуцироваться в значительно более высокой концентрации при применении индуцибельного промотора или промотора, обеспечивающего высокий уровень экспрессии, за счет чего белок продуцируется с повышенными уровнями концентрации. Определение включает продуцирование антитела в самых разнообразных организмах и/или клетках-хозяевах, которые известны из уровня техники.
[0104] В случае аминокислотных последовательностей идентичность и/или сходство последовательности могут быть определены с применением стандартных методик, известных из уровня техники, включая без ограничения алгоритм локальной идентичности последовательностей из Smith and Waterman (1981) Adv. Appl. Math. 2:482, алгоритм выравнивания идентичности последовательностей из Needleman and Wunsch (1970) J. моль. Biol. 48:443, способ поиска подобия из Pearson и Lipman (1988) Proc. Nat. Acad. Sci. USA 85:2444, компьютеризированные реализации этих алгоритмов (GAP, BESTFIT, FASTA и TFASTA в программном пакете Wisconsin Genetics Software Package, Genetics Computer Group, 575 Science Drive, Медисон, штат Висконсин, США), программу Best Fit sequence, описанную Devereux et al. (1984) Nucl. Acid Res. 12:387-95, например, с использованием настроек по умолчанию или путем проверки. Процент идентичности можно рассчитывать со ссылкой на "Current Methods in Sequence Comparison and Analysis", Macromolecule Sequencing and Synthesis, Selected Methods and Applications, стр. 127-149 (1988), Alan R. Liss, Inc) или рассчитывают предпочтительно с помощью Fast DB на основе следующих параметров.
Штраф за несовпадение: 1
Штраф за введение гэпа: 1
Штраф за удлинение гэпа: 0,33
Штраф за соединение: 30
[0105] Примером применимого алгоритма является PILEUP. PILEUP создает выравнивание множественных последовательностей из группы родственных последовательностей с применением прогрессивных попарных выравниваний. Он также может строить дерево, показывающее кластеризующие взаимосвязи, применяемые для создания выравнивания. PILEUP использует упрощение способа прогрессивного выравнивания из Feng & Doolittle (1987) J моль Evol. Evol. 35:351-60; причем способ подобен способу, описанному в работе Higgins and Sharp (1989) CABIOS 5:151-3. Применимые параметры в PILEUP включают штраф за введение гэпа по умолчанию - 3,00, штраф за удлинение гэпа по умолчанию - 0,10 и оцениваемые концевые гэпы.
[0106] Другим примером применимого алгоритма является алгоритм BLAST, описанный в Altschul et al. (1990) J. Mol. Biol. 215:403-10; Altschul et al. (1997) Остатки нуклеиновых кислот. 25:3389-402 и Karin et al. (1993) Proc. Natl. Acad. Sci. USA 90:5873-87. Особенно применимой программой BLAST является программа WU-BLAST-2, которую получили из Altschul et al. (1996) Methods in Enzymology 266:460-80. WU-BLAST-2 применяет несколько параметров поиска, большинство из которых установлены как значения по умолчанию. Регулируемые параметры установлены на следующие значения: длина перекрывания=l, доля перекрывания=0,125, пороговая длина слова (T)=II. Параметры HSP S и HSP S2 представляют собой динамические значения и устанавливаются программой самостоятельно в зависимости от состава специфический последовательности и состава специфический базы данных, относительно которой производится поиск представляющей интерес последовательности; однако значения можно корректировать для повышения чувствительности.
[0107] Дополнительным применимым алгоритмом является BLAST с введением гэпов, сообщаемый в работе Altschul et al. (1993) Nucl. Acid Res. 25:3389-402. BLAST с введением гэпов применяет матрицу замен BLOSUM-62; пороговый параметр T, установленный на 9; метод "двух совпадений" для запуска продлений без гэпов, штраф за удлинение гэпов на k составляет 10+k; Xu установлен на 16, и Xg установлен на 40 для стадии поиска в базе данных и на 67 для стадии вывода результатов алгоритмов. Выравнивания с введением гэпов запускаются при показателе, соответствующем приблизительно 22 битам.
[0108] Обычно гомология аминокислот, сходство или идентичность между белками, раскрытыми в данном документе, и их вариантами, включая варианты FRA, варианты her2, варианты последовательностей тубулина и варианты вариабельных доменов антител (включая отдельные варианты CDR), составляет по меньшей мере 80% с последовательностями, изображенными в данном документе, и, что более типично, предусматривается предпочтительно возрастающая гомология или идентичность по меньшей мере 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% и почти 100% или 100%.
[0109] Аналогичным образом, "процент (%) идентичности последовательности нуклеиновой кислоты" в отношении последовательности нуклеиновой кислоты антител и других белков, идентифицированных в данном документе, определяется как процент нуклеотидных остатков в кандидатной последовательности, которые идентичны нуклеотидным остаткам в кодирующей последовательности антигенсвязывающего белка. В специфическом способе используется модуль BLASTN из WU-BLAST-2, установленный на параметры по умолчанию, при этом длина перекрывания и доля перекрывания установлены на 1 и 0,125 соответственно.
[0110] Поскольку сайт или область введения вариации аминокислотной последовательности предварительно определены, то мутацию саму по себе не нужно предварительно определять. Например, чтобы оптимизировать свойства мутации в заданном сайте, в кодоне- или области-мишени можно выполнять случайный мутагенез, а экспрессированные варианты CDR антигенсвязывающих белков подвергать скринингу в отношении оптимальной комбинации требуемой активности. Широко известны методики получения мутаций, представляющих собой замены в предварительно определенных сайтах в ДНК с известной последовательностью, например мутагенез с праймером MI3 и ПЦР-мутагенез.
[0111] Далее в данном документе будет описан способ получения ADC, представленного Формулой (I), в соответствии с вариантом осуществления настоящего изобретения.
[0112] Вариант осуществления настоящего изобретения относится к способу получения конъюгата антитело-лекарственное средство (ADC), представленного Формулой (I), и включает следующие стадии 1 и 2.
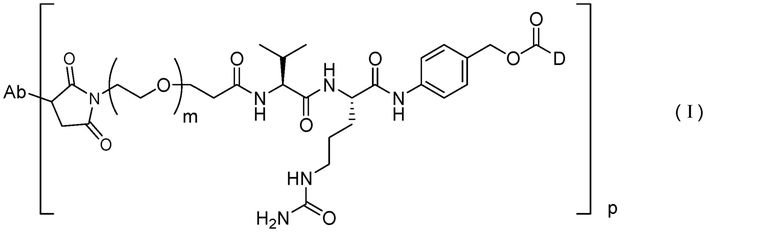
[причем в Формуле:
Ab представляет собой антитело или его антигенсвязывающий фрагмент,
D представляет собой эрибулин,
m представляет собой целое число от 1 до 10, и
p представляет собой целое число от 1 до 8]
Стадия 1: стадия получения соединения, представленного Формулой (B), путем осуществления реакции эрибулина или его соли с соединением, представленным Формулой (A),
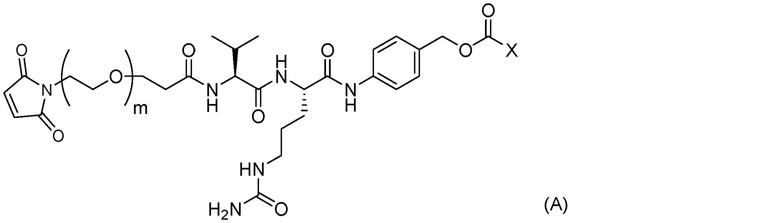
[причем в Формуле: m представляет собой целое число от 1 до 10, и X представляет собой феноксигруппу или нитрофеноксигруппу.]
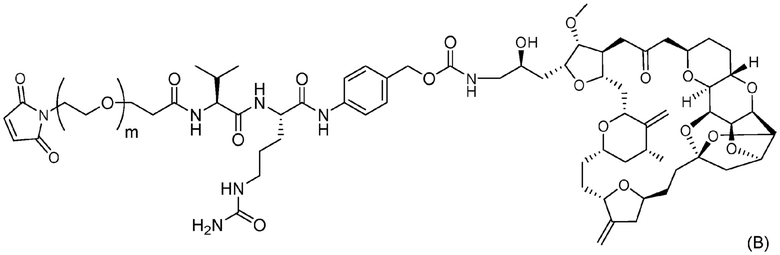
[причем в Формуле: m представляет собой целое число от 1 до 10]
Стадия 2: стадия получения конъюгата антитело-лекарственное средство, представленного Формулой (I), путем осуществления реакции соединения, представленного Формулой (B), с Ab.
[0113] Стадия 1 представляет собой стадию получения соединения, представленного Формулой (B), путем осуществления реакции эрибулина или его соли с соединением, представленным Формулой (A).
[0114] Эрибулин может представлять собой как свободную Форму эрибулина, так и соль эрибулина. Примеры соли эрибулина включают в себя эрибулин мезилат. Количество применяемого эрибулина или его соли может составлять от 1 до 1000 г или может составлять от 10 до 300 г в пересчете на свободную Форму эрибулина.
[0115] Соединение, представленное Формулой (A), представляет собой соединение, соответствующее линкерному фрагменту, в ADC, является реакционно-способным в отношении антитела в терминальной малеимидной структуре и является реакционноспособным в отношении эрибулина в терминале X на противоположной стороне. X представляет собой феноксигруппу или нитрофеноксигруппу. Нитрофеноксигруппа может представлять собой любую из о-нитрофеноксигруппы, м-нитрофеноксигруппы и п-нитрофеноксигруппы. В случаях, когда X представляет собой феноксигруппу или нитрофеноксигруппу, X является реакционноспособным в отношении первичной аминогруппы на конце эрибулина. Соединение, представленное Формулой (A), может быть получено с помощью способа, приведенного ниже.
[0116] Количество применяемого соединения, представленного Формулой (A), может составлять от 0,5 до 2,0 моль, от 0,6 до 3,0 моль, от 1,0 до 2,0 моль или от 1,3 до 1,8 моль на 1 моль эрибулина.
[0117] На стадии 1 может применяться основание. Основание не ограничено, при условии, что оно не ингибирует реакцию эрибулина и соединения, представленного Формулой (A), при этом примеры основания включают третичный амин, такой как триэтиламин или N,N-диизопропилэтиламин, и азотсодержащее ароматическое соединение, такое как пиридин или 2,6-лутидин. Количество применяемого основания может составлять от 0,5 до 3,0 моль, от 1,0 до 2,0 моль или от 1,1 до 1,5 моль на 1 моль эрибулина.
[0118] Стадию 1 можно выполнять при отсутствии растворителя или в растворителе, и предпочтительно ее осуществляют в растворителе. Растворитель не ограничен, при условии, что он не ингибирует реакцию эрибулина и соединения, представленного Формулой (A), при этом примеры растворителя включают N,N-диметилформамид (DMF), диметилсульфоксид (DMSO), N-метилпирролидон (NMP) и пиридин. Количество применяемого растворителя может составлять от 5 до 20 мл или от 6 до 15 мл на 1 г эрибулина.
[0119] Температура реакции на стадии 1 не ограничена, при условии, что это температура, при которой протекает реакция эрибулина и соединения, представленного Формулой (A). Температура реакции может представлять собой комнатную температуру или составлять от 20°C до 25°C.
[0120] Для ускорения реакции на стадии 1 может применяться ускоритель, такой как 4-диметиламинопиридин. Количество применяемого ускорителя может составлять от 0,01 до 0,8 г или от 0,1 до 0,3 г на 1 моль эрибулина.
[0121] Далее в данном документе будет описан пример способа очистки. Однако способ очистки не ограничен данным примером, и очистку можно выполнять с применением известного в химии способа. После завершения реакции со стадии 1 реакционную смесь можно очищать на колонке с обращенной фазой. Колонка с обращенной фазой представляет собой, например, колонку, в которой силикагель с октадецильной группой (C18) применяют как наполнитель. Реакционную смесь помещают на верхнюю часть колонки с обращенной фазой и экстрагируют полярным растворителем, таким как ацетонитрил или вода. Необязательно предпочтительно, что уксусную кислоту или подобную применяют так, чтобы pH экстрагируемого растворителя был кислым. Метиленхлорид добавляют к полученному экстракту и полученное соединение, представленное Формулой (B), переносят в метиленхлоридный слой (органический слой). В ходе экстракции необязательно pH можно корректировать водным раствором бикарбоната натрия. Полученный органический слой может быть нейтрализован с помощью остаточной кислоты, такой как водный раствор бикарбоната натрия. Полученный органический слой концентрируют при пониженном давлении для растворения остатка в метиленхлориде, метаноле, или подобном и раствор добавляют по каплям в пентан. В результате соединение, представленное Формулой (B), осаждается. Полученное твердое вещество промывают пентаном и высушивают при пониженном давлении. В результате получают необходимое соединение.
[0122] Стадия 2 представляет собой стадию получения конъюгата антитело-лекарственное средство, представленного Формулой (I), путем осуществления реакции соединения, представленного Формулой (B), с Ab. Цистеиновый остаток в фрагменте, представляющем собой антитело (Ab), подвергается сопряженному присоединению по Михаэлю с малеимидной структурой в соединении, представленном Формулой (B), с образованием между ними ковалентной связи. Множество соединений, представленных Формулой (B), могут связываться с одним фрагментом, представляющим собой антитело Ab. Число образованных связей соответствует p в Формуле (A).
[0123] Количество применяемого соединения, представленного Формулой (B), может составлять от 1,0 до 8,0 моль или от 3,0 до 5,0 моль на фрагмент, представляющий собой антитело Ab.
[0124] Как правило, стадию 2 проводят в буферном растворе. Буферный раствор не ограничен, при условии, что он не модифицирует подлежащее применению антитело Ab и не ингибирует связывание с соединением, представленным Формулой (B). Буферный раствор может представлять собой фосфатный буферный раствор, боратный буферный раствор, буферный раствор, содержащий трис(гидроксиметил)аминометан, буферный раствор, содержащий этилендиаминтетрауксусную кислоту, или любую их комбинацию. pH буферного раствора предпочтительно составляет от 6,0 до 8,0 и более предпочтительно от 6,5 до 7,5.
[0125] На стадии 2 в буферный раствор может быть добавлен полярный органический растворитель. Полярный органический растворитель не ограничен, при условии, что он может быть смешан с буферным раствором, и способен увеличить растворимость соединения, представленного Формулой (B). Например, раствор, в котором соединение, представленное Формулой (B), растворено в полярном органическом растворителе, может быть добавлен к буферному раствору, в котором растворено антитело Ab.
[0126] Примеры полярного органического растворителя включают N,N-диметилформамид, N,N-диметилацетамид и диметилсульфоксид. Количество применяемого органического растворителя может составлять от 60 до 300 мл, от 110 до 240 мл, от 130 до 210 мл, или от 140 до 180 мл на 1 мг соединения, представленного Формулой (B).
[0127] Температура реакции на стадии 2 не ограничена, при условии, что это температура, при которой протекает реакция соединения, представленного Формулой (B), и антитела Ab. Температура реакции может представлять собой комнатную температуру или составлять от 20°C до 25°C.
[0128] Более конкретно температура реакции является следующей. Во-первых, антитело Ab фильтруют сквозь фильтр (проницаемая мембрана) и растворяют путем добавления к нему буферного раствора. Путем добавления TCEP-HCl (трис(2-карбоксиэтил)фосфингидрохлорид) к полученному раствору для частичного восстановления в молекуле антитела расщепляется дисульфидная связь с образованием сульфгидрильной группы. Затем добавляют соединение, представленное Формулой (B), или раствор, в котором соединение, представленное Формулой (B), растворяют в полярном органическом растворителе так, что соединение, представленное Формулой (B), и антитело связываются друг с другом. После завершения реакции 2, например, можно добавить N-ацетилцистеин. N-ацетилцистеин вызывает реакцию с оставшимся соединением, представленным Формулой (B), и также вызывает реакцию с сульфгидрильной группой, образованной частичным восстановлением.
[0129] Далее в данном документе будет описан пример способа очистки. Однако способ очистки не ограничен данным примером, и очистку можно выполнять с применением известного в химии способа. После завершения реакции буферный раствор в реакционном растворе заменяют другим буферным раствором с применением фильтрации с тангенциальным потоком (TFF). Затем добавляют водный раствор лимонной кислоты, фильтруют сквозь фильтр и очищают буферным раствором.
[0130] В данном документе будет описан способ получения соединения, представленного Формулой (A). Соединение, представленное Формулой (A), можно получить, например, из соединения, представленного Формулой (1), и соединения, представленного Формулой (2), за две стадии, как показано ниже.
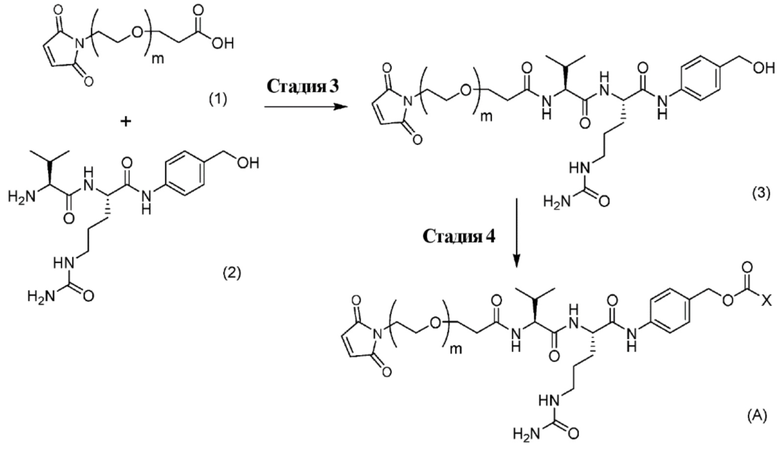
[0131] Стадия 3 представляет собой стадию активации карбоксигруппы соединения, представленного Формулой (1), и конденсирования соединения, представленного Формулой (1), с соединением, представленным Формулой (2). Соединение, представленное Формулой (3), получают путем конденсации соединения, представленного Формулой (1), и соединения, представленного Формулой (2).
[0132] Соединение, представленное Формулой (1), доступно в Tokyo Chemical Industry Co., Ltd. под торговым названием "Mal-PEG2-acid" (код по каталогу: M3203). Кроме того, соединение, представленное Формулой (1), может быть получено известным в органической химии способом с применением трет-бутилакрилата и т.п. с полиэтиленгликолем соответствующей длины в качестве исходного материала.
[0133] Количество применяемого соединения, представленного Формулой (1), может составлять от 1,0 до 1,5 моль или от 1,1 до 2,0 моль на 1 моль соединения, представленного Формулой (2).
[0134] Соединение, представленное Формулой (2), доступно от Tokyo Chemical Industry Co., Ltd. под торговым названием "Fmoc-Val-Cit-PAB-OH" (код по каталогу: F1223). Кроме того, соединение, представленное Формулой (2), может быть получено известным в органической химии способом с применением N-Fmoc-цитруллина, п-аминобензилового спирта и N-Fmoc-валина. "Fmoc" представляет собой защитную группу для аминогруппы и представляет собой 9-флуоренилметилоксикарбонильную группу.
[0135] Предпочтительно, чтобы стадию 3 проводили в присутствии конденсирующего средства. Конденсирующее средство не ограничено, при условии, что оно ускоряет реакцию конденсации карбоновой кислоты и первичного амина, и примеры конденсирующего средства включают дициклогексилкарбодиимид (DCC), 1-(3-диметиламинопропил)-3-этилкарбодиимид и 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилморфолиниум хлорид (DMT-MM).
[0136] Количество применяемого конденсирующего средства может составлять от 1,0 до 2,0 моль или от 1,3 до 1,5 моль на 1 моль соединения, представленного Формулой (1).
[0137] На стадии 3 может применяться основание. Основание не ограничено, при условии, что оно не ингибирует реакцию соединения, представленного Формулой (1), и соединения, представленного Формулой (2), и примеры основания включают третичный амин, такой как триэтиламин или N,N-диизопропилэтиламин, и азотсодержащее ароматическое соединение, такое как пиридин или 2,6-лутидин. Количество применяемого основания может быть от 0,5 до 2,0 моль, от 1,0 до 1,5 моль или от 1,1 до 1,3 моль на 1 моль соединения, представленного Формулой (1).
[0138] Стадию 3 можно выполнять при отсутствии растворителя или в растворителе, и предпочтительно ее осуществляют в растворителе. Растворитель не ограничен, при условии, что он не ингибирует реакцию соединения, представленного Формулой (1), и соединения, представленного Формулой (2), и примеры растворителя включают N,N-диметилформамид (DMF), тетрагидрофуран (THF), метанол (MeOH) и смешанный из них растворитель. Количество применяемого растворителя может составлять от 10 до 40 мл или от 20 до 30 мл на 1 г соединения, представленного Формулой (1).
[0139] Температура реакции на стадии 3 не ограничена, при условии, что это температура, при которой протекает реакция соединения, представленного Формулой (1), и соединения, представленного Формулой (2). Температура реакции может представлять собой комнатную температуру или составлять от 15°C до 35°C.
[0140] Стадия 4 представляет собой стадию получения соединения, представленного Формулой (A), путем ацилирования гидроксильной группы в соединении, представленном Формулой (3), с применением ацилирующего средства.
[0141] Количество применяемого соединения, представленного Формулой (3), может быть соответствующим образом выбрано в зависимости от реакции. Например, количество применяемого соединения, представленного Формулой (3), может составлять от 10 до 500 г или от 100 до 300 г.
[0142] Примеры ацилирующего средства включают дифенилкарбонат, бис(4-нитрофенил)карбонат, бис(2-нитрофенил)карбонат, бис(3-нитрофенил)карбонат, фенилхлорформиат, 4-нитрофенилхлорформиат, 2-нитрофенилхлорформиат и 3-нитрофенилхлорформиат. Часть ацилирующего средства соответствует X в Формуле (A) и вид ацилирующего средства может быть выбран в зависимости от выбора требуемой X-группы.
[0143] Количество применяемого ацилирующего средства может составлять от 1,0 до 5,0 моль или от 2,0 до 4,0 моль на 1 моль соединения, представленного Формулой (3).
[0144] Стадию 4 можно выполнять при отсутствии растворителя или в растворителе, и предпочтительно ее осуществляют в растворителе. Растворитель не ограничен, при условии, что он не ингибирует реакцию ацилирования соединения, представленного Формулой (3), и примеры растворителя включают N,N-диметилформамид (DMF), N,N-диметилацетамид, толуол, диметилсульфоксид (DMSO) и N,N-диметилацетамид (DMA). Количество применяемого растворителя может составлять от 5 до 20 мл или от 6 до 15 мл на 1 г соединения, представленного Формулой (3).
[0145] Температура реакции на стадии 4 не ограничена при условии, что это температура, при которой протекает реакция ацилирования соединения, представленного Формулой (3). Температура реакции может представлять собой комнатную температуру или составлять от 20°C до 25°C.
Примеры
[0146] Далее в данном документе настоящее изобретение будет подробно описано с помощью примеров получения и сравнительных примеров получения.
Аббревиатуры, используемые в примерах, используются так же, как они описаны в уровне техники, и они, например, представлены далее.
DIPEA: N,N-диизопропилэтиламин
DMA: N,N-диметилацетамид
DMF: N,N-диметилформамид
DMT-MM: 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилморфолиния хлорид
EDTA: этилендиаминтетрауксусная кислота
THF: тетрагидрофуран
[0147] <Пример получения 1>
(11S,14S)-14-[3-(Карбамоиламино)пропил]-1-(2,5-диоксо-2,5-дигидро-1H-пиррол-1-ил)-N-[4-(гидроксиметил)фенил]-9,12-диоксо-11-(пропан-2-ил)-3,6-диокса-10,13-диазапентадекан-15-амид
[0148] Смесь (2S)-2-{[(2S)-2-амино-3-метилбутаноил]амино}-5-(карбамоиламино)-N-[4-(гидроксиметил)фенил]пентанамида (184 г), 3-{2-[2-(2,5-диоксо-2,5-дигидро-1H-пиррол-1-ил)этокси]этокси}пропановой кислоты (150 г), DMT-MM (174 г), метанола (2,76 л) и THF (2,76 л) перемешивали в атмосфере азота при температуре от 15°C до 35°C в течение 24 часов. Реакционную смесь концентрировали при пониженном давлении, и к ней добавляли ацетонитрил. Осажденный осадок фильтровали и дополнительно промывали ацетонитрилом. Полученное твердое вещество смешивали с ацетонитрилом и фильтровали с получением твердого вещества. Полученное твердое вещество высушивали при пониженном давлении с получением указанного в заголовке соединения (267 г, выход 89%).
[0149] <Пример получения 2>
(4-{[(11S,14S)-14-[3-(Карбамоиламино)пропил]-1-(2,5-диоксо-2,5-дигидро-1H-пиррол-1-ил)-9,12,15-триоксо-11-(пропан-2-ил)-3,6-диокса-10,13-диазапентадекан-15-ил]амино}фенил)метил=4-нитрофенил=карбонат
[0150] Смесь указанного в примерах получения соединения 1 (250 г), бис(4-нитрофенил)карбоната (615 г), DIPEA (157 г) и DMF (5,0 л) перемешивали в атмосфере азота при температуре от 15°C до 35°C в течение 3 часов. Реакционную смесь концентрировали при пониженном давлении и очищали на силикагелевой колонке (метиленхлорид/ацетон) и фракцию, включая указанное в заголовке соединение, концентрировали при пониженном давлении. В результате указанное в заголовке соединение (162 г, выход 51%) получали в виде твердого вещества.
[0151] <Пример получения 3>
(4-{[(11S,14S)-14-[3-(Карбамоиламино)пропил]-1-(2,5-диоксо-2,5-дигидро-1H-пиррол-1-ил)-9,12,15-триоксо-11-(пропан-2-ил)-3,6-диокса-10,13-диазапентадекан-15-ил]амино}фенил)метил={(2S)-2-гидрокси-3-[(2R,3R,3aS,7R,8aS,9S,10aR,11S,12R,13aR,13bS,15S,18S,21S,24S,26R,28R,29aS)-3-метокси-26-метил-20,27-диметилиденгексакозагидро-11,15:18,21:24,28-триэпокси-7,9-этано-12,15-метано-9H,15H-фуро[3,2-i]фуро[2',3':5,6]пирано[4,3-b][1,4]диоксациклопентакозин-5(4H)-он-2-ил]пропил}карбамат
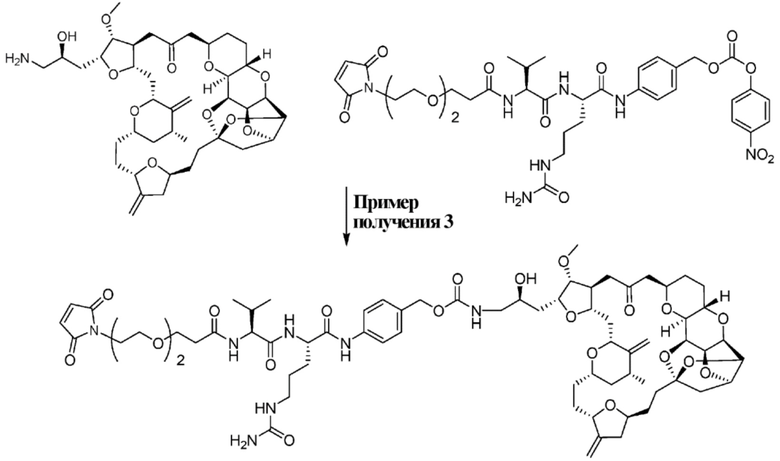
[0152] Смесь эрибулина мезилата (93 г), DIPEA (26 мл), соединения, полученного в примере получения 2 (116 г), и DMF (930 мл) перемешивали в атмосфере азота при температуре от 20°C до 25°C в течение 20 часов. Реакционную смесь очищали на колонке с обращенной фазой (торговое название; Kromasil C18) (ацетонитрил/вода/уксусная кислота), и фракцию, включая указанное в заголовке соединение, экстрагировали с метиленхлоридом. Затем органический слой промывали водным раствором бикарбоната натрия и водой и затем концентрировали при пониженном давлении. Концентрированный остаток растворяли в смешанном растворителе из метиленхлорида, метанола и уксусной кислоты и раствор добавляли по каплям в пентан. Осажденный осадок фильтровали и полученное твердое вещество промывали пентаном и высушивали при пониженном давлении. В результате получали указанное в заголовке соединение (109,6 г, выход 71%).
1H-ЯМР (400 МГц, CD3OD): δ (ppm) 7,59 (d, J=8,4 Гц, 2H), 7,31 (d, J=8,4 Гц, 2H), 6,81 (s, 2H), 5,13 (s, 1H), 5,06 (d, J=12,4 Гц, 1H), 5,02 (s, 1H), 5,01 (d, J=12,4 Гц, 1H), 4,87 (s, 1H), 4,82 (s, 1H), 4,71 (t, J=4,0 Гц, 1H), 4,61 (t, J=4,4 Гц, 1H), 4,50 (dd, J=5,2, 9,2 Гц, 1H), 4,47 (d, J=10,8 Гц, 1H), 4,32-4,27 (m, 2H), 4,19 (dd, J=6,8, 11,6 Гц, 1H), 4,13-4,07 (m, 2H), 3,98 (t, J=10,4 Гц,1H), 3,88-3,82 (m, 3H), 3,76-3,64 (m, 6H), 3,62-3,51 (m, 6H), 3,38 (s, 3H), 3,22-3,08 (m, 4H), 2,93 (dd, J=2,4, 9,6 Гц, 1H), 2,92-2,84 (m, 1H), 2,76-2,63 (m, 2H), 2,52 (t, J=6,0 Гц, 2H), 2,44-2,29 (m, 5H), 2,21-1,97 (m, 8H), 1,93-1,83 (m, 3H), 1,80-1,66 (m, 5H), 1,66-1,28 (m, 10H), 1,11 (d, J=6,4 Гц, 3H), 1,07-1,01 (m, 1H), 0,99 (d, J=6,8 Гц, 3H), 0,97 (d, J=6,4 Гц, 3H).
LCMS (M+H): масса/заряд 1374,9
[0153] <Сравнительный пример получения 1>
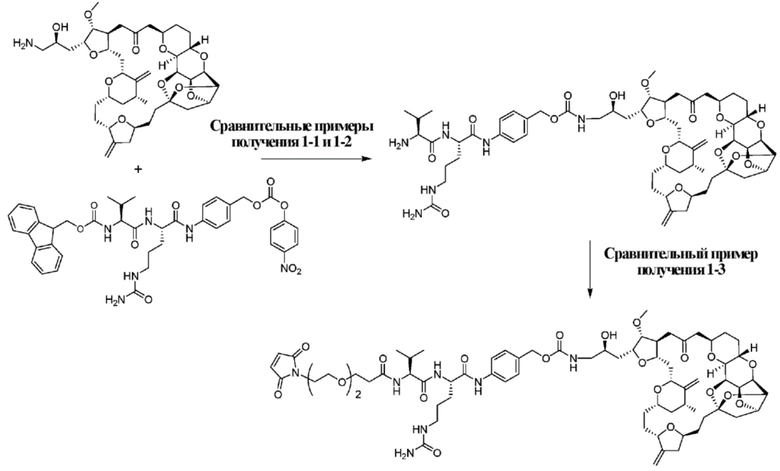
[0154] <Сравнительный пример получения 1-1>
4-{[(2S)-5-(Карбамоиламино)-2-{[(2S)-2-{[(9H-флуорен-9-илметокси)карбонил]амино}3-метилбутаноил]амино}пентаноил]амино}бензил={(2S)-2-гидрокси-3-[(2R,3R,3aS,7R,8aS,9S,10aR,11S,12R,13aR,13bS,15S,18S,21S,24S,26R,28R,29aS)-3-метокси-26-метил-20,27-диметилиденгексакосагидро-11,15:18,21:24,28-триэпокси-7,9-этано-12,15-метано-9H,15H-фуро[3,2-i]фуро[2',3':5,6]пирано[4,3-b][1,4]диоксациклопентакозин-5(4H)-он-2-ил]пропил}карбамат
[0155] Смесь эрибулина мезилата (93 г), DIPEA (25 мл), 4-{[(2S)-5-(карбамоиламино)-2-{[(2S)-2-{[(9H-флуорен-9-илметокси)карбонил]амино}3-метилбутаноил]амино}пентаноил]амино}бензил=4-нитрофенилкарбоната (103,6 г) и DMF (930 мл) перемешивали в атмосфере азота при температуре от 20°C до 25°C в течение 16 часов.
[0156] <Сравнительный пример получения 1-2>
4-{[(2S)-2-{[(2S)-2-Амино-3-метилбутаноил]амино}-5-(карбамоиламино)пентаноил]амино}бензил={(2S)-2-гидрокси-3-[(2R,3R,3aS,7R,8aS,9S,10aR,11S,12R,13aR,13bS,15S,18S,21S,24S,26R,28R,29aS)-3-метокси-26-метил-20,27-диметилиденгексакозагидро-11,15:18,21:24,28-триэпокси-7,9-этано-12,15-метано-9H,15H-фуро[3,2-i]фуро[2',3':5,6]пирано[4,3-b][1,4]диоксациклопентакосин-5(4H)-он-2-ил]пропил}карбамат
[0157] Диэтиламин (234 мл) добавляли в реакционную смесь и ее перемешивали при температуре от 20°C до 25°C в течение 0,5 часа. Этилацетат и хлористоводородную кислоту добавляли в реакционную смесь и водный слой промывали гептаном. Метилтетрагидрофуран и водный раствор карбоната калия, хлорида натрия добавляли в водный слой, и органический слой промывали водным раствором хлорида натрия. Органический слой высушивали сульфатом магния и концентрировали при пониженном давлении.
1H-ЯМР (400 МГц, CD3OD): δ (ppm) 7,56 (d, J=8,4 Гц, 2H), 7,32 (d, J=8,4 Гц, 2H), 5,14 (s, 1H), 5,06 (d, J=12,4 Гц, 1H), 5,03 (s, 1H), 5,01 (d, J=12,4 Гц, 1H), 4,87 (s, 1H), 4,83 (s, 1H), 4,71 (t, J=4,4 Гц, 1H), 4,62 (t, J=4,4 Гц, 1H), 4,57 (dd, J=4,8, 8,8 Гц, 1H), 4,47 (d, J=10,8 Гц, 1H), 4,32-4,27 (m, 2H), 4,18 (dd, J=4,8, 6,4 Гц, 1H), 4,13-4,07 (m, 2H), 3,98 (t, J=10,4 Гц, 1H), 3,88-3,82 (m, 3H), 3,76-3,70 (m, 4H), 3,60 (d, J=6,0 Гц, 1H), 3,38 (s, 3H), 3,26-3,10 (m, 3H), 2,93 (dd, J =2,0, 11,2 Гц, 1H), 2,91-2,84 (m, 1H), 2,75-2,64 (m, 2H), 2,44-2,29 (m, 5H), 2,21-1,97 (m, 8H), 1,93-1,83 (m, 3H), 1,79-1,72 (m, 5H), 1,68-1,29 (m, 8H), 1,11 (d, J=6,8 Гц, 3H), 1,07-1,01 (m, 1H), 1,06 (d, J=7,2 Гц, 3H), 1,02 (d, J=7,2 Гц, 3H)
LCMS (M+H): масса/заряд 1135,7
[0158] <Сравнительный Пример получения 1-3>
(4-{[(11S,14S)-14-[3-(Карбамоиламино)пропил]-1-(2,5-диоксо-2,5-дигидро-1H-пиррол-1-ил)-9,12,15-триоксо-11-(пропан-2-ил)-3,6-диокса-10,13-диазапентадекан-15-ил]амино}фенил)метил={(2S)-2-гидрокси-3-[(2R,3R,3aS,7R,8aS,9S,10aR,11S,12R,13aR,13bS,15S,18S,21S,24S,26R,28R,29aS)-3-метокси-26-метил-20,27-диметилиденгексакозагидро-11,15:18,21:24,28-триэпокси-7,9-этано-12,15-метано-9H,15H-фуро[3,2-i]фуро[2',3':5,6]пирано[4,3-b][1,4]диоксациклопентакозин-5(4H)-он-2-ил]пропил}карбамат
[0159] 41-[2-(2-{3-[(2,5-Диоксопирролидин-1-ил)окси]-3-оксопропокси}этокси)этил]-1H-пиррол-2,5-дион (47,9 г), DIPEA (20 мл) и DMF (913 мл) добавляли в концентрированный остаток, полученный в сравнительном примере получения 1-2 и перемешивали при температуре от 20°C до 25°C в течение 3 часов.
Реакционную смесь очищали на колонке с обращенной фазой (торговое название; SILMERCK 10013) (ацетонитрил/вода/уксусная кислота) и фракцию, содержащую указанное в заголовке соединение, экстрагировали с метиленхлоридом. Органический слой промывали водным раствором бикарбоната натрия и водой и затем концентрировали при пониженном давлении. Концентрированный остаток растворяли в метиленхлориде, метаноле и уксусной кислоте и раствор добавляли по каплям в пентан. В результате профильтровали осажденный осадок. Полученное твердое вещество промывали пентаном и высушивали при пониженном давлении. В результате получали указанное в заголовке соединение (88,1 г, выход 57% в три стадии).
[0160] <Пример получения 4>
1493 мл буферного водного раствора для разведения (10 ммоль/л тринатрия фосфата, 100 ммоль/л хлорида натрия, 3 вес./об. % сахарозы и pH 6,5) и 1098 мл буферного раствора для корректировки pH (0,25 моль/л трис(гидроксиметил)аминометана гидрохлорид, 20 ммоль/л EDTA, pH 7,7) добавляли к 7854 мл MORAb-003-содержащему буферному водному раствору (26,6 мг/мл MORAb-003, 10 ммоль/л тринатрия фосфата, 100 ммоль/л хлорида натрия, 3 вес./об. % сахарозы и pH 6,5). Водный раствор трис(2-карбоксиэтил)фосфина (10 ммоль/л, 311 г) добавляли при температуре 20°C и перемешивали в течение 2,5 часов.
DMA-раствор соединения, полученного в примере получения 3 (8,37 ммоль/л, 809 мл) добавляли и перемешивали в течение 0,5 часа. Водный раствор N-ацетилцистеина (30 ммоль/л, 452 г) добавили для остановки реакции и перемешивали в течение 0,5 часа. Конъюгат антитело-лекарственное средство (ADC) очищали путем диафильтрации при следующих условиях.
(Условия Очистки)
Фильтр (проницаемая мембрана): Pellicon 3 (1,14 м2, 30 кДа x1, 0,57 м2, 30 кДа x1)
TMP (трансмембранный перепад давления): 15 фунтов на квадратный дюйм
Дополнительный буферный раствор: 25 ммоль/л водного раствора лимонной кислоты (pH 6,3)
Температура: от 17,0°C до 23,0°C
Проникновение: 163,2 кг
[0161] Путем добавления 25 ммоль/л водного раствора лимонной кислоты (3013 г, pH 6,3) и 5668 г буферного водного раствора для создания условий (25 ммоль/л лимонной кислоты, 1 моль/л сахарозы, 0,24 вес./об. %, Полисорбат 80, pH 6,3), получали водный раствор ADC (концентрация белка: 10,6 мг/мл, общий вес: 20,9 кг, содержание ADC: 213,430 г, выход 99%). Затем водный раствор ADC подвергали стерильной фильтрации (Millipore Durapore PVDF).
[Перечень последовательностей]
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Eisai R&D Management
<120> СПОСОБ ПОЛУЧЕНИЯ КОНЪЮГАТА АНТИТЕЛО-ЛЕКАРСТВЕННОЕ
СРЕДСТВО НА ОСНОВЕ ЭРИБУЛИНА
<130> FP20-0574-00
<160> 347
<170> PatentIn версия 3.5
<210> 1
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь MORAb-003
<400> 1
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ser Ala Ser Gly Phe Thr Phe Ser Gly Tyr
20 25 30
Gly Leu Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Ser Ser Gly Gly Ser Tyr Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Ala Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asp Ser Leu Arg Pro Glu Asp Thr Gly Val Tyr Phe Cys
85 90 95
Ala Arg His Gly Asp Asp Pro Ala Trp Phe Ala Tyr Trp Gly Gln Gly
100 105 110
Thr Pro Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 2
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи MORAb-003
<400> 2
Gly Tyr Gly Leu Ser
1 5
<210> 3
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи MORAb-003
<400> 3
Met Ile Ser Ser Gly Gly Ser Tyr Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 4
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи MORAb-003
<400> 4
His Gly Asp Asp Pro Ala Trp Phe Ala Tyr
1 5 10
<210> 5
<211> 468
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Аминокислотная последовательность тяжелой цепи
полноразмерного белка-предшественника MORAb-003
<400> 5
Met Gly Trp Ser Cys Ile Ile Leu Phe Leu Val Ala Thr Ala Thr Gly
1 5 10 15
Val His Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln
20 25 30
Pro Gly Arg Ser Leu Arg Leu Ser Cys Ser Ala Ser Gly Phe Thr Phe
35 40 45
Ser Gly Tyr Gly Leu Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu
50 55 60
Glu Trp Val Ala Met Ile Ser Ser Gly Gly Ser Tyr Thr Tyr Tyr Ala
65 70 75 80
Asp Ser Val Lys Gly Arg Phe Ala Ile Ser Arg Asp Asn Ala Lys Asn
85 90 95
Thr Leu Phe Leu Gln Met Asp Ser Leu Arg Pro Glu Asp Thr Gly Val
100 105 110
Tyr Phe Cys Ala Arg His Gly Asp Asp Pro Ala Trp Phe Ala Tyr Trp
115 120 125
Gly Gln Gly Thr Pro Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
130 135 140
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
145 150 155 160
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
165 170 175
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
180 185 190
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
195 200 205
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
210 215 220
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
225 230 235 240
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
245 250 255
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
260 265 270
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
275 280 285
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
290 295 300
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
305 310 315 320
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
325 330 335
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
340 345 350
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
355 360 365
Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val
370 375 380
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
385 390 395 400
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
405 410 415
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
420 425 430
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
435 440 445
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
450 455 460
Ser Pro Gly Lys
465
<210> 6
<211> 217
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легка цепь MORAb-003
<400> 6
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Ile Ser Ser Asn
20 25 30
Asn Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro Trp
35 40 45
Ile Tyr Gly Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Phe Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Tyr Pro
85 90 95
Tyr Met Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr
100 105 110
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu
115 120 125
Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro
130 135 140
Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly
145 150 155 160
Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr
165 170 175
Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His
180 185 190
Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val
195 200 205
Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 7
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи MORAb-003
<400> 7
Ser Val Ser Ser Ser Ile Ser Ser Asn Asn Leu His
1 5 10
<210> 8
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи MORAb-003
<400> 8
Gly Thr Ser Asn Leu Ala Ser
1 5
<210> 9
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи MORAb-003
<400> 9
Gln Gln Trp Ser Ser Tyr Pro Tyr Met Tyr Thr
1 5 10
<210> 10
<211> 236
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Аминокислотная последовательность легкой цепи
полноразмерного белка-предшественника MORAb-003
<400> 10
Met Gly Trp Ser Cys Ile Ile Leu Phe Leu Val Ala Thr Ala Thr Gly
1 5 10 15
Val His Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala
20 25 30
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Ile
35 40 45
Ser Ser Asn Asn Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
50 55 60
Lys Pro Trp Ile Tyr Gly Thr Ser Asn Leu Ala Ser Gly Val Pro Ser
65 70 75 80
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Phe Thr Ile Ser
85 90 95
Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Trp Ser
100 105 110
Ser Tyr Pro Tyr Met Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile
115 120 125
Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp
130 135 140
Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn
145 150 155 160
Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
165 170 175
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp
180 185 190
Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr
195 200 205
Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser
210 215 220
Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
225 230 235
<210> 11
<211> 1407
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Нуклеотиды тяжелой цепи MORAb-003
<400> 11
atgggatgga gctgtatcat cctcttcttg gtagcaacag ctacaggtgt ccactccgag 60
gtccaactgg tggagagcgg tggaggtgtt gtgcaacctg gccggtccct gcgcctgtcc 120
tgctccgcat ctggcttcac cttcagcggc tatgggttgt cttgggtgag acaggcacct 180
ggaaaaggtc ttgagtgggt tgcaatgatt agtagtggtg gtagttatac ctactatgca 240
gacagtgtga agggtagatt tgcaatatcg cgagacaacg ccaagaacac attgttcctg 300
caaatggaca gcctgagacc cgaagacacc ggggtctatt tttgtgcaag acatggggac 360
gatcccgcct ggttcgctta ttggggccaa gggaccccgg tcaccgtctc ctcagcctcc 420
accaagggcc catcggtctt ccccctggca ccctcctcca agagcacctc tgggggcaca 480
gcggccctgg gctgcctggt caaggactac ttccccgaac cggtgacggt gtcgtggaac 540
tcaggcgccc tgaccagcgg cgtgcacacc ttcccggctg tcctacagtc ctcaggactc 600
tactccctca gcagcgtggt gaccgtgccc tccagcagct tgggcaccca gacctacatc 660
tgcaacgtga atcacaagcc cagcaacacc aaggtggaca agaaagttga gcccaaatct 720
tgtgacaaaa ctcacacatg cccaccgtgc ccagcacctg aactcctggg gggaccgtca 780
gtcttcctct tccccccaaa acccaaggac accctcatga tctcccggac ccctgaggtc 840
acatgcgtgg tggtggacgt gagccacgaa gaccctgagg tcaagttcaa ctggtacgtg 900
gacggcgtgg aggtgcataa tgccaagaca aagccgcggg aggagcagta caacagcacg 960
taccgtgtgg tcagcgtcct caccgtcctg caccaggact ggctgaatgg caaggagtac 1020
aagtgcaagg tctccaacaa agccctccca gcccccatcg agaaaaccat ctccaaagcc 1080
aaagggcagc cccgagaacc acaggtgtac accctgcccc catcccggga tgagctgacc 1140
aagaaccagg tcagcctgac ctgcctggtc aaaggcttct atcccagcga catcgccgtg 1200
gagtgggaga gcaatgggca gccggagaac aactacaaga ccacgcctcc cgtgctggac 1260
tccgacggct ccttcttctt atattcaaag ctcaccgtgg acaagagcag gtggcagcag 1320
gggaacgtct tctcatgctc cgtgatgcat gaggctctgc acaaccacta cacgcagaag 1380
agcctctccc tgtctcccgg gaaatga 1407
<210> 12
<211> 711
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Нуклеотиды легкой цепи MORAb-003
<400> 12
atgggatgga gctgtatcat cctcttcttg gtagcaacag ctacaggtgt ccactccgac 60
atccagctga cccagagccc aagcagcctg agcgccagcg tgggtgacag agtgaccatc 120
acctgtagtg tcagctcaag tataagttcc aacaacttgc actggtacca gcagaagcca 180
ggtaaggctc caaagccatg gatctacggc acatccaacc tggcttctgg tgtgccaagc 240
agattcagcg gtagcggtag cggtaccgac tacaccttca ccatcagcag cctccagcca 300
gaggacatcg ccacctacta ctgccaacag tggagtagtt acccgtacat gtacacgttc 360
ggccaaggga ccaaggtgga aatcaaacga actgtggctg caccatctgt cttcatcttc 420
ccgccatctg atgagcagtt gaaatctgga actgcctctg ttgtgtgcct gctgaataac 480
ttctatccca gagaggccaa agtacagtgg aaggtggata acgccctcca atcgggtaac 540
tcccaggaga gtgtcacaga gcaggacagc aaggacagca cctacagcct cagcagcacc 600
ctgacgctga gcaaagcaga ctacgagaaa cacaaagtct acgcctgcga agtcacccat 660
cagggcctga gctcgcccgt cacaaagagc ttcaacaggg gagagtgtta a 711
<210> 13
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи MORAb-003; IMGT
<400> 13
Gly Phe Thr Phe Ser Gly Tyr Gly
1 5
<210> 14
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи MORAb-003; IMGT
<400> 14
Ile Ser Ser Gly Gly Ser Tyr Thr
1 5
<210> 15
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи MORAb-003; IMGT
<400> 15
Ala Arg His Gly Asp Asp Pro Ala Trp Phe Ala Tyr
1 5 10
<210> 16
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи MORAb-003; IMGT
<400> 16
Ser Ser Ile Ser Ser Asn Asn
1 5
<210> 17
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи MORAb-003; IMGT
<400> 17
Gly Thr Ser
1
<210> 18
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи MORAb-003; IMGT
<400> 18
Gln Gln Trp Ser Ser Tyr Pro Tyr Met Tyr Thr
1 5 10
<210> 19
<211> 257
<212> БЕЛОК
<213> Homo sapiens
<400> 19
Met Ala Gln Arg Met Thr Thr Gln Leu Leu Leu Leu Leu Val Trp Val
1 5 10 15
Ala Val Val Gly Glu Ala Gln Thr Arg Ile Ala Trp Ala Arg Thr Glu
20 25 30
Leu Leu Asn Val Cys Met Asn Ala Lys His His Lys Glu Lys Pro Gly
35 40 45
Pro Glu Asp Lys Leu His Glu Gln Cys Arg Pro Trp Arg Lys Asn Ala
50 55 60
Cys Cys Ser Thr Asn Thr Ser Gln Glu Ala His Lys Asp Val Ser Tyr
65 70 75 80
Leu Tyr Arg Phe Asn Trp Asn His Cys Gly Glu Met Ala Pro Ala Cys
85 90 95
Lys Arg His Phe Ile Gln Asp Thr Cys Leu Tyr Glu Cys Ser Pro Asn
100 105 110
Leu Gly Pro Trp Ile Gln Gln Val Asp Gln Ser Trp Arg Lys Glu Arg
115 120 125
Val Leu Asn Val Pro Leu Cys Lys Glu Asp Cys Glu Gln Trp Trp Glu
130 135 140
Asp Cys Arg Thr Ser Tyr Thr Cys Lys Ser Asn Trp His Lys Gly Trp
145 150 155 160
Asn Trp Thr Ser Gly Phe Asn Lys Cys Ala Val Gly Ala Ala Cys Gln
165 170 175
Pro Phe His Phe Tyr Phe Pro Thr Pro Thr Val Leu Cys Asn Glu Ile
180 185 190
Trp Thr His Ser Tyr Lys Val Ser Asn Tyr Ser Arg Gly Ser Gly Arg
195 200 205
Cys Ile Gln Met Trp Phe Asp Pro Ala Gln Gly Asn Pro Asn Glu Glu
210 215 220
Val Ala Arg Phe Tyr Ala Ala Ala Met Ser Gly Ala Gly Pro Trp Ala
225 230 235 240
Ala Trp Pro Phe Leu Leu Ser Leu Ala Leu Met Leu Leu Trp Leu Leu
245 250 255
Ser
<210> 20
<211> 982
<212> ДНК
<213> Homo sapiens
<400> 20
cattccttgg tgccactgac cacagctctt tcttcaggga cagacatggc tcagcggatg 60
acaacacagc tgctgctcct tctagtgtgg gtggctgtag taggggaggc tcagacaagg 120
attgcatggg ccaggactga gcttctcaat gtctgcatga acgccaagca ccacaaggaa 180
aagccaggcc ccgaggacaa gttgcatgag cagtgtcgac cctggaggaa gaatgcctgc 240
tgttctacca acaccagcca ggaagcccat aaggatgttt cctacctata tagattcaac 300
tggaaccact gtggagagat ggcacctgcc tgcaaacggc atttcatcca ggacacctgc 360
ctctacgagt gctcccccaa cttggggccc tggatccagc aggtggatca gagctggcgc 420
aaagagcggg tactgaacgt gcccctgtgc aaagaggact gtgagcaatg gtgggaagat 480
tgtcgcacct cctacacctg caagagcaac tggcacaagg gctggaactg gacttcaggg 540
tttaacaagt gcgcagtggg agctgcctgc caacctttcc atttctactt ccccacaccc 600
actgttctgt gcaatgaaat ctggactcac tcctacaagg tcagcaacta cagccgaggg 660
agtggccgct gcatccagat gtggttcgac ccagcccagg gcaaccccaa tgaggaggtg 720
gcgaggttct atgctgcagc catgagtggg gctgggccct gggcagcctg gcctttcctg 780
cttagcctgg ccctaatgct gctgtggctg ctcagctgac ctccttttac cttctgatac 840
ctggaaatcc ctgccctgtt cagccccaca gctcccaact atttggttcc tgctccatgg 900
tcgggcctct gacagccact ttgaataaac cagacaccgc acatgtgtct tgagaattat 960
ttggaaaaaa aaaaaaaaaa aa 982
<210> 21
<211> 1255
<212> БЕЛОК
<213> Homo sapiens
<400> 21
Met Glu Leu Ala Ala Leu Cys Arg Trp Gly Leu Leu Leu Ala Leu Leu
1 5 10 15
Pro Pro Gly Ala Ala Ser Thr Gln Val Cys Thr Gly Thr Asp Met Lys
20 25 30
Leu Arg Leu Pro Ala Ser Pro Glu Thr His Leu Asp Met Leu Arg His
35 40 45
Leu Tyr Gln Gly Cys Gln Val Val Gln Gly Asn Leu Glu Leu Thr Tyr
50 55 60
Leu Pro Thr Asn Ala Ser Leu Ser Phe Leu Gln Asp Ile Gln Glu Val
65 70 75 80
Gln Gly Tyr Val Leu Ile Ala His Asn Gln Val Arg Gln Val Pro Leu
85 90 95
Gln Arg Leu Arg Ile Val Arg Gly Thr Gln Leu Phe Glu Asp Asn Tyr
100 105 110
Ala Leu Ala Val Leu Asp Asn Gly Asp Pro Leu Asn Asn Thr Thr Pro
115 120 125
Val Thr Gly Ala Ser Pro Gly Gly Leu Arg Glu Leu Gln Leu Arg Ser
130 135 140
Leu Thr Glu Ile Leu Lys Gly Gly Val Leu Ile Gln Arg Asn Pro Gln
145 150 155 160
Leu Cys Tyr Gln Asp Thr Ile Leu Trp Lys Asp Ile Phe His Lys Asn
165 170 175
Asn Gln Leu Ala Leu Thr Leu Ile Asp Thr Asn Arg Ser Arg Ala Cys
180 185 190
His Pro Cys Ser Pro Met Cys Lys Gly Ser Arg Cys Trp Gly Glu Ser
195 200 205
Ser Glu Asp Cys Gln Ser Leu Thr Arg Thr Val Cys Ala Gly Gly Cys
210 215 220
Ala Arg Cys Lys Gly Pro Leu Pro Thr Asp Cys Cys His Glu Gln Cys
225 230 235 240
Ala Ala Gly Cys Thr Gly Pro Lys His Ser Asp Cys Leu Ala Cys Leu
245 250 255
His Phe Asn His Ser Gly Ile Cys Glu Leu His Cys Pro Ala Leu Val
260 265 270
Thr Tyr Asn Thr Asp Thr Phe Glu Ser Met Pro Asn Pro Glu Gly Arg
275 280 285
Tyr Thr Phe Gly Ala Ser Cys Val Thr Ala Cys Pro Tyr Asn Tyr Leu
290 295 300
Ser Thr Asp Val Gly Ser Cys Thr Leu Val Cys Pro Leu His Asn Gln
305 310 315 320
Glu Val Thr Ala Glu Asp Gly Thr Gln Arg Cys Glu Lys Cys Ser Lys
325 330 335
Pro Cys Ala Arg Val Cys Tyr Gly Leu Gly Met Glu His Leu Arg Glu
340 345 350
Val Arg Ala Val Thr Ser Ala Asn Ile Gln Glu Phe Ala Gly Cys Lys
355 360 365
Lys Ile Phe Gly Ser Leu Ala Phe Leu Pro Glu Ser Phe Asp Gly Asp
370 375 380
Pro Ala Ser Asn Thr Ala Pro Leu Gln Pro Glu Gln Leu Gln Val Phe
385 390 395 400
Glu Thr Leu Glu Glu Ile Thr Gly Tyr Leu Tyr Ile Ser Ala Trp Pro
405 410 415
Asp Ser Leu Pro Asp Leu Ser Val Phe Gln Asn Leu Gln Val Ile Arg
420 425 430
Gly Arg Ile Leu His Asn Gly Ala Tyr Ser Leu Thr Leu Gln Gly Leu
435 440 445
Gly Ile Ser Trp Leu Gly Leu Arg Ser Leu Arg Glu Leu Gly Ser Gly
450 455 460
Leu Ala Leu Ile His His Asn Thr His Leu Cys Phe Val His Thr Val
465 470 475 480
Pro Trp Asp Gln Leu Phe Arg Asn Pro His Gln Ala Leu Leu His Thr
485 490 495
Ala Asn Arg Pro Glu Asp Glu Cys Val Gly Glu Gly Leu Ala Cys His
500 505 510
Gln Leu Cys Ala Arg Gly His Cys Trp Gly Pro Gly Pro Thr Gln Cys
515 520 525
Val Asn Cys Ser Gln Phe Leu Arg Gly Gln Glu Cys Val Glu Glu Cys
530 535 540
Arg Val Leu Gln Gly Leu Pro Arg Glu Tyr Val Asn Ala Arg His Cys
545 550 555 560
Leu Pro Cys His Pro Glu Cys Gln Pro Gln Asn Gly Ser Val Thr Cys
565 570 575
Phe Gly Pro Glu Ala Asp Gln Cys Val Ala Cys Ala His Tyr Lys Asp
580 585 590
Pro Pro Phe Cys Val Ala Arg Cys Pro Ser Gly Val Lys Pro Asp Leu
595 600 605
Ser Tyr Met Pro Ile Trp Lys Phe Pro Asp Glu Glu Gly Ala Cys Gln
610 615 620
Pro Cys Pro Ile Asn Cys Thr His Ser Cys Val Asp Leu Asp Asp Lys
625 630 635 640
Gly Cys Pro Ala Glu Gln Arg Ala Ser Pro Leu Thr Ser Ile Ile Ser
645 650 655
Ala Val Val Gly Ile Leu Leu Val Val Val Leu Gly Val Val Phe Gly
660 665 670
Ile Leu Ile Lys Arg Arg Gln Gln Lys Ile Arg Lys Tyr Thr Met Arg
675 680 685
Arg Leu Leu Gln Glu Thr Glu Leu Val Glu Pro Leu Thr Pro Ser Gly
690 695 700
Ala Met Pro Asn Gln Ala Gln Met Arg Ile Leu Lys Glu Thr Glu Leu
705 710 715 720
Arg Lys Val Lys Val Leu Gly Ser Gly Ala Phe Gly Thr Val Tyr Lys
725 730 735
Gly Ile Trp Ile Pro Asp Gly Glu Asn Val Lys Ile Pro Val Ala Ile
740 745 750
Lys Val Leu Arg Glu Asn Thr Ser Pro Lys Ala Asn Lys Glu Ile Leu
755 760 765
Asp Glu Ala Tyr Val Met Ala Gly Val Gly Ser Pro Tyr Val Ser Arg
770 775 780
Leu Leu Gly Ile Cys Leu Thr Ser Thr Val Gln Leu Val Thr Gln Leu
785 790 795 800
Met Pro Tyr Gly Cys Leu Leu Asp His Val Arg Glu Asn Arg Gly Arg
805 810 815
Leu Gly Ser Gln Asp Leu Leu Asn Trp Cys Met Gln Ile Ala Lys Gly
820 825 830
Met Ser Tyr Leu Glu Asp Val Arg Leu Val His Arg Asp Leu Ala Ala
835 840 845
Arg Asn Val Leu Val Lys Ser Pro Asn His Val Lys Ile Thr Asp Phe
850 855 860
Gly Leu Ala Arg Leu Leu Asp Ile Asp Glu Thr Glu Tyr His Ala Asp
865 870 875 880
Gly Gly Lys Val Pro Ile Lys Trp Met Ala Leu Glu Ser Ile Leu Arg
885 890 895
Arg Arg Phe Thr His Gln Ser Asp Val Trp Ser Tyr Gly Val Thr Val
900 905 910
Trp Glu Leu Met Thr Phe Gly Ala Lys Pro Tyr Asp Gly Ile Pro Ala
915 920 925
Arg Glu Ile Pro Asp Leu Leu Glu Lys Gly Glu Arg Leu Pro Gln Pro
930 935 940
Pro Ile Cys Thr Ile Asp Val Tyr Met Ile Met Val Lys Cys Trp Met
945 950 955 960
Ile Asp Ser Glu Cys Arg Pro Arg Phe Arg Glu Leu Val Ser Glu Phe
965 970 975
Ser Arg Met Ala Arg Asp Pro Gln Arg Phe Val Val Ile Gln Asn Glu
980 985 990
Asp Leu Gly Pro Ala Ser Pro Leu Asp Ser Thr Phe Tyr Arg Ser Leu
995 1000 1005
Leu Glu Asp Asp Asp Met Gly Asp Leu Val Asp Ala Glu Glu Tyr
1010 1015 1020
Leu Val Pro Gln Gln Gly Phe Phe Cys Pro Asp Pro Ala Pro Gly
1025 1030 1035
Ala Gly Gly Met Val His His Arg His Arg Ser Ser Ser Thr Arg
1040 1045 1050
Ser Gly Gly Gly Asp Leu Thr Leu Gly Leu Glu Pro Ser Glu Glu
1055 1060 1065
Glu Ala Pro Arg Ser Pro Leu Ala Pro Ser Glu Gly Ala Gly Ser
1070 1075 1080
Asp Val Phe Asp Gly Asp Leu Gly Met Gly Ala Ala Lys Gly Leu
1085 1090 1095
Gln Ser Leu Pro Thr His Asp Pro Ser Pro Leu Gln Arg Tyr Ser
1100 1105 1110
Glu Asp Pro Thr Val Pro Leu Pro Ser Glu Thr Asp Gly Tyr Val
1115 1120 1125
Ala Pro Leu Thr Cys Ser Pro Gln Pro Glu Tyr Val Asn Gln Pro
1130 1135 1140
Asp Val Arg Pro Gln Pro Pro Ser Pro Arg Glu Gly Pro Leu Pro
1145 1150 1155
Ala Ala Arg Pro Ala Gly Ala Thr Leu Glu Arg Pro Lys Thr Leu
1160 1165 1170
Ser Pro Gly Lys Asn Gly Val Val Lys Asp Val Phe Ala Phe Gly
1175 1180 1185
Gly Ala Val Glu Asn Pro Glu Tyr Leu Thr Pro Gln Gly Gly Ala
1190 1195 1200
Ala Pro Gln Pro His Pro Pro Pro Ala Phe Ser Pro Ala Phe Asp
1205 1210 1215
Asn Leu Tyr Tyr Trp Asp Gln Asp Pro Pro Glu Arg Gly Ala Pro
1220 1225 1230
Pro Ser Thr Phe Lys Gly Thr Pro Thr Ala Glu Asn Pro Glu Tyr
1235 1240 1245
Leu Gly Leu Asp Val Pro Val
1250 1255
<210> 22
<211> 3768
<212> ДНК
<213> Homo sapiens
<400> 22
atggagctgg cggccttgtg ccgctggggg ctcctcctcg ccctcttgcc ccccggagcc 60
gcgagcaccc aagtgtgcac cggcacagac atgaagctgc ggctccctgc cagtcccgag 120
acccacctgg acatgctccg ccacctctac cagggctgcc aggtggtgca gggaaacctg 180
gaactcacct acctgcccac caatgccagc ctgtccttcc tgcaggatat ccaggaggtg 240
cagggctacg tgctcatcgc tcacaaccaa gtgaggcagg tcccactgca gaggctgcgg 300
attgtgcgag gcacccagct ctttgaggac aactatgccc tggccgtgct agacaatgga 360
gacccgctga acaataccac ccctgtcaca ggggcctccc caggaggcct gcgggagctg 420
cagcttcgaa gcctcacaga gatcttgaaa ggaggggtct tgatccagcg gaacccccag 480
ctctgctacc aggacacgat tttgtggaag gacatcttcc acaagaacaa ccagctggct 540
ctcacactga tagacaccaa ccgctctcgg gcctgccacc cctgttctcc gatgtgtaag 600
ggctcccgct gctggggaga gagttctgag gattgtcaga gcctgacgcg cactgtctgt 660
gccggtggct gtgcccgctg caaggggcca ctgcccactg actgctgcca tgagcagtgt 720
gctgccggct gcacgggccc caagcactct gactgcctgg cctgcctcca cttcaaccac 780
agtggcatct gtgagctgca ctgcccagcc ctggtcacct acaacacaga cacgtttgag 840
tccatgccca atcccgaggg ccggtataca ttcggcgcca gctgtgtgac tgcctgtccc 900
tacaactacc tttctacgga cgtgggatcc tgcaccctcg tctgccccct gcacaaccaa 960
gaggtgacag cagaggatgg aacacagcgg tgtgagaagt gcagcaagcc ctgtgcccga 1020
gtgtgctatg gtctgggcat ggagcacttg cgagaggtga gggcagttac cagtgccaat 1080
atccaggagt ttgctggctg caagaagatc tttgggagcc tggcatttct gccggagagc 1140
tttgatgggg acccagcctc caacactgcc ccgctccagc cagagcagct ccaagtgttt 1200
gagactctgg aagagatcac aggttaccta tacatctcag catggccgga cagcctgcct 1260
gacctcagcg tcttccagaa cctgcaagta atccggggac gaattctgca caatggcgcc 1320
tactcgctga ccctgcaagg gctgggcatc agctggctgg ggctgcgctc actgagggaa 1380
ctgggcagtg gactggccct catccaccat aacacccacc tctgcttcgt gcacacggtg 1440
ccctgggacc agctctttcg gaacccgcac caagctctgc tccacactgc caaccggcca 1500
gaggacgagt gtgtgggcga gggcctggcc tgccaccagc tgtgcgcccg agggcactgc 1560
tggggtccag ggcccaccca gtgtgtcaac tgcagccagt tccttcgggg ccaggagtgc 1620
gtggaggaat gccgagtact gcaggggctc cccagggagt atgtgaatgc caggcactgt 1680
ttgccgtgcc accctgagtg tcagccccag aatggctcag tgacctgttt tggaccggag 1740
gctgaccagt gtgtggcctg tgcccactat aaggaccctc ccttctgcgt ggcccgctgc 1800
cccagcggtg tgaaacctga cctctcctac atgcccatct ggaagtttcc agatgaggag 1860
ggcgcatgcc agccttgccc catcaactgc acccactcct gtgtggacct ggatgacaag 1920
ggctgccccg ccgagcagag agccagccct ctgacgtcca tcatctctgc ggtggttggc 1980
attctgctgg tcgtggtctt gggggtggtc tttgggatcc tcatcaagcg acggcagcag 2040
aagatccgga agtacacgat gcggagactg ctgcaggaaa cggagctggt ggagccgctg 2100
acacctagcg gagcgatgcc caaccaggcg cagatgcgga tcctgaaaga gacggagctg 2160
aggaaggtga aggtgcttgg atctggcgct tttggcacag tctacaaggg catctggatc 2220
cctgatgggg agaatgtgaa aattccagtg gccatcaaag tgttgaggga aaacacatcc 2280
cccaaagcca acaaagaaat cttagacgaa gcatacgtga tggctggtgt gggctcccca 2340
tatgtctccc gccttctggg catctgcctg acatccacgg tgcagctggt gacacagctt 2400
atgccctatg gctgcctctt agaccatgtc cgggaaaacc gcggacgcct gggctcccag 2460
gacctgctga actggtgtat gcagattgcc aaggggatga gctacctgga ggatgtgcgg 2520
ctcgtacaca gggacttggc cgctcggaac gtgctggtca agagtcccaa ccatgtcaaa 2580
attacagact tcgggctggc tcggctgctg gacattgacg agacagagta ccatgcagat 2640
gggggcaagg tgcccatcaa gtggatggcg ctggagtcca ttctccgccg gcggttcacc 2700
caccagagtg atgtgtggag ttatggtgtg actgtgtggg agctgatgac ttttggggcc 2760
aaaccttacg atgggatccc agcccgggag atccctgacc tgctggaaaa gggggagcgg 2820
ctgccccagc cccccatctg caccattgat gtctacatga tcatggtcaa atgttggatg 2880
attgactctg aatgtcggcc aagattccgg gagttggtgt ctgaattctc ccgcatggcc 2940
agggaccccc agcgctttgt ggtcatccag aatgaggact tgggcccagc cagtcccttg 3000
gacagcacct tctaccgctc actgctggag gacgatgaca tgggggacct ggtggatgct 3060
gaggagtatc tggtacccca gcagggcttc ttctgtccag accctgcccc gggcgctggg 3120
ggcatggtcc accacaggca ccgcagctca tctaccagga gtggcggtgg ggacctgaca 3180
ctagggctgg agccctctga agaggaggcc cccaggtctc cactggcacc ctccgaaggg 3240
gctggctccg atgtatttga tggtgacctg ggaatggggg cagccaaggg gctgcaaagc 3300
ctccccacac atgaccccag ccctctacag cggtacagtg aggaccccac agtacccctg 3360
ccctctgaga ctgatggcta cgttgccccc ctgacctgca gcccccagcc tgaatatgtg 3420
aaccagccag atgttcggcc ccagccccct tcgccccgag agggccctct gcctgctgcc 3480
cgacctgctg gtgccactct ggaaaggccc aagactctct ccccagggaa gaatggggtc 3540
gtcaaagacg tttttgcctt tgggggtgcc gtggagaacc ccgagtactt gacaccccag 3600
ggaggagctg cccctcagcc ccaccctcct cctgccttca gcccagcctt cgacaacctc 3660
tattactggg accaggaccc accagagcgg ggggctccac ccagcacctt caaagggaca 3720
cctacggcag agaacccaga gtacctgggt ctggacgtgc cagtgtga 3768
<210> 23
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь MORAb-003 (таблица 2)
<400> 23
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ser Ala Ser Gly Phe Thr Phe Ser Gly Tyr
20 25 30
Gly Leu Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Ser Ser Gly Gly Ser Tyr Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Ala Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asp Ser Leu Arg Pro Glu Asp Thr Gly Val Tyr Phe Cys
85 90 95
Ala Arg His Gly Asp Asp Pro Ala Trp Phe Ala Tyr Trp Gly Gln Gly
100 105 110
Thr Pro Val Thr Val Ser Ser
115
<210> 24
<211> 110
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь MORAb-003 (таблица 2)
<400> 24
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Val Ser Ser Ser Ile Ser Ser Asn
20 25 30
Asn Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro Trp
35 40 45
Ile Tyr Gly Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Phe Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Tyr Pro
85 90 95
Tyr Met Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 25
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь MORAb-009 (таблица 2)
<400> 25
Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Glu Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Thr Met Asn Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Leu Ile Thr Pro Tyr Asn Gly Ala Ser Ser Tyr Asn Gln Lys Phe
50 55 60
Arg Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Asp Leu Leu Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Arg Gly Gly Tyr Asp Gly Arg Gly Phe Asp Tyr Trp Gly Ser Gly
100 105 110
Thr Pro Val Thr Val Ser Ser
115
<210> 26
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь MORAb-009 (таблица 2)
<400> 26
Asp Ile Glu Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Gly Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Asn Ser Tyr Ser Leu Thr Ile Ser Ser Val Glu Ala Glu
65 70 75 80
Asp Asp Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Lys His Pro Leu Thr
85 90 95
Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105
<210> 27
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь трастузумаба
<400> 27
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 28
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь трастузумаба
<400> 28
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 29
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 33011-xi
<400> 29
Gln Ser Val Glu Glu Ser Gly Gly Arg Leu Val Thr Pro Gly Thr Pro
1 5 10 15
Leu Thr Leu Thr Cys Thr Val Ser Gly Ile Ser Leu Ser Ser Asp Ala
20 25 30
Ile Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Tyr Ile Gly
35 40 45
Ile Ile Asn Gly Gly Gly Asn Thr Tyr Tyr Ala Ser Trp Ala Lys Gly
50 55 60
Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp Leu Lys Ile Thr
65 70 75 80
Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Ala Arg Gly Ile
85 90 95
Gln His Gly Gly Gly Asn Ser Asp Tyr Tyr Tyr Tyr Gly Met Asp Leu
100 105 110
Trp Gly Pro Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 30
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 33011-xi
<400> 30
Glu Val Leu Met Thr Gln Thr Pro Ser Ser Val Ser Ala Ala Val Gly
1 5 10 15
Asp Thr Val Thr Ile Lys Cys Gln Ala Ser Gln Ser Ile Ser Ser Val
20 25 30
Leu Ser Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile
35 40 45
Tyr Leu Ala Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Asp Leu Glu Cys
65 70 75 80
Asp Asp Ala Ala Thr Tyr Tyr Cys Gln Thr Asn Tyr Gly Thr Ser Ser
85 90 95
Ser Asn Tyr Gly Phe Ala Phe Gly Gly Gly Thr Glu Val Val Val Lys
100 105 110
<210> 31
<211> 126
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 33011-zu
<400> 31
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Ile Ser Leu Ser Ser Asp
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Tyr Ile
35 40 45
Gly Ile Ile Asn Gly Gly Gly Asn Thr Tyr Tyr Ala Ser Trp Ala Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg His Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Ile Gln His Gly Gly Gly Asn Ser Asp Tyr Tyr Tyr Tyr Gly
100 105 110
Met Asp Leu Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 32
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 33011-zu
<400> 32
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Ser Ile Ser Ser Val
20 25 30
Leu Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Leu Ala Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Cys
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Thr Asn Tyr Gly Thr Ser Ser
85 90 95
Ser Asn Tyr Gly Phe Ala Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 33
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 111B10-xi
<400> 33
Gln Ser Val Glu Glu Ser Gly Gly Arg Leu Val Thr Pro Gly Thr Pro
1 5 10 15
Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Asn Asn Tyr Ala
20 25 30
Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile Gly
35 40 45
Ser Ile Ser Thr Gly Gly Leu Ala Phe Tyr Ala Asn Trp Ala Lys Gly
50 55 60
Arg Phe Thr Ile Ser Arg Thr Ser Thr Thr Val Asp Leu Lys Met Thr
65 70 75 80
Ser Leu Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Gly Arg Asn Gly
85 90 95
Gly Gly Ser Tyr Ile Phe Tyr Tyr Phe Asp Leu Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 34
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 111B10-xi
<400> 34
Ala Phe Glu Leu Thr Gln Thr Pro Ser Ser Val Glu Ala Ala Val Gly
1 5 10 15
Gly Thr Ile Thr Ile Lys Cys Gln Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Ser Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Thr Leu Ala Ser Gly Val Ser Ser Arg Phe Lys Gly
50 55 60
Ser Gly Ser Gly Thr Glu Tyr Thr Leu Thr Ile Ser Asp Leu Glu Cys
65 70 75 80
Ala Asp Ala Ala Thr Tyr Phe Cys Gln Ser Tyr Tyr Asp Ile Gly Thr
85 90 95
Ser Thr Phe Gly Gly Gly Thr Glu Val Val Val Lys
100 105
<210> 35
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 111B10-zu
<400> 35
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Leu Asn Asn Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Ser Thr Gly Gly Leu Ala Phe Tyr Ala Asn Trp Ala Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Asn Gly Gly Gly Ser Tyr Ile Phe Tyr Tyr Phe Asp Leu Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 36
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 111B10-zu
<400> 36
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Cys
65 70 75 80
Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Ser Tyr Tyr Asp Ile Gly Thr
85 90 95
Ser Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 37
<211> 114
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 201C15-xi
<400> 37
Gln Ser Val Lys Glu Ser Gly Gly Arg Leu Val Thr Pro Gly Thr Pro
1 5 10 15
Leu Thr Leu Thr Cys Thr Val Ser Gly Ile Asp Leu Ser Ser Tyr Ala
20 25 30
Met Gly Trp Phe Arg Gln Ala Pro Gly Lys Gly Leu Glu Tyr Ile Gly
35 40 45
Thr Ile Asn Ile Gly Gly Arg Val Tyr Tyr Ala Ser Trp Ala Lys Gly
50 55 60
Arg Phe Thr Ile Ser Arg Thr Ser Thr Thr Val Asp Leu Lys Ala Pro
65 70 75 80
Ser Leu Thr Ala Glu Asp Thr Ala Thr Tyr Phe Cys Ala Arg Tyr Tyr
85 90 95
Asn Gly Gly Ser Tyr Asp Ile Trp Gly Pro Gly Thr Leu Val Thr Val
100 105 110
Ser Leu
<210> 38
<211> 110
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 201C15-xi
<400> 38
Asp Val Val Met Thr Gln Thr Pro Ala Ser Ala Ser Glu Pro Val Gly
1 5 10 15
Gly Thr Val Thr Ile Lys Cys Gln Ala Ser Glu Ser Ile Tyr Arg Val
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile
35 40 45
Tyr Asp Thr Ser Thr Leu Ala Ser Gly Ala Pro Ser Arg Phe Lys Gly
50 55 60
Ser Gly Tyr Gly Thr Glu Phe Thr Leu Thr Ile Ser Gly Val Gln Cys
65 70 75 80
Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gly Gly Tyr Tyr Ala Asp Ser
85 90 95
Tyr Gly Ile Ala Phe Gly Gly Gly Thr Glu Val Val Val Lys
100 105 110
<210> 39
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 201C15-zu
<400> 39
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ser Ala Ser Gly Ile Asp Leu Ser Ser Tyr
20 25 30
Ala Met Gly Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Tyr Ile
35 40 45
Gly Thr Ile Asn Ile Gly Gly Arg Val Tyr Tyr Ala Ser Trp Ala Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Tyr Tyr Asn Gly Gly Ser Tyr Asp Ile Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 40
<211> 110
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 201C15-zu
<400> 40
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Glu Ser Ile Tyr Arg Val
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asp Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Cys
65 70 75 80
Asp Asp Ala Ala Thr Tyr Tyr Cys Gln Gly Gly Tyr Tyr Ala Asp Ser
85 90 95
Tyr Gly Ile Ala Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 41
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 346C6-xi
<400> 41
Gln Ser Val Glu Glu Ser Gly Gly Arg Leu Val Lys Pro Asp Glu Ser
1 5 10 15
Leu Thr Leu Thr Cys Thr Ala Ser Gly Phe Ser Leu Ser Ser Tyr Ala
20 25 30
Met Ile Trp Val Arg Gln Ala Pro Gly Glu Gly Leu Glu Trp Ile Gly
35 40 45
Thr Ile Ser Thr Gly Gly Ile Thr Tyr Tyr Ala Ser Trp Ala Lys Gly
50 55 60
Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp Leu Lys Ile Thr
65 70 75 80
Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Ala Arg Gly Gly
85 90 95
Tyr Ala Ala Ser Ser Ala Tyr Tyr Leu Pro Tyr Tyr Phe Asp Leu Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 42
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 346C6-xi
<400> 42
Ala Ala Val Leu Thr Gln Thr Pro Ser Pro Val Ser Ala Ala Val Gly
1 5 10 15
Gly Thr Val Thr Ile Ser Cys Gln Ser Ser Gln Ser Val Tyr Asn Asn
20 25 30
Asn Asn Leu Ala Trp Phe Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu
35 40 45
Leu Ile Tyr Leu Ala Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe
50 55 60
Ser Gly Ser Gly Ser Gly Thr Gln Phe Thr Leu Thr Ile Ser Gly Val
65 70 75 80
Gln Cys Asp Asp Ala Ala Thr Tyr Tyr Cys Leu Gly Gly Cys Asp Asp
85 90 95
Asp Ala Asp Thr Phe Ala Phe Gly Gly Gly Thr Glu Val Val Val Lys
100 105 110
<210> 43
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 346C6-zu
<400> 43
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Leu Ser Ser Tyr
20 25 30
Ala Met Ile Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Thr Ile Ser Thr Gly Gly Ile Thr Tyr Tyr Ala Ser Trp Ala Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Gly Tyr Ala Ala Ser Ser Ala Tyr Tyr Leu Pro Tyr Tyr Phe
100 105 110
Asp Leu Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 44
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 346C6-zu
<400> 44
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gln Ser Ser Gln Ser Val Tyr Asn Asn
20 25 30
Asn Asn Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu
35 40 45
Leu Ile Tyr Leu Ala Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe
50 55 60
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
65 70 75 80
Gln Cys Glu Asp Ala Ala Thr Tyr Tyr Cys Leu Gly Gly Cys Asp Asp
85 90 95
Asp Ala Asp Thr Phe Ala Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 45
<211> 357
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь MORAb-003 (таблица 3)
<400> 45
gaggtccaac tggtggagag cggtggaggt gttgtgcaac ctggccggtc cctgcgcctg 60
tcctgctccg catctggctt caccttcagc ggctatgggt tgtcttgggt gagacaggca 120
cctggaaaag gtcttgagtg ggttgcaatg attagtagtg gtggtagtta tacctactat 180
gcagacagtg tgaagggtag atttgcaata tcgcgagaca acgccaagaa cacattgttc 240
ctgcaaatgg acagcctgag acccgaagac accggggtct atttttgtgc aagacatggg 300
gacgatcccg cctggttcgc ttattggggc caagggaccc cggtcaccgt ctcctca 357
<210> 46
<211> 330
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Легкая цепь MORAb-003 (таблица 3)
<400> 46
gacatccagc tgacccagag cccaagcagc ctgagcgcca gcgtgggtga cagagtgacc 60
atcacctgta gtgtcagctc aagtataagt tccaacaact tgcactggta ccagcagaag 120
ccaggtaagg ctccaaagcc atggatctac ggcacatcca acctggcttc tggtgtgcca 180
agcagattca gcggtagcgg tagcggtacc gactacacct tcaccatcag cagcctccag 240
ccagaggaca tcgccaccta ctactgccaa cagtggagta gttacccgta catgtacacg 300
ttcggccaag ggaccaaggt ggaaatcaaa 330
<210> 47
<211> 357
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь MORAb-009 (таблица 3)
<400> 47
caggtacaac tgcagcagtc tgggcctgag ctggagaagc ctggcgcttc agtgaagata 60
tcctgcaagg cttctggtta ctcattcact ggctacacca tgaactgggt gaagcagagc 120
catggaaaga gccttgagtg gattggactt attactcctt acaatggtgc ttctagctac 180
aaccagaagt tcaggggcaa ggccacatta actgtagaca agtcatccag cacagcctac 240
atggacctcc tcagtctgac atctgaagac tctgcagtct atttctgtgc aagggggggt 300
tacgacggga ggggttttga ctactgggga tccgggaccc cggtcaccgt ctcctca 357
<210> 48
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Легкая цепь MORAb-009 (таблица 3)
<400> 48
gacatcgagc tcactcagtc tccagcaatc atgtctgcat ctccagggga gaaggtcacc 60
atgacctgca gtgccagctc aagtgtaagt tacatgcact ggtaccagca gaagtcaggc 120
acctccccca aaagatggat ttatgacaca tccaaactgg cttctggagt cccaggtcgc 180
ttcagtggca gtgggtctgg aaactcttac tctctcacaa tcagcagcgt ggaggctgaa 240
gatgatgcaa cttattactg ccagcagtgg agtaagcacc ctctcacgtt cggatccggg 300
accaaggtgg aaatcaaa 318
<210> 49
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 33011-xi (таблица 3)
<400> 49
cagtcggtgg aggagtccgg gggtcgcctg gtcacgcctg ggacacccct gacactcacc 60
tgcaccgtct ctggaatctc cctcagtagc gatgcaataa gctgggtccg ccaggctcca 120
gggaaggggc tcgaatacat cggaatcatt aatggtggtg gtaacacata ctacgcgagc 180
tgggcgaaag gccgattcac catctccaaa acctcgacca cggtggatct gaaaatcacc 240
agtccgacaa ccgaggacac ggccacctat ttctgtgcca gaggcattca acatggtggt 300
ggtaatagtg attattatta ttacggcatg gacctctggg gcccaggcac cctggtcact 360
gtctcttca 369
<210> 50
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 33011-xi (таблица 3)
<400> 50
gaagtgttga tgacccagac tccatcctcc gtgtctgcag ctgtgggaga cacagtcacc 60
atcaagtgcc aggccagtca gagcattagt agtgtcttgt cctggtatca gcagaaacca 120
gggcagcctc ccaagctcct gatctatctg gcatccactc tggcatctgg ggtcccatcg 180
cggttcagcg gcagtagatc tgggacagag ttcactctca ccatcagcga cctggagtgt 240
gacgatgctg ccacttacta ctgtcaaacc aattatggta ctagtagtag taattatggt 300
tttgctttcg gcggagggac cgaggtggtc gtcaaa 336
<210> 51
<211> 378
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 33011-zu (таблица 3)
<400> 51
gaagtccaac tggtggaaag cgggggagga ctggtgcagc cgggcggatc cctccggctg 60
tcatgtgctg catcgggaat ttccctctcc tccgacgcga ttagctgggt cagacaggcc 120
cccggaaagg ggctggagta catcggtatc atcaacggcg gcggaaacac ctactacgcc 180
tcctgggcca agggccgctt caccatctcg cggcataatt ccaagaacac tctgtacttg 240
caaatgaact ccctgagggc cgaggacacc gccgtgtact actgcgcgcg cggcatccag 300
cacggtggtg gaaacagcga ctactactac tatgggatgg atctgtgggg ccagggaact 360
cttgtgaccg tgtcgtca 378
<210> 52
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 33011-zu (таблица 3)
<400> 52
gacattcaga tgacccagtc cccaagctcg ctgtccgcct ccgtgggcga ccgcgtgacc 60
atcacgtgcc aggcgtccca gtcaattagc agcgtgctct cctggtacca acagaagccg 120
gggaaagcac ccaagctgct gatctacttg gcctccactc tggcctcggg agtgccttca 180
cggttctccg gatcgggatc tggtactgat ttcaccctca ccatctcgag ccttcagtgc 240
gaggacatcg ctacttacta ttgtcaaacc aactacggaa cctccagctc caactacggc 300
tttgccttcg gtggcgggac caaggtcgaa atcaaa 336
<210> 53
<211> 354
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 111B10-xi (таблица 3)
<400> 53
cagtcggtgg aggagtccgg gggtcgcctg gtcacgcctg ggacacccct gacactcacc 60
tgcacagtct ctggattctc cctcaataac tatgcaatga gctgggtccg ccaggctcca 120
gggaaggggc tggaatggat cggatccatt agtactggtg gtctcgcatt ctacgcgaac 180
tgggcaaaag gccgattcac catctccaga acctcgacca cggtggatct gaaaatgacc 240
agtctgacaa ccgaggacac ggccacctat ttctgtggca gaaatggtgg tggtagttat 300
attttctatt attttgactt gtggggccaa ggcaccctcg tcactgtctc ttca 354
<210> 54
<211> 324
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 111B10-xi (таблица 3)
<400> 54
gcattcgaat tgacccagac tccatcctcc gtggaggcag ctgtgggagg cacaatcacc 60
atcaagtgcc aggccagtca gagcattagt agttacttat cctggtatca gcagaaacca 120
gggcagcctc ccaagctcct gatctattct gcatccactc tggcatctgg ggtctcatcg 180
cggttcaaag gcagtggatc tgggacagag tacactctca ccatcagcga cctggagtgt 240
gccgatgctg ccacttactt ctgtcaaagc tattatgata ttggtactag tactttcggc 300
ggagggaccg aggtggtcgt caaa 324
<210> 55
<211> 363
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 111B10-zu (таблица 3)
<400> 55
gaagtgcagc tggtggaatc tggcggcgga ctggtgcagc ctggcggatc tctgagactg 60
tcttgtgccg cctccggctt ctccctgaac aactacgcca tgtcctgggt gcgacaggcc 120
cctggcaaag gcctggaatg gatcggctcc atcagcacag gcggcctggc cttctacgcc 180
aattgggcca agggccggtt caccatcagc cgggacaact ccaagaacac cctgtacctc 240
cagatgaact ccctgcgggc cgaggacacc gccgtgtact actgtgccag aaacggcgga 300
ggctcctaca tcttctacta cttcgacctg tggggccagg gcaccctcgt gacagtgtca 360
tct 363
<210> 56
<211> 324
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 111B10-zu (таблица 3)
<400> 56
gatattcaga tgacccagtc cccctccagc ctgtccgctt ctgtgggcga cagagtgacc 60
atcacctgtc aggcctccca gtccatctcc tcctacctgt cctggtatca gcagaagccc 120
ggcaaggccc ccaagctgct gatctactct gcctccacac tggcctccgg cgtgccctct 180
agattctccg gctctggctc tggcaccgac tttaccctga ccatcagctc cctccagtgc 240
gaggatgccg ccacctacta ctgccagtcc tactacgaca tcggcacctc caccttcggc 300
ggaggcacca aggtggaaat caaa 324
<210> 57
<211> 342
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 201C15-xi (таблица 3)
<400> 57
cagtcagtga aggagtccgg gggtcgcctg gtcacgcctg ggacacccct gacactcacc 60
tgcacagtct ctggaatcga cctcagtagc tatgcaatgg gctggttccg ccaggctcca 120
gggaaggggc tggaatacat cggaaccatt aatattggtg gtcgcgtata ttacgcgagc 180
tgggcaaaag gccgattcac catctccaga acctcgacca cggtggatct gaaagcgccc 240
agtctgacag ccgaggacac ggccacctat ttctgtgcca gatattataa tggtggtagt 300
tatgacatct ggggcccagg caccctggtc accgtctctt ta 342
<210> 58
<211> 330
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 201C15-xi (таблица 3)
<400> 58
gatgttgtga tgacccagac tccagcctcc gcgtctgaac ctgtgggagg cacagtcacc 60
atcaagtgcc aggccagtga gagcatttat cgcgtattgg cctggtatca gcagaaacca 120
gggcagcctc ccaagctcct gatctatgat acatccactc tggcatctgg ggccccatcg 180
cggttcaaag gcagtggata tgggacagag ttcactctca ccatcagcgg cgtgcagtgt 240
gaagatgctg ccacttacta ctgtcaaggc ggttattatg ctgatagtta tggtattgct 300
ttcggcggag ggaccgaggt ggtggtcaaa 330
<210> 59
<211> 351
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 201C15-zu (таблица 3)
<400> 59
caggtgcagc tggtggaatc tggcggagga ctggtgcagc ctggcggctc tctgagactg 60
tcctgttccg cctccggaat cgacctgtcc tcctacgcta tgggctgggt gcgacaggct 120
cctggcaagg gcctggagta catcggcacc atcaacatcg gcggcagagt gtactacgcc 180
tcctgggcca agggccggtt caccatctcc agagacaact ccaagaacac cctgtacctc 240
cagatgaact ccctgcgggc cgaggacacc gccgtgtact actgcgcccg gtactacaac 300
ggcggctcct acgatatctg gggccagggc acactcgtga ccgtgtcctc t 351
<210> 60
<211> 330
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 201C15-zu (таблица 3)
<400> 60
gatatccaga tgacccagtc cccctccacc ctgtctgcct ctgtgggcga cagagtgacc 60
atcacctgtc aggcctccga gtccatctac cgggtgctgg cctggtatca gcagaagcct 120
ggcaaggccc ccaagctgct gatctacgac accagcacac tggcctccgg cgtgccctct 180
agattctccg gctctggctc tggcaccgag tttaccctga ccatctccag cctccagtgc 240
gacgacgccg ccacctacta ttgtcagggc ggctactacg ccgactccta cggaatcgct 300
ttcggcggag gcaccaaggt ggaaatcaaa 330
<210> 61
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 346C6-xi (таблица 3)
<400> 61
cagtcggtgg aggagtccgg cggtcgcctg gtaaagcctg acgaatccct gacactcacc 60
tgcacagcct ctggattctc cctcagtagt tatgcaatga tctgggtccg ccaggctcca 120
ggggaggggc tggaatggat cggaaccatt agtactggtg gtatcacata ctacgcgagc 180
tgggcgaaag gccgattcac catctccaaa acctcgacca cggtggatct gaaaatcacc 240
agtccgacaa ccgaggacac ggccacctat ttctgtgcca gagggggata tgctgctagt 300
agtgcttatt atctcccgta ctactttgac ttgtggggcc aagggaccct ggtcaccgtc 360
tcctca 366
<210> 62
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 346C6-xi (таблица 3)
<400> 62
gcagccgtgc tgacccagac accatcaccc gtgtctgcag ctgtgggagg cacagtcacc 60
atcagttgcc agtccagtca gagtgtttat aataataaca acttagcctg gtttcagcag 120
aaacccgggc agcctcccaa gcttctgatc tatctggcat ccactctggc atctggggtc 180
ccatcacggt tcagcggcag tggatctggg acacagttca ctctcaccat cagcggcgtg 240
cagtgtgacg atgctgccac ttattactgt ctaggtggtt gtgatgatga tgctgatact 300
tttgctttcg gcggagggac tgaggtggtg gtcaaa 336
<210> 63
<211> 375
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 346C6-zu (таблица 3)
<400> 63
gaagtgcagc tggtggaatc tggcggcgga ctggtgcagc ctggcggatc tctgagactg 60
tcttgtgccg cctccggctt ctccctgtcc tcctacgcta tgatctgggt gcgacaggcc 120
cctggcaagg gcctggaatg gatcggcacc atctctaccg gcggaattac ctactacgcc 180
tcctgggcca agggccggtt caccatctcc agagacaact ccaagaacac cctgtacctc 240
cagatgaact ccctgcgggc cgaggacacc gccgtgtact attgtgctag aggcggctac 300
gccgccagct ccgcttacta cctgccctac tacttcgacc tgtggggcca gggcaccctc 360
gtgacagtgt catct 375
<210> 64
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 346C6-zu (таблица 3)
<400> 64
gatattcaga tgacccagtc cccctccagc ctgtccgctt ctgtgggcga cagagtgacc 60
atcacctgtc agtcctccca gtccgtgtat aacaacaaca acctggcctg gtatcagcag 120
aaacccggca aggtgcccaa gctgctgatc tacctggcct ccacactggc ctctggcgtg 180
ccctctagat tctccggctc tggctctggc accgacttta ccctgaccat cagctccctc 240
cagtgcgagg atgccgccac ctactattgc ctgggcggct gcgacgacga cgccgatacc 300
tttgcttttg gcggaggcac caaggtggaa atcaaa 336
<210> 65
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи MORAb-009 (таблица 4)
<400> 65
Gly Tyr Thr Met Asn
1 5
<210> 66
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи MORAb-009 (таблица 4)
<400> 66
Leu Ile Thr Pro Tyr Asn Gly Ala Ser Ser Tyr Asn Gln Lys Phe Arg
1 5 10 15
Gly
<210> 67
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи MORAb-009 (таблица 4)
<400> 67
Gly Gly Tyr Asp Gly Arg Gly Phe Asp Tyr
1 5 10
<210> 68
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи MORAb-009 (таблица 4)
<400> 68
Ser Ala Ser Ser Ser Val Ser Tyr Met His
1 5 10
<210> 69
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи MORAb-009 (таблица 4)
<400> 69
Asp Thr Ser Lys Leu Ala Ser
1 5
<210> 70
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи MORAb-009 (таблица 4)
<400> 70
Gln Gln Trp Ser Lys His Pro Leu Thr
1 5
<210> 71
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи трастузумаба (таблица 4)
<400> 71
Asp Thr Tyr Ile His
1 5
<210> 72
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи трастузумаба (таблица 4)
<400> 72
Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 73
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи трастузумаба (таблица 4)
<400> 73
Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr
1 5 10
<210> 74
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи трастузумаба (таблица 4)
<400> 74
Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ala
1 5 10
<210> 75
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи трастузумаба (таблица 4)
<400> 75
Ser Ala Ser Phe Leu Tyr Ser
1 5
<210> 76
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи трастузумаба (таблица 4)
<400> 76
Gln Gln His Tyr Thr Thr Pro Pro Thr
1 5
<210> 77
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 33011-xi (таблица 4)
<400> 77
Ser Asp Ala Ile Ser
1 5
<210> 78
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 33011-xi (таблица 4)
<400> 78
Ile Ile Asn Gly Gly Gly Asn Thr Tyr Tyr Ala Ser Trp Ala Lys Gly
1 5 10 15
<210> 79
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 33011-xi (таблица 4)
<400> 79
Gly Ile Gln His Gly Gly Gly Asn Ser Asp Tyr Tyr Tyr Tyr Gly Met
1 5 10 15
Asp Leu
<210> 80
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 33011-xi (таблица 4)
<400> 80
Gln Ala Ser Gln Ser Ile Ser Ser Val Leu Ser
1 5 10
<210> 81
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 33011-xi (таблица 4)
<400> 81
Leu Ala Ser Thr Leu Ala Ser
1 5
<210> 82
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 33011-xi (таблица 4)
<400> 82
Gln Thr Asn Tyr Gly Thr Ser Ser Ser Asn Tyr Gly Phe Ala
1 5 10
<210> 83
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 33011-zu (таблица 4)
<400> 83
Ser Asp Ala Ile Ser
1 5
<210> 84
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 33011-zu (таблица 4)
<400> 84
Ile Ile Asn Gly Gly Gly Asn Thr Tyr Tyr Ala Ser Trp Ala Lys Gly
1 5 10 15
<210> 85
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 33011-zu (таблица 4)
<400> 85
Gly Ile Gln His Gly Gly Gly Asn Ser Asp Tyr Tyr Tyr Tyr Gly Met
1 5 10 15
Asp Leu
<210> 86
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 33011-zu (таблица 4)
<400> 86
Gln Ala Ser Gln Ser Ile Ser Ser Val Leu Ser
1 5 10
<210> 87
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 33011-zu (таблица 4)
<400> 87
Leu Ala Ser Thr Leu Ala Ser
1 5
<210> 88
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 33011-zu (таблица 4)
<400> 88
Gln Thr Asn Tyr Gly Thr Ser Ser Ser Asn Tyr Gly Phe Ala
1 5 10
<210> 89
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 111B10-xi (таблица 4)
<400> 89
Asn Tyr Ala Met Ser
1 5
<210> 90
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 111B10-xi (таблица 4)
<400> 90
Ser Ile Ser Thr Gly Gly Leu Ala Phe Tyr Ala Asn Trp Ala Lys Gly
1 5 10 15
<210> 91
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 111B10-xi (таблица 4)
<400> 91
Asn Gly Gly Gly Ser Tyr Ile Phe Tyr Tyr Phe Asp Leu
1 5 10
<210> 92
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 111B10-xi (таблица 4)
<400> 92
Gln Ala Ser Gln Ser Ile Ser Ser Tyr Leu Ser
1 5 10
<210> 93
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 111B10-xi (таблица 4)
<400> 93
Ser Ala Ser Thr Leu Ala Ser
1 5
<210> 94
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 111B10-xi (таблица 4)
<400> 94
Gln Ser Tyr Tyr Asp Ile Gly Thr Ser Thr
1 5 10
<210> 95
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 111B10-zu (таблица 4)
<400> 95
Asn Tyr Ala Met Ser
1 5
<210> 96
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 111B10-zu (таблица 4)
<400> 96
Ser Ile Ser Thr Gly Gly Leu Ala Phe Tyr Ala Asn Trp Ala Lys Gly
1 5 10 15
<210> 97
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 111B10-zu (таблица 4)
<400> 97
Asn Gly Gly Gly Ser Tyr Ile Phe Tyr Tyr Phe Asp Leu
1 5 10
<210> 98
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 111B10-zu (таблица 4)
<400> 98
Gln Ala Ser Gln Ser Ile Ser Ser Tyr Leu Ser
1 5 10
<210> 99
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 111B10-zu (таблица 4)
<400> 99
Ser Ala Ser Thr Leu Ala Ser
1 5
<210> 100
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 111B10-zu (таблица 4)
<400> 100
Gln Ser Tyr Tyr Asp Ile Gly Thr Ser Thr
1 5 10
<210> 101
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 201C15-xi (таблица 4)
<400> 101
Ser Tyr Ala Met Gly
1 5
<210> 102
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 201C15-xi (таблица 4)
<400> 102
Thr Ile Asn Ile Gly Gly Arg Val Tyr Tyr Ala Ser Trp Ala Lys Gly
1 5 10 15
<210> 103
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 201C15-xi (таблица 4)
<400> 103
Tyr Tyr Asn Gly Gly Ser Tyr Asp Ile
1 5
<210> 104
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 201C15-xi (таблица 4)
<400> 104
Gln Ala Ser Glu Ser Ile Tyr Arg Val Leu Ala
1 5 10
<210> 105
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 201C15-xi (таблица 4)
<400> 105
Asp Thr Ser Thr Leu Ala Ser
1 5
<210> 106
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 201C15-xi (таблица 4)
<400> 106
Gln Gly Gly Tyr Tyr Ala Asp Ser Tyr Gly Ile Ala
1 5 10
<210> 107
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 201C15-zu (таблица 4)
<400> 107
Ser Tyr Ala Met Gly
1 5
<210> 108
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 201C15-zu (таблица 4)
<400> 108
Thr Ile Asn Ile Gly Gly Arg Val Tyr Tyr Ala Ser Trp Ala Lys Gly
1 5 10 15
<210> 109
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 201C15-zu (таблица 4)
<400> 109
Tyr Tyr Asn Gly Gly Ser Tyr Asp Ile
1 5
<210> 110
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 201C15-zu (таблица 4)
<400> 110
Gln Ala Ser Glu Ser Ile Tyr Arg Val Leu Ala
1 5 10
<210> 111
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 201C15-zu (таблица 4)
<400> 111
Asp Thr Ser Thr Leu Ala Ser
1 5
<210> 112
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 201C15-zu (таблица 4)
<400> 112
Gln Gly Gly Tyr Tyr Ala Asp Ser Tyr Gly Ile Ala
1 5 10
<210> 113
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 346C6-xi (таблица 4)
<400> 113
Ser Tyr Ala Met Ile
1 5
<210> 114
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 346C6-xi (таблица 4)
<400> 114
Thr Ile Ser Thr Gly Gly Ile Thr Tyr Tyr Ala Ser Trp Ala Lys Gly
1 5 10 15
<210> 115
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 346C6-xi (таблица 4)
<400> 115
Gly Gly Tyr Ala Ala Ser Ser Ala Tyr Tyr Leu Pro Tyr Tyr Phe Asp
1 5 10 15
Leu
<210> 116
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 346C6-xi (таблица 4)
<400> 116
Gln Ser Ser Gln Ser Val Tyr Asn Asn Asn Asn Leu Ala
1 5 10
<210> 117
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 346C6-xi (таблица 4)
<400> 117
Leu Ala Ser Thr Leu Ala Ser
1 5
<210> 118
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 346C6-xi (таблица 4)
<400> 118
Leu Gly Gly Cys Asp Asp Asp Ala Asp Thr Phe Ala
1 5 10
<210> 119
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 346C6-zu (таблица 4)
<400> 119
Ser Tyr Ala Met Ile
1 5
<210> 120
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 346C6-zu (таблица 4)
<400> 120
Thr Ile Ser Thr Gly Gly Ile Thr Tyr Tyr Ala Ser Trp Ala Lys Gly
1 5 10 15
<210> 121
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 346C6-zu (таблица 4)
<400> 121
Gly Gly Tyr Ala Ala Ser Ser Ala Tyr Tyr Leu Pro Tyr Tyr Phe Asp
1 5 10 15
Leu
<210> 122
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 346C6-zu (таблица 4)
<400> 122
Gln Ser Ser Gln Ser Val Tyr Asn Asn Asn Asn Leu Ala
1 5 10
<210> 123
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 346C6-zu (таблица 4)
<400> 123
Leu Ala Ser Thr Leu Ala Ser
1 5
<210> 124
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 346C6-zu (таблица 4)
<400> 124
Leu Gly Gly Cys Asp Asp Asp Ala Asp Thr Phe Ala
1 5 10
<210> 125
<211> 15
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи MORAb-003 (таблица 5)
<400> 125
ggctatgggt tgtct 15
<210> 126
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи MORAb-003 (таблица 5)
<400> 126
atgattagta gtggtggtag ttatacctac tatgcagaca gtgtgaaggg t 51
<210> 127
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи MORAb-003 (таблица 5)
<400> 127
catggggacg atcccgcctg gttcgcttat 30
<210> 128
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи MORAb-003 (таблица 5)
<400> 128
agtgtcagct caagtataag ttccaacaac ttgcac 36
<210> 129
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи MORAb-003 (таблица 5)
<400> 129
ggcacatcca acctggcttc t 21
<210> 130
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи MORAb-003 (таблица 5)
<400> 130
caacagtgga gtagttaccc gtacatgtac acg 33
<210> 131
<211> 15
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи MORAb-009 (таблица 5)
<400> 131
ggctacacca tgaac 15
<210> 132
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи MORAb-009 (таблица 5)
<400> 132
cttattactc cttacaatgg tgcttctagc tacaaccaga agttcagggg c 51
<210> 133
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи MORAb-009 (таблица 5)
<400> 133
gggggttacg acgggagggg ttttgactac 30
<210> 134
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи MORAb-009 (таблица 5)
<400> 134
agtgccagct caagtgtaag ttacatgcac 30
<210> 135
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи MORAb-009 (таблица 5)
<400> 135
gacacatcca aactggcttc t 21
<210> 136
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи MORAb-009 (таблица 5)
<400> 136
cagcagtgga gtaagcaccc tctcacg 27
<210> 137
<211> 15
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 33011-xi (таблица 5)
<400> 137
agcgatgcaa taagc 15
<210> 138
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 33011-xi (таблица 5)
<400> 138
atcattaatg gtggtggtaa cacatactac gcgagctggg cgaaaggc 48
<210> 139
<211> 54
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 33011-xi (таблица 5)
<400> 139
ggcattcaac atggtggtgg taatagtgat tattattatt acggcatgga cctc 54
<210> 140
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 33011-xi (таблица 5)
<400> 140
caggccagtc agagcattag tagtgtcttg tcc 33
<210> 141
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 33011-xi (таблица 5)
<400> 141
ctggcatcca ctctggcatc t 21
<210> 142
<211> 42
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 33011-xi (таблица 5)
<400> 142
caaaccaatt atggtactag tagtagtaat tatggttttg ct 42
<210> 143
<211> 15
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 33011-zu (таблица 5)
<400> 143
tccgacgcga ttagc 15
<210> 144
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 33011-zu (таблица 5)
<400> 144
atcatcaacg gcggcggaaa cacctactac gcctcctggg ccaagggc 48
<210> 145
<211> 54
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 33011-zu (таблица 5)
<400> 145
ggcatccagc acggtggtgg aaacagcgac tactactact atgggatgga tctg 54
<210> 146
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 33011-zu (таблица 5)
<400> 146
caggcgtccc agtcaattag cagcgtgctc tcc 33
<210> 147
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 33011-zu (таблица 5)
<400> 147
ttggcctcca ctctggcctc g 21
<210> 148
<211> 42
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 33011-zu (таблица 5)
<400> 148
caaaccaact acggaacctc cagctccaac tacggctttg cc 42
<210> 149
<211> 15
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 111B10-xi (таблица 5)
<400> 149
aactatgcaa tgagc 15
<210> 150
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 111B10-xi (таблица 5)
<400> 150
tccattagta ctggtggtct cgcattctac gcgaactggg caaaaggc 48
<210> 151
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 111B10-xi (таблица 5)
<400> 151
aatggtggtg gtagttatat tttctattat tttgacttg 39
<210> 152
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 111B10-xi (таблица 5)
<400> 152
caggccagtc agagcattag tagttactta tcc 33
<210> 153
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 111B10-xi (таблица 5)
<400> 153
tctgcatcca ctctggcatc t 21
<210> 154
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 111B10-xi (таблица 5)
<400> 154
caaagctatt atgatattgg tactagtact 30
<210> 155
<211> 15
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 111B10-zu (таблица 5)
<400> 155
aactacgcca tgtcc 15
<210> 156
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 111B10-zu (таблица 5)
<400> 156
tccatcagca caggcggcct ggccttctac gccaattggg ccaagggc 48
<210> 157
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 111B10-zu (таблица 5)
<400> 157
aacggcggag gctcctacat cttctactac ttcgacctg 39
<210> 158
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 111B10-zu (таблица 5)
<400> 158
caggcctccc agtccatctc ctcctacctg tcc 33
<210> 159
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 111B10-zu (таблица 5)
<400> 159
tctgcctcca cactggcctc c 21
<210> 160
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 111B10-zu (таблица 5)
<400> 160
cagtcctact acgacatcgg cacctccacc 30
<210> 161
<211> 15
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 201C15-xi (таблица 5)
<400> 161
agctatgcaa tgggc 15
<210> 162
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 201C15-xi (таблица 5)
<400> 162
accattaata ttggtggtcg cgtatattac gcgagctggg caaaaggc 48
<210> 163
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 201C15-xi (таблица 5)
<400> 163
tattataatg gtggtagtta tgacatc 27
<210> 164
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 201C15-xi (таблица 5)
<400> 164
caggccagtg agagcattta tcgcgtattg gcc 33
<210> 165
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 201C15-xi (таблица 5)
<400> 165
gatacatcca ctctggcatc t 21
<210> 166
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 201C15-xi (таблица 5)
<400> 166
caaggcggtt attatgctga tagttatggt attgct 36
<210> 167
<211> 15
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 201C15-zu (таблица 5)
<400> 167
tcctacgcta tgggc 15
<210> 168
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 201C15-zu (таблица 5)
<400> 168
accatcaaca tcggcggcag agtgtactac gcctcctggg ccaagggc 48
<210> 169
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 201C15-zu (таблица 5)
<400> 169
tactacaacg gcggctccta cgatatc 27
<210> 170
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 201C15-zu (таблица 5)
<400> 170
caggcctccg agtccatcta ccgggtgctg gcc 33
<210> 171
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 201C15-zu (таблица 5)
<400> 171
gacaccagca cactggcctc c 21
<210> 172
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 201C15-zu (таблица 5)
<400> 172
cagggcggct actacgccga ctcctacgga atcgct 36
<210> 173
<211> 15
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 346C6-xi (таблица 5)
<400> 173
agttatgcaa tgatc 15
<210> 174
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 346C6-xi (таблица 5)
<400> 174
accattagta ctggtggtat cacatactac gcgagctggg cgaaaggc 48
<210> 175
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 346C6-xi (таблица 5)
<400> 175
gggggatatg ctgctagtag tgcttattat ctcccgtact actttgactt g 51
<210> 176
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 346C6-xi (таблица 5)
<400> 176
cagtcctccc agtccgtgta taacaacaac aacctggcc 39
<210> 177
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 346C6-xi (таблица 5)
<400> 177
ctggcatcca ctctggcatc t 21
<210> 178
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 346C6-xi (таблица 5)
<400> 178
ctaggtggtt gtgatgatga tgctgatact tttgct 36
<210> 179
<211> 15
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 346C6-zu (таблица 5)
<400> 179
tcctacgcta tgatc 15
<210> 180
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 346C6-zu (таблица 5)
<400> 180
accatctcta ccggcggaat tacctactac gcctcctggg ccaagggc 48
<210> 181
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 346C6-zu (таблица 5)
<400> 181
ggcggctacg ccgccagctc cgcttactac ctgccctact acttcgacct g 51
<210> 182
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 346C6-zu (таблица 5)
<400> 182
cagtcctccc agtccgtgta taacaacaac aacctggcc 39
<210> 183
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 346C6-zu (таблица 5)
<400> 183
ctggcctcca cactggcctc t 21
<210> 184
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 346C6-zu (таблица 5)
<400> 184
ctgggcggct gcgacgacga cgccgatacc tttgct 36
<210> 185
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи MORAb-009 (таблица 6)
<400> 185
Gly Tyr Ser Phe Thr Gly Tyr Thr
1 5
<210> 186
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи MORAb-009 (таблица 6)
<400> 186
Ile Thr Pro Tyr Asn Gly Ala Ser
1 5
<210> 187
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи MORAb-009 (таблица 6)
<400> 187
Ala Arg Gly Gly Tyr Asp Gly Arg Gly Phe Asp Tyr
1 5 10
<210> 188
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи MORAb-009 (таблица 6)
<400> 188
Ser Ser Val Ser Tyr
1 5
<210> 189
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи MORAb-009 (таблица 6)
<400> 189
Asp Thr Ser
1
<210> 190
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи MORAb-009 (таблица 6)
<400> 190
Gln Gln Trp Ser Lys His Pro Leu Thr
1 5
<210> 191
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи трастузумаба (таблица 6)
<400> 191
Gly Phe Asn Ile Lys Asp Thr Tyr
1 5
<210> 192
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи трастузумаба (таблица 6)
<400> 192
Ile Tyr Pro Thr Asn Gly Tyr Thr
1 5
<210> 193
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи трастузумаба (таблица 6)
<400> 193
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr
1 5 10
<210> 194
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи трастузумаба (таблица 6)
<400> 194
Gln Asp Val Asn Thr Ala
1 5
<210> 195
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи трастузумаба (таблица 6)
<400> 195
Ser Ala Ser
1
<210> 196
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи трастузумаба (таблица 6)
<400> 196
Gln Gln His Tyr Thr Thr Pro Pro Thr
1 5
<210> 197
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 33011-xi (таблица 6)
<400> 197
Gly Ile Ser Leu Ser Ser Asp Ala
1 5
<210> 198
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 33011-xi (таблица 6)
<400> 198
Ile Asn Gly Gly Gly Asn Thr
1 5
<210> 199
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 33011-xi (таблица 6)
<400> 199
Ala Arg Gly Ile Gln His Gly Gly Gly Asn Ser Asp Tyr Tyr Tyr Tyr
1 5 10 15
Gly Met Asp Leu
20
<210> 200
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 33011-xi (таблица 6)
<400> 200
Gln Ser Ile Ser Ser Val
1 5
<210> 201
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 33011-xi (таблица 6)
<400> 201
Leu Ala Ser
1
<210> 202
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 33011-xi (таблица 6)
<400> 202
Gln Thr Asn Tyr Gly Thr Ser Ser Ser Asn Tyr Gly Phe Ala
1 5 10
<210> 203
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 33011-zu (таблица 6)
<400> 203
Gly Ile Ser Leu Ser Ser Asp Ala
1 5
<210> 204
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 33011-zu (таблица 6)
<400> 204
Ile Asn Gly Gly Gly Asn Thr
1 5
<210> 205
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 33011-zu (таблица 6)
<400> 205
Ala Arg Gly Ile Gln His Gly Gly Gly Asn Ser Asp Tyr Tyr Tyr Tyr
1 5 10 15
Gly Met Asp Leu
20
<210> 206
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 33011-zu (таблица 6)
<400> 206
Gln Ser Ile Ser Ser Val
1 5
<210> 207
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 33011-zu (таблица 6)
<400> 207
Leu Ala Ser
1
<210> 208
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 33011-zu (таблица 6)
<400> 208
Gln Thr Asn Tyr Gly Thr Ser Ser Ser Asn Tyr Gly Phe Ala
1 5 10
<210> 209
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 111B10-xi (таблица 6)
<400> 209
Gly Phe Ser Leu Asn Asn Tyr Ala
1 5
<210> 210
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 111B10-xi (таблица 6)
<400> 210
Ile Ser Thr Gly Gly Leu Ala
1 5
<210> 211
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 111B10-xi (таблица 6)
<400> 211
Gly Arg Asn Gly Gly Gly Ser Tyr Ile Phe Tyr Tyr Phe Asp Leu
1 5 10 15
<210> 212
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 111B10-xi (таблица 6)
<400> 212
Gln Ser Ile Ser Ser Tyr
1 5
<210> 213
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 111B10-xi (таблица 6)
<400> 213
Ser Ala Ser
1
<210> 214
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 111B10-xi (таблица 6)
<400> 214
Gln Ser Tyr Tyr Asp Ile Gly Thr Ser Thr
1 5 10
<210> 215
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 111B10-zu (таблица 6)
<400> 215
Gly Phe Ser Leu Asn Asn Tyr Ala
1 5
<210> 216
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 111B10-zu (таблица 6)
<400> 216
Ile Ser Thr Gly Gly Leu Ala
1 5
<210> 217
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 111B10-zu (таблица 6)
<400> 217
Ala Arg Asn Gly Gly Gly Ser Tyr Ile Phe Tyr Tyr Phe Asp Leu
1 5 10 15
<210> 218
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 111B10-zu (таблица 6)
<400> 218
Gln Ser Ile Ser Ser Tyr
1 5
<210> 219
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 111B10-zu (таблица 6)
<400> 219
Ser Ala Ser
1
<210> 220
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 111B10-zu (таблица 6)
<400> 220
Gln Ser Tyr Tyr Asp Ile Gly Thr Ser Thr
1 5 10
<210> 221
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 201C15-xi (таблица 6)
<400> 221
Gly Ile Asp Leu Ser Ser Tyr Ala
1 5
<210> 222
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 201C15-xi (таблица 6)
<400> 222
Ile Asn Ile Gly Gly Arg Val
1 5
<210> 223
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 201C15-xi (таблица 6)
<400> 223
Ala Arg Tyr Tyr Asn Gly Gly Ser Tyr Asp Ile
1 5 10
<210> 224
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 201C15-xi (таблица 6)
<400> 224
Glu Ser Ile Tyr Arg Val
1 5
<210> 225
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 201C15-xi (таблица 6)
<400> 225
Asp Thr Ser
1
<210> 226
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 201C15-xi (таблица 6)
<400> 226
Gln Gly Gly Tyr Tyr Ala Asp Ser Tyr Gly Ile Ala
1 5 10
<210> 227
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 201C15-zu (таблица 6)
<400> 227
Gly Ile Asp Leu Ser Ser Tyr Ala
1 5
<210> 228
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 201C15-zu (таблица 6)
<400> 228
Ile Asn Ile Gly Gly Arg Val
1 5
<210> 229
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 201C15-zu (таблица 6)
<400> 229
Ala Arg Tyr Tyr Asn Gly Gly Ser Tyr Asp Ile
1 5 10
<210> 230
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 201C15-zu (таблица 6)
<400> 230
Glu Ser Ile Tyr Arg Val
1 5
<210> 231
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 201C15-zu (таблица 6)
<400> 231
Asp Thr Ser
1
<210> 232
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 201C15-zu (таблица 6)
<400> 232
Gln Gly Gly Tyr Tyr Ala Asp Ser Tyr Gly Ile Ala
1 5 10
<210> 233
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 346C6-xi (таблица 6)
<400> 233
Gly Phe Ser Leu Ser Ser Tyr Ala
1 5
<210> 234
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 346C6-xi (таблица 6)
<400> 234
Ile Ser Thr Gly Gly Ile Thr
1 5
<210> 235
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 346C6-xi (таблица 6)
<400> 235
Ala Arg Gly Gly Tyr Ala Ala Ser Ser Ala Tyr Tyr Leu Pro Tyr Tyr
1 5 10 15
Phe Asp Leu
<210> 236
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 346C6-xi (таблица 6)
<400> 236
Gln Ser Val Tyr Asn Asn Asn Asn
1 5
<210> 237
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 346C6-xi (таблица 6)
<400> 237
Leu Ala Ser
1
<210> 238
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 346C6-xi (таблица 6)
<400> 238
Leu Gly Gly Cys Asp Asp Asp Ala Asp Thr Phe Ala
1 5 10
<210> 239
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 346C6-zu (таблица 6)
<400> 239
Gly Phe Ser Leu Ser Ser Tyr Ala
1 5
<210> 240
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 346C6-zu (таблица 6)
<400> 240
Ile Ser Thr Gly Gly Ile Thr
1 5
<210> 241
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 346C6-zu (таблица 6)
<400> 241
Ala Arg Gly Gly Tyr Ala Ala Ser Ser Ala Tyr Tyr Leu Pro Tyr Tyr
1 5 10 15
Phe Asp Leu
<210> 242
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 346C6-zu (таблица 6)
<400> 242
Gln Ser Val Tyr Asn Asn Asn Asn
1 5
<210> 243
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 346C6-zu (таблица 6)
<400> 243
Leu Ala Ser
1
<210> 244
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 346C6-zu (таблица 6)
<400> 244
Leu Gly Gly Cys Asp Asp Asp Ala Asp Thr Phe Ala
1 5 10
<210> 245
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи MORAb-003 (таблица 7)
<400> 245
ggcttcacct tcagcggcta tggg 24
<210> 246
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи MORAb-003 (таблица 7)
<400> 246
attagtagtg gtggtagtta tacc 24
<210> 247
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи MORAb-003 (таблица 7)
<400> 247
gcaagacatg gggacgatcc cgcctggttc gcttat 36
<210> 248
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи MORAb-003 (таблица 7)
<400> 248
tcaagtataa gttccaacaa c 21
<210> 249
<211> 9
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи MORAb-003 (таблица 7)
<400> 249
ggcacatcc 9
<210> 250
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи MORAb-003 (таблица 7)
<400> 250
caacagtgga gtagttaccc gtacatgtac acg 33
<210> 251
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи MORAb-009 (таблица 7)
<400> 251
ggttactcat tcactggcta cacc 24
<210> 252
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи MORAb-009 (таблица 7)
<400> 252
attactcctt acaatggtgc ttct 24
<210> 253
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи MORAb-009 (таблица 7)
<400> 253
gcaagggggg gttacgacgg gaggggtttt gactac 36
<210> 254
<211> 15
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи MORAb-009 (таблица 7)
<400> 254
tcaagtgtaa gttac 15
<210> 255
<211> 9
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи MORAb-009 (таблица 7)
<400> 255
gacacatcc 9
<210> 256
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи MORAb-009 (таблица 7)
<400> 256
cagcagtgga gtaagcaccc tctcacg 27
<210> 257
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 33011-xi (таблица 7)
<400> 257
ggaatctccc tcagtagcga tgca 24
<210> 258
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 33011-xi (таблица 7)
<400> 258
attaatggtg gtggtaacac a 21
<210> 259
<211> 60
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 33011-xi (таблица 7)
<400> 259
gccagaggca ttcaacatgg tggtggtaat agtgattatt attattacgg catggacctc 60
<210> 260
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 33011-xi (таблица 7)
<400> 260
cagagcatta gtagtgtc 18
<210> 261
<211> 9
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 33011-xi (таблица 7)
<400> 261
ctggcatct 9
<210> 262
<211> 42
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 33011-xi (таблица 7)
<400> 262
caaaccaatt atggtactag tagtagtaat tatggttttg ct 42
<210> 263
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 33011-zu (таблица 7)
<400> 263
ggaatttccc tctcctccga cgcg 24
<210> 264
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 33011-zu (таблица 7)
<400> 264
atcaacggcg gcggaaacac c 21
<210> 265
<211> 60
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 33011-zu (таблица 7)
<400> 265
gcgcgcggca tccagcacgg tggtggaaac agcgactact actactatgg gatggatctg 60
<210> 266
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 33011-zu (таблица 7)
<400> 266
cagtcaatta gcagcgtg 18
<210> 267
<211> 9
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 33011-zu (таблица 7)
<400> 267
ttggcctcc 9
<210> 268
<211> 42
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 33011-zu (таблица 7)
<400> 268
caaaccaact acggaacctc cagctccaac tacggctttg cc 42
<210> 269
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 111B10-xi (таблица 7)
<400> 269
ggattctccc tcaataacta tgca 24
<210> 270
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 111B10-xi (таблица 7)
<400> 270
attagtactg gtggtctcgc a 21
<210> 271
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 111B10-xi (таблица 7)
<400> 271
ggcagaaatg gtggtggtag ttatattttc tattattttg acttg 45
<210> 272
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 111B10-xi (таблица 7)
<400> 272
cagagcatta gtagttac 18
<210> 273
<211> 9
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 111B10-xi (таблица 7)
<400> 273
tctgcatcc 9
<210> 274
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 111B10-xi (таблица 7)
<400> 274
caaagctatt atgatattgg tactagtact 30
<210> 275
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 111B10-zu (таблица 7)
<400> 275
ggcttctccc tgaacaacta cgcc 24
<210> 276
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 111B10-zu (таблица 7)
<400> 276
atcagcacag gcggcctggc c 21
<210> 277
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 111B10-zu (таблица 7)
<400> 277
gccagaaacg gcggaggctc ctacatcttc tactacttcg acctg 45
<210> 278
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 111B10-zu (таблица 7)
<400> 278
cagtccatct cctcctac 18
<210> 279
<211> 9
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 111B10-zu (таблица 7)
<400> 279
tctgcctcc 9
<210> 280
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 111B10-zu (таблица 7)
<400> 280
cagtcctact acgacatcgg cacctccacc 30
<210> 281
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 201C15-xi (таблица 7)
<400> 281
ggaatcgacc tcagtagcta tgca 24
<210> 282
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 201C15-xi (таблица 7)
<400> 282
attaatattg gtggtcgcgt a 21
<210> 283
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 201C15-xi (таблица 7)
<400> 283
gccagatatt ataatggtgg tagttatgac atc 33
<210> 284
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 201C15-xi (таблица 7)
<400> 284
gagagcattt atcgcgta 18
<210> 285
<211> 9
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 201C15-xi (таблица 7)
<400> 285
gatacatcc 9
<210> 286
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 201C15-xi (таблица 7)
<400> 286
caaggcggtt attatgctga tagttatggt attgct 36
<210> 287
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 201C15-zu (таблица 7)
<400> 287
ggaatcgacc tgtcctccta cgct 24
<210> 288
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 201C15-zu (таблица 7)
<400> 288
atcaacatcg gcggcagagt g 21
<210> 289
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 201C15-zu (таблица 7)
<400> 289
gcccggtact acaacggcgg ctcctacgat atc 33
<210> 290
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 201C15-zu (таблица 7)
<400> 290
gagtccatct accgggtg 18
<210> 291
<211> 9
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 201C15-zu (таблица 7)
<400> 291
gacaccagc 9
<210> 292
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 201C15-zu (таблица 7)
<400> 292
cagggcggct actacgccga ctcctacgga atcgct 36
<210> 293
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 346C6-xi (таблица 7)
<400> 293
ggattctccc tcagtagtta tgca 24
<210> 294
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 346C6-xi (таблица 7)
<400> 294
attagtactg gtggtatcac a 21
<210> 295
<211> 57
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 346C6-xi (таблица 7)
<400> 295
gccagagggg gatatgctgc tagtagtgct tattatctcc cgtactactt tgacttg 57
<210> 296
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 346C6-xi (таблица 7)
<400> 296
cagagtgttt ataataataa caac 24
<210> 297
<211> 9
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 346C6-xi (таблица 7)
<400> 297
ctggcatcc 9
<210> 298
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 346C6-xi (таблица 7)
<400> 298
ctaggtggtt gtgatgatga tgctgatact tttgct 36
<210> 299
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 тяжелой цепи 346C6-zu (таблица 7)
<400> 299
ggcttctccc tgtcctccta cgct 24
<210> 300
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 тяжелой цепи 346C6-zu (таблица 7)
<400> 300
atctctaccg gcggaattac c 21
<210> 301
<211> 57
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи 346C6-zu (таблица 7)
<400> 301
gctagaggcg gctacgccgc cagctccgct tactacctgc cctactactt cgacctg 57
<210> 302
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR1 легкой цепи 346C6-zu (таблица 7)
<400> 302
cagtccgtgt ataacaacaa caac 24
<210> 303
<211> 9
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR2 легкой цепи 346C6-zu (таблица 7)
<400> 303
ctggcctcc 9
<210> 304
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи 346C6-zu (таблица 7)
<400> 304
ctgggcggct gcgacgacga cgccgatacc tttgct 36
<210> 305
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь MORAb-009 (таблица 8)
<400> 305
Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Glu Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Thr Met Asn Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Leu Ile Thr Pro Tyr Asn Gly Ala Ser Ser Tyr Asn Gln Lys Phe
50 55 60
Arg Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Asp Leu Leu Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Arg Gly Gly Tyr Asp Gly Arg Gly Phe Asp Tyr Trp Gly Ser Gly
100 105 110
Thr Pro Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 306
<211> 213
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь MORAb-009 (таблица 8)
<400> 306
Asp Ile Glu Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Gly Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Asn Ser Tyr Ser Leu Thr Ile Ser Ser Val Glu Ala Glu
65 70 75 80
Asp Asp Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Lys His Pro Leu Thr
85 90 95
Phe Gly Ser Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 307
<211> 451
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь трастузумаба (таблица 8)
<400> 307
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 308
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь трастузумаба (таблица 8)
<400> 308
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 309
<211> 453
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 33011-xi (таблица 8)
<400> 309
Gln Ser Val Glu Glu Ser Gly Gly Arg Leu Val Thr Pro Gly Thr Pro
1 5 10 15
Leu Thr Leu Thr Cys Thr Val Ser Gly Ile Ser Leu Ser Ser Asp Ala
20 25 30
Ile Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Tyr Ile Gly
35 40 45
Ile Ile Asn Gly Gly Gly Asn Thr Tyr Tyr Ala Ser Trp Ala Lys Gly
50 55 60
Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp Leu Lys Ile Thr
65 70 75 80
Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Ala Arg Gly Ile
85 90 95
Gln His Gly Gly Gly Asn Ser Asp Tyr Tyr Tyr Tyr Gly Met Asp Leu
100 105 110
Trp Gly Pro Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
195 200 205
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
210 215 220
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
260 265 270
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
275 280 285
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
305 310 315 320
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
325 330 335
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
340 345 350
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
355 360 365
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
370 375 380
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
385 390 395 400
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
405 410 415
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
435 440 445
Leu Ser Pro Gly Lys
450
<210> 310
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 33011-xi (таблица 8)
<400> 310
Glu Val Leu Met Thr Gln Thr Pro Ser Ser Val Ser Ala Ala Val Gly
1 5 10 15
Asp Thr Val Thr Ile Lys Cys Gln Ala Ser Gln Ser Ile Ser Ser Val
20 25 30
Leu Ser Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile
35 40 45
Tyr Leu Ala Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Asp Leu Glu Cys
65 70 75 80
Asp Asp Ala Ala Thr Tyr Tyr Cys Gln Thr Asn Tyr Gly Thr Ser Ser
85 90 95
Ser Asn Tyr Gly Phe Ala Phe Gly Gly Gly Thr Glu Val Val Val Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 311
<211> 456
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 33011-zu (таблица 8)
<400> 311
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Ile Ser Leu Ser Ser Asp
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Tyr Ile
35 40 45
Gly Ile Ile Asn Gly Gly Gly Asn Thr Tyr Tyr Ala Ser Trp Ala Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg His Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Ile Gln His Gly Gly Gly Asn Ser Asp Tyr Tyr Tyr Tyr Gly
100 105 110
Met Asp Leu Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
210 215 220
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
325 330 335
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
355 360 365
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 312
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 33011-zu (таблица 8)
<400> 312
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Ser Ile Ser Ser Val
20 25 30
Leu Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Leu Ala Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Cys
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Thr Asn Tyr Gly Thr Ser Ser
85 90 95
Ser Asn Tyr Gly Phe Ala Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 313
<211> 448
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 111B10-xi (таблица 8)
<400> 313
Gln Ser Val Glu Glu Ser Gly Gly Arg Leu Val Thr Pro Gly Thr Pro
1 5 10 15
Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Asn Asn Tyr Ala
20 25 30
Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile Gly
35 40 45
Ser Ile Ser Thr Gly Gly Leu Ala Phe Tyr Ala Asn Trp Ala Lys Gly
50 55 60
Arg Phe Thr Ile Ser Arg Thr Ser Thr Thr Val Asp Leu Lys Met Thr
65 70 75 80
Ser Leu Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Gly Arg Asn Gly
85 90 95
Gly Gly Ser Tyr Ile Phe Tyr Tyr Phe Asp Leu Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
260 265 270
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
405 410 415
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 314
<211> 215
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 111B10-xi (таблица 8)
<400> 314
Ala Phe Glu Leu Thr Gln Thr Pro Ser Ser Val Glu Ala Ala Val Gly
1 5 10 15
Gly Thr Ile Thr Ile Lys Cys Gln Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Ser Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Thr Leu Ala Ser Gly Val Ser Ser Arg Phe Lys Gly
50 55 60
Ser Gly Ser Gly Thr Glu Tyr Thr Leu Thr Ile Ser Asp Leu Glu Cys
65 70 75 80
Ala Asp Ala Ala Thr Tyr Phe Cys Gln Ser Tyr Tyr Asp Ile Gly Thr
85 90 95
Ser Thr Phe Gly Gly Gly Thr Glu Val Val Val Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 315
<211> 451
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 111B10-zu (таблица 8)
<400> 315
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Leu Asn Asn Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Ser Thr Gly Gly Leu Ala Phe Tyr Ala Asn Trp Ala Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Asn Gly Gly Gly Ser Tyr Ile Phe Tyr Tyr Phe Asp Leu Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 316
<211> 215
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 111B10-zu (таблица 8)
<400> 316
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Cys
65 70 75 80
Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Ser Tyr Tyr Asp Ile Gly Thr
85 90 95
Ser Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 317
<211> 444
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 201C15-xi (таблица 8)
<400> 317
Gln Ser Val Lys Glu Ser Gly Gly Arg Leu Val Thr Pro Gly Thr Pro
1 5 10 15
Leu Thr Leu Thr Cys Thr Val Ser Gly Ile Asp Leu Ser Ser Tyr Ala
20 25 30
Met Gly Trp Phe Arg Gln Ala Pro Gly Lys Gly Leu Glu Tyr Ile Gly
35 40 45
Thr Ile Asn Ile Gly Gly Arg Val Tyr Tyr Ala Ser Trp Ala Lys Gly
50 55 60
Arg Phe Thr Ile Ser Arg Thr Ser Thr Thr Val Asp Leu Lys Ala Pro
65 70 75 80
Ser Leu Thr Ala Glu Asp Thr Ala Thr Tyr Phe Cys Ala Arg Tyr Tyr
85 90 95
Asn Gly Gly Ser Tyr Asp Ile Trp Gly Pro Gly Thr Leu Val Thr Val
100 105 110
Ser Leu Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser
115 120 125
Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys
130 135 140
Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu
145 150 155 160
Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu
165 170 175
Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr
180 185 190
Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val
195 200 205
Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro
210 215 220
Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe
225 230 235 240
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
245 250 255
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
260 265 270
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
275 280 285
Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
290 295 300
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
305 310 315 320
Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
325 330 335
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg
340 345 350
Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
355 360 365
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
370 375 380
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
385 390 395 400
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
405 410 415
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
420 425 430
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440
<210> 318
<211> 217
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 201C15-xi (таблица 8)
<400> 318
Asp Val Val Met Thr Gln Thr Pro Ala Ser Ala Ser Glu Pro Val Gly
1 5 10 15
Gly Thr Val Thr Ile Lys Cys Gln Ala Ser Glu Ser Ile Tyr Arg Val
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile
35 40 45
Tyr Asp Thr Ser Thr Leu Ala Ser Gly Ala Pro Ser Arg Phe Lys Gly
50 55 60
Ser Gly Tyr Gly Thr Glu Phe Thr Leu Thr Ile Ser Gly Val Gln Cys
65 70 75 80
Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gly Gly Tyr Tyr Ala Asp Ser
85 90 95
Tyr Gly Ile Ala Phe Gly Gly Gly Thr Glu Val Val Val Lys Arg Thr
100 105 110
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu
115 120 125
Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro
130 135 140
Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly
145 150 155 160
Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr
165 170 175
Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His
180 185 190
Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val
195 200 205
Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 319
<211> 447
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 201C15-zu (таблица 8)
<400> 319
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ser Ala Ser Gly Ile Asp Leu Ser Ser Tyr
20 25 30
Ala Met Gly Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Tyr Ile
35 40 45
Gly Thr Ile Asn Ile Gly Gly Arg Val Tyr Tyr Ala Ser Trp Ala Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Tyr Tyr Asn Gly Gly Ser Tyr Asp Ile Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
115 120 125
Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys
130 135 140
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
145 150 155 160
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
165 170 175
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
180 185 190
Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn
195 200 205
Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His
210 215 220
Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 320
<211> 217
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 201C15-zu (таблица 8)
<400> 320
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Glu Ser Ile Tyr Arg Val
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asp Thr Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Cys
65 70 75 80
Asp Asp Ala Ala Thr Tyr Tyr Cys Gln Gly Gly Tyr Tyr Ala Asp Ser
85 90 95
Tyr Gly Ile Ala Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr
100 105 110
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu
115 120 125
Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro
130 135 140
Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly
145 150 155 160
Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr
165 170 175
Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His
180 185 190
Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val
195 200 205
Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 321
<211> 452
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 346C6-xi (таблица 8)
<400> 321
Gln Ser Val Glu Glu Ser Gly Gly Arg Leu Val Lys Pro Asp Glu Ser
1 5 10 15
Leu Thr Leu Thr Cys Thr Ala Ser Gly Phe Ser Leu Ser Ser Tyr Ala
20 25 30
Met Ile Trp Val Arg Gln Ala Pro Gly Glu Gly Leu Glu Trp Ile Gly
35 40 45
Thr Ile Ser Thr Gly Gly Ile Thr Tyr Tyr Ala Ser Trp Ala Lys Gly
50 55 60
Arg Phe Thr Ile Ser Lys Thr Ser Thr Thr Val Asp Leu Lys Ile Thr
65 70 75 80
Ser Pro Thr Thr Glu Asp Thr Ala Thr Tyr Phe Cys Ala Arg Gly Gly
85 90 95
Tyr Ala Ala Ser Ser Ala Tyr Tyr Leu Pro Tyr Tyr Phe Asp Leu Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
210 215 220
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
225 230 235 240
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
260 265 270
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val
355 360 365
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Pro Gly Lys
450
<210> 322
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 346C6-xi (таблица 8)
<400> 322
Ala Ala Val Leu Thr Gln Thr Pro Ser Pro Val Ser Ala Ala Val Gly
1 5 10 15
Gly Thr Val Thr Ile Ser Cys Gln Ser Ser Gln Ser Val Tyr Asn Asn
20 25 30
Asn Asn Leu Ala Trp Phe Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu
35 40 45
Leu Ile Tyr Leu Ala Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe
50 55 60
Ser Gly Ser Gly Ser Gly Thr Gln Phe Thr Leu Thr Ile Ser Gly Val
65 70 75 80
Gln Cys Asp Asp Ala Ala Thr Tyr Tyr Cys Leu Gly Gly Cys Asp Asp
85 90 95
Asp Ala Asp Thr Phe Ala Phe Gly Gly Gly Thr Glu Val Val Val Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 323
<211> 455
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 346C6-zu (таблица 8)
<400> 323
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Leu Ser Ser Tyr
20 25 30
Ala Met Ile Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Thr Ile Ser Thr Gly Gly Ile Thr Tyr Tyr Ala Ser Trp Ala Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Gly Tyr Ala Ala Ser Ser Ala Tyr Tyr Leu Pro Tyr Tyr Phe
100 105 110
Asp Leu Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu
210 215 220
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
225 230 235 240
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
275 280 285
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
290 295 300
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
305 310 315 320
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
325 330 335
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
340 345 350
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys
355 360 365
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
370 375 380
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
385 390 395 400
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
405 410 415
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
420 425 430
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
435 440 445
Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 324
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 346C6-zu (таблица 8)
<400> 324
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gln Ser Ser Gln Ser Val Tyr Asn Asn
20 25 30
Asn Asn Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu
35 40 45
Leu Ile Tyr Leu Ala Ser Thr Leu Ala Ser Gly Val Pro Ser Arg Phe
50 55 60
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
65 70 75 80
Gln Cys Glu Asp Ala Ala Thr Tyr Tyr Cys Leu Gly Gly Cys Asp Asp
85 90 95
Asp Ala Asp Thr Phe Ala Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 325
<211> 1350
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь MORAb-003 (таблица 9)
<400> 325
gaggtccaac tggtggagag cggtggaggt gttgtgcaac ctggccggtc cctgcgcctg 60
tcctgctccg catctggctt caccttcagc ggctatgggt tgtcttgggt gagacaggca 120
cctggaaaag gtcttgagtg ggttgcaatg attagtagtg gtggtagtta tacctactat 180
gcagacagtg tgaagggtag atttgcaata tcgcgagaca acgccaagaa cacattgttc 240
ctgcaaatgg acagcctgag acccgaagac accggggtct atttttgtgc aagacatggg 300
gacgatcccg cctggttcgc ttattggggc caagggaccc cggtcaccgt ctcctcagcc 360
tccaccaagg gcccatcggt cttccccctg gcaccctcct ccaagagcac ctctgggggc 420
acagcggccc tgggctgcct ggtcaaggac tacttccccg aaccggtgac ggtgtcgtgg 480
aactcaggcg ccctgaccag cggcgtgcac accttcccgg ctgtcctaca gtcctcagga 540
ctctactccc tcagcagcgt ggtgaccgtg ccctccagca gcttgggcac ccagacctac 600
atctgcaacg tgaatcacaa gcccagcaac accaaggtgg acaagaaagt tgagcccaaa 660
tcttgtgaca aaactcacac atgcccaccg tgcccagcac ctgaactcct ggggggaccg 720
tcagtcttcc tcttcccccc aaaacccaag gacaccctca tgatctcccg gacccctgag 780
gtcacatgcg tggtggtgga cgtgagccac gaagaccctg aggtcaagtt caactggtac 840
gtggacggcg tggaggtgca taatgccaag acaaagccgc gggaggagca gtacaacagc 900
acgtaccgtg tggtcagcgt cctcaccgtc ctgcaccagg actggctgaa tggcaaggag 960
tacaagtgca aggtctccaa caaagccctc ccagccccca tcgagaaaac catctccaaa 1020
gccaaagggc agccccgaga accacaggtg tacaccctgc ccccatcccg ggatgagctg 1080
accaagaacc aggtcagcct gacctgcctg gtcaaaggct tctatcccag cgacatcgcc 1140
gtggagtggg agagcaatgg gcagccggag aacaactaca agaccacgcc tcccgtgctg 1200
gactccgacg gctccttctt cttatattca aagctcaccg tggacaagag caggtggcag 1260
caggggaacg tcttctcatg ctccgtgatg catgaggctc tgcacaacca ctacacgcag 1320
aagagcctct ccctgtctcc cgggaaatga 1350
<210> 326
<211> 654
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Легкая цепь MORAb-003 (таблица 9)
<400> 326
gacatccagc tgacccagag cccaagcagc ctgagcgcca gcgtgggtga cagagtgacc 60
atcacctgta gtgtcagctc aagtataagt tccaacaact tgcactggta ccagcagaag 120
ccaggtaagg ctccaaagcc atggatctac ggcacatcca acctggcttc tggtgtgcca 180
agcagattca gcggtagcgg tagcggtacc gactacacct tcaccatcag cagcctccag 240
ccagaggaca tcgccaccta ctactgccaa cagtggagta gttacccgta catgtacacg 300
ttcggccaag ggaccaaggt ggaaatcaaa cgaactgtgg ctgcaccatc tgtcttcatc 360
ttcccgccat ctgatgagca gttgaaatct ggaactgcct ctgttgtgtg cctgctgaat 420
aacttctatc ccagagaggc caaagtacag tggaaggtgg ataacgccct ccaatcgggt 480
aactcccagg agagtgtcac agagcaggac agcaaggaca gcacctacag cctcagcagc 540
accctgacgc tgagcaaagc agactacgag aaacacaaag tctacgcctg cgaagtcacc 600
catcagggcc tgagctcgcc cgtcacaaag agcttcaaca ggggagagtg ttaa 654
<210> 327
<211> 1350
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь MORAb-009 (таблица 9)
<400> 327
caggtacaac tgcagcagtc tgggcctgag ctggagaagc ctggcgcttc agtgaagata 60
tcctgcaagg cttctggtta ctcattcact ggctacacca tgaactgggt gaagcagagc 120
catggaaaga gccttgagtg gattggactt attactcctt acaatggtgc ttctagctac 180
aaccagaagt tcaggggcaa ggccacatta actgtagaca agtcatccag cacagcctac 240
atggacctcc tcagtctgac atctgaagac tctgcagtct atttctgtgc aagggggggt 300
tacgacggga ggggttttga ctactgggga tccgggaccc cggtcaccgt ctcctcagcc 360
tccaccaagg gcccatcggt cttccccctg gcaccctcct ccaagagcac ctctgggggc 420
acagcggccc tgggctgcct ggtcaaggac tacttccccg aaccggtgac ggtgtcgtgg 480
aactcaggcg ccctgaccag cggcgtgcac accttcccgg ctgtcctaca gtcctcagga 540
ctctactccc tcagcagcgt ggtgaccgtg ccctccagca gcttgggcac ccagacctac 600
atctgcaacg tgaatcacaa gcccagcaac accaaggtgg acaagaaagt tgagcccaaa 660
tcttgtgaca aaactcacac atgcccaccg tgcccagcac ctgaactcct ggggggaccg 720
tcagtcttcc tcttcccccc aaaacccaag gacaccctca tgatctcccg gacccctgag 780
gtcacatgcg tggtggtgga cgtgagccac gaagaccctg aggtcaagtt caactggtac 840
gtggacggcg tggaggtgca taatgccaag acaaagccgc gggaggagca gtacaacagc 900
acgtaccgtg tggtcagcgt cctcaccgtc ctgcaccagg actggctgaa tggcaaggag 960
tacaagtgca aggtctccaa caaagccctc ccagccccca tcgagaaaac catctccaaa 1020
gccaaagggc agccccgaga accacaggtg tacaccctgc ccccatcccg ggatgagctg 1080
accaagaacc aggtcagcct gacctgcctg gtcaaaggct tctatcccag cgacatcgcc 1140
gtggagtggg agagcaatgg gcagccggag aacaactaca agaccacgcc tcccgtgctg 1200
gactccgacg gctccttctt cctctacagc aagctcaccg tggacaagag caggtggcag 1260
caggggaacg tcttctcatg ctccgtgatg catgaggctc tgcacaacca ctacacgcag 1320
aagagcctct ccctgtctcc cgggaaatga 1350
<210> 328
<211> 642
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Легкая цепь MORAb-009 (таблица 9)
<400> 328
gacatcgagc tcactcagtc tccagcaatc atgtctgcat ctccagggga gaaggtcacc 60
atgacctgca gtgccagctc aagtgtaagt tacatgcact ggtaccagca gaagtcaggc 120
acctccccca aaagatggat ttatgacaca tccaaactgg cttctggagt cccaggtcgc 180
ttcagtggca gtgggtctgg aaactcttac tctctcacaa tcagcagcgt ggaggctgaa 240
gatgatgcaa cttattactg ccagcagtgg agtaagcacc ctctcacgtt cggatccggg 300
accaaggtgg aaatcaaacg aactgtggct gcaccatctg tcttcatctt cccgccatct 360
gatgagcagt tgaaatctgg aactgcctct gttgtgtgcc tgctgaataa cttctatccc 420
agagaggcca aagtacagtg gaaggtggat aacgccctcc aatcgggtaa ctcccaggag 480
agtgtcacag agcaggacag caaggacagc acctacagcc tcagcagcac cctgacgctg 540
agcaaagcag actacgagaa acacaaagtc tacgcctgcg aagtcaccca tcagggcctg 600
agctcgcccg tcacaaagag cttcaacagg ggagagtgtt aa 642
<210> 329
<211> 1362
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 33011-xi (таблица 9)
<400> 329
cagtcggtgg aggagtccgg gggtcgcctg gtcacgcctg ggacacccct gacactcacc 60
tgcaccgtct ctggaatctc cctcagtagc gatgcaataa gctgggtccg ccaggctcca 120
gggaaggggc tcgaatacat cggaatcatt aatggtggtg gtaacacata ctacgcgagc 180
tgggcgaaag gccgattcac catctccaaa acctcgacca cggtggatct gaaaatcacc 240
agtccgacaa ccgaggacac ggccacctat ttctgtgcca gaggcattca acatggtggt 300
ggtaatagtg attattatta ttacggcatg gacctctggg gcccaggcac cctggtcact 360
gtctcttcag catccaccaa gggcccatcg gtcttccccc tggcaccctc ctccaagagc 420
acctctgggg gcacagcggc cctgggctgc ctggtcaagg actacttccc cgaaccggtg 480
acggtgtcgt ggaactcagg cgccctgacc agcggcgtgc acaccttccc ggctgtccta 540
cagtcctcag gactctactc cctcagcagc gtggtgaccg tgccctccag cagcttgggc 600
acccagacct acatctgcaa cgtgaatcac aagcccagca acaccaaggt ggacaagaaa 660
gttgagccca aatcttgtga caaaactcac acatgcccac cgtgcccagc acctgaactc 720
ctggggggac cgtcagtctt cctcttcccc ccaaaaccca aggacaccct catgatctcc 780
cggacccctg aggtcacatg cgtggtggtg gacgtgagcc acgaagaccc tgaggtcaag 840
ttcaactggt acgtggacgg cgtggaggtg cataatgcca agacaaagcc gcgggaggag 900
cagtacaaca gcacgtaccg tgtggtcagc gtcctcaccg tcctgcacca ggactggctg 960
aatggcaagg agtacaagtg caaggtctcc aacaaagccc tcccagcccc catcgagaaa 1020
accatctcca aagccaaagg gcagccccga gaaccacagg tgtacaccct gcccccatcc 1080
cgggatgagc tgaccaagaa ccaggtcagc ctgacctgcc tggtcaaagg cttctatccc 1140
agcgacatcg ccgtggagtg ggagagcaat gggcagccgg agaacaacta caagaccacg 1200
cctcccgtgc tggactccga cggctccttc ttcttatatt caaagctcac cgtggacaag 1260
agcaggtggc agcaggggaa cgtcttctca tgctccgtga tgcatgaggc tctgcacaac 1320
cactacacgc agaagagcct ctccctgtct cccgggaaat ga 1362
<210> 330
<211> 660
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 33011-xi (таблица 9)
<400> 330
gaagtgttga tgacccagac tccatcctcc gtgtctgcag ctgtgggaga cacagtcacc 60
atcaagtgcc aggccagtca gagcattagt agtgtcttgt cctggtatca gcagaaacca 120
gggcagcctc ccaagctcct gatctatctg gcatccactc tggcatctgg ggtcccatcg 180
cggttcagcg gcagtagatc tgggacagag ttcactctca ccatcagcga cctggagtgt 240
gacgatgctg ccacttacta ctgtcaaacc aattatggta ctagtagtag taattatggt 300
tttgctttcg gcggagggac cgaggtggtc gtcaaacgaa ctgtggctgc accatctgtc 360
ttcatcttcc cgccatctga tgagcagttg aaatctggaa ctgcctctgt tgtgtgcctg 420
ctgaataact tctatcccag agaggccaaa gtacagtgga aggtggataa cgccctccaa 480
tcgggtaact cccaggagag tgtcacagag caggacagca aggacagcac ctacagcctc 540
agcagcaccc tgacgctgag caaagcagac tacgagaaac acaaagtcta cgcctgcgaa 600
gtcacccatc agggcctgag ctcgcccgtc acaaagagct tcaacagggg agagtgttga 660
<210> 331
<211> 1371
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 33011-zu (таблица 9)
<400> 331
gaagtccaac tggtggaaag cgggggagga ctggtgcagc cgggcggatc cctccggctg 60
tcatgtgctg catcgggaat ttccctctcc tccgacgcga ttagctgggt cagacaggcc 120
cccggaaagg ggctggagta catcggtatc atcaacggcg gcggaaacac ctactacgcc 180
tcctgggcca agggccgctt caccatctcg cggcataatt ccaagaacac tctgtacttg 240
caaatgaact ccctgagggc cgaggacacc gccgtgtact actgcgcgcg cggcatccag 300
cacggtggtg gaaacagcga ctactactac tatgggatgg atctgtgggg ccagggaact 360
cttgtgaccg tgtcgtcagc atccaccaag ggcccatcgg tcttccccct ggcaccctcc 420
tccaagagca cctctggggg cacagcggcc ctgggctgcc tggtcaagga ctacttcccc 480
gaaccggtga cggtgtcgtg gaactcaggc gccctgacca gcggcgtgca caccttcccg 540
gctgtcctac agtcctcagg actctactcc ctcagcagcg tggtgaccgt gccctccagc 600
agcttgggca cccagaccta catctgcaac gtgaatcaca agcccagcaa caccaaggtg 660
gacaagaaag ttgagcccaa atcttgtgac aaaactcaca catgcccacc gtgcccagca 720
cctgaactcc tggggggacc gtcagtcttc ctcttccccc caaaacccaa ggacaccctc 780
atgatctccc ggacccctga ggtcacatgc gtggtggtgg acgtgagcca cgaagaccct 840
gaggtcaagt tcaactggta cgtggacggc gtggaggtgc ataatgccaa gacaaagccg 900
cgggaggagc agtacaacag cacgtaccgt gtggtcagcg tcctcaccgt cctgcaccag 960
gactggctga atggcaagga gtacaagtgc aaggtctcca acaaagccct cccagccccc 1020
atcgagaaaa ccatctccaa agccaaaggg cagccccgag aaccacaggt gtacaccctg 1080
cccccatccc gggatgagct gaccaagaac caggtcagcc tgacctgcct ggtcaaaggc 1140
ttctatccca gcgacatcgc cgtggagtgg gagagcaatg ggcagccgga gaacaactac 1200
aagaccacgc ctcccgtgct ggactccgac ggctccttct tcttatattc aaagctcacc 1260
gtggacaaga gcaggtggca gcaggggaac gtcttctcat gctccgtgat gcatgaggct 1320
ctgcacaacc actacacgca gaagagcctc tccctgtctc ccgggaaatg a 1371
<210> 332
<211> 660
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 33011-zu (таблица 9)
<400> 332
gacattcaga tgacccagtc cccaagctcg ctgtccgcct ccgtgggcga ccgcgtgacc 60
atcacgtgcc aggcgtccca gtcaattagc agcgtgctct cctggtacca acagaagccg 120
gggaaagcac ccaagctgct gatctacttg gcctccactc tggcctcggg agtgccttca 180
cggttctccg gatcgggatc tggtactgat ttcaccctca ccatctcgag ccttcagtgc 240
gaggacatcg ctacttacta ttgtcaaacc aactacggaa cctccagctc caactacggc 300
tttgccttcg gtggcgggac caaggtcgaa atcaaacgaa ctgtggctgc accatctgtc 360
ttcatcttcc cgccatctga tgagcagttg aaatctggaa ctgcctctgt tgtgtgcctg 420
ctgaataact tctatcccag agaggccaaa gtacagtgga aggtggataa cgccctccaa 480
tcgggtaact cccaggagag tgtcacagag caggacagca aggacagcac ctacagcctc 540
agcagcaccc tgacgctgag caaagcagac tacgagaaac acaaagtcta cgcctgcgaa 600
gtcacccatc agggcctgag ctcgcccgtc acaaagagct tcaacagggg agagtgttga 660
<210> 333
<211> 1347
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 111B10-xi (таблица 9)
<400> 333
cagtcggtgg aggagtccgg gggtcgcctg gtcacgcctg ggacacccct gacactcacc 60
tgcacagtct ctggattctc cctcaataac tatgcaatga gctgggtccg ccaggctcca 120
gggaaggggc tggaatggat cggatccatt agtactggtg gtctcgcatt ctacgcgaac 180
tgggcaaaag gccgattcac catctccaga acctcgacca cggtggatct gaaaatgacc 240
agtctgacaa ccgaggacac ggccacctat ttctgtggca gaaatggtgg tggtagttat 300
attttctatt attttgactt gtggggccaa ggcaccctcg tcactgtctc ttcagcatcc 360
accaagggcc catcggtctt ccccctggca ccctcctcca agagcacctc tgggggcaca 420
gcggccctgg gctgcctggt caaggactac ttccccgaac cggtgacggt gtcgtggaac 480
tcaggcgccc tgaccagcgg cgtgcacacc ttcccggctg tcctacagtc ctcaggactc 540
tactccctca gcagcgtggt gaccgtgccc tccagcagct tgggcaccca gacctacatc 600
tgcaacgtga atcacaagcc cagcaacacc aaggtggaca agaaagttga gcccaaatct 660
tgtgacaaaa ctcacacatg cccaccgtgc ccagcacctg aactcctggg gggaccgtca 720
gtcttcctct tccccccaaa acccaaggac accctcatga tctcccggac ccctgaggtc 780
acatgcgtgg tggtggacgt gagccacgaa gaccctgagg tcaagttcaa ctggtacgtg 840
gacggcgtgg aggtgcataa tgccaagaca aagccgcggg aggagcagta caacagcacg 900
taccgtgtgg tcagcgtcct caccgtcctg caccaggact ggctgaatgg caaggagtac 960
aagtgcaagg tctccaacaa agccctccca gcccccatcg agaaaaccat ctccaaagcc 1020
aaagggcagc cccgagaacc acaggtgtac accctgcccc catcccggga tgagctgacc 1080
aagaaccagg tcagcctgac ctgcctggtc aaaggcttct atcccagcga catcgccgtg 1140
gagtgggaga gcaatgggca gccggagaac aactacaaga ccacgcctcc cgtgctggac 1200
tccgacggct ccttcttctt atattcaaag ctcaccgtgg acaagagcag gtggcagcag 1260
gggaacgtct tctcatgctc cgtgatgcat gaggctctgc acaaccacta cacgcagaag 1320
agcctctccc tgtctcccgg gaaatga 1347
<210> 334
<211> 648
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 111B10-xi (таблица 9)
<400> 334
gcattcgaat tgacccagac tccatcctcc gtggaggcag ctgtgggagg cacaatcacc 60
atcaagtgcc aggccagtca gagcattagt agttacttat cctggtatca gcagaaacca 120
gggcagcctc ccaagctcct gatctattct gcatccactc tggcatctgg ggtctcatcg 180
cggttcaaag gcagtggatc tgggacagag tacactctca ccatcagcga cctggagtgt 240
gccgatgctg ccacttactt ctgtcaaagc tattatgata ttggtactag tactttcggc 300
ggagggaccg aggtggtcgt caaacgaact gtggctgcac catctgtctt catcttcccg 360
ccatctgatg agcagttgaa atctggaact gcctctgttg tgtgcctgct gaataacttc 420
tatcccagag aggccaaagt acagtggaag gtggataacg ccctccaatc gggtaactcc 480
caggagagtg tcacagagca ggacagcaag gacagcacct acagcctcag cagcaccctg 540
acgctgagca aagcagacta cgagaaacac aaagtctacg cctgcgaagt cacccatcag 600
ggcctgagct cgcccgtcac aaagagcttc aacaggggag agtgttga 648
<210> 335
<211> 1356
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 111B10-zu (таблица 9)
<400> 335
gaagtgcagc tggtggaatc tggcggcgga ctggtgcagc ctggcggatc tctgagactg 60
tcttgtgccg cctccggctt ctccctgaac aactacgcca tgtcctgggt gcgacaggcc 120
cctggcaaag gcctggaatg gatcggctcc atcagcacag gcggcctggc cttctacgcc 180
aattgggcca agggccggtt caccatcagc cgggacaact ccaagaacac cctgtacctc 240
cagatgaact ccctgcgggc cgaggacacc gccgtgtact actgtgccag aaacggcgga 300
ggctcctaca tcttctacta cttcgacctg tggggccagg gcaccctcgt gacagtgtca 360
tctgcatcca ccaagggccc atcggtcttc cccctggcac cctcctccaa gagcacctct 420
gggggcacag cggccctggg ctgcctggtc aaggactact tccccgaacc ggtgacggtg 480
tcgtggaact caggcgccct gaccagcggc gtgcacacct tcccggctgt cctacagtcc 540
tcaggactct actccctcag cagcgtggtg accgtgccct ccagcagctt gggcacccag 600
acctacatct gcaacgtgaa tcacaagccc agcaacacca aggtggacaa gaaagttgag 660
cccaaatctt gtgacaaaac tcacacatgc ccaccgtgcc cagcacctga actcctgggg 720
ggaccgtcag tcttcctctt ccccccaaaa cccaaggaca ccctcatgat ctcccggacc 780
cctgaggtca catgcgtggt ggtggacgtg agccacgaag accctgaggt caagttcaac 840
tggtacgtgg acggcgtgga ggtgcataat gccaagacaa agccgcggga ggagcagtac 900
aacagcacgt accgtgtggt cagcgtcctc accgtcctgc accaggactg gctgaatggc 960
aaggagtaca agtgcaaggt ctccaacaaa gccctcccag cccccatcga gaaaaccatc 1020
tccaaagcca aagggcagcc ccgagaacca caggtgtaca ccctgccccc atcccgggat 1080
gagctgacca agaaccaggt cagcctgacc tgcctggtca aaggcttcta tcccagcgac 1140
atcgccgtgg agtgggagag caatgggcag ccggagaaca actacaagac cacgcctccc 1200
gtgctggact ccgacggctc cttcttctta tattcaaagc tcaccgtgga caagagcagg 1260
tggcagcagg ggaacgtctt ctcatgctcc gtgatgcatg aggctctgca caaccactac 1320
acgcagaaga gcctctccct gtctcccggg aaatga 1356
<210> 336
<211> 648
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 111B10-zu (таблица 9)
<400> 336
gatattcaga tgacccagtc cccctccagc ctgtccgctt ctgtgggcga cagagtgacc 60
atcacctgtc aggcctccca gtccatctcc tcctacctgt cctggtatca gcagaagccc 120
ggcaaggccc ccaagctgct gatctactct gcctccacac tggcctccgg cgtgccctct 180
agattctccg gctctggctc tggcaccgac tttaccctga ccatcagctc cctccagtgc 240
gaggatgccg ccacctacta ctgccagtcc tactacgaca tcggcacctc caccttcggc 300
ggaggcacca aggtggaaat caaacgaact gtggctgcac catctgtctt catcttcccg 360
ccatctgatg agcagttgaa atctggaact gcctctgttg tgtgcctgct gaataacttc 420
tatcccagag aggccaaagt acagtggaag gtggataacg ccctccaatc gggtaactcc 480
caggagagtg tcacagagca ggacagcaag gacagcacct acagcctcag cagcaccctg 540
acgctgagca aagcagacta cgagaaacac aaagtctacg cctgcgaagt cacccatcag 600
ggcctgagct cgcccgtcac aaagagcttc aacaggggag agtgttga 648
<210> 337
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 201C15-xi (таблица 9)
<400> 337
cagtcagtga aggagtccgg gggtcgcctg gtcacgcctg ggacacccct gacactcacc 60
tgcacagtct ctggaatcga cctcagtagc tatgcaatgg gctggttccg ccaggctcca 120
gggaaggggc tggaatacat cggaaccatt aatattggtg gtcgcgtata ttacgcgagc 180
tgggcaaaag gccgattcac catctccaga acctcgacca cggtggatct gaaagcgccc 240
agtctgacag ccgaggacac ggccacctat ttctgtgcca gatattataa tggtggtagt 300
tatgacatct ggggcccagg caccctggtc accgtctctt tagcatccac caagggccca 360
tcggtcttcc ccctggcacc ctcctccaag agcacctctg ggggcacagc ggccctgggc 420
tgcctggtca aggactactt ccccgaaccg gtgacggtgt cgtggaactc aggcgccctg 480
accagcggcg tgcacacctt cccggctgtc ctacagtcct caggactcta ctccctcagc 540
agcgtggtga ccgtgccctc cagcagcttg ggcacccaga cctacatctg caacgtgaat 600
cacaagccca gcaacaccaa ggtggacaag aaagttgagc ccaaatcttg tgacaaaact 660
cacacatgcc caccgtgccc agcacctgaa ctcctggggg gaccgtcagt cttcctcttc 720
cccccaaaac ccaaggacac cctcatgatc tcccggaccc ctgaggtcac atgcgtggtg 780
gtggacgtga gccacgaaga ccctgaggtc aagttcaact ggtacgtgga cggcgtggag 840
gtgcataatg ccaagacaaa gccgcgggag gagcagtaca acagcacgta ccgtgtggtc 900
agcgtcctca ccgtcctgca ccaggactgg ctgaatggca aggagtacaa gtgcaaggtc 960
tccaacaaag ccctcccagc ccccatcgag aaaaccatct ccaaagccaa agggcagccc 1020
cgagaaccac aggtgtacac cctgccccca tcccgggatg agctgaccaa gaaccaggtc 1080
agcctgacct gcctggtcaa aggcttctat cccagcgaca tcgccgtgga gtgggagagc 1140
aatgggcagc cggagaacaa ctacaagacc acgcctcccg tgctggactc cgacggctcc 1200
ttcttcttat attcaaagct caccgtggac aagagcaggt ggcagcaggg gaacgtcttc 1260
tcatgctccg tgatgcatga ggctctgcac aaccactaca cgcagaagag cctctccctg 1320
tctcccggga aatga 1335
<210> 338
<211> 654
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 201C15-xi (таблица 9)
<400> 338
gatgttgtga tgacccagac tccagcctcc gcgtctgaac ctgtgggagg cacagtcacc 60
atcaagtgcc aggccagtga gagcatttat cgcgtattgg cctggtatca gcagaaacca 120
gggcagcctc ccaagctcct gatctatgat acatccactc tggcatctgg ggccccatcg 180
cggttcaaag gcagtggata tgggacagag ttcactctca ccatcagcgg cgtgcagtgt 240
gaagatgctg ccacttacta ctgtcaaggc ggttattatg ctgatagtta tggtattgct 300
ttcggcggag ggaccgaggt ggtggtcaaa cgaactgtgg ctgcaccatc tgtcttcatc 360
ttcccgccat ctgatgagca gttgaaatct ggaactgcct ctgttgtgtg cctgctgaat 420
aacttctatc ccagagaggc caaagtacag tggaaggtgg ataacgccct ccaatcgggt 480
aactcccagg agagtgtcac agagcaggac agcaaggaca gcacctacag cctcagcagc 540
accctgacgc tgagcaaagc agactacgag aaacacaaag tctacgcctg cgaagtcacc 600
catcagggcc tgagctcgcc cgtcacaaag agcttcaaca ggggagagtg ttga 654
<210> 339
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 201C15-zu (таблица 9)
<400> 339
caggtgcagc tggtggaatc tggcggagga ctggtgcagc ctggcggctc tctgagactg 60
tcctgttccg cctccggaat cgacctgtcc tcctacgcta tgggctgggt gcgacaggct 120
cctggcaagg gcctggagta catcggcacc atcaacatcg gcggcagagt gtactacgcc 180
tcctgggcca agggccggtt caccatctcc agagacaact ccaagaacac cctgtacctc 240
cagatgaact ccctgcgggc cgaggacacc gccgtgtact actgcgcccg gtactacaac 300
ggcggctcct acgatatctg gggccagggc acactcgtga ccgtgtcctc tgcatccacc 360
aagggcccat cggtcttccc cctggcaccc tcctccaaga gcacctctgg gggcacagcg 420
gccctgggct gcctggtcaa ggactacttc cccgaaccgg tgacggtgtc gtggaactca 480
ggcgccctga ccagcggcgt gcacaccttc ccggctgtcc tacagtcctc aggactctac 540
tccctcagca gcgtggtgac cgtgccctcc agcagcttgg gcacccagac ctacatctgc 600
aacgtgaatc acaagcccag caacaccaag gtggacaaga aagttgagcc caaatcttgt 660
gacaaaactc acacatgccc accgtgccca gcacctgaac tcctgggggg accgtcagtc 720
ttcctcttcc ccccaaaacc caaggacacc ctcatgatct cccggacccc tgaggtcaca 780
tgcgtggtgg tggacgtgag ccacgaagac cctgaggtca agttcaactg gtacgtggac 840
ggcgtggagg tgcataatgc caagacaaag ccgcgggagg agcagtacaa cagcacgtac 900
cgtgtggtca gcgtcctcac cgtcctgcac caggactggc tgaatggcaa ggagtacaag 960
tgcaaggtct ccaacaaagc cctcccagcc cccatcgaga aaaccatctc caaagccaaa 1020
gggcagcccc gagaaccaca ggtgtacacc ctgcccccat cccgggatga gctgaccaag 1080
aaccaggtca gcctgacctg cctggtcaaa ggcttctatc ccagcgacat cgccgtggag 1140
tgggagagca atgggcagcc ggagaacaac tacaagacca cgcctcccgt gctggactcc 1200
gacggctcct tcttcttata ttcaaagctc accgtggaca agagcaggtg gcagcagggg 1260
aacgtcttct catgctccgt gatgcatgag gctctgcaca accactacac gcagaagagc 1320
ctctccctgt ctcccgggaa atga 1344
<210> 340
<211> 654
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 201C15-zu (таблица 9)
<400> 340
gatatccaga tgacccagtc cccctccacc ctgtctgcct ctgtgggcga cagagtgacc 60
atcacctgtc aggcctccga gtccatctac cgggtgctgg cctggtatca gcagaagcct 120
ggcaaggccc ccaagctgct gatctacgac accagcacac tggcctccgg cgtgccctct 180
agattctccg gctctggctc tggcaccgag tttaccctga ccatctccag cctccagtgc 240
gacgacgccg ccacctacta ttgtcagggc ggctactacg ccgactccta cggaatcgct 300
ttcggcggag gcaccaaggt ggaaatcaaa cgaactgtgg ctgcaccatc tgtcttcatc 360
ttcccgccat ctgatgagca gttgaaatct ggaactgcct ctgttgtgtg cctgctgaat 420
aacttctatc ccagagaggc caaagtacag tggaaggtgg ataacgccct ccaatcgggt 480
aactcccagg agagtgtcac agagcaggac agcaaggaca gcacctacag cctcagcagc 540
accctgacgc tgagcaaagc agactacgag aaacacaaag tctacgcctg cgaagtcacc 600
catcagggcc tgagctcgcc cgtcacaaag agcttcaaca ggggagagtg ttga 654
<210> 341
<211> 1359
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 346C6-xi (таблица 9)
<400> 341
cagtcggtgg aggagtccgg cggtcgcctg gtaaagcctg acgaatccct gacactcacc 60
tgcacagcct ctggattctc cctcagtagt tatgcaatga tctgggtccg ccaggctcca 120
ggggaggggc tggaatggat cggaaccatt agtactggtg gtatcacata ctacgcgagc 180
tgggcgaaag gccgattcac catctccaaa acctcgacca cggtggatct gaaaatcacc 240
agtccgacaa ccgaggacac ggccacctat ttctgtgcca gagggggata tgctgctagt 300
agtgcttatt atctcccgta ctactttgac ttgtggggcc aagggaccct ggtcaccgtc 360
tcctcagcat ccaccaaggg cccatcggtc ttccccctgg caccctcctc caagagcacc 420
tctgggggca cagcggccct gggctgcctg gtcaaggact acttccccga accggtgacg 480
gtgtcgtgga actcaggcgc cctgaccagc ggcgtgcaca ccttcccggc tgtcctacag 540
tcctcaggac tctactccct cagcagcgtg gtgaccgtgc cctccagcag cttgggcacc 600
cagacctaca tctgcaacgt gaatcacaag cccagcaaca ccaaggtgga caagaaagtt 660
gagcccaaat cttgtgacaa aactcacaca tgcccaccgt gcccagcacc tgaactcctg 720
gggggaccgt cagtcttcct cttcccccca aaacccaagg acaccctcat gatctcccgg 780
acccctgagg tcacatgcgt ggtggtggac gtgagccacg aagaccctga ggtcaagttc 840
aactggtacg tggacggcgt ggaggtgcat aatgccaaga caaagccgcg ggaggagcag 900
tacaacagca cgtaccgtgt ggtcagcgtc ctcaccgtcc tgcaccagga ctggctgaat 960
ggcaaggagt acaagtgcaa ggtctccaac aaagccctcc cagcccccat cgagaaaacc 1020
atctccaaag ccaaagggca gccccgagaa ccacaggtgt acaccctgcc cccatcccgg 1080
gatgagctga ccaagaacca ggtcagcctg acctgcctgg tcaaaggctt ctatcccagc 1140
gacatcgccg tggagtggga gagcaatggg cagccggaga acaactacaa gaccacgcct 1200
cccgtgctgg actccgacgg ctccttcttc ttatattcaa agctcaccgt ggacaagagc 1260
aggtggcagc aggggaacgt cttctcatgc tccgtgatgc atgaggctct gcacaaccac 1320
tacacgcaga agagcctctc cctgtctccc gggaaatga 1359
<210> 342
<211> 660
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 346C6-xi (таблица 9)
<400> 342
gcagccgtgc tgacccagac accatcaccc gtgtctgcag ctgtgggagg cacagtcacc 60
atcagttgcc agtccagtca gagtgtttat aataataaca acttagcctg gtttcagcag 120
aaacccgggc agcctcccaa gcttctgatc tatctggcat ccactctggc atctggggtc 180
ccatcacggt tcagcggcag tggatctggg acacagttca ctctcaccat cagcggcgtg 240
cagtgtgacg atgctgccac ttattactgt ctaggtggtt gtgatgatga tgctgatact 300
tttgctttcg gcggagggac tgaggtggtg gtcaaacgaa ctgtggctgc accatctgtc 360
ttcatcttcc cgccatctga tgagcagttg aaatctggaa ctgcctctgt tgtgtgcctg 420
ctgaataact tctatcccag agaggccaaa gtacagtgga aggtggataa cgccctccaa 480
tcgggtaact cccaggagag tgtcacagag caggacagca aggacagcac ctacagcctc 540
agcagcaccc tgacgctgag caaagcagac tacgagaaac acaaagtcta cgcctgcgaa 600
gtcacccatc agggcctgag ctcgcccgtc acaaagagct tcaacagggg agagtgttga 660
<210> 343
<211> 1368
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь 346C6-zu (таблица 9)
<400> 343
gaagtgcagc tggtggaatc tggcggcgga ctggtgcagc ctggcggatc tctgagactg 60
tcttgtgccg cctccggctt ctccctgtcc tcctacgcta tgatctgggt gcgacaggcc 120
cctggcaagg gcctggaatg gatcggcacc atctctaccg gcggaattac ctactacgcc 180
tcctgggcca agggccggtt caccatctcc agagacaact ccaagaacac cctgtacctc 240
cagatgaact ccctgcgggc cgaggacacc gccgtgtact attgtgctag aggcggctac 300
gccgccagct ccgcttacta cctgccctac tacttcgacc tgtggggcca gggcaccctc 360
gtgacagtgt catctgcatc caccaagggc ccatcggtct tccccctggc accctcctcc 420
aagagcacct ctgggggcac agcggccctg ggctgcctgg tcaaggacta cttccccgaa 480
ccggtgacgg tgtcgtggaa ctcaggcgcc ctgaccagcg gcgtgcacac cttcccggct 540
gtcctacagt cctcaggact ctactccctc agcagcgtgg tgaccgtgcc ctccagcagc 600
ttgggcaccc agacctacat ctgcaacgtg aatcacaagc ccagcaacac caaggtggac 660
aagaaagttg agcccaaatc ttgtgacaaa actcacacat gcccaccgtg cccagcacct 720
gaactcctgg ggggaccgtc agtcttcctc ttccccccaa aacccaagga caccctcatg 780
atctcccgga cccctgaggt cacatgcgtg gtggtggacg tgagccacga agaccctgag 840
gtcaagttca actggtacgt ggacggcgtg gaggtgcata atgccaagac aaagccgcgg 900
gaggagcagt acaacagcac gtaccgtgtg gtcagcgtcc tcaccgtcct gcaccaggac 960
tggctgaatg gcaaggagta caagtgcaag gtctccaaca aagccctccc agcccccatc 1020
gagaaaacca tctccaaagc caaagggcag ccccgagaac cacaggtgta caccctgccc 1080
ccatcccggg atgagctgac caagaaccag gtcagcctga cctgcctggt caaaggcttc 1140
tatcccagcg acatcgccgt ggagtgggag agcaatgggc agccggagaa caactacaag 1200
accacgcctc ccgtgctgga ctccgacggc tccttcttct tatattcaaa gctcaccgtg 1260
gacaagagca ggtggcagca ggggaacgtc ttctcatgct ccgtgatgca tgaggctctg 1320
cacaaccact acacgcagaa gagcctctcc ctgtctcccg ggaaatga 1368
<210> 344
<211> 660
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Легкая цепь 346C6-zu (таблица 9)
<400> 344
gatattcaga tgacccagtc cccctccagc ctgtccgctt ctgtgggcga cagagtgacc 60
atcacctgtc agtcctccca gtccgtgtat aacaacaaca acctggcctg gtatcagcag 120
aaacccggca aggtgcccaa gctgctgatc tacctggcct ccacactggc ctctggcgtg 180
ccctctagat tctccggctc tggctctggc accgacttta ccctgaccat cagctccctc 240
cagtgcgagg atgccgccac ctactattgc ctgggcggct gcgacgacga cgccgatacc 300
tttgcttttg gcggaggcac caaggtggaa atcaaacgaa ctgtggctgc accatctgtc 360
ttcatcttcc cgccatctga tgagcagttg aaatctggaa ctgcctctgt tgtgtgcctg 420
ctgaataact tctatcccag agaggccaaa gtacagtgga aggtggataa cgccctccaa 480
tcgggtaact cccaggagag tgtcacagag caggacagca aggacagcac ctacagcctc 540
agcagcaccc tgacgctgag caaagcagac tacgagaaac acaaagtcta cgcctgcgaa 600
gtcacccatc agggcctgag ctcgcccgtc acaaagagct tcaacagggg agagtgttga 660
<210> 345
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пример эпитопа 1
<400> 345
Ala His Lys Asp
1
<210> 346
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Пример эпитопа 2
<400> 346
Asn Thr Ser Gln Glu Ala His Lys Asp Val Ser Tyr Leu
1 5 10
<210> 347
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь трастузумаба
<400> 347
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| КОНЪЮГАТЫ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ОСНОВЕ ЭРИБУЛИНА И СПОСОБЫ ПРИМЕНЕНИЯ | 2017 |
|
RU2754369C2 |
| АНТИТЕЛО ПРОТИВ LILRB1 И ЕГО ПРИМЕНЕНИЯ | 2021 |
|
RU2813373C1 |
| АНТИ-LILRB1 АНТИТЕЛО И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2801535C1 |
| АНТИТЕЛА К ТАУ И ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2787779C2 |
| АНТИТЕЛА, СВЯЗЫВАЮЩИЕСЯ С ЧЕЛОВЕЧЕСКИМ КАННАБИНОИДНЫМ РЕЦЕПТОРОМ 1 (СВ1) | 2015 |
|
RU2730674C2 |
| БИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА | 2020 |
|
RU2818588C2 |
| ПОЛИПЕПТИД, ВКЛЮЧАЮЩИЙ АНТИГЕНСВЯЗЫВАЮЩИЙ ДОМЕН И ТРАНСПОРТИРУЮЩИЙ СЕГМЕНТ | 2018 |
|
RU2815452C2 |
| АНТИТЕЛА ПРОТИВ БЕЛКА-1 ЗАПРОГРАММИРОВАННОЙ КЛЕТОЧНОЙ СМЕРТИ (PD-1) И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2725950C1 |
| АНТИ-PVRIG АНТИТЕЛА И СПОСОБЫ ПРИМЕНЕНИЯ | 2016 |
|
RU2732042C2 |
| ГЕТЕРОДИМЕРНЫЕ Fc-СЛИТЫЕ БЕЛКИ IL15/IL15Rα | 2017 |
|
RU2779938C2 |
Изобретение относится к способу получения конъюгата антитело-лекарственное средство, представленного Формулой (I), где Ab представляет собой антитело или его антигенсвязывающий фрагмент; D представляет собой эрибулин; m представляет собой целое число 1-10; и p представляет собой целое число 1-8, причем указанный способ включает: (i) осуществление реакции соединения Формулы (1), где m в Формуле (1) представляет собой целое число от 1 до 10, с соединением Формулы (2) для получения соединения Формулы (3), (ii) ацилирование гидроксильной группы в соединении Формулы (3) с использованием ацилирующего средства, и где ацилирующее средство включает феноксигруппу или нитрофеноксигруппу, получая таким образом соединение, представленное Формулой (A), (iii) осуществление реакции эрибулина или его соли с соединением, представленным Формулой (A) для получения соединения, представленного Формулой (B), (iv) осуществление реакции соединения, представленного Формулой (B), с антителом или его антигенсвязывающим фрагментом для получения конъюгата антитело-лекарственное средство, представленного Формулой (I). Способ обеспечивает получение конъюгата антитело-лекарственное средство с высоким выходом. 2 н. и 8 з.п. ф-лы, 10 табл., 4 пр.
Формула (I):
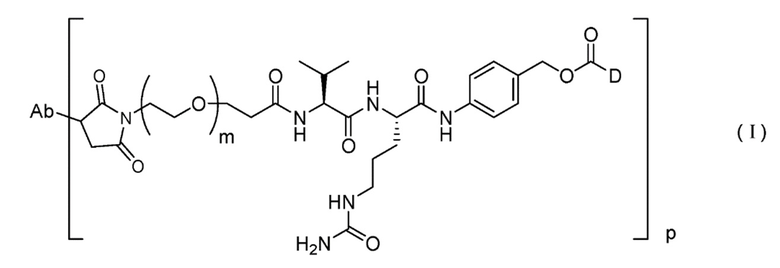
Формула (1):
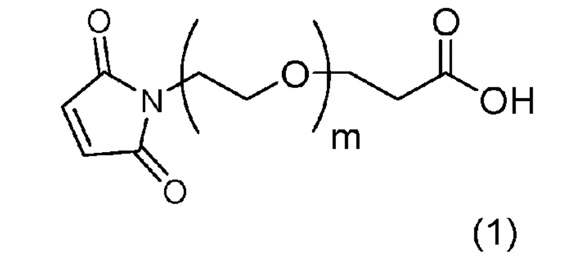
Формула (2):
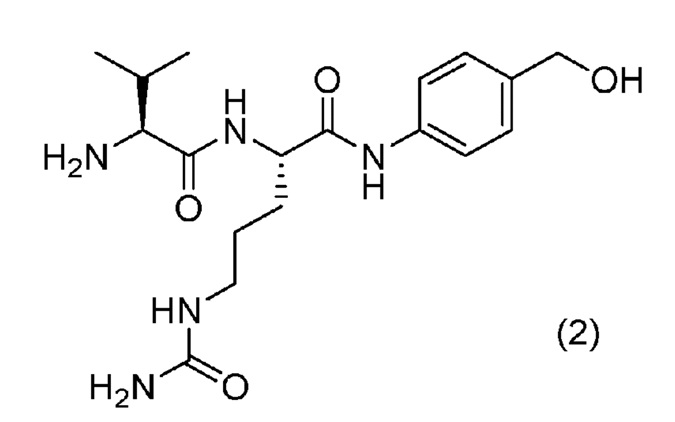
Формула (3):
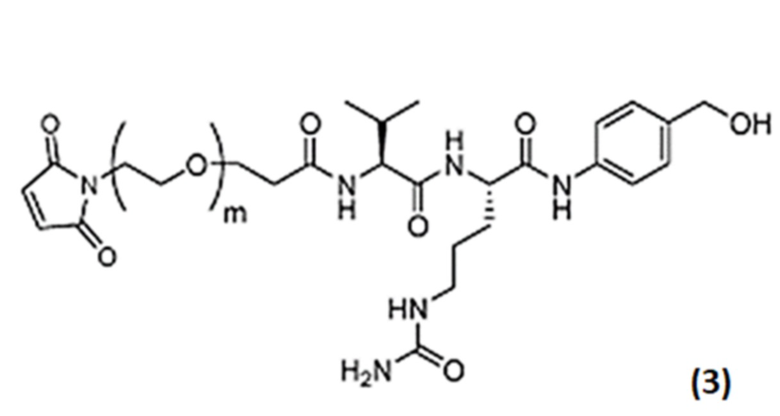
Формула (A):
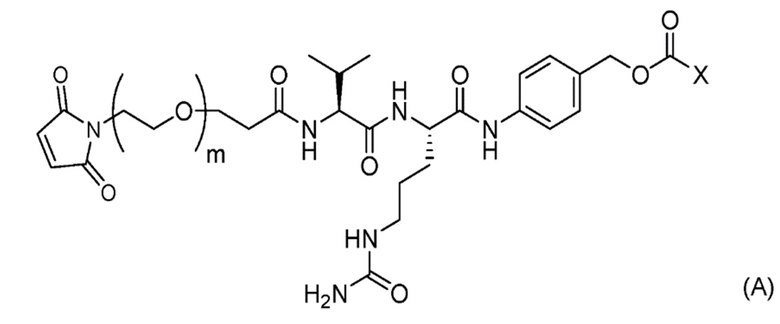
1. Способ получения соединения, представленного Формулой (B),
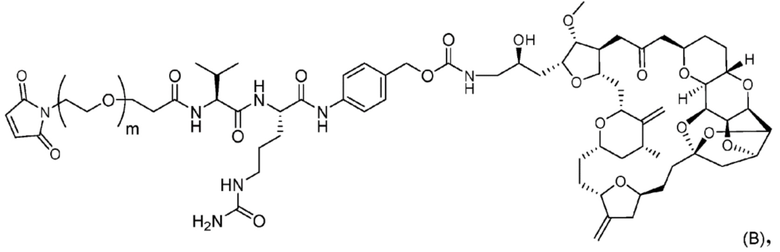
где m в Формуле (B) представляет собой целое число от 1 до 10, где способ включает:
(i) осуществление реакции соединения Формулы (1):
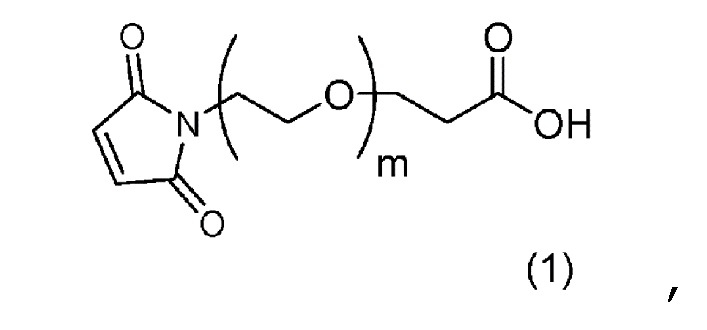
где m в Формуле (1) представляет собой целое число от 1 до 10, с соединением Формулы (2):
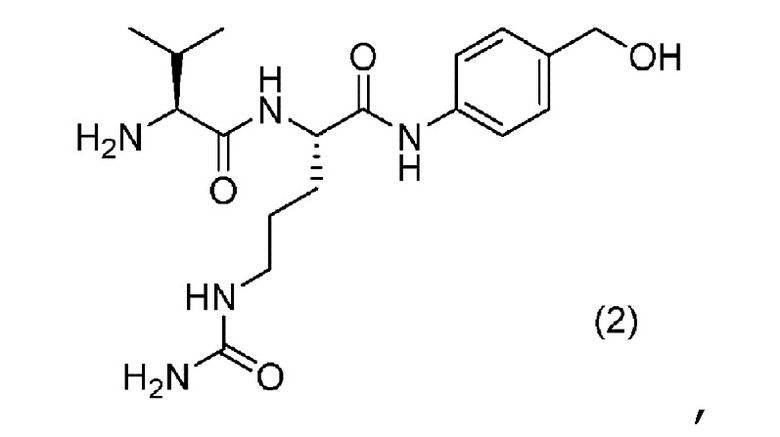
с получением соединения Формулы (3):
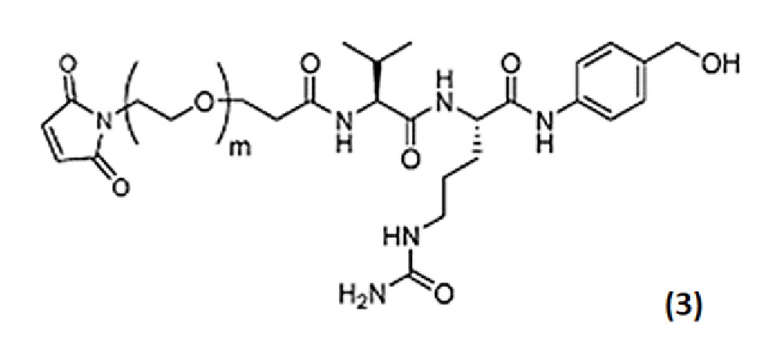 ;
;
(ii) ацилирование гидроксильной группы в соединении Формулы (3) с использованием ацилирующего средства, где m в Формуле (3) представляет собой целое число от 1 до 10, и где ацилирующее средство включает феноксигруппу или нитрофеноксигруппу, получая таким образом соединение, представленное Формулой (A),
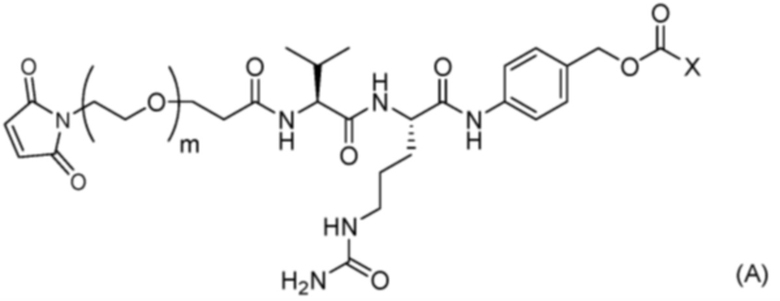
где m в Формуле (A) представляет собой целое число от 1 до 10, и X в Формуле (A) представляет собой феноксигруппу или нитрофеноксигруппу; и
(iii) осуществление реакции соединения Формулы (A) с эрибулином или его солью, получая таким образом соединение, представленное Формулой (B).
2. Способ по п. 1, в котором эрибулин или его соль представляет собой эрибулина метансульфонат.
3. Способ по п. 1, в котором стадия осуществления реакции соединения Формулы (A) с эрибулином или его солью, осуществляют в присутствии основания.
4. Способ по п. 3, в котором основание включает: третичный амин, необязательно триэтиламин или N,N-диизопропилэтиламин, или азотсодержащее ароматическое соединение, необязательно пиридин или 2,6-лутидин.
5. Способ по п. 1, в котором ацилирующее средство включает: дифенилкарбонат, бис(4-нитрофенил)карбонат, бис(2-нитрофенил)карбонат, бис(3-нитрофенил)карбонат, фенилхлорформиат, 4-нитрофенилхлорформиат, 2-нитрофенилхлорформиат или 3-нитрофенилхлорформиат.
6. Способ получения конъюгата антитело-лекарственное средство, представленного Формулой (I),
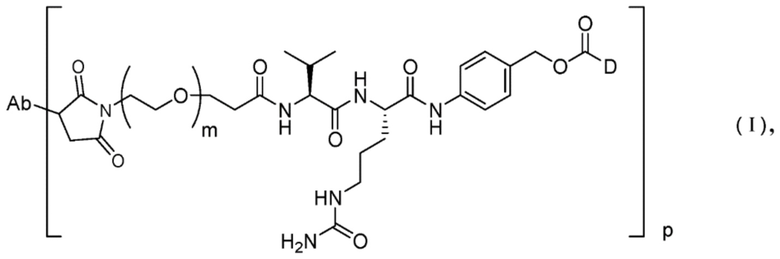
где Ab представляет собой антитело или его антигенсвязывающий фрагмент,
D представляет собой эрибулин,
m представляет собой целое число от 1 до 10, и
p представляет собой целое число от 1 до 8,
где способ включает:
(i) осуществление реакции соединения Формулы (1):

где m в Формуле (1) представляет собой целое число от 1 до 10, с соединением Формулы (2):

для получения соединения Формулы (3):
 ,
,
(ii) ацилирование гидроксильной группы в соединении Формулы (3) с использованием ацилирующего средства, где m в Формуле (3) представляет собой целое число от 1 до 10, и где ацилирующее средство включает феноксигруппу или нитрофеноксигруппу, получая таким образом соединение, представленное Формулой (A),
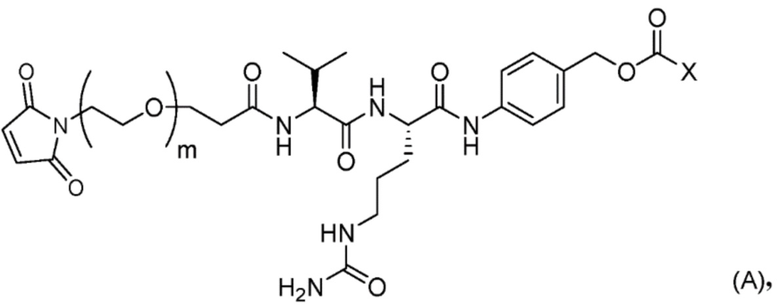
где m в Формуле (A) представляет собой целое число от 1 до 10, и X в Формуле (A) представляет собой феноксигруппу или нитрофеноксигруппу;
(iii) осуществление реакции эрибулина или его соли с соединением, представленным Формулой (A) для получения соединения, представленного Формулой (B),

где m в Формуле (B) представляет собой целое число от 1 до 10, и
(iv) осуществление реакции соединения, представленного Формулой (B), с антителом или его антигенсвязывающим фрагментом для получения конъюгата антитело-лекарственное средство, представленного Формулой (I).
7. Способ по п. 6, в котором:
(A) Ab включает антитело или антигенсвязывающий фрагмент, который связывается с фолатным рецептором альфа (FRA), где антитело или антигенсвязывающий фрагмент содержит:
(i) три последовательности CDR тяжелой цепи, представленные SEQ ID NO: 2 (HCDR1), SEQ ID NO: 3 (HCDR2) и SEQ ID NO: 4 (HCDR3), и три последовательности CDR легкой цепи, представленные SEQ ID NO: 7 (LCDR1), SEQ ID NO: 8 (LCDR2) и SEQ ID NO: 9 (LCDR3), которые определены согласно системе нумерации Kabat,
(ii) три последовательности CDR тяжелой цепи, представленные SEQ ID NO: 13 (HCDR1), SEQ ID NO: 14 (HCDR2) и SEQ ID NO: 15 (HCDR3), и три последовательности CDR легкой цепи, представленные SEQ ID NO: 16 (LCDR1), SEQ ID NO: 17 (LCDR2) и SEQ ID NO: 18 (LCDR3), которые определены согласно системе нумерации IMGT,
(iii) домен тяжелой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 1, и домен легкой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 6, или
(iv) вариабельный домен тяжелой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 23, и вариабельный домен легкой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 24;
(B) Ab включает антитело или антигенсвязывающий фрагмент, который связывается с рецептором-2 эпидермального фактора роста человека (HER2), где антитело или антигенсвязывающий фрагмент содержит:
(v) три последовательности CDR тяжелой цепи, представленные SEQ ID NO: 71 (HCDR1), SEQ ID NO: 72 (HCDR2) и SEQ ID NO: 73 (HCDR3), и три последовательности CDR легкой цепи, представленные SEQ ID NO: 74 (LCDR1), SEQ ID NO: 75 (LCDR2) и SEQ ID NO: 76 (LCDR3), которые определены согласно системе нумерации Kabat,
(vi) три последовательности CDR тяжелой цепи, представленные SEQ ID NO: 191 (HCDR1), SEQ ID NO: 192 (HCDR2) и SEQ ID NO: 193 (HCDR3), и три последовательности CDR легкой цепи, представленные SEQ ID NO: 194 (LCDR1), SEQ ID NO: 195 (LCDR2) и SEQ ID NO: 196 (LCDR3), которые определены согласно системе нумерации IMGT,
(vii) вариабельный домен тяжелой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 27, и вариабельный домен легкой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 28, или
(viii) домен тяжелой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 307 или 347, и домен легкой цепи, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 308; или
(C) Ab включает антитело или антигенсвязывающий фрагмент, который связывается с мезотелином, где антитело или антигенсвязывающий фрагмент содержит:
(ix) три последовательности CDR тяжелой цепи, представленные SEQ ID NO: 65 (HCDR1), SEQ ID NO: 66 (HCDR2) и SEQ ID NO: 67 (HCDR3), и три последовательности CDR легкой цепи, представленные SEQ ID NO: 68 (LCDR1), SEQ ID NO: 69 (LCDR2) и SEQ ID NO: 70 (LCDR3), которые определены согласно системе нумерации Kabat,
(x) три последовательности CDR тяжелой цепи, представленные SEQ ID NO: 185 (HCDR1), SEQ ID NO: 186 (HCDR2) и SEQ ID NO: 187 (HCDR3), и три последовательности CDR легкой цепи, представленные SEQ ID NO: 188 (LCDR1), SEQ ID NO: 189 (LCDR2) и SEQ ID NO: 190 (LCDR3), которые определены согласно системе нумерации IMGT,
(xi) вариабельный домен тяжелой цепи, содержащий аминокислотную последовательность, представленную SEQ ID NO: 25, и вариабельный домен легкой цепи, представленный SEQ ID NO: 26, или
(xii) домен тяжелой цепи, содержащий аминокислотную последовательность, представленную SEQ ID NO: 305, и домен легкой цепи, содержащий аминокислотную последовательность, представленную SEQ ID NO: 306.
8. Способ по п. 6, где p равняется 3 или 4.
9. Способ по п. 6, где эрибулин или его соль представляет собой эрибулина метансульфонат.
10. Способ по п. 6, в котором ацилирующее средство включает: дифенилкарбонат, бис(4-нитрофенил)карбонат, бис(2-нитрофенил)карбонат, бис(3-нитрофенил)карбонат, фенилхлорформиат, 4-нитрофенилхлорформиат, 2-нитрофенилхлорформиат или 3-нитрофенилхлорформиат.
| WO 2016151432 A1, 29.09.2016 | |||
| WO 2017151979 A1, 08.09.2017 | |||
| Cazzamalli Samuel et al., In Vivo Antitumor Activity of a Novel Acetazolamide-Cryptophycin Conjugate for the Treatment of Renal Cell Carcinomas, ACS Omega, 2018, v | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| 14726-14731 | |||
| WO 2018200812 A1, 01.11.2018 | |||
| WO 2019232449 A1, 05.12.2019. | |||
Авторы
Даты
2025-05-15—Публикация
2020-12-21—Подача