Изобретение относится к медицине и биологии, к области экспериментальной дерматологии. Способ может быть использован для ускорения заживления ран, в том числе и послеоперационных.
Миграция кератиноцитов является критическим этапом в тщательно организованном процессе заживления ран, который необходим для поддержания барьерной функции кожи. Первым шагом для восстановления кожного барьера после повреждения или операции является повторная эпителизация, при которой восстанавливается первый слой кератиноцитов и предотвращается возможное инфицирование раны [Seeger, M. A., & Paller, A. S. (2015). Advances in Wound Care. 4(4):213-224. doi: 10.1089/wound.2014.0540]. В базальном слое кожи этот процесс включает мобилизацию, митоз и миграцию кератиноцитов из окружающего эпидермиса с последующей дифференцировкой клеток и полным восстановлением эпидермального барьера, таким образом, миграция эпидермальных кератиноцитов является основой для реэпителизации кожи во время заживления ран [Seeger, M. A., & Paller, A. S. (2015). Advances in Wound Care. 4(4):213-224. doi:10.1089/wound.2014.0540]. Хронические раны характеризуются гиперпролиферативным и немигрирующим эпидермисом [Sabine A. Eming, Paul Martin, and Marjana Tomic-Canic Sci Transl Med. 2014 6(265): 265sr6. doi: 10.1126/scitranslmed.3009337].
Миграция кератиноцитов контролируется различными факторами роста и сигнальными путями, в том числе никотиновыми и мускариновыми рецепторами ацетилхолина (nAChR и mAChR, соответственно). Известно, что активация mAChR приводит к усилению роста клеток кожи [Słoniecka M, Backman LJ, Danielson P. (2015). Int Immunopharmacol. 29(1):57-62. doi:10.1016/j.intimp.2015.05.039]. Также известно, что активация nAChR ослабляет миграцию кератиноцитов, нарушая врожденный кожный иммунитет [Mari Kishibe, Tina M. Griffin, Katherine A. Radek Int Immunopharmacol. 2015 Nov; 29(1): 63-70.]. Таким образом, модуляция nAChR и mAChR в клетках эпителия представляет перспективную стратегию для усиления реэпителизации ран.
Известен способ усиления пролиферации и миграции кератиноцитов низкими концентрациями ацетилхолина [Uberti F., Bardelli C., Morsanuto V., Ghirlanda S., Cochis A., Molinari C., Cells Tissues Organs 2017;203:215-230 doi.org/10.1159/000451023]. Однако ацетилхолин активирует и mAChR и nAChR, а активация nAChR ингибирует миграцию кератиноцитов [Mari Kishibe, Tina M. Griffin, Katherine A. Radek Int Immunopharmacol. 2015 Nov; 29(1): 63-70].
Существуют различные эндогенные модуляторы ацетилхолиновых рецепторов клеток кожи, одним из которых является секретируемый ауто/паракринный регулятор эпителиального гомеостаза SLURP-2 [Arredondo J, Chernyavsky AI, Grando SA. (2007). Life Sci. 80(24-25):2243-2247. doi:10.1016/j.lfs.2007.01.003]. Рекомбинантный аналог белка человека SLURP-2 (rSLURP-2, SEQ ID NO: 1) ингибирует токи через α4β2- и α3β2-nAChR и является аллостерическим модулятором M1 и M3 mAChR человека. Взаимодействуя с α3β2-nAChR и М3-mAChR, rSLURP-2 увеличивает пролиферацию кератиноцитов человека [Lyukmanova EN, Shulepko MA, Shenkarev ZO, Bychkov ML, Paramonov AS, Chugunov AO, Kulbatskii DS, Arvaniti M, Dolejsi E, Schaer T, Arseniev AS, Efremov RG, Thomsen MS, Dolezal V, Bertrand D, Dolgikh DA, Kirpichnikov MP. (2016). Sci Rep. 3;6:30698. doi:10.1038/srep30698]. Кроме того, SLURP-2 увеличивает экспрессию интегринов α5 и αV, участвующих в миграции клеток при ранозаживлении [Chernyavsky AI, Kalantari-Dehaghi M, Phillips C, Marchenko S, Grando SA. (2012). Wound Repair Regen. 20(1):103-13. doi: 10.1111/j.1524-475X.2011.00753.x]. Эти данные свидетельствуют о том, что SLURP-2 является важным участником эпителизации ран и рекомбинантный аналог белка человека SLURP-2 может использоваться для ускорения ранозаживления.
Наиболее близким к заявленному является способ ускорения миграции кератиноцитов с использованием rSLURP-2 (SEQ ID NO: 1) [Люкманова Е.Н. (2019). Диссертация на соискание ученой степени доктора биологических наук по специальности 03.01.03-молекулярная биология]. Однако, инкубация кератиноцитов с rSLURP-2 усиливает как миграцию, так и пролиферацию клеток [Lyukmanova EN, Shulepko MA, Shenkarev ZO, Bychkov ML, Paramonov AS, Chugunov AO, Kulbatskii DS, Arvaniti M, Dolejsi E, Schaer T, Arseniev AS, Efremov RG, Thomsen MS, Dolezal V, Bertrand D, Dolgikh DA, Kirpichnikov MP. (2016). Sci Rep. 3;6:30698. doi:10.1038/srep30698]. Известно, что усиление пролиферации кератиноцитов при ранозаживлении опасно утолщением эпидермального слоя и формированием келоидных рубцов на месте ран [Chua AW, Ma D, Gan SU, Fu Z, Han HC, Song C, Sabapathy K, Phan TT. (2010). J Invest Dermatol. 131(3):644-654. doi: 10.1038/jid.2010.371]. Таким образом, использование rSLURP-2 в качестве ранозаживляющего агента может иметь побочное действие в виде формирования келоидных рубцов. Технической проблемой, на решение которой направлено заявляемое изобретение, является создание нового способа, который позволит усилить миграцию кератиноцитов без увеличения их пролиферации. Поставленная техническая проблема решается за счет рекомбинантного белка rSLURP-2[R20A], имеющего аминокислотную последовательность SEQ ID NO: 2 и являющегося специфическим регуляторным фактором эпителиальных клеток, в частности кератиноцитов, т.е. специфическим стимулятором, вызывающим ускоренную миграцию кератиноцитов без увеличения их пролиферации.
Рекомбинантный препарат rSLURP-2[R20A] (SEQ ID NO: 2) получают в бактериальной системе экспрессии, при которой белок ренатурируют из цитоплазматических телец включения E. coli, как описано в примерах 2-4. Рекомбинантный препарат rSLURP-2[R20A] (SEQ ID NO: 2), как и рекомбинантный аналог белка человека rSLURP-2 имеет аминокислотный остаток метионина на N-конце, но отличается от rSLURP-2 (SEQ ID NO: 1) заменой аминокислотного остатка аргинина в 20-м положении на аминокислотный остаток аланина.
Изобретение иллюстрируют графические материалы:
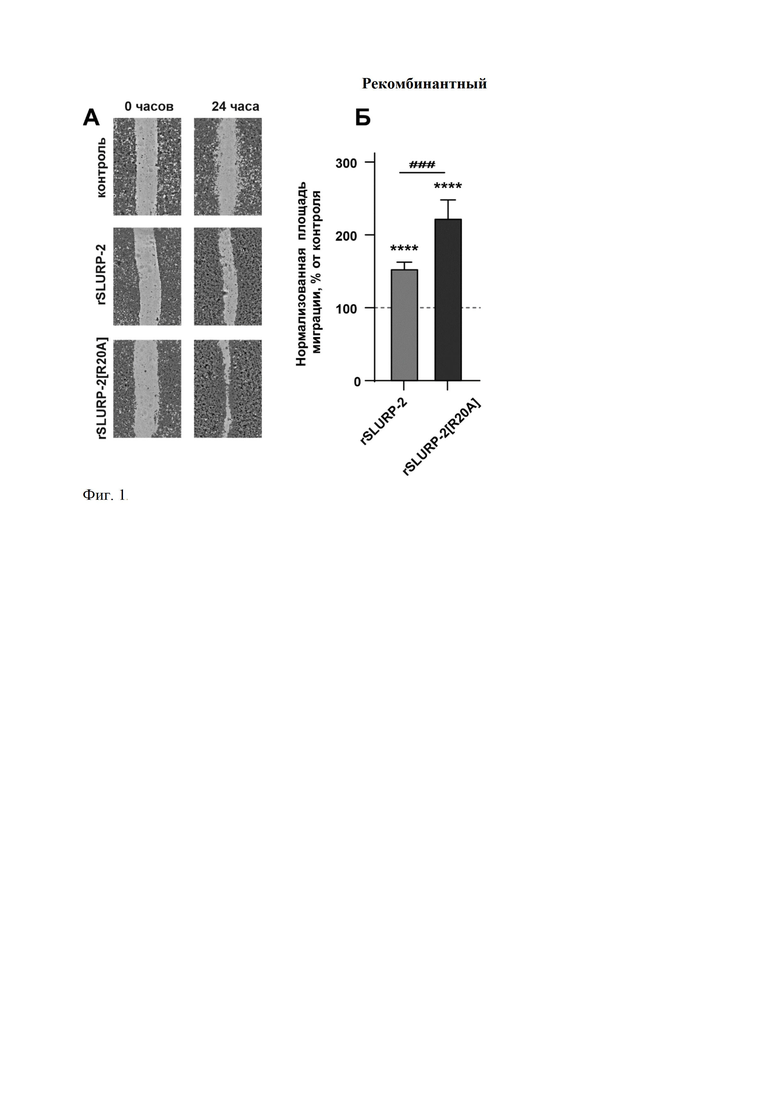
На фиг. 1 представлен эффект rSLURP-2 (SEQ ID NO: 1) и rSLURP-2[R20A] (SEQ ID NO: 2) на миграцию кератиноцитов Het1A согласно данным скрэтч-теста. Клетки (7×104 клеток/см2) высевали за 24 часа до эксперимента на 96-луночный культуральный планшет для образования монослоя клеток, затем в монослое клеток делали царапину и инкубировали с 100 нМ rSLURP-2 (SEQ ID NO: 1) или 100 нМ rSLURP-2[R20A] (SEQ ID NO: 2) в течение 24 часов. С помощью прибора CloneSelect (Molecular Devices) определяли площадь, занимаемую мигрирующими кератиноцитами. А. Репрезентативные микрофотографии, показывающие эффект препаратов на миграцию кератиноцитов. Б. Оценка скорости миграции кератиноцитов в контроле и под действием препаратов rSLURP-2 и rSLURP-2[R20A]. Скорость миграции оценивали по изменению площади прироста монослоя клеток в зону царапины через 24 часа. **** (p<0.0001) означает достоверное отличие между группами данных и контрольным значением (100%, пунктирная линия) согласно ANOVA с последующим тестом Dunnet. ### (p<0.001) означает отличие между группами данных «rSLURP-2» (SEQ ID NO: 1) и «rSLURP-2[R20A]» (SEQ ID NO: 2) согласно ANOVA с последующим тестом Dunnet.
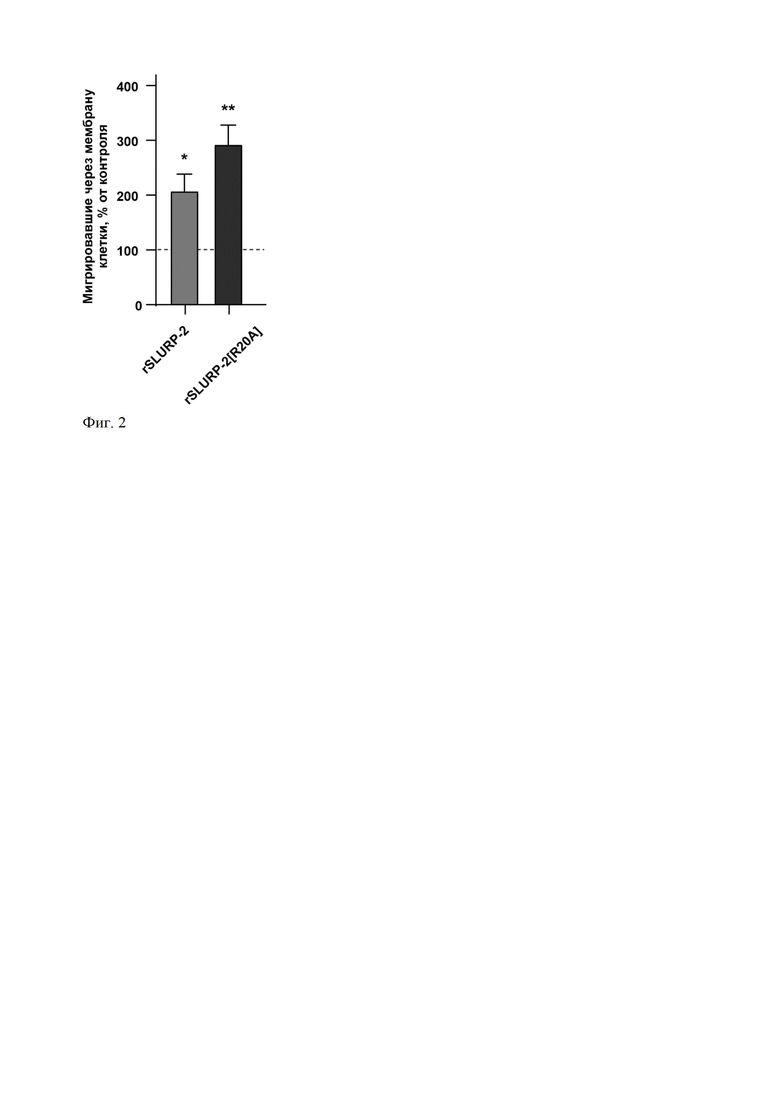
На фиг. 2 представлены данные по влиянию rSLURP-2 (SEQ ID NO: 1) и rSLURP-2[R20A] (SEQ ID NO: 2) на миграцию кератиноцитов Het1A согласно данным теста на миграцию клеток через пористую базальную мембрану. Клетки суспендировали с 100 нМ rSLURP-2 (SEQ ID NO: 1) или 100 нМ rSLURP-2[R20A] (SEQ ID NO: 2), после чего высевали в 24-луночный культуральный планшет, содержащий вставки c дном из пористой мембраны, покрытой коллагеном, фибронектином и ламинином. Клетки в вставках инкубировали с препаратами в течение 72 часов с заменой среды каждые 24 часа. После инкубации, мигрировавшие через пористую мембрану клетки открепляли от дна культурального планшета и окрашивали при помощи флуорексона. Уровень флуоресценции определяли на планшетном ридере Promega Glomax LT, а количество клеток вычисляли при помощи калибровочной кривой. * (p<0.05), ** (p<0.01) означает достоверное отличие между группами данных и контрольным значением (100%, пунктирная линия) согласно ANOVA с последующим тестом Dunnet.
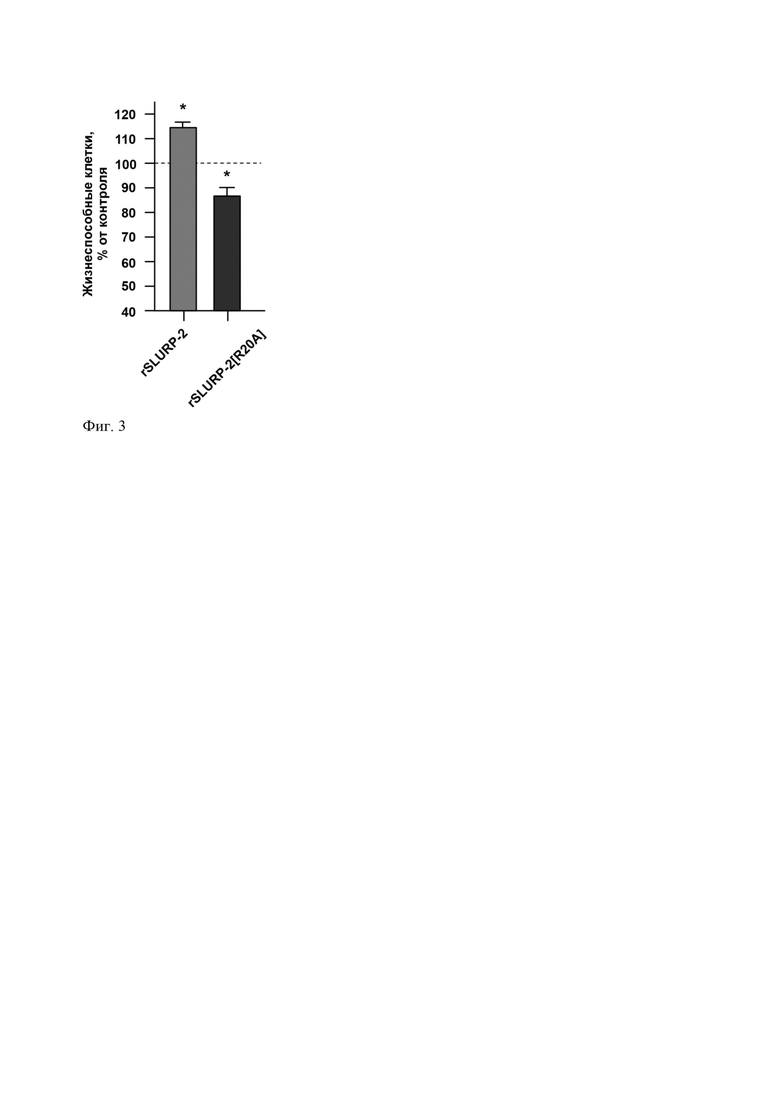
На фиг. 3 приведены данные о влиянии rSLURP-2 (SEQ ID NO: 1) и rSLURP-2[R20A] (SEQ ID NO: 2) на пролиферацию кератиноцитов Het1A. Клетки (2,8×104 клеток/см2) высевали за 24 часа до эксперимента на 96-луночный культуральный планшет и через 24 часа добавляли к клеткам 100 нМ rSLURP-2 (SEQ ID NO: 1) или 100 нМ rSLURP-2[R20A] (SEQ ID NO: 2), после чего инкубировали 48 часов. Жизнеспособность клеток определяли тестом WST-1. * (p<0.05) означает достоверное отличие между группами данных и контрольным значением (100%, пунктирная линия) согласно ANOVA с последующим тестом Dunnet.
Изобретение иллюстрируют примеры.
Пример 1. Конструирование рекомбинантной плазмидной ДНК pET22b(+)/rSLURP-2[R20A].
Рекомбинантную плазмидную ДНК pET22b(+)/rSLURP-2[R20A] конструируют на основе вектора pET22b(+)/slurp-2, содержащего ген slurp-2 (SEQ ID NO: 3, патент РФ № 2015109082(014406), с помощью сайт-направленного мутагенеза. Для этого фрагмент ДНК, содержащий ген slurp-2 амплифицируют методом двухстадийной ПЦР. На первой стадии с использованием пар олигонуклеотидов (SEQ ID NO: 4), (SEQ ID NO: 5) и (SEQ ID NO: 6), (SEQ ID NO: 7) нарабатывают фрагменты, соответствующие 5' и 3' концам гена slurp-2[R20A]. На второй стадии полученные фрагменты используют в качестве матрицы для ПЦР и получения фрагмента ДНК, содержащего полноразмерный ген slurp-2[R20A].
ПЦР продукт, содержащий ген slurp-2[R20A] (SEQ ID NO: 8), обрабатывают последовательно рестриктазами NdeI и HindIII (Thermo Scientific) и из полученного гидролизата выделяют в 2%-ном геле легкоплавкой агарозы фрагмент длиной 240 п.о., содержащий ген SLURP-2[R20A].
2 мкг плазмидной ДНК рЕТ22b(+) (Novagen, США) обрабатывают последовательно рестриктазами NdeI и HindIII и из полученного гидролизата выделяют в 1%-ном геле легкоплавкой агарозы векторную ДНК длиной 5382 п.о.
ПЦР продукт, содержащий ген slurp-2[R20A] (SEQ ID NO: 8) и обработанный рестриктазами NdeI и HindIII, и плазмидную ДНК рЕТ22b(+), обработанную рестриктазами NdeI и HindIII, соединяют при помощи лигазной реакции в 10 мкл буфера для лигирования (Thermo Scientific), содержащего 1 ед. Т4 ДНК-лигазы (Thermo Scientific). 1 мкл реакционной смеси используют для трансформации 100 мкл компетентных клеток XL-1 Blue (Stratagene, США). 1/10 клеток, использованных для трансформации, высевают на LB-агар, содержащий 100 мкг/мл ампициллина. Из выросших клонов выделяют целевую плазмидную pET22b(+)/rSLURP-2[R20A] и анализируют ее путем обработки набором эндонуклеаз рестрикции NdeI и HindIII с последующим электрофоретическим анализом длин рестрикционных фрагментов в 2% агарозном геле.
Окончательно структуру рекомбинантной ДНК pET22b(+)/rSLURP-2[R20A] подтверждают определением нуклеотидной последовательности в области фрагмента синтетического гена, кодирующего rSLURP-2[R20A] (SEQ ID NO: 8).
Пример 2. Получение штамма-продуцента rSLURP-2[R20A].
Рекомбинантной плазмидной ДНК pET22b(+)/rSLURP-2[R20A] трансформируют компетентные клетки Escherichia coli BL21(DE3) (Novagen). Для этого к 200 мкл компетентных клеток добавляют 20 нг плазмидной ДНК pET22b(+)/rSLURP-2[R20A], хорошо перемешивают и инкубируют во льду в течение 30 мин. Затем клетки подвергают тепловому шоку в течение 90 сек при 42°C, после чего вновь помещают в лед и инкубируют 4-5 мин. Затем к клеточной суспензии добавляют 300 мкл среды SOB, и инкубируют клетки в течение 60 мин при 37°С и хорошей аэрации. Затем клетки высевают по 100 мкл на чашки Петри с питательной твердой средой, содержащей ампициллин (100 мкг/мл). В результате получают штамм-продуцент rSLURP-2[R20A].
Собранные с чашек Петри колонии с клетками E. coli BL21(DE3)/pET22b(+)/rSLURP-2[R20A] ресуспендируют в 50 мл жидкой среды Terrific Brouth (TB), содержащей ампициллин (100 мкг/мл). Культивирование проводят при 37°С с умеренным перемешиванием (250 об./мин.) до достижения клеточной плотности в культуре, соответствующей величине поглощения при 600 нм 0.6. Далее клеточную культуру переносят в 1 л ТВ и продолжают выращивание в ферментере (Bioflow 3000, New Brunswick Scientific, США). Культивирование осуществляют при 37°С в условиях автоматического поддержания относительного содержания кислорода в системе не менее 30% от максимально достижимого. Регулируемыми параметрами являются обороты мешалки и скорость подачи воздуха. Экспрессию гена, кодирующего rSLURP-2[R20A] индуцируют добавлением изопропилтио-β-D-галактопиранозида до конечной концентрации 0.05 мМ при клеточной плотности в культуре, соответствующей величине поглощения при 600 нм 1.0. После индукции культивирование клеток осуществляют в течение 12 часов.
Отбирают пробу 1 мл и центрифугируют 5 мин при скорости 6000 об/мин, после чего клетки суспендируют в 100 мкл буфера, содержащего 125 мМ трис-HCl, pH 6,8, 20% глицерин, 3% додецилсульфат натрия, 3% меркаптоэтанол, 0,005% бромфеноловый синий, инкубируют 10 мин в кипящей водяной бане, образцы объемом 5 мкл анализируют электрофорезом в 13% полиакриламидном геле с додецилсульфатом натрия. Гель окрашивают Кумасси G-250, сканируют и рассчитывают процентное содержание рекомбинантного белка в лизатах с использованием программы Scion Image (Scion Corp., США). По данным сканирования белок rSLURP-2[R20A] составляет 10% от общего клеточного белка.
Пример 3. Выделение рекомбинантного белка rSLURP-2[R20A].
Клетки собирают центрифугированием (10000 g, 20 мин., 4°С) и ресуспендируют в холодном буфере 20 мМ Tris/HCl, 100 мМ NaCl, 1 мМ EDTA, pH 8.0 в соотношении 10 мл буфера на 1 г осадка. Далее суспензию клеток дезинтегрируют ультразвуком (Branson Digital Sonifier, США) при выходной мощности 50 Вт и 4°С в течение 5 минут. Полученную взвесь центрифугируют при 36000 g в течение 20 мин. Образовавшийся осадок ресуспендируют в исходном буфере с добавлением 2 М мочевины. Суспензию переносят в охлажденный стакан, дезинтегрируют 10 секунд и центрифугируют в тех же условиях, что и ранее. Процедуру повторяют дважды. После отмывания 2 М мочевиной осадок два раза промывают исходным буфером, содержащим 1% Тритон Х-100, и затем два раза деионизованной водой (MilliQ, Millipore, США). Отмытые тельца включения хранят при -70°С.
Отмытые тельца включения ресуспендируют в 30 мМ трис-глициновом буфере, pH 9.2 содержащем 8 M мочевину (Carl Roth, Германия), из расчета 10 мл буфера на 1 г телец включения. Суспензию дезинтегрируют при выходной мощности прибора 50 Вт и 4°С в течение 30 сек. Затем суспензию тел включения сульфируют добавлением 0,4 М сульфита натрия, цистина до концентрации 0.4 мМ и NiCl2 до концентрации 5 мМ. В таком виде тельца оставляют на 18 часов в открытом стакане при перемешивании и 25°С. Затем смесь центрифугируют при 36000 g 1 час и супернатант разводят в 10 раз 2 М мочевиной. После этого сульфированный SLURP-2 наносят на колонку с ДЕАП-Сферонит-ОН, предварительно уравновешенную 30 мМ Tris-HСl, pH 8.0 (буфер А). rSLURP-2[R20A] элюируют буфером А, содержащим 300 мМ NaCl и 8 M мочевину.
Во фракцию белка, содержащую rSLURP-2[R20A], добавляют дитиотреитол до конечной концентрации 50 мМ и дополнительно чистят с помощью обратнофазной ВЭЖХ с помощью хроматографической колонки Jupiter С4, А300, 10×250 мм (Phenomenex, США) на приборе “Smartline” (Knauer, Германия). Элюцию SLURP-2 проводят градиентом ацетонитрила от 10% до 45% за 30 мин в присутствии 0,1 % трифторуксусной кислоты. Полученный препарат SLURP-2 с восстановленными дисульфидными связями лиофилизируют.
Пример 4. Ренатурация рекомбинантного белка rSLURP-2[R20A].
Лиофилизированный и восстановленный rSLURP-2[R20A] растворяют в буфере для ренатурации, содержащем 50 мМ Tris/HCl, 2 М мочевину, 0.5 M L-аргинин, 2 мМ GSH и 2 мМ GSSG, рН 9.0, до конечной концентрации белка 0.1 мг/мл. Ренатурацию проводят при 4°С в течение 3 суток.
Раствор rSLURP-2[R20A] концентрируют в 4 раза на концентрационной ячейке с размером пор мембраны 1 кДа (Millipore, США). Очистку ренатурированного rSLURP-2[R20A] проводят с помощью обратнофазной ВЭЖХ на колонке Jupiter С4, А300, 4,6×250 мм (Phenomenex, США). Элюцию rSLURP-2[R20A] проводят градиентом ацетонитрила от 20% до 45% за 30 мин в присутствии 0,1% трифторуксусной кислоты. Полученный препарат ренатурированного rSLURP-2[R20A] лиофилизируют.
Описываемый способ выделения позволяет получить 5 мг ренатурированного rSLURP-2[R20A] из 1 г влажной биомассы, что соответствует 5 мг белка из 100 мг лиофилизированной биомассы.
Спектры, измеренные на времяпролетном масс-спектрометре UltraFlex TOF/TOF фирмы Bruker Daltonics (Германия), оснащенном источником ионизации MALDI, показали соответствие молекулярной массы рекомбинантного rSLURP-2[R20A] расчетным данным, полученным для аминокислотной последовательности (SEQ ID NO: 2). Формирование дисульфидных связей было также подтверждено с помощью реактива Элмана.
Пример 5. Изобретение раскрывается на примере монослоя кератиноцитов человека Het1A. Клетки культивируются в питательной среде BEBM. Клетки Het1A культивируют в культуральных флаконах объемом 75 мл и пересаживают минимум 2 раза в неделю. Клетки высевают в лунки культурального 96-луночного планшета (25000 клеток на лунку), через сутки в монослое клеток делают царапину и добавляют 100 нМ rSLURP-2 (SEQ ID NO: 1) или 100 нМ rSLURP-2[R20A] (SEQ ID NO: 2), после чего инкубируют 24 часа. С помощью прибора CloneSelect (Molecular Devices) определяют площадь, занимаемую мигрирующими кератиноцитами, через 24 часа. Пример показывает, что rSLURP-2 (SEQ ID NO: 1) усиливает миграцию клеток при 24-часовой инкубации до 114,2 ± 5,1% относительно контроля, однако при инкубации кератиноцитов с rSLURP-2[R20A] (SEQ ID NO: 2), миграция кератиноцитов увеличивается до 135,6 ± 9,9 % относительно контроля. Эффект препарата rSLURP-2[R20A] (SEQ ID NO: 2) на миграцию кератиноцитов значительно превышает эффект rSLURP-2 (SEQ ID NO: 1).
Пример 6. Изобретение раскрывается на примере прохождения кератиноцитов человека Het1A через поры базальной мембраны. Клетки культивируются в питательной среде BEBM. Клетки Het1A культивируют в культуральных флаконах объемом 75 мл и пересаживают минимум 2 раза в неделю. Клетки суспендируют с 100 нМ rSLURP-2 (SEQ ID NO: 1) или 100 нМ rSLURP-2[R20A] (SEQ ID NO: 2), после чего высевают в 24-луночный культуральный планшет, содержащий вставки c дном из пористой базальной мембраны, покрытой коллагеном, фибронектином и ламинином. Диаметр пор составляет 8 мкм. Клетки во вставках инкубируют с препаратами в течение 72 часов с заменой среды каждые 24 часа. После инкубации, мигрировавшие через пористую мембрану и прикрепившиеся к дну 24-луночного культурального планшета клетки открепляют от дна культурального планшета и окрашивают при помощи флуорексона. Уровень флуоресценции определяют на флуоресцентном планшетном ридере Promega Glomax LT, а количество клеток вычисляют при помощи калибровочной кривой. Пример показывает, что препарат rSLURP-2[R20A] (SEQ. №2) более эффективно стимулирует миграцию кератиноцитов через базальную мембрану при 24-часовой инкубации, чем препарат rSLURP-2 (фиг. 2).
Пример 7. Изобретение раскрывается на примере монослоя кератиноцитов человека Het1A. Клетки культивируются в питательной среде BEBM. Клетки Het1A культивируют в культуральных флаконах объемом 75 мл и пересаживают минимум 2 раза в неделю. Клетки высевают в лунки культурального 96-луночного планшета (10000 клеток на лунку), через сутки к клеткам добавляют 100 нМ rSLURP-2 (SEQ ID NO: 1) или 100 нМ rSLURP-2[R20A] (SEQ ID NO: 2), после чего инкубируют клетки 48 часов. Жизнеспособность клеток определяют тестом WST-1. Для этого, к клеткам добавляют растворы WST-1 и электроноакцептора 1-m-PMS (0,5 мM и 20 мкM на лунку), инкубируют 4 часа и определяют оптическую плотность лунок планшета при 450 нм с выравниванием фона при 655 нм. Пример показывает, что rSLURP-2 (SEQ ID NO: 1) увеличивает пролиферацию кератиноцитов, в то время как rSLURP-2[R20A] (SEQ ID NO: 2), наоборот, тормозит рост кератиноцитов. Таким образом, эффект rSLURP-2[R20A] (SEQ ID NO: 2), в отличие от эффекта rSLURP-2 (SEQ ID NO: 1) не связан с увеличением пролиферации кератиноцитов, а проявляется в усилении миграции клеток кожи, т.е. является специфическим стимулятором миграции эпителиальных клеток человека.
Последовательности
Последовательность 1: "рекомбинантный белок rSLURP-2 "
Характеристики
ORGANISM = synthetic construct
--->
Последовательность
MIWCHQCTGF GGCSHGSRCL RDSTHCVTTA TRVLSNTEDL PLVTKMCHIG CPDIPSLGLG 60
PYVSIACCQT SLCNHD 76
<---
Последовательность 2: "Рекомбинантный белок rSLURP-2[R20A]"
Характеристики
ORGANISM = synthetic construct
--->
Последовательность
MIWCHQCTGF GGCSHGSRCL ADSTHCVTTA TRVLSNTEDL PLVTKMCHIG CPDIPSLGLG 60
PYVSIACCQT SLCNHD 76
<---
Последовательность 3: "ген slurp-2 "
Характеристики
organism = synthetic construct
--->
Последовательность
tagcgtgaag acgacagaac catatgattt ggtgccatca gtgcaccggc tttggcggct 60
gctcccatgg ctcccgttgc ctgcgtgatt ccacccattg cgtgaccacc gcgacccgtg 120
tgctgtccaa taccgaagat ctgccgctgg tgaccaaaat gtgccatatt ggctgcccgg 180
atattccgtc cctgggcctg ggcccgtatg tgtccattgc gtgctgccag acctccctgt 240
gcaatcatga ttagtagaag cttgttgtac tgagttc 277
<---
Последовательность 4: "олигонуклеотид для введения мутации NO 4"
Характеристики
organism = synthetic construct
Последовательность 5: "олигонуклеотид для введения мутации NO 5"
Характеристики
organism = synthetic construct
--->
Последовательность
atgctagtta ttgctcag 18
<---
Последовательность 6: "олигонуклеотид для введения мутации NO 6"
Характеристики
organism = synthetic construct
--->
Последовательность
gcaatgggtg gaatcagcca ggcaacggga gcc 33
<---
Последовательность 7: "олигонуклеотид для введения мутации NO 7"
Характеристики
organism = synthetic construct
Последовательность 8: "ген slurp-2[R20A]"
Характеристики
organism = synthetic construct
--->
Последовательность
tagcgtgaag acgacagaac catatgattt ggtgccatca gtgcaccggc tttggcggct 60
gctcccatgg ctcccgttgc ctggctgatt ccacccattg 100
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Набор олигонуклеотидных праймеров и зондов для выявления Herpesvirus Saimiri в клеточных культурах методом ПЦР в реальном времени | 2020 |
|
RU2753767C1 |
| Рекомбинантный штамм Herpesvirus saimiri для получения популяций иммортализованных аутологичных Т-лимфоцитов, экспрессирующих парные химерные рецепторы против опухолевых антигенов CD44 и CD133 | 2020 |
|
RU2771081C2 |
| Штамм гибридных культивируемых клеток животных Mus musculus 5B9 - продуцент мышиного моноклонального антитела 5B9, антитело моноклональное мышиное 5В9 и антитело рекомбинантное химерное (мышь-человек) xi5В9, нейтрализующие рицин Ricinus communis | 2022 |
|
RU2802436C1 |
| Нуклеотидная последовательность, кодирующая фермент литиказу, и панель олигонуклеотидов для получения синтетической нуклеотидной последовательности гена литиказы | 2023 |
|
RU2826150C1 |
| Плазмида для экспрессии рекомбинантного хорионического гонадотропина человека (ХГЧ), плазмида для экспрессии рекомбинантных альфа- и бета-субъединиц ХГЧ, моноклональная линия клеток млекопитающих - продуцент ХГЧ, способ получения рекомбинантного ХГЧ | 2024 |
|
RU2834784C1 |
| АНТИТЕЛА ПРОТИВ ПРОПЕРДИНА И ИХ ПОЛУЧЕНИЕ | 2021 |
|
RU2830308C1 |
| Способ получения генно-модифицированных лабораторных животных с индуцируемой системной и тканеспецифической экспрессией циклофилин А человека | 2022 |
|
RU2800264C1 |
| Способ получения генно-модифицированных лабораторных животных с нуль-аллелем гена P2rx3 | 2022 |
|
RU2805173C1 |
| BCMA-СПЕЦИФИЧЕСКИЕ ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, СОДЕРЖАЩИЕ БЛОКАТОР ПЕРЕДАЧИ СИГНАЛА IL-6 | 2023 |
|
RU2828294C1 |
| Моноклональные антитела, специфичные к белку рустицианин, и использование антител для диагностики и лечения злокачественных новообразований | 2024 |
|
RU2823344C1 |
Изобретение относится к медицине и биологии, к области экспериментальной дерматологии, и позволяет добиться ускорения заживления ран. Предлагается рекомбинантный белок rSLURP-2[R20A], который является специфическим стимулятором, вызывающим ускоренную миграцию кератиноцитов без увеличения их пролиферации. 3 н. и 2 з.п. ф-лы, 3 ил., 7 пр.
1. Рекомбинантный белок rSLURP-2[R20A], имеющий аминокислотную последовательность SEQ ID NO 2.
2. Применение белка по п. 1, в качестве специфического стимулятора миграции эпителиальных клеток человека.
3. Способ стимуляции миграции эпителиальных клеток человека, заключающийся в контактировании указанных клеток с эффективным количеством белка по п. 1.
4. Способ по п. 3, отличающийся тем, что белок продуцируется бактериальными клетками.
5. Способ по п. 4, отличающийся тем, что бактериальные клетки представляют собой E.
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pET22b(+)/slurp-2, КОДИРУЮЩАЯ БЕЛОК SLURP-2, И ШТАММ БАКТЕРИЙ Escherichia coli BL21(DE3) pET22b(+)/slurp-2- ПРОДУЦЕНТ БЕЛКА SLURP-2 ЧЕЛОВЕКА | 2015 |
|
RU2583307C2 |
| Lyukmanova E.N | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Rep., 2016, 6:30698, DOI: 10.1038/srep30698. | |||
Авторы
Даты
2021-01-28—Публикация
2020-07-23—Подача