Область техники, к которой относится настоящее изобретение
Настоящее описание относится к молекулам антител против вируса BK или к их связывающим фрагментам. Кроме того, настоящее описание относится к нуклеиновым кислотам, кодирующим молекулы антител или их связывающих фрагментов, векторам экспрессии, клеткам-хозяевам и способам получения молекул антител или их связывающих фрагментов. Также представлены фармацевтические композиции, содержащие молекулы антител или их связывающих фрагментов. Молекулы антител против вируса BK или их связывающих фрагментов согласно настоящему описанию можно использовать (отдельно или в комбинации с другими средствами или терапевтическими методами) для лечения или профилактики инфекции вируса BK и/или связанного с вирусом BK нарушения. Таким образом, настоящее описание также относится к молекулам антител против вируса BK или к их связывающим фрагментам или к фармацевтическим композициям, содержащим молекулы антител против вируса BK или их связывающие фрагменты, для применения в лечении или профилактики инфекции вируса BK и/или связанного с вирусом BK нарушения. Также представлена диагностическая композиция, содержащая молекулу антитела или его связывающего фрагмента.
Предшествующий уровень техники настоящего изобретения
Иммуносупрессивные лекарственные средства являются стандартом лечения реципиентов трансплантатов, чтобы обеспечить приживление и для предотвращения отторжения трансплантата. Иммуносупрессия может запускать реактивацию полиомавируса BK человека, например у 40-50% реципиентов трансплантатов почки (Hurdiss et al., Structure, 2016 Apr 5;24(4):528-536), и в 10% случаев это приводит к связанной с вирусом BK (BKV) нефропатии (BKVAN) (Bennett et al., Microbes Infect, 2012 Aug;14(9):672-83, Rinaldo et al, APMIS, 2013 Aug;121(8):728-45). BKVAN представляет собой серьезную угрозу, которая может приводить к потере функции трансплантата или даже к потере трансплантата (Ramos et al., Transplantation, 2009 Mar 15;87(5):621-30). Применение противовирусных средств дало противоречивые результаты по эффективности и не считается ценным вариантом лечения (Santeusanio et al. Am J Health Syst Pharm, 2017 Dec 15;74(24):2037-2045; Kable et al., Transplant Direct, 2017 Mar 10;3(4):e142).
Таким образом, стандартом лечения острой виремии является снижение иммуносупрессии, чтобы иммунная система могла бороться с вирусом. Однако это приводит к значительному риску краткосрочной и долгосрочной дисфункции трансплантата из-за иммунных реакций хозяина против трансплантата, таких как образование донор-специфических антител.
Ввиду постоянной потребности в улучшенных стратегиях профилактической или лечебной терапии у пациентов с подавленным иммунитетом весьма нужны новые композиции для нейтрализации активности вируса ВК.
Сущность настоящего изобретения
Аспект A
В одном аспекте A1 настоящее описание относится к молекуле антитела против вируса BK или к его фрагменту, связывающему вирус BK.
Структурные свойства
В некоторых вариантах осуществления аспекта A1 настоящее описание относится к молекуле антитела против вируса BK или его фрагмента, связывающего вирус BK, где молекула антитела или связывающего фрагмента содержит по меньшей мере одну, две, три, четыре, пять или шесть определяющих комплементарность областей (CDR) (или все CDR вместе) вариабельной области тяжелой цепи (VH) и/или вариабельной области легкой цепи (VL), содержащих аминокислотную последовательность, показанную в таблице 3, где одна или несколько CDR (или все CDR вместе) могут иметь одно, два, три, четыре, пять, шесть или более изменений, например аминокислотных замен (например консервативных аминокислотных замен), вставок или делеций, по сравнению с аминокислотной последовательностью, показанной в таблице 3.
В некоторых вариантах осуществления аспекта A1 настоящее описание относится к молекуле антитела против вируса BK или его фрагмента, связывающего вирус BK, содержащей:
вариабельную область тяжелой цепи (VH), содержащую один, два или три элемента из: аминокислотной последовательности SEQ ID NO:21 определяющей комплементарность области 1 тяжелой цепи (VHCDR1) или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции, аминокислотной последовательности SEQ ID NO:22 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции, и аминокислотной последовательности SEQ ID NO:23 определяющей комплементарность области 3 тяжелой цепи (VHCDR3) или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции; и/или вариабельную область легкой цепи (VL), содержащую один, два или три элемента из: аминокислотной последовательности SEQ ID NO:24 определяющей комплементарность области 1 легкой цепи (VLCDR1) или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции, аминокислотной последовательности SEQ ID NO:25 определяющей комплементарность области 2 легкой цепи (VLCDR2) или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции, и аминокислотной последовательности SEQ ID NO:26 определяющей комплементарность области 3 легкой цепи (VLCDR3) или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции.
В некоторых вариантах осуществления аспекта A1 настоящее описание относится к молекуле антитела против вируса BK или его фрагмента, связывающего вирус BK, содержащей:
вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:23 определяющей комплементарность области 3 тяжелой цепи (VHCDR3) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены); и/или
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:26 определяющей комплементарность области 3 легкой цепи (VLCDR3) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены).
В некоторых вариантах осуществления аспекта A1 настоящее описание относится к молекуле антитела против вируса BK или его фрагмента, связывающего вирус BK, содержащей:
вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:21 определяющей комплементарность области 1 тяжелой цепи (VHCDR1) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), аминокислотную последовательность SEQ ID NO:22 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), и аминокислотную последовательность SEQ ID NO:23 определяющей комплементарность области 3 тяжелой цепи (VHCDR3) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены); и/или
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:24 определяющей комплементарность области 1 легкой цепи (VLCDR1) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), аминокислотную последовательность SEQ ID NO:25 определяющей комплементарность области 2 легкой цепи (VLCDR2) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), и аминокислотную последовательность SEQ ID NO:26 определяющей комплементарность области 3 легкой цепи (VLCDR3) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены).
В некоторых вариантах осуществления аспекта A1 настоящее описание относится к молекуле антитела против вируса BK или его фрагмента, связывающего вирус BK, содержащей:
вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:21 определяющей комплементарность области 1 тяжелой цепи (VHCDR1), аминокислотную последовательность SEQ ID NO:22 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) или последовательность, имеющую одну, две или три аминокислотные замены, и аминокислотную последовательность SEQ ID NO:23 определяющей комплементарность области 3 тяжелой цепи (VHCDR3); и/или
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:24 определяющей комплементарность области 1 легкой цепи (VLCDR1) или последовательность, имеющую одну или две аминокислотные замены, аминокислотную последовательность SEQ ID NO:25 определяющей комплементарность области 2 легкой цепи (VLCDR2) и аминокислотную последовательность SEQ ID NO:26 определяющей комплементарность области 3 легкой цепи (VLCDR3) или последовательность, имеющую одну, две, три или четыре аминокислотные замены.
В некоторых вариантах осуществления аспекта A1 молекула антитела против вируса BK или его связывающего вирус BK фрагмента содержит:
вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:21 определяющей комплементарность области 1 тяжелой цепи (VHCDR1), аминокислотную последовательность SEQ ID NO:22 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) и аминокислотную последовательность SEQ ID NO:23 определяющей комплементарность области 3 тяжелой цепи (VHCDR3); и
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:24 определяющей комплементарность области 1 легкой цепи (VLCDR1), аминокислотную последовательность SEQ ID NO:25 определяющей комплементарность области 2 легкой цепи (VLCDR2) и аминокислотную последовательность SEQ ID NO:26 определяющей комплементарность области 3 легкой цепи (VLCDR3),
где одна или две аминокислоты в CDR были вставлены, удалены или заменены.
В некоторых вариантах осуществления аспекта A1 молекула антитела против вируса BK или его связывающего вирус BK фрагмента содержит:
вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:21 определяющей комплементарность области 1 тяжелой цепи (VHCDR1), аминокислотную последовательность SEQ ID NO:22 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) и аминокислотную последовательность SEQ ID NO:23 определяющей комплементарность области 3 тяжелой цепи (VHCDR3); и
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:24 определяющей комплементарность области 1 легкой цепи (VLCDR1), аминокислотную последовательность SEQ ID NO:25 определяющей комплементарность области 2 легкой цепи (VLCDR2) и аминокислотную последовательность SEQ ID NO:26 определяющей комплементарность области 3 легкой цепи (VLCDR3).
В некоторых вариантах осуществления аспекта A1 молекула антитела против вируса BK или его связывающего вирус BK фрагмента содержит вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:27 или аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:27.
В некоторых вариантах осуществления аспекта A1 молекула антитела против вируса BK или его связывающего вирус BK фрагмента содержит (i) вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:28 или аминокислотную последовательность имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:28; или (ii)
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:31 или аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:31.
В некоторых вариантах осуществления аспекта A1 молекула антитела против вируса BK или его связывающего вирус BK фрагмента содержит
(i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:27 или аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:27; и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:28 или аминокислотную последовательность имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:28; или
(ii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:27 или аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:27; и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:31 или аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:31.
В некоторых вариантах осуществления аспекта A1 молекула антитела против вируса BK или его связывающего вирус BK фрагмента содержит
(i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:27 и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:28; или
(ii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:27 и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:31.
Функциональные свойства
В некоторых вариантах осуществления аспекта A1 молекула антитела против вируса BK или его связывающего вирус BK фрагмента имеет одно или несколько (например, 2, 3, 4, 5, 6, 7, 8 или 9) следующих свойств:
(i) связывается с вирусом BK серотип I VP1 с EC50 менее примерно 10 нМ, 1 нМ, 0,9 нМ, 0,8 нМ, 0,7 нМ, 0,6 нМ, 0,5 нМ, 0,4 нМ, 0,3 нМ, 0,2 нМ, 0,19 нМ, 0,18 нМ, 0,17 нМ, 0,16 нМ, 0,15 нМ, 0,14 нМ, 0,13 нМ, 0,12 нМ, 0,11 нМ, 0,10 нМ, 0,09 нМ, 0,08 нМ, 0,07 нМ, 0,06 нМ, 0,05 нМ, 0,04 нМ, 0,03 нМ или 0,02 нМ, например, когда молекулу антитела или его связывающего фрагмента тестируют как бивалентную молекулу с использованием ELISA, например, как описано в примере 2;
(ii) связывается с вирусом BK серотип II VP1 с EC50 менее примерно 10 нМ, 1 нМ, 0,9 нМ, 0,8 нМ, 0,7 нМ, 0,6 нМ, 0,5 нМ, 0,4 нМ, 0,3 нМ, 0,2 нМ, 0,19 нМ, 0,18 нМ, 0,17 нМ, 0,16 нМ, 0,15 нМ, 0,14 нМ, 0,13 нМ, 0,12 нМ, 0,11 нМ, 0,10 нМ, 0,09 нМ, 0,08 нМ, 0,07 нМ, 0,06 нМ, 0,05 нМ, 0,04 нМ, 0,03 нМ или 0,02 нМ, например, когда молекулу антитела или его связывающего фрагмента тестируют как бивалентную молекулу с использованием ELISA, например, как описано в примере 2;
(iii) связывается с вирусом BK серотип III VP1 с EC50 менее примерно 10 нМ, 1 нМ, 0,9 нМ, 0,8 нМ, 0,7 нМ, 0,6 нМ, 0,5 нМ, 0,4 нМ, 0,3 нМ, 0,2 нМ, 0,19 нМ, 0,18 нМ, 0,17 нМ, 0,16 нМ, 0,15 нМ, 0,14 нМ, 0,13 нМ, 0,12 нМ, 0,11 нМ, 0,10 нМ, 0,09 нМ, 0,08 нМ, 0,07 нМ, 0,06 нМ, 0,05 нМ, 0,04 нМ, 0,03 нМ или 0,02 нМ, например, когда молекулу антитела или его связывающего фрагмента тестируют как бивалентную молекулу с использованием ELISA, например, как описано в примере 2;
(iv) связывается с вирусом BK серотип IV VP1 с EC50 менее примерно 10 нМ, 1 нМ, 0,9 нМ, 0,8 нМ, 0,7 нМ, 0,6 нМ, 0,5 нМ, 0,4 нМ, 0,3 нМ, 0,2 нМ, 0,19 нМ, 0,18 нМ, 0,17 нМ, 0,16 нМ, 0,15 нМ, 0,14 нМ, 0,13 нМ, 0,12 нМ, 0,11 нМ, 0,10 нМ, 0,09 нМ, 0,08 нМ, 0,07 нМ, 0,06 нМ, 0,05 нМ, 0,04 нМ, 0,03 нМ или 0,02 нМ, например, когда молекулу антитела или его связывающего фрагмента тестируют как бивалентную молекулу с использованием ELISA, например, как описано в примере 2;
(v) не связывается с вирусом JC VP1; например, как описано в примере 6;
(vi) нейтрализует вирус BK серотип I;
(vii) нейтрализует вирус BK серотип II;
(viii) нейтрализует вирус BK серотип III;
(ix) нейтрализует вирус BK серотип IV.
В одном аспекте A2 настоящее описание относится к молекуле антитела или его связывающего фрагмента, которая конкурирует за связывание с вирусом BK серотип I VP1, вирусом BK серотип II VP1, вирусом BK серотип III VP1 и/или вирусом BK серотип IV VP1 с молекулой антитела или его связывающего фрагмента, описанной в настоящем документе. В некоторых вариантах осуществления аспекта A2 настоящее описание относится к молекуле антитела или его связывающего фрагмента, которая конкурирует за связывание с вирусом BK генотип I VP1, вирусом BK генотип II VP1, вирусом BK генотип III VP1 и/или вирусом BK генотип IV VP1 с молекулой антитела или его связывающего фрагмента, которая содержит вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:21 определяющей комплементарность области 1 тяжелой цепи (VHCDR1), аминокислотную последовательность SEQ ID NO:22 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) и аминокислотную последовательность SEQ ID NO:23 определяющей комплементарность области 3 тяжелой цепи (VHCDR3); и
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:24 определяющей комплементарность области 1 легкой цепи (VLCDR1), аминокислотную последовательность SEQ ID NO:25 определяющей комплементарность области 2 легкой цепи (VLCDR2) и аминокислотную последовательность SEQ ID NO:26 определяющей комплементарность области 3 легкой цепи (VLCDR3).
В некоторых вариантах осуществления аспекта A2 настоящее описание относится к молекуле антитела или его связывающего фрагмента, которая конкурирует за связывание с вирусом BK генотип I VP1, вирусом BK генотип II VP1, вирусом BK генотип III VP1 и/или вирусом BK генотип IV VP1 с молекулой антитела или его связывающего фрагмента, которая содержит (i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:27 и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:28; или
(ii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:27 и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:31.
В одном аспекте A3 настоящее описание относится к фармацевтической композиции, содержащей молекулу антитела или его связывающего фрагмента, описанную в настоящем документе, и фармацевтически приемлемый носитель, вспомогательное средство или стабилизатор.
В одном аспекте A4 настоящее описание относится к молекулам антител против вируса BK или их связывающих фрагментов, описанным в настоящем документе, или к фармацевтическим композициям, содержащим молекулы антител против вируса BK или их связывающих фрагментов, описанные в настоящем документе, для применения при лечении или профилактике инфекции вируса BK и/или связанного с вирусом BK нарушения. В некоторых вариантах осуществления аспекта A4 связанное с вирусом BK нарушение выбирают из группы, состоящей из нефропатии, связанной с вирусом BK нефропатии (BKVAN), геморрагического цистита (HC).
В одном аспекте A5 настоящее описание относится к нуклеиновой кислоте, кодирующей вариабельную область тяжелой и/или легкой цепи молекулы антитела или его связывающего фрагмента, описанной в настоящем документе.
В одном аспекте A6 настоящее описание относится к вектору экспрессии, содержащему нуклеиновую кислоту, описанную в настоящем документе.
В одном аспекте A7 настоящее описание относится к клетке-хозяину, содержащей нуклеиновую кислоту, описанную в настоящем документе, или вектор экспрессии, описанный в настоящем документе.
В одном аспекте A8 настоящее описание относится к способу получения молекулы антитела, где способ включает культивирование клетки-хозяина, описанной в настоящем документе, в условиях, подходящих для экспрессии гена.
В одном аспекте A9 настоящее описание относится к диагностической композиции, содержащей молекулу антитела или его связывающего фрагмента, описанную в настоящем документе.
Аспект B
В одном аспекте B1 настоящее описание относится к молекуле антитела против вируса BK или его связывающего вирус BK фрагмента.
Структурные свойства
В некоторых вариантах осуществления аспекта B1 настоящее описание относится к молекуле антитела против вируса BK или его фрагмента, связывающего вирус BK, где молекула антитела или связывающего фрагмента содержит по меньшей мере одну, две, три, четыре, пять или шесть определяющих комплементарность областей (CDR) (или все CDR вместе) из вариабельной области тяжелой цепи (VH) и/или из вариабельной области легкой цепи (VL), содержащих аминокислотную последовательность, показанную в таблице 4, где одна или несколько CDR (или все CDR вместе) могут иметь одно, два, три, четыре, пять, шесть или более изменений, например аминокислотных замен (например консервативных аминокислотных замен), вставок или делеций, по сравнению с аминокислотной последовательностью, показанной в таблице 4.
В некоторых вариантах осуществления аспекта B1 настоящее описание относится к молекуле антитела против вируса BK или его фрагмента, связывающего вирус BK, содержащей:
(i) вариабельную область тяжелой цепи (VH), содержащую один, два или три элемента из: аминокислотной последовательности определяющей комплементарность области 1 тяжелой цепи (VHCDR1) SEQ ID NO:34 или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции, аминокислотной последовательности SEQ ID NO:35 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции, и аминокислотной последовательности SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3) или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции; и/или вариабельную область легкой цепи (VL), содержащую один, два или три элемента из: аминокислотной последовательности SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1) или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции, аминокислотной последовательности SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции, и аминокислотной последовательности SEQ ID NO:39 определяющей комплементарность области 3 легкой цепи (VLCDR3) или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции; или
(ii) вариабельную область тяжелой цепи (VH), содержащую один, два или три элемента из: аминокислотной последовательности определяющей комплементарность области 1 тяжелой цепи (VHCDR1) SEQ ID NO:34 или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции, аминокислотной последовательности SEQ ID NO:44 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции, и аминокислотной последовательности SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3) или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции; и/или вариабельную область легкой цепи (VL), содержащую один, два или три элемента из: аминокислотной последовательности SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1) или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции, аминокислотной последовательности SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции, и аминокислотной последовательности SEQ ID NO:39 определяющей комплементарность области 3 легкой цепи (VLCDR3) или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции; или
(iii) вариабельную область тяжелой цепи (VH), содержащую один, два или три элемента из: аминокислотной последовательности определяющей комплементарность области 1 тяжелой цепи (VHCDR1) SEQ ID NO:34 или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции, аминокислотной последовательности SEQ ID NO:44 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции, и аминокислотной последовательности SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3) или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции; и/или вариабельную область легкой цепи (VL), содержащую один, два или три элемента из: аминокислотной последовательности SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1) или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции, аминокислотной последовательности SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции, и аминокислотной последовательности SEQ ID NO:48 определяющей комплементарность области 3 легкой цепи (VLCDR3) или последовательности, имеющей одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), вставки или делеции.
В некоторых вариантах осуществления аспекта B1 настоящее описание относится к молекуле антитела против вируса BK или его фрагмента, связывающего вирус BK, содержащей:
(i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены); и/или
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:39 определяющей комплементарность области 3 легкой цепи (VLCDR3) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены); или
(ii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены); и/или
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:48 определяющей комплементарность области 3 легкой цепи (VLCDR3) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены).
В некоторых вариантах осуществления аспекта B1 настоящее описание относится к молекуле антитела против вируса BK или его фрагмента, связывающего вирус BK, содержащей:
(i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:34 определяющей комплементарность области 1 тяжелой цепи (VHCDR1) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), аминокислотную последовательность SEQ ID NO:35 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), и аминокислотную последовательность SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены); и/или
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), аминокислотную последовательность SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), и аминокислотную последовательность SEQ ID NO:39 определяющей комплементарность области 3 легкой цепи (VLCDR3) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены); или
(ii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:34 определяющей комплементарность области 1 тяжелой цепи (VHCDR1) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), аминокислотную последовательность SEQ ID NO:44 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), и аминокислотную последовательность SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены); и/или
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), аминокислотную последовательность SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), и аминокислотную последовательность SEQ ID NO:39 определяющей комплементарность области 3 легкой цепи (VLCDR3) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены); или
(iii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:34 определяющей комплементарность области 1 тяжелой цепи (VHCDR1) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), аминокислотную последовательность SEQ ID NO:44 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), и аминокислотную последовательность SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены); и/или
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), аминокислотную последовательность SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены), и аминокислотная последовательность SEQ ID NO:48 определяющей комплементарность области 3 легкой цепи (VLCDR3) или последовательность, имеющую одну, две, три или четыре аминокислотные замены (например консервативные аминокислотные замены).
В некоторых вариантах осуществления аспекта B1 настоящее описание относится к молекуле антитела против вируса BK или его фрагмента, связывающего вирус BK, содержащей:
(i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:34 определяющей комплементарность области 1 тяжелой цепи (VHCDR1), аминокислотную последовательность SEQ ID NO:35 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) или последовательность, имеющую одну, две или три аминокислотные замены, и аминокислотную последовательность SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3); и/или
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1) или последовательность, имеющую одну или две аминокислотные замены, аминокислотную последовательность SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) и аминокислотную последовательность SEQ ID NO:39 определяющей комплементарность области 3 легкой цепи (VLCDR3) или последовательность, имеющую одну, две, три или четыре аминокислотные замены; или
(ii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:34 определяющей комплементарность области 1 тяжелой цепи (VHCDR1), аминокислотную последовательность SEQ ID NO:44 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) или последовательность, имеющую одну, две или три аминокислотные замены, и аминокислотную последовательность SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3); и/или
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1) или последовательность, имеющую одну или две аминокислотные замены, аминокислотную последовательность SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) и аминокислотную последовательность SEQ ID NO:39 определяющей комплементарность области 3 легкой цепи (VLCDR3) или последовательность, имеющую одну, две, три или четыре аминокислотные замены; или
(iii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:34 определяющей комплементарность области 1 тяжелой цепи (VHCDR1), аминокислотную последовательность SEQ ID NO:44 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) или последовательность, имеющую одну, две или три аминокислотные замены, и аминокислотную последовательность SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3); и/или
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1) или последовательность, имеющую одну или две аминокислотные замены, аминокислотную последовательность SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) и аминокислотная последовательность SEQ ID NO:48 определяющей комплементарность области 3 легкой цепи (VLCDR3) или последовательность, имеющую одну, две, три или четыре аминокислотные замены.
В некоторых вариантах осуществления аспекта B1 молекула антитела против вируса BK или его связывающего вирус BK фрагмента содержит:
(i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:34 определяющей комплементарность области 1 тяжелой цепи (VHCDR1), аминокислотную последовательность SEQ ID NO:35 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) и аминокислотную последовательность SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3); и
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1), аминокислотную последовательность SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) и аминокислотную последовательность SEQ ID NO:39 определяющей комплементарность области 3 легкой цепи (VLCDR3);
где одна или две аминокислоты в CDR были вставлены, удалены или заменены;
или
(ii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:34 определяющей комплементарность области 1 тяжелой цепи (VHCDR1), аминокислотную последовательность SEQ ID NO:44 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) и аминокислотную последовательность SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3); и
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1), аминокислотную последовательность SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) и аминокислотную последовательность SEQ ID NO:39 определяющей комплементарность области 3 легкой цепи (VLCDR3);
где одна или две аминокислоты в CDR были вставлены, удалены или заменены;
или
(iii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:34 определяющей комплементарность области 1 тяжелой цепи (VHCDR1), аминокислотную последовательность SEQ ID NO:44 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) и аминокислотную последовательность SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3); и
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1), аминокислотную последовательность SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) и аминокислотная последовательность SEQ ID NO:48 определяющей комплементарность области 3 легкой цепи (VLCDR3);
где одна или две аминокислоты в CDR были вставлены, удалены или заменены.
В некоторых вариантах осуществления аспекта B1 молекула антитела против вируса BK или его связывающего вирус BK фрагмента содержит:
(i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:34 определяющей комплементарность области 1 тяжелой цепи (VHCDR1), аминокислотную последовательность SEQ ID NO:35 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) и аминокислотную последовательность SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3); и
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1), аминокислотную последовательность SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) и аминокислотную последовательность SEQ ID NO:39 определяющей комплементарность области 3 легкой цепи (VLCDR3); или
(ii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:34 определяющей комплементарность области 1 тяжелой цепи (VHCDR1), аминокислотную последовательность SEQ ID NO:44 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) и аминокислотную последовательность SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3); и
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1), аминокислотную последовательность SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) и аминокислотную последовательность SEQ ID NO:39 определяющей комплементарность области 3 легкой цепи (VLCDR3); или
(iii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:34 определяющей комплементарность области 1 тяжелой цепи (VHCDR1), аминокислотную последовательность SEQ ID NO:44 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) и аминокислотную последовательность SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3); и
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1), аминокислотную последовательность SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) и аминокислотная последовательность SEQ ID NO:48 определяющей комплементарность области 3 легкой цепи (VLCDR3).
В некоторых вариантах осуществления аспекта B1 молекула антитела против вируса BK или его связывающего вирус BK фрагмента содержит (i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:40 или аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:40; или (ii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:45 или аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:45; или (iii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:49 или аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:49.
В некоторых вариантах осуществления аспекта B1 молекула антитела против вируса BK или его связывающего вирус BK фрагмента содержит (i) вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:41 или аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:41; или (ii) вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:50 или аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:50.
В некоторых вариантах осуществления аспекта B1 молекула антитела против вируса BK или его связывающего вирус BK фрагмента содержит
(i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:40 или аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:40; и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:41 или аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:41; или
(ii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:45 или аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:45; и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:41 или аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:41; или
(iii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:49 или аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:49; и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:50 или аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:50.
В некоторых вариантах осуществления аспекта B1 молекула антитела против вируса BK или его связывающего вирус BK фрагмента содержит
(i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:40, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:41; или
(ii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:45, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:41; или
(iii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:49, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:50.
Функциональные свойства
В некоторых вариантах осуществления аспекта B1 молекула антитела против вируса BK или его связывающего вирус BK фрагмента имеет одно или несколько (например 2, 3, 4, 5, 6, 7, 8 или 9) следующих свойств:
(i) связывается с вирусом BK серотип I VP1 с EC50 менее примерно 10 нМ, 1 нМ, 0,9 нМ, 0,8 нМ, 0,7 нМ, 0,6 нМ, 0,5 нМ, 0,4 нМ, 0,3 нМ, 0,2 нМ, 0,19 нМ, 0,18 нМ, 0,17 нМ, 0,16 нМ, 0,15 нМ, 0,14 нМ, 0,13 нМ, 0,12 нМ, 0,11 нМ, 0,10 нМ, 0,09 нМ, 0,08 нМ, 0,07 нМ, 0,06 нМ, 0,05 нМ, 0,04 нМ, 0,03 нМ или 0,02 нМ, например, когда молекулу антитела или его связывающего фрагмента тестируют как бивалентную молекулу с использованием ELISA, например, как описано в примере 2;
(ii) связывается с вирусом BK серотип II VP1 с EC50 менее примерно 10 нМ, 1 нМ, 0,9 нМ, 0,8 нМ, 0,7 нМ, 0,6 нМ, 0,5 нМ, 0,4 нМ, 0,3 нМ, 0,2 нМ, 0,19 нМ, 0,18 нМ, 0,17 нМ, 0,16 нМ, 0,15 нМ, 0,14 нМ, 0,13 нМ, 0,12 нМ, 0,11 нМ, 0,10 нМ, 0,09 нМ, 0,08 нМ, 0,07 нМ, 0,06 нМ, 0,05 нМ, 0,04 нМ, 0,03 нМ или 0,02 нМ, например, когда молекулу антитела или его связывающего фрагмента тестируют как бивалентную молекулу с использованием ELISA, например, как описано в примере 2;
(iii) связывается с вирусом BK серотип III VP1 с EC50 менее примерно 10 нМ, 1 нМ, 0,9 нМ, 0,8 нМ, 0,7 нМ, 0,6 нМ, 0,5 нМ, 0,4 нМ, 0,3 нМ, 0,2 нМ, 0,19 нМ, 0,18 нМ, 0,17 нМ, 0,16 нМ, 0,15 нМ, 0,14 нМ, 0,13 нМ, 0,12 нМ, 0,11 нМ, 0,10 нМ, 0,09 нМ, 0,08 нМ, 0,07 нМ, 0,06 нМ, 0,05 нМ, 0,04 нМ, 0,03 нМ или 0,02 нМ, например, когда молекулу антитела или его связывающего фрагмента тестируют как бивалентную молекулу с использованием ELISA, например, как описано в примере 2;
(iv) связывается с вирусом BK серотип IV VP1 с EC50 менее примерно 10 нМ, 1 нМ, 0,9 нМ, 0,8 нМ, 0,7 нМ, 0,6 нМ, 0,5 нМ, 0,4 нМ, 0,3 нМ, 0,2 нМ, 0,19 нМ, 0,18 нМ, 0,17 нМ, 0,16 нМ, 0,15 нМ, 0,14 нМ, 0,13 нМ, 0,12 нМ, 0,11 нМ, 0,10 нМ, 0,09 нМ, 0,08 нМ, 0,07 нМ, 0,06 нМ, 0,05 нМ, 0,04 нМ, 0,03 нМ или 0,02 нМ, например, когда молекулу антитела или его связывающего фрагмента тестируют как бивалентную молекулу с использованием ELISA, например, как описано в примере 2;
(v) не связывается с вирусом JC VP1; например, как описано в примере 6;
(vi) нейтрализует вирус BK серотип I;
(vii) нейтрализует вирус BK серотип II;
(viii) нейтрализует вирус BK серотип III;
(ix) нейтрализует вирус BK серотип IV.
В одном аспекте B2 настоящее описание относится к молекуле антитела или его связывающего фрагмента, которая конкурирует за связывание с вирусом BK серотип I VP1, вирусом BK серотип II VP1, вирусом BK серотип III VP1 и/или вирусом BK серотип IV VP1 с молекулой антитела или его связывающего фрагмента, описанной в настоящем документе. В некоторых вариантах осуществления аспекта B2 настоящее описание относится к молекуле антитела или его связывающего фрагмента, которая конкурирует за связывание с вирусом BK генотип I VP1, вирусом BK генотип II VP1, вирусом BK генотип III VP1 и/или вирусом BK генотип IV VP1 с молекулой антитела или его связывающего фрагмента, которая содержит
(i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:34 определяющей комплементарность области 1 тяжелой цепи (VHCDR1), аминокислотную последовательность SEQ ID NO:35 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) и аминокислотную последовательность SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3); и
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1), аминокислотную последовательность SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) и аминокислотную последовательность SEQ ID NO:39 определяющей комплементарность области 3 легкой цепи (VLCDR3); или
(ii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:34 определяющей комплементарность области 1 тяжелой цепи (VHCDR1), аминокислотную последовательность SEQ ID NO:44 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) и аминокислотную последовательность SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3); и
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1), аминокислотную последовательность SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) и аминокислотную последовательность SEQ ID NO:39 определяющей комплементарность области 3 легкой цепи (VLCDR3); или
(iii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:34 определяющей комплементарность области 1 тяжелой цепи (VHCDR1), аминокислотную последовательность SEQ ID NO:44 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) и аминокислотную последовательность SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3); и
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1), аминокислотную последовательность SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) и аминокислотная последовательность SEQ ID NO:48 определяющей комплементарность области 3 легкой цепи (VLCDR3).
В некоторых вариантах осуществления аспекта B2 настоящее описание относится к молекуле антитела или его связывающего фрагмента, которая конкурирует за связывание с вирусом BK генотип I VP1, вирусом BK генотип II VP1, вирусом BK генотип III VP1 и/или вирусом BK генотип IV VP1 с молекулой антитела или его связывающего фрагмента, которая содержит
(i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:40, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:41; или
(ii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:45, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:41; или
(iii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:49, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:50.
В одном аспекте B3 настоящее описание относится к фармацевтической композиции, содержащей молекулу антитела или его связывающего фрагмента, описанную в настоящем документе, и фармацевтически приемлемый носитель, вспомогательное средство или стабилизатор.
В одном аспекте B4 настоящее описание относится к молекулам антител против вируса BK или их связывающих фрагментов, описанным в настоящем документе, или к фармацевтическим композициям, содержащим молекулы антител против вируса BK или их связывающих фрагментов, описанные в настоящем документе, для применения при лечении или профилактике инфекции вируса BK и/или связанного с вирусом BK нарушения. В некоторых вариантах осуществления аспекта B4 связанное с вирусом BK нарушение выбирают из группы, состоящей из нефропатии, связанной с вирусом BK нефропатии (BKVAN), геморрагического цистита (HC).
В одном аспекте B5 настоящее описание относится к нуклеиновой кислоте, кодирующей вариабельную область тяжелой и/или легкой цепи молекулы антитела или его связывающего фрагмента, описанной в настоящем документе.
В одном аспекте B6 настоящее описание относится к вектору экспрессии, содержащему нуклеиновую кислоту, описанную в настоящем документе.
В одном аспекте B7 настоящее описание относится к клетке-хозяину, содержащей нуклеиновую кислоту, описанную в настоящем документе, или вектор экспрессии, описанный в настоящем документе.
В одном аспекте B8 настоящее описание относится к способу получения молекулы антитела, где способ включает культивирование клетки-хозяина, описанной в настоящем документе, в условиях, подходящих для экспрессии гена.
В одном аспекте B9 настоящее описание относится к диагностической композиции, содержащей молекулу антитела или его связывающего фрагмента, описанную в настоящем документе.
Краткое описание чертежей
Фиг. 1. Связывание антител против вируса ВК с серотипами I-IV BKV-VP1 в ELISA. Эти данные использовали для определения значений EC50E с помощью трехпараметрического анализа в программном обеспечении GraphPad Prism.
Фиг. 2. Количественная оценка опосредованной антителами нейтрализации штаммов BKV (серотипы Ia, Ib, II, III и IV). Клетки 293TT использовали в качестве мишени для инфицирования экспрессирующим люциферазу псевдовирусом BK с серотипом Ia, Ib, II, III и IV VP1. Антитела против вируса ВК использовали в указанных концентрациях.
Фиг. 3. Длительная нейтрализация вируса BKV дикого типа на эпителиальных клетках первичных почечных канальцев человека антителами против вируса BK. Показана остаточная вирусная нагрузка после длительной совместной инкубации клеток, вируса ВК и антител против вируса ВК в указанных концентрациях. Концентрации антител соответствуют EC 95 (1,500), EC50 (0,15) и EC5 (0,015). На этой фигуре P8D11 помечен «BM2».
Фиг. 4. Связывание антител против вируса BK с конформационным эпитопом.
Фиг. 5. Оценка силы связывания в ELISA с мутантами VP1 и JCV- антитела 319C07 и антитела 336F07 по сравнению с антителом P8D11. Значения EC50 для различных мутантных форм VP1 и JC-VP1 определяли по сравнению с VP1 дикого типа. Мутанты VP1 обозначены в стандартном формате, где номер относится к положению в последовательности VP1-STI, которое было изменено с аминокислоты слева от номера на аминокислоту справа от номера.
На графиках показано связывание антитела 319C07, антитела 336F07, изотипического контрольного антитела 24C03 и антитела P8D11 с выбранными мутантами BKV-VP1 и JCV-VP1, а также пентамерами нерелевантного антигена CMV-gH.
В таблице представлены данные для всех протестированных мутантов BKV-VP1 и JCV-VP1. «+» использован для обозначения того, что между исходной последовательностью и мутантной последовательностью не наблюдается различий в аффинности связывания. «Красный» обозначает пониженное связывание, «-» обозначает отсутствие связывания.
Фиг. 6. Ингибирование распространения BKV на HRPTEC антителами против вируса BK (на этой фигуре P8D11 помечен как «BM2»).
Фиг. 7. Активность ADCC антител против BKV на инфицированных и неинфицированных HPRTEC.
Фиг. 8. Активность CDC антител против BKV на инфицированных и неинфицированных HPRTEC в присутствии сыворотки человека.
Подробное раскрытие настоящего изобретения
Настоящее изобретение, иллюстративно описанное ниже, может быть надлежащим образом осуществлено на практике при отсутствии какого-либо элемента или элементов, ограничения или ограничений, конкретно не раскрытых в данном документе.
Настоящее изобретение будет описано в отношении конкретных вариантов осуществления и со ссылкой на определенные фигуры, но изобретение ими не ограничено, а ограничено только формулой изобретения.
В тех случаях, когда термин «содержащий» использован в настоящем описании и формуле изобретения, он не исключает другие элементы. Для целей настоящего изобретения термин «состоящий из» считается предпочтительным вариантом осуществления термина «содержащий». Если далее определено, что группа включает по меньшей мере определенное количество вариантов осуществления, это также следует понимать как раскрытие группы, которая предпочтительно состоит только из этих вариантов осуществления.
Если не указано иное, использование существительного в единственном числе включает множественное число этого существительного. Термины «примерно» или «приблизительно» в контексте настоящего изобретения обозначают интервал точности, который будет понятен специалисту в данной области для обеспечения технического эффекта рассматриваемого признака. Термин указывает на отклонение от указанного числового значения ±20%, предпочтительно ±10% и более предпочтительно ±5%.
Технические термины использованы в их обычном значении. Если определенным терминам придается особое значение, ниже будут даны определения терминов, в контексте которых эти термины использованы.
Некоторые аспекты настоящего изобретения основаны, по крайней мере частично, на идентификации молекул антител против вируса BK или их связывающих фрагментов, которые
- связывают и нейтрализуют вирус ВК серотипа I; и/или
- связывают и связывают вирус ВК серотипа II; и/или
- связывают и нейтрализуют вирус ВК серотипа III; и/или
- связываться и нейтрализуют вирус ВК серотипа IV; и/или
- не связываются с вирусом JC VP1.
В предпочтительном варианте осуществления молекулы антител против вируса BK или их связывающие фрагменты нейтрализуют вирусы BK серотипов I, II, III и IV.
В другом предпочтительном варианте осуществления молекулы антител против вируса BK или их связывающие фрагменты не связываются с вирусом JC VP1. Повышенная специфичность проявляется в виде отсутствия связывания с близкородственным вирусом JC VP1. Повышенная специфичность считается лучшей безопасностью из-за меньшего риска нецелевой реактивности.
Как упоминалось выше, в настоящем изобретении рассмотрены молекулы антител против вируса BK или их связывающие фрагменты. Полноразмерное антитело содержит константный домен и вариабельный домен. Константная область не обязательно должна присутствовать в связывающем антигене фрагменте антитела.
Таким образом, связывающие фрагменты могут содержать части интактного полноразмерного антитела, такие как антигенсвязывающая или вариабельная область полного антитела. Примеры фрагментов антител включают фрагменты Fab, F(ab')2, Id и Fv; диатела; линейные антитела; молекулы одноцепочечных антител (например, scFv); фрагменты мультиспецифических антител, например биспецифических, триспецифических и мультиспецифических антител (например диатела, триатела, тетратела); минитела; хелатирующие рекомбинантные антитела; тритела или битела; интратела; нанотела; малые модульные иммунофармацевтические препараты (SMIP), слитые белки связывающего домена иммуноглобулина; верблюжьи антитела; антитела, содержащие VHH; и любые другие полипептиды, образованные из фрагментов антител. Специалисту известно, что антигенсвязывающую функцию антитела могут выполнять фрагменты полноразмерного антитела.
В настоящем документе раскрыты полипептиды, имеющие указанные последовательности или последовательности, по существу идентичные или сходные с ними, например последовательности, имеющие по меньшей мере около 85%, 90%, 95% или 99% идентичности указанной последовательности.
Определение процента идентичности между двумя последовательностями предпочтительно осуществляют с использованием математического алгоритма Karlin and Altschul (1993) Proc. Natl. Acad. Sci USA 90: 5873-5877. Такой алгоритм включен в программу BLASTp (Protein BLAST) program of Altschul et al. (1990) J. Mol. Biol. 215: 403-410, доступную на сайте NCBI (https://blast.ncbi.nlm.nih.gov/). Определение процента идентичности может быть выполнено со стандартными параметрами программы BLASTp. Для общих параметров в поле «Максимальные целевые последовательности» можно установить 100, в поле «Короткие запросы» можно установить галочку, в поле «Порог ожидания» можно установить 10, в поле «Размер слова» можно установить значение «3», и можно установить «0» в поле «Максимальное количество совпадений в диапазоне запроса». Для параметров оценки в поле «Матрица» можно установить «BLOSUM62», в поле «Стоимость гэпа» можно установить «Existence: 11 Extension: 1», в поле «Композиционные корректировки» можно установить «условная композиционная корректировка матрицы замен». В поле параметров «Фильтры и маскирование» можно не ставить галочку «Области низкой сложности», нельзя ставить галочку «только согласно таблице поиска» и нельзя ставить галочку «скрыть строчные символы».
В соответствии с описанием «консервативная аминокислотная замена» представляет собой аминокислотную замену, при которой аминокислотный остаток заменяется аминокислотным остатком, имеющим аналогичную боковую цепь. В данной области определены семейства аминокислотных остатков, имеющих аналогичные боковые цепи. Эти семейства включают аминокислоты с основными боковыми цепями (например лизин, аргинин, гистидин), кислыми боковыми цепями (например аспарагиновая кислота, глутаминовая кислота), незаряженными полярными боковыми цепями (например глицин, аспарагин, глутамин, серин, треонин, тирозин, цистеин), неполярными боковыми цепями (например аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин, триптофан), бета-разветвленными боковыми цепями (например треонин, валин, изолейцин) и ароматическими боковыми цепями (например тирозин, фенилаланин, триптофан, гистидин).
Как уже упоминалось, изобретение также относится в некоторых вариантах осуществления к нуклеиновой кислоте, кодирующей молекулы антител или их связывающие фрагменты, векторам, содержащим такие нуклеиновые кислоты, и клеткам-хозяевам, содержащим такие нуклеиновые кислоты или векторы.
Молекулы антител или их связывающие фрагменты могут кодироваться одной нуклеиновой кислотой (например одной нуклеиновой кислотой, содержащей нуклеотидные последовательности, которые кодируют полипептиды легкой и тяжелой цепи антитела) или двумя или более отдельными нуклеиновыми кислотами, каждая из которых кодирует другую часть молекулы антитела или фрагмент антитела. Нуклеиновые кислоты могут представлять собой ДНК, кДНК, РНК и т.п.
Описанные в данном документе нуклеиновые кислоты могут быть вставлены в векторы. «Вектор» представляет собой любую молекулу или композицию, способную переносить последовательность нуклеиновой кислоты в подходящую клетку, где может происходить синтез кодируемого полипептида.
Настоящее описание в некоторых аспектах дополнительно относится к клетке-хозяину (например выделенной или очищенной клетке), содержащей нуклеиновую кислоту или вектор согласно изобретению. Клетка-хозяин может представлять собой клетку любого типа, способную трансформироваться нуклеиновой кислотой или вектором согласно изобретению с получением кодируемого ими полипептида.
Молекулы антител против вируса BK или их фрагменты, связывающие вирус против BK, могут быть включены в состав композиций, особенно фармацевтических композиций. Такие композиции содержат терапевтически эффективное количество антитела или его связывающего фрагмента в смеси с фармацевтически приемлемым носителем, вспомогательным средством или стабилизатором.
Кроме того, молекулы антител против вируса BK или против их связывающих вирус BK фрагментов и фармацевтические композиции, которые описаны в настоящем документе, можно вводить в способах лечения или профилактики инфекции вируса BK и/или связанного с вирусом BK нарушения.
Предпочтительными вариантами осуществления аспектов B1-B9 настоящего изобретения являются:
1. Молекула антитела против вируса BK или его фрагмента, связывающего вирус BK, содержащая:
(i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:34 определяющей комплементарность области 1 тяжелой цепи (VHCDR1) или последовательность, имеющую одну или две аминокислотные замены, аминокислотную последовательность SEQ ID NO:35 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) или последовательность, имеющую одну или две аминокислотные замены, и аминокислотную последовательность SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3) или последовательность, имеющую одну или две аминокислотные замены; и
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1) или последовательность, имеющую одну или две аминокислотные замены, аминокислотную последовательность SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) или последовательность, имеющую одну или две аминокислотные замены, и аминокислотную последовательность SEQ ID NO:39 определяющей комплементарность области 3 легкой цепи (VLCDR3) или последовательность, имеющую одну или две аминокислотные замены; или
(ii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:34 определяющей комплементарность области 1 тяжелой цепи (VHCDR1) или последовательность, имеющую одну или две аминокислотные замены, аминокислотную последовательность SEQ ID NO:44 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) или последовательность, имеющую одну или две аминокислотные замены, и аминокислотную последовательность SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3) или последовательность, имеющую одну или две аминокислотные замены; и
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1) или последовательность, имеющую одну или две аминокислотные замены, аминокислотную последовательность SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) или последовательность, имеющую одну или две аминокислотные замены, и аминокислотную последовательность SEQ ID NO:39 определяющей комплементарность области 3 легкой цепи (VLCDR3) или последовательность, имеющую одну или две аминокислотные замены; или
(iii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:34 определяющей комплементарность области 1 тяжелой цепи (VHCDR1) или последовательность, имеющую одну или две аминокислотные замены, аминокислотную последовательность SEQ ID NO:44 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) или последовательность, имеющую одну или две аминокислотные замены, и аминокислотную последовательность SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3) или последовательность, имеющую одну или две аминокислотные замены; и
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1) или последовательность, имеющую одну или две аминокислотные замены, аминокислотную последовательность SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) или последовательность, имеющую одну или две аминокислотные замены, и аминокислотная последовательность SEQ ID NO:48 определяющей комплементарность области 3 легкой цепи (VLCDR3) или последовательность, имеющую одну или две аминокислотные замены.
2. Молекула антитела или его связывающего фрагмента по п. 1, содержащая:
(i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:34 определяющей комплементарность области 1 тяжелой цепи (VHCDR1), аминокислотную последовательность SEQ ID NO:35 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) и аминокислотную последовательность SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3); и
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1), аминокислотную последовательность SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) и аминокислотную последовательность SEQ ID NO:39 определяющей комплементарность области 3 легкой цепи (VLCDR3); или
(ii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:34 определяющей комплементарность области 1 тяжелой цепи (VHCDR1), аминокислотную последовательность SEQ ID NO:44 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) и аминокислотную последовательность SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3); и
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1), аминокислотную последовательность SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) и аминокислотную последовательность SEQ ID NO:39 определяющей комплементарность области 3 легкой цепи (VLCDR3); или
(iii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:34 определяющей комплементарность области 1 тяжелой цепи (VHCDR1), аминокислотную последовательность SEQ ID NO:44 определяющей комплементарность области 2 тяжелой цепи (VHCDR2) и аминокислотную последовательность SEQ ID NO:36 определяющей комплементарность области 3 тяжелой цепи (VHCDR3); и
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:37 определяющей комплементарность области 1 легкой цепи (VLCDR1), аминокислотную последовательность SEQ ID NO:38 определяющей комплементарность области 2 легкой цепи (VLCDR2) и аминокислотная последовательность SEQ ID NO:48 определяющей комплементарность области 3 легкой цепи (VLCDR3).
3. Молекула антитела или его связывающего фрагмента по пп. 1 или 2, содержащая
(i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:40 или аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:40, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:41 или аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:41; или
(ii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:45 или аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:45, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:41 или аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:41; или
(iii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:49 или аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:49, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:50 или аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере примерно 85%, 90%, 95% или 99% с SEQ ID NO:50.
4. Молекула антитела или его связывающего фрагмента по любому из пп. 1-3, содержащая
(i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:40, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:41; или
(ii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:45, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:41; или
(iii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO:49, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO:50.
5. Молекула антитела или его связывающего фрагмента по любому из пп. 1-4,
имеющая одно или несколько (например 2, 3, 4, 5, 6, 7, 8 или 9) следующих свойств:
(i) связывается с вирусом BK серотип I VP1 с EC50 менее примерно 10 нМ, 1 нМ, 0,9 нМ, 0,8 нМ, 0,7 нМ, 0,6 нМ, 0,5 нМ, 0,4 нМ, 0,3 нМ, 0,2 нМ, 0,19 нМ, 0,18 нМ, 0,17 нМ, 0,16 нМ, 0,15 нМ, 0,14 нМ, 0,13 нМ, 0,12 нМ, 0,11 нМ, 0,10 нМ, 0,09 нМ, 0,08 нМ, 0,07 нМ, 0,06 нМ, 0,05 нМ, 0,04 нМ, 0,03 нМ или 0,02 нМ, например, когда молекулу антитела или его связывающего фрагмента тестируют как бивалентную молекулу с использованием ELISA, например, как описано в примере 2;
(ii) связывается с вирусом BK серотип II VP1 с EC50 менее примерно 10 нМ, 1 нМ, 0,9 нМ, 0,8 нМ, 0,7 нМ, 0,6 нМ, 0,5 нМ, 0,4 нМ, 0,3 нМ, 0,2 нМ, 0,19 нМ, 0,18 нМ, 0,17 нМ, 0,16 нМ, 0,15 нМ, 0,14 нМ, 0,13 нМ, 0,12 нМ, 0,11 нМ, 0,10 нМ, 0,09 нМ, 0,08 нМ, 0,07 нМ, 0,06 нМ, 0,05 нМ, 0,04 нМ, 0,03 нМ или 0,02 нМ, например, когда молекулу антитела или его связывающего фрагмента тестируют как бивалентную молекулу с использованием ELISA, например, как описано в примере 2;
(iii) связывается с вирусом BK серотип III VP1 с EC50 менее примерно 10 нМ, 1 нМ, 0,9 нМ, 0,8 нМ, 0,7 нМ, 0,6 нМ, 0,5 нМ, 0,4 нМ, 0,3 нМ, 0,2 нМ, 0,19 нМ, 0,18 нМ, 0,17 нМ, 0,16 нМ, 0,15 нМ, 0,14 нМ, 0,13 нМ, 0,12 нМ, 0,11 нМ, 0,10 нМ, 0,09 нМ, 0,08 нМ, 0,07 нМ, 0,06 нМ, 0,05 нМ, 0,04 нМ, 0,03 нМ или 0,02 нМ, например, когда молекулу антитела или его связывающего фрагмента тестируют как бивалентную молекулу с использованием ELISA, например, как описано в примере 2;
(iv) связывается с вирусом BK серотип IV VP1 с EC50 менее примерно 10 нМ, 1 нМ, 0,9 нМ, 0,8 нМ, 0,7 нМ, 0,6 нМ, 0,5 нМ, 0,4 нМ, 0,3 нМ, 0,2 нМ, 0,19 нМ, 0,18 нМ, 0,17 нМ, 0,16 нМ, 0,15 нМ, 0,14 нМ, 0,13 нМ, 0,12 нМ, 0,11 нМ, 0,10 нМ, 0,09 нМ, 0,08 нМ, 0,07 нМ, 0,06 нМ, 0,05 нМ, 0,04 нМ, 0,03 нМ или 0,02 нМ, например, когда молекулу антитела или его связывающего фрагмента тестируют как бивалентную молекулу с использованием ELISA, например, как описано в примере 2;
(v) не связывается с вирусом JC VP1;
(vi) нейтрализует вирус BK серотип I;
(vii) нейтрализует вирус BK серотип II;
(viii) нейтрализует вирус BK серотип III;
(ix) нейтрализует вирус BK серотип IV.
6. Молекула антитела или его связывающего фрагмента, которая конкурирует за связывание с вирусом BK серотип I VP1, вирусом BK серотип II VP1, вирусом BK серотип III VP1 и/или вирусом BK серотип IV VP1 с молекулой антитела или его связывающего фрагмента по любому из пп. 1-5.
7. Фармацевтическая композиция, содержащая молекулу антитела или его связывающего фрагмента по любому из пп. 1-6 и фармацевтически приемлемый носитель, вспомогательное средство или стабилизатор.
8. Молекула антитела или его связывающего фрагмента по любому из пп. 1-6 или фармацевтическая композиция по п. 7 для применения при лечении или профилактике инфекции вируса BK и/или связанного с вирусом BK нарушения.
9. Нуклеиновая кислота, кодирующая вариабельную область тяжелой и/или легкой цепи молекулы антитела или его связывающего фрагмента по любому из пп. 1-6.
10. Вектор экспрессии, содержащий нуклеиновую кислоту по п. 9.
11. Клетка-хозяин, содержащая нуклеиновую кислоту по п. 9 или вектор экспрессии по п. 10.
12. Способ получения молекулы антитела, где способ включает культивирование клетки-хозяина по п. 11 в условиях, подходящих для экспрессии гена.
13. Диагностическая композиция, содержащая молекулу антитела или его связывающего фрагмента по любому из пп. 1-6.
Примеры
Вводные комментарии
Аминокислотные последовательности конструкций белка VP1, использованные в следующих примерах, кратко изложены в таблице 1 ниже.
Таблица 1. Аминокислотные последовательности конструкций белка VP1
Сравнительные антитела
P8D11 (WO 2017/046676) клонировали, как описано для других антител. VH и VL P8D11, как описано в WO 2017/046676, слили с идентичными константными доменами IgG, как описано ниже. Аминокислотные последовательности для сравнительного антитела P8D11 изложены в таблице 2 ниже.
Отрицательный контроль 24C3 представляет собой антитело против столбнячного токсина, полученное у здоровых людей. Вариабельные фрагменты слили с идентичными константными доменами IgG, как описано ниже.
Таблица 2. Аминокислотные последовательности для сравнительного антитела P8D11 (WO 2017/046676)
Обнаружение Антител
Пример 1
В-клетки памяти периферической крови от здоровых людей доноров или реципиентов трансплантата почки использовали для получения экспрессионных библиотек репертуара антител путем клонирования вариабельных областей легкой и тяжелой цепи иммуноглобулина в экспрессионную кассету, обеспечивающую константную область тяжелой цепи иммуноглобулина человека в сочетании с трансмембранным доменом, полученным из CD8 человека, чтобы обеспечить дисплей антител в клетках млекопитающих. Скрининг библиотек антител проводили после трансдукции библиотеки в клетки HEK 293T методом антиген-специфической сортировки с использованием флуоресцентно меченных VP1-пентамеров вируса BK.
Эта сортировка давала клоны клеток HEK, экспрессирующих антитело, специфичное против вируса BK, которые далее размножали для увеличения производства антител для последующего анализа свойств антител, таких как дополнительные анализы связывания в ELISA или нейтрализация вируса BK. Нейтрализующую способность антител тестировали с использованием псевдовирусов BK (BK-PsV), несущих репортерную плазмиду, экспрессирующую люциферазу, и BKV дикого типа. Затем специфичные для вируса BK антитела с высокой аффинностью и способностью нейтрализовать вирус субклонировали в экспрессионные векторы для экспрессии растворимых антител и экспрессировали после временной трансфекции в клетках HEK 293F или CHO. Затем антитела очищали над белком G или белком А для характеристики в различных анализах. Аминокислотные последовательности, относящиеся к идентифицированному антителу 319C07, приведены в таблице 3 ниже. Кроме того, были получены варианты, и в таблице 3 ниже также приведены соответствующие аминокислотные последовательности. Аминокислотные последовательности, относящиеся к идентифицированному антителу 336F07, приведены в Таблице 4 ниже. Кроме того, были получены варианты, и в Таблице 4 ниже также приведены соответствующие аминокислотные последовательности.
Таблица 3. Аминокислотные последовательности антител 319C07 и 319C07-var1 против вируса BK
Таблица 4. Аминокислотные последовательности антител 336F07, 336F07-var1 и 336F07-var4 против вируса BK
Анализы
Пример 2 - Связывание с пентамером VP1 в ELISA
Материал и методы
Связывание антител против вируса BK с пентамерами BKV-VP1 анализировали с помощью ELISA. Вкратце, 96-луночные планшеты для анализа Costar®, планшеты с высоким связыванием с половинной площадью лунок (Corning Inc. #3690) покрывали по 30 мкл/лунку 1 мкг/мл пентамеров BKV-VP1 в течение ночи при 4°C. Затем планшет блокировали с помощью 5% сухого обезжиренного молока (Rapilait, Migros #7610200017598), разведенного в PBS. Антитела серийно разводили в PBS с 0,5% сухого обезжиренного молока и на 1,5 часа добавляли в планшеты, покрытые антигеном. Затем планшеты промывали PBS 0,05% Tween20 (AppliChem, A4974) и инкубировали с меченым ферментом вторичным антителом (конъюгированным с HRP козьим античеловеческим IgG, Jackson-Immuno #109-035-098), разбавленным 1:10000 в PBS с 0,5% сухого обезжиренного молока в течение 45 мин. Планшеты трижды промывали PBS, содержащим 0,05% Tween 20. Реакцию проводили, используя 30 мкл/лунку жидкого субстрата TMB (Sigma-Aldrich, #T0440), и останавливали 15 мкл/лунку H2SO4. Поглощение определяли при 450 нм (Tecan, CM INFINITE MONO 200). Данные подгоняли, и кажущиеся значения EC50 ELISA (EC50E) определяли с помощью трехпараметрического анализа в GraphPad Prism (GraphPad Software).
Результаты
Антитело 319C07 показало сильное и селективное связывание со всеми серотипами BKV-VP1 (фиг. 1, значения EC50E ниже). По сравнению со сравнительным антителом P8D11 антитело 319C07 показало более высокую аффинность к серотипам I, II и IV и показало сравнимую аффинность к серотипу III BKV-VP1.
Также антитело 336F07 показало сильное и селективное связывание со всеми серотипами BKV-VP1 (фиг. 1, значения EC50E ниже). По сравнению со сравнительным антителом P8D11 антитело 336F07 показало более высокую аффинность ко всем четырем серотипам.
Пример 3. Нейтрализация псевдовируса BK антителами против вируса BK
Материал и методы
Псевдовирус BK (BK-PsV), несущий репортерный ген NanoLuc, получали, как описано (Pastrana et al., J Virol, 2013 Sep; 87(18):10105-13). Было получено пять различных генотипов: BKV-Ia (BK-D; JF894228), BKV-Ib2 (PittVR2; DQ989796), BKV-II (Q85238; CAA79596), BKV-III (Q0PDA6; BAF03017) и BKV-IVc2 (A-66H; АВ369093). VP1 очищали на шариках агарозного геля, как описано (Buck et al., J Virol, 2008 Jun; 82(11):5190-7, и Buck et al., Curr Protoc Cell Biol, 2007 Dec; Chapter 26; 26.21). Инфекционный титр вируса определяли на клетках 293ТТ. Различные разведения BK-PsV тестировали в 96-луночном планшете с ингибитором и без него. Разведение, выбранное для дальнейших анализов, приводило к высокому сигналу люминесценции в неингибированных клетках.
20000 клеток (293ТТ) высевали в 96-луночный планшет с использованием среды DMEM, содержащей 9% FBS, HEPES и пенициллин/стрептавидин. После 5-часовой инкубации в каждую лунку добавляли антитела в различных концентрациях и фиксированное количество ВК-псевдовируса, и планшет инкубировали при 37°С, 5% СО2. Через 3 дня инкубации активность люциферазы в супернатанте измеряли с использованием реагента для анализа NanoGlo™ (Promega, #N1130).
40 мкл клеточной культуры или вируса-клетки-антитела-совместной культуры-супернатанта переносили в 96-луночные планшеты с белым дном, добавляли 40 мкл субстрата NanoGlo™ и инкубировали в течение 2 минут перед определением активности люциферазы с использованием люминесцентного ридера (BioTek Synergy). Данные наносили на кривую зависимости сигнала от концентрации антител. Значения IC50 определяли с помощью GraphPad Prism с использованием нелинейной регрессии (подбор кривой) и формулы «логарифм (ингибитор) против нормализованного ответа (переменный угловой коэффициент)» (программное обеспечение GraphPad).
Результаты
319C07 и вариант 319C07-var1 демонстрируют сильное ингибирование псевдовирусов BK всех серотипов. 319C07 значительно превосходит P8D11 (фиг. 2, значения IC50 ниже).
Также антитело 336F07 и варианты 336F07-var1 и 336F07-var4 демонстрируют сильное ингибирование BK-псевдовируса всех серотипов. 336F07 значительно превосходит P8D11 (фиг. 2, значения IC50 ниже).
Пример 4. Длительная нейтрализация вируса антителами против вируса BK
Материал и методы
Для обеспечения долговременной нейтрализации вируса антителами против вируса BK in vitro использовали повторяющиеся циклы совместного культивирования эпителиальных клеток первичных почечных канальцев человека (HPRTEC), штамма I вируса BK дикого типа (ATCC® VR-837™) и антител против вируса BK.
В начале исследования добавляли антитела против вируса BK в трех различных концентрациях, соответствующих их ЕС95; эффективность вирусного ингибирования EC50 и EC5 в отношении совместных культур клеток и вирусов в течение 1 недели. По истечении этого периода вирус брали из клеток и оставшегося супернатанта с помощью 3 циклов замораживания-оттаивания. Затем 10 мкл этого вирусного экстракта добавляли к свежепосеянным клеткам HRPTEC в присутствии антител в различных концентрациях. Через 2 недели после прививки снова количественно оценивали вирусную нагрузку, и получали экстракты вируса для использования в следующем цикле заражения. Эту процедуру повторяли 3 раза, в результате чего общее время совместного культивирования составило 8 недель.
Анализ проводили в трех повторениях в 96-луночных планшетах для культивирования клеток с плоским дном. Количественную оценку вирусной нагрузки в культуральном супернатанте проводили путем сбора 15 мкл среды, которую затем инактивировали нагреванием при 95°C в течение 10 минут и использовали для количественной ПЦР с праймерами 5'-GGATGGGCAGCCTATGTATG-3' (SEQ ID NO:53), и 5'-TCATATCTGGGTCCCCTGGA-3' (SEQ ID NO:54) и зондом TaqMan™ FAM-AGGGTGTTTGATGGCACAGA-TAMRA (SEQ ID NO:55). ПЦР проводили с использованием PerfeCTa qPCR ToughMix (Quantabio, #95140) при следующих условиях: 95°C в течение 8 мин и 40 циклов 95°C в течение 10 с и 60°C в течение 60 с.
Результаты
Антитело 319C07 демонстрирует более полную нейтрализацию вируса по сравнению с P8D11. Это становится наиболее очевидным при рассмотрении последнего цикла нейтрализации инфекции через 8 недель, когда при концентрациях, соответствующих EC95 и EC50, вирус больше не обнаруживается, тогда как P8D11 показывает измеримую вирусную нагрузку как при EC95, так и при EC50. (фиг. 3, P8D11 помечен на этом рисунке как «BM2»).
Также антитело 336F07 демонстрирует более полную нейтрализацию вируса по сравнению с P8D11. Это становится наиболее очевидным при взгляде на последний цикл нейтрализации инфекции через 8 недель (фиг. 3, на этом рисунке P8D11 помечен «BM2»).
Пример 5. Антитела против вируса BK связываются с конформационным эпитопом
Материал и методы
Чтобы определить, связываются ли антитела против вируса BK с конформационным эпитопом, проводили дот-блоты VP1 в нативном состоянии и в денатурированном состоянии. Пентамеры BKV-VP1 серотипов I, II, III и IV наносили на нитроцеллюлозную мембрану либо в нативном виде, либо после химической и термической денатурации с использованием буфера Tris, содержащего SDS и β-меркаптоэтанол, и нагревания при 85°С в течение 5 мин. Обе мембраны инкубировали с антителами против вируса BK, и их связывание выявляли с использованием конъюгированных с HRP вторичных антител, направленных против Fc человека. Детекцию проводили с использованием колориметрического субстрата (Sigma Fast DAB).
Результаты
Антитело 319C07 и антитело 336F07 демонстрируют селективное связывание с конформационным эпитопом (фиг. 4). Благодаря отсутствию окрашивания денатурированного антигена можно исключить связывание с линейным эпитопом. Коммерчески доступное контрольное антитело (Ab53977, Abcam, IgG кролика), о котором известно, что оно распознает линейный эпитоп, обнаруживало как денатурированный, так и неденатурированный VP1.
Пример 6. Связывание с мутациями пентамера BKV-VP1 и пентамера JCV-VP1 в ELISA
Материал и методы
Последовательность дикого типа VP1-серотип Ib использовали в качестве основы для введения мутаций в различные положения. Аналогичным образом использовали VP1 вируса JC. Связывание антител против вируса ВК с пентамерами VP1 дикого типа и вариантами анализировали с помощью ELISA. Вкратце, 96-луночные планшеты для анализа Costar®, планшеты с половиной площади лунок с высоким связыванием (Corning Inc. #3690) покрывали 30 мкл/лунку 1 мкг/мл вариантов пентамера BKV-VP1 в течение ночи при 4°C. Через 16 часов неспецифическое связывание блокировали с помощью 5% сухого обезжиренного молока (Rapilait, Migros #7610200017598), разведенного в PBS. Антитела последовательно разбавляли от 67 нМ до 0,02 нМ в PBS, содержащем 0,5% сухого обезжиренного молока, и инкубировали на планшетах, покрытых антигеном, в течение 1,5 часов. Затем планшеты трижды промывали PBS 0,05% Tween20 (AppliChem, A4974) и затем инкубировали со вторичным антителом (конъюгированным с HRP козьим античеловеческим IgG, Jackson-Immuno #109-035-098), разведенным 1:10000 в PBS с 0,5% сухого обезжиренного молока в течение 45 мин. Активность HRP связанных вторичных антител выявляли, используя 30 мкл/лунку жидкого субстрата TMB (Sigma-Aldrich, #T0440). Реакцию останавливали через 2,5 мин путем добавления 15 мкл/лунку 1М H2SO4. Поглощение определяли при 450 нм (Tecan, CM INFINITE MONO 200). Данные наносили на график, и значения EC50 определяли с помощью трехпараметрического анализа в GraphPad Prism (программное обеспечение GraphPad) и обозначали EC50ELISA (EC50E).
Результаты
Связывание с мутантными формами BKV VP1 по сравнению с VP1 дикого типа и с VP1 близкородственного вируса полиомы JC тестировали на антитело 319C07 по сравнению с антителом P8D11. Антитело 319C07 вообще не связывается с VP1 вируса JC, тогда как антитело P8D11 демонстрирует слабое, но значительное связывание. Если аминокислоты в положениях N62, D175 или S275 заменены на аланин, 319C07 демонстрирует слегка сниженную аффинность связывания. Замена аминокислоты K172 на аланин не снижает связывание. С другой стороны, P8D11 демонстрирует пониженное связывание с мутантом VP1-I-K172A, в то время как мутации N62A, D175A или S275A не влияют на связывание. По сравнению с антителом P8D11, 319C07 в данном случае демонстрирует четко различимую картину, предполагающую, что оно взаимодействует с другими аминокислотами VP1 по сравнению с P8D11 (фиг. 5).
Связывание с мутантными формами BKV VP1 по сравнению с VP1 дикого типа и с VP1 близкородственного вируса полиомы JC также тестировали на антитело 336F07 по сравнению с антителом P8D11. Антитело 336F07 вообще не связывается с VP1 вируса JC, тогда как антитело P8D11 демонстрирует слабое, но значительное связывание. Если аминокислоты в положении N62 или E73 мутированы, 336FC07 демонстрирует слегка сниженную аффинность связывания. Замена аминокислоты K172 на аланин не снижает связывание. С другой стороны, P8D11 демонстрирует пониженное связывание с мутантом VP1-I-K172A, в то время как мутации N62A или E73Q не влияют на связывание. По сравнению с антителом P8D11, 336F07 демонстрирует в данном случае четко различимую картину, предполагающую, что оно взаимодействует с другими аминокислотами VP1 по сравнению с P8D11 (фиг. 5).
Пример 7 - Ингибирование распространения вируса из инфицированных клеток HRPTEC
Материал и методы
Первичные эпителиальные клетки проксимальных канальцев почек человека (HRPTEC) инфицировали BKV (штамм 33-1, ATCC® 45024™). Через 5 дней клетки осторожно соскабливали клеточным скребком и тщательно промывали PBS для удаления всего бесклеточного вируса. Затем клетки добавляли в лунки, содержащие растущие HRPTEC и различные разведения нейтрализующих BKV антител. Через 8 дней после инокуляции клеток из каждой лунки удаляли по 10 мкл супернатанта, и определяли вирусную нагрузку с помощью количественной ПЦР с использованием праймеров 5'-GGATGGGCAGCCTATGTATG-3' (SEQ ID NO:53), 5'-TCATATCTGGGTCCCCTGGA-3' (SEQ ID NO:54) и зонда FAM-5'-AGGGTGTTTGATGGCACAGA-3'-TAMRA (SEQ ID NO:55), как описано (Martelli et al., Viruses, 2018 Aug 30;10(9):466).
Результаты
Антитело 319C07 демонстрирует примерно 100-кратное превосходство над P8D11 в ингибировании распространения BKV среди HRPTEC; также антитело 336F07 демонстрирует значительное превосходство над P8D11 в отношении ингибирования распространения BKV среди HRPTEC (фиг. 6, P8D11 помечен на этой фигуре как «BM2»).
Пример 8. Антителозависимая клеточная цитотоксичность (ADCC)
Материал и методы
В качестве клеток-мишеней использовали HPRTEC, посеянные в плоскодонные 96-луночные планшеты, либо инфицированные штаммом I вируса BK дикого типа (ATCC® VR-837™), либо оставленные неинфицированными. В качестве эффекторных клеток использовали сконструированные клетки Jurkat, компоненты ADCC Reporter Bioassay G7015 от Promega. В этом анализе, в качестве суррогата активности ADCC, сигнальный путь Fc-γRIIIa эффекторными клетками количественно оценивает посредством считывания люминесценции.
Антитела против BKV или контрольные антитела в серийных разведениях добавляли в культуру HPRTEC вместе с эффекторными клетками и инкубировали в течение 6 часов перед проявлением и измерением биолюминесценции, как описано производителем набора для анализа.
Результаты
319C7 и 336F07 показали сравнимую активность ADCC в отношении инфицированных HPRTEC, которая, в свою очередь, была сравнима с активностью P8D11. ADCC не наблюдалось на HPRTEC, которые не были инфицированы 319C7 и 336F07 или P8D11 (фиг. 7).
Пример 9 - Комплементзависимая токсичность
Материал и методы
В качестве клеток-мишеней использовали HPRTEC, посеянные в плоскодонные 96-луночные планшеты, либо инфицированные штаммом I вируса BK дикого типа (ATCC® VR-837™), либо оставленные неинфицированными. Клетки инкубировали с антителами против BKV при серийных разведениях, начиная со 100 мкг/мл и 20% сыворотки человека, в течение ночи, и количественно определяли жизнеспособность клеток, определяя соотношение живых клеток с использованием критерия FSC/SSC в цитометре.
Результаты
319C7 и 336F07 не проявляли активности CDC в концентрации 100 мкг/мл на инфицированных HPRTEC, и такое же наблюдение было сделано с антителом P8D11 и контрольным антителом ритуксимабом, направленным против нерелевантной мишени на HRPTEC (фиг. 8).
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> МЕМО ТЕРАПЬЮТИКС АГ
УНИВЕРЗИТЕТ ЦЮРИХ
УНИВЕРЗИТЕТ БЕРН
<120> Молекулы антител против вируса bk
<130> M11468WO
<160> 55
<170> PatentIn version 3.5
<210> 1
<211> 270
<212> PRT
<213> Полиомавирус человека 1
<400> 1
Gly Gly Val Glu Val Leu Glu Val Lys Thr Gly Val Asp Ala Ile Thr
1 5 10 15
Glu Val Glu Cys Phe Leu Asn Pro Glu Met Gly Asp Pro Asp Glu Asn
20 25 30
Leu Arg Gly Phe Ser Leu Lys Leu Ser Ala Glu Asn Asp Phe Ser Ser
35 40 45
Asp Ser Pro Glu Arg Lys Met Leu Pro Cys Tyr Ser Thr Ala Arg Ile
50 55 60
Pro Leu Pro Asn Leu Asn Glu Asp Leu Thr Cys Gly Asn Leu Leu Met
65 70 75 80
Trp Glu Ala Val Thr Val Gln Thr Glu Val Ile Gly Ile Thr Ser Met
85 90 95
Leu Asn Leu His Ala Gly Ser Gln Lys Val His Glu His Gly Gly Gly
100 105 110
Lys Pro Ile Gln Gly Ser Asn Phe His Phe Phe Ala Val Gly Gly Asp
115 120 125
Pro Leu Glu Met Gln Gly Val Leu Met Asn Tyr Arg Thr Lys Tyr Pro
130 135 140
Asp Gly Thr Ile Thr Pro Lys Asn Pro Thr Ala Gln Ser Gln Val Met
145 150 155 160
Asn Thr Asp His Lys Ala Tyr Leu Asp Lys Asn Asn Ala Tyr Pro Val
165 170 175
Glu Cys Trp Val Pro Asp Pro Ser Arg Asn Glu Asn Thr Arg Tyr Phe
180 185 190
Gly Thr Phe Thr Gly Gly Glu Asn Val Pro Pro Val Leu His Val Thr
195 200 205
Asn Thr Ala Thr Thr Val Leu Leu Asp Glu Gln Gly Val Gly Pro Leu
210 215 220
Cys Lys Ala Asp Ser Leu Tyr Val Ser Ala Ala Asp Ile Cys Gly Leu
225 230 235 240
Phe Thr Asn Ser Ser Gly Thr Gln Gln Trp Arg Gly Leu Ala Arg Tyr
245 250 255
Phe Lys Ile Arg Leu Arg Lys Arg Ser Val Lys Asn Pro Tyr
260 265 270
<210> 2
<211> 362
<212> PRT
<213> Искусственная последовательность
<220>
<223> Псевдовирус BK, VP1-Ia
<400> 2
Met Ala Pro Thr Lys Arg Lys Gly Glu Cys Pro Gly Ala Ala Pro Lys
1 5 10 15
Lys Pro Lys Glu Pro Val Gln Val Pro Lys Leu Leu Ile Lys Gly Gly
20 25 30
Val Glu Val Leu Glu Val Lys Thr Gly Val Asp Ala Ile Thr Glu Val
35 40 45
Glu Cys Phe Leu Asn Pro Glu Met Gly Asp Pro Asp Glu Asn Leu Arg
50 55 60
Gly Phe Ser Leu Lys Leu Ser Ala Glu Asn Asp Phe Ser Ser Asp Ser
65 70 75 80
Pro Glu Arg Lys Met Leu Pro Cys Tyr Ser Thr Ala Arg Ile Pro Leu
85 90 95
Pro Asn Leu Asn Glu Asp Leu Thr Cys Gly Asn Leu Leu Met Trp Glu
100 105 110
Ala Val Thr Val Gln Thr Glu Val Ile Gly Ile Thr Ser Met Leu Asn
115 120 125
Leu His Ala Gly Ser Gln Lys Val His Glu His Gly Gly Gly Lys Pro
130 135 140
Ile Gln Gly Ser Asn Phe His Phe Phe Ala Val Gly Gly Asp Pro Leu
145 150 155 160
Glu Met Gln Gly Val Leu Met Asn Tyr Arg Thr Lys Tyr Pro Asp Gly
165 170 175
Thr Ile Thr Pro Lys Asn Pro Thr Ala Gln Ser Gln Val Met Asn Thr
180 185 190
Asp His Lys Ala Tyr Leu Asp Lys Asn Asn Ala Tyr Pro Val Glu Cys
195 200 205
Trp Val Pro Asp Pro Ser Arg Asn Glu Asn Thr Arg Tyr Phe Gly Thr
210 215 220
Phe Thr Gly Gly Glu Asn Val Pro Pro Val Leu His Val Thr Asn Thr
225 230 235 240
Ala Thr Thr Val Leu Leu Asp Glu Gln Gly Val Gly Pro Leu Cys Lys
245 250 255
Ala Asp Ser Leu Tyr Val Ser Ala Ala Asp Ile Cys Gly Leu Phe Thr
260 265 270
Asn Ser Ser Gly Thr Gln Gln Trp Arg Gly Leu Ala Arg Tyr Phe Lys
275 280 285
Ile Arg Leu Arg Lys Arg Ser Val Lys Asn Pro Tyr Pro Ile Ser Phe
290 295 300
Leu Leu Ser Asp Leu Ile Asn Arg Arg Thr Gln Arg Val Asp Gly Gln
305 310 315 320
Pro Met Tyr Gly Met Glu Ser Gln Val Glu Glu Val Arg Val Phe Asp
325 330 335
Gly Thr Glu Arg Leu Pro Gly Asp Pro Asp Met Ile Arg Tyr Ile Asp
340 345 350
Lys Gln Gly Gln Leu Gln Thr Lys Met Leu
355 360
<210> 3
<211> 362
<212> PRT
<213> Искусственная последовательность
<220>
<223> Псевдовирус BK, VP1-Ib
<400> 3
Met Ala Pro Thr Lys Arg Lys Gly Glu Cys Pro Gly Ala Ala Pro Lys
1 5 10 15
Lys Pro Lys Glu Pro Val Gln Val Pro Lys Leu Leu Ile Lys Gly Gly
20 25 30
Val Glu Val Leu Glu Val Lys Thr Gly Leu Asp Ala Ile Thr Glu Val
35 40 45
Glu Cys Phe Leu Asn Pro Glu Met Gly Asp Pro Asp Glu Asn Leu Arg
50 55 60
Gly Phe Ser Leu Lys Leu Ser Ala Glu Asn Asp Phe Ser Ser Asp Ser
65 70 75 80
Pro Asp Arg Lys Met Leu Pro Cys Tyr Ser Thr Ala Arg Ile Pro Leu
85 90 95
Pro Asn Leu Asn Glu Asp Leu Thr Cys Gly Asn Leu Leu Met Trp Glu
100 105 110
Ala Val Thr Val Gln Thr Glu Val Ile Gly Ile Thr Ser Met Leu Asn
115 120 125
Leu His Ala Gly Ser Gln Lys Val His Glu His Gly Gly Gly Lys Pro
130 135 140
Ile Gln Gly Ser Asn Phe His Phe Phe Ala Val Gly Gly Asp Pro Leu
145 150 155 160
Glu Met Gln Gly Val Leu Met Asn Tyr Arg Thr Lys Tyr Pro Glu Gly
165 170 175
Thr Ile Thr Pro Lys Asn Pro Thr Ala Gln Ser Gln Val Met Asn Thr
180 185 190
Asp His Lys Ala Tyr Leu Asp Lys Asn Asn Ala Tyr Pro Val Glu Cys
195 200 205
Trp Ile Pro Asp Pro Ser Arg Asn Glu Asn Thr Arg Tyr Phe Gly Thr
210 215 220
Phe Thr Gly Gly Glu Asn Val Pro Pro Val Leu His Val Thr Asn Thr
225 230 235 240
Ala Thr Thr Val Leu Leu Asp Glu Gln Gly Val Gly Pro Leu Cys Lys
245 250 255
Ala Asp Ser Leu Tyr Val Ser Ala Ala Asp Ile Cys Gly Leu Phe Thr
260 265 270
Asn Ser Ser Gly Thr Gln Gln Trp Arg Gly Leu Ala Arg Tyr Phe Lys
275 280 285
Ile Arg Leu Arg Lys Arg Ser Val Lys Asn Pro Tyr Pro Ile Ser Phe
290 295 300
Leu Leu Ser Asp Leu Ile Asn Arg Arg Thr Gln Arg Val Asp Gly Gln
305 310 315 320
Pro Met Tyr Gly Met Glu Ser Gln Val Glu Glu Val Arg Val Phe Asp
325 330 335
Gly Thr Glu Arg Leu Pro Gly Asp Pro Asp Met Ile Arg Tyr Ile Asp
340 345 350
Lys Gln Gly Gln Leu Gln Thr Lys Met Leu
355 360
<210> 4
<211> 270
<212> PRT
<213> Полиомавирус человека 1
<400> 4
Gly Gly Val Glu Val Leu Glu Val Lys Thr Gly Val Asp Ala Ile Thr
1 5 10 15
Glu Val Glu Cys Phe Leu Asn Pro Glu Met Gly Asp Pro Asp Asp Asn
20 25 30
Leu Arg Gly Tyr Ser Leu Lys Leu Thr Ala Glu Asn Ala Phe Asp Ser
35 40 45
Asp Ser Pro Asp Lys Lys Met Leu Pro Cys Tyr Ser Thr Ala Arg Ile
50 55 60
Pro Leu Pro Asn Leu Asn Glu Asp Leu Thr Cys Gly Asn Leu Leu Met
65 70 75 80
Trp Glu Ala Val Thr Val Lys Thr Glu Val Ile Gly Ile Thr Ser Met
85 90 95
Leu Asn Leu His Ala Gly Ser Gln Lys Val His Glu Asn Gly Gly Gly
100 105 110
Lys Pro Val Gln Gly Ser Asn Phe His Phe Phe Ala Val Gly Gly Asp
115 120 125
Pro Leu Glu Met Gln Gly Val Leu Met Asn Tyr Arg Thr Lys Tyr Pro
130 135 140
Gln Gly Thr Ile Thr Pro Lys Asn Pro Thr Ala Gln Ser Gln Val Met
145 150 155 160
Asn Thr Asp His Lys Ala Tyr Leu Asp Lys Asn Asn Ala Tyr Pro Val
165 170 175
Glu Cys Trp Ile Pro Asp Pro Ser Arg Asn Glu Asn Thr Arg Tyr Phe
180 185 190
Gly Thr Tyr Thr Gly Gly Glu Asn Val Pro Pro Val Leu His Val Thr
195 200 205
Asn Thr Ala Thr Thr Val Leu Leu Asp Glu Gln Gly Val Gly Pro Leu
210 215 220
Cys Lys Ala Asp Ser Leu Tyr Val Ser Ala Ala Asp Ile Cys Gly Leu
225 230 235 240
Phe Thr Asn Ser Ser Gly Thr Gln Gln Trp Arg Gly Leu Ala Arg Tyr
245 250 255
Phe Lys Ile Arg Leu Arg Lys Arg Ser Val Lys Asn Pro Tyr
260 265 270
<210> 5
<211> 362
<212> PRT
<213> Искусственная последовательность
<220>
<223> Псевдовирус BK, VP1-II
<400> 5
Met Ala Pro Thr Lys Arg Lys Gly Glu Cys Pro Gly Ala Ala Pro Lys
1 5 10 15
Lys Pro Lys Glu Pro Val Gln Val Pro Lys Leu Leu Ile Lys Gly Gly
20 25 30
Val Glu Val Leu Glu Val Lys Thr Gly Val Asp Ala Ile Thr Glu Val
35 40 45
Glu Cys Phe Leu Asn Pro Glu Met Gly Asp Pro Asp Asp Asn Leu Arg
50 55 60
Gly Tyr Ser Leu Lys Leu Thr Ala Glu Asn Ala Phe Asp Ser Asp Ser
65 70 75 80
Pro Asp Lys Lys Met Leu Pro Cys Tyr Ser Thr Ala Arg Ile Pro Leu
85 90 95
Pro Asn Leu Asn Glu Asp Leu Thr Cys Gly Asn Leu Leu Met Trp Glu
100 105 110
Ala Val Thr Val Lys Thr Glu Val Ile Gly Ile Thr Ser Met Leu Asn
115 120 125
Leu His Ala Gly Ser Gln Lys Val His Glu Asn Gly Gly Gly Lys Pro
130 135 140
Val Gln Gly Ser Asn Phe His Phe Phe Ala Val Gly Gly Asp Pro Leu
145 150 155 160
Glu Met Gln Gly Val Leu Met Asn Tyr Arg Thr Lys Tyr Pro Gln Gly
165 170 175
Thr Ile Thr Pro Lys Asn Pro Thr Ala Gln Ser Gln Val Met Asn Thr
180 185 190
Asp His Lys Ala Tyr Leu Asp Lys Asn Asn Ala Tyr Pro Val Glu Cys
195 200 205
Trp Ile Pro Asp Pro Ser Arg Asn Glu Asn Thr Arg Tyr Phe Gly Thr
210 215 220
Tyr Thr Gly Gly Glu Asn Val Pro Pro Val Leu His Val Thr Asn Thr
225 230 235 240
Ala Thr Thr Val Leu Leu Asp Glu Gln Gly Val Gly Pro Leu Cys Lys
245 250 255
Ala Asp Ser Leu Tyr Val Ser Ala Ala Asp Ile Cys Gly Leu Phe Thr
260 265 270
Asn Ser Ser Gly Thr Gln Gln Trp Arg Gly Leu Ala Arg Tyr Phe Lys
275 280 285
Ile Arg Leu Arg Lys Arg Ser Val Lys Asn Pro Tyr Pro Ile Ser Phe
290 295 300
Leu Leu Ser Asp Leu Ile Asn Arg Arg Thr Gln Arg Val Asp Gly Gln
305 310 315 320
Pro Met Tyr Gly Met Glu Ser Gln Val Glu Glu Val Arg Val Phe Asp
325 330 335
Gly Thr Glu Gln Leu Pro Gly Asp Pro Asp Met Ile Arg Tyr Ile Asp
340 345 350
Arg Gln Gly Gln Leu Gln Thr Lys Met Val
355 360
<210> 6
<211> 362
<212> PRT
<213> Полиомавирус человека 1
<400> 6
Met Ala Pro Thr Lys Arg Lys Gly Glu Cys Pro Gly Ala Ala Pro Lys
1 5 10 15
Lys Pro Lys Glu Pro Val Gln Val Pro Lys Leu Leu Ile Lys Gly Gly
20 25 30
Val Glu Val Leu Glu Val Lys Thr Gly Val Asp Ala Ile Thr Glu Val
35 40 45
Glu Cys Phe Leu Asn Pro Glu Met Gly Asp Pro Asp Asp Asn Leu Arg
50 55 60
Gly Tyr Ser Gln His Leu Ser Ala Glu Asn Ala Phe Glu Ser Asp Ser
65 70 75 80
Pro Asp Arg Lys Met Leu Pro Cys Tyr Ser Thr Ala Arg Ile Pro Leu
85 90 95
Pro Asn Leu Asn Glu Asp Leu Thr Cys Gly Asn Leu Leu Met Trp Glu
100 105 110
Ala Val Thr Val Lys Thr Glu Val Ile Gly Ile Thr Ser Met Leu Asn
115 120 125
Leu His Ala Gly Ser Gln Lys Val His Glu Asn Gly Gly Gly Lys Pro
130 135 140
Val Gln Gly Ser Asn Phe His Phe Phe Ala Val Gly Gly Asp Pro Leu
145 150 155 160
Glu Met Gln Gly Val Leu Met Asn Tyr Arg Thr Lys Tyr Pro Gln Gly
165 170 175
Thr Ile Thr Pro Lys Asn Pro Thr Ala Gln Ser Gln Val Met Asn Thr
180 185 190
Asp His Lys Ala Tyr Leu Asp Lys Asn Asn Ala Tyr Pro Val Glu Cys
195 200 205
Trp Ile Pro Asp Pro Ser Arg Asn Glu Asn Thr Arg Tyr Phe Gly Thr
210 215 220
Tyr Thr Gly Gly Glu Asn Val Pro Pro Val Leu His Val Thr Asn Thr
225 230 235 240
Ala Thr Thr Val Leu Leu Asp Glu Gln Gly Val Gly Pro Leu Cys Lys
245 250 255
Ala Asp Ser Leu Tyr Val Ser Ala Ala Asp Ile Cys Gly Leu Phe Thr
260 265 270
Asn Ser Ser Gly Thr Gln Gln Trp Arg Gly Leu Ala Arg Tyr Phe Lys
275 280 285
Ile Arg Leu Arg Lys Arg Ser Val Lys Asn Pro Tyr Pro Ile Ser Phe
290 295 300
Leu Leu Ser Asp Leu Ile Asn Arg Arg Thr Gln Lys Val Asp Gly Gln
305 310 315 320
Pro Met Tyr Gly Met Glu Ser Gln Val Glu Glu Val Arg Val Phe Asp
325 330 335
Gly Thr Glu Gln Leu Pro Gly Asp Pro Asp Met Ile Arg Tyr Ile Asp
340 345 350
Arg Gln Gly Gln Leu Gln Thr Lys Met Val
355 360
<210> 7
<211> 362
<212> PRT
<213> Искусственная последовательность
<220>
<223> Псевдовирус BK, VP1-III
<400> 7
Met Ala Pro Thr Lys Arg Lys Gly Glu Cys Pro Gly Ala Ala Pro Lys
1 5 10 15
Lys Pro Lys Glu Pro Val Gln Val Pro Lys Leu Leu Ile Lys Gly Gly
20 25 30
Val Glu Val Leu Glu Val Lys Thr Gly Val Asp Ala Ile Thr Glu Val
35 40 45
Glu Cys Phe Leu Asn Pro Glu Met Gly Asp Pro Asp Asp Asn Leu Arg
50 55 60
Gly Tyr Ser Gln His Leu Ser Ala Glu Asn Ala Phe Glu Ser Asp Ser
65 70 75 80
Pro Asp Arg Lys Met Leu Pro Cys Tyr Ser Thr Ala Arg Ile Pro Leu
85 90 95
Pro Asn Leu Asn Glu Asp Leu Thr Cys Gly Asn Leu Leu Met Trp Glu
100 105 110
Ala Val Thr Val Lys Thr Glu Val Ile Gly Ile Thr Ser Met Leu Asn
115 120 125
Leu His Ala Gly Ser Gln Lys Val His Glu Asn Gly Gly Gly Lys Pro
130 135 140
Val Gln Gly Ser Asn Phe His Phe Phe Ala Val Gly Gly Asp Pro Leu
145 150 155 160
Glu Met Gln Gly Val Leu Met Asn Tyr Arg Thr Lys Tyr Pro Gln Gly
165 170 175
Thr Ile Thr Pro Lys Asn Pro Thr Ala Gln Ser Gln Val Met Asn Thr
180 185 190
Asp His Lys Ala Tyr Leu Asp Lys Asn Asn Ala Tyr Pro Val Glu Cys
195 200 205
Trp Ile Pro Asp Pro Ser Arg Asn Glu Asn Thr Arg Tyr Phe Gly Thr
210 215 220
Tyr Thr Gly Gly Glu Asn Val Pro Pro Val Leu His Val Thr Asn Thr
225 230 235 240
Ala Thr Thr Val Leu Leu Asp Glu Gln Gly Val Gly Pro Leu Cys Lys
245 250 255
Ala Asp Ser Leu Tyr Val Ser Ala Ala Asp Ile Cys Gly Leu Phe Thr
260 265 270
Asn Ser Ser Gly Thr Gln Gln Trp Arg Gly Leu Ala Arg Tyr Phe Lys
275 280 285
Ile Arg Leu Arg Lys Arg Ser Val Lys Asn Pro Tyr Pro Ile Ser Phe
290 295 300
Leu Leu Ser Asp Leu Ile Asn Arg Arg Thr Gln Arg Val Asp Gly Gln
305 310 315 320
Pro Met Tyr Gly Met Glu Ser Gln Val Glu Glu Val Arg Val Phe Asp
325 330 335
Gly Thr Glu Gln Leu Pro Gly Asp Pro Asp Met Ile Arg Tyr Ile Asp
340 345 350
Arg Gln Gly Gln Leu Gln Thr Lys Met Val
355 360
<210> 8
<211> 270
<212> PRT
<213> Полиомавирус человека 1
<400> 8
Gly Gly Val Glu Val Leu Glu Val Lys Thr Gly Val Asp Ala Ile Thr
1 5 10 15
Glu Val Glu Cys Phe Leu Asn Pro Glu Met Gly Asp Pro Asp Asn Asp
20 25 30
Leu Arg Gly Tyr Ser Leu Arg Leu Thr Ala Glu Thr Ala Phe Asp Ser
35 40 45
Asp Ser Pro Asp Arg Lys Met Leu Pro Cys Tyr Ser Thr Ala Arg Ile
50 55 60
Pro Leu Pro Asn Leu Asn Glu Asp Leu Thr Cys Gly Asn Leu Leu Met
65 70 75 80
Trp Glu Ala Val Thr Val Lys Thr Glu Val Ile Gly Ile Thr Ser Met
85 90 95
Leu Asn Leu His Ala Gly Ser Gln Lys Val His Glu Asn Gly Gly Gly
100 105 110
Lys Pro Ile Gln Gly Ser Asn Phe His Phe Phe Ala Val Gly Gly Asp
115 120 125
Pro Leu Glu Met Gln Gly Val Leu Met Asn Tyr Arg Thr Lys Tyr Pro
130 135 140
Glu Gly Thr Val Thr Pro Lys Asn Pro Thr Ala Gln Ser Gln Val Met
145 150 155 160
Asn Thr Asp His Lys Ala Tyr Leu Asp Lys Asn Asn Ala Tyr Pro Val
165 170 175
Glu Cys Trp Ile Pro Asp Pro Ser Arg Asn Glu Asn Thr Arg Tyr Phe
180 185 190
Gly Thr Tyr Thr Gly Gly Glu Asn Val Pro Pro Val Leu His Val Thr
195 200 205
Asn Thr Ala Thr Thr Val Leu Leu Asp Glu Gln Gly Val Gly Pro Leu
210 215 220
Cys Lys Ala Asp Ser Leu Tyr Val Ser Ala Ala Asp Ile Cys Gly Leu
225 230 235 240
Phe Thr Asn Ser Ser Gly Thr Gln Gln Trp Arg Gly Leu Pro Arg Tyr
245 250 255
Phe Lys Ile Arg Met Arg Lys Arg Ser Val Lys Asn Pro Tyr
260 265 270
<210> 9
<211> 362
<212> PRT
<213> Искусственная последовательность
<220>
<223> Псевдовирус BK, VP1-IVc
<400> 9
Met Ala Pro Thr Lys Arg Lys Gly Glu Cys Pro Gly Ala Ala Pro Lys
1 5 10 15
Lys Pro Lys Glu Pro Val Gln Val Pro Lys Leu Leu Ile Lys Gly Gly
20 25 30
Val Glu Val Leu Glu Val Lys Thr Gly Val Asp Ala Ile Thr Glu Val
35 40 45
Glu Cys Phe Leu Asn Pro Glu Met Gly Asp Pro Asp Asn Asp Leu Arg
50 55 60
Gly Tyr Ser Leu Arg Leu Thr Ala Glu Thr Ala Phe Asp Ser Asp Ser
65 70 75 80
Pro Asp Arg Lys Met Leu Pro Cys Tyr Ser Thr Ala Arg Ile Pro Leu
85 90 95
Pro Asn Leu Asn Glu Asp Leu Thr Cys Gly Asn Leu Leu Met Trp Glu
100 105 110
Ala Val Thr Val Lys Thr Glu Val Ile Gly Ile Thr Ser Met Leu Asn
115 120 125
Leu His Ala Gly Ser Gln Lys Val His Glu Asn Gly Gly Gly Lys Pro
130 135 140
Ile Gln Gly Ser Asn Phe His Phe Phe Ala Val Gly Gly Asp Pro Leu
145 150 155 160
Glu Met Gln Gly Val Leu Met Asn Tyr Arg Thr Lys Tyr Pro Glu Gly
165 170 175
Thr Val Thr Pro Lys Asn Pro Thr Ala Gln Ser Gln Val Met Asn Thr
180 185 190
Asp His Lys Ala Tyr Leu Asp Lys Asn Asn Ala Tyr Pro Val Glu Cys
195 200 205
Trp Ile Pro Asp Pro Ser Lys Asn Glu Asn Thr Arg Tyr Phe Gly Thr
210 215 220
Tyr Thr Gly Gly Glu Asn Val Pro Pro Val Leu His Val Thr Asn Thr
225 230 235 240
Ala Thr Thr Val Leu Leu Asp Glu Gln Gly Val Gly Pro Leu Cys Lys
245 250 255
Ala Asp Ser Leu Tyr Val Ser Ala Ala Asp Ile Cys Gly Leu Phe Thr
260 265 270
Asn Ser Ser Gly Thr Gln Gln Trp Arg Gly Leu Pro Arg Tyr Phe Lys
275 280 285
Ile Arg Leu Arg Lys Arg Ser Val Lys Asn Pro Tyr Pro Ile Ser Phe
290 295 300
Leu Leu Ser Asp Leu Ile Asn Arg Arg Thr Gln Arg Val Asp Gly Gln
305 310 315 320
Pro Met Tyr Gly Met Glu Ser Gln Val Glu Glu Val Arg Val Phe Asp
325 330 335
Gly Thr Glu Gln Leu Pro Gly Asp Pro Asp Met Ile Arg Tyr Ile Asp
340 345 350
Arg Gln Gly Gln Leu Gln Thr Lys Met Val
355 360
<210> 10
<211> 270
<212> PRT
<213> полиомавирус JC
<400> 10
Gly Gly Val Glu Val Leu Glu Val Lys Thr Gly Val Asp Ser Ile Thr
1 5 10 15
Glu Val Glu Cys Phe Leu Thr Pro Glu Met Gly Asp Pro Asp Glu His
20 25 30
Leu Arg Gly Phe Ser Lys Ser Ile Ser Ile Ser Asp Thr Phe Glu Ser
35 40 45
Asp Ser Pro Asn Arg Asp Met Leu Pro Cys Tyr Ser Val Ala Arg Ile
50 55 60
Pro Leu Pro Asn Leu Asn Glu Asp Leu Thr Cys Gly Asn Ile Leu Met
65 70 75 80
Trp Glu Ala Val Thr Leu Lys Thr Glu Val Ile Gly Val Thr Ser Leu
85 90 95
Met Asn Val His Ser Asn Gly Gln Ala Thr His Asp Asn Gly Ala Gly
100 105 110
Lys Pro Val Gln Gly Thr Ser Phe His Phe Phe Ser Val Gly Gly Glu
115 120 125
Ala Leu Glu Leu Gln Gly Val Leu Phe Asn Tyr Arg Thr Lys Tyr Pro
130 135 140
Asp Gly Thr Ile Phe Pro Lys Asn Ala Thr Val Gln Ser Gln Val Met
145 150 155 160
Asn Thr Glu His Lys Ala Tyr Leu Asp Lys Asn Lys Ala Tyr Pro Val
165 170 175
Glu Cys Trp Val Pro Asp Pro Thr Arg Asn Glu Asn Thr Arg Tyr Phe
180 185 190
Gly Thr Leu Thr Gly Gly Glu Asn Val Pro Pro Val Leu His Ile Thr
195 200 205
Asn Thr Ala Thr Thr Val Leu Leu Asp Glu Phe Gly Val Gly Pro Leu
210 215 220
Cys Lys Gly Asp Asn Leu Tyr Leu Ser Ala Val Asp Val Cys Gly Met
225 230 235 240
Phe Thr Asn Arg Ser Gly Ser Gln Gln Trp Arg Gly Leu Ser Arg Tyr
245 250 255
Phe Lys Val Gln Leu Arg Lys Arg Arg Val Lys Asn Pro Tyr
260 265 270
<210> 11
<211> 5
<212> PRT
<213> Искусственная последовательность
<220>
<223> определяющая комплементарность область 1 тяжелой цепи
<400> 11
Asn Tyr Trp Met Thr
1 5
<210> 12
<211> 17
<212> PRT
<213> Искусственная последовательность
<220>
<223> определяющая комплементарность область 2 тяжелой цепи
<400> 12
Asn Ile Lys Lys Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val Arg
1 5 10 15
Gly
<210> 13
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<223> определяющая комплементарность область 3 тяжелой цепи
<400> 13
Val Arg Ser Gly Arg Tyr Phe Ala Leu Asp Asp
1 5 10
<210> 14
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<223> определяющая комплементарность область 1 легкой цепи
<400> 14
Gly Gly Asp Asn Ile Gly Ser Arg Pro Val His
1 5 10
<210> 15
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> определяющая комплементарность область 2 легкой цепи
<400> 15
Asp Asp Ser Asn Arg Pro Ser
1 5
<210> 16
<211> 10
<212> PRT
<213> Искусственная последовательность
<220>
<223> определяющая комплементарность область 3 легкой цепи
<400> 16
Gln Val Trp Ser Ser Ser Thr Asp His Pro
1 5 10
<210> 17
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> вариабельная область тяжелой цепи
<400> 17
Gln Val Gln Leu Val Glu Ser Gly Gly Thr Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Asn Tyr
20 25 30
Trp Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Lys Lys Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val
50 55 60
Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Phe Cys
85 90 95
Ala Thr Val Arg Ser Gly Arg Tyr Phe Ala Leu Asp Asp Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 18
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> вариабельная область легкой цепи
<400> 18
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Val Ala Pro Gly Lys
1 5 10 15
Thr Ala Arg Ile Thr Cys Gly Gly Asp Asn Ile Gly Ser Arg Pro Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Ile Leu Val Val Tyr
35 40 45
Asp Asp Ser Asn Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Arg Val Glu Ala Gly
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp Ser Ser Ser Thr Asp His
85 90 95
Pro Phe Gly Gly Gly Thr Lys Val Thr Val Leu
100 105
<210> 19
<211> 450
<212> PRT
<213> Искусственная последовательность
<220>
<223> полноразмерная тяжелая цепь
<400> 19
Gln Val Gln Leu Val Glu Ser Gly Gly Thr Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Asn Tyr
20 25 30
Trp Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Lys Lys Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val
50 55 60
Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Phe Cys
85 90 95
Ala Thr Val Arg Ser Gly Arg Tyr Phe Ala Leu Asp Asp Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 20
<211> 213
<212> PRT
<213> Искусственная последовательность
<220>
<223> полноразмерная легкая цепь
<400> 20
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Val Ala Pro Gly Lys
1 5 10 15
Thr Ala Arg Ile Thr Cys Gly Gly Asp Asn Ile Gly Ser Arg Pro Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Ile Leu Val Val Tyr
35 40 45
Asp Asp Ser Asn Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Arg Val Glu Ala Gly
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Val Trp Ser Ser Ser Thr Asp His
85 90 95
Pro Phe Gly Gly Gly Thr Lys Val Thr Val Leu Gly Gln Pro Lys Ala
100 105 110
Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu Glu Leu Gln Ala
115 120 125
Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe Tyr Pro Gly Ala
130 135 140
Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro Val Lys Ala Gly Val
145 150 155 160
Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys Tyr Ala Ala Ser
165 170 175
Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser His Arg Ser Tyr
180 185 190
Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu Lys Thr Val Ala
195 200 205
Pro Thr Glu Cys Ser
210
<210> 21
<211> 5
<212> PRT
<213> Искусственная последовательность
<220>
<223> определяющая комплементарность область 1 тяжелой цепи
<400> 21
Ala Tyr Tyr Trp Thr
1 5
<210> 22
<211> 16
<212> PRT
<213> Искусственная последовательность
<220>
<223> определяющая комплементарность область 2 тяжелой цепи
<400> 22
Glu Ile Asn His Arg Gly Tyr Thr Asn Tyr Asn Pro Ser Leu Arg Gly
1 5 10 15
<210> 23
<211> 13
<212> PRT
<213> Искусственная последовательность
<220>
<223> определяющая комплементарность область 3 тяжелой цепи
<400> 23
Leu Arg Ser Thr Ser Gly Trp His Asp Tyr Phe Asp Tyr
1 5 10
<210> 24
<211> 12
<212> PRT
<213> Искусственная последовательность
<220>
<223> определяющая комплементарность область 1 легкой цепи
<400> 24
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 25
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> определяющая комплементарность область 2 легкой цепи
<400> 25
Gly Ala Ser Ser Arg Ala Thr
1 5
<210> 26
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<223> определяющая комплементарность область 3 легкой цепи
<400> 26
Leu Gln Tyr Gly Ser Ser Pro Leu Thr
1 5
<210> 27
<211> 121
<212> PRT
<213> Искусственная последовательность
<220>
<223> вариабельная область тяжелой цепи
<400> 27
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Arg Gly Ser Phe Ser Ala Tyr
20 25 30
Tyr Trp Thr Trp Phe Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asn His Arg Gly Tyr Thr Asn Tyr Asn Pro Ser Leu Arg
50 55 60
Gly Arg Val Ser Ile Ser Val Asp Thr Ser Lys Lys Gln Phe Ser Leu
65 70 75 80
Lys Leu Arg Ser Val Asn Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Thr Leu Arg Ser Thr Ser Gly Trp His Asp Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 28
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> вариабельная область легкой цепи
<400> 28
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Thr Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Val Val Tyr Phe Cys Leu Gln Tyr Gly Ser Ser Pro
85 90 95
Leu Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 29
<211> 451
<212> PRT
<213> Искусственная последовательность
<220>
<223> полноразмерная тяжелая цепь
<400> 29
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Arg Gly Ser Phe Ser Ala Tyr
20 25 30
Tyr Trp Thr Trp Phe Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asn His Arg Gly Tyr Thr Asn Tyr Asn Pro Ser Leu Arg
50 55 60
Gly Arg Val Ser Ile Ser Val Asp Thr Ser Lys Lys Gln Phe Ser Leu
65 70 75 80
Lys Leu Arg Ser Val Asn Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Thr Leu Arg Ser Thr Ser Gly Trp His Asp Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 30
<211> 215
<212> PRT
<213> Искусственная последовательность
<220>
<223> полноразмерная легкая цепь
<400> 30
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Thr Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Val Val Tyr Phe Cys Leu Gln Tyr Gly Ser Ser Pro
85 90 95
Leu Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 31
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> вариабельная область легкой цепи
<400> 31
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Phe Cys Leu Gln Tyr Gly Ser Ser Pro
85 90 95
Leu Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 32
<211> 451
<212> PRT
<213> Искусственная последовательность
<220>
<223> полноразмерная тяжелая цепь
<400> 32
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Tyr Arg Gly Ser Phe Ser Ala Tyr
20 25 30
Tyr Trp Thr Trp Phe Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asn His Arg Gly Tyr Thr Asn Tyr Asn Pro Ser Leu Arg
50 55 60
Gly Arg Val Ser Ile Ser Val Asp Thr Ser Lys Lys Gln Phe Ser Leu
65 70 75 80
Lys Leu Arg Ser Val Asn Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Thr Leu Arg Ser Thr Ser Gly Trp His Asp Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 33
<211> 215
<212> PRT
<213> Искусственная последовательность
<220>
<223> полноразмерная легкая цепь
<400> 33
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Phe Cys Leu Gln Tyr Gly Ser Ser Pro
85 90 95
Leu Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 34
<211> 5
<212> PRT
<213> Искусственная последовательность
<220>
<223> определяющая комплементарность область 1 тяжелой цепи
<400> 34
Leu Tyr Ala Met Asn
1 5
<210> 35
<211> 17
<212> PRT
<213> Искусственная последовательность
<220>
<223> определяющая комплементарность область 2 тяжелой цепи
<400> 35
Leu Ile Ser Gly Ser Gly Thr Ala Thr Tyr Tyr Ala Asp Ser Val Thr
1 5 10 15
Gly
<210> 36
<211> 15
<212> PRT
<213> Искусственная последовательность
<220>
<223> определяющая комплементарность область 3 тяжелой цепи
<400> 36
Thr Tyr Pro Thr Trp Gly Gly Val Val Ile Gly Ala Ile Asp Val
1 5 10 15
<210> 37
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<223> определяющая комплементарность область 1 легкой цепи
<400> 37
Arg Ala Ser Gln Ser Ile Gln Arg Trp Leu Ala
1 5 10
<210> 38
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> определяющая комплементарность область 2 легкой цепи
<400> 38
Asp Ala Ser Thr Leu Glu Ser
1 5
<210> 39
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<223> определяющая комплементарность область 3 легкой цепи
<400> 39
Gln Gln Tyr Asn Gly His Ala Ser Thr
1 5
<210> 40
<211> 124
<212> PRT
<213> Искусственная последовательность
<220>
<223> вариабельная область тяжелой цепи
<400> 40
Glu Glu Pro Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Leu Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Leu Ile Ser Gly Ser Gly Thr Ala Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Thr Gly Arg Phe Ser Ile Ser Arg Asp Asn Tyr Lys Asn Arg Val Tyr
65 70 75 80
Leu Gln Met Asp Ser Leu Arg Ala Asp Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Lys Thr Tyr Pro Thr Trp Gly Gly Val Val Ile Gly Ala Ile Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 41
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> вариабельная область легкой цепи
<400> 41
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Gln Arg Trp
20 25 30
Leu Ala Trp His Gln Gln Lys Pro Gly Arg Ala Pro Lys Val Leu Ile
35 40 45
His Asp Ala Ser Thr Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Gly His Ala Ser
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 42
<211> 454
<212> PRT
<213> Искусственная последовательность
<220>
<223> полноразмерная тяжелая цепь
<400> 42
Glu Glu Pro Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Leu Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Leu Ile Ser Gly Ser Gly Thr Ala Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Thr Gly Arg Phe Ser Ile Ser Arg Asp Asn Tyr Lys Asn Arg Val Tyr
65 70 75 80
Leu Gln Met Asp Ser Leu Arg Ala Asp Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Lys Thr Tyr Pro Thr Trp Gly Gly Val Val Ile Gly Ala Ile Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys
115 120 125
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
130 135 140
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
145 150 155 160
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
165 170 175
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
180 185 190
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
195 200 205
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
210 215 220
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
325 330 335
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly Lys
450
<210> 43
<211> 214
<212> PRT
<213> Искусственная последовательность
<220>
<223> полноразмерная легкая цепь
<400> 43
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Gln Arg Trp
20 25 30
Leu Ala Trp His Gln Gln Lys Pro Gly Arg Ala Pro Lys Val Leu Ile
35 40 45
His Asp Ala Ser Thr Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Gly His Ala Ser
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 44
<211> 17
<212> PRT
<213> Искусственная последовательность
<220>
<223> определяющая комплементарность область 2 тяжелой цепи
<400> 44
Leu Ile Ser Gly Ser Gly Thr Ala Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 45
<211> 124
<212> PRT
<213> Искусственная последовательность
<220>
<223> вариабельная область тяжелой цепи
<400> 45
Glu Glu Pro Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Leu Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Leu Ile Ser Gly Ser Gly Thr Ala Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Ser Ile Ser Arg Asp Asn Ser Lys Asn Arg Val Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Asp Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Lys Thr Tyr Pro Thr Trp Gly Gly Val Val Ile Gly Ala Ile Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 46
<211> 454
<212> PRT
<213> Искусственная последовательность
<220>
<223> полноразмерная тяжелая цепь
<400> 46
Glu Glu Pro Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Leu Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Leu Ile Ser Gly Ser Gly Thr Ala Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Ser Ile Ser Arg Asp Asn Ser Lys Asn Arg Val Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Asp Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Lys Thr Tyr Pro Thr Trp Gly Gly Val Val Ile Gly Ala Ile Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys
115 120 125
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
130 135 140
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
145 150 155 160
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
165 170 175
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
180 185 190
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
195 200 205
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
210 215 220
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
325 330 335
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly Lys
450
<210> 47
<211> 214
<212> PRT
<213> Искусственная последовательность
<220>
<223> полноразмерная легкая цепь
<400> 47
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Gln Arg Trp
20 25 30
Leu Ala Trp His Gln Gln Lys Pro Gly Arg Ala Pro Lys Val Leu Ile
35 40 45
His Asp Ala Ser Thr Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Gly His Ala Ser
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 48
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<223> определяющая комплементарность область 3 легкой цепи
<400> 48
Gln Gln Tyr Ser Gly His Ala Ser Thr
1 5
<210> 49
<211> 124
<212> PRT
<213> Искусственная последовательность
<220>
<223> вариабельная область тяжелой цепи
<400> 49
Glu Glu Pro Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Leu Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Leu Ile Ser Gly Ser Gly Thr Ala Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Arg Val Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Thr Tyr Pro Thr Trp Gly Gly Val Val Ile Gly Ala Ile Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 50
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> вариабельная область легкой цепи
<400> 50
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Gln Arg Trp
20 25 30
Leu Ala Trp His Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
His Asp Ala Ser Thr Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Ser Gly His Ala Ser
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 51
<211> 454
<212> PRT
<213> Искусственная последовательность
<220>
<223> полноразмерная тяжелая цепь
<400> 51
Glu Glu Pro Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Leu Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Leu Ile Ser Gly Ser Gly Thr Ala Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Arg Val Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ala Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Thr Tyr Pro Thr Trp Gly Gly Val Val Ile Gly Ala Ile Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys
115 120 125
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
130 135 140
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
145 150 155 160
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
165 170 175
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
180 185 190
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
195 200 205
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
210 215 220
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
325 330 335
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly Lys
450
<210> 52
<211> 214
<212> PRT
<213> Искусственная последовательность
<220>
<223> полноразмерная легкая цепь
<400> 52
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Gln Arg Trp
20 25 30
Leu Ala Trp His Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
His Asp Ala Ser Thr Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Ser Gly His Ala Ser
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 53
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> праймер для кПЦР
<400> 53
ggatgggcag cctatgtatg 20
<210> 54
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> праймер для кПЦР
<400> 54
tcatatctgg gtcccctgga 20
<210> 55
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> зонд для кПЦР
<400> 55
agggtgtttg atggcacaga 20
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| МОЛЕКУЛЫ АНТИ-SIGLEC-9 АНТИТЕЛА | 2020 |
|
RU2833330C1 |
| ИММУНОДОМИНАНТНЫЕ БЕЛКИ И ФРАГМЕНТЫ ПРИ РАССЕЯННОМ СКЛЕРОЗЕ | 2019 |
|
RU2828590C2 |
| УЛУЧШЕННЫЕ АНТИ-FLT3 АНТИГЕНСВЯЗЫВАЮЩИЕ БЕЛКИ | 2019 |
|
RU2830982C2 |
| СПОСОБ СНИЖЕНИЯ ОШИБОЧНОГО ВКЛЮЧЕНИЯ НЕКАНОНИЧЕСКИХ АМИНОКИСЛОТ С РАЗВЕТВЛЕННОЙ ЦЕПЬЮ | 2019 |
|
RU2816654C2 |
| БИСПЕЦИФИЧЕСКОЕ АНТИТЕЛО ПРОТИВ ВИРУСА БЕШЕНСТВА И ЕГО ПРИМЕНЕНИЕ | 2019 |
|
RU2764740C1 |
| АНТИТЕЛО К ЦИТОМЕГАЛОВИРУСУ ЧЕЛОВЕКА И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2817217C1 |
| НОВЫЙ КОРОНАВИРУС РЫБ | 2020 |
|
RU2813731C2 |
| ТРИСПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ ДЛЯ ЛЕЧЕНИЯ ВИРУСНОЙ ИНФЕКЦИИ ГЕПАТИТА В И СВЯЗАННЫХ СОСТОЯНИЙ | 2016 |
|
RU2733496C2 |
| КОНЪЮГАТЫ ЛЕКАРСТВЕННЫХ СРЕДСТВ, СОДЕРЖАЩИЕ АНТИТЕЛА ПРОТИВ КЛАУДИНА 18.2 | 2016 |
|
RU2841168C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ С ИСПОЛЬЗОВАНИЕМ АНТИТЕЛ ПРОТИВ КЛАУДИНА 18.2 ДЛЯ ЛЕЧЕНИЯ РАКА | 2014 |
|
RU2792932C2 |
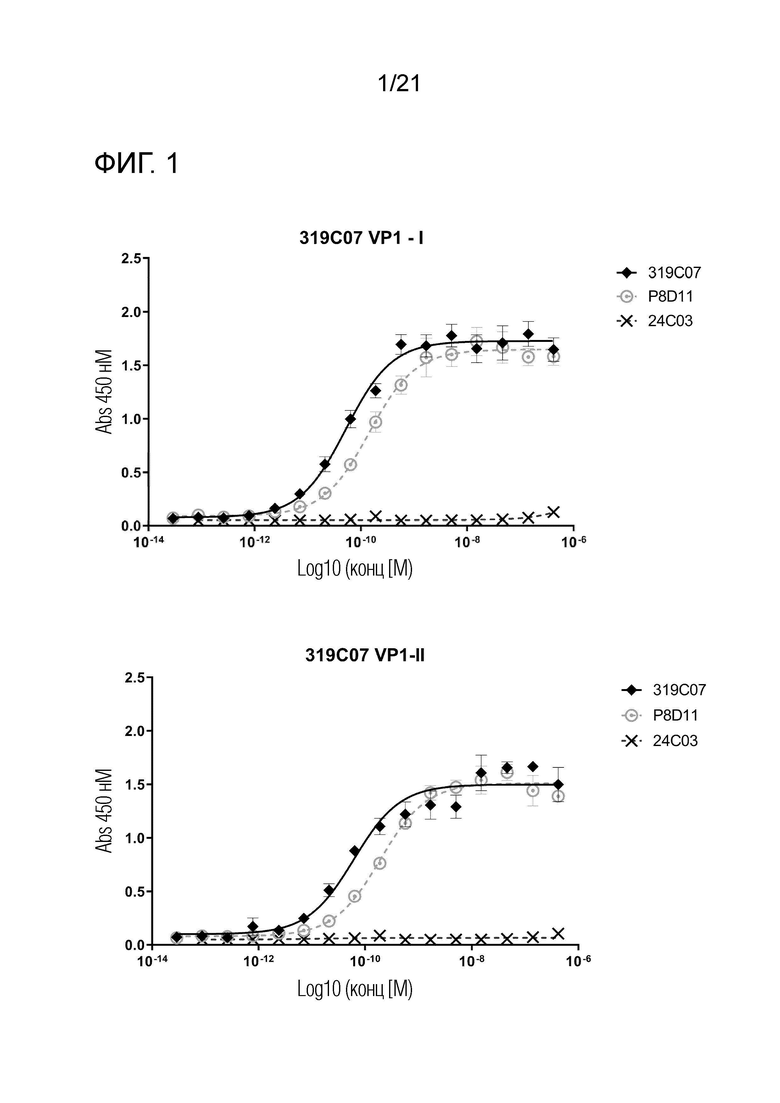
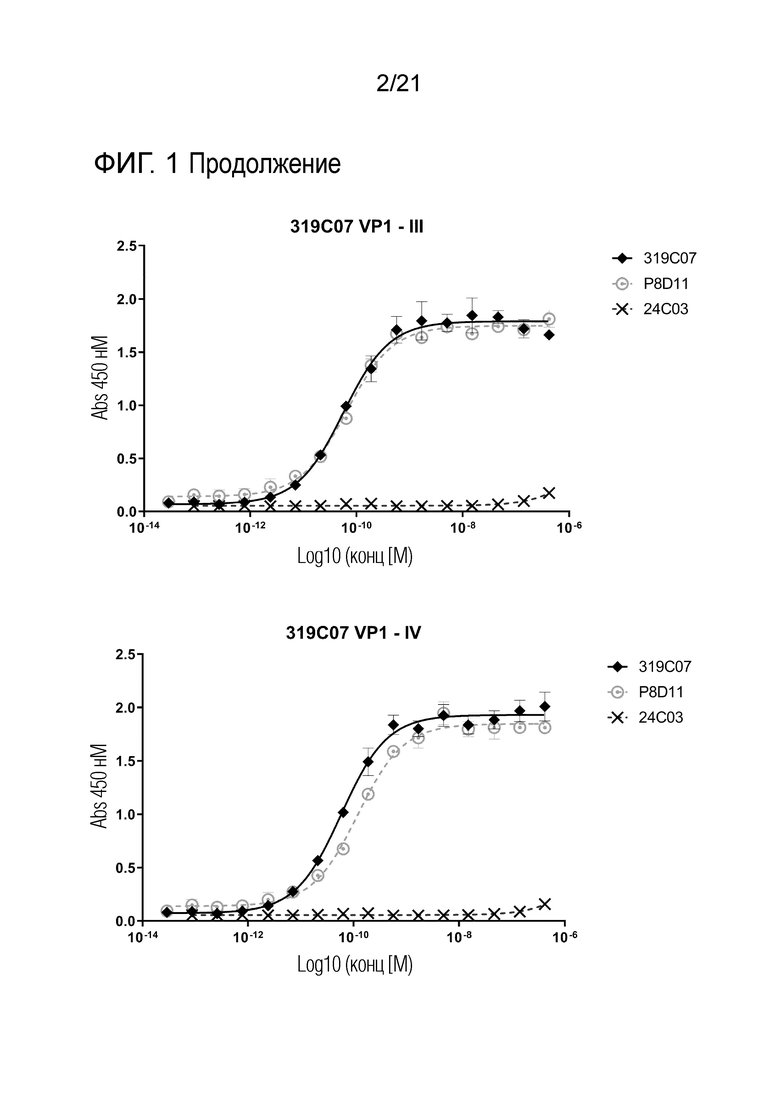
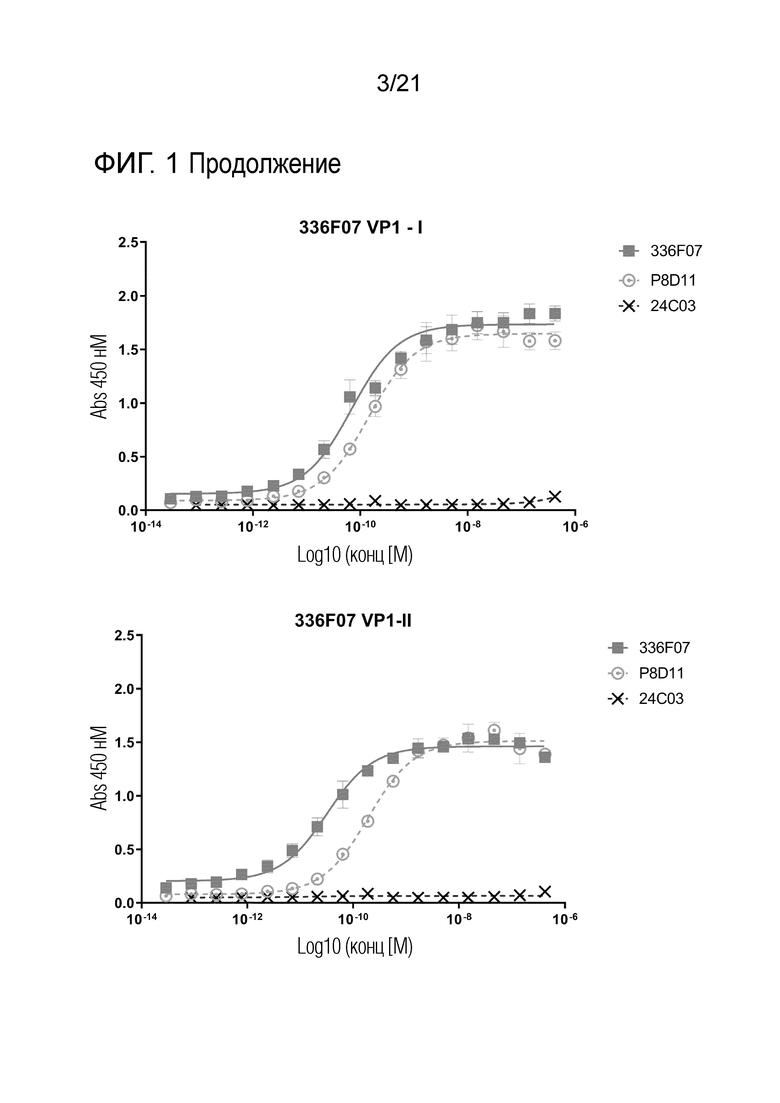
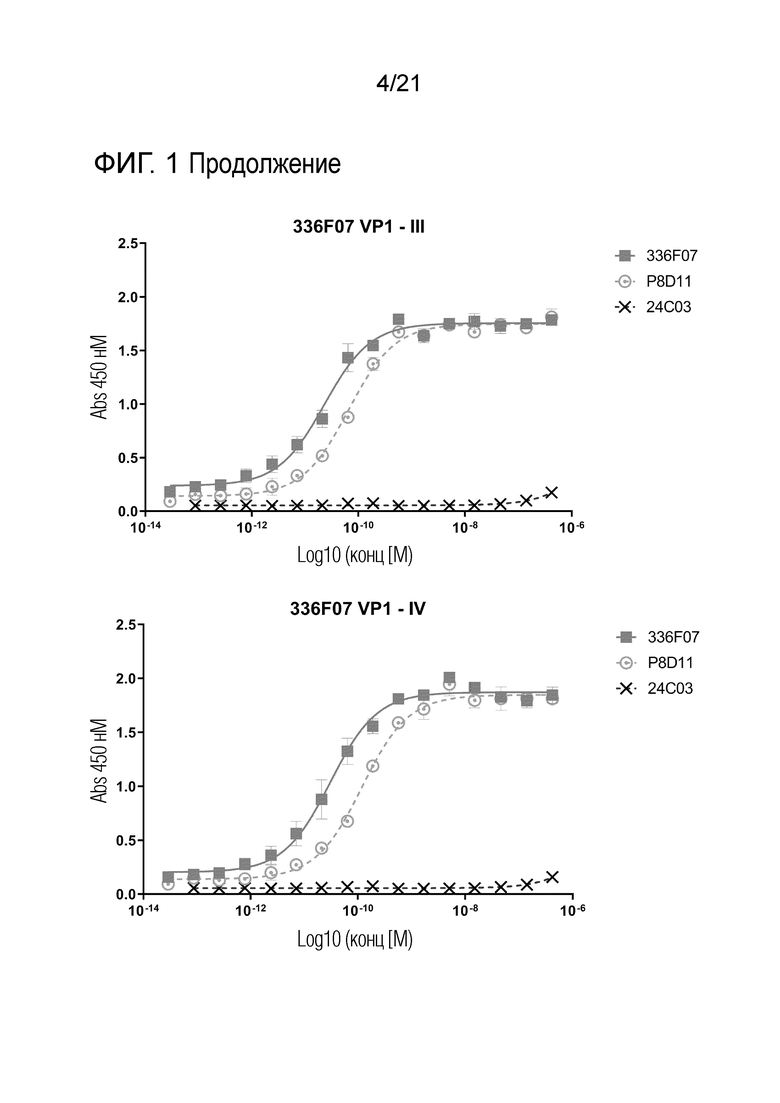
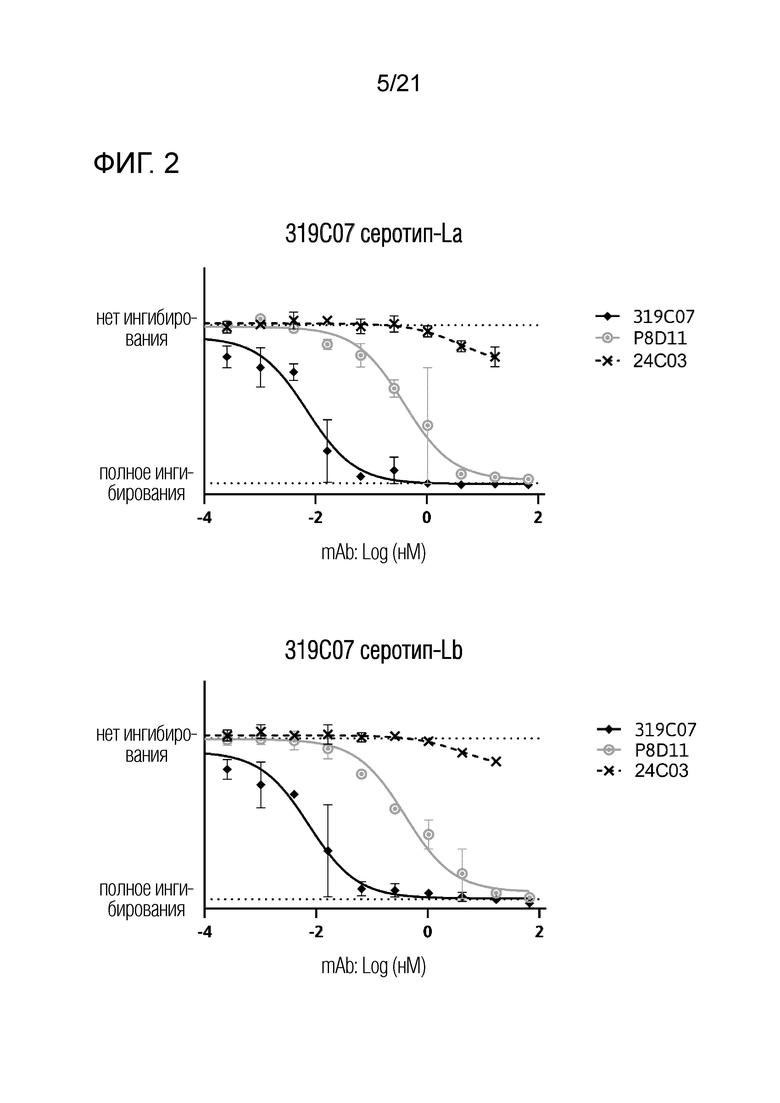
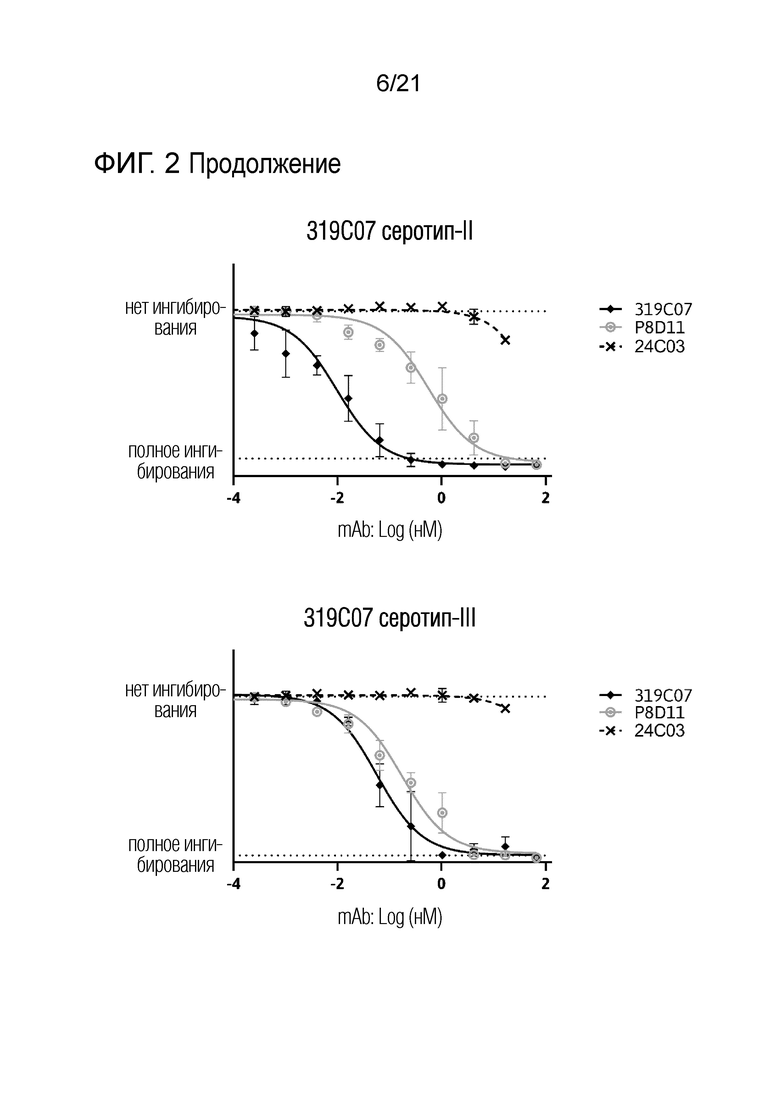
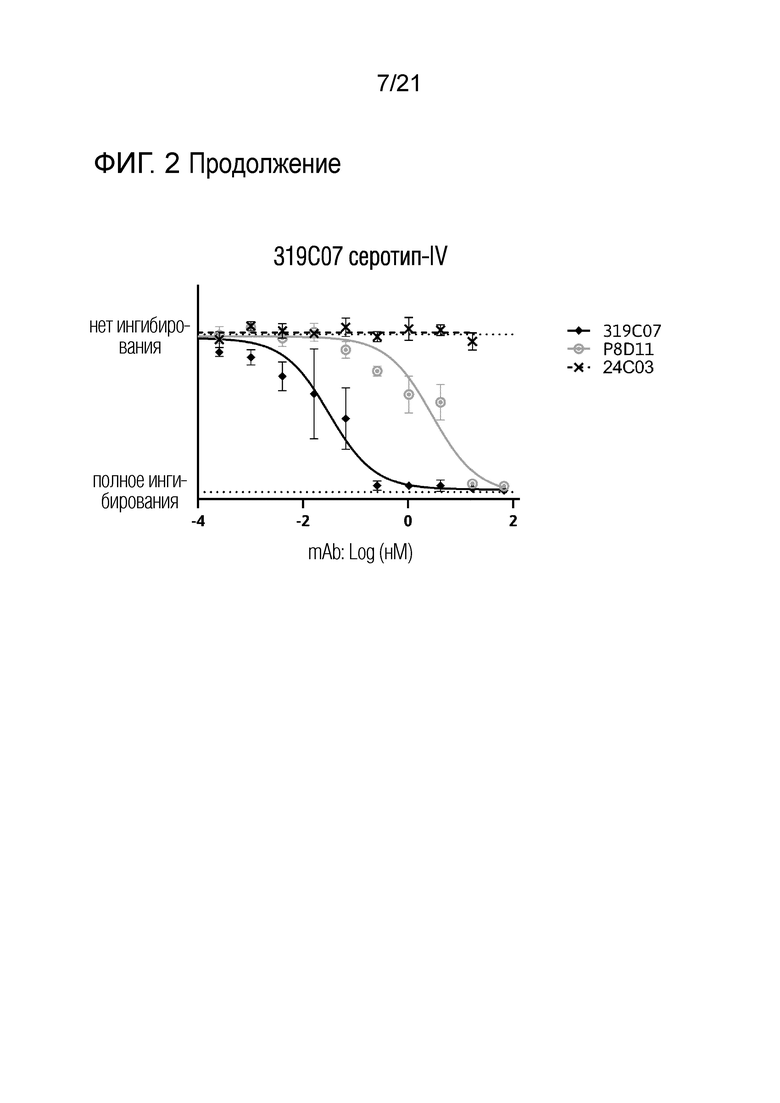
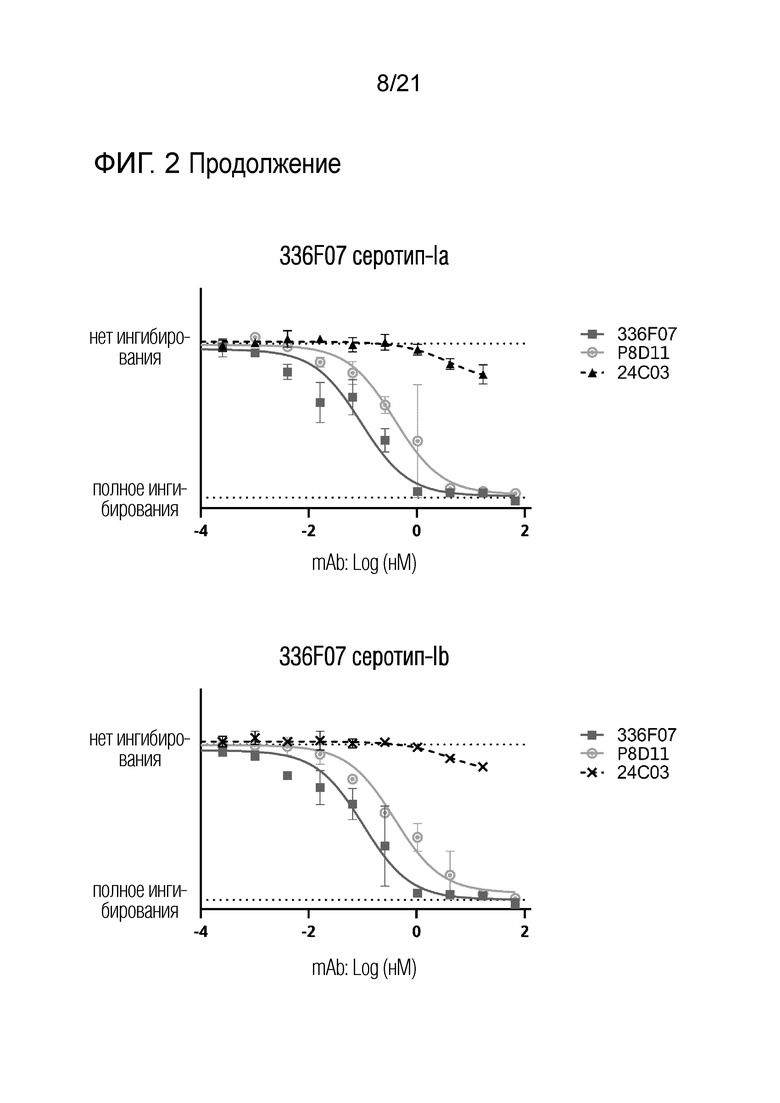
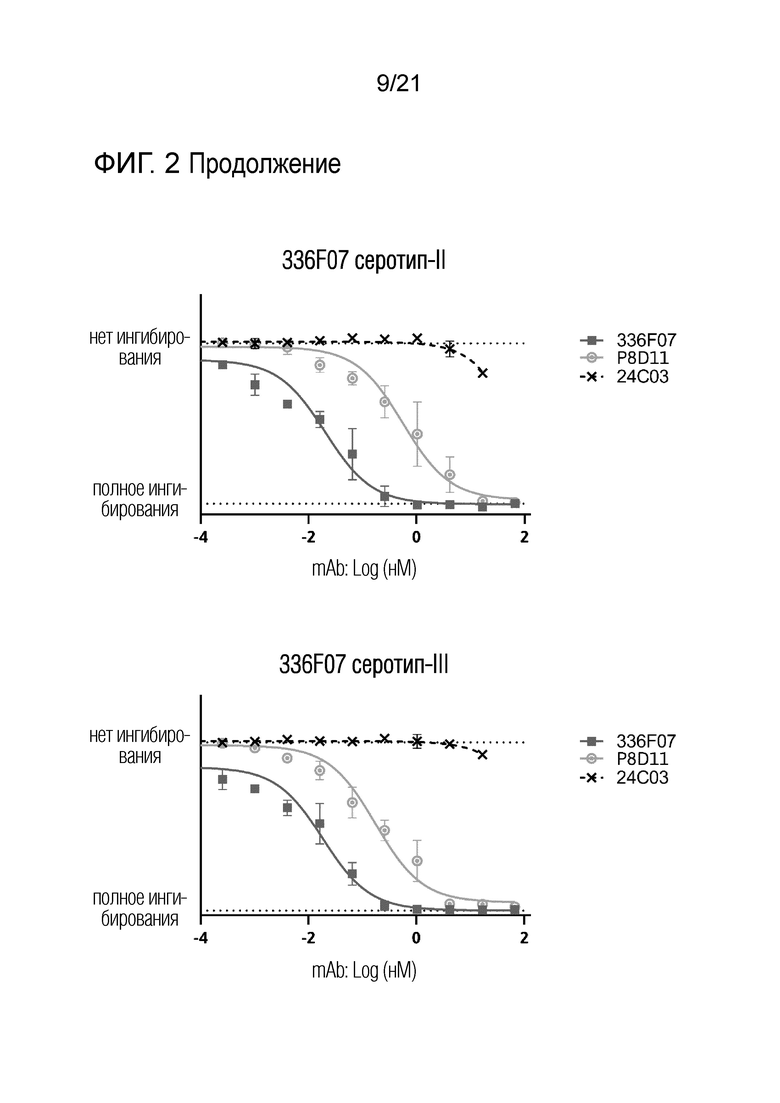
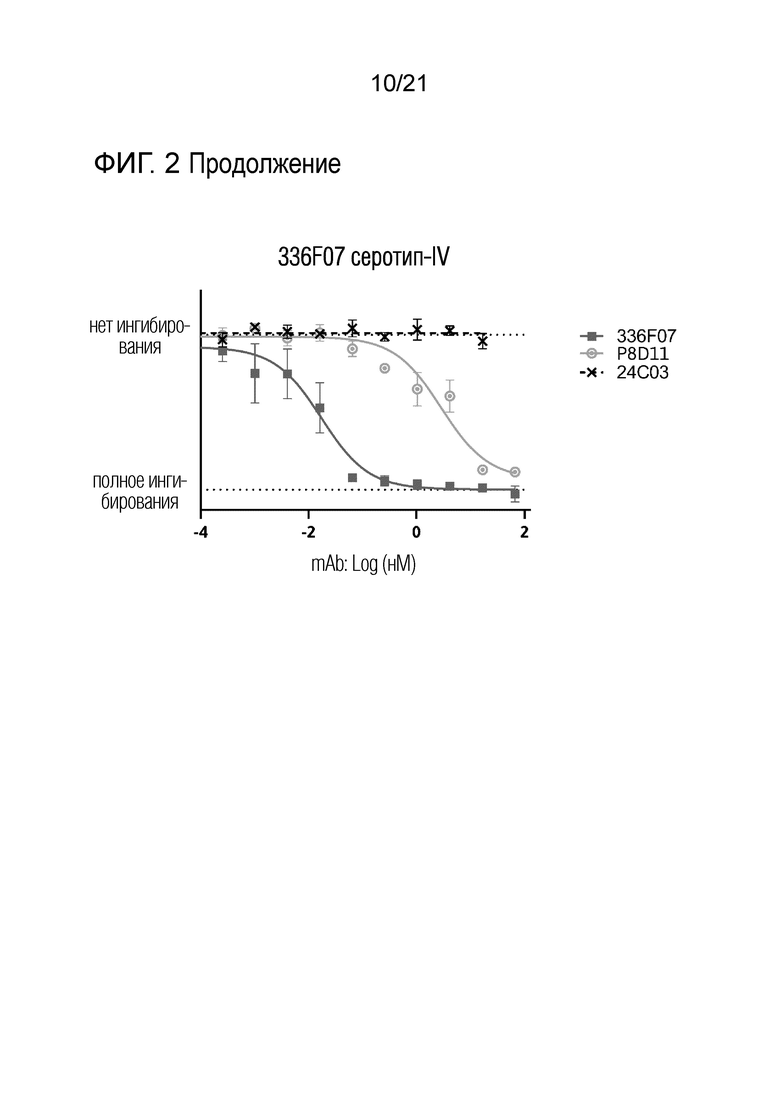
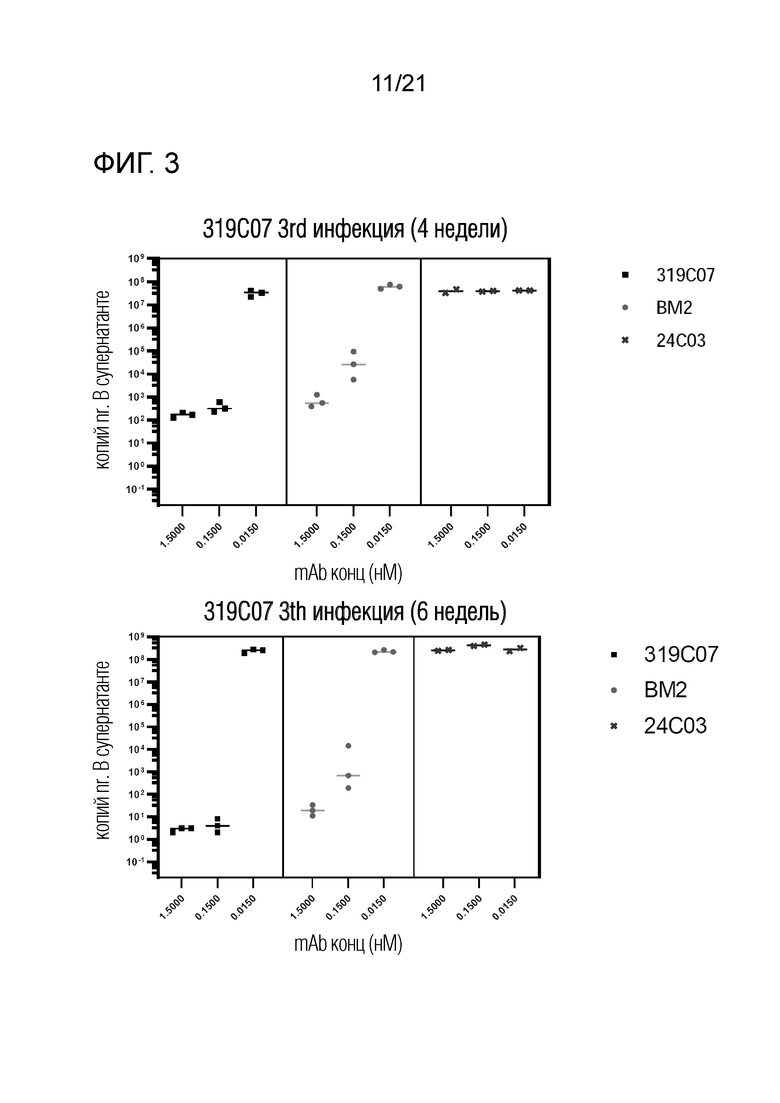
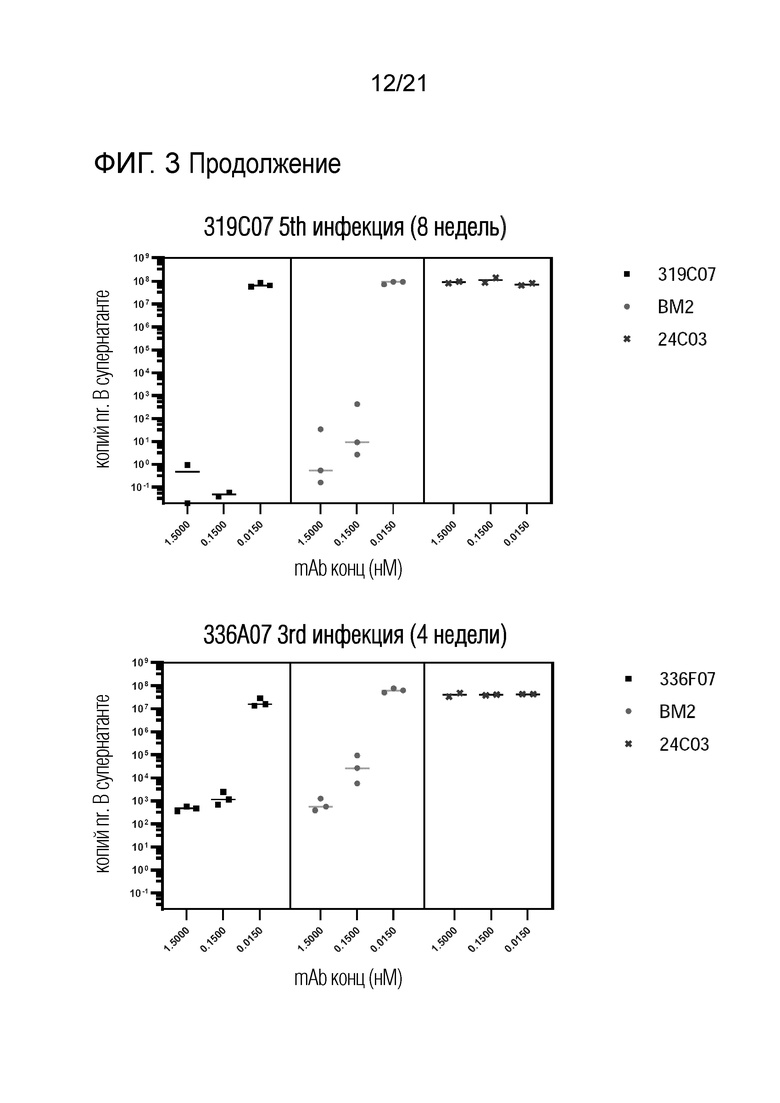
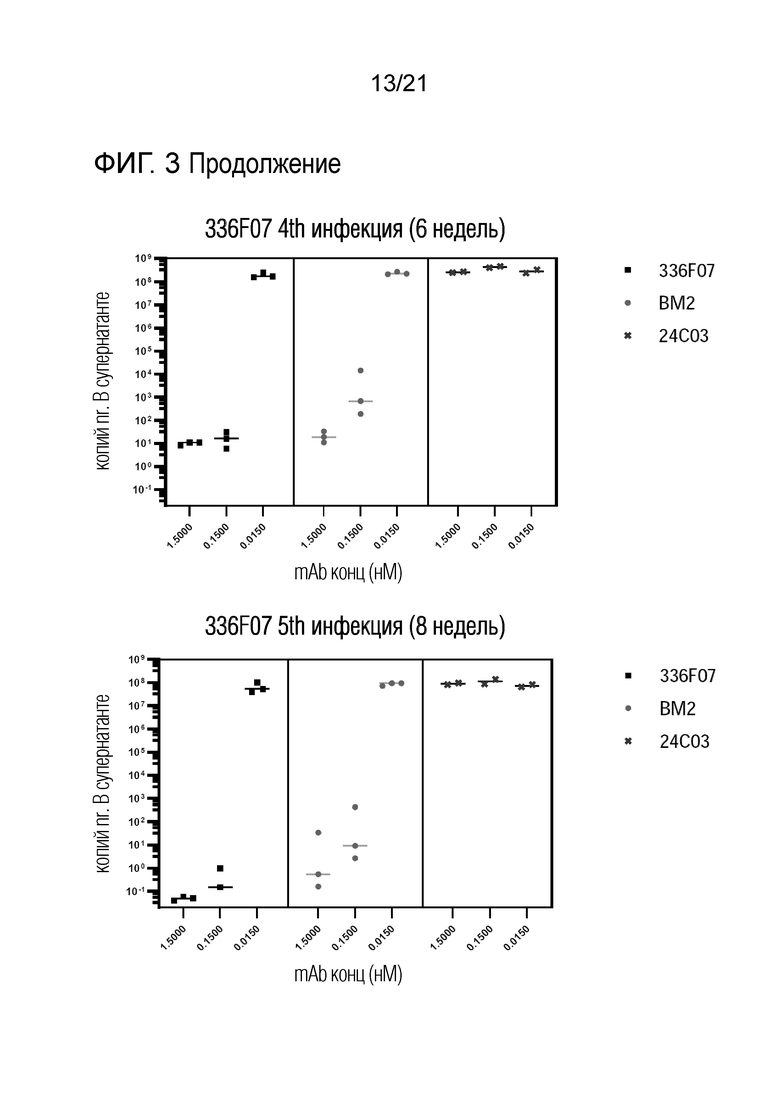
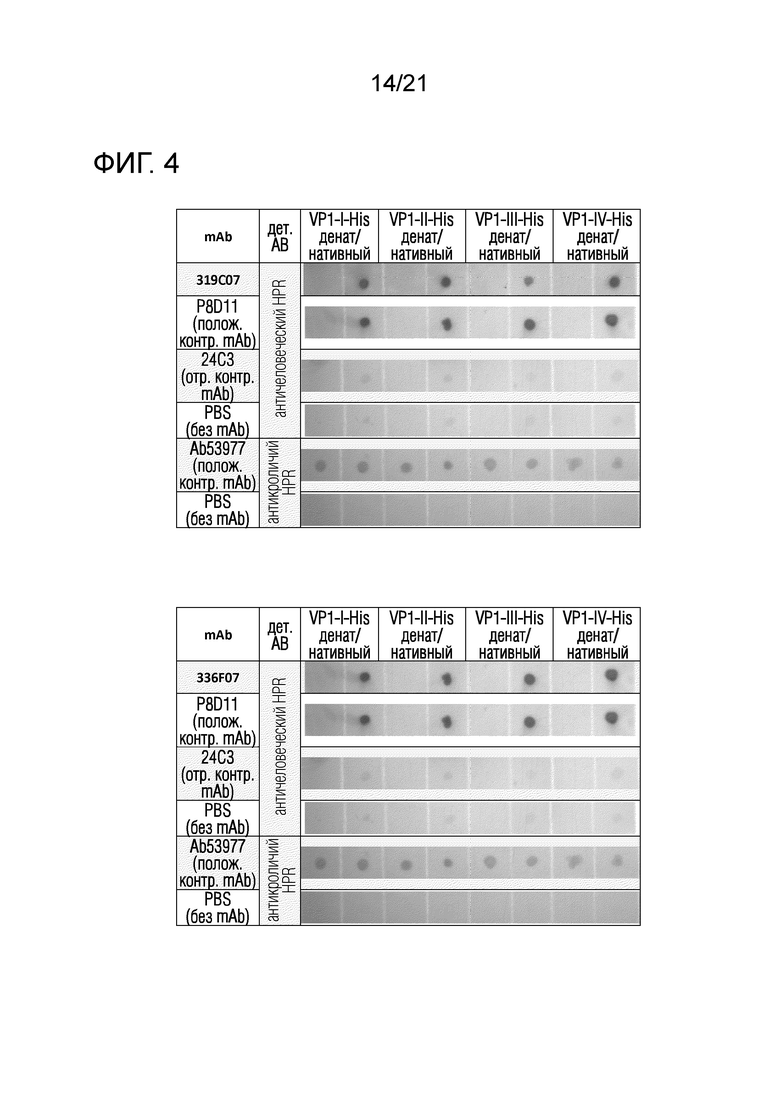
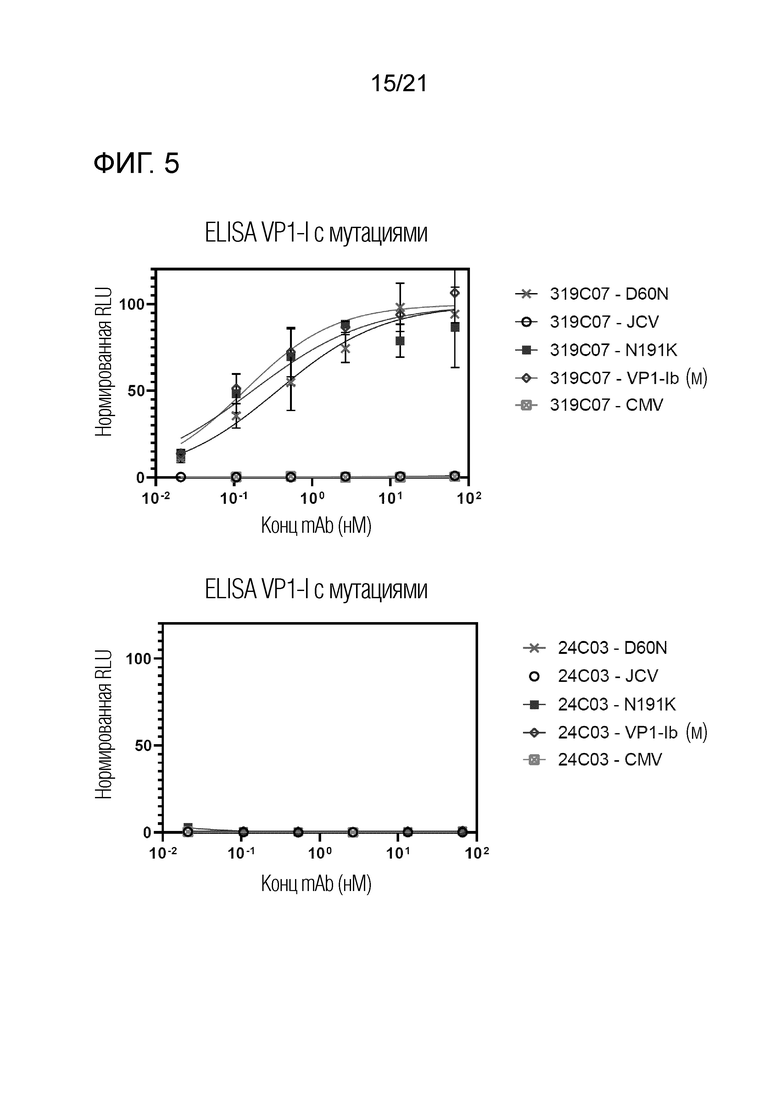
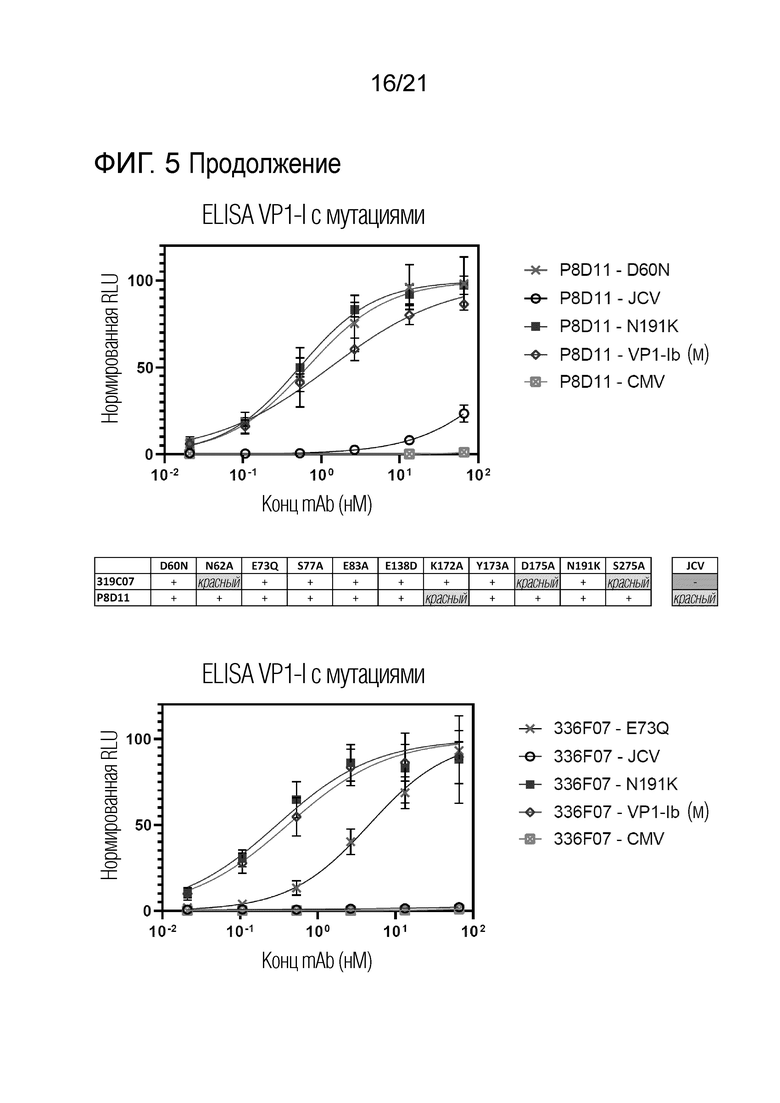
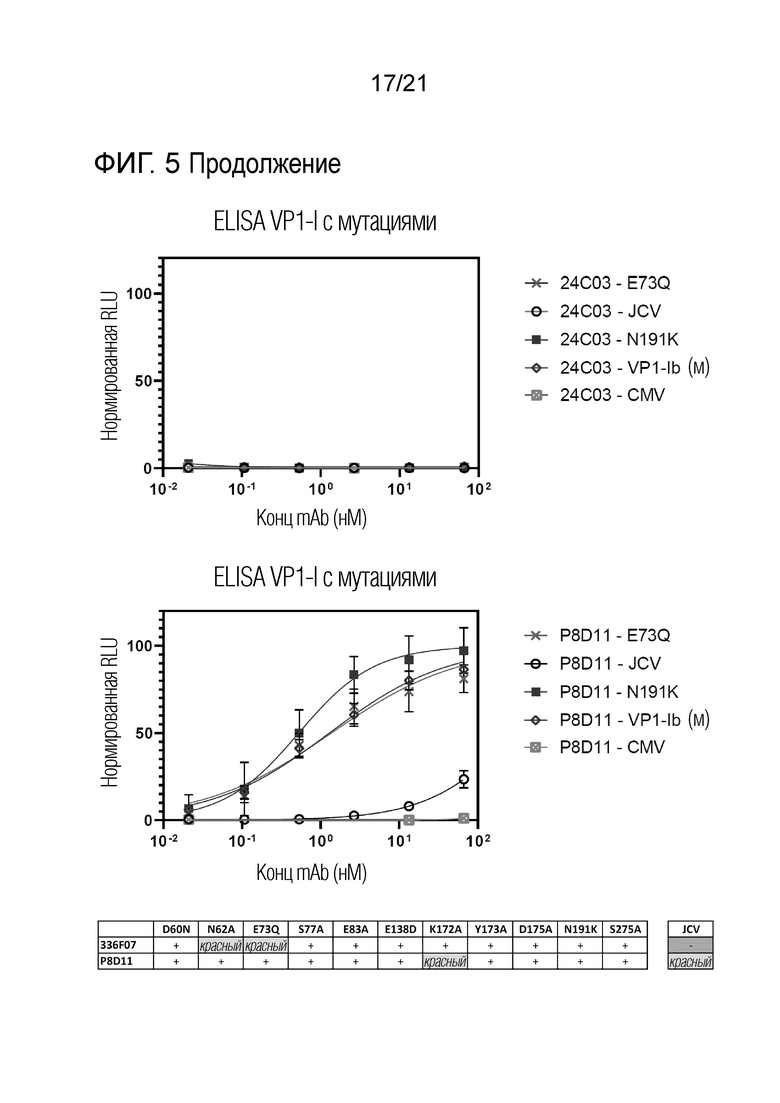
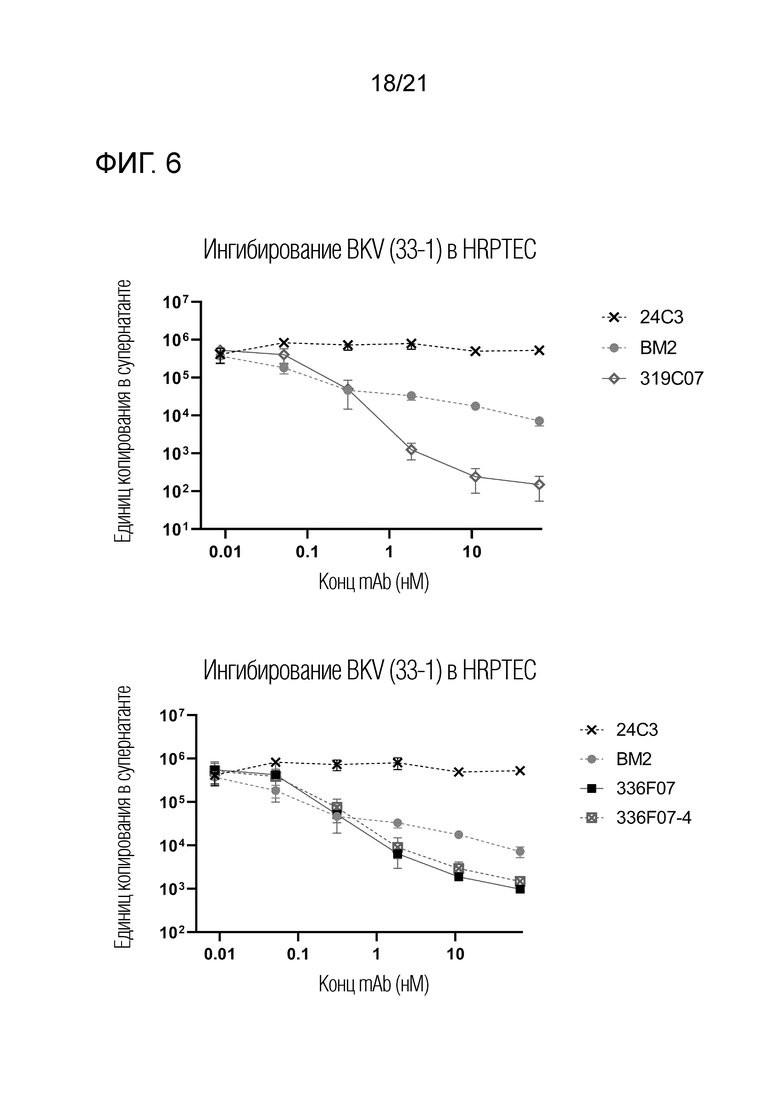
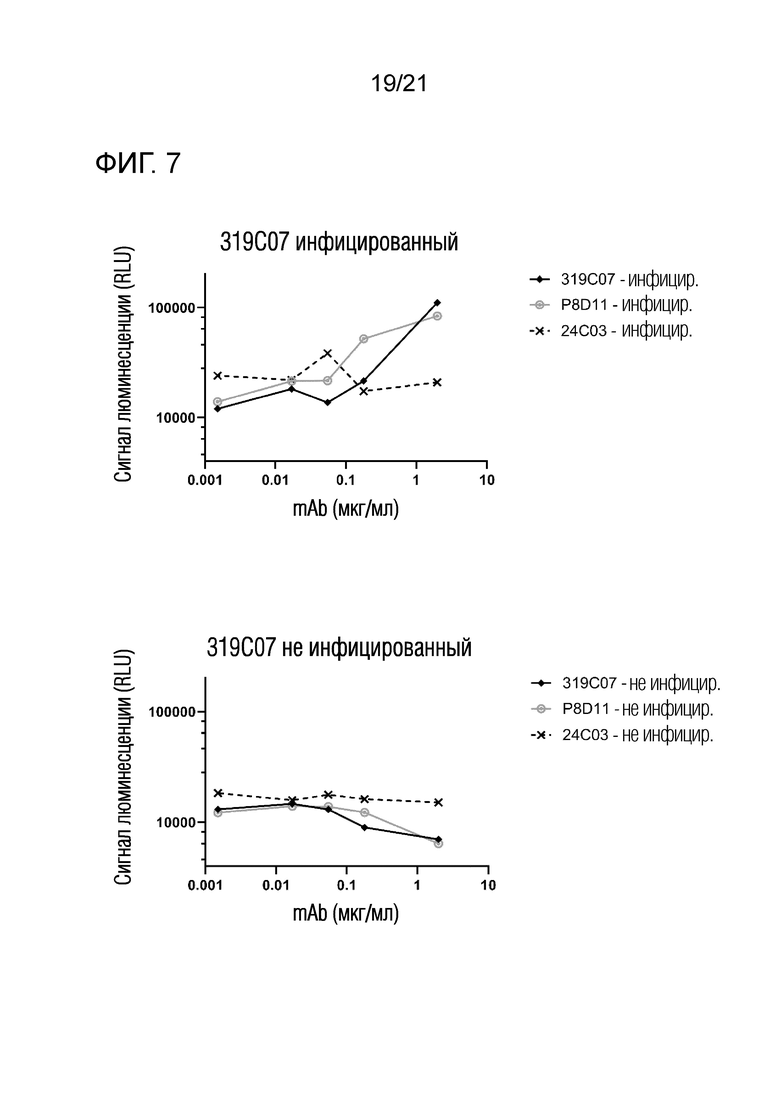
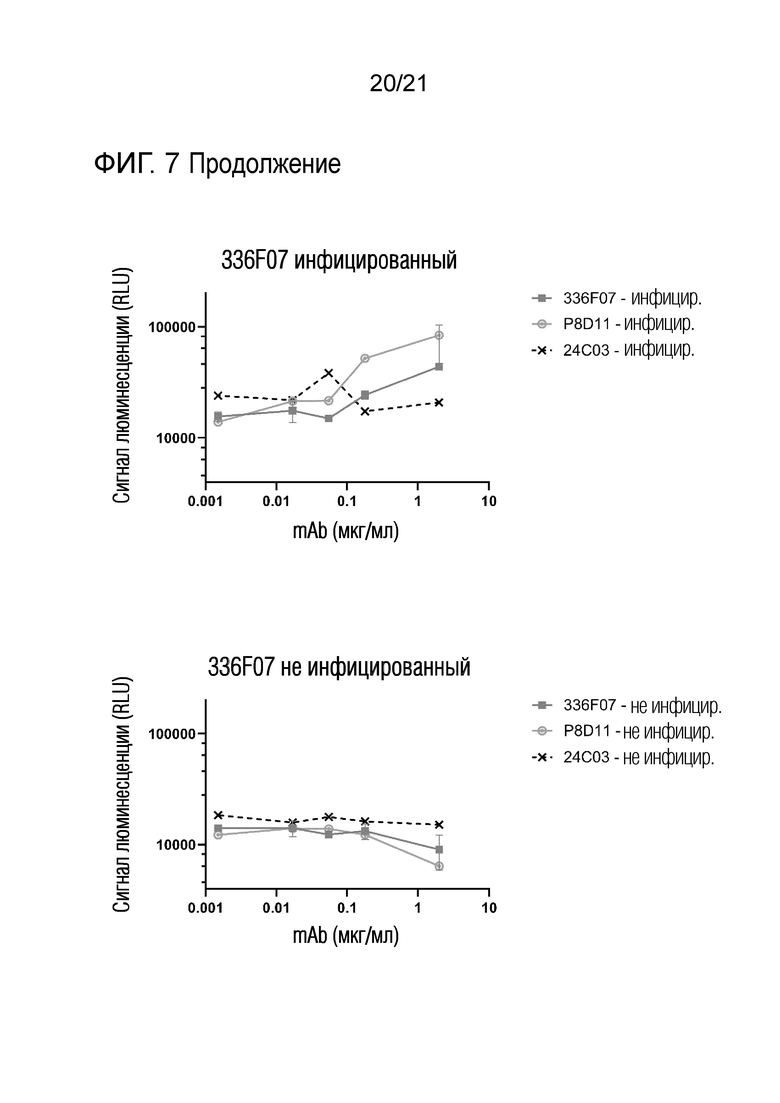
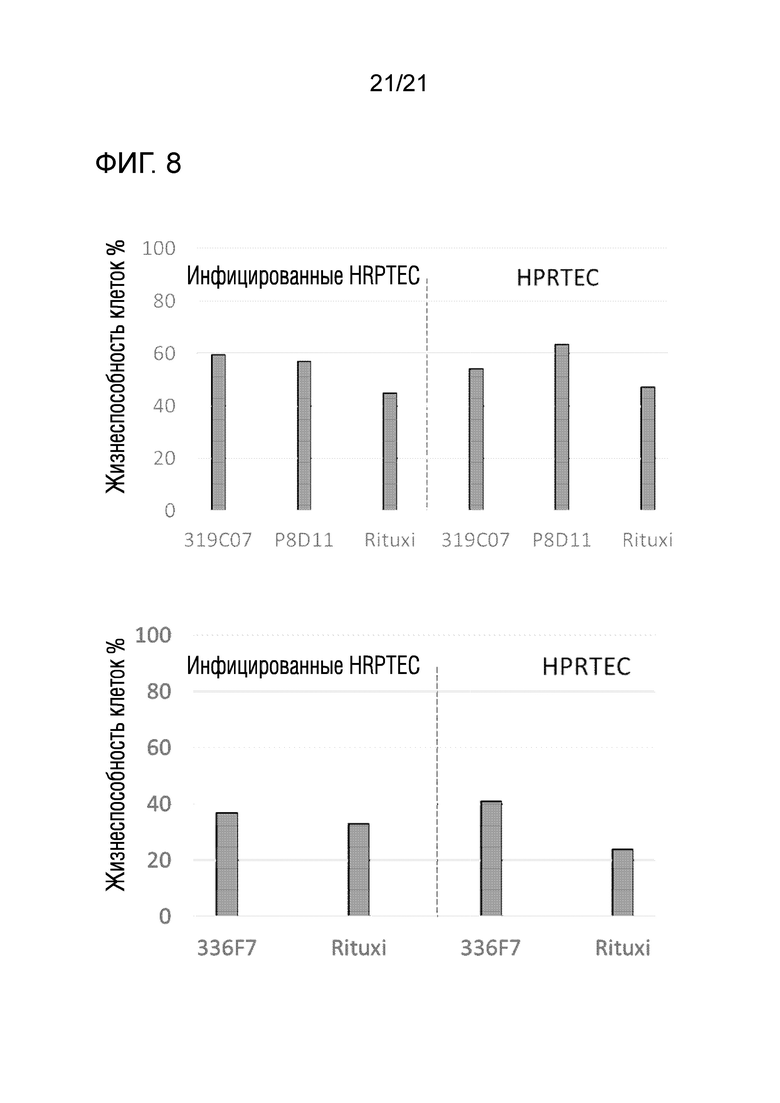
Изобретение относится к области биотехнологии, а именно к молекуле антитела против вируса BK, или его фрагменту, связывающему вирус BK. Изобретение эффективно для применения при лечении или профилактике инфекции вируса BK и/или связанного с вирусом BK нарушения. 4 з.п. ф-лы, 8 ил., 4 табл., 8 пр.
1. Молекула антитела против вируса BK, или его фрагмента, связывающего вирус BK, содержащая:
вариабельную область тяжелой цепи (VH), содержащую
определяющую комплементарность область 1 тяжелой цепи (VHCDR1) с аминокислотной последовательностью SEQ ID NO: 21,
определяющую комплементарность область 2 тяжелой цепи (VHCDR2) с аминокислотной последовательностью SEQ ID NO: 22, и
определяющую комплементарность область 3 тяжелой цепи (VHCDR3) с аминокислотной последовательностью SEQ ID NO: 23; и
вариабельную область легкой цепи (VL), содержащую
определяющую комплементарность область 1 легкой цепи (VLCDR1) с аминокислотной последовательностью SEQ ID NO: 24,
определяющей комплементарность области 2 легкой цепи (VLCDR2) с аминокислотной последовательностью SEQ ID NO: 25, и
определяющей комплементарность области 3 легкой цепи (VLCDR3) с аминокислотной последовательностью SEQ ID NO: 26.
2. Молекула антитела, или его связывающего фрагмента, по п. 1, содержащая
(i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO: 27 или аминокислотную последовательность, которая по меньшей мере приблизительно на 85%, 90%, 95% или 99% идентична SEQ ID NO: 27, и
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO: 28 или аминокислотную последовательность, которая по меньшей мере приблизительно на 85%, 90%, 95% или 99% идентична SEQ ID NO: 28; или
(ii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO: 27 или аминокислотную последовательность, которая по меньшей мере приблизительно на 85%, 90%, 95% или 99% идентична SEQ ID NO: 27, и
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO: 31 или аминокислотную последовательность, которая по меньшей мере приблизительно на 85%, 90%, 95% или 99% идентична SEQ ID NO: 31.
3. Молекула антитела, или его связывающего фрагмента, по п. 1 или 2, содержащая
(i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO: 27, и
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO: 28; или
(ii) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO: 27, и
вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO: 31.
4. Молекула антитела, или его связывающего фрагмента, по любому из пп. 1-3,
содержащая одно или несколько следующих свойств:
(i) связывается с вирусом BK серотипа I VP1 с ЕС50, равным менее чем приблизительно 10 нМ, 1 нМ, 0,9 нМ, 0,8 нМ, 0,7 нМ, 0,6 нМ, 0,5 нМ, 0,4 нМ, 0,3 нМ, 0,2 нМ, 0,19 нМ, 0,18 нМ, 0,17 нМ, 0,16 нМ, 0,15 нМ, 0,14 нМ, 0,13 нМ, 0,12 нМ, 0,11 нМ, 0,10 нМ, 0,09 нМ, 0,08 нМ, 0,07 нМ, 0,06 нМ, 0,05 нМ, 0,04 нМ, 0,03 нМ или 0,02 нМ, например, когда молекулу антитела, или его связывающего фрагмента тестируют как бивалентную молекулу с использованием ELISA;
(ii) связывается с вирусом BK серотипа II VP1 с ЕС50, равным менее чем приблизительно 10 нМ, 1 нМ, 0,9 нМ, 0,8 нМ, 0,7 нМ, 0,6 нМ, 0,5 нМ, 0,4 нМ, 0,3 нМ, 0,2 нМ, 0,19 нМ, 0,18 нМ, 0,17 нМ, 0,16 нМ, 0,15 нМ, 0,14 нМ, 0,13 нМ, 0,12 нМ, 0,11 нМ, 0,10 нМ, 0,09 нМ, 0,08 нМ, 0,07 нМ, 0,06 нМ, 0,05 нМ, 0,04 нМ, 0,03 нМ или 0,02 нМ, например, когда молекулу антитела или его связывающего фрагмента тестируют как бивалентную молекулу с использованием ELISA;
(iii) связывается с вирусом BK серотипа III VP1 с ЕС50, равным менее чем приблизительно 10 нМ, 1 нМ, 0,9 нМ, 0,8 нМ, 0,7 нМ, 0,6 нМ, 0,5 нМ, 0,4 нМ, 0,3 нМ, 0,2 нМ, 0,19 нМ, 0,18 нМ, 0,17 нМ, 0,16 нМ, 0,15 нМ, 0,14 нМ, 0,13 нМ, 0,12 нМ, 0,11 нМ, 0,10 нМ, 0,09 нМ, 0,08 нМ, 0,07 нМ, 0,06 нМ, 0,05 нМ, 0,04 нМ, 0,03 нМ или 0,02 нМ, например, когда молекулу антитела или его связывающего фрагмента тестируют как бивалентную молекулу с использованием ELISA;
(iv) связывается с вирусом BK серотипа IV VP1 с ЕС50, равным менее чем приблизительно 10 нМ, 1 нМ, 0,9 нМ, 0,8 нМ, 0,7 нМ, 0,6 нМ, 0,5 нМ, 0,4 нМ, 0,3 нМ, 0,2 нМ, 0,19 нМ, 0,18 нМ, 0,17 нМ, 0,16 нМ, 0,15 нМ, 0,14 нМ, 0,13 нМ, 0,12 нМ, 0,11 нМ, 0,10 нМ, 0,09 нМ, 0,08 нМ, 0,07 нМ, 0,06 нМ, 0,05 нМ, 0,04 нМ, 0,03 нМ или 0,02 нМ, например, когда молекулу антитела или его связывающего фрагмента тестируют как бивалентную молекулу с использованием ELISA;
(v) не связывается с вирусом JC VP1;
(vi) нейтрализует вирус BK серотипа I;
(vii) нейтрализует вирус BK серотипа II;
(viii) нейтрализует вирус BK серотипа III;
(ix) нейтрализует вирус BK серотипа IV.
5. Молекула антитела, или его связывающего фрагмента, по любому из пп. 1-4 для применения при лечении или профилактике инфекции вируса BK и/или связанного с вирусом BK нарушения.
| WO 2014102399 A1, 03.07.2014 | |||
| SUNDARAM HARIHARAN et al., BK Virus-Specific Antibodies and BKV DNA in Renal Transplant Recipients with BKV Nephritis, American Journal of Transplantation 2005; 5: 2719-2724 | |||
| WO 2017046676 A1, 23.03.2017, реферат, формула | |||
| P | |||
| RANDHAWA et al., Commercially Available Immunoglobulins Contain Virus Neutralizing |
Авторы
Даты
2025-03-04—Публикация
2021-06-09—Подача