ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка испрашивает приоритет предварительной заявки на патент США № 62/775246, поданной 4 декабря 2018 г., предварительной заявки на патент США № 62/641869, поданной 12 марта 2018 г., предварительной заявки на патент США № 62/641873, поданной 12 марта 2018 г., предварительной заявки на патент США № 62/625009, поданной 1 февраля 2018 г., и предварительной заявки на патент США № 62/625019, поданной 1 февраля 2018 г., каждая из которых включена в данный документ посредством ссылки в ее полном объеме.
ССЫЛКА НА ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Данная заявка подана в электронном виде посредством EFS-Web и включает перечень последовательностей, поданный в электронном виде в формате txt. Файл с расширением.txt содержит перечень последовательностей под названием «ALGN_014_03WO_SeqList_ST25.txt», созданный 24 января 2019 г. и имеющий размер ~725 килобайт. Перечень последовательностей, содержащийся в этом файле с расширением.txt, является частью описания и включен в данный документ посредством ссылки в его полном объеме.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к химерным антигенным рецепторам (CAR). CAR способны перенаправлять специфичность и реактивность иммунных клеток на выбранную мишень с использованием свойств лиганд-связывающего домена. В частности, настоящее изобретение относится к CAR, которые специфически связываются с кластером дифференцировки 70 (CAR, специфическими к CD70). Настоящее изобретение также относится к полинуклеотидам, кодирующим CAR, специфические к CD70, и выделенным клеткам, экспрессирующим на своей поверхности CAR, специфические к CD70. Настоящее изобретение также относится к способам конструирования иммунных клеток, экспрессирующих на своей поверхности CAR, специфические к CD70. Настоящее изобретение, в частности, применимо для лечения рака, как, например, лимфомы, лейкоза, глиомы или почечно-клеточной карциномы (RCC). Настоящее изобретение также относится к иммунным клеткам, содержащим CAR, специфические к CD70 (CAR-T-клетки, специфические к CD70), композициям, содержащим CAR-T-клетки, специфические к CD70, и способам применения CAR-T-клеток, специфических к CD70, для лечения состояний, ассоциированных со злокачественными клетками, экспрессирующими CD70 (например, рака).
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Адаптивный перенос иммунных клеток, генетически модифицированных для распознавания антигенов, ассоциированных со злокачественными новообразованиями, является перспективным новым подходом к лечению рака (см., например, Brenner et al., Current Opinion in Immunology, 22(2): 251-257 (2010); Rosenberg et al., Nature Reviews Cancer, 8(4): 299-308 (2008)). Т-клетки могут быть генетически модифицированы для экспрессии химерных антигенных рецепторов (CAR), слитых белков, состоящих из антигенраспознающего фрагмента и доменов активации Т-клеток (см., например, Eshhar et al., Proc. Natl. Acad. Sci. USA, 90(2): 720-724 (1993), а также Sadelain et al., Curr. Opin. Immunol, 21(2): 215-223 (2009)).
Кластер дифференцировки 70 (CD70, CD27LG или TNFSF7) является представителем суперсемейства фактора некроза опухолей (TNF) и лиганда для CD27, рецептора суперсемейства TNF. Временное взаимодействие между CD27 и CD70 обеспечивает костимуляцию Т-клеток, комплементарную той, которая обеспечивается CD28. CD70 экспрессируется при гемобластозах, таких как неходжкинская лимфома и болезнь Ходжкина, а также на солидных опухолях, таких как глиобластома и почечно-клеточная карцинома; при этом его экспрессия на ccRCC является практически однородной (см., например, Grewal I., et al., Expert Opinion on Therapeutic Targets, 12(3): 341-351 (2008)). Адаптивный перенос Т-клеток, генетически модифицированных для распознавания антигенов, ассоциированных со злокачественными новообразованиями, является перспективным новым подходом лечения рака (см., например, Brenner et al., Current Opinion in Immunology, 22(2): 251-257 (2010); Rosenberg et al., Nature Reviews Cancer, 8(4): 299-308 (2008)). Т-клетки могут быть генетически модифицированы для экспрессии химерных антигенных рецепторов (CAR), которые представляют собой слитые белки, состоящие из антигенраспознающего фрагмента и доменов активации Т-клеток (см., например, Eshhar et al., Proc. Natl. Acad. Sci. USA, 90(2): 720-724 (1993), and Sadelain et al., Current Opinion in Immunology, 21(2): 215-223 (2009)). Экспрессия CD70 в нормальных тканях ограничивается активированными Т-клетками, В-клетками, NK-клетками и дендритными клетками. Однако экспрессия CD70 на активированных Т-клетках может вызывать определенную обеспокоенность в плане продуцирования CAR-Т-клеток из-за потенциальной целенаправленной дифференцировки Т-клеток, истощения и взаимного уничтожения в ходе способа получения.
Почечно-клеточная карцинома (RCC) представляет собой рак, который возникает в корковом веществе почки и составляет приблизительно 90% форм рака почки. На основе гистологии RCC можно классифицировать на несколько подтипов, из которых светлоклеточная почечно-клеточная карцинома (ccRCC) является наиболее распространенной и приводит к самой высокой смертности. Каждый год сообщалось о свыше 320000 случаях RCC, приводящих во всем мире к приблизительно 140000 смертей. В течение последних 10 лет частота возникновения RCC стабильно повышалась и составляет 2-3% от всех злокачественных новообразований у взрослых. Пациенты с локализованными опухолями на ранней стадии могут отказаться от хирургической резекции; однако локализованное заболевание может подвергаться ранней гематогенной диссеминации, что приводит к метастазированию. Очаги ранних метастазов включают легкие, лимфоузлы, печень, кость и головной мозг; реже надпочечники и контралатеральную почку. Пациенты с заболеванием на поздней стадии сталкиваются с высокими показателями смертности: 5-летняя медиана выживаемости составляет 53% для III стадии заболевания и лишь 8% для заболевания с метастазами. Существующие в настоящее время виды лечения первой линии для заболевания на поздней стадии включают низкомолекулярные ингибиторы тирозинкиназы (TKI), такие как сунитиниб и пазопаниб, которые нацеливаются на рецептор фактора роста эндотелия сосудов (VEGF), моноклональные антитела, которые нацеливаются на VEGF, такие как бевацизумаб, мишень для темсиролимуса - ингибитора рапамицина у млекопитающих (mTOR), а также высокие дозы IL-2. Хотя эти средства терапии, целенаправленно воздействующие на VEGF, характеризуются обеспечивают улучшенную общую выживаемость, долговременная устойчивость к лекарственным средствам приводит к рецидиву заболевания, и при этом лечение заболевания на поздней стадии все еще остается неудовлетворенной потребностью (см., например, Zarrabi, K. et al., Journal of Hematology and Oncology, 10:38 (2017)).
Соответственно, существует потребность в альтернативных способах и средствах лечения рака и, в частности, злокачественных новообразований, в которые вовлечена аберрантная экспрессия CD70. Новые средства иммунотерапии, такие как терапия с помощью CAR-T-клеток, могут значительно улучшить исход у пациентов с раком, у которых экспрессируется CD70, например, при mRCC. Соответственно, лечение рака (такого как, например, mRCC) с применением CAR, специфических к CD70, и CAR-T-клеток, специфических к CD70, может стать перспективной терапевтической стратегией. В данном документе представлены способы и композиции, удовлетворяющие такую потребность.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В данном документе представлены химерные антигенные рецепторы (CAR), которые связываются с CD70, а также способы их получения и способы их применения. В данном документе также представлены иммунные клетки, например Т-клетки, содержащие такие CD70-специфические CAR. Показано, что определенные CAR, специфические к CD70, эффективны, когда они экспрессируются в Т-клетках с активацией Т-клеток при приведении в контакт с CD70. Преимущественно CAR, специфические к CD70, представленные в данном документе, связываются с CD70 человека. Также преимущественно CAR-T-клетки, специфические к CD70, представленные в данном документе, проявляют цитотоксическую активность при приведении в контакт с клетками, экспрессирующими CD70. В данном документе также представлены антитела, которые связываются с CD70, а также способы их получения и способы их применения. Представленные в данном документе антитела, специфические к CD70, связываются с CD70 человека.
В одном аспекте настоящего изобретения представлен химерный антигенный рецептор (CAR), специфический к кластеру дифференцировки 70 (CD70), содержащий внеклеточный лиганд-связывающий домен, первый трансмембранный домен и внутриклеточный сигнальный домен, где внеклеточный домен содержит одноцепочечный Fv-фрагмент (scFv), связывающийся с внеклеточным доменом CD70.
В некоторых вариантах осуществления настоящего изобретения представлен CAR, специфический к CD70, где внеклеточный домен CAR, представленный в данном документе, содержит scFv, содержащий вариабельную область тяжелой цепи (VH), содержащую три CDR из области VH, содержащей последовательность, представленную под SEQ ID NO: 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38, 40, 42, 44, 46, 48, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379 или 381; и вариабельную область легкой цепи (VL), содержащую три CDR из области VL, представленной под SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 338, 340, 342, 344, 346, 348, 350, 352, 354, 356, 358, 360, 362, 364, 366, 368, 370, 372, 374, 376, 378 или 380. В некоторых вариантах осуществления область VH содержит последовательность, представленную под SEQ ID NO: 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38, 40, 42, 44, 46, 48, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379 или 381, или ее вариант с одной или более консервативными аминокислотными заменами по остаткам, которые не присутствуют в CDR, и/или область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 338, 340, 342, 344, 346, 348, 350, 352, 354, 356, 358, 360, 362, 364, 366, 368, 370, 372, 374, 376, 378 или 380, или ее варианта с одной или более аминокислотными заменами по аминокислотам, которые не присутствуют в CDR.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 49, 50 или 51; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 52 или 53; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 54; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 193; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 194; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 195.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:2, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 1.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 55, 56 или 57; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 58 или 59; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 60; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 196; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 197; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 198.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:4, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 3.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 61, 62 или 63; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 64 или 65; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 66; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 199; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 200; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 201.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:6, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 5.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 67, 68 или 69; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 70 или 71; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 72; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 202; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 203; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 204.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:8, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 7.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 73, 74 или 75; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 76 или 77; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 78; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 205; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 206; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 207.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:10, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 9.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 79, 80 или 81; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 82 или 83; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 84; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 208; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 209; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 210.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:12, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 11.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 85, 86 или 87; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 88 или 89; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 90; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 211; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 212; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 213.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:14, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 13.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 91, 92 или 93; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 94 или 95; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 96; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 214; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 215; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 216.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:16, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 15.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 97, 98 или 99; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 100 или 101; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 102; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 217; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 218; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 219.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:18, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 17.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 103, 104 или 105; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 106 или 107; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 108; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 220; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 221; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 222.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:20, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 19.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 109, 110 или 111; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 112 или 113; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 114; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 223; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 224; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 225.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:22, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 21.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 115, 116 или 117; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 118 или 119; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 120; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 226; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 227; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 228.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:24, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 23.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 121, 122 или 123; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 124 или 125; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 126; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 229; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 230; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 231.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:26, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 25.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 127, 128 или 129; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 130 или 131; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 132; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 232; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 233; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 234.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:28, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 27.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 133, 134 или 135; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 136 или 137; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 138; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 235; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 236; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 237.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:30, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 29.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 139, 140 или 141; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 142 или 143; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 144; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 238; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 239; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 240.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:32, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 31.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 145, 146 или 147; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 148 или 149; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 150; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 241; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 242; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 243.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:34, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 33.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 151, 152 или 153; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 154 или 155; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 156; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 244; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 245; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 246.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:36, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 35.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 157, 158 или 159; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 160 или 161; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 162; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 247; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 248; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 249.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:38, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 37.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 163, 164 или 165; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 166 или 167; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 168; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 250; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 251; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 252.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:40, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 39.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 169, 170 или 171; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 172 или 173; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 174; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 253; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 254; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 255.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:42, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 41.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 175, 176 или 177; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 178 или 179; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 180; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 256; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 257; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 258.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:44, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 43.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 181, 182 или 183; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 184 или 185; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 186; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 259; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 260; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 261.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:46, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 45.
В некоторых вариантах осуществления область VH содержит CDR1 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 187, 188 или 189; CDR2 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 190 или 191; и CDR3 VH, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 192; и область VL содержит CDR1 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 262; CDR2 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 263; и CDR3 VL, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 264.
В некоторых вариантах осуществления область VH содержит аминокислотную последовательность, представленную под SEQ ID NO:48, и область VL содержит аминокислотную последовательность, представленную под SEQ ID NO: 47.
В некоторых вариантах осуществления каждая CDR определена в соответствии с определением по Кабату, определением по Чотиа, комбинацией определения по Кабату и определения по Чотиа, определением AbM или контактным определением CDR.
В некоторых вариантах осуществления каждая из CDR определена в соответствии с определением по Кабату, определением по Чотиа, расширенным определением, комбинацией определения по Кабату и определения по Чотиа, определением AbM, контактным определением и/или конформационным определением CDR.
В некоторых вариантах осуществления внутриклеточный сигнальный домен предусматривает сигнальный домен CD3ζ. В некоторых вариантах осуществления внутриклеточный сигнальный домен предусматривает домен 4-1BB. В некоторых вариантах осуществления CAR дополнительно содержит второй внутриклеточный сигнальный домен. В некоторых вариантах осуществления второй внутриклеточный сигнальный домен предусматривает домен 4-1BB. В некоторых вариантах осуществления CAR содержит первый внутриклеточный сигнальный домен CD3ζ и второй внутриклеточный сигнальный домен 4-1BB.
В некоторых вариантах осуществления внутриклеточный сигнальный домен предусматривает сигнальный домен CD3ζ. В некоторых вариантах осуществления внутриклеточный сигнальный домен предусматривает домен 4-1BB. В некоторых вариантах осуществления CAR дополнительно содержит два внутриклеточных сигнальных домена. В некоторых вариантах осуществления CAR дополнительно содержит 3, 4, 5 или 6 внутриклеточных сигнальных доменов. В некоторых вариантах осуществления CAR содержит первый внутриклеточный сигнальный домен и второй внутриклеточный сигнальный домен, где второй внутриклеточный сигнальный домен предусматривает домен 4-1BB. В некоторых вариантах осуществления CAR содержит внутриклеточный сигнальный домен CD3ζ и внутриклеточный сигнальный домен 4-1BB.
В некоторых вариантах осуществления CAR может содержать домен «стебля» между внеклеточным лиганд-связывающим доменом и первым трансмембранным доменом. В некоторых вариантах осуществления домен «стебля» выбран из группы, состоящей из шарнирного участка из CD8α человека, шарнирного участка из IgG1 и шарнирного участка из FcγRIIIα. В некоторых вариантах осуществления домен «стебля» представляет собой шарнирный участок из CD8α человека, шарнирный участок из IgG1 человека или шарнирный участок из FcγRIIIα человека.
В некоторых вариантах осуществления CAR может содержать эпитоп CD20. В некоторых вариантах осуществления эпитоп CD20 содержит аминокислотную последовательность, представленную под SEQ ID NO: 293, или SEQ ID NO: 294, или SEQ ID NO: 609.
В некоторых вариантах осуществления CAR может содержать аминокислотную последовательность, представленную под SEQ ID NO: 311-334, перечисленных в таблице 5. В некоторых вариантах осуществления CAR может содержать аминокислотную последовательность, представленную под SEQ ID NO: 319 или 327.
В некоторых вариантах осуществления первый трансмембранный домен предусматривает трансмембранный домен цепи CD8α.
В некоторых вариантах осуществления CAR может содержать другой внеклеточный лиганд-связывающий домен, который не является специфическим в отношении CD70.
В некоторых вариантах осуществления внеклеточный лиганд-связывающий домен (домены), первый трансмембранный домен и внутриклеточный сигнальный домен (домены) расположены в одном полипептиде.
В некоторых вариантах осуществления CAR может содержать второй трансмембранный домен, где первый трансмембранный домен и внеклеточный лиганд-связывающий домен (домены) расположены в первом полипептиде, и где второй трансмембранный домен и внутриклеточный сигнальный домен (домены) расположены во втором полипептиде, где первый трансмембранный домен содержит трансмембранный домен из α-цепи высокоаффинного рецептора для IgE (FcεRI), а второй трансмембранный домен содержит трансмембранный домен из γ- или β-цепи FcεRI.
В некоторых вариантах осуществления CAR может содержать третий полипептид, содержащий третий трансмембранный домен, слитый с внутриклеточным сигнальным доменом из костимулирующей молекулы, где третий трансмембранный домен предусматривает трансмембранный домен из γ- или β-цепи FcεRI.
В другом аспекте настоящего изобретения представлен выделенный полинуклеотид, содержащий последовательность нуклеиновой кислоты, кодирующую CAR, специфический к CD70, описанный в данном документе.
В другом аспекте настоящего изобретения представлен вектор экспрессии, содержащий полинуклеотид, кодирующий CAR, специфический к CD70, описанный в данном документе.
В другом аспекте настоящего изобретения представлена сконструированная иммунная клетка, экспрессирующая на своей внешней клеточной мембране CAR, специфический к CD70, описанный в данном документе. В некоторых вариантах осуществления сконструированная иммунная клетка может содержать другой CAR, который не является специфическим в отношении CD70. В некоторых вариантах осуществления сконструированная иммунная клетка может содержать полинуклеотид, кодирующий «суицидный» полипептид. В некоторых вариантах осуществления «суицидный» полипептид представляет собой RQR8.
В некоторых вариантах осуществления сконструированная иммунная клетка получена из воспалительного Т-лимфоцита, цитотоксического Т-лимфоцита, регуляторного Т-лимфоцита или хелперного Т-лимфоцита.
В некоторых вариантах осуществления сконструированная иммунная клетка может характеризоваться разрушением одного или более эндогенных генов, где эндогенный ген кодирует TCRα, TCRβ, CD52, глюкокортикоидный рецептор (GR), дезоксицитидинкиназу (dCK), CD70 или белок контрольной точки иммунного ответа, такой как, например, белок запрограммированной смерти-1 (PD-1).
В некоторых вариантах осуществления сконструированная иммунная клетка получена от здорового донора. В некоторых вариантах осуществления сконструированная иммунная клетка получена от пациента.
В другом аспекте настоящего изобретения представлена сконструированная иммунная клетка, экспрессирующая на своей внешней клеточной мембране CAR, специфический к CD70, описанный в данном документе, для применения в качестве лекарственного препарата. В некоторых вариантах осуществления лекарственный препарат предназначен для применения в лечении рака. В некоторых вариантах осуществления лекарственный препарат предназначен для лечения почечно-клеточной карциномы, глиобластомы, глиомы, например, глиомы низкой степени злокачественности, неходжкинской лимфомы (NHL), болезни Ходжкина (HD), макроглобулинемии Вальденстрема, острого миелоидного лейкоза, множественной миеломы, диффузной крупноклеточной лимфомы, фолликулярной лимфомы или немелкоклеточного рака легкого.
В другом аспекте настоящего изобретения представлен способ конструирования иммунной клетки, предусматривающий: обеспечение иммунной клетки и обеспечение экспрессии на поверхности клетки по меньшей мере одного CAR, специфического к CD70, описанного в данном документе. В некоторых вариантах осуществления способ предусматривает: обеспечение иммунной клетки; введение в клетку по меньшей мере одного полинуклеотида, кодирующего указанный CAR, специфический к CD70; и обеспечение экспрессии указанного полинуклеотида в клетке.
В некоторых вариантах осуществления способ предусматривает обеспечение иммунной клетки; введение в клетку по меньшей мере одного полинуклеотида, кодирующего указанный CAR, специфический к CD70; и введение по меньшей мере одного другого CAR, не являющегося специфическим к CD70.
В другом аспекте настоящего изобретения представлен способ лечения субъекта, страдающего от состояния, ассоциированного со злокачественными клетками, при этом способ предусматривает: обеспечение иммунной клетки, экспрессирующей на поверхности CAR, специфический к CD70, описанный в данном документе; и введение указанных иммунных клеток указанному пациенту.
В другом аспекте настоящего изобретения представлена фармацевтическая композиция, содержащая сконструированную иммунную клетку, описанную в данном документе.
В другом аспекте настоящего изобретения представлен способ лечения состояния, ассоциированного со злокачественными клетками, экспрессирующими CD70, у субъекта, предусматривающий введение нуждающемуся в этом субъекту, эффективного количества фармацевтической композиции, содержащей сконструированную иммунную клетку, описанную в данном документе. В некоторых вариантах осуществления состояние представляет собой рак. В некоторых вариантах осуществления рак представляет собой почечно-клеточную карциному, глиобластому, глиому, такую как глиома низкой степени злокачественности, неходжкинскую лимфому (NHL), болезнь Ходжкина (HD), макроглобулинемию Вальденстрема, острый миелоидный лейкоз, множественную миелому, диффузную крупноклеточную лимфому, фолликулярную лимфому или немелкоклеточный рак легкого.
В другом аспекте настоящего изобретения представлен способ подавления роста или прогрессирования опухоли у субъекта, у которого имеются злокачественные клетки, экспрессирующие CD70, предусматривающий введение нуждающемуся в этом субъекту эффективного количества фармацевтической композиции, содержащей сконструированную иммунную клетку, описанную в данном документе.
В другом аспекте настоящего изобретения представлен способ подавления метастазирования злокачественных клеток, экспрессирующих CD70, у субъекта, предусматривающий введение нуждающемуся в этом субъекту эффективного количества фармацевтической композиции, содержащей сконструированную иммунную клетку, описанную в данном документе.
В другом аспекте настоящего изобретения представлен способ индуцирования регрессии опухоли у субъекта, у которого имеются злокачественные клетки, экспрессирующие CD70, предусматривающий введение нуждающемуся в этом субъекту эффективного количества фармацевтической композиции, содержащей сконструированную иммунную клетку, описанную в данном документе.
В некоторых вариантах осуществления любой из вышеуказанных способов дополнительно предусматривает введение одного или более дополнительных терапевтических средств, как, например, моноклонального антитела и/или химиотерапевтического средства. В некоторых вариантах осуществления моноклональное антитело может представлять собой, например, антитело, которое связывается с ингибитором контрольной точки, таким как, например, антитело к PD-1 или антитело к PD-L1. В некоторых вариантах осуществления любой из вышеуказанных способов дополнительно предусматривает введение ингибитора рецепторной тирозинкиназы, такого как сунитиниб или акситиниб.
В некоторых вариантах осуществления настоящего изобретения представлен CAR, специфический к CD70, содержащий внеклеточный лиганд-связывающий домен, трансмембранный домен и внутриклеточный сигнальный домен, где внеклеточный домен содержит одноцепочечный Fv-фрагмент (scFv), связывающийся с внеклеточным доменом CD70, имеющим вариабельную область тяжелой цепи (VH) и вариабельную область легкой цепи (VL); где область VH содержит аминокислотную последовательность, которая на по меньшей мере 95%, 96%, 97%, 98%, 99% или 100% идентична SEQ ID NO: 18, и область VL содержит аминокислотную последовательность, которая на по меньшей мере 95%, 96%, 97%, 98%, 99% или 100% идентична SEQ ID NO: 17; или область VH содержит аминокислотную последовательность, которая на по меньшей мере 95%, 96%, 97%, 98%, 99% или 100% идентична SEQ ID NO: 34, и область VL содержит аминокислотную последовательность, которая на по меньшей мере 95%, 96%, 97%, 98%, 99% или 100% идентична SEQ ID NO: 33.
В некоторых вариантах осуществления внеклеточный домен содержит аминокислотную последовательность, которая на по меньшей мере 95%, 96%, 97%, 98%, 99% или 100% идентична SEQ ID NO: 319. В некоторых вариантах осуществления внеклеточный домен содержит аминокислотную последовательность, которая на по меньшей мере 95%, 96%, 97%, 98%, 99% или 100% идентична SEQ ID NO: 327.
В некоторых вариантах осуществления настоящего изобретения представлен полинуклеотид, кодирующий CAR, специфический к CD70, где полинуклеотид содержит последовательность нуклеиновой кислоты, которая на по меньшей мере 95%, 96%, 97%, 98%, 99% или 100% идентична SEQ ID. NO: 297 и на по меньшей мере 95%, 96%, 97%, 98%, 99% или на 100% идентична SEQ ID NO: 298 или на по меньшей мере 95%, 96%, 97%, 98%, 99% или 100% идентична SEQ ID NO: 307 и на по меньшей мере 95%, 96%, 97%, 98%, 99% или 100% идентична SEQ ID NO: 308.
В некоторых вариантах осуществления настоящего изобретения представлен CAR, содержащий антигенсвязывающую молекулу, которая специфически связывается с CD70, где антигенсвязывающая молекула содержит по меньшей мере одно из следующего: CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 49-51, 55-57, 61-63, 67-69, 73-75, 79-81, 85-87, 91-93, 97-99, 103-105, 109-111, 115-117, 121-123, 127-129, 133-135, 139-141, 145-147, 151-153, 157-159, 163-165, 169-171, 175-177, 181-183, 187-189, 382-384, 388-390, 394-396, 400-402, 406-408, 412-414, 418-420, 424-426, 430-432, 436-438, 442-444, 448-450, 454-456, 460-462, 466-468, 472-474, 478-480, 484-486, 490-492, 496-498, 502-504 и 508-510; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ NO: 52, 53, 58, 59, 64, 65, 70, 71, 76, 77, 82, 83, 88, 89, 94, 95, 100, 101, 106, 107, 112, 113, 118, 119, 124, 125, 130, 131, 136, 137, 142, 143, 148, 149, 154, 155, 160, 161, 166, 167, 172, 173, 178, 179, 184, 185, 190, 191, 385, 386, 391, 392, 397, 398, 403, 404, 409, 410, 415, 416, 421, 422, 427, 428, 433, 434, 439, 440, 445, 446, 451, 452, 457, 458, 463, 464, 469, 470, 475, 476, 481, 482, 487, 488, 493, 494, 499, 500, 505, 506, 511 и 512; CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 54, 60, 66, 72, 78, 84, 90, 96, 102, 108, 114, 120, 126, 132, 138, 144, 150, 156, 162, 168, 174, 180, 186, 192, 387, 393, 399, 405, 411, 417, 423, 429, 435, 441, 447, 453, 459, 465, 471, 477, 483, 489, 495, 501, 507 и 513; CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ NO: 193, 196, 199, 202, 205, 208, 211, 214, 217, 220, 223, 226, 229, 232, 235, 238, 241, 244, 247, 250, 253, 256, 259, 262, 514, 517, 520, 523, 526, 529, 532, 535, 538, 541, 544, 547, 550, 553, 556, 559, 562, 565, 568, 571, 574 и 577; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 194, 197, 200, 203, 206, 209, 212, 215, 218, 221, 224, 227, 230, 233, 236, 239, 242, 245, 248, 251, 254, 257, 260, 263, 515, 518, 521, 524, 527, 530, 533, 536, 539, 542, 545, 548, 551, 554, 557, 560, 563, 566, 569, 572, 575 и 578; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 195, 198, 201, 204, 207, 210, 213, 216, 219, 222, 225, 228, 231, 234, 237, 240, 243, 246, 249, 252, 255, 258, 261, 264, 516, 519, 522, 525, 528, 531, 534, 537, 540, 543, 546, 549, 552, 555, 558, 561, 564, 567, 570, 573, 576 и 579.
В некоторых вариантах осуществления антигенсвязывающая молекула содержит вариабельный домен тяжелой цепи, содержащий аминокислотные последовательности CDRH1, CDRH2 и CDRH3 соответственно, выбранные из одной из SEQ ID NO: 49-51, 52-53, 54; 55-57, 58-59, 60; 61-63, 64-65, 66; 67-69, 70-71, 72; 73-75, 76-77, 78; 79-81, 82-83, 84; 85-87, 88-89, 90; 91-93, 94-95, 96; 97-99, 100-101, 102; 103-105, 106-107, 108; 109-111, 112-113, 114; 115-117, 118-119, 120; 121-123, 124-125, 126; 127-129, 130-131, 132; 133-135, 136-137, 138; 139-141, 142-143, 144; 145-147, 148-149, 150; 151-153, 154-155, 156; 157-159, 160-161, 162; 163-165, 166-167, 168; 169-171, 172-173, 174; 175-177, 178-179, 180; 181-183, 184-185, 186; 187-189, 190-191, 192; 382-384, 385-386, 387; 388-390, 391-392, 393; 394-396, 397-398, 399; 400-402, 403-404, 405; 406-408, 409-410, 411; 412-414, 415-416, 417; 418-420, 421-422, 423; 424-426, 427-428, 429; 430-432, 433-434, 435; 436-438, 439-440, 441; 442-444, 445-446, 447; 448-450, 451-452, 453; 454-456, 457-458, 459; 460-462, 463-464, 465; 466-468, 469-470, 471; 472-474, 475-476, 477; 478-480, 481-482, 483; 484-486, 487-488, 489; 490-492, 493-494, 495; 496-498, 499-500, 501; 502-504, 505-506, 507 или 508-510, 511-512, 513; и вариабельный домен легкой цепи, содержащий, соответственно, аминокислотные последовательности CDRL1, CDRL2 и CDRL3, выбранные из одной из SEQ ID NO: 193, 194, 195; 196, 197, 198; 199, 200, 201; 202, 203, 204; 205, 206, 207; 208, 209, 210; 211, 212, 213; 214, 215, 216; 217, 218, 219; 220, 221, 222; 223, 224, 225; 226, 227, 228; 229, 230, 231; 232, 233, 234; 235, 236, 237; 238, 239, 240; 241, 242, 243; 244, 245, 246; 247, 248, 249; 250, 251, 252; 253, 254, 255; 256, 257, 258; 259, 260, 261; 262, 263, 264; 514, 515, 516; 517, 518, 519; 520, 521, 522; 523, 524, 525; 526, 527, 528; 529, 530, 531; 532, 533, 534; 535, 536, 537; 538, 539, 540; 541, 542, 543; 544, 545, 546; 547, 548, 549; 550, 551, 552; 553, 554, 555; 556, 557, 558; 559, 560, 561; 562, 563, 564; 565, 566, 567; 568, 569, 570; 571, 572, 573; 574, 575, 576 и 577, 578, 579.
В некоторых вариантах осуществления антигенсвязывающая молекула содержит аминокислотные последовательности CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3 соответственно, выбранные из одной из SEQ ID NO 49-51, 52-53, 54, 193, 194, 195; 55-57, 58-59, 60, 196, 197, 198; 61-63, 64-65, 66, 199, 200, 201; 67-69, 70-71, 72, 202, 203, 204; 73-75, 76-77, 78, 205, 206, 207; 79-81, 82-83, 84, 208, 209, 210; 85-87, 88-89, 90, 211, 212, 213; 91-93, 94-95, 96, 214, 215, 216; 97-99, 100-101, 102, 217, 218, 219; 103-105, 106-107, 108, 220, 221, 222; 109-111, 112-113, 114, 223, 224, 225; 115-117, 118-119, 120, 226, 227, 228; 121-123, 124-125, 126, 229, 230, 231; 127-129, 130-131, 132, 232, 233, 234; 133-135, 136-137, 138, 235, 236, 237; 139-141, 142-143, 144, 238, 239, 240; 145-147, 148-149, 150, 241, 242, 243; 151-153, 154-155, 156, 244, 245, 246; 157-159, 160-161, 162, 247, 248, 249; 163-165, 166-167, 168, 250, 251, 252; 169-171, 172-173, 174, 253, 254, 255; 175-177, 178-179, 180, 256, 257, 258; 181-183, 184-185, 186, 259, 260, 261; 187-189, 190-191, 192, 262, 263, 264; 382-384, 385-386, 387, 514, 515, 516; 388-390, 391-392, 393, 517, 518, 519; 394-396, 397-398, 399, 520, 521, 522; 400-402, 403-404, 405, 523, 524, 525; 406-408, 409-410, 411, 526, 527, 528; 412-414, 415-416, 417, 529, 530, 531; 418-420, 421-422, 423, 532, 533, 534; 424-426, 427-428, 429, 535, 536, 537; 430-432, 433-434, 435, 538, 539, 540; 436-438, 439-440, 441, 541, 542, 543; 442-444, 445-446, 447, 544, 545, 546; 448-450, 451-452, 453, 547, 548, 549; 454-456, 457-458, 459, 550, 551, 552; 460-462, 463-464, 465, 553, 554, 555; 466-468, 469-470, 471, 556, 557, 558; 472-474, 475-476, 477, 559, 560, 561; 478-480, 481-482, 483, 562, 563, 564; 484-486, 487-488, 489, 565, 566, 567; 490-492, 493-494, 495, 568, 569, 570; 496-498, 499-500, 501, 571, 572, 573; 502-504, 505-506, 507, 574, 575, 576 и 508-510, 511-512, 513, 577, 578, 579.
В некоторых вариантах осуществления антигенсвязывающая молекула содержит вариабельный домен легкой цепи, содержащий аминокислотные последовательности CDRH1, CDRH2 и CDRH3 соответственно, выбранные из одной из SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 338, 340, 342, 344, 346, 348, 350, 352, 354, 356, 358, 360, 362, 364, 366, 368, 370, 372, 374, 376, 378 и 380; и вариабельный домен тяжелой цепи, содержащий аминокислотные последовательности CDRL1, CDRL2 и CDRL3 соответственно, выбранные из одной из SEQ ID NO: 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38, 40, 42, 44, 46, 48, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379 и 381.
В некоторых вариантах осуществления антигенсвязывающая молекула содержит аминокислотные последовательности вариабельного домена легкой цепи и вариабельного домена тяжелой цепи соответственно, выбранные из одной из SEQ ID NO: 1 и 2; 3 и 4; 5 и 6; 7 и 8; 9 и 10; 11 и 12; 13 и 14; 15 и 16; 17 и 18; 19 и 20; 21 и 22; 23 и 24; 25 и 26; 27 и 28; 29 и 30; 31 и 32; 33 и 34; 35 и 36; 37 и 38; 39 и 40; 41 и 42; 43 и 44; 45 и 46; 47 и 48; 338 и 339; 340 и 341; 342 и 343; 344 и 345; 346 и 347; 348 и 349; 350 и 351; 352 и 353; 354 и 355; 356 и 357; 358 и 359; 360 и 361; 362 и 363; 364 и 365; 366 и 367; 368 и 369; 370 и 371; 372 и 373; 374 и 375; 376 и 377; 378 и 379 и 380 и 381.
В другом аспекте настоящего изобретения представлены антитела, которые специфически связываются с кластером дифференцировки 70 (CD70).
В некоторых вариантах осуществления антитело содержит область VH, представленную под SEQ ID NO: 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38, 40, 42, 44, 46, 48, 339, 341, 343, 345, 347, 349, 351, 353, 355, 662, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379 или 381; и/или область VL, представленную под SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 338, 340, 342, 344, 346, 348, 350, 352, 354, 661, 356, 358, 360, 362, 364, 366, 368, 370, 372, 374, 376, 378 или 380.
В некоторых вариантах осуществления антитело содержит вариабельную область тяжелой цепи (VH), содержащую (i) CDR1 VH, содержащую последовательность, представленную под SEQ ID NO: 49, 50, 51, 55, 56, 57, 61, 62, 63, 67, 68, 69, 73, 74, 75, 79, 80, 81, 85, 86, 87, 91, 92, 93, 97, 98, 99, 103, 104, 105, 109, 110, 111, 115, 116, 117, 121, 122, 123, 127, 128, 129, 133, 134, 135, 139, 140, 141, 145, 146, 147, 151, 152, 153, 157, 158, 159, 163, 164, 165, 169, 170, 171, 175, 176, 177, 181, 182, 183, 187, 188, 189, 382, 383, 384, 388, 389, 390, 394, 395, 396, 400, 401, 402, 406, 407, 408, 412, 413, 414, 418, 419, 420, 424, 425, 426, 430, 431, 432, 663, 664, 665, 436, 437, 438, 442, 443, 444, 448, 449, 450, 454, 455, 456, 460, 461, 462, 466, 467, 468, 472, 473, 474, 478, 479, 480, 484, 485, 486, 490, 491, 492, 496, 497, 498, 502, 503, 504, 508, 509 или 510; (ii) CDR2 VH, содержащую последовательность, представленную под SEQ ID NO: 52, 53, 58, 59, 64, 65, 70, 71, 76, 77, 82, 83, 88, 89, 94, 95, 100, 101, 106, 107, 112, 113, 118, 119, 124, 125, 130, 131, 136, 137, 142, 143, 148, 149, 154, 155, 160, 161, 166, 167, 172, 173, 178, 179, 184, 185, 190, 191, 385, 386, 391, 392, 397, 398, 403, 404, 409, 410, 415, 416, 421, 422, 427, 428, 433, 434, 666, 667, 439, 440, 445, 446, 451, 452, 457, 458, 463, 464, 469, 470, 475, 476, 481, 482, 487, 488, 493, 494, 499, 500, 505, 506, 511 или 512; и iii) CDR3 VH, содержащую последовательность, представленную под SEQ ID NO: 54, 60, 66, 72, 78, 84, 90, 96, 102, 108, 114, 120, 126, 132, 138, 144, 150, 156, 162, 168, 174, 180, 186, 192, 387, 393, 399, 405, 411, 417, 423, 429, 435, 668, 441, 447, 453, 459, 465, 471, 477, 483, 489, 495, 501, 507 или 513; и/или вариабельную область легкой цепи (VL), содержащую (i) CDR1 VL, содержащую последовательность, представленную под SEQ ID NO: 193, 196, 199, 202, 205, 208, 211, 214, 217, 220, 223, 226, 229, 232, 235, 238, 241, 244, 247, 250, 253, 256, 259, 262, 514, 517, 520, 523, 526, 529, 532, 535, 538, 669, 541, 544, 547, 550, 553, 556, 559, 562, 565, 568, 571, 574 или 577; (ii) CDR2 VL, содержащую последовательность, представленную под SEQ ID NO: 194, 197, 200, 203, 206, 209, 212, 215, 218, 221, 224, 227, 230, 233, 236, 239, 242, 245, 248, 251, 254, 257, 260, 263, 515, 518, 521, 524, 527, 530, 533, 536, 539, 670, 542, 545, 548, 551, 554, 557, 560, 563, 566, 569, 572, 575 или 578; и (iii) CDR3 VL, содержащую последовательность, представленную под SEQ ID NO: 195, 198, 201, 204, 207, 210, 213, 216, 219, 222, 225, 228, 231, 234, 237, 240, 243, 246, 249, 252, 255, 258, 261, 264, 516, 519, 522, 525, 528, 531, 534, 537, 540, 671, 543, 546, 549, 552, 555, 558, 561, 564, 567, 570, 573, 576 или 579.
В некоторых вариантах осуществления антитело содержит область VH, содержащую CDR1 VH, CDR2 VH и CDR3 VH из последовательности VH, представленной под SEQ ID NO: 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38, 40, 42, 44, 46, 48, 339, 341, 343, 345, 347, 349, 351, 353, 355, 662, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379 или 381; и/или область VL, содержащую CDR1 VL, CDR2 VL и CDR3 VL из последовательности VL, представленной под SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 338, 340, 342, 344, 346, 348, 350, 352, 354, 661, 356, 358, 360, 362, 364, 366, 368, 370, 372, 374, 376, 378 или 380.
В дополнительных аспектах настоящего изобретения представлены нуклеиновые кислоты, векторы, клетки-хозяева, фармацевтические композиции, способы получения и способ лечения состояний с помощью раскрытых антител.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На фиг. 1 показан график, отображающий объемы опухолей у мышей, которых обрабатывали 4F11 CAR-Т-клетками в разных дозах в модели подкожного ксенотрансплантата.
На фиг. 2 показан график, отображающий показатели веса тела мышей, которых обрабатывали 4F11 CAR-Т-клетками в разных дозах в модели подкожного ксенотрансплантата.
На фиг. 3 показан график, отображающий объемы опухолей у мышей, которых обрабатывали с помощью 4F11- и P08F08 CAR-T-клетки с KO по CD70 или без него, в модели подкожного ксенотрансплантата.
На фиг. 4 представлен график, отображающий показатели веса тела у мышей, которых обрабатывали с помощью 4F11- и P08F08 CAR-T-клетки с KO по CD70 или без него, в модели подкожного ксенотрансплантата.
На фиг. 5A - 5C представлен ряд графиков, отображающих значения потока опухолевых клеток у мышей, получавших контрольные клетки, клеток, экспрессирующих 4F11 CAR, с KO по CD70 или без него и с KO по TCRa или без него, и мышей, получавших клетки, экспрессирующие P08F08 CAR, с KO по CD70 или без него и с KO по TCRa или без него, у 3 доноров в модели ACHN с легочными метастазами.
На фиг. 5А показаны результаты, полученные при использовании контрольных клеток, клеток, экспрессирующих 4F11 CAR, с CD70, TCRa или как с KO по CD70, так и с KO по TCR, и клеток, экспрессирующих P08F08 CAR, с KO по TCR; при этом клетки были получены от донора D419.
На фиг. 5В показаны результаты, полученные при использовании контрольных клеток, клеток, экспрессирующих 4F11 CAR, c KO по CD70 или без него, и клеток, экспрессирующих P08F08 CAR; при этом клетки были получены от донора D710.
На фиг. 5С показаны результаты, полученные при использовании контрольных клеток, клеток, экспрессирующих 4F11 CAR, c KO по CD70 или без него, и клеток, экспрессирующих P08F08 CAR; при этом клетки были получены от донора D503.
На фиг. 6A - 6F показаны пять иллюстративных неограничивающих конструкций на основе CAR. На каждой из фиг. 6A - 6F примерное расстояние от антигенсвязывающего фрагмента домена, специфического к CD70, до клеточной мембраны показано двойной стрелкой, обозначенной числом аминокислотных остатков (аа) между scFv и трансмембранным доменом.
На фиг. 6А показана конструкция на основе CAR второго поколения, включающая внеклеточный домен, содержащий scFv, специфический к CD70, шарнирный участок, трансмембранный домен, первый внутриклеточный домен (домен 4-1BB) и второй внутриклеточный домен (сигнальный домен CD3ζ).
На фиг. 6B показан формат SR2 CAR, в котором «суицидный» переключатель создан путем вставки двух эпитопов RTX (т. Е. эпитопов CD20) между шарнирным участком и scFv.
На фиг. 6C показан формат RSRQR CAR, в котором добавлен третий эпитоп RTX и эпитоп CD34.
На фиг. 6D показан формат RSR, в котором два эпитопа RTX фланкируют scFv.
На фиг. 6E показана модификация формата RSR CAR, в которой шарнирный домен укорочен (называется RSR-short).
На фиг. 6F показан формат R2S CAR, в котором два эпитопа RTX формата R2 CAR перемещены на N-конец scFv.
На фиг. 7 показана жизнеспособность клеток-мишеней после воздействия CAR, специфических к CD70, в четырех форматах или нетрансдуцированных (NTD) контрольных клеток.
На фиг. 8A - 8D представлена серия графиков, показывающих уничтожение клеток 786-0, ACHN или REH при использовании CAR-Т-клеток, специфических к CD70, где внеклеточный домен CAR содержит scFv, указанные в пояснениях на фиг. 8D.
На фиг. 8A показано уничтожение клеток 786-0, где внеклеточный домен CAR содержит scFv, указанные в пояснениях на фиг. 8D.
На фиг. 8В показано уничтожение клеток ACHN, где внеклеточный домен CAR содержит scFv, указанные в пояснениях на фиг. 8D.
На фиг. 8С показано уничтожение клеток REH, где внеклеточный домен CAR содержит scFv, указанные в пояснениях на фиг. 8D.
На фиг. 9A - 9D представлены серии графиков, показывающих последовательное уничтожение клеток 786-0, ACHN или REH при использовании CAR-Т-клеток, специфических к CD70, где внеклеточный домен CAR содержит scFv, указанные в пояснениях на фиг. 9D.
На фиг. 9A представлен график, отображающий эффективность CAR, специфических к CD70, при повторном воздействии на меченные люциферазой клетки-мишени 786-O (каждые 2-3 дня CAR-T-клетки переносили в 96-луночный планшет, содержащий свежие мишени). Соотношение E:T составляло 3:1. CAR экспрессировали в клетках от донора D503.
На фиг. 9В представлен график, отображающий эффективность CAR, специфических к CD70, при повторном воздействии на меченные люциферазой клетки-мишени ACHN (каждые 2-3 дня CAR-T-клетки переносили в 96-луночный планшет, содержащий свежие мишени). Соотношение E:T составляло 10:1. CAR экспрессировали в клетках от донора D503.
На фиг. 9С представлен график, отображающий эффективность CAR, специфических к CD70, при повторном воздействии на клетки-мишени REH, меченные люциферазой (2×106 клеток добавили в указанные моменты времени). Соотношение E:T составляло 1:5. CAR экспрессировали в клетках от донора D503.
На фиг. 10 представлен ряд графиков, показывающих эффективность CAR, специфических к CD70, в формате R2S, SR2 или RSRQR при многократном воздействии на клетки-мишени REH, меченные люциферазой (2×106 клеток добавили в указанные моменты времени). Соотношение E:T составляло 1:5. CAR экспрессировали в клетках от донора D772.
На фиг. 11 представлен график, показывающий значения потока опухолевых клеток у мышей, получавших контрольные клетки или клетки, экспрессирующие различные scFv CAR в модели ACHN с легочными метастазами.
На фиг. 12A - 12C представлен ряд графиков, отображающих количественную оценку экспрессии CD70 в контексте связывающей способности антитела (ABC) к CD70 на различных исследуемых клеточных линиях или клеточных линиях и клетках, полученных от пациентов с RCC. Также показаны данные по клеткам, полученным от пациентов с RCC.
На фиг. 12A показана количественная оценка экспрессии CD70 в контексте связывающей способности антитела (ABC) к CD70 на различных исследуемых клеточных линиях.
На фиг. 12B показана количественная оценка экспрессии CD70 в контексте связывающей способности антитела (ABC) к CD70 на клетках, полученных от пациентов с RCC.
На фиг. 12С показаны данные по клеткам, полученным от пациентов с RCC.
На фиг. 13A - 13C представлен ряд графиков, отображающих уничтожение клеток-мишеней от пациента WD-59279 с RCC, клеточных линий, полученных от пациентов, или ACHN, при этом связывающая способность антител указана на каждой панели.
На фиг. 13A - B показано уничтожение клеток-мишеней от пациентов с RCC и связывающая способность антител.
На фиг. 13C показано уничтожение клеток-мишеней ACHN и связывающая способность антител.
На фиг. 14A - 14B представлен ряд гистограмм, показывающих количественную оценку числа рецепторов CD70 и уничтожение гемовых опухолевых клеток с помощью 4F11 CAR в формате QR3 при 1:1 E:T для дополнительных линий клеток, экспрессирующих CD70 на различных уровнях.
На фиг. 14A представлена гистограмма, отображающая количественную оценку числа рецепторов CD70 у CAR 4F11 в формате QR3 при E:T 1:1 для дополнительных линий клеток, экспрессирующих CD70 на различных уровнях.
На фиг. 14B представлена гистограмма, отображающая уничтожение гемовых опухолевых клеток с помощью CAR 4F11 в формате QR3 при 1:1 E:T для дополнительных линий клеток, экспрессирующих CD70 на различных уровнях.
На фиг. 15А - 15В представлен ряд графиков, отображающих показатели объема опухоли и веса тела у мышей, которых обрабатывали с помощью 4F11- и P08F08-CAR-T-клетки в дозе 10×106 клеток или 5×106 клеток, в модели подкожного ксенотрансплантата.
На фиг. 15А представлен график, отображающий показатели объема опухоли у мышей, которых обрабатывали с помощью 4F11- и P08F08-CAR-T-клетки в дозе 10×106 клеток или 5×106 клеток, в модели подкожного ксенотрансплантата.
На фиг. 15В представлен график, отображающий показатели веса тела у мышей, которых обрабатывали с помощью 4F11- и P08F08-CAR-T-клетки в дозе 10×106 клеток или 5×106 клеток, в модели подкожного ксенотрансплантата.
ПОДРОБНОЕ ОПИСАНИЕ
В описании, раскрытом в данном документе, представлены химерные антигенные рецепторы (CAR) и иммунные клетки, содержащие CAR (например, CAR-T-клетки), которые специфически связываются с CD70 (например, CD70 человека). В описании также представлены полинуклеотиды, кодирующие такие CAR, композиции, содержащие эти CAR-T-клетки, а также способы получения и применения этих CAR и CAR-T-клеток. В описании также представлены способы лечения у субъекта состояния, ассоциированного со злокачественными клетками, экспрессирующими CD70, например при раке.
Общие методики
В композициях и способах по настоящему изобретению, если не указано иное, будут использоваться традиционные методики молекулярной биологии (в том числе рекомбинантные методики), микробиологии, клеточной биологии, биохимии и иммунологии, которые находятся в пределах компетенции специалиста в данной области техники. Такие методики в полном объеме объяснены в литературе, такой как Molecular Cloning: A Laboratory Manual, second edition (Sambrook et al., 1989) Cold Spring Harbor Press; Oligonucleotide Synthesis (M.J. Gait, ed., 1984); Methods in Molecular Biology, Humana Press; Cell Biology: A Laboratory Notebook (J.E. Cellis, ed., 1998) Academic Press; Animal Cell Culture (R.I. Freshney, ed., 1987); Introduction to Cell and Tissue Culture (J.P. Mather and P.E. Roberts, 1998) Plenum Press; Cell and Tissue Culture: Laboratory Procedures (A. Doyle, J.B. Griffiths, and D.G. Newell, eds., 1993-1998) J. Wiley and Sons; Methods in Enzymology (Academic Press, Inc.); Handbook of Experimental Immunology (D.M. Weir and C.C. Blackwell, eds.); Gene Transfer Vectors for Mammalian Cells (J.M. Miller and M.P. Calos, eds., 1987); Current Protocols in Molecular Biology (F.M. Ausubel et al., eds., 1987); PCR: The Polymerase Chain Reaction, (Mullis et al., eds., 1994); Current Protocols in Immunology (J.E. Coligan et al., eds., 1991); Short Protocols in Molecular Biology (Wiley and Sons, 1999); Immunobiology (C.A. Janeway and P. Travers, 1997); Antibodies (P. Finch, 1997); Antibodies: a practical approach (D. Catty., ed., IRL Press, 1988-1989); Monoclonal antibodies: a practical approach (P. Shepherd and C. Dean, eds., Oxford University Press, 2000); Using antibodies: a laboratory manual (E. Harlow and D. Lane (Cold Spring Harbor Laboratory Press, 1999); The Antibodies (M. Zanetti and J.D. Capra, eds., Harwood Academic Publishers, 1995).
Определения
Используемый в данном документе термин «внеклеточный лиганд-связывающий домен» относится к олиго- или полипептиду, который способен связывать лиганд. В некоторых иллюстративных вариантах осуществления домен будет способен взаимодействовать с молекулой клеточной поверхности. Например, внеклеточный лиганд-связывающий домен может быть выбран для распознавания лиганда, который действует в качестве маркера клеточной поверхности на клетках-мишенях, ассоциированных с конкретным патологическим состоянием.
Термин «стеблевой домен» или «шарнирный домен» используются в данном документе взаимозаменяемо для обозначения любого олиго- или полипептида, который функционирует для связывания трансмембранного домена с внеклеточным лиганд-связывающим доменом в CAR. В частности, домены «стебля» используются для придания большей гибкости и доступности внеклеточному лиганд-связывающему домену.
Термин «внутриклеточный сигнальный домен» относится к части белка, которая трансдуцирует сигнал эффекторной сигнальной функции и направляет клетку на выполнение специализированной функции.
Термин «костимулирующая молекула» в контексте настоящего изобретения относится к родственному партнеру по связыванию на иммунной клетке, например, Т-клетке, которая специфически связывается с костимулирующим лигандом, за счет чего опосредуется костимулирующий ответ клетки, например, без ограничения пролиферация. Костимулирующие молекулы включают без ограничения молекулу MHC класса I, BTLA и рецептор лиганда Toll. Примеры костимулирующих молекул включают CD27, CD28, CD8, 4-1BB (CD137), OX40, CD30, CD40, PD-1, ICOS, антиген-1, ассоциированный с функцией лимфоцитов (LFA-1), CD2, CD7, LIGHT, NKG2C, B7-H3 и лиганд, который специфически связывается с CD83 и т. п.
«Костимулирующий лиганд» относится к молекуле на антигенпрезентирующей клетке, которая специфически связывает родственную молекулу костимулирующего сигнала на иммунной клетке, например, Т-клетке, за счет чего обеспечивается сигнал, который в дополнение к первичному сигналу обеспечивается, к примеру, путем связывания комплекса TCR/CD3 с молекулой MHC, нагруженной пептидом, опосредует Т-клеточный ответ, в том числе без ограничения активацию пролиферации, дифференцировку и т. п. Костимулирующий лиганд может включать без ограничения CD7, B7-1 (CD80), B7-2 (CD86), PD-L1, PD-L2, 4-1BBL, OX40L, индуцируемый костимулирующий лиганд (ICOS-L), молекулу межклеточной адгезии (ICAM, CD30L, CD40, CD70, CD83, HLA-G, MICA, M1CB, HVEM, рецептор β-лимфотоксина, 3/TR6, ILT3, ILT4, агонист или антитело, которое связывает лиганд Toll-подобного рецептора, и лиганд, который специфически связывается с B7-H3. Костимулирующий лиганд также охватывает среди прочего антитело, которое специфически связывается с костимулирующей молекулой, присутствующей на Т-клетке, например, без ограничения CD27, CD28, 4-1BB, OX40, CD30, CD40, PD-1, ICOS, антиген-1, ассоциированный с функцией лимфоцитов (LFA-1), CD2, CD7, LTGHT, NKG2C, B7-H3, лиганд, который специфически связывается с CD83.
«Антитело» представляет собой молекулу иммуноглобулина, способную специфически связываться с мишенью, такой как углевод, полинуклеотид, липид, полипептид и т. д., посредством по меньшей мере одного антигенраспознающего участка, расположенного в вариабельной области молекулы иммуноглобулина. Используемый в данном документе термин охватывает не только интактные поликлональные или моноклональные антитела, но также и фрагменты (такие как Fab, Fab’, F(ab’)2, Fv), одноцепочечные (scFv) и доменные антитела (в том числе, например, антитела акул и верблюдовых), и слитые белки, содержащие антитело и любую другую модифицированную конфигурацию молекулы иммуноглобулина, которая содержит антигенраспознающий участок. Антитело включает антитело любого класса, как, например, IgG, IgA, IgE, IgD или IgM (или их подкласса), и при этом антитело необязательно должно относиться к какому-либо конкретному классу. В зависимости от аминокислотной последовательности антитела константной области его тяжелых цепей иммуноглобулины могут относиться к разным классам. Существует пять основных классов иммуноглобулинов: IgA, IgD, IgE, IgG и IgM, при этом некоторые из них могут дополнительно подразделяться на подклассы (изотипы), например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2. Константные области тяжелой цепи, которые соответствуют различным классам иммуноглобулинов, соответственно, называются альфа, дельта, эпсилон, гамма и мю. Хорошо известны структуры субъединиц и трехмерные конфигурации различных классов иммуноглобулинов.
Термины «антигенсвязывающий фрагмент» или «антигенсвязывающая часть» антитела, используемые в данном документе, относятся к одному или более фрагментам интактного антитела, которые сохраняют способность к специфическому связыванию с указанным антигеном (например, CD70). Антигенсвязывающие функции антитела могут выполняться фрагментами интактного антитела. Примеры связывающих фрагментов, охваченных термином «антигенсвязывающий фрагмент антитела», включают Fab; Fab’; F(ab’)2; Fd-фрагмент, состоящий из доменов VH и СН1; Fv-фрагмент, состоящий из доменов VL и VH одного плеча антитела, однодоменный (dAb) фрагмент (Ward et al., Nature 341:544-546, 1989) и выделенную область, определяющую комплементарность (CDR).
Антитело, антигенсвязывающий фрагмент, конъюгат на основе антитела или полипептид, который «предпочтительно связывается» или «специфически связывается» (используется взаимозаменяемо в данном документе) с мишенью (например, белком CD70) является термином, хорошо известным в данной области техники, и способы определения такого специфического или предпочтительного связывания также хорошо известны в данной области техники. Считается, что молекула демонстрирует «специфическое связывание» или «преимущественное связывание», если она вступает в реакцию или соединяется чаще, быстрее, с большей продолжительностью и/или с большей аффинностью с конкретной клеткой или веществом, чем с альтернативными клетками или веществами. Антитело «специфически связывается» или «преимущественно связывается» с мишенью, если оно связывается с большей аффинностью, авидностью, более легко и/или с большей продолжительностью, чем оно связывается с другими веществами. Например, антитело, которое специфически или преимущественно связывается с эпитопом CD70, представляет собой антитело, которое связывается с этим эпитопом с большей аффинностью, авидностью, более легко и/или с большей продолжительностью, чем оно связывается с другими эпитопами CD70 или эпитопами, не являющимися CD70. Также при ознакомлении с этим определением следует понимать, что, например, антитело (или частица, или эпитоп), которое специфически или преимущественно связывается с первой мишенью, может либо связываться, либо не связываться специфическим или предпочтительным образом со второй мишенью. Таким образом, «специфическое связывание» или «предпочтительное связывание» необязательно требует (хотя оно может включать) исключительное связывание. В целом, но не обязательно, ссылка на связывание означает преимущественное связывание.
«Вариабельная область» антитела относится к вариабельной области легкой цепи антитела или вариабельной области тяжелой цепи антитела либо отдельно, либо в комбинации. Как известно из уровня техники, каждая вариабельная область тяжелой и легкой цепей состоит из четырех каркасных областей (FR), соединенных тремя областями определяющими комплементарность (CDR), также известными как гипервариабельные области. CDR в каждой цепи удерживаются вместе в непосредственной близости с помощью FR и CDR из другой цепи, участвуя в образовании антигенсвязывающего участка антител. Существуют по меньшей мере две методики определения CDR: (1) подход, основанный на межвидовой вариабельности последовательностей (т. e. Kabat et al. Sequences of Proteins of Immunological Interest, (5th ed., 1991, National Institutes of Health, Bethesda Md.)); и (2) подход, основанный на кристаллографических исследованиях комплексов антиген-антитело (Al-lazikani et al. (1997) J. Molec. Biol. 273:927-948). Используемая в данном документе CDR может относиться к таким CDR, которые определяют либо с помощью любого из подходов, либо с помощью комбинации обоих подходов.
«CDR» вариабельного домена представляют собой аминокислотные остатки в пределах вариабельной области, которые идентифицируют в соответствии с суммированием определений согласно Кабату, Чотиа, суммированием определением как согласно Кабату, так и согласно Чотиа, AbM, контактными и/или конформационными определениями или в соответствии с любой методикой определения CDR, хорошо известных из уровня техники. CDR антитела можно идентифицировать как гипервариабельные области, первоначально определенные Kabat et al. См., например, Кабат et al., 1992, Sequences of Proteins of Immunological Interest, 5th ed., Public Health Service, NIH, Washington D.C. Положения CDR можно также идентифицировать как структурные петлевые структуры, первоначально описанные Чотиа и др. См., например, Чотиа et al., Nature 342:877-883, 1989. Другие подходы к идентификации CDR включают «определение AbM», которое представляет собой оптимальное сочетание Кабат и Чотиа и получены с использованием программного обеспечения для построения моделей антител AbM Oxford Molecular (в настоящее время Accelrys®), или «определение контакта» CDR на основе наблюдаемых контактов с антигенами, как это изложено в MacCallum et al., J. Mol. Biol., 262:732-745, 1996. При другом подходе, называемом в данном документе как «определение конформационного положения» CDR, положения CDR можно идентифицировать как остатки, которые создают энтальпийные вклады в связывание антигена. См., например, Makabe et al., Journal of Biological Chemistry, 283:1156-1166, 2008. Тем не менее, другие определения границ CDR могут не строго следовать одному из вышеприведенных подходов, однако тем не менее будут перекрываться с по меньшей мере частью CDR согласно Кабату, хотя они могут быть сокращены или удлинены в свете прогнозирования или экспериментальных данных о том, что конкретные остатки или группы остатков или даже целые CDR не оказывают значительного влияния на связывание антигена. Используемая в данном документе CDR может относиться к таким CDR, которые определяются любым подходом, известным в данной области техники, включая комбинации подходов. В способах, применяемых в данном документе, можно использовать CDR, определенные в соответствии с любым из этих подходов. Для любого данного варианта осуществления, предусматривающего более одной CDR, CDR можно определить в соответствии с любым из определений по Кабату, Чотиа, расширенного, AbM, контактного и/или конформационного определения.
Используемый в данном документе термин «моноклональное антитело» относится к антителу, полученному из популяции фактически однородных антител, т. е. отдельные антитела, составляющие популяцию, являются идентичными за исключением возможных встречающихся в природе мутаций, которые могут присутствовать в незначительных количествах. Моноклональные антитела являются высокоспецифическими, направленными против одного антигенного участка. Кроме того, в отличие от препаратов на основе поликлонального антитела, которые обычно содержат разные антитела, направленные против разных детерминантов (эпитопов), каждое моноклональное антитело направлено на один детерминант на антигене. Определение «моноклональное» указывает на характер антитела, как полученного из фактически однородной популяции антител, и не должен истолковываться как требующий получения антитела любым конкретным способом. Например, моноклональные антитела, подлежащие применению в соответствии с настоящим изобретением, можно получать посредством гибридомного способа, впервые описанного Kohler, Nature 256:495, 1975, или можно получать с помощью способов рекомбинантной ДНК, таких как описанные в патенте США № 4816567. Моноклональные антитела также можно выделять из фаговых библиотек, созданных с применением методик, описанных, например, McCafferty et al., Nature 348:552-554, 1990.
Используемый в данном документе термин «гуманизированное» антитело относится к формам антител, отличных от человеческих (например, к мышиным), которые представляют собой химерные иммуноглобулины, цепи иммуноглобулинов или их фрагменты (такие как Fv, Fab, Fab’, F(ab')2 или другие антигенсвязывающие подпоследовательности антител), которые содержат минимальную последовательность, полученную из иммуноглобулина, отличного от человеческого. В некоторых иллюстративных вариантах осуществления гуманизированные антитела представляют собой человеческие иммуноглобулины (реципиентное антитело), в которых остатки из области, определяющей комплементарность (CDR), реципиента заменены остатками из CDR вида, отличного от человека (донорное антитело), такого как мышь, крыса или кролик, характеризующиеся требуемой специфичностью, аффинностью и активностью. В некоторых случаях остатки каркасной области Fv (FR) человеческого иммуноглобулина замещены соответствующими остатками, отличными от человеческих. Кроме того, гуманизированное антитело может содержать остатки, которые не обнаружены ни в реципиентном антителе, ни во внесенных последовательностях CDR или каркасных областях, однако включены для дополнительного уточнения и оптимизации характеристик антител. В целом гуманизированное антитело будет содержать фактически все из по меньшей мере одного и, как правило, двух вариабельных доменов, в которых все или фактически все области CDR соответствуют тем, которые находятся в иммуноглобулине, отличном от человеческого, и все или фактически все из областей FR являются таковыми в консенсусной последовательности человеческого иммуноглобулина. Оптимально гуманизированное антитело также будет содержать по меньшей мере часть константной области или домена иммуноглобулина (Fc), как правило, человеческого иммуноглобулина. Иллюстративные варианты осуществления представляют собой антитела, имеющие Fc-области, модифицированные так, как это описано в WO 99/58572. Другие формы гуманизированных антител содержат одну или более CDR (CDR L1, CDR L2, CDR L3, CDR H1, CDR H2 или CDR H3), которые изменены по сравнению с исходным антителом, которые также обозначают одну или более CDR, «полученных из» одной или более CDR из исходного антитела.
Используемый в данном документе термин «человеческое антитело» означает антитело, имеющее аминокислотную последовательность, соответствующую последовательности антитела, продуцируемого человеком, и/или которое было получено с помощью любой из методик получения человеческих антител, известных специалистам в данной области техники и раскрытых в данном документе. Это определение человеческого антитела включает антитела, содержащие по меньшей мере один полипептид тяжелой цепи человека или по меньшей мере один полипептид легкой цепи человека. Одним из таких примеров является антитело, содержащее полипептиды легкой цепи мыши и тяжелой цепи человека. Человеческие антитела можно получать с помощью различных методик, известных из уровня техники. В некоторых вариантах осуществления человеческое антитело выбрано из фаговой библиотеки, где в фаговой библиотеке экспрессируются человеческие антитела (Vaughan et al., Nature Biotechnology, 14:309-314, 1996; Sheets et al., Proc. Natl. Acad. Sci. (USA) 95:6157-6162, 1998; Hoogenboom and Winter, J. Mol. Biol., 227:381, 1991; Marks et al., J. Mol. Biol., 222:581, 1991). Человеческие антитела также можно получать путем иммунизации животных, которым трансгенно вводили локусы человеческого иммуноглобулина вместо эндогенных локусов, например, мышей, у которых гены эндогенного иммуноглобулина были частично или полностью разрушены или инактивированы. Этот подход описан в патентах США №№ 5545807; 5545806; 5569825; 5625126; 5633425 и 5661016. Альтернативно человеческое антитело можно получать путем иммортализации человеческих В-лимфоцитов, которые продуцируют антитело, направленное против целевого антигена (такие В-лимфоциты можно выделить у субъекта или можно иммунизировать in vitro). См., например, Cole et al. Monoclonal Antibodies and Cancer Therapy, Alan R. Liss, p. 77, 1985; Boerner et al., J. Immunol., 147 (1):86-95, 1991 и патент США № 5750373.
Термин «химерное антитело» предназначен для обозначения антител, в которых последовательности вариабельной области получены от одного вида, а последовательности константной области получены от других видов, как, например, антитело, в котором последовательности вариабельной области получены из антитела мыши, а последовательности константной области получены из человеческого антитела.
Термины «полипептид», «олигопептид», «пептид» и «белок» используются в данном документе взаимозаменяемо для обозначения цепей аминокислот любой длины - в некоторых вариантах относительно короткие (например, 10-100 аминокислот). Цепь может быть линейной или разветвленной, она может содержать модифицированные аминокислоты и/или может прерываться кислотами, не относящимися к аминокислотам. Термины также охватывают аминокислотную цепь, которая была модифицирована естественным образом или путем вмешательства; например, путем образования дисульфидной связи, гликозилирования, липидизации, ацетилирования, фосфорилирования или любой другой манипуляции или модификации, такой как конъюгация с метящим компонентом. Также в определение включены, например, полипептиды, содержащие один или более аналогов аминокислот (включая, например, аминокислоты неприродного происхождения и т. д.), а также другие модификации, известные из в данной области техники. Понятно, что полипептиды могут встречаться в виде отдельных цепей или ассоциированных цепей.
«Моновалентное антитело» содержит один антигенсвязывающий участок на молекулу (например, IgG или Fab). В некоторых случаях моновалентное антитело может содержать более одного антигенсвязывающего участка, но участки связывания из разных антигенов.
«Бивалентное антитело» содержит два антигенсвязывающих участка на молекулу (например, IgG). В некоторых случаях два связывающих участка характеризуются одинаковыми видами специфичности в отношении антигена. Однако бивалентные антитела могут быть биспецифическими.
Антитела по настоящему изобретению можно получать с применением методик, хорошо известных из уровня техники, например, рекомбинантных технологий, технологий фагового дисплея, синтетических технологий или комбинаций таких технологий или других технологий, хорошо известных из уровня техники (см., например, Jayasena, S.D., Clin. Chem., 45: 1628-50, 1999 и Fellouse, F.A., et al, J. MoI. Biol., 373(4): 924-40, 2007).
В данной области техники известно, что термины «полинуклеотид» или «нуклеиновая кислота», используемые в данном документе взаимозаменяемо, относятся к цепям нуклеотидов любой длины и включают ДНК и РНК. Нуклеотиды могут представлять собой дезоксирибонуклеотиды, рибонуклеотиды, модифицированные нуклеотиды или основания и/или их аналоги, или любую подложку, которая может быть встроена в цепь с помощью ДНК- или РНК-полимеразы. Полинуклеотид может содержать модифицированные нуклеотиды, такие как метилированные нуклеотиды и их аналоги. Модификацию нуклеотидной структуре, при ее наличии, можно придать до или после сборки цепи. Последовательность нуклеотидов может прерываться компонентами, не являющимися нуклеотидами. Полинуклеотид можно дополнительно модифицировать после полимеризации, например, путем конъюгации с метящим компонентом. Другие типы модификаций включают, например, «кэпы», замену одного или более встречающихся в природе нуклеотидов на аналог, межнуклеотидные модификации, такие как, например, модификации с незаряженными связями (например, метилфосфонаты, сложные фосфотриэфиры, фосфоамидаты, карбаматы и т. д.) и с заряженными связями (например, фосфоротиоаты, фосфородитиоаты и т. д.), содержащие боковые фрагменты, такие как, например, белки (например, нуклеазы, токсины, антитела, сигнальные пептиды, поли-L-лизин и т. д.), с интеркаляторами (например, акридин, псорален и т. д.), с хелаторами (например, металлы, радиоактивные металлы, бор, окисляющие металлы и т. д.), с алкилаторами, с модифицированными связями (например, альфа-аномерные нуклеиновые кислоты и т. д.), а также немодифицированные формы полинуклеотида (полинуклеотидов). Кроме того, любая из гидроксильных групп, обычно присутствующая в сахарах, может быть замещена, например, фосфонатными группами, фосфатными группами, защищена стандартными защитными группами или активирована с получением дополнительных связей с дополнительными нуклеотидами, или может быть конъюгирована с твердыми подложками. 5’- и 3’-концевой OH может быть фосфорилирован или замещен аминами или органическими фрагментами кэппирующих групп с 1-20 атомами углерода. Другие гидроксилы также можно получать в стандартных защитных группах. Полинуклеотиды также могут содержать аналогичные формы сахаров рибозы или дезоксирибозы, которые в целом известны в данной области техники, в том числе, например, 2’-O-метил-, 2’-O-аллил, 2’-фтор- или 2’-азидорибоза, карбоциклические аналоги сахаров, альфа- или бета-аномерные сахара, эпимерные сахара, такие как арабиноза, ксилозы или ликсозы, пиранозные сахара, фуранозные сахара, седогептулозы, ациклические аналоги и нуклеозидные аналоги с удаленным азотистым основанием, такие как метилрибозид. Одна или более сложных фосфодиэфирных связей могут быть заменены чередующимися связывающими группами. Эти альтернативные связывающие группы включают без ограничения варианты, в которых фосфат заменен P(O)S («тиоатом»), P(S)S («дитиоатом»), (O)NR2 («амидатом»), P(O)R, P(O)OR’, CO или CH2 («формацеталем»), в которых каждый R или R’ независимо представляет собой H или замещенный или незамещенный алкил (C1-20), необязательно содержащий простую эфирную (-O-) связь, арил, алкенил, циклоалкил, циклоалкенил или аралдил. Не все связи в полинуклеотиде должны быть идентичными. Предыдущее описание применимо ко всем полинуклеотидам в данном документе, в том числе к РНК и ДНК.
В данной области техники известно, что «константная область» антитела относится к константной области легкой цепи антитела или константной области тяжелой цепи антитела отдельно или в комбинации.
Используемый в данном документе термин «фактически чистый» относится к материалу, который является чистым на по меньшей мере 50% (т. е. не содержит загрязняющих веществ), чистым на по меньшей мере 90%, чистым на по меньшей мере 95%, чистым на по меньшей мере 98% и чистым на по меньшей мере 99%.
«Клетка-хозяин» включает отдельную клетку или культуру клеток, которые могут являться или являются реципиентом вектора (векторов) для включения полинуклеотидных вставок. Клетки-хозяева включают потомство одной клетки-хозяина, и при этом потомство может необязательно являться полностью идентичным (по морфологии или по комплементарной геномной ДНК) в исходной родительской клетке вследствие естественной, случайной или преднамеренной мутации. Клетка-хозяин включает клетки, трансфицированные in vivo полинуклеотидом (полинуклеотидами) по настоящему изобретению.
Используемый в данном документе термин «иммунная клетка» относится к клетке гемопоэтического происхождения, функционально вовлеченной в инициацию и/или функционирование врожденного и/или адаптивного иммунного ответа.
В данной области техники известно, что термин «Fc-область» используется для определения C-концевой области тяжелой цепи иммуноглобулина. «Fc-область» может представлять собой последовательность с нативной Fc-областью или вариант Fc-области. Хотя границы Fc-области тяжелой цепи иммуноглобулина могут варьироваться, Fc-область IgG тяжелой цепи человека обычно определяется как фрагмент аминокислотного остатка в положении Cys226 или от Pro230 к его карбоксильному концу. Нумерация остатков в Fc-области соответствует таковой согласно индексу EU, как у Кабата. Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, Md., 1991. Fc-область иммуноглобулина, как правило, содержит две константные области - CH2 и CH3.
Используемые в данной области техники термины «Fc-рецептор» и «FcR» описывают рецептор, который связывается с Fc-областью антитела. В некоторых вариантах осуществления FcR представляет собой человеческий FcR с нативной последовательностью. Более того, в некоторых вариантах осуществления FcR является таким, который связывает IgG-антитело (гамма-рецептор) и включает рецепторы подклассов FcγRI, FcγRII, и FcγRIII, в том числе аллельные варианты и подвергнутые альтернативному сплайсингу формы данных рецепторов. Рецепторы FcγRII включают FcγRIIA («активирующий рецептор») и FcγRIIB («ингибирующий рецептор»), которые имеют сходные аминокислотные последовательности, отличающиеся в первую очередь своими цитоплазматическими доменами. FcR рассматриваются в Ravetch and Kinet, Ann. Rev. Immunol., 9:457-92, 1991; Capel et al., Immunomethods, 4:25-34, 1994; и de Haas et al., J. Lab. Clin. Med., 126:330-41, 1995. «FcR» также включает неонатальный рецептор FcRn, который отвечает за передачу материнских иммуноглобулинов плоду (Guyer et al., J. Immunol., 117:587, 1976; и Kim et al., J. Immunol., 24:249, 1994).
Термин «конкуренция», используемый в данном документе в отношении антитела, означает, что первое антитело или его антигенсвязывающий фрагмент (или часть) связывается с эпитопом способом, в значительной степени сходным со связыванием второго антитела или его антигенсвязывающей части, за счет чего результат связывания первого антитела с его когнатным эпитопом заметно уменьшается в присутствии второго антитела по сравнению со связыванием первого антитела в отсутствие второго антитела. Может иметь место альтернатива, где связывание второго антитела с его эпитопом также выявляемо снижается в присутствии первого антитела, но необязательно. То есть первое антитело может подавлять связывание второго антитела с его эпитопом без подавления этим вторым антителом связывания первого антитела с его соответствующим эпитопом. Однако в тех случаях, когда каждое антитело выявляемо подавляет связывание другого антитела с его родственным эпитопом или лигандом, либо в одинаковой, большей либо меньшей степени, антитела считаются «перекрестно конкурирующими» друг с другом для связывания их соответствующего (соответствующих) эпитопа (эпитопов). Настоящее изобретение охватывает как конкурирующие, так и перекрестно конкурирующие антитела. Независимо от механизма, с помощью которого происходит такая конкуренция или перекрестная конкуренция (например, стерическое несоответствие, конформационное изменение или связывание с общим эпитопом или его частью), специалист в данной области техники оценил бы, исходя из представленных в данном документе идей, что такие конкурирующие и/или перекрестно конкурирующие антитела охватываются и могут быть применимы для способов, раскрытых в данном документе.
Используемый в данном документе термин «аутологичный» означает, что клетки, линия клеток или популяция клеток, используемые для лечения пациентов, получены от указанного пациента.
Используемый в данном документе термин «аллогенный» означает, что клетки или популяция клеток, используемые для лечения пациентов, получены не от указанного пациента, а от донора.
Используемый в данном документе термин «лечение» представляет собой подход для получения благоприятных или требуемых клинических результатов. Для целей настоящего изобретения благоприятные или требуемые клинические результаты включают без ограничения одно или более из следующего: уменьшение пролиферации (или уничтожение) неопластических или раковых клеток, подавление метастазирования неопластических клеток, сокращение или уменьшение размера опухоли, экспрессирующей CD70, например, почечно-клеточной карциномы (RCC), лимфомы, лейкоза или глиомы, ремиссия заболевания, ассоциированного с CD70 (например, рака), уменьшение симптомов, возникающих в результате заболевания, ассоциированного с CD70 (например, рака), повышение качества жизни пациентов, страдающих от заболевания, ассоциированного с CD70 (например, рака), уменьшение дозы других лекарственных препаратов, необходимых для лечения заболевания, ассоциированного с CD70 (например, рака), задержка прогрессирования заболевания, ассоциированного с CD70 (например, рака), излечение заболевания, ассоциированного с CD70 (например, рака) и/или продление выживаемости пациентов, имеющих заболевание, ассоциированное с CD70 (например, рак).
«Уменьшение тяжести» означает ослабление или улучшение одного или более симптомов по сравнению с такими симптомами при отсутствии введения CAR, специфического к CD70, или CAR-T-клетки, специфической к CD70. «Уменьшение тяжести» также включает сокращение или уменьшение продолжительности симптома.
Используемые в данном документе термины «эффективная доза» или «эффективное количество» лекарственного средства, соединения, или фармацевтической композиции представляет собой количество, достаточное для достижения любого из одного или более благоприятных или требуемых результатов. В случае профилактического применения благоприятные или требуемые результаты включают устранение или уменьшение риска возникновения, сокращение степени тяжести или отсрочку возникновения заболевания, в том числе биохимических, гистологических и/или поведенческих симптомов заболевания, его осложнений и промежуточных патологических фенотипов, появляющихся в ходе развития заболевания. В случае терапевтического применения благоприятные или требуемые результаты включают клинические результаты, такие как снижение частоты возникновения или уменьшение тяжести одного или более симптомов различных заболеваний или состояний, ассоциированных с CD70 (таких как, например, множественная миелома), снижение дозы других лекарственных препаратов, необходимых для лечения заболевания, усиления эффекта другого лекарственного препарата и/или замедления прогрессирования заболевания, ассоциированного с CD70, у пациентов. Эффективную дозу можно вводить за одно или более введений. Для целей настоящего изобретения эффективная доза лекарственного средства, соединения или фармацевтической композиции представляет собой количество, достаточное для осуществления профилактического или терапевтического лечения непосредственно или опосредствованно. В клиническом контексте понятно, что эффективная доза лекарственного средства, соединения или фармацевтической композиции может обеспечиваться или может не обеспечиваться в сочетании с другим лекарственным средством, соединением или фармацевтической композицией. Таким образом, «эффективную дозу» можно рассматривать в контексте введения одного или более терапевтических средств, и можно считать, что одно средство подлежит введению в эффективном количестве, если в сочетании с одним или более другими средствами требуемый результат может быть достигнут или достигается.
«Индивидуум», «пациент» или «субъект» представляет собой млекопитающее - в некоторых вариантах осуществления человека. Млекопитающие включают без ограничения людей, обезьян, свиней и других сельскохозяйственных животных, животных, используемых в спорте, домашних питомцев, приматов, лошадей, собак, кошек, грызунов, в том числе мышей, крыс, морских свинок и т. д. Субъектом является млекопитающее, и эти термины используются в данном документе взаимозаменяемо. В некоторых вариантах осуществления субъект представляет собой человека. В некоторых вариантах осуществления субъектом является примат, отличный от человека. В некоторых вариантах осуществления субъект представляет собой человека или обезьяну, например, макака-крабоеда.
Используемый в данном документе термин «вектор» означает конструкцию, которая способна доставлять, а в некоторых вариантах осуществления обеспечивать экспрессию одного или более из представляющих интерес гена (генов) или последовательности (последовательностей) в клетке-хозяине. Примеры векторов включают без ограничения вирусные векторы, векторы для экспрессии голой ДНК или РНК, плазмиды, космиды или фаговые векторы, векторы для экспрессии ДНК или РНК, ассоциированные с катионными конденсирующими средствами, инкапсулированные в липосомы векторы для экспрессии ДНК или РНК и определенные эукариотические клетки, такие как клетки-продуценты.
Используемый в данном документе термин «последовательность контроля экспрессии» означает последовательность нуклеиновой кислоты, которая направляет транскрипцию нуклеиновой кислоты. Последовательность контроля экспрессии может представлять собой промотор, такой как конститутивный или индуцируемый промотор, или энхансер. Последовательность контроля экспрессии функционально связана с последовательностью нуклеиновой кислоты, подлежащей транскрипции.
Используемые в данном документе термины «фармацевтически приемлемый носитель» или «фармацевтически приемлемое вспомогательное вещество» включают любой материал, который в комбинации с активным ингредиентом предоставляет возможность ингредиенту сохранять биологическую активность и не вступать в реакцию с иммунной системой субъекта. Примеры включают без ограничения любые стандартные фармацевтические носители, такие как фосфатно-буферный солевой раствор, воду, эмульсии, такие как эмульсия масло/вода, и различные типы смачивающих средств. Иллюстративными разбавителями для аэрозольного или парентерального введения являются фосфатно-буферный солевой раствор (PBS) или нормальный (0,9%) солевой раствор. Композиции, содержащие такие носители, составлены с помощью хорошо известных общепринятых способов (см., например, Remington's Pharmaceutical Sciences, 18th edition, A. Gennaro, ed., Mack Publishing Co., Easton, PA, 1990; и Remington, The Science and Practice of Pharmacy 21st Ed. Mack Publishing, 2005).
Термин «kon», используемый в данном документе, относится к константе скорости связывания антитела, или scFv, или CAR с антигеном.
Термин «koff», используемый в данном документе, относится к константе скорости диссоциации антитела, или scFv, или CAR из комплекса антитело/антиген.
Термин «KD», используемый в данном документе, относится к равновесной константе диссоциации взаимодействия антитело-антиген, или scFv-антиген, или CAR-антиген.
Ссылка на «приблизительно» в отношении значения или параметра в данном документе включает (и описывает) варианты осуществления, которые направлены per se на данное значение или параметр. Например, описание, относящееся к «приблизительно X» включает описание «X». Числовые диапазоны включают числа, определяющие диапазон.
Понятно, что какие бы варианты осуществления ни описывались в данном документе с формулировкой «содержащий», также предусмотрены другие аналогичные варианты осуществления, описываемые терминами «состоящий из» и/или «состоящий фактически из».
В тех случаях, когда аспекты или варианты осуществления изобретения описаны терминами группы Маркуша или другой группы альтернатив, настоящее изобретение охватывает не только всю группу, указанную в целом, но и каждого члена группы по отдельности и все возможные подгруппы основной группы, но также в основной группе отсутствует один или более членов группы. В настоящем изобретении также предусмотрено явное исключение любого одного или более из членов группы в заявленном изобретении.
Если не указано иное, то все технические и научные термины, используемые в данном документе, имеют то же значение, которое обычно понимается специалистами в области техники, к которой относится настоящее изобретение. В случае противоречия настоящее описание, включая определения, будет иметь преимущество. По всему описанию и формуле изобретения слово «содержать» или его варианты, такие как «содержит» или «содержащий», следует понимать как подразумевающие включение указанного целого числа или группы целых чисел, но не исключение какого-либо другого целого числа или группы целых чисел. Если согласно контексту не требуется иное, то термины в единственном числе будут охватывать формы множественного числа, и термины во множественном числе будут включать форму единственного числа.
В данном документе описаны иллюстративные способы и материалы, хотя способы и материалы, подобные или эквивалентные тем, которые описаны в данном документе, также можно применять в практическом осуществлении или тестировании по настоящему изобретению. Указанные материалы, способы и примеры являются лишь иллюстративными и не предназначены для ограничения.
CAR, СПЕЦИФИЧЕСКИЕ К CD70, И СПОСОБЫ ИХ ПОЛУЧЕНИЯ
В настоящем изобретении представлены CAR, которые связываются с CD70 (например, человеческим CD70 (например, SEQ ID NO: 335), например, депонированными в соответствии с положениями Будапештского договора и с присвоенным регистрационным номером: P32970-1. CAR, специфические к CD70, представленные в данном документе, включают одноцепочечные CAR и многоцепочечные CAR. В некоторых вариантах осуществления CAR характеризуются способностью перенаправлять Т-клеточную специфичность и реактивность по отношению к CD70 без ограничения MHC, используя антигенсвязывающие свойства моноклональных антител. Неограниченное MHC распознавание антигена наделяет Т-клетки, экспрессирующие CAR, способностью распознавать антиген независимо от процессинга антигена, обходя таким образом основной механизм избегания опухоли.
В некоторых вариантах осуществления CAR, представленные в данном документе, содержат внеклеточный лиганд-связывающий домен (например, одноцепочечный вариабельный фрагмент (scFv)), трансмембранный домен и внутриклеточный сигнальный домен. В некоторых вариантах осуществления CAR, представленные в данном документе, дополнительно содержат «шарнирный» или «стеблевой» домен, который может располагаться между внеклеточным лиганд-связывающим доменом и трансмембранным доменом. В некоторых вариантах осуществления внеклеточный лиганд-связывающий домен, трансмембранный домен и внутриклеточный сигнальный домен расположены в одном полипептиде, т. е. в одной цепи. В данном документе также представлены многоцепочечные CAR и полипептиды. В некоторых вариантах осуществления многоцепочечные CAR содержат: первый полипептид, содержащий трансмембранный домен и по меньшей мере один внеклеточный лиганд-связывающий домен, и второй полипептид, содержащий трансмембранный домен и по меньшей мере один внутриклеточный сигнальный домен, где полипептиды собраны вместе с образованием многоцепочечного CAR. В некоторых вариантах осуществления CAR индуцируются, например, с помощью малой молекулы (например, AP1903) или белка (например, Epo, Tpo или PD-1). В некоторых вариантах осуществления многоцепочечный CAR, специфический к CD70, основан на высокоаффинном рецепторе для IgE (FcεRI). FcεRI, экспрессируемый на тучных клетках и базофилах, вызывает аллергические реакции. FcεRI представляет собой тетрамерный комплекс, состоящий из одной α-субъединицы, одной β-субъединицы и двух дисульфид-связанных γ-субъединиц. α-Субъединица содержит IgE-связывающий домен. β- и γ-субъединицы содержат ITAM, которые опосредуют передачу сигнала. В некоторых вариантах осуществления внеклеточный домен цепи FcRα удален и заменен внеклеточным лиганд-связывающим доменом, специфическим к CD70. В некоторых вариантах осуществления многоцепочечный CAR, специфический к CD70, содержит scFv, который специфически связывается с CD70, шарнирным участком CD8α и ITAM цепи FcRβ. В некоторых вариантах осуществления CAR может содержать или не содержать цепь FcRγ.
В некоторых вариантах осуществления внеклеточный лиганд-связывающий домен содержит scFv, содержащий вариабельную область легкой цепи (VL) и вариабельную область тяжелой цепи (VH) моноклонального антитела, специфического к целевому антигену (т. е. CD70), соединенного гибким линкером. Фрагменты одноцепочечной вариабельной области получают путем связывания вариабельных областей легкой и/или тяжелой цепи с использованием короткого связывающего пептида (Bird et al., Science 242:423-426, 1988). Примером связывающего пептида является линкер GS, имеющий аминокислотную последовательность (GGGGS)3 (SEQ ID NO: 296), который образует мостик размером примерно 3,5 нм между карбоксиконцом одной вариабельной области и аминоконцом другой вариабельной области. Были сконструированы и использованы линкеры других последовательностей (Bird et al., 1988, см. выше). Другие иллюстративные линкеры, как правило, могут включать другие линкеры GS, которые, как правило, могут включать (GGGGS)x, где x равен 1, 2, 3, 4, 5 (SEQ ID NO: 613). В некоторых вариантах осуществления x равен 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или любому целому числу меньше приблизительно 20. В некоторых вариантах осуществления линкер представляет собой (GGGGS)4 (SEQ ID NO: 602). В некоторых вариантах осуществления линкер представляет собой GSTSGSGKPGSGEGSTKG (SEQ ID NO: 612), как описано в Whitlow et al, Protein Eng. (1993) 6(8): 989-895. Как правило, линкеры могут представлять собой короткие гибкие полипептиды, которые в некоторых вариантах осуществления состоят из приблизительно 20 или меньше аминокислотных остатков. Линкеры, в свою очередь, можно модифицировать для придания им дополнительных функций, таких как присоединение лекарственных средств или присоединение к твердой подложке. Одноцепочечные варианты могут быть получены либо рекомбинантным, либо синтетическим путем. С целью синтетического получения scFv можно использовать автоматический синтезатор. Для рекомбинантного получения scFv подходящая плазмида, содержащая полинуклеотид, кодирующий scFv, может быть введена в подходящую клетку-хозяин, либо эукариотическую, такую как клетки дрожжей, растений, насекомых или млекопитающих, либо прокариотическую, такую как E. coli. Полинуклеотиды, кодирующие представляющий интерес scFv, можно получить с помощью стандартных манипуляций, например, лигирования полинуклеотидов. Полученный scFv можно выделить с применением стандартных методик очистки белков, известных в данной области техники.
В другом аспекте представлен CAR, который специфически связывается с CD70, где CAR содержит внеклеточный лиганд-связывающий домен, содержащий: область VH, содержащую CDR1 VH, CDR2 VH и CDR3 VH из последовательности VH, представленной под SEQ ID NO: 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38, 40, 42, 44, 46 или 48; и/или область VL, содержащую CDR1 VL, CDR2 VL и CDR3 VL из последовательности VL, представленной под SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45 или 47. В некоторых вариантах осуществления VH и VL связаны друг с другом с помощью гибкого линкера. В некоторых вариантах осуществления гибкий линкер содержит аминокислотную последовательность, представленную под SEQ ID NO: 296.
В некоторых вариантах осуществления CAR по настоящему изобретению содержит внеклеточный лиганд-связывающий домен, имеющий любую одну из частичных последовательностей легкой цепи, указанных в таблице 1, и/или любую одну из частичных последовательностей тяжелой цепи, указанных в таблице 1. В таблице 1 подчеркнутые последовательности представляют собой последовательности CDR согласно Кабату и жирным шрифтом согласно Чотиа.
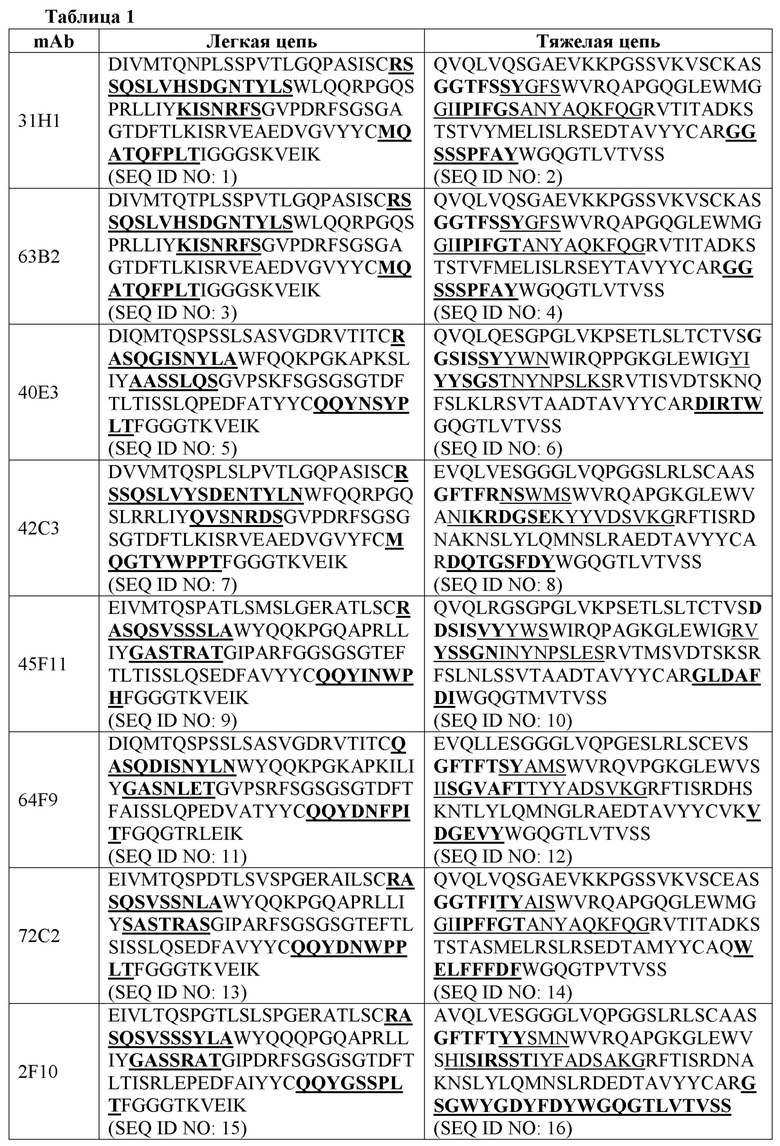
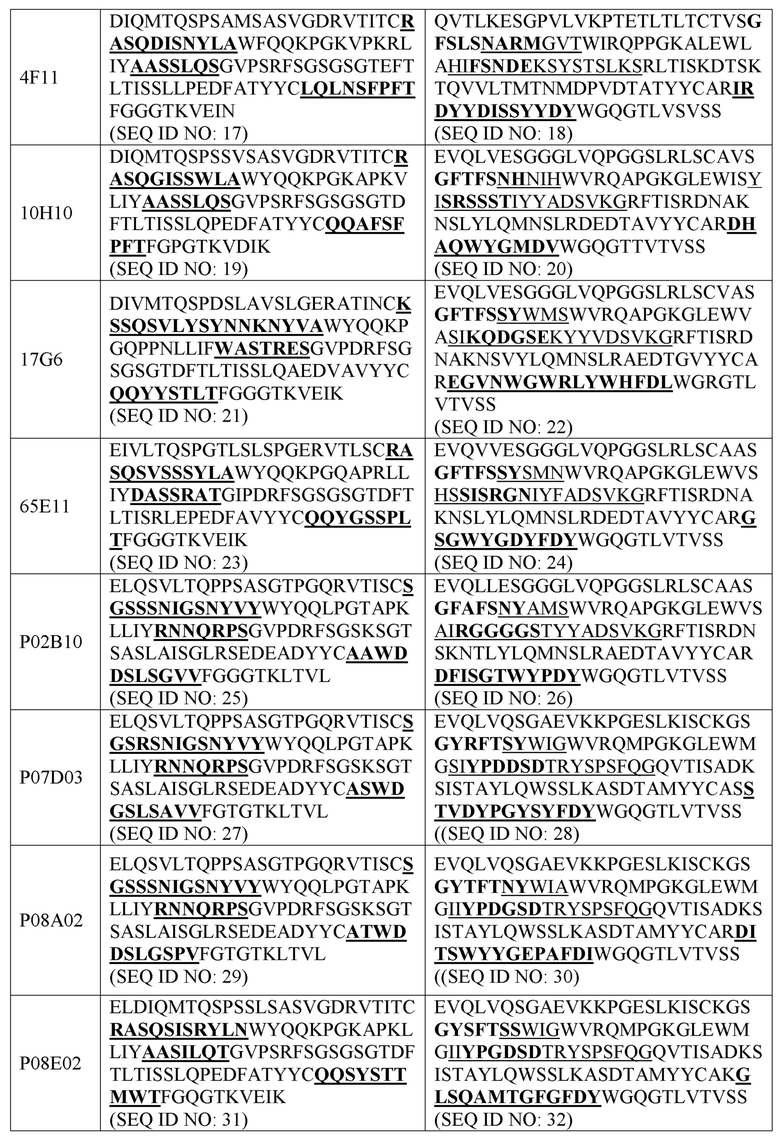
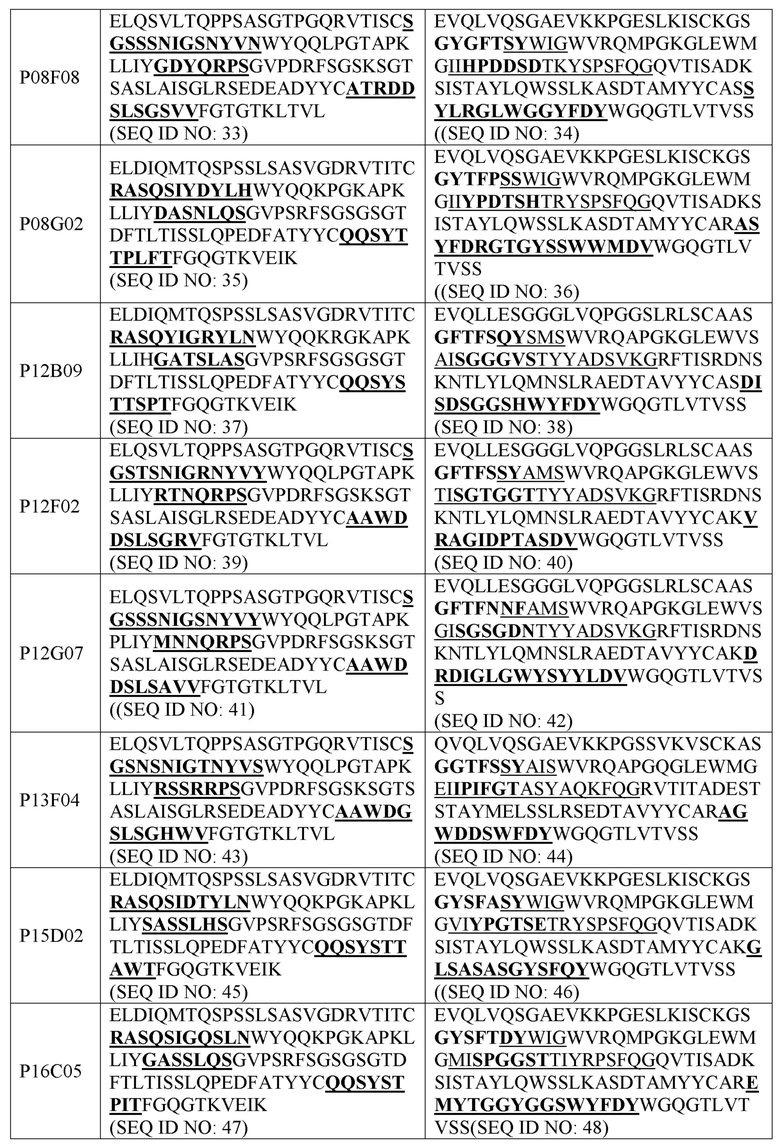
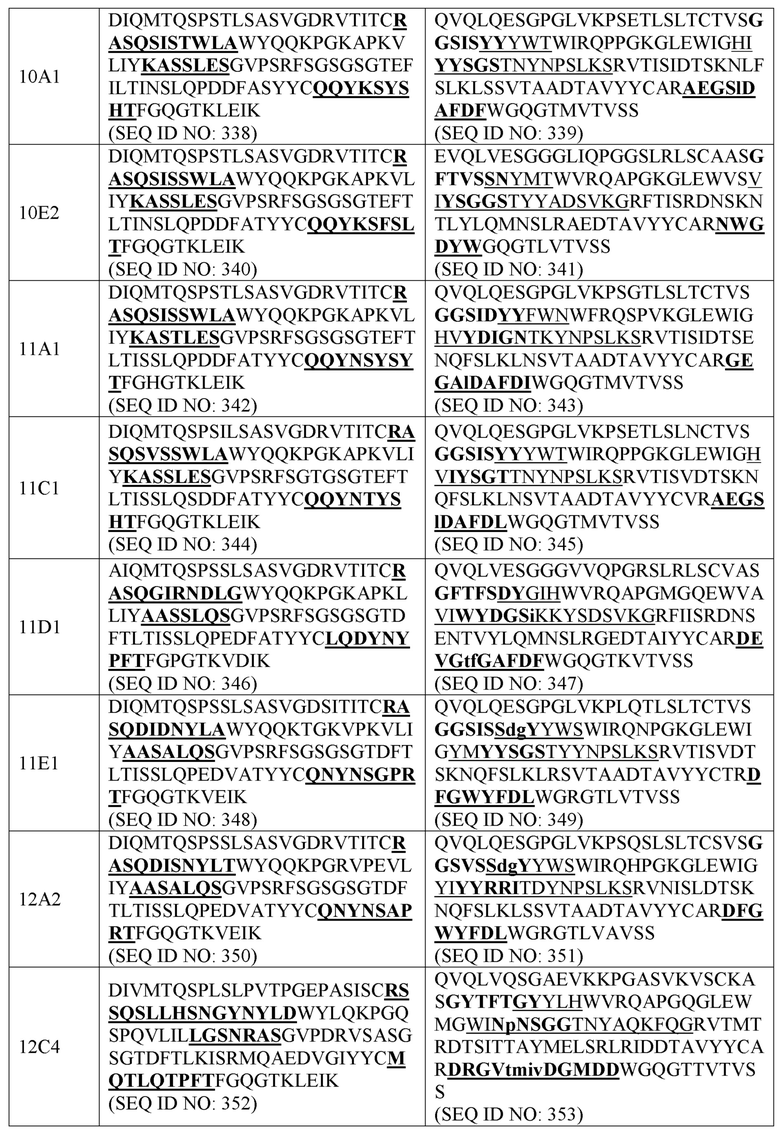
Также в данном документе представлены части CDR внеклеточных лиганд-связывающих доменов CAR к CD70 (включая CDR согласно Чотиа, Кабату и контактные области CDR). Определение областей CDR хорошо известно специалистам в данной области техники. Следует понимать, что в некоторых вариантах осуществления CDR могут представлять собой комбинацию CDR согласно Кабату и Чотиа (также называемые как «комбинированные CR» или «расширенные CDR»). В некоторых вариантах осуществления CDR представляют собой CDR согласно Кабату. В других вариантах осуществления CDR представляют собой CDR согласно Чотиа. Другими словами, в вариантах осуществления с более чем одной CDR, CDR могут быть любыми: согласно Кабату, Чотиа, комбинированными CDR или их комбинациями. В таблицах 2A - 2B представлены примеры последовательностей CDR, представленных в данном документе.
Таблица 2A
GGTFSSY (SEQ ID NO: 50) (Чотиа);
GGTFSSYGFS (SEQ ID NO: 51) (расширенная)
IPIFGS (SEQ ID NO: 53) (Чотиа)
GGTFSSY (SEQ ID NO: 56) (Чотиа)
GGTFSSYGFS (расширенная) (SEQ ID NO: 57)
IPIFGT (SEQ ID NO: 59) (Чотиа)
GGSISSY (SEQ ID NO: 62) (Чотиа);
GGSISSYYWN (SEQ ID NO: 63) (расширенная)
YYSGS (SEQ ID NO: 65) (Чотиа)
GFTFRNS (SEQ ID NO: 68) (Чотиа);
GFTFRNSWMS (SEQ ID NO: 69) (расширенная)
KRDGSE (SEQ ID NO: 71) (Чотиа)
DDSISVY (SEQ ID NO: 74) (Чотиа);
DDSISVYYWS (SEQ ID NO: 75) (расширенная)
YSSGN (SEQ ID NO: 77) (Чотиа)
GFTFTSY (SEQ ID NO: 80) (Чотиа);
GFTFTSYAMS (SEQ ID NO: 81) (расширенная)
YSSGN (SEQ ID NO: 83) (Чотиа)
GGTFITY (SEQ ID NO: 86) (Чотиа);
GGTFITYAIS (SEQ ID NO: 87) (расширенная)
IPFFGT (SEQ ID NO: 89) (Чотиа)
GFTFTYY (SEQ ID NO: 92) (Чотиа);
GFTFTYYSMN (SEQ ID NO: 93) (расширенная)
SIRSST (SEQ ID NO: 95) (Чотиа)
GFSLSNARM (SEQ ID NO: 98) (Чотиа);
GFSLSNARMGVT (SEQ ID NO: 99) (расширенная)
FSNDE (SEQ ID NO: 101) (Чотиа)
GFTFSNH (SEQ ID NO: 104) (Чотиа);
GFTFSNHNIH (SEQ ID NO: 105) (расширенная)
SRSSST (SEQ ID NO: 107) (Чотиа)
GFTFSSY (SEQ ID NO: 110) (Чотиа);
GFTFSSYWMS (SEQ ID NO: 111) (расширенная)
KQDGSE (SEQ ID NO: 113) (Чотиа)
GFTFSSY (SEQ ID NO: 116) (Чотиа);
GFTFSSYSMN (SEQ ID NO: 117) (расширенная)
SISRGN (SEQ ID NO: 119) (Чотиа)
GFAFSNY (SEQ ID NO: 122) (Чотиа);
GFAFSNYAMS (SEQ ID NO: 123) (расширенная)
RGGGGS (SEQ ID NO: 125) (Чотиа)
GYRFTSY (SEQ ID NO: 128) (Чотиа);
GYRFTSYWIG (SEQ ID NO: 129) (расширенная)
YPDDSD (SEQ ID NO: 131) (Чотиа)
GYTFTNY (SEQ ID NO: 134) (Чотиа);
GYTFTNYWIA (SEQ ID NO: 135) (расширенная)
YPDGSD (SEQ ID NO: 137) (Чотиа)
(SEQ ID NO: 138)
GYSFTSS (SEQ ID NO: 140) (Чотиа);
GYSFTSSWIG (SEQ ID NO: 141) (расширенная)
YPGDSD (SEQ ID NO: 143) (Чотиа)
GYGFTSY (SEQ ID NO: 146) (Чотиа);
GYGFTSYWIG (SEQ ID NO: 147) (расширенная)
HPDDSD (SEQ ID NO: 149) (Чотиа)
GYTFPSS (SEQ ID NO: 152) (Чотиа);
GYTFPSSWIG (SEQ ID NO: 153) (расширенная)
YPDTSH (SEQ ID NO: 155) (Чотиа)
GFTFSQY (SEQ ID NO: 158) (Чотиа);
GFTFSQYSMS (SEQ ID NO: 159) (расширенная)
SGGGVS (SEQ ID NO: 161) (Чотиа)
GFTFSSY (SEQ ID NO: 164) (Чотиа);
GFTFSSYAMS (SEQ ID NO: 165) (расширенная)
SGTGGT (SEQ ID NO: 167) (Чотиа)
GFTFNNF (SEQ ID NO: 170) (Чотиа);
GFTFNNFAMS (SEQ ID NO: 171) (расширенная)
SGSGDN (SEQ ID NO: 173) (Чотиа)
GGTFSSY (SEQ ID NO: 176) (Чотиа);
GGTFSSYAIS (SEQ ID NO: 177) (расширенная)
IPIFGT (SEQ ID NO: 179) (Чотиа)
GYSFASY (SEQ ID NO: 182) (Чотиа);
GYSFASYWIG (SEQ ID NO: 183) (расширенная)
YPGTSE (SEQ ID NO: 185) (Чотиа)
GYSFTDY (SEQ ID NO: 188) (Чотиа);
GYSFTDYWIG (SEQ ID NO: 189) (расширенная)
SPGGST (SEQ ID NO: 191) (Чотиа)
GGSISYY (SEQ ID NO: 383) (Чотиа);
GGSISYYYWT (SEQ ID NO: 384) (расширенная)
YYSGS (SEQ ID NO: 386) (Чотиа)
GFTVSSN (SEQ ID NO: 389) (Чотиа);
GFTVSSNYMT (SEQ ID NO: 390) (расширенная)
YSGGS (SEQ ID NO: 392) (Чотиа)
GGSIDYY (SEQ ID NO: 395) (Чотиа);
GGSIDYYFWN (SEQ ID NO: 396) (расширенная)
YDIGN (SEQ ID NO: 398) (Чотиа)
GGSISYY (SEQ ID NO: 401) (Чотиа);
GGSISYYYWT (SEQ ID NO: 402) (расширенная)
IYSGT (SEQ ID NO: 404) (Чотиа)
GFTFSDY (SEQ ID NO: 407) (Чотиа);
GFTFSDYGIH (SEQ ID NO: 408) (расширенная)
WYDGSi (SEQ ID NO: 410) (Чотиа)
GGSISSdgY (SEQ ID NO: 413) (Чотиа);
GGSISSdgYYWS (SEQ ID NO: 414) (расширенная)
YYSGS (SEQ ID NO: 416) (Чотиа)
GGSVSSdgY (SEQ ID NO: 419) (Чотиа);
GGSVSSdgYYWS (SEQ ID NO: 420) (расширенная)
YYRRI (SEQ ID NO: 422) (Чотиа)
GYTFTGY (SEQ ID NO: 425) (Чотиа);
GYTFTGYYLH (SEQ ID NO: 426) (расширенная)
NpNSGG (SEQ ID NO: 428) (Чотиа)
GFTFSDY (SEQ ID NO: 431) (Чотиа);
GFTFSDYGMH (SEQ ID NO: 432) (расширенная)
WYDGSn (SEQ ID NO: 434) (Чотиа)
GFTFSDY (SEQ ID NO: 664) (Чотиа);
GFTFSDYGMH (SEQ ID NO: 665) (расширенная)
WYDGSn (SEQ ID NO: 667) (Чотиа)
GGSISSdgY (SEQ ID NO: 437) (Чотиа);
GGSISSdgYYWS (SEQ ID NO: 438) (расширенная)
YYSGI (SEQ ID NO: 440) (Чотиа)
GGSISSdaY (SEQ ID NO: 443) (Чотиа);
GGSISSdaYYWS (SEQ ID NO: 444) (расширенная)
YYSGI (SEQ ID NO: 446) (Чотиа)
GFTFSDY (SEQ ID NO: 449) (Чотиа);
GFTFSDYGIH (SEQ ID NO: 450) (расширенная)
WYDGSi (SEQ ID NO: 452) (Чотиа)
GFTFSNA (SEQ ID NO: 455) (Чотиа);
GFTFSNAWMS (SEQ ID NO: 456) (расширенная)
KsktGGGT (SEQ ID NO: 458) (Чотиа)
GGSISYY (SEQ ID NO: 461) (Чотиа);
GGSISYYFWT (SEQ ID NO: 462) (расширенная)
YYSGN (SEQ ID NO: 464) (Чотиа)
GFTFSSY (SEQ ID NO: 467) (Чотиа);
GFTFSSYSMN (SEQ ID NO: 468) (расширенная)
StSSNY (SEQ ID NO: 470) (Чотиа)
GFTFSSY (SEQ ID NO: 473) (Чотиа);
GFTFSSYGMH (SEQ ID NO: 474) (расширенная)
WYDGSn (SEQ ID NO: 476) (Чотиа)
GGSISYY (SEQ ID NO: 479) (Чотиа);
GGSISYYYWS (SEQ ID NO: 480) (расширенная)
NYMGN (SEQ ID NO: 482) (Чотиа)
GYIFTGY (SEQ ID NO: 485) (Чотиа);
GYIFTGYYIY (SEQ ID NO: 486) (расширенная)
NpSSGG (SEQ ID NO: 488) (Чотиа)
GYTFTSH (SEQ ID NO: 491) (Чотиа);
GYTFTSHYIY (SEQ ID NO: 492) (расширенная)
NpNSGG (SEQ ID NO: 494) (Чотиа)
GFTFTSH (SEQ ID NO: 497) (Чотиа);
GFTFTSHYIY (SEQ ID NO: 498) (расширенная)
NpNSGG (SEQ ID NO: 500) (Чотиа)
GFTLSIY (SEQ ID NO: 503) (Чотиа);
GFTLSIYAIH (SEQ ID NO: 504) (расширенная)
GgRGSS (SEQ ID NO: 506) (Чотиа)
GFTFSNY (SEQ ID NO: 509) (Чотиа);
GFTFSNYSMN (SEQ ID NO: 510) (расширенная)
SsSTIY (SEQ ID NO: 512) (Чотиа)
Таблица 2B
В настоящем изобретении охвачены модификации CAR и полипептидов, содержащих последовательности, показанные в таблицах 1 или 2A - 2B, включая функционально эквивалентные CAR, имеющие модификации, которые существенно не влияют на их свойства, и варианты, которые имеют повышенную или пониженную активность и/или аффинность. Например, аминокислотную последовательность можно подвергать мутации с получением антитела с требуемой аффинностью связывания с CD70. Модификация полипептидов является стандартной практикой в данной области техники и не нуждается в подробном описании в данном документе. Примеры модифицированных полипептидов включают полипептиды с консервативными заменами аминокислотных остатков, одну или более делеций или добавлений аминокислот, которые в значительной степени не оказывают вредного воздействия на функциональную активность, или которые обеспечивают созревание (усиливают) аффинность полипептида к его лиганду, или используют химические аналоги.
Вставки аминокислотной последовательности включают амино- и/или карбоксиконцевые слияния, варьирующееся по длине от одного остатка до полипептидов, содержащих сто или более остатков, а также вставки внутри последовательности из одного или множества аминокислотных остатков. Примеры концевых вставок включают антитело с N-концевым остатком метионила или антитело, слитое с эпитопной меткой. Другие вставочные варианты молекулы антитела включают слияние фермента или полипептида с N- или C-концом антитела, что увеличивает время полужизни антитела в кровотоке.
Варианты замещения имеют по меньшей мере один удаленный аминокислотный остаток в молекуле антитела и другой остаток, вставленный на это место. Сайты, представляющие наибольший интерес для замещающего мутагенеза, включают гипервариабельные области, но изменения FR также предусмотрены. Консервативные замены показаны в таблице 3 под заголовком «консервативные замены». Если такие замены в результате приводят к изменению биологической активности, то можно ввести более значительные изменения, обозначенные в таблице 3 как «иллюстративные замены», или дополнительно описанные ниже в ссылке на классы аминокислот, а продукты подвергнуть скринингу.
Таблица 3. Аминокислотные замены
(встречающаяся в природе аминокислота)
В некоторых вариантах осуществления настоящего изобретения представлен CAR, содержащий внеклеточный лиганд-связывающий домен, который связывается с CD70 и за связывание с CD70 конкурирует с CAR, описанным в данном документе, в том числе CAR, содержащим внеклеточный домен, который содержит ScFv, содержащий последовательности 31H1, 63B2, 40E3, 42C3, 45F11, 64F9, 72C2, 2F10, 4F11, 10H10, 17G6, 65E11, P02B10, P07D03, P08A02, P08E02, P08F08, P08G02, P12B09, P12F02, P12G07, P13F04, P15D02, P16C05, 10A1, 10E2, 11A1, 11C1, 11D1, 11E1, 12A2, 12C4, 12C5, 12D3, 12D6, 12D7, 12F5, 12H4, 8C8, 8F7, 8F8, 9D8, 9E10, 9E5, 9F4 или 9F8.
В некоторых вариантах осуществления настоящего изобретения представлен CAR, который специфически связывается с CD70, где CAR содержит область VH, содержащую последовательность, представленную под SEQ ID NO: 20; и/или область VL, содержащую последовательность, представленную под SEQ ID NO: 19. В некоторых вариантах осуществления настоящего изобретения представлен CAR, который специфически связывается с CD70, где CAR содержит область VH, содержащую последовательность, представленную под SEQ ID NO: 22; и/или область VL, содержащую последовательность, представленную под SEQ ID NO: 21. В некоторых вариантах осуществления настоящего изобретения представлен CAR, который специфически связывается с CD70, где CAR содержит область VH, содержащую последовательность, представленную под SEQ ID NO: 28; и/или область VL, содержащую последовательность, представленную под SEQ ID NO: 27. В некоторых вариантах осуществления настоящего изобретения представлен CAR, который специфически связывается с CD70, где CAR содержит область VH, содержащую последовательность, представленную под SEQ ID NO: 36; и/или область VL, содержащую последовательность, представленную под SEQ ID NO: 35. В некоторых вариантах осуществления настоящего изобретения представлен CAR, который специфически связывается с CD70, где CAR содержит область VH, содержащую последовательность, представленную под SEQ ID NO: 46; и/или область VL, содержащую последовательность, представленную под SEQ ID NO: 45. В некоторых вариантах осуществления настоящего изобретения представлен CAR, который специфически связывается с CD70, где CAR содержит область VH, содержащую последовательность, представленную под SEQ ID NO: 18; и/или область VL, содержащую последовательность, представленную под SEQ ID NO: 17. В некоторых вариантах осуществления настоящего изобретения представлен CAR, который специфически связывается с CD70, где CAR содержит область VH, содержащую последовательность, представленную под SEQ ID NO: 34; и/или область VL, содержащую последовательность, представленную под SEQ ID NO: 33. В некоторых вариантах осуществления настоящего изобретения также представлены CAR, содержащие части CDR антител к CD70 на основе контактных областей CDR. Контактные области CDR являются областями антитела, которые придают специфичность антителу к антигену. В целом контактные области CDR включают положения остатков в CDR и верньерных зонах, которые ограничены для поддержания надлежащей структуры петли с целью обеспечения связывания антитела со специфическим антигеном. См., например, Makabe et al., J. Biol. Chem., 283:1156-1166, 2007. Определение контактных областей CDR хорошо известно специалистам в данной области техники.
Аффинность связывания (KD) лиганд-связывающего домена в CAR, специфическом к CD70, описанного в данном документе, с CD70 (например, человеческим CD70) может составлять, например, от приблизительно 0,1 до приблизительно 1000 нМ, например, от приблизительно 0,5 нм до приблизительно 500 нМ, или например, от приблизительно 1 нм до приблизительно 250 нм. В некоторых вариантах осуществления аффинность связывания составляет приблизительно любое значение из 1000 нм, 750 нм, 500 нм, 400 нм, 300 нм, 250 нм, 200 нм, 100 нм, 90 нм, 80 нм, 70 нм, 60 нм, 50 нм, 45 нм, 40 нм, 35 нм, 30 нм, 25 нм, 20 нм, 19 нм, 18 нм, 17 нм, 16 нм, 15 нм, 10 нм, 8 нм, 7,5 нм, 7 нм, 6,5 нм, 6 нм, 5,5 нм, 5 нм, 4 нм, 3 нм, 2 нм, 1 нм, 0,5 нм, 0,3 нм или 0,1 нм.
В некоторых вариантах осуществления аффинность связывания (KD) scFv лиганд-связывающего домена в CAR, специфическом к CD70, описанном в данном документе, с CD70 составляет от приблизительно 10 нМ до приблизительно 100 нМ, от приблизительно 10 нМ до приблизительно 90 нМ, от приблизительно 10 нМ до приблизительно 80 нМ, от приблизительно 20 нМ до приблизительно 70 нМ, от приблизительно 25 нМ до приблизительно 75 нМ или от приблизительно 40 нМ до приблизительно 110 нМ. В некоторых вариантах осуществления аффинность связывания scFv, описанная в этом абзаце, относится к CD70 человека.
В некоторых вариантах осуществления аффинность связывания составляет меньше приблизительно любого из значений 1000 нм, 900 нм, 800 нм, 250 нМ, 200 нМ, 100 нМ, 50 нМ, 30 нМ, 20 нМ, 10 нМ, 7,5 нМ, 7 нМ, 6,5 нМ, 6 нМ, 5 нМ.
Внутриклеточный сигнальный домен CAR согласно настоящему изобретению отвечает за внутриклеточную передачу сигнала после связывания внеклеточного лиганд-связывающего домена с мишенью, что приводит к активации иммунной клетки и иммунного ответа. Внутриклеточный сигнальный домен обладает способностью активировать по меньшей мере одну из нормальных эффекторных функций иммунной клетки, при которой экспрессируется CAR. Например, эффекторная функция Т-клетки может представлять собой цитолитическую активность или хелперную активность, включающую секрецию цитокинов.
В некоторых вариантах осуществления внутриклеточный сигнальный домен для применения в CAR может представлять собой цитоплазматические последовательности, например, без ограничения, Т-клеточного рецептора и корецепторов, которые действуют совместно, инициируя передачу сигнала после взаимодействия с антигенным рецептором, а также любое производное или вариант этих последовательностей и любая синтетическая последовательность, которая имеет такие же функциональные возможности. Внутриклеточные сигнальные домены включают два разных класса цитоплазматических сигнальных последовательностей: те, которые инициируют антиген-зависимую первичную активацию, и те, которые действуют антиген-независимым образом, обеспечивая вторичный или костимулирующий сигнал. Первичные цитоплазматические сигнальные последовательности могут содержать сигнальные мотивы, которые известны как иммунорецепторные тирозиновые активирующие мотивы - ITAM. ITAM представляют собой четко определенные сигнальные мотивы, обнаруженные в интрацитоплазматическом хвосте у множества рецепторов, которые служат сайтами связывания для тирозинкиназ класса syk/zap70. Примеры ITAM, используемых в настоящем изобретении, могут включать в качестве неограничивающих примеров те, которые получены из TCRζ, FcRγ, FcRβ, FcRε, CD3γ, CD3δ, CD3ε, CD5, CD22, CD79a, CD79b и CD66d. В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR может содержать сигнальный домен CD3ζ, имеющий аминокислотную последовательность, которая на по меньшей мере приблизительно 70%, по меньшей мере 80%, по меньшей мере 90%, 95%, 97% или 99% идентична аминокислотной последовательности, представленной под SEQ ID NO: 272 или 683. В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR по настоящему изобретению содержит домен костимулирующей молекулы.
В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR по настоящему изобретению содержит часть костимулирующей молекулы, выбранной из группы, состоящей из фрагмента 41BB (GenBank: AAA53133.) и CD28 (NP_006130.1). В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR по настоящему изобретению содержит аминокислотную последовательность, которая на по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90%, 95%, 97% или 99% идентична аминокислотной последовательности, представленной под SEQ ID NO: 271 или 682 и SEQ ID NO: 275. В некоторых вариантах осуществления внутриклеточный сигнальный домен CAR по настоящему изобретению содержит аминокислотную последовательность, которая на по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90%, 95%, 97% или 99% идентична аминокислотной последовательностью, представленной под SEQ ID NO: 271 или 682, и/или на по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90%, 95%, 97% или 99% идентична аминокислотной последовательности, представленной под SEQ ID NO: 276.
CAR экспрессируются на поверхности мембраны клетки. Таким образом, CAR может содержать трансмембранный домен. Подходящие трансмембранные домены для CAR, раскрытого в данном документе, характеризуются способностью (а) экспрессироваться на поверхности клетки, которая в некоторых вариантах осуществления является иммунной клеткой, такой как, например, без ограничения, лимфоцитарная клетка, например, Т-хелперная (Th) клетка, цитотоксическая T (Tc) клетка, регуляторная T (Treg) или естественные клетки-киллеры (NK), и/или (b) взаимодействовать с лиганд-связывающим доменом и внутриклеточным сигнальным доменом для управления клеточным ответом иммунной клетки на заранее определенную клетку-мишень. Трансмембранный домен может быть получен либо из природного, либо из синтетического источника. Трансмембранный домен может быть получен из любого мембраносвязанного или трансмембранного белка. В качестве неограничивающих примеров трансмембранный полипептид может представлять собой подпоследовательность или субъединицу Т-клеточного рецептора, например, α, β, γ или δ, полипептид, составляющий комплекс CD3, рецептор IL-2 p55 (цепь), p75 (β-цепь) или γ-цепь, субъединичная цепь Fc-рецепторов, в частности Fcγ-рецептор III или белки CD. Альтернативно трансмембранный домен может быть синтетическим и может содержать преимущественно гидрофобные остатки, такие как лейцин и валин. В некоторых вариантах осуществления указанный трансмембранный домен получен из цепи CD8α человека (например, NP_001139345.1). Трансмембранный домен может дополнительно содержать домен «стебля» между внеклеточным лиганд-связывающим доменом и указанным трансмембранным доменом. Домен «стебля» может содержать до 300 аминокислот - в некоторых вариантах осуществления от 10 до 100 аминокислот или в некоторых вариантах осуществления от 25 до 50 аминокислот. Стеблевая область может быть получена из всех или части встречающихся в природе молекул, например, из всей или части внеклеточной области CD8, CD4, CD28, 4-1BB или IgG (в частности, шарнирной области из IgG), или из всей или части константной области тяжелой цепи антитела. Альтернативно домен «стебля» может представлять собой синтетическую последовательность, которая соответствует встречающейся в природе стеблевой последовательности, или может быть полностью синтетической стеблевой последовательностью. В некоторых вариантах осуществления указанный домен «стебля» является частью цепи CD8α человека (например, NP_001139345.1). В другом конкретном варианте осуществления указанные шарнирный и трансмембранный домены содержат часть цепи CD8α человека, которая в некоторых вариантах осуществления характеризуется по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90%, 95%, 97% или 99% идентичностью последовательности с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 268 и 270. В некоторых вариантах осуществления описанный в данном документе домен «стебля» в CAR содержит подпоследовательность CD8α, IgG1 или FcγRIIIα, в частности шарнирную область из любого из CD8α, IgG1 или FcγRIIIα. В некоторых вариантах осуществления домен «стебля» содержит шарнирный участок из CD8α человека, шарнирный участок из IgG1 человека или шарнирный участок из FcγRIIIα человека. В некоторых вариантах осуществления CAR, раскрытые в данном документе, могут содержать внеклеточный лиганд-связывающий домен, который специфически связывается с CD70. В некоторых вариантах осуществления CAR, раскрытые в данном документе, содержат scFv, шарнирный и трансмембранный домены CD8α человека, сигнальный домен CD3ζ и сигнальный домен 4-1BB.
В таблице 4 представлены иллюстративные последовательности доменов, которые можно использовать в описанных в данном документе CAR.
Таблица 4. Иллюстративные последовательности компонентов CAR
Понижающая регуляция или мутация антигенов-мишеней, как правило, наблюдается в раковых клетках с образованием вариантов ускользания с потерей антигена. Таким образом, чтобы компенсировать ускользание опухоли и придать иммунной клетке большую специфичность к мишени, CAR, специфический к CD70, может содержать один или более дополнительных внеклеточных лиганд-связывающих доменов, предназначенных для одновременного связывания различных элементов в мишени, за счет чего повышается активация и функция иммунных клеток. В некоторых вариантах осуществления внеклеточные лиганд-связывающие домены могут быть расположены в тандеме на одном и том же трансмембранном полипептиде, при этом необязательно они могут быть разделены линкером. В некоторых вариантах осуществления указанные разные внеклеточные связывающие лиганд домены могут быть расположены на разных трансмембранных полипептидах, образующих CAR. В некоторых вариантах осуществления настоящее изобретение относится к популяции CAR, каждый из которых содержит разный внеклеточный лиганд-связывающий домен. В частности, настоящее изобретение относится к способу конструирования иммунных клеток, предусматривающему обеспечение иммунной клетки и экспрессии на поверхности клетки популяции CAR, каждый из которых содержит разные внеклеточные лиганд-связывающие домены. В другом конкретном варианте осуществления настоящее изобретение относится к способу конструирования иммунной клетки, предусматривающему обеспечение иммунной клетки и введение в клетку полинуклеотидов, кодирующих полипептиды, составляющие популяцию CAR, каждый из которых содержит разные внеклеточные лиганд-связывающие домены. Под популяцией CAR подразумевают по меньшей мере два, три, четыре, пять, шесть или более CAR, каждый из которых содержит разные внеклеточные лиганд-связывающие домены. Разные внеклеточные лиганд-связывающие домены в соответствии с настоящим изобретением могут в некоторых вариантах осуществления одновременно связывать разные элементы в мишени, за счет чего повышается активация и функция иммунных клеток. Настоящее изобретение также относится к выделенной иммунной клетке, которая содержит популяцию CAR, каждый из которых содержит разные внеклеточные лиганд-связывающие домены.
В другом аспекте настоящего изобретения представлены полинуклеотиды, кодирующие любой из CAR и полипептидов, описанных в данном документе. Полинуклеотиды можно получать и экспрессировать с помощью процедур, известных в данной области техники.
В другом аспекте настоящего изобретения представлены композиции (такие как фармацевтические композиции), содержащие любую из клеток по настоящему изобретению. В некоторых вариантах осуществления композиция содержит клетку, содержащую полинуклеотид, кодирующий любые из CAR, описанных в данном документе. В других вариантах осуществления композиция содержит один или оба полинуклеотида, представленных под SEQ ID NO: 297 и SEQ ID NO:298, SEQ ID NO: 299 и SEQ ID NO:300, SEQ ID NO: 301 и SEQ ID NO:302, SEQ ID NO: 303 и SEQ ID NO:304, SEQ ID NO: 305 и SEQ ID NO:306, SEQ ID NO: 307 и SEQ ID NO:308 или SEQ ID NO: 309 и SEQ ID NO:310 ниже:
вариабельная область тяжелой цепи 4F11
CAGGTCACCTTGAAGGAGTCTGGTCCTGTGCTGGTGAAACCCACAGAGACCCTCACGCTGACCTGCACCGTCTCTGGGTTCTCACTCAGTAATGCTAGAATGGGTGTGACCTGGATCCGTCAGCCCCCAGGGAAGGCCCTGGAGTGGCTTGCACACATTTTTTCGAATGACGAAAAATCCTACAGTACATCTCTGAAGAGCAGGCTCACCATCTCCAAGGACACTTCCAAAACCCAGGTGGTCCTTACCATGACCAACATGGACCCTGTGGACACAGCCACATATTACTGTGCACGGATACGAGATTACTATGACATTAGTAGTTATTATGACTACTGGGGCCAGGGAACCCTGGTCAGCGTCTCCTCA (SEQ ID NO: 297)
вариабельная область легкой цепи 4F11
GACATCCAGATGACCCAGTCTCCATCTGCCATGTCTGCATCTGTAGGAGACAGAGTCACCATCACTTGTCGGGCGAGTCAGGACATTAGCAATTATTTAGCCTGGTTTCAGCAGAAACCAGGGAAAGTCCCTAAGCGCCTGATCTATGCTGCATCCAGTTTGCAAAGTGGGGTCCCATCAAGGTTCAGCGGCAGTGGATCGGGGACAGAATTCACTCTCACAATCAGCAGCCTGCTGCCTGAAGATTTTGCAACTTATTACTGTCTACAGCTTAATAGTTTCCCGTTCACTTTTGGCGGAGGGACCAAGGTGGAGATCAAC (SEQ ID NO: 298).
В еще одних вариантах осуществления композиция содержит один или оба полинуклеотида, представленных под SEQ ID NO: 299 и SEQ ID NO: 300 ниже:
вариабельная область тяжелой цепи 17G6
GAGGTGCAGCTGGTGGAGTCTGGGGGAGGCTTGGTCCAGCCTGGGGGGTCCCTGAGACTCTCCTGTGTAGCCTCTGGATTCACCTTTAGTAGTTATTGGATGAGCTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAGTGGGTGGCCAGCATAAAGCAAGATGGAAGTGAGAAATACTATGTGGACTCTGTGAAGGGCCGATTCACCATCTCCAGAGACAACGCCAAGAACTCAGTGTATCTGCAAATGAACAGCCTGAGAGCCGAGGACACGGGTGTGTATTACTGTGCGAGAGAAGGAGTCAACTGGGGATGGAGACTCTACTGGCACTTCGATCTCTGGGGCCGTGGAACCCTGGTCACTGTCTCCTCA (SEQ ID NO: 299)
вариабельная область легкой цепи 17G6
GACATCGTGATGACCCAGTCTCCAGACTCCCTGGCTGTGTCTCTGGGCGAGAGGGCCACCATCAACTGCAAGTCCAGCCAGAGTGTTTTATACAGCTACAACAATAAGAACTACGTAGCTTGGTACCAGCAGAAACCAGGACAACCTCCTAACCTACTCATTTTCTGGGCATCTACCCGGGAATCCGGGGTCCCTGACCGATTCAGTGGCAGCGGGTCTGGGACAGATTTCACTCTCACCATCAGCAGCCTGCAGGCTGAAGATGTGGCAGTTTACTACTGTCAGCAATATTATAGTACGCTCACTTTCGGCGGAGGGACCAAGGTGGAGATCAAA (SEQ ID NO: 300).
В еще одних вариантах осуществления композиция содержит один или оба полинуклеотида, представленных под SEQ ID NO: 301 и SEQ ID NO: 302 ниже:
вариабельная область тяжелой цепи 10H10
GAGGTGCAGCTGGTGGAGTCTGGGGGAGGCTTGGTACAGCCTGGGGGGTCCCTGAGACTCTCCTGTGCAGTCTCTGGATTCACCTTCAGTAACCATAACATACACTGGGTCCGCCAGGCTCCAGGGAAGGGGCTGGAGTGGATTTCATACATTAGTCGAAGTAGTAGTACCATATATTACGCAGACTCTGTGAAGGGCCGATTCACAATCTCCAGAGACAATGCCAAGAACTCACTGTATCTGCAAATGAACAGCCTGAGAGACGAAGACACGGCTGTGTATTACTGTGCGAGAGATCACGCTCAGTGGTACGGTATGGACGTTTGGGGCCAAGGGACCACGGTCACCGTCTCCTCA (SEQ ID NO: 301).
Вариабельная область легкой цепи 10H10
GACATCCAGATGACCCAGTCTCCATCTTCCGTGTCTGCATCGGTAGGAGACAGAGTCACCATCACTTGTCGGGCGAGTCAGGGTATTAGCAGCTGGTTAGCCTGGTATCAGCAGAAACCAGGGAAAGCCCCTAAGGTCCTGATCTATGCTGCATCCAGTTTGCAAAGTGGGGTCCCATCAAGGTTCAGCGGCAGTGGATCTGGGACAGATTTCACTCTCACCATCAGCAGCCTGCAGCCTGAAGATTTTGCAACTTACTATTGTCAACAGGCTTTCAGTTTCCCATTCACTTTCGGCCCTGGGACCAAAGTGGATATCAAA (SEQ ID NO: 302).
В еще одних вариантах осуществления композиция содержит один или оба полинуклеотида, представленных под SEQ ID NO: 303 и SEQ ID NO: 304 ниже:
вариабельная область тяжелой цепи P07D03
GAAGTGCAGCTTGTCCAGAGCGGAGCCGAAGTGAAGAAGCCTGGCGAGAGCCTGAAGATCAGCTGCAAGGGCTCCGGATATCGCTTCACAAGTTACTGGATAGGGTGGGTGCGCCAGATGCCTGGTAAGGGACTGGAATGGATGGGCTCTATATATCCTGATGATTCCGACACACGTTATAGCCCAAGCTTTCAGGGCCAGGTCACAATCAGCGCTGACAAGAGCATCAGCACCGCCTACCTTCAGTGGTCGTCTCTGAAGGCCAGCGACACCGCAATGTACTACTGCGCCTCTAGCACAGTTGACTACCCGGGATACAGTTACTTCGACTACTGGGGCCAAGGTACACTGGTCACCGTCAGCAGC (SEQ ID NO: 303)
вариабельная область легкой цепи P07D03
GAGCTCCAGAGCGTGCTGACCCAGCCTCCTAGCGCAAGCGGCACCCCTGGACAGCGTGTGACAATTAGCTGTAGCGGAAGTCGTAGCAATATCGGATCAAACTATGTGTATTGGTATCAGCAATTGCCCGGTACAGCACCCAAATTGCTCATATATAGAAATAATCAGAGACCTAGCGGAGTGCCTGATCGTTTTAGCGGTAGCAAAAGCGGCACCAGCGCATCACTGGCAATTTCAGGCCTGCGTAGCGAAGATGAGGCGGATTATTACTGTGCGAGTTGGGATGGTTCGCTGAGTGCTGTTGTGTTCGGCACCGGTACAAAACTGACCGTTCTG (SEQ ID NO: 304).
В еще одних вариантах осуществления композиция содержит один или оба полинуклеотида, представленных под SEQ ID NO: 305 и SEQ ID NO: 306 ниже:
вариабельная область тяжелой цепи P08G02
GAAGTGCAGCTTGTCCAGAGCGGAGCCGAAGTGAAGAAGCCTGGCGAGAGCCTGAAGATCAGCTGCAAGGGCTCCGGATACACCTTTCCTTCATCATGGATAGGTTGGGTGCGCCAGATGCCTGGTAAGGGACTGGAATGGATGGGCATCATATACCCTGATACTAGCCATACCCGTTACAGCCCAAGCTTTCAGGGCCAGGTCACAATCAGCGCTGACAAGAGCATCAGCACCGCCTACCTTCAGTGGTCGTCTCTGAAGGCCAGCGACACCGCAATGTACTACTGTGCCCGTGCGAGCTATTTCGATCGTGGAACAGGGTATAGTTCTTGGTGGATGGATGTGTGGGGCCAAGGTACACTGGTCACCGTCAGCAGC (SEQ ID NO: 305).
ариабельная область легкой цепи P08G02
GAGCTCGATATTCAGATGACCCAGAGCCCTAGCAGCCTGAGCGCAAGCGTGGGCGATAGAGTGACCATTACCTGTAGGGCCTCACAATCCATATACGACTATTTGCACTGGTATCAGCAGAAACCCGGGAAAGCACCCAAACTGCTGATTTACGATGCTTCCAACCTACAGAGTGGCGTTCCTTCACGTTTTAGCGGTAGCGGTTCAGGCACCGATTTCACCCTGACCATTAGCAGCCTTCAGCCCGAAGATTTCGCTACGTATTATTGCCAGCAATCATACACCACGCCGTTGTTTACATTCGGCCAGGGTACCAAAGTGGAAATCAAA (SEQ ID NO: 306).
В еще одних вариантах осуществления композиция содержит один или оба полинуклеотида, представленных под SEQ ID NO: 307 и SEQ ID NO: 308 ниже:
вариабельная область тяжелой цепи P08F08
GAAGTGCAGCTTGTCCAGAGCGGAGCCGAAGTGAAGAAGCCTGGCGAGAGCCTGAAGATCAGCTGCAAGGGCTCCGGATACGGATTCACAAGTTATTGGATAGGTTGGGTGCGCCAGATGCCTGGTAAGGGACTGGAATGGATGGGTATCATTCATCCCGATGATAGCGACACCAAATACAGCCCAAGCTTTCAGGGCCAGGTCACAATCAGCGCTGACAAGAGCATCAGCACCGCCTACCTTCAGTGGTCGTCTCTGAAGGCCAGCGACACCGCAATGTACTACTGTGCCTCTAGCTATTTGCGTGGCTTGTGGGGAGGCTATTTTGACTATTGGGGCCAAGGTACACTGGTCACCGTCAGCAGC (SEQ ID NO: 307)
вариабельная область легкой цепи P08F08
GAGCTCCAGAGCGTGCTGACCCAGCCTCCTAGCGCAAGCGGCACCCCTGGACAGCGTGTGACAATTAGCTGTAGCGGATCAAGCTCAAACATTGGCTCAAATTATGTGAATTGGTATCAGCAATTGCCCGGTACAGCACCCAAACTGCTCATTTATGGAGATTATCAACGACCTAGCGGAGTGCCTGATCGTTTTAGCGGTAGCAAAAGCGGCACCAGCGCATCACTGGCAATTTCAGGCCTGCGTAGCGAAGATGAGGCGGATTATTACTGTGCTACCCGCGACGATTCGTTATCTGGGTCTGTCGTTTTTGGCACCGGTACAAAACTGACCGTGCTG (SEQ ID NO: 308).
В еще одних вариантах осуществления композиция содержит один или оба полинуклеотида, представленных под SEQ ID NO: 309 и SEQ ID NO: 310 ниже:
вариабельная область тяжелой цепи P15D02
GAAGTGCAGCTTGTCCAGAGCGGAGCCGAAGTGAAGAAGCCTGGCGAGAGCCTGAAGATCAGCTGCAAGGGCTCCGGATACAGTTTTGCCTCATACTGGATCGGTTGGGTGCGCCAGATGCCTGGTAAGGGACTGGAATGGATGGGCGTAATTTACCCCGGAACTAGCGAGACACGTTACAGCCCAAGCTTTCAGGGCCAGGTCACAATCAGCGCTGACAAGAGCATCAGCACCGCCTACCTTCAGTGGTCGTCTCTGAAGGCCAGCGACACCGCAATGTACTACTGCGCTAAAGGGTTGAGTGCGAGTGCAAGTGGATATTCTTTCCAATATTGGGGCCAAGGTACACTGGTCACCGTCAGCAGC (SEQ ID NO: 309)
вариабельная область легкой цепи P15D032
GAGCTCGATATTCAGATGACCCAGAGCCCTAGCAGCCTGAGCGCAAGCGTGGGCGATAGAGTGACCATTACCTGTAGGGCCTCACAAAGCATCGACACATATTTAAACTGGTATCAGCAGAAACCCGGGAAAGCACCCAAACTGCTGATTTATTCAGCTAGTAGCCTACACAGTGGCGTTCCTTCACGTTTTAGCGGTAGCGGTTCAGGCACCGATTTCACCCTGACCATTAGCAGCCTTCAGCCCGAAGATTTCGCTACGTATTATTGCCAACAATCATACAGCACAACTGCTTGGACATTCGGCCAGGGTACCAAAGTGGAAATCAAA (SEQ ID NO: 310).
В данном документе дополнительно описаны векторы экспрессии и введение композиций полинуклеотида.
В другом аспекте настоящего изобретения представлен способ получения любого из полинуклеотидов, описанных в данном документе.
Настоящим изобретением также охвачены полинуклеотиды, комплементарные любым таким последовательностям. Полинуклеотиды могут являться однонитевыми (кодирующими или антисмысловыми) или двухнитевыми и могут представлять собой ДНК (геномную, кДНК или синтетическую) или молекулы РНК. Молекулы РНК включают молекулы HnRNA, которые содержат интроны и соответствуют молекуле ДНК «один-к-одному» и молекулы мРНК, которые не содержат интронов. Дополнительные кодирующие или некодирующие последовательности могут, но необязательно, быть представлены в полинуклеотиде по настоящему изобретению, и при этом полинуклеотид может, но необязательно, быть связанным с другими молекулами и/или вспомогательными материалами.
Полинуклеотиды могут содержать нативную последовательность (т. е. эндогенную последовательность, которая кодирует антитело или его часть) или могут содержать вариант такой последовательности. Полинуклеотидные варианты содержат одну или более замен, добавлений, делеций и/или вставок, при условии, что иммунореактивность кодирующего полипептида не уменьшается по сравнению с нативной иммунореактивной молекулой. Эффект в отношении иммунореактивности кодируемого полипептида в целом можно оценить так, как это описано в данном документе. Варианты в вариантах осуществления характеризуются по меньшей мере приблизительно 70% идентичностью, по меньшей мере приблизительно 80% идентичностью, по меньшей мере приблизительно 90% идентичностью или по меньшей мере приблизительно 95% идентичностью с полинуклеотидной последовательностью, которая кодирует нативное антитело или его часть.
Две полинуклеотидные или полипептидные последовательности называются «идентичными», если последовательность нуклеотидов или аминокислот в этих двух последовательностях одинакова при выравнивании для установления максимального сходства, как это описано ниже. Сравнения двух последовательностей, как правило, выполняют путем сравнения последовательностей в окне сравнения для идентификации и сравнения локальных областей сходства последовательности. Термин «окно сравнения», используемый в данном документе, относится к сегменту из по меньшей мере приблизительно 20 смежных положений, обычно от 30 до приблизительно 75 или от 40 до приблизительно 50, в которых последовательность можно сравнить с эталонной последовательностью такого же количества смежных положений после того, как две последовательности оптимально выровнены.
Оптимальное выравнивание последовательностей для сравнения можно проводить с использованием программы Megalign в комплекте программного обеспечения для биоинформатики Lasergene (DNASTAR, Inc., Мадисон, Висконсин, США) с использованием стандартных параметров. Данная компьютерная программа реализует несколько схем выравнивания, описанных в следующих ссылках: Dayhoff, M.O., 1978, A model of evolutionary change in proteins - Matrices for detecting distant relationships. In Dayhoff, M.O. (ed.) Atlas of Protein Sequence and Structure, National Biomedical Research Foundation, Washington DC Vol. 5, Suppl. 3, pp. 345-358; Hein J., 1990, Unified Approach to Alignment and Phylogenes pp. 626-645 Methods in Enzymology vol. 183, Academic Press, Inc., San Diego, CA; Higgins, D.G. and Sharp, P.M., 1989, CABIOS 5:151-153; Myers, E.W. and Muller W., 1988, CABIOS 4:11-17; Robinson, E.D., 1971, Comb. Theor. 11:105; Santou, N., Nes, M., 1987, Mol. Biol. Evol. 4:406-425; Sneath, P.H.A. and Sokal, R.R., 1973, Numerical Taxonomy the Principles and Practice of Numerical Taxonomy, Freeman Press, San Francisco, CA; Wilbur, W.J. and Lipman, D.J., 1983, Proc. Natl. Acad. Sci. USA 80:726-730.
«Процентное значение идентичности последовательности» определяют путем сравнения двух оптимально выровненных последовательностей в окне сравнения из по меньшей мере 20 положений, где часть полинуклеотидной или полипептидной последовательности в окне сравнения может содержать добавления или делеции (т. е. гэпы), составляющие 20 процентов или меньше, обычно от 5 до 15 процентов или от 10 до 12 процентов по сравнению с эталонными последовательностями (которые не содержат добавлений или делеций) для оптимального выравнивания двух последовательностей. Процентное значение рассчитывают путем определения числа положений, в которых встречаются идентичные основания нуклеиновых кислот или аминокислотный остаток в обоих последовательностях с получением количества совпавших положений, разделения количества совпавших положений на общее количество положений в эталонной последовательности (т. е. размер окна) и умножения результатов на 100 с получением процентного значения идентичности последовательности.
Также или в качестве альтернативы варианты могут являться по сути гомологичными нативному гену или его части или их комплементарной последовательности. Эти полинуклеотидные варианты способны к гибридизации в умеренно-жестких условиях со встречающейся в природе последовательностью ДНК, кодирующей нативное антитело (или комплементарной последовательностью).
Подходящие «умеренно-жесткие условия» включают предварительную отмывку в растворе 5 X SSC, 0,5% SDS, 1,0 мМ EDTA (pH 8,0); гибридизацию при 50°C - 65°C, 5 X SSC в течение ночи с последующей двухкратной отмывкой при 65°C в течение 20 минут с каждым из 2X, 0,5X и 0,2X SSC, содержащим 0,1% SDS.
Используемые в данном документе «очень жесткие условия» или «условия с высокой жесткостью» являются следующими: (1) использование низкой ионной силы и высокой температуры для отмывки, например, 0,015 M хлорида натрия/0,0015 M цитрата натрия/0,1% натрий додецилсульфата при 50°C; (2) использование в ходе гибридизации средства для денатурации, такого как формамид, например, 50% (об./об.) формамида с 0,1% бычьим сывороточным альбумином/0,1% фиколла/0,1% поливинилпирролидона/50 мМ натрий-фосфатного буфера при pH 6,5 с 750 мМ хлорида натрия, 75 мМ цитрата натрия при 42°C; или (3) использование 50% формамида, 5 x SSC (0,75 M NaCl, 0,075 M цитрата натрия), 50 мМ фосфата натрия (pH 6,8), 0,1% пирофосфата натрия, 5 x раствора Денхардта, подвергнутый воздействию ультразвука раствор ДНК спермы лосося (50 мкг/мл), 0,1% SDS и 10% сульфат декстрана при 42°C с отмывкой при 42°C в 0,2 x SSC (хлорид натрия/цитрат натрия) и 50% формамида при 55°C с последующей отмывкой в условиях высокой жесткости, состоящий из 0,1 x SSC, содержащий EDTA при 55°C. Специалист в данной области техники поймет как отрегулировать температуру, ионную силу и т. д., в случае необходимости подстроиться под такие факторы, как длина зонда и т. п.
Специалистам в данной области техники будет понятно, что в результате вырожденности генетического кода существует множество нуклеотидных последовательностей, которые кодируют полипептид, описанный в данном документе. Некоторые из этих полинуклеотидов обладают минимальной гомологией с нуклеотидной последовательностью любого нативного гена. Тем не менее, полинуклеотиды, которые различаются из-за отличий в используемости кодонов, специально представлены в настоящем изобретении. Кроме того, аллели генов, содержащих полинуклеотидные последовательности, представленные в данном документе, находятся в пределах объема настоящего изобретения. Аллели представляют собой эндогенные гены, которые изменяются в результате одной или более мутаций, такой как делеции, добавления и/или замены нуклеотидов. Полученные мРНК и белок могут, но необязательно, иметь измененные структуру или функцию. Аллели можно идентифицировать с применением стандартных методик (например, гибридизации, амплификации и/или сравнения базы данных последовательностей).
Полинуклеотиды по настоящему изобретению можно получать с применением химического синтеза, рекомбинантных способов или ПЦР. Способы химического синтеза полинуклеотидов хорошо известны из уровня техники и не нуждаются в подробном описании в данном документе. Специалист в данной области может применять последовательности, представленные в данном документе, и коммерческий ДНК-синтезатор для получения требуемой последовательности ДНК.
Для получения полинуклеотидов с применением рекомбинантных способов, полинуклеотид, содержащий требуемую последовательность можно поместить в подходящий вектор, и вектор, в свою очередь, можно внедрить в подходящую клетку-хозяина для репликации и амплификации, как дополнительно рассмотрено в данном документе. Полинуклеотиды можно поместить в клетки-хозяева с помощью способов, известных из уровня техники. Клетки трансформируют путем введения экзогенного полинуклеотида с помощью непосредственного введения, эндоцитоза, трансфекции, F-спаривания или электропорации. После введения экзогенный полинуклеотид можно сохранять в клетке в качестве неинтегрируемого вектора (такого как плазмида) или интегрировать в геном клетки-хозяина. Амплифицированный таким образом полинуклеотид можно выделить из клетки-хозяина с помощью способов, хорошо известных из уровня техники. См., например, Sambrook et al., 1989.
В качестве альтернативы ПЦР обеспечивает возможность воспроизведения последовательностей ДНК. Технология ПЦР хорошо известна из уровня техники и описана в патентах США № 4683195, 4800159, 4754065 и 4683202, а также ПЦР: The Polymerase Chain Reaction, Mullis et al. eds., Birkauswer Press, Boston, 1994.
РНК можно получать путем использования выделенной ДНК в подходящем векторе и введения его в подходящую клетку-хозяина. Когда клетки воспроизводятся путем клеточного деления и ДНК транскрибируется в РНК, РНК затем можно выделить с применением способов, хорошо известных специалистам в данной области техники, как это представлено ранее, например в Sambrook et al., 1989.
Подходящие клонирующие векторы могут быть сконструированы согласно стандартным методикам или могут быть выбраны из большого количества клонирующих векторов, доступных в данной области техники. Хотя выбираемый клонирующий вектор может варьироваться в зависимости от клетки-хозяина, предназначенной для использования, применимые клонирующие векторы будут, как правило, обладать способностью к саморепликации, могут содержать отдельную мишень для конкретной рестрикционной эндонуклеазы и/или могут нести гены для маркера, который может использоваться при отборе клонов, содержащих вектор. Подходящие примеры включают плазмиды и бактериальные вирусы, например, pUC18, pUC19, Bluescript (например, pBS SK+) и их производные, mp18, mp19, pBR322, pMB9, ColE1, pCR1, RP4, ДНК фагов и бифункциональные векторы, например pSA3 и pAT28. Эти и многие другие клонирующие векторы доступны от коммерческих производителей, таких как BioRad, Strategene и Invitrogen.
Векторы экспрессии обычно представляют собой конструкции на основе реплицируемых полинуклеотидов, которые содержат полинуклеотид в соответствии с настоящим изобретением. Предполагается, что вектор экспрессии должен быть способен к репликации в клетках-хозяевах либо в виде эписом, либо в виде составляющей хромосомной ДНК. Подходящие векторы экспрессии включают без ограничения плазмиды, вирусные векторы, в том числе аденовирусы, аденоассоциированные вирусы, ретровирусы, космиды и вектор (векторы) экспрессии, раскрытые в публикации по PCT № WO87/04462, или лентивирусные векторы pLVX, доступные от Clonetech. Компоненты вектора обычно могут включать без ограничения одно или более из следующего: сигнальную последовательность; точку начала репликации; один или более маркерных генов; подходящие элементы контроля транскрипции (такие как промоторы, энхансеры и терминатор). Для экспрессии (т. е. трансляции) также обычно требуются один или более элементов контроля транскрипции, например, сайты связывания рибосом, сайты инициации трансляции и стоп-кодоны.
Векторы, содержащие представляющие интерес полинуклеотиды, можно вводить в клетку-хозяина с помощью любого ряда подходящих способов, включая электропорацию, трансфекцию с использованием хлорида кальция, хлорида рубидия, фосфата кальция, DEAE-декстрана или других веществ; бомбардировку микрочастицами; липофекцию и инфекцию (например, где вектор представляет собой инфицирующее средство, например вирус осповакцины). Выбор вводимых векторов или полинуклеотидов будет часто зависеть от свойств клетки-хозяина.
Полинуклеотид, кодирующий CAR, специфический к CD70, раскрытый в данном документе, может присутствовать в кассете экспрессии или векторе экспрессии (например, плазмиде, предназначенной для введения в бактериальную клетку-хозяина, или в вирусном векторе, таком как бакуловирусный вектор, предназначенный для трансфекции клетки-хозяина насекомого, или в плазмидном или вирусном векторе, таком как лентивирус, предназначенном для трансфекции клетки-хозяина млекопитающего). В некоторых вариантах осуществления полинуклеотид или вектор может включать последовательность нуклеиновой кислоты, кодирующую последовательности с рибосомным «проскоком», такие как, например, без ограничения, последовательность, кодирующая пептид 2А. Пептиды 2А, которые были идентифицированы в подгруппе афтовирусы пикорнавирусов, вызывают рибосомный «проскок» от одного кодона к другому без образования пептидной связи между двумя аминокислотами, кодируемыми кодонами (см. (Donnelly and Elliott 2001; Atkins, Wills et al. 2007; Doronina, Wu et al. 2008)). Под «кодоном» подразумевают три нуклеотида на мРНК (или на смысловой нити молекулы ДНК), которые транслируются рибосомой в один аминокислотный остаток. Таким образом, два полипептида могут быть синтезированы из одной непрерывной открытой рамки считывания в мРНК, когда полипептиды разделены последовательностью олигопептида 2А, которая находится в рамке. Такие механизмы рибосомного «проскока» хорошо известны в данной области техники и, как известно, используются несколькими векторами для экспрессии нескольких белков, кодируемых одной информационной РНК.
Для направления трансмембранных полипептидов в секреторный путь клетки-хозяина в некоторых вариантах осуществления секреторная сигнальная последовательность (также известная как лидерная последовательность, препропоследовательность или пре-последовательность) предоставляется в полинуклеотидной последовательности или последовательности вектора. Секреторная сигнальная последовательность функционально связана с трансмембранной последовательностью нуклеиновой кислоты, т. е. две последовательности соединены в правильной рамке считывания и расположены так, чтобы направлять вновь синтезированный полипептид в секреторный путь клетки-хозяина. Как правило, секреторные сигнальные последовательности располагаются в 5’-направлении от последовательности нуклеиновой кислоты, кодирующей представляющий интерес полипептид, хотя некоторые секреторные сигнальные последовательности могут быть расположены в другом месте в представляющей интерес последовательности нуклеиновой кислоты (см., например, Welch et al., патент США № 5037743; Holland et al., патент США № 5143830). В некоторых вариантах осуществления сигнальный пептид содержит аминокислотную последовательность, представленную под SEQ ID NO: 266 или 277. Специалисты в данной области техники поймут, что ввиду вырожденности генетического кода между указанными полинуклеотидными молекулами возможны значительные вариации последовательности. В некоторых вариантах осуществления последовательности нуклеиновой кислоты по настоящему изобретению оптимизированы по кодонам для экспрессии в клетках млекопитающих или в некоторых вариантах осуществления для экспрессии в клетках человека. Оптимизация кодонов относится к замене кодонов в представляющей интерес последовательности, которые, как правило, являются редкими в генах с высокой экспрессией у данного вида, на кодоны, которые, как правило, часто встречаются в генах с высокой экспрессией у таких видов, такими кодонами, кодирующими аминокислоты, как кодоны, которые подвергаются обмену.
АНТИТЕЛА, СПЕЦИФИЧЕСКИЕ К CD70, И СПОСОБЫ ИХ ПОЛУЧЕНИЯ
В данном документе представлены антитела к CD70.
В некоторых вариантах осуществления антитело к CD70 по настоящему изобретению содержит любую из частичных последовательностей легкой цепи, перечисленных в таблице 1, и/или любую одну из частичных последовательностей тяжелой цепи, перечисленных в таблице 1. В таблице 1 подчеркнутые последовательности представляют собой последовательности CDR согласно Кабату и жирным шрифтом согласно Чотиа.
В таблицах 2A - 2B представлены примеры последовательностей CDR антител к CD70, представленных в данном документе.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело (например, включающее фрагменты антитела, такие как одноцепочечные вариабельные фрагменты (scFv), которые специфически связываются с кластером дифференцировки 70 (CD70)), где антитело содержит (а) вариабельную область тяжелой цепи (VH), содержащую (i) первую область, определяющую комплементарность (CDR1), VH, содержащую последовательность, представленную под SEQ ID NO: 49, 50, 51, 55, 56, 57, 61, 62, 63, 67, 68, 69, 73, 74, 75, 79, 80, 81, 85, 86, 87, 91, 92, 93, 97, 98, 99, 103, 104, 105, 109, 110, 111, 115, 116, 117, 121, 122, 123, 127, 128, 129, 133, 134, 135, 139, 140, 141, 145, 146, 147, 151, 152, 153, 157, 158, 159, 163, 164, 165, 169, 170, 171, 175, 176, 177, 181, 182, 183, 187, 188, 189, 382, 383, 384, 388, 389, 390, 394, 395, 396, 400, 401, 402, 406, 407, 408, 412, 413, 414, 418, 419, 420, 424, 425, 426, 430, 431, 432, 663, 664, 665, 436, 437, 438, 442, 443, 444, 448, 449, 450, 454, 455, 456, 460, 461, 462, 466, 467, 468, 472, 473, 474, 478, 479, 480, 484, 485, 486, 490, 491, 492, 496, 497, 498, 502, 503, 504, 508, 509 или 510; (ii) CDR2 VH, содержащую последовательность, представленную под SEQ ID NO: 52, 53, 58, 59, 64, 65, 70, 71, 76, 77, 82, 83, 88, 89, 94, 95, 100, 101, 106, 107, 112, 113, 118, 119, 124, 125, 130, 131, 136, 137, 142, 143, 148, 149, 154, 155, 160, 161, 166, 167, 172, 173, 178, 179, 184, 185, 190, 191, 385, 386, 391, 392, 397, 398, 403, 404, 409, 410, 415, 416, 421, 422, 427, 428, 433, 434, 666, 667, 439, 440, 445, 446, 451, 452, 457, 458, 463, 464, 469, 470, 475, 476, 481, 482, 487, 488, 493, 494, 499, 500, 505, 506, 511 или 512; и iii) CDR3 VH, содержащую последовательность, представленную под SEQ ID NO: 54, 60, 66, 72, 78, 84, 90, 96, 102, 108, 114, 120, 126, 132, 138, 144, 150, 156, 162, 168, 174, 180, 186, 192, 387, 393, 399, 405, 411, 417, 423, 429, 435, 668, 441, 447, 453, 459, 465, 471, 477, 483, 489, 495, 501, 507 или 513; и/или вариабельную область легкой цепи (VL), содержащую (i) CDR1 VL, содержащую последовательность, представленную под SEQ ID NO: 193, 196, 199, 202, 205, 208, 211, 214, 217, 220, 223, 226, 229, 232, 235, 238, 241, 244, 247, 250, 253, 256, 259, 262, 514, 517, 520, 523, 526, 529, 532, 535, 538, 669, 541, 544, 547, 550, 553, 556, 559, 562, 565, 568, 571, 574 или 577; (ii) CDR2 VL, содержащую последовательность, представленную под SEQ ID NO: 194, 197, 200, 203, 206, 209, 212, 215, 218, 221, 224, 227, 230, 233, 236, 239, 242, 245, 248, 251, 254, 257, 260, 263, 515, 518, 521, 524, 527, 530, 533, 536, 539, 670, 542, 545, 548, 551, 554, 557, 560, 563, 566, 569, 572, 575 или 578; и (iii) CDR3 VL, содержащую последовательность, представленную под SEQ ID NO: 195, 198, 201, 204, 207, 210, 213, 216, 219, 222, 225, 228, 231, 234, 237, 240, 243, 246, 249, 252, 255, 258, 261, 264, 516, 519, 522, 525, 528, 531, 534, 537, 540, 671, 543, 546, 549, 552, 555, 558, 561, 564, 567, 570, 573, 576 или 579.
В некоторых вариантах осуществления настоящего изобретения представлено антитело (например, scFv), которое специфически связывается с кластером дифференцировки 70 (CD70), где указанное антитело содержит вариабельную область тяжелой цепи (VH), содержащую CDR1 VH, CDR2 VH и CDR3 VH из последовательности VH, представленной под SEQ ID NO: 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38, 40, 42, 44, 46, 48, 339, 341, 343, 345, 347, 349, 351, 353, 355, 662, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379 или 381; и/или вариабельную область (VL) легкой цепи, содержащую CDR1 VL, CDR2 VL и CDR3 VL из последовательности VL, представленной под SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 338, 340, 342, 344, 346, 348, 350, 352, 354, 661, 356, 358, 360, 362, 364, 366, 368, 370, 372, 374, 376, 378 или 380.
В некоторых вариантах осуществления настоящего изобретения представлено выделенное антитело, которое специфически связывается с CD70 и конкурирует с любым из вышеуказанных антител.
В некоторых вариантах осуществления настоящего изобретения представлено антитело, которое связывается с CD70 и конкурирует с антителом, описанным в данном документе, включая 31H1, 63B2, 40E3, 42C3, 45F11, 64F9, 72C2, 2F10, 4F11, 10H10, 17G6, 65E11, P02B10, P07D03, P08A02, P08E02, P08F08, P08G02, P12B09, P12F02, P12G07, P13F04, P15D02, P16C05, 10A1, 10E2, 11A1, 11C1, 11D1, 11E1, 12A2, 12C4, 12C5, 12D3, 12D6, 12D7, 12F5, 12H4, 8C8, 8F7, 8F8, 9D8, 9E10, 9E5, 9F4 или 9F8.
В некоторых вариантах осуществления настоящего изобретения также представлены части CDR антител к CD70 на основе контактных областей CDR. Контактные области CDR являются областями антитела, которые придают специфичность антителу к антигену. В целом контактные области CDR включают положения остатков в CDR и верньерных зонах, которые ограничены для поддержания надлежащей структуры петли с целью обеспечения связывания антитела со специфическим антигеном. См., например, Makabe et al., J. Biol. Chem., 283:1156-1166, 2007. Определение контактных областей CDR хорошо известно специалистам в данной области техники.
Аффинность связывания (KD) антитела к CD70, описанного в данном документе, с CD70 (например, CD70 человека (например, (SEQ ID NO: 335)) может составлять от приблизительно 0,001 до приблизительно 5000 нМ. В некоторых вариантах осуществления аффинность связывания составляет приблизительно 5000 нМ, 4500 нМ, 4000 нМ, 3500 нМ, 3000 нМ, 2500 нМ, 2000 нМ, 1789 нМ, 1583 нМ, 1540 нМ, 1500 нМ, 1490 нМ, 1064 нМ, 1000 нМ, 933 нМ, 894 нМ, 750 нМ, 705 нМ, 678 нМ, 532 нМ, 500 нМ, 494 нМ, 400 нМ, 349 нМ, 340 нМ, 353 нМ, 300 нМ, 250 нМ, 244 нМ, 231 нМ, 225 нМ, 207 нМ, 200 нМ, 186 нМ, 172 нМ, 136 нМ, 113 нМ, 104 нМ, 101 нМ, 100 нМ, 90 нМ, 83 нМ, 79 нМ, 74 нМ, 54 нМ, 50 нМ, 45 нМ, 42 нМ, 40 нМ, 35 нМ, 32 нМ, 30 нМ, 25 нМ, 24 нМ, 22 нМ, 20 нМ, 19 нМ, 18 нМ, 17 нМ, 16 нМ, 15 нМ, 12 нМ, 10 нМ, 9 нМ, 8 нМ, 7,5 нМ, 7 нМ, 6,5 нМ, 6 нМ, 5,5 нМ, 5 нМ, 4 нМ, 3 нМ, 2 нМ, 1 нМ, 0,5 нМ, 0,3 нМ, 0,1 нМ, 0,01 нМ или 0,001 нМ. В некоторых вариантах осуществления аффинность связывания составляет меньше приблизительно любого из значений 5000 нМ, 4000 нМ, 3000 нМ, 2000 нМ, 1000 нМ, 900 нМ, 800 нМ, 250 нМ, 200 нМ, 100 нМ, 50 нМ, 30 нМ, 20 нМ, 10 нМ, 7,5 нМ, 7 нМ, 6,5 нМ, 6 нМ, 5 нМ, 4,5 нМ, 4 нМ, 3,5 нМ, 3 нМ, 2,5 нМ, 2 нМ, 1,5 нМ, 1 нМ или 0,5 нМ.
В некоторых вариантах осуществления настоящего изобретения представлена нуклеиновая кислота, кодирующая любое из указанных выше выделенных антител. В некоторых вариантах осуществления настоящего изобретения представлен вектор, содержащий такую нуклеиновую кислоту. В некоторых вариантах осуществления настоящего изобретения представлена клетка-хозяин, содержащая такую нуклеиновую кислоту.
В настоящем изобретении также представлены любые антитела из вышеуказанных антител для применения в качестве лекарственного препарата. В некоторых вариантах осуществления лекарственный препарат предназначен для применения в лечении видов рака, связанных с CD70, выбранных из группы, состоящей из почечно-клеточной карциномы, глиобластомы, глиомы, такой как глиома низкой степени злокачественности, неходжкинской лимфомы (NHL), болезни Ходжкина (HD), макроглобулинемии Вальденстрема, острого миелоидного лейкоза, множественной миеломы, диффузной крупноклеточной лимфомы, фолликулярной лимфомы или немелкоклеточного рака легкого.
В некоторых вариантах осуществления настоящего изобретения представлен способ лечения нуждающегося в этом субъекта, предусматривающий предоставление любого из вышеуказанных антител и введение указанного антитела указанному субъекту.
В некоторых вариантах осуществления настоящего изобретения представлена фармацевтическая композиция, содержащая любое из вышеуказанных антител.
В некоторых вариантах осуществления настоящего изобретения представлен способ лечения состояния, ассоциированного со злокачественными клетками, экспрессирующими CD70, у субъекта, предусматривающий введение нуждающемуся в этом субъекту эффективного количества любого из вышеуказанных антител или фармацевтической композиции, содержащей любое из вышеуказанных антител. В некоторых вариантах осуществления состояние представляет собой рак. В некоторых вариантах осуществления рак представляет собой рак, связанный с CD70, выбранный из группы, состоящей из почечно-клеточной карциномы, глиобластомы, глиомы, такой как глиома низкой степени злокачественности, неходжкинской лимфомы (NHL), болезни Ходжкина (HD), макроглобулинемии Вальденстрема, острого миелоидного лейкоза, множественной миеломы, диффузной крупноклеточной лимфомы, фолликулярной лимфомы или немелкоклеточного рака легкого.
В некоторых вариантах осуществления настоящего изобретения представлен способ подавления роста или прогрессирования опухоли у субъекта, у которого имеются злокачественные клетки, экспрессирующие CD70, предусматривающий введение нуждающемуся в этом субъекту эффективного количества фармацевтической композиции по настоящему изобретению.
В некоторых вариантах осуществления настоящего изобретения представлен способ подавления метастазирования злокачественных клеток, экспрессирующих CD70, у субъекта, предусматривающий введение нуждающемуся в этом субъекту эффективного количества фармацевтической композиции по настоящему изобретению.
В некоторых вариантах осуществления настоящего изобретения представлен способ индуцирования регрессии опухоли у субъекта, у которого имеются злокачественные клетки, экспрессирующие CD70, предусматривающий введение нуждающемуся в этом субъекту эффективного количества фармацевтической композиции по настоящему изобретению.
В некоторых вариантах осуществления для получения антитела предусмотрено культивирование клетки-хозяина в условиях, которые приводят к продуцированию антитела, и выделение антитела из клетки-хозяина или культуры клеток.
Антитела, применимые в настоящем изобретении, могут охватывать моноклональные антитела, поликлональные антитела, фрагменты антител (например, Fab, Fab’, F(ab’)2, Fv, Fc и т. д.), химерные антитела, биспецифические антитела, гетероконъюгатные антитела, одноцепочечные (ScFv) антитела, их мутантные формы, слитые белки, содержащие часть антитела (например, домен антитела), гуманизированные антитела и любую другую модифицированную конфигурацию молекулы иммуноглобулина, которая содержит антигенраспознающий участок требуемой специфичности, включая варианты гликозилирования антител, варианты аминокислотной последовательности антител и ковалентно модифицированные антитела. Антитела могут быть мышиными, крысиными, человеческими или любого другого происхождения (в том числе химерными или гуманизированными антителами).
В некоторых вариантах осуществления описанное в данном документе моноспецифическое антитело к CD70 представляет собой моноклональное антитело. Например, моноспецифическое антитело к CD70 представляет собой моноклональное антитело человека.
В настоящем изобретении также представлены следующие иллюстративные варианты осуществления:
1. Выделенное антитело, которое специфически связывается с кластером дифференцировки 70 (CD70), где антитело содержит:
(а) вариабельную область тяжелой цепи (VH), содержащую (i) область один, определяющую комплементарность (CDR1), VH, которая содержит последовательность, представленную под SEQ ID NO: 49, 50, 51, 55, 56, 57, 61, 62, 63, 67, 68, 69, 73, 74, 75, 79, 80, 81, 85, 86, 87, 91, 92, 93, 97, 98, 99, 103, 104, 105, 109, 110, 111, 115, 116, 117, 121, 122, 123, 127, 128, 129, 133, 134, 135, 139, 140, 141, 145, 146, 147, 151, 152, 153, 157, 158, 159, 163, 164, 165, 169, 170, 171, 175, 176, 177, 181, 182, 183, 187, 188, 189, 382, 383, 384, 388, 389, 390, 394, 395, 396, 400, 401, 402, 406, 407, 408, 412, 413, 414, 418, 419, 420, 424, 425, 426, 430, 431, 432, 663, 664, 665, 436, 437, 438, 442, 443, 444, 448, 449, 450, 454, 455, 456, 460, 461, 462, 466, 467, 468, 472, 473, 474, 478, 479, 480, 484, 485, 486, 490, 491, 492, 496, 497, 498, 502, 503, 504, 508, 509 или 510 (ii) CDR2 VH, содержащую последовательность, представленную под SEQ ID NO: 52, 53, 58, 59, 64, 65, 70, 71, 76, 77, 82, 83, 88, 89, 94, 95, 100, 101, 106, 107, 112, 113, 118, 119, 124, 125, 130, 131, 136, 137, 142, 143, 148, 149, 154, 155, 160, 161, 166, 167, 172, 173, 178, 179, 184, 185, 190, 191, 385, 386, 391, 392, 397, 398, 403, 404, 409, 410, 415, 416, 421, 422, 427, 428, 433, 434, 666, 667, 439, 440, 445, 446, 451, 452, 457, 458, 463, 464, 469, 470, 475, 476, 481, 482, 487, 488, 493, 494, 499, 500, 505, 506, 511 или 512; и iii) CDR3 VH, содержащую последовательность, представленную под SEQ ID NO: 54, 60, 66, 72, 78, 84, 90, 96, 102, 108, 114, 120, 126, 132, 138, 144, 150, 156, 162, 168, 174, 180, 186, 192, 387, 393, 399, 405, 411, 417, 423, 429, 435, 668, 441, 447, 453, 459, 465, 471, 477, 483, 489, 495, 501, 507 или 513; и/или
(b) вариабельную область легкой цепи (VL), содержащую (i) CDR1 VL, которая содержит последовательность, представленную под SEQ ID NO: 193, 196, 199, 202, 205, 208, 211, 214, 217, 220, 223, 226, 229, 232, 235, 238, 241, 244, 247, 250, 253, 256, 259, 262, 514, 517, 520, 523, 526, 529, 532, 535, 538, 669, 541, 544, 547, 550, 553, 556, 559, 562, 565, 568, 571, 574 или 577; (ii) CDR2 VL, содержащую последовательность, представленную под SEQ ID NO: 194, 197, 200, 203, 206, 209, 212, 215, 218, 221, 224, 227, 230, 233, 236, 239, 242, 245, 248, 251, 254, 257, 260, 263, 515, 518, 521, 524, 527, 530, 533, 536, 539, 670, 542, 545, 548, 551, 554, 557, 560, 563, 566, 569, 572, 575 или 578; и (iii) CDR3 VL, содержащую последовательность, представленную под SEQ ID NO: 195, 198, 201, 204, 207, 210, 213, 216, 219, 222, 225, 228, 231, 234, 237, 240, 243, 246, 249, 252, 255, 258, 261, 264, 516, 519, 522, 525, 528, 531, 534, 537, 540, 671, 543, 546, 549, 552, 555, 558, 561, 564, 567, 570, 573, 576 или 579.
2. Выделенное антитело, которое специфически связывается с кластером дифференцировки 70 (CD70), где антитело содержит:
(a) область VH, содержащую CDR1 VH, CDR2 VH и CDR3 VH из последовательности VH, представленной под SEQ ID NO: 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38, 40, 42, 44, 46, 48, 339, 341, 343, 345, 347, 349, 351, 353, 355, 662, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379 или 381; и/или
(b) область VL, содержащую CDR1 VL, CDR2 VL и CDR3 VL из последовательности VL, представленной под SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 338, 340, 342, 344, 346, 348, 350, 352, 354, 661, 356, 358, 360, 362, 364, 366, 368, 370, 372, 374, 376, 378 или 380.
3. Выделенное антитело, которое специфически связывается с CD70 и конкурирует с антителом согласно варианту осуществления 1.
4. Нуклеиновая кислота, кодирующая антитело согласно любому из вариантов осуществления 1-3.
5. Вектор, содержащий нуклеиновую кислоту согласно варианту осуществления 4.
6. Клетка-хозяин, содержащая нуклеиновую кислоту согласно варианту осуществления 4.
7. Антитело согласно любому из вариантов осуществления 1-3 для применения в качестве лекарственного препарата.
8. Антитело согласно варианту осуществления 7, где лекарственный препарат предназначен для применения в лечении рака, связанного с CD70, выбранного из группы, состоящей из почечно-клеточной карциномы, глиобластомы, глиомы, такой как глиома низкой степени злокачественности, неходжкинской лимфомы (NHL), болезни Ходжкина (HD), макроглобулинемии Вальденстрема, острого миелоидного лейкоза, множественной миеломы, диффузной крупноклеточной лимфомы, фолликулярной лимфомы или немелкоклеточного рака легкого.
9. Способ лечения субъекта, нуждающегося в этом, предусматривающий:
обеспечение антитела согласно любому из вариантов осуществления 1-3 и
введение указанного антитела указанному субъекту.
10. Фармацевтическая композиция, содержащая антитело согласно любому из вариантов осуществления 1-3.
11. Способ лечения состояния, ассоциированного со злокачественными клетками, экспрессирующими CD70, у субъекта, предусматривающий введение нуждающемуся в этом субъекту эффективного количества антитела согласно любому из вариантов осуществления 1-3 или фармацевтической композиции согласно варианту осуществления 10.
12. Способ согласно варианту осуществления 11, где состояние представляет собой рак.
13. Способ согласно варианту осуществления 12, где рак представляет собой рак, связанный с CD70, выбранный из группы, состоящей из почечно-клеточной карциномы, глиобластомы, глиомы, такой как глиома низкой степени злокачественности, неходжкинской лимфомы (NHL), болезни Ходжкина (HD), макроглобулинемии Вальденстрема, острого миелоидного лейкоза, множественной миеломы, диффузной крупноклеточной лимфомы, фолликулярной лимфомы или немелкоклеточного рака легкого.
14. Способ подавления роста или прогрессирования опухоли у субъекта, у которого имеются злокачественные клетки, экспрессирующие CD70, предусматривающий введение нуждающемуся в этом субъекту эффективного количества фармацевтической композиции согласно варианту осуществления 10.
15. Способ подавления метастазирования злокачественных клеток, экспрессирующих CD70, у субъекта, предусматривающий введение нуждающемуся в этом субъекту эффективного количества фармацевтической композиции согласно варианту осуществления 10.
16. Способ индуцирования регрессии опухоли у субъекта, у которого имеются злокачественные клетки, экспрессирующие CD70, предусматривающий введение нуждающемуся в этом субъекту эффективного количества фармацевтической композиции согласно варианту осуществления 10.
17. Способ получения антитела, предусматривающий культивирование клетки-хозяина согласно варианту осуществления 6 в условиях, которые приводят к продуцированию антитела, и выделение антитела из клетки-хозяина или культуры клеток.
Способы конструирования иммунной клетки
В данном документе представлены способы получения иммунных клеток для применения в иммунотерапии. В некоторых вариантах осуществления способы предусматривают введение CAR в соответствии с настоящим изобретением в иммунные клетки и размножение клеток. В некоторых вариантах осуществления настоящее изобретение относится к способу конструирования иммунной клетки, предусматривающему: обеспечение клетки и обеспечение экспрессии на поверхности клетки по меньшей мере одного CAR, описанного выше. Способы конструирования иммунных клеток описаны, например, в публикациях патентных заявок по РСТ № WO/2014/039523, WO/2014/184741, WO/2014/191128, WO/2014/184744 и WO/2014/184143, каждая из которых во всей своей полноте включена в данный документ посредством ссылки. В некоторых вариантах осуществления способ предусматривает трансфицирование клетки по меньшей мере одним полинуклеотидом, кодирующим CAR, как описано выше, и экспрессию полинуклеотидов в клетке.
В некоторых вариантах осуществления полинуклеотиды присутствуют в лентивирусных векторах для стабильной экспрессии в клетках.
В некоторых вариантах осуществления способ может дополнительно предусматривать стадию генетического модифицирования клетки путем разрушения или инактивации по меньшей мере одного гена, экспрессирующего, например, без ограничения компонент TCR, мишень для иммуносупрессивного средства, ген HLA, CD70 и/или белок контрольной точки иммунного ответа, такой как, например, PDCD1 или CTLA-4. Под разрушением или инактивацией гена подразумевается, что представляющий интерес ген не экспрессируется в функциональной белковой форме. В некоторых вариантах осуществления ген, который подлежит разрушению или инактивации, выбран из группы, состоящей из, например, без ограничения TCRα, TCRβ, CD52, GR, PD-1, CD70 и CTLA-4. В некоторых вариантах осуществления способ предусматривает разрушение или инактивацию одного или более генов путем введения в клетки редкощепящей эндонуклеазы, способной селективно инактивировать ген путем селективного расщепления ДНК. В некоторых вариантах осуществления редкощепящая эндонуклеаза может представлять собой, например, нуклеазу с цинковыми пальцами (ZFN), нуклеазу megaTAL, мегануклеазу, эффекторную нуклеазу, подобную активатору транскрипции (TALE-нуклеазу), или эндонуклеазу, ассоциированную с CRISPR.
В некоторых вариантах осуществления дополнительный каталитический домен используется с редкощепящей эндонуклеазой для повышения ее способности инактивировать целевые гены. Например, дополнительный каталитический домен может быть ферментом процессинга конца ДНК. Неограничивающие примеры ферментов процессинга концов ДНК включают 5-3'-экзонуклеазы, 3-5'-экзонуклеазы, 5-3'-щелочные экзонуклеазы, 5'-флэп-эндонуклеазы, хеликазы, фосфатазы, гидролазы и матрично-независимые ДНК-полимеразы. Неограничивающие примеры такого каталитического домена включают белковый домен или каталитически активное производное белкового домена, выбранного из группы, состоящей из hExoI (EXO1_HUMAN), ExoI дрожжей (EXO1_YEAST), ExoI E. coli, TREX2 человека, TREX1 мыши, TREX1 человека, бычий TREX1, крысиный TREX1, TdT (терминальная дезоксинуклеотидилтрансфераза) ДНК2 человека, ДНК2 дрожжей (DNA2_YEAST). В некоторых вариантах осуществления дополнительный каталитический домен может характеризоваться 3'-5'-экзонуклеазной активностью, и в некоторых вариантах осуществления указанный дополнительный каталитический домен представляет собой TREX, как, например, каталитический домен TREX2 (WO2012/058458). В некоторых вариантах осуществления указанный каталитический домен кодируется одноцепочечным полипептидом TREX. Дополнительный каталитический домен может быть слит с белком, гибридизированным с нуклеазой, или с химерным белком. В некоторых вариантах осуществления дополнительный каталитический домен слит с применением, например, пептидного линкера.
В некоторых вариантах осуществления способ дополнительно предусматривает стадию введения в клетки экзогенной нуклеиновой кислоты, содержащей по меньшей мере последовательность, гомологичную части последовательности целевой нуклеиновой кислоты, таким образом, что гомологичная рекомбинация происходит между последовательностью целевой нуклеиновой кислоты и экзогенной нуклеиновой кислотой. В некоторых вариантах осуществления указанная экзогенная нуклеиновая кислота содержит первую и вторую части, которые гомологичны 5’- и 3'-областям последовательности целевой нуклеиновой кислоты соответственно. Экзогенная нуклеиновая кислота может также содержать третью часть, расположенную между первой и второй частями, которая не имеет гомологии с 5’- и 3'-областями последовательности целевой нуклеиновой кислоты. После расщепления последовательности целевой нуклеиновой кислоты стимулируется событие гомологичной рекомбинации между последовательностью целевой нуклеиновой кислоты и экзогенной нуклеиновой кислотой. В некоторых вариантах осуществления в донорской матрице можно использовать гомологичные последовательности, размер которых составляет по меньшей мере приблизительно 50 п.о., более приблизительно 100 п.о. или более приблизительно 200 п.о. Размер экзогенной нуклеиновой кислоты может составлять, например, без ограничения от приблизительно 200 п.о. до приблизительно 6000 п.о. или от приблизительно 1000 п.о. до приблизительно 2000 п.о. Участки общей гомологии нуклеиновых кислот расположены в областях, фланкирующих сайт внесения разрыва в 3'-5'-направлении и 5'-3'-направлении, а последовательность нуклеиновой кислоты, которая подлежит введению, расположена между двумя плечами.
В некоторых вариантах осуществления нуклеиновая кислота последовательно содержит первую область гомологии с последовательностями, расположенную выше указанного сайта расщепления; последовательность для инактивации целевого гена, выбранного из группы, состоящей из TCRα, TCRβ, CD52, CD70, глюкокортикоидного рецептора (GR), дезоксицитидинкиназы (DCK) и белка контрольной точки иммунного ответа, такого как, например, белок программируемой смерти-1 (PD-1); и вторую область гомологии с последовательностями, расположенную ниже сайта расщепления. Стадия введения полинуклеотида может осуществляться одновременно, до или после введения или экспрессии редкощепящей эндонуклеазы. В зависимости от местоположения целевой последовательности нуклеиновой кислоты, в которой произошло событие разрыва, такую экзогенную нуклеиновую кислоту можно использовать для нокаута гена, например, когда экзогенная нуклеиновая кислота находится в открытой рамке считывания гена, или для введения новых последовательностей или представляющих интерес генов. Вставки последовательностей с применением такой экзогенной нуклеиновой кислоты можно использовать для модифицирования существующего целевого гена путем внесения коррекции или замены гена (обмен аллелями - в качестве неограничивающего примера) или для повышения или понижения экспрессии целевого гена (обмен промоторами - в качестве неограничивающего примера), внесения коррекции или замены целевого гена. В некоторых вариантах осуществления инактивация гена, выбранного из группы, состоящей из TCRα, TCRβ, CD52, CD70, GR, DCK и белков иммунных контрольных точек, может быть проведена в точном геномном местоположении, на которое нацеливается специфическая TALE-нуклеаза, где указанная специфическая TALE-нуклеаза катализирует расщепление, и где экзогенная нуклеиновая кислота последовательно содержит по меньшей мере область гомологии и последовательность для инактивации одного целевого гена, выбранного из группы, состоящей из TCRα, TCRβ, CD52, CD70, GR, DCK, белков контрольных точек иммунного ответа, которые интегрируются посредством гомологичной рекомбинации. В некоторых вариантах осуществления несколько генов могут быть последовательно или одновременно разрушены или инактивированы с применением нескольких TALE-нуклеаз соответственно и специфического целенаправленного воздействия на один определенный ген и несколько конкретных полинуклеотидов для инактивации конкретного гена.
В некоторых вариантах осуществления способ предусматривает инактивацию одного или более дополнительных генов, выбранных из группы, состоящей из TCRα, TCRβ, CD52, CD70, GR, DCK и белков контрольных точек иммунного ответа. В некоторых вариантах осуществления инактивация гена может быть достигнута за счет введения в клетки по меньшей мере одной редкощепящей эндонуклеазы таким образом, что редкощепящая эндонуклеаза специфически катализирует расщепление целевой последовательности клеточного генома; и необязательного введения в клетки экзогенной нуклеиновой кислоты, последовательно содержащей первую область гомологии с последовательностями выше сайта расщепления, последовательность, которая должна быть вставлена в геном клетки, и вторую область гомологии с последовательностями ниже сайта расщепления; где введенная экзогенная нуклеиновая кислота инактивирует ген и интегрирует по меньшей мере одну экзогенную полинуклеотидную последовательность, кодирующую по меньшей мере один представляющий интерес рекомбинантный белок. В некоторых вариантах осуществления экзогенная полинуклеотидная последовательность интегрирована в ген, кодирующий белок, выбранный из группы, состоящей из TCRα, TCRβ, CD52, CD70, GR, DCK и белка контрольной точки иммунного ответа.
В другом аспекте стадия генетического модифицирования клеток может предусматривать модифицирование Т-клеток путем разрушения или инактивации по меньшей мере одного гена, экспрессирующего мишень для иммуносупрессивного средства, и размножение клеток необязательно в присутствии иммуносупрессивного средства. Иммуносупрессивное средство представляет собой средство, подавляющее иммунную функцию с помощью одного из нескольких механизмов действия. Иммуносупрессивное средство может уменьшать активность и/или выраженность иммунного ответа. Неограничивающие примеры иммуносупрессивных средств включают ингибиторы кальциневрина, мишени рапамицина, блокаторы α-цепи интерлейкина-2, ингибиторы инозинмонофосфатдегидрогеназы, ингибиторы дигидрофолатредуктазы, кортикостероиды и иммуносупрессивные антиметаболиты. Некоторые цитотоксические иммуносупрессоры действуют путем ингибирования синтеза ДНК. Другие могут действовать посредством активации Т-клеток или подавления активации хелперных клеток. Способы согласно настоящему изобретению наделяют Т-клетки иммуносупрессивной устойчивости при иммунотерапии путем разрушения или инактивации мишени для иммуносупрессивного средства в Т-клетках. В качестве неограничивающих примеров мишени для иммуносупрессивного средства могут представлять собой рецептор для иммуносупрессивного средства, такой как, например, без ограничения CD52, глюкокортикоидный рецептор (GR), представители семейства генов FKBP и представители семейства генов циклофилинов.
В некоторых вариантах осуществления генетическая модификация согласно данному способу включает экспрессию в предоставленных для конструирования клетках одной редкощепящей эндонуклеазы, вследствие чего редкощепящая эндонуклеаза специфически катализирует расщепление в одном целевом гене, за счет чего обеспечивается разрушение или инактивация целевого гена. В некоторых вариантах осуществления способ конструирования клеток предусматривает по меньшей мере одну из следующих стадий: обеспечение Т-клетки, такой как, например, из культуры клеток или из образца крови; выбор гена в Т-клетке, экспрессирующей мишень для иммуносупрессивного средства; введение в Т-клетку редкощепящей эндонуклеазы, способной посредством расщепления ДНК (в некоторых вариантах осуществления путем введения двухнитевого разрыва) селективно инактивировать ген, кодирующий мишень для иммуносупрессивного средства, и размножение клеток необязательно в присутствии иммуносупрессивного средства.
В некоторых вариантах осуществления способ предусматривает: обеспечение Т-клетки, такой как, например, из культуры клеток или из образца крови; выбор гена в Т-клетке, где ген экспрессирует мишень для иммуносупрессивного средства; трансфицирование Т-клетки посредством нуклеиновой кислоты, кодирующей редкощепящую эндонуклеазу, способную посредством расщепления ДНК (в некоторых вариантах осуществления путем введения двухнитевого разрыва) селективно инактивировать ген, кодирующий мишень для иммуносупрессивного средства, и экспрессирование редкощепящих эндонуклеаз в Т-клетках; и размножение клеток необязательно в присутствии иммуносупрессивного средства.
В некоторых вариантах осуществления редкощепящая эндонуклеаза специфически нацеливается на CD52 или GR. В некоторых вариантах осуществления выбранный для инактивации ген кодирует CD52, а иммуносупрессивное лечение предусматривает гуманизированное антитело, нацеливающееся на антиген CD52. В некоторых вариантах осуществления выбранный для инактивации ген кодирует GR, а иммуносупрессивное лечение предусматривает использование кортикостероида, например дексаметазона. В некоторых вариантах осуществления ген, выбранный для инактивации, является представителем семейства генов FKBP или его вариантом, а иммуносупрессивное лечение предусматривает использованием FK506, также известного как такролимус или фуджимицин. В некоторых вариантах осуществления представителем семейства генов FKBP является FKBP12 или его вариант. В некоторых вариантах осуществления ген, выбранный для инактивации, является представителем семейства генов циклофилинов или его вариантом, а иммуносупрессивное лечение предусматривает использование циклоспорина.
В некоторых вариантах осуществления редкощепящая эндонуклеаза может представлять собой, например, нуклеазу с цинковыми пальцами (ZFN), нуклеазу megaTAL, мегануклеазу, эффекторную нуклеазу, подобную активатору транскрипции (TALE-нуклеазу), или эндонуклеазу, ассоциированную с CRISPR. В некоторых вариантах осуществления редкощепящая эндонуклеаза представляет собой TALE-нуклеазу. В некоторых вариантах осуществления редкощепящая нуклеаза представляет собой нуклеазу CRISPR с направляющей РНК, которая по меньшей мере, частично или полностью комплементарна целевому сайту.
Как правило, нуклеаза, ассоциированная с CRISPR, обеспечивается с направляющей РНК (gRNA) или ее функциональным эквивалентом. gRNA состоит из двух частей; crispr-РНК (crRNA), которая является специфической к целевой последовательности геномной ДНК, и трансактивирующая РНК (tracrRNA), которая способствует связыванию Cas с ДНК. В некоторых вариантах осуществления crRNA и tracrRNA могут присутствовать в одном и том же РНК-олигонуклеотиде, называемом одиночной направляющей РНК (sgRNA). В некоторых вариантах осуществления crRNA и tracrRNA могут присутствовать в виде отдельных РНК-олигонуклеотидов. Используемый в данном документе термин «направляющая РНК» или «gRNA» относится к комбинации tracrRNA и crRNA, представленной либо в виде sgRNA, либо в виде дуплекса crRNA:tracrRNA. В некоторых вариантах осуществления нуклеаза, ассоциированная с CRISPR, представляет собой нуклеазу Cas9. В некоторых вариантах осуществления белок Cas9 может быть получен из Streptococcus pyogenes (SpCas9). В некоторых вариантах осуществления белок Cas9 может быть получен из других штаммов бактерий, в том числе Staphylococcus aureus (SaCas9). В некоторых вариантах осуществления эндонуклеаза Cas выбрана из группы, включающей SpCas9, SpCas9-HF1, SpCas9-HF2, SpCas9-HF3, SpCas9-HF4, SaCas9, FnCpf, FnCas9, eSpCas9, C2C1, C2C3, Cpf1, Casl, CaslB, Cas2, Cas3, Cas4, Cas5, Cas6, Cas7, Cas8, Cas9 (также известную как Csnl и Csx12), Cas10, Csyl, Csy2, Csy3, Csel, Cse2, Cscl, Csc2, Csa5, Csn2, Csm2, Csm3, Csm4, Csm5, Csm6, Cmrl, Cmr3, Cmr4, Cmr5, Cmr6, Csbl, Csb2, Csb3, Csxl7, Csxl4, Csx10, Csx16, CsaX, Csx3, Csxl, Csxl5, Csfl, Csf2, Csf3 или Csf4.
Исследования показывают, что адоптивный перенос Т-клеток, полученных из менее дифференцированной (т. е. TSCM или TCM) субпопуляции, приводит к длительной персистенции in vivo (см., например, Berger, C. et al., The Journal of Clinical Investigation, 118(1): 294-305 (2008)). Таким образом, генетический нокдаун CD70 в продукте CAR-T является важным фактором предотвращения дифференцировки Т-клеток.
В некоторых вариантах осуществления генетическая модификация согласно данному способу включает экспрессию в предоставленных для конструирования клетках одной редкощепящей эндонуклеазы, вследствие чего редкощепящая эндонуклеаза специфически катализирует расщепление в гене CD70, за счет чего обеспечивается разрушение или инактивация гена CD70. В некоторых вариантах осуществления способ конструирования клеток предусматривает по меньшей мере одну из следующих стадий: обеспечение Т-клетки, такой как, например, из культуры клеток или из образца крови; введение в Т-клетку редкощепящей эндонуклеазы, способной посредством расщепления ДНК селективно инактивировать (в некоторых вариантах осуществления путем введения двухнитевого разрыва) ген, кодирующий CD70, и размножение клеток.
В некоторых вариантах осуществления способ предусматривает: обеспечение Т-клетки, например, из культуры клеток или из образца крови; трансфицирование Т-клетки посредством нуклеиновой кислоты, кодирующей редкощепящую эндонуклеазу, способную избирательно инактивировать путем расщепления ДНК (в некоторых вариантах осуществления путем введения двухнитевого разрыва) ген, кодирующий CD70, и экспрессию редкощепящих эндонуклеаз в Т-клетках; и размножение клеток.
В некоторых вариантах осуществления редкощепящая эндонуклеаза может представлять собой, например, мегануклеазу, нуклеазу с цинковыми пальцами или TALE-нуклеазу (TALEN). В некоторых вариантах осуществления редкощепящая эндонуклеаза представляет собой TALE-нуклеазу. В некоторых вариантах осуществления редкощепящая нуклеаза представляет собой нуклеазу, ассоциированную с CRISPR, вместе с направляющей РНК, которая по меньшей мере частично или полностью комплементарна целевому сайту.
В данном документе также представлены способы конструирования Т-клеток, подходящих для иммунотерапии, при этом способы предусматривают генетическое модифицирование Т-клеток путем разрушения или инактивации по меньшей мере белка контрольной точки иммунного ответа. В некоторых вариантах осуществления белок контрольной точки иммунного ответа представляет собой, например, PD-1 и/или CTLA-4. В некоторых вариантах осуществления способы генетического модифицирования клетки предусматривают модифицирование Т-клеток путем разрушения или инактивации по меньшей мере одного белка контрольной точки иммунного ответа и размножение клеток. Белки контрольных точек иммунного ответа включают без ограничения белок программируемой гибели 1 (PD-1, также известный как PDCD1 или CD279, номер доступа: NM-005018), цитотоксический T-лимфоцитарный антиген 4 (CTLA-4, также известный как CD152, номер доступа AF414120.1 в GenBank), LAG3 (также известный как CD223, номер доступа: NM-002286.5), Tim3 (также известный как HAVCR2, номер доступа в GenBank: JX049979.1), BTLA (также известный как CD272, номер доступа: NM-181780.3), BY55 (также известный как CD160, номер доступа в GenBank: CR541888.1), TIGIT (также известный как VSTM3, номер доступа: NM-173799), B7H5 (также известный как C10orf54, гомолог мышиного гена vista, номер доступа: NM-022153.1), LAIR1 (также известный как CD305, номер доступа в GenBank: CR542051.1), SIGLEC10 (номер доступа в GeneBank: AY358337.1), 2B4 (также известный как CD244, номер доступа: NM-001166664.1), которые непосредственно подавляют иммунные клетки. Например, CTLA-4 представляет собой белок клеточной поверхности, экспрессируемый некоторыми CD4 и CD8 Т-клетками; когда его лиганды (B7-1 и B7-2) взаимодействуют с антигенпрезентирующими клетками, активация Т-клеток и эффекторная функция подавляются.
В некоторых вариантах осуществления указанный способ конструирования клеток предусматривает по меньшей мере одну из следующих стадий: обеспечение Т-клетки, такой как, например, из культуры клеток или из образца крови; введение в Т-клетку редкощепящей эндонуклеазы, способной посредством расщепления ДНК селективно инактивировать (в некоторых вариантах осуществления путем введения двухнитевого разрыва) один ген, кодирующий белок контрольной точки иммунного ответа, и размножение клеток. В некоторых вариантах осуществления способ предусматривает обеспечение Т-клетки, например, из культуры клеток или из образца крови; трансфицирование указанной Т-клетки посредством нуклеиновой кислоты, кодирующей редкощепящую эндонуклеазу, способную избирательно инактивировать путем расщепления ДНК (в некоторых вариантах осуществления путем введения двухнитевого разрыва) ген, кодирующий белок контрольной точки иммунного ответа, и экспрессию редкощепящих эндонуклеаз в Т-клетках; размножение клеток. В некоторых вариантах осуществления редкощепящая эндонуклеаза специфически нацеливается на ген, выбранный из группы, состоящей из: PD-1, CTLA-4, LAG3, Tim3, BTLA, BY55, TIGIT, B7H5, LAIR1, SIGLEC10, 2B4, TCRα и TCRβ. В некоторых вариантах осуществления редкощепящая эндонуклеаза может представлять собой мегануклеазу, нуклеазу с цинковыми пальцами или TALE-нуклеазу. В некоторых вариантах осуществления редкощепящая эндонуклеаза представляет собой TALE-нуклеазу. В некоторых вариантах осуществления редкощепящая нуклеаза представляет собой Cas9 с направляющей РНК, которая по меньшей мере частично или полностью комплементарна целевому сайту.
В некоторых вариантах осуществления настоящее изобретение может быть, в частности, подходящим для аллогенной иммунотерапии. В таких вариантах осуществления клетки можно модифицировать посредством способа, предусматривающего разрушение или инактивацию по меньшей мере одного гена, кодирующего компонент Т-клеточного рецептора (TCR) в Т-клетках, и размножение Т-клеток. В некоторых вариантах осуществления генетическая модификация в соответствии с указанным способом обусловлена экспрессией в предоставляемых для конструирования клетках одной редкощепящей эндонуклеазы, вследствие чего редкощепящая эндонуклеаза специфически катализирует расщепление одного целевого гена, обеспечивая тем самым разрушение или инактивацию целевого гена. В некоторых вариантах осуществления указанный способ конструирования клеток предусматривает по меньшей мере одну из следующих стадий: обеспечение Т-клетки, такой как, например, из культуры клеток или из образца крови; введение в Т-клетку редкощепящей эндонуклеазы, способной селективно инактивировать посредством расщепления ДНК (в некоторых вариантах осуществления путем введения двухнитевого разрыва) по меньшей мере один ген, кодирующий компонент Т-клеточного рецептора (TCR); и размножение клеток.
В некоторых вариантах осуществления способ предусматривает обеспечение Т-клетки, такой как, например, из культуры клеток или из образца крови; трансфицирование указанной Т-клетки посредством нуклеиновой кислоты, кодирующей редкощепящую эндонуклеазу, способную избирательно инактивировать путем расщепления ДНК (в некоторых вариантах осуществления путем введения двухнитевого разрыва) по меньшей мере один ген, кодирующий компонент Т-клеточного рецептора (TCR); экспрессию редкощепящих эндонуклеаз в T-клетках; сортировку трансформированных Т-клеток, которые не экспрессируют TCR на своей клеточной поверхности; и размножение клеток.
В некоторых вариантах осуществления редкощепящая эндонуклеаза может представлять собой мегануклеазу, нуклеазы с цинковыми пальцами или TALE-нуклеазу. В некоторых вариантах осуществления редкощепящая эндонуклеаза представляет собой TALE-нуклеазу. В некоторых вариантах осуществления TALE-нуклеазы распознают и расщепляют последовательность, кодирующую TCRα или TCRβ. В некоторых вариантах осуществления TALE-нуклеаза содержит полипептидную последовательность, выбранную из аминокислотной последовательности, представленной под SEQ ID NO: 281, 282, 283, 284, 285, 286, 287, 288, 289 или 290.
Полипептидные последовательности TALE-нуклеазы:
повтор TRAC_T01-L
LTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASNIGGKQALETVQALLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASNIGGKQALETVQALLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPEQVVAIASNIGGKQALETVQALLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPEQVVAIASNIGGKQALETVQALLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGRPALE (SEQ ID NO: 281).
Повтор TRAC_T01-R
LTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASNIGGKQALETVQALLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPEQVVAIASNIGGKQALETVQALLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASNIGGKQALETVQALLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGRPALE (SEQ ID NO: 282).
Повтор TRBC_T01-L
LTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPEQVVAIASNIGGKQALETVQALLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASNIGGKQALETVQALLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASNIGGKQALETVQALLPVLCQAHGLTPQQVVAIASNGGGRPALE (SEQ ID NO: 283).
Повтор TRBC_T01-R
NPQRSTVWYLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGRPALE (SEQ ID NO: 284).
Повтор TRBC_T02-L
LTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASNIGGKQALETVQALLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPEQVVAIASNIGGKQALETVQALLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGRPALE (SEQ ID NO: 285).
Повтор TRBC_T02-R
LTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPEQVVAIASNIGGKQALETVQALLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPEQVVAIASNIGGKQALETVQALLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGRPALE (SEQ ID NO: 286).
Повтор CD52_T02-L
LTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPEQVVAIASNIGGKQALETVQALLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASNIGGKQALETVQALLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASNIGGKQALETVQALLPVLCQAHGLTPQQVVAIASNGGGRPALE (SEQ ID NO: 287).
Повтор CD52_T02-R
LTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPEQVVAIASNIGGKQALETVQALLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPEQVVAIASNIGGKQALETVQALLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGRPALE (SEQ ID NO: 288).
Повтор CD70-L
LTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASNIGGKQALETVQALLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGRPALE (SEQ ID NO: 289)
Повтор CD70-R
LTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPEQVVAIASNIGGKQALETVQALLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPEQVVAIASNIGGKQALETVQALLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNNGGKQALETVQRLLPVLCQAHGLTPEQVVAIASHDGGKQALETVQRLLPVLCQAHGLTPQQVVAIASNGGGRPALE (SEQ ID NO: 290)
В другом аспекте еще одна стадия генетического модифицирования клетки может представлять собой способ размножения T-клеток с дефицитом TCRα, предусматривающий введение в T-клетку pTα (также известного как preTCRα) или его функционального варианта и размножение клеток необязательно посредством стимуляции CD3-комплекса. В некоторых вариантах осуществления способ предусматривает: а) трансфицирование клеток нуклеиновой кислотой, кодирующей по меньшей мере фрагмент pTα, для поддержания экспрессии на поверхности CD3; б) экспрессию указанного pTα в клетках; и c) размножение клеток необязательно посредством стимуляции CD3-комплекса.
Также представлены способы получения Т-клеток для иммунотерапии, предусматривающие стадии способа размножения Т-клеток. В некоторых вариантах осуществления полинуклеотидная последовательность pTα может быть введена случайным образом или путем гомологичной рекомбинации. В некоторых вариантах осуществления вставка может быть ассоциирована с инактивацией гена TCRα.
Можно использовать различные функциональные варианты pTα. «Функциональный вариант» пептида относится к молекуле, которая по сути сходна либо с полным пептидом, либо с его фрагментом. «Фрагмент» pTα или его функционального варианта относится к любой субпопуляции молекулы, то есть к пептиду, более короткому, чем полноразмерный pTα. В некоторых вариантах осуществления pTα или функциональные варианты могут представлять собой, например, полноразмерный pTα или вариант pTα, усеченный с С-конца. В усеченном на С-конце pTα отсутствуют один или более С-концевых остатков. В качестве неограничивающих примеров в усеченном с С-конца варианте pTα отсутствуют 18, 48, 62, 78, 92, 110 или 114 остатков, начиная с С-конца белка. Варианты аминокислотной последовательности пептида могут быть получены путем мутаций в ДНК, кодирующей пептид. Такие функциональные варианты включают, например, делеции, вставки или замены остатков в аминокислотной последовательности. Для получения конечной конструкции также можно осуществить любую комбинацию делеции, вставки и замены при условии, что конечная конструкция обладает требуемой активностью, в частности, восстановлением функционального CD3-комплекса. В некоторых вариантах осуществления для воздействия на димеризацию необходимо ввести по меньшей мере одну мутацию в разные варианты pTα, как это описано выше. В качестве неограничивающего примера мутантный остаток может представлять собой по меньшей мере W46R, D22A, K24A, R102A или R117A из человеческого белка pTα или положения, выровненные с использованием способа CLUSTALW, на представителе семейства pTα или представителе-гомологе. В некоторых вариантах осуществления pTα или его вариант, описанные выше, содержат мутантный остаток W46R или мутантные остатки D22A, K24A, R102A и R117A. В некоторых вариантах осуществления указанные pTα или варианты также слиты с доменом, передающим сигнал, таким как, например, CD28, OX40, ICOS, CD27, CD137 (4-1BB) и CD8, представленные в качестве неограничивающих примеров. Внеклеточный домен pTα или варианты, описанные выше, могут быть слиты с фрагментом белка TCRα, в частности с трансмембранным и внутриклеточным доменом TCRα. Варианты pTα также могут быть слиты с внутриклеточным доменом TCRα.
В некоторых вариантах осуществления варианты pTα могут быть слиты с внеклеточным лиганд-связывающим доменом. В некоторых вариантах осуществления pTα или его функциональный вариант слиты с одноцепочечным фрагментом антитела (scFv), содержащим вариабельный фрагмент легкой и тяжелой цепей целевого антиген-специфического моноклонального антитела, соединенных гибким линкером.
Термин «Т-клетка с дефицитом TCRα» относится к выделенной Т-клетке, в которой отсутствует экспрессия функциональной цепи TCRα. Это может быть достигнуто различными способами, представленными в качестве неограничивающих примеров: путем конструирования Т-клетки таким образом, чтобы она не экспрессировала какой-либо функциональный TCRα на своей клеточной поверхности, или путем конструирования Т-клетки таким образом, чтобы она продуцировала лишь небольшое количество функциональной цепи TCRα на своей поверхности, или путем конструирования Т-клетки для экспрессии мутированной или усеченной формы цепи TCRα. Клетки с дефицитом TCRα больше не способны размножаться за счет CD3-комплекса. Таким образом, чтобы преодолеть эту проблему и сделать возможной пролиферацию клеток с дефицитом TCRα, в клетки вводят pTα или его функциональный вариант, за счет чего восстанавливается функциональный CD3-комплекс. В некоторых вариантах осуществления способ дополнительно предусматривает введение в указанные Т-клетки редкощепящих эндонуклеаз, способных селективно инактивировать путем расщепления ДНК один ген, кодирующий один компонент Т-клеточного рецептора (TCR). В некоторых вариантах осуществления редкощепящая эндонуклеаза представляет собой TALE-нуклеазу.
В другом аспекте сконструированные Т-клетки, полученные посредством описанных в данном документе способов, можно приводить в контакт с биспецифическими антителами. Например, Т-клетки можно приводить в контакт с биспецифическими антителами ex vivo до введения пациенту или in vivo после введения пациенту. Биспецифические антитела содержат две вариабельные области с различными антигенными свойствами, которые способствуют сближению сконструированных клеток с целевым антигеном. В качестве неограничивающего примера биспецифическое антитело может быть направлено против онкомаркера и лимфоцитарного антигена, такого как, например, без ограничения CD3, и может перенаправлять и активировать любые циркулирующие в крови Т-клетки против опухолей.
В некоторых вариантах осуществления полинуклеотиды, кодирующие полипептиды по настоящему изобретению, могут представлять собой мРНК, которую вводят непосредственно в клетки, например, путем электропорации. В некоторых вариантах осуществления может использоваться технология cytoPulse для обеспечения временной повышенной проницаемости живых клеток с целью доставки материала в клетки. Параметры могут быть изменены для определения условий высокой эффективности трансфекции с минимальной гибелью.
В данном документе также представлены способы трансфицирования Т-клеток. В некоторых вариантах осуществления способ предусматривает приведение в контакт Т-клетки с РНК и приложение к Т-клетке последовательности быстрых импульсов, состоящей из: (а) электрического импульса с диапазоном напряжения, составляющим от приблизительно 2250 до 3000 В на сантиметр; (b) продолжительности импульса, составляющей 0,1 мс; (c) импульсного интервала между электрическими импульсами на стадиях (а) и (b), составляющего от приблизительно 0,2 до 10 мс; (d) электрического импульса с диапазоном напряжения, составляющим от приблизительно 2250 до 3000 В, с продолжительностью импульса, составляющей приблизительно 100 мс, и импульсным интервалом, составляющим приблизительно 100 мс, между электрическим импульсом на стадии (b) и первым электрическим импульсом на стадии (c); и (e) четырех электрических импульсов с напряжением, составляющим приблизительно 325 В, с продолжительностью импульса, составляющей приблизительно 0,2 мс, и импульсным интервалом, составляющим 2 мс, между каждым из 4 электрических импульсов. В некоторых вариантах осуществления способ трансфицирования Т-клетки предусматривает приведение указанной Т-клетки в контакт с РНК и приложение к Т-клетке последовательности быстрых импульсов, предусматривающей: (а) электрический импульс с напряжением, составляющим приблизительно 2250, 2300, 2350, 2400, 2450, 2500, 2550, 2400, 2450, 2500, 2600, 2700, 2800, 2900 или 3000 В на сантиметр; (b) продолжительность импульса, составляющую 0,1 мс; (c) и импульсный интервал между электрическими импульсами на стадии (а) и (b), составляющий приблизительно 0,2, 0,5, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мс; (d) один электрический импульс с диапазоном напряжения, составляющим от приблизительно 2250, 2250, 2300, 2350, 2400, 2450, 2500, 2550, 2400, 2450, 2500, 2600, 2700, 2800, 2900 или 3000 В, с продолжительностью импульса, составляющей 100 мс, и импульсным интервалом, составляющим 100 мс, между электрическим импульсом на стадии (b) и первым электрическим импульсом на стадии (c); и (e) 4 электрических импульса с напряжением, составляющим приблизительно 325 В, с продолжительностью импульса, составляющей приблизительно 0,2 мс, и импульсным интервалом, составляющим приблизительно 2 мс, между каждым из 4 электрических импульсов. Любые значения, входящие в диапазон значений, описанный выше, раскрыты в настоящей заявке. Среда для электропорации может быть любой подходящей средой, известной в данной области техники, например BTXpress Cytoporation® Media T4, доступная от BTX. В некоторых вариантах осуществления среда для электропорации характеризуется проводимостью в диапазоне, составляющем от приблизительно 0,01 до приблизительно 1,0 мСм.
В некоторых вариантах осуществления в качестве неограничивающих примеров РНК кодирует редкощепящую эндонуклеазу, один мономер редкощепящей эндонуклеазы, например, полу-TALE-нуклеазу, CAR, по меньшей мере один компонент многоцепочечного химерного антигенного рецептора, pTα или его функциональный вариант, экзогенную нуклеиновую кислоту и/или один дополнительный каталитический домен.
Сконструированные иммунные клетки
В настоящем изобретении также представлены сконструированные иммунные клетки, содержащие любой из полинуклеотидов CAR, описанных в данном документе. В некоторых вариантах осуществления CAR можно ввести в иммунную клетку в виде трансгена посредством плазмидного вектора. В некоторых вариантах осуществления плазмидный вектор также может содержать, например, маркер для отбора, который обеспечивает идентификацию и/или отбор клеток, которые получили вектор.
Полипептиды CAR можно синтезировать in situ в клетке после введения в клетку полинуклеотидов, кодирующих полипептиды CAR. Альтернативно полипептиды CAR можно получать вне клеток, а затем вводить в клетки. Способы введения полинуклеотидной конструкции в клетки известны в данной области техники. В некоторых вариантах осуществления можно использовать способы стабильной трансформации для интеграции полинуклеотидной конструкции в геном клетки. В других вариантах осуществления способы временной трансформации могут быть использованы для временной экспрессии полинуклеотидной конструкции, и при этом полинуклеотидная конструкция не интегрируется в геном клетки. В других вариантах осуществления можно использовать способы, опосредованные вирусом. Полинуклеотиды можно вводить в клетку посредством любых подходящих средств, таких как, например, рекомбинантные вирусные векторы (например, ретровирусы, аденовирусы), липосомы и им подобные. Методики временной трансформации включают, например, без ограничения микроинъекцию, электропорацию или бомбардировку частицами. Полинуклеотиды могут быть включены в векторы, такие как, например, плазмидные векторы или вирусные векторы.
В данном документе также представлены выделенные клетки и клеточные линии, полученные посредством описанных выше способов конструирования клеток, представленных в данном документе. В некоторых вариантах осуществления выделенная клетка содержит по меньшей мере один CAR, описанный выше. В некоторых вариантах осуществления выделенная клетка содержит популяцию CAR, при этом каждый CAR содержит разные внеклеточные лиганд-связывающие домены.
В данном документе также представлены выделенные иммунные клетки, полученные с помощью любого из описанных выше способов. Любая иммунная клетка, способная экспрессировать гетерологичные ДНК, может быть использована для экспрессии CAR, представляющего интерес. В некоторых вариантах осуществления иммунная клетка представляет собой Т-клетку. В некоторых вариантах осуществления иммунная клетка может быть получена из, например, без ограничения стволовой клетки. Стволовые клетки могут представлять собой стволовые клетки взрослого, эмбриональные стволовые клетки, отличные от человеческих, в частности стволовые клетки, отличные от человеческих, стволовые клетки из пуповинной крови, клетки-предшественники, стволовые клетки костного мозга, индуцированные плюрипотентные стволовые клетки, тотипотентные стволовые клетки или гемопоэтические стволовые клетки. Типичными человеческими клетками являются клетки CD34+. Выделенная клетка также может представлять собой дендритную клетку, киллерную дендритную клетку, тучную клетку, NK-клетку, B-клетку или T-клетку, выбранную из группы, состоящей из воспалительных T-лимфоцитов, цитотоксических T-лимфоцитов, регуляторных T-лимфоцитов или хелперных Т-лимфоцитов. В некоторых вариантах осуществления клетка может быть получена из группы, состоящей из CD4+ Т-лимфоцитов и CD8+ Т-лимфоцитов.
В некоторых вариантах осуществления сконструированные иммунные клетки, экспрессирующие на своей клеточной поверхностной мембране CAR, специфический к CD70, по настоящему изобретению, содержат процентную долю стволовых клеток памяти и центральных клеток памяти, превышающую 10%, 20%, 30%, 40%, 50% или 60%. В некоторых вариантах осуществления сконструированные иммунные клетки, экспрессирующие на своей клеточной поверхностной мембране CAR, специфический к CD70, по настоящему изобретению, содержат процентную долю стволовых клеток памяти и центральных клеток памяти, составляющую от приблизительно 10% до приблизительно 60%, от приблизительно 10% до приблизительно 50%, от приблизительно 10% до приблизительно 40%, от приблизительно 15% до приблизительно 50%, от приблизительно 15% до приблизительно 40%, от приблизительно 20% до приблизительно 60% или от приблизительно 20% до приблизительно 70%.
В некоторых вариантах осуществления иммунная клетка представляет собой воспалительный Т-лимфоцит, который экспрессирует любой из CAR, описанных в данном документе. В некоторых вариантах осуществления иммунная клетка представляет собой цитотоксический Т-лимфоцит, который экспрессирует любой из CAR, описанных в данном документе. В некоторых вариантах осуществления иммунная клетка представляет собой регуляторный Т-лимфоцит, который экспрессирует любой из CAR, описанных в данном документе. В некоторых вариантах осуществления иммунная клетка представляет собой хелперный Т-лимфоцит, который экспрессирует любой из CAR, описанных в данном документе.
Перед размножением и генетической модификацией источник клеток может быть получен от субъекта посредством ряда неограничивающих способов. Клетки можно получить из ряда неограничивающих источников, в том числе из мононуклеарных клеток периферической крови, костного мозга, ткани лимфатических узлов, пуповинной крови, ткани тимуса, ткань из очага инфекции, асцитной жидкости, плеврального выпота, ткани селезенки и опухоли. В некоторых вариантах осуществления можно использовать любое количество линий Т-клеток, доступных и известных специалистам в данной области техники. В некоторых вариантах осуществления клетки могут быть получены от здорового донора, от пациента, у которого диагностирован рак, или от пациента, у которого диагностирована инфекция. В некоторых вариантах осуществления клетки могут быть частью смешанной популяции клеток, которые обладают разными фенотипическими характеристиками.
В данном документе также представлены клеточные линии, полученные из трансформированных Т-клеток в соответствии с любым из описанных выше способов. В данном документе также представлены модифицированные клетки, резистентные к иммуносупрессивному лечению. В некоторых вариантах осуществления выделенная клетка по настоящему изобретению содержит полинуклеотид, кодирующий CAR.
Иммунные клетки по настоящему изобретению могут быть активированы и размножены либо до, либо после генетической модификации Т-клеток с применением способов, в общем описанных, например, без ограничения в патентах США №№ 6352694; 6534055; 6905680; 6692964; 5858358; 6887466; 6905681; 7144575; 7067318; 7172869; 7232566; 7175843; 5883223; 6905874; 6797514; 6867041; а также публикации заявки на патент США № 20060121005. Т-клетки можно размножать in vitro или in vivo. Как правило, Т-клетки по настоящему изобретению могут быть размножены, например, путем приведения в контакт со средством, которое стимулирует комплекс CD3 TCR и костимулирующей молекулой на поверхности Т-клеток для создания сигнала активации для Т-клетки. Например, химические вещества, такие как ионофор кальция A23187, форбол 12-миристат-13-ацетат (PMA) или митогенные лектины, такие как фитогемагглютинин (PHA), могут быть использованы для создания сигнала активации для Т-клетки.
В некоторых вариантах осуществления популяции Т-клеток можно стимулировать in vitro путем приведения в контакт, например, с антителом к CD3 или его антигенсвязывающим фрагментом, или с антителом к CD2, иммобилизованным на поверхности, или путем приведения в контакт с активатором белка протеинкиназы C (например, бриостатином) в сочетании с ионофором кальция. Для костимуляции вспомогательной молекулы на поверхности Т-клеток используется лиганд, который связывает вспомогательную молекулу. Например, популяция Т-клеток может быть приведена в контакт с антителом к CD3 и антителом к CD28 в условиях, подходящих для стимуляции пролиферации Т-клеток. Антитело к CD3 и антитело к CD28 могут быть размещены на грануле, планшете или другом субстрате. Условия, подходящие для культуры Т-клеток, включают подходящую среду (например, Minimal Essential Media, или RPMI Media 1640, или X-vivo 5 (Lonza)), которая может содержать факторы, необходимые для пролиферации и жизнеспособности, включая сыворотку крови (например, фетальную бычью или человеческую сыворотку крови), интерлейкин-2 (IL-2), инсулин, IFN-γ, IL-4, IL-7, GM-CSF, IL-10, IL-2, IL-15, TGFp и TNF или любые другие добавки для роста клеток, известные специалисту в данной области техники. Другие добавки для роста клеток включают без ограничения поверхностно-активное вещество, плазманат и восстанавливающие средства, такие как N-ацетилцистеин и 2-меркаптоэтанол. Среды могут включать RPMI 1640, A1M-V, DMEM, MEM, a-MEM, F-12, X-Vivo 1 и X-Vivo 20, Optimizer, дополненные аминокислотами, пируватом натрия и витаминами, либо без сыворотки крови, либо дополненные соответствующим количеством сыворотки крови (или плазмы крови) или определенным набором гормонов и/или количеством цитокина (цитокинов), достаточного для роста и размножения Т-клеток (например, IL-7 и/или IL-15). Антибиотики, например пенициллин и стрептомицин, добавляют только в экспериментальные культуры, но не в культуры клеток, которые должны быть введены субъекту. Целевые клетки поддерживаются в условиях, необходимых для поддержания роста, например, при соответствующей температуре (например, 37°C) и атмосфере (например, атмосферный воздух плюс 5% CO2). Т-клетки, которые подвергались воздействию различного времени стимуляции, могут проявлять разные характеристики.
В некоторых вариантах осуществления клетки по настоящему изобретению могут быть размножены путем совместного культивирования с тканью или клетками. Клетки также можно размножать in vivo, например, в крови субъекта после введения клетки субъекту.
В некоторых вариантах осуществления выделенная клетка по настоящему изобретению содержит один разрушенный или инактивированный ген, выбранный из группы, состоящей из CD52, CD70, GR, PD-1, CTLA-4, LAG3, Tim3, BTLA, BY55, TIGIT, B7H5, LAIR1, SIGLEC10, 2B4, HLA, TCRα и TCRβ, и/или экспрессирует CAR, многоцепочечный CAR и/или трансген pTα. В некоторых вариантах осуществления выделенная клетка содержит полинуклеотиды, кодирующие полипептиды, содержащие многоцепочечный CAR. В некоторых вариантах осуществления выделенная клетка по настоящему изобретению содержит два разрушенных или инактивированных гена, выбранных из группы, состоящей из: CD52 и GR, CD52 и TCRα, CDR52 и TCRβ, CD70 и CD52, CD70 и TCRα, CD70 и TCRβ, GR и TCRα, GR и TCRβ, TCRα и TCRβ, PD-1 и TCRα, PD-1 и TCRβ, CTLA-4 и TCRα, CTLA-4 и TCRβ, LAG3 и TCRα, LAG3 и TCRβ, Tim3 и TCRα, Tim3 и TCRβ, BTLA и TCRα, BTLA и TCRβ, BY55 и TCRα, BY55 и TCRβ, TIGIT и TCRα, TIGIT и TCRβ, B7H5 и TCRα, B7H5 и TCRβ, LAIR1 и TCRα, LAIR1 и TCRβ, SIGLEC10 и TCRα, SIGLEC10 и TCRβ, 2B4 и TCRα, 2B4 и TCRβ, и/или экспрессирует CAR, многоцепочечный CAR и трансген pTα.
В некоторых вариантах осуществления выделенная клетка по настоящему изобретению содержит три разрушенных или инактивированных гена, выбранных из CD52, CD70 и TCRα или CD52, CD70 и TCRβ, и/или экспрессирует CAR, многоцепочечный CAR и трансген pTα.
В некоторых вариантах осуществления TCR становится нефункциональным в клетках по настоящему изобретению путем разрушения или инактивирования гена TCRα и/или гена (генов) TCRβ. В некоторых вариантах осуществления представлен способ получения модифицированных клеток, получаемых от индивидуума, где клетки могут пролиферировать независимо от пути передачи сигнала главного комплекса гистосовместимости (MHC). Модифицированные клетки, которые могут пролиферировать независимо от пути передачи сигнала MHC, чувствительные к получению посредством данного способа, входят в объем настоящего изобретения. Модифицированные клетки, раскрытые в данном документе, могут быть использованы для лечения пациентов, нуждающихся в этом, в отношении отторжения по типу «хозяин против трансплантата» (HvG) и заболевания «трансплантат против хозяина» (GvHD); следовательно, в объеме настоящего изобретения находится способ лечения пациентов, нуждающихся в этом, в отношении отторжения по типу «хозяин против трансплантата» (HvG) и заболевания «трансплантат против хозяина» (GvHD), предусматривающий лечение указанного пациента путем введения указанному пациенту эффективного количества модифицированных клеток, содержащих разрушенные или инактивированные гены TCRα и/или TCRβ.
В некоторых вариантах осуществления иммунные клетки сконструированы так, чтобы они были резистентны к одному или более химиотерапевтическим лекарственным средствам. Химиотерапевтическое лекарственное средство может представлять собой, например, аналог пуринового нуклеотида (PNA), что делает иммунную клетку подходящей для противораковой терапии, сочетающей адоптивную иммунотерапию и химиотерапию. Иллюстративные PNA включают, например, клофарабин, флударабин, циклофосфамид и цитарабин, по отдельности или в комбинации. PNA метаболизируются дезоксицитидинкиназой (dCK) в моно-, ди- и трифосфатные PNA. Их трифосфатные формы конкурируют с АТФ за синтез ДНК, действуют как проапоптотические средства и являются высокоактивными ингибиторами рибонуклеотидредуктазы (RNR), которая вовлечена в продуцирование тринуклеотидов. В данном документе представлены CAR-T-клетки, специфические к CD70, содержащие разрушенный или инактивированный ген dCK. В некоторых вариантах осуществления клетки с нокаутом dCK получают путем трансфекции Т-клеток с применением полинуклеотидов, кодирующих специфическую TAL-нуклеазу, направленную против генов dCK, например, путем электропорации мРНК. CAR-T-клетки, специфические к CD70, с нокаутом по dCK могут быть резистентными к PNA, в том числе, например, к клорофарабину и/или флударабину, и поддерживать цитотоксическую активность Т-клеток в отношении клеток, экспрессирующих CD70.
В некоторых вариантах осуществления выделенные клетки или клеточные линии по настоящему изобретению могут содержать pTα или его функциональный вариант. В некоторых вариантах осуществления выделенная клетка или клеточная линия может быть дополнительно генетически модифицирована путем разрушения или инактивации гена TCRα.
Эпитопы, специфические в отношении моноклональных антител
В некоторых вариантах осуществления внеклеточный домен любого из CAR, специфических к CD70, описанных в данном документе, может содержать один или более эпитопов, специфических для (т. е. специфически распознаваемых) моноклонального антитела. Данные эпитопы также называются в данном документе mAb-специфическими эпитопами. Иллюстративные mAb-специфические эпитопы раскрыты в международной патентной публикации № WO 2016/120126, которая полностью включена в данный документ во всей своей полноте. В данных вариантах осуществления внеклеточный домен содержит полипептиды VH и VL, которые специфически связываются с CD70, и один или более эпитопов, которые связываются с одним или более моноклональными антителами (mAb). CAR, содержащие mAb-специфические эпитопы, могут быть одноцепочечными или многоцепочечными.
Включение эпитопов, специфических к моноклональным антителам, во внеклеточный домен CAR, описанных в данном документе, позволяет осуществлять сортировку и истощать сконструированные иммунные клетки, экспрессирующие CAR. В некоторых вариантах осуществления данное свойство также способствует восстановлению эндогенных клеток, экспрессирующих CD70, которые были истощены посредством введения сконструированных иммунных клеток, экспрессирующих CAR.
Соответственно, в некоторых вариантах осуществления настоящее изобретение относится к способу сортировки и/или истощения сконструированных иммунных клеток, имеющих CAR, содержащие mAb-специфические эпитопы, и к способу стимулирования восстановления эндогенных CD70-экспрессирующих клеток, таких как клетки-предшественники костного мозга.
Для получения CAR, содержащих эпитопы, специфические для моноклональных антител, могут быть использованы несколько пар эпитоп-моноклональное антитело; в частности, те, которые уже одобрены для медицинского применения, такие как эпитоп CD20/ритуксимаб - в качестве неограничивающего примера.
Настоящее изобретение также охватывает способы сортировки сконструированных иммунных клеток, имеющих CAR, специфические к CD70, экспрессирующие mAb-специфический эпитоп (эпитопы), и терапевтические способы, где активацию сконструированных иммунных клеток, имеющих такие CAR, модулируют путем истощения клеток с применением антитела, которое нацеливается на внешний лиганд-связывающий домен указанных CAR.
В некоторых вариантах осуществления CAR-T-клетка содержит полинуклеотид, кодирующий «суицидный» полипептид, такой как, например, RQR8. См., например, WO2013153391A, который включен в данный документ посредством ссылки во всей своей полноте. В CAR-T-клетках, содержащих полинуклеотид, «суицидный» полипептид экспрессируется на поверхности CAR-T-клетки. В некоторых вариантах осуществления «суицидный» полипептид содержит аминокислотную последовательность, представленную под SEQ ID NO: 291.
CPYSNPSLCSGGGGSELPTQGTFSNVSTNVSPAKPTTTACPYSNPSLCSGGGGSPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCNHRNRRRVCKCPRPVV (SEQ ID NO: 291).
«Суицидный» полипептид также может содержать сигнальный пептид на амино-конце, например, MGTSLLCWMALCLLGADHADA (SEQ ID NO: 611). В некоторых вариантах осуществления «суицидный» полипептид содержит аминокислотную последовательность, представленную под SEQ ID NO: 292, которая включает сигнальную последовательность под SEQ ID NO: 611.
mgtsllcwmalcllgadhadacpysnpslcsggggselptqgtfsnvstnvspakptttacpysnpslcsggggspaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlycnhrnrrrvckcprpvv (SEQ ID NO: 292).
В некоторых вариантах осуществления суицидный полипептид содержит аминокислотную последовательность под SEQ ID NO: 611
Если «суицидный» полипептид экспрессируется на поверхности CAR-T-клетки, связывание ритуксимаба с R-эпитопами полипептида вызывает лизис клетки. Более одной молекулы ритуксимаба может связываться с одним полипептидом, экспрессируемым на поверхности клетки. Каждый R-эпитоп полипептида может связываться с отдельной молекулой ритуксимаба. Удаление CAR-T-клеток, специфических к CD70, может происходить in vivo, например, путем введения пациенту ритуксимаба. Решение об удалении перенесенных клеток может быть вызвано обнаружением у пациента нежелательных эффектов, которые связаны с перенесенными клетками, например, при обнаружении неприемлемых уровней токсичности.
В некоторых вариантах осуществления при введении пациенту сконструированные иммунные клеток, экспрессирующие на своей клеточной поверхности любой из CAR, специфических к CD70, описанных в данном документе, могут снижать уровень, уничтожать или лизировать эндогенные CD70-экспрессирующие клетки у пациента. В одном варианте осуществления процентная доля снижения уровня или лизиса эндогенных клеток, экспрессирующих CD70, или клеток из линии клеток, экспрессирующих CD70, посредством сконструированных иммунных клеток, экспрессирующих любой из CAR, специфических к CD70, описанных в данном документе, составляет по меньшей мере приблизительно 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90% или 95% или превышает указанные значения. В одном варианте осуществления процентная доля снижения уровня или лизиса эндогенных клеток, экспрессирующих CD70, или клеток из линии клеток, экспрессирующих CD70, посредством сконструированных иммунных клеток, экспрессирующих любой из CAR, специфических к CD70, описанных в данном документе, составляет от приблизительно 5% до приблизительно 95%, от приблизительно 10% до приблизительно 95%, от приблизительно 10% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 10% до приблизительно 60%, от приблизительно 10% до приблизительно 50%, от приблизительно 10% до приблизительно 40%, от приблизительно 20% до приблизительно 90%, от приблизительно 20% до приблизительно 80%, от приблизительно 20% до приблизительно 70%, от приблизительно 20% до приблизительно 60%, от приблизительно 20% до приблизительно 50%, от приблизительно 25% до приблизительно 75% или от приблизительно 25% до приблизительно 60%. В одном варианте осуществления эндогенные CD70-экспрессирующие клетки представляют собой эндогенные CD70-экспрессирующие клетки костного мозга.
В одном варианте осуществления процентную долю снижения уровня или лизиса целевых клеток, например, клеточной линии, экспрессирующей CD70, посредством сконструированных иммунных клеток, экспрессирующих на своей клеточной поверхностной мембране CAR, специфический к CD70, по настоящему изобретению можно измерить с использованием анализа, описанного в данном документе.
Способ сортировки CAR-положительных иммунных клеток
В одном из аспектов представлены способы in vitro сортировки популяции иммунных клеток, где субпопуляция иммунных клеток содержит сконструированные иммунные клетки, экспрессирующие любой из CAR, специфических к CD70, содержащих эпитопы, специфические к моноклональным антителам, описанным в данном документе. Способ предусматривает приведение в контакт популяции иммунных клеток с моноклональным антителом, специфическим к эпитопам, и отбор иммунных клеток, которые связываются с моноклональным антителом, для получения популяции клеток, обогащенных сконструированными иммунными клетками, экспрессирующими CAR, специфический к CD70.
В некоторых вариантах осуществления указанное моноклональное антитело, специфическое к указанному эпитопу, необязательно конъюгировано с флуорофором. В этом варианте осуществления стадию отбора клеток, которые связываются с моноклональным антителом, можно выполнить с помощью сортировки клеток с активацией флуоресценции (FACS). В некоторых вариантах осуществления указанное моноклональное антитело, специфическое к указанному эпитопу, необязательно конъюгировано с магнитными частицами. В данном варианте осуществления стадию отбора клеток, которые связываются с моноклональным антителом, можно выполнить с помощью активируемой магнитным полем сортировки клеток (MACS).
В некоторых вариантах осуществления внеклеточный связывающий домен в CAR содержит mAb-специфический эпитоп с одной или более из SEQ ID NO: 294 или 601-610. В некоторых вариантах осуществления внеклеточный связывающий домен в CAR содержит mAb-специфический эпитоп под SEQ ID NO: 609. В некоторых вариантах осуществления внеклеточный связывающий домен в CAR содержит mAb-специфический эпитоп под SEQ ID NO: 295. В некоторых вариантах осуществления внеклеточный связывающий домен в CAR содержит mAb-специфический эпитоп под SEQ ID NO: 609, и антитело, используемое для приведения в контакт с популяцией иммунных клеток, представляет собой QBEND-10. В некоторых вариантах осуществления внеклеточный связывающий домен в CAR содержит mAb-специфический эпитоп под SEQ ID NO: 295, и антитело, используемое для приведения в контакт с популяцией иммунных клеток, представляет собой QBEND-10.
В некоторых вариантах осуществления внеклеточный связывающий домен в CAR содержит mAb-специфический эпитоп под SEQ ID NO: 294. В некоторых вариантах осуществления внеклеточный связывающий домен в CAR содержит mAb-специфический эпитоп под SEQ ID NO: 294, и антитело, используемое для приведения в контакт с популяцией иммунных клеток, представляет собой ритуксимаб.
В некоторых вариантах осуществления популяция CAR-экспрессирующих иммунных клеток, полученная с применением способа in vitro сортировки иммунных клеток, описанного выше, содержит по меньшей мере 60%, 65%, 70%, 75%, 80%, 85%, 90% или 95% CAR-экспрессирующих иммунных клеток. В некоторых вариантах осуществления популяция CD70 CAR-экспрессирующих иммунных клеток, полученная с применением описанного выше способа in vitro сортировки CAR-экспрессирующих иммунных клеток, содержит по меньшей мере 85% CAR-экспрессирующих иммунных клеток.
Согласно настоящему изобретению клетки, которые подлежат введению реципиенту, могут быть обогащены in vitro из исходной популяции. Способы размножения исходных популяций хорошо известны в данной области техники и могут включать отбор клеток, которые экспрессируют антиген, такой как, например, антиген CD34, с применением комбинаций центрифугирования в градиенте плотности, очистки иммуномагнитными гранулами, аффинной хроматографии и сортировки флуоресцентно активированных клеток, известных специалистам в данной области техники.
Проточная цитометрия широко используется в данной области техники и представляет собой способ, хорошо известный специалисту в данной области техники, предназначенный для сортировки и количественной оценки конкретных типов клеток в популяции клеток. В общем проточная цитометрия представляет собой способ количественной оценки компонентов или структурных характеристик клеток, главным образом с помощью оптических средств. Поскольку различные типы клеток можно отличить путем количественной оценки структурных характеристик, проточная цитометрия и сортировка клеток могут использоваться для подсчета и сортировки клеток с разными фенотипами в смеси.
Анализ с помощью проточной цитометрии включает две основные стадии: 1) маркировку выбранных типов клеток одним или более метящими маркерами и 2) определение количества меченых клеток по отношению к общему количеству клеток в популяции.
Первичный способ маркировки типов клеток заключается в связывании меченых антител с маркерами, экспрессируемыми конкретным типом клеток. Антитела либо непосредственно метят флуоресцентным соединением, либо косвенно метят, используя, например, второе антитело, меченное флуоресцентной меткой, которое распознает первое антитело.
В некоторых вариантах осуществления способ, используемый для сортировки иммунных клеток, экспрессирующих CAR, представляет собой активируемую магнитным полем сортировку клеток (MACS). Активируемая магнитным полем сортировка клеток (MACS) представляет собой способ разделения разных популяций клеток в зависимости от их поверхностных антигенов (молекул CD) с применением суперпарамагнитных наночастиц и колонок. Чтобы получить чистые популяции клеток, нужно выполнить несколько простых стадий. Клетки в одноклеточной суспензии метят микрогранулами с использованием магнитного поля. Образец наносят на колонку, состоящую из ферромагнитных сфер, покрытых безвредным для клеток покрытием, обеспечивающим быстрое и бережное разделение клеток. Не подвергшиеся мечению клетки проходят, а клетки с магнитной меткой остаются внутри колонки. Проходящий поток можно собрать в виде немеченой фракции клеток. После короткой стадии промывки колонку удаляют из разделителя, и клетки с магнитной меткой элюируются из колонки.
В некоторых вариантах осуществления mAb, используемое в способе сортировки иммунных клеток, экспрессирующих CAR, выбрано из алемтузумаба, ибритумомаба тиуксетана, муромонаба-CD3, тозитумомаба, абциксимаба, базиликсимаба, брентуксимаба ведотина, цетуксимаба, инфликсимаба, ритуксимаба, бевацизумаба, цертолизумаба пегола, даклизумаба, экулизумаба, эфализумаба, гемтузумаба, натализумаба, омализумаба, паливизумаба, ранибизумаба, тоцилизумаба, трастузумаба, ведолизумаба, адалимумаба, белимумаба, канакинумаба, деносумаба, голимумаба, ипилимумаба, офатумумаба, панитумумаба, QBEND-10 и/или устекинумаба. В некоторых вариантах осуществления указанное mAb представляет собой ритуксимаб. В другом варианте осуществления указанное mAb представляет собой QBEND-10.
В некоторых вариантах осуществления CAR-T-клетка содержит выбранный эпитоп в scFv, характеризующийся специфичностью, которая распознается конкретным антителом. См., например, WO2016/120216, которая полностью включена в данный документ посредством ссылки. Такой эпитоп облегчает сортировку и/или истощение CAR-T-клеток. Эпитоп может быть выбран из любого количества эпитопов, известных в данной области техники. В некоторых вариантах осуществления эпитоп может быть мишенью для моноклонального антитела, одобренного для медицинского применения, такого как, например, без ограничения эпитоп CD20, распознаваемый ритуксимабом. В некоторых вариантах осуществления эпитоп содержит аминокислотную последовательность CPYSNPSLC (SEQ ID NO: 293)
В некоторых вариантах осуществления эпитоп расположен в CAR. Например, без ограничения, эпитоп может располагаться между scFv и шарнирным участком CAR. В некоторых вариантах осуществления в CAR могут использоваться два экземпляра одного и того же эпитопа, разделенные линкерами. Например, полипептид, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 294, или SEQ ID NO: 609, или SEQ ID NO: 295, можно использовать в CAR, с расположением между вариабельной областью легкой цепи и шарнирным участком.
gsggggscpysnpslcsggggscpysnpslcsggggs (SEQ ID NO: 294)
ELPTQGTFSNVSTNVS (SEQ ID NO: 609)
ELPTQGTFSNVSTNVSPAKPTTTA (SEQ ID NO: 295)
В некоторых вариантах осуществления внеклеточный связывающий домен CAR содержит следующую последовательность:
V1-L1-V2-(L)x-эпитоп 1-(L)x-;
V1-L1-V2-(L)x-эпитоп 1-(L)x-эпитоп 2-(L)x-;
V1-L1-V2-(L)x-эпитоп 1-(L)x-эпитоп 2-(L)x-эпитоп 3-(L)x-;
(L)x-эпитоп 1-(L)x-V1-L1-V2;
(L)x-эпитоп 1-(L)x-эпитоп 2-(L)x-V1-L1-V2;
эпитоп 1-(L)x-эпитоп 2-(L)x-эпитоп 3-(L)x-V1-L1-V2;
(L)x-эпитоп 1-(L)x-V1-L1-V2-(L)x-эпитоп 2-(L)x;
(L)x-эпитоп 1-(L)x-V1-L1-V2-(L)x-эпитоп 2-(L)x-эпитоп 3-(L)x-;
(L)x-эпитоп 1-(L)x-V1-L1-V2-(L)x-эпитоп 2-(L)x-эпитоп 3-(L)x-эпитоп 4-(L)x-;
(L)x-эпитоп 1-(L)x-эпитоп 2-(L)x-V1-L1-V2-(L)x-эпитоп 3-(L)x-;
(L)x-эпитоп 1-(L)x-эпитоп 2-(L)x-V1-L1-V2-(L)x-эпитоп 3-(L)x-эпитоп 4-(L)x-;
V1-(L)x-эпитоп 1-(L)x-V2;
V1-(L)x-эпитоп 1-(L)x-V2-(L)x-эпитоп 2-(L)x;
V1-(L)x-эпитоп 1-(L)x-V2-(L)x-эпитоп 2-(L)x-эпитоп 3-(L)x;
V1-(L)x-эпитоп 1-(L)x-V2-(L)x-эпитоп 2-(L)x-эпитоп 3-(L)x-эпитоп 4-(L)x;
(L)x-эпитоп 1-(L)x-V1-(L)x-эпитоп 2-(L)x-V2 или
(L)x-эпитоп 1-(L)x-V1-(L)x-эпитоп 2-(L)x-V2-(L)x-эпитоп 3-(L)x;
где
V1 представляет собой VL, и V2 представляет собой VH или V1 представляет собой VH, и V2 представляет собой VL;
L1 представляет собой линкер, подходящий для связывания цепи VH с цепью VL;
L представляет собой линкер, содержащий глициновые и сериновые остатки, и каждый случай L во внеклеточном связывающем домене может быть идентичным или отличаться от другого случая L в том же внеклеточном связывающем домене, который в определенных вариантах осуществления содержит или представляет собой SGGGG (SEQ ID NO: 614), GGGGS (SEQ ID NO: 615) или SGGGGS (SEQ ID NO: 616), и
x равен 0, или 1, или 2, и при этом каждый случай x выбран независимо от других; и
эпитоп 1, эпитоп 2, эпитоп 3 и эпитоп 4 представляют собой mAb-специфические эпитопы и могут быть идентичными или разными, и где VH представляет собой вариабельный фрагмент тяжелой цепи, и VL представляет собой вариабельный фрагмент легкой цепи. В некоторых вариантах осуществления эпитоп 1, эпитоп 2 и эпитоп 4 представляют собой mAb-специфический эпитоп, имеющий аминокислотную последовательность под SEQ ID NO: 293, а эпитоп 3 представляет собой mAb-специфический эпитоп, имеющий аминокислотную последовательность под SEQ ID NO: 295.
В некоторых вариантах осуществления внеклеточный связывающий домен CAR содержит следующую последовательность:
V1-L1-V2-(L)x-эпитоп 1-(L)x-;
V1-L1-V2-(L)x-эпитоп 1-(L)x-эпитоп 2-(L)x-;
V1-L1-V2-(L)x-эпитоп 1-(L)x-эпитоп 2-(L)x-эпитоп 3-(L)x-;
(L)x-эпитоп 1-(L)x-V1-L1-V2;
(L)x-эпитоп 1-(L)x-эпитоп 2-(L)x-V1-L1-V2;
эпитоп 1-(L)x-эпитоп 2-(L)x-эпитоп 3-(L)x-V1-L1-V2;
(L)x-эпитоп 1-(L)x-V1-L1-V2-(L)x-эпитоп 2-(L)x;
(L)x-эпитоп 1-(L)x-V1-L1-V2-(L)x-эпитоп 2-(L)x-эпитоп 3-(L)x-;
(L)x-эпитоп 1-(L)x-V1-L1-V2-(L)x-эпитоп 2-(L)x-эпитоп 3-(L)x-эпитоп 4-(L)x-;
(L)x-эпитоп 1-(L)x-эпитоп 2-(L)x-V1-L1-V2-(L)x-эпитоп 3-(L)x-;
(L)x-эпитоп 1-(L)x-эпитоп 2-(L)x-V1-L1-V2-(L)x-эпитоп 3-(L)x-эпитоп 4-(L)x-;
V1-(L)x-эпитоп 1-(L)x-V2;
V1-(L)x-эпитоп 1-(L)x-V2-(L)x-эпитоп 2-(L)x;
V1-(L)x-эпитоп 1-(L)x-V2-(L)x-эпитоп 2-(L)x-эпитоп 3-(L)x;
V1-(L)x-эпитоп 1-(L)x-V2-(L)x-эпитоп 2-(L)x-эпитоп 3-(L)x-эпитоп 4-(L)x;
(L)x-эпитоп 1-(L)x-V1-(L)x-эпитоп 2-(L)x-V2 или
(L)x-эпитоп 1-(L)x-V1-(L)x-эпитоп 2-(L)x-V2-(L)x-эпитоп 3-(L)x;
где
V1 представляет собой VL, и V2 представляет собой VH или V1 представляет собой VH, и V2 представляет собой VL;
L1 представляет собой линкер, подходящий для связывания цепи VH с цепью VL;
L представляет собой линкер, содержащий глициновые и сериновые остатки, и каждый случай L во внеклеточном связывающем домене может быть идентичным или отличаться от другого случая L в том же внеклеточном связывающем домене, который в определенных вариантах осуществления содержит или представляет собой SGGGG (SEQ ID NO: 614), GGGGS (SEQ ID NO: 615) или SGGGGS (SEQ ID NO: 616), и
x равен 0, или 1, или 2, и при этом каждый случай x выбран независимо от других; и
эпитоп 1, эпитоп 2, эпитоп 3 и эпитоп 4 представляют собой mAb-специфические эпитопы и могут быть идентичными или разными, и где VH представляет собой вариабельный фрагмент тяжелой цепи, и VL представляет собой вариабельный фрагмент легкой цепи. В некоторых вариантах осуществления эпитоп 1, эпитоп 2 и эпитоп 4 представляют собой mAb-специфический эпитоп, имеющий аминокислотную последовательность под SEQ ID NO: 293, а эпитоп 3 представляет собой mAb-специфический эпитоп, имеющий аминокислотную последовательность под SEQ ID NO: 609.
В некоторых вариантах осуществления внеклеточный связывающий домен CAR содержит следующую последовательность:
V1-L1-V2-(L)x-эпитоп 1-(L)x-эпитоп 2-(L)x- или
(L)x-эпитоп 1-(L)x-V1-L1-V2-(L)x-эпитоп 2-(L)x-эпитоп 3-(L)x-эпитоп 4-(L)x-, где V1, V2, L1, L, x и эпитоп 1, эпитоп 2, эпитоп 3 и эпитоп 4 определены выше.
В некоторых вариантах осуществления внеклеточный связывающий домен CAR содержит следующую последовательность:
(L)x-эпитоп 1-(L)x-V1-L1-V2-(L)x-эпитоп 2-(L)x-эпитоп 3-(L)x-эпитоп 4-(L)x- где V1, V2, L1, L, x определены выше, и где (L)x-эпитоп 1-(L)x представляет собой GGGGSCPYSNPSLCSGGGGSGGGGS (SEQ ID NO: 617),
(L)x-эпитоп 2-(L)x-эпитоп 3-(L)x-эпитоп 4 представляет собой GSGGGGSCPYSNPSLCSGGGGSELPTQGTFSNVSTNVSPAKPTTTACPYSNPSLC (SEQ ID NO: 618)
и V1, V2, L1, L, x определены выше.
В некоторых вариантах осуществления эпитоп-специфическое антитело может быть конъюгировано с цитотоксическим лекарственным средством. Существует также возможность усиления цитотоксичности CDC с применением сконструированных антител, на которые прививают компонент (компоненты) системы комплемента. В некоторых вариантах осуществления активацию CAR-T-клеток можно модулировать путем истощения клеток с применением антитела, которое распознает эпитоп.
Варианты применения в терапии
Выделенные клетки, полученные посредством описанных выше способов, или клеточные линии, полученные из таких выделенных клеток, можно применять в качестве лекарственного препарата. В некоторых вариантах осуществления такой лекарственный препарат может использоваться для лечения рака. В некоторых вариантах осуществления рак представляет собой почечно-клеточную карциному, глиобластому, глиому, такую как глиома низкой степени злокачественности, неходжкинскую лимфому (NHL), болезнь Ходжкина (HD), макроглобулинемию Вальденстрема, острый миелоидный лейкоз, множественную миелому, диффузную крупноклеточную лимфому, фолликулярную лимфому или немелкоклеточный рак легкого.
В некоторых вариантах осуществления рак представляет собой рак гематопоэтического происхождения, такой как лимфома или лейкоз. В некоторых вариантах осуществления рак выбран из группы, состоящей из множественной миеломы, злокачественного новообразования из плазматических клеток, лимфомы Ходжкина, узловой лимфомы Ходжкина с преобладанием лимфоцитов, болезни Калера и миеломатоза, лейкоза из плазматических клеток, плазмацитомы, B-клеточного пролимфоцитарного лейкоза, волосатоклеточного лейкоза, В-клеточной неходжкинской лимфомы (NHL), острого миелоидного лейкоза (AML), хронического лимфоцитарного лейкоза (CLL), острого лимфоцитарного лейкоза (ALL), хронического миелоидного лейкоза (CML), фолликулярной лимфомы, лимфомы Беркитта, лимфомы из клеток маргинальной зоны, лимфомы из клеток мантийной зоны, крупноклеточной лимфомы, B-лимфобластной лимфомы из клеток-предшественников, миелоидного лейкоза, макроглобулинемии Вальденстрема, диффузной крупноклеточной лимфомы, фолликулярной лимфомы, лимфомы лимфоидной ткани слизистых оболочек, мелкоклеточной лимфоцитарной лимфомы, первичной медиастинальной (тимусной) крупноклеточной лимфомы, лимфоплазматической лимфомы, узловой B-клеточной лимфомы из клеток маргинальной зоны, лимфомы маргинальной зоны селезенки, внутрисосудистой В-крупноклеточной лимфомы, первичной выпотной лимфомы, лимфоматоидного гранулематоза, T-клеточной/гистиоцитарной B-крупноклеточной лимфомы, первичной лимфомы центральной нервной системы, первичной кожной диффузной B-крупноклеточной лимфомы (ножной тип), EBV-положительной диффузной крупноклеточной B-лимфомы у пожилых людей, диффузной B-крупноклеточной лимфомы, ассоциированной с воспалением, внутрисосудистой B-крупноклеточной лимфомы, ALK-положительной B-крупноклеточной лимфомы, плазмабластной лимфомы, B-крупноклеточной лимфомы, возникающей при многоочаговой болезни Кастлемана, ассоциированной с HHV8, неклассифицированной B-клеточной лимфомы с признаками, промежуточными между диффузной B-крупноклеточной лимфомой и лимфомой Беркитта, неклассифицированной B-клеточной лимфомы с признаками, промежуточными между диффузной B-крупноклеточной лимфомой и классической лимфомой Ходжкина, и других видов рака, связанных с гемопоэтическими клетками, например ALL или AML.
В некоторых вариантах осуществления выделенная клетка по настоящему изобретению или клеточная линия, полученная из выделенных клеток, может быть использована в изготовлении лекарственного препарата для лечения рака у нуждающегося в этом пациента.
В данном документе также представлены способы лечения пациентов. В некоторых вариантах осуществления способ предусматривает обеспечение иммунной клеткой по настоящему изобретению нуждающегося в этом пациента. В некоторых вариантах осуществления способ предусматривает стадию введения трансформированных иммунных клеток по настоящему изобретению нуждающемуся в этом пациенту.
В некоторых вариантах осуществления Т-клетки по настоящему изобретению могут быть подвергнуты устойчивому размножению Т-клеток in vivo и могут сохраняться в течение продолжительного периода времени.
Способы лечения по настоящему изобретению могут быть улучшающими состояние, лечебными или профилактическими. Способ по настоящему изобретению может быть либо частью аутологичной иммунотерапии, либо частью лечения посредством аллогенной иммунотерапии. Настоящее изобретение является особенно подходящим для аллогенной иммунотерапии. Т-клетки от доноров можно трансформировать в отличные от аллореактивных клетки с применением стандартных протоколов и воспроизводить при необходимости с получением тем самым CAR-T-клеток, которые можно вводить одному или более пациентам. Такая терапия посредством CAR-T-клеток может быть сделана доступной в виде готового к реализации терапевтического продукта.
Клетки, которые можно использовать в способах по настоящему изобретению, описаны в предыдущем разделе. Данное лечение можно использовать для лечения пациентов, у которых диагностирован, например, рак. Виды рака, которые могут быть подвергнуты лечению, включают, например, без ограничения раковые заболевания, в которые вовлечены В-лимфоциты, включая любой из перечисленных выше видов рака. Типы рака, подлежащие лечению с помощью CAR и CAR-T-клеток по настоящему изобретению, включают без ограничения определенные лейкозы или лимфоидные злокачественные новообразования. Также включены опухоли/виды рака у взрослых и опухоли/виды рака у детей. В некоторых вариантах осуществления лечение может осуществляться в комбинации с одним или более средствами противораковой терапии, выбранными из группы из терапии с помощью антител, химиотерапии, терапии с помощью цитокинов, терапии с помощью дендритных клеток, генной терапии, гормональной терапии, терапии с помощью лазерного излучения и лучевой терапии.
В некоторых вариантах осуществления можно проводить лечение пациентов, проходящих иммуносупрессивную терапию. Более того, в некоторых вариантах осуществления способы по настоящему изобретению основаны на клетках или популяции клеток, которые стали резистентными к по меньшей мере одному иммуносупрессивному средству вследствие инактивации гена, кодирующего рецептор для такого иммуносупрессивного средства. В данном аспекте иммуносупрессивное лечение должно способствовать отбору и размножению Т-клеток в соответствии с настоящим изобретением в организме пациента. Введение клеток или популяции клеток в соответствии с настоящим изобретением можно осуществлять любым удобным способом, в том числе с помощью аэрозольной ингаляции, инъекции, перорального приема, инфузии, трансфузии, имплантации или трансплантации. Композиции, описанные в данном документе, можно вводить пациенту подкожно, внутрикожно, интратуморально, интранодально, интрамедуллярно, внутримышечно, посредством внутривенной или внутрилимфатической инъекции или инфузии или внутрибрюшинно. В некоторых вариантах осуществления клеточные композиции по настоящему изобретению вводят путем внутривенной инъекции или инфузии.
В некоторых вариантах осуществления введение клеток или популяции клеток может предусматривать введение, например, от приблизительно 104 до приблизительно 109 клеток на кг веса тела, включая все целые значения количества клеток в этих диапазонах. В некоторых вариантах осуществления введение клеток или популяции клеток может предусматривать введение от приблизительно 105 до приблизительно 106 клеток на кг веса тела, включая все целые значения количества клеток в этих диапазонах. Клетки или популяцию клеток можно вводить в одной или более дозах. В некоторых вариантах осуществления указанное эффективное количество клеток можно вводить в виде одной дозы. В некоторых вариантах осуществления указанное эффективное количество клеток можно вводить в виде более чем одной дозы в течение определенного периода времени. Определение сроков введения является компетенцией главного лечащего врача и зависит от клинического состояния пациента. Клетки или популяция клеток могут быть получены из любого источника, например от пациента, из банка крови или от донора. Хотя индивидуальные потребности варьируются, определение оптимальных диапазонов эффективных количеств данного типа клеток для конкретного заболевания или условий находится в пределах компетенции специалиста в данной области техники. Эффективное количество означает количество, которое обеспечивает терапевтическую или профилактическую пользу. Вводимая доза будет зависеть от возраста, состояния здоровья и веса реципиента, вида сопутствующего лечения при его наличии, частоты лечения и природы требуемого эффекта. В некоторых вариантах осуществления эффективное количество клеток или композиции, содержащей эти клетки, вводят парентерально. В некоторых вариантах осуществления введение может быть внутривенным. В некоторых вариантах осуществления введение можно осуществлять непосредственно с помощью инъекции в опухоль.
В некоторых вариантах осуществления способы предусматривают (а) введение субъекту с заболеванием первой дозы аллогенных CAR-T-клеток. В некоторых вариантах осуществления первая доза содержит приблизительно 1×104 клеток, приблизительно 5×104 клеток, приблизительно 1×105 клеток, приблизительно 5×105 клеток, приблизительно 1×106 клеток, приблизительно 5×106 клеток, приблизительно 6×106 клеток, приблизительно 1×107 клеток, приблизительно 6×107 клеток, приблизительно 1×108, приблизительно 1,8×108 клеток или приблизительно 4,8×108 клеток. В некоторых вариантах осуществления способы дополнительно предусматривают (b) введение субъекту последующей дозы CAR-T-клеток в момент времени, который составляет по меньшей мере или более приблизительно 5 недель после и через менее приблизительно 24 недель от начала введения в (а).
В некоторых вариантах осуществления субъекту с рецидивирующим/рефрактерным заболеванием (например, рецидивирующей/рефрактерной RCC) вводят первую и последующую дозу аллогенных CAR-T-клеток, каждая из которых содержит приблизительно 6×106 клеток, и последующую дозу CAR-T-клеток в (b) вводят через приблизительно 99 дней после начала введения в (а).
В некоторых вариантах осуществления способы дополнительно предусматривают введение дополнительных последующих или последующих доз, так что вводят первую и несколько последующих доз, например, в соответствии с количествами вводимых доз и графиками, указанными для первой и последующих доз. В некоторых вариантах осуществления первую из одной или более последующих доз вводят в момент времени, который составляет по меньшей мере или более 5 недель от начала введения следующей дозы. В некоторых вариантах осуществления введение первой, последующей и последующих доз включает введение по меньшей мере трех доз в пределах 5 недель или в течение приблизительно 5 недель. В некоторых вариантах осуществления последующую дозу вводят через приблизительно 16 недель от начала введения первой дозы, а дополнительную последующую или последующую дозу вводят на 17 неделе от начала введения первой дозы. В некоторых вариантах осуществления дополнительные последующие дозы вводят на 17 неделе и/или 34 неделе от начала введения первой дозы.
В некоторых аспектах время введения последующей (последующих) дозы (доз) дополнительно является временем, в течение которого субъект не проявляет иммунного ответа, например, не проявляет выявляемого адаптивного иммунного ответа хозяина, специфического для CAR-T, указанного для первой (или предшествующей) дозы.
В некоторых вариантах осуществления время между введением первой дозы (начальной дозы), например, между началом введения первой или предыдущей дозы и началом введения последующей дозы (например, началом введения следующей дозы) составляет более приблизительно 4 недель, например, более приблизительно 5, 6, 7, 8 или 9 дней, например, более приблизительно 20 недель, например, от приблизительно 9 до приблизительно 35 недель, от приблизительно 14 до приблизительно 28 недель, от 15 до 27 недель или от приблизительно 16 до приблизительно 18 недель; и/или приблизительно 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26 или 27 недель. В некоторых вариантах осуществления введение следующей дозы (например, от начала введения) проводят через более приблизительно 5 недель после и через менее приблизительно 24 недели после введения первой или предшествующей дозы (например, от начала введения). В некоторых вариантах осуществления введение следующей дозы начинают через 17 недель от введения первой дозы. В некоторых вариантах осуществления время между введением первой и последующей дозы (например, от начало введения) или до и последующей дозы составляет более приблизительно 5 недель и менее приблизительно 24 недель, например, от 10 до 24 недель, например приблизительно 17 недель. В некоторых вариантах осуществления время между введением первой и последующей дозы (например, от начала введения) составляет приблизительно 17 недель.
В некоторых вариантах осуществления настоящего изобретения клетки вводят пациенту в сочетании (например, до, одновременно или после) с любым количеством подходящих средств для лечения, включая среди прочего лечение с помощью таких средств, как терапия с использованием моноклональных антител, антагониста CCR2 (например, INC-8761), противовирусная терапия, цидофовира и интерлейкина-2, цитарабина (также известного как ARA-C), или лечение пациентов с MS с помощью натализумаба, или лечение пациентов с псориазом с помощью эфализумаба, или другие варианты лечения пациентов с PML. В некоторых вариантах осуществления CAR-T-клетки, специфические к CD70, вводят пациенту в сочетании с одним или более из следующего: с антителом к PD-1 (например, ниволумабом, пембролизумабом или PF-06801591), антителом к PD-L1 (например, авелумабом, атезолизумабом или дурвалумабом), антителом к OX40 (например, PF-04518600), антителом к 4-1BB (например, PF-05082566), антителом к MCSF (например, PD-0360324), антителом к GITR и/или антителом к TIGIT. В некоторых вариантах осуществления CAR, специфический к CD70, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 319 или 327, вводят пациенту в сочетании с авелумабом, представляющим собой антитело к PD-L1. В дополнительных вариантах осуществления Т-клетки по настоящему изобретению можно использовать в комбинации с химиотерапией, лучевой терапией, иммунодепрессантами, такими как циклоспорин, азатиоприн, метотрексат, микофенолат и FK506, антителами или другими иммунодеструктивными средствами, такими как CAMPATH, с антителами к CD3 или другими способами терапии с помощью антител, цитоксином, флударабином, циклоспорином, FK506, рапамицином, микофеноловой кислотой, стероидами, FR901228, цитокинами и/или ионизирующим излучением. Данные лекарственные средства ингибируют кальциневрин (циклоспорин и FK506) или кальций-зависимую фосфатазу, или ингибируют киназу p70S6, которая важна для передачи сигналов, индуцированной фактором роста (рапамицин) (Henderson, Naya et al. 1991; Liu, Albers et al. 1992; Bierer, Hollander et al. 1993). В дополнительных вариантах осуществления Т-клетки по настоящему изобретению можно использовать в комбинации с ингибиторами рецепторной тирозинкиназы, такими как мидостаурин, сунитиниб и акситаниб, ингибиторами mTOR, такими как рапамацин и эверолимус, эпигенетическими модуляторами, такими как вориностат, ингибиторами протеасом, такими как бортезомиб, иммуномодулирующими средствами, такими как леналидомид, ингибиторами Hedgehog, такими как эрисмодегиб и PF-04449913, или ингибиторами изоцитратдегидрогеназы (IDH), такими как AG-120 и AG-221. В дополнительном варианте осуществления клеточные композиции по настоящему изобретению вводят пациенту в сочетании с (например, до, одновременно или после) трансплантацией костного мозга, терапией по деструкции Т-лимфоцитов с использованием химиотерапевтических средств, таких как флударабин, наружной дистанционной лучевой терапией (XRT), циклофосфамидом или антителами, например, OKT3 или CAMPATH. В некоторых вариантах осуществления клеточные композиции по настоящему изобретению вводят после терапии по деструкции B-клеток, например, с помощью средств, которые взаимодействуют с CD20, например, ритуксана. Например, в некоторых вариантах осуществления субъекты могут получать стандартное лечение с использованием высокодозовой химиотерапии с последующей трансплантацией стволовых клеток периферической крови. В некоторых вариантах осуществления после трансплантации субъекты получают инфузию размноженных иммунных клеток по настоящему изобретению. В некоторых вариантах осуществления размноженные клетки вводят до или после хирургического вмешательства.
В некоторых вариантах осуществления представлены способы истощения сконструированных иммунных клеток, экспрессирующих CAR, специфический к CD70, у субъекта, которому вводят указанные клетки. Истощение может осуществлять путем подавления или устранения.
В одном аспекте способ истощения сконструированных иммунных клеток, экспрессирующих CAR, специфический к CD70, содержащий эпитоп, специфический к моноклональному антителу, предусматривает приведение в контакт указанной сконструированной иммунной клетки с моноклональным антителом, специфическим к данному эпитопу.
В некоторых вариантах осуществления способ истощения у субъекта, которому ввели сконструированные иммунные клетки, экспрессирующие CAR, специфический к CD70, содержащий эпитоп, специфический к моноклональному антителу, предусматривает введение субъекту моноклонального антитела, специфического к эпитопу. В данных вариантах осуществления введение субъекту моноклонального антитела, специфического к эпитопу, присутствующему во внеклеточном домене CAR, устраняет или подавляет активность сконструированных CAR-экспрессирующих иммунных клеток у субъекта. В одном аспекте истощение сконструированных иммунных клеток, экспрессирующих CAR, позволяет восстановить эндогенную популяцию CD70-экспрессирующих клеток.
В одном аспекте настоящее изобретение относится к способу стимулирования восстановления эндогенных клеток, экспрессирующих CD70, у субъекта, которому ввели сконструированные иммунные клетки, экспрессирующие на поверхности клетки CAR, специфический к CD70, содержащий эпитоп, специфический к моноклональному антителу, при этом способ предусматривает введение субъекту моноклонального антитела, специфического к эпитопу. В некоторых вариантах осуществления эндогенные CD70-экспрессирующие клетки представляют собой эндогенные CD70-экспрессирующие клетки костного мозга. В одном аспекте термин «восстановление» относится к повышению количества эндогенных CD70-экспрессирующих клеток. Количество эндогенных CD70-экспрессирующих клеток может повышаться вследствие увеличения пролиферации эндогенных CD70-экспрессирующих клеток и/или вследствие снижения устранения эндогенных CD70-экспрессирующих клеток с помощью CAR-экспрессирующих сконструированных иммунных клеток. В некоторых вариантах осуществления введение моноклонального антитела субъекту обеспечивает истощение сконструированных иммунных клеток, экспрессирующих CAR, и повышает у субъекта количество эндогенных CD70-экспрессирующих клеток, например эндогенных CD70-экспрессирующих клеток-предшественников костного мозга. В одном варианте осуществления введение моноклонального антитела субъекту обеспечивает повышение количества эндогенных клеток, экспрессирующих CD70, на по меньшей мере приблизительно 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%. %, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90% или 95% по сравнению с количеством эндогенных клеток, экспрессирующих CD70, до введения моноклонального антитела.
В одном аспекте представлен способ лечения CD70-опосредованного состояния у субъекта, при этом способ предусматривает: (a) введение субъекту сконструированных иммунных клеток, экспрессирующих на клеточной поверхности CAR, специфические к CD70, содержащие один или более эпитопов, специфических к одному или более моноклональным антителам; и (b) последующее истощение сконструированных иммунных клеток у субъекта путем введения субъекту одного или более моноклональных антител, специфических к эпитопу.
В некоторых вариантах осуществления mAb, используемые в способе истощения сконструированных CAR-экспрессирующих иммунных клеток, выбраны из алемтузумаба, ибритумомаба тиуксетана, муромонаба-CD3, тозитумомаба, абциксимаба, базиликсимаба, брентуксимаба ведотина, цетуксимаба, инфликсимаба, ритуксимаба, бевацизумаба, цертолизумаба пегола, даклизумаба, экулизумаба, эфализумаба, гемтузумаба, натализумаба, омализумаба, паливизумаба, ранибизумаба, тоцилизумаба, трастузумаба, ведолизумаба, адалимумаба, белимумаба, канакинумаба, деносумаба, голимумаба, ипилимумаба, офатумумаба, панитумумаба, QBEND-10, устекинумаба или их комбинаций.
В некоторых вариантах осуществления указанный эпитоп, специфический к моноклональному антителу (mAb-специфический эпитоп), представляет собой эпитоп или мимотоп CD20, например SEQ ID NO: 609, SEQ ID NO: 294 или SEQ ID NO: 295, а также mAb, специфическое к эпитопу, представляет собой ритуксимаб.
В некоторых вариантах осуществления стадия введения субъекту моноклонального антитела предусматривает инфузию субъекту моноклонального антитела. В некоторых вариантах осуществления количество эпитоп-специфического mAb, вводимое субъекту, достаточно для устранения по меньшей мере 20%, 30%, 40%, 50%, 60%, 70%, 80% или 90% CAR-экспрессирующих иммунных клеток у субъекта.
В некоторых вариантах осуществления стадия введения субъекту моноклонального антитела предусматривает инфузию субъекту 375 мг/м2 ритуксимаба один или более раз в неделю.
В некоторых вариантах осуществления, если иммунные клетки, экспрессирующие CAR, содержащий mAb-специфический эпитоп (CAR-экспрессирующие иммунные клетки), истощают в анализе CDC с использованием эпитоп-специфических mAb, то количество жизнеспособных CAR-экспрессирующих иммунных клеток уменьшается, например, по меньшей мере на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80% или 90%.
В некоторых вариантах осуществления цитотоксическое лекарственное средство связано с эпитоп-специфическими mAb, которые используются для истощения CAR-экспрессирующих иммунных клеток. Объединяя активности моноклональных антител по целенаправленному воздействию с цитотоксической активностью цитотоксических лекарственных средств, конъюгат антитело-лекарственное средство (ADC) позволяет осуществлять тонкое распознавание здоровой и пораженной ткани по сравнению с применением только лекарственного средства. Для нескольких ADC были получены разрешения на продажу; при этом технология их получения, в частности на линкерах, широко представлена в следующем уровне техники (Payne, G. (2003) Cancer Cell 3:207-212; Trail et al (2003) Cancer Immunol. Immunother. 52:328-337; Syrigos and Epenetos (1999) Anticancer Research 19:605-614; Niculescu-Duvaz and Springer (1997) Adv. Drug Del. Rev. 26:151-172; патент США № 4975278).
В некоторых вариантах осуществления эпитоп-специфическое mAb, подлежащее инфузии, предварительно конъюгировано с молекулой, способной стимулировать комплемент-зависимую цитотоксичность (CDC). Таким образом, система комплемента помогает или дополняет способность антител очищать организм от патогенов. При стимуляции с помощью одного из нескольких запускается каскад активации в виде массивного усиления ответа и активации мембраноатакующего комплекса уничтожения клеток. Для конъюгирования mAb можно использовать другую молекулу, например, гликаны [Courtois, A, Gac-Breton, S., Berthou, C, Guezennec, J., Bordron, A. and Boisset, C. (2012), Complement dependent cytotoxicity activity of therapeutic antibody fragments is acquired by immunogenic glycan coupling, Electronic Journal of Biotechnology ISSN: 0717-3458; http://www.ejbiotechnology.info DOI: 10.2225/voll5-issue5).
Наборы
В настоящем изобретении представлены наборы для применения в способах по настоящему изобретению. Наборы по настоящему изобретению включают один или более контейнеров, содержащих полинуклеотид, кодирующий CAR, специфический к CD70, или сконструированную иммунную клетку, содержащую полинуклеотид, кодирующий CAR, специфический к CD70, описанный в данном документе, и инструкции по применению в соответствии с любым из способов по настоящему изобретению, описанных в данном документе. Как правило, эти инструкции содержат описание введения сконструированной иммунной клетки для описанных выше видов терапевтического лечения. Набор может включать одно или более средств для лимфодеплеции (например, алемтузумаб, цитоксан, флударабин, циклофосфамид или темозоломид).
Инструкции, относящиеся к применению сконструированных иммунных клеток, описанных в данном документе, как правило, включают информацию о дозировке, схеме введения доз и пути введения для предполагаемого лечения. Контейнеры могут представлять собой однократные дозы, общие упаковки (например, многодозовые упаковки) или субъединицы доз. Инструкции, предоставляемые в наборе по настоящему изобретению, как правило, представляют собой письменные инструкции на этикетке или листке-вкладыше (например, бумажном листке, включенном в набор), однако приемлемыми также являются машиночитаемые инструкции (например, инструкции, хранящиеся на магнитном или оптическом диске для хранения). В некоторых вариантах осуществления контейнеры можно идентифицировать (например, по этикетке, штрих-коду или радиочастотной идентификации (RFID)), отслеживать или фиксировать с помощью машиночитаемого идентификатора контейнера.
Наборы по настоящему изобретению помещены в подходящую упаковку. Подходящая упаковка включает без ограничения флаконы, бутылки, банки, гибкую упаковку (например, герметичные майларовые или пластиковые пакеты) и им подобные. В некоторых вариантах осуществления контейнер (например, пластиковый пакет) является подходящим для внутривенной инфузии. Также предусмотрены упаковки для применения в комбинации со специальным устройством, таким как ингалятор, устройство для назального введения (например, распылитель) или инфузионное устройство, такое как мининасос. Набор может иметь стерильный порт доступа (например, контейнер может представлять собой мешок для внутривенного раствора или флакон с пробкой, прокалываемой иглой для подкожных инъекций). Контейнер также может иметь стерильный порт доступа (например, контейнер может представлять собой мешок для внутривенного раствора или флакон с пробкой, прокалываемой иглой для подкожных инъекций). По меньшей мере одно действующее вещество в композиции представляет собой CAR, специфический к CD70. Контейнер может дополнительно содержать второе фармацевтически активное средство.
В наборах могут необязательно предоставляться дополнительные компоненты, такие как буферы и интерпретирующая информация. Обычно набор содержит контейнер и этикетку или листок-вкладыш (листки-вкладыши) на контейнере, или они связаны с ним.
Следующие примеры предложены лишь в иллюстративных целях, но не предназначены для ограничения объема настоящего изобретения. В действительности, различные модификации настоящего изобретения в дополнение к представленным и описанным в данном документе будут очевидны специалистам в данной области техники, исходя из вышеизложенного описания, и попадают в объем прилагаемой формулы изобретения.
Депозиты были созданы в соответствии с положениями Будапештского договора о международном признании депонирования микроорганизмов для целей патентной процедуры и правил к нему (Будапештский договор). Это гарантирует сохранение жизнеспособной культуры в депозите в течение 30 лет от даты депонирования. Депозит будет доступен через ATCC в соответствии с условиями Будапештского договора и при условии соглашения между Pfizer, Inc. и ATCC, которое гарантирует постоянный и неограниченный доступ к потомству культуры депозита для общественности после выдачи соответствующего патента США или при обнародовании любой заявки на патент США или иностранного государства в зависимости от того, что наступит раньше, и обеспечивает доступность потомства для лиц, определенных Комиссаром США по патентам и товарным знакам, имеющим право на него в соответствии с 35 USC Раздел 122 и правила Уполномоченного в соответствии с ним (включая раздел 1.14 37 C.F.R. с конкретной ссылкой на 886 OG 638).
Правопреемник настоящей заявки согласился с тем, что если культура материалов в депозите погибнет, будет утеряна или уничтожена при культивировании в подходящих условиях, материалы будут незамедлительно заменены такими же при получении уведомления. Доступность депонированного материала не должна толковаться как лицензия на практическую реализацию настоящего изобретения в нарушение прав, предоставленных в соответствии с полномочиями любого правительства в соответствии с его патентным законодательством.
ПРИМЕРЫ
Пример 1. Получение CAR-T-клеток, специфических к CD70
Следующие кодон-оптимизированные последовательности CAR, специфических к CD70, перечисленные в таблице 5 ниже, синтезировали и субклонировали в следующие лентивирусные векторы: pLVX-EF1a-TurboGFP-P2A-CD70 CAR (Clontech) или pCLS-EF1a-BFP-P2A-CD70 CAR (Cellectis), используя сайты рестрикции XmaI (5 ') и MluI (3') (клонируя таким образом CAR после сайта P2A).
Таблица 5. Иллюстративные CAR, специфические к CD70
(SEQ ID NO: 311)
VH 31H1;
линкер GS;
VL 31H1;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
(SEQ ID NO: 312)
VH 63B2;
линкер GS;
VL 63B2;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
(SEQ ID NO: 313)
VH 40E3;
линкер GS;
VL 40E3;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
(SEQ ID NO: 314)
VH 42C3;
линкер GS;
VL 42C3;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
(SEQ ID NO: 315)
VH 45F11;
линкер GS;
VL 45F11;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
(SEQ ID NO: 316)
VH 64F9;
линкер GS;
VL 64F9;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
(SEQ ID NO: 317)
VH 72C2;
линкер GS;
VL 72C2;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
(SEQ ID NO: 318)
VH 2F10;
линкер GS;
VL 2F10;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
(SEQ ID NO: 319)
VH 4F11;
линкер GS;
VL 4F11;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
(SEQ ID NO: 320)
VH 10H10;
линкер GS;
VL 10H10;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
(SEQ ID NO: 321)
VH 17G6;
линкер GS;
VL 17G6;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
(SEQ ID NO: 322)
VH 65E11;
линкер GS;
VL 65E11;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
(SEQ ID NO: 323)
VH P02B10;
линкер GS;
VL P02B10;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
(SEQ ID NO: 324)
VH P07D03;
линкер GS;
VL P07D03;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
(SEQ ID NO: 325)
VH P08A02;
линкер GS;
VL P08A02;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
(SEQ ID NO: 326)
VH P08E02;
линкер GS;
VL P08E02;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
(SEQ ID NO: 327)
VH P08F08;
линкер GS;
VL P08F08;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
(SEQ ID NO: 328)
VH P08G02;
линкер GS;
VL P08G02;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
(SEQ ID NO: 329)
VH P12B09;
линкер GS;
VL P12B09;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
(SEQ ID NO: 330)
VH P12F02;
линкер GS;
VL P12F02;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
(SEQ ID NO: 331)
VH P12G07;
линкер GS;
VL P12G07;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
(SEQ ID NO: 332)
VH P13F04;
линкер GS;
VL P13F04;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
(SEQ ID NO: 333)
VH P15D02;
линкер GS;
VL P15D02;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
(SEQ ID NO: 334)
VH P16C05;
линкер GS;
VL P16C05;
линкер GS;
шарнирный участок из CD8α;
домен TM из CD8α;
ISD 41BB;
ISD CD3ζ
Также получены CAR, содержащие ScFv на основе последовательностей 10A1, 10E2, 11A1, 11C1, 11D1, 11E1, 12A2, 12C4, 12C5, 12D3, 12D6, 12D7, 12F5, 12H4, 8C8, 8F7, 8F8, 9D8, 9E10, 9E5, 9F4 или 9F8, и они содержат последовательности, представленные под SEQ ID NO: 580, 581, 582, 583, 584, 585, 586, 587, 588, 589, 590, 591, 592, 593, 594, 595, 596, 597, 598, 599, 600 и 601.
Пример 2. Скрининг с использованием клеток Jurkat для in vitro определения характеристик CAR к CD70
Клетки Jurkat представляют собой иммортализованную линию Т-клеток человека и подобно первичным Т-клеткам экспрессируют CD70 при активации или трансдукции. Таким образом, эти клетки были выбраны для трансдукции посредством CAR к CD70 для изучения их профиля активации. Клетки Jurkat, модифицированные с использованием CRISPR/Cas9 с нокаутом по CD70 («KO Jurkat»), или первичные Jurkat («WT Jurkat») трансдуцировали с помощью CAR к CD70. Их профиль аутоактивации определяли путем сравнения процентной доли экспрессии CD69 на WT Jurkat (аутоактивация и мишень-зависимая активация, поскольку WT Jurkat при трансдукции экспрессируют мишень, т. е. CD70) с таким показателем у KO Jurkat (только аутоактивация в отсутствие мишени, т. е. CD70) посредством проточной цитометрии. Клоны, которые продемонстрировали мишень-специфическую активацию и минимальную аутоактивацию, затем отбирали на основании «коэффициента активации» (определение термина см. ниже). Аутоактивация является термином, используемым для описания мишень-независимой кластеризации и активации CAR. Аутоактивация CAR может варьироваться от минимальной/нулевой до высокой и считается неотъемлемой характеристикой или тенденцией scFv к агрегации и кластеризации. Аутоактивация приводит к длительной передаче сигналов и может привести к дифференцировке Т-клеток, истощению и снижению цитолитического потенциала. Скрининг и устранение аутоактивирующихся с высокой частотой CAR является важным шагом в оптимальной идентификации CAR. В идеале у CAR аутоактивация минимальна.
Связывание CAR с рекомбинантным антигеном представляет собой один из способов определения характеристик CAR и их объединения в уникальные группы. Сильное связывание может указывать на то, что CAR высокоэкспрессируется на поверхности клетки и характеризуется аффинностью от умеренной до высокой по отношению к их антигену-мишени. Низкое или минимальное связывание может указывать на низкую экспрессию и/или более слабую аффинность. CAR с высокой и низкой степенью связывания следует дополнительно охарактеризовать, поскольку оптимальная аффинность и экспрессия на клеточной поверхности неизвестны.
Материалы и способы
Нокаут CD70, опосредованный CRISPR/Cas9, в клетках Jurkat
Клетки Jurkat трансфицировали направляющими РНК-векторами, нацеливающимися на CD70, содержащими Cas9 и GFP, полученными из ДНК 2.0, с использованием Lipofectamine 3000 (Invitrogen). Через сорок восемь часов после трансфекции проводили сортировку отдельных клеток с активацией флуоресценции для отбора клеток GFP+ CD70-. Затем отдельные клоны размножали и путем грубого лизиса клеток получали геномную ДНК для ПЦР. Продукты ПЦР секвенировали для идентификации клонов со вставками/делециями или сдвигами рамки считывания, указывающими на нокаут CD70.
Трансдукция клеток Jurkat с помощью CAR к CD70
Клетки HEK293T высевали из расчета 0,5 миллиона клеток на мл в 2 мл DMEM (Gibco), дополненной 10% FBS (Hyclone или JR Scientific), на лунку в 6-луночном планшете в день 0. В день 1 лентивирус получали путем смешивания лентивирусных упаковывающих векторов: 1,5 мкг psPAX2, 0,5 мкг pMD2G и 2 мкг соответствующего вектора для переноса CAR, содержащего метку GFP, в 250 мкл Opti-MEM (Gibco) на лунку в 6-луночном планшете («смесь ДНК»). 10 мкл Lipofectamine 2000 (Invitrogen) в 250 мкл Opti-MEM инкубировали при комнатной температуре в течение 5 минут, а затем добавляли к смеси ДНК. Вирус инкубировали при комнатной температуре в течение 20 минут, и в общем объеме 500 мкл медленно добавляли по стенкам в лунки, содержащие HEK293T. В день 2 среду из каждой лунки 6-луночного планшета заменяли на 2 мл на лунку средой для клеток Jurkat, т. е. RPMI (Gibco), дополненной 10% FBS. В день 3 клетки Jurkat (KO или WT) ресуспендировали в количестве 0,5 миллиона клеток на мл в 2 мл RPMI, дополненной 10% FBS, на лунку 6-луночного планшета. Лентивирусные супернатанты клеток HEK293T собирали и пропускали через фильтр 0,45 микрон (EMD Millipore) с удалением клеточного дебриса, а затем добавляли к клеткам Jurkat. В день 6 эффективность трансдукции определяли путем выявления сигнала GFP с помощью проточной цитометрии. При необходимости клетки размножали в колбах большего размера, используя RPMI, дополненную 10% FBS.
Профиль активации и способность связывать белок CD70
В день 5 трансдуцированные клетки окрашивали человеческим антителом к CD69, конъюгированным с PE-Cy7, и анализировали на проточном цитометре с получением процентной доли популяции CD69+ для каждого CAR. Клетки также инкубировали с рекомбинантным биотинилированным человеческим белком CD70, окрашивали стрептавидином, конъюгированным с PE, и анализировали на проточном цитометре для определения связывания белка. Коэффициенты активации (активация WT/активация KO) и связывание белка использовали для ранжирования CAR.
Таблица 6
(WT/KO)
Коэффициент активации и связывание CAR с белками гибридомы определяли в скрининге с использованием клеток Jurkat и использовали для in vitro определения характеристик CAR. Коэффициент активации определяли путем расчета соотношения экспрессии CD69 в процентах на клетках Jurkat дикого типа, трансдуцированных CAR к CD70 (WT), и экспрессии в процентах на клетках Jurkat с нокаутом по CD70, трансдуцированных CAR к CD70 (KO). Более высокий коэффициент активации указывает на мишень-зависимую активацию. Связывание с белками определяли путем связывания с рекомбинантным биотинилированным белком hCD70, и его выявляли с использованием стрептавидина, конъюгированного с красителем фикоэритрином (РЕ), с помощью проточной цитометрии. Значения связывания белков указывают на процентную долю CD3+ CAR-Т-клеток, которые связываются с человеческим белком CD70.
Таблица 7
(WT/KO)
Таблица 7. Коэффициент активации и связывание с белками фаговых CAR определяли с помощью скрининга с использованием клеток Jurkat. Коэффициент активации использовали для in vitro определения характеристик CAR. Коэффициент активации определяли путем расчета соотношения экспрессии CD69 в процентах на клетках Jurkat дикого типа, трансдуцированных CAR к CD70 (WT), и экспрессии в процентах на клетках Jurkat с нокаутом по CD70, трансдуцированных CAR к CD70 (KO). Более высокий коэффициент активации указывает на мишень-зависимую активацию. Связывание с белками определяли путем связывания с рекомбинантным биотинилированным белком hCD70, и его выявляли с использованием стрептавидина, конъюгированного с красителем фикоэритрином (РЕ), с помощью проточной цитометрии. Значения связывания белков указывают на процентную долю CD3+ CAR-Т-клеток, которые связываются с человеческим белком CD70.
CAR, которые демонстрировали минимальную аутоактивацию, т. е. минимальную экспрессию CD69 при трансдуцировании в Jurkat с KO по CD70, считались более желательными по сравнению с такими, которые активировались с высокой степенью даже в отсутствие мишени, поскольку это может привести к более истощенному фенотипу CAR. Аналогично CAR с более высокой степенью связывания с человеческим белком CD70 считались более желательными, поскольку это свидетельствовало о надлежащих экспрессии и фолдинге CAR на поверхности.
Пример 3. Скрининг с использованием первичных Т-клеток для in vitro определения характеристик фаговых и гибридомных CAR
Первичные человеческие Т-клетки трансдуцировали с помощью CAR к CD70 для определения эффективности трансдукции, экспрессии CD70 на Т-клетках в культуре и субпопуляциях Т-клеток. Затем трансдуцированные CAR-Т-клетки замораживали для использования в функциональных анализах.
Эффективность трансдукции конструкциями на основе CAR может сильно варьировать между разными клонами. Большая эффективность трансдукции приводит к увеличению количества CAR-Т-клеток и более эффективному процессу получения, в то время как CAR с низкой эффективностью трансдукции могут не подходить для крупномасштабного производства. В некоторых вариантах осуществления предпочтительна высокая эффективность трансдукции.
Т-клетки обладают рядом фенотипов или субпопуляций, указывающих на состояние дифференцировки и воздействие антигена. Метки на клеточной поверхности помогают идентифицировать субпопуляции Т-клеток, при этом маркер CD62L, как правило, обнаруживается на наивных, стволовых клетках памяти и центральных Т-клетках памяти. Эти клетки являются менее дифференцированными по сравнению с другими субпопуляциями, такими как эффекторные Т-клетки памяти и эффекторные Т-клетки, поэтому CAR-Т-клетки с более высокой процентной долей CD62L-положительных клеток в некоторых вариантах осуществления являются предпочтительными.
Экспрессия CD70 на поверхности также варьируется между различными трансдуцированными CAR: некоторые CAR-T-клетки экспрессируют 20-40% CD70 из-за активации и трансдукции T-клеток, а другие не экспрессируют.
Материалы и способы
Выделение первичных Т-клеток
Т-клетки выделяли из образцов лейкоцитарных пленок, полученных из Стэнфордского университета, с использованием среды с градиентом плотности фиколла (Ficoll Paque PLUS/GE Healthcare Life Sciences). Выделяли слой РВМС, а Т-клетки очищали с использованием коммерчески доступного набора для выделения Т-клеток (Miltenyi Biotec).
Трансдукция Т-клеток с помощью CAR к CD70
Клетки HEK293T высевали из расчета 0,5 миллиона клеток на мл в 2 мл DMEM (Gibco), дополненной 10% FBS (Hyclone или JR Scientific), на лунку в 6-луночном планшете в день 0. В день 1 лентивирус получали путем смешивания лентивирусных упаковывающих векторов: 1,5 мкг psPAX2, 0,5 мкг pMD2G и 2 мкг соответствующего вектора для переноса CAR, содержащего метку GFP, в 250 мкл Opti-MEM (Gibco) на лунку в 6-луночном планшете («смесь ДНК»). 10 мкл Lipofectamine 2000 (Invitrogen) в 250 мкл Opti-MEM инкубировали при комнатной температуре в течение 5 минут, а затем добавляли к смеси ДНК. Вирус инкубировали при комнатной температуре в течение 20 минут, и в общем объеме 500 мкл медленно добавляли по стенкам в лунки, содержащие HEK293T. Очищенные Т-клетки активировали в среде X-Vivo-15 (Lonza), дополненной 100 МЕ/мл IL-2 человека (Miltenyi Biotec), 10% FBS (Hyclone или JR Scientific), и с добавлением гранул CD2/CD3/CD28 для активации Т-клеток человека при соотношении гранула:клетка 1:2 (Miltenyi Biotec). В день 2 среду из каждой лунки 6-луночного планшета заменяли на 2 мл на лунку средой для трансдукции Т-клеток, т. е. X-Vivo-15, дополненной 10% FBS. В 3 день Т-клетки ресуспендировали в количестве 0,5 миллиона клеток на мл в 2 мл среды для трансдукции Т-клеток на лунку 6-луночного планшета. Лентивирусные супернатанты клеток HEK293T собирали и пропускали через фильтр 0,45 микрон (EMD Millipore) с удалением клеточного дебриса, а затем добавляли к Т-клеткам вместе со 100 МЕ/мл IL-2 человека. В день 6 эффективность трансдукции определяли путем выявления сигнала GFP с помощью проточной цитометрии. Клетки размножали в больших колбах или сосудах G-Rex (Wilson Wolf) при необходимости, используя среду для размножения Т-клеток, т. е. X-Vivo-15, дополненную 5% сыворотки крови группы AB человека (Gemini Bio).
Экспрессия CD70 и Т-клеточные субпопуляции в CAR-Т-клетках
В 13 день после активации трансдуцированные CAR-Т-клетки окрашивали антителом к CD70 человека, конъюгированным с PE, и антителом к CD62L человека, конъюгированным с BV605, и анализировали на проточном цитометре с получением процентной доли популяций CD70+ и CD62L+ для каждого CAR. Затем размноженные CAR-Т-клетки замораживали в FBS, содержащей 10% DMSO (Sigma Aldrich), для дальнейшего использования в функциональных анализах.
Таблица 8
(%)
(%)
(%)
Таблица 8 Фенотип CAR-Т-клеток на 13 день после активации использовали для определения характеристик CAR фага и гибридомы in vitro. Популяцию CAR+ определяли путем гейтирования по CD3+ клеткам; популяцию, экспрессирующую CD70, определяли путем гейтирования живых CD3+ клеток; популяцию, экспрессирующую CD62L, определяли путем гейтирования живых CD3+ CAR+ CD8+ клеток.
Исследуемые конструкции на основе CAR показали различные уровни эффективности трансдукции. Клоны, которые в результате давали низкую эффективность трансдукции, считались менее желательными, поскольку они будут менее подходящими для крупномасштабного производства. CAR-Т-клеточные продукты также демонстрировали разный фенотип (измеренный по экспрессии CD62L) и разные уровни экспрессии CD70 на поверхности. Как правило, CAR-Т-клетки, которые экспрессировали более высокие уровни CD62L, считались более желательными, поскольку они, вероятно, являются менее дифференцированными.
Пример 4. Стресс-тест с фаговыми CAR
Получали CAR-Т-клетки с 12 разными scFv из фаговой библиотеки, и их замораживали так, как это описано в предыдущем примере. Данные CAR-Т-клетки затем оттаивали и смешивали с клетками-мишенями Raji, которые, как известно, экспрессируют CD70, при соотношении эффектор:мишень (E:T), составляющем 1:1, в RPMI, дополненной 10% FBS. После чего клетки Raji добавляли к CAR-T-клеткам каждые 2 дня, чтобы поддерживать соотношение E:T 1:1. Процентную долю лизиса клеток-мишеней и кратность увеличения количества эффекторных CAR-Т-клеток определяли в каждый момент времени.
Стресс-тест представляет собой скрининговый анализ, который включает повторяющееся воздействие CAR-Т-клеток на их мишень, что вызывает пролиферацию CAR, а в некоторых случаях дифференцировку и истощение. Стресс-тест использовали для отбора оптимальных клонов с высоким уровнем лизиса клеток-мишеней и пролиферативными способностями после нескольких циклов воздействия на клетки-мишени.
Материалы и способы
В день 0 CAR-Т-клетки, полученные с 12 разными scFv из фаговой библиотеки, размораживали и смешивали с клетками Raji при соотношении Е:Т 1:1. В день 2 200 мкл клеток из анализа смешивали с 50 мкл гранул для подсчета клеток (CountBright, Invitrogen) и анализировали на проточном цитометре. Для определения общего количества GFP+ CAR-Т-клеток (гейтированных по CD3+) и клеток Raji (гейтированных по CD3-) для каждой CAR-обработки использовали гранулы для подсчета. На основании общего количества CAR-Т-клеток рассчитывали количество клеток Raji, необходимое для поддержания соотношения E:T 1:1, и их добавляли в соответствующую лунку для анализа. Данный процесс повторяли в день 5 и день 7. Процентную долю лизиса клеток-мишеней рассчитывали в каждый момент времени путем вычисления процентной доли живых клеток Raji для каждой CAR-обработки с последующей нормализацией к нетрансдуцированному контролю. Кратность увеличения количества CAR-Т-клеток по сравнению с количеством CAR-Т-клеток, высеянных в день 0, рассчитывали в каждый момент времени.
Оптимальными клонами считали клоны с наивысшим уровнем лизиса клеток-мишеней и наибольшей кратностью увеличения их количества в конце анализа на 7 день, например P08F08.
Таблица 9
Таблица 9. Лизис клеток-мишеней и кратность увеличения количества CAR-Т-клеток в стресс-тесте использовали для in vitro определения характеристик фаговых CAR. Фенотип CAR-Т-клеток определяли на 13 день после активации, а затем на 14 день клетки замораживали. Стресс-тест проводили с использованием размороженных CAR-Т-клеток с клетками-мишенями Raji при соотношении E:T 1:1. Лизис клеток-мишеней определяли с помощью проточной цитометрии путем гейтирования клеток-мишеней CD3- через 2, 5 и 7 дней после совместного культивирования с CAR-Т-клетками. Кратность увеличения количества CAR-Т-клеток определяли с использованием гранул для подсчета клеток и расчета количества клеток в дни 2, 5 и 7 по сравнению с количеством клеток, добавленных в начале анализа. CAR, выделенные жирным шрифтом, демонстрируют высокий уровень лизиса клеток-мишеней и кратность увеличения количества.
Пример 5. Повторение стресс-теста с оптимальными CAR, полученными от второго донора
Получали и замораживали CAR-Т-клетки (P07D03, P08F08, P08G02, P15D02) с 4 scFv из фаговой библиотеки и с 2 scFv из гибридомной библиотеки (4F11, 17G6) так, как это описано в примере 3. Данные CAR-Т-клетки затем оттаивали и смешивали с клетками-мишенями Raji, которые, как известно, экспрессируют CD70, при соотношении эффектор:мишень (E:T), составляющем 1:1, в RPMI, дополненной 10% FBS. После чего клетки Raji добавляли к CAR-T-клеткам каждые 2 дня, чтобы поддерживать соотношение E:T 1:1. Процентную долю лизиса клеток-мишеней и кратность увеличения количества эффекторных CAR-Т-клеток определяли в каждый момент времени.
Все клоны показали хорошие результаты в отношении лизиса клеток-мишеней. P08F08 и 4F11 характеризовались отличными показателями кратности увеличения количества.
Таблица 10
(%)
(%)
(%)
Таблица 10. Лизис клеток-мишеней и кратность увеличения количества CAR-Т-клеток в стресс-тесте использовали для in vitro определения характеристик оптимальных CAR. Фенотип CAR-Т-клеток определяли на 14 день после активации, а затем в тот же день клетки замораживали. Стресс-тест проводили с использованием размороженных CAR-Т-клеток с клетками-мишенями Raji при соотношении E:T 1:1. Лизис клеток-мишеней определяли с помощью проточной цитометрии путем гейтирования клеток-мишеней CD3- через 2, 5 и 7 дней после совместного культивирования с CAR-Т-клетками. Кратность увеличения количества CAR-Т-клеток определяли с использованием гранул для подсчета клеток и расчета количества клеток в дни 2, 5 и 7 по сравнению с количеством клеток, добавленных в начале анализа. CAR, выделенные жирным шрифтом, демонстрируют высокий уровень лизиса клеток-мишеней и кратность увеличения количества.
Пример 6. Дозозависимая in vivo эффективность CAR-T в подкожной опухолевой модели RCC
CAR-Т-клетки получали из scFv 4F11 так, как это описано в примере 3. Мышам NOD scid gamma (NSG) подкожно имплантировали опухоли 786-O, и как только опухоли достигали объема 200 мм3, мышей обрабатывали CAR-Т-клетками 4F11 в различных дозах посредством внутривенной инъекции в хвостовую вену для определения оптимальной дозы CAR-T-клеток. Клетки 786-O доступны в ATCC® под названием CRL-1932™. CAR-T-клетки 4F11 были высокоэффективными in vivo и вызывали полную регрессию опухоли в дозе 5×106 CAR-T-клеток.
Материалы и способы
Пятьдесят мышей NOD scid gamma (NSG) обривали и готовили к подкожной имплантации опухоли на правый бок. Опухолевые клетки 786-O, которые, как известно, экспрессируют CD70, размножали в RPMI, дополненной 10% FBS. В день 0 клетки 786-O ресуспендировали в бессывороточной RPMI в концентрации, необходимой для введения 5 миллионов клеток на животное. Опухолевые клетки инъецировали подкожно в 100 мкл бессывороточной RPMI в комбинации со 100 мкл Matrigel (Corning) на животное. Показатели веса тела исходного уровня в день 0 у всех животных регистрировали сразу же после имплантации опухоли. Размер опухоли измеряли дважды в неделю, начиная с дня 9, с использованием электронно-цифровых штангельциркулей (Mitutoyo) и регистрировали показатели веса тела. В день 14, когда опухоли достигали 200 мм3 (стандартная погрешность 8,39), 40 мышей, несущих опухоль, рандомизировали в 4 группы по 10 мышей в каждой. 4F11 CAR-Т-клетки оттаивали в RPMI, дополненной 10% FBS, и ресуспендировали в бессывороточной RPMI при концентрации, необходимой для инъекции 1, 3 или 5 миллионов CAR+ Т-клеток на животное (рассчитано на основе эффективности трансдукции у 4F11, составляющей 57,2%). Количество нетрансдуцированных Т-клеток (NTD), необходимое для поддержания равного общего количества Т-клеток в каждой группе, рассчитывали и добавляли к соответствующим образцам. CAR-Т-клетки или контрольные нетрансдуцированные Т-клетки вводили в 200 мкл бессывороточной RPMI на животное внутривенно в хвостовую вену. Опухоли измеряли и показатели веса тела регистрировали два раза в неделю до дня 43, когда группа NTD достигала конечной точки исследования (объем опухоли 1500 мм3).
Показатели объема опухолей (среднее значение и погрешность SEM) наносили на график с использованием GraphPad Prism, при этом статистические данные рассчитывали с использованием однофакторного дисперсионного анализа с повторными измерениями (см. фиг. 1 и фиг. 2). Хотя опухоли были полностью устранены с помощью дозы CAR, составляющей 5 миллионов, доза 1 миллион CAR+ не показала эффективность по сравнению с группой NTD. Таким образом, дозу CAR+, составляющую 3 миллиона, выбрали в качестве оптимальной дозы для дальнейших исследований in vivo.
Пример 7. In vivo сравнение CAR к CD70 с TALEN-опосредованным нокаутом по CD70 или без него в клетках 786-O
4F11 и P08F08 CAR-Т-клетки получали так, как это описано в примере 1, с электропорацией ДНК TALEN CD70 или без нее в день 6 после активации. Мышам NSG подкожно имплантировали опухоли 786-O, и после того, как опухоли достигали объема 200 мм3, мышей обрабатывали CAR-Т-клетками посредством внутривенной инъекции в хвостовую вену для определения CAR и условия с наиболее оптимальной эффективностью. CAR-T-клетки P08F08 были высокоэффективными in vivo и вызывали полную регрессию опухоли при дозе CAR-T-клеток, составляющей 3×106, независимо от нокаута CD70 (KO). 4F11 CAR-Т-клетки показали высокую эффективность при нокауте CD70, но в отсутствие нокаута CD70 они лишь контролировали рост опухоли. Эти результаты дают возможность предположить, что нокаут CD70 может повысить активность CAR к CD70.
Материалы и способы
Семьдесят пять мышей NSG обривали и их готовили к подкожной имплантации опухоли на правый бок. Опухолевые клетки 786-O, которые, как известно, экспрессируют CD70, размножали в RPMI, дополненной 10% FBS. В день 0 клетки 786-O ресуспендировали в бессывороточной RPMI в концентрации, необходимой для введения 5 миллионов клеток на животное. Опухолевые клетки инъецировали подкожно в 100 мкл бессывороточной RPMI в комбинации со 100 мкл Matrigel (Corning) на животное. Показатели веса тела исходного уровня в день 0 у всех животных регистрировали сразу же после имплантации опухоли. Размер опухоли измеряли дважды в неделю, начиная с дня 7, с использованием электронно-цифровых штангельциркулей (Mitutoyo) и регистрировали показатели веса тела. В день 20, когда опухоли достигали 200 мм3 (стандартная погрешность 9,69), 60 мышей, несущих опухоль, рандомизировали в 6 групп по 10 мышей в каждой. В день 21 CAR-Т-клетки оттаивали в RPMI, дополненной 10% FBS, и ресуспендировали в бессывороточной RPMI в количестве, составляющем 3 миллиона CAR+ Т-клеток на животное (рассчитано на основе индивидуальных показателей эффективности трансдукции). Количество клеток NTD, необходимое для поддержания равной процентной доли CAR+ Т-клеток, а также равного количества общих Т-клеток в каждой группе, рассчитывали и добавляли к соответствующим образцам. CAR-Т-клетки или контрольные NTD вводили в 200 мкл бессывороточной RPMI на животное внутривенно через хвостовую вену. Опухоли измеряли и показатели веса тела регистрировали два раза в неделю до дня 56, когда группа NTD достигала конечной точки исследования (объем опухоли 1500 мм3) (см. фиг. 3 и фиг. 4).
Показатели объема опухолей (среднее значение и погрешность SEM) наносили на график с использованием GraphPad Prism, при этом статистические данные рассчитывали с использованием однофакторного дисперсионного анализа с повторными измерениями. В группах CAR-T P08F08, как с нокаутом по CD70, так и без него была достигнута полная регрессия опухоли при дозе CAR+, составляющей 3 миллиона. В группе CAR-T 4F11 с нокаутом по CD70 также была достигнута полная регрессия опухоли при дозе CAR+, составляющей 3 миллиона. Однако группа CAR-T 4F11 без нокаута по CD70 не вызывала полной регрессии.
На фиг. 3 и фиг. 4 статистическая значимость по сравнению с соответствующим контролем NTD приведена справа от пояснений (например, P08F08 с KO по CD70 по сравнению с NTD с KO по CD70). Статистическая значимость для каждой группы CAR с KO по CD70 по сравнению с соответствующей группой CAR без КО по CD70 приведена слева от пояснений. Статистика представляет собой однофакторный дисперсионный анализ RM с апостериорным критерием Даннета (ns (не значимо) p>0,05, *p<0,05, **p<0,01, ***p<0,001, ****p<0,0001).
Пример 8. In vivo сравнение CAR к CD70 с TALEN-опосредованным нокаутом по CD70 или без него в опухолевой модели ACHN с метастазами
4F11 CAR-Т-клетки и P08F08 из примера 7 дополнительно тестировали на клетках ACHN, полученных из клеток почечно-клеточного рака (RCC). Клетки ACHN описаны в Simmons et al. Animal Models of Bone Metastasis. Veterinary Pathology 52:827-841, 834 (2015). Каждой из мышей NSG внутривенно имплантировали 1 миллион опухолевых клеток ACHN, и через 15 дней после инъекции опухолевых клеток мышам внутривенно вводили CAR-Т-клетки посредством инъекции в хвостовую вену для определения CAR и условия с наиболее оптимальной эффективностью. CAR-Т-клетки 4F11, введенные в дозе 3 миллиона CAR+ клеток на мышь, являлись эффективными у всех 3 исследованных доноров независимо от нокаута по CD70 (KO). CAR-Т-клетки P08F08 не продемонстрировали какой-либо эффективности, и их тестировали лишь в отсутствие нокаута по CD70.
Материалы и способы
Сорок пять мышей NSG готовили для внутривенного введения опухоли через хвостовую вену. Опухолевые клетки ACHN, которые, как известно, экспрессируют CD70, размножали в MEM, дополненной 10% FBS. В день 0 опухолевые клетки ACHN ресуспендировали в бессывороточной МЕМ в концентрации, необходимой для введения 1 миллиона клеток на животное. Опухолевые клетки ACHN вводили внутривенно в 200 мкл бессывороточной среды MEM. Показатели веса тела исходного уровня в день 4 регистрировали у всех животных. Поток опухолевых клеток измеряли дважды в неделю, начиная с дня 7, с использованием биолюминесценции (IVIS Spectrum Imager™ от PerkinElmer™; автоэкспозиция с максимальным временем экспозиции 120 секунд), и регистрировали показатели веса тела. В день 20, когда опухоли достигали 200 мм3 (стандартная погрешность 9,69), 20 мышей, несущих опухоль, рандомизировали в 4 группы по 5 мышей в каждой. В день 15 CAR-Т-клетки оттаивали в МЕМ, дополненной 10% FBS, и ресуспендировали в бессывороточной МЕМ в количестве, составляющем 3 миллиона CAR+ Т-клеток на животное (рассчитано на основе индивидуальных показателей эффективности трансдукции). Количество клеток NTD, необходимое для поддержания равной процентной доли CAR+ Т-клеток, а также равного количества общих Т-клеток в каждой группе, рассчитывали и добавляли к соответствующим образцам. CAR-Т-клетки или контрольные NTD вводили в 200 мкл бессывороточной МЕМ на животное внутривенно через хвостовую вену. Измеряли поток опухолевых клеток и регистрировали показатели веса тела дважды в неделю до дней 35-49, когда группа NTD достигала конечной точки исследования (потеря веса тела> 20%) (см. фиг. 5a, 5b и 5c).
Показатели биолюминесценции (среднее значение и погрешность SEM) наносили на график с использованием GraphPad Prism, при этом статистические данные рассчитывали с использованием однофакторного дисперсионного анализа с повторными измерениями. Группы CAR-T 4F11, как с нокаутом по CD70, так и без него продемонстрировали противоопухолевую эффективность при дозе CAR+, составляющей 3 миллиона. Группа CAR-T P08F08 без нокаута по CD70 продемонстрировала незначительную эффективность или ее отсутствие при дозе CAR+, составляющей 3 миллиона.
Пример 9. Активность CAR-Т-клеток, специфических к CD70, экспрессирующих эпитопы CD20
Часть A: активность in vitro
CAR-Т-клетки, специфические к CD70, экспрессирующие эпитопы CD20, являются эффективными против клеток-мишеней 786-0 в киллинг-анализе клеток.
Сконструировали шесть форматов CAR, специфических к CD70 (фиг. 6A - 6F). Последовательности сконструированных CAR показаны в таблицах 11A - 11F:
таблица 11A
(фиг. 6A)
Таблица 11B
(фиг. 6B)
Таблица 11C
(фиг. 6C)
Таблица 11D
(фиг. 6D)
Таблица 11E
(фиг. 6E)
Тестирование проводили в отношении следующего: контроль NTD; формат RSRQR (показанный выше и схематически на фиг. 6C) для 4F11 CAR; формат SR2 (показан выше и схематически на фиг. 6B) для P08F08 CAR; формат R2S (показан выше и схематически на фиг. 6F) для P08F08 CAR и формат RSR-short (показан выше и схематически на фиг. 6E) для P08F08 CAR.
Получали CAR-Т-клетки, которые экспрессируют каждый из форматов CAR. Эти CAR-Т-клетки затем оттаивали и смешивали с клетками-мишенями 786-0, которые, как известно, экспрессируют CD70, при соотношении эффектор:мишень (E:T), составляющем 3:1, 1:1, 1:3 или 1:9 (или 0 контроль), в RPMI, дополненной 10% FBS. Определяли процентную долю лизиса клеток-мишеней и кратность увеличения количества эффекторных CAR-Т-клеток (фиг. 7).
Процентную долю лизиса клеток-мишеней рассчитывали в каждый момент времени путем вычисления процентной доли живых клеток 786-0 для каждой CAR-обработки с последующей нормализацией к необработанному контролю. Кратность увеличения количества CAR-Т-клеток по сравнению с количеством CAR-Т-клеток, высеянных в день 0, рассчитывали в каждый момент времени.
Данные результаты демонстрируют, что CAR-T-клетки, специфические к CD70, экспрессирующие эпитопы CD20, могут эффективно уничтожать клетки-мишени при соотношениях E:T 3:1, 1:1, 1:3 и 1:9 и при соотношениях в диапазонах между ними, а также потенциально при соотношениях, выходящих за пределы диапазона от 3:1 до 1:9, которые не тестировали в данном эксперименте.
Часть B: чувствительность к ритуксимабу in vivo
Истощение CAR-Т-клеток, специфических к CD70, после введения ритуксимаба обеспечивает восстановление лимфоцитов, экспрессирующих CD70, у мышей NSG.
На мышах тестировали способность ритуксимаба, представляющего собой антитело к CD20, опосредовать истощение CAR-Т-клеток, специфических к CD70, экспрессирующих эпитопы CD20, и способствовать восстановлению лимфоцитов. В данном эксперименте мышей обрабатывали Т-клетками, экспрессирующими либо CAR, специфический к CD70, который может связываться с белком CD70 мыши на поверхности лимфоцитов (α-мышиные CD70 CAR-T) и содержащий эпитоп CD20, распознаваемый ритуксимабом, либо контрольный CAR, который в незначительной степени связывается с белком FLT3 мыши. Анализ лимфоцитов с помощью проточной цитометрии использовали для демонстрации цитотоксической активности CAR-T-клеток в отношении лимфоцитов, экспрессирующих CD70, что проявляется в уменьшении количества лимфоцитов по сравнению с мышами, получавшими контрольные CAR-T-клетки, или с необработанными мышами. После подтверждения киллинг-активности CAR-Т-клеток мышам вводили ритуксимаб в течение четырех последовательных дней, а циркулирующие в крови остаточные CAR-Т-клетки подсчитывали с помощью проточной цитометрии в день 13. CAR-Т-клетки, специфические к CD70, в крови у этих мышей истощены по сравнению с контрольной группой, которая не получала ритуксимаб. И в завершении, анализ лимфоцитов посредством проточной цитометрии показал, что только у мышей, получавших ритуксимаб (день 20), наблюдалось восстановление лимфоцитов.
Данный эксперимент демонстрирует, что ритуксимаб-зависимое истощение CAR-Т-клеток, специфических к CD70, которые экспрессируют эпитопы CD20, ослабевает повреждение тканей, экспрессирующих CD70, обеспечивая быстрое восстановление лимфоцитов.
Пример 10. Активность CAR-Т-клеток, специфических к CD70
Уничтожение клеток-мишеней оценивали с использованием того же анализа и экспериментальных параметров, аналогичных описанным в примере 9, части A. Тестируемыми линиями были 786-0, ACHN и REH (линия клеток острого лимфоцитарного лейкоза человека). Клеточная линия REH демонстрировала лучшую дифференцировку CAR-Т-клеток, специфических к CD70, поэтому ее можно использовать для ранжирования scFv во всех дальнейших экспериментах. На фиг. 8A - 8D показано уничтожение клеток 786-0 (фиг. 8A), ACHN (фиг. 8B) или REH (фиг. 8C) с использованием CAR-Т-клеток, специфических к CD70, где внеклеточный домен CAR содержит scFv, указанный в пояснениях (фиг. 8D). Во всех экспериментах использовали «голый» формат CAR.
В таблице 12 представлены основные данные для фиг. 8A - 8D и дополнительно измеренная процентная доля положительных клеток для флуоресцентно меченых антител к CD70, CD25 и 4-1BB (маркеры активации); процентная доля стволовых Т-клеток памяти (TSCM), процентная доля BFP (CAR+) перед проведением анализа цитотоксичности.
Таблица 12
На фиг. 9A показана эффективность CAR, специфических к CD70, при повторном воздействии на меченные люциферазой клетки-мишени 786-O (CAR-T-клетки переносили в 96-луночный планшет, содержащий свежие мишени, каждые 2-3 дня). Соотношение E:T составляло 3:1. CAR экспрессировали в клетках от донора D503. Аналогично результатам, описанным в примере 4, для in vitro определения характеристик CAR scFv использовали лизис клеток-мишеней в стресс-тесте.
На фиг. 9В показана эффективность CAR, специфических к CD70, при повторном воздействии на меченные люциферазой клетки-мишени ACHN (CAR-T-клетки переносили в 96-луночный планшет, содержащий свежие мишени, каждые 2-3 дня). Соотношение E:T составляло 10:1. CAR экспрессировали в клетках от донора D503. Аналогично результатам, описанным в примере 4, для in vitro определения характеристик CAR scFv использовали лизис клеток-мишеней в стресс-тесте.
На фиг. 9С показана эффективность CAR, специфических к CD70, при повторном воздействии на клетки-мишени REH, меченные люциферазой (2×106 клеток добавили в указанные моменты времени). Соотношение E:T составляло 1:5. CAR экспрессировали в клетках от донора D503. Аналогично результатам, описанным в примере 4, для in vitro определения характеристик CAR scFv использовали лизис клеток-мишеней в стресс-тесте.
На фиг. 10 показана эффективность CAR, специфических к CD70, в различных форматах (как указано в примере 9, части А) при повторном воздействии на клетки-мишени REH, меченные люциферазой (2×106 клеток добавили в указанные моменты времени). Соотношение E:T составляло 1:5. Аналогично результатам, описанным в примере 4, для in vitro определения характеристик CAR scFv использовали лизис клеток-мишеней в стресс-тесте.
Пример 11. In vivo сравнение CAR CD70 в модели ACHN с метастазами
CAR-Т-клетки, содержащие различные scFv CD70, получали и тестировали на клетках ACHN, клеточной линии, полученной из клеток почечно-клеточного рака (RCC). Клетки ACHN описаны в Simmons et al. Animal Models of Bone Metastasis. Veterinary Pathology 52:827-841, 834 (2015). Каждой из мышей NSG внутривенно имплантировали 1 миллион опухолевых клеток ACHN, и через 15 дней после инъекции опухолевых клеток мышам внутривенно вводили CAR-Т-клетки посредством инъекции в хвостовую вену для определения CAR и условия с наиболее оптимальной эффективностью. CAR-Т-клетки 12C5, введенные в дозе 3 миллиона CAR+ клеток на мышь, продемонстрировали наилучшую эффективность.
Материалы и способы
сорок пять мышей NSG готовили для внутривенного введения опухоли через хвостовую вену. Опухолевые клетки ACHN, которые, как известно, экспрессируют CD70, размножали в MEM, дополненной 10% FBS. В день 0 опухолевые клетки ACHN ресуспендировали в бессывороточной МЕМ в концентрации, необходимой для введения 1 миллиона клеток на животное. Опухолевые клетки ACHN вводили внутривенно в 200 мкл бессывороточной среды MEM. Показатели веса тела исходного уровня в день 4 регистрировали у всех животных. Поток опухолевых клеток измеряли дважды в неделю, начиная с дня 7, с использованием биолюминесценции (IVIS Spectrum Imager™ от PerkinElmer™; автоэкспозиция с максимальным временем экспозиции 120 секунд), и регистрировали показатели веса тела. В день 20, когда опухоли достигали 200 мм3 (стандартная погрешность 9,69), 35 мышей, несущих опухоль, рандомизировали в 7 групп по 5 мышей в каждой. В день 15 CAR-Т-клетки оттаивали в МЕМ, дополненной 10% FBS, и ресуспендировали в бессывороточной МЕМ в количестве, составляющем 3 миллиона CAR+ Т-клеток на животное (рассчитано на основе индивидуальных показателей эффективности трансдукции). Количество клеток NTD, необходимое для поддержания равной процентной доли CAR+ Т-клеток, а также равного количества общих Т-клеток в каждой группе, рассчитывали и добавляли к соответствующим образцам. CAR-Т-клетки или контрольные NTD вводили в 200 мкл бессывороточной МЕМ на животное внутривенно через хвостовую вену. Измеряли поток опухолевых клеток и регистрировали показатели веса тела дважды в неделю до дня 32, когда группа NTD достигала конечной точки исследования (потеря веса тела> 20%) (см. фиг. 11).
Показатели биолюминесценции (среднее значение и погрешность SEM) наносили на график с использованием GraphPad Prism, при этом статистические данные рассчитывали с использованием однофакторного дисперсионного анализа с повторными измерениями. Группа CAR-T 12C5 продемонстрировала противоопухолевую эффективность при дозе CAR+, составляющей 3 миллиона.
Пример 12. Уровни экспрессии CD70 в образцах RCC, полученных от пациентов, и лизис образцов RCC, полученных от пациентов, CAR-Т-клетками, специфическими к CD70
Образцы первичных клеток от пациентов с RCC получали из Conversant Bio (замороженные диссоциированные опухолевые клетки) или из CHTN Western/NDRI (свежие фрагменты опухоли, которые затем подвергали диссоциации на месте отбора в лабораторных условиях с использованием набора для диссоциации опухолей человека Miltenyi MACS и GentleMACS). Первичные опухолевые клетки поддерживали в RPMI, дополненной 20% FBS. Для определения экспрессии белка CD70 на клеточной поверхности в этих клетках наряду с соответствующими линиями клеток RCC, авторы настоящего изобретения проводили проточную цитометрию и количественное определение рецепторов с использованием антитела к CD70, конъюгированного с фикоэритрином при соотношении 1:1. Рецепторы клеточной поверхности количественно определяли с использованием гранул Quantibrite от BD Biosciences, а значения связывающей способности антител (ABC) рассчитывали в соответствии с рекомендациями производителя. CD70-специфические CAR-Т-клетки получали так, как это описано ранее, и их цитотоксичность к первичным клеткам RCC и линии клеток RCC ACHN оценивали с использованием того же анализа и экспериментальных параметров, аналогичных описанным в примере 9, части А.
Результаты
Подтвердили, что первичные клетки RCC экспрессируют CD70 со значениями ABC, варьирующими в диапазоне от ~2000 рецепторов CD70 на клетку (рецепторы/клетка) до ~25000 рецепторов/клетка (фиг. 12B), с экспрессией на линиях клеток RCC, варьирующей в диапазоне от ~25000 рецепторов/клетка до ~400000 рецепторов/клетка (фиг. 12A). Авторы настоящего изобретения также подтвердили, что клетки, экспрессирующие 7000 рецепторов CD70 на клетку (рецепторы/клетка) (фиг. 13B), 24000 рецепторов/клетка (фиг. 13A) или 40000 рецепторов/клетка (фиг. 13C), эффективно уничтожаются посредством CD70-специфических CAR-Т-клеток, в которых CAR получен либо из scFv 4F11, либо из P08F08.
Пример 13. Уровни экспрессии CD70 на различных гематологических опухолевых клеточных линиях и лизис данных клеток посредством CAR-Т-клеток, специфических к CD70
Охарактеризовали способность нацеливать CD70 на целый ряд гемовых опухолей, в том числе на лимфомы, лейкозы и миеломы. Определение характеристик включало анализ экспрессии как РНК CD70, так и белка клеточной поверхности при множественных злокачественных новообразованиях с последующим анализом эффективности CAR-Т-клеток в отношении клеточных линий.
Результаты
Анализ экспрессии РНК при остром миелоидном лейкозе (AML), остром лимфобластном лейкозе (ALL), неходжкинской лимфоме (NHL) и множественной миеломе (клетки MM) с использованием Атласа ракового генома (TCGA) показал, что экспрессия CD70 может наблюдаться для всех 4 типов рака, что указывает на потенциальную применимость целенаправленного воздействия на данные виды рака с помощью CD70-специфических CAR-Т-клеток. Чтобы определить экспрессию белка CD70 на клеточной поверхности при данных видах рака, авторы настоящего изобретения проводили проточную цитометрию и количественную оценку рецепторов на панели клеточных линий, полученных из выбранных типов опухолей. Паттерны экспрессии белков клеточной поверхности были аналогичны анализам РНК, подтверждающим, что экспрессия CD70 широко распространена в клеточных линиях всех типов опухолей (фиг. 14A). Затем авторы настоящего изобретения получали CAR-Т-клетки, специфические к CD70, для проверки их эффективности в анализе цитотоксичности in vitro в отношении тех же клеточных линий. CAR-Т-клетки, специфические к CD70, проявляли устойчивую специфическую активность в отношении клеток-мишеней, экспрессирующих антиген CD70 (фиг. 14B). Различные клеточные линии могут быть уничтожены посредством CAR, специфических к CD70, (фиг. 14B), что указывает на то, что CAR, специфические к CD70, могут уничтожать даже те клетки, которые экспрессируют CD70 на низком уровне. Это демонстрирует, что активность CAR, специфических к CD70, не ограничена конкретными типами клеток. И наконец, авторы настоящего изобретения показали, что данные CAR эффективны в отношении линии клеток MM1S в in vivo анализе, проводимом так, как это показано в примере 7 (фиг. 15A и фиг. 15B). MM1S представляет собой линию клеток множественной миеломы, экспрессирующую умеренное количество рецепторов CD70 на клетку (фиг. 14A). И в заключение, было отмечено, что CD70 имеет широкий профиль экспрессии в целом ряде гематологических злокачественных новообразований. Использование CD70-специфических CAR-T-клеток по отдельности или в комбинации с другими мишенями, связанными с гемом, дает возможность целенаправленного воздействия на опухолевый антиген или предотвращать его ускользание при широком диапазоне гематологических злокачественных новообразований.
Пример 14. Определение кинетических параметров и аффинности взаимодействий антител к CD70/CD70 человека при 37°C
В данном примере определяли кинетические параметры связывания и/или аффинность разных антител к CD70 к CD70 человека. ScFv получали путем клонирования вариабельных областей антител к CD70, фланкирующих линкер (GGGGS)4 (SEQ ID NO: 602), а затем части шарнирного участка и Fc из модифицированной последовательности человеческого IgG2, что дало слитую конструкцию scFv-Fc, которую экспрессировали с использованием Expi293, а затем очищали посредством аффинной хроматографии на основе связывания с белком А. Рекомбинантный человеческий CD70 получали путем слияния AviTag™, полигистидиновой метки и домена тримеризации куриного тенасцина с N-концом внеклеточного домена (ECD) человеческого CD70, который экспрессировали с использованием Expi293, затем очищали с помощью аффинной хроматографии с иммобилизованными ионами металлов (IMAC) с последующей эксклюзионной хроматографией (SEC) при необходимости.
Кинетические параметры связывания антител определяли с помощью поверхностного плазмонного резонанса (Biacore 8K, GE Healthcare Bio-Sciences, Питтсбург, Пенсильвания) при 37°C в HBS-T+ (0,01 M HEPES, pH 7,4, 0,15 M NaCl, 0,05% об./об. Tween20, 1 мг/мл BSA). Рекомбинантный человеческий CD70, разведенный в HBS-T+, подвергали захвату на чипе C1, на котором было иммобилизовано антитело с меткой AviTag™. Очищенные слитые конструкции на основе scFv-Fc к CD70 последовательно разводили в HBS-T+, вводили со скоростью 30 мкл/мин в течение 2-4 минут, диссоциацию отслеживали в течение 10 минут, а затем поверхность регенерировали 75 мМ фосфорной кислотой между введениями. Буферы в ходе циклов отбирали для каждой слитой конструкции на основе scFv-Fc к CD70 с целью осуществления двойного контроля («двойной контроль» описан в Myszka, D.G. Improving biosensor analysis. J. Mol. Recognit. 12, 279-284 (1999)). Кинетические константы скорости ассоциации (kon) и константы скорости диссоциации (koff) получали одновременно путем глобального согласования сенсограмм с двойным контролем с моделью Ленгмюра 1:1 с моделью массопереноса с использованием программного обеспечения Biacore 8K Evaluation Software (GE Healthcare Bio-Sciences, Питтсбург, Пенсильвания), а затем их использовали для расчета равновесной константы диссоциации (KD) из кинетических констант скорости реакции (KD=koff/kon). Данные согласовывали с моделью аффинности в стационарном состоянии 1:1 с использованием программного обеспечения Biacore 8K Evaluation Software для определения равновесной константы диссоциации в стационарном состоянии (SS KD) по мере необходимости.
Кинетические параметры связывания и параметры аффинности для тестируемых антител к CD70 показаны в таблице 13. Антитела, показанные в таблице 13, имеют ту же последовательность scFv, что и CAR, показанные в таблицах 5 и 11 с таким же названием.
Таблица 13
Хотя раскрытые идеи были описаны со ссылкой на различные варианты применения, способы, наборы и композиции, следует понимать, что различные изменения и модификации могут быть сделаны без отклонения от идей данного документа и заявленной формулы изобретения, представленной ниже. Вышеуказанные примеры предусмотрены для лучшего иллюстрирования раскрытых идей и не предназначены для ограничения объема идей, представленных в данном документе. Хотя настоящие идеи были описаны в определениях этих иллюстративных вариантов осуществления, специалист в данной области легко поймет, что многочисленные вариации и модификации этих иллюстративных вариантов осуществления возможны без излишних экспериментов. Все такие вариации и модификации находятся в рамках действующих идей.
Все ссылки, цитируемые в данном документе, в том числе патенты, заявки на патенты, научные статьи, пособия и т. п., а также ссылки, цитируемые в них, в той степени, в которой они уже не являются таковыми, включены в данный документ с помощью ссылки в их полном объеме. В случае если одна или более из ссылок на литературные источники и аналогичные материалы отличаются или противоречат данной заявке, включая без ограничения определенные термины, термины относительно использования, описанные методики и т. п., данная заявка имеет преимущественную силу.
В изложенных выше описании и примерах подробно определены некоторые конкретные варианты осуществления настоящего изобретения и описан наилучший способ осуществления, предлагаемый авторами настоящего изобретения. Однако будет понятно, что независимо от того, насколько подробно изложенное выше может быть представлено в тексте, настоящее изобретение может быть реализовано на практике многими путями, и при этом настоящее изобретение следует истолковывать в соответствии с прилагаемой формулой изобретения и любыми ее эквивалентами.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ПФАЙЗЕР ИНК.
<120> ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, НАЦЕЛИВАЮЩИЕСЯ НА CD70
<130> ALGN-014/03WO 333466-2233
<150> US 62/775246
<151> 2018-12-04
<150> US 62/641873
<151> 2018-03-12
<150> US 62/641869
<151> 2018-03-12
<150> US 62/625019
<151> 2018-02-01
<150> US 62/625009
<151> 2018-02-01
<160> 683
<170> PatentIn версии 3.5
<210> 1
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 1
Asp Ile Val Met Thr Gln Asn Pro Leu Ser Ser Pro Val Thr Leu Gly
1. 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asp Gly Asn Thr Tyr Leu Ser Trp Leu Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Ile Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ala Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Thr Gln Phe Pro Leu Thr Ile Gly Gly Gly Ser Lys Val Glu Ile Lys
100 105 110
<210> 2
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 2
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Gly Phe Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Ser Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ile Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Ser Ser Ser Pro Phe Ala Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 3
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 3
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Ser Pro Val Thr Leu Gly
1. 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asp Gly Asn Thr Tyr Leu Ser Trp Leu Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Ile Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ala Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Thr Gln Phe Pro Leu Thr Ile Gly Gly Gly Ser Lys Val Glu Ile Lys
100 105 110
<210> 4
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 4
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Gly Phe Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Val Phe
65 70 75 80
Met Glu Leu Ile Ser Leu Arg Ser Glu Tyr Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Ser Ser Ser Pro Phe Ala Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 5
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 5
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Asn Tyr
20 25 30
Leu Ala Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Lys Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 6
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 6
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1. 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Tyr
20 25 30
Tyr Trp Asn Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Tyr Tyr Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Arg Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Asp Ile Arg Thr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
100 105 110
<210> 7
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 7
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1. 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val Tyr Ser
20 25 30
Asp Glu Asn Thr Tyr Leu Asn Trp Phe Gln Gln Arg Pro Gly Gln Ser
35 40 45
Leu Arg Arg Leu Ile Tyr Gln Val Ser Asn Arg Asp Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Phe Cys Met Gln Gly
85 90 95
Thr Tyr Trp Pro Pro Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 8
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 8
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Asn Ser
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Lys Arg Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gln Thr Gly Ser Phe Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 9
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 9
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Met Ser Leu Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Thr Arg Ala Thr Gly Ile Pro Ala Arg Phe Gly Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Ile Asn Trp Pro His
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 10
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 10
Gln Val Gln Leu Arg Gly Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1. 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Asp Asp Ser Ile Ser Val Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Ala Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Arg Val Tyr Ser Ser Gly Asn Ile Asn Tyr Asn Pro Ser Leu Glu
50 55 60
Ser Arg Val Thr Met Ser Val Asp Thr Ser Lys Ser Arg Phe Ser Leu
65 70 75 80
Asn Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Leu Asp Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr
100 105 110
Val Ser Ser
115
<210> 11
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 11
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ile Leu Ile
35 40 45
Tyr Gly Ala Ser Asn Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Ala Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Gln Tyr Asp Asn Phe Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 12
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 12
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Glu
1. 5 10 15
Ser Leu Arg Leu Ser Cys Glu Val Ser Gly Phe Thr Phe Thr Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ile Ile Ser Gly Val Ala Phe Thr Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp His Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Gly Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Lys Val Asp Gly Glu Val Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 13
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 13
Glu Ile Val Met Thr Gln Ser Pro Asp Thr Leu Ser Val Ser Pro Gly
1. 5 10 15
Glu Arg Ala Ile Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Asn
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Thr Arg Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Ser Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Asp Asn Trp Pro Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 14
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 14
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1. 5 10 15
Ser Val Lys Val Ser Cys Glu Ala Ser Gly Gly Thr Phe Ile Thr Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Phe Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Ser
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Gln Trp Glu Leu Phe Phe Phe Asp Phe Trp Gly Gln Gly Thr Pro
100 105 110
Val Thr Val Ser Ser
115
<210> 15
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 15
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Gln Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Ile Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 16
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 16
Ala Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Tyr Tyr
20 25 30
Ser Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser His Ile Ser Ile Arg Ser Ser Thr Ile Tyr Phe Ala Asp Ser Ala
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ser Gly Trp Tyr Gly Asp Tyr Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 17
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 17
Asp Ile Gln Met Thr Gln Ser Pro Ser Ala Met Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu Ala Trp Phe Gln Gln Lys Pro Gly Lys Val Pro Lys Arg Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Leu Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Leu Asn Ser Phe Pro Phe
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Asn
100 105
<210> 18
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 18
Gln Val Thr Leu Lys Glu Ser Gly Pro Val Leu Val Lys Pro Thr Glu
1. 5 10 15
Thr Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Asn Ala
20 25 30
Arg Met Gly Val Thr Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu
35 40 45
Trp Leu Ala His Ile Phe Ser Asn Asp Glu Lys Ser Tyr Ser Thr Ser
50 55 60
Leu Lys Ser Arg Leu Thr Ile Ser Lys Asp Thr Ser Lys Thr Gln Val
65 70 75 80
Val Leu Thr Met Thr Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Ala Arg Ile Arg Asp Tyr Tyr Asp Ile Ser Ser Tyr Tyr Asp Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Ser Val Ser Ser
115 120
<210> 19
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 19
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Phe Ser Phe Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 20
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 20
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Thr Phe Ser Asn His
20 25 30
Asn Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Ser Tyr Ile Ser Arg Ser Ser Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Ala Gln Trp Tyr Gly Met Asp Val Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 21
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 21
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1. 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Val Leu Tyr Ser
20 25 30
Tyr Asn Asn Lys Asn Tyr Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Asn Leu Leu Ile Phe Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Ser Thr Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 22
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 22
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Val Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Lys Gln Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Val Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Gly Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Val Asn Trp Gly Trp Arg Leu Tyr Trp His Phe Asp
100 105 110
Leu Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 23
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 23
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Val Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Asp Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 24
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 24
Glu Val Gln Val Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ser Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser His Ser Ser Ile Ser Arg Gly Asn Ile Tyr Phe Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ser Gly Trp Tyr Gly Asp Tyr Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 25
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 25
Glu Leu Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro
1. 5 10 15
Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly
20 25 30
Ser Asn Tyr Val Tyr Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys
35 40 45
Leu Leu Ile Tyr Arg Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg
50 55 60
Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly
65 70 75 80
Leu Arg Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp
85 90 95
Ser Leu Ser Gly Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 26
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 26
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ala Phe Ser Asn Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Arg Gly Gly Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Phe Ile Ser Gly Thr Trp Tyr Pro Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 27
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 27
Glu Leu Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro
1. 5 10 15
Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Arg Ser Asn Ile Gly
20 25 30
Ser Asn Tyr Val Tyr Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys
35 40 45
Leu Leu Ile Tyr Arg Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg
50 55 60
Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly
65 70 75 80
Leu Arg Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ser Trp Asp Gly
85 90 95
Ser Leu Ser Ala Val Val Phe Gly Thr Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 28
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 28
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1. 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr Arg Phe Thr Ser Tyr
20 25 30
Trp Ile Gly Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Ser Ile Tyr Pro Asp Asp Ser Asp Thr Arg Tyr Ser Pro Ser Phe
50 55 60
Gln Gly Gln Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Ser Ser Thr Val Asp Tyr Pro Gly Tyr Ser Tyr Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 29
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 29
Glu Leu Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro
1. 5 10 15
Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly
20 25 30
Ser Asn Tyr Val Tyr Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys
35 40 45
Leu Leu Ile Tyr Arg Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg
50 55 60
Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly
65 70 75 80
Leu Arg Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Thr Trp Asp Asp
85 90 95
Ser Leu Gly Ser Pro Val Phe Gly Thr Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 30
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 30
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1. 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Trp Ile Ala Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Tyr Pro Asp Gly Ser Asp Thr Arg Tyr Ser Pro Ser Phe
50 55 60
Gln Gly Gln Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Asp Ile Thr Ser Trp Tyr Tyr Gly Glu Pro Ala Phe Asp Ile
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 31
<211> 110
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 31
Glu Leu Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
1. 5 10 15
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser
20 25 30
Arg Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu
35 40 45
Leu Ile Tyr Ala Ala Ser Ile Leu Gln Thr Gly Val Pro Ser Arg Phe
50 55 60
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
65 70 75 80
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr
85 90 95
Thr Met Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 32
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 32
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1. 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Ser Ser
20 25 30
Trp Ile Gly Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Tyr Pro Gly Asp Ser Asp Thr Arg Tyr Ser Pro Ser Phe
50 55 60
Gln Gly Gln Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Lys Gly Leu Ser Gln Ala Met Thr Gly Phe Gly Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 33
<211> 113
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 33
Glu Leu Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro
1. 5 10 15
Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly
20 25 30
Ser Asn Tyr Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys
35 40 45
Leu Leu Ile Tyr Gly Asp Tyr Gln Arg Pro Ser Gly Val Pro Asp Arg
50 55 60
Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly
65 70 75 80
Leu Arg Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Thr Arg Asp Asp
85 90 95
Ser Leu Ser Gly Ser Val Val Phe Gly Thr Gly Thr Lys Leu Thr Val
100 105 110
Leu
<210> 34
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 34
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1. 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr Gly Phe Thr Ser Tyr
20 25 30
Trp Ile Gly Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile His Pro Asp Asp Ser Asp Thr Lys Tyr Ser Pro Ser Phe
50 55 60
Gln Gly Gln Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Ser Ser Tyr Leu Arg Gly Leu Trp Gly Gly Tyr Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 35
<211> 110
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 35
Glu Leu Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
1. 5 10 15
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Tyr
20 25 30
Asp Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu
35 40 45
Leu Ile Tyr Asp Ala Ser Asn Leu Gln Ser Gly Val Pro Ser Arg Phe
50 55 60
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
65 70 75 80
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Thr Thr
85 90 95
Pro Leu Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 36
<211> 126
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 36
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1. 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr Thr Phe Pro Ser Ser
20 25 30
Trp Ile Gly Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Tyr Pro Asp Thr Ser His Thr Arg Tyr Ser Pro Ser Phe
50 55 60
Gln Gly Gln Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Ala Ser Tyr Phe Asp Arg Gly Thr Gly Tyr Ser Ser Trp Trp
100 105 110
Met Asp Val Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 37
<211> 110
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 37
Glu Leu Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
1. 5 10 15
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Tyr Ile Gly
20 25 30
Arg Tyr Leu Asn Trp Tyr Gln Gln Lys Arg Gly Lys Ala Pro Lys Leu
35 40 45
Leu Ile His Gly Ala Thr Ser Leu Ala Ser Gly Val Pro Ser Arg Phe
50 55 60
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
65 70 75 80
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr
85 90 95
Thr Ser Pro Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 38
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 38
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Gln Tyr
20 25 30
Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Gly Gly Val Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Asp Ile Ser Asp Ser Gly Gly Ser His Trp Tyr Phe Asp Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 39
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 39
Glu Leu Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro
1. 5 10 15
Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Thr Ser Asn Ile Gly
20 25 30
Arg Asn Tyr Val Tyr Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys
35 40 45
Leu Leu Ile Tyr Arg Thr Asn Gln Arg Pro Ser Gly Val Pro Asp Arg
50 55 60
Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly
65 70 75 80
Leu Arg Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp
85 90 95
Ser Leu Ser Gly Arg Val Phe Gly Thr Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 40
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 40
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Thr Ile Ser Gly Thr Gly Gly Thr Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Val Arg Ala Gly Ile Asp Pro Thr Ala Ser Asp Val Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 41
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 41
Glu Leu Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro
1. 5 10 15
Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly
20 25 30
Ser Asn Tyr Val Tyr Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys
35 40 45
Pro Leu Ile Tyr Met Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg
50 55 60
Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly
65 70 75 80
Leu Arg Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp
85 90 95
Ser Leu Ser Ala Val Val Phe Gly Thr Gly Thr Lys Leu Thr Val Leu
100 105 110
<210> 42
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 42
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Asn Phe
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Gly Ser Gly Asp Asn Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Arg Asp Ile Gly Leu Gly Trp Tyr Ser Tyr Tyr Leu Asp
100 105 110
Val Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 43
<211> 113
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 43
Glu Leu Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro
1. 5 10 15
Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Asn Ser Asn Ile Gly
20 25 30
Thr Asn Tyr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys
35 40 45
Leu Leu Ile Tyr Arg Ser Ser Arg Arg Pro Ser Gly Val Pro Asp Arg
50 55 60
Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly
65 70 75 80
Leu Arg Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Gly
85 90 95
Ser Leu Ser Gly His Trp Val Phe Gly Thr Gly Thr Lys Leu Thr Val
100 105 110
Leu
<210> 44
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 44
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Ile Ile Pro Ile Phe Gly Thr Ala Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Gly Trp Asp Asp Ser Trp Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 45
<211> 110
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 45
Glu Leu Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
1. 5 10 15
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Asp
20 25 30
Thr Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu
35 40 45
Leu Ile Tyr Ser Ala Ser Ser Leu His Ser Gly Val Pro Ser Arg Phe
50 55 60
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
65 70 75 80
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr
85 90 95
Thr Ala Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 46
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 46
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1. 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Ala Ser Tyr
20 25 30
Trp Ile Gly Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Val Ile Tyr Pro Gly Thr Ser Glu Thr Arg Tyr Ser Pro Ser Phe
50 55 60
Gln Gly Gln Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Lys Gly Leu Ser Ala Ser Ala Ser Gly Tyr Ser Phe Gln Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 47
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 47
Glu Leu Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
1. 5 10 15
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Gly
20 25 30
Gln Ser Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu
35 40 45
Leu Ile Tyr Gly Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe
50 55 60
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
65 70 75 80
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr
85 90 95
Pro Ile Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 48
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 48
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1. 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Asp Tyr
20 25 30
Trp Ile Gly Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Ser Pro Gly Gly Ser Thr Thr Ile Tyr Arg Pro Ser Phe
50 55 60
Gln Gly Gln Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Glu Met Tyr Thr Gly Gly Tyr Gly Gly Ser Trp Tyr Phe Asp
100 105 110
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 49
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 49
Ser Tyr Gly Phe Ser
1. 5
<210> 50
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 50
Gly Gly Thr Phe Ser Ser Tyr
1. 5
<210> 51
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 51
Gly Gly Thr Phe Ser Ser Tyr Gly Phe Ser
1. 5 10
<210> 52
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 52
Gly Ile Ile Pro Ile Phe Gly Ser Ala Asn Tyr Ala Gln Lys Phe Gln
1. 5 10 15
Gly
<210> 53
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 53
Ile Pro Ile Phe Gly Ser
1. 5
<210> 54
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 54
Gly Gly Ser Ser Ser Pro Phe Ala Tyr
1. 5
<210> 55
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 55
Ser Tyr Gly Phe Ser
1. 5
<210> 56
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 56
Gly Gly Thr Phe Ser Ser Tyr
1. 5
<210> 57
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 57
Gly Gly Thr Phe Ser Ser Tyr Gly Phe Ser
1. 5 10
<210> 58
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 58
Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe Gln
1. 5 10 15
Gly
<210> 59
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 59
Ile Pro Ile Phe Gly Thr
1. 5
<210> 60
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 60
Gly Gly Ser Ser Ser Pro Phe Ala Tyr
1. 5
<210> 61
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 61
Ser Tyr Tyr Trp Asn
1. 5
<210> 62
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 62
Gly Gly Ser Ile Ser Ser Tyr
1. 5
<210> 63
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 63
Gly Gly Ser Ile Ser Ser Tyr Tyr Trp Asn
1. 5 10
<210> 64
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 64
Tyr Ile Tyr Tyr Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys Ser
1. 5 10 15
<210> 65
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 65
Tyr Tyr Ser Gly Ser
1. 5
<210> 66
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 66
Asp Ile Arg Thr Trp
1. 5
<210> 67
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 67
Asn Ser Trp Met Ser
1. 5
<210> 68
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 68
Gly Phe Thr Phe Arg Asn Ser
1. 5
<210> 69
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 69
Gly Phe Thr Phe Arg Asn Ser Trp Met Ser
1. 5 10
<210> 70
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 70
Asn Ile Lys Arg Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val Lys
1. 5 10 15
Gly
<210> 71
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 71
Lys Arg Asp Gly Ser Glu
1. 5
<210> 72
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 72
Asp Gln Thr Gly Ser Phe Asp Tyr
1. 5
<210> 73
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 73
Val Tyr Tyr Trp Ser
1. 5
<210> 74
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 74
Asp Asp Ser Ile Ser Val Tyr
1. 5
<210> 75
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 75
Asp Asp Ser Ile Ser Val Tyr Tyr Trp Ser
1. 5 10
<210> 76
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 76
Val Tyr Ser Ser Gly Asn Ile Asn Tyr Asn Pro Ser Leu Glu Ser
1. 5 10 15
<210> 77
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 77
Tyr Ser Ser Gly Asn
1. 5
<210> 78
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 78
Gly Leu Asp Ala Phe Asp Ile
1. 5
<210> 79
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 79
Ser Tyr Ala Met Ser
1. 5
<210> 80
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 80
Gly Phe Thr Phe Thr Ser Tyr
1. 5
<210> 81
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 81
Gly Phe Thr Phe Thr Ser Tyr Ala Met Ser
1. 5 10
<210> 82
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 82
Arg Val Tyr Ser Ser Gly Asn Ile Asn Tyr Asn Pro Ser Leu Glu Ser
1. 5 10 15
<210> 83
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 83
Tyr Ser Ser Gly Asn
1. 5
<210> 84
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 84
Gly Leu Asp Ala Phe Asp Ile
1. 5
<210> 85
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 85
Thr Tyr Ala Ile Ser
1. 5
<210> 86
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 86
Gly Gly Thr Phe Ile Thr Tyr
1. 5
<210> 87
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 87
Gly Gly Thr Phe Ile Thr Tyr Ala Ile Ser
1. 5 10
<210> 88
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 88
Gly Ile Ile Pro Phe Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe Gln
1. 5 10 15
Gly
<210> 89
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 89
Ile Pro Phe Phe Gly Thr
1. 5
<210> 90
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 90
Trp Glu Leu Phe Phe Phe Asp Phe
1. 5
<210> 91
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 91
Tyr Tyr Ser Met Asn
1. 5
<210> 92
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 92
Gly Phe Thr Phe Thr Tyr Tyr
1. 5
<210> 93
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 93
Gly Phe Thr Phe Thr Tyr Tyr Ser Met Asn
1. 5 10
<210> 94
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 94
His Ile Ser Ile Arg Ser Ser Thr Ile Tyr Phe Ala Asp Ser Ala Lys
1. 5 10 15
Gly
<210> 95
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 95
Ser Ile Arg Ser Ser Thr
1. 5
<210> 96
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 96
Gly Ser Gly Trp Tyr Gly Asp Tyr Phe Asp Tyr
1. 5 10
<210> 97
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 97
Asn Ala Arg Met Gly Val Thr
1. 5
<210> 98
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 98
Gly Phe Ser Leu Ser Asn Ala Arg Met
1. 5
<210> 99
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 99
Gly Phe Ser Leu Ser Asn Ala Arg Met Gly Val Thr
1. 5 10
<210> 100
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 100
His Ile Phe Ser Asn Asp Glu Lys Ser Tyr Ser Thr Ser Leu Lys Ser
1. 5 10 15
<210> 101
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 101
Phe Ser Asn Asp Glu
1. 5
<210> 102
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 102
Ile Arg Asp Tyr Tyr Asp Ile Ser Ser Tyr Tyr Asp Tyr
1. 5 10
<210> 103
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 103
Asn His Asn Ile His
1. 5
<210> 104
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 104
Gly Phe Thr Phe Ser Asn His
1. 5
<210> 105
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 105
Gly Phe Thr Phe Ser Asn His Asn Ile His
1. 5 10
<210> 106
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 106
Tyr Ile Ser Arg Ser Ser Ser Thr Ile Tyr Tyr Ala Asp Ser Val Lys
1. 5 10 15
Gly
<210> 107
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 107
Ser Arg Ser Ser Ser Thr
1. 5
<210> 108
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 108
Asp His Ala Gln Trp Tyr Gly Met Asp Val
1. 5 10
<210> 109
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 109
Ser Tyr Trp Met Ser
1. 5
<210> 110
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 110
Gly Phe Thr Phe Ser Ser Tyr
1. 5
<210> 111
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 111
Gly Phe Thr Phe Ser Ser Tyr Trp Met Ser
1. 5 10
<210> 112
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 112
Ser Ile Lys Gln Asp Gly Ser Glu Lys Tyr Tyr Val Asp Ser Val Lys
1. 5 10 15
Gly
<210> 113
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 113
Lys Gln Asp Gly Ser Glu
1. 5
<210> 114
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 114
Glu Gly Val Asn Trp Gly Trp Arg Leu Tyr Trp His Phe Asp Leu
1. 5 10 15
<210> 115
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 115
Ser Tyr Ser Met Asn
1. 5
<210> 116
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 116
Gly Phe Thr Phe Ser Ser Tyr
1. 5
<210> 117
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 117
Gly Phe Thr Phe Ser Ser Tyr Ser Met Asn
1. 5 10
<210> 118
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 118
His Ser Ser Ile Ser Arg Gly Asn Ile Tyr Phe Ala Asp Ser Val Lys
1. 5 10 15
Gly
<210> 119
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 119
Ser Ile Ser Arg Gly Asn
1. 5
<210> 120
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 120
Gly Ser Gly Trp Tyr Gly Asp Tyr Phe Asp Tyr
1. 5 10
<210> 121
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 121
Asn Tyr Ala Met Ser
1. 5
<210> 122
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 122
Gly Phe Ala Phe Ser Asn Tyr
1. 5
<210> 123
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 123
Gly Phe Ala Phe Ser Asn Tyr Ala Met Ser
1. 5 10
<210> 124
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 124
Ala Ile Arg Gly Gly Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1. 5 10 15
Gly
<210> 125
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 125
Arg Gly Gly Gly Gly Ser
1. 5
<210> 126
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 126
Asp Phe Ile Ser Gly Thr Trp Tyr Pro Asp Tyr
1. 5 10
<210> 127
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 127
Ser Tyr Trp Ile Gly
1. 5
<210> 128
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 128
Gly Tyr Arg Phe Thr Ser Tyr
1. 5
<210> 129
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 129
Gly Tyr Arg Phe Thr Ser Tyr Trp Ile Gly
1. 5 10
<210> 130
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 130
Ser Ile Tyr Pro Asp Asp Ser Asp Thr Arg Tyr Ser Pro Ser Phe Gln
1. 5 10 15
Gly
<210> 131
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 131
Tyr Pro Asp Asp Ser Asp
1. 5
<210> 132
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 132
Ser Thr Val Asp Tyr Pro Gly Tyr Ser Tyr Phe Asp Tyr
1. 5 10
<210> 133
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 133
Asn Tyr Trp Ile Ala
1. 5
<210> 134
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 134
Gly Tyr Thr Phe Thr Asn Tyr
1. 5
<210> 135
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 135
Gly Tyr Thr Phe Thr Asn Tyr Trp Ile Ala
1. 5 10
<210> 136
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 136
Ile Ile Tyr Pro Asp Gly Ser Asp Thr Arg Tyr Ser Pro Ser Phe Gln
1. 5 10 15
Gly
<210> 137
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 137
Tyr Pro Asp Gly Ser Asp
1. 5
<210> 138
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 138
Asp Ile Thr Ser Trp Tyr Tyr Gly Glu Pro Ala Phe Asp Ile
1. 5 10
<210> 139
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 139
Ser Ser Trp Ile Gly
1. 5
<210> 140
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 140
Gly Tyr Ser Phe Thr Ser Ser
1. 5
<210> 141
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 141
Gly Tyr Ser Phe Thr Ser Ser Trp Ile Gly
1. 5 10
<210> 142
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 142
Ile Ile Tyr Pro Gly Asp Ser Asp Thr Arg Tyr Ser Pro Ser Phe Gln
1. 5 10 15
Gly
<210> 143
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 143
Tyr Pro Gly Asp Ser Asp
1. 5
<210> 144
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 144
Gly Leu Ser Gln Ala Met Thr Gly Phe Gly Phe Asp Tyr
1. 5 10
<210> 145
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 145
Ser Tyr Trp Ile Gly
1. 5
<210> 146
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 146
Gly Tyr Gly Phe Thr Ser Tyr
1. 5
<210> 147
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 147
Gly Tyr Gly Phe Thr Ser Tyr Trp Ile Gly
1. 5 10
<210> 148
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 148
Ile Ile His Pro Asp Asp Ser Asp Thr Lys Tyr Ser Pro Ser Phe Gln
1. 5 10 15
Gly
<210> 149
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 149
His Pro Asp Asp Ser Asp
1. 5
<210> 150
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 150
Ser Tyr Leu Arg Gly Leu Trp Gly Gly Tyr Phe Asp Tyr
1. 5 10
<210> 151
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 151
Ser Ser Trp Ile Gly
1. 5
<210> 152
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 152
Gly Tyr Thr Phe Pro Ser Ser
1. 5
<210> 153
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 153
Gly Tyr Thr Phe Pro Ser Ser Trp Ile Gly
1. 5 10
<210> 154
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 154
Ile Ile Tyr Pro Asp Thr Ser His Thr Arg Tyr Ser Pro Ser Phe Gln
1. 5 10 15
<210> 155
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 155
Tyr Pro Asp Thr Ser His
1. 5
<210> 156
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 156
Ala Ser Tyr Phe Asp Arg Gly Thr Gly Tyr Ser Ser Trp Trp Met Asp
1. 5 10 15
Val
<210> 157
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 157
Gln Tyr Ser Met Ser
1. 5
<210> 158
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 158
Gly Phe Thr Phe Ser Gln Tyr
1. 5
<210> 159
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 159
Gly Phe Thr Phe Ser Gln Tyr Ser Met Ser
1. 5 10
<210> 160
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 160
Ala Ile Ser Gly Gly Gly Val Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1. 5 10 15
Gly
<210> 161
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 161
Ser Gly Gly Gly Val Ser
1. 5
<210> 162
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 162
Asp Ile Ser Asp Ser Gly Gly Ser His Trp Tyr Phe Asp Tyr
1. 5 10
<210> 163
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 163
Ser Tyr Ala Met Ser
1. 5
<210> 164
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 164
Gly Phe Thr Phe Ser Ser Tyr
1. 5
<210> 165
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 165
Gly Phe Thr Phe Ser Ser Tyr Ala Met Ser
1. 5 10
<210> 166
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 166
Thr Ile Ser Gly Thr Gly Gly Thr Thr Tyr Tyr Ala Asp Ser Val Lys
1. 5 10 15
Gly
<210> 167
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 167
Ser Gly Thr Gly Gly Thr
1. 5
<210> 168
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 168
Val Arg Ala Gly Ile Asp Pro Thr Ala Ser Asp Val
1. 5 10
<210> 169
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 169
Asn Phe Ala Met Ser
1. 5
<210> 170
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 170
Gly Phe Thr Phe Asn Asn Phe
1. 5
<210> 171
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 171
Gly Phe Thr Phe Asn Asn Phe Ala Met Ser
1. 5 10
<210> 172
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 172
Gly Ile Ser Gly Ser Gly Asp Asn Thr Tyr Tyr Ala Asp Ser Val Lys
1. 5 10 15
Gly
<210> 173
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 173
Ser Gly Ser Gly Asp Asn
1. 5
<210> 174
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 174
Asp Arg Asp Ile Gly Leu Gly Trp Tyr Ser Tyr Tyr Leu Asp Val
1. 5 10 15
<210> 175
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 175
Ser Tyr Ala Ile Ser
1. 5
<210> 176
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 176
Gly Gly Thr Phe Ser Ser Tyr
1. 5
<210> 177
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 177
Gly Gly Thr Phe Ser Ser Tyr Ala Ile Ser
1. 5 10
<210> 178
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 178
Glu Ile Ile Pro Ile Phe Gly Thr Ala Ser Tyr Ala Gln Lys Phe Gln
1. 5 10 15
Gly
<210> 179
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 179
Ile Pro Ile Phe Gly Thr
1. 5
<210> 180
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 180
Ala Gly Trp Asp Asp Ser Trp Phe Asp Tyr
1. 5 10
<210> 181
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 181
Ser Tyr Trp Ile Gly
1. 5
<210> 182
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 182
Gly Tyr Ser Phe Ala Ser Tyr
1. 5
<210> 183
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 183
Gly Tyr Ser Phe Ala Ser Tyr Trp Ile Gly
1. 5 10
<210> 184
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 184
Val Ile Tyr Pro Gly Thr Ser Glu Thr Arg Tyr Ser Pro Ser Phe Gln
1. 5 10 15
Gly
<210> 185
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 185
Tyr Pro Gly Thr Ser Glu
1. 5
<210> 186
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 186
Gly Leu Ser Ala Ser Ala Ser Gly Tyr Ser Phe Gln Tyr
1. 5 10
<210> 187
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 187
Asp Tyr Trp Ile Gly
1. 5
<210> 188
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 188
Gly Tyr Ser Phe Thr Asp Tyr
1. 5
<210> 189
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 189
Gly Tyr Ser Phe Thr Asp Tyr Trp Ile Gly
1. 5 10
<210> 190
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 190
Met Ile Ser Pro Gly Gly Ser Thr Thr Ile Tyr Arg Pro Ser Phe Gln
1. 5 10 15
Gly
<210> 191
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 191
Ser Pro Gly Gly Ser Thr
1. 5
<210> 192
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 192
Met Tyr Thr Gly Gly Tyr Gly Gly Ser Trp Tyr Phe Asp Tyr
1. 5 10
<210> 193
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 193
Arg Ser Ser Gln Ser Leu Val His Ser Asp Gly Asn Thr Tyr Leu Ser
1. 5 10 15
<210> 194
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 194
Lys Ile Ser Asn Arg Phe Ser
1. 5
<210> 195
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 195
Met Gln Ala Thr Gln Phe Pro Leu Thr
1. 5
<210> 196
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 196
Arg Ser Ser Gln Ser Leu Val His Ser Asp Gly Asn Thr Tyr Leu Ser
1. 5 10 15
<210> 197
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 197
Lys Ile Ser Asn Arg Phe Ser
1. 5
<210> 198
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 198
Met Gln Ala Thr Gln Phe Pro Leu Thr
1. 5
<210> 199
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 199
Arg Ala Ser Gln Gly Ile Ser Asn Tyr Leu Ala
1. 5 10
<210> 200
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 200
Ala Ala Ser Ser Leu Gln Ser
1. 5
<210> 201
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 201
Gln Gln Tyr Asn Ser Tyr Pro Leu Thr
1. 5
<210> 202
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 202
Arg Ser Ser Gln Ser Leu Val Tyr Ser Asp Glu Asn Thr Tyr Leu Asn
1. 5 10 15
<210> 203
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 203
Gln Val Ser Asn Arg Asp Ser
1. 5
<210> 204
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 204
Met Gln Gly Thr Tyr Trp Pro Pro Thr
1. 5
<210> 205
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 205
Arg Ala Ser Gln Ser Val Ser Ser Ser Leu Ala
1. 5 10
<210> 206
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 206
Gly Ala Ser Thr Arg Ala Thr
1. 5
<210> 207
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 207
Gln Gln Tyr Ile Asn Trp Pro His
1. 5
<210> 208
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 208
Gln Ala Ser Gln Asp Ile Ser Asn Tyr Leu Asn
1. 5 10
<210> 209
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 209
Gly Ala Ser Asn Leu Glu Thr
1. 5
<210> 210
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 210
Gln Gln Tyr Asp Asn Phe Pro Ile Thr
1. 5
<210> 211
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 211
Arg Ala Ser Gln Ser Val Ser Ser Asn Leu Ala
1. 5 10
<210> 212
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 212
Ser Ala Ser Thr Arg Ala Ser
1. 5
<210> 213
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 213
Gln Gln Tyr Asp Asn Trp Pro Pro Leu Thr
1. 5 10
<210> 214
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 214
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1. 5 10
<210> 215
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 215
Gly Ala Ser Ser Arg Ala Thr
1. 5
<210> 216
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 216
Gln Gln Tyr Gly Ser Ser Pro Leu Thr
1. 5
<210> 217
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 217
Arg Ala Ser Gln Asp Ile Ser Asn Tyr Leu Ala
1. 5 10
<210> 218
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 218
Ala Ala Ser Ser Leu Gln Ser
1. 5
<210> 219
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 219
Leu Gln Leu Asn Ser Phe Pro Phe Thr
1. 5
<210> 220
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 220
Arg Ala Ser Gln Gly Ile Ser Ser Trp Leu Ala
1. 5 10
<210> 221
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 221
Ala Ala Ser Ser Leu Gln Ser
1. 5
<210> 222
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 222
Gln Gln Ala Phe Ser Phe Pro Phe Thr
1. 5
<210> 223
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 223
Lys Ser Ser Gln Ser Val Leu Tyr Ser Tyr Asn Asn Lys Asn Tyr Val
1. 5 10 15
Ala
<210> 224
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 224
Trp Ala Ser Thr Arg Glu Ser
1. 5
<210> 225
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 225
Gln Gln Tyr Tyr Ser Thr Leu Thr
1. 5
<210> 226
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 226
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1. 5 10
<210> 227
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 227
Asp Ala Ser Ser Arg Ala Thr
1. 5
<210> 228
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 228
Gln Gln Tyr Gly Ser Ser Pro Leu Thr
1. 5
<210> 229
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 229
Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn Tyr Val Tyr
1. 5 10
<210> 230
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 230
Arg Asn Asn Gln Arg Pro Ser
1. 5
<210> 231
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 231
Ala Ala Trp Asp Asp Ser Leu Ser Gly Val Val
1. 5 10
<210> 232
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 232
Ser Gly Ser Arg Ser Asn Ile Gly Ser Asn Tyr Val Tyr
1. 5 10
<210> 233
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 233
Arg Asn Asn Gln Arg Pro Ser
1. 5
<210> 234
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 234
Ala Ser Trp Asp Gly Ser Leu Ser Ala Val Val
1. 5 10
<210> 235
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 235
Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn Tyr Val Tyr
1. 5 10
<210> 236
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 236
Arg Asn Asn Gln Arg Pro Ser
1. 5
<210> 237
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 237
Ala Thr Trp Asp Asp Ser Leu Gly Ser Pro Val
1. 5 10
<210> 238
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 238
Arg Ala Ser Gln Ser Ile Ser Arg Tyr Leu Asn
1. 5 10
<210> 239
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 239
Ala Ala Ser Ile Leu Gln Thr
1. 5
<210> 240
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 240
Gln Gln Ser Tyr Ser Thr Thr Met Trp Thr
1. 5 10
<210> 241
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 241
Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn Tyr Val Asn
1. 5 10
<210> 242
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 242
Gly Asp Tyr Gln Arg Pro Ser
1. 5
<210> 243
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 243
Ala Thr Arg Asp Asp Ser Leu Ser Gly Ser Val Val
1. 5 10
<210> 244
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 244
Arg Ala Ser Gln Ser Ile Tyr Asp Tyr Leu His
1. 5 10
<210> 245
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 245
Asp Ala Ser Asn Leu Gln Ser
1. 5
<210> 246
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 246
Gln Gln Ser Tyr Thr Thr Pro Leu Phe Thr
1. 5 10
<210> 247
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 247
Arg Ala Ser Gln Tyr Ile Gly Arg Tyr Leu Asn
1. 5 10
<210> 248
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 248
Gly Ala Thr Ser Leu Ala Ser
1. 5
<210> 249
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 249
Gln Gln Ser Tyr Ser Thr Thr Ser Pro Thr
1. 5 10
<210> 250
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 250
Ser Gly Ser Thr Ser Asn Ile Gly Arg Asn Tyr Val Tyr
1. 5 10
<210> 251
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 251
Arg Thr Asn Gln Arg Pro Ser
1. 5
<210> 252
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 252
Ala Ala Trp Asp Asp Ser Leu Ser Gly Arg Val
1. 5 10
<210> 253
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 253
Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn Tyr Val Tyr
1. 5 10
<210> 254
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 254
Met Asn Asn Gln Arg Pro Ser
1. 5
<210> 255
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 255
Ala Ala Trp Asp Asp Ser Leu Ser Ala Val Val
1. 5 10
<210> 256
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 256
Ser Gly Ser Asn Ser Asn Ile Gly Thr Asn Tyr Val Ser
1. 5 10
<210> 257
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 257
Arg Ser Ser Arg Arg Pro Ser
1. 5
<210> 258
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 258
Ala Ala Trp Asp Gly Ser Leu Ser Gly His Trp Val
1. 5 10
<210> 259
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 259
Arg Ala Ser Gln Ser Ile Asp Thr Tyr Leu Asn
1. 5 10
<210> 260
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 260
Ser Ala Ser Ser Leu His Ser
1. 5
<210> 261
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 261
Gln Gln Ser Tyr Ser Thr Thr Ala Trp Thr
1. 5 10
<210> 262
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 262
Arg Ala Ser Gln Ser Ile Gly Gln Ser Leu Asn
1. 5 10
<210> 263
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 263
Gly Ala Ser Ser Leu Gln Ser
1. 5
<210> 264
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 264
Gln Gln Ser Tyr Ser Thr Pro Ile Thr
1. 5
<210> 265
<400> 265
000
<210> 266
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 266
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro
20
<210> 267
<211> 16
<212> БЕЛОК
<213> Homo sapiens
<400> 267
Gly Leu Ala Val Ser Thr Ile Ser Ser Phe Phe Pro Pro Gly Tyr Gln
1. 5 10 15
<210> 268
<211> 45
<212> БЕЛОК
<213> Homo sapiens
<400> 268
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
1. 5 10 15
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
20 25 30
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
35 40 45
<210> 269
<211> 231
<212> БЕЛОК
<213> Homo sapiens
<400> 269
Glu Pro Lys Ser Pro Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1. 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys
130 135 140
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 270
<211> 24
<212> БЕЛОК
<213> Homo sapiens
<400> 270
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
1. 5 10 15
Ser Leu Val Ile Thr Leu Tyr Cys
20
<210> 271
<211> 42
<212> БЕЛОК
<213> Homo sapiens
<400> 271
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
1. 5 10 15
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
20 25 30
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
35 40
<210> 272
<211> 112
<212> БЕЛОК
<213> Homo sapiens
<400> 272
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
1. 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 273
<211> 52
<212> БЕЛОК
<213> Homo sapiens
<400> 273
Phe Phe Ile Pro Leu Leu Val Val Ile Leu Phe Ala Val Asp Thr Gly
1. 5 10 15
Leu Phe Ile Ser Thr Gln Gln Gln Val Thr Phe Leu Leu Lys Ile Lys
20 25 30
Arg Thr Arg Lys Gly Phe Arg Leu Leu Asn Pro His Pro Lys Pro Asn
35 40 45
Pro Lys Asn Asn
50
<210> 274
<211> 215
<212> БЕЛОК
<213> Homo sapiens
<400> 274
Met Asp Thr Glu Ser Asn Arg Arg Ala Asn Leu Ala Leu Pro Gln Glu
1. 5 10 15
Pro Ser Ser Val Pro Ala Phe Glu Val Leu Glu Ile Ser Pro Gln Glu
20 25 30
Val Ser Ser Gly Arg Leu Leu Lys Ser Ala Ser Ser Pro Pro Leu His
35 40 45
Thr Trp Leu Thr Val Leu Lys Lys Glu Gln Glu Phe Leu Gly Val Thr
50 55 60
Gln Ile Leu Thr Ala Met Ile Cys Leu Cys Phe Gly Thr Val Val Cys
65 70 75 80
Ser Val Leu Asp Ile Ser His Ile Glu Gly Asp Ile Phe Ser Ser Phe
85 90 95
Lys Ala Gly Tyr Pro Phe Trp Gly Ala Ile Phe Phe Ser Ile Ser Gly
100 105 110
Met Leu Ser Ile Ile Ser Glu Arg Arg Asn Ala Thr Tyr Leu Val Arg
115 120 125
Gly Ser Leu Gly Ala Asn Thr Ala Ser Ser Ile Ala Gly Gly Thr Gly
130 135 140
Ile Thr Ile Leu Ile Ile Asn Leu Lys Lys Ser Leu Ala Tyr Ile His
145 150 155 160
Ile His Ser Cys Gln Lys Phe Phe Glu Thr Lys Cys Phe Met Ala Ser
165 170 175
Phe Ser Thr Glu Ile Val Val Met Met Leu Phe Leu Thr Ile Leu Gly
180 185 190
Leu Gly Ser Ala Val Ser Leu Thr Ile Cys Gly Ala Gly Glu Glu Leu
195 200 205
Lys Gly Asn Lys Val Pro Glu
210 215
<210> 275
<211> 42
<212> БЕЛОК
<213> Homo sapiens
<400> 275
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
1. 5 10 15
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
20 25 30
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
35 40
<210> 276
<211> 41
<212> БЕЛОК
<213> Homo sapiens
<400> 276
Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp Tyr Met Asn Met Thr
1. 5 10 15
Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro
20 25 30
Pro Arg Asp Phe Ala Ala Tyr Arg Ser
35 40
<210> 277
<211> 18
<212> БЕЛОК
<213> Homo sapiens
<400> 277
Met Ile Pro Ala Val Val Leu Leu Leu Leu Leu Leu Val Glu Gln Ala
1. 5 10 15
Ala Ala
<210> 278
<211> 43
<212> БЕЛОК
<213> Homo sapiens
<400> 278
Leu Gly Glu Pro Gln Leu Cys Tyr Ile Leu Asp Ala Ile Leu Phe Leu
1. 5 10 15
Tyr Gly Ile Val Leu Thr Leu Leu Tyr Cys Arg Leu Lys Ile Gln Val
20 25 30
Arg Lys Ala Ala Ile Thr Ser Tyr Glu Lys Ser
35 40
<210> 279
<211> 22
<212> БЕЛОК
<213> Homo sapiens
<400> 279
Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val
1. 5 10 15
Glu Glu Asn Pro Gly Pro
20
<210> 280
<211> 21
<212> БЕЛОК
<213> Homo sapiens
<400> 280
Gly Ser Gly Glu Gly Arg Gly Ser Leu Leu Thr Cys Gly Asp Val Glu
1. 5 10 15
Glu Asn Pro Gly Pro
20
<210> 281
<211> 530
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 281
Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys
1. 5 10 15
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
20 25 30
His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly
35 40 45
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
50 55 60
Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn
65 70 75 80
Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
85 90 95
Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala
100 105 110
Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu
115 120 125
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala
130 135 140
Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
145 150 155 160
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val
165 170 175
Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val
180 185 190
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu
195 200 205
Gln Val Val Ala Ile Ala Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu
210 215 220
Thr Val Gln Ala Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
225 230 235 240
Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala
245 250 255
Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly
260 265 270
Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser Asn Ile Gly Gly Lys
275 280 285
Gln Ala Leu Glu Thr Val Gln Ala Leu Leu Pro Val Leu Cys Gln Ala
290 295 300
His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly
305 310 315 320
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
325 330 335
Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser Asn
340 345 350
Ile Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Ala Leu Leu Pro Val
355 360 365
Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala
370 375 380
Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu
385 390 395 400
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala
405 410 415
Ile Ala Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Ala
420 425 430
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val
435 440 445
Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val
450 455 460
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu
465 470 475 480
Gln Val Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu
485 490 495
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
500 505 510
Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Arg Pro Ala
515 520 525
Leu Glu
530
<210> 282
<211> 530
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 282
Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly Gly Lys
1. 5 10 15
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
20 25 30
His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly
35 40 45
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
50 55 60
Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His
65 70 75 80
Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
85 90 95
Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala
100 105 110
Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Ala Leu Leu
115 120 125
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala
130 135 140
Ile Ala Ser Asn Asn Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
145 150 155 160
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val
165 170 175
Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val
180 185 190
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln
195 200 205
Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu
210 215 220
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
225 230 235 240
Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys Gln Ala
245 250 255
Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly
260 265 270
Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys
275 280 285
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
290 295 300
His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly
305 310 315 320
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
325 330 335
Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser Asn
340 345 350
Ile Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Ala Leu Leu Pro Val
355 360 365
Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala
370 375 380
Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu
385 390 395 400
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala
405 410 415
Ile Ala Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Ala
420 425 430
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val
435 440 445
Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val
450 455 460
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln
465 470 475 480
Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys Gln Ala Leu Glu
485 490 495
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
500 505 510
Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Arg Pro Ala
515 520 525
Leu Glu
530
<210> 283
<211> 530
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 283
Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys
1. 5 10 15
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
20 25 30
His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly
35 40 45
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
50 55 60
Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn
65 70 75 80
Asn Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
85 90 95
Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala
100 105 110
Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu
115 120 125
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala
130 135 140
Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
145 150 155 160
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val
165 170 175
Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val
180 185 190
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln
195 200 205
Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys Gln Ala Leu Glu
210 215 220
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
225 230 235 240
Pro Glu Gln Val Val Ala Ile Ala Ser Asn Ile Gly Gly Lys Gln Ala
245 250 255
Leu Glu Thr Val Gln Ala Leu Leu Pro Val Leu Cys Gln Ala His Gly
260 265 270
Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys
275 280 285
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
290 295 300
His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly
305 310 315 320
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
325 330 335
Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His
340 345 350
Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
355 360 365
Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala
370 375 380
Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Ala Leu Leu
385 390 395 400
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala
405 410 415
Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
420 425 430
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val
435 440 445
Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val
450 455 460
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu
465 470 475 480
Gln Val Val Ala Ile Ala Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu
485 490 495
Thr Val Gln Ala Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
500 505 510
Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Arg Pro Ala
515 520 525
Leu Glu
530
<210> 284
<211> 539
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 284
Asn Pro Gln Arg Ser Thr Val Trp Tyr Leu Thr Pro Gln Gln Val Val
1. 5 10 15
Ala Ile Ala Ser Asn Asn Gly Gly Lys Gln Ala Leu Glu Thr Val Gln
20 25 30
Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln
35 40 45
Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr
50 55 60
Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro
65 70 75 80
Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys Gln Ala Leu
85 90 95
Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu
100 105 110
Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys Gln
115 120 125
Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His
130 135 140
Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly Gly
145 150 155 160
Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln
165 170 175
Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp
180 185 190
Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu
195 200 205
Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser
210 215 220
Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro
225 230 235 240
Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile
245 250 255
Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu
260 265 270
Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val
275 280 285
Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln
290 295 300
Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln
305 310 315 320
Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr
325 330 335
Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro
340 345 350
Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys Gln Ala Leu
355 360 365
Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu
370 375 380
Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys Gln
385 390 395 400
Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His
405 410 415
Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly
420 425 430
Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln
435 440 445
Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly
450 455 460
Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu
465 470 475 480
Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser
485 490 495
Asn Asn Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro
500 505 510
Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile
515 520 525
Ala Ser Asn Gly Gly Gly Arg Pro Ala Leu Glu
530 535
<210> 285
<211> 530
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 285
Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly Gly Lys
1. 5 10 15
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
20 25 30
His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly
35 40 45
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
50 55 60
Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His
65 70 75 80
Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
85 90 95
Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala
100 105 110
Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Ala Leu Leu
115 120 125
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala
130 135 140
Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
145 150 155 160
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val
165 170 175
Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val
180 185 190
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu
195 200 205
Gln Val Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu
210 215 220
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
225 230 235 240
Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys Gln Ala
245 250 255
Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly
260 265 270
Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser Asn Ile Gly Gly Lys
275 280 285
Gln Ala Leu Glu Thr Val Gln Ala Leu Leu Pro Val Leu Cys Gln Ala
290 295 300
His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly
305 310 315 320
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
325 330 335
Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn
340 345 350
Asn Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
355 360 365
Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala
370 375 380
Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu
385 390 395 400
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala
405 410 415
Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
420 425 430
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val
435 440 445
Val Ala Ile Ala Ser Asn Asn Gly Gly Lys Gln Ala Leu Glu Thr Val
450 455 460
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu
465 470 475 480
Gln Val Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu
485 490 495
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
500 505 510
Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Arg Pro Ala
515 520 525
Leu Glu
530
<210> 286
<211> 530
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 286
Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys
1. 5 10 15
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
20 25 30
His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly
35 40 45
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
50 55 60
Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn
65 70 75 80
Asn Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
85 90 95
Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala
100 105 110
Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Ala Leu Leu
115 120 125
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala
130 135 140
Ile Ala Ser Asn Asn Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
145 150 155 160
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val
165 170 175
Val Ala Ile Ala Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu Thr Val
180 185 190
Gln Ala Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln
195 200 205
Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu
210 215 220
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
225 230 235 240
Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala
245 250 255
Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly
260 265 270
Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys
275 280 285
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
290 295 300
His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly
305 310 315 320
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
325 330 335
Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn
340 345 350
Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
355 360 365
Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala
370 375 380
Ser Asn Asn Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu
385 390 395 400
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala
405 410 415
Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
420 425 430
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val
435 440 445
Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val
450 455 460
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln
465 470 475 480
Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu
485 490 495
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
500 505 510
Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Arg Pro Ala
515 520 525
Leu Glu
530
<210> 287
<211> 530
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 287
Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys
1. 5 10 15
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
20 25 30
His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly
35 40 45
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
50 55 60
Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His
65 70 75 80
Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
85 90 95
Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala
100 105 110
Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu
115 120 125
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala
130 135 140
Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
145 150 155 160
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val
165 170 175
Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val
180 185 190
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln
195 200 205
Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu
210 215 220
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
225 230 235 240
Pro Glu Gln Val Val Ala Ile Ala Ser Asn Ile Gly Gly Lys Gln Ala
245 250 255
Leu Glu Thr Val Gln Ala Leu Leu Pro Val Leu Cys Gln Ala His Gly
260 265 270
Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly Gly Lys
275 280 285
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
290 295 300
His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly
305 310 315 320
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
325 330 335
Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His
340 345 350
Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
355 360 365
Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala
370 375 380
Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Ala Leu Leu
385 390 395 400
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala
405 410 415
Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
420 425 430
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val
435 440 445
Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val
450 455 460
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu
465 470 475 480
Gln Val Val Ala Ile Ala Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu
485 490 495
Thr Val Gln Ala Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
500 505 510
Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Arg Pro Ala
515 520 525
Leu Glu
530
<210> 288
<211> 530
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 288
Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys
1. 5 10 15
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
20 25 30
His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly
35 40 45
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
50 55 60
Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His
65 70 75 80
Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
85 90 95
Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala
100 105 110
Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu
115 120 125
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala
130 135 140
Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
145 150 155 160
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val
165 170 175
Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val
180 185 190
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln
195 200 205
Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu
210 215 220
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
225 230 235 240
Pro Glu Gln Val Val Ala Ile Ala Ser Asn Ile Gly Gly Lys Gln Ala
245 250 255
Leu Glu Thr Val Gln Ala Leu Leu Pro Val Leu Cys Gln Ala His Gly
260 265 270
Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly Gly Lys
275 280 285
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
290 295 300
His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly
305 310 315 320
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
325 330 335
Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn
340 345 350
Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
355 360 365
Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala
370 375 380
Ser Asn Asn Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu
385 390 395 400
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala
405 410 415
Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
420 425 430
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val
435 440 445
Val Ala Ile Ala Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu Thr Val
450 455 460
Gln Ala Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu
465 470 475 480
Gln Val Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu
485 490 495
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
500 505 510
Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Arg Pro Ala
515 520 525
Leu Glu
530
<210> 289
<211> 530
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 289
Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys
1. 5 10 15
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
20 25 30
His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly
35 40 45
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
50 55 60
Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn
65 70 75 80
Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
85 90 95
Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala
100 105 110
Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu
115 120 125
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala
130 135 140
Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
145 150 155 160
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val
165 170 175
Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val
180 185 190
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln
195 200 205
Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu
210 215 220
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
225 230 235 240
Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala
245 250 255
Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly
260 265 270
Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly Gly Lys
275 280 285
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
290 295 300
His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly
305 310 315 320
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
325 330 335
Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn
340 345 350
Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
355 360 365
Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala
370 375 380
Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu
385 390 395 400
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala
405 410 415
Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
420 425 430
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val
435 440 445
Val Ala Ile Ala Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu Thr Val
450 455 460
Gln Ala Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln
465 470 475 480
Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys Gln Ala Leu Glu
485 490 495
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
500 505 510
Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Arg Pro Ala
515 520 525
Leu Glu
530
<210> 290
<211> 530
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 290
Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys
1. 5 10 15
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
20 25 30
His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly
35 40 45
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
50 55 60
Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn
65 70 75 80
Asn Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
85 90 95
Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala
100 105 110
Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu
115 120 125
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala
130 135 140
Ile Ala Ser Asn Asn Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
145 150 155 160
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val
165 170 175
Val Ala Ile Ala Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu Thr Val
180 185 190
Gln Ala Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln
195 200 205
Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu
210 215 220
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
225 230 235 240
Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala
245 250 255
Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly
260 265 270
Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly Gly Lys
275 280 285
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
290 295 300
His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser Asn Ile Gly
305 310 315 320
Gly Lys Gln Ala Leu Glu Thr Val Gln Ala Leu Leu Pro Val Leu Cys
325 330 335
Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn
340 345 350
Asn Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
355 360 365
Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala
370 375 380
Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu
385 390 395 400
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala
405 410 415
Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
420 425 430
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val
435 440 445
Val Ala Ile Ala Ser Asn Asn Gly Gly Lys Gln Ala Leu Glu Thr Val
450 455 460
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu
465 470 475 480
Gln Val Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu
485 490 495
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
500 505 510
Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Arg Pro Ala
515 520 525
Leu Glu
530
<210> 291
<211> 136
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 291
Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser Glu
1. 5 10 15
Leu Pro Thr Gln Gly Thr Phe Ser Asn Val Ser Thr Asn Val Ser Pro
20 25 30
Ala Lys Pro Thr Thr Thr Ala Cys Pro Tyr Ser Asn Pro Ser Leu Cys
35 40 45
Ser Gly Gly Gly Gly Ser Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
50 55 60
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
65 70 75 80
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
85 90 95
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
100 105 110
Ser Leu Val Ile Thr Leu Tyr Cys Asn His Arg Asn Arg Arg Arg Val
115 120 125
Cys Lys Cys Pro Arg Pro Val Val
130 135
<210> 292
<211> 157
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 292
Met Gly Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1. 5 10 15
Asp His Ala Asp Ala Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly
20 25 30
Gly Gly Gly Ser Glu Leu Pro Thr Gln Gly Thr Phe Ser Asn Val Ser
35 40 45
Thr Asn Val Ser Pro Ala Lys Pro Thr Thr Thr Ala Cys Pro Tyr Ser
50 55 60
Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser Pro Ala Pro Arg Pro
65 70 75 80
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
85 90 95
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
100 105 110
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
115 120 125
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Asn His Arg
130 135 140
Asn Arg Arg Arg Val Cys Lys Cys Pro Arg Pro Val Val
145 150 155
<210> 293
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 293
Cys Pro Tyr Ser Asn Pro Ser Leu Cys
1. 5
<210> 294
<211> 37
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 294
Gly Ser Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys
1. 5 10 15
Ser Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser
20 25 30
Gly Gly Gly Gly Ser
35
<210> 295
<211> 24
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
пептид
<400> 295
Glu Leu Pro Thr Gln Gly Thr Phe Ser Asn Val Ser Thr Asn Val Ser
1. 5 10 15
Pro Ala Lys Pro Thr Thr Thr Ala
20
<210> 296
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 296
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1. 5 10 15
<210> 297
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 297
caggtcacct tgaaggagtc tggtcctgtg ctggtgaaac ccacagagac cctcacgctg
60
acctgcaccg tctctgggtt ctcactcagt aatgctagaa tgggtgtgac ctggatccgt
120
cagcccccag ggaaggccct ggagtggctt gcacacattt tttcgaatga cgaaaaatcc
180
tacagtacat ctctgaagag caggctcacc atctccaagg acacttccaa aacccaggtg
240
gtccttacca tgaccaacat ggaccctgtg gacacagcca catattactg tgcacggata
300
cgagattact atgacattag tagttattat gactactggg gccagggaac cctggtcagc
360
gtctcctca
369
<210> 298
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 298
gacatccaga tgacccagtc tccatctgcc atgtctgcat ctgtaggaga cagagtcacc
60
atcacttgtc gggcgagtca ggacattagc aattatttag cctggtttca gcagaaacca
120
gggaaagtcc ctaagcgcct gatctatgct gcatccagtt tgcaaagtgg ggtcccatca
180
aggttcagcg gcagtggatc ggggacagaa ttcactctca caatcagcag cctgctgcct
240
gaagattttg caacttatta ctgtctacag cttaatagtt tcccgttcac ttttggcgga
300
gggaccaagg tggagatcaa c
321
<210> 299
<211> 372
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 299
gaggtgcagc tggtggagtc tgggggaggc ttggtccagc ctggggggtc cctgagactc
60
tcctgtgtag cctctggatt cacctttagt agttattgga tgagctgggt ccgccaggct
120
ccagggaagg ggctggagtg ggtggccagc ataaagcaag atggaagtga gaaatactat
180
gtggactctg tgaagggccg attcaccatc tccagagaca acgccaagaa ctcagtgtat
240
ctgcaaatga acagcctgag agccgaggac acgggtgtgt attactgtgc gagagaagga
300
gtcaactggg gatggagact ctactggcac ttcgatctct ggggccgtgg aaccctggtc
360
actgtctcct ca
372
<210> 300
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 300
gacatcgtga tgacccagtc tccagactcc ctggctgtgt ctctgggcga gagggccacc
60
atcaactgca agtccagcca gagtgtttta tacagctaca acaataagaa ctacgtagct
120
tggtaccagc agaaaccagg acaacctcct aacctactca ttttctgggc atctacccgg
180
gaatccgggg tccctgaccg attcagtggc agcgggtctg ggacagattt cactctcacc
240
atcagcagcc tgcaggctga agatgtggca gtttactact gtcagcaata ttatagtacg
300
ctcactttcg gcggagggac caaggtggag atcaaa
336
<210> 301
<211> 357
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 301
gaggtgcagc tggtggagtc tgggggaggc ttggtacagc ctggggggtc cctgagactc
60
tcctgtgcag tctctggatt caccttcagt aaccataaca tacactgggt ccgccaggct
120
ccagggaagg ggctggagtg gatttcatac attagtcgaa gtagtagtac catatattac
180
gcagactctg tgaagggccg attcacaatc tccagagaca atgccaagaa ctcactgtat
240
ctgcaaatga acagcctgag agacgaagac acggctgtgt attactgtgc gagagatcac
300
gctcagtggt acggtatgga cgtttggggc caagggacca cggtcaccgt ctcctca
357
<210> 302
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 302
gacatccaga tgacccagtc tccatcttcc gtgtctgcat cggtaggaga cagagtcacc
60
atcacttgtc gggcgagtca gggtattagc agctggttag cctggtatca gcagaaacca
120
gggaaagccc ctaaggtcct gatctatgct gcatccagtt tgcaaagtgg ggtcccatca
180
aggttcagcg gcagtggatc tgggacagat ttcactctca ccatcagcag cctgcagcct
240
gaagattttg caacttacta ttgtcaacag gctttcagtt tcccattcac tttcggccct
300
gggaccaaag tggatatcaa a
321
<210> 303
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 303
gaagtgcagc ttgtccagag cggagccgaa gtgaagaagc ctggcgagag cctgaagatc
60
agctgcaagg gctccggata tcgcttcaca agttactgga tagggtgggt gcgccagatg
120
cctggtaagg gactggaatg gatgggctct atatatcctg atgattccga cacacgttat
180
agcccaagct ttcagggcca ggtcacaatc agcgctgaca agagcatcag caccgcctac
240
cttcagtggt cgtctctgaa ggccagcgac accgcaatgt actactgcgc ctctagcaca
300
gttgactacc cgggatacag ttacttcgac tactggggcc aaggtacact ggtcaccgtc
360
agcagc
366
<210> 304
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 304
gagctccaga gcgtgctgac ccagcctcct agcgcaagcg gcacccctgg acagcgtgtg
60
acaattagct gtagcggaag tcgtagcaat atcggatcaa actatgtgta ttggtatcag
120
caattgcccg gtacagcacc caaattgctc atatatagaa ataatcagag acctagcgga
180
gtgcctgatc gttttagcgg tagcaaaagc ggcaccagcg catcactggc aatttcaggc
240
ctgcgtagcg aagatgaggc ggattattac tgtgcgagtt gggatggttc gctgagtgct
300
gttgtgttcg gcaccggtac aaaactgacc gttctg
336
<210> 305
<211> 378
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 305
gaagtgcagc ttgtccagag cggagccgaa gtgaagaagc ctggcgagag cctgaagatc
60
agctgcaagg gctccggata cacctttcct tcatcatgga taggttgggt gcgccagatg
120
cctggtaagg gactggaatg gatgggcatc atataccctg atactagcca tacccgttac
180
agcccaagct ttcagggcca ggtcacaatc agcgctgaca agagcatcag caccgcctac
240
cttcagtggt cgtctctgaa ggccagcgac accgcaatgt actactgtgc ccgtgcgagc
300
tatttcgatc gtggaacagg gtatagttct tggtggatgg atgtgtgggg ccaaggtaca
360
ctggtcaccg tcagcagc
378
<210> 306
<211> 330
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 306
gagctcgata ttcagatgac ccagagccct agcagcctga gcgcaagcgt gggcgataga
60
gtgaccatta cctgtagggc ctcacaatcc atatacgact atttgcactg gtatcagcag
120
aaacccggga aagcacccaa actgctgatt tacgatgctt ccaacctaca gagtggcgtt
180
ccttcacgtt ttagcggtag cggttcaggc accgatttca ccctgaccat tagcagcctt
240
cagcccgaag atttcgctac gtattattgc cagcaatcat acaccacgcc gttgtttaca
300
ttcggccagg gtaccaaagt ggaaatcaaa
330
<210> 307
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 307
gaagtgcagc ttgtccagag cggagccgaa gtgaagaagc ctggcgagag cctgaagatc
60
agctgcaagg gctccggata cggattcaca agttattgga taggttgggt gcgccagatg
120
cctggtaagg gactggaatg gatgggtatc attcatcccg atgatagcga caccaaatac
180
agcccaagct ttcagggcca ggtcacaatc agcgctgaca agagcatcag caccgcctac
240
cttcagtggt cgtctctgaa ggccagcgac accgcaatgt actactgtgc ctctagctat
300
ttgcgtggct tgtggggagg ctattttgac tattggggcc aaggtacact ggtcaccgtc
360
agcagc
366
<210> 308
<211> 339
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 308
gagctccaga gcgtgctgac ccagcctcct agcgcaagcg gcacccctgg acagcgtgtg
60
acaattagct gtagcggatc aagctcaaac attggctcaa attatgtgaa ttggtatcag
120
caattgcccg gtacagcacc caaactgctc atttatggag attatcaacg acctagcgga
180
gtgcctgatc gttttagcgg tagcaaaagc ggcaccagcg catcactggc aatttcaggc
240
ctgcgtagcg aagatgaggc ggattattac tgtgctaccc gcgacgattc gttatctggg
300
tctgtcgttt ttggcaccgg tacaaaactg accgtgctg
339
<210> 309
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 309
gaagtgcagc ttgtccagag cggagccgaa gtgaagaagc ctggcgagag cctgaagatc
60
agctgcaagg gctccggata cagttttgcc tcatactgga tcggttgggt gcgccagatg
120
cctggtaagg gactggaatg gatgggcgta atttaccccg gaactagcga gacacgttac
180
agcccaagct ttcagggcca ggtcacaatc agcgctgaca agagcatcag caccgcctac
240
cttcagtggt cgtctctgaa ggccagcgac accgcaatgt actactgcgc taaagggttg
300
agtgcgagtg caagtggata ttctttccaa tattggggcc aaggtacact ggtcaccgtc
360
agcagc
366
<210> 310
<211> 330
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 310
gagctcgata ttcagatgac ccagagccct agcagcctga gcgcaagcgt gggcgataga
60
gtgaccatta cctgtagggc ctcacaaagc atcgacacat atttaaactg gtatcagcag
120
aaacccggga aagcacccaa actgctgatt tattcagcta gtagcctaca cagtggcgtt
180
ccttcacgtt ttagcggtag cggttcaggc accgatttca ccctgaccat tagcagcctt
240
cagcccgaag atttcgctac gtattattgc caacaatcat acagcacaac tgcttggaca
300
ttcggccagg gtaccaaagt ggaaatcaaa
330
<210> 311
<211> 494
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 311
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly
35 40 45
Thr Phe Ser Ser Tyr Gly Phe Ser Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Phe Gly Ser Ala Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser
85 90 95
Thr Ser Thr Val Tyr Met Glu Leu Ile Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Gly Ser Ser Ser Pro Phe Ala Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Val Met Thr Gln Asn Pro Leu Ser Ser Pro Val Thr Leu Gly Gln
165 170 175
Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser Asp
180 185 190
Gly Asn Thr Tyr Leu Ser Trp Leu Gln Gln Arg Pro Gly Gln Ser Pro
195 200 205
Arg Leu Leu Ile Tyr Lys Ile Ser Asn Arg Phe Ser Gly Val Pro Asp
210 215 220
Arg Phe Ser Gly Ser Gly Ala Gly Thr Asp Phe Thr Leu Lys Ile Ser
225 230 235 240
Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala Thr
245 250 255
Gln Phe Pro Leu Thr Ile Gly Gly Gly Ser Lys Val Glu Ile Lys Thr
260 265 270
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
275 280 285
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
290 295 300
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
305 310 315 320
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
325 330 335
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
340 345 350
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
355 360 365
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
370 375 380
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
385 390 395 400
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
405 410 415
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
420 425 430
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
435 440 445
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
450 455 460
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
465 470 475 480
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 312
<211> 494
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 312
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly
35 40 45
Thr Phe Ser Ser Tyr Gly Phe Ser Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser
85 90 95
Thr Ser Thr Val Phe Met Glu Leu Ile Ser Leu Arg Ser Glu Tyr Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Gly Ser Ser Ser Pro Phe Ala Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Val Met Thr Gln Thr Pro Leu Ser Ser Pro Val Thr Leu Gly Gln
165 170 175
Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser Asp
180 185 190
Gly Asn Thr Tyr Leu Ser Trp Leu Gln Gln Arg Pro Gly Gln Ser Pro
195 200 205
Arg Leu Leu Ile Tyr Lys Ile Ser Asn Arg Phe Ser Gly Val Pro Asp
210 215 220
Arg Phe Ser Gly Ser Gly Ala Gly Thr Asp Phe Thr Leu Lys Ile Ser
225 230 235 240
Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala Thr
245 250 255
Gln Phe Pro Leu Thr Ile Gly Gly Gly Ser Lys Val Glu Ile Lys Thr
260 265 270
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
275 280 285
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
290 295 300
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
305 310 315 320
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
325 330 335
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
340 345 350
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
355 360 365
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
370 375 380
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
385 390 395 400
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
405 410 415
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
420 425 430
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
435 440 445
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
450 455 460
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
465 470 475 480
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 313
<211> 483
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 313
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Ser Tyr Tyr Trp Asn Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Tyr Ile Tyr Tyr Ser Gly Ser Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Arg Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Asp Ile Arg Thr Trp Gly Gln Gly Thr Leu
115 120 125
Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser
145 150 155 160
Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys
165 170 175
Arg Ala Ser Gln Gly Ile Ser Asn Tyr Leu Ala Trp Phe Gln Gln Lys
180 185 190
Pro Gly Lys Ala Pro Lys Ser Leu Ile Tyr Ala Ala Ser Ser Leu Gln
195 200 205
Ser Gly Val Pro Ser Lys Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
210 215 220
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr
225 230 235 240
Cys Gln Gln Tyr Asn Ser Tyr Pro Leu Thr Phe Gly Gly Gly Thr Lys
245 250 255
Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
260 265 270
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
275 280 285
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
290 295 300
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
305 310 315 320
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
325 330 335
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
340 345 350
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
355 360 365
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
370 375 380
Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
385 390 395 400
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
405 410 415
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
420 425 430
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
435 440 445
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
450 455 460
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
465 470 475 480
Pro Pro Arg
<210> 314
<211> 493
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 314
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Arg Asn Ser Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ala Asn Ile Lys Arg Asp Gly Ser Glu Lys Tyr
65 70 75 80
Tyr Val Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Gln Thr Gly Ser Phe Asp Tyr Trp
115 120 125
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val
145 150 155 160
Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly Gln Pro
165 170 175
Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val Tyr Ser Asp Glu
180 185 190
Asn Thr Tyr Leu Asn Trp Phe Gln Gln Arg Pro Gly Gln Ser Leu Arg
195 200 205
Arg Leu Ile Tyr Gln Val Ser Asn Arg Asp Ser Gly Val Pro Asp Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg
225 230 235 240
Val Glu Ala Glu Asp Val Gly Val Tyr Phe Cys Met Gln Gly Thr Tyr
245 250 255
Trp Pro Pro Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 315
<211> 485
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 315
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Arg Gly Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Asp Asp
35 40 45
Ser Ile Ser Val Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Ala Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Arg Val Tyr Ser Ser Gly Asn Ile Asn Tyr
65 70 75 80
Asn Pro Ser Leu Glu Ser Arg Val Thr Met Ser Val Asp Thr Ser Lys
85 90 95
Ser Arg Phe Ser Leu Asn Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Gly Leu Asp Ala Phe Asp Ile Trp Gly Gln
115 120 125
Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met
145 150 155 160
Thr Gln Ser Pro Ala Thr Leu Ser Met Ser Leu Gly Glu Arg Ala Thr
165 170 175
Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser
195 200 205
Thr Arg Ala Thr Gly Ile Pro Ala Arg Phe Gly Gly Ser Gly Ser Gly
210 215 220
Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser Glu Asp Phe Ala
225 230 235 240
Val Tyr Tyr Cys Gln Gln Tyr Ile Asn Trp Pro His Phe Gly Gly Gly
245 250 255
Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
260 265 270
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
275 280 285
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
290 295 300
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
305 310 315 320
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
325 330 335
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
340 345 350
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
355 360 365
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
370 375 380
Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
385 390 395 400
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
405 410 415
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
420 425 430
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
435 440 445
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
450 455 460
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
465 470 475 480
Ala Leu Pro Pro Arg
485
<210> 316
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 316
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Glu Ser Leu Arg Leu Ser Cys Glu Val Ser Gly Phe
35 40 45
Thr Phe Thr Ser Tyr Ala Met Ser Trp Val Arg Gln Val Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ile Ile Ser Gly Val Ala Phe Thr Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp His Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Gly Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Val Lys Val Asp Gly Glu Val Tyr Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met
145 150 155 160
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
165 170 175
Ile Thr Cys Gln Ala Ser Gln Asp Ile Ser Asn Tyr Leu Asn Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Lys Ala Pro Lys Ile Leu Ile Tyr Gly Ala Ser
195 200 205
Asn Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Phe Ala Ile Ser Ser Leu Gln Pro Glu Asp Val Ala
225 230 235 240
Thr Tyr Tyr Cys Gln Gln Tyr Asp Asn Phe Pro Ile Thr Phe Gly Gln
245 250 255
Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 317
<211> 489
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 317
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Glu Ala Ser Gly Gly
35 40 45
Thr Phe Ile Thr Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Phe Phe Gly Thr Ala Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser
85 90 95
Thr Ser Thr Ala Ser Met Glu Leu Arg Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Gln Trp Glu Leu Phe Phe Phe Asp Phe Trp
115 120 125
Gly Gln Gly Thr Pro Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile
145 150 155 160
Val Met Thr Gln Ser Pro Asp Thr Leu Ser Val Ser Pro Gly Glu Arg
165 170 175
Ala Ile Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Asn Leu Ala
180 185 190
Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Ser
195 200 205
Ala Ser Thr Arg Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly
210 215 220
Ser Gly Thr Glu Phe Thr Leu Ser Ile Ser Ser Leu Gln Ser Glu Asp
225 230 235 240
Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Asp Asn Trp Pro Pro Leu Thr
245 250 255
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
325 330 335
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
340 345 350
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
355 360 365
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
370 375 380
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
385 390 395 400
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
405 410 415
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
420 425 430
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
435 440 445
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
450 455 460
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
465 470 475 480
Leu His Met Gln Ala Leu Pro Pro Arg
485
<210> 318
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 318
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Ala Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Thr Tyr Tyr Ser Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser His Ile Ser Ile Arg Ser Ser Thr Ile Tyr
65 70 75 80
Phe Ala Asp Ser Ala Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Ser Gly Trp Tyr Gly Asp Tyr Phe
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro
165 170 175
Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser
180 185 190
Ser Tyr Leu Ala Trp Tyr Gln Gln Gln Pro Gly Gln Ala Pro Arg Leu
195 200 205
Leu Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu
225 230 235 240
Glu Pro Glu Asp Phe Ala Ile Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser
245 250 255
Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 319
<211> 494
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 319
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Thr Leu Lys Glu Ser Gly Pro Val Leu
20 25 30
Val Lys Pro Thr Glu Thr Leu Thr Leu Thr Cys Thr Val Ser Gly Phe
35 40 45
Ser Leu Ser Asn Ala Arg Met Gly Val Thr Trp Ile Arg Gln Pro Pro
50 55 60
Gly Lys Ala Leu Glu Trp Leu Ala His Ile Phe Ser Asn Asp Glu Lys
65 70 75 80
Ser Tyr Ser Thr Ser Leu Lys Ser Arg Leu Thr Ile Ser Lys Asp Thr
85 90 95
Ser Lys Thr Gln Val Val Leu Thr Met Thr Asn Met Asp Pro Val Asp
100 105 110
Thr Ala Thr Tyr Tyr Cys Ala Arg Ile Arg Asp Tyr Tyr Asp Ile Ser
115 120 125
Ser Tyr Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Ser Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
145 150 155 160
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ala Met Ser
165 170 175
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
180 185 190
Ile Ser Asn Tyr Leu Ala Trp Phe Gln Gln Lys Pro Gly Lys Val Pro
195 200 205
Lys Arg Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
210 215 220
Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser
225 230 235 240
Ser Leu Leu Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Leu Asn
245 250 255
Ser Phe Pro Phe Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Asn Thr
260 265 270
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
275 280 285
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
290 295 300
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
305 310 315 320
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
325 330 335
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
340 345 350
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
355 360 365
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
370 375 380
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
385 390 395 400
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
405 410 415
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
420 425 430
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
435 440 445
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
450 455 460
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
465 470 475 480
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 320
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 320
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe
35 40 45
Thr Phe Ser Asn His Asn Ile His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Ser Tyr Ile Ser Arg Ser Ser Ser Thr Ile Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp His Ala Gln Trp Tyr Gly Met Asp
115 120 125
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
165 170 175
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
180 185 190
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val Leu Ile
195 200 205
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
225 230 235 240
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Phe Ser Phe Pro Phe
245 250 255
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 321
<211> 500
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 321
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Val Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ala Ser Ile Lys Gln Asp Gly Ser Glu Lys Tyr
65 70 75 80
Tyr Val Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Val Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Gly Val Tyr Tyr Cys Ala Arg Glu Gly Val Asn Trp Gly Trp Arg Leu
115 120 125
Tyr Trp His Phe Asp Leu Trp Gly Arg Gly Thr Leu Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu
165 170 175
Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln
180 185 190
Ser Val Leu Tyr Ser Tyr Asn Asn Lys Asn Tyr Val Ala Trp Tyr Gln
195 200 205
Gln Lys Pro Gly Gln Pro Pro Asn Leu Leu Ile Phe Trp Ala Ser Thr
210 215 220
Arg Glu Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
225 230 235 240
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val
245 250 255
Tyr Tyr Cys Gln Gln Tyr Tyr Ser Thr Leu Thr Phe Gly Gly Gly Thr
260 265 270
Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro
275 280 285
Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys
290 295 300
Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala
305 310 315 320
Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu
325 330 335
Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys
340 345 350
Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr
355 360 365
Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly
370 375 380
Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala
385 390 395 400
Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg
405 410 415
Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu
420 425 430
Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn
435 440 445
Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met
450 455 460
Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly
465 470 475 480
Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala
485 490 495
Leu Pro Pro Arg
500
<210> 322
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 322
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Val Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ser Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser His Ser Ser Ile Ser Arg Gly Asn Ile Tyr
65 70 75 80
Phe Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Ser Gly Trp Tyr Gly Asp Tyr Phe
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro
165 170 175
Gly Glu Arg Val Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser
180 185 190
Ser Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu
195 200 205
Leu Ile Tyr Asp Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu
225 230 235 240
Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser
245 250 255
Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 323
<211> 496
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 323
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Ala Phe Ser Asn Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Arg Gly Gly Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Phe Ile Ser Gly Thr Trp Tyr Pro
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Glu Leu Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr
165 170 175
Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile
180 185 190
Gly Ser Asn Tyr Val Tyr Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro
195 200 205
Lys Leu Leu Ile Tyr Arg Asn Asn Gln Arg Pro Ser Gly Val Pro Asp
210 215 220
Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser
225 230 235 240
Gly Leu Arg Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp
245 250 255
Asp Ser Leu Ser Gly Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val
260 265 270
Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
275 280 285
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
290 295 300
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
305 310 315 320
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
325 330 335
Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
340 345 350
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
355 360 365
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
370 375 380
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
385 390 395 400
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
405 410 415
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
420 425 430
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
435 440 445
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
450 455 460
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
465 470 475 480
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 324
<211> 498
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 324
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Glu Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr
35 40 45
Arg Phe Thr Ser Tyr Trp Ile Gly Trp Val Arg Gln Met Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Ser Ile Tyr Pro Asp Asp Ser Asp Thr Arg
65 70 75 80
Tyr Ser Pro Ser Phe Gln Gly Gln Val Thr Ile Ser Ala Asp Lys Ser
85 90 95
Ile Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Ser Ser Thr Val Asp Tyr Pro Gly Tyr Ser
115 120 125
Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Glu Leu Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser
165 170 175
Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Arg Ser
180 185 190
Asn Ile Gly Ser Asn Tyr Val Tyr Trp Tyr Gln Gln Leu Pro Gly Thr
195 200 205
Ala Pro Lys Leu Leu Ile Tyr Arg Asn Asn Gln Arg Pro Ser Gly Val
210 215 220
Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala
225 230 235 240
Ile Ser Gly Leu Arg Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ser
245 250 255
Trp Asp Gly Ser Leu Ser Ala Val Val Phe Gly Thr Gly Thr Lys Leu
260 265 270
Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
275 280 285
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
290 295 300
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
305 310 315 320
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
325 330 335
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
340 345 350
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
355 360 365
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
370 375 380
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
385 390 395 400
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
405 410 415
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
420 425 430
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
435 440 445
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
450 455 460
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
465 470 475 480
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
485 490 495
Pro Arg
<210> 325
<211> 499
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 325
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Glu Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr
35 40 45
Thr Phe Thr Asn Tyr Trp Ile Ala Trp Val Arg Gln Met Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Ile Ile Tyr Pro Asp Gly Ser Asp Thr Arg
65 70 75 80
Tyr Ser Pro Ser Phe Gln Gly Gln Val Thr Ile Ser Ala Asp Lys Ser
85 90 95
Ile Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Arg Asp Ile Thr Ser Trp Tyr Tyr Gly Glu
115 120 125
Pro Ala Phe Asp Ile Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
145 150 155 160
Gly Gly Gly Ser Glu Leu Gln Ser Val Leu Thr Gln Pro Pro Ser Ala
165 170 175
Ser Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser
180 185 190
Ser Asn Ile Gly Ser Asn Tyr Val Tyr Trp Tyr Gln Gln Leu Pro Gly
195 200 205
Thr Ala Pro Lys Leu Leu Ile Tyr Arg Asn Asn Gln Arg Pro Ser Gly
210 215 220
Val Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu
225 230 235 240
Ala Ile Ser Gly Leu Arg Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala
245 250 255
Thr Trp Asp Asp Ser Leu Gly Ser Pro Val Phe Gly Thr Gly Thr Lys
260 265 270
Leu Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
275 280 285
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
290 295 300
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
305 310 315 320
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
325 330 335
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
340 345 350
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
355 360 365
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
370 375 380
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
385 390 395 400
Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
405 410 415
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
420 425 430
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
435 440 445
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
450 455 460
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
465 470 475 480
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
485 490 495
Pro Pro Arg
<210> 326
<211> 496
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 326
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Glu Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr
35 40 45
Ser Phe Thr Ser Ser Trp Ile Gly Trp Val Arg Gln Met Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Ile Ile Tyr Pro Gly Asp Ser Asp Thr Arg
65 70 75 80
Tyr Ser Pro Ser Phe Gln Gly Gln Val Thr Ile Ser Ala Asp Lys Ser
85 90 95
Ile Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Lys Gly Leu Ser Gln Ala Met Thr Gly Phe
115 120 125
Gly Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Glu Leu Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
165 170 175
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
180 185 190
Ser Ile Ser Arg Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
195 200 205
Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ile Leu Gln Thr Gly Val Pro
210 215 220
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
225 230 235 240
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser
245 250 255
Tyr Ser Thr Thr Met Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile
260 265 270
Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
275 280 285
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
290 295 300
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
305 310 315 320
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
325 330 335
Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
340 345 350
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
355 360 365
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
370 375 380
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
385 390 395 400
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
405 410 415
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
420 425 430
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
435 440 445
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
450 455 460
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
465 470 475 480
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 327
<211> 499
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 327
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Glu Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr
35 40 45
Gly Phe Thr Ser Tyr Trp Ile Gly Trp Val Arg Gln Met Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Ile Ile His Pro Asp Asp Ser Asp Thr Lys
65 70 75 80
Tyr Ser Pro Ser Phe Gln Gly Gln Val Thr Ile Ser Ala Asp Lys Ser
85 90 95
Ile Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Ser Ser Tyr Leu Arg Gly Leu Trp Gly Gly
115 120 125
Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Glu Leu Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser
165 170 175
Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser
180 185 190
Asn Ile Gly Ser Asn Tyr Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr
195 200 205
Ala Pro Lys Leu Leu Ile Tyr Gly Asp Tyr Gln Arg Pro Ser Gly Val
210 215 220
Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala
225 230 235 240
Ile Ser Gly Leu Arg Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Thr
245 250 255
Arg Asp Asp Ser Leu Ser Gly Ser Val Val Phe Gly Thr Gly Thr Lys
260 265 270
Leu Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
275 280 285
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
290 295 300
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
305 310 315 320
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
325 330 335
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
340 345 350
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
355 360 365
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
370 375 380
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
385 390 395 400
Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
405 410 415
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
420 425 430
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
435 440 445
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
450 455 460
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
465 470 475 480
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
485 490 495
Pro Pro Arg
<210> 328
<211> 500
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 328
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Glu Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr
35 40 45
Thr Phe Pro Ser Ser Trp Ile Gly Trp Val Arg Gln Met Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Ile Ile Tyr Pro Asp Thr Ser His Thr Arg
65 70 75 80
Tyr Ser Pro Ser Phe Gln Gly Gln Val Thr Ile Ser Ala Asp Lys Ser
85 90 95
Ile Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Arg Ala Ser Tyr Phe Asp Arg Gly Thr Gly
115 120 125
Tyr Ser Ser Trp Trp Met Asp Val Trp Gly Gln Gly Thr Leu Val Thr
130 135 140
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Gly Gly Gly Gly Ser Glu Leu Asp Ile Gln Met Thr Gln Ser
165 170 175
Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys
180 185 190
Arg Ala Ser Gln Ser Ile Tyr Asp Tyr Leu His Trp Tyr Gln Gln Lys
195 200 205
Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Asp Ala Ser Asn Leu Gln
210 215 220
Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
225 230 235 240
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr
245 250 255
Cys Gln Gln Ser Tyr Thr Thr Pro Leu Phe Thr Phe Gly Gln Gly Thr
260 265 270
Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro
275 280 285
Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys
290 295 300
Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala
305 310 315 320
Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu
325 330 335
Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys
340 345 350
Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr
355 360 365
Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly
370 375 380
Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala
385 390 395 400
Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg
405 410 415
Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu
420 425 430
Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn
435 440 445
Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met
450 455 460
Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly
465 470 475 480
Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala
485 490 495
Leu Pro Pro Arg
500
<210> 329
<211> 497
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 329
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Gln Tyr Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Gly Gly Val Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Ser Asp Ile Ser Asp Ser Gly Gly Ser His
115 120 125
Trp Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
145 150 155 160
Gly Gly Gly Ser Glu Leu Asp Ile Gln Met Thr Gln Ser Pro Ser Ser
165 170 175
Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser
180 185 190
Gln Tyr Ile Gly Arg Tyr Leu Asn Trp Tyr Gln Gln Lys Arg Gly Lys
195 200 205
Ala Pro Lys Leu Leu Ile His Gly Ala Thr Ser Leu Ala Ser Gly Val
210 215 220
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
225 230 235 240
Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln
245 250 255
Ser Tyr Ser Thr Thr Ser Pro Thr Phe Gly Gln Gly Thr Lys Val Glu
260 265 270
Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
275 280 285
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
290 295 300
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
305 310 315 320
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
325 330 335
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
340 345 350
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
355 360 365
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
370 375 380
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
385 390 395 400
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
405 410 415
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
420 425 430
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
435 440 445
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
450 455 460
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
465 470 475 480
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
485 490 495
Arg
<210> 330
<211> 497
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 330
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Thr Ile Ser Gly Thr Gly Gly Thr Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Val Arg Ala Gly Ile Asp Pro Thr Ala
115 120 125
Ser Asp Val Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Glu Leu Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly
165 170 175
Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Thr Ser Asn
180 185 190
Ile Gly Arg Asn Tyr Val Tyr Trp Tyr Gln Gln Leu Pro Gly Thr Ala
195 200 205
Pro Lys Leu Leu Ile Tyr Arg Thr Asn Gln Arg Pro Ser Gly Val Pro
210 215 220
Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile
225 230 235 240
Ser Gly Leu Arg Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp
245 250 255
Asp Asp Ser Leu Ser Gly Arg Val Phe Gly Thr Gly Thr Lys Leu Thr
260 265 270
Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
275 280 285
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
290 295 300
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
305 310 315 320
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
325 330 335
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
340 345 350
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
355 360 365
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
370 375 380
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
385 390 395 400
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
405 410 415
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
420 425 430
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
435 440 445
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
450 455 460
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
465 470 475 480
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
485 490 495
Arg
<210> 331
<211> 500
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 331
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Asn Asn Phe Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Ser Gly Ser Gly Asp Asn Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Asp Arg Asp Ile Gly Leu Gly Trp Tyr
115 120 125
Ser Tyr Tyr Leu Asp Val Trp Gly Gln Gly Thr Leu Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Glu Leu Gln Ser Val Leu Thr Gln Pro Pro Ser
165 170 175
Ala Ser Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser
180 185 190
Ser Ser Asn Ile Gly Ser Asn Tyr Val Tyr Trp Tyr Gln Gln Leu Pro
195 200 205
Gly Thr Ala Pro Lys Pro Leu Ile Tyr Met Asn Asn Gln Arg Pro Ser
210 215 220
Gly Val Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser
225 230 235 240
Leu Ala Ile Ser Gly Leu Arg Ser Glu Asp Glu Ala Asp Tyr Tyr Cys
245 250 255
Ala Ala Trp Asp Asp Ser Leu Ser Ala Val Val Phe Gly Thr Gly Thr
260 265 270
Lys Leu Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro
275 280 285
Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys
290 295 300
Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala
305 310 315 320
Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu
325 330 335
Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys
340 345 350
Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr
355 360 365
Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly
370 375 380
Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala
385 390 395 400
Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg
405 410 415
Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu
420 425 430
Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn
435 440 445
Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met
450 455 460
Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly
465 470 475 480
Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala
485 490 495
Leu Pro Pro Arg
500
<210> 332
<211> 496
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 332
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly
35 40 45
Thr Phe Ser Ser Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Glu Ile Ile Pro Ile Phe Gly Thr Ala Ser
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Ala Gly Trp Asp Asp Ser Trp Phe Asp
115 120 125
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Glu Leu Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro
165 170 175
Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Asn Ser Asn Ile Gly
180 185 190
Thr Asn Tyr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys
195 200 205
Leu Leu Ile Tyr Arg Ser Ser Arg Arg Pro Ser Gly Val Pro Asp Arg
210 215 220
Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly
225 230 235 240
Leu Arg Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Gly
245 250 255
Ser Leu Ser Gly His Trp Val Phe Gly Thr Gly Thr Lys Leu Thr Val
260 265 270
Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
275 280 285
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
290 295 300
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
305 310 315 320
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
325 330 335
Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
340 345 350
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
355 360 365
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
370 375 380
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
385 390 395 400
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
405 410 415
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
420 425 430
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
435 440 445
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
450 455 460
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
465 470 475 480
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 333
<211> 496
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 333
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Glu Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr
35 40 45
Ser Phe Ala Ser Tyr Trp Ile Gly Trp Val Arg Gln Met Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Val Ile Tyr Pro Gly Thr Ser Glu Thr Arg
65 70 75 80
Tyr Ser Pro Ser Phe Gln Gly Gln Val Thr Ile Ser Ala Asp Lys Ser
85 90 95
Ile Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Lys Gly Leu Ser Ala Ser Ala Ser Gly Tyr
115 120 125
Ser Phe Gln Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Glu Leu Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
165 170 175
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
180 185 190
Ser Ile Asp Thr Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
195 200 205
Pro Lys Leu Leu Ile Tyr Ser Ala Ser Ser Leu His Ser Gly Val Pro
210 215 220
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
225 230 235 240
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser
245 250 255
Tyr Ser Thr Thr Ala Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile
260 265 270
Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
275 280 285
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
290 295 300
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
305 310 315 320
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
325 330 335
Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
340 345 350
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
355 360 365
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
370 375 380
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
385 390 395 400
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
405 410 415
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
420 425 430
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
435 440 445
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
450 455 460
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
465 470 475 480
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 334
<211> 497
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 334
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Glu Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr
35 40 45
Ser Phe Thr Asp Tyr Trp Ile Gly Trp Val Arg Gln Met Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Met Ile Ser Pro Gly Gly Ser Thr Thr Ile
65 70 75 80
Tyr Arg Pro Ser Phe Gln Gly Gln Val Thr Ile Ser Ala Asp Lys Ser
85 90 95
Ile Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Arg Glu Met Tyr Thr Gly Gly Tyr Gly Gly
115 120 125
Ser Trp Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Glu Leu Asp Ile Gln Met Thr Gln Ser Pro Ser
165 170 175
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
180 185 190
Ser Gln Ser Ile Gly Gln Ser Leu Asn Trp Tyr Gln Gln Lys Pro Gly
195 200 205
Lys Ala Pro Lys Leu Leu Ile Tyr Gly Ala Ser Ser Leu Gln Ser Gly
210 215 220
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
225 230 235 240
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln
245 250 255
Gln Ser Tyr Ser Thr Pro Ile Thr Phe Gly Gln Gly Thr Lys Val Glu
260 265 270
Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
275 280 285
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
290 295 300
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
305 310 315 320
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
325 330 335
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
340 345 350
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
355 360 365
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
370 375 380
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
385 390 395 400
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
405 410 415
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
420 425 430
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
435 440 445
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
450 455 460
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
465 470 475 480
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
485 490 495
Arg
<210> 335
<211> 193
<212> БЕЛОК
<213> Homo sapiens
<400> 335
Met Pro Glu Glu Gly Ser Gly Cys Ser Val Arg Arg Arg Pro Tyr Gly
1. 5 10 15
Cys Val Leu Arg Ala Ala Leu Val Pro Leu Val Ala Gly Leu Val Ile
20 25 30
Cys Leu Val Val Cys Ile Gln Arg Phe Ala Gln Ala Gln Gln Gln Leu
35 40 45
Pro Leu Glu Ser Leu Gly Trp Asp Val Ala Glu Leu Gln Leu Asn His
50 55 60
Thr Gly Pro Gln Gln Asp Pro Arg Leu Tyr Trp Gln Gly Gly Pro Ala
65 70 75 80
Leu Gly Arg Ser Phe Leu His Gly Pro Glu Leu Asp Lys Gly Gln Leu
85 90 95
Arg Ile His Arg Asp Gly Ile Tyr Met Val His Ile Gln Val Thr Leu
100 105 110
Ala Ile Cys Ser Ser Thr Thr Ala Ser Arg His His Pro Thr Thr Leu
115 120 125
Ala Val Gly Ile Cys Ser Pro Ala Ser Arg Ser Ile Ser Leu Leu Arg
130 135 140
Leu Ser Phe His Gln Gly Cys Thr Ile Ala Ser Gln Arg Leu Thr Pro
145 150 155 160
Leu Ala Arg Gly Asp Thr Leu Cys Thr Asn Leu Thr Gly Thr Leu Leu
165 170 175
Pro Ser Arg Asn Thr Asp Glu Thr Phe Phe Gly Val Gln Trp Val Arg
180 185 190
Pro
<210> 336
<211> 933
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<220>
<221> модифицированное_основание
<222> (793)..(793)
<223> a, c, t или g
<220>
<221> модифицированное_основание
<222> (797)..(797)
<223> a, c, t или g
<400> 336
atggctctcc cggtcacggc cctgctgctg cctctggcgc tgctcctgca cgcggcgcgc
60
ccgcaggtca ccttgaagga gtctggtcct gtgctggtga aacccacaga gaccctcacg
120
ctgacctgca ccgtctctgg gttctcactc agtaatgcta gaatgggtgt gacctggatc
180
cgtcagcccc cagggaaggc cctggagtgg cttgcacaca ttttttcgaa tgacgaaaaa
240
tcctacagta catctctgaa gagcaggctc accatctcca aggacacttc caaaacccag
300
gtggtcctta ccatgaccaa catggaccct gtggacacag ccacatatta ctgtgcacgg
360
atacgagatt actatgacat tagtagttat tatgactact ggggccaggg aaccctggtc
420
agcgtctcct caggcggagg cggttctggc ggaggtggca gcggtggtgg cggaagtggg
480
ggtggcggct ccgacatcca gatgacccag tctccatctg ccatgtctgc atctgtagga
540
gacagagtca ccatcacttg tcgggcgagt caggacatta gcaattattt agcctggttt
600
cagcagaaac cagggaaagt ccctaagcgc ctgatctatg ctgcatccag tttgcaaagt
660
ggggtcccat caaggttcag cggcagtgga tcggggacag aattcactct cacaatcagc
720
agcctgctgc ctgaagattt tgcaacttat tactgtctac agcttaatag tttcccgttc
780
acttttggcg ganggancaa ggtggagatc aacactacca caccagcacc tcgaccacca
840
actccagcac caaccattgc atcacagcca ctgagcctgc gaccagaggc ctgtagacct
900
gctgcaggag gagctgtgca tacccgagga ctg
933
<210> 337
<211> 948
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 337
atggctctcc cggtcacggc cctgctgctg cctctggcgc tgctcctgca cgcggcgcgc
60
ccggaagtgc agcttgtcca gagcggagcc gaagtgaaga agcctggcga gagcctgaag
120
atcagctgca agggctccgg atacggattc acaagttatt ggataggttg ggtgcgccag
180
atgcctggta agggactgga atggatgggt atcattcatc ccgatgatag cgacaccaaa
240
tacagcccaa gctttcaggg ccaggtcaca atcagcgctg acaagagcat cagcaccgcc
300
taccttcagt ggtcgtctct gaaggccagc gacaccgcaa tgtactactg tgcctctagc
360
tatttgcgtg gcttgtgggg aggctatttt gactattggg gccaaggtac actggtcacc
420
gtcagcagcg gcggaggcgg ttctggcgga ggtggcagcg gtggtggcgg aagtgggggt
480
ggcggctccg agctccagag cgtgctgacc cagcctccta gcgcaagcgg cacccctgga
540
cagcgtgtga caattagctg tagcggatca agctcaaaca ttggctcaaa ttatgtgaat
600
tggtatcagc aattgcccgg tacagcaccc aaactgctca tttatggaga ttatcaacga
660
cctagcggag tgcctgatcg ttttagcggt agcaaaagcg gcaccagcgc atcactggca
720
atttcaggcc tgcgtagcga agatgaggcg gattattact gtgctacccg cgacgattcg
780
ttatctgggt ctgtcgtttt tggcaccggt acaaaactga ccgtgctgac taccacacca
840
gcacctcgac caccaactcc agcaccaacc attgcatcac agccactgag cctgcgacca
900
gaggcctgta gacctgctgc aggaggagct gtgcataccc gaggactg
948
<210> 338
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 338
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Thr Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val Leu Ile
35 40 45
Tyr Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Ile Leu Thr Ile Asn Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Ser Tyr Tyr Cys Gln Gln Tyr Lys Ser Tyr Ser His
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 339
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 339
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1. 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Tyr Tyr
20 25 30
Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly His Ile Tyr Tyr Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Ile Asp Thr Ser Lys Asn Leu Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Ala Glu Gly Ser Leu Asp Ala Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 340
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 340
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val Leu Ile
35 40 45
Tyr Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Asn Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Lys Ser Phe Ser Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 341
<211> 113
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 341
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Ile Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Ser Asn
20 25 30
Tyr Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Val Ile Tyr Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Asn Trp Gly Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
100 105 110
Ser
<210> 342
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 342
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val Leu Ile
35 40 45
Tyr Lys Ala Ser Thr Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Ser Tyr
85 90 95
Thr Phe Gly His Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 343
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 343
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gly
1. 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Asp Tyr Tyr
20 25 30
Phe Trp Asn Trp Phe Arg Gln Ser Pro Val Lys Gly Leu Glu Trp Ile
35 40 45
Gly His Val Tyr Asp Ile Gly Asn Thr Lys Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Ile Asp Thr Ser Glu Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Asn Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Gly Glu Gly Ala Leu Asp Ala Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 344
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 344
Asp Ile Gln Met Thr Gln Ser Pro Ser Ile Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Val Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val Leu Ile
35 40 45
Tyr Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Thr Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Thr Tyr Ser His
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 345
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 345
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1. 5 10 15
Thr Leu Ser Leu Asn Cys Thr Val Ser Gly Gly Ser Ile Ser Tyr Tyr
20 25 30
Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly His Val Ile Tyr Ser Gly Thr Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Asn Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Val
85 90 95
Arg Ala Glu Gly Ser Leu Asp Ala Phe Asp Leu Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 346
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 346
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp
20 25 30
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Asn Tyr Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 347
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 347
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1. 5 10 15
Ser Leu Arg Leu Ser Cys Val Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Gly Ile His Trp Val Arg Gln Ala Pro Gly Met Gly Gln Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Ile Lys Lys Tyr Ser Asp Ser Val
50 55 60
Lys Gly Arg Phe Ile Ile Ser Arg Asp Asn Ser Glu Asn Thr Val Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Gly Glu Asp Thr Ala Ile Tyr Tyr Cys
85 90 95
Ala Arg Asp Glu Val Gly Thr Phe Gly Ala Phe Asp Phe Trp Gly Gln
100 105 110
Gly Thr Lys Val Thr Val Ser Ser
115 120
<210> 348
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 348
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Ser Ile Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Asp Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Thr Gly Lys Val Pro Lys Val Leu Ile
35 40 45
Tyr Ala Ala Ser Ala Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Asn Tyr Asn Ser Gly Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 349
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 349
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Leu Gln
1. 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Asp
20 25 30
Gly Tyr Tyr Trp Ser Trp Ile Arg Gln Asn Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Tyr Met Tyr Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Arg Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Thr Arg Asp Phe Gly Trp Tyr Phe Asp Leu Trp Gly Arg Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 350
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 350
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu Thr Trp Tyr Gln Gln Lys Pro Gly Arg Val Pro Glu Val Leu Ile
35 40 45
Tyr Ala Ala Ser Ala Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Asn Tyr Asn Ser Ala Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 351
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 351
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1. 5 10 15
Ser Leu Ser Leu Thr Cys Ser Val Ser Gly Gly Ser Val Ser Ser Asp
20 25 30
Gly Tyr Tyr Trp Ser Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Tyr Ile Tyr Tyr Arg Arg Ile Thr Asp Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Asn Ile Ser Leu Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Asp Phe Gly Trp Tyr Phe Asp Leu Trp Gly Arg Gly Thr
100 105 110
Leu Val Ala Val Ser Ser
115
<210> 352
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 352
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1. 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Val Leu Ile Leu Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Val Ser Ala Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Met Gln Ala Glu Asp Val Gly Ile Tyr Tyr Cys Met Gln Thr
85 90 95
Leu Gln Thr Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 353
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 353
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Leu His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Thr Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ile Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Gly Val Thr Met Ile Val Asp Gly Met Asp Asp Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 354
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 354
Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Ile Ile Thr Cys Arg Ala Ser Gln Gly Ile Asn Ser His
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Ser Thr Leu Pro Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Val Thr Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Leu Asn His Tyr Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Asp Ile Asn
100 105
<210> 355
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 355
Glu Val Glu Leu Val Glu Ser Gly Gly Gly Met Val Gln Pro Gly Arg
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Met Gly Leu Glu Trp Val
35 40 45
Thr Val Ile Trp Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Glu Val Gly Phe Val Gly Ala Phe Asp Ile Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 356
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 356
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Thr Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Lys Tyr Asn Ser Ala Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 357
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 357
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1. 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Asp
20 25 30
Gly Tyr Tyr Trp Ser Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Tyr Met Tyr Tyr Ser Gly Ile Thr Tyr His Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Asp Phe Gly Trp Tyr Phe Asp Leu Trp Gly Arg Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 358
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 358
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Thr Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Ala Tyr Tyr Cys Gln Lys Tyr Asn Ser Ala Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 359
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 359
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1. 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Asp
20 25 30
Ala Tyr Tyr Trp Ser Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Tyr Met Tyr Tyr Ser Gly Ile Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Asp Phe Gly Trp Tyr Phe Asp Leu Trp Gly Arg Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 360
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 360
Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Ser Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Ser Phe
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Val Leu Leu Ile
35 40 45
Tyr Val Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Val Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Leu His Val Tyr Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Arg
100 105
<210> 361
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 361
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1. 5 10 15
Ser Leu Arg Leu Ser Cys Val Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Gly Ile His Trp Val Arg Gln Ala Pro Gly Met Gly Gln Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Ile Lys Lys Tyr Ser Asp Ser Val
50 55 60
Lys Gly Arg Phe Ile Ile Ser Arg Asp Asn Ser Glu Asn Thr Val Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Gly Glu Asp Thr Ala Ile Tyr Tyr Cys
85 90 95
Ala Arg Asp Glu Val Gly Thr Phe Gly Ala Phe Asp Phe Trp Gly Gln
100 105 110
Gly Thr Lys Val Thr Val Ser Ser
115 120
<210> 362
<211> 113
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 362
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Pro Val Thr Pro Gly
1. 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Asp Asp Gly Asn Thr Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln
35 40 45
Ser Pro Gln Leu Leu Ile Tyr Thr Leu Ser Tyr Arg Ala Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys
65 70 75 80
Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln
85 90 95
Arg Ile Glu Phe Pro Phe Thr Phe Gly Pro Gly Thr Lys Val Asp Ile
100 105 110
Lys
<210> 363
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 363
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Lys Ser Lys Thr Gly Gly Gly Thr Thr Asp Tyr Ala Ala
50 55 60
Pro Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Thr Ser Leu Ile Val Gly Ala Ile Ser Leu Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 364
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 364
Asp Ile Gln Met Thr Gln Ser Pro Ser Ala Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Ala Ile Thr Cys Arg Ala Ser Gln Thr Ile Ser Thr Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val Leu Ile
35 40 45
Tyr Lys Ala Ser Asn Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Asn Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Gln Thr Phe Ser His
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 365
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 365
Gln Val Gln Leu Arg Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1. 5 10 15
Thr Leu Ser Leu Thr Cys Thr Ile Ser Gly Gly Ser Ile Ser Tyr Tyr
20 25 30
Phe Trp Thr Trp Ile Arg Gln Pro Pro Gly Arg Gly Leu Glu Trp Ile
35 40 45
Gly Gln Ile Tyr Tyr Ser Gly Asn Thr Asn Ser Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Ile Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Thr Ser Val Thr Val Ala Asp Thr Ala Val Tyr Tyr Cys Val
85 90 95
Arg Ala Glu Gly Ser Leu Asp Ala Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Ala Val Ser Ser
115
<210> 366
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 366
Asp Met Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Leu Thr Cys Arg Ala Ser Gln Gly Ile Ser Asn Tyr
20 25 30
Leu Ala Trp Phe Gln Leu Lys Pro Gly Lys Val Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Ala Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Lys Tyr Asn Ser Ala Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 367
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 367
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Val Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ser Met Asn Trp Val Arg Gln Phe Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Ser Thr Ser Ser Asn Tyr Ile His Tyr Ala Asp Ser Leu
50 55 60
Gln Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Val Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Arg Asp Lys Gly Thr Thr Leu Thr Asn Trp Tyr Phe Asp Leu Trp
100 105 110
Gly Arg Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 368
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 368
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1. 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Thr Leu Val His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asn Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Ser Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Met Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Ile Gln Thr Pro Tyr Thr Phe Gly Gln Gly Thr Asn Val Glu Ile Lys
100 105 110
<210> 369
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 369
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1. 5 10 15
Ser Leu Arg Leu Ser Cys Gly Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Leu
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Tyr Ser Gly Ser Ser Asp Ala Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 370
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 370
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val Leu Ile
35 40 45
Tyr Lys Ala Ser Asn Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Ser Cys
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 371
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 371
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Gln Pro Ser Glu
1. 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Tyr Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Asn Ile Asn Tyr Met Gly Asn Thr Ile Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asp Gln Phe Ser Leu
65 70 75 80
Lys Leu Thr Ser Val Ser Ala Ala Asp Thr Ala Val Tyr Tyr Cys Val
85 90 95
Arg Ala Glu Gly Ser Leu Asp Ala Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Leu Val Ala Val Ser Leu
115
<210> 372
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 372
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Ile Ile Phe Thr Cys Gln Ala Ser Gln Asp Ile Asn Asn Tyr
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asp Trp Glu Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Tyr Asp His Leu Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Val Glu Ile Lys
100 105
<210> 373
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 373
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Thr Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Gly Tyr
20 25 30
Tyr Ile Tyr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Ser Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Ala Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Lys Arg Glu Tyr Tyr Tyr Asn Phe Gly Met Asp Val
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Thr
115 120
<210> 374
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 374
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Ile Leu Thr Cys Gln Ala Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asp Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Ala Asp Phe Thr Phe Thr Ile Ser Asn Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asp His Leu Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 375
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 375
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Thr Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser His
20 25 30
Tyr Ile Tyr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Asp Arg Val Thr Met Ala Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Arg Lys Arg Glu Tyr Tyr Tyr Asn Phe Gly Met Asp Val
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ala
115 120
<210> 376
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 376
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Ile Leu Thr Cys Gln Ala Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asp Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Ala Asp Phe Thr Phe Thr Ile Ser Asn Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asp His Leu Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 377
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 377
Gln Val Gln Leu Val Gln Phe Gly Val Glu Val Arg Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Val Ser Gly Phe Thr Phe Thr Ser His
20 25 30
Tyr Ile Tyr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Lys Tyr Ala Gln Lys Phe
50 55 60
Gln Asp Arg Val Thr Met Ala Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ser Val Tyr Tyr Cys
85 90 95
Val Lys Asp Arg Lys Arg Glu Tyr Tyr Tyr Asn Phe Gly Met Asp Val
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 378
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 378
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Tyr Asp Asn Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 379
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 379
Glu Val Gln Met Leu Glu Ser Gly Gly Gly Leu Ile Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Lys Thr Ser Gly Phe Thr Leu Ser Ile Tyr
20 25 30
Ala Ile His Trp Val Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Ser Ser Phe Gly Gly Arg Gly Ser Ser Thr Tyr Phe Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Ala Ser Glu Asn Ser Leu Tyr
65 70 75 80
Leu His Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Glu Lys Asp Trp Gly Arg Gly Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 380
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 380
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1. 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu Tyr Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Phe Leu Asn Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Phe Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 381
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 381
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Ser Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Ser Ser Ser Thr Ile Tyr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Lys Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ile Gly Trp Glu Val Phe Thr Leu Gly Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Gln Val Thr Val Ser Ser
115 120
<210> 382
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 382
Tyr Tyr Tyr Trp Thr
1. 5
<210> 383
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 383
Gly Gly Ser Ile Ser Tyr Tyr
1. 5
<210> 384
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 384
Gly Gly Ser Ile Ser Tyr Tyr Tyr Trp Thr
1. 5 10
<210> 385
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 385
His Ile Tyr Tyr Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys Ser
1. 5 10 15
<210> 386
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 386
Tyr Tyr Ser Gly Ser
1. 5
<210> 387
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 387
Ala Glu Gly Ser Leu Asp Ala Phe Asp Phe
1. 5 10
<210> 388
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 388
Ser Asn Tyr Met Thr
1. 5
<210> 389
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 389
Gly Phe Thr Val Ser Ser Asn
1. 5
<210> 390
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 390
Gly Phe Thr Val Ser Ser Asn Tyr Met Thr
1. 5 10
<210> 391
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 391
Val Ile Tyr Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys Gly
1. 5 10 15
<210> 392
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 392
Tyr Ser Gly Gly Ser
1. 5
<210> 393
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 393
Asn Trp Gly Asp Tyr Trp
1. 5
<210> 394
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 394
Tyr Tyr Phe Trp Asn
1. 5
<210> 395
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 395
Gly Gly Ser Ile Asp Tyr Tyr
1. 5
<210> 396
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 396
Gly Gly Ser Ile Asp Tyr Tyr Phe Trp Asn
1. 5 10
<210> 397
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 397
His Val Tyr Asp Ile Gly Asn Thr Lys Tyr Asn Pro Ser Leu Lys Ser
1. 5 10 15
<210> 398
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 398
Tyr Asp Ile Gly Asn
1. 5
<210> 399
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 399
Gly Glu Gly Ala Leu Asp Ala Phe Asp Ile
1. 5 10
<210> 400
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 400
Tyr Tyr Tyr Trp Thr
1. 5
<210> 401
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 401
Gly Gly Ser Ile Ser Tyr Tyr
1. 5
<210> 402
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 402
Gly Gly Ser Ile Ser Tyr Tyr Tyr Trp Thr
1. 5 10
<210> 403
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 403
His Val Ile Tyr Ser Gly Thr Thr Asn Tyr Asn Pro Ser Leu Lys Ser
1. 5 10 15
<210> 404
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 404
Ile Tyr Ser Gly Thr
1. 5
<210> 405
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 405
Ala Glu Gly Ser Leu Asp Ala Phe Asp Leu
1. 5 10
<210> 406
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 406
Asp Tyr Gly Ile His
1. 5
<210> 407
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 407
Gly Phe Thr Phe Ser Asp Tyr
1. 5
<210> 408
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 408
Gly Phe Thr Phe Ser Asp Tyr Gly Ile His
1. 5 10
<210> 409
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 409
Val Ile Trp Tyr Asp Gly Ser Ile Lys Lys Tyr Ser Asp Ser Val Lys
1. 5 10 15
Gly
<210> 410
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 410
Trp Tyr Asp Gly Ser Ile
1. 5
<210> 411
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 411
Asp Glu Val Gly Thr Phe Gly Ala Phe Asp Phe
1. 5 10
<210> 412
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 412
Ser Asp Gly Tyr Tyr Trp Ser
1. 5
<210> 413
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 413
Gly Gly Ser Ile Ser Ser Asp Gly Tyr
1. 5
<210> 414
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 414
Gly Gly Ser Ile Ser Ser Asp Gly Tyr Tyr Trp Ser
1. 5 10
<210> 415
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 415
Tyr Met Tyr Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser
1. 5 10 15
<210> 416
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 416
Tyr Tyr Ser Gly Ser
1. 5
<210> 417
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 417
Asp Phe Gly Trp Tyr Phe Asp Leu
1. 5
<210> 418
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 418
Ser Asp Gly Tyr Tyr Trp Ser
1. 5
<210> 419
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 419
Gly Gly Ser Val Ser Ser Asp Gly Tyr
1. 5
<210> 420
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 420
Gly Gly Ser Val Ser Ser Asp Gly Tyr Tyr Trp Ser
1. 5 10
<210> 421
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 421
Tyr Ile Tyr Tyr Arg Arg Ile Thr Asp Tyr Asn Pro Ser Leu Lys Ser
1. 5 10 15
<210> 422
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 422
Tyr Tyr Arg Arg Ile
1. 5
<210> 423
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 423
Asp Phe Gly Trp Tyr Phe Asp Leu
1. 5
<210> 424
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 424
Gly Tyr Tyr Leu His
1. 5
<210> 425
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 425
Gly Tyr Thr Phe Thr Gly Tyr
1. 5
<210> 426
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 426
Gly Tyr Thr Phe Thr Gly Tyr Tyr Leu His
1. 5 10
<210> 427
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 427
Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln
1. 5 10 15
Gly
<210> 428
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 428
Asn Pro Asn Ser Gly Gly
1. 5
<210> 429
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 429
Asp Arg Gly Val Thr Met Ile Val Asp Gly Met Asp Asp
1. 5 10
<210> 430
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 430
Asp Tyr Gly Met His
1. 5
<210> 431
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 431
Gly Phe Thr Phe Ser Asp Tyr
1. 5
<210> 432
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 432
Gly Phe Thr Phe Ser Asp Tyr Gly Met His
1. 5 10
<210> 433
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 433
Val Ile Trp Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1. 5 10 15
Gly
<210> 434
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 434
Trp Tyr Asp Gly Ser Asn
1. 5
<210> 435
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 435
Asp Glu Val Gly Phe Val Gly Ala Phe Asp Ile
1. 5 10
<210> 436
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 436
Ser Asp Gly Tyr Tyr Trp Ser
1. 5
<210> 437
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 437
Gly Gly Ser Ile Ser Ser Asp Gly Tyr
1. 5
<210> 438
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 438
Gly Gly Ser Ile Ser Ser Asp Gly Tyr Tyr Trp Ser
1. 5 10
<210> 439
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 439
Tyr Met Tyr Tyr Ser Gly Ile Thr Tyr His Asn Pro Ser Leu Lys Ser
1. 5 10 15
<210> 440
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 440
Tyr Tyr Ser Gly Ile
1. 5
<210> 441
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 441
Asp Phe Gly Trp Tyr Phe Asp Leu
1. 5
<210> 442
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 442
Ser Asp Ala Tyr Tyr Trp Ser
1. 5
<210> 443
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 443
Gly Gly Ser Ile Ser Ser Asp Ala Tyr
1. 5
<210> 444
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 444
Gly Gly Ser Ile Ser Ser Asp Ala Tyr Tyr Trp Ser
1. 5 10
<210> 445
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 445
Tyr Met Tyr Tyr Ser Gly Ile Thr Tyr Tyr Asn Pro Ser Leu Lys Ser
1. 5 10 15
<210> 446
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 446
Tyr Tyr Ser Gly Ile
1. 5
<210> 447
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 447
Asp Phe Gly Trp Tyr Phe Asp Leu
1. 5
<210> 448
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 448
Asp Tyr Gly Ile His
1. 5
<210> 449
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 449
Gly Phe Thr Phe Ser Asp Tyr
1. 5
<210> 450
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 450
Gly Phe Thr Phe Ser Asp Tyr Gly Ile His
1. 5 10
<210> 451
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 451
Val Ile Trp Tyr Asp Gly Ser Ile Lys Lys Tyr Ser Asp Ser Val Lys
1. 5 10 15
Gly
<210> 452
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 452
Trp Tyr Asp Gly Ser Ile
1. 5
<210> 453
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 453
Asp Glu Val Gly Thr Phe Gly Ala Phe Asp Phe
1. 5 10
<210> 454
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 454
Asn Ala Trp Met Ser
1. 5
<210> 455
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 455
Gly Phe Thr Phe Ser Asn Ala
1. 5
<210> 456
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 456
Gly Phe Thr Phe Ser Asn Ala Trp Met Ser
1. 5 10
<210> 457
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 457
Arg Ile Lys Ser Lys Thr Gly Gly Gly Thr Thr Asp Tyr Ala Ala Pro
1. 5 10 15
Val Lys Gly
<210> 458
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 458
Lys Ser Lys Thr Gly Gly Gly Thr
1. 5
<210> 459
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 459
Leu Ile Val Gly Ala Ile Ser Leu Phe Asp Tyr
1. 5 10
<210> 460
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 460
Tyr Tyr Phe Trp Thr
1. 5
<210> 461
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 461
Gly Gly Ser Ile Ser Tyr Tyr
1. 5
<210> 462
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 462
Gly Gly Ser Ile Ser Tyr Tyr Phe Trp Thr
1. 5 10
<210> 463
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 463
Gln Ile Tyr Tyr Ser Gly Asn Thr Asn Ser Asn Pro Ser Leu Lys Ser
1. 5 10 15
<210> 464
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 464
Tyr Tyr Ser Gly Asn
1. 5
<210> 465
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 465
Ala Glu Gly Ser Leu Asp Ala Phe Asp Ile
1. 5 10
<210> 466
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 466
Ser Tyr Ser Met Asn
1. 5
<210> 467
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 467
Gly Phe Thr Phe Ser Ser Tyr
1. 5
<210> 468
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 468
Gly Phe Thr Phe Ser Ser Tyr Ser Met Asn
1. 5 10
<210> 469
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 469
Ser Ile Ser Thr Ser Ser Asn Tyr Ile His Tyr Ala Asp Ser Leu Gln
1. 5 10 15
Gly
<210> 470
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 470
Ser Thr Ser Ser Asn Tyr
1. 5
<210> 471
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 471
Asp Lys Gly Thr Thr Leu Thr Asn Trp Tyr Phe Asp Leu
1. 5 10
<210> 472
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 472
Ser Tyr Gly Met His
1. 5
<210> 473
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 473
Gly Phe Thr Phe Ser Ser Tyr
1. 5
<210> 474
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 474
Gly Phe Thr Phe Ser Ser Tyr Gly Met His
1. 5 10
<210> 475
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 475
Val Ile Trp Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Leu Lys
1. 5 10 15
Gly
<210> 476
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 476
Trp Tyr Asp Gly Ser Asn
1. 5
<210> 477
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 477
Asp Gly Tyr Ser Gly Ser Ser Asp Ala Phe Asp Ile
1. 5 10
<210> 478
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 478
Tyr Tyr Tyr Trp Ser
1. 5
<210> 479
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 479
Gly Gly Ser Ile Ser Tyr Tyr
1. 5
<210> 480
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 480
Gly Gly Ser Ile Ser Tyr Tyr Tyr Trp Ser
1. 5 10
<210> 481
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 481
Asn Ile Asn Tyr Met Gly Asn Thr Ile Tyr Asn Pro Ser Leu Lys Ser
1. 5 10 15
<210> 482
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 482
Asn Tyr Met Gly Asn
1. 5
<210> 483
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 483
Ala Glu Gly Ser Leu Asp Ala Phe Asp Phe
1. 5 10
<210> 484
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 484
Gly Tyr Tyr Ile Tyr
1. 5
<210> 485
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 485
Gly Tyr Ile Phe Thr Gly Tyr
1. 5
<210> 486
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 486
Gly Tyr Ile Phe Thr Gly Tyr Tyr Ile Tyr
1. 5 10
<210> 487
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 487
Trp Ile Asn Pro Ser Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln
1. 5 10 15
Gly
<210> 488
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 488
Asn Pro Ser Ser Gly Gly
1. 5
<210> 489
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 489
Asp Arg Lys Arg Glu Tyr Tyr Tyr Asn Phe Gly Met Asp Val
1. 5 10
<210> 490
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 490
Ser His Tyr Ile Tyr
1. 5
<210> 491
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 491
Gly Tyr Thr Phe Thr Ser His
1. 5
<210> 492
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 492
Gly Tyr Thr Phe Thr Ser His Tyr Ile Tyr
1. 5 10
<210> 493
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 493
Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln
1. 5 10 15
Asp
<210> 494
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 494
Asn Pro Asn Ser Gly Gly
1. 5
<210> 495
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 495
Asp Arg Lys Arg Glu Tyr Tyr Tyr Asn Phe Gly Met Asp Val
1. 5 10
<210> 496
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 496
Ser His Tyr Ile Tyr
1. 5
<210> 497
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 497
Gly Phe Thr Phe Thr Ser His
1. 5
<210> 498
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 498
Gly Phe Thr Phe Thr Ser His Tyr Ile Tyr
1. 5 10
<210> 499
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 499
Trp Ile Asn Pro Asn Ser Gly Gly Thr Lys Tyr Ala Gln Lys Phe Gln
1. 5 10 15
Asp
<210> 500
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 500
Asn Pro Asn Ser Gly Gly
1. 5
<210> 501
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 501
Asp Arg Lys Arg Glu Tyr Tyr Tyr Asn Phe Gly Met Asp Val
1. 5 10
<210> 502
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 502
Ile Tyr Ala Ile His
1. 5
<210> 503
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 503
Gly Phe Thr Leu Ser Ile Tyr
1. 5
<210> 504
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 504
Gly Phe Thr Leu Ser Ile Tyr Ala Ile His
1. 5 10
<210> 505
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 505
Ser Phe Gly Gly Arg Gly Ser Ser Thr Tyr Phe Ala Asp Ser Val Lys
1. 5 10 15
Gly
<210> 506
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 506
Gly Gly Arg Gly Ser Ser
1. 5
<210> 507
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 507
Glu Lys Asp Trp Gly Arg Gly Phe Asp Tyr
1. 5 10
<210> 508
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 508
Asn Tyr Ser Met Asn
1. 5
<210> 509
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 509
Gly Phe Thr Phe Ser Asn Tyr
1. 5
<210> 510
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 510
Gly Phe Thr Phe Ser Asn Tyr Ser Met Asn
1. 5 10
<210> 511
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 511
Ser Ile Ser Ser Ser Thr Ile Tyr Ile Tyr Tyr Ala Asp Ser Val Lys
1. 5 10 15
Gly
<210> 512
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 512
Ser Ser Ser Thr Ile Tyr
1. 5
<210> 513
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 513
Asp Ile Gly Trp Glu Val Phe Thr Leu Gly Phe Asp Tyr
1. 5 10
<210> 514
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 514
Arg Ala Ser Gln Ser Ile Ser Thr Trp Leu Ala
1. 5 10
<210> 515
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 515
Lys Ala Ser Ser Leu Glu Ser
1. 5
<210> 516
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 516
Gln Gln Tyr Lys Ser Tyr Ser His Thr
1. 5
<210> 517
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 517
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1. 5 10
<210> 518
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 518
Lys Ala Ser Ser Leu Glu Ser
1. 5
<210> 519
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 519
Gln Gln Tyr Lys Ser Phe Ser Leu Thr
1. 5
<210> 520
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 520
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1. 5 10
<210> 521
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 521
Lys Ala Ser Thr Leu Glu Ser
1. 5
<210> 522
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 522
Gln Gln Tyr Asn Ser Tyr Ser Tyr Thr
1. 5
<210> 523
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 523
Arg Ala Ser Gln Ser Val Ser Ser Trp Leu Ala
1. 5 10
<210> 524
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 524
Lys Ala Ser Ser Leu Glu Ser
1. 5
<210> 525
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 525
Gln Gln Tyr Asn Thr Tyr Ser His Thr
1. 5
<210> 526
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 526
Arg Ala Ser Gln Gly Ile Arg Asn Asp Leu Gly
1. 5 10
<210> 527
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 527
Ala Ala Ser Ser Leu Gln Ser
1. 5
<210> 528
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 528
Leu Gln Asp Tyr Asn Tyr Pro Phe Thr
1. 5
<210> 529
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 529
Arg Ala Ser Gln Asp Ile Asp Asn Tyr Leu Ala
1. 5 10
<210> 530
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 530
Ala Ala Ser Ala Leu Gln Ser
1. 5
<210> 531
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 531
Gln Asn Tyr Asn Ser Gly Pro Arg Thr
1. 5
<210> 532
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 532
Arg Ala Ser Gln Asp Ile Ser Asn Tyr Leu Thr
1. 5 10
<210> 533
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 533
Ala Ala Ser Ala Leu Gln Ser
1. 5
<210> 534
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 534
Gln Asn Tyr Asn Ser Ala Pro Arg Thr
1. 5
<210> 535
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 535
Arg Ser Ser Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr Leu Asp
1. 5 10 15
<210> 536
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 536
Leu Gly Ser Asn Arg Ala Ser
1. 5
<210> 537
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 537
Met Gln Thr Leu Gln Thr Pro Phe Thr
1. 5
<210> 538
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 538
Arg Ala Ser Gln Gly Ile Asn Ser His Leu Ala
1. 5 10
<210> 539
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 539
Tyr Ala Ser Thr Leu Pro Ser
1. 5
<210> 540
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 540
Gln Gln Leu Asn His Tyr Pro Ile Thr
1. 5
<210> 541
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 541
Arg Ala Ser Gln Gly Ile Ser Asn Tyr Leu Ala
1. 5 10
<210> 542
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 542
Ala Ala Ser Thr Leu His Ser
1. 5
<210> 543
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 543
Gln Lys Tyr Asn Ser Ala Pro Arg Thr
1. 5
<210> 544
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 544
Arg Ala Ser Gln Asp Ile Ser Asn Tyr Leu Ala
1. 5 10
<210> 545
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 545
Ala Ala Ser Thr Leu His Ser
1. 5
<210> 546
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 546
Gln Lys Tyr Asn Ser Ala Pro Arg Thr
1. 5
<210> 547
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 547
Arg Ala Ser Gln Asp Ile Ser Ser Phe Leu Ala
1. 5 10
<210> 548
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 548
Val Ala Ser Thr Leu Gln Ser
1. 5
<210> 549
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 549
Gln Gln Leu His Val Tyr Pro Ile Thr
1. 5
<210> 550
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 550
Arg Ser Ser Gln Ser Leu Leu Asp Ser Asp Asp Gly Asn Thr Tyr Leu
1. 5 10 15
Asp
<210> 551
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 551
Thr Leu Ser Tyr Arg Ala Ser
1. 5
<210> 552
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 552
Met Gln Arg Ile Glu Phe Pro Phe Thr
1. 5
<210> 553
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 553
Arg Ala Ser Gln Thr Ile Ser Thr Trp Leu Ala
1. 5 10
<210> 554
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 554
Lys Ala Ser Asn Leu Glu Ser
1. 5
<210> 555
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 555
Gln Gln Tyr Gln Thr Phe Ser His Thr
1. 5
<210> 556
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 556
Arg Ala Ser Gln Gly Ile Ser Asn Tyr Leu Ala
1. 5 10
<210> 557
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 557
Ala Ala Ser Thr Leu Gln Ser
1. 5
<210> 558
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 558
Gln Lys Tyr Asn Ser Ala Pro Leu Thr
1. 5
<210> 559
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 559
Arg Ser Ser Gln Thr Leu Val His Ser Asn Gly Tyr Asn Tyr Leu Asn
1. 5 10 15
<210> 560
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 560
Leu Gly Ser Asn Arg Ala Ser
1. 5
<210> 561
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 561
Met Gln Ala Ile Gln Thr Pro Tyr Thr
1. 5
<210> 562
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 562
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1. 5 10
<210> 563
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 563
Lys Ala Ser Asn Leu Glu Ser
1. 5
<210> 564
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 564
Gln Gln Tyr Asn Ser Tyr Ser Cys Thr
1. 5
<210> 565
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 565
Gln Ala Ser Gln Asp Ile Asn Asn Tyr Leu His
1. 5 10
<210> 566
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 566
Asp Ala Ser Asp Trp Glu Thr
1. 5
<210> 567
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 567
Gln Gln Tyr Asp His Leu Pro Ile Thr
1. 5
<210> 568
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 568
Gln Ala Ser Gln Asp Ile Ser Asn Tyr Leu His
1. 5 10
<210> 569
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 569
Asp Ala Ser Asp Leu Glu Thr
1. 5
<210> 570
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 570
Gln Gln Tyr Asp His Leu Pro Ile Thr
1. 5
<210> 571
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 571
Gln Ala Ser Gln Asp Ile Ser Asn Tyr Leu His
1. 5 10
<210> 572
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 572
Asp Ala Ser Asp Leu Glu Thr
1. 5
<210> 573
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 573
Gln Gln Tyr Asp His Leu Pro Ile Thr
1. 5
<210> 574
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 574
Gln Ala Ser Gln Asp Ile Ser Asn Tyr Leu Asn
1. 5 10
<210> 575
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 575
Asp Ala Ser Asn Leu Glu Thr
1. 5
<210> 576
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 576
Gln Gln Tyr Asp Asn Leu Pro Tyr Thr
1. 5
<210> 577
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 577
Arg Ser Ser Gln Ser Leu Leu Tyr Ser Asn Gly Tyr Asn Tyr Leu Asp
1. 5 10 15
<210> 578
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 578
Leu Asn Ser Asn Arg Ala Ser
1. 5
<210> 579
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 579
Met Gln Ala Leu Gln Thr Pro Leu Thr
1. 5
<210> 580
<211> 489
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 580
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Tyr Tyr Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly His Ile Tyr Tyr Ser Gly Ser Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Ile Asp Thr Ser Lys
85 90 95
Asn Leu Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Ala Glu Gly Ser Leu Asp Ala Phe Asp Phe
115 120 125
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Thr Trp Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val Leu Ile Tyr
195 200 205
Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Glu Phe Ile Leu Thr Ile Asn Ser Leu Gln Pro Asp
225 230 235 240
Asp Phe Ala Ser Tyr Tyr Cys Gln Gln Tyr Lys Ser Tyr Ser His Thr
245 250 255
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
325 330 335
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
340 345 350
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
355 360 365
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
370 375 380
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
385 390 395 400
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
405 410 415
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
420 425 430
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
435 440 445
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
450 455 460
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
465 470 475 480
Leu His Met Gln Ala Leu Pro Pro Arg
485
<210> 581
<211> 484
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 581
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Ile Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Val Ser Ser Asn Tyr Met Thr Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Val Ile Tyr Ser Gly Gly Ser Thr Tyr Tyr
65 70 75 80
Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys
85 90 95
Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Asn Trp Gly Asp Tyr Trp Gly Gln Gly Thr
115 120 125
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
145 150 155 160
Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
165 170 175
Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala Trp Tyr Gln Gln
180 185 190
Lys Pro Gly Lys Ala Pro Lys Val Leu Ile Tyr Lys Ala Ser Ser Leu
195 200 205
Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu
210 215 220
Phe Thr Leu Thr Ile Asn Ser Leu Gln Pro Asp Asp Phe Ala Thr Tyr
225 230 235 240
Tyr Cys Gln Gln Tyr Lys Ser Phe Ser Leu Thr Phe Gly Gln Gly Thr
245 250 255
Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro
260 265 270
Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys
275 280 285
Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala
290 295 300
Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu
305 310 315 320
Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys
325 330 335
Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr
340 345 350
Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly
355 360 365
Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala
370 375 380
Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg
385 390 395 400
Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu
405 410 415
Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn
420 425 430
Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met
435 440 445
Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly
450 455 460
Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala
465 470 475 480
Leu Pro Pro Arg
<210> 582
<211> 489
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 582
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gly Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Asp Tyr Tyr Phe Trp Asn Trp Phe Arg Gln Ser Pro Val Lys
50 55 60
Gly Leu Glu Trp Ile Gly His Val Tyr Asp Ile Gly Asn Thr Lys Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Ile Asp Thr Ser Glu
85 90 95
Asn Gln Phe Ser Leu Lys Leu Asn Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Gly Glu Gly Ala Leu Asp Ala Phe Asp Ile
115 120 125
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val Leu Ile Tyr
195 200 205
Lys Ala Ser Thr Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp
225 230 235 240
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Ser Tyr Thr
245 250 255
Phe Gly His Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
325 330 335
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
340 345 350
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
355 360 365
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
370 375 380
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
385 390 395 400
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
405 410 415
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
420 425 430
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
435 440 445
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
450 455 460
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
465 470 475 480
Leu His Met Gln Ala Leu Pro Pro Arg
485
<210> 583
<211> 489
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 583
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Asn Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Tyr Tyr Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly His Val Ile Tyr Ser Gly Thr Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Asn Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Val Arg Ala Glu Gly Ser Leu Asp Ala Phe Asp Leu
115 120 125
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Ile Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Val Ser Ser Trp Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val Leu Ile Tyr
195 200 205
Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Thr
210 215 220
Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser Asp
225 230 235 240
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Thr Tyr Ser His Thr
245 250 255
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
325 330 335
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
340 345 350
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
355 360 365
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
370 375 380
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
385 390 395 400
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
405 410 415
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
420 425 430
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
435 440 445
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
450 455 460
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
465 470 475 480
Leu His Met Gln Ala Leu Pro Pro Arg
485
<210> 584
<211> 491
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 584
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Val Ala Ser Gly Phe
35 40 45
Thr Phe Ser Asp Tyr Gly Ile His Trp Val Arg Gln Ala Pro Gly Met
50 55 60
Gly Gln Glu Trp Val Ala Val Ile Trp Tyr Asp Gly Ser Ile Lys Lys
65 70 75 80
Tyr Ser Asp Ser Val Lys Gly Arg Phe Ile Ile Ser Arg Asp Asn Ser
85 90 95
Glu Asn Thr Val Tyr Leu Gln Met Asn Ser Leu Arg Gly Glu Asp Thr
100 105 110
Ala Ile Tyr Tyr Cys Ala Arg Asp Glu Val Gly Thr Phe Gly Ala Phe
115 120 125
Asp Phe Trp Gly Gln Gly Thr Lys Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
165 170 175
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn
180 185 190
Asp Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
195 200 205
Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Asn Tyr Pro
245 250 255
Phe Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 585
<211> 489
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 585
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Leu Gln Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Ser Asp Gly Tyr Tyr Trp Ser Trp Ile Arg Gln Asn Pro
50 55 60
Gly Lys Gly Leu Glu Trp Ile Gly Tyr Met Tyr Tyr Ser Gly Ser Thr
65 70 75 80
Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr
85 90 95
Ser Lys Asn Gln Phe Ser Leu Lys Leu Arg Ser Val Thr Ala Ala Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Thr Arg Asp Phe Gly Trp Tyr Phe Asp Leu
115 120 125
Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp
165 170 175
Ser Ile Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Asp Asn Tyr Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Thr Gly Lys Val Pro Lys Val Leu Ile Tyr
195 200 205
Ala Ala Ser Ala Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
225 230 235 240
Asp Val Ala Thr Tyr Tyr Cys Gln Asn Tyr Asn Ser Gly Pro Arg Thr
245 250 255
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
325 330 335
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
340 345 350
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
355 360 365
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
370 375 380
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
385 390 395 400
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
405 410 415
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
420 425 430
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
435 440 445
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
450 455 460
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
465 470 475 480
Leu His Met Gln Ala Leu Pro Pro Arg
485
<210> 586
<211> 489
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 586
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Ser Leu Ser Leu Thr Cys Ser Val Ser Gly Gly
35 40 45
Ser Val Ser Ser Asp Gly Tyr Tyr Trp Ser Trp Ile Arg Gln His Pro
50 55 60
Gly Lys Gly Leu Glu Trp Ile Gly Tyr Ile Tyr Tyr Arg Arg Ile Thr
65 70 75 80
Asp Tyr Asn Pro Ser Leu Lys Ser Arg Val Asn Ile Ser Leu Asp Thr
85 90 95
Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Ala Arg Asp Phe Gly Trp Tyr Phe Asp Leu
115 120 125
Trp Gly Arg Gly Thr Leu Val Ala Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Asn Tyr Leu
180 185 190
Thr Trp Tyr Gln Gln Lys Pro Gly Arg Val Pro Glu Val Leu Ile Tyr
195 200 205
Ala Ala Ser Ala Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
225 230 235 240
Asp Val Ala Thr Tyr Tyr Cys Gln Asn Tyr Asn Ser Ala Pro Arg Thr
245 250 255
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
325 330 335
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
340 345 350
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
355 360 365
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
370 375 380
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
385 390 395 400
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
405 410 415
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
420 425 430
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
435 440 445
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
450 455 460
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
465 470 475 480
Leu His Met Gln Ala Leu Pro Pro Arg
485
<210> 587
<211> 498
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 587
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Gly Tyr Tyr Leu His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Ile Thr Thr Ala Tyr Met Glu Leu Ser Arg Leu Arg Ile Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Arg Gly Val Thr Met Ile Val Asp
115 120 125
Gly Met Asp Asp Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val
165 170 175
Thr Pro Gly Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu
180 185 190
Leu His Ser Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro
195 200 205
Gly Gln Ser Pro Gln Val Leu Ile Leu Leu Gly Ser Asn Arg Ala Ser
210 215 220
Gly Val Pro Asp Arg Val Ser Ala Ser Gly Ser Gly Thr Asp Phe Thr
225 230 235 240
Leu Lys Ile Ser Arg Met Gln Ala Glu Asp Val Gly Ile Tyr Tyr Cys
245 250 255
Met Gln Thr Leu Gln Thr Pro Phe Thr Phe Gly Gln Gly Thr Lys Leu
260 265 270
Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
275 280 285
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
290 295 300
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
305 310 315 320
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
325 330 335
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
340 345 350
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
355 360 365
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
370 375 380
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
385 390 395 400
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
405 410 415
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
420 425 430
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
435 440 445
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
450 455 460
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
465 470 475 480
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
485 490 495
Pro Arg
<210> 588
<211> 491
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 588
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Glu Leu Val Glu Ser Gly Gly Gly Met
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Asp Tyr Gly Met His Trp Val Arg Gln Ala Pro Gly Met
50 55 60
Gly Leu Glu Trp Val Thr Val Ile Trp Tyr Asp Gly Ser Asn Lys Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Val Phe Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Glu Val Gly Phe Val Gly Ala Phe
115 120 125
Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val
165 170 175
Gly Asp Arg Val Ile Ile Thr Cys Arg Ala Ser Gln Gly Ile Asn Ser
180 185 190
His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
195 200 205
Ile Tyr Tyr Ala Ser Thr Leu Pro Ser Gly Val Pro Ser Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Val Thr Ser Leu Gln
225 230 235 240
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Leu Asn His Tyr Pro
245 250 255
Ile Thr Phe Gly Gln Gly Thr Arg Leu Asp Ile Asn Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 589
<211> 489
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 589
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Ser Asp Gly Tyr Tyr Trp Ser Trp Ile Arg Gln His Pro
50 55 60
Gly Lys Gly Leu Glu Trp Ile Gly Tyr Met Tyr Tyr Ser Gly Ile Thr
65 70 75 80
Tyr His Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr
85 90 95
Ser Lys Asn Gln Phe Ser Leu Arg Leu Ser Ser Val Thr Ala Ala Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Ala Arg Asp Phe Gly Trp Tyr Phe Asp Leu
115 120 125
Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Asn Tyr Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu Ile Tyr
195 200 205
Ala Ala Ser Thr Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
225 230 235 240
Asp Val Ala Thr Tyr Tyr Cys Gln Lys Tyr Asn Ser Ala Pro Arg Thr
245 250 255
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
325 330 335
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
340 345 350
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
355 360 365
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
370 375 380
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
385 390 395 400
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
405 410 415
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
420 425 430
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
435 440 445
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
450 455 460
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
465 470 475 480
Leu His Met Gln Ala Leu Pro Pro Arg
485
<210> 590
<211> 489
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 590
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Ser Asp Ala Tyr Tyr Trp Ser Trp Ile Arg Gln His Pro
50 55 60
Gly Lys Gly Leu Glu Trp Ile Gly Tyr Met Tyr Tyr Ser Gly Ile Thr
65 70 75 80
Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr
85 90 95
Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Ala Arg Asp Phe Gly Trp Tyr Phe Asp Leu
115 120 125
Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Asn Tyr Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu Ile Tyr
195 200 205
Ala Ala Ser Thr Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp
225 230 235 240
Asp Phe Ala Ala Tyr Tyr Cys Gln Lys Tyr Asn Ser Ala Pro Arg Thr
245 250 255
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
325 330 335
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
340 345 350
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
355 360 365
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
370 375 380
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
385 390 395 400
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
405 410 415
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
420 425 430
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
435 440 445
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
450 455 460
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
465 470 475 480
Leu His Met Gln Ala Leu Pro Pro Arg
485
<210> 591
<211> 491
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 591
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Val Ala Ser Gly Phe
35 40 45
Thr Phe Ser Asp Tyr Gly Ile His Trp Val Arg Gln Ala Pro Gly Met
50 55 60
Gly Gln Glu Trp Val Ala Val Ile Trp Tyr Asp Gly Ser Ile Lys Lys
65 70 75 80
Tyr Ser Asp Ser Val Lys Gly Arg Phe Ile Ile Ser Arg Asp Asn Ser
85 90 95
Glu Asn Thr Val Tyr Leu Gln Met Asn Ser Leu Arg Gly Glu Asp Thr
100 105 110
Ala Ile Tyr Tyr Cys Ala Arg Asp Glu Val Gly Thr Phe Gly Ala Phe
115 120 125
Asp Phe Trp Gly Gln Gly Thr Lys Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val
165 170 175
Gly Asp Arg Val Ser Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Ser
180 185 190
Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Val Leu Leu
195 200 205
Ile Tyr Val Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Val Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Leu His Val Tyr Pro
245 250 255
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Arg Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 592
<211> 499
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 592
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Lys Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Asn Ala Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Gly Arg Ile Lys Ser Lys Thr Gly Gly Gly Thr
65 70 75 80
Thr Asp Tyr Ala Ala Pro Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
85 90 95
Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu
100 105 110
Asp Thr Ala Val Tyr Tyr Cys Thr Ser Leu Ile Val Gly Ala Ile Ser
115 120 125
Leu Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Pro Val
165 170 175
Thr Pro Gly Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu
180 185 190
Leu Asp Ser Asp Asp Gly Asn Thr Tyr Leu Asp Trp Tyr Leu Gln Lys
195 200 205
Pro Gly Gln Ser Pro Gln Leu Leu Ile Tyr Thr Leu Ser Tyr Arg Ala
210 215 220
Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
225 230 235 240
Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr
245 250 255
Cys Met Gln Arg Ile Glu Phe Pro Phe Thr Phe Gly Pro Gly Thr Lys
260 265 270
Val Asp Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
275 280 285
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
290 295 300
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
305 310 315 320
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
325 330 335
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
340 345 350
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
355 360 365
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
370 375 380
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
385 390 395 400
Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
405 410 415
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
420 425 430
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
435 440 445
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
450 455 460
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
465 470 475 480
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
485 490 495
Pro Pro Arg
<210> 593
<211> 489
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 593
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Arg Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Ile Ser Gly Gly
35 40 45
Ser Ile Ser Tyr Tyr Phe Trp Thr Trp Ile Arg Gln Pro Pro Gly Arg
50 55 60
Gly Leu Glu Trp Ile Gly Gln Ile Tyr Tyr Ser Gly Asn Thr Asn Ser
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Ile Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Thr Ser Val Thr Val Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Val Arg Ala Glu Gly Ser Leu Asp Ala Phe Asp Ile
115 120 125
Trp Gly Gln Gly Thr Met Val Ala Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Ala Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Ala Ile Thr Cys Arg Ala Ser Gln Thr Ile Ser Thr Trp Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val Leu Ile Tyr
195 200 205
Lys Ala Ser Asn Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Asn Ser Leu Gln Pro Asp
225 230 235 240
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Gln Thr Phe Ser His Thr
245 250 255
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
325 330 335
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
340 345 350
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
355 360 365
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
370 375 380
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
385 390 395 400
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
405 410 415
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
420 425 430
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
435 440 445
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
450 455 460
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
465 470 475 480
Leu His Met Gln Ala Leu Pro Pro Arg
485
<210> 594
<211> 493
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 594
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Lys Pro Gly Gly Ser Leu Arg Leu Ser Cys Val Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ser Met Asn Trp Val Arg Gln Phe Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ser Ile Ser Thr Ser Ser Asn Tyr Ile His
65 70 75 80
Tyr Ala Asp Ser Leu Gln Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Ser Ser Leu Arg Val Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Val Arg Asp Lys Gly Thr Thr Leu Thr Asn Trp
115 120 125
Tyr Phe Asp Leu Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Met Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala
165 170 175
Ser Val Gly Asp Arg Val Thr Leu Thr Cys Arg Ala Ser Gln Gly Ile
180 185 190
Ser Asn Tyr Leu Ala Trp Phe Gln Leu Lys Pro Gly Lys Val Pro Lys
195 200 205
Leu Leu Ile Tyr Ala Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Ala Leu Thr Ile Ser Ser
225 230 235 240
Leu Gln Pro Glu Asp Val Ala Thr Tyr Tyr Cys Gln Lys Tyr Asn Ser
245 250 255
Ala Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 595
<211> 497
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 595
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Gly Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Gly Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ala Val Ile Trp Tyr Asp Gly Ser Asn Lys Tyr
65 70 75 80
Tyr Ala Asp Ser Leu Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Gly Tyr Ser Gly Ser Ser Asp Ala
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr
165 170 175
Pro Gly Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Thr Leu Val
180 185 190
His Ser Asn Gly Tyr Asn Tyr Leu Asn Trp Tyr Leu Gln Lys Pro Gly
195 200 205
Gln Ser Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly
210 215 220
Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Ser Asp Phe Thr Leu
225 230 235 240
Lys Ile Ser Arg Met Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met
245 250 255
Gln Ala Ile Gln Thr Pro Tyr Thr Phe Gly Gln Gly Thr Asn Val Glu
260 265 270
Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
275 280 285
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
290 295 300
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
305 310 315 320
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
325 330 335
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
340 345 350
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
355 360 365
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
370 375 380
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
385 390 395 400
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
405 410 415
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
420 425 430
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
435 440 445
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
450 455 460
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
465 470 475 480
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
485 490 495
Arg
<210> 596
<211> 489
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 596
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Gln Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Tyr Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Asn Ile Asn Tyr Met Gly Asn Thr Ile Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asp Gln Phe Ser Leu Lys Leu Thr Ser Val Ser Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Val Arg Ala Glu Gly Ser Leu Asp Ala Phe Asp Phe
115 120 125
Trp Gly Gln Gly Thr Leu Val Ala Val Ser Leu Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val Leu Ile Tyr
195 200 205
Lys Ala Ser Asn Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp
225 230 235 240
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Ser Cys Thr
245 250 255
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
325 330 335
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
340 345 350
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
355 360 365
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
370 375 380
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
385 390 395 400
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
405 410 415
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
420 425 430
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
435 440 445
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
450 455 460
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
465 470 475 480
Leu His Met Gln Ala Leu Pro Pro Arg
485
<210> 597
<211> 494
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 597
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Thr Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Ile Phe Thr Gly Tyr Tyr Ile Tyr Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Ser Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Ala Arg Asp Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Arg Lys Arg Glu Tyr Tyr Tyr Asn
115 120 125
Phe Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Thr
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
145 150 155 160
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
165 170 175
Ala Ser Val Gly Asp Arg Ile Ile Phe Thr Cys Gln Ala Ser Gln Asp
180 185 190
Ile Asn Asn Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
195 200 205
Lys Leu Leu Ile Tyr Asp Ala Ser Asp Trp Glu Thr Gly Val Pro Ser
210 215 220
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser
225 230 235 240
Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Tyr Asp
245 250 255
His Leu Pro Ile Thr Phe Gly Gln Gly Thr Arg Val Glu Ile Lys Thr
260 265 270
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
275 280 285
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
290 295 300
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
305 310 315 320
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
325 330 335
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
340 345 350
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
355 360 365
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
370 375 380
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
385 390 395 400
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
405 410 415
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
420 425 430
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
435 440 445
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
450 455 460
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
465 470 475 480
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 598
<211> 494
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 598
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Thr Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser His Tyr Ile Tyr Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Asp Arg Val Thr Met Ala Arg Asp Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Asp Arg Lys Arg Glu Tyr Tyr Tyr Asn
115 120 125
Phe Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ala
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
145 150 155 160
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
165 170 175
Ala Ser Val Gly Asp Arg Val Ile Leu Thr Cys Gln Ala Ser Gln Asp
180 185 190
Ile Ser Asn Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
195 200 205
Lys Leu Leu Ile Tyr Asp Ala Ser Asp Leu Glu Thr Gly Val Pro Ser
210 215 220
Arg Phe Ser Gly Ser Gly Ser Gly Ala Asp Phe Thr Phe Thr Ile Ser
225 230 235 240
Asn Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asp
245 250 255
His Leu Pro Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Thr
260 265 270
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
275 280 285
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
290 295 300
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
305 310 315 320
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
325 330 335
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
340 345 350
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
355 360 365
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
370 375 380
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
385 390 395 400
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
405 410 415
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
420 425 430
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
435 440 445
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
450 455 460
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
465 470 475 480
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 599
<211> 494
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 599
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Phe Gly Val Glu Val
20 25 30
Arg Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Val Ser Gly Phe
35 40 45
Thr Phe Thr Ser His Tyr Ile Tyr Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Lys
65 70 75 80
Tyr Ala Gln Lys Phe Gln Asp Arg Val Thr Met Ala Arg Asp Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ser Val Tyr Tyr Cys Val Lys Asp Arg Lys Arg Glu Tyr Tyr Tyr Asn
115 120 125
Phe Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
145 150 155 160
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
165 170 175
Ala Ser Val Gly Asp Arg Val Ile Leu Thr Cys Gln Ala Ser Gln Asp
180 185 190
Ile Ser Asn Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
195 200 205
Lys Leu Leu Ile Tyr Asp Ala Ser Asp Leu Glu Thr Gly Val Pro Ser
210 215 220
Arg Phe Ser Gly Ser Gly Ser Gly Ala Asp Phe Thr Phe Thr Ile Ser
225 230 235 240
Asn Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asp
245 250 255
His Leu Pro Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Thr
260 265 270
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
275 280 285
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
290 295 300
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
305 310 315 320
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
325 330 335
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
340 345 350
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
355 360 365
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
370 375 380
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
385 390 395 400
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
405 410 415
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
420 425 430
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
435 440 445
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
450 455 460
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
465 470 475 480
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 600
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 600
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Met Leu Glu Ser Gly Gly Gly Leu
20 25 30
Ile Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Lys Thr Ser Gly Phe
35 40 45
Thr Leu Ser Ile Tyr Ala Ile His Trp Val Arg Gln Ala Pro Gly Arg
50 55 60
Gly Leu Glu Trp Val Ser Ser Phe Gly Gly Arg Gly Ser Ser Thr Tyr
65 70 75 80
Phe Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Ala Ser
85 90 95
Glu Asn Ser Leu Tyr Leu His Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Glu Lys Asp Trp Gly Arg Gly Phe Asp
115 120 125
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
165 170 175
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Asp Ile Ser Asn Tyr
180 185 190
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
195 200 205
Tyr Asp Ala Ser Asn Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Gln Pro
225 230 235 240
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Tyr Asp Asn Leu Pro Tyr
245 250 255
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 601
<211> 498
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетическая
конструкция
<400> 601
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Lys Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Asn Tyr Ser Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ser Ile Ser Ser Ser Thr Ile Tyr Ile Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Lys Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Ile Gly Trp Glu Val Phe Thr Leu
115 120 125
Gly Phe Asp Tyr Trp Gly Gln Gly Thr Gln Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val
165 170 175
Thr Pro Gly Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu
180 185 190
Leu Tyr Ser Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro
195 200 205
Gly Gln Ser Pro Gln Leu Leu Ile Phe Leu Asn Ser Asn Arg Ala Ser
210 215 220
Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
225 230 235 240
Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Phe Cys
245 250 255
Met Gln Ala Leu Gln Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val
260 265 270
Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
275 280 285
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
290 295 300
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
305 310 315 320
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
325 330 335
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
340 345 350
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
355 360 365
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
370 375 380
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
385 390 395 400
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
405 410 415
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
420 425 430
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
435 440 445
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
450 455 460
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
465 470 475 480
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
485 490 495
Pro Arg
<210> 602
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 602
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1. 5 10 15
Gly Gly Gly Ser
20
<210> 603
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 603
Cys Gln Phe Asp Leu Ser Thr Arg Arg Leu Lys Cys
1. 5 10
<210> 604
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 604
Cys Gln Tyr Asn Leu Ser Ser Arg Ala Leu Lys Cys
1. 5 10
<210> 605
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 605
Cys Val Trp Gln Arg Trp Gln Lys Ser Tyr Val Cys
1. 5 10
<210> 606
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 606
Cys Met Trp Asp Arg Phe Ser Arg Trp Tyr Lys Cys
1. 5 10
<210> 607
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 607
Ser Phe Val Leu Asn Trp Tyr Arg Met Ser Pro Ser Asn Gln Thr Asp
1. 5 10 15
Lys Leu Ala Ala Phe Pro Glu Asp Arg
20 25
<210> 608
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 608
Ser Gly Thr Tyr Leu Cys Gly Ala Ile Ser Leu Ala Pro Lys Ala Gln
1. 5 10 15
Ile Lys Glu
<210> 609
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 609
Glu Leu Pro Thr Gln Gly Thr Phe Ser Asn Val Ser Thr Asn Val Ser
1. 5 10 15
<210> 610
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 610
Gly Gln Asn Asp Thr Ser Gln Thr Ser Ser Pro Ser
1. 5 10
<210> 611
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 611
Met Gly Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1. 5 10 15
Asp His Ala Asp Ala
20
<210> 612
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 612
Gly Ser Thr Ser Gly Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr
1. 5 10 15
Lys Gly
<210> 613
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> ИНАЯ ХАРАКТЕРИСТИКА
<222> (1)..(25)
<223> Данная последовательность может охватывать 1-5 повторяющихся
звеньев «Gly Gly Gly Gly Ser»
<400> 613
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1. 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser
20 25
<210> 614
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 614
Ser Gly Gly Gly Gly
1. 5
<210> 615
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 615
Gly Gly Gly Gly Ser
1. 5
<210> 616
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 616
Ser Gly Gly Gly Gly Ser
1. 5
<210> 617
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 617
Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly
1. 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser
20 25
<210> 618
<211> 55
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 618
Gly Ser Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys
1. 5 10 15
Ser Gly Gly Gly Gly Ser Glu Leu Pro Thr Gln Gly Thr Phe Ser Asn
20 25 30
Val Ser Thr Asn Val Ser Pro Ala Lys Pro Thr Thr Thr Ala Cys Pro
35 40 45
Tyr Ser Asn Pro Ser Leu Cys
50 55
<210> 619
<211> 489
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 619
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Thr Leu Lys Glu Ser Gly Pro Val Leu
20 25 30
Val Lys Pro Thr Glu Thr Leu Thr Leu Thr Cys Thr Val Ser Gly Phe
35 40 45
Ser Leu Ser Asn Ala Arg Met Gly Val Thr Trp Ile Arg Gln Pro Pro
50 55 60
Gly Lys Ala Leu Glu Trp Leu Ala His Ile Phe Ser Asn Asp Glu Lys
65 70 75 80
Ser Tyr Ser Thr Ser Leu Lys Ser Arg Leu Thr Ile Ser Lys Asp Thr
85 90 95
Ser Lys Thr Gln Val Val Leu Thr Met Thr Asn Met Asp Pro Val Asp
100 105 110
Thr Ala Thr Tyr Tyr Cys Ala Arg Ile Arg Asp Tyr Tyr Asp Ile Ser
115 120 125
Ser Tyr Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Ser Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Ala Met Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Asn Tyr Leu
180 185 190
Ala Trp Phe Gln Gln Lys Pro Gly Lys Val Pro Lys Arg Leu Ile Tyr
195 200 205
Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Leu Pro Glu
225 230 235 240
Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Leu Asn Ser Phe Pro Phe Thr
245 250 255
Phe Gly Gly Gly Thr Lys Val Glu Ile Asn Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
325 330 335
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
340 345 350
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
355 360 365
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
370 375 380
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
385 390 395 400
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
405 410 415
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
420 425 430
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
435 440 445
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
450 455 460
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
465 470 475 480
Leu His Met Gln Ala Leu Pro Pro Arg
485
<210> 620
<211> 526
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 620
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Thr Leu Lys Glu Ser Gly Pro Val Leu
20 25 30
Val Lys Pro Thr Glu Thr Leu Thr Leu Thr Cys Thr Val Ser Gly Phe
35 40 45
Ser Leu Ser Asn Ala Arg Met Gly Val Thr Trp Ile Arg Gln Pro Pro
50 55 60
Gly Lys Ala Leu Glu Trp Leu Ala His Ile Phe Ser Asn Asp Glu Lys
65 70 75 80
Ser Tyr Ser Thr Ser Leu Lys Ser Arg Leu Thr Ile Ser Lys Asp Thr
85 90 95
Ser Lys Thr Gln Val Val Leu Thr Met Thr Asn Met Asp Pro Val Asp
100 105 110
Thr Ala Thr Tyr Tyr Cys Ala Arg Ile Arg Asp Tyr Tyr Asp Ile Ser
115 120 125
Ser Tyr Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Ser Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Ala Met Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Asn Tyr Leu
180 185 190
Ala Trp Phe Gln Gln Lys Pro Gly Lys Val Pro Lys Arg Leu Ile Tyr
195 200 205
Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Leu Pro Glu
225 230 235 240
Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Leu Asn Ser Phe Pro Phe Thr
245 250 255
Phe Gly Gly Gly Thr Lys Val Glu Ile Asn Gly Ser Gly Gly Gly Gly
260 265 270
Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser
275 280 285
Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser Thr
290 295 300
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
305 310 315 320
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
325 330 335
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
340 345 350
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
355 360 365
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
370 375 380
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
385 390 395 400
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
405 410 415
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
420 425 430
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
435 440 445
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
450 455 460
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
465 470 475 480
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
485 490 495
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
500 505 510
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520 525
<210> 621
<211> 536
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 621
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Glu Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr
35 40 45
Gly Phe Thr Ser Tyr Trp Ile Gly Trp Val Arg Gln Met Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Ile Ile His Pro Asp Asp Ser Asp Thr Lys
65 70 75 80
Tyr Ser Pro Ser Phe Gln Gly Gln Val Thr Ile Ser Ala Asp Lys Ser
85 90 95
Ile Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Ser Ser Tyr Leu Arg Gly Leu Trp Gly Gly
115 120 125
Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Glu Leu Gln Ser Val Leu Thr Gln Pro Pro Ser Ala Ser
165 170 175
Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser
180 185 190
Asn Ile Gly Ser Asn Tyr Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr
195 200 205
Ala Pro Lys Leu Leu Ile Tyr Gly Asp Tyr Gln Arg Pro Ser Gly Val
210 215 220
Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala
225 230 235 240
Ile Ser Gly Leu Arg Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Thr
245 250 255
Arg Asp Asp Ser Leu Ser Gly Ser Val Val Phe Gly Thr Gly Thr Lys
260 265 270
Leu Thr Val Leu Gly Ser Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn
275 280 285
Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
290 295 300
Ser Leu Cys Ser Gly Gly Gly Gly Ser Thr Thr Thr Pro Ala Pro Arg
305 310 315 320
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
325 330 335
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
340 345 350
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
355 360 365
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg
370 375 380
Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro
385 390 395 400
Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu
405 410 415
Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala
420 425 430
Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
435 440 445
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
450 455 460
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
465 470 475 480
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
485 490 495
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
500 505 510
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
515 520 525
His Met Gln Ala Leu Pro Pro Arg
530 535
<210> 622
<211> 526
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 622
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Tyr Tyr Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly His Ile Tyr Tyr Ser Gly Ser Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Ile Asp Thr Ser Lys
85 90 95
Asn Leu Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Ala Glu Gly Ser Leu Asp Ala Phe Asp Phe
115 120 125
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Thr Trp Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val Leu Ile Tyr
195 200 205
Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Glu Phe Ile Leu Thr Ile Asn Ser Leu Gln Pro Asp
225 230 235 240
Asp Phe Ala Ser Tyr Tyr Cys Gln Gln Tyr Lys Ser Tyr Ser His Thr
245 250 255
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Ser Gly Gly Gly Gly
260 265 270
Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser
275 280 285
Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser Thr
290 295 300
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
305 310 315 320
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
325 330 335
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
340 345 350
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
355 360 365
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
370 375 380
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
385 390 395 400
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
405 410 415
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
420 425 430
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
435 440 445
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
450 455 460
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
465 470 475 480
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
485 490 495
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
500 505 510
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520 525
<210> 623
<211> 526
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 623
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Asn Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Tyr Tyr Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly His Val Ile Tyr Ser Gly Thr Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Asn Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Val Arg Ala Glu Gly Ser Leu Asp Ala Phe Asp Leu
115 120 125
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Ile Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Val Ser Ser Trp Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val Leu Ile Tyr
195 200 205
Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Thr
210 215 220
Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser Asp
225 230 235 240
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Thr Tyr Ser His Thr
245 250 255
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Ser Gly Gly Gly Gly
260 265 270
Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser
275 280 285
Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser Thr
290 295 300
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
305 310 315 320
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
325 330 335
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
340 345 350
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
355 360 365
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
370 375 380
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
385 390 395 400
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
405 410 415
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
420 425 430
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
435 440 445
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
450 455 460
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
465 470 475 480
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
485 490 495
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
500 505 510
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520 525
<210> 624
<211> 526
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 624
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Leu Gln Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Ser Asp Gly Tyr Tyr Trp Ser Trp Ile Arg Gln Asn Pro
50 55 60
Gly Lys Gly Leu Glu Trp Ile Gly Tyr Met Tyr Tyr Ser Gly Ser Thr
65 70 75 80
Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr
85 90 95
Ser Lys Asn Gln Phe Ser Leu Lys Leu Arg Ser Val Thr Ala Ala Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Thr Arg Asp Phe Gly Trp Tyr Phe Asp Leu
115 120 125
Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp
165 170 175
Ser Ile Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Asp Asn Tyr Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Thr Gly Lys Val Pro Lys Val Leu Ile Tyr
195 200 205
Ala Ala Ser Ala Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
225 230 235 240
Asp Val Ala Thr Tyr Tyr Cys Gln Asn Tyr Asn Ser Gly Pro Arg Thr
245 250 255
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Ser Gly Gly Gly Gly
260 265 270
Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser
275 280 285
Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser Thr
290 295 300
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
305 310 315 320
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
325 330 335
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
340 345 350
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
355 360 365
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
370 375 380
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
385 390 395 400
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
405 410 415
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
420 425 430
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
435 440 445
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
450 455 460
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
465 470 475 480
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
485 490 495
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
500 505 510
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520 525
<210> 625
<211> 526
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 625
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Ser Leu Ser Leu Thr Cys Ser Val Ser Gly Gly
35 40 45
Ser Val Ser Ser Asp Gly Tyr Tyr Trp Ser Trp Ile Arg Gln His Pro
50 55 60
Gly Lys Gly Leu Glu Trp Ile Gly Tyr Ile Tyr Tyr Arg Arg Ile Thr
65 70 75 80
Asp Tyr Asn Pro Ser Leu Lys Ser Arg Val Asn Ile Ser Leu Asp Thr
85 90 95
Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Ala Arg Asp Phe Gly Trp Tyr Phe Asp Leu
115 120 125
Trp Gly Arg Gly Thr Leu Val Ala Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Asn Tyr Leu
180 185 190
Thr Trp Tyr Gln Gln Lys Pro Gly Arg Val Pro Glu Val Leu Ile Tyr
195 200 205
Ala Ala Ser Ala Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
225 230 235 240
Asp Val Ala Thr Tyr Tyr Cys Gln Asn Tyr Asn Ser Ala Pro Arg Thr
245 250 255
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Ser Gly Gly Gly Gly
260 265 270
Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser
275 280 285
Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser Thr
290 295 300
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
305 310 315 320
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
325 330 335
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
340 345 350
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
355 360 365
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
370 375 380
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
385 390 395 400
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
405 410 415
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
420 425 430
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
435 440 445
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
450 455 460
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
465 470 475 480
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
485 490 495
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
500 505 510
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520 525
<210> 626
<211> 528
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 626
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Glu Leu Val Glu Ser Gly Gly Gly Met
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Asp Tyr Gly Met His Trp Val Arg Gln Ala Pro Gly Met
50 55 60
Gly Leu Glu Trp Val Thr Val Ile Trp Tyr Asp Gly Ser Asn Lys Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Val Phe Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Glu Val Gly Phe Val Gly Ala Phe
115 120 125
Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val
165 170 175
Gly Asp Arg Val Ile Ile Thr Cys Arg Ala Ser Gln Gly Ile Asn Ser
180 185 190
His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
195 200 205
Ile Tyr Tyr Ala Ser Thr Leu Pro Ser Gly Val Pro Ser Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Val Thr Ser Leu Gln
225 230 235 240
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Leu Asn His Tyr Pro
245 250 255
Ile Thr Phe Gly Gln Gly Thr Arg Leu Asp Ile Asn Gly Ser Gly Gly
260 265 270
Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly
275 280 285
Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly
290 295 300
Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
305 310 315 320
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
325 330 335
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
340 345 350
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
355 360 365
Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
370 375 380
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
385 390 395 400
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
405 410 415
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
420 425 430
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
435 440 445
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
450 455 460
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
465 470 475 480
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
485 490 495
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
500 505 510
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520 525
<210> 627
<211> 526
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 627
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Gln Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Tyr Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Asn Ile Asn Tyr Met Gly Asn Thr Ile Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asp Gln Phe Ser Leu Lys Leu Thr Ser Val Ser Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Val Arg Ala Glu Gly Ser Leu Asp Ala Phe Asp Phe
115 120 125
Trp Gly Gln Gly Thr Leu Val Ala Val Ser Leu Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val Leu Ile Tyr
195 200 205
Lys Ala Ser Asn Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp
225 230 235 240
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Ser Cys Thr
245 250 255
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Ser Gly Gly Gly Gly
260 265 270
Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser
275 280 285
Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser Thr
290 295 300
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
305 310 315 320
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
325 330 335
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
340 345 350
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
355 360 365
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
370 375 380
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
385 390 395 400
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
405 410 415
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
420 425 430
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
435 440 445
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
450 455 460
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
465 470 475 480
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
485 490 495
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
500 505 510
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520 525
<210> 628
<211> 569
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 628
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val
35 40 45
Thr Leu Lys Glu Ser Gly Pro Val Leu Val Lys Pro Thr Glu Thr Leu
50 55 60
Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Asn Ala Arg Met
65 70 75 80
Gly Val Thr Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu Trp Leu
85 90 95
Ala His Ile Phe Ser Asn Asp Glu Lys Ser Tyr Ser Thr Ser Leu Lys
100 105 110
Ser Arg Leu Thr Ile Ser Lys Asp Thr Ser Lys Thr Gln Val Val Leu
115 120 125
Thr Met Thr Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Tyr Cys Ala
130 135 140
Arg Ile Arg Asp Tyr Tyr Asp Ile Ser Ser Tyr Tyr Asp Tyr Trp Gly
145 150 155 160
Gln Gly Thr Leu Val Ser Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
165 170 175
Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro
180 185 190
Ser Ala Met Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg
195 200 205
Ala Ser Gln Asp Ile Ser Asn Tyr Leu Ala Trp Phe Gln Gln Lys Pro
210 215 220
Gly Lys Val Pro Lys Arg Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser
225 230 235 240
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr
245 250 255
Leu Thr Ile Ser Ser Leu Leu Pro Glu Asp Phe Ala Thr Tyr Tyr Cys
260 265 270
Leu Gln Leu Asn Ser Phe Pro Phe Thr Phe Gly Gly Gly Thr Lys Val
275 280 285
Glu Ile Asn Gly Ser Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
290 295 300
Ser Leu Cys Ser Gly Gly Gly Gly Ser Glu Leu Pro Thr Gln Gly Thr
305 310 315 320
Phe Ser Asn Val Ser Thr Asn Val Ser Pro Ala Lys Pro Thr Thr Thr
325 330 335
Ala Cys Pro Tyr Ser Asn Pro Ser Leu Cys Thr Thr Thr Pro Ala Pro
340 345 350
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
355 360 365
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
370 375 380
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
385 390 395 400
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
405 410 415
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
420 425 430
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
435 440 445
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
450 455 460
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
465 470 475 480
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
485 490 495
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
500 505 510
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
515 520 525
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
530 535 540
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
545 550 555 560
Leu His Met Gln Ala Leu Pro Pro Arg
565
<210> 629
<211> 579
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 629
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val
35 40 45
Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu Ser Leu
50 55 60
Lys Ile Ser Cys Lys Gly Ser Gly Tyr Gly Phe Thr Ser Tyr Trp Ile
65 70 75 80
Gly Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met Gly Ile
85 90 95
Ile His Pro Asp Asp Ser Asp Thr Lys Tyr Ser Pro Ser Phe Gln Gly
100 105 110
Gln Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr Leu Gln
115 120 125
Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys Ala Ser
130 135 140
Ser Tyr Leu Arg Gly Leu Trp Gly Gly Tyr Phe Asp Tyr Trp Gly Gln
145 150 155 160
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
165 170 175
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Leu Gln Ser
180 185 190
Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln Arg Val
195 200 205
Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn Tyr Val
210 215 220
Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu Ile Tyr
225 230 235 240
Gly Asp Tyr Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser Gly Ser
245 250 255
Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Arg Ser Glu
260 265 270
Asp Glu Ala Asp Tyr Tyr Cys Ala Thr Arg Asp Asp Ser Leu Ser Gly
275 280 285
Ser Val Val Phe Gly Thr Gly Thr Lys Leu Thr Val Leu Gly Ser Gly
290 295 300
Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly
305 310 315 320
Gly Gly Ser Glu Leu Pro Thr Gln Gly Thr Phe Ser Asn Val Ser Thr
325 330 335
Asn Val Ser Pro Ala Lys Pro Thr Thr Thr Ala Cys Pro Tyr Ser Asn
340 345 350
Pro Ser Leu Cys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
355 360 365
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
370 375 380
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
385 390 395 400
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
405 410 415
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
420 425 430
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
435 440 445
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
450 455 460
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
465 470 475 480
Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
485 490 495
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
500 505 510
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
515 520 525
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
530 535 540
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
545 550 555 560
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
565 570 575
Pro Pro Arg
<210> 630
<211> 569
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 630
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val
35 40 45
Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu
50 55 60
Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Tyr Tyr Tyr Trp
65 70 75 80
Thr Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly His
85 90 95
Ile Tyr Tyr Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys Ser Arg
100 105 110
Val Thr Ile Ser Ile Asp Thr Ser Lys Asn Leu Phe Ser Leu Lys Leu
115 120 125
Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ala
130 135 140
Glu Gly Ser Leu Asp Ala Phe Asp Phe Trp Gly Gln Gly Thr Met Val
145 150 155 160
Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
165 170 175
Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro
180 185 190
Ser Thr Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg
195 200 205
Ala Ser Gln Ser Ile Ser Thr Trp Leu Ala Trp Tyr Gln Gln Lys Pro
210 215 220
Gly Lys Ala Pro Lys Val Leu Ile Tyr Lys Ala Ser Ser Leu Glu Ser
225 230 235 240
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Ile
245 250 255
Leu Thr Ile Asn Ser Leu Gln Pro Asp Asp Phe Ala Ser Tyr Tyr Cys
260 265 270
Gln Gln Tyr Lys Ser Tyr Ser His Thr Phe Gly Gln Gly Thr Lys Leu
275 280 285
Glu Ile Lys Gly Ser Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
290 295 300
Ser Leu Cys Ser Gly Gly Gly Gly Ser Glu Leu Pro Thr Gln Gly Thr
305 310 315 320
Phe Ser Asn Val Ser Thr Asn Val Ser Pro Ala Lys Pro Thr Thr Thr
325 330 335
Ala Cys Pro Tyr Ser Asn Pro Ser Leu Cys Thr Thr Thr Pro Ala Pro
340 345 350
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
355 360 365
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
370 375 380
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
385 390 395 400
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
405 410 415
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
420 425 430
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
435 440 445
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
450 455 460
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
465 470 475 480
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
485 490 495
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
500 505 510
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
515 520 525
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
530 535 540
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
545 550 555 560
Leu His Met Gln Ala Leu Pro Pro Arg
565
<210> 631
<211> 569
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 631
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val
35 40 45
Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu
50 55 60
Ser Leu Asn Cys Thr Val Ser Gly Gly Ser Ile Ser Tyr Tyr Tyr Trp
65 70 75 80
Thr Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly His
85 90 95
Val Ile Tyr Ser Gly Thr Thr Asn Tyr Asn Pro Ser Leu Lys Ser Arg
100 105 110
Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu
115 120 125
Asn Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Val Arg Ala
130 135 140
Glu Gly Ser Leu Asp Ala Phe Asp Leu Trp Gly Gln Gly Thr Met Val
145 150 155 160
Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
165 170 175
Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro
180 185 190
Ser Ile Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg
195 200 205
Ala Ser Gln Ser Val Ser Ser Trp Leu Ala Trp Tyr Gln Gln Lys Pro
210 215 220
Gly Lys Ala Pro Lys Val Leu Ile Tyr Lys Ala Ser Ser Leu Glu Ser
225 230 235 240
Gly Val Pro Ser Arg Phe Ser Gly Thr Gly Ser Gly Thr Glu Phe Thr
245 250 255
Leu Thr Ile Ser Ser Leu Gln Ser Asp Asp Phe Ala Thr Tyr Tyr Cys
260 265 270
Gln Gln Tyr Asn Thr Tyr Ser His Thr Phe Gly Gln Gly Thr Lys Leu
275 280 285
Glu Ile Lys Gly Ser Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
290 295 300
Ser Leu Cys Ser Gly Gly Gly Gly Ser Glu Leu Pro Thr Gln Gly Thr
305 310 315 320
Phe Ser Asn Val Ser Thr Asn Val Ser Pro Ala Lys Pro Thr Thr Thr
325 330 335
Ala Cys Pro Tyr Ser Asn Pro Ser Leu Cys Thr Thr Thr Pro Ala Pro
340 345 350
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
355 360 365
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
370 375 380
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
385 390 395 400
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
405 410 415
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
420 425 430
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
435 440 445
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
450 455 460
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
465 470 475 480
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
485 490 495
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
500 505 510
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
515 520 525
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
530 535 540
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
545 550 555 560
Leu His Met Gln Ala Leu Pro Pro Arg
565
<210> 632
<211> 569
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 632
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val
35 40 45
Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Leu Gln Thr Leu
50 55 60
Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Asp Gly Tyr
65 70 75 80
Tyr Trp Ser Trp Ile Arg Gln Asn Pro Gly Lys Gly Leu Glu Trp Ile
85 90 95
Gly Tyr Met Tyr Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys
100 105 110
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
115 120 125
Lys Leu Arg Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Thr
130 135 140
Arg Asp Phe Gly Trp Tyr Phe Asp Leu Trp Gly Arg Gly Thr Leu Val
145 150 155 160
Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
165 170 175
Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro
180 185 190
Ser Ser Leu Ser Ala Ser Val Gly Asp Ser Ile Thr Ile Thr Cys Arg
195 200 205
Ala Ser Gln Asp Ile Asp Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Thr
210 215 220
Gly Lys Val Pro Lys Val Leu Ile Tyr Ala Ala Ser Ala Leu Gln Ser
225 230 235 240
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
245 250 255
Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Val Ala Thr Tyr Tyr Cys
260 265 270
Gln Asn Tyr Asn Ser Gly Pro Arg Thr Phe Gly Gln Gly Thr Lys Val
275 280 285
Glu Ile Lys Gly Ser Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
290 295 300
Ser Leu Cys Ser Gly Gly Gly Gly Ser Glu Leu Pro Thr Gln Gly Thr
305 310 315 320
Phe Ser Asn Val Ser Thr Asn Val Ser Pro Ala Lys Pro Thr Thr Thr
325 330 335
Ala Cys Pro Tyr Ser Asn Pro Ser Leu Cys Thr Thr Thr Pro Ala Pro
340 345 350
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
355 360 365
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
370 375 380
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
385 390 395 400
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
405 410 415
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
420 425 430
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
435 440 445
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
450 455 460
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
465 470 475 480
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
485 490 495
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
500 505 510
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
515 520 525
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
530 535 540
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
545 550 555 560
Leu His Met Gln Ala Leu Pro Pro Arg
565
<210> 633
<211> 569
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 633
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val
35 40 45
Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln Ser Leu
50 55 60
Ser Leu Thr Cys Ser Val Ser Gly Gly Ser Val Ser Ser Asp Gly Tyr
65 70 75 80
Tyr Trp Ser Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu Trp Ile
85 90 95
Gly Tyr Ile Tyr Tyr Arg Arg Ile Thr Asp Tyr Asn Pro Ser Leu Lys
100 105 110
Ser Arg Val Asn Ile Ser Leu Asp Thr Ser Lys Asn Gln Phe Ser Leu
115 120 125
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
130 135 140
Arg Asp Phe Gly Trp Tyr Phe Asp Leu Trp Gly Arg Gly Thr Leu Val
145 150 155 160
Ala Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
165 170 175
Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro
180 185 190
Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg
195 200 205
Ala Ser Gln Asp Ile Ser Asn Tyr Leu Thr Trp Tyr Gln Gln Lys Pro
210 215 220
Gly Arg Val Pro Glu Val Leu Ile Tyr Ala Ala Ser Ala Leu Gln Ser
225 230 235 240
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
245 250 255
Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Val Ala Thr Tyr Tyr Cys
260 265 270
Gln Asn Tyr Asn Ser Ala Pro Arg Thr Phe Gly Gln Gly Thr Lys Val
275 280 285
Glu Ile Lys Gly Ser Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
290 295 300
Ser Leu Cys Ser Gly Gly Gly Gly Ser Glu Leu Pro Thr Gln Gly Thr
305 310 315 320
Phe Ser Asn Val Ser Thr Asn Val Ser Pro Ala Lys Pro Thr Thr Thr
325 330 335
Ala Cys Pro Tyr Ser Asn Pro Ser Leu Cys Thr Thr Thr Pro Ala Pro
340 345 350
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
355 360 365
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
370 375 380
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
385 390 395 400
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
405 410 415
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
420 425 430
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
435 440 445
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
450 455 460
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
465 470 475 480
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
485 490 495
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
500 505 510
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
515 520 525
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
530 535 540
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
545 550 555 560
Leu His Met Gln Ala Leu Pro Pro Arg
565
<210> 634
<211> 571
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 634
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val
35 40 45
Glu Leu Val Glu Ser Gly Gly Gly Met Val Gln Pro Gly Arg Ser Leu
50 55 60
Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr Gly Met
65 70 75 80
His Trp Val Arg Gln Ala Pro Gly Met Gly Leu Glu Trp Val Thr Val
85 90 95
Ile Trp Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys Gly
100 105 110
Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Phe Leu Gln
115 120 125
Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg
130 135 140
Asp Glu Val Gly Phe Val Gly Ala Phe Asp Ile Trp Gly Gln Gly Thr
145 150 155 160
Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
165 170 175
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Leu Thr Gln
180 185 190
Ser Pro Ser Phe Leu Ser Ala Ser Val Gly Asp Arg Val Ile Ile Thr
195 200 205
Cys Arg Ala Ser Gln Gly Ile Asn Ser His Leu Ala Trp Tyr Gln Gln
210 215 220
Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Tyr Ala Ser Thr Leu
225 230 235 240
Pro Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu
245 250 255
Phe Thr Leu Thr Val Thr Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
260 265 270
Tyr Cys Gln Gln Leu Asn His Tyr Pro Ile Thr Phe Gly Gln Gly Thr
275 280 285
Arg Leu Asp Ile Asn Gly Ser Gly Gly Gly Gly Ser Cys Pro Tyr Ser
290 295 300
Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser Glu Leu Pro Thr Gln
305 310 315 320
Gly Thr Phe Ser Asn Val Ser Thr Asn Val Ser Pro Ala Lys Pro Thr
325 330 335
Thr Thr Ala Cys Pro Tyr Ser Asn Pro Ser Leu Cys Thr Thr Thr Pro
340 345 350
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
355 360 365
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
370 375 380
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
385 390 395 400
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
405 410 415
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
420 425 430
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
435 440 445
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
450 455 460
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
465 470 475 480
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
485 490 495
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
500 505 510
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
515 520 525
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
530 535 540
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
545 550 555 560
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
565 570
<210> 635
<211> 569
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 635
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val
35 40 45
Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Gln Pro Ser Glu Thr Leu
50 55 60
Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Tyr Tyr Tyr Trp
65 70 75 80
Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Asn
85 90 95
Ile Asn Tyr Met Gly Asn Thr Ile Tyr Asn Pro Ser Leu Lys Ser Arg
100 105 110
Val Thr Ile Ser Val Asp Thr Ser Lys Asp Gln Phe Ser Leu Lys Leu
115 120 125
Thr Ser Val Ser Ala Ala Asp Thr Ala Val Tyr Tyr Cys Val Arg Ala
130 135 140
Glu Gly Ser Leu Asp Ala Phe Asp Phe Trp Gly Gln Gly Thr Leu Val
145 150 155 160
Ala Val Ser Leu Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
165 170 175
Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro
180 185 190
Ser Thr Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg
195 200 205
Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala Trp Tyr Gln Gln Lys Pro
210 215 220
Gly Lys Ala Pro Lys Val Leu Ile Tyr Lys Ala Ser Asn Leu Glu Ser
225 230 235 240
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr
245 250 255
Leu Thr Ile Ser Ser Leu Gln Pro Asp Asp Phe Ala Thr Tyr Tyr Cys
260 265 270
Gln Gln Tyr Asn Ser Tyr Ser Cys Thr Phe Gly Gln Gly Thr Lys Leu
275 280 285
Glu Ile Lys Gly Ser Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
290 295 300
Ser Leu Cys Ser Gly Gly Gly Gly Ser Glu Leu Pro Thr Gln Gly Thr
305 310 315 320
Phe Ser Asn Val Ser Thr Asn Val Ser Pro Ala Lys Pro Thr Thr Thr
325 330 335
Ala Cys Pro Tyr Ser Asn Pro Ser Leu Cys Thr Thr Thr Pro Ala Pro
340 345 350
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
355 360 365
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
370 375 380
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
385 390 395 400
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
405 410 415
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
420 425 430
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
435 440 445
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
450 455 460
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
465 470 475 480
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
485 490 495
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
500 505 510
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
515 520 525
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
530 535 540
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
545 550 555 560
Leu His Met Gln Ala Leu Pro Pro Arg
565
<210> 636
<211> 527
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 636
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Gln Val Thr Leu Lys Glu Ser Gly
35 40 45
Pro Val Leu Val Lys Pro Thr Glu Thr Leu Thr Leu Thr Cys Thr Val
50 55 60
Ser Gly Phe Ser Leu Ser Asn Ala Arg Met Gly Val Thr Trp Ile Arg
65 70 75 80
Gln Pro Pro Gly Lys Ala Leu Glu Trp Leu Ala His Ile Phe Ser Asn
85 90 95
Asp Glu Lys Ser Tyr Ser Thr Ser Leu Lys Ser Arg Leu Thr Ile Ser
100 105 110
Lys Asp Thr Ser Lys Thr Gln Val Val Leu Thr Met Thr Asn Met Asp
115 120 125
Pro Val Asp Thr Ala Thr Tyr Tyr Cys Ala Arg Ile Arg Asp Tyr Tyr
130 135 140
Asp Ile Ser Ser Tyr Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Ser
145 150 155 160
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
165 170 175
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ala Met Ser Ala Ser
180 185 190
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser
195 200 205
Asn Tyr Leu Ala Trp Phe Gln Gln Lys Pro Gly Lys Val Pro Lys Arg
210 215 220
Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe
225 230 235 240
Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu
245 250 255
Leu Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Leu Asn Ser Phe
260 265 270
Pro Phe Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Asn Gly Gly Gly
275 280 285
Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Gly Gly Gly Gly Ser
290 295 300
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
305 310 315 320
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
325 330 335
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
340 345 350
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
355 360 365
Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
370 375 380
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
385 390 395 400
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
405 410 415
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
420 425 430
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
435 440 445
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
450 455 460
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
465 470 475 480
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
485 490 495
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
500 505 510
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520 525
<210> 637
<211> 537
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 637
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Glu Val Gln Leu Val Gln Ser Gly
35 40 45
Ala Glu Val Lys Lys Pro Gly Glu Ser Leu Lys Ile Ser Cys Lys Gly
50 55 60
Ser Gly Tyr Gly Phe Thr Ser Tyr Trp Ile Gly Trp Val Arg Gln Met
65 70 75 80
Pro Gly Lys Gly Leu Glu Trp Met Gly Ile Ile His Pro Asp Asp Ser
85 90 95
Asp Thr Lys Tyr Ser Pro Ser Phe Gln Gly Gln Val Thr Ile Ser Ala
100 105 110
Asp Lys Ser Ile Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala
115 120 125
Ser Asp Thr Ala Met Tyr Tyr Cys Ala Ser Ser Tyr Leu Arg Gly Leu
130 135 140
Trp Gly Gly Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
145 150 155 160
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
165 170 175
Ser Gly Gly Gly Gly Ser Glu Leu Gln Ser Val Leu Thr Gln Pro Pro
180 185 190
Ser Ala Ser Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly
195 200 205
Ser Ser Ser Asn Ile Gly Ser Asn Tyr Val Asn Trp Tyr Gln Gln Leu
210 215 220
Pro Gly Thr Ala Pro Lys Leu Leu Ile Tyr Gly Asp Tyr Gln Arg Pro
225 230 235 240
Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala
245 250 255
Ser Leu Ala Ile Ser Gly Leu Arg Ser Glu Asp Glu Ala Asp Tyr Tyr
260 265 270
Cys Ala Thr Arg Asp Asp Ser Leu Ser Gly Ser Val Val Phe Gly Thr
275 280 285
Gly Thr Lys Leu Thr Val Leu Gly Gly Gly Gly Ser Cys Pro Tyr Ser
290 295 300
Asn Pro Ser Leu Cys Gly Gly Gly Gly Ser Thr Thr Thr Pro Ala Pro
305 310 315 320
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
325 330 335
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
340 345 350
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
355 360 365
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
370 375 380
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
385 390 395 400
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
405 410 415
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
420 425 430
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
435 440 445
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
450 455 460
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
465 470 475 480
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
485 490 495
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
500 505 510
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
515 520 525
Leu His Met Gln Ala Leu Pro Pro Arg
530 535
<210> 638
<211> 527
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 638
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly
35 40 45
Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val
50 55 60
Ser Gly Gly Ser Ile Ser Tyr Tyr Tyr Trp Thr Trp Ile Arg Gln Pro
65 70 75 80
Pro Gly Lys Gly Leu Glu Trp Ile Gly His Ile Tyr Tyr Ser Gly Ser
85 90 95
Thr Asn Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Ile Asp
100 105 110
Thr Ser Lys Asn Leu Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala
115 120 125
Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ala Glu Gly Ser Leu Asp Ala
130 135 140
Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
165 170 175
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser
180 185 190
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser
195 200 205
Thr Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val
210 215 220
Leu Ile Tyr Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe
225 230 235 240
Ser Gly Ser Gly Ser Gly Thr Glu Phe Ile Leu Thr Ile Asn Ser Leu
245 250 255
Gln Pro Asp Asp Phe Ala Ser Tyr Tyr Cys Gln Gln Tyr Lys Ser Tyr
260 265 270
Ser His Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly
275 280 285
Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Gly Gly Gly Gly Ser
290 295 300
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
305 310 315 320
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
325 330 335
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
340 345 350
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
355 360 365
Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
370 375 380
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
385 390 395 400
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
405 410 415
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
420 425 430
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
435 440 445
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
450 455 460
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
465 470 475 480
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
485 490 495
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
500 505 510
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520 525
<210> 639
<211> 527
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 639
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly
35 40 45
Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Asn Cys Thr Val
50 55 60
Ser Gly Gly Ser Ile Ser Tyr Tyr Tyr Trp Thr Trp Ile Arg Gln Pro
65 70 75 80
Pro Gly Lys Gly Leu Glu Trp Ile Gly His Val Ile Tyr Ser Gly Thr
85 90 95
Thr Asn Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp
100 105 110
Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Asn Ser Val Thr Ala Ala
115 120 125
Asp Thr Ala Val Tyr Tyr Cys Val Arg Ala Glu Gly Ser Leu Asp Ala
130 135 140
Phe Asp Leu Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
165 170 175
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ile Leu Ser Ala Ser
180 185 190
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Val Ser
195 200 205
Ser Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val
210 215 220
Leu Ile Tyr Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe
225 230 235 240
Ser Gly Thr Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu
245 250 255
Gln Ser Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Thr Tyr
260 265 270
Ser His Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly
275 280 285
Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Gly Gly Gly Gly Ser
290 295 300
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
305 310 315 320
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
325 330 335
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
340 345 350
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
355 360 365
Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
370 375 380
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
385 390 395 400
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
405 410 415
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
420 425 430
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
435 440 445
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
450 455 460
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
465 470 475 480
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
485 490 495
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
500 505 510
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520 525
<210> 640
<211> 527
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 640
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly
35 40 45
Pro Gly Leu Val Lys Pro Leu Gln Thr Leu Ser Leu Thr Cys Thr Val
50 55 60
Ser Gly Gly Ser Ile Ser Ser Asp Gly Tyr Tyr Trp Ser Trp Ile Arg
65 70 75 80
Gln Asn Pro Gly Lys Gly Leu Glu Trp Ile Gly Tyr Met Tyr Tyr Ser
85 90 95
Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser
100 105 110
Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Arg Ser Val Thr
115 120 125
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Thr Arg Asp Phe Gly Trp Tyr
130 135 140
Phe Asp Leu Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
165 170 175
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
180 185 190
Val Gly Asp Ser Ile Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Asp
195 200 205
Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Thr Gly Lys Val Pro Lys Val
210 215 220
Leu Ile Tyr Ala Ala Ser Ala Leu Gln Ser Gly Val Pro Ser Arg Phe
225 230 235 240
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
245 250 255
Gln Pro Glu Asp Val Ala Thr Tyr Tyr Cys Gln Asn Tyr Asn Ser Gly
260 265 270
Pro Arg Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly
275 280 285
Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Gly Gly Gly Gly Ser
290 295 300
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
305 310 315 320
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
325 330 335
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
340 345 350
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
355 360 365
Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
370 375 380
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
385 390 395 400
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
405 410 415
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
420 425 430
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
435 440 445
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
450 455 460
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
465 470 475 480
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
485 490 495
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
500 505 510
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520 525
<210> 641
<211> 527
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 641
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly
35 40 45
Pro Gly Leu Val Lys Pro Ser Gln Ser Leu Ser Leu Thr Cys Ser Val
50 55 60
Ser Gly Gly Ser Val Ser Ser Asp Gly Tyr Tyr Trp Ser Trp Ile Arg
65 70 75 80
Gln His Pro Gly Lys Gly Leu Glu Trp Ile Gly Tyr Ile Tyr Tyr Arg
85 90 95
Arg Ile Thr Asp Tyr Asn Pro Ser Leu Lys Ser Arg Val Asn Ile Ser
100 105 110
Leu Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr
115 120 125
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Phe Gly Trp Tyr
130 135 140
Phe Asp Leu Trp Gly Arg Gly Thr Leu Val Ala Val Ser Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
165 170 175
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
180 185 190
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser
195 200 205
Asn Tyr Leu Thr Trp Tyr Gln Gln Lys Pro Gly Arg Val Pro Glu Val
210 215 220
Leu Ile Tyr Ala Ala Ser Ala Leu Gln Ser Gly Val Pro Ser Arg Phe
225 230 235 240
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
245 250 255
Gln Pro Glu Asp Val Ala Thr Tyr Tyr Cys Gln Asn Tyr Asn Ser Ala
260 265 270
Pro Arg Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly
275 280 285
Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Gly Gly Gly Gly Ser
290 295 300
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
305 310 315 320
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
325 330 335
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
340 345 350
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
355 360 365
Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
370 375 380
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
385 390 395 400
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
405 410 415
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
420 425 430
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
435 440 445
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
450 455 460
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
465 470 475 480
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
485 490 495
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
500 505 510
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520 525
<210> 642
<211> 529
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 642
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Glu Val Glu Leu Val Glu Ser Gly
35 40 45
Gly Gly Met Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala
50 55 60
Ser Gly Phe Thr Phe Ser Asp Tyr Gly Met His Trp Val Arg Gln Ala
65 70 75 80
Pro Gly Met Gly Leu Glu Trp Val Thr Val Ile Trp Tyr Asp Gly Ser
85 90 95
Asn Lys Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg
100 105 110
Asp Asn Ser Lys Asn Thr Val Phe Leu Gln Met Asn Ser Leu Arg Ala
115 120 125
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Glu Val Gly Phe Val
130 135 140
Gly Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
145 150 155 160
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
165 170 175
Gly Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser
180 185 190
Ala Ser Val Gly Asp Arg Val Ile Ile Thr Cys Arg Ala Ser Gln Gly
195 200 205
Ile Asn Ser His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
210 215 220
Lys Leu Leu Ile Tyr Tyr Ala Ser Thr Leu Pro Ser Gly Val Pro Ser
225 230 235 240
Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Val Thr
245 250 255
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Leu Asn
260 265 270
His Tyr Pro Ile Thr Phe Gly Gln Gly Thr Arg Leu Asp Ile Asn Gly
275 280 285
Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Gly Gly Gly
290 295 300
Gly Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
305 310 315 320
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
325 330 335
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
340 345 350
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
355 360 365
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
370 375 380
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
385 390 395 400
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
405 410 415
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
420 425 430
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
435 440 445
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
450 455 460
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
465 470 475 480
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
485 490 495
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
500 505 510
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
515 520 525
Arg
<210> 643
<211> 527
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 643
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly
35 40 45
Pro Gly Leu Val Gln Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val
50 55 60
Ser Gly Gly Ser Ile Ser Tyr Tyr Tyr Trp Ser Trp Ile Arg Gln Pro
65 70 75 80
Pro Gly Lys Gly Leu Glu Trp Ile Gly Asn Ile Asn Tyr Met Gly Asn
85 90 95
Thr Ile Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp
100 105 110
Thr Ser Lys Asp Gln Phe Ser Leu Lys Leu Thr Ser Val Ser Ala Ala
115 120 125
Asp Thr Ala Val Tyr Tyr Cys Val Arg Ala Glu Gly Ser Leu Asp Ala
130 135 140
Phe Asp Phe Trp Gly Gln Gly Thr Leu Val Ala Val Ser Leu Gly Gly
145 150 155 160
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
165 170 175
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser
180 185 190
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser
195 200 205
Ser Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val
210 215 220
Leu Ile Tyr Lys Ala Ser Asn Leu Glu Ser Gly Val Pro Ser Arg Phe
225 230 235 240
Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu
245 250 255
Gln Pro Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr
260 265 270
Ser Cys Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly
275 280 285
Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Gly Gly Gly Gly Ser
290 295 300
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
305 310 315 320
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
325 330 335
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
340 345 350
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
355 360 365
Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
370 375 380
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
385 390 395 400
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
405 410 415
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
420 425 430
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
435 440 445
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
450 455 460
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
465 470 475 480
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
485 490 495
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
500 505 510
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520 525
<210> 644
<211> 522
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 644
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Gln Val Thr Leu Lys Glu Ser Gly
35 40 45
Pro Val Leu Val Lys Pro Thr Glu Thr Leu Thr Leu Thr Cys Thr Val
50 55 60
Ser Gly Phe Ser Leu Ser Asn Ala Arg Met Gly Val Thr Trp Ile Arg
65 70 75 80
Gln Pro Pro Gly Lys Ala Leu Glu Trp Leu Ala His Ile Phe Ser Asn
85 90 95
Asp Glu Lys Ser Tyr Ser Thr Ser Leu Lys Ser Arg Leu Thr Ile Ser
100 105 110
Lys Asp Thr Ser Lys Thr Gln Val Val Leu Thr Met Thr Asn Met Asp
115 120 125
Pro Val Asp Thr Ala Thr Tyr Tyr Cys Ala Arg Ile Arg Asp Tyr Tyr
130 135 140
Asp Ile Ser Ser Tyr Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Ser
145 150 155 160
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
165 170 175
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ala Met Ser Ala Ser
180 185 190
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser
195 200 205
Asn Tyr Leu Ala Trp Phe Gln Gln Lys Pro Gly Lys Val Pro Lys Arg
210 215 220
Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe
225 230 235 240
Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu
245 250 255
Leu Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Leu Asn Ser Phe
260 265 270
Pro Phe Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Asn Gly Gly Gly
275 280 285
Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Thr Thr Thr Pro Ala
290 295 300
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
305 310 315 320
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
325 330 335
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
340 345 350
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
355 360 365
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
370 375 380
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
385 390 395 400
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
405 410 415
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
420 425 430
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
435 440 445
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
450 455 460
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
465 470 475 480
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
485 490 495
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
500 505 510
Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520
<210> 645
<211> 532
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 645
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Glu Val Gln Leu Val Gln Ser Gly
35 40 45
Ala Glu Val Lys Lys Pro Gly Glu Ser Leu Lys Ile Ser Cys Lys Gly
50 55 60
Ser Gly Tyr Gly Phe Thr Ser Tyr Trp Ile Gly Trp Val Arg Gln Met
65 70 75 80
Pro Gly Lys Gly Leu Glu Trp Met Gly Ile Ile His Pro Asp Asp Ser
85 90 95
Asp Thr Lys Tyr Ser Pro Ser Phe Gln Gly Gln Val Thr Ile Ser Ala
100 105 110
Asp Lys Ser Ile Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala
115 120 125
Ser Asp Thr Ala Met Tyr Tyr Cys Ala Ser Ser Tyr Leu Arg Gly Leu
130 135 140
Trp Gly Gly Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
145 150 155 160
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
165 170 175
Ser Gly Gly Gly Gly Ser Glu Leu Gln Ser Val Leu Thr Gln Pro Pro
180 185 190
Ser Ala Ser Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly
195 200 205
Ser Ser Ser Asn Ile Gly Ser Asn Tyr Val Asn Trp Tyr Gln Gln Leu
210 215 220
Pro Gly Thr Ala Pro Lys Leu Leu Ile Tyr Gly Asp Tyr Gln Arg Pro
225 230 235 240
Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala
245 250 255
Ser Leu Ala Ile Ser Gly Leu Arg Ser Glu Asp Glu Ala Asp Tyr Tyr
260 265 270
Cys Ala Thr Arg Asp Asp Ser Leu Ser Gly Ser Val Val Phe Gly Thr
275 280 285
Gly Thr Lys Leu Thr Val Leu Gly Gly Gly Gly Ser Cys Pro Tyr Ser
290 295 300
Asn Pro Ser Leu Cys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro
305 310 315 320
Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys
325 330 335
Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala
340 345 350
Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu
355 360 365
Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys
370 375 380
Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr
385 390 395 400
Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly
405 410 415
Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala
420 425 430
Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg
435 440 445
Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu
450 455 460
Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn
465 470 475 480
Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met
485 490 495
Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly
500 505 510
Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala
515 520 525
Leu Pro Pro Arg
530
<210> 646
<211> 522
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 646
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly
35 40 45
Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val
50 55 60
Ser Gly Gly Ser Ile Ser Tyr Tyr Tyr Trp Thr Trp Ile Arg Gln Pro
65 70 75 80
Pro Gly Lys Gly Leu Glu Trp Ile Gly His Ile Tyr Tyr Ser Gly Ser
85 90 95
Thr Asn Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Ile Asp
100 105 110
Thr Ser Lys Asn Leu Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala
115 120 125
Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ala Glu Gly Ser Leu Asp Ala
130 135 140
Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
165 170 175
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser
180 185 190
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser
195 200 205
Thr Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val
210 215 220
Leu Ile Tyr Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe
225 230 235 240
Ser Gly Ser Gly Ser Gly Thr Glu Phe Ile Leu Thr Ile Asn Ser Leu
245 250 255
Gln Pro Asp Asp Phe Ala Ser Tyr Tyr Cys Gln Gln Tyr Lys Ser Tyr
260 265 270
Ser His Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly
275 280 285
Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Thr Thr Thr Pro Ala
290 295 300
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
305 310 315 320
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
325 330 335
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
340 345 350
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
355 360 365
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
370 375 380
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
385 390 395 400
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
405 410 415
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
420 425 430
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
435 440 445
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
450 455 460
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
465 470 475 480
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
485 490 495
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
500 505 510
Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520
<210> 647
<211> 522
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 647
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly
35 40 45
Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Asn Cys Thr Val
50 55 60
Ser Gly Gly Ser Ile Ser Tyr Tyr Tyr Trp Thr Trp Ile Arg Gln Pro
65 70 75 80
Pro Gly Lys Gly Leu Glu Trp Ile Gly His Val Ile Tyr Ser Gly Thr
85 90 95
Thr Asn Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp
100 105 110
Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Asn Ser Val Thr Ala Ala
115 120 125
Asp Thr Ala Val Tyr Tyr Cys Val Arg Ala Glu Gly Ser Leu Asp Ala
130 135 140
Phe Asp Leu Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
165 170 175
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ile Leu Ser Ala Ser
180 185 190
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Val Ser
195 200 205
Ser Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val
210 215 220
Leu Ile Tyr Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe
225 230 235 240
Ser Gly Thr Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu
245 250 255
Gln Ser Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Thr Tyr
260 265 270
Ser His Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly
275 280 285
Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Thr Thr Thr Pro Ala
290 295 300
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
305 310 315 320
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
325 330 335
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
340 345 350
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
355 360 365
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
370 375 380
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
385 390 395 400
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
405 410 415
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
420 425 430
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
435 440 445
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
450 455 460
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
465 470 475 480
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
485 490 495
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
500 505 510
Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520
<210> 648
<211> 522
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 648
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly
35 40 45
Pro Gly Leu Val Lys Pro Leu Gln Thr Leu Ser Leu Thr Cys Thr Val
50 55 60
Ser Gly Gly Ser Ile Ser Ser Asp Gly Tyr Tyr Trp Ser Trp Ile Arg
65 70 75 80
Gln Asn Pro Gly Lys Gly Leu Glu Trp Ile Gly Tyr Met Tyr Tyr Ser
85 90 95
Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser
100 105 110
Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Arg Ser Val Thr
115 120 125
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Thr Arg Asp Phe Gly Trp Tyr
130 135 140
Phe Asp Leu Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
165 170 175
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
180 185 190
Val Gly Asp Ser Ile Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Asp
195 200 205
Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Thr Gly Lys Val Pro Lys Val
210 215 220
Leu Ile Tyr Ala Ala Ser Ala Leu Gln Ser Gly Val Pro Ser Arg Phe
225 230 235 240
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
245 250 255
Gln Pro Glu Asp Val Ala Thr Tyr Tyr Cys Gln Asn Tyr Asn Ser Gly
260 265 270
Pro Arg Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly
275 280 285
Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Thr Thr Thr Pro Ala
290 295 300
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
305 310 315 320
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
325 330 335
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
340 345 350
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
355 360 365
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
370 375 380
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
385 390 395 400
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
405 410 415
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
420 425 430
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
435 440 445
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
450 455 460
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
465 470 475 480
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
485 490 495
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
500 505 510
Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520
<210> 649
<211> 522
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 649
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly
35 40 45
Pro Gly Leu Val Lys Pro Ser Gln Ser Leu Ser Leu Thr Cys Ser Val
50 55 60
Ser Gly Gly Ser Val Ser Ser Asp Gly Tyr Tyr Trp Ser Trp Ile Arg
65 70 75 80
Gln His Pro Gly Lys Gly Leu Glu Trp Ile Gly Tyr Ile Tyr Tyr Arg
85 90 95
Arg Ile Thr Asp Tyr Asn Pro Ser Leu Lys Ser Arg Val Asn Ile Ser
100 105 110
Leu Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr
115 120 125
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Phe Gly Trp Tyr
130 135 140
Phe Asp Leu Trp Gly Arg Gly Thr Leu Val Ala Val Ser Ser Gly Gly
145 150 155 160
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
165 170 175
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
180 185 190
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser
195 200 205
Asn Tyr Leu Thr Trp Tyr Gln Gln Lys Pro Gly Arg Val Pro Glu Val
210 215 220
Leu Ile Tyr Ala Ala Ser Ala Leu Gln Ser Gly Val Pro Ser Arg Phe
225 230 235 240
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
245 250 255
Gln Pro Glu Asp Val Ala Thr Tyr Tyr Cys Gln Asn Tyr Asn Ser Ala
260 265 270
Pro Arg Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly
275 280 285
Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Thr Thr Thr Pro Ala
290 295 300
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
305 310 315 320
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
325 330 335
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
340 345 350
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
355 360 365
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
370 375 380
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
385 390 395 400
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
405 410 415
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
420 425 430
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
435 440 445
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
450 455 460
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
465 470 475 480
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
485 490 495
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
500 505 510
Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520
<210> 650
<211> 524
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 650
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Glu Val Glu Leu Val Glu Ser Gly
35 40 45
Gly Gly Met Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala
50 55 60
Ser Gly Phe Thr Phe Ser Asp Tyr Gly Met His Trp Val Arg Gln Ala
65 70 75 80
Pro Gly Met Gly Leu Glu Trp Val Thr Val Ile Trp Tyr Asp Gly Ser
85 90 95
Asn Lys Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg
100 105 110
Asp Asn Ser Lys Asn Thr Val Phe Leu Gln Met Asn Ser Leu Arg Ala
115 120 125
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Glu Val Gly Phe Val
130 135 140
Gly Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
145 150 155 160
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
165 170 175
Gly Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser
180 185 190
Ala Ser Val Gly Asp Arg Val Ile Ile Thr Cys Arg Ala Ser Gln Gly
195 200 205
Ile Asn Ser His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
210 215 220
Lys Leu Leu Ile Tyr Tyr Ala Ser Thr Leu Pro Ser Gly Val Pro Ser
225 230 235 240
Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Val Thr
245 250 255
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Leu Asn
260 265 270
His Tyr Pro Ile Thr Phe Gly Gln Gly Thr Arg Leu Asp Ile Asn Gly
275 280 285
Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Thr Thr Thr
290 295 300
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
305 310 315 320
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
325 330 335
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
340 345 350
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
355 360 365
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
370 375 380
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
385 390 395 400
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
405 410 415
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
420 425 430
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
435 440 445
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
450 455 460
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
465 470 475 480
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
485 490 495
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
500 505 510
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520
<210> 651
<211> 522
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 651
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly
35 40 45
Pro Gly Leu Val Gln Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val
50 55 60
Ser Gly Gly Ser Ile Ser Tyr Tyr Tyr Trp Ser Trp Ile Arg Gln Pro
65 70 75 80
Pro Gly Lys Gly Leu Glu Trp Ile Gly Asn Ile Asn Tyr Met Gly Asn
85 90 95
Thr Ile Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp
100 105 110
Thr Ser Lys Asp Gln Phe Ser Leu Lys Leu Thr Ser Val Ser Ala Ala
115 120 125
Asp Thr Ala Val Tyr Tyr Cys Val Arg Ala Glu Gly Ser Leu Asp Ala
130 135 140
Phe Asp Phe Trp Gly Gln Gly Thr Leu Val Ala Val Ser Leu Gly Gly
145 150 155 160
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
165 170 175
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser
180 185 190
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser
195 200 205
Ser Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val
210 215 220
Leu Ile Tyr Lys Ala Ser Asn Leu Glu Ser Gly Val Pro Ser Arg Phe
225 230 235 240
Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu
245 250 255
Gln Pro Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr
260 265 270
Ser Cys Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly
275 280 285
Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Thr Thr Thr Pro Ala
290 295 300
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
305 310 315 320
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
325 330 335
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
340 345 350
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
355 360 365
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
370 375 380
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
385 390 395 400
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
405 410 415
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
420 425 430
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
435 440 445
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
450 455 460
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
465 470 475 480
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
485 490 495
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
500 505 510
Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520
<210> 652
<211> 522
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 652
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu
35 40 45
Cys Gly Gly Gly Gly Ser Gln Val Thr Leu Lys Glu Ser Gly Pro Val
50 55 60
Leu Val Lys Pro Thr Glu Thr Leu Thr Leu Thr Cys Thr Val Ser Gly
65 70 75 80
Phe Ser Leu Ser Asn Ala Arg Met Gly Val Thr Trp Ile Arg Gln Pro
85 90 95
Pro Gly Lys Ala Leu Glu Trp Leu Ala His Ile Phe Ser Asn Asp Glu
100 105 110
Lys Ser Tyr Ser Thr Ser Leu Lys Ser Arg Leu Thr Ile Ser Lys Asp
115 120 125
Thr Ser Lys Thr Gln Val Val Leu Thr Met Thr Asn Met Asp Pro Val
130 135 140
Asp Thr Ala Thr Tyr Tyr Cys Ala Arg Ile Arg Asp Tyr Tyr Asp Ile
145 150 155 160
Ser Ser Tyr Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Ser Val Ser
165 170 175
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
180 185 190
Asp Ile Gln Met Thr Gln Ser Pro Ser Ala Met Ser Ala Ser Val Gly
195 200 205
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Asn Tyr
210 215 220
Leu Ala Trp Phe Gln Gln Lys Pro Gly Lys Val Pro Lys Arg Leu Ile
225 230 235 240
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
245 250 255
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Leu Pro
260 265 270
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Leu Asn Ser Phe Pro Phe
275 280 285
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Asn Thr Thr Thr Pro Ala
290 295 300
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
305 310 315 320
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
325 330 335
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
340 345 350
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
355 360 365
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
370 375 380
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
385 390 395 400
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
405 410 415
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
420 425 430
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
435 440 445
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
450 455 460
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
465 470 475 480
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
485 490 495
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
500 505 510
Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520
<210> 653
<211> 532
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 653
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu
35 40 45
Cys Gly Gly Gly Gly Ser Glu Val Gln Leu Val Gln Ser Gly Ala Glu
50 55 60
Val Lys Lys Pro Gly Glu Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly
65 70 75 80
Tyr Gly Phe Thr Ser Tyr Trp Ile Gly Trp Val Arg Gln Met Pro Gly
85 90 95
Lys Gly Leu Glu Trp Met Gly Ile Ile His Pro Asp Asp Ser Asp Thr
100 105 110
Lys Tyr Ser Pro Ser Phe Gln Gly Gln Val Thr Ile Ser Ala Asp Lys
115 120 125
Ser Ile Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp
130 135 140
Thr Ala Met Tyr Tyr Cys Ala Ser Ser Tyr Leu Arg Gly Leu Trp Gly
145 150 155 160
Gly Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
165 170 175
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
180 185 190
Gly Gly Gly Ser Glu Leu Gln Ser Val Leu Thr Gln Pro Pro Ser Ala
195 200 205
Ser Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser
210 215 220
Ser Asn Ile Gly Ser Asn Tyr Val Asn Trp Tyr Gln Gln Leu Pro Gly
225 230 235 240
Thr Ala Pro Lys Leu Leu Ile Tyr Gly Asp Tyr Gln Arg Pro Ser Gly
245 250 255
Val Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu
260 265 270
Ala Ile Ser Gly Leu Arg Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala
275 280 285
Thr Arg Asp Asp Ser Leu Ser Gly Ser Val Val Phe Gly Thr Gly Thr
290 295 300
Lys Leu Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro
305 310 315 320
Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys
325 330 335
Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala
340 345 350
Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu
355 360 365
Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys
370 375 380
Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr
385 390 395 400
Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly
405 410 415
Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala
420 425 430
Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg
435 440 445
Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu
450 455 460
Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn
465 470 475 480
Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met
485 490 495
Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly
500 505 510
Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala
515 520 525
Leu Pro Pro Arg
530
<210> 654
<211> 522
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 654
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu
35 40 45
Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly
50 55 60
Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly
65 70 75 80
Gly Ser Ile Ser Tyr Tyr Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly
85 90 95
Lys Gly Leu Glu Trp Ile Gly His Ile Tyr Tyr Ser Gly Ser Thr Asn
100 105 110
Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Ile Asp Thr Ser
115 120 125
Lys Asn Leu Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr
130 135 140
Ala Val Tyr Tyr Cys Ala Arg Ala Glu Gly Ser Leu Asp Ala Phe Asp
145 150 155 160
Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
165 170 175
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
180 185 190
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
195 200 205
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Thr Trp
210 215 220
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val Leu Ile
225 230 235 240
Tyr Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
245 250 255
Ser Gly Ser Gly Thr Glu Phe Ile Leu Thr Ile Asn Ser Leu Gln Pro
260 265 270
Asp Asp Phe Ala Ser Tyr Tyr Cys Gln Gln Tyr Lys Ser Tyr Ser His
275 280 285
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala
290 295 300
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
305 310 315 320
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
325 330 335
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
340 345 350
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
355 360 365
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
370 375 380
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
385 390 395 400
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
405 410 415
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
420 425 430
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
435 440 445
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
450 455 460
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
465 470 475 480
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
485 490 495
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
500 505 510
Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520
<210> 655
<211> 522
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 655
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu
35 40 45
Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly
50 55 60
Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Asn Cys Thr Val Ser Gly
65 70 75 80
Gly Ser Ile Ser Tyr Tyr Tyr Trp Thr Trp Ile Arg Gln Pro Pro Gly
85 90 95
Lys Gly Leu Glu Trp Ile Gly His Val Ile Tyr Ser Gly Thr Thr Asn
100 105 110
Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser
115 120 125
Lys Asn Gln Phe Ser Leu Lys Leu Asn Ser Val Thr Ala Ala Asp Thr
130 135 140
Ala Val Tyr Tyr Cys Val Arg Ala Glu Gly Ser Leu Asp Ala Phe Asp
145 150 155 160
Leu Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
165 170 175
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
180 185 190
Asp Ile Gln Met Thr Gln Ser Pro Ser Ile Leu Ser Ala Ser Val Gly
195 200 205
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Val Ser Ser Trp
210 215 220
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val Leu Ile
225 230 235 240
Tyr Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
245 250 255
Thr Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
260 265 270
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Thr Tyr Ser His
275 280 285
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala
290 295 300
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
305 310 315 320
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
325 330 335
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
340 345 350
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
355 360 365
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
370 375 380
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
385 390 395 400
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
405 410 415
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
420 425 430
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
435 440 445
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
450 455 460
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
465 470 475 480
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
485 490 495
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
500 505 510
Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520
<210> 656
<211> 522
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 656
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu
35 40 45
Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly
50 55 60
Leu Val Lys Pro Leu Gln Thr Leu Ser Leu Thr Cys Thr Val Ser Gly
65 70 75 80
Gly Ser Ile Ser Ser Asp Gly Tyr Tyr Trp Ser Trp Ile Arg Gln Asn
85 90 95
Pro Gly Lys Gly Leu Glu Trp Ile Gly Tyr Met Tyr Tyr Ser Gly Ser
100 105 110
Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp
115 120 125
Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Arg Ser Val Thr Ala Ala
130 135 140
Asp Thr Ala Val Tyr Tyr Cys Thr Arg Asp Phe Gly Trp Tyr Phe Asp
145 150 155 160
Leu Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly
165 170 175
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
180 185 190
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
195 200 205
Asp Ser Ile Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Asp Asn Tyr
210 215 220
Leu Ala Trp Tyr Gln Gln Lys Thr Gly Lys Val Pro Lys Val Leu Ile
225 230 235 240
Tyr Ala Ala Ser Ala Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
245 250 255
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
260 265 270
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Asn Tyr Asn Ser Gly Pro Arg
275 280 285
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
290 295 300
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
305 310 315 320
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
325 330 335
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
340 345 350
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
355 360 365
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
370 375 380
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
385 390 395 400
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
405 410 415
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
420 425 430
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
435 440 445
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
450 455 460
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
465 470 475 480
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
485 490 495
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
500 505 510
Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520
<210> 657
<211> 522
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 657
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu
35 40 45
Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly
50 55 60
Leu Val Lys Pro Ser Gln Ser Leu Ser Leu Thr Cys Ser Val Ser Gly
65 70 75 80
Gly Ser Val Ser Ser Asp Gly Tyr Tyr Trp Ser Trp Ile Arg Gln His
85 90 95
Pro Gly Lys Gly Leu Glu Trp Ile Gly Tyr Ile Tyr Tyr Arg Arg Ile
100 105 110
Thr Asp Tyr Asn Pro Ser Leu Lys Ser Arg Val Asn Ile Ser Leu Asp
115 120 125
Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala
130 135 140
Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Phe Gly Trp Tyr Phe Asp
145 150 155 160
Leu Trp Gly Arg Gly Thr Leu Val Ala Val Ser Ser Gly Gly Gly Gly
165 170 175
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
180 185 190
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
195 200 205
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Asn Tyr
210 215 220
Leu Thr Trp Tyr Gln Gln Lys Pro Gly Arg Val Pro Glu Val Leu Ile
225 230 235 240
Tyr Ala Ala Ser Ala Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
245 250 255
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
260 265 270
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Asn Tyr Asn Ser Ala Pro Arg
275 280 285
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
290 295 300
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
305 310 315 320
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
325 330 335
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
340 345 350
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
355 360 365
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
370 375 380
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
385 390 395 400
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
405 410 415
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
420 425 430
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
435 440 445
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
450 455 460
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
465 470 475 480
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
485 490 495
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
500 505 510
Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520
<210> 658
<211> 524
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 658
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu
35 40 45
Cys Gly Gly Gly Gly Ser Glu Val Glu Leu Val Glu Ser Gly Gly Gly
50 55 60
Met Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
65 70 75 80
Phe Thr Phe Ser Asp Tyr Gly Met His Trp Val Arg Gln Ala Pro Gly
85 90 95
Met Gly Leu Glu Trp Val Thr Val Ile Trp Tyr Asp Gly Ser Asn Lys
100 105 110
Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn
115 120 125
Ser Lys Asn Thr Val Phe Leu Gln Met Asn Ser Leu Arg Ala Glu Asp
130 135 140
Thr Ala Val Tyr Tyr Cys Ala Arg Asp Glu Val Gly Phe Val Gly Ala
145 150 155 160
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
165 170 175
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
180 185 190
Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser
195 200 205
Val Gly Asp Arg Val Ile Ile Thr Cys Arg Ala Ser Gln Gly Ile Asn
210 215 220
Ser His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu
225 230 235 240
Leu Ile Tyr Tyr Ala Ser Thr Leu Pro Ser Gly Val Pro Ser Arg Phe
245 250 255
Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Val Thr Ser Leu
260 265 270
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Leu Asn His Tyr
275 280 285
Pro Ile Thr Phe Gly Gln Gly Thr Arg Leu Asp Ile Asn Thr Thr Thr
290 295 300
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
305 310 315 320
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
325 330 335
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
340 345 350
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
355 360 365
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
370 375 380
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
385 390 395 400
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
405 410 415
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
420 425 430
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
435 440 445
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
450 455 460
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
465 470 475 480
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
485 490 495
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
500 505 510
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520
<210> 659
<211> 522
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 659
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu
35 40 45
Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly
50 55 60
Leu Val Gln Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly
65 70 75 80
Gly Ser Ile Ser Tyr Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly
85 90 95
Lys Gly Leu Glu Trp Ile Gly Asn Ile Asn Tyr Met Gly Asn Thr Ile
100 105 110
Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser
115 120 125
Lys Asp Gln Phe Ser Leu Lys Leu Thr Ser Val Ser Ala Ala Asp Thr
130 135 140
Ala Val Tyr Tyr Cys Val Arg Ala Glu Gly Ser Leu Asp Ala Phe Asp
145 150 155 160
Phe Trp Gly Gln Gly Thr Leu Val Ala Val Ser Leu Gly Gly Gly Gly
165 170 175
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
180 185 190
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
195 200 205
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp
210 215 220
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val Leu Ile
225 230 235 240
Tyr Lys Ala Ser Asn Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
245 250 255
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
260 265 270
Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Ser Cys
275 280 285
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala
290 295 300
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
305 310 315 320
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
325 330 335
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
340 345 350
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
355 360 365
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
370 375 380
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
385 390 395 400
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
405 410 415
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
420 425 430
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
435 440 445
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
450 455 460
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
465 470 475 480
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
485 490 495
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
500 505 510
Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520
<210> 660
<211> 24
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 660
Asn Ser Glu Leu Leu Ser Leu Ile Asn Asp Met Pro Ile Thr Asn Asp
1. 5 10 15
Gln Lys Lys Leu Met Ser Asn Asn
20
<210> 661
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 661
Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Ile Ile Thr Cys Arg Ala Ser Gln Gly Ile Asn Ser His
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Ser Thr Leu Pro Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Val Thr Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Leu Asn His Tyr Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 662
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 662
Glu Val Glu Leu Val Glu Ser Gly Gly Gly Met Val Gln Pro Gly Arg
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Met Gly Leu Glu Trp Val
35 40 45
Thr Val Ile Trp Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Glu Val Gly Phe Val Gly Ala Phe Asp Ile Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 663
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 663
Asp Tyr Gly Met His
1. 5
<210> 664
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 664
Gly Phe Thr Phe Ser Asp Tyr
1. 5
<210> 665
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 665
Gly Phe Thr Phe Ser Asp Tyr Gly Met His
1. 5 10
<210> 666
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 666
Val Ile Trp Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1. 5 10 15
Gly
<210> 667
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 667
Trp Tyr Asp Gly Ser Asn
1. 5
<210> 668
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 668
Asp Glu Val Gly Phe Val Gly Ala Phe Asp Ile
1. 5 10
<210> 669
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 669
Arg Ala Ser Gln Gly Ile Asn Ser His Leu Ala
1. 5 10
<210> 670
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 670
Tyr Ala Ser Thr Leu Pro Ser
1. 5
<210> 671
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 671
Gln Gln Leu Asn His Tyr Pro Ile Thr
1. 5
<210> 672
<211> 494
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 672
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Thr Leu Lys Glu Ser Gly Pro Val Leu
20 25 30
Val Lys Pro Thr Glu Thr Leu Thr Leu Thr Cys Thr Val Ser Gly Phe
35 40 45
Ser Leu Ser Asn Ala Arg Met Gly Val Thr Trp Ile Arg Gln Pro Pro
50 55 60
Gly Lys Ala Leu Glu Trp Leu Ala His Ile Phe Ser Asn Asp Glu Lys
65 70 75 80
Ser Tyr Ser Thr Ser Leu Lys Ser Arg Leu Thr Ile Ser Lys Asp Thr
85 90 95
Ser Lys Thr Gln Val Val Leu Thr Met Thr Asn Met Asp Pro Val Asp
100 105 110
Thr Ala Thr Tyr Tyr Cys Ala Arg Ile Arg Asp Tyr Tyr Asp Ile Ser
115 120 125
Ser Tyr Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Ser Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
145 150 155 160
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ala Met Ser
165 170 175
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
180 185 190
Ile Ser Asn Tyr Leu Ala Trp Phe Gln Gln Lys Pro Gly Lys Val Pro
195 200 205
Lys Arg Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
210 215 220
Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser
225 230 235 240
Ser Leu Leu Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Leu Asn
245 250 255
Ser Phe Pro Phe Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Asn Thr
260 265 270
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
275 280 285
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
290 295 300
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
305 310 315 320
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
325 330 335
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
340 345 350
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
355 360 365
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
370 375 380
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
385 390 395 400
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
405 410 415
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
420 425 430
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
435 440 445
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
450 455 460
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
465 470 475 480
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 673
<211> 491
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 673
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Glu Leu Val Glu Ser Gly Gly Gly Met
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Asp Tyr Gly Met His Trp Val Arg Gln Ala Pro Gly Met
50 55 60
Gly Leu Glu Trp Val Thr Val Ile Trp Tyr Asp Gly Ser Asn Lys Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Val Phe Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Glu Val Gly Phe Val Gly Ala Phe
115 120 125
Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val
165 170 175
Gly Asp Arg Val Ile Ile Thr Cys Arg Ala Ser Gln Gly Ile Asn Ser
180 185 190
His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
195 200 205
Ile Tyr Tyr Ala Ser Thr Leu Pro Ser Gly Val Pro Ser Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Val Thr Ser Leu Gln
225 230 235 240
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Leu Asn His Tyr Pro
245 250 255
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 674
<211> 531
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 674
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Thr Leu Lys Glu Ser Gly Pro Val Leu
20 25 30
Val Lys Pro Thr Glu Thr Leu Thr Leu Thr Cys Thr Val Ser Gly Phe
35 40 45
Ser Leu Ser Asn Ala Arg Met Gly Val Thr Trp Ile Arg Gln Pro Pro
50 55 60
Gly Lys Ala Leu Glu Trp Leu Ala His Ile Phe Ser Asn Asp Glu Lys
65 70 75 80
Ser Tyr Ser Thr Ser Leu Lys Ser Arg Leu Thr Ile Ser Lys Asp Thr
85 90 95
Ser Lys Thr Gln Val Val Leu Thr Met Thr Asn Met Asp Pro Val Asp
100 105 110
Thr Ala Thr Tyr Tyr Cys Ala Arg Ile Arg Asp Tyr Tyr Asp Ile Ser
115 120 125
Ser Tyr Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Ser Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
145 150 155 160
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ala Met Ser
165 170 175
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
180 185 190
Ile Ser Asn Tyr Leu Ala Trp Phe Gln Gln Lys Pro Gly Lys Val Pro
195 200 205
Lys Arg Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
210 215 220
Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser
225 230 235 240
Ser Leu Leu Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Leu Asn
245 250 255
Ser Phe Pro Phe Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Asn Gly
260 265 270
Ser Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser
275 280 285
Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly
290 295 300
Gly Gly Gly Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
305 310 315 320
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
325 330 335
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
340 345 350
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
355 360 365
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
370 375 380
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
385 390 395 400
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
405 410 415
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
420 425 430
Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
435 440 445
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
450 455 460
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
465 470 475 480
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
485 490 495
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
500 505 510
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
515 520 525
Pro Pro Arg
530
<210> 675
<211> 528
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 675
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Glu Leu Val Glu Ser Gly Gly Gly Met
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Asp Tyr Gly Met His Trp Val Arg Gln Ala Pro Gly Met
50 55 60
Gly Leu Glu Trp Val Thr Val Ile Trp Tyr Asp Gly Ser Asn Lys Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Val Phe Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Glu Val Gly Phe Val Gly Ala Phe
115 120 125
Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val
165 170 175
Gly Asp Arg Val Ile Ile Thr Cys Arg Ala Ser Gln Gly Ile Asn Ser
180 185 190
His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
195 200 205
Ile Tyr Tyr Ala Ser Thr Leu Pro Ser Gly Val Pro Ser Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Val Thr Ser Leu Gln
225 230 235 240
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Leu Asn His Tyr Pro
245 250 255
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Gly Ser Gly Gly
260 265 270
Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly
275 280 285
Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly
290 295 300
Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
305 310 315 320
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
325 330 335
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
340 345 350
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
355 360 365
Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
370 375 380
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
385 390 395 400
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
405 410 415
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
420 425 430
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
435 440 445
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
450 455 460
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
465 470 475 480
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
485 490 495
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
500 505 510
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520 525
<210> 676
<211> 574
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 676
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val
35 40 45
Thr Leu Lys Glu Ser Gly Pro Val Leu Val Lys Pro Thr Glu Thr Leu
50 55 60
Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Asn Ala Arg Met
65 70 75 80
Gly Val Thr Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu Trp Leu
85 90 95
Ala His Ile Phe Ser Asn Asp Glu Lys Ser Tyr Ser Thr Ser Leu Lys
100 105 110
Ser Arg Leu Thr Ile Ser Lys Asp Thr Ser Lys Thr Gln Val Val Leu
115 120 125
Thr Met Thr Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Tyr Cys Ala
130 135 140
Arg Ile Arg Asp Tyr Tyr Asp Ile Ser Ser Tyr Tyr Asp Tyr Trp Gly
145 150 155 160
Gln Gly Thr Leu Val Ser Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
165 170 175
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
180 185 190
Met Thr Gln Ser Pro Ser Ala Met Ser Ala Ser Val Gly Asp Arg Val
195 200 205
Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Asn Tyr Leu Ala Trp
210 215 220
Phe Gln Gln Lys Pro Gly Lys Val Pro Lys Arg Leu Ile Tyr Ala Ala
225 230 235 240
Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
245 250 255
Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Leu Pro Glu Asp Phe
260 265 270
Ala Thr Tyr Tyr Cys Leu Gln Leu Asn Ser Phe Pro Phe Thr Phe Gly
275 280 285
Gly Gly Thr Lys Val Glu Ile Asn Gly Ser Gly Gly Gly Gly Ser Cys
290 295 300
Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser Glu Leu
305 310 315 320
Pro Thr Gln Gly Thr Phe Ser Asn Val Ser Thr Asn Val Ser Pro Ala
325 330 335
Lys Pro Thr Thr Thr Ala Cys Pro Tyr Ser Asn Pro Ser Leu Cys Thr
340 345 350
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
355 360 365
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
370 375 380
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
385 390 395 400
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
405 410 415
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
420 425 430
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
435 440 445
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
450 455 460
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
465 470 475 480
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
485 490 495
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
500 505 510
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
515 520 525
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
530 535 540
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
545 550 555 560
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
565 570
<210> 677
<211> 571
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 677
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val
35 40 45
Glu Leu Val Glu Ser Gly Gly Gly Met Val Gln Pro Gly Arg Ser Leu
50 55 60
Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr Gly Met
65 70 75 80
His Trp Val Arg Gln Ala Pro Gly Met Gly Leu Glu Trp Val Thr Val
85 90 95
Ile Trp Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys Gly
100 105 110
Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Phe Leu Gln
115 120 125
Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg
130 135 140
Asp Glu Val Gly Phe Val Gly Ala Phe Asp Ile Trp Gly Gln Gly Thr
145 150 155 160
Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
165 170 175
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Leu Thr Gln
180 185 190
Ser Pro Ser Phe Leu Ser Ala Ser Val Gly Asp Arg Val Ile Ile Thr
195 200 205
Cys Arg Ala Ser Gln Gly Ile Asn Ser His Leu Ala Trp Tyr Gln Gln
210 215 220
Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Tyr Ala Ser Thr Leu
225 230 235 240
Pro Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu
245 250 255
Phe Thr Leu Thr Val Thr Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
260 265 270
Tyr Cys Gln Gln Leu Asn His Tyr Pro Ile Thr Phe Gly Gln Gly Thr
275 280 285
Arg Leu Glu Ile Lys Gly Ser Gly Gly Gly Gly Ser Cys Pro Tyr Ser
290 295 300
Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser Glu Leu Pro Thr Gln
305 310 315 320
Gly Thr Phe Ser Asn Val Ser Thr Asn Val Ser Pro Ala Lys Pro Thr
325 330 335
Thr Thr Ala Cys Pro Tyr Ser Asn Pro Ser Leu Cys Thr Thr Thr Pro
340 345 350
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
355 360 365
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
370 375 380
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
385 390 395 400
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
405 410 415
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
420 425 430
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
435 440 445
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
450 455 460
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
465 470 475 480
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
485 490 495
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
500 505 510
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
515 520 525
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
530 535 540
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
545 550 555 560
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
565 570
<210> 678
<211> 532
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 678
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Gln Val Thr Leu Lys Glu Ser Gly
35 40 45
Pro Val Leu Val Lys Pro Thr Glu Thr Leu Thr Leu Thr Cys Thr Val
50 55 60
Ser Gly Phe Ser Leu Ser Asn Ala Arg Met Gly Val Thr Trp Ile Arg
65 70 75 80
Gln Pro Pro Gly Lys Ala Leu Glu Trp Leu Ala His Ile Phe Ser Asn
85 90 95
Asp Glu Lys Ser Tyr Ser Thr Ser Leu Lys Ser Arg Leu Thr Ile Ser
100 105 110
Lys Asp Thr Ser Lys Thr Gln Val Val Leu Thr Met Thr Asn Met Asp
115 120 125
Pro Val Asp Thr Ala Thr Tyr Tyr Cys Ala Arg Ile Arg Asp Tyr Tyr
130 135 140
Asp Ile Ser Ser Tyr Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Ser
145 150 155 160
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
165 170 175
Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser
180 185 190
Ala Met Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
195 200 205
Ser Gln Asp Ile Ser Asn Tyr Leu Ala Trp Phe Gln Gln Lys Pro Gly
210 215 220
Lys Val Pro Lys Arg Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly
225 230 235 240
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu
245 250 255
Thr Ile Ser Ser Leu Leu Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu
260 265 270
Gln Leu Asn Ser Phe Pro Phe Thr Phe Gly Gly Gly Thr Lys Val Glu
275 280 285
Ile Asn Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys
290 295 300
Gly Gly Gly Gly Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro
305 310 315 320
Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys
325 330 335
Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala
340 345 350
Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu
355 360 365
Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys
370 375 380
Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr
385 390 395 400
Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly
405 410 415
Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala
420 425 430
Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg
435 440 445
Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu
450 455 460
Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn
465 470 475 480
Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met
485 490 495
Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly
500 505 510
Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala
515 520 525
Leu Pro Pro Arg
530
<210> 679
<211> 529
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 679
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Glu Val Glu Leu Val Glu Ser Gly
35 40 45
Gly Gly Met Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala
50 55 60
Ser Gly Phe Thr Phe Ser Asp Tyr Gly Met His Trp Val Arg Gln Ala
65 70 75 80
Pro Gly Met Gly Leu Glu Trp Val Thr Val Ile Trp Tyr Asp Gly Ser
85 90 95
Asn Lys Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg
100 105 110
Asp Asn Ser Lys Asn Thr Val Phe Leu Gln Met Asn Ser Leu Arg Ala
115 120 125
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Glu Val Gly Phe Val
130 135 140
Gly Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
145 150 155 160
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
165 170 175
Gly Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser
180 185 190
Ala Ser Val Gly Asp Arg Val Ile Ile Thr Cys Arg Ala Ser Gln Gly
195 200 205
Ile Asn Ser His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
210 215 220
Lys Leu Leu Ile Tyr Tyr Ala Ser Thr Leu Pro Ser Gly Val Pro Ser
225 230 235 240
Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Val Thr
245 250 255
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Leu Asn
260 265 270
His Tyr Pro Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Gly
275 280 285
Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Gly Gly Gly
290 295 300
Gly Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
305 310 315 320
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
325 330 335
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
340 345 350
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
355 360 365
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
370 375 380
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
385 390 395 400
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
405 410 415
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
420 425 430
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
435 440 445
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
450 455 460
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
465 470 475 480
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
485 490 495
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
500 505 510
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
515 520 525
Arg
<210> 680
<211> 527
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 680
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Gln Val Thr Leu Lys Glu Ser Gly
35 40 45
Pro Val Leu Val Lys Pro Thr Glu Thr Leu Thr Leu Thr Cys Thr Val
50 55 60
Ser Gly Phe Ser Leu Ser Asn Ala Arg Met Gly Val Thr Trp Ile Arg
65 70 75 80
Gln Pro Pro Gly Lys Ala Leu Glu Trp Leu Ala His Ile Phe Ser Asn
85 90 95
Asp Glu Lys Ser Tyr Ser Thr Ser Leu Lys Ser Arg Leu Thr Ile Ser
100 105 110
Lys Asp Thr Ser Lys Thr Gln Val Val Leu Thr Met Thr Asn Met Asp
115 120 125
Pro Val Asp Thr Ala Thr Tyr Tyr Cys Ala Arg Ile Arg Asp Tyr Tyr
130 135 140
Asp Ile Ser Ser Tyr Tyr Asp Tyr Trp Gly Gln Gly Thr Leu Val Ser
145 150 155 160
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
165 170 175
Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser
180 185 190
Ala Met Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
195 200 205
Ser Gln Asp Ile Ser Asn Tyr Leu Ala Trp Phe Gln Gln Lys Pro Gly
210 215 220
Lys Val Pro Lys Arg Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly
225 230 235 240
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu
245 250 255
Thr Ile Ser Ser Leu Leu Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu
260 265 270
Gln Leu Asn Ser Phe Pro Phe Thr Phe Gly Gly Gly Thr Lys Val Glu
275 280 285
Ile Asn Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys
290 295 300
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
305 310 315 320
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
325 330 335
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
340 345 350
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
355 360 365
Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
370 375 380
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
385 390 395 400
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
405 410 415
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
420 425 430
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
435 440 445
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
450 455 460
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
465 470 475 480
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
485 490 495
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
500 505 510
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520 525
<210> 681
<211> 524
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 681
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
20 25 30
Ser Leu Cys Gly Gly Gly Gly Ser Glu Val Glu Leu Val Glu Ser Gly
35 40 45
Gly Gly Met Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala
50 55 60
Ser Gly Phe Thr Phe Ser Asp Tyr Gly Met His Trp Val Arg Gln Ala
65 70 75 80
Pro Gly Met Gly Leu Glu Trp Val Thr Val Ile Trp Tyr Asp Gly Ser
85 90 95
Asn Lys Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg
100 105 110
Asp Asn Ser Lys Asn Thr Val Phe Leu Gln Met Asn Ser Leu Arg Ala
115 120 125
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Glu Val Gly Phe Val
130 135 140
Gly Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
145 150 155 160
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
165 170 175
Gly Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser
180 185 190
Ala Ser Val Gly Asp Arg Val Ile Ile Thr Cys Arg Ala Ser Gln Gly
195 200 205
Ile Asn Ser His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
210 215 220
Lys Leu Leu Ile Tyr Tyr Ala Ser Thr Leu Pro Ser Gly Val Pro Ser
225 230 235 240
Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Val Thr
245 250 255
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Leu Asn
260 265 270
His Tyr Pro Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Gly
275 280 285
Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Thr Thr Thr
290 295 300
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
305 310 315 320
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
325 330 335
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
340 345 350
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
355 360 365
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
370 375 380
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
385 390 395 400
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
405 410 415
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
420 425 430
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
435 440 445
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
450 455 460
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
465 470 475 480
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
485 490 495
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
500 505 510
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520
<210> 682
<211> 40
<212> БЕЛОК
<213> Homo sapiens
<400> 682
Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro
1. 5 10 15
Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu
20 25 30
Glu Glu Glu Gly Gly Cys Glu Leu
35 40
<210> 683
<211> 112
<212> БЕЛОК
<213> Homo sapiens
<400> 683
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly
1. 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<---
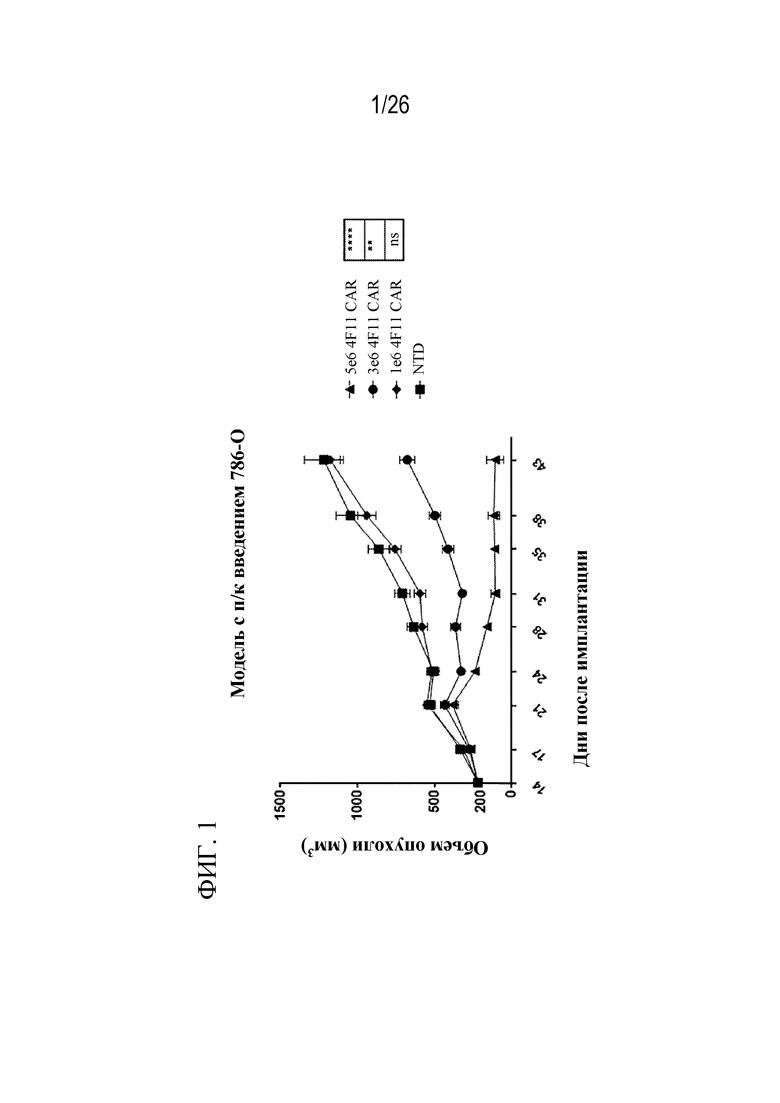
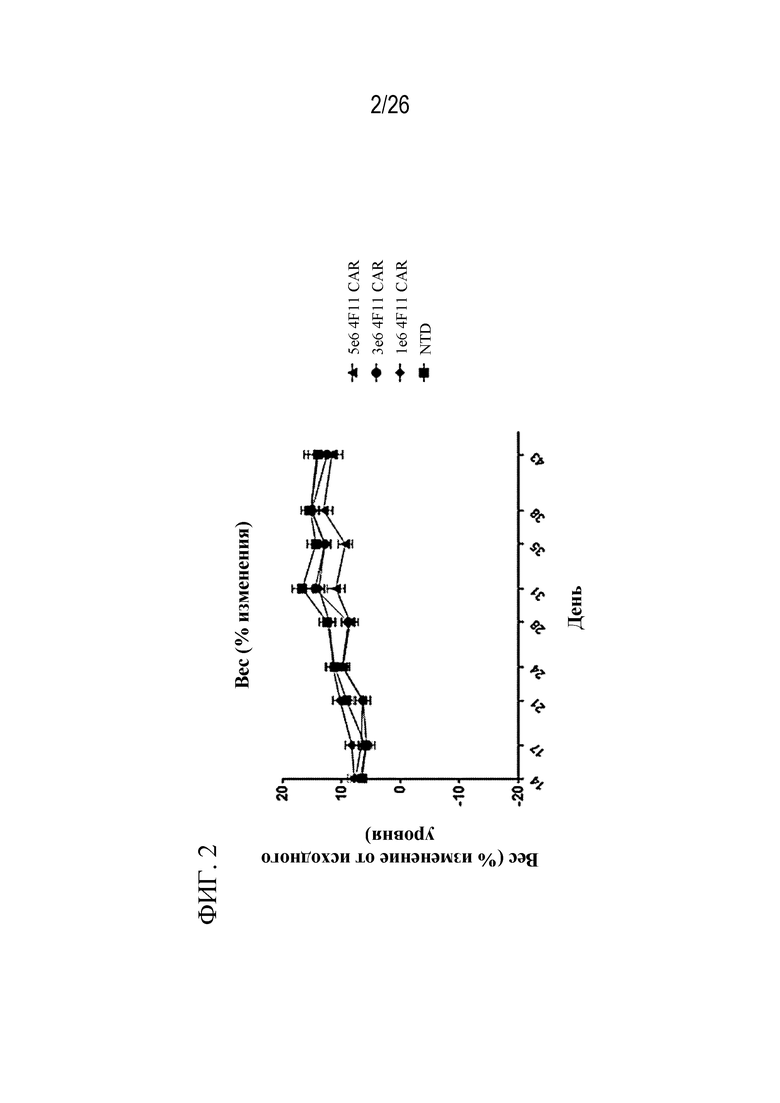
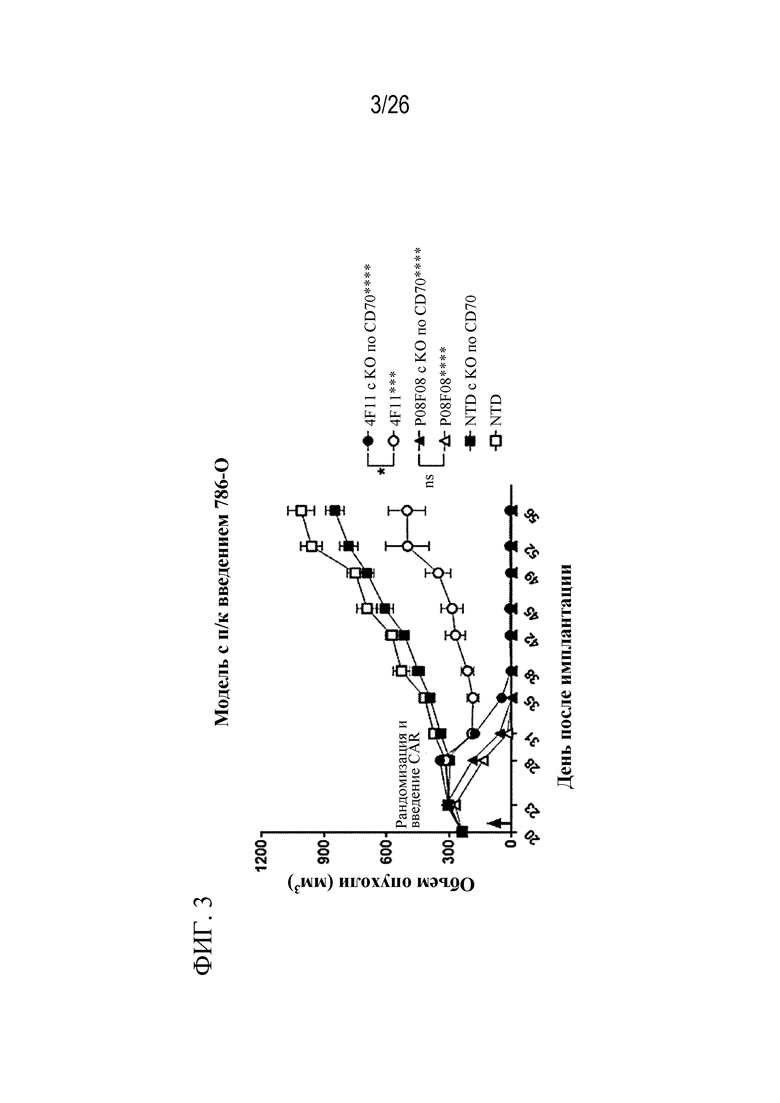
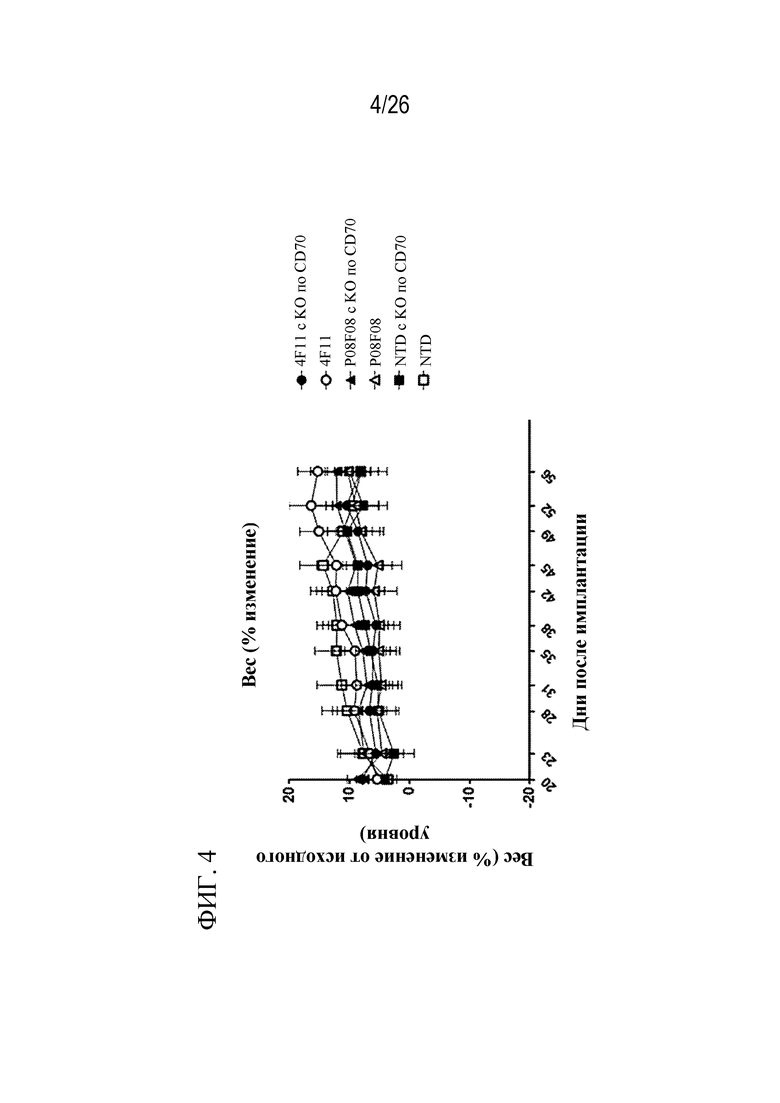
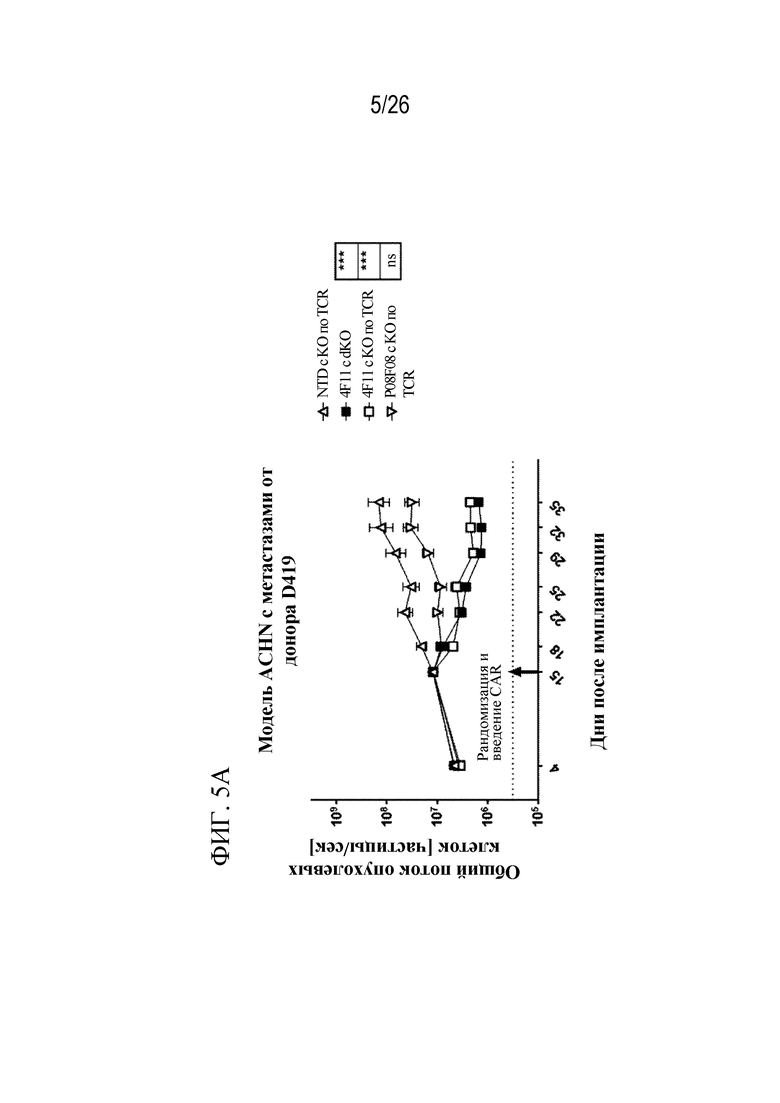
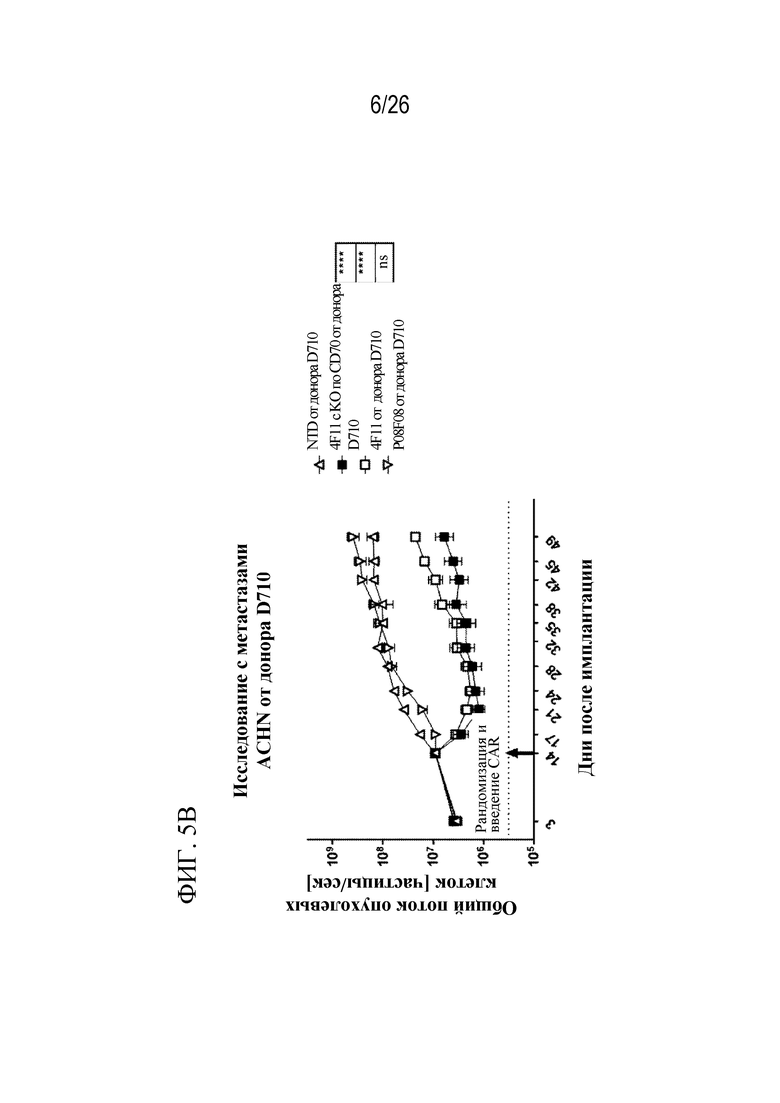
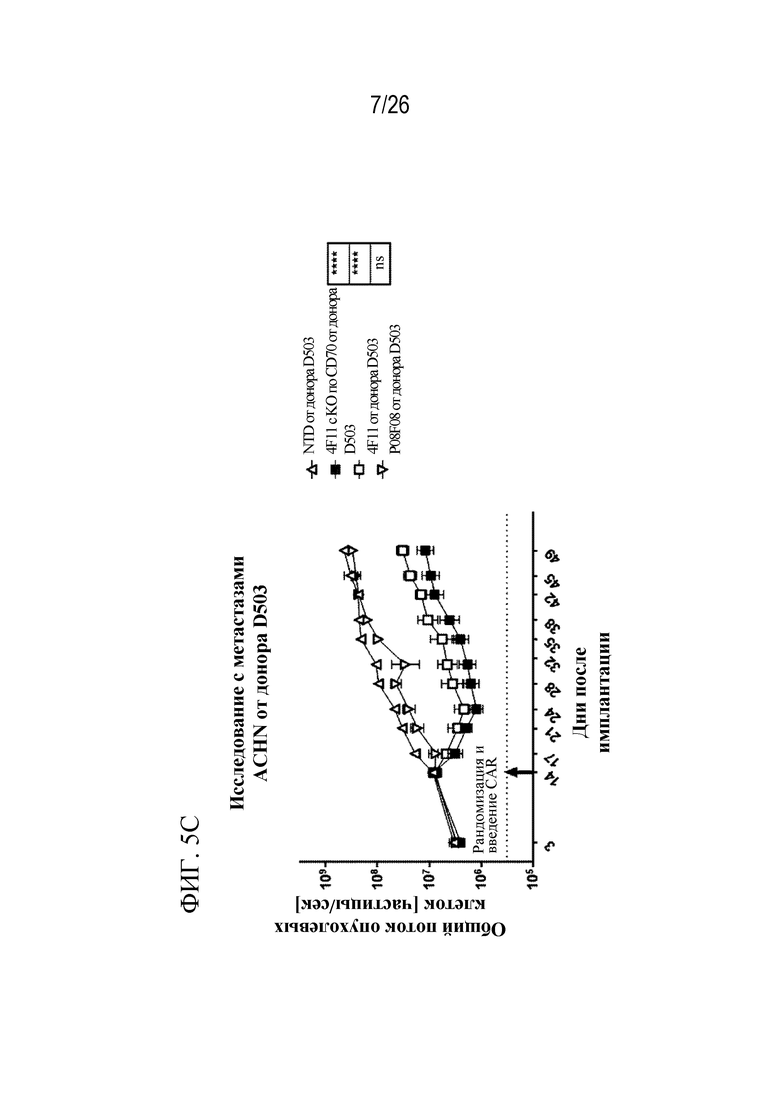
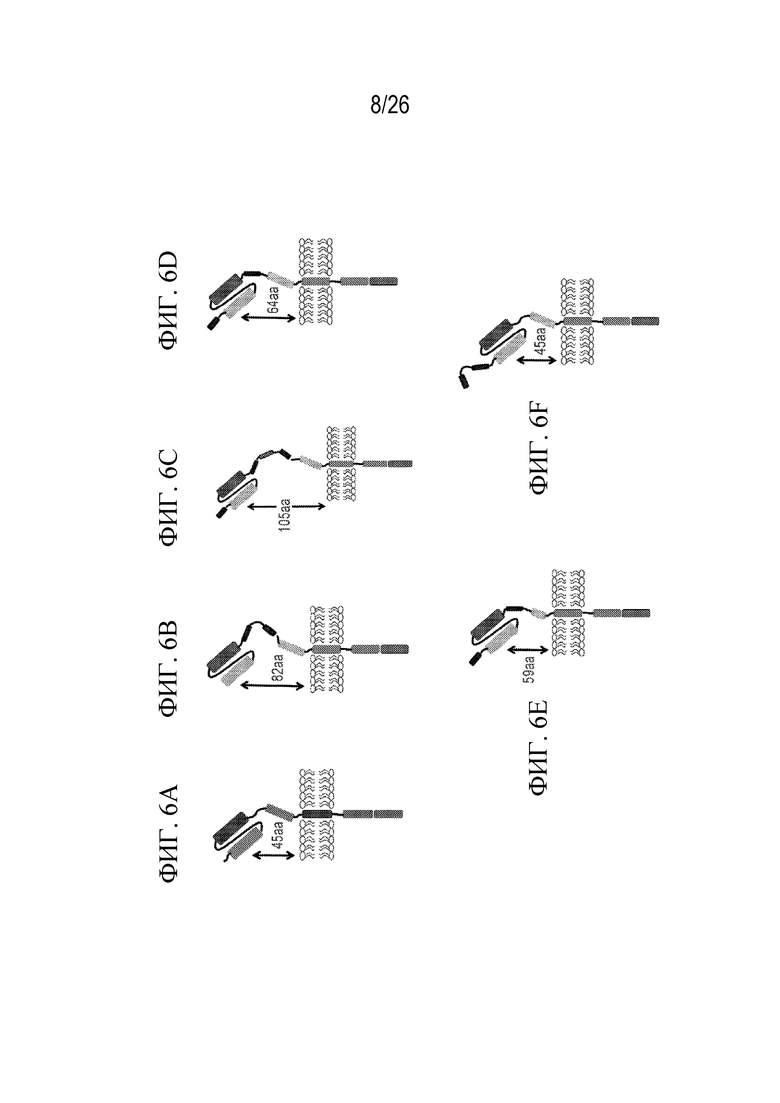
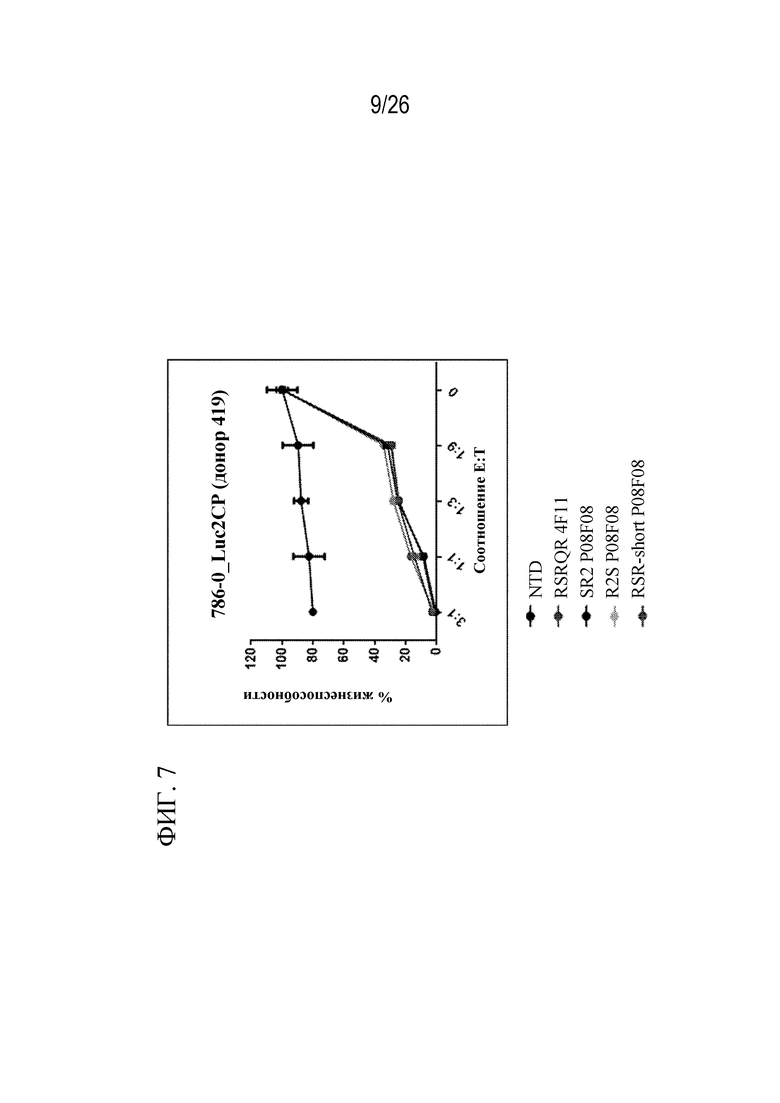
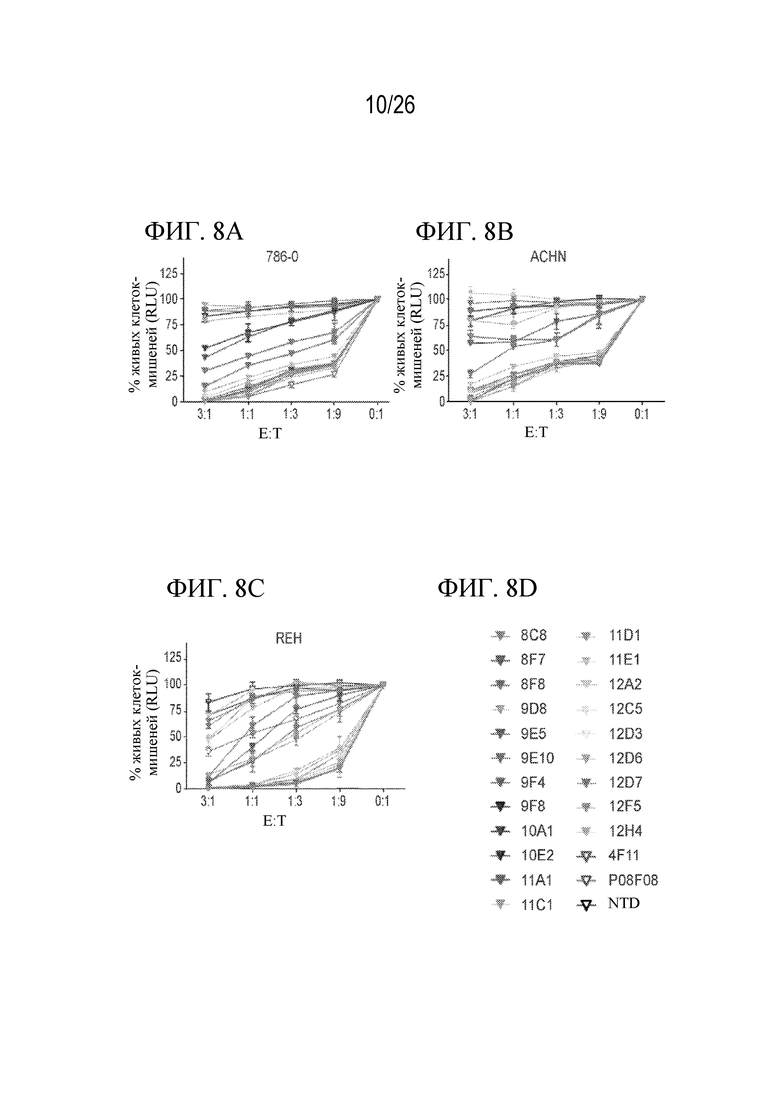
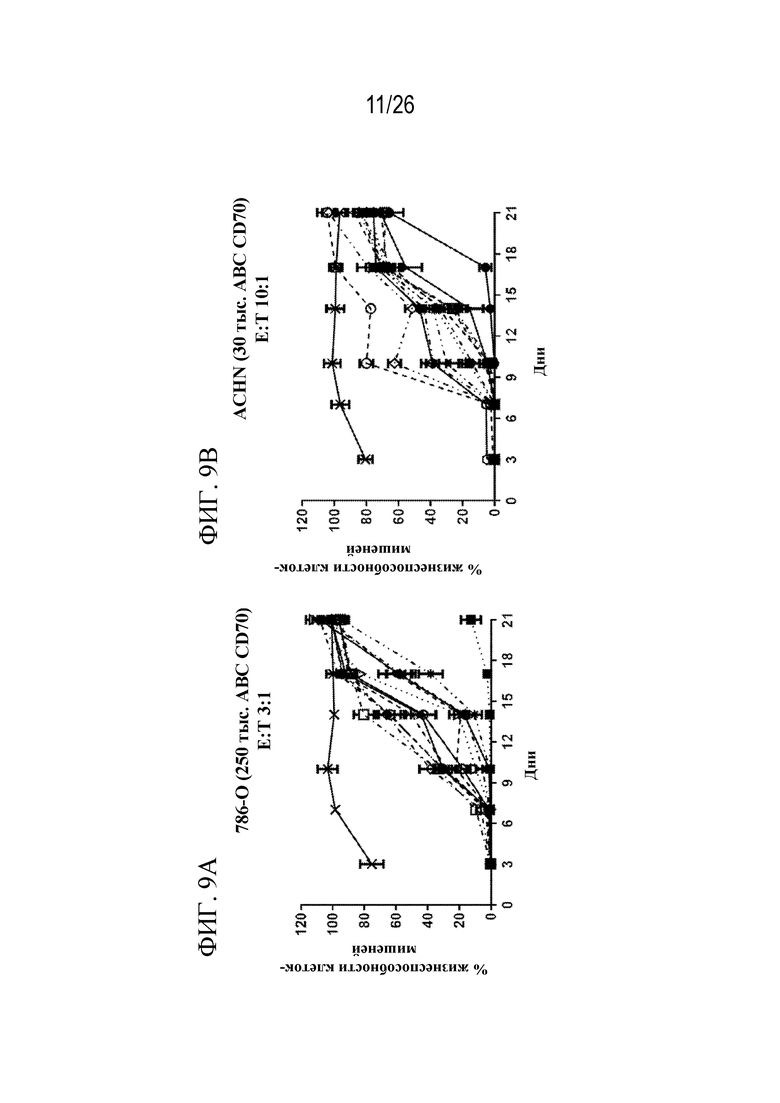
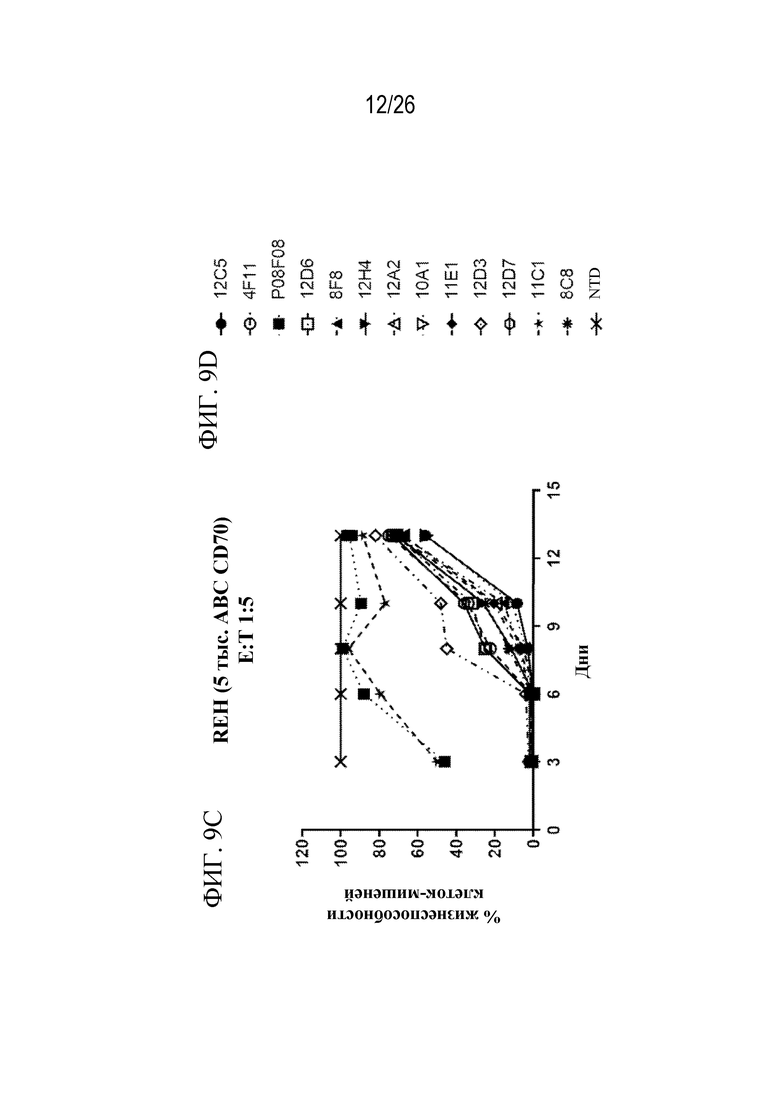

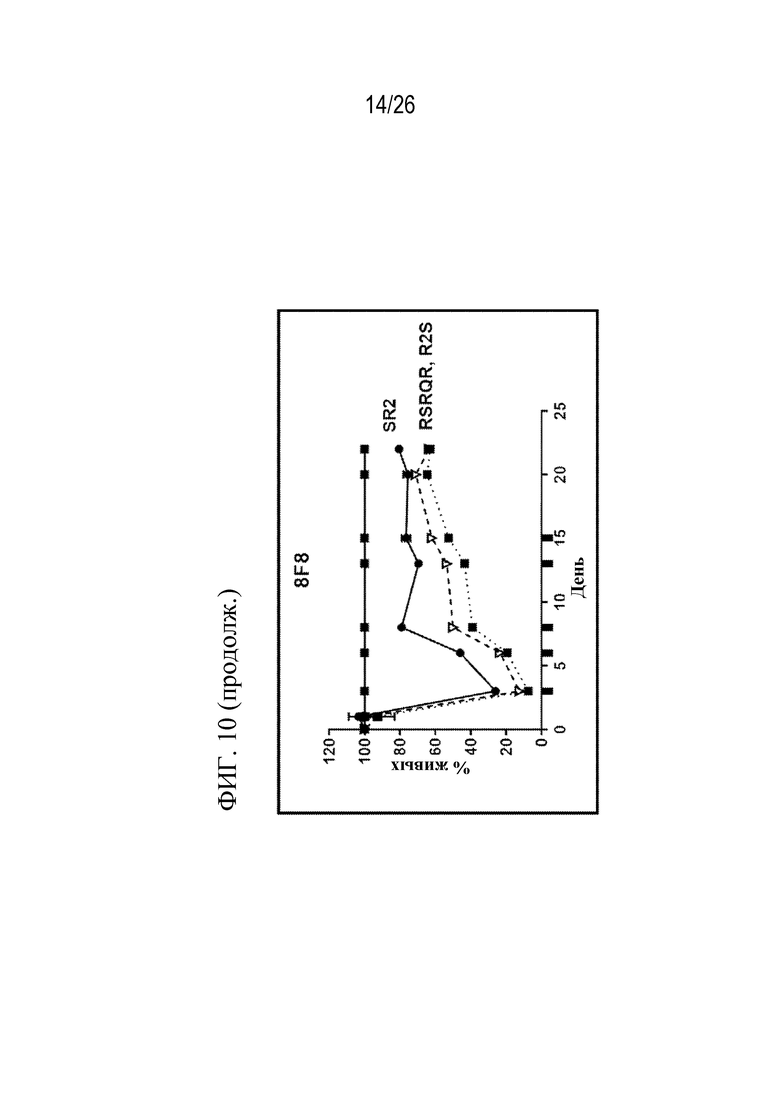
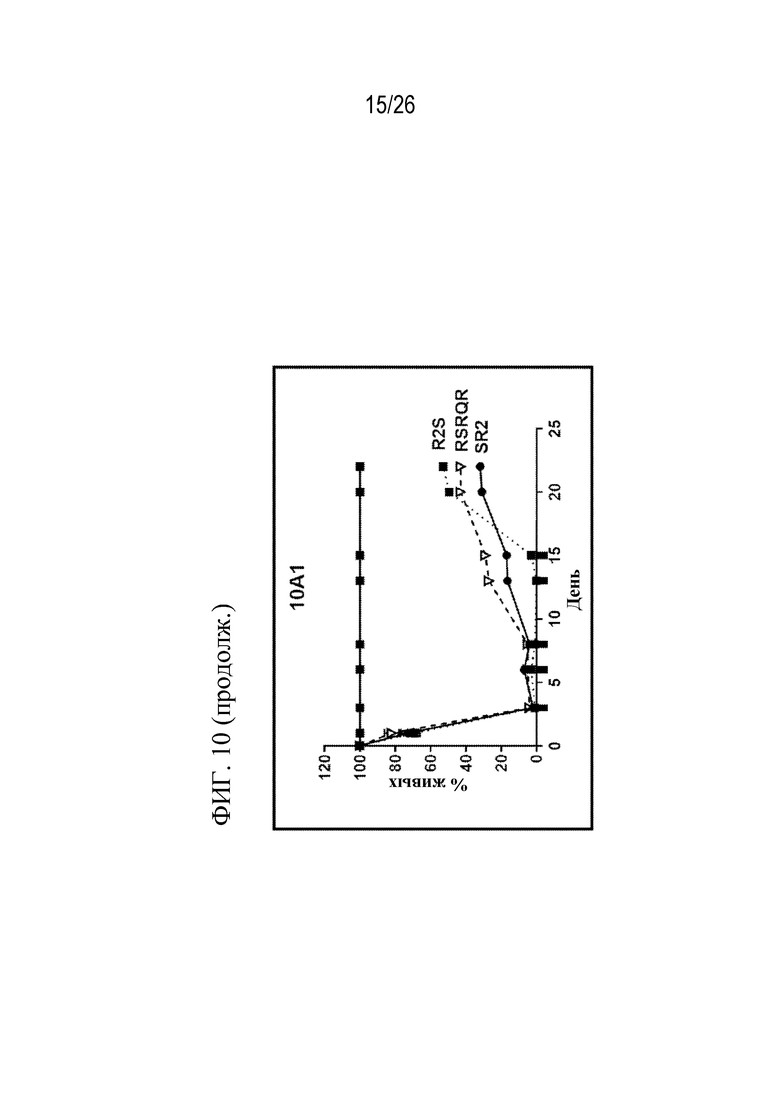
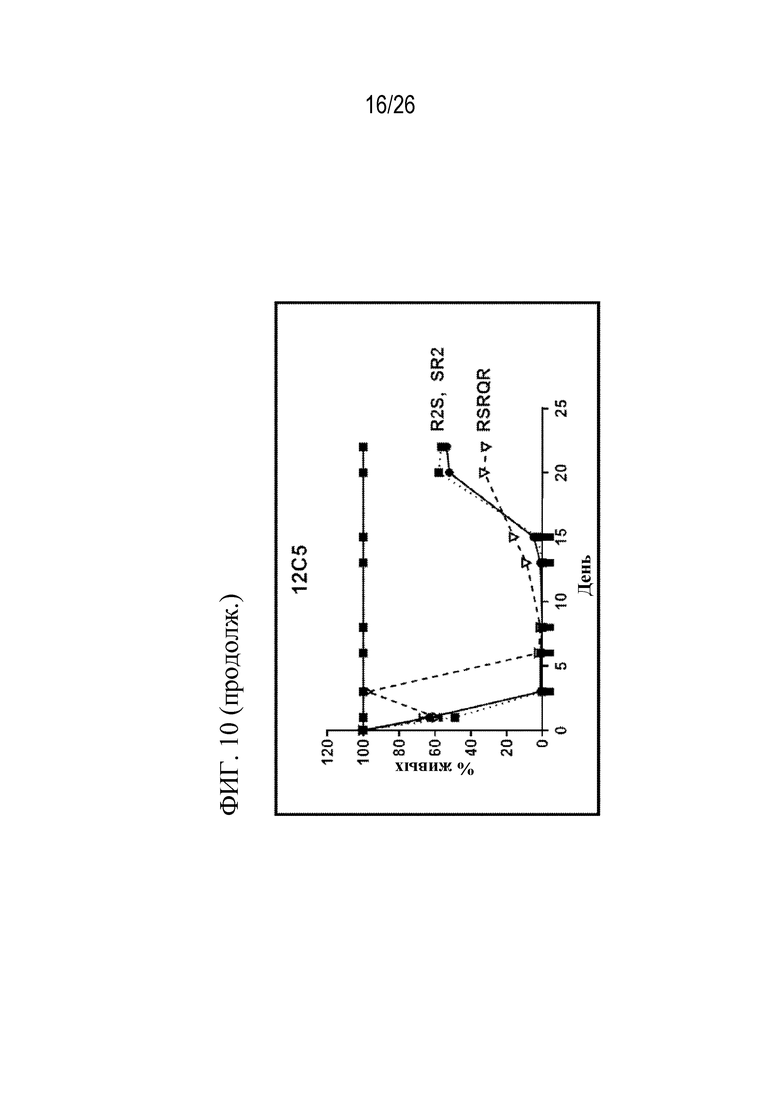

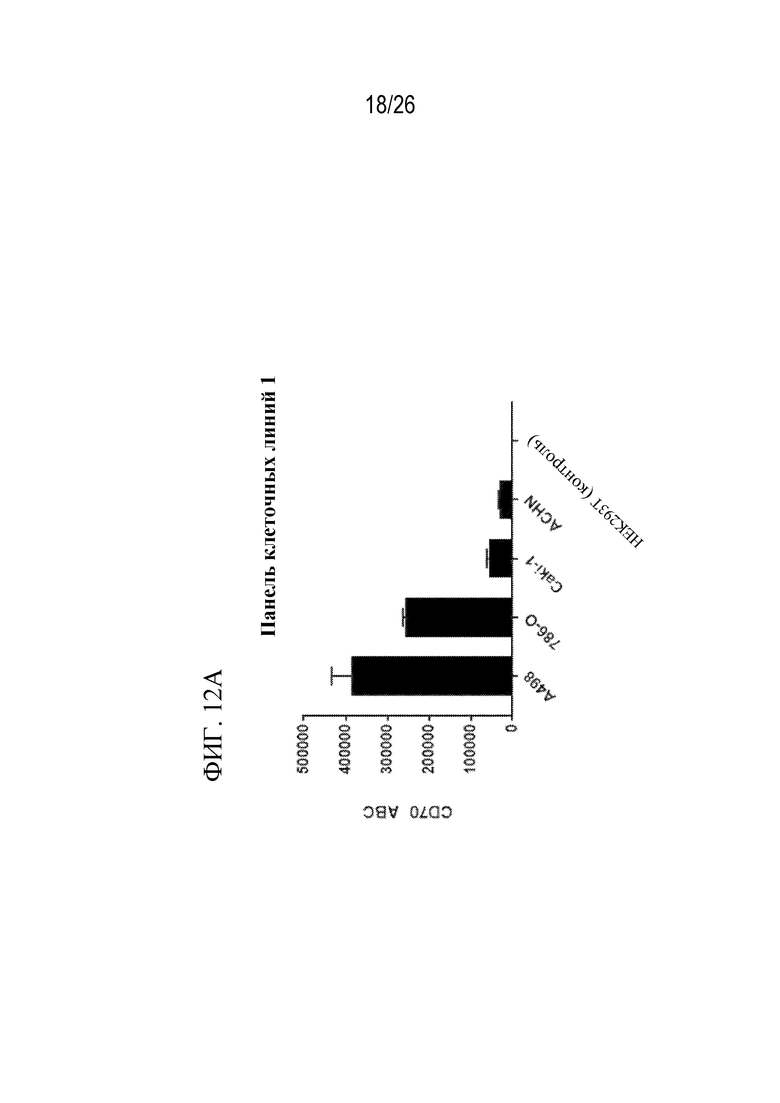
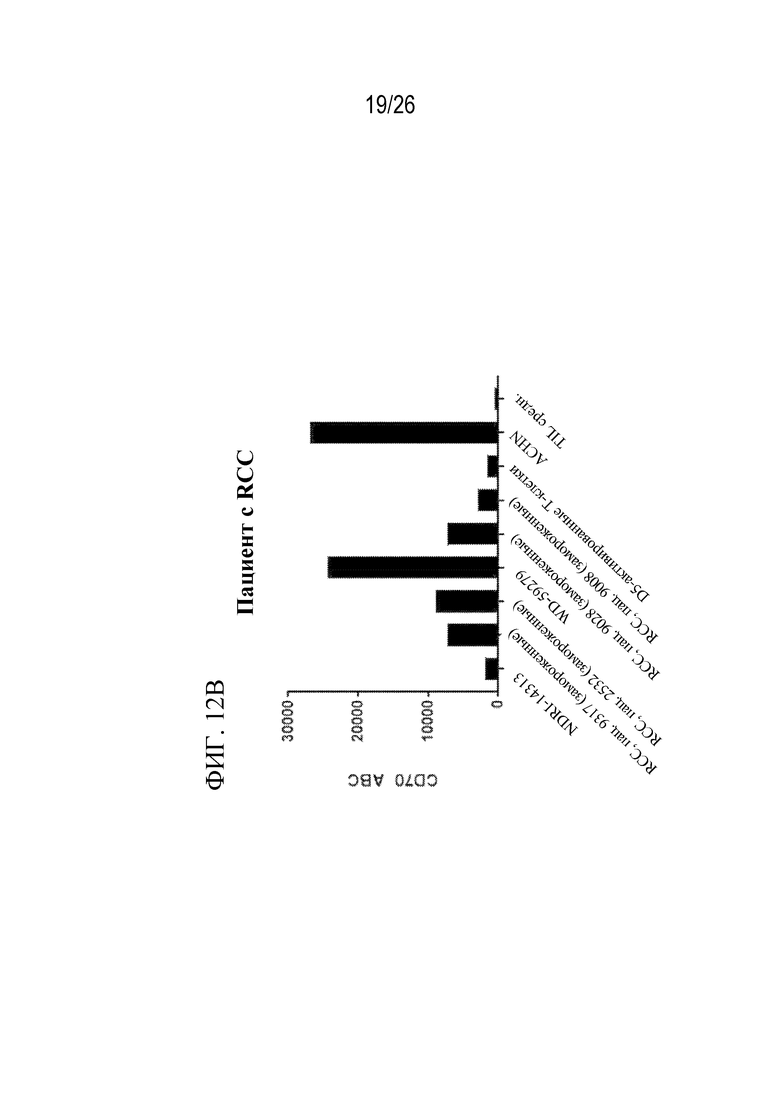
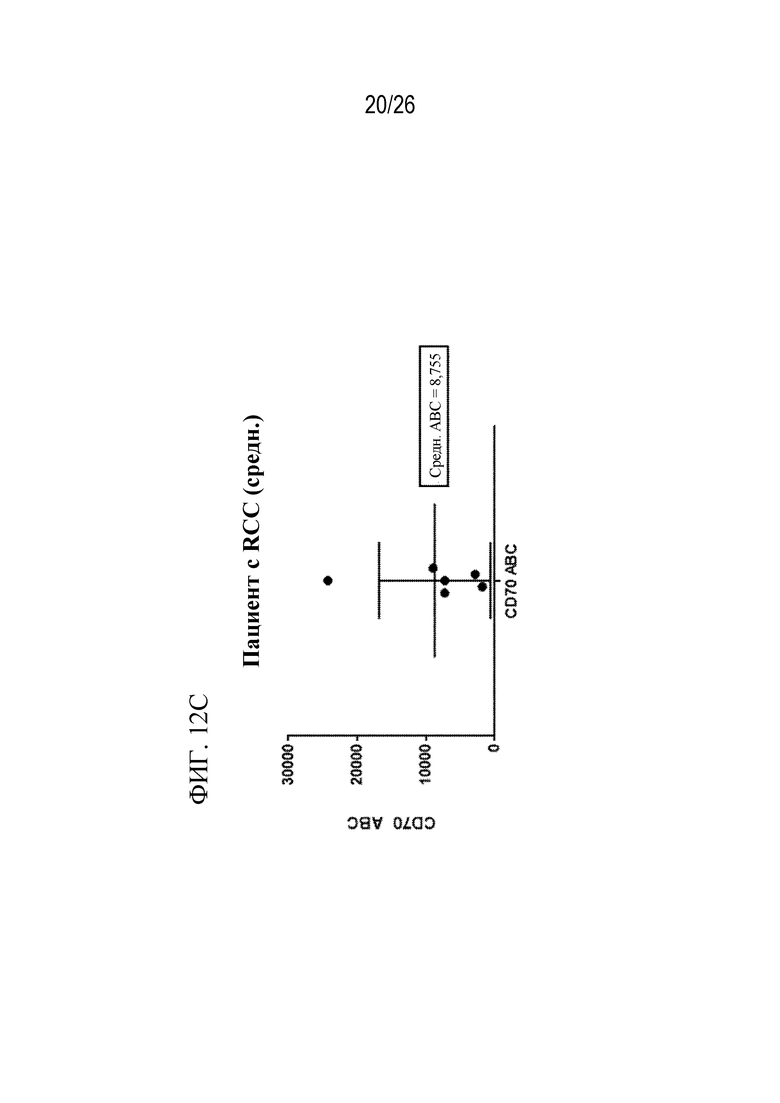
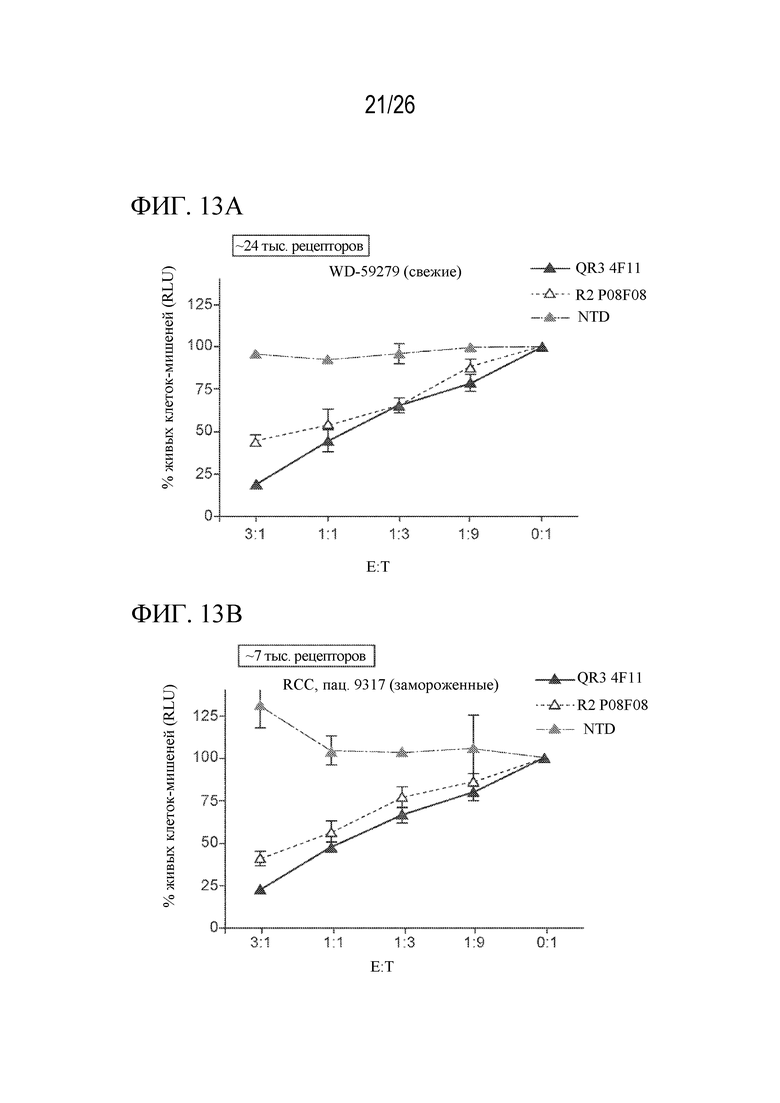
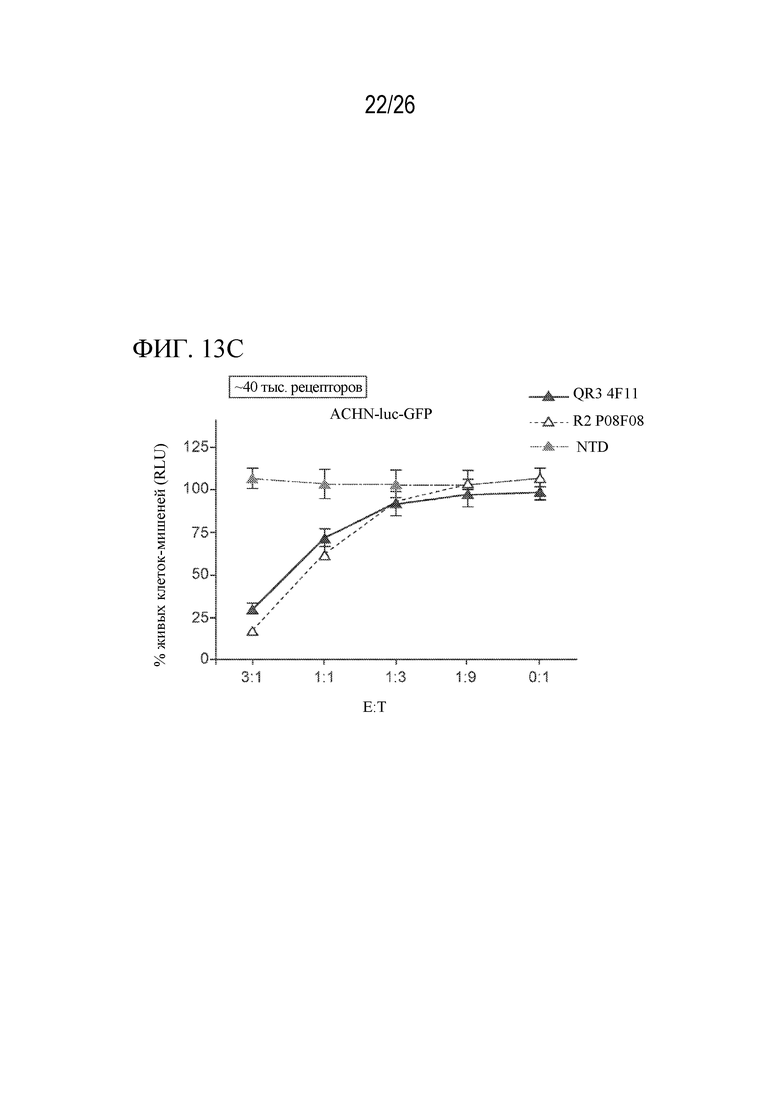
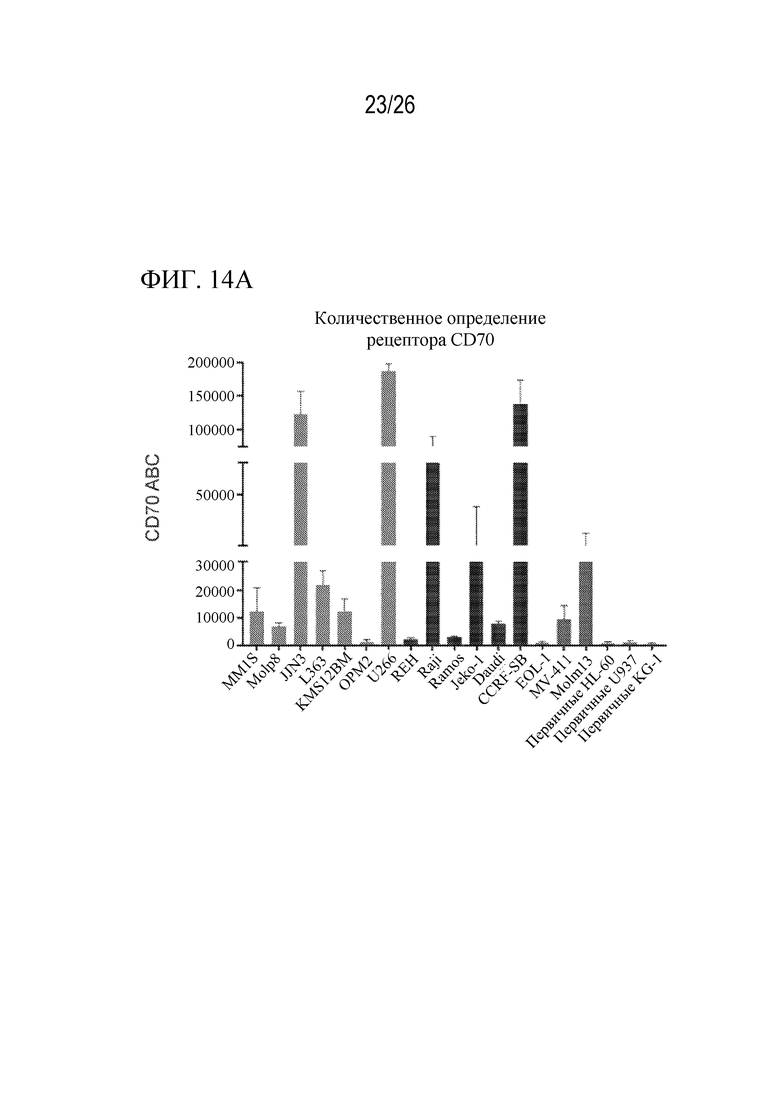
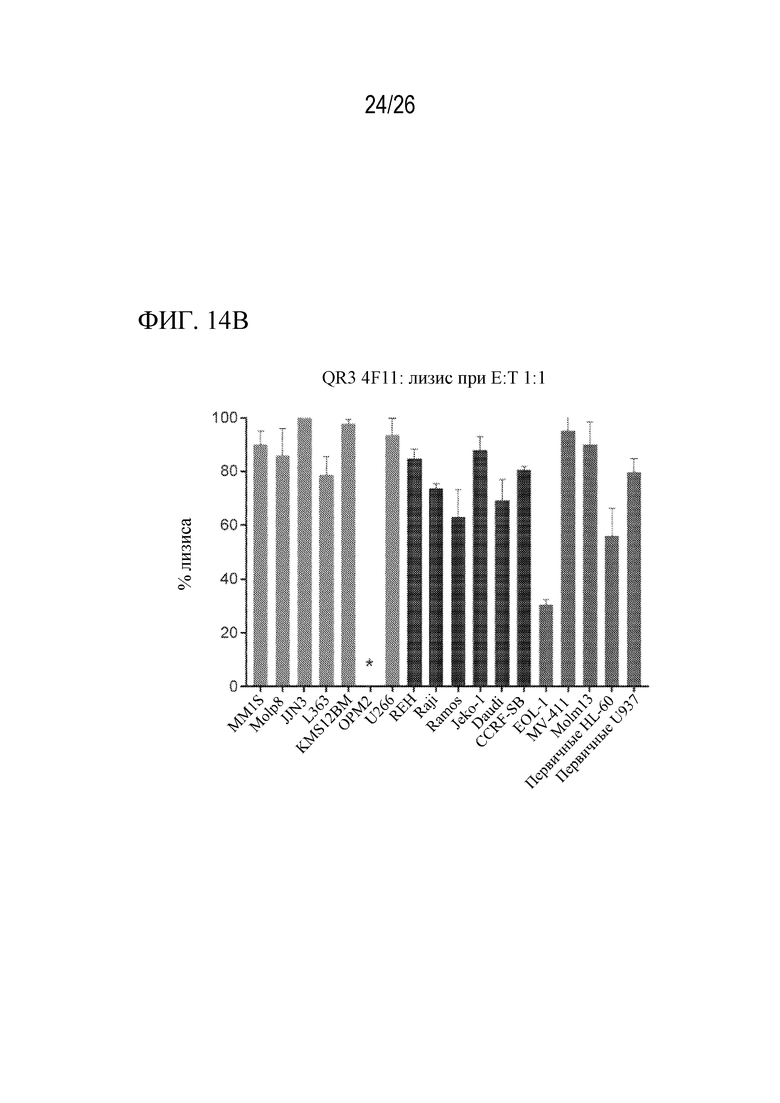


Настоящее изобретение относится к области биотехнологии, а именно к CAR (химерным антигенным рецепторам), которые специфически связываются с CD70. Также раскрыты сконструированные иммунные клетки, содержащие данные CAR, нуклеиновые кислоты, кодирующие CAR, и способы получения CAR, сконструированных иммунных клеток и нуклеиновых кислот. Изобретение эффективно в лечении состояния, ассоциированного со злокачественными клетками, экспрессирующими CD70. 12 н. и 46 з.п. ф-лы, 15 ил., 13 табл., 14 пр.
1. Химерный антигенный рецептор (CAR), специфический к кластеру дифференцировки 70 (CD70), содержащий внеклеточный лиганд-связывающий домен, первый трансмембранный домен и внутриклеточный сигнальный домен, где внеклеточный домен содержит одноцепочечный Fv-фрагмент (scFv), связывающийся с внеклеточным доменом CD70, где scFv содержит аминокислотные последовательности CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3, соответственно, выбранные из одной из SEQ ID NO:
a) 97-99, 100-101, 102, 217, 218, 219;
b) 478-480, 481-482, 483, 562, 563, 564;
c) 49-51, 52-53, 54, 193, 194, 195;
d) 55-57, 58-59, 60, 196, 197, 198;
e) 61-63, 64-65, 66, 199, 200, 201;
f) 67-69, 70-71, 72, 202, 203, 204;
g) 73-75, 76-77, 78, 205, 206, 207;
h) 79-81, 82-83, 84, 208, 209, 210;
i) 85-87, 88-89, 90, 211, 212, 213;
j) 91-93, 94-95, 96, 214, 215, 216;
k) 103-105, 106-107, 108, 220, 221, 222;
l) 109-111, 112-113, 114, 223, 224, 225;
m) 115-117, 118-119, 120, 226, 227, 228;
n) 121-123, 124-125, 126, 229, 230, 231;
o) 127-129, 130-131, 132, 232, 233, 234;
p) 133-135, 136-137, 138, 235, 236, 237;
q) 139-141, 142-143, 144, 238, 239, 240;
r) 145-147, 148-149, 150, 241, 242, 243;
s) 151-153, 154-155, 156, 244, 245, 246;
t) 157-159, 160-161, 162, 247, 248, 249;
u) 163-165, 166-167, 168, 250, 251, 252;
v) 169-171, 172-173, 174, 253, 254, 255;
w) 175-177, 178-179, 180, 256, 257, 258;
x) 181-183, 184-185, 186, 259, 260, 261;
y) 187-189, 190-191, 192, 262, 263, 264;
z) 382-384, 385-386, 387, 514, 515, 516;
aa) 388-390, 391-392, 393, 517, 518, 519;
bb) 394-396, 397-398, 399, 520, 521, 522;
cc) 400-402, 403-404, 405, 523, 524, 525;
dd) 406-408, 409-410, 411, 526, 527, 528;
ee) 412-414, 415-416, 417, 529, 530, 531;
ff) 418-420, 421-422, 423, 532, 533, 534;
gg) 424-426, 427-428, 429, 535, 536, 537;
hh) 430-432, 433-434, 435, 538, 539, 540;
ii) 436-438, 439-440, 441, 541, 542, 543;
jj) 442-444, 445-446, 447, 544, 545, 546;
kk) 448-450, 451-452, 453, 547, 548, 549;
ll) 454-456, 457-458, 459, 550, 551, 552;
mm) 460-462, 463-464, 465, 553, 554, 555;
nn) 466-468, 469-470, 471, 556, 557, 558;
oo) 472-474, 475-476, 477, 559, 560, 561;
pp) 484-486, 487-488, 489, 565, 566, 567;
qq) 490-492, 493-494, 495, 568, 569, 570;
rr) 496-498, 499-500, 501, 571, 572, 573;
ss) 502-504, 505-506, 507, 574, 575, 576;
tt) 508-510, 511-512, 513, 577, 578, 579; и
uu) 663-665, 666-667, 668, 669, 670, 671.
2. CAR, специфический к CD70, по п. 1, где scFv содержит CDRH1, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 97, 98 или 99; CDRH2, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 100 или 101; и CDRH3, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 102; CDRL1, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 217; CDRL2, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 218; и CDRL3, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 219.
3. CAR, специфический к CD70, по п. 1, где scFv содержит область VH, которая содержит аминокислотную последовательность, представленную под SEQ ID NO: 18, и область VL, которая содержит аминокислотную последовательность, представленную под SEQ ID NO: 17.
4. CAR, специфический к CD70, по п. 1, где scFv содержит CDRH1, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 478, 479 или 480; CDRH2, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 481 или 482; и CDRH3, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 483; CDRL1, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 562; CDRL2, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 563; и CDRL3, содержащую аминокислотную последовательность, представленную под SEQ ID NO: 564.
5. CAR, специфический к CD70, по п. 1, где scFv содержит область VH, которая содержит аминокислотную последовательность, представленную под SEQ ID NO: 371, и область VL, которая содержит аминокислотную последовательность, представленную под SEQ ID NO: 370.
6. CAR, специфический к CD70, по любому из пп. 1-5, где внутриклеточный сигнальный домен предусматривает сигнальный домен CD3ζ или домен 4-1BB.
7. CAR, специфический к CD70, по любому из пп. 1-6, содержащий второй внутриклеточный сигнальный домен.
8. CAR, специфический к CD70, по п. 7, где CAR содержит внутриклеточный сигнальный домен CD3ζ и внутриклеточный сигнальный домен 4-1BB.
9. CAR, специфический к CD70, по любому из пп. 1-8, содержащий шарнирный домен между внеклеточным лиганд-связывающим доменом и первым трансмембранным доменом.
10. CAR, специфический к CD70, по п. 9, где шарнирный домен выбран из группы, состоящей из шарнирного участка из CD8α человека, шарнирного участка из IgG1 и шарнирного участка из FcγRIIIα.
11. CAR, специфический к CD70, по любому из пп. 1-10, содержащий эпитоп CD20.
12. CAR, специфический к CD70, по п. 11, где эпитоп CD20 содержит аминокислотную последовательность, представленную под SEQ ID NO: 293, или SEQ ID NO: 294, или SEQ ID NO: 609.
13. CAR, специфический к CD70, по любому из пп. 1-12, где первый трансмембранный домен предусматривает трансмембранный домен цепи CD8α.
14. CAR, специфический к CD70, по любому из пп. 1-13, содержащий другой внеклеточный лиганд-связывающий домен, который не является специфическим к CD70.
15. CAR, специфический к CD70, по любому из пп. 1-14, где внеклеточный (внеклеточные) лиганд-связывающий (лиганд-связывающие) домен (домены), первый трансмембранный домен и внутриклеточный (внутриклеточные) сигнальный (сигнальные) домен (домены) расположены в одном полипептиде.
16. CAR, специфический к CD70, по любому из пп. 1-15, содержащий второй трансмембранный домен, где первый трансмембранный домен и внеклеточный (внеклеточные) лиганд-связывающий (лиганд-связывающие) домен (домены) расположены в первом полипептиде и где второй трансмембранный домен и внутриклеточный (внутриклеточные) сигнальный (сигнальные) домен (домены) расположены во втором полипептиде.
17. CAR, специфический к CD70, по п. 16, содержащий третий полипептид, содержащий третий трансмембранный домен, слитый с внутриклеточным сигнальным доменом из костимулирующей молекулы.
18. CAR, специфический к CD70, по п. 1, где CAR, специфический к CD70, содержит аминокислотную последовательность, представленную под SEQ ID NO: 311 - 334.
19. CAR, специфический к CD70, по п. 1, где CAR, специфический к CD70, содержит аминокислотную последовательность, представленную под SEQ ID NO: 319 или 596.
20. CAR, специфический к CD70, по п. 1, где CAR, специфический к CD70, содержит аминокислотную последовательность, представленную под SEQ ID NO: 596, 619, 620, 627, 628, 635, 636, 643, 644, 651, 672, 674, 676, 678 или 680.
21. CAR, специфический к CD70, по п. 1, где CAR, специфический к CD70, содержит аминокислотную последовательность, представленную под SEQ ID NO: 580-601.
22. Нуклеиновая кислота, кодирующая CAR, специфический к CD70, содержащая последовательность нуклеиновой кислоты, кодирующую CAR, специфический к CD70, по любому из пп. 18-21.
23. Нуклеиновая кислота по п. 22, содержащая последовательность нуклеиновой кислоты, представленную под SEQ ID NO: 336 или 337, или последовательность нуклеиновой кислоты, которая кодирует аминокислотную последовательность SEQ ID NO: 319 или SEQ ID NO: 596.
24. Вектор экспрессии, содержащий нуклеиновую кислоту по любому из пп. 22 или 23.
25. Сконструированная иммунная клетка, экспрессирующая на своей внешней клеточной мембране CAR, специфический к CD70, кодируемый нуклеиновой кислотой по любому из пп. 22-23 или вектором экспрессии по п. 24, где сконструированная иммунная клетка представляет собой естественную клетку-киллера (NK) или Т-клетку, где Т-клетка представляет собой Т-клетку, выбранную из группы, состоящей из воспалительных Т-лимфоцитов, цитотоксических Т-лимфоцитов и хелперных Т-лимфоцитов, или Т-клетка получена из группы, состоящей из CD4+ T-лимфоцитов и CD8+ T-лимфоцитов.
26. Сконструированная иммунная клетка по п. 25, дополнительно содержащая полинуклеотид, кодирующий «суицидный» полипептид, содержащий аминокислотную последовательность согласно любой из SEQ ID NO: 291, 292, 293, 295, 603-611, 660.
27. Сконструированная иммунная клетка по п. 26, где «суицидный» полипептид имеет аминокислотную последовательность SEQ ID NO: 291.
28. Сконструированная иммунная клетка по любому из пп. 25-27, дополнительно характеризующаяся разрушением одного или более эндогенных генов, где эндогенный ген кодирует TCRα, TCRβ, CD52, глюкокортикоидный рецептор (GR), дезоксицитидинкиназу (dCK), CD70 или белок контрольной точки иммунного ответа, такой как, например, белок запрограммированной смерти-1 (PD-1).
29. Сконструированная иммунная клетка по любому из пп. 25-27, дополнительно характеризующаяся разрушением TCRα и CD52 или TCRα, CD52 и CD70.
30. Сконструированная иммунная клетка по любому из пп. 25-29, где иммунная клетка получена от здорового донора.
31. Сконструированная иммунная клетка по любому из пп. 25-29, где иммунная клетка получена от пациента.
32. Сконструированная иммунная клетка по любому из пп. 25-31 для применения в качестве лекарственного препарата.
33. Сконструированная иммунная клетка по п. 32, где лекарственный препарат предназначен для применения в лечении рака.
34. Сконструированная иммунная клетка по п. 33, где рак выбран из группы, состоящей из почечно-клеточной карциномы, глиобластомы, глиомы, такой как глиома низкой степени злокачественности, неходжкинской лимфомы (NHL), болезни Ходжкина (HD), макроглобулинемии Вальденстрема, острого миелоидного лейкоза, множественной миеломы, диффузной крупноклеточной лимфомы, фолликулярной лимфомы и немелкоклеточного рака легкого.
35. Популяция сконструированных иммунных клеток по любому из пп. 25-34, где
a) указанная популяция клеток содержит процентную долю стволовых клеток памяти и центральных клеток памяти, составляющую более 20%, 30% или 40%, и/или
b) указанная популяция клеток обеспечивает достижение процентной доли лизиса клеток, экспрессирующих CD70, к дню 6, превышающей 10%, 20%, 30% или 40%, в случае рекурсивных клеток, экспрессирующих CD70, согласно измерению с применением подходящего скринингового анализа на основе стресс-теста.
36. Популяция сконструированных иммунных клеток по п. 35, где указанная популяция клеток обеспечивает достижение процентной доли лизиса клеток, экспрессирующих CD70, к дню 6, превышающей 20%, в случае рекурсивных клеток, экспрессирующих CD70, согласно измерению с применением подходящего скринингового анализа на основе стресс-теста.
37. Способ конструирования иммунной клетки, экспрессирующей CAR, специфический к CD70, кодируемый полинуклеотидом по любому из пп. 22, 23 или вектором экспрессии по п. 24, предусматривающий:
а) обеспечение иммунной клетки, где иммунная клетка представляет собой Т-клетку, дендритную клетку, киллерную дендритную клетку, тучную клетку, NK-клетку, B-клетку или T-клетку, выбранную из группы, состоящей из воспалительных T-лимфоцитов, цитотоксических T-лимфоцитов, регуляторных T-лимфоцитов и хелперных Т-лимфоцитов, или получена из стволовых клеток, клеток-предшественников, индуцированных плюрипотентных стволовых клеток, тотипотентных стволовых клеток или гемопоэтических стволовых клеток;
b) введение в клетку по меньшей мере одного полинуклеотида по п. 22 или 23 или вектора экспрессии по п. 24; и
с) обеспечение экспрессии указанного полинуклеотида или вектора в иммунной клетке.
38. Способ лечения состояния, ассоциированного со злокачественными клетками, экспрессирующими CD70, у субъекта, нуждающегося в этом, предусматривающий:
a) обеспечение эффективного количества сконструированной иммунной клетки по любому из пп. 25-34 или популяции сконструированных иммунных клеток по п. 35 или 36; и
b) введение указанных иммунных клеток или указанной популяции сконструированных иммунных клеток указанному пациенту.
39. Фармацевтическая композиция для лечения состояния, ассоциированного со злокачественными клетками, экспрессирующими CD70, содержащая эффективное количество сконструированной иммунной клетки по любому из пп. 25-34 или эффективное количество популяции сконструированных иммунных клеток по пп. 35, 36.
40. Способ лечения состояния, ассоциированного со злокачественными клетками, экспрессирующими CD70, у субъекта, предусматривающий введение нуждающемуся в этом субъекту эффективного количества фармацевтической композиции по п. 39.
41. Способ по п. 40, где состояние представляет собой рак.
42. Способ по п. 41, где рак выбран из группы, состоящей из почечно-клеточной карциномы, глиобластомы, глиомы, такой как глиома низкой степени злокачественности, неходжкинской лимфомы (NHL), болезни Ходжкина (HD), макроглобулинемии Вальденстрема, острого миелоидного лейкоза, множественной миеломы, диффузной крупноклеточной лимфомы, фолликулярной лимфомы и немелкоклеточного рака легкого.
43. Способ подавления роста или прогрессирования опухоли у субъекта, у которого имеются злокачественные клетки, экспрессирующие CD70, предусматривающий введение нуждающемуся в этом субъекту эффективного количества фармацевтической композиции по п. 39.
44. Способ подавления метастазирования злокачественных клеток, экспрессирующих CD70, у субъекта, предусматривающий введение нуждающемуся в этом субъекту эффективного количества фармацевтической композиции по п. 39.
45. Способ индуцирования регрессии опухоли у субъекта, у которого имеются злокачественные клетки, экспрессирующие CD70, предусматривающий введение нуждающемуся в этом субъекту эффективного количества фармацевтической композиции по п. 39.
46. CAR, специфический к CD70, по п. 1, где scFv содержит аминокислотные последовательности вариабельного домена легкой цепи и вариабельного домена тяжелой цепи, соответственно, выбранные из одной из SEQ ID NO:
a) 17 и 18;
b) 370 и 371;
c) 1 и 2;
d) 3 и 4;
e) 5 и 6;
f) 7 и 8;
g) 9 и 10;
h) 11 и 12;
i) 13 и 14;
j) 15 и 16;
k) 19 и 20;
l) 21 и 22;
m) 23 и 24;
n) 25 и 26;
o) 27 и 28;
p) 29 и 30;
q) 31 и 32;
r) 33 и 34;
s) 35 и 36;
t) 37 и 38;
u) 39 и 40;
v) 41 и 42;
w) 43 и 44;
x) 45 и 46;
y) 47 и 48;
z) 338 и 339;
aa) 340 и 341;
bb) 342 и 343;
cc) 344 и 345;
dd) 346 и 347;
ee) 348 и 349;
ff) 350 и 351;
gg) 352 и 353;
hh) 354 и 355;
ii) 356 и 357;
jj) 358 и 359;
kk) 360 и 361;
ll) 362 и 363;
mm) 364 и 365;
nn) 366 и 367;
oo) 368 и 369;
pp) 372 и 373;
qq) 374 и 375;
rr) 376 и 377;
ss) 378 и 379;
tt) 380 и 381; и
uu) 661 и 662; или
антигенсвязывающая молекула конкурирует за связывание с CD70 с антигенсвязывающей молекулой по любому из (a)-(uu).
47. CAR, специфический к CD70, по п. 46, где внутриклеточный сигнальный домен предусматривает сигнальный домен CD3ζ или домен 4-1ВВ.
48. CAR, специфический к CD70, по любому из пп. 46, 47, содержащий второй внутриклеточный сигнальный домен.
49. CAR, специфический к CD70, по п. 48, где CAR содержит внутриклеточный сигнальный домен CD3ζ и внутриклеточный сигнальный домен 4-1BB.
50. CAR, специфический к CD70, по любому из пп. 46-49, содержащий шарнирный домен между внеклеточным лиганд-связывающим доменом и первым трансмембранным доменом.
51. CAR, специфический к CD70, по п. 50, где шарнирный домен выбран из группы, состоящей из шарнирного участка из CD8α человека, шарнирного участка из IgG1 и шарнирного участка из FcγRIIIα.
52. CAR, специфический к CD70, по любому из пп. 46-50, дополнительно содержащий эпитоп CD20.
53. CAR, специфический к CD70, по п. 53, где эпитоп CD20 содержит аминокислотную последовательность, представленную под SEQ ID NO: 293, или SEQ ID NO: 294, или SEQ ID NO: 609.
54. CAR, специфический к CD70, по любому из пп. 46-53, где первый трансмембранный домен предусматривает трансмембранный домен цепи CD8α.
55. CAR, специфический к CD70, по любому из пп. 46-54, содержащий другой внеклеточный лиганд-связывающий домен, который не является специфическим к CD70.
56. CAR, специфический к CD70, по любому из пп. 46-55, где внеклеточный (внеклеточные) лиганд-связывающий (лиганд-связывающие) домен (домены), первый трансмембранный домен и внутриклеточный (внутриклеточные) сигнальный (сигнальные) домен (домены) расположены в одном полипептиде.
57. CAR, специфический к CD70, по любому из пп. 46-56, содержащий второй трансмембранный домен, где первый трансмембранный домен и внеклеточный (внеклеточные) лиганд-связывающий (лиганд-связывающие) домен (домены) расположены в первом полипептиде и где второй трансмембранный домен и внутриклеточный (внутриклеточные) сигнальный (сигнальные) домен (домены) расположены во втором полипептиде.
58. CAR, специфический к CD70, по п. 57, содержащий третий полипептид, содержащий третий трансмембранный домен, слитый с внутриклеточным сигнальным доменом из костимулирующей молекулы.
| WO 2015121454 A1, 20.08.2015 | |||
| JIN L | |||
| et al., CD70, a novel target of CAR T-cell therapy for gliomas | |||
| Neuro Oncol | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Vol | |||
| Прибор для промывания газов | 1922 |
|
SU20A1 |
| No | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Pp | |||
| Устройство двукратного усилителя с катодными лампами | 1920 |
|
SU55A1 |
| US 2013323214 A1, 05.12.2013 | |||
| ОДНОЦЕПОЧЕЧНЫЕ МУЛЬТИВАЛЕНТНЫЕ СВЯЗЫВАЮЩИЕ БЕЛКИ С ЭФФЕКТОРНОЙ ФУНКЦИЕЙ | 2007 |
|
RU2487888C2 |
| WO 2018027197 A1, 08.02.2018. | |||
Авторы
Даты
2023-08-16—Публикация
2019-01-31—Подача