В декабре 2019 г. в Китае произошла вспышка тяжелой острой респираторной инфекции COVID-19 (CoronaVirus Disease-19), вызванной новым коронавирусом SARS CoV-2. С момента своего появления вирус распространился почти на все страны мира. Всемирная организация здравоохранения объявила, что вспышка приняла характер пандемии. Эпидемия COVID-19 стала третьей по счету, вызванной коронавирусами, после эпидемий тяжелого острого респираторного синдрома 2002-2003 гг. и ближневосточного респираторного синдрома. По данным ВОЗ на начало декабря 2020 года зафиксировано более 65 млн заразившихся и более 1,4 млн умерших от короновирусной инфекции. Продолжающаяся эпидемия COVID-19 представляет серьезную угрозу человечеству, включая прямое влияние на повседневную жизнь миллионов людей и негативное воздействие на мировую экономику.
В настоящее время отсутствуют эффективные средства этиотропной и патогенетической терапии короновирусных инфекций. Основными задачами этиотропной и патогенетической терапии коронавирусных инфекций являются снижение вирусной нагрузки и/или уменьшение выраженности воспаления в легких. Одобренных этиотропных препаратов против SARS-CoV-2 на сегодня нет, хотя имеется довольно большое количество кандидатных препаратов, протестированных в доклинических исследованиях. Применяется также патогенетическая и симптоматическая терапия, направленная на уменьшение выраженности интоксикакции и воспалительного процесса в легких, восстановление оксигенации крови, коррекцию водно-солевого баланса и т.д. Поэтому основным подходом борьбы с COVID-19 должна стать своевременная вакцинопрофилактика.
Одобренных к клиническому применению вакцин против SARS-CoV-2 нет, хотя разработано много кандидатных препаратов. Кандидатные вакцины относятся к следующим типам:
1) субъединичные вакцины (как правило, на основе рекомбинантного белка S или его рецептор-связывающего домена);
2) ДНК-вакцины на основе генетических конструкций, кодирующих цельный белок S или его рецепторсвязывающий домен;
3) векторные вакцины на основе непатогенных вирусов (аденовирусов, вируса Vaccinia и др.), в геном которых встроен один или несколько генов коронавирусов;
4) убитые цельновирионные вакцины;
5) ослабленные живые вакцины, полученные путем генно-инженерных модификаций вируса дикого типа, направленных на удаление или инактивацию факторов вирулентности (ингибиторов интерферонового ответа, медиаторов цитопатического эффекта).
Все перечисленные вакцины, возможно, позволят создать защитные титры нейтрализующих антител. С целью повышения эффективности вакцинации целесообразно вводить в состав вакцинных препаратов иммуноадъюванты.
При использовании адъювантов появляется возможность повысить иммуногенность вакцин в отношении набора антигенно отличных штаммов, а также при иммунизации различных популяционных групп, в том числе групп риска. Кроме того, при значительном повышении иммуногенности за счет добавления адъюванта к вакцине появляется возможность перехода на простые (однократные) схемы иммунизации, а также снижения дозы антигена. Это особенно важно для вакцин в условиях пандемии, поскольку при той же мощности производства будет получено больше доз вакцины, и, как следствие, иммунизировано больше людей.
Таким образом, разработка отечественного безопасного и эффективного препарата -вакцины против коронавирусной инфекции, содержащей корпускулярный адьювант, -представляется стратегически важным аспектом защиты населения Российской Федерации от тяжелых социальных и экономических последствий пандемии, которые возможно контролировать с помощью вакцинопрофилактики.
Перечень иллюстраций
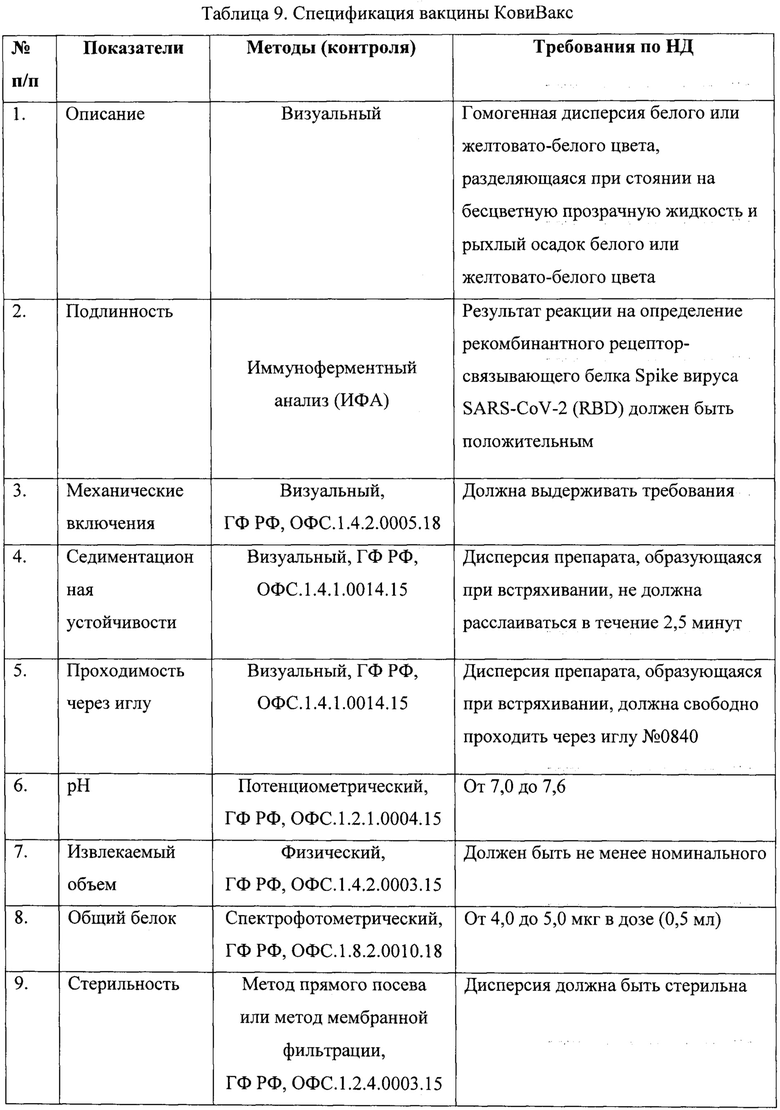
Рис. 1. Структурная формула бетулина
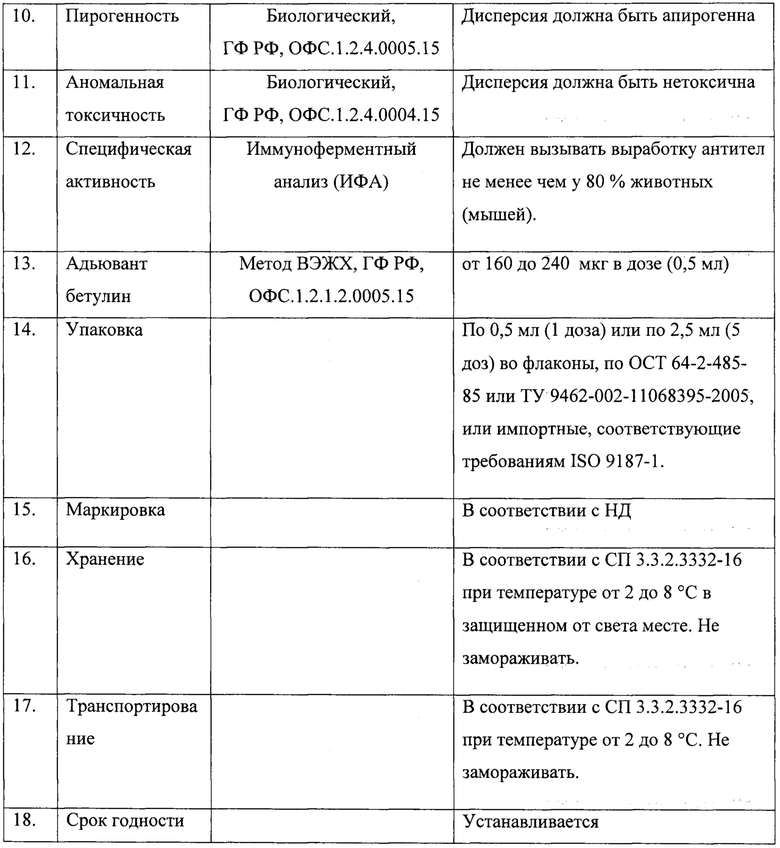
Рис. 2. Хроматографический профиль ТГФ в образце КА после стадии ультрафильтрации
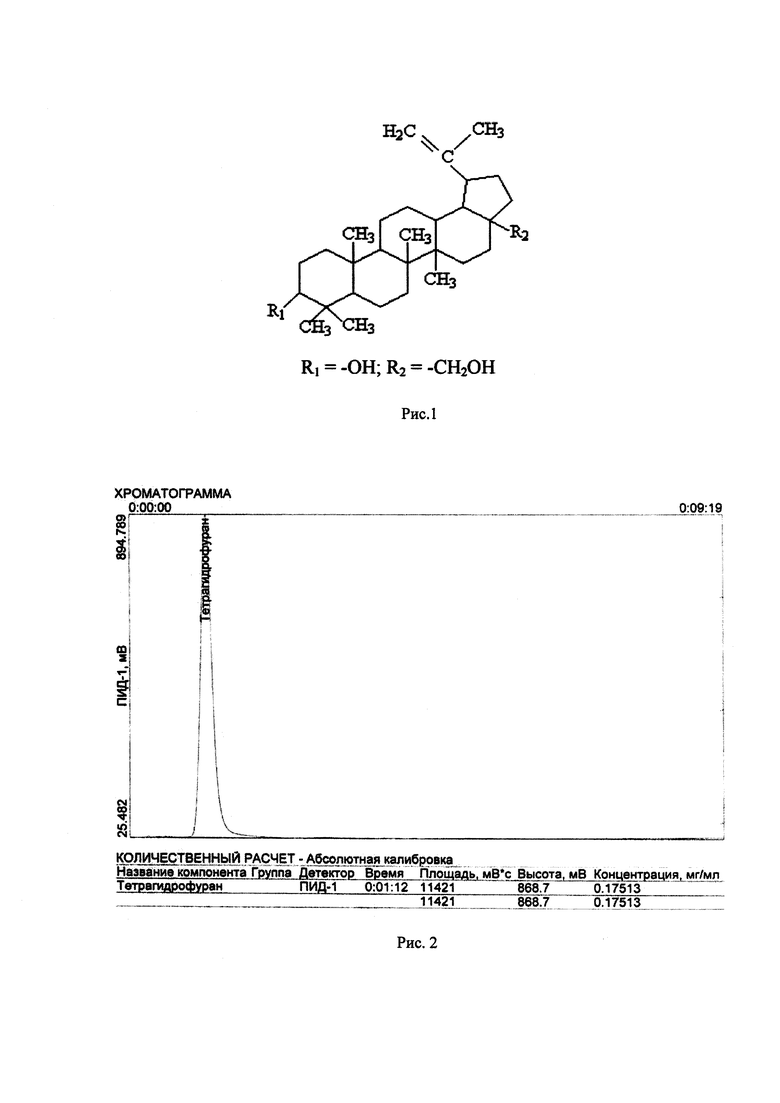
Рис. 3 Размер сферических аморфных наночастиц КА САНЧ
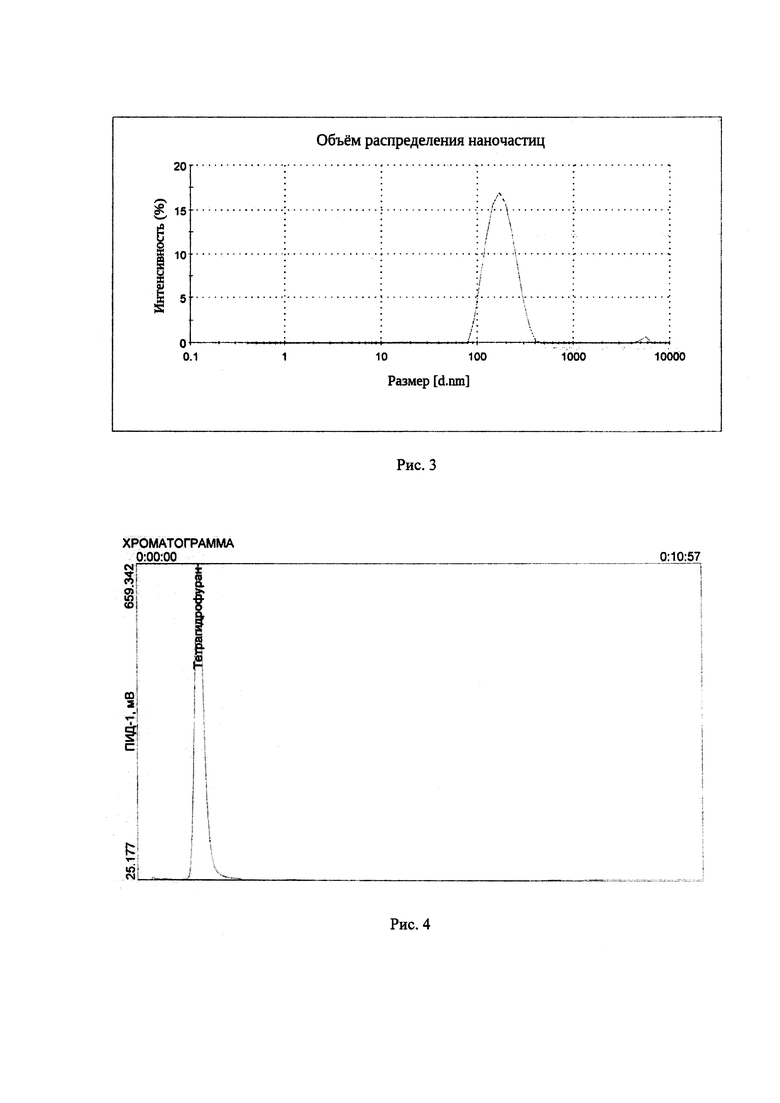
Рис. 4. Хроматографический профиль ТГФ в образце КА после стадии ультрафильтрации
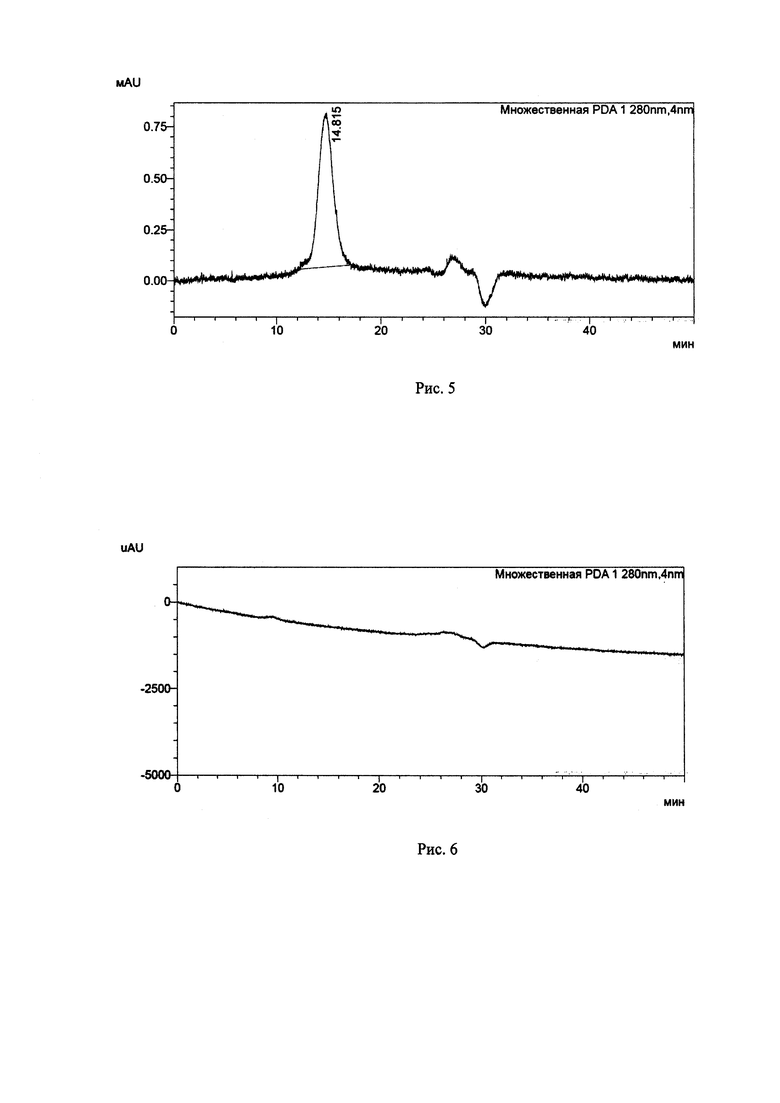
Рис. 5 и 6. Хроматографический профиль образца фармацевтической субстанции.
Описание изобретения
Нами была разработана лабораторная технология получения корпускулярного адъюванта (КА) на основе природного бетулина для последующего его использования при производстве вакцины. Объектом разработки являлся корпускулярный адъювант на основе природного пентациклического тритерпенового вещества - бетулина (бетуленол, бетулинол, лупендиол). Препарат предназначен для использования в качестве адъюванта профилактических вакцин.
Бетулин является тритерпеновым спиртом, обладающим двумя гидроксильными группами (рис. 1). Растворимость бетулина составляет менее 1 мкг/мл, поэтому создание водорастворимой формы весьма актуально. Поиск таких форм привел к созданию сферических аморфных наночастиц на основе бересты.
К адъювантам, используемым в производстве вакцинных препаратов, в соответствии с руководством ВОЗ и нормативными документами, действующими в России, предъявляются следующие требования: они должны быть стерильными, апирогенными, нетоксичными. Однако, как в лабораторной технологии получения КА, разработанной на кафедре биотехнологии и нанобиотехнологии Московского государственного университета тонких химических технологий имени М. В. Ломоносова (МИТХТ им. М.В. Ломоносова), так и в масштабированном ее варианте не предусмотрена стадия стерилизации [RU 2355423 "Адъювант"; A61K 47/06; С08Н 5/04; опубликован 20.05.2009]. Согласно данному способу адъювант получают путем растворения коммерчески доступного сухого экстракта бересты в органическом растворителе, тетрагидрофуране (ТГФ), при концентрации 2,5-5 г/л; добавляют к указанному раствору большое количество воды (до 25 объемов воды по отношению к объему раствора); удаляют растворитель и основную часть воды. К полученному водному раствору наночастиц добавляют криопротектор (например, сорбит) и осуществляют лиофилизацию. Перед использованием адъюванты растворяют в фосфатном буфере (рН 7,5), обрабатывают ультразвуком в течение 15 минут, после чего охлаждают.
Задачей изобретения являлось создание технологии получения КА из природного бетулина, отвечающего требованиям к вакцинным препаратам для парентерального введения по показателям стерильности, пирогенности, иммуногенности и безопасности.
Техническим результатом является разработка способа получения корпускулярного бетулина с оптимальным методом стерилизации для использования в качестве адъюванта в вакцине против коронавируса SARS-COV2.
Отработка методов стерилизации КА
На первых этапах наших исследований был проведен подбор оптимального метода стерилизации КА, который можно было бы использовать на заключительной технологической стадии производства. Для получения стерильного адъюванта оценивалась возможность использования термических и мембранных методов стерилизации.
В качестве термического метода применили паровую стерилизацию при следующих режимах: 120°С - 0,5 атмосферы (0,5 кгс/см2) - 10 минут; 120°С - 1,0 атмосфера (1,0 кгс/см2) - 45 минут. В результате проведенных исследований было установлено, что испытанные условия термической обработки не пригодны: после стерилизации образуются крупные хлопьевидные частицы, не распадающиеся при интенсивном перемешивании, которые при длительном хранении всплывают на поверхность. Термическая обработка, нарушая структуру аморфных наночастиц, вызывала их агрегацию.
С целью отработки мембранных методов стерилизации проводились исследования по изучению возможности применения мембран из нейлона, полиэфирсульфона, ацетатацеллюлозы. При выполнении экспериментов было отмечено, что на поверхности таких фильтров происходит сорбция частиц: фильтруемый материал над мембраной становился прозрачным за счет образования осадка частиц на ней, при этом снижалась фильтрующая способность мембраны. Следовательно, данные фильтроэлементы оказались непригодными для стерилизующей фильтрации КА.
Таким образом, было установлено, что стерилизация КА мембранными и термическими методами на конечных этапах производства невозможна.
Получение стерильного раствора бетулина в тетрагидрофуране, как основы для производства КА.
Для получения адъюванта, отвечающего требованиям к препаратам для парентерального введения, нами предложена технология, в которой все исходные растворы должны стерилизоваться на начальных этапах производства КА, и весь дальнейший технологический процесс должен проходить в стерильных условиях.
При отработке условий стерилизующей фильтрации раствора бетулина в тетрагидрофуране (10 мг/мл) использовали нейлоновую мембрану с диаметром пор 0,22 мкм марки NRG Pall N66+. Данный фильтроэлемент является гидрофильным с модифицированным зарядом, поэтому первоначально нам представлялось целесообразным оценить его сорбционную способность, которая могла отрицательно отразиться на выходе готового продукта. Для этого Исполнителем были проведены опыты, в ходе которых было определено содержание бетулина методом высокоэффективной жидкостной хроматографии ВЭЖХ до и после фильтрации и затем рассчитывали процент сорбции бетулина (табл. 1).
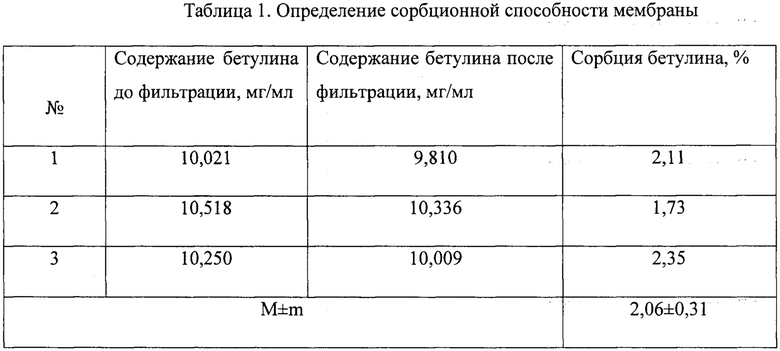
Из представленных в табл. 1 данных видно, что используемая мембрана обладает низкой сорбционной способностью: содержание бетулина в растворе до и после фильтрации различаются очень незначительно, только около 2% активного вещества сорбировалось мембраной. Таким образом, сорбционные свойства испытанного в опытах фильтроэлемента марки NRG Pall N66+ позволяют его использовать для стерилизующей фильтрации КА.
Далее необходимо было установить химическую стойкость мембранного материала по отношению к органическому растворителю тетрагидрофурану ТГФ. Для этого был применен метод "точки пузырька", рекомендованный методическими указаниями МУ 42-51-19-93 Минздрава РФ. При использовании фильтрационных систем, в соответствии с требованиями GMP, необходима проверка целостности мембранных фильтрующих элементов. Согласно МУ 42-51-19-93 при стерилизующей фильтрации следует проводить тестирование на целостность до и после каждого процесса фильтрации. Следует отметить, что нарушение целостности фильтроэлемента (мембраны) также может произойти и во время его стерилизации, когда фильтр подвергается воздействию высокой температуры и повышенному давлению. В опытах по определению целостности мембран до и после фильтрования ТГФ-содержащего раствора бетулина с использованием метода "точки пузырька" также проводили визуальный осмотр мембран после процесса стерилизующей фильтрации.
Тест "точка пузырька" по окончании фильтрации осуществляется автоматически. Когда весь объем жидкости отфильтровывался, поток газа, используемый для передавливания, должен автоматически прекратиться, как только газ достигнет поверхности насыщенной жидкостью мембраны. При этом в стеклянном приемнике не должно наблюдаться появление пузырьков газа.
В результате проведенных испытаний было установлено, что фильтрующая мембрана в течение 20 минут сохраняла избыточное давление, созданное в фильтрующей системе, и через слой жидкости не проходили пузырьки газа. Визуальный осмотр мембран после процесса фильтрации также подтверждал целостность фильтроэлемента (мембраны). Полученные результаты показали высокую химическую стойкость стерилизующей мембраны.
Таким образом, проведенные эксперименты, в которых была установлена низкая сорбционная способность стерилизующей мембраны марки NRG Pall N66+ по отношению к раствору бетулина в тетрагидрофуране и ее устойчивость к действию ТГФ, показали возможность использования мембранного способа стерилизации исходного раствора в технологии получения КА.
Получение гомогенной дисперсии КА
С целью получения гомогенных дисперсии КА к стерильной смеси 1% раствора бетулина в тетрагидрофуране, в соответствии с технологией, добавляли 25-кратный объем стерильного 0,01 М трис-буфера (рН-9,0±0,1) с помощью перистальтического насоса при постоянном перемешивании в течение 15 минут магнитной мешалкой пропеллерного типа. После добавления буфера содержание ТГФ в растворе составляло 3,85%. Далее полученную суспензию обрабатывали ультразвуком при 35 кГц в течение 10 минут. Для этого стеклянную емкость с полученной суспензией подвергали обработке в ультразвуковой бане. В результате обработки получали белую равномерную суспензию без конгламератов и включений. За гомогенностью суспензии следили по светорассеянию, последовательно обрабатывая по 30 секунд до получения двух одинаковых спектров распределения частиц в диапазоне 100-150 нанометров.
Ультрафильтрация. Отработка метода очистки
На следующем этапе отрабатывали метод очистки дисперсии КА. С целью удаления токсичного ТГФ применяли ультрафильтрацию на полых волокнах с номинальной отсекающей молекулярной массой 100 или 300 кДа в режиме фильтрации. На первых этапах ультрафильтрации при быстром снижении концентрации ТГФ происходила частичная сорбция КА на мембранах установки, при этом скорость фильтрации снижалась незначительно, а выход готового продукта уменьшался. Поэтому необходимо было отработать параметры ультрафильтрационного процесса, препятствующие сорбции на мембранах КА и обеспечивающие эффективное удаление ТГФ. В результате проведенных экспериментов по оптимизации условий очистки было показано, что для предотвращения сорбции необходимо использовать 2-3-кратное разведение исходной дисперсии КА. При этом скорость ультрафильтрации составляла 1,0-1,2 л/минуту, давление устанавливали в пределах 0,6-0,8 атм. Для диафильтрации использовали 10-кратный объем 0,01 М трис-буфера с рН 9,00 ал для повышения выхода адъюванта после каждого объема диафильтрующего буферного раствора включали обратный поток с последующей обработкой суспензии ультразвуком в течение 3 минут при 35 кГц
Затем дисперсии концентрировали до содержания бетулина 1,0-2,0 мг/мл. Концентрацию бетулина определяли методом ВЭЖХ. После ультрафильтрации в КА контролировали остаточное количество ТГФ газо-жидкостной хроматографией (рис. 2).
После ультрафильтрации было установлено, что содержание ТГФ составляло 0,176±0,009 мг/мл.
Таким образом, отработанные условия процесса ультрафильтрации обеспечивают эффективное удаление токсичного тетрагидрофурана.
Характеристика полученных частиц КА
По внешнему виду полученный адъювант КА представлял собой дисперсию белого или желтовато-белого цвета, разделяющаяся при хранении на прозрачную надосадочную жидкость и легкий осадок, полностью разбивающийся при встряхивании.
Первоначально мы провели оценку готового препарата по показателю стерильности методом прямого посева на питательную среду. В пробирки с тиогликолевой питательной средой вносили по 1 мл адъюванта с концентрацией КА 1 мг/мл, восстановленного из лиофилизата. Посевы инкубировали при температуре 32,5±2,5°С и 22,5±2,5°С. После 14-суточной инкубации питательная среда в пробирках оставалась прозрачной, т.е. роста микроорганизмов не наблюдалось. Таким образом, было установлено, что полученные лиофилизированные образцы КА стерильны.
Для проверки на пирогенность образцы КА вводили кроликам по 200 мкг на килограмм массы внутривенно. При этом максимальная сумма изменения температуры у трех кроликов составила 0,9°С (табл. 2), что свидетельствует об апирогенности КА.
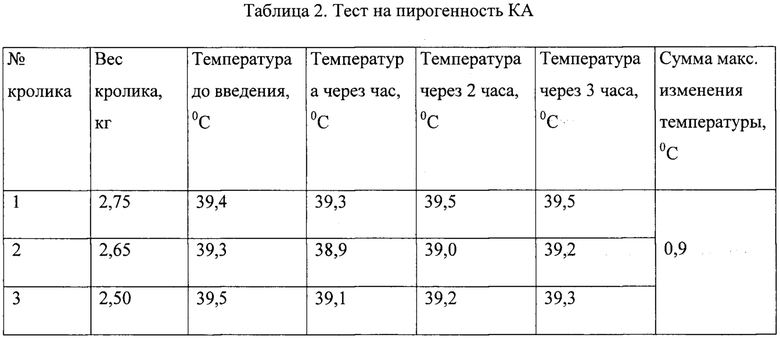
Таким образом, разработанная технология позволяет получать препарат КА стерильным и апирогеными, что удовлетворяет требованиям, предъявляемым к препаратам для парентерального введения, и позволяет их использовать в качестве вакцинных адъювантов.
Основной характеристикой адъювантов на основе наночастиц является размер и дзета-потенциал, т.к. от размера и заряда частиц зависит их адъювантная способность. Во многих работах отмечают, что именно размер частиц играет определяющую роль в эффективности адъювантов. Причем, наиболее эффективны в качестве иммунологических адъювантов частицы субмикронной области. По данным P.L. Mottram. Туре 1 and 2 immunity following vaccination is influenced by nanoparticle size: formulation of a model vaccine for respiratory syncytial virus / P. Mottram [et al.] // Mol. Pharm. - 2006. - Vol.4, №1. - P. 73-84, частицы с размером до 500 нм являлись оптимальными для поглощения макрофагами.
На этапах отработки технологии корпускулярного адъюванта определяли дзета-потенциал и размер частиц. Дзета-потенциал определяли методом электрофоретического рассеяния по изменению распределения частиц в электрическом поле с помощью прибора Zetasizer Nano фирмы Malvern. Дзета-потенциал - электрический потенциал, который возникает при движении частиц между адсорбционным слоем ионов, располагающимся на поверхности частиц, и диффузионным слоем ионов среды, окружающим частицу. Размер КА определяли на приборе Zetasizer Nano ZS фирмы Malvern методом лазерного корреляционного светорассеяния под углом 170° с длиной волны λ=633 нм. Метод определения размеров дисперсных частиц основан на анализе спектра рассеянного света. Метод является абсолютным, не требующим предварительной калибровки с использованием стандартных образцов. Лазерное корреляционное светорассеяние - это метод измерения средней скорости движения дисперсных частиц путем анализа динамических флуктуаций интенсивности рассеянного света, т.е. определение спектральной плотности или временной корреляционной функции рассеянного света. Хаотическое броуновское движение дисперсных частиц приводит к микроскопическим флуктуациям их локальной концентрации, что, в свою очередь, вызывает локальные флуктуации показателя преломления среды. При прохождении лазерного луча, представляющего собой плоскую, монохроматическую, линейно поляризованную волну, через такую среду часть света будет рассеяна на этих локальных неоднородностях. Флуктуации интенсивности рассеянного света будут соответствовать флуктуациям локальной концентрации дисперсных частиц, что позволит измерить коэффициент диффузии дисперсных частиц в жидкости. Поскольку коэффициент диффузии дисперсных частиц однозначно связан с размером частиц, лазерное корреляционное светорассеяние, по существу, является методом измерения размеров таких субмикронных частиц. Размер частиц рассчитывается по формуле Стокса-Эйнштейна, которая связывает размер частиц с их коэффициентом диффузии и вязкостью жидкости.
Как видно из данных, представленных на рис. 3, частицы в полученных образцах КА имеют средние размеры 160-180 нм. Значение дзета-потенциала составило минус 44,3 мВ. Наличие отрицательного заряда может способствовать эффективному связыванию с антигеном.
Таким образом, с использованием предлагаемой технологии можно получать частицы, эффективно связывающие антиген и обладающие адъювантным действием.
Методики контроля качества образцов КА
Определение концентрации бетулина в дисперсиях КА
При отработке технологического процесса получения КА и оценке готового продукта одним из важных контрольных параметров является содержание бетулина. Наиболее простой способ определения концентрации дисперсии по оценке рассеивания света не может дать точной информации, поскольку здесь имеет место зависимость не только от количества частиц, но и от их размера и формы. Незначительные изменения размера и формы наночастиц могут вызвать существенные различия в рассеивании света.
При выполнении данных исследований был разработан оригинальный метод определения содержания бетулина с использованием высокоэффективной жидкостной хроматографии. Высокоэффективная жидкостная хроматография (ВЭЖХ), интенсивно развиваясь несколько последних десятилетий, зарекомендовала себя в качестве одного из самых универсальных методов разделения и фармакопейного анализа субстанций и лекарственных средств.
Метод ВЭЖХ применим для разделения значительно более широкого круга веществ, чем газовая хроматография, поскольку большая часть веществ не обладает летучестью, а многие биологически активные вещества неустойчивы при высоких температурах.
Из всех вариантов ВЭЖХ, обращенно-фазовый применяется в настоящее время наиболее широко. Его привлекательность определяется методической простотой и универсальностью, во многих случаях - простотой механизма сорбции и предсказуемостью поведения веществ на основании их строения. На сегодняшний день большинство анализов выполняется на неполярных привитых фазах с применением следующих типов детекторов: ультрафиолетовые, флуориметрические, электрохимические, масс-спектрометрические.
Метод ВЭЖХ отличается большой селективностью и чувствительностью, а также универсальностью, позволяющей проводить качественный и количественный анализ в субстанциях и готовых лекарственных формах в одних и тех же условиях.
Ранее были установлено, что для идентификации бетулина предпочтительно использовать его раствор в этиловом спирте. Спектр поглощения полученного раствора имеет максимум в ультрафиолетовой области спектра при длине волны 210 нм, которая была выбрана рабочей при количественном определении бетулина методом ВЭЖХ. Использование тетрагидрофурана в качестве растворителя недопустимо из-за своей непрозрачности при данной длине волны.
Хроматографический анализ проводили с использованием хроматографической системы LC-20 Prominence производства «Shimadzu» (Япония), снабженной спектрофотометрическим детектором на диодной матрице, насосом для подачи подвижной фазы, дегазатором, автоматическим инжектором с возможностью поддержания температуры образцов +4°С, термостатируемым колоночным отделением и компьютером с установленной программой сбора и обработки хроматографических данных.
В ходе работы исследовали параметры разделения исследуемого раствора бетулина на двух аналитических колонках: Kromasil 100-С18 (5 мкм, 150 × 4.8 мм) и Kromasil 100-С8 (5 мкм, 150 × 4.8 мм) производства AkzoNobel (Голландия). В результате эксперимента было установлено, что селективное разделение основного вещества и наиболее близко элюирующих пиков наблюдалось на колонке С18, которую использовали в дальнейшей работе.
При выборе состава подвижной фазы были использованы следующие компоненты: метанол, ацетонитрил, вода.
Исследования показали, что в изократическом режиме элюирования, при использовании подвижных фаз с содержанием водного компонента 30-40% по объему наблюдалась значительное уширение пика и недостаточное разрешение пика исследуемого вещества и соседнего пика (Rs не превышала 1,3).
Кроме того, при концентрации бетулина в растворе 1,0 мг/мл наблюдалось уширение переднего фронта пика, что приводило к потере эффективности разделения бетулина. Таким образом, была подобрана оптимальная рабочая концентрация раствора бетулина, которая составила 0,2 мг/мл.
В ходе дальнейших исследований удалось добиться удовлетворительных показателей разделения бетулина в изократическом режиме элюирования. Сильным компонентом элюента являлся ацетонитрил.
Исследование зависимости площади пика бетулина от его концентрации в испытуемом растворе было проведено в эксперименте на модельных смесях субстанции бетулина в соотношении, эквивалентном их соотношению в КА лиофилизате. Диапазон концентраций бетулина составлял от 0,16 до 0,24 мг/мл.
Для построения калибровочного графика готовили раствор стандартного образца (СО). Около 10 мг (точная навеска) стандартного образца бетулина помещали в мерную колбу вместимостью 50 мл, прибавляли 10 мл спирта этилового, растворяля, доводили объем раствора тем же растворителем до метки и перемешивали. Полученный раствор фильтровали через фильтр типа «Миллипор» с диаметром пор 0,45 мкм или аналогичный, отбрасывая первые 2 мл фильтрата (0,2 мг/мл).
Приготовление стандартных растворов для построения калибровочного графика.
Непосредственно перед анализом готовили 5 стандартных растворов бетулина, как указанно в табл. 3.

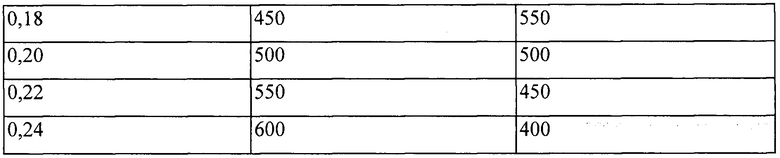
Для приготовления испытуемого раствора отбирали 1 флакон с адъювантом, содержимое которого растворяли в 10,0 мл этилового спирта (около 1,0 мг/мл бетулина). Полученный раствор помещали в темное место на 2 часа, затем обрабатывали ультразвуком в течение 10 мин, охлаждали и перемешивали. Порцию полученного раствора фильтровали через нейлоновый фильтр типа «Миллипор» с диаметром пор 0,45 мкм или аналогичный, отбрасывая первые 2 мл фильтрата.
5,0 мл фильтрата помещали в мерную колбу вместимостью 25,0 мл, доводили объем раствора этиловым спиртом до метки и перемешивали (около 0,2 мг/мл).
Хроматографическую систему перед началом анализа кондиционировали, пропуская подвижную фазу не менее 30 минут, до достижения стабильной базовой линии.
Последовательно хроматографировали по 20 мкл растворителя, РСО, получая не менее 3-х хроматограмм для каждого разведения. Строили калибровочную кривую. Далее хроматографировали по 20 мкл испытуемого раствора, получая не менее 3-х хроматограмм. Время регистрации хроматограммы испытуемого раствора соответствует двукратному времени удерживания основного пика.
Содержание бетулина в испытуемом образце в миллиграммах (X) вычисляли по формуле:
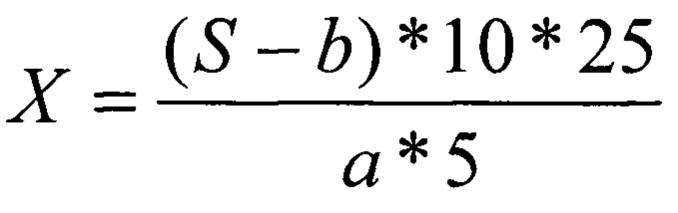
где: а - тангенс угла наклона линейной регрессии к оси абсцисс;
b - координата точки пересечения линейной регрессии с осью ординат;
S - площадь пика испытуемого образца.
Определение концентрации ТГФ
Предлагаемая Исполнителем технология получения КА включает стадию ультрафильтрации для удаления ТГФ, который является слаботоксичным веществом (ЛД50=2.3 г/кг; ПДК=100 мг/м3). Контроль качества ультрафильтрационной очистки проводили по содержанию ТГФ в дисперсии и в пермеате. Также определять остаточную концентрацию растворителя нужно и в готовом препарате. Для этих целей мы использовали метод ГЖХ.
Данные по анализу проб, полученных на стадии ультрафильтрации в пермеате (1) и концентрате (2), представлены в табл. 4. В исходной пробе до стадии ультрафильтрации количество тетрагидрофурана составляло 3,85%.
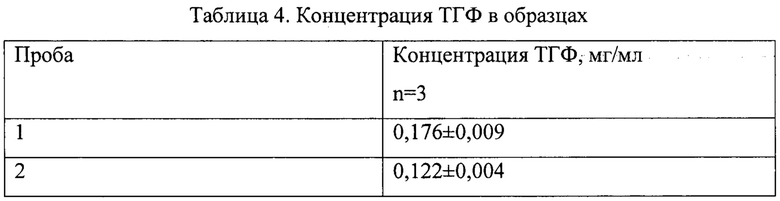
Анализ полученных результатов показал, что стадия ультрафильтрации способствует снижению остаточной концентрации ТГФ почти до 0,122 мг/мл (рис. 4). Таким образом, при введении вакцинной дозы (200 мкг в 0,5 мл) в организм попадет доза ТГФ, которая значительно меньше ЛД50. Подобранный метод ультрафильтрации обеспечивает значительное снижение концентрации ТГФ.
Определение фотометрического показателя дисперсности
С целью стандартизации КА в процессе производства целесообразно использование фотометрического показателя дисперсности (ФПД). Метод определения ФПД основывается на том, что в довольно широких пределах рассеивание света дисперсиями прямо пропорционально зависит от концентрации, размера частиц и их формы и заключается в определении оптической плотности при двух длинах волн с последующим вычислением показателя дисперсности; небольшие изменения в этих параметрах приводят к существенному изменению рассеивания света. Определяя ФПД, можно оперативно следить за технологическим процессом, контролировать формирование частиц.
Анализ 6 серий КА показал, что при соблюдении всех параметров технологического процесса получаются стандартные дисперсии (табл. 5)

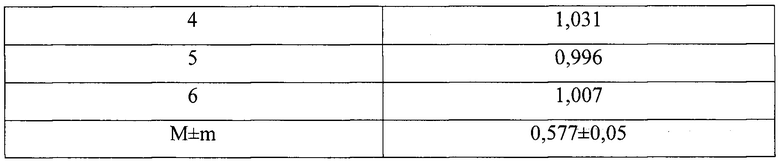
В результате проведенных экспериментов было установлено, что ФПД для КА в концентрации 0,5 мг/мл имеет значение 0,577±0,05.
Таким образом, ФПД может быть использован для стандартизации процесса получения и характеристики готового адъюванта КА на основе природного бетулина.
Далее была разработана лабораторная технология получения вакцины для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2, рекомбинантной жидкой, 10, 40 мкг/мл с использованием КА.
Первый этап заключался в разработке технологии рекомбинантного RBD-FC белка, созданного на основе генома коронавируса SARS-CoV-19.
Второй этап состоял из выбора оптимальных концентраций антигенного компонента и содержания адъюванта в вакцине с целью оптимизации дозы вакцины.
Третий этап заключался в оптимизации процесса сведения антигенного компонента и адъюванта для формулирования готовой к применению формы вакцины.
Фармацевтическую субстанцию для вакцины для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2, получали с применением рекомбинантных технологий. Фармацевтическая субстанция представляет собой высокоочищенный рекомбинантный рецептор-связывающий домен (RBD) шиловидного белка (S белка) вируса SARS-CoV-2.
Технология рекомбинантного RBD белка включает следующее стадии: клонирование последовательности гена RBD в экспрессионный вектор, индуцирование клеток штамма-продуцента, культивирование клеток продуцентов, осаждение клеток из культуральной среды центрифугированием, лизис и разрушение клеток, разделение дифференциальным центрифугированием белков легко растворимой фракции и нерастворимых белков, очистка рекомбинантного белков с помощью аффинной хроматографии на агарозном носителе, содержащим присоединенный ковалентной связью белок protein А, стерилизующая фильтрация. Разработанная методика позволяет очищать рекомбинантный белок из биомассы штамма-продуцента с возможностью последующего масштабирования этого процесса до промышленных объемов.
Разработка технологии вакцины
В результате проведенных исследований предложен следующий состав одной дозы (0,5 мл):

Примеры получения вакцинных препаратов.
Были проведены работы по отработке и оптимизации лабораторной технологии получения вакцины. В результате чего был разработан лабораторного регламента производства препарата «Вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2, рекомбинантной жидкой, 10 мкг/мл.
Пример 1. Стерильный рекомбинантный рецептор-связывающий домен белка Spike вируса SARS-CoV-2 (антиген RBD) добавляли в емкость с предварительно приготовленным стерильным адъювантом в Трис-HCl буферном растворе. Адъювант готовили в этой же емкости, помещенной в ультразвуковую баню. В емкость со стерильным буферным раствором подавали стерильный раствор бетулина в тетрагидрофуране с включенным ультразвуком при 35 КГц в течение 10 минут После подачи и перемешивания раствора бетулина полученную суспензию подвергали ультрафильтрации для удаления ТГФ, по завершению ультрафильтрации суспензию обрабатывали ультразвуком при 35 кГц в течение 3 минут. Далее в емкость подавали стерильный рекомбинантный антиген, растворенный в Трис-HCl буферном растворе из расчета, чтобы конечная концентрация антигена RBD составила 40 мкг/мл или 10 мкг/мл, а адъюванта- 400 мкг/мл. Емкость тщательно перемешивали и помещали в шейкере в холодильник на 3 часа. Затем бутыли с антигеном RBD и адъювантом хранили в холодильной камере при температуре от 2 до 8°С Полученный вакцинный балк после проведения контролей разлили во флаконы по 0,5 мл. Получили серии вакцины П1 40 мкг/мл 905 флаконов и 10 мкг/мл в количестве 840 флаконов для доклинических исследований.
Пример 2. В емкость со стерильным буферным раствором 0,01 М рН 8,8 объемом 5,5 литров подавали 200 мл. 2% раствор бетулина в тетрагидрофуране (ТГФ)в течение 10 мин. при включенном ультразвуке мощностью 40 кГц. Полученную суспензию подвергают ультрафильтрации с применением буферного раствора и мембран с порогом исключения 100 КДа. Для повышения выхода адъюванта после каждого объема диафильтрующего буферного раствора (5 л × 3) включают обратный поток с последующей обработкой суспензии ультразвуком в течение 3 минут при 35 кГц. Доводят объем суспензии до 5 литров. Далее в емкость, при интенсивном перемещивании, добавляют 5 л раствора антигена, состоящего из белка, представляющего нуклеопротеин (N) вируса SARS CoV-2 и RBD этого же вируса в 0,05 М трис-HCl буфере рН 7,6, содержащего 0,15 М NaCl. Конечная концентрация антигена в суспензии составляла 10 мкг/мл, а адъюванта 400 мкг/мл.
Затем емкость с суспензией помещали в холодильник на +4 С, а через сутки разливали по 0,5 мл в во флаконы.
Оценку полноты сорбции вакцин проводили методом ВЭЖХ с использованием жидкостного хроматографа Shimadzu LC-2010 (Япония) и аналитической колонки Superdex 200 Increase 10/300GL. Испытуемый образец вакцины (0,5 мл) центрифугировали при 4000 об/мин в течение 30 мин. Наличие RBD белка в надосадочной жидкости контролировали по наличию пика со временем удерживания основного компонента близким ко времени удерживания образца сравнения (субстанции RBD-Fc). На рис. 5 и 6 представлены хроматографические профили образца фармацевтической субстанции и испытуемого образца вакцины.
Отсутствие пика в образце вакцины со временем удерживания 14,8 мин свидетельствует о полноте сорбции антигена на адьюванте бетулине.
Оценка специфической активности вакцины
Целью исследования являлось сравнительное изучение иммуногенности вакцины в опытах на животных. В ходе исследования сравнивали выработку антител у иммунизированных опытными вакцинами мышей линии Balb/c массой 12 - 14 г обоего пола. Испытуемые препараты вводили двукратно (по схеме 0-14) внутрибрюшинно по 0,5 мл шприцем вместимостью 1 мл. Аналогично контрольным группам животных вводили натрия хлорид, раствор для инфузий 0,9%. Забор крови осуществляли на 14 день после однократной иммунизации и на 14 день после двукратной иммунизации. Антитела определяли в сыворотках с помощью метода ИФА.
Исследовали специфическую активность вакцины содержащей только RBD (в двух дозировках: 5 и 20 мкг рекомбинантного белка в дозе (0,5 мл), вакцину N+RBD в дозировке 5 мкг антигена в дозе (0,5 мл)а также вакцину без адьюванта.
Данные о числе животных, о вакцинах и их дозировке при иммунизации представлены в табл. 6.
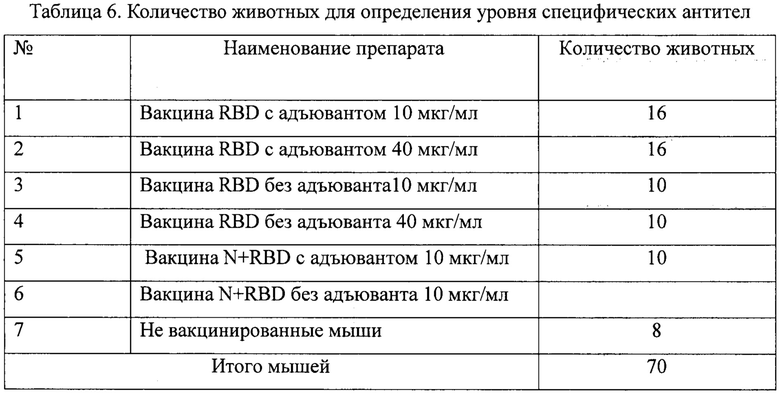
Полученные из крови мышей сыворотки (индивидуально от каждого животного) контролировали на наличие антител к антигену SARS-CoV-2 методом иммуноферментного анализа с использованием экспериментальной тест-системы (ИФТС). При конструировании ИФТС использовались коммерческие реагенты: a/mouse IgG (H+L) Strong Zyme HRP Conjugate (фирмы «SDT», Германия); хромоген - 3,3,5,5-тетраметилбензидин (фирмы «Хема», Россия); блокатор - белково-солевой раствор, в качестве стоп-реагента применялся 5% раствор серной кислоты. Иммуноферментную реакцию выполняли на полистироловых планшетах фирмы Greiner bio-one, Германия. На подложку наносили 1 мкг антигена SARS-CoV-2 и сорбировали в течение суток. Результаты иммуноферментного анализа регистрировали на спектрофотометре PR 2100 производства фирмы «Sanofi Diagnostiks Pasteur» (Франция) при двух длинах волн 450/620 нм.

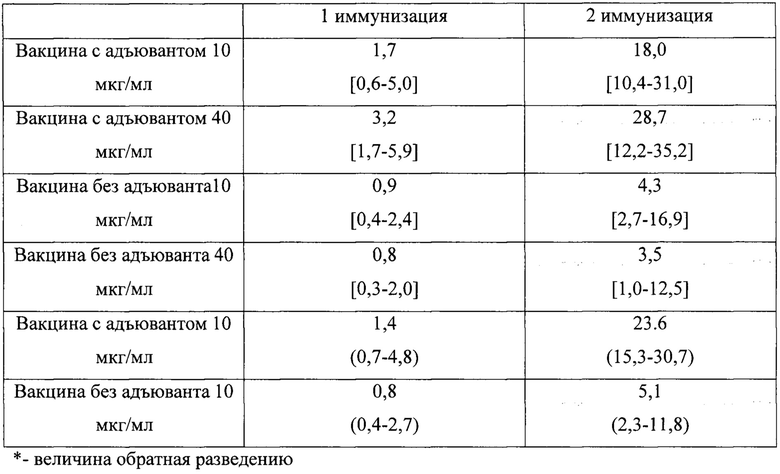
Таким образом, иммунизация животных вакциной с адъювантом способствует нарастанию титра антител, при этом следует отметить, что более выраженным действием обладает препарат, в состав которого входит адъювант.
Определение содержания адьюванта (КА).
Определение проводили методом обращено-фазовой ВЭЖХ в соответствии с ГФ РФ, ОФС.1.2.1.2.0005.15. Исследование проводили с использованием жидкостного хроматографа Shimadzu LC-2010 (Япония) и аналитической колонки Kromasil 300-5С8 250 × 4.6 мм с размером частиц 5 мкм, AkzoNobel (Голландия) в изократическом режиме элюирования и детектировании при 210 нм.

Таким образом, на основании проведенных исследований был разработан проект спецификации на препарат «Вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2, рекомбинантная жидкая, 10 и 40 мкг/мл, максимально отражающий все требования, предъявляемые Государственной Фармакопеей к препаратам такого класса. Проект спецификации представлен в табл. 9.
Таким образом, установлено, что вакцина, содержащая корпускулярный адъювант на основе природного бетулина, обладает высокой антигенной активностью.
| название | год | авторы | номер документа |
|---|---|---|---|
| Пентавалентная субъединичная вакцина против респираторных инфекций и способ ее получения | 2022 |
|
RU2804948C2 |
| Гибридный ген, состоящий из рецептора RBD поверхностного белка S коронавируса SARS-CoV-2, эпитопов S14P5 и S21P2, Fc-фрагмента, для получения рекомбинантного антигена и его применения в составе вакцинной композиции против коронавирусной инфекции | 2022 |
|
RU2795160C1 |
| СПОСОБ ПОЛУЧЕНИЯ АДЪЮВАНТА ДЛЯ ВИРУСНЫХ ВАКЦИН | 2014 |
|
RU2545714C1 |
| СПОСОБ ПОЛУЧЕНИЯ АДЪЮВАНТА ДЛЯ ВАКЦИН | 2014 |
|
RU2545717C1 |
| Генная конструкция для экспрессии рекомбинантных белков на основе участка S-белка SARS-CoV-2, включающего RBD и SD1, слитого с Fc фрагментом IgG, способ получения рекомбинантных белков, антигены и антигенные композиции для индукции длительного антительного и клеточного иммунитета против вируса SARS-CoV-2 | 2021 |
|
RU2802825C2 |
| Вакцина на основе вирусоподобных частиц (VLP) для профилактики COVID-19 для парентерального применения | 2024 |
|
RU2834060C1 |
| Интегративный плазмидный вектор pVEAL3-RBDdel, обеспечивающий синтез и секрецию рекомбинантного белка рецепторсвязывающего домена RBDdelta коронавируса SARS-CoV-2 в клетках млекопитающих, рекомбинантный штамм клеточной линии CHO-K1- RBDdelta и рекомбинантный белок RBDdelta SARS-CoV-2, продуцируемый штаммом клеточной линии | 2023 |
|
RU2816175C1 |
| Рекомбинантные вирусоподобные частицы для индукции специфического иммунитета против вируса тяжелого острого респираторного синдрома SARS-CoV-2 | 2021 |
|
RU2769224C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ S-АНТИГЕНА В ЦЕЛЬНОВИРИОННЫХ ИНАКТИВИРОВАННЫХ АДСОРБИРОВАННЫХ НА ГИДРООКИСИ АЛЮМИНИЯ, СУБЪЕДИНИЧНЫХ НА ОСНОВЕ S-БЕЛКА, РЕКОМБИНАНТНЫХ ИЛИ ПОЛИПЕПТИДНЫХ, СОДЕРЖАЩИХ ДОМЕН RBD SPIKE-БЕЛКА ВИРУСА SARS-COV ВАКЦИНАХ ДЛЯ ПРОФИЛАКТИКИ КОРОНАВИРУСНОЙ ИНФЕКЦИИ COVID-19 И/ИЛИ ДРУГИХ КОРОНАВИРУСНЫХ ИНФЕКЦИЙ | 2023 |
|
RU2825291C1 |
| Рекомбинантный вакцинный штамм для живой интраназальной вакцины, обеспечивающей сочетанную профилактику гриппозной и коронавирусной инфекций | 2022 |
|
RU2782531C1 |
Изобретение относится к способу получения адъюванта на основе бетулина для вакцины против коронавируса SARS-CоV-2, предусматривающему стерилизующую фильтрацию раствора бетулина в тетрагидрофуране через нейлоновую мембрану с диаметром пор 0,22 мкм, снижение содержания тетрагидрофурана путем добавления 25-кратного объема стерильного 0,01 М трис-буфера (рН-9,0±0,1) с помощью перистальтического насоса при постоянном перемешивании в течение 15 минут магнитной мешалкой пропеллерного типа с последующей гомогенизацией ультразвуком при 35-40 кГц в течение 10 минут до получения гомогенной суспензии с образованием сферических аморфных гомогенных частиц, на которых сорбируют белки вируса SARS-CoV-2. Технический результат: предложен способ получения адъюванта на основе бетулина для вакцины против коронавируса SARS-CоV-2, с высокой стерильностью и иммуногенностью, что повышает качество вакцины против коронавируса. 3 з.п. ф-лы, 6 ил., 9 табл., 2 пр.
1. Способ получения адъюванта на основе бетулина для вакцины против коронавируса SARS-CoV-2, предусматривающий стерилизующую фильтрацию раствора бетулина в тетрагидрофуране через нейлоновую мембрану с диаметром пор 0,22 мкм, снижение содержания тетрагидрофурана путем добавления 25-кратного объема стерильного 0,01 М трис-буфера (рН-9,0±0,1) с помощью перистальтического насоса при постоянном перемешивании в течение 15 минут магнитной мешалкой пропеллерного типа с последующей гомогенизацией ультразвуком при 35-40 кГц в течение 10 минут до получения гомогенной суспензии с образованием сферических аморфных гомогенных частиц, на которых сорбируют белки вируса SARS-CoV-2.
2. Способ по п. 1, отличающийся тем, что ультрафильтрацию осуществляют с применением половолоконных мембран или фильтров с номинальной отсекающей молекулярной массой 100-300 КДа
3. Способ по п. 1, отличающийся тем, что для получения гомогенной суспензии обработку суспензии корпускулярного адъюванта проводят ультразвуком после ультрафильтрации в режиме 35-40 кГц.
4. Способ по п. 1, отличающийся тем, что для повышения выхода адъюванта после каждого объема диафильтрующего буферного раствора включают обратный поток с последующей обработкой суспензии ультразвуком в течение 3 минут при 35-40 кГц.
| СПОСОБ ПОЛУЧЕНИЯ АДЪЮВАНТА ДЛЯ ВАКЦИН | 2014 |
|
RU2545717C1 |
| СПОСОБ ПОЛУЧЕНИЯ АДЪЮВАНТА ДЛЯ ВИРУСНЫХ ВАКЦИН | 2014 |
|
RU2545714C1 |
| АДЪЮВАНТ | 2007 |
|
RU2355423C1 |
| НОСИТЕЛЬ ЛЕКАРСТВЕННЫХ И ДИАГНОСТИЧЕСКИХ СРЕДСТВ | 2006 |
|
RU2322998C1 |
| ВАКЦИНА ПРОТИВ ГРИППА | 2014 |
|
RU2546861C1 |
Авторы
Даты
2021-06-07—Публикация
2020-12-29—Подача