Область техники, к которой относится изобретение
Настоящее изобретение относится к антителу против VISTA или его антигенсвязывающему фрагменту, кодирующей указанное нуклеиновой кислоте, к вектору, включающему эту нуклеиновую кислоту, клетке, трансформированной этим вектором, способу получения указанного антитела или его антигенсвязывающего фрагмента, композиции, включающей указанное для профилактики или лечения аутоиммунного заболевания, и к композиции, включающей указанное для введения в комбинации с антителом против PD-1 или антителом против PD-L1.
Уровень техники
Иммунная система представляет собой сетевую систему, включающую клетки и ткани для реагирования на чужеродные патогены. Иммунная система при ответе на несобственные антигены, с которыми она неоднократно встречалась, главным образом, подразделяется на B-клеточный ответ с применением антител и T-клеточный ответ, который опосредуется клетками. В дополнение к этому, существуют иммунные системы, которые могут немедленно реагировать на патогены, и такие клетки, как макрофаги, NK-клетки и нейтрофилы, непосредственно участвуют в удалении антигенов. Что касается иммунной системы, то клональный отбор или ему подобный отбор действует в начале индивидуального развития для предотвращения воздействия иммунной системы на собственный антиген. Однако иммунная система часто может действовать на собственные антигены, что может вызывать заболевания.
Ревматоидный артрит представляет собой типичное аутоиммунное заболевание. Многочисленные исследования показали, что такие механизмы ускользания от иммунологического надзора действуют даже в опухолях. Механизм уклонения от иммунитета может подавлять или повышать иммунитет к антигенам путем подавления или стимулирования активности иммунных клеток. Вещества, вовлеченные в этот фактор, называются «иммунными контрольными точками». В последнее время предпринимали различные попытки лечения опухолей путем вмешательства в иммуносупрессивные функции этих опухолей или путем дополнительного усиления факторов, вовлеченных в иммунную активность.
Поскольку антитела, блокирующие CTLA-4 (цитотоксический антиген 4, связанный с Т-лимфоцитами), который представляет собой иммунную контрольную точку, впервые были применены к пациентам со злокачественной меланомой в 2010 году, и их терапевтический эффект примерно у 20% пациентов был четко продемонстрирован, то появился новый терапевтический подход к лечению рака путем усиления противоракового иммунного ответа путем ингибирования его действия с применением терапевтического антитела, нацеленного на иммунную контрольную точку, которая функционирует как негативный регулятор иммунитета.
Впоследствии разработанное антитело против PD-1 или против PD-L1 продемонстрировало лучший эффект, чем антитело против CTLA-4, и, в особенности, продемонстрировало значительное снижение серьезных побочных эффектов, возникающих у пациентов, проходящих лечение антителом CTLA-4, таким образом, его стали очень активно применять при злокачественной меланоме, немелкоклеточном раке легкого и раке мочевого пузыря.
В особенности, противораковую иммунотерапию иногда выбирали для пациентов, у которых традиционные способы лечения рака, такие как хирургическое вмешательство, противораковые лекарственные средства и лучевая терапия, оказывались неудачными, но все чаще выбирали в качестве основного способа лечения, основанного на разработке антител против PD-1/PD-L1, обладающих уменьшенными побочными эффектами, и активно применяли в клинических испытаниях в рамках объема лечения, распространяющегося на различные карциномы, не отвечающие на традиционные терапевтические агенты, такие как рак желудка и рак печени.
Терапевтические агенты, нацеленные на PD-1, имеют механизм для активации иммунного надзора Т-клеток, а PD-L1 представляет собой лиганд PD-1, который связывается с PD-L1, экспрессируемым в опухолевых клетках, чтобы препятствовать иммуносупрессии Т-клетками и тем самым обеспечивать противоопухолевую активность. Чтобы дополнительно максимизировать эту активность, требуется композиция, обладающая иммуносупрессивным механизмом, который не перекрывается с PD-1/PD-L1. Ожидается, что комбинированная терапия, в которой эти вещества применяют вместе с обычными терапевтическими средствами, окажется очень полезным инструментом повышения эффективности лечения пациентов с опухолями.
VISTA (V-домен-содержащий Ig-супрессор активации T-клеток) - это недавно идентифицированное вещество со свойствами иммунной контрольной точки, которое, как известно, непосредственно ингибирует активность T-клеток. VISTA последовательно экспрессируется в гематопоэтических компартментах, в клетках миелоидного семейства экспрессируется на самом высоком уровне, а в CD4+, CD8+ T-клетках и Foxp3+ CD4+ регуляторных T-клетках экспрессируется на относительно низких уровнях. VISTA экспрессируется в большинстве иммунных клеток, включая Т-клетки, но известно, что он экспрессируется на самом высоком уровне в миелоидных клетках. Следовательно, молекула, которая подавляет VISTA, имеет целевую точку, отличную от PD-1 или PD-L1, что, как можно ожидать, повысит эффективность комбинированной терапии с терапевтическими средствами PD-1/PD-L1.
VISTA имеет структурное сходство с семейством TIM, поскольку он имеет внеклеточный домен иммуноглобулина V (IgV), и было обнаружено, что аминокислотные последовательности VISTA человека и мыши имеют между собой гомологию, равную приблизительно 90%. Некоторые эксперименты показали, что VISTA ингибирует пролиферацию Т-клеток и связанную с этим экспрессию цитокинов, в качестве лиганда экспрессируется антиген-презентирующими клетками (АРС) в виде полной аминокислотной последовательности VISTA или VISTA-Fc, имеющего внеклеточный домен VISTA, связанный с Fc-частью тяжелой цепи антитела. Кроме того, известно, что VISTA-специфические антитела увеличивают тяжесть заболевания в модели аутоиммунного энцефаломиелита, а также повышают противоопухолевую иммунную активность (Le Mercier I., et al., 2014).
Также возможно разработать терапевтическое средство для подавления опухоли, применяя иммунодепрессивную активность VISTA, но также возможно разработать терапевтическое средство для GvHD (реакция «трансплантат против хозяина») и аутоиммунных заболеваний путем дальнейшего повышения иммуносупрессивной активности VISTA. Например, было обнаружено, что антитела против VISTA мыши подавляют GvHD, индуцированную Т-клетками дикого типа (Files, D.B. et al., 2011). Это указывает на то, что активность антитела может действовать как агонист или антагонист в зависимости от эпитопа. Следовательно, антитела, имеющие две функции, могут быть выбраны в качестве антител против VISTA.
На этом техническом уровне авторы настоящего изобретения попытались разработать антитела против VISTA. В результате авторы настоящего изобретения разработали антитело против VISTA, которое обладает желаемой способностью связываться с VISTA, и обнаружили, что антитело против VISTA может служить в качестве целевого противоракового средства или терапевтического средства против аутоиммунного заболевания. На основании этого открытия настоящее изобретение было завершено.
Раскрытие изобретения
Техническая проблема
Одна из целей настоящего изобретения заключается в создании нового антитела против VISTA или его антигенсвязывающего фрагмента.
Другая цель настоящего изобретения заключается в обеспечении нуклеиновой кислоты, кодирующей антитело или его антигенсвязывающий фрагмент.
Другая цель настоящего изобретения заключается в обеспечении вектора, включающего нуклеиновую кислоту, клетку, трансформированную вектором, и способа ее получения.
Другая цель настоящего изобретения заключается в обеспечении композиции, включающей антитело или его антигенсвязывающий фрагмент, для профилактики или лечения опухоли, рака или аутоиммунного заболевания.
Другая цель настоящего изобретения заключается в обеспечении композиции, включающей антитело или его антигенсвязывающий фрагмент, для введения в комбинации с антителом против PD-1 или антителом против PD-L1.
Техническое решение
В соответствии с одним из аспектов настоящего изобретения вышеуказанные и другие цели могут быть достигнуты путем обеспечения антитела или его антигенсвязывающего фрагмента, связывающегося с V-доменным Ig-супрессором активации Т-клеток (VISTA), включающего вариабельную область тяжелой цепи, включающую CDR1 тяжелой цепи, выбранную из группы, состоящей из последовательностей SEQ ID NO: 1, 7, 13 и 19;
CDR2 тяжелой цепи, выбранную из группы, состоящей из последовательностей SEQ ID NO: 2, 8, 14 и 20; и
CDR3 тяжелой цепи, выбранную из группы, состоящей из последовательностей SEQ ID NO: 3, 9, 15 и 21; а также
вариабельную область легкой цепи, включающую: CDR1 легкой цепи, выбранную из группы, состоящей из последовательностей SEQ ID NO: 4, 10, 16 и 22;
CDR2 легкой цепи, выбранную из группы, состоящей из последовательностей SEQ ID NO: 5, 11, 17 и 23; и
CDR3 легкой цепи, выбранную из группы, состоящей из последовательностей SEQ ID NO: 6, 12, 18, 24 и 34-40.
В другом аспекте настоящего изобретения предложена нуклеиновая кислота, кодирующая антитело или его антигенсвязывающий фрагмент.
В другом аспекте настоящего изобретения обеспечивают вектор, включающий нуклеиновую кислоту.
В другом аспекте настоящего изобретения обеспечивают клетку, трансформированную вектором.
В другом аспекте настоящего изобретения обеспечивают способ получения антитела или его антигенсвязывающего фрагмента, включающий: (а) культивирование клетки; и (b) выделение антитела или его антигенсвязывающего фрагмента из культивируемой клетки.
В другом аспекте настоящего изобретения обеспечивают композицию, включающую антитело или его антигенсвязывающий фрагмент в качестве активного ингредиента для предотвращения или лечения опухоли, рака или аутоиммунного заболевания. В другом аспекте настоящего изобретения обеспечивают способ предотвращения или лечения опухоли, рака или аутоиммунного заболевания, включающий введение антитела или его антигенсвязывающего фрагмента пациенту с опухолью, раком или аутоиммунным заболеванием. В другом аспекте настоящего изобретения обеспечивают применение антитела или его антигенсвязывающего фрагмента для ингибирования иммуносупрессивного механизма VISTA и применение антитела или его антигенсвязывающего фрагмента для профилактики или лечения опухоли, рака или применение антитела или его антигенсвязывающего фрагмента для улучшения иммуносупрессивной способности VISTA и применение антитела или его антигенсвязывающего фрагмента для профилактики или лечения аутоиммунного заболевания.
В другом аспекте настоящего изобретения обеспечивают композицию, включающую антитело или его антигенсвязывающий фрагмент, для введения в комбинации с антителом против PD-1 или антителом против PD-L1. В другом аспекте настоящего изобретения обеспечивают способ профилактики или лечения опухоли или рака, включая введение пациенту антитела или его антигенсвязывающего фрагмента в сочетании с антителом против PD-1 или антителом против PD-L1. В другом аспекте настоящего изобретения обеспечивают применение антитела или его антигенсвязывающего фрагмента для введения в комбинации с антителом против PD-1 или антителом против PD-L1 для лечения опухоли или рака.
Полезные эффекты
Антитело против VISTA или его антигенсвязывающий фрагмент в соответствии с настоящим изобретением проявляет желаемую способность к связыванию с VISTA и может быть полезным для профилактики или лечения целевого рака/опухоли или аутоиммунного заболевания. Настоящее изобретение позволяет разработать терапевтическое средство, имеющее целевую точку, отличающуюся от целевой точки традиционного терапевтического средства, направленного на иммунную контрольную точку, тем самым обеспечивая комбинированную терапию с обычным терапевтическим средством и монотерапию для лечения опухолей, и может усиливать активность контрольных точек, подавляя иммунную активность и обеспечивая тем самым новую иммуносупрессивную терапию.
Описание рисунков
Фиг. 1 показывает результат определения того, связываются ли VISTA-экспрессирующие клетки с моноклональными scFv-фагами путем взаимодействия моноклональных scFv-фагов с клетками CHO-K1, экспрессирующими VISTA.
Фиг. 2 показывает результат измерений способом ELISA для определения того, существует ли перекрестная реактивность между выбранным антителом против VISTA и антигенами VISTA человека и мыши.
Фиг. 3 показывает результат определения способности к связыванию выбранного антитела против VISTA с клетками CHO-K1, экспрессирующими VISTA человека и мыши.
Фиг. 4 показывает результат измерения IFN-γ, продуцируемого в реакции алло-MLR периферической крови человека способом ELISA.
На фиг. 5 приведен результат, показывающий, что группа введения антитела против VISTA теряет значительное количество массы.
На фиг. 6 приведен результат, показывающий, что группа введения анти-VISTA-антитела претерпевает значительное снижение массы опухоли.
На фиг. 7 приведен результат, демонстрирующий посредством смешанной реакции лимфоцитов (MLR) эффективную пролиферацию клеток для оценки функции оптимизированного антитела против VISTA.
На фиг. 8 приведен результат, демонстрирующий посредством реакции смешанной культуры лимфоцитов (MLR), увеличение секреции цитокинов для оценки функции оптимизированного анти-VISTA антитела.
На фиг. 9 приведен результат, показывающий, что оптимизированная группа введения антител против VISTA теряет значительное количество веса.
На фиг. 10 приведен результат, показывающий, что в группе с оптимизированным введением анти-VISTA-антитела происходит значительное снижение массы опухоли.
Лучший вариант осуществления изобретения
Если не указано иное, все технические и научные термины, применяемые в настоящем документе, имеют те же значения, которые понятны специалисты в области, к которой относится настоящее изобретение. В общем, применяемая в настоящем документе номенклатура хорошо известна в данной области техники и применена обычным образом.
Таким образом, в одном из аспектов настоящее изобретение направлено на связывание антитела с V-доменным Ig-супрессором активации T-клеток (VISTA) или его антигенсвязывающим фрагментом, включая вариабельную область тяжелой цепи, включающую CDR1 тяжелой цепи, выбранную из группы, состоящей из последовательностей SEQ ID NOS: 1, 7, 13 и 19;
CDR2 тяжелой цепи, выбранную из группы, состоящей из последовательностей SEQ ID NOS: 2, 8, 14 и 20; и
CDR3 тяжелой цепи, выбранную из группы, состоящей из последовательностей SEQ ID NOS: 3, 9, 15 и 21; и
вариабельную область легкой цепи, включающую CDR1 легкой цепи, выбранную из группы, состоящей из последовательностей SEQ ID NOS: 4, 10, 16 и 22;
CDR2 легкой цепи, выбранную из группы, состоящей из последовательностей SEQ ID NOS: 5, 11, 17 и 23; и
CDR3 легкой цепи, выбранную из группы, состоящей из последовательностей SEQ ID NOS: 6, 12, 18, 24 и 34-40.
Как применен в настоящем документе, термин «антитело» относится к антителу против VISTA, которое специфически связывается с VISTA. В объем настоящего изобретения входит не только полное антитело, специфически связывающееся с VISTA, но также антигенсвязывающий фрагмент молекулы антитела.
Термин «полное антитело» относится к структуре, имеющей две легкие цепи полной длины и две тяжелые цепи полной длины, в которой каждая легкая цепь связана с соответствующей тяжелой цепью дисульфидной связью. Константная область тяжелой цепи имеет типы гамма (γ), мю (μ), альфа (α), дельта (δ) и эпсилон (ε) и подразделяются на гамма 1 (γ1), гамма 2 (γ2), гамма 3 (γ3), гамма 4 (γ4), альфа 1 (α1) и альфа 2 (α2). Константная область легкой цепи имеет типы каппа (κ) и лямбда (λ).
Термин «антигенсвязывающий фрагмент антитела» или «фрагмент антитела» относится к фрагменту, который, по меньшей мере, обладает антигенсвязывающей способностью и включает Fab, F(ab'), F(ab’)2, Fv и тому подобные фрагменты. Среди фрагментов антитела Fab относится к структуре, включающей вариабельную область каждой из тяжелой цепи и легкой цепи, константную область легкой цепи и первый константный домен (CH1) тяжелой цепи, каждый из которых имеет один антиген-связывающий сайт. Fab' отличается от Fab тем, что он дополнительно включает шарнирную область, включающую, по меньшей мере, один остаток цистеина на С-конце домена CH1 тяжелой цепи. F(ab')2 создается дисульфидной связью между остатками цистеина в шарнирной области Fab'. Fv представляет собой минимальный фрагмент антитела, имеющий только вариабельную область тяжелой цепи и вариабельную область легкой цепи, рекомбинантная технология получения Fv раскрыта в международных публикациях PCT, таких как WO 88/10649, WO 88/106630, WO 88/07085, WO 88/07086 и WO 88/09344. Двухцепочечный Fv представляет собой фрагмент, в котором вариабельная область тяжелой цепи и вариабельная область легкой цепи связаны нековалентной связью, а одноцепочечный Fv (scFv) представляет собой фрагмент, в котором вариабельная область тяжелой цепи цепь и вариабельная область легкой цепи обычно связаны ковалентной связью через пептидный линкер между ними или непосредственно связаны на С-конце, образуя димерообразную структуру, такую как двухцепочечный Fv. Такие фрагменты антител могут быть получены с применением протеаз (например, Fab может быть получен путем рестрикционного расщепления всего антитела папаином, а фрагмент F(ab')2 может быть получен путем рестрикционного расщепления всего антитела пепсином) и может быть получен способами генетической рекомбинации.
В одном из воплощений, антитело по настоящему изобретению находится в форме Fv (например, scFv) или в форме полного антитела. Кроме того, константная область тяжелой цепи может быть выбрана из изотипов гамма (γ), мю (μ), альфа (α), дельта (δ) и эпсилон (ε). Например, константной областью может быть гамма 1 (IgG1), гамма 3 (IgG3) или гамма 4 (IgG4). Константная область легкой цепи может представлять собой каппу или лямбду.
Как применен в настоящем документе, термин «тяжелая цепь» охватывает как полноразмерную тяжелую цепь, которая включает вариабельный домен (VH), содержащий аминокислотную последовательность, имеющую последовательность вариабельной области, достаточную для придания специфичности антигену, и три константных домена (СН1, СН2 и СН3) и его фрагмент. Как применен в настоящем документе, термин «легкая цепь» охватывает как полноразмерную легкую цепь, которая включает вариабельный домен (VL), содержащий аминокислотную последовательность, имеющую последовательность вариабельной области, достаточную для придания специфичности антигену, и константный домен (CL) и его фрагмент.
Антитело по настоящему изобретению включает, без ограничений, моноклональные антитела, полиспецифические антитела, антитела человека, гуманизированные антитела, химерные антитела, одноцепочечные Fv (scFV), одноцепочечные антитела, фрагменты Fab, F(ab') фрагменты, дисульфидные связи Fvs (sdFVs), антиидиотипические (анти-Id) антитела, эпитоп-связывающие фрагменты таких антител и тому подобное.
Термин «моноклональное антитело» относится к идентичному антителу, исключая возможные встречающиеся в природе мутации, когда антитело, полученное из популяции по существу гомогенных антител, то есть каждое антитело, составляющее эту популяцию, может присутствовать в небольшом количестве. Моноклональные антитела представляют собой высокоспецифичные антитела и, следовательно, индуцируются против одного антигенного сайта. В отличие от обычных (поликлональных) препаратов антител, которые обычно включают разные антитела, направленные против разных детерминант (эпитопов), каждое моноклональное антитело направлено против одной детерминанты на антигене.
Термин «эпитоп» относится к детерминанте белка, с которой антитело может специфически связываться. Эпитопы обычно состоят из группы химически активных поверхностных молекул, таких как боковые цепи аминокислот или сахаров, и, как правило, имеют не только конкретные трехмерные структурные характеристики, но также специфические характеристики заряда. Трехмерные эпитопы отличаются от нетрехмерных эпитопов тем, что связь с первыми разрывается в присутствии денатурирующего растворителя, тогда как связь с последними не разрывается.
Антитело, не являющееся человеческим (например, мышиное), «гуманизированной» формы - это химерное антитело, содержащее минимальную последовательность, полученную из иммуноглобулина вида, не относящегося к человеку. В большинстве случаев гуманизированное антитело представляет собой человеческий иммуноглобулин (рецепторное антитело), в котором остаток гипервариабельной области рецептора заменен остатком гипервариабельной области вида, не относящегося к человеку (донорское антитело), такого как мышь, крысы, кролики или приматы, не относящиеся к человеку, имеющим желаемую специфичность, аффинность и способность.
Как применен в настоящем документе, термин «человеческое антитело» относится к молекуле, полученной из человеческого иммуноглобулина, в которой все аминокислотные последовательности, составляющие антитело, включая определяющую комплементарность область и структурную область, состоят из человеческих иммуноглобулинов.
Антитело человека включает не только «химерное» антитело (иммуноглобулин), в котором части тяжелой цепи и/или легкой цепи получены из определенного вида или идентичны или гомологичны соответствующим последовательностям в антителе, принадлежащем к определенному классу или подклассу антител, а оставшаяся цепь (цепи) происходят от другого вида или идентичны или гомологичны соответствующим последовательностям антитела, принадлежащего к другому классу или подклассу антитела, а также фрагменту антитела, который проявляет желаемую биологическую активность.
Как применен в настоящем документе, термин «вариабельный домен антитела» относится к областям легкой и тяжелой цепи молекулы антитела, включая аминокислотную последовательность определяющей комплементарность области (CDR; т.е. CDR1, CDR2 и CDR3) и каркасной области (FR). VH относится к вариабельному домену тяжелой цепи. VL относится к вариабельному домену легкой цепи.
Термин «определяющая комплементарность область» (CDR; то есть CDR1, CDR2 и CDR3) относится к аминокислотному остатку вариабельного домена антитела, который необходим для связывания антигена. Каждый вариабельный домен обычно имеет три области CDR, идентифицированные как CDR1, CDR2 и CDR3.
В настоящем изобретении антитело, связывающееся с VISTA или его антигенсвязывающим фрагментом, может включать вариабельную область тяжелой цепи, включающую CDR1 тяжелой цепи последовательности SEQ ID NO: 1, CDR2 тяжелой цепи последовательности SEQ ID NO: 2 и CDR3 тяжелой цепи последовательности SEQ ID NO: 3, и вариабельную область легкой цепи, включающую CDR1 легкой цепи последовательности SEQ ID NO: 4, CDR2 легкой цепи последовательности SEQ ID NO: 5 и CDR3 легкой цепи последовательности SEQ ID NO: 6,
вариабельную область тяжелой цепи, включающую CDR1 тяжелой цепи последовательности SEQ ID NO: 1, CDR2 тяжелой цепи последовательности SEQ ID NO: 2 и CDR3 тяжелой цепи последовательности SEQ ID NO: 3, и вариабельную область легкой цепи, включающую CDR1 легкой цепи последовательности SEQ ID NO: 4, CDR2 легкой цепи последовательности SEQ ID NO: 5 и CDR3 легкой цепи последовательности SEQ ID NO: 33,
вариабельную область тяжелой цепи, включающую CDR1 тяжелой цепи последовательности SEQ ID NO: 1, CDR2 тяжелой цепи последовательности SEQ ID NO: 2 и CDR3 тяжелой цепи последовательности SEQ ID NO: 3, и вариабельную область легкой цепи, включающую CDR1 легкой цепи последовательности SEQ ID NO: 4, CDR2 легкой цепи последовательности SEQ ID NO: 5 и CDR3 легкой цепи последовательности SEQ ID NO: 34,
вариабельную область тяжелой цепи, включающую CDR1 тяжелой цепи последовательности SEQ ID NO: 1, CDR2 тяжелой цепи последовательности SEQ ID NO: 2 и CDR3 тяжелой цепи последовательности SEQ ID NO: 3, и вариабельную область легкой цепи, включающую CDR1 легкой цепи последовательности SEQ ID NO: 4, CDR2 легкой цепи последовательности SEQ ID NO: 5 и CDR3 легкой цепи последовательности SEQ ID NO: 35,
вариабельную область тяжелой цепи, включающую CDR1 тяжелой цепи последовательности SEQ ID NO: 1, CDR2 тяжелой цепи последовательности SEQ ID NO: 2 и CDR3 тяжелой цепи последовательности SEQ ID NO: 3, и вариабельную область легкой цепи, включающую CDR1 легкой цепи последовательности SEQ ID NO: 4, CDR2 легкой цепи последовательности SEQ ID NO: 5 и CDR3 легкой цепи последовательности SEQ ID NO: 36,
вариабельную область тяжелой цепи, включающую CDR1 тяжелой цепи последовательности SEQ ID NO: 1, CDR2 тяжелой цепи последовательности SEQ ID NO: 2 и CDR3 тяжелой цепи последовательности SEQ ID NO: 3, и вариабельную область легкой цепи, включающую CDR1 легкой цепи последовательности SEQ ID NO: 4, CDR2 легкой цепи последовательности SEQ ID NO: 5 и CDR3 легкой цепи последовательности SEQ ID NO: 37,
вариабельную область тяжелой цепи, включающую CDR1 тяжелой цепи последовательности SEQ ID NO: 1, CDR2 тяжелой цепи последовательности SEQ ID NO: 2 и CDR3 тяжелой цепи последовательности SEQ ID NO: 3, и вариабельную область легкой цепи, включающую CDR1 легкой цепи последовательности SEQ ID NO: 4, CDR2 легкой цепи последовательности SEQ ID NO: 5 и CDR3 легкой цепи последовательности SEQ ID NO: 38,
вариабельную область тяжелой цепи, включающую CDR1 тяжелой цепи последовательности SEQ ID NO: 1, CDR2 тяжелой цепи последовательности SEQ ID NO: 2 и CDR3 тяжелой цепи последовательности SEQ ID NO: 3, и вариабельную область легкой цепи, включающую CDR1 легкой цепи последовательности SEQ ID NO: 4, CDR2 легкой цепи последовательности SEQ ID NO: 5 и CDR3 легкой цепи последовательности SEQ ID NO: 39,
вариабельную область тяжелой цепи, включающую CDR1 тяжелой цепи последовательности SEQ ID NO: 1, CDR2 тяжелой цепи последовательности SEQ ID NO: 2 и CDR3 тяжелой цепи последовательности SEQ ID NO: 3, и вариабельную область легкой цепи, включающую CDR1 легкой цепи последовательности SEQ ID NO: 4, CDR2 легкой цепи последовательности SEQ ID NO: 5 и CDR3 легкой цепи последовательности SEQ ID NO: 40,
вариабельную область тяжелой цепи, включающую CDR1 тяжелой цепи последовательности SEQ ID NO: 7, CDR2 тяжелой цепи последовательности SEQ ID NO: 8 и CDR3 тяжелой цепи последовательности SEQ ID NO: 9, и вариабельную область легкой цепи, включающую CDR1 легкой цепи последовательности SEQ ID NO: 10, CDR2 легкой цепи последовательности SEQ ID NO: 11, и CDR3 легкой цепи последовательности SEQ ID NO: 12,
вариабельную область тяжелой цепи, включающую CDR1 тяжелой цепи последовательности SEQ ID NO: 13, CDR2 тяжелой цепи последовательности SEQ ID NO: 14 и CDR3 тяжелой цепи последовательности SEQ ID NO: 15, и вариабельную область легкой цепи, включающую CDR1 легкой цепи последовательности SEQ ID NO: 16, CDR2 легкой цепи последовательности SEQ ID NO: 17, и CDR3 легкой цепи последовательности SEQ ID NO: 18, или
вариабельную область тяжелой цепи, включающую CDR1 тяжелой цепи последовательности SEQ ID NO: 19, CDR2 тяжелой цепи последовательности SEQ ID NO: 20 и CDR3 тяжелой цепи последовательности SEQ ID NO: 21, и вариабельную область легкой цепи, включающую CDR1 легкой цепи последовательности SEQ ID NO: 22, CDR2 легкой цепи последовательности SEQ ID NO: 23, и CDR3 легкой цепи последовательности SEQ ID NO: 24.
Термин «каркасная область» (FR) относится к остатку вариабельного домена, отличному от остатка CDR. Каждый вариабельный домен обычно имеет четыре FR, обозначаемые как FR1, FR2, FR3 и FR4.
Фрагмент «Fv» представляет собой фрагмент антитела, содержащий полные сайты распознавания и связывания антител. Такая область включает димер, например, scFv, который состоит из одного вариабельного домена тяжелой цепи и одного вариабельного домена легкой цепи, в значительной степени прочно ковалентно связанных друг с другом.
Фрагмент «Fab» содержит вариабельный домен и константный домен легкой цепи, а также вариабельный домен и первый константный домен (CH1) тяжелой цепи. Фрагмент антитела F(ab')2 обычно включает пару фрагментов Fab, ковалентно связанных через цистеин шарнира, расположенный между ними вблизи его карбоксильного конца.
«Одноцепочечный Fv» или «scFv» фрагмент антитела включает домены антитела VH и VL, в котором эти домены присутствуют в одной полипептидной цепи. Полипептид Fv может дополнительно включать полипептидный линкер между доменом VH и доменом VL для того, чтобы scFv образовывал желаемую структуру для связывания антигена.
Антитело VISTA может включать одинарные или двойные цепи. Функционально, аффинность связывания антитела VISTA варьирует от 10-5 M до 10-12 M. Например, аффинность связывания антитела VISTA составляет от 10-6 M до 10-12 M, от 10-7 M до 10-12 M, от 10-8 M до 10-12 M, от 10-9 M до 10-12 M, от 10-5 M до 10-11 M, от 10-6 M до 10-11 M, от 10-7 M до 10-11 M, от 10-8 M до 10-11 M, от 10-9 M до 10-11 M, от 10-10 M до 10-11 M, от 10-5 M до 10-10 M, от 10-6 M до 10-10 M, от 10-7 M до 10-10 M, от 10-8 M до 10-10 M, от 10-9 M до 10-10 M, от 10-5 M до 10-9 M, от 10-6 M до 10-9 M, от 10-7 M до 10-9 M, от 10-8 M до 10-9 M, от 10-5 M до 10-8 M, от 10-6 M до 10-8 M, от 10-7 M до 10-8 M, от 10-5 M до 10-7 M, от 10-6 M до 10-7 M или от 10-5 M до 10-6 M.
Связывание антитела с VISTA или его антигенсвязывающим фрагментом может включать вариабельную область тяжелой цепи, выбранную из группы, состоящей из последовательностей SEQ ID NOS: 25, 27, 29, 31 и 49. Кроме того, антитело, связывающееся с VISTA или с его антигенсвязывающим фрагментом, может включать вариабельную область легкой цепи, выбранную из группы, состоящей из последовательностей SEQ ID NOS: 26, 28, 30, 32, 41-48 и 50.
В конкретном воплощении в соответствии с настоящим изобретением антитело, связывающееся с VISTA или его антигенсвязывающим фрагментом, может включать: вариабельную область тяжелой цепи последовательности SEQ ID NO: 25 и вариабельную область легкой цепи последовательности SEQ ID NO: 26;
вариабельную область тяжелой цепи последовательности SEQ ID NO: 25 и вариабельную область легкой цепи последовательности SEQ ID NO: 41;
вариабельную область тяжелой цепи последовательности SEQ ID NO: 25 и вариабельную область легкой цепи последовательности SEQ ID NO: 42;
вариабельную область тяжелой цепи последовательности SEQ ID NO: 25 и вариабельную область легкой цепи последовательности SEQ ID NO: 43;
вариабельную область тяжелой цепи последовательности SEQ ID NO: 25 и вариабельную область легкой цепи последовательности SEQ ID NO: 44;
вариабельную область тяжелой цепи последовательности SEQ ID NO: 25 и вариабельную область легкой цепи последовательности SEQ ID NO: 45;
вариабельную область тяжелой цепи последовательности SEQ ID NO: 25 и вариабельную область легкой цепи последовательности SEQ ID NO: 46;
вариабельную область тяжелой цепи последовательности SEQ ID NO: 25 и вариабельную область легкой цепи последовательности SEQ ID NO: 47;
вариабельную область тяжелой цепи последовательности SEQ ID NO: 25 и вариабельную область легкой цепи последовательности SEQ ID NO: 48;
вариабельную область тяжелой цепи последовательности SEQ ID NO: 25 и вариабельную область легкой цепи последовательности SEQ ID NO: 50;
вариабельную область тяжелой цепи последовательности SEQ ID NO: 49 и вариабельную область легкой цепи последовательности SEQ ID NO: 48;
вариабельную область тяжелой цепи последовательности SEQ ID NO: 49 и вариабельную область легкой цепи последовательности SEQ ID NO: 50;
вариабельную область тяжелой цепи последовательности SEQ ID NO: 27 и вариабельную область легкой цепи последовательности SEQ ID NO: 28;
вариабельную область тяжелой цепи последовательности SEQ ID NO: 29 и вариабельную область легкой цепи последовательности SEQ ID NO: 30; или
вариабельную область тяжелой цепи последовательности SEQ ID NO: 31 и вариабельную область легкой цепи последовательности SEQ ID NO: 32.
«Фаговый дисплей» представляет собой способ отображения мутантного полипептида в виде слитого белка, по меньшей мере, с частью белка оболочки на поверхности фаговой частицы, например, нитчатого фага. Полезность фагового дисплея заключается в быстрой и эффективной классификации последовательностей, которые связываются с антигенами-мишенями с высокой аффинностью, в больших библиотеках рандомизированных мутантов белка. Отображение пептидов и библиотек белков на фагах применяют для скрининга миллионов полипептидов с целью идентификации полипептидов со специфическими свойствами связывания.
Технология фагового дисплея предложила мощный инструмент для производства и скрининга новых белков, которые связываются со специфическими лигандами (например, антигенами). Применяя технологию фагового дисплея, можно создавать большие библиотеки мутантов белка и быстро отсортировать последовательности, связывающиеся с высоким сродством с антигенами-мишенями. Нуклеиновую кислоту, кодирующую мутантные полипептиды, сливают с последовательностью нуклеиновой кислоты, кодирующей белок вирусной оболочки, например ген III или белок VIII. Была разработана монофазная система фагового дисплея, в которой последовательность нуклеиновой кислоты, кодирующую белок или полипептид, сливают с последовательностью нуклеиновой кислоты, кодирующей часть белка гена III. В монофазной системе отображения слитый ген экспрессируется на низком уровне, белок гена III дикого типа также экспрессируется, и, таким образом, сохраняется инфекционность частиц.
Важно продемонстрировать экспрессию пептидов на поверхности фиброзного фага и экспрессию функциональных фрагментов антител в периферической цитоплазме E.coli для разработки библиотек фагового дисплея антител. Библиотеки антител- или антиген-связывающих полипептидов получают с помощью ряда способов, например, способов модификации одного гена путем вставки случайной последовательности ДНК или клонирования связанной последовательности гена. Скрининг может быть выполнен в библиотеках в отношении экспрессии антител- или антиген-связывающих белков, имеющих желаемые характеристики.
Технология фагового дисплея имеет несколько преимуществ по сравнению с обычными гибридомными и рекомбинантными способами получения антител, имеющих желаемые характеристики. Этот способ обеспечивает создание больших библиотек антител с различными последовательностями в течение короткого времени без применения животных. Производство гибридом и производство гуманизированных антител может занять нескольких месяцев. Кроме того, поскольку иммунитет не требуется, то библиотеки фаговых антител могут генерировать антитела против антигенов, которые токсичны или имеют низкую антигенность. Библиотеки фаговых антител также можно применять для получения и идентификации новых терапевтических антител.
Могут быть применены способы получения человеческих антител из иммунизированных или неиммунизированных людей, последовательностей зародышевой линии или репертуаров наивных B-клеточных Ig с помощью библиотек фагового дисплея. Наивные или неиммуногенные антигенсвязывающие библиотеки могут быть получены с применением различных лимфатических тканей.
Способы идентификации и отделения высокоаффинных антител из библиотек фагового дисплея важны для разделения новых терапевтических антител. Выделение высокоаффинных антител из библиотек зависит от размера библиотек, эффективности продукции в бактериальных клетках и разнообразия библиотек. Размер библиотек уменьшается из-за неправильного сворачивания белка антитела или антигенсвязывающего белка и неэффективной продукции из-за присутствия стоп-кодона. Экспрессия в бактериальных клетках может быть заингибирована неправильным сворачиванием антитела или антигенсвязывающего домена. Экспрессия может быть улучшена путем попеременного мутирования остатков на поверхности границ вариабельных/константных или выбранных остатков CDR. Последовательность каркасной области представляет собой элемент, который обеспечивает правильное сворачивание при создании фаговых библиотек антител в бактериальных клетках.
Важно создавать разнообразные библиотеки антител- или антигенсвязывающих белков для отделения высокоаффинных антител. Обнаружено, что области CDR3 часто участвуют в связывании антигена. Поскольку область CDR3 в тяжелой цепи значительно различается по размеру, последовательности и структурной/размерной морфологии, то различные библиотеки могут быть получены с применением того же.
В конкретном воплощении в соответствии с настоящим изобретением была проведена оптимизация антител для повышения аффинности клона 1B8 антитела против VISTA, в CDR3 легкой цепи и в CDR3 тяжелой цепи из 1B8 ввели случайные мутации, и выполнили биопэннинг с применением библиотеки мутантов фага scFv. В результате было получено 8 типов оптимизированных клонов, включающих, по меньшей мере, одну вариабельную область легкой цепи CDR3, выбранную из группы, состоящей из последовательностей SEQ ID NO: 33-40.
Кроме того, разнообразие может быть создано путем рандомизации областей CDR вариабельных тяжелых и легких цепей с применением всех 20 аминокислот в каждой позиции. Применение всех 20 аминокислот приводит к получению последовательностей антител, имеющих повышенное разнообразие и повышенную вероятность идентификации новых антител.
Антитело или фрагмент антитела по настоящему изобретению может включать последовательность упомянутого в настоящем документе антитела, а также его биологические эквиваленты, при условии, что они могут специфически распознавать VISTA. Например, могут быть внесены дополнительные изменения в аминокислотную последовательность антитела, чтобы дополнительно улучшить аффинность связывания и/или другие биологические свойства антитела. Такие вариации включают, например, делецию, вставку и/или замену остатков аминокислотной последовательности антитела. Такие вариации аминокислот основаны на относительном сходстве заместителей боковых цепей аминокислот, таких как гидрофобность, гидрофильность, заряд и их размер. Анализ размера, формы и типа заместителей боковых цепей аминокислот позволяет увидеть, что каждый из аргинина, лизина и гистидина представляет собой положительно заряженный остаток; аланин, глицин и серин имеют одинаковые размеры, а фенилаланин, триптофан и тирозин имеют сходные формы. Таким образом, исходя из этих соображений, аргинин, лизин и гистидин; аланин, глицин и серин; и фенилаланин, триптофан и тирозин считаются биологически функциональными эквивалентами.
Принимая во внимание вариации, имеющие биологически эквивалентную активность, антитело или кодирующую его молекулу нуклеотида, в соответствии с настоящим изобретением интерпретируют как включение последовательности, имеющей существенную идентичность с последовательностью, указанной в номере последовательности. Термин «существенная идентичность» означает, что последовательность имеет гомологию по меньшей мере 90%, наиболее предпочтительно, гомологию по меньшей мере 95% по меньшей мере 96% по меньшей мере 97% по меньшей мере 98% или по меньшей мере 99%, при выравнивании последовательности по настоящему изобретению и любой другой последовательности так, чтобы они максимально соответствовали друг другу и выровненной последовательности могли быть проанализированы с помощью алгоритмов, обычно применяемых в данной области техники. Способы выравнивания для сравнения последовательностей хорошо известны в данной области техники. Основное средство поиска локального выравнивания от NCBI (BLAST) доступен через NCBI и т.п. и может быть применен вместе с программами анализа последовательностей, такими как BLASTP, BLASTM, BLASTX, TBLASTN и TBLASTX через Интернет. BLAST доступен по адресу www.ncbi.nlm.nih.gov/BLAST/. Способ сравнения гомологии последовательностей с применением этой программы можно найти по адресу www.ncbi.nlm.nih.gov/BLAST/blast_help.html.
Исходя из этого, антитело или его антигенсвязывающий фрагмент в соответствии с настоящим изобретением может иметь гомологию 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% или более по сравнению с раскрытой в настоящем документе последовательностью или соответствовать ей по всей длине. Такая гомология может быть определена путем сравнения последовательностей и/или выравнивания способами, известными в данной области техники. Например, процент гомологии последовательности нуклеиновой кислоты или белка в соответствии с настоящим изобретением может быть определен с применением алгоритма сравнения последовательностей (то есть, с помощью BLAST или BLAST 2.0), ручного выравнивания или визуального контроля.
В другом аспекте настоящее изобретение относится к нуклеиновой кислоте, кодирующей антитело или его антигенсвязывающий фрагмент.
Выделив нуклеиновую кислоту, кодирующую антитело или его антигенсвязывающий фрагмент в соответствии с настоящим изобретением, антитело или его антигенсвязывающий фрагмент можно получить рекомбинантным способом. Нуклеиновую кислоту выделяют и встраивают в реплицируемый вектор с последующим дальнейшим клонированием (амплификацией ДНК) или дальнейшей экспрессией. Исходя из этого, в другом аспекте настоящее изобретение направлено на вектор, включающий нуклеиновую кислоту.
Термин «нуклеиновая кислота» предназначен для охвата молекул ДНК (гДНК и кДНК) и РНК, а нуклеотид, который представляет собой основной компонент нуклеиновой кислоты, включает нуклеотиды природного происхождения, а также их аналоги, в которых модифицированы фрагменты сахара или оснований. Последовательность нуклеиновой кислоты, кодирующая вариабельные области тяжелой и легкой цепи по настоящему изобретению, может варьироваться. Такое изменение включает добавление, делецию или неконсервативную или консервативную замену нуклеотидов.
ДНК, кодирующая антитело, может быть легко выделена или синтезирована с помощью обычных процедур (например, с применением олигонуклеотидного зонда, способного специфически связываться с ДНК, кодирующей тяжелые и легкие цепи антитела). Доступно множество разнообразных векторов. Компоненты вектора, как правило, включают, без ограничений, один или несколько из следующих компонентов: сигнальные последовательности, точки начала репликации, один или несколько маркерных генов, энхансерные элементы, промоторы и последовательности терминации транскрипции.
Как применен в настоящем документе, термин «вектор» относится к средству для экспрессии генов-мишеней в клетках-хозяевах и включает плазмидные векторы, космидные векторы и вирусные векторы, такие как бактериофаговые векторы, аденовирусные векторы, ретровирусные векторы и аденоассоциированные вирусные векторы. Нуклеиновая кислота, кодирующая антитело в векторе, функционально связана с промотором.
Термин «функционально связанный» означает функциональную связь между последовательностью регуляции экспрессии нуклеиновой кислоты (например, массивом сайта связывания промотора, сигнальной последовательностью или регулятором транскрипции) и другой последовательностью нуклеиновой кислоты и позволяет регуляторной последовательности регулировать транскрипцию и/или трансляцию другой последовательности нуклеиновой кислоты.
Если прокариотическую клетку применяют в качестве хозяина, то она обычно включает мощный промотор, способный осуществлять транскрипцию (такой как tac-промотор, lac-промотор, lacUV5-промотор, lpp-промотор, pLλ-промотор, pRλ-промотор, rac5-промотор, amp-промотор, recA-промотор, SP-промотор, trp-промотор или T7-промотор), сайт связывания рибосомы для инициации трансляции и последовательность терминации транскрипции/трансляции. Кроме того, например, если в качестве хозяина применяют эукариотическую клетку, то она включает промотор, полученный из генома клеток млекопитающих (например, промотор металлотионеина, промотор β-актина, промотор гемоглобина человека или промотор креатина мышц человека ) или промотор, полученный из вируса млекопитающего (например, поздний промотор аденовируса, промотор вируса коровьей оспы 7,5K, промотор SV40, цитомегаловирусный (CMV) промотор, промотор HSV tk, промотор вируса опухоли молочной железы мыши (MMTV), промотор LTR HIV, промотор вируса Молони, промотор вируса Эпштейна-Барра (EBV) и промотор вируса саркомы Рауса (RSV)), и обычно имеет последовательность полиаденилирования в качестве последовательности терминации транскрипции.
Необязательно, вектор может быть слит с другой последовательностью, чтобы облегчить очистку экспрессируемого из него антитела. Последовательность для слияния включает, например, глутатион-S-трансферазу («Pharmacia», США), мальтозосвязывающий белок («NEB», США), FLAG («IBI», США), 6x His (гексагистидин; «Qiagen», США) и тому подобное.
Вектор включает гены устойчивости к антибиотикам, обычно применяемые в данной области техники в качестве селектируемых маркеров, и их примеры включают гены, обеспечивающие устойчивость к ампициллину, гентамицину, карбенициллину, хлорамфениколу, стрептомицину, канамицину, генетицину, неомицину и тетрациклину.
В другом аспекте настоящее изобретение направлено на клетку, трансформированную вышеуказанным вектором. Клетка, применяемая для продуцирования антитела по настоящему изобретению, может представлять собой прокариотическую, дрожжевую клетку или клетку высших эукариот, но не ограничивается ими.
Можно применять прокариотические клетки-хозяева, такие как Escherichia coli, штаммы рода Bacillus, такие как Bacillus subtilis и Bacillus thuringiensis, Streptomyces spp., Pseudomonas spp. (например, Pseudomonas putida), Proteus mirabilis и Staphylococcus spp. (например, Staphylococcus carnosus).
Клетки животных представляют наибольший интерес, и примеры полезных линий клеток-хозяев включают, COS-7, BHK, CHO, CHOK1, DXB-11, DG-44, CHO/-DHFR, CV1, COS-7, HEK293, BHK, TM4, VERO, HELA, MDCK, BRL 3A, W138, Hep G2, SK-Hep, MMT, TRI, MRC 5, FS4, 3T3, RIN, A549, PC12, K562, PER.C6, SP2/0, NS-0, U20S и HT1080, но не ограничиваются ими.
В другом аспекте настоящее изобретение относится к способу получения антитела или его антигенсвязывающего фрагмента, включающему: (а) культивирование клетки; и (b) выделение антитела или его антигенсвязывающего фрагмента из культивируемой клетки.
Клетки можно культивировать в различных средах. В качестве культуральной среды может быть без ограничений применена любая коммерчески доступная среда. Все другие необходимые добавки, хорошо известные специалистам в данной области техники, могут быть включены в соответствующих концентрациях. Условия культивирования, такие как температура и рН, обычно применяют с клетками-хозяевами, выбранными для экспрессии, что будет очевидно специалистам в данной области техники.
Восстановление антитела или его антигенсвязывающего фрагмента может быть осуществлено, например, центрифугированием или ультрафильтрацией для удаления примесей и очистки полученного продукта с применением, например, аффинной хроматографии. Могут быть применены другие дополнительные способы очистки, такие как анионообменная или катионообменная хроматография, хроматография гидрофобного взаимодействия и хроматография на гидроксиапатите (HA).
В другом аспекте настоящее изобретение относится к композиции для предотвращения или лечения опухоли или рака, включающей антитело в качестве активного ингредиента. Антитело может представлять собой IgG или фрагмент, включающий вариабельную область, а именно ScFv или Fab. Кроме того, вариабельная область тяжелой цепи может представлять собой IgG1, IgG2, IgG3 или IgG4.
Настоящее изобретение может обеспечивать, например, фармацевтическую композицию для профилактики или лечения опухоли или рака, содержащую: (а) фармацевтически эффективное количество антитела к VISTA или его антигенсвязывающего фрагмента в соответствии с настоящим изобретением; и (б) фармацевтически приемлемый носитель. Настоящее изобретение также относится к способу профилактики или лечения опухоли или рака, включающему введение антитела или его антигенсвязывающего фрагмента в соответствии с настоящим изобретением пациенту с опухолью или раком. Настоящее изобретение может обеспечить применение антитела или его антигенсвязывающего фрагмента для ингибирования иммуносупрессивного механизма VISTA и его применение для профилактики или лечения опухоли или рака.
Опухоли, которые представляют собой заболевания, к которым может быть применена композиция, включают типичные опухоли или раковые заболевания, которые реагируют на иммунотерапию, а также опухоли или раковые заболевания, которые до настоящего времени не подвергались иммунотерапии. Неограничивающие примеры опухолей или раковых заболеваний, которые представляют собой мишени для лечения, включают меланому (например, метастатическую злокачественную меланому), рак почки (например, светлоклеточный рак почки), рак предстательной железы (например, гормонорефрактерную аденокарциному простаты), аденокарциному поджелудочной железы, рак молочной железы, рак толстой кишки, рак легких (например, немелкоклеточный рак легкого), рак пищевода, плоскоклеточный рак головы и шеи, рак печени, рак яичников, рак шейки матки, рак щитовидной железы, глиобластому, глиому, лейкоз, лимфому и другие неопластические карциномы. Кроме того, опухоли или раки в соответствии с настоящим изобретением включают рефрактерные или рецидивирующие раки, которые можно лечить с применением антитела по настоящему изобретению.
В другом аспекте настоящее изобретение относится к композиции для предотвращения или лечения аутоиммунного заболевания, включающей антитело в качестве активного ингредиента. Антитело может представлять собой IgG или фрагмент, включающий вариабельную область, а именно ScFv или Fab. Кроме того, вариабельная область тяжелой цепи может представлять собой IgG1, IgG2, IgG3 или IgG4.
Настоящее изобретение может обеспечивать, например, композицию для профилактики или лечения аутоиммунного заболевания, содержащую: (а) фармацевтически эффективное количество антитела к VISTA или его антигенсвязывающего фрагмента в соответствии с настоящим изобретением; и (б) фармацевтически приемлемый носитель. Настоящее изобретение также относится к способу профилактики или лечения аутоиммунного заболевания, включающему введение антитела или его антигенсвязывающего фрагмента в соответствии с настоящим изобретением пациенту с аутоиммунным заболеванием. Настоящее изобретение может обеспечить применение антитела или его антигенсвязывающего фрагмента для улучшения иммуносупрессивного механизма VISTA и его применения для профилактики или лечения аутоиммунного заболевания.
Аутоиммунное заболевание может включать, например, лейкоз; синдром хронической усталости; болезнь трансплантат против хозяина (GVHD); гипералгезию; воспалительные заболевания кишечника; нейровоспалительные заболевания; травмы ишемии/реперфузии, включая церебральную ишемию, повреждение головного мозга в результате травмы, эпилепсию, кровотечение или судороги, которые могут вызвать нейродегенерацию; диабет, например, диабет 1-го типа; рассеянный склероз; заболевания глаз; боль; панкреатит; легочный фиброз; ревматоидные заболевания, такие как ревматоидный артрит, остеоартрит, ювенильный ревматоидный артрит, серопозитивный полиартрит, анкилозирующий спондилит, синдром Рейтера и реактивный артрит, псориатический артрит, энтеропатический артрит, полимиозит, дерматомиозит, склеродермия, системный склероз, васкулит, церебральный васкулит, синдром Шёгрена, ревматическая лихорадка, полихондрит и множественная миалгия, ревматоидный и гигантоклеточный артериит; септический шок; побочные эффекты в результате лучевой терапии; системная красная волчанка; заболевание височно-нижнечелюстного сустава; тиреоидит и тому подобное.
Как применен в настоящем документе, термин «предотвращение» относится к любому действию, вызывающему подавление рака или аутоиммунного заболевания или задержку его прогрессирования при введении композиции в соответствии с настоящим изобретением. Термин «лечение» означает подавление, облегчение или устранение прогрессирования рака, или подавление, облегчение или устранение прогрессирования аутоиммунного заболевания.
В некоторых случаях, существует возможность эффективно воздействовать на опухолевые клетки, применяя антитело в сочетании с другим противораковым терапевтическим агентом, и существует возможность усиливать иммунный ответ, направленный на опухолевые клетки, путем повышения активности противоопухолевых Т-клеток. Антитело может быть применено в комбинации с другими противоопухолевыми или иммуногенными средствами [например, аттенуированными раковыми клетками, опухолевыми антигенами (включая рекомбинационные белки, пептиды и молекулы углеводов), клетками переноса антигенов, например, антигенов, происходящих из опухоли, или дендритными клетками, сенсибилизированными нуклеиновыми кислотами, иммуностимулирующими цитокинами (например, IL-2, IFNα2 и GM-CSF) и клетками, трансфицированными генами, кодирующими иммуностимулирующие цитокины (включая, например, GM-CSF, но не ограничиваясь ими)]; со стандартной терапией рака (например, химиотерапией, лучевой терапией или хирургическим вмешательством); или другими антителами (включая, но не ограничиваясь, VEGF, EGFR, Her2/neu, рецепторы VEGF, рецепторы других факторов роста, CD20, CD40, CTLA-4, OX-40, 4-IBB и ICOS).
В другом аспекте настоящее изобретение относится к композиции, содержащей антитело или его антигенсвязывающий фрагмент, для введения в комбинации с антителом к PD-1 или антителом к PD-L1. В другом аспекте настоящего изобретения обеспечивают способ профилактики или лечения опухоли или рака, включающий введение антитела или его антигенсвязывающего фрагмента в сочетании с антителом к PD-1 или антителом к PD-L1 пациенту с опухолью или раком. В другом аспекте настоящего изобретения обеспечивают применение антитела или его антигенсвязывающего фрагмента для введения в комбинации с антителом к PD-1 или антителом к PD-L1 для лечения опухоли или рака.
Антитело или его антигенсвязывающий фрагмент можно вводить одновременно с антителом к PD-1 или антителом к PD-L1 или можно вводить отдельно от него с интервалом времени между ними. Отдельное введение антитела к PD-1 или антитела к PD-L1 можно проводить до или после введения антитела или его антигенсвязывающего фрагмента.
Поскольку в композиции в качестве активного ингредиента применяют антитело против VISTA или его антигенсвязывающий фрагмент в соответствии с настоящим изобретением, их общие описания опущены.
Фармацевтически приемлемый носитель, содержащийся в фармацевтической композиции, может включать фармацевтически приемлемый носитель, обычно применяемый в препаратах, и может включать, без ограничения, лактозу, декстрозу, сахарозу, сорбит, маннит, крахмал, аравийскую камедь, фосфат кальция, альгинат, желатин, силикат кальция, микрокристаллическую целлюлозу, поливинилпирролидон, воду, сироп, метилцеллюлозу, метилгидроксибензоат, пропилгидроксибензоат, тальк, стеарат магния, минеральное масло и тому подобное. Композиция в соответствии с настоящим изобретением может дополнительно содержать смазывающее вещества, смачивающее средство, подсластитель, ароматизатор, эмульгатор, суспендирующее средство, консервант или тому подобное, в дополнение к описанным выше ингредиентам.
Фармацевтическую композицию в соответствии с настоящим изобретением можно вводить перорально или парентерально. Парентеральное введение может представлять собой внутривенную инъекцию, подкожную инъекцию, внутримышечную инъекцию, внутрибрюшинную инъекцию, эндотелиальное введение, местное введение, интраназальное введение, ингаляционное введение, ректальное введение или тому подобное.
При пероральном введении, поскольку белки или пептиды перевариваются, пероральная композиция должна быть покрыта активным лекарственным средством или составлена таким образом, чтобы защитить его от деградации в желудке. Кроме того, фармацевтическую композицию можно вводить с применением любого устройства, способного доставлять активное вещество к клеткам-мишеням.
Подходящую дозу фармацевтической композиции в соответствии с настоящим изобретением можно варьировать в зависимости от таких факторов, как способ составления, способ введения и возраст, масса тела, пол, патологические состояния, диета, время введения, способ введения, скорость выведения и чувствительность пациента, и врач общей практики обычной квалификации может легко определить и назначить дозу, эффективную для желаемого лечения или профилактики. Например, суточная доза фармацевтической композиции в соответствии с настоящим изобретением может находиться в диапазоне от 0,001 до 100 мг/кг. Термин «фармацевтически эффективное количество» может означать количество, достаточное для предотвращения или лечения рака или аутоиммунного заболевания.
Фармацевтическая композиция в соответствии с настоящим изобретением может быть приготовлена в форме единичной дозы или может быть включена в многодозовый контейнер посредством получения композиции с применением фармацевтически приемлемого носителя и/или вспомогательного вещества в соответствии со способом, который может быть легко осуществлен специалистами в области техники, к которой относится настоящее изобретение. В этом случае композиция может находиться в форме раствора, суспензии, сиропа или эмульсии в масляной или водной среде или может находиться в форме экстракта, порошка, гранулы, таблетки или капсулы. Композиция может дополнительно содержать диспергатор или стабилизатор.
Примеры
Далее настоящее изобретение будет описано более подробно с отсылкой к примерам. Однако специалистам в данной области техники будет очевидно, что эти примеры приведены только для иллюстрации настоящего изобретения и не должны рассматриваться как ограничивающие объем настоящего изобретения.
Пример 1. Скрининг антител, связывающихся с VISTA
Библиотеки наивных человеческих ScFv (scFv), раскрытые в выложенном корейском патенте № 10-2008-0109417, применяли для библиотек антител для скрининга антител, связывающихся с VISTA, и получения библиотек. 100 мкл антигена (hVISTA-Fc, «R&D systems», № по каталогу 7126-B7) наносили в количестве 2 мкл/мл на 96-луночный иммунопланшет и инкубировали в течение ночи при 4°C. На следующий день покрытый антигеном планшет промывали три раза PBS, а затем проводили реакцию с 200 мкл блокирующего буфера с 2%-ным BSA при комнатной температуре в течение 2-х часов. 50 мкл исходного раствора XL1-Blue добавляли к 2 мл 2x среды для роста клеток YT-TET (тетрациклин 10 мкг/мл) и инкубировали при 37°C в течение 2-х часов при 200 об/мин, а затем добавляли еще 13 мл этой среды и инкубировали до тех пор, пока OD 600 не достигала 0,5. После блокирования в течение 2-х часов лунку промывали 3 раза 1XPBS. Группу фаговой библиотеки объединяли с каждой промытой лункой, и фаговую библиотеку и 4% BSA смешивали в равных количествах, а затем к ним добавляли 200 мкл смеси с последующей инкубацией на качалке при комнатной температуре в течение 30-ти минут, позволяя реакции протекать в течение 2-х часов. После завершения реакции с библиотекой фагов супернатант отбрасывали, остаток промывали 5 раз 0,05% PBST и промывали 5 раз PBS, в каждую лунку добавляли по 100 мкл 100 мМ TEA (триметиламина) и полученную смесь перемешивали встряхиванием при комнатной температуре в течение 10-ти минут. Через 10 минут в каждую лунку добавляли по 50 мкл 1М Трис (рН 7,5) с последующим перемешиванием. Супернатант добавляли к 10 мл XL1-синего, имевшего OD600, равную 0,5, для проведения заражения при 37°С в течение 30-ти минут. После завершения заражения, 100 мкл применяли в качестве выходного титра, а остаток центрифугировали при 7000 об/мин в течение 10-ти минут. Супернатант отбрасывали, а осадок распределяли по большой квадратной чашке (СМ 34 мкг/мл + 1% глюкоза) и инкубировали при 30°С в течение ночи. 100 мкл, оставленные в качестве выходного титра, разбавляли до 1/10, 1/100 и 1/1000, распределяли по чашке CM и инкубировали в течение ночи при 37°C. На следующий день колонии, выращенные на квадратной чашке, соскребали с помощью петли после добавления в чашку 50 мл 2х среды YT и центрифугировали при 7000 об/мин в течение 10-ти минут, супернатант отбрасывали, а осадок применяли для приготовления первичного исходного продукта для пэннинга. 100 мл культуральной среды 2х YT (среда для роста клеток: СМ 34 мкг/мл + 1% глюкоза) помещали в колбу Эрленмейера на 500 мл, туда добавляли клетки так, чтобы довести значение OD600 до 0,2, и выращивали при 200 об/мин и 37°С до OD600, равной 0,5. После культивирования клеток до достижения OD600 величины, равной 0,5, добавляли фаг-помощник (мутант M13KO7) в количестве, в 20 раз превышающем количество клеток. После заражения фагом-помощником при 37°С в течение 30-ти минут проводили центрифугирование при 7000 об/мин в течение 10-ти минут. Супернатант отбрасывали и клетки инкубировали в течение ночи в 100 мл свежей среды 2xYT (CM 34 мкг/мл + кан. 70 мкг/мл + 1 мМ IPTG + 5 мМ MgCl2) при 200 об/мин и 30°C. На следующий день выращенные клетки центрифугировали при 7000 об/мин в течение 10-ти минут и снова центрифугировали таким же образом, как описано выше. Собранный супернатант осаждали на льду в присутствии 1/5 (объем/объем) 20% ПЭГ/2,5 мМ NaCl по отношению к супернатанту в течение 1-го часа. После осаждения проводили центрифугирование при 7000 об/мин в течение 1-го часа. Супернатант отбрасывали, а осадок высвобождали с 3 мл PBS, фильтровали через фильтр 0,45 мкм, хранили при 4°C и применяли в следующем процессе пэннинга. Этот процесс повторяли 3-4 раза, и связывание антитела с антигеном идентифицировали с помощью ELISA.
Пример 2. ELISA для моноклонального фага ScFv
После того, как процесс пэннинга был завершен, конечную стоковую суспензию круглых клеток разводили с образованием 200-500 колоний, распределяли по чашке с агаром CM и затем инкубировали в течение ночи при 37°C. На следующий день, когда колонии росли, на 96-луночный глубокий планшет вносили 200 мкл среды 2xYT (CM 34 мкг/мл + 1% глюкозы), в каждую лунку вносили колонию по одной, а затем планшет инкубировали в течение ночи при 37°С и 3000 об/мин. На следующий день 200 мкл среды 2xYT (CM 34 мкг/мл + 1% глюкоза) вносили на новый 96-луночный глубокий планшет, и 20 мл клеток, выращенных накануне, вносили в каждую лунку и выращивали при 37°С и 3000 об/мин в течение 1-го часа и 10-ти минут. Оставшиеся клетки хранили при -70°С в 100 мкл 50%-ного глицерина. Когда клетки росли, 1 мкл хелперного фага смешивали с 19 мкл среды 2xYT, и 20 мкл полученной смеси вносили в каждую лунку и инкубировали в течение 30-ти минут при 37°C. После инкубации проводили центрифугирование при 3000 об/мин в течение 10-ти минут. Супернатант отбрасывали и к остатку добавляли 200 мкл 2×YT среды (CM 34 мкг/мл + Кан. 70 мкг/мл + 1 мМ IPTG + 5 мМ MgCl2) с последующей инкубацией в MegaGrow при 30°C и 3000 об/мин в течение ночи.
1 мкг/мл Ag (hVISTA-Fc, mVISTA-Fc) вносили по 100 мкл/лунку на 96-луночный иммунопланшет и затем инкубировали в течение ночи при 4°C. На следующий день клетки, выращенные накануне, центрифугировали при 3000 об/мин в течение 10-ти минут и хранили при 4°С. Посаженный на планшет Ag промывали 3 раза 0,05% PBST, а затем добавляли 200 мкл блокирующего буфера с 2%-ным BSA с последующей инкубацией при 25°C в течение 2-х часов. После того, как блокирование было завершено, полученное в результате промывали 3 раза 0,05% PBST. 50 мкл 4%-ного BSA смешивали с 50 мкл фага, хранившегося при пониженной температуре, равной 4°С, и оставляли при встряхивании при комнатной температуре в течение 1-го часа для протекании между ними реакции. После завершения связывания фага продукт реакции трижды промывали 0,05% PBST, к нему добавляли 100 мкл HRP-конъюгированного мышиного анти-М13-антитела (1:3000, GE, № по кат. 27-9421-01), и оставляли для протекания реакции при 25°С в течение 1-го часа. После завершения реакции полученный продукт промывали 3 раза 0,05% PBST, к нему добавляли 100 мкл TMB (набор реагентов субстрата #BD TMB 555214), окраска развивалась в течение 3-5 минут, к этому добавляли 50 мкл стоп-раствора, а затем проводили анализ с помощью считывающего устройства для ELISA.
Таблица 1. Результат измерения способом ELISA для выбора связывания моноклонального фага scFv с антигеном VISTA после процесса пэннинга
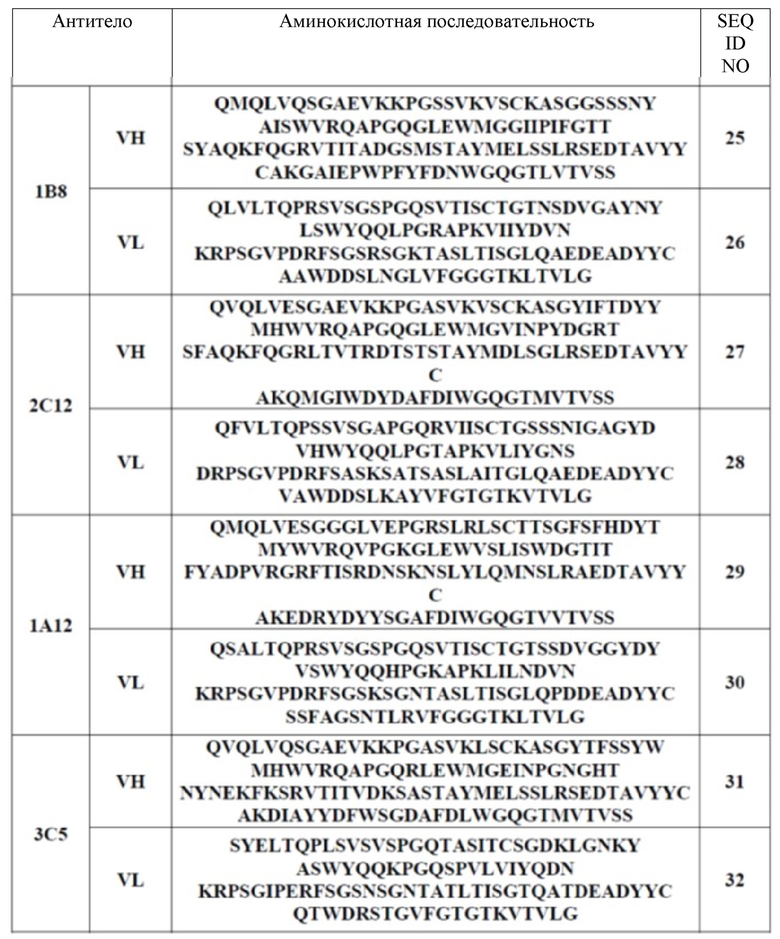
Отобранные антитела показаны в приведенной ниже таблице 2.
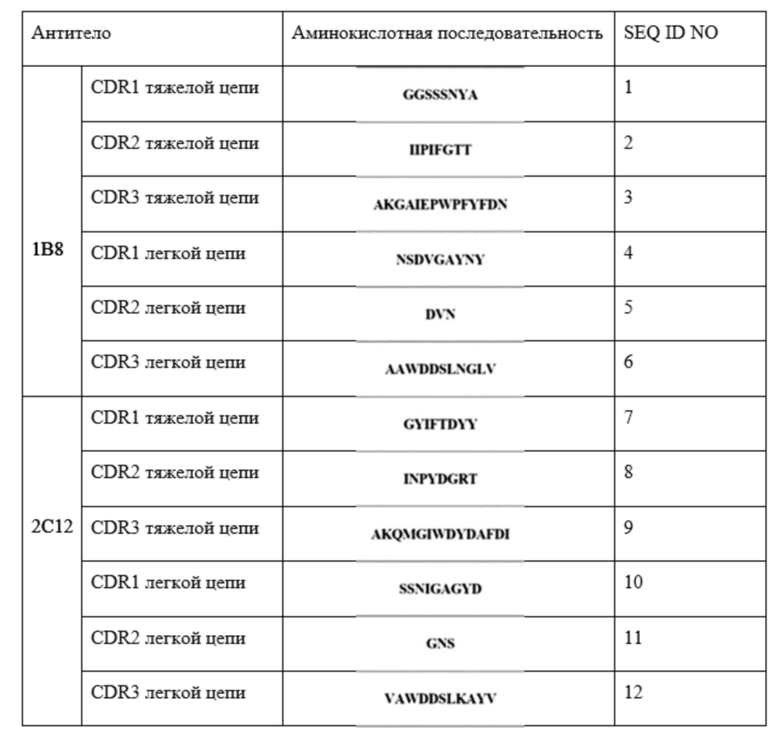
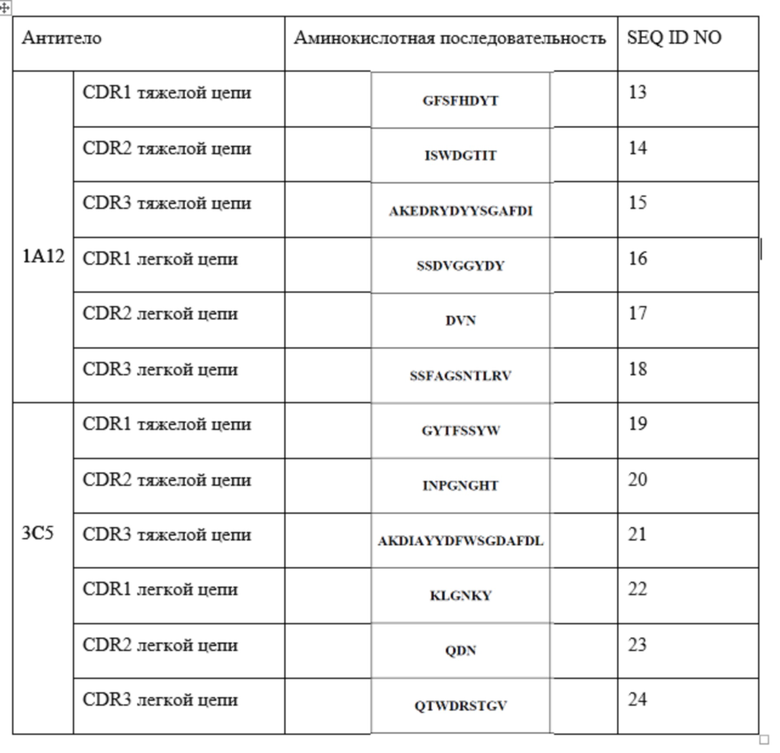
Таблица 3
Пример 3. Связывание анти-VISTA ScFV-фага с VISTA-экспрессирующими клетками CHO-K1
Клетки CHO-K1, экспрессирующие VISTA человека и VISTA мыши, были получены для определения того, связывается ли прошедшее скрининг антитело с клетками, экспрессирующими VISTA. 50 мкл полученных клеток высевали на 96-луночный глубокий планшет при плотности, равной 4×106 клеток/мл, в буфере FACS (2% FBS, 0,05% азида натрия в PBS), к этому добавляли 50 мкл супернатанта фага, подвергающегося фаговой инкубации, и инкубировали при комнатной температуре в течение 1-го часа. После инкубации в каждую лунку добавляли по 400 мкл буфера FACS с последующим центрифугированием при 2000 об/мин в течение 5-ти минут. Супернатант отбрасывали и к остатку добавляли 100 мкл анти-М13-антитела (1:1000) с последующим проведением реакции при 4°С в течение 1-го часа. После завершения реакции в каждую лунку добавляли по 400 мкл буфера FACS с последующим центрифугированием при 2000 об/мин в течение 5-ти минут. Супернатант отбрасывали, добавляли по 100 мкл анти-мышиного антитела IgG-PE (1:500) и оставляли для протекания реакции при 4°С в течение 1-го часа. После завершения реакции в каждую лунку добавляли по 400 мкл буфера FACS с последующим центрифугированием при 2000 об/мин в течение 5-ти минут. Супернатант отбрасывали, и к нему добавляли 200 мкл буфера FACS,а затем анализировали с применением FACS («Beckton Dickinson», FACSCalibur). Результаты приведены на фиг. 1.
Как показано на фиг. 1, все отобранные антитела связывались с клетками CHO-K1, полученными для сверхэкспрессии человеческого VISTA. 6A6, применяемый в качестве группы отрицательного контроля, не связывался с ними, а антитело против VISTA («R&D systems», № по кат. FAB71261A), применяемое в качестве группы положительного контроля, хорошо связывалось с клетками, как и ожидалось.
Пример 4. Экспрессия анти-VISTA IgG
Превращение прошедшего скрининг фага scFv в форму IgG проводили с применением способов молекулярной биологии. Фагемиду экстрагировали из прошедшего скрининг клона E. coli и дважды разрезали рестриктазой Sfi I (R0123, «New England Biolabs», США) для получения фрагмента ДНК вариабельной области тяжелой цепи, вектор pIgGHD-6A6Hvy, включавший константную область тяжелой цепи, обрабатывали Sfi I, а затем вставляли фрагмент ДНК вариабельной области. Таким же способом, как описано выше, фагемиду дважды разрезали рестриктазой BstX I (R0113, «New England Biolabs») для получения фрагмента ДНК вариабельной области легкой цепи, вектор pIgGLD-6A6Lgt, включавший константную область легкой цепи, дважды разрезали с помощью BstX I, и фрагмент ДНК вариабельной области вставляли для завершения клонирования ДНК в форму IgG.
Временную экспрессию IgG осуществляли с помощью набора для системы экспрессии Expi293F («Thermo Fisher Scientific», США). Клетки Expi293, включенные в набор, культивировали в суспензии на орбитальном шейкере при 125 об/мин, 37°C и 5% CO2 с применением специальной среды. Каждые 3 дня клетки культивировали путем пассирования до 3×105 клеток/мл, и когда вводили вектор экспрессии, то количество клеток доводили до 3×106 клеток/мл перед применением. Введение гена проводили с помощью «ExpiFectamine» в качестве специального реагента, готовили комплекс липид-ДНК, содержащий 1 мкг ДНК вектора экспрессии, и 2,7 мкл «ExpiFectamine» на 1 мл клеточной суспензии, и добавляли к клеточной суспензии. Через 16-18 часов после введения добавляли половину (1/2) энхансера для индукции экспрессии. Затем клетки культивировали в тех же условиях, как указано выше, в течение 3-4 дней и центрифугировали для получения супернатанта, содержащего IgG.
Пример 5. Очистка анти-PD-L1 антитела
Полученный супернатант наносили на колонку с белком A («GE Healthcare») и очищали IgG с помощью аффинной хроматографии. После уравновешивания колонки с помощью 20 мМ Трис-HCl, 50 мМ NaCl и 5 мМ ЭДТА (рН 7,0) наносили супернатант, промывали 50 мМ Трис-HCl, 500 мМ NaCl, 5 мМ ЭДТА и 0,2%-ным раствором полисорбата 20 (рН 7,0 элюировали 50 мМ NaCl, 0,1 М глицин-HCl (рН 3,5) и нейтрализовали 1 М Трис. Элюированный белок диализовали с применением диализной мембраны MWCO 10000 spectra/por («Spectrum Labs», США) для смены растворителя на PBS. Затем белок концентрировали до необходимой концентрации с помощью Vivaspin («Sartorius», DE), распределяли и хранили при -80°C.
После очистки каждое антитело обрабатывали невосстанавливающими и восстанавливающими буферами LDS для образцов («Thermo Fisher Scientific») и анализировали с помощью электрофореза, применяя систему NuPAGE («Thermo Fisher Scientific»). В результате был получен IgG, имеющий общую молекулярную массу около 150 кДа, включающий тяжелую цепь 50 кДа и легкую цепь 25 кДа.
Пример 6. Связывающая способность антитела против VISTA к антигену
Связывающая способность прошедшего скрининг антитела к антигену измеряли с помощью Octet («ForteBio»). Для этой цели антитело иммобилизовали на биосенсоре, различные концентрации антигена добавляли в 96-луночный планшет, а затем измеряли способность к связыванию.
Таблица 4. Результаты определения способности к связыванию различных анти-VISTA-антител с антигеном VISTA для измерения способности к связыванию между ними
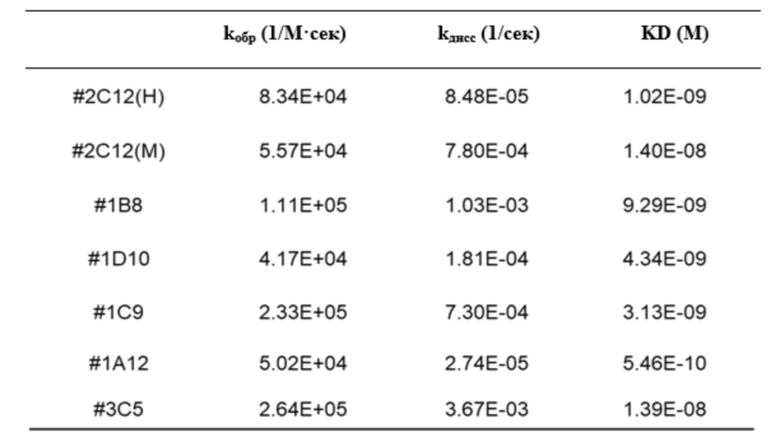
Пример 7. Перекрестная реактивность анти-VISTA-антитела к VISTA человека и мыши
Анализ ELISA: 1 мкг/мл Ag (человеческий VISTA-Fc или мышиный VISTA-Fc) высевали в объеме 100 мкл/лунку на 96-луночный планшет и инкубировали при 4°C в течение ночи. На следующий день прикрепленный к планшету Ag промывали 3 раза 0,05% PBST и добавляли 200 мкл 2% блокирующего буфера BSA с последующей инкубацией при 25°C в течение 2-х часов. После завершения блокировки полученный продукт промывали 3 раза 0,05% PBST. 1 мкг/мл каждого антитела вносили в объеме 100 мкл/лунку и инкубировали при 25°С в течение 1-го часа. После завершения инкубации полученный продукт промывали 3 раза 0,05% PBST и добавляли к нему 100 мкл пероксидазы, конъюгированной с козьим антителами к человеческому IgG (каппа) (1:2000, «Bethyl Lab», № по кат. A80-115P), с последующей инкубацией при 25°С в течение 30-ти минут. После инкубации полученный продукт промывали 3 раза 0,05% PBST, добавляли 100 мкл TMB (набор реагентов BD TMB для субстрата # 555214), окрашивали в течение 3-5 минут, к этому добавляли 50 мкл стоп-раствора, и затем проводили анализ с помощью считывающего устройства для микропланшетов для ELISA. Результаты приведены на фиг. 2.
Как показано на фиг. 2, все прошедшие скрининг антитела связываются с VISTA человека, в частности, антитело 2C12 хорошо связывается с VISTA мыши, а также с VISTA человека.
Анализ FACS: для выявления сверхэкспрессии VISTA человека и мыши в клетках CHO-K1, клеточный раствор (5×105 клеток/100 мкл/пробирка FACS) в концентрации 5×106/мл в буфере FACS (2% FBS, 0,05% азида натрия в PBS), готовили 2 мкг/мл прошедшего скрининг антитела и 100 мкл клеточного раствора, 100 мкл антитела помещали в пробирку FACS и затем инкубировали при 4°C в течение 30-ти минут. После завершения инкубации в каждую пробирку добавляли по 2 мл буфера FACS с последующим центрифугированием при 1500 об/мин в течение 5-ти минут. Супернатант отбрасывали, в каждую пробирку добавляли 100 мкл козьего PE, конъюгированного с IgG-Fc человека (A80-248PE, 1:500), и реакция протекала при 4°C в течение 20-ти минут. В случае положительной контрольной группы, 5 мкл APC-конъюгированного анти-hVISTA (R&D, № по кат. 71261A) добавляли к клеткам со сверхэкспрессией hVISTA (в том же количестве, что и к образцу), а в случае мышей 1 мкл APC-конъюгированный анти-mVISTA («BioLegend», № по кат. 143710) добавляли к клеткам со сверхэкспрессией mVISTA (в том же количестве, что и образец) с последующей реакцией при 4°C в течение 20-ти минут. После завершения реакции, в каждую лунку добавляли по 2 мл буфера FACS с последующим центрифугированием при 1500 об/мин в течение 5-ти минут. Супернатант отбрасывали, и туда добавляли 200 мкл буфера FACS с последующим анализом с применением BD FACSCalibur. Результаты приведены на фиг. 3.
Как показано на фиг. 3, при обработке клеток CHO-K1, полученных для сверхэкспрессии VISTA, с помощью прошедшего скрининг анти-VISTA, как в ELISA, все прошедшего скрининг антитела связываются с CHO-K1, экспрессирующими VISTA человека на своей поверхности, и антитело 2C12 также связывается с CHO-K1, экспрессирующими VISTA мыши на своей поверхности.
Пример 8. Алло-MLR анализ антитела против VISTA
У донора-человека отбирали 50 мл периферической крови и разбавляли в 3 раза PBS, содержавшим 2 мМ ЭДТА. 15 мл Ficoll-Paque (GE, № по кат. 17-1440-03) вносили в свежую пробирку на 50 мл и медленно загружали 30 мл разбавленной крови с последующим центрифугированием при 2000 об/мин в течение 40 минут. Слой РВМС извлекали, переносили в пробирку на 50 мл и промывали промывочным буфером (среда RPMI1640, содержавшая 2% FBS и 10 мМ HEPES) путем центрифугирования при 1600 об/мин в течение 10-ти минут. После центрифугирования супернатант отбрасывали и многократно промывали. Клеточные осадки, оставшиеся после центрифугирования, разбивали на отдельные клетки с помощью 50 мл промывочного буфера, а затем удаляли мертвую клеточную массу с помощью клеточного фильтра (40 мкм). Клетки (донор A или B), которые планировали применять в качестве респондеров Allo-MLR, разбавляли до концентрации 4×106 клеток/мл средой MLR (среда RPMI1640, содержавшая 10% FBS, 10 мМ HEPES, 1 мМ пируват, NEAA (100X), 2 мМ L-глютамин, 1% антибиотики, 10-5M β-ME). Клетки (доноры B или A), которые планировали применять в качестве стимуляторов, обрабатывали митомицином C (MMC) для ингибирования пролиферации клеток. Способ будет подробно описан следующим образом. Клетки, применяемые в качестве стимуляторов, разводили в среде MLR в концентрации 4×106 клеток/мл в пробирке на 50 мл и добавляли ММС для достижения общего объема 25 мкг/мл с последующей реакцией в течение 30 минут при 37°С. После того как реакция была завершена, пробирку на 50 мл полностью заполняли промывочным буфером и проводили центрифугирование при 1200 об/мин в течение 10 минут с последующей промывкой. Этот процесс был выполнен 4 раза для полного удаления MMC. Наконец, остаток разводили в среде MLR до концентрации 4×106 клеток/мл. Полученные клетки разделяли на аликвоты по 2×105 клеток/лунку (50 мкл) в 96-луночный планшет для культивирования клеток. 50 мкл анализируемого антитела добавляли для достижения конечных концентраций 30 мкг/мл и 10 мкг/мл. Антитело тестировали, применяя по 3 лунки для каждой концентрации. После инкубации в течение 5-ти дней в СО2-инкубаторе при 37°С 50 мкл супернатанта клеточной культуры хранили отдельно для измерения продукции IFN-γ, а оставшиеся клетки применяли для анализа пролиферации клеток. Пролиферацию клеток анализировали путем измерения количества ATP, продуцируемого в клетках, оставшихся после алло-MLR. Способ подробно описан следующим образом. К культивируемым клеткам добавляли 100 мкл (эквивалентно раствору для культивирования клеток) раствора для анализа жизнеспособности по люминесцентности клеток CellTiter-Glo® Luminescent cell viability assay («Promega») и проводили реакцию в течение 10-ти минут при комнатной температуре, чтобы вызвать лизис клеток. Жизнеспособность клеток измеряли с помощью люминометра. Результаты приведены на фиг. 4.
Как показано на фиг. 4, конкуренты (группа положительного контроля) и клоны 1B8 индуцировали экспрессию большего количества гамма-интерферона, чем группа, обработанная неспецифическим антителом (полный IgG), а все другие клоны индуцировали более низкую экспрессию интерферона-гамма, чем полный IgG. Другими словами, эти клоны представляют собой клоны, которые подавляют экспрессию интерферона-гамма. Среди них 2C12, 1A12 и 3C5 продемонстрировали превосходную способность подавлять экспрессию интерферона-гамма.
Пример 9. Противоопухолевая активность антитела против VISTA
Противораковую эффективность терапевтических средств человеческих PBMC и JNJ61610588, пембролизумаба и анти-VISTA mAb 1B8 определяли путем введения их в хвостовую вену мышей NSG, имевших подушечки, трансплантированные с клетками линии рака молочной железы человека, подушка из жировой ткани молочной железы MDA-MB-231, для оценки противоопухолевой активности антитела против VISTA. Эксперимент проводили совместно с Центром ресурсов лабораторных животных Корейского научно-исследовательского института биологии и биотехнологии.
Клеточную линию рака молочной железы человека, MDA-MB-231, размораживали и культивировали в инкубаторе с CO2 («Forma», США) при температуре 37°C и концентрации CO2, равной 5%. В последний день культивирования все раковые клетки собирали и подсчитывали, и концентрацию клеток доводили до 3×107 клеток/мл с применением бессывороточной среды. Раствор культуры клеток, отрегулированный таким образом, вводили с помощью инъекции по 0,1 мл (3×106 клеток/мышь) в подушечку из жировой ткани каждой из левой и правой областей груди.
После трансплантации раковых клеток, когда средний размер опухоли для каждой группы достигал 46,9 мм3, вводили PBMC (4×107 клеток/мл) типа A (мышь № 1 в каждой группе), типа B (мышь № 2 в каждой группа), типа C (мышь № 3 в каждой группе), типа D (мышь № 4 в каждой группе), типа E (мышь № 5 в каждой группе) и типа F (мышь № 6 в каждой группе) с помощью инъекции в дозе 0,16 мл (0,64×107 клеток/мышь) в хвостовую вену.
Для отделения PBMC у донора-человека отбирали 50 мл периферической крови и разбавляли в 3 раза PBS, содержащим 2 мМ EDTA. 15 мл Ficoll-Paque (GE, № по кат. 17-1440-03) вносили в свежую пробирку на 50 мл и медленно загружали в нее 30 мл разбавленной крови, а затем центрифугировали при 2000 об/мин в течение 40 минут. Слой РВМС извлекали и переносили в пробирку на 50 мл, и клетки промывали промывочным буфером (среда RPMI1640, содержащая 2% FBS и 10 мМ HEPES) центрифугированием при 1600 об/мин в течение 10-ти минут. После центрифугирования супернатант отбрасывали и промывали четыре раза. Клеточные осадки, оставшиеся после центрифугирования, разбивали на отдельные клетки в 50 мл промывочного буфера и затем разбавляли до концентрации 2×107 клеток/мл в среде PBS.
Для формирования группы мышей и введения лекарственного средства группе мышей после инъекции РВМС начинали введение лекарственного средства. Препарат вводили через хвостовую вену в дозе 5 мг/кг в каждую группу группы 1: РВМС + полный IgG человека (контроль); группу 2: PBMC + конкурент (JNJ 61610588); группу 3: РВМС + пембролизумаб; группу 4: РВМС + анти VISTA mAb (1B8); и группу 5: РВМС + пембролизумаб + анти-VISTA mAb (1B8).
После инъекции РВМС препарат сначала вводили по 0,2 мл на мышь два раза в неделю в общей сложности 7 раз.
Всех животных наблюдали на предмет проявления общих клинических симптомов и изменения массы тела и размера опухоли в начале введения и непосредственно перед каждым введением в течение экспериментального периода.
Изменение размера опухоли выражали с помощью формулы длина×ширина×высота/2 после измерения левой и правой опухолей в трех направлениях с применением штангенциркуля Вернье для каждого из 12 субъектов с момента, когда средний размер опухоли в каждой группе трансплантации раковых клеток достигал 46,9 мм3 до 25-го дня после этого.
На 25-й день от начала введения лекарства отбирали по 3 здоровые мыши в каждой группе, из их орбитальных вен (пробирка с ЭДТА) брали кровь, мышей умерщвляли с применением газа CO2, селезенку извлекали и иммобилизовали в PBS и опухоли разделяли на правую и левую части. Опухоли взвешивали с применением химических весов, а затем регистрировали их внешний вид и иммобилизовали в жидком азоте и формалине.
В результате ни одна из групп введения не проявила специфических общих симптомов в течение испытательного периода, но мышь № 2 группы контроля растворителя (PBMC + PBS) и мышь № 5 группы введения PBMC + анти-VISTA mob 1B8 показали потерю веса с 17-го дня и 21-го дня, соответственно, до последнего дня, по сравнению с их первоначальным весом (таблица 5 и фиг. 5).
Таблица 5. Изменение веса мыши по дням (%)
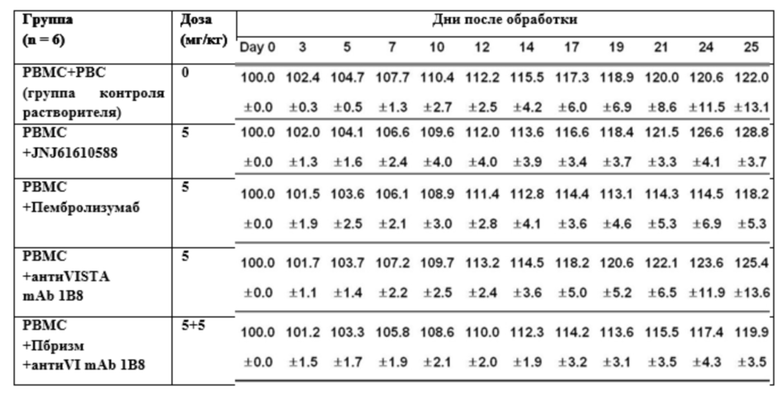
На 25-й день после начала приема препарата опухоль MDA-MB-231 иссекали и взвешивали. В результате в группах введения PBMC + JNJ61610588 (5 мг/кг), PBMC + пембролизумаб (5 мг/кг), PBMC + анти-VISTA mAb 1B8 (5 мг/кг) и PBMC + пембролизумаб + анти-VISTA mAb (5+5 мг/кг) наблюдали статистически значимое снижение массы опухоли на 18,9% (р <0,05), 32,9% (р < 0,001), 37,8% (р < 0,001) и 60,6% (р < 0,001), соответственно (таблица 6, фиг. 6), по сравнению с группой контроля с растворителем (РВМС + полный IgG человека).
Таблица 6. Изменение размера опухоли и веса опухоли в последний день
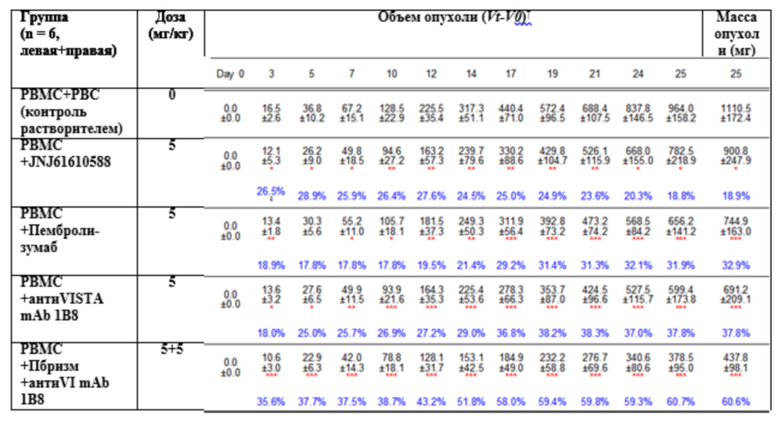
Значащие цифры (t-TEST): * р < 0,05, ** р < 0,01, *** р < 0,001 (против РВМС + PBS);
† Δt=Vt-Vo, Vt (измерение объема опухоли), Vo (начальный объем опухоли);
‡ Уровень ингибирования (против РВМС + PBS).
Пример 10. Изготовление и скрининг вариантов для улучшения сродства
Оптимизацию антител проводили для повышения аффинности клона 1B8 антитела против VISTA. Праймер, имеющий случайные мутации, введенные в CDR3 легкой цепи и CDR3 тяжелой цепи 1B8, получали с применением способа мягкой рандомизации, который сохраняет 80% исходной последовательности ДНК 1B8 и рандомизирует ее. Фрагмент ДНК, кодирующий вариабельную область легкой цепи 1B8 и вариабельную область тяжелой цепи ME4, в которую была введена мутация, получали с помощью ПЦР с применением праймера. Каждая из вариабельной области легкой цепи и вариабельной области тяжелой цепи фагемиды фага 1B8 scFv была заменена фрагментом ДНК для получения библиотеки 1B8 варианта CDR3 легкой цепи scFv-фага и библиотеки ДНК варианта CDR3 тяжелой цепи scFv-фага, соответственно.
Библиотеку ДНК вариантов scFv-фага очищали с применением фенол-хлороформа и затем трансформировали в штамм E.coli XL-1 Blue с помощью электропорации. Полученное разнообразие идентифицировали с помощью анализа эффективности трансформации и анализа последовательности ДНК, экспрессию фагов индуцировали культивированием в масштабе 500 мл, и способом осаждения с помощью PEG получали библиотеку вариантов CDR3 легкой цепи 1B8 фага scFv.
Биопэннинг проводили с применением каждого варианта из библиотеки фагов scFv таким же образом, как в примере 1. Затем в процессе скрининга измеряли константу скорости диссоциации (kdis) scFv в качестве количественного показателя для оценки способности удерживать связывание. Результат показал, что 7 подвергнутых скринингу оптимизированных клонов сохраняли вариабельную область тяжелой цепи 1B8. Показаны результаты измерения констант скорости диссоциации (таблица 7) и аминокислотные последовательности (Таблицы 8 и 9) 7-ми подвергнутых скринингу оптимизированных клонов.
Результат измерения констант скорости диссоциации семи оптимизированных анти-VISTA-антител показал, что последовательность PMC-309.3.3 была получена путем замены N (Aps) части CDR3 лучшего анти-VISTA.H2 на Y (Tyr). Результат сравнения и анализа последовательности PMC-309.3.3 с базовой последовательностью зародышевой линии человека с применением программного обеспечения IMGT (http://imgt.cines.fr/IMGT_vquest/share/textes/) показал, что вариабельная область тяжелой цепи была получена из IGHV1-69*06. Результат сравнения с аминокислотной последовательностью IGHV1-69*06 группы зародышевой линии показал, что были замещены 4 аминокислотных остатка каркасной области (FR). Для повышения эффективности свертывания при сохранении антигенсвязывающей способности, был получен РМС 309.3.4 с повышенной эффективностью за счет замены части FR. Конкретная последовательность PMC 309.3.4 показана в таблице10.
Таблица 7
Таблица 8
Таблица 9
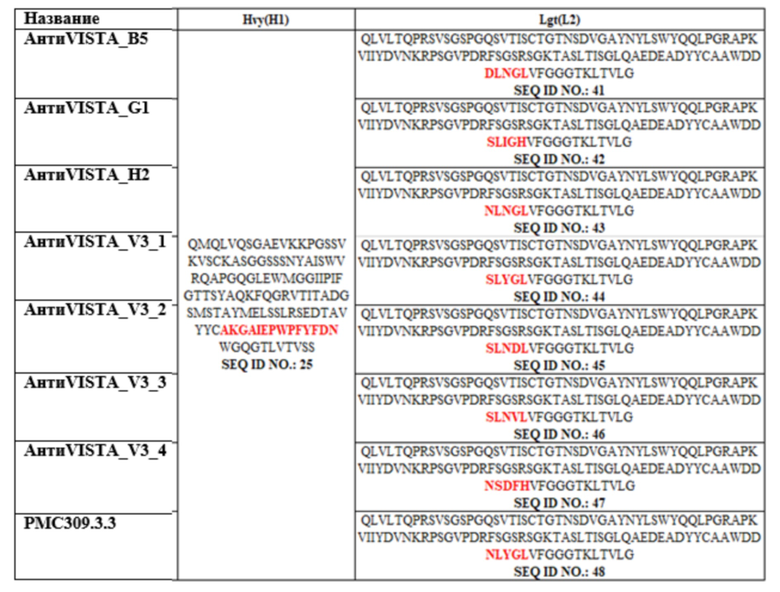
Таблица 10

Пример 11. Анализ физико-химических свойств оптимизированного антитела против VISTA
Каждый оптимизированный клон scFv-фага был преобразован в форму IgG. Конкретные способы клонирования, получения и очистки ДНК для преобразования формы проводили с применением тех же способов, которые были описаны в примерах 4 и 5.
Октет применяли для оценки силы связывания оптимизированного анти-VISTA-антитела, исключая при этом клоны с низкой продуктивностью, эксперимент выполняли так же, как способ, представленный в примере 6 (таблица 11). Как видно из таблицы 11, сила связывания с человеческим VISTA была значительно увеличена за счет оптимизации.
Таблица 11
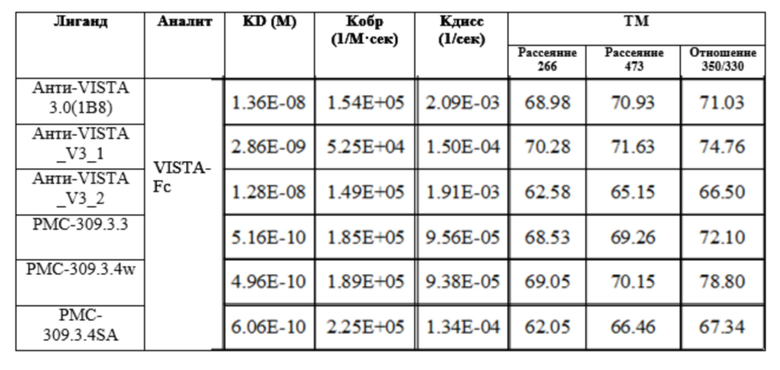
Пример 12. Анализ алло-MLR оптимизированного антитела против VISTA
Для оценки функции оптимизированного антитела, реакцию смешанной культуры лимфоцитов (MLR) проводили таким же образом, как в примере 8, для измерения реактивности иммунных клеток, содержащихся в периферической крови in vitro. Таким образом, было подтверждено, что были индуцированы клеточная пролиферация и продуцирование цитокинов (IFN-γ).
Результаты приведены на фиг. 7 и 8. Как видно из фиг. 7 и 8, препарат PMC-309.3.3 значительно превосходил сравнительную группу, и зависящая от его концентрация пролиферации клеток и секреции цитокинов увеличилась.
Пример 13. Противоопухолевая активность оптимизированных антител против VISTA
Для оценки противоопухолевой активности антитела против VISTA, противораковую эффективность препаратов, которые вводили в хвостовую вену (PMC-309.3.4W, PMC-309.3.4SA), с измененными вариабельными областями легкой цепи, включая человеческие PBMC и JNJ61610588, PMC-309.3.3 и анти-VISTA 3.4, оценивали так же, как в примере 7, с применением мышей NSG, имевших подушечки с трансплантированной клеточной линией рака молочной железы человека, подушки жировой ткани молочной железы MDA-MB-231.
Как видно из результатов, представленных в таблице 12, таблице 13 и на фиг. 9 и 10, PMC-309.3.3 показал наилучшую противораковую активность, что соответствует результату в реакции смешанной культуры лимфоцитов.
Таблица 12
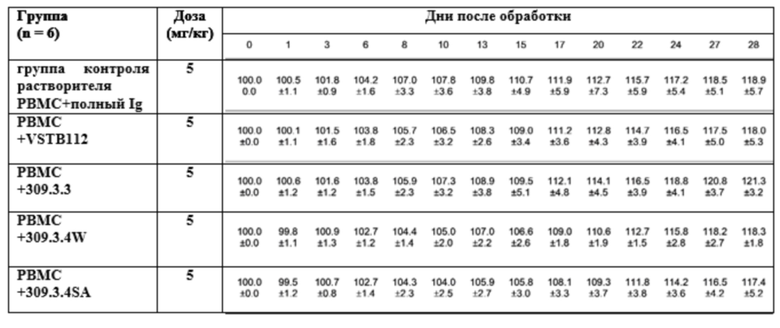
Таблица 13
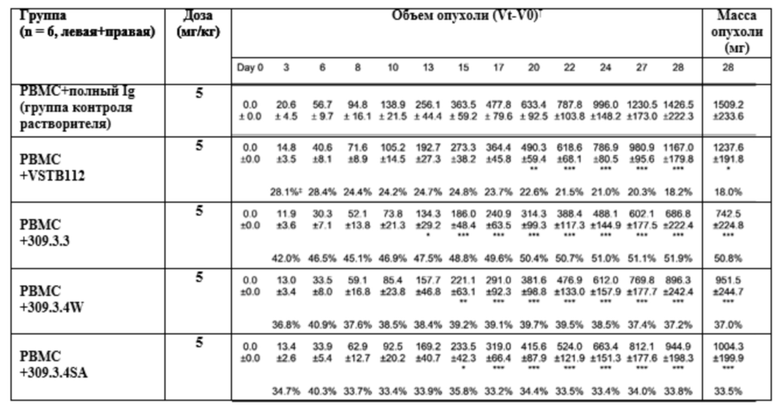
Значащие цифры (t-TEST): * р < 0,05, ** р < 0,01, *** р < 0,001 (против РВМС + полный IgG);
† Δt=Vt-Vo, Vt (измерение объема опухоли), Vo (начальный объем опухоли);
‡ Уровень ингибирования (против РВМС + полный IgG).
Хотя конкретные воплощения настоящего изобретения были описаны подробно, специалистам в данной области техники должно быть понятно, что это настоящее описание обеспечено для изложения предпочтительных воплощений в иллюстративных целях и не должно рассматриваться как ограничивающее объем настоящего изобретения. Следовательно, существенный объем настоящего изобретения определяется прилагаемой формулой изобретения и ее эквивалентами.
--->
Перечень последовательностей
<110> ФАРМАБЦИН ИНК.
<120> АНТИТЕЛА ПРОТИВ VISTA И ИХ ПРИМЕНЕНИЕ
<130> PP-B2107
<150> KR 17/136632
<151> 2017-10-20
<160> 50
<170> KopatentIn 2.0
<210> 1
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> Heavy-chain CDR1 of 1B8
<400> 1
Gly Gly Ser Ser Ser Asn Tyr Ala
1 5
<210> 2
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> Heavy-chain CDR2 of 1B8
<400> 2
Ile Ile Pro Ile Phe Gly Thr Thr
1 5
<210> 3
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Heavy-chain CDR3 of 1B8
<400> 3
Ala Lys Gly Ala Ile Glu Pro Trp Pro Phe Tyr Phe Asp Asn
1 5 10
<210> 4
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Light-chain CDR1 of 1B8
<400> 4
Asn Ser Asp Val Gly Ala Tyr Asn Tyr
1 5
<210> 5
<211> 3
<212> PRT
<213> Artificial Sequence
<220>
<223> Light-chain CDR2 of 1B8
<400> 5
Asp Val Asn
1
<210> 6
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Light-chain CDR3 of 1B8
<400> 6
Ala Ala Trp Asp Asp Ser Leu Asn Gly Leu Val
1 5 10
<210> 7
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> Heavy-chain CDR1 of 2C12
<400> 7
Gly Tyr Ile Phe Thr Asp Tyr Tyr
1 5
<210> 8
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> Heavy-chain CDR2 of 2C12
<400> 8
Ile Asn Pro Tyr Asp Gly Arg Thr
1 5
<210> 9
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> Heavy-chain CDR3 of 2C12
<400> 9
Ala Lys Gln Met Gly Ile Trp Asp Tyr Asp Ala Phe Asp Ile
1 5 10
<210> 10
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Light-chain CDR1 of 2C12
<400> 10
Ser Ser Asn Ile Gly Ala Gly Tyr Asp
1 5
<210> 11
<211> 3
<212> PRT
<213> Artificial Sequence
<220>
<223> Light-chain CDR2 of 2C12
<400> 11
Gly Asn Ser
1
<210> 12
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Light-chain CDR3 of 2C12
<400> 12
Val Ala Trp Asp Asp Ser Leu Lys Ala Tyr Val
1 5 10
<210> 13
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> Heavy-chain CDR1 of 1A12
<400> 13
Gly Phe Ser Phe His Asp Tyr Thr
1 5
<210> 14
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> Heavy-chain CDR2 of 1A12
<400> 14
Ile Ser Trp Asp Gly Thr Ile Thr
1 5
<210> 15
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Heavy-chain CDR3 of 1A12
<400> 15
Ala Lys Glu Asp Arg Tyr Asp Tyr Tyr Ser Gly Ala Phe Asp Ile
1 5 10 15
<210> 16
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Light-chain CDR1 of 1A12
<400> 16
Ser Ser Asp Val Gly Gly Tyr Asp Tyr
1 5
<210> 17
<211> 3
<212> PRT
<213> Artificial Sequence
<220>
<223> Light-chain CDR2 of 1A12
<400> 17
Asp Val Asn
1
<210> 18
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Light-chain CDR3 of 1A12
<400> 18
Ser Ser Phe Ala Gly Ser Asn Thr Leu Arg Val
1 5 10
<210> 19
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> Heavy-chain CDR1 of 3C5
<400> 19
Gly Tyr Thr Phe Ser Ser Tyr Trp
1 5
<210> 20
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> Heavy-chain CDR2 of 3C5
<400> 20
Ile Asn Pro Gly Asn Gly His Thr
1 5
<210> 21
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> Heavy-chain CDR3 of 3C5
<400> 21
Ala Lys Asp Ile Ala Tyr Tyr Asp Phe Trp Ser Gly Asp Ala Phe Asp
1 5 10 15
Leu
<210> 22
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<223> Light-chain CDR1 of 3C5
<400> 22
Lys Leu Gly Asn Lys Tyr
1 5
<210> 23
<211> 3
<212> PRT
<213> Artificial Sequence
<220>
<223> Light-chain CDR2 of 3C5
<400> 23
Gln Asp Asn
1
<210> 24
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> Light-chain CDR3 of 3C5
<400> 24
Gln Thr Trp Asp Arg Ser Thr Gly Val
1 5
<210> 25
<211> 121
<212> PRT
<213> Artificial Sequence
<220>
<223> VH of 1B8
<400> 25
Gln Met Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Ser Ser Ser Asn Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Gly Ser Met Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Gly Ala Ile Glu Pro Trp Pro Phe Tyr Phe Asp Asn Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 26
<211> 112
<212> PRT
<213> Artificial Sequence
<220>
<223> VL of 1B8
<400> 26
Gln Leu Val Leu Thr Gln Pro Arg Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Val Thr Ile Ser Cys Thr Gly Thr Asn Ser Asp Val Gly Ala Tyr
20 25 30
Asn Tyr Leu Ser Trp Tyr Gln Gln Leu Pro Gly Arg Ala Pro Lys Val
35 40 45
Ile Ile Tyr Asp Val Asn Lys Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Arg Ser Gly Lys Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser
85 90 95
Leu Asn Gly Leu Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
<210> 27
<211> 121
<212> PRT
<213> Artificial Sequence
<220>
<223> VH of 2C12
<400> 27
Gln Val Gln Leu Val Glu Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Val Ile Asn Pro Tyr Asp Gly Arg Thr Ser Phe Ala Gln Lys Phe
50 55 60
Gln Gly Arg Leu Thr Val Thr Arg Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Asp Leu Ser Gly Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Gln Met Gly Ile Trp Asp Tyr Asp Ala Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 28
<211> 112
<212> PRT
<213> Artificial Sequence
<220>
<223> VL of 2C12
<400> 28
Gln Phe Val Leu Thr Gln Pro Ser Ser Val Ser Gly Ala Pro Gly Gln
1 5 10 15
Arg Val Ile Ile Ser Cys Thr Gly Ser Ser Ser Asn Ile Gly Ala Gly
20 25 30
Tyr Asp Val His Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Val
35 40 45
Leu Ile Tyr Gly Asn Ser Asp Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Ala Ser Lys Ser Ala Thr Ser Ala Ser Leu Ala Ile Thr Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Val Ala Trp Asp Asp Ser
85 90 95
Leu Lys Ala Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu Gly
100 105 110
<210> 29
<211> 122
<212> PRT
<213> Artificial Sequence
<220>
<223> VH of 1A12
<400> 29
Gln Met Gln Leu Val Glu Ser Gly Gly Gly Leu Val Glu Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Thr Thr Ser Gly Phe Ser Phe His Asp Tyr
20 25 30
Thr Met Tyr Trp Val Arg Gln Val Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Leu Ile Ser Trp Asp Gly Thr Ile Thr Phe Tyr Ala Asp Pro Val
50 55 60
Arg Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Glu Asp Arg Tyr Asp Tyr Tyr Ser Gly Ala Phe Asp Ile Trp
100 105 110
Gly Gln Gly Thr Val Val Thr Val Ser Ser
115 120
<210> 30
<211> 112
<212> PRT
<213> Artificial Sequence
<220>
<223> VL of 1A12
<400> 30
Gln Ser Ala Leu Thr Gln Pro Arg Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Val Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asp Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Ile Leu Asn Asp Val Asn Lys Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Pro Asp Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Phe Ala Gly Ser
85 90 95
Asn Thr Leu Arg Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
<210> 31
<211> 124
<212> PRT
<213> Artificial Sequence
<220>
<223> VH of 3C5
<400> 31
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Glu Ile Asn Pro Gly Asn Gly His Thr Asn Tyr Asn Glu Lys Phe
50 55 60
Lys Ser Arg Val Thr Ile Thr Val Asp Lys Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Ile Ala Tyr Tyr Asp Phe Trp Ser Gly Asp Ala Phe Asp
100 105 110
Leu Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 32
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> VL of 3C5
<400> 32
Ser Tyr Glu Leu Thr Gln Pro Leu Ser Val Ser Val Ser Pro Gly Gln
1 5 10 15
Thr Ala Ser Ile Thr Cys Ser Gly Asp Lys Leu Gly Asn Lys Tyr Ala
20 25 30
Ser Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Val Leu Val Ile Tyr
35 40 45
Gln Asp Asn Lys Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Gly Thr Gln Ala Thr
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Thr Trp Asp Arg Ser Thr Gly Val
85 90 95
Phe Gly Thr Gly Thr Lys Val Thr Val Leu Gly
100 105
<210> 33
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic Sequence
<400> 33
Ala Ala Trp Asp Asp Asp Leu Asn Gly Leu Val
1 5 10
<210> 34
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic Sequence
<400> 34
Ala Ala Trp Asp Asp Ser Leu Ile Gly His Val
1 5 10
<210> 35
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic Sequence
<400> 35
Ala Ala Trp Asp Asp Asn Leu Asn Gly Leu Val
1 5 10
<210> 36
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic Sequence
<400> 36
Ala Ala Trp Asp Asp Ser Leu Tyr Gly Leu Val
1 5 10
<210> 37
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic Sequence
<400> 37
Ala Ala Trp Asp Asp Ser Leu Asn Asp Leu Val
1 5 10
<210> 38
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic Sequence
<400> 38
Ala Ala Trp Asp Asp Ser Leu Asn Val Leu Val
1 5 10
<210> 39
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic Sequence
<400> 39
Ala Ala Trp Asp Asp Asn Ser Asp Phe His Val
1 5 10
<210> 40
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic Sequence
<400> 40
Ala Ala Trp Asp Asp Asn Leu Tyr Gly Leu Val
1 5 10
<210> 41
<211> 112
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic Sequence
<400> 41
Gln Leu Val Leu Thr Gln Pro Arg Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Val Thr Ile Ser Cys Thr Gly Thr Asn Ser Asp Val Gly Ala Tyr
20 25 30
Asn Tyr Leu Ser Trp Tyr Gln Gln Leu Pro Gly Arg Ala Pro Lys Val
35 40 45
Ile Ile Tyr Asp Val Asn Lys Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Arg Ser Gly Lys Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Asp
85 90 95
Leu Asn Gly Leu Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
<210> 42
<211> 112
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic Sequence
<400> 42
Gln Leu Val Leu Thr Gln Pro Arg Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Val Thr Ile Ser Cys Thr Gly Thr Asn Ser Asp Val Gly Ala Tyr
20 25 30
Asn Tyr Leu Ser Trp Tyr Gln Gln Leu Pro Gly Arg Ala Pro Lys Val
35 40 45
Ile Ile Tyr Asp Val Asn Lys Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Arg Ser Gly Lys Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser
85 90 95
Leu Ile Gly His Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
<210> 43
<211> 112
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic Sequence
<400> 43
Gln Leu Val Leu Thr Gln Pro Arg Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Val Thr Ile Ser Cys Thr Gly Thr Asn Ser Asp Val Gly Ala Tyr
20 25 30
Asn Tyr Leu Ser Trp Tyr Gln Gln Leu Pro Gly Arg Ala Pro Lys Val
35 40 45
Ile Ile Tyr Asp Val Asn Lys Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Arg Ser Gly Lys Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Asn
85 90 95
Leu Asn Gly Leu Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
<210> 44
<211> 112
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic Sequence
<400> 44
Gln Leu Val Leu Thr Gln Pro Arg Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Val Thr Ile Ser Cys Thr Gly Thr Asn Ser Asp Val Gly Ala Tyr
20 25 30
Asn Tyr Leu Ser Trp Tyr Gln Gln Leu Pro Gly Arg Ala Pro Lys Val
35 40 45
Ile Ile Tyr Asp Val Asn Lys Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Arg Ser Gly Lys Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser
85 90 95
Leu Tyr Gly Leu Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
<210> 45
<211> 112
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic Sequence
<400> 45
Gln Leu Val Leu Thr Gln Pro Arg Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Val Thr Ile Ser Cys Thr Gly Thr Asn Ser Asp Val Gly Ala Tyr
20 25 30
Asn Tyr Leu Ser Trp Tyr Gln Gln Leu Pro Gly Arg Ala Pro Lys Val
35 40 45
Ile Ile Tyr Asp Val Asn Lys Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Arg Ser Gly Lys Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser
85 90 95
Leu Asn Asp Leu Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
<210> 46
<211> 112
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic Sequence
<400> 46
Gln Leu Val Leu Thr Gln Pro Arg Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Val Thr Ile Ser Cys Thr Gly Thr Asn Ser Asp Val Gly Ala Tyr
20 25 30
Asn Tyr Leu Ser Trp Tyr Gln Gln Leu Pro Gly Arg Ala Pro Lys Val
35 40 45
Ile Ile Tyr Asp Val Asn Lys Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Arg Ser Gly Lys Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser
85 90 95
Leu Asn Val Leu Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
<210> 47
<211> 112
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic Sequence
<400> 47
Gln Leu Val Leu Thr Gln Pro Arg Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Val Thr Ile Ser Cys Thr Gly Thr Asn Ser Asp Val Gly Ala Tyr
20 25 30
Asn Tyr Leu Ser Trp Tyr Gln Gln Leu Pro Gly Arg Ala Pro Lys Val
35 40 45
Ile Ile Tyr Asp Val Asn Lys Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Arg Ser Gly Lys Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Asn
85 90 95
Ser Asp Phe His Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
<210> 48
<211> 112
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic Sequence
<400> 48
Gln Leu Val Leu Thr Gln Pro Arg Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Val Thr Ile Ser Cys Thr Gly Thr Asn Ser Asp Val Gly Ala Tyr
20 25 30
Asn Tyr Leu Ser Trp Tyr Gln Gln Leu Pro Gly Arg Ala Pro Lys Val
35 40 45
Ile Ile Tyr Asp Val Asn Lys Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Arg Ser Gly Lys Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Asn
85 90 95
Leu Tyr Gly Leu Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
<210> 49
<211> 121
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic Sequence
<400> 49
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Ser Ser Ser Asn Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Gly Ala Ile Glu Pro Trp Pro Phe Tyr Phe Asp Asn Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 50
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic Sequence
<400> 50
Gln Ser Ala Leu Thr Gln Pro Arg Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Val Thr Ile Ser Cys Thr Gly Thr Asn Ser Asp Val Gly Ala Tyr
20 25 30
Asn Tyr Leu Ser Trp Tyr Gln Gln Leu Pro Gly Arg Ala Pro Lys Val
35 40 45
Ile Ile Tyr Asp Val Asn Lys Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Arg Ser Gly Lys Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Asn
85 90 95
Leu Tyr Gly Leu Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105 110
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА ПРОТИВ БЕЛКА-1 ЗАПРОГРАММИРОВАННОЙ КЛЕТОЧНОЙ СМЕРТИ (PD-1) И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2725950C1 |
| АНТИ-CEACAM1 АНТИТЕЛО И ЕГО ПРИМЕНЕНИЕ | 2018 |
|
RU2754876C2 |
| Биспецифическое антитело анти-HER2/анти-4-1BB и его применение | 2020 |
|
RU2831838C2 |
| БИСПЕЦИФИЧЕСКОЕ АНТИТЕЛО АНТИ-EGFR/АНТИ-4-1ВВ И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2831836C2 |
| Антитела против лиганда-1 запрограммированной смерти (PD-L1) и их применение | 2017 |
|
RU2721582C1 |
| НОВОЕ АНТИ-С-МЕТ АНТИТЕЛО И ЕГО ПРИМЕНЕНИЕ | 2018 |
|
RU2751720C2 |
| АНТИТЕЛО ПРОТИВ ANG2 И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2788088C1 |
| АНТИТЕЛО ПРОТИВ TIE-2 И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2795455C2 |
| C3-СВЯЗЫВАЮЩИЕ АГЕНТЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2802307C2 |
| АНТИ-PRE-S1 HBV АНТИТЕЛА | 2016 |
|
RU2739955C2 |
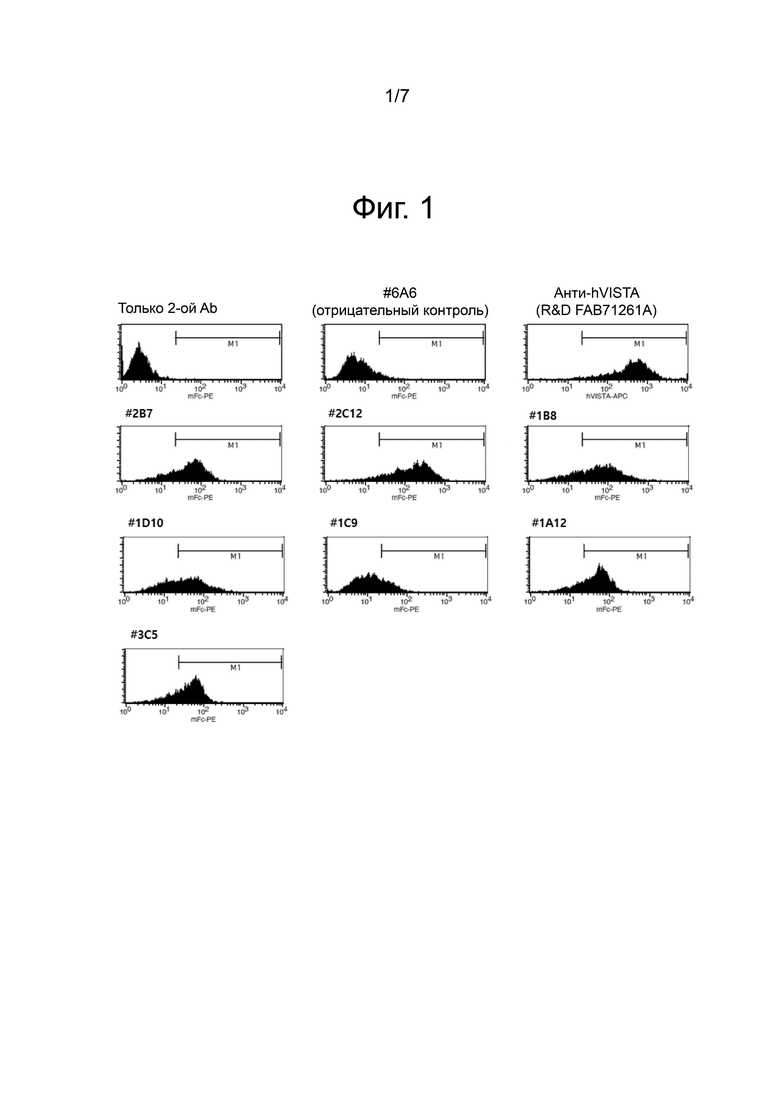
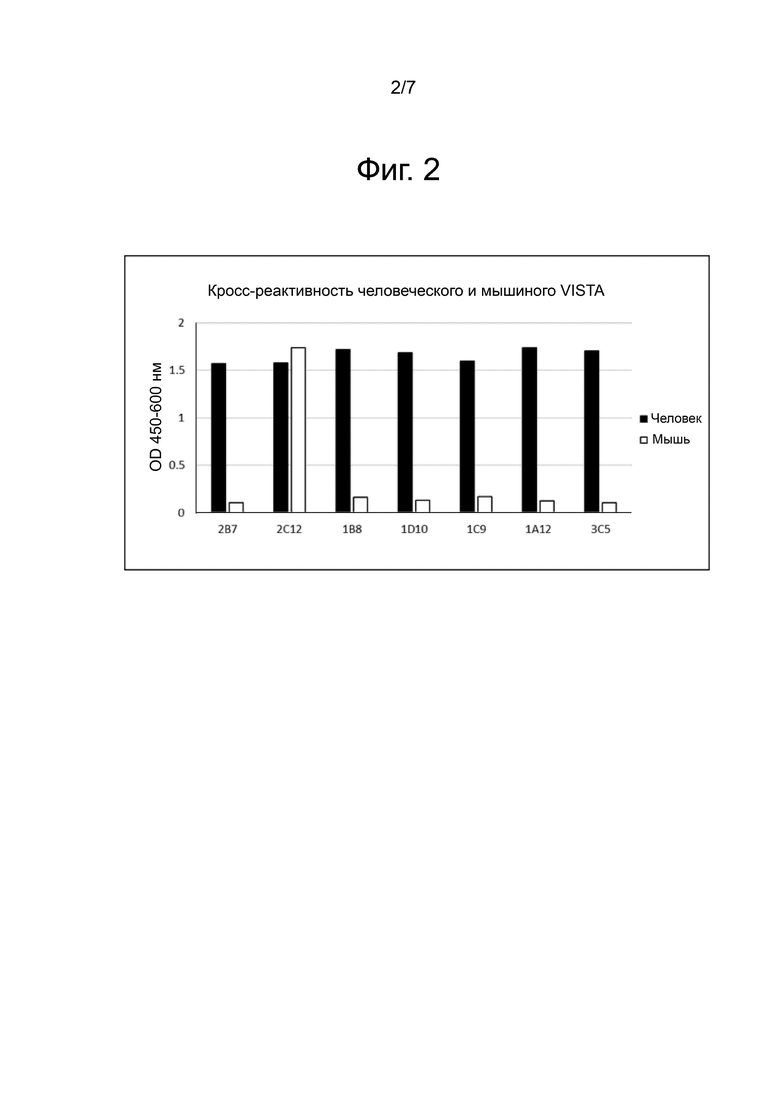
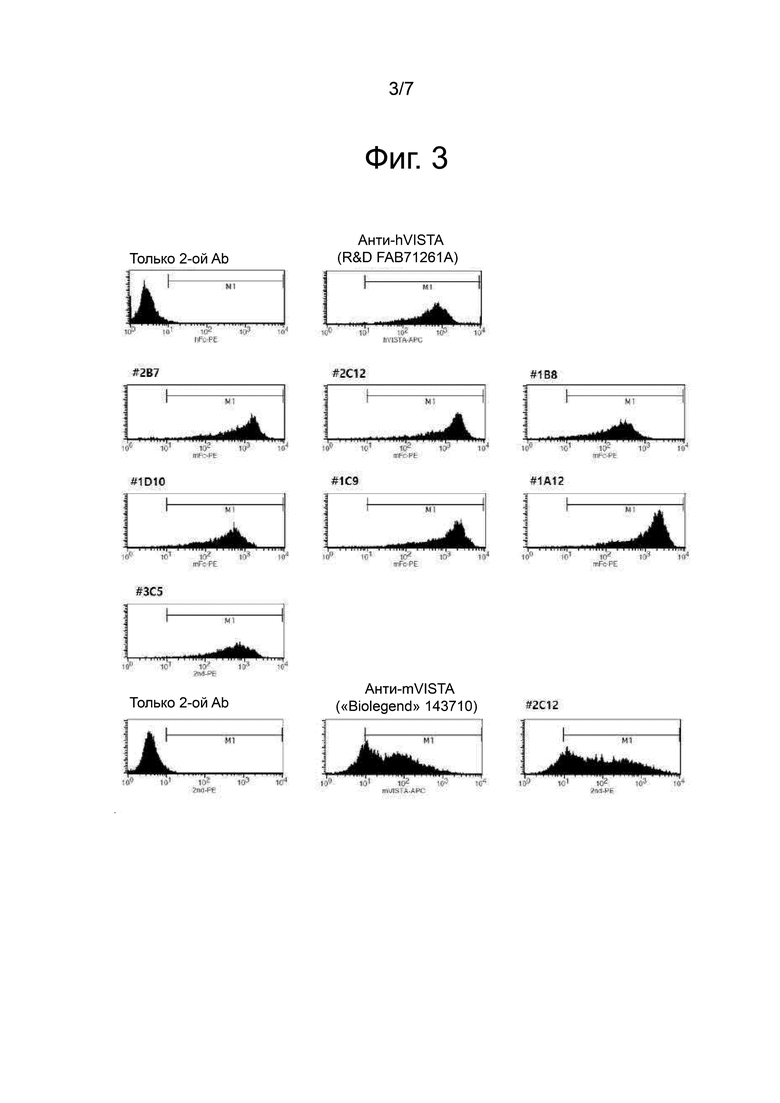
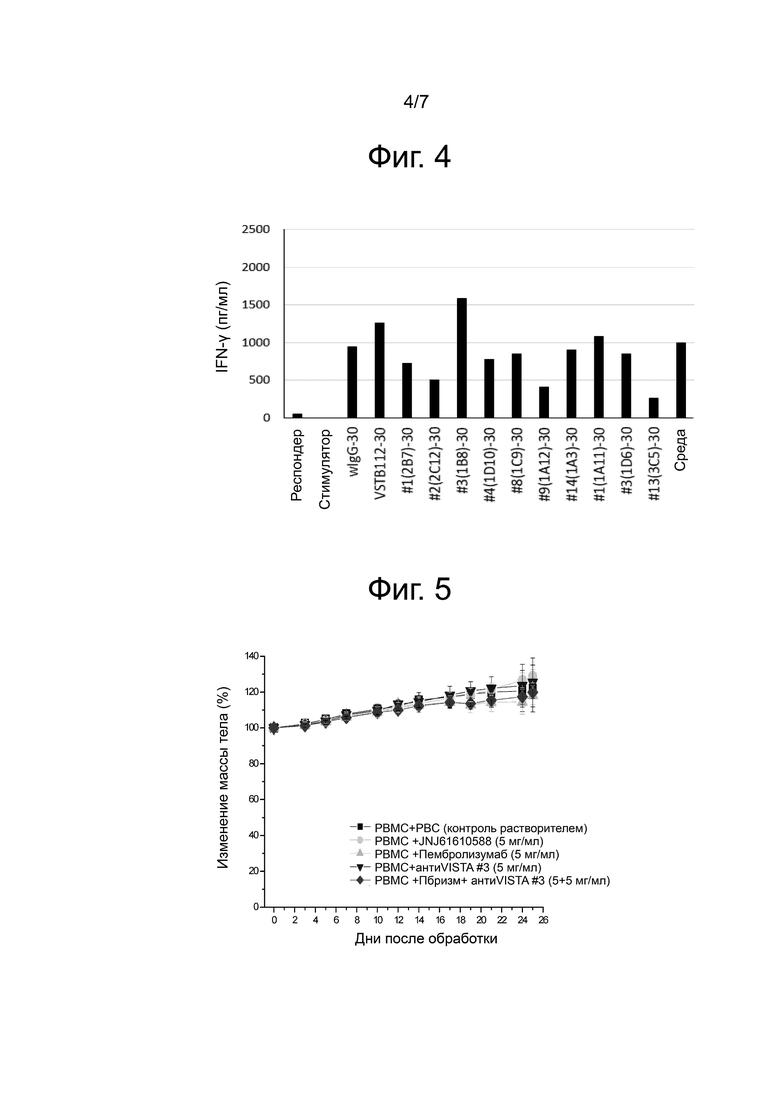
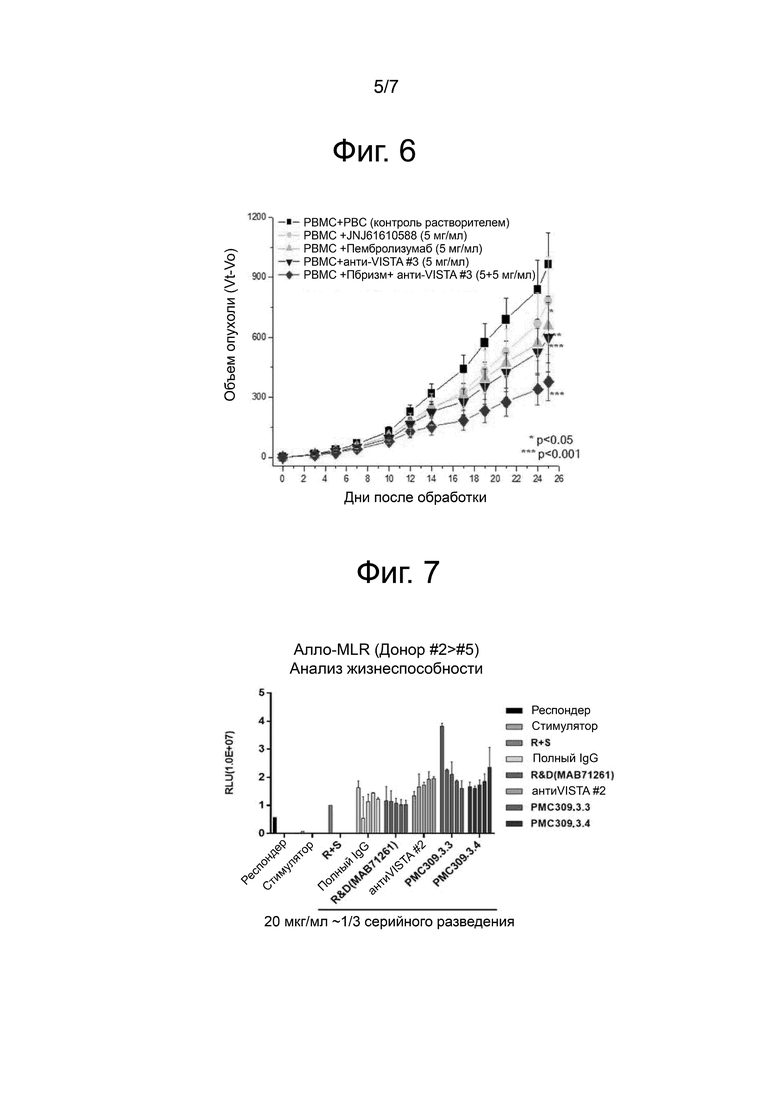
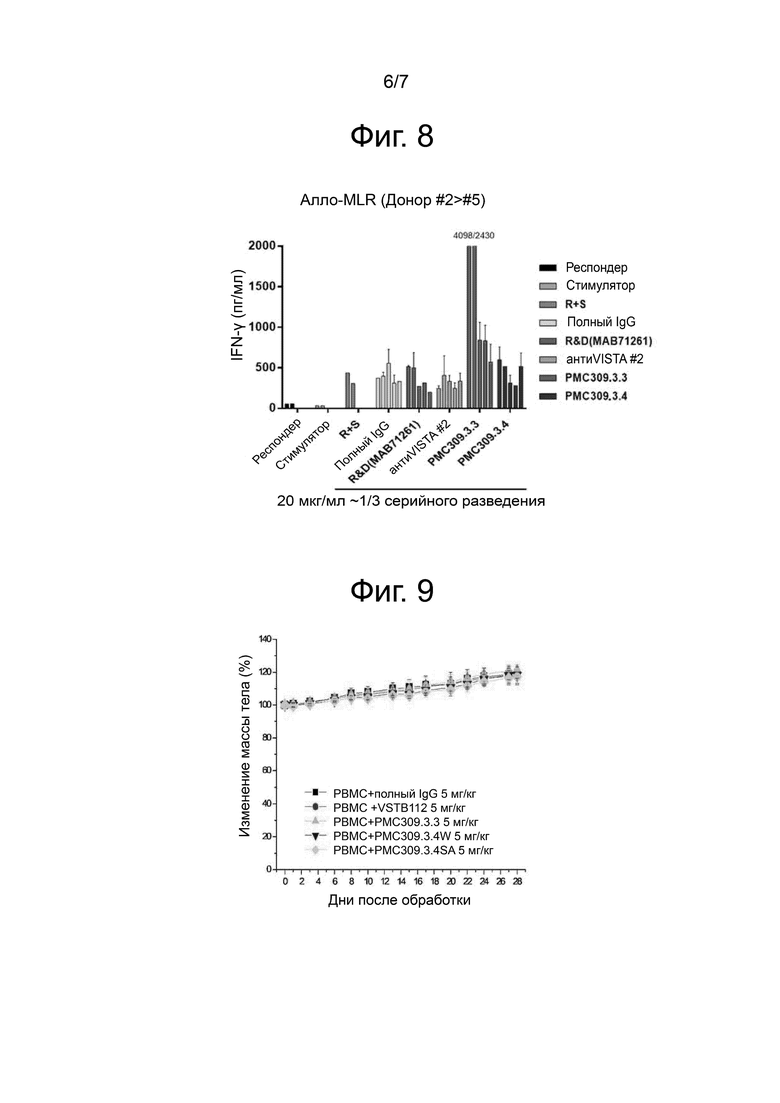
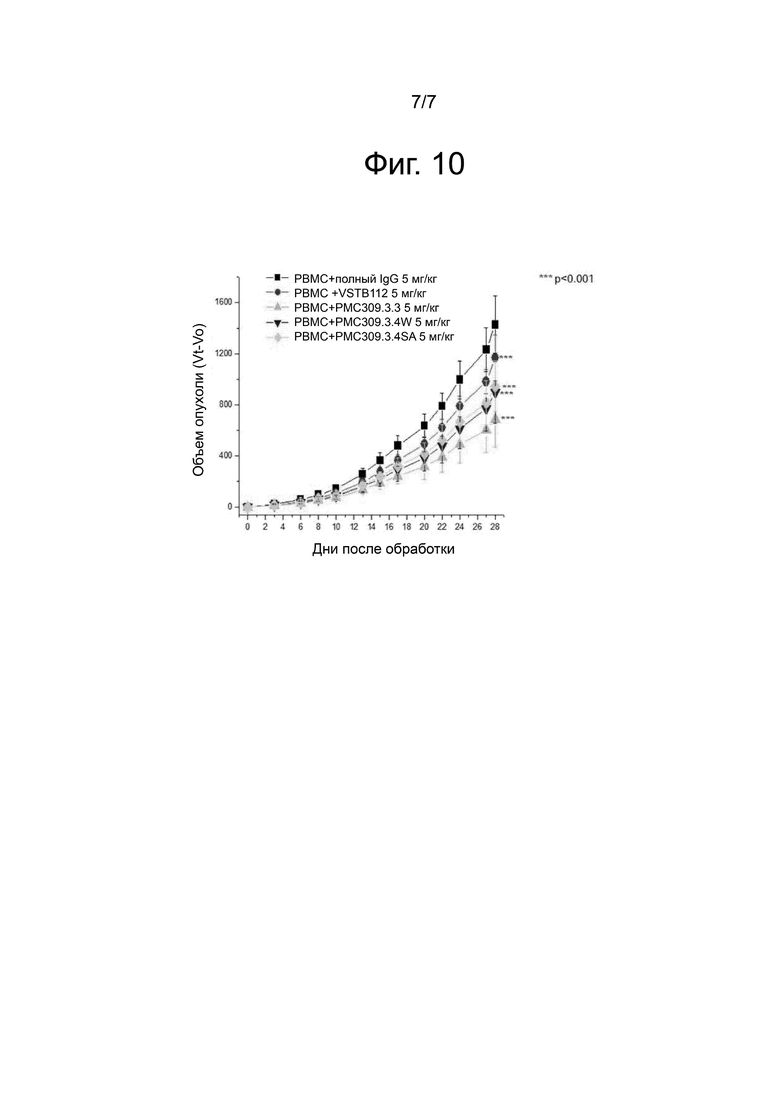
Настоящее изобретение относится к области иммунологии. Заявлено антитело против VISTA или его антигенсвязывающий фрагмент, нуклеиновая кислота, экспрессионный вектор, клетка. Кроме того, предложен способ получения антитела или его антигенсвязывающего фрагмента, композиция для профилактики или лечения и композиции для одновременного введения в комбинации с антителом к PD-1 или антителом к PD-L1. Настоящее изобретение может найти дальнейшее применение в терапии опухолей или аутоиммунных заболеваний, экспрессирующих V-доменный Ig-супрессор активации Т-клеток (VISTA). 7 н. и 2 з.п. ф-лы, 13 табл., 13 пр., 10 ил.
1. Антитело или его антигенсвязывающий фрагмент, связывающееся с V-доменным Ig-супрессором активации Т-клеток (VISTA), включающие:
вариабельную область тяжелой цепи, включающую CDR1 тяжелой цепи согласно SEQ ID NO: 1, CDR2 тяжелой цепи согласно SEQ ID NO: 2, CDR3 тяжелой цепи согласно SEQ ID NO: 3, вариабельную область легкой цепи, содержащую CDR1 легкой цепи согласно SEQ ID NO: 4, CDR2 легкой цепи согласно SEQ ID NO: 5, CDR3 легкой цепи согласно SEQ ID NO: 6,
вариабельную область тяжелой цепи, содержащую CDR1 тяжелой цепи согласно SEQ ID NO: 7, CDR2 тяжелой цепи согласно SEQ ID NO: 8, CDR3 тяжелой цепи согласно SEQ ID NO: 9, вариабельную область легкой цепи, содержащую CDR1 легкой цепи согласно SEQ ID NO: 10, CDR2 легкой цепи согласно SEQ ID NO: 11, CDR3 легкой цепи согласно SEQ ID NO: 12,
вариабельную область тяжелой цепи, содержащую CDR1 тяжелой цепи согласно SEQ ID NO: 13, CDR2 тяжелой цепи согласно SEQ ID NO: 14, CDR3 тяжелой цепи согласно SEQ ID NO: 15, вариабельную область легкой цепи, содержащую CDR1 легкой цепи согласно SEQ ID NO: 16, CDR2 легкой цепи согласно SEQ ID NO: 17, CDR3 легкой цепи согласно SEQ ID NO: 18,
вариабельную область тяжелой цепи, содержащую CDR1 тяжелой цепи согласно SEQ ID NO: 19, CDR2 тяжелой цепи согласно SEQ ID NO: 20, CDR3 тяжелой цепи согласно SEQ ID NO: 21, вариабельную область легкой цепи, содержащую CDR1 легкой цепи согласно SEQ ID NO: 22, CDR2 легкой цепи согласно SEQ ID NO: 23, CDR3 легкой цепи согласно SEQ ID NO: 24,
вариабельную область тяжелой цепи, содержащую CDR1 тяжелой цепи согласно SEQ ID NO: 1, CDR2 тяжелой цепи согласно SEQ ID NO: 2, CDR3 тяжелой цепи согласно SEQ ID NO: 3, вариабельную область легкой цепи, содержащую CDR1 легкой цепи согласно SEQ ID NO: 4, CDR2 легкой цепи согласно SEQ ID NO: 5, CDR3 легкой цепи согласно SEQ ID NO: 33,
вариабельную область тяжелой цепи, содержащую CDR1 тяжелой цепи согласно SEQ ID NO: 1, CDR2 тяжелой цепи согласно SEQ ID NO: 2, CDR3 тяжелой цепи согласно SEQ ID NO: 3, вариабельную область легкой цепи, содержащую CDR1 легкой цепи согласно SEQ ID NO: 4, CDR2 легкой цепи согласно SEQ ID NO: 5, CDR3 легкой цепи согласно SEQ ID NO: 34,
вариабельную область тяжелой цепи, содержащую CDR1 тяжелой цепи согласно SEQ ID NO: 1, CDR2 тяжелой цепи согласно SEQ ID NO: 2, CDR3 тяжелой цепи согласно SEQ ID NO: 3, вариабельную область легкой цепи, содержащую CDR1 легкой цепи согласно SEQ ID NO: 4, CDR2 легкой цепи согласно SEQ ID NO: 5, CDR3 легкой цепи согласно SEQ ID NO: 35,
вариабельную область тяжелой цепи, содержащую CDR1 тяжелой цепи согласно SEQ ID NO: 1, CDR2 тяжелой цепи согласно SEQ ID NO: 2, CDR3 тяжелой цепи согласно SEQ ID NO: 3, вариабельную область легкой цепи, содержащую CDR1 легкой цепи согласно SEQ ID NO: 4, CDR2 легкой цепи согласно SEQ ID NO: 5, CDR3 легкой цепи согласно SEQ ID NO: 36,
вариабельную область тяжелой цепи, содержащую CDR1 тяжелой цепи согласно SEQ ID NO: 1, CDR2 тяжелой цепи согласно SEQ ID NO: 2, CDR3 тяжелой цепи согласно SEQ ID NO: 3, вариабельную область легкой цепи, содержащую CDR1 легкой цепи согласно SEQ ID NO: 4, CDR2 легкой цепи согласно SEQ ID NO: 5, CDR3 легкой цепи согласно SEQ ID NO: 37,
вариабельную область тяжелой цепи, содержащую CDR1 тяжелой цепи согласно SEQ ID NO: 1, CDR2 тяжелой цепи согласно SEQ ID NO: 2, CDR3 тяжелой цепи согласно SEQ ID NO: 3, вариабельную область легкой цепи, содержащую CDR1 легкой цепи согласно SEQ ID NO: 4, CDR2 легкой цепи согласно SEQ ID NO: 5, CDR3 легкой цепи согласно SEQ ID NO: 38,
вариабельную область тяжелой цепи, содержащую CDR1 тяжелой цепи согласно SEQ ID NO: 1, CDR2 тяжелой цепи согласно SEQ ID NO: 2, CDR3 тяжелой цепи согласно SEQ ID NO: 3, вариабельную область легкой цепи, содержащую CDR1 легкой цепи согласно SEQ ID NO: 4, CDR2 легкой цепи согласно SEQ ID NO: 5, CDR3 легкой цепи согласно SEQ ID NO: 39, или
вариабельную область тяжелой цепи, содержащую CDR1 тяжелой цепи согласно SEQ ID NO: 1, CDR2 тяжелой цепи согласно SEQ ID NO: 2, CDR3 тяжелой цепи согласно SEQ ID NO: 3, вариабельную область легкой цепи, содержащую CDR1 легкой цепи согласно SEQ ID NO: 4, CDR2 легкой цепи согласно SEQ ID NO: 5, CDR3 легкой цепи согласно SEQ ID NO: 40.
2. Антитело или его антигенсвязывающий фрагмент по п. 1, где антитело или его антигенсвязывающий фрагмент включают вариабельную область тяжелой цепи, выбранную из группы, состоящей из последовательностей SEQ ID NO: 25, 27, 29, 31 и 49.
3. Антитело или его антигенсвязывающий фрагмент по п. 1, где антитело или его антигенсвязывающий фрагмент включают вариабельную область легкой цепи, выбранную из группы, состоящей из последовательностей SEQ ID NO: 26, 28, 30, 32, 41-48 и 50.
4. Нуклеиновая кислота, кодирующая антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3.
5. Экспрессионный вектор, включающий нуклеиновую кислоту по п. 4.
6. Клетка для продуцирования антитела или его антигенсвязывающего фрагмента по любому из пп. 1-3, трансформированная экспрессионным вектором по п. 5.
7. Способ получения антитела, связывающегося с VISTA, или его антигенсвязывающего фрагмента, включающий:
(a) культивирование клетки по п. 6; а также
(b) выделение антитела или его антигенсвязывающего фрагмента из культивируемой клетки.
8. Композиция для профилактики или лечения опухоли или аутоиммунного заболевания, экспрессирующих V-доменный Ig-супрессор активации Т-клеток (VISTA), включающая фармацевтически эффективное количество антитела или его антигенсвязывающего фрагмента по любому из пп. 1-3 в качестве активного ингредиента.
9. Композиция для введения в комбинации с антителом к PD-1 или антителом к PD-L1, включающая антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3 и фармацевтически приемлемый носитель.
| Токарный резец | 1924 |
|
SU2016A1 |
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
Авторы
Даты
2021-07-01—Публикация
2018-10-22—Подача