Изобретение относится к аналитической химии, а именно к определению концентрации привитых аминогрупп на поверхности минеральных наполнителей, что может быть использовано при производстве композиционных материалов, модифицированных минеральных наполнителей и различных сорбентов на их основе.
При производстве композиционных материалов модификацию минеральных наполнителей проводят с целью увеличения смачиваемости, адгезии, а также создания химической связи между полимером и наполнителем. При этом количество функциональных групп, привитых после модификации, будет влиять на свойства получаемого материала.
Известен способ определения концентрации привитых аминогрупп на поверхности модифицированного силикагеля путем обратного кислотно-основного титрования [Химия привитых поверхностных соединений/ под ред. Г.В. Лисичкина.- М.: ФИЗМАТЛИТ, 2003. - С. 282]. При этом происходит контакт модифицированного силикагеля с соляной кислотой, в результате чего привитые аминогруппы реагируют с последней с образованием соответствующего катиона аммония. Затем избыток соляной кислоты оттитровывают щелочью. Данный способ прост в исполнении, не требует применения дорогостоящих реактивов, однако не может быть использован для определения концентрации привитых аминогрупп на поверхности многих минеральных наполнителей, таких как базальт, слюда, тальк и т.д. Причиной этого является наличие в них основных оксидов, которые тоже реагируют с соляной кислотой. При этом расход соляной кислоты на основные оксиды в холостом опыте может быть гораздо больше, чем при титровании модифицированного наполнителя. Поэтому определить концентрацию привитых аминогрупп на поверхности многих минеральных наполнителей данным методом невозможно.
Известен способ определения концентрации привитых аминогрупп на поверхности минеральных наполнителей, заключающийся в количественном определении углерода, водорода и азота посредством анализа продуктов сжигания образца. Концентрация аминогрупп рассчитывается по данным элементного анализа [Liu, Y.-H., Lin, Н.-Р., &Mou, C.-Y. (2004). Direct method for surface silyl functionalization of mesoporous silica./ Langmuir: the ACS journal of surfaces and colloids, 20(8), p.3231-3239].
Известен также способ определения концентрации привитых аминогрупп на поверхности минеральных наполнителей рентгеновской фотоэлектронной спектрометрией [Okusa, Н., Kurihara, К., &Kunitake, Т. (1994). Chemical modification of molecularly smooth mica surface and protein attachment. Langmuir, 10(10), p.3577-3581].
Однако указанные способы требуют применения дорогостоящего сложного оборудования, поэтому не могут быть реализованы на многих предприятиях, производящих модифицированные наполнители и композиционные материалы.
Известен способ определения аминогрупп методом ацилирования, применяемый для определения аминогрупп в жидких или твердых растворимых образцах, например, по методу Магнусона и Черри [Сиггиа С., Ханна Дж.Г. Количественный органический анализ по функциональным группам: пер. с англ.- М.: Химия, 1983. - С. 25]. Ацилирование проводят 1 М раствором уксусного ангидрида в дихлорэтане, содержащем 0,15 моль/л хлорной кислоты в качестве катализатора. К навеске жидкой пробы, содержащей 4-5 ммоль аминогрупп прибавляют 10 мл ацилирующего раствора, выдерживают 5 минут и приливают 35-40 мл гидролизующей смеси (диметилформамид: пиридин: вода в соотношении 6:3:1). Выдерживают 5-10 минут, затем прибавляют несколько капель индикатора и титруют спиртовым раствором гидроксида калия. Содержание аминогрупп рассчитывают по разности результатов холостого титрования и титрования пробы. Преимущества данного метода заключаются в легкости приготовления ацилирующего раствора, поскольку его не надо охлаждать при приготовлении. Раствор ангидрида в дихлорэтане практически бесцветен и хранится не менее 2 месяцев. Кроме того, отмечается наибольшая скорость реакции ацилирования в данном растворителе. Однако данный способ не применим для анализа модифицированных минеральных наполнителей. Концентрация функциональных групп на их поверхности составляет обычно 0,4-1,5 ммоль/г, т.е. для анализа в среднем необходима навеска вещества массой 5 г. При этом 10 мл ацилирующего раствора недостаточно для хорошего смачивания образца, а, следовательно, и количественного протекания реакции. При разбавлении ацилирующего раствора дихлорэтаном для лучшего смачивания пробы реакция ацилирования аминогрупп протекает не полностью, давая заниженные результаты, а при увеличении количества ацилирующего раствора той же концентрации относительно навески образца сильно возрастает погрешность эксперимента, в том числе из-за увеличения количества хлорной кислоты относительно количества определяемых групп.
Известен способ определения аминогрупп методом ацилирования по методу Фрица и Шенка [Сиггиа С., Ханна Дж.Г. Количественный органический анализ по функциональным группам: пер. с англ. - М.: Химия, 1983 - С. 21]. Ацилирование проводят 2 М раствором уксусного ангидрида в этилацетате или пиридине, содержащем 0,15 моль/л хлорной кислоты в качестве катализатора. К навеске жидкой пробы, содержащей 3-4 ммоль аминогрупп, прибавляют 5 мл ацилирующего раствора в этилацетате или пиридине, выдерживают около 5 минут и приливают 2 мл воды и 10 мл раствора пиридина в воде (3:1). Выдерживают 5-10 минут, затем прибавляют несколько капель индикатора и титруют раствором щелочи, напримергидроксидом калия.
Данный метод не применим для анализа модифицированных минеральных наполнителей. Концентрация функциональных групп на их поверхности составляет обычно 0,4-1,5 ммоль/г, т.е. для анализа в среднем необходима навеска вещества массой 5 г. При этом 5 мл ацилирующего раствора недостаточно для хорошего смачивания образца, а, следовательно, и количественного протекания реакции. Так же, при анализе твердых образцов, необходимо отделение анализируемого раствора от твердой фазы, что невозможно сделать при приведенных соотношениях количества анализируемого образца и раствора. При увеличении количества ацилирующего раствора той же концентрации относительно навески образца сильно возрастает погрешность эксперимента, в том числе из-за увеличения количества хлорной кислоты относительно количества определяемых групп. Разбавление раствора, или снижение количества хлорной кислоты в данных ацилирующих растворах невозможно, поскольку при ее концентрации менее 0,15 моль/л ацилирование протекает не полностью. Таким образом, данный способ трудоемкий и не может быть применен к анализу модифицированных минеральных наполнителей.
Наиболее близким аналогом к предлагаемому техническому решению является способ определения концентрации привитых аминогрупп на поверхности минеральных наполнителей, основанный на использовании в качестве ацилирующего раствора 0,5-0,6 М раствора уксусного ангидрида в смешанном растворителе дихлорэтан - пиридин в соотношении от 0,5:1 до 2:1, содержащий 0,025-0,15 моль/л хлорной кислоты в качестве катализатора. Ацилирующий раствор готовят, смешивая необходимые соотношения раствора уксусного ангидрида в дихлорэтане и пиридина. К навеске пробы модифицированного минерального наполнителя добавляют 0,5-0,6 М ацилирующий раствор в смешанном растворителе, содержащий хлорную кислоту. Соотношение навески пробы к объему ацилирующего раствора составляет 1:4 - 1:5. Выдерживают для количественного протекания реакции, добавляют гидролизующую смесь, содержащею диметилформамид: пиридин: вода в соотношении 6:3:1 соответственно, центрифугируют для отделения осадка и отбирают аликвоту раствора для титрования. Содержание аминогрупп рассчитывают по разности результатов холостого титрования и титрования пробы [Патент 2541759 РФ, МПК G01N 31/16 (2006.01), G01N 21/78 (2006.01)].
Недостатком данного способа является использование для определения концентрации привитых аминогрупп веществ ограниченного пользования, а также искажение результатов определения концентрации привитых аминогрупп из-за использования хлорной кислоты в качестве катализатора.
Техническим результатом является упрощение способа определения концентрации привитых аминогрупп за счет сокращения ассортимента и количества реагентов, необходимых для их определения, а также доступности используемых реагентов.
Для достижения технического результата предлагается в качестве ацилирующего раствора использовать 0,5 М раствор пиромеллитового диангидрида (ПМДА) в смешанном растворителе (диметилсульфоксид (ДМСО) - пиридин). К навеске пробы модифицированного минерального наполнителя добавляют 0,5 М ацилирующий раствор в смешанном растворителе. Соотношение навески пробы к объему ацилирующего раствора составляет 1:5 - 1:12,5. Выдерживают для количественного протекания реакции на водяной бане не менее 5 минут при 95°С, после чего добавляют воду для гидролиза и греют. Полученную смесь центрифугируют для отделения осадка и отбирают аликвоту раствора для титрования. Титрование проводят водным раствором щелочи в присутствие индикатора. Содержание аминогрупп рассчитывают по разности результатов холостого титрования и титрования пробы.
Отличительными признаками от прототипа являются:
- использование 0,5 М раствора пиромеллитового диангидрида (ПМДА) в смешанном растворителе (ДМСО - пиридин);
- использование соотношения массы навески к объему ацетилирующего раствора, составляющее от 1:5 до 1:12,5;
- нагревание на водяной бане не менее 5 минут при 95°С для количественного протекания реакции;
- использование для гидролиза воды без органических растворителей.
Совокупность указанных отличительных признаков позволяет упростить способ определения аминогрупп в различных, в том числе и твердых нерастворимых материалах, т.к. ПМДА является доступным реагентом, не требующим разрешений, специальных условий хранения и учета. Кроме того, ПМДА, в отличие от уксусного ангидрида, является нелетучим, что исключает ошибки, связанные с испарением реагентов при анализе. Отсутствие хлорной кислоты в составе ацилирующей смеси позволяет проводить анализ минеральных наполнителей, содержащих в составе реакционноспособные основные оксиды. Такие преимущества, по сравнению с прототипом, позволяют снизить расход исходных реагентов при анализе одного образца.
Пример 1. В емкость помещают навеску модифицированного силикагеля, содержащего 1,00±0,03 ммоль/г привитых аминогрупп, массой 0,2000 г. Добавляют 0,5 мл 0,5 М раствора ПМДА в смешанном растворителе ДМСО - пиридин. Выдерживают реакционную смесь на водяной бане в течение 30 минут при температуре 95°С, после чего добавляют 6 мл воды и греют еще 2 минуты (из литературных источников известно, данного времени достаточно для протекания гидролиза [Сиггиа С., Ханна Дж.Г. Количественный органический анализ по функциональным группам: пер. с англ. - М.: Химия, 1983. - С. 31]). Далее смесь центрифугируют для отделения осадка и отбирают аликвоту раствора объемом 1 мл для титрования. Титрование проводят в присутствии индикатора фенолфталеина до перехода окраски из бесцветной в малиновый цвет 0,1 М водным раствором гидроксида калия. Содержание аминогрупп рассчитывают по разности результатов холостого титрования и титрования пробы. Найденное количество аминогрупп составило 0,73±0,03 ммоль/г.
Примеры 2-15 проводят по аналогичной методике с варьированием температуры нагревания, времени нагревания и объема ацилирующей смеси. Условия проведения эксперимента и полученные результаты представлены в таблице.
Пример 16. В емкость помещают навеску модифицированной микрослюды, содержащей0,37±0,03 ммоль/г привитых аминогрупп, массой 0,2000 г. Добавляют 1 мл 0,5 М раствора ПМДА в смешанном растворителе ДМСО - пиридин. Выдерживают реакционную смесь на водяной бане в течение 5 минут при температуре 95°С, после чего добавляют 6 мл воды и греют еще 2 минуты. Далее смесь центрифугируют для отделения осадка и отбирают аликвоту раствора объемом 1 мл для титрования. Титрование проводят в присутствии индикатора фенолфталеина до перехода окраски из бесцветной в малиновый цвет 0,1 М водным раствором гидроксида калия. Найденное количество аминогрупп составило 0,36±0,03 ммоль/г.
Пример 17. В емкость помещают навеску модифицированной микрослюды, содержащей 0,16±0,03 ммоль/г привитых аминогрупп, массой 0,2000 г. Добавляют 1 мл 0,5 М раствора ПМДА в смешанном растворителе ДМСО - пиридин. Выдерживают реакционную смесь на водяной бане в течение 5 минут при температуре 95°С, после чего добавляют 6 мл воды и греют еще 2 минуты. Далее смесь центрифугируют для отделения осадка и отбирают аликвоту раствора объемом 1 мл для титрования. Титрование проводят в присутствии индикатора фенолфталеина до перехода окраски из бесцветной в малиновый цвет 0,1 М водным раствором гидроксида калия. Найденное количество аминогрупп составило 0,17±0,03 ммоль/г.
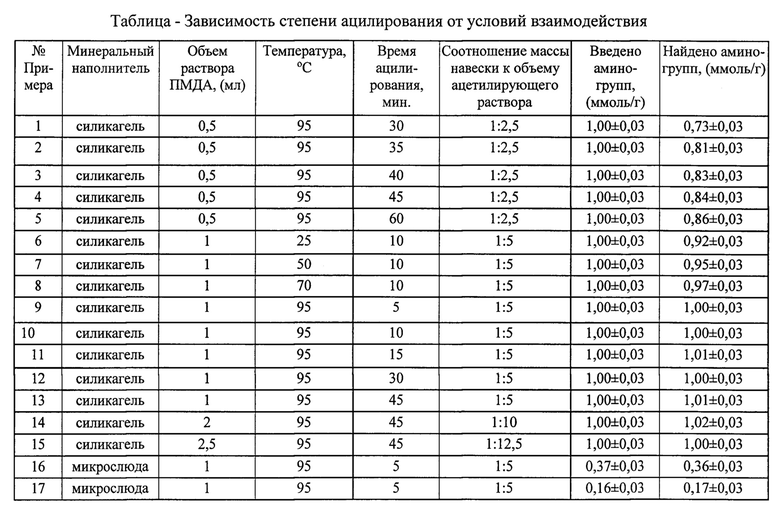
Содержание аминогрупп в образцах, взятых для анализа по предложенному методу, определялось для силикагеля обратным кислотно-основным титрованием, для остальных минеральных наполнителей - методом термогравиметрического анализа.
Как видно из приведенных примеров использование 0,5 М раствора ПМДА в смешанном растворителе ДМСО - пиридин позволяет применять соотношения массы навески к объему ацетилирующего раствора от 1:5 до 1:12,5, в зависимости от удельной поверхности и плотности анализируемого материала, а также концентрации привитых аминогрупп. Как видно из примеров №№1-5 при недостаточном избытке ПМДА ацилирование не протекает количественно. Количество ПМДА должно превышать количество определяемых аминогрупп как минимум в 5 раз для количественного протекания реакции, что иллюстрируют примеры 9-17.
Для количественного протекания реакции необходимо нагревание реакционной смеси до 95°С в течение 5 минут (пример 9). При более низких температурах реакция не протекает количественно (примеры 6-8). Данные таблицы свидетельствуют о нецелесообразности времени нагревания большего, чем 5 мин.
Применение большого избытка ПМДА не вносит дополнительных ошибок в определение концентрации (примеры 14-15) и может быть использовано при анализе наполнителей с высокой концентрацией привитых аминогрупп.
Примеры 16-17 иллюстрируют возможность применения данного метода для анализа модифицированных наполнителей, анализ которых не возможен методами кислотно-основного титрования из-за содержания основных оксидов.
Итак, по сравнению с прототипом мы видим, что для анализа применены доступные реактивы, сокращено использование органических растворителей (примерно 1 мл на один анализ, против почти 7 мл по прототипу). Также не используется хлорная кислота, что способствует снижению протекания побочных реакций, таких как взаимодействие хлорной кислоты с аминогруппами или основными оксидами, входящими в состав наполнителей, что повышает точность определения. Не используются для определения концентрации привитых аминогрупп вещества ограниченного пользования, что обеспечивает доступность выполнения способа на предприятиях, занимающихся модификацией минеральных наполнителей и их использованием. Также предложенный способ приводит к сокращению ассортимента и количества реагентов, необходимых для определения.
Предлагаемый способ обладает новизной, существенными отличиями, промышленно применим, а следовательно, соответствует критериям охраноспособности.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ ПРИВИТЫХ АМИНОГРУПП НА ПОВЕРХНОСТИ МИНЕРАЛЬНЫХ НАПОЛНИТЕЛЕЙ | 2013 |
|
RU2541759C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ АЗОТСОДЕРЖАЩИХ КРЕМНИЙОРГАНИЧЕСКИХ СОЕДИНЕНИЙ | 1970 |
|
SU268737A1 |
| Способ получения @ -аминобензамидопропилкремнезема | 1990 |
|
SU1725950A1 |
| Способ определения окси- и аминопроизводных в водной среде | 1983 |
|
SU1133548A1 |
| ИОННЫЕ МОЛЕКУЛЯРНЫЕ КОНЪЮГАТЫ N-АЦИЛИРОВАННЫХ ПРОИЗВОДНЫХ ПОЛИ(2-АМИНО-2-ДЕОКСИ-D-ГЛЮКОЗЫ) И ПОЛИПЕПТИДОВ | 1996 |
|
RU2172323C2 |
| СПОСОБ СЕЛЕКТИВНОГО АЦИЛИРОВАНИЯ ПРОИНСУЛИНА, ИНСУЛИНА ИЛИ ИНСУЛИНОВОГО АНАЛОГА, ИМЕЮЩИХ СВОБОДНЫЕ ε- И α-АМИНОГРУППЫ | 1995 |
|
RU2155773C2 |
| Способ количественного определения 4,4 -дипиридила | 1976 |
|
SU650004A1 |
| АЦИЛИРОВАННЫЕ АНАЛОГИ ИНСУЛИНА | 1995 |
|
RU2160118C2 |
| СПОСОБ ПОЛУЧЕНИЯ КРИСТАЛЛИЧЕСКОГО МОНО- ИЛИ ДИГИДРАТА ДИГИДРОХЛОРИДА 7-[2-(2- АМИНОТИАЗОЛ -4-ИЛ)-2(Z)- МЕТОКСИИМИНОАЦЕТАМИДО] -3-[(1- МЕТИЛ-1- ПИРРОЛИДИНИО) МЕТИЛ] -ЦЕФ- 3-ЕМ- 4-КАРБОКСИЛАТА, ПО СУЩЕСТВУ СВОБОДНОГО ОТ АНТИИЗОМЕРА И Δ -ИЗОМЕРА | 1992 |
|
RU2039059C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ АНГИДРИДНЫХ ГРУПП В ПИРОМЕЛЛИТОВОМ ДИАНГИДРИДЕ И 2(5)-(N-АМИНОФЕНИЛ)-5(2)-ФЕНИЛПИРИМИДИН В КАЧЕСТВЕ РЕАГЕНТА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1985 |
|
SU1311394A1 |
Изобретение относится к аналитической химии, а именно к определению концентрации привитых аминогрупп на поверхности минеральных наполнителей, что может быть использовано при производстве композиционных материалов, модифицированных минеральных наполнителей и различных сорбентов на их основе. Способ определения концентрации привитых аминогрупп на поверхности минеральных наполнителей включает приготовление ацилирующего раствора, добавление его к навеске пробы модифицированного минерального наполнителя, выдерживание для количественного протекания реакции, центрифугирование полученной смеси для отделения осадка, титрование раствором щелочи в присутствии индикатора, вычисление концентрации аминогрупп по разности результатов холостого титрования и титрования пробы, при этом в качестве ацилирующего раствора используют 0,5 М раствор пиромеллитового диангидрида в смешанном растворителе диметилсульфоксид - пиридин, соотношение массы навески пробы к объему ацетилирующего раствора составляет 1:5-1:12,5, полученную смесь выдерживают на водяной бане не менее 5 минут при 95°С, после чего добавляют воду для гидролиза и нагревают. Техническим результатом является упрощение способа определения концентрации привитых аминогрупп. 1 табл.
Способ определения концентрации привитых аминогрупп на поверхности минеральных наполнителей, включающий приготовление ацилирующего раствора, добавление его к навеске пробы модифицированного минерального наполнителя, выдерживание для количественного протекания реакции, центрифугирование полученной смеси для отделения осадка, титрование раствором щелочи в присутствии индикатора, вычисление концентрации аминогрупп по разности результатов холостого титрования и титрования пробы, отличающийся тем, что в качестве ацилирующего раствора используют 0,5 М раствор пиромеллитового диангидрида в смешанном растворителе диметилсульфоксид - пиридин, соотношение массы навески пробы к объему ацетилирующего раствора составляет 1:5-1:12,5, полученную смесь выдерживают на водяной бане не менее 5 минут при 95°С, после чего добавляют воду для гидролиза и нагревают.
| СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ ПРИВИТЫХ АМИНОГРУПП НА ПОВЕРХНОСТИ МИНЕРАЛЬНЫХ НАПОЛНИТЕЛЕЙ | 2013 |
|
RU2541759C1 |
| СИГГИА С., ХАННА ДЖ.Г | |||
| КОЛИЧЕСТВЕННЫЙ ОРГАНИЧЕСКИЙ АНАЛИЗ ПО ФУНКЦИОНАЛЬНЫМ ГРУППАМ | |||
| ПЕР | |||
| С АНГЛ., с | |||
| Выбрасывающий ячеистый аппарат для рядовых сеялок | 1922 |
|
SU21A1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ, СОДЕРЖАЩИХ АМИНОГРУППУ | 0 |
|
SU379872A1 |
| Способ количественного определения аминогрупп в алкиламиносилохромах | 1978 |
|
SU767644A1 |
Авторы
Даты
2021-12-02—Публикация
2021-03-25—Подача