ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к применению графенового продукта, композициям, содержащим указанный продукт, и их применению в терапии.
УРОВЕНЬ ТЕХНИКИ
Семейство материалов на основе графена или родственных материалов недавно оказалось в центре внимания после присуждения Нобелевской премии по физике 2010 г. и последующего бурного развития многочисленных применений этих материалов в области энергетики, электроники, сенсоров, DLP (от англ. digital light processing - цифровая обработка света), медицины и охраны окружающей среды. «Основоположник» этого семейства - графен - представляет собой двумерный материал, состоящий из sp2-гибридизованных атомов углерода, расположенных в гексагональной сотовой решетке.
Расширенное семейство материалов, родственных графену, включает графен (одно- и многослойный), графит, полициклические ароматические углеводороды, углеродные нанотрубки, фуллерены, различные графеновые наноструктуры разной размерности (например, графеновые нановолокна, графеновые наночастицы, графеновые квантовые точки, графеновые наноленты, графеновые наносетки, графеновые нанодиски, графеновые пены, графеновые наностолбики), любые комбинации других родственных графену материалов, замещенные материалы, родственные графену (например, в результате замещения атомов углерода на N, В, Р, S, Si или другие атомы), и родственные графену материалы, функционализированные реакционноспособными функциональными группами (например, карбоксильными группами, сложными эфирами, амидами, тиолами, гидроксильными группами, диольными группами, кетонными группами, сульфонатными группами, карбонильными группами, арильными группами, эпоксигруппами, фенольными группами, фосфоновыми кислотами, аминогруппами, порфиринами, пиридинами, полимерами и их комбинациями).
В нескольких публикациях описано применение графеновых материалов в медицинских целях.
В патенте US 2006/0134096 описаны композиции и способы медицинского применения композиций, содержащих графен, в частности непористый углерод, кроме фуллерена или нанотрубок, включающий графен. Их применяют наружно на ранах, в качестве сорбентов для токсинов или при гемодиализе.
В патенте ЕР 313353 предложены фармацевтические композиции на основе графеновых наноструктур для предотвращения или лечения нейродегенеративных заболеваний. Графеновая наноструктура препятствует образованию фибрилл, вызванному неправильным сворачиванием белка.
В патенте US 2014/0120081 предложено применение углеродных наноматериалов для лечения окислительного стресса у субъекта путем снижения уровня активных форм кислорода. Углеродный наноматериал выбран из нанотрубок, графена, графеновых нанолент, графита, оксида графита и т.д., которые могут быть функционализированы.
В патенте GB 2532449 описан функционализированный наноматериал для применения для лечения, профилактики или предотвращения рака путем ингибирования пролиферации раковых стволовых клеток, где указанный наноматериал представляет собой однослойный графен, малослойный графен, нанографит, одностенные или многостенные углеродные нанотрубки, фуллерены, углеродные рупорообразные нановыступы, углеродные нановолокна или аморфный или частично аморфизированный наноуглерод или их смеси. Оксид графена является предпочтительным.
В работе Guranathan S. и Kim J-H. в International Journal of Nanomedicine, 2016:11, cc. 1927-1945, приведен обзор синтеза, токсичности, биосовместимости и биомедицинских применений графена и родственных материалов. Как отмечается в данном документе, многие из этих продуктов по-прежнему создают проблемы, связанные с токсичностью и биосовместимостью. На токсический эффект графена могут влиять физико-химические свойства, такие как размер и распределение по размеру, поверхностный заряд, площадь поверхности, число слоев, поперечные размеры, поверхностные явления, чистота, состояние частиц, поверхностные функциональные группы и форма. Противоопухолевая терапия, фототермическая терапия, доставка лекарств, трансфекция генов, биозондирование, визуализация и тканевая инженерия относятся к числу биомедицинских применений, упомянутых в данном обзоре.
По-прежнему существует потребность в новых материалах на основе графена с низкой или отсутствующей токсичностью и хорошей биосовместимостью, способных обеспечивать полезный биологический эффект и подходящих для применения в терапии.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Авторами настоящего изобретения обнаружены новые графеновые продукты, обладающие примечательными свойствами, имеющие крайне низкую или нулевую токсичность и подходящие для применения в терапии.
Согласно первому аспекту, настоящее изобретение относится к применению графенового наноматериала, представляющего собой графеновые нановолокна, где указанный графеновый наноматериал имеет количественное распределение частиц по размерам с dn(90), равным 0,60 мкм или менее, и объемное распределение частиц по размерам с dv(90), равным 80,00 мкм или менее, измеренное при помощи лазерного дифракционного анализатора размеров частиц.
Предпочтительно удельная площадь поверхности графенового наноматериала, измеренная методом БЭТ, составляет 100-500 м2/г, и более предпочтительно 300-350 м2/г.
Согласно другому варианту реализации, объем пор графенового наноматериала составляет 0,35-0,40 см3/г.
Также предпочтительно, чтобы примеси в графеновом наноматериале составляли менее 0,01 масс. %.
Согласно другому аспекту, настоящее изобретение относится к применению вышеуказанного графенового наноматериала в качестве лекарственного средства. Согласно одному варианту реализации, лекарственное средство предназначено для лечения поражений кожи, выбранных из ран, экземы, кожных ожогов и кожных язв. Согласно другому аспекту, настоящее изобретение относится к фармацевтическим композициям, содержащим вышеуказанный графеновый наноматериал.
ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фигура 1. - Рамановская спектроскопия GMC-1.
Фигура 2 - Адсорбция-десорбция в N2GMC-L
Фигура 3А. - Рентгеновская дифракция исходного материала GNF.
Фигура 3В. - Рентгеновская дифракция GMC-1.
Фигура 4А. - Сравнение количественного распределения частиц по размерам для исходного материала GNF и GMC-1.
Фигура 4В. - Сравнение объемного распределения частиц по размерам в зависимости от процентного содержания частиц для исходного материала GNF и GMC-1.
Фигура 5. - Количественные анализы токсичности на культивированных клетках Hep-G2, обработанных GMC-1 в течение 24 часов. А) Жизнеспособность, определенная по методу вытеснения трипанового синего, и В) клеточный метаболизм, определенный с помощью МТТ-теста с 1- и 10-кратной концентрацией GMC-1 в носителе. Значения представлены как среднее ± СОС (стандартная ошибка среднего).
Фигура 6. - Модель заживления кожной раны на грызунах (Rattus Norvegicus), основанная на биопсиях, проведенных в дорсальной области, которую обрабатывали наружно каждые 2 дня препаратом, содержащим 2-кратное количество GMC-1 или не содержащим его (контрольный тест). А) Динамика закрытия области раны, В) регенерация дермы (коллагенизация и реэпителизация) и С) острый воспалительный инфильтрат на 4-й день. Значения выражены в процентах относительно внутренней контрольной раны на животное (не обрабатывалась каким-либо препаратом) и представлены как среднее ± СОС.*=Р<0,05 по сравнению с контрольным тестом, значение считается статистически значимым.
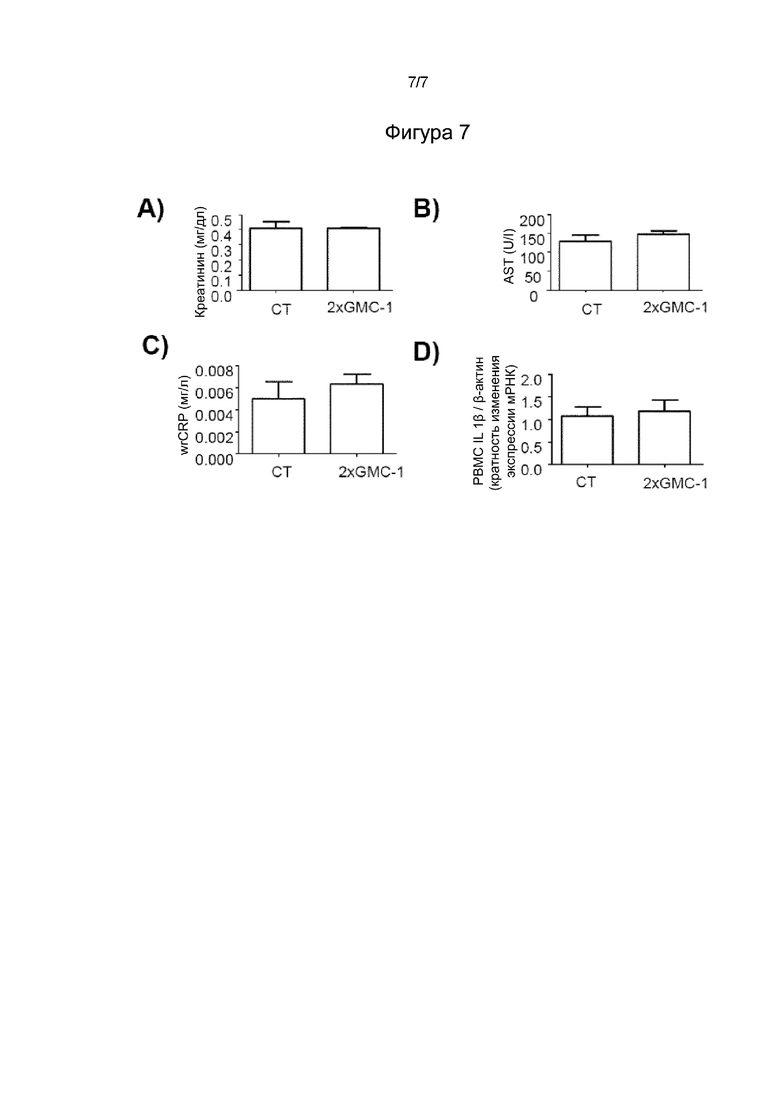
Фигура 7. - Системный биохимический анализ модели заживления кожной раны на грызунах (Rattus Norvegicus), основанный на биопсиях, проведенных в дорсальной области, которую обрабатывали наружно каждые 2 дня препаратом, содержащим 2-хкратное количество GMC-1 или не содержащим его (контрольный тест). На 4-й день и после эвтаназии определяли плазматический А) креатинин, В) аспартатаминотрансферазу (AST) и wrCRP (С-реактивный белок широкого диапазона). D) В мононуклеарных клетках периферической крови (РВМС) кратность изменения экспрессии мРНК определяли с помощью RT-qPCR для экспрессии маркера системного воспаления интерлейкина 1-бета (IL-1-бета). Значения представлены как среднее ± СОС.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Графеновое сырье
В настоящем изобретении термин «графен» относится к материалу, образующему полициклическую ароматическую молекулу с множеством атомов углерода, ковалентно связанных друг с другом. Ковалентно связанные атомы углерода образуют шестичленное кольцо, являющееся повторяющимся звеном.
Термин «графеновые нановолокна» (GNF) относится к цилиндрическим наноструктурам со слоями графена, расположенными в виде сложенных стопкой конусов, чаш или пластин. Поверхность плоскости графена наклонена относительно оси волокна, что открывает края плоскости, присутствующие на внутренней и внешней поверхностях углеродных на но волокон.
Термин «графеновые нанотрубки» (GNT) относится к одностенным или многостенным концентрическим цилиндрам из графена, в которых базальные плоскости образуют менее реакционноспособную поверхность по сравнению с поверхностью графеновых нановолокон, поскольку они являются цилиндрическими и полыми, как трубки, а графеновые нановолокна подобны стержням, и, как правило, в них нет внутреннего пустого пространства.
Продукт согласно настоящему изобретению представляет собой наноматериал на основе углерода, полученный из GNF, который подвергается ряду процедур очистки и обработки для получения материала с достаточной для фармацевтических целей чистотой, обладающего неожиданными биологическими свойствами.
Исходный углеродный наноматериал представляет собой материал на основе графена (графеновые нановолокна). Согласно одному варианту реализации, графеновые нановолокна, применяемые для получения продукта согласно настоящему изобретению, имеют количественное распределение частиц по размерам dn(90), равное 4,0 мкм или менее, и объемное распределение частиц по размерам dv(90), равное 105,00 мкм или менее. Предпочтительно они имеют площадь поверхности примерно 250-400 м2/г.
Сырье, используемое для получения продукта согласно настоящему изобретению, можно синтезировать с помощью широкого спектра методов, таких как эпитаксиальный рост на карбиде кремния, химическое осаждение из газовой фазы, микромеханическое или механическое расслоение графита, химическое окисление графита, восстановление оксида графита с использованием термического, химического или многостадийного восстановления, каталитическое разложение углеводородов на металлическом катализаторе, разворачивание углеродных нанотрубок, электропрядение и т.д.
Эпитаксиальный рост на карбиде кремния представляет собой способ, в котором отделенные от графена монослои могут быть синтезированы на монокристаллическом кристалле карбида кремния (SiC), который применяют в качестве субстрата. Этот способ состоит в нагревании подложки из SiC до высоких температур (>1100°С) при высоком вакууме. В указанных условиях атомы кремния сублимируются, что приводит к эпитаксиальному росту графена на поверхности подложки (атомы углерода перегруппировываются, образуя графен) [Sutter, P., Epitaxial graphene: How silicon leaves the scene. Nature Materials, 2009. 8(3): 171-172].
В способе химического разложения из газовой фазы источник углерода каталитически разлагается на каталитическом субстрате. После термического разложения углеводородов каталитическая поверхность вызывает растворение атомов углерода, образовавшихся внутри металла [Jacobberger, R.M., et al., Simple Graphene Synthesis via Chemical Vapor Deposition. Journal of Chemical Education, 2015. 92(11): 1903-1907, Lavin-Lopez, M.P., et al., Thickness control of graphene deposited over polycrystalline nickel. New Journal of Chemistry, 2015. 39(6): 4414-4423].
Микромеханическое расслоение графита заключается в отделении самого внешнего слоя указанного твердого вещества в виде чешуек с помощью тонкого соскабливания с использованием объекта с твердой поверхностью или клейкой ленты [Geim, А.K.; K.S. Novoselov, The rise of graphene. Nature Materials, 2007. 6(3): 183-191]. Механическое расслоение позволяет разделять листы, которые образуются из графита, суспендированного в органических или водных растворителях, посредством воздействия ультразвуковых волн. Получаемый материал имеет высокое качество, однако он не представляет значительного промышленного интереса с учетом его низкого выхода и высокой стоимости изготовления [Lotya, М., et al., Liquid phase production of graphene by exfoliation of graphite in surfactant/water solutions. Journal of the American Chemical Society, 2009. 131(10): 3611-3620].
Для синтеза графеновых нановолокон (GNF) также можно применять широкий спектр методов, которые в особенности предпочтительны для получения продукта согласно настоящему изобретению. Например, метод химического осаждения из газовой фазы для получения углеродного нановолокна представляет собой каталитический метод, в котором источник углерода разлагается в присутствии катализатора до сформированных GNF. В качестве катализатора применяются каталитические частицы переходных металлов, таких как железо, никель, кобальт и медь. Процесс CVD происходит при температурах от 500 до 1200°С [Martin-Gullon, I., et al., Differences between carbon nanofibers produced using Fe and Ni catalysts in a floating catalyst reactor. Carbon, 2006. 44(8): 1572-1580]. Электропрядение представляет собой альтернативный способ получения GNF. В этом способе применяется процесс золь-гель, для которого необходима игла с тонким острием. Для этого на каплю иглы подается высокое напряжение, в результате чего раствор выходит из иглы по направлению к мишени. Когда поверхностное натяжение раствора достаточно велико, и предотвращается вхождение мелкой капли, волокнистая структура может быть получена и собрана в объективе [Zhang, L, et al., A review: Carbon nanofibers from electrospun polyacrylonitrile and their applications. Journal of Materials Science, 2014. 49(2): 463-480].
Средние диаметры и длины пористого графитового материала, применяемого для получения композита согласно настоящему изобретению, измеряются с помощью просвечивающей электронной микроскопии (ПЭМ).
Очистка и обработка
Графеновый наноматериал, синтезированный по описанным выше способам, применяется в качестве сырья для синтеза материала на основе графена, имеющего фармацевтическую степень чистоты, согласно настоящему изобретению. Затем неочищенный графеновый наноматериал подвергается процессу очистки, предпочтительно с использованием сильной кислоты (H2SO4, HCl, HF, HNO3, HBr и т.д.), для удаления возможных металлов или примесей, внесенных в структуру графенового наноматериала в процессе синтеза. Можно применять любой процесс, способный удалять примеси и не оказывающий влияния на свойства графенового материала. Среди кислот особенно предпочтительна соляная или фтористоводородная кислота, однако специалист может выбрать кислоту и условия в зависимости от количества и типа присутствующих примесей. Процесс очистки предпочтительно проводится при низких температурах (20-50°С) в течение нескольких часов (12-24 часов). Если для процесса очистки применяется раствор, очищенный графеновый наноматериал можно затем промыть очищенной при помощи системы Millipore водой до нейтрального значения рН, а затем высушить, например, в вакууме.
Очищенный графеновый наноматериал также обрабатывается для достижения уменьшенного распределения по размерам частиц, что делает продукт подходящим для медицинского и косметического применения. Очищенный графеновый наноматериал, например, подвергается процессу уменьшения размера и модификации свойств. Согласно одному варианту реализации, он подвергается процессу расслоения при комнатной температуре, например, посредством обработки ультразвуком, мокрого размола или гибридных процессов. Особенно предпочтительна обработка ультразвуком вследствие простоты процесса, который может дополнительно контролироваться при помощи проб для проверки достижения требуемого распределения частиц по размерам. После этого может быть проведен необязательный процесс разделения частиц по размеру для контроля размера частиц в диапазоне 10-100 мкм. Специалист легко определит методику, необходимую для выбора распределения по размерам частиц. Например, эта стадия может быть осуществлена посредством фильтрования или центрифугирования, предпочтительно вакуумного фильтрования, например, через фильтр из спеченного стекла. Указанная стадия разделения частиц по размеру может обеспечивать преимущество, состоящее в получении частиц, имеющих количественное распределение частиц по размерам dn(90), равное 0,60 мкм или менее, и объемное распределение частиц по размерам dv(90), равное 80,00 мкм или менее.
В заключение для контроля наличия в материале следов других токсичных соединений, включая бактериологическое загрязнение или эндотоксины, и с целью поддержания асептических и стерильных условий материал также может быть подвергнут стандартному процессу депирогенизации путем нагревания, предпочтительно при 200-500°С в течение 10-60 мин.
Полученное значение распределения частиц по размерам может быть определено при помощи обычных средств, применяемых в данной области, таких как анализатор размера частиц, например Mastersizer 2000 от Malvern Panalytical, использованный в примерах.
В контексте настоящего изобретения количественное распределение частиц по размерам dn(90), равное 0,60 мкм или менее, и объемное распределение частиц по размерам dv(90), равное 80,00 мкм или менее, может быть получено путем проведения стадии (b), необязательно включая дополнительную стадию разделения частиц по размеру, предпочтительно стадию фильтрования. Предпочтительно фильтрование представляет собой вакуумное фильтрование при помощи фильтра из спеченного стекла с размером пор от 1 до 20 мкм, предпочтительно от 4 до 20 мкм, более предпочтительно от 5 до 16 мкм.
Продукт
Продукт согласно настоящему изобретению представляет собой очищенный графеновый наноматериал с количественным распределением частиц по размерам dn(90), равным примерно 0,60 мкм или менее, и объемным распределением частиц по размерам dv(90), равным 80,00 мкм или менее, предпочтительно 70,00 мкм или менее.
Распределение частиц по размерам измеряется с помощью лазерного дифракционного анализатора размеров частиц. Распределение частиц по размерам D50 представляет собой значение диаметра частицы при 50% совокупного распределения. Если D50 имеет определенное значение, то 50% частиц в образце имеют размер, больший этого значения, а 50% - меньший. Распределение частиц по размерам представляет собой количество частиц, которые попадают в каждый из различных диапазонов размеров, выраженное в процентах от общего количества всех размеров в рассматриваемом образце. Наиболее широко применяемым способом описания распределения частиц по размерам являются значения d (d10, d50 и d90), которые представляют собой отсечки для 10%, 50% и 90% от совокупной массы.
Эти значения могут толковаться как диаметр материала, который делит массу образца на определенные процентные доли при расположении частиц по возрастанию массы. Параметр d10 представляет собой диаметр, при котором 10% массы образца состоит из частиц с диаметром, меньшим этого значения. Параметр d50 представляет собой диаметр частицы, при котором 50% массы образца меньше, а 50% массы образца больше, чем это значение, и d90 представляет собой диаметр, при котором 90% массы образца состоит из частиц с диаметром, меньшим этого значения. Эти значения можно применять для количественного распределения частиц по размерам (dn) и объемного распределения частиц по размерам (dv).
Количественное распределение частиц по размерам dn(90) означает точку в распределении по размерам, вплоть до которой включительно содержится 90% от общего количества материала в образце.
Объемное распределение частиц по размерам dv(90) означает точку в распределении по размерам, вплоть до которой включительно содержится 90% от общего объема материала в образце.
Распределение частиц по размерам продукта согласно настоящему изобретению измерялось с помощью прибора Mastersizer 3000 от Malvern Panalytical.
В контексте настоящего изобретения термин «удельная площадь поверхности (УПП)» относится к общей площади поверхности материала на единицу массы.
Пористость и удельная площадь поверхности, описанные в настоящей заявке, измеряются посредством методов Брунауэра-Эммета-Теллера («БЭТ»), применяемых в хорошо известной специалисту в данной области техники методике физической адсорбции с использованием азота в качестве адсорбционного материала.
Согласно одному варианту реализации, площадь поверхности по методу БЭТ продукта согласно настоящему изобретению составляет 300-350 м2/г.
Согласно другому варианту реализации, объем пор продукта согласно настоящему изобретению составляет 0,35-0,40 см3/г.
Согласно предпочтительному варианту реализации, продукт согласно настоящему изобретению имеет площадь поверхности по методу БЭТ, составляющую 300-350 м2/г, и объем пор, составляющий 0,35-0,40 см3/г.
Продукт согласно настоящему изобретению представляет собой графеновые нановолокна.
Композиция
Согласно другому аспекту, настоящее изобретение относится к фармацевтической композиции, содержащей графеновый продукт согласно настоящему изобретению и одно или более фармацевтически приемлемых вспомогательных веществ.
Используемый в настоящей заявке термин «фармацевтическая композиция» относится к композициям и молекулярным структурам, которые являются физиологически переносимыми и обычно не вызывают аллергической реакции или подобной неблагоприятной реакции, такой как желудочные расстройства, головокружение и т.п., при введении человеку или животному. Предпочтительно термин «фармацевтически приемлемый» означает, что вещество одобрено надзорным органом государства или федерального правительства и/или включено в Европейскую фармакопею или Фармакопею США и/или другие общепризнанные фармакопеи для применения на животных и, в частности, на людях.
Термин «вспомогательное вещество» относится к носителю, разбавителю или адъюванту, которые вводятся с действующим веществом. Эти фармацевтические вспомогательные вещества могут представлять собой стерильные жидкости, такие как воду и масла, в том числе нефтяного, животного, растительного или синтетического происхождения, например, арахисовое масло, соевое масло, минеральное масло, кунжутное масло и т.п.
Согласно предпочтительному варианту реализации, фармацевтическая композиция согласно настоящему изобретению подходит для наружного применения на коже, например, в виде кремов, лосьонов, мазей, микроэмульсий, жирных мазей, гелей, эмульсий-гелей, паст, пен, настоек, растворов, пластырей, повязок и трансдермальных терапевтических систем. Наиболее предпочтительны кремы или эмульсии-гели.
Кремы или лосьоны представляют собой эмульсии типа «масло в воде». Подходящие масляные основы представляют собой жирные спирты, в частности, содержащие от 12 до 18 атомов углерода, например, лауриловый, цетиловый или стеариловый спирт, жирные кислоты, в частности, содержащие от 10 до 18 атомов углерода, например, пальмитиновая или стеариновая кислота, сложные эфиры жирных кислот, например, глицерилтрикаприлокапрат (нейтральное масло) или цетилпальмитат, воски от жидких до твердых, например, изопропилмиристат, шерстяной воск или пчелиный воск, и/или углеводороды, в частности жидкие, полутвердые или твердые вещества или их смеси, например, вазелиновое масло (петролатум, Вазелин) или парафиновое масло. Подходящие эмульгаторы представляют собой поверхностно-активные вещества, обладающие преимущественно гидрофильными свойствами, такие как соответствующие неионные эмульгаторы, например, сложные эфиры жирных кислот и полиспиртов, и/или их аддукты с этиленоксидом, в частности соответствующие сложные эфиры жирных кислот с (поли)этиленгликолем, (пол и) про пилен гликолем или сорбитолом, где фрагмент жирной кислоты содержит, в частности, от 10 до 18 атомов углерода, в частности неполные сложные эфиры глицерина и жирных кислот или неполные сложные эфиры жирных кислот и полигидроксиэтиленсорбитана, такие как сложные эфиры полиглицерина и жирных кислот или сложные эфиры полигидроксиэтиленсорбитана и жирных кислот (Tween), а также простые эфиры полигидроксиэтилена и жирных спиртов или сложные эфиры жирных кислот, где фрагмент жирного спирта содержит, в частности, от 12 до 18 атомов углерода, а фрагмент жирной кислоты содержит, в частности, от 10 до 18 атомов углерода, такие как сложный эфир пол и гид роксиэтилен глицерина и жирной кислоты (например, Tagat S), или соответствующие ионные эмульгаторы, такие как соли щелочных металлов сульфатов жирных спиртов, в частности, содержащие от 12 до 18 атомов углерода во фрагменте жирного спирта, например, лаурилсульфат натрия, цетилсульфат натрия или стеарилсульфат натрия, которые обычно применяются в присутствии жирных спиртов, например, цетилового спирта или стеарилового спирта. Добавки к водной фазе представляют собой, среди прочего, агенты, предотвращающие высыхание кремов, например, увлажнители, такие как полиспирты, такие как глицерин, сорбитол, пропиленгликоль и/или полиэтиленгликоли, а также консерванты, отдушки, гелеобразующие агенты и т.д.
Мази представляют собой эмульсии типа "вода в масле", которые содержат до 70% воды или водной фазы, предпочтительно от примерно 20% до примерно 50%. Особенно подходящими в качестве масляной фазы являются углеводороды, например, вазелиновое масло, парафиновое масло и/или твердые парафины, которые для улучшения способности к связыванию воды предпочтительно содержат подходящие гидроксисоединения, такие как жирные спирты или их сложные эфиры, например, цетиловый спирт, спирты шерстяного воска, шерстяной воск или пчелиный воск. Эмульгаторы представляют собой соответствующие липофильные вещества, например, указанного выше типа, такие как сложные эфиры жирных кислот и сорбитана (Span), например, сорбитанолеат и/или сорбитанизостеарат. Добавки к водной фазе представляют собой, среди прочего, увлажнители, такие как полиспирты, например глицерин, пропиленгликоль, сорбитол и/или полиэтиленгликоль, а также консерванты, отдушки и т.д.
Микроэмульсии представляют собой изотропные системы на основе следующих четырех компонентов: вода, поверхностно-активное вещество, например, тензиоактивный агент, липид, такой как неполярное или полярное масло, например, парафиновое масло, природные масла, такие как оливковое или кукурузное масло, и спирт или полиспирт, содержащий липофильные группы, например, 2-октилдодеканол или этоксилированные эфиры глицерина или полиглицерина. При необходимости к микроэмульсиям могут быть добавлены другие добавки. Микроэмульсии имеют мицеллы или частицы с размерами менее 200 нм и представляют собой прозрачные или полупрозрачные системы, которые формируются самопроизвольно и являются устойчивыми. Жирные мази не содержат воды и содержат в качестве основы, в частности, углеводороды, например, парафин, вазелиновое масло и/или жидкие парафины, а также природные или частично синтетические жиры, такие как сложные эфиры жирных кислот и глицерина, например, триглицерид кокосовой жирной кислоты, или предпочтительно отвержденные жиры, например, гидрированное арахисовое масло, касторовое масло или воски, также неполные сложные эфиры глицерина и жирных кислот, например, моно- и дистеарат глицерина, а также, например, жирные спирты, увеличивающие способность к связыванию воды, эмульгаторы и/или добавки, указанные выше применительно к мазям.
Касательно гелей, различают водные гели, безводные гели и гели с низким содержанием воды, состоящие из набухающих гелеобразующих материалов. В частности, применяются прозрачные гидрогели на основе неорганических или органических макромолекул. Высокомолекулярные неорганические компоненты, обладающие гелеобразующими свойствами, преимущественно представляют собой водосодержащие силикаты, такие как силикаты алюминия, например, бентонит, алюмосиликат магния, например, вигум, или коллоидную кремниевую кислоту, например, аэросил. В качестве высокомолекулярных органических веществ применяются, например, природные, полусинтетические или синтетические макромолекулы. Природные и полусинтетические полимеры получают, например, из полисахаридов, содержащих разнообразные углеводные компоненты, такие как целлюлозу, крахмалы, трагакант, аравийскую камедь и агар-агар, и желатин, альгиновую кислоту и ее соли, например, альгинат натрия, и их производные, такие как низшие алкилцеллюлозы, например, метил- или этил целлюлоза, низшие карбокси- или гидроксиалкилцеллюлозы, например, карбоксиметил- или гидроксиэтилцеллюлоза. Компоненты синтетических гелеобразующих макромолекул представляют собой, например, соответствующим образом замещенные ненасыщенные алифатические соединения, такие как виниловый спирт, винилпирролидин, акриловая или метакриловая кислота.
Эмульсии-гели, также называемые "эмульгели", представляют собой композиции для наружного применения, сочетающие свойства геля и эмульсии типа "масло в воде". В отличие от гелей, они содержат липидную фазу, которая вследствие ее восстанавливающих жир свойств позволяет втирать лекарственную форму, и в то же время прямая абсорбция в кожу ощущается как приятный эффект. Кроме того, может наблюдаться повышенная растворимость липофильных действующих веществ. Одно преимущество эмульсий-гелей по сравнению с эмульсиями типа «масло в воде» состоит в усиленном охлаждающем эффекте, который обусловлен охлаждением вследствие испарения дополнительного спиртового компонента в случае его присутствия.
Пены наносят, например, из контейнеров под давлением и они представляют собой жидкие эмульсии типа «масло-в-воде» в форме аэрозоля; в качестве пропеллента применяются незамещенные углеводороды, такие как алканы, например, пропан и/или бутан. В качестве масляной фазы применяются, среди прочего, углеводороды, например, парафиновое масло, жирные спирты, например, цетиловый спирт, сложные эфиры жирных кислот, например, изопропилмиристат и/или другие воски. В качестве эмульгаторов применяются, среди прочего, смеси эмульгаторов, обладающих преимущественно гидрофильными свойствами, такие как сложные эфиры полигидроксиэтиленсорбитана и жирных кислот (Tween), и эмульгаторов, обладающих преимущественно липофильными свойствами, такие как сложные эфиры сорбитана и жирных кислот (Span). Также добавляются обычные добавки, такие как консерванты и т.д. Настойки и растворы, как правило, имеют этанольную основу, к которой может быть добавлена вода и к которой добавляются, среди прочего, полиспирты, например, глицерин, гликоли и/или полиэтиленгликоль в качестве увлажнителей для уменьшения испарения, и восстанавливающие жир вещества, такие как сложные эфиры жирных кислот с низкомолекулярными полиэтиленгликолями, пропиленгликолем или глицерином, то есть липофильные вещества, которые являются растворимыми в водной смеси, в качестве замены жирных веществ, удаляемых с кожи под воздействием этанола, и при необходимости другие вспомогательные вещества и добавки. Подходящие настойки или растворы также могут наноситься в виде спрея с помощью соответствующих устройств.
Трансдермальные терапевтические системы, в частности, с местной доставкой графенового продукта согласно настоящему изобретению содержат эффективное количество графенового продукта, необязательно вместе с носителем. Подходящие носители включают абсорбируемые фармакологически подходящие растворители, способствующие прохождению действующего вещества через кожу. Трансдермальные системы доставки имеют вид, например, пластыря, включающего (а) субстрат (поддерживающий слой или пленка), (b) матрицу, содержащую действующее вещество, необязательно носители и необязательно (но предпочтительно) специальный адгезив для закрепления системы на коже и, как правило, (с) защитную пленку (антиадгезионное покрытие). Матрица (b) обычно присутствует в виде смеси всех компонентов или может состоять из отдельных слоев.
Мембраны и матрицы, содержащие графеновый продукт согласно настоящему изобретению, также подходят для наружного применения продукта либо самостоятельно, либо в качестве части более сложного продукта, такого как повязка на рану, бинт и т.д. Примером таких мембран или матриц являются природные полимеры, такие как полисахариды (альгинаты, хитин, хитозан, гепарин, хондроитин, каррагинан), протеогликаны и белки (коллаген, желатин, фибрин, кератин, шелковый фиброин, мембрана яичной скорлупы); синтетические полимеры, такие как гидрогели или микро/наноразмерные волокна биомиметического внеклеточного матрикса на основе полигликолевой кислоты, полимолочной кислоты, полиакриловой кислоты, поли-ε-капролактона, поливинилпирролидона, поливинилового спирта, полиэтиленгликоля и т.д.
Все эти системы хорошо известны специалисту в данной области техники. Изготовление фармацевтического препарата для наружного применения осуществляется по известному способу, например, путем суспендирования графенового продукта согласно настоящему изобретению в основе или при необходимости в части основы.
Композиции согласно настоящему изобретению могут также включать обычные для дерматологических применений добавки и адъюванты, такие как консерванты, в частности сложные эфиры парабена, такие как метилпарабен, этилпарабен, пропилпарабен, бутилпарабен или четвертичные аммониевые соединения, такие как хлорид бензалкония, или формальдегидные доноры, такие как имидазонидинилмочевина, или спирты, такие как бензиловый спирт, феноксиэтанол, или кислоты, такие как бензойная кислота, сорбиновая кислота; кислоты или основания, используемые в качестве рН-буферных вспомогательных компонентов; антиоксиданты, в частности фенольные антиоксиданты, такие как гидрохинон, токоферол и их производные, а также флавоноиды, или различные антиоксиданты, такие как аскорбиновая кислота, аскорбилпальмитат; отдушки; наполнители, такие как каолин или крахмал; пигменты или красители; UV-экранирующие агенты; увлажняющие компоненты, в частности глицерин, бутиленгликоль, гексиленгликоль, мочевина, гиалуроновая кислота или их производные; антисвободнорадикальные агенты, такие как витамин Е или его производные; усилители всасывания, в частности пропиленгликоль, этанол, изопропанол, диметилсульфоксид, N-метил-2-пирролидон; жирные кислоты/спирты, такие как олеиновая кислота, олеиловый спирт; терпены, такие как лимонен, ментол, 1,8-цинеол; алкильные сложные эфиры, такие как этилацетат, бутилацетат; агенты для образования ионных пар, такие как салициловая кислота.
Дальнейшая подробная информация относительно подходящих лекарственных форм для наружного применения может быть получена в стандартных учебниках, например, в Remington, "The science and practice of pharmacy», 22-е издание (2012 г.).
Количество продукта на основе графенового наноматериала согласно настоящему изобретению в лекарственной форме может находиться в диапазоне от 0,01% до 10% масс./масс., предпочтительно от 0,01% до 5% масс./масс., более предпочтительно от 0,1% до 3% масс./масс.
Благоприятные эффекты и применения
Как можно видеть из приведенных ниже примеров, продукт согласно настоящему изобретению не токсичен также при наружном применении и обладает хорошей биосовместимостью.
Кроме того, продукт согласно настоящему изобретению неожиданно показал эффективность при восстановлении кожи и заживлении ран, что продемонстрировано в примерах.
Следовательно, графеновый продукт согласно настоящему изобретению и содержащие его композиции подходят для применения в качестве лекарственного средства в терапии.
Термин «терапия» или «терапевтический» означает лечение или предотвращение заболевания у людей или животных и восстановление, коррекцию или изменение физиологических функций человека или животных.
Многие патологические состояния могут нарушать целостность кожи и кожные функции, например, сахарный диабет, травмы, воспалительные заболевания, метаболические нарушения, нарушения свертываемости крови, аутоиммунные заболевания, такие как псориаз, и прочее. Поэтому способствование заживлению кожных повреждений, независимо от природы причинного фактора, имеет первостепенное значение. После повреждения кожи закрытие раны обусловлено образованием нового эпителия за счет пролиферации и направленной миграции различных типов клеток, таких как кератиноциты или фибробласты, к краям раны [Bennet NT et al., Am J Surg 1993, 166:74-81; Wong VW et al., J Biomed Biotechnol. 2011:969618].
Графеновый продукт согласно настоящему изобретению оказался эффективным при заживлении ран в опытах на крысах и безвредным с точки зрения системных изменений почечных, гепатических или воспалительных маркеров in vivo.
Следовательно, его можно применять при лечении состояния, приводящего к нарушению целостности кожи, такого как раны, кожные ожоги и кожные язвы.
Способ применения
Применяемую в настоящем способе композицию предпочтительно наносят местно.
Суточная доза лекарственной формы для местного применения, включающая графеновый продукт согласно настоящему изобретению, может зависеть от различных факторов, таких как пол, возраст, вес и индивидуальное состояние пациента.
ПРИМЕРЫ
Пример 1:
ПОЛУЧЕНИЕ И ФИЗИКО-ХИМИЧЕСКАЯ ХАРАКТЕРИЗАЦИЯ GMC-1
Сырье
Текстурные характеристики, степень графитизации и основные физико-химические и термические свойства сырья, которое можно применять для получения графеновых наноматериалов согласно настоящему изобретению, представлены в Таблице 1 ниже.


В данном примере для получения материала согласно настоящему изобретению применяли графеновые нановолокна (GNF).
Необработанный углеродный наноматериал на основе графена (GNF) подвергали процессу очистки с использованием HF для удаления металлов и примесей, внесенных в структуру GNF в процессе синтеза. Процесс очистки проводили при низких температурах (20-50°С) в течение нескольких часов (12-24 часов). Затем очищенный углеродный наноматериал сушили в вакууме и промывали очищенной при помощи системы Millipore водой до нейтрального значения рН.
Затем очищенные GNF подвергали процессу расслоения в течение нескольких часов (2-5 часов) при комнатной температуре в растворе при помощи воды или других растворителей. В заключение материал подвергали стандартному процессу депирогенизации путем нагревания (200-500°С в течение 10-60 минут). Полученный продукт (GMC-1) был охарактеризован следующим образом: Элементный анализ GMC-1
Основное различие между GMC-1 и сырьем можно наблюдать по результатам их элементного анализа (Таблица 2). По сравнению с необработанными GNF GMC-1 состоит только из углерода и кислорода. Он не содержит следов примесей, которые могли бы нанести вред здоровью человека, что подтверждается токсикологическими экспериментами.

Рамановская спектроскопия GMC-1
Рамановский спектр GMC-1 получали с использованием лазера с длиной волны 512 нм. Он демонстрирует характерные пики углеродных материалов (Фигура 1). Пик D на 1332 см"1 и пик G на 1580 см-1. Полоса G соответствует сеткам атомов углерода, то есть идеальной графитовой структуре, а полоса D обусловлена наличием дефектов как в базисной плоскости, так и на краях. Для графеновых нановолокон полоса D имеет более высокую интенсивность, чем полоса G. Большой пик D может появляться в графитовых материалах, имеющих большое количество краев, как в случае этих нановолокон. Тот факт, что обе полосы D и G имеют не слишком большую ширину, также свидетельствует о кристалличности нановолокон.
Анализ GMC-1 методом адсорбции-десорбции азота
Основополагающим принципом измерения общей площади поверхности твердого тела путем физической адсорбции газа является определение количества молекул газа, необходимых для покрытия поверхности твердого тела. Если известна площадь, занимаемая молекулой, то площадь поверхности твердого тела можно оценить по количеству молекул поглощенного газа, измеренному волюметрическим или гравиметрическим методом (Брунауэр, Эммет и Теллер).
Общую площадь поверхности рассчитывали по многоточечному уравнению БЭТ, а общий объем пор определяли по количеству пара, адсорбированного при относительном давлении Р/Po=0,99, предполагая, что поры впоследствии заполняются жидким адсорбатом. Средний размер пор, форма которых принималась за цилиндрическую, оценивался по величине общего объема пор и площади поверхности, предполагая, что поры, не заполненные при относительном давлении менее 1, не влияли на объем и площадь поверхности пор образца.
Анализ площади поверхности, объема пор и площади пор проводили путем адсорбции-десорбции N2 при 77 К с использованием прибора QUANTACHROM QUADRASORB SI с шестью портами дегазации и тремя портами анализа под управлением программного обеспечения (QUADRAWIN), записывающего значения относительного давления для каждого дозированного объема N2. На Фигуре 2 изображены площадь поверхности, объем пор и размер пор GMC-1.
Площадь поверхности по методу БЭТ: 300-350 м2/г
Объем пор: 0,35-0,4 см3/г
Размер пор: 5-6 нм
Рентгеновская дифракция GMC-1
Была получена рентгеновская дифрактограмма, соответствующая образцу GNF (Фигура 3А). Как можно видеть, дифрактограмма содержит пик при примерно 25,9°, который соответствует расстоянию между плоскостями 002 графита, или расстоянию между листами графена. В высококристаллическом графите межслоевое расстояние составляет 0,334 нм. В данном случае нановолокна имеют немного большее расстояние, равное 0,343 нм, что указывает на то, что они обладают ближней кристалличностью и являются турбостратными. Размер кристалла в направлении, перпендикулярном плоскости 002 (Lc), составляет 4,64 нм, что свидетельствует о вышеуказанном факте.
На Фигуре 3В изображена дифрактограмма, соответствующая образцу материала согласно настоящему изобретению GMC-1. GNF и GMC-1 демонстрируют одинаковые пики, однако в GMC-1 эти пики соответствуют более низкому значению 2θ.
В Таблице 3 приведены характеристические кристаллографические параметры GNF и GMC-1:
Межслоевое расстояние (d002)
Высота стопки кристаллов (Lc)
Размер кристаллитов в плоскости (La)
Число графеновых слоев в кристалле (npg)

где:
λ - длина волны излучения (λ=0,15404 нм)
θ1 - положение дифракционного пика (°)
θ2 - положение дифракционного пика (°)
k1 - коэффициент формы (k=0,9)
k2 - постоянная коэффициента ф ормы Уоррена (k=1,84)
FWHM - ширина на половине высоты соответствующего дифракционного пика (рад)
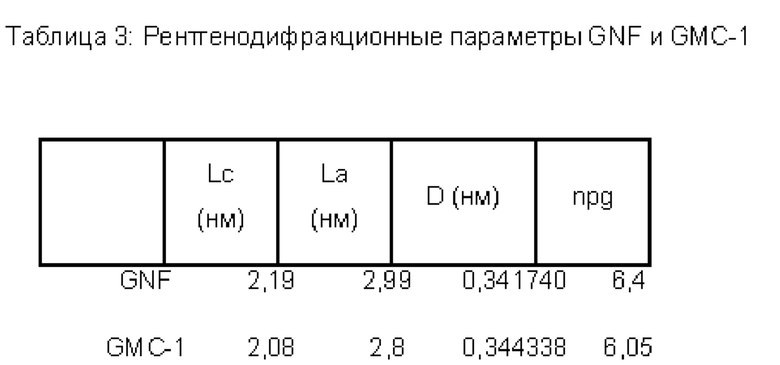
При превращении GNF в GMC-1 кристаллическая структура материала изменяется. Таким образом, в GMC-1, подвергнутом процессу очистки, промывки и расслоения, наблюдается уменьшение высоты стопки кристаллов (Lc), размера кристаллитов в плоскости (La) и числа графеновых слоев в кристалле (Nc). Межслоевое расстояние в GMC-1 увеличивается вследствие процесса расслоения, которому подвергали материал. Высота стопки кристаллов (Lc) и размер кристаллитов в плоскости (La) претерпевают уменьшение вследствие процесса очистки и расслоения.
Распределение частиц по размерам
Распределение частиц по размерам для исходного материала GNF и продукта согласно настоящему изобретению GMC-1 измеряли с помощью прибора Mastersizer 3000 от Malvern Panalytical. В приборе Mastersizer 3000 для измерения размера частиц применяется метод лазерной дифракции. Этот результат достигается путем измерения интенсивности света, рассеянного при прохождении лазерного луча через образец диспергированных частиц. Затем эти данные анализируются для расчета размера частиц, создавших картину рассеяния.
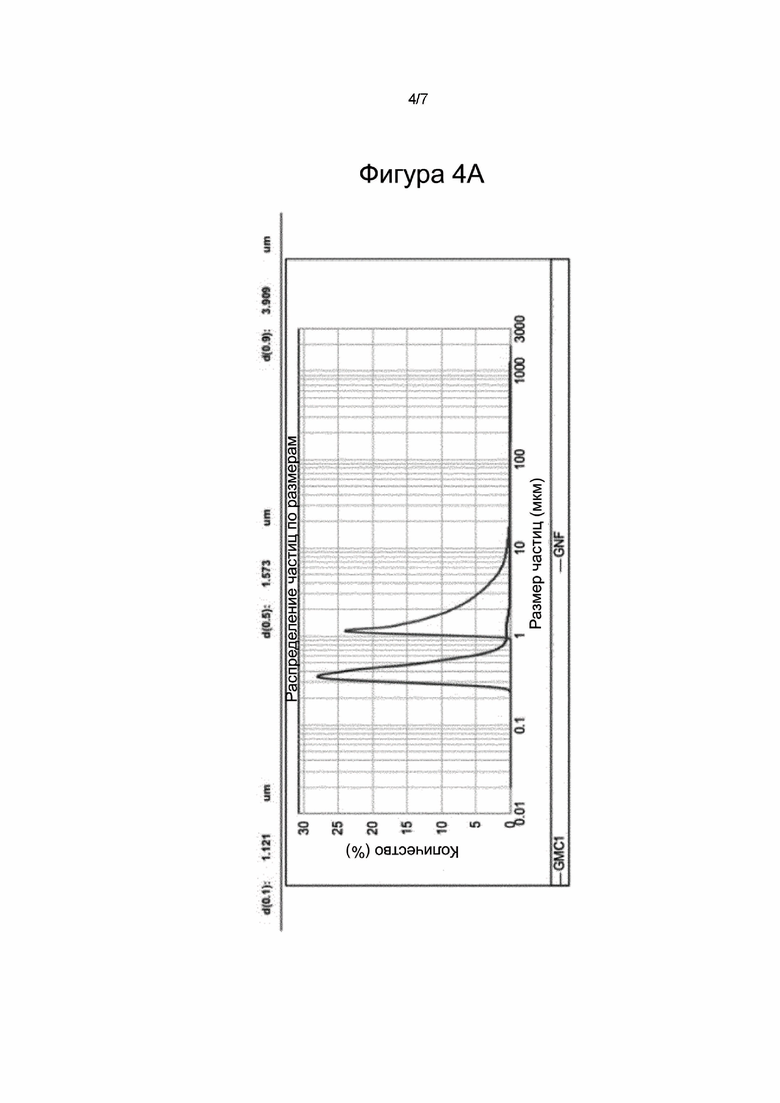
На Фигуре 4А изображено количественное распределение частиц по размерам для GNF и GMC-1.
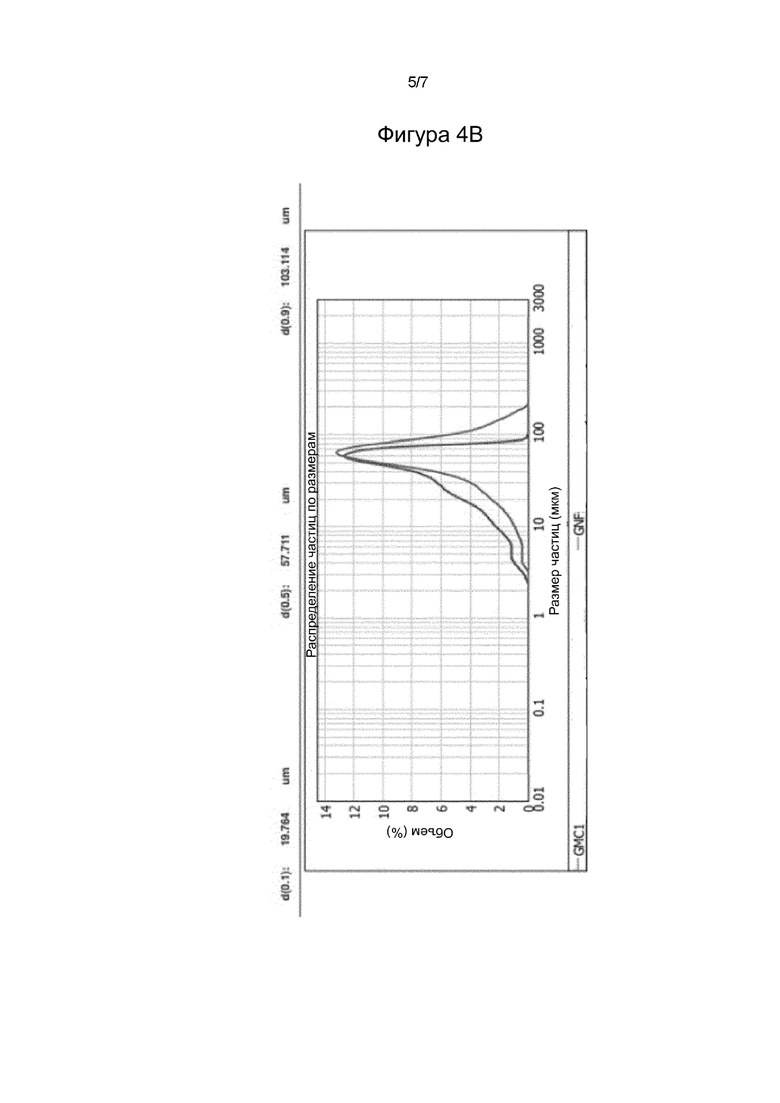
На Фигуре 4В изображено сравнение объемного распределения частиц по размерам в зависимости от процентного содержания частиц для GNF и GMC-1.
Параметры d(0,1), d(0,5) и d(0,9) показаны на Фигурах; dn относится к количеству частиц, a dv относится к объему частиц.
Для GNF параметр dn(10) означает, что 10% от числа частиц имеют размер 1,121 мкм или менее, параметр dn(50) означает, что 50% от числа частиц имеют размер 1,573 мкм или менее и параметр dn(90) означает, что 90% от числа частиц имеют размер 3,909 мкм или менее. Для GNF параметр dv(10) означает, что 10% объема образца занято частицами с размером 19,764 мкм или менее, параметр dv(50) означает, что 50% объема образца занято частицами с размером 57,711 мкм или менее и параметр dv(90) означает, что 90% образца занято частицами с размером 103,114 мкм или менее.
В случае GMC-1 параметр dn(10) означает, что 10% от числа частиц имеют размер 0,313 мкм или менее, параметр dn(50) означает, что 50% от числа частиц имеют размер 0,394 мкм или менее и параметр dn(90) означает, что 90% от числа частиц имеют размер 0,577 мкм или менее. Для GMC-1 параметр dv(10) означает, что 10% объема образца занято частицами с размером 10,549 мкм или менее, параметр dv(50) означает, что 50% объема образца занято частицами с размером 39,693 мкм или менее и параметр dv(90) означает, что 90% образца занято частицами с размером 69,576 мкм или менее.
Сравнение количественного и объемного распределения частиц по размерам между GNF и GMC-1 показывает, что GMC-1 имеет более низкое распределение частиц по размерам. Обобщая вышеизложенное, dn(90) для GNF имеет размер 3,909 мкм или менее по числу частиц, и dv(90) имеет размер 103,114 мкм или менее по объему частиц, тогда как dn(90) для GMC-1 имеет размер 0,577 мкм или менее по числу частиц, и dv(90) имеет размер 69,576 мкм или менее по объему частиц. Фигуры 4А и 4В четко демонстрируют это уменьшение числа и объема частиц в GMC-1 по сравнению с используемым сырьем (GNF).
БИОЛОГИЧЕСКАЯ АКТИВНОСТЬ
Статистика
Приведенные данные представлены как средние значения ± СОС для переменного числа экспериментов. t-Критерий Стьюдента использовался для двух выборок, а для более чем двух выборок использовался одно- или двухфакторный дисперсионный анализ (ANOVA) в парной или непарной форме с последующим критерием множественного сравнения. Статистически значимыми считались значения Р<0,05.
Пример 2: АНАЛИЗ ТОКСИЧНОСТИ НА КЛЕТОЧНЫХ ЛИНИЯХ HEP-G2
Были проведены испытания с GMC-1 на культивированных клетках (гепатоцитная линия Hep-G2), применявшихся в фармакологических и токсикологических исследованиях.
В 6-луночных чашках для культивирования высевали 300000 клеток на одну лунку и выращивали в 10% питательной среде с добавлением фетальной бычьей сыворотки (по умолчанию DMEM). Клетки поддерживали в контролируемых условиях инкубатора при 37°С, 5% CO2 и влажности. При достижении конфлюэнтности их лишали сыворотки на 16 часов. Продукт добавляли в виде суспензии при различных концентрациях, сохраняя одинаковый конечный объем, поддерживая постоянные контролируемые условия в течение 24 часов. Затем клетки обрабатывали и их жизнеспособность/токсичность испытывали при помощи двух взаимодополняющих тестов, указанных в вышеупомянутом ISO:
a) Вытеснение трипанового синего, который позволяет различить живые и мертвые клетки и
b) Метаболическая активность по окрашиванию клеток МТТ (бромид 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия).
Результаты представлены на Фигуре 5. Данные демонстрируют, что GMC-1 нетоксичен для культивированной клеточной линии Hep-G2.
Пример 3: ЗАЖИВЛЕНИЕ РАН НА ЖИВОТНОЙ МОДЕЛИ
Заживление кожных ран представляет собой универсальный регенеративный процесс закрытия раны и восстановления эпителиального барьера и подлежащей соединительной ткани.
Многие факторы и системные состояния являются причиной нарушения кожной функции. После повреждения кожи для закрытия раны должен образоваться новый эпителий.
Заживление раны включает миграцию, пролиферацию и дифференцировку клеток и образование внеклеточного матрикса. Хронические раны, такие как венозные раны, диабетическая стопа или пролежни, характеризуются незавершенными процессами заживления, включая повышенную бактериальную колонизацию и/или инфекцию, и они вызываются другими состояниями и заболеваниями, такими как сахарный диабет, травмы, воспалительные заболевания, метаболические нарушения, нарушения свертываемости крови, курение, иммуносупрессия, недоедание и ожирение.
Был проведен анализ дермальной регенерации на модели заживления ран на грызунах. Лекарственная форма GMC-1 была основана на гидрогеле с желатином в качестве основного вспомогательного вещества [X.J. Yang, et al., Polym. Int. 44 (1997) 448-452].
Использованная животная модель представляла собой Rattus norvegicus, самцов или самок в возрасте 3-8 месяцев с массой тела 300-500 в начале экспериментов, n=18). Крыс разделили на две группы, одну из которых обрабатывали лекарственной формой, содержащей продукт, а другую обрабатывали такой же лекарственной формой, не содержащей продукт. Животных анестезировали при помощи изофлурана и брили кожу спинной области. После дезинфекции 70% этанолом на кожу спинной области наносили пять глубоких ран с помощью дермальных биопсийных щипцов диаметром 4 мм. Четыре раны обрабатывали пластырем на основе лекарственной формы, который содержал или не содержал GMC-1 (контрольная группа). Пятую биопсию оставляли открытой для контроля закрытия ран. Лекарственную форму наносили раз в два дня. За закрытием ран следили с течением времени при помощи планиметрических измерений, в ходе которых делали фотографии каждой раны с использованием цифровой камеры (PowerShot Рго1, Canon) через 0-2 и 4 дня после нанесения ран. Анализировали площадь ран (Jimage, NIH). Процент закрытия раны в каждый момент времени получали по следующей формуле: (1 - [текущий размер раны/исходный размер раны]) × 100. Это значение выражено в процентах относительно значения закрытия для пятой биопсии (внутренний контроль животного).
На 4-й день животных умерщвляли, иссекали зажившую область раны, фиксировали в 10% нейтрализованном формальдегиде в течение 24 ч и заливали парафином. Срезы толщиной три мкм депарафинизировали в ксилоле, регидратировали путем последовательного погружения в растворы этанола нисходящей концентрации и проводили гистопатологические определения (реэпителизация, коллагенизация и острая воспалительная инфильтрация). Эпителизацию каждой раны оценивали на основании индивидуальных оценок, определенных путем вышеуказанного гистопатологического анализа.
Результаты представлены на Фигуре 6. При наружном применении GMC-1 регенерирует дерму in vivo.
После эвтаназии плазму и мононуклеарные клетки периферической крови (основная популяция лейкоцитов, циркулирующих в крови) консервировали и исследовали. Проводили общий биохимический анализ плазмы и исследовали разные почечные, печеночные и воспалительные маркеры (креатинин, трансаминазы и С-реактивный белок широкого диапазона). Обрабатывали мононуклеарные клетки периферической крови (РВМС) для изучения экспрессии провоспалительного маркера интерлейкина 1-бета. Это изменение экспрессии определяли с помощью количественной полимеразной цепной реакции с обратной транскрипцией (RT-qPCR). 100 нг конвертированной ДНК (кДНК) из исходной мРНК, экстрагированной из разных образцов, амплифицировали с помощью коммерческих тестов экспрессии генов (TaqMan, Life Technologies). Значения нормировали относительно эндогенного контроля (бета-актин), а затем проводили исследование кратности изменения экспрессии с использованием метода 2∧-deltadeltaCt.
Результаты представлены на Фигуре 7. Наружное нанесение GMC-1 на поврежденный участок кожи безвредно с точки зрения системных изменений почечных, печеночных или воспалительных маркеров in vivo.
| название | год | авторы | номер документа |
|---|---|---|---|
| ГРАФЕНОВЫЙ ПРОДУКТ И ЕГО КОСМЕТИЧЕСКИЕ ПРИМЕНЕНИЯ | 2019 |
|
RU2764771C1 |
| Добавки на основе графеновых наноматериалов для улучшения цементирующих композиций, цементирующая композиция, способ получения армированного бетона, армированный бетон и его применение | 2019 |
|
RU2768920C1 |
| ЧЕРНИЛА-ГЛАЗУРЬ ДЛЯ ЦИФРОВОЙ ПЕЧАТИ | 2013 |
|
RU2620808C2 |
| НОВЫЕ ЭЛЕКТРОДЫ С ПОЛИМЕРНОЙ МАТРИЦЕЙ | 2020 |
|
RU2822818C2 |
| КОНЦЕНТРИРОВАННАЯ СЕЛЬСКОХОЗЯЙСТВЕННАЯ КОМПОЗИЦИЯ | 2014 |
|
RU2619989C2 |
| СПОСОБ УЛУЧШЕНИЯ ИЗОЛИРУЮЩЕЙ СПОСОБНОСТИ ВСПЕНЕННЫХ ВИНИЛАРОМАТИЧЕСКИХ ПОЛИМЕРОВ И ТАКИМ ОБРАЗОМ ПОЛУЧЕННЫЕ ПРОДУКТЫ | 2006 |
|
RU2412218C2 |
| ВЕЕРООБРАЗНОЕ АЭРОЗОЛЬНОЕ УСТРОЙСТВО ДЛЯ УКЛАДКИ ВОЛОС | 2011 |
|
RU2623154C2 |
| УЛЬТРАЗВУКОВЫЕ КОНТРАСТНЫЕ ВЕЩЕСТВА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2004 |
|
RU2345793C2 |
| СТАБИЛЬНАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ), ЛЕКАРСТВЕННОЕ СРЕДСТВО (ВАРИАНТЫ) И СПОСОБЫ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ КОЖНЫХ ИНФЕКЦИЙ И ИНФЕКЦИЙ КОЖНЫХ СТРУКТУР, ВЫЗВАННЫХ БАКТЕРИЯМИ, ЗАБОЛЕВАНИЙ, ПЕРЕДАЮЩИХСЯ ПОЛОВЫМ ПУТЕМ, И ИНФЕКЦИЙ ПОЛОВЫХ ПУТЕЙ, ВЫЗВАННЫХ БАКТЕРИЯМИ, И ИНФЕКЦИЙ НОСОГЛОТКИ, ВЫЗВАННЫХ БАКТЕРИЯМИ, У ЧЕЛОВЕКА ИЛИ ЖИВОТНОГО | 2009 |
|
RU2478367C2 |
| ВСПЕНИВАЮЩИЕСЯ ВИНИЛАРОМАТИЧЕСКИЕ ПОЛИМЕРЫ С УЛУЧШЕННОЙ ТЕПЛОИЗОЛЯЦИЕЙ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2007 |
|
RU2406734C1 |




Изобретение может быть использовано в медицине. Предложено применение графенового наноматериала, представляющего собой графеновые нановолокна, для лечения поражений кожи, выбранных из ран, экземы, кожных ожогов и кожных язв. Графеновый наноматериал имеет количественное распределение частиц по размерам с dn(90), равным 0,60 мкм или менее, и объемное распределение частиц по размерам с dv(90), равным 80,00 мкм или менее, измеренным при помощи лазерного дифракционного анализатора размеров частиц. Также предложена фармацевтическая композиция, содержащая продукт из указанного графенового наноматериала. Изобретения позволяют обеспечить заживление ран и восстановление кожи при помощи безвредного продукта. 2 н. и 3 з.п. ф-лы, 7 ил., 3 табл., 3 пр.
1. Применение графенового наноматериала, представляющего собой графеновые нановолокна, где указанный графеновый наноматериал имеет количественное распределение частиц по размерам с dn(90), равным 0,60 мкм или менее, и объемное распределение частиц по размерам с dv(90), равным 80,00 мкм или менее, измеренным при помощи лазерного дифракционного анализатора размеров частиц, для лечения поражений кожи, выбранных из ран, экземы, кожных ожогов и кожных язв.
2. Фармацевтическая композиция для лечения поражений кожи, выбранных из ран, экземы, кожных ожогов и кожных язв, содержащая продукт из графенового наноматериала, определенного в п. 1, и фармацевтически приемлемое вспомогательное вещество.
3. Фармацевтическая композиция по п. 2, подходящая для местного применения.
4. Фармацевтическая композиция по п. 3, отличающаяся тем, что указанная композиция представлена в форме, выбранной из крема, мази, микроэмульсии, геля, эмульсии-геля, пасты, пены, настойки, пластыря, повязки, мембраны, матрицы или трансдермальной системы доставки.
5. Фармацевтическая композиция по п. 4, отличающаяся тем, что указанная композиция представляет собой гидрогель или крем.
| SANGILIYANDI GURUNATHAN et al., Synthesis, toxicity, biocompatibility, and biomedical applications of graphene and graphene-related materials, International Journal of Nanomedicine, 2016, v | |||
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| Паровая радиальная турбина двойного вращения | 1925 |
|
SU1927A1 |
| WO 2015034930 A1, 12.03.2015 | |||
| СПОСОБЫ ИЗГОТОВЛЕНИЯ ГРАФЕНОВЫХ НАНОЛЕНТ С ПРИМЕНЕНИЕМ РАСТВОРИТЕЛЯ | 2012 |
|
RU2609915C2 |
| СПОСОБ ПРЯДЕНИЯ ВОЛОКОН ИЗ ГРАФЕНОВЫХ ЛЕНТ | 2011 |
|
RU2550850C2 |
| CN 106521719 A, 22.03.2017 | |||
| CN 103482620 B, 20.01.2016. | |||
Авторы
Даты
2022-01-28—Публикация
2019-07-17—Подача