Изобретение относится к области аналитической химии, точнее к ионометрии, способу количественного определения одного из цефалоспориновых антибиотиков цефтриаксона (Ceftr) в жидкости ротовой полости (ЖРП) и в цельной крови больных ковидом. Изобретение также может использоваться в медицине для токсического и технического анализа лекарственных средств, в биосистемах (сыворотке крови, слюне и т.д.) а также для фармакокинетических исследований с целью регулирования введения оптимальных доз антибиотика при лечении различных инфекционных заболеваний.
Антибиотики применяются в медицине, ветеринарии, пищевой промышленности при консервировании, для обработки пищевых продуктов при их транспортировке. В связи с этим требуется контроль содержания Ceftr в лекарственных формах, в биологических жидкостях организма человека и животных, продуктов питания, сточных водах фармацевтических предприятий и других объектов.
Аналоги
Из уровня техники известны различные способы количественного определения антибиотиков: микробиологические, спектрофотометрические, флуориметрические, хемилюминесцентные, различные варианты хроматографических методов, в т.ч. высокоэффективная жидкостная хроматография (ВЭЖХ), хроматомасспектрометрия, инверсионная вольтамперометрия, электроаналитическое определение с модифицированными электродами.
Для определения β-лактамных антибиотиков применяют спектроскопические способы, основанные на использовании определенных свойств антибиотиков: собственное поглощение, цветные реакции, появление или исчезновение характерных полос в УФ, видимой или ИК-областях спектра под воздействием различных реагентов.
Известен спектрофотометрический способ определения антибиотиков пеницилленовой группы - ампициллина, амоксициллина, клоксациллина, сулбенициллина, карбенициллина, тикарциллина в готовых лекарственных формах (Amin A.S. Pyrocatechol violet in pharmaceutical analysis. Part I. A spectrophotometric method for the determination of some pMactam antibiotics in pure and in pharmaceutical dosage forms // Farmaco. - 2001. - V. 56, №3. - P. 211-218), основанный на измерении поглощения (λ=323-346 нм) продуктом реакции пенициллинов с раствором 1,2,4-триазола, содержащим хлорид ртути (II). Данный способ применим преимущественно для определения вещества в лекарственных формах, составляющих его основу.
Известны спектрофотометрический и спектрофлуориметрический способы определения 4 пенициллинов (амоксициллина, бакампициллина, пиперациллина и сультамициллина) и 10 цефалоспориновых антибиотиков в фармацевтических препаратах, которые основаны на окислении антибиотиков церием (IV) в среде ОДМ H2SO4 при 100°С. Способы включают операцию измерения уменьшения светопоглощения церия (IV) при λ=317 нм или интенсивности флуоресценции образовавшегося церия (III) при длинах волн возбуждения и испускания 256 и 356 нм.
Belal S. Use of cerium (IV) in the spectrophotometric and spectrofluorimetric determinations of penicillins and cephalosporins in their pharmaceutical preparations // Spectrosc Lett, 2000. - Vol. 33. - №6. - P. 931-948).
Известен спектрофотометрический способ определения ампициллина, амоксициллина и карбенициллина с применением фенольного реактива Фолина-Чокальтеу (Ахмад А.С., Рахман Н., Ислам Ф. Спектрофотометрическое определение ампициллина, амоксициллина и карбенициллина с применением фенольного реактива Фолина-Чокальтеу // Журн. аналит. химии, 2004. - Т. 12. - №2. - С. 138-142). Смесь определяемых пенициллинов с реактивом при рН 2,25 нагревают в термостатируемой водяной бане при 95±2°С и возникающую синюю окраску образующихся гетерополисоединений измеряют спектрофотометрически при λ=750 нм для ампициллина и карбенициллина и при λ=770 нм для амоксициллина.
Известен способ определения натриевых солей цефотаксима и моногидрата цефадроксила в двух составляющих смесях методом производной спектрофотометрии (Morelli В. Derivative spectrophotometry in the analysis of mixtures of cefotaxime sodium and cefadroxil monohydrate // J Pharm and Biomed Anal., 2003. - Vol. 32. - №2. - P. 257-267). Способ заключается в снятии спектров поглощения антибиотиков и оценке первой и второй производных спектров поглощения. Пределы чувствительности от 0,28 до 0,51 мг/мл.
Разработаны потенциометрические сенсоры на основе ионных ассоциатов цефуроксима с катионами тетраалкиламмония. Сенсоры обеспечивают широкий диапозон определяемных содержаний антибиотиков 1⋅10-4-1⋅10-2 М; предел обнаружения антибиотиков составляет 8⋅10-6М. (О.И. Кулапина, М.С. Михайлова, Е.Г. Кулапина Ионометрическое определение цефуроксима и цефуроксим аксетила в биологических и лекарственных средах // Известия Саратовского ун-та. Сер. Химия. Экология. 2013. Т. 15. вып. 3. С. 40-45).
Сенсоры для определения цефуроксима и цефуроксим аксетила позволяет определять в биологический средах (ротовой жидкости) для корректировки и оптимизации курса лечения, а также для определения основного вещества в лекарственных препаратах. Известен также способ определения цефазолина в биологических средах с применением ионселективных электродов (О.И. Кулапина, В.В. Барагузина, Н.В. Скобликова. Определение цефазолина в биологических средах с применением ионселективных электродов // Химико-фармацевтический журнал. 2008. Т. 42, №8. С. 41-44).Оценено соотношение компонентов в ионном ассоциате, растворимость, термическая устойчивость до 70 градусов. Показано, что зависимость ЭДС от концентрации цефазолина выполняется в интервале 1⋅10-1-1⋅10-5 моль; угловой коэффициент электродных функций составляет 56±2 мВ/рС. Ксел.к некоторым неорганическим ионам (CI-, Br-, НСО3-, НРО42-, SO42-) позволяет использовать данные электроды для определения цефазолина в биологических жидкостях.
Критика аналогов
Однако фармакокинетические исследования, проводимые на биологических средах, требуют определения низких концентраций антибиотиков Cmin<10 мкг/мл, а следовательно, для данных целей необходим более чувствительный и экспрессный метод.
Известные способы предназначены для определения антибиотиков в лекарственных средах и в силу недостаточной чувствительности и длительности не могут быть использованы для анализа биологических сред на содержание антибиотиков.
Однако обычно применяемые наполнители фармацевтических композиций (например, сахар) влияют на результат определения, поэтому такие наполнители должны быть удалены из анализируемых материалов перед определением пенициллинов в капсулах и таблетках. Метод предложен для определения антибиотиков в модельных растворах. Данный способ характеризуется также длительностью процесса, требует операции нагрева, которая отрицательно сказывается на состоянии антибиотика и, следовательно, на метрологических параметрах методики определения. В последних аналогах отсутствует интервал кислотности при которых должен функционировать разработанные электроды. Интервал определяемых концентраций варьируется в двух порядках. Не изучена селективность к антибиотикам бета-цифолоспаринового ряда.
Прототип
Наиболее близким к предлагаемому техническому решению является определение цефтриаксона в крови и тканях методом ионообменной хроматографии (В.В. Хасанов, Е.Г. Соколович, К.А. Дычко // Химико-фармацевтический журнал. Том 40. №2, 2006), который выбран в качестве прототипа.
Прототип заключается в следующем.
Процедура определения включает предварительную твердофазную экстракцию на концентрирующем патроне из небольшого объема крови (200 мкл) с последующей обращенно-фазовой ВЭЖХ с ион-парным модифицированием. Механизм разделения комплексный с участием электростатических взаимодействий анионов цефтриаксона с положительно заряженной аминогруппой. Предел обнаружения цефтриаксона составил 0,4 мкг/мл в плазме крови и 0,03 мг/л в слюне (табл. 1.). Рабочий раствор устойчив при хранении в темноте при 4° в течение 10 час.
Образцы печени, легких в крови были взяты у здоровых Kpbic (Vistar, Maccoft тела 250-280 г) спустя различное время после внутримышечного введения цефтриаксона в дозе 25 мг/кг веса. Образец ткани взвешивался, замораживался в жидком азоте, после заливали физиологическим раствором, тщательно гомогенизировали и центрифугировали 5 мин. при 6000 мин-1. Надосадочную жидкость отбирали и смешивали ацетонитрилом в соотношении 1:3, фильтровали через мембрану 0.45 мкм и вводили в колонку. Образцы крови смешивали с ацетонитрилом (1:3), тщательно перемешивали и центрифугировали, супернатант далее обрабатывали, как указано выше. Подготовленные образцы загружались в колонку с использованием петли для ввода образца постоянного объема 100 или 500 мкл. Калибровочный график оказался линейным в диапазоне цефтриаксона 10-400 нг в колонке с коэффициентом корреляции 0,999.
Критика прототипа
Так как цефтриаксон - высокополярное соединение, он трудно экстрагируется из биологических жидкостей. Пробоподготовка обычно содержит депротенизацию этанолом, ацетонитрилом или метанолом, а раствор цефтриаксона неустойчив в спирте, поэтому анализ необходим проводить в течение 2-х часов. При увеличении концентрации противоионов, а также защелачивании среды возможно повреждение наполнителя колонки.
Таким образом применение прототипа для определения цефтриаксона очень длителен, требует дорогостоящей аппаратуры, многостадийная подготовка пробы, интервал определяемых концентраций узок (табл. 1).
Цель изобретения
Целью изобретения является разработка экспресс способа ионометрического определения цефтриаксона для регулирования введения оптимальных доз антибиотика при лечении различных инфекционных заболеваний, в том числе у больных ковидом, а также при исследовании фармакокинетики.
Задачей предлагаемого изобретения является создание экспрессного, доступного, недорогого количественного способа определения цефалоспоринового антибиотика, в частности цефтриаксона цефтриаксон-селективным электродом (Ceftr-СЭ) в биологических средах в т.ч. жидкости ротовой полости, плазме крови и др.
Сущность изобретения
Предлагается экспресс способ количественного определения цефтриаксона, включающий отбор проб реальных объектов, содержащих Ceftr у больных ковидом, пробоподготовка и измерение разности потенциала (ЭДС) электрода сравнения и индикаторного электрода с мембраной на основе электродноактивного компонента (ЭАК) в виде ионного ассоциата цефтриаксона и октадециламина(ОДА). Ионометрическое определение Ceftr проводят по градуировочному графику, построенному по эталонным растворам, в диапозоне рН 7-8, при этом градировочный график строят по измеренным значениям электродного потенциала от концентраций Ceftr в эталонных растворах; а при использовании в качестве пробы цельной крови предварительно осаждают белок по ГОСТу и удаляют форменные элементы. Вышеописанный способ позволяет в течение 1 мин определить содержания Ceftr, при этом отпадает применение дорогостоящихся приборов, органических растворителей, отсутствует многостадийность процесса, уменьшается время и погрешность обнаружения, повышается точность определения.
Поставленная задача решается тем, что способ количественного определения цефалоспоринового антибиотика в биологических средах проводят отбор пробы биологической среды, содержащей цефтриаксон, ее пробоподготовки, включающей удаление твердых элементов с последующим осаждением и удалением белков, измерения равновесного потенциала (ЭДС) и определения концентрации антибиотика по градуировочному графику (фиг. 1), построенному по эталонной среде, в качестве которой используют биологическую среду без содержания цефтриаксима, прошедшую аналогичную пробоподготовку, с последующим введением в подготовленную пробу раствора определяемого антибиотика в различных концентрациях, при этом градуировочный график строят по измеренным значениям потенциала цефтриаксон-селективного электрода относительно электрода сравнения в зависимости от содержания цефтриаксона в исследуемом растворе. Для удаления твердых элементов из пробы биологической среды без содержания антибиотика и с содержанием антибиотика, пробу предварительно центрифугируют 10-20 мин при 2000-3500 об/мин, а осаждение белков проводят сульфатом цинка в среде гидроксида натрия, удаление белков осуществляют центрифугированием в течение 10-20 мин при 2000-3500 об/мин. В качестве биологической среды может быть использована жидкость ротовой полости и плазма крови или цельная кровь, при этом в процессе пробоподготовки из жидкости ротовой полости удаляют твердые остатки пищи, а из цельной крови - форменные элементы.
Предлагаемый способ заключается в следующем: сначала готовят раствор цефтриаксона с концентрацией 0,1 М, растворением рассчитанного количества в дистиллированной воде, затем последовательным разбавлением готовят растворы меньших концентраций 1⋅10-2; 1⋅10-3; 1⋅10-4; 1⋅10-5 М. Далее помещают различные количества препарата в стакан, емкостью 25 мл и до 2-3 мл добавляют биологической среды, например смешанной слюны (жидкости ротовой полости - ЖРП) или сыворотки крови практически здорового человека (не принимающего в течение 7-10 дней цефтриаксона). Объем исследуемого раствора задается объемом мерной колбы на 25 мл, в которой осуществляют перемешивание компонентов. Затем готовят пробы больных ковидом, проводивших лечение цефтриоксоном, центрифугируют и осаждают белки при аналогичных режимах, измеряют равновесный потенциал относительно биопробы без антибиотика и по градуировочному графику. На фиг. 1 отражен градуировочный график для определения содержания цефтриаксона с содержанием Ceftr 10 и 50 ммоль/л в мембране. По фиг. 1 рассчитывают содержание цефтриаксона в исследуемой среде.
Примеры конкретного выполнения способа
Пример 1.
Для проведения экспресс способа определения цефтриаксона в смешанной слюне больных ковидом-19, проводили отбор проб смешанной слюны у больного ковид-19 путем забора ротовой жидкости в сухие полиэтиленовые пробирки. Пробу отбирали спустя 1-2 часа после приема пищи, перед сбором ротовую полость ополаскивали водой. Пробу ЖРП центрифугировали в течение 15 минут при 3500 об/мин. Затем добавляли в пробу 1 мл NaOH (с=0,12 моль/л) и 4 мл ZnSO4 (с=5,4 г/л) и нагревали на водяной бане. После осаждения белков отбирали надосадочную жидкость и снова центрифугировали 15 минут при 3500 об/мин.
Концентрацию цефтриаксона в смешанной слюне определяли способом градуировочного графика. Для приготовления серии водных растворов цефтриаксона навеску порошка 1,4439 г, растворяли в мерной колбе вместимостью 25 мл и до метки доводили дистиллированной водой (концентрации исходного раствора 1⋅10-1 М, разбавляя на порядок получали растворы нужной концентраций). Отбирали 2,5 мл исходного раствора Ceftr в мерную колбу вместимостью 25 мл, получали раствор с концентрацией 1⋅10-2 М. и т.д.
Минимально определяемое содержание антибиотика составило 0,05 мкг/мл.
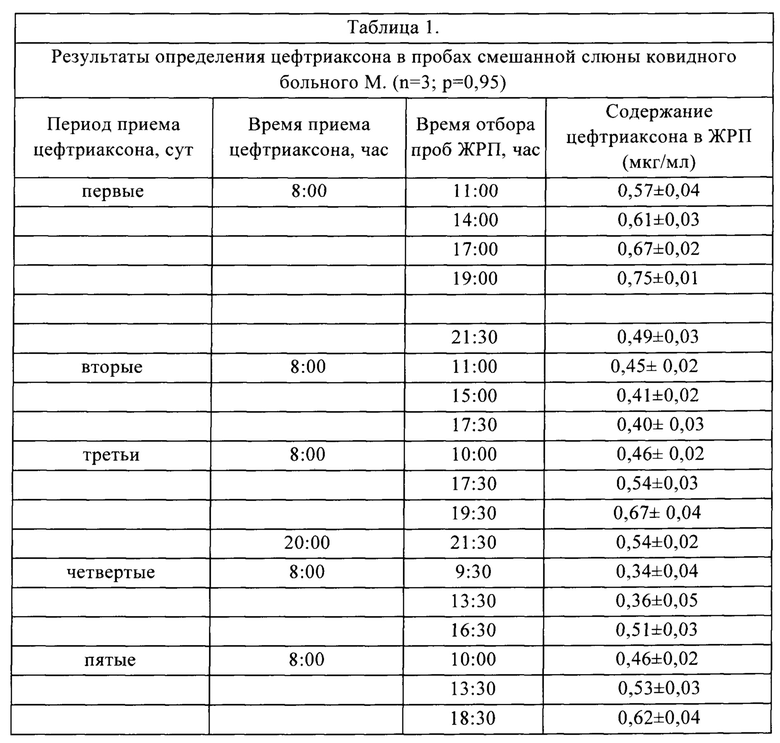
Потенциометрические исследования проводили с помошью 8-Канальной компьютеризованной системы сбора потенциометрических данных на базе ПК, Экотест-120 и коммутатора КМ-8 (НПП «ЭКОНИКС», Москва, Россия); Для отделения белковых компонентов из смешанной слюны использовали центрифугу Wirowka MPW-6. Результаты определения цефтриаксона в смешанной слюне больного М. приведены в таблице 1.
В таблице 1 представлена зависимость концентрации цефтриаксона в смешанной слюне больного М. от времени забора пробы. Показано, что максимальная концентрация Ceftr в ЖРП достигается к 18-19 часам после приема в 8 часов утра 20 мг препарата, затем происходит уменьшение концентрации до начальных значений. После вечернего приема 20 мг Ceftr концентрация препарата в ЖРП снова повышается.
С учетом сложности анализируемых объектов и самого определяемого вещества достоверность полученных результатов при реализации способа оценивалась методом «введено-найдено». Погрешность определения не превышала 4%.
Полученные данные свидетельствуют о возможности ионометрического определения цефтриаксона в жидкости ротовой полости больных ковидом при фармакокинетических исследованиях.
Пример 2.
Для ионометрического определения цефтриаксона в сыворотке крови больного ковидом способ был опробован на сыворотке крови здорового человека с внесенными добавками цефтриаксона. Кровь (4-5 мл), отобранную из локтевой вены, выдерживали в течение 30 минут без стабилизатора при комнатной температуре, затем центрифугировали для отделения форменных элементов. Осаждение белков, измерения ЭДС, построение градуировочных графиков проводили по технологиям, представленным в примере 1. Результаты потенциометрического поведения цефтриаксима в сыворотке крови характеризовались параметрами, аналогичными Примеру 1. Правильность результатов определения цефтриаксона контролировали с применением методом добавок по формуле:

Результаты определения цефтриаксона в пламе крови больного ковидом М. методом «введено найдено» приведены в таблице 2.
Технический результат, полученный от применения предлагаемого способа
Техническим результатом заявляемого способа является сокращение времени определения цефтриоксима, повышение интервала обнаружения цефтриаксона и оптимизации метрологических характеристик способа (увеличение точности, снижение погрешности определения результатов) (табл. 1).
Кроме того, одним из преимуществ заявляемого способа является возможность использования в качестве биологической среды смешанной слюны, что, по сравнению с анализом крови, характеризуется безболезненностью взятия пробы, простотой, удобством, отсутствием риска внесения инфекции, невозможностью травмы кожи и стенки сосудов, адекватностью концентрации вещества фармакотерапевтическому эффекту в полости рта.
Таким образом, заявляемый способ расширяет функциональные возможности экспрессного определения цефтриаксона в биологических жидкостях за счет расширения спектра используемых объектов цефалоспоринового антибиотика. Способ отличается высокой экспрессностью, возможностью определения активной концентрации антибиотика в широком концентрационном интервале, простотой, доступностью и дешевизной.
Диапазон определяемых концентраций 0,05-55,4 мкг/мл дает возможность определения Ceftr в смешанной слюне и крови больных при инфекционных заболеваниях, например у больных ковидом. Сравнительная характеристика хроматографического и ионометрического способов определения цефтриаксона дана в таблице 3. Таким образом, способ отличается высокой экспрессностью, дешевизной и широким диапазоном определяемых содержаний.
Полученные данные свидетельствуют о возможности экспрессного определения цефтриаксона в плазме крови с применением цефтриаксон-селективного электрода. В отличие от других цефалоспоринов цефтриаксон характеризуется большим периодом полураспада (7-8 ч.), из-за чего рекомендуется ежедневный контроль при употреблении этого препарата. Спустя сутки концентрация антибиотика в плазме крови достигает в пределах 10 мкг/мл (табл. 2).


| название | год | авторы | номер документа |
|---|---|---|---|
| МЕМБРАНА ИОНОСЕЛЕКТИВНОГО ЭЛЕКТРОДА ДЛЯ ОПРЕДЕЛЕНИЯ ЦЕФАЛОСПОРИНОВЫХ АНТИБИОТИКОВ В ЛЕКАРСТВЕННЫХ И БИОЛОГИЧЕСКИХ СРЕДАХ | 2011 |
|
RU2469304C1 |
| Мембрана ионселективного электрода для определения цефтриаксона в биосистемах | 2022 |
|
RU2789107C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ЦЕФАЛОСПОРИНОВЫХ АНТИБИОТИКОВ В БИОСРЕДАХ | 2010 |
|
RU2445624C2 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ АМИНОГЛИКОЗИТНЫХ АНТИБИОТИКОВ В ЛЕКАРСТВЕННЫХ И БИОЛОГИЧЕСКИХ СРЕДАХ | 2003 |
|
RU2235995C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ БИОЦИДНОГО АЗОТСОДЕРЖАЩЕГО ОРГАНИЧЕСКОГО СОЕДИНЕНИЯ В ВОДНОМ РАСТВОРЕ ЭТОГО СОЕДИНЕНИЯ | 2013 |
|
RU2567335C2 |
| Способ обнаружения биоцидного азотсодержащего органического соединения в водном растворе этого соединения | 2015 |
|
RU2611047C2 |
| Способ определения лекарственного препарата метформин в смешанной слюне пациента, страдающего сахарным диабетом | 2019 |
|
RU2705363C1 |
| СПОСОБ ИОНОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ЖЕЛЕЗА (III) | 2010 |
|
RU2444728C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ ЦЕФТРИАКСОНА В СЫВОРОТКЕ КРОВИ ЧЕЛОВЕКА | 2022 |
|
RU2805079C1 |
| Способ количественного определения биоцидного азотсодержащего органического соединения гидразида изоникотиновой кислоты (изониазида) в водном растворе этого соединения | 2016 |
|
RU2633080C2 |

Изобретение относится к медицине, а именно к аналитической химии, ионометрии, и может быть использовано для определения цефтриаксона в смешанной слюне и плазме крови. Осуществляют осаждение, удаление белков и форменных элементов, построение и определение концентраций антибиотика по градуировочному графику ЭДС, мВ. 2 мл биологической жидкости помещают в емкость размером 25 мл, доводят рН до 7-8, опускают в раствор цефтриаксон-селективный электрод с мембраной на основе электродноактивного компонента в виде ионного ассоциата цефтриаксона и октадециламина, и электрод сравнения. В течение одной минуты определяют содержание цефтриаксона в исследуемой среде. Способ обеспечивает возможность сокращения времени определения цефтриаксона, повышения интервала обнаружения цефтриаксона и оптимизации метрологических характеристик способа (увеличение точности, снижение погрешности определения результатов) за счет ионометрического количественного определения содержания цефалоспоринового антибиотика - цефтриаксона с помощью цефтриаксон-селективного электрода в смешанной слюне и плазме крови пациента в течение одной минуты. 1 ил., 3 табл., 2 пр.
Экспресс-способ определения цефтриаксона в смешанной слюне и плазме крови, включающей осаждение, удаление белков и форменных элементов, построение и определение концентраций антибиотика по градуировочному графику ЭДС, мВ, отличающийся тем, что 2 мл биологической жидкости помещают в емкость размером 25 мл, доводят рН до 7-8, опускают в раствор цефтриаксон-селективный электрод с мембраной на основе электродноактивного компонента в виде ионного ассоциата цефтриаксона и октадециламина, и электрод сравнения, и в течение одной минуты определяют содержание цефтриаксона в исследуемой среде.
| Линия задержки изменяющихся во времени сигналов | 1961 |
|
SU151112A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ТЕТРАЦИКЛИНОВ С ПОМОЩЬЮ ПЬЕЗОЭЛЕКТРИЧЕСКОГО СЕНСОРА | 2017 |
|
RU2687742C1 |
| МЕМБРАНА ИОНОСЕЛЕКТИВНОГО ЭЛЕКТРОДА ДЛЯ ОПРЕДЕЛЕНИЯ ЦЕФАЛОСПОРИНОВЫХ АНТИБИОТИКОВ В ЛЕКАРСТВЕННЫХ И БИОЛОГИЧЕСКИХ СРЕДАХ | 2011 |
|
RU2469304C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ЛЕВОМИЦЕТИНА В ПИЩЕВЫХ ПРОДУКТАХ И ФАРМПРЕПАРАТАХ | 2000 |
|
RU2180748C1 |
| RU 2019129941 A, 24.03.2021 | |||
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ АМИНОГЛИКОЗИТНЫХ АНТИБИОТИКОВ В ЛЕКАРСТВЕННЫХ И БИОЛОГИЧЕСКИХ СРЕДАХ | 2003 |
|
RU2235995C1 |
| Электрохимический способ определения концентрации эритромицина | 1981 |
|
SU987503A1 |
| TUTUNATU B | |||
| et al | |||
| Ceftriaxone Degradation in the Presence of Sodium Halides Investigated by Electrochemical Methods Assisted by UV-Vis Spectrophotometry | |||
Авторы
Даты
2022-05-12—Публикация
2021-07-06—Подача