Изобретение относится к области органической химии, к новым биологически активным веществам класса замещенных 4,5-дигидрофуран-2,3-дионов, а именно к 5-гидрокси-4-{[(4-метоксифенил)(4-нитрофенил)амино]метилиден}-5-(трифторметил)дигидрофуран-2,3-диону (1), формулы:
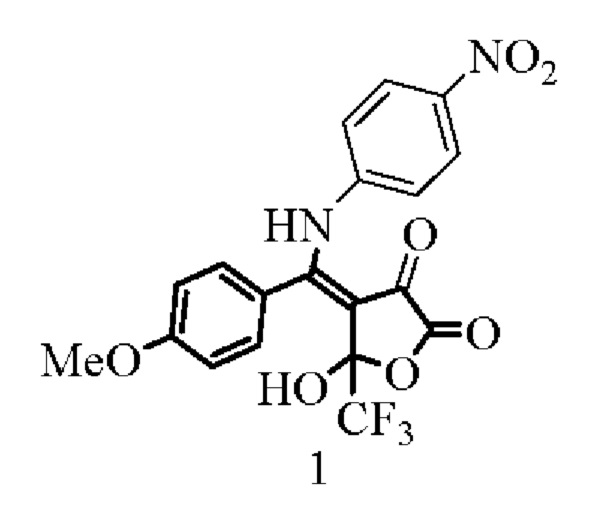
обладающему противомикробной активностью, что позволяет предположить его использование в медицине в качестве противомикробного препарата.
Аналогом по структуре заявляемому соединению является 3-[(тиен-2-ил)(4-этоксифенил)метил]дигидрофуран-2,5-дион, проявляющий противомикробную активность [Raghavendra K.R. An accessible route for the synthesis of novel lignan derivatives and their biological evaluation / K.R. Raghavendra, N. Renuka, K.A. Kumar, S. Shashikanth // Pharm. Chem. J. - 2017 - Vol. 51, №. 8 - P. 661-669] формулы:
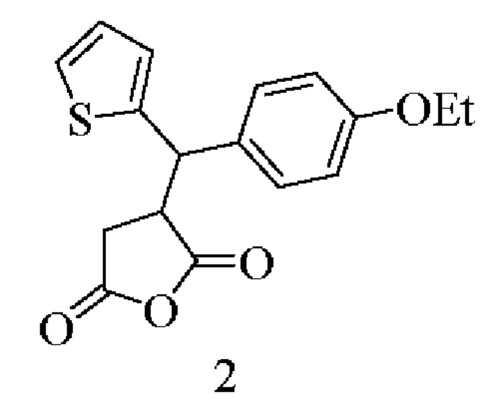
В качестве эталона сравнения противомикробной активности взяты фенилсалицилат и флуконазол [М.Д. Машковский, Лекарственные средства. - М.: Новая волна, 2012 - с. 950, 920].
Целью предлагаемого изобретения является поиск в ряду замещенных 4,5-дигидрофуран-2,3-дионов веществ с выраженной противомикробной активностью.
Поставленная задача достигается получением 5-гидрокси-4-{[(4-метоксифенил)(4-нитрофенил)амино]метилиден}-5-(трифторметил)дигидрофуран-2,3-диона, который обладает противомикробной активностью.
Заявляемое вещество (1) синтезируют взаимодействием 5-(4-метоксифенил)-4-(2,2,2-трифторацетил)фуран-2,3-диона (Н.Ю. Лисовенко, Е.П. Козлова, С.С. Харитонова, М.В. Дмитриев Взаимодействие 5-замещенных 4-(трифторацетил)фуран-2,3-дионов с основаниями Шиффа / ЖОрХ. 2018. Вып. 5. С. 705-709.) с 4-нитроанилином при перемешивании в среде абсолютного хлороформа с последующим выделением целевого продукта известными методами по схеме:
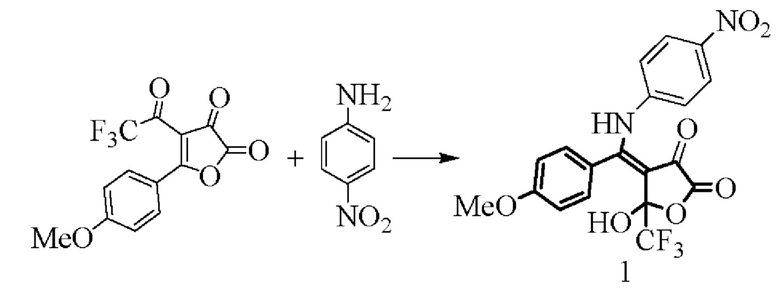
Технический результат заключается в расширении арсенала средств воздействия на живой организм.
Изобретение иллюстрируется следующими примерами:
Пример 1. Получение соединения (1).
К раствору 2 ммоль 5-(4-метоксифенил)-4-(2,2,2-трифторацетил)фуран-2,3-диона в 5 мл абсолютного хлороформа при перемешивании прикапывают раствор 2 ммоль 4-нитроанилина в 5 мл абсолютного хлороформа. Реакционную смесь оставляют при перемешивании на 3-5 часов. По истечении времени осадок отфильтровывают и перекристаллизовывают из толуола. Выход 80%. Тразл.=180-182°С. (ИК спектр (ФСМ 1202, вазелиновое масло, ν, см-1): 3217 уш. (NH, ОН), 1799 (С2=O), 1609 (С3=O). Спектр ЯМР ТТ, (Braker Avance III HD (рабочая частота 400 MHz), внутренний стандарт - ТМС, ДМСО-d6, δ, м.д.): 3.79 с (3Н, СН3О), 6.97 д (2Н, Наром., J 8.0 Гц), 7.18 д (2Н, Наром., J 8.0 Гц), 7.81 д (2Н, Наром., J 8.0 Гц), 8.09 д (2Н, Наром, J 8.0 Гц), 8.30 уш. с (1H, ОН), 10.56 с (1H, NH). Спектр ЯМР 13С, (Bruker Avance III HD (рабочая частота 100 MHz), внутренний стандарт - ТМС, ДМСО-d6, δ, м.д.): 55.6, 100.1, 112.3, 113.8, 114.0, 117.7, 124.3, 126.2, 128.0, 129.4, 131.4, 135.7, 140.5, 147.0, 155.5, 163.8, 164.1, 165.2, 186.4. Спектр ЯМР 19F, (Bruker Avance III HD (рабочая частота 376 MHz), внутренний стандарт - ТМС, ДМСО-d6, δ, м.д.): -80.89. Найдено, %: С, 52.06; Н, 2.99; F, 13.00; N, 6.39; О, 25.55. C19H13F3N2O7. Вычислено, %: С, 52.06; Н, 2.97; F, 13.01; N, 6.39; О, 25.57.
Полученное соединение (1) представляет собой ярко-желтое кристаллическое вещество, хорошо растворимое в этилацетате, ацетоне и ДМСО, трудно растворимое в хлороформе, ацетонитриле и толуоле и нерастворимое в гексане и воде.
Пример 2. Противомикробная активность соединения (1).
Противомикробные свойства заявленного соединения (1) изучали на 3-х коллекционных условно-патогенных штаммах микроорганизмов: Staphylococcus aureus (штамм 906), Escherichia coli (штамм 1257) и Candida albicans (РКПГУ 1353/1277).
Для исследования противомикробного действия использовали общепринятый метод двукратных серийных разведений в жидкой питательной среде микрометодом [Хабриев Р.У. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. - М.: И-во Медицина, 2005. - 832 с.]. Готовили исходные разведения микроорганизмов в физиологическом растворе из суточной агаровой культуры по оптическому стандарту мутности (ОСО) на 5 ME с использованием денситометра. После ряда разведений конечная концентрация клеток в опыте составляла 2.5×105 клеток/мл. В лунках стерильного 96 луночного плоскодонного микропланшета готовили два параллельных ряда двукратных серийных разведений химических соединений в бульоне РПБ, Сабуро. В каждой лунке содержалось 150 мкл определенной концентрации испытуемого вещества и 150 мкл инокулята культуры. В последних рядах содержалась питательная среда и культура в равных объемах (контроль). Максимально испытанная концентрация соответствовала 1000.0 мкг/мл, минимальная - 1.0 мкг/мл. Результаты оценивали с помощью программного обеспечения Gen 5 спектрофотометра для микропланшет Epoch. Последняя лунка ряда с задержкой роста и показателями ОП равной оптической плотности контрольной лунки соответствовала минимальной подавляющей концентрацией соединения.
Проведенные исследования показали (см. таблицу), что заявленное соединение (1) ингибирует рост бактерий Staphylococcus aureus в концентрации 125,0 мкг/мл, обладает фунгистатическим действием в отношении культуры Candida albicans в концентрации 250,0 мкг/мл, проявляет слабую бактериостатическую активность в отношении бактерий Escherichia coli в концентрации 500,0 мкг/мл.
Результаты исследований по заявленному соединению (1) изложены в таблице 1.
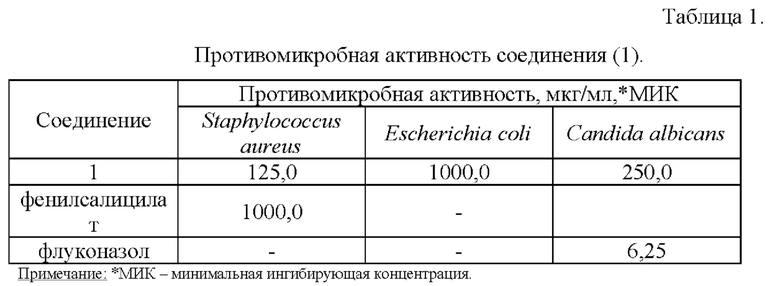
Заявленное соединение 5-гидрокси-4-{[(4-метоксифенил)(4-нитрофенил)амино]метилиден}-5-(трифторметил)дигидрофуран-2,3-дион, обладающее противомикробной активностью, может найти применение в фармакологии, медицине и ветеринарии.
Изобретение относится к 5-гидрокси-4-{[(4-метоксифенил)(4-нитрофенил)амино]метилиден}-5-(трифторметил)дигидрофуран-2,3-диону формулы (1), проявляющему противомикробную активность. Технический результат заключается в противомикробной активности, обеспечиваемой соединением формулы (1). 1 табл., 2 пр.
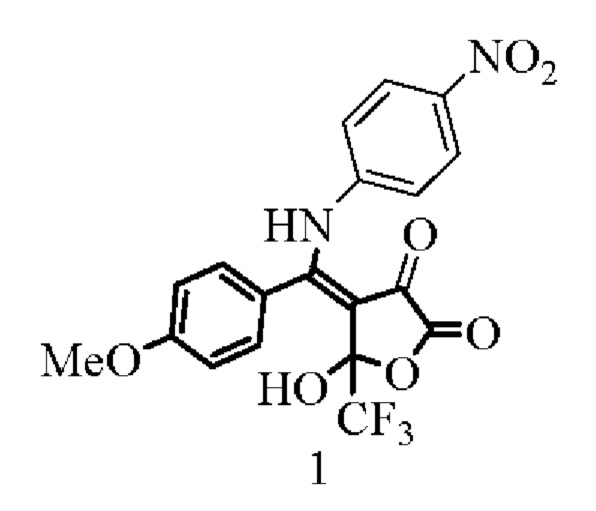
5-гидрокси-4-{[(4-метоксифенил)(4-нитрофенил)амино]метилиден}-5-(трифторметил)дигидрофуран-2,3-дион формулы (1)
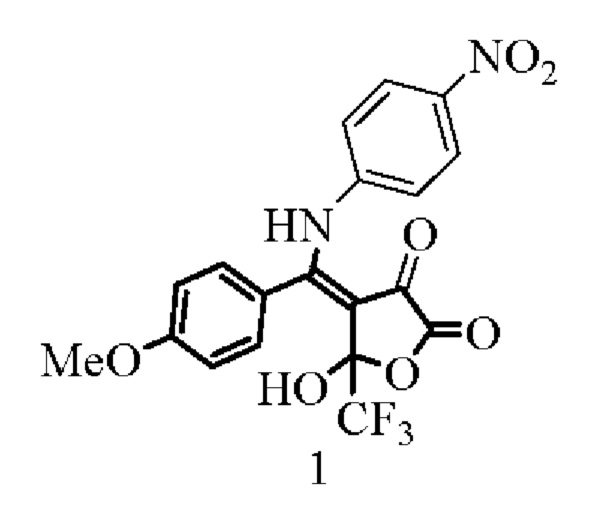
проявляющий противомикробную активность.
| Raghavendra, K.R., Renuka, N., Kumar, K.A | |||
| et al | |||
| An Accessible Route for the Synthesis of Novel Lignan Derivatives and Their Biological Evaluation | |||
| Способ запрессовки не выдержавших гидравлической пробы отливок | 1923 |
|
SU51A1 |
| Применение 3-(2-(4-нитрофенил)-2-оксоэтилиден)морфолин-2-она в качестве средства, обладающего противомикробной активностью | 2021 |
|
RU2763728C1 |
| 4-[2-(гидроксиметил)-фениламино]-6',6'-диметил-1'-(2-фторфенил)-3-(4-хлорбензоил)-6',7'-дигидро-5Н-спиро[фуран-2,3'-индол]-2',4',5(1'H,5'H)-трион в качестве средства, обладающего противомикробной активностью | 2021 |
|
RU2763140C1 |
| ПРИМЕНЕНИЕ ПРОТИВОМИКРОБНОГО СРЕДСТВА ДЛЯ ЗОЛОТИСТОГО СТАФИЛОКОККА С МНОЖЕСТВЕННОЙ ЛЕКАРСТВЕННОЙ УСТОЙЧИВОСТЬЮ НА ОСНОВЕ 2-((4-R-5-R-3-(ЭТОКСИКАРБОНИЛ)ТИОФЕН-2-ИЛ)АМИНО)-4-ОКСО-4-R-БУТ-2-ЕНОВЫХ КИСЛОТ | 2021 |
|
RU2763735C1 |
| Валок пресса | 1974 |
|
SU572191A3 |
Авторы
Даты
2022-10-11—Публикация
2022-02-18—Подача