Предлагаемое изобретение относится к области экспериментальной медицины, а именно к профилактике инфекционных болезней, касающейся использования препаратов бактериофагов для предотвращения развития холеры у экспериментальных животных.
Основной профилактической мерой против холеры, по рекомендации ВОЗ, является массовая вакцинация (1). Но у противохолерных вакцин есть ограничения и противопоказания. Это аллергия, возраст, беременность и грудное вскармливание (2). Кроме того, необходимость лечения больных холерой, зараженных антибиотикоустойчивыми штаммами, диктует необходимость разработки новых средств и методов профилактики и терапии этого заболевания. Перспективными в этом плане могут быть препараты бактериофагов.
Бактериофаги - это уникальные микроорганизмы, на основе которых создана особая по своим свойствам и характеристикам группа лечебно-профилактических препаратов (3). Они успешно применяются для лечения сальмонеллеза, дизентерии, брюшного тифа и т.д. (4), в том числе у детей и беременных женщин. С терапевтической целью используют вирулентные (литические) фаги, поскольку только они способны уничтожать клеток бактерий-хозяев. Вирулентные фаги, проникая внутрь бактериальной клетки, переключают ее метаболизм на воспроизведение новых фагов, которое завершается лизисом бактерии. Этот процесс повторяется с другими бактериальными клетками. Благодаря строгой специфичности действия, бактериофаги, в отличие от антибиотиков, не вызывают побочных реакций, не угнетают нормальную микрофлору макроорганизма, стимулируют факторы специфического и неспецифического иммунитета (что особенно значимо при лечении рецидивирующих воспалительных заболеваний); не обладают токсическим действием (5). Несомненным преимуществом этих препаратов является полная совместимость с любыми лекарственными средствами; пребиотиками, моно- и полипробиотиками, ферментными препаратами, возможность применения их у пациентов с аллергическими реакциями на антибиотики; сокращение длительности лечения за счет быстрого действия и глубокого проникновения в очаг инфекции (6).
Коммерческих профилактических препаратов на основе холерных бактериофагов в настоящее время не зарегистрировано.
Известна методика санации и профилактики с использованием сальмонеллезного бактериофага лиц (пациенты и медицинский персонал), поступающих в очаг нозокомиального сальмонеллеза (7). Для профилактики этого заболевания адаптированный сальмонеллезный бактериофаг назначают всем поступающим в отделения пациентам с высоким риском заражения, а так же контактным лицам из расчета по 2 табл. 2-3 раза в сутки (первые 5 дней), затем по 2 табл. однократно ежедневно в течение времени пребывания в очаге. Также для профилактики бактериофаг назначается сотрудникам отделений с высоким риском заражения из расчета по 2-4 табл. 3 раза в сутки (5-7 дней), с плавным переходом на фагопрофилактику с назначением бактериофага по 2 табл. 3 раза в неделю в течение времени существования эпидемического очага.
Однако, хотя предлагаемый метод является высокоэффективным и безвредным при лечении заболевших, а также при профилактике сальмонеллеза в эпидемическом очаге этого заболевания, он не пригоден для профилактики холеры, так как бактериофаги обладают высокой специфичностью, лизируя не только отдельные виды бактерий, но и штаммы только одного вида.
За прототип выбран способ отбора бактериофагов для лечения экспериментальной холеры, вызванной классическими холерными вибрионами (8), заключающийся в однократном внутрибрюшинном применении вирулентного холерного фага М3 в титре 7*109 БОЕ/мл, осуществленное сразу после заражения животных вирулентными фагочувствительными штаммами Vibrio cholerae 1082 (0,3*109 м.к./мл) и V. cholerae 1084 (5*109 м.к./мл), приводило к снижению вибриотитра культур в 2,6-2,7 раза, кроме того, фаг М3, пропассированный через организм животных, увеличил лизирующую активность в отношении еще трех штаммов (11131, 13570, 13603), устойчивых к исходному фагу.
Эти данные могут быть полезны при создании лечебных препаратов для фаготерапии холеры, но не отражают возможности применения холерных бактериофагов для профилактики этой инфекции.
Техническая задача предлагаемого изобретения состояла в разработке нового эффективного препарата для профилактики холеры.
Поставленная задача достигалась тем, что в способе профилактики холеры с помощью бактериофагов, характеризующийся тем, что для профилактики развития холеры в эксперименте до заражения вирулентными штаммами холеры путем введения в изолированную петлю тонкого кишечника 1×109 клеток смеси в соотношении 1:1 24-часовых культур Vibrio cholerae биоваров El Tor и Classical 01 серогруппы, выращенных в пептонной воде и суспендированных в 1 мл пептонного раствора, кроликам весом 1,5-2 кг внутрижелудочно через зонд вводят смесь фагов Rostov-M3 5×108 БОЕ/мл и Rostov- 13 2×108 БОЕ/мл в соотношении 1:1 объемом 3 мл в течение 3,5, или 7 дней.
Способ осуществляется по следующей технологии:
Взрослым кроликам, весом 1,5 - 2 кг, внутрижелудочно через зонд вводят по 3 мл бактериофагов Rostov-M3 5×108 БОЭ/мл, либо Rostov-13 2×108 БОЭ/мл, либо смесь этих фагов (1:1) в течение 3, 5 и 7 дней. Контрольным животным вводят в том же количестве физиологический раствор. После 3, 5 и 7 дней фагопрофилактики опытных и контрольных животных, после 24-х часового голодания, заражают вирулентным штаммом холеры. Все штаммы взяты из коллекции музея Ростовского противочумного института.
После введения миорелаксанта ксилозина (из расчета 0,15 мл на 1 кг веса) делают разрез по средней линии живота и извлекают петли тонкого кишечника. На 60 см проксимальнее аппендикса накладывают лигатуры, перевязывая одинаковые участки кишечника длинной 12 см с промежутками между ними 4-5 см. В одну лигированную петлю вводят 1 мл 0,9% раствора хлорида натрия (контрольная петля), в другую (опытная петля) - 1×109 клеток выращенной в пептошюй воде и суспендированной в 1 мл пептонного раствора 24-часовой культуры Vibrio choleras El Tor 18898 или V choleras Classical 145, или смесь этих культур (1:1). После этого брюшную стенку зашивают. Спустя 16-18 часов животных забивают воздушной эмболией и вскрывают.
Об эффективности использования бактериофагов для профилактики холеры судят по наличию и выраженности энтеропатогенного и холерогенного эффектов.
Энтеропатогенный эффект оценивают по патологоанатомической картине в опытной перевязанной петле тонкого кишечника: наличию отека слизистой и подслизистой оболочек, кровоизлияний и некрозов покровного эпителия ворсин. Отсутствие подобных нарушений свидетельствует об эффективности использования бактериофагов.
Холерогенный эффект оценивают по коэффициенту растяжения опытной петли, рассчитываемого по формуле:
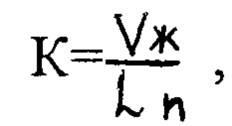
где К - коэффициент растяжения петли;
V ж - объем жидкости;
L п - длина петли
Если К<1,0, холерогенный эффект отсутствует, что свидетельствует об эффективности использования бактериофагов для профилактики холеры.
Профилактическое использование бактериофагов как по отдельности, так и в смеси в течение 5 и 7 дней перед заражением препятствовало развитию холеры в тонком кишечнике экспериментальных животных.
Предложенный способ основан на использовании смеси холерных бактериофагов, лизирующих штаммы холеры, относящиеся к разным биоварам (Classical и El Tor) O1 серогруппы возбудителя для профилактики этой особо опасной инфекции. В способе использовали бактериофаг Rostov-13, выделенный из водных объектов окружающей среды в 2017 г., а также Rostov-М3, выделенный из водных объектов окружающей среды в 2015 г (фаг Мукерджи), из коллекции холерных фагов ФКУЗ Ростовский-на-Дону противочумный институт Роспотребнадзора. Rostov-13 лизирует V. cholerae O1 серогруппы биовара El Tor с литической активностью 97%, Rostov-МЗ -V. cholerae O1 серогруппы биовара Classical с литической активностью 83,3%. Полный геном фага Rostov-М3 зарегистрирован и доступен в Genbank (NCBI) под номером MN3 79463
Эффективность предложенного способа подтверждается следующими примерами:
Пример 1: Определение профилактического действия бактериофага Rostov-13 на модели изолированной петли тонкого кишечника взрослых кроликов, зараженных V. cholerae El Tor.
Четыре группы (но 3 штуки) взрослых кроликов (1,5-2 кг) с профилактической целью внутрижелудочно через зонд получают по 3 мл препарата бактериофага Rostov-13 2×108 БОЕ/мл в течение 3, 5 и 7 дней. Контролем служат кролики, которым в таком же количестве вводят физиологический раствор. После 3, 5 и 7 дней фагопрофилактики опытные и контрольные животные, после 24-х часового голодания, заражают вирулентным штаммом холеры. Для этого перевязывают две петли тонкого кишечника: в одну лигированную петлю вводят 1 мл 0,9% раствора хлорида натрия (контрольная петля), в другую (опытная петля) - 1×109 клеток 24-часовой культуры V. cholerae El Tor 18898, выращенной в пептонной воде и суспендированной в 1 мл пептонного раствора.
О профилактическом эффекте препарата фага судят по отсутствию/развитию признаков, характерных для холеры: наличию жидкости в опытных петлях (К>1 - холерогенный эффект) и отека слизистой и подслизистой оболочек, кровоизлияний (энтеропатогенный эффект).
При оценке результатов выявлено, что у всех животных контрольной группы в опытной петле с возбудителем холеры регистрировались выраженный холерогенный и энтеропатогенный эффекты.
У получавших фаг в течение 3 дней кроликов, инфицированных V. cholerae El Tor 18898, наблюдали холерогенный эффект, аналогичный контрольной группе животных и более слабо выраженный, по сравнению с контролем, энтеропатогенный эффект.
В таблице 1 дана оценка профилактического действия бактериофага Rostov-13 по наличию/выраженности холерогенного и энтеропатогенного эффектов в изолированной петле тонкого кишечника взрослого кролика.

После пятидневного профилактического приема препарата бактериофага Rostov-13 холерогенного эффекта у зараженных животных не обнаружено, наблюдались незначительные кровоизлияния в стенках тонкого кишечника.
У зараженных после семидневного приема бактериофага экспериментальных животных признаков развития холеры выявлено не было.
Пример 2: Определение профилактического действия бактериофага Rostov-М3 на модели изолированной петли тонкого кишечника взрослых кроликов, зараженных V. cholerae O1 Classical
12-и взрослым кроликам (по 3 в группе), весом 1,5-2 кг, внутрижелудочно через зонд вводят с целью профилактики холеры 3 мл 5×108 БОЕ/мл бактериофага Rostov-М3. Первая группа получала препарат в течение 3 дней, вторая - 5 дней и третья - 7 дней. Кроликам контрольной группы в таком же количестве вводят физиологический раствор. После фагопрофилактики опытных и контрольных животных, после 24-х часового голодания, заражают вирулентным штаммом холеры в изолированную петлю тонкого кишечника. В одну лигированную петлю вводят 1 мл 0,9% раствора хлорида натрия (контрольная петля), в другую (опытная петля) - 1×109 клеток 24-часовой культуры V. cholerae Classical 145, выращенной в пептонной воде и суспендированной в 1 мл пептонного раствора.
При анализе полученных результатов выявлено, что прием фага Rostov-МЗ в течение 3 дней оказался недостаточным для предотвращения развития экспериментальной холеры: у животных этой группы развивался выраженный холерогенный и энтеропатогенный эффекты.
В таблице 2 отражена оценка профилактического действия препарата бактериофага Rostov-М3 по наличию/выраженности холерогенного и энтеропатогенного эффектов в изолированной петле тонкого кишечника взрослого кролика.

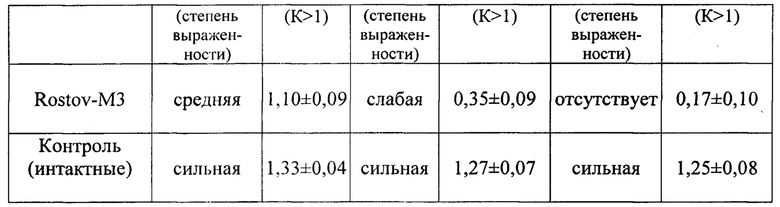
Однако, уже после 5 дней профилактического приема бактериофага Rostov-М3 признаков развития холеры у экспериментальных животных не было выявлено: опытная петля была сдута, жидкость, свидетельствующая о наличии холерогенного эффекта, отсутствовала, отеков не было, наблюдались незначительные кровоизлияния на стенках тонкого кишечника. У животных, получавших бактериофаг в течение 7 дней, опытная петля не отличалась от контрольной. Следует отметить, что у животных контрольной группы опытные петли тонкого кишечника были сильно раздуты, заполнены мутной жидкостью, наблюдались ярко выраженные кровоизлияния на их стенках.
Пример 3. Определение профилактического действия коктейля из бактериофагов Rostov-М3 и Rostov-13 в отношении штаммов холеры O1 серогруппы биоваров Classical и El Tor
Постановку эксперимента осуществляли аналогично описанному в примерах 1 и 2.
После профилактики 3 мл смеси фагов (1:1) в течение 3, 5 и 7 дней опытных и контрольных животных заражают смесью (1:1) вирулентных штаммов холеры в изолированную петлю тонкого кишечника. В контрольную петлю вводят 1 мл 0,9% раствора хлорида натрия, в опытную петлю - 1×109 клеток смеси (1:1) 24-часовых культур V. cholerae El Tor 18899 и V. cholerae Classical 569 В, выращенных в пептонной воде и суспендированных в 1 мл понтонного раствора.
При подведении итогов эксперимента выявлено, что трехдневный прием смеси фагов снижает, по сравнению с контролем, выраженность патоморфологических изменений в опытных петлях тонкого кишечника животных, но полностью не препятствует развитию экспериментальной холеры.
В таблице 3 отражена оценка профилактического действия препарата смеси бактериофагов Rostov-13 и Rostov-МЗ по наличию/выраженности холерогенного и энтеропатогенного эффектов в изолированной петле тонкого кишечника взрослого кролика.
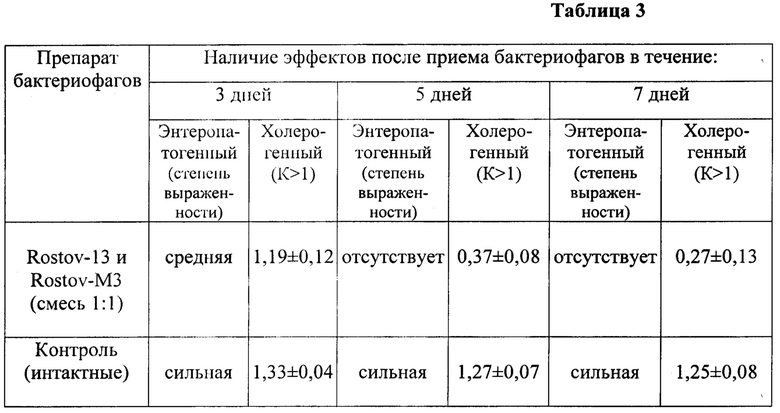
Смесь фагов Rostov-М3 и Rostov-13 оказывает эффективное профилактическое действие в отношении холерных вибрионов после пятидневного курса приема. Аналогичные результаты получены при использовании смеси бактериофагов в течение 7 дней.
Таким образом, отраженные в примерах полученные результаты свидетельствуют о том, что предложенный нами способ профилактики холеры является эффективным. Курсовой, в течение пяти дней, прием бактериофагов Rostov-М3 и Rostov-13 отдельно, и, особенно, в смеси, препятствуют развитию экспериментальной холеры.
Профилактическое использование смеси (коктейля) этих бактериофагов предотвращает инфицирование экспериментальных животных как штаммами, относящимися к биовару El Тог, так и штаммами биовара Classical. Эти результаты могут быть полезны для разработки новых иммунобиологических препаратов для профилактики холеры у людей и будут учтены при создании экспериментального профилактического препарата на основе холерных бактериофагов.
Источники информации:
1. Qadri F., Wierzba T.F., АН М., Chowdhury F., Khan A.I., Saha A.et al Efficacy of a single-dose, inactivated oral cholera vaccine in Bangladesh. // N. Engl. J. Med. -2016. - Vol.374. - Pp.1723-1732
2. Wong K.K., Burdette E., Mahon B.E., Mintz E.D., Ryan E.T., Reingold A.L. Recommendations of the Advisory Committee on Immunization Practices for Use of Cholera Vaccine // MMWR Morb Mortal Wkly Rep.- 2017. - Vol.66 (18). -Pp.482-485.
3. Захаренко СМ. Бактериофаги: Современные аспекты применения, перспективы на будущее // Медицинский совет.- 2013. - №10. - С.72-74.
4. Дарбеева О.С., Майская Л.М., Парфенюк Р.Л., Дурманова З.В. Пути совершенствования лечебно-профилактических бактериофагов // Биопрепараты. - 2010. - №3(39). - С.53-54.
5. Чушков Ю.В. Бактериофаги в лечении и профилактике инфекционных заболеваний // Фарматека. - 2011. - 6. - С.34-41
6. Буданов П.В., Новахова Ж.Д., Чурганова А.А. Альтернатива антибактериальной терапии в акушерстве и гинекологии // РМЖ. - 2015. - №1.-С.14-15.
7. Акимкин В.Г. Современные аспекты эпидемиологии и профилактики нозокомиального сальмонеллеза // Медицинский совет. Госпитальная терапия, 2013. - №5-6 (1). - С.33-39.
8. Гаевская Н.Е., Кудрякова Т.А., Качкина Г.В., Алиева А.А., Саямов С.Р. Отбор бактериофагов для лечения экспериментальной холеры, вызванной классическими холерными вибрионами // Современные наукоемкие технологии. - 2004- №3. - С11-15.
9. Ситников И.Г., Шошин А.А., Волхов А.Р. Возможность управления инфекцией // Инфекция и иммунитет.- 2014. - С.110
10. Щербенков И.М. Бактериофаги. Что мы знаем о них? // Медицинский совет.- 2013. - №2. - С.56-62.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ идентификации холерных вибрионов O1 серогруппы биоваров Classical и El Tor | 2019 |
|
RU2729575C1 |
| Способ повышения эффективности противохолерной вакцинации для профилактики на экспериментальных животных | 2018 |
|
RU2691411C1 |
| Способ идентификации Vibrio cholerae 01 серогруппы биовара El Tor | 2022 |
|
RU2797369C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА БЕЛКА ОМР Т ДЛЯ МОДЕЛИРОВАНИЯ ПРОТИВОХОЛЕРНОГО ИММУНИТЕТА У ЭКСПЕРИМЕНТАЛЬНЫХ ЖИВОТНЫХ | 2017 |
|
RU2663102C2 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ ПРИМЕНЕНИЯ ИММУНОМОДУЛЯТОРА ИМУНОФАНА ПРИ ЭКСПЕРИМЕНТАЛЬНОЙ ХОЛЕРЕ | 2011 |
|
RU2481791C2 |
| Способ обнаружения жизнеспособных холерных вибрионов 01 серогруппы биоваров Classical и El Tor в окружающей среде с помощью бактериофага M3 методом количественной ПЦР | 2023 |
|
RU2808577C1 |
| Способ профилактики холеры с использованием везикул для моделирования противохолерного иммунитета у экспериментальных животных | 2022 |
|
RU2792160C1 |
| Набор штаммов бактерий для обучения вопросам микробиологии и методам лабораторной диагностики холеры | 2019 |
|
RU2743454C1 |
| АВИРУЛЕНТНЫЙ ТЕСТ-ШТАММ БАКТЕРИЙ Vibrio cholerae БИОВАРА eltor СЕРОВАРА Ogawa (ctxA-, tcpA-, toxR-, zot-), ИСПОЛЬЗУЕМЫЙ В ИММУНОЛОГИЧЕСКИХ, ГЕНЕТИЧЕСКИХ ИССЛЕДОВАНИЯХ И УЧЕБНОМ ПРОЦЕССЕ | 2004 |
|
RU2254371C1 |
| АВИРУЛЕНТНЫЙ ШТАММ БАКТЕРИЙ Vibrio cholerae KM 263 БИОВАРА ЭЛЬТОР СЕРОВАРА ИНАБА - ПРОДУЦЕНТ ПРОТЕКТИВНОГО О1 АНТИГЕНА | 2010 |
|
RU2425867C1 |
Изобретение относится к области экспериментальной медицины, а именно к профилактике инфекционных болезней, касающейся использования препаратов бактериофагов для предотвращения развития холеры у экспериментальных животных. Сущность изобретения заключается в том, что для профилактики развития экспериментальной холеры до заражения вирулентными штаммами холеры путем введения в изолированную петлю тонкого кишечника 1×109 клеток смеси в соотношении 1:1 24-часовых культур Vibrio cholerae биоваров El Tor и Classical 01 серогруппы, выращенных в пептонной воде и суспендированных в 1 мл пептонного раствора, кроликам весом 1,5-2 кг внутрижелудочно через зонд вводят смесь фагов Rostov-М3 5×108 БОЕ/мл и Rostov-13 2×108 БОЕ/мл в соотношении 1:1 объемом 3 мл в течение 3, 5 или 7 дней. Изобретение обеспечивает эффективный способ профилактики холеры. 3 пр., 3 табл.
Способ профилактики холеры с помощью бактериофагов, характеризующийся тем, что для профилактики развития холеры в эксперименте до заражения вирулентными штаммами холеры путем введения в изолированную петлю тонкого кишечника 1×109 клеток смеси в соотношении 1:1 24-часовых культур Vibrio cholerae биоваров El Tor и Classical 01 серогруппы, выращенных в пептонной воде и суспендированных в 1 мл пептонного раствора, кроликам весом 1,5-2 кг внутрижелудочно через зонд вводят смесь фагов Rostov-М3 5×108 БОЕ/мл и Rostov-13 2×108 БОЕ/мл в соотношении 1:1 объемом 3 мл в течение 3, 5 или 7 дней.
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ ПРИМЕНЕНИЯ ИММУНОМОДУЛЯТОРА ИМУНОФАНА ПРИ ЭКСПЕРИМЕНТАЛЬНОЙ ХОЛЕРЕ | 2011 |
|
RU2481791C2 |
| ТЮРИНА А.В | |||
| и др | |||
| Активность препарата бактериофагов в отношении антибиотикорезистентных штаммов холерных вибрионов El Tor / АНТИБИОТИКИ И ХИМИОТЕРАПИЯ, 2018, 63; 7-8, стр | |||
| Солесос | 1922 |
|
SU29A1 |
| ПОГОЖОВА М.П | |||
| и др | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Аппарат для испытания прессованных хлебопекарных дрожжей | 1921 |
|
SU117A1 |
Авторы
Даты
2022-11-08—Публикация
2021-12-16—Подача