Область техники
Изобретение относится к биотехнологии, а именно, к новым ферментам – Cas нуклеазам систем CRISPR-Cas, применяемым для разрезания ДНК и редактирования геномов различных организмов. Данная технология может применяться в будущем для генной терапии наследственных заболеваний человека, а также для редактирования геномов других организмов.
Работа выполнена при финансовой поддержке Министерства Науки и Высшего образования Российской Федерации в рамках Соглашения №075-15-2019-1661 от 31.10.2019.
Уровень техники
Изменение последовательности ДНК – одна из актуальных задач биотехнологии на сегодняшний день. Редактирование и изменение геномов эукариотических и прокариотических организмов, а также манипуляции с ДНК in vitro, требуют направленного внесения двунитевых разрывов в последовательности ДНК.
Для решения этой задачи в настоящее время используют следующие методики: искусственные нуклеазные системы, содержащей домены типа «цинковые пальцы» (ZFN), эффекторные нуклеазы, подобные активатору транскрипции (TALEN-системы) и бактериальные CRISPR-Cas системы. Первые два метода требуют трудозатратой оптимизации аминокислотной последовательности нуклеазы для узнавания конкретной последовательности ДНК. В отличие от них в случае CRISPR-Cas систем структурами, узнающими ДНК мишень, являются не белки, а короткие направляющие РНК. Разрезание конкретной ДНК мишени не требует синтеза нуклеазы или ее гена de novo, а обеспечивается за счет использования направляющих РНК, комплементарных целевой последовательности. Это делает CRISPR-Cas системы удобными и эффективными инструментами разрезания различных ДНК-последовательностей. Методика позволяет осуществлять единовременное разрезание ДНК в нескольких участках при использовании направляющих РНК разной последовательностей. Такой подход используется в том числе для одновременного изменения нескольких генов в эукариотических организмах.
По своей природе CRISPR-Cas системы являются иммунными системами прокариот, способными высоко специфично вносить разрывы в генетический материал вирусов
(Mojica F. J. M., 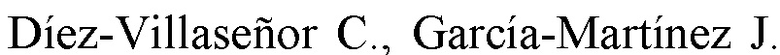 & Soria E. Intervening sequences of regularly spaced prokaryotic repeats derive from foreign genetic elements // Journal of molecular evolution. – 2005. – Т. 60. – №. 2. – С. 174-182). Аббревиатура CRISPR-Cas расшифровывается как «Clustered Regularly Interspaced Short Palindromic Repeats and CRISPR associated genes» (Jansen R., Embden J. D., Gaastra W. & Schouls L. M. Identification of genes that are associated with DNA repeats in prokaryotes // Molecular microbiology. – 2002. – Т. 43. – №. 6. – С. 1565-1575), что переводе с английского обозначает «короткие палиндромные повторы, регулярно расположенные группами, и ассоциированные с ними гены». Все CRISPR-Cas системы состоят из CRISPR кассет и генов, кодирующих различные Cas белки (Jansen R. et al., Molecular microbiology. – 2002. – Т. 43. – №. 6. – С. 1565-1575). CRISPR кассеты состоят из последовательностей спейсеров, каждый из которых имеет уникальную нуклеотидную последовательность, и повторяющихся палиндромных повторов (Jansen R. et al., Molecular microbiology. – 2002. – Т. 43. – №. 6. – С. 1565-1575). В результате транскрипции CRISPR кассет и их последующего процессинга образуются направляющие крРНК, которые вместе с Cas белками формируют эффекторный комплекс
& Soria E. Intervening sequences of regularly spaced prokaryotic repeats derive from foreign genetic elements // Journal of molecular evolution. – 2005. – Т. 60. – №. 2. – С. 174-182). Аббревиатура CRISPR-Cas расшифровывается как «Clustered Regularly Interspaced Short Palindromic Repeats and CRISPR associated genes» (Jansen R., Embden J. D., Gaastra W. & Schouls L. M. Identification of genes that are associated with DNA repeats in prokaryotes // Molecular microbiology. – 2002. – Т. 43. – №. 6. – С. 1565-1575), что переводе с английского обозначает «короткие палиндромные повторы, регулярно расположенные группами, и ассоциированные с ними гены». Все CRISPR-Cas системы состоят из CRISPR кассет и генов, кодирующих различные Cas белки (Jansen R. et al., Molecular microbiology. – 2002. – Т. 43. – №. 6. – С. 1565-1575). CRISPR кассеты состоят из последовательностей спейсеров, каждый из которых имеет уникальную нуклеотидную последовательность, и повторяющихся палиндромных повторов (Jansen R. et al., Molecular microbiology. – 2002. – Т. 43. – №. 6. – С. 1565-1575). В результате транскрипции CRISPR кассет и их последующего процессинга образуются направляющие крРНК, которые вместе с Cas белками формируют эффекторный комплекс
(Brouns S. J., Jore M. M., Lundgren M., Westra E. R., Slijkhuis R. J., Snijders A. P., Dickman M. J., Makarova K. S., Koonin E. V. & van der Oost J. Small CRISPR RNAs guide antiviral defense in prokaryotes // Science. – 2008. – Т. 321. – №. 5891. – С. 960-964). За счет комплементарного спаривания крРНК с целевым участком ДНК, именуемым протоспейсером, Cas-нуклеаза узнает ДНК-мишень и высоко специфично вносит в нее разрыв.
CRISPR-Cas системы, представленными одиночным белком-эффектором, разделяют на шесть различных типов (от I до VI) в зависимости от Cas белков, входящих в состав систем. В 2013 году впервые было предложено использовать систему CRISPR-Cas9, относящуюся к типу II, для редактирования геномной ДНК клеток человека (Cong L., Ran F. A., Cox D., Lin S., Barretto R., Habib N., Hsu P. D., Wu X., Jiang W., Marraffini L. A. & Zhang F. Multiplex genome engineering using CRISPR/Cas systems // Science. – 2013. – Т. 339. – № 6121. – С. 819-823). Система CRISPR-Cas9 II типа отличается простотой состава и механизма работы: для ее функционирования необходимо формирование эффекторного комплекса, состоящего лишь из одного белка Cas9 и двух коротких РНК: крРНК (crRNA) и трейсерной РНК (tracrRNA, трРНК). Трейсерная РНК комплементарно спаривается с участком крРНК, происходящим из CRISPR повтора, образуя вторичную структуру, необходимую для связывания направляющих РНК с Cas эффектором. Определение последовательности направляющих РНК является важным шагом в характеризации неизученных ранее Cas-ортологов. Эффекторный белок Cas9 является РНК-зависимой ДНК эндонуклеазой с двумя нуклеазными доменами (HNH и RuvC), вносящими разрывы в комплементарные нити целевой ДНК, таким образом образуя двунитевой разрыв ДНК (Deltcheva E., Chylinski K., Sharma C. M., Gonzales K., Chao Y., Pirzada Z. A., Eckert M. R., Vogel J. & Charpentier E. CRISPR RNA maturation by trans-encoded small RNA and host factor RNase III // Nature. – 2011. – Т. 471. – №. 7340. – С. 602).
Технология CRISPR-Cas9 является одной из самых современных и быстроразвивающихся методик внесения разрывов в ДНК различных организмов, начиная от бактериальных штаммов и заканчивая клетками человека, а также in vitro (Song M. The CRISPR/Cas9 system: Their delivery, in vivo and ex vivo applications and clinical development by startups // Biotechnology Progress. – 2017. – Т. 33. – № 4. – С. 1035–1045).
Эффекторному рибонуклеиновому комплексу, состоящему из Cas9 и дуплекса крРНК и трейсерной РНК, для распознавания и последующего гидролиза ДНК помимо комплементарного соответствия спейсера крРНК и протоспейсера необходимо присутствие PAM (от англ. «PAM» - protospacer adjusted motif) на ДНК мишени (Mojica F. J. M. et al., Journal of molecular evolution. – 2005. – Т. 60. – №. 2. – С. 174-182). PAM представляет собой строго определенную последовательность из нескольких нуклеотидов, расположенных в системах типа II вплотную либо в нескольких нуклеотидах от 3'-конца протоспейсера на нетаргетной цепи. При отсутствии PAM гидролиза связей в ДНК с образованием двунитевого разрыва не происходит. Необходимость присутствия PAM последовательности на мишени повышает специфичность узнавания, но в то же время накладывает ограничение в выборе целевых участков ДНК, в которые необходимо внести разрыв. Таким образом, наличие нужной PAM последовательности, фланирующей ДНК-мишень с 3'-конца, является характеристикой, ограничивающей применение CRISPR-Cas систем на любых участках ДНК.
На сегодняшний день известно несколько CRISPR-Cas нуклеаз, способных направлено и специфично вносить двунитевые разрывы в ДНК. Например, NmeCas9 из Neisseria meningitidis strain 8013 (Esvelt K. M., Mali P., Braff J. L., Moosburner M., Yaung S. J. & Church G. M. Orthogonal Cas9 proteins for RNA-guided gene regulation and editing // Nature Methods. – 2013. – Т. 10. – С. 1116–1121), Nme2Cas9 из Neisseria meningitidis strain De11444 (Edraki A., Mir A., Ibraheim R., Gainetdinov I., Yoon Y., Song C.-Q., Cao Y., Gallant J., Xue W., Rivera-Perez J. A. & Sontheimer E. J. A compact, high-accuracy Cas9 with a dinucleotide PAM for in vivo genome editing // Molecular Cell. – 2019. – Т. 73. – С. 714–726), CjCas9 из Campylobacter jejuni (Kim E., Koo T., Park S. W., Kim D., Kim K., Cho H. Y., Song D. W., Lee K. J., Jung M. H., Kim S., Kim J. H., Kim J. H. & Kim J. S. In vivo genome editing with a small Cas9 orthologue derived from Campylobacter jejuni // Nature Communications. – 2017. – Т. 8. – С. 14500), CdCas9 из Corynebacterium diphtheriae (Hirano S., Abudayyeh O. O., Gootenberg J. S., Horii T., Ishitani R., Hatada I., Zhang F., Nishimasu H. & Nureki O. Structural basis for the promiscuous PAM recognition by Corynebacterium diphtheriae Cas9 // Nature Communications. – 2019. – Т. 10. – С. 1968), GeoCas9 из Geobacillus stearothermophilus (Harrington L. B., Paez-Espino D., Staahl B. T., Chen J. S., Ma E., Kyrpides N. C. & Doudna J. A. A thermostable Cas9 with increased lifetime in human plasma // Nature Communications. – 2017. – Т. 8. – С. 1424.), SaCas9 из Staphylococcus aureus (Ran F. A., Cong L., Yan W. X., Scott D. A., Gootenberg J. S., Kriz A. J., Zetsche B., Shalem O., Wu X., Makarova K. S., Koonin E. V., Sharp P. A. & Zhang F. In vivo genome editing using Staphylococcus aureus Cas9 // Nature. – 2015. – Т. 520. – С. 186–191), SauriCas9 из Staphylococcus auricularis (Hu Z., Wang S., Zhang C., Gao N., Li M., Wang D., Wang D., Liu D., Liu H., Ong S.-G., Wang H., Wang Y. A compact Cas9 ortholog from Staphylococcus Auricularis (SauriCas9) expands the DNA targeting scope // PLOS Biology. – 2020. – Т. 18. – e3000686).
Различные CRISPR-Cas белки используют для своей работы разные, оригинальные PAM последовательности. Однако большинство из описанных характеризуются длинной и сложной PAM последовательностью.
Использование CRISPR-Cas белков с новыми разнообразными PAM последовательностями необходимо для обеспечения возможности изменения любого участка ДНК, как in vitro, так и в геноме живых организмов. Изменение эукариотических геномов также требует использования нуклеаз малого размера для обеспечения доставки CRISPR-Cas систем в клетки посредством AAV вирусов.
Несмотря на известность ряда способов разрезания ДНК и изменения последовательности геномной ДНК, на сегодняшний день сохраняется потребность в новых эффективных инструментах для модификации ДНК в различных организмах и в строго определенных местах последовательности ДНК.
Краткое описание изобретения
Задачей настоящего изобретения является создание новых инструментов для изменения последовательности геномной ДНК одноклеточных или многоклеточных организмов на основе систем CRISPR-Cas9. Существующие в настоящее время системы имеют ограниченное применение из-за специфичной последовательности РАМ, которая должна присутствовать на 3'-конце участка ДНК, подвергающегося модификации. Поиск новых ферментов Cas9 с другими РАМ последовательностями позволит расширить арсенал имеющихся средств для образования двунитевого разрыва в необходимых, строго определенных местах в молекулах ДНК разных организмов. Для решения этой задачи авторами была охарактеризована ранее биоинформатически предсказанная система из бактерии Streptococcus uberis NCTC3858.
CRISPR нуклеаза II типа SuCas9, которая может быть применена для внесения направленных изменений в геном как этого, так и других организмов. Существенным признаком, отличающим настоящее изобретение, является отличающаяся от других известных последовательность PAM, а также малый размер белка SuCas9.
Указанная задача решается путем применения белка, содержащего аминокислотную последовательность SEQ ID NO: 1, или содержащего аминокислотную последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности SEQ ID NO: 1 и имеет отличия по сравнению с SEQ ID NO: 1 только в неконсервативных аминокислотных остатках, для образования двунитевого разрыва в молекуле ДНК, расположенного непосредственно перед нуклеотидной последовательностью 5'-NNAAR-3' в указанной молекуле ДНК. В некоторых вариантах изобретения данное применение характеризуется тем, что образование двунитевого разрыва в молекуле ДНК происходит при температуре от 25°C до 45°C.
Указанная задача также решается путем создания способа изменения последовательности геномной ДНК одноклеточного или многоклеточного организма, включающего введение в по меньшей мере одну клетку этого организма эффективного количества: а) либо белка, содержащего аминокислотную последовательность SEQ ID NO: 1, либо нуклеиновой кислоты, кодирующей белок, содержащий аминокислотную последовательность SEQ ID NO: 1, и б) либо направляющей РНК, содержащей последовательность, образующую дуплекс с нуклеотидной последовательностью участка геномной ДНК организма, непосредственно примыкающей к нуклеотидной последовательности 5'-NNAAR-3', и взаимодействующей с указанным белком после образования дуплекса, либо последовательности ДНК, кодирующей указанную направляющую РНК; при этом взаимодействие указанного белка с направляющей РНК и нуклеотидной последовательностью 5'-NNAAR-3' приводит к образованию двунитевого разрыва в последовательности геномной ДНК, непосредственно примыкающей к последовательности 5'-NNAAR-3'. В некоторых вариантах изобретения данный способ характеризуется тем, что дополнительно включающий введение экзогенной последовательности ДНК одновременно с направляющей РНК.
В качестве направляющей РНК может быть использована смесь из крРНК (crRNA) и трейсерной РНК (tracrRNA), способных образовать комплекс с участком целевой ДНК и белком SuCas9. В предпочтительных вариантах изобретения в качестве направляющей РНК может быть использована гибридная РНК, сконструированная на основе крРНК и трейсерной РНК. Методы конструирования гибридной направляющей РНК известны специалистам (Hsu P. D., Scott D. A., Weinstein J. A., Ran F. A., Konermann S., Agarwala V., Li Y., Fine E. J., Wu X., Shalem O., Cradick T. J., Marraffini L. A., Bao G. & Zhang F. DNA targeting specificity of RNA-guided Cas9 nucleases // Nature Biotechnology. – 2013. – Т. 31. – №9. – С. 827-832).
Изобретение может быть использовано как для разрезания целевой ДНК in vitro, так и для модификации генома какого-либо живого организма. Модификация генома может проводиться прямым способом – разрезанием генома в соответствующем сайте, а также вставкой экзогенной последовательности ДНК за счет гомологичной репарации.
В качестве экзогенной последовательности ДНК может быть использован любой участок двунитевой или однонитевой ДНК из генома организма, отличного от организма, используемого при введении (или смесь таких участков между собой и с другими фрагментами ДНК), при этом этот участок (или смесь участков) предназначен для интеграции в место двуцепочечного разрыва в целевой ДНК, образованного под действием нуклеазы SuCas9. В некоторых вариантах изобретения в качестве экзогенной последовательности ДНК может быть использован участок двуцепочечной ДНК из генома организма, используемого при введении белка SuCas9, но при этом измененный мутациями (заменой нуклеотидов), а также вставками или делециями одного или нескольких нуклеотидов.
Техническим результатом настоящего изобретения является повышение универсальности доступных систем CRISPR-Cas9, позволяющее использовать нуклеазу Cas9 для разрезания геномной или плазмидной ДНК в большем количестве специфических сайтов и специфических условий.
Краткое описание рисунков
Фиг. 1. Схема устройства локуса CRISPR SuCas9 системы.
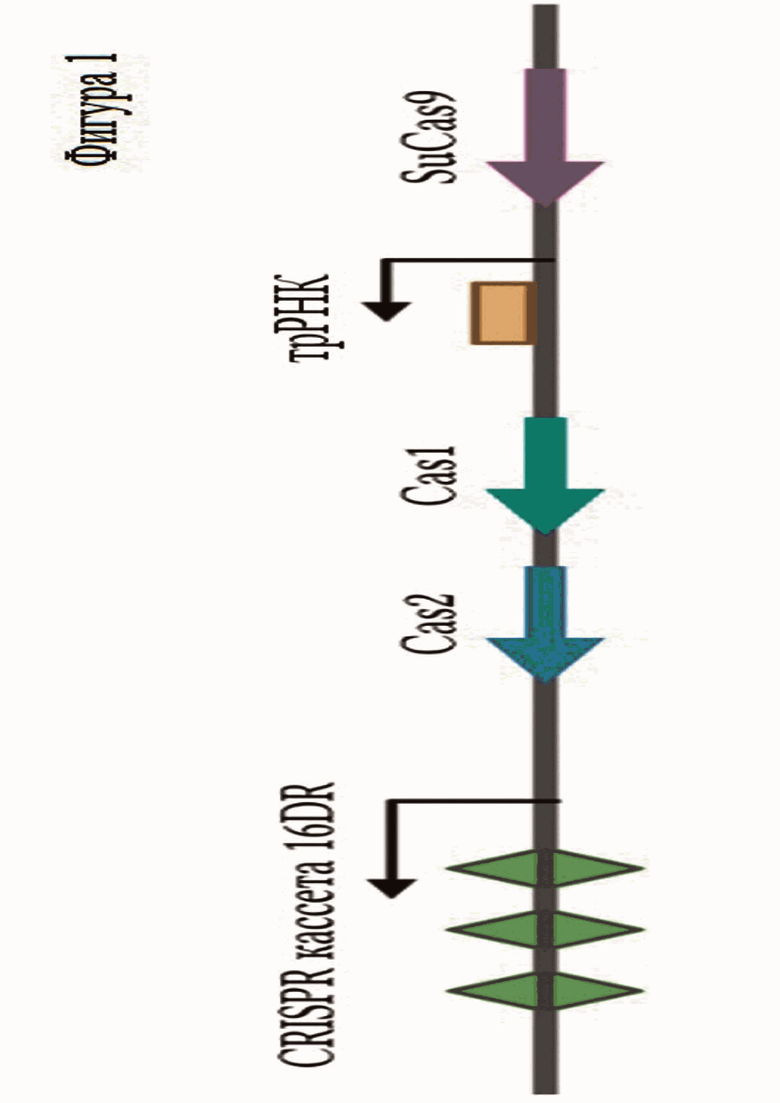
Фиг. 2. PAM скрининг in vitro. Схема эксперимента.
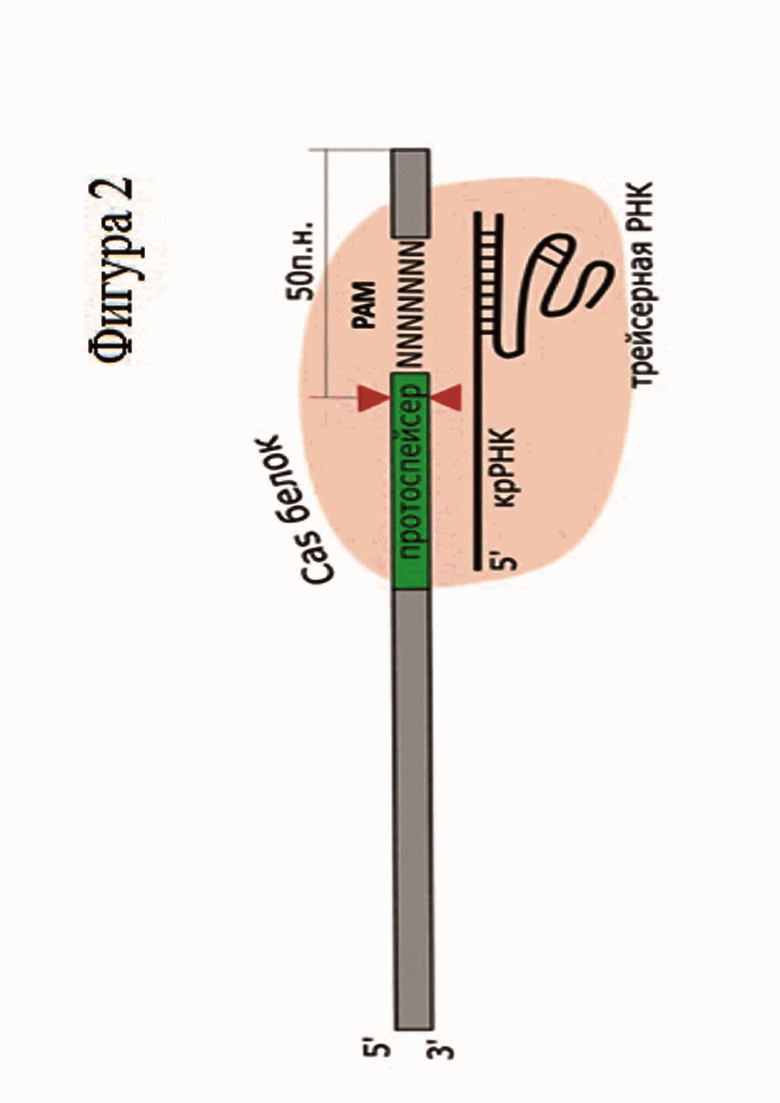
Фиг. 3. Разрезание нуклеазой SuCas9 фрагментов 7N библиотеки при использовании крРНК с длиной прямого повтора DR 35 нуклеотидов и длиной спейсерной части 20 нуклеотидов (SP20). Красной стрелкой отмечено положение разрезанного фрагмента.
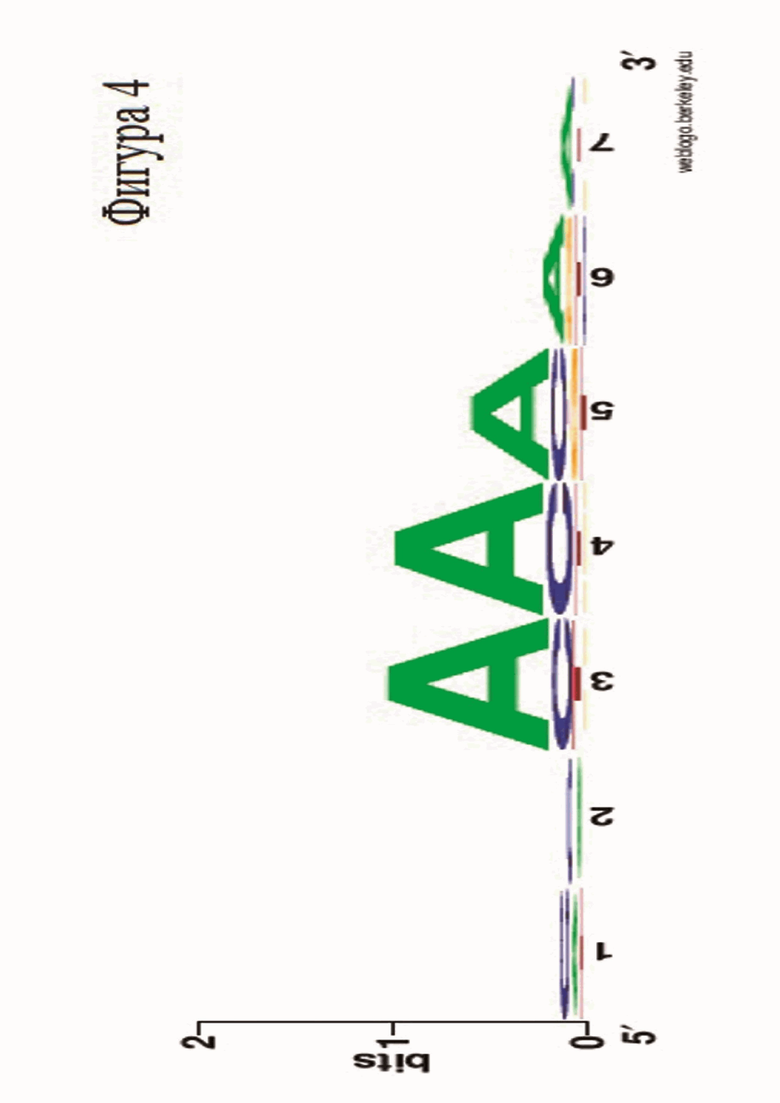
Фиг. 4. PAM Logo нуклеазы SuCas9, полученное в результате скрининга 7N PAM библиотек.
Фиг. 5. Разрезание нуклеазой SuCas9 ДНК-мишеней с конкретными PAM последовательностями, выбранными по результатам PAM-скрининга. «+» - образцы в которые была добавлена направляющая РНК, «-» - образцы без направляющей РНК, выступающие в роли отрицательного контроля. Красными стрелками отмечено положение разрезанного фрагмента ДНК.
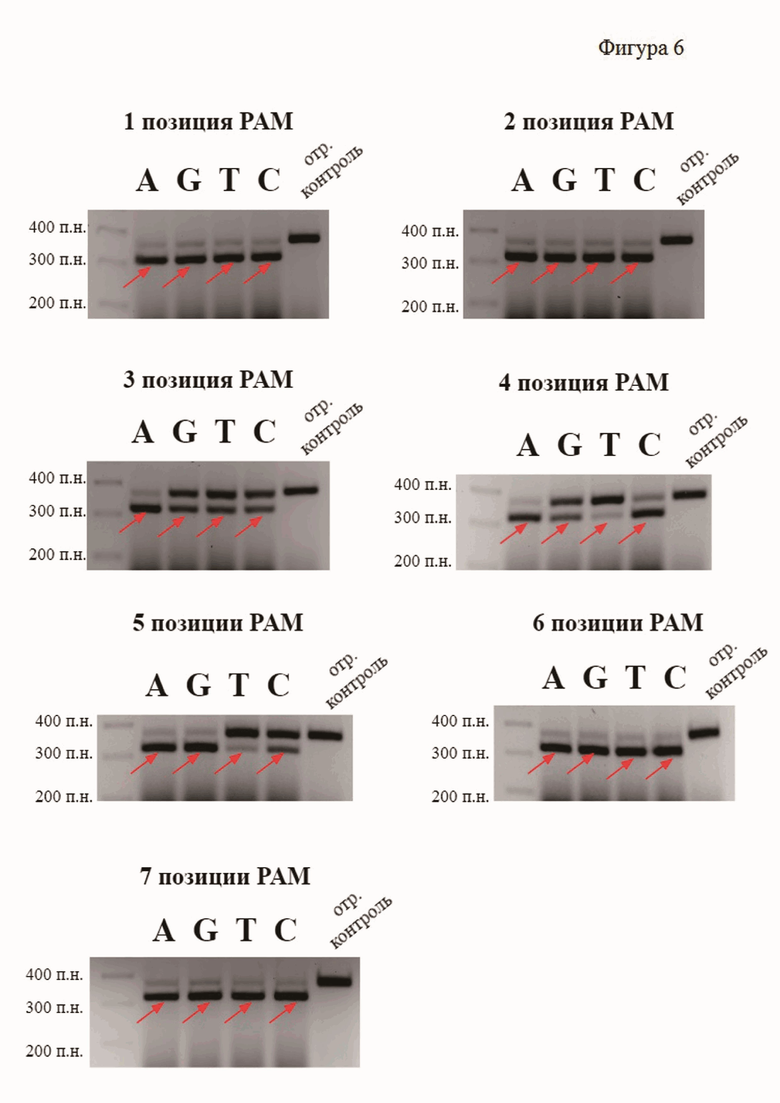
Фиг. 6. Проверка влияния однонуклеотидных замен в каждой позиции PAM на эффективность разрезания нуклеазой SuCas9 ДНК-мишени. В качестве отрицательного контроля выступает образец без добавления направляющей РНК. Красными стрелками отмечено положение разрезанного фрагмента ДНК.
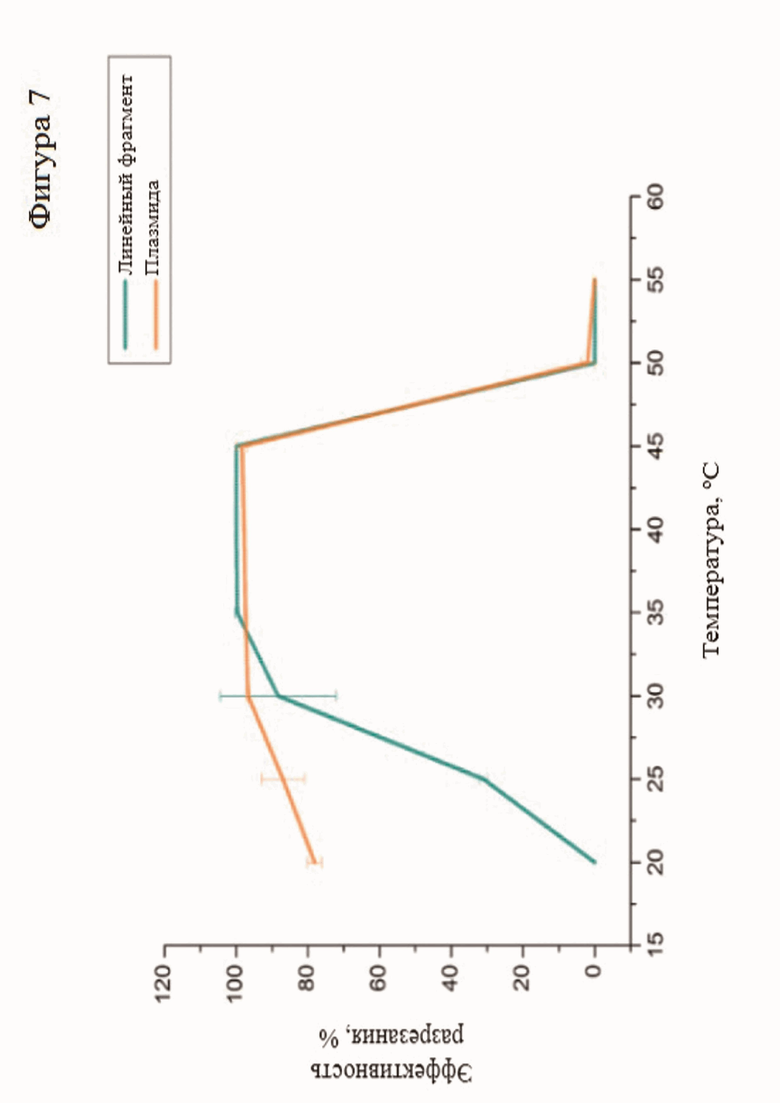
Фиг. 7. Эффективность разрезания ДНК белком SuCas9 при разных температурах. Эффективность разрезания (в процентах) рассчитывали как отношение интенсивности свечения фрагментов ДНК на геле, соответствующих молекулам, разрезанным SuCas9 к суммарной интенсивности свечения ДНК в образце. На графике показаны средние значения и стандартные отклонения, полученные в трех независимых экспериментах.
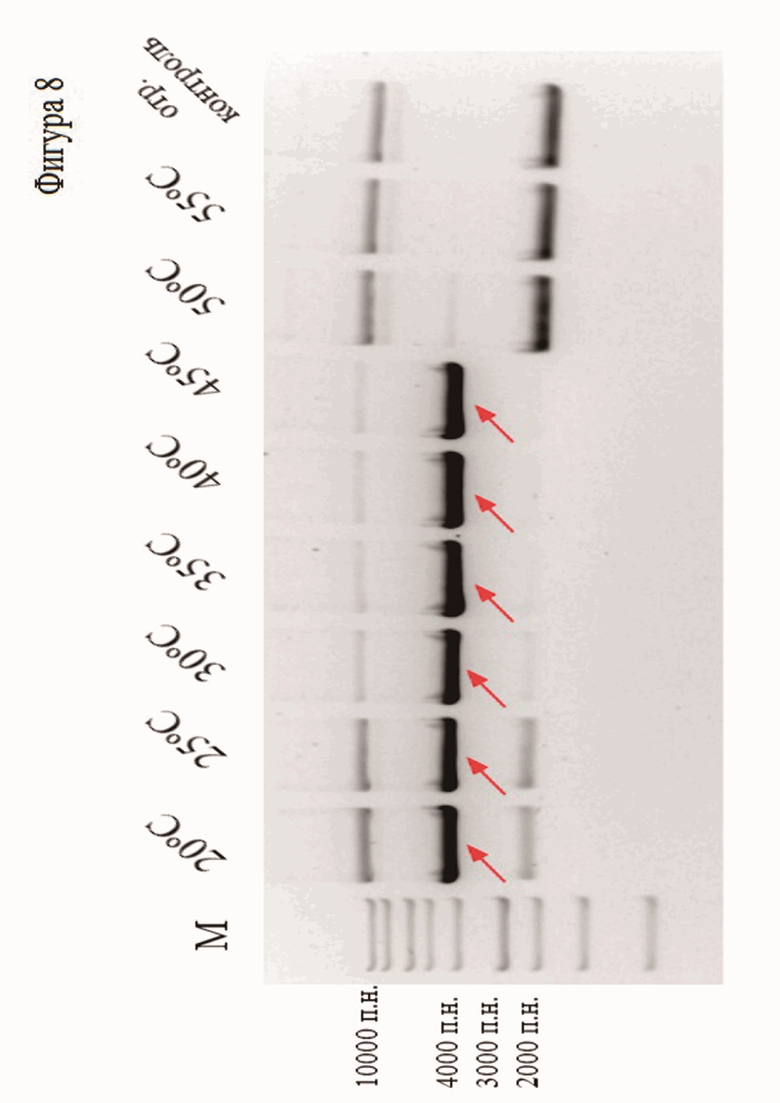
Фиг. 8. Эффективность разрезания плазмидной ДНК белком SuCas9 при разных температурах. SuCas9 инкубировали с трРНК и крРНК и плазмидной ДНК длиной 2,7 т.п.н., содержащим целевые последовательности при указанных температурах в течение 10 минут. Красными стрелками отмечено положение разрезанного фрагмента ДНК.
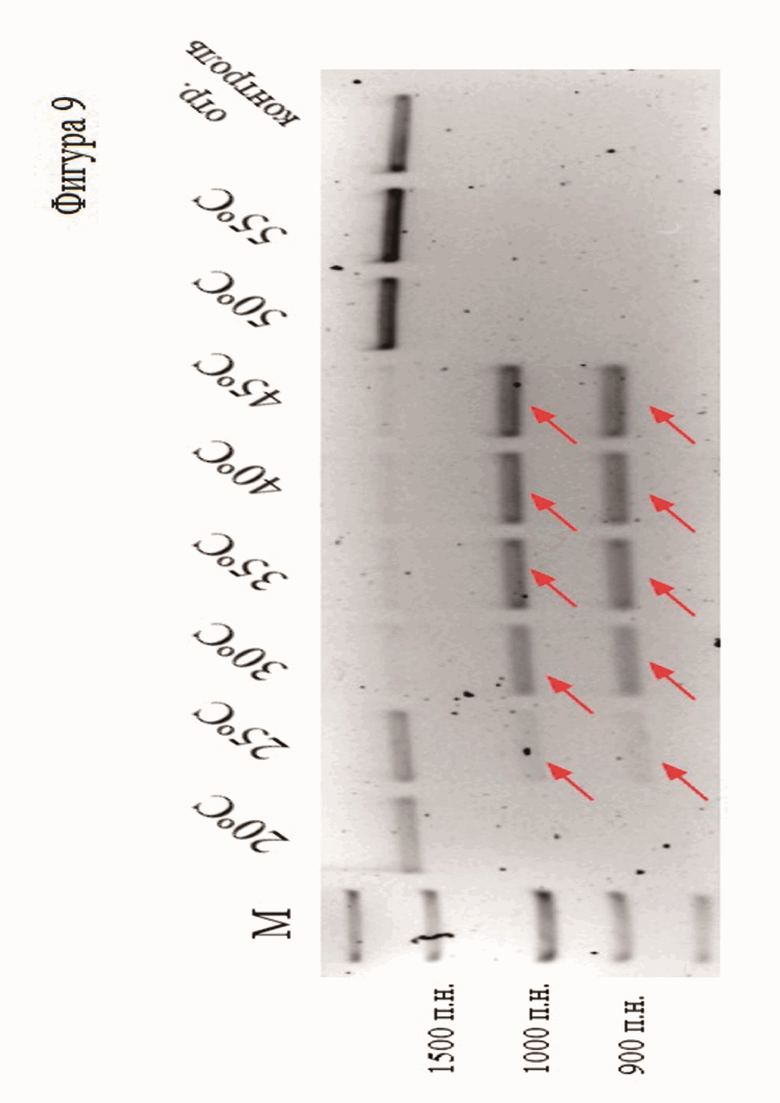
Фиг. 9. Эффективность разрезания линейной ДНК белком SuCas9 при разных температурах. SuCas9 инкубировали с трРНК и крРНК и линейным фрагментом ДНК длиной 1526 п.н., содержащим целевую последовательность при указанных температурах в течение 10 минут. Красными стрелками отмечено положение разрезанного фрагмента ДНК.
Фиг. 10. Сравнение эффективности разрезания SuCas9 нуклеазой ДНК-мишени с последовательностью PAM CCAAAAA при использовании различных форм гРНК и крРНК с трРНК.
Фиг. 11. Выравнивание аминокислотных последовательностей белков SuCas9 и SgoCas9 из Streptococcus gordonii.
Осуществление изобретения
В описании данного изобретения термины «включает» и «включающий» интерпретируются как означающие «включает, помимо всего прочего». Указанные термины не предназначены для того, чтобы их истолковывали как «состоит только из». Если не определено отдельно, технические и научные термины в данной заявке имеют стандартные значения, общепринятые в научной и технической литературе.
Используемый здесь термин «процент гомологии двух последовательностей» эквивалентен термину «процент идентичности двух последовательностей». Идентичность последовательностей определяется на основании референсной последовательности. Алгоритмы для анализа последовательности известны в данной области, такие как BLAST, описанный в Altschul et al. (Basic local alignment search tool // Journal of Molecular Biology. – 1990. – Т. 215. – С. 403-410). Для целей настоящего изобретения для определения уровня идентичности и сходства между нуклеотидными последовательностями и аминокислотными последовательностями может быть использовано сравнение нуклеотидных и аминокислотных последовательностей, производимое с помощью пакета программ BLAST, предоставляемого National Center for Biotechnology Information (http://www.ncbi.nlm.nih.gov/blast) с использованием содержащего разрывы выравнивания со стандартными параметрами. Процент идентичности двух последовательностей определяется числом положений идентичных аминокислот в этих двух последовательностях с учетом числа пробелов и длины каждого пробела, которые необходимо ввести для оптимального сопоставления двух последовательностей путем выравнивания. Процент идентичности равен числу идентичных аминокислот в данных положениях с учетом выравнивания последовательностей, разделенному на общее число положений и умноженному на 100.
Термин «специфически гибридизуется» относится к ассоциации между двумя одноцепочечными молекулами нуклеиновых кислот или в достаточной степени комплементарными последовательностями, что разрешает такую гибридизацию в предопределенных условиях, обычно использующихся в данной области.
Фраза «двунитевой разрыв, расположенный непосредственно перед нуклеотидной последовательностью РАМ» означает, что двунитевой разрыв в целевой последовательности ДНК будет произведен на расстоянии от 0 до 25 нуклеотидов перед нуклеотидной последовательностью РАМ.
Под экзогенной последовательностью ДНК, вводимой одновременно с направляющей РНК, следует понимать последовательность ДНК, подготовленную специально для специфической модификации двуцепочечной целевой ДНК в месте разрыва, определяемого специфичностью направляющей РНК. Подобной модификацией может быть, например, вставка или делеция определенных нуклеотидов в месте разрыва целевой ДНК. Экзогенной ДНК может служить как участок ДНК из другого организма, так и участок ДНК из того же организма, что и целевая ДНК.
Под белком, содержащим определенную аминокислотную последовательность следует понимать белок, имеющий аминокислотную последовательность, составленную из указанной аминокислотной последовательности и, возможно, других последовательностей, соединенных пептидными связями с указанной аминокислотной последовательностью. Примером других последовательностей может служить последовательность сигнала ядерной локализации (NLS), или другие последовательности, обеспечивающие повышенную функциональность для указанной аминокислотной последовательности.
Под экзогенной последовательностью ДНК, вводимой одновременно с направляющей РНК, следует понимать последовательность ДНК, подготовленную специально для специфической модификации двуцепочечной целевой ДНК в месте разрыва, определяемого специфичностью направляющей РНК. Подобной модификацией может быть, например, вставка или делеция определенных нуклеотидов в месте разрыва целевой ДНК. Экзогенной ДНК может служить как участок ДНК из другого организма, так и участок ДНК из того же организма, что и целевая ДНК.
Под эффективным количеством вводимых в клетку белка и РНК следует понимать такое количество белка и РНК, которое при попадании в указанную клетку будет способно образовать функциональный комплекс, то есть комплекс, который будет специфически связываться с целевой ДНК и производить в ней двунитевой разрыв в месте, определяемом направляющей РНК и РАМ последовательностью на ДНК. Эффективность этого процесса может быть оценена при помощи анализа целевой ДНК, выделенной из указанной клетки с помощью стандартных методов, известных специалистам.
Доставка белка и РНК в клетку может быть осуществлена различными способами. Например, белок может быть доставлен в виде ДНК-плазмиды, которая кодирует ген этого белка, как мРНК для трансляции этого белка в цитоплазме клетки, или как рибонуклеопротеидный комплекс, включающий этот белок и направляющую РНК. Доставка может быть осуществлена различными методами, известными специалистам.
Нуклеиновая кислота, кодирующая компоненты системы, может быть введена в клетку, непосредственно или опосредованно: за счет трансфекции или трансформации клеток известными специалистам способами, за счет использования рекомбинантного вируса, за счет манипуляций с клеткой, таких как микроинъекция ДНК и т. п.
Доставка рибонуклеинового комплекса, состоящего из нуклеазы и направляющих РНК и экзогенной ДНК (при необходимости) может осуществляться путем трансфекции комплексов в клетку или за счет механического введения комплекса внутрь клетки, например, микроинъекции.
Молекула нуклеиновой кислоты, кодирующая белок, который необходимо ввести в клетку, может быть интегрирована в хромосому или может представлять собой внехромосомно реплицирующуюся ДНК. В некоторых вариантах для обеспечения эффективной экспрессии гена белка с вводимой в клетку ДНК необходимо изменить последовательность этой ДНК в соответствии с типом клетки в целях оптимизации кодонов при экспрессии, обусловленное неравномерностью частот встречаемости синонимичных кодонов в кодирующих областях генома различных организмов. Оптимизация кодонов необходима для увеличения экспрессии в клетках животных, растений, грибов или микроорганизмов.
Для функционирования белка, имеющего последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности SEQ ID NO: 1, в эукариотической клетке необходимо, чтобы этот белок оказался в ядре этой клетки. Поэтому, в некоторых вариантах изобретения, для образования двунитевых разрывов в целевой ДНК используют белок, имеющий последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности SEQ ID NO: 1, и который дополнительно модифицирован с одного или с обоих концов добавлением одного или нескольких сигналов ядерной локализации. Например, может быть использован сигнал ядерной локализации из вируса SV40. Для эффективной доставки в ядро сигнал ядерной локализации может быть отделен от основной последовательности белка спейсерной последовательностью, например, описанной в Shen B, et al. (Generation of gene-modified mice via Cas9/RNA-mediated gene targeting // Cell Research. – 2013. – Т. 23. – №5. – С. 720-723). Также, в других вариантах осуществления, может быть использован другой сигнал ядерной локализации, или альтернативный метод доставки указанного белка в ядро клетки.
Настоящее изобретение охватывает применение белка из организма Streptococcus uberis NCTC3858, гомологичного ранее охарактеризованным белкам Cas9, для внесения двуцепочечных разрывов в молекулы ДНК в строго определенных положениях. Использование CRISPR нуклеаз для внесения направленных изменений в геном имеет ряд преимуществ. Во-первых, специфичность действия системы определяется последовательностью крРНК, что позволяет использовать один тип нуклеазы для всех локусов-мишеней. Во-вторых, методика позволяет доставить в клетку сразу несколько направляющих РНК, комплементарных разным генам-мишеням, что позволяет осуществлять единовременное изменение сразу нескольких генов.
SuCas9 – Cas нуклеаза, найденная в бактериях Streptococcus uberis NCTC3858, являющихся одним из самых распространенным возбудителем мастита у коров. Streptococcus uberis NCTC3858 CRISPR-Cas9 система (далее CRISPR SuCas9) относится к II C типу CRISPR Cas систем и состоит из CRISPR кассеты, несущей шестнадцать прямых повторов (direct repeats, DR) последовательностью 5'-GTTTTTGTACTCTCAAGATTTAAGTAACTATAAAAC-3' (SEQ ID NO: 2) разделенных последовательностями уникальных спейсеров. Биоинформатический анализ спейсерного состава CRISPR кассеты SuCas9 обнаружил, что несколько спейсеров системы совпадают по последовательности с фрагментами генома бактериофагов, инфицирующих организмы Streptococcus. Анализ протоспейсерных последовательностей с помощью программного обеспечения CRISPRTarget определил несколько мишеней, фланкированных PAM последовательностью 5’-NNAAAR-3’.
К CRISPR кассете прилегает ген эффекторного белка SuCas9. Рядом с Cas геном была обнаружена последовательность, частично комплементарная прямым повторам, складывающаяся в характерную вторичную структуру, - предполагаемая трейсерная РНК (трРНК).
Знание характерной архитектуры РНК-Cas белкового комплекса систем II-C типа позволила предсказать направление транскрипции CRISPR кассеты: пре-крРНК транскрибируется в том же направлении, что и Cas гены (Фиг.1).
Таким образом, анализ последовательности локуса SuCas9 позволил предсказать последовательности трейсерной и направляющих РНК (Таблица 1).
Таблица 1. Определенные биоинформатическиими методами последовательности направляющих РНК системы CRISPR SuCas9. Жирным шрифтом обозначена последовательность прямого повтора DR. Знаками “x” обозначены нуклеотиды вариабельной спейсерной части крРНК.
Для проверки активности SuCas9 нуклеазы и определения требуемого SuCas9 PAM мотива, были проведены эксперименты по воссозданию реакции разрезания ДНК in vitro. Для определения PAM последовательности белка SuCas9 использовали in vitro разрезание двунитевых PAM библиотек. Для этого необходимо было получить все компоненты эффекторного комплекса SuCas9: направляющие РНК и нуклеазу в рекомбинантной форме. Определение последовательности направляющих РНК позволило синтезировать in vitro молекулы крРНК и трРНК. Синтез осуществляли с помощью набора NEB HiScribe T7 RNA synthesis. Двунитевые ДНК библиотеки представляли собой фрагменты размером 374 пар нуклеотидов (п. н.), содержащие последовательность протоспейсера, фланкированную рандомизированными семью нуклеотидами (5'-NNNNNNN-3') c 3' конца:
5'-cccggggtaccacggagagatggtggaaatcatctttctcgtgggcatccttgatggccacctcgtcggaagtgcccacgagg
atgacagcaatgccaatgctgggggggctcttctgagaacgagctctgctgcctgacacggccaggacggccaacaccaaccag
aacttgggagaacagcactccgctctgggcttcatcttcaactcgtcgactccctgcaaacacaaagaaagagcatgttaaaatagg
atctacatcacgtaacctgtcttagaagaggctagatactgcaattcaaggaccttatctcctttcattgagcacNNNNNNNaa
ctccatctaccagcctactctcttatctctggtatt -3' (SEQ ID NO: 4)
Для разрезания этой мишени использовали направляющие РНК следующей последовательности:
трРНК:
5'- AUAGUUACUUAAAUCUUGCUGAGCCUACAAAGAUAAGGCUUCAUGCCGAAUUCAAGCACCCCAUCAUUGAUGGGGUGCUUUUCGUAUUGUG -3' (SEQ ID NO: 3)
и крРНК:
5'-uaucuccuuucauugagcacGUUUUUGUACUCUCAAGAUUUAAGUAACUAUAAAAC -3' (SEQ ID NO: 5)
Жирным шрифтом выделена последовательность крРНК, комплементарная протоспейсеру (целевой ДНК последовательности).
Для получения рекомбинантного белка SuCas9 его ген был клонирован в плазмиду pET21a. В качестве кодирующей ген ДНК, использовалась ДНК, амплифицированная с геномной ДНК Streptococcus uberis NCTC3858, заказанной из коллекции DSMZ (Leibniz Institute DSMZ-German Collection of Microorganisms and Cell Cultures GmbH). Клетки E. coli Rosetta были трансформированы полученной плазмидой pET21a-6xHis-SuCas9.
500 мкл ночной культуры разводили в 500 мл среды LB, и растили клетки при температуре 37°C до достижения оптической плотности 0.6 отн. ед. Синтез целевого белка индуцировали добавлением ИПТГ до концентрации 1 мМ, после чего клетки инкубировали при температуре 16°C в течение 16 часов. Затем проводили центрифугирование клеток на скорости 5000 g в течение 30 минут, полученные осадки клеток замораживали при температуре -20°C.
Осадки размораживали на льду в течение 30 минут, ресуспензировали в 15 мл лизисного буфера (Tris-HCl 50мМ pH 8, 500 мМ NaCl, β-меркаптоэтанол 1мМ, имидазол 10 мМ) с добавлением 15 мг лизоцима и снова инкубировали на льду в течение 30 минут. Затем клетки разрушали воздействием ультразвука в течение 30 минут и центрифугировали в течение 40 минут на скорости 16000 g. Полученный супернатант пропускали через фильтр 0.2 мкм и наносили на колонку HisTrap HP 1 mL (GE Healthcare) на скорости 1 мл/мин.
Хроматографию проводили при помощи FPLC хроматографа AKTA (GE Healthcare) на скорости 1 мл/мин. Колонку с нанесенным белком промывали 20 мл лизисного буфера с добавлением 10 мМ имидазола, после чего белок смывали лизисным буфером с добавлением 300 мМ имидазола.
Затем, фракцию белка, полученную в ходе афинной хроматографии, пропускали через гель-фильтрационную колонку Superdex 200 10/300 GL (24 мл), уравновешенную следующим буфером: Tris-HCl 50 мМ pH 8, 500 мМ NaCl, 1 мМ DTT. При помощи концентратора Аmicon (с фильтром на 30 кДа) фракции, соответствующие мономерной форме белка SuCas9, сконцентрировали до 2 мг/мл, после чего очищенный белок хранили при температуре -80°C в буфере, содержащем 10% глицерин.
In vitro реакцию порезки линейных PAM библиотек проводили в объёме 20 мкл в следующих условиях. Реакционная смесь состояла из: 1X CutSmart буфера (NEB), 5 мМ DTT, 100 нМ PAM-библиотеки, 2 мкМ трРНК/крРНК, 400 нМ белка SuCas9. В качестве контроля аналогичным образом были приготовлены пробы, не содержащие РНК. Пробы инкубировали при различных температурах и анализировали методом гель-электрофореза в 2% агарозном геле. В случае правильного узнавания и специфического разрезания ДНК белком SuCas9 должны формироваться два фрагмента ДНК длиной порядка 326 и 48 пар оснований (см. Фиг. 2).
Результаты опыта показали, что SuCas9 обладает нуклеазной активностью и разрезает часть фрагментов PAM библиотеки (Фиг. 3).
Реакцию разрезания библиотеки повторяли в подобранных условиях. Продукты реакции наносили на 2% агарозный гель и подвергали электрофорезу. Непорезанные фрагменты ДНК длиной 374 п.н. экстрагировали из геля и подготавливали для высокоэффективного секвенирования с помощью набора NEB NextUltra II. Образцы секвенировали на платформе Illumina и далее проводили анализ последовательностей биоформатическими методами: определяли разницу в представленности нуклеотидов в отдельных позициях PAM (NNNNNNN) в сравнении с контрольным образцом. Для анализа результатов было построено PAM лого (Фиг. 4).
PAM лого выявило значимость 3, 4 и 5 позиций в PAM и предпочтение в этих позициях аденину, что находится в согласии с предстказанными PAM последовательностями протоспейсеров бактериофагов. Исходя из этих результатов, была предположена PAM последовательность для SuCas9: 5'-NNAAA-3'.
Для подтверждения наличия нуклеазной активности у SuCas9 проводили реакции разрезания ДНК фрагментов, содержащих ДНК-мишень 5'-atctcctttcattgagcac-3', фланкированную PAM последовательностями, выбранными по результатам PAM скрининга (5’-CCAAAAA-3’, 5’-ACAAAAA-3’, 5’-CCAAACA-3’, 5’-CCAACAA-3’, 5’-AAAAAAA-3’, 5’-CCAAAGA-3’, 5’-CCACAAA-3’, 5’-CAAACAA-3’, 5’-ACCAAAA-3’, 5’-CCAATAA-3’, 5’-AGAAACC-3’, 5’-CCAATGA-3’; последовательности PAM расположены в порядке уменьшения эффективности узнавания согласно результатам анализа PAM скринига).
SuCas9 разрезал большинство мишеней, фланкированных выбранными PAM, менее эффективно разрезав 5’-CAAACAA-3’, 5’-ACCAAAA-3’, 5’-CCAATAA-3’ показавшие меньшую долю разрезания в эксперименте PAM скрининга (Фиг.5).
Далее для уточнения PAM последовательности была произведена проверка значимости отдельных нуклеотидных позиций.
Для этого эксперимента была выбрана последовательность PAM 5’-CCAAAAA-3’, на которой SuCas9 продемонстрировал высокую нуклеазную активность (Фиг. 5).
Реакции разрезания (Фиг. 6) проводили in vitro с использованием ДНК фрагментов, содержащих ДНК-мишень 5'-atctcctttcattgagcac-3', фланкированную PAM последовательностью 5’-CCAAAAA-3’ (или ее производных):
5'-cccggggtaccacggagagatggtggaaatcatctttctcgtgggcatccttgatggccacctcgtcggaagtgcccacgaggat
gacagcaatgccaatgctgggggggctcttctgagaacgagctctgctgcctgacacggccaggacggccaacaccaaccagaact
tgggagaacagcactccgctctgggcttcatcttcaactcgtcgactccctgcaaacacaaagaaagagcatgttaaaataggatctac
atcacgtaacctgtcttagaagaggctagatactgcaattcaaggaccttatctcctttcattgagcacCCAAAAAaactccatcta
ccagcctactctcttatctctggtatt-3' (SEQ ID NO: 6)
Все реакции разрезания ДНК проводили в следующих условиях:
1x CutSmart буфер
200 нM SuCas9
40 нM ДНК
2 мкM крРНК
2 мкM трРНК
Время инкубации - 10 минут, температура проведения реакции 37°C.
Замена нуклеотидов в каждом положении PAM показала, что значимыми являются только 3, 4, 5 позиции, подтвердив результаты PAM скрининга (Фиг.6).
В позициях 3 и 4 SuCas9 требует наличия аденина, в позиции 5 требует аденин или гуанин. (Фиг.5)
В результате проведенных исследований удалось сделать следующий вывод: PAM, распознаваемый нуклеазой SuCas9, соответствует следующей формуле 5'- NNAA(A/G)-3' (5'-NNAAR-3').
Дополнительно был исследован температурный оптимум нуклеазной активности белка SuCas9 (Фиг. 7, Фиг. 8 и Фиг. 9). В результате было показано, что белок активен в диапазоне температур 25–45 °С.
Нижеследующие примеры осуществления способа приведены в целях раскрытия характеристик настоящего изобретения и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения.
Пример 1. Использование гибридной направляющей РНК для разрезания ДНК мишени.
гРНК(гайд РНК) - форма направляющих РНК, которая представляет собой слитые воедино трРНК и крРНК. Для подбора оптимальной гРНК были сконструированы два варианта этой последовательности, отличающиеся длиной трРНК – крРНК дуплекса. РНК синтезировали in vitro и проводили с ними эксперименты по разрезанию ДНК –мишени.
В качестве гибридных РНК были использованы следующие РНК последовательности:
1 - гРНК 1 31DR:
UAUCUCCUUUCAUUGAGCACGUUUUUGUACUCUCAAGAUUUAAGUAACUAUGAAAAUAGUUACUUAAAUCUUGCUGAGCCUACAAAGAUAAGGCUUCAUGCCGAAUUCAAGCACCCCAUCAUUGAUGGGGUGCUUUUCGUAUUGUG (SEQ ID NO: 7)
2 - гРНК 2 36DR
UAUCUCCUUUCAUUGAGCACGUUUUUGUACUCUCAAGAUUUAAGUAACUAUAAAACGAAAAUAGUUACUUAAAUCUUGCUGAGCCUACAAAGAUAAGGCUUCAUGCCGAAUUCAAGCACCCCAUCAUUGAUGGGGUGCUUUUCGUAUUGUG (SEQ ID NO: 8)
Жирным шрифтом обозначена 20-нуклеотидная последовательность, обеспечивающая спаривание с ДНК -мишенью (вариабельная часть гРНК). Кроме того, в эксперименте делали контрольную пробу без РНК, а также положительный контроль - разрезание мишени с помощью крРНК с трРНК.
В качестве ДНК мишени использовалась последовательность, содержащую сайт узнавания 5'-tatctcctttcattgagcac-3' с соответствующим консенсусу PAM CСAAAАА:
5'-cccggggtaccacggagagatggtggaaatcatctttctcgtgggcatccttgatggccacctcgtcggaagtgcccacgagg
atgacagcaatgccaatgctgggggggctcttctgagaacgagctctgctgcctgacacggccaggacggccaacaccaaccag
aacttgggagaacagcactccgctctgggcttcatcttcaactcgtcgactccctgcaaacacaaagaaagagcatgttaaaatagg
atctacatcacgtaacctgtcttagaagaggctagatactgcaattcaaggaccttatctcctttcattgagcacCСAAAААca
actccatctaccagcctactctcttatctctggtatt-3'(SEQ ID NO: 9)
Жирным шрифтом обозначен сайт узнавания, заглавными буквами PAM.
Реакцию проводили в следующих условиях: концентрация ДНК последовательности, содержащей PAM (CСAAAАА) – 40 нM, концентрация белка – 400 нM, концентрация РНК - 2 мкM; время инкубирования - 30 минут, температура инкубирования - 37°С.
Подобранные гРНК 1 и гРНК 2 оказались так же эффективны, как и нативные последовательности трРНК и крРНК (Фиг. 10).
Эти варианты гибридной РНК могут быть использованы для разрезания любой другой целевой ДНК при изменении последовательности, непосредственно спаривающейся с ДНК -мишенью.
Пример 2. Белки Cas9 из близкородственных организмов, относящихся к Streptococcus uberis NCTC3858.
На сегодняшний день в Streptococcus uberis NCTC3858 не охарактеризовано ни одного фермента системы CRISPR-Cas9. Сравнимый по размерам белок SgoCas9 из Streptococcus gordonii (также относится к белкам Cas9) идентичен SuCas9 на 63.92% (Фиг. 11, степень идентичности была рассчитана по программе BLASTp, «default parameters»).
Таким образом, белок SuCas9 существенно отличается по аминокислотной последовательности от других Cas9 белков, изученных на сегодняшний день.
Специалисту в области генетической инженерии очевидно, что полученный и охарактеризованный в данном Описании вариант последовательности белка SuCas9 может быть изменен без изменения функции самого белка (например, направленным мутагенезом аминокислотных остатков, напрямую не влияющих на функциональную активность (Sambrook et al., Molecular Cloning: A Laboratory Manual, (1989), CSH Press, pp. 15.3-15.108)). В частности, специалисту известно, что могут быть изменены неконсервативные аминокислотные остатки, не затрагивающие остатки, определяющие функциональность белка (определяющие его функцию или структуру). Примерами таких изменений могут служить замены неконсервативных аминокислотных остатков на гомологичные. В некоторых вариантах осуществления изобретения возможно использование белка, содержащего аминокислотную последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности SEQ ID NO: 1 и имеет отличия по сравнению с SEQ ID NO: 1 только в неконсервативных аминокислотных остатках, для образования двунитевого разрыва в молекуле ДНК, расположенного непосредственно перед нуклеотидной последовательностью 5'-NNAAR-3' в указанной молекуле ДНК. Гомологичные белки могут быть получены путем мутагенеза (например, сайт-направленного или ПЦР-опосредуемого мутагенеза) соответствующих молекул нуклеиновых кислот с последующим тестированием кодируемого модифицированного белка Cas9 на сохранение его функций в соответствии с описанными здесь функциональными анализами.
Пример 3. Описанная в настоящем изобретении система SuCas9 в комплексе с направляющими РНК может быть использована для изменения последовательности геномной ДНК многоклеточного организма, в том числе эукариотического. Для введения система SuCas9 в комплексе с направляющими РНК в клетки этого организма (во все клетки или в часть клеток) могут быть применены различные подходы, известные специалистам. Например, методы доставки CRISPR-Cas9 систем в клетки организмов раскрыты в источниках (Liu C et al., Delivery strategies of the CRISPR-Cas9 gene-editing system for therapeutic applications. J Control Release. 2017 Nov 28;266:17-26; Lino CA et al., Delivering CRISPR: a review of the challenges and approaches. Drug Deliv. 2018 Nov;25(1):1234-1257), и в источниках, раскрытых внутри этих источников.
Для эффективной экспрессии нуклеазы SuCas9 в эукариотических клетках будет желательно провести оптимизацию кодонов для аминокислотной последовательности белка SuCas9 методами, известными специалистам (например, IDT codon optimization tool).
Для эффективной работы нуклеазы SuCas9 в эукариотических клетках необходимо обеспечить импорт этого белка внутрь ядра эукариотической клетки. Для этого можно использовать сигнал ядерной локализации из Т-антигена вируса SV40 (Lanford et al., Cell, 1986, 46: 575–582), соединённый с последовательностью SuCas9 с помощью спейсерной последовательности, описанной в Shen B, et al. "Generation of gene-modified mice via Cas9/RNA-mediated gene targeting", Cell Res. 2013 May;23(5):720-3 или без нее. Таким образом, полная аминокислотная последовательность нуклеазы, транспортируемой внутрь ядра эукариотической клетки, будет представлять собой следующую последовательность: MAPKKKRKVGIHGVPAA-SuCas9-KRPAATKKAGQAKKKK (далее SuCas9 NLS). Для доставки белка с приведенной выше аминокислотной последовательностью, могут быть использованы по меньшей мере два подхода.
Доставка в виде гена осуществляется путем создания плазмиды, несущей ген SuCas9 NLS под регуляцией промотора (например, CMV промотора) и последовательности, кодирующей направляющие РНК под регуляцией U6 промотора. В качестве ДНК- мишеней используются ДНК последовательности, фланкированные 5'-NNAAR-3', например, последовательности гена grin2b человека:
5’- CTGAAGGAAAGCAAGGCCAG-3’
Таким образом, кассета для экспрессии sgРНК выглядит следующим образом:
gagggcctatttcccatgattccttcatatttgcatatacgatacaaggctgttagagagataattggaattaatttgactgtaaacacaaagatattagtacaaaatacgtgacgtagaaagtaataatttcttgggtagtttgcagttttaaaattatgttttaaaatggactatcatatgcttaccgtaacttgaaagtatttcgatttcttggctttatatatcttgtggaaaggacgaaacaccg CTGAAGGAAAGCAAGGCCAGGTTTTTGTACTCTCAAGATTTAAGTAACTATAAAACGAAAATAGTTACTTAAATCTTGCTGAGCCTACAAAGATAAGGCTTCATGCCGAATTCAAGCACCCCATCATTGATGGGGTGCTTTTCGTATTGTGTTTTTT (SEQ ID NO: 10)
Жирным шрифтом выделена последовательность U6 промотора, далее идет последовательность, необходимая для узнавания целевой ДНК, а далее идет последовательность, образующая структуру гРНК, которая выделена курсивом.
Плазмидную ДНК очищают и трансфицируют в клетки человека HEK293 c помощью реагента Lipofectamine 2000 (Thermo Fisher Scientific). Клетки инкубируют в течение 72 часов, после чего из них выделяется геномная ДНК с помощью колонок для очистки геномной ДНК (Thermo Fisher Scientific). Целевой ДНК сайт анализируется с помощью секвенирования на платформе Illumina с целью определения числа вставок-делеций в ДНК, происходящих в целевом сайте по причине направленного двунитевого разрыва и последующей его репарации.
Для амплификации целевых фрагментов используют праймеры, фланкирующие предположительное место внесения разрыва.
После амплификации пробы готовятся по протоколу реагента Ultra II DNA Library Prep Kit for Illumina (NEB) для подготовки образцов к высокопроизводительному секвенированию. Затем проводится секвенирование на платформе Illumina 300cycles, прямое прочтение. Результаты секвенирования анализируются биоинформатическими методами. В качестве детекции разрезания принимается вставка или делеция нескольких нуклеотидов в целевой последовательности ДНК.
Доставка в виде рибонуклеинового комплекса осуществляется путем инкубации рекомбинантной формы SuCas9 NLS c направляющими РНК в CutSmart буфере (NEB). Рекомбинантный белок получают из бактериальных клеток-продуцентов, очищая его с помощью аффинной хроматографии (NiNTA, Qiagen) разделением по размеру (Superdex 200).
Белок смешивают с РНК в соотношении 1:2 (SuCas9 NLS : гРНК), инкубируют в течение 10 минут на комнатной температуре, затем смесь трансфицируют в клетки.
Далее проводится анализ экстрагированной из них ДНК на предмет вставок-делеций в целевом ДНК сайте (как описано выше).
Охарактеризованная в настоящем изобретении нуклеаза SuCas9 из бактерии Streptococcus uberis NCTC3858 имеет ряд преимуществ относительно ранее охарактеризованных Cas9 белков.
SuCas9 обладает коротким отличным от других известных Cas нуклеаз PAM мотивом, необходимым для функционирования системы.
Известные на сегодняшний день большинство Cas нуклеаз, способных вносить двунитевые разрывы в ДНК, имеют сложные многобуквенные PAM последовательности, ограничивающие выбор последовательностей, пригодных для разрезания. Среди изученных Cas нуклеаз, распознающих короткие PAM, только SuCas9 может распознавать последовательности, фланкированные NNDAR мотивом.
SuСas9 – новая Cas нуклеаза, имеющая простой в использовании PAM, отличающийся от известных на сегодняшний день PAM последовательностей других нуклеаз. Белок SuCas9 разрезает с высокой эффективностью различные ДНК-мишени, в том числе и при 37°С, и может стать основой нового инструмента геномного редактирования.
Несмотря на то, что изобретение описано со ссылкой на раскрываемые варианты воплощения, для специалистов в данной области должно быть очевидно, что конкретные подробно описанные случаи приведены лишь в целях иллюстрирования настоящего изобретения, и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения. Должно быть, понятно, что возможно осуществление различных модификаций без отступления от сути настоящего изобретения.
--->
<110> Федеральное государственное бюджетное учреждение науки Институт биологии
гена Российской академии наук (Institute of Gene Biology Russian Academy
of Sciences)
<120> Средство разрезания ДНК на основе Cas9 белка из бактерии Streptococcus
uberis NCTC3858
<160> 10
<210> 1
<211> 1126
<212> PRT
<213> Streptococcus uberis NCTC3858
<400> 1
MTNGMILGLD IGVASVGVGI IEADSGKIVH ASSRIFPSAN ADNNVDRRKF RGSRRLLRRK 60
KHRVKRLQDL FDKYDIVTNF DNLNLNPYEL RVKGLNEPLS NEELFASLRN ITKHRGISYL 120
DDGEDDSSGN GTEYAKAIEL NQQLLKEKTP GQIQFDRLNQ YGQLRGNFDI VDENGEIHHV 180
INVFSTSSYR KEAEQILKKQ SETNTSISTD FINDFIQLLI SKRKYYHGPG NPKSRTDYGR 240
YRTDGTDLDN IFDVLIGKCS FYPEEYRASK TSYTAQEFNF LNDLNNLTLP TETGKLSEQQ 300
KIDLVNWAKE TKILGPKKLL QEIAKRNNCK FEDIRGYRLD NKDNPDMHVF DVYRKMNFDL 360
ETISVKDLSV DSLNQLARIL TLNTEREGIE EAIKKLMPNQ FTEKQMLELI AFRKSNSSIF 420
GKGWHSLSIK LMKELIPELY HTSDEQMTIL NRFGKFKLTK LDSKRTNYID ENSVTDEIYN 480
PVVAKSVRQA IKIINASIKK WGDFDKIVIE MPRDKNEEEE RKRIADGQKV NAKEKEQAEK 540
HAAKLFNGKE ELPSEVFHGY KELALRIRLW YQQDQKCLYS GKEITISDLI YNRELFEIDH 600
ILPLSLSFDD SLSNKVLVYC WANQEKGQRT PFQALDSMKS AWSYREFKNA ILHNSKISRK 660
KRDYFLTEQD ISKIEVKQKF IERNLVDTRY ASRTVLNVLQ QSLKNLEKET KVSVVRGQFT 720
SQLRRKWHID KTRDTYHHHA VDALIIAASA KLRYWKKQGD ILFENYLINR HVDRVTGEIQ 780
SDDSYKEEVF TPPYDGFVQT ISNPGFEDEI LFSYQVDSKV NRKISDATIY ATRSAKLEKD 840
KKEQTYVLGK IKDIYSQTGF ENFLKIYNKD KSKFLIYQKD PETWEKIIEP ILKNYREFDN 900
KGKDIVNPFE KYRNDNGPIC KYSRKGNGPE IKQFKYYDTV LGKYIEITPE SSRNIVALRS 960
LNPWRTDVYF NEKTLKYEFL GLKYSDLNIQ NKEEYGISEE NYQKIKKEEG VSEESIFKFT 1020
LYRNDLIIIK DLSKGKSQIF RFWSRTGKVN EKHKLELKPY NKSSFEKGES LEVIRNLYPS 1080
SNQFQEKLNK SDLSIYKLKT DILGNKFISK NENLFPKLIY KKIKRK 1126
<210> 2
<211> 36
<212> ДНК
<213> Streptococcus uberis
<400> 2
gtttttgtac tctcaagatt taagtaacta taaaac 36
<210> 3
<211> 91
<212> РНК
<213> artificial sequence
<220>
<223> SuCas9 трРНК
<400> 3
auaguuacuu aaaucuugcu gagccuacaa agauaaggcu ucaugccgaa uucaagcacc 60
ccaucauuga uggggugcuu uucguauugu g 91
<210> 4
<211> 374
<212> ДНК
<213> artificial sequence
<220>
<223> ДНК-библиотека
<400> 4
cccggggtac cacggagaga tggtggaaat catctttctc gtgggcatcc ttgatggcca 60
cctcgtcgga agtgcccacg aggatgacag caatgccaat gctggggggg ctcttctgag 120
aacgagctct gctgcctgac acggccagga cggccaacac caaccagaac ttgggagaac 180
agcactccgc tctgggcttc atcttcaact cgtcgactcc ctgcaaacac aaagaaagag 240
catgttaaaa taggatctac atcacgtaac ctgtcttaga agaggctaga tactgcaatt 300
caaggacctt atctcctttc attgagcacN NNNNNNaact ccatctacca gcctactctc 345
ttatctctgg tatt 374
<210> 5
<211> 56
<212> РНК
<213> artificial sequence
<220>
<223> крРНК
<400> 5
uaucuccuuu cauugagcac GUUUUUGUAC UCUCAAGAUU UAAGUAACUA UAAAAC 56
<210> 6
<211> 374
<212> ДНК
<213> artificial sequence
<220>
<223> ДНК-библиотека, содержащих ДНК-мишень 5'-atctcctttcattgagcac-3',
фланкированную PAM последовательностью 5’-CCAAAAA-3’ (или ее производных)
<400> 6
cccggggtac cacggagaga tggtggaaat catctttctc gtgggcatcc ttgatggcca 60
cctcgtcgga agtgcccacg aggatgacag caatgccaat gctggggggg ctcttctgag 120
aacgagctct gctgcctgac acggccagga cggccaacac caaccagaac ttgggagaac 180
agcactccgc tctgggcttc atcttcaact cgtcgactcc ctgcaaacac aaagaaagag 240
catgttaaaa taggatctac atcacgtaac ctgtcttaga agaggctaga tactgcaatt 300
caaggacctt atctcctttc attgagcacC CAAAAAaact ccatctacca gcctactctc 345
ttatctctgg tatt 374
<210> 7
<211> 146
<212> РНК
<213> artificial sequence
<220>
<223> гРНК 1 31DR
<400> 7
uaucuccuuu cauugagcac guuuuuguac ucucaagauu uaaguaacua ugaaaauagu 60
uacuuaaauc uugcugagcc uacaaagaua aggcuucaug ccgaauucaa gcaccccauc 120
auugaugggg ugcuuuucgu auugug 146
<210> 8
<211> 151
<212> РНК
<213> artificial sequence
<220>
<223> гРНК 2 36DR
<400> 8
uaucuccuuu cauugagcac guuuuuguac ucucaagauu uaaguaacua uaaaacgaaa 60
auaguuacuu aaaucuugcu gagccuacaa agauaaggcu ucaugccgaa uucaagcacc 120
ccaucauuga uggggugcuu uucguauugu g 151
<210> 9
<211> 375
<212> ДНК
<213> artificial sequence
<220>
<223> ДНК мишень, содержащую сайт узнавания 5'-tatctcctttcattgagcac-3'
с соответствующим консенсусу PAM CСAAAАА
<400> 9
cccggggtac cacggagaga tggtggaaat catctttctc gtgggcatcc ttgatggcca 60
cctcgtcgga agtgcccacg aggatgacag caatgccaat gctggggggg ctcttctgag 120
aacgagctct gctgcctgac acggccagga cggccaacac caaccagaac ttgggagaac 180
agcactccgc tctgggcttc atcttcaact cgtcgactcc ctgcaaacac aaagaaagag 240
catgttaaaa taggatctac atcacgtaac ctgtcttaga agaggctaga tactgcaatt 300
caaggacctt atctcctttc attgagcacC СAAAААcaac tccatctacc agcctactct 345
cttatctctg gtatt 375
<210> 10
<211> 408
<212> ДНК
<213> artificial sequence
<220>
<223> кассета для экспрессии sgРНК
<400> 10
gagggcctat ttcccatgat tccttcatat ttgcatatac gatacaaggc tgttagagag 60
ataattggaa ttaatttgac tgtaaacaca aagatattag tacaaaatac gtgacgtaga 120
aagtaataat ttcttgggta gtttgcagtt ttaaaattat gttttaaaat ggactatcat 180
atgcttaccg taacttgaaa gtatttcgat ttcttggctt tatatatctt gtggaaagga 240
cgaaacaccg ctgaaggaaa gcaaggccag gtttttgtac tctcaagatt taagtaacta 300
taaaacgaaa atagttactt aaatcttgct gagcctacaa agataaggct tcatgccgaa 345
ttcaagcacc ccatcattga tggggtgctt ttcgtattgt gtttttt 408
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СИСТЕМА РЕДАКТИРОВАНИЯ ГЕНОМНОЙ ДНК ЭУКАРИОТИЧЕСКОЙ КЛЕТКИ НА ОСНОВЕ НУКЛЕОТИДНОЙ ПОСЛЕДОВАТЕЛЬНОСТИ, КОДИРУЮЩЕЙ БЕЛОК SUCAS9NLS | 2022 |
|
RU2804422C1 |
| Средство разрезания ДНК на основе Cas9 белка из бактерии Capnocytophaga ochracea | 2021 |
|
RU2778156C1 |
| СРЕДСТВО РАЗРЕЗАНИЯ ДНК НА ОСНОВЕ CAS9 БЕЛКА ИЗ БАКТЕРИИ DEMEQUINA SEDIMINICOLA | 2019 |
|
RU2722933C1 |
| Средство разрезания ДНК на основе ScCas12a белка из бактерии Sedimentisphaera cyanobacteriorum | 2022 |
|
RU2791447C1 |
| ПРИМЕНЕНИЕ CAS9 БЕЛКА ИЗ БАКТЕРИИ PASTEURELLA PNEUMOTROPICA ДЛЯ МОДИФИКАЦИИ ГЕНОМНОЙ ДНК В КЛЕТКАХ | 2019 |
|
RU2724470C1 |
| СРЕДСТВО РАЗРЕЗАНИЯ ДНК НА ОСНОВЕ CAS9 БЕЛКА ИЗ DEFLUVIIMONAS SP. | 2018 |
|
RU2712492C1 |
| СРЕДСТВО РАЗРЕЗАНИЯ ДНК НА ОСНОВЕ CAS9 БЕЛКА ИЗ БАКТЕРИИ PASTEURELLA PNEUMOTROPICA | 2019 |
|
RU2722934C1 |
| Средство разрезания ДНК на основе Cas9 белка из биотехнологически значимой бактерии Clostridium cellulolyticum | 2018 |
|
RU2712497C1 |
| Средство разрезания двунитевой ДНК с помощью Cas12d белка из Katanobacteria и гибридной РНК, полученной путем слияния направляющей CRISPR РНК и scout РНК | 2020 |
|
RU2771626C1 |
| Средство обнаружения нуклеиновых кислот на основе ScCas12a белка из бактерии Sedimentisphaera cyanobacteriorum | 2023 |
|
RU2820345C1 |



Изобретение относится к области биотехнологии, в частности к применению нуклеазы Cas9 для образования двунитевого разрыва в молекуле ДНК. Также раскрыт способ изменения последовательности геномной ДНК одноклеточного или многоклеточного организма, включающий введение в по меньшей мере одну клетку этого организма эффективного количества вышеуказанной нуклеазы Cas9. Изобретение эффективно для повышения универсальности доступных систем CRISPR-Cas9 и позволяет использовать нуклеазу Cas9 для разрезания геномной или плазмидной ДНК в большем количестве специфических сайтов и специфических условий. 2 н. и 3 з.п. ф-лы, 11 ил., 1 табл., 3 пр.
1. Применение белка, содержащего аминокислотную последовательность SEQ ID NO: 1 или содержащего аминокислотную последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности SEQ ID NO: 1 и имеет отличия по сравнению с SEQ ID NO: 1 только в неконсервативных аминокислотных остатках, для образования двунитевого разрыва в молекуле ДНК, расположенного непосредственно перед нуклеотидной последовательностью 5'-NNAAR-3' в указанной молекуле ДНК.
2. Применение белка по п. 1, характеризующееся тем, что образование двунитевого разрыва в молекуле ДНК происходит при температуре от 25 до 45°C.
3. Применение белка по п. 1, где белок содержит аминокислотную последовательность SEQ ID NO: 1.
4. Способ изменения последовательности геномной ДНК одноклеточного или многоклеточного организма, включающий введение в по меньшей мере одну клетку этого организма эффективного количества: а) либо белка, содержащего аминокислотную последовательность SEQ ID NO: 1, либо нуклеиновой кислоты, кодирующей белок, содержащий аминокислотную последовательность SEQ ID NO: 1, и б) либо направляющей РНК, содержащей последовательность, образующую дуплекс с нуклеотидной последовательностью участка геномной ДНК организма, непосредственно примыкающей к нуклеотидной последовательности 5'-NNAAR-3', и взаимодействующей с указанным белком после образования дуплекса, либо последовательности ДНК, кодирующей указанную направляющую РНК;
при этом взаимодействие указанного белка с направляющей РНК и нуклеотидной последовательностью 5'-NNAAR-3' приводит к образованию двунитевого разрыва в последовательности геномной ДНК, непосредственно примыкающей к последовательности 5'-NNAAR-3'.
5. Способ по п. 4, дополнительно включающий введение экзогенной последовательности ДНК одновременно с направляющей РНК.
| База данных: NCBI Reference Sequence: WP_037591994.1, 28.02.2022 | |||
| Средство разрезания ДНК на основе Cas9 белка из биотехнологически значимой бактерии Clostridium cellulolyticum | 2018 |
|
RU2712497C1 |
| ZIYING HU et al., A compact Cas9 ortholog from Staphylococcus Auricularis (SauriCas9) expands the DNA targeting scope, e | |||
| PLoS Biol, 2020, 18(3): e3000686 | |||
| F | |||
| ANN RAN et al., In vivo genome editing using Staphylococcus aureus Cas9, Nature | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
Авторы
Даты
2023-01-17—Публикация
2022-03-16—Подача