Изобретения относятся к области органической химии, а именно к новым индивидуальным соединениям класса метил 3-ароил-1-(1,5-диметил-3-оксо-2-фенил-2,3-дигидро-1Н-пиразол-4-ил)-4-гидрокси-5-оксо-2-хлор-2,5-дигидро-1Н-пиррол-2-карбоксилатов, обладающих противомикробной активностью, и способу их получения. Данные соединения могут использоваться также для синтеза новых гетероциклических соединений и лекарственных препаратов в фармакологии.
Известен структурный аналог заявленных соединений [Gang Sun, Yuxi Sun, Cheng Yu, Zengwei Liu , Changliang Huang , Laixiang Xu. Synthesis, crystal structure, vibrational spectral and density functional studies of 4-(2,5-dioxo-2H-pyrrol-1(5H)-yl)antipyrine. Journal of Molecular Structure, 2011, vol. 1006, no. 1-3, pp. 383-394], который получают по следующей схеме:
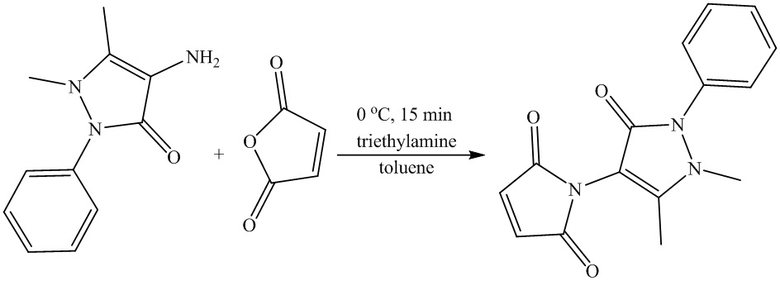
К недостаткам данного способа относится невозможность получения метил 3-ароил-1-(1,5-диметил-3-оксо-2-фенил-2,3-дигидро-1Н-пиразол-4-ил)-4-гидрокси-5-оксо-2-хлор-2,5-дигидро-1Н-пиррол-2-карбоксилатов.
Задачей изобретения является разработка простого способа синтеза неописанных в литературе метил 3-ароил-1-(1,5-диметил-3-оксо-2-фенил-2,3-дигидро-1Н-пиразол-4-ил)-4-гидрокси-5-оксо-2-хлор-2,5-дигидро-1Н-пиррол-2-карбоксилатов, проявляющих противомикробную активность и которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем.
Поставленная задача решается путем взаимодействия метил 4-арил-2-(1,5-диметил-3-оксо-2-фенил-2,3-дигидро-1Н-пиразол-4-иламино)-4-оксо-2-бутеноатов (Iа-д) с оксалилхлоридом (II), взятыми в соотношении 1:1 при температуре 40-61°С в течение 10-30 минут по схеме:
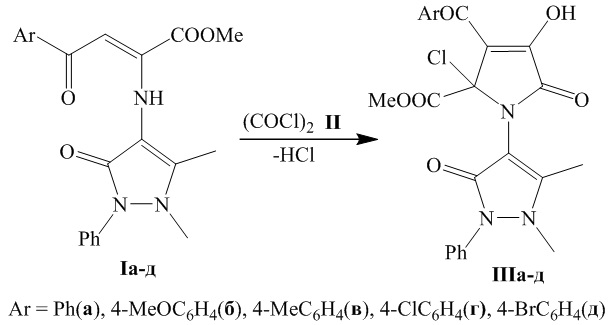
Поставленная задача также решается применением метил 3-(4-бромбензоил)-1-(1,5-диметил-3-оксо-2-фенил-2,3-дигидро-1Н-пиразол-4-ил)-4-гидрокси-5-оксо-2-хлор-1Н-пиррол-2-карбоксилата в качестве средства, обладающего противомикробной активностью.
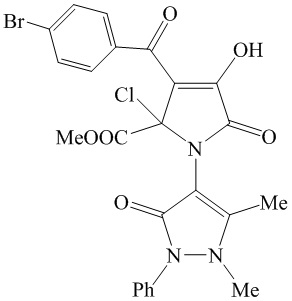
Из патентной и технической литературы не были выявлены способы получения метил 3-ароил-1-(1,5-диметил-3-оксо-2-фенил-2,3-дигидро-1Н-пиразол-4-ил)-4-гидрокси-5-оксо-2-хлор-2,5-дигидро-1Н-пиррол-2-карбоксилатов, имеющие сходные признаки с заявляемым способом, а именно не использовались исходные продукты и интервал времени реакции.
Также неизвестно применение метил 3-(4-бромбензоил)-1-(1,5-диметил-3-оксо-2-фенил-2,3-дигидро-1Н-пиразол-4-ил)-4-гидрокси-5-оксо-2-хлор-1Н-пиррол-2-карбоксилата в качестве средства, обладающего противомикробной активностью. На основании этого можно сделать вывод о соответствии заявленных технических решений критерию «новизна» и «изобретательный уровень».
Изобретения иллюстрируются следующими примерами.
Пример 1. Метил 3-бензоил-1-(1,5-диметил-3-оксо-2-фенил-2,3-дигидро-1Н-пиразол-4-ил)-4-гидрокси-5-оксо-2-хлор-1Н-пиррол-2-карбоксилат (IIIа).
Получение (IIIа): Соединение (Iа) 1,955 г (5 ммоль) смешивают с 25 мл безводного дихлорметана, добавляют в смесь 0,6355 г (5 ммоль) соединения (II). Нагревают реакционную смесь в течение 30 минут при температуре 40°С, затем остужают до температуры 20-22°С. Выпавшие кристаллы фильтруют, сушат. Выход 2,047 г (85%), т.пл. 165-167°С (с разложением).
Соединения (IIIа) - светло-желтое кристаллическое вещество, легкорастворимое в ДМСО, ДМФА, ацетонитриле, труднорастворимое в этилацетате и ацетоне, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях.
Спектр ЯМР 1Н соединения (IIIа) снят в растворе ДМСО-d6 при частоте 400 МГц, δ, м.д.: 2.17 с (3H, Me-С), 3.20 с (3H, Me-N), 3.64 с (3H, OMe), 7.34-7.80 гр.с (10Н, 2Ph), 12.10 (1Н, уш.с, ОН).
Спектр ЯМР 13С соединения (IIIа) снят в растворе ДМСО-d6 при частоте 100 МГц, δ, м.д.: 188.3, 168.3, 164.8, 161.2 (2C), 155.0, 137.7, 134.6, 132.6, 129.1 (2C), 128.8, 128.0, 126.8, 124.3, 119.3, 101.2, 52.5, 35.6, 10.6.
Соединение (IIIа) C24H20ClN3O6. Найдено, %: С 60.08, H 4.15, N 8.59, Сl 7.62. Вычислено, %: С 59.82, H 4.18, N 8.72, Cl 7.36.
Пример 2. Метил 1-(1,5-диметил-3-оксо-2-фенил-2,3-дигидро-1Н-пиразол-4-ил)-3-(4-метоксибензоил)-4-гидрокси-5-оксо-2-хлор-1Н-пиррол-2-карбоксилат (IIIб).
Получение (IIIб): Соединение (Iб) 2,105 г (5 ммоль) смешивают с 25 мл безводного дихлорметана, добавляют в смесь 0,6355 г (5 ммоль) соединения (II). Нагревают реакционную смесь в течение 20 минут при температуре 40°С, затем остужают до температуры 20-22°С. Выпавшие кристаллы фильтруют, сушат. Выход 2,300 г (90%), т.пл. 196-198°С (с разложением).
Соединения (IIIб) - светло-желтое кристаллическое вещество, легкорастворимое в ДМСО, ДМФА, ацетонитриле, труднорастворимое в этилацетате и ацетоне, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях.
Спектр ЯМР 1Н соединения (IIIб) снят в растворе ДМСО-d6 при частоте 400 МГц, δ, м.д.: 2.16 с (3H, Me-С), 3.19 с (3H, Me-N), 3.63 с (3H, OMe), 3.86 с (3H, MeO-С6H4), 7.29-7.82 гр.с (9Н, Ph,С6H4), 12.15 (1Н, уш.с, ОН).
Спектр ЯМР 13С соединения (IIIб) снят в растворе ДМСО-d6 при частоте 100 МГц, δ, м.д.: 186.7, 168.9, 164.9, 163.0, 161.2 (2C), 155.0, 134.6, 131.4, 130.2, 129.1 (2C), 126.8, 124.4, 119.8, 113.4, 101.3, 55.5, 52.5, 35.2, 10.6.
Соединение (IIIб) C25H22ClN3O7. Найдено, %: С 58.74, H 4.39, N 8.14, Cl 7.13. Вычислено, %: С 58.66, H 4.33, N 8.21, Cl 6.92.
Пример 3. Метил 1-(1,5-диметил-3-оксо-2-фенил-2,3-дигидро-1Н-пиразол-4-ил)-3-(4-метилбензоил)-4-гидрокси-5-оксо-2-хлор-1Н-пиррол-2-карбоксилат (IIIв).
Получение (IIIв): Соединение (Iв) 2,025 г (5 ммоль) смешивают с 25 мл безводного дихлорметана, добавляют в смесь 0,6355 г (5 ммоль) соединения (II). Нагревают реакционную смесь в течение 10 минут при температуре 61°С, затем остужают до температуры 20-22°С. Выпавшие кристаллы фильтруют, сушат. Выход 2,203 г (89%), т.пл. 177-179°С (с разложением).
Соединения (IIIв) - светло-желтое кристаллическое вещество, легкорастворимое в ДМСО, ДМФА, ацетонитриле, труднорастворимое в этилацетате и ацетоне, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях.
Спектр ЯМР 1Н соединения (IIIв) снят в растворе ДМСО-d6 при частоте 400 МГц, δ, м.д.: 2.18 с (3H, Me-С), 2.39 с (3H, Me-С6H4), 3.21 с (3H, Me-N), 3.64 с (3H, OMe), 7.31-7.72 гр.с (9Н, Ph,С6H4), 12.13 (1Н, уш.с, ОН).
Спектр ЯМР 13С соединения (IIIв) снят в растворе ДМСО-d6 при частоте 100 МГц, δ, м.д.: 187.9, 168.4, 164.9, 161.2 (2C), 155.0, 143.0, 135.1, 134.5, 129.1 (2C), 129.0, 128.6, 126.8, 124.4, 119.6, 101.3, 52.5, 35.2, 21.1, 10.6.
Соединение (IIIв) C25H22ClN3O6. Найдено, %: С 60.14, H 4.45, N 8.26, Сl 7.32. Вычислено, %: С 60.55, H 4.47, N 8.47, Сl 7.15.
Пример 4. Метил 1-(1,5-диметил-3-оксо-2-фенил-2,3-дигидро-1Н-пиразол-4-ил)-3-(4-хлорбензоил)-4-гидрокси-5-оксо-2-хлор-1Н-пиррол-2-карбоксилат (IIIг).
Получение (IIIг): Соединение (Iг) 2,125 г (5 ммоль) смешивают с 25 мл безводного дихлорметана, добавляют в смесь 0,6355 г (5 ммоль) соединения (II). Нагревают реакционную смесь в течение 10 минут при температуре 40°С, затем остужают до температуры 20-22°С. Выпавшие кристаллы фильтруют, сушат. Выход 2,292 г (89%), т.пл. 186-188°С (с разложением).
Соединения (IIIг) - светло-желтое кристаллическое вещество, легкорастворимое в ДМСО, ДМФА, ацетонитриле, труднорастворимое в этилацетате и ацетоне, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях.
Спектр ЯМР 1Н соединения (IIIг) снят в растворе ДМСО-d6 при частоте 400 МГц, δ, м.д.: 2.17 с (3H, Me-С), 3.19 с (3H, Me-N), 3.63 с (3H, OMe), 7.33-7.80 гр.с (9Н, Ph,С6H4), 12.18 (1Н, уш.с, ОН).
Спектр ЯМР 13С соединения (IIIг) снят в растворе ДМСО-d6 при частоте 100 МГц, δ, м.д.: 187.1, 168.1, 164.6, 161.2 (2C), 155.0, 137.4, 136.4, 134.5, 130.7, 129.1 (2C), 128.2, 126.8, 124.4, 119.1, 101.2, 52.6, 35.1, 10.6.
Соединение (IIIг) C24H18Cl2N3O6. Найдено, %: С 54.06, H 3.65, N 8.48, Cl 13.55. Вычислено, %: С 55.83, H 3.71, N 8.14, Cl 13.43.
Пример 5. Метил 3-(4-бромбензоил)-1-(1,5-диметил-3-оксо-2-фенил-2,3-дигидро-1Н-пиразол-4-ил)-4-гидрокси-5-оксо-2-хлор-1Н-пиррол-2-карбоксилат (IIIд).
Получение (IIIд): Соединение (Iд) 2,345 г (5 ммоль) смешивают с 25 мл безводного дихлорметана, добавляют в смесь 0,6355 г (5 ммоль) соединения (II). Нагревают реакционную смесь в течение 10 минут при температуре 40°С, затем остужают до температуры 20-22°С. Выпавшие кристаллы фильтруют, сушат. Выход 2,432 г (87%), т.пл. 176-178°С (с разложением).
Соединения (IIIд) - светло-желтое кристаллическое вещество, легкорастворимое в ДМСО, ДМФА, ацетонитриле, труднорастворимое в этилацетате и ацетоне, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях.
Спектр ЯМР 1Н соединения (IIIд) снят в растворе ДМСО-d6 при частоте 400 МГц, δ, м.д.: 2.18 с (3H, Me-С), 3.21 с (3H, Me-N), 3.64 с (3H, OMe), 7.34-7.73 гр.с (9Н, Ph,С6H4), 12.11 (1Н, уш.с, ОН).
Спектр ЯМР 13С соединения (IIIд) снят в растворе ДМСО-d6 при частоте 100 МГц, δ , м.д.: 187.3, 168.2, 164.6, 161.1 (2C), 155.0, 137.4, 136.7, 134.5, 130.8, 129.1 (2C), 126.8, 126.5, 124.4, 119.0, 101.1, 52.6, 35.2, 10.6.
Соединение (IIIд) C24H18BrClN3O6. Найдено, %: С 51.17, H 3.45, N 7.21, Br 14.54, Cl 6.09. Вычислено, %: С 51.40, H 3.42, N 7.49, Br 14.25, Cl 6.32.
Пример 6. Фармакологическое исследование соединения (IIIд) на наличие противомикробной активности.
Для исследований использовали общепринятый метод двукратных серийных разведений в жидкой питательной среде микрометодом [Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ - М.: И-во Медицина, 2005]. Готовили исходные разведения микроорганизмов в физиологическом растворе из суточной агаровой культуры по оптическому стандарту мутности (ОСО) на 5 МЕ с использованием денситометра. После ряда разведений конечная концентрация клеток в опыте составляла 2,5×105 клеток/мл.
Противомикробные свойства химических веществ изучали на 3-х коллекционных условно-патогенных штаммах микроорганизмов: Staphylococcus aureus (АТСС 25923), Escherichia coli (АТСС 25922), Candida albicans ( РКПГY 1353/1277).
Результаты исследования противомикробных свойств
Примечание: *МИК - минимальная ингибирующая концентрация; **МБК - минимальная бактерицидная концентрация
В лунках стерильного 96 луночного плоскодонного микропланшета готовили два параллельных ряда двукратных серийных разведений химических соединений в бульоне РПБ, Сабуро. В каждой лунке содержалось 150мкл определенной концентрации испытуемого вещества и 150 мкл инокулята культуры. В последних рядах содержалась питательная среда и культура в равных объемах (контроль). Максимально испытанная концентрация соответствовала 1000,0 мкг/мл, минимальная - 1,0 мкг/мл. Микропланшет помещали в термостат спектрофотометра Epoch и замеряли оптическую плотности (ОП) при длине волны 540нм. Через 24 часа и 7 суток вновь регистрировали ОП культуральной жидкости.
Результаты оценивали с помощью программного обеспечения Gen 5 спектрофотометра для микропланшет Epoch. Последняя лунка ряда с задержкой роста и показателями ОП равной оптической плотности контрольной лунки соответствует минимальной подавляющей концентрацией соединения.
Умеренным антимикробным действием обладает соединение ЛВА-75, ингибирует рост культур S. аureus и C. albicans в концентрациях 125,0-250,0 мкг/мл.
Предлагаемый способ прост в осуществлении, и позволяет получить новые индивидуальные соединения класса метил 3-ароил-1-(1,5-диметил-3-оксо-2-фенил-2,3-дигидро-1Н-пиразол-4-ил)-4-гидрокси-5-оксо-2-хлор-2,5-дигидро-1Н-пиррол-2-карбоксилаты, обладающие противомикробной активностью. Заявляемые соединения могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем и лекарственных препаратов в фармакологии.
Изобретение относится к новым соединениям - метил 3-ароил-1-(1,5-диметил-3-оксо-2-фенил-2,3-дигидро-1Н-пиразол-4-ил)-4-гидрокси-5-оксо-2-хлор-2,5-дигидро-1Н-пиррол-2-карбоксилатам, где Ar означает Ph (IIIа), 4-MeOC6H4 (IIIб), 4-MeC6H4 (IIIв), 4-ClC6H4 (IIIг) или 4-BrC6H4 (IIIд), и способу их получения. Соединения обладают противомикробной активностью и могут быть использованы также для синтеза новых гетероциклических соединений и лекарственных препаратов в фармакологии. 3 н.п. ф-лы, 1 табл., 6 пр.
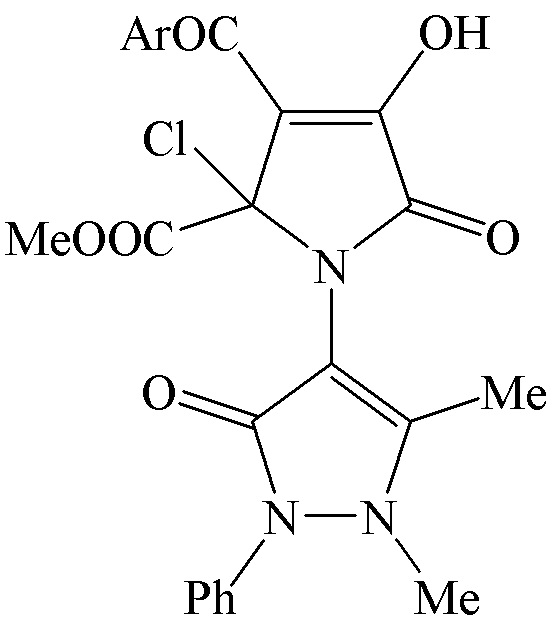
1. Метил 3-ароил-1-(1,5-диметил-3-оксо-2-фенил-2,3-дигидро-1Н-пиразол-4-ил)-4-гидрокси-5-оксо-2-хлор-2,5-дигидро-1Н-пиррол-2-карбоксилаты общей формулы:
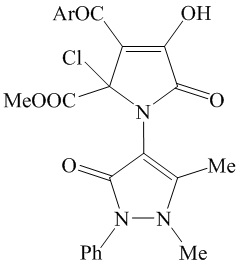
где Ar означает Ph (IIIа), 4-MeOC6H4 (IIIб), 4-MeC6H4 (IIIв), 4-ClC6H4 (IIIг) или 4-BrC6H4 (IIIд).
2. Способ получения метил 3-ароил-1-(1,5-диметил-3-оксо-2-фенил-2,3-дигидро-1Н-пиразол-4-ил)-4-гидрокси-5-оксо-2-хлор-2,5-дигидро-1Н-пиррол-2-карбоксилатов общей формулы:

где Ar означает Ph (IIIа), 4-MeOC6H4 (IIIб), 4-MeC6H4 (IIIв), 4-ClC6H4 (IIIг) или 4-BrC6H4 (IIIд), отличающийся тем, что метил 4-арил-2-(1,5-диметил-3-оксо-2-фенил-2,3-дигидро-1Н-пиразол-4-иламино)-4-оксо-2-бутеноатов (Iа-д) подвергают взаимодействию с оксалилхлоридом (II), взятыми в соотношении 1:1 при температуре 40-61 °С в течение 10-30 минут по схеме:
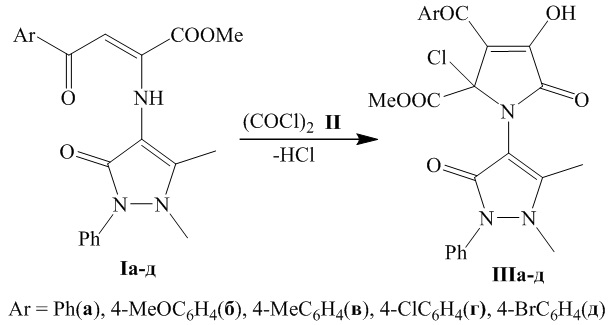
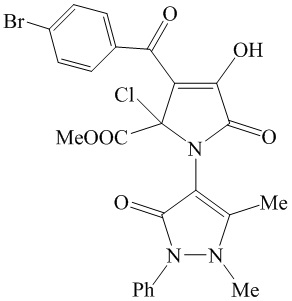
3. Применение метил 3-(4-бромбензоил)-1-(1,5-диметил-3-оксо-2-фенил-2,3-дигидро-1Н-пиразол-4-ил)-4-гидрокси-5-оксо-2-хлор-1Н-пиррол-2-карбоксилата в качестве средства, обладающего противомикробной активностью
| (Е)-4-((5-(4-БРОМФЕНИЛ)-1-((2,4-ДИНИТРОФЕНИЛ)АМИНО)-2-ОКСО-1,2-ДИГИДРО-3Н-ПИРРОЛ-3-ИЛИДЕН)АМИНО)-1,5-ДИМЕТИЛ-2-ФЕНИЛ-1,2-ДИГИДРО-3Н-ПИРАЗОЛ-3-ОН, ОБЛАДАЮЩИЙ ПРОТИВОМИКРОБНОЙ АКТИВНОСТЬЮ | 2021 |
|
RU2776067C1 |
| В.А | |||
| Лядов, Е.С | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| ЭКОЛОГИЯ | |||
| УРБАНИСТИКА, 2021, т.4, стр.110-113 | |||
| Gein, V | |||
| L | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2023-03-22—Публикация
2022-07-28—Подача