ОБЛАСТЬ ИЗОБРЕТЕНИЯ
[1] Настоящее изобретение относится к антигенсвязывающим белкам (ABP) со специфичностью связывания для индуцируемого глюкокортикоидами белка, родственного рецептору фактора некроза опухоли (GITR), и к композициям, содержащим такие ABP, включая фармацевтические композиции, диагностические композиции и наборы. Изобретение относится к способам получения ABP GITR, и к способам применения ABP GITR, например, для терапевтических целей, диагностических целей и исследовательских целей.
УРОВЕНЬ ТЕХНИКИ
[2] GITR является членом суперсемейства рецептора фактора некроза опухоли (TNFR). GITR экспрессируется во многих клетках врожденной и адаптивной иммунной системы, и экспрессия на поверхности мембраны увеличивается в активированных T-клетках. См. Hanabuchib et al., Blood, 2006, 107:3617-3623; и Nocentini et al., Eur. J. Immunol., 2005, 35:1016-1022; полное содержание всех из которых приведено в настоящем описании в качестве ссылки. GITR активируется посредством лиганда GITR (GITRL).
[3] Агонизм GITR оказывает костимулирующий эффект на эффекторные T-клетки. См. Schaer et al., Curr. Opin. Immunol., 2012, 24:217-224, полное содержание которого приведено в качестве ссылки. Агонисты GITR предложены в качестве лекарственных средств для терапии злокачественных опухолей. См. Schaer et al., выше; Melero et al., Clin Cancer Res., 2013, 19:1044-1053; Cohen et al., J. Clin. Oncol., 2007, 25:3058; Cohen et al., PLoS One, 2010, 5:e10436; Nocentini et al., Br. J. Pharmacol., 2012, 165:2089-2099; и Патентную публикацию США No. 2007/0098719; полное содержание всех из которых приведено в настоящем описании в качестве ссылки.
[4] Хотя показано, что антитела-агонисты GITR являются многообещающими в моделях на мышах, сложно получать агонистические антитела против GITR человека. В Nocentini et al. (Br. J. Pharmacol., 2012, 165:2089-2099) отмечено, что «mAb против GITR имеют намного более слабый запускающий потенциал у человека, чем у мышей». Авторы статьи выдвинули предположение, что это может являться результатом того факта, что GITR человека должен быть мультимеризован в стабильные тримеры или суперкластеры (например, тетрамеры тримеров), чтобы подвергаться сильной активации.
[5] Таким образом, существует необходимость ABP, которые могут выступать в роли агониста GITR человека более активно, чем известные антитела. Настоящее изобретение относится к ABP, удовлетворяющим эту необходимость.
СУЩНОСТЬ ИЗОБРЕТЕННИЯ
[6] Настоящее изобретение относится к ABP, которые специфически связывают GITR, и к способам применения таких ABP.
[7] В одном аспекте настоящее изобретение относится к выделенному мультивалентному антигенсвязывающему белку (ABP), специфически связывающему GITR человека (hGITR; SEQ ID NO: 1), содержащему следующие шесть последовательностей CDR: (a) CDR-H3, имеющую последовательность X1X2X3X4X5RGYGDYGGHHAFDI, где X1 представляет собой A или V, X2 представляет собой H, D, L или R, X3 представляет собой E или D, X4 представляет собой R, N, S или A, и X5 представляет собой V, D или G (SEQ ID NO:141); (b) CDR-H2, имеющую последовательность X1IX2X3SGX4TYYNPSLKS, где X1 представляет собой G, L, или S, X2 представляет собой Y, A, или V, X3 представляет собой E, Y или H, и X4 представляет собой S или K (SEQ ID NO:142); (c) CDR-H1, имеющую последовательность X1SISSX2X3X4X5WX6, где X1 представляет собой Y или G, X2 представляет собой G, S, или E, X3 представляет собой L, G, S, Y, или A, X4 представляет собой G, A, Y, M, или G, X5 представляет собой V, A, или отсутствует, и X6 представляет собой S или G (SEQ ID NO:143); (d) CDR-L3, имеющую последовательность QQEYX1TPPX2, где X1 представляет собой A или N, и X2 представляет собой T или S (SEQ ID NO:144); (e) CDR-L2, имеющую последовательность X1AX2SLX3X4, где X1 представляет собой A или S, X2 представляет собой D или S, X3 представляет собой Q, D, K или E, и X4 представляет собой S или Y (SEQ ID NO:145); и (f) CDR-L1, имеющую последовательность X1ASX2SIX3X4YLN, где X1 представляет собой G или R, X2 представляет собой Q или K, X3 представляет собой S, D или N, и X4 представляет собой S или T (SEQ ID NO:146).
[8] В одном варианте осуществления, ABP из (a) содержит последовательность VH из SEQ ID NO:9 и последовательность VL из SEQ ID NO:10; в другом варианте осуществления, ABP из (b) содержит последовательность VH из SEQ ID NO:19 и последовательность VL из SEQ ID NO:20; в другом варианте осуществления, ABP из (c) содержит последовательность VH из SEQ ID NO:26 и последовательность VL из SEQ ID NO:27; в другом варианте осуществления, ABP из (d) содержит последовательность VH из SEQ ID NO:26 или SEQ ID NO:34 и последовательность VL из SEQ ID NO:35; в другом варианте осуществления, ABP из (e) содержит последовательность VH из SEQ ID NO:26 и последовательность VL из SEQ ID NO:40; в другом варианте осуществления, ABP из (f) содержит последовательность VH из SEQ ID NO:44 и последовательность VL из SEQ ID NO:45; в другом варианте осуществления, ABP из (g) содержит последовательность VH из SEQ ID NO:44 и последовательность VL из SEQ ID NO:53; в другом варианте осуществления, ABP из (h) содержит последовательность VH из SEQ ID NO:58 и последовательность VL из SEQ ID NO:10; в другом варианте осуществления, ABP из (i) содержит последовательность VH из SEQ ID NO:104 и последовательность VL из SEQ ID NO:10; и в другом варианте осуществления, ABP из (j) содержит последовательность VH из SEQ ID NO:105 и последовательность VL из SEQ ID NO:10.
[9] В одном варианте осуществления, ABP из (b) содержит тяжелую цепь из SEQ ID NO:7 и легкую цепь из SEQ ID NO:8; В другом варианте осуществления, ABP из (b) содержит тяжелую цепь из SEQ ID NO:17 и легкую цепь из SEQ ID NO:18. В другом варианте осуществления, ABP из (c) содержит тяжелую цепь из SEQ ID NO:24 и легкую цепь из SEQ ID NO:25. В другом варианте осуществления, ABP из (d) содержит (i) тяжелую цепь из SEQ ID NO:32 и легкую цепь из SEQ ID NO:33, или (ii) тяжелую цепь из SEQ ID NO:37 и легкую цепь из SEQ ID NO:33. В другом варианте осуществления, ABP из (e) содержит (i) тяжелую цепь из SEQ ID NO:38 и легкую цепь из SEQ ID NO:39. В другом варианте осуществления, ABP из (f) содержит тяжелую цепь из SEQ ID NO:42 и легкую цепь из SEQ ID NO:43; в другом варианте осуществления, ABP из (g) содержит (i) тяжелую цепь из SEQ ID NO:51 и легкую цепь из SEQ ID NO:52; В другом варианте осуществления, ABP из (h) содержит (i) тяжелую цепь из SEQ ID NO:57 и легкую цепь из SEQ ID NO:8; В другом варианте осуществления, ABP из (i) содержит (i) тяжелую цепь из SEQ ID NO:114 и легкую цепь из SEQ ID NO:8, или (ii) тяжелую цепь из SEQ ID NO:120 и легкую цепь из SEQ ID NO:8; или (iii) тяжелую цепь из SEQ ID NO:122 и легкую цепь из SEQ ID NO:8; или в другом варианте осуществления, ABP из (j) содержит (i) тяжелую цепь из SEQ ID NO:115 и легкую цепь из SEQ ID NO:8, или (ii) тяжелую цепь из SEQ ID NO:121 и легкую цепь из SEQ ID NO:8; или (iii) тяжелую цепь из SEQ ID NO:123 и легкую цепь из SEQ ID NO:8.
[10] В другом варианте осуществления, ABP содержит тяжелую цепь из SEQ ID NO:7 и легкую цепь из SEQ ID NO:8; или тяжелую цепь из SEQ ID NO:17 и легкую цепь из SEQ ID NO:18; или тяжелую цепь из SEQ ID NO:24 и легкую цепь из SEQ ID NO:25; тяжелую цепь из SEQ ID NO:32 и легкую цепь из SEQ ID NO:33, или (ii) тяжелую цепь из SEQ ID NO:37 и легкую цепь из SEQ ID NO:33; тяжелую цепь из SEQ ID NO:38 и легкую цепь из SEQ ID NO:39; тяжелую цепь из SEQ ID NO:42 и легкую цепь из SEQ ID NO:43; тяжелую цепь из SEQ ID NO:51 и легкую цепь из SEQ ID NO:52; тяжелую цепь из SEQ ID NO:57 и легкую цепь из SEQ ID NO:8; тяжелую цепь из SEQ ID NO:114 и легкую цепь из SEQ ID NO:8, или (ii) тяжелую цепь из SEQ ID NO:120 и легкую цепь из SEQ ID NO:8; или (iii) тяжелую цепь из SEQ ID NO:122 и легкую цепь из SEQ ID NO:8; или тяжелую цепь из SEQ ID NO:115 и легкую цепь из SEQ ID NO:8, или (ii) тяжелую цепь из SEQ ID NO:121 и легкую цепь из SEQ ID NO:8; или (iii) тяжелую цепь из SEQ ID NO:123 и легкую цепь из SEQ ID NO:8.
[11] В другом аспекте настоящее изобретение относится к выделенному мультивалентному антигенсвязывающему белку (ABP), специфически связывающему GITR человека (hGITR; SEQ ID NO: 1), содержащему следующие шесть последовательностей CDR: (a) CDR-H3, имеющую последовательность, указанную в SEQ ID NO:66; (b) CDR-H2, имеющую последовательность, указанную в SEQ ID NO:65; (c) CDR-H1, имеющую последовательность, указанную в SEQ ID NO:64; (d) CDR-L3, имеющую последовательность, указанную в SEQ ID NO:69; (e) CDR-L2, имеющую последовательность, указанную в SEQ ID NO:68; и (f) CDR-L1, имеющую последовательность, указанную в SEQ ID NO:67.
[12] В одном варианте осуществления, ABP содержит последовательность VH из SEQ ID NO:62 и последовательность VL из SEQ ID NO:63; последовательность VH из SEQ ID NO:70 и последовательность VL из SEQ ID NO:63; или последовательность VH из SEQ ID NO:97 и последовательность VL из SEQ ID NO:63.
[13] В другом варианте осуществления, ABP содержит (i) тяжелую цепь из SEQ ID NO:171 и легкую цепь из SEQ ID NO:172; тяжелую цепь из SEQ ID NO:173 и легкую цепь из SEQ ID NO:174; последовательность тяжелой цепи из SEQ ID NO:106 и последовательность легкой цепи из SEQ ID NO:107; или (ii) последовательность тяжелой цепи из SEQ ID NO:116 и последовательность легкой цепи из SEQ ID NO:107.
[14] В другом аспекте настоящее изобретение относится к выделенному мультивалентному антигенсвязывающему белку (ABP), специфически связывающему GITR человека (hGITR; SEQ ID NO: 1), содержащему следующие шесть последовательностей CDR: (a) CDR-H3, имеющую последовательность, указанную в SEQ ID NO:75; (b) CDR-H2, имеющую последовательность, указанную в SEQ ID NO:74; (c) CDR-H1, имеющую последовательность, указанную в SEQ ID NO:73; (d) CDR-L3, имеющую последовательность, указанную в SEQ ID NO:78; (e) CDR-L2, имеющую последовательность, указанную в SEQ ID NO:77; и (f) CDR-L1, имеющую последовательность, указанную в SEQ ID NO:75.
[15] В одном варианте осуществления, ABP содержит последовательность VH из SEQ ID NO:71 и последовательность VL из SEQ ID NO:72; или последовательность VH из SEQ ID NO:98 и последовательность VL из SEQ ID NO:72.
[16] В другом варианте осуществления, ABP содержит тяжелую цепь из SEQ ID NO:173 и легкую цепь из SEQ ID NO:109; или ABP содержит (i) тяжелую цепь из SEQ ID NO:108 и легкую цепь из SEQ ID NO:109; или (ii) тяжелую цепь из SEQ ID NO:117 и легкую цепь из SEQ ID NO:109.
[17] В другом аспекте настоящее изобретение относится к выделенному мультивалентному антигенсвязывающему белку (ABP), специфически связывающему GITR человека (hGITR; SEQ ID NO: 1), содержащему следующие шесть последовательностей CDR: (a) CDR-H3, имеющую последовательность, указанную в SEQ ID NO:83; (b) CDR-H2, имеющую последовательность, указанную в (i) SEQ ID NO:82, или (ii) SEQ ID NO:100; (c) CDR-H1, имеющую последовательность, указанную в SEQ ID NO:81; (d) CDR-L3, имеющую последовательность, указанную в SEQ ID NO:86; (e) CDR-L2, имеющую последовательность, указанную в SEQ ID NO:85; и (f) CDR-L1, имеющую последовательность, указанную в SEQ ID NO:84.
[18] В одном варианте осуществления, ABP содержит последовательность CDR-H2 из (b)(i) из вышеуказанного абзаца и последовательность VH из SEQ ID NO:79, и последовательность VL из SEQ ID NO:80. В другом варианте осуществления, ABP содержит последовательность CDR-H2 из (b)(i) из вышеуказанного абзаца и последовательность VH из SEQ ID NO:87, и последовательность VL из SEQ ID NO:80. В другом варианте осуществления, ABP содержит последовательность CDR-H2 из (b)(i) из вышеуказанного абзаца и последовательность VH из SEQ ID NO:88, и последовательность VL из SEQ ID NO:80. В другом варианте осуществления, ABP содержит последовательность CDR-H2 из (b)(ii) из вышеуказанного абзаца и последовательность VH из SEQ ID NO:99, и последовательность VL из SEQ ID NO:80.
[19] В одном варианте осуществления, ABP содержит тяжелую цепь из SEQ ID NO:174 и легкую цепь из SEQ ID NO:111; В другом варианте осуществления, ABP содержит тяжелую цепь из SEQ ID NO:175 и легкую цепь из SEQ ID NO:111; в другом варианте осуществления, ABP содержит тяжелую цепь из SEQ ID NO:176 и легкую цепь из SEQ ID NO:111; В другом варианте осуществления, ABP содержит тяжелую цепь из SEQ ID NO:110 и легкую цепь из SEQ ID NO:111; или (ii) тяжелую цепь из SEQ ID NO:118 и легкую цепь из SEQ ID NO:111.
[20] В другом аспекте настоящее изобретение относится к выделенному мультивалентному антигенсвязывающему белку (ABP), специфически связывающему GITR человека (hGITR; SEQ ID NO:1), содержащему следующие шесть последовательностей CDR: (a) CDR-H3, имеющую последовательность, указанную в SEQ ID NO:93; (b) CDR-H2, имеющую последовательность GIIPIFGEAQYAQX1FX2G, где X1 представляет собой K или R, и X2 представляет собой Q или R (SEQ ID NO:215); (c) CDR-H1, имеющую последовательность, указанную в SEQ ID NO:91; (d) CDR-L3, имеющую последовательность, указанную в SEQ ID NO:94; (d) CDR-L2, имеющую последовательность, указанную в SEQ ID NO:85; и (e) CDR-L1, имеющую последовательность, указанную в SEQ ID NO:84.
[21] В одном варианте осуществления, ABP содержит: CDR-H2 из SEQ ID NO:92; CDR-H2 из SEQ ID NO:96; или CDR-H2 из SEQ ID NO:102.
[22] В другом варианте осуществления, ABP содержит последовательность VH из SEQ ID NO:89 и последовательность VL из SEQ ID NO:90. В другом варианте осуществления, ABP содержит последовательность VH из SEQ ID NO:95 и последовательность VL из SEQ ID NO:90. В другом варианте осуществления, ABP содержит последовательность VH из SEQ ID NO:101 и последовательность VL из SEQ ID NO:90.
[23] В другом варианте осуществления, ABP содержит тяжелую цепь из SEQ ID NO:177 и легкую цепь из SEQ ID NO:113. В другом варианте осуществления, ABP содержит тяжелую цепь из SEQ ID NO:178 и легкую цепь из SEQ ID NO:113. В другом варианте осуществления, ABP содержит тяжелую цепь из SEQ ID NO:112 и легкую цепь из SEQ ID NO:113; или (ii) тяжелую цепь из SEQ ID NO:119 и легкую цепь из SEQ ID NO:113.
[24] В другом аспекте настоящее изобретение относится к выделенному мультивалентному антигенсвязывающему белку (ABP), специфически связывающему GITR человека (hGITR; SEQ ID NO: 1), содержащему следующие шесть последовательностей CDR: (a) CDR-H3, имеющую последовательность, указанную в SEQ ID NO:134; (b) CDR-H2, имеющую последовательность, указанную в SEQ ID NO:133;CDR-H1, имеющую последовательность, указанную в SEQ ID NO:132; (c) CDR-L3, имеющую последовательность, указанную в SEQ ID NO:135; (d) CDR-L2, имеющую последовательность, указанную в SEQ ID NO:68; и (e) CDR-L1, имеющую последовательность, указанную в SEQ ID NO:67.
[25] В одном варианте осуществления, ABP содержит (i) последовательность VH из SEQ ID NO:126 и последовательность VL из SEQ ID NO:128; или (ii) последовательность VH из SEQ ID NO:127 и последовательность VL из SEQ ID NO:128.
[26] В одном варианте осуществления, ABP содержит (i) тяжелую цепь из SEQ ID NO:124 и легкую цепь из SEQ ID NO:125; или (ii) тяжелую цепь из SEQ ID NO:136 и легкую цепь из SEQ ID NO:125.
[27] В другом аспекте настоящее изобретение относится к выделенному мультивалентному антигенсвязывающему белку (ABP), специфически связывающему GITR человека (hGITR; SEQ ID NO: 1), содержащему: (a) CDR-H3, имеющую по меньшей мере приблизительно 60%, по меньшей мере приблизительно 70%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 90%, или по меньшей мере приблизительно 95% идентичности с CDR-H3 из области VH, выбранной из SEQ ID NO: 9, 19, 26, 34, 44, 58, 62, 70, 71, 79, 87, 88, 89, 95, 97, 98, 99, 101, 104, 105, 126 и 127; (b) CDR-H2, имеющую по меньшей мере приблизительно 60%, по меньшей мере приблизительно 70%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 90%, или по меньшей мере приблизительно 95% идентичности с CDR-H2 из области VH, выбранной из SEQ ID NO: 9, 19, 26, 34, 44, 58, 62, 70, 71, 79, 87, 88, 89, 95, 97, 98, 99, 101, 104, 105, 126 и 127; (c) CDR-H1, имеющую по меньшей мере приблизительно 60%, по меньшей мере приблизительно 70%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 90%, или по меньшей мере приблизительно 95% идентичности с CDR-H1 из области VH, выбранной из SEQ ID NO: 9, 19, 26, 34, 44, 58, 62, 70, 71, 79, 87, 88, 89, 95, 97, 98, 99, 101, 104, 105, 126 и 127; (d) CDR-L3, имеющую по меньшей мере приблизительно 60%, по меньшей мере приблизительно 70%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 90%, или по меньшей мере приблизительно 95% идентичности с CDR-L3 из области VL, выбранной из SEQ ID NO: 10, 20, 27, 35, 40, 45, 53, 63, 72, 80, 90 и 128; (e) CDR-L2, имеющую по меньшей мере приблизительно 60%, по меньшей мере приблизительно 70%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 90%, или по меньшей мере приблизительно 95% идентичности с CDR-L2 из области VL, выбранной из SEQ ID NO: 10, 20, 27, 35, 40, 45, 53, 63, 72, 80, 90, и 128; и (f) CDR-L1, имеющую по меньшей мере приблизительно 60%, по меньшей мере приблизительно 70%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 90%, или по меньшей мере приблизительно 95% идентичности с CDR-L1 из области VL, выбранной из SEQ ID NO: 10, 20, 27, 35, 40, 45, 53, 63, 72, 80, 90, и 128.
[28] В одном варианте осуществления, каждая из CDR-H3, CDR-H2, CDR-H1, CDR-L3, CDR-L2 и CDR-L1 идентифицирована в соответствии со схемой нумерации, выбранной из схемы нумерации Kabat, схемы нумерации Chothia или схемы нумерации IMGT. В другом варианте осуществления, CDR-H1 идентифицирована, как определено по обеим схемам нумерации Chothia и Kabat, включая границы обеих схем нумерации.
[29] В одном варианте осуществления, CDR-H3 содержит CDR-H3, выбранную из SEQ ID NO: 13, 23, 30, 48, 61, 66, 75, 83, 93, 103, 131, или ее вариант, имеющий 1, 2 или 3 аминокислотных замены. В другом варианте осуществления, CDR-H2 содержит CDR-H2, выбранную из SEQ ID NO: 12, 22, 29, 47, 60, 65, 74, 82, 92, 96, 100, 102, 130 и 133, или ее вариант, имеющий 1, 2 или 3 аминокислотных замены. В другом варианте осуществления, CDR-H1 содержит CDR-H1, выбранную из SEQ ID NO: 11, 21, 28, 46, 59, 64, 73, 81, 91, 129, 132, или ее вариант, имеющий 1 или 2 аминокислотных замены. В другом варианте осуществления, CDR-L3 содержит CDR-L3, выбранную из SEQ ID NO: 16, 17, 56, 69, 78, 86, 94, 135, или ее вариант, имеющий 1, 2 или 3 аминокислотных замены. В другом варианте осуществления, CDR-L2 содержит CDR-L2, выбранную из SEQ ID NO: 15, 31, 41, 50, 55, 68, 77 и 85, или ее вариант, имеющий 1 аминокислотную замену. В другом варианте осуществления, CDR-L1 содержит CDR-L1, выбранную из SEQ ID NO: 14, 36, 49, 54, 67, 76 и 84, или ее вариант, имеющий 1, 2 или 3 аминокислотных замены. В одном варианте осуществления, аминокислотные замены представляют собой консервативные аминокислотные замены.
[30] В одном варианте осуществления любого из вышеуказанных аспектов, ABP: (a) конкурирует за связывание с GITR с антителом, выбранным из ABP1, ABP2, ABP3, ABP4, ABP5, ABP6, ABP7, ABP8, ABP9, ABP10, ABP11, ABP12, ABP13, ABP14, ABP15, ABP16, ABP17, ABP18, ABP19, ABP20, ABP21, ABP22, ABP23, ABP24, ABP25, ABP26, ABP27, ABP28, ABP29, ABP30, ABP31, ABP32, ABP33 и ABP34, каждое как представлено в Приложении A этого описания; или (b) имеет по меньшей мере три антигенсвязывающих домена, специфически связывающие эпитоп на GITR; или (c) имеет по меньшей мере три антигенсвязывающих домена, специфически связывающие один эпитоп на GITR; или (d) имеет по меньшей мере четыре антигенсвязывающих домена, специфически связывающие эпитоп на GITR; или (e) имеет по меньшей мере четыре антигенсвязывающих домена, специфически связывающие один эпитоп на GITR; или (f) выступает в роли агониста GITR, экспрессированного на поверхности клетки-мишени; или (g) усиливает связывание GITRL с GITR; или (h) костимулирет эффекторную T-клетку в комбинации с представлением антигена от антигенпредставляющей клетки; или (i) ингибирует супрессию эффекторной T-клетки посредством регуляторной T-клетки; или (j) уменьшает количество регуляторных T-клеток в ткани или в системном кровотоке; (k) является способным связываться с одним или несколькими из остатков GITR (SEQ ID NO:1) из группы, состоящей из R56, C58, R59, D60, Y61, P62, E64, E65, C66 и C67; или (l) является способным к любой комбинации из (a) - (k).
[31] В одном варианте осуществления любого из вышеуказанных аспектов, GITR выбран из hGITR (SEQ ID NO: 1), hGITR-T43R (SEQ ID NO: 2), cGITR (SEQ ID NO: 3), mGITR (SEQ ID NO: 4) и их комбинаций. В другом варианте осуществления, ABP (a) специфически связывает GITR яванского макака (cGITR; SEQ ID NO: 3); (b) связывает GITR мыши (mGITR; SEQ ID NO: 4) с аффинностью, более низкой (как показано по более высокой KD), чем аффинность ABP для hGITR, или не связывает mGITR; или (c) является способным к любой комбинации из (a) - (b). В другом варианте осуществления, ABP: (a) специфически связывает cGITR (SEQ ID NO: 3); (b) связывает mGITR (SEQ ID NO: 4) с аффинностью, более низкой (как показано по более высокой KD), чем аффинность ABP для hGITR и cGITR; и (c) усиливает связывание GITRL с GITR.
[32] В другом аспекте настоящее изобретение относится к ABP, который конкурирует за связывание с GITR с ABP по любому из пп. 1-26, где ABP: (a) специфически связывает cGITR (SEQ ID NO: 3); (b) связывает mGITR (SEQ ID NO: 4) с аффинностью, более низкой (как показано по более высокой KD), чем аффинность ABP для hGITR и cGITR; и (c) усиливает связывание GITRL с GITR. В одном варианте осуществления, ABP содержит антитело. В другом варианте осуществления, антитело представляет собой моноклональное антитело. В другом варианте осуществления, антитело выбрано из человеческого антитела, гуманизированного антитела или химерного антитела. В другом варианте осуществления, ABP является мультивалентным. В другом варианте осуществления, ABP содержит фрагмент антитела.
[33] В другом варианте осуществления, ABP содержит альтернативный каркас. В другом варианте осуществления, ABP содержит константную область иммуноглобулина. В другом варианте осуществления, ABP содержит константную область тяжелой цепи из класса, выбранного из IgA, IgD, IgE, IgG или IgM. В другом варианте осуществления, ABP содержит константную область тяжелой цепи из класса IgG и подкласса, выбранного из IgG4, IgG1, IgG2, или IgG3.
[34] В одном варианте осуществления любого из вышеуказанных аспектов, по меньшей мере один Fab является слитым с C-концом домена Fc IgG. В другом варианте осуществления, ABP дополнительно содержит по меньшей мере один линкер. В другом варианте осуществления, IgG представляет собой IgG4. В другом варианте осуществления, IgG представляет собой IgG1. В другом варианте осуществления, по меньшей мере один Fab является слитым с N-концом домена Fc IgG. В одном варианте осуществления, по меньшей мере один Fab представляет собой по меньшей мере два Fab. В другом варианте осуществления, по меньшей мере один Fab представляет собой по меньшей мере три Fab. В другом варианте осуществления, по меньшей мере один Fab представляет собой по меньшей мере четыре Fab. В другом варианте осуществления, два Fab являются независимо слитыми с N-концом IgG. В другом варианте осуществления, два Fab являются независимо слитыми с C-концом IgG. В другом варианте осуществления, Fab присоединен к каждому N-концу IgG, линкер присоединен к каждому указанному Fab, и Fab присоединен к каждому линкеру. В другом варианте осуществления, Fab присоединен к каждому C-концу IgG, линкер присоединен к каждому указанному Fab, и Fab присоединен к каждому линкеру. В другом варианте осуществления, при этом каждый линкер содержит SEQ ID NO:5. В другом варианте осуществления, каждый линкер содержит SEQ ID NO:6.
[35] В одном варианте осуществления любого из вышеуказанных аспектов, ABP содержит антитело с общей легкой цепью, антитело с модификацией выступы-во-впадины, scFv, присоединенный к IgG, Fab, присоединенный к IgG, диатело, тетравалентное биспецифическое антитело, DVD-Ig™, DART™, DuoBody®, CovX-Body, антитело Fcab, TandAb®, тандемный Fab, Zybody™, или их комбинации. В одном варианте осуществления, ABP связывает более одной молекулы GITR. В другом варианте осуществления, ABP является независимым от связывания GITRL. В другом варианте осуществления, ABP усиливает связывание GITRL с GITR по меньшей мере приблизительно на 10%, по меньшей мере приблизительно на 20%, по меньшей мере приблизительно на 30%, по меньшей мере приблизительно на 40%, по меньшей мере приблизительно на 50%, по меньшей мере приблизительно на 60%, по меньшей мере приблизительно на 70%, по меньшей мере приблизительно на 80%, или по меньшей мере приблизительно на 90%. В другом варианте осуществления, ABP усиливает связывание GITRL с GITR по меньшей мере приблизительно на 50%. В другом варианте осуществления, клетка-мишень выбрана из эффекторной T-клетки, регуляторной T-клетки, клетки естественного киллера (NK), T-клетки естественного киллера (NKT), дендритной клетки и B-клетки. В другом варианте осуществления, клетка-мишень представляет собой эффекторную T-клетку, выбранную из T-клетки-помощника (CD4+), цитотоксической T-клетки (CD8+) и их комбинаций. В другом варианте осуществления, клетка-мишень представляет собой регуляторную T-клетку, выбранную из CD4+CD25+Foxp3+ регуляторной T-клетки, CD8+CD25+ регуляторной T-клетки и их комбинаций. В другом варианте осуществления, ткань представляет собой опухоль.
[36] В одном варианте осуществления любого из вышеуказанных аспектов, KD первого антигенсвязывающего домена для hGITR (SEQ ID NO: 1) или hGITR-T43R (SEQ ID NO: 2) составляет менее, чем приблизительно 20 нМ. В одном варианте осуществления, KD первого антигенсвязывающего домена для cGITR (SEQ ID NO: 3) составляет менее, чем приблизительно 200 нМ. В другом варианте осуществления, KD второго антигенсвязывающего домена для hGITR (SEQ ID NO: 1) или hGITR-T43R (SEQ ID NO: 2) составляет менее, чем приблизительно 100 нМ. В другом варианте осуществления, KD второго антигенсвязывающего домена для cGITR (SEQ ID NO: 3) составляет менее, чем приблизительно 1 мкМ. В другом варианте осуществления, ABP содержит домен Fc с уменьшенной эффекторной функцией по сравнению с доменом Fc IgG1. В другом варианте осуществления, ABP содержит агликозилированный домен Fc. В другом варианте осуществления, ABP содержит домен Fc IgG1 с аланином в одном или нескольких из положений 234, 235, 265 и 297.
[37] В одном варианте осуществления любого из вышеуказанных аспектов, GITR экспрессируется на поверхности клетки-мишени. В одном варианте осуществления, ABP вызывает мультимеризацию GITR, экспрессированного на поверхности клетки-мишени. В одном варианте осуществления, ABP вызывает мультимеризацию 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 молекул GITR.
[38] В одном варианте осуществления любого из вышеуказанных аспектов, ABP специфически связывает эпитоп GITR человека (hGITR; SEQ ID NO:1) и является способным связывать один или несколько остатков из группы, состоящей из R56, C58, R59, D60, Y61, P62, E64, E65, C66 и C67.
[39] В одном варианте осуществления любого из вышеуказанных аспектов, ABP содержит иммуноглобулин, состоящий по меньшей мере из двух различных (т.е., имеющих различные последовательности и/или связывающихся с различными остатками) вариабельных областей тяжелой цепи, где каждая спарена с вариабельной областью общей легкой цепи. В другом варианте осуществления, вариабельная область общей легкой цепи формирует отдельный антигенсвязывающий домен с каждой из двух различных вариабельных областей тяжелой цепи. В другом варианте осуществления, ABP содержит первый вариабельный домен VH, имеющий SEQ ID NO:189, второй вариабельный домен VH, имеющий SEQ ID NO:215, и общую вариабельную легкую цепь, имеющую SEQ ID NO:190. В другом варианте осуществления, ABP содержит первый вариабельный домен VH, имеющий SEQ ID NO:199, второй вариабельный домен VH, имеющий SEQ ID NO:216, и общую вариабельную легкую цепь, имеющую SEQ ID NO:200.
[40] В другом аспекте настоящее изобретение относится к набору, содержащему ABP из любого из вышеуказанных аспектов или указанный в Приложении A, и инструкции для использования ABP. В одном варианте осуществления, ABP является лиофилизированным. В другом варианте осуществления, набор дополнительно содержит жидкость для разведения лиофилизированного ABP.
[41] Известно, что когда антитело экспрессируется в клетках, антитело подвергается модификации после трансляции. Примеры посттрансляционной модификации включают отщепление лизина на C-конце тяжелой цепи посредством карбоксипептидазы; модификацию глутамина или глутаминовой кислоты на N-конце тяжелой цепи и легкой цепи до пиролутаминовой кислоты посредством пироглутамилирования; гликозилирование; окисление; дезамидирование; и гликирование, и известно, что такие посттрансляционные модификации возникают в различных антителах (См. journal of Pharmaceutical Sciences, 2008, Vol. 97, p. 2426-2447, полное содержание которого приведено в качестве ссылки). В некоторых вариантах осуществления, ABP по изобретению представляет собой антитело или его антигенсвязывающий фрагмент, подвергшиеся посттрансляционной модификации. Примеры антитела или его антигенсвязывающего фрагмента, подвергшихся посттрансляционной модификации, включают антитело или его антигенсвязывающие фрагменты, подвергшиеся пироглутамилированию на N-конце вариабельной области тяжелой цепи и/или делеции лизина на C-конце тяжелой цепи. В данной области известно, что такая посттрансляционная модификация, обусловленная пироглутамилированием на N-конце и делецией лизина на C-конце, не оказывает какого-либо влияния на активность антитела или его фрагмента (Analytical Biochemistry, 2006, Vol. 348, p. 24-39, полное содержание которого приведено в качестве ссылки).
[42] В одном варианте осуществления любого из вышеуказанных аспектов, ABP содержит полипептидную последовательность, имеющую остаток пироглутамата (pE) на N-конце. В одном варианте осуществления, ABP содержит последовательность VH, в которой N-концевой Q заменен на pE. В другом варианте осуществления, ABP содержит последовательность VL, в которой N-концевой E заменен на pE. В другом варианте осуществления, ABP содержит последовательность тяжелой цепи, в которой N-концевой Q заменен на pE.
[43] В одном варианте осуществления любого из вышеуказанных аспектов, ABP содержит последовательность легкой цепи, в которой N-концевой E заменен на pE. В другом варианте осуществления, ABP предназначен для использования в качестве лекарственного средства. В другом варианте осуществления, ABP предназначен для использования в лечении злокачественной опухоли или вирусной инфекции.
[44] В одном варианте осуществления, ABP предназначен для использования в лечении злокачественной опухоли, где злокачественная опухоль выбрана из солидной опухоли и гематологической опухоли.
[45] В другом аспекте настоящее изобретение относится к представляет выделенному полинуклеотиду, кодирующему ABP из любого из вышеуказанных аспектов или указанный в Приложении A, его VH, его VL, его легкую цепь, его тяжелую цепь или его антигенсвязывающую часть.
[46] В другом аспекте настоящее изобретение относится к вектору, содержащему представляющий интерес полинуклеотид из вышеуказанного аспекта. В другом аспекте настоящее изобретение относится к клетке-хозяину, содержащей полинуклеотид или вектор из любого из вышеуказанных аспектов. В одном варианте осуществления, клетка-хозяин выбрана из клетки бактерии, клетки гриба и клетки млекопитающего. В другом варианте осуществления, клетка-хозяин выбрана из клетки E. coli, клетки Saccharomyces cerevisiae и клетки CHO.
[47] В другом аспекте настоящее изобретение относится к реакционной смеси для бесклеточной экспрессии, содержащей полинуклеотид или вектор из вышеуказанных аспектов.
[48] В другом аспекте настоящее изобретение относится к способу получения ABP из любого из вышеуказанных аспектов или указанного в Приложении A, включающему экспрессию ABP в клетке-хозяине и выделение экспрессированного ABP.
[49] В другом аспекте настоящее изобретение относится к фармацевтической композиции, содержащей ABP из любого из вышеуказанных аспектов или указанный в Приложении A, и фармацевтически приемлемый наполнитель. В одном варианте осуществления, количество ABP в фармацевтической композиции является достаточным для (a) уменьшения супрессии эффекторных T-клеток регуляторными T-клетками; (b) активации эффекторных T-клеток; (c) уменьшения количества регуляторных T-клеток в ткани или системно; (d) индукции или усиления пролиферации эффекторных T-клеток; (e) замедления скорости роста опухоли; (f) индукции регрессии опухоли; или (g) их комбинации, у субъекта. В одном варианте осуществления, фармацевтическая композиция предназначена для использования в качестве лекарственного средства, например, для использования в лечении злокачественной опухоли или вирусной инфекции. В одном варианте осуществления, фармацевтическая композиция предназначена для использования в лечении злокачественной опухоли, где злокачественная опухоль выбрана из солидной опухоли и гематологической опухоли.
[50] В другом варианте осуществления, количество ABP в фармацевтической композиции является достаточным для (a) уменьшения супрессии эффекторных T-клеток регуляторными T-клетками; (b) активации эффекторных T-клеток; (c) уменьшения количества регуляторных T-клеток в ткани или системно; (d) индукции или усиления пролиферации эффекторных T-клеток; (e) замедления скорости роста опухоли; (f) индукции регрессии опухоли; или (g) их комбинации, у субъекта.
[51] В другом аспекте настоящее изобретение относится к способу лечения или предотвращения заболевания или состояния у нуждающегося в этом субъекта, включающему введение субъекту эффективного количества ABP из любого из вышеуказанных аспектов или указанного в Приложении A, или его фармацевтической композиции.
[52] В другом аспекте настоящее изобретение относится к способу из числа способов увеличения активации иммуноцитов у субъекта, включающему введение субъекту эффективного количества ABP из любого из вышеуказанных аспектов или указанного в Приложении A, или его фармацевтической композиции. В одном варианте осуществления, заболевание или состояние представляет собой злокачественную опухоль.
[53] В другом варианте осуществления, способ индуцирует или усиливает иммунный ответ на ассоциированный с злокачественной опухолью антиген. В другом варианте осуществления, ABP вводят в количестве, достаточном для (a) уменьшения супрессии эффекторных T-клеток регуляторными T-клетками; (b) активации эффекторных T-клеток; (c) уменьшения количества регуляторных T-клеток в ткани или системно; (d) индукции или усиления пролиферации эффекторных T-клеток; (e) замедления скорости роста опухоли; (f) индукции регрессии опухоли; или (g) их комбинации. В другом варианте осуществления, злокачественная опухоль представляет собой солидную опухоль. В другом варианте осуществления, злокачественная опухоль представляет собой гематологическую опухоль. В другом варианте осуществления, способ дополнительно включает введение одного или нескольких дополнительных лекарственных средств. В одном варианте осуществления, дополнительное лекарственное средство выбрано из радиоактивного облучения, цитотоксического средства, химиотерапевтического средства, цитостатического средства, противогормонального средства, ингибитора EGFR, иммуностимулирующего средства, антиангиогенного средства и их комбинаций. В одном варианте осуществления, дополнительное лекарственное средство представляет собой иммуностимулирующее средство. В одном варианте осуществления, иммуностимулирующее средство содержит средство, блокирующее передачу сигналов ингибирующего рецептора, экспрессированного иммуноцитом, или его лиганда. В одном варианте осуществления, ингибирующий рецептор, экспрессированный иммуноцитом, или его лиганд выбран из CTLA-4, PD-1, PD-L1, NRP1, LAG-3, Tim3, TIGIT, невритина, BTLA, KIR и их комбинаций. В одном варианте осуществления, иммуностимулирующее средство содержит агонист стимулирующего рецептора, экспрессированный иммуноцитом. В другом варианте осуществления, стимулирующий рецептор, экспрессированный иммуноцитом, выбран из OX40, ICOS, CD27, CD28, 4-1BB, CD40 и их комбинаций. В другом варианте осуществления, иммуностимулирующее средство содержит цитокин. В другом варианте осуществления, цитокин выбран из IL-2, IL-5, IL-7, IL-12, IL-15, IL-21 и их комбинаций. В другом варианте осуществления, иммуностимулирующее средство содержит онколитический вирус. В другом варианте осуществления, онколитический вирус выбран из вируса простого герпеса, вируса везикулярного стоматита, аденовируса, вируса болезни Ньюкасла, вируса осповакцины, вируса Мараба и их комбинаций. В другом варианте осуществления, иммуностимулирующее средство содержит T-клетку, экспрессирующую химерный рецептор антигена. В другом варианте осуществления, иммуностимулирующее средство содержит би- или мультиспецифическое нацеленное на T-клетку антитело. В другом варианте осуществления, иммуностимулирующее средство содержит антитело против TGF-β, ловушку TGF-β или их комбинацию. В другом варианте осуществления, иммуностимулирующее средство содержит вакцину против ассоциированного с злокачественной опухолью антигена.
[54] В другом аспекте настоящее изобретение относится к способу модуляции иммунного ответа у нуждающегося в этом субъекта, включающему введение субъекту эффективного количества ABP из любого из вышеуказанных аспектов или указанного в Приложении A, или его фармацевтической композиции. В одном варианте осуществления, способ дополнительно включает введение одного или нескольких дополнительных лекарственных средств субъекту. В одном варианте осуществления, дополнительное лекарственное средство представляет собой агонист стимулирующего рецептора иммуноцита, и стимулирующий рецептор иммуноцита выбран из OX40, CD2, CD27, CDS, ICAM-1, LFA-1 (CD11a/CD18), ICOS (CD278), 4-1BB (CD137), CD28, CD30, CD40, BAFFR, HVEM, CD7, LIGHT, NKG2C, SLAMF7, NKp80, CD160, B7-H3, лиганда CD83, и их комбинаций. В одном варианте осуществления, дополнительное лекарственное средство представляет собой цитокин, выбранный из IL-2, IL-5, IL-7, IL-12, IL-15, IL-21 и их комбинаций. В одном варианте осуществления, дополнительное лекарственное средство представляет собой онколитический вирус, выбранный из вируса простого герпеса, вируса везикулярного стоматита, аденовируса, вируса болезни Ньюкасла, вируса осповакцины, вируса Мараба и их комбинаций. В одном варианте осуществления, дополнительное лекарственное средство составлено в той же самой фармацевтической композиции, что и ABP. В одном варианте осуществления, дополнительное лекарственное средство составлено в фармацевтической композиции, отличной от ABP. В одном варианте осуществления, дополнительное лекарственное средство вводят до введения ABP. В одном варианте осуществления, дополнительное лекарственное средство вводят после введения ABP. В одном варианте осуществления, дополнительное лекарственное средство вводят одновременно с ABP.
[55] В другом аспекте настоящее изобретение относится к выделенному мультивалентному антигенсвязывающему белку (ABP), специфически связывающему GITR человека (hGITR; SEQ ID NO: 1), где ABP конкурирует за связывание с одним или несколькими из ABP1, ABP2, ABP3, ABP4, ABP5, ABP6, ABP7, ABP8, ABP9, ABP10, ABP11, ABP12, ABP13, ABP14, ABP15, ABP16, ABP17, ABP18, ABP19, ABP20, ABP21, ABP22, ABP23, ABP24, ABP25, ABP26, ABP27, ABP28, ABP29, ABP30, ABP31, ABP32, ABP33, и ABP34, ABP50, ABP51, ABP52, ABP53, ABP54, ABP55, ABP56, ABP57, ABP62, ABP63, ABP64, ABP65, ABP66, ABP67, ABP68, ABP67, ABP68, ABP69, ABP70, ABP71, ABP72, ABP73, ABP74, ABP75, ABP76, ABP77, ABP78, ABP79, ABP80, ABP812, ABP82, ABP83, ABP84, ABP85, ABP86, ABP87, ABP88, ABP89, ABP90, ABP91, ABP92, ABP93, ABP94, ABP95, ABP96, ABP97, ABP98, ABP99, ABP100, ABP102, ABP103, ABP104, ABP105, ABP106, ABP107, ABP108 и ABP109, каждое как представлено в Приложении A этого описания.
[56] В другом аспекте настоящее изобретение относится к антителу против GITR человека или его антигенсвязывающему фрагменту, содержащему четыре вариабельные области тяжелой цепи и четыре вариабельные области легкой цепи, где вариабельная область тяжелой цепи содержит CDR-H3, состоящую из SEQ ID NO:13, CDR-H2, состоящую из SEQ ID NO:12, и CDR-H1, состоящую из SEQ ID NO:11; и вариабельная область легкой цепи содержит CDR-L3, состоящую из SEQ ID NO:16, CDR-L2, состоящую из SEQ ID NO:15, и CDR-L1, состоящую из SEQ ID NO:14; и одна вариабельная область тяжелой цепи и одна вариабельная область легкой цепи составляют один антигенсвязывающий участок, и антитело или антигенсвязывающий фрагмент содержит четыре антигенсвязывающих участка.
[57] В одном варианте осуществления, антитело против GITR человека или его антигенсвязывающий фрагмент содержит четыре вариабельные области тяжелой цепи и четыре вариабельные области легкой цепи, в которых вариабельная область тяжелой цепи состоит из SEQ ID NO: 9, вариабельная область легкой цепи состоит из SEQ ID NO: 10, и одна вариабельная область тяжелой цепи и одна вариабельная область легкой цепи составляют один антигенсвязывающий участок, и антитело или антигенсвязывающий фрагмент содержит четыре антигенсвязывающих участка.
[58] В одном варианте осуществления, антитело против GITR человека или его антигенсвязывающий фрагмент содержит четыре вариабельные области тяжелой цепи и четыре вариабельные области легкой цепи, в которых вариабельная область тяжелой цепи состоит из SEQ ID NO: 9, где Q в положении 1 последовательности модифицирован до пироглутамата, вариабельная область легкой цепи состоит из SEQ ID NO: 10, и одна вариабельная область тяжелой цепи и одна вариабельная область легкой цепи составляют один антигенсвязывающий участок, и антитело или антигенсвязывающий фрагмент содержит четыре антигенсвязывающих участка.
[59] В одном варианте осуществления, антитело против GITR человека содержит две тяжелые цепи и четыре легкие цепи, каждая тяжелая цепь содержит две структуры, состоящие из вариабельной области тяжелой цепи и области CH1, области CH2 и области CH3, и C-конец одной из структур связан с N-концом другой структуры посредством линкера, и каждая легкая цепь содержит вариабельную область легкой цепи и константную область легкой цепи (левая панель на ФИГ. 1B).
[60] В одном варианте осуществления, антитело против GITR человека содержит две тяжелые цепи и четыре легкие цепи, где каждая тяжелая цепь содержит первую вариабельную область тяжелой цепи и первую область CH1, линкер, вторую вариабельную область тяжелой цепи, вторую область CH1, область CH2 и область CH3, и каждая легкая цепь содержит вариабельную область легкой цепи и константную область легкой цепи (левая панель на ФИГ. 1B).
[61] В одном варианте осуществления, антитело против GITR человека содержит две тяжелые цепи и четыре легкие цепи; каждая тяжелая цепь содержит две структуры, состоящие из вариабельной области тяжелой цепи, содержащей CDR-H3, состоящую из SEQ ID NO:13, CDR-H2, состоящую из SEQ ID NO:12, и CDR-H1, состоящую из SEQ ID NO:11, и области CH1, области CH2 и области CH3, и карбокси-конец (C-конец) одной из структур связан с амино-концом (N-концом) другой структуры посредством линкера; и каждая легкая цепь содержит вариабельную область легкой цепи, содержащую CDR-L3, состоящую из SEQ ID NO:16, CDR-L2, состоящую из SEQ ID NO:15, и CDR-L1, состоящую из SEQ ID NO:14.
[62] В одном варианте осуществления, антитело против GITR человека содержит две тяжелые цепи и четыре легкие цепи; каждая тяжелая цепь содержит первую вариабельную область тяжелой цепи и вторую вариабельную область тяжелой цепи, где каждая содержит CDR-H3, состоящую из SEQ ID NO:13, CDR-H2 состоящую из SEQ ID NO:12, и CDR-H1, состоящую из SEQ ID NO:11; первую область CH1, линкер, вторую область CH1, область CH2 и область CH3; и каждая легкая цепь содержит вариабельную область легкой цепи, содержащую CDR-L3, состоящую из SEQ ID NO:16, CDR-L2, состоящую из SEQ ID NO:15, и CDR-L1, состоящую из SEQ ID NO:14.
[63] В одном варианте осуществления, антитело против GITR человека содержит две тяжелые цепи и четыре легкие цепи, в которых каждая тяжелая цепь содержит две структуры, состоящие из вариабельной области тяжелой цепи из SEQ ID NO: 9 и области CH1, области CH2 и области CH3, и C-конец одной из структур связан с N-концом другой структуры посредством линкера, и каждая легкая цепь содержит вариабельную область легкой цепи из SEQ ID NO: 10, и константная область легкой цепи.
[64] В одном варианте осуществления, антитело против GITR человека содержит две тяжелые цепи и четыре легкие цепи, где каждая тяжелая цепь содержит первую вариабельную область тяжелой цепи и вторую вариабельную область тяжелой цепи, каждая, как указано в SEQ ID NO: 9; первую область CH1, линкер, вторую область CH1, область CH2 и область CH3; и где каждая легкая цепь содержит вариабельную область легкой цепи из SEQ ID NO: 10, и константную область легкой цепи.
[65] В одном варианте осуществления, антитело против GITR человека содержит две тяжелые цепи и четыре легкие цепи, в которой каждая тяжелая цепь содержит две структуры, состоящие из вариабельной области тяжелой цепи из SEQ ID NO: 9 и области CH1, области CH2 и области CH3, и C-конец одной из структур связан с N-концом другой структуры посредством линкера, где Q в положении 1 последовательности модифицирован до пироглутамата, и каждая легкая цепь содержит вариабельную область легкой цепи из SEQ ID NO: 10 и константную область легкой цепи.
[66] В одном варианте осуществления, антитело против GITR человека содержит две тяжелые цепи и четыре легкие цепи, где каждая тяжелая цепь содержит первую вариабельную область тяжелой цепи и вторую вариабельную область тяжелой цепи, каждая, как указано в SEQ ID NO: 9; первую область CH1, линкер, вторую область CH1, область CH2 и область CH3; где Q в положении 1 последовательности модифицирован до пироглутамата, и каждая легкая цепь содержит вариабельную область легкой цепи из SEQ ID NO: 10 и a константную область легкой цепи.
[67] В одном варианте осуществления, антитело против GITR человека содержит две тяжелые цепи, где каждая имеет две вариабельные области, из SEQ ID NO: 7, и четыре легкие цепи из SEQ ID NO: 8.
[68] В одном варианте осуществления, антитело против GITR человека содержит две тяжелые цепи, где каждая имеет две вариабельные области, из SEQ ID NO: 7, где Q в положении 1 последовательности модифицирован до пироглутамата, и четыре легкие цепи из SEQ ID NO: 8.
[69] В одном варианте осуществления, антитело против GITR человека содержит две тяжелые цепи, где каждая имеет две вариабельные области, состоящие из аминокислотной последовательности в диапазоне от Q в положении 1 до G в положении 686 из SEQ ID NO: 7, и четыре легкие цепи из SEQ ID NO: 8.
[70] В одном варианте осуществления, антитело против GITR человека содержит две тяжелые цепи, состоящие из аминокислотной последовательности в диапазоне от Q в положении 1 до G в положении 686 из SEQ ID NO: 7, где Q модифицирован до пироглутамата, и четыре легкие цепи из SEQ ID NO: 8.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[71] На ФИГ. 1 представлена схематическая иллюстрация механизма действия конкретных иллюстративных ABP GITR, представленных в настоящем описании. На ФИГ. 1A показаны три молекулы GITR (одна обозначена 101), погруженные в мембрану клетки (102). Показан рисунок антитела традиционного формата, связывающего всего две молекулы GITR (103). На ФИГ. 1B показан рисунок антитела тетравалентного моноспецифического (TM) формата, описанного в настоящем описании: на левой панели (105) показано TM, содержащее два N-концевых Fab IgG1, с C-концевым антителом IgG4 S228P; на правой панели (106) показано TM, содержащее два C-концевых Fab IgG1 и N-концевое антитело IgG4 S228P. Антигенсвязывающие домены проиллюстрированы незакрашенными кругами (107). На ФИГ. 1C показан рисунок антитела тетравалентного биспецифического формата, описанного в настоящем описании: на левой панели (105) показано биспецифическое антитело, содержащее два N-концевых Fab IgG1, с C-концевым антителом IgG4 S228P; на правой панели (106) показано биспецифическое антитело, содержащее два C-концевых Fab IgG1 и N-концевое антитело IgG4 S228P. Антигенсвязывающие домены, имеющие специфичность для двух не перекрывающихся эпитопных специфичностей, проиллюстрированы незакрашенными кругами (107 и 108). На ФИГ. 1D показана мультимеризация GITR после связывания трех иллюстративных ABP тетравалентного моноспецифического (TM) формата. Ожидают, что мультимеризация выступает в роли агониста передачи сигналов GITR, как описано в другом месте настоящего описания.
[72] ФИГ. 2 представляет собой график, показывающий иллюстративные результаты определения KD посредством OCTET для ABP формата с N-концевым Fab 1-8.
[73] ФИГ. 3 представляет собой серии графиков, показывающих результаты анализа FACS, показывающие связывание иллюстративной панели ABP формата TM с N-концевым Fab с CD4+ (фигура 3A) и CD8+ (фигура 3B) T-клетками. Распределение CD4+ и CD8+ показано на верхней левой панели каждой фигуры. В верхнем ряду, слева направо, показан положительный контроль против GITR и контроль изотипа против IgG4 человека, ABP9, ABP2, ABP1, и ABP7. В нижнем ряду показаны ABP8, ABP3, ABP4, ABP5, ABP6, ABP23 и ABP24. Указан процент положительно окрашенных IgG4+ CD4/8+ клеток; MRI указана в скобках.
[74] ФИГ. 4 представляет собой серии графиков, показывающих активность восьми оптимизированных агонистических антител в формате TM с N-концевым Fab. Клетки HT1080, стабильно экспрессирующие GITR человека (левые панели) или яванского макака (правые панели), затем инкубировали с ABP1 (ФИГ. 4A), ABP2 (ФИГ. 4B), ABP3 (ФИГ. 4C), ABP4 (ФИГ. 4D), ABP5 (ФИГ. 4E), ABP6 (ФИГ. 4F), ABP7 (ФИГ. 4G) и ABP8 (FIG 4H) (показаны как круги на ФИГ.), и измеряли индукцию IL-8. GITRL использовали в качестве контроля (квадраты). Таблица значений EC50 показана внизу каждой панели на каждой ФИГ.
[75] ФИГ. 5 представляет собой серии графиков, сравнивающие агонистическую активность в экспрессирующих GITR клетках HT1080 исходного антитела формата TM с N-концевым Fab, ABP43, с радом дополнительно оптимизированных антител, имеющих либо N-концевой, либо C-концевой формат. На ФИГ. 5A показаны ABP43 (квадраты), ABP23 (круги), ABP24 (треугольники) и ABP29 (незакрашенные круги), ABP30 (незакрашенные треугольники), ABP31 (незакрашенные круги) и ABP32 (незакрашенные треугольники), все по сравнению с GITRL (знак +). На ФИГ. 5B показаны ABP19 (N-концевой Fab, треугольники) и ABP25 (C-концевой Fab, перевернутые треугольники). GITRL показан как знаки плюс. На ФИГ. 5C показаны ABP21 (N-концевой Fab, треугольники) и ABP27 (C-концевой Fab, перевернутые треугольники). GITRL показан как знаки плюс. На ФИГ. 5D показаны ABP20 (N-концевой Fab, треугольники) и ABP26 (C-концевой Fab, перевернутые треугольники). GITRL показан как знаки плюс. На ФИГ. 5E показаны ABP22 (N-концевой Fab, треугольники) и ABP28 (C-концевой Fab, перевернутые треугольники). GITRL показан как знаки плюс. Контроль IgG4 показан как знак X на каждой фигуре.
[76] На ФИГ. 6 показаны результаты определения EC50 для ABP33 и ABP34 в анализе HT1080, как описано в примерах. ABP33 (тетравалентный вариант, объединяющий IgG4 ABP61 с Fab IgG1 из ABP58 на N-конце) и ABP34 (тетравалентный вариант, объединяющий IgG4 из ABP61 с Fab IgG1 из ABP58 на C-конце) сравнивали с двухвалентными ABP 59 и 61 (IgG4 S228P), которые являлись основой для ABP33 и ABP34. Как показано на ФИГ., оба биспецифических тетравалентных антитела имеют превосходящую EC50, как измерено по индукции IL-8, по сравнению с индивидуальными двухвалентными антителами, использованными для конструирования биспецифических тетравалентных антител.
[77] На ФИГ. 7 показаны результаты определения EC50 в анализе T-клеток Jurkat, как описано для клеток HT1080 выше. Оптимизированные ABP формата TM с N-концевым Fab сравнивали с GITRL по их способности выступать в роли агониста GITR, как измерено по продукцию IL-8. На ФИГ. 7A-7H показаны ABP 1-8, соответственно.
[78] На ФИГ. 8A показан анализ FACS для количественных оценок в трех повторах T-клеток, выделенных от двух доноров-людей, и показан процент GITR+ CD4+ клеток (слева) и CD8+ клеток (справа) в различных временных точках, +/- стимуляция с использованием PHA.
[79] На ФИГ. 8B-8M показаны результаты обработки T-бластов от 4 различных доноров после контрольных обработок или обработок ABP, и полученная продукция IL-2 (данные нормализованы по уровням продукции IL-2, достигнутыми в контрольных средах). На каждой ФИГ. верхний ряд, слева направо, представляет собой измерение FACS связывания ABP с CD4+ клетками, продукция IL-2 в клетках от донора 1, продукция IL-2 в клетках от донора 2. В нижнем ряду, слева направо, представлено измерение FACS связывания ABP с CD8+ клетками, продукция IL-2 в клетках от донора 3, продукция IL-2 в клетках от донора 4. Данные показаны следующим образом: 8B: контроль изотипа IgG4; 8C: антитело SEC4; 8D: отрицательный контроль IgG4 формата TM; 8E: ABP9 (IgG4 формата TM, неоптимизированный предшественник ABP 1-8). 8F: ABP1; 8G: ABP2; 8H: ABP3; 8I: ABP4; 8J: ABP5; 8K:ABP6; 8L: ABP7; 8M: ABP8.
[80] ФИГ. 9A-9H представляет собой серии графиков, показывающих сравнение активности оптимизированного ABP TM с N-концевым Fab («IgG4 TM») против соответствующего оптимизированного не относящегося к TM ABP IgG1 N297A («IgG1»). Клетки HT1080, стабильно экспрессирующие GITR человека (левая панель) или яванского макака (правая панель), затем обрабатывали каждым TM с N-концевым Fab ABP и соответствующим ABP IgG1 следующим образом: ABP1 IgG4 TM /ABP35 IgG1 (ФИГ. 9A), ABP2 IgG4 TM /ABP36 IgG1 (ФИГ. 9B), ABP3 IgG4 TM /ABP37 IgG1 (ФИГ. 9C), ABP4 IgG4 TM /ABP38 IgG1 (ФИГ. 9D), ABP5 IgG4 TM /ABP38 P45L IgG1 (ФИГ. 9E), ABP6 IgG4 TM /ABP39 IgG1 (ФИГ. 9F), ABP7 IgG4 TM /ABP40 IgG1 (ФИГ. 9G) и ABP8 IgG4 TM /ABP41 IgG1 (ФИГ. 9H) и IgG4 в качестве положительного контроля. Индукция IL-8 посредством GITRL показана как круги, посредством ABP IgG4 формата TM как треугольники, посредством соответствующего ABP IgG1 как ромбы и посредством контрольных антител IgG4 как квадраты. Таблица значений EC50 показана внизу каждой панели на каждой ФИГ.
[81] ФИГ. 10 представляет собой график, показывающий данные EC50 в анализе HT1080, как описано, сравнивающие не относящееся к TM исходное антитело с соответствующими вариантами формата TM. ABP43 (ромбы) представляет собой не относящийся к TM IgG4 S228P предшественник ABP9 (IgG4 N-концевой Fab, квадраты) и ABP10 (IgG4 C-концевой Fab, круги). Индукция IL-8 посредством GITRL (положительный контроль) показана как одиночная точка данных (звезда). Продукция IL-8 показана в пг/мл.
[82] ФИГ. 11A представляет собой график, показывающий индукцию IL-8 репрезентативными эталонными антителами SEC4 и SEC9 в клетках HT1080, модифицированных для стабильной экспрессии GITR человека. Культивированные клетки обрабатывали в течение шести часов с использованием диапазона концентраций двух эталонных агонистических антител, SEC4 (35E6, форматированное для наличия мышиных вариабельных областей с человеческими областями IgG4 S228P/каппа, ромбы) и SEC9 (гуманизированное 6C8 N62Q IgG1 N297A, круги), так же как отрицательного контроля IgG4 (закрашенные треугольники), отрицательного контроля IgG1 отрицательного контроля (незакрашенные треугольники), и тримерного лиганда GITR человека («hGITRL», квадраты) в качестве положительного контроля. Индукцию IL-8 измеряли посредством ELISA. Как показано на фигуре, GITRL имел лучшую EC50 (врезка) и максимальную индукцию, по сравнению как с SEC4, так и с SEC9. На ФИГ. 11B-11I показано сравнение ABP 1-8, соответственно, с SEC4 и SEC9. TM ABP указаны кругами, SEC4 квадратами и SEC9 треугольниками. Продукция IL-8 показана в пг/мл.
[83] ФИГ. 12 представляет собой два графика, показывающие продукцию цитокинов в стимулированных выделенных клетках аденокарциномы человека NSCLC после обработки с использованием ABP1 формата TM, отдельно или в комбинации с пембролизумабом. Клетки либо представляли собой нестимулированный контроль, либо были стимулированы с использованием 1 мкг/мл αCD3 (растворимого)+2 мкг/мл αCD28 (растворимого)+IL-2 (50 нг/мл); клетки либо не подвергали иммунотерапевтической обработке (для оценки уровней белка контрольной точки), либо подвергали обработке пембролизумабом (10 мкг/мл), контрольным ABP формата TM (2 мкг/мл), ABP1 (2 мкг/мл), или ABP1+пембролизумабом. Клетки инкубировали в течение 48 часов перед сбором супернатантов, и клетки окрашивали по экспрессии белка контрольной точки. В некоторых образцах, брефелдин A (ингибитор секреции цитокинов) добавляли на последние пять часов стимуляции для детекции цитокинов посредством внутриклеточного окрашивания цитокинов. Показана продукция TNF (ФИГ. 12A) и продукция IFNγ (ФИГ. 12B).
[84] ФИГ. 13 представляет собой серии графиков, показывающих кластеризацию и интернализацию GITR после связывания антитела. Интернализацию GITR измеряли в CD4+ клетках (ФИГ. 13A-E) и CD8+ клетках (фигуры 13F-J) либо от донора 1 (фигуры 13A-B, 13F-G), либо от донора 2 (фигуры 13C-D, 13H-I). Клетки обрабатывали либо ABP1 в формате TM антитела, либо стандартным двухвалентным антителом ABP35. Как можно наблюдать, инкубация либо с ABP1, либо с ABP35 ингибирует последующее окрашивание с использованием ABP1Dylight650 (фигуры 13A, 13C, 13F, 13H), но только инкубация с ABP1 индуцирует интернализацию GITR, как измерено по окрашиванию с использованием не конкурирующего клона 108-17 (фигуры 13B, 13D, 13G, 13I). Определение EC50 ABP1 на клетках от обоих доноров показано на фигуре 13E (CD4+ клетки) и фигуре 13J (CD8+ клетки).
[85] На ФИГ. 14 показана продукция цитокина (IL-2) активированными T-бластами от двух здоровых доноров-людей (донора 1 и донора 2, ФИГ. 14A и 14B, соответственно) после обработки ABP1 против GITR формата TM антитела IgG4, его эквивалентом ABP35 формата IgG1 и контролями изотипа IgG4 формата TM и IgG1. Активированные CD4+/CD8+ T-клетки обрабатывали только средой, рекомбинантным GITR-лигандом, ABP1, контролем изотипа hIgG4 формата TM, ABP35 или контролем изотипа hIgG1 стандартного формата, в девяти дозах каждый: 10 мкг/мл, 2 мкг/мл, 0,4 мкг/мл, 80 нг/мл, 16 нг/мл, 3,2 нг/мл, 0,64 нг/мл, 0,13 нг/мл, и 0,026 нг/мл. Клетки стимулировали посредством добавления 1 мкг/мл антител против CD3 и 2 мкг/мл антител против CD28. На ФИГ. 14C показаны такие же данные для ABP1, как на ФИГ. 14A и 14B, с расчетом определения EC50 у каждого донора.
[86] На ФИГ. 15 показана продукция цитокина (IL-2) активированными T-бластами от двух здоровых доноров-людей (донора 1 и донора 2, ФИГ. 15A и 15B, соответственно) после обработки ABP1 против GITR формата TM антитела IgG4, контролем IgG4 формата TM («Изо-TM»), SEC4, SEC9, рекомбинантным hGITRL и контролями изотипа IgG1 и IgG4. Активированные CD4+/CD8+ T-клетки обрабатывали только средой, рекомбинантным GITR-лигандом, ABP1, контролем изотипа hIgG4 формата TM, SEC4, SEC9, контролем изотипа IgG1 стандартного формата или контролем изотипа hIgG1 стандартного формата, в девяти дозах каждый: 10 мкг/мл, 2 мкг/мл, 0,4 мкг/мл, 80 нг/мл, 16 нг/мл, 3,2 нг/мл, 0,64 нг/мл, 0,13 нг/мл, и 0,026 нг/мл. Клетки стимулировали посредством добавления 1 мкг/мл антител против CD3 и 2 мкг/мл антител против CD28. На ФИГ. 15C (донор 1) и 15D (донор 2) показаны такие же данные для ABP1, как на 15A и 15B, с расчетом определения EC50 у каждого донора.
ПОДРОБНОЕ ОПИСАНИЕ
Определения
[87] Если не определено иное, все термины из данной области, обозначения и другая научная терминология, используемые в настоящем описании, имеют значение, общеизвестное для специалиста в области, к которой относится это изобретение. В некоторых случаях, термины с общеизвестными значениями определены в настоящем описании для ясности и/или для удобства ссылки, и включение таких определений в настоящее описание необязательно следует рассматривать как представляющее отличие от того, что является общеизвестным в данной области. Техники и способы, описанные или процитированные в настоящем описании, в основном, хорошо понятны и широко применяются с использованием общепринятых способов, специалистами в данной области, например, такие как широко применяемые способы молекулярного клонирования, описанные в Sambrook et al., Molecular Cloning: A Laboratory Manual 4th ed. (2012) Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY. Подходящим образом, способы, включающие использование коммерчески доступных наборов и реагентов, как правило, осуществляют в соответствии с определенными производителем протоколами и условиями, если не указано иное.
[88] В рамках изобретения, формы единственного числа включают ссылки на множественное число, если контекст явно не указывает на иное. Термины «включают», «такой как» и т.п. предназначены для выражения включения без ограничения, если конкретно не указано иное.
[89] Как используют в настоящем описании, термин «содержащий» также конкретно включает варианты «состоящий из» и «в основном состоящий из» перечисленных элементов, если конкретно не указано иное. Например, мультиспецифический ABP, «содержащий диатело», включает мультиспецифический ABP, «состоящий из диатела», и мультиспецифический ABP «в основном состоящий из диатела».
[90] Термин «приблизительно» обозначает и включает указанное значение и диапазон выше и ниже этого значения. В конкретных вариантах осуществления, термин «приблизительно» обозначает указанное значение±10%,±5% или±1%. В конкретных вариантах осуществления, термин «приблизительно» обозначает указанное значение±одно стандартное отклонение от этого значения.
[91] Термины «GITR», «белок GITR» и «антиген GITR» используют в настоящем описании взаимозаменяемо для обозначения GITR человека или любых вариантов (например, вариантов сплайсинга и аллельных вариантов), изоформ и видовых гомологов GITR человека, которые естественным образом экспрессированы в клетках, или которые экспрессированы в клетках, трансфицированных геном gitr. В некоторых аспектах, белок GITR представляет собой белок GITR, естественным образом экспрессированный у примата (например, обезьяны или человека), грызуна (например, мыши или крысы), собаки, верблюда, кошки, коровы, козы, лошади или овцы. В некоторых аспектах, белок GITR представляет собой GITR человека (hGITR; SEQ ID NO: 1). В некоторых аспектах, белок GITR представляет собой вариант T43R GITR человека (hGITR-T43R; SEQ ID NO: 2). В некоторых аспектах, белок GITR содержит внеклеточный домен hGITR, локализованный в положениях 26-162 из SEQ ID NO: 1-2. В некоторых аспектах, белок GITR представляет собой GITR яванского макака (cGITR; SEQ ID NO: 3). В некоторых аспектах, белок GITR содержит внеклеточный домен cGITR, локализованный в положениях 20-156 из SEQ ID NO: 3. В некоторых аспектах, белок GITR представляет собой GITR мыши (mGITR; SEQ ID NO: 4). В некоторых аспектах, белок GITR содержит внеклеточный домен mGITR, локализованный в положениях 20-153 из SEQ ID NO: 4. В некоторых аспектах, белок GITR представляет собой полноразмерный или непроцессированный белок GITR. В некоторых аспектах, белок GITR представляет собой укороченный или процессированный белок GITR, полученный посредством посттрансляционной модификации. GITR известен также под множеством синонимов, включая член 18 суперсемейства рецепторов фактора некроза опухоли, (TNFRSF18); AITR, индуцируемый глюкокортикоидами родственный TNFR белок; индуцируемый активацией рецептор семейства TNFR; индуцируемый активацией белок суперсемейства рецепторов TNF; CD357; и GITR-D.
[92] Термин «иммуноглобулин» относится к классу структурно родственных белков, как правило, содержащих две пары полипептидных цепей: одну пару легких (L) цепей и одну пару тяжелых (H) цепей. В «интактном иммуноглобулине», все четыре из этих цепей соединены друг с другом дисульфидными связями. Структура иммуноглобулинов хорошо охарактеризована. См., например, Paul, Fundamental Immunology 7th ed., Ch. 5 (2013) Lippincott Williams & Wilkins, Philadelphia, PA. Кратко, каждая тяжелая цепь, как правило, содержит вариабельную область тяжелой цепи (VH) и константную область тяжелой цепи (CH). Константная область тяжелой цепи, как правило, содержит три домена, обозначенные CH1, CH2, и CH3. Каждая легкая цепь, как правило, содержит вариабельную область легкой цепи (VL) и константную область легкой цепи. Константная область легкой цепи, как правило, содержит один домен, обозначенный CL.
[93] Термин «антигенсвязывающий белок» (ABP) относится к белку, содержащему один или несколько антигенсвязывающих доменов, которые специфически связывают антиген или эпитоп. В некоторых вариантах осуществления, антигенсвязывающий домен связывает антиген или эпитоп со специфичностью и аффинностью, сходными со специфичностью и аффинностью природных антител. В некоторых вариантах осуществления, ABP содержит, состоит из или в основном состоит из антитела. В некоторых вариантах осуществления, ABP содержит, состоит из или в основном состоит из фрагмента антитела. В некоторых вариантах осуществления, ABP содержит, состоит из или в основном состоит из альтернативного каркаса. «ABP GITR», «ABP против GITR» или «специфический для GITR ABP» представляет собой ABP, в рамках изобретения, который специфически связывает антиген GITR. В некоторых вариантах осуществления, ABP связывает внеклеточный домен GITR. В конкретных вариантах осуществления, ABP GITR, в рамках изобретения, связывает эпитоп GITR, консервативный между белками GITR или среди белков GITR из различных видов.
[94] Термин «антитело» использован в настоящем описании в самом широком смысле и включает конкретные типы молекул иммуноглобулинов, содержащие один или несколько антигенсвязывающих доменов, специфически связывающих антиген или эпитоп. Антитело конкретно включает интактные антитела (например, интактные иммуноглобулины), фрагменты антител и мультиспецифические антитела. Одним примером антигенсвязывающего домена является антигенсвязывающий домен, сформированный посредством димера VH -VL. Антитело представляет собой один тип ABP.
[95] Термин «альтернативный каркас» относится к молекуле, в которой одна или несколько областей может быть подвергнута диверсификации для получения одного или нескольких антигенсвязывающих доменов, специфически связывающих антиген или эпитоп. В некоторых вариантах осуществления, антигенсвязывающий домен связывает антиген или эпитоп со специфичностью и аффинностью, сходными со специфичностью и аффинностью природных антител. Иллюстративные альтернативные каркасы включают каркасы, происходящие из фибронектина (например, аднектины™), β-сэндвича (например, iMab), липокалина (например, антикалины®), EETI-II/AGRP, BPTI/LACI-D1/ITI-D2 (например, домены Куница), пептидных аптамеров на основе тиоредоксина, белка A (например, аффитело®), анкириновых повторов (например, дарпины), гамма-B-кристаллина/убиквитина (например, аффилины), CTLD3 (например, тетранектины), финомеров и модуля LDLR-A (например, авимеры). Дополнительная информация об альтернативных каркасах представлена в Binz et al., Nat. Biotechnol., 2005 23:1257-1268; Skerra, Current Opin. in Biotech., 2007 18:295-304; и Silacci et al., J. Biol. Chem., 2014, 289:14392-14398; полное содержание всех из которых приведено в настоящем описании в качестве ссылки. Альтернативный каркас представляет собой один тип ABP.
[96] Термин «антигенсвязывающий домен» обозначает часть ABP, способную специфически связывать антиген или эпитоп.
[97] Термины «полноразмерное антитело», «интактное антитело» и «полное антитело» используют в настоящем описании взаимозаменяемо для обозначения антитела, имеющего структуру, по существу сходную со структурой природного антитела и имеющего тяжелые цепи, содержащие область Fc.
[98] Термин «область Fc» обозначает C-концевую область тяжелой цепи иммуноглобулина, которая, в природных антителах, взаимодействует с рецепторами Fc и определенными белками системы комплемента. Структуры областей Fc различных иммуноглобулинов и содержащиеся в них участки гликозилирования известны в данной области. См. Schroeder and Cavacini, J. Allergy Clin. Immunol., 2010, 125:S41-52, полное содержание которого приведено в качестве ссылки. Область Fc может представлять собой природную область Fc, или область Fc, модифицированную, как описано в другом месте настоящего описания.
[99] Области VH и VL можно далее подразделять на области гипервариабельности («гипервариабельные области (HVR);» также называемые «определяющими комплементарность областями» (CDR)), перемежающиеся с областями, которые являются более консервативными. Более консервативные области называют каркасными областями (FR). Каждая VH и VL, как правило, содержит три CDR и четыре FR, расположенные в следующем порядке (от N-конца до C-конца): FR1 - CDR1 - FR2 - CDR2 - FR3 - CDR3 - FR4. CDR вовлечены в связывание антигена и влияют на антигенную специфичность и аффинность связывания антитела. См. Kabat et al., Sequences of Proteins of Immunological Interest 5th ed. (1991) Public Health Service, National Institutes of Health, Bethesda, MD, полное содержание которого приведено в качестве ссылки.
[100] Легкую цепь из любого вида позвоночных можно отнести к одному из двух типов, называемых каппа (κ) и лямбда (λ), на основании последовательности ее константного домена.
[101] Тяжелую цепь из любого вида позвоночных можно отнести к одному из пяти различных классов (или изотипов): IgA, IgD, IgE, IgG и IgM. Эти классы обозначены также α, δ, ε, γ и μ, соответственно. Классы IgG и IgA далее подразделяют на подклассы на основании различий в последовательности и функции. У человека экспрссируются следующие подклассы: IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2.
[102] Границы аминокислотной последовательности CDR специалист в данной области может определять с использованием любой из ряда известных схем нумерации, включая описанные в Kabat et al., выше (схема нумерации «Kabat»); Al-Lazikani et al., 1997, J. Mol. Biol., 273:927-948 (схема нумерации «Chothia»); MacCallum et al., 1996, J. Mol. Biol. 262:732-745 («контактная» схема нумерации); Lefranc et al., Dev. Comp. Immunol., 2003, 27:55-77 (схема нумерации «IMGT»); и Honegge and Plückthun, J. Mol. Biol., 2001, 309:657-70 (схема нумерации «AHo»); полное содержание всех из которых приведено в настоящем описании в качестве ссылки.
[103] В таблице 1 представлены положения CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3, как идентифицировано посредством схем Kabat и Chothia. Для CDR-H1, представлена нумерация остатков с использованием обеих схем нумерации Kabat и Chothia.
[104] Если не указано иное, схема нумерации, используемая для идентификации конкретной CDR в настоящем описании, представляет собой схему нумерации Kabat/Chothia. Когда остатки, охваченные этими двумя схемами нумерации, отличаются (например, CDR-H1 и/или CDR-H2), схема нумерации определена либо как Kabat, либо как Chothia. Для удобства, CDR-H3 иногда обозначают в настоящем описании либо как Kabat, либо как Chothia. Однако, это не предназначено для введения различий в последовательности, когда они не существуют, и специалист в данной области может легко подтвердить, являются ли последовательности одинаковыми или различными, посредством проверки последовательностей.
[105] CDR можно приписывать, например, с использованием программного обеспечения для нумерации антител, такого как Abnum, доступного на www.bioinf.org.uk/abs/abnum/, и описанного в Abhinandan and Martin, Immunology, 2008, 45:3832-3839, полное содержание которого приведено в качестве ссылки.
Таблица 1. Остатки в CDR в соответствии со схемами нумерации Kabat и Chothia.
* C-конец CDR-H1, при нумерации с использованием системы нумерации Kabat, отличается между H32 и H34, в зависимости от длины CDR.
[106] «Схему нумерации EU», как правило, используют при ссылке на остаток в константной области тяжелой цепи антитела (например, как опубликовано в Kabat et al., выше). Если не указано иное, схему нумерации EU используют для обозначения остатков в константных областях тяжелой цепи антитела, описанных в настоящем описании.
[107] «Фрагмент антитела» или «антигенсвязывающий фрагмент» содержит часть интактного антитела, такого как антигенсвязывающая или вариабельная область интактного антитела. фрагменты антител включают, например, фрагменты Fv, фрагменты Fab, фрагменты F(ab')2, фрагменты Fab', фрагменты scFv (sFv) и фрагменты scFv-Fc.
[108] Фрагменты «Fv» содержат нековалентно связанный димер вариабельного домена одной тяжелой цепи и вариабельного домена одной легкой цепи.
[109] Фрагменты «Fab» содержат, в дополнение к вариабельным доменам тяжелой и легкой цепи, константный домен легкой цепи и первый константный домен (CH1) тяжелой цепи. Фрагменты Fab можно получать, например, рекомбинантными способами или посредством расщепления папаином полноразмерного антитела.
[110] Фрагменты «F(ab')2» содержат два фрагмента Fab', соединенные, рядом с шарнирной областью, дисульфидными связями. Фрагменты F(ab')2 можно получать, например, рекомбинантными способами или посредством расщепления пепcином интактного антитела. фрагменты F(ab') можно диссоциировать, например, посредством обработки β-меркаптоэтанолом.
[111] Фрагменты антител «одноцепоченый Fv» или «sFv», или «scFv» содержат домен VH и домен VL на одной полипептидной цепи. VH и VL, как правило, связаны посредством пептидного линкера. См. Plückthun A. (1994). В некоторых вариантах осуществления, линкер представляет собой (GGGGS)n (SEQ ID NO: 5). В других вариантах осуществления, линкер представляет собой GGGGSGGGGSGGGGS (SEQ ID NO:6). В некоторых вариантах осуществления, n=1, 2, 3, 4, 5, или 6. См. Antibodies from Escherichia coli. In Rosenberg M. & Moore G.P. (Eds.), The Pharmacology of Monoclonal Antibodies vol. 113 (pp. 269-315). Springer-Verlag, New York, полное содержание которого приведено в качестве ссылки.
[112] Фрагменты «scFv-Fc» содержат scFv, присоединенный к домену Fc. Например, домен Fc может быть присоединен к C-концу scFv. За доменом Fc может следовать VH или VL, в зависимости от ориентации вариабельных доменов в scFv (т.е., VH -VL или VL -VH ). Можно использовать любой подходящий домен Fc, известный в данной области или описанный в настоящем описании. В некоторых случаях, домен Fc содержит домен Fc IgG4.
[113] Термин «однодоменное антитело» относится к молекуле, в которой один вариабельный домен антитела специфически связывает антиген без присутствия другого вариабельного домена. Однодоменные антитела и их фрагменты описаны в Arabi Ghahroudi et al., FEBS Letters, 1998, 414:521-526 и Muyldermans et al., Trends in Biochem. Sci., 2001, 26:230-245, полное содержание всех из которых приведено в настоящем описании в качестве ссылки.
[114] «Мультиспецифический ABP» представляет собой ABP, содержащий два или более различных антигенсвязывающих доменов, совместно специфически связывающих два или более различных эпитопа. Два или более различных эпитопа могут представлять собой эпитопы на одном и том же антигене (например, отдельной молекуле GITR, экспрессированной в клетке) или на различных антигенах (например, различных молекулах GITR, экспрессированных в одной и той же клетке). В некоторых аспектах, мультиспецифический ABP связывает два различных эпитопа (т.е., «биспецифический ABP»). В некоторых аспектах, мультиспецифический ABP связывает три различных эпитопа (т.е., «триспецифический ABP»). В некоторых аспектах, мультиспецифический ABP связывает четыре различных эпитопа (т.е., «квадроспецифический ABP»). В некоторых аспектах, мультиспецифический ABP связывает шесть различных эпитопов (т.е., «квинтоспецифический ABP»). В некоторых аспектах, мультиспецифический ABP связывает 6, 7, 8 или более различных эпитопов. Каждая специфичность связывания может присутствовать с любой подходящей валентностью. Примеры мультиспецифического ABP представлены в другом мете настоящего описания.
[115] «Моноспецифический ABP» представляет собой ABP, который содержит участок связывания, специфически связывающий одиночный эпитоп. Примером моноспецифического ABP является природная молекула IgG, которая, в то время как является двухвалентной, узнает один и тот же эпитоп на каждом антигенсвязывающем домене. Специфичность связывания может присутствовать с любой подходящей валентностью.
[116] Термин «моноклональное антитело» относится к антителу из популяции по существу гомогенных антител. Популяция по существу гомогенных антител содержит антитела, которые являются по существу сходными и которые связывают одинаковый эпитоп(ы), за исключением вариантов, которые могут в норме возникать в ходе получения моноклонального антитела. Такие варианты, как правило, присутствуют только в незначительных количествах. Моноклональное антитело, как правило, получают способом, включающим отбор одного антитела из множества антител. Например, способ отбора может представлять собой отбор уникального клона из множества клонов, таких как пул клонов гибридомы, клонов фага, клонов дрожжей, клонов бактерий или клонов другой рекомбинантной ДНК. Отобранное антитело можно далее изменять, например, для улучшения аффинности для мишени («аффинное созревание»), для гуманизации антитела, для улучшения его продукции в культуре клеток и/или для уменьшения его иммуногенности у субъекта.
[117] Термин «химерное антитело» относится к антителу, в котором часть тяжелой и/или легкой цепи происходит из конкретного источника или вида, в то время как остальная часть тяжелой и/или легкой цепи происходит из другого источника или вида.
[118] «Гуманизированные» формы не относящегося к человеку антитела представляют собой химерные антитела, содержащие минимальную последовательность, происходящую из не относящегося к человеку антитела. Гуманизированное антитело, как правило, представляет собой человеческое антитело (реципиентное антитело), в котором остатки из одной или нескольких CDR заменены на остатки одной или несколько CDR из не относящегося к человеку антитела (донорного антитела). Донорное антитело может представлять собой любое подходящее не относящееся к человеку антитело, такое как антитело мыши, крысы, кролика, курицы или не относящегося к человеку примата, имеющее желательную специфичность, аффинность или биологический эффект. В некоторых случаях, выбранные остатки каркасной области реципиентного антитела заменяют на соответствующие остатки каркасной области из донорного антитела. Гуманизированные антитела могут также содержать остатки, не обнаруженные в реципиентном антителе или донорном антителе. Такие модификации можно осуществлять для дальнейшего уточнения функции антитела. Дополнительные подробности См. в Jones et al., Nature, 1986, 321:522-525; Riechmann et al., Nature, 1988, 332:323-329; и Presta, Curr. Op. Struct. Biol., 1992, 2:593-596, полное содержание всех из которых приведено в настоящем описании в качестве ссылки.
[119] «Человеческое антитело» представляет собой антитело, имеющее аминокислотную последовательность, соответствующую аминокислотной последовательности антитела, продуцированного человеком или клеткой человека, или полученные от не относящегося к человеку источника, в котором использован репертуар человеческих антител или кодирующие человеческое антитело последовательности (например, полученные из человеческих источников или сконструированные de novo). Человеческие антитела конкретно исключают гуманизированные антитела.
[120] «Выделенный ABP» или «выделенная нуклеиновая кислота» представляет собой ABP или нуклеиновую кислоту, отделенные от и/или выделенные из компонента их природного окружения. Компоненты природного окружения могут включать ферменты, гормоны и другие белковые или небелковые материалы. В некоторых вариантах осуществления, выделенный ABP является очищенным до степени, достаточной для получения по меньшей мере 15 остатков N-концевой или внутренней аминокислотной последовательности, например, с использованием секвенатора с вращающимся стаканом. В некоторых вариантах осуществления, выделенный ABP является очищенным до гомогенности посредством электрофореза в геле (например, SDS-PAGE) в восстанавливающих или невосстанавливающих условиях, с детекцией окрашиванием Кумасси® синим или серебром. Выделенный ABP включает в себя ABP in situ внутри рекомбинантной клетки, поскольку по меньшей мере один компонент природного окружения ABP не присутствует. В некоторых аспектах, выделенный ABP или выделенная нуклеиновая кислота получены посредством по меньшей мере одной стадии очистки. В некоторых вариантах осуществления, выделенный ABP или выделенная нуклеиновая кислота являются очищенными до по меньшей мере 80%, 85%, 90%, 95% или 99% по массе. В некоторых вариантах осуществления, выделенный ABP или выделенная нуклеиновая кислота являются очищенными до по меньшей мере 80%, 85%, 90%, 95% или 99% по объему. В некоторых вариантах осуществления, выделенный ABP или выделенная нуклеиновая кислота представлены в форме раствора, содержащего по меньшей мере 85%, 90%, 95%, 98%, 99%-100% ABP или нуклеиновой кислоты по массе. В некоторых вариантах осуществления, выделенный ABP или выделенная нуклеиновая кислота представлены в форме раствора, содержащего по меньшей мере 85%, 90%, 95%, 98%, 99%-100% ABP или нуклеиновой кислоты по объему.
[121] «Аффинность» относится к силе общих суммарных нековалентных взаимодейстий одного участка связывания молекулы (например, an ABP) и ее партнера по связыванию (например, антигена или эпитопа). Если не указано иное, как применяют в настоящем описании, «аффинность» относится к собственной аффинности связывания, отражающей взаимодействие 1:1 меду членами связывающейся пары (например, ABP и антигена или эпитопа). Аффинность молекулы X для ее партнера Y можно представлять посредством равновесной константы диссоциации (KD). Кинетические компоненты, вносящие вклад в равновесную константу диссоциации, более подробно описаны ниже. Аффинность можно измерять общепринятыми способами, известными в данной области, включая описанные в настоящем описании. Аффинность можно определять, например, с использованием способа поверхностного плазмонного резонанса (SPR) (например, BIACORE®) или интерферометрии биослоя (например, FORTEBIO®).
[122] Применительно к связыванию ABP с молекулой-мишенью, термины «связывать», «специфическое связывание», «специфически связывает», «специфический для», «избирательно связывает» и «избирательный для» конкретного антигена (например, полипептидной мишени) или эпитопа конкретного антигена, обозначают связывание, которое является измеримо отличным от неспецифического или неизбирательного взаимодействия (например, с не относящейся к мишени молекулой). Специфическое связывание можно измерять, например, посредством измерения связывания с молекулой-мишенью и сравнения со связыванием с не относящейся к мишени молекулой. Специфическое связывание можно также определять по конкуренции с контрольной молекулой, имитирующей эпитоп, узнаваемый на молекуле-мишени. В этом случае, специфическое связывание показывают, если связывание ABP с молекулой-мишенью конкурентно ингибируется контрольной молекулой. В некоторых аспектах, аффинность ABP GITR для не относящейся к мишени молекулы составляет менее, чем приблизительно 50% аффинности для GITR. В некоторых аспектах, аффинность ABP GITR для не относящейся к мишени молекулы составляет менее, чем приблизительно 40% аффинности для GITR. В некоторых аспектах, аффинность ABP GITR для не относящейся к мишени молекулы составляет менее, чем приблизительно 30% аффинности для GITR. В некоторых аспектах, аффинность ABP GITR для не относящейся к мишени молекулы составляет менее, чем приблизительно 20% аффинности для GITR. В некоторых аспектах, аффинность ABP GITR для не относящейся к мишени молекулы составляет менее, чем приблизительно 10% аффинности для GITR. В некоторых аспектах, аффинность ABP GITR для не относящейся к мишени молекулы составляет менее, чем приблизительно 1% аффинности для GITR. В некоторых аспектах, аффинность ABP GITR для не относящейся к мишени молекулы составляет менее, чем приблизительно 0,1% аффинности для GITR.
[123] Термин «kd» (с-1), в рамках изобретения, относится к константе скорости диссоциации для конкретного взаимодействия ABP-антиген. Это значение также обозначают как значение koff.
[124] Термин «ka» (M-1×с-1), в рамках изобретения, относится к константе скорости связывания для конкретного взаимодействия ABP-антиген. Это значение также обозначают как значение kon.
[125] Термин «KD» (M), в рамках изобретения, относится к равновесной константе диссоциации конкретного взаимодействия ABP-антиген. KD=kd/ka.
[126] Термин «KA» (M-1), в рамках изобретения, относится к равновесной константе связывания конкретного взаимодействия ABP-антиген. KA=ka/kd.
[127] «Подвергнутый аффинному созреванию» ABP представляет собой ABP с одним или несколькими изменениями (например, в одной или нескольких CDR или FR), приводящим к улучшению аффинности ABP для его антигена, по сравнению с исходным ABP, не имеющим изменения(изменений). В одном варианте осуществления, подвергнутый аффинному созреванию ABP имеет наномолярную или пикомолярную аффинность для антигена-мишени. Подвергнутый аффинному созреванию ABP можно получать с использованием множества способов, известных в данной области. Например, в Marks et al. (Bio/Technology, 1992, 10:779-783, полное содержание которого приведено в качестве ссылки), описано аффинное созревание посредством перетасовки доменов VH и VL. Случайный мутагенез CDR и/или каркасных остатков описан, например, в Barbas et al. (Proc. Nat. Acad. Sci. U.S.A., 1994, 91:3809-3813); Schier et al., Gene, 1995, 169:147-155; Yelton et al., J. Immunol., 1995, 155:1994-2004; Jackson et al., J. Immunol., 1995, 154:3310-33199; и Hawkins et al, J. Mol. Biol., 1992, 226:889-896; полное содержание всех из которых приведено в настоящем описании в качестве ссылки.
[128] «Иммуноконъюгат» представляет собой ABP, конъюгированный с одной или несколькими гетерологичной молекулой(молекулми).
[129] «Эффекторные функции» относятся к тем видам биологической активности, опосредованным областью Fc антитела, активность которых может меняться в зависимости от изотипа антитела. Примеры эффекторных функций антитела включают связывание C1q для активации комплементзависимой цитотоксичности (CDC), связывание рецептора Fc для активации антителозависимой клеточной цитотоксичности (ADCC) и антителозависимого клеточного фагоцитоза (ADCP).
[130] При использовании в настоящем описании в контексте двух или более ABP, термин «конкурирует с» или «проявляет перекрестную конкуренцию с» показывает, что два или более ABP конкурируют за связывание с антигеном (например, GITR). В одном иллюстративном анализе, поверхность покрывают GITR и подвергают контакту с первым ABP GITR, после чего добавляют второй ABP GITR. В другом иллюстративном анализе, поверхность покрывают первым ABP GITR и подвергают контакту с GITR, и затем добавляют второй ABP GITR. Если присутствие первого ABP GITR уменьшает связывание второго ABP GITR, в любом анализе, тогда ABP конкурируют. Термин «конкурирует с» включает также комбинации ABP, где ABP уменьшает связывание другого ABP, но где не наблюдают конкуренции, когда ABP добавляют в обратном порядке. Однако, в некоторых вариантах осуществления, первый и второй ABP ингибируют связывание друг друга, независимо от порядка, в котором их добавляют. В некоторых вариантах осуществления, один ABP уменьшает связывание другого ABP с его антигеном по меньшей на мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80% или по меньшей мере на 90%.
[131] Термин «эпитоп» обозначает часть антигена, которая специфически связывается с ABP. Эпитопы часто состоят из доступных на поверхности боковых цепей аминокислотных остатков и/или сахаров и могут иметь специфические характеристики трехмерной структуры, так же как специфические характеристики заряда. Конформационные и неконформационные эпитопы отличаются тем, что связывание с первыми, но не с последними, может быть потеряно в присутствии денатурирующих растворителей. Эпитоп может содержать аминокислотные остатки, непосредственно вовлеченные в связывание, и другие аминокислотные остатки, не вовлеченные непосредственно в связывание. Эпитоп, с которым связывается ABP, можно определять с использованием известных способов определения эпитопов, например, таких как тестирование связывания ABP с вариантами GITR с различными точечными мутациями или с химерными вариантами GITR.
[132] Процент «идентичности» между полипептидной последовательностью и контрольной последовательностью определяют как процент аминокислотных остатков в полипептидной последовательности, которые являются идентичными аминокислотным остаткам в контрольной последовательности, поле выравнивания последовательностей и введения пропусков, если необходимо, для достижения максимального процента идентичности последовательностей. Выравнивание с целью определения процента идентичности аминокислотных последовательностей можно осуществлять различными способами, лежащими в компетенции специалиста в данной области, например, с использованием публично доступного компьютерного программного обеспечения, такого как программное обеспечение BLAST, BLAST-2, ALIGN, MEGALIGN (DNASTAR), CLUSTALW, CLUSTAL OMEGA или MUSCLE. Специалист в данной области может определять подходящие параметры для выравнивания последовательностей, включая любые алгоритмы, необходимые для достижения максимального выравнивания на протяжении полной длины сравниваемых последовательностей.
[133] «Консервативная замена» или «консервативная аминокислотная замена» относится к замене аминокислоты на химически или функционально сходную аминокислоту. Таблицы консервативных замен, предоставляющие сходные аминокислоты, хорошо известны в данной области. В качестве примера, группы аминокислот, представленные в таблицах 2-4, рассматривают, в некоторых вариантах осуществления, как консервативные замены друг для друга.
Таблица 2. Избранные группы аминокислот, которые считают консервативными заменами друг для друга, в конкретных вариантах осуществления.
Таблица 3. Дополнительные избранные группы аминокислот, которые считают консервативными заменами друг для друга, в конкретных вариантах осуществления.
Таблица 4. Дополнительные избранные группы аминокислот, которые считают консервативными заменами друг для друга, в конкретных вариантах осуществления.
[134] Дополнительные консервативные замены можно обнаружить, например, в Creighton, Proteins: Structures and Molecular Properties 2nd ed. (1993) W. H. Freeman & Co., New York, NY. ABP, полученный посредством введения одной или нескольких консервативных замен аминокислотных остатков в исходный ABP, обозначают как «консервативно модифицированный вариант».
[135] Термин «аминокислота» относится к двадцати обычным природным аминокислотам. Природные аминокислоты включают аланин (Ala; A), аргинин (Arg; R), аспарагин (Asn; N), аспарагиновую кислоту (Asp; D), цистеин (Cys; C); глутаминовую кислоту (Glu; E), глутамин (Gln; Q), глицин (Gly; G); гистидин (His; H), изолейцин (Ile; I), лейцин (Leu; L), лизин (Lys; K), метионин (Met; M), фенилаланин (Phe; F), пролин (Pro; P), серин (Ser; S), треонин (Thr; T), триптофан (Trp; W), тирозин (Tyr; Y) и валин (Val; V).
[136] Термин «вектор», в рамках изобретения, обозначает молекулу нуклеиновой кислоты, способную размножать другую нуклеиновую кислоту, с которой она связана. Термин включает вектор как самореплицирующуюся структуру нуклеиновой кислоты, так же как вектор, встроенный в геном клетки-хозяина, в которую он был введен. Определенные векторы являются способными управлять экспрессией нуклеиновых кислот, с которыми они функционально связаны. Такие векторы обозначены в настоящем описании как «экспрессирующие векторы».
[137] Термины «клетка-хозяин», «линия клеток-хозяев» и «культура клеток-хозяев» использованы взаимозаменяемо и обозначают клетки, в которые введена экзогенная нуклеиновая кислота, включая потомство таких клеток. Клетки-хозяева включают «трансфрманты» (или «трансформированные клетки») и «трансфектанты» (или «трансфицированные клетки»), где каждые включают первичную трансформированную или трансфицированную клетку и происходящее из нее потомство. Такое потомство может не являться полностью идентичным родительской клетке по содержанию нуклеиновой кислоты и может содержать мутации.
[138] Термин «лечение» (и его варианты, такие как «лечить» или «подвергание лечению») относится к клиническому вмешательству с целью изменения естественного течения заболевания или состояния у нуждающегося в этом субъекта. Лечение можно проводить как для профилактики, так и в ходе течения клинической патологии. Желательные эффекты лечения включают предотвращение возникновения или рецидива заболевания, облегчение симптомов, уменьшение любых прямых или непрямых патологических последствий заболевания, предотвращение метастазирования, уменьшение скорости прогрессирования заболевания, облегчение или смягчение состояния заболевания и ремиссию или улучшенный прогноз.
[139] В рамках изобретения, термин «терапевтически эффективное количество» или «эффективное количество» относится к количеству ABP или фармацевтической композиции, в рамках изобретения, которое, при введении субъекту, является эффективным для лечения заболевания или нарушение.
[140] В рамках изобретения, термин «субъект» относится к субъекту-млекопитающему. Иллюстративные субъекты включают людей, обезьян, собак, кошек, мышей, крыс, коров, лошадей, верблюдов, коз, кроликов и овец. В конкретных вариантах осуществления, субъект представляет собой человека. В некоторых вариантах осуществления, субъект имеет заболевание или состояние, которое можно лечить с использованием ABP, в рамках изобретения. В некоторых аспектах, заболевание или состояние представляет собой злокачественную опухоль.
[141] Термин «вкладыш в упаковку» используют для обозначения инструкций, обычно включенных в коммерческие упаковки терапевтических или диагностических продуктов (например, наборов), которые содержат информацию относительно показаний, применения, дозирования, введения, комбинированной терапии, противопоказаний и/или предостережений, касающихся использования таких терапевтических или диагностических продуктов.
[142] Термин «цитотоксическое средство», в рамках изобретения, относится к веществу, которое ингибирует или предотвращает клеточную функцию и/или вызывает гибель или разрушение клеток.
[143] «Химиотерапевтическое средство» относится к химическому соединению, которое можно использовать в лечении злокачественной опухоли. Химиотерапевтические средства включают «противогормональные средства» или «эндокринные лекарственные средства», которые действуют для регуляции, уменьшения, блокирования или подавления эффектов гормонов, которые могут стимулировать рост злокачественных опухолей.
[144] Термин «цитостатическое средство» относится к соединению или композиции, вызывающим арест роста клеток in vitro или in vivo. В некоторых вариантах осуществления, цитостатическое средство представляет собой средство, уменьшающее процент клеток в S-фазе. В некоторых вариантах осуществления, цитостатическое средство уменьшает процент клеток в S-фазе по меньшей мере приблизительно на 20%, по меньшей мере приблизительно на 40%, по меньшей мере приблизительно на 60%, или по меньшей мере приблизительно на 80%.
[145] Термин «опухоль» относится к любым росту и пролиферации неопластических клеток, либо злокачественным, либо доброкачественным, и ко всем предзлокачественным и злокачественным клеткам и тканям. Термины «злокачественная опухоль», «злокачественный», «нарушение пролиферации клеток», «нарушение пролиферации» и «опухоль» не являются взаимоисключающими, как обозначено в настоящем описании. Термины «нарушение пролиферации клеток» и «нарушение пролиферации» относятся к нарушениям, ассоциированным с некоторой степенью аномальной пролиферации клеток. В некоторых вариантах осуществления, нарушение пролиферации клеток представляет собой злокачественную опухоль.
[146] Термин «фармацевтическая композиция» относится к препарату, который находится в такой форме, чтобы обеспечивать эффективность биологической активности содержащегося в нем активного ингредиента в лечении субъекта, и который не содержит дополнительных компонентов, неприемлемо токсичных для субъекта.
[147] Термины «модулировать» и «модуляция» относятся к уменьшению или ингибированию или, альтернативно, к активации или увеличению, указанной переменной.
[148] Термины «увеличивать» и «активировать» относятся к увеличению на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 75%, 80%, 85%, 90%, 95%, 100%, в 2 раза, 3 раза, 4 раза, 5 раз, 10 раз, 20 раз, 50 раз, 100 раз или более, указанной переменной, такой как активность передачи сигналов GITR.
[149] Термины «уменьшать» и «ингибировать» относятся к уменьшению на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 75%, 80%, 85%, 90%, 95%, в 2 раза, 3 раза, 4 раза, 5 раз, 10 раз, 20 раз, 50 раз, 100 раз или более, указанной переменной, такой как (a) количество регуляторных T-клеток и/или (b) симптомы заболевания или состояния, такие как наличие или размер метастазов или размер первичной опухоли.
[150] Термин «выступать в роли агониста» относится к активации передачи сигналов рецептора для индукции биологического ответа, ассоциированного с активацией рецептора. «Агонист» представляет собой молекулу, такую как ABP, в рамках изобретения, которая связывает рецептор и выступает в роли его агониста.
[151] Термин «выступать в роли антагониста» относится к ингибированию передачи сигналов рецептора для ингибирования биологического ответа, ассоциированного с активацией рецептора. «Антагонист» представляет собой молекулу, такую как ABP, которая связывает рецептор и выступает в роли его антагониста.
[152] Термин «мультимеризоваться» относится к акту формирования «мультимеров» молекулы посредством сборки молекулы для формирования надмолекулярной структуры, удерживаемой вместе посредством нековалентных или ковалентных взаимодействий. Мультимеры включают «гомомультимеры», представляющие собой ансамбли, сформированные из множества единиц одной и той же молекулы, или «гетеромультимеры», представляющие собой ансамбли, содержащие по меньшей мере одну единицу первой молекулы и по меньшей мере одну единицу второй молекулы. При использовании в настоящем описании применительно к GITR, термин мультимеризоваться относится к ансамблю молекул GITR, экспрессированных на поверхности клетки, индуцированной, например, посредством связывания ABP, в рамках изобретения, или посредством GITRL. Такая мультимеризация ассоциирована с активацией передачи сигналов GITR. См. Nocentini et al., Br. J. Pharmacol., 2012, 165:2089-2099, полное содержание которого приведено в качестве ссылки.
[153] Термин «эффекторная T-клетка» включает T-клетки-помощники (т.е., CD4+) и цитотоксические (т.е., CD8+) T-клетки. CD4+ эффекторные T-клетки вносят вклад в развитие нескольких иммунологических процессов, включая созревание B-клеток в плазматические клетки и B-клетки памяти, и активацию цитотоксических T-клеток и макрофагов. CD8+ эффекторные T-клетки разрушают инфицированные вирусом клетки и клетки опухолей. См. в Seder and Ahmed, Nature Immunol., 2003, 4:835-842, полное содержание которого приведено в качестве ссылки, дополнительную информацию об эффекторных T-клетках.
[154] Термин «регуляторные T-клетки» включает клетки, регулирующие иммунологическую устойчивость, например, посредством супрессии эффекторных T-клеток. В некоторых аспектах, регуляторная T-клетка имеет фенотип CD4+CD25+Foxp3+. В некоторых аспектах, регуляторная T-клетка имеет фенотип CD8+CD25+. См. в Nocentini et al., Br. J. Pharmacol., 2012, 165:2089-2099, полное содержание которого приведено в качестве ссылки, дополнительную информацию о регуляторных T-клетках, экспрессирующих GITR.
[155] Термин «дендритная клетка» относится к профессиональной антигенпредставляющей клетке, способной активировать наивную T-клетку и стимулировать рост и дифференцировку B-клетки.
Антигенсвязывающие белки против GITR
1.1. Связывание GITR и клетки-мишени
[156] Настоящее изобретение относится к ABP, специфически связывающим GITR. В некоторых аспектах, GITR представляет собой hGITR (SEQ ID NO: 1). В некоторых аспектах, GITR представляет собой hGITR-T43R (SEQ ID NO: 2). В некоторых аспектах, GITR представляет собой cGITR (SEQ ID NO: 3). В некоторых вариантах осуществления, GITR представляет собой mGITR (SEQ ID NO: 4).
[157] В некоторых вариантах осуществления, ABP, в рамках изобретения, специфически связывают hGITR (SEQ ID NO: 1), hGITR-T43R (SEQ ID NO: 2), cGITR (SEQ ID NO: 3) и mGITR (SEQ ID NO: 4). В некоторых вариантах осуществления, ABP, в рамках изобретения, специфически связывают hGITR (SEQ ID NO: 1), hGITR-T43R (SEQ ID NO: 2) и cGITR (SEQ ID NO: 3). В некоторых вариантах осуществления, ABP, в рамках изобретения, специфически связывают hGITR (SEQ ID NO: 1) и hGITR-T43R (SEQ ID NO: 2). В некоторых вариантах осуществления, ABP, в рамках изобретения, не связывают mGITR (SEQ ID NO: 4).
[158] В некоторых вариантах осуществления, ABP, в рамках изобретения, специфически связывают внеклеточный домен GITR.
[159] GITR может быть экспрессирован на поверхности любой подходящей клетки-мишени. В некоторых вариантах осуществления, клетка-мишень представляет собой эффекторную T-клетку. В некоторых вариантах осуществления, клетка-мишень представляет собой регуляторную T-клетку. В некоторых вариантах осуществления, клетка-мишень представляет собой клетку естественного киллера (NK). В некоторых вариантах осуществления, клетка-мишень представляет собой T-клетку естественного киллера (NKT). В некоторых вариантах осуществления, клетка-мишень представляет собой дендритную клетку. В некоторых аспектах, дендритная клетка представляет собой плазмацитоидную дендритную клетку. В некоторых вариантах осуществления, клетка-мишень представляет собой B-клетку. В некоторых аспектах, B-клетка представляет собой плазматическую клетку. См. Nocentini et al., Br. J. Pharmacol., 2012, 165:2089-2099, полное содержание которого приведено в качестве ссылки.
[160] В некоторых вариантах осуществления, ABP, в рамках изобретения, специфически связывают мономер GITR.
[161] В некоторых вариантах осуществления, ABP, в рамках изобретения, специфически связывают мультимер GITR. В некоторых аспектах, мультимер содержит две молекулы GITR. В некоторых аспектах, мультимер содержит три молекулы GITR. В некоторых аспектах, мультимер содержит четыре молекулы GITR. В некоторых аспектах, мультимер содержит пять молекул GITR. В некоторых аспектах, мультимер содержит шесть молекул GITR. В некоторых аспектах, мультимер содержит более шести молекул GITR.
[162] В некоторых вариантах осуществления, ABP, в рамках изобретения, содержит, состоит из или в основном состоит из молекулы иммуноглобулина. В некоторых аспектах, молекула иммуноглобулина содержит, состоит из или в основном состоит из антитела.
[163] В некоторых вариантах осуществления, ABP, в рамках изобретения, содержит легкую цепь. В некоторых аспектах, легкая цепь представляет собой легкую цепь каппа. В некоторых аспектах, the легкая цепь представляет собой легкую цепь лямбда.
[164] В некоторых вариантах осуществления, ABP, в рамках изобретения, содержит тяжелую цепь. В некоторых аспектах, тяжелая цепь представляет собой IgA. В некоторых аспектах, тяжелая цепь представляет собой IgD. В некоторых аспектах, тяжелая цепь представляет собой IgE. В некоторых аспектах, тяжелая цепь представляет собой IgG. В некоторых аспектах, тяжелая цепь представляет собой IgM. В некоторых аспектах, тяжелая цепь представляет собой IgG1. В некоторых аспектах, тяжелая цепь представляет собой IgG2. В некоторых аспектах, тяжелая цепь представляет собой IgG3. В некоторых аспектах, тяжелая цепь представляет собой IgG4. В некоторых аспектах, тяжелая цепь представляет собой IgA1. В некоторых аспектах, тяжелая цепь представляет собой IgA2.
[165] В некоторых вариантах осуществления, ABP, в рамках изобретения, содержит, состоит из или в основном состоит из фрагмента антитела. В некоторых аспектах, фрагмент антитела представляет собой an фрагмент Fv. В некоторых аспектах, фрагмент антитела представляет собой фрагмент Fab. В некоторых аспектах, фрагмент антитела представляет собой фрагмент F(ab')2. В некоторых аспектах, фрагмент антитела представляет собой фрагмент Fab'. В некоторых аспектах, фрагмент антитела представляет собой фрагмент scFv (sFv). В некоторых аспектах, фрагмент антитела представляет собой scFv-Fc. В некоторых аспектах, фрагмент антитела представляет собой фрагмент однодоменного антитела.
[166] В некоторых вариантах осуществления, ABP, в рамках изобретения, представляют собой моноклональные антитела. В некоторых вариантах осуществления, ABP, в рамках изобретения, представляют собой поликлональные антитела.
[167] В некоторых вариантах осуществления, ABP, в рамках изобретения, содержат, состоят из или в основном состоят из химерных антител. В некоторых вариантах осуществления, ABP, в рамках изобретения, содержат, состоят из или в основном состоят из гуманизированных антител. В некоторых вариантах осуществления, ABP, в рамках изобретения, содержат, состоят из или в основном состоят из человеческих антител.
[168] В некоторых вариантах осуществления, ABP, в рамках изобретения, содержат, состоят из или в основном состоят из подвергнутых аффинному созреванию ABP. В некоторых аспектах, ABP представляют собой подвергнутые аффинному созреванию ABP, происходящие из ABP, в рамках изобретения.
[169] В некоторых вариантах осуществления, ABP, в рамках изобретения, содержат, состоят из или в основном состоят из альтернативного каркаса. Можно использовать любой подходящий альтернативный каркас. В некоторых аспектах, ABP, в рамках изобретения, содержат, состоят из или в основном состоят из альтернативного каркаса, выбранного из аднектина™, iMab, антикалина®, EETI-II/AGRP, домена Куница, пептидного аптамера на основе тиоредоксина, аффитела®, дарпина, аффилина, тетранектина, финомера и авимера.
[170] В некоторых вариантах осуществления, ABP, в рамках изобретения, ингибирует связывание GITR с GITRL. В некоторых аспектах, ABP ингибирует связывание GITR с GITRL по меньшей мере приблизительно на 50%. В некоторых аспектах, ABP ингибирует связывание GITR с GITRL по меньшей мере приблизительно на 75%. В некоторых аспектах, ABP ингибирует связывание GITR с GITRL по меньшей мере приблизительно на 90%. В некоторых аспектах, ABP ингибирует связывание GITR с GITRL по меньшей мере приблизительно на 95%.
1.2. Моноспецифические и мультиспецифические антигенсвязывающие белки против GITR
[171] В некоторых вариантах осуществления, ABP, в рамках изобретения, представляют собой моноспецифические ABP. В некоторых аспектах, моноспецифические ABP связывают один и тот же эпитоп на двух или более различных молекулах GITR. В некоторых аспектах, моноспецифические ABP связывают один и тот же эпитоп на двух молекулах GITR. В некоторых аспектах, моноспецифические ABP связывают один и тот же эпитоп на трех молекулах GITR. В некоторых аспектах, моноспецифические ABP связывают один и тот же эпитоп на четырех молекулах GITR. В некоторых аспектах, моноспецифические ABP связывают один и тот же эпитоп на пяти молекулах GITR. В некоторых аспектах, моноспецифические ABP связывают один и тот же эпитоп на шести молекулах GITR. В некоторых аспектах, моноспецифические ABP связывают один и тот же эпитоп на более, чем шести молекулах GITR.
[172] В некоторых вариантах осуществления, моноспецифические ABP, в рамках изобретения, являются мультивалентными. В рамках изобретения, термин «мультивалентный» относится к антителу, например, более чем с двумя связывающими областями (т.е., содержащими области VH и VL). В некоторых аспектах, моноспецифические ABP являются двухвалентными. В некоторых аспектах, моноспецифические ABP являются трехвалентными. В некоторых аспектах, моноспецифические ABP являются тетравалентными. В некоторых аспектах, моноспецифические ABP являются пентавалентными. В некоторых аспектах, моноспецифические ABP являются гексавалентными. В некоторых аспектах, моноспецифические ABP являются септивалентными. В некоторых аспектах, моноспецифические ABP являются октавалентными.
[173] В некоторых вариантах осуществления, моноспецифические мультивалентные ABP, описанные в настоящем описании, являются тетравалентными.
[174] В некоторых вариантах осуществления, ABP, в рамках изобретения, представляют собой мультиспецифические ABP. В некоторых аспектах, мультиспецифические ABP связывают два или более эпитопов на двух или более различных молекулах GITR. В некоторых аспектах, мультиспецифические ABP связывают два или более эпитопов на двух молекулах GITR. В некоторых аспектах, мультиспецифические ABP связывают два или более эпитопов на трех молекулах GITR. В некоторых аспектах, мультиспецифические ABP связывают два или более эпитопов на четырех молекулах GITR. В некоторых аспектах, мультиспецифические ABP связывают два или более эпитопов на пяти молекулах GITR. В некоторых аспектах, мультиспецифические ABP связывают два или более эпитопов на шести молекулах GITR. В некоторых аспектах, мультиспецифические ABP связывают два или более эпитопов на семи молекулах GITR. В некоторых аспектах, мультиспецифические ABP связывают два или более эпитопов на восьми молекулах GITR. В некоторых аспектах, мультиспецифические ABP связывают два или более эпитопов на девяти молекулах GITR. В некоторых аспектах, мультиспецифические ABP связывают два или более эпитопов на десяти молекулах GITR. В некоторых аспектах, мультиспецифические ABP связывают два или более эпитопов на одиннадцати молекулах GITR. В некоторых аспектах, мультиспецифические ABP связывают два или более эпитопов на двенадцати молекулах GITR. В некоторых аспектах, мультиспецифические ABP связывают два или более эпитопов на более, чем двенадцати молекулах GITR.
[175] Мультиспецифические ABP, в рамках изобретения, могут связывать любое подходящее количество эпитопов на GITR. В некоторых аспектах, мультиспецифические ABP связывают два эпитопа на GITR. В некоторых аспектах, мультиспецифические ABP связывают три эпитопа на GITR. В некоторых аспектах, мультиспецифические ABP связывают четыре эпитопа на GITR. В некоторых аспектах, мультиспецифические ABP связывают пять эпитопов на GITR. В некоторых аспектах, мультиспецифические ABP связывают шесть эпитопов на GITR. В некоторых аспектах, мультиспецифические ABP связывают семь эпитопов на GITR. В некоторых аспектах, мультиспецифические ABP связывают восемь эпитопов на GITR. В некоторых аспектах, мультиспецифические ABP связывают девять эпитопов на GITR. В некоторых аспектах, мультиспецифические ABP связывают десять эпитопов на GITR. В некоторых аспектах, мультиспецифические ABP связывают одиннадцать эпитопов на GITR. В некоторых аспектах, мультиспецифические ABP связывают двенадцать эпитопов на GITR. В некоторых аспектах, мультиспецифические ABP связывают более двенадцати эпитопов на GITR.
[176] В некоторых аспектах, мультиспецифический ABP, в рамках изобретения, связывает по меньшей мере два различных эпитопа на по меньшей мере двух различных молекулах GITR. В некоторых аспектах, мультиспецифический ABP, в рамках изобретения, связывает по меньшей мере три различных эпитопа на по меньшей мере трех различных молекулах GITR. В некоторых аспектах, мультиспецифический ABP, в рамках изобретения, связывает по меньшей мере четыре различных эпитопа на по меньшей мере четырех различных молекулах GITR. В некоторых аспектах, мультиспецифический ABP, в рамках изобретения, связывает по меньшей мере пять различных эпитопов на по меньшей мере пяти различных молекулах GITR.
[177] В некоторых вариантах осуществления, мультиспецифический ABP, в рамках изобретения, содержит первый антигенсвязывающий домен, который специфически связывает первый эпитоп на GITR и второй антигенсвязывающий домен, который специфически связывает второй эпитоп на GITR, где первый эпитоп и второй эпитоп являются различными. В некоторых аспектах, мультиспецифический ABP дополнительно содержит один или несколько дополнительных антигенсвязывающих доменов, которые специфически связывают один или несколько дополнительных эпитопов на GITR, где каждый из дополнительных эпитопов является отличным от эпитопов, связываемых первым антигенсвязывающим доменом, вторым антигенсвязывающим доменом или любыми другими следующими антигенсвязывающими доменами ABP.
[178] В некоторых вариантах осуществления, мультиспецифический ABP, в рамках изобретения, связывает эпитоп на молекуле GITR и эпитоп на другой молекуле, не представляющей собой GITR. Любую подходящую не относящуюся к GITR молекулу можно связывать посредством ABP, в рамках изобретения. В некоторых аспектах, не относящаяся к GITR молекула представляет собой другой член суперсемейства рецепторов фактора некроза опухоли (TNFRSF). В некоторых аспектах, другой член TNFRSF выбран из CD27, CD40, EDA2R, EDAR, FAS, LTBR, NGFR, RELT, TNFRSF1A, TNFRSF1B, TNFRSF4, TNFRSF6B, TNFRSF8, TNFRSF9, TNFRSF10A, TNFRSF10B, TNFRSF10C, TNFRSF10D, TFNRSF11A, TNFRSF11B, TNFRSF12A, TNFRSF13B, TNFRSF13C, TNFRSF14, TNFRSF17, TNFRSF18, TNFRSF19, TNFRSF21 и TNFRSF25.
[179] Множество конструкций мультиспецифического ABP известно в данной области, и ABP, в рамках изобретения, можно предоставлять в форме любой подходящей мультиспецифической конструкции.
[180] В некоторых вариантах осуществления, мультиспецифический ABP содержит иммуноглобулин, содержащий по меньшей мере две различные вариабельные области тяжелой цепи, где каждая спарена с вариабельной областью общей легкой цепи (т.е., «антитело с общей легкой цепью»). Вариабельная область общей легкой цепи формирует отдельный антигенсвязывающий домен с каждой из двух различных вариабельных областей тяжелых цепей. См. Merchant et al., Nature Biotechnol., 1998, 16:677-681, полное содержание которого приведено в качестве ссылки.
[181] В некоторых вариантах осуществления, мультивалентные ABP, описанные в настоящем описании, содержат иммуноглобулин, содержащий антитело или его фрагмент, присоединенные к одному или нескольким из N- или C-концов тяжелых или легких цепей такого иммуноглобулина. См., например, Патент США No. 8722859 и Coloma and Morrison, Nature Biotechnol., 1997, 15:159-163, полное содержание каждого из которых приведено в качестве ссылки. В некоторых аспектах, такой ABP содержит тетравалентное биспецифическое антитело. В некоторых аспектах, такой ABP содержит тетравалентное моноспецифическое (TM) антитело.
[182] В некоторых вариантах осуществления, мультивалентный ABP содержит гибридный иммуноглобулин, содержащий по меньшей мере две различные вариабельные области тяжелой цепи и по меньшей мере две различные вариабельные области легкой цепи. См. Milstein and Cuello, Nature, 1983, 305:537-540; и Staerz and Bevan, Proc. Natl. Acad. Sci. USA, 1986, 83:1453-1457; полное содержание всех из которых приведено в настоящем описании в качестве ссылки.
[183] В некоторых вариантах осуществления, мультивалентный ABP содержит цепи иммуноглобулинов с изменениями для уменьшения образования побочных продуктов, которые не имеют мультиспецифичности. В некоторых аспектах, ABP содержат одну или несколько модификаций «выступы-во-впадины», как описано в Патенте США No. 5731168, полное содержание которого приведено в качестве ссылки.
[184] В некоторых вариантах осуществления, мультивалентный ABP содержит цепи иммуноглобулинов с одной или несколькими электростатическими модификациями для стимуляции сборки гетеромультимеров Fc. См. WO 2009/089004, полное содержание которого приведено в качестве ссылки.
[185] В некоторых вариантах осуществления, мультивалентный ABP содержит биспецифическую одноцепочечную молекулу. См. Traunecker et al., EMBO J., 1991, 10:3655-3659; и Gruber et al., J. Immunol., 1994, 152:5368-5374; полное содержание всех из которых приведено в настоящем описании в качестве ссылки.
[186] В некоторых вариантах осуществления, мультивалентный ABP содержит вариабельный домен тяжелой цепи и вариабельный домен легкой цепи, или домен VHH однодоменного антитела, соединенные полипептидным линкером, где длина линкера выбрана для стимуляции сборки мультивалентного ABP с желательной мультиспецифичностью. Например, моноспецифические scFv, как правило, образуются, когда остатки V тяжелой цепи предотвращают спаривание вариабельных доменов тяжелой и легкой цепи на одной той же полипептидной цепи, таким образом, позволяя спаривание вариабельных доменов тяжелой и легкой цепи из одной цепи с комплементарными доменами на другой цепи. Полученные ABP, таким образом, имеют мультиспецифичность, со специфичностью каждого участка связывания, в которую вносят вклад более одной полипептидной цепи. Полипептидные цепи, содержащие вариабельные домены тяжелых и легких цепей, соединенные линкерами из между 3 и 12 аминокислотных остатков преимущественно формируют димеры (называемые диателами). С линкерами из между 0 и 2 аминокислотных остатков, преимущественно формируются тримеры (называемые триотелами) и тетрамеры (называемые тетрателами). Однако, точный тип олигомеризации, по-видимому, зависит от состава аминокислотных остатков и порядка вариабельных доменов в каждой полипептидной цепи (например, VH-линкер-VL по сравнению с VL-линкер-VH), в дополнение к длине линкера. Специалист в данной области может выбирать подходящую длину линкера на основании желательной мультиспецифичности.
[187] В некоторых вариантах осуществления, моноспецифический или мультиспецифический ABP содержит диатело. См. Hollinger et al., Proc. Natl. Acad. Sci. USA, 1993, 90:6444-6448, полное содержание которого приведено в качестве ссылки. В некоторых вариантах осуществления, моноспецифический или мультиспецифический ABP содержит триотело. См. Todorovska et al., J. Immunol. Methods, 2001, 248:47-66, полное содержание которого приведено в качестве ссылки. В некоторых вариантах осуществления, моноспецифический или мультиспецифический ABP содержит тетратело. См. в том же документе, полное содержание которого приведено в качестве ссылки.
[188] В некоторых вариантах осуществления, мультиспецифический ABP содержит триспецифическое производное F(ab')3. См. Tutt et al. J. Immunol., 1991, 147:60-69, полное содержание которого приведено в качестве ссылки.
[189] В некоторых вариантах осуществления, моноспецифический или мультиспецифический ABP содержит перекрестно сшитое антитело. См. Патент США No. 4676980; Brennan et al., Science, 1985, 229:81-83; Staerz, et al. Nature, 1985, 314:628-631; и EP 0453082; полное содержание всех из которых приведено в настоящем описании в качестве ссылки.
[190] В некоторых вариантах осуществления, моноспецифический или мультиспецифический ABP содержит антигенсвязывающие домены, собранные посредством лейциновых молний. См. Kostelny et al., J. Immunol., 1992, 148:1547-1553, полное содержание которого приведено в качестве ссылки.
[191] В некоторых вариантах осуществления, моноспецифический или мультиспецифический ABP содержит комплементарные белковые домены. В некоторых аспектах, комплементарные белковые домены содержат заякоривающий домен (AD) и димеризующий и причаливающий домены (DDD). В некоторых вариантах осуществления, AD и DDD связываются друг с другом и таким образом, позволяют сборку структур мультиспецифического ABP способом «замок на причале» (DNL). Можно собирать ABP со множеством специфичностей, включая биспецифические ABP, триспецифические ABP, тетраспецифические ABP, пентаспецифические ABP и гексаспецифические ABP. Мультиспецифические ABP, содержащие комплементарные белковые домены, описаны, например, в Патентах США No. 7521056; 7550143; 7534866; и 7527787; полное содержание всех из которых приведено в настоящем описании в качестве ссылки.
[192] В некоторых вариантах осуществления, моноспецифический или мультиспецифический ABP содержит гибрид молекулы антитела и не относящейся к антителу молекулы со специфичностью для GITR или другой мишени. См. в WO 93/08829, полное содержание которого приведено в качестве ссылки, примеры таких ABP. В некоторых аспектах не относящаяся к антителу молекула представляет собой GITRL.
[193] В некоторых вариантах осуществления, моноспецифический или мультиспецифический ABP содержит антитело с Fab двойного действия (DAF), как описано в Патентной публикации США No. 2008/0069820, полное содержание которой приведено в качестве ссылки.
[194] В некоторых вариантах осуществления, мультиспецифический ABP содержит антитело, сформированное посредством восстановления двух исходных молекул с последующим смешиванием этих двух исходных молекул и повторным окислением для сборки гибридной структуры. См. Carlring et al., PLoS One, 2011, 6:e22533, полное содержание которого приведено в качестве ссылки.
[195] В некоторых вариантах осуществления, моноспецифический или мультиспецифический ABP содержит a DVD-Ig™. DVD-Ig™ представляет собой иммуноглобулин с двойным вариабельным доменом, который может связывать два или более антигенов. DVD-Ig™ описаны в Патенте США No. 7612181, полное содержание которого приведено в качестве ссылки.
[196] В некоторых вариантах осуществления, моноспецифический или мультиспецифический ABP содержит DART™. DART™ описаны в Moore et al., Blood, 2011, 117:454-451, полное содержание которого приведено в качестве ссылки.
[197] В некоторых вариантах осуществления, мультиспецифический ABP содержит DuoBody®. DuoBodies® описаны в Labrijn et al., Proc. Natl. Acad. Sci. USA, 2013, 110:5145-5150; Gramer et al., mAbs, 2013, 5:962-972; и Labrijn et al., Nature Protocols, 2014, 9:2450-2463; полное содержание всех из которых приведено в настоящем описании в качестве ссылки.
[198] В некоторых вариантах осуществления, моноспецифический или мультиспецифический ABP, описанный в настоящем описании, содержит фрагмент антитела, присоединенный к другому антителу или фрагменту. Присоединение может являться ковалентным или нековалентным. Когда присоединение является ковалентным, оно может присутствовать в форме слитого белка или происходить посредством химического линкера. Иллюстративные примеры мультиспецифических ABP, содержащих фрагменты антител, присоединенные к другим антителам, включают тетравалентные биспецифические антитела, где scFv является слитым с C-концом CH3 из IgG. См. Coloma and Morrison, Nature Biotechnol., 1997, 15:159-163. Другие примеры включают антитела, в которых молекула Fab присоединена к константной области иммуноглобулина. См. Miler et al., J. Immunol., 2003, 170:4854-4861, полное содержание которого приведено в качестве ссылки. Можно использовать любой подходящий фрагмент, включая любой из фрагментов, описанных в настоящем описании или известных в данной области.
[199] В некоторых вариантах осуществления, моноспецифический или мультиспецифический ABP содержит CovX-Body. CovX-Bodies описаны, например, в Doppalapudi et al., Proc. Natl. Acad. Sci. USA, 2010, 107:22611-22616, полное содержание которого приведено в качестве ссылки.
[200] В некоторых вариантах осуществления, моноспецифический или мультиспецифический ABP содержит антитело Fcab, где один или несколько антигенсвязывающих доменов введены в область Fc. Антитела Fcab описаны в Wozniak-Knopp et al., Белок Eng. Des. Sel., 2010, 23:289-297, полное содержание которого приведено в качестве ссылки.
[201] В некоторых вариантах осуществления, моноспецифический или мультиспецифический ABP содержит антитело TandAb®. Антитела TandAb® описаны в Kipriyanov et al., J. Mol. Biol., 1999, 293:41-56 и Zhukovsky et al., Blood, 2013, 122:5116, полное содержание всех из которых приведено в настоящем описании в качестве ссылки.
[202] В некоторых вариантах осуществления, мультиспецифический ABP содержит тандемный Fab. Тандемные Fab описаны в WO 2015/103072, полное содержание которого приведено в качестве ссылки.
[203] В некоторых вариантах осуществления, мультиспецифический ABP содержит Zybody™. Zybodies™ описаны в LaFleur et al., mAbs, 2013, 5:208-218, полное содержание которого приведено в качестве ссылки.
1.3. Антигенсвязывающие белки, вызывающие мультимеризацию GITR
[204] В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию GITR, экспрессированного на поверхности клетки-мишени. ABP, в рамках изобретения, можно разрабатывать, на основании их валентности и специфичности, чтобы вызывать мультимеризацию любого подходящего количества молекул GITR.
[205] В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию двух молекул GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию трех молекул GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию четырех молеку GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию пяти молекул GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию шести молекул GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию семи молекул GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию восьми молекул GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию девяти молекул GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию десяти молекул GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию одиннадцати молекул GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию двенадцати молекулы GITR.
[206] В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию по меньшей мере двух молекул GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию по меньшей мере трех молекул GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию по меньшей мере четырех молекул GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию по меньшей мере пяти молекул GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию по меньшей мере шести молекул GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию по меньшей мере семи молекул GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию по меньшей мере восьми молекул GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию по меньшей мере девяти молекул GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию по меньшей мере десяти молекул GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию по меньшей мере одиннадцати молекул GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию по меньшей мере двенадцати молекул GITR.
[207] В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию от двух до двенадцати молекул GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию от трех до десяти молекул GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию от трех до шести молекул GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию от трех до пяти молекул GITR. В некоторых вариантах осуществления, ABP, в рамках изобретения, вызывают мультимеризацию от трех до четырех молекул GITR.
1.4. Агонизм GITR
[208] В некоторых вариантах осуществления, ABP, в рамках изобретения, выступает в роли агониста GITR при связывании. Такой агонизм может возникать в результате мультимеризации GITR посредством ABP, как описано в другом месте настоящего описания. См. ФИГ. 1.
[209] В некоторых вариантах осуществления, агонизм GITR посредством ABP, в рамках изобретения, приводит к модуляции активности NF-κB в клетке-мишени. См. Патент США No. 7812135, полное содержание которого приведено в настоящем описании в качестве ссылки. В некоторых аспектах, агонизм GITR приводит к модуляции активности или стабильности IκB в клетке-мишени.
[210] В некоторых вариантах осуществления, агонизм GITR посредством ABP, в рамках изобретения, приводит к активации пути MAPK в клетке-мишени. В некоторых аспектах, компоненты пути MAPK, активируемые посредством ABP, в рамках изобретения, включают один или несколько из p38, JNK, и ERK. См. Nocentini et al., Proc. Natl. Acad. Sci. USA, 1997, 94:6216-6221; Ronchetti et al., Eur. J. Immunol., 2004, 34:613-622; и Esparza et al., J. Immunol., 2005, 174:7869-7874; полное содержание всех из которых приведено в настоящем описании в качестве ссылки.
[211] В некоторых вариантах осуществления, агонизм GITR посредством ABP, в рамках изобретения, приводит к увеличенной продукции IL-2Rα, IL-2, IL-8 и/или IFNγ в клетке-мишени. См. Ronchetti et al., Eur. J. Immunol., 2004, 34:613-622, полное содержание которого приведено в качестве ссылки.
[212] В некоторых вариантах осуществления, агонизм GITR посредством ABP, в рамках изобретения, усиливает пролиферацию, выживаемость и/или функцию эффекторной T-клетки. В некоторых аспектах эффекторная T-клетка представляет собой CD4+ эффекторную T-клетку. В некоторых аспектах, эффекторная T-клетка представляет собой CD8+ эффекторную T-клетку.
[213] В некоторых вариантах осуществления, агонизм GITR посредством ABP, в рамках изобретения, прекращает супрессию эффекторной T-клетки посредством регуляторной T-клетки. В некоторых аспектах, регуляторная T-клетка представляет собой CD4+CD25+Foxp3+ регуляторную T-клетку. В некоторых аспектах, регуляторная T-клетка представляет собой CD8+CD25+ регуляторную T-клетку.
[214] В некоторых вариантах осуществления, агонизм GITR посредством ABP, в рамках изобретения, изменяет встречаемость или распределение регуляторных T-клеток. В некоторых аспектах, частота регуляторных T-клеток уменьшена. В некоторых аспектах, частота регуляторных T-клеток уменьшена в конкретной ткани. В некоторых аспектах, накопление регуляторных T-клеток внутри опухоли уменьшено, что приводит к более благоприятному соотношению эффекторных T-клеток к регуляторным T-клеткам, и к усилению активности CD8+ T-клеток. См. Cohen et al., PLoS One, 2010, 5:e10436.
[215] В некоторых вариантах осуществления, агонизм GITR посредством ABP, в рамках изобретения, увеличивает активность клетки естественного киллера (NK). В некоторых вариантах осуществления, агонизм GITR посредством ABP, в рамках изобретения, увеличивает активность антигенпредставляющей клетки. В некоторых вариантах осуществления, агонизм GITR посредством ABP, в рамках изобретения, увеличивает активность дендритной клетки. В некоторых вариантах осуществления, агонизм GITR посредством ABP, в рамках изобретения, увеличивает активность B-клетки.
[216] В некоторых вариантах осуществления, агонизм GITR посредством ABP, в рамках изобретения, приводит к усилению иммунного ответа. В некоторых вариантах осуществления, агонизм GITR посредством ABP, в рамках изобретения, приводит к задержке начала развития опухоли. В некоторых вариантах осуществления, агонизм GITR посредством ABP, в рамках изобретения, приводит к уменьшению размера опухоли. В некоторых вариантах осуществления, агонизм GITR посредством ABP, в рамках изобретения, приводит к уменьшению количества метастазов.
[217] В некоторых вариантах осуществления, агонизм GITR посредством мультивалентного моноспецифического ABP, в рамках изобретения, приводит к большему максимальному уровню агонизма, чем для двухвалентного моноспецифического антитела. В некоторых вариантах осуществления, дополнительная валентность приводит к эффекту на EC50, превышающему аддитивные эффекты каждого из связывающих доменов. В некоторых вариантах осуществления, тетравалентный моноспецифический ABP, в рамках изобретения, имеет больший максимальный уровень агонизма, чем двухвалентное моноспецифическое антитело.
[218] В некоторых вариантах осуществления, мультиспецифические ABP, в рамках изобретения, являются более сильными агонистами GITR, чем смеси соответствующих моноспецифических ABP. Например, если мультиспецифический ABP, в рамках изобретения, содержит две различные эпитопные специфичности (например, A и B), тогда, в некоторых вариантах осуществления, агонизм GITR посредством такого мультиспецифического ABP превышает агонизм GITR посредством смеси двух моноспецифических ABP, каждый из которых содержит одну из двух специфичностей (например, A или B). В некоторых вариантах осуществления, дополнительные специфичности мультиспецифического ABP, в рамках изобретения, приводят к синергическому (т.е., большему, чем аддитивное) увеличению активности по сравнению со смесями моноспецифических ABP, каждый из которых имеет только одну из специфичностей мультиспецифического ABP.
1.5. Аффинность антигенсвязывающих белков для GITR
[219] В некоторых вариантах осуществления, аффинность ABP, в рамках изобретения, для GITR, как показано по KD, составляет менее, чем приблизительно 10-5 M, менее, чем приблизительно 10-6 M, менее, чем приблизительно 10-7 M, менее, чем приблизительно 10-8 M, менее, чем приблизительно 10-9 M, менее, чем приблизительно 10-10 M, менее, чем приблизительно 10-11 M, или менее, чем приблизительно 10-12 M. В некоторых вариантах осуществления, аффинность ABP составляет между приблизительно 10-7 M и 10-12 M. В некоторых вариантах осуществления, аффинность ABP составляет между приблизительно 10-7 M и 10-11 M. В некоторых вариантах осуществления, аффинность ABP составляет между приблизительно 10-7 M и 10-10 M. В некоторых вариантах осуществления, аффинность ABP составляет между приблизительно 10-7 M и 10-9 M. В некоторых вариантах осуществления, аффинность ABP составляет между приблизительно 10-7 M и 10-8 M. В некоторых вариантах осуществления, аффинность ABP составляет между приблизительно 10-8 M и 10-12 M. В некоторых вариантах осуществления, аффинность ABP составляет между приблизительно 10-8 M и 10-11 M. В некоторых вариантах осуществления, аффинность ABP составляет между приблизительно 10-9 M и 10-11 M. В некоторых вариантах осуществления, аффинность ABP составляет между приблизительно 10-10 M и 10-11 M.
[220] В некоторых вариантах осуществления, ABP, в рамках изобретения, специфически связывают hGITR (SEQ ID NO: 1) с KD X и cGITR с KD ≤10X. В некоторых вариантах осуществления, ABP, в рамках изобретения, специфически связывают hGITR (SEQ ID NO: 1) с KD X и cGITR с KD ≤5X. В некоторых вариантах осуществления, ABP, в рамках изобретения, специфически связывают hGITR (SEQ ID NO: 1) с KD X и cGITR с KD ≤2X. В некоторых аспектах, X представляет собой любую KD, описанную в этом описании. В некоторых аспектах, X представляет собой 0,01 нМ, 0,1 нМ, 1 нМ, 10 нМ, 20 нМ, 50 нМ или 100 нМ.
[221] В некоторых вариантах осуществления, KD, ka и kd определяют с использованием поверхностного плазмонного резонанса (SPR). В некоторых аспектах, в анализе SPR используют устройство BIACORE®. В некоторых аспектах, антиген иммобилизуют на биосенорном чипе из карбоксиметилированного декстрана (CM4 или CM5) и приводят в контакт с ABP, в рамках изобретения. Константы скорости связывания и диссоциации можно рассчитывать с использованием программного обеспечения BIAevaluation® и модели связывания один-к-одному Ленгмюра. В некоторых аспектах, анализ проводят при 25°C. В некоторых аспектах, анализ проводят при 37°C.
[222] В некоторых вариантах осуществления, KD, ka и kd определяют с использованием интерферометрии биослоя (BLI). Можно использовать любой подходящий способ BLI. В некоторых аспектах, в анализе BLI используют устройство FORTEBIO®. В некоторых аспектах, биосенсор для связывания Fc IgG человека (AHC) используют для фиксации ABP на поверхности сенсора. Затем, ассоциацию ABP и антигена мониторируют посредством приведения иммобилизованного ABP в контакт с различными концентрациями GITR. Затем диссоциацию антигена и ABP измеряют в буфере без GITR. Константы скорости связывания и диссоциации рассчитывают с использованием кинетических модулей программного обеспечения для анализа FORTEBIO®. В некоторых аспектах, анализ проводят при 30°C.
[223] В других вариантах осуществления, KD можно определять посредством анализа связывания радиоактивно меченного антигена, как описано в Chen et al. J. Mol. Biol., 1999, 293:865-881, полное содержание которого приведено в качестве ссылки.
1.5.1. Варианты гликозилирования
[224] В конкретных вариантах осуществления, ABP, в рамках изобретения, можно изменять для увеличения, уменьшения или уничтожения степени, в которой он гликозилирован. Гликозилирование полипептидов является, как правило, либо «N-связанным», либо «O-связанным».
[225] «N-связанное» гликозилирование относится к присоединению углеводной группы к боковой цепи остатка аспарагина. Трипептидные последовательности аспарагин-X-серин и аспарагин-X-треонин, где X представляет собой любую аминокислоту, за исключением пролина, представляют собой последовательности узнавания для ферментного присоединения группы углевода к боковой цепи аспарагина. Таким образом, присутствие любой из этих трипептидных последовательностей в полипептиде создает потенциальный участок гликозилирования.
[226] «O-связанное» гликозилирование относится к присоединению одного из сахаров N-ацетилгалактозамина, галактозы или ксилозы к гидроксиаминокислоте, наиболее обычно, серину или треонину, хотя может быть использован также 5-гидроксипролин или 5-гидроксилизин.
[227] Добавление или делецию участков N-связанного гликозилирования к или из ABP, в рамках изобретения, можно осуществлять посредством изменения аминокислотной последовательности таким образом, чтобы создавать или удалять одну или несколько из вышеописанных трипептидных последовательностей. Добавление или делецию участков O- связанного гликозилирования можно осуществлять посредством добавления, делеции или замены одного или нескольких остатков серина или треонина в последовательность или к последовательности (в зависимости от обстоятельств) ABP.
[228] В некоторых вариантах осуществления, ABP, в рамках изобретения, содержит мотив гликозилирования, который отличается от природного ABP. Любой подходящий природный мотив гликозилирования можно модифицировать в ABP, в рамках изобретения. Структурные свойства и свойства гликозилирования иммуноглобулинов, например, известны в данной области и обобщены, например, в Schroeder and Cavacini, J. Allergy Clin. Immunol., 2010, 125:S41-52, полное содержание которого приведено в качестве ссылки.
[229] В некоторых вариантах осуществления, ABP, в рамках изобретения, содержит область Fc IgG1 с модификацией олигосахарида, присоединенного к аспарагину 297 (Asn 297). Природные антитела IgG1, продуцированные клетками млекопитающих, как правило, содержат разветвленный, двухантенный олигосахарид, который, как правило, присоединен посредством N-связи к Asn 297 домена CH2 области Fc. См. Wright et al., TIBTECH, 1997, 15:26-32, полное содержание которого приведено в качестве ссылки. Олигосахарид, присоединенный к Asn 297, может включать различные углеводы, такие как манноза, N-ацетилглюкозамин (GlcNAc), галактоза и сиаловая кислота, так же как фукоза, присоединенная к GlcNAc в «стебле» двухантенной структуры олигосахарида.
[230] В некоторых вариантах осуществления, олигосахарид, присоединенный к Asn 297, модифицируют для получения ABP, имеющий измененную ADCC. В некоторых вариантах осуществления, олигосахарид изменяют для улучшения ADCC. В некоторых вариантах осуществления, олигосахарид изменяют для уменьшения ADCC.
[231] В некоторых аспектах, ABP, в рамках изобретения, содержит домен IgG1 с уменьшенным содержанием фукозы в положении Asn 297 по сравнению с природным доменом IgG1. Известно, что такие домены Fc имеют улучшенную ADCC. См. Shields et al., J. Biol. Chem., 2002, 277:26733-26740, полное содержание которого приведено в качестве ссылки. В некоторых аспектах, такой ABP не содержит фукозы в положении Asn 297. Количество фукозы можно определять с использованием любого подходящего способа, например, как описано в WO 2008/077546, полное содержание которого приведено в качестве ссылки.
[232] В некоторых вариантах осуществления, ABP, в рамках изобретения, содержит разделенный надвое олигосахарид, такой как двухантенный олигосахарид, присоединенный к области Fc ABP, разделенный посредством GlcNAc. Такие варианты ABP могут иметь уменьшенное фукозилирование и/или улучшенную функцию ADCC. Примеры таких вариантов ABP описаны, например, в WO 2003/011878; Патенте США No. 6602684; и Патентной публикации США No. 2005/0123546; полное содержание всех из которых приведено в настоящем описании в качестве ссылки.
[233] Другие иллюстративные варианты гликозилирования описаны, например, в Патентных публикациях США No. 2003/0157108, 2004/0093621, 2003/0157108, 2003/0115614, 2002/0164328, 2004/0093621, 2004/0132140, 2004/0110704, 2004/0110282, 2004/0109865; в Международных патентных публикациях No. 2000/61739, 2001/29246, 2003/085119, 2003/084570, 2005/035586, 2005/035778; 2005/053742, 2002/031140; Okazaki et al., J. Mol. Biol., 2004, 336:1239-1249; и Yamane-Ohnuki et al., Biotech. Bioeng., 2004, 87: 614-622; полное содержание всех из которых приведено в настоящем описании в качестве ссылки.
[234] В некоторых вариантах осуществления, ABP, в рамках изобретения, содержит область Fc по меньшей мере с одним остатком галактозы в олигосахариде, присоединенном к области Fc. Такие варианты ABP могут иметь улучшенную функцию CDC. Примеры таких вариантов ABP описаны, например, в WO 1997/30087; WO 1998/58964; и WO 1999/22764; полное содержание каждого из которых приведено в качестве ссылки.
[235] Примеры линий клеток, способных продуцировать дефукозилированные ABP, включают клетки Lec13 CHO, имеющие недостаточность фукозилирования белка (См. Ripka et al., Arch. Biochem. Biophys., 1986, 249:533-545; Патентную публикацию США No.. 2003/0157108; WO 2004/056312; полное содержание всех из которых приведено в настоящем описании в качестве ссылки), и линии клеток с нокаутом, такие как клетки с нокаутом гена альфа-1,6-фукозилтрансферазы или FUT8 (См. Yamane-Ohnuki et al., Biotech. Bioeng., 2004, 87: 614-622; Kanda et al., Biotechnol. Bioeng., 2006, 94:680-688; и WO 2003/085107; полное содержание всех из которых приведено в настоящем описании в качестве ссылки).
[236] В некоторых вариантах осуществления, ABP, в рамках изобретения, представляет собой агликозилированный ABP. Агликозилированный ABP можно получать с использованием любого способа, известного в данной области или описанного в настоящем описании. В некоторых аспектах, агликозилированный ABP получают посредством модификации ABP для удаления всех участков гликозилирования. В некоторых аспектах, участки гликозилирования удаляют только из области Fc ABP. В некоторых аспектах, агликозилированный ABP получают посредством экспрессии ABP в организме, неспособном к гликозилированию, таком как E. coli, или посредством экспрессии ABP в бесклеточной реакционной смеси.
[237] В некоторых вариантах осуществления, ABP, в рамках изобретения, имеет константную область с уменьшенной эффекторной функцией по сравнению с природным антителом IgG1. В некоторых вариантах осуществления, аффинность константной области из области Fc ABP, в рамках изобретения, для рецептора Fc меньше, чем аффинность константной области природного IgG1 для такого рецептора Fc.
1.6. Варианты аминокислотной последовательности области Fc
[238] В конкретных вариантах осуществления, ABP, в рамках изобретения, содержит область Fc с одной или несколькими аминокислотными заменами, вставками или делециями по сравнению с природной областью Fc. В некоторых аспектах, такие замены, вставки или делеции приводят к получению ABP с измененными стабильностью, гликозилированием или другими характеристиками. В некоторых аспектах, такие замены, вставки или делеции приводят к получению агликозилированного ABP.
[239] В некоторых аспектах, область Fc ABP, в рамках изобретения, модифицируют для получения ABP с измененной аффинностью для рецептора Fc, или ABP, который является более иммунологически инертным. В некоторых вариантах осуществления, варианты ABP, в рамках изобретения, имеют некоторые, но не все, эффекторные функции. Такой ABP можно использовать, например, когда время полужизни ABP является важным in vivo, но когда конкретные эффекторные функции (например, активация комплемента и ADCC) не являются необходимыми или являются вредными.
[240] В некоторых вариантах осуществления, область Fc ABP, в рамках изобретения, представляет собой область Fc IgG4 человека, содержащую стабилизирующую шарнирную область мутацию S228P или L235E. В некоторых вариантах осуществления, область Fc IgG4 содержит стабилизирующие шарнирную область мутации S228P и L235E. См. Aalberse et al., Immunology, 2002, 105:9-19, полное содержание которого приведено в качестве ссылки. В некоторых вариантах осуществления, область Fc IgG4 содержит одну или несколько из следующих мутаций: E233P, F234V, и L235A. См. Armour et al., Mol. Immunol., 2003, 40:585-593, полное содержание которого приведено в качестве ссылки. В некоторых вариантах осуществления, область Fc IgG4 содержит делецию в положении G236.
[241] В некоторых вариантах осуществления, область Fc из ABP, в рамках изобретения, представляет собой область Fc IgG1 человека, содержащую одну или несколько мутаций для уменьшения связывания рецептора Fc. В некоторых аспектах, одна или несколько мутаций присутствуют в остатках, выбранных из S228 (например, S228A), L234 (например, L234A), L235 (например, L235A), D265 (например, D265A), и N297 (например, N297A). В некоторых аспектах, ABP содержит мутацию PVA236. PVA236 означает, что аминокислотная последовательность ELLG, из положений аминокислот 233-236 из IgG1 или EFLG из IgG4, заменена на PVA. См. Патентную публикацию США No. 2013/0065277, полное содержание которого приведено в качестве ссылки.
[242] В некоторых вариантах осуществления, область Fc из ABP, в рамках изобретения, модифицируют, как описано в Armour et al., Eur. J. Immunol., 1999, 29:2613-2624; WO 1999/058572; и/или U.K. Pat. App. No. 98099518; полное содержание всех из которых приведено в настоящем описании в качестве ссылки.
[243] В некоторых вариантах осуществления, область Fc ABP, в рамках изобретения, представляет собой область Fc IgG2 человека, содержащую одну или несколько из мутаций A330S и P331S.
[244] В некоторых вариантах осуществления, область Fc из ABP, в рамках изобретения, имеет аминокислотную замену в одном или нескольких положениях, выбранных из 238, 265, 269, 270, 297, 327 и 329. См. Патент США No. 6737056, полное содержание которого приведено в качестве ссылки. Такие мутанты Fc включают мутанты Fc с заменами в двух или более из положений аминокислот 265, 269, 270, 297 и 327, включая так называемый мутант Fc «DANA» с заменой остатков 265 и 297 на аланин. См. Патент США No. 7332581, полное содержание которого приведено в качестве ссылки. В некоторых вариантах осуществления, ABP содержит аланин в положении аминокислоты 265. В некоторых вариантах осуществления, ABP содержит аланин в положении аминокислоты 297.
[245] В конкретных вариантах осуществления, ABP, в рамках изобретения, содержит область Fc с одной или несколькими аминокислотными заменами, улучшающими ADCC, такими как замена в одном или нескольких из положений 298, 333 и 334 области Fc. В некоторых вариантах осуществления, ABP, в рамках изобретения, содержит область Fc с одной или несколькими аминокислотными заменами в положениях 239, 332 и 330, как описано в Lazar et al., Proc. Natl. Acad. Sci. USA, 2006,103:4005-4010, полное содержание которого приведено в качестве ссылки.
[246] В некоторых вариантах осуществления, ABP, в рамках изобретения, содержит одно или несколько изменений, улучшающих или уменьшающих связывание C1q и/или CDC. См. Патент США No. 6194551; WO 99/51642; и Idusogie et al., J. Immunol., 2000, 164:4178-4184; полное содержание всех из которых приведено в настоящем описании в качестве ссылки.
[247] В некоторых вариантах осуществления, ABP, в рамках изобретения, содержит один или несколько изменений для увеличения времени полужизни. ABP с увеличенным временем полужизни и улучшенным связыванием с неонатальным рецептором Fc (FcRn) описаны, например, в Hinton et al., J. Immunol., 2006, 176:346-356; и Патентной публикации США No. 2005/0014934; полное содержание всех из которых приведено в настоящем описании в качестве ссылки. Такие варианты Fc включают варианты с заменами в одном или нескольких из остатков из области Fc: 238, 250, 256, 265, 272, 286, 303, 305, 307, 311, 312, 314, 317, 340, 356, 360, 362, 376, 378, 380, 382, 413, 424, 428 и 434 из IgG.
[248] В некоторых вариантах осуществления, ABP, в рамках изобретения, содержит один или несколько вариантов области Fc, как описано в Патенте США No. 7371826 5648260 и 5624821; Duncan and Winter, Nature, 1988, 322:738-740; и WO 94/29351; полное содержание всех из которых приведено в настоящем описании в качестве ссылки.
1.7. Сконструированные с использованием цистеина варианты антигенсвязывающего белка
[249] В конкретных вариантах осуществления, настоящее изобретение относится к сконструированным с использованием цистеина ABP, также известным как «тиоMAb», в которых один или несколько остатков ABP заменены на остатки цистеина. В конкретных вариантах осуществления, замененные остатки встречаются в доступных для растворителя остатках ABP. Посредством замены таких остатков на цистеин, реакционноспособные тиольные группы вводят в доступные для растворителя участки ABP, и их можно использовать для конъюгации ABP с другими группами, такими как группы лекарственного средства или группы линкера-лекарственного средства, например, для получения иммуноконъюгата.
[250] В конкретных вариантах осуществления, любые один или несколько из следующих остатков можно заменять на цистеин: V205 легкой цепи; A118 области Fc тяжелой цепи; и S400 области Fc тяжелой цепи. Сконструированные с использованием цистеина ABP можно получать, как описано, например, в Патенте США No. 7521541, полное содержание которого приведено в качестве ссылки.
1.7.1. Иммуноконъюгаты
1.7.1.1. Конъюгаты антигенсвязывающий белок-полимер
[251] В некоторых вариантах осуществления, ABP, в рамках изобретения, дериватизируют посредством конъюгации с полимером. Любой подходящий полимер можно конъюгировать с ABP.
[252] В некоторых вариантах осуществления, полимер представляет собой водорастворимый полимер. Иллюстративные примеры водорастворимых полимеров включают полиэтиленгликоль (PEG), сополимеры этиленгликоля/пропиленгликоля, карбоксиметилцеллюлозу, декстран, поливиниловый спирт, поливинилпирролидон, поли-1,3-диоксолан, поли-1,3,6-триоксан, сополимер этилена/малеинового ангидрида, полиаминокислоты (либо гомополимеры, либо случайные сополимеры), сополимер(н-винилпирролидона)-полиэтиленгликоля, гомополимеры пропропиленгликоля, сополимеры полипропиленоксида/этиленоксида, полиоксиэтилированные полиолы (например, глицерин), поливиниловый спирт и их смеси. В некоторых аспектах, пропионовый альдегид полиэтиленгликоля может обеспечивать преимущества при изготовлении благодаря его стабильности в воде.
[253] Полимер может иметь любую молекулярную массу, и может являться разветвленными или неразветвленными. Количество полимеров, присоединенных к каждому ABP, может меняться, и если присоединено более одного полимера, они могут представлять собой один и тот же полимер или различные полимеры. Как правило, количество и/или тип полимеров, используемых для дериватизации, можно определять на основе соображений, включающих конкретные свойства или функции ABP, подлежащие улучшению, и намеченное применение ABP.
1.7.1.2. Конъюгаты антигенсвязывающий белок-лекарственное средство
[254] В некоторых вариантах осуществления, ABP, в рамках изобретения, являются конъюгированными с одним или несколькими лекарственными средствами. Любое подходящее лекарственное средство можно конъюгировать с ABP. Иллюстративные лекарственные средства включают цитокины, хемокины и другие средства, индуцирующие желательную активность T-клеток, такие как GITRL, OX40L, 4-1BBL, TNF-альфа, IL-2, слитый с IL-15 белок, CXCL9, CXCL10, ловушка IL-10, ловушка IL-27 и ловушка IL-35. Ловушки цитокинов и их применение известны в данной области и описаны, например, в Economides et al., Nature Medicine, 2003, 9:47-52, полное содержание которого приведено в качестве ссылки.
Способы получения антигенсвязывающих белков против GITR
1.8. Получение антигена GITR
[255] Антиген GITR, используемый для выделения ABP, в рамках изобретения, может представлять собой интактный GITR или фрагмент GITR. Антиген GITR может находиться в форме выделенного белка или белка, экспрессированного на поверхности клетки.
[256] В некоторых вариантах осуществления, антиген GITR представляет собой неприродный вариант GITR, такой как белок GITR, имеющий аминокислотную последовательность или посттрансляционную моификацию не встречающиеся в природе.
[257] В некоторых вариантах осуществления, антиген GITR укорачивают посредством удаления, например, внутриклеточных или пересекающих мембрану последовательностей, или сигнальных последовательностей. В некоторых вариантах осуществления, антиген GITR является слитым на C-конце с доменом Fc IgG1 человека или полигистидиновой меткой.
1.9. Способы получения моноклональных антител
[258] Моноклональные антитела можно получать, например, с использованием способа гибридомы, впервые описанного в Kohler et al., Nature, 1975, 256:495-497 (полное содержание которого приведено в качестве ссылки), и/или посредством способов рекомбинантной ДНК (См., например, Патент США No. 4816567, полное содержание которого приведено в качестве ссылки). Моноклональные антитела можно также получать, например, с использованием библиотек на основе фагов или дрожжей. См., например, Патенты США No. 8258082 и 8691730, полное содержание всех из которых приведено в настоящем описании в качестве ссылки.
[259] В способе гибридомы, мышь или другого подходящего животного-хозяина, иммунизируют для активации лимфоцитов, которые продуцируют или способны продуцировать антитела, которые могут специфически связывать белок, использованный для иммунизации. Альтернативно, можно иммунизировать лимфоциты in vitro. Затем лимфоциты сливают с клетками миеломы с использованием подходящего вызывающего слияние клеток средства, такого как полиэтиленгликоль, для получения клеток гибридомы. См. Goding J.W., Monoclonal Antibodies: Principles and Practice 3rd ed. (1986) Academic Press, San Diego, CA, полное содержание которого приведено в качестве ссылки.
[260] Клетки гибридомы рассевают и выращивают в подходящей культуральной среде, содержащей одно или несколько веществ, подавляющих рост или выживание не слитых, родительских клеток миеломы. Например, если в родительских клетках миеломы отсутствует фермент гипоксантин-гуанин-фосфорибозилтрансфераза (HGPRT или HPRT), культуральная среда для гибридомы, как правило, содержит гипоксантин, аминоптерин и тимидин (среда HAT), которые предотвращают рост клеток с недостаточностью HGPRT.
[261] Клетки миеломы, которые можно использовать, представляют собой клетки, которые эффективно сливаются, поддерживают стабильно высокий уровень экспрессии антитела выбранными продуцирующими антитело клетками и являются чувствительными к условиям среды, таким как присутствие или отсутствие среды HAT. Из них, предпочтительными линиями клеток миеломы являются линии миеломы мыши, такие как линии, происходящие из опухолей мышей MOP-21 и MC-11 (доступные из Salk Institute Cell Distribution Center, San Diego, CA), и клетки SP-2 или X63-Ag8-653 (доступные из Американской коллекции типовых культур, Rockville, MD). Описаны также линии клеток миеломы человека и гетеромиеломы мыши-человека для продукции человеческих моноклональных антител. См., например, Kozbor, J. Immunol., 1984, 133:3001, полное содержание которого приведено в качестве ссылки.
[262] После идентификации клеток гибридомы, продуцирующих антитела с желательной специфичностью, аффинностью и/или биологической активностью, отобранные клоны можно субклонировать способами лимитирующих разведений и выращивать стандартными способами. См. Goding, выше. Подходящие для данной цели культуральные среды включаетю, например, среду D-MEM или RPMI-1640. Кроме того, клетки гибридомы можно выращивать in vivo в форме асцитных опухолей у животного.
[263] ДНК, кодирующую моноклональные антитела, можно легко выделять и секвенировать с использованием общепринятых способов (например, с использованием олигонуклеотидных зондов, способных специфически связываться с генами, кодирующими тяжелые и легкие цепи моноклональных антител). Таким образом, клетки гибридомы могут служить полезным источником ДНК, кодирующей антитела с желательными свойствами. После выделения, ДНК можно помещать в экспрессирующие векторы, которыми затем трансфицируют клетки-хозяева, такие как бактерии (например, E. coli), дрожжи (например, Saccharomyces или виды Pichia), клетки COS, клетки яичника китайского хомяка (CHO) или клетки миеломы, которые в ином случае не продуцируют антитело, для продукции моноклональных антител.
1.10. Способы получения химерных антител
[264] Иллюстративные способы получения химерных антител описаны, например, в Патенте США No. 4816567; и Morrison et al., Proc. Natl. Acad. Sci. USA, 1984, 81:6851-6855; полное содержание всех из которых приведено в настоящем описании в качестве ссылки. В некоторых вариантах осуществления, химерное антитело получают с использованием рекомбинантных способов для комбинации не относящейся к человеку вариабельной области (например, вариабельной области, происходящей из мыши, крысы, хомяка, кролика или нечеловекообразного примата, такого как обезьяна), с человеческой константной областью.
1.11. Способы получения гуманизированных антител
[265] Гуманизированные антитела можно получать посредством замены большинства, или всех, из структурных частей не относящегося к человеку моноклонального антитела, на соответствующие последовательности человеческого антитела. Следовательно, получают гибридную молекулу, в которой только антигенспецифическая вариабельная область, или CDR, состоит из не относящейся к человеку последовательности. Способы получения гуманизированных антител включают способы, описанные, например, в Winter and Milstein, Nature, 1991, 349:293-299; Rader et al., Proc. Nat. Acad. Sci. U.S.A., 1998, 95:8910-8915; Steinberger et al., J. Biol. Chem., 2000, 275:36073-36078; Queen et al., Proc. Natl. Acad. Sci. U.S.A., 1989, 86:10029-10033; и Патентах США No. 5585089, 5693761, 5693762 и 6180370; полное содержание всех из которых приведено в настоящем описании в качестве ссылки.
1.12. Способы получения человеческих антител
[266] Человеческие антитела можно получать множеством способов, известных в данной области, например, с использованием трансгенных животных (например, гуманизированных мышей). См., например, Jakobovits et al., Proc. Natl. Acad. Sci. U.S.A., 1993, 90:2551; Jakobovits et al., Nature, 1993, 362:255-258; Bruggermann et al., Year in Immuno., 1993, 7:33; и Патенты США No. 5591669, 5589369 и 5545807; полное содержание всех из которых приведено в настоящем описании в качестве ссылки. Человеческие антитела можно получать также из библиотек фагового дисплея (См., например, Hoogenboom et al., J. Mol. Biol., 1991, 227:381-388; Marks et al., J. Mol. Biol., 1991, 222:581-597; и Патенты США No. 5565332 и 5573905; полное содержание всех из которых приведено в настоящем описании в качестве ссылки). Человеческие антитела можно получать также посредством активированных in vitro B-клеток (См., например, Патенты США. No. 5567610 и 5229275, полное содержание всех из которых приведено в настоящем описании в качестве ссылки). Человеческие антитела можно получать также из библиотек на основе дрожжей (См., например, Патент США No. 8691730, полное содержание которого приведено в качестве ссылки).
1.13. Способы получения фрагментов антител
[267] Фрагменты антител, в рамках изобретения, можно получать любым подходящим способом, включая иллюстративные способы, описанные в настоящем описании, или способы, известные в данной области. Подходящие способы включают рекомбинантные способы и протеолитическое расщепление полноразмерных антител. Иллюстративные способы получения фрагментов антител описаны, например, в Hudson et al., Nat. Med., 2003, 9:129-134, полное содержание которого приведено в качестве ссылки. Способы получения scFv антител описаны, например, в Plückthun, in The Pharmacology of Monoclonal Antibodies, vol. 113, Rosenburg and Moore eds., Springer-Verlag, New York, pp. 269-315 (1994); WO 93/16185; и Патентах США No. 5571894 и 5587458; полное содержание всех из которых приведено в настоящем описании в качестве ссылки.
1.14. Способы получения альтернативных каркасов
[268] Альтернативные каркасы, в рамках изобретения, можно получать любым подходящим способом, включая иллюстративные способы, описанные в настоящем описании, или способы, известные в данной области. Например, способы получения аднектинов™ описаны в Emanuel et al., mAbs, 2011, 3:38-48, полное содержание которого приведено в качестве ссылки. Способы получения iMabs описаны в Патентной публикации США No. 2003/0215914, полное содержание которого приведено в качестве ссылки. Способы получения антикалинов® описаны в Vogt and Skerra, Chem. Biochem., 2004, 5:191-199, полное содержание которого приведено в качестве ссылки. Способы получения доменов Куница описаны в Wagner et al., Biochem. & Biophys. Res. Comm., 1992, 186:118-1145, полное содержание которого приведено в качестве ссылки. Способы получения пептидных аптамеров на основе тиоредоксина представлены в Geyer and Brent, Meth. Enzymol., 2000, 328:171-208, полное содержание которого приведено в качестве ссылки. Способы получения аффител представлены в Fernandez, Curr. Opinion in Biotech., 2004, 15:364-373, полное содержание которого приведено в качестве ссылки. Способы получения дарпинов представлены в Zahnd et al., J. Mol. Biol., 2007, 369:1015-1028, полное содержание которого приведено в качестве ссылки. Способы получения аффилинов представлены в Ebersbach et al., J. Mol. Biol., 2007, 372:172-185, полное содержание которого приведено в качестве ссылки. Способы получения тетранектинов представлены в Graversen et al., J. Biol. Chem., 2000, 275:37390-37396, полное содержание которого приведено в качестве ссылки. Способы получения авимеров представлены в Silverman et al., Nature Biotech., 2005, 23:1556-1561, полное содержание которого приведено в качестве ссылки. Способы получения финомеров представлены в Silacci et al., J. Biol. Chem., 2014, 289:14392-14398, полное содержание которого приведено в качестве ссылки.
[269] Дополнительная информация об альтернативных каркасах представлена в Binz et al., Nat. Biotechnol., 2005 23:1257-1268; и Skerra, Current Opin. in Biotech., 2007 18:295-304, полное содержание всех из которых приведено в настоящем описании в качестве ссылки.
1.15. Способы получения мультиспецифических ABP
[270] Мультиспецифические или мультивалентные моноспецифические ABP, в рамках изобретения, можно получать любым подходящим способом, включая иллюстративные способы, описанные в настоящем описании, или способы, известные в данной области. Способы получения антитела с общей легкой цепью описаны в Merchant et al., Nature Biotechnol., 1998, 16:677-681, полное содержание которого приведено в качестве ссылки. Способы получения тетравалентных биспецифических антител описаны в Coloma and Morrison, Nature Biotechnol., 1997, 15:159-163, полное содержание которого приведено в качестве ссылки. Способы получения гибридных иммуноглобулинов описаны в Milstein and Cuello, Nature, 1983, 305:537-540; и Staerz and Bevan, Proc. Natl. Acad. Sci. USA, 1986, 83:1453-1457; полное содержание всех из которых приведено в настоящем описании в качестве ссылки. Способы получения иммуноглобулинов с модификацией выступы-во-впадины описаны в Патенте США No. 5731168, полное содержание которого приведено в качестве ссылки. Способы получения иммуноглобулинов с электростатическими модификациями представвлены в WO 2009/089004, полное содержание которого приведено в качестве ссылки. Способы получения мультивалентных (например, тетравалентных) моноспецифических антител описаны в Miller et al., 2003, Патент США No. 8722859, полное содержание которого приведено в качестве ссылки. Способы получения биспецифических одноцепочечных антител описаны в Traunecker et al., EMBO J., 1991, 10:3655-3659; и Gruber et al., J. Immunol., 1994, 152:5368-5374; полное содержание всех из которых приведено в настоящем описании в качестве ссылки. Способы получения одноцепочечеых антител, длину линкера которых можно менять, описаны в Патентах США No. 4946778 и 5132405, полное содержание всех из которых приведено в настоящем описании в качестве ссылки. Способы получения диател описаны в Hollinger et al., Proc. Natl. Acad. Sci. USA, 1993, 90:6444-6448, полное содержание которого приведено в качестве ссылки. Способы получения триотел и тетрател описаны в Todorovska et al., J. Immunol. Methods, 2001, 248:47-66, полное содержание которого приведено в качестве ссылки. Способы получения триспецифических производных F(ab')3 описаны в Tutt et al. J. Immunol., 1991, 147:60-69, полное содержание которого приведено в качестве ссылки. Способы получения перекрестно сшитых антител описаны в Патенте США No. 4676980; Brennan et al., Science, 1985, 229:81-83; Staerz, et al. Nature, 1985, 314:628-631; и EP 0453082; полное содержание всех из которых приведено в настоящем описании в качестве ссылки. Способы получения антигенсвязывающих доменов, собранных посредством лейциновых молний, описаны в Kostelny et al., J. Immunol., 1992, 148:1547-1553, полное содержание которого приведено в качестве ссылки. Способы получения ABP способом DNL описаны в Патентах США No. 7521056; 7550143; 7534866; и 7527787; полное содержание всех из которых приведено в настоящем описании в качестве ссылки. Способы получения гибридов антител и не относящихся к антителам молекул описаны в WO 93/08829, полное содержание которого приведено в качестве ссылки, для примеров таких ABP. Способы получения антител DAF описаны в Патентной публикации США No. 2008/0069820, полное содержание которой приведено в качестве ссылки. Способы получения ABP посредством восстановления и окисления описаны в Carlring et al., PLoS One, 2011, 6:e22533, полное содержание которого приведено в качестве ссылки. Способы получения DVD-Ig™ описаны в Патенте США No. 7612181, полное содержание которого приведено в качестве ссылки. Способы получения DART™ описаны в Moore et al., Blood, 2011, 117:454-451, полное содержание которого приведено в качестве ссылки. Способы получения DuoBodies® описаны в Labrijn et al., Proc. Natl. Acad. Sci. USA, 2013, 110:5145-5150; Gramer et al., mAbs, 2013, 5:962-972; и Labrijn et al., Nature Protocols, 2014, 9:2450-2463; полное содержание всех из которых приведено в настоящем описании в качестве ссылки. Способы получения антител, содержащих scFv, слитые с C-концом CH3 из IgG описаны в Coloma and Morrison, Nature Biotechnol., 1997, 15:159-163, полное содержание которого приведено в качестве ссылки. Способы получения антител, в которых молекула Fab присоединена к константной области иммуноглобулина, описаны в Miler et al., J. Immunol., 2003, 170:4854-4861, полное содержание которого приведено в качестве ссылки. Способы получения CovX-Bodies описаны в Doppalapudi et al., Proc. Natl. Acad. Sci. USA, 2010, 107:22611-22616, полное содержание которого приведено в качестве ссылки. Способы получения антител Fcab описаны в Wozniak-Knopp et al., Protein Eng. Des. Sel., 2010, 23:289-297, полное содержание которого приведено в качестве ссылки. Способы получения антител TandAb® описаны в Kipriyanov et al., J. Mol. Biol., 1999, 293:41-56 и Zhukovsky et al., Blood, 2013, 122:5116, полное содержание всех из которых приведено в настоящем описании в качестве ссылки. Способы получения тандемных Fab описаны в WO 2015/103072, полное содержание которого приведено в качестве ссылки. Способы получения Zybodies™ описаны в LaFleur et al., mAbs, 2013, 5:208-218, полное содержание которого приведено в качестве ссылки.
[271] В другом аспекте настоящее изобретение относится к способу полугчения антитела против GITR человека или его антигенсвязывающего фрагмента, включающему культивирование клетки-хозяина(клеток-хозяев), выбранной из группы, состоящей из (a) - (c) ниже, для экспрессии тетравалентного антитела против GITR человека или его антигенсвязывающего фрагмента: (a) клетки-хозяина, трансформированной экспрессирующим вектором, содержащим полинуклеотид, содержащий последовательность оснований, кодирующую вариабельную область тяжелой цепи антитела против GITR человека или его антигенсвязывающего фрагмента, в рамках изобретения, и полинуклеотид, содержащий последовательность оснований, кодирующую вариабельную область легкой цепи антитела или его антигенсвязывающего фрагмента; (b) клетки-хозяина, трансформированной экспрессирующим вектором, содержащим полинуклеотид, содержащий последовательность оснований, кодирующую вариабельную область тяжелой цепи антитела против GITR человека или его антигенсвязывающего фрагмента, в рамках изобретения, и экспрессирующим вектором, содержащим полинуклеотид, содержащий последовательность оснований, кодирующую вариабельную область легкой цепи антитела или его антигенсвязывающего фрагмента; и (c) клетки-хозяина, трансформированной экспрессирующим вектором, содержащим полинуклеотид, содержащий последовательность оснований, кодирующую вариабельную область тяжелой цепи антитела против GITR человека или его антигенсвязывающего фрагмента, в рамках изобретения, и клетки-хозяина, трансформированной экспрессирующим вектором, содержащим полинуклеотид, содержащий последовательность оснований, кодирующую вариабельную область легкой цепи антитела или его антигенсвязывающего фрагмента.
[272] В другом аспекте настоящее изобретение относится к способу получения антитела против GITR человека, включающему культивирование клетки-хозяина(клеток-хозяев), выбранной из группы, состоящей из (a) - (c) ниже, для экспрессии антитела против GITR человека: (a) клетки-хозяина, трансформированной экспрессирующим вектором, содержащим полинуклеотид, содержащий последовательность оснований, кодирующую тяжелую цепь антитела против GITR человека, в рамках изобретения, и полинуклеотид, содержащий последовательность оснований, кодирующую легкую цепь антитела; (b) клетки-хозяина, трансформированной экспрессирующим вектором, содержащим полинуклеотид, содержащий последовательность оснований, кодирующую тяжелую цепь антитела против GITR человека, в рамках изобретения, и экспрессирующим вектором, содержащим полинуклеотид, содержащий последовательность оснований, кодирующую легкую цепь антитела; и (c) клетки-хозяина, трансформированной экспрессирующим вектором, содержащим полинуклеотид, содержащий последовательность оснований, кодирующую тяжелую цепь антитела против GITR человека, в рамках изобретения, и клетки-хозяина, трансформированной экспрессирующим вектором, содержащим полинуклеотид, содержащий последовательность оснований, кодирующую легкую цепь антитела.
1.16. Способы получения вариантов
[273] В некоторых вариантах осуществления, ABP, в рамках изобретения, представляет собой подвергнутый аффинному созреванию вариант исходного ABP, который можно получать, например, с использованием способов аффинного созревания на основе фагового дисплея. Кратко, в один или несколько остатков CDR можно вносить мутации, и вариант ABP или его часть экспонируют на фаге и подвергают скринингу по аффинности. Такие изменения можно осуществлять в «горячих точках» CDR, или в остатках, кодируемых кодонами, которые подвержены мутациям с высокой частотой в ходе процесса соматического созревания (См. Chowdhury, Methods Mol. Biol., 2008, 207:179-196, полное содержание которого приведено в качестве ссылки), и/или в остатках, контактирующих с антигеном. В некоторых вариантах осуществления, аффинное созревание можно использовать для изменения или введения видов для связывания, т.е., антитело против мыши можно модифицировать для связывания с вариантами такого же антигена-мишени из человека и яванского макака, и т.д.
[274] Любой подходящий способ можно использовать для введения изменчивости в полинуклеотидную последовательность(последовательности), кодирующую ABP, включая ПЦР с пониженной точностью, перетасовку цепей и направляемый олигонуклеотидами мутагенез, такой как направляемый тринуклеотидами мутагенез (TRIM). В некоторых аспектах, рандомизируют несколько остатков CDR (например, 4-6 остатков за один раз). Остатки CDR, вовлеченные в связывание антигена, можно специфически идентифицировать, например, с использованием аланинового сканирующего мутагенеза или моделирования. CDR-H3 и CDR-L3 особенно часто являются мишенями для мутации.
[275] Введение разнообразия в вариабельные области и/или CDR можно использовать для получения вторичной библиотеки. Затем проводят скрининг вторичной библиотеки для идентификации вариантов ABP с улучшенной аффинностью. Аффинное созревание посредством конструирования и повторного отбора из вторичных библиотек описано, например, в Hoogenboom et al., Methods in Molecular Biology, 2001, 178:1-37, полное содержание которого приведено в качестве ссылки.
1.17. Векторы, клетки-хозяева и рекомбинантные способы
[276] Настоящее изобретение относится также к выделенным нуклеиновым кислотам, кодирующим ABP GITR, векторам, содержащим нуклеиновые кислоты, и к клеткам-хозяевам, содержащим векторы и нуклеиновые кислоты, так же как к рекомбинантным способам получения ABP.
[277] В другом аспекте настоящее изобретение относится к полинуклеотиду, содержащему последовательность оснований, кодирующую вариабельную область тяжелой цепи антитела против GITR человека или его антигенсвязывающего фрагмента, в рамках изобретения. В другом аспекте настоящее изобретение относится к полинуклеотиду, содержащему последовательность оснований, кодирующую вариабельную область легкой цепи антитела против GITR человека или его антигенсвязывающего фрагмента, в рамках изобретения.
[278] В другом аспекте настоящее изобретение относится к полинуклеотиду, содержащему последовательность оснований, кодирующую тяжелую цепь антитела против GITR человека, в рамках изобретения. В другом аспекте настоящее изобретение относится к полинуклеотиду, содержащему последовательность оснований, кодирующую легкую цепь антитела против GITR человека, в рамках изобретения.
[279] Для рекомбинантного получения ABP, нуклеиновую кислоту(кислоты), кодирующую его, можно выделять и вставлять в способный к репликации вектор для дальнейшего клонирования (т.е., амплификации ДНК) или экспрессии. В некоторых аспектах, нуклеиновую кислоту можно получать посредством гомологичной рекомбинации, например, как описано в Патенте США No. 5204244, полное содержание которого приведено в качестве ссылки.
[280] В другом аспекте настоящее изобретение относится к экспрессирующему вектору, содержащему (a) полинуклеотид, содержащий последовательность оснований, кодирующую вариабельную область тяжелой цепи антитела против GITR человека или его антигенсвязывающего фрагмента, в рамках изобретения, и/или (b) полинуклеотид, содержащий последовательность оснований, кодирующую вариабельную область легкой цепи антитела против GITR человека или его антигенсвязывающий фрагмент.
[281] В другом аспекте настоящее изобретение относится к экспрессирующему вектору, содержащему (a) полинуклеотид, содержащий последовательность оснований, кодирующую тяжелую цепь антитела против GITR человека, в рамках изобретения, и/или (b) полинуклеотид, содержащий последовательность оснований, кодирующую легкую цепь антитела против GITR человека.
[282] Множество различных векторов известно в данной области. Компоненты вектора, как правило, включают одно или несколько из следующего: сигнальная последовательность, точка начала репликации, один или несколько маркерных генов, энхансерный элемент, промотор и последовательность терминации транскрипции, например, как описано в Патенте США No. 5534615, полное содержание которого приведено в качестве ссылки.
[283] Иллюстративные примеры подходящих клеток-хозяев представлены ниже. Эти клетки-хозяева не являются ограничивающими, и любую подходящую клетку-хозяина можно использовать для получения ABP, в рамках изобретения.
[284] В другом аспекте настоящее изобретение относится к клетке-хозяину, трансформированной экспрессирующим вектором, выбранной из группы, состоящей из (a) - (d): (a) клетки-хозяина, трансформированной экспрессирующим вектором, содержащим полинуклеотид, содержащий последовательность оснований, кодирующую вариабельную область тяжелой цепи антитела против GITR человека или его антигенсвязывающего фрагмента, в рамках изобретения, и полинуклеотид, содержащий последовательность оснований, кодирующую вариабельную область легкой цепи антитела или его антигенсвязывающего фрагмента; (b) клетки-хозяина, трансформированной экспрессирующим вектором, содержащим полинуклеотид, содержащий последовательность оснований, кодирующую вариабельную область тяжелой цепи антитела против GITR человека или его антигенсвязывающего фрагмента, в рамках изобретения, и экспрессирующим вектором, содержащим полинуклеотид, содержащий последовательность оснований, кодирующую вариабельную область легкой цепи антитела или его антигенсвязывающего фрагмента; (c) клетки-хозяина, трансформированной экспрессирующим вектором, содержащим полинуклеотид, содержащий последовательность оснований, кодирующую вариабельную область тяжелой цепи антитела против GITR человека или его антигенсвязывающего фрагмента, в рамках изобретения; и (d) клетки-хозяина, трансформированной экспрессирующим вектором, содержащим полинуклеотид, содержащий последовательность оснований, кодирующую вариабельную область легкой цепи антитела против GITR человека или его антигенсвязывающего фрагмента, в рамках изобретения.
[285] В другом аспекте настоящее изобретение относится к клетке-хозяину, трансформированной экспрессирующим вектором, выбранной из группы, состоящей из (a) - (d): (a) клетки-хозяина, трансформированной экспрессирующим вектором, содержащим полинуклеотид, содержащий последовательность оснований, кодирующую тяжелую цепь антитела против GITR человека, в рамках изобретения, и полинуклеотид, содержащий последовательность оснований, кодирующую легкую цепь антитела; (b) клетки-хозяина, трансформированной экспрессирующим вектором, содержащим полинуклеотид, содержащий последовательность оснований, кодирующую тяжелую цепь антитела против GITR человека, в рамках изобретения, и экспрессирующим вектором, содержащим полинуклеотид, содержащий последовательность оснований, кодирующую легкую цепь антитела; (c) клетки-хозяина, трансформированной экспрессирующим вектором, содержащим полинуклеотид, содержащий последовательность оснований, кодирующую тяжелую цепь антитела против GITR человека, в рамках изобретения; и (d) клетки-хозяина, трансформированной экспрессирующим вектором, содержащим полинуклеотид, содержащий последовательность оснований, кодирующую легкую цепь антитела против GITR человека, в рамках изобретения.
[286] Подходящие клетки-хозяева включают любые клетки прокариот (например, бактерий), низших эукариот (например, дрожжей), или высших эукариот (например, млекопитающих). Подходящие прокариот включают эубактерии, такие как грамотрицательные или грамположительные организмы, например, Enterobacteriaceae, такие как Escherichia (E. coli), Enterobacter, Erwinia, Klebsiella, Proteus, Salmonella (S. typhimurium), Serratia (S. marcescans), Shigella, Bacilli (B. subtilis и B. licheniformis), Pseudomonas (P. aeruginosa), и Streptomyces. Одним из полезных клонирующих хозяев E. coli является E. coli 294, хотя другие штаммы, такие как E. coli B, E. coli X1776 и E. coli W3110, также являются подходящими.
[287] В дополнение к прокариотам, эукариотические микроорганизмы, такие как мицелиальные грибы или дрожжи, также являются пригодными клонирующими или экспрессирующими хозяевами для векторов, кодирующих ABP GITR. Saccharomyces cerevisiae, или обычные пекарские дрожжи, являются общеупотребительным микроорганизмом-хозяином из низших эукариот. Однако, ряд других родов, видов и штаммов являются доступными и могут быть использованы, такие как Schizosaccharomyces pombe, Kluyveromyces (K. lactis, K. fragilis, K. bulgaricus K. wickeramii, K. waltii, K. drosophilarum, K. thermotolerans и K. marxianus), Yarrowia, Pichia pastoris, Candida (C. albicans), Trichoderma reesia, Neurospora crassa, Schwanniomyces (S. occidentalis), и мицелиальные грибы например, такие как Penicillium, Tolypocladium и Aspergillus (A. nidulans и A. niger).
[288] Клетки-хозяева млекопитающих, которые можно использовать, включают клетки COS-7, клетки HEK293; клетки почки детеныша хомяка (BHK); клетки яичника китайского хомяка (CHO); клетки Сертоли мышей; клетки почки африканской зеленой мартышки (VERO-76) и т.п.
[289] Клетки-хозяева, используемые для получения ABP GITR по этому изобретению, можно культивировать во множестве сред. Коммерчески доступные среды, например, такие как среда Хэма F10, минимальная поддерживающая среда (MEM), RPMI-1640 и модифицированная способом Дульбекко среда Игла (DMEM), являются пригодными для культивирования клеток-хозяев. Кроме того, можно использовать любую из сред, описанных в Ham et al., Meth. Enz., 1979, 58:44; Barnes et al., Anal. Biochem., 1980, 102:255; и Патентах США No. 4767704, 4657866, 4927762, 4560655 и 5122469; или WO 90/03430 и WO 87/00195. Полное содержание каждой из вышеуказанных ссылок приведено в качестве ссылки.
[290] Любую из этих сред можно дополнять по необходимости гормонами и/или другими факторами роста (такими как инсулин, трансферрин или эпидермальный фактор роста), солями (такими как хлорид натрия, кальций, магний, и фосфат), буферами (такими как HEPES), нуклеотидами (такими как аденозин и тимидин), антибиотиками, микроэлементами (определенными как неорганические соединения, обычно присутствующие в конечных концентрациях в микромолярном диапазоне) и глюкозой или эквивалентным источником энергии. Любые другие необходимые добавки также можно включать в подходящих концентрациях, известных специалисту в данной области.
[291] Условия культивирования, такие как температура, pH, и т.п, представляют собой условия, ранее использованные для клетки-хозяина, выбранной для экспрессии, и являются очевидными для специалиста в данной области.
[292] При использовании рекомбинантных способов, ABP может продуцироваться внутри клеток, в периплазматическом пространстве, или напрямую секретироваться в среду. Если ABP продуцируется внутри клеток, в качестве первой стадии, дебрис твердых частиц, либо клеток-хозяев, либо лизированных фрагментов, удаляют, например, посредством центрифугирования или ультрафильтрации. Например, в Carter et al. (Bio/Technology, 1992, 10:163-167, полное содержание которого приведено в качестве ссылки) описан способ выделения ABP, который секретируется в периплазматическое пространство E. coli. Кратко, клеточную массу размораживают в присутствии ацетата натрия (pH 3,5), ЭДТА и фенилметилсульфонилфторида (PMSF) в течение приблизительно 30 мин. Клеточный дебрис можно удалять посредством центрифугирования.
[293] В некоторых вариантах осуществления, ABP получают в бесклеточной системе. В некоторых аспектах, бесклеточная система представляет собой систему для транскрипции и трансляции in vitro, как описано в Yin et al., mAbs, 2012, 4:217-225, полное содержание которого приведено в качестве ссылки. В некоторых аспектах, в бесклеточной системе используют бесклеточный экстракт из эукариотической клетки или из прокариотической клетки. В некоторых аспектах, прокариотическая клетка представляет собой E. coli. Бесклеточная экспрессия ABP может являться полезной, например, когда ABP накапливается в клетке в форме нерастворимого агрегата, или когда выходы после периплазматической экспрессии являются низкими.
[294] Когда ABP секретируется в среду, супернатанты из таких систем для экспрессии, как правило, сначала концентрируют с использованием коммерчески доступного фильтра для концентрации белка, например, установки для ультрафильтрации Amicon® или Millipore®, Pellcon®. Ингибитор протеаз, такой как PMSF, можно включать в любую из вышеуказанных стадий для ингибирования протеолиза, и антибиотики можно включать для предотвращения роста непредусмотренных загрязняющих организмов.
[295] Композицию ABP полученную из клеток, можно очищать с использованием, например, хроматографии на гидроксилапатите, электрофореза в геле, диализа и аффинной хроматографии, где аффинная хроматография является особенно полезным способом очистки. Пригодность белка A в качестве аффинного лиганда зависит от вида и изотипа любого домена Fc иммуноглобулина, который присутствует в ABP. Белок A можно использовать для очистки ABP, содержащих тяжелые цепи γ1, γ2 или γ4 человека (Lindmark et al., J. Immunol. Meth., 1983, 62:1-13, полное содержание которого приведено в качестве ссылки). Белок G представляет можно использовать для всех изотипов мыши и для γ3 человека (Guss et al., EMBO J., 1986, 5:1567-1575, полное содержание которого приведено в качестве ссылки).
[296] Матрица, к которой присоединяют аффинный лиганд, наиболее часто представляет собой агарозу, однако, доступны другие матрицы. Механически стабильные матрицы, такие как стекло с контролируемым размером пор или поли(стиролдивинил)бензол, обеспечивают более высокие скорости потока и более короткие периоды времени обработки, чем можно достигать с использованием агарозы. Когда ABP содержит домен CH3, смолу BakerBond ABX® можно использовать для очистки.
[297] Другие способы очистки белка, такие как фракционирование на ионообменной колонке, преципитация этанолом, обращеннофазовая HPLC, хроматография на силикагеле, хроматография на гепарин-сефарозе®, хроматофокусировка, SDS-PAGE, и преципитация сульфатом аммония, также являются доступными, и их может использовать специалист в данной области.
[298] После любой стадии(стадий) предварительной очистки, смесь, содержащую представляющий интерес ABP и загрязняющие примеси, можно подвергать хроматографии с гидрофобным взаимодействием при низком pH с использованием буфера для элюции с pH между приблизительно 2,5 и приблизительно 4,5, как правило, проводимой при низкой концентрации солей (например, от приблизительно 0 до приблизительно 0,25 M соли).
Анализы
[299] Множество анализов, известных в данной области, можно использовать для идентификации и характеризации ABP GITR, в рамках изобретения.
1.18. Анализы связывания, конкуренции и эпитопного картирования
[300] Специфическую активность связывания антигена для ABP, в рамках изобретения, можно оценивать любым подходящим способом, включая использование SPR, BLI и RIA, как описано в другом месте настоящего описания. Кроме того, активность связывания антигена можно оценивать посредством анализов ELISA и анализов Вестерн-блоттинга.
[301] Анализы для измерения конкуренции между двумя ABP, или между ABP и другой молекулой (например, GITRL) описаны в другомм мессте настоящего описания и, например, в Harlow and Lane, Antibodies: A Laboratory Manual ch.14, 1988, Cold Spring Harbor Laboratory, Cold Spring Harbor, N.Y, полное содержание которого приведено в качестве ссылки.
[302] Анализы для картирования эпитопов, которые связывают ABP, в рамках изобретения, описаны, например, в Morris «Epitope Mapping Protocols», in Methods in Molecular Biology vol. 66, 1996, Humana Press, Totowa, N.J., полное содержание которого приведено в качестве ссылки. В некоторых вариантах осуществления, эпитоп определяют посредством конкуренции пептидов. В некоторых вариантах осуществления, эпитоп определяют посредством масс-спектрометрии. В некоторых вариантах осуществления, эпитоп определяют посредством кристаллографии.
1.19. Анализы агонизма GITR
[303] В некоторых вариантах осуществления, ABP, в рамках изобретения, подвергают скринингу для идентификации или характеризации ABP с агонистическойй активностью против GITR. Любой подходящий анализ можно использовать для идентификации или характеризации таких ABP. В некоторых аспектах, анализ измеряет количество цитокина, секретируемое эффекторной T-клеткой после приведения эффекторной T-клетки в контакт с ABP, в рамках изобретения. В некоторых аспектах, цитокин выбран из IL-2Rα, IL-2, IL-8, IFNγ и их комбинаций. В некоторых аспектах, цитокин выбран из sCD40L, VEGF, TNF-β, TNF-α, TGF-α, RANTES, PDGF-AB/BB, PDGF-AA, MIP-1β, MIP-1α, MDC (CCL22), MCP-3, MCP-1, IP-10, IL-17A, IL-15, IL-13, IL-12 (p70), IL-12 (p40), IL-10, IL-9, IL-8, IL-7, IL-6, IL-5, IL-4, IL-3, IL-2, IL-2Rα, IL-1RA, IL-1β, IL-1α, IFNγ, IFNα2, GRO, GM-CSF, G-CSF, фракталкина, лиганда Flt-3, FGF-2, эотаксина, EGF и их комбинаций.
[304] В некоторых вариантах осуществления, эффекторные клетки костимулируют с использованием агониста CD3, для стимуляции секреции цитокинов эффекторной клеткой. В некоторых аспектах, агонист CD3 предоставляют на субмаксимальном уровне.
[305] В некоторых вариантах осуществления, используют функциональные анализы, такие как анализы на основе клеток HT1080 или Jurkat, более подробно описанные в примере 2. Дополнительные анализы описаны в Wyzgol et al., J Immunol 2009; 183:1851-1861, содержание которого приведено в настоящем описании в качестве ссылки.
[306] В некоторых аспектах, такие анализы могут измерять пролиферацию эффекторной T-клетки после приведения эффекторной T-клетки в контакт с ABP, в рамках изобретения. В некоторых аспектах, пролиферацию эффекторной T-клетки измеряют посредством разведения красителя (например, сукцинимидилового сложного эфира диацетата карбоксифлуоресцеина; CFSE), посредством поглощения тритированного тимидина, посредством люминесцентных анализов жизнеспособности клеток, или посредством других анализов, известных в данной области.
[307] В некоторых аспектах, такие анализы могут измерять дифференцировку, продукцию цитокинов, жизнеспособность (например, выживаемость), пролиферацию или супрессорную активность регуляторной T-клетки после приведения регуляторной T-клетки в контакт с ABP, в рамках изобретения.
[308] В некоторых аспектах, такие анализы могут измерять цитотоксическую активность клетки NK после приведения клетки NK в контакт с ABP, в рамках изобретения. В некоторых аспектах, цитотоксическую активность клетки NK измеряют с использованием анализа цитотоксичности, количественно оценивающего опосредованное NK уничтожение клеток-мишеней (например, линии клеток K562). См. Jang et al., Ann. Clin. Lab. Sci., 2012, 42:42-49, полное содержание которого приведено в качестве ссылки.
[309] Дополнительные анализы для измерения агонизма GITR описаны в другом месте этого описания, включая Примеры, и известны в данной области. Специалист в данной области может легко выбрать подходящий анализ для оценки агонизма GITR.
1.20. Анализы эффекторных Функций
[310] Эффекторную функцию ABP, в рамках изобретения, можно оценивать с использованием множества in vitro и in vivo анализов, известных в данной области, включая анализы, описанные в Ravetch and Kinet, Annu. Rev. Immunol., 1991, 9:457-492; Патентах США No. 5500362, 5821337; Hellstrom et al., Proc. Nat'l Acad. Sci. USA, 1986, 83:7059-7063; Hellstrom et al., Proc. Nat'l Acad. Sci. USA, 1985, 82:1499-1502; Bruggemann et al., J. Exp. Med., 1987, 166:1351-1361; Clynes et al., Proc. Nat'l Acad. Sci. USA, 1998, 95:652-656; WO 2006/029879; WO 2005/100402; Gazzano-Santoro et al., J. Immunol. Methods, 1996, 202:163-171; Cragg et al., Blood, 2003, 101:1045-1052; Cragg et al. Blood, 2004, 103:2738-2743; и Petkova et al., Int'l. Immunol., 2006, 18:1759-1769; полное содержание всех из которых приведено в настоящем описании в качестве ссылки.
Фармацевтические композиции
[311] ABP, в рамках изобретения, можно составлять в любую подходящую фармацевтическую композицию и вводить любым подходящим способом введения. Подходящие способы введения включают, но без ограничения, внутриартериальные, внутрикожные, внутримышечные, внутрибрюшинные, внутривенные, назальные, парентеральные, пульмональные и подкожные способы.
[312] В другом аспекте настоящее изобретение относится к фармацевтической композиции, содержащей множество видов антител против GITR человека или их антигенсвязывающих фрагментов, в рамках изобретения. Например, фармацевтическая композиция содержит антитело или его антигенсвязывающий фрагмент, которые не подвергали посттрансляционной модификации, и антитело или его антигенсвязывающий фрагмент, полученные в результате посттрансляционной модификации антитела или его антигенсвязывающего фрагмента.
[313] В одном варианте осуществления, фармацевтическая композиция содержит по меньшей мере два вида антител против GITR человека, выбранных из (1) - (4): (1) антитела против GITR человека, содержащего две тяжелые цепи, состоящие из SEQ ID NO: 7 и четыре легкие цепи, состоящие из SEQ ID NO: 8; (2) антитела против GITR человека, содержащего две тяжелые цепи, состоящие из SEQ ID NO: 7, где Q в положении 1 модифицирован до пироглутамата, и четыре легкие цепи, состоящие из SEQ ID NO: 8; (3) антитела против GITR человека, содержащего две тяжелые цепи, состоящие из аминокислотной последовательности в диапазоне от Q в положении 1 до G в положении 686 из SEQ ID NO: 7, и четыре легкие цепи, состоящие из SEQ ID NO: 8; и (4) антитела против GITR человека, содержащего две тяжелые цепи, состоящие из аминокислотной последовательности в диапазоне от Q в положении 1 to G в положении 686 из SEQ ID NO: 7, где Q в положении 1 модифицирован до пироглутамата, и четыре легкие цепи из SEQ ID NO: 8.
[314] В одном варианте осуществления, фармацевтическая композиция содержит антитело против GITR человека, содержащее две тяжелые цепи, состоящие из SEQ ID NO: 7, и четыре легкие цепи, состоящие из SEQ ID NO: 8; и антитело против GITR человека, содержащее две тяжелые цепи, состоящие из аминокислотной последовательности в диапазоне от Q в положении 1 до G в положении 686 из SEQ ID NO: 7, где Q в положении 1 модифицирован до пироглутамата, и четыре легкие цепи из SEQ ID NO: 8, и фармацевтически приемлемый наполнитель.
[315] Фармацевтическая композиция может содержать один или несколько фармацевтических наполнителей. Можно использовать любой подходящий фармацевтический наполнитель, и специалист в данной области способен выбирать подходящие фармацевтические наполнители. Соответственно, фармацевтические наполнители, представленные ниже, являются иллюстративными, а не ограничивающими. Дополнительные фармацевтические наполнители включают, например, фармацевтические наполнители, описанные в Handbook of Pharmaceutical Excipients, Rowe et al. (Eds.) 6th Ed. (2009), полное содержание которого приведено в качестве ссылки.
[316] В некоторых вариантах осуществления, фармацевтическая композиция содержит средство против пенообразования. Можно использовать любое подходящее средство против пенообразования. В некоторых аспектах, средство против пенообразования выбрано из спирта, эфира, масла, воска, силикона, поверхностно-активного вещества и их комбинаций. В некоторых аспектах, средство против пенообразования выбрано из минерального масла, растительного масла, этилен-бис-стеарамида, парафинового воска, сложноэфирного воска, воска из жирного спирта, жирного спирта с длинной цепью, мыла жирной кислоты, сложного эфира жирной кислоты, силиконгликоля, фторсиликона, сополимера полиэтиленгликоля-полипропиленгликоля, полидиметилсилоксана-диоксида кремния, эфира, октилового спирта, каприловвого спирта, триолеата сорбитана, этилового спирта, 2-этил-гексанола, диметикона, олеилового спирта, симетикона и их комбинаций.
[317] В некоторых вариантах осуществления, фармацевтическая композиция содержит coрастворитель. Иллюстративные примеры coрастворителей включают этанол, поли(этилен)гликоль, бутиленгликоль, диметилацетамид, глицерин, пропиленгликоль и их комбинации.
[318] В некоторых вариантах осуществления, фармацевтическая композиция содержит буфер. Иллюстративные примеры буферов включают ацетат, борат, карбонат, лактат, малат, фосфат, цитрат, гидроксид, диэтаноламин, моноэтаноламин, глицин, метионин, гуаровую камедь, моноглутамат натрия и их комбинации.
[319] В некоторых вариантах осуществления, фармацевтическая композиция содержит носитель или наполнитель. Иллюстративные примеры носителей или наполнителей включают лактозу, мальтодекстрин, маннит, сорбит, хитозан, стеариновую кислоту, ксантановую смолу, гуаровую камедь и их комбинации.
[320] В некоторых вариантах осуществления, фармацевтическая композиция содержит поверхностно-активное вещество. Иллюстративные примеры поверхностно-активных веществ включают d-альфа-токоферол, хлорид бензалкония, хлорид бензэтония, цетримид, хлорид цетилпиридиния, докузат натрия, глицерилбегенат, глицерилмоноолеат, лауриновую кислоту, макрогол-15-гидроксистеарат, миристиловый спирт, фосфолипиды, эфиры полиоксиэтиленалкила, полиоксиэтиленсорбитановые сложные эфиры жирных кислот, полиоксиэтиленстеараты, полиоксилглицериды, лаурилсульфат натрия, сложные эфиры сорбитана, витамин E полиэтилен(гликоль)сукцинат и их комбинации.
[321] В некоторых вариантах осуществления, фармацевтическая композиция содержит средство против слеживания. Иллюстративные примеры средств против слеживания включают фосфат кальция (трехосновный), гидроксиметилцеллюлозу, гидроксипропилцеллюлозу, оксид магния и их комбинации.
[322] Другие наполнители, которые можно использовать в фармацевтических композициях, включают, например, альбумин, антиоксиданты, антибактериальные средства, противогрибковые средства, биоадсорбируемые полимеры, хелатирующие агенты, контролирующие высвобождение средства, разбавители, диспергирующие средства, усилители растворения, эмульгаторы, гелеобразующие средства, основы мазей, усилители проницаемости, консерванты, солюбилизирующие средства, растворители, стабилизаторы, сахара и их комбинации. Конкретные примеры каждого из этих средств описаны, например, в Handbook of Pharmaceutical Excipients, Rowe et al. (Eds.) 6th Ed. (2009), The Pharmaceutical Press, полное содержание которого приведено в качестве ссылки.
[323] В некоторых вариантах осуществления, фармацевтическая композиция содержит растворитель. В некоторых аспектах, растворитель представляет собой солевой раствор, такой как стерильный солевой раствор или раствор декстрозы. В некоторых аспектах, растворитель представляет собой воду для инъекций.
[324] В некоторых вариантах осуществления, фармацевтические композиции находятся в форме твердых частиц, таких как микрочастица или наночастица. Микрочастицы и наночастицы можно формировать из любого подходящего материала, такого как полимер или липид В некоторых аспектах, микрочастицы или наночастицы представляют собой мицеллы, липосомы или полимеросомы.
[325] Кроме того, настоящее изобретение относится к безводным фармацевтическим композициям и лекарственным формам, содержащим ABP, поскольку вода может облегчать деградацию некоторых ABP.
[326] Безводные фармацевтические композиции и лекарственные формы, в рамках изобретения, можно получать с использованием безводных ингредиентов или ингредиентов с низким содержанием влажности или в условиях низкой влажности. Фармацевтические композиции и лекарственные формы, которые содержат лактозу и по меньшей мере один активный ингредиент, содержащий первичный или вторичный амин, могут являться безводными, если ожидают значительный контакт с увлажнением и/или влажностью в ходе изготовления, упаковки и/или хранения представляет собой.
[327] Безводную фармацевтическую композицию следует получать и хранить таким образом, чтобы поддерживать ее безводное состояние. Соответственно, безводные композиции можно упаковывать с использованием материалов, как известно, предотвращающих воздействие воды, так что их можно включать в подходящие наборы для составления. Примеры подходящей упаковки включают, но без ограничения, герметично запаянную фольгу, пластики, контейнеры для единичной дозы (например, ампулы), блистерные упаковки и контурные упаковки.
1.21. Парентеральные лекарственные формы
[328] В конкретных вариантах осуществления, ABP, в рамках изобретения, составляют в парентеральные лекарственные формы. Парентеральные лекарственные формы можно вводить субъектам различными способами, включая, но без ограничения, подкожный, внутривенный (включающий инфузии и болюсные инъекции), внутримышечный и внутриартериальный. Поскольку их введение, как правило, обходит способы природной защиты субъекта против загрязняющих примесей, парентеральные лекарственные формы, как правило, являются стерильными или пригодными для стерилизации перед введением субъекту. Примеры парентеральных лекарственных форм включают, но без ограничения, растворы, готовые для инъекции, сухие (например, лиофилизированные) продукты, готовые для растворения или суспендирования в фармацевтически приемлемом носителе, суспензии, готовые для инъекции, и эмульсии.
[329] Пригодные носители, которые можно использовать для получения парентеральных лекарственных форм, хорошо известны специалистам в данной области. Примеры включают, но без ограничения: воду для инъекций USP; водные носители, такие как, но без ограничения, хлорид натрия для инъекций, раствор Рингера для инъекций, декстроза для инъекций, декстроза и хлорид натрия для инъекций и лактированный раствор Рингера для инъекций; смешивающиеся с водой носители, такие как, но без ограничения, этиловый спирт, полиэтиленгликоль и полипропиленгликоль; и неводные ноители, такие как, но без ограничения, кукурузное масло, хлопковое масло, арахисовое масло, кунжутное масло, этилолеат, изопропилмиристат и бензилбензоат.
[330] Наполнители, увеличивающие растворимость одного или нескольких ABP, описанных в настоящем описании, также можно включать в парентеральные лекарственные формы.
[331] В некоторых вариантах осуществления, парентеральная лекарственная форма является лиофилизированной. Иллюстративные лиофилизированные составы описаны, например, в Патентах США No. 6267958 и 6171586; и WO 2006/044908; полное содержание всех из которых приведено в настоящем описании в качестве ссылки.
Дозы и единичные дозированные формы
[332] В случае лекарственных средств для человека, медицинский работник может определять позологию, которую следует считать наиболее подходящей в соответствии с профилактическим или излечивающим лечением и в соответствии с возрастом, массой, состоянием и другими факторами, специфическими для субъекта, подлежащего лечению.
[333] В конкретных вариантах осуществления, композиция, в рамках изобретения, представляет собой фармацевтическую композицию или однократную единичную дозированную форму. Фармацевтические композиции и однократные единичные дозированные формы, в рамках изобретения, содержат профилактически или терапевтически эффективное количество одного или нескольких профилактических или терапевтических ABP.
[334] Количество ABP или композиции, которое может являться эффективным для предотвращения или лечения нарушения или его одного или нескольких симптомов, можно менять в зависимости от характера и тяжести заболевания или состояния, и способа, которым вводят ABP. Частоту и дозу можно также менять в соответствии с факторами, специфическими для каждого субъекта, в зависимости от специфических водимых лекарственных средств (например, терапевтических или профилактических средств), тяжести нарушения, заболевания или состояния, способа введения, также как возраста, массы тела, ответа и предшествующего анамнеза субъекта. Эффективные дозы можно экстраполировать из кривых зависимости ответа от дозы, выведенных из тестовых систем in vitro или тестовых систем в моделях на животных.
[335] В конкретных вариантах осуществления, иллюстративные дозы композиции включают миллиграммовые или микрограммовые количества ABP на килограмм массы субъекта или образца (например, от приблизительно 100 микрограмм на килограмм до приблизительно 25 миллиграмм на килограмм, или от приблизительно 100 микрограмм на килограмм до приблизительно 10 миллиграмм на килограмм). В конкретном варианте осуществления, доза ABP, в рамках изобретения, на основании массы ABP, вводимая для предотвращения, лечения, управления течением или облегчения нарушения, или одного или нескольких его симптомов у субъекта, составляет 0,1 мг/кг, 1 мг/кг, 2 мг/кг, 3 мг/кг, 4 мг/кг, 5 мг/кг, 6 мг/кг, 10 мг/кг, 15 мг/кг, 20 мг/кг, 25 мг/кг, 30 мг/кг или 40 мг/кг или более, на массу тела субъекта.
[336] Дозу можно вводить в соответствии с подходящим расписанием, например, еженедельно, один раз в каждые две недели, один раз в каждые три недели, или один раз в каждые четыре недели. В некоторых вариантах осуществления, антитело, подлежащее введению один раз в каждые три или четыре недели, можно вводить в более высокой дозе, чем антитело, вводимое каждую одну или две недели. В некоторых вариантах осуществления, вводимая нагрузочная доза выше, чем поддерживающая доза, вводимая позднее. Может являться необходимым использовать дозы ABP за пределами диапазонов, описанных в настоящем описании, в некоторых случаях, как очевидно специалисту в данной области. Кроме того, следует отметить, что медицинскому работнику или лечащему терапевту известно, как и когда прерывать, корректировать или прекращать терапию в соответствии с ответом субъекта.
[337] Различные терапевтически эффективные количества могут являться применимыми для различных заболеваний и состояний, как хорошо известно специалисту в данной области. Подобным образом, количества, достаточные для предотвращения, управления течением, лечения или облегчения таких нарушений, но недостаточные для вызова, или достаточные для уменьшения, неблагоприятных эффектов, ассоциированных с ABP, в рамках изобретения, также включены в уровни дозирования и расписания частоты дозирования, в рамках изобретения. Кроме того, когда субъекту вводят множественные дозы композиции, в рамках изобретения, не все из доз обязательно должны быть одинаковыми. Например, дозу, водимую субъекту, можно увеличивать для улучшения профилактического или терапевтического эффекта композиции или ее можно уменьшать для уменьшения одного или нескольких побочных эффектов, испытываемых конкретным субъектом.
[338] В конкретных вариантах осуществления, лечение или предотвращение можно начинать с одной или нескольких нагрузочных доз ABP или композиции, в рамках изобретения, за которыми следуют одна или несколько поддерживающих доз.
[339] В конкретных вариантах осуществления, дозу ABP или композиции, в рамках изобретения, можно вводить для достижения состояния равновесия концентрации ABP в крови или сыворотке субъекта. Концентрацию в состоянии равновесия можно определять посредством измерения в соответствии со способами, доступными специалисту в данной области, или она может быть основана на физических характеристиках субъекта, таких как рост, масса и возраст.
[340] В конкретных вариантах осуществления, введение одной и той же композиции можно повторять, и введения могут быть разделены по меньшей мере 1 сутками, 2 сутками, 3 сутками, 5 сутками, 10 сутками, 15 сутками, 30 сутками, 45 сутками, 2 месяцами, 75 сутками, 3 месяцами или 6 месяцами.
[341] Как более подробно обсуждают в другом месте этого описания, ABP, в рамках изобретения, можно, необязательно, вводить вместе с одним или несколькими дополнительными средствами, которые можно использовать для предотвращения или лечения заболевания или нарушения. Эффективное количество таких дополнительных средств может зависеть от количества ABP, присутствующего в составе, типа нарушения или лечения, и других факторов, известных в данной области или описанных в настоящем описании.
Терапевтические применения
[342] Для терапевтических применений, ABP по изобретению вводят млекопитающему, как правило, человеку, в фармацевтически приемлемой лекарственной форме, такой как известные в данной области и описанные выше. Например, ABP по изобретению можно вводить человеку внутривенно в форме болюса или посредством непрерывной инфузии в течение некоторого периода времени, посредством внутримышечного, внутрибрюшинного, интрацереброспинального, подкожного, интраартикулярного, внутрисуставного, интратекального или внутриопухолевого способов. ABP моно также подходящим образом вводить перитуморальным, внутриочаговым способами или по периферии очага, для достижения местных, так же как системных, терапевтических эффектов. Внутрибрюшинный способ может являться особенно полезным, например, для лечения опухолей яичников.
[343] ABP, в рамках изобретения, можно использовать для лечения любого заболевания или состояния, вовлекающего GITR. В некоторых вариантах осуществления, заболевание или состояние представляет собой заболевание или состояние, при котором можно обеспечивать преимущество от лечения с использованием ABP против GITR. В некоторых вариантах осуществления, заболевание или состояние представляет собой опухоль. В некоторых вариантах осуществления, заболевание или состояние представляет собой нарушение пролиферации клеток. В некоторых вариантах осуществления, заболевание или состояние представляет собой злокачественную опухоль.
[344] В некоторых вариантах осуществления, ABP, в рамках изобретения, предназначены для использования в качестве лекарственного средства. В некоторых вариантах осуществления, ABP, в рамках изобретения, предназначены для использования в изготовлении или получении лекарственного средства. В некоторых вариантах осуществления, лекарственное средство предназначено для лечения заболевания или состояния, при котором можно получать преимущество от ABP против GITR. В некоторых вариантах осуществления, заболевание или состояние представляет собой опухоль. В некоторых вариантах осуществления, заболевание или состояние представляет собой нарушение пролиферации клеток. В некоторых вариантах осуществления, заболевание или состояние представляет собой злокачественную опухоль.
[345] Любую подходящую злокачественную опухоль можно лечить с использованием ABP, в рамках изобретения. Иллюстративные подходящие злокачественные опухоли включают, например, острый лимфобластный лейкоз (ALL), острый миелоидный лейкоз (AML), адренокортикальную карциному, злокачественную опухоль анального канала, злокачественную опухоль аппендикса, астроцитому, базальноклеточную карциному, опухоль головного мозга, злокачественную опухоль желчных протоков, рак мочевого пузыря, рак кости, рак молочной железы, бронхиальную опухоль, карциному неизвестного первичного происхождения, опухоль сердца, рак шейки матки, хордому, рак толстого кишечника, колоректальный рак, краниофарингиому, карциному протоков, эмбриональную опухоль, рак эндометрия, эпендимому, рак пищевода, эстезионейробластому, фиброзную гистиоцитому, саркому Юинга, офтальмологическую злокачественную опухоль, опухоль из зародышевых клеток, рак желчного пузыря, рак желудка, карциноидную опухоль желудочно-кишечного тракта, стромальную опухоль желудочно-кишечного тракта, гестационную трофобластическую опухоль, глиому, рак головы и шеи, печеночноклеточную злокачественную опухоль, гистиоцитоз, лимфому Ходжкина, гипофарингеальную злокачественную опухоль, внутриглазную меланому, опухоль островков поджелудочной железы, саркому Капоши, рак почки, лангергансоклеточный гистиоцитоз, злокачественную опухоль гортани, злокачественную опухоль губ и полости рта, рак печени, лобулярную карциному in situ, рак легкого, макроглобулинемию, злокачественную фиброзную гистиоцитому, меланому, карциному из клеток Меркеля, мезотелиому, клинически неидентифицированную метастазирующую первичную плоскоклеточную карциному шеи, карциному срединной линии с вовлечением гена NUT, злокачественную опухоль полости рта, синдром множественной эндокринной неоплазии, множественную миелому, фунгоидный микоз, миелодиспластический синдром, миелодиспластическую/миелопролиферативную неоплазию, злокачественную опухоль носовой полости и околоносовых пазух, злокачественную опухоль носоглотки, нейробластому, немелкоклеточный рак легкого, злокачественную опухоль ротоглотки, остеосаркому, рак яичника, рак поджелудочной железы, папилломатоз, параганглиому, рак паращитовидной железы, рак полового члена, злокачественную опухоль глотки, феохромоцитомы, опухоль гипофиза, плевролегочную бластому, первичную лимфому центральной нервной системы, рак предстательной железы, рак прямой кишки, почечноклеточный рак, злокачественную опухоль почечной лоханки и мочеточника, ретинобластому, рабдоидную опухоль, злокачественную опухоль слюнных желез, синдром Сезари, рак кожи, мелкоклеточный рак легкого, рак тонкого кишечника, саркому мягких тканей, опухоль спинного мозга, рак желудка, T-клеточную лимфому, тератоидную опухоль, рак яичка, злокачественную опухоль горла, тимому и карциному тимуса, рак щитовидной железы, злокачественную опухоль мочеиспускательного канала, рак тела матки, рак влагалища, рак вульвы и опухоль Вильмса.
[346] В некоторых вариантах осуществления, настоящее изобретение относится к способу лечения заболевания или состояния у нуждающегося в этом субъекта посредством введения эффективного количества ABP, в рамках изобретения, субъекту. В некоторых аспектах, заболевание или состояние представляет собой злокачественную опухоль.
[347] В некоторых вариантах осуществления, настоящее изобретение относится к способу мультимеризации GITR в клетке-мишени нуждающегося в этом субъекта посредством введения эффективного количества ABP, в рамках изобретения, субъекту.
[348] В некоторых вариантах осуществления, настоящее изобретение относится к способу агонизма GITR в клетке-мишени нуждающегося в этом субъекта посредством введения эффективного количества ABP, в рамках изобретения, субъекту. В некоторых аспектах, агонизм GITR посредством ABP, в рамках изобретения, приводит к увеличенной секреции IL-2Rα, IL-2, IL-8 и/или IFNγ клеткой-мишенью.
[349] В некоторых вариантах осуществления, настоящее изобретение относится к способу модуляции активности NF-κB в клетке-мишени нуждающегося в этом субъекта посредством введения эффективного количества ABP, в рамках изобретения, субъекту.
[350] В некоторых вариантах осуществления, настоящее изобретение относится к способу модуляции деградации IκB в клетке-мишени нуждающегося в этом субъекта посредством введения эффективного количества ABP, в рамках изобретения, субъекту.
[351] В некоторых вариантах осуществления, настоящее изобретение относится к способу активации пути MAPK в клетке-мишени нуждающегося в этом субъекта посредством введения эффективного количества ABP, в рамках изобретения, субъекту. В некоторых аспектах, компоненты пути MAPK, активируемые посредством ABP, в рамках изобретения, включают один или несколько из p38, JNK и ERK.
[352] В некоторых вариантах осуществления, настоящее изобретение относится к способу увеличения пролиферации, выживаемости и/или функции эффекторной T-клетки у нуждающегося в этом субъекта посредством введения эффективного количества ABP, в рамках изобретения, субъекту. В некоторых аспектах эффекторная T-клетка представляет собой CD4+ эффекторную T-клетку. В некоторых аспектах, эффекторная T-клетка представляет собой CD8+ эффекторную T-клетку.
[353] В некоторых вариантах осуществления, настоящее изобретение относится к способу прекращения супрессии эффекторной T-клетки посредством регуляторной T-клетки у нуждающегося в этом субъекта посредством введения эффективного количества ABP, в рамках изобретения, субъекту. В некоторых аспектах, регуляторная T-клетка представляет собой CD4+CD25+Foxp3+ регуляторную T-клетку. В некоторых аспектах, регуляторная T-клетка представляет собой CD8+CD25+ регуляторную T-клетку.
[354] В некоторых вариантах осуществления, настоящее изобретение относится к способу изменения частоты встречаемости или распределения или регуляторные T-клетки у нуждающегося в этом субъекта посредством введения эффективного количества ABP, в рамках изобретения, субъекту. В некоторых аспектах, частота регуляторных T-клеток уменьшена. В некоторых аспектах, частота регуляторных T-клеток уменьшена в конкретной ткани. В некоторых аспектах, накопление регуляторных T-клеток внутри опухоли уменьшено, что приводит к более благоприятному соотношению эффекторных T-клеток к регуляторным T-клеткам, и к усилению активности CD8+ T-клеток.
[355] В некоторых вариантах осуществления, настоящее изобретение относится к способу увеличения активности клетки естественного киллера (NK) у нуждающегося в этом субъекта посредством введения эффективного количества ABP, в рамках изобретения, субъекту.
[356] В некоторых вариантах осуществления, настоящее изобретение относится к способу увеличения активности дендритной клетки у нуждающегося в этом субъекта посредством введения эффективного количества ABP, в рамках изобретения, субъекту.
[357] В некоторых вариантах осуществления, настоящее изобретение относится к способу увеличения активности B-клетки у нуждающегося в этом субъекта посредством введения эффективного количества ABP, в рамках изобретения, субъекту.
[358] В некоторых вариантах осуществления, настоящее изобретение относится к способу усиления иммунного ответа у нуждающегося в этом субъекта посредством введения эффективного количества ABP, в рамках изобретения, субъекту.
[359] В некоторых вариантах осуществления, настоящее изобретение относится к способу задержки начала развития опухоли у нуждающегося в этом субъекта посредством введения эффективного количества ABP, в рамках изобретения, субъекту.
[360] В некоторых вариантах осуществления, настоящее изобретение относится к способу задержки начала развития злокачественной опухоли у нуждающегося в этом субъекта посредством введения эффективного количества ABP, в рамках изобретения, субъекту.
[361] В некоторых вариантах осуществления, настоящее изобретение относится к способу уменьшения размера опухоли у нуждающегося в этом субъекта посредством введения эффективного количества ABP, в рамках изобретения, субъекту.
[362] В некоторых вариантах осуществления, настоящее изобретение относится к способу уменьшения количества метастазов у нуждающегося в этом субъекта посредством введения эффективного количества ABP, в рамках изобретения, субъекту.
Способы комбинированной терапии
[363] В некоторых вариантах осуществления, ABP, в рамках изобретения, вводят по меньшей мере с одним дополнительным лекарственным средством. Любое подходящее дополнительное лекарственное средство можно вводить с ABP, в рамках изобретения. В некоторых аспектах, дополнительное лекарственное средство выбрано из радиоактивного облучения, цитотоксического средства, химиотерапевтического средства, цитостатического средства, противогормонального средства, ингибитора EGFR, иммуностимулирующего средства, антиангиогенного средства и их комбинаций.
[364] В некоторых вариантах осуществления, дополнительное лекарственное средство содержит иммуностимулирующее средство.
[365] В некоторых вариантах осуществления, иммуностимулирующее средство представляет собой средство, блокирующее передачу сигналов ингибирующим рецептором иммуноцита или его лигандом. В некоторых аспектах, ингибирующий рецептор или лиганд выбран из CTLA-4, PD-1, PD-L1, NRP-1, LAG-3, Tim3, TIGIT, невритина, BTLA, KIR и их комбинаций. В некоторых аспектах, средство выбрано из пембролизумаба (антитела против PD-1), ниволумаба (антитела против PD-1), атезолизумаба (антитела против PD-L1), ипилимумаба (антитела против CTLA-4, и их комбинаций.
[366] В некоторых вариантах осуществления, иммуностимулирующее средство представляет собой агонист костимулирующего рецептора иммуноцита. В некоторых аспектах, костимулирующий рецептор выбран из OX40, ICOS, CD27, CD28, 4-1BB или CD40. В некоторых вариантах осуществления, агонист представляет собой антитело.
[367] В некоторых вариантах осуществления, иммуностимулирующее средство представляет собой цитокин. В некоторых аспектах, цитокин выбран из IL-2, IL-5, IL-7, IL-12, IL-15, IL-21 и их комбинаций.
[368] В некоторых вариантах осуществления, иммуностимулирующее средство представляет собой онколитический вирус. В некоторых аспектах, онколитический вирус выбран из вируса простого герпеса, вируса везикулярного стоматита, аденовируса, вируса болезни Ньюкасла, вируса осповакцины и вируса Мараба.
[369] В некоторых вариантах осуществления, иммуностимулирующее средство представляет собой T-клетку с химерным рецептором антигена (CAR-T-клетку). В некоторых вариантах осуществления, иммуностимулирующее средство представляет собой би- или мультиспецифическое нацеленное на T-клетку антитело. В некоторых вариантах осуществления, иммуностимулирующее средство представляет собой антитело против TGF-β. В некоторых вариантах осуществления, иммуностимулирующее средство представляет собой ловушку TGF-β.
[370] В некоторых вариантах осуществления, дополнительное лекарственное средство представляет собой вакцину против антигена опухоли. Вакцина может быть нацелена на любой подходящий антиген, при условии, что он присутствует в опухоли, подвергаемой лечению способами, в рамках изобретения. В некоторых аспектах, антиген опухоли представляет собой антиген опухоли, сверхэкспрессированный по сравнению с его уровнями экспрессии в нормальной ткани. В некоторых аспектах, антиген опухоли выбран из раково-тестикулярного антигена, антигена дифференцировки, NY-ESO-1, MAGE-A1, MART и их комбинаций.
[371] Дополнительные примеры дополнительны лекарственных средств включают таксан (например, паклитаксел или доцетаксел); средство на основе платины (например, карбоплатин, оксалиплатин, и/или цисплатин); ингибитор топоизомеразы (например, иринотекан, топотекан, этопозид и/или митоксантрон); фолиновую кислоту (например, лейковорин); или нуклеозидный ингибитор метаболизма (например, фторурацил, капецитабин и/или гемцитабин). В некоторых вариантах осуществления, дополнительное лекарственное средство представляет собой фолиновую кислоту, 5-фторурацил и/или оксалиплатин. В некоторых вариантах осуществления, дополнительное лекарственное средство представляет собой 5-фторурацил и иринотекан. В некоторых вариантах осуществления, дополнительное лекарственное средство представляет собой таксан и средство на основе платины. В некоторых вариантах осуществления, дополнительное лекарственное средство представляет собой паклитаксел и карбоплатин. В некоторых вариантах осуществления, дополнительное лекарственное средство представляет собой пеметрексат. В некоторых вариантах осуществления, дополнительное лекарственное средство представляет собой направленное лекарственное средство, такое как средство, нацеленное на EGFR, RAF или MEK.
[372] Дополнительное лекарственное средство можно вводить любыми подходящими способами. В некоторых вариантах осуществления, ABP, в рамках изобретения, и дополнительное лекарственное средство включены в одну и ту же фармацевтическую композицию. В некоторых вариантах осуществления, ABP, в рамках изобретения, и дополнительное лекарственное средство включены в различные фармацевтические композиции.
[373] В вариантах осуществления, когда ABP, в рамках изобретения, и дополнительное лекарственное средство включены в различные фармацевтические композиции, введение ABP можно осуществлять до, во время и/или после введения дополнительного лекарственного средства. В некоторых аспектах, введение ABP, в рамках изобретения, и дополнительного лекарственного средства осуществляют в пределах приблизительно одного месяца друг от друга. В некоторых аспектах, введение ABP, в рамках изобретения, и дополнительного лекарственного средства осуществляют в пределах приблизительно одной недели друг от друга. В некоторых аспектах, введение ABP, в рамках изобретения, и дополнительного лекарственного средства осуществляют в пределах приблизительно одних суток друг от друга. В некоторых аспектах, введение ABP, в рамках изобретения, и дополнительного лекарственного средства осуществляют в пределах приблизительно двенадцати часов друг от друга. В некоторых аспектах, введение ABP, в рамках изобретения, и дополнительного лекарственного средства осуществляют в пределах приблизительно одного часа друг от друга.
Диагностические способы
[374] Настоящее изобретение относится также к способам детекции присутствия GITR на клетках от субъекта. Такие способы можно использовать, например, для прогнозирования и оценки способности отвечать на лечение ABP, в рамках изобретения.
[375] В некоторых вариантах осуществления, образец крови получают от субъекта, и определяют фракцию клеток, экспрессирующих GITR. В некоторых аспектах, определяют относительное количество GITR, экспрессированного такими клетками. фракцию клеток, экспрессирующих GITR и относительное количество GITR, экспрессированного такими клетками, можно определять любым подходящим способом. В некоторых вариантах осуществления, проточную цитометрию используют для проведения таких измерений. В некоторых вариантах осуществления, активированную флуоресценцией сортировку клеток (FACS) представляет используют для проведения такого измерения. См. в Li et al., J. Autoimmunity, 2003, 21:83-92 способы оценки экспрессии GITR в периферической крови.
Наборы
[376] Настоящее изобретение относится также к наборам, содержащим ABP. Наборы можно использовать для лечения, предотвращения и/или диагностики заболевания или нарушения, как описано в настоящем описании.
[377] В некоторых вариантах осуществления, набор содержит контейнер и этикетку или листовку-вкладыш на контейнере или приложенные к контейнеру. Подходящие контейнеры включают, например, флаконы, ампулы, шприцы и пакеты для IV раствора. Контейнеры можно изготавливать из множества материалов, таких как стекло или пластик. Контейнер содержит композицию, которая, самостоятельно или в комбинации с другой композицией, является эффективной для лечения, предотвращения и/или диагностики заболевания или нарушения. Контейнер может иметь стерильное отверстие для доступа. Например, если контейнер может представляет собой пакет или флакон с раствором для внутривенного введения, он может иметь выход, который можно прокалывать иглой. По меньшей мере один действующее вещество в композиции представляет собой ABP, в рамках изобретения. На этикетке или в листовке-вкладыше указано, что композицию используют для лечения выбранного состояния.
[378] В некоторых вариантах осуществления, набор содержит (a) первый контейнер с содержащейся в нем первой композицией, где первая композиция содержит ABP, в рамках изобретения; и (b) второй контейнер с содержащейся в нем второй композицией, где вторая композиция содержит дополнительное лекарственное средство. Набор в этом варианте осуществления изобретения может дополнительно содержать листовку-вкладыш, где указано, что композицию можно использовать для лечения конкретного состояния.
[379] Альтернативно или дополнительно, набор может дополнительно содержать второй (или третий) контейнер, содержащий фармацевтически приемлемый наполнитель. В некоторых аспектах, наполнитель представляет собой буфер. Набор может дополнительно включать другие материалы, желательные с коммерческой и пользовательской точки зрения, включая фильтры, иглы и шприцы.
Другие иллюстративные варианты осуществления
[380] Варианты осуществления, представленные ниже, не являются ограничивающими и представлены с целью иллюстрации конкретных вариантов осуществления и аспектов изобретения, в дополнение к описанным на протяжении этого описания.
[381] Вариант осуществления 1: ABP, который специфически связывает GITR человека и/или комплекс GITR человека и является способным по меньшей мере один к одному из следующего: a) проявляет перекрестную конкуренцию с GITRL за связывание с GITR; b) может подвергаться интернализации в клетку человека; c) ингибирует супрессию эффекторной T-клетки; d) подавляет ингибирование эффекторных T-клеток регуляторными T-клетками; e) уменьшает количество регуляторных T-клеток в тканях или в кровотоке; f) активирует эффекторную T-клетку; g) осуществляет ассоциацию GITR в комплекс GITR; h) модулирует активность GITR человека и/или комплекса GITR.
[382] Вариант осуществления 2: ABP из варианта осуществления 1, где ABP имеет одну или несколько из следующих характеристик: a) представляет собой моноклональное антитело; b) представляет собой человеческое антитело, гуманизированное антитело или химерное антитело; c) представляет собой мультиспецифическое или мультивалентное антитело, например, тетравалентное антитело; d) содержит по меньшей мере один Fab на N-конце или C-конце; e) принадлежит к типу IgG1, IgG2, IgG3 или IgG4; f) представляет собой антигенсвязывающий фрагмент антитела; g) представляет собой фрагмент Fab, фрагмент Fab', фрагмент F(ab')2 или фрагмент Fv; h) представляет собой биспецифическое антитело, диатело, одноцепочечное антитело, однодоменное антитело, доменное антитело VH или нанотело.
[383] Вариант осуществления 3: ABP из варианта осуществления 1, где ABP имеет одну или несколько из следующих характеристик: a) связывает полипептид GITR человека из SEQ ID NO: 1-2 или его вариант, или как иным образом описано в настоящем описании, с KD менее, чем приблизительно 20 нМ; или b) связывает полипептид GITR яванского макака из SEQ ID NO: 3 или его вариант, или как иным образом описано в настоящем описании, с KD менее, чем приблизительно 200 нМ.
[384] Вариант осуществления 4: ABP из варианта осуществления 1, содержащий первый антигенсвязывающий домен, который специфически связывает первый домен узнавания антитела на GITR человека и второй антигенсвязывающий домен, который специфически связывает второй домен узнавания антитела на GITR человека, где первый домен узнавания антитела и второй домен узнавания антитела не являются идентичными.
[385] Вариант осуществления 5: ABP из варианта осуществления 4, содержащий биспецифический связывающий белок в формате, выбранном из группы, состоящей из молекулы DVD-Ig™, молекулы BiTe®, молекулы DART™, молекулы DuoBody®, молекулы scFv/диатела-IgG, молекулы с перекрестной мультиспецифичностью, биспецифической молекулы 2-в-1, мультиспецифической молекулы типа выступ-во-впадину, молекулы Fab+IgG, молекулы CovX-Body, молекулы аффитела, биспецифической молекулы scFv/диатело-CH2/CH3, мультиспецифической молекулы на основе IgG-не относящегося к Ig белкового каркаса, молекулы финомера®, молекулы Fcab™, TandAb®, Zybody™ и биспецифической молекулы scFV/диатела, связанного с нормальным белком человека, подобным человеческому сывороточному альбумину.
[386] Вариант осуществления 6: ABP из варианта осуществления 4, где первый антигенсвязывающий домен имеет KD менее, чем приблизительно 20 нМ и способен проявлять агонизм к GITR человека, и где второй антигенсвязывающий домен имеет KD менее, чем приблизительно 100 нМ.
[387] Вариант осуществления 7: ABP, конкурирующий или способный к конкуренции за связывание с GITR человека с эталонным ABP, где эталонный ABP представляет собой ABP из варианта осуществления 1.
[388] Вариант осуществления 8: ABP из варианта осуществления 7, где ABP и эталонное антитело проявляют перекрестную конкуренцию или являются способными к перекрестной конкуренции за связывание с GITR человека.
[389] Вариант осуществления 9: ABP из варианта осуществления 1, содержащий константную область тяжелой цепи, содержащую человеческую константную область тяжелой цепи или ее фрагмент или вариант, где вариант константной области содержит вплоть до 20 модифицированных аминокислотных замен, где от 0 до вплоть до 20 модифицированных аминокислотных замен представляют собой консервативные аминокислотные замены.
[390] Вариант осуществления 10: ABP из варианта осуществления 1, конкурирующий или способный к конкуренции за связывание с GITRL человека с белком GITR.
[391] Вариант осуществления 11: ABP из варианта осуществления 1, способный к активации передачи сигналов GITR не зависимым от лиганда образом.
[392] Вариант осуществления 12: ABP из варианта осуществления 1, способный к усилению зависимого от лиганда связывания GITR и GITRL.
[393] Вариант осуществления 13: Фармацевтическая композиция, содержащая ABP из любого из вариантов осуществления 1-12 в фармацевтически приемлемом носителе.
[394] Вариант осуществления 14: Биспецифическое антитело, содержащее первый антигенсвязывающий домен, который специфически связывает первый домен узнавания антитела на GITR человека и второй антигенсвязывающий домен, который специфически связывает второй домен узнавания антитела на GITR человека, где первый домен узнавания антитела и второй домен узнавания антитела не являются идентичными.
[395] Вариант осуществления 15: Биспецифическое антитело из варианта осуществления 14, где первый домен узнавания антитела и второй домен узнавания антитела присутствуют в внеклеточном домене GITR человека.
[396] Вариант осуществления 16: Биспецифическое антитело из варианта осуществления 14, где первый домен узнавания антитела и второй домен узнавания антитела являются способными осуществлять ассоциацию по меньшей мере двух белков GITR человека в функциональный комплекс.
[397] Вариант осуществления 17: Комплексообразующий ABP, содержащий первый антигенсвязывающий домен, который специфически связывает первый домен узнавания антитела на белке GITR человека или на комплексе GITR человека, содержащем по меньшей мере два белка GITR, и является способным по меньшей мере к одному из следующего: a) проявляет перекрестную конкуренцию с GITRL за связывание с GITR; b) может подвергаться интернализации в клетку человека; c) ингибирует супрессию эффекторной T-клетки; d) подавляет ингибирование эффекторных T-клеток регуляторными T-клетками; e) уменьшает количество регуляторных T-клеток в тканях или в кровотоке; f) активирует эффекторную T-клетку; g) осуществляет ассоциацию GITR в комплекс GITR; h) модулирует активность GITR человека и/или комплекса GITR.
[398] Вариант осуществления 18: Выделенная нуклеиновая кислота, кодирующая ABP по любому из вариантов осуществления 1-12 или биспецифическое антитело по любому из вариантов осуществления 14-16, или комплексообразующий ABP из варианта осуществления 17.
[399] Вариант осуществления 19: Экспрессирующий вектор, содержащий нуклеиновую кислоту в соответствии с вариантом осуществления 18.
[400] Вариант осуществления 20: Прокариотическая или эукариотическая клетка-хозяин, содержащая вектор из варианта осуществления 19.
[401] Вариант осуществления 21: Способ получения рекомбинантного белка, включающий стадии экспрессии нуклеиновой кислоты из варианта осуществления 18 в прокариотической или эукариотической клетке-хозяине и выделения указанного белка из указанной клетки или супернатанта культуры клеток.
[402] Вариант осуществления 22: Способ лечения субъекта, страдающего злокачественной опухолью или воспалительным заболеванием, включающий стадию введения субъекту фармацевтической композиции, содержащей ABP по любому из вариантов осуществления 1-12 или биспецифическое антитело по любому из вариантов осуществления 14-16, или комплексообразующий ABP из варианта осуществления 17.
[403] Вариант осуществления 23: Способ индукции или усиления иммунного ответа у субъекта, включающий стадию введения субъекту фармацевтической композиции, содержащей ABP по любому из вариантов осуществления 1-12 или биспецифическое антитело по любому из вариантов осуществления 14-16, или комплексообразующий ABP из варианта осуществления 17, где иммунный ответ вызывают против антигена опухоли.
[404] Вариант осуществления 24: Способ из варианта осуществления 23, где ABP, биспецифическое антитело или комплексообразующий ABP вводят в количестве, достаточном для достижения одного или нескольких из следующего у субъекта: a) уменьшения супрессии активности эффекторных T-клеток регуляторными T-клетками; b) уменьшения уровней регуляторных T-клеток; c) активации эффекторных T-клеток; d) индукции или усиления пролиферации эффекторных T-клеток; e) замедления скорости роста опухоли; и f) индукции регрессии опухоли.
[405] Вариант осуществления 25: Способ из варианта осуществления 22, где злокачественная опухоль представляет собой солидную опухоль.
[406] Вариант осуществления 26: Способ из варианта осуществления 22, где злокачественная опухоль представляет собой гематологическую опухоль.
[407] Вариант осуществления 27: Способ по любому из вариантов осуществления 22-26, где способ дополнительно включает одно или несколько из следующего a) проведения химиотерапии; b) проведения радиотерапии; или c) введения одного или нескольких дополнительных лекарственных средств.
[408] Вариант осуществления 28: Способ из варианта осуществления 27, где дополнительное лекарственное средство содержит иммуностимулирующее средство.
[409] Вариант осуществления 29: Способ из варианта осуществления 27, где иммуностимулирующее средство содержит антагонист ингибирующего рецептора иммуноцита.
[410] Вариант осуществления 30: Способ из варианта осуществления 29, где ингибирующий рецептор содержит CTLA-4, PD-1, PD-L1, LAG-3, Tim3, TIGIT, невритин, BTLA или KIR, или его функциональный фрагмент.
[411] Вариант осуществления 31: Способ из варианта осуществления 27, где иммуностимулирующее средство содержит агонист костимулирующего рецептора иммуноцита, или его функциональный фрагмент.
[412] Вариант осуществления 32: Способ из варианта осуществления 31, где костимулирующий рецептор содержит OX40, ICOS, CD27, CD28, 4-1BB или CD40.
[413] Вариант осуществления 33: Способ из варианта осуществления 27, где иммуностимулирующее средство содержит цитокин.
[414] Вариант осуществления 34: Способ из варианта осуществления 27, где цитокин содержит IL-2, IL-5, IL-7, IL-12, IL-15 или IL-21.
[415] Вариант осуществления 35: Способ из варианта осуществления 27, где иммуностимулирующее средство содержит онколитический вирус.
[416] Вариант осуществления 36: Способ из варианта осуществления 35, где онколитический вирус содержит вирус простого герпеса, вирус везикулярного стоматита, аденовирус, вирус болезни Ньюкасла, вирус осповакцины или вирус Мараба.
[417] Вариант осуществления 37: Способ из варианта осуществления 27, где иммуностимулирующее средство содержит T-клетку со сконструированным химерным антигеном.
[418] Вариант осуществления 38: Способ из варианта осуществления 27, где иммуностимулирующее средство содержит би- или мультиспецифическое нацеленное на T-клетку антитело.
[419] Вариант осуществления 39: Способ из варианта осуществления 27, где дополнительное лекарственное средство содержит антитело против TGF-β или ловушку рецептора TGF-β.
[420] Вариант осуществления 40: Способ по любому из вариантов осуществления 22-39, где введение фармацевтической композиции приводит к индукции или усилению пролиферации эффекторной T-клетки, или I-каппаB и/или NF-κB в T-клетке, или к модуляции активности GITR в T-клетке, или к индуцированной T-клеточным рецептором передаче сигналов в эффекторной T-клетке, или к их комбинации.
[421] Вариант осуществления 41: Способ скрининга тестируемых соединений, содержащих ABP по любому из вариантов осуществления 1-12, способных ингибировать взаимодействие GITRL с комплексом GITR, включающий стадии: приведения образца, содержащего GITRL и комплекс GITR, в контакт с соединением; и определения того, уменьшено ли взаимодействие GITRL с комплексом GITR в образце, по сравнению с взаимодействием GITRL с комплексом GITR в образце, не приводимом в контакт с соединением, на основании чего по уменьшению взаимодействия GITRL с GITR в образце, приводимом в контакт с соединением, идентифицируют соединение как соединение, ингибирующее взаимодействие GITRL с комплексом GITR.
ПРИМЕРЫ
[422] Ниже приведены примеры способов и композиций по изобретению. Понятно, что различные другие варианты осуществления можно осуществлять на практике, принимая во внимание общее описание, представленное в настоящем описании.
Пример 1: Отбор антигенсвязывающих белков против GITR
Материалы и способы
Антигены биотинилировали с использованием набора для сульфо-NHS-биотинилирования EZ-Link® от Pierce. Антитело козы F(ab')2 против каппа человека с FITC (LC-FITC), экстравидин®-PE (EA-PE) и стрептавидин-AF633 (SA-633) получены из Southern Biotech, Sigma, и Molecular Probes, соответственно. MicroBeads® с стрептавидином и колонки для разделения MACS LC закупали из Miltenyi Biotec. Антитело козы против IgG человека с PE (Human-PE) получено из Southern Biotech.
Исследование наивной библиотеки
Восемь наивных человеческих синтетических библиотек в дрожжах, каждая с разнообразием ~109, размножали, как описано ранее (См., например, Y. Xu et al, Addressing polyspecificity of antibodies selected from an in vitro yeast presentation system: a FACS-based, high-throughput selection and analytical tool. PEDS 26.10, 663-70 (2013); WO2009036379; WO2010105256; и WO2012009568.) Для первых двух циклов отбора, осуществляли способ сортировки на магнитных бусинах с использованием системы Miltenyi MACS, как описано ранее (См., например, Siegel et al, High efficiency recovery and epitope-specific sorting of an scFv yeast display library. J Immunol Methods 286(1-2), 141-153 (2004).) Кратко, клетки дрожжей (~1010 клеток/библиотеку) инкубировали с 5 мл 10 нМ биотинилированного слитого с Fc антигена в течение 30 мин при 30°C в буфере для промывки (фосфатно-солевой буфер (PBS)/0,1% бычий сывороточный альбумин (BSA)). После промывки один раз 40 мл ледяного буфера для промывки, осадок клеток ресуспендировали в 20 мл буфера для промывки, и бусины MicroBeads® с стрептавидином (500 мкл) добавляли к дрожжам и инкубировали в течение 15 мин при 4°C. Затем дрожжи осаждали, ресуспендировали в 20 мл буфера для промывки, и наносили на колонку Miltenyi LS. После нанесения 20 мл, колонку промывали 3 раза с использованием 3 мл буфера для промывки. Затем колонку убирали из магнитного поля, и дрожжи элюировали с использованием 5 мл сред для роста и затем выращивали в течение ночи. Следующие циклы отбора проводили с использованием проточной цитометрии. Приблизительно 2×107 дрожжей осаждали, промывали три раза буфером для промывки и инкубировали при 30°C либо с уменьшающимися концентрациями биотинилированного слитого с Fc антигена (10-1 нМ) в условиях равновесия, 10 нМ биотинилированных слитых с Fc антигенов различных видов для получения перекрестной реакционной способности видов, либо с полиспецифическим истощающим реагентом (PSR) для удаления неспецифических антител из отбора. Для истощения PSR, библиотеки инкубировали с разведением 1:10 биотинилированного реагента PSR, как описано ранее (См., например, Y. Xu et al, Addressing polyspecificity of antibodies selected from an in vitro yeast presentation system: a FACS-based, high-throughput selection and analytical tool. PEDS 26.10, 663-70 (2013).) Затем дрожжи промывали дважды буфером для промывки и окрашивали с использованием LC-FITC (разведенного 1:100) и либо SA-633 (разведенного 1:500), либо EAPE (разведенного 1:50) вторичных реагентов в течение 15 мин при 4°C. После промывки дважды буфером для промывки, осадки клеток ресуспендировали в 0,3 мл буфера для промывки и переносили в закрытые фильтром пробирки для сортировки. Сортировку проводили с использованием сортировщика FACS ARIA (BD Biosciences) и окна сортировки определяли для отбора антител с желательными характеристиками. Циклы отбора повторяли до получения популяции со всеми желательными характеристиками. После конечного цикла сортировки, дрожжи рассевали, и индивидуальные колонии отбирали для характеризации.
Оптимизация антител
Оптимизацию антител проводили способом диверсификации легкой цепи, и затем посредством введения разнообразия в вариабельные области тяжелой цепи и легкой цепи, как описано ниже. Комбинацию некоторых из этих способов использовали для каждого антитела.
Способ периодической диверсификации легких цепей: плазмиды с тяжелыми цепями, полученные на выходе отбора из наивной библиотеки, выделяли из дрожжей посредством разрушения и сбора, размножали в E.coli и впоследствии очищали из E.coli, и трансформировали в библиотеку легких цепей с разнообразием 5×106. Отборы проводили с использованием одного цикла MACS и четырех циклов FACS, с использованием таких же условий, как при исследовании наивной библиотеки.
Диверсификация легких цепей: Вариабельную область тяжелой цепи отдельного антитела амплифицировали посредством ПЦР и трансформировали, вместе с вектором для экспрессии тяжелой цепи, в библиотеку легких цепей с разнообразием 5×106. Отборы проводили с использованием одного цикла MACS и трех циклов FACS, с использованием таких же условий, как при исследовании наивной библиотеки. Для каждого цикла FACS библиотеки проверяли по связыванию PSR, перекрестной реакционной способности видов и аффинному давлению, и сортировку проводили для получения популяции с желательными характеристиками.
Отбор CDRH1 и CDRH2: CDRH3 отдельного антитела вводили способом рекомбинации в предварительно полученную библиотеку с вариантами CDRH1 и CDRH2 с разнообразием 1×108, и отборы проводили с использованием одного цикла MACS и четырех циклов FACS, как описано для исследования наивной библиотеки. Для каждого цикла FACS библиотеки проверяли по связыванию PSR, перекрестной реакционной способности видов и аффинному давлению, и сортировку проводили для получения популяции с желательными характеристиками. Для этих отборов аффинное давление прилагали посредством предварительной инкубации биотинилированного антигена с исходным IgG в течение 30 минут и затем добавления этой смеси с предварительно сформированными комплексами к библиотеке дрожжей на период времени, позволяющий достигать равновесия в смеси для отбора. Тогда получали возможность сортировки антител с более высокой аффинностью.
Отбор мутантных CDRH3/VH: Из IDT заказывали олигонуклеотиды («олиги»), содержащие CDRH3, также как фланкирующую область с каждой стороны от CDRH3. Положения аминокислот в кодирующей CDRH3 части олигонуклеотида меняли посредством разнообразия NNK. Олигонуклеотиды CDRH3 делали двухцепочечными с использованием праймеров, гибридизующихся с фланкирующей областью CDRH3. Оставшуюся часть вариабельной области тяжелой цепи подвергали мутагенезу посредством ПЦР с внесением ошибок для введения дополнительного разнообразия в не относящиеся к CDR3 области тяжелой цепи. Затем получали библиотеку посредством трансформации двухцепочечного олигонуклеотида CDRH3, подвергнутой мутагенезу остальной части вариабельной области тяжелой цепи и вектора для экспрессии тяжелой цепи в дрожжи, уже содержащие родительскую плазмиду с легкой цепью. Отборы проводили подобно предшествующим циклам, с использованием четырех циклов сортировки FACS. Для каждого цикла FACS библиотеки проверяли по связыванию PSR, перекрестной реакционной способности видов и аффинному давлению, и сортировку проводили для получения популяции с желательными характеристиками. Аффинное давление для этих отборов прилагали, как описано выше для отбора CDRH1 и CDRH2.
Отбор CDRL1, CDRL2 и CDRL3: Из IDT заказывали олигонуклеотиды, содержащие CDRL3, также как фланкирующую область с каждой стороны от CDRL3. Положения аминокислот в кодирующей CDRL3 части олигонуклеотида меняли посредством разнообразия NNK. Олигонуклеотиды CDRL3 делали двухцепочечными с использованием праймеров, гибридизующихся с фланкирующей областью CDRL3. Затем эти двухцепочечные олигонуклеотиды CDRL3 вводили способом рекомбинации в предварительно полученную библиотеку с вариантами CDRL1 и CDRL2 с разнообразием 3×105, и отборы проводили с использованием одного цикла MACS и четырех циклов FACS, как описано для исследования наивной библиотеки. Для каждого цикла FACS библиотеки проверяли по связыванию PSR, перекрестной реакционной способности видов и аффинному давлению, и сортировку проводили для получения популяции с желательными характеристиками. Аффинное давление для этих отборов прилагали, как описано выше для отбора CDRH1 и CDRH2.
Продукция и очистка антител
Клоны дрожжей выращивали до насыщения и затем подвергали индукции в течение 48 час при 30°C с встряхиванием. После индукции, клетки дрожжей осаждали, и супернатанты собирали для очистки. IgG очищали с использованием колонки с белком A и элюировали с использованием уксусной кислоты, pH 2,0. Фрагменты Fab получали посредством расщепления папаином и очищали с использованием KappaSelect® (GE Healthcare LifeSciences).
Измерения KD с использованием ForteBio
Измерения аффинности с использованием ForteBio® проводили в Octet® RED384, в основном, как описано ранее (См., например, Estep et al, High throughput solution-based measurement of antibody-antigen affinity and epitope binning. Mabs 5(2), 270-278 (2013)). Кратко, измерения аффинности с использованием ForteBio проводили посредством нанесения IgG в режиме управления компьютером на сенсоры AHQ. Сенсоры уравновешивали в автономном режиме в буфере для анализа в течение 30 мин, и затем мониторировали в режиме управления компьютером в течение 60 секунд для определения фона. Сенсоры с загруженными IgG подвергали воздействию 100 нМ антигена в течение 3 минут, и после этого переносили в буфер для анализа на 3 мин для измерения скорости диссоциации. Для оценки моновалентной аффинности использовали Fab вместо IgG. Для этой оценки, небиотинилированный слитый с Fc антиген наносили в режиме управления компьютером на сенсоры AHQ. Сенсоры уравновешивали в автономном режиме в буфере для анализа в течение 30 мин и затем мониторировали в режиме управления компьютером в течение 60 секунд для определения фона. Сенсоры с загруженным антигеном подвергали воздействию 200 нМ Fab в течение 3 минут, и после этого переносили в буфер для анализа на 3 мин для измерения скорости диссоциации. Всю кинетику анализировали с использованием модели связывания 1:1.
Группировка эпитопов/блокирование лиганда с использованием ForteBio
Группировку эпитопов/блокирование лиганда проводили с использованием стандартного анализа перекрестного блокирования в сэндвич-формате. Контрольное IgG против мишени наносили на сенсоры AHQ, и незанятые участки связывания Fc на сенсоре блокировали с использованием не относящегося к делу человеческого антитела IgG1. Затем сенсоры подвергали воздействию 100 нМ антигена-мишени, с последующим воздействием второго антитела против мишени или лиганда. Дополнительное связывание вторым антителом или лигандом после ассоциации антигена указывает на незанятый эпитоп (не конкурент), в то время как отсутствие связывания указывает на блокирование эпитопа (конкурент или блокирование лиганда).
Анализ связывания клеток
Приблизительно 100000 клеток, сверхэкспрессирующих антиген, промывали буфером для промывки и инкубировали с 100 мкл 100 нМ IgG в течение 5 минут при комнатной температуре. Затем клетки дважды промывали буфером для промывки и инкубировали с 100 мкл 1:100 Human-PE в течение 15 минут на льду. Затем клетки дважды промывали буфером для промывки и анализировали в анализаторе FACS Canto II (BD Biosciences.)
Эксклюзионная хроматография
Колонку TSKgel® SuperSW mAb HTP (22855) использовали для быстрого анализа SEC продуцированных млекопитающими mAb при 0,4 мл/мин со временем цикла 6 мин/цикл. 200 мМ фосфат натрия и 250 мМ хлорид натрия использовали в качестве подвижной фазы.
Динамическая сканирующая флуорометрия
10 мкл 20x Sypro Orange добавляют к 20 мкл раствора 0,2-1 мг/мл mAb или Fab. Устройство для RT-ПЦР (BioRad CFX96 RT PCR) используют для линейного изменения температуры планшета для образца от 40 до 95 C с шагом 0,5 C, с уравновешиванием 2 мин при каждой температуре. Отрицательную первую производную необработанных данных используют для выведения Tm.
Пример 2: Характеристики антител формата TM
Аффинность ABP формата IgG1 и TM для GITR из нескольких видов
[423] ABP GITR оценивали по их способности связывать рекомбинантный hGITR (SEQ ID NO: 1), hGITR-T43R (SEQ ID NO: 2), cGITR (SEQ ID NO: 3) и mGITR (SEQ ID NO: 4) с использованием устройства FORTEBIO® OCTET. Анализ проводили при 30°C, с использованием 1× кинетического буфера (ForteBio, Inc.) в качестве буфера для анализа. Биосенсоры для связывания против Fc IgG человека (AHC) (ForteBio, Inc.) использовали для связывания ABP GITR на сенсорах. Сенсоры уравновешивали в буфере для анализа в течение 600 секунд перед анализом. Фон устанавливали посредством погружения сенсоров в 1× буфер для анализа на 60 секунд. ABP загружали на сенсоры посредством погружения сенсоров в раствор ABP на 300 секунд. Фон устанавливали посредством погружения сенсоров в 1× буфер для анализа на 120 секунд. Реакцию на сенсорах останавливали посредством погружения в 200 мкг/мл IgG человека на 300 секунд для предотвращения неспецифического связывания антигенов GITR-Fc с сенсором. Фон устанавливали посредством погружения сенсоров в 1× буфер для анализа на 60 секунд. Затем связывание мониторировали в течение 300 секунд в 25 нМ рекомбинантных антигенах, и диссоциацию отслеживали в течение 1200 секунд только в буфере. KD определяли с использованием функции кинетики программного обеспечения для анализа FORTEBIO® с использованием модели связывания 1:1. Результаты показаны в таблице 5.
Таблица 5: KD ABP по OCTET с использованием кинетики для одной концентрации
[424] Другие ABP GITR оценивали по их способности связывать рекомбинантный hGITR и cGITR (SEQ ID NO: 3) с использованием устройства FORTEBIO® Octet RED384, в общем, как описано ранее (См., например, Estep et al, High throughput solution-based measurement of antibody-antigen affinity and epitope binning. Mabs 5(2), 270-278 (2013)). Биосенсоры AHQ (ForteBio, Inc.) использовали для связывания ABP GITR на сенсорах. Реакцию на сенсорах останавливали посредством погружения в неродственное антитело IgG1 человека для предотвращения неспецифического связывания антигенов GITR-Fc с сенсором. Сенсоры уравновешивали в буфере для анализа в течение 30 минут. Фон устанавливали посредством погружения сенсоров в буфер для анализа в течение 60 секунд. Связывание мониторировали в течение 180 секунд в 100 нМ рекомбинантных антигенах, и диссоциацию отслеживали в течение 180 секунд только в буфере. KD определяли с использованием функции кинетики программного обеспечения для анализа FORTEBIO® с использованием модели связывания 1:1. Результаты показаны в таблице 6.
Таблица 6: ABP KD по OCTET с использованием кинетики для одной концентрации
* неоптимизированный, не относящийся к TM ABP IgG1, соответствующий ABP в скобках
# H1H2-оптимизированный, не относящийся к TM ABP IgG1, соответствующий ABP в скобках
[425] Дополнительные измерения KD проводили для 8 антител формата TM с N-концевым Fab с использованием кинетики для множества концентраций. ABP GITR оценивали по их способности связывать рекомбинантный hGITR (SEQ ID NO: 1), hGITR-T43R (SEQ ID NO: 2) и cGITR (SEQ ID NO: 3) с использованием устройства FORTEBIO® OCTET. Анализ проводили при 30°C, с использованием 1× кинетического буфера (ForteBio, Inc.) в качестве буфера для анализа. Биосенсоры для связывания против Fc IgG человека (AHC) (ForteBio, Inc.) использовали для связывания ABP GITR на сенсорах. Сенсоры насыщали в буфере для анализа в течение 600 секунд перед анализом. Фон устанавливали посредством погружения сенсоров в 1× буфер для анализа на 60 секунд. ABP загружали на сенсоры посредством погружения сенсоров в раствор ABP на 300 секунд. Фон устанавливали посредством погружения сенсоров в 1× буфер для анализа на 120 секунд. Затем связывание мониторировали в течение 300 секунд при различных концентрациях рекомбинантных антигенов (50 нМ - 0,78 нМ, 2-кратные разведения в буфере для анализа), и диссоциацию отслеживали в течение 600 или 1200 секунд только в буфере. KD определяли с использованием функции кинетики программного обеспечения для анализа FORTEBIO® с использованием модели связывания 1:1. Результаты определения KD посредством OCTET показаны на ФИГ.2 и в таблице 7. Как можно видеть на фигуре, каждая из KD для GITR человека составляла менее 1нМ, и KD для GITR яванского макака находятся в пределах 15-кратных KD для человека. Кроме того, антитела формата TM связывают вариант GITR человека с SNP T43R.
Таблица 7. Характеристики связывания ABP формата TM с N-концевым Fab
KD (M), n=3
KD (M), n=1
KD (M), n=3
Анализы связывания GITR
[426] Мононуклеарные клетки периферической крови (PBMC) культивировали в среде для роста в присутствии фитогемагглютинина (PHA) в течение 5 суток при 37°C для повышающей регуляции экспрессии GITR. T-клетки собирали и промывали, и затем инкубировали при 4°C с одним из восьми ABP GITR формата TM или контрольным антителом для изотипа человека. После промывки, клетки инкубировали при 4°C с конъюгированным с флуорохромом антителом против CD4 человека и антителом против CD8 человека, так же как с конъюгированным с флуорохромом антителом против IgG человека для детекции связанного ABP против GITR человека. Процент GITR+ CD4 и CD8 клеток, так же как среднюю интенсивность флуоресценции (MFI) определяют посредством проточной цитометрии.
[427] Иллюстративные результаты показаны на ФИГ. 3. На фигуре 3A показаны CD4+ клетки, и на фигуре 3B показаны CD8+ клетки. В верхнем ряду, слева направо, показан положительный контроль против GITR и контроль изотипа против IgG4 человека, и ABP формата TM с N-концевым Fab ABP9, ABP2, ABP1, и ABP7. В нижнем ряду показаны ABP8, ABP3, ABP4, ABP5, ABP6, ABP23 и ABP24. Указан процент IgG4+ CD4/8+ клеток.
[428] Связывание с GITR человека, яванского макака и мыши на поверхности клеток оценивают посредством трансфекции клеток HT1080, CHO или 293T-с использованием соответствующего GITR (человека, яванского макака или мыши). Связывание с GITR яванского макака дополнительно оценивают с использованием первичных T-клеток яванского макака и линии T-клеток HSC-F, каждые после стимуляции с использованием антитела против CD3, для увеличения экспрессии GITR.
Анализы активности антигенсвязывающих белков для GITR
[429] ABP GITR тестировали по их способности выступать в роли агониста GITR. В одном анализе, клетки HT1080, стабильно экспрессирующие GITR человека или яванского макака, приводили в контакт с ABP GITR формата TM или тримерным GITRL человека. Через 24 часа, количество IL-8, секретированного клетками, оценивали посредством анализа ELISA. Увеличенная секреция IL-8 соответствует увеличению агонизма GITR. Результаты для антител 1-8 формата TM с N-концевым Fab показаны на ФИГ. 4. Показан выход IL-8 на основании концентрации антитела или лиганда для ABP1 (ФИГ. 4A), ABP2 (ФИГ. 4B), ABP3 (ФИГ. 4C), ABP4 (ФИГ. 4D), ABP5 (ФИГ. 4E), ABP6 (ФИГ. 4F), ABP7 (ФИГ. 4G) и ABP8 (FIG 4H). Антитела показаны как круги на ФИГ., и контроль GITRL показан как квадраты. Значения EC50 сравнивают с значениями для лиганда GITR (GITRL).
[430] Таблица 8. Агонистическая активность антител формата TM по отношению к GITR человека и яванского макака на клетках HT1080
[431] Такой же анализ проводили с использованием не относящихся к TM вариантов ABP 1-8 из IgG1 N297A (См. ФИГ. 4), и данные обобщены в таблице 9.
Таблица 9. Активность антител IgG1 N297A по отношению к GITR человека и яванского макака на клетках HT1080
[432] Анализ снова использовали для тестирования активности дополнительный антител формата TM с N-концевым Fab и с C-концевым Fab, так же как вариантов IgG1 N297A этих антител. Данные обобщены в таблице 10 и таблице 11, и показаны на ФИГ. 5. На ФИГ. 5A показаны ABP43 (квадраты), ABP23 (круги), ABP24 (треугольники) и ABP29 (незакрашенные круги), ABP30 (незакрашенные треугольники), ABP31 (незакрашенные круги) и ABP32 (незакрашенные треугольники), все по сравнению с GITRL (знак +). На ФИГ. 5B показаны ABP19 (N-концевой Fab, треугольники) и ABP25 (C-концевой Fab, перевернутые треугольники). GITRL показан как знаки плюс. На ФИГ. 5C показаны ABP21 (N-концевой Fab, треугольники) и ABP27 (C-концевой Fab, перевернутые треугольники). GITRL показан как знаки плюс. На ФИГ. 5D показаны ABP20 (N-концевой Fab, треугольники) и ABP26 (C-концевой Fab, перевернутые треугольники). GITRL показан как знаки плюс. На ФИГ. 5E показаны ABP22 (N-концевой Fab, треугольники) и ABP28 (C-концевой Fab, перевернутые треугольники). GITRL показан как знаки плюс. Как показано на ФИГ., ABP формата с N-концевым Fab проявляли тенденцию к индукции большего уровня IL-8, чем их эквиваленты с C-концевым Fab.
[433] На ФИГ. 10 показано дополнительное сравнение ABP43 (неоптимизированного формата IgG4) с двумя соответствующими ABP формата TM, где эквивалент Fab IgG1 ABP43 добавлен к N- или C-концу ABP43. Как можно видеть на фигуре, ABP9 формата TM с N-концевым Fab (квадраты) индуцировал наибольший уровень IL-8 (и имел наилучшую EC50) по сравнению с ABP10 формата TM с C-концевым Fab (круги) и ABP43, не относящимся к формату TM (ромбы). Оба ABP формата TM имели лучшую активность, чем исходный ABP, не относящийся к формату TM, так же как GITRL. Индукция IL-8 посредством GITRL (положительный контроль) показана как одиночная точка данных (звезда). Продукция IL-8 показана в пг/мл.
Таблица 10. Агонистическая активность антител формата TM с N-концевым Fab и C-концевым Fab по отношению к GITR человека на клетках HT1080
Таблица 11. Агонистическая активность антител формата IgG1 N297A по отношению к GITR человека на клетках HT1080
[434] Получены дополнительные варианты IgG1 N297A оптимизированных антител H1H2/VH и показаны ниже в таблице 12, и указана их агонистическая активность, определенная в анализе HT1080, как описано выше. Эти антитела являются подходящими для получения в формате TM.
Таблица 12. Агонистическая активность антител формата IgG1 N297A по отношению к GITR человека на клетках HT1080
[435] Сходный анализ проводили на клетках Jurkat, линии клеток на основе T-клеток, модифицированной для экспрессии GITR человека и люциферазного репортера NF-κB (Promega®). Восемь оптимизированных антител формата TM с N-концевым Fab, ABP 1-8, сравнивали с GITRL по их способности индуцировать IL-8 в T-клетках. Как показано на ФИГ. 7A-H (для ABP 1-8) и в таблице 13, все восемь ABP являлись лучшими, чем GITRL, в индукции продукции цитокина.
Таблица 13. 8 оптимизированных форматов TM с N-концевым Fab превосходят GITRL
Агонистическая активность антител TM-формата с N-концевым Fab в первичных клетках
[436] В одном варианте осуществления, ABP GITR дополнительно тестируют по их способности подавать костимулирующий сигнал CD4+CD25- эффекторным T-клеткам в сочетании с передачей сигналов TCR посредством антитела против CD3. Увеличение активации T-клеток измеряют посредством количественной оценки пролиферации, и/или измерения увеличения продукции и секреции цитокинов, включая IFN-гамма, с использованием анализа ELISA.
[437] В другом варианте осуществления, ABP GITR дополнительно анализируют для оценки их способности предотвращать супрессию эффекторных T-клеток регуляторными T-клетками. CD4+ T-клетки человека выделяют с использованием набора для выделения CD4+ T-клеток человека (Miltenyi #130-096). Регуляторные T-клетки дополнительно обогащают с использованием бусин против CD25 человека MicroBeads® II (Miltenyi #130-092-983), следуя инструкциям производителя. Истощенные по CD25 CD4+ T-клетки используют в качестве эффекторных T-клеток в анализе супрессии. Бусины, конъюгированные с антителами против CD2, CD3 и CD28 человека, используют для активации эффекторных T-клеток в анализе (Treg Suppression Inspector; назывемый также бусинами для активации T-клеток, Miltenyi #130-092-909). В 96-луночный планшет, 50000 каждых из регуляторных T-клеток и эффекторных T-клеток рассевают в каждую лунку и инкубируют с эквивалентным количеством бусин для активации T-клеток. Смеси клеток и бусин приводят в контакт с различными концентрациями ABP GITR на пять суток. Пролиферацию эффекторных T-клеток измеряют посредством стимуляции культур клеток с использованием тритированного тимидина в течение последних 16 часов культивирования, промывки и измерения уровня радиоактивности, включенной в клетки.
Агонистическая активность антител TM-формата с N-концевым Fab в анализе первичных клеток T-бластов
Предварительно стимулированные T-клетки (T-бласты) использовали для оценки активности восьми антител формата TM с N-концевым Fab (ABP 1-8).
Для получения T-бластов, PBMC стимулируют с использованием PHA в течение 5-7 суток для размножения клеток и индукции экспрессии GITR. Клетки промывают и замораживают до подготовки проведения функционального анализа.
Для оценки функциональной активности ABP 1-8, клетки стимулируют посредством добавления 1 мг/мл антитела против CD3+2 мг/мл антитела против CD28, 0,003-10 мг/мл ABP 1-8, и 10 мг/мл GITRL в качестве положительного контроля. Клетки инкубируют при 37°C, и супернатанты собирают через 48 часов. Продукцию IL-2 измеряют посредством AlphaLISA® (Perkin Elmer®). На ФИГ. 8A показан процент GITR+ CD4+ клеток (слева) и CD8+ клеток (справа) в клетках от двух доноров-людей в различных временных точках, +/- стимуляция с использованием PHA.
На ФИГ. 8B-8M показаны результаты обработки T-бластов от 4 различных доноров после контрольных обработок или обработок ABP, и полученная продукция IL-2. На каждой ФИГ. верхний ряд, слева направо, представляет собой измерение FACS связывания ABP с CD4+ клетками, продукция IL-2 в клетках от донора 1, продукция IL-2 в клетках от донора 2. В нижнем ряду, слева направо, представлено измерение FACS связывания ABP с CD8+ клетками, продукция IL-2 в клетках от донора 3, продукция IL-2 в клетках от донора 4. Данные показаны следующим образом: 8B: контроль изотипа IgG4; 8C: антитело SEC4; 8D: отрицательный контроль IgG4 формата TM; 8E: не относящийся к TM IgG4 неоптимизированный предшественник линии ABP 1-8 (ABP9). 8F: ABP1; 8G: ABP2; 8H: ABP3; 8I: ABP4; 8J: ABP5; 8K: ABP6; 8L: ABP7; 8M:ABP8.
Как показано на ФИГ., T-бласты от различных доноров проявляли изменчивость ответа на обработку ABP 1-8; однако, обработка с использованием всех восьми ABP формата TM имела агонистическую активность при большинстве тестированных концентраций, как измерено по продукции IL-2 и по сравнению с контрольными антителами.
Сравнение активности агонизма GITR оптимизированных ABP формата TM с N-концевым Fab и не относящихся к формату TM ABP IgG1
[438] Те же самые восемь оптимизированных ABP формата TM с N-концевым Fab (1-8), что и в вышеуказанных примерах, сравнивали с неоптимизированными контрольными предшественниками в таком же анализе индукции IL-8, описанном выше, и это показано на ФИГ. 4. На каждой ФИГ. показано сравнение ABP 1-8 формата TM с N-концевым Fab (IgG4 S228P с N-концевым Fab IgG1, «IgG4 TM») и соответствующего ABP IgG1, не относящегося к формату TM (IgG1 N297, «IgG1»), так же как GITRL в качестве положительного контроля и отрицательного контроля IgG4 (GITRL и IgG4 анализировали в планшете, отдельном от ABP). На левых панелях показаны результаты для клеток, экспрессирующих hGITR, и на правых панелях показаны результаты для клеток, экспрессирующих cGITR. Индукция IL-8 как функция от концентрации ABP показана для ABP 1 (ФИГ. 9A), ABP 2 (ФИГ. 9B), ABP3 (ФИГ. 9C), ABP4 (ФИГ. 9D), ABP5 (ФИГ. 9E), ABP6 (ФИГ. 9F), ABP7 (ФИГ. 9G) и ABP8 (ФИГ. 9H). Индукция IL-8 посредством GITRL показана как круги, посредством антител формата TM как треугольники, посредством исходных антител IgG1 как ромбы, и посредством контрольных антител IgG4 как квадраты. Таблица значений EC50 показана внизу каждой панели на каждой ФИГ.
[439] Результаты, показанные на фигуре 9, демонстрируют, что восемь оптимизированных ABP являются способными индуцировать продукцию IL-8 в клетках, экспрессирующих GITR человека или яванского макака, в намного большей степени в форме антител формата TM с N-концевым Fab, по сравнению с двухвалентным IgG1 N297A. Антитела формата TM с N-концевым Fab имели меньшие значения EC50 и большую максимальную продукцию IL-8 по сравнению форматом двухвалентного IgG1 N297A. Кроме того, все антитела TM имели более высокую аффинность для GITR, чем не относящаяся к TM форма исходного антитела (ср. таблицы 5 и 7 с таблицей 6).
Оценка блокирования GITRL
[440] В другом варианте осуществления, блокирование GITR оценивали с использованием устройства FORTEBIO® OCTET. Анализ проводили при 30°C с использованием 1× кинетического буфера (ForteBio, Inc.) в качестве буфера для анализа. Биосенсоры для связывания против Fc IgG человека (AHC) (ForteBio, Inc.) использовали для связывания ABP GITR человека на сенсорах. Сенсоры насыщали в буфере для анализа в течение 300 секунд перед анализом. ABP загружали на сенсоры посредством погружения сенсоров в раствор супернатанта ABP на 300 секунд. Фон устанавливали посредством погружения сенсоров в 1× буфер для анализа на 200 секунд. Затем связывание рекомбинантного GITR мониторировали в течение 180 секунд. Способность рекомбинантного GITRL впоследствии связываться с ABP/комплексом GITR определяли посредством погружения сенсоров в GITRL на 180 секунд.
[441] Блокирование GITR оценивали в соответствии с вышеуказанными способами с использованием ABP 1-8. Все восемь ABP являлись способными блокировать связывание GITRL.
[442] В одном варианте осуществления, для оценки того, блокируют ли ABP против GITR человека связывание лиганда GITR (GITRL, R&D Systems #6987-GL-CF) с GITR, различные концентрации немеченого ABP GITR инкубируют с пан-T-клетками человека при 4°C в буфере для окрашивания (например, фосфатно-солевом буфере с 0,5% бычьим сывороточным альбумином) в течение 10 мин. Без промывки, 4 нМ меченного HA GITRL человека добавляют и инкубируют при 4°C в течение следующих 30 мин. Затем клетки дважды промывают буфером для окрашивания, и инкубируют с антителом против HA с PE (Miltenyi #130-092-257) в буфере для окрашивания при 4°C в течение 30 мин. Затем клетки дважды промывают буфером для окрашивания и фиксируют с использованием 2% параформальдегида в PBS для анализа проточной цитометрии. Уменьшение уровня окрашивания PE показывает, что ABP блокирует взаимодействие GITR-GITRL.
Пример 3: Мультиспецифические антигенсвязывающие белки
[443] Один вариант осуществления мультиспецифических ABP, агонистических для GITR, включает антитело с общей легкой цепью. Идентифицированы ABP, связывающие два отдельных эпитопа на GITR. Эти два ABP разделяют одну и ту же легкую цепь. ABP61 представляет собой агонистическое антитело, и ABP59 имеет меньшую агонистическую активность, но не конкурирует с ABP61 за связывание с GITR. Мультивалентные мультиспецифические антитела с общими легкими цепями получали посредством трансфекции клеток-хозяев HEK-293 векторами, кодирующими две тяжелые цепи и одну общую легкую цепь. Первый иллюстративный ABP, описанный в настоящем описании, с общей легкой цепью (SEQ ID NO:125) представляет собой ABP33, имеющий тяжелую цепь IgG4 (ABP61) с N-концевым Fab (из ABP58 (IgG1-эквивалента ABP59)), и полноразмерную последовательность SEQ ID NO:124 (HC) и SEQ ID NO:125 (LC). Второй иллюстративный ABP, описанный в настоящем описании, с общей легкой цепью, представляет собой ABP34, имеющий тяжелую цепь IgG4 (ABP61) с C-концевым Fab (из ABP58 (IgG1-эквивалента ABP59) и полноразмерную последовательность SEQ ID NO:136 (HC) и SEQ ID NO:125 (LC).
[444] Каждый мультиспецифический ABP связывает два отдельных эпитопа на GITR. ABP характеризуют, как описано в примерах выше. Другие мультиспецифические ABP, описанные в настоящем описании, получали и характеризовали сходным образом. На ФИГ. 6 показаны результаты определения EC50 для ABP33 и ABP34 в анализе HT1080, как описано выше в примере 2. ABP33 (тетравалентный вариант, объединяющий ABP61 IgG4 с Fab IgG1 из ABP58 [IgG1-эквивалента ABP59] на N-конце) и ABP34 (тетравалентный вариант, объединяющий ABP61 IgG4 с Fab IgG1 из ABP58 [IgG1-эквивалента ABP59] на C-конце) сравнивали с двухвалентными ABP 59 и 61 (IgG4 S228P). Как показано на ФИГ., оба тетравалентных антитела имели превосходящую EC50, как измерено посредством индукции IL-8, по сравнению с их двухвалентными эквивалентами.
Пример 4: Сравнение антитела TM-формата с эталонными антителами против GITR
[445] Активность антител TM-формата с N-концевым Fab тестировали по сравнению с двумя известными антителами против GITR, SEC4 и SEC9, в клетках HT1080, модифицированных для стабильной экспрессии GITR человека. Культивированные клетки обрабатывали в течение шести часов с использованием диапазона концентраций двух эталонных агонистических антител, SEC4 («35E6», форматированное для наличия мышиных вариабельных областей с человеческими областями IgG4 S228P/каппа, оранжевые ромбы) и SEC9 (гуманизированное 6C8 N62Q IgG1 N297A). SEC4 описано, например, в Патенте США No. 8709424; вариабельные области обнаружены в SEQ ID NO 1 и 12. SEC9 описано, например, в Патенте США No. 7812135; полноразмерные последовательности приведены в SEQ ID NO 58 и 63. Доза 1 мкг/мл двухвалентного антитела является эквивалентной 6,67 нМ; доза 1 мкг/мл тетравалентного антитела является эквивалентной 4 нМ.
[446] Индукцию IL-8 измеряли посредством ELISA и рассчитывали EC50. На ФИГ. 11A показано сравнение hGITRL с SEC4 (ромбы) и SEC9 (круги), так же как с отрицательным контролем IgG4 (закрашенные треугольники), с отрицательным контролем IgG1 (незакрашенные треугольники), и тримерным лигандом GITR человека («hGITRL», квадраты) в качестве положительного контроля. GITRL имел лучшую EC50 (врезка) и максимальную индукцию по сравнению как с SEC4, так и с SEC9.
[447] Показаны также сравнения GITRL с ABP1 (ФИГ. 11B), ABP2 (ФИГ. 11C), ABP3 (ФИГ. 11D), ABP4 (ФИГ. 11E), ABP5 (ФИГ. 11F), ABP6 (ФИГ. 11G), ABP7 (ФИГ. 11H) и ABP8 (ФИГ. 11I). Как показано на фигуре, все восемь антител формата TM с N-концевым Fab имели более преимущественные EC50, чем либо SEC4, либо SEC9. Все восемь антител формата TM с N-концевым Fab имели также более высокую индукцию продукции IL-8, чем либо SEC4, либо SEC9.
[448] SEC4 тестировали также, как описано выше, в анализе первичных клеток T-бластов. Как показано на ФИГ. 8, индукция IL-2 в первичных клетках посредством SEC4 была меньше для всех четырех доноров, чем антител формата TM.
Пример 5: ABP против GITR увеличивают продукцию цитокинов в инфильтрующих опухоль пациента лимфоцитах и в GITR+ T-клетках
Материалы и способы
[449] Образцы диссоциированных опухолей закупали из Conversant Bio. Образцы представляли собой аденокарциному NSCLC, выделенную от мужчины в возрасте 75 лет, ранее курящего, с заболеванием стадии Ia, до какого-либо лечения. Образец быстро размораживали, затем подвергали повторной стимуляции в нескольких условиях, в присутствии и в отсутствие иммунотерапевтических средств следующим образом: клетки либо представляли собой контроль без стимуляции, либо были стимулированы с использованием 1 мкг/мл αCD3 (растворимого)+2 мкг/мл αCD28 (растворимого)+IL-2 (50 нг/мл); клетки либо не подвергали иммунотерапевтической обработке (для оценки уровней белков контрольной точки), либо подвергали обработке пембролизумабом (10 мкг/мл), контрольным ABP формата TM (2 мкг/мл), ABP1 (2 мкг/мл) или ABP1+пембролизумабом. Клетки инкубировали в течение 48 часов перед сбором супернатантов и окрашиванием по экспрессии белков контрольной точки. В некоторых образцах, брефелдин A (ингибитор секреции цитокинов) добавляли на последние пять часов стимуляции для детекции цитокинов посредством внутриклеточного окрашивания цитокинов.
Результаты
[450] Клетки отбирали как положительные по GITR T-клетки, и результаты показаны на фигуре 12A (продукция TNF) и фигуре 12B (продукция IFNγ). Как показано на фигурах, обработка единственным средством против GITR (ABP1) приводила к увеличению продукции цитокинов. В этом анализе не присутствовало значительного увеличения продукции цитокинов в клетках, подвергнутых комбинированной обработке ABP1+пембролизумаб.
Пример 6: Анализ посредством мутагенеза для определения эпитопов: аланиновое сканирование
[451] Для идентификации эпитопа для связывания ABP1 с GITR человека, одиночные точечные мутации вводили в внеклеточный домен GITR человека для определения того, уменьшается ли связывание APB1. Использовали либо замены на аланин, либо специфические мышиные остатки (ABP1 не связывает GITR мыши). Белки экспрессировали в клетках HEK-293 с меткой Fc, секретировали в форме растворимого белка, очищали на смоле MabSelect® Sure® Lx и характеризовали посредством SDS-PAGE. Связывание оценивали посредством интерферометрии биослоя (BLI) с использованием платформы Octet. GITR человека дикого типа-Fc или GITR-мутант-Fc связывали с сенсорами против Fc человека, промывали и подвергали воздействию ABP1 Fab. Для остатков, считаемых частью связывающего эпитопа, показано уменьшение или отсутствие связывания (например, KD, более чем в 3 раза слабее, чем для связывания с GITR человека дикого типа). Замены на аланин остатков C58, R59, Y61, E64, C67 и замена на аспарагиновую кислоту в положении C66 приводили к отсутствию связывания, в то время как замены на аланин остатков R56, D60, P62 или E65 приводили к уменьшению связывания.
Пример 7: Оценка антигенсвязывающих белков против GITR in vivo
[452] Исследования in vivo проводят для демонстрации способности ABP уменьшать количество циркулирующих регуляторных T-клеток в гуманизированной модели на мышах NSG. Новорожденным мышам NSG трансплантируют CD34+ клетки фетальной печени человека посредством ретроорбитальной инъекции. Через 16 недель, у животных развивается разнообразный репертуар иммуноцитов человека, включая CD4+ и CD8+ эффекторные T-клетки, и регуляторные T-клетки. Однократную внутрибрюшинную дозу 25 мг/кг ABP против GITR человека или контроль изотипа человека вводят мышам, и процент циркулирующих CD4+ T-клеток человека, экспрессирующих маркер регуляторных T-клеток FoxP3 определяют посредством проточной цитометрии на сутки 4 после дозирования.
Пример 8. Инкубация активированных T-клеток с ABP1 формата TM или его предшественником общепринятого формата ABP35
Получение активированных T-бластов
[453] Активированные T-бласты получали посредством стимуляции свежевыделенных PBMC от двух здоровых доноров в течение 7 суток с использованием PHA (конечная конц. 10 мкг/мл) и IL-2 (конечная конц. 4 нг/мл, добавленных только на последние 24 час) при 37°C и 5% CO2.
Интернализация GITR после связывания антитела
[454] Активированные CD4+/CD8+ T-бласты рассевали при 2×105 на лунку в 96-луночные планшеты с U-образным дном. Лунки обрабатывали только средой, рекомбинантным GITR-лигандом (10 мкг/мл, R&D Systems, кат.# 6987-GL-025/CF), ABP1 (~250 кДа), контролем изотипа hIgG4 формата TM, ABP35 (~150 кДа) или контролем изотипа hIgG1 стандартного формата, в девяти дозах каждый: 10 мкг/мл, 2 мкг/мл, 0,4 мкг/мл, 80 нг/мл, 16 нг/мл, 3,2 нг/мл, 0,64 нг/мл, 0,13 нг/мл и 0,026 нг/мл.
Интернализация GITR после связывания антитела
[455] Опосредованная антителом кластеризация стимулирует эндоцитоз и передачу сигналов членами суперсемейства рецепторов TNF, таких как GITR. Измеряли способность ABP1 и ABP35 (так же как контролей изотипа) опосредовать кластеризацию и интернализацию.
[456] Активированные T-бласты сначала окрашивали для сортировки FACS. Рецепторы Fc блокировали с использованием TruStain® FcX человека в течение 10 минут при комнатной температуре. Клетки инкубировали с конъюгированными с флуоресцентной меткой антителами в течение 30 минут при 4°C, как в таблице 14. Затем клетки промывали 2X буфером для FACS, фиксировали в параформальдегиде в течение 30 минут в темноте, снова промывали и ресуспендировали в 200 мкл буфера для FACS, и собирали данные в устройстве BD Fortessa.
[457] Интернализацию GITR измеряли в CD4+ клетках (фигуры 13A-E) и CD8+ клетках (фигуры 13F-J) либо от донора 1 (фигуры 13A-B, 13F-G), либо от донора 2 (фигуры 13C-D, 13H-I). Клетки обрабатывали либо ABP1 в формате TM антитела, либо стандартным двухвалентным антителом ABP35. Как можно наблюдать, инкубация либо с ABP1, либо с ABP35 ингибирует последующее окрашивание с использованием ABP1Dylight650 (фигуры 13A, 13C, 13F, 13H), но только инкубация с ABP1 индуцирует интернализацию GITR, как измерено по окрашиванию с использованием не конкурирующего клона 108-17 (фигуры 13B, 13D, 13G, 13I). Определение EC50 ABP1 на клетках от обоих доноров показано на фигуре 13E (CD4+ клетки) и фигуре 13J (CD8+ клетки).
Таблица 14. Мечение флуорохромом
Продукция цитокинов в активированных T-клетках, обработанных ABP1 или ABP35
[458] Активированные CD4+/CD8+ T-бласты рассевали при 5×104 на лунку в 96-луночные планшеты с U-образным дном. Лунки обрабатывали только средой, рекомбинантным GITR-лигандом (10 мкг/мл, R&D Systems, кат.# 6987-GL-025/CF), ABP1, контролем изотипа hIgG4 формата TM, ABP35, или контролем изотипа hIgG1 стандартного формата в девяти дозах каждый: 10 мкг/мл, 2 мкг/мл, 0,4 мкг/мл, 80 нг/мл, 16 нг/мл, 3,2 нг/мл, 0,64 нг/мл, 0,13 нг/мл и 0,026 нг/мл.
[459] Клетки стимулировали посредством добавления 1 мкг/мл антител против CD3 (антитело мыши против белка человека, клон UCHT-1), R&D Systems, кат.# MAB100) и 2 мкг/мл антител против CD28 (антитело мыши против белка человека, клон 37407), R&D Systems, кат.# MAB342) антитела. Реакционные смеси для анализа инкубировали при 37°C и 5% CO2 в течение 48 час. Продукцию IL-2 измеряли посредством AlphaLISA® (Perkin Elmer).
[460] Инкубация T-бластов с антителом ABP1 формата TM, но не с таким же антителом в стандартном двухвалентном формате (ABP35) или с любым из контролей изотипа, приводит к интернализации GITR посредством активированных CD4+ и CD8+ T-клеток (ФИГ. 13).
[461] Кроме того, суперкластеризация рецептора GITR посредством ABP1, но не связывание посредством общепринятого двухвалентного ABP, стимулирует секрецию IL-2 активированными T-бластами зависимым от дозы образом (ФИГ. 14). Совместно, эти данные показывают, что T-бласты, не отвечающие на общепринятую терапию против GITR, могут отвечать на соответствующее антитело в формате TM.
Пример 9: Продукция цитокинов в активированных T-клетках, обработанных ABP1, по сравнению с двумя эталонными антителами, SEC4 и SEC9
[462] Активированные T-бласты получали, как описано в примере 8, и использовали для сравнения активности ABP1 с эталонными антителами против GITR SEC4 и SEC9. Активированные T-бласты получали посредством стимуляции свежевыделенных PBMC от двух здоровых доноров в течение 7 суток с использованием PHA (конечная конц. 10 мкг/мл) и IL-2 (конечная конц. 4 нг/мл, добавленных только на последние 24 час) при 37°C и 5% CO2.
[463] Активированные CD4+/CD8+ T-бласты рассевали при 5×104 на лунку в 96-луночные планшеты с U-образным дном. Лунки обрабатывали только средой, рекомбинантным GITR-лигандом, ABP1, SEC4, SEC9, контролем изотипа hIgG4 формата TM («Изо-TM»), контролем изотипа hIgG1 стандартного формата и контролем изотипа hIgG4 стандартного формата, в девяти дозах каждый: 10 мкг/мл, 2 мкг/мл, 0,4 мкг/мл, 80 нг/мл, 16 нг/мл, 3,2 нг/мл, 0,64 нг/мл, 0,13 нг/мл и 0,026 нг/мл.
Продукция цитокинов в активированных T-клетках, обработанных ABP1, SEC4 и SEC9
[464] Клетки стимулировали посредством добавления 1 мкг/мл антитела против CD3 и 2 мкг/мл антитела против CD28. Клетки инкубировали при 37°C и 5% CO2 в течение 48 час. Продукцию IL-2 измеряли посредством AlphaLISA® (Perkin Elmer). Как видно в примере 8, ABP формата TM1 стимулирует секрецию IL-2 активированными T-бластами зависимым от дозы образом. Продукция IL-2 активированными T-клетками показана на фигуре 15A (донор 1) и 15B (донор 2). Соответствующая EC50 показана на фигуре 15C (донор 1) и 15D (донор 2).
[465] Как можно видеть на фигурах, SEC4 и SEC9 эффективно не индуцируют IL-2 зависимым от дозы образом, ABP1 индуцировал продукцию IL-2 в большей степени, чем SEC4 и SEC9, явно зависимым от дозы образом. Совместно, эти данные поддерживают вывод, что T-бласты, не отвечающие на общепринятую терапию против GITR, могут отвечать на соответствующее антитело в формате TM.
ЭКВИВАЛЕНТЫ
[466] Описание, приведенное выше, может включать множество отдельных изобретений с независимой полезностью. Несмотря на то, что каждое из этих изобретений описано в его предпочтительной форме(формах), конкретные варианты его осуществления, как описано и проиллюстрировано в настоящем описании, не следует рассматривать в ограничивающем смысле, поскольку возможны многочисленные варианты. Объект изобретения включает все новые и неочевидные комбинации и подкомбинации различных элементов, признаков, функций и/или свойств, описанных в настоящем описании. В нижеследующей формуле изобретения особенно выделены конкретные комбинации и подкомбинации, рассматриваемые как новые и неочевидные. Изобретения, осуществленные в других комбинациях и подкомбинациях признаков, функций, элементов и/или свойств, могут быть заявлены в этой заявке, в заявках, по которым испрашивается приоритет этой заявки, или в родственных заявках. Такие пункты формулы изобретения, независимо от того, относятся ли они к другому изобретению или к тому же самому изобретению, и имеют ли они более широкий, более узкий, равный или другой объем по сравнению с оригинальными пунктами формулы изобретения, также рассматривают как включенные в объект изобретения по настоящему описанию.ПРИЛОЖЕНИЕ A: ПОСЛЕДОВАТЕЛЬНОСТИ
IgG4 S228P
IgG4 S228P
IgG1 N297A
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> POTENZA THERAPEUTICS, INC.
<120> АНТИГЕНСВЯЗЫВАЮЩИЕ БЕЛКИ ПРОТИВ GITR И СПОСОБЫ ИХ ПРИМЕНЕНИЯ
<130> 32248-38337/PCT
<140> PCT/US2017/062443
<141> 2017-11-19
<150> GC 2017/34287
<151> 2017-11-19
<150> 62/448,644
<151> 2017-01-20
<150> 62/497,428
<151> 2016-11-19
<160> 233
<170> PatentIn версии 3.5
<210> 1
<211> 241
<212> БЕЛОК
<213> Homo sapiens
<400> 1
Met Ala Gln His Gly Ala Met Gly Ala Phe Arg Ala Leu Cys Gly Leu
1 5 10 15
Ala Leu Leu Cys Ala Leu Ser Leu Gly Gln Arg Pro Thr Gly Gly Pro
20 25 30
Gly Cys Gly Pro Gly Arg Leu Leu Leu Gly Thr Gly Thr Asp Ala Arg
35 40 45
Cys Cys Arg Val His Thr Thr Arg Cys Cys Arg Asp Tyr Pro Gly Glu
50 55 60
Glu Cys Cys Ser Glu Trp Asp Cys Met Cys Val Gln Pro Glu Phe His
65 70 75 80
Cys Gly Asp Pro Cys Cys Thr Thr Cys Arg His His Pro Cys Pro Pro
85 90 95
Gly Gln Gly Val Gln Ser Gln Gly Lys Phe Ser Phe Gly Phe Gln Cys
100 105 110
Ile Asp Cys Ala Ser Gly Thr Phe Ser Gly Gly His Glu Gly His Cys
115 120 125
Lys Pro Trp Thr Asp Cys Thr Gln Phe Gly Phe Leu Thr Val Phe Pro
130 135 140
Gly Asn Lys Thr His Asn Ala Val Cys Val Pro Gly Ser Pro Pro Ala
145 150 155 160
Glu Pro Leu Gly Trp Leu Thr Val Val Leu Leu Ala Val Ala Ala Cys
165 170 175
Val Leu Leu Leu Thr Ser Ala Gln Leu Gly Leu His Ile Trp Gln Leu
180 185 190
Arg Ser Gln Cys Met Trp Pro Arg Glu Thr Gln Leu Leu Leu Glu Val
195 200 205
Pro Pro Ser Thr Glu Asp Ala Arg Ser Cys Gln Phe Pro Glu Glu Glu
210 215 220
Arg Gly Glu Arg Ser Ala Glu Glu Lys Gly Arg Leu Gly Asp Leu Trp
225 230 235 240
Val
<210> 2
<211> 241
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 2
Met Ala Gln His Gly Ala Met Gly Ala Phe Arg Ala Leu Cys Gly Leu
1 5 10 15
Ala Leu Leu Cys Ala Leu Ser Leu Gly Gln Arg Pro Thr Gly Gly Pro
20 25 30
Gly Cys Gly Pro Gly Arg Leu Leu Leu Gly Arg Gly Thr Asp Ala Arg
35 40 45
Cys Cys Arg Val His Thr Thr Arg Cys Cys Arg Asp Tyr Pro Gly Glu
50 55 60
Glu Cys Cys Ser Glu Trp Asp Cys Met Cys Val Gln Pro Glu Phe His
65 70 75 80
Cys Gly Asp Pro Cys Cys Thr Thr Cys Arg His His Pro Cys Pro Pro
85 90 95
Gly Gln Gly Val Gln Ser Gln Gly Lys Phe Ser Phe Gly Phe Gln Cys
100 105 110
Ile Asp Cys Ala Ser Gly Thr Phe Ser Gly Gly His Glu Gly His Cys
115 120 125
Lys Pro Trp Thr Asp Cys Thr Gln Phe Gly Phe Leu Thr Val Phe Pro
130 135 140
Gly Asn Lys Thr His Asn Ala Val Cys Val Pro Gly Ser Pro Pro Ala
145 150 155 160
Glu Pro Leu Gly Trp Leu Thr Val Val Leu Leu Ala Val Ala Ala Cys
165 170 175
Val Leu Leu Leu Thr Ser Ala Gln Leu Gly Leu His Ile Trp Gln Leu
180 185 190
Arg Ser Gln Cys Met Trp Pro Arg Glu Thr Gln Leu Leu Leu Glu Val
195 200 205
Pro Pro Ser Thr Glu Asp Ala Arg Ser Cys Gln Phe Pro Glu Glu Glu
210 215 220
Arg Gly Glu Arg Ser Ala Glu Glu Lys Gly Arg Leu Gly Asp Leu Trp
225 230 235 240
Val
<210> 3
<211> 235
<212> БЕЛОК
<213> Macaca fascicularis
<400> 3
Met Cys Ala Cys Gly Thr Leu Cys Cys Leu Ala Leu Leu Cys Ala Ala
1 5 10 15
Ser Leu Gly Gln Arg Pro Thr Gly Gly Pro Gly Cys Gly Pro Gly Arg
20 25 30
Leu Leu Leu Gly Thr Gly Lys Asp Ala Arg Cys Cys Arg Val His Pro
35 40 45
Thr Arg Cys Cys Arg Asp Tyr Gln Ser Glu Glu Cys Cys Ser Glu Trp
50 55 60
Asp Cys Val Cys Val Gln Pro Glu Phe His Cys Gly Asn Pro Cys Cys
65 70 75 80
Thr Thr Cys Gln His His Pro Cys Pro Ser Gly Gln Gly Val Gln Pro
85 90 95
Gln Gly Lys Phe Ser Phe Gly Phe Arg Cys Val Asp Cys Ala Leu Gly
100 105 110
Thr Phe Ser Arg Gly His Asp Gly His Cys Lys Pro Trp Thr Asp Cys
115 120 125
Thr Gln Phe Gly Phe Leu Thr Val Phe Pro Gly Asn Lys Thr His Asn
130 135 140
Ala Val Cys Val Pro Gly Ser Pro Pro Ala Glu Pro Pro Gly Trp Leu
145 150 155 160
Thr Ile Val Leu Leu Ala Val Ala Ala Cys Val Leu Leu Leu Thr Ser
165 170 175
Ala Gln Leu Gly Leu His Ile Trp Gln Leu Gly Ser Gln Pro Thr Gly
180 185 190
Pro Arg Glu Thr Gln Leu Leu Leu Glu Val Pro Pro Ser Thr Glu Asp
195 200 205
Ala Ser Ser Cys Gln Phe Pro Glu Glu Glu Arg Gly Glu Arg Leu Ala
210 215 220
Glu Glu Lys Gly Arg Leu Gly Asp Leu Trp Val
225 230 235
<210> 4
<211> 228
<212> БЕЛОК
<213> Mus musculus
<400> 4
Met Gly Ala Trp Ala Met Leu Tyr Gly Val Ser Met Leu Cys Val Leu
1 5 10 15
Asp Leu Gly Gln Pro Ser Val Val Glu Glu Pro Gly Cys Gly Pro Gly
20 25 30
Lys Val Gln Asn Gly Ser Gly Asn Asn Thr Arg Cys Cys Ser Leu Tyr
35 40 45
Ala Pro Gly Lys Glu Asp Cys Pro Lys Glu Arg Cys Ile Cys Val Thr
50 55 60
Pro Glu Tyr His Cys Gly Asp Pro Gln Cys Lys Ile Cys Lys His Tyr
65 70 75 80
Pro Cys Gln Pro Gly Gln Arg Val Glu Ser Gln Gly Asp Ile Val Phe
85 90 95
Gly Phe Arg Cys Val Ala Cys Ala Met Gly Thr Phe Ser Ala Gly Arg
100 105 110
Asp Gly His Cys Arg Leu Trp Thr Asn Cys Ser Gln Phe Gly Phe Leu
115 120 125
Thr Met Phe Pro Gly Asn Lys Thr His Asn Ala Val Cys Ile Pro Glu
130 135 140
Pro Leu Pro Thr Glu Gln Tyr Gly His Leu Thr Val Ile Phe Leu Val
145 150 155 160
Met Ala Ala Cys Ile Phe Phe Leu Thr Thr Val Gln Leu Gly Leu His
165 170 175
Ile Trp Gln Leu Arg Arg Gln His Met Cys Pro Arg Glu Thr Gln Pro
180 185 190
Phe Ala Glu Val Gln Leu Ser Ala Glu Asp Ala Cys Ser Phe Gln Phe
195 200 205
Pro Glu Glu Glu Arg Gly Glu Gln Thr Glu Glu Lys Cys His Leu Gly
210 215 220
Gly Arg Trp Pro
225
<210> 5
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 5
Gly Gly Gly Gly Ser
1 5
<210> 6
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 6
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 7
<211> 687
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 7
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Leu Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Gly Ile Tyr Glu Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Glu Arg Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
225 230 235 240
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
245 250 255
Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly Leu Gly Trp Gly Trp Ile
260 265 270
Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Gly Ile Tyr Glu
275 280 285
Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile
290 295 300
Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val
305 310 315 320
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala His Glu Arg Val Arg
325 330 335
Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly Gln
340 345 350
Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
355 360 365
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
370 375 380
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
385 390 395 400
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
405 410 415
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
420 425 430
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
435 440 445
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
450 455 460
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
465 470 475 480
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
485 490 495
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
500 505 510
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
515 520 525
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
530 535 540
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
545 550 555 560
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
565 570 575
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
580 585 590
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
595 600 605
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
610 615 620
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
625 630 635 640
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
645 650 655
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
660 665 670
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
675 680 685
<210> 8
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 8
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Glu Tyr Ala Thr Pro Pro
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 9
<211> 126
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 9
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Leu Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Gly Ile Tyr Glu Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Glu Arg Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 10
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 10
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Glu Tyr Ala Thr Pro Pro
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 11
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 11
Tyr Ser Ile Ser Ser Gly Leu Gly Trp Gly
1 5 10
<210> 12
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 12
Gly Ile Tyr Glu Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 13
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 13
Ala His Glu Arg Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
1 5 10 15
Phe Asp Ile
<210> 14
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 14
Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn
1 5 10
<210> 15
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 15
Ala Ala Ser Ser Leu Gln Ser
1 5
<210> 16
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 16
Gln Gln Glu Tyr Ala Thr Pro Pro Thr
1 5
<210> 17
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 17
Gln Gln Glu Tyr Asn Thr Pro Pro Thr
1 5
<210> 18
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 18
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Glu Tyr Asn Thr Pro Pro
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 19
<211> 127
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 19
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Gly
20 25 30
Gly Ala Val Trp Ser Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Gly Ile Ala Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Asp Glu Asn Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His
100 105 110
Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 20
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 20
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Glu Tyr Asn Thr Pro Pro
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 21
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 21
Gly Ser Ile Ser Ser Gly Gly Ala Val Trp Ser
1 5 10
<210> 22
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 22
Gly Ile Ala Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 23
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 23
Ala Asp Glu Asn Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
1 5 10 15
Phe Asp Ile
<210> 24
<211> 687
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 24
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Ala Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Glu Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
225 230 235 240
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
245 250 255
Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly Ala Gly Trp Gly Trp Ile
260 265 270
Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Leu Ile Val His
275 280 285
Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile
290 295 300
Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val
305 310 315 320
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Val Leu Glu Ser Val Arg
325 330 335
Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly Gln
340 345 350
Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
355 360 365
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
370 375 380
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
385 390 395 400
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
405 410 415
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
420 425 430
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
435 440 445
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
450 455 460
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
465 470 475 480
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
485 490 495
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
500 505 510
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
515 520 525
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
530 535 540
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
545 550 555 560
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
565 570 575
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
580 585 590
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
595 600 605
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
610 615 620
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
625 630 635 640
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
645 650 655
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
660 665 670
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
675 680 685
<210> 25
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 25
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Lys Tyr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Glu Tyr Asn Thr Pro Pro
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 26
<211> 126
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 26
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Ala Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Glu Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 27
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 27
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Lys Tyr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Glu Tyr Asn Thr Pro Pro
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 28
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 28
Tyr Ser Ile Ser Ser Gly Ala Gly Trp Gly
1 5 10
<210> 29
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 29
Leu Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 30
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 30
Val Leu Glu Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
1 5 10 15
Phe Asp Ile
<210> 31
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 31
Ala Ala Ser Ser Leu Lys Tyr
1 5
<210> 32
<211> 687
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 32
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Ala Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Pro Glu Trp
35 40 45
Ile Gly Leu Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Glu Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
225 230 235 240
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
245 250 255
Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly Ala Gly Trp Gly Trp Ile
260 265 270
Arg Gln Pro Pro Gly Lys Gly Pro Glu Trp Ile Gly Leu Ile Val His
275 280 285
Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile
290 295 300
Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val
305 310 315 320
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Val Leu Glu Ser Val Arg
325 330 335
Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly Gln
340 345 350
Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
355 360 365
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
370 375 380
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
385 390 395 400
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
405 410 415
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
420 425 430
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
435 440 445
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
450 455 460
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
465 470 475 480
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
485 490 495
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
500 505 510
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
515 520 525
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
530 535 540
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
545 550 555 560
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
565 570 575
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
580 585 590
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
595 600 605
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
610 615 620
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
625 630 635 640
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
645 650 655
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
660 665 670
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
675 680 685
<210> 33
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 33
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Lys Ser Ile Asp Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Glu Tyr Asn Thr Pro Pro
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 34
<211> 126
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 34
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Ala Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Pro Glu Trp
35 40 45
Ile Gly Leu Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Glu Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 35
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 35
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Lys Ser Ile Asp Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Glu Tyr Asn Thr Pro Pro
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 36
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 36
Arg Ala Ser Lys Ser Ile Asp Ser Tyr Leu Asn
1 5 10
<210> 37
<211> 687
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 37
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Ala Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Glu Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
225 230 235 240
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
245 250 255
Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly Ala Gly Trp Gly Trp Ile
260 265 270
Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Leu Ile Val His
275 280 285
Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile
290 295 300
Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val
305 310 315 320
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Val Leu Glu Ser Val Arg
325 330 335
Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly Gln
340 345 350
Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
355 360 365
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
370 375 380
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
385 390 395 400
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
405 410 415
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
420 425 430
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
435 440 445
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
450 455 460
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
465 470 475 480
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
485 490 495
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
500 505 510
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
515 520 525
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
530 535 540
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
545 550 555 560
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
565 570 575
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
580 585 590
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
595 600 605
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
610 615 620
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
625 630 635 640
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
645 650 655
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
660 665 670
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
675 680 685
<210> 38
<211> 687
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 38
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Ala Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Glu Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
225 230 235 240
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
245 250 255
Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly Ala Gly Trp Gly Trp Ile
260 265 270
Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Leu Ile Val His
275 280 285
Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile
290 295 300
Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val
305 310 315 320
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Val Leu Glu Ser Val Arg
325 330 335
Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly Gln
340 345 350
Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
355 360 365
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
370 375 380
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
385 390 395 400
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
405 410 415
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
420 425 430
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
435 440 445
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
450 455 460
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
465 470 475 480
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
485 490 495
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
500 505 510
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
515 520 525
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
530 535 540
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
545 550 555 560
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
565 570 575
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
580 585 590
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
595 600 605
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
610 615 620
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
625 630 635 640
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
645 650 655
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
660 665 670
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
675 680 685
<210> 39
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 39
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Asp Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Glu Tyr Asn Thr Pro Pro
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 40
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 40
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Asp Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Glu Tyr Asn Thr Pro Pro
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 41
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 41
Ala Ala Asp Ser Leu Gln Ser
1 5
<210> 42
<211> 687
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 42
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu
20 25 30
Tyr Met Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Tyr His Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Ala Asp Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
225 230 235 240
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
245 250 255
Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu Tyr Met Trp Gly Trp Ile
260 265 270
Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Leu Ile Tyr His
275 280 285
Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile
290 295 300
Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val
305 310 315 320
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Glu Ala Asp Arg
325 330 335
Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly Gln
340 345 350
Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
355 360 365
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
370 375 380
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
385 390 395 400
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
405 410 415
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
420 425 430
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
435 440 445
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
450 455 460
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
465 470 475 480
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
485 490 495
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
500 505 510
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
515 520 525
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
530 535 540
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
545 550 555 560
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
565 570 575
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
580 585 590
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
595 600 605
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
610 615 620
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
625 630 635 640
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
645 650 655
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
660 665 670
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
675 680 685
<210> 43
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 43
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Asn Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Asp Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Glu Tyr Asn Thr Pro Pro
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 44
<211> 126
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 44
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu
20 25 30
Tyr Met Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Tyr His Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Ala Asp Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 45
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 45
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Asn Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Asp Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Glu Tyr Asn Thr Pro Pro
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 46
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 46
Tyr Ser Ile Ser Ser Glu Tyr Met Trp Gly
1 5 10
<210> 47
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 47
Leu Ile Tyr His Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 48
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 48
Ala Arg Glu Ala Asp Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
1 5 10 15
Phe Asp Ile
<210> 49
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 49
Arg Ala Ser Gln Ser Ile Asn Ser Tyr Leu Asn
1 5 10
<210> 50
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 50
Ala Ala Ser Ser Leu Asp Ser
1 5
<210> 51
<211> 687
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 51
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu
20 25 30
Tyr Met Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Tyr His Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Ala Asp Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
225 230 235 240
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
245 250 255
Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu Tyr Met Trp Gly Trp Ile
260 265 270
Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Leu Ile Tyr His
275 280 285
Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile
290 295 300
Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val
305 310 315 320
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Glu Ala Asp Arg
325 330 335
Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly Gln
340 345 350
Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
355 360 365
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
370 375 380
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
385 390 395 400
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
405 410 415
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
420 425 430
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
435 440 445
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
450 455 460
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
465 470 475 480
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
485 490 495
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
500 505 510
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
515 520 525
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
530 535 540
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
545 550 555 560
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
565 570 575
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
580 585 590
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
595 600 605
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
610 615 620
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
625 630 635 640
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
645 650 655
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
660 665 670
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
675 680 685
<210> 52
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 52
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gly Ala Ser Gln Ser Ile Ser Thr Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Glu Tyr Asn Thr Pro Pro
85 90 95
Ser Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 53
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 53
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gly Ala Ser Gln Ser Ile Ser Thr Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Glu Tyr Asn Thr Pro Pro
85 90 95
Ser Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 54
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 54
Gly Ala Ser Gln Ser Ile Ser Thr Tyr Leu Asn
1 5 10
<210> 55
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 55
Ser Ala Ser Ser Leu Glu Ser
1 5
<210> 56
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 56
Gln Gln Glu Tyr Asn Thr Pro Pro Ser
1 5
<210> 57
<211> 689
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 57
Gln Leu Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Ser
20 25 30
Ser Tyr Ala Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Asp Ser Gly Arg Gly Tyr Gly Asp Tyr Gly Gly His His
100 105 110
Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala
115 120 125
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser
130 135 140
Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
145 150 155 160
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
165 170 175
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
180 185 190
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr
195 200 205
Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg
210 215 220
Val Glu Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Leu Gln Leu Gln
225 230 235 240
Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr
245 250 255
Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Ser Ser Tyr Ala Trp Gly
260 265 270
Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Ser Ile
275 280 285
Tyr Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val
290 295 300
Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser
305 310 315 320
Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser
325 330 335
Gly Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp
340 345 350
Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
355 360 365
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
370 375 380
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
385 390 395 400
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
405 410 415
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
420 425 430
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
435 440 445
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
450 455 460
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro
465 470 475 480
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
485 490 495
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
500 505 510
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
515 520 525
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val
530 535 540
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
545 550 555 560
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
565 570 575
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
580 585 590
Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr
595 600 605
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
610 615 620
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
625 630 635 640
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys
645 650 655
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
660 665 670
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
675 680 685
Lys
<210> 58
<211> 127
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 58
Gln Leu Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Ser
20 25 30
Ser Tyr Ala Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Asp Ser Gly Arg Gly Tyr Gly Asp Tyr Gly Gly His His
100 105 110
Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 59
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 59
Gly Ser Ile Ser Ser Ser Ser Tyr Ala Trp Gly
1 5 10
<210> 60
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 60
Ser Ile Tyr Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 61
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 61
Ala Arg Asp Ser Gly Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
1 5 10 15
Phe Asp Ile
<210> 62
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 62
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Arg Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Tyr Ile Ser Trp Val Arg Gln Val Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Val Pro Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Gly Gly Gly Tyr Ala Arg Gly Asp His Tyr Tyr Gly Met
100 105 110
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 63
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 63
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Lys
85 90 95
Ile Gly Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 64
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 64
Gly Thr Phe Ser Ser Tyr Tyr Ile Ser
1 5
<210> 65
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 65
Gly Ile Ile Pro Val Pro Gly Thr Ala Asn Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 66
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 66
Ala Arg Ala Gly Gly Gly Tyr Ala Arg Gly Asp His Tyr Tyr Gly Met
1 5 10 15
Asp Val
<210> 67
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 67
Arg Ser Ser Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr Leu Asp
1 5 10 15
<210> 68
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 68
Leu Gly Ser Asn Arg Ala Ser
1 5
<210> 69
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 69
Met Gln Lys Ile Gly Thr Pro Leu Thr
1 5
<210> 70
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 70
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Tyr Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Val Pro Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Gly Gly Gly Tyr Ala Arg Gly Asp His Tyr Tyr Gly Met
100 105 110
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 71
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 71
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Arg Gly
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Glu Gly Thr Ala Tyr Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Gly Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Ser Asp Tyr Gly Leu Pro Arg Gly Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 72
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 72
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Ser Leu Phe Pro Pro
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 73
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 73
Gly Thr Phe Ser Arg Gly Ala Ile Ser
1 5
<210> 74
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 74
Gly Ile Ile Pro Ile Glu Gly Thr Ala Tyr Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 75
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 75
Ala Arg Gln Ser Asp Tyr Gly Leu Pro Arg Gly Met Asp Val
1 5 10
<210> 76
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 76
Arg Ala Ser Gln Gly Ile Ser Ser Trp Leu Ala
1 5 10
<210> 77
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 77
Gly Ala Ser Ser Leu Gln Ser
1 5
<210> 78
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 78
Gln Gln Ala Ser Leu Phe Pro Pro Thr
1 5
<210> 79
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 79
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 80
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 80
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Leu Val Phe Pro Pro
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 81
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 81
Gly Thr Phe Ser Ser Tyr Ala Ile Ser
1 5
<210> 82
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 82
Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 83
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 83
Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr
1 5 10
<210> 84
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 84
Arg Ala Ser Gln Ser Val Ser Ser Tyr Leu Ala
1 5 10
<210> 85
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 85
Asp Ala Ser Asn Arg Ala Thr
1 5
<210> 86
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 86
Gln Gln Arg Leu Val Phe Pro Pro Thr
1 5
<210> 87
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 87
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 88
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 88
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Lys Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 89
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 89
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Val Arg Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala Gln Arg Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 90
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 90
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln His Ser Val Phe Pro Pro
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 91
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 91
Gly Thr Phe Val Arg Tyr Ala Ile Ser
1 5
<210> 92
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 92
Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala Gln Arg Phe Gln
1 5 10 15
Gly
<210> 93
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 93
Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr
1 5 10
<210> 94
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 94
Gln Gln His Ser Val Phe Pro Pro Thr
1 5
<210> 95
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 95
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Val Arg Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala Gln Lys Phe
50 55 60
Arg Gly Arg Ala Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 96
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 96
Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala Gln Lys Phe Arg
1 5 10 15
Gly
<210> 97
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 97
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Tyr Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Val Pro Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Gly Gly Gly Tyr Ala Arg Gly Asp His Tyr Tyr Gly Met
100 105 110
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 98
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 98
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Arg Gly
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Glu Gly Thr Ala Tyr Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Ser Asp Tyr Gly Leu Pro Arg Gly Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 99
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 99
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Ser Gly Phe Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 100
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 100
Gly Ile Ile Pro Ile Ser Gly Phe Ala Asn Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 101
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 101
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Val Arg Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 102
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 102
Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 103
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 103
Ala Arg Asp Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
1 5 10 15
Phe Asp Ile
<210> 104
<211> 126
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 104
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu
20 25 30
Tyr Met Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Tyr His Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Gly Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 105
<211> 127
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 105
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Gly
20 25 30
Gly Ala Val Trp Ser Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Gly Ile Ala Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Asp Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His
100 105 110
Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 106
<211> 684
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 106
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Tyr Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Val Pro Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Gly Gly Gly Tyr Ala Arg Gly Asp His Tyr Tyr Gly Met
100 105 110
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser
225 230 235 240
Gly Ala Glu Val Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys
245 250 255
Ala Ser Gly Gly Thr Phe Ser Ser Tyr Tyr Ile Ser Trp Val Arg Gln
260 265 270
Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Val Pro
275 280 285
Gly Thr Ala Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr
290 295 300
Ala Asp Glu Ser Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg
305 310 315 320
Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ala Gly Gly Gly Tyr
325 330 335
Ala Arg Gly Asp His Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr
340 345 350
Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
355 360 365
Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly
370 375 380
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
385 390 395 400
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
405 410 415
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
420 425 430
Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser
435 440 445
Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys
450 455 460
Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu
465 470 475 480
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
485 490 495
Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln
500 505 510
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
515 520 525
Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu
530 535 540
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
545 550 555 560
Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys
565 570 575
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
580 585 590
Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
595 600 605
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
610 615 620
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
625 630 635 640
Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln
645 650 655
Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
660 665 670
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
675 680
<210> 107
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 107
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Lys
85 90 95
Ile Gly Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 108
<211> 676
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 108
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Arg Gly
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Glu Gly Thr Ala Tyr Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Ser Asp Tyr Gly Leu Pro Arg Gly Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
210 215 220
Gly Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
225 230 235 240
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly
245 250 255
Thr Phe Ser Arg Gly Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln
260 265 270
Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Glu Gly Thr Ala Tyr
275 280 285
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser
290 295 300
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
305 310 315 320
Ala Val Tyr Tyr Cys Ala Arg Gln Ser Asp Tyr Gly Leu Pro Arg Gly
325 330 335
Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser
340 345 350
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr
355 360 365
Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
370 375 380
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
385 390 395 400
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
405 410 415
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr
420 425 430
Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
435 440 445
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe
450 455 460
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
465 470 475 480
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
485 490 495
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
500 505 510
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
515 520 525
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
530 535 540
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
545 550 555 560
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
565 570 575
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
580 585 590
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
595 600 605
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
610 615 620
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
625 630 635 640
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
645 650 655
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
660 665 670
Leu Ser Leu Gly
675
<210> 109
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 109
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Ser Leu Phe Pro Pro
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 110
<211> 674
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 110
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Ser Gly Phe Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Gly
210 215 220
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
225 230 235 240
Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr
245 250 255
Phe Ser Ser Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly
260 265 270
Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Ser Gly Phe Ala Asn Tyr
275 280 285
Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr
290 295 300
Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
305 310 315 320
Val Tyr Tyr Cys Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro
325 330 335
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys
340 345 350
Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu
355 360 365
Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
370 375 380
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
385 390 395 400
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
405 410 415
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn
420 425 430
Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser
435 440 445
Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly
450 455 460
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
465 470 475 480
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln
485 490 495
Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val
500 505 510
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr
515 520 525
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
530 535 540
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile
545 550 555 560
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
565 570 575
Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser
580 585 590
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
595 600 605
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
610 615 620
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val
625 630 635 640
Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met
645 650 655
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
660 665 670
Leu Gly
<210> 111
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 111
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Leu Val Phe Pro Pro
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 112
<211> 672
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 112
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Val Arg Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Gly Gly
210 215 220
Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys
225 230 235 240
Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe
245 250 255
Val Arg Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu
260 265 270
Glu Trp Met Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala
275 280 285
Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser
290 295 300
Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val
305 310 315 320
Tyr Tyr Cys Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp
325 330 335
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
340 345 350
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
355 360 365
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
370 375 380
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
385 390 395 400
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
405 410 415
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
420 425 430
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
435 440 445
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro
450 455 460
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
465 470 475 480
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
485 490 495
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
500 505 510
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val
515 520 525
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
530 535 540
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
545 550 555 560
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
565 570 575
Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr
580 585 590
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
595 600 605
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
610 615 620
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys
625 630 635 640
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
645 650 655
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
660 665 670
<210> 113
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 113
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln His Ser Val Phe Pro Pro
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 114
<211> 686
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 114
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu
20 25 30
Tyr Met Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Tyr His Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Gly Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
225 230 235 240
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
245 250 255
Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu Tyr Met Trp Gly Trp Ile
260 265 270
Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Leu Ile Tyr His
275 280 285
Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile
290 295 300
Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val
305 310 315 320
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Gly Arg
325 330 335
Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly Gln
340 345 350
Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
355 360 365
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
370 375 380
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
385 390 395 400
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
405 410 415
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
420 425 430
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
435 440 445
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
450 455 460
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
465 470 475 480
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
485 490 495
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
500 505 510
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
515 520 525
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
530 535 540
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
545 550 555 560
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
565 570 575
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
580 585 590
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
595 600 605
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
610 615 620
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
625 630 635 640
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
645 650 655
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
660 665 670
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
675 680 685
<210> 115
<211> 688
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 115
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Gly
20 25 30
Gly Ala Val Trp Ser Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Gly Ile Ala Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Asp Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His
100 105 110
Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala
115 120 125
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser
130 135 140
Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
145 150 155 160
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
165 170 175
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
180 185 190
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr
195 200 205
Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg
210 215 220
Val Glu Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln
225 230 235 240
Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln Thr Leu Ser Leu Thr
245 250 255
Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Gly Gly Ala Val Trp Ser
260 265 270
Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu Trp Ile Gly Gly Ile
275 280 285
Ala Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val
290 295 300
Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser
305 310 315 320
Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser
325 330 335
Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp
340 345 350
Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
355 360 365
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
370 375 380
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
385 390 395 400
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
405 410 415
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
420 425 430
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
435 440 445
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
450 455 460
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro
465 470 475 480
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
485 490 495
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
500 505 510
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
515 520 525
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val
530 535 540
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
545 550 555 560
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
565 570 575
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
580 585 590
Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr
595 600 605
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
610 615 620
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
625 630 635 640
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys
645 650 655
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
660 665 670
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
675 680 685
<210> 116
<211> 694
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 116
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Tyr Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Val Pro Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Gly Gly Gly Tyr Ala Arg Gly Asp His Tyr Tyr Gly Met
100 105 110
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser
130 135 140
Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys
195 200 205
Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu
225 230 235 240
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
260 265 270
Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val
355 360 365
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Leu Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
450 455 460
Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro
465 470 475 480
Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser
485 490 495
Ser Tyr Tyr Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu
500 505 510
Trp Met Gly Gly Ile Ile Pro Val Pro Gly Thr Ala Asn Tyr Ala Gln
515 520 525
Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr
530 535 540
Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr
545 550 555 560
Tyr Cys Ala Arg Ala Gly Gly Gly Tyr Ala Arg Gly Asp His Tyr Tyr
565 570 575
Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala
580 585 590
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser
595 600 605
Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
610 615 620
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
625 630 635 640
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
645 650 655
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr
660 665 670
Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg
675 680 685
Val Glu Pro Lys Ser Cys
690
<210> 117
<211> 686
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 117
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Arg Gly
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Glu Gly Thr Ala Tyr Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Ser Asp Tyr Gly Leu Pro Arg Gly Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly
210 215 220
Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro
260 265 270
Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser
405 410 415
Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Gly
435 440 445
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val
450 455 460
Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser Ser Val
465 470 475 480
Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Arg Gly Ala Ile
485 490 495
Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Gly
500 505 510
Ile Ile Pro Ile Glu Gly Thr Ala Tyr Tyr Ala Gln Lys Phe Gln Gly
515 520 525
Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr Met Glu
530 535 540
Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg
545 550 555 560
Gln Ser Asp Tyr Gly Leu Pro Arg Gly Met Asp Val Trp Gly Gln Gly
565 570 575
Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
580 585 590
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
595 600 605
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
610 615 620
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
625 630 635 640
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
645 650 655
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
660 665 670
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
675 680 685
<210> 118
<211> 684
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 118
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Ser Gly Phe Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
210 215 220
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Gly Gly
435 440 445
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln
450 455 460
Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser Ser Val Lys
465 470 475 480
Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr Ala Ile Ser
485 490 495
Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile
500 505 510
Ile Pro Ile Ser Gly Phe Ala Asn Tyr Ala Gln Lys Phe Gln Gly Arg
515 520 525
Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr Met Glu Leu
530 535 540
Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Glu
545 550 555 560
Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr Trp Gly Gln Gly Thr Leu
565 570 575
Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
580 585 590
Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys
595 600 605
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
610 615 620
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
625 630 635 640
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
645 650 655
Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn
660 665 670
Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
675 680
<210> 119
<211> 682
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 119
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Val Arg Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val
260 265 270
Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Gly Gly Gly
435 440 445
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu
450 455 460
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser Ser Val Lys Val
465 470 475 480
Ser Cys Lys Ala Ser Gly Gly Thr Phe Val Arg Tyr Ala Ile Ser Trp
485 490 495
Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Ile
500 505 510
Pro Ile Phe Gly Glu Ala Gln Tyr Ala Gln Lys Phe Gln Gly Arg Val
515 520 525
Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr Met Glu Leu Ser
530 535 540
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Glu Gly
545 550 555 560
Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp Gly Gln Gly Thr Leu Val Thr
565 570 575
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
580 585 590
Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val
595 600 605
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
610 615 620
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
625 630 635 640
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
645 650 655
Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys
660 665 670
Val Asp Lys Arg Val Glu Pro Lys Ser Cys
675 680
<210> 120
<211> 696
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 120
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu
20 25 30
Tyr Met Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Tyr His Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Gly Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr
130 135 140
Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr
195 200 205
Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
260 265 270
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
275 280 285
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
305 310 315 320
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
325 330 335
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
340 345 350
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
355 360 365
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
370 375 380
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
385 390 395 400
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
405 410 415
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
435 440 445
Leu Ser Leu Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
450 455 460
Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys
465 470 475 480
Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile
485 490 495
Ser Ser Glu Tyr Met Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly
500 505 510
Leu Glu Trp Ile Gly Leu Ile Tyr His Ser Gly Lys Thr Tyr Tyr Asn
515 520 525
Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn
530 535 540
Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val
545 550 555 560
Tyr Tyr Cys Ala Arg Asp Ser Gly Arg Gly Tyr Gly Asp Tyr Gly Gly
565 570 575
His His Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser
580 585 590
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
595 600 605
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
610 615 620
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
625 630 635 640
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
645 650 655
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
660 665 670
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
675 680 685
Lys Arg Val Glu Pro Lys Ser Cys
690 695
<210> 121
<211> 698
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 121
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Gly
20 25 30
Gly Ala Val Trp Ser Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Gly Ile Ala Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Asp Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His
100 105 110
Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala
115 120 125
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser
130 135 140
Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
145 150 155 160
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
165 170 175
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
180 185 190
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr
195 200 205
Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg
210 215 220
Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
325 330 335
Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Leu Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
450 455 460
Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val
465 470 475 480
Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser
485 490 495
Ile Ser Ser Gly Gly Ala Val Trp Ser Trp Ile Arg Gln His Pro Gly
500 505 510
Lys Gly Leu Glu Trp Ile Gly Gly Ile Ala Tyr Ser Gly Ser Thr Tyr
515 520 525
Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser
530 535 540
Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr
545 550 555 560
Ala Val Tyr Tyr Cys Ala Arg Asp Ser Val Arg Gly Tyr Gly Asp Tyr
565 570 575
Gly Gly His His Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr
580 585 590
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
595 600 605
Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val
610 615 620
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
625 630 635 640
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
645 650 655
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
660 665 670
Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys
675 680 685
Val Asp Lys Arg Val Glu Pro Lys Ser Cys
690 695
<210> 122
<211> 686
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 122
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu
20 25 30
Tyr Met Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Tyr His Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Gly Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr
130 135 140
Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr
195 200 205
Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
260 265 270
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
275 280 285
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
305 310 315 320
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
325 330 335
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
340 345 350
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
355 360 365
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
370 375 380
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
385 390 395 400
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
405 410 415
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
435 440 445
Leu Ser Leu Gly Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser
450 455 460
Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala
465 470 475 480
Val Ser Gly Tyr Ser Ile Ser Ser Glu Tyr Met Trp Gly Trp Ile Arg
485 490 495
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Leu Ile Tyr His Ser
500 505 510
Gly Lys Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser
515 520 525
Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr
530 535 540
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Gly Arg Gly
545 550 555 560
Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly Gln Gly
565 570 575
Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
580 585 590
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
595 600 605
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
610 615 620
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
625 630 635 640
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
645 650 655
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
660 665 670
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
675 680 685
<210> 123
<211> 688
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 123
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Gly
20 25 30
Gly Ala Val Trp Ser Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Gly Ile Ala Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Asp Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His
100 105 110
Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala
115 120 125
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser
130 135 140
Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
145 150 155 160
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
165 170 175
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
180 185 190
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr
195 200 205
Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg
210 215 220
Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
325 330 335
Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Leu Gly Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
450 455 460
Ser Gly Pro Gly Leu Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys
465 470 475 480
Thr Val Ser Gly Gly Ser Ile Ser Ser Gly Gly Ala Val Trp Ser Trp
485 490 495
Ile Arg Gln His Pro Gly Lys Gly Leu Glu Trp Ile Gly Gly Ile Ala
500 505 510
Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr
515 520 525
Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser
530 535 540
Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser Val
545 550 555 560
Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly
565 570 575
Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
580 585 590
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
595 600 605
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
610 615 620
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
625 630 635 640
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
645 650 655
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
660 665 670
Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
675 680 685
<210> 124
<211> 672
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 124
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Thr Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gln Tyr Gly Tyr Tyr Gly Gly Arg Leu Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
210 215 220
Gly Gly Gly Gly Ser Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val
225 230 235 240
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
245 250 255
Thr Phe Ser Ser Tyr Gly Met His Trp Val Arg Gln Ala Pro Gly Lys
260 265 270
Gly Leu Glu Trp Val Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr
275 280 285
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
290 295 300
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
305 310 315 320
Ala Val Tyr Tyr Cys Ala Arg Asp Gly Leu Gly Tyr Met Ala Trp Gly
325 330 335
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
340 345 350
Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala
355 360 365
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
370 375 380
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
385 390 395 400
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
405 410 415
Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His
420 425 430
Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly
435 440 445
Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser
450 455 460
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
465 470 475 480
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro
485 490 495
Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
500 505 510
Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val
515 520 525
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
530 535 540
Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr
545 550 555 560
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
565 570 575
Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
580 585 590
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
595 600 605
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
610 615 620
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser
625 630 635 640
Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
645 650 655
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
660 665 670
<210> 125
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 125
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Ile Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 126
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 126
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Thr Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gln Tyr Gly Tyr Tyr Gly Gly Arg Leu Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 127
<211> 116
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 127
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Leu Gly Tyr Met Ala Trp Gly Gln Gly Thr Thr Val
100 105 110
Thr Val Ser Ser
115
<210> 128
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 128
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Ile Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 129
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 129
Tyr Thr Phe Thr Ser Tyr Tyr Met His
1 5
<210> 130
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 130
Ile Ile Asn Pro Ser Gly Gly Ser Thr Thr Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 131
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 131
Ala Arg Gly Gln Tyr Gly Tyr Tyr Gly Gly Arg Leu Asp Val
1 5 10
<210> 132
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 132
Phe Thr Phe Ser Ser Tyr Gly Met His
1 5
<210> 133
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 133
Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 134
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 134
Ala Arg Asp Gly Leu Gly Tyr Met Ala
1 5
<210> 135
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 135
Met Gln Ala Leu Gln Thr Pro Ile Thr
1 5
<210> 136
<211> 672
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 136
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Leu Gly Tyr Met Ala Trp Gly Gln Gly Thr Thr Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro
210 215 220
Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
225 230 235 240
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
245 250 255
Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn
260 265 270
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
275 280 285
Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
290 295 300
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
305 310 315 320
Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys
325 330 335
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu
340 345 350
Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
355 360 365
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
370 375 380
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
385 390 395 400
Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly
405 410 415
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
420 425 430
Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys Gly Gly Gly Gly Ser
435 440 445
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
450 455 460
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
465 470 475 480
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
485 490 495
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Thr Tyr Ala Gln Lys Phe
500 505 510
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
515 520 525
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
530 535 540
Ala Arg Gly Gln Tyr Gly Tyr Tyr Gly Gly Arg Leu Asp Val Trp Gly
545 550 555 560
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
565 570 575
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
580 585 590
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
595 600 605
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
610 615 620
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
625 630 635 640
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
645 650 655
Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
660 665 670
<210> 137
<211> 103
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 137
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Pro Lys Ser Cys
100
<210> 138
<211> 327
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 138
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro
100 105 110
Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Leu Gly Lys
325
<210> 139
<211> 326
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 139
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro
100 105 110
Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Leu Gly
325
<210> 140
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 140
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 141
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="Val"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /замена="Asp" или "Leu", или "Arg"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Asp"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Asn" или "Ser", или "Ala"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Asp" или "Gly"
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (1)..(19)
<223> /примечание="Варианты остатков, приведенные в
последовательности, не имеют преимущества по отношению к остаткам в
аннотациях положений вариантов"
<400> 141
Ala His Glu Arg Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
1 5 10 15
Phe Asp Ile
<210> 142
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="Leu" или "Ser"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Ala" или "Val"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Tyr" или "His"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Lys"
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (1)..(16)
<223> /примечание="Варианты остатков, приведенные в
последовательности, не имеют преимущества по отношению к остаткам в
аннотациях положений вариантов"
<400> 142
Gly Ile Tyr Glu Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 143
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="Gly"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Ser" или "Glu"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Gly" или "Ser", или "Tyr", или "Ala"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="Ala" или "Tyr", или "Met"
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /замена="Ala" или " "
<220>
<221> ВАРИАНТ
<222> (11)..(11)
<223> /замена="Gly"
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (1)..(11)
<223> /примечание="Варианты остатков, приведенные в
последовательности, не имеют преимущества по отношению к остаткам в
аннотациях положений вариантов"
<400> 143
Tyr Ser Ile Ser Ser Gly Leu Gly Val Trp Ser
1 5 10
<210> 144
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Asn"
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /замена="Ser"
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (1)..(9)
<223> /примечание="Варианты остатков, приведенные в
последовательности, не имеют преимущества по отношению к остаткам в
аннотациях положений вариантов"
<400> 144
Gln Gln Glu Tyr Ala Thr Pro Pro Thr
1 5
<210> 145
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="Ser"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Ser"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Asp" или "Lys", или "Glu"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Tyr"
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (1)..(7)
<223> /примечание="Варианты остатков, приведенные в
последовательности, не имеют преимущества по отношению к остаткам в
аннотациях положений вариантов"
<400> 145
Ala Ala Asp Ser Leu Gln Ser
1 5
<210> 146
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="Arg"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Lys"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Asp" или "Asn"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="Thr"
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (1)..(11)
<223> /примечание="Варианты остатков, приведенные в
последовательности, не имеют преимущества по отношению к остаткам в
аннотациях положений вариантов"
<400> 146
Gly Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn
1 5 10
<210> 147
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический
пептид"
<220>
<221> ВАРИАНТ
<222> (14)..(14)
<223> /замена="Arg"
<220>
<221> ВАРИАНТ
<222> (16)..(16)
<223> /замена="Arg"
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (1)..(17)
<223> /примечание="Варианты остатков, приведенные в
последовательности, не имеют преимущества по отношению к остаткам в
аннотациях положений вариантов"
<400> 147
Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 148
<211> 456
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 148
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Leu Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Gly Ile Tyr Glu Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Glu Arg Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
210 215 220
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Tyr Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
325 330 335
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
355 360 365
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 149
<211> 457
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 149
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Gly
20 25 30
Gly Ala Val Trp Ser Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Gly Ile Ala Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Asp Glu Asn Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His
100 105 110
Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala
115 120 125
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser
130 135 140
Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
145 150 155 160
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
165 170 175
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
180 185 190
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr
195 200 205
Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys
210 215 220
Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
225 230 235 240
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
245 250 255
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
260 265 270
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
275 280 285
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
290 295 300
Gln Tyr Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
305 310 315 320
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
325 330 335
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
340 345 350
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
355 360 365
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
370 375 380
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
385 390 395 400
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
405 410 415
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
420 425 430
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
435 440 445
Lys Ser Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 150
<211> 456
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 150
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Ala Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Glu Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
210 215 220
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Tyr Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
325 330 335
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
355 360 365
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 151
<211> 456
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 151
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Ala Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Pro Glu Trp
35 40 45
Ile Gly Leu Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Glu Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
210 215 220
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Tyr Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
325 330 335
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
355 360 365
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 152
<211> 456
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 152
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Ala Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Glu Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
210 215 220
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Tyr Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
325 330 335
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
355 360 365
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 153
<211> 456
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 153
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu
20 25 30
Tyr Met Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Tyr His Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Ala Asp Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
210 215 220
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Tyr Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
325 330 335
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
355 360 365
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 154
<211> 456
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 154
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu
20 25 30
Tyr Met Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Tyr His Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Ala Asp Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
210 215 220
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Tyr Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
325 330 335
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
355 360 365
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 155
<211> 457
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 155
Gln Leu Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Ser
20 25 30
Ser Tyr Ala Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Asp Ser Gly Arg Gly Tyr Gly Asp Tyr Gly Gly His His
100 105 110
Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala
115 120 125
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser
130 135 140
Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
145 150 155 160
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
165 170 175
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
180 185 190
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr
195 200 205
Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys
210 215 220
Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
225 230 235 240
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
245 250 255
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
260 265 270
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
275 280 285
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
290 295 300
Gln Tyr Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
305 310 315 320
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
325 330 335
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
340 345 350
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
355 360 365
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
370 375 380
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
385 390 395 400
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
405 410 415
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
420 425 430
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
435 440 445
Lys Ser Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 156
<211> 454
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 156
Gln Leu Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Ser
20 25 30
Ser Tyr Ala Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Asp Ser Gly Arg Gly Tyr Gly Asp Tyr Gly Gly His His
100 105 110
Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala
115 120 125
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser
130 135 140
Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
145 150 155 160
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
165 170 175
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
180 185 190
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr
195 200 205
Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg
210 215 220
Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
325 330 335
Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Leu Gly Lys
450
<210> 157
<211> 455
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 157
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Tyr Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Val Pro Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Gly Gly Gly Tyr Ala Arg Gly Asp His Tyr Tyr Gly Met
100 105 110
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu
210 215 220
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
225 230 235 240
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
275 280 285
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
290 295 300
Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
305 310 315 320
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
325 330 335
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
340 345 350
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys
355 360 365
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
370 375 380
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
385 390 395 400
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
405 410 415
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
420 425 430
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
435 440 445
Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 158
<211> 451
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 158
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Arg Gly
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Glu Gly Thr Ala Tyr Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Ser Asp Tyr Gly Leu Pro Arg Gly Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 159
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 159
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Ser Gly Phe Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 160
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 160
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Val Arg Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 161
<211> 456
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 161
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu
20 25 30
Tyr Met Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Tyr His Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Gly Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
210 215 220
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Tyr Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
325 330 335
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
355 360 365
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 162
<211> 457
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 162
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Gly
20 25 30
Gly Ala Val Trp Ser Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Gly Ile Ala Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Asp Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His
100 105 110
Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala
115 120 125
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser
130 135 140
Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
145 150 155 160
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
165 170 175
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
180 185 190
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr
195 200 205
Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys
210 215 220
Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
225 230 235 240
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
245 250 255
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
260 265 270
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
275 280 285
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
290 295 300
Gln Tyr Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
305 310 315 320
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
325 330 335
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
340 345 350
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
355 360 365
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
370 375 380
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
385 390 395 400
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
405 410 415
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
420 425 430
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
435 440 445
Lys Ser Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 163
<211> 685
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 163
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Arg Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Tyr Ile Ser Trp Val Arg Gln Val Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Val Pro Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Gly Gly Gly Tyr Ala Arg Gly Asp His Tyr Tyr Gly Met
100 105 110
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser
225 230 235 240
Gly Ala Glu Val Lys Arg Pro Gly Ser Ser Val Lys Val Ser Cys Lys
245 250 255
Ala Ser Gly Gly Thr Phe Ser Ser Tyr Tyr Ile Ser Trp Val Arg Gln
260 265 270
Val Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Val Pro
275 280 285
Gly Thr Ala Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr
290 295 300
Ala Asp Glu Ser Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg
305 310 315 320
Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ala Gly Gly Gly Tyr
325 330 335
Ala Arg Gly Asp His Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr
340 345 350
Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
355 360 365
Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly
370 375 380
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
385 390 395 400
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
405 410 415
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
420 425 430
Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser
435 440 445
Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys
450 455 460
Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu
465 470 475 480
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
485 490 495
Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln
500 505 510
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
515 520 525
Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu
530 535 540
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
545 550 555 560
Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys
565 570 575
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
580 585 590
Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
595 600 605
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
610 615 620
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
625 630 635 640
Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln
645 650 655
Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
660 665 670
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
675 680 685
<210> 164
<211> 685
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 164
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Tyr Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Val Pro Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Gly Gly Gly Tyr Ala Arg Gly Asp His Tyr Tyr Gly Met
100 105 110
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser
225 230 235 240
Gly Ala Glu Val Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys
245 250 255
Ala Ser Gly Gly Thr Phe Ser Ser Tyr Tyr Ile Ser Trp Val Arg Gln
260 265 270
Ala Pro Gly Gln Arg Leu Glu Trp Met Gly Gly Ile Ile Pro Val Pro
275 280 285
Gly Thr Ala Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr
290 295 300
Ala Asp Glu Ser Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg
305 310 315 320
Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ala Gly Gly Gly Tyr
325 330 335
Ala Arg Gly Asp His Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr
340 345 350
Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
355 360 365
Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly
370 375 380
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
385 390 395 400
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
405 410 415
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
420 425 430
Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser
435 440 445
Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys
450 455 460
Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu
465 470 475 480
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
485 490 495
Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln
500 505 510
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
515 520 525
Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu
530 535 540
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
545 550 555 560
Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys
565 570 575
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
580 585 590
Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
595 600 605
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
610 615 620
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
625 630 635 640
Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln
645 650 655
Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
660 665 670
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
675 680 685
<210> 165
<211> 677
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 165
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Arg Gly
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Glu Gly Thr Ala Tyr Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Gly Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Ser Asp Tyr Gly Leu Pro Arg Gly Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
210 215 220
Gly Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
225 230 235 240
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly
245 250 255
Thr Phe Ser Arg Gly Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln
260 265 270
Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Glu Gly Thr Ala Tyr
275 280 285
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser
290 295 300
Thr Gly Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
305 310 315 320
Ala Val Tyr Tyr Cys Ala Arg Gln Ser Asp Tyr Gly Leu Pro Arg Gly
325 330 335
Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser
340 345 350
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr
355 360 365
Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
370 375 380
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
385 390 395 400
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
405 410 415
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr
420 425 430
Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
435 440 445
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe
450 455 460
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
465 470 475 480
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
485 490 495
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
500 505 510
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
515 520 525
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
530 535 540
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
545 550 555 560
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
565 570 575
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
580 585 590
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
595 600 605
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
610 615 620
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
625 630 635 640
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
645 650 655
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
660 665 670
Leu Ser Leu Gly Lys
675
<210> 166
<211> 675
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 166
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Gly
210 215 220
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
225 230 235 240
Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr
245 250 255
Phe Ser Ser Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly
260 265 270
Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr
275 280 285
Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr
290 295 300
Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
305 310 315 320
Val Tyr Tyr Cys Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro
325 330 335
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys
340 345 350
Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu
355 360 365
Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
370 375 380
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
385 390 395 400
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
405 410 415
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn
420 425 430
Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser
435 440 445
Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly
450 455 460
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
465 470 475 480
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln
485 490 495
Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val
500 505 510
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr
515 520 525
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
530 535 540
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile
545 550 555 560
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
565 570 575
Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser
580 585 590
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
595 600 605
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
610 615 620
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val
625 630 635 640
Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met
645 650 655
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
660 665 670
Leu Gly Lys
675
<210> 167
<211> 675
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 167
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Gly
210 215 220
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
225 230 235 240
Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr
245 250 255
Phe Ser Ser Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Arg
260 265 270
Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr
275 280 285
Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr
290 295 300
Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
305 310 315 320
Val Tyr Tyr Cys Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro
325 330 335
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys
340 345 350
Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu
355 360 365
Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
370 375 380
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
385 390 395 400
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
405 410 415
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn
420 425 430
Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser
435 440 445
Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly
450 455 460
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
465 470 475 480
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln
485 490 495
Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val
500 505 510
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr
515 520 525
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
530 535 540
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile
545 550 555 560
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
565 570 575
Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser
580 585 590
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
595 600 605
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
610 615 620
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val
625 630 635 640
Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met
645 650 655
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
660 665 670
Leu Gly Lys
675
<210> 168
<211> 675
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 168
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Lys Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Gly
210 215 220
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
225 230 235 240
Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr
245 250 255
Phe Ser Ser Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly
260 265 270
Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr
275 280 285
Ala Gln Lys Phe Gln Gly Lys Val Thr Ile Thr Ala Asp Glu Ser Thr
290 295 300
Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
305 310 315 320
Val Tyr Tyr Cys Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro
325 330 335
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys
340 345 350
Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu
355 360 365
Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
370 375 380
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
385 390 395 400
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
405 410 415
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn
420 425 430
Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser
435 440 445
Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly
450 455 460
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
465 470 475 480
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln
485 490 495
Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val
500 505 510
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr
515 520 525
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
530 535 540
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile
545 550 555 560
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
565 570 575
Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser
580 585 590
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
595 600 605
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
610 615 620
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val
625 630 635 640
Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met
645 650 655
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
660 665 670
Leu Gly Lys
675
<210> 169
<211> 673
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 169
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Val Arg Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala Gln Arg Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Gly Gly
210 215 220
Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys
225 230 235 240
Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe
245 250 255
Val Arg Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu
260 265 270
Glu Trp Met Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala
275 280 285
Gln Arg Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser
290 295 300
Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val
305 310 315 320
Tyr Tyr Cys Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp
325 330 335
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
340 345 350
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
355 360 365
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
370 375 380
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
385 390 395 400
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
405 410 415
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
420 425 430
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
435 440 445
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro
450 455 460
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
465 470 475 480
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
485 490 495
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
500 505 510
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val
515 520 525
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
530 535 540
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
545 550 555 560
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
565 570 575
Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr
580 585 590
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
595 600 605
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
610 615 620
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys
625 630 635 640
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
645 650 655
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
660 665 670
Lys
<210> 170
<211> 673
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 170
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Val Arg Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala Gln Lys Phe
50 55 60
Arg Gly Arg Ala Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Gly Gly
210 215 220
Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys
225 230 235 240
Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe
245 250 255
Val Arg Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu
260 265 270
Glu Trp Met Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala
275 280 285
Gln Lys Phe Arg Gly Arg Ala Thr Ile Thr Ala Asp Glu Ser Thr Ser
290 295 300
Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val
305 310 315 320
Tyr Tyr Cys Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp
325 330 335
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
340 345 350
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
355 360 365
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
370 375 380
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
385 390 395 400
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
405 410 415
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
420 425 430
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
435 440 445
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro
450 455 460
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
465 470 475 480
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
485 490 495
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
500 505 510
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val
515 520 525
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
530 535 540
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
545 550 555 560
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
565 570 575
Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr
580 585 590
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
595 600 605
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
610 615 620
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys
625 630 635 640
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
645 650 655
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
660 665 670
Lys
<210> 171
<211> 455
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 171
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Arg Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Tyr Ile Ser Trp Val Arg Gln Val Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Val Pro Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Gly Gly Gly Tyr Ala Arg Gly Asp His Tyr Tyr Gly Met
100 105 110
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu
210 215 220
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
225 230 235 240
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
275 280 285
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
290 295 300
Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
305 310 315 320
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
325 330 335
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
340 345 350
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys
355 360 365
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
370 375 380
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
385 390 395 400
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
405 410 415
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
420 425 430
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
435 440 445
Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 172
<211> 455
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 172
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Tyr Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Val Pro Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Gly Gly Gly Tyr Ala Arg Gly Asp His Tyr Tyr Gly Met
100 105 110
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu
210 215 220
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
225 230 235 240
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
275 280 285
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
290 295 300
Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
305 310 315 320
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
325 330 335
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
340 345 350
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys
355 360 365
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
370 375 380
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
385 390 395 400
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
405 410 415
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
420 425 430
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
435 440 445
Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 173
<211> 451
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 173
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Arg Gly
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Glu Gly Thr Ala Tyr Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Gly Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Ser Asp Tyr Gly Leu Pro Arg Gly Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 174
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 174
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 175
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 175
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 176
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 176
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Lys Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 177
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 177
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Val Arg Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala Gln Arg Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 178
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 178
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Val Arg Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala Gln Lys Phe
50 55 60
Arg Gly Arg Ala Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 179
<211> 451
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 179
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Thr Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gln Tyr Gly Tyr Tyr Gly Gly Arg Leu Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 180
<211> 448
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 180
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Thr Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gln Tyr Gly Tyr Tyr Gly Gly Arg Leu Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly
210 215 220
Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro
260 265 270
Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser
405 410 415
Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 181
<211> 446
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 181
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Leu Gly Tyr Met Ala Trp Gly Gln Gly Thr Thr Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 182
<211> 443
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 182
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Leu Gly Tyr Met Ala Trp Gly Gln Gly Thr Thr Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro
210 215 220
Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
225 230 235 240
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
245 250 255
Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn
260 265 270
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
275 280 285
Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
290 295 300
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
305 310 315 320
Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys
325 330 335
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu
340 345 350
Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
355 360 365
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
370 375 380
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
385 390 395 400
Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly
405 410 415
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
420 425 430
Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440
<210> 183
<211> 690
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 183
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Leu Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Gly Ile Tyr Glu Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Glu Arg Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
225 230 235 240
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
245 250 255
Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly Leu Gly Trp Gly Trp Ile
260 265 270
Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Gly Ile Tyr Glu
275 280 285
Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile
290 295 300
Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val
305 310 315 320
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala His Glu Arg Val Arg
325 330 335
Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly Gln
340 345 350
Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
355 360 365
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
370 375 380
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
385 390 395 400
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
405 410 415
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
420 425 430
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
435 440 445
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp
450 455 460
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
465 470 475 480
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
485 490 495
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
500 505 510
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
515 520 525
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
530 535 540
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
545 550 555 560
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
565 570 575
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
580 585 590
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
595 600 605
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
610 615 620
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
625 630 635 640
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
645 650 655
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
660 665 670
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
675 680 685
Gly Lys
690
<210> 184
<211> 692
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 184
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Gly
20 25 30
Gly Ala Val Trp Ser Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Gly Ile Ala Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Asp Glu Asn Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His
100 105 110
Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala
115 120 125
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser
130 135 140
Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
145 150 155 160
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
165 170 175
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
180 185 190
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr
195 200 205
Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg
210 215 220
Val Glu Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln
225 230 235 240
Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln Thr Leu Ser Leu Thr
245 250 255
Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Gly Gly Ala Val Trp Ser
260 265 270
Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu Trp Ile Gly Gly Ile
275 280 285
Ala Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val
290 295 300
Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser
305 310 315 320
Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Asp Glu Asn
325 330 335
Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp
340 345 350
Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
355 360 365
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
370 375 380
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
385 390 395 400
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
405 410 415
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
420 425 430
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
435 440 445
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser
450 455 460
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
465 470 475 480
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
485 490 495
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
500 505 510
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
515 520 525
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
530 535 540
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
545 550 555 560
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
565 570 575
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
580 585 590
Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val
595 600 605
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
610 615 620
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
625 630 635 640
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
645 650 655
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
660 665 670
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
675 680 685
Ser Pro Gly Lys
690
<210> 185
<211> 690
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 185
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Ala Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Glu Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
225 230 235 240
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
245 250 255
Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly Ala Gly Trp Gly Trp Ile
260 265 270
Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Leu Ile Val His
275 280 285
Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile
290 295 300
Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val
305 310 315 320
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Val Leu Glu Ser Val Arg
325 330 335
Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly Gln
340 345 350
Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
355 360 365
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
370 375 380
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
385 390 395 400
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
405 410 415
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
420 425 430
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
435 440 445
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp
450 455 460
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
465 470 475 480
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
485 490 495
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
500 505 510
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
515 520 525
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
530 535 540
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
545 550 555 560
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
565 570 575
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
580 585 590
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
595 600 605
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
610 615 620
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
625 630 635 640
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
645 650 655
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
660 665 670
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
675 680 685
Gly Lys
690
<210> 186
<211> 690
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 186
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Ala Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Pro Glu Trp
35 40 45
Ile Gly Leu Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Glu Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
225 230 235 240
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
245 250 255
Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly Ala Gly Trp Gly Trp Ile
260 265 270
Arg Gln Pro Pro Gly Lys Gly Pro Glu Trp Ile Gly Leu Ile Val His
275 280 285
Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile
290 295 300
Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val
305 310 315 320
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Val Leu Glu Ser Val Arg
325 330 335
Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly Gln
340 345 350
Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
355 360 365
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
370 375 380
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
385 390 395 400
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
405 410 415
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
420 425 430
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
435 440 445
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp
450 455 460
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
465 470 475 480
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
485 490 495
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
500 505 510
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
515 520 525
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
530 535 540
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
545 550 555 560
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
565 570 575
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
580 585 590
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
595 600 605
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
610 615 620
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
625 630 635 640
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
645 650 655
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
660 665 670
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
675 680 685
Gly Lys
690
<210> 187
<211> 690
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 187
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Ala Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Glu Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
225 230 235 240
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
245 250 255
Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly Ala Gly Trp Gly Trp Ile
260 265 270
Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Leu Ile Val His
275 280 285
Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile
290 295 300
Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val
305 310 315 320
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Val Leu Glu Ser Val Arg
325 330 335
Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly Gln
340 345 350
Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
355 360 365
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
370 375 380
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
385 390 395 400
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
405 410 415
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
420 425 430
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
435 440 445
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp
450 455 460
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
465 470 475 480
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
485 490 495
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
500 505 510
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
515 520 525
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
530 535 540
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
545 550 555 560
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
565 570 575
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
580 585 590
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
595 600 605
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
610 615 620
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
625 630 635 640
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
645 650 655
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
660 665 670
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
675 680 685
Gly Lys
690
<210> 188
<211> 690
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 188
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Ala Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Glu Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
225 230 235 240
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
245 250 255
Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly Ala Gly Trp Gly Trp Ile
260 265 270
Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Leu Ile Val His
275 280 285
Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile
290 295 300
Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val
305 310 315 320
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Val Leu Glu Ser Val Arg
325 330 335
Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly Gln
340 345 350
Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
355 360 365
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
370 375 380
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
385 390 395 400
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
405 410 415
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
420 425 430
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
435 440 445
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp
450 455 460
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
465 470 475 480
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
485 490 495
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
500 505 510
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
515 520 525
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
530 535 540
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
545 550 555 560
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
565 570 575
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
580 585 590
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
595 600 605
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
610 615 620
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
625 630 635 640
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
645 650 655
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
660 665 670
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
675 680 685
Gly Lys
690
<210> 189
<211> 690
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 189
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu
20 25 30
Tyr Met Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Tyr His Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Ala Asp Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
225 230 235 240
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
245 250 255
Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu Tyr Met Trp Gly Trp Ile
260 265 270
Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Leu Ile Tyr His
275 280 285
Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile
290 295 300
Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val
305 310 315 320
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Glu Ala Asp Arg
325 330 335
Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly Gln
340 345 350
Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
355 360 365
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
370 375 380
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
385 390 395 400
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
405 410 415
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
420 425 430
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
435 440 445
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp
450 455 460
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
465 470 475 480
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
485 490 495
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
500 505 510
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
515 520 525
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
530 535 540
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
545 550 555 560
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
565 570 575
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
580 585 590
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
595 600 605
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
610 615 620
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
625 630 635 640
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
645 650 655
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
660 665 670
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
675 680 685
Gly Lys
690
<210> 190
<211> 690
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 190
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu
20 25 30
Tyr Met Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Tyr His Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Ala Asp Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
225 230 235 240
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
245 250 255
Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu Tyr Met Trp Gly Trp Ile
260 265 270
Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Leu Ile Tyr His
275 280 285
Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile
290 295 300
Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val
305 310 315 320
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Glu Ala Asp Arg
325 330 335
Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly Gln
340 345 350
Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
355 360 365
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
370 375 380
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
385 390 395 400
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
405 410 415
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
420 425 430
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
435 440 445
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp
450 455 460
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
465 470 475 480
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
485 490 495
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
500 505 510
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
515 520 525
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
530 535 540
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
545 550 555 560
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
565 570 575
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
580 585 590
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
595 600 605
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
610 615 620
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
625 630 635 640
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
645 650 655
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
660 665 670
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
675 680 685
Gly Lys
690
<210> 191
<211> 690
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 191
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Leu Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Gly Ile Tyr Glu Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Glu Arg Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
325 330 335
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr
355 360 365
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Pro Gly Lys Gly Gly Gly Gly Ser Gln Val Gln
450 455 460
Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser
465 470 475 480
Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly Leu Gly Trp
485 490 495
Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Gly
500 505 510
Ile Tyr Glu Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg
515 520 525
Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu
530 535 540
Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala His Glu
545 550 555 560
Arg Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile
565 570 575
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly
580 585 590
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
595 600 605
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
610 615 620
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
625 630 635 640
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
645 650 655
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
660 665 670
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys
675 680 685
Ser Cys
690
<210> 192
<211> 692
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 192
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Gly
20 25 30
Gly Ala Val Trp Ser Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Gly Ile Ala Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Asp Glu Asn Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His
100 105 110
Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala
115 120 125
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser
130 135 140
Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
145 150 155 160
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
165 170 175
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
180 185 190
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr
195 200 205
Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg
210 215 220
Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
225 230 235 240
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
245 250 255
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
260 265 270
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
275 280 285
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
290 295 300
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
305 310 315 320
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
325 330 335
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
340 345 350
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
355 360 365
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
370 375 380
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
385 390 395 400
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
405 410 415
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
420 425 430
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
435 440 445
Lys Ser Leu Ser Leu Ser Pro Gly Lys Gly Gly Gly Gly Ser Gln Val
450 455 460
Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln Thr Leu
465 470 475 480
Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Gly Gly Ala
485 490 495
Val Trp Ser Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu Trp Ile
500 505 510
Gly Gly Ile Ala Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys
515 520 525
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
530 535 540
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
545 550 555 560
Asp Glu Asn Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe
565 570 575
Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr
580 585 590
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
595 600 605
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
610 615 620
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
625 630 635 640
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
645 650 655
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
660 665 670
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
675 680 685
Pro Lys Ser Cys
690
<210> 193
<211> 690
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 193
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Ala Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Glu Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
325 330 335
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr
355 360 365
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Pro Gly Lys Gly Gly Gly Gly Ser Gln Val Gln
450 455 460
Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser
465 470 475 480
Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly Ala Gly Trp
485 490 495
Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Leu
500 505 510
Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg
515 520 525
Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu
530 535 540
Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Val Leu Glu
545 550 555 560
Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile
565 570 575
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly
580 585 590
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
595 600 605
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
610 615 620
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
625 630 635 640
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
645 650 655
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
660 665 670
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys
675 680 685
Ser Cys
690
<210> 194
<211> 690
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 194
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Ala Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Pro Glu Trp
35 40 45
Ile Gly Leu Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Glu Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
325 330 335
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr
355 360 365
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Pro Gly Lys Gly Gly Gly Gly Ser Gln Val Gln
450 455 460
Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser
465 470 475 480
Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly Ala Gly Trp
485 490 495
Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Pro Glu Trp Ile Gly Leu
500 505 510
Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg
515 520 525
Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu
530 535 540
Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Val Leu Glu
545 550 555 560
Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile
565 570 575
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly
580 585 590
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
595 600 605
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
610 615 620
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
625 630 635 640
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
645 650 655
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
660 665 670
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys
675 680 685
Ser Cys
690
<210> 195
<211> 690
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 195
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Ala Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Glu Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
325 330 335
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr
355 360 365
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Pro Gly Lys Gly Gly Gly Gly Ser Gln Val Gln
450 455 460
Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser
465 470 475 480
Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly Ala Gly Trp
485 490 495
Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Leu
500 505 510
Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg
515 520 525
Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu
530 535 540
Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Val Leu Glu
545 550 555 560
Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile
565 570 575
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly
580 585 590
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
595 600 605
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
610 615 620
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
625 630 635 640
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
645 650 655
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
660 665 670
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys
675 680 685
Ser Cys
690
<210> 196
<211> 690
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 196
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Ala Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Glu Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
325 330 335
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr
355 360 365
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Pro Gly Lys Gly Gly Gly Gly Ser Gln Val Gln
450 455 460
Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser
465 470 475 480
Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly Ala Gly Trp
485 490 495
Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Leu
500 505 510
Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg
515 520 525
Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu
530 535 540
Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Val Leu Glu
545 550 555 560
Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile
565 570 575
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly
580 585 590
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
595 600 605
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
610 615 620
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
625 630 635 640
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
645 650 655
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
660 665 670
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys
675 680 685
Ser Cys
690
<210> 197
<211> 690
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 197
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu
20 25 30
Tyr Met Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Tyr His Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Ala Asp Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
325 330 335
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr
355 360 365
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Pro Gly Lys Gly Gly Gly Gly Ser Gln Val Gln
450 455 460
Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser
465 470 475 480
Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu Tyr Met Trp
485 490 495
Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Leu
500 505 510
Ile Tyr His Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg
515 520 525
Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu
530 535 540
Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Glu
545 550 555 560
Ala Asp Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile
565 570 575
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly
580 585 590
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
595 600 605
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
610 615 620
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
625 630 635 640
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
645 650 655
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
660 665 670
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys
675 680 685
Ser Cys
690
<210> 198
<211> 690
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 198
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu
20 25 30
Tyr Met Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Tyr His Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Ala Asp Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
325 330 335
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr
355 360 365
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Pro Gly Lys Gly Gly Gly Gly Ser Gln Val Gln
450 455 460
Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser
465 470 475 480
Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu Tyr Met Trp
485 490 495
Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Leu
500 505 510
Ile Tyr His Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg
515 520 525
Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu
530 535 540
Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Glu
545 550 555 560
Ala Asp Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile
565 570 575
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly
580 585 590
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
595 600 605
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
610 615 620
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
625 630 635 640
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
645 650 655
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
660 665 670
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys
675 680 685
Ser Cys
690
<210> 199
<211> 688
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 199
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Arg Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Tyr Ile Ser Trp Val Arg Gln Val Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Val Pro Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Gly Gly Gly Tyr Ala Arg Gly Asp His Tyr Tyr Gly Met
100 105 110
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser
225 230 235 240
Gly Ala Glu Val Lys Arg Pro Gly Ser Ser Val Lys Val Ser Cys Lys
245 250 255
Ala Ser Gly Gly Thr Phe Ser Ser Tyr Tyr Ile Ser Trp Val Arg Gln
260 265 270
Val Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Val Pro
275 280 285
Gly Thr Ala Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr
290 295 300
Ala Asp Glu Ser Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg
305 310 315 320
Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ala Gly Gly Gly Tyr
325 330 335
Ala Arg Gly Asp His Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr
340 345 350
Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
355 360 365
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
370 375 380
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
385 390 395 400
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
405 410 415
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
420 425 430
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
435 440 445
Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr
450 455 460
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
465 470 475 480
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
485 490 495
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
500 505 510
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
515 520 525
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
530 535 540
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
545 550 555 560
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
565 570 575
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
580 585 590
Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
595 600 605
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
610 615 620
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
625 630 635 640
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
645 650 655
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
660 665 670
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
675 680 685
<210> 200
<211> 688
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 200
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Tyr Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Val Pro Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Gly Gly Gly Tyr Ala Arg Gly Asp His Tyr Tyr Gly Met
100 105 110
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser
225 230 235 240
Gly Ala Glu Val Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys
245 250 255
Ala Ser Gly Gly Thr Phe Ser Ser Tyr Tyr Ile Ser Trp Val Arg Gln
260 265 270
Ala Pro Gly Gln Arg Leu Glu Trp Met Gly Gly Ile Ile Pro Val Pro
275 280 285
Gly Thr Ala Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr
290 295 300
Ala Asp Glu Ser Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg
305 310 315 320
Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ala Gly Gly Gly Tyr
325 330 335
Ala Arg Gly Asp His Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr
340 345 350
Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
355 360 365
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
370 375 380
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
385 390 395 400
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
405 410 415
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
420 425 430
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
435 440 445
Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr
450 455 460
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
465 470 475 480
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
485 490 495
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
500 505 510
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
515 520 525
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
530 535 540
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
545 550 555 560
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
565 570 575
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
580 585 590
Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
595 600 605
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
610 615 620
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
625 630 635 640
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
645 650 655
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
660 665 670
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
675 680 685
<210> 201
<211> 680
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 201
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Arg Gly
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Glu Gly Thr Ala Tyr Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Gly Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Ser Asp Tyr Gly Leu Pro Arg Gly Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
210 215 220
Gly Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
225 230 235 240
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly
245 250 255
Thr Phe Ser Arg Gly Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln
260 265 270
Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Glu Gly Thr Ala Tyr
275 280 285
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser
290 295 300
Thr Gly Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
305 310 315 320
Ala Val Tyr Tyr Cys Ala Arg Gln Ser Asp Tyr Gly Leu Pro Arg Gly
325 330 335
Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser
340 345 350
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
355 360 365
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
370 375 380
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
385 390 395 400
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
405 410 415
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
420 425 430
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
435 440 445
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
450 455 460
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
465 470 475 480
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
485 490 495
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
500 505 510
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
515 520 525
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
530 535 540
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
545 550 555 560
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
565 570 575
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr
580 585 590
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
595 600 605
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
610 615 620
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
625 630 635 640
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
645 650 655
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
660 665 670
Ser Leu Ser Leu Ser Pro Gly Lys
675 680
<210> 202
<211> 678
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 202
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Gly
210 215 220
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
225 230 235 240
Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr
245 250 255
Phe Ser Ser Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly
260 265 270
Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr
275 280 285
Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr
290 295 300
Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
305 310 315 320
Val Tyr Tyr Cys Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro
325 330 335
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys
340 345 350
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
355 360 365
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
370 375 380
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
385 390 395 400
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
405 410 415
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
420 425 430
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro
435 440 445
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
450 455 460
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
465 470 475 480
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
485 490 495
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
500 505 510
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
515 520 525
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
530 535 540
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
545 550 555 560
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
565 570 575
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
580 585 590
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
595 600 605
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
610 615 620
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
625 630 635 640
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
645 650 655
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
660 665 670
Ser Leu Ser Pro Gly Lys
675
<210> 203
<211> 678
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 203
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Gly
210 215 220
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
225 230 235 240
Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr
245 250 255
Phe Ser Ser Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Arg
260 265 270
Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr
275 280 285
Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr
290 295 300
Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
305 310 315 320
Val Tyr Tyr Cys Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro
325 330 335
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys
340 345 350
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
355 360 365
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
370 375 380
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
385 390 395 400
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
405 410 415
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
420 425 430
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro
435 440 445
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
450 455 460
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
465 470 475 480
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
485 490 495
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
500 505 510
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
515 520 525
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
530 535 540
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
545 550 555 560
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
565 570 575
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
580 585 590
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
595 600 605
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
610 615 620
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
625 630 635 640
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
645 650 655
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
660 665 670
Ser Leu Ser Pro Gly Lys
675
<210> 204
<211> 678
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 204
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Lys Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Gly
210 215 220
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
225 230 235 240
Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr
245 250 255
Phe Ser Ser Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly
260 265 270
Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr
275 280 285
Ala Gln Lys Phe Gln Gly Lys Val Thr Ile Thr Ala Asp Glu Ser Thr
290 295 300
Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
305 310 315 320
Val Tyr Tyr Cys Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro
325 330 335
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys
340 345 350
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
355 360 365
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
370 375 380
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
385 390 395 400
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
405 410 415
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
420 425 430
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro
435 440 445
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
450 455 460
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
465 470 475 480
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
485 490 495
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
500 505 510
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
515 520 525
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
530 535 540
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
545 550 555 560
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
565 570 575
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
580 585 590
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
595 600 605
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
610 615 620
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
625 630 635 640
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
645 650 655
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
660 665 670
Ser Leu Ser Pro Gly Lys
675
<210> 205
<211> 676
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 205
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Val Arg Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala Gln Arg Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Gly Gly
210 215 220
Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys
225 230 235 240
Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe
245 250 255
Val Arg Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu
260 265 270
Glu Trp Met Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala
275 280 285
Gln Arg Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser
290 295 300
Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val
305 310 315 320
Tyr Tyr Cys Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp
325 330 335
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
340 345 350
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
355 360 365
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
370 375 380
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
385 390 395 400
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
405 410 415
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
420 425 430
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser
435 440 445
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
450 455 460
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
465 470 475 480
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
485 490 495
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
500 505 510
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
515 520 525
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
530 535 540
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
545 550 555 560
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
565 570 575
Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val
580 585 590
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
595 600 605
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
610 615 620
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
625 630 635 640
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
645 650 655
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
660 665 670
Ser Pro Gly Lys
675
<210> 206
<211> 676
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 206
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Val Arg Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala Gln Lys Phe
50 55 60
Arg Gly Arg Ala Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Gly Gly
210 215 220
Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys
225 230 235 240
Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe
245 250 255
Val Arg Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu
260 265 270
Glu Trp Met Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala
275 280 285
Gln Lys Phe Arg Gly Arg Ala Thr Ile Thr Ala Asp Glu Ser Thr Ser
290 295 300
Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val
305 310 315 320
Tyr Tyr Cys Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp
325 330 335
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
340 345 350
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
355 360 365
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
370 375 380
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
385 390 395 400
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
405 410 415
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
420 425 430
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser
435 440 445
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
450 455 460
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
465 470 475 480
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
485 490 495
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
500 505 510
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
515 520 525
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
530 535 540
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
545 550 555 560
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
565 570 575
Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val
580 585 590
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
595 600 605
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
610 615 620
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
625 630 635 640
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
645 650 655
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
660 665 670
Ser Pro Gly Lys
675
<210> 207
<211> 688
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 207
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Arg Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Tyr Ile Ser Trp Val Arg Gln Val Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Val Pro Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Gly Gly Gly Tyr Ala Arg Gly Asp His Tyr Tyr Gly Met
100 105 110
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
225 230 235 240
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
275 280 285
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
290 295 300
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
305 310 315 320
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
325 330 335
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
340 345 350
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
355 360 365
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
370 375 380
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
385 390 395 400
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
405 410 415
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
420 425 430
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
435 440 445
Leu Ser Leu Ser Pro Gly Lys Gly Gly Gly Gly Ser Gln Val Gln Leu
450 455 460
Val Gln Ser Gly Ala Glu Val Lys Arg Pro Gly Ser Ser Val Lys Val
465 470 475 480
Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr Tyr Ile Ser Trp
485 490 495
Val Arg Gln Val Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Ile
500 505 510
Pro Val Pro Gly Thr Ala Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val
515 520 525
Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr Met Glu Leu Ser
530 535 540
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ala Gly
545 550 555 560
Gly Gly Tyr Ala Arg Gly Asp His Tyr Tyr Gly Met Asp Val Trp Gly
565 570 575
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
580 585 590
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
595 600 605
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
610 615 620
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
625 630 635 640
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
645 650 655
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
660 665 670
Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
675 680 685
<210> 208
<211> 688
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 208
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Tyr Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Val Pro Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Gly Gly Gly Tyr Ala Arg Gly Asp His Tyr Tyr Gly Met
100 105 110
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
225 230 235 240
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
275 280 285
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
290 295 300
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
305 310 315 320
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
325 330 335
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
340 345 350
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
355 360 365
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
370 375 380
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
385 390 395 400
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
405 410 415
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
420 425 430
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
435 440 445
Leu Ser Leu Ser Pro Gly Lys Gly Gly Gly Gly Ser Gln Val Gln Leu
450 455 460
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser Ser Val Lys Val
465 470 475 480
Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr Tyr Ile Ser Trp
485 490 495
Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met Gly Gly Ile Ile
500 505 510
Pro Val Pro Gly Thr Ala Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val
515 520 525
Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr Met Glu Leu Ser
530 535 540
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ala Gly
545 550 555 560
Gly Gly Tyr Ala Arg Gly Asp His Tyr Tyr Gly Met Asp Val Trp Gly
565 570 575
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
580 585 590
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
595 600 605
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
610 615 620
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
625 630 635 640
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
645 650 655
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
660 665 670
Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
675 680 685
<210> 209
<211> 680
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 209
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Arg Gly
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Glu Gly Thr Ala Tyr Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Gly Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Ser Asp Tyr Gly Leu Pro Arg Gly Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys Gly Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly
450 455 460
Ala Glu Val Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala
465 470 475 480
Ser Gly Gly Thr Phe Ser Arg Gly Ala Ile Ser Trp Val Arg Gln Ala
485 490 495
Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Glu Gly
500 505 510
Thr Ala Tyr Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala
515 520 525
Asp Glu Ser Thr Gly Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser
530 535 540
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Gln Ser Asp Tyr Gly Leu
545 550 555 560
Pro Arg Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser
565 570 575
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
580 585 590
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
595 600 605
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
610 615 620
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
625 630 635 640
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
645 650 655
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
660 665 670
Lys Arg Val Glu Pro Lys Ser Cys
675 680
<210> 210
<211> 678
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 210
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys Gly Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala
450 455 460
Glu Val Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser
465 470 475 480
Gly Gly Thr Phe Ser Ser Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro
485 490 495
Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Ser Gly Phe
500 505 510
Thr Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp
515 520 525
Glu Ser Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu
530 535 540
Asp Thr Ala Val Tyr Tyr Cys Ala Arg Glu Gly Gly His Tyr Tyr Ser
545 550 555 560
Gly Trp Pro Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala
565 570 575
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser
580 585 590
Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
595 600 605
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
610 615 620
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
625 630 635 640
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr
645 650 655
Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg
660 665 670
Val Glu Pro Lys Ser Cys
675
<210> 211
<211> 678
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 211
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys Gly Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala
450 455 460
Glu Val Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser
465 470 475 480
Gly Gly Thr Phe Ser Ser Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro
485 490 495
Gly Gln Arg Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Ser Gly Phe
500 505 510
Thr Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp
515 520 525
Glu Ser Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu
530 535 540
Asp Thr Ala Val Tyr Tyr Cys Ala Arg Glu Gly Gly His Tyr Tyr Ser
545 550 555 560
Gly Trp Pro Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala
565 570 575
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser
580 585 590
Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
595 600 605
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
610 615 620
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
625 630 635 640
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr
645 650 655
Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg
660 665 670
Val Glu Pro Lys Ser Cys
675
<210> 212
<211> 678
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 212
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Lys Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys Gly Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala
450 455 460
Glu Val Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser
465 470 475 480
Gly Gly Thr Phe Ser Ser Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro
485 490 495
Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Ser Gly Phe
500 505 510
Thr Asn Tyr Ala Gln Lys Phe Gln Gly Lys Val Thr Ile Thr Ala Asp
515 520 525
Glu Ser Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu
530 535 540
Asp Thr Ala Val Tyr Tyr Cys Ala Arg Glu Gly Gly His Tyr Tyr Ser
545 550 555 560
Gly Trp Pro Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala
565 570 575
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser
580 585 590
Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
595 600 605
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
610 615 620
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
625 630 635 640
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr
645 650 655
Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg
660 665 670
Val Glu Pro Lys Ser Cys
675
<210> 213
<211> 676
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 213
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Val Arg Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala Gln Arg Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys Gly Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu
450 455 460
Val Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly
465 470 475 480
Gly Thr Phe Val Arg Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly
485 490 495
Gln Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala
500 505 510
Gln Tyr Ala Gln Arg Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu
515 520 525
Ser Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp
530 535 540
Thr Ala Val Tyr Tyr Cys Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu
545 550 555 560
Pro Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr
565 570 575
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
580 585 590
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
595 600 605
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
610 615 620
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
625 630 635 640
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
645 650 655
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
660 665 670
Pro Lys Ser Cys
675
<210> 214
<211> 676
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 214
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Val Arg Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala Gln Lys Phe
50 55 60
Arg Gly Arg Ala Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys Gly Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu
450 455 460
Val Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly
465 470 475 480
Gly Thr Phe Val Arg Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly
485 490 495
Gln Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala
500 505 510
Gln Tyr Ala Gln Lys Phe Arg Gly Arg Ala Thr Ile Thr Ala Asp Glu
515 520 525
Ser Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp
530 535 540
Thr Ala Val Tyr Tyr Cys Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu
545 550 555 560
Pro Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr
565 570 575
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
580 585 590
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
595 600 605
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
610 615 620
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
625 630 635 640
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
645 650 655
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
660 665 670
Pro Lys Ser Cys
675
<210> 215
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (14)..(14)
<223> /замена="Arg"
<220>
<221> ВАРИАНТ
<222> (16)..(16)
<223> /замена="Arg"
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (1)..(17)
<223> /примечание="Варианты остатков, приведенные в
последовательности, не имеют преимущества по отношению к остаткам в
аннотациях положений вариантов"
<400> 215
Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 216
<211> 675
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 216
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
210 215 220
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys Gly
435 440 445
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
450 455 460
Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr
465 470 475 480
Phe Ser Ser Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Arg
485 490 495
Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr
500 505 510
Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr
515 520 525
Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
530 535 540
Val Tyr Tyr Cys Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro
545 550 555 560
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys
565 570 575
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
580 585 590
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
595 600 605
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
610 615 620
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
625 630 635 640
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
645 650 655
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro
660 665 670
Lys Ser Cys
675
<210> 217
<211> 675
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 217
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Lys Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
210 215 220
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys Gly
435 440 445
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
450 455 460
Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr
465 470 475 480
Phe Ser Ser Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly
485 490 495
Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr
500 505 510
Ala Gln Lys Phe Gln Gly Lys Val Thr Ile Thr Ala Asp Glu Ser Thr
515 520 525
Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
530 535 540
Val Tyr Tyr Cys Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro
545 550 555 560
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys
565 570 575
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
580 585 590
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
595 600 605
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
610 615 620
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
625 630 635 640
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
645 650 655
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro
660 665 670
Lys Ser Cys
675
<210> 218
<211> 673
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 218
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Val Arg Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala Gln Arg Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val
260 265 270
Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys Gly Gly
435 440 445
Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys
450 455 460
Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe
465 470 475 480
Val Arg Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu
485 490 495
Glu Trp Met Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala
500 505 510
Gln Arg Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser
515 520 525
Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val
530 535 540
Tyr Tyr Cys Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp
545 550 555 560
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
565 570 575
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
580 585 590
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
595 600 605
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
610 615 620
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
625 630 635 640
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
645 650 655
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser
660 665 670
Cys
<210> 219
<211> 673
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 219
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Val Arg Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala Gln Lys Phe
50 55 60
Arg Gly Arg Ala Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val
260 265 270
Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys Gly Gly
435 440 445
Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys
450 455 460
Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe
465 470 475 480
Val Arg Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu
485 490 495
Glu Trp Met Gly Gly Ile Ile Pro Ile Phe Gly Glu Ala Gln Tyr Ala
500 505 510
Gln Lys Phe Arg Gly Arg Ala Thr Ile Thr Ala Asp Glu Ser Thr Ser
515 520 525
Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val
530 535 540
Tyr Tyr Cys Ala Arg Glu Gly Tyr Tyr Tyr Gly Ala Leu Pro Tyr Trp
545 550 555 560
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
565 570 575
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
580 585 590
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
595 600 605
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
610 615 620
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
625 630 635 640
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
645 650 655
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser
660 665 670
Cys
<210> 220
<211> 689
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 220
Gln Leu Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Ser
20 25 30
Ser Tyr Ala Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Asp Ser Gly Arg Gly Tyr Gly Asp Tyr Gly Gly His His
100 105 110
Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala
115 120 125
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser
130 135 140
Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
145 150 155 160
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
165 170 175
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
180 185 190
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr
195 200 205
Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg
210 215 220
Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
325 330 335
Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Leu Gly Lys Gly Gly Gly Gly Ser Gln Leu Gln Leu Gln
450 455 460
Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr
465 470 475 480
Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Ser Ser Tyr Ala Trp Gly
485 490 495
Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Ser Ile
500 505 510
Tyr Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val
515 520 525
Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser
530 535 540
Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Ser
545 550 555 560
Gly Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp
565 570 575
Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
580 585 590
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
595 600 605
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
610 615 620
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
625 630 635 640
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
645 650 655
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
660 665 670
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser
675 680 685
Cys
<210> 221
<211> 689
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 221
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Gly
20 25 30
Gly Ala Val Trp Ser Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Gly Ile Ala Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Asp Glu Asn Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His
100 105 110
Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala
115 120 125
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser
130 135 140
Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
145 150 155 160
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
165 170 175
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
180 185 190
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr
195 200 205
Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg
210 215 220
Val Glu Pro Lys Ser Cys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln
225 230 235 240
Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln Thr Leu Ser Leu Thr
245 250 255
Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Gly Gly Ala Val Trp Ser
260 265 270
Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu Trp Ile Gly Gly Ile
275 280 285
Ala Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val
290 295 300
Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser
305 310 315 320
Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Asp Glu Asn
325 330 335
Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp
340 345 350
Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
355 360 365
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
370 375 380
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
385 390 395 400
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
405 410 415
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
420 425 430
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
435 440 445
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
450 455 460
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro
465 470 475 480
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
485 490 495
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
500 505 510
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
515 520 525
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val
530 535 540
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
545 550 555 560
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
565 570 575
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
580 585 590
Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr
595 600 605
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
610 615 620
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
625 630 635 640
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys
645 650 655
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
660 665 670
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
675 680 685
Lys
<210> 222
<211> 687
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 222
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Leu Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Gly Ile Tyr Glu Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Glu Arg Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr
130 135 140
Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr
195 200 205
Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
260 265 270
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
275 280 285
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
305 310 315 320
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
325 330 335
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
340 345 350
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
355 360 365
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
370 375 380
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
385 390 395 400
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
405 410 415
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
435 440 445
Leu Ser Leu Gly Lys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
450 455 460
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
465 470 475 480
Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly Leu Gly Trp Gly Trp Ile
485 490 495
Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Gly Ile Tyr Glu
500 505 510
Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile
515 520 525
Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val
530 535 540
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala His Glu Arg Val Arg
545 550 555 560
Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly Gln
565 570 575
Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
580 585 590
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
595 600 605
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
610 615 620
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
625 630 635 640
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
645 650 655
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
660 665 670
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
675 680 685
<210> 223
<211> 689
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 223
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Gly
20 25 30
Gly Ala Val Trp Ser Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Gly Ile Ala Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Asp Glu Asn Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His
100 105 110
Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala
115 120 125
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser
130 135 140
Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
145 150 155 160
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
165 170 175
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
180 185 190
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr
195 200 205
Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg
210 215 220
Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
325 330 335
Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Leu Gly Lys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln
450 455 460
Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln Thr Leu Ser Leu Thr
465 470 475 480
Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Gly Gly Ala Val Trp Ser
485 490 495
Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu Trp Ile Gly Gly Ile
500 505 510
Ala Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val
515 520 525
Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser
530 535 540
Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Asp Glu Asn
545 550 555 560
Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp
565 570 575
Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
580 585 590
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
595 600 605
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
610 615 620
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
625 630 635 640
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
645 650 655
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
660 665 670
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser
675 680 685
Cys
<210> 224
<211> 687
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 224
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Ala Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Glu Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr
130 135 140
Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr
195 200 205
Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
260 265 270
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
275 280 285
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
305 310 315 320
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
325 330 335
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
340 345 350
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
355 360 365
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
370 375 380
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
385 390 395 400
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
405 410 415
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
435 440 445
Leu Ser Leu Gly Lys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
450 455 460
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
465 470 475 480
Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly Ala Gly Trp Gly Trp Ile
485 490 495
Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Leu Ile Val His
500 505 510
Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile
515 520 525
Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val
530 535 540
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Val Leu Glu Ser Val Arg
545 550 555 560
Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly Gln
565 570 575
Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
580 585 590
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
595 600 605
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
610 615 620
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
625 630 635 640
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
645 650 655
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
660 665 670
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
675 680 685
<210> 225
<211> 687
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 225
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Ala Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Pro Glu Trp
35 40 45
Ile Gly Leu Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Glu Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr
130 135 140
Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr
195 200 205
Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
260 265 270
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
275 280 285
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
305 310 315 320
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
325 330 335
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
340 345 350
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
355 360 365
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
370 375 380
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
385 390 395 400
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
405 410 415
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
435 440 445
Leu Ser Leu Gly Lys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
450 455 460
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
465 470 475 480
Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly Ala Gly Trp Gly Trp Ile
485 490 495
Arg Gln Pro Pro Gly Lys Gly Pro Glu Trp Ile Gly Leu Ile Val His
500 505 510
Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile
515 520 525
Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val
530 535 540
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Val Leu Glu Ser Val Arg
545 550 555 560
Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly Gln
565 570 575
Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
580 585 590
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
595 600 605
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
610 615 620
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
625 630 635 640
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
645 650 655
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
660 665 670
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
675 680 685
<210> 226
<211> 687
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 226
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Ala Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Glu Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr
130 135 140
Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr
195 200 205
Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
260 265 270
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
275 280 285
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
305 310 315 320
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
325 330 335
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
340 345 350
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
355 360 365
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
370 375 380
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
385 390 395 400
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
405 410 415
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
435 440 445
Leu Ser Leu Gly Lys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
450 455 460
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
465 470 475 480
Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly Ala Gly Trp Gly Trp Ile
485 490 495
Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Leu Ile Val His
500 505 510
Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile
515 520 525
Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val
530 535 540
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Val Leu Glu Ser Val Arg
545 550 555 560
Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly Gln
565 570 575
Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
580 585 590
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
595 600 605
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
610 615 620
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
625 630 635 640
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
645 650 655
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
660 665 670
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
675 680 685
<210> 227
<211> 687
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 227
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly
20 25 30
Ala Gly Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Val His Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Glu Ser Val Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr
130 135 140
Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr
195 200 205
Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
260 265 270
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
275 280 285
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
305 310 315 320
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
325 330 335
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
340 345 350
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
355 360 365
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
370 375 380
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
385 390 395 400
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
405 410 415
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
435 440 445
Leu Ser Leu Gly Lys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
450 455 460
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
465 470 475 480
Ala Val Ser Gly Tyr Ser Ile Ser Ser Gly Ala Gly Trp Gly Trp Ile
485 490 495
Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Leu Ile Val His
500 505 510
Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile
515 520 525
Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val
530 535 540
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Val Leu Glu Ser Val Arg
545 550 555 560
Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly Gln
565 570 575
Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
580 585 590
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
595 600 605
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
610 615 620
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
625 630 635 640
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
645 650 655
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
660 665 670
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
675 680 685
<210> 228
<211> 687
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 228
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu
20 25 30
Tyr Met Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Tyr His Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Ala Asp Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr
130 135 140
Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr
195 200 205
Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
260 265 270
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
275 280 285
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
305 310 315 320
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
325 330 335
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
340 345 350
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
355 360 365
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
370 375 380
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
385 390 395 400
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
405 410 415
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
435 440 445
Leu Ser Leu Gly Lys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
450 455 460
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
465 470 475 480
Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu Tyr Met Trp Gly Trp Ile
485 490 495
Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Leu Ile Tyr His
500 505 510
Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile
515 520 525
Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val
530 535 540
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Glu Ala Asp Arg
545 550 555 560
Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly Gln
565 570 575
Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
580 585 590
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
595 600 605
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
610 615 620
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
625 630 635 640
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
645 650 655
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
660 665 670
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
675 680 685
<210> 229
<211> 687
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 229
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu
20 25 30
Tyr Met Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Leu Ile Tyr His Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Ala Asp Arg Gly Tyr Gly Asp Tyr Gly Gly His His Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr
130 135 140
Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr
195 200 205
Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
210 215 220
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
260 265 270
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
275 280 285
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
305 310 315 320
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
325 330 335
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
340 345 350
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
355 360 365
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
370 375 380
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
385 390 395 400
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
405 410 415
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
435 440 445
Leu Ser Leu Gly Lys Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
450 455 460
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
465 470 475 480
Ala Val Ser Gly Tyr Ser Ile Ser Ser Glu Tyr Met Trp Gly Trp Ile
485 490 495
Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Leu Ile Tyr His
500 505 510
Ser Gly Lys Thr Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile
515 520 525
Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val
530 535 540
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Glu Ala Asp Arg
545 550 555 560
Gly Tyr Gly Asp Tyr Gly Gly His His Ala Phe Asp Ile Trp Gly Gln
565 570 575
Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
580 585 590
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
595 600 605
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
610 615 620
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
625 630 635 640
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
645 650 655
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
660 665 670
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
675 680 685
<210> 230
<211> 685
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 230
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Arg Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Tyr Ile Ser Trp Val Arg Gln Val Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Val Pro Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Gly Gly Gly Tyr Ala Arg Gly Asp His Tyr Tyr Gly Met
100 105 110
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser
130 135 140
Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys
195 200 205
Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu
225 230 235 240
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
260 265 270
Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val
355 360 365
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Leu Gly Lys Gly Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser
450 455 460
Gly Ala Glu Val Lys Arg Pro Gly Ser Ser Val Lys Val Ser Cys Lys
465 470 475 480
Ala Ser Gly Gly Thr Phe Ser Ser Tyr Tyr Ile Ser Trp Val Arg Gln
485 490 495
Val Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Val Pro
500 505 510
Gly Thr Ala Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr
515 520 525
Ala Asp Glu Ser Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg
530 535 540
Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ala Gly Gly Gly Tyr
545 550 555 560
Ala Arg Gly Asp His Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr
565 570 575
Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
580 585 590
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
595 600 605
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
610 615 620
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
625 630 635 640
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
645 650 655
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
660 665 670
Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
675 680 685
<210> 231
<211> 685
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 231
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Tyr Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Val Pro Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Gly Gly Gly Tyr Ala Arg Gly Asp His Tyr Tyr Gly Met
100 105 110
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser
130 135 140
Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys
195 200 205
Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu
225 230 235 240
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
260 265 270
Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val
355 360 365
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Leu Gly Lys Gly Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser
450 455 460
Gly Ala Glu Val Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys
465 470 475 480
Ala Ser Gly Gly Thr Phe Ser Ser Tyr Tyr Ile Ser Trp Val Arg Gln
485 490 495
Ala Pro Gly Gln Arg Leu Glu Trp Met Gly Gly Ile Ile Pro Val Pro
500 505 510
Gly Thr Ala Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr
515 520 525
Ala Asp Glu Ser Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg
530 535 540
Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ala Gly Gly Gly Tyr
545 550 555 560
Ala Arg Gly Asp His Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr
565 570 575
Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
580 585 590
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
595 600 605
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
610 615 620
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
625 630 635 640
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
645 650 655
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
660 665 670
Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
675 680 685
<210> 232
<211> 677
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 232
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Arg Gly
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Glu Gly Thr Ala Tyr Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Gly Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Ser Asp Tyr Gly Leu Pro Arg Gly Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly
210 215 220
Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro
260 265 270
Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser
405 410 415
Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
Gly Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
450 455 460
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly
465 470 475 480
Thr Phe Ser Arg Gly Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln
485 490 495
Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Glu Gly Thr Ala Tyr
500 505 510
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser
515 520 525
Thr Gly Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
530 535 540
Ala Val Tyr Tyr Cys Ala Arg Gln Ser Asp Tyr Gly Leu Pro Arg Gly
545 550 555 560
Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser
565 570 575
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
580 585 590
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
595 600 605
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
610 615 620
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
625 630 635 640
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
645 650 655
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
660 665 670
Glu Pro Lys Ser Cys
675
<210> 233
<211> 675
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 233
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
210 215 220
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys Gly
435 440 445
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
450 455 460
Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr
465 470 475 480
Phe Ser Ser Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly
485 490 495
Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Ser Gly Phe Thr Asn Tyr
500 505 510
Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr
515 520 525
Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
530 535 540
Val Tyr Tyr Cys Ala Arg Glu Gly Gly His Tyr Tyr Ser Gly Trp Pro
545 550 555 560
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys
565 570 575
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
580 585 590
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
595 600 605
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
610 615 620
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
625 630 635 640
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
645 650 655
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro
660 665 670
Lys Ser Cys
675
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИГЕНСВЯЗЫВАЮЩИЕ БЕЛКИ ПРОТИВ TIGIT И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2776714C2 |
| УЛУЧШЕННЫЕ АНТИ-FLT3 АНТИГЕНСВЯЗЫВАЮЩИЕ БЕЛКИ | 2019 |
|
RU2830982C2 |
| ПОЛИВАЛЕТНЫЕ И ПОЛИСПЕЦИФИЧНЫЕ GITR-СВЯЗЫВАЮЩИЕ СЛИТЫЕ БЕЛКИ | 2016 |
|
RU2753439C2 |
| АНТИТЕЛО ПРОТИВ ПРОТЕИНТИРОЗИНФОСФАТАЗЫ σ РЕЦЕПТОРНОГО ТИПА ЧЕЛОВЕКА | 2012 |
|
RU2715642C2 |
| АНТИТЕЛА К ENTPD2, ВИДЫ КОМБИНИРОВАННОЙ ТЕРАПИИ И СПОСОБЫ ПРИМЕНЕНИЯ АНТИТЕЛ И ВИДОВ КОМБИНИРОВАННОЙ ТЕРАПИИ | 2019 |
|
RU2790991C2 |
| АНТИТЕЛА К РЕЦЕПТОРУ IL4 ДЛЯ ПРИМЕНЕНИЯ В ВЕТЕРИНАРИИ | 2019 |
|
RU2837141C2 |
| СКОНСТРУИРОВАННЫЕ PH-ЗАВИСИМЫЕ АНТИТЕЛА К CD3, А ТАКЖЕ СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2020 |
|
RU2832079C2 |
| АНТИ-IL31 АНТИТЕЛА ДЛЯ ПРИМЕНЕНИЯ В ВЕТЕРИНАРИИ | 2020 |
|
RU2835543C1 |
| PD-L1 специфические антитела | 2017 |
|
RU2756236C2 |
| ПОЛИВАЛЕНТНЫЕ И ПОЛИСПЕЦИФИЧЕСКИЕ ОХ40-СВЯЗЫВАЮЩИЕ СЛИТЫЕ БЕЛКИ | 2017 |
|
RU2773052C2 |
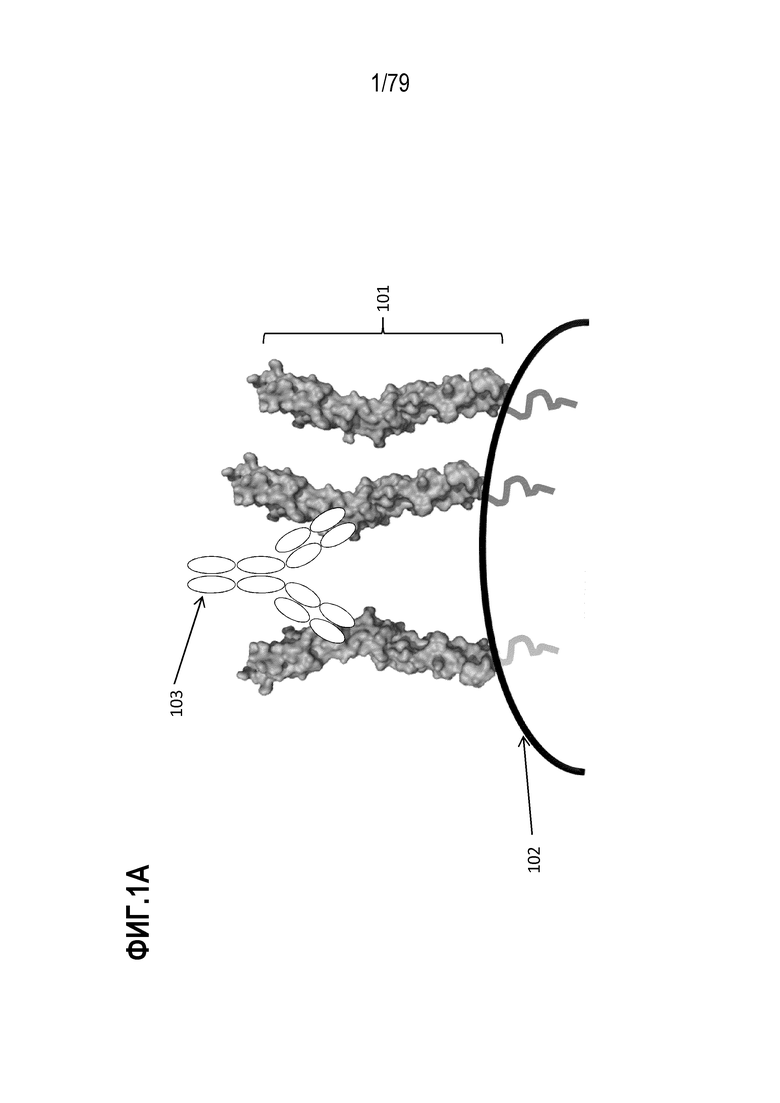
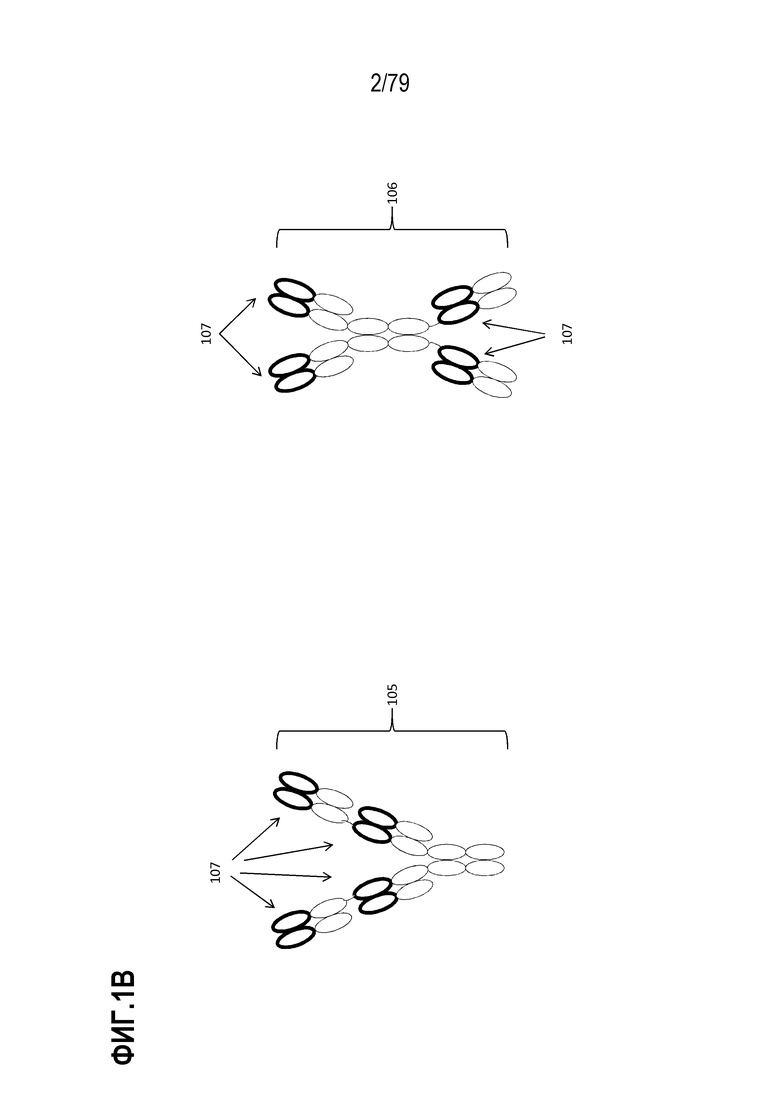
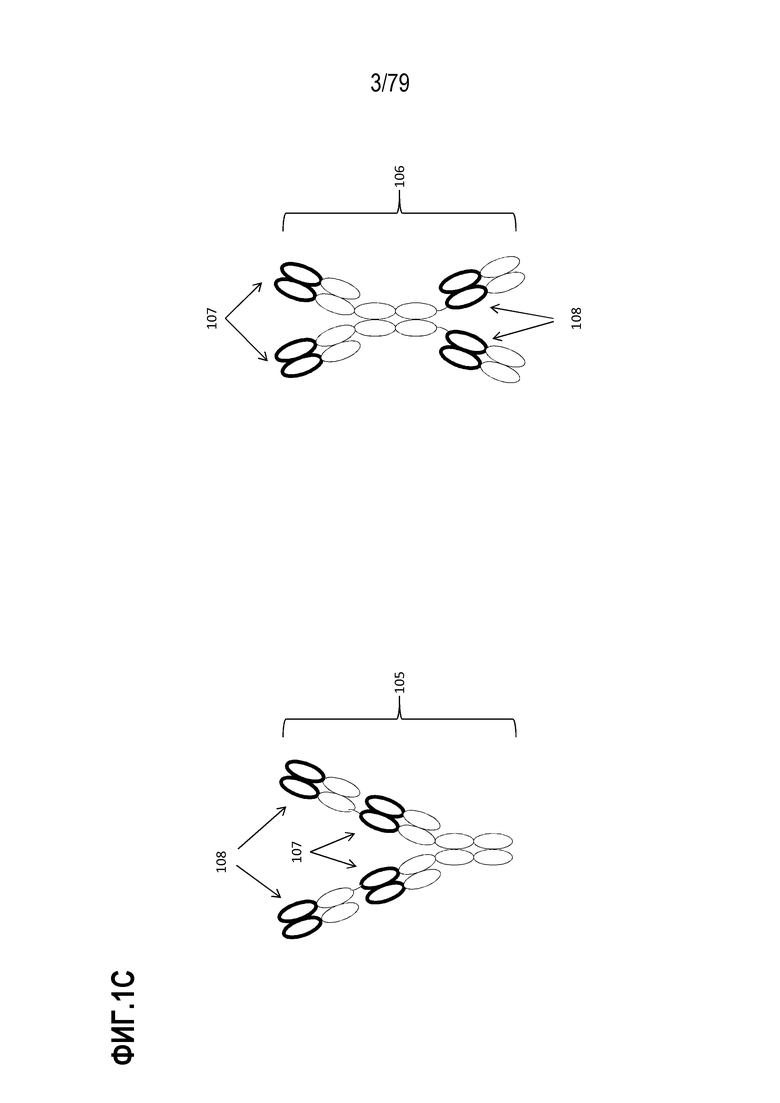


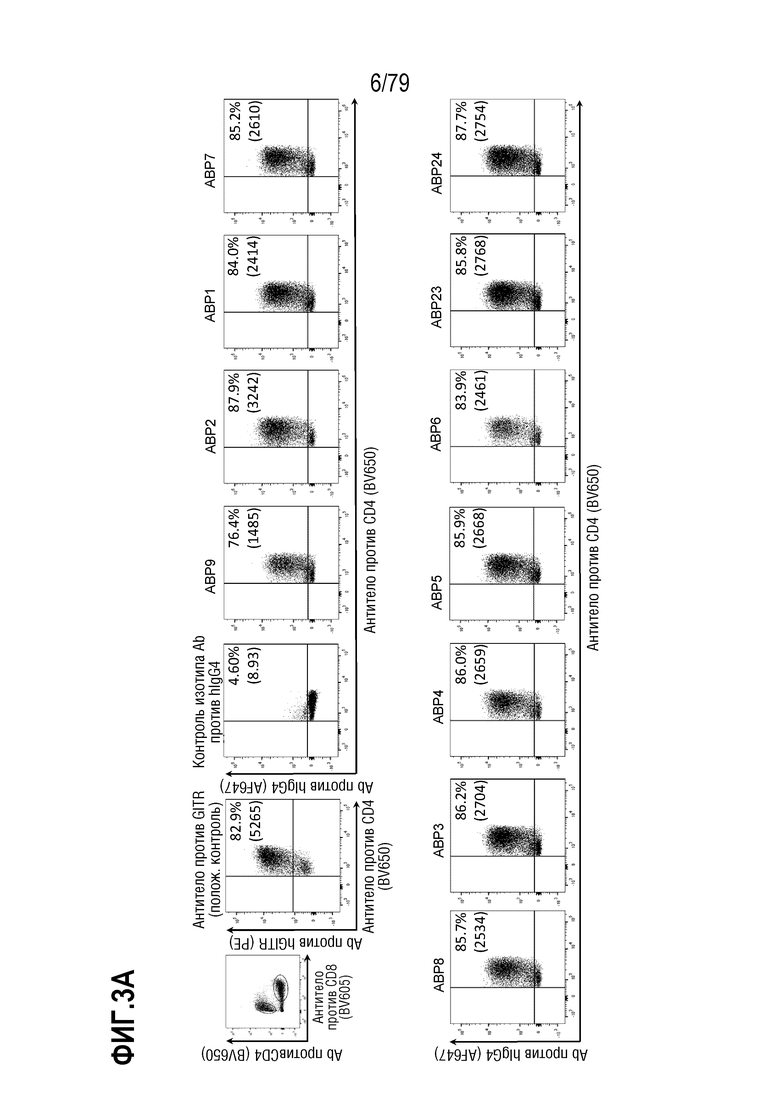

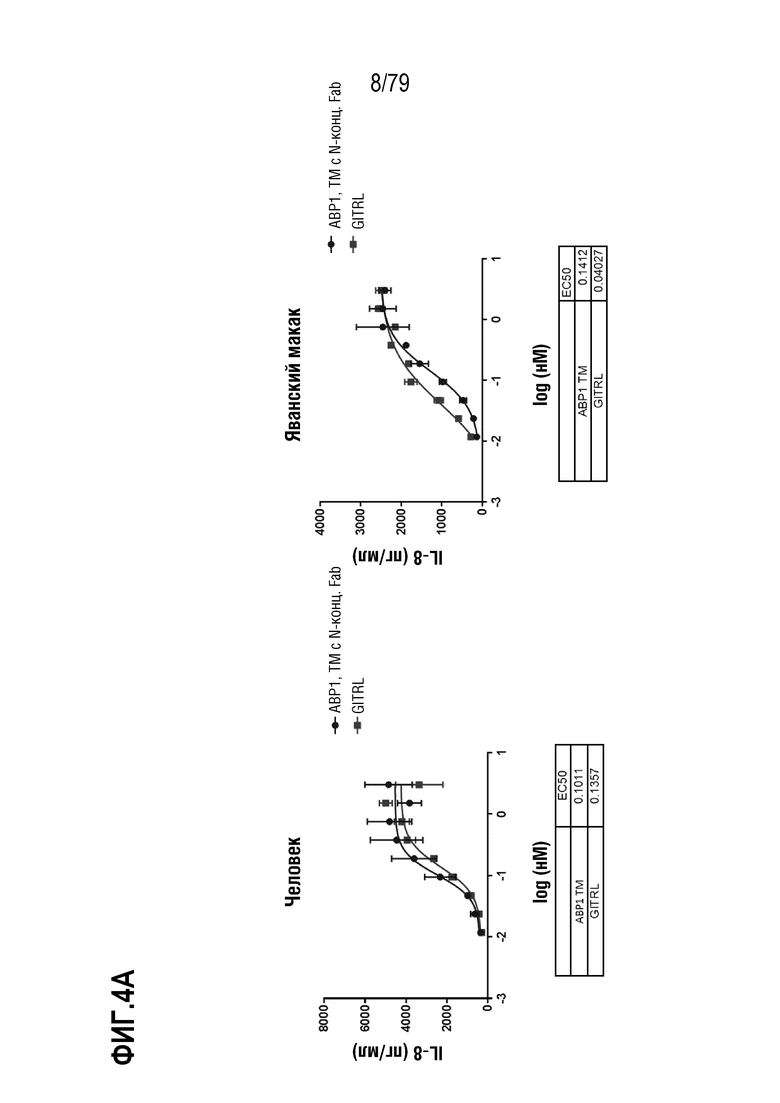
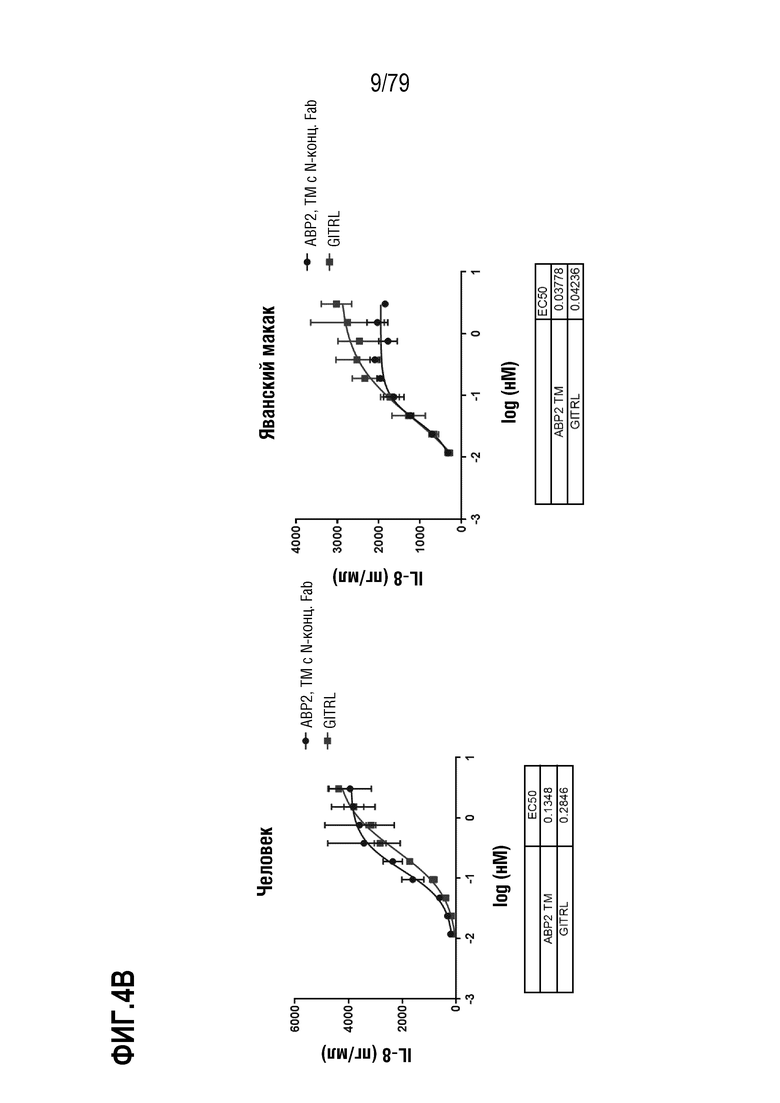
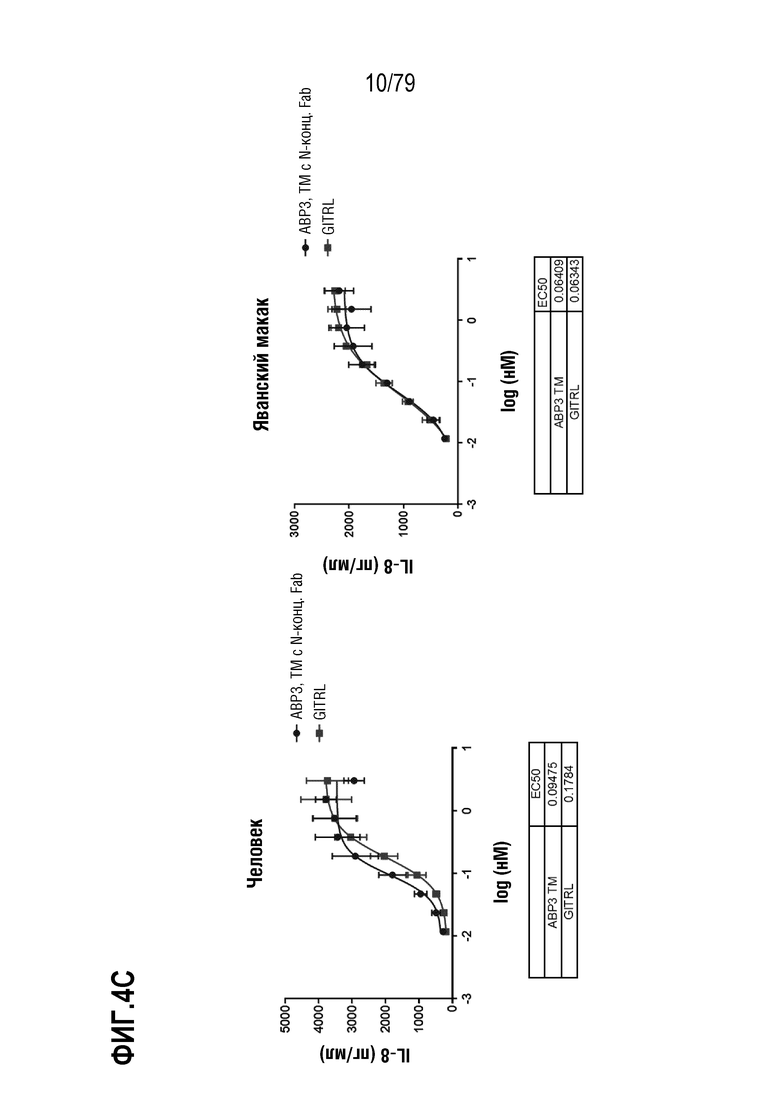
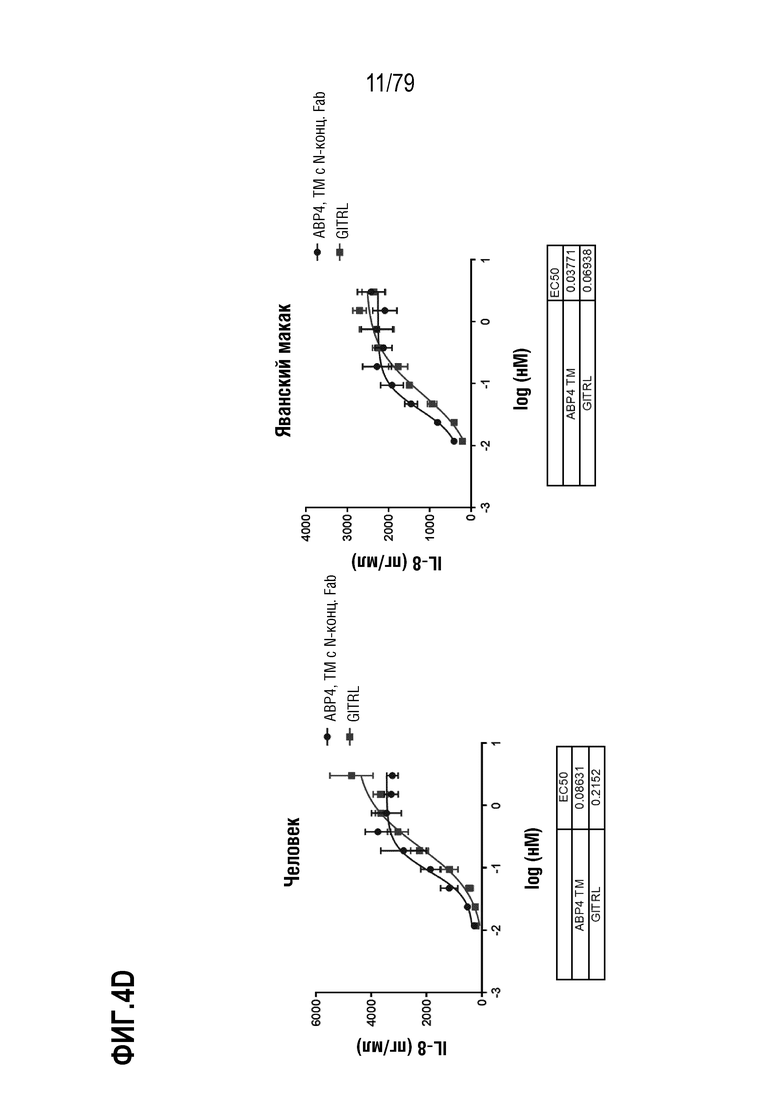

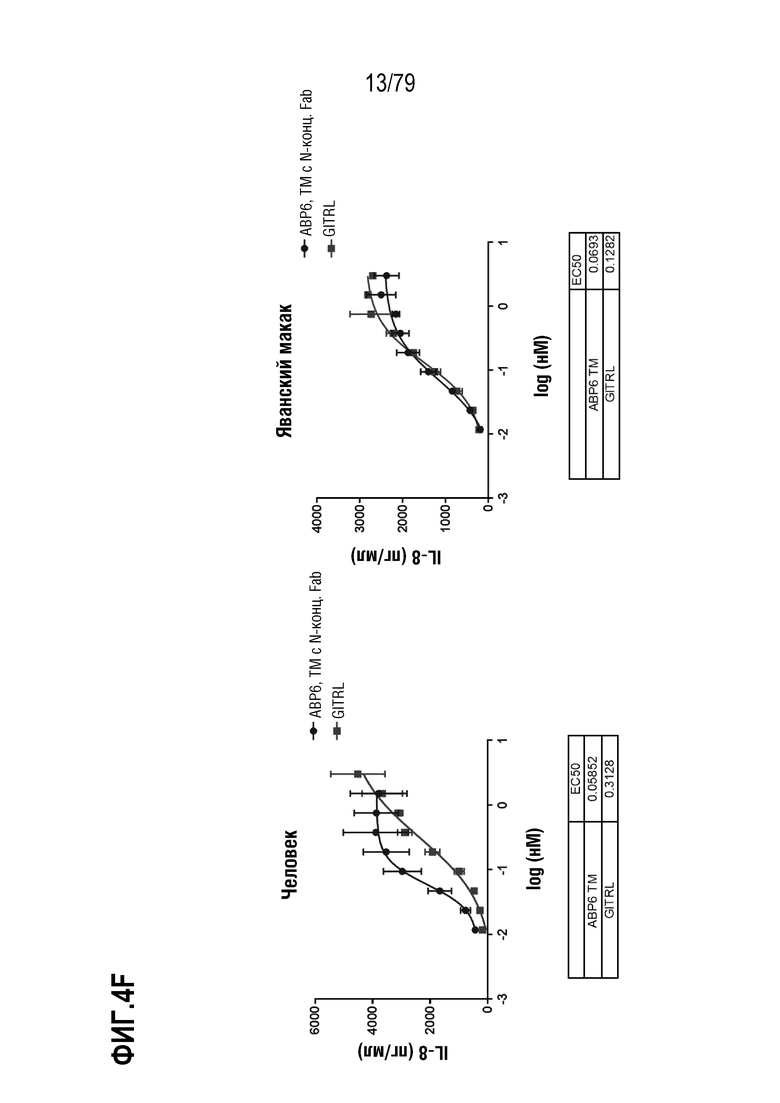
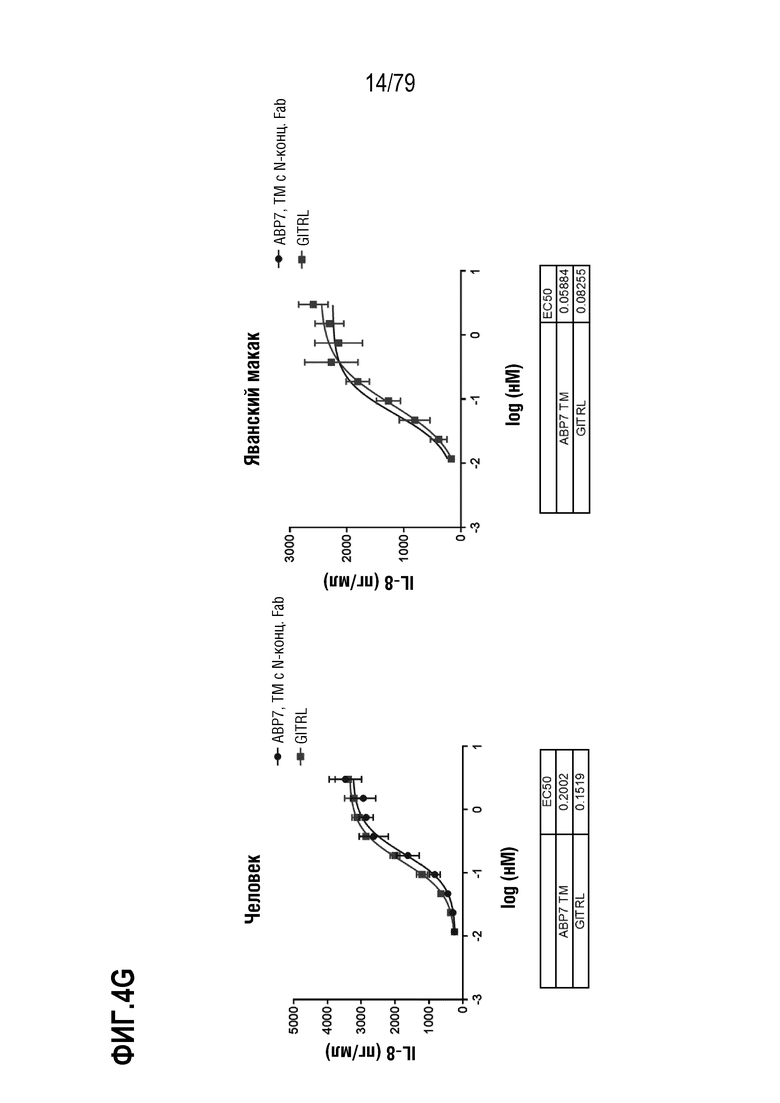
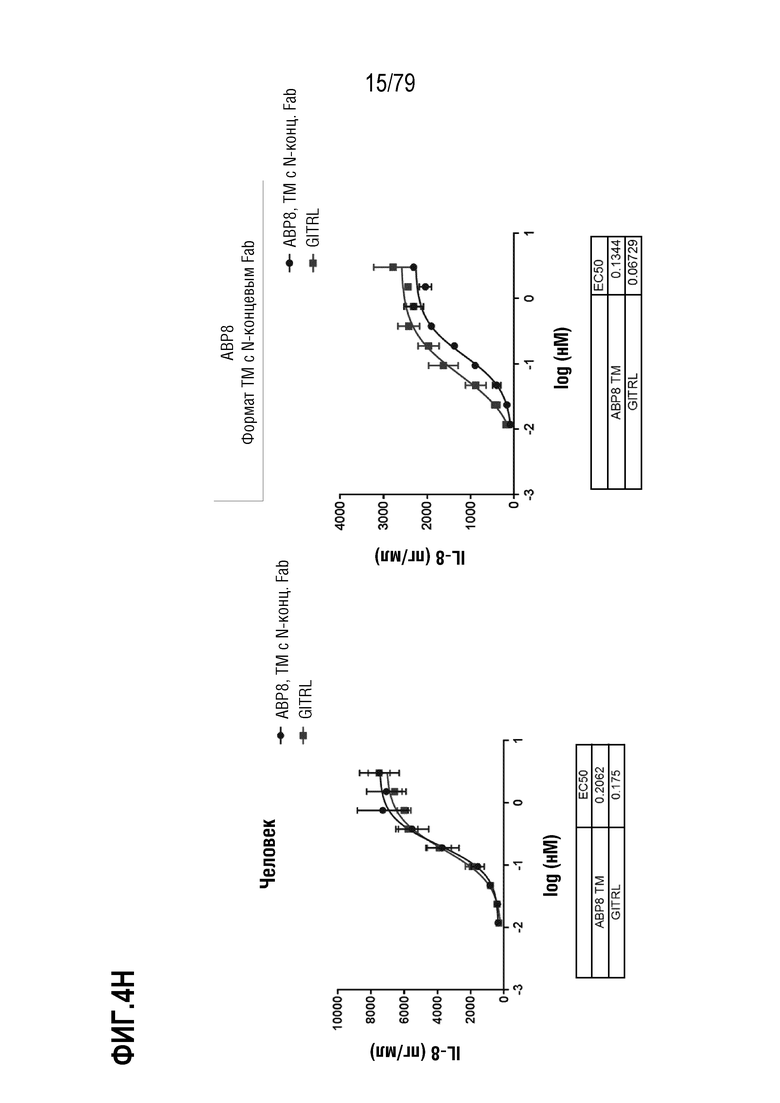
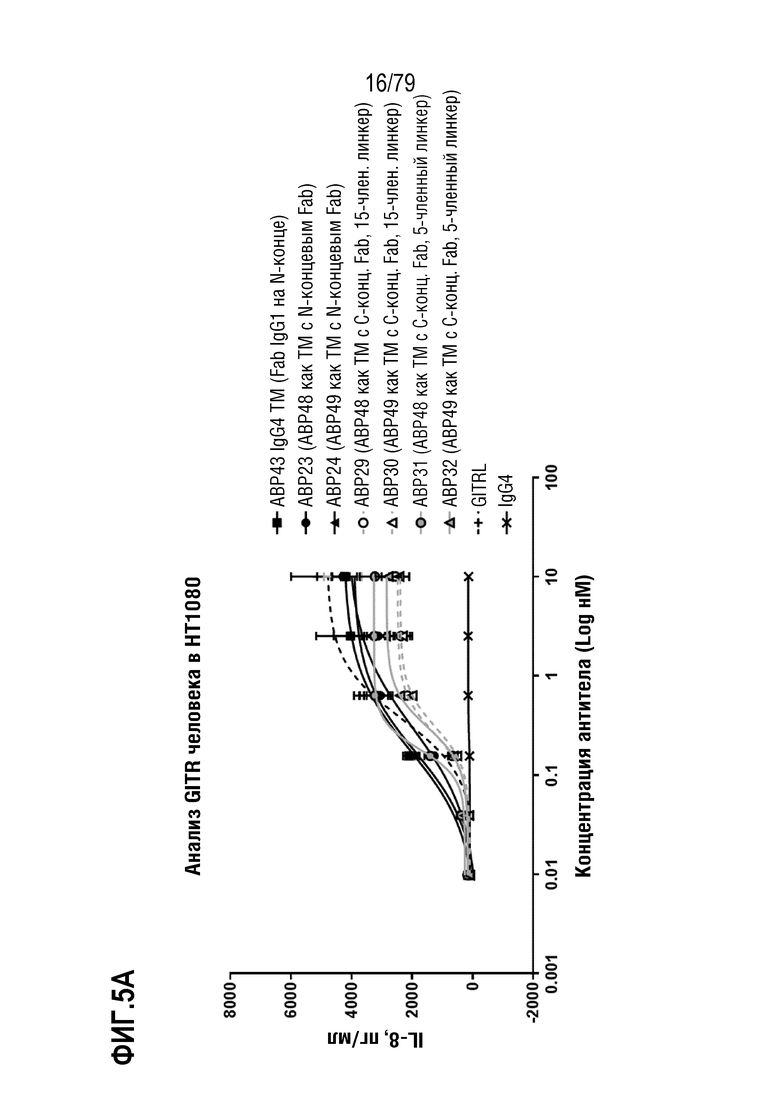

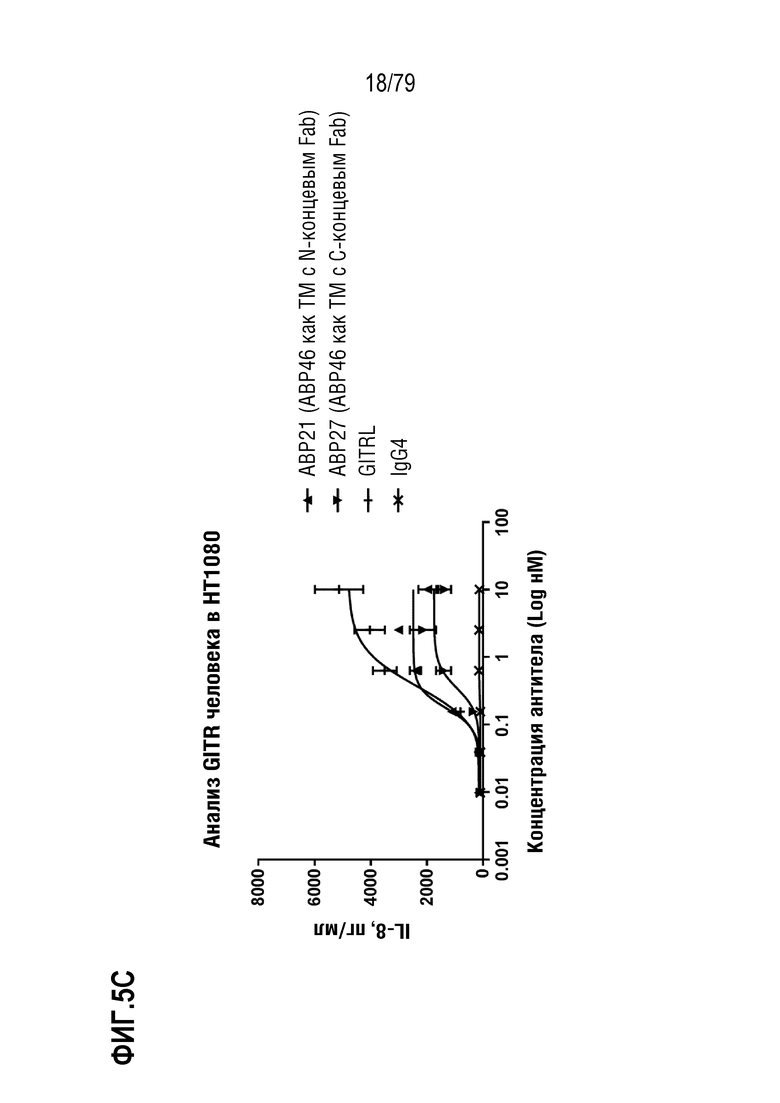
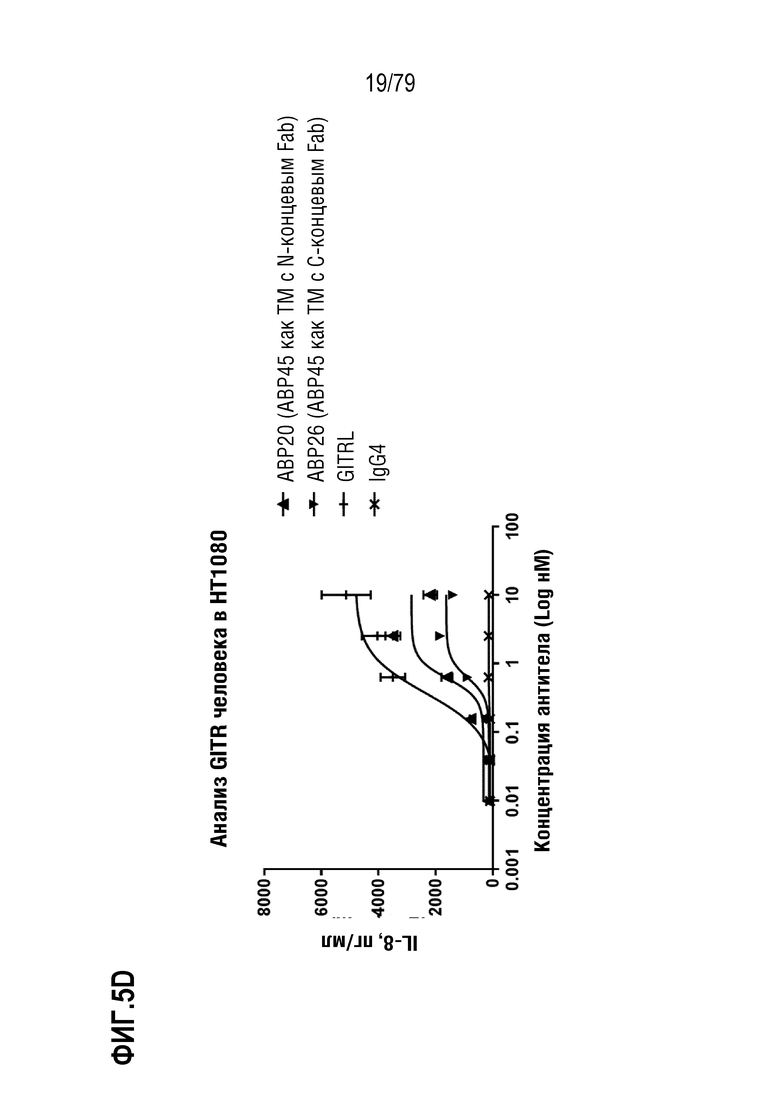
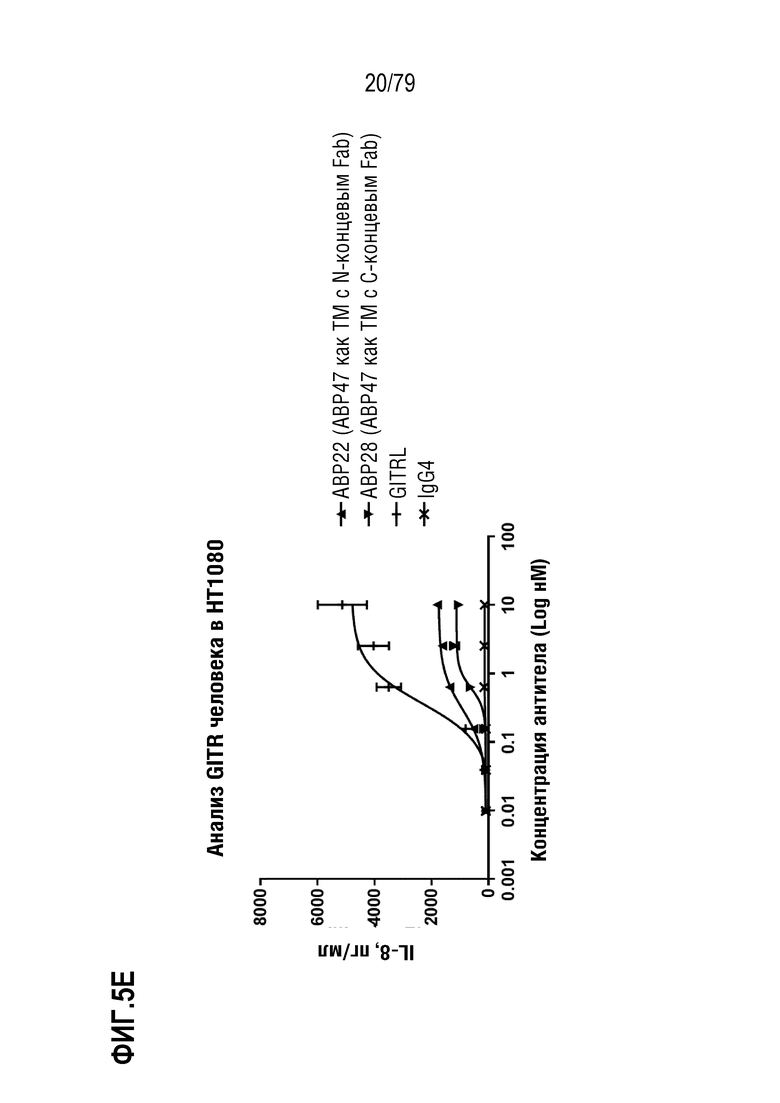
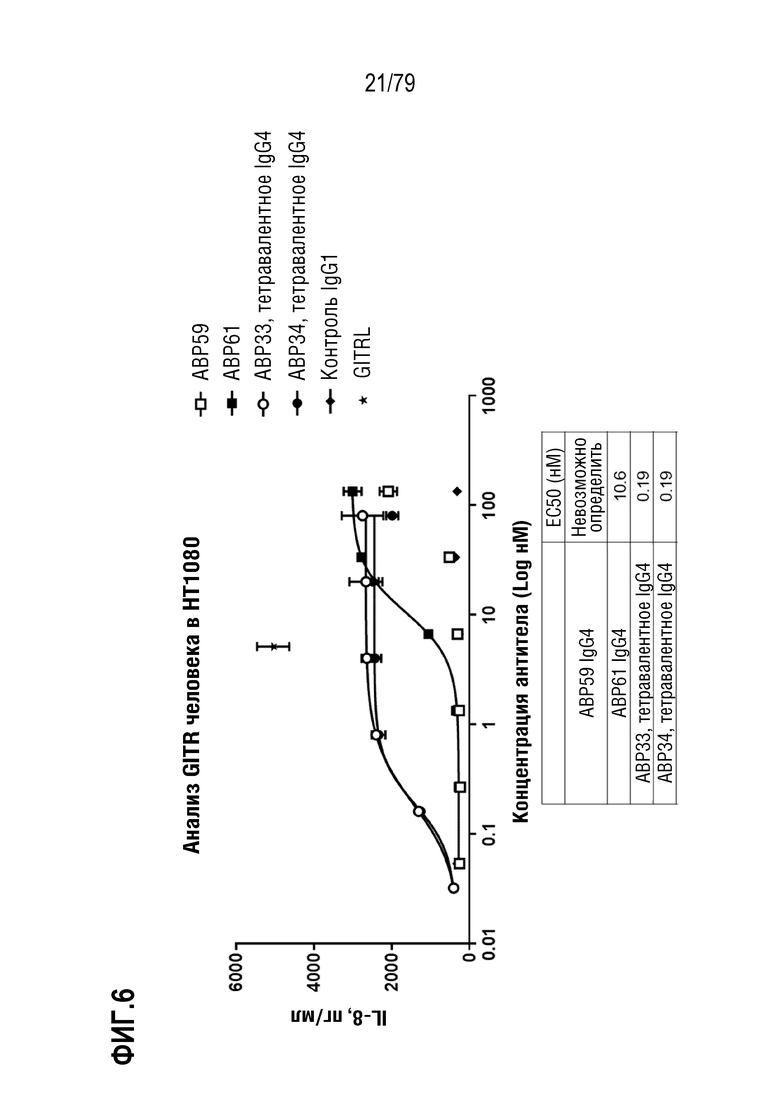
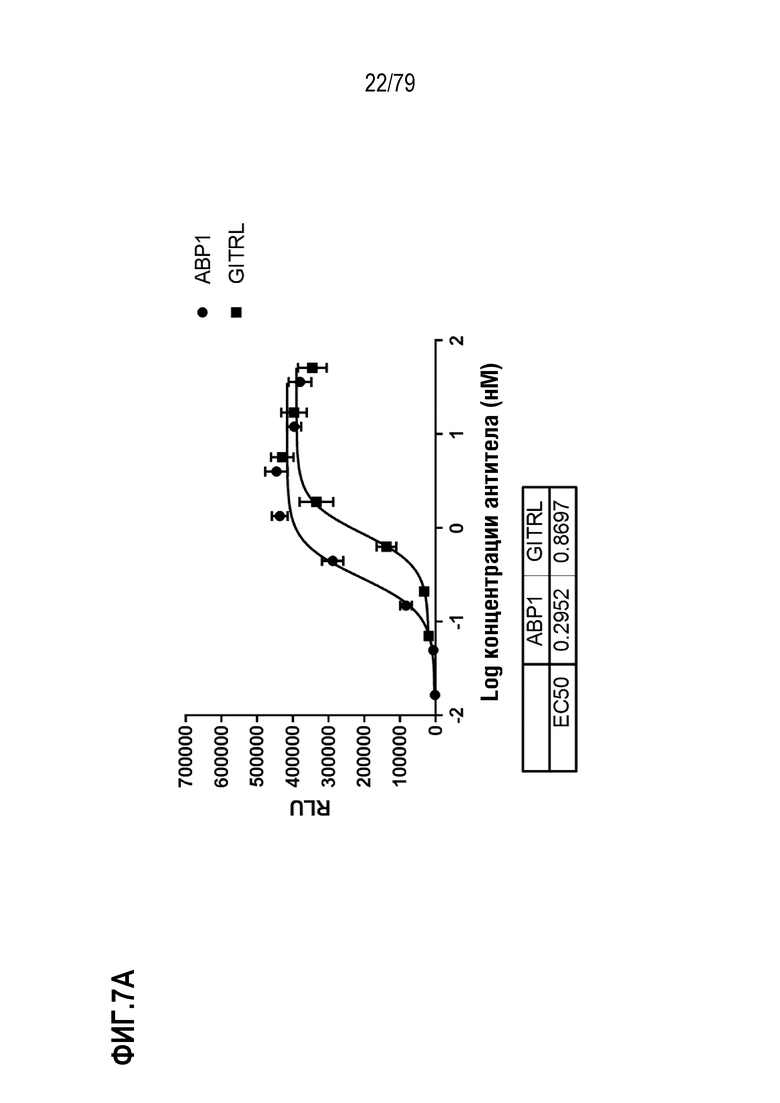
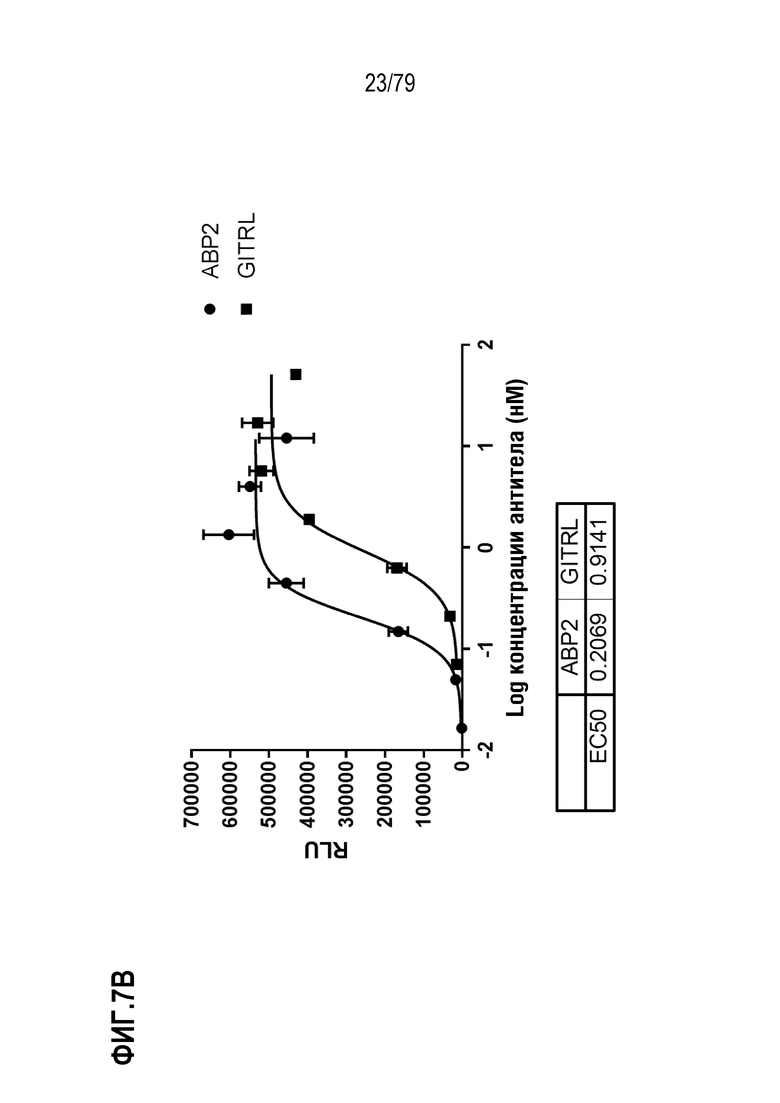
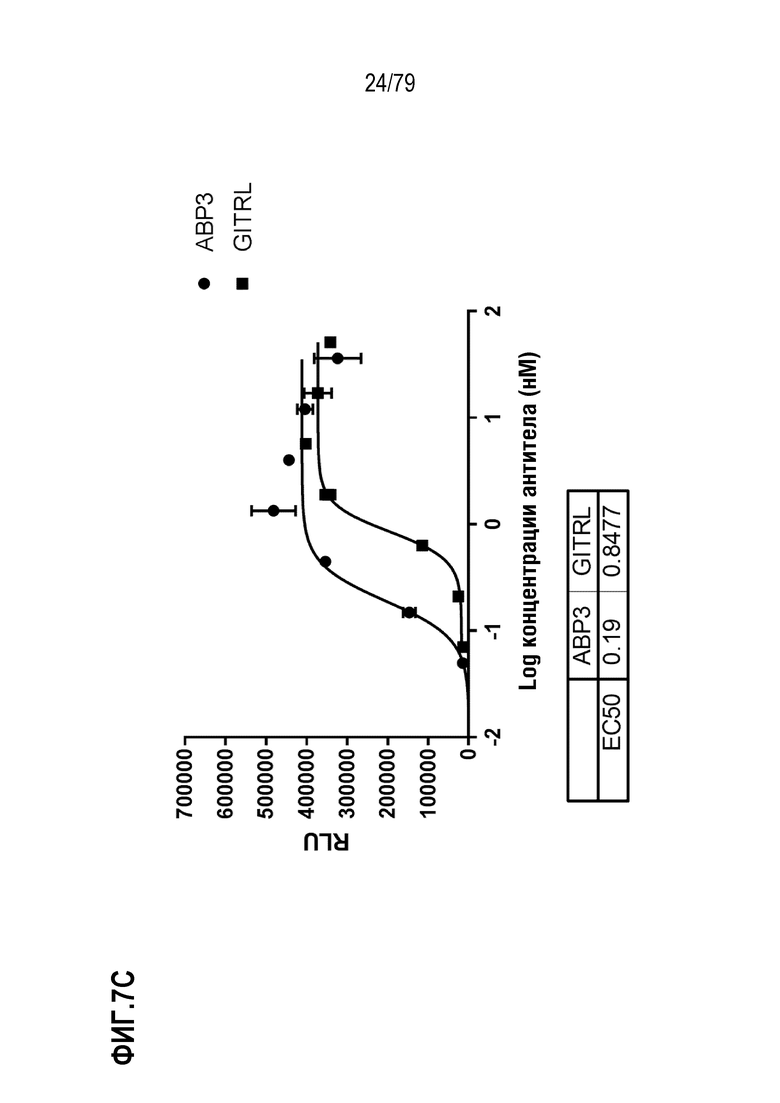
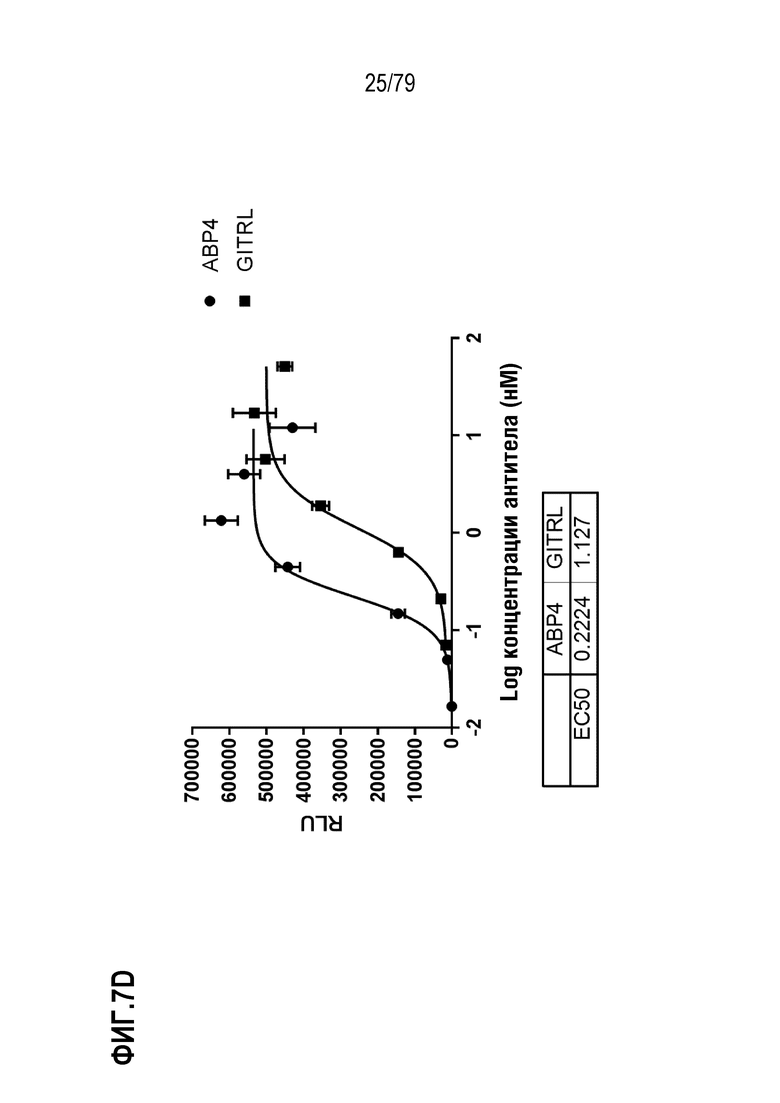
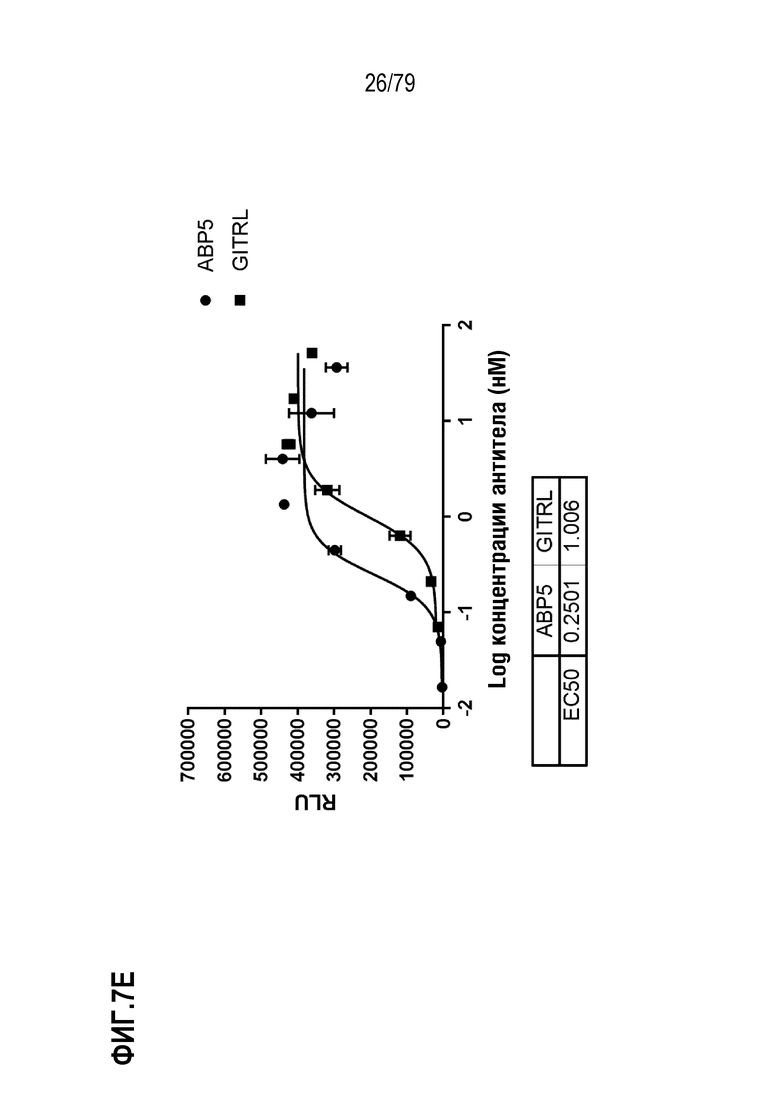
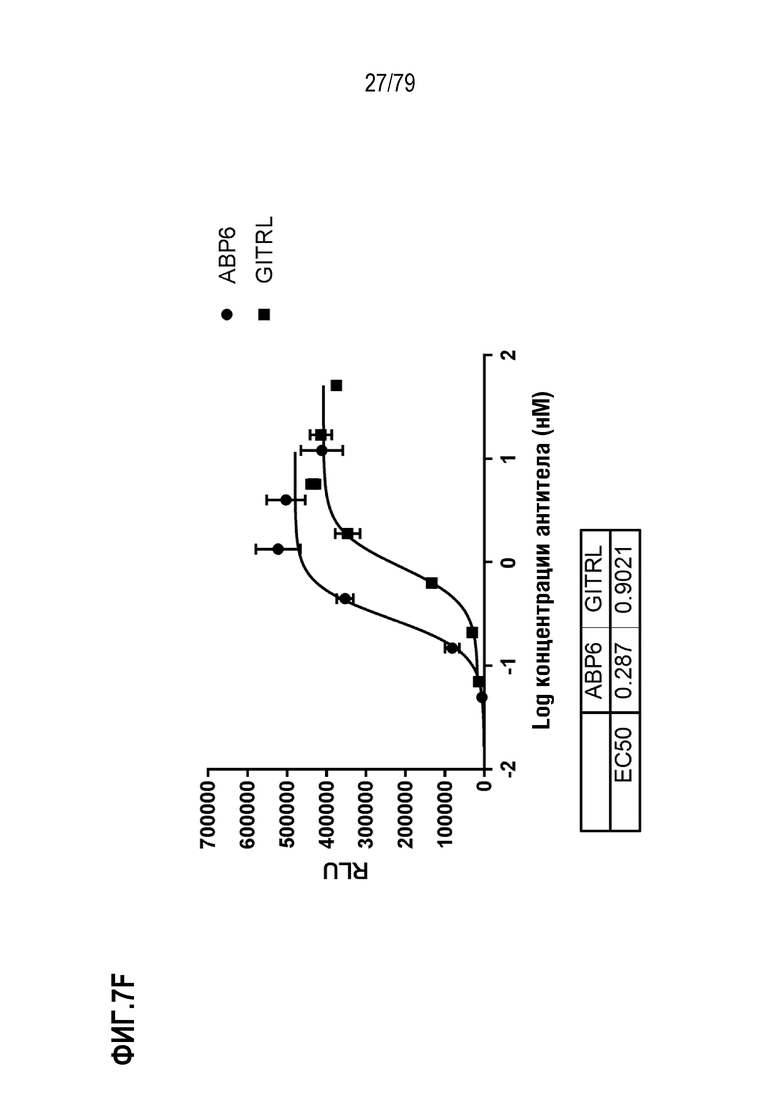
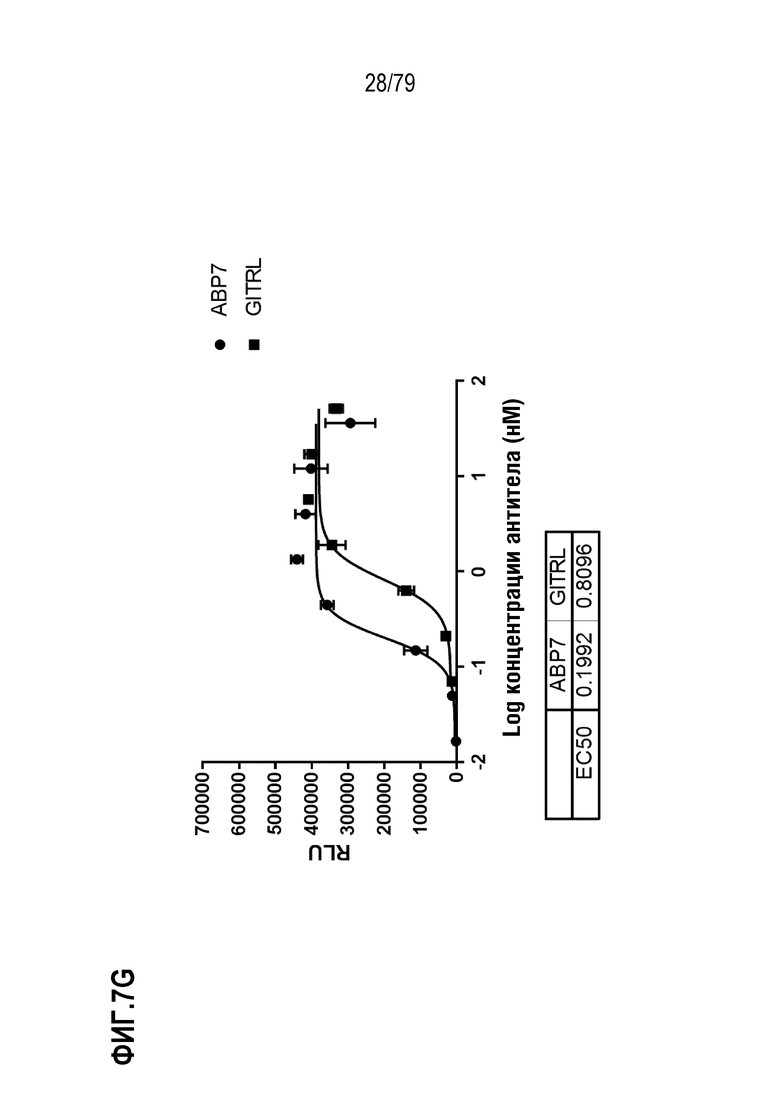
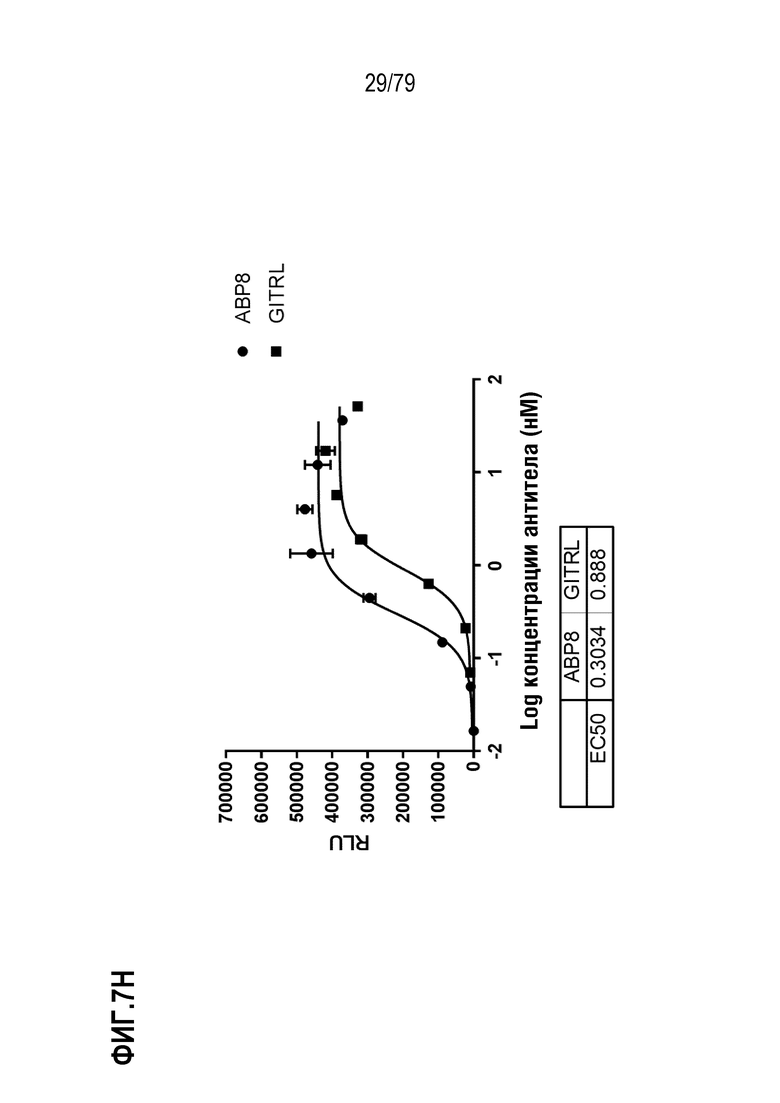
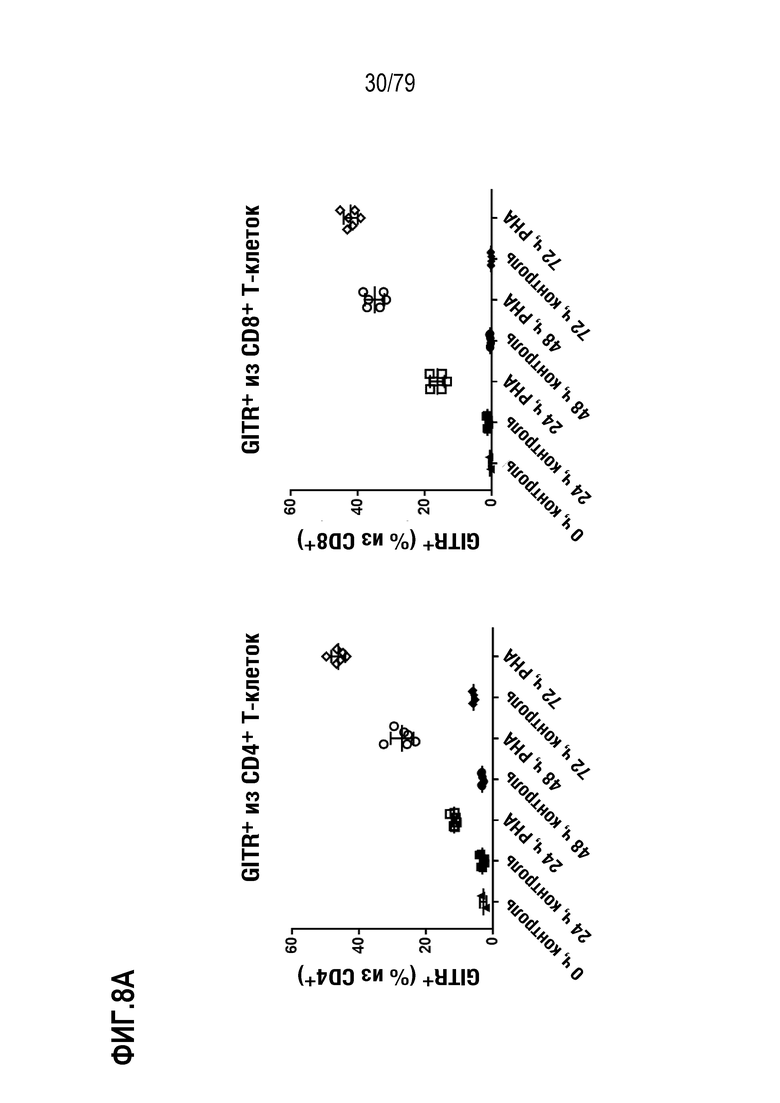
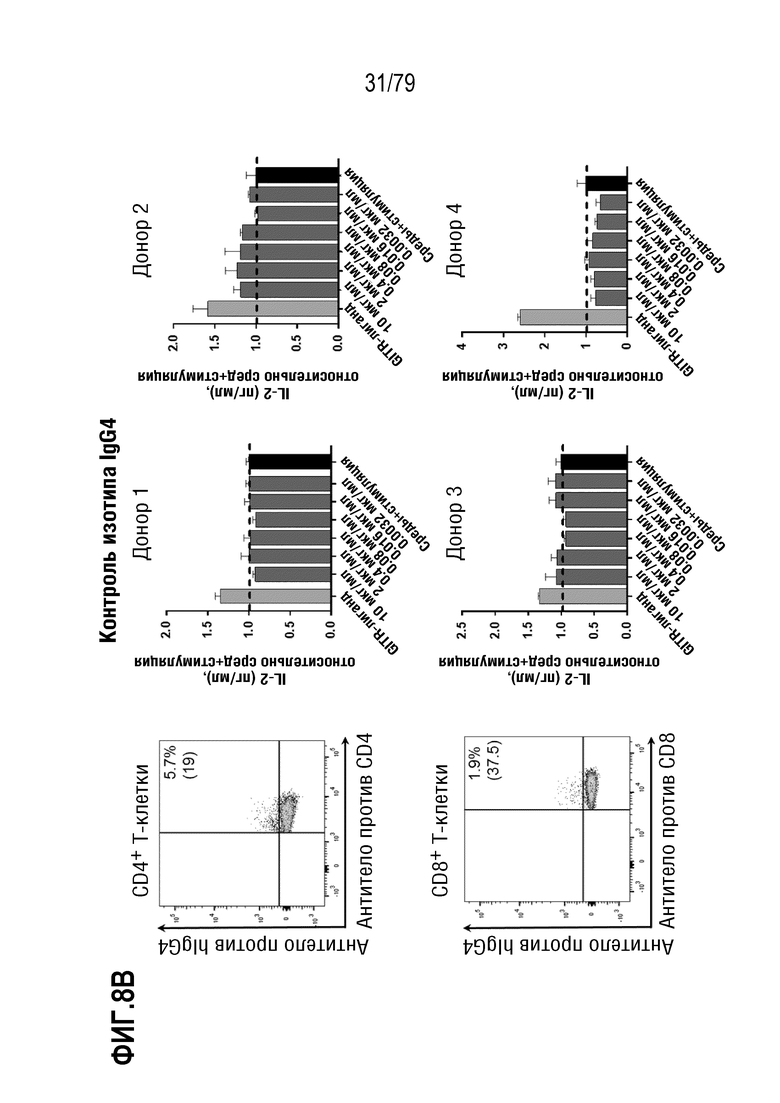
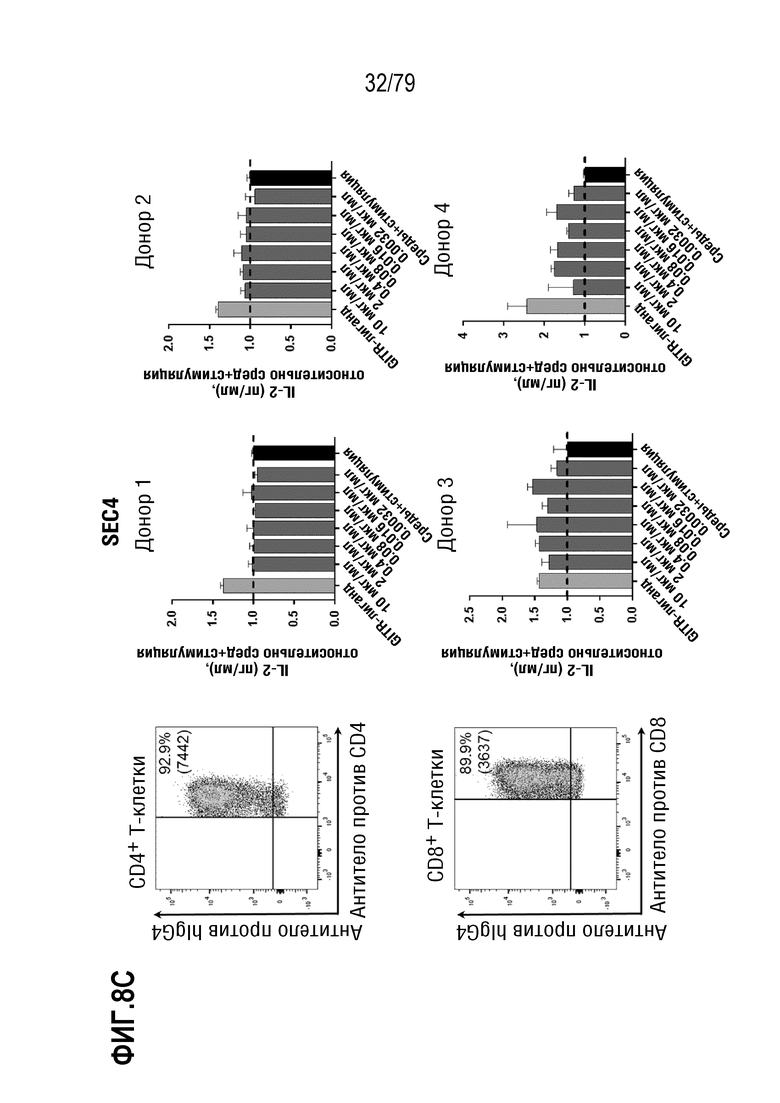
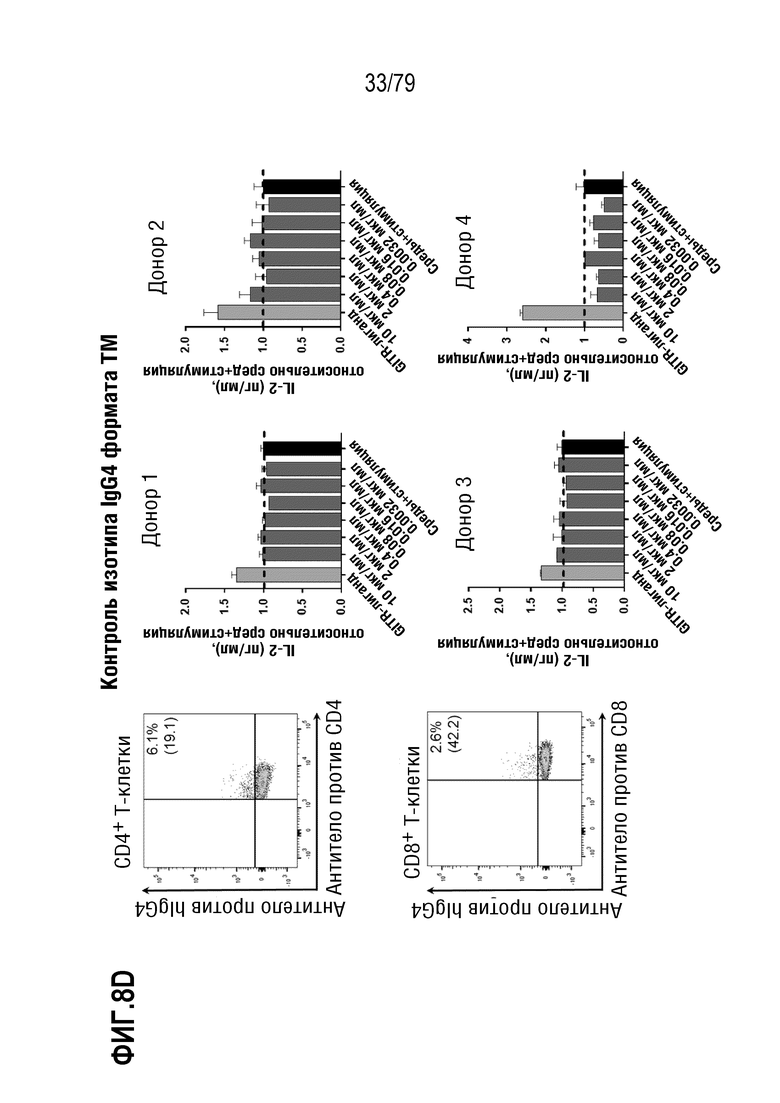
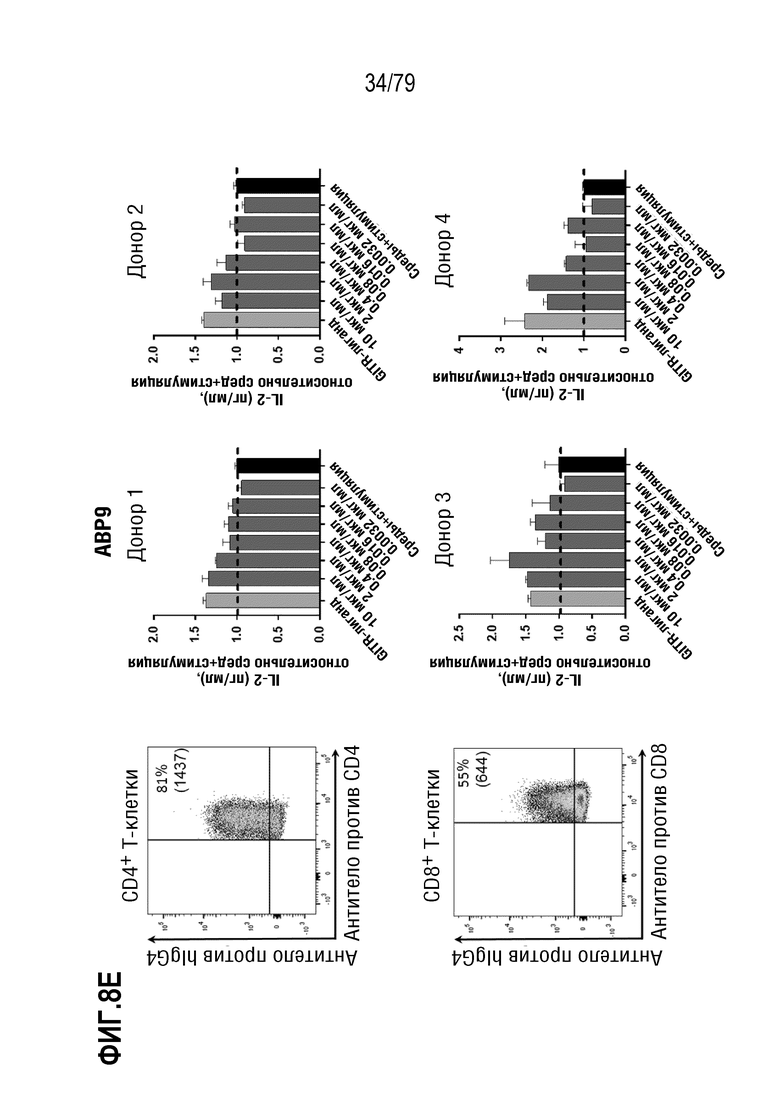
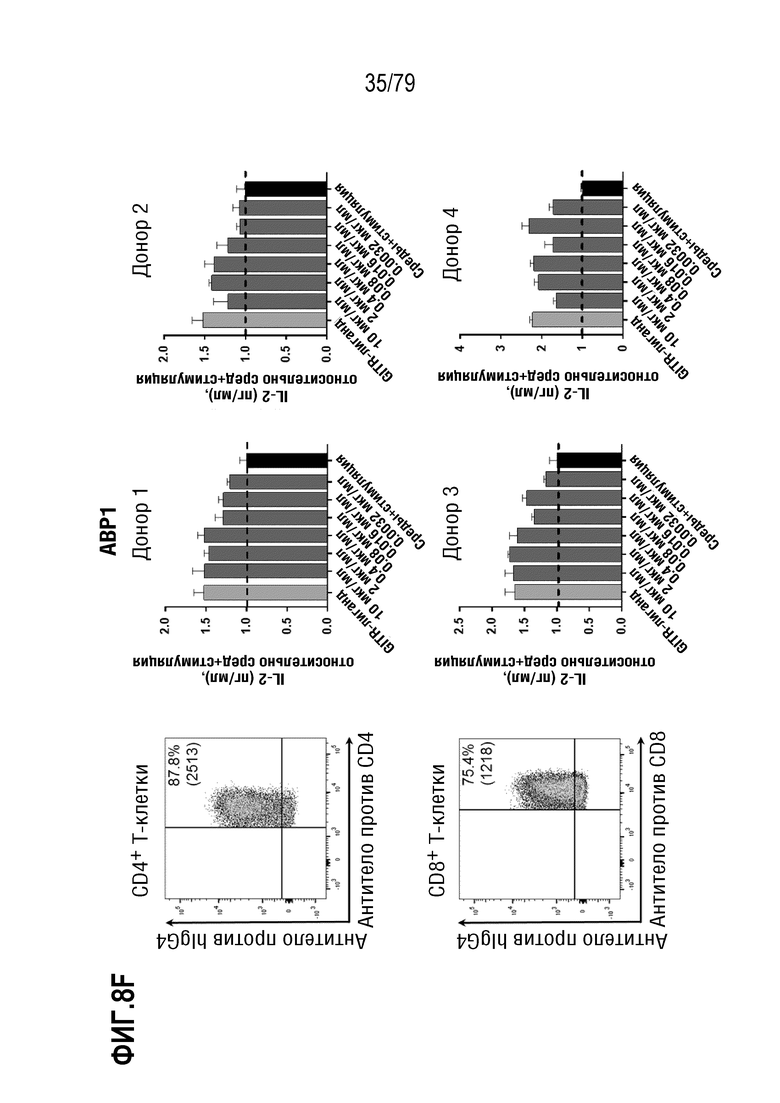
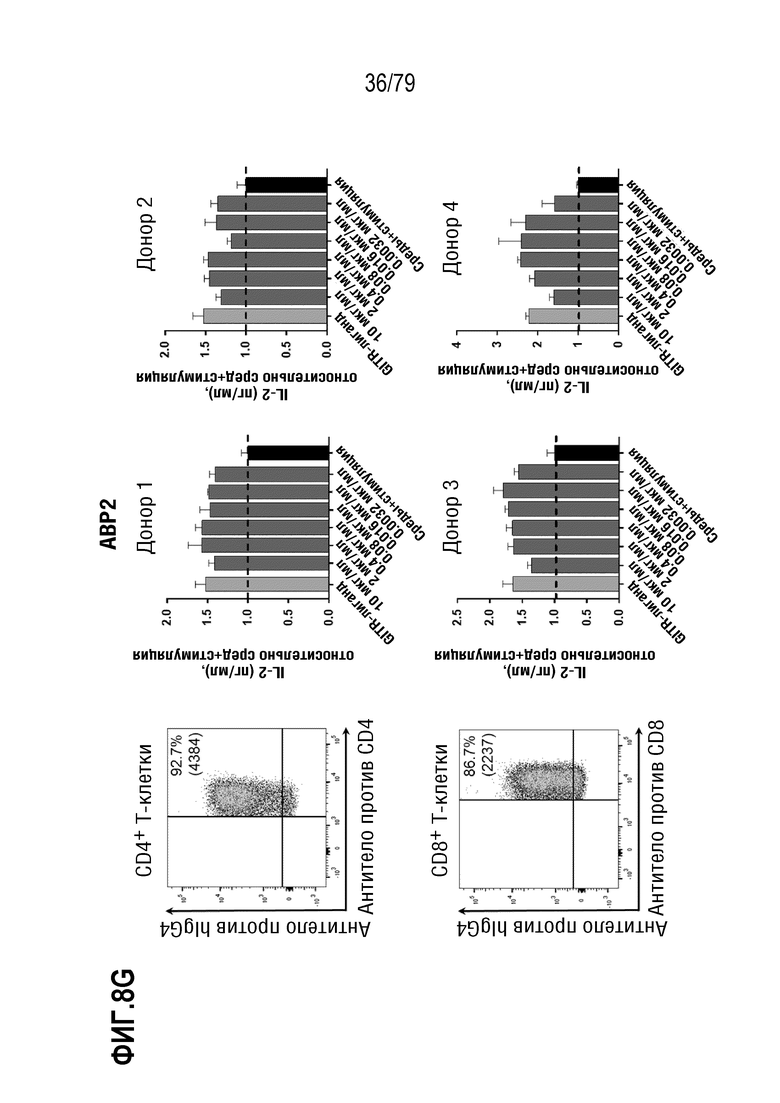
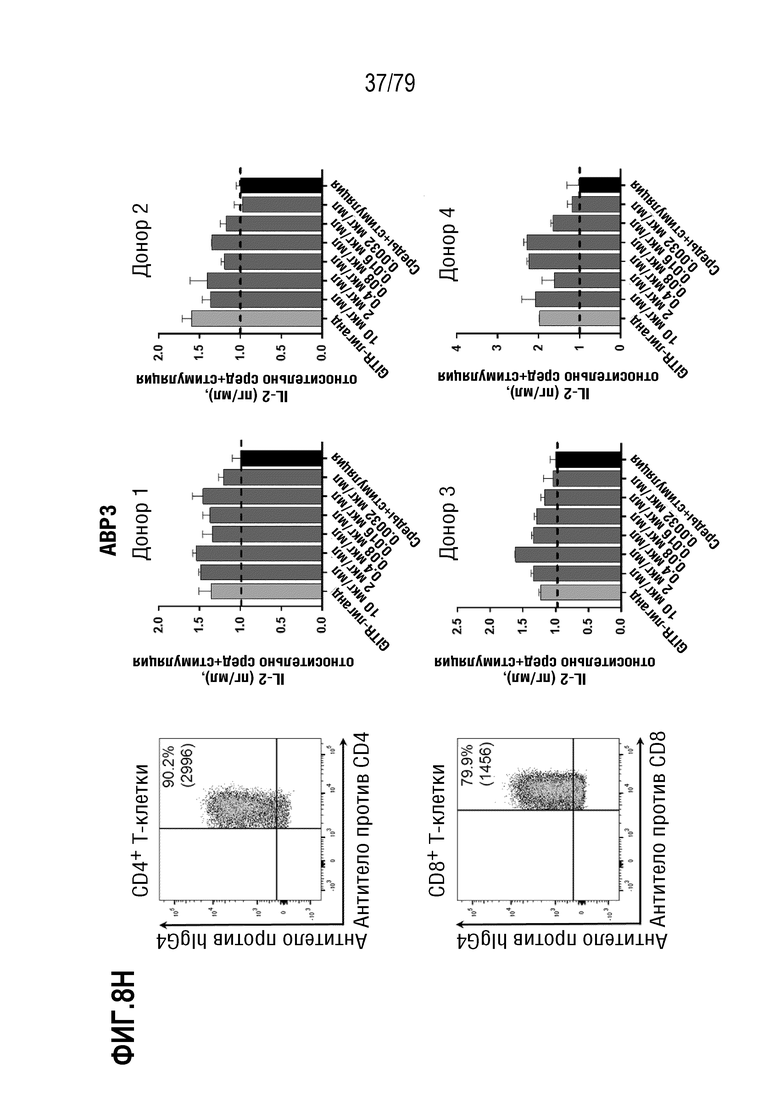
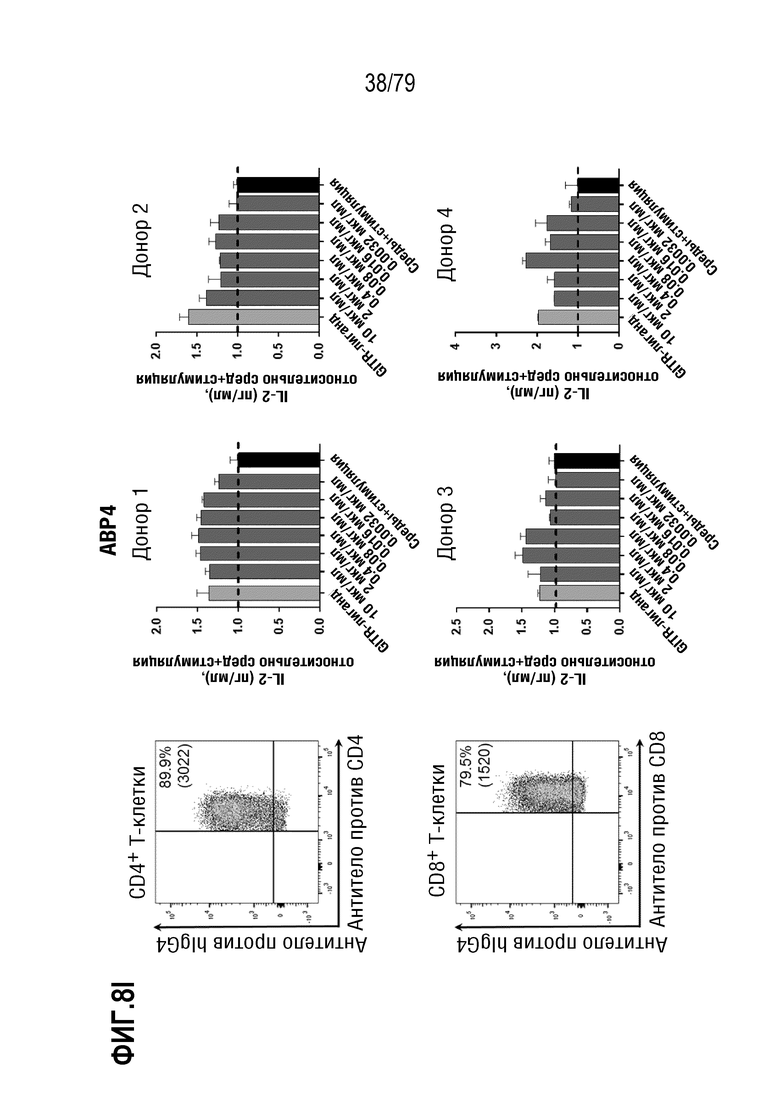
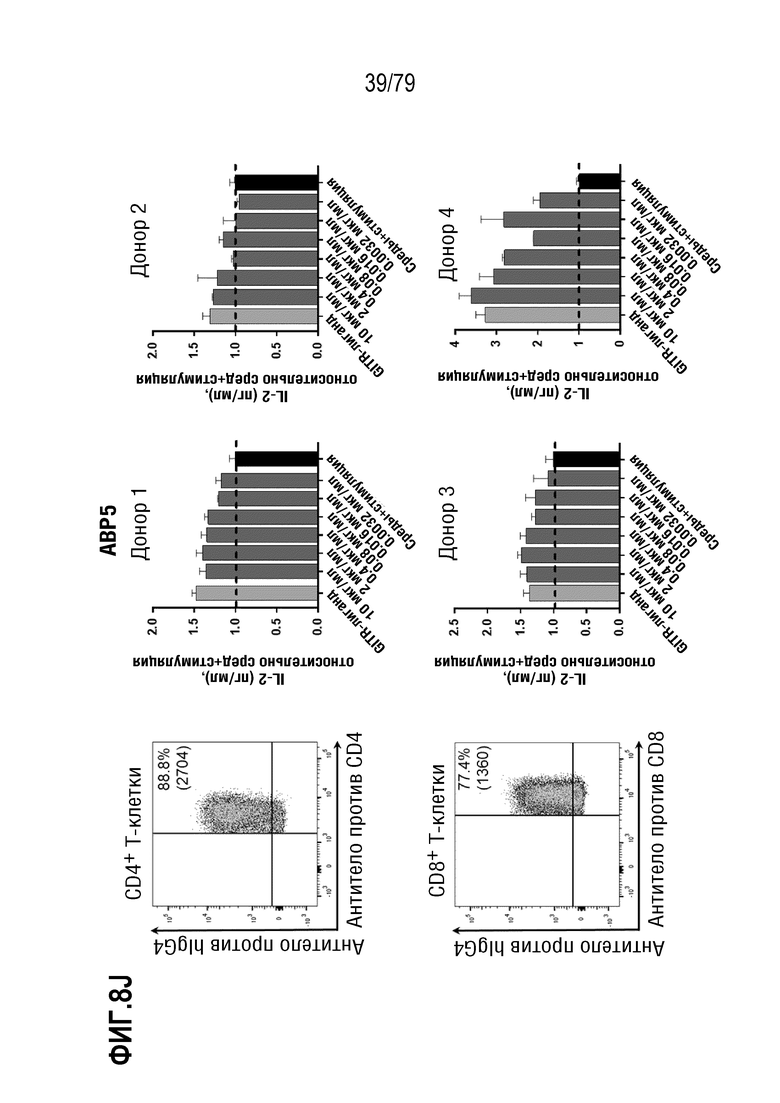

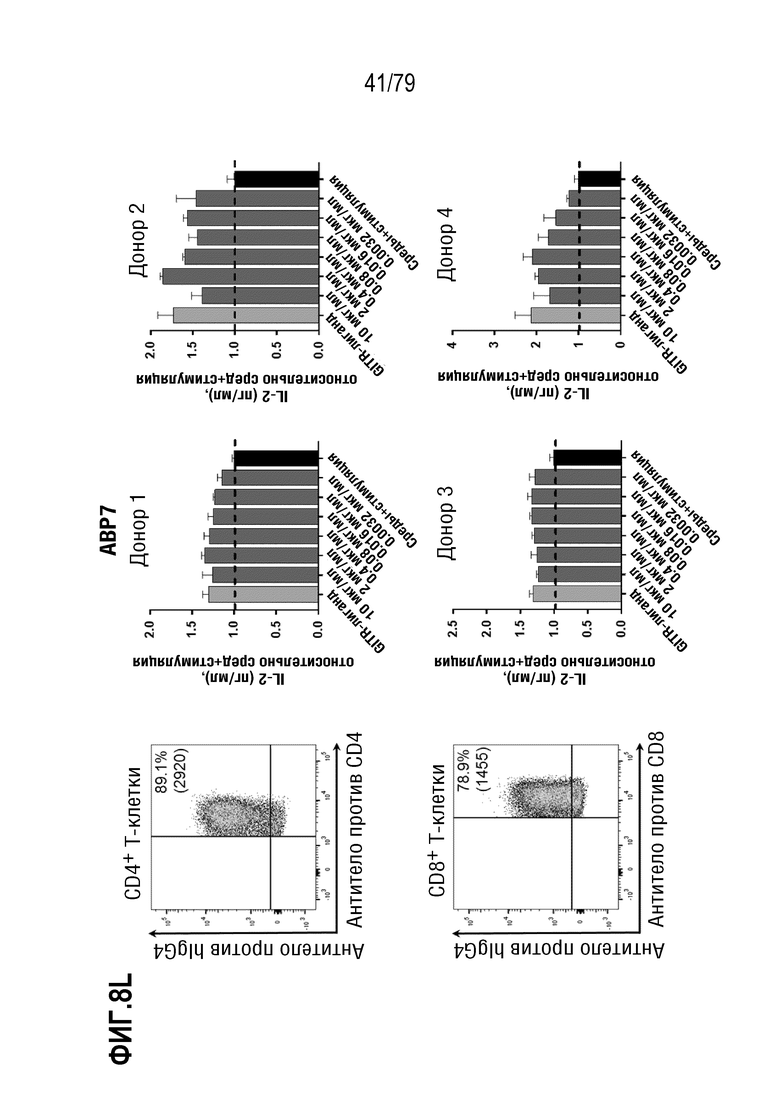
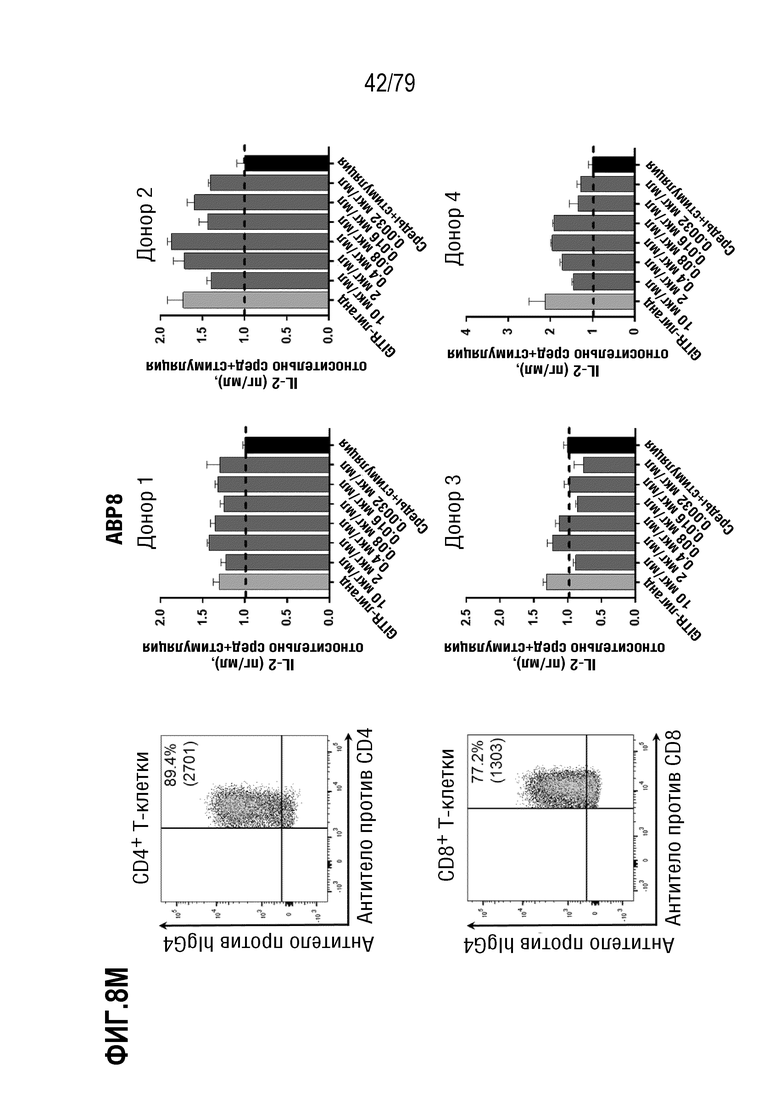
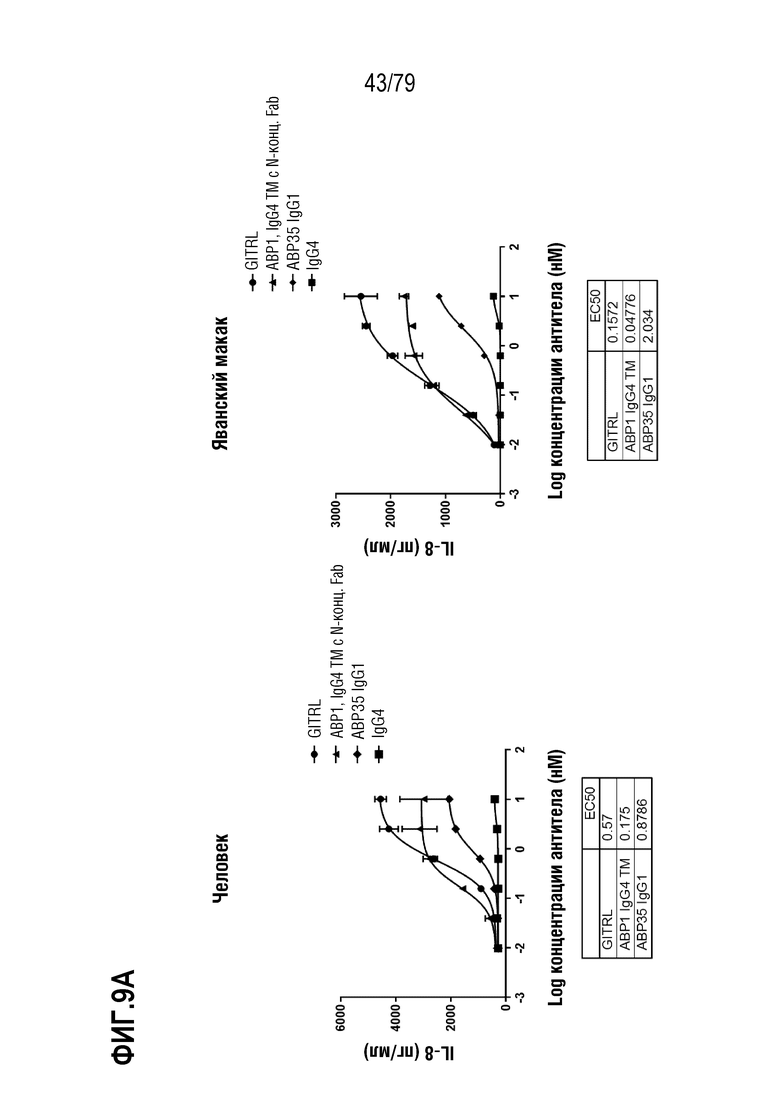
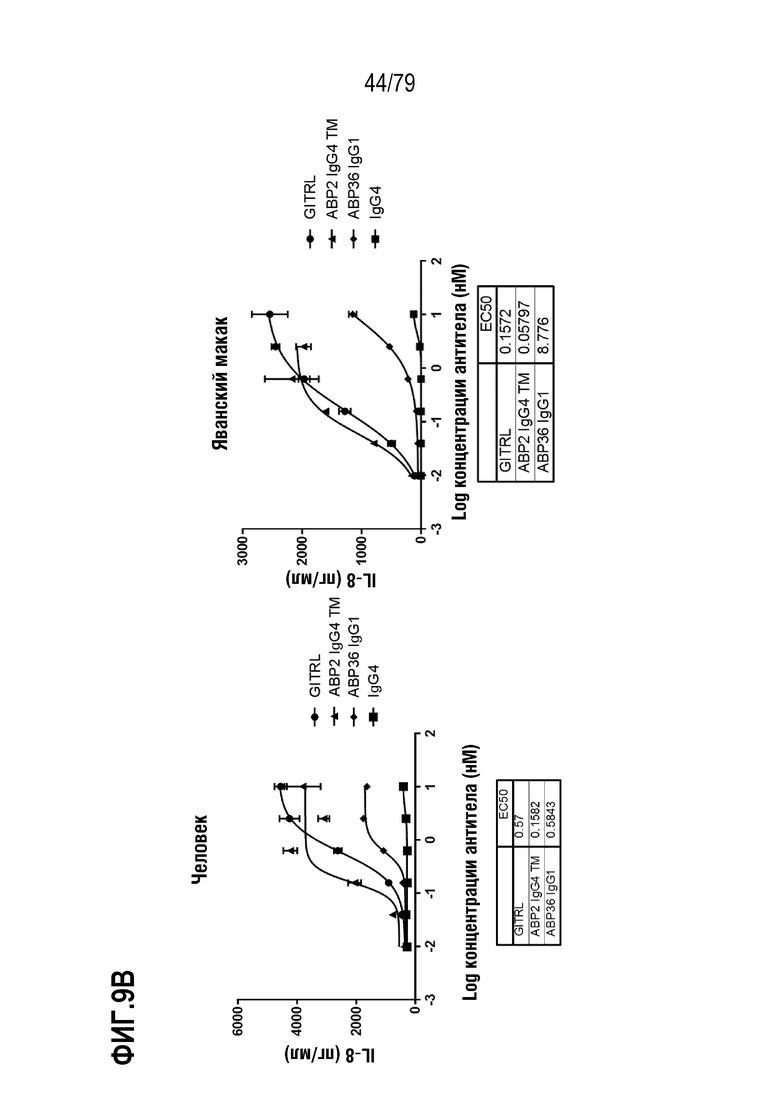
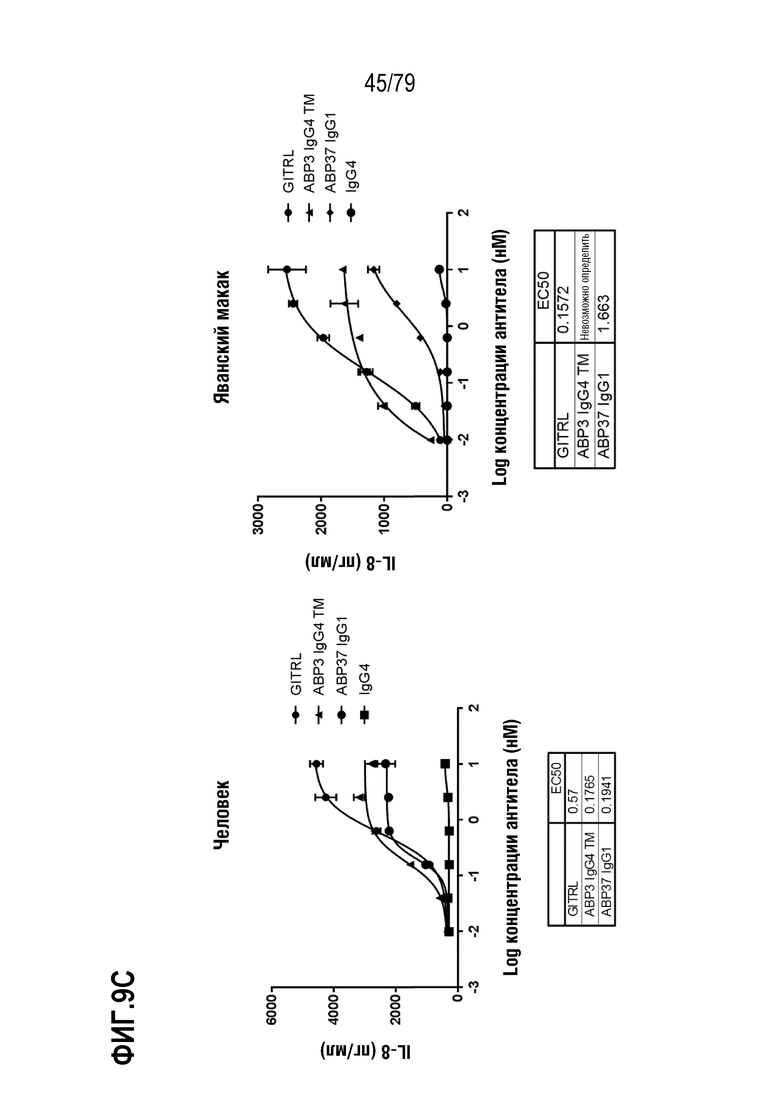
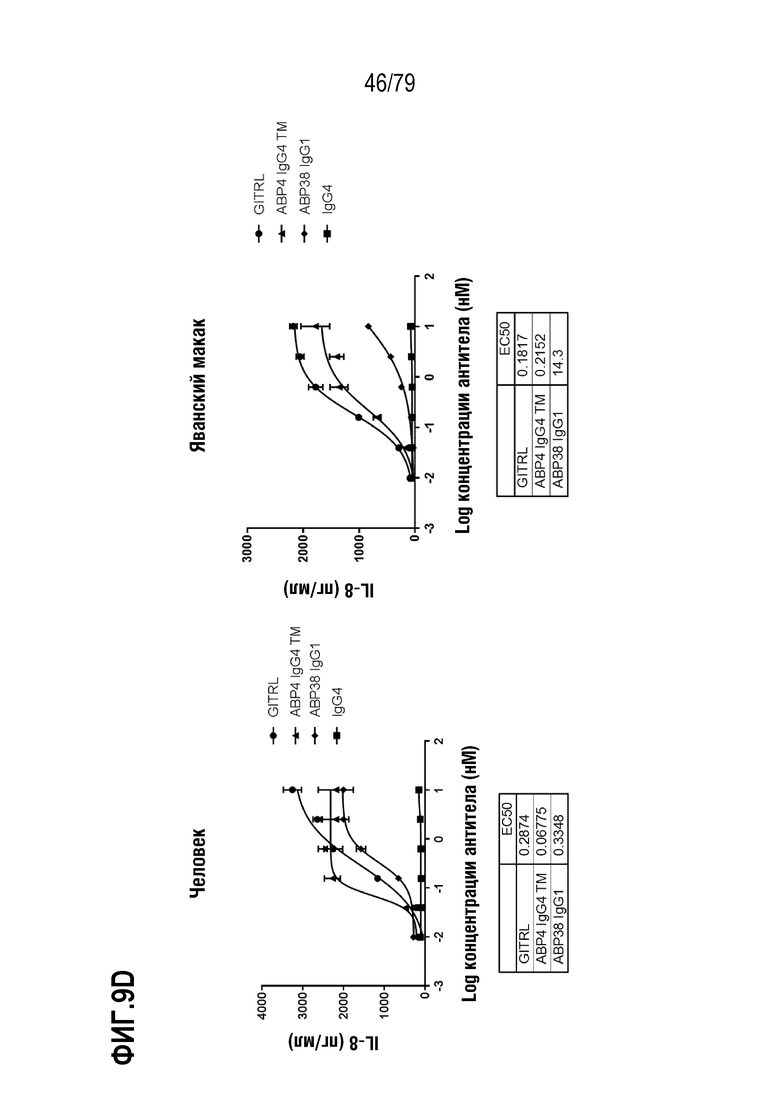
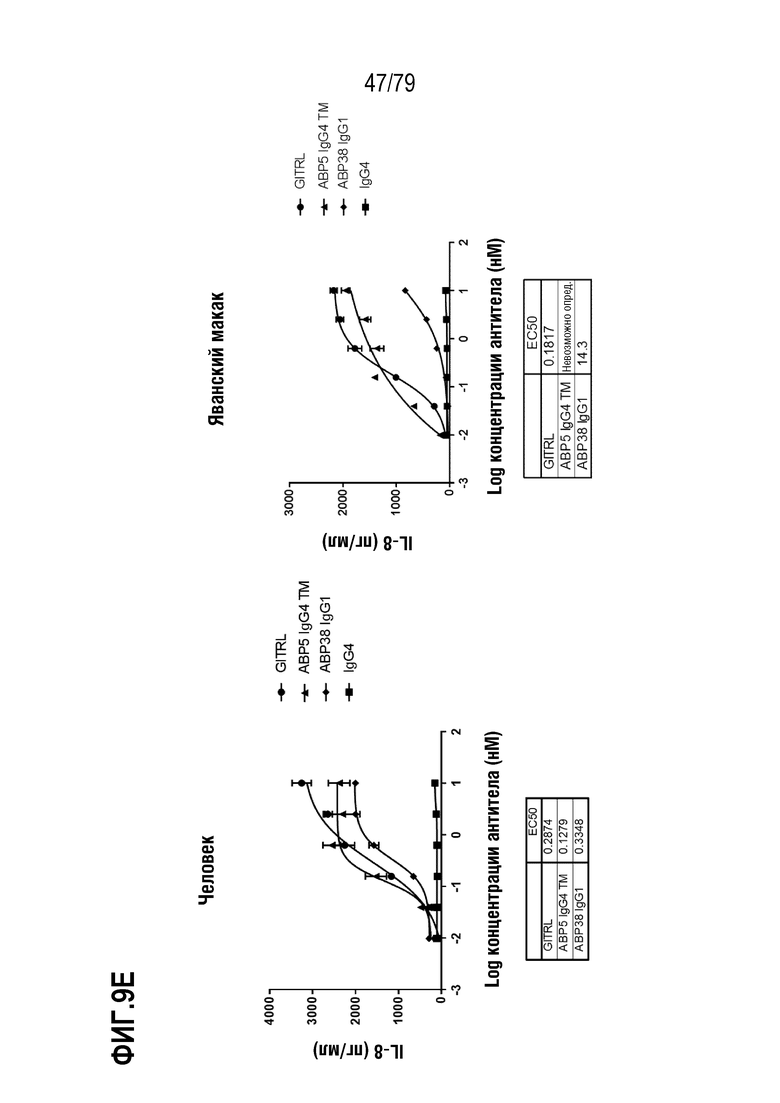
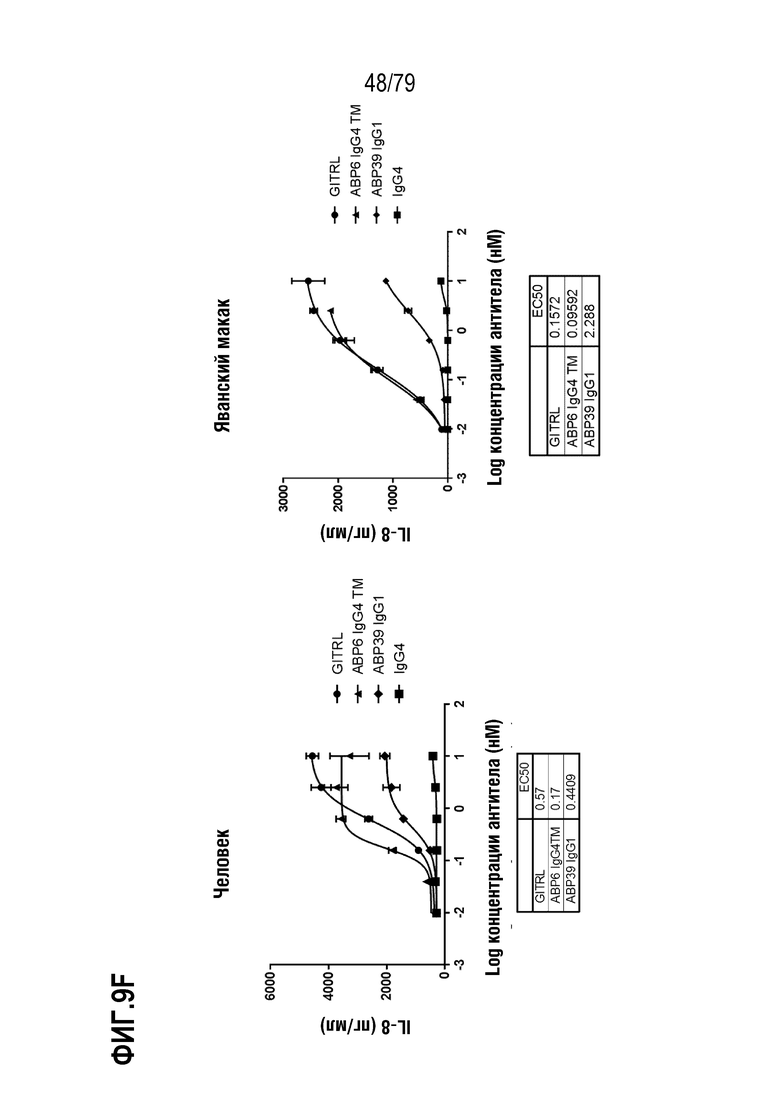
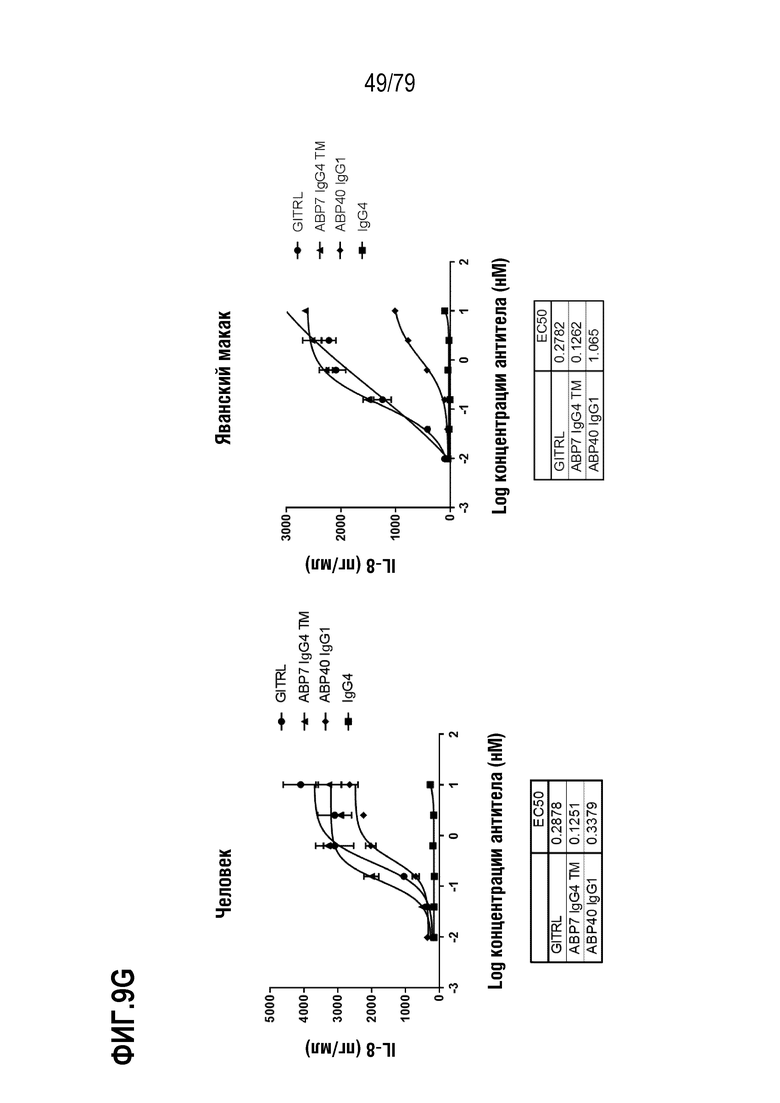
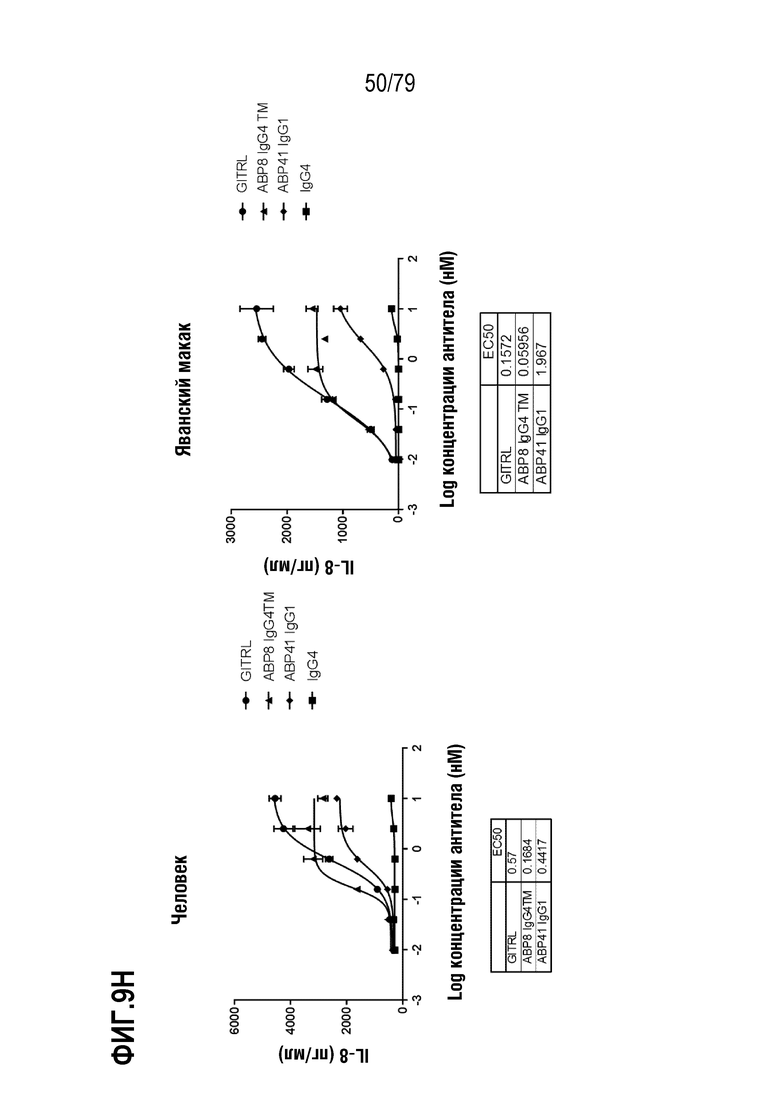
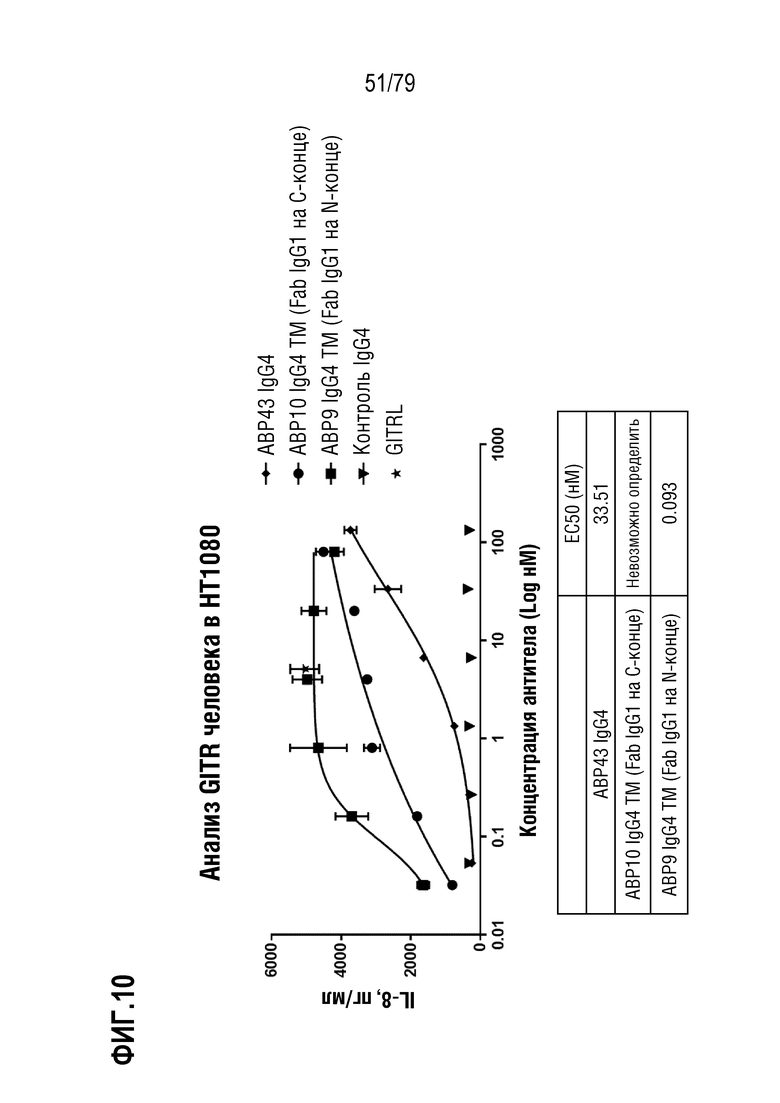
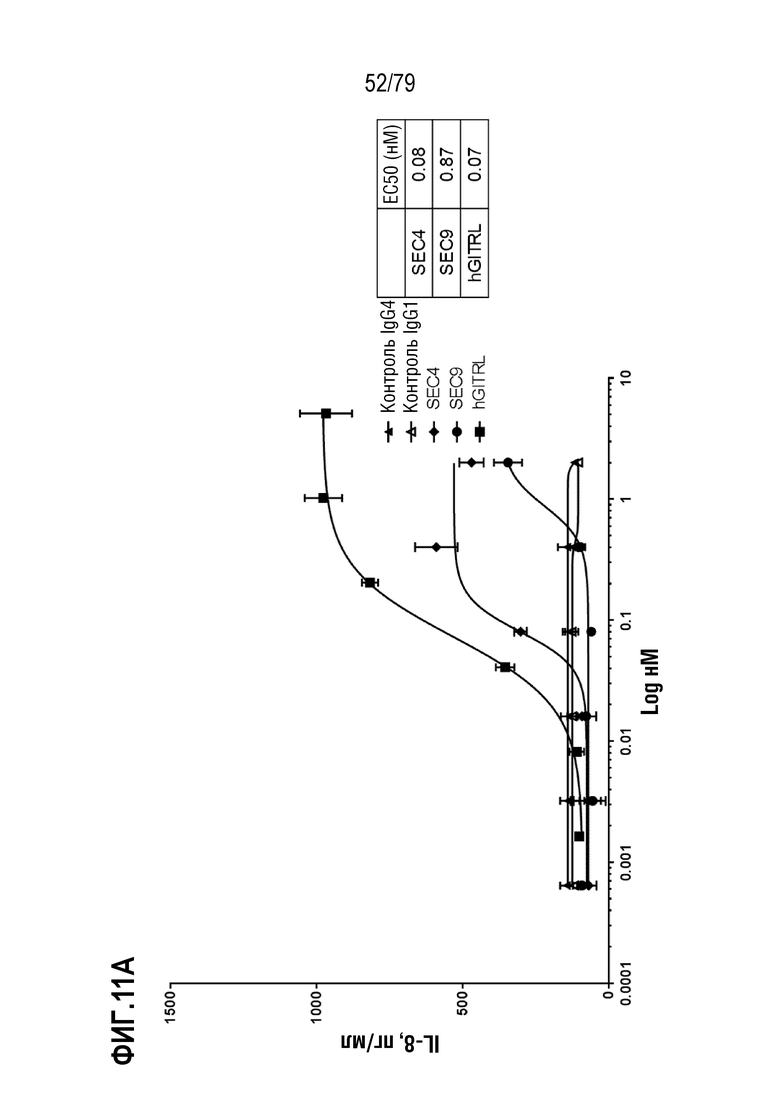
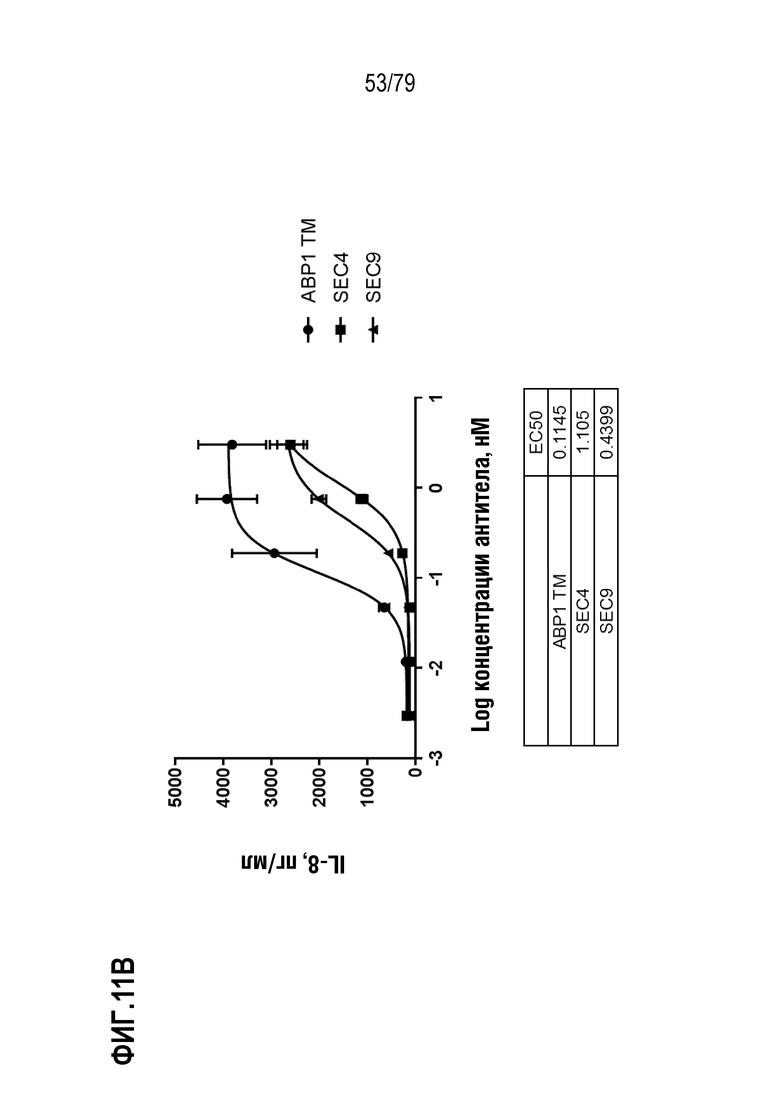
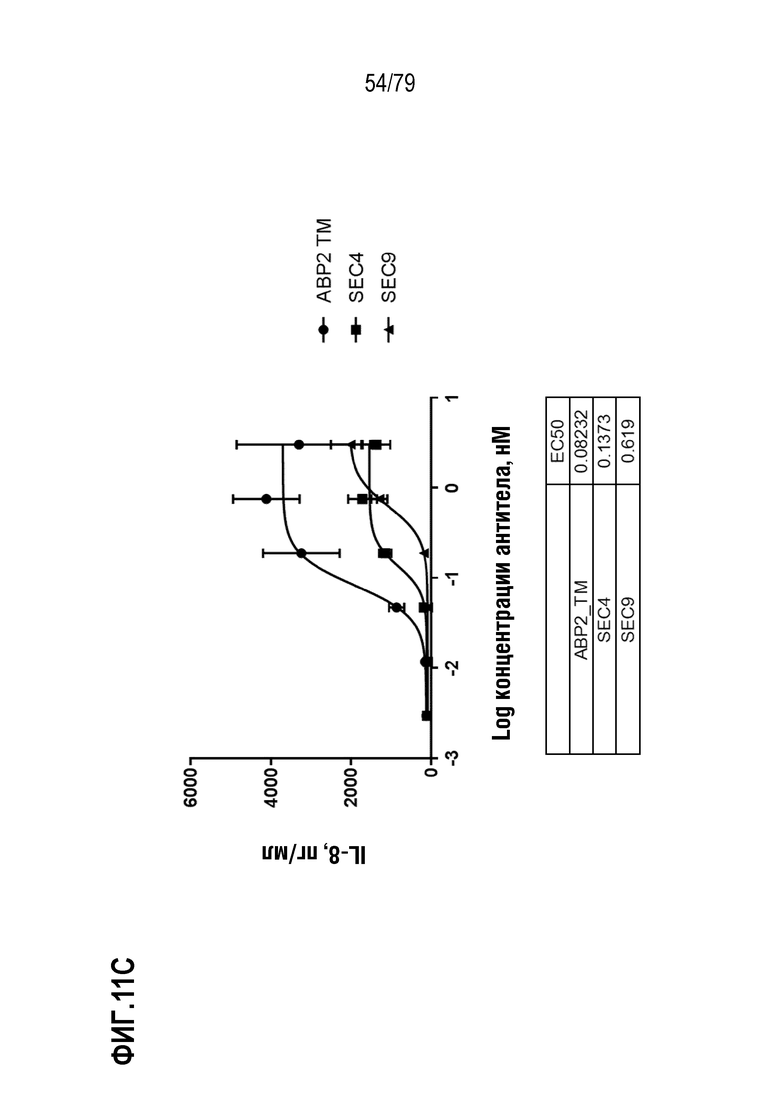
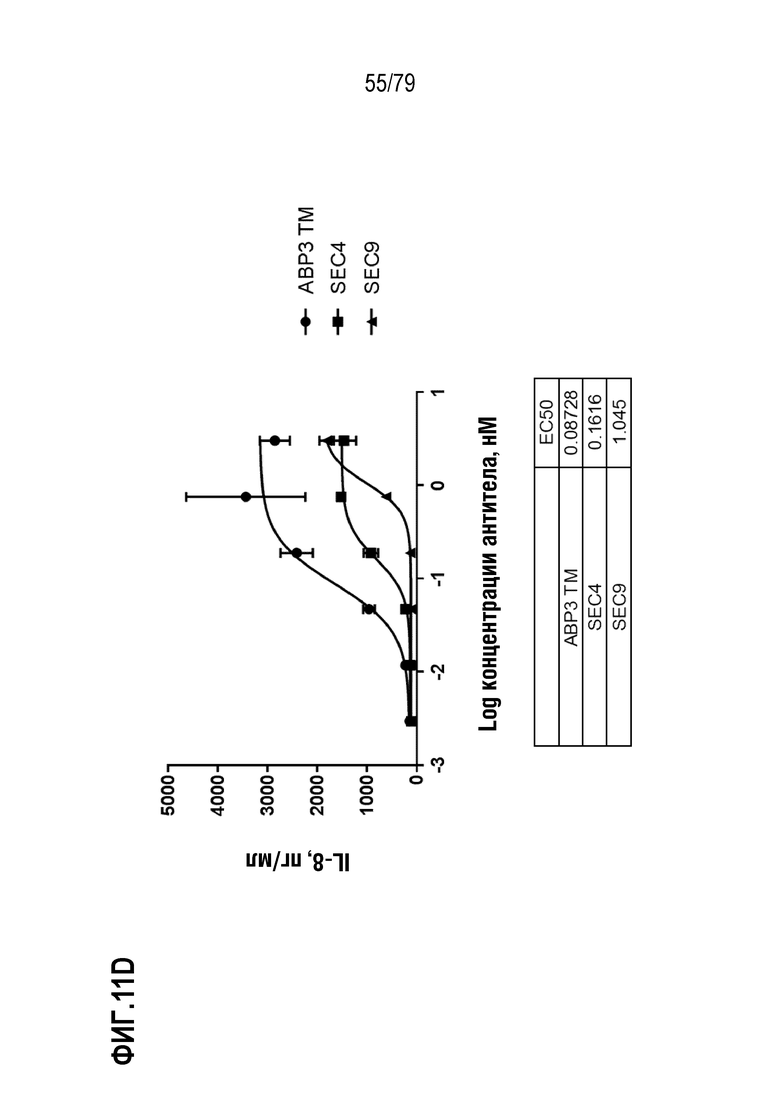
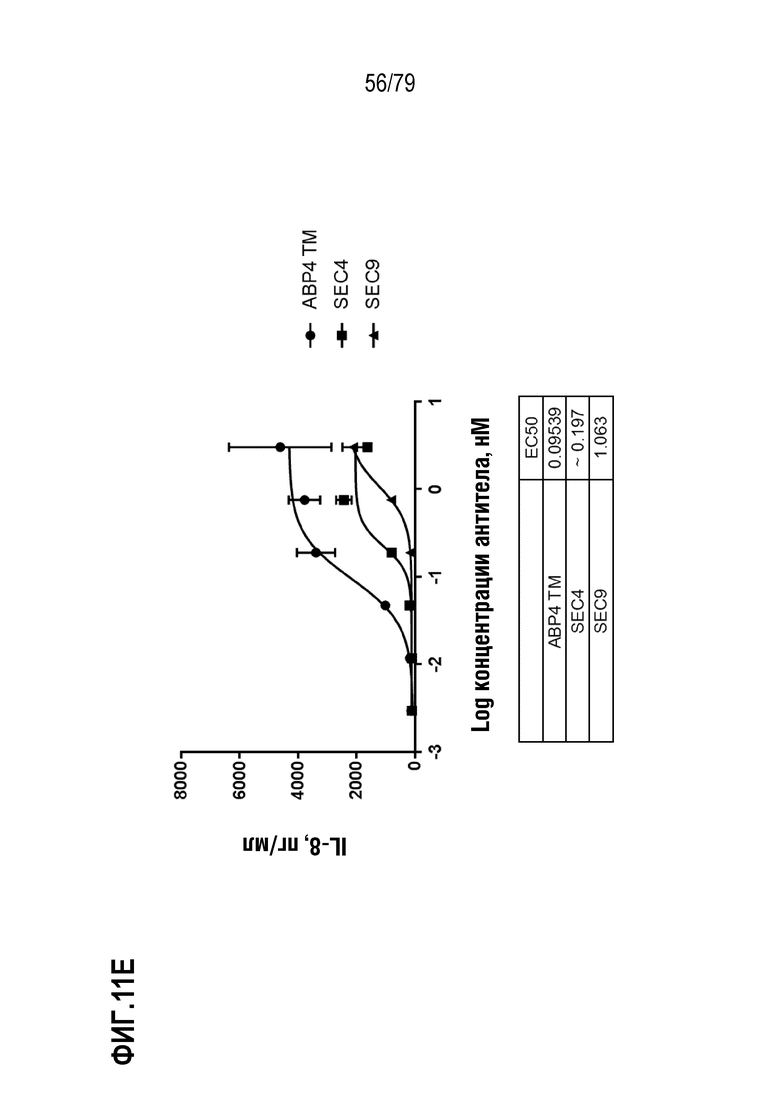
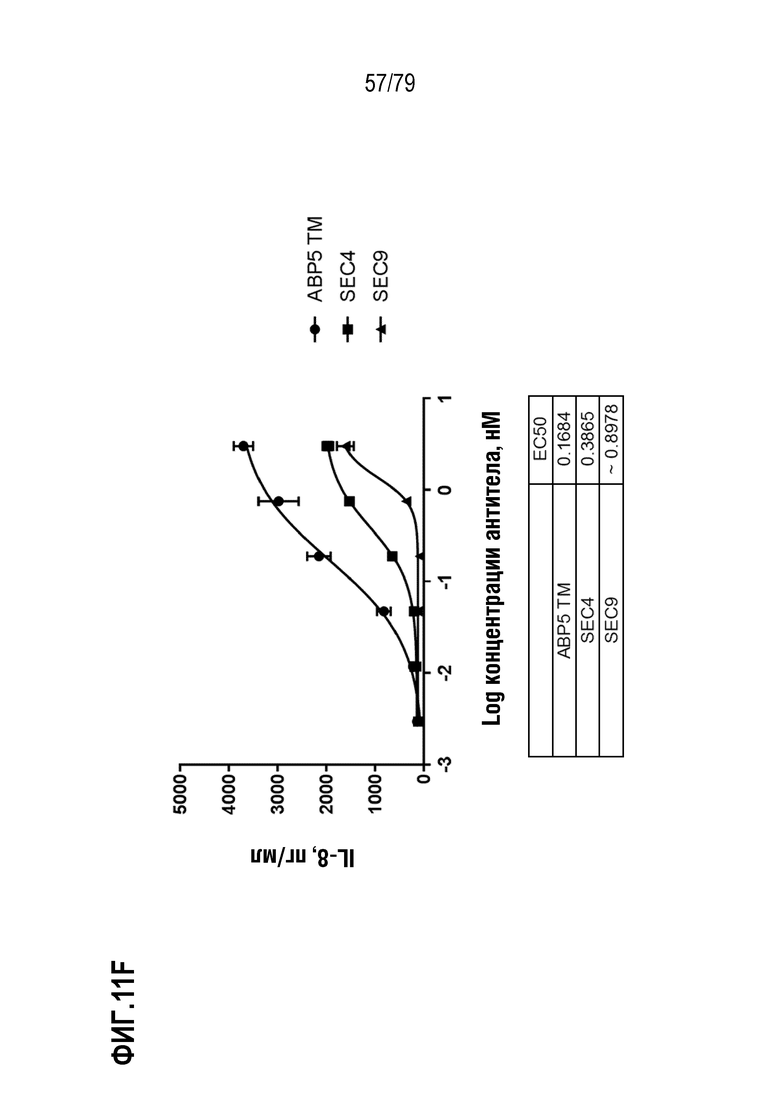
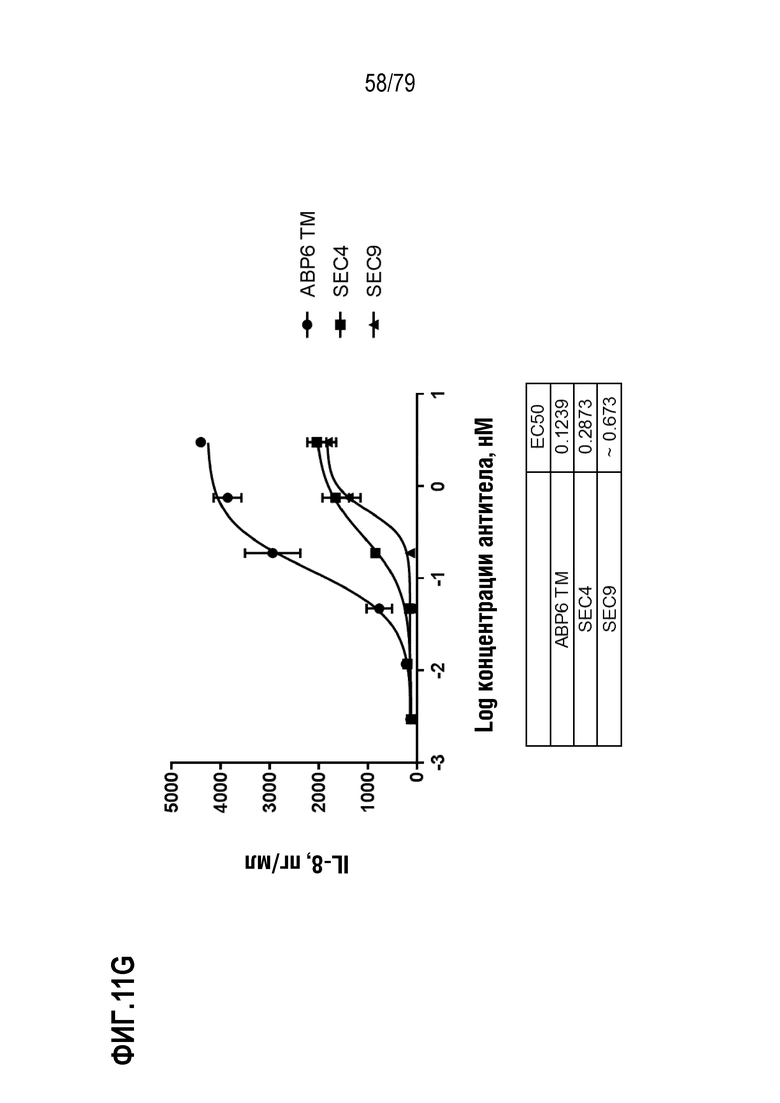
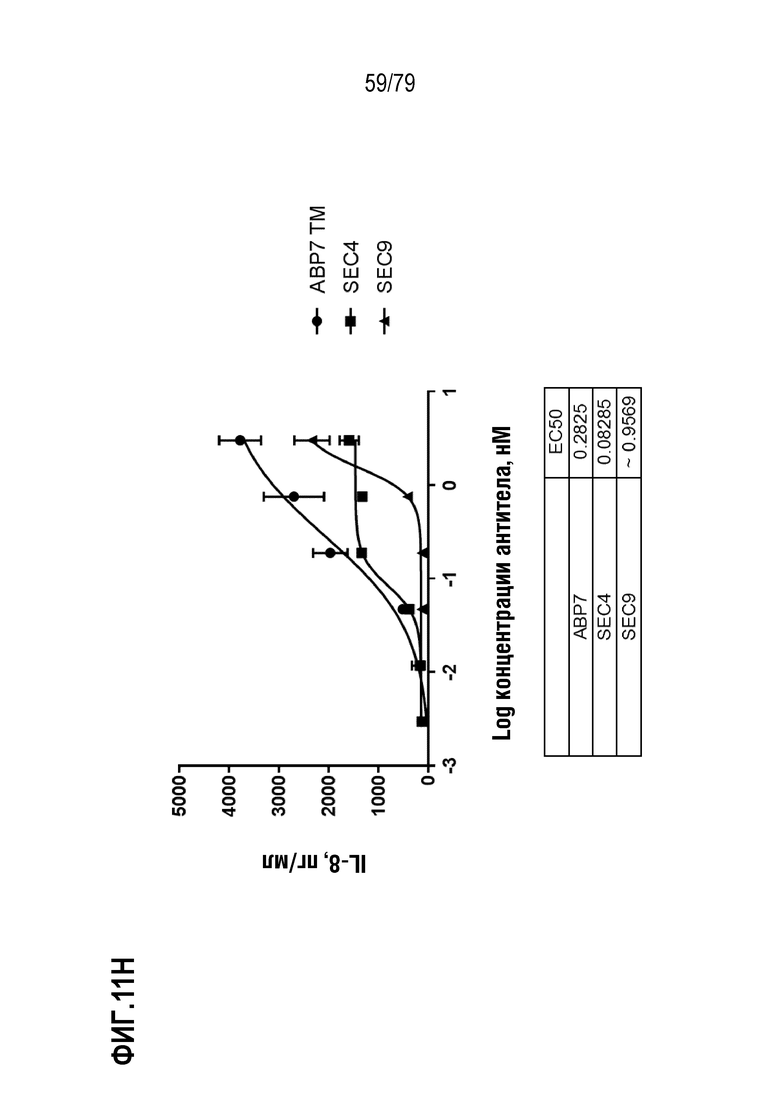
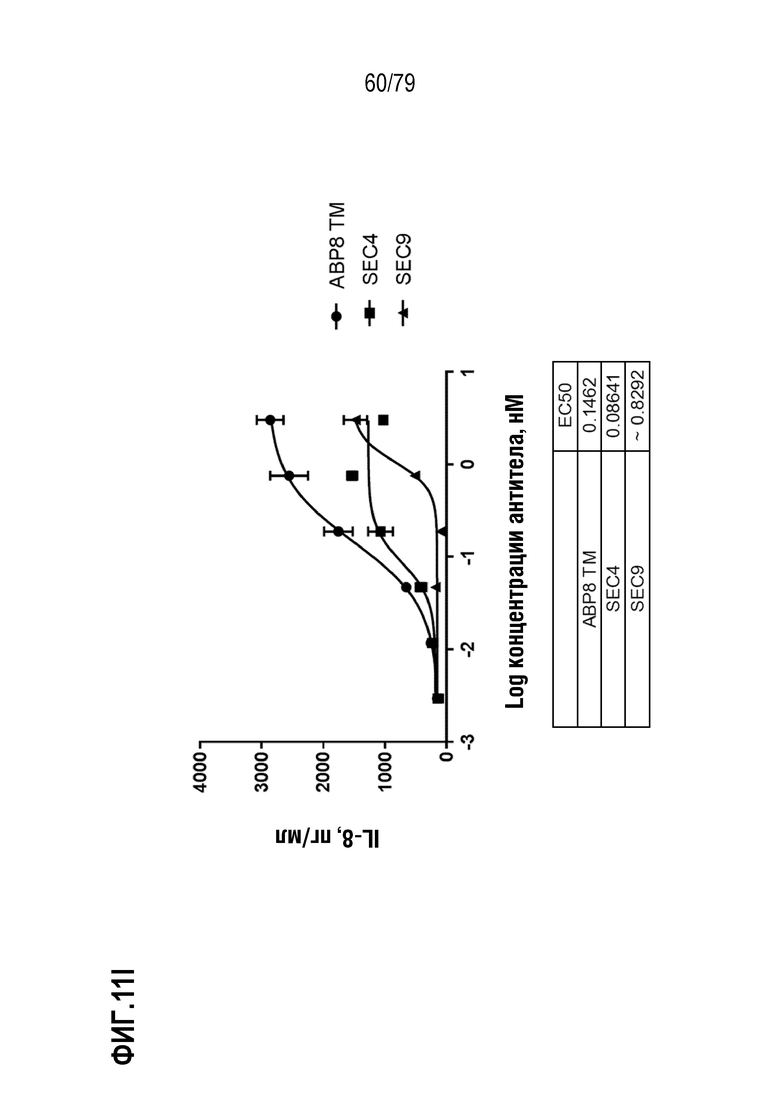
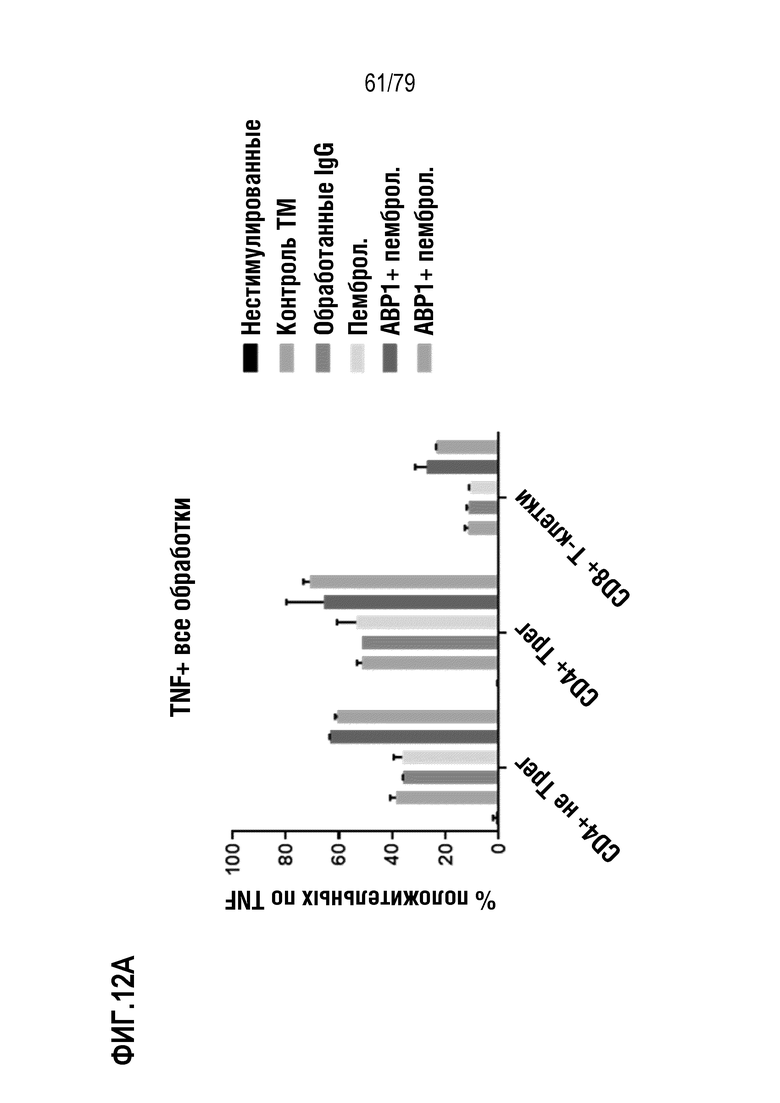
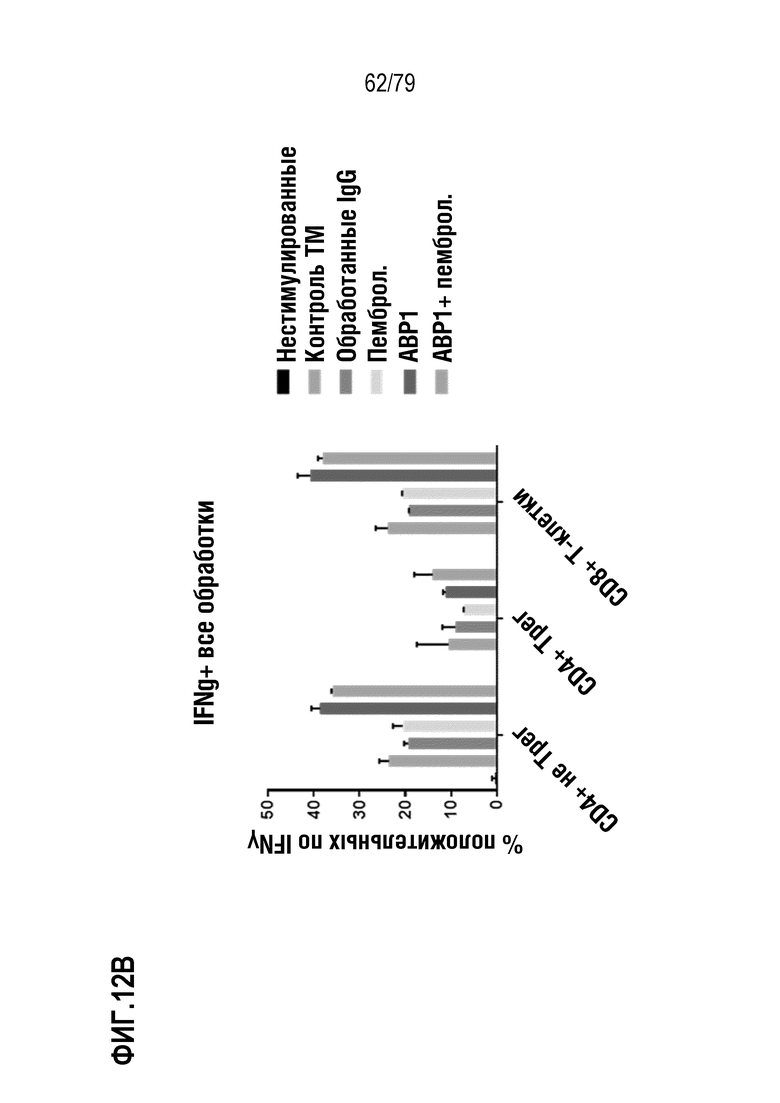
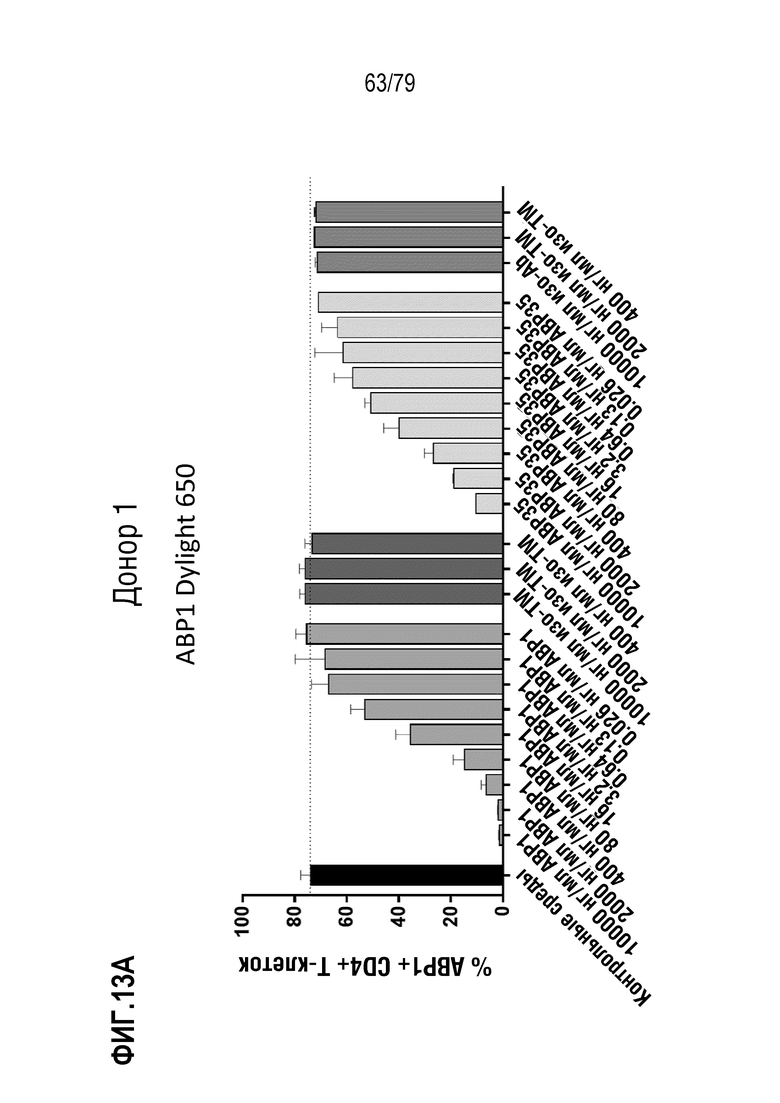
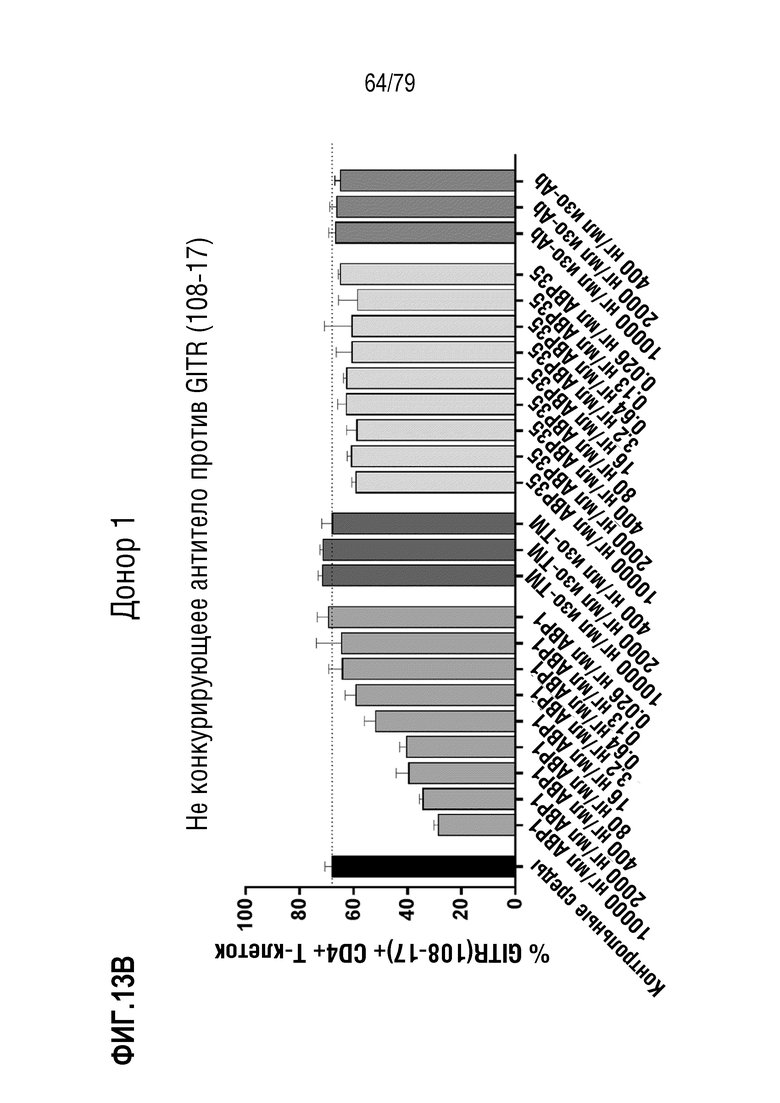
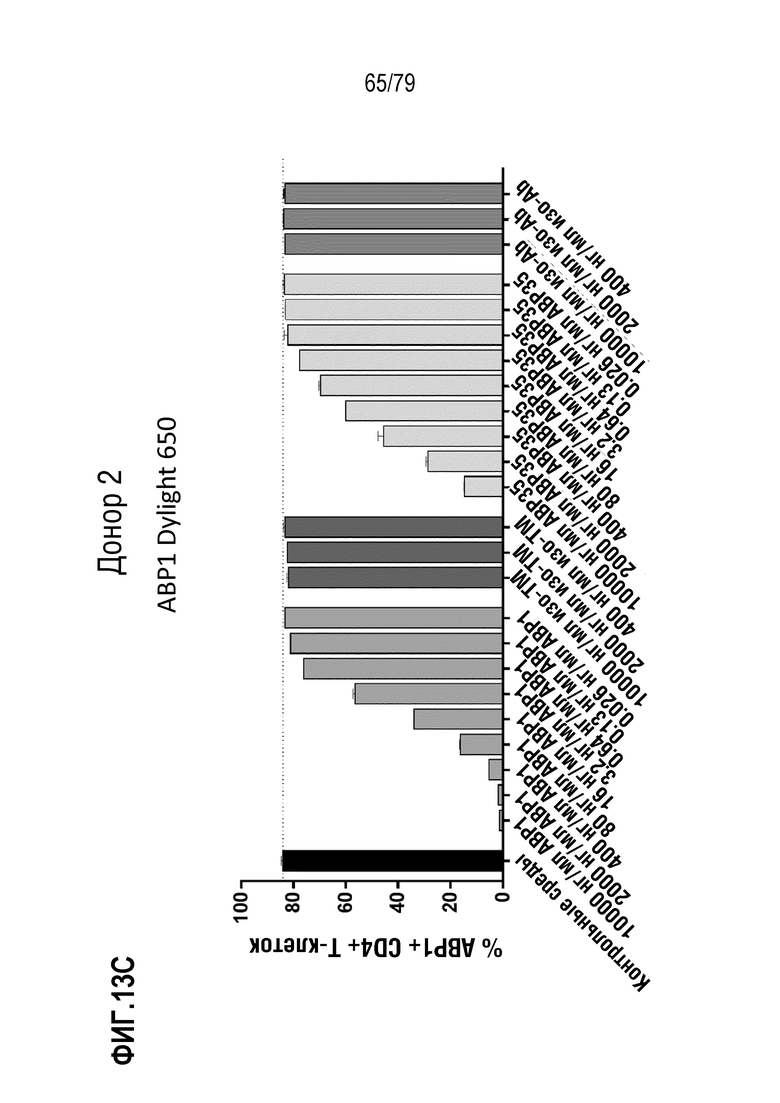

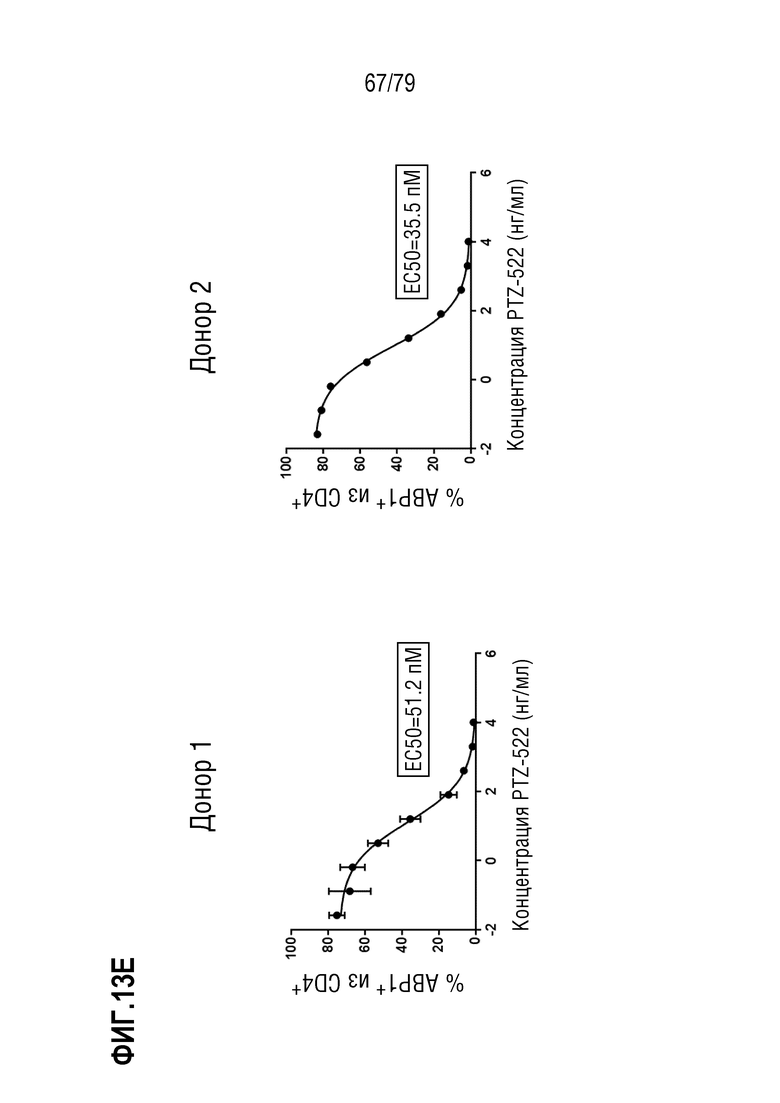
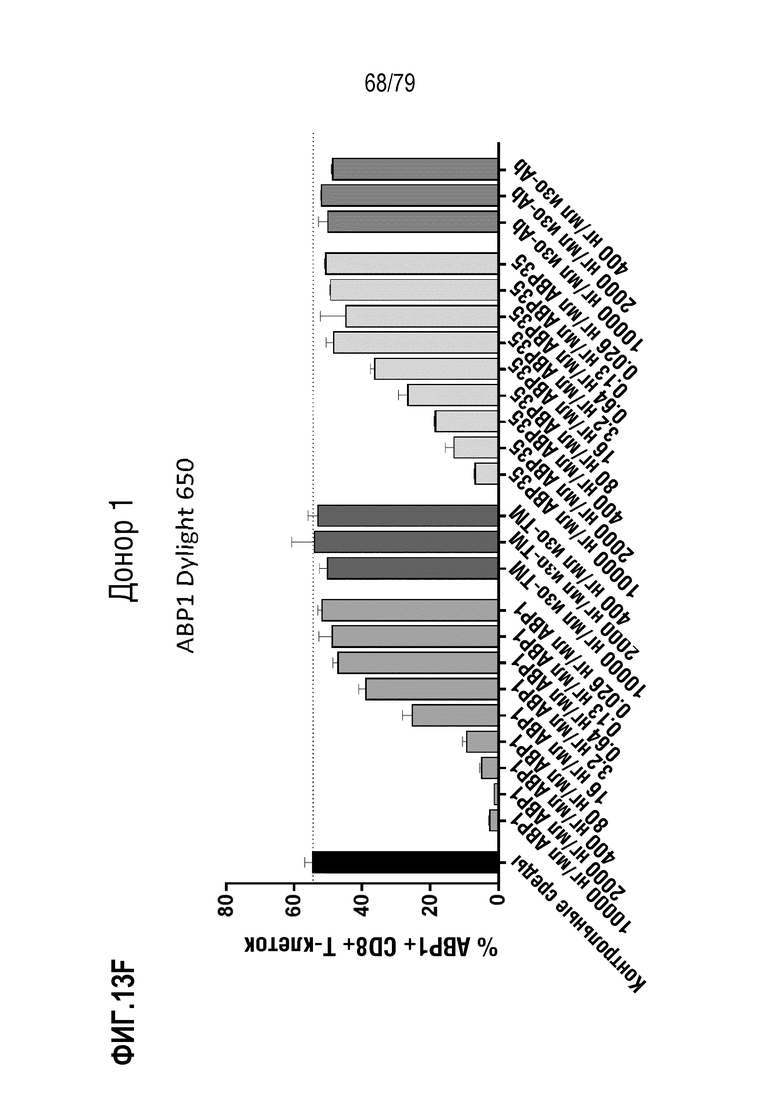
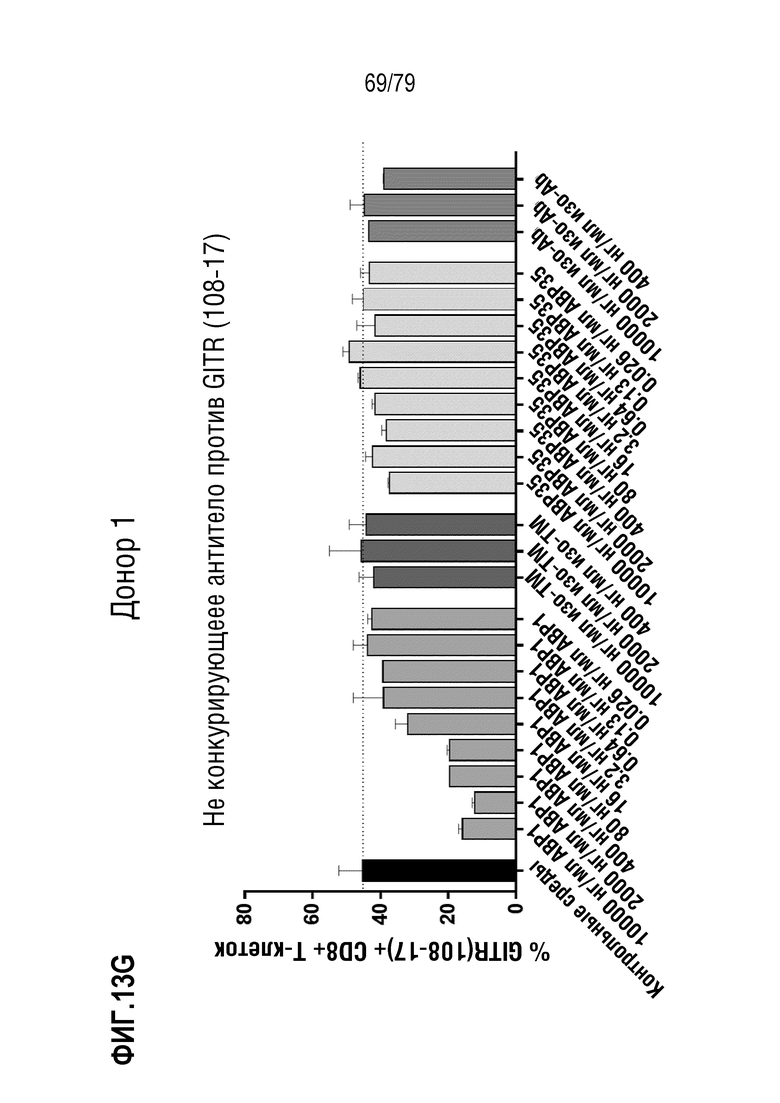
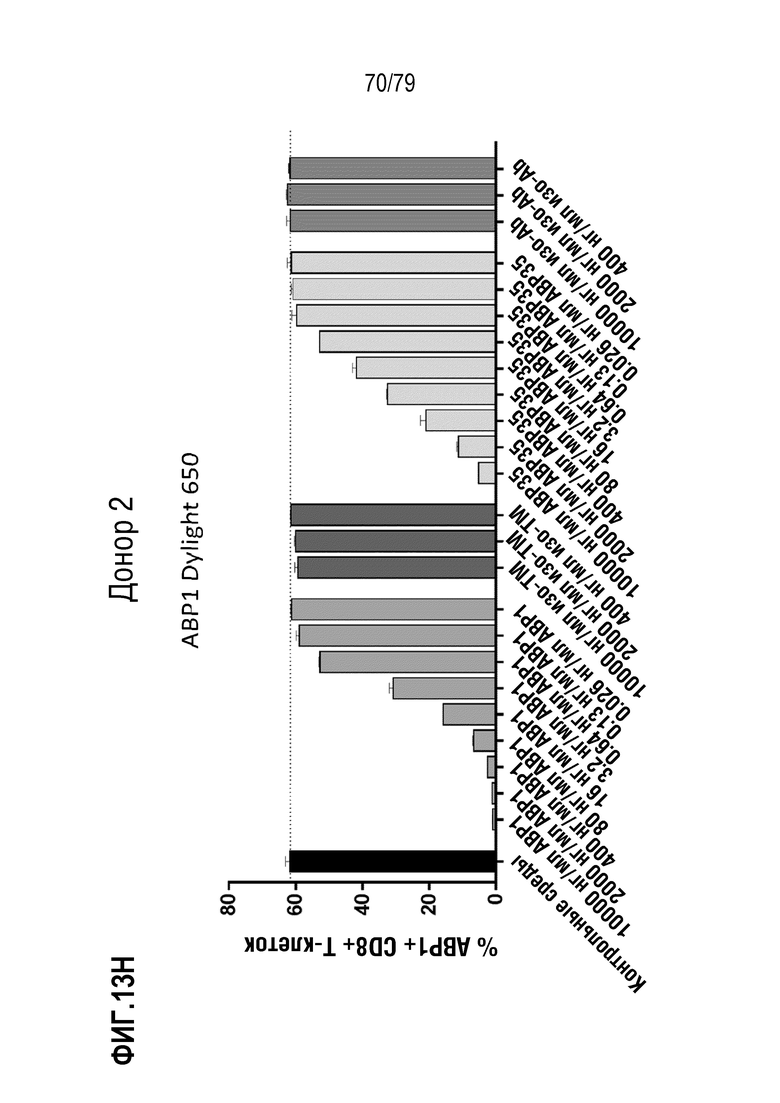
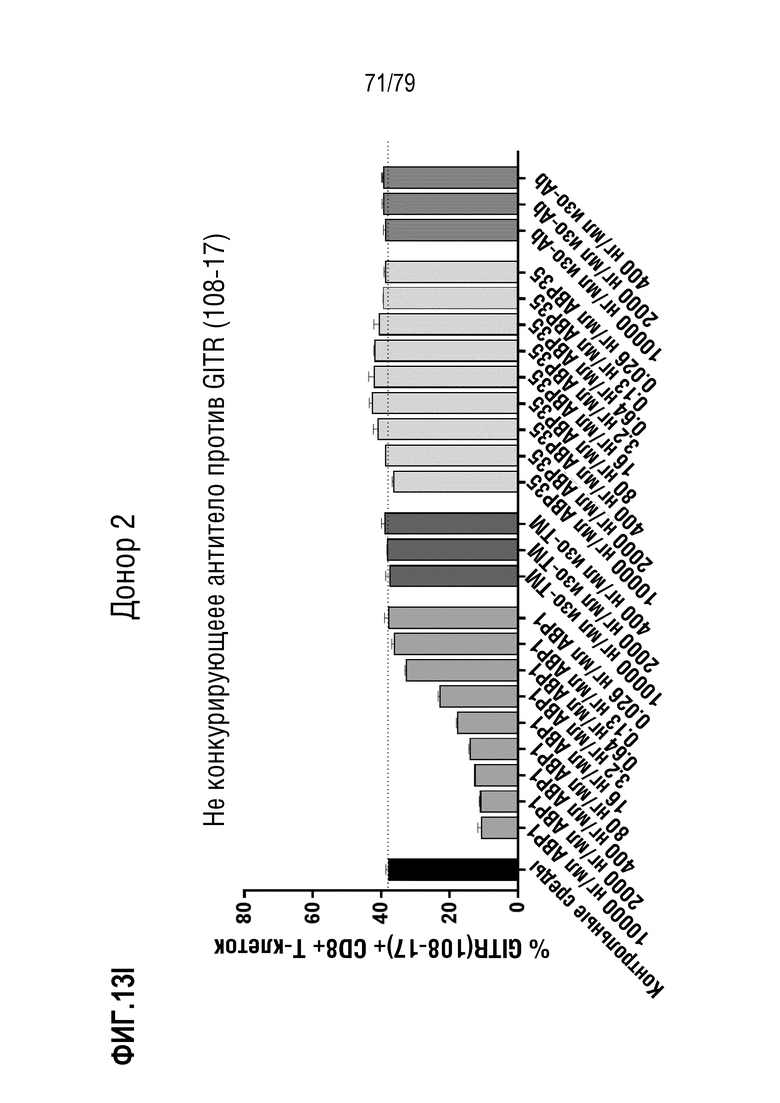
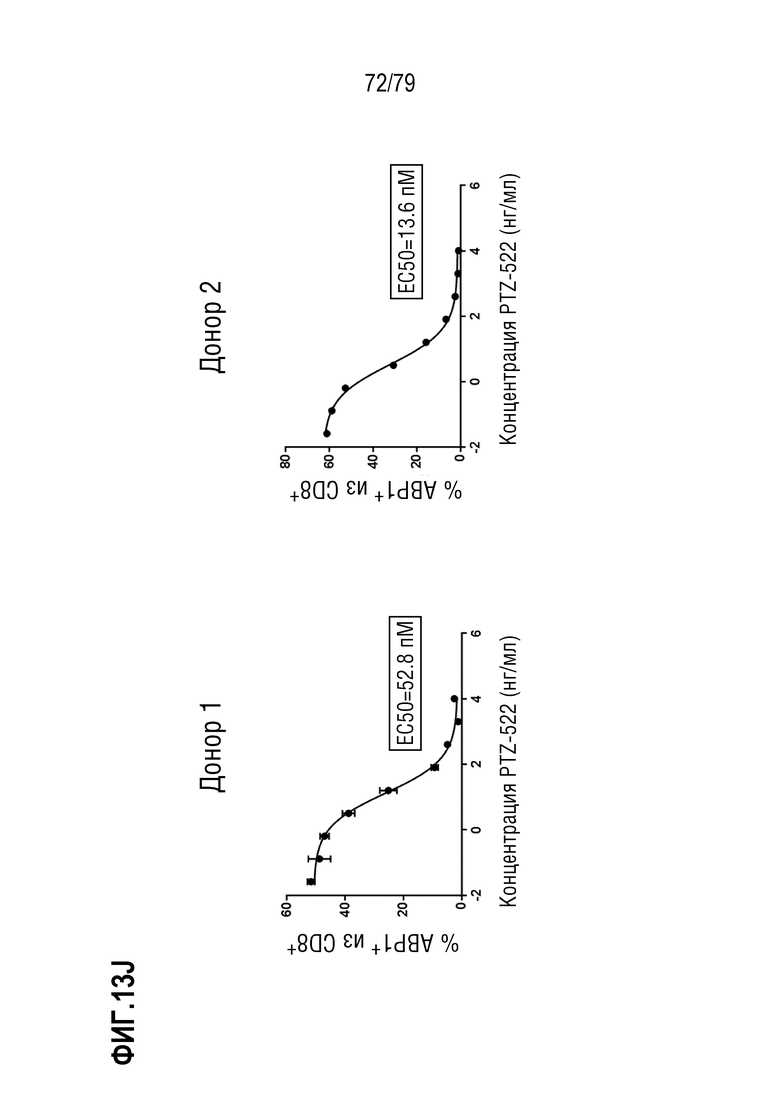
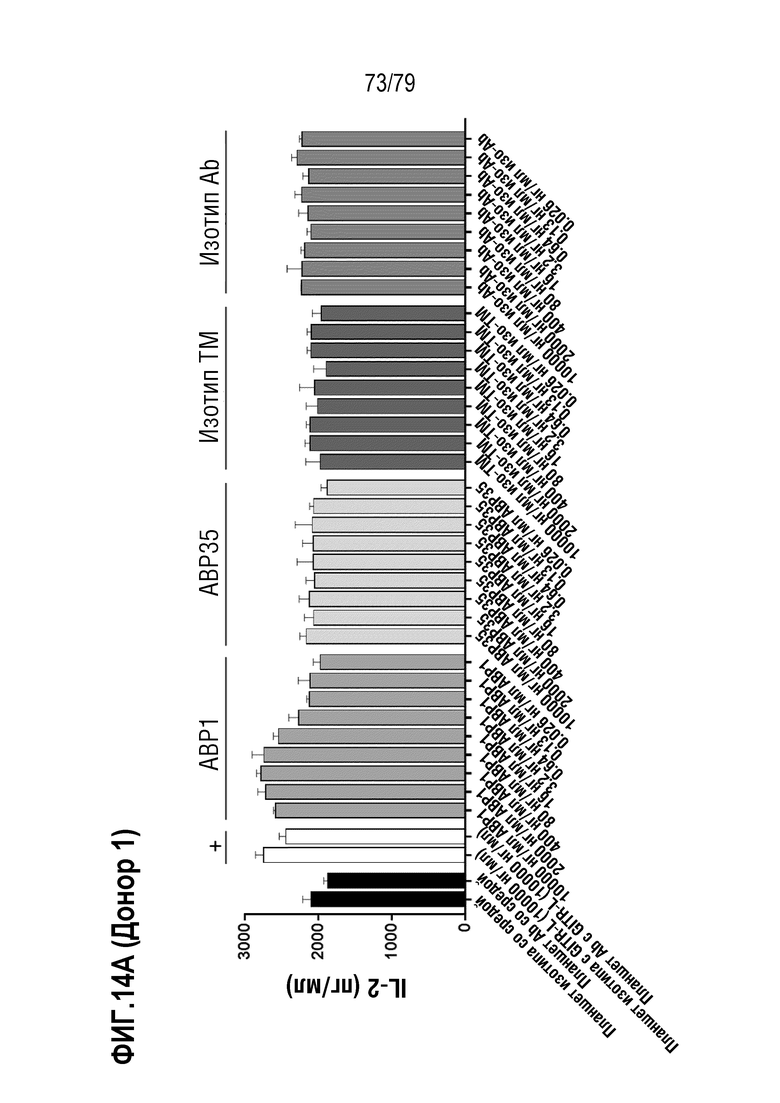
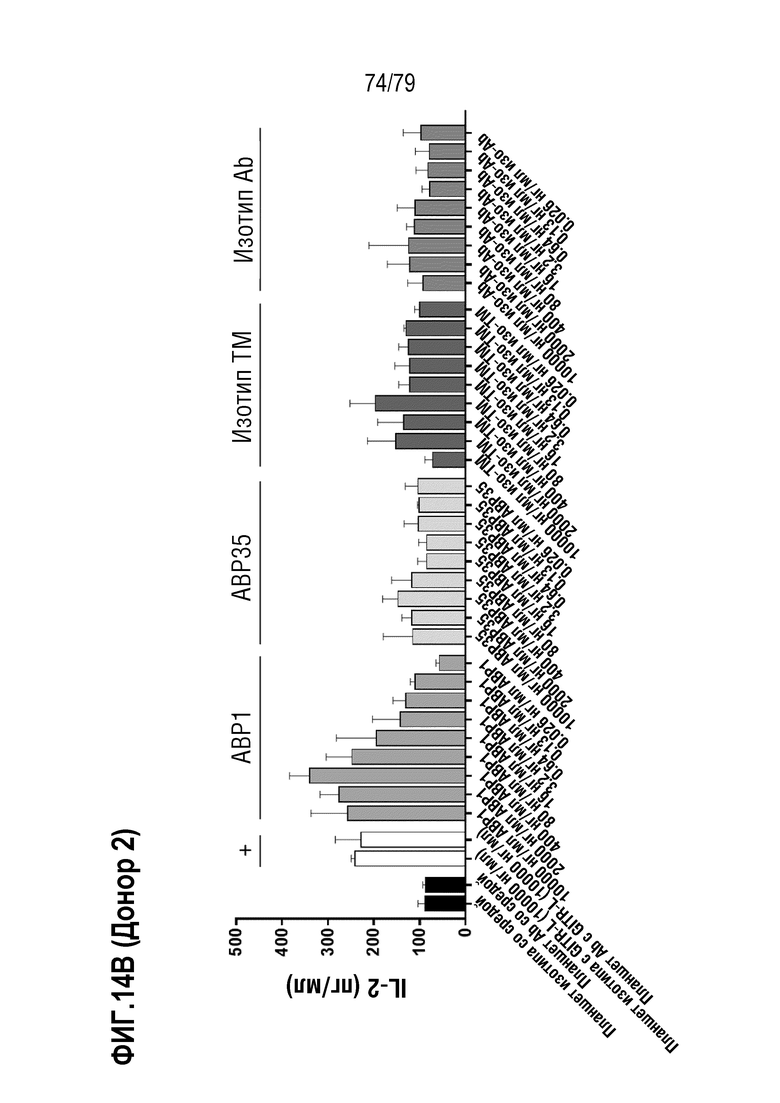
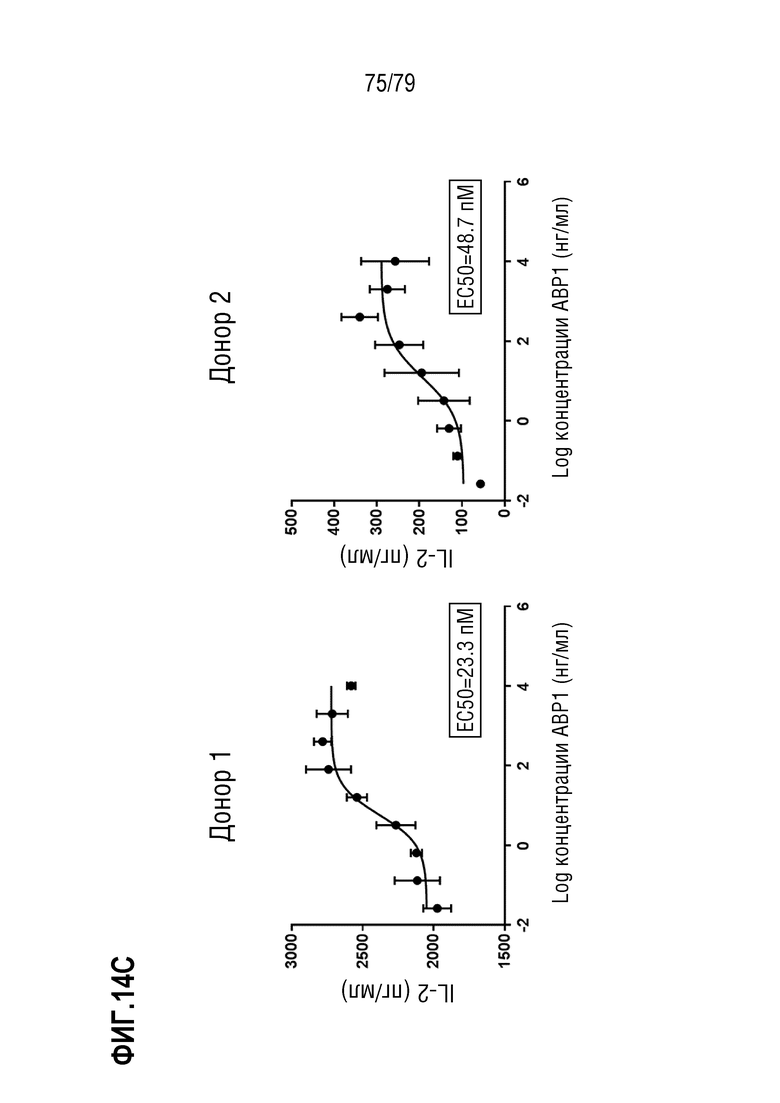
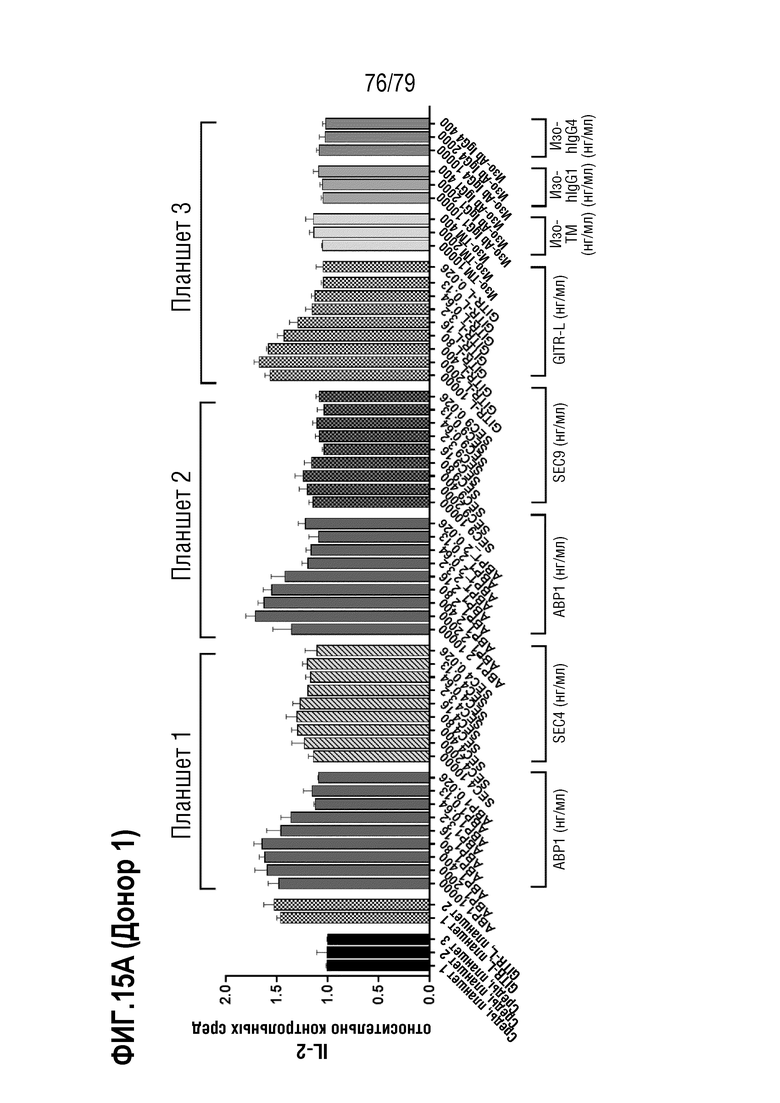
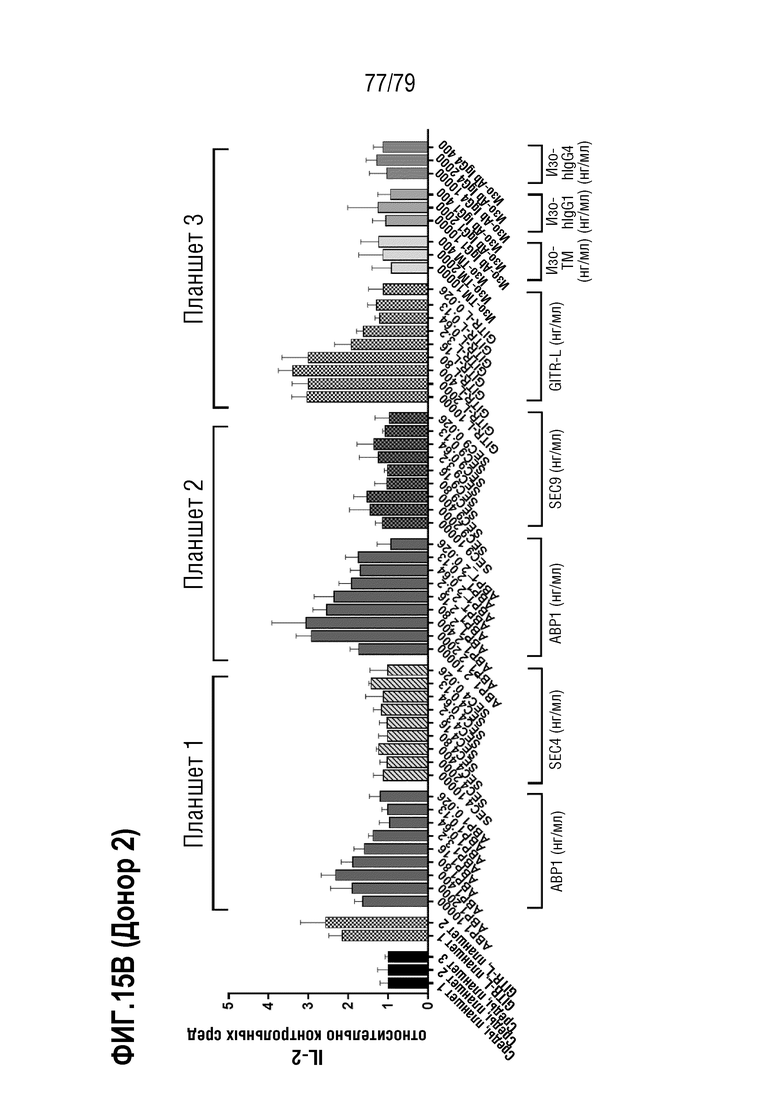
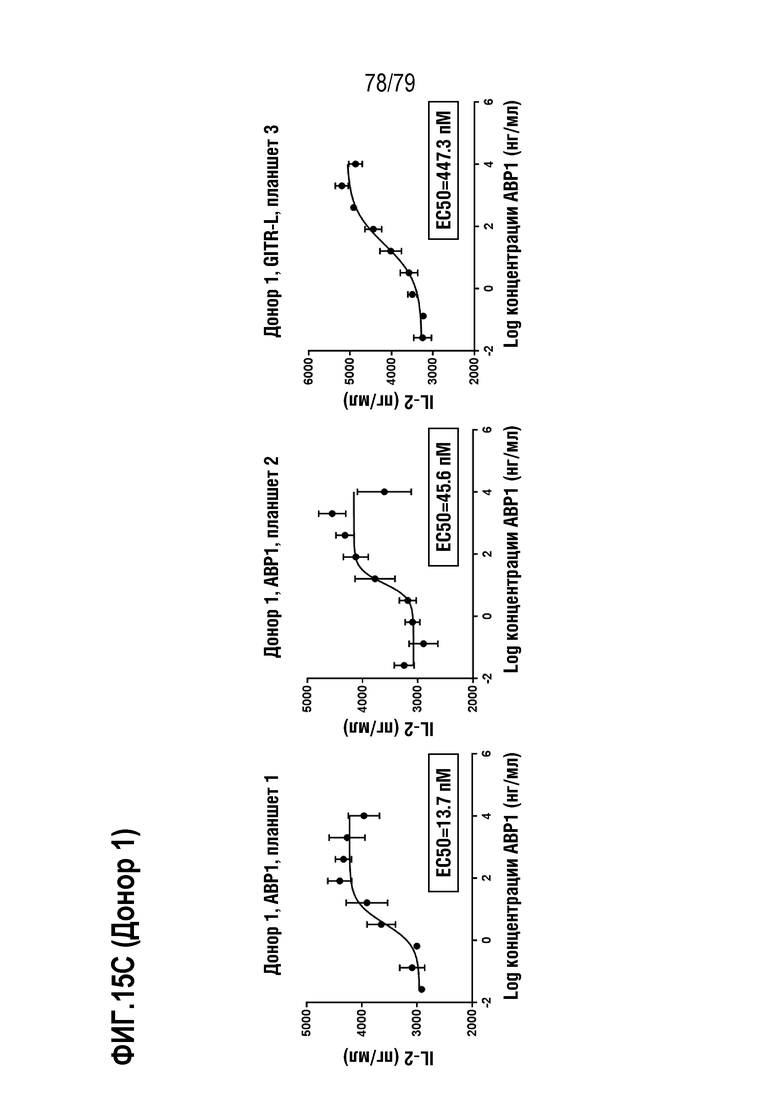
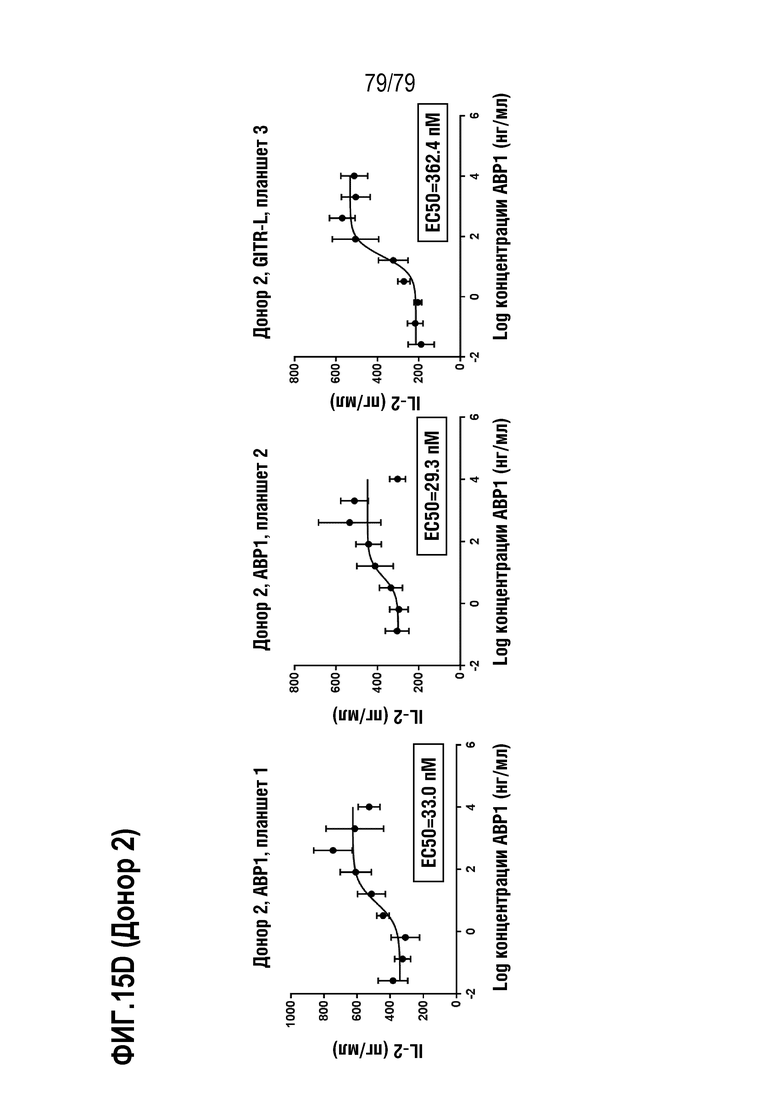
Изобретение относится к области биотехнологии, конкретно к рекомбинантному получению антитела или его антигенсвязывающего фрагмента, связывающего GITR, и может быть использовано в медицине для терапии опухолей. Изобретение позволяет получить антитело или его антигенсвязывающий фрагмент, способный специфически связывать GITR и выступающий в роли агониста GITR человека с улучшенной активностью. 19 н. и 91 з.п. ф-лы, 15 ил., 14 табл., 9 пр.
1. Выделенное антитело или его антигенсвязывающий фрагмент, специфически связывающий GITR человека с SEQ ID NO: 1, где антитело или его антигенсвязывающий фрагмент содержит:
a. CDR-H3 из SEQ ID NO:13, CDR-H2 из SEQ ID NO:12, CDR-H1 из SEQ ID NO:11, CDR-L3 из SEQ ID NO:16, CDR-L2 из SEQ ID NO:15 и CDR-L1 из SEQ ID NO:14;
b. CDR-H3 из SEQ ID NO:23, CDR-H2 из SEQ ID NO:22, CDR-H1 из SEQ ID NO:21, CDR-L3 из SEQ ID NO:17, CDR-L2 из SEQ ID NO:15 и CDR-L1 из SEQ ID NO:14;
c. CDR-H3 из SEQ ID NO:30, CDR-H2 из SEQ ID NO:29, CDR-H1 из SEQ ID NO:28, CDR-L3 из SEQ ID NO:17, CDR-L2 из SEQ ID NO:31 и CDR-L1 из SEQ ID NO:14;
d. CDR-H3 из SEQ ID NO:30, CDR-H2 из SEQ ID NO:29, CDR-H1 из SEQ ID NO:28, CDR-L3 из SEQ ID NO:17, CDR-L2 из SEQ ID NO:15 и CDR-L1 из SEQ ID NO:36;
e. CDR-H3 из SEQ ID NO:30, CDR-H2 из SEQ ID NO:29, CDR-H1 из SEQ ID NO:28, CDR-L3 из SEQ ID NO:17, CDR-L2 из SEQ ID NO:41 и CDR-L1 из SEQ ID NO:14;
f. CDR-H3 из SEQ ID NO:48, CDR-H2 из SEQ ID NO:47, CDR-H1 из SEQ ID NO:46, CDR-L3 из SEQ ID NO:17, CDR-L2 из SEQ ID NO:50 и CDR-L1 из SEQ ID NO:49;
g. CDR-H3 из SEQ ID NO:48, CDR-H2 из SEQ ID NO:47, CDR-H1 из SEQ ID NO:46, CDR-L3 из SEQ ID NO:56, CDR-L2 из SEQ ID NO:55 и CDR-L1 из SEQ ID NO:54;
h. CDR-H3 из SEQ ID NO:61, CDR-H2 из SEQ ID NO:60, CDR-H1 из SEQ ID NO:59, CDR-L3 из SEQ ID NO:16, CDR-L2 из SEQ ID NO:15 и CDR-L1 из SEQ ID NO:14;
i. CDR-H3 из SEQ ID NO:61, CDR-H2 из SEQ ID NO:47, CDR-H1 из SEQ ID NO:46, CDR-L3 из SEQ ID NO:16, CDR-L2 из SEQ ID NO:15 и CDR-L1 из SEQ ID NO:14; или
j. CDR-H3 из SEQ ID NO:103, CDR-H2 из SEQ ID NO:22, CDR-H1 из SEQ ID NO:21, CDR-L3 из SEQ ID NO:16, CDR-L2 из SEQ ID NO:15 и CDR-L1 из SEQ ID NO:14.
2. Антитело или его антигенсвязывающий фрагмент по п. 1, где:
a. антитело или его антигенсвязывающий фрагмент содержит последовательность VH из SEQ ID NO:9 и последовательность VL из SEQ ID NO:10;
b. антитело или его антигенсвязывающий фрагмент содержит последовательность VH из SEQ ID NO:19 и последовательность VL из SEQ ID NO:20;
c. антитело или его антигенсвязывающий фрагмент содержит последовательность VH из SEQ ID NO:26 и последовательность VL из SEQ ID NO:27;
d. антитело или его антигенсвязывающий фрагмент содержит последовательность VH из SEQ ID NO:26 или SEQ ID NO:34 и последовательность VL из SEQ ID NO:35;
e. антитело или его антигенсвязывающий фрагмент содержит последовательность VH из SEQ ID NO:26 и последовательность VL из SEQ ID NO:40;
f. антитело или его антигенсвязывающий фрагмент содержит последовательность VH из SEQ ID NO:44 и последовательность VL из SEQ ID NO:45;
g. антитело или его антигенсвязывающий фрагмент содержит последовательность VH из SEQ ID NO:44 и последовательность VL из SEQ ID NO:53;
h. антитело или его антигенсвязывающий фрагмент содержит последовательность VH из SEQ ID NO:58 и последовательность VL из SEQ ID NO:10;
i. антитело или его антигенсвязывающий фрагмент содержит последовательность VH из SEQ ID NO:104 и последовательность VL из SEQ ID NO:10; или
j. антитело или его антигенсвязывающий фрагмент содержит последовательность VH из SEQ ID NO:105 и последовательность VL из SEQ ID NO:10.
3. Антитело или его антигенсвязывающий фрагмент по п. 2, где:
a. антитело или его антигенсвязывающий фрагмент содержит тяжелую цепь из SEQ ID NO:7 и легкую цепь из SEQ ID NO:8;
b. антитело или его антигенсвязывающий фрагмент содержит тяжелую цепь из SEQ ID NO:17 и легкую цепь из SEQ ID NO:18;
c. антитело или его антигенсвязывающий фрагмент содержит тяжелую цепь из SEQ ID NO:24 и легкую цепь из SEQ ID NO:25;
d. антитело или его антигенсвязывающий фрагмент содержит (i) тяжелую цепь из SEQ ID NO:32 и легкую цепь из SEQ ID NO:33 или (ii) тяжелую цепь из SEQ ID NO:37 и легкую цепь из SEQ ID NO:33;
e. антитело или его антигенсвязывающий фрагмент содержит (i) тяжелую цепь из SEQ ID NO:38 и легкую цепь из SEQ ID NO:39;
f. антитело или его антигенсвязывающий фрагмент содержит (i) тяжелую цепь из SEQ ID NO:42 и легкую цепь из SEQ ID NO:43;
g. антитело или его антигенсвязывающий фрагмент содержит (i) тяжелую цепь из SEQ ID NO:51 и легкую цепь из SEQ ID NO:52;
h. антитело или его антигенсвязывающий фрагмент содержит (i) тяжелую цепь из SEQ ID NO:57 и легкую цепь из SEQ ID NO:8;
i. антитело или его антигенсвязывающий фрагмент содержит (i) тяжелую цепь из SEQ ID NO:114 и легкую цепь из SEQ ID NO:8, или (ii) тяжелую цепь из SEQ ID NO:120 и легкую цепь из SEQ ID NO:8; или (iii) тяжелую цепь из SEQ ID NO:122 и легкую цепь из SEQ ID NO:8; или
j. антитело или его антигенсвязывающий фрагмент содержит (i) тяжелую цепь из SEQ ID NO:115 и легкую цепь из SEQ ID NO:8, или (ii) тяжелую цепь из SEQ ID NO:121 и легкую цепь из SEQ ID NO:8; или (iii) тяжелую цепь из SEQ ID NO:123 и легкую цепь из SEQ ID NO:8.
4. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где аминокислотные замены представляют собой консервативные аминокислотные замены.
5. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где антитело или его антигенсвязывающий фрагмент:
a. имеет по меньшей мере три антигенсвязывающих домена, специфически связывающие эпитоп на GITR;
b. имеет по меньшей мере три антигенсвязывающих домена, специфически связывающие один эпитоп на GITR;
c. имеет по меньшей мере четыре антигенсвязывающих домена, специфически связывающие эпитоп на GITR;
d. имеет по меньшей мере четыре антигенсвязывающих домена, специфически связывающие один эпитоп на GITR;
e. выступает в роли агониста GITR, экспрессированного на поверхности клетки-мишени;
f. блокирует связывание GITRL с GITR;
g. костимулирет эффекторную T-клетку в комбинации с представлением антигена от антигенпредставляющей клетки;
h. ингибирует супрессию эффекторной T-клетки посредством регуляторной T-клетки;
i. уменьшает количество регуляторных T-клеток в ткани или в системном кровотоке;
j. является способным связываться с одним или несколькими из остатков GITR с SEQ ID NO:1, выбранных из группы, состоящей из R56, C58, R59, D60, Y61, P62, E64, E65, C66 и C67; или
k. является способным к любой комбинации из (a) - (j).
6. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где GITR выбран из hGITR с SEQ ID NO: 1, hGITR-T43R с SEQ ID NO: 2, cGITR с SEQ ID NO: 3, mGITR с SEQ ID NO: 4 и их комбинаций.
7. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где антитело представляет собой моноклональное антитело.
8. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где антитело выбрано из человеческого антитела, гуманизированного антитела или химерного антитела.
9. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где антитело или его антигенсвязывающий фрагмент является трехвалентным, тетравалентным, пентавалентным, гексавалентным, септивалентным или октавалентным.
10. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где антитело или его антигенсвязывающий фрагмент содержит фрагмент антитела.
11. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где антитело или его антигенсвязывающий фрагмент содержит альтернативный каркас.
12. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где антитело или его антигенсвязывающий фрагмент содержит константную область иммуноглобулина.
13. Антитело или его антигенсвязывающий фрагмент по п. 12, где антитело или его антигенсвязывающий фрагмент содержит константную область тяжелой цепи из класса, выбранного из IgA, IgD, IgE, IgG или IgM.
14. Антитело или его антигенсвязывающий фрагмент по п. 13, где антитело или его антигенсвязывающий фрагмент содержит константную область тяжелой цепи из класса IgG и подкласса, выбранного из IgG4, IgG1, IgG2 или IgG3.
15. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где по меньшей мере один Fab является слитым с C-концом домена Fc IgG.
16. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, дополнительно содержащий по меньшей мере один линкер.
17. Антитело или его антигенсвязывающий фрагмент по п. 14, где IgG представляет собой IgG4.
18. Антитело или его антигенсвязывающий фрагмент по п. 14, где IgG представляет собой IgG1.
19. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где по меньшей мере один Fab является слитым с N-концом домена Fc IgG.
20. Антитело или его антигенсвязывающий фрагмент по п. 19, где по меньшей мере один Fab представляет собой по меньшей мере два Fab.
21. Антитело или его антигенсвязывающий фрагмент по п. 19, где по меньшей мере один Fab представляет собой по меньшей мере три Fab.
22. Антитело или его антигенсвязывающий фрагмент по п. 19, где по меньшей мере один Fab представляет собой по меньшей мере четыре Fab.
23. Антитело или его антигенсвязывающий фрагмент по любому из пп. 20-22, где два Fab являются независимо слитыми с N-концом IgG.
24. Антитело или его антигенсвязывающий фрагмент по любому из пп. 20-22, где два Fab являются независимо слитыми с C-концом IgG.
25. Антитело или его антигенсвязывающий фрагмент по п. 23, где Fab присоединен к каждому N-концу IgG, линкер присоединен к каждому указанному Fab и Fab присоединен к каждому линкеру.
26. Антитело или его антигенсвязывающий фрагмент по п. 24, где Fab присоединен к каждому C-концу IgG, линкер присоединен к каждому указанному Fab и Fab присоединен к каждому линкеру.
27. Антитело или его антигенсвязывающий фрагмент по п. 25 или 26, где каждый линкер содержит SEQ ID NO:5.
28. Антитело или его антигенсвязывающий фрагмент по п. 25 или 26, где каждый линкер содержит SEQ ID NO:6.
29. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где антитело или его антигенсвязывающий фрагмент содержит антитело с общей легкой цепью, антитело с модификацией выступы-во-впадины, scFv, присоединенный к IgG, Fab, присоединенный к IgG, диатело, тетравалентное биспецифическое антитело, CovX-Body, антитело Fcab, тандемный Fab или их комбинацию.
30. Антитело или его антигенсвязывающий фрагмент по п. 9, где антитело или его антигенсвязывающий фрагмент связывает более одной молекулы GITR.
31. Антитело или его антигенсвязывающий фрагмент по п. 5, где антитело или его антигенсвязывающий фрагмент выступает в роли агониста GITR, экспрессированного на поверхности клетки-мишени, и агонизм GITR посредством антитела или его антигенсвязывающего фрагмента является независимым от связывания GITRL.
32. Антитело или его антигенсвязывающий фрагмент по п. 5, где антитело или его антигенсвязывающий фрагмент выступает в роли агониста GITR, экспрессированного на поверхности клетки-мишени, и антитело или его антигенсвязывающий фрагмент усиливает связывание GITRL с GITR по меньшей мере приблизительно на 10%, по меньшей мере приблизительно на 20%, по меньшей мере приблизительно на 30%, по меньшей мере приблизительно на 40%, по меньшей мере приблизительно на 50%, по меньшей мере приблизительно на 60%, по меньшей мере приблизительно на 70%, по меньшей мере приблизительно на 80% или по меньшей мере приблизительно на 90%.
33. Антитело или его антигенсвязывающий фрагмент по п. 32, где антитело или его антигенсвязывающий фрагмент усиливает связывание GITRL с GITR по меньшей мере приблизительно на 50%.
34. Антитело или его антигенсвязывающий фрагмент по п. 5, где клетка-мишень выбрана из эффекторной T-клетки, регуляторной T-клетки, клетки естественного киллера (NK), T-клетки естественного киллера (NKT), дендритной клетки и B-клетки.
35. Антитело или его антигенсвязывающий фрагмент по п. 5, где клетка-мишень представляет собой эффекторную T-клетку, выбранную из T-клетки-помощника (CD4+), цитотоксической T-клетки (CD8+) и их комбинаций.
36. Антитело или его антигенсвязывающий фрагмент по п. 5, где клетка-мишень представляет собой регуляторную T-клетку, выбранную из CD4+CD25+Foxp3+ регуляторной T-клетки, CD8+CD25+ регуляторной T-клетки и их комбинаций.
37. Антитело или его антигенсвязывающий фрагмент по п. 5, где ткань представляет собой опухоль.
38. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где KD первого антигенсвязывающего домена для hGITR с SEQ ID NO: 1 или hGITR-T43R с SEQ ID NO: 2 составляет менее чем приблизительно 20 нМ.
39. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где KD первого антигенсвязывающего домена для cGITR с SEQ ID NO: 3 составляет менее чем приблизительно 200 нМ.
40. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где KD второго антигенсвязывающего домена для hGITR с SEQ ID NO: 1 или hGITR-T43R с SEQ ID NO: 2 составляет менее чем приблизительно 100 нМ.
41. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где KD второго антигенсвязывающего домена для cGITR с SEQ ID NO: 3 составляет менее чем приблизительно 1 мкМ.
42. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где антитело или его антигенсвязывающий фрагмент содержит домен Fc с уменьшенной эффекторной функцией по сравнению с доменом Fc IgG1.
43. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где антитело или его антигенсвязывающий фрагмент содержит агликозилированный домен Fc.
44. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где антитело или его антигенсвязывающий фрагмент содержит домен Fc IgG1 с аланином в одном или нескольких из положений 234, 235, 265 и 297.
45. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где GITR экспрессируется на поверхности клетк
и-мишени.
46. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где антитело или его антигенсвязывающий фрагмент вызывает мультимеризацию GITR, экспрессированного на поверхности клетки-мишени.
47. Антитело или его антигенсвязывающий фрагмент по п. 46, где антитело или его антигенсвязывающий фрагмент вызывает мультимеризацию 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 молекул GITR.
48. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где антитело или его антигенсвязывающий фрагмент содержит иммуноглобулин, содержащий по меньшей мере две различные вариабельные области тяжелой цепи, где каждая спарена с вариабельной областью общей легкой цепи.
49. Антитело или его антигенсвязывающий фрагмент по п. 48, где вариабельная область общей легкой цепи формирует отдельный антигенсвязывающий домен с каждой из двух различных вариабельных областей тяжелой цепи.
50. Антитело или его антигенсвязывающий фрагмент по п. 48, где антитело или его антигенсвязывающий фрагмент содержит первый вариабельный домен VH, имеющий SEQ ID NO:189, второй вариабельный домен VH, имеющий SEQ ID NO:215, и общую вариабельную легкую цепь, имеющую SEQ ID NO:190.
51. Антитело или его антигенсвязывающий фрагмент по п. 48, где антитело или его антигенсвязывающий фрагмент содержит первый вариабельный домен VH, имеющий SEQ ID NO:199, второй вариабельный домен VH, имеющий SEQ ID NO:216, и общую вариабельную легкую цепь, имеющую SEQ ID NO:200.
52. Набор для специфического связывания с GITR человека (hGITR) с SEQ ID NO:1, содержащий антитело или его антигенсвязывающий фрагмент по любому из пп. 1-51 и инструкции для применения антитела или его антигенсвязывающего фрагмента.
53. Набор по п. 52, где антитело или его антигенсвязывающий фрагмент является лиофилизированным.
54. Набор по п. 53, дополнительно содержащий жидкость для разведения лиофилизированного антитела или его антигенсвязывающего фрагмента.
55. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где антитело или его антигенсвязывающий фрагмент содержит полипептидную последовательность, имеющую остаток пироглутамата (pE) на N-конце.
56. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где антитело или его антигенсвязывающий фрагмент содержит последовательность VH, в которой N-концевой Q заменен на pE.
57. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где антитело или его антигенсвязывающий фрагмент содержит последовательность VL, в которой N-концевой E заменен на pE.
58. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где антитело или его антигенсвязывающий фрагмент содержит последовательность тяжелой цепи, в которой N-концевой Q заменен на pE.
59. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, где антитело или его антигенсвязывающий фрагмент содержит последовательность легкой цепи, в которой N-концевой E заменен на pE.
60. Применение антитела или его антигенсвязывающего фрагмента по любому из пп. 1-51 в лечении злокачественной опухоли.
61. Применение по п. 60, где злокачественная опухоль выбрана из солидной опухоли и гематологической опухоли.
62. Выделенный полинуклеотид, кодирующий антитело или его антигенсвязывающий фрагмент, специфически связывающий GITR человека (hGITR) с SEQ ID NO: 1, где полинуклеотид кодирует антитело или антигенсвязывающий фрагмент по любому из пп. 1-51.
63. Вектор для размножения полинуклеотида, кодирующего антитело или его антигенсвязывающий фрагмент, специфически связывающий GITR человека (hGITR) с SEQ ID NO: 1, где вектор содержит полинуклеотид по п. 62.
64. Клетка-хозяин для размножения полинуклеотида, кодирующего антитело или его антигенсвязывающий фрагмент, специфически связывающий GITR человека (hGITR) с SEQ ID NO: 1, где клетка-хозяин содержит полинуклеотид по п. 62 или вектор по п. 63 и где клетка-хозяин выбрана из группы, состоящей из бактериальной клетки, грибковой клетки, клетки COS-7, клетки почки детеныша хомячка (BHK); клетки яичника китайского хомячка (СНО); клетки Сертоли мышей и клетки почек африканской зеленой мартышки.
65. Клетка-хозяин по п. 64, выбранная из клетки бактерии, клетки гриба и клетки млекопитающего.
66. Клетка-хозяин по п. 64, выбранная из клетки E. coli, клетки Saccharomyces cerevisiae и клетки CHO.
67. Способ получения антитела или его антигенсвязывающего фрагмента по любому из пп. 1-51, включающий экспрессию антитела или его антигенсвязывающего фрагмента в клетке-хозяине по п. 65 и выделение экспрессированного антитела или его антигенсвязывающего фрагмента.
68. Фармацевтическая композиция для использования в лечении злокачественной опухоли, содержащая терапевтически эффективное количество антитела или его антигенсвязывающего фрагмента по любому из пп. 1-51 и фармацевтически приемлемый наполнитель.
69. Фармацевтическая композиция по п. 68, где количество антитела или его антигенсвязывающего фрагмента в фармацевтической композиции является достаточным для (a) уменьшения супрессии эффекторных T-клеток регуляторными T-клетками; (b) активации эффекторных T-клеток; (c) уменьшения количества регуляторных T-клеток в ткани или системно; (d) индукции или усиления пролиферации эффекторных T-клеток; (e) замедления скорости роста опухоли; (f) индукции регрессии опухоли или (g) их комбинации у субъекта.
70. Фармацевтическая композиция по п. 68 или 69, где злокачественная опухоль выбрана из солидной опухоли и гематологической опухоли.
71. Способ лечения или предотвращения злокачественной опухоли у нуждающегося в этом субъекта, включающий введение субъекту эффективного количества антитела или его антигенсвязывающего фрагмента по любому из пп. 1-51 или фармацевтической композиции по п. 68 или 69.
72. Способ активации иммуноцитов, экспрессирующих GITR, у субъекта, включающий введение субъекту эффективного количества антитела или его антигенсвязывающего фрагмента по любому из пп. 1-51 или фармацевтической композиции по п. 68 или 69.
73. Способ по п. 71 или 72, индуцирующий или усиливающий иммунный ответ на ассоциированный с злокачественной опухолью антиген.
74. Способ по любому из пп. 71-73, где антитело или его антигенсвязывающий фрагмент вводят в количестве, достаточном для (a) уменьшения супрессии эффекторных T-клеток регуляторными T-клетками; (b) активации эффекторных T-клеток; (c) индукции или усиления пролиферации эффекторных T-клеток; (d) замедления скорости роста опухоли; (e) индукции регрессии опухоли или (f) их комбинации.
75. Способ по п. 73 или 74, где злокачественная опухоль представляет собой солидную опухоль.
76. Способ по п. 73 или 74, где злокачественная опухоль представляет собой гематологическую опухоль.
77. Способ по любому из пп. 71-76, дополнительно включающий введение одного или нескольких дополнительных лекарственных средств.
78. Способ по п. 77, где дополнительное лекарственное средство выбрано из цитотоксического средства, химиотерапевтического средства, цитостатического средства, противогормонального средства, ингибитора EGFR, иммуностимулирующего средства, антиангиогенного средства и их комбинаций.
79. Способ по п. 77, где дополнительное лекарственное средство представляет собой иммуностимулирующее средство.
80. Способ по п. 79, где иммуностимулирующее средство содержит средство, блокирующее передачу сигналов ингибирующим рецептором, экспрессированным иммуноцитом, или его лигандом.
81. Способ по п. 80, где ингибирующий рецептор, экспрессированный иммуноцитом, или его лиганд выбран из CTLA-4, PD-1, PD-L1, NRP-1, LAG-3, Tim3, TIGIT, невритина, BTLA, KIR и их комбинаций.
82. Способ по п. 79, где иммуностимулирующее средство содержит агонист стимулирующего рецептора, экспрессированного иммуноцитом.
83. Способ по п. 81, где стимулирующий рецептор, экспрессированный иммуноцитом, выбран из OX40, CD2, CD27, CDS, ICAM-1, LFA-1 (CD11a/CD18), ICOS (CD278), 4-1BB (CD137), CD28, CD30, CD40, BAFFR, HVEM, CD7, LIGHT, NKG2C, SLAMF7, NKp80, CD160, B7-H3, лиганда CD83 и их комбинаций.
84. Способ по п. 79, где иммуностимулирующее средство содержит цитокин.
85. Способ по п. 84, где цитокин выбран из IL-2, IL-5, IL-7, IL-12, IL-15, IL-21 и их комбинаций.
86. Способ по п. 79, где иммуностимулирующее средство содержит онколитический вирус.
87. Способ по п. 86, где онколитический вирус выбран из вируса простого герпеса, вируса везикулярного стоматита, аденовируса, вируса болезни Ньюкасла, вируса осповакцины, вируса Мараба и их комбинаций.
88. Способ по п. 79, где иммуностимулирующее средство содержит T-клетку, экспрессирующую химерный рецептор антигена.
89. Способ по п. 79, где иммуностимулирующее средство содержит би- или мультиспецифическое нацеленное на T-клетку антитело.
90. Способ по п. 79, где иммуностимулирующее средство содержит антитело против TGF-β, ловушку TGF-β или их комбинацию.
91. Способ по п. 79, где иммуностимулирующее средство содержит вакцину против ассоциированного с злокачественной опухолью антигена.
92. Способ усиления иммунного ответа у нуждающегося в этом субъекта, включающий введение субъекту эффективного количества антитела или его антигенсвязывающего фрагмента по любому из пп. 1-51 или фармацевтической композиции по любому из пп. 86-70, где иммунный ответ вызван против антигена опухоли.
93. Способ по любому из пп. 77-91, где дополнительное лекарственное средство составлено в той же самой фармацевтической композиции, что и антитело или его антигенсвязывающий фрагмент.
94. Способ по любому из пп. 77-91, где дополнительное лекарственное средство составлено в фармацевтической композиции, отличной от антитела или его антигенсвязывающего фрагмента.
95. Способ по любому из пп. 77-91 или 94, где дополнительное лекарственное средство вводят до введения антитела или его антигенсвязывающего фрагмента.
96. Способ по любому из пп. 77-91 или 94, где дополнительное лекарственное средство вводят после введения антитела или его антигенсвязывающего фрагмента.
97. Способ по любому из пп. 77-91 и 93-96, где дополнительное лекарственное средство вводят одновременно с антителом или его антигенсвязывающим фрагментом.
98. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-51, специфически связывающий эпитоп GITR человека (hGITR) с SEQ ID NO:1 и являющийся способным связывать один или несколько остатков из группы, состоящей из R56, C58, R59, D60, Y61, P62, E64, E65, C66 и C67.
99. Антитело против GITR человека или его антигенсвязывающий фрагмент, содержащие четыре вариабельные области тяжелой цепи и четыре вариабельные области легкой цепи,
где вариабельные области тяжелой цепи содержат CDR-H3, состоящую из SEQ ID NO:13, CDR-H2, состоящую из SEQ ID NO:12, и CDR-H1, состоящую из SEQ ID NO:11;
и вариабельные области легкой цепи содержат CDR-L3, состоящую из SEQ ID NO:16, CDR-L2, состоящую из SEQ ID NO:15, и CDR-L1, состоящую из SEQ ID NO:14; и
где одна вариабельная область тяжелой цепи и одна вариабельная область легкой цепи составляют один антигенсвязывающий участок и где антитело против GITR человека или антигенсвязывающий фрагмент содержит всего четыре антигенсвязывающих участка.
100. Антитело против GITR человека или его антигенсвязывающий фрагмент по п. 99, выбранные из (1) или (2):
(1) антитела против GITR человека или его антигенсвязывающего фрагмента, содержащего четыре вариабельные области тяжелой цепи и четыре вариабельные области легкой цепи, в котором вариабельная область тяжелой цепи состоит из SEQ ID NO: 9,
вариабельная область легкой цепи состоит из SEQ ID NO: 10, и
одна вариабельная область тяжелой цепи и одна вариабельная область легкой цепи составляют один антигенсвязывающий участок и антитело или антигенсвязывающий фрагмент содержит четыре антигенсвязывающих участка; и
(2) антитела против GITR человека или его антигенсвязывающего фрагмента, содержащего четыре вариабельные области тяжелой цепи и четыре вариабельные области легкой цепи, в котором каждая вариабельная область тяжелой цепи состоит из SEQ ID NO: 9, где Q в положении 1 последовательности модифицирован до пироглутамата,
вариабельная область легкой цепи состоит из SEQ ID NO: 10, и
одна вариабельная область тяжелой цепи и одна вариабельная область легкой цепи составляют один антигенсвязывающий участок и антитело или антигенсвязывающий фрагмент содержит четыре антигенсвязывающих участка.
101. Антитело против GITR человека по п. 99, содержащее две тяжелые цепи и четыре легкие цепи; где каждая тяжелая цепь содержит первую вариабельную область тяжелой цепи и вторую вариабельную область тяжелой цепи, где каждая содержит CDR-H3, состоящую из SEQ ID NO:13, CDR-H2, состоящую из SEQ ID NO:12, и CDR-H1, состоящую из SEQ ID NO:11; первую область CH1, линкер, вторую область CH1, область CH2, область CH3; и каждая легкая цепь содержит вариабельную область легкой цепи, содержащую CDR-L3, состоящую из SEQ ID NO:16, CDR-L2, состоящую из SEQ ID NO:15, и CDR-L1, состоящую из SEQ ID NO:14.
102. Антитело против GITR человека по п. 99, выбранное из (1) или (2):
(1) антитела против GITR человека, содержащего две тяжелые цепи и четыре легкие цепи, в которой
каждая тяжелая цепь содержит две структуры, состоящие из вариабельной области тяжелой цепи из SEQ ID NO: 9 и области CH1, области CH2 и области CH3, и C-конец одной из структур связан с N-концом другой структуры посредством линкера; и
каждая легкая цепь содержит вариабельную область легкой цепи из SEQ ID NO: 10 и константную область легкой цепи; и
(2) антитела против GITR человека, содержащего две тяжелые цепи и четыре легкие цепи, в котором
каждая тяжелая цепь содержит две структуры, состоящие из вариабельной области тяжелой цепи из SEQ ID NO: 9 и области CH1, области CH2 и области CH3, и C-конец одной из структур связан с N-концом другой структуры посредством линкера, где Q в положении 1 последовательности модифицирован до пироглутамата; и
каждая легкая цепь содержит вариабельную область легкой цепи из SEQ ID NO: 10 и константную область легкой цепи.
103. Антитело против GITR человека по п. 99, выбранное из (1) - (4):
(1) антитела против GITR человека, содержащего две тяжелые цепи, состоящие из SEQ ID NO: 7, и четыре легкие цепи, состоящие из SEQ ID NO: 8,
(2) антитела против GITR человека, содержащего две тяжелые цепи, состоящие из SEQ ID NO: 7, где Q в положении 1 модифицирован до пироглутамата, и четыре легкие цепи, состоящие из SEQ ID NO: 8,
(3) антитела против GITR человека, содержащего две тяжелые цепи, состоящие из аминокислотной последовательности в диапазоне от Q в положении 1 до G в положении 686 из SEQ ID NO: 7, и четыре легкие цепи, состоящие из SEQ ID NO: 8,
(4) антитела против GITR человека, содержащего две тяжелые цепи, состоящие из аминокислотной последовательности в диапазоне от Q в положении 1 до G в положении 686 из SEQ ID NO: 7, где Q в положении 1 модифицирован до пироглутамата, и четыре легкие цепи, состоящие из SEQ ID NO: 8.
104. Полинуклеотид, кодирующий вариабельную область антитела против GITR человека или его антигенсвязывающего фрагмента, где полинуклеотид выбран из группы, состоящей из (a) и (b):
(a) полинуклеотида, кодирующего вариабельную область тяжелой цепи антитела против GITR человека или его антигенсвязывающего фрагмента по п. 103, где вариабельная область тяжелой цепи состоит из SEQ ID NO:9; и
(b) полинуклеотида, кодирующего вариабельную область легкой цепи антитела против GITR человека или его антигенсвязывающего фрагмента по п. 103, где вариабельная область легкой цепи состоит из SEQ ID NO:10.
105. Полинуклеотид, кодирующий тяжелую цепь или легкую цепь антитела против GITR человека, где полинуклеотид выбран из группы, состоящей из (a) и (b):
(a) полинуклеотида, кодирующего тяжелую цепь антитела против GITR человека по п. 103, где тяжелая цепь состоит из SEQ ID NO:7; и
(b) полинуклеотида, кодирующего легкую цепь антитела против GITR человека по п. 103, где легкая цепь состоит из SEQ ID NO:8.
106. Экспрессирующий вектор для экспрессии вариабельной области тяжелой цепи и/или вариабельной области легкой цепи антитела против GITR человека или его антигенсвязывающего фрагмента, содержащий:
(a) полинуклеотид, кодирующий вариабельную область тяжелой цепи антитела против GITR человека или его антигенсвязывающего фрагмента по п. 100, где вариабельная область тяжелой цепи состоит из SEQ ID NO:9, и/или
(b) полинуклеотид, кодирующий вариабельную область легкой цепи антитела против GITR человека или его антигенсвязывающего фрагмента по п. 100, где вариабельная область легкой цепи состоит из SEQ ID NO:10.
107. Экспрессирующий вектор для экспрессии вариабельной области тяжелой цепи и/или вариабельной области легкой цепи антитела против GITR человека или его антигенсвязывающего фрагмента, содержащий:
(a) полинуклеотид, кодирующий тяжелую цепь антитела против GITR человека по п. 103, где тяжелая цепь состоит из SEQ ID NO:7, и/или
(b) полинуклеотид, кодирующий легкую цепь антитела против GITR человека по п. 103, где легкая цепь состоит из SEQ ID NO:8.
108. Фармацевтическая композиция для специфического связывания GITR человека, содержащая терапевтически эффективное количество антитела против GITR человека по п. 103 и фармацевтически приемлемый наполнитель.
109. Применение антитела против GITR человека по п. 103 для изготовления фармацевтической композиции для предотвращения или лечения злокачественной опухоли.
110. Способ предотвращения или лечения злокачественной опухоли, включающий введение терапевтически эффективного количества антитела против GITR человека по п. 103.
| WO 2015184099 A1, 03.12.2015 | |||
| ЛИГАНД GITR И СВЯЗАННЫЕ С ЛИГАНДОМ GITR МОЛЕКУЛЫ И АНТИТЕЛА И ВАРИАНТЫ ИХ ПРИМЕНЕНИЯ | 2004 |
|
RU2369636C2 |
| NOCENTINI G | |||
| et al | |||
| Pharmacological modulation of GITRL/GITR system: therapeutic perspectives, British journal of pharmacology, 2012, V | |||
| Устройство для отыскания металлических предметов | 1920 |
|
SU165A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| SCUMPIA P | |||
| O | |||
| et al | |||
| Treatment with GITR agonistic antibody corrects adaptive immune dysfunction in sepsis, Blood, The Journal of | |||
Авторы
Даты
2023-05-05—Публикация
2017-11-19—Подача