Область, к которой относится изобретение
[1] Настоящее изобретение относится к новым белкам, связывающимся с антигеном fms-подобной тирозинкиназы 3 (FLT3) человека, таким как антитела, имеющие улучшенную аффинность связывания с FLT3 и/или противоопухолевую активность. Антитела к FLT3 по изобретению были получены путем мутации родительского антитела к FLT3 и протестированы in vitro в анализах связывания, а также in vivo на модели опухоли мышей и в образцах опухолей пациента-человека. Антитела по изобретению представлены в виде моноспецифических конструкций или в формате биспецифического антитела FLT3xCD3 и демонстрируют превосходную аффинность к мишени и/или уничтожение опухолевых клеток. Настоящее изобретение также относится к способам получения антигенсвязывающих белков по изобретению, а также кодирующих их нуклеиновых кислот, к векторам и клеткам-хозяевам для их экспрессии. Изобретение также относится к способам лечения или диагностики заболевания, такого как лейкоз, с использованием FLT3 антигенсвязывающего белка (ABP) по изобретению.
Описание
[2] В процессе научной работы, начавшейся в 1980-е годы, было установлено, что биспецифические антитела, направленные на опухоль-ассоциированный антиген (TAA) и комплекс T-клеточный рецептор (TCR)/CD3, способны к активации T-клеток, приводящей к лизису TAA-экспрессирующих опухолевых клеток активированными T-клетками (Staerz et al. Nature 1985, 314:628-631; Perez et al. Nature 1985, 316:354-356; Jung et al. Proc Natl Acad Sci USA 1986, 83:4479-4483). Поскольку антитела к CD3, связанные с Fc рецепторами (FcRs) через их Fc-часть, чрезвычайно эффективны для индукции T-клеточной активации и высвобождения цитокинов как нежелательных побочных эффектов, очень важно сконструировать Fc-обедненные или -аттенуированные биспецифические TAAxCD3-антитела, чтобы предотвратить связывание FcR и обеспечить возможность для активации T-клеток, ограниченной клеткой-мишенью, а не FcR-опосредованной (Jung et al. Immunol Today 1988; 9:257-260; Jung et al. Eur J Immunol 1991; 21:2431-2435).
[3] Получение биспецифических антител, отвечающих этим этим необходимым требованиям, в промышленном качестве и количестве остается сложной задачей. Недавно было продемонстрировано, что рекомбинантное биспецифическое одноцепочечное (bssc) антитело с CD19xCD3-специфичностью, называемое Блинатумомабом, обладает существенной эффективностью в лечении пациентов с ALL (Bargou et al. Science 2008, 321:974-977), и оно было одобрено FDA как важное открытие. Следует отметить, что это лекарственное средство применяют в виде непрерывной 24-часовой инфузии в течение нескольких недель из-за его низкого периода полужизни в сыворотке и достаточно высокой токсичности: безопасно приемлемые дозы составляют примерно 30 мкг на пациента в день, что в 10000 раз ниже, чем используемые для лечения общепринятыми моноспецифическими противоопухолевыми антителами (Adams and Weiner. Nat Biotechnol 2005, 23:1147-57). Достигаемые концентрации лекарственного средства в сыворотке ниже 1 нг/мл (Topp et al. J Clin Oncol 2011; 29:2493-2498). Причиной этого существенного ограничения доз, также наблюдаемого в предыдущих клинических испытаниях с другими биспецифическими антителами (Kroesen et al. Br J Cancer 1994; 70:652-661; Tibben et al. Int J Cancer 1996; 66:477-483), является нецелевая T-клеточная активация, приводящая к системному высвобождению цитокинов. Очевидно, это явление препятствует оптимальной терапевтической активности биспецифических антител, стимулирующих TCR/CD3 комплекс.
[4] В принципе, дозоограничивающая нецелевая T-клеточная активация и возникающая в результате проблема токсичности могут быть вызваны двумя разными механизмами. T-клеточная активация не является - как должна бы - ограничиваемой клеткой-мишенью, т.е. даже одновалентный сайт связывания эффектора CD3 в конструкции биспецифического антитела способен индуцировать некоторую T-клеточную активацию в отсутствие клеток-мишеней, с которыми антитело связывается при помощи его нацеливающего фрагмента. Это представляет собой нецелевую активацию в строгом смысле, поскольку клетки, несущие целевой антиген, не требуются для индукции этого явления. Было замечено, что это явление значительно варьирует, если используют разные антитела к CD3 в разных форматах, и если добавляют некоторые стимулирующие фоновые клетки (SBCs), такие как клетки лимфомы (SKW6.4) или эндотелиальные клетки (HUVECs), которые обеспечивают костимулы для T-клеточной активации. Таким образом, следует выбрать CD3 фрагмент, индуцирующий минимальную “нецелевую” T-клеточную активацию для конструирования биспецифических антител.
[5] TAA, на который нацелено биспецифическое антитело, не является полностью опухоль-специфическим, что приводит к антитело-опосредованной Т-клеточной активации из-за связывания с нормальными TAA-экспрессирующими клетками. В строгом смысле это не является нецелевой активацией, поскольку она индуцируется антиген-экспрессирующими клетками-мишенями, хотя и “неправильными”, т.е. нормальными, а не злокачественными клетками. Блинатумомаб, биспецифическое CD19xCD3-антитело, указанное выше, безусловно, сталкивается с этой проблемой, поскольку его антиген-мишень CD19 экспрессируется на нормальных В-лимфоцитах. Очевидно, что специфичность таргетирования антигена для злокачественной ткани имеет решающее значение для предотвращения нецелевой Т-клеточной активации такого типа. Fms-подобная тирозинкиназа 3 (FLT3) представляет собой гематопоэтический рецепторный тирозинкиназный белок класса III, который имеет гомологию с другими членами семейства класса III, включая рецептор фактора стволовых клеток (c-KIT), рецептор макрофагального колониестимулирующего фактора (FMS) и рецептор тромбоцитарного фактора роста (PDGFR). После связывания с лигандом FLT3 рецептор FLT3 подвергается гомодимеризации, тем самым обеспечивая аутофосфорилирование специфических тирозиновых остатков в юкстамембранном домене и нисходящую активацию через PI3K Akt, MAPK и STAT5 пути. Таким образом, FLT3 играет решающую роль в качестве сигнального компонента в контроле пролиферации, выживания и дифференцировки нормальных гемопоэтических клеток.
[6] Человеческий FLT3 экспрессируется в CD34+CD38-гематопоэтических стволовых клетках (HSC), а также в субпопуляции дендритных клеток-предшественников. Экспрессия FLT3 также может быть обнаружена в мультипотентных клетках-предшественниках, таких как CD34+CD38+CD45RA-CD123|0W обший миелоидный предшественник (CMP), CD34+CD38+CD45RA+CD123|0W предшественники гранулоцитов и макрофагов (GMP) и CD34+CD38+CD10+CD19-общие лимфоидные клетки-предшественники (CLP). Интересно то, что, экспрессия FLT3 почти отсутствует в CD34+CD38-CD45RA-CD123-клетках-предшественниках мегакариоцитов и эристроцитов (MEP). Таким образом, экспрессия FLT3 преимущественно ограничивается ранними миелоидными и лимфоидными клетками-предшественниками, с некоторым уровнем экспрессии в более зрелых клетках моноцитарной линии. При остром миелоиднном лейкозе (AML) и остром лимфоцитарном лейкозе (ALL) FLT3 экспрессируется при очень высоких уровнях. FLT3 также экспрессируется при хроническом миелоидном лейкозе (CML) при бластном кризе, но не в хронической фазе. В целом, FLT3 экспрессируется у примерно 98% пред-B ALL пациентов и у примерно 90% AML пациентов.
[7] У от 15% до 34% пациентов с AML присутствуют мутации FLT3/ITD, с меньшей частотой у детей и с большей частотой у пожилых людей. Как взрослые, так и детские пациенты с AML с мутациями FLT3/ITD имеют очень плохой прогноз (Rombouts WJ, Blokland I,  Ploemacher RELeukemia. 2000 Apr; 14 (4): 675-83), и поэтому FLT3 является многообещающей мишенью для терапии AML, а также ALL. Мутировавший FLT3 постоянно активируется, и FLT3 передает сигналы по путям, которые включают ras/MAP киназу, STAT5 и PI3 киназу/AKT, что способствует блокированию апоптоза и дифференцировки, а также стимулирует пролиферацию. Для нацеленного воздействия на FLT3 можно использовать подход на основе антител для терапии как AML, так и ALL. Были разработаны антитела, которые связываются с FLT3 и ингибируют связывание FL с рецептором. Антитело IMC-EB10 от Imclone оценивали у пациентов с рецидивом AML в исследовании фазы I, однако исследование было прекращено из-за недостаточной эффективности (ClinicalTrials.gov Identifier: NCT00887926). Таким образом, сохраняется острая необходимость в оценке моноклональных антител второго поколения, включая биспецифические антитела, для лечения AML.
Ploemacher RELeukemia. 2000 Apr; 14 (4): 675-83), и поэтому FLT3 является многообещающей мишенью для терапии AML, а также ALL. Мутировавший FLT3 постоянно активируется, и FLT3 передает сигналы по путям, которые включают ras/MAP киназу, STAT5 и PI3 киназу/AKT, что способствует блокированию апоптоза и дифференцировки, а также стимулирует пролиферацию. Для нацеленного воздействия на FLT3 можно использовать подход на основе антител для терапии как AML, так и ALL. Были разработаны антитела, которые связываются с FLT3 и ингибируют связывание FL с рецептором. Антитело IMC-EB10 от Imclone оценивали у пациентов с рецидивом AML в исследовании фазы I, однако исследование было прекращено из-за недостаточной эффективности (ClinicalTrials.gov Identifier: NCT00887926). Таким образом, сохраняется острая необходимость в оценке моноклональных антител второго поколения, включая биспецифические антитела, для лечения AML.
[8] В дополнение к Т-клеточной активации, индуцируемой стимуляцией подлинно мономерного CD3, в недавней статье предлагается альтернативный механизм нецелевой активации, включающий нацеливающую часть биспецифического антитела; если эта часть состоит из одноцепочечного фрагмента, который индуцирует кластеризацию эффекторной части биспецифического антитела на поверхности Т-клеток, может индуцироваться тоническая передача сигналов, приводящая к истощению Т-клеток (Long et al. Nat Med 2015; 6: 581), которая практически не обнаруживается обычными краткосрочных анализами in vitro, но серьезно влияет на эффективность in vivo. Эти наблюдения были сделаны с использованием Т-клеток, трансфицированных химерным антигенным рецептором (CAR Т-клетки). Химерные Т-клеточные рецепторы включают одноцепочечные антитела в качестве нацеливающих групп. Весьма вероятно, что результаты Long et al. (2015) аналогичным образом применимы к биспецифическим антителам с такой нацеливающей частью, поскольку эти реагенты, после связывания с Т-клеткой, функционально эквивалентны Т-клетке, трансфицированной соответствующим CAR. В данной области хорошо известно, что большинство одноцепочечных антител имеют тенденцию к образованию мультимеров и агрегатов (Worn et al. J Mol Biol 2001, 305: 989-1010), и поэтому неудивительно, что все, кроме одного из CAR, испытанных Long et al. (2015), показали феномен кластеризации и тонической передачи сигналов CD3, хотя и в разной степени (Long et al. 2015). Обозначенная выше проблема требует биспецифического формата, который предотвращает мультимеризацию нацеливающей части и вызываемую ею кластеризацию.
[9] Недостатком большинства биспецифических форматов является очень короткий период полужизни в сыворотке (1-3 часа) из-за пониженной молекулярной массы и отсутствия CH3 доменов. Таким образом, прототипическое антитело Блинатумомаб применяют путем непрерывной 24-часовой в/в инфузии в течение нескольких недель. Применение полных форматов на основе IgG с повышенным периодом полужизни в сыворотке, таких как IgGsc, показанные на Фиг. 1, считается неподходящим из-за возможной повышенной нецелевой активации, индуцируемой двухвалентной C-концевой CD3-связывающей группой.
[10] Учитывая вышеизложенное, в данной области техники существует необходимость в улучшенных ABP, нацеленных на FLT3, которые решают по меньшей мере одну из проблем, обозначенных выше.
Сущность изобретения
[11] В общем виде и путем краткого описания основные аспекты настоящего изобретения могут быть описаны следующим образом:
[12] В первом аспекте изобретение относится к антигенсвязывающему белку (ABP), способному связываться с человеческой fms-подобной тирозинкиназой 3 (FLT3), включающему:
(i) один, предпочтительно два вариабельных домена тяжелой цепи, включающих CDRH1 область, представленную в SEQ ID NO: 01 (SYWMH), CDRH2 область, представленную в SEQ ID NO: 02 (EIDPSDSYKDYNQKFKD), и CDRH3 область, представленную в SEQ ID NO: 03 (AITTTPFDF), или где в каждом случае независимо CDRH1, CDRH2 и/или CDRH3 включают последовательность, имеющую не более трех или двух, предпочтительно не более одной аминокислотной замены, делеции или инсерции по сравнению с SEQ ID NO: 01, SEQ ID NO: 02 или SEQ ID NO: 03, соответственно; и
(ii) один, предпочтительно два вариабельных домена легкой цепи, включающих CDRL1 область, представленную в SEQ ID NO: 05 (RASQSISNNLH), CDRL2 область, представленную в SEQ ID NO: 06 (YASQSIS), и CDRL3 область, представленную в SEQ ID NO: 07 (QQSNTWPYT), или где в каждом случае независимо CDRL1, CDRL2 и/или CDRL3 включают последовательность, имеющую не более трех или двух, предпочтительно не более одной аминокислотной замены, делеции или инсерции по сравнению с SEQ ID NO: 05, SEQ ID NO: 06 или SEQ ID NO: 07, соответственно;
отличающемуся тем, что указанный один, предпочтительно два вариабельных домена тяжелой цепи и указанный один, предпочтительно два вариабельных домена легкой цепи, каждый включают каркасную область антитела, содержащую по меньшей мере часть консенсусной каркасной последовательности человеческого антитела.
[13] Во втором аспекте изобретение относится к антигенсвязывающему белку (ABP) или его антигенсвязывающему фрагменту, способному связываться с fms-подобной тирозинкиназой 3 (FLT3), и который способен конкурировать со связыванием ABP первого аспекта с FLT3.
[14] В третьем аспекте изобретение относится к биспецифическому антигенсвязывающему белку (ABP), который включает первый антигенсвязывающий домен, способный связываться с антигеном fms-подобной тирозинкиназы 3 (FLT3) человека, и второй антигенсвязывающий домен, способный связываться с антигеном кластера дифференцировки 3 (CD3) человека, где биспецифический ABP:
a. связывается с FLT3 с EC50 меньше чем 10 нМ, как определено в анализе связывания биспецифического ABP с FLT3-положительными клетками методом проточной цитометрии с использованием устройства для сортировки флуоресцентно-активированных клеток (FACS); и
b. связывается с CD3 с EC50 меньше чем 200 нМ, как определено в анализе связывания биспецифического ABP с CD3-положительными клетками методом проточной цитометрии с использованием устройства для сортировки флуоресцентно-активированных клеток (FACS) .
[15] В четвертом аспекте изобретение относится к выделенной нуклеиновой кислоте, включающей последовательность, кодирующую ABP, или антигенсвязывающий фрагмент или мономер, такой как тяжелая или легкая цепь, ABP первого или второго аспекта, или кодирующую биспецифический ABP в соответствии с третьим аспектом.
[16] В пятом аспекте изобретение относится к нуклеиновокислотной конструкции (NAC), включающей нуклеиновую кислоту четвертого аспекта и один или более дополнительных элементов последовательности, обеспечивающих возможность экспрессии кодируемого антигенсвязывающего белка (ABP) или биспецифического ABP, или компонента указанного ABP или биспецифического ABP (такого тяжелая цепь или легкая цепь антитела) в клетке.
[17] В шестом аспекте изобретение относится к рекомбинантной клетке-хозяину, включающей нуклеиновую кислоту четвертого аспекта или нуклеиновокислотную конструкцию (NAC) в соответствии со вторым аспектом.
[18] В седьмом аспекте изобретение относится к фармацевтической композиции, включающей: (i) антигенсвязывающий белок (ABP) или биспецифический ABP первого-третьего аспекта, или (ii) нуклеиновую кислоту четвертого аспекта или NAC в соответствии с пятым, или (iii) рекомбинантную клетку-хозяин в соответствии с шестым аспектом и фармацевтически приемлемый носитель, стабилизатор и/или эксципиент.
[19] В восьмом аспекте изобретение относится к компоненту для применения в медицине, где компонент выбран из перечня, включающего: (i) антигенсвязывающий белок(ABP) или биспецифический ABP первого-третьего аспекта, или (ii) нуклеиновую кислоту четвертого аспекта или NAC в соответствии с пятым, или (iii) рекомбинантную клетку-хозяин в соответствии с шестым аспектом и фармацевтическую композицию в соответствии с седьмым аспектом.
[20] В девятом аспекте изобретение относится к способу усиления клеточно-опосредованного иммунного ответа на человеческую клетку, которая экспрессирует человеческий FLT3, включающему контактирование указанной клетки с антигенсвязывающим белком (ABP) первого или второго аспекта, или биспецифическим ABP в соответствии с третьим аспектом, или нуклеиновой кислотой, кодирующий указанный ABP или биспецифический ABP, в соответствии с четвертым аспектом в присутствии иммунной клетки, такой как T-клетка или природная киллерная (NK) клетка, усиливая таким образом клеточно-опосредованный иммунный ответа против указанной человеческой клетки.
[21] В десятом аспекте изобретение относится к способу профилактики и/или лечения пролиферативного расстройства у субъекта, включающему введение субъекту терапевтически эффективного количества компонента, указанного в восьмом аспекте; и где пролиферативное расстройство характеризуется экспрессией человеческой fms-подобной тирозинкиназы 3 (FLT3) в клетках, ассоциированных с пролиферативным расстройством.
Подробное описание изобретения
[22] Далее будут описаны элементы изобретения. Эти элементы перечислены с конкретными вариантами осуществления, однако следует понимать, что они могут быть объединены любым способом и в любом количестве для создания дополнительных вариантов осуществления. Различные описанные примеры и предпочтительные варианты осуществления не должны толковаться как ограничение настоящего изобретения только конкретно описанными вариантами осуществления. Следует понимать, что настоящее описание поддерживает и охватывает варианты осуществления, которые объединяют два или более конкретно описанных варианта осуществления или которые объединяют один или более конкретно описанных вариантов осуществления с любым количеством раскрытых и/или предпочтительных элементов. Кроме того, любые перестановки и комбинации всех описанных элементов в настоящей заявке должны считаться раскрытыми в описании настоящей заявки, если контекст не указывает иное.
В первом аспекте настоящее изобретение относится к антигенсвязывающему белку (ABP), способному связываться с человеческой fms-подобной тирозинкиназой 3 (FLT3), включающему: (i) вариабельный домен тяжелой цепи, включающий CDRH1 область, представленную в SEQ ID NO: 01 (SYWMH), CDRH2 область, представленную в SEQ ID NO: 02 (EIDPSDSYKDYNQKFKD), и CDRH3 область, представленную в SEQ ID NO: 03 (AITTTPFDF), или где в каждом случае независимо CDRH1, CDRH2 и/или CDRH3 включают последовательность, имеющую не более трех или двух, предпочтительно не более одной аминокислотной замены, делеции или инсерции по сравнению с SEQ ID NO: 01, SEQ ID NO: 02 или SEQ ID NO: 03, соответственно; или включающий последовательность CDRH1, CDRH2 или CDRH3, имеющую по меньшей мере 75% идентичность последовательности или по меньшей мере 80%, предпочтительно 90% идентичность последовательности с SEQ ID NO: 01, SEQ ID NO: 02, или SEQ ID NO: 03; и (ii) вариабельный домен легкой цепи, включающий CDRL1 область, представленную в SEQ ID NO: 05 (RASQSISNNLH), CDRL2 область, представленную в SEQ ID NO: 06 (YASQSIS), и CDRL3 область, представленную в SEQ ID NO: 07 (QQSNTWPYT), или где в каждом случае независимо CDRL1, CDRL2 и/или CDRL3 включают последовательность, имеющую не более трех или двух, предпочтительно не более одной аминокислотной замены, делеции или инсерции по сравнению с SEQ ID NO: 05, SEQ ID NO: 06 или SEQ ID NO: 07, соответственно; или включающий последовательность CDRL1, CDRL2 или CDRL3, имеющую по меньшей мере 75% идентичность последовательности или по меньшей мере 80% идентичность последовательности с SEQ ID NO: 05, SEQ ID NO: 06, или SEQ ID NO: 07, отличающемуся тем, что указанная вариабельная область тяжелой цепи и указанная вариабельная область легкой цепи каждая включают человеческие каркасные последовательности вариабельной области. Предпочтительно указанный вариабельный домен(домены) тяжелой цепи и указанный вариабельный домен(домены) легкой цепи, каждый включают каркасную область антитела, содержащую по меньшей мере часть консенсусной каркасной последовательности человеческого антитела.
[23] Настоящее изобретение также относится к новым высокоаффинным и эффективным конструкциям антител, полученным из гуманизированной версии анти-FLT3 антитела 4G8 (мышиное анти-FLT3 антитело, полностью раскрытое в WO 2011/076922), которое впервые было гуманизировано прививкой CDR, означающей, что CDR области мышиного антитела 4G8 вставлены в каркасную область тяжелой цепи и легкой цепи человеческого антитела. Однако затем гуманизированное антитело 4G8 было значительно изменено по формату, константным и вариабельным областям для получения ABP по настоящему изобретению. В принципе, любая вариабельная область легкой цепи человека и/или вариабельная область тяжелой цепи могут служить каркасом для CDR прививки. В одном иллюстративном примере гуманизированного антитела по изобретению CDR области легкой цепи антитела 4G8 (что означает CDR петли в SEQ ID NO: 5 - SEQ ID NO: 7) могут быть вставлены в (вариабельный домен) человеческой последовательности κ-легкой цепи IGKV3-15*1, которая депонирована в базе данных IMGT/LIGM под номером доступа M23090, см. также Ichiyoshi Y., Zhou M., Casali P. A human anti-insulin IgG autoantibody apparently arises through clonal selection from an insulin-specific 'germ-line' natural antibody template. Analysis by V gene segment reassortment and site-directed mutagenesis' J. Immunol. 154(1):226-238 (1995). В другом иллюстративном примере гуманизированного антитела по изобретению CDR области тяжелой цепи антитела 4G8 (что означает петли CDR в SEQ ID NO: 1 - SEQ ID NO: 3) могут быть включены в (вариабельные домены) последовательности тяжелой цепи IGHV1-46*03, которая депонирована в базе данных IMGT/LIGM под номером доступа L06612 (см. также Watson C.T., et al. Complete haplotype sequence of the human immunoglobulin heavy-chain variable, diversity, and joining genes and characterization of allelic and copy-number variation. Am. J. Hum. Genet. 92(4):530-546 (2013).
[24] Термин “антигенсвязывающий белок” или “ABP” в контексте настоящей заявки означает белок, который специфически связывается с антигеном-мишенью, например с одним или несколькими эпитопами, представленными или присутствующими на антигене-мишени. Антиген для ABPs по изобретению представляет собой FLT3, или в случае биспецифических молекул - FLT3 и CD3. Типично антигенсвязывающий белок представляет собой антитело (или его фрагмент), предпочтительно биспецифическое антитело; однако другие формы антигенсвязывающего белка также предусматриваются изобретением. Например, ABP может представлять собой другой (не антитело) рецепторный белок, полученный из небольших и устойчивых не-иммуноглобулиновых “каркасов”, таких как те, которые наделены связывающими функциями, например с использованием способов комбинаторного конструирования белков (Gebauer & Skerra, 2009; Curr Opin Chem Biol, 13:245). Конкретные примеры таких отличных от антител ABP включают: Молекулы аффител на основе Z домена Белка A (Nygren, 2008; FEBS J 275:2668); Аффилины на основе кристаллического гамма-B и/или убиквитина (Ebersbach et al, 2007; J Mo Biol, 372:172); Аффимеры на основе цистатина (Johnson et al, 2012; Anal Chem 84:6553); Аффитины на основе Sac7d из Sulfolobus acidcaldarius (Krehenbrink et al, 2008; J Mol Biol 383:1058); Альфатела на основе трехспиральной суперспирали (Desmet et al, 2014; Nature Comms 5:5237); Антикалины на основе липокалинов (Skerra, 2008; FEBS J 275:2677); Авимеры на основе A доменов различных мембранных рецепторов (Silverman et al, 2005; Nat Biotechnol 23:1556); ДАРпины на основе анкиринового повторного мотива (Strumpp et al, 2008; Drug Discov Today, 13:695); Финомеры на основе SH3 домена Fyn (Grabulovski et al, 2007; J Biol Chem 282:3196); пептиды с доменами Куница на основе доменов Куница различных ингибиторов протеаз (Nixon et al, Curr opin Drug Discov Devel, 9:261) и Центрины и Монотела на основе 10-го III типа домена фибронектина (Diem et al., 2014; Protein Eng Des Sel 27:419 doi: 10.1093/protein/gzu016; Koide & Koide, 2007; Methods Mol Biol 352:95). В контексте ABP по настоящему изобретению, ABP представлен предпочтительно в биспецифическом формате, включающем антигенсвязывающие домены для человеческого FLT3 и человеческого CD3.
[25] Термин “определяющая комплементарность область” (или “CDR”, или “гипервариабельная область”) в контексте настоящей заявки в широком смысле относится к одной или нескольким гипервариабельным или определяющим комплементарность областям (CDR), присутствующим в вариабельных областях легкой или тяжелой цепи антитела. См., например: “IMGT”, Lefranc et al, 20003, Dev Comp Immunol 27:55; Honegger & Plückthun, 2001, J Mol Biol 309:657, Abhinandan & Martin, 2008, Mol Immunol 45:3832, Kabat, et al. (1987): Sequences of Proteins of Immunological Interest National Institutes of Health, Bethesda, Md. Эти термины включают гипервариабельные области, определенные Kabat et al (1983) Sequences of Proteins of Immunological Interest, US Dept of Health and Human Services, или гипервариабельные петли в 3-мерных структурах антител (Chothia and Lesk, 1987; J Mol Biol 196:901). CDRs в каждой цепи удерживаются в непосредственной близости каркасными областями и, с CDRs из другой цепи, способствуют образованию антигенсвязывающего сайта. В CDR находятся выбранные аминокислоты, которые были описаны как области, определяющие селективность (SDR), которые представляют собой критические контактные остатки, используемые CDR во взаимодействии антитело-антиген. (Kashmiri, 2005; Methods 36:25).
[26] Термин “антитело”, как правило, относится к белковой связывающей молекуле, которая основана на иммуноглобулине. Типичными примерами такого антитела являются производные или функциональные фрагменты иммуноглобулина, которые сохраняют специфичность связывания. Способы получения антител и фрагментов антител хорошо известны в данной области техники. Термин “антитело” также включает иммуноглобулины (Ig) различных классов (т.е. IgA, IgG, IgM, IgD и IgE) и подклассов (таких как IgG1, lgG2 и т.д.). Как также указано выше, иллюстративные примеры производного или молекулы антитела включают Fab фрагменты, F(ab’)2, Fv фрагменты, одноцепочечные Fv фрагменты (scFv), диатела или доменные антитела (Holt LJ et al., Trends Biotechnol. 21(11), 2003, 484-490). Определение термина “антитело”, таким образом, также включает варианты осуществления, такие как химерные, одноцепочечные и гуманизированные антитела.
[27] “ABP”, в контексте настоящей заявки, может нести один или более доменов, которые содержат последовательность, имеющую по меньшей мере приблизительно 60%, по меньшей мере приблизительно 70%, по меньшей мере приблизительно 75%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 85%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 92%, по меньшей мере приблизительно 95%, по меньшей мере приблизительно 96%, по меньшей мере приблизительно 97%, по меньшей мере приблизительно 98% или по меньшей мере приблизительно 99% идентичности последовательности с соответствующим природным доменом иммуноглобулина M, иммуноглобулина G, иммуноглобулина A, иммуноглобулина D или иммуноглобулина E. В этой связи следует отметить, что термин “приблизительно” или “примерно” в контексте настоящей заявки означает отклонение в пределах 20%, например отклонение в пределах 10% или в пределах 5% от данного значения или диапазона.
[28] “Процент (%) идентичности последовательностей” в контексте настоящей заявки означает процент попарно идентичных остатков - после гомологического выравнивания последовательности полипептида по настоящему изобретению с рассматриваемой последовательностью - относительно количества остатков в более длинной из этих двух последовательностей. Выравнивание с целью определения процента идентичности аминокислотной последовательности может достигаться различными способами, которые известны специалистам в данной области, например, с использованием общедоступного компьютерного программного обеспечения, такого как программное обеспечение BLAST, ALIGN или Megalign (DNASTAR). Специалисты в данной области могут определить подходящие параметры для измерения выравнивания, включая любые алгоритмы, необходимые для достижения максимального выравнивания по всей длине сравниваемых последовательностей. То же самое верно и для нуклеотидных последовательностей, раскрытых в настоящей заявке.
[29] “Иммуноглобулин” в контексте настоящей заявки обычно представляет собой тетрамерный гликозилированный белок, состоящий из двух легких (L) цепей, каждая примерно 25 кДа, и двух тяжелых (H) цепей, каждая примерно 50 кДа. Два типа легкой цепи, названные лямбда и каппа, можно найти в иммуноглобулинах. В зависимости от аминокислотной последовательности константного домена тяжелых цепей иммуноглобулины могут быть отнесены к пяти основным классам: A, D, E, G и M, и некоторые из них далее могут подразделяться на подклассы (изотипы), например, IgG1, lgG2, IgG3, IgG4, IgA1 и IgA2. IgM иммуноглобулин состоит из 5 основных гетеротетрамерных единиц вместе с дополнительным полипептидом, называемым J цепью, и содержит 10 антигенсвязывающих сайтов, тогда как IgA иммуноглобулины содержат 2-5 основных 4-цепочечных единиц, которые могут полимеризоваться с образованием поливалентных агрегатов, в комбинации с J цепью. В случае IgGs, 4-цепочечная единица, как правило, имеет молекулярную массу приблизительно 150000 Дальтон.
[30] В IgG классе иммуноглобулинов имеется несколько иммуноглобулиновых доменов в тяжелой цепи. Под “иммуноглобулиновым (Ig) доменом” подразумевается область иммуноглобулина, имеющая четкую третичную структуру. В контексте IgG антител, каждый из IgG изотипов имеет три CH области: “CH1” относится к положениям 118-220, “CH2” относится к положениям 237-340, и “CH3” относится к положениям 341-447 в соответствии с EU индексом, как в Kabat et al. Под “шарниром”, или “шарнирной областью”, или “шарнирной областью антитела”, или “шарнирной областью иммуноглобулина”, или “H” подразумевается гибкий полипептид, включающий аминокислоты между первым и вторым константными доменами антитела. Структурно, IgG CH1 домен заканчивается в EU положении 220, а IgG CH2 домен начинается с остатка в EU положении 237. Таким образом, IgG шарнир в настоящем изобретении определяется как включающий положения 221 (D221 в IgG1) - 236 (G236 в IgG1), где нумерация указана в соответствии с EU индексом, как в Kabat et al. Константная область тяжелой цепи, как определено в настоящей заявке, относится к N-концу CH1 домена до C-конца CH3 домена, таким образом, включает положения 118-447, где нумерация указана в соответствии с EU индексом.
[31] Термин “вариабельный” относится к частям иммуноглобулиновых доменов, которые демонстрируют вариабельность в их последовательности и которые участвуют в определении специфичности и аффинности связывания конкретного антитела (т.е. “вариабельный домен(домены)”). Вариабельность не распределяется равномерно по вариабельным доменам антител; она сконцентрирована в субдоменах каждой из вариабельных областей тяжелых и легких цепей. Эти субдомены называются “гипервариабельными областями” “HVR” или “HV”, или “определяющими комплементарность областями” (CDR). Более консервативные (т.е. не гипервариабельные) части вариабельных доменов называются “каркасными” областями (FR). Вариабельные домены природных тяжелых и легких цепей каждый включают четыре FR области, большей частью принимающие β-листовую конфигурацию, соединенные тремя гипервариабельными областями, которые образуют петли, соединяющие β-листовую структуру, а в некоторых случаях образующие ее часть. Гипервариабельные области в каждой цепи удерживаются вместе в непосредственной близости посредством FR и, с гипервариабельными областями из другой цепи, способствуют образованию антигенсвязывающего сайта (см. Kabat et al., ниже). Как правило, природные иммуноглобулины включают шесть CDR (см. ниже); три в VH (CDRH1, CDRH2, CDRH3) и три в VL (CDRL1, CDRL2, CDRL3). В природных иммуноглобулинах CDRH3 и CDRL3 демонстрируют наибольшее разнообразие из шести CDR, и, в частности, считается, что CDRH3 играет уникальную роль в придании точной специфичности иммуноглобулинам. Константные домены не вовлечены непосредственно в связывание антигена, но демонстрируют различные эффекторные функции, такие как, например, антитело-зависимую клеточно-опосредованную цитотоксичность и активацию комплемента.
[32] Термины “VH” (также указываемый как VH) и “VL” (также указываемый как VL) используются в настоящей заявке как относящиеся к вариабельному домену тяжелой цепи и вариабельному домену легкой цепи, соответственно, иммуноглобулина. Вариабельная область легкой или тяжелой цепи иммуноглобулина состоит из “каркасной” области, прерываемой тремя гипервариабельными областями. Таким образом, термин “гипервариабельная область” относится к аминокислотным остаткам антитела, которые ответственны за связывание с антигеном. Гипервариабельная область включает аминокислотные остатки из “определяющей комплементарность области” или “CDR”. В вариабельной части иммуноглобулина имеются три CDR тяжелой цепи и три легкой цепи (или CDR области). Таким образом, “CDR” в контексте настоящей заявки относятся ко всем трем CDR тяжелой цепи (CDRH1, CDRH2 и CDRH3) или всем трем CDR легкой цепи (CDRL1, CDRL2 и CDRL3), или ко всем CDR тяжелой и всем легкой цепи, в зависимости от ситуации. Три CDR формируют характер связывания вариабельной области легкой цепи и три формируют характер связывания вариабельной области тяжелой цепи. CDR определяют антиген-специфичность молекулы иммуноглобулина и разделены аминокислотными последовательностями, которые включают поддерживающие или каркасные области. Для точного определения границ и длин CDR используют различные системы классификации и нумерации. Структура и укладка белка антитела могут означать, что другие остатки считаются частью антигенсвязывающей области и должны таким образом рассматриваться специалистами в данной области. CDR обеспечивают  часть контактирующих остатков для связывания иммуноглобулина с антигеном или эпитопом.
часть контактирующих остатков для связывания иммуноглобулина с антигеном или эпитопом.
[33] CDR3 обычно является наиболее важным источником молекулярного разнообразия в сайте связывания с антителом. H3, например, может иметь такую короткую длину, как два аминокислотных остатка, или длину больше чем 26 аминокислот. Структуры субъединиц и трехмерные конфигурации различных классов иммуноглобулинов хорошо известны в данной области техники. Обзор структуры антител см. в Antibodies: A Laboratory Manual, Cold Spring Harbor Laboratory, eds. Harlow et al., 1988. Специалистам в данной области техники должно быть понятно, что структура каждой субъединицы, например, структура CH, VH, CL, VL, CDR, FR, включает активные фрагменты, например, часть VH, VL или CDR субъединицы связывается с антигеном, т.е. антигенсвязывающий фрагмент, или, например, часть CH субъединицы, которая связывается, например, с Fc рецептором и/или комплементом и/или активирует их. CDR типично относятся к CDRs по Кабату, как описано в Sequences of Proteins of immunological Interest, US Department of Health and Human Services (1991), eds. Kabat et al. Другой стандарт для характеристики сайта связывания с антигеном включает ссылку на гипервариабельные петли, как описано Chothia. См., например, Chothia, et al. (1992; J. MoI. Biol. 227:799-817; and Tomlinson et al. (1995) EMBO J. 14:4628-4638. Еще один стандарт включает определение AbM, используемое в программе моделирования антител Oxford Molecular's AbM. См., например, Protein Sequence and Structure Analysis of Antibody Variable Domains. In: Antibody Engineering Lab Manual (Ed.: Duebel, S. and Kontermann, R., Springer-Verlag, Heidelberg). Варианты осуществления, описанные применительно к CDRs по Кабату, альтернативно можно осуществить с использованием аналогичных описанных взаимосвязей применительно к гипервариабельным петлям по Чотиа или к AbM-определенным петлям.
[34] Соответствующая тяжелая цепь мю иммуноглобулина, тяжелая цепь гамма, тяжелая цепь альфа, тяжелая цепь дельта, тяжелая цепь эпсилон, легкая цепь лямбда или легкая цепь каппа могут происходить от любого вида, например вида млекопитающих, включая вид грызунов, амфибию, например подкласса Lissamphibia, который включает, например, лягушек, жаб, саламандр или тритонов, или вида беспозвоночных. Примеры млекопитающих включают, но не ограничиваются этим, крысу, мышь, кролика, морскую свинку, белку, хомяка, ежа, утконоса, американскую пищуху, броненосца, собаку, лемура, козу, свинью, корову, опоссума, лошадь, летучую мышь, сурка, орангутанга, макаку-резус, шерстистую обезьяну, макака, шимпанзе, тамарина (saguinus oedipus), мартышку или человека.
[35] Как указано в настоящей заявке, иммуноглобулин типично представляет собой гликопротеин, который включает по меньшей мере две тяжелые (H) цепи и две легкие (L) цепи, связанные дисульфидными связями, или их антигенсвязывающую часть. Каждая тяжелая цепь имеет вариабельную область тяжелой цепи (сокращенно указана как VH) и константную область тяжелой цепи. В некоторых вариантах осуществления константная область тяжелой цепивключает три домена CH1, CH2 и CH3. Каждая легкая цепь имеет вариабельную область легкой цепи (сокращенно указана как VL) и константную область легкой цепи. Константная областя легкой цепи включает один домен CL. VH и VL области далее могут подразделяться на области гипервариабельности, называемые определяющими комплементарность областями (CDR), чередующиеся с областями, которые являются более консервативными, называемыми каркасными областями (FR). CDR содержат  часть остатков, ответственных за специфические взаимодействия антитела с антигеном. Каждая VH и VL имеет три CDR и четыре FR, расположенные от амино-конца к карбокси-концу в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. Вариабельные области тяжелой и легкой цепи содержат связывающий домен, который взаимодействует с эпитопом антигена.
часть остатков, ответственных за специфические взаимодействия антитела с антигеном. Каждая VH и VL имеет три CDR и четыре FR, расположенные от амино-конца к карбокси-концу в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. Вариабельные области тяжелой и легкой цепи содержат связывающий домен, который взаимодействует с эпитопом антигена.
[36] Остатки “каркасной области” или “FR” представляют собой остатки вариабельного домена, отличные от гипервариабельной области. Последовательности каркасных областей различных легких или тяжелых цепей относительно консервативны в пределах одного вида. Таким образом, “человеческая каркасная область” представляет собой каркасную область, которая по существу идентична (примерно на 85% или более, обычно 90-95% или более) каркасной области природного иммуноглобулина человека. Каркасная область антитела, которая представляет собой комбинированные каркасные области составляющих его легкой и тяжелой цепей, служит для позиционирования и выравнивания CDR. CDR в первую очередь ответственны за связывание с эпитопом антигена.
[37] Термины “Fab”, “Fab область”, “Fab часть” или “Fab фрагмент” означают полипептид, который включает VH, CH1, VL и CL домен иммуноглобулина. Fab может относиться к этой области как таковой или к этой области в контексте ABP, а также полноразмерного иммуноглобулина или фрагмента иммуноглобулина. Типично Fab область содержит всю легкую цепь антитела. Fab область может быть взята для определения “плеча” молекулы иммуноглобулина. Она содержит эпитоп-связывающуюся часть этого Ig. Fab область природного иммуноглобулина можно получить в виде протеолитического фрагмента методом папаинового гидролиза. “F(ab’)2 часть” представляет собой протеолитический фрагмент, полученный путем пепсинового гидролиза иммуноглобулина. “Fab’ часть” представляет собой продукт, являющийся результатом восстановления дисульфидных связей F(ab’)2 части. В контексте настоящей заявки термины “Fab”, “Fab область”, “Fab часть” или “Fab фрагмент” могут также включать шарнирную область, которая определяет C-концевой конец плеча антитела. Эта шарнирная область соответствует шарнирной области, присутствующей в направлении C-конца от CH1 домена в полноразмерном иммуноглобулине, где плечи ABP могут быть взяты для определения Y. Термин шарнирная область используется в данной области техники, поскольку иммуноглобулин обладает некоторой гибкостью в этой области. “Тяжелая цепь Fab” в контексте настоящей заявки означает такую часть (или полипептид) Fab фрагмента, которая включает VH и CH1, тогда как “легкая цепь Fab” в контексте настоящей заявки означает такую часть (или полипептид) Fab фрагмента, которая включает VL и CL.
[38] Термин “Fc область” или “Fc фрагмент” используется для определения С-концевой области тяжелой цепи иммуноглобулина, включая Fc-области с нативной последовательностью и вариантные Fc-области. Fc часть опосредует эффекторную функцию антител, например активацию системы комплемента и иммунных эффекторных клеток, несущих Fc-рецептор, таких как NK-клетки. В молекулах IgG человека Fc-область образуется в результате расщепления папаином N-концевой области до Cys226. Хотя границы Fc-области тяжелой цепи иммуноглобулина могут варьировать, Fc-область тяжелой цепи человеческого IgG обычно определяется как простирающаяся от аминокислотного остатка в положении Cys226 или от Pro230 до его карбоксильного конца. С-концевой лизин (остаток 447 в соответствии с системой нумерации EU) Fc области может быть удален, например, в процессе получения или очистки ABP или при помощи рекомбинантной нуклеиновой кислоты, кодирующей тяжелую цепь ABP. Fc-области с нативной последовательностью включают IgG1, IgG2 (IgG2A, IgG2B), IgG3 и IgG4 млекопитающих, например человеческие или мышиные. Fc область содержит два или три константных домена, в зависимости от класса антитела. В вариантах осуществления, где иммуноглобулин представляет собой IgG, Fc область имеет СН2 и СН3 домен.
[39] Термин “одноцепочечный вариабельный фрагмент” (scFv) используется для определения фрагмента антитела, в котором вариабельные области тяжелой (VH) и легкой цепей (VL) иммуноглобулина слиты вместе посредством короткого линкерного пептида от десяти до приблизительно 25 аминокислот. Линкер обычно богат глицином для гибкости, а также серином или треонином для растворимости и может либо соединять N-конец VH с C-концом VL, либо соединять N-конец VL с С-концом VH. scFv фрагмент сохраняет специфический сайт связывания антигена, но не имеет константных доменов иммуноглобулинов.
[40] Термин “эпитоп”, также известный как “антигенная детерминанта”, относится к части антигена, с которой специфически связывается антитело или Т-клеточный рецептор, образуя таким образом комплекс. Таким образом, термин “эпитоп” включает любую молекулу или детерминанту белка, способную к специфическому связыванию с иммуноглобулином или Т-клеточным рецептором. Сайт(сайты) связывания (паратоп) ABP, описанного в настоящей заявке, могут специфически связываться/взаимодействовать с конформационными или непрерывными эпитопами, которые уникальны для являющейся мишенью структуры. Эпитопные детерминанты обычно состоят из химически активных поверхностных групп молекул, таких как аминокислоты или боковые цепи сахаров, и обычно имеют специфические трехмерные структурные характеристики, а также специфические характеристики заряда. В некоторых вариантах осуществления эпитопные детерминанты включают химически активные поверхностные группы молекул, такие как аминокислоты, боковые цепи сахаров, фосфорил или сульфонил, и в некоторых вариантах осуществления могут иметь определенные трехмерные структурные характеристики и/или специфические характеристики заряда. Что касается полипептидных антигенов, конформационный или прерывистый эпитоп характеризуется присутствием двух или более дискретных аминокислотных остатков, разделенных в первичной последовательности, но собирающихся в согласованную структуру на поверхности молекулы, когда полипептид укладывается в нативный белок/антиген (SeIa, M., Science (1969) 166, 1365-1374; Laver, WG, et al. Cell (1990) 61, 553-556). Два или более дискретных аминокислотных остатка, вносящих вклад в эпитоп, могут присутствовать на отдельных участках одной или нескольких полипептидных цепей. Эти остатки объединяются на поверхности молекулы, когда полипептидная цепь(цепи) укладывается в трехмерную структуру с образованием эпитопа. Напротив, непрерывный или линейный эпитоп состоит из двух или более дискретных аминокислотных остатков, которые присутствуют в одном линейном сегменте полипептидной цепи.
[41] Термин "специфический" в данном контексте или "специфически связывающийся", также используемый как "направленный на", означает в соответствии с данным изобретением, что антитело или фрагмент иммунного рецептора способен специфически взаимодействовать и/или связываться с специфическим антигеном или лигандом, или с множеством специфических антигенов или лигандов, но по существу не связывается с другими антигенами или лигандами. Такое связывание может быть проиллюстрировано спецификой "принципа замка и ключа". Считается, что антитела "связываются с одним и тем же эпитопом", если антитела перекрестно конкурируют, так что только одно антитело может связываться с эпитопом в данный момент времени, то есть одно антитело предотвращает связывание или модулирующий эффект другого.
[42] Термин "выделенный ABP" в контексте настоящей заявки относится к ABP, который был идентифицирован и отделен и/или выделен из компонента его естественной среды. Загрязняющие компоненты его естественной окружающей среды представляют собой вещества, которые могут мешать диагностическому или терапевтическому использованию антитела, и могут включать ферменты, гормоны и другие белковые или небелковые растворенные вещества. В некоторых вариантах осуществления ABP очищен до более чем 95% по массе антитела, как определено методом Лоури, например до более чем 99% по массе. В некоторых вариантах осуществления антитело очищают до гомогенности, как показывает SDS-PAGE в восстанавливающих или невосстанавливающих условиях с использованием кумасси синего или, предпочтительно, окрашивания серебром. Выделенный ABP в некоторых вариантах осуществления может присутствовать в рекомбинантных клетках, при этом один или более компонентов природного окружения антитела не присутствуют. Обычно выделенное антитело получают с использованием по меньшей мере одной стадии очистки.
[43] (Рекомбинантный) ABP по изобретению, который связывается с FLT3 и/или FLT3-экспрессирующими раковыми клетками, как описано в настоящей заявке, можно использовать в любом подходящем формате рекомбинантного антитела, например, в виде Fv фрагмента, scFv, одновалентного антитела без шарнирной области, миниантитела, Fab фрагмента, Fab' фрагмента, F(ab')2 фрагмента. Рекомбинантный ABP по изобретению может также включать константные домены (области), такие как константная область человеческого IgG, CH1 домен (как в Fab фрагментах) и/или всю Fc область. Альтернативно, ABP по изобретению также может представлять собой полноразмерное (целое) антитело, предпочтительно в биспецифическом формате.
[44] Существует ряд возможных механизмов, посредством которых антитела опосредуют клеточные эффекты, включая антипролиферацию через блокировку необходимых путей роста, внутриклеточную передачу сигналов, ведущую к апоптозу, усиленную даунрегуляцию и/или оборот рецепторов, комплемент-зависимую цитотоксичность (CDC), антитело-зависимую клеточно-опосредованную цитотоксичность (ADCC), антитело-зависимый клеточно-опосредованный фагоцитоз (ADCP) и стимулирование адаптивного иммунного ответа (Cragg et al, 1999, Curr Opin Immunol 11 541-547, Glennie et al, 2000, Immunol Today 21 403-410). Эффективность антител может быть обусловлена комбинацией этих механизмов, и их относительная важность в клинической терапии для онкологии, по-видимому, зависит от рака.
[45] Важность FcγR-опосредованных эффекторных функций для активности некоторых антител была продемонстрирована на мышах (Clynes et al, 1998, Proc Natl Acad Sci USA 95 652-656, Clynes et al, 2000, Nat Med 6 443-446,), а также из наблюдаемых корреляций между клинической эффективностью у людей и их аллотипом высоко(V158)- или низко(F158)-аффинных полиморфных форм FcγRIIIa (Cartron et al , 2002, Blood 99 754-758, Weng & Levy, 2003, Journal of Clinical Oncology, 21 3940-3947). Вместе эти данные предполагают, что антитело, оптимизированное для связывания с определенными FcγR, может лучше опосредовать эффекторные функции и, таким образом, более эффективно разрушать клетки-мишени у пациентов. Таким образом, многообещающим средством для повышения противоопухолевой активности антител является усиление их способности опосредовать цитотоксические эффекторные функции, такие как ADCC, ADCP и CDC. Кроме того, антитела могут опосредовать противоопухолевый механизм через сигналы ингибирования роста или апоптоза, которые могут возникать, когда антитело связывается со своей мишенью на опухолевых клетках. Такая передача сигналов может быть усилена при презентации антител опухолевым клеткам, связанным с иммунными клетками через FcγR. Следовательно, повышенная аффинность антител к FcγR может привести к усилению антипролиферативных эффектов.
[46] Некоторый успех был достигнут в модификации антител с селективно усиленным связыванием с FcγR для обеспечения усиленной эффекторной функции. Конструирование антител для оптимизированной эффекторной функции было достигнуто с использованием аминокислотных модификаций (см., например, патентную заявку США US 2004-0132101 или патентную заявку США 2006-0024298.
[47] ABP по настоящему изобретению способен связываться с человеческим FLT3. Термин "fms-подобная тирозинкиназа 3" или "FLT3" используются в настоящей заявке взаимозаменяемо и включают варианты, изоформы и видовые гомологи FLT3 человека. Белок FLT3 человека имеет номер доступа UniProt P36888 (версия от 9 сентября 2018 г.). Ген FLT3 человека расположен на хромосоме 13 и имеет HGNC номер доступа HGNC:3765 (www.genenames.org - версия HGNC от 9 сентября 2018 г.). FLT3 человека также известен под названиями CD135, FLK2, STK1. Однако в некоторых предпочтительных случаях антитела по изобретению могут не вступать в перекрестную реакцию с FLT3 других видов, кроме человека.
[48] Для определения эпитопа можно использовать стандартные методы картирования эпитопа, известные в данной области. Например, фрагменты (пептиды) FLT3 (например, синтетические пептиды), которые связывают антитело, можно использовать для определения того, связывается ли антитело-кандидат или его антигенсвязывающий фрагмент с одним и тем же эпитопом. Для линейных эпитопов синтезируют перекрывающиеся пептиды определенной длины (например, 8 или более аминокислот). Пептиды могут отклоняться на 1 аминокислоту, так что получают серию пептидов, покрывающих каждый 8-аминокислотный фрагмент последовательности белка FLT3. Меньшее количество пептидов может быть получено с использованием больших отклонений, например, 2 или 3 аминокислоты. Кроме того, можно синтезировать более длинные пептиды (например, 9-, 10- или 11-мерные). Связывание пептидов с антителами или антигенсвязывающими фрагментами можно определить с использованием стандартных методов, включая поверхностный плазмонный резонанс (BIACORE) и ELISA анализы. Для исследования конформационных эпитопов можно использовать более крупные FLT3 фрагменты. Были описаны и могут быть описаны другие методы, в которых используют масс-спектрометрию для определения конформационных эпитопов (см., например, Baerga-Ortiz et al., Protein Science 11:1300-1308, 2002 и цитируемые там ссылки). Другие методы определения эпитопа представлены в стандартных лабораторных справочниках, таких как Unit 6.8 (“Phage Display Selection and Analysis of B-cell Epitopes”) и Unit 9.8 (“Identification of Antigenic Determinants Using Synthetic Peptide Combinatorial Libraries”) Current Protocols in Immunology, Coligan et al., eds., John Wiley & Sons. Эпитопы могут быть подтверждены путем введения точечных мутаций или делеций в известный эпитоп, а затем тестирования связывания с одним или несколькими антителами или антигенсвязывающими фрагментами, чтобы определить, какие мутации уменьшают связывание антител или антигенсвязывающих фрагментов.
[49] ABP по изобретению в некоторых предпочтительных вариантах осуществления включают в их первом антигенсвязывающем домене вариабельную область тяжелой цепи, включающую человеческие каркасные области аллеля IGHV1-46, предпочтительно IGHV1-46*3. В легких цепях ABP по изобретению включают вариабельные области, имеющие каркас IGKV3D-15*01. В некоторых вариантах осуществления антитело по изобретению представляет собой полностью привитое гуманизированное антитело, которое обозначается как V0-V6 и включает последовательности вариабельных доменов тяжелой и легкой цепи SEQ ID NO: 76 и 77 соответственно. Однако одним достижением настоящего изобретения является обеспечение мутантных вариантов гуманизированного анти-FLT3 антитела с улучшенной аффинностью связывания, авидностью и/или активностью для рекрутинга и активации T-клеток и T-клеточно-опосредованной противоопухолевой цитотоксичности. Поэтому в соответствии с настоящим изобретением предпочтительно, чтобы ABP по изобретению в FLT3-специфическом первом антигенсвязывающем домене включал вариабельные области тяжелой цепи с мутацией(мутациями) в одном или нескольких положениях, выбранных из 16, 18, 19, 20, 22, 48, 57, 60, 69, 70, 75, 76, 78, 80, 81, 87 и 108, в соответствии с нумерацией по Кабату. Наиболее предпочтительно мутации представляют собой любую одну, или любую комбинацию, или все из K16G, V18L, K19R, V20L, K22A, M48I, K57T, N60A, M69I, T70S, T75K, S76N, V78L, M80L, E81Q, S87A и T108L, в соответствии с нумерацией по Кабату. Кроме того, ABP по изобретению может также включать, в его FLT3-специфическом первом антигенсвязывающем домене, последовательность вариабельной области легкой цепи, имеющую одну или несколько мутаций, выбранных из 49, 87 и 55, предпочтительно Y49K, I55A и Y87F, где нумерация указана в соответствии с системой Кабата. В некоторых вариантах осуществления ABP по изобретению, в его первом антигенсвязывающем домене, может включать мутации в последовательности вариабельной области тяжелой цепи, и предпочтительно как единственные мутации, K16G, V18L, K19R, V20L, K22A, K57T, N60A, M69I, T70S, T75K, S76N, V78L, M80L, E81Q, S87A и T108L, и мутацию I55A в последовательности вариабельной области легкой цепи, или не включает никаких мутаций в вариабельной области легкой цепи. Или ABP по изобретению может включать K16G, V18L, K19R, V20L, K22A, M69I, T70S, T75K, S76N, V78L, M80L, E81Q, S87A, T108L, предпочтительно как единственные мутации, и отсутствие мутаций в последовательности вариабельной области легкой цепи. Еще один пример относится к ABP, который в анти-FLT3 связывающем домене не включает никаких мутаций в последовательности вариабельной области тяжелой цепи и включает I55A мутации в последовательностм вариабельной области соответствующей легкой цепи. Более предпочтительны ABP по изобретению, включающие в анти-FLT3 первом антигенсвязывающем домене последовательность вариабельной области тяжелой цепи с мутацией в положении 48, предпочтительно 48I, и в последовательности вариабельной области соответствующей легкой цепи мутации 49K и 87F. Нумерация в соответствии с системой Кабата.
[50] Еще один вариант осуществления изобретения относится к ABP, включающим в их первом антигенсвязывающем домене, направленном на FLT3, вариабельную область тяжелой цепи антитела и вариабельную область легкой цепи антитела, где вариабельная область тяжелой цепи включает аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере 70%, 80%, 90%, 95%, 96%, 97%, 98% или 99%, предпочтительно 100%, с аминокислотной последовательностью, выбранной из SEQ ID NO: 15, 17, 19, 21, 23 или 76, или, в каждом случае независимо, необязательно с не более чем десятью, девятью, восемью, семью, шестью, пятью, четырьмя, предпочтительно не более чем тремя, двумя или одной аминокислотной заменой(заменами), инсерцией(инсерциями) или делецией(делециями) по сравнению с этими последовательностями; и/или где вариабельная область легкой цепи включает аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере 70%, 80%, 90%, 95%, 96%, 97%, 98% или 99%, предпочтительно 100%, с аминокислотной последовательностью, выбранной из SEQ ID NO: 16, 18, 20, 22, 24 или 77, или, в каждом случае независимо, необязательно с не более чем десятью, девятью, восемью, семью, шестью, пятью, четырьмя, предпочтительно не более чем тремя, двумя или одной аминокислотной заменой(заменами), инсерцией(инсерциями) или делецией(делециями) по сравнению с этими последовательностями. Где такие аминокислотные замены предпочтительно являются консервативными заменами. Наиболее предпочтительно легкая и тяжелая цепь в этих ABP спарены в соответствии с антителами, раскрытыми в таблице 1 ниже. Кроме того, предпочтительные ABP в соответствии с изобретением включают в вариабельной области тяжелой цепи аминокислотные положения 16, 18, 19, 20, 22, 48, 57, 60, 69, 70, 75, 76, 78, 80, 81, 87 и 108, как представлено в любой из SEQ ID NO: 15, 17, 19, 21 или 23; и/или включают в вариабельной области легкой цепи аминокислотные положения 49, 55 и 87, как представлено в любой из SEQ ID NO: 16, 18, 20, 22 или 24; где нумерация указана в соответствии с системой Кабата.
[51] В некоторых вариантах осуществления изобретения вариабельная область тяжелой цепи ABP включает аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% с аминокислотной последовательностью, представленной в SEQ ID NO: 21, и вариабельная область легкой цепи включает аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере 95% с аминокислотной последовательностью, представленной в SEQ ID NO: 22.
[52] В некоторых вариантах осуществления изобретения вариабельная область тяжелой цепи включает аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% с аминокислотной последовательностью, представленной в SEQ ID NO: 76, и вариабельная область легкой цепи включает аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере 95% с аминокислотной последовательностью, представленной в SEQ ID NO: 77.
[53] В некоторых конкретных вариантах осуществления изобретения предпочтительным является ABP, где вариабельная область тяжелой цепи включает 48I, и где вариабельная область легкой цепи включает 87F, где нумерация указана в соответствии с системой Кабата. Еще более предпочтительным является ABP по изобретению, где вариабельная область легкой цепи дополнительно включает 49K, где нумерация указана в соответствии с системой Кабата.
[54] ABP по изобретению, как объясняется в настоящей заявке, предпочтительно представляют собой биспецифические молекулы, где указанный второй антигенсвязывающий домен связывается с CD3, предпочтительно где указанный второй антигенсвязывающий домен слит с тяжелой цепью первого связывающего домена антитела. Предпочтительно, второй антигенсвязывающий домен включает scFv фрагмент, включающий аминокислотную последовательность, имеющую по меньшей мере 70%, 80%, 90%, 95%, 96%, 97%, 98% или 99%, предпочтительно 100%, идентичность последовательности с последовательностью, выбранной из SEQ ID NO: 14, 25, 26 и 27, или, в каждом случае независимо, необязательно с не более чем десятью, девятью, восемью, семью, шестью, пятью, четырьмя, предпочтительно не более чем тремя, двумя или одной аминокислотной заменой(заменами), инсерцией(инсерциями) или делецией(делециями) по сравнению с такой последовательностью.
[55] ABP в соответствии с изобретением в некоторых вариантах осуществления может представлять собой ABP, включающий по меньшей мере одну тяжелую цепь антитела, имеющую аминокислотную последовательность с по меньшей мере 70%, 80%, 90%, 95%, 96%, 97%, 98% или 99%, предпочтительно 100% идентичностью последовательности с, или имеющую не больше двадцати, пятнадцати, десяти, девяти, восьми, семи, шести, четырех, предпочтительно трех или двух, предпочтительно не более одной аминокислотной замены, делеции или инсерции по сравнению с последовательностью, выбранной из SEQ ID NO: 28, 30, 32, 34, 36, 38, 40, 42, 44, 46, 48, 50, 52, 54, 56, 58, 60, 62, 64, 66, 68, 70, 72, 74 и 78; и/или включающий по меньшей мере одну легкую цепь антитела, имеющую аминокислотную последовательность с по меньшей мере 70%, 80%, 90%, 95%, 96%, 97%, 98% или 99%, предпочтительно 100% идентичностью последовательности с, или имеющую не больше двадцати, пятнадцати, десяти, девяти, восьми, семи, шести, четырех, предпочтительно трех или двух, предпочтительно не более одной аминокислотной замены, делеции или инсерции по сравнению с последовательностью, выбранной из SEQ ID NO: 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75 и 79. В предпочтительных вариантах осуществления ABP по изобретению представляет собой ABP, описанный в этом параграфе, при условии, что легкая и тяжелая цепь спарены, как показано для раскрытых антител в таблице 1 ниже.
[56] ABP по изобретению предпочтительно представляет собой ABP, включающий одну, предпочтительно две тяжелых цепи антитела и одну, предпочтительно две легких цепи антитела, каждая из которых включает аминокислотную последовательность с по меньшей мере 70%, 80%, 90%, 95%, 96%, 97%, 98% или 99%, предпочтительно 100% идентичностью последовательности с, или имеет не больше двадцати, пятнадцати, десяти, девяти, восьми, семи, шести, четырех, предпочтительно трех или двух, предпочтительно не более одной аминокислотной замены, делеции или инсерции по сравнению с:
a. последовательностью, выбранной из SEQ ID NO: 28 для тяжелой цепи и SEQ ID NO: 29 для легкой цепи (антитело V1-V6);
b. последовательностью, выбранной из SEQ ID NO: 30 для тяжелой цепи и SEQ ID NO: 31 для легкой цепи (антитело V2-V6);
c. последовательностью, выбранной из SEQ ID NO: 32 для тяжелой цепи и SEQ ID NO: 33 для легкой цепи (антитело V3-V6);
d. последовательностью, выбранной из SEQ ID NO: 34 для тяжелой цепи и SEQ ID NO: 35 для легкой цепи (антитело V4-V6);
e. последовательностью, выбранной из SEQ ID NO: 36 для тяжелой цепи и SEQ ID NO: 37 для легкой цепи (антитело V5-V6);
f. последовательностью, выбранной из SEQ ID NO: 38 для тяжелой цепи и SEQ ID NO: 39 для легкой цепи (антитело V1-V7);
g. последовательностью, выбранной из SEQ ID NO: 40 для тяжелой цепи и SEQ ID NO: 41 для легкой цепи (антитело V2-V7);
h. последовательностью, выбранной из SEQ ID NO: 42 для тяжелой цепи и SEQ ID NO: 43 для легкой цепи (антитело V3-V7);
i. последовательностью, выбранной из SEQ ID NO: 44 для тяжелой цепи и SEQ ID NO: 45 для легкой цепи (антитело V4-V7);
j. последовательностью, выбранной из SEQ ID NO: 46 для тяжелой цепи и SEQ ID NO: 47 для легкой цепи (антитело V5-V7);
k. последовательностью, выбранной из SEQ ID NO: 48 для тяжелой цепи и SEQ ID NO: 49 для легкой цепи (антитело V1-V8);
l. последовательностью, выбранной из SEQ ID NO: 50 для тяжелой цепи и SEQ ID NO: 51 для легкой цепи (антитело V2-V8);
m. последовательностью, выбранной из SEQ ID NO: 52 для тяжелой цепи и SEQ ID NO: 53 для легкой цепи (антитело V3-V8);
n. последовательностью, выбранной из SEQ ID NO: 54 для тяжелой цепи и SEQ ID NO: 55 для легкой цепи (антитело V4-V8);
o. последовательностью, выбранной из SEQ ID NO: 56 для тяжелой цепи и SEQ ID NO: 57 для легкой цепи (антитело V5-V8);
p. последовательностью, выбранной из SEQ ID NO: 58 для тяжелой цепи и SEQ ID NO: 59 для легкой цепи (антитело V1-V9);
q. последовательностью, выбранной из SEQ ID NO: 60 для тяжелой цепи и SEQ ID NO: 61 для легкой цепи (антитело V2-V9);
r. последовательностью, выбранной из SEQ ID NO: 62 для тяжелой цепи и SEQ ID NO: 63 для легкой цепи (антитело V3-V9);
s. последовательностью, выбранной из SEQ ID NO: 64 для тяжелой цепи и SEQ ID NO: 65 для легкой цепи (антитело V4-V9);
t. последовательностью, выбранной из SEQ ID NO: 66 для тяжелой цепи и SEQ ID NO: 67 для легкой цепи (антитело V5-V9);
u. последовательностью, выбранной из SEQ ID NO: 68 для тяжелой цепи и SEQ ID NO: 69 для легкой цепи (антитело V6-V6);
v. последовательностью, выбранной из SEQ ID NO: 70 для тяжелой цепи и SEQ ID NO: 71 для легкой цепи (антитело V6-V7);
w. последовательностью, выбранной из SEQ ID NO: 72 для тяжелой цепи и SEQ ID NO: 73 для легкой цепи (антитело V6-V8);
x. последовательностью, выбранной из SEQ ID NO: 74 для тяжелой цепи и SEQ ID NO: 75 для легкой цепи (антитело V6-V9).
y. последовательностью, выбранной из SEQ ID NO: 78 для тяжелой цепи и SEQ ID NO: 79 для легкой цепи (антитело V0-V6).
[57] Повсеместно в настоящем раскрытии предпочтительные варианты вариабельных областей антитела обозначаются как “Vx” или “Vx-Vy”. “Vx”, где x может иметь значение 0, 1, 2, 3, 4, 5, 6, 7, 8 или 9, означает вариант вариабельной области, раскрытый в настоящем изобретении в таблице 1, или в разделе Примеры, в частности, описанный в примере 3. В частности, FLT3 антигенсвязывающий домен гуманизированного 4G8 обозначен как Вариант 0 или V0. Термины V0, V1, V2, V3, V4, V5 и V6 могут относиться к вариантам вариабельной области FLT3-связывающего сайта антитела по изобретению. С другой стороны, термины V6, V7, V8 и V9 относятся к определенным вариантам CD3-связывающего сайта антител (биспецифических) по изобретению. Термин “Vx-Vy” используется в настоящей заявке для описания предпочтительных биспецифических FLT3xCD3 ABP по изобретению, где Vx означает вариант анти-FLT3 связывающего сайта, а Vy означает вариант анти-CD3 связывающего сайта. В этом контексте Vx может быть одним из V0, V1, V2, V3, V4, V5 и V6; тогда как Vy может быть одним из V6, V7 V8 или V9. Должно быть понятно, что V6 может использоваться как в контексте варианта анти-FLT3 связывающего сайта, так и варианта анти-CD3 связывающего сайта по изобретению. Использование будет очевидно из контекста. Последовательность вариантов и номенклатура конструкции в целом также будут очевидны из таблицы 1 ниже.
[58] Тяжелая и легкая цепи указанных выше ABP (a.) - (y.) предпочтительно спарены друг с другом. Предпочтительные АВР по изобретению выбирают в соответствии с их способностью индуцировать Т-клеточно-опосредованный киллинг и/или ингибирование роста лейкозных раковых клеток, например, в соответствии с данными, приведенными в разделе Примеры настоящего раскрытия. Например, определенные конструкции, такие как V5-V9, демонстрируют наивысшее комбинированное сродство к FLT3 и CD3. Хотя каждая конструкция, содержащая либо CD3, либо FLT3 антигенсвязывающий домен V5-V9, является предпочтительным ABP в этом отношении, для некоторых применений может потребоваться такое сильное FLT3/CD3 связующее. Однако также антитела, имеющие несколько пониженную аффинность, но, следовательно, лучшую переносимость (гуманизация) или биологическую активность (противораковую активность) также включены в качестве предпочтительных конструкций по изобретению. Поэтому описанные выше ABP a.-х. все являются предпочтительными, в частности, все гуманизированные варианты, не включающие FLT3 (первый) антигенсвязывающий домен V6-V6.
[59] Другой аспект изобретения относится к биспецифическому антигенсвязывающему белку (ABP), который включает первый антигенсвязывающий домен, способный связываться с антигеном fms-подобной тирозинкиназы 3 (FLT3) человека, и второй антигенсвязывающий домен, связывающийся с человеческим антигеном кластера дифференцировки 3 (CD3). Биспецифические ABP, как описано для этого аспекта, в предпочтительных вариантах осуществления могут включать любой из, или комбинацию, вариантов осуществления ABP, описанных выше. ABP, описанный выше, может во всех его вариантах осуществления представлять собой биспецифический ABP, как описано далее.
[60] В некоторых вариантах осуществления предпочтительно, чтобы биспецифический ABP связывался с FLT3 с EC50 меньше чем 10 нМ, предпочтительно меньше чем 9 нМ, более предпочтительно меньше чем 8 нМ, более предпочтительно меньше чем 7 нМ, более предпочтительно меньше чем 6 нМ или меньше чем 5,5 нМ. Альтернативно или дополнительно, биспецифический ABP по изобретению связывает FLT3 с EC50 больше чем 0,5 нМ, более предпочтительно больше чем 1 нМ, более предпочтительно больше чем 1,3 нМ, более предпочтительно больше чем 2 нМ, более предпочтительно больше чем 3 нМ, или 4 нМ, или больше чем 4,5 нМ. Также альтернативно или дополнительно, биспецифический ABP в соответствии с изобретением связывает FLT3 с EC50 меньше чем 10 нМ и больше чем 0,5 нМ, более предпочтительно меньше чем 9 нМ и больше чем 1 нМ, предпочтительно меньше чем 8 нМ и больше чем 1,3 нМ, предпочтительно меньше чем 7 нМ и больше чем 3 нМ, предпочтительно меньше чем 6 нМ и больше чем 4 нМ, предпочтительно меньше чем 5,5 нМ и больше чем 4,5 нМ. EC50 связывания биспецифического ABP с FLT3 имеет значение, определенное в анализе связывания биспецифического ABP с FLT3-положительными клетками методом проточной цитометрии с использованием устройства для сортировки флуоресцентно-активированных клеток (FACS); предпочтительно, где FLT3-положительные клетки представляют собой лейкозные клетки из B-клеток предшественников, предпочтительно NALM-16 клетки (депонированные под номером ACC 680 в DSMZ); и/или предпочтительно, где связывание определяют с использованием флуоресцентно-меченного вторичного антитела; и/или где биспецифический ABP инкубируют с FLT3-положительными клетками приблизительно 30 минут перед проточной цитометрией. В этом варианте осуществления изобретение относится к антителам, в отношении которых к удивлению было обнаружено, что определенная предпочтительная аффинность связывания со связывающей антиген - мишень молекулой может привести к улучшенному терапевтическому эффекту. В этом отношении, как показано в примерах, некоторые антитела, хотя и имеют более низкое сродство к FLT3 по сравнению с другими антителами, обладают значительно улучшенным эффектом опосредования цитотоксичности. В некоторых предпочтительных аспектах и вариантах осуществления предпочтительны антитела, попадающие в такое “окно” аффинности, как раскрыто в настоящей заявке.
[61] В дополнение или альтернативно, биспецифический ABP по изобретению связывает FLT3 с kD меньше чем 50 мкМ, более предпочтительно меньше чем 20 мкМ, более предпочтительно меньше чем 10 мкМ, более предпочтительно меньше чем 5 мкМ, более предпочтительно меньше чем 1 мкМ; и/или связывает FLT3 с kD больше чем 50 нМ, более предпочтительно больше чем 100 нМ, более предпочтительно больше чем 160 нМ, более предпочтительно больше чем 200 нМ, более предпочтительно больше чем 300 нМ. Наиболее предпочтительно биспецифический ABP по изобретению связывается с FLT3 в определенном предпочтительном диапазоне, таком как с kD меньше чем 50 мкМ и больше чем 50 нМ, более предпочтительно меньше чем 20 мкМ и больше чем 100 нМ, более предпочтительно меньше чем 10 мкМ и больше чем 160 нМ, более предпочтительно меньше чем 5 мкМ и больше чем 200 нМ, более предпочтительно меньше чем 1 мкМ и больше чем 300 нМ; где kD имеет значение, измеренное методом поверхностного плазмонного резонанса, например в Анализе Аффинности BIAcore, например, который описан в разделе Примеры.
[62] В другом варианте осуществления биспецифический ABP в соответствии с изобретением связывается с CD3 с EC50 меньше чем 200 нМ, предпочтительно меньше чем 90 нМ, более предпочтительно меньше чем 50 нМ, более предпочтительно меньше чем 20 нМ, более предпочтительно меньше чем 15 нМ, и/или связывается с CD3 с EC50 of больше чем 1 нМ, предпочтительно больше чем 2 нМ, более предпочтительно больше чем 4,1 нМ, более предпочтительно больше чем 6 нМ, более предпочтительно больше чем 8 нМ; и/или В некоторых вариантах осуществления предпочтительны определенные диапазоны аффинности для связывания CD3, такие как ABP, который связывается с CD3 с EC50 меньше чем 200 нМ и больше чем 1 нМ, предпочтительно меньше чем 200 нМ и больше чем 2 нМ, более предпочтительно меньше чем 90 нМ и больше чем 4,1 нМ, более предпочтительно меньше чем 20 нМ и больше чем 6 нМ, более предпочтительно меньше чем 15 нМ и больше чем 8 нМ. EC50 связывания биспецифического ABP с CD3 имеет значение, определенное в анализе связывания биспецифического ABP с CD3-положительными клетками методом проточной цитометрии с использованием устройства для сортировки флуоресцентно-активированных клеток (FACS); предпочтительно, где CD3-положительные клетки представляют собой клетки T-клеточного лейкоза, предпочтительно клетки Jurkat (депонированные под номером ACC 282 в DSMZ); и/или предпочтительно, где связывание определяют с использованием флуоресцентно-меченного вторичного антитела; и/или где биспецифический ABP инкубируют с CD3-положительными клетками приблизительно 30 минут перед проточной цитометрией.
[63] Альтернативно или дополнительно, в некоторых вариантах осуществления ABP по изобретению характеризуются своей способностью убивать или ингибировать пролиферацию раковых клеток, экспрессирующих человеческий FLT3, таких как клетки ALL или AML. Следовательно, предпочтительным в контексте изобретения является биспецифический ABP, описанный в настоящей заявке, который ингибирует пролиферацию и/или жизнеспособность лейкозных мононуклеарных клеток крови пациента, страдающего острым лейкозом, в анализе in vitro по сравнению с независимым контролем, до степени равной или меньше 50%, более предпочтительно равной или меньше 40%, более предпочтительно равной или меньше 30%, наиболее предпочтительно равной или меньше 25%. Примерами таких предпочтительных биспецифических АВР по изобретению являются V3-V6, V3-V8, V3-V9, V4-V6, V4-V8, V4-V9, V5-V6, V5-V8 и V5-V9 и их варианты, раскрытые в настоящей заявке.
[64] Кроме того, некоторые варианты осуществления изобретения относятся к ABP, которые конкурируют с ABP по настоящему изобретению за связывание с FLT3, например для конкурентного ингибирования связывания антитела по изобретению с FLT3. Для определения конкурентного ингибирования можно использовать различные анализы, известные среднему специалисту в данной области. Например, анализы перекрестной конкуренции можно использовать для определения конкурентного ингибирования антителом или его антигенсвязывающим фрагментом связывания FLT3 другим антителом или его антигенсвязывающим фрагментом. К ним относятся клеточные анализы с использованием проточной цитометрии или твердофазный анализ связывания. Также можно использовать другие анализы, которые оценивают способность антител или их антигенсвязывающих фрагментов перекрестно конкурировать за молекулы FLT3, которые не экспрессируются на поверхности клеток, в твердой фазе или в фазе раствора.
[65] ABP в соответствии с изобретением может иметь две цепи: более короткую цепь, которая в некоторых вариантах осуществления может представлять собой легкую цепь, и основную цепь, которая в некоторых вариантах осуществления также может называться тяжелой цепью. ABP обычно представляет собой димер из этих двух цепей.
[66] ABP по изобретению предпочтительно может представлять собой биспецифический ABP. Биспецифический ABP может включать (i) вариабельную область, включающую вариабельный домен тяжелой цепи и вариабельный домен легкой цепи, как определено в любом из предшествующих пунктов, где указанная вариабельная область включает первый антигенсвязывающий домен, способный связываться с человеческим FLT3, и (ii) вариабельную область тяжелой цепи и вариабельную область легкой цепи ABP, включающую второй антигенсвязывающий домен. Должно быть понятно, что сайт связывания для FLT3 предпочтительно представляет собой сайт связывания FLT3-связывающего антитела по изобретению, описанного в настоящей заявке.
[67] “Биспецифический” или “бифункциональный” ABP представляет собой ABP, который имеет два разных эпитоп/антигенсвязывающих домена (или “сайта”), и соответственно имеет специфичности связывания в отношении двух разных целевых эпитопов. Эти два эпитопа могут быть эпитопами одного и того же антигена или, как предпочтительно в настоящем изобретении, разных антигенов, таких как разные антигены FLT3 и CD3.
[68] "Биспецифический ABP" может представлять собой ABP, который связывается с одним антигеном или эпитопом одним из двух или более связывающими плечами, определяемыми первой парой тяжелой и легкой цепи или основной и более короткой/меньшей цепи, и связывается с другим антигеном или эпитопом на втором плече, определяемом второй парой тяжелой и легкой цепи или основной и меньшей цепи. Такой вариант осуществления биспецифического ABP имеет два разных антигенсвязывающих плеча, как по специфичности, так и по последовательностям CDR. Обычно биспецифический ABP является одновалентным для каждого антигена, с которым он связывается, т.е. он связывается только одним плечом с соответствующим антигеном или эпитопом. Однако биспецифические антитела также могут быть димеризованы или мультимеризованы, что предпочтительно в контексте настоящего изобретения. Например, в димерном IgGsc формате, как описано в настоящей заявке, антитело может иметь два сайта связывания для каждого антигена (Фиг. 1). Биспецифическое антитело может представлять собой гибридный ABP, который может иметь первую связывающую область, которая определяется первой вариабельной областью легкой цепи и первой вариабельной областью тяжелой цепи, и вторую связывающую область, которая определяется второй вариабельной областью легкой цепи и второй вариабельной областью тяжелой цепи. Настоящим изобретением предусматриваются, что одна из этих связывающих областей может определяться парой тяжелой/легкой цепи. В контексте настоящего изобретения биспецифический ABP может иметь первый сайт связывания, определяемый вариабельными областями основной цепи и меньшей цепи, и второй, другой сайт связывания, определяемый вариабельной областью scFv фрагмента, включенного в основную цепь ABP.
[69] Способы получения биспецифического ABP известны в данной области техники, например, химическая конъюгация двух разных моноклональных антител или, например, также химическая конъюгация двух фрагментов антител, например, двух Fab фрагментов. Альтернативно, биспецифические ABP получают квадрогибридомным методом, т.е. путем слияния гибридом, продуцирующих исходные антитела. Из-за случайного распределения H и L цепей получают потенциальную смесь десяти различных структур антител, из которых только одна имеет желаемую специфичность связывания.
[70] Биспецифический ABP по изобретению может действовать как моноклональное антитело (mAb) в отношении каждой мишени. В некоторых вариантах осуществления антитело является химерным, гуманизированным или полностью человеческим. Биспецифический ABP, например, может представлять собой биспецифический тандемный одноцепочечный Fv, биспецифический Fab2 или биспецифическое диатело.
[71] На основании доменов, включенных в ABP по изобретению, биспецифический ABP по изобретению может включать Fab фрагмент, который, как правило, может включать шарнирную область, CH2 домен и одноцепочечный Fv фрагмент. Такие биспецифические ABP называются “Fabsc”-ABPs, и они впервые были описаны в Международной патентной заявке WO 2013/092001. Более конкретно, “Fabsc” формат ABP, как используется в настоящем изобретении, типично относится к биспецифическому ABP по изобретению, содержащему Fab фрагмент, который, как правило, включает шарнирную область, которая находится на C-конце Fab фрагмента, который связан с N-концом CH2 домена, C-конец которого, в свою очередь, связан с N-концом scFv фрагмента. Такой “Fabsc” не включает или по существу не включает CH3 домен. В этом контексте, “не включающий” или “ по существу не включающий” означает, что ABP не включает полноразмерный CH3 домен. Это предпочтительно означает, что ABP включает 10 или меньше, предпочтительно 5 или меньше, предпочтительно 3 или даже меньше аминокислот из CH3 домена. Иллюстративный пример для Fabsc формата ABP показан на Фиг. 1A, другой иллюстративный пример для Fabsc формата ABP показан на Фиг. 12. В иллюстративных вариантах осуществления (в этой связи см. также Фиг. 1A, Fabsc ABP по изобретению может включать CH2 домен, который не обладает способностью к димеризации дисульфидными связями, которые образованы цистеиновым остатком в положении последовательности 226 шарнирной области и/или цистеиновым остатком в положении последовательности 229 одного из шарнирных доменов, в соответствии с нумерацией по Кабату [EU-Индекс]. Таким образом, в этих вариантах осуществления, цистеиновые остатки в положении 226в последовательности и/или положении 229 в последовательности либо удалены, либо заменены, например, сериновым остатком. В дополнение или альтернативно, “Fabsc” ABP по изобретению также может иметь “Fc-аттенуированный” CH2 домен (который включает шарнирную область). Это “Fc-аттенуирование” достигается путем делеции и/или замены (мутирования) по меньшей мере одного из выбранных аминокислотных остатков в CH2 домене, которые способны опосредовать связывание с Fc-рецептором. В иллюстративных вариантах осуществления по меньшей мере один аминокислотный остаток шарнирной области или CH2 домена, который способен опосредовать связывание с Fc рецепторами и который отсутствует или мутирован, выбран из группы, состоящей из положения 228, 230, 231, 232, 233, 234, 235, 236, 237, 238, 265, 297, 327 и 330 в последовательности (нумерация положений в последовательности в соответствии с EU-индексом). В иллюстративном примере такой Fc-аттенуированный ABP может содержать по меньшей мере одну мутацию, выбранную из группы, состоящей из делеции аминокислоты 228, делеции аминокислоты 229, делеции аминокислоты 230, делеции аминокислоты 231, делеции аминокислоты 232, делеции аминокислоты 233, замены Glu233→Pro, замены Leu234→Val, делеции аминокислоты 234, замены Leu235→Ala, делеции аминокислоты 235, делеции аминокислоты 236, делеции аминокислоты 237, делеции аминокислоты 238, замены Asp265→Gly, замены Asn297→Gln, замены Ala327→Gln и замены Ala330→Ser (нумерация положений в последовательности в соответствии с EU-индексом, см. в этой связи, например, также Фиг. 1O и Фиг. 1P Международной патентной заявки WO 2013/092001). В случае биспецифических антител, который активируют T-клетки, например, против опухолевых клеток, Fc-аттенуирование может быть желаемым для предотвращения связывания антител с несущими Fc-рецептор клетками, что может привести к нежелательной нецелевой активации T-клеток.
[72] В соответствии с публикацией Coloma and Morrison (Nat Biotechnol 15:159-63, 1997), биспецифический ABP по изобретению также может иметь CH3 домен, как правило, расположенный в направлении к C-концу от CH2 домена. Такая молекула также указана в настоящей заявке как “IgGsc” формат ABP и означает биспецифический ABP по изобретению, содержащий Fab фрагмент, который, как правило, включает шарнирную область, которая находится на C-конце Fab фрагмента, который типично связан с N-концом CH2 домена, C-конец которого, в свою очередь, типично связан с N-концом CH3 домена, C-конец которого, в свою очередь, типично связан с N-концом scFv фрагмента. Иллюстративный пример IgGsc формата ABP показан на Фиг. 1. Такой биспецифический ABP формат предпочтителен в контексте настоящего изобретения.
[73] Общим для форматов антител Fabsc и IgGsc является то, что N-концевая таргетирующая часть состоит из “физиологических” Fab- или Fab2 областей, соответственно, избегая, таким образом, использования одноцепочечных фрагментов в этой части молекулы. Если эти форматы должны использоваться для ограниченной клетками-мишенями T-клеточной активации, можно использовать аттенуирование связывания Fc рецептора (FcR) (если это желательно или необходимо) для предотвращения FcR-опосредованной активации. Это можно осуществить например, путем введения определенных и хорошо известных мутаций в CH2 домен молекулы, как описано выше, а также в Международной патентной заявке WO 2013/092001 и в Armour et al. Eur J Immunol 1999; 29:2613. Соответственно, также IgGsc ABP по изобретению может иметь CH2 домен (включая шарнирную область), в котором по меньшей мере один аминокислотный остаток шарнирной области или CH2 домена, который способен опосредовать связывание с Fc рецепторами, отсутствует или мутирован. Как объясняется выше, этот остаток в CH2 и шарнирной области, соответственно, может быть выбран из группы, состоящей из положения 228, 230, 231, 232, 233, 234, 235, 236, 237, 238, 265, 297, 327 и 330 в последовательности (нумерации положений последовательности в соответствии с EU-индексом). Однако из-за присутствия CH3 домена в молекуле IgGsc две отдельные молекулы будут (спонтанно) гомодимеризоваться через CH3 домен с образованием четырехвалентной молекулы (в этой связи снова см. Фиг. 1B). Таким образом, необходима делеция или мутация цистеиновых остатков в положении 226 в последовательности и/или положении 229 в последовательности шарнирной области. Таким образом, такой тетрамерный IgGsc ABP по изобретению может иметь цистеиновый остаток в положении 226 в последовательности и/или в положении 229 в последовательности одного из соответствующих шарнирных доменов, в соответствии с нумерацией по Кабату [EU-Индекс].
[74] В соответствии с представленным выше раскрытием биспецифических ABP, которые содержат ряд CDR областей, которые опосредуют связывание с FLT3 и/или связывание с лейкозными раковыми клетками, ABP по настоящему изобретению может включать второй сайт связывания, который специфически связывается с рецептором на иммунной клетке, такой как T-клетка или NK клетки. Этот рецептор, присутствующий на иммунной клетке, может представлять собой рецептор, который способен к активации иммунной клетки или стимулированию иммунного ответа иммунной клетки. Индуцированный иммунный ответ предпочтительно может представлять собой цитотоксический иммунный ответ. Такой подходящий рецептор может представлять собой, например, CD3, антигенспецифический T-клеточный рецептор (TCR), CD28, CD16, NKG2D, Ox40, 4-1 BB, CD2, CD5, белок 1 запрограммированной клеточной гибели (PD-1) и CD95. Особенно предпочтительным является ABP, в котором второй сайт связывания связывается с CD3, TCR или CD16. Наиболее предпочтительным является ABP, в котором второй сайт связывания специфически связывается с CD3. Один предпочтительный ABP включает второй сайт связывания, который соответствует антигенсвязывающему сайту анти-CD3 антитела OKT3. Аминокислотные последовательности вариабельного домена тяжелой цепи и вариабельного домена легкой цепи антитела OKT3, например, также описаны в Arakawa et al J. Biochem. 120, 657-662 (1996) и Международной Патентной заявке WO 2015/158868 (см. SEQ ID NOS: 17 и 18 в перечнях последовательностей WO 2015/158868). Другой предпочтительный ABP включает второй сайт связывания, который соответствует антигенсвязывающему сайту анти-CD3 антитела UCHT1. Последовательности VH и VL гуманизированного UCHT1 антитела описаны в Международной патентной заявке WO 2013/092001. Другие примеры CD3-связывающих ABP, которые можно использовать в настоящем изобретении, включают ABP, описанные в Европейском патенте 2155783 B1 или Европейском патенте EP 2155788 B1, которые способны связываться с эпитопом цепи CD3ε человека и Callithrix jacchus, Saguinus oedipus или Saimiri sciureus.
[75] Соответственно, биспецифический ABP по изобретению может представлять собой биспецифический ABP, такой как молекула IgGsc, которая содержит Fab фрагмент и scFv фрагмент, как описано в настоящей заявке. В этой молекуле первый сайт связывания может связываться с FLT3 и может содержаться в Fab (или двухвалентном FLT3 F(ab)2 в контексте формата IgGsc) фрагменте, как описано в настоящей заявке, а второй сайт связывания (который может связываться с иммунным рецептором) может содержаться в scFv фрагменте, таком как scFv, специфически связывающийся с CD3. Альтернативно, первый сайт связывания, который связывается с FLT3, содержится в одноцепочечном Fv фрагменте, а второй сайт связывания (который может связываться с CD3) содержится в Fab фрагменте.
[76] В некоторых вариантах осуществления биспецифический ABP по изобретению сам по себе не активирует иммунную клетку, например Т-клетку, после связывания, например связывания с CD3. Вместо этого, только когда оба сайта связывания, например FLT3-специфическое связывание и CD3-специфический сайт связывания связаны с рецептором на Т-клетке и с FLT3 на раковой клетке-мишени, первый может перекрестно связывать активирующий рецептор, заставляя эффекторные клетки убивать специфическую клетку-мишень. Стандартные функциональные анализы для оценки способности лимфоцитов уничтожать клетки-мишени в присутствии и в отсутствие биспецифического ABP по изобретению могут быть настроены на оценку и/или скрининг способности ABP активировать рецептор, с которым он связывается.
[77] В некоторых вариантах осуществления изобретения биспецифический ABP содержит в качестве второго антигенсвязывающего домена scFv и анти-CD3 антитело, такое как UCHT1 или его варианты, которые, например, раскрыты в настоящей заявке в SEQ ID NO: 14 и 25-27.
[78] В этом контексте следует отметить, что в объеме изобретения ABP может содержать один или более мутантных аминокислотных остатков. Термины "мутантный", "мутант" и "мутация" применительно к нуклеиновой кислоте или полипептиду относятся к замене, делеции или вставке одного или нескольких нуклеотидов или аминокислот, соответственно, по сравнению с "природной" или "исходной" (если указана ссылка) нуклеиновой кислотой или полипептидом, т.е. с эталонной последовательностью, которая может быть взята для определения дикого типа. Например, вариабельные домены ABP по изобретению, полученные путем множественных мутационных изменений исходной молекулы 4G8 и описанные в настоящей заявке, могут быть взяты в качестве исходной последовательности.
[79] В этом отношении следует понимать, что термин "положение", когда он используется в соответствии с настоящим изобретением, означает положение аминокислоты в аминокислотной последовательности, описанной в настоящей заявке. Это положение может быть указано относительно похожей нативной последовательности, например последовательности природного IgG домена или цепи. Термин "соответствующий" в контексте настоящей заявки также означает, что положение не обязательно, или не только, определяется числом предшествующих нуклеотидов/аминокислот. Таким образом, положение данной аминокислоты в соответствии с настоящим изобретением, которая может быть заменена, может варьировать из-за делеции или добавления аминокислот в другом месте цепи антитела.
[80] Таким образом, под "соответствующим положением" в соответствии с настоящим изобретением следует понимать, что аминокислоты могут различаться по указанному количеству, но все же могут иметь аналогичные смежные аминокислоты. Указанные аминокислоты, которые могут быть заменены, удалены или добавлены, также охватываются термином "соответствующее положение". Чтобы определить, соответствует ли аминокислотный остаток в данной аминокислотной последовательности определенному положению в аминокислотной последовательности природного домена или цепи иммуноглобулина, специалист может использовать средства и методы, хорошо известные в данной области, например, выравнивания вручную или при помощи компьютерных программ, таких как BLAST2.0, что означает Basic Local Alignment Search Tool или ClustalW, или любой другой подходящей программы, которая подходит для выравниваний последовательностей.
[81] В некоторых вариантах осуществления замена (или замещение) представляет собой консервативную замену. Консервативные замены, как правило, представляют собой следующие замены, перечисленные в соответствии с аминокислотами, подлежащими мутации, за каждой следует одна или несколько замен, которые можно считать консервативными: Ala → Gly, Ser, Val; Arg → Lys; Asn → Gln, His; Asp → Glu; Cys → Ser; Gln → Asn; Glu → Asp; Gly → Ala; His → Arg, Asn, Gln; Ile → Leu, Val; Leu → Ile, Val; Lys → Arg, Gln, Glu; Met → Leu, Tyr, Ile; Phe → Met, Leu, Tyr; Ser → Thr; Thr → Ser; Trp → Tyr; Tyr → Trp, Phe; Val → Ile, Leu. Другие замены также допустимы и могут быть определены эмпирически или в соответствии с другими известными консервативными или не консервативными заменами. Для лучшего ориентирования, каждая из следующих восьми групп содержит аминокислоты, которые, как правило, можно рассматривтаь как определяющие консервативные замены друг для друга:
- Аланин (Ala), Глицин (Gly);
- Аспарагиновая кислота (Asp), Глутаминовая кислота (Glu);
- Аспарагин (Asn), Глутамин (Gln);
- Аргинин (Arg), Лизин (Lys);
- Изолейцин (Ile), Лейцин (Leu), Метионин (Met), Валин (Val);
- Фенилаланин (Phe), Тирозин (Tyr), Триптофан (Trp);
- Серин (Ser), Треонин (Thr); и
- Цистеин (Cys), Метионин (Met)
[82] Если такие замены приводят к изменению биологической активности, тогда можно ввести более существенные изменения, такие как следующие или которые дополнительно описаны ниже в связи с классами аминокислот, и скринировать продукты на желаемую характеристику. Примерами таких более существенных изменений являются: Ala → Leu, Ile; Arg → Gln; Asn → Asp, Lys, Arg, His; Asp → Asn; Cys → Ala; Gln → Glu; Glu → Gln; His → Lys; Ile → Met, Ala, Phe; Leu → Ala, Met, Норлейцин; Lys → Asn; Met → Phe; Phe → Val, Ile, Ala; Trp → Phe; Tyr → Thr, Ser; Val → Met, Phe, Ala.
[83] В некоторых вариантах осуществления ABP в соответствии с изобретением включает один или более аминокислотных остатков, включая два, три, четыре, пять, шесть, семь, восемь, девять, десять, одиннадцать, двенадцать, тринадцать, четырнадцать, пятнадцать, шестнадцать, семнадцать или восемнадцать аминокислотных остатков, которые мутированы для предотвращения димеризации через цистеиновые остатки или для модуляции Fc-функции (см. выше). В некоторых из этих вариантов осуществления один или более аминокислотных остатков CH2 домена и/или шарнирной области, который способен опосредовать связывание с Fc рецепторами, мутированы. Если они присутствуют, один или более аминокислотных остатков, способные опосредовать связывание с Fc рецепторами, могут представлять собой аминокислотные остатки, которые способны активировать антитело-зависимую клеточную цитотоксичность (ADCC) или комплемент-опосредованную цитотоксичность (CDC). В некоторых вариантах осуществления соответствующий аминокислотный остаток, способный опосредовать связывание с Fc рецепторами, заменен другой аминокислотой, как правило, при сравнении последовательности с последовательностью соответствующего природного домена в иммуноглобулине, таком как IgG. В некоторых вариантах осуществления такой аминокислотный остаток, способный опосредовать связывание с Fc рецепторами, делетирован, как правило, по сравнению с последовательностью соответствующего природного домена в иммуноглобулине, таком как IgG.
[84] В некоторых вариантах осуществления один или более мутантных, например, замененных или делетированных, аминокислотных остатков представляет/представляют собой аминокислоту, находящуюся в одном из положений 226, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 265, 297, 327 и 330. Здесь так же используемая нумерация аминокислот соответствует положениям в последовательности в соответствии с нумерациией Кабата [EU-Индекс]. Соответствующая делеция аминокислоты, например, может представлять собой делецию аминокислоты 228, обычно пролина в IgG, делецию аминокислоты 229, обычно цистеина в IgG, делецию аминокислоты 230, обычно пролина в IgG, делецию аминокислоты 231, обычно аланина в IgG, делецию аминокислоты 232, обычно пролина в IgG, делецию аминокислоты 233, обычно глутаминовой кислоты в IgG, делецию аминокислоты 234, обычно лейцина в IgG, делецию аминокислоты 235, обычно лейцина в IgG, делецию аминокислоты 236, обычно глицина в IgG, делецию аминокислоты 237, обычно глицина в IgG, делецию аминокислоты 238, обычно пролина в IgG, и делецию аминокислоты 265, обычно аспарагиновой кислоты в IgG. Соответствующая замена аминокислоты, например, может представлять собой замену аминокислоты 226, обычно цистеина в IgG, замену аминокислоты 228, обычно пролина в IgG, замену аминокислоты 229, обычно цистеина в IgG, замену аминокислоты 230, обычно пролина в IgG, замену аминокислоты 231, обычно аланина в IgG, замену аминокислоты 232, обычно пролина в IgG, замену аминокислоты 233, обычно глутаминовой кислоты в IgG, замену аминокислоты 234, обычно лейцина в IgG, замену аминокислоты 235, обычно лейцина в IgG, замену аминокислоты 265, обычно аспарагиновой кислоты в IgG, замену аминокислоты 297, обычно аспарагина в IgG, замену аминокислоты 327, обычно аланина в IgG, и замену аминокислоты 330, обычно аланина в IgG. Соответствующая замена может представлять собой одну из замены Cys226→Ser, замены Cys229→Ser, замены Glu233→Pro, замены Leu234→Val, замены Leu235→Ala, замены Asp265→Gly, замены Asn297→Gln, замены Ala327→Gln, замены Ala327→Gly и замены Ala330→Ser. Как можно видеть из представленного выше, в некоторых вариантах осуществления один или два цистеиновых остатка в положенииях 226 и 229 в шарнирной области заменяются другой аминокислотой, например сериновым остатком. Таким образом, образование дисульфидной связи с другой основной цепью можно предотвратить. Кроме того, и как также объясняется ниже, делеция и/или замена (мутирование) выбранных аминокислотных остатков в CH2 домене, который способен опосредовать связывание с Fc-рецепторами, может привести к ABP по изобретению, имеющему меньшую или вообще никакой активности, что касается антитело-зависимой клеточно-опосредованной цитотоксичности и фиксации комплемента.
[85] Другой тип аминокислотного варианта антитела изменяет исходный паттерн гликозилирования (если таковой имеется) ABP. Под изменением подразумевается делеция одного или нескольких углеводных фрагментов, присутствующих в антителе, и/или добавление одного или нескольких сайтов гликозилирования, которые отсутствуют в антителе. Гликозилирование антител обычно является либо N-связанным, либо O-связанным. N-связанный относится к присоединению углеводного фрагмента к боковой цепи аспарагинового остатка. Трипептидные последовательности аспарагин-X-серин и аспарагин-X-треонин, где X представляет собой любую аминокислоту, кроме пролина, представляют собой последовательности распознавания для ферментативного присоединения углеводного фрагмента к боковой цепи аспарагина. Таким образом, присутствие любой из этих трипептидных последовательностей в полипептиде создает потенциальный сайт гликозилирования. О-связанное гликозилирование относится к присоединению одного из сахаров N-ацетилгалактозамина, галактозы или ксилозы к гидроксиаминокислоте, чаще всего к серину или треонину, хотя также можно использовать 5-гидроксипролин или 5-гидроксилизин. Добавление сайтов гликозилирования к антителу обычно осуществляют путем изменения аминокислотной последовательности так, чтобы она содержала одну или несколько из описанных выше трипептидных последовательностей (для сайтов N-связанного гликозилирования). Изменение также можно осуществить путем добавления или замены одним или несколькими сериновыми или треониновыми остатками в последовательности исходного антитела (для сайтов O-связанного гликозилирования).
[86] В контексте настоящего изобретения в некоторых вариантах осуществления часть основной цепи ABP по настоящему изобретению, которая представляет Fc-область иммуноглобулина, обычно инертна или по меньшей мере практически не влияет на связывание с Fc-рецепторами. Как было сказано, это достигается удалением и/или заменой (мутацией) по меньшей мере одного из выбранных аминокислотных остатков в домене CH2, которые способны опосредовать связывание с Fc-рецептором. Такие молекулы также указаны в настоящей заявке как “Fc-аттенуированные” ABP или “Fcko” ABP. Часть цепи антитела в соответствии с изобретением, которую можно считать как представляющую часть Fc фрагмента, т.е. домен CH2 и, если он присутствует, домен CH3, таким образом, может определять “каркас”, не обеспечивая конкретной биологической функции, например эффекторной функции. Однако в настоящем изобретении было обнаружено, что этот каркас может обеспечить значительные преимущества с точки зрения очистки, эффективности производства и/или стабильности ABP по настоящему изобретению по сравнению с известными ABP.
[87] В некоторых вариантах осуществления распознавание, и соответственно, связывание этой Fc-соответствующей части с данным рецептором Fc примерно в 2 раза, примерно в 5 раз, примерно в 8 раз, примерно в 10 раз, примерно в 12 раз, примерно в 15 раз, примерно в 20 раз или еще ниже, чем у Fc области природного иммуноглобулина. В некоторых вариантах осуществления эта Fc-соответствующая часть полностью лишена своей способности связываться с рецепторами Fc. Связывание антитела с рецепторами Fc, включая определение константы диссоциации, может легко определить квалифицированный специалист с использованием стандартных методов, таких как поверхностный плазмонный резонанс, например используя BiacoreTM измерение. Аналогичным образом можно использовать любой другой метод измерения биомолекулярного связывания, который, например, может основываться на спектроскопических, фотохимических, фотометрических или радиологических средствах. Примерами соответствующих методов детекции являются флуоресцентная корреляционная спектроскопия, фотохимическое сшивание и использование фотоактивных или радиоактивных меток, соответственно. Некоторые из этих методов могут включать дополнительные методы разделения, такие как электрофорез или ВЭЖХ.
[88] При необходимости с этой целью можно осуществить замену или удаление аминокислотных остатков, как объяснено выше. Подходящие мутации можно взять из Armor et al. (Eur. J. Immunol. [1999] 29, 2613-2624), например. Дополнительные подходящие положения для мутаций в последовательности цепи антитела могут быть взяты из данных кристаллической структуры, опубликованных для комплекса между FcγRIII и Fc-фрагментом человеческого IgG1 (Sondermann et al., Nature [2000] 406, 267-273). Помимо измерения аффинности связывания, как описано выше, для оценки уровня “аттенуации Fc” или потери аффинности связывания, также можно функционально оценить способность (отсутствие) опосредовать связывание с Fc-рецептором. В случае ABP, которые связывают CD3 как одну мишень, можно, например, оценить связывание по митогенности таких CD3-связывающих ABP на клетках. Митогенность опосредуется связыванием антител к CD3 с Fc-рецепторами на дополнительных клетках, таких как моноциты. Если ABP по изобретению, имеющее один сайт связывания для CD3, не проявляет какого-либо митогенного эффекта, тогда как исходное моноклональное анти-CD3 антитело, которое имеет функциональную Fc часть, индуцирует сильный митоз в Т-клетках, очевидно, что из-за отсутствия митоза ABP по настоящему изобретению не обладает способностью связываться с Fc и, таким образом, может рассматриваться как молекула с “Fc-нокаутом”. Иллюстративные примеры метода оценки анти-CD3-опосредованной митогенности описаны Davis, Vida & Lipsky (J.Immunol (1986) 137, 3758) и Ceuppens, JL, & van Vaeck, F. (см. J.Immunol. (1987) 139, 4067, или Cell. Immunol. (1989) 118, 136). Дополнительные иллюстративные подходящие примеры анализа для оценки митогенности антитела описаны Rosenthal-Allieri et al. (Rosenthal-Allieri MA, Ticcioni M, Deckert M, Breittmeyer JP, Rochet N, Rouleaux M и Senik A, Bernerd A, Cell Immunol. 1995 163 (1):88-95) и Grosse-Hovest et al. (Grosse-Hovest L, Hartlapp I., Marwan W., Brem G, Rammensee H-G and Jung G, Eur J Immunol. [2003] May;33(5):1334-1340). Кроме того, отсутствие связывания Fc можно оценить по способности ABP по изобретению опосредовать одну или несколько хорошо известных эффекторных функций Fc части.
[89] Как отмечалось выше, замены или делеции цистеиновых остатков можно осуществить для того, чтобы ввести или удалить одну или несколько дисульфидных связей, включая введение или удаление потенциальной или ранее существовавшей дисульфидной связи. Таким образом, связь между основной цепью и цепью с меньшей массой/меньшей длиной ABP в соответствии с изобретением может контролироваться, включая установление, усиление или отмену. Путем введения или удаления одного или нескольких цистеиновых остатков можно ввести или удалить дисульфидный мостик. В качестве иллюстративного примера, тетрамерный ABP в соответствии с изобретением обычно имеет одну или несколько дисульфидных связей, которые связывают два димерных ABP. Одна такая дисульфидная связь обычно определяется цистеином в основной цепи первого димерного ABP и цистеином в шарнирной области второго димерного ABP. В связи с этим, в некоторых вариантах осуществления антитело по изобретению может включать аминокислотную замену нативного цистеинового остатка в положениях 226 и/или 229 относительно последовательности иммуноглобулина IgG человека, в соответствии с нумерацией по Кабату [EU-Индекс], другим аминокислотным остатком.
[90] Замены или делеции аминокислотных остатков, таких как аргининовый, аспарагиновый, сериновый, треониновый или тирозиновый остатки, также можно осуществить для модификации паттерна гликозилирования антитела. В качестве иллюстративного примера, молекула IgG имеет единственный N-связанный двухантенарный углевод по Asn297 домена CH2. Что касается IgG либо из сыворотки, либо из полученных ex vivo гибридом или сконструированных клеток, IgG являются гетерогенными по отношению к связанному с Asn297 углеводу. Что касается человеческого IgG, сердцевинный олигосахарид обычно состоит из GlcNAc2Man3GlcNAc с разными количествами внешних остатков.
[91] Как указано, помимо связывания антигенов/эпитопов иммуноглобулин, как известно, обладает дополнительными "эффекторными функциями", биологической активностью, обусловленной Fc областью (Fc областью нативной последовательности или Fc областью варианта аминокислотной последовательности) иммуноглобулина, и варьирует в зависимости от изотипа иммуноглобулина. Примеры эффекторных функций антитела включают: связывание Clq и комплемент-зависимую цитотоксичность (CDC); связывание с рецептором Fc; антитело-зависимую клеточно-опосредованную цитотоксичность (ADCC); фагоцитоз; даун-регуляцию рецепторов клеточной поверхности (например, В-клеточных рецепторов); и В-клеточную активацию. Осуществление эффекторных функций антитела обычно включает рекрутирование эффекторных клеток. Некоторые эффекторные функции иммуноглобулина опосредуются Fc рецепторами (FcR), которые связывают Fc-область антитела. FcR определяются по их специфичности к изотипам иммуноглобулинов; Fc рецепторы для IgG антител обозначаются как FcγR, для IgE как FcεR, для IgA как FcαR и т.д. Любая из этих эффекторных функций (или потеря таких эффекторных функций), такая как CDC или ADCC, может использоваться для оценки отсутствия способности ABP по настоящему изобретению к связыванию с Fc.
[92] В этом контексте следует отметить, что термин "Fc рецептор" или "FcR" означает рецептор, обычно белок, который способен связываться с Fc областью антитела. Рецепторы Fc находятся на поверхности определенных клеток иммунной системы организма, например природных киллерных клеток, макрофагов, нейтрофилов и тучных клеток. Рецепторы Fc in vivo связываются с иммуноглобулинами, которые иммобилизуются на инфицированных клетках или присутствуют на инвазивных патогенах. Их активность стимулирует фагоцитарные или цитотоксические клетки к уничтожению микробов или инфицированных клеток путем антитело-опосредованного фагоцитоза или антитело-зависимой клеточно-опосредованной цитотоксичности. Некоторые вирусы, такие как флавивирусы, используют рецепторы Fc, чтобы помочь им инфицировать клетки посредством механизма, известного как антитело-зависимое усиление инфекции. Обзор FcR см. в Ravetch and Kinet, Annu. Rev. Immunol. 9: 457-92 (1991); Capel et al., Immunomethods 4: 25-34 (1994); и de Haas et al., J. Lab. Clin. Med. 126: 330-41 (1995).
[93] "Комплемент-зависимая цитотоксичность" или "CDC" относится к лизису клетки-мишени в присутствии комплемента. Активация классического пути комплемента инициируется связыванием первого компонента системы комплемента (Clq) с антителами (соответствующего подкласса), которые связаны с их родственным антигеном. Для оценки активации комплемента можно осуществить анализ CDC, например, как описано в Gazzano-Santoro et al., J. Immunol. Методы 202: 163 (1997).
[94] Термин "система комплемента" используется в данной области для обозначения ряда небольших белков, называемых факторами комплемента, обнаруженных в крови, обычно циркулирующих в виде неактивных предшественников (про-протеинов). Термин относится к способности этой неизменяемой и неадаптируемой системы "дополнять" способность антител и фагоцитарных клеток выводить из организма патогены, такие как бактерии, а также комплексы антиген-антитело. Примером факторов комплемента является комплекс C1, который включает C1q и две сериновые протазы, C1r и C1s. Комплекс C1 является компонентом пути CDC. C1q представляет собой шестивалентную молекулу с молекулярной массой приблизительно 460000 и структурой, подобной букету тюльпанов, в которой шесть коллагеновых "стеблей" соединены с шестью областями типа шаровидной головки. Чтобы активировать каскад комплемента, C1q должен связываться как минимум с двумя молекулами IgG1, IgG2 или IgG3.
[95] "Антитело-зависимая клеточная цитотоксичность" или ADCC относится к форме цитотоксичности, при которой молекулы иммуноглобулина, связанные с рецепторами Fc (FcR), присутствующие на определенных цитотоксических клетках, таких как природные киллерные клетки (NK), нейтрофилы и макрофаги, обеспечивают возможность специфического связывания этих цитотоксических эффекторных клеток с антиген-несущей клеткой-мишенью и последующего уничтожения этой клетки-мишени цитотоксинами. Антитела "вооружают" цитотоксические клетки и необходимы для уничтожения клетки-мишени посредством этого механизма. Первичные клетки для опосредования ADCC, NK-клетки, экспрессируют только FcγRIII, тогда как моноциты экспрессируют FcγRI, FcγRlI и FcγRIII. Экспрессия FcR на гемопоэтических клетках показана в Таблице 3 на стр. 464 Ravetch and Kinet, Annu. Rev. Immunol. 9: 457-92 (1991). Для оценки ADCC активности представляющей интерес молекулы можно осуществить анализ ADCC in vitro, такой как описанный в патентах США №№5500362 или 5821337. Подходящие эффекторные клетки для таких анализов включают, но не ограничиваются этим, мононуклеарные клетки периферической крови (PBMC) и природные киллерные клетки (NK). В некоторых вариантах осуществления ADCC активность представляющей интерес молекулы может быть оценена in vivo, например, на животной модели, такой, которая описана в Clynes et al., PNAS USA 95: 652-656 (1998).
[96] ABP по изобретению может быть получен с использованием любой известной и хорошо зарекомендовавшей себя системы экспрессии и технологии культивирования рекомбинантных клеток, например, путем экспрессии в бактериальных хозяевах (прокариотических системах) или эукариотических системах, таких как дрожжи, грибы, клетки насекомых или клетки млекопитающих. Например, ABP по изобретению при использовании в формате "IgGsc" можно (конечно) получить, как описано Coloma and Morrison (Nat Biotechnol 15:159-63, 1997) или как описано в разделе "Примеры" в настоящей заявке. Аналогичным образом, ABP по изобретению, используемые в формате "Fabsc", можно получить, как описано в Международной патентной заявке WO 2013/092001 или как описано в настоящей заявке в разделе "Примеры". ABP по настоящему изобретению также могут продуцироваться в трансгенных организмах, таких как коза, растение или трансгенная мышь XENOMOUSE, сконструированный штамм мышей, который имеет большие фрагменты локусов иммуноглобулина человека и является дефицитным по продукции мышиного антитела. Антитело также может быть получено путем химического синтеза.
[97] Для получения рекомбинантного ABP по изобретению обычно выделяют полинуклеотид, кодирующий антитело, и вставляют в реплицируемый вектор, такой как плазмида, для дальнейшего клонирования (амплификации) или экспрессии. Иллюстративным примером подходящей системы экспрессии является система глутаматсинтетазы (например, продаваемая Lonza Biologics), при этом клеткой-хозяином является, например, CHO или NS0. Полинуклеотид, кодирующий антитело, легко выделить и секвенировать с использованием обычных процедур. Векторы, которые можно использовать, включают плазмиду, вирус, фаг, транспозоны, минихромсомы, из которых типичным вариантом осуществления являются плазмиды. Обычно такие векторы дополнительно включают сигнальную последовательность, точку начала репликации, один или более маркерных генов, энхансерный элемент, промотор и последовательности терминации транскрипции, функционально связанные с полинуклеотидом легкой и/или тяжелой цепи для облегчения экспрессии. Полинуклеотиды, кодирующие легкую и тяжелую цепи, могут быть вставлены в отдельные векторы и трансфицированы в одну и ту же клетку-хозяин, или, при желании, тяжелая цепь и легкая цепь могут быть вставлены в один и тот же вектор для трансфекции в клетку-хозяин. Обе цепи могут находиться, например, под контролем дицистронного оперона и экспрессироваться, приводя к получению функционального и правильно уложенного ABP, как описано в Skerra, A. (1994) Use of the tetracycline promoter for the tightly regulated production of a murine antibody fragment in Escherichia coli, Gene 151, 131-135, или Skerra, A. (1994) A general vector, pASK84, for cloning, bacterial production, and single-step purification of antibody Fab fragments, Gene 141, 79-8. Таким образом, в соответствии с одним аспектом, настоящее изобретение относится к способу конструирования вектора, кодирующего легкую и/или тяжелую цепи антитела или его антигенсвязывающего фрагмента по изобретению, который включает встраивание в вектор полинуклеотида, кодирующего легкую цепь и/или тяжелую цепь ABP по изобретению.
[98] При использовании рекомбинантных методов ABP может продуцироваться внутриклеточно, в периплазматическом пространстве, или непосредственно секретироваться в среду (см. Также Skerra 1994, выше). Если антитело продуцируется внутриклеточно, на первой стадии частицы дебриса, либо клетки-хозяева, либо лизированные фрагменты, удаляют, например, центрифугированием или ультрафильтрацией. Carter et al., Bio/Technology 10: 163-167 (1992) описывают процедуру выделения антител, которые секретируются в периплазматическое пространство E. coli. Антитело также может продуцироваться в любой окислительной среде. Такая окислительная среда может быть обеспечена периплазмой грамотрицательных бактерий, таких как E. coli, во внеклеточной среде грамположительных бактерий или в просвете эндоплазматического ретикулума эукариотических клеток (включая клетки животных, такие как клетки насекомых или млекопитающих) и обычно способствует образованию структурных дисульфидных связей. Однако также возможно продуцировать ABP по изобретению в цитозоле клетки-хозяина, такой как E. coli. В этом случае полипептид может быть либо непосредственно получен в растворимом и свернутом состоянии, либо выделен в форме телец включения с последующей ренатурацией in vitro. Еще одним вариантом является использование специфических штаммов-хозяев, имеющих окислительную внутриклеточную среду, которая, таким образом, может способствовать образованию дисульфидных связей в цитозоле (Venturi M, Seifert C, Hunte C. (2002) “High level production of functional antibody Fab fragments in an oxidizing bacterial cytoplasm.” J. Mol. Biol. 315, 1-8).
[99] ABP, продуцируемый клетками, может быть очищен с использованием любого общепринятого метода очистки, например, хроматографии на гидроксилапатите, гель-электрофореза, диализа и аффинной хроматографии, при этом аффинная хроматография является одним из предпочтительных методов очистки. ABP могут быть очищены посредством аффинной очистки с белками/лигандами, которые специфически и обратимо связывают константные домены, такие как домены CH1 или CL. Примерами таких белков являются иммуноглобулин-связывающие бактериальные белки, такие как белок A, белок G, белок A/G или белок L, где связывание белка L ограничено ABP, которые содержат легкие цепи каппа. Альтернативным методом очистки антител с κ-легкими цепями является использование связанных с гранулами анти-каппа антител (KappaSelect). Пригодность белка А в качестве аффинного лиганда зависит от вида и изотипа любого Fc-домена иммуноглобулина, присутствующего в антителе. Белок А можно использовать для очистки антител (Lindmark et al., J. Immunol. Meth. 62: 1-13 (1983)). Белок G рекомендован для всех мышиных изотипов и для человеческого гамма-3 (Guss et al., EMBO J. 5: 15671575 (1986)). Выбор метода очистки, который используется для конкретного ABP по изобретению, находится в компетенции специалиста со средней квалификацией в данной области.
[100] Также возможно снабдить одну из цепей ABP по настоящему изобретению одной или несколькими аффинными метками. Аффинные метки, такие как Strep-tag® или Strep-tag® II (Schmidt, TGM et al. (1996) J. Mol. Biol. 255, 753-766), myc-tag, FLAG TM-tag, His6-tag или HA-tag, обеспечивают легкую детекцию, а также простой способ очистки рекомбинантного ABP.
[101] Что касается нуклеиновых кислот по изобретению, молекула нуклеиновой кислоты, кодирующая одну или несколько цепей антитела по изобретению, может быть любой нуклеиновой кислотой в любой возможной конфигурации, такой как одноцепочечная, двухцепочечная или их комбинация. Нуклеиновые кислоты включают, например, молекулы ДНК, молекулы РНК, аналоги ДНК или РНК, полученные с использованием нуклеотидных аналогов или с использованием химии нуклеиновых кислот, заблокированные молекулы нуклеиновых кислот (LNA) и молекулы белковых нуклеиновых кислот (PNA). ДНК или РНК могут иметь геномное или синтетическое происхождение и могут быть одноцепочечными или двухцепочечными. Такая нуклеиновая кислота может представлять собой, например, мРНК, кРНК, синтетическую РНК, геномную ДНК, кДНК, синтетическую ДНК, сополимер ДНК и РНК, олигонуклеотиды и т.д. Соответствующая нуклеиновая кислота может, кроме того, содержать неприродные нуклеотидные аналоги и/или быть связана с аффинным тэгом или меткой.
[102] В некоторых вариантах осуществления нуклеиновокислотная последовательность, кодирующая цепь, такую как основная цепь и/или меньшая цепь антитела в соответствии с изобретением, включена в вектор, такой как плазмида. Если замена или делеция должны быть включены в цепь антитела, по сравнению с природным доменом или областью антитела, кодирующую последовательность соответствующего нативного домена/области, например включенную в последовательность иммуноглобулина, можно использовать в качестве начальной точки для мутагенеза. Для мутагенеза выбранных аминокислотных положений специалист в данной области техники имеет в своем распоряжении различные установленные стандартные методы сайт-направленного мутагенеза. Обычно используемый метод представляет собой введение мутаций посредством ПЦР (полимеразной цепной реакции) с использованием смесей синтетических олигонуклеотидов, которые содержат композицию вырожденных оснований в желаемых положениях последовательности. Например, использование кодона NNK или NNS (где N=аденин, гуанин или цитозин или тимин; K=гуанин или тимин; S=аденин или цитозин) позволяет включать все 20 аминокислот плюс янтарный стоп-кодон во время мутагенеза, тогда как кодон VVS ограничивает количество возможных включенных аминокислот до 12, поскольку он исключает аминокислоты Cys, Ile, Leu, Met, Phe, Trp, Tyr, Val от включения в выбранное положение полипептидной последовательности; использование кодона NMS (где M=аденин или цитозин), например, ограничивает количество возможных аминокислот до 11 в выбранном положении в последовательности, поскольку он исключает аминокислоты Arg, Cys, Gly, Ile, Leu, Met, Phe , Trp, Val от включения в выбранное положение в последовательности. В этом отношении следует отметить, что кодоны для других аминокислот (помимо обычных 20 встречающихся в природе аминокислот), таких как селеноцистеин или пирролизин, также могут быть включены в нуклеиновую кислоту ABP. Также возможно, как описано Wang, L., et al. (2001) Science 292, 498-500, или Wang, L., and Schultz, P.G. (2002) Chem. Comm. 1, 1-11, использовать "искусственные" кодоны, такие как UAG, которые обычно распознаются как стоп-кодоны, для вставки других необычных аминокислот, например о-метил-L-тирозина или пара-аминофенилаланина.
[103] Использование нуклеотидных строительных блоков с пониженной специфичностью пары оснований, таких как, например, инозин, 8-оксо-2'-дезоксигуанозин или 6(2-дезокси-β-D-рибофуранозил)-3,4-дигидро-8H-пиримин-до-1,2-оксазин-7-он (Zaccolo et al. (1996) J. Mol. Biol. 255, 589-603), представляет собой еще один вариант введения мутаций в выбранный сегмент последовательности. Еще одной возможностью является так называемый триплет-мутагенез. В этом методе используются смеси различных нуклеотидных триплетов, каждый из которых кодирует одну аминокислоту, для включения в кодирующую последовательность ( et al., 1994 Nucleic Acids Res 22, 5600-5607).
et al., 1994 Nucleic Acids Res 22, 5600-5607).
[104] Молекулу нуклеиновой кислоты, кодирующую цепь, такую как основная цепь и/или меньшая цепь антитела в соответствии с изобретением, можно экспрессировать с использованием любой подходящей системы экспрессии, например, в подходящей клетке-хозяине или в бесклеточной системе. Полученный ABP может быть обогащен посредством селекции и/или выделения. Предпочтительно нуклеиновые кислоты по изобретению представлены в контексте генетических конструкций, таких как векторы/плазмиды.
[105] Также изобретение относится к системе нуклеиновых кислот или конструкциям, включающим такую нуклеиновую кислоту по изобретению, где система по изобретению включает по меньшей мере две нуклеиновых кислоты по изобретению, каждая из которых кодирует один мономер ABP по изобретению, например, одна нуклеиновая кислота, кодирующая последовательность тяжелой цепи, и вторая нуклеиновая кислота, кодирующая последовательность легкой цепи.
[106] В некоторых вариантах осуществления полипептиды ABP по изобретению могут кодироваться нуклеиновыми кислотами для экспрессии in vivo или in vitro. Таким образом, в некоторых вариантах осуществления обеспечивается выделенная нуклеиновая кислота, кодирующая ABP по изобретению. В некоторых вариантах осуществления нуклеиновая кислота кодирует одну часть или мономер ABP по изобретению (например, одну из двух (тяжелой и легкой) цепей антитела), и/или другая нуклеиновая кислота кодирует другую часть или мономер ABP изобретение (например, другую из двух цепей антитела). Такие нуклеиновые кислоты могут обеспечиваться в комбинации или в виде системы вместе. В некоторых вариантах осуществления нуклеиновая кислота кодирует две или несколько полипептидных цепей ABP, например, по меньшей мере 2 цепи антитела. Нуклеиновые кислоты, кодирующие несколько цепей ABP, могут включать сайты расщепления нуклеиновых кислот между по меньшей мере двумя последовательностями цепей, могут кодировать сайт начала транскрипции или трансляции между последовательностями двух или более цепей и/или могут кодировать протеолитические сайты-мишени между двумя или более цепями ABP.
[107] Еще один аспект изобретения относится к вектору (такому как вектор экспрессии), который содержит нуклеиновую кислоту, кодирующую ABP, как раскрыто в настоящей заявке, или часть или мономер ABP. Например, в некоторых вариантах осуществления, где ABP представляет собой мультимерный белок, нуклеиновая кислота кодирует только одну полипептидную цепь антигенной конструкции. Следовательно, для экспрессии такой антигенсвязывающей конструкции вектор экспрессии по изобретению может содержать две или более нуклеиновых кислот, каждая из которых кодирует отдельную часть или мономер ABP, которые в комбинации будут экспрессировать полный ABP. Аналогично, вектор экспрессии по изобретению, который содержит нуклеиновую кислоту, которая кодирует только часть или мономер антигенсвязывающей конструкции, может использоваться в комбинации с другими отдельными векторами экспрессии по изобретению, каждый из которых кодирует отдельную часть или мономер ABP. В других вариантах осуществления нуклеиновая кислота кодирует несколько полипептидных цепей ABP по изобретению. В некоторых вариантах осуществления вектор экспрессии включает вектор pcDNA3.1™/myc-His(-)Version A для экспрессии в клетках млекопитающих (Invitrogen, Inc.) или его вариант. Вектор экспрессии pcDNA3.1 содержит промотор CMV для экспрессии в клетках млекопитающих и селективные маркеры как млекопитающих (неомицин), так и бактериальные (ампициллин). В некоторых вариантах осуществления вектор экспрессии включает плазмиду. В некоторых вариантах осуществления вектор включает вирусный вектор, например ретровирусный или аденовирусный вектор. В вариантах осуществления изобретения вектор включает космиду, YAC или BAC.
[108] В другом соответствующем аспекте изобретение относится к клетке (такой как клетка-хозяин и/или рекомбинантная клетка-хозяин), включающей одну или несколько нуклеиновых кислот по изобретению. Предпочтительно такая клетка способна экспрессировать ABP (или его компонент), кодируемый указанными нуклеиновыми кислотами. Например, если ABP по изобретению содержит две отдельные полипептидные цепи (например, тяжелую и легкую цепь IgG), тогда клетка по изобретению может включать первую нуклеиновую кислоту, которая кодирует (и может экспрессировать) тяжелую цепь такого ABP, а также вторую нуклеиновую кислоту, которая кодирует (и может экспрессировать) легкую цепь такого ABP; альтернативно, клетка может включать одну нуклеиновую кислоту, которая кодирует обе цепи такого ABP. Таким образом, такая клетка по изобретению будет способна экспрессировать функциональный ABP по изобретению. Клетка (хозяин) по изобретению может представлять собой одну из клеток-хозяев млекопитающих, прокариотических или эукариотических, как описано в другом разделе настоящей заявки, в частности, клетка представляет собой клетку яичника китайского хомячка (СНО).
[109] В некоторых вариантах осуществления такого аспекта клетка (хозяин) представляет собой клетку человека; в частности, это может быть человеческая клетка, выделенная у конкретного субъекта (например, аутологичная человеческая клетка). В таких вариантах осуществления такую человеческую клетку можно размножать и/или осуществлять манипуляции in vitro, чтобы ввести нуклеиновую кислоту по настоящему изобретению. Использование и манипуляции с человеческой клеткой от конкретного субъекта может быть в целях получения ABP по изобретению, в том числе для повторного введения популяции таких обработанных человеческих клеток человеку, например, для применения в терапии. В некоторых из таких применений манипулируемая человеческая клетка может быть введена тому же человеку, у которого она была изначально взята; например, как аутологичная человеческая клетка.
[110] Человеческая клетка, которая подвергается такой манипуляции, может относиться к любому типу зародышевых или соматических клеток организма. Например, донорская клетка может быть зародышевой клеткой или соматической клеткой, выбранной из группы, состоящей из фибробластов, В-клеток, Т-клеток, дендритных клеток, кератиноцитов, жировых клеток, эпителиальных клеток, эпидермальных клеток, хондроцитов, кумулюсных клеток, нервных клеток, глиальных клеток, астроцитов, сердечных клеток, клеток пищевода, мышечных клеток, меланоцитов, гематопоэтических клеток, макрофагов, моноцитов и мононуклеарных клеток. Донорская клетка может быть получена из любого органа или ткани организма; например, это может быть клетка из органа, выбранного из группы, состоящей из печени, желудка, кишечника, легких, поджелудочной железы, роговицы, кожи, желчного пузыря, яичников, мужских половых желез, почек, сердца, мочевого пузыря и уретры.
[111] Изобретение также относится к фармацевтической композиции, которая включает ABP по изобретению и, необязательно, фармацевтически приемлемый эксципиент.
[112] ABP в соответствии с изобретением можно вводить любым парентеральным или непарентеральным (энтеральным) путем, который терапевтически эффективен для белковых лекарственных средств. Способы парентерального применения включают, например, внутрикожные, подкожные, внутримышечные, интратрахеальные, интраназальные, интравитреальные или внутривенные инъекции и методы инфузии, например в виде растворов для инъекций, инфузионных растворов или настоек, а также в виде аэрозольных инстилляций и ингаляций, например в виде аэрозольных смесей, спреев или порошков. Обзор доставки лекарств в легкие, т.е. либо путем ингаляции аэрозолей (которые также можно использовать для интраназального введения), либо внутрихеальной инстилляцией, см., например, в J.S. Patton et al. The lungs as a portal of entry for systemic drug delivery. Proc. Amer. Thoracic Soc. 2004 Vol. 1 pages 338-344). Непарентеральные способы доставки представляют собой, например, пероральный, например в форме пилюль, таблеток, капсул, растворов или суспензий, или ректальный, например в виде суппозиториев. ABP по изобретению можно вводить системно или местно в композициях, содержащих обычные нетоксичные фармацевтически приемлемые эксципиенты или носители, добавки и носители, по желанию.
[113] В одном варианте осуществления настоящего изобретения фармацевтический препарат вводят млекопитающему и, в частности, человеку парентерально. Соответствующие методы введения включают, но не ограничиваются этим, например, внутрикожные, подкожные, внутримышечные, интратрахеальные или внутривенные инъекции и методы инфузии, например в виде растворов для инъекций, инфузионных растворов или настоек, а также в виде аэрозольных инстилляций и ингаляций, например в виде аэрозольных смесей, спреев или порошков. Комбинация внутривенной и подкожной инфузии и/или инъекции может быть наиболее удобной в случае соединений с относительно коротким периодом полужизни в сыворотке. Фармацевтическая композиция может представлять собой водный раствор, эмульсию масло-в-воде или эмульсию вода-в-масле.
[114] В этой связи следует отметить, что технологии чрескожной доставки, например ионтофорез, сонофорез или доставка с использованием микроигл, как описано в Meidan VM and Michniak BB 2004 Am. J. Ther. 11 (4):312-316, также можно использовать для чрескожной доставки ABP, описанного в настоящей заявке. Непарентеральными способами доставки являются, например, пероральное, например в форме пилюль, таблеток, капсул, растворов или суспензий, или ректальное введение, например в виде суппозиториев. ABP по изобретению можно вводить системно или местно в композициях, содержащих различные обычно используемые нетоксичные фармацевтически приемлемые эксципиенты или носители, добавки и наполнители.
[115] Дозировка используемого ABP может варьировать в широких пределах для достижения желаемого профилактического эффекта или терапевтического ответа. Это, например, зависит от сродства ABP к выбранной мишени, а также от периода полужизни комплекса между ABP и лигандом in vivo. Кроме того, оптимальная дозировка будет зависеть от биодистрибуции ABP или его конъюгата, способа введения, тяжести заболевания/расстройства, которое лечат, а также состояния здоровья пациента. Например, при использовании в виде мази для местного применения может использоваться высокая концентрация ABP. Однако, при желании, ABP также можно вводить в композиции с замедленным высвобождением, например в форме липосомальных дисперсий или полимерных микросфер на основе гидрогеля, таких как PolyActive™ или OctoDEX™ (см. Bos et al., Business Briefing: Pharmatech 2003: 1-6). Другие доступные композиции с замедленным высвобождением представляют собой, например, полимеры на основе PLGA (PR Pharmaceuticals), гидрогели на основе PLA-PEG (Medincell) и полимеры на основе PEA (Medivas).
[116] Соответственно, ABP по настоящему изобретению могут быть составлены в композиции с использованием фармацевтически приемлемых ингредиентов, а также принятых способов получения (Gennaro, A.L. and Gennaro, A.R. (2000) Remington: The Science and Practice of Pharmacy, 20th Ed., Lippincott Williams & Wilkins, Philadelphia, PA). Для получения фармацевтических композиций можно использовать фармацевтически инертные неорганические или органические эксципиенты. Для получения, например, пилюль, порошков, желатиновых капсул или суппозиториев можно использовать, например, лактозу, тальк, стеариновую кислоту и ее соли, жиры, воски, твердые или жидкие полиолы, натуральные и отвержденные масла. Подходящие эксципиенты для получения растворов, суспензий, эмульсий, аэрозольных смесей или порошков для восстановления в растворы или аэрозольные смеси перед использованием включают воду, спирты, глицерин, полиолы и их подходящие смеси, а также растительные масла.
[117] Фармацевтическая композиция может также содержать добавки, такие как, например, наполнители, связующие, смачивающие агенты, глиданты, стабилизаторы, консерванты, эмульгаторы и, кроме того, растворители или солюбилизаторы или агенты для достижения эффекта депо. Последнее заключается в том, что слитые белки могут быть включены в системы медленного или замедленного высвобождения или адресной доставки, такие как липосомы и микрокапсулы.
[118] Композиции можно стерилизовать различными способами, включая фильтрацию через фильтр, задерживающий бактерии, или путем включения стерилизующих агентов в форме стерильных твердых композиций, которые можно растворять или диспергировать в стерильной воде или другой стерильной среде непосредственно перед использованием.
[119] ABP может быть подходящим и может использоваться для лечения или профилактики заболевания. Соответственно, в некоторых вариантах осуществления ABP в соответствии с изобретением можно использовать в способе лечения и/или профилактики медицинского состояния, такого как расстройство или заболевание. Точно так же ABP по настоящему изобретению можно использовать при лечении заболевания. Заболевание, которое необходимо лечить или предотвращать, может быть пролиферативным заболеванием. Такое пролиферативное заболевание предпочтительно может представлять собой опухоль или рак. Благодаря способности ABP по изобретению связывать FLT3, этот ABP можно использовать для лечения рака, который состоит из клеток, экспрессирующих FLT3, как дикого типа, так и мутированный FLT3. Что касается лечений по изобретению, рак может представлять собой любой рак, включая любой из острого лимфоцитарного рака, острого миелоидного лейкоза (AMI), альвеолярной рабдомиосаркомы, рака мочевого пузыря (например, карциномы мочевого пузыря), рака костей, рака мозга (например, медуллобластомы), рака молочной железы, рака заднего прохода, анального канала или аноректального рака, рак глаза, рак внутрипеченочного желчного протока, рака суставов, рака шеи, желчного пузыря или плевры, рака носа, полости носа или среднего уха, рака полости рта, рака вульвы, хронического лимфоцитарного лейкоза, хронического миелоидного рака, рака толстой кишки, рака пищевода, рака шейки матки, фибросаркомы, карциноидной опухоли желудочно-кишечного тракта, рака головы и шеи (например, плоскоклеточный рак головы и шеи), лимфомы Ходжкина, рака гипофаринкса, рака почки, рака гортани, лейкоза, жидких опухолей, рака печени, рака легких (например, немелкоклеточная карцинома легких и длинная аденокарцинома), лимфомы, мезотелиомы, мастоцитомы, меланомы, множественной миеломы, рака носоглотки, неходжкинской лимфомы, B-хронического лимфоцитарного лейкоза, волосистоклеточного лейкоза, острого лимфоцитарного лейкоза (ALL) и лимфомы Беркета, рака яичников, рака поджелудочной железы, рака брюшной полости, сальника и брыжейки, рака глотки, рака предстательной железы, рака прямой кишки, рака почек, рака кожи, рака тонкой кишки, рака мягких тканей, солидных опухолей, синовиальной саркомы, гастрального рака, тестикулярного рака, рака щитовидной железы и рака мочеточника. Предпочтительно рак характеризуется экспрессией FLT3. Наиболее предпочтительно рак представляет собой FLT3-положительный лейкоз, такой как AML или ALL.
[120] Субъект, которого лечат слитым белком, может быть человеком или животным, отличным от человека. Таким животным предпочтительно является млекопитающее, например человек, свинья, крупный рогатый скот, кролик, мышь, крыса, примат, коза, овца, курица или лошадь, наиболее предпочтительно человек.
[121] ABP по настоящему изобретению также можно использовать для диагностики заболевания, такого как заболевание, описанное в настоящей заявке. Для этого ABP может быть помечен подходящей детектируемой сигнальной меткой. Такой меченый ABP может обеспечить возможность детекции или количественного определения уровня FLT3 или рака, такого как лейкоз, или любого из вышеперечисленных видов рака, у субъекта. При назначении для использования in vivo указанная детектируемая сигнальная метка предпочтительно является обнаруживаемой in vivo.
[122] Меченый ABP может использоваться в методах иммуно-визуализации. Обнаруживаемая сигнальная метка в этом случае может быть выбрана, например, на основе метода иммуно-визуализации, используемого для диагностики, например, гамма-излучающего радионуклида (или гамма-излучателя) в случае метода визуализации с использованием гамма-камеры/SPECT, металло- или позитрон-излучателя в случае методов МРТ или ПЭТ, соответственно. В этом отношении одна или несколько обнаруживаемых сигнальных меток настоящего раскрытия включают агенты для визуализации с использованием гамма-камеры, агенты для ПЭТ-визуализации и агенты для МРТ-визуализации, такие как радионуклиды, флуоресцентные агенты, флюорогены, хромофоры, хромогены, фосфоресцирующие вещества, хемилюминесцентные агенты и биолюминесцентные агенты.
[123] Подходящей детектируемой сигнальной меткой может быть радионуклид. Указанный радионуклид может быть выбран из группы, состоящей из 3H, 14C, 35S, 99Tc, 123I, 125I, 131I, mIn, 97Ru, 67Ga, 68Ga, 72As, 89Zr и 201Tl.
[124] Подходящей детектируемой сигнальной меткой также может быть флуорофор или флуороген. Указанный флуорофор или флуороген можно выбрать из группы, состоящей из флуоресцеина, родамина, дансила, фикоэритрина, фикоцианина, аллофикоцианина, о-фталальдегида, флуорескамина, производного флуоресцеина, орегонового зеленого, родаминового зеленого, родолового зеленого или техасского красного.
[125] Меченый ABP может быть прямо или косвенно связан с обнаруживаемой сигнальной меткой. Например, ABP может быть связан либо непосредственно (например, через тирозиновые остатки в ABP), либо опосредованно (например, через линкер - как металл-хелатирующий агент) с детектируемой сигнальной меткой. В некоторых других вариантах осуществления ABP может быть связан с молекулой, которая может быть связана (in vitro или in vivo) с детектируемой сигнальной меткой во время и в месте использования.
[126] Детектируемая сигнальная метка может быть связана с ABP через один или более остатков диэтилентриаминпентауксусной кислоты (DTPA), которые связаны с ABP.
[127] Изобретение также относитсся к способу in vitro обнаружения или диагностики заболевания, определенного в настоящей заявке. Такой способ может включать контактирование образца, полученного от субъекта, с предпочтительно меченным ABP по изобретению. Образец может быть образцом крови, мочи или спинномозговой жидкости, но предпочтительно может быть жидким образцом или образцом биопсии. Подлежащее обнаружению или диагностированию заболевание предпочтительно представляет собой лейкоз, такой как ALL или AML.
[128] Термины "по [настоящему] изобретению", "в соответствии с изобретением", "согласно изобретению" и т.п., используемые в настоящей заявке, предназначены для обозначения всех аспектов и вариантов осуществления изобретения, описанных и/или заявленных в настоящей заявке.
[129] В контексте настоящей заявки термин "включающий" следует истолковывать как охватывающий как "включающий в себя", так и "состоящий из", причем оба значения являются специально предусмотренными и, следовательно, индивидуально раскрытыми вариантами осуществления в соответствии с настоящим изобретением. При использовании в настоящей заявке "и/или" следует понимать как конкретное раскрытие каждой из двух определяемых функций или компонентов с другим или без другого. Например, "А и/или В" следует рассматривать как конкретное раскрытие каждого из (i) A, (ii) B и (iii) A и B, как если бы каждый был индивидуально раскрыт в настоящей заявке. В контексте настоящего изобретения термины "приблизительно" и "примерно" обозначают интервал точности, который специалист в данной области техники поймет, чтобы по-прежнему гарантировать технический эффект рассматриваемого признака. Термин обычно указывает отклонение от указанного числового значения на ±20%, ±15%, ±10% и, например, ±5%. Специалистам с обычной квалификацией должно быть понятно, что конкретное такое отклонение численного значения для данного технического эффекта будет зависеть от характера технического эффекта. Например, естественный или биологический технический эффект обычно может иметь большее отклонение, чем искусственный или инженерно-технический эффект. Если используется ссылка на существительное в единственном числе, она также включает множественное число этого существительного, если специально не указано иное.
[130] Следует понимать, что применение раскрытия настоящего изобретения к конкретной проблеме или условиям, а также включение вариаций настоящего изобретения или его дополнительных характерных признаков (таких как дополнительные аспекты и варианты осуществления) будет в пределах возможности специалиста в данной области техники в свете раскрытия, содержащегося в настоящей заявке.
[131] Если контекст не диктует иное, описания и определения функций, изложенных выше, не ограничиваются каким-либо конкретным аспектом или вариантом осуществления изобретения и в равной степени применимы ко всем аспектам и вариантам осуществления, которые описаны.
[132] Все ссылочные документы, патенты и публикации, цитируемые в настоящей заявке, полностью включены в настоящую заявку посредством ссылки.
[133] В свете вышеизложенного, будет понятно, что настоящее изобретение также относится к следующим перечисленным вариантам осуществления:
Пункт 1: Биспецифический антигенсвязывающий белок (ABP), который включает первый антигенсвязывающий домен, способный связываться с антигеном fms-подобной тирозинкиназы 3 (FLT3) человека, и второй антигенсвязывающий домен, связывающийся с человеческим антигеном кластера дифференцировки 3 (CD3).
Пункт 2: Биспецифический ABP в соответствии с пунктом 1, где биспецифический ABP связывается с FLT3 с EC50 меньше чем 10 нМ, предпочтительно меньше чем 9 нМ, более предпочтительно меньше чем 8 нМ, более предпочтительно меньше чем 7 нМ, более предпочтительно меньше чем 6 нМ или меньше чем 5,5 нМ.
Пункт 3: Биспецифический ABP в соответствии с пунктом 1 или 2, где биспецифический ABP связывается с FLT3 с EC50 больше чем 0,5 нМ, более предпочтительно больше чем 1 нМ, более предпочтительно больше чем 1,3 нМ, более предпочтительно больше чем 2 нМ, более предпочтительно больше чем 3 нМ или 4 нМ, или больше чем 4,5 нМ.
Пункт 4: Биспецифический ABP в соответствии с любым из пунктов 1-3, где биспецифический ABP связывается с FLT3 с EC50 меньше чем 10 нМ и больше чем 0,5 нМ, более предпочтительно меньше чем 9 нМ и больше чем 1 нМ, предпочтительно меньше чем 8 нМ и больше чем 1,3 нМ, предпочтительно меньше чем 7 нМ и больше чем 3 нМ, предпочтительно меньше чем 6 нМ и больше чем 4 нМ, предпочтительно меньше чем 5,5 нМ и больше чем 4,5 нМ,
Пункт 5: Биспецифический ABP в соответствии с любым из пунктов 2-4, где EC50 связывания биспецифического ABP с FLT3 имеет значение, определенное в анализе связывания биспецифического ABP с FLT3-положительными клетками методом проточной цитометрии с использованием устройства для сортировки флуоресцентно-активированных клеток (FACS); предпочтительно где FLT3-положительные клетки представляют собой лейкозные клетки из B-клеток предшественников, предпочтительно NALM-16 клетки (депонированные под номером ACC 680 в DSMZ); и/или предпочтительно, где связывание определяют с использованием флуоресцентно-меченного вторичного антитела; и/или где биспецифический ABP инкубируют с FLT3-положительными клетками приблизительно 30 минут перед проточной цитометрией.
Пункт 6: Биспецифический ABP в соответствии с любым из пунктов 1-5, где биспецифический ABP связывается FLT3 с kD меньше чем 50 мкМ, более предпочтительно меньше чем 20 мкМ, более предпочтительно меньше чем 10 мкМ, более предпочтительно меньше чем 5 мкМ, более предпочтительно меньше чем 1 мкМ.
Пункт 7: Биспецифический ABP в соответствии с любым из пунктов 1-5, где биспецифический ABP связывается FLT3 с kD больше чем 50 нМ, более предпочтительно больше чем 100 нМ, более предпочтительно больше чем 160 нМ, более предпочтительно больше чем 200 нМ, более предпочтительно больше чем 300 нМ.
Пункт 8: Биспецифический ABP в соответствии с любым из пунктов 1-5, где биспецифический ABP связывается FLT3 с kD меньше чем 50 мкМ и больше чем 50 нМ, более предпочтительно меньше чем 20 мкМ и больше чем 100 нМ, более предпочтительно меньше чем 10 мкМ и больше чем 160 нМ, более предпочтительно меньше чем 5 мкМ и больше чем 200 нМ, более предпочтительно меньше чем 1 мкМ и больше чем 300 нМ.
Пункт 9: Биспецифический ABP в соответствии с любым из пунктов 6-8, где kD имеет значение, измеренное методом поверхностного плазмонного резонанса, например в анализе аффинности BIAcore.
Пункт 10: Биспецифический ABP в соответствии с любым из пунктов 1-9, где биспецифический ABP связывается с CD3 с EC50 меньше чем 200 нМ, предпочтительно меньше чем 90 нМ, более предпочтительно меньше чем 50 нМ, более предпочтительно меньше чем 20 нМ, более предпочтительно меньше чем 15 нМ.
Пункт 11: Биспецифический ABP в соответствии с любым из пунктов 1-10, где биспецифический ABP связывается с CD3 с EC50 больше чем 1 нМ, предпочтительно больше чем 2 нМ, более предпочтительно больше чем 4,1 нМ, более предпочтительно больше чем 6 нМ, более предпочтительно больше чем 8 нМ.
Пункт 12: Биспецифический ABP в соответствии с любым из пунктов 1-11, где биспецифический ABP связывается с CD3 с EC50 меньше чем 200 нМ и больше чем 1 нМ, предпочтительно меньше чем 200 нМ и больше чем 2 нМ, более предпочтительно меньше чем 90 нМ и больше чем 4,1 нМ, более предпочтительно меньше чем 20 нМ и больше чем 6 нМ, более предпочтительно меньше чем 15 нМ и больше чем 8 нМ.
Пункт 13: Биспецифический ABP в соответствии с любым из пунктов 10-12, где EC50 связывания биспецифического ABP с CD3 имеет значение, определенное в анализе связывания биспецифического ABP с CD3-положительными клетками методом проточной цитометрии с использованием устройства для сортировки флуоресцентно-активированных клеток (FACS); предпочтительно где CD3-положительные клетки представляют собой клетки T-клеточного лейкоза, предпочтительно Jurkat клетки (депонированные под номером ACC 282 в DSMZ); и/или предпочтительно, где связывание определяют с использованием флуоресцентно-меченного вторичного антитела; и/или где биспецифический ABP инкубируют с CD3-положительными клетками приблизительно 30 минут перед проточной цитометрией.
Пункт 14: Биспецифический ABP в соответствии с любым из пунктов 1-13, который ингибирует пролиферацию и/или жизнеспособность лейкозных мононуклеарных клеток крови пациента, страдающего острым лейкозом, в анализе in vitro по сравнению с независимым контролем, до уровня равного или меньше чем 50%, более предпочтительно равного или меньше чем 40%, более предпочтительно равного или меньше чем 30%, наиболее предпочтительно равного или меньше чем 25%.
Пункт 15: Биспецифический ABP в соответствии с любым из пунктов 1-14, где биспецифический ABP включает два сайта связывания с первым антигеном.
Пункт 16: Биспецифический ABP в соответствии с любым из пунктов 1-15, где биспецифический ABP включает два сайта связывания с вторым антигеном.
Пункт 17: Биспецифический ABP в соответствии с любым из пунктов 1-16, который представляет собой антитело или вариант антитела.
Пункт 18: Биспецифический ABP в соответствии с пунктом 17, где антигенсвязывающий домен состоит из вариабельного домена тяжелой цепи антитела и вариабельного домена легкой цепи антитела.
Пункт 19: Биспецифический ABP в соответствии с любым из пунктов 1-18, который представляет собой четырехвалентное и гомодимерное биспецифическое антитело, включающее в каждом мономере: (i) N-концевой Fab фрагмент, включающий вариабельную область, включающую вариабельный домен тяжелой цепи и вариабельный домен легкой цепи, где указанная вариабельная область включает первый антигенсвязывающий сайт; (ii) C-концевой scFv фрагмент, включающий второй антигенсвязывающий сайт, и где (i) и (ii) соединены CH2 и CH3 доменом.
Пункт 20: Биспецифический ABP в соответствии с любым из пунктов 17-19, где по меньшей мере один аминокислотный остаток CH2 домена, который способен опосредовать связывание с Fc рецепторами, в указанном антителе отсутствует или мутирован.
Пункт 21: Биспецифический ABP в соответствии с любым из пунктов 1-20, где второй антигенсвязывающий сайт включает в ориентации от C- к N-концу вариабельный домен тяжелой цепи антитела и вариабельный домен легкой цепи антитела.
Пункт 22: ABP, способный связываться с человеческой fms-подобной тирозинкиназой 3 (FLT3), включающий: (i) вариабельный домен тяжелой цепи, включающий CDRH1 область, представленную в SEQ ID NO: 01 (SYWMH), CDRH2 область, представленную в SEQ ID NO: 02 (EIDPSDSYKDYNQKFKD), и CDRH3 область, представленную в SEQ ID NO: 03 (AITTTPFDF), или где в каждом случае независимо CDRH1, CDRH2 и/или CDRH3 включают последовательность, имеющую не более трех или двух, предпочтительно не более одной аминокислотной замены, делеции или инсерции по сравнению с SEQ ID NO: 01, SEQ ID NO: 02, или SEQ ID NO: 03, соответственно; или включающий последовательность CDRH1, CDRH2 или CDRH3, имеющую по меньшей мере 75% идентичности последовательности или по меньшей мере 80%, предпочтительно 90% идентичности последовательности с SEQ ID NO: 01, SEQ ID NO: 02 или SEQ ID NO: 03; и (ii) вариабельный домен легкой цепи, включающий CDRL1 область, представленную в SEQ ID NO: 05 (RASQSISNNLH), CDRL2 область, представленную в SEQ ID NO: 06 (YASQSIS), и CDRL3 область, представленную в SEQ ID NO: 07 (QQSNTWPYT), или где в каждом случае независимо CDRL1, CDRL2 и/или CDRL3 включают последовательность, имеющую не более трех или двух, предпочтительно не более одной аминокислотной замены, делеции или инсерции по сравнению с SEQ ID NO: 05, SEQ ID NO: 06 или SEQ ID NO: 07, соответственно; или включающий последовательность CDRL1, CDRL2 или CDRL3, имеющую по меньшей мере 75% идентичности последовательности или по меньшей мере 80% идентичности последовательности с SEQ ID NO: 05, SEQ ID NO: 06 или SEQ ID NO: 07; отличающийся тем, что каждая из указанной вариабельной области тяжелой цепи и указанной вариабельной области легкой цепи включает человеческие каркасные последовательности вариабельной области.
Пункт 23: ABP в соответствии с пунктом 22, который представляет собой биспецифический ABP в соответствии с любым из пунктов 1-21, и где указанные CDR области (i) и (ii) в пункте 22 содержатся в указанном первом антигенсвязывающем домене.
Пункт 24: ABP в соответствии с любым пунктом 22 или 23, где человеческие каркасные последовательности вариабельных доменов тяжелой цепи получены из IGHV1-46, предпочтительно IGHV1-46*3, и/или где человеческие каркасные последовательности вариабельных доменов тяжелой цепи получены из IGKV3D-15.
Пункт 25: ABP в соответствии с пунктом 24, где вариабельная область тяжелой цепи включает любую из или комбинацию следующих мутаций: K16G, V18L, K19R, V20L, K22A, M48I, K57T, N60A, M69I, T70S, T75K, S76N, V78L, M80L, E81Q, S87A и T108L, где нумерация указана в соответствии с системой Кабата.
Пункт 26: ABP в соответствии с пунктом 24 или 25, где вариабельная область легкой цепи включает любую из или комбинацию следующих мутаций: Y49K, Y87F, и I55A, где нумерация указана в соответствии с системой Кабата.
Пункт 27: ABP по пункту 1, где вариабельная область тяжелой цепи включает аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере 80% с аминокислотной последовательностью, выбранной из SEQ ID NO: 15, 17, 19, 21 или 23, или, в каждом случае независимо, необязательно с не более чем десятью, девятью, восемью, семью, шестью, пятью, четырьмя, предпочтительно не более чем тремя, двумя или одной аминокислотной заменой(заменами), инсерцией(инсерциями) или делецией(делециями) по сравнению с этими последовательностями; и/или где вариабельная область легкой цепи включает аминокислотную последовательность, имеющую идентичность последовательности по меньшей мере 80% с аминокислотной последовательностью, выбранной из SEQ ID NO: 16, 18, 20, 22 или 24, или, в каждом случае независимо, необязательно с не более чем десятью, девятью, восемью, семью, шестью, пятью, четырьмя, предпочтительно не более чем тремя, двумя или одной аминокислотной заменой(заменами), инсерцией(инсерциями) или делецией(делециями) по сравнению с этими последовательностями.
Пункт 28: ABP в соответствии с пунктом 27, где в вариабельной области тяжелой цепи аминокислотные положения 16, 18, 19, 20, 22, 48, 57, 60, 69, 70, 75, 76, 78, 80, 81, 87 и 108 такие же, как в любой из SEQ ID NO: 15, 17, 19, 21 или 23; и/или где в вариабельной области легкой цепи аминокислотные положения 49, 55, и 87 такие же, как в любой из SEQ ID NO: 16, 18, 20, 22 или 24; где нумерация указана в соответствии с системой Кабата.
Пункт 29: ABP в соответствии с любым из пунктов 1-28, включающий по меньшей мере один, предпочтительно два связывающих второй антиген домена, где указанный второй антигенсвязывающий домен связывается с CD3, предпочтительно где указанный второй антигенсвязывающий домен слит с тяжелой цепью первого связывающего домена антитела.
Пункт 30: ABP в соответствии с пунктом 29, где второй антигенсвязывающий домен включает scFv фрагмент, включающий аминокислотную последовательность, имеющую по меньшей мере 80% идентичности последовательности с, или, в каждом случае независимо, необязательно с не более чем десятью, девятью, восемью, семью, шестью, пятью, четырьмя, предпочтительно не более чем тремя, двумя или одной аминокислотной заменой(заменами), инсерцией(инсерциями) или делецией(делециями) по сравнению с последовательностью, выбранной из SEQ ID NO: 14, 25, 26 и 27.
Пункт 31: ABP в соответствии с пунктом 27 или 28, включающий по меньшей мере одну тяжелую цепь антитела, имеющую аминокислотную последовательность с по меньшей мере 80% идентичности последовательности с, или имеющую не больше двадцати, пятнадцати, десяти, девяти, восьми, семи, шести, четырех, предпочтительно трех или двух, предпочтительно не более одной аминокислотной замены, делеции или инсерции по сравнению с последовательностью, выбранной из SEQ ID NO: 28, 30, 32, 34, 36, 38, 40, 42, 44, 46, 48, 50, 52, 54, 56, 58, 60, 62, 64, 66, 68, 70, 72 и 74; и/или включающий по меньшей мере одну легкую цепь антитела, имеющую аминокислотную последовательность с по меньшей мере 80% идентичности последовательности с, или имеющую не больше двадцати, пятнадцати, десяти, девяти, восьми, семи, шести, четырех, предпочтительно трех или двух, предпочтительно не более одной аминокислотной замены, делеции или инсерции по сравнению с последовательностью, выбранной из SEQ ID NO: 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73 и 75.
Пункт 32: ABP в соответствии с пунктом 31, включающий одну, предпочтительно две тяжелые цепи антитела и одну, предпочтительно две легкие цепи антитела, каждая из которых включает аминокислотную последовательность с по меньшей мере 80% идентичности последовательности с, или имеет не больше двадцати, пятнадцати, десяти, девяти, восьми, семи, шести, четырех, предпочтительно трех или двух, предпочтительно не более одной аминокислотной замены, делеции или инсерции по сравнению с:
a. последовательностью, выбранной из SEQ ID NO: 28 для тяжелой цепи и SEQ ID NO: 29 для легкой цепи;
b. последовательностью, выбранной из SEQ ID NO: 30 для тяжелой цепи и SEQ ID NO: 31 для легкой цепи;
c. последовательностью, выбранной из SEQ ID NO: 32 для тяжелой цепи и SEQ ID NO: 33 для легкой цепи;
d. последовательностью, выбранной из SEQ ID NO: 34 для тяжелой цепи и SEQ ID NO: 35 для легкой цепи;
e. последовательностью, выбранной из SEQ ID NO: 36 для тяжелой цепи и SEQ ID NO: 37 для легкой цепи;
f. последовательностью, выбранной из SEQ ID NO: 38 для тяжелой цепи и SEQ ID NO: 39 для легкой цепи;
g. последовательностью, выбранной из SEQ ID NO: 40 для тяжелой цепи и SEQ ID NO: 41 для легкой цепи;
h. последовательностью, выбранной из SEQ ID NO: 42 для тяжелой цепи и SEQ ID NO: 43 для легкой цепи;
i. последовательностью, выбранной из SEQ ID NO: 44 для тяжелой цепи и SEQ ID NO: 45 для легкой цепи;
j. последовательностью, выбранной из SEQ ID NO: 46 для тяжелой цепи и SEQ ID NO: 47 для легкой цепи;
k. последовательностью, выбранной из SEQ ID NO: 48 для тяжелой цепи и SEQ ID NO: 49 для легкой цепи;
l. последовательностью, выбранной из SEQ ID NO: 50 для тяжелой цепи и SEQ ID NO: 51 для легкой цепи;
m. последовательностью, выбранной из SEQ ID NO: 52 для тяжелой цепи и SEQ ID NO: 53 для легкой цепи;
n. последовательностью, выбранной из SEQ ID NO: 54 для тяжелой цепи и SEQ ID NO: 55 для легкой цепи;
o. последовательностью, выбранной из SEQ ID NO: 56 для тяжелой цепи и SEQ ID NO: 57 для легкой цепи;
p. последовательностью, выбранной из SEQ ID NO: 58 для тяжелой цепи и SEQ ID NO: 59 для легкой цепи;
q. последовательностью, выбранной из SEQ ID NO: 60 для тяжелой цепи и SEQ ID NO: 61 для легкой цепи;
r. последовательностью, выбранной из SEQ ID NO: 62 для тяжелой цепи и SEQ ID NO: 63 для легкой цепи;
s. последовательностью, выбранной из SEQ ID NO: 64 для тяжелой цепи и SEQ ID NO: 65 для легкой цепи;
t. последовательностью, выбранной из SEQ ID NO: 66 для тяжелой цепи и SEQ ID NO: 67 для легкой цепи;
u. последовательностью, выбранной из SEQ ID NO: 68 для тяжелой цепи и SEQ ID NO: 69 для легкой цепи;
v. последовательностью, выбранной из SEQ ID NO: 70 для тяжелой цепи и SEQ ID NO: 71 для легкой цепи;
w. последовательностью, выбранной из SEQ ID NO: 72 для тяжелой цепи и SEQ ID NO: 73 для легкой цепи;
x. последовательностью, выбранной из SEQ ID NO: 74 для тяжелой цепи и SEQ ID NO: 75 для легкой цепи;
где тяжелая цепь и легкая цепь спарены друг с другом.
Пункт 33: ABP или его антигенсвязывающий фрагмент, способный связываться с человеческим FLT3, который способен конкурировать со связыванием ABP в соответствии с любым из пунктов 1-32.
Пункт 34: ABP по любому из пунктов 1-33, обладающий активностью связывания с T-клеткой и с FLT3-экспрессирующей опухолевой клеткой, предпочтительно где антитело повышает рекрутинг T-клеток к FLT3-экспрессирующей опухолевой клетке путем связывания с FLT3 и CD3.
Пункт 35: ABP в соответствии с любым из пунктов 1-34, где вариабельная область тяжелой цепи и вариабельная область легкой цепи молекулы антитела, включающей второй связывающий домен, представляет собой вариабельную область тяжелой цепи и вариабельную область легкой цепи UCHT1.
Пункт 36: ABP в соответствии с любым из пунктов 1-35, включающий константные области тяжелой цепи CH1-CH3, и где по меньшей мере один аминокислотный остаток человеческого CH2 домена, который способен опосредовать связывание с Fc рецепторами, отсутствует или мутирован.
Пункт 37: ABP по любому из пунктов 1-36, где ABP представляет собой молекулу тетрамерного антитела или молекулу гомодимерного и четырехвалентного антитела.
Пункт 38: Выделенная нуклеиновая кислота, кодирующая ABP или антигенсвязывающий фрагмент или мономер ABP по любому из пунктов 1-37.
Пункт 39: Рекомбинантная клетка-хозяин, включающая нуклеиновую кислоту по пункту 38.
Пункт 40: Фармацевтическая композиция, включающая: (i) ABP по любому из пунктов 1-37, или (ii) нуклеиновую кислоту по пункту 38, или (iii) рекомбинантную клетку-хозяин в соответствии с пунктом 39 и фармацевтически приемлемый носитель, стабилизатор и/или эксципиент.
Пункт 41: Компонент для применения в медицине, где компонент выбран из перечня, включающего: ABP по любому из пунктов 1-37, выделенную нуклеиновую кислоту по пункту 38, рекомбинантную клетку-хозяина в соответствии с пунктом 39 и фармацевтическую композицию в соответствии с пунктом 40.
Пункт 42: Компонент для применения по пункту 41, где применение в медицине представляет собой применение в лечении пролиферативного расстройства, которое связано с экспрессией FLT3.
Пункт 43: Компонент для применения по пунктам 41 или 42, где компонент предназначен для применения для усиления T-клеточно-опосредованного киллинга и/или ингибирования пролиферации FLT3-положительных опухолевых клеток.
Пункт 44: Компонент для применения в соответствии с любым из пунктов 41-43, где компонент предназначен для применения в диагностике, профилактике и/или лечении пролиферативного заболевания, где пролиферативное заболевание предпочтительно представляет собой рак, где рак выбран из лейкоза, такого как острый миелоидный лейкоз (AML) или острый лимфобластный лейкоз (ALL), или солидный рак, выбранный из рака предстательной железы, колоректального рака, рака желудка, карциномы легкого, остеосаркомы, рака молочной железы, рака поджелудочной железы, или плоскоклеточной карциномы; предпочтительно рак представляет собой лейкоз, такой как AML или ALL.
Пункт 45: Компонент для применения в соответствии с пунктом 44, где рак ассоциирован с опухолевыми клетками, экспрессирующими FLT3.
Краткое описание чертежей и последовательностей
[134] Чертежи показывают:
[135] Фиг. 1 представляет Fc-аттенуированный IgGsc-формат, который использовали для конструирования вариантов биспецифического FLT3xCD3 антитела, описанных в настоящем изобретении. Варианты FLT3 антигенсвязывающего домена (V1-V5) получали, начиная с гуманизации V-областей анти-FLT3 антитела 4G8 путем CDR-прививки с использованием стратегий замены с разной жесткостью. Для получения различных CD3-антигенсвязывающих доменов (V6-V9) использовали последовательности UCHT1 scFv.
[136] Фиг. 2 показывает аминокислотную последовательность тяжелой и легкой цепи CC-2. A: последовательность тяжелой цепи молекулы биспецифического FLT3(4G8)XCD3 (гуманизированный hUCHT1) антитела формата IgGsc (SEQ ID NO: 68). Тяжелая цепь включает вариабельную область мышиной тяжелой цепи (HC) 4G8, домен IgG1 CH1, шарнирную область IgG1, модифицированный домен CH2 IgG1, домен CH3 IgG1 и одноцепочечный фрагмент Fv гуманизированного CD3 (UCHT1). B: показывает аминокислотную последовательность легкой цепи каппа FLT3 (4G8) x CD3 (гуманизированный hUCHT1) (SEQ ID NO: 69). Эта легкая цепь дополняет конструкции тяжелой цепи SEQ ID NO: 68 с образованием химерной 4G8xUCHT1 IgGsc- и Fabsc-молекулы, соответственно (см. Фиг. 1).
[137] Фиг. 3 показывает связывание различных вариантов CC-2 с растворимым рекомбинантным белком FLT3. Соответствующие варианты антител иммобилизовали на чипе Biacore, покрытом белком А, и связывание His-меченного рекомбинантного FLT3 белка (Sino Biologicals) определяли с использованием устройства Biacore X (GE Healthcare). Показаны результаты различных мутировавших вариантов антигенсвязывающего домена FLT3 (V1 - V5).
[138] Фиг. 4 показывает связывание вариантов CC-2 с клетками Nalm16, экспрессирующими FLT3. Рассчитанные значения ЕС50 указаны на соответствующих полосах на Фиг. 3. Испытывали мутированные варианты FLT3 антигенсвязывающего домена (V1 - V5).
[139] Фиг. 5 показывает истощение лейкозных клеток в образцах крови пациентов с AML с использованием различных конструкций CC-2 по настоящему изобретению. Показывает сравнение мутированных вариантов FLT3 антигенсвязывающего домена (V1 - V5). Также указаны значения результатов Biacore Фиг. 3 и EC50 проточной цитометрии Фиг. 4.
[140] Фиг. 6 показывает связывание CC-2 вариантов с клетками Jurkat, экспрессирующими CD3. Рассчитанные значения ЕС50 указаны на соответствующих полосах на фиг. 5. Испытывали мутированные варианты CD3 антигенсвязывающего домена (V7 - V9).
[141] Фиг. 7 показывает истощение лейкозных клеток в образцах крови пациентов с AML с использованием различных конструкций CC-2 по настоящему изобретению. Показано сравнение мутированных вариантов CD3 антигенсвязывающего домена (V7 - V9). Также указаны значения проточной цитометрии EC50 Фиг.6.
[142] Фиг. 8 показывает результаты активации Т-клеток и уменьшения бластов различными вариантами CC-2 в анализе проточной цитометрии. Используемые варианты CC2 различаются как по их FLT3 антигенсвязывающим доменам, так и по CD3 антигенсвязывающим доменам (используемые антитела: V6-V6 (V6); V6-V9 (V9); V4-V6 (V4)). A: уменьшение CD4-положительных клеток; B: уменьшение CD8-положительных клеток; C: количество бластов.
[143] Фиг. 9 показывает истощение лейкозных клеток NALM16 различными вариантами CC-2 в анализе проточной цитометрии. Используемые варианты CC2 различаются как по их FLT3 антигенсвязывающим доменам, так и по CD3 антигенсвязывающим доменам (используемые антитела: V6-V6 (V6); V6-V8 (V8); V4-V6 (V4); V6-V7 (V7)).
[144] Фиг. 10 показывает антилейкозную активность CC-2 варианта 4 in vivo у иммунодефицитных мышей NSG с привитым первичным AML (A) или ALL (B). В качестве примера показаны варианты CC-2, содержащие FLT3 антигенсвязывающий домен V4 (V4-V6).
[145] Фиг. 11 показывает антитело-зависимую клеточную цитотоксичность (ADCC) варианта моноспецифического анти-FLT3 антитела. Показан специфический лизис FLT3+ лейкозных клеток (SEM; DSMZ № ACC 546) аллогенными поликлональными природными киллерными клетками (pNKC) в присутствии указанных FLT3 конструкций или Fc-контроля (каждый 5 мкг/мл), измеренный с использованием 2 ч анализов цитотоксичности с использованием BATDA-европия.
[146] ABP по изобретению все описаны в перечне последовательностей и в следующей таблице 1:
ПРИМЕРЫ
[147] Некоторые аспекты и варианты осуществления изобретения будут проиллюстрированы при помощи примеров и со ссылкой на описание, чертежи и таблицы, представленные в настоящей заявке. Такие примеры способов, применений и других аспектов настоящего изобретения являются только репрезентативными, и не должны рассматриваться как ограничение объема настоящего изобретения только такими репрезентативными примерами.
[148] Примеры показывают:
[149] Пример 1: Получение рекомбинантных биспецифических FLT3xCD3 ABP (CC-2)
[150] 4G8 анти-FLT3 антитело использовали для конструирования рекомбинантных биспецифических ABP в IgGsc формате (Фиг. 1), т.е. вариабельный домен мышиного антитела к FLT3, 4G8, сливали с человеческими константными областями и вариабельными областями антитела к CD3, UCHT1, в следующем порядке. VL-CL для легкой цепи и VH-CH1-CH2mod-CH3-scFv(UCHT1) для тяжелой цепи (см. Фиг. 1). В этих ABP FLT3-связывающий сайт присутствует в виде Fab2 фрагмента, тогда как CD3-связывающий сайт присутствует в виде scFv фрагмента (снова см. Фиг. 1). Для подавления FcR-связывания следующие модификации были введены в шарнирную область и CH2 домен (EU-индекс): E233P; L234V; L235A; ΔG236; D265G;; A327Q; A330S (см. в этой связи также Международную патентную заявку WO 2013/092001). Конструкции клонировали в вектор экспрессии, полученный из pcDNA3.1 (InVitrogen, Thermo Fisher), как также описано в Международной патентной заявке WO 2013/092001, и транзиентно трансфицировали в CHO-клетки. ABPs очищали из супернатантов трансфицированных клеток аффинной хроматографией со смолами с Белком A. (закупали у GE Health Care Freiburg, Germany). Полученное мышиное FLT3xCD3 биспецифическое антитело обозначается как V6-V6.
[151] Пример 2: Получение гуманизированных 4G8 антител
[152] Анти-FLT3 антитело 4G8 гуманизировали путем прививки CDR областей легкой цепи антитела 4G8 (что означает CDR петли из SEQ ID NO: 5 - SEQ ID NO: 7) в (вариабельный домен) человеческой последовательности κ-легкой цепи IGKV3-15*01, которая депонирована в базе данных IMGT/LIGM под номером доступа M23090, см. также Ichiyoshi Y., Zhou M., Casali P. A human anti-insulin IgG autoantibody apparently arises through clonal selection from an insulin-specific 'germ-line' natural antibody template. Analysis by V gene segment reassortment and site-directed mutagenesis' J. Immunol. 154(1):226-238 (1995). Затем CDR области тяжелой цепи антитела 4G8 (что означает CDR петли из SEQ ID NO: 01 - SEQ ID NO: 03) включали в (вариабельные домены) последовательности тяжелой цепи IGHV1-46*03, которая депонирована в базе данных IMGT/LIGM под номером доступа L06612 (см. также Watson C.T., et al. Complete haplotype sequence of the human immunoglobulin heavy-chain variable, diversity, and joining genes and characterization of allelic and copy-number variation. Am. J. Hum. Genet. 92(4):530-546 (2013). Полученное гуманизированное 4G8 использовали в качестве основы для мутационного анализа/вариантов настоящего изобретения.
[153] Пример 3: Получение вариантов биспецифических FLT3xCD3 ABP (CC-2) по изобретению
[154] Были получены несколько вариантов (V1-V5) FLT3-связывающего домена гуманизированного 4G8. Кроме того, несколько описанных в публикациях вариантов CD3-связывающего домена scFv, полученных из гуманизированного анти-CD3 антитела UCHT1 (V7 - V9), использовали в различных комбинациях с вариантами FLT3-связывающего домена по изобретению. Были идентифицированы следующие предпочтительные мутированные варианты, обладающие специфическими техническими эффектами, которые желательны для использования таких гуманизированных вариантов 4G8 (CDR подчеркнуты, а мутации указаны относительно соответствующих тяжелых и легких цепей, присутствующих в FLT3 антиген - связывающем домене гуманизированного 4G8, которые обозначены как вариант 0 или V0)
[155] Вариант 1 (V1) Вариабельные области гуманизированного 4G8 к FLT3
Вариабельная область тяжелой цепи:
Мутации: K16G, V18L, K19R, V20L, K22A, K57T, N60A, M69I, T70S, T75K, S76N, V78L, M80L, E81Q, S87A, T108L
QVQLVQSGAEVKKPGGSLRLSCAASGYTFTSYWMHWVRQAPGQGLEWIGEIDPSDSYTDYAQKFKDRVTISRDTSKNTLYLQLSSLRAEDTAVYYCARAITTTPFDFWGQGTLVTVSS.
Вариабельная область легкой цепи:
Мутации: K49Y, I55A
EIVMTQSPATLSVSPGERATLSCRASQSISNNLHWYQQKPGQAPRLLIYYASQSASGIPARFSGSGSGTEFTLTISSLQSEDFAVYFCQQSNTWPYTFGGGTKLEIK
[156] Вариант 2 (V2) Вариабельные области гуманизированного 4G8 к FLT3
Вариабельная область тяжелой цепи:
Мутации: K16G, V18L, K19R, V20L, K22A, K57T, N60A, M69I, T70S, T75K, S76N, V78L, M80L, E81Q, S87A, T108L
QVQLVQSGAEVKKPGGSLRLSCAASGYTFTSYWMHWVRQAPGQGLEWIGEIDPSDSYTDYAQKFKDRVTISRDTSKNTLYLQLSSLRAEDTAVYYCARAITTTPFDFWGQGTLVTVSS
Вариабельная область легкой цепи:
EIVMTQSPATLSVSPGERATLSCRASQSISNNLHWYQQKPGQAPRLLIKYASQSISGIPARFSGSGSGTEFTLTISSLQSEDFAVYFCQQSNTWPYTFGGGTKLEIK
[157] Вариант 3 (V3) Вариабельные области гуманизированного 4G8 к FLT3
Вариабельная область тяжелой цепи:
Мутации: 48I
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVRQAPGQGLEWIGEIDPSDSYKDYNQKFKDRVTMTRDTSTSTVYMELSSLRSEDTAVYYCARAITTTPFDFWGQGTTVTVSS
Вариабельная область легкой цепи:
Мутации: K49Y, I55A
EIVMTQSPATLSVSPGERATLSCRASQSISNNLHWYQQKPGQAPRLLIYYASQSASGIPARFSGSGSGTEFTLTISSLQSEDFAVYFCQQSNTWPYTFGGGTKLEIK
[158] Вариант 4 (V4) Вариабельные области гуманизированного 4G8 к FLT3
Вариабельная область тяжелой цепи:
Мутации: 48I
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWMHWVRQAPGQGLEWIGEIDPSDSYKDYNQKFKDRVTMTRDTSTSTVYMELSSLRSEDTAVYYCARAITTTPFDFWGQGTTVTVSS
Вариабельная область легкой цепи:
Мутации: 49K, 87F
EIVMTQSPATLSVSPGERATLSCRASQSISNNLHWYQQKPGQAPRLLIKYASQSISGIPARFSGSGSGTEFTLTISSLQSEDFAVYFCQQSNTWPYTFGGGTKLEIK
[159] Вариант 5 (V5) Вариабельные области гуманизированного 4G8 к FLT3
Вариабельная область тяжелой цепи:
Мутации: K16G, V18L, K19R, V20L, K22A, M69I, T70S, T75K, S76N, V78L, M80L, E81Q, S87A, T108L
QVQLVQSGAEVKKPGGSLRLSCAASGYTFTSYWMHWVRQAPGQGLEWIGEIDPSDSYKDYNQKFKDRVTISRDTSKNTLYLQLSSLRAEDTAVYYCARAITTTPFDFWGQGTLVTVSS
Вариабельная область легкой цепи:
EIVMTQSPATLSVSPGERATLSCRASQSISNNLHWYQQKPGQAPRLLIKYASQSISGIPARFSGSGSGTEFTLTISSLQSEDFAVYFCQQSNTWPYTFGGGTKLEIK
[160] Вариант 1 (V7) scFv гуманизированного UCHT1 к CD3
Мутации: N60A, Q61D, K62S, D65G, K73D
DIQMTQSPSSLSASVGDRVTITCRASQDIRNYLNWYQQKPGKAPKLLIYYTSRLESGVPSRFSGSGSGTDYTLTISSLQPEDFATYYCQQGNTLPWTFGQGTKVEIKGGGGSGGGGSGGGGSEVQLVESGGGLVQPGGSLRLSCAASGYSFTGYTMNWVRQAPGKGLEWVALINPYKGVSTYADSFKGRFTISVDDSKNTAYLQMNSLRAEDTAVYYCARSGYYGDSDWYFDVWGQGTLVTVSS
[161] Вариант 2 (V8) scFv гуманизированного UCHT1 к CD3
Мутации: K73D
DIQMTQSPSSLSASVGDRVTITCRASQDIRNYLNWYQQKPGKAPKLLIYYTSRLESGVPSRFSGSGSGTDYTLTISSLQPEDFATYYCQQGNTLPWTFGQGTKVEIKGGGGSGGGGSGGGGSEVQLVESGGGLVQPGGSLRLSCAASGYSFTGYTMNWVRQAPGKGLEWVALINPYKGVSTYNQKFKDRFTISVDDSKNTAYLQMNSLRAEDTAVYYCARSGYYGDSDWYFDVWGQGTLVTVSS
[162] Вариант 3 (V9) scFv гуманизированного UCHT1 к CD3
Мутации: замена легкая цепь - тяжелая цепь (VL-VH → VH-VL):
EVQLVESGGGLVQPGGSLRLSCAASGYSFTGYTMNWVRQAPGKGLEWVALINPYKGVSTYNQKFKDRFTISVDKSKNTAYLQMNSLRAEDTAVYYCARSGYYGDSDWYFDVWGQGTLVTVSSGGGGSGGGGSGGGGSDIQMTQSPSSLSASVGDRVTITCRASQDIRNYLNWYQQKPGKAPKLLIYYTSRLESGVPSRFSGSGSGTDYTLTISSLQPEDFATYYCQQGNTLPWTFGQGTKVEIK
Представленные выше варианты использовали для создания вариантов биспецифических ABP, как показано в таблице 1 выше.
[163] Пример 4: Аффинность связывания вариантов FLT3 антигенсвязывающего домена гуманизированного 4G8.
[164] На Фиг. 3 показано связывание различных вариантов V1-V5 FLT3-связывающего домена, описанных выше, которые были испытаны на их константу диссоциации с использованием растворимого рекомбинантного белка FLT3. Соответствующие варианты антител иммобилизовывали на чипе Biacore, покрытом белком A, и определяли связывание His-меченного рекомбинантного белка FLT3 (Sino Biologicals) с использованием устройства Biacore X (GE Healthcare). Результаты показаны в таблице 2:
[165] Кроме того, аффинность связывания антитела также испытывали с использованием связывания антитела с его мишенью (мишенями), экспрессированными на клетках. Проанализировано связывание вариантов CC-2 с клетками Nalm16, экспрессирующими FLT3 (Фиг. 4), или клетками Jurkat, экспрессирующими CD3 (Фиг. 6). Варианты V1-V9 (где V6 представляет собой V6-V6) были получены после транзиентной трансфекции клеток СНО с использованием вставленных последовательностей, перечисленных выше. Антитела очищали аффинной хроматографией с белком А и эксклюзионной хроматографией. V1-V5 содержат различные варианты антитела к FLT3, как указано выше, и идентичного CD3-связывающего антитела (вариант UCHT1, который связывается с CD3 с EC50 ~ 10 нМ). V6-V9 содержат исходное антитело 4G8, которое связывается с FLT3 с EC50 ~ 1 нМ, и различные варианты UCHT1. Для измерения связывания антител с FLT3 и CD3 клетки NALM16 (FLT3+) и Jurkat (CD3+) инкубировали с соответствующими вариантами в течение 30 минут, промывали, окрашивали козьим анти-человеческим Fcγ-специфическим и PE-конъюгированным вторичным антителом (Jackson Immuno Research), снова промывали и анализировали с использованием метода проточной цитометрии (FACSCalibur, BD Biosciences).
[166] Выводы: Как показано на Фиг. 3 и 4, вариант 5 имеет наивысшее сродство связывания с FLT3, за которым следует V4, как измерено методами поверхностного плазмонного резонанса (Biacore) и проточной цитометрии, соответственно.
[167] Пример 5: Истощение лейкозных клеток из образцов крови пациентов с AML с использованием различных вариантов FLT3-связывающего или CD3-связывающего домена.
Мононуклеарные клетки периферической крови (PBMC) получали от пациентов с острым лейкозом путем центрифугирования в градиенте плотности, инкубировали в течение 5 дней с указанными вариантами CC-2 при 1 мкг/мл и анализировали методом проточной цитометрии с использованием FACSCanto-II (BD Biosciences). Лейкозные клетки идентифицировали с использованием антител к CD33, CD34 или CD117. Для калибровки количества клеток к каждому образцу добавляли определенное количество компенсационных шариков (BD Biosciences). Данные получали из трех (V4, V5, V6, V9) и двух (V3) независимых экспериментов с клетками от двух разных доноров. Все значения сопоставляли с данными, полученными с контрольным антителом IgGsc с независимой специфичностью. Результаты для FLT3-связывающих вариантов показаны на Фиг. 5, для CD3-связывающих вариантов на Фиг. 7.
[169] Выводы: Антилейкозная активность изначально соответствует значениям сродства на обеих сторонах биспецифической молекулы. Высокоактивным и аффинным к FLT3 является вариант V5. Однако неожиданно, что менее аффинный вариант V4 имеет значительно лучший цитотоксический потенциал против лейкозных клеток по сравнению с другими вариантами, указывая на то, что для определенных применений может быть выбран более низкий диапазон аффинности для анти-FLT3 антител. Аналогичный результат наблюдали для CD3-связывающей части.
[170] Активность Т-клеток и уменьшение бластных клеток анализировали для различных концентраций антител, как показано на Фиг. 8 и 9. Получали препарат PBMC от пациента MM2 и инкубировали с указанными концентрациями вариантов CC-2. Через 5 дней активацию Т-клеток и истощение лейкозных клеток оценивали методом проточной цитометрии (Фиг. 8). Клетки Nalm16 инкубировали в течение 3 дней с указанными концентрациями вариантов CC-2 при соотношении E:T 2:1, а затем анализировали методом проточной цитометрии (Фиг. 9).
[171] Пример 6: Противолейкозная активность ABP по изобретению in vivo.
[172] Для испытания in vivo применения вариантов CC-2 по изобретению предпочтительные варианты для связывания FLT3 и CD3 были испытаны на их терапевтический потенциал на модели иммунодефицитных мышей (Фиг. 10). Мммунодефицитным NSG мышам прививали клетки первичного AML (слева) или ALL (справа). На 7-й день инъецировали РВМС вместе с CC-2 (V4-V6) или контрольным антителом, и bsAb-обработку повторяли на 10-й день. На 17-й день лейкозную нагрузку (соотношение клеток hCD45+/mCD45+) в костном мозге определяли методом проточной цитометрии.
[173] Выводы: эксперимент демонстрирует терапевтический потенциал для даже менее аффинных вариантов CC2, таких как V4.
[174] Изобретение, иллюстративно описанное в настоящей заявке, может быть подходящим образом реализовано на практике при отсутствии какого-либо элемента или элементов, ограничений или ограничений, конкретно не раскрытых в настоящей заявке. Таким образом, например, термины “включающий”, “включая”, “содержащий” и т.д. следует рассматривать широко и без ограничения. Кроме того, используемые в настоящей заявке термины и выражения использовались как термины описания, а не ограничения, и при использовании таких терминов и выражений нет намерения исключать какие-либо эквиваленты показанных и описанных функций или их частей, но признано, что в объеме заявленного изобретения возможны различные модификации. Таким образом, следует понимать, что, хотя настоящее изобретение было конкретно раскрыто посредством иллюстративных вариантов осуществления и дополнительных функций, специалисты могут использовать модификации и вариации изобретений, раскрытых в настоящей заявке, и что такие модификации и вариации считаются входящим в объем данного изобретения.
[175] Пример 7. Гуманизированные варианты 4G8 в формате моноспецифического IgG.
[176] Чтобы протестировать превосходство созданных вариантов антител по изобретению, новые последовательности вариабельных доменов были клонированы в формат моноспецифического анти-FLT3 человеческого IgG. Для этого соответствующие вариабельные последовательности тяжелой и легкой цепи клонировали в формат моноспецифического человеческого IgG. Для этого гены антител были кодон-оптимизированы для экспрессии в клетках человека и сконструированы с сайтами рестрикции NheI и Not на 5’ и 3’ концах. Гены синтезировали и затем клонировали в вектор экспрессии млекопитающих, следуя стандартным процедурам. После проверки последовательностей получали плазмиды в количестве, достаточном для трансфекции, с использованием наборов для очистки Plasmid Plus (Qiagen).
[177] Клетки млекопитающих HEK293 (эмбриональные клетки почки человека 293) пассировали до оптимальной стадии для транзиентной трансфекции. Клетки транзиентно трансфицировали вектором экспрессии и культивировали еще 6 дней.
[178] Культуры собирали центрифугированием при 4000 об/мин и фильтровали через фильтр 0,22 мм. Первую стадию очистки осуществляли методом аффинной хроматографии на никеле с элюированием с использованием PBS, содержащего 400 мМ имидазола. Вторую стадию очистки осуществляли методом эксклюзионной хроматографии с элюированием в PBS (фосфатно-солевой буфер) pH 7,2. Концентрацию антител определяли УФ-спектроскопией и антитела концентрировали, при необходимости. Чистоту антител определяли методом SDS-PAGE (электрофорез в полиакриламидном геле с додецилсульфатом натрия) и ВЭЖХ (высокоэффективная жидкостная хроматография). ВЭЖХ осуществляли на устройстве Agilent серии 1100 с использованием эксклюзионной колонки MabPac, в PBS при 0,2 мл/мин.
[179] Чтобы выяснить превосходство полученных вариантов 4G8, моноспецифический IgG с последовательностями вариабельных доменов тяжелой и легкой цепей варианта V4 (последовательности вариабельных доменов тяжелой и легкой цепей, как показано в SEQ ID NO: 21 и 22, соответственно) сравнивали с исходным (мышиным) IgG V6 (последовательности вариабельных доменов тяжелой и легкой цепей, как показано в SEQ ID NO: 4 и 8, соответственно) и Fc контролем в анализе ADCC. Для этого pNKC были получены путем инкубации не пластик-адгезивных PBMC с питающими клетками K562-41BBL-IL15, полученными от St Jude's Children's Research Hospital, как описано ранее (Schmiedel BJ et al. Int J Cancer 2011; 128: 2911-2922; Fujisaki H et al. Cancer Res 2009; 69: 4010-4017). Киллинг с использованием BATDA-Европия осуществляли, как описано ранее (Baessler T. et al. Cancer Res 2009: 69: 1037-1045). Результаты показаны на Фиг. 11.
[180] Данные на Фиг. 11 показывают иллюстративные результаты для одного pNKC донора при указанных соотношениях эффектор:мишень. Превосходные скорости лизиса для вариантов V4 по сравнению V6 FLT3 моноспецифического IgG могут наблюдаться в этих экспериментальных условиях, что демонстрирует улучшенный терапевтический потенциал вариантов по настоящему изобретению по сравнению с исходным антителом 4G8.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Deutsches Krebsforschungszentrum Stiftung des oeffentlichen
Rechts
Eberhard Karls Universitaet Tuebingen
<120> УЛУЧШЕННЫЕ АНТИ-FLT3 АНТИГЕНСВЯЗЫВАЮЩИЕ БЕЛКИ
<130> D31605WO
<150> EP18193889.5
<151> 2018-09-11
<150> EP19189566.3
<151> 2019-08-01
<160> 79
<170> PatentIn version 3.5
<210> 1
<211> 5
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 1
Ser Tyr Trp Met His
1 5
<210> 2
<211> 17
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 2
Glu Ile Asp Pro Ser Asp Ser Tyr Lys Asp Tyr Asn Gln Lys Phe Lys
1 5 10 15
Asp
<210> 3
<211> 9
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 3
Ala Ile Thr Thr Thr Pro Phe Asp Phe
1 5
<210> 4
<211> 118
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 4
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Leu Lys Leu Ser Cys Lys Ser Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Arg Pro Gly His Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Lys Asp Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Val Asp Arg Ser Ser Asn Thr Ala Tyr
65 70 75 80
Met His Leu Ser Ser Leu Thr Ser Asp Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Thr Leu Thr Val Ser Ser
115
<210> 5
<211> 11
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 5
Arg Ala Ser Gln Ser Ile Ser Asn Asn Leu His
1 5 10
<210> 6
<211> 7
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 6
Tyr Ala Ser Gln Ser Ile Ser
1 5
<210> 7
<211> 9
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 7
Gln Gln Ser Asn Thr Trp Pro Tyr Thr
1 5
<210> 8
<211> 107
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 8
Asp Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Val Thr Pro Gly
1 5 10 15
Asp Ser Val Ser Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Ser His Glu Ser Pro Arg Leu Leu Ile
35 40 45
Lys Tyr Ala Ser Gln Ser Ile Ser Gly Ile Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Ser Ile Asn Ser Val Glu Thr
65 70 75 80
Glu Asp Phe Gly Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 9
<211> 107
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 9
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 10
<211> 98
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 10
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val
<210> 11
<211> 15
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 11
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
1 5 10 15
<210> 12
<211> 109
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 12
Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
1 5 10 15
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
20 25 30
Val Gly Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
35 40 45
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
50 55 60
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
65 70 75 80
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gln
85 90 95
Leu Pro Ser Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
100 105
<210> 13
<211> 109
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 13
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp
1 5 10 15
Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
20 25 30
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
35 40 45
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
50 55 60
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
65 70 75 80
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
85 90 95
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser Gly
100 105
<210> 14
<211> 244
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 14
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu
115 120 125
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
130 135 140
Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val Arg
145 150 155 160
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Leu Ile Asn Pro Tyr
165 170 175
Lys Gly Val Ser Thr Tyr Asn Gln Lys Phe Lys Asp Arg Phe Thr Ile
180 185 190
Ser Val Asp Lys Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu
195 200 205
Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Gly Tyr Tyr
210 215 220
Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp Gly Gln Gly Thr Leu Val
225 230 235 240
Thr Val Ser Ser
<210> 15
<211> 118
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 15
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Thr Asp Tyr Ala Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 16
<211> 107
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 16
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Tyr Ala Ser Gln Ser Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 17
<211> 118
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 17
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Thr Asp Tyr Ala Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 18
<211> 107
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 18
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Lys Tyr Ala Ser Gln Ser Ile Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 19
<211> 118
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 19
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Lys Asp Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser
115
<210> 20
<211> 107
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 20
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Tyr Ala Ser Gln Ser Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 21
<211> 118
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 21
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Lys Asp Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser
115
<210> 22
<211> 107
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 22
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Lys Tyr Ala Ser Gln Ser Ile Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 23
<211> 118
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 23
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Lys Asp Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 24
<211> 107
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 24
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Lys Tyr Ala Ser Gln Ser Ile Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 25
<211> 244
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 25
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu
115 120 125
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
130 135 140
Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val Arg
145 150 155 160
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Leu Ile Asn Pro Tyr
165 170 175
Lys Gly Val Ser Thr Tyr Ala Asp Ser Phe Lys Gly Arg Phe Thr Ile
180 185 190
Ser Val Asp Asp Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu
195 200 205
Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Gly Tyr Tyr
210 215 220
Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp Gly Gln Gly Thr Leu Val
225 230 235 240
Thr Val Ser Ser
<210> 26
<211> 244
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 26
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu
115 120 125
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
130 135 140
Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val Arg
145 150 155 160
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Leu Ile Asn Pro Tyr
165 170 175
Lys Gly Val Ser Thr Tyr Asn Gln Lys Phe Lys Asp Arg Phe Thr Ile
180 185 190
Ser Val Asp Asp Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu
195 200 205
Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Gly Tyr Tyr
210 215 220
Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp Gly Gln Gly Thr Leu Val
225 230 235 240
Thr Val Ser Ser
<210> 27
<211> 244
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 27
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Thr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Leu Ile Asn Pro Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Gly Tyr Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser
130 135 140
Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys
145 150 155 160
Arg Ala Ser Gln Asp Ile Arg Asn Tyr Leu Asn Trp Tyr Gln Gln Lys
165 170 175
Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Tyr Thr Ser Arg Leu Glu
180 185 190
Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr
195 200 205
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr
210 215 220
Cys Gln Gln Gly Asn Thr Leu Pro Trp Thr Phe Gly Gln Gly Thr Lys
225 230 235 240
Val Glu Ile Lys
<210> 28
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 28
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Thr Asp Tyr Ala Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
450 455 460
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn
465 470 475 480
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
485 490 495
Ile Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro Ser Arg Phe Ser
500 505 510
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
515 520 525
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro
530 535 540
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly
545 550 555 560
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
565 570 575
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
580 585 590
Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val
595 600 605
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Leu Ile Asn Pro
610 615 620
Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys Phe Lys Asp Arg Phe Thr
625 630 635 640
Ile Ser Val Asp Lys Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
645 650 655
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Gly Tyr
660 665 670
Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp Gly Gln Gly Thr Leu
675 680 685
Val Thr Val Ser Ser
690
<210> 29
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 29
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Tyr Ala Ser Gln Ser Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 30
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 30
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Thr Asp Tyr Ala Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
450 455 460
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn
465 470 475 480
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
485 490 495
Ile Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro Ser Arg Phe Ser
500 505 510
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
515 520 525
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro
530 535 540
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly
545 550 555 560
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
565 570 575
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
580 585 590
Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val
595 600 605
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Leu Ile Asn Pro
610 615 620
Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys Phe Lys Asp Arg Phe Thr
625 630 635 640
Ile Ser Val Asp Lys Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
645 650 655
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Gly Tyr
660 665 670
Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp Gly Gln Gly Thr Leu
675 680 685
Val Thr Val Ser Ser
690
<210> 31
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 31
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Lys Tyr Ala Ser Gln Ser Ile Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 32
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 32
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Lys Asp Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
450 455 460
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn
465 470 475 480
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
485 490 495
Ile Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro Ser Arg Phe Ser
500 505 510
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
515 520 525
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro
530 535 540
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly
545 550 555 560
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
565 570 575
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
580 585 590
Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val
595 600 605
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Leu Ile Asn Pro
610 615 620
Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys Phe Lys Asp Arg Phe Thr
625 630 635 640
Ile Ser Val Asp Lys Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
645 650 655
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Gly Tyr
660 665 670
Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp Gly Gln Gly Thr Leu
675 680 685
Val Thr Val Ser Ser
690
<210> 33
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 33
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Tyr Ala Ser Gln Ser Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 34
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 34
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Lys Asp Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
450 455 460
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn
465 470 475 480
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
485 490 495
Ile Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro Ser Arg Phe Ser
500 505 510
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
515 520 525
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro
530 535 540
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly
545 550 555 560
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
565 570 575
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
580 585 590
Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val
595 600 605
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Leu Ile Asn Pro
610 615 620
Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys Phe Lys Asp Arg Phe Thr
625 630 635 640
Ile Ser Val Asp Lys Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
645 650 655
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Gly Tyr
660 665 670
Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp Gly Gln Gly Thr Leu
675 680 685
Val Thr Val Ser Ser
690
<210> 35
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 35
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Lys Tyr Ala Ser Gln Ser Ile Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 36
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 36
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Lys Asp Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
450 455 460
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn
465 470 475 480
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
485 490 495
Ile Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro Ser Arg Phe Ser
500 505 510
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
515 520 525
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro
530 535 540
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly
545 550 555 560
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
565 570 575
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
580 585 590
Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val
595 600 605
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Leu Ile Asn Pro
610 615 620
Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys Phe Lys Asp Arg Phe Thr
625 630 635 640
Ile Ser Val Asp Lys Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
645 650 655
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Gly Tyr
660 665 670
Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp Gly Gln Gly Thr Leu
675 680 685
Val Thr Val Ser Ser
690
<210> 37
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 37
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Lys Tyr Ala Ser Gln Ser Ile Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 38
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 38
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Thr Asp Tyr Ala Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
450 455 460
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn
465 470 475 480
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
485 490 495
Ile Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro Ser Arg Phe Ser
500 505 510
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
515 520 525
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro
530 535 540
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly
545 550 555 560
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
565 570 575
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
580 585 590
Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val
595 600 605
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Leu Ile Asn Pro
610 615 620
Tyr Lys Gly Val Ser Thr Tyr Ala Asp Ser Phe Lys Gly Arg Phe Thr
625 630 635 640
Ile Ser Val Asp Asp Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
645 650 655
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Gly Tyr
660 665 670
Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp Gly Gln Gly Thr Leu
675 680 685
Val Thr Val Ser Ser
690
<210> 39
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 39
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Tyr Ala Ser Gln Ser Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 40
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 40
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Thr Asp Tyr Ala Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
450 455 460
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn
465 470 475 480
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
485 490 495
Ile Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro Ser Arg Phe Ser
500 505 510
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
515 520 525
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro
530 535 540
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly
545 550 555 560
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
565 570 575
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
580 585 590
Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val
595 600 605
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Leu Ile Asn Pro
610 615 620
Tyr Lys Gly Val Ser Thr Tyr Ala Asp Ser Phe Lys Gly Arg Phe Thr
625 630 635 640
Ile Ser Val Asp Asp Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
645 650 655
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Gly Tyr
660 665 670
Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp Gly Gln Gly Thr Leu
675 680 685
Val Thr Val Ser Ser
690
<210> 41
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 41
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Lys Tyr Ala Ser Gln Ser Ile Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 42
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 42
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Lys Asp Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
450 455 460
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn
465 470 475 480
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
485 490 495
Ile Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro Ser Arg Phe Ser
500 505 510
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
515 520 525
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro
530 535 540
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly
545 550 555 560
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
565 570 575
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
580 585 590
Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val
595 600 605
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Leu Ile Asn Pro
610 615 620
Tyr Lys Gly Val Ser Thr Tyr Ala Asp Ser Phe Lys Gly Arg Phe Thr
625 630 635 640
Ile Ser Val Asp Asp Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
645 650 655
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Gly Tyr
660 665 670
Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp Gly Gln Gly Thr Leu
675 680 685
Val Thr Val Ser Ser
690
<210> 43
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 43
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Tyr Ala Ser Gln Ser Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 44
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 44
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Lys Asp Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
450 455 460
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn
465 470 475 480
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
485 490 495
Ile Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro Ser Arg Phe Ser
500 505 510
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
515 520 525
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro
530 535 540
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly
545 550 555 560
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
565 570 575
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
580 585 590
Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val
595 600 605
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Leu Ile Asn Pro
610 615 620
Tyr Lys Gly Val Ser Thr Tyr Ala Asp Ser Phe Lys Gly Arg Phe Thr
625 630 635 640
Ile Ser Val Asp Asp Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
645 650 655
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Gly Tyr
660 665 670
Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp Gly Gln Gly Thr Leu
675 680 685
Val Thr Val Ser Ser
690
<210> 45
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 45
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Lys Tyr Ala Ser Gln Ser Ile Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 46
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 46
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Lys Asp Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
450 455 460
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn
465 470 475 480
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
485 490 495
Ile Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro Ser Arg Phe Ser
500 505 510
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
515 520 525
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro
530 535 540
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly
545 550 555 560
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
565 570 575
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
580 585 590
Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val
595 600 605
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Leu Ile Asn Pro
610 615 620
Tyr Lys Gly Val Ser Thr Tyr Ala Asp Ser Phe Lys Gly Arg Phe Thr
625 630 635 640
Ile Ser Val Asp Asp Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
645 650 655
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Gly Tyr
660 665 670
Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp Gly Gln Gly Thr Leu
675 680 685
Val Thr Val Ser Ser
690
<210> 47
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 47
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Lys Tyr Ala Ser Gln Ser Ile Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 48
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 48
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Thr Asp Tyr Ala Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
450 455 460
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn
465 470 475 480
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
485 490 495
Ile Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro Ser Arg Phe Ser
500 505 510
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
515 520 525
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro
530 535 540
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly
545 550 555 560
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
565 570 575
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
580 585 590
Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val
595 600 605
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Leu Ile Asn Pro
610 615 620
Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys Phe Lys Asp Arg Phe Thr
625 630 635 640
Ile Ser Val Asp Asp Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
645 650 655
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Gly Tyr
660 665 670
Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp Gly Gln Gly Thr Leu
675 680 685
Val Thr Val Ser Ser
690
<210> 49
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 49
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Tyr Ala Ser Gln Ser Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 50
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 50
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Thr Asp Tyr Ala Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
450 455 460
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn
465 470 475 480
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
485 490 495
Ile Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro Ser Arg Phe Ser
500 505 510
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
515 520 525
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro
530 535 540
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly
545 550 555 560
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
565 570 575
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
580 585 590
Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val
595 600 605
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Leu Ile Asn Pro
610 615 620
Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys Phe Lys Asp Arg Phe Thr
625 630 635 640
Ile Ser Val Asp Asp Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
645 650 655
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Gly Tyr
660 665 670
Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp Gly Gln Gly Thr Leu
675 680 685
Val Thr Val Ser Ser
690
<210> 51
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 51
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Lys Tyr Ala Ser Gln Ser Ile Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 52
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 52
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Lys Asp Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
450 455 460
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn
465 470 475 480
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
485 490 495
Ile Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro Ser Arg Phe Ser
500 505 510
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
515 520 525
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro
530 535 540
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly
545 550 555 560
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
565 570 575
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
580 585 590
Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val
595 600 605
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Leu Ile Asn Pro
610 615 620
Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys Phe Lys Asp Arg Phe Thr
625 630 635 640
Ile Ser Val Asp Asp Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
645 650 655
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Gly Tyr
660 665 670
Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp Gly Gln Gly Thr Leu
675 680 685
Val Thr Val Ser Ser
690
<210> 53
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 53
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Tyr Ala Ser Gln Ser Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 54
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 54
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Lys Asp Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
450 455 460
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn
465 470 475 480
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
485 490 495
Ile Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro Ser Arg Phe Ser
500 505 510
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
515 520 525
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro
530 535 540
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly
545 550 555 560
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
565 570 575
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
580 585 590
Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val
595 600 605
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Leu Ile Asn Pro
610 615 620
Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys Phe Lys Asp Arg Phe Thr
625 630 635 640
Ile Ser Val Asp Asp Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
645 650 655
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Gly Tyr
660 665 670
Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp Gly Gln Gly Thr Leu
675 680 685
Val Thr Val Ser Ser
690
<210> 55
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 55
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Lys Tyr Ala Ser Gln Ser Ile Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 56
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 56
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Lys Asp Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
450 455 460
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn
465 470 475 480
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
485 490 495
Ile Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro Ser Arg Phe Ser
500 505 510
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
515 520 525
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro
530 535 540
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly
545 550 555 560
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
565 570 575
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
580 585 590
Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val
595 600 605
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Leu Ile Asn Pro
610 615 620
Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys Phe Lys Asp Arg Phe Thr
625 630 635 640
Ile Ser Val Asp Asp Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
645 650 655
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Gly Tyr
660 665 670
Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp Gly Gln Gly Thr Leu
675 680 685
Val Thr Val Ser Ser
690
<210> 57
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 57
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Lys Tyr Ala Ser Gln Ser Ile Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 58
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 58
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Thr Asp Tyr Ala Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
450 455 460
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly
465 470 475 480
Tyr Thr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
485 490 495
Val Ala Leu Ile Asn Pro Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys
500 505 510
Phe Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ser Lys Asn Thr Ala
515 520 525
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
530 535 540
Cys Ala Arg Ser Gly Tyr Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val
545 550 555 560
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
565 570 575
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
580 585 590
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
595 600 605
Cys Arg Ala Ser Gln Asp Ile Arg Asn Tyr Leu Asn Trp Tyr Gln Gln
610 615 620
Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Tyr Thr Ser Arg Leu
625 630 635 640
Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
645 650 655
Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
660 665 670
Tyr Cys Gln Gln Gly Asn Thr Leu Pro Trp Thr Phe Gly Gln Gly Thr
675 680 685
Lys Val Glu Ile Lys
690
<210> 59
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 59
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Tyr Ala Ser Gln Ser Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 60
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 60
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Thr Asp Tyr Ala Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
450 455 460
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly
465 470 475 480
Tyr Thr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
485 490 495
Val Ala Leu Ile Asn Pro Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys
500 505 510
Phe Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ser Lys Asn Thr Ala
515 520 525
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
530 535 540
Cys Ala Arg Ser Gly Tyr Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val
545 550 555 560
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
565 570 575
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
580 585 590
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
595 600 605
Cys Arg Ala Ser Gln Asp Ile Arg Asn Tyr Leu Asn Trp Tyr Gln Gln
610 615 620
Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Tyr Thr Ser Arg Leu
625 630 635 640
Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
645 650 655
Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
660 665 670
Tyr Cys Gln Gln Gly Asn Thr Leu Pro Trp Thr Phe Gly Gln Gly Thr
675 680 685
Lys Val Glu Ile Lys
690
<210> 61
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 61
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Lys Tyr Ala Ser Gln Ser Ile Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 62
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 62
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Lys Asp Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
450 455 460
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly
465 470 475 480
Tyr Thr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
485 490 495
Val Ala Leu Ile Asn Pro Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys
500 505 510
Phe Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ser Lys Asn Thr Ala
515 520 525
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
530 535 540
Cys Ala Arg Ser Gly Tyr Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val
545 550 555 560
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
565 570 575
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
580 585 590
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
595 600 605
Cys Arg Ala Ser Gln Asp Ile Arg Asn Tyr Leu Asn Trp Tyr Gln Gln
610 615 620
Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Tyr Thr Ser Arg Leu
625 630 635 640
Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
645 650 655
Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
660 665 670
Tyr Cys Gln Gln Gly Asn Thr Leu Pro Trp Thr Phe Gly Gln Gly Thr
675 680 685
Lys Val Glu Ile Lys
690
<210> 63
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 63
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Tyr Ala Ser Gln Ser Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 64
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 64
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Lys Asp Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
450 455 460
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly
465 470 475 480
Tyr Thr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
485 490 495
Val Ala Leu Ile Asn Pro Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys
500 505 510
Phe Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ser Lys Asn Thr Ala
515 520 525
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
530 535 540
Cys Ala Arg Ser Gly Tyr Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val
545 550 555 560
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
565 570 575
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
580 585 590
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
595 600 605
Cys Arg Ala Ser Gln Asp Ile Arg Asn Tyr Leu Asn Trp Tyr Gln Gln
610 615 620
Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Tyr Thr Ser Arg Leu
625 630 635 640
Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
645 650 655
Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
660 665 670
Tyr Cys Gln Gln Gly Asn Thr Leu Pro Trp Thr Phe Gly Gln Gly Thr
675 680 685
Lys Val Glu Ile Lys
690
<210> 65
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 65
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Lys Tyr Ala Ser Gln Ser Ile Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 66
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 66
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Lys Asp Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
450 455 460
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly
465 470 475 480
Tyr Thr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
485 490 495
Val Ala Leu Ile Asn Pro Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys
500 505 510
Phe Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ser Lys Asn Thr Ala
515 520 525
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
530 535 540
Cys Ala Arg Ser Gly Tyr Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val
545 550 555 560
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
565 570 575
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
580 585 590
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
595 600 605
Cys Arg Ala Ser Gln Asp Ile Arg Asn Tyr Leu Asn Trp Tyr Gln Gln
610 615 620
Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Tyr Thr Ser Arg Leu
625 630 635 640
Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
645 650 655
Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
660 665 670
Tyr Cys Gln Gln Gly Asn Thr Leu Pro Trp Thr Phe Gly Gln Gly Thr
675 680 685
Lys Val Glu Ile Lys
690
<210> 67
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 67
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Lys Tyr Ala Ser Gln Ser Ile Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 68
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 68
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Leu Lys Leu Ser Cys Lys Ser Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Arg Pro Gly His Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Lys Asp Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Val Asp Arg Ser Ser Asn Thr Ala Tyr
65 70 75 80
Met His Leu Ser Ser Leu Thr Ser Asp Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Thr Leu Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
450 455 460
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn
465 470 475 480
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
485 490 495
Ile Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro Ser Arg Phe Ser
500 505 510
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
515 520 525
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro
530 535 540
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly
545 550 555 560
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
565 570 575
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
580 585 590
Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val
595 600 605
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Leu Ile Asn Pro
610 615 620
Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys Phe Lys Asp Arg Phe Thr
625 630 635 640
Ile Ser Val Asp Lys Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
645 650 655
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Gly Tyr
660 665 670
Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp Gly Gln Gly Thr Leu
675 680 685
Val Thr Val Ser Ser
690
<210> 69
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 69
Asp Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Val Thr Pro Gly
1 5 10 15
Asp Ser Val Ser Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Ser His Glu Ser Pro Arg Leu Leu Ile
35 40 45
Lys Tyr Ala Ser Gln Ser Ile Ser Gly Ile Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Ser Ile Asn Ser Val Glu Thr
65 70 75 80
Glu Asp Phe Gly Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 70
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 70
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Leu Lys Leu Ser Cys Lys Ser Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Arg Pro Gly His Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Lys Asp Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Val Asp Arg Ser Ser Asn Thr Ala Tyr
65 70 75 80
Met His Leu Ser Ser Leu Thr Ser Asp Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Thr Leu Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
450 455 460
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn
465 470 475 480
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
485 490 495
Ile Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro Ser Arg Phe Ser
500 505 510
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
515 520 525
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro
530 535 540
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly
545 550 555 560
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
565 570 575
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
580 585 590
Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val
595 600 605
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Leu Ile Asn Pro
610 615 620
Tyr Lys Gly Val Ser Thr Tyr Ala Asp Ser Phe Lys Gly Arg Phe Thr
625 630 635 640
Ile Ser Val Asp Asp Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
645 650 655
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Gly Tyr
660 665 670
Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp Gly Gln Gly Thr Leu
675 680 685
Val Thr Val Ser Ser
690
<210> 71
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 71
Asp Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Val Thr Pro Gly
1 5 10 15
Asp Ser Val Ser Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Ser His Glu Ser Pro Arg Leu Leu Ile
35 40 45
Lys Tyr Ala Ser Gln Ser Ile Ser Gly Ile Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Ser Ile Asn Ser Val Glu Thr
65 70 75 80
Glu Asp Phe Gly Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 72
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 72
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Leu Lys Leu Ser Cys Lys Ser Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Arg Pro Gly His Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Lys Asp Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Val Asp Arg Ser Ser Asn Thr Ala Tyr
65 70 75 80
Met His Leu Ser Ser Leu Thr Ser Asp Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Thr Leu Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
450 455 460
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn
465 470 475 480
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
485 490 495
Ile Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro Ser Arg Phe Ser
500 505 510
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
515 520 525
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro
530 535 540
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly
545 550 555 560
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
565 570 575
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
580 585 590
Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val
595 600 605
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Leu Ile Asn Pro
610 615 620
Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys Phe Lys Asp Arg Phe Thr
625 630 635 640
Ile Ser Val Asp Asp Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
645 650 655
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Gly Tyr
660 665 670
Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp Gly Gln Gly Thr Leu
675 680 685
Val Thr Val Ser Ser
690
<210> 73
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 73
Asp Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Val Thr Pro Gly
1 5 10 15
Asp Ser Val Ser Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Ser His Glu Ser Pro Arg Leu Leu Ile
35 40 45
Lys Tyr Ala Ser Gln Ser Ile Ser Gly Ile Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Ser Ile Asn Ser Val Glu Thr
65 70 75 80
Glu Asp Phe Gly Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 74
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 74
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Leu Lys Leu Ser Cys Lys Ser Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Arg Pro Gly His Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Lys Asp Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Val Asp Arg Ser Ser Asn Thr Ala Tyr
65 70 75 80
Met His Leu Ser Ser Leu Thr Ser Asp Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Thr Leu Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
450 455 460
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly
465 470 475 480
Tyr Thr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
485 490 495
Val Ala Leu Ile Asn Pro Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys
500 505 510
Phe Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ser Lys Asn Thr Ala
515 520 525
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
530 535 540
Cys Ala Arg Ser Gly Tyr Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val
545 550 555 560
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
565 570 575
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
580 585 590
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
595 600 605
Cys Arg Ala Ser Gln Asp Ile Arg Asn Tyr Leu Asn Trp Tyr Gln Gln
610 615 620
Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Tyr Thr Ser Arg Leu
625 630 635 640
Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
645 650 655
Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
660 665 670
Tyr Cys Gln Gln Gly Asn Thr Leu Pro Trp Thr Phe Gly Gln Gly Thr
675 680 685
Lys Val Glu Ile Lys
690
<210> 75
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 75
Asp Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Val Thr Pro Gly
1 5 10 15
Asp Ser Val Ser Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Ser His Glu Ser Pro Arg Leu Leu Ile
35 40 45
Lys Tyr Ala Ser Gln Ser Ile Ser Gly Ile Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Ser Ile Asn Ser Val Glu Thr
65 70 75 80
Glu Asp Phe Gly Val Tyr Phe Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 76
<211> 118
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 76
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Lys Asp Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser
115
<210> 77
<211> 107
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 77
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Tyr Ala Ser Gln Ser Ile Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 78
<211> 693
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 78
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Glu Ile Asp Pro Ser Asp Ser Tyr Lys Asp Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ile Thr Thr Thr Pro Phe Asp Phe Trp Gly Gln Gly Thr
100 105 110
Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Gly Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gln Leu Pro Ser Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser
435 440 445
Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
450 455 460
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn
465 470 475 480
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
485 490 495
Ile Tyr Tyr Thr Ser Arg Leu Glu Ser Gly Val Pro Ser Arg Phe Ser
500 505 510
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
515 520 525
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro
530 535 540
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly
545 550 555 560
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val
565 570 575
Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser
580 585 590
Cys Ala Ala Ser Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn Trp Val
595 600 605
Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Leu Ile Asn Pro
610 615 620
Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys Phe Lys Asp Arg Phe Thr
625 630 635 640
Ile Ser Val Asp Lys Ser Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser
645 650 655
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Gly Tyr
660 665 670
Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp Gly Gln Gly Thr Leu
675 680 685
Val Thr Val Ser Ser
690
<210> 79
<211> 214
<212> Белок
<213> искусственная
<220>
<223> вариантная последовательность антитела
<400> 79
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Asn
20 25 30
Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Tyr Ala Ser Gln Ser Ile Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Ser
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Asn Thr Trp Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИГЕНСВЯЗЫВАЮЩИЕ БЕЛКИ ПРОТИВ TIGIT И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2776714C2 |
| АНТИГЕНСВЯЗЫВАЮЩИЕ БЕЛКИ ПРОТИВ GITR И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2795625C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, НАЦЕЛЕННЫЕ НА FLT3 | 2018 |
|
RU2820859C2 |
| АНТИТЕЛА, СПЕЦИФИЧНЫЕ К FLT3, И ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2758513C2 |
| АНТИТЕЛО ПРОТИВ ПРОТЕИНТИРОЗИНФОСФАТАЗЫ σ РЕЦЕПТОРНОГО ТИПА ЧЕЛОВЕКА | 2012 |
|
RU2715642C2 |
| АНТИТЕЛА И КОМПОЗИЦИИ ПРОТИВ FLT3 | 2021 |
|
RU2836004C1 |
| АНТИТЕЛА К РЕЦЕПТОРУ IL4 ДЛЯ ПРИМЕНЕНИЯ В ВЕТЕРИНАРИИ | 2019 |
|
RU2837141C2 |
| АНТИ-IL31 АНТИТЕЛА ДЛЯ ПРИМЕНЕНИЯ В ВЕТЕРИНАРИИ | 2020 |
|
RU2835543C1 |
| ВЫДЕЛЕННОЕ АНТИТЕЛО (ВАРИАНТЫ), СПОСОБ ПОЛУЧЕНИЯ АНТИТЕЛА, ВЫДЕЛЕННАЯ НУКЛЕИНОВАЯ КИСЛОТА, ЭКСПРЕССИОННАЯ КАССЕТА (ВАРИАНТЫ), ПЛАЗМИДА (ВАРИАНТЫ), КЛЕТКА-ХОЗЯИН, ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ, НАБОР, СПОСОБ ЛЕЧЕНИЯ БОЛЬНОГО, ПОДВЕРЖЕННОГО РИСКУ ИЛИ СТРАДАЮЩЕГО ОТ ИНФЕКЦИИ E.COLI, И СПОСОБ ДИАГНОСТИКИ ОПРЕДЕЛЕНИЯ ИНФЕКЦИЙ E.COLI | 2014 |
|
RU2724530C2 |
| СЛИТЫЙ БЕЛОК, ВКЛЮЧАЮЩИЙ IL-12 И АНТИТЕЛО ПРОТИВ FAP, И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2831612C1 |
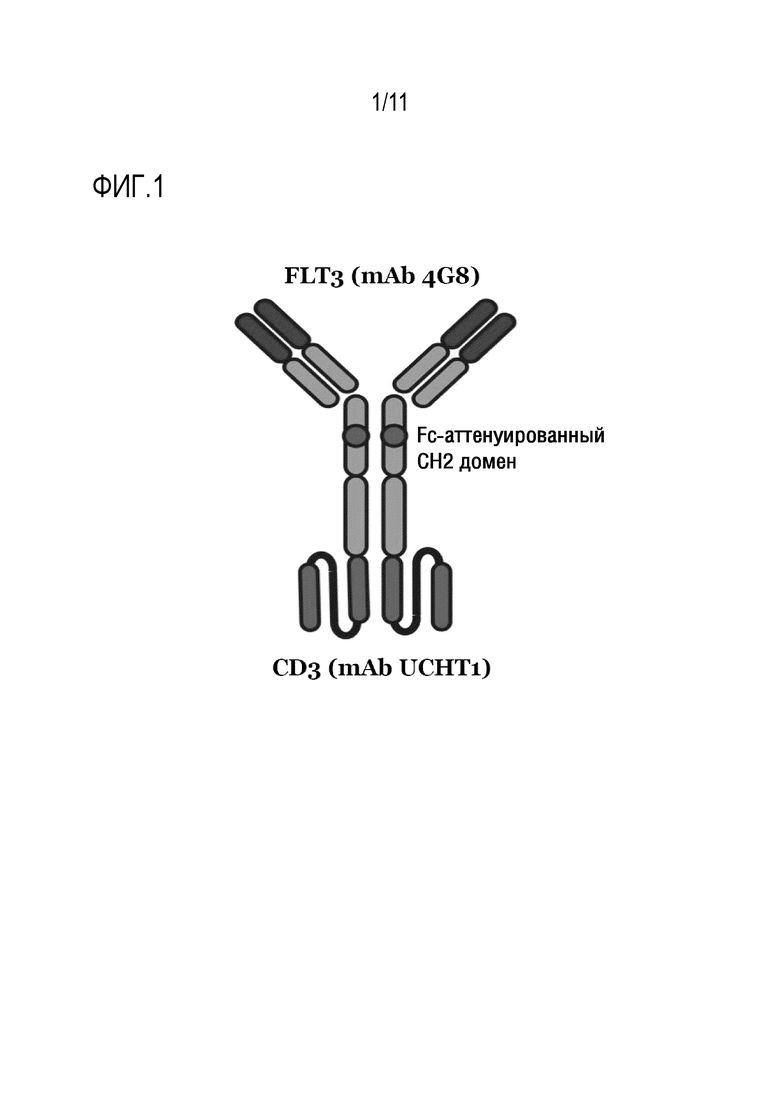

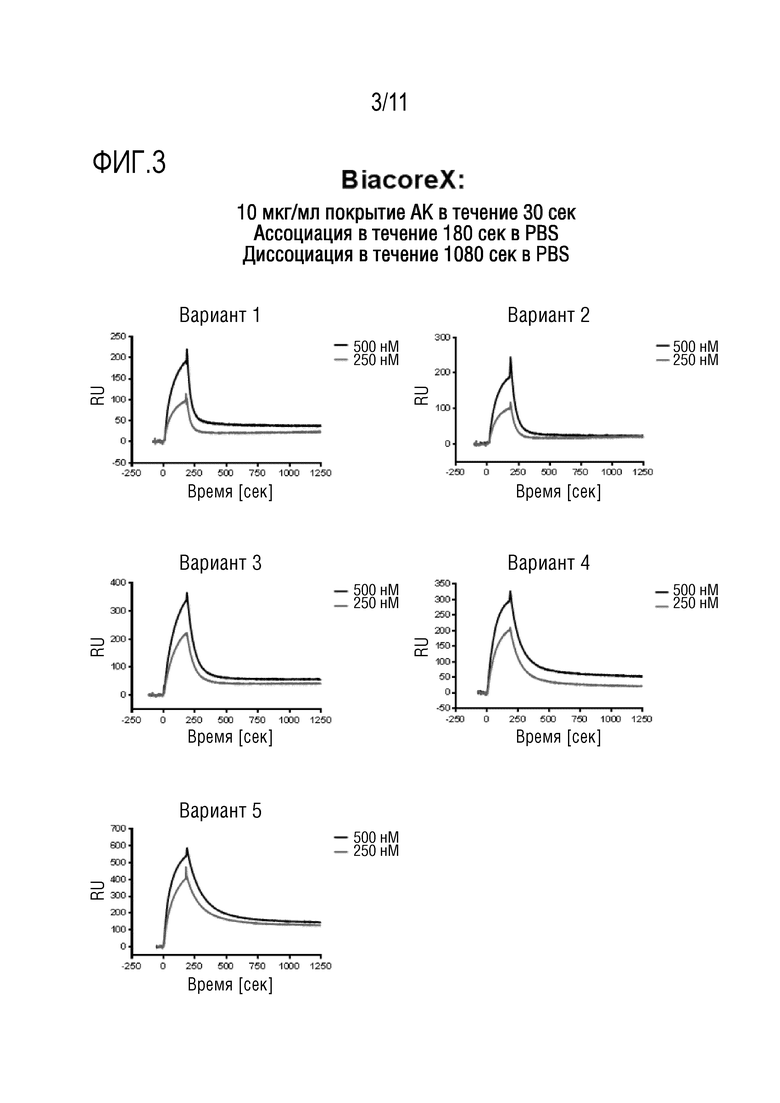
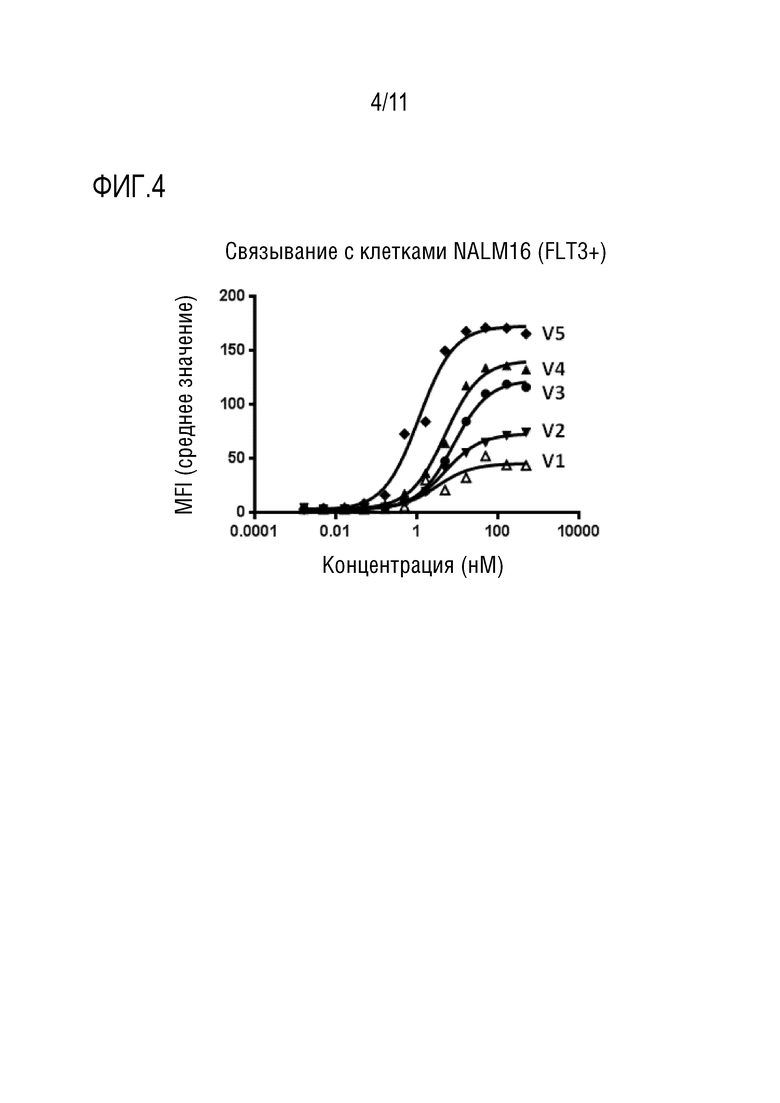
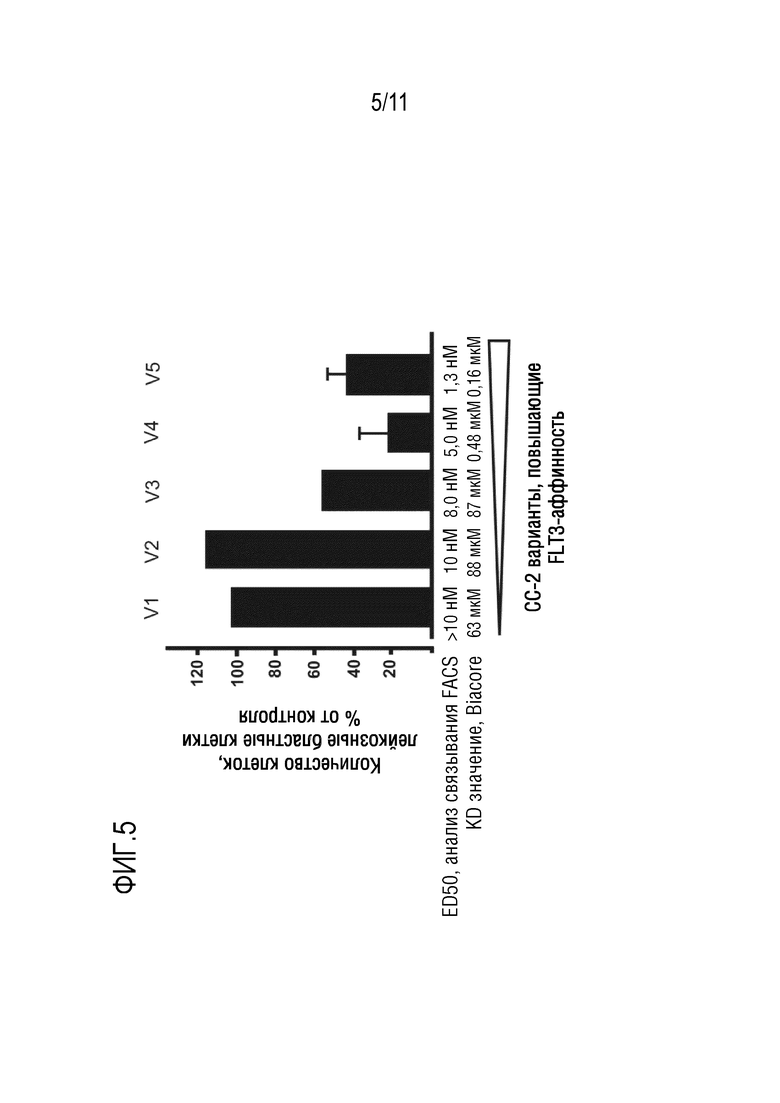
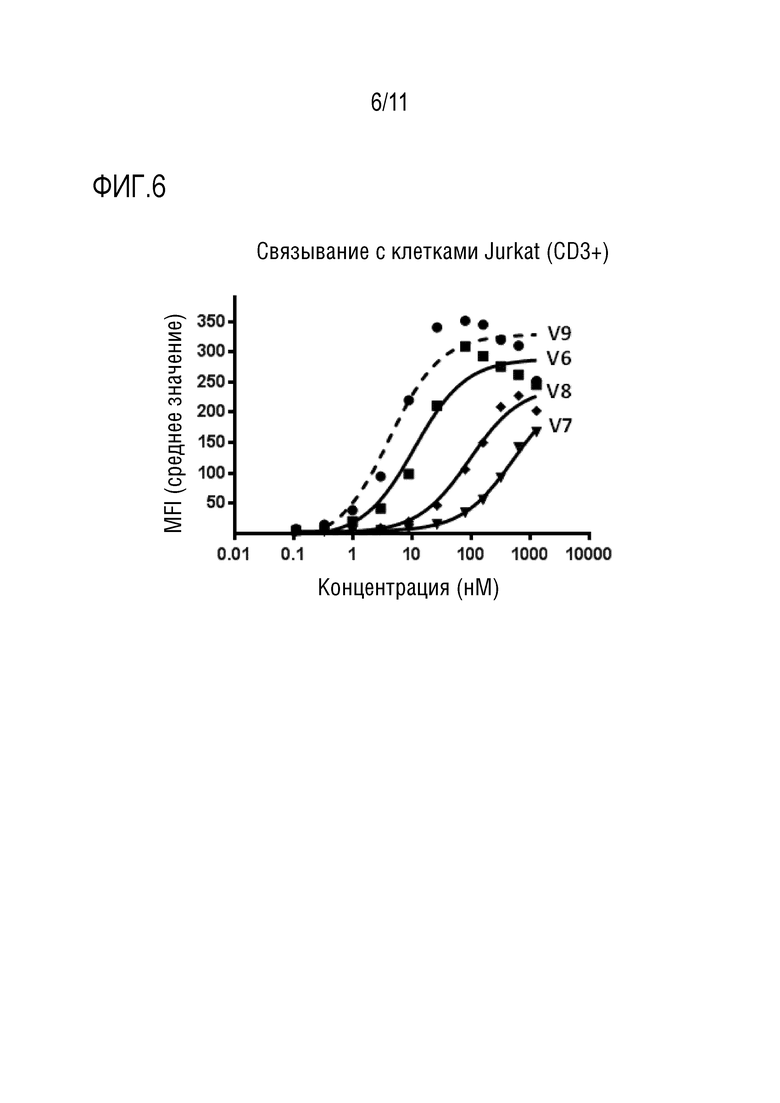
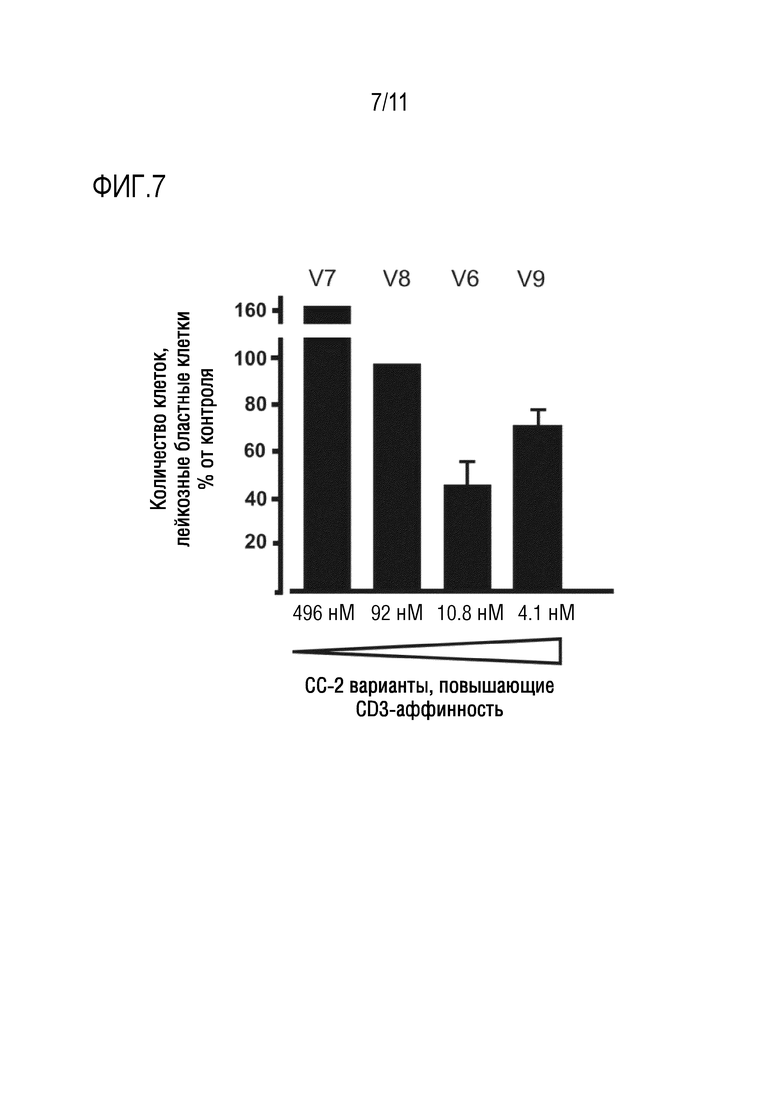
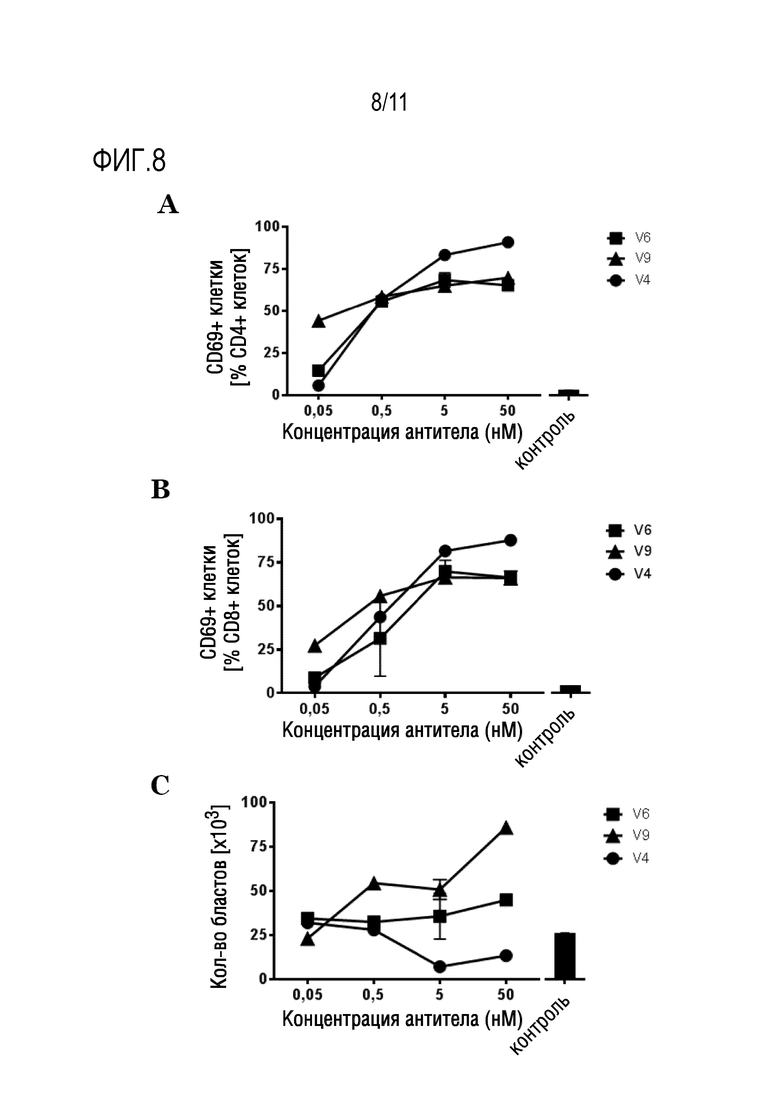
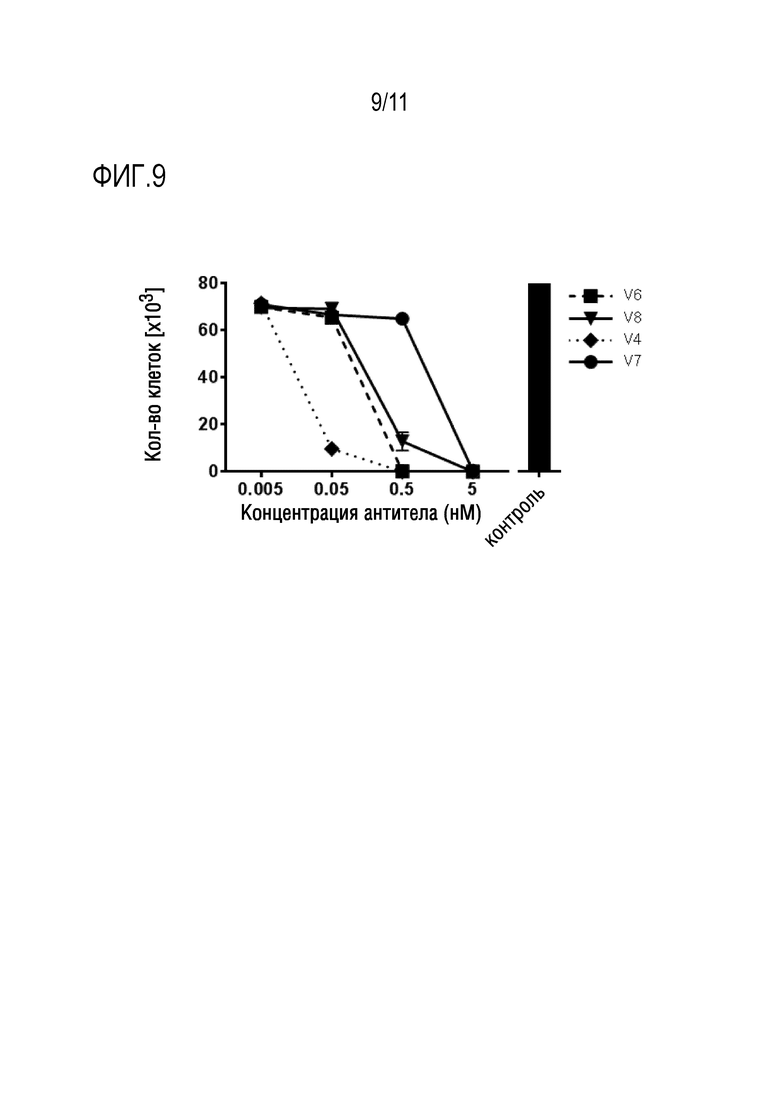
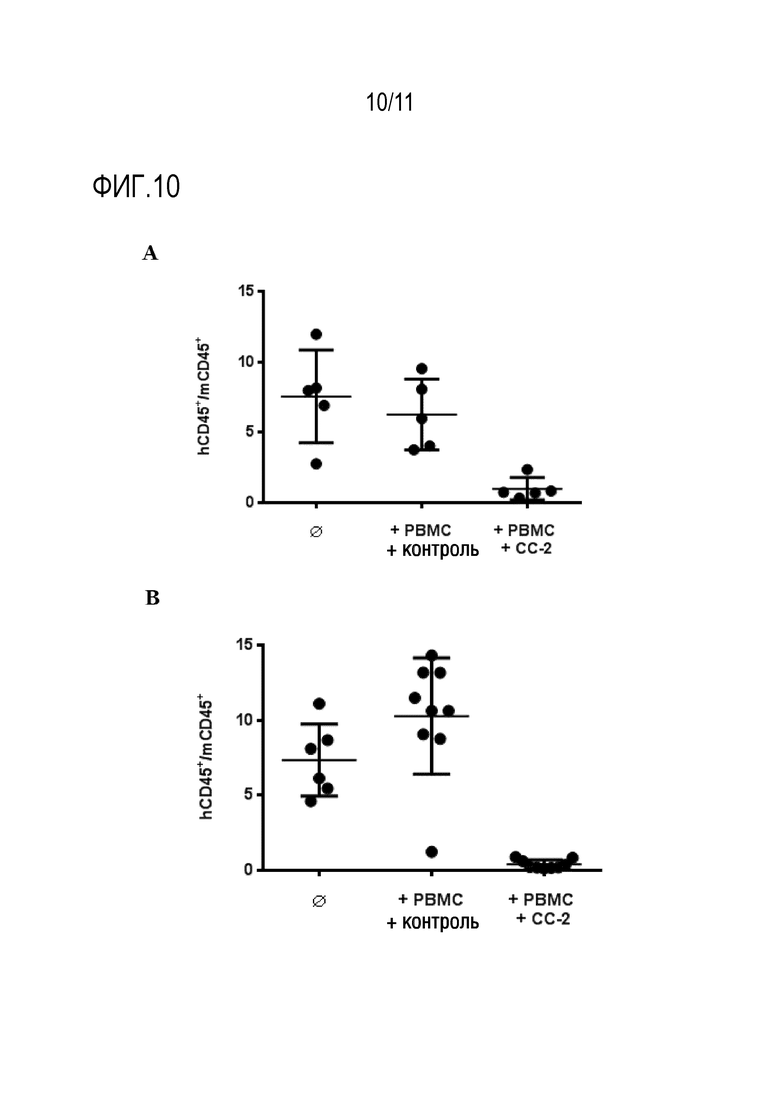
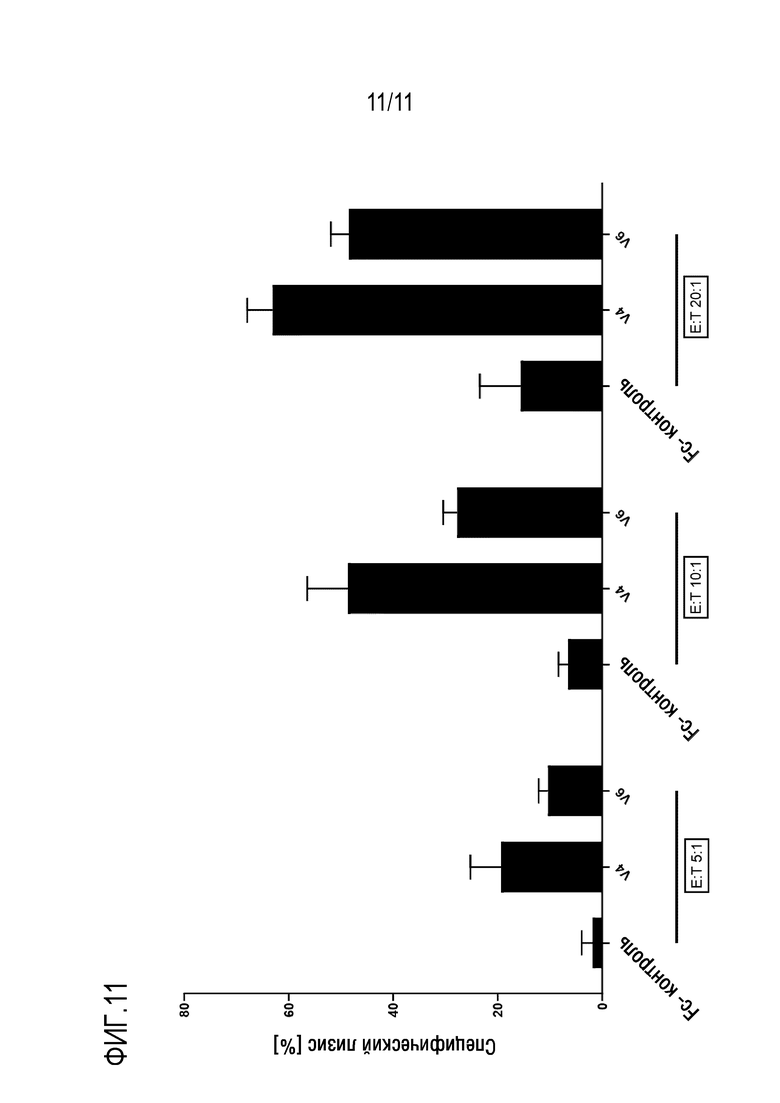
Группа изобретений относится к биотехнологии. Представлен антигенсвязывающий белок (ABP), способный связываться с человеческой fms-подобной тирозинкиназой 3 (FLT3), причем ABP представляет собой антитело или его антигенсвязывающий фрагмент, включающий: вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, выбранную из SEQ ID NO: 15, 17, 19, 21, 23 или 76, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, выбранную из SEQ ID NO: 16, 18, 20, 22, 24 или 77. Также раскрыты: фармацевтическая композиция для профилактики или лечения пролиферативного заболевания, способ усиления клеточно-опосредованного иммунного ответа на человеческую клетку, которая экспрессирует человеческий FLT3, и способ лечения пролиферативного расстройства у субъекта, включающий введение субъекту терапевтически эффективного количества фармацевтической композиции. Изобретение применяется для лечения пролиферативных расстройств, связанных с экспрессией FLT3, где расстройство представляет собой рак, в частности, такой как лейкоз, солидный рак, рак предстательной железы, колоректальный рак, рак желудка, карцинома легкого, остеосаркома, рак молочной железы, рак поджелудочной железы или плоскоклеточная карцинома. 4 н. и 18 з.п. ф-лы, 11 ил., 2 табл., 7 пр.
1. Антигенсвязывающий белок (ABP), способный связываться с человеческой fms-подобной тирозинкиназой 3 (FLT3), причем ABP представляет собой антитело или его антигенсвязывающий фрагмент, включающий:
вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, выбранную из SEQ ID NO: 15, 17, 19, 21, 23 или 76, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, выбранную из SEQ ID NO: 16, 18, 20, 22, 24 или 77.
2. ABP по п. 1, где в вариабельной области тяжелой цепи аминокислотные положения 16, 18, 19, 20, 22, 48, 57, 60, 69, 70, 75, 76, 78, 80, 81, 87 и 108 являются такими же, как в любой из SEQ ID NO: 15, 17, 19, 21 или 23, и/или где в вариабельной области легкой цепи аминокислотные положения 49, 55 и 87 являются такими же, как в любой из SEQ ID NO: 16, 18, 20, 22 или 24, где нумерация указана в соответствии с системой Кабата.
3. ABP по п. 1 или 2, где вариабельная область тяжелой цепи включает аминокислотную последовательность, представленную в SEQ ID NO: 21, и вариабельная область легкой цепи включает аминокислотную последовательность, представленную в SEQ ID NO: 22.
4. ABP по п. 1 или 2, где вариабельная область тяжелой цепи включает аминокислотную последовательность, представленную в SEQ ID NO: 76, и вариабельная область легкой цепи включает аминокислотную последовательность, представленную в SEQ ID NO: 77.
5. ABP по любому из пп. 1-4, где вариабельная область тяжелой цепи включает 48I и где вариабельная область легкой цепи включает 87F, где нумерация указана в соответствии с системой Кабата.
6. ABP по п. 5, где вариабельная область легкой цепи включает 49K, где нумерация указана в соответствии с системой Кабата.
7. ABP по любому из пп. 1-6, где ABP состоит из по меньшей мере одной, предпочтительно двух, последовательности (последовательностей) тяжелой цепи антитела, и по меньшей мере одной, предпочтительно двух, последовательности (последовательностей) легкой цепи, где указанная последовательность (последовательности) тяжелой цепи антитела и последовательность (последовательности) легкой цепи включает (включают) каждую последовательность вариабельной области в одной из следующих комбинаций V0-V5:
(SEQ ID NO)
(SEQ ID NO)
8. ABP по любому из пп. 1-7, который связывается с указанным FLT3 с kD меньше чем 50 мкМ и больше чем 50 нМ; предпочтительно который связывается с указанным FLT3 с kD меньше чем 1 мкМ и больше чем 300 нМ.
9. ABP по любому из пп. 1-8, который связывается с человеческой клеткой, экспрессирующей FLT3, с EC50 меньше чем 10 нМ и больше чем 0,5 нМ.
10. ABP по любому из пп. 1-9, который связывается с человеческой клеткой, экспрессирующей FLT3, с EC50 меньше чем 5,5 нМ и больше чем 4,5 нМ.
11. ABP по любому из пп. 1-10, который является выделенным и/или по существу чистым.
12. ABP по любому из пп. 1-11, который представляет собой моноклональное антитело.
13. ABP по любому из пп. 1-12, где указанное антитело представляет собой химерное антитело, такое как человеческое химерное антитело.
14. ABP по п.12 или 13, где указанное антитело представляет собой IgG, IgE, IgD, IgA или IgM иммуноглобулин; предпочтительно IgG иммуноглобулин.
15. ABP по любому из пп. 12-14, где антигенсвязывающий фрагмент выбран из перечня, состоящего из: Fab, Fab’-SH, Fv, scFv и F(ab’)2.
16. ABP по любому из пп. 1-15, где указанный ABP модифицирован или сконструирован для повышения антителозависимой клеточной цитотоксичности (ADCC), предпочтительно где указанный ABP является афукозилированным.
17. ABP по любому из пп. 1-16, включающий две последовательности тяжелой цепи антитела и две последовательности легкой цепи антитела, где указанные последовательности тяжелой цепи антитела и последовательности легкой цепи антитела включают, каждая, аминокислотные последовательности в любой из следующих комбинаций V0-V5:
(SEQ ID NO)
(SEQ ID NO)
18. ABP по любому из пп. 1-17, содержащий: (i) область CDRH1, представленную в SEQ ID NO: 01 (SYWMH), область CDRH2, представленную в SEQ ID NO: 02 (EIDPSDSYKDYNQKFKD), и область CDRH3, представленную в SEQ ID NO: 03 (AITTTPFDF); и (ii) область CDRL1, представленную в SEQ ID NO: 05 (RASQSISNNLH), область CDRL2, представленную в SEQ ID NO: 06 (YASQSIS), и область CDRL3, представленную в SEQ ID NO: 07 (QQSNTWPYT).
19. Фармацевтическая композиция для профилактики или лечения пролиферативного заболевания, где пролиферативное расстройство связано с экспрессией FLT3, включающая: ABP по любому из пп. 1-18 и фармацевтически приемлемый носитель, стабилизатор и/или эксципиент.
20. Фармацевтическая композиция по п. 19, где пролиферативное расстройство, связанное с экспрессией FLT3, представляет собой рак, такой как рак, выбранный из лейкоза, такого как острый миелоидный лейкоз (AML) или острый лимфобластный лейкоз (ALL), или солидный рак, выбранный из рака предстательной железы, колоректального рака, рака желудка, карциномы легкого, остеосаркомы, рака молочной железы, рака поджелудочной железы или плоскоклеточной карциномы; предпочтительно рак представляет собой лейкоз, такой как AML или ALL.
21. Способ усиления клеточно-опосредованного иммунного ответа на человеческую клетку, которая экспрессирует человеческий FLT3, включающий контактирование указанной клетки с ABP по любому из пп. 1-18, с усилением таким образом клеточно-опосредованного иммунного ответа против указанной человеческой клетки.
22. Способ лечения пролиферативного расстройства у субъекта, включающий введение субъекту терапевтически эффективного количества фармацевтической композиции по п. 19 и где пролиферативное расстройство характеризуется экспрессией FLT3 в клетках, ассоциированных с пролиферативным расстройством.
| WO 2011076922 A1, 30.06.2011 | |||
| WO 2017176760 A2, 12.10.2017 | |||
| LI YIWEN et al | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Счетная таблица | 1919 |
|
SU104A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| RU 2011146088 A, 27.06.2013. | |||
Авторы
Даты
2024-11-28—Публикация
2019-09-11—Подача