ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0001]
Настоящее изобретение относится к производному пара-борфенилаланина (в дальнейшем в данном документе также называемому «производным BPA»), композиции, содержащей таковое, и набору для получения таковых.
УРОВЕНЬ ТЕХНИКИ
[0002]
Бор-нейтронозахватная терапия (BNCT) представляет собой способ, который включает в себя накопление бора (10В) в пораженной части и проведение облучения ее нейтронами с обеспечением ядерной реакции, которая позволяет локально вырабатывать α-лучи, которые уничтожают клетки-мишени. Накопление бора в пораженной части осуществляют введением борсодержащего лекарственного средства. Лекарственные средства, которые применяются на людях по состоянию на текущий момент, включают кластер бора меркаптоундекагидрододекаборат (BSH), который является борсодержащим лекарственным средством первого поколения, и пара-борфенилаланин (BPA), который является борсодержащим лекарственным средством второго поколения. Кроме того, появились сообщения о борсодержащих лекарственных средствах третьего поколения, где кластер бора является нанесенным на носитель, такой как липосома, полимер, полимерная мицелла, и т.д. (NPL1).
[0003]
BSH имеет превосходную растворимость в воде, но имеет плохую селективность в отношении опухолей. Борсодержащие лекарственные средства третьего поколения, содержащие BSH, могут селективно доставлять бор к опухолям благодаря эффекту улучшенной проницаемости и удерживания (эффекту EPR) в результате использования носителей, таких как липосомы, полимеры и полимерные мицеллы. Однако, поскольку эффект EPR, как правило, реализуется носителем, проявляющим длительное удерживание в крови, трудно повысить соотношение концентраций бора в опухоли/крови при использовании борсодержащих лекарственных средств третьего поколения.
[0004]
Известно, что фенилаланиновая структура в BPA распознается, например, аминокислотным транспортером (LAT1), который сверхэкспрессируется в опухолевых клетках, и BPA селективно захватывается опухолевыми клетками (NPL2). Однако, BPA имеет плохую растворимость в воде.
[0005]
Сделано сообщение, что проблемный аспект, связанный с плохой растворимостью BPA, может быть улучшен в результате получения комплексов с сахарами, такими как фруктоза или сорбит, взятыми в качестве солюбилизаторов (PTL1).
[СПИСОК ПРОТИВОПОСТАВЛЕННЫХ МАТЕРИАЛОВ]
[ПАТЕНТНАЯ ЛИТЕРАТУРА]
[0006]
[PTL 1] Публикация Японского нерассмотренного патента (Kokai) № 2009-51766
[НЕПАТЕНТНАЯ ЛИТЕРАТУРА]
[0007]
[NPL1] Luderer M.J. et al., Phar. Res., 32, 2824-2836 (2015)
[NPL2] Wongthai P. et al., Cancer Sci. 106, 279-286 (2015)
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[ТЕХНИЧЕСКАЯ ЗАДАЧА]
[0008]
В случае борсодержащих лекарственных средств первого поколения и третьего поколения, трудно повысить их способность накапливаться в опухолях при поддерживании соотношения концентраций бора в опухолевой/нормальной ткани и соотношения концентраций бора в опухоли/крови на высоком уровне. С другой стороны, это может быть достигнуто в некоторый момент времени с помощью BPA второго поколения.
[0009]
Однако, поскольку BPA захватывается раковыми клетками в основном посредством аминокислотного транспортера LAT1, который является обменным транспортером, по мере снижения концентрации внеклеточного BPA, внутриклеточный BPA вытекает из клетки. Таким образом, существует проблема, состоящая в том, что после накопления бора в опухолевой ткани, концентрация бора в опухоли будет снижаться на ранней стадии.
[0010]
Способ в PTL 1 может позволить улучшить растворимость в воде BPA, но не может разрешить проблему раннего выведения BPA из опухолевых клеток. В качестве подхода для решения этой проблемы, осуществляют способ, в котором BPA вводят постепенно для поддержания концентрации внутриопухолевого бора на уровне, требуемом для лечения при проведении облучения нейтронами пораженной части. Однако, в этом случае, поскольку в нормальных кровяных сосудах присутствует большое количество бора, возникает сложность, состоящая в том, что нормальная ткань подвергается воздействию излучения.
[0011]
Таким образом, задачей настоящего изобретения является разрешение проблемы раннего выведения BPA из опухолевых клеток с тем, чтобы реализовать селективное накопление и длительное удерживание бора в опухолях, при одновременном достижении превосходного соотношения концентраций бора в опухолевых/нормальных тканях и соотношения концентраций бора в опухоли/крови.
[РЕШЕНИЕ ЗАДАЧИ]
[0012]
В отношении вышеупомянутой проблемы, в результате обширного исследования, выполненного авторами настоящего изобретения, обнаружено, что система доставки бора, в которой BPA нанесен на полимер, захватывается опухолевыми клетками в ходе эндоцитоза посредством аминокислотного транспортера, и, что высокие концентрации внутриклеточного бора могут поддерживаться в течение длительного времени в сравнении с обычно применяемым BPA. В результате этого обнаружения сделано настоящее изобретение.
[0013]
Конкретно, настоящее изобретение охватывает следующие пункты <1> - <21>.
<1>
Производное пара-борфенилаланина, включающее:
полимер, связанный, либо непосредственно, либо через линкер, с группой, представленной формулой (I), приведенной ниже.
[Хим. стр. 1]

где,
стрелки показывают связь со смежным атомом, и
X1-X4, каждый независимо, представляют собой Н, 18F или 19F.
<2>
Производное пара-борфенилаланина согласно пункту <1>, где две или более групп, представленных формулой (I), связаны непосредственно или через линкер с полимером, и
где группы, представленные формулой (I), могут быть одинаковыми или различными.
<3>
Производное пара-борфенилаланина согласно пункту <1> или <2>, где его среднечисловая молекулярная масса составляет 1000 Да или более.
<4>
Производное пара-борфенилаланина согласно любому из пунктов <1> - <3>, где полимер выбирают из группы, состоящей из поливинилового спирта, сложного полиэфира, простого полиэфира, полиакрилата, полиакриламида, полипептида, полисахарида и их сополимеров.
<5>
Производное пара-борфенилаланина согласно любому из пунктов <1> - <4>, где полимер представляет собой поливиниловый спирт.
<6>
Производное пара-борфенилаланина согласно пункту <5>, где производное пара-борфенилаланина представлено соединением формулы (II), приведенной ниже, или его фармацевтически приемлемой солью.
[Хим. стр. 2]
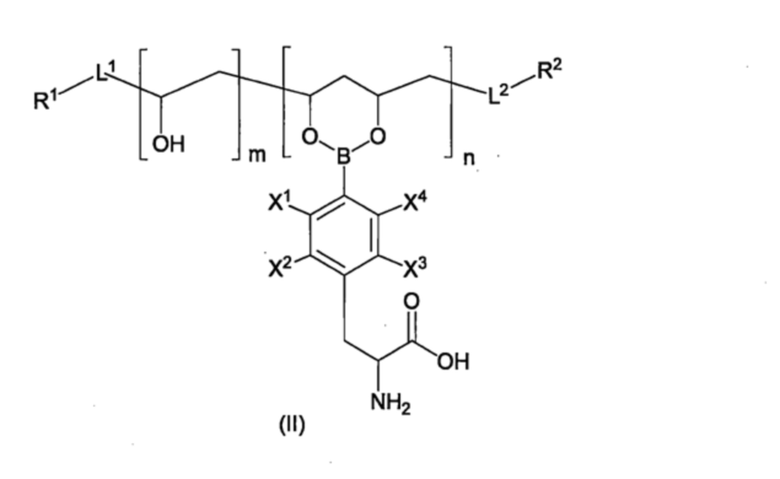
где,
X1-X4, каждый независимо, представляют собой Н, 18F или 19F,
L1 и L2, каждый независимо, представляют собой линкер или отсутствуют,
R1 и R2, каждый независимо, представляют собой водород, гидроксильную группу, карбоксильную группу, аминогруппу, С1-10-алкильную группу, которая может быть замещена галогеном, С1-10-алкоксигруппу, которая может быть замещена галогеном, тиольную группу, цианогруппу, азидогруппу, -CH(OA1)2, или детектируемую метку,
А1 представляет собой С1-6-алкильную группу,
m имеет значение от 0 до 3998,
n имеет значение от 1 до 2000,
m+2n=от 10 до 4000, и
порядок следования повторяющихся звеньев является произвольным.
<7>
Производное пара-борфенилаланина согласно любому из пунктов <1> - <4>, где полимер представляет собой полипептид.
<8>
Производное пара-борфенилаланина согласно пункту <7>, где производное пара-борфенилаланина представлено соединением формулы (III), приведенной ниже, или его фармацевтически приемлемой солью.
[Хим. стр. 3]

где,
L3 и L4, каждый независимо, представляют собой линкер или отсутствуют,
R3 и R4, каждый независимо, представляют собой водород, гидроксильную группу, карбоксильную группу, аминогруппу, С1-10-алкильную группу, которая может быть замещена галогеном, С1-10-алкоксигруппу, которая может быть замещена галогеном, тиольную группу, цианогруппу, азидогруппу, -CH(OA1)2, или детектируемую метку,
А1 представляет собой С1-6-алкильную группу,
R5a, каждый независимо, представляют собой группу, представленную формулой (IV-a) или (IV-b), приведенной ниже,
[Хим. стр. 4]
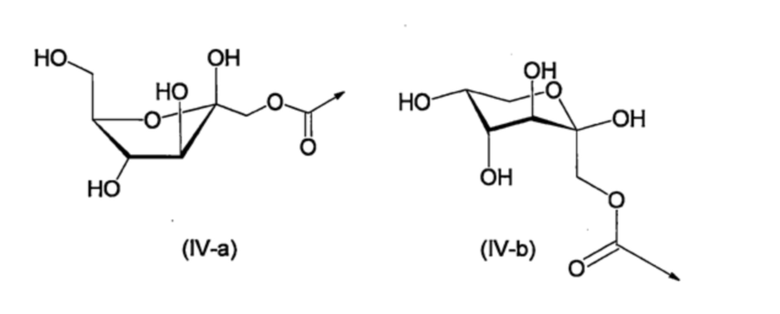
где, стрелки показывают связь с NH,
R5b, каждый независимо, представляют собой группу, выбранную из группы, состоящей из групп, представленных следующими формулами (IV-с) - (IV-g),
[Хим. стр. 5]
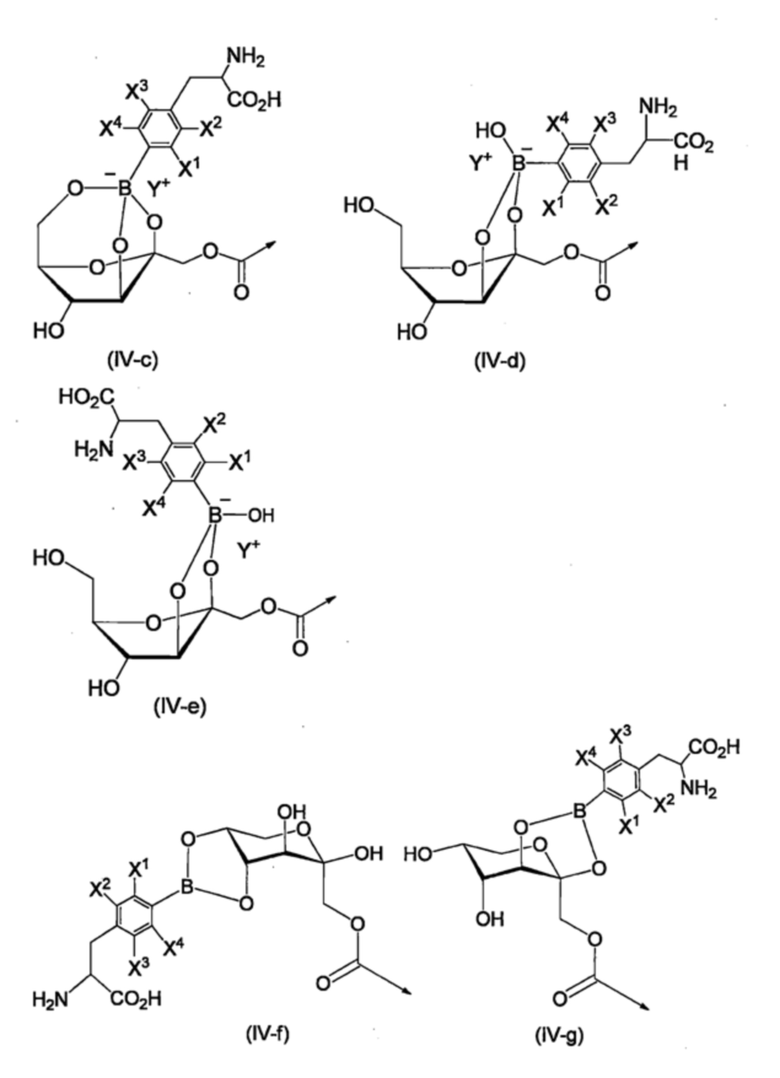
где,
стрелки показывают связь с NH,
X1-X4, каждый независимо, представляют собой Н, 18F или 19F,
Y+ представляет собой H+, ион щелочного металла, или ион тетра-С1-6-алкил-аммония,
p=от 0 до 299,
q=от 1 до 300,
r=от 0 до 299,
p+q+r=от 10 до 300, и
порядок следования повторяющихся звеньев является произвольным.
<9>
Производное пара-борфенилаланина согласно пункту <7>, где производное пара-борфенилаланина представлено соединением формулы (V), приведенной ниже, или его фармацевтически приемлемой солью,
[Хим. стр. 6]
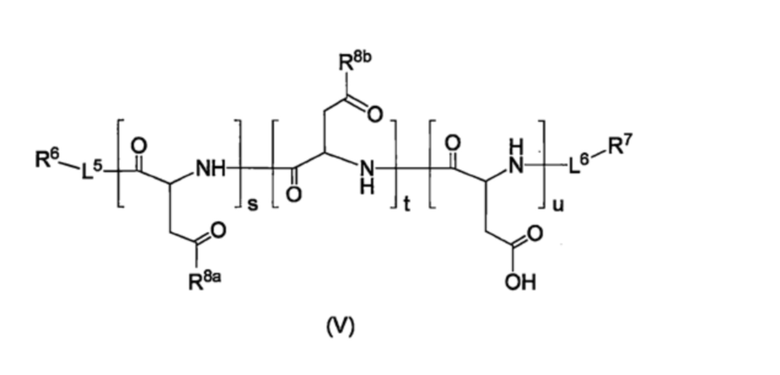
где,
L5 и L6, каждый независимо, представляют собой линкер или отсутствуют,
R6 и R7, каждый независимо, представляют собой водород, гидроксильную группу, карбоксильную группу, аминогруппу, С1-10-алкильную группу, которая может быть замещена галогеном, С1-10-алкоксигруппу, которая может быть замещена галогеном, тиольную группу, цианогруппу, азидогруппу, -CH(OA1)2, или детектируемую метку,
А1 представляет собой С1-6-алкильную группу,
R8a означает группу, представленную формулой (VI-a), приведенной ниже,
[Хим. стр. 7]

где, стрелка показывает связь с карбонильным углеродом,
R8b, каждый независимо, представляют собой группу, выбранную из группы, состоящей из групп, представленных формулами (VI-b) - (VI-h), приведенными ниже,
[Хим. стр. 8]
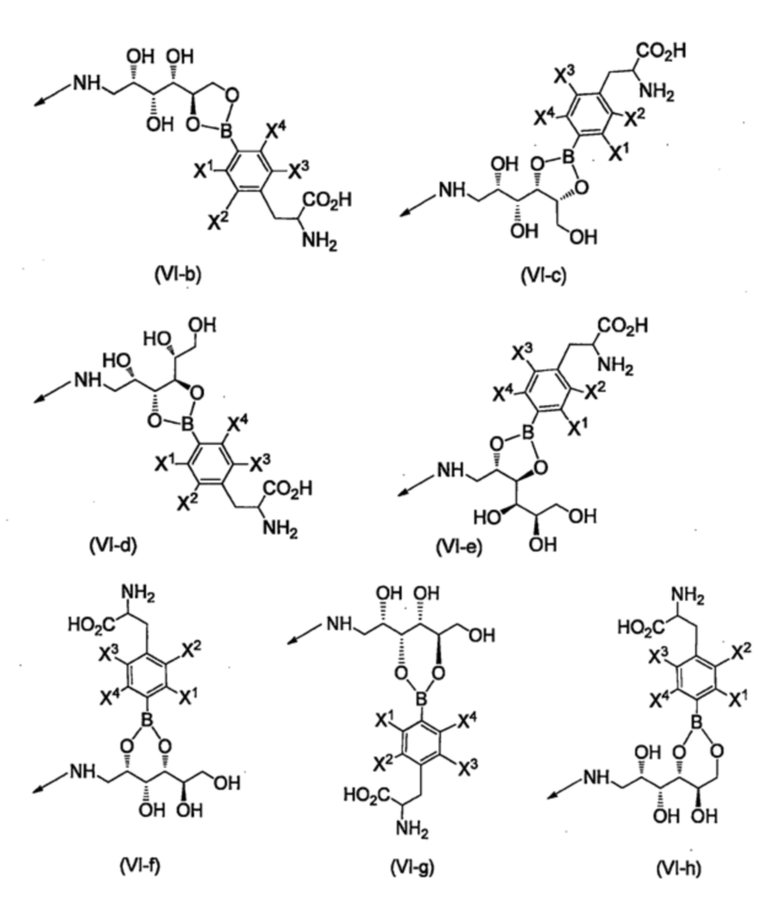
где,
стрелки показывают связь с карбонильным углеродом,
X1-X4, каждый независимо, представляют собой Н, 18F или 19F,
s=от 0 до 299,
t=от 1 до 300,
u=от 0 до 299,
s+t+u=от 2 до 300, и
порядок следования повторяющихся звеньев является произвольным.
<10>
Производное пара-борфенилаланина согласно пункту <7>, где производное пара-борфенилаланина представлено соединением формулы (XX), приведенной ниже, или его фармацевтически приемлемой солью,
[Хим. стр. 9]
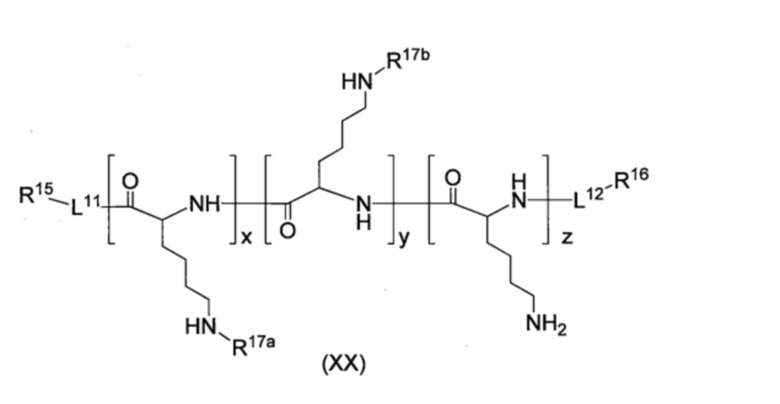
где,
L11 и L12, каждый независимо, представляют собой линкер или отсутствуют,
R15 и R16, каждый независимо, представляют собой водород, гидроксильную группу, карбоксильную группу, аминогруппу, С1-10-алкильную группу, которая может быть замещена галогеном, С1-10-алкоксигруппу, которая может быть замещена галогеном, тиольную группу, цианогруппу, азидогруппу, -CH(OA1)2, или детектируемую метку,
А1 представляет собой С1-6-алкильную группу,
R17a означает группу, представленную формулой (XXI-a), приведенной ниже,
[Хим. стр. 10]

где, стрелка показывает связь с NH,
R17b, каждый независимо, представляют собой группу, выбранную из группы, состоящей из групп, представленных формулами (XXI-b) - (XXI-h), приведенными ниже,
[Хим. стр. 11]
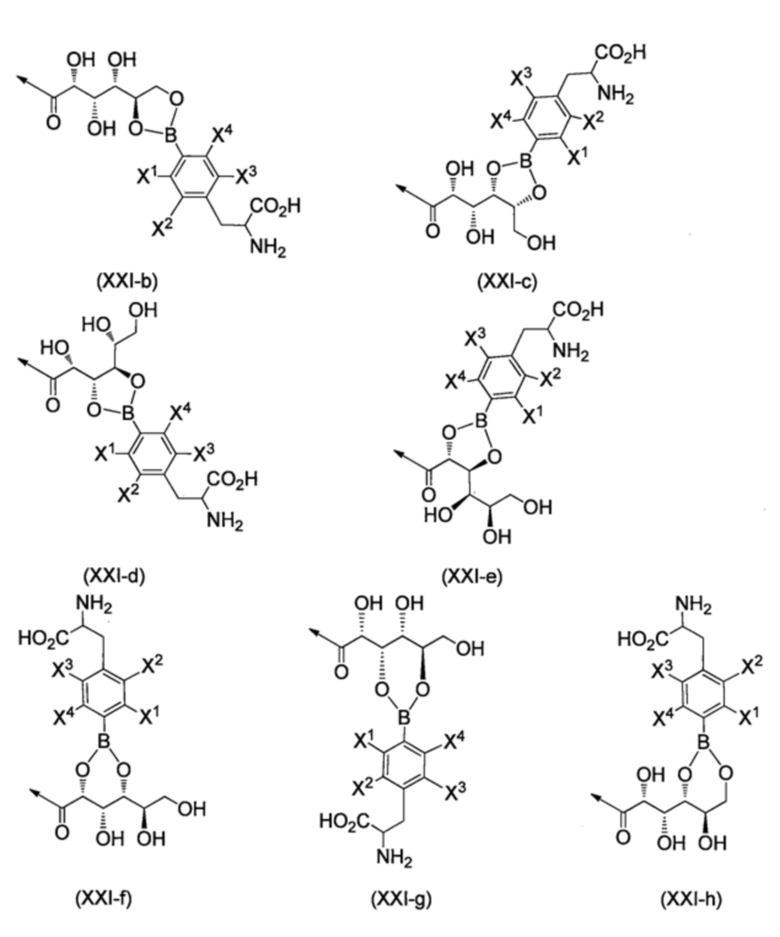
где,
стрелки показывают связь с NH,
X1-X4, каждый независимо, представляют собой Н, 18F или 19F,
x=от 0 до 299,
y=от 1 до 300,
z=от 0 до 299,
x+y+z=от 10 до 300, и
порядок следования повторяющихся звеньев является произвольным.
<11>
Производное пара-борфенилаланина согласно пункту <5>, где производное пара-борфенилаланина представлено соединением формулы (XXII), приведенной ниже, или его фармацевтически приемлемой солью,
[Хим. стр. 12]

где,
X1-X4, каждый независимо, представляют собой Н, 18F или 19F,
L13 и L14, каждый независимо, представляют собой линкер или отсутствуют,
R18 и R19, каждый независимо, представляют собой водород, гидроксильную группу, карбоксильную группу, аминогруппу, С1-10-алкильную группу, которая может быть замещена галогеном, С1-10-алкоксигруппу, которая может быть замещена галогеном, тиольную группу, цианогруппу, азидогруппу, -CH(OA1)2, или детектируемую метку,
А1 представляет собой С1-6-алкильную группу,
R20, каждый независимо, представляют собой С1-10-алкильную группу, которая может быть замещена галогеном, -NR21R22-группу, или следующую группу,
[Хим. стр. 13]
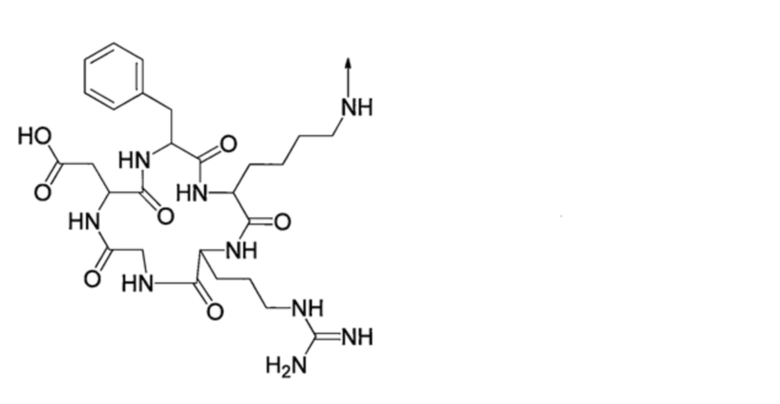
где, стрелка показывает связь с карбонильным углеродом,
R21 и R22, каждый независимо, представляют собой водород или С1-10-алкильную группу, которая может быть замещена галогеном,
а=от 1 до 3998,
b=от 0 до 3997,
с=от 1 до 2000,
a+b+2c=от 10 до 4000, и
порядок следования повторяющихся звеньев является произвольным.
<12>
Композиция, содержащая производное пара-борфенилаланина согласно любому из пунктов <1> - <11>.
<13>
Композиция согласно пункту <12> для лечения опухолей.
<14>
Композиция согласно пункту <12> для диагностирования и обнаружения опухолей.
<15>
Набор для получения композиции согласно любому из пунктов <10> - <12> или для получения производного пара-борфенилаланина согласно любому из пунктов <1> - <9>, включающий в себя соединение, представленное формулой (VII),
[Хим. стр. 14]
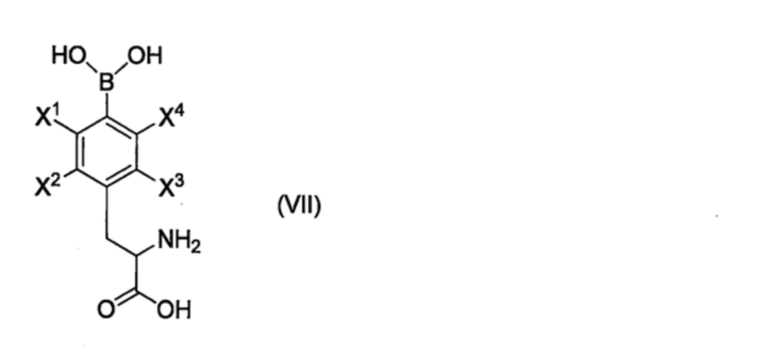
где,
X1-X4, каждый независимо, представляют собой Н, 18F или 19F, и
полимер, который может вступать в реакцию с соединением, представленным формулой (VII), с образованием производного пара-борфенилаланина согласно любому из пунктов <1> - <11>.
<16>
Способ лечения опухоли, включающий в себя введение субъекту, нуждающемуся в том, эффективной дозировки производного пара-борфенилаланина согласно любому из пунктов <1> - <11>.
<17>
Способ обнаружения или диагностирования опухолей, включающий в себя введение субъекту, нуждающемуся в том, эффективной дозировки производного пара-борфенилаланина согласно любому из пунктов <1> - <11>.
<18>
Производное пара-борфенилаланина согласно любому из пунктов <1> - <11> для лечения опухолей.
<19>
Производное пара-борфенилаланина согласно любому из пунктов <1> - <11> для диагностирования и обнаружения опухолей.
<20>
Применение производного пара-борфенилаланина согласно любому из пунктов <1> - <11> в получении лекарственного средства для лечения опухолей.
<21>
Применение производного пара-борфенилаланина согласно любому из пунктов <1> - <11> в получении лекарственного средства для диагностирования и обнаружения опухолей.
[ПРЕИМУЩЕСТВЕННЫЕ ЭФФЕКТЫ ИЗОБРЕТЕНИЯ]
[0014]
При помощи использования производного пара-борфенилаланина по настоящему изобретению, может быть реализовано селективное накопление и длительное удерживание бора в опухолях, при одновременном достижении превосходного соотношения концентраций бора в опухолевой/нормальной ткани и соотношение концентраций бора в опухоли/крови.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0015]
[ФИГ. 1] показывает результат измерений 11B-NMR (500 МГц, D2O) для 11B-BPA, Fru-11B-BPA и PVA-11B-BPA.
[ФИГ. 2] показывает полученные методом конфокальной микроскопии изображения клеток ВхPC3, обработанных посредством Cy5-PVA-BPA и Fru-BPA. На фигуре, контрольные пробы представляют собой клетки ВхPC3, которые не были обработаны каким-либо из образцов (были добавлены Lysotracker (флуоресцентный краситель) для окрашивания и реагент для обнаружения BPA (DAHMI)).
[ФИГ. 3-1] предоставляет график, показывающий концентрацию внутриклеточного бора. Результаты показаны в виде среднего значения ± стандартное отклонение (S.D.) (n=3). Статистическую значимость вычисляют с помощью t-критерия Стьюдента. *p<0,05, **p<0,01.
[ФИГ. 3-2] предоставляет график, показывающий концентрацию внутриклеточного бора. Результаты показаны в виде среднего значения ± стандартное отклонение (S.D.) (n=3). Статистическую значимость вычисляют с помощью t-критерия Стьюдента. *p<0,05, **p<0,01. На фигуре, «+ 30-минутное вытеснение метки» означает 30 минут дополнительного выдерживания.
[ФИГ. 4-1] показывает результаты внутриклеточного захвата Cy5-PVA и Cy5-PVA-BPA в том случае, когда BCH не добавляют. Данные показаны в виде среднего значения ± стандартное отклонение (S.D.) (n=3). P-значение вычисляют с помощью t-критерия Стьюдента. *p<0,05, **p<0,01.
[ФИГ. 4-2] показывает результаты внутриклеточного захвата Cy5-PVA и Cy5-PVA-BPA в том случае, когда BCH добавляют. Данные показаны в виде среднего значения ± стандартное отклонение (S.D.) (n=3). P-значение вычисляют с помощью t-критерия Стьюдента. *p<0,05, **p<0,01.
[ФИГ. 5-1] показывает результаты накопления в опухолях PVA-BPA и Fru-BPA у подвергнутых трансплантации клеток CT-26 мышей. Данные показаны в виде среднего значения ± стандартное отклонение (S.D.) (n=3). P-значение вычисляют с помощью t-критерия Стьюдента. *p<0,05, **p<0,01.
[ФИГ. 5-2] показывает соотношение накопления в опухоли/крови PVA-BPA и Fru-BPA у подвергнутых трансплантации клеток CT-26 мышей. Данные показаны в виде среднего значения ± стандартное отклонение (S.D.) (n=4). P-значение вычисляют с помощью t-критерия Стьюдента. *p<0,05, **p<0,01.
[ФИГ. 6-1] показывает результаты накопления в опухолях PVA-BPA и Fru-BPA у подвергнутых трансплантации BxPC3 мышей. Данные показаны в виде среднего значения ± стандартное отклонение (S.D.) (n=4). P-значение вычисляют с помощью t-критерия Стьюдента. *p<0,05, **p<0,01.
[ФИГ. 6-2] показывает соотношение накопления в опухоли/крови PVA-BPA и Fru-BPA у подвергнутых трансплантации BxPC3 мышей. Данные показаны в виде среднего значения ± стандартное отклонение (S.D.) (n=4). P-значение вычисляют с помощью t-критерия Стьюдента. *p<0,05, **p<0,01.
[ФИГ. 7] показывает CLSM-изображение опухоли CT26 через шесть часов после внутривенной инъекции Cy5-PVA-BPA. Красный: Cy5; Голубой: Hoechst33342 (клеточное ядро); Зеленый: DyLight488 (кровеносные сосуды).
[ФИГ. 8-1] показывает относительное изменение размера опухолей с течением времени после введения образцов. Данные показаны в виде среднего значения ± стандартное отклонение (S.D.) (n= 4 или 8). P-значение вычисляют с помощью критерия множественных сравнений Бонферрони. *p<0,05, **p<0,01.
[ФИГ. 8-2] показывает кривые Каплана-Мейера в отношении относительного размера опухоли после введения образца.
[ФИГ. 9-1] показывает изображения окрашенных гематоксилин-эозином (HE) опухолей после обработки для Контрольной группы (Холодная).
[ФИГ. 9-2] показывает изображения HE-окрашенных опухолей после обработки для Контрольной группы (Горячая).
[ФИГ. 9-3] показывает изображения HE-окрашенных опухолей через 3 часа после обработки посредством Fru-BPA (Горячая группа).
[ФИГ. 9-4] показывает изображения HE-окрашенных опухолей через 3 часа после обработки посредством PVA-BPA (Горячая группа).
[ФИГ. 10-1] показывает спектр 19F-NMR для 19F-BPA.
[ФИГ. 10-2] показывает спектр 19F-NMR для Fru-19F-BPA.
[ФИГ. 10-3] показывает спектр 19F-NMR для PVA-19F-BPA.
[ФИГ. 11] показывает результаты накопления в опухолях PVA-19F-BPA и Fru-19F-BPA. На фигуре, Fru-BPA представляет результаты для Fru-19F-BPA, и PVA-BPA представляет результаты для PVA-19F-BPA.
[ФИГ. 12-1] показывает результаты накопления в опухолях PEG-P[Lys(Fru)/Lys]-BPA.
[ФИГ. 12-2] показывает соотношение накопления в опухоли/крови PEG-P[Lys(Fru)/Lys]-BPA.
[ФИГ. 13-1] показывает относительное изменение размера опухолей с течением времени после введения образцов. Статистически значимое различие вычисляют с помощью критерия наименьшей значимой разности (LSD) Фишера на 18-ый день.
[ФИГ. 13-2] показывает подвергнутую облучению пучком нейтронов группу, изъятую из ФИГ. 13-1. Статистически значимое различие вычисляют с помощью критерия наименьшей значимой разности (LSD) Фишера на 18-ый день. На фигуре, «Полимер-BPA» относится к PEG-P[Lys(Fru)/Lys]-BPA.
[ФИГ. 14-1] показывает накопление в опухолях P[Asp(Глюкамин)/Asp]-BPA.
[ФИГ. 14-2] показывает соотношение накопления в опухоли/крови P[Asp(Глюкамин)/Asp]-BPA.
[ФИГ. 15] показывает относительное изменение размера опухолей с течением времени после введения образцов. Данные показаны в виде среднего значения ± стандартное отклонение (S.D.) (Контрольная группа: n=8, фруктоза-BPA: n= 6, PVA-BPA: n=6).
[ФИГ. 16] показывает относительное изменение размера опухолей с течением времени после введения образцов. Данные показаны в виде среднего значения ± стандартное отклонение (S.D.) (n=8).
[ФИГ. 17] показывает результаты оценивания констант взаимодействия в ПРИМЕРЕ 19. На фигуре, (А), (В) и (С), соответственно, представляют N3-P[Lys(Глюконат)/Lys]_(A), N3-P[Lys(Глюконат)/Lys]_(B), и N3-P[Lys(Глюконат)/Lys]_(C).
[ФИГ. 18] показывает полученные методом конфокальной микроскопии изображения клеток ВхPC3, обработанных посредством Cy5-P[Lys(Глюконат)/Lys](C)-BPA и Сорбит-BPA. На фигуре, «Полимер» относится к «Cy5- P[Lys(Глюконат)/Lys](C)».
[ФИГ. 19] показывает результаты накопления в опухолях N3-P[Lys(Глюконат)/Lys]_(A)-BPA ((A)-BPA на фигуре), N3-P[Lys(Глюконат)/Lys]_(B)-BPA ((B)-BPA на фигуре), N3-P[Lys(Глюконат)/Lys]_(C)-BPA ((C)-BPA на фигуре), mPEG10k-P[Lys(Глюконат)/Lys]_-BPA ((D)-BPA на фигуре) и Сорбит-BPA. Данные показаны в виде среднего значения ± стандартное отклонение (S.D.) (n=3).
[ФИГ. 20] показывает относительное изменение размера опухолей с течением времени после введения образцов в ПРИМЕРЕ 22. Данные показаны в виде среднего значения ± стандартное отклонение (S.D.) (n=6).
[ФИГ. 21] показывает кривые Каплана-Мейера в отношении относительного размера опухоли после введения образца в ПРИМЕРЕ 22.
ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
[0016]
<<Определения>>
В данном документе, «С1-10-алкильная группа» относится к линейной или разветвленной алкильной группе, имеющей 1-10 атомов углерода. Примеры С1-10-алкильной группы включают метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, изопентил, неопентил, 1-этилпропил, н-гексил, изогексил, 1,1-диметилбутил, 2,2-диметилбутил, 3,3-диметилбутил, 2-этилбутил, н-гептил, н-октил, н-нонил, и н-децил. С1-10-алкильные группы включают С1-8-алкильные группы, С1-7-алкильные группы, С1-6-алкильные группы, С1-5-алкильные группы, и С1-4-алкильные группы.
[0017]
В данном документе, «С1-10-алкоксигруппа» относится к группе, где атом кислорода связан с С1-10-алкилом. Примеры С1-10-алкоксигруппы включают метокси-, этокси-, пропокси-, изопропокси-, бутокси-, изобутокси-, втор-бутокси-, трет-бутокси-, пентилокси-, изопентилокси-, неопентилокси-, 1-этилпропокси-, гексилокси-, изогексилокси-, 1,1-диметилбутокси-, 2,2-диметилбутокси-, 3,3-диметилбутокси-, 2-этилбутокси-, гептилокси-, октилокси-, нонилокси-, и децилокси-группы. С1-10-алкоксигруппы включают С1-8-алкоксигруппы, С1-7-алкоксигруппы, С1-6-алкоксигруппы, С1-5-алкоксигруппы, и С1-4-алкоксигруппы.
[0018]
В данном документе, «атом галогена» относится к атомам фтора, атомам хлора, атомам брома или атомам йода.
[0019]
В данном документе, «С1-10-алкильная группа, которая может быть замещена галогеном», включает «С1-10-алкильные группы», где замещаемые атомы водорода в них замещены одним или более, например, одним - пятью атомами галогена. Конкретные примеры включают дифторметил, трифторметил, 2,2,2-трифторэтил, 3,3,3-трифторпропил, 4-фторбутил, и 4,4,4-трифторбутил.
[0020]
В данном документе, «С1-10-алкоксигруппа, которая может быть замещена галогеном», включает «С1-10-алкоксигруппы», где замещаемые атомы водорода в них замещены одним или более, например, одним - пятью атомами галогена. Конкретные примеры включают дифторметокси-, трифторметокси-, 2,2,2-трифторэтокси-, 3,3,3-трифторпропокси-, 4-фторбутокси-, и 4,4,4-трифторбутокси-группы.
[0021]
В данном документе, «С1-40-алкиленовая группа» относится к линейной или разветвленной алкильной группе, имеющей 1-40 атомов углерода. Конкретные примеры включают метиленовую группу, этиленовую группу, пропиленовую группу, бутиленовую группу, пентиленовую группу, гексиленовую группу, гептиленовую группу, октиленовую группу, нониленовую группу, дециленовую группу, ундециленовую группу, додециленовую группу, тридециленовую группу, тетрадециленовую группу, пентадециленовую группу, гексадециленовую группу, гептадециленовую группу, октадециленовую группу, нонадециленовую группу, эйкозаниленовую группу, геникозаниленовую группу, докозаниленовую группу, трикозаниленовую группу, тетракозаниленовую группу, пентакозаниленовую группу, гексакозаниленовую группу, гептакозаниленовую группу, октакозаниленовую группу, нонакозаниленовую группу, триаконтаниленовую группу, гентриаконтаниленовую группу, дотриаконтаниленовую группу, тритриаконтаниленовую группу, тетратриаконтаниленовую группу, пентатриаконтаниленовую группу, гексатриаконтаниленовую группу, гептатриаконтаниленовую группу, октатриаконтаниленовую группу, нонатриаконтаниленовую группу, и тетраконтаниленовую группу. С1-40-алкиленовые группы включают С1-20-алкиленовые группы, С1-10-алкиленовые группы, и С1-5-алкиленовые группы.
[0022]
В данном документе, «С6-14-ариленовая группа» относится к двухвалентной группе, содержащей ароматический карбоцикл, имеющий 6-14 атомов углерода, например, к фениленовой группе, нафтиленовой группе, и антрацениленовой группе.
[0023]
В данном документе, «5-10-членная гетероариленовая группа» относится к двухвалентной группе, включающей 5-10-членный ароматический гетероцикл. Примеры ароматического гетероцикла включают пиррольное кольцо, индольное кольцо, тиофеновое кольцо, бензотиофеновое кольцо, фурановое кольцо, бензофурановое кольцо, пиридиновое кольцо, хинолиновое кольцо, изохинолиновое кольцо, тиазольное кольцо, бензотиазольное кольцо, изотиазольное кольцо, бензисотиазольное кольцо, пиразольное кольцо, индазольное кольцо, оксазольное кольцо, бензоксазольное кольцо, изоксазольное кольцо, бензисоксазольное кольцо, имидазольное кольцо, бензимидазольное кольцо, триазольное кольцо, бензотриазольное кольцо, пиримидиновое кольцо, уридиновое кольцо, пиразиновое кольцо, и пиридазиновое кольцо.
[0024]
В данном документе, «оксогруппа» относится к группе, которая образует карбонильную группу с атомом углерода, с которым она связана.
[0025]
В данном документе, «полимер» относится к соединению, имеющему, по меньшей мере, 2 повторяющихся звена, предпочтительно 3 повторяющихся звена, более предпочтительно, по меньшей мере, 5 повторяющихся звеньев, и даже более предпочтительно, по меньшей мере, 10 повторяющихся звеньев.
[0026]
В данном документе, «фармацевтически приемлемая соль» относится к соли свободного соединения, которая является фармацевтически приемлемой и имеет желательную фармакологическую активность. «Фармацевтически приемлемая соль» особым образом не ограничивается, но может представлять собой, например:
соль неорганической кислоты, такой как серная кислота, соляная кислота, бромистоводородная кислота, фосфорная кислота или азотная кислота;
соль органической кислоты, такой как уксусная кислота, щавелевая кислота, молочная кислота, винная кислота, фумаровая кислота, малеиновая кислота, лимонная кислота, бензолсульфоновая кислота, метансульфоновая кислота, пара-толуолсульфоновая кислота, бензойная кислота, камфорсульфоновая кислота, этансульфоновая кислота, глюкогептоновая кислота, глюконовая кислота, глутаминовая кислота, гликолевая кислота, яблочная кислота, малоновая кислота, миндальная кислота, галактаровая кислота, или нафталин-2-сульфоновая кислота;
соль одного или нескольких ионов металла, таких как ионы лития, ионы натрия, ионы калия, ионы кальция, ионы магния, ионы цинка, ионы алюминия; или
соль амина, такого как аммиак, аргинин, лизин, пиперазин, холин, диэтиламин, 4-фенилциклогексиламин, 2-аминоэтанол, или бензатин.
[0027]
В данном документе, «опухоль» относится к клеточной совокупности, которая проявляет неконтролируемую пролиферацию вследствие генетической мутации и включает доброкачественные и злокачественные опухоли. В данном документе, термин «злокачественная опухоль» может быть использован взаимозаменяемо с термином «рак». Термин «рак» используется в широком смысле с включением раковых заболеваний, которые представляют собой карциномы эпителиального происхождения, саркомы, и гематологические злокачественные образования, такие как лейкемия. Примеры раковых заболеваний, которые представляют собой карциномы эпителиального происхождения, включают рак желудка, рак толстой кишки, рак желчного пузыря, рак желчного протока, рак поджелудочной железы, рак двенадцатиперстной кишки, рак почки, рак предстательной железы, рак яичника, рак матки, рак молочной железы, рак кожи, печеночноклеточный рак, рак языка, рак пищевода, и фарингеальный рак, но не ограничиваются этим. Примеры сарком включают фибросаркому, злокачественную фиброзную гистиоцитому, кожную фибросаркому, липосаркому, миосаркому, ангиосаркому, саркому Капоши, лимфангиосаркому, синовиальную саркому, и остеосаркому, но не ограничиваются этим. Примеры гематологических злокачественных заболеваний включют лейкемию, злокачественную лимфому, и множественную миелому, но не ограничиваются этим. В данном документе, «клетки опухоли» представляют собой клетки, которые образуют опухоли и относятся к клеткам, которые обычно пролиферируют аномально независимо от нормальной окружающей ткани (то есть, клеткам, которые стали раковыми).
[0028]
В данном документе, «субъект» относится к любому млекопитающему. «Субъект» особым образом не ограничивается, но включает, например, людей, приматов, мышей, крыс, собак, кошек, коров, лошадей, свиней, овец, коз, и верблюдов. Субъект предпочтительно представляет собой человека.
[0029]
<<Производное пара-борфенилаланина (BPA)>>
BPA-производное по настоящему изобретению включает полимер, связанный напрямую или через линкер с полученной от BPA группой, представленной формулой (I), приведенной ниже:
[Хим. стр. 15]

где,
стрелки показывают связь со смежным атомом и
X1-X4, каждый независимо, представляют собой Н, 18F, или 19F.
[0030]
Производное BPA по настоящему изобретению связывается с аминокислотным транспортером (в частности, LAT1) на опухолевых клетках с помощью группы, представленной формулой (I), присутствующей в производном BPA. После связывания с аминокислотным транспортером, BPA-производное по настоящему изобретению захватывается опухолевой клеткой в результате эндоцитоза. Таким образом, BPA-производное по настоящему изобретению обеспечивает селективное накопление бора в опухолевых клетках. Далее, BPA-производное по настоящему изобретению перемещается в эндосому. В результате, скорость клеточной экскреции бора из опухолевых клеток сравнительно ниже, чем при использовании BPA как такового. Таким образом, бор может удерживаться в течение длительного периода в опухолевых клетках. Кроме того, BPA-производное по настоящему изобретению может позволить достигать превосходного соотношения концентраций бора в опухоли/нормальной ткани и соотношения концентраций бора в опухоли/крови.
[0031]
Трехмерная структура группы, представленной формулой (I), особым образом не ограничивается при условии, что селективный захват BPA-производного в опухолевые клетки при этом не затрудняется, и форма трехмерных структур может быть представлена формулой (I-a) или (I-b), приведенной ниже. Кроме того, обе нижеприведенные группы, представленные формулой (I-a) и формулой (I-b), могут быть внедрены в BPA-производное по настоящему изобретению. Группа формулы (I) предпочтительно представляет собой группу, представленную формулой (I-a), имеющую L-фенилаланиновый фрагмент.
[Хим. стр. 16]
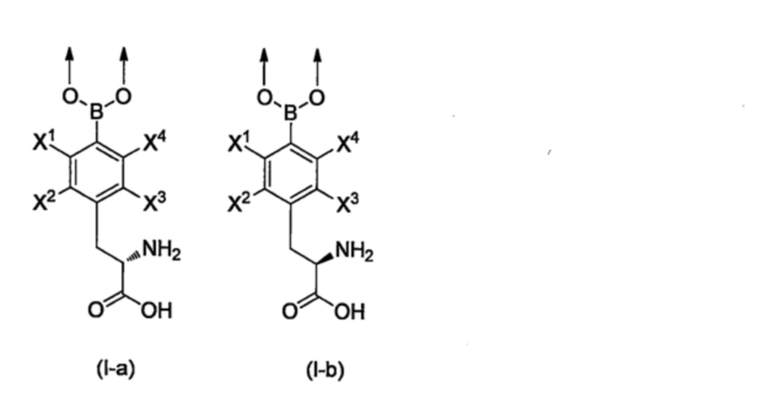
[0032]
Если, по меньшей мере, один из X1-X4 в формуле (1) представляет собой 18F, BPA-производное по настоящему изобретению может быть использовано для диагностики и обнаружения опухолей при использовании, например, PET (позитронно-эмиссионной томографии). Если, по меньшей мере, один из X1-X4 в формуле (1) представляет собой 19F, BPA-производное по настоящему изобретению может быть использовано для диагностики и обнаружения опухолей при использовании, например, 19F-MRI (магнитно-резонансной визуализации).
[0033]
Способ, которым связывают группу формулы (I) с полимером или линкером, особым образом не ограничивается. Например, фрагмент бороновой кислоты может быть подвергнут реакции с диольным фрагментом, присутствующим в полимере или линкере, с получением структуры сложного эфира бороновой кислоты, представленной следующими формулами (VIII-a)-(VIIIc).
[Хим. стр. 17]
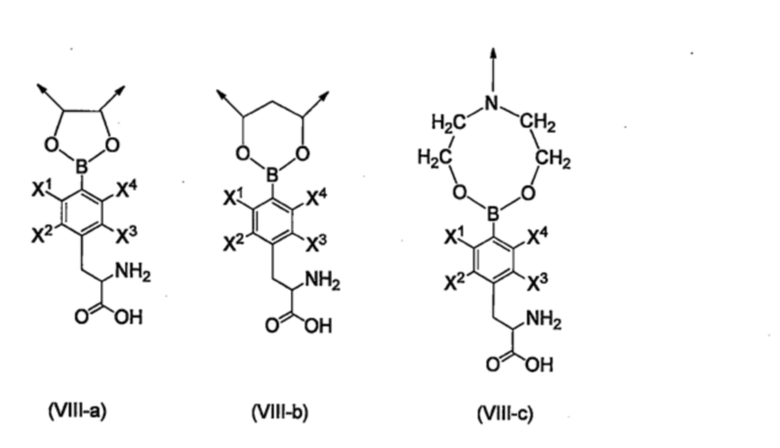
где,
стрелки показывают связь со смежным атомом, и
X1-X4, каждый независимо, представляют собой Н, 18F, или 19F.
[0034]
Далее, если получают сложноэфирную структуру, такую как в формулах (VIII-a) и (VIII-b), приведенных выше, то она может быть подвергнута реакции с дополнительной гидроксильной группой, присутствующей в полимере или линкере, с получением триольно-боратной структуры. Триольно-боратная структура представляет собой структуру, представленную, например, формулой (IV-a), приведенной ниже.
[Хим. стр. 18]
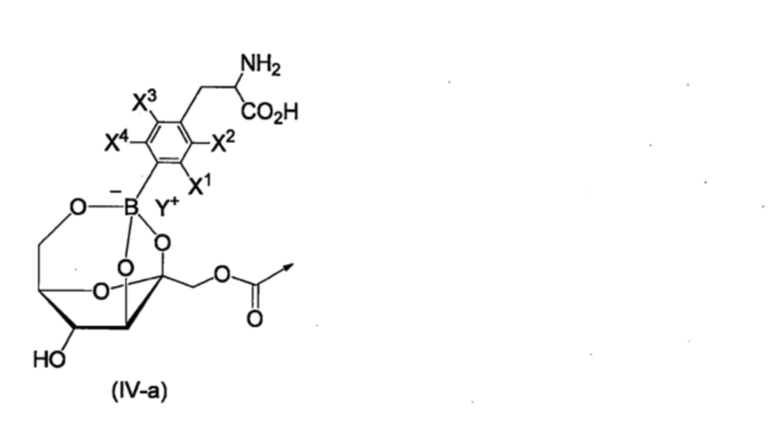
где,
стрелка показывает связь со смежным атомом,
X1-X4, каждый независимо, представляют собой Н, 18F, или 19F, и
Y+ представляет собой, например, Н+, ион щелочного металла, или ион тетра-С1-6-алкил-аммония.
[0035]
Далее, если получают сложноэфирную структуру, такую как в формулах (VIII-a) и (VIII-b), приведенных выше, то может быть получена структура сложного эфира бороновой кислоты, где гидроксильная группа связана с бором, в водном растворе. Такие структуры сложного эфира бороновой кислоты имеют структуры, представленные, например, формулами (IV-b) и (IV-c), приведенными ниже.
[Хим. стр. 19]
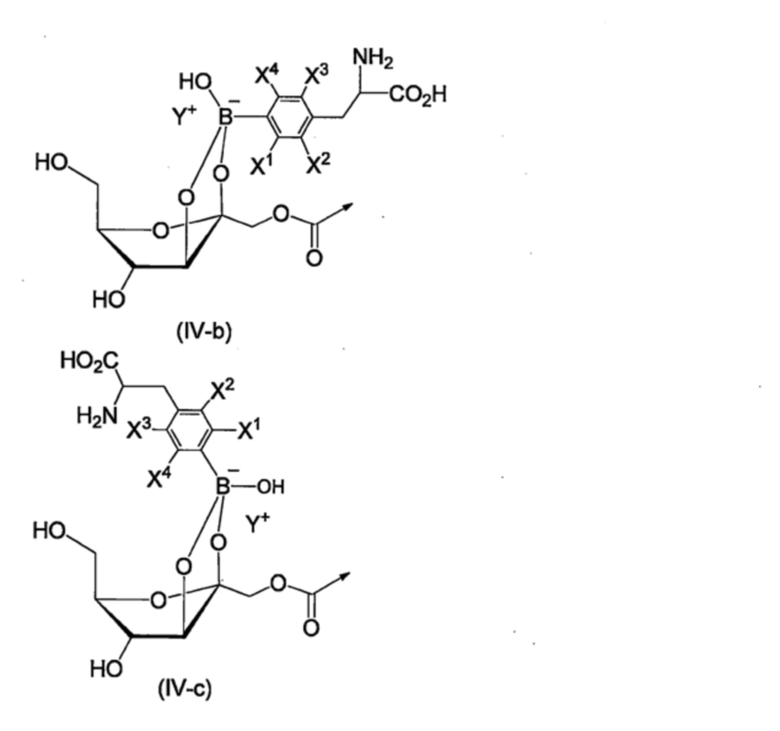
где,
стрелки показывают связь со смежным атомом,
X1-X4, каждый независимо, представляют собой Н, 18F, или 19F, и
Y+ представляет собой, например, Н+, ион щелочного металла, или ион тетра-С1-6-алкил-аммония.
[0036]
Кроме того, например, фрагмент бороновой кислоты может быть подвергнут реакции с фрагментом дикарбоновой кислоты, присутствующим на полимере или линкере, с получением структуры, такой как структура, представленная формулой (VIII-d), приведенной ниже.
[Хим. стр. 20]
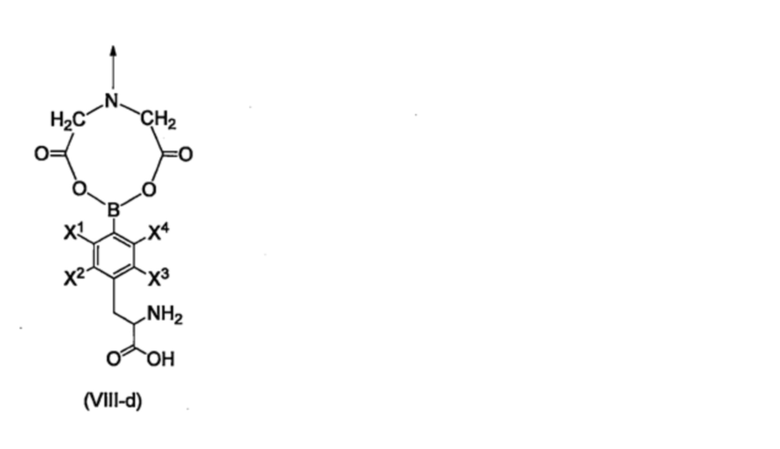
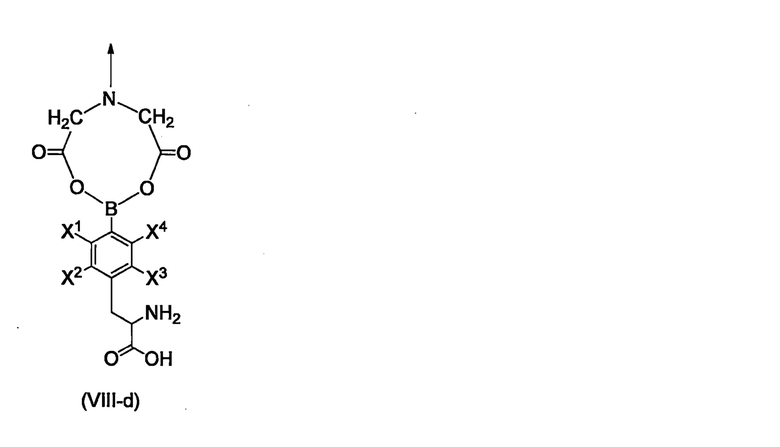

где,
стрелка показывает связь со смежным атомом, и
X1-X4, каждый независимо, представляют собой Н, 18F, или 19F.
[0037]
Число групп, представленных формулой (I), в производном BPA по настоящему изобретению особым образом не ограничивается при условии, что действие производного BPA не ингибируется. Нижний предел числа вышеупомянутых групп составляет, например, 1, 2, 3, 4, 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 60, 70, 80, 90, или 100, и верхний предел числа вышеупомянутых групп составляет, например, 200, 300, 400, 500, 600, 700, 800, 900, 1000, 2000, 3000, или 5000. Число вышеупомянутых групп составляет предпочтительно 2 или более. В том случае, когда число групп, представленных формулой (I), в производном BPA по настоящему изобретению составляет 2 или более, группы, представленные формулой (I), могут быть одинаковыми или различными. В результате образования многочисленных связей со множеством аминокислотных транспортеров (в частности, LAT1) на опухолевых клетках посредством множества групп, представленных формулой (I), способность к связыванию производного BPA по настоящему изобретению с аминокислотными транспортерами значительно повышается по сравнению со способностью к связыванию BPA как такового с аминокислотным транспортером. Более предпочтительно, число групп, представленных формулой (I), составляет 2-5000, 2-2000, 2-1000, 2-500, 2-300, 2-200, 10-5000, 10-2000, 10-1000, 10-500, 10-300, или 10-200. Следует отметить, что реакция между бороновой кислотой и гидроксильной группой является равновесной реакцией. Так, в том случае, когда производное BPA по настоящему изобретению имеет структуру сложного эфира бороновой кислоты, число групп, представленных формулой (I), содержащихся в производном BPA по настоящему изобретению, варьируется в зависимости от концентрации бороновой кислоты и полимера в растворе, который образует производное BPA по настоящему изобретению.
[0038]
Полимер, содержащийся в производном BPA по настоящему изобретению, особым образом не ограничивается при условии, что не ингибируется действие производного BPA. Полимер может быть линейным или разветвленным и может представлять собой гомополимер или сополимер. В случае сополимеров, сополимер может быть статистическим сополимером или блок-сополимером. Полимер, содержащийся в производном BPA по настоящему изобретению, предпочтительно представляет собой водорастворимый полимер. Полимеры, которые могут быть использованы в производном BPA по настоящему изобретению, включают, например, поливиниловый спирт, полиуретан, сложный полиэфир, полиамид, поликарбонат, полиимид, простой полиэфир, полиакрилат, полиакриламид, полисилоксан, поливинил, полипептид, полисахарид, полинуклеотид, и их сополимеры. Предпочтительно, полимер представляет собой поливиниловый спирт, сложный полиэфир, простой полиэфир, полиакрилат, полиакриламид, полипептид, полисахарид, и их сополимеры. Более предпочтительно, полимер представляет собой поливиниловый спирт или полипептид.
[0039]
Нижний предел среднечисловой молекулярной массы производного BPA по настоящему изобретению составляет, например, 1000 Да, 2000 Да, 3000 Да, 4000 Да, 5000 Да, 6000 Да или 7000 Да (предпочтительно 5000 Да), и ее верхний предел, хотя и не ограничивается особым образом, составляет, например, 1500000 Да, 1000000 Да, 500000 Да, 300000 Да, 100000 Да, 70000 Да или 50000 Да. Среднечисловая молекулярная масса производного BPA по настоящему изобретению составляет предпочтительно 1000 Да или более, более предпочтительно от 3000 Да до 150000 Да, и еще более предпочтительно от 6000 Да до 70000 Да. В данном документе, если не задано иное, среднечисловая молекулярная масса имеет значение, определяемое вычислением на основе интегрированного значения по 1Н-ЯМР спектру.
[0040]
В том случае, когда группа, представленная формулой (I), связана с полимером через линкер, линкер содержит группу, которая может связываться с BPA. Предпочтительно, эта группа представляет собой гидроксильную группу или карбоксильную группу. Предпочтительно, линкер содержит, по меньшей мере, 2 гидроксильные группы или, по меньшей мере, 2 карбоксильные группы. Линкер особым образом не ограничивается при условии, что не ингибируется функция производного BPA по настоящему изобретению, но может представлять собой, например, С1-40-алкиленовую группу, замещенную посредством 2 гидроксильных групп. В данном документе, метильные группы в С1-40-алкиленовой группе могут быть замещены посредством 1-10 оксогрупп, метиленовые группы в С1-40-алкиленовой группе могут быть замещены посредством 1-10 галогенов, метиленовые группы в С1-40-алкиленовой группе могут быть замещены посредством 1-10 гидроксильных групп, смежные метиленовые группы могут быть соединены друг с другом посредством 1-10 ненасыщенных связей, и из числа метиленовых групп в алкиленовой группе, 1-20 метиленовых групп могут быть заменены на NH, N(C1-10-алкил), O, S, C6-14-арилен, или 5-10-членный гетероарилен. Кроме того, линкер включает, например, полиолы (например, катехолы и полифенолы), сахара (например, фруктозу), сахарные спирты (например, сорбит) и глюкамин. К тому же, линкер включает, например, соединения, представленные формулой (X-a) и формулой (XII-a), приведенными ниже.
[Хим. стр. 21]
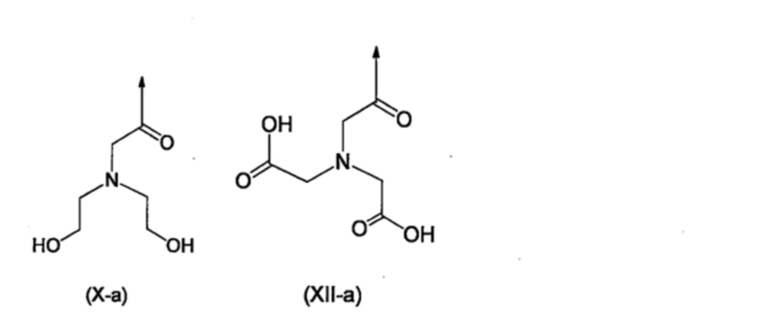
где,
стрелки показывают связь со смежным атомом.
[0041]
Производное BPA по настоящему изобретению может содержать, по меньшей мере, один тип детектируемой метки. В данном документе, «детектируемая метка» представляет собой любой атом или соединение, который(-ое) может быть детектирован(-о) любым существующим средством детектирования. Средство детектирования особым образом не ограничивается, но может включать, например, визуальное обследование, использование оптических контрольно-измерительных приборов (например, оптического микроскопа, флюоресцентного микроскопа, фазоконтрастного микроскопа, оборудования для визуализации in vivo), рентгеновского оборудования (например, простого рентгеновского прибора, оборудования для CT (компьютерной томографии)), оборудования для MRI (магнитно-резонансной визуализации), оборудования для обследования методом медицинской радиологии (например, оборудования для сцинтиграфии, оборудования для PET (позитронно-эмиссионной томографии), оборудования для SPECT (однофотонной эмиссионной компьютерной томографии)), оборудования для ультразвукового обследования и оборудования для термографии. Специалист в данной области знает соответственные метки для каждого средства обнаружения, что раскрыто, например, в публикации Lecchi et al., Q J Nucl Med Mol Imaging. 2007; 51 (2): pp. 111-26. Детектируемая метка особым образом не ограничивается, но может, например, включать флуоресцентные метки, люминесцентные метки, контрастные агенты, атомы металла, соединения, содержащие один или более атомов металла, радиоизотопы, соединения, содержащие один или более радиоизотопов, наночастицы, и липосомы. Местоположение, в которое вводят детектируемую метку в производное BPA по настоящему изобретению, особым образом не ограничивается. Например, детектируемая метка может быть введена в концевые группы полимера или может быть введена напрямую или через линкер в заместитель (например, гидроксильную группу), имеющийся в полимере.
[0042]
Метки, подходящие для детектирования путем визуального обследования или путем использования оптических контрольно-измерительных приборов, включают, например, различные флуоресцентные и люминесцентные метки. Конкретные флуоресцентные метки не ограничиваются особым образом, но могут быть использованы, например, серия Cy™ (например, Cy™ 2, 3, 5, 5.5, 7, и т.д.), серия DyLight™ (например, DyLight™ 405, 488, 549, 594, 633, 649, 680, 750, 800, и т.д.), серия Alexa Fluor® (например, Alexa Fluor® 405, 488, 549, 594, 633, 647, 680, 750, и т.д.), серия HiLyte Fluor® (например, HiLyte Fluor™ 488, 555, 647, 680, 750, и т.д.), серия ATTO (например, ATTO 488, 550, 633, 647N, 655, 740, и т.д.), FAM, FITC, Texas Red, GFP, RFP, Qdot, IRDye® (например, IRDye® 700DX).
[0043]
Далее, конкретные люминесцентные метки особым образом не ограничиваются, но могут быть использованы, например, люминол, люциферин, люцигенин, и экворин.
[0044]
Метки, подходящие для детектирования при помощи использования рентгеновского оборудования, включают, например, различные контрастные агенты. Конкретные контрастные агенты особым образом не ограничиваются, но могут быть использованы, например, атомы йода, ионы йода, и йод-содержащие соединения.
[0045]
Метки, подходящие для детектирования с использованием оборудования для MRI, включают, например, различные атомы металла или соединения, содержащие1 или более типов атома металла, например, комплекс, содержащий один или более атомов металла. Конкретно, метки особым образом не ограничиваются, но могут включать, например, гадолиний (III) (Gd(III)), иттрий-88 (88Y), индий-111 (111In); их комплексы с лигандами, такими как диэтилентриаминпентауксусная кислота (DTPA), тетраазациклододекан-1,4,7,10-тетрауксуснаякислота (DOTA), (1,2-этандиилдинитрило)тетрауксусная кислота (EDTA), этилендиамин, 2,2'-бипиридин (bipy), 1,10-фенантролин (phen), 1,2-бис(дифенилфосфино)этан (DPPE), 2,4-пентандион (acac), оксалат (ox); и суперпарамагнитный оксид железа (SPIO), и оксид марганца (MnO).
[0046]
Примеры меток, подходящих для детектирования с использованием оборудования для обследования методом медицинской радиологии, включают, например, различные радиоизотопы и соединения, содержащие один или более радиоизотопов, например, комплекс одного или более радиоизотопов. Радиоизотопы особым образом не ограничиваются, но могут включать, например, технеций-99m (99mTc), индий-111 (111In), йод-123 (123I), йод-124 (124I), йод-125 (125I), йод-131 (131I), таллий-201 (201Tl), углерод-11 (11C), азот-13 (13C), кислород-15 (15O), фтор-18 (18F), медь-64 (64Cu), галлий-67 (67Ga), криптон-81m (81mKr), ксенон-133 (133Xe), стронций-89 (89Sr), иттрий-90 (90Y). Кроме того, соединения, которые содержат радиоизотопы, особым образом не ограничиваются, но могут включать, например, 123I-IMP, 99mTc-HMPAO, 99mTc-ECD, 99mTc-MDP, 99mTc-тетрофосмин, 99mTc-MIBI, 99mTcO4-, 99mTc-MAA, 99mTc-MAG3, 99mTc-DTPA, 99mTc-DMSA, 18F-FDG.
[0047]
Метки, подходящие для детектирования с помощью оборудования для ультразвукового обследования, особым образом не ограничиваются, но могут включать, например, наночастицы или липосомы.
[0048]
В одном варианте осуществления настоящего изобретения, производное BPA по настоящему изобретению представляет собой соединение, представленное формулой (II), приведенной ниже, или его фармацевтически приемлемую соль.
[Хим. стр. 22]
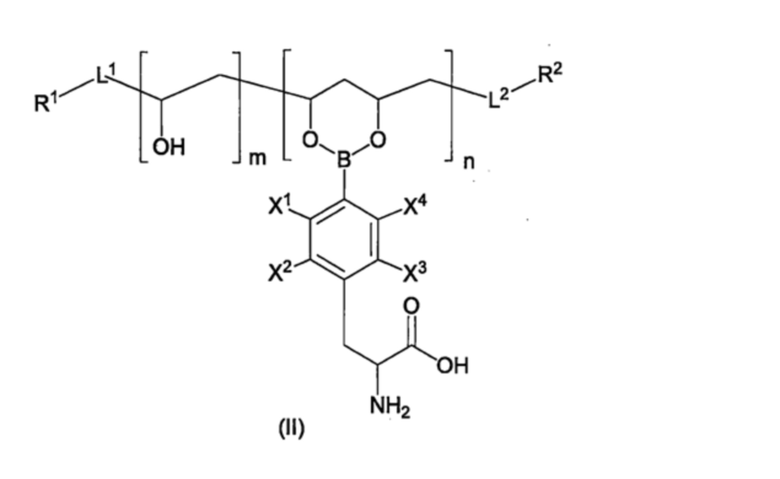
где,
X1-X4, каждый независимо, представляют собой Н, 18F или 19F,
L1 и L2, каждый независимо, представляют собой линкер или отсутствуют,
R1 и R2, каждый независимо, представляют собой водород, гидроксильную группу, карбоксильную группу, аминогруппу, С1-10-алкильную группу, которая может быть замещена галогеном, С1-10-алкоксигруппу, которая может быть замещена галогеном, тиольную группу, цианогруппу, азидогруппу, -CH(OA1)2, или детектируемую метку,
А1 представляет собой С1-6-алкильную группу,
m имеет значение от 0 до 3998,
n имеет значение от 1 до 2000,
m+2n=от 10 до 4000, и
порядок следования повторяющихся звеньев является произвольным (то есть, сополимер может представлять собой статистический сополимер или блок-сополимер).
[0049]
m и n представляют собой степень полимеризации. Нижний предел для m составляет 0, но предпочтительно составляет 0, 1, 2, 3, 4, 5, 6, 7, 8, или 9. Верхний предел для m имеет значение 3998, но предпочтительно имеет значение 3998, 3500, 3000, 2500, 2000, 1500, 1000, 900, 800, 700, 600, 500, 400, 300, 200, 100, 50, 40, 30, 20, или 10. Нижний предел для n имеет значение 1, но предпочтительно составляет 1, 2, 3, 4, 5, 6, 7, 8, 9, или 10. Верхний предел для n составляет 2000, но предпочтительно имеет значение 2000, 1990, 1980, 1970, 1960, 1950, 1900, 1800, 1700, 1600, 1500, 1400, 1300, 1200, 1100, или 500. Нижний предел для (m+2n) составляет 10, но предпочтительно имеет значение 10, 20, 30, 40, или 50. Верхний предел для (m+2n) составляет 4000, но предпочтительно имеет значение 4000, 3500, 3000, 2500, 2000, 1500, 1000, 900, 800, 700, 600, 500, 400, 300, или 200. m и n могут быть вычислены проведением количественной оценки в расчете на интегрированное значение по спектру 1Н-ЯМР.
[0050]
L1 и/или L2, в том случае, когда они являются линкерами, особым образом не ограничиваются, но могут представлять собой, например, С1-40-алкиленовую группу. В данном документе, метильные группы в С1-40-алкиленовой группе могут быть замещены посредством 1-10 оксогрупп, метиленовые группы в С1-40-алкиленовой группе могут быть замещены посредством 1-10 галогенов, смежные метиленовые группы могут быть связаны друг с другом посредством 1-10 ненасыщенных связей, и из числа метиленовых групп в алкиленовой группе, 1-20 метиленовых групп могут быть заменены на NH, N(C1-10-алкил), O, S, C6-14-арилен, 5-10-членный гетероарилен, или полиоксиалкилен, имеющий степень полимеризации 2-2000, 2-1000, 2-500, 2-400, 2-300, 2-200, 2-100, 2-50, или 2-10. Линкер может иметь, например, следующую структуру.
[Хим. стр. 23]
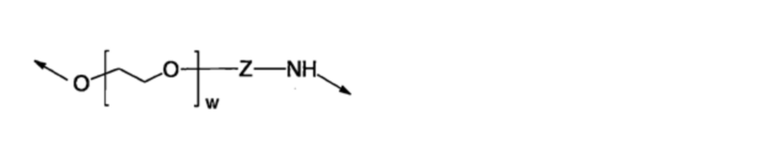
где, w имеет значение 1-2000, и Z представляет собой С1-5-алкиленовую группу.
Кроме того, линкер может иметь, например, следующую структуру.
[Хим. стр. 24]

где, w имеет значение 1-2000, и Z представляет собой С1-5-алкиленовую группу.
[0051]
В одном варианте осуществления настоящего изобретения, производное BPA по настоящему изобретению представляет собой соединение, представленное формулой (III), приведенной ниже, или его фармацевтически приемлемую соль.
[Хим. стр. 25]
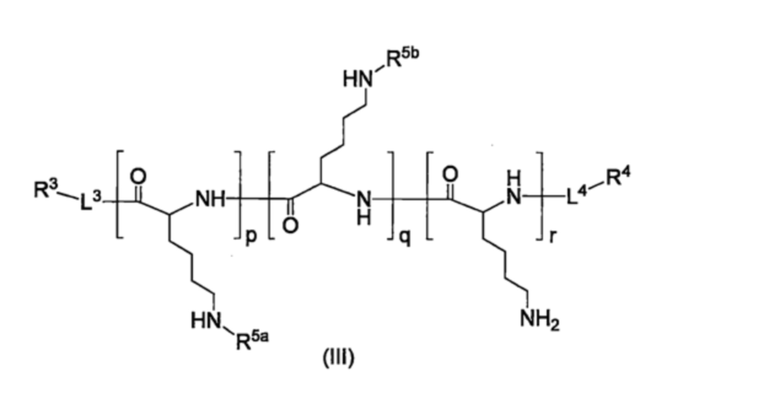
где,
L3 и L4, каждый независимо, представляют собой линкер или отсутствуют,
R3 и R4, каждый независимо, представляют собой водород, гидроксильную группу, карбоксильную группу, аминогруппу, С1-10-алкильную группу, которая может быть замещена галогеном, С1-10-алкоксигруппу, которая может быть замещена галогеном, тиольную группу, цианогруппу, азидогруппу, -CH(OA1)2, или детектируемую метку,
А1 представляет собой С1-6-алкильную группу,
R5a, каждый независимо, представляют собой группу, представленную формулой (IV-a) или (IV-b), приведенной ниже,
[Хим. стр. 26]

где, стрелки показывают связь с NH,
R5b, каждый независимо, представляют собой группу, выбранную из группы, состоящей из групп, представленных формулами (IV-с) - (IV-g), приведенными ниже,
[Хим. стр. 27]

где,
стрелки показывают связь с NH,
X1-X4, каждый независимо, представляют собой Н, 18F или 19F,
Y+ представляет собой H+, ион щелочного металла, или ион тетра-С1-6-алкил-аммония (например, тетраметиламмония, тетраэтиламмония, тетра-n-пропиламмония, тетра-n-бутиламмония, тетра-n-пентиламмония, тетра-n-гексиламмония),
p=от 0 до 299,
q=от 1 до 300,
r=от 0 до 299,
p+q+r=от 10 до 300, и
порядок следования повторяющихся звеньев является произвольным (то есть, сополимер может представлять собой статистический сополимер или блок-сополимер).
[0052]
В данном документе, «R5a, каждый независимо,» означает, что, когда имеется множество повторяющихся звеньев, также имеется множество R5a, которые находятся в повторяющихся звеньях, но эти R5a могут совпадать или отличаться друг от друга. «R5b, каждый независимо,» имеет притом аналогичное значение.
[0053]
p, q и r представляют собой степень полимеризации. Нижний предел для p составляет 0, но предпочтительно имеет значение 0, 1, 2, 3, 4, 5, 6, 7, 8, или 9. Верхний предел для p составляет 299, но предпочтительно имеет значение 299, 290, 280, 270, 260, или 250. Нижний предел для q составляет 1, но предпочтительно имеет значение 1, 2, 3, 4, 5, 6, 7, 8, или 9. Верхний предел для q составляет 300, но предпочтительно имеет значение 300, 290, 280, 270, 260, или 250. Нижний предел для r составляет 0, но предпочтительно имеет значение 0, 1, 2, 3, 4, 5, 6, 7, 8, или 9. Верхний предел для r составляет 299, но предпочтительно имеет значение 299, 290, 280, 270, 260, или 250. Нижний предел для (p+q+r) составляет 10, но предпочтительно имеет значение 10, 20 или 30. Верхний предел для (p+q+r) составляет 300, но предпочтительно имеет значение 300, 290, 280, 270, 260, или 250. p, q и r могут быть вычислены в результате проведения количественной оценки в расчете на интегрированное значение по спектру 1Н-ЯМР.
[0054]
L3 и/или L4, в том случае, когда они являются линкерами, особым образом не ограничиваются, но могут представлять собой, например, С1-40-алкиленовую группу. В данном документе, метильные группы в С1-40-алкиленовой группе могут быть замещены посредством 1-10 оксогрупп, метиленовые группы в С1-40-алкиленовой группе могут быть замещены посредством 1-10 галогенов, смежные метиленовые группы могут быть связаны друг с другом посредством 1-10 ненасыщенных связей, и из числа метиленовых групп в алкиленовой группе, 1-20 метиленовых групп могут быть заменены на NH, N(C1-10-алкил), O, S, C6-14-арилен, 5-10-членный гетероарилен, или полиоксиалкилен, имеющий степень полимеризации 2-2000, 2-1000, 2-500, 2-400, 2-300, 2-200, 2-100, 2-50, или 2-10. Линкер может иметь, например, следующую структуру.
[Хим. стр. 28]

где, w имеет значение 1-2000, и Z представляет собой С1-5-алкиленовую группу.
Кроме того, линкер может иметь, например, следующую структуру.
[Хим. стр. 29]

где, w имеет значение 1-2000, и Z представляет собой С1-5-алкиленовую группу.
[0055]
В одном варианте осуществления настоящего изобретения, производное BPA по настоящему изобретению представляет собой соединение, представленное формулой (V), приведенной ниже, или его фармацевтически приемлемую соль.
[Хим. стр. 30]
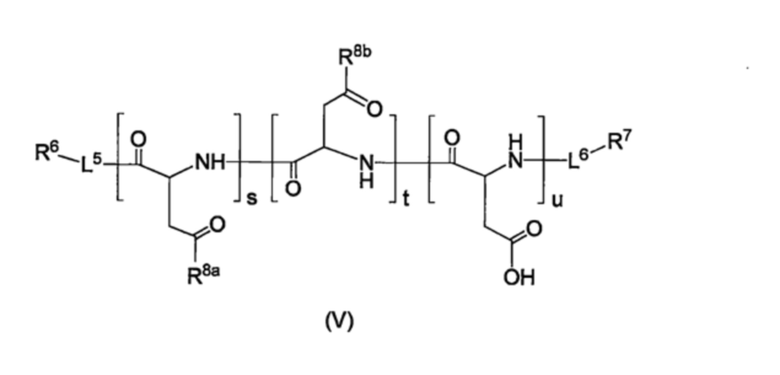
где,
L5 и L6, каждый независимо, представляют собой линкер или отсутствуют,
R6 и R7, каждый независимо, представляют собой водород, гидроксильную группу, карбоксильную группу, аминогруппу, С1-10-алкильную группу, которая может быть замещена галогеном, С1-10-алкоксигруппу, которая может быть замещена галогеном, тиольную группу, цианогруппу, азидогруппу, -CH(OA1)2, или детектируемую метку,
А1 представляет собой С1-6-алкильную группу,
R8a, каждый независимо, представляют собой группу, представленную формулой (VI-a), приведенной ниже,
[Хим. стр. 31]

где, стрелка показывает связь с карбонильным углеродом,
R8b, каждый независимо, представляют собой группу, выбранную из группы, состоящей из групп, представленных формулами (VI-b)-(VI-h), приведенными ниже,
[Хим. стр. 32]
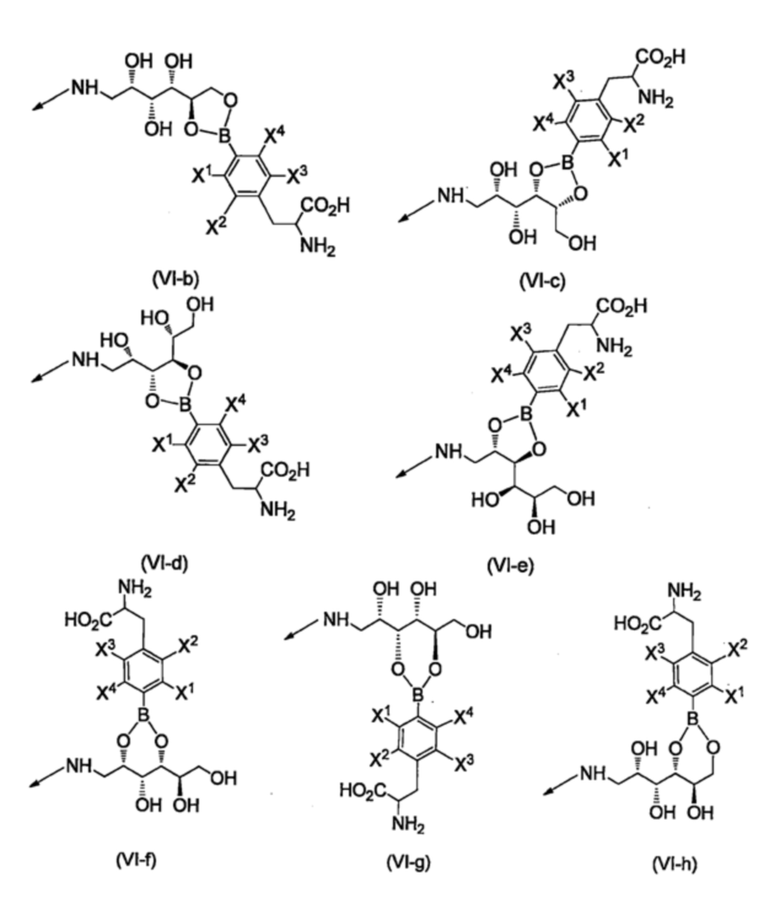
где,
стрелки показывают связь с карбонильным углеродом,
X1-X4, каждый независимо, представляют собой Н, 18F или 19F,
s=от 0 до 299,
t=от 1 до 300,
u=от 0 до 299,
s+t+u=от 2 до 300, и
порядок следования повторяющихся звеньев является произвольным (то есть, сополимер может представлять собой статистический сополимер или блок-сополимер).
[0056]
В данном документе, «R8b, каждый независимо,» означает, что, когда имеется множество повторяющихся звеньев, также существует множество R8b, которые находятся в повторяющихся звеньях, но эти R8b могут совпадать или отличаться друг от друга.
[0057]
s, t и u представляют собой степень полимеризации. Нижний предел для s составляет 0, но предпочтительно имеет значение 0, 1, 2, 3, 4, 5, 6, 7, 8, или 9. Верхний предел для s составляет 299, но предпочтительно имеет значение 299, 290, 280, 270, 260, или 250. Нижний предел для t составляет 1, но предпочтительно имеет значение 1, 2, 3, 4, 5, 6, 7, 8, или 9. Верхний предел для t составляет 300, но предпочтительно имеет значение 300, 290, 280, 270, 260, или 250. Нижний предел для u составляет 0, но предпочтительно имеет значение 0, 1, 2, 3, 4, 5, 6, 7, 8, или 9. Верхний предел для u составляет 299, но предпочтительно имеет значение 299, 290, 280, 270, 260, или 250. Нижний предел для (s+t+u) составляет 2, но предпочтительно имеет значение 2, 3, 4 или 5. Верхний предел для (s+t+u) составляет 300, но предпочтительно имеет значение 300, 290, 280, 270, 260, или 250. s, t и u могут быть вычислены в результате проведения количественной оценки в расчете на интегрированное значение по спектру 1Н-ЯМР.
[0058]
L5 и/или L6, в том случае, когда они являются линкерами, особым образом не ограничиваются, но могут представлять собой, например, С1-40-алкиленовую группу. В данном документе, метильные группы в С1-40-алкиленовой группе могут быть замещены посредством 1-10 оксогрупп, метиленовые группы в С1-40-алкиленовой группе могут быть замещены посредством 1-10 галогенов, смежные метиленовые группы могут быть связаны друг с другом посредством 1-10 ненасыщенных связей, и из числа метиленовых групп в алкиленовой группе, 1-20 метиленовых групп могут быть заменены на NH, N(C1-10-алкил), O, S, C6-14-арилен, 5-10-членный гетероарилен, или полиоксиалкилен, имеющий степень полимеризации 50-500. Линкер может иметь, например, следующую структуру,
[Хим. стр. 33]

где, w имеет значение 1-2000, и Z представляет собой С1-5-алкиленовую группу.
Кроме того, линкер может иметь, например, следующую структуру.
[Хим. стр. 34]

где, w имеет значение 1-2000, и Z представляет собой С1-5-алкиленовую группу.
[0059]
В одном варианте осуществления настоящего изобретения, производное BPA по настоящему изобретению представляет собой соединение, представленное формулой (IX), приведенной ниже, или его фармацевтически приемлемую соль.
[Хим. стр. 35]
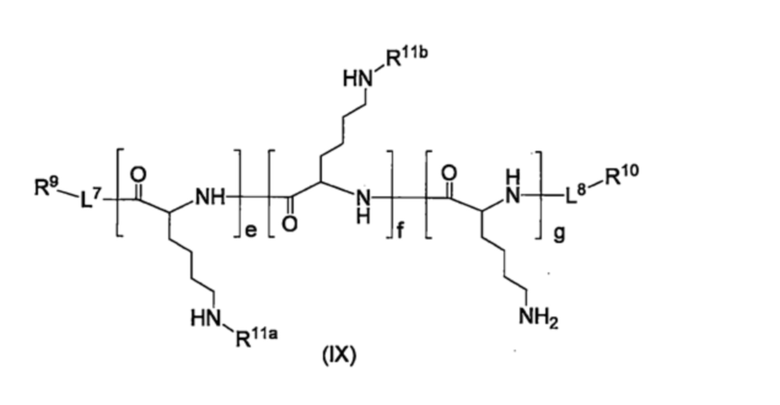
где,
L7 и L8, каждый независимо, представляют собой линкер или отсутствуют,
R9 и R10, каждый независимо, представляют собой водород, гидроксильную группу, карбоксильную группу, аминогруппу, С1-10-алкильную группу, которая может быть замещена галогеном, С1-10-алкоксигруппу, которая может быть замещена галогеном, тиольную группу, цианогруппу, азидогруппу, -CH(OA1)2, или детектируемую метку,
А1 представляет собой С1-6-алкильную группу,
R11a представлено формулой (X-a), приведенной ниже,
[Хим. стр. 36]

где, стрелка показывает связь с NH,
R11b, каждый независимо, представляют собой группу, представленную формулой (X-b), приведенной ниже,
[Хим. стр. 37]
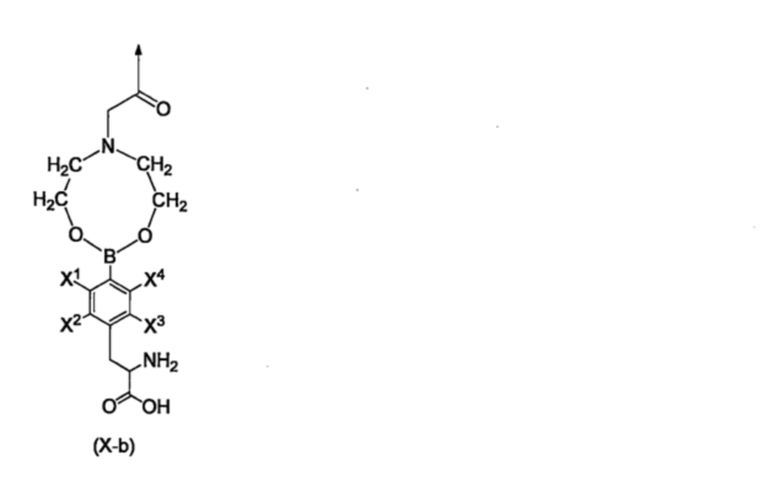
где,
стрелка показывает связь с NH,
X1-X4, каждый независимо, представляют собой Н, 18F или 19F,
Y+ представляет собой H+, ион щелочного металла, или ион тетра-С1-6-алкил-аммония (например, тетраметиламмония, тетраэтиламмония, тетра-n-пропиламмония, тетра-n-бутиламмония, тетра-n-пентиламмония, тетра-n-гексиламмония),
e=от 0 до 299,
f=от 1 до 300,
g=от 0 до 299,
e+f+g=от 10 до 300, и
порядок следования повторяющихся звеньев является произвольным (то есть, сополимер может представлять собой статистический сополимер или блок-сополимер).
[0060]
В данном документе, «R11b, каждый независимо,» означает, что, когда имеется множество повторяющихся звеньев, также имеется множество R11b, которые находятся в повторяющихся звеньях, но эти R11b могут совпадать или отличаться друг от друга.
[0061]
e, f и g представляют собой степень полимеризации. Нижний предел для e составляет 0, но предпочтительно имеет значение 0, 1, 2, 3, 4, 5, 6, 7, 8, или 9. Верхний предел для e составляет 299, но предпочтительно имеет значение 299, 290, 280, 270, 260, или 250. Нижний предел для f составляет 1, но предпочтительно имеет значение 1, 2, 3, 4, 5, 6, 7, 8, или 9. Верхний предел для f составляет 300, но предпочтительно имеет значение 300, 290, 280, 270, 260, или 250. Нижний предел для g составляет 0, но предпочтительно имеет значение 0, 1, 2, 3, 4, 5, 6, 7, 8, или 9. Верхний предел для g составляет 299, но предпочтительно имеет значение 299, 290, 280, 270, 260, или 250. Нижний предел для (e+f+g) составляет 10, но предпочтительно имеет значение 10, 20 или 30. Верхний предел для (e+f+g) составляет 300, но предпочтительно имеет значение 300, 290, 280, 270, 260, или 250. e, f и g могут быть вычислены в результате проведения количественной оценки в расчете на интегрированное значение по спектру 1Н-ЯМР.
[0062]
L7 и/или L8, в том случае, когда они являются линкерами, особым образом не ограничиваются, но могут представлять собой, например, С1-40-алкиленовую группу. В данном документе, метильные группы в С1-40-алкиленовой группе могут быть замещены посредством 1-10 оксогрупп, метиленовые группы в С1-40-алкиленовой группе могут быть замещены посредством 1-10 галогенов, смежные метиленовые группы могут быть связаны друг с другом посредством 1-10 ненасыщенных связей, и из числа метиленовых групп в алкиленовой группе, 1-20 метиленовых групп могут быть заменены на NH, N(C1-10-алкил), O, S, C6-14-арилен, 5-10-членный гетероарилен, или полиоксиалкилен, имеющий степень полимеризации 2-2000, 2-1000, 2-500, 2-400, 2-300, 2-200, 2-100, 2-50, или 2-10. Линкер может иметь, например, следующую структуру.
[Хим. стр. 38]

где, w имеет значение 1-2000, и Z представляет собой С1-5-алкиленовую группу.
Кроме того, линкер может иметь, например, следующую структуру,
[Хим. стр. 39]

где, w имеет значение 1-2000, и Z представляет собой С1-5-алкиленовую группу.
[0063]
В одном варианте осуществления настоящего изобретения, производное BPA по настоящему изобретению представляет собой соединение, представленное формулой (XI), приведенной ниже, или его фармацевтически приемлемую соль,
[Хим. стр. 40]
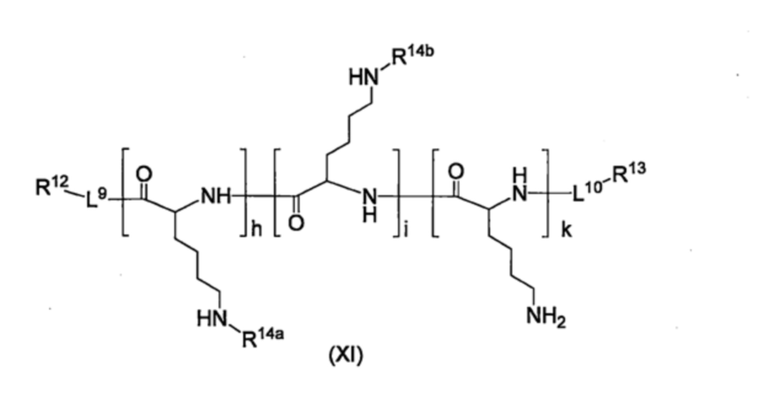
где,
L9 и L10, каждый независимо, представляют собой линкер или отсутствуют,
R12 и R13, каждый независимо, представляют собой водород, гидроксильную группу, карбоксильную группу, аминогруппу, С1-10-алкильную группу, которая может быть замещена галогеном, С1-10-алкоксигруппу, которая может быть замещена галогеном, тиольную группу, цианогруппу, азидогруппу, -CH(OA1)2, или детектируемую метку,
А1 представляет собой С1-6-алкильную группу,
R14a представлено формулой (XII-a), приведенной ниже,
[Хим. стр. 41]

где, стрелка показывает связь с NH,
R14b, каждый независимо, представлен формулой (XII-b), приведенной ниже,
[Хим. стр. 42]
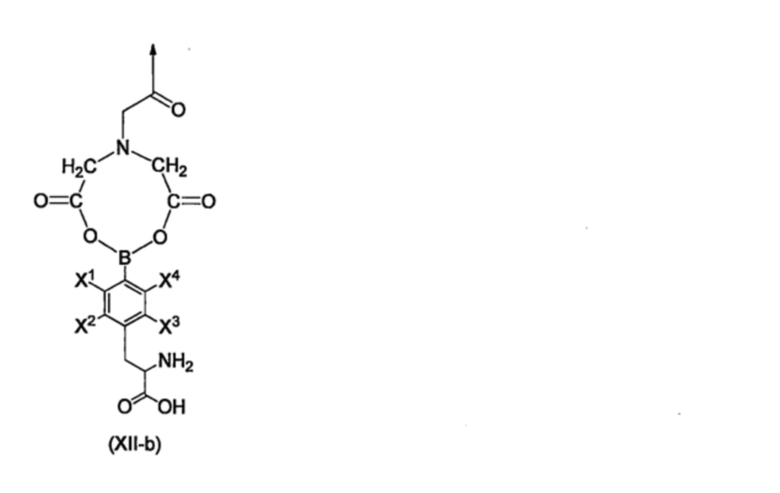
где,
стрелка показывает связь с NH,
X1-X4, каждый независимо, представляют собой Н, 18F или 19F,
Y+ представляет собой H+, ион щелочного металла, или ион тетра-С1-6-алкил-аммония (например, тетраметиламмония, тетраэтиламмония, тетра-n-пропиламмония, тетра-n-бутиламмония, тетра-n-пентиламмония, тетра-n-гексиламмония),
h=от 0 до 299,
i=от 1 до 300,
k=от 0 до 299,
h+i+k=от 10 до 300, и
порядок следования повторяющихся звеньев является произвольным (то есть, сополимер может представлять собой статистический сополимер или блок-сополимер).
[0064]
В данном документе, «R14b, каждый независимо,» означает, что, когда имеется множество повторяющихся звеньев, также имеется множество R14b, которые находятся в повторяющихся звеньях, но эти R14b могут совпадать или отличаться друг от друга.
[0065]
h, i и k представляют собой степень полимеризации. Нижний предел для h составляет 0, но предпочтительно имеет значение 0, 1, 2, 3, 4, 5, 6, 7, 8, или 9. Верхний предел для h составляет 299, но предпочтительно имеет значение 299, 290, 280, 270, 260, или 250. Нижний предел для i составляет 1, но предпочтительно имеет значение 1, 2, 3, 4, 5, 6, 7, 8, или 9. Верхний предел для i составляет 300, но предпочтительно имеет значение 300, 290, 280, 270, 260, или 250. Нижний предел для k составляет 0, но предпочтительно имеет значение 0, 1, 2, 3, 4, 5, 6, 7, 8, или 9. Верхний предел для k составляет 299, но предпочтительно имеет значение 299, 290, 280, 270, 260, или 250. Нижний предел для (h+i+k) составляет 10, но предпочтительно имеет значение 10, 20 или 30. Верхний предел для (h+i+k) составляет 300, но предпочтительно имеет значение 300, 290, 280, 270, 260, или 250. h, i и k могут быть вычислены в результате проведения количественной оценки в расчете на интегрированное значение по спектру 1Н-ЯМР.
[0066]
L9 и/или L10, в том случае, когда они являются линкерами, особым образом не ограничиваются, но могут представлять собой, например, С1-40-алкиленовую группу. В данном документе, метильные группы в С1-40-алкиленовой группе могут быть замещены посредством 1-10 оксогрупп, метиленовые группы в С1-40-алкиленовой группе могут быть замещены посредством 1-10 галогенов, смежные метиленовые группы могут быть связаны друг с другом посредством 1-10 ненасыщенных связей, и из числа метиленовых групп в алкиленовой группе, 1-20 метиленовых групп могут быть заменены на NH, N(C1-10-алкил), O, S, C6-14-арилен, 5-10-членный гетероарилен, или полиоксиалкилен, имеющий степень полимеризации 2-2000, 2-1000, 2-500, 2-400, 2-300, 2-200, 2-100, 2-50, или 2-10. Линкер может иметь, например, следующую структуру.
[Хим. стр. 43]

где, w имеет значение 1-2000, и Z представляет собой С1-5-алкиленовую группу.
Кроме того, линкер может иметь, например, следующую структуру,
[Хим. стр. 44]

где, w имеет значение 1-2000, и Z представляет собой С1-5-алкиленовую группу.
[0067]
В одном варианте осуществления настоящего изобретения, производное BPA по настоящему изобретению представляет собой соединение, представленное формулой (XX), приведенной ниже, или его фармацевтически приемлемую соль,
[Хим. стр. 45]
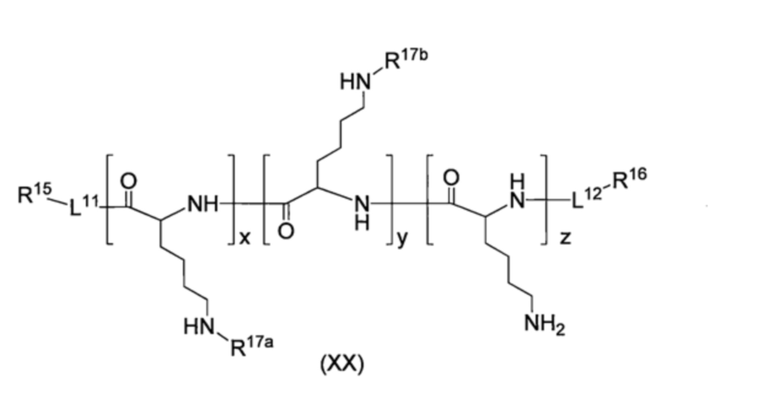
где,
L11 и L12, каждый независимо, представляют собой линкер или отсутствуют,
R15 и R16, каждый независимо, представляют собой водород, гидроксильную группу, карбоксильную группу, аминогруппу, С1-10-алкильную группу, которая может быть замещена галогеном, С1-10-алкоксигруппу, которая может быть замещена галогеном, тиольную группу, цианогруппу, азидогруппу, -CH(OA1)2, или детектируемую метку,
А1 представляет собой С1-6-алкильную группу,
R17a означает группу, представленную формулой (XXI-a), приведенной ниже,
[Хим. стр. 46]

где, стрелка показывает связь с NH,
R17b, каждый независимо, представляет собой группу, выбранную из группы, состоящей из групп, представленных формулами (XXI-b)-(XXI-h), приведенными ниже,
[Хим. стр. 47]
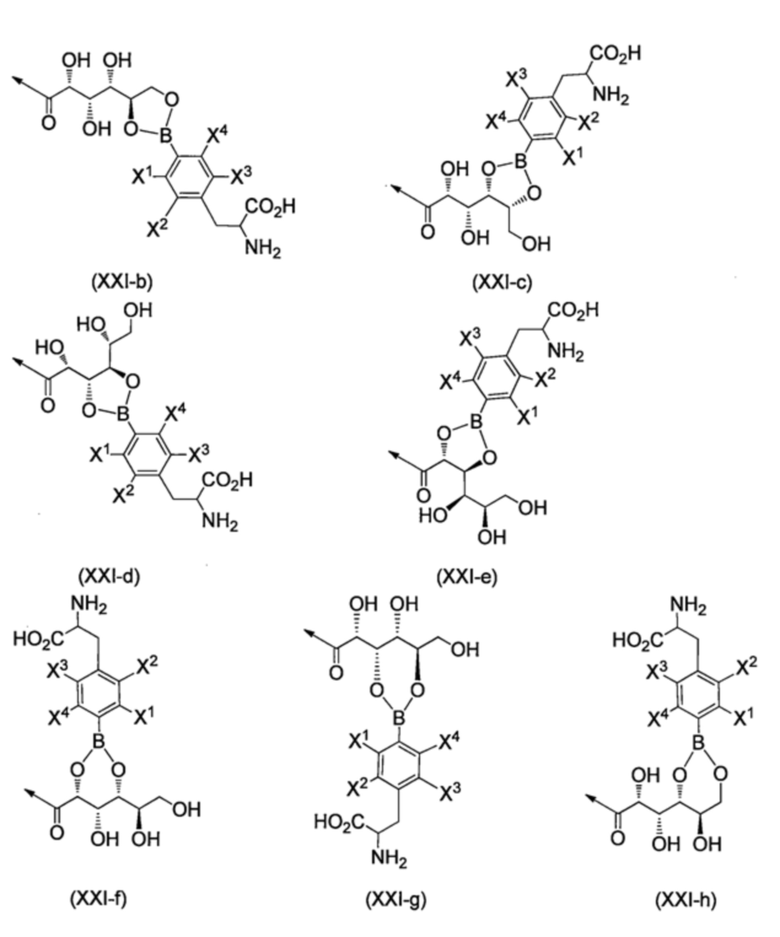
где,
стрелки показывают связь с NH,
X1-X4, каждый независимо, представляют собой Н, 18F или 19F,
x=от 0 до 299,
y=от 1 до 300,
z=от 0 до 299,
x+y+z=от 10 до 300, и
порядок следования повторяющихся звеньев является произвольным (то есть, сополимер может представлять собой статистический сополимер или блок-сополимер).
[0068]
В данном документе, «R17b, каждый независимо,» означает, что, когда имеется множество повторяющихся звеньев, также имеется множество R17b, которые находятся в повторяющихся звеньях, но эти R17b могут совпадать или отличаться друг от друга.
[0069]
x, y и z представляют собой степень полимеризации. Нижний предел для x составляет 0, но предпочтительно имеет значение 0, 1, 2, 3, 4, 5, 6, 7, 8, или 9. Верхний предел для x составляет 299, но предпочтительно имеет значение 299, 290, 280, 270, 260, или 250. Нижний предел для y составляет 1, но предпочтительно имеет значение 1, 2, 3, 4, 5, 6, 7, 8, или 9. Верхний предел для y составляет 300, но предпочтительно имеет значение 300, 290, 280, 270, 260, или 250. Нижний предел для z составляет 0, но предпочтительно имеет значение 0, 1, 2, 3, 4, 5, 6, 7, 8, или 9. Верхний предел для z составляет 299, но предпочтительно имеет значение 299, 290, 280, 270, 260, или 250. Нижний предел для (x+y+z) составляет 10, но предпочтительно имеет значение 10, 20 или 30. Верхний предел для (x+y+z) составляет 300, но предпочтительно имеет значение 300, 290, 280, 270, 260, или 250. x, y и z могут быть вычислены в результате проведения количественной оценки в расчете на интегрированное значение по спектру 1Н-ЯМР.
[0070]
L11 и/или L12, в том случае, когда они являются линкерами, особым образом не ограничиваются, но могут представлять собой, например, С1-40-алкиленовую группу. В данном документе, метильные группы в С1-40-алкиленовой группе могут быть замещены посредством 1-10 оксогрупп, метиленовые группы в С1-40-алкиленовой группе могут быть замещены посредством 1-10 галогенов, смежные метиленовые группы могут быть связаны друг с другом посредством 1-10 ненасыщенных связей, и из числа метиленовых групп в алкиленовой группе, 1-20 метиленовых групп могут быть заменены на NH, N(C1-10-алкил), O, S, C6-14-арилен, 5-10-членный гетероарилен, или полиоксиалкилен, имеющий степень полимеризации 2-1000, 2-500, 2-400, 2-300, 2-200, 2-100, 2-50, или 2-10. Линкер может иметь, например, следующую структуру.
[Хим. стр. 48]

где, w имеет значение 1-2000, и Z представляет собой С1-5-алкиленовую группу.
[0071]
В одном варианте осуществления настоящего изобретения, производное BPA по настоящему изобретению представляет собой соединение, представленное формулой (XXII), приведенной ниже, или его фармацевтически приемлемую соль,
[Хим. стр. 49]
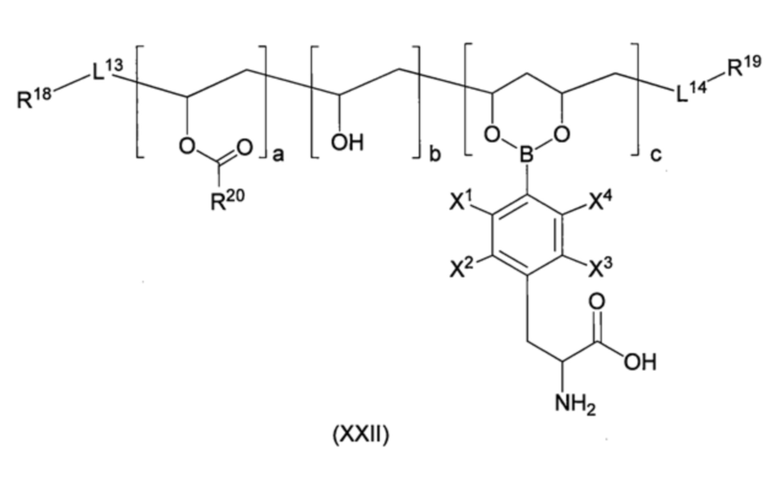
где,
X1-X4, каждый независимо, представляют собой Н, 18F или 19F,
L13 и L14, каждый независимо, представляют собой линкер или отсутствуют,
R18 и R19, каждый независимо, представляют собой водород, гидроксильную группу, карбоксильную группу, аминогруппу, С1-10-алкильную группу, которая может быть замещена галогеном, С1-10-алкоксигруппу, которая может быть замещена галогеном, тиольную группу, цианогруппу, азидогруппу, -CH(OA1)2, или детектируемую метку,
А1 представляет собой С1-6-алкильную группу,
R20, каждый независимо, представляют собой С1-10-алкильную группу, которая может быть замещена галогеном, -NR21R22-группу, или следующую группу,
[Хим. стр. 50]
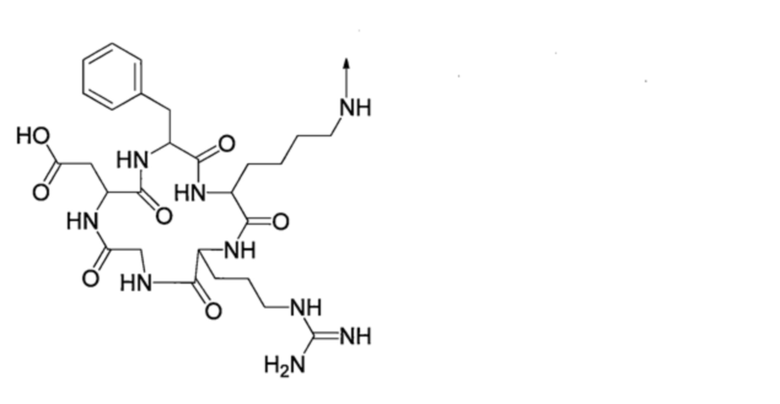
где, стрелка показывает связь с карбонильным углеродом,
R21 и R22 представляют собой, каждый независимо, водород или С1-10-алкильную группу, которая может быть замещена галогеном,
а=от 1 до 3998,
b=от 0 до 3997,
с=от 1 до 2000,
a+b+2c=от 10 до 4000, и
порядок следования повторяющихся звеньев является произвольным.
[0072]
a, b и c представляют собой степень полимеризации. Нижний предел для a составляет 1, но предпочтительно имеет значение 1, 2, 3, 4, 5, 6, 7, 8, или 9. Верхний предел для a составляет 3998, но предпочтительно имеет значение 3998, 3500, 3000, 2500, 2000, 1500, 1000, 900, 800, 700, 600, 500, 400, 300, 200, 100, 50, 40, 30, 20, или 10. Нижний предел для b составляет 0, но предпочтительно имеет значение 0, 1, 2, 3, 4, 5, 6, 7, 8, или 9. Верхний предел для b составляет 3997, но предпочтительно имеет значение 3997, 3500, 3000, 2500, 2000, 1500, 1000, 900, 800, 700, 600, 500, 400, 300, 200, 100, 50, 40, 30, 20, или 10. Нижний предел для c составляет 1, но предпочтительно имеет значение 1, 2, 3, 4, 5, 6, 7, 8, 9, или 10. Верхний предел для с составляет 2000, но предпочтительно имеет значение 2000, 1990, 1980, 1970, 1960, 1950, 1900, 1800, 1700, 1600, 1500, 1400, 1300, 1200, 1100, или 500. Нижний предел для (a+b+2c) составляет 10, но предпочтительно имеет значение 10, 20, 30, 40, или 50. Верхний предел для (a+b+2c) составляет 4000, но предпочтительно имеет значение 4000, 3500, 3000, 2500, 2000, 1500, 1000, 900, 800, 700, 600, 500, 400, 300, или 200. a, b, и c могут быть вычислены в результате проведения количественной оценки в расчете на интегрированное значение по спектру 1Н-ЯМР.
[0073]
L13 и/или L14, в том случае, когда они являются линкерами, особым образом не ограничиваются, но могут представлять собой, например, С1-40-алкиленовую группу. В данном документе, метильные группы в С1-40-алкиленовой группе могут быть замещены посредством 1-10 оксогрупп, метиленовые группы в С1-40-алкиленовой группе могут быть замещены посредством 1-10 галогенов, смежные метиленовые группы могут быть связаны друг с другом посредством 1-10 ненасыщенных связей, и из числа метиленовых групп в алкиленовой группе, 1-20 метиленовых групп могут быть заменены на NH, N(C1-10-алкил), O, S, C6-14-арилен, 5-10-членный гетероарилен, или полиоксиалкилен, имеющий степень полимеризации 2-2000, 2-1000, 2-500, 2-400, 2-300, 2-200, 2-100, 2-50, или 2-10. Линкер может иметь, например, следующую структуру,
[Хим. стр. 51]

где, w имеет значение 1-2000, и Z представляет собой С1-5-алкиленовую группу.
[0074]
Производное BPA по настоящему изобретению может быть получено в результате введения группы, представленной формулой (I), в полимер с применением любого из различных общеизвестных способов. Например, соединение, представленное формулой (VII), приведенной ниже,
[Хим. стр. 52]

где,
X1-X4 представляют собой, каждый независимо, Н, 18F или 19F, и
полимер, который, при реагировании с соединением, представленным формулой (VII), может образовывать группу, представленную формулой (I), приведенной ниже
[Хим. стр. 53]

где,
стрелки показывают связь со смежным атомом, и
X1-X4 представляют собой, каждый независимо, Н, 18F или 19F,
смешивают в воде или в содержащем воду растворителе (например, забуференном фосфатом физиологическом растворе) и подвергают реакции, например, при 4-100°С в течение 10 минут - 1 часа с получением производного BPA.
[0075]
<<КОМПОЗИЦИЯ>>
Композиция по настоящему изобретению содержит производное BPA по настоящему изобретению. Композиция по настоящему изобретению может дополнительно содержать фармацевтически приемлемые носители, разбавители, буферные растворы, эксципиенты и их комбинации. Композиция по настоящему изобретению может быть использована в лечении, диагностировании и детектировании опухолей. В том случае, когда композицию по настоящему изобретению вводят субъекту, путь введения особым образом не ограничивается, но может включать внутривенное, подкожное, внутримышечное, внутрисуставное, интраперитонеальное и внутриглазное введение. Кроме того, дозировку выбирают надлежащим образом в зависимости от типа заболевания и возраста, веса, и пола субъекта.
[0076]
<<НАБОР>>
Набор по настоящему изобретению содержит соединение, представленное формулой (VII), приведенной ниже,
[Хим. стр. 54]

где,
X1-X4 представляют собой, каждый независимо, Н, 18F или 19F, и
полимер, который, при реагировании с соединением, представленным формулой (VII), может образовывать группу, представленную формулой (I), приведенной ниже
[Хим. стр. 55]

где,
стрелки показывают связь со смежным атомом, и
X1-X4 представляют собой, каждый независимо, Н, 18F или 19F.
[0077]
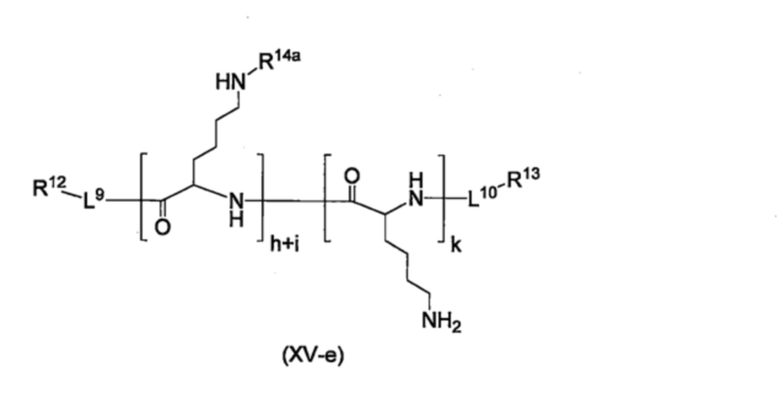
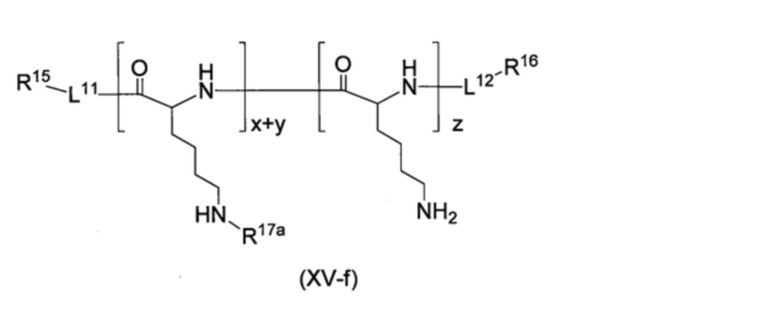
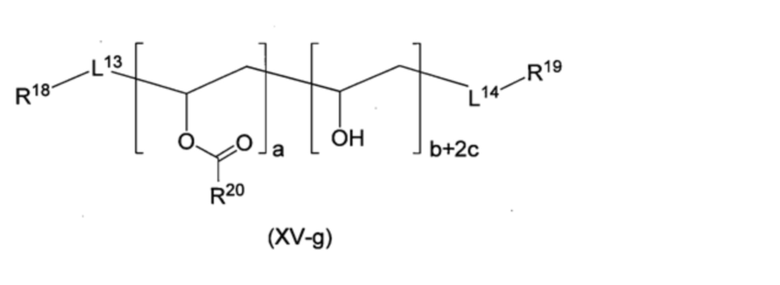
Полимер, который может образовывать группу, представленную формулой (I), в результате реакции с соединением, представленным формулой (VII), может быть линейным или разветвленным и может представлять собой гомополимер или сополимер. В случае сополимеров, сополимер может быть статистическим сополимером или блок-сополимером. Полимер предпочтительно представляет собой водорастворимый полимер. Полимер может включать, например, поливиниловый спирт, полиуретан, сложный полиэфир, полиамид, поликарбонат, полиимид, простой полиэфир, полиакрилат, полиакриламид, полисилоксан, поливинил, полипептид, полисахарид, полинуклеотид, и их сополимеры. Предпочтительно, полимер включает поливиниловый спирт, сложный полиэфир, простой полиэфир, полиакрилат, полиакриламид, полипептид, полисахарид, или их сополимеры, и более предпочтительно, полимер включает поливиниловый спирт или полипептид. Полимер, который может образовывать группу, представленную формулой (I), в результате реакции с соединением, представленным формулой (VII), может иметь фрагмент, который образует группу, представленную формулой (I), при реагировании с соединением, представленным формулой (VII), связанный с боковой цепью. Этот фрагмент может образовывать линкер между полимером и группой, представленной формулой (I).
[0078]
Полимер, который может образовывать группу, представленную формулой (I), в результате реакции с соединением, представленным формулой (VII), может быть представлен формулами (XV-a)-(XV-g), приведенными ниже. Определение символов в формулах и их диапазоны являются такими, как описано выше.
[Хим. стр. 56]
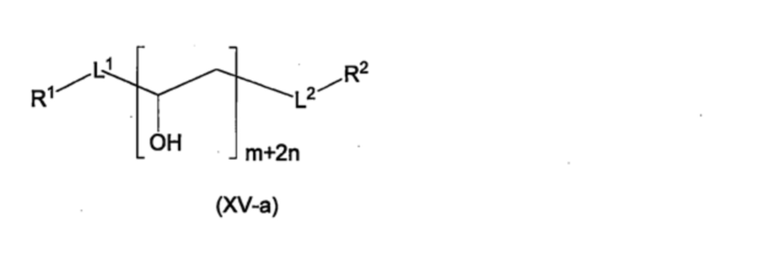
[Хим. стр. 57]
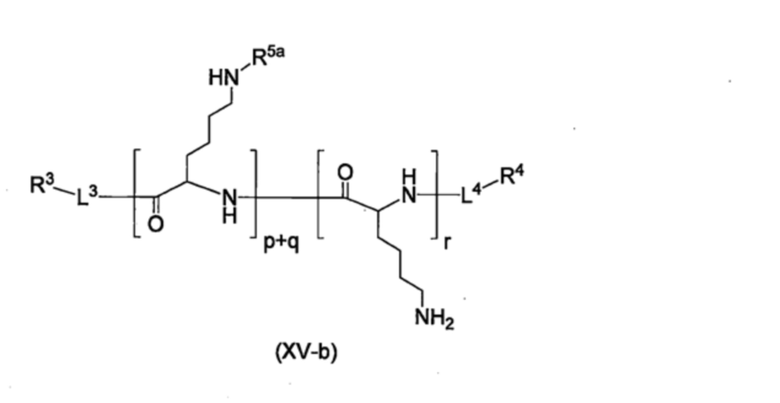
[Хим. стр. 58]

[Хим. стр. 59]
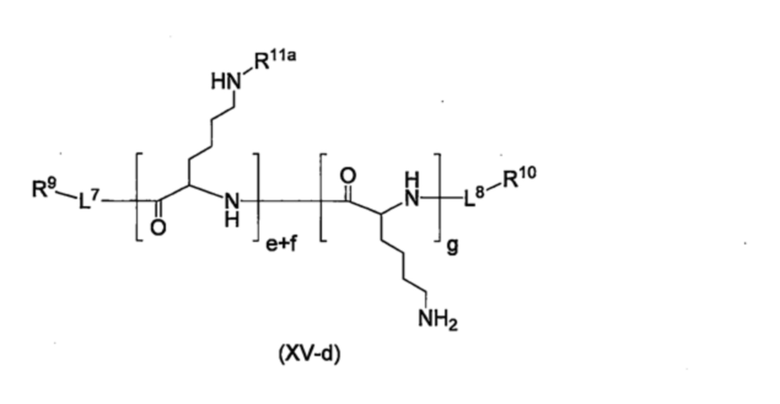
[Хим. стр. 60]
[Хим. стр. 61]
[Хим. стр. 62]
[0079]
Набор по настоящему изобретению может включать инструкции в отношении способа получения производного BPA по настоящему изобретению. Набор также может включать инструкции в отношении способа применения производного BPA по настоящему изобретению в лечении, диагностировании, и детектировании опухолей.
[0080]
Все документы, упомянутые в этом описании, включены в данный документ посредством ссылки в полном их объеме.
[0081]
Варианты осуществления настоящего изобретения, описанные ниже, предоставляются лишь с иллюстративными целями и не ограничивают технический объем настоящего изобретения. Технический объем настоящего изобретения ограничивается только пунктами Формулы изобретения. Модификации настоящего изобретения, например, добавление, исключение и замена составляющих признаков настоящего изобретения, могут быть сделаны при условии, что при этом не возникнет никакого отклонения от сущности настоящего изобретения.
ПРИМЕРЫ
[0082]
ПРИМЕР 1
Синтез Поливинилового Спирта (PVA)
<Реагенты>
Если не задано иное, то коммерчески доступные реагенты и растворители используются так, как они есть.
Винилацетат: используют товарный продукт (), подвергнутый перегонке в атмосфере аргона.
Цианометил-метил(фенил)карбамодитиоат: Sigma Aldrich
α,α’-азобисизобутиронитрил (AIBN): Sigma Aldrich
Метанол (MeOH) (особая степень чистоты): Nacalai Tesque
Соляная кислота 5 моль/л (для масс-спектрометрии): Wako Pure Chemical Industries, Ltd.
Гидроксид натрия 5 моль/л (для масс-спектрометрии): Wako Pure Chemical Industries, Ltd.
Бензол (особая степень чистоты): Wako Pure Chemical Industries, Ltd.
Тетрагидрофуран (THF): Wako Pure Chemical Industries, Ltd.
Дигидрофосфат натрия (NaH2PO3): Wako Pure Chemical Industries, Ltd.
Гидрофосфат динатрия: Nacalai Tesque
<Оборудование>
NMR (Ядерный Магнитный Резонанс=ЯМР): BRUKER AVANCE III 400 (400 МГц, BRUKER BioSpin)
GPC (Гельпроникающая хроматография): JASCO Corporation
Колонка для измерения PVAc: колонка TSK-gel superAW3000, superAW4000, и superAWL-guard (Tosoh Corporation)
Колонка для измерения PVA: Superdex 200 Increase 10/300 GL (GE Healthcare)
Детектор: RI-2031
[0083]
(1) Синтез поли(винилацетата) (PVAc)
[Хим. стр. 63]
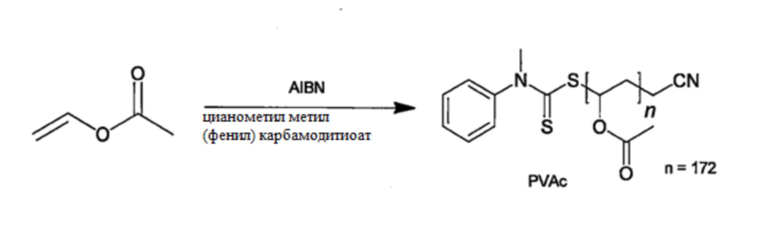
2,86 мг (0,0174 ммоль) инициатора AIBN и 38,68 мг (0,174 ммоль) агента RAFT (обратимой передачи цепи по механизму присоединение-фрагментация) цианометил-метил(фенил)-карбамодитиоата взвешивают и добавляют в двугорлую грушевидную колбу объемом 100 мл в атмосфере аргона в ледяной бане. После этого, 3,22 мл (34,8 ммоль) винилацетата добавляют в систему в атмосфере аргона, и проводят дегазирование по схеме замораживание-откачивание-оттаивание 4 раза. Систему заполняют аргоном и перемешивают при 60°С в течение 24 часов. После этого, реакционный раствор помещают в диализную мембрану (MWCO (показатель пористости ультрамембран) = 3,5 кД), диализируют 3 раза в течение 12 часов против 300 мл раствора THF и затем лиофилизируют из раствора бензола. Целевой PVAc получают в виде твердого вещества светло-желтого цвета с выходом 2,97 г. Получающийся в результате PVAc анализируют методами 1Н-NMR и GPC.
[0084]
На основе данных 1Н-NMR, вычисляют, что степень полимеризации PVAc составляет 172 и Mn=14800. Конкретно, с использованием полученного от агента RAFT сигнала ароматического кольца (7,56-7,28 ppm (м.д.), (шир., Ar-H)) в качестве эталона (5Н), среднечисловую молекулярную массу вычисляют на основе полученного от каркаса основной цепи сигнала (1,84-1,66 ppm (шир., -СН2)) и полученного от сложноэфирной группы сигнала (2,04-1,85 ppm (шир., О-СО-СН3)). Кривая GPC является унимодальной, молекулярно-массовое распределение Mw/Mn=1,31 является узким, и молекулярную массу вычисляют как Mn=12800. Поскольку молекулярная масса, определяемая методом GPC, является относительной молекулярной массой, рассчитанной относительно стандартного полиэтиленгликоля, в дальнейшем в данном документе, Mn будет означать молекулярную массу, которая получена методом 1Н-NMR.
[Хим. стр. 64]
1Н-NMR (400 МГц, DMSO-d6): δ 7,56-7,28 (шир., -Ar-H), 4,90-4,68 (шир., -СНСН2-), 2,04-1,85 (шир., -ОСОСН3), 1,84-1,66 (шир., -СНСН2-)
[0085]
(2) Синтез Поливинилового Спирта (PVA)
[Хим. стр. 65]
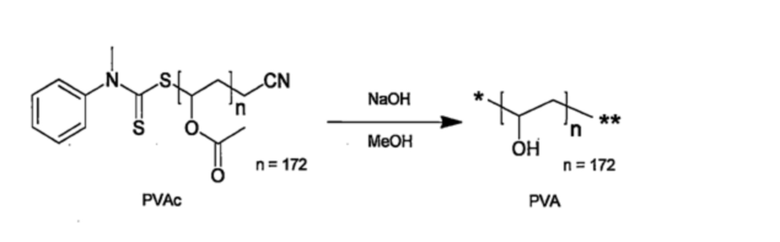
1,00 г (0,062 ммоль) PVAc, полученного в приведенном выше пункте (1), взвешивают и растворяют в 30 мл MeOH в грушевидной колбе объемом 300 мл. 2,32 г (57,94 ммоль) гидроксида натрия (5 эквивалентов) добавляют к сложному эфиру PVAc, к этому дополнительно добавляют чистую воду, затем смесь перемешивают при 60°С в течение 24 часов. Реакционный раствор помещают в диализную мембрану (MWCO=3,5 кД) и диализируют 3 раза против 2 л чистой воды. Получающийся в результате полимерный раствор фильтруют через фильтр с размером ячеек 0,45 мкм и затем лиофилизируют. Целевой PVA получают в виде твердого вещества светло-желтого цвета с выходом 240 мг. Полученный PVA анализируют методами 1Н-NMR и GPC. На основе данных 1Н-NMR, определяют, что степень омыления составляет 99% по моль. Кроме того, подтверждают, что кривая GPC для полученного PVA является унимодальной. Следует отметить, что «*» и «**» в вышеприведенных химических формулах означают неустановленные структуры.
[Хим. стр. 66]
1Н-NMR (400 МГц, DMSO-d6): δ 4,76-4,18 (шир., -ОH), 4,08-3,75 (шир., -СНСН2-), 1,78-1,08 (шир., -СНСН2-)
[0086]
ПРИМЕР 2
Оценивание связывания производного BPA (PVA-BPA), в котором BPA связан с PVA
<Реагенты>
Если не задано иное, то коммерчески доступные реагенты и растворители используются так, как они есть.
Соляная кислота 5 моль/л (для масс-спектрометрии): Wako Pure Chemical Industries, Ltd.
Гидроксид натрия 5 моль/л (для масс-спектрометрии): Wako Pure Chemical Industries, Ltd.
Дигидрофосфат натрия (NaH2PO3): Wako Pure Chemical Industries, Ltd.
4-Бороно-L-фенилаланин (BPA) (бор в этом реагенте представляет собой 10B): Katchem
4-Бороно-L-фенилаланин (11B-BPA) (бор в этом реагенте имеет смешанную форму: 11B-BPA и 10B-BPA): Sigma-Aldrich
Ализариновый красный С (ARS): Wako Pure Chemical Industries, Ltd.
Гидрофосфат динатрия: Nacalai Tesque
D-фруктоза (также называемая «Fru» ниже по тексту): Wako Pure Chemical Industries, Ltd.
Следует отметить, что производное BPA, полученное проведением реакции между Fru и BPA, также называется «Fru-BPA» ниже по тексту.
<Оборудование>
NMR (Ядерный Магнитный Резонанс=ЯМР): BRUKER AVANCE III HD500 (500 МГц, BRUKER BioSpin)
Флуоресцентный спектрофотометр (FP8300): JASCO Corporation
[0087]
Раствор 11В-BPA, раствор Fru-11B-BPA и раствор PVA-11B-BPA приготавливают в следующих концентрациях с использованием 10 мМ PBS (140 мМ NaCl, рН 9,5).
Раствор 11В-BPA: концентрация 11В-BPA 191,3 мМ=40 мг/мл
Раствор Fru-11B-BPA: концентрация 11В-BPA 191,3 мМ=40 мг/мл, концентрация фруктозы 103,2 мг/мл
Раствор PVA-11B-BPA: концентрация 11В-BPA 191,3 мМ=40 мг/мл, концентрация диола в PVA 573,9 мМ=50,4 мг/мл
[0088]
450 мкл каждого образца и 50 мкл D2O смешивают, и 11В-ЯМР измеряют. Результат 11В-ЯМР-спектроскопии проиллюстрирован на ФИГ. 1. Пик с самой высокой интенсивностью сигнала соответствует раствору BPA (шир., 2,1 ppm до 10,0 ppm). Пики для раствора PVA-BPA и раствора Fru-BPA отчетливо отличаются от сигнала раствора BPA, и, кроме того, так как интенсивность сигнала BPA самого по себе снижается, качественно определено, что PVA и BPA связываются.
[0089]
В вышеупомянутом растворе 11В-BPA, вычислено, с учетом константы равновесия (рН 7,4), что (свободный BPA):(BPA, связанный с PVA) = 10:90-0:100 (молярное соотношение). Следует отметить, что поскольку рН для раствора PVA-11B-BPA имеет значение 9,5, и чем выше рН, тем выше константа равновесия, предполагается, что почти 100% BPA является связанным с PVA в растворе.
[0090]
Константу равновесия для PVA и BPA вычисляют с использованием способа ARS в соответствии со способом, описанным в публикации Springsteen G., Wang B. H. Tetrahedron 58, 5291-5300 (2002). Первоначально, приготавливают каждый из следующих растворов A, B, C, и D.
Раствор A: ARS (9,0 × 10-6 M)
Раствор B: ARS (9,0 × 10-6 M) + BPA (2,0 × 10-3 M )
Раствор C: ARS (9,0 × 10-6 M) + BPA (2,0 × 10-3 M) + PVA (концентрация диола=5,0 × 10-1 M)
Раствор D: ARS (9,0 × 10-6 M) + BPA (2,0 × 10-3 M) + фруктоза (0,8 × 10-1 M)
Раствор E: ARS (9,0 × 10-6 M) + BPA (2,0 × 10-3 M) + глюкоза (0,8 × 10-1 M)
[0091]
Раствор А и Раствор В смешивают в различных соотношениях, и измеряют флуоресценцию с использованием одноразовой ячейки (PS, TGK) (Ex=468 нм, Em=572 нм). Константу равновесия К0 для ARS-BPA вычисляют на основе полученной интенсивности флуоресценции. Далее, Раствор В смешивают с Раствором C, D, или E, каждый из которых содержит диольное соединение, в различных соотношениях, и измеряют флуоресценцию с использованием одноразовой ячейки (Ex=468 нм, Em=572 нм). Кажущуюся константу относительного равновесия К1 для каждого соединения (эквивалент с концентрацией диола [2ОН])-BPA вычисляют с использованием этих результатов и вышеупомянутого значения К0. Результаты проиллюстрированы ниже в Таблице 1.
[Таблица 1]
Таблица 1
(диол)-BPA
(диол)-BPA
[0092]
В упомянутом растворе С, вычислено, на основе константы равновесия (рН 7,4), что (свободный BPA):(BPA, связанный с PVA) = приблизительно 50:50 (молярное соотношение).
[0093]
ПРИМЕР 3
Внутриклеточный захват PVA-BPA
<Реагенты>
Питательная среда, Онкологический институт Розуэлла Парка (RPMI): Sigma Aldrich
Фосфатно-солевой буфер D-PBS (-): Wako Pure Chemical Industries, Ltd.
Фетальная бычья сыворотка (FBS): Biosera
Раствор Трипсин-EDTA: Sigma life science
Пенициллин/ Стрептомицин: Sigma life science
Cy5-NHS: Thermo Fisher Scientific
Флуоресцентный краситель LysoTracker® Красный DND-99: Thermo Fisher Scientific
4-Диэтиламиносалицилальдегид: Tokyo Chemical Industry Co., Ltd.
Метиламин: Tokyo Chemical Industry Co., Ltd.
DMSO: Nacalai Tesque
2-Аминонорборнан-2-карбоновая кислота (BCH): Sigma-Aldrich
Hoechst® 33342: Thermo Fischer Scientific.
4-Бром-L-фенилаланин (BPA): Katchem
PVA, произведенный тем же способом, что и в ПРИМЕРЕ 1 (Mn=6500-9500)
Гидрофосфат динатрия: Nacalai Tesque
DAHMI: Полученный согласно способу, описанному в публикации Springsteen G., et al., Acs Sensors 1, 1394-1397 (2016).
Клеточное сито: клеточное сито Falcon с размером ячеек 35 мкм для пробирок на 5 мл
Клетки BxPC3 (клеточная линия рака поджелудочной железы человека): Американская коллекция типовых культур (Manassas, VA)
<Оборудование>
Проточный цитометр (FCM): Guava easy Cyte 6-2L (Merck Millipore)
Конфокальный лазерный сканирующий микроскоп (CLSM): LSM710 (Carl Zeiss)
Прибор для ICP-MS Agilent 7900 (Масс-спектрометрия с индуктивно связанной плазмой) (Agilent Technology Co., Ltd.)
ЯМР=NMR (Ядерный Магнитный Резонанс): BRUKER AVANCE III 400 (400 МГц, BRUKER BioSpin)
[0094]
(1) Синтез производного BPA (Cy5-PVA-BPA), в котором Cy5 связан с PVA-BPA
125 мг (1,67 × 10-2) PVA взвешивают в ампуле объемом 6 мл и растворяют в 2,5 мл DMSO. Далее, 1,23 мл (2,00 × 10-2 ммоль) Cy5-NHS (1,2 эквивалента) добавляют в раствор PVA, и эту смесь перемешивают при комнатной температуре в течение 3 часов. Реакционный раствор помещают в диализную мембрану (MWCO=3,5 кД) и диализируют 3 раза против 2 л чистой воды. Для полного удаления свободного Cy5 в диализном растворе, продукт очищают с использованием колонки PD-10 и затем лиофилизируют с получением продукта реакции PVA и Cy5-NHS (Cy5-PVA) в виде твердого вещества голубого цвета (выход 122 мг). Cy5-PVA-BPA получают смешением Cy5-PVA и BPA в 10 мМ PBS (140 мМ NaCl, рН 9,5), из условия, чтобы концентрация диола в PVA составляла 0,34 мМ, и концентрация BPA составляла 0,11 мМ. В полученном растворе, вычислено, на основе константы равновесия (рН 7,4), что (свободный BPA):(BPA, связанный с PVA) = приблизительно 60:40 (молярное соотношение)
[0095]
(2) Оценивание клеточного захвата Cy5-PVA-BPA с использованием конфокальной микроскопии
Клетки B×PC3 инокулируют в чашке со стеклянным дном (AGC Technoglass) в количестве 5 × 104 клеток/ чашку и подвергают предварительному выращиванию культуры в течение 24 часов. Раствор Cy5-PVA-BPA или раствор Fru-BPA (концентрация фруктозы=0,28 мМ, концентрация BPA=0,11 мМ), получение которого описано в вышеупомянутом пункте (1), приготавливают в смешанном растворе культуральной среды D-PBS/RPMI (содержащей 10% FBS, 1% Пенициллин-Стрептомицина) (PBS:RPMI=1:4), и 1 мл каждого из этих образцов добавляют в каждую лунку и инкубируют в течение 30 минут. После удаления культуральной среды, раствор ‘2 мМ DAHMI (соединения для флуоресцентного детектирования BPA)/10 мкл DMSO’ и раствор ‘50 нМ Lyso Tracker® красный DND-99/990 мкл PBS’ добавляют в каждую лунку и инкубируют в течение 30 минут. Клетки промывают три раза посредством 1 мл PBS, затем к тому добавляют 1 мл PBS, и затем клетки изучают с помощью CLSM. Результаты проиллюстрированы на ФИГ. 2. Подтверждено, что в том случае, когда Fru-BPA подвергается внутриклеточному захвату, BPA распределяется по всей цитоплазме. С другой стороны, ФИГ. 2 показывает, что Cy5-PVA и BPA колокализируются с лизосомами, что позволяет предположить, что Cy5-PVA-BPA включается в результате эндоцитоза.
[0096]
ПРИМЕР 4
Оценивание внутриклеточного захвата PVA-BPA и его опосредование посредством аминокислотного транспортера (LAT1)
Клетки B×PC3 инокулируют в чашке Петри в количестве 5 × 106 клеток/ лунку и подвергают предварительному выращиванию культуры в течении 24 часов. Далее, раствор культуральной среды D-PBS/ RPMI (10% FBS, 1% пенициллин-стрептомицина) (D-PBS: RPMI=1:4) используют в получении следующих образцов.
Раствор PVA-BPA (концентрация диола=3,03 мМ, концентрация BPA=3,03 мМ)
Раствор Fru-BPA (концентрация фруктозы=7,82 мМ, концентрация BPA=3,03 мМ)
Вышеупомянутый раствор PVA-BPA+BCH (ингибитор LAT1)(20 мМ)
Вышеупомянутый раствор Fru-BPA+BCH (20 мМ)
[0097]
В упомянутом растворе PVA-BPA, вычислено, на основе константы равновесия (pH 7,4), что (свободный BPA):(BPA, связанный с PVA) = приблизительно 30:70 (молярное соотношение).
[0098]
10 мл этих образцов добавляют в каждую чашку петри и инкубируют в течение 3 часов. Каждую лунку промывают посредством 10 мл D-PBS, затем к тому добавляют 1,0 мл трипсин-EDTA и затем проводят инкубирование в течение 10 минут. Следует отметить, что в отношении PVA-BPA и Fru-BPA, также приготавливают образцы, где, после промывания посредством D-PBS, добавляют свежую культуральную жидкость и проводят инкубирование в течение дополнительных 30 минут. После этого, проводят промывание посредством D-PBS, затем добавляют 1,0 мл раствора трипсин-EDTA и выполняют инкубирование в течение 10 минут. После подтверждения того, что клетки отсоединились (разъединились), с помощью оптического микроскопа, добавляют 9,0 мл культуральной среды RPMI, содержащей 10% FBS, и приготавливают клеточную суспензию. Проводят центрифугирование при 1500 rpm (оборотах в минуту) в течение 5 минут при 24°С и удаляют супернатант. Подсчитывают число клеток, затем раствор образца вливают в пробирку фирмы Falcon объемом 15 мл и добавляют 1 мл 70%-ной азотной кислоты. После этого, каждый образец инкубируют при 50°С в течение 15 минут, 70°С в течение 15 минут, и 90°С в течение 1 часа. Образцы разбавляют до 10 мл чистой водой, фильтруют через гидрофобный фильтр, затем оценивают с использованием ICP-MS. Результаты проиллюстрированы на ФИГ. 3-1 и 3-2.
[0099]
Как видно на ФИГ. 3-1, по сравнению с Fru-BPA, PVA-BPA демонстрирует приблизительно трехкратную концентрацию внутриклеточного бора. С другой стороны, в том случае, когда используют ингибитор LAT1 BCH(2-аминобицикло[2.2.1]гептан-2-карбоновую кислоту), внутриклеточный захват как Fru-BPA, так и PVA-BPA значительно снижается. Эти результаты позволяют предположить, что внутриклеточный захват PVA-BPA происходит через LAT1-опосредованный эндоцитоз. Кроме того, ФИГ. 3-2 показывает, что в результате проведения дополнительных 30 минут инкубирования, Fru-BPA значительно снижает концентрацию внутриклеточного бора. В противоположность тому, PVA-BPA демонстрирует чрезвычайно высокие концентрации бора даже после проведения дополнительного инкубирования.
[0100]
ПРИМЕР 5
Влияние BPA на внутриклеточный захват PVA
Клетки B×PC3 инокулируют на 12-луночный планшет в количестве 1 × 105 клеток/лунку и подвергают предварительному выращиванию культуры в течение 24 часов (n=3). Далее, используют раствор культуральной среды D-PBS/ RPMI (10 FBS, 1% пенициллин-стрептомицина) (D-PBS:RPMI=1:4) в приготовлении следующих образцов.
Раствор Cy5-PVA-BPA (концентрация диола в PVA=0,34 мМ, концентрация BPA=0,11 мМ)
Вышеупомянутый раствор Cy5-PVA-BPA+BCH (20,0 мМ)
[0101]
В упомянутом растворе Cy5-PVA-BPA, вычислено, на основе константы равновесия (pH 7,4), что (свободный BPA):(BPA, связанный с PVA) = приблизительно 60:40 (молярное соотношение).
[0102]
1 мл этих образцов добавляют в каждую лунку и инкубируют в течение 30 минут, 3 часов и 6 часов. Каждую лунку промывают посредством 1 мл PBS, затем к тому добавляют 0,5 мл раствора трипсин-EDTA и затем проводят инкубирование в течение 10 минут. После подтверждения с помощью оптического микроскопа того, что клетки отсоединились, добавляют 0,5 мл культуральной среды RPMI, содержащей 10% FBS, и приготавливают клеточную суспензию. Полученную клеточную суспензию фильтруют через клеточное сито, затем проводят количественную оценку интенсивности флуоресценции Cy5 клеток с использованием проточного цитометра. Результаты проиллюстрированы на ФИГ. 4-1 и 4-2.
[0103]
Cy5-PVA-BPA проявляет значительно более высокий внутриклеточный захват, чем Cy5-PVA (ФИГ. 4-1). В противоположность тому, такое различие в захвате исчезает в том случае, когда LAT1 ингибируют посредством BCH (ФИГ. 4-2). Сходно с ПРИМЕРОМ 4, эти результаты позволяют предположить, что внутриклеточный захват PVA-BPA происходит через LAT1-опосредованный эндоцитоз.
[0104]
ПРИМЕР 6
Влияние на модель подкожной опухоли
<Реагенты, клетки и животные>
PVA произведен тем же способом, что и в ПРИМЕРЕ 1 (Mn=6500-9500)
Соляная кислота 5 моль/л (для масс-спектрометрии): Wako Pure Chemical Industries, Ltd.
Гидроксид натрия 5 моль/л (для масс-спектрометрии): Wako Pure Chemical Industries, Ltd.
4-Бороно-L-фенилаланин (BPA): Katchem
Гидрофосфат динатрия: Nacalai Tesque
Lemosol: Wako Pure Chemical Industries, Ltd.
Drysol: Kanto Chemical Co., Inc.
Криостат: Leica CM 3050S, Leica Microsystems, Nussloch GmbH, Германия
Реактив O.C.T: Sakura Finetek Japan, Inc.
Hoechst® 33342: Thermo Fischer Scientific
Конъюгат: Лектин томатов, DyLight 488: Funakoshi
Клетки BxPC3 (клеточная линия рака поджелудочной железы человека): Американская коллекция типовых культур (Manassas, VA)
Клетки CT26 (клеточная линия рака толстой кишки мышей): Американская коллекция типовых культур (Manassas, VA)
Мышь BALB/c: Charles River Japan
‘Голая’ (бестимусная) мышь BALB/c: Charles River Japan
<Оборудование>
Прибор для ICP-MS Agilent 7900: Agilent Technology Co., Ltd.
Конфокальный лазерный сканирующий микроскоп (CLSM): LSM710 (Carl Zeiss)
Fuji Drychem NX500: Fujifilm Corporation
Установка нейтронного облучения с использованием тяжелой воды: KUR
флуоресцентный микроскоп 'все-в-одном' (BZ-X710): KEYENCE
[0105]
Модели подкожной опухоли получают подкожной инъекцией клеток CT26 мышам BALB/c в количестве 2,0 × 105 клеток/мышь и подкожной инъекцией клеток BxPC3 'голым' мышам BALB/c в количестве 5,0 × 106 клеток/мышь. Как только размер опухоли достигает примерно 200 мм3, 200 мкл следующих образцов медленно вводят через хвостовую вену (8 мг BPA/мышь).
PVA-BPA (концентрация BPA=191 мМ, концентрация диола в PVA=574 мМ) в PBS (pH 9,5)
Fru-BPA (концентрация BPA=191 мМ, концентрация фруктозы=574 мМ) в PBS (pH 9,5)
[0106]
По истечении заданного времени после введения образца, мышей препарируют, кровь собирают, и опухоли удаляют. Кровь и различные органы помещают в пробирку фирмы Falcon объемом 10 мл, и добавляют 1 мл 70%-ной азотной кислоты. После этого, каждый образец инкубируют при 50°С в течение 15 минут, 70°С в течение 15 минут, и 90°С в течение 1 часа. Образцы разбавляют до 10 мл чистой водой, фильтруют через гидрофобный фильтр, затем оценивают с использованием ICP-MS. Результаты фармакокинетического анализа мышей с трансплантированными клетками CT-26 проиллюстрированы на ФИГ. 5-1 и 5-2, и результаты фармакокинетического анализа мышей с трансплантированными клетками BxPC3 проиллюстрированы на ФИГ. 6-1 и 6-2. PVA-BPA показывает превосходное накопление в опухоли для всех типов опухолей и может поддерживать высокую концентрацию внутриопухолевого бора в течение длительного времени. Также, соотношение опухоль/кровь является сравнимым с соотношением для обычно применяемого Fru-BPA.
[0107]
ПРИМЕР 7
Испытание по проникновению в опухоль Cy5-PVA-BPA
Таким же способом, как в ПРИМЕРЕ 6, получают раствор Cy5-PVA-BPA и модель подкожной опухоли CT26, и, как только размер опухоли достигает примерно 200 мм3, 200 мкл образца медленно вводят через хвостовую вену (8 мг BPA/мышь). По истечении 5,5 часов после введения, внутривенно вводят раствор конъюгата лектин томатов-DyLight488 (50 мкг) и Hoechst 33342 (50 мкг). Опухоль удаляют через 6 часов после введения образца, опухоль срезают посередине, и срезанный сегмент помещают на стеклянную чашку и изучают методом CLSM. Результаты проиллюстрированы на ФИГ. 7. Общее распределение C5-PVA позволяет предположить, что BPA может быть доставлено по всей опухоли.
[0108]
ПРИМЕР 8
Противоопухолевое действие
Клетки СT-26 подкожно имплантируют (2,0 × 105 клеток/ мышь) около правого бедра мышей BALB/ c, и 250 мкл следующих образцов медленно вводят через хвостовую вену мышей, имеющих размер опухоли приблизительно 50-100 мм3, (10 мг BPA/мышь).
PVA-BPA (концентрация BPA=191 мМ, концентрация диола в PVA=574 мМ) в PBS (pH 9,5)
Fru-BPA (концентрация BPA=191 мМ, концентрация фруктозы=574 мМ) в PBS (pH 9,5)
[0109]
В упомянутом растворе PVA-11В-BPA, вычислено, на основе константы равновесия (pH 7,4), что (свободный BPA):(BPA, связанный с PVA) = 10:90-0:100 (молярное соотношение). Следует отметить, что, поскольку рН раствора PVA-BPA имеет значение 9,5, и чем выше рН, тем больше константа равновесия, то установлено, что почти 100% BPA является связанным с PVA в растворе.
[0110]
В группе нейтронного облучения, нейтронное облучение проводят в течение 50 минут только вокруг правого бедра мыши через 3 часа и 6 часов после введения образца. С учетом дня облучения, установленного в качестве первого дня, диаметр опухоли измеряют каждые 2-3 дня с помощью электронных циркулей, и массу тела измеряют с помощью электронных весов в течение всех 25 дней. Измеренный диаметр опухоли используют в формуле эллиптической аппроксимации объема (ab2 × 1/2, где a представляет собой длинную сторону, и b означает короткую сторону), что дает объем опухоли. Оцененные группы сведены вместе ниже.
[0111]
Контрольная группа (ХОЛОДНАЯ) (n=8): необработанная группа.
Fru-BPA (ХОЛОДНАЯ) (n=8): сделана инъекция только Fru-BPA.
PVA-BPA (ХОЛОДНАЯ) (n=8): сделана инъекция только PVA-BPA.
Контрольная группа (ГОРЯЧАЯ) (n=8): выполнено только облучение нейтронами.
Fru-BPA (ГОРЯЧАЯ) 3 часа (n=8): сделана инъекция посредством Fru-BPA, затем выполнено облучение нейтронами через 3 часа после этого.
PVA-BPA (ГОРЯЧАЯ) 3 часа (n=4): сделана инъекция посредством PVA-BPA, затем через 3 часа после этого выполнено облучение нейтронами.
PVA-BPA (ГОРЯЧАЯ) 6 часов (n=8): сделана инъекция посредством PVA-BPA, затем через 6 часов после этого выполнено облучение нейтронами.
[0112]
Изменение размера опухоли с течением времени и кривые Каплана-Мейера показаны на ФИГУРАХ 8-1 и 8-2. PVA-BPA показывает значительное ингибирующее действие на рост опухоли в нейтронозахватной терапии по сравнению с Fru-BPA.
[0113]
Через двадцать пять дней после облучения тепловыми нейтронами, опухоль удаляют и погружают в раствор формалина на 4 дня. Опухоль вынимают из раствора формалина и разрезают тонкими слоями посередине опухолевой ткани. Удаленные органы обрабатывают заливочной средой (реактивом O.C.T) для изготовления замороженных срезов, и затем тканевый срез толщиной 4 мкм изготавливают с использованием криостата и подвергают окрашиванию гематоксилин-эозином. Результаты проиллюстрированы на ФИГУРАХ 9-1-9-4. PVA-BPA (ГОРЯЧАЯ ГРУППА) 3 часа (ФИГ. 9-4) позволяет предположить, что во всей опухоли индуцируется апоптоз, что согласуется с эффектами эксперимента по противоопухолевому действию.
[0114]
ПРИМЕР 9
Сигнал ядерного магнитного резонанса 19F и накопление в опухоли PVA-19F-BPA
<Реагенты, клетки и животные>
PVA произведен тем же способом, что и в ПРИМЕРЕ 1 (Mn=6500-9500)
Соляная кислота 5 моль/л (для масс-спектрометрии): Wako Pure Chemical Industries, Ltd.
Гидроксид натрия 5 моль/л (для масс-спектрометрии): Wako Pure Chemical Industries, Ltd.
70%-ная азотная кислота (1,42): Wako Pure Chemical Industries, Ltd.
Гидрофосфат динатрия: Nacalai Tesque
2-Амино-3-(4-бороно-2-фторфенил)пропановая кислота (19F-BPA) (рацемический): Fluorotech LLC
Клетки CT26 (клеточная линия рака толстой кишки мыши): Американская коллекция типовых культур (Manassas, VA)
Мышь BALB/c: Charles River Japan
<Оборудование>
Прибор для NMR (Ядерный Магнитный Резонанс=ЯМР): BRUKER AVANCE III 400 (400 МГц, BRUKER BioSpin)
Прибор для ICP-MS Agilent 7900: Agilent Technology Co., Ltd.
[0115]
Следующие образцы приготавливают в следующих концентрациях с использованием 10 мМ PBS (140 мМ NaCl, рН 9,5).
19F-BPA (концентрация 19F-BPA=176 мМ)
Fru-19F-BPA (концентрация 19F-BPA=176 мМ, концентрация фруктозы=573,9 мМ)
PVA-19F-BPA (концентрация 19F-BPA=176 мМ, концентрация диола в PVA=573,9 мМ)
[0116]
450 мкл каждого образца и 50 мкл D2O смешивают, и измеряют 19F-NMR. Результаты проиллюстрированы на ФИГУРАХ 10-1-10-3. NMR-сигнал для PVA-19F-BPA можно легко обнаружить (ФИГ. 10-3). Полагают, что PVA-19F-BPA применим в 19F-MRI в последующих диагностических методах.
[0117]
ПРИМЕР 10
Фармакокинетика PVA-19F-BPA и Fru-19F-BPA
Модели подкожной опухоли получают подкожной инъекцией клеток CT26 мышам BALB/c в количестве 2,0 × 105 клеток/мышь. Как только размер опухоли достигает примерно 200 мм3, 200 мкл следующих образцов медленно вводят через хвостовую вену мышей (8 мг 19F-BPA/мышь).
PVA-19F-BPA (концентрация BPA=176 мМ, концентрация диола в PVA=574 мМ) в PBS (pH 9,5)
Fru-19F-BPA (концентрация BPA=176 мМ, концентрация фруктозы=574 мМ) в PBS (pH 9,5)
[0118]
По истечении заданного времени после введения образца, мышей препарируют, и опухоли удаляют. Опухоли помещают в пробирку фирмы Falcon объемом 10 мл, и добавляют к тому 1 мл 70%-ной азотной кислоты. После этого, каждый образец инкубируют при 50°С в течение 15 минут, 70°С в течение 15 минут, и 90°С в течение 1 часа. Образцы разбавляют до 10 мл чистой водой, фильтруют через гидрофобный фильтр, затем оценивают количество бора с использованием ICP-MS. Результаты проиллюстрированы на ФИГ. 11. Поскольку PVA-19F-BPA удерживается в опухоли в высокой концентрации в течение длительного времени, ожидают улучшение отношения 'сигнал/шум’ в 19F-MRI (магнитно-резонансной визуализации).
[0119]
ПРИМЕР 11
Синтез PEG-P[Lys(Fru)Lys]
<Реагенты>
Диметилсульфоксид (DMSO) (дегидратированный гидридом кальция, затем очищенный перегонкой): Wako Pure Chemical Industries, Ltd.
Lys(TFA)-NCA (лизин(трифторацетил)-N-карбоксиангидрид): Chuo Kasei Co., Ltd.
MeO-PEG-NH2 (молекулярная масса PEG (ПЭГ): 10 КДа): NOF corporation
Метанол: Wako Pure Chemical Industries, Ltd.
NaOH: Wako Pure Chemical Industries, Ltd.
HCl: Wako Pure Chemical Industries, Ltd.
Бензол: Wako Pure Chemical Industries, Ltd.
Диэтиловый простой эфир: Kanto Chemical Co.
2,3,4,5-ди-O-изопропилиден-бета-D-фруктопираноза (DiOFru): Tokyo Chemical Industry Co., Ltd.
1,1'-Карбонилдиимидазол (CDI): Sigma-Aldrich
Трифторуксусная кислота (TFA): Wako Pure Chemical Industries, Ltd.
4-Броно-L-фенилаланин (BPA) (B): KatChem
<Оборудование>
NMR (Ядерный Магнитный Резонанс=ЯМР): BRUKER AVANCE III 400 (400 МГц, BRUKER BioSpin)
GPC (Гельпроникающая хроматография): JASCO Corporation
Колонка для измерения PEG-PLys (TFA): колонка TSK-gel superAW3000, superAW4000, и superAWL-guard (Tosoh Corporation)
Колонка для измерения PEG-PLys: Superdex 200 Increase 10/300 GL (GE Healthcare)
Детектор: RI-2031
[0120]
(1) Синтез MeO-PEG-PLys (TFA)
[Хим. стр. 67]
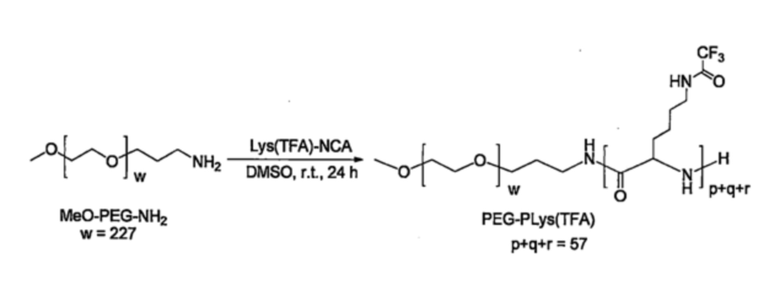
1,00 г MeO-PEG-NH2 растворяют в бензоле и лиофилизируют в течение ночи, затем это растворяют в 10 мл перегнанного DMSO, который добавляют туда в атмосфере аргона. Тем временем, 1,60 г Lys(TFA)-NCA растворяют в 15 мл перегнанного DMSO в атмосфере аргона. Эти растворы смешивают в атмосфере аргона и перемешивают в течение 24 часов при комнатной температуре. После этого, реакционный раствор добавляют к избыточному количеству диэтилового эфира с получением осадка, который собирают вакуумной фильтрацией и сушат при пониженном давлении в течении ночи с получением PEG-PLys(TFA). Молекулярно-массовое распределение для полученного PEG-PLys(TFA) подтверждается методом GPC, и Mw/Mn=1,12. Кроме того, степень полимеризации для PLys(TFA) на основе результатов 1Н-NMR составляет 57.
[Хим. стр. 68]
1Н-ЯМР (400 МГц, DMSO-d6): δ 9,48-9,10 (шир., -NH-C=O-CF3), 8,61-7,60 (шир., C-NН-С=O-), 4,10-3,72 (шир., СH-NН-), 3,70-3,45 (шир., -СН2-СН2-O-), 3,25-3,00 (шир., -СH2-NH-C=O-), 2,22-1,00 (шир., -СН2-СН2-СН2-)
[0121]
(2) Синтез PEG-PLys
[Хим. стр. 69]
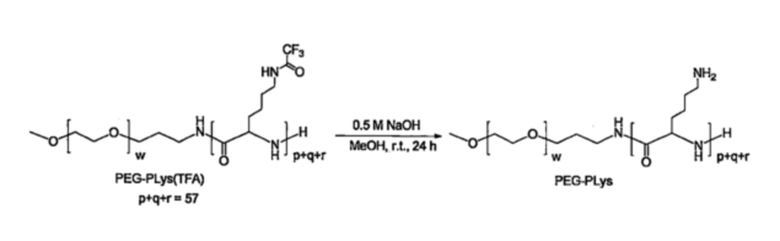
1,2 г PEG-PLys(TFA) растворяют в смеси ‘водный раствор NaOH (5М)/вода/метанол' (10 мл/5 мл/ 35 мл) и перемешивают в течение 20 часов при 35°С. Затем это диализируют дважды против 0,01N-ной HCl и три раза против чистой воды (MWCO для диализной мембраны: 6-8 кДа). Затем это лиофилизируют и получают 600 мг PEG-PLys.
[Хим. стр. 70]
1Н-ЯМР (400 МГц, D2O): δ 4,43-4,24 (шир., CH-NH-), 3,85-3,61 (шир., -CH2-CH2-O-), 2,07-1,28 (шир., -CH2-CH2-CH2-), 3,14-2,94 (шир., -CH2-NH-C=O-)
[0122]
(3) Синтез PEG-P[Lys(Fru-ISP)/Lys]
[Хим. стр. 71]
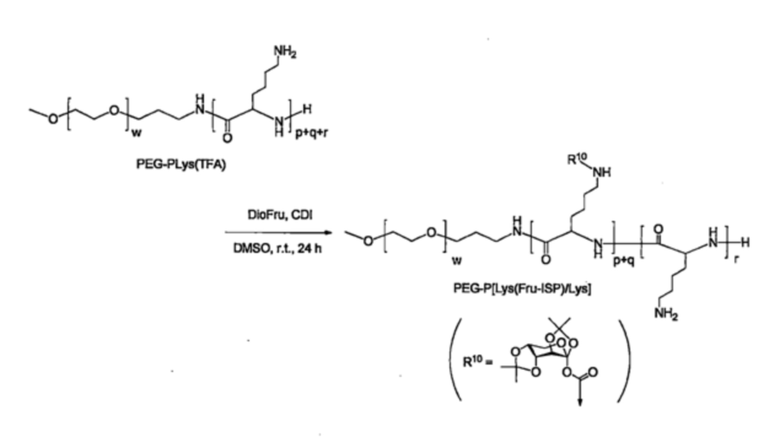
1,21 г CDI и 3,88 г DiOfru растворяют в 15 мл перегнанного DMSO в атмосфере аргона и перемешивают в течение 20 часов при 45°С. Далее, 300 мг MeO-PEG-PLys растворяют в 5 мл перегнанного DMSO, к тому добавляют раствор, полученный реакционным взаимодействием CDI и DiOfru, и это оставляют реагировать в течение 20 часов при комнатной температуре. По завершении реакции, затем в отношении этого проводят диализ дважды против метанола и дважды против чистой воды (MWCO диализной мембраны: 6-8 кДа). Наконец, это лиофилизируют и получают 360 мг PEG-P[Lys(Fru-ISP)/Lys]. Молекулярно-массовое распределение для него измеряют методом GPC, и MW/Mn=1,17. Степень введения DiOFru в полимер составляет 58%, что вычислено методом 1Н-ЯМР. На основе результатов 1Н-ЯМР, (p+q) имеет значение 33, и r имеет значение 24 в вышеупомянутой химической формуле.
[Хим. стр. 72]
1Н-ЯМР (400 МГц, D2O): δ 3,85-3,61 (шир., -CH2-CH2-O-), 3,32-3,02 (шир., -СН2-NH-R10), 3,02-2,81 (шир., -CH2-NH2), 2,25-1,20 (шир., -CH2-CH2-CH2-, CH3-С-CН3)
[0123]
(4) Синтез PEG-P[Lys(Fru)/Lys]
[Хим. стр. 73]

PEG-P[Lys(Fru-ISP)/Lys] растворяют в TFA/H2O (95/5 объем./объем) в концентрации 20 мг/мл и перемешивают в течение ночи при комнатной температуре. Затем реакционный раствор диализируют однократно против чистой воды, дважды против 0,01N-ной HCl, и дополнительно дважды против чистой воды (MWCO для диализной мембраны: 6-8 кДа). После диализа, это лиофилизируют и получают PEG-P[Lys(Fru)/Lys]. Mn=24100.
[Хим. стр. 74]
1Н-ЯМР (400 МГц, D2O): δ 4,35-4,20 (шир., CH-NH-), 3,75-3,55 (шир., -CH2-CH2-O-), 3,32-3,02 (шир., -СН2-NH-R11), 3,02-2,81 (шир., -CH2-NH2), 1,98-1,15 (шир., -CH2-CH2-CH2-)
[0124]
ПРИМЕР 12
Оценивание накопления в опухоли и противоопухолевое действие производного BPA (PEG-P[Lys(Fru)/Lys]-BPA), где BPA связан с PEG-P[Lys(Fru)/Lys]
<Реагенты, клетки, и животные>
PEG-P[Lys(Fru)/Lys] произведен тем же способом, что и в ПРИМЕРЕ 11 (Mn=24100)
Соляная кислота 5 моль/л (для масс-спектрометрии): Wako Pure Chemical Industries, Ltd.
Гидроксид натрия 5 моль/л (для масс-спектрометрии): Wako Pure Chemical Industries, Ltd.
4-Бороно-L-фенилаланин (BPA): Katchem
Гидрофосфат динатрия: Nacalai Tesque
Клетки BxPC3 (клеточная линия рака поджелудочной железы человека): Американская коллекция типовых культур (Manassas, VA)
Клетки CT26 (клеточная линия рака толстой кишки мышей): Американская коллекция типовых культур (Manassas, VA)
Мышь BALB/c: Charles River Japan
‘Голая’ (бестимусная) мышь BALB/c: Charles River Japan
<Оборудование>
Прибор для ICP-MS Agilent 7900: Agilent Technology Co., Ltd.
Установка нейтронного облучения с использованием тяжелой воды: KUR
[0125]
Клетки BxPC3 подкожно вводят инъекцией ‘голым’ мышам BALB/c в количестве 1 × 107 клеток/мышь. Как только размер опухоли достигает примерно 200 мм3, следующий образец внутривенно вводят инъекцией.
PEG-P[Lys(Fru)/Lys]-BPA в PBS (33 мг PEG-P[Lys(Fru)/Lys]/ мышь, 8 мг BPA/ мышь)
[0126]
По истечении заданного времени после введения образца, мышей препарируют, кровь собирают, и опухоли удаляют. Опухоли помещают в пробирку фирмы Falcon объемом 10 мл, и добавляют 1 мл 70%-ной азотной кислоты. После этого, каждый образец инкубируют при 50°С в течение 15 минут, 70°С в течение 15 минут, и 90°С в течение 1 часа. Образцы разбавляют до 10 мл чистой водой, фильтруют через гидрофобный фильтр, затем оценивают количество бора с использованием ICP-MS. Результаты проиллюстрированы на ФИГУРАХ 12-1 и 12-2.
[0127]
ПРИМЕР 13
Противоопухолевое действие PEG-P[Lys(Fru)/Lys]-BPA на модель подкожной опухоли CT26
Клетки СT-26 подкожно имплантируют (2,0 × 105 клеток/ мышь) около правого бедра мышей BALB/c, и 250 мкл следующих образцов медленно вводят через хвостовую вену мышей, имеющих размер опухоли приблизительно 15-150 мм3, (10 мг BPA/мышь).
Fru-BPA (концентрация BPA=192 мМ, концентрация фруктозы:концентрация BPA=3:1) в PBS (pH 8,5)
PEG-P[Lys(Fru)/Lys]-BPA (концентрация BPA=192 мМ, концентрация фруктозы боковой цепи полимера:концентрация BPA=1,2:1) в PBS (pH 8,5)
[0128]
В группе нейтронного облучения, нейтронное облучение проводят в течение 50 минут только вокруг правого бедра мыши через 3 часа и 6 часов после введения образца. С учетом дня облучения, установленного в качестве первого дня, диаметр опухоли измеряют каждые 2-3 дня с помощью электронных циркулей, и массу тела измеряют с помощью электронных весов в течение всех 25 дней. Измеренный диаметр опухоли используют в формуле эллиптической аппроксимации объема (ab2 × 1/2, где a представляет собой длинную сторону, и b означает короткую сторону), что дает объем опухоли. Оцененные группы сведены вместе ниже.
[0129]
Контрольная группа (ХОЛОДНАЯЙ) (n=7): необработанная группа.
Fru-BPA (ХОЛОДНАЯ) (n=7): сделана инъекция только Fru-BPA.
PEG-P[Lys(Fru)/Lys]-BPA (ХОЛОДНАЯ) (n=4): сделана инъекция только PEG-P[Lys(Fru)/Lys]-BPA.
Контрольная группа (ГОРЯЧАЯ) (n=6): выполнено только облучение нейтронами.
Fru-BPA (ГОРЯЧАЯ) 3 часа (n=7): сделана инъекция посредством Fru-BPA, затем выполнено облучение нейтронами через 3 часа после этого.
Fru-BPA (ГОРЯЧАЯ) 6 часов (n=7): сделана инъекция посредством Fru-BPA, затем выполнено облучение нейтронами через 6 часов после этого.
PEG-P[Lys(Fru)/Lys]-BPA (ГОРЯЧАЯ) 3 часа (n=6): сделана инъекция посредством PEG-P[Lys(Fru)/Lys]-BPA, затем через 3 часа после этого выполнено облучение нейтронами.
PEG-P[Lys(Fru)/Lys]-BPA (ГОРЯЧАЯ) 6 часов (n=5): сделана инъекция посредством PEG-P[Lys(Fru)/Lys]-BPA, затем через 6 часов после этого выполнено облучение нейтронами.
[0130]
Изменение размера опухоли с течением времени показано на ФИГУРАХ 13-1 и 13-2. PEG-P[Lys(Fru)/Lys]-BPA показывает значительное ингибирующее действие на рост опухоли в нейтронозахватной терапии по сравнению с Fru-BPA.
[0131]
ПРИМЕР 14
Синтез P[Asp(глюкамин)/Asp]
<Реагенты>
Диметилсульфоксид (DMSO) (дегидратированный гидридом кальция и очищенный перегонкой): Wako Pure Chemical Industries, Ltd.
BLA-NCA: NanoCarrier Co., Ltd.
4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилморфолиния хлорид (DMTMM): Wako Pure Chemical Industries, Ltd.
Триэтиламин (TEA): Wako Pure Chemical Industries, Ltd.
Диэтиловый эфир: Kanto Chemical Co.
Метанол: Wako Pure Chemical Industries, Ltd.
NaOH: Wako Pure Chemical Industries, Ltd.
HCl: Wako Pure Chemical Industries, Ltd.
N, N-диметилформамид (DMF): Wako Pure Chemical Industries, Ltd. (используемый после дегидратации и перегонки)
Дихлорметан (DCM): Wako Pure Chemical Industries, Ltd. (используемый после дегидратации и перегонки)
4-Бороно-L-фенилаланин (BPA) (B): KatChem
D-глюкамин: Tokyo Chemical Industry Co., Ltd.
<Оборудование>
Прибор для NMR (Ядерный Магнитный Резонанс=ЯМР): BRUKER AVANCE III 400 (400 МГц, BRUKER BioSpin)
GPC (Гельпроникающая хроматография): JASCO Corporation
Колонка для измерения PBLA: колонка TSK-gel super AW3000, super AW4000, и super AWL-guard (Tosoh Corporation)
Колонка для измерения PAsp: Superdex 200 Increase 10/300 GL (GE Healthcare)
Детектор: UV-2070 (канал 1), RI-2031 (канал 2)
[0132]
(1) Получение поли(β-бензил-L-аспартат) (PBLA)
[Хим. стр. 75]

1,44 г BLA-NCA растворяют в смешанном растворителе, состоящем из 3 мл DMF и 27 мл DCM, в атмосфере аргона, к этому добавляют 3,9 мкл пропиламина и проводят перемешивание в течение 48 часов. После перемешивания, реакционный раствор добавляют по каплям к диэтиловому эфиру с получением осадка, который отфильтровывают через нутч-фильтр и сушат при пониженном давлении с получением PBLA. Молекулярно-массовое распределение, как определено методом GPC, составляет Mw/Mn=1,11, и степень полимеризации составляет 73 на основе результата 1Н-NMR.
[Хим. стр. 76]
1Н-ЯМР (400 МГц, DMSO-d6): δ 8,35-8,00 (шир., C-NH-C=O-), 7,40-7,19 (шир., -C6Н5), 5,15-4,92 (шир., -О-СH2-С6Н5), 4,70-4,51 (шир., СН-NН-), 2,90-2,49 (шир., CH-СH2-C=O-O-), 0,78-0,71 (шир., -СН3)
[0133]
(2) Получение полиаспартовой кислоты (PAsp)
[Хим. стр. 77]
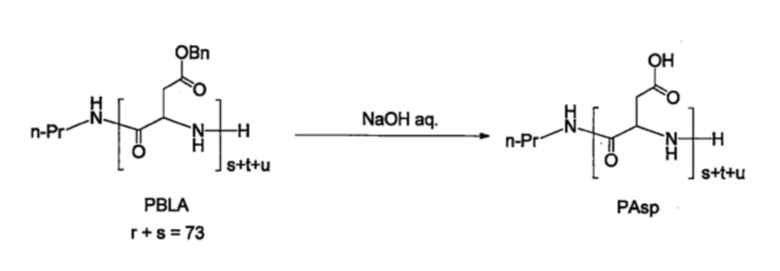
1 г PBLA добавляют к 0,5М-ному водному раствору NaOH и перемешивают в течение 20 часов при 35°С. Реакционный раствор диализируют против чистой воды четыре раза (MWCO для диализной мембраны: 3,5 кДа) и лиофилизируют с получением 0,2 г PAsp.
[Хим. стр. 78]
1Н-ЯМР (400 МГц, D2O): δ 2,91-2,48 (шир., СН-СН2-COOH), 0,94-0,82 (шир., -СН3)
[0134]
(3) Получение P[Asp(глюкамин)/Asp]
[Хим. стр. 79]
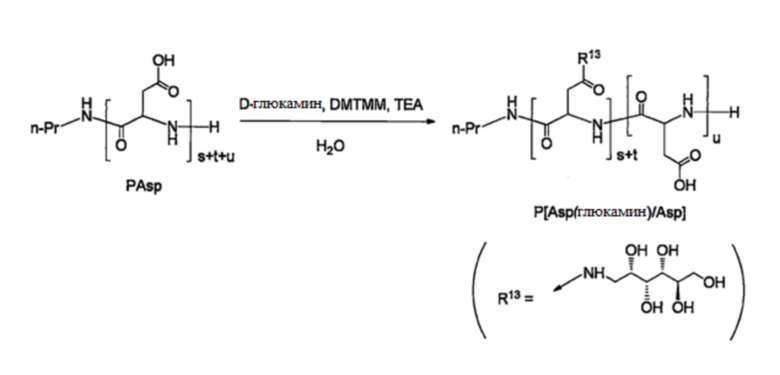
0,2 г PAsp, 3 г DMTMM, и 2,6 г D-глюкамина растворяют в чистой воде, добавляют несколько капель TEA, и смесь перемешивают при комнатной температуре в течение 24 часов. После перемешивания, реакционный раствор диализируют против чистой воды четыре раза (MWCO диализной мембраны: 3,5 кДа) и лиофилизируют с получением P[Asp(глюкамин)/Asp]. Физические свойства оценивают методом GPC и 1H-NMR, и данные 1H-NMR показывают, что степень введения глюкамина составляет 30%. На основе результатов 1H-NMR, в вышеупомянутой химической формуле (s+t) имеет значение 17, и u имеет значение 56.
[Хим. стр. 80]
1Н-ЯМР (400 МГц, D2O): δ 4,18-3,00 (шир., -R13), 2,91-2,48 (шир., СН-СН2-COOH), 0,94-0,82 (шир., -СН3)
[0135]
ПРИМЕР 15
Накопление в опухоли производного BPA (P[Asp(глюкамин)/Asp]-BPA), где BPA является связанным с P[Asp(глюкамин)/Asp]
Модели подкожной опухоли получают подкожной инъекцией клеток CT26 мышам BALB/c в количестве 2,0 × 105 клеток/мышь. Как только размер опухоли достигает примерно 200 мм3, 200 мкл следующего образца медленно вводят через хвостовую вену мышей (8 мг BPA/мышь).
P[Asp(глюкамин)/Asp]-BPA (концентрация BPA=192 мМ, концентрация BPA:концентрация глюкамина=1:1,2) в PBS (pH 9)
[0136]
По истечении заданного времени после введения образца, кровь собирают, мышей препарируют, и опухоли удаляют. Опухоли помещают в пробирку фирмы Falcon объемом 10 мл, и добавляют 1 мл 70%-ной азотной кислоты. После этого, каждый образец инкубируют при 50°С в течение 15 минут, 70°С в течение 15 минут, и 90°С в течение 1 часа. Образцы разбавляют до 10 мл чистой водой, фильтруют через гидрофобный фильтр, затем количество бора оценивают с использованием ICP-MS. Результаты проиллюстрированы на ФИГ. 14-1 и 14-2, позволяют предположить, что использование P[Asp(глюкамин)/Asp]-BPA может улучшить свойства накопления в опухоли и соотношение накопления в опухоли/крови.
[0137]
ПРИМЕР 16
Противоопухолевое действие PVA-BPA на модель подкожной опухоли BxPC3
Клетки BxPC3 подкожно вводят инъекцией (5 × 106 клеток/мышь) около правого бедра мышей BALB/c, и 250 мкл следующих образцов медленно вводят через хвостовую вену мышей, имеющих размер опухоли примерно 500 мм3 (10 мг BPA/ мышь).
PVA-BPA (концентрация BPA=191 мМ, концентрация диола в PVA=574 мМ) в воде (рН 9,2)
Fru-BPA (концентрация BPA=191 мМ, концентрация фруктозы=574 мМ) в воде (рН 9,2)
(рН корректируют с использованием водного раствора HCl и водного раствора NaOH)
[0138]
Нейтронное облучение проводят в течение 50 минут только вокруг правого бедра мыши через 3 часа после введения образца. С учетом дня облучения, установленного в качестве первого дня, диаметр опухоли измеряют с течением времени с помощью электронных циркулей, и массу тела измеряют с помощью электронных весов в течение всех 55 дней. Измеренный диаметр опухоли используют в формуле эллиптической аппроксимации объема (ab2 × 1/2, где a представляет собой длинную сторону, и b означает короткую сторону) с получением объема опухоли. Оцененные группы сведены вместе ниже.
[0139]
Контрольная группа (ХОЛОДНАЯ) (n=8): необработанная группа.
Fru-BPA (ГОРЯЧАЯ) (n=6): сделана инъекция Fru-BPA, затем выполнено облучение нейтронами через 3 часа после этого.
PVA-BPA (ГОРЯЧАЯ) (n=6): сделана инъекция PVA-BPA, затем выполнено облучение нейтронами через 3 часа после этого.
[0140]
Результаты проиллюстрированы на ФИГ. 15. На 55-ый день, наблюдается статистически значимое различие между Fru-BPA и PVA-BPA (p < 0,05 [t-критерия Стьюдента]).
[0141]
ПРИМЕР 17
Противоопухолевое действие PEG-P[Lys(Fru)/Lys]-BPA на модель подкожной опухоли BxPC3
Клетки BxPC3 подкожно вводят инъекцией (5 × 106 клеток/мышь) около правого бедра мышей BALB/c, и 250 мкл следующих образцов медленно вводят через хвостовую вену мышей, имеющих размер опухоли примерно 15-150 мм3 (10 мг BPA/ мышь).
Fru-BPA (концентрация BPA=192 мМ, концентрация фруктозы:концентрация BPA=3:1) в PBS (рН 8,5)
PEG-P[Lys(Fru)/Lys]-BPA (концентрация BPA=192 мМ, концентрация фруктозы боковой цепи полимера:концентрация BPA=1,2:1) в PBS (рН 8,5)
[0142]
В группе нейтронного облучения, нейтронное облучение проводят в течение 50 минут только вокруг правого бедра мыши через 3 часа и 6 часов после введения образца. С учетом дня облучения, установленного в качестве первого дня, диаметр опухоли измеряют каждые 2-3 дня с помощью электронных циркулей, и массу тела измеряют с помощью электронных весов в течение всех 25 дней. Измеренный диаметр опухоли используют в формуле эллиптической аппроксимации объема (ab2 × 1/2, где a представляет собой длинную сторону, и b означает короткую сторону), что дает объем опухоли. Оцененные группы сведены вместе ниже.
[0143]
Контрольная группа (ГОРЯЧАЯ) (n=8): выполнено только облучение нейтронами.
Fru-BPA (ГОРЯЧАЯ) (n=8): сделана инъекция Fru-BPA, затем через 3 часа после этого выполнено облучение нейтронами.
PEG-P[Lys(Fru)/Lys]-BPA (ГОРЯЧАЯ) (n=8): сделана инъекция PEG-P[Lys(Fru)/Lys]-BPA, затем выполнено облучение нейтронами через 3 часа после этого.
[0144]
Изменение размера опухоли с течением времени показано на ФИГУРАХ 16.
[0145]
ПРИМЕР 18
Синтез N3-P[Lys(Глюконат)/Lys] и mPEG10k-P[Lys(Глюконат)/Lys]
[Хим. стр. 81]

[0146]
<Реагенты>
11-Азид-3,6,9-триоксаундекан-1-амин: Sigma Aldrich
Метокси-PEG10k-NH2: NOF Co.
NCA-L-Lys(Tfa): Chuo Kasei Co.
D-глюконо-1,5-лактон: Tokyo Chemical Industry Co.
Триэтиламин (TEA): Nacalai Tesque
Диметилсульфоксид (DMSO): DMSO, приобретенный в Wako Pure Chemical Industries, Ltd., очищают перегонкой в атмосфере аргона и используют.
Метанол: Wako Pure Chemical Industries, Ltd.
Бензол: Nacalai Tesque
Диэтиловый эфир: Kanto Chemical Co.
Водный раствор гидроксида натрия 5 моль/л: Wako Pure Chemical Industries, Ltd.
Соляная кислота 5 моль/л: Nacalai Tesque
Тяжелая вода (0,05% по массе 3-(триметилсилил)пропионовой-2,2,3,3-d4 кислоты, натриевая соль):Sigma Aldrich
<Оборудование>
NMR (Ядерный Магнитный Резонанс=ЯМР): BRUKER AVANCE III 400 (400 МГц, BRUKER BioSpin)
GPC (Гельпроникающая хроматография): JASCO Corporation
Superdex 200 Increase 10/300 GL (GE Healthcare)
Детектор: RI-2031
[0147]
(1-1)
Синтез N3-Plys_(A)
3,2 г (11,9 ммоль) NCA-Lys(Tfa) взвешивают и добавляют в двугорлую грушевидную колбу объемом 100 мл в атмосфере аргона. К этому добавляют 33 мл очищенного перегонкой DMSO и растворяют NCA. После этого, добавляют 30 мкл (0,151 ммоль) инициатора 11-азид-3,6,9-триоксаундекан-1-амина, и смесь перемешивают на водяной бане при 40°С в течение 3 дней. После этого, реакционный раствор помещают в диализную мембрану (MWCO=3,5 кД) и диализируют 3 раза против 500 мл метанола в течение 4 часов. Растворитель испаряют из диализированного раствора образца с помощью ротационного испарителя и затем сушат при пониженном давлении в течение ночи. 100 мл метанола, 2 мл 5М-ого водного раствора гидроксида натрия, и 8 мл воды сверхвысокой чистоты добавляют к полученному твердому веществу, которое растворяют. Это перемешивают в течение ночи на водяной бане, установленной на 40°С. После этого, реакционный раствор помещают в диализную мембрану (MWCO=3,5 кД) и диализируют дважды против 1 л 0,01М-ого водного раствора гидроксида натрия в течение 4 часов и затем диализируют четыре раза против 3 л воды сверхвысокой чистоты в течение 4 часов. Диализированный образец помещают в грушевидную колбу объемом 500 мл, и растворитель удаляют лиофилизированием с получением твердого вещества белого цвета N3-Plys_(A). На основе данных 1Н-NMR, степень полимеризации полученного соединения составляет 64,4.
[Хим. стр. 82]
1Н-ЯМР (400 МГц, D2O): δ 1,35-1,90 (шир., -СН2-), 3,02 (т, -СН2-NH2), 3,70 (шир., -СН2-О-), 4,32 (т, -СН-СОNH-).
[0148]
(1-2)
(2) Синтез N3-Plys_(B)
В результате проведения реакции с применением такого же способа, что и в вышеупомянутом разделе (1-1), за исключением использования 20 мкл (0,101 ммоль) инициатора 11-азид-3,6,9-триоксаундекан-1-амина, получают твердое вещество белого цвета N3-PLys_(B). На основе данных 1Н-ЯМР, степень полимеризации полученного соединения составляет 98,4.
[Хим. стр. 83]
1Н-ЯМР (400 МГц, D2O): δ 1,35-1,90 (шир., -СН2-), 3,02 (т, -СН2-NH2), 3,70 (шир., -СН2-О-), 4,32 (т, -СН-СОNH-).
[0149]
(1-3)
Синтез N3-Plys_(C)
В результате проведения реакции с применением такого же способа, что и в вышеупомянутом разделе (1-1), за исключением использования 15 мкл (0,0755 ммоль) инициатора 11-азид-3,6,9-триоксаундекан-1-амина, получают твердое вещество белого цвета N3-PLys_(С). На основе данных 1Н-ЯМР, степень полимеризации полученного соединения составляет 130,4.
[Хим. стр. 84]
1Н-ЯМР (400 МГц, D2O): δ 1,35-1,90 (шир., -СН2-), 3,02 (т, -СН2-NH2), 3,70 (шир., -СН2-О-), 4,32 (т, -СН-СОNH-).
[0150]
(1-4)
Синтез mPEG10k-PLys
Такую же реакцию полимеризации, что и в вышеупомянутом разделе (1-1), проводят с использованием, в качестве инициатора, полиэтиленгликоля, имеющего группу -ОМе на одном конце и группу -NH2 на другом конце и имеющего среднечисловую молекулярную массу 10000 (в дальнейшем в данном документе называемого mPEG10k-NH2). Взвешивают 1,00 г (0,100 ммоль) mPEG10k-PLys, добавляют в двугорлую грушевидную колбу и растворяют в 2 мл бензола. Далее, растворитель испаряют лиофилизированием. К этому добавляют 10 мл очищенного перегонкой DMSO в атмосфере аргона и растворяют лиофилизированный продукт. Далее, взвешивают 1,61 г NCA-Lys(Tfa) в атмосфере аргона и добавляют в отдельную двугорлую грушевидную колбу. К тому добавляют 16 мл очищенного перегонкой DMSO и NCA-Lys(Tfa) растворяют. Раствор NCA/DMSO добавляют к раствору PEG/DMSO с помощью шприца, и смесь перемешивают на водяной бане при 40°С в течение 2 дней. Реакционный раствор добавляют по каплям к 500 мл диэтилового эфира и очищают методом переосаждения. Осадок собирают фильтрацией через нутч-фильтр и сушат при пониженном давлении в течение ночи с получением твердого вещества белого цвета. Полученный полимер добавляют в грушевидную колбу объемом 100 мл и к тому добавляют 100 мл метанола, 2 мл 5М-ого водного раствора гидроксида натрия и 8 мл воды сверхвысокой чистоты и перемешивают в течение ночи на водяной бане, установленной на 40°С. Раствор образца помещают в диализную мембрану (MWCO=3,5 кД) и диализируют дважды против 1 л 0,01М-ого водного раствора гидроксида натрия в течение 4 часов и затем диализируют четыре раза против 3 л воды сверхвысокой чистоты в течение 4 часов. Раствор диализированного образца добавляют в грушевидную колбу объемом 500 мл, и растворитель удаляют лиофилизированием с получением 1,3 г твердого вещества белого цвета mPEG10k-Plys. На основе данных 1Н-NMR, степень полимеризации полученного соединения составляет 52,1.
[Хим. стр. 85]
1Н-ЯМР (400 МГц, D2O): δ 1,35-1,90 (шир., -СН2-), 3,02 (т, -СН2-NH2), 3,68 (шир., -СН2-О-), 4,32 (т, -СН-СОNH-).
[0151]
(2-1)
Синтез N3-P[Lys(Глюконат)/Lys (А)
1,3 г (0,066 ммоль) N3-PLys_(A), получение которого описано в разделе (1-1) выше, 2,73 г (15,3 ммоль) D-глюконо-1,5-лактона, и 2,1 мл TEA (15 ммоль) добавляют в грушевидную колбу объемом 200 мл и растворяют в 100 мл метанола, и смесь перемешивают при кипячении с обратным холодильником в течение 24 часов. После этого растворитель испаряют с помощью ротационного испарителя, и полученный осадок растворяют в 30 мл 0,01М-ой соляной кислоты. После этого, раствор помещают в диализную мембрану (MWCO=3,5 кД) и диализируют однократно против 1 л 0,01М-ой соляной кислоты в течение 4 часов и затем диализируют четыре раза против 3 л воды сверхвысокой чистоты в течение 4 часов. Диализированный раствор фильтруют с помощью фильтра с размером ячеек 0,45 мкм и после этого растворитель испаряют лиофилизированием с получением 2,5 г твердого вещества белого цвета N3-P[Lys(Глюконат)/Lys]_(A). На основе данных 1Н-ЯМР, степень введения глюконовой кислоты в полимер составляет 98,0%. Кроме того, на основании степени полимеризации и степени введения, Mn=19763. К тому же, на основании данных GPC, коэффициент полидисперсности (PDI) имеет значение 1,22.
[Хим. стр. 86]
1Н-ЯМР (400 МГц, D2O): δ 1,30-2,05 (шир., -СН2-), 3,01 (шир., -СН2-NH2), 3,25 (шир., -СН2-NHCО-), 3,64-4,33 (шир., -CH-OH), 4,32 (шир., -СН-СОNH-).
[0152]
(2-2)
Синтез N3-P[Lys(Глюконат)/Lys (В)
В результате проведения реакции с применением такого же способа, что и в вышеупомянутом разделе (2-1), за исключением использования 1,6 г (0,054 ммоль) N3-PLys_(B) вместо N3-PLys_(А) и использования 3,36 г (18,9 ммоль) D-глюконо-1,5-лактона и 2,6 мл (19 ммоль) TEA, получают 3,0 г твердого вещества белого цвета N3-P[Lys(Глюконат)/Lys] (B). На основе данных 1Н-ЯМР, степень введения глюконовой кислоты в полимер составляет 98,4%. Кроме того, на основании степени полимеризации и степени введения, Mn=29712. К тому же, исходя из данных GPC, коэффициент полидисперсности (PDI) имеет значение 1,24.
[Хим. стр. 87]
1Н-ЯМР (400 МГц, D2O): δ 1,30-2,05 (шир., -СН2-), 3,01 (шир., -СН2-NH2), 3,25 (шир., -СН2-NHCО-), 3,64-4,33 (шир., -CH-OH), 4,32 (шир., -СН-СОNH-).
[0153]
(2-3)
Синтез N3-P[Lys(Глюконат)/Lys] (C)
В результате проведения реакции с применением такого же способа, что и в вышеупомянутом разделе (2-1), за исключением использования 1,5 г (0,038 ммоль) N3-PLys_(C) вместо N3-PLys_(А), и использования 3,15 г (17,7 ммоль) D-глюконо-1,5-лактона и 2,4 мл (17 ммоль) TEA, получают 2,9 г твердого вещества белого цвета N3-P[Lys(Глюконат)/Lys]_(С). На основе данных 1Н-ЯМР, степень введения глюконовой кислоты в полимер составляет 97,8%. Кроме того, на основании степени полимеризации и степени введения, Mn=39636. К тому же, исходя из данных GPC, коэффициент полидисперсности (PDI) имеет значение 1,35.
[Хим. стр. 88]
1Н-ЯМР (400 МГц, D2O): δ 1,30-2,05 (шир., -СН2-), 3,01 (шир., -СН2-NH2), 3,25 (шир., -СН2-NHCО-), 3,64-4,33 (шир., -CH-OH), 4,32 (шир., -СН-СОNH-).
[0154]
(2-4)
Синтез mPEG10k-P[Lys(Глюконат)/Lys]
1,3 г (0,050 ммоль) mPEG10k-PLys, получение которого описано в разделе (1-4) выше, 1,5 г (8,43 ммоль) D-глюконо-1,5-лактона, и 0,83 мл TEA (8,4 ммоль) добавляют в грушевидную колбу объемом 50 мл и растворяют в 10 мл метанола, который туда добавляют. Смесь перемешивают при кипячении с обратным холодильником в течение 24 часов. После этого, растворитель испаряют с помощью ротационного испарителя, и полученный осадок растворяют в 10 мл 0,01М-ой соляной кислоты. Раствор образца помещают в диализную мембрану (MWCO=3,5 кД) и диализируют однократно против 1 л 0,01М-ой соляной кислоты в течение 4 часов и затем диализируют четыре раза против 3 л воды сверхвысокой чистоты в течение 4 часов. Диализированный раствор фильтруют с помощью фильтра с размером ячеек 0,45 мкм и после этого растворитель испаряют лиофилизированием с получением 1,8 г твердого вещества белого цвета mPEG10k-P[Lys(Глюконат)/Lys]. На основе данных 1Н-ЯМР, степень введения глюконовой кислоты в полимер составляет 98,9%. Кроме того, К тому же, исходя из данных GPC, коэффициент полидисперсности (PDI) имеет значение 1,16.
[Хим. стр. 89]
1Н-ЯМР (400 МГц, D2O): δ 1,30-2,05 (шир., -СН2-), 3,01 (шир., -СН2-NH2), 3,25 (шир., -СН2-NHCО-), 3,64-4,33 (шир., -CH-OH), 3,68 (шир., -СН2-О-), 4,32 (шир., -СН-СОNH-).
[0155]
ПРИМЕР 19
Оценивание связывания N3-P[Lys(Глюконат)/Lys]-BPA
<Реагенты>
Соляная кислота 5 моль/л: Nacalai Tesque
Водный раствор гидроксида натрия 5 моль/л: Wako Pure Chemical Industries, Ltd.
Дигидрофосфат натрия (NaH2PO3): Nacalai Tesque
[10B-обогащенный] 4-бороно-L-фенилаланин (BPA): Katchem
Ализариновый красный С (ARS): Wako Pure Chemical Industries, Ltd.
D-фруктоза: Wako Pure Chemical Industries, Ltd.
D-глюкоза: Nacalai Tesque
D-сорбит: Tokyo Chemical Industry Co.
<Оборудование>
Флуоресцентный спектрофотометр (FP8300): JASCO Corporation
[0156]
Константу равновесия N3-P[Lys(Глюконат)/Lys] и BPA вычисляют с использованием способа ARS в соответствии со способом, описанным в публикации Springsteen G., Wang B. H. Tetrahedron 58, 5291-5300 (2002). Первоначально, приготавливают каждый из следующих растворов A, B, C, и D.
•Раствор A: ARS (9,0 × 10-6 M)
•Раствор B: ARS (9,0 × 10-6 M), BPA (2,0 × 10-3 M )
•Раствор C1: ARS (9,0 × 10-6 M), BPA (2,0 × 10-3 M), Сорбит (0,05 М)
•Раствор С2: ARS (9,0 × 10-6 M), BPA (2,0 × 10-3 M), Глюкоза (1,5 M)
•Раствор С3: ARS (9,0 × 10-6 M), BPA (2,0 × 10-3 M), Фруктоза (0,1 M)
•Раствор С4: ARS (9,0 × 10-6 M), BPA (2,0 × 10-3 M), N3-P[Lys(Глюконат)/Lys]_(A) (0,01 M: эталон глюконовой кислоты боковой цепи)
•Раствор С5: ARS (9,0 × 10-6 M), BPA (2,0 × 10-3 M), N3-P[Lys(Глюконат)/Lys]_(В) (0,01 M: эталон глюконовой кислоты боковой цепи)
•Раствор С6: ARS (9,0 × 10-6 M), BPA (2,0 × 10-3 M), N3-P[Lys(Глюконат)/Lys]_(С) (0,01 M: эталон глюконовой кислоты боковой цепи)
[0157]
Раствор А и Раствор В смешивают в различных соотношениях, и измеряют флуоресценцию с использованием одноразовых ячеек (PS, TGK) (Ex=468 нм, Em=572 нм). Константу равновесия К0 для ARS-BPA вычисляют на основе полученной интенсивности флуоресценции. Далее, Раствор В смешивают с Раствором C в различных соотношениях, и измеряют флуоресценцию с использованием одноразовых ячеек (Ex=468 нм, Em=572 нм). Кажущуюся константу связывания каждого соединения и BPA вычисляют с использованием этих результатов и вышеупомянутого значения К0. Результаты проиллюстрированы на ФИГ. 17.
[0158]
Установлено, что N3-P[Lys(Глюконат)Lys], синтезированный в ПРИМЕРЕ 18, имеет высокую прочность связывания с BPA. Прочность связывания является примерно в 4 раза выше, чем прочность связывания сорбита, который имеет высокую прочность связывания среди соединений сахаров, и примерно в 500 раз выше, чем прочность связывания глюкозы, которая часто присутствует в крови. На основании этих результатов, предполагают, что N3-P[Lys(Глюконат)Lys]-BPA будет проявлять высокую стабильность в крови.
[0159]
ПРИМЕР 20
Клеточный захват Cy5-P[Lys(Глюконат)/Lys]-BPA
(1) Синтез Cy5-P[Lys(Глюконат)/Lys]_(С)
100 мг (2,5 мкмоль) N3-P[Lys(Глюконат)/Lys]_(С), синтезированный в ПРИМЕРЕ 18 (2-3), взвешивают во флаконе объемом 6 мл и растворяют в 1,8 мл DMSO. Далее, к тому добавляют 224 мкл (2,8 мкмоль) раствора Cy5-DBCO/DMSO с концентрацией 12,5 мг/мл, и смесь перемешивают в течение ночи при комнатной температуре. Реакционный раствор помещают в ультрафильтрационную мембрану (MWCO=10 кД), к нему добавляют 10 мл воды сверхвысокой чистоты, и проводят ультрафильтрацию. Добавляют 15 мл воды сверхвысокой чистоты, и проводят ультрафильтрацию дополнительные два раза. Для дополнительной очистки очищенного ультрафильтрацией образца, образец очищают с использованием колонки PD-10 (GE Healthcare), раствор собранного образца лиофилизируют с испарением растворителя, и получают 97 мг Cy5-P[Lys(Глюконат)/Lys](С) в виде твердого вещества голубого цвета.
[0160]
(2) Оценивание клеточного захвата Cy5-P[Lys(Глюконат)/Lys]_(С)-BPA
Клетки BxPC-3 инокулируют в количестве 5 × 104 клеток/лунку на 8-луночный планшет (Система с камерой Lab-Tek из боросиликатного покровного стекла № 1,0) для исследований под микроскопом и инкубируют в течение ночи при 37°С в атмосфере 5%-ого СО2 (культуральная среда: RPMI-1640, содержащая 10% FBS и 1% Пенициллин-Стрептомицина). После инкубации, культуральную среду удаляют при помощи аспиратора, и добавляют 500 мкл растворов следующих образцов.
•Сорбит-BPA: BPA (3,03 мМ), Сорбит (3,64 мМ)/ культуральная среда 10% PBS-90% RPMI
•Cy5-P[Lys(Глюконат)/Lys](C)-BPA: BPA (3,03 мМ), Cy5-P[Lys(Глюконат)/Lys](C)·(3,64 мМ: эталон глюконовой кислоты боковой цепи)/культуральная среда 10% PBS-90% RPMI
Вышеупомянутые растворы образцов корректируют с доведением до 10-кратной концентрации с помощью фосфатного буферного раствора (10 мМ NaH2PO4, 140 мМ NaCl, pH 7,4) и затем разбавляют культуральной средой RPMI перед использованием. К этому добавляют растворы образцов и затем инкубируют в течение 1 часа. После этого, растворы образцов удаляют с помощью аспиратора, и добавляют 20 мкМ DAHMI, раствор ‘50 нМ LysoTracker Зеленый/PBS’ (500 мкл), и проводят инкубирование в течение 30 минут. После этого, растворы удаляют с помощью аспиратора и проводят промывание три раза посредством 500 мкл PBS. После трехкратного промывания, к этому добавляют 500 мкл PBS, и затем изучают флуоресценцию с помощью конфокального микроскопа. Результаты проиллюстрированы на ФИГ. 18.
[0161]
В результате наблюдения под микроскопом, подтверждено, что Cy5-P[Lys(Глюконат)/Lys](C) является локализованным в эндосоме, не во всей цитоплазме. Поскольку Cy5-P[Lys(Глюконат)/Lys](C) локализуется вместе с BPA, это позволяет предположить, что Cy5-P[Lys(Глюконат)/Lys](C)-BPA внедряется в клетки в результате эндоцитоза.
[0162]
ПРИМЕР 21
Фармакокинетика N3-P[Lys(Глюконат)/Lys]-BPA и сорбит-BPA
<Реагенты, клетки, и животные>
N3-P[Lys(Глюконат)/Lys]_(A), N3-P[Lys(Глюконат)/Lys]_(B), N3-P[Lys(Глюконат)/Lys]_(C) и mPEG10k-P[Lys(Глюконат)/Lys], синтезированные в ПРИМЕРЕ 18
D-сорбит: Tokyo Chemical Industry Co.
Соляная кислота 5 моль/л: Nacalai Tesque
Гидроксид натрия 5 моль/л (для масс-спектрометрии): Wako Pure Chemical Industries, Ltd.
L-4-боронофенил-аланин (BPA): Katchem
Азотная кислота (1,42): Wako Pure Chemical Industries, Ltd.
Клетки CT26 (клеточная линия рака толстой кишки мышей): Американская коллекция типовых культур (Manassas, VA)
Мышь BALB/c: Charles River Japan
<Оборудование>
Прибор для ICP-MS Agilent 7900: Agilent Technology Co., Ltd.
Установка нейтронного облучения с использованием тяжелой воды: KUR
[0163]
Модели подкожной опухоли получают подкожной инъекцией клеток CT26 мышам BALB/c в количестве 1,0 × 105 клеток/мышь. Как только размер опухоли достигает примерно 200 мм3, 200 мкл растворов следующих образцов (рН 7,4) вводят через хвостовую вену (10 мг BPA/мышь). Растворы следующих образцов приготавливают путем растворения сахара или полимера и BPA в соответственном количестве воды сверхвысокой чистоты, добавления водного раствора гидроксида натрия и получения щелочного раствора, полного растворения растворяемого вещества и затем добавления соляной кислоты с доведением рН до 7,4, добавления воды сверхвысокой чистоты, разбавления растворов до конечных концентраций, приведенных ниже, и проведения стерилизации фильтрацией с использованием фильтра с размером ячеек 0,22 мкм.
•N3-P[Lys(Глюконат)/Lys]_(A)-BPA (BPA 240 мМ)
•N3-P[Lys(Глюконат)/Lys]_(В)-BPA (BPA 240 мМ)
•N3-P[Lys(Глюконат)/Lys]_(С)-BPA (BPA 240 мМ)
•mPEG10k-P[Lys(Глюконат)/Lys]-BPA (BPA 240 мМ)
•Сорбит-BPA (BPA 240 мМ, Сорбит 288 мМ)
[0164]
Через три часа после введения образца, мышей препарируют, и опухоли удаляют. Опухоли помещают в пробирку объемом 14 мл (кругло-донная пробирка PP, Falcon), и добавляют 1 мл азотной кислоты (1,42). После этого, каждый образец инкубируют при 50°С в течение 15 минут, 70°С в течение 15 минут, и 90°С в течение 1 часа. Добавляют воду сверхвысокой чистоты вплоть до 10 мл. После фильтрации через гидрофобный фильтр, оценивают количество бора с использованием ICP-MS. Результаты фармакокинетического анализа в отношении мышей с трансплантированными клетками CT-26 проиллюстрированы на ФИГ. 19.
[0165]
ПРИМЕР 22
Противоопухолевое действие N3-P[Lys(Глюконат)/Lys]-BPA
Клетки СT-26 подкожно имплантируют (1,0 × 105 клеток/ мышь) около правого бедра мышей BALB/ c, и 200 мкл следующих образцов медленно вводят через хвостовую вену мышей, имеющих размер опухоли приблизительно 50-100 мм3, (10 мг BPA/мышь).
•N3-P[Lys(Глюконат)/Lys](В)-BPA (BPA 240 мМ)
•N3-P[Lys(Глюконат)/Lys](С)-BPA (BPA 240 мМ)
•Сорбит-BPA (BPA 240 мМ, Сорбит 288 мМ)
[0166]
В группе нейтронного облучения, нейтронное облучение проводят в течение 50 минут только вокруг правого бедра мыши через 2,5 часа после введения образца. С учетом дня облучения, установленного в качестве первого дня, диаметр опухоли измеряют каждые 2-3 дня с помощью электронных циркулей, и массу тела измеряют с помощью электронных весов в течение всех 30 дней. Измеренный диаметр опухоли используют в формуле эллиптической аппроксимации объема (ab2 × 1/2, где a представляет собой длинную сторону, и b означает короткую сторону), что дает объем опухоли. Оцененные группы сведены вместе ниже (n=6).
[0167]
Контрольная группа (ХОЛОДНАЯ): необработанная группа.
Контрольная группа (ГОРЯЧАЯ): выполнено только облучение нейтронами.
Сорбит-BPA (ГОРЯЧАЯ): сделана инъекция посредством сорбит-BPA, затем выполнено облучение нейтронами через 2,5 часа после этого.
N3-P[Lys(Глюконат)/Lys](В)-BPA (ГОРЯЧАЯ): сделана инъекция посредством N3-P[Lys(Глюконат)/Lys](В)-BPA, затем выполнено облучение нейтронами через 2,5 часа после этого.
N3-P[Lys(Глюконат)/Lys](С)-BPA (ГОРЯЧАЯ): сделана инъекция посредством N3-P[Lys(Глюконат)/Lys](С)-BPA, затем выполнено облучение нейтронами через 2,5 часа после этого.
[0168]
Изменение размера опухоли с течением времени и кривые Каплана-Мейера в отношении этого показаны на ФИГУРАХ 20 и 21 (кривую выживаемости строят с объемом опухоли 1600 мм3 в качестве конечной точки). Сорбит-BPA, N3-P[Lys(Глюконат)/Lys](B)-BPA (ГОРЯЧАЯ ГРУППА) и N3-P[Lys(Глюконат)/Lys](С)-BPA (ГОРЯЧАЯ ГРУППА) показывают более сильное противоопухолевое действие и более высокие показатели выживаемости по сравнению с контрольными группами (Контрольная группа (ХОЛОДНАЯ) и Контрольная группа (ГОРЯЧАЯ)). Кроме того, N3-P[Lys(Глюконат)/Lys](С)-BPA (ГОРЯЧАЯ) показывает более высокий показатель выживаемости по сравнению с другими группами.
[0169]
ПРИМЕР 23
Синтез P[VA(RGD)VA]
Циклический пептид RGDfK, имеющий сильное сродство к интегрину αvβ3, который, как сообщается, сверхэкспрессируется в связанных с опухолью кровеносных сосудах и в опухолевых клетках, вводят в боковую цепь PVA.
[Хим. стр. 90]
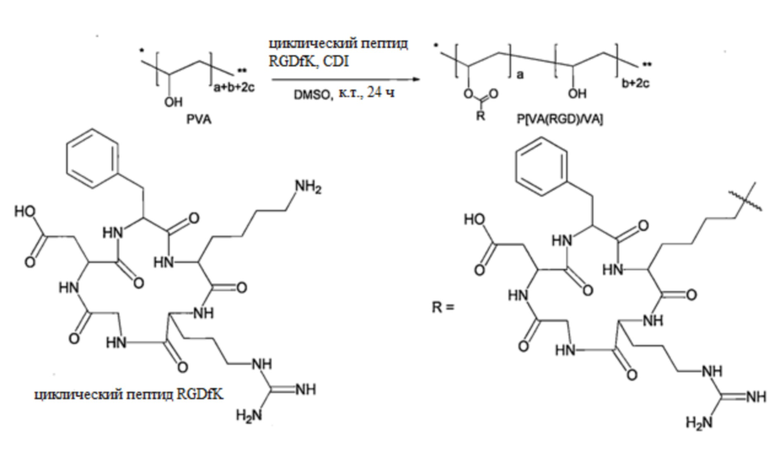
[0170]
<Реагенты>
Если не задано иное, то коммерчески доступные реагенты и растворители используют так, как они есть.
PVA (Mn=9200): синтезированный согласно способу ПРИМЕРА 1 (2).
Циклический пептид RGDfK: приобретенный в Synpeptide
CDI: приобретенный в Sigma Aldrich
DMSO: приобретенный в Wako Pure Chemical Industries, Ltd.
DMSO-d6: приобретенный в Wako Pure Chemical Industries, Ltd.
[0171]
100 мг PVA и 17,7 мг CDI растворяют в 10 мл DMSO, и смесь перемешивают при комнатной температуре в течение 2 часов. После этого, к тому добавляют 19,7 мг циклического пептида RGDfK, и перемешивают в течение 24 часов при комнатной температуре. Продукт диализируют против воды три раза. После диализа, образец лиофилизируют и собирают. Результаты 1H-NMR-анализа показывают, что один или два циклических пептида RGDfK связан(-ы) с одним полимером.
[Хим. стр. 91]
1Н-ЯМР (400 МГц, DMSO-d6): δ 7,28-7,12 (Ph-H циклического RGDfK), 4,76-4,18 (-ОН), 4,08-3,75 (-СНСН2- основной цепи полимера), 4,7-3,5 (СНα циклического RGDfK), 1,78-1,08 (-СНСН2- основной цепи полимера), 1,8-1,4 (-СН2СН2СН2NH-).
[0172]
ПРИМЕР 24
Оценивание накопления в опухоли P[VA(RGD)/VA]-BPA
<Реагенты, клетки, и животные>
P[VA(RGD)/VA]: полученный в ПРИМЕРЕ 23
BPA: KatChem
Клетки BxPC3: Американская коллекция типовых культур (Manassas, VA)
‘Голая’ (бестимусная) мышь BALB/c: Charles River Japan
[0173]
Клетки BxPC3 подкожно вводят инъекцией ‘голым’ мышам BALB/c в количестве 5 × 106 клеток/мышь. Как только размер опухоли достигает примерно 200 мм3, следующий образец внутривенно вводят инъекцией (8 мг BPA/мышь).
P[VA(RGD)/VA]-BPA (концентрация BPA: 191 мМ, концентрация диола P[VA(RGD)/VA]: 91 мМ) в PBS (рН 10)
[0174]
По истечении шести часов после внутривенной инъекции, мышей подвергают эвтаназии с применением цервикальной дислокации, и затем препарируют с удалением опухолей. Опухоли помещают в пробирку фирмы Falcon объемом 10 мл, и добавляют 1 мл 70%-ой азотной кислоты. После этого, каждый образец инкубируют при 50°С в течение 15 минут, 70°С в течение 15 минут, и при 90°С в течение 1 часа. Образцы разбавляют до 10 мл чистой водой, фильтруют через гидрофобный фильтр, затем оценивают количество бора с использованием ICP-MS. В результате, P[VA(RGD)/VA]-BPA показывает высокое накопление, составляющее 6,2 ± 2,4% дозы/г опухоли, в опухоли даже через 6 часов после введения.
ПРОМЫШЛЕННАЯ ПРИМЕНИМОСТЬ
[0175]
Согласно настоящему изобретению, можно доставлять большое количество бора селективным в отношении опухоли образом в BNCT. Кроме того, это может быть применено к модифицированному фтором BPA в качестве диагностического агента и также может быть использовано в качестве диагностического агента на основе бора.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ И СПОСОБ ДВОЙНОГО НАЦЕЛИВАНИЯ ПРИ ЛЕЧЕНИИ НЕЙРОЭНДОКРИННЫХ ОПУХОЛЕЙ | 2019 |
|
RU2789198C2 |
| ПРОИЗВОДНЫЕ АМАТОКСИНА | 2014 |
|
RU2695370C2 |
| КОМПОЗИЦИИ И СПОСОБЫ, ОТНОСЯЩИЕСЯ К КОНЪЮГАТАМ ЛЕКАРСТВЕННЫХ СРЕДСТВ С АНТИТЕЛАМИ ПРОТИВ CD19 | 2019 |
|
RU2806333C2 |
| КОМПОЗИЦИЯ ПРОТИВОРАКОВОЙ ВАКЦИНЫ, СОДЕРЖАЩАЯ ПЕПТИД WT1, ДЛЯ ТРАНСДЕРМАЛЬНОГО ВВЕДЕНИЯ | 2014 |
|
RU2685933C2 |
| БИЛИГАНДНЫЙ КОНЪЮГАТ ЛЕКАРСТВЕННОГО СРЕДСТВА И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2820346C2 |
| ПРОИЗВОДНОЕ ПИРАЗОЛА | 2014 |
|
RU2632884C2 |
| КОНЪЮГАТ ФЛУОРЕСЦЕНТНОГО КРАСИТЕЛЯ С ВЕЩЕСТВОМ ПЕПТИДНОЙ ПРИРОДЫ, ВКЛЮЧАЮЩИМ ПСМА-СВЯЗЫВАЮЩИЙ ЛИГАНД НА ОСНОВЕ ПРОИЗВОДНОГО МОЧЕВИНЫ ДЛЯ ВИЗУАЛИЗАЦИИ КЛЕТОК, ЭКСПРЕССИРУЮЩИХ ПСМА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2019 |
|
RU2713151C1 |
| КОНЪЮГАТЫ ДИСОРАЗОЛОВ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ, НАЗВАННЫЕ КОНЪЮГАТЫ ДЛЯ ИЗГОТОВЛЕНИЯ ЛЕКАРСТВЕННОГО СРЕДСТВА, НАБОР И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2007 |
|
RU2473562C2 |
| КОМПЛЕКС ПРОИЗВОДНОГО МОЧЕВИНЫ С РАДИОНУКЛИДНОЙ МЕТКОЙ Tс ДЛЯ ДИАГНОСТИКИ ОПУХОЛЕЙ, ЭКСПРЕССИРУЮЩИХ ПРОСТАТСПЕЦИФИЧЕСКИЙ МЕМБРАННЫЙ АНТИГЕН, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2023 |
|
RU2825402C1 |
| КОМПОЗИЦИЯ ПРОТИВОРАКОВОЙ ВАКЦИНЫ, СОДЕРЖАЩЕЙ ПЕПТИД WT1, ДЛЯ ТРАНСДЕРМАЛЬНОГО ВВЕДЕНИЯ | 2014 |
|
RU2687144C2 |

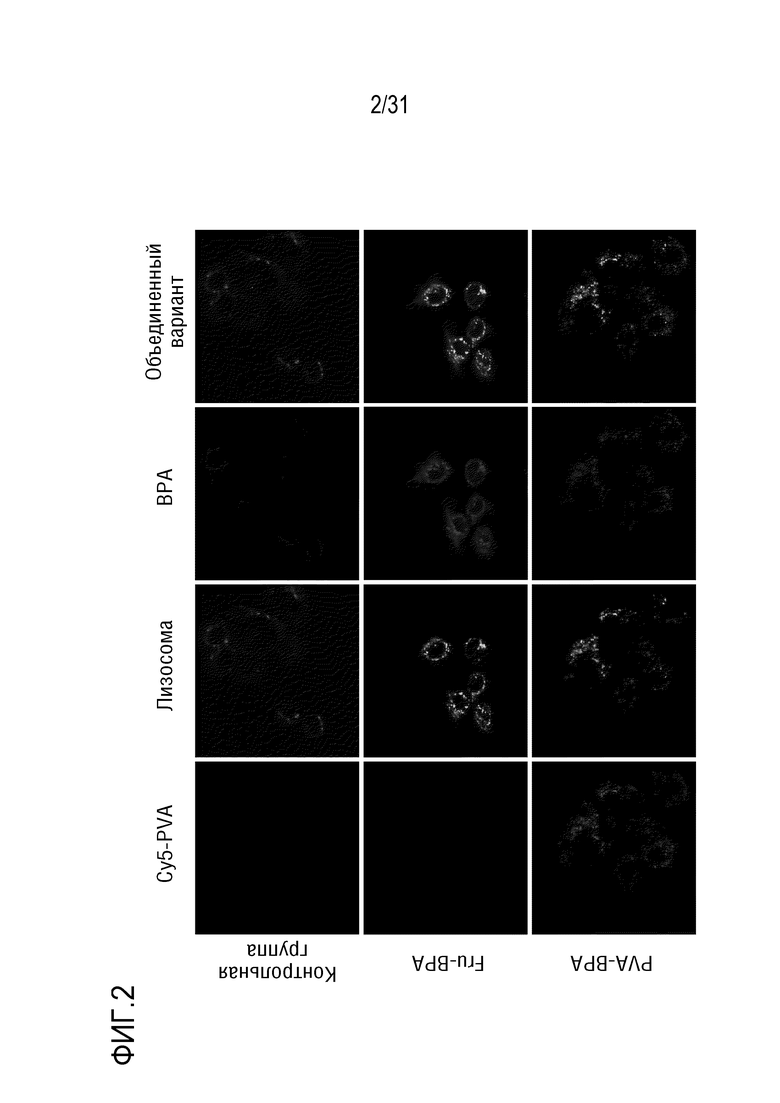
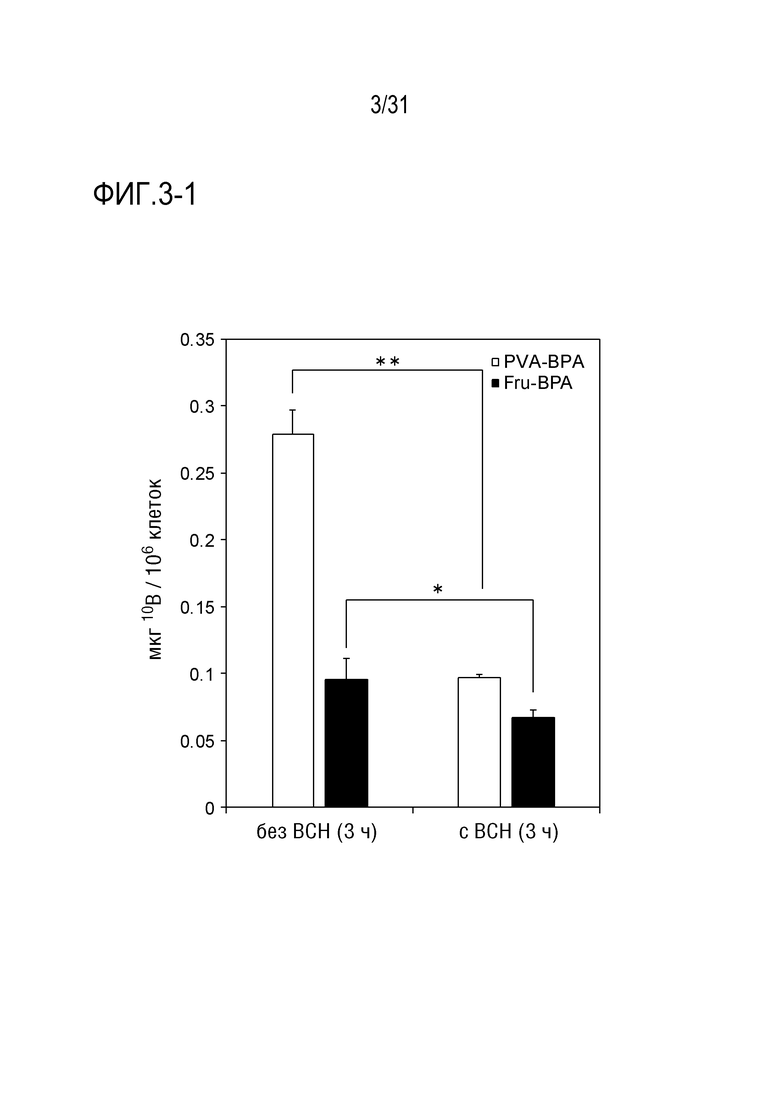
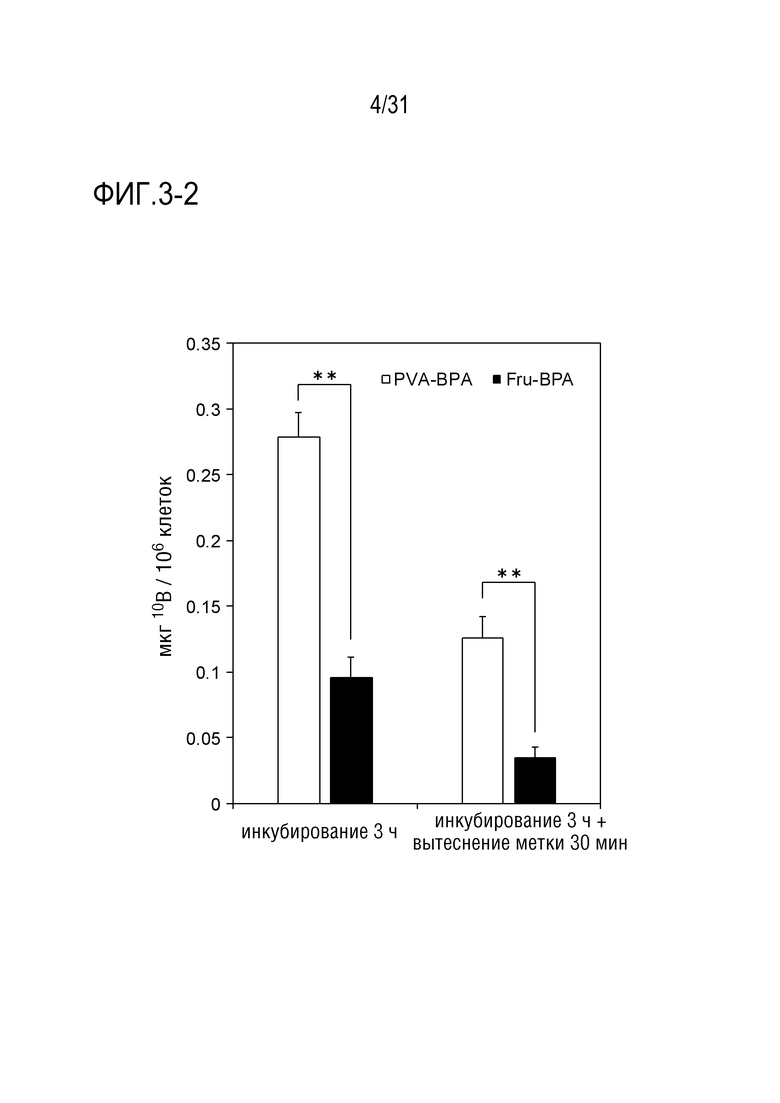
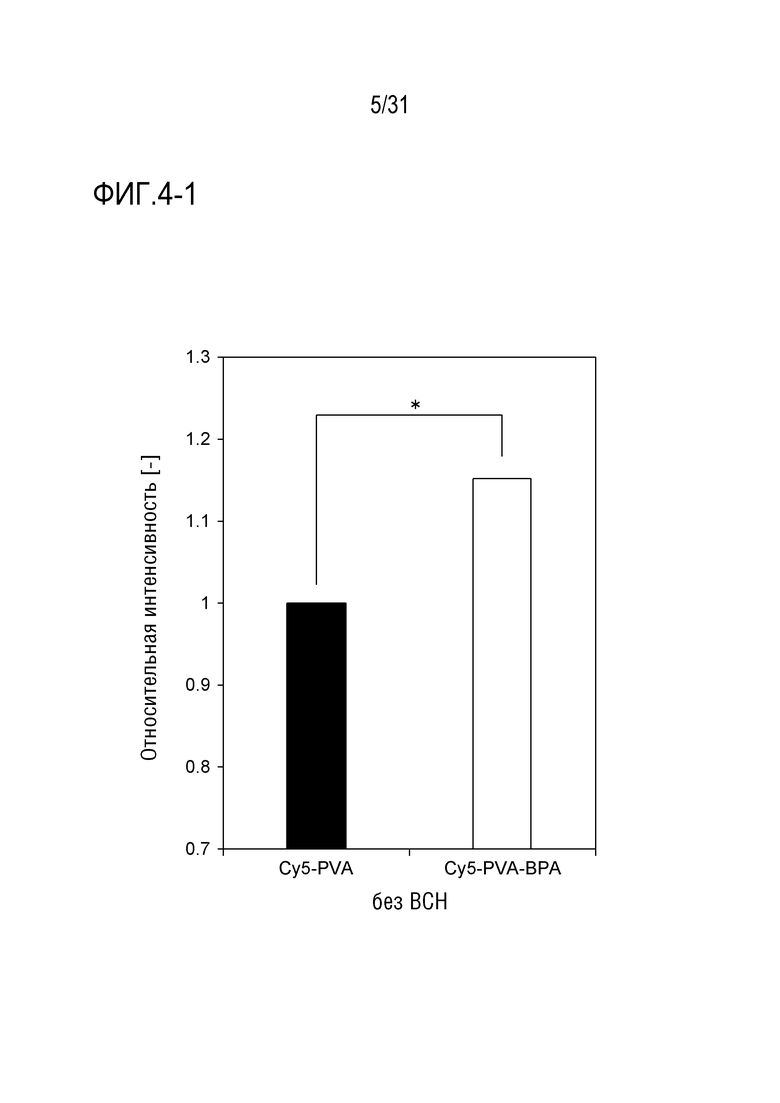
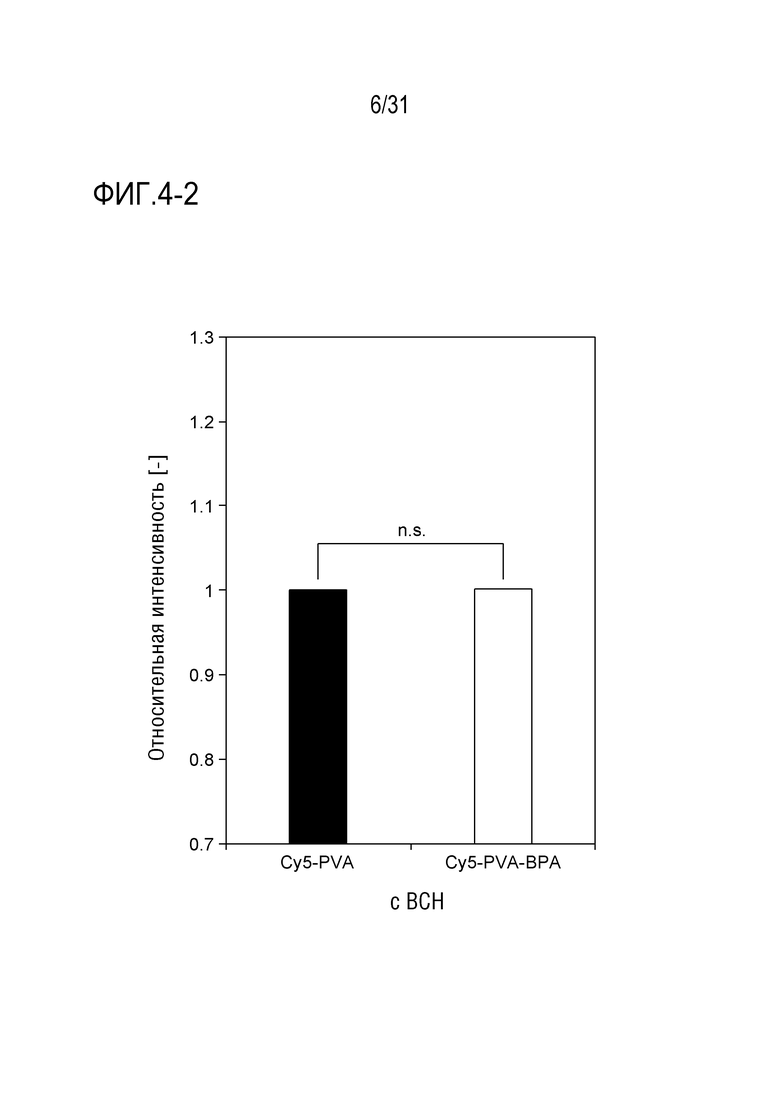
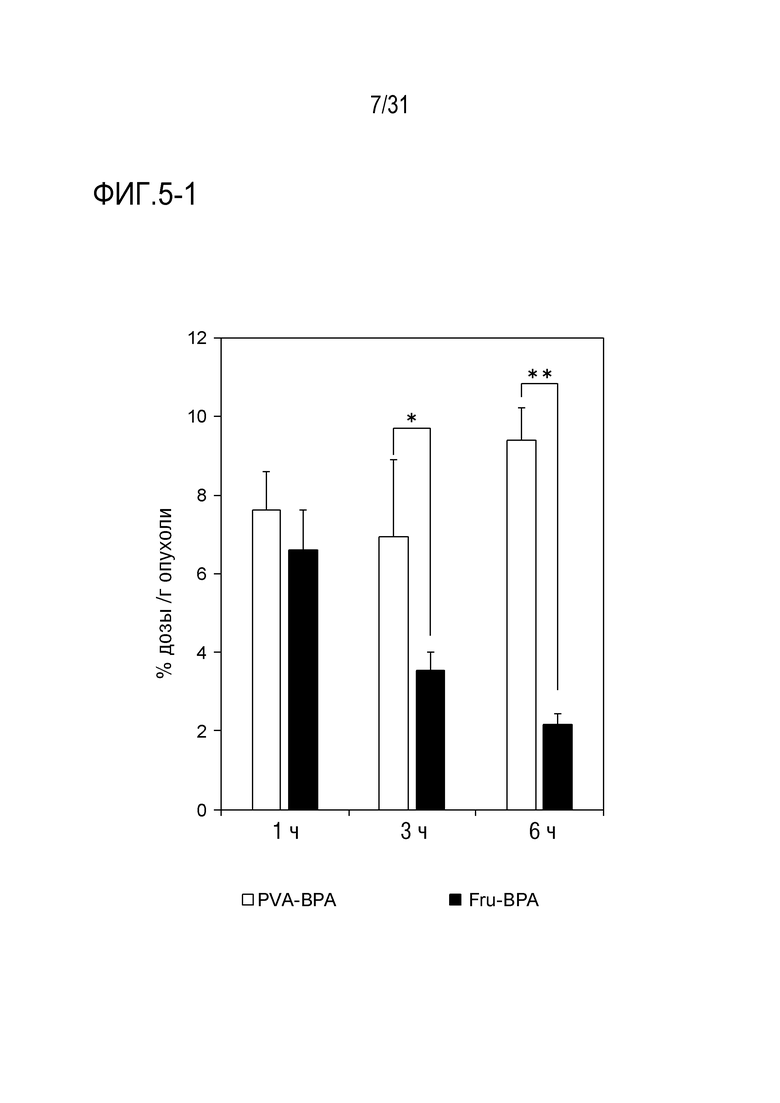
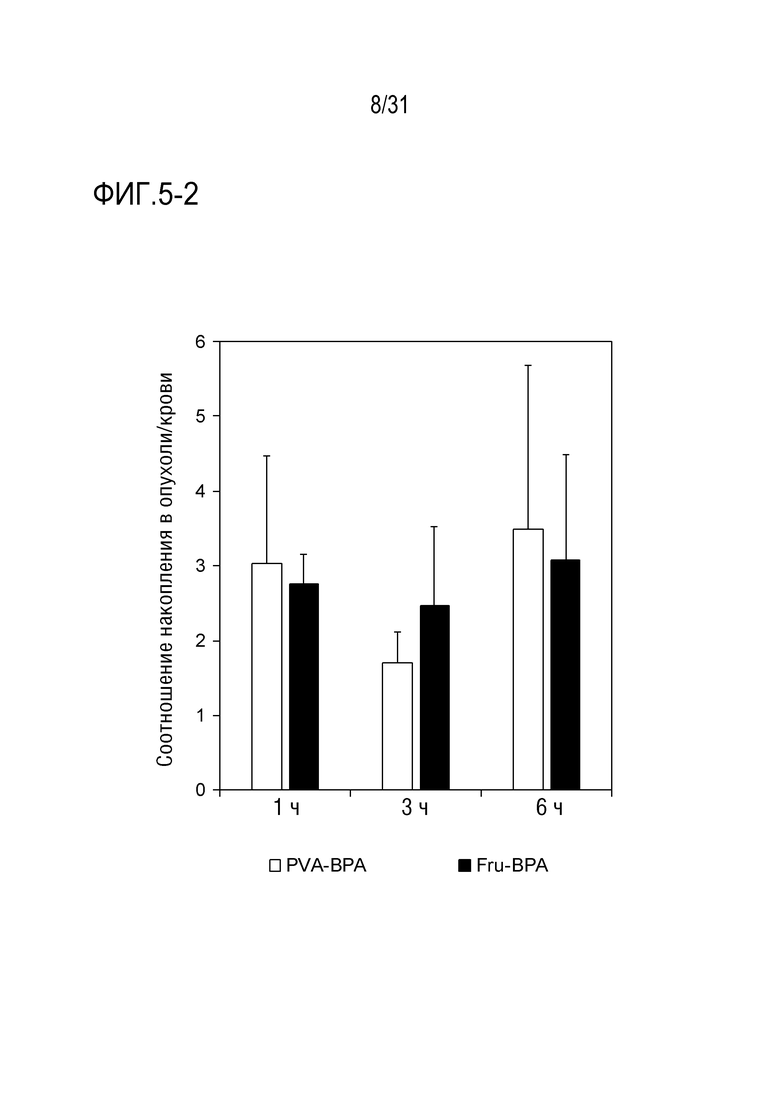
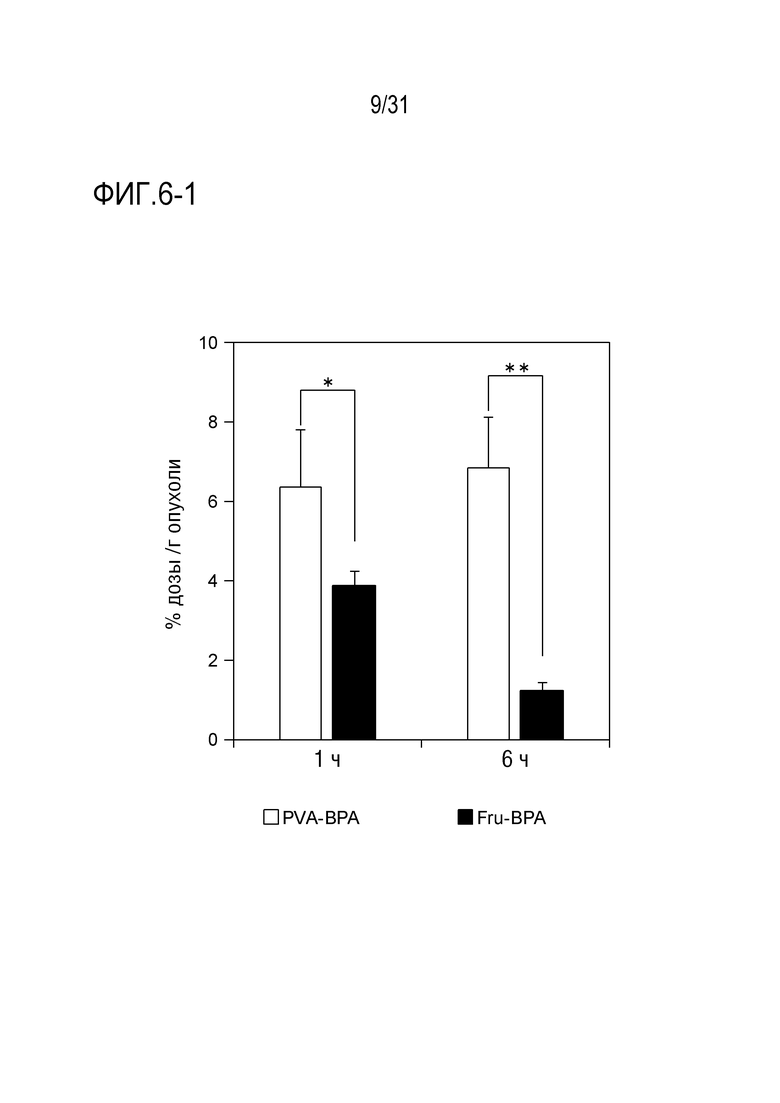
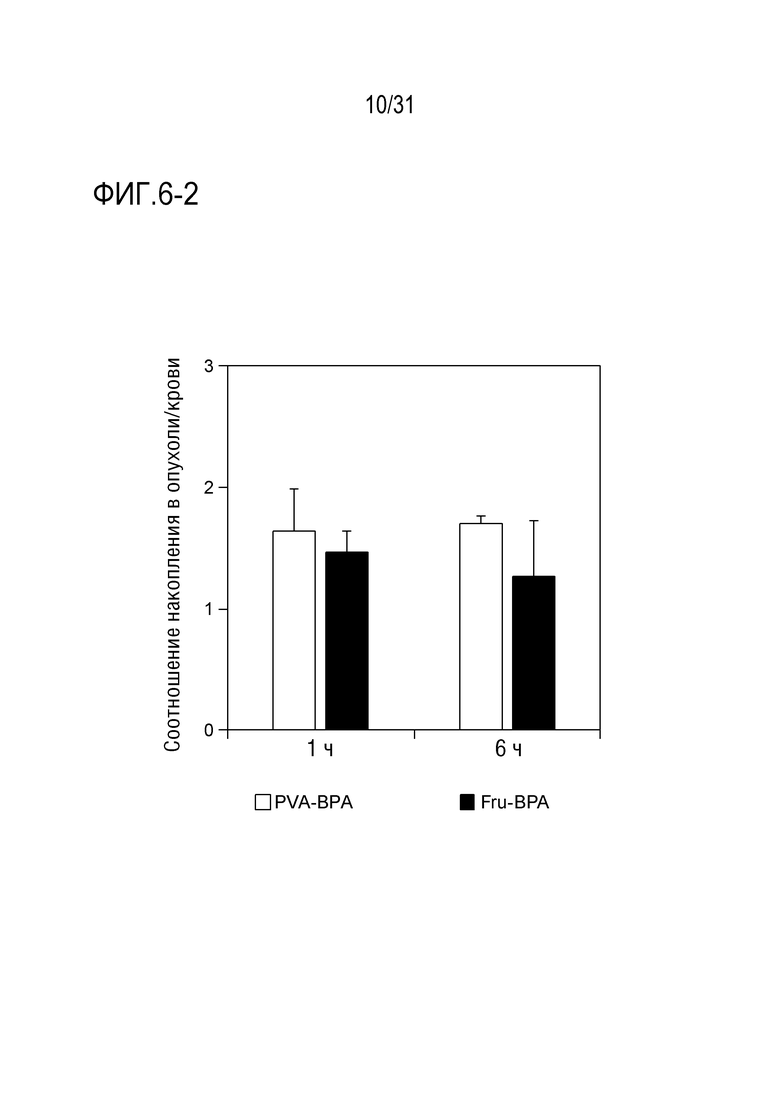

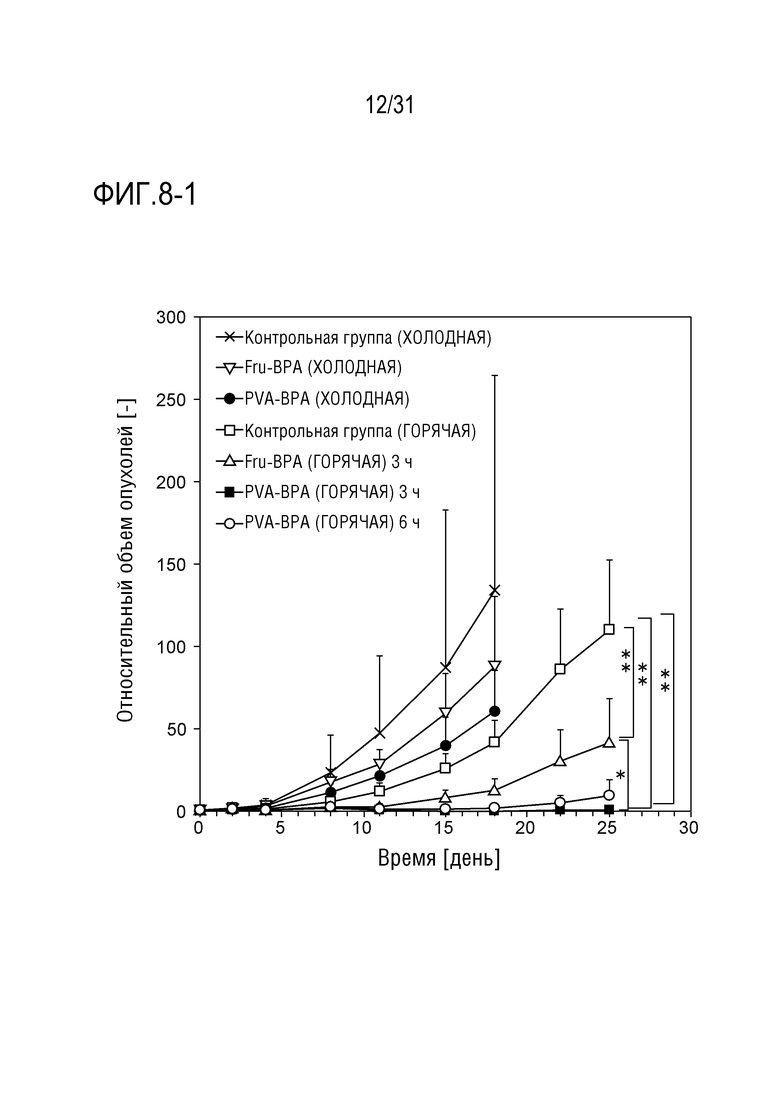
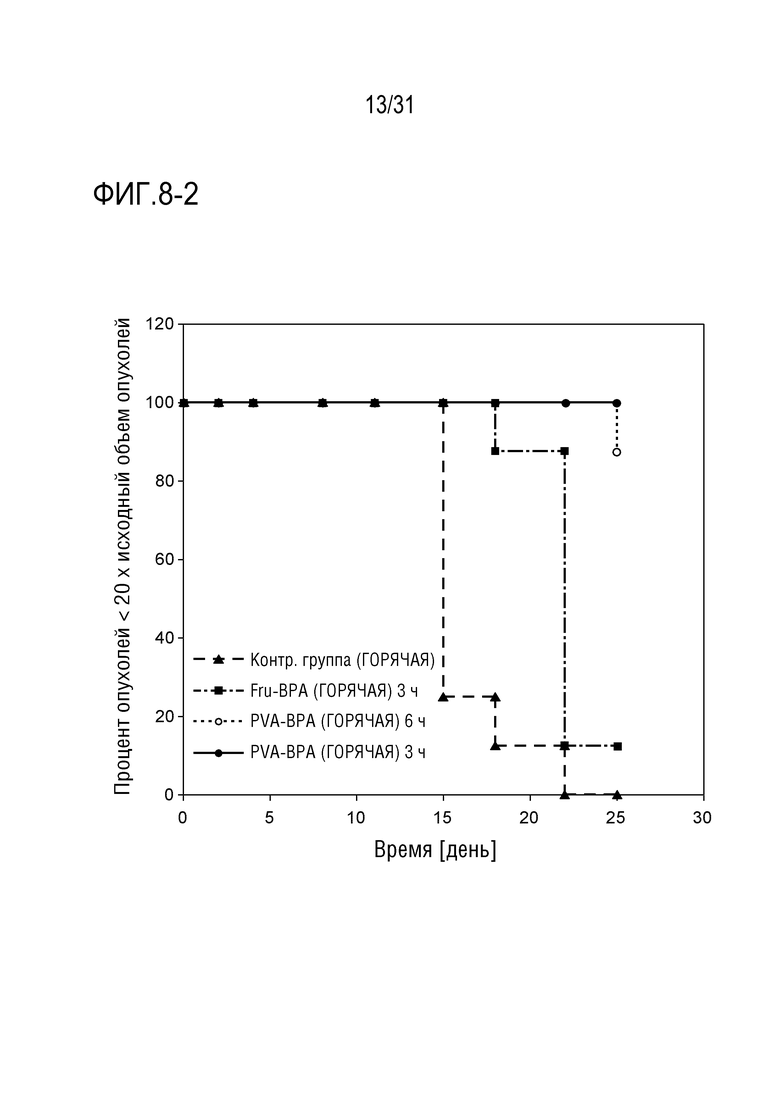
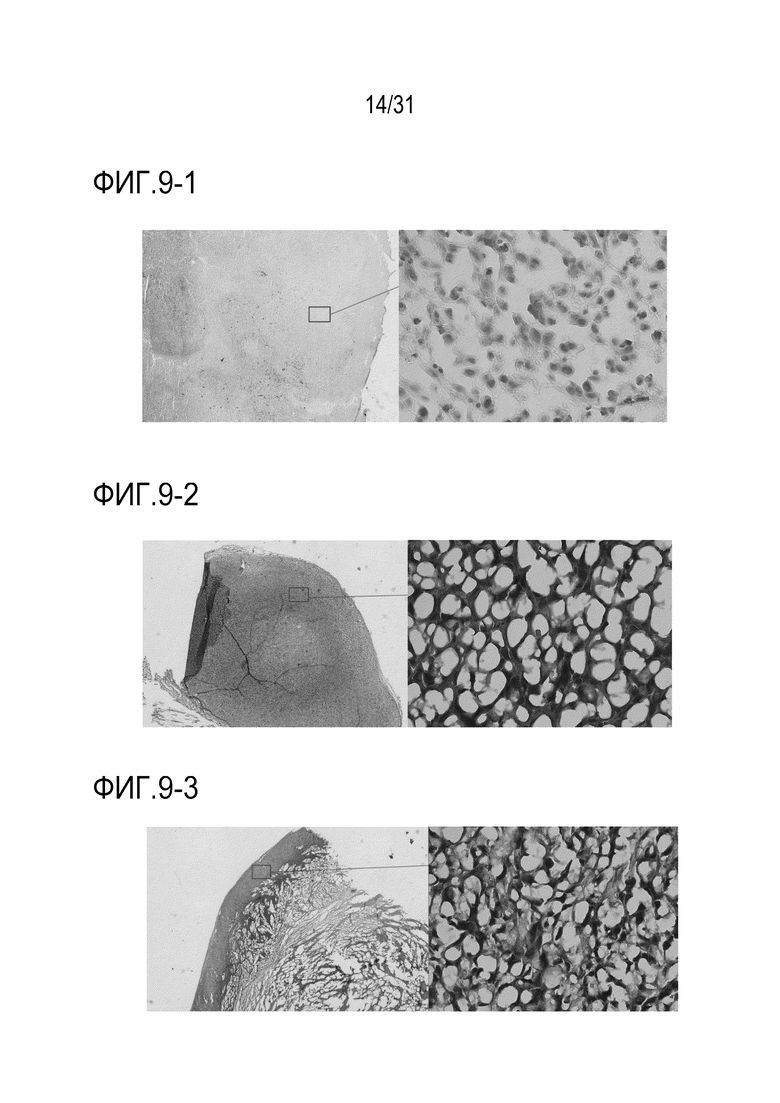

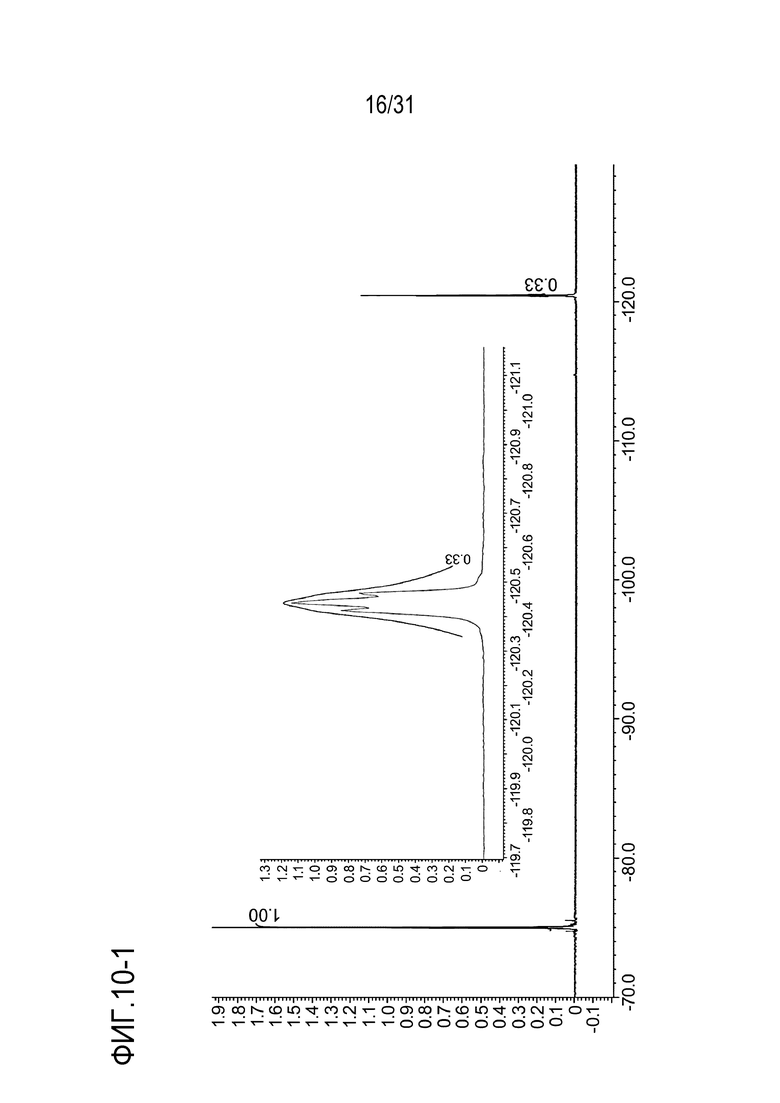


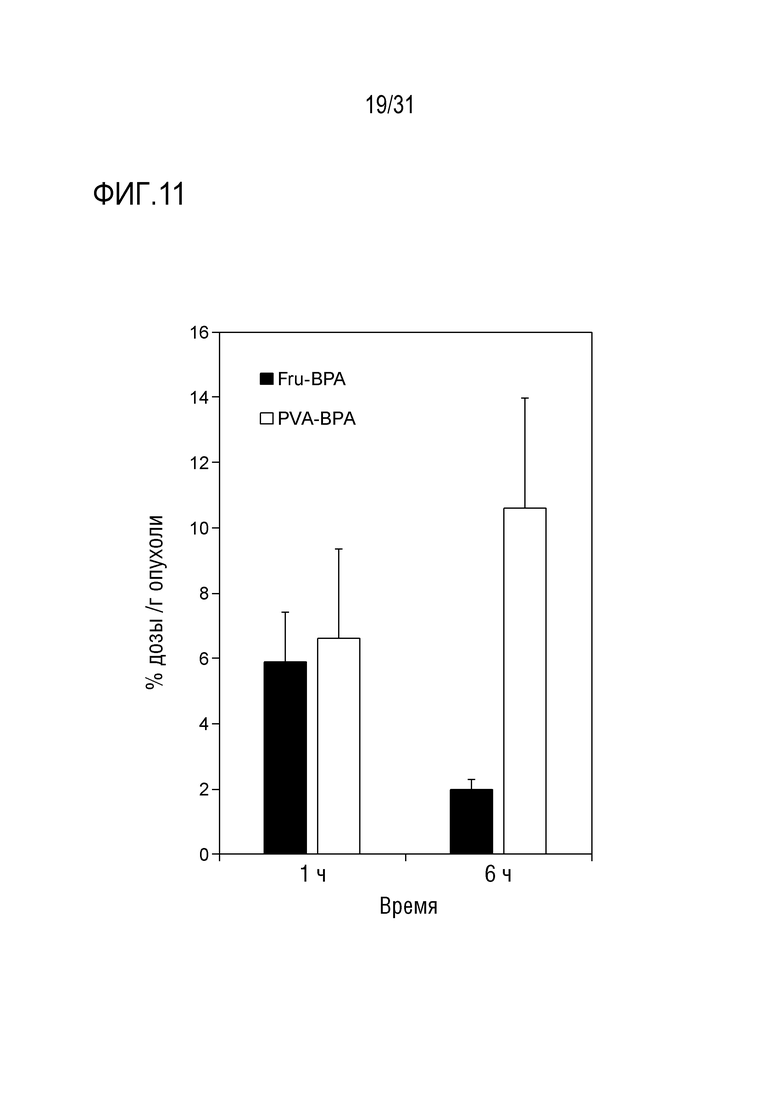
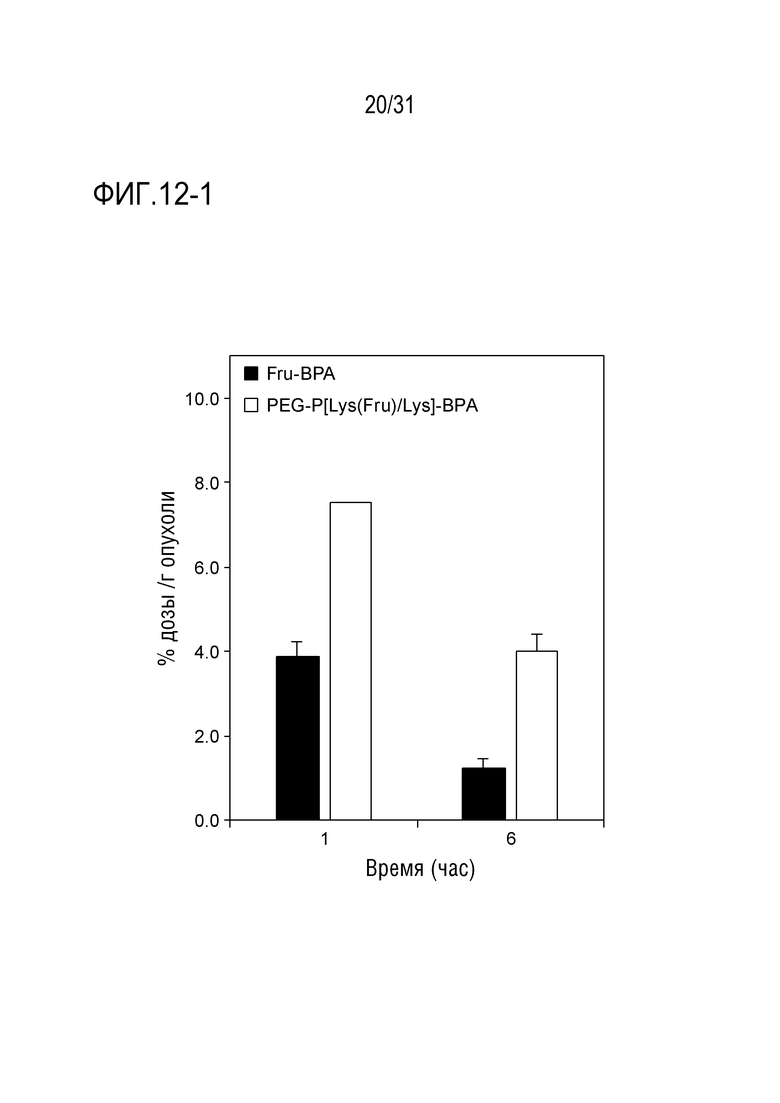
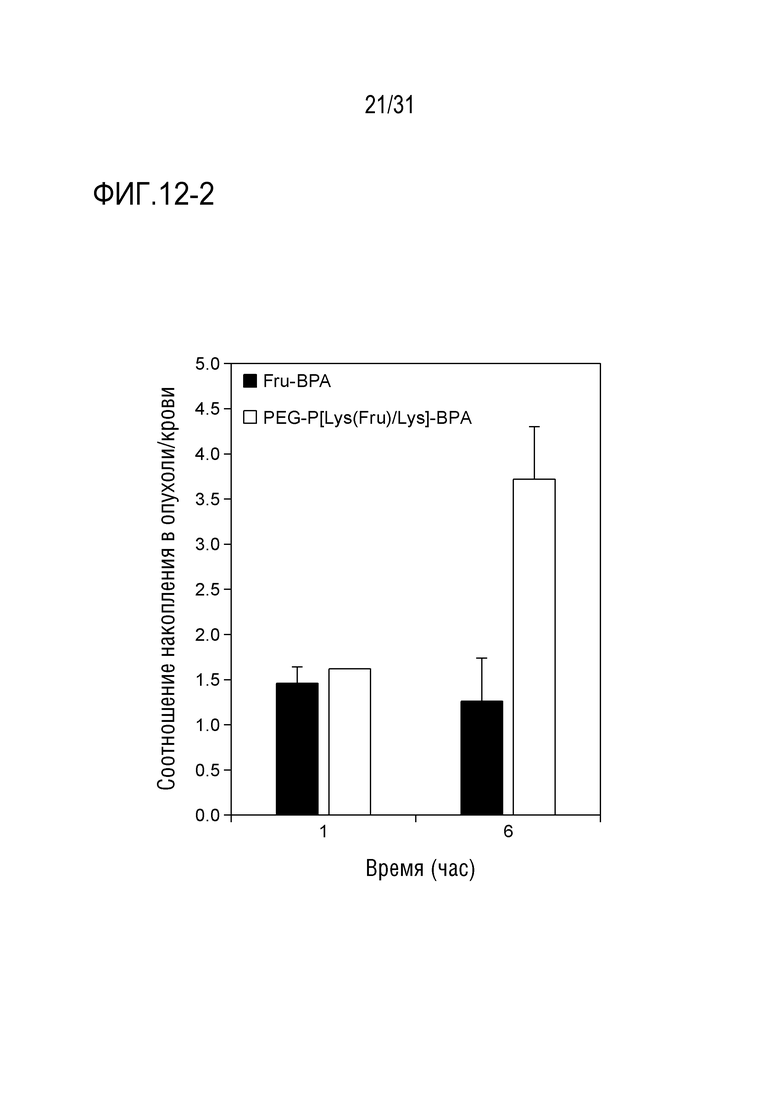
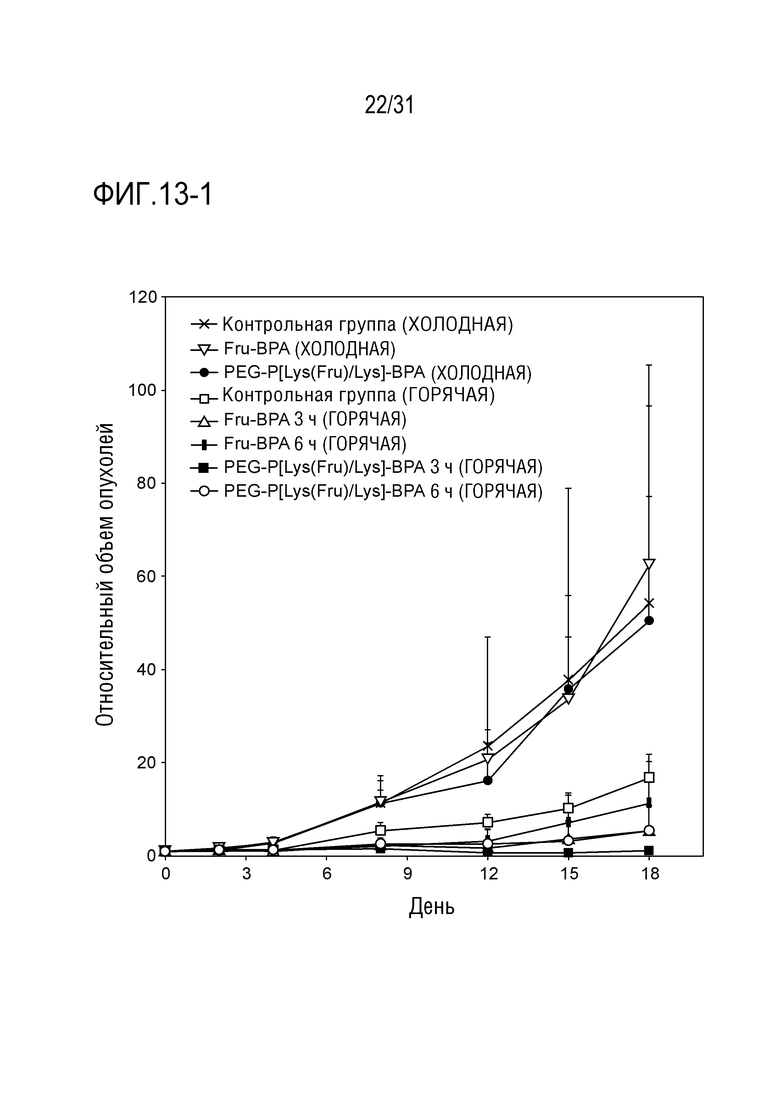
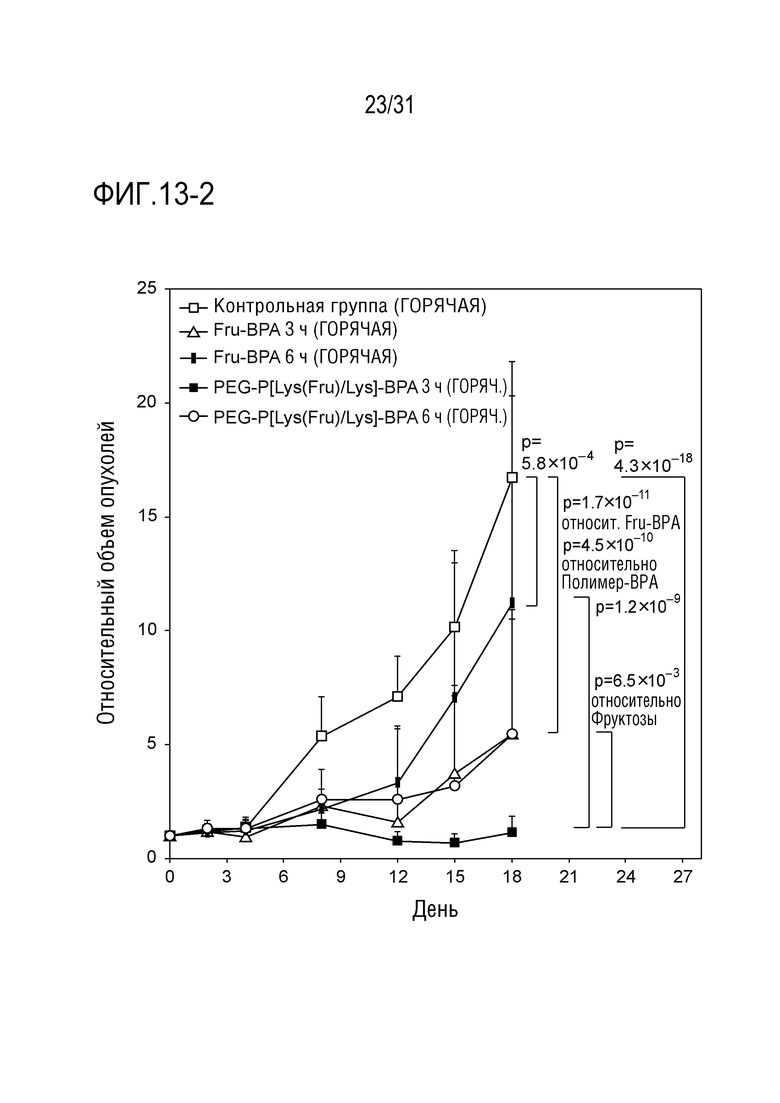
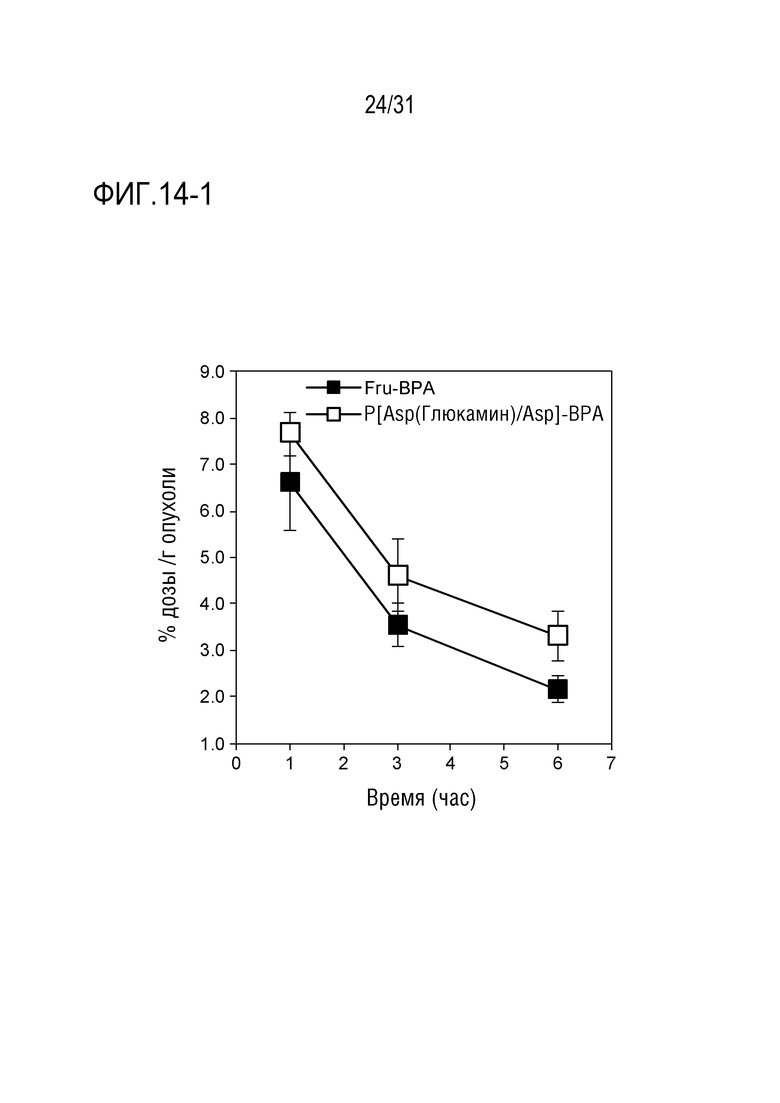
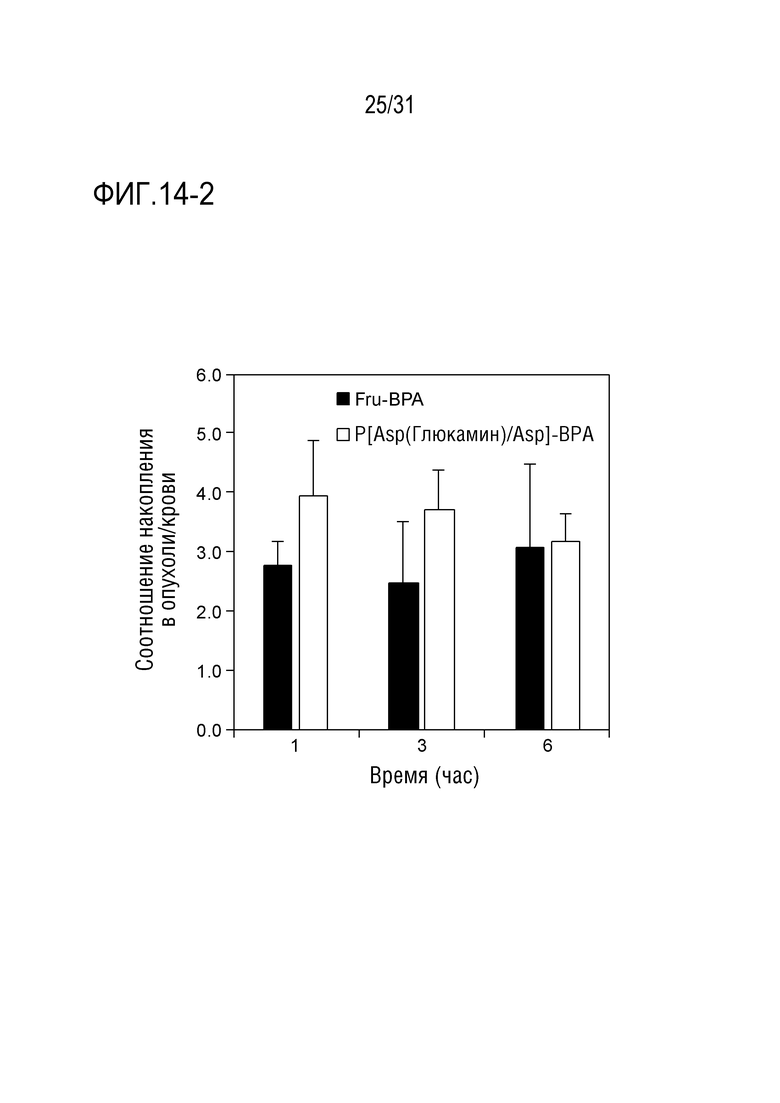
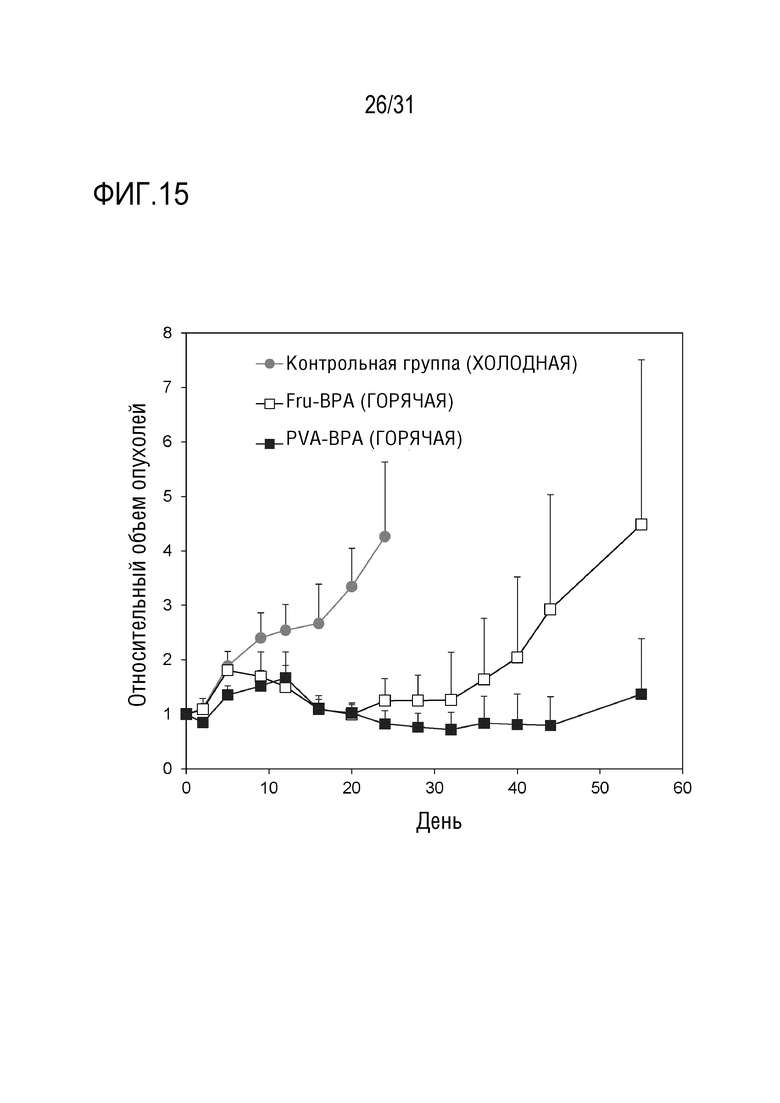
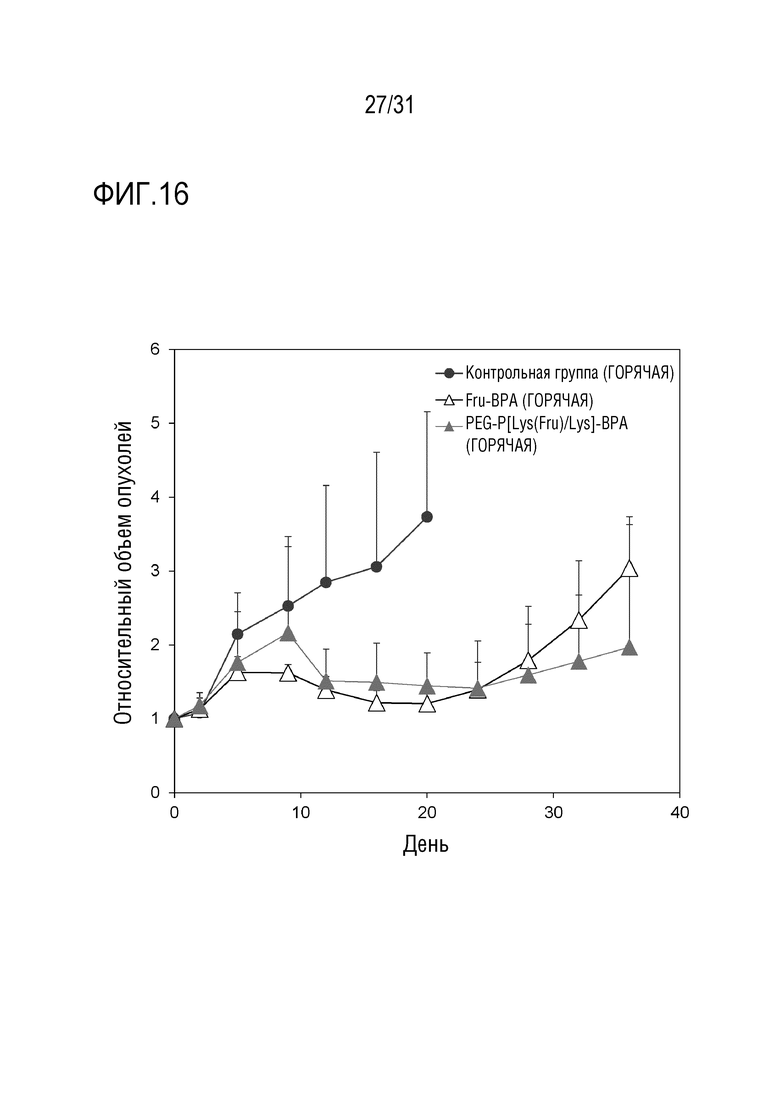

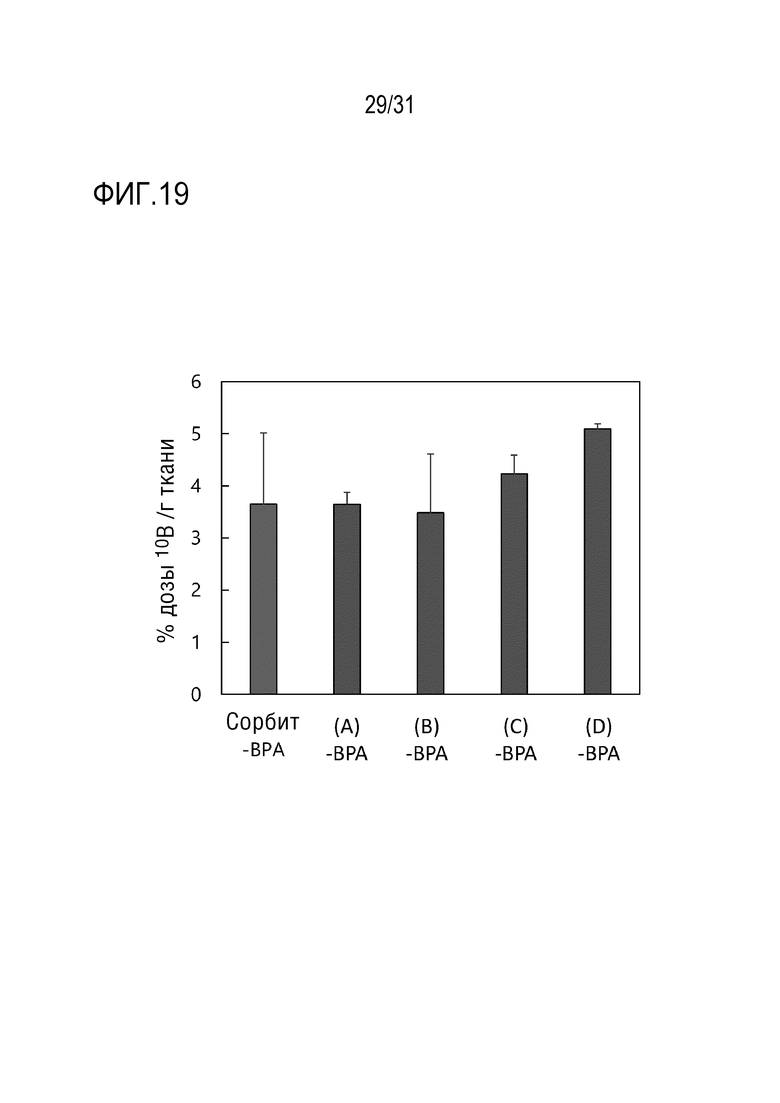
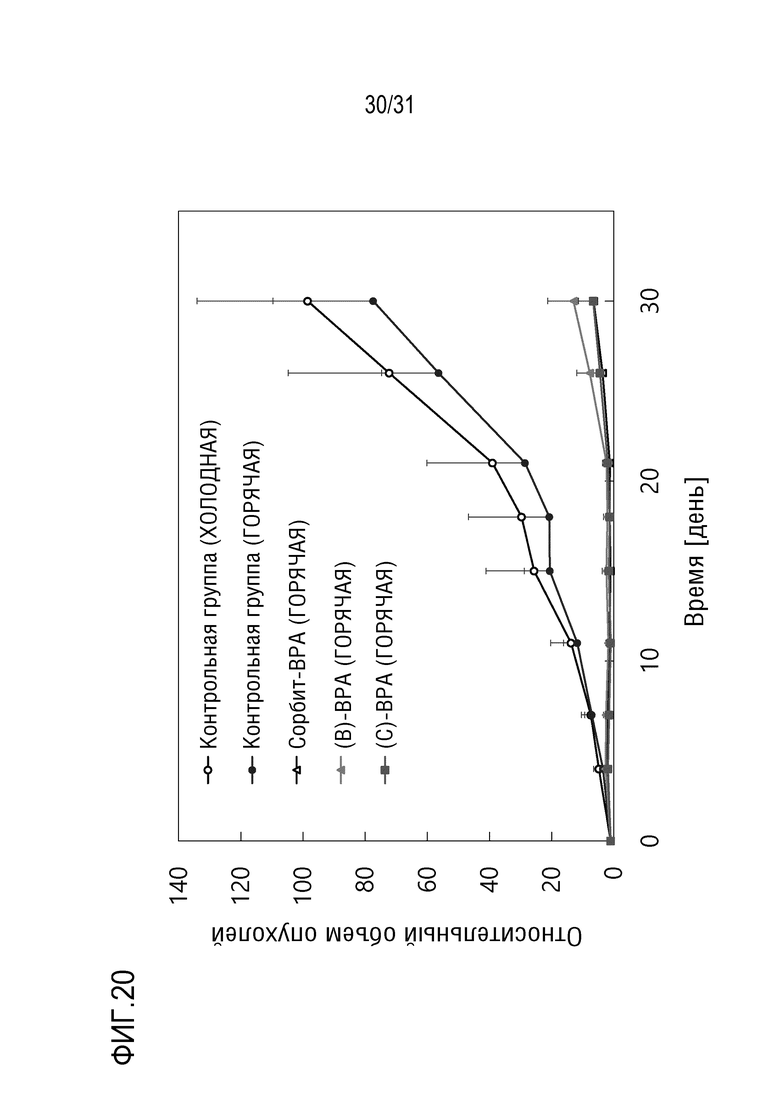
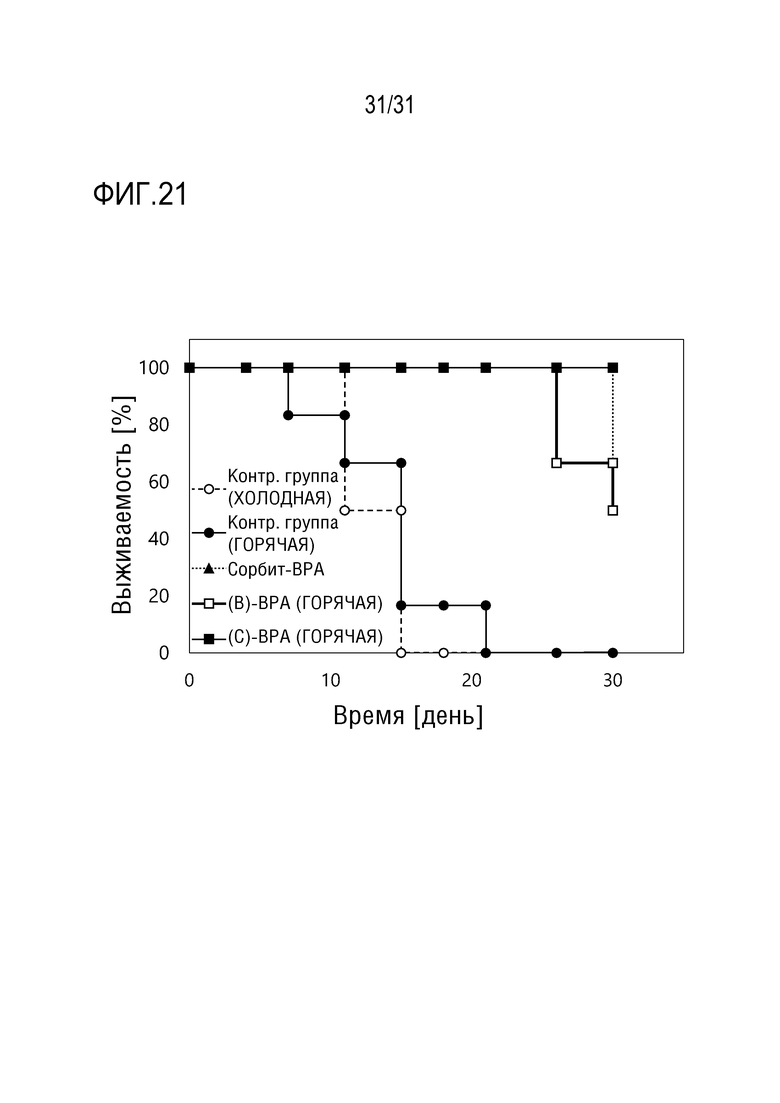
Изобретение относится к производному пара-борфенилаланина, включающему полимер, связанный, либо непосредственно, либо через линкер, с группой, представленной формулой (I). В формуле (I): стрелки показывают связь со смежным атомом, X1-X4 представляют собой, каждый независимо, Н, 18F или 19F. При этом полимер выбирают из группы, состоящей из поливинилового спирта, простого полиэфира и полипептида, и среднечисловая молекулярная масса производного пара-борфенилаланина составляет 1000 Да или более. Также предложены фармацевтические композиции, содержащие производное пара-борфенилаланина, и набор для получения фармацевтических композиций. Изобретение позволяет реализовать селективное накопление и длительное удерживание бора в опухолях, при одновременном достижении превосходного соотношения концентраций бора в опухолевых/нормальных тканях и соотношения концентраций бора в опухоли/крови. 4 н. и 8 з.п. ф-лы, 34 ил., 1 табл., 24 пр.
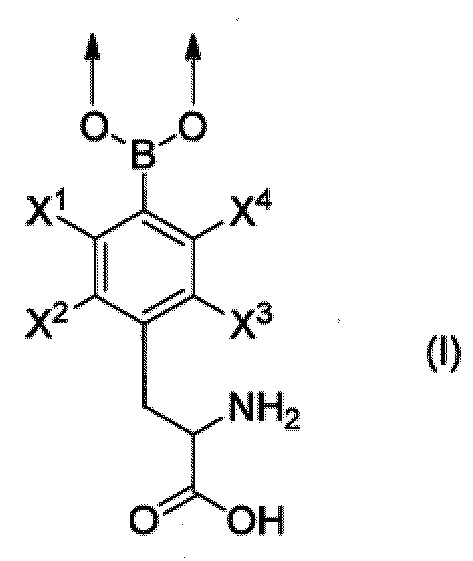
1. Производное пара-борфенилаланина, включающее:
полимер, связанный, либо непосредственно, либо через линкер, с группой, представленной формулой (I) ниже:
[Хим. стр. 1]
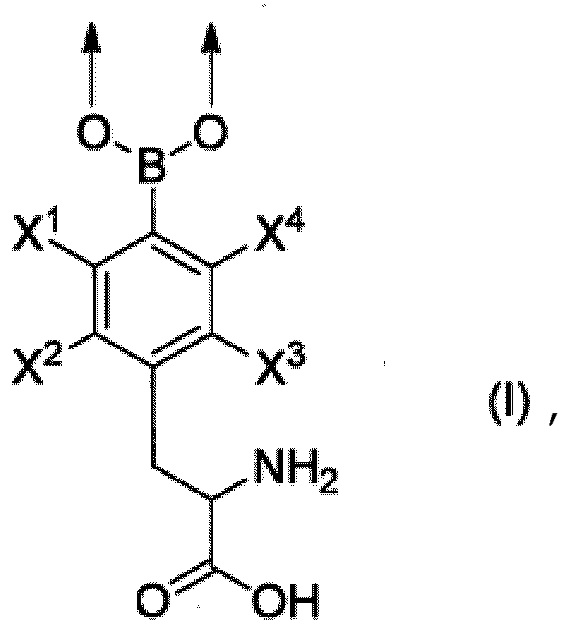
где стрелки показывают связь со смежным атомом и
X1-X4 представляют собой, каждый независимо, Н, 18F или 19F,
где полимер выбирают из группы, состоящей из поливинилового спирта, простого полиэфира и полипептида, и где его среднечисловая молекулярная масса производного пара-борфенилаланина составляет 1000 Да или более.
2. Производное пара-борфенилаланина по п. 1, где две или более групп, представленных формулой (I), связаны напрямую или через линкер с полимером и
где группы, представленные формулой (I), могут быть одинаковыми или различными.
3. Производное пара-борфенилаланина по п.1 или 2, где полимер представляет собой поливиниловый спирт.
4. Производное пара-борфенилаланина по п. 3, где производное пара-борфенилаланина представлено соединением формулы (II), приведенной ниже, или его фармацевтически приемлемой солью:
[Хим. стр. 2]
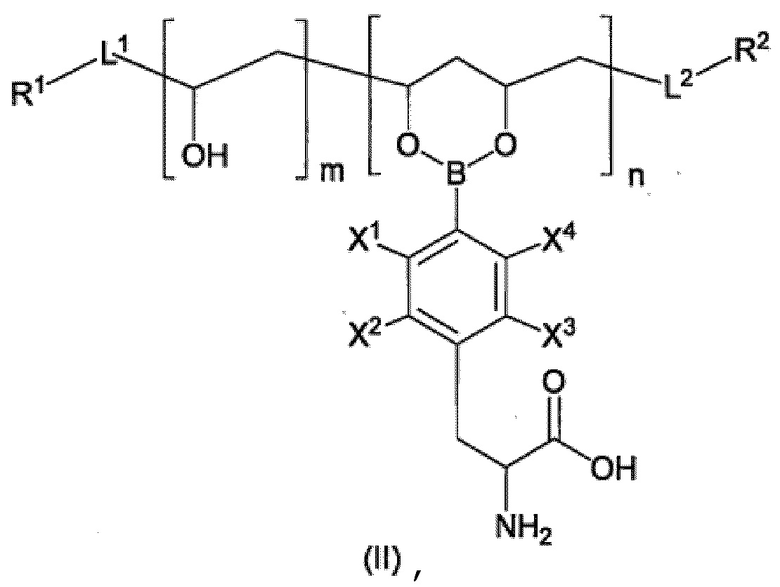
где X1-X4 представляют собой, каждый независимо, Н, 18F или 19F,
L1 и L2 представляют собой, каждый независимо, линкер или отсутствуют,
R1 и R2 представляют собой, каждый независимо, водород, гидроксильную группу, карбоксильную группу, аминогруппу, С1-10-алкильную группу, которая может быть замещена галогеном, С1-10-алкоксигруппу, которая может быть замещена галогеном, тиольную группу, цианогруппу, азидогруппу, -CH(OA1)2 или детектируемую метку,
А1 представляет собой С1-6-алкильную группу,
m имеет значение от 1 до 3998,
n имеет значение от 1 до 2000,
m+2n = от 10 до 4000, и
порядок следования повторяющихся звеньев является произвольным.
5. Производное пара-борфенилаланина по п.1 или 2, где полимер представляет собой полипептид.
6. Производное пара-борфенилаланина по п. 5, где производное пара-борфенилаланина представлено соединением формулы (III), приведенной ниже, или его фармацевтически приемлемой солью:
[Хим. стр. 3]
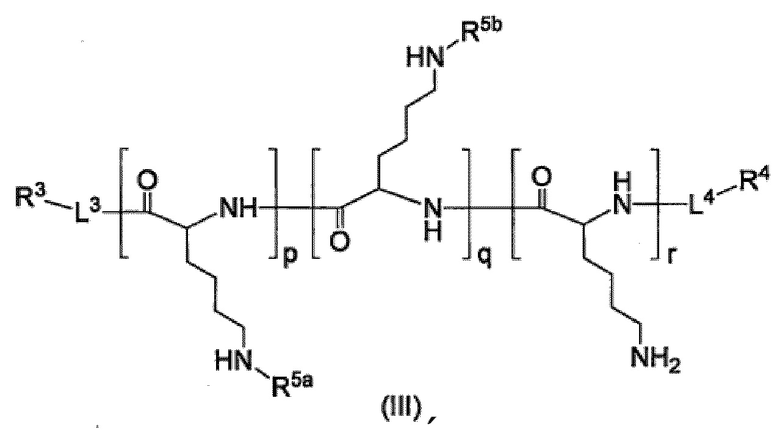
где L3 и L4 представляют собой, каждый независимо, линкер или отсутствуют,
R3 и R4 представляют собой, каждый независимо, водород, гидроксильную группу, карбоксильную группу, аминогруппу, С1-10-алкильную группу, которая может быть замещена галогеном, С1-10-алкоксигруппу, которая может быть замещена галогеном, тиольную группу, цианогруппу, азидогруппу, -CH(OA1)2 или детектируемую метку,
А1 представляет собой С1-6-алкильную группу,
R5a представляют собой, каждый независимо, группу, представленную ниже формулой (IV-a) или (IV-b):
[Хим. стр. 4]
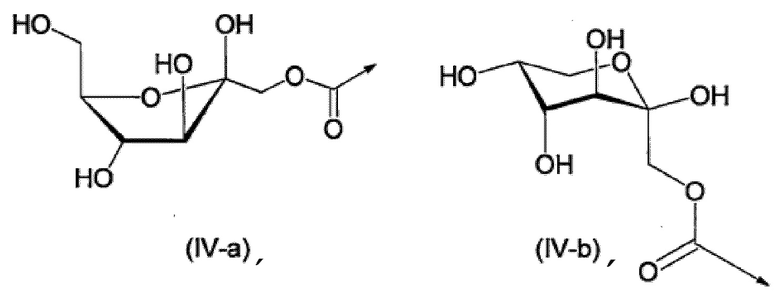
где стрелки показывают связь с NH,
R5b представляют собой, каждый независимо, группу, выбранную из группы, состоящей из групп, представленных следующими формулами (IV-с) - (IV-g):
[Хим. стр. 5]
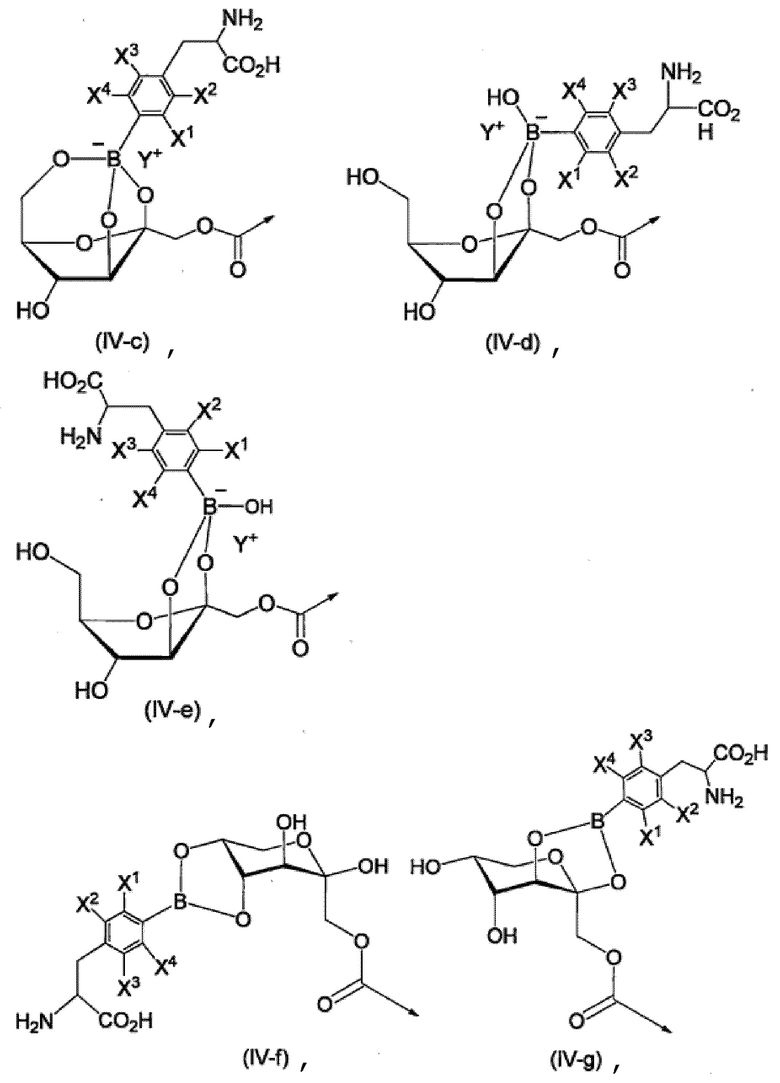
где стрелки показывают связь с NH,
X1-X4 представляют собой, каждый независимо, Н, 18F или 19F,
Y+ представляет собой H+, ион щелочного металла или ион тетра-С1-6-алкил-аммония,
p = от 0 до 299,
q = от 1 до 300,
r = от 0 до 299,
p+q+r = от 10 до 300, и
порядок следования повторяющихся звеньев является произвольным.
7. Производное пара-борфенилаланина по п. 5, где производное пара-борфенилаланина представлено соединением формулы (V), приведенной ниже, или его фармацевтически приемлемой солью:
[Хим. стр. 6]
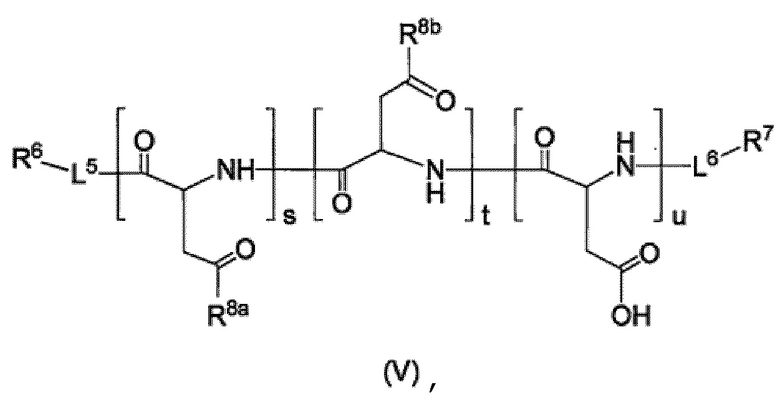
где L5 и L6 представляют собой, каждый независимо, линкер или отсутствуют,
R6 и R7, каждый независимо, представляют собой водород, гидроксильную группу, карбоксильную группу, аминогруппу, С1-10-алкильную группу, которая может быть замещена галогеном, С1-10-алкоксигруппу, которая может быть замещена галогеном, тиольную группу, цианогруппу, азидогруппу, -CH(OA1)2 или детектируемую метку,
А1 представляет собой С1-6-алкильную группу,
R8a означает группу, представленную ниже формулой (VI-a)
[Хим. стр. 7]
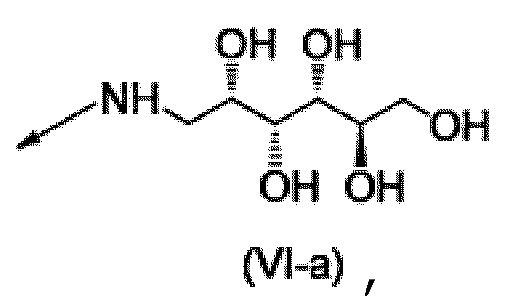
где стрелка показывает связь с карбонильным углеродом,
R8b представляют собой, каждый независимо, группу, выбранную из группы, состоящей из групп, представленных ниже формулами (VI-b) - (VI-h):
[Хим. стр. 8]
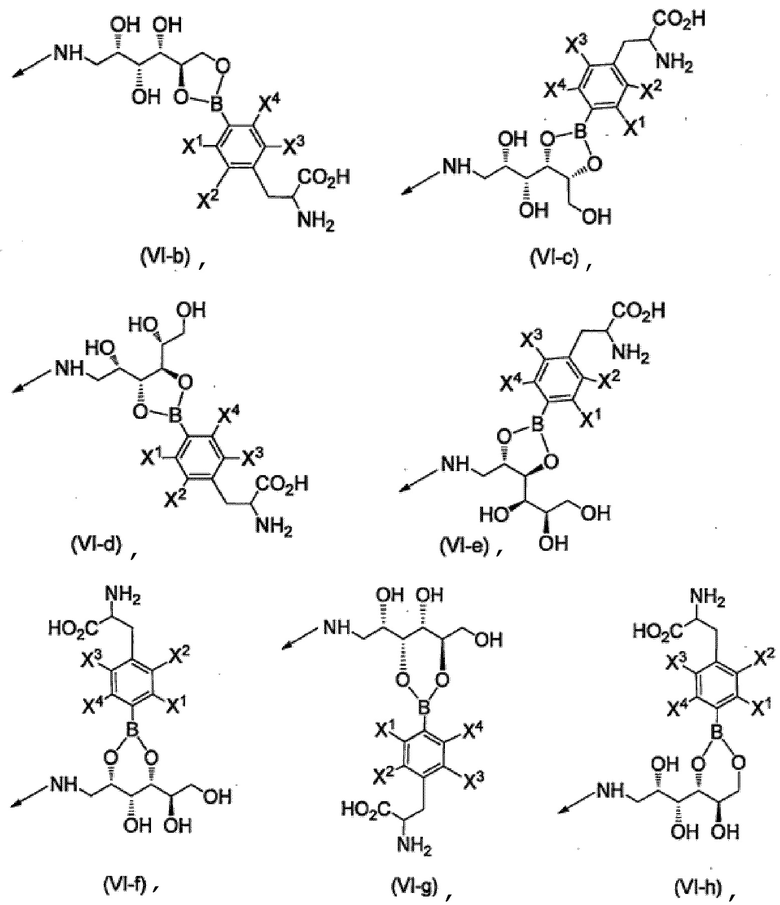
где стрелки показывают связь с карбонильным углеродом,
X1-X4 представляют собой, каждый независимо, Н, 18F или 19F,
s = от 0 до 299,
t = от 1 до 300,
u = от 0 до 299,
s+t+u = от 2 до 300, и
порядок следования повторяющихся звеньев является произвольным.
8. Производное пара-борфенилаланина по п. 5, где производное пара-борфенилаланина представлено соединением формулы (XX), приведенной ниже, или его фармацевтически приемлемой солью:
[Хим. стр. 9]
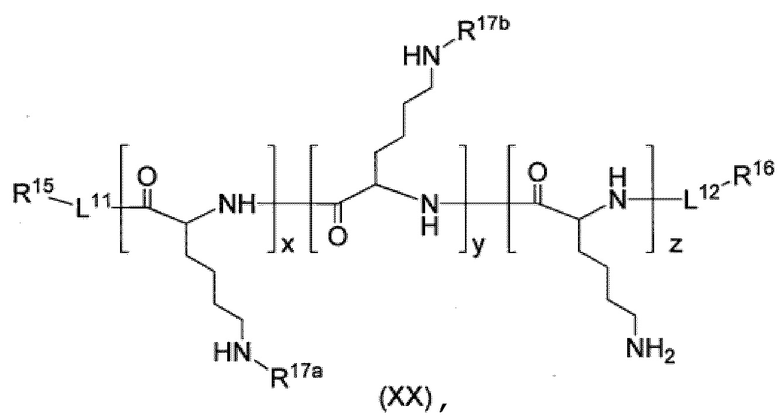
где L11 и L12 представляют собой, каждый независимо, линкер или отсутствуют,
R15 и R16 представляют собой, каждый независимо, водород, гидроксильную группу, карбоксильную группу, аминогруппу, С1-10-алкильную группу, которая может быть замещена галогеном, С1-10-алкоксигруппу, которая может быть замещена галогеном, тиольную группу, цианогруппу, азидогруппу, -CH(OA1)2 или детектируемую метку,
А1 представляет собой С1-6-алкильную группу,
R17a означает группу, представленную ниже формулой (XXI-a)
[Хим. стр. 10]

где стрелка показывает связь с NH,
R17b представляют собой, каждый независимо, группу, выбранную из группы, состоящей из групп, представленных ниже формулами (XXI-b) - (XXI-h):
[Хим. стр. 11]
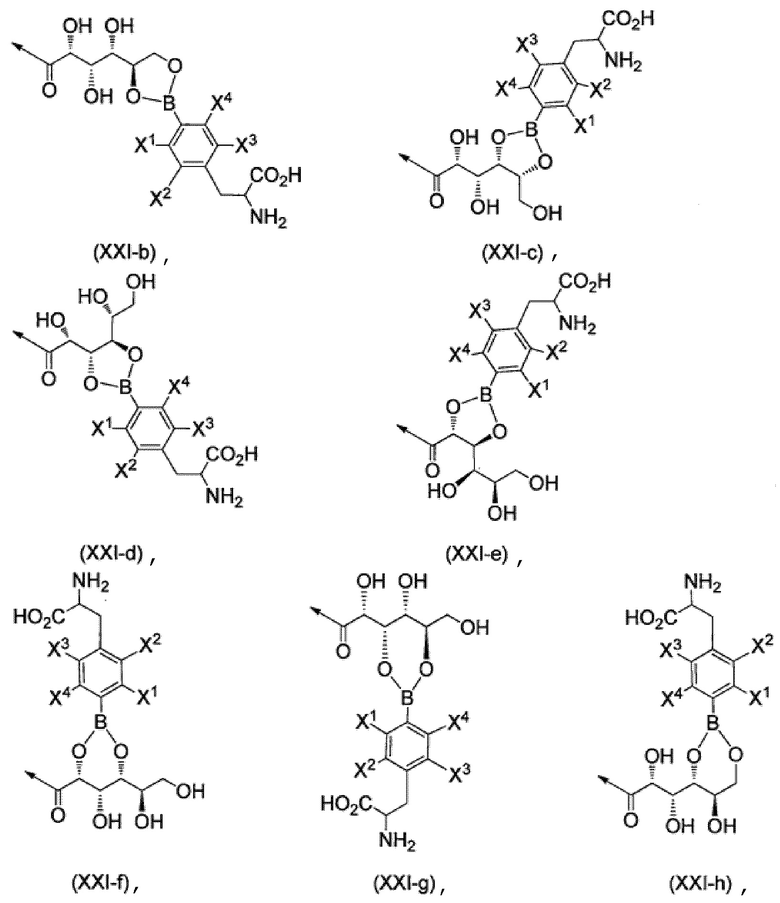
где стрелки показывают связь с NH,
X1-X4 представляют собой, каждый независимо, Н, 18F или 19F,
x = от 0 до 299,
y = от 1 до 300,
z = от 0 до 299,
x+y+z = от 10 до 300, и
порядок следования повторяющихся звеньев является произвольным.
9. Производное пара-борфенилаланина по п. 3, где производное пара-борфенилаланина представлено соединением формулы (XXII), приведенной ниже, или его фармацевтически приемлемой солью:
[Хим. стр. 12]
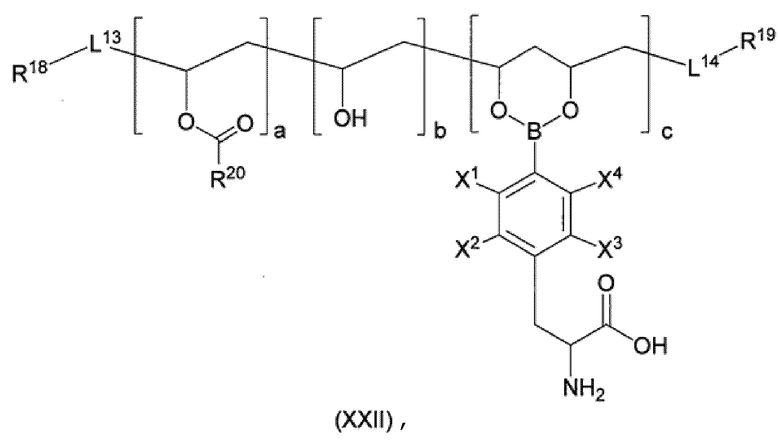
где X1-X4 представляют собой, каждый независимо, Н, 18F или 19F,
L13 и L14 представляют собой, каждый независимо, линкер или отсутствуют,
R18 и R19 представляют собой, каждый независимо, водород, гидроксильную группу, карбоксильную группу, аминогруппу, С1-10-алкильную группу, которая может быть замещена галогеном, С1-10-алкоксигруппу, которая может быть замещена галогеном, тиольную группу, цианогруппу, азидогруппу, -CH(OA1)2 или детектируемую метку,
А1 представляет собой С1-6-алкильную группу,
R20 представляют собой, каждый независимо, С1-10-алкильную группу, которая может быть замещена галогеном, -NR21R22-группу, или следующую группу:
[Хим. стр. 13]
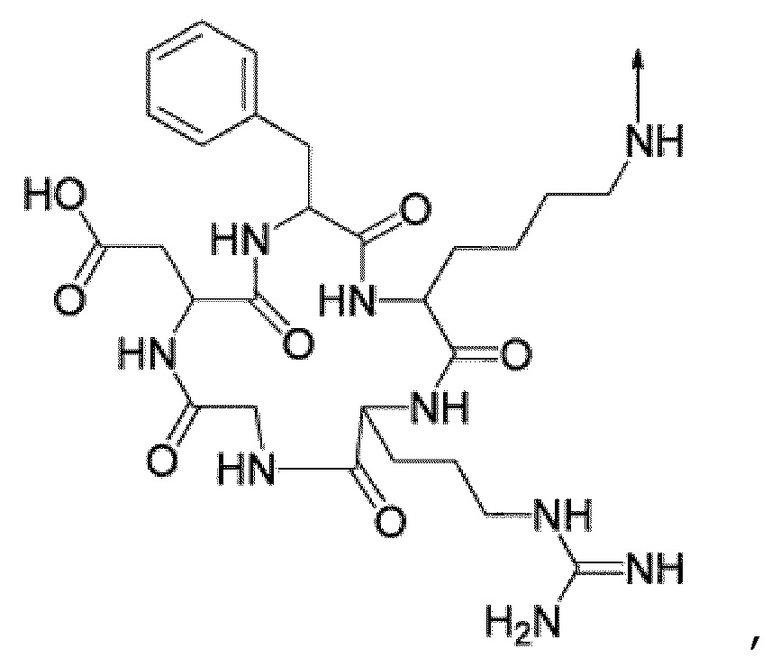
где стрелка показывает связь с карбонильным углеродом,
R21 и R22 представляют собой, каждый независимо, водород или С1-10-алкильную группу, которая может быть замещена галогеном,
а = от 1 до 3998,
b = от 1 до 3997,
с = от 1 до 2000,
a+b+2c = от 10 до 4000, и
порядок следования повторяющихся звеньев является произвольным.
10. Фармацевтическая композиция для лечения опухолей, содержащая производное пара-борфенилаланина по любому из пп. 1-9.
11. Фармацевтическая композиция для диагностирования и обнаружения опухолей, содержащая производное пара-борфенилаланина по любому из пп. 1-9.
12. Набор для получения композиции по п. 10 или 11 или для получения производного пара-борфенилаланина по любому из пп. 1-9, включающий в себя соединение, представленное формулой (VII)
[Хим. стр. 14]
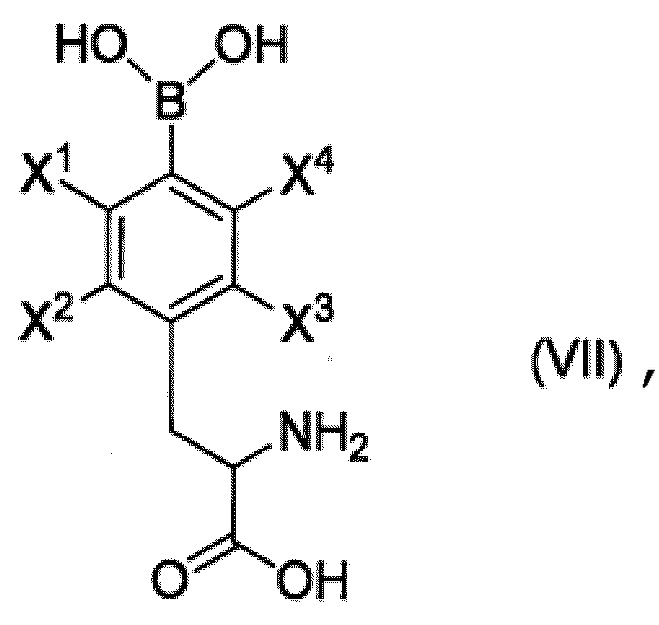
где X1-X4 представляют собой, каждый независимо, Н, 18F или 19F, и
полимер, который может вступать в реакцию с соединением, представленным формулой (VII), с образованием производного пара-борфенилаланина по любому из пп. 1-9.
| WO 2000057887 A1, 05.10.2000 | |||
| WO 2004009135 A2, 29.01.2004 | |||
| JP 2006096870 A, 13.04.2006 | |||
| СИВАЕВ И.Б | |||
| и др | |||
| Бор-нейтронозахватная терапия рака | |||
| Химический аспект, Рос | |||
| хим | |||
| ж | |||
| (Ж | |||
| Рос | |||
| Хим | |||
| Об-ва им | |||
| Д.И | |||
| Менделеева), 2004, т | |||
| XLVIII, N 4, с | |||
| Шкив для канатной передачи | 1920 |
|
SU109A1 |
| стр | |||
| Говорящий кинематограф | 1920 |
|
SU111A1 |
| СПОСОБ ДОСТАВКИ БОРСОДЕРЖАЩИХ ПРЕПАРАТОВ ДЛЯ БОР-НЕЙТРОНОЗАХВАТНОЙ ТЕРАПИИ | 2014 |
|
RU2589822C2 |
Авторы
Даты
2023-06-02—Публикация
2019-02-19—Подача