Область техники
Изобретение относится к области технической медицины и, более конкретно, относится к применению филлирина и/или его производных, и/или композиции филлирина/филлигенина, который(ая) подавляет и ингибирует белок 3CLpro вируса COVID-19 и может быть использована для производства лекарственных средств против коронавируса, в частности, против вируса COVID-19, и других ему подобных вирусов.
Уровень техники
COVID-19 - коронавирусная болезнь 2019 года (также известна как коронавирусная пневмония нового типа). Возбудителем болезни COVID-19 является вирус COVID-19 (также известный как коронавирус нового типа), который принадлежит к семейству коронавирусов, имеющий высокую гомологию с атипичной пневмонией (SARS), вспыхнувшей в 2003 году. До сих пор отсутствуют специфические лекарственные средства против вируса COVID-19. До сих пор также, отсутствуют специфические лекарственные средства против ранее вспыхнувшей атипичной пневмонии.
Авторы настоящего изобретения посвятили себя исследованию экстрактов лекарственных средств традиционной китайской медицины, и случайно и неожиданно обнаружили, что лекарственная композиция из филлирина и небольшого количества филлигенина обладает синергетическим лечебным, а также явно выраженным синергетическим лекарственным эффектом в части противовирусной активности. Например, китайская патентная заявка CN105362283A, раскрывает композицию филлирина/филлигенина и ее применение для уменьшения или/и лечения вирусных заболеваний, среди этих вирусных заболеваний есть заболевания, вызываемые вирусом гриппа, вирусом парагриппа, вирусом Коксаки CoxA16, респираторно-синцитиальным вирусом RSV, вирусом простого опоясывающего лишая HSV-I, вирусом простого герпеса HSV-II, вирусом простого герпеса CVB3, аденовирусом ADV или энтеровирусом EV71.
Тем не менее, существует много антивирусных средств с различными механизмами действия, и невозможно предсказать, какие из существующих противовирусных препаратов будут оказывают ингибирующее действие на возникший вирус COVID-19. В частности, поскольку коронавирус в значительной степени отличается от вышеперечисленных вирусов, на который нацелена композиция филлирина/филлигенина, и исследования вируса COVID-19 и воздействия на него терапевтического механизма еще не завершены, специалисты в данной области не могут предсказать ингибирующий эффект композиции филлирина/филлигенина на коронавирус (особенно вирус COVID-19).
Кроме того, не сообщалось о влиянии филлирина, филлигенина или их производных на 3-химотрипсин-подобный белок цистеина (сокращенно 3CL pro protein) вируса COVID-19.
Тем не менее, авторы настоящего изобретения неожиданно обнаружили, что композиция филлирина/филлигенина проявляет превосходное ингибирующее действие на вирус COVID-19, а, что касается его высокого уровня безопасности, то клиническое одобрение этой композиции для других применений близится к завершению. Таким образом, данная композиция имеет перспективу стать лекарственным средством от COVID-19, и может быть быстро введена в клиническую практику. Кроме того, авторы настоящего изобретения обнаружили, что филлирин, филлигенин или их производные обладают специфическим ингибирующим действием на белок 3CL pro вируса COVID-19, и могут быть использованы в качестве ингибиторов данного белка.
Краткое описание изобретения
Настоящее изобретение решает техническую проблему, связанную с предоставлением нового средства, целенаправленно ингибирующего белок 3CLpro вируса COVID-19, и лекарственного средства для борьбы с коронавирусом (особенно вирусом COVID-19) или для лечения заболеваний, вызванных коронавирусом (особенно COVID-19).
В частности, в первом варианте осуществления настоящего изобретения предлагает применение филлирина и/или его производных в приготовлении средства для ингибирования белка 3CLpro вируса COVID-19. Средство для ингибирования белка 3CLpro вируса COVID-19 включает филлирин и/или его производные.
Применение в первом варианте осуществления изобретения может представлять собой отдельное применение филлирина или его производных или комбинированное применение филлирина и его производных, такое как применение композиции филлирина/филлигенина. При применении в первом варианте осуществления настоящего изобретения ингибирование может быть in vivo или in vitro.
Предпочтительно, при применении в первом варианте осуществления настоящего изобретения производное представляет собой KD-2-GLU или KD-2-SO3H.
Соответственно, в втором варианте осуществления настоящего изобретения предлагается способ ингибирования белка 3CLpro вируса COVID-19, включающий стадию взаимодействия белка 3CLpro вируса COVID-19 с филлирином и/или его производными. Данный способ может быть in vivo или in vitro.
Предпочтительно, в способе во втором варианте осуществления настоящего изобретения производное представляет собой KD-2-GLU или KD-2-SO3H.
В третьем варианте настоящего изобретения обеспечивается применение композиции филлирина/филлигенина в приготовлении лекарственных средств для борьбы с коронавирусом, а также обеспечивается применение композиции филлирина/филлигенина в приготовлении лекарственного средства для лечения заболеваний, вызванных коронавирусом. Борьба с коронавирусом может быть in vitro, например, ингибирование пролиферации коронавируса прироста, но предпочтительнее борьба с коронавирусом проводится in vivo, т.е. заболевания, вызванные коронавирусом, лечатся.
В настоящем документе, если не указано обратное, термины «филлирин/филлигенин», «филлирин и филлигенин» и «филлирин и композиция филлигенина» могут быть использоваться взаимозаменяемо для обозначения композиции, состоящей из филлирина и филлигенина, то есть филлирин/филлигенин считается целой, не разделяемой композицией. Предпочтительно в настоящем изобретении весовое соотношение филлирина к филлигенину составляет 2~98: 2~98, предпочтительно 80~98: 2~20, и более предпочтительно 90~98: 2~10, например, 90:10 или 98:2.
Предпочтительно, при применении в третьем варианте осуществления настоящего изобретения, под коронавирусом понимают вирус COVID-19, или заболевание вызванное коронавирусом являющееся COVID-19. Предпочтительно, композиция филлирина/филлигенина ингибирует белок 3CLpro вируса COVID-19, то есть, при применении в третьем варианте осуществления настоящего изобретения, композиция филлирина/филлигенина противодействует вирусу COVID-19 или лечит заболевание, вызванное вирусом COVID-19, ингибируя белок 3CLpro вируса COVID-19.
Композицию филлирина/филлигенина можно использовать в сочетании с другим лекарственным средством (лекарствами) против коронавируса (например, вируса COVID-19) или для лечения заболевания (заболеваний), вызванного коронавирусом (например, COVID-19), или можно использовать отдельно. Авторы настоящего изобретения обнаружили, что механизм действия композиции филлирина/филлигенина против вируса COVID-19 включает ингибирование белка 3CLpro вируса COVID-19.
Предпочтительно, при применении в третьем варианте осуществления настоящего изобретения композиция филлирина/филлигенина применяется в качестве единственного активного фармацевтического ингредиента, то есть, единственным активным ингредиентом в лекарственном средстве является композиция филлирина/филлигенина. Таким образом, в третьем варианте осуществления настоящего изобретения, предпочтительно, предлагается применение композиции филлирина/филлигенина в качестве единственного активного фармацевтического ингредиента в приготовлении лекарственного средства для борьбы с коронавирусом (например, вирусом COVID-19), или применение композиции филлирина/филлигенина в качестве единственного активного фармацевтического ингредиента при производстве лекарственного средства для лечения заболеваний вызванных коронавирусом (например, COVID-19).
Лекарственное средство может включать фармацевтически приемлемый носитель так, чтобы можно было приготовить фармацевтический состав. Это действие хорошо известно специалистам в данной области техники. При применении согласно третьему варианту настоящего изобретения указанное лекарственное средство предпочтительно присутствует в форме таблетки, капсулы, пилюли, порошка, гранулы, сиропа, раствора, эмульсии, инъекции, спрея, аэрозоля, геля, крема, катаплазмата, адгезивного пластыря или пластыря.
Соответственно, настоящее изобретение также предлагает второе медицинское применение композиции филлирина/филлигенина и способ лечения с ее использованием.
В четвертом варианте осуществления настоящего изобретения предлагается применение композиции филлирина/филлигенина для борьбы с коронавирусом (например, вирусом COVID-19). Настоящее изобретение также предлагает композицию филлирина/филлигенина для лечения заболеваний, вызванных коронавирусом (например, COVID-19); или альтернативно, настоящее изобретение также предлагает применение композиции филлирина/филлигенина для ингибирования белка 3CLpro вируса COVID-19.
Кроме того, настоящее изобретение предлагает лекарственное средство, содержащее композицию филлирина/филлигенина, которое используется для борьбы с коронавирусом (например, вирусом COVID-19). Также настоящее изобретение предлагает лекарственное средство, содержащее композицию филлирина/филлигенина, которое используется для лечения заболеваний, вызванных коронавирусом (например, COVID-19); альтернативно, настоящее изобретение также предлагает лекарственное средство, содержащее композицию филлирина/филлигенина, которое используется для ингибирования белка 3CLpro вируса COVID-19.
Предпочтительно, в лекарственном средстве, включающем композицию филлирина/филлигенина, данная композиция является единственным активным фармацевтическом ингредиентом.
Также предпочтительно, лекарственное средство, включающее композицию филлирина/филлигенина, обеспечивается в форме таблеток, капсул, пилюль, порошков, гранул, сиропов, растворов, эмульсий, инъекций, спреев, аэрозолей, гелей, кремов, катаплазм, адгезивных пластырей или пластырей.
В пятом варианте осуществления настоящего изобретения предлагается способ борьбы с коронавирусом (например, вирусом COVID-19), включающий в себя введение эффективного количества композиции филлирина/филлигенина нуждающемуся пациенту. Соответственно, настоящее изобретение также предлагает способ лечения заболеваний, вызванных коронавирусом (например, COVID-19), который включает в себя введение эффективного количества композиции филлирина/филлигенина нуждающемуся пациенту. Предпочтительно композиция филлирина/филлигенина противодействует вирусу COVID-19 или лечит заболевание(я), вызванное вирусом COVID-19, путем ингибирования белка 3CLpro вируса COVID-19.
Кроме того, настоящее изобретение предлагает способ борьбы с вирусом COVID-19, включающий в себя введение эффективного количества лекарственного средства, содержащего композицию филлирина/филлигенина, нуждающемуся пациенту. Соответственно, настоящее изобретение также предлагает способ лечения заболеваний, вызванных коронавирусом (например, COVID-19), который включает в себя введение лекарственного средства, содержащего эффективное количество композиции филлирина/филлигенина нуждающемуся пациенту.
В данном документе, определении дозы (эффективного количества) и путь введения лекарственного средства обычно определяются врачом в соответствии с индивидуальными показателями пациента (такими как возраст, вес, пол, время болезни, физическое состояние и тяжесть инфекции и т.д.). Поскольку индивидуальные показатели пациента изменяются, доза введения также быть изменена, и выбор подходящей дозы определяется лечащим врачом. Путь введения определяется по лекарственной форме фармацевтической композиции, и подходящие пути введения включают пероральный, парентеральный, введение через слизистую оболочку, внутримышечный, внутривенный, подкожный, внутриглазной, внутрикожный, трансдермальный и т.п. Путь введения предпочтительно является пероральным.
Предпочтительно, в этом способе композиция филлирина/филлигенина является единственным активным фармацевтическим ингредиентом в данном лекарственном средстве.
Также предпочтительно, в этом способе лекарственные средства представлены в форме таблеток, капсул, пилюль, порошков, гранул, сиропов, растворов, эмульсий, инъекций, спреев, аэрозолей, гелей, кремов, катаплазм, адгезивных пластырей или пластырей.
Полезный эффект настоящего изобретения состоит в том, что предложены средство и способ для ингибирования белка 3CLpro вируса COVID-19. Композиция филлирина/филлигенина может эффективно ингибировать вирус COVID-19 и другие коронавирусы даже при низких концентрациях, и комбинация филлирина и филлигенина, которая обладает синергетическим эффектом, может стать перспективным лекарственным средством для борьбы с коронавирусом, таким как вирус COVID-19, и может быть быстро введена в клиническую практику.
Для облегчения понимания настоящее изобретение подробно описано ниже со ссылкой на частные варианты осуществления и чертежи. Следует отметить, что описания являются только иллюстративными и не накладывают ограничения на объем настоящего изобретения. В соответствии с данным описанием, различные варианты настоящего изобретения очевидны для специалистов в данной области. Кроме того, описание настоящего изобретения ссылается на общедоступную литературу, которая предназначена для более ясного описания настоящего изобретения. Полный текст этой опубликованной литературы включен в данный документ для справки, как если бы их полный текст был продублирован в данном документе.
Короткое описание чертежей
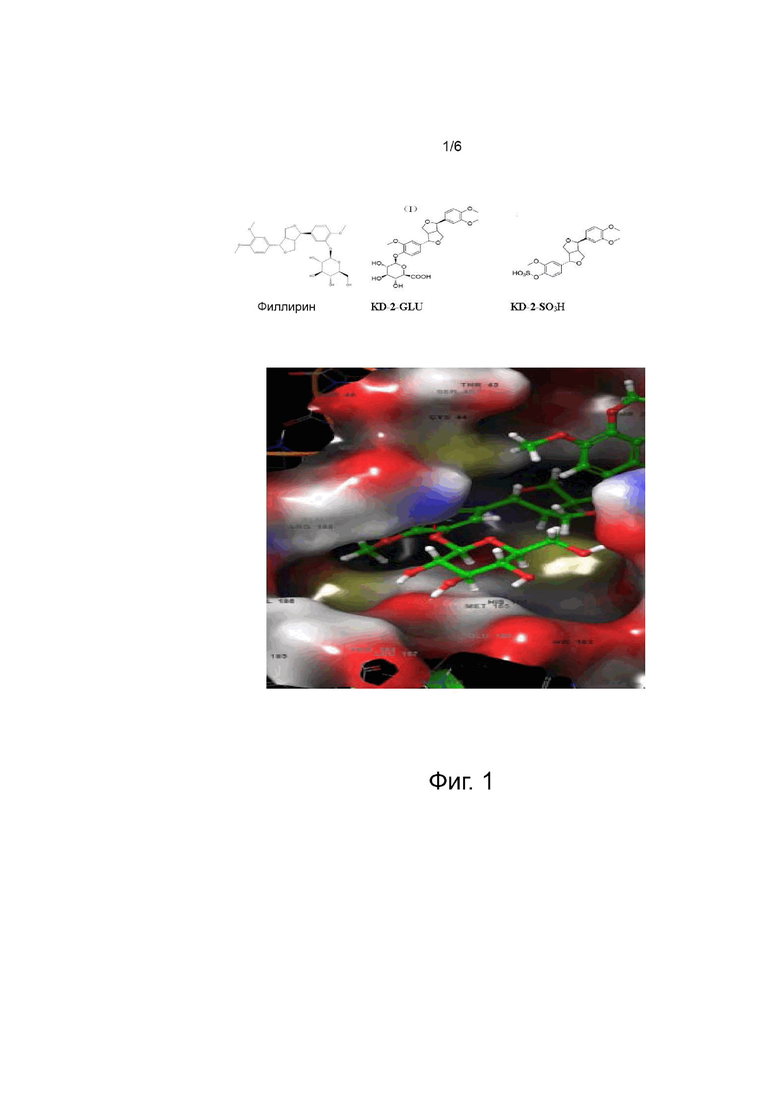
Фиг. 1 показывает структуру филлирина и его производного.
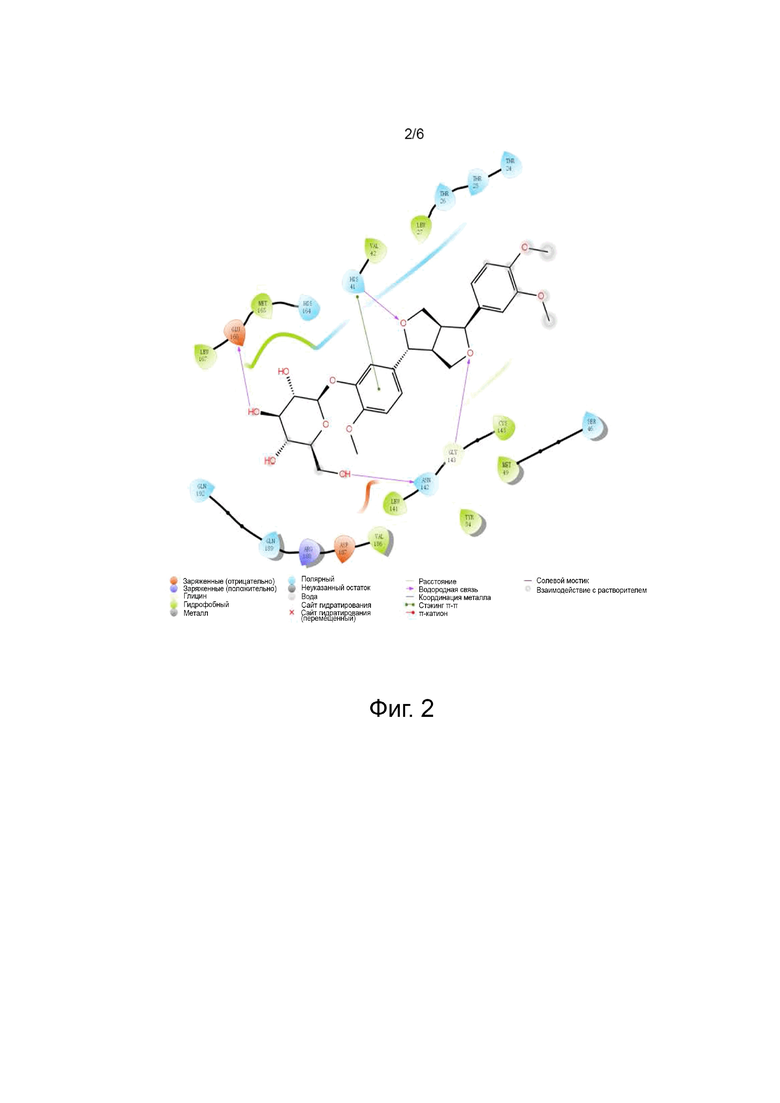
Фиг. 2 показывает моделирование связи KD-1 с белком-мишенью 3CLpro вируса COVID-19.
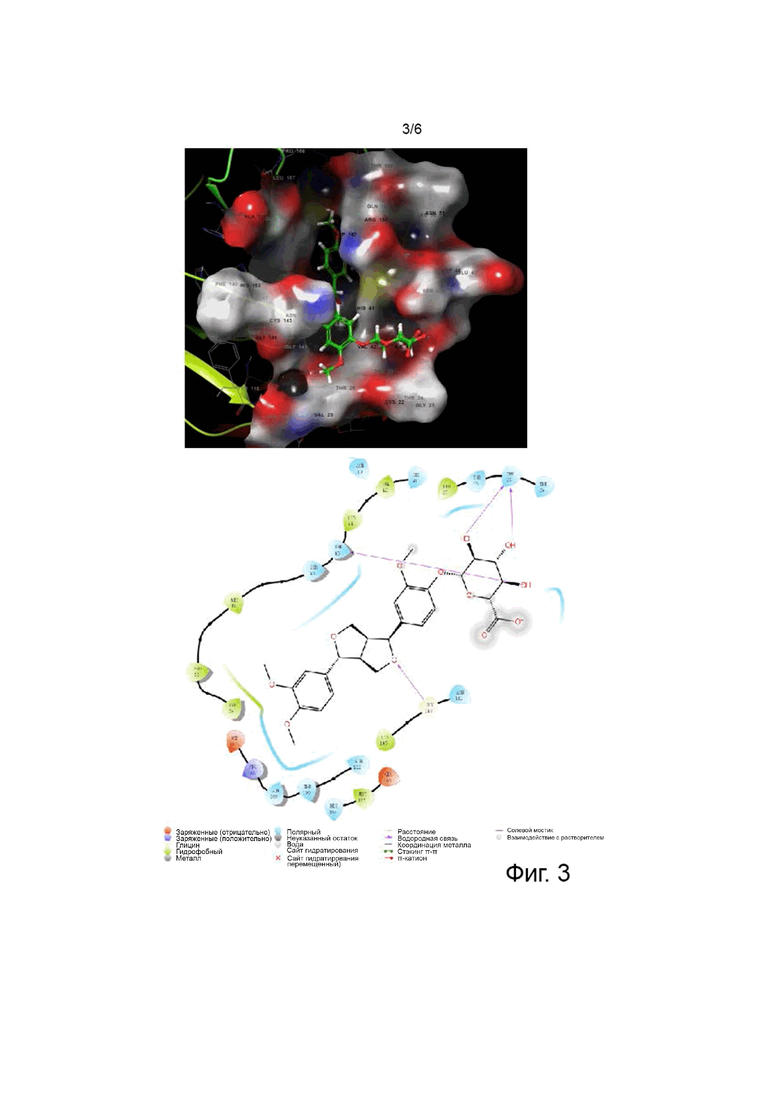
Фиг. 3 показывает моделирование связи KD-2 с белком-мишенью вируса COVID-19.
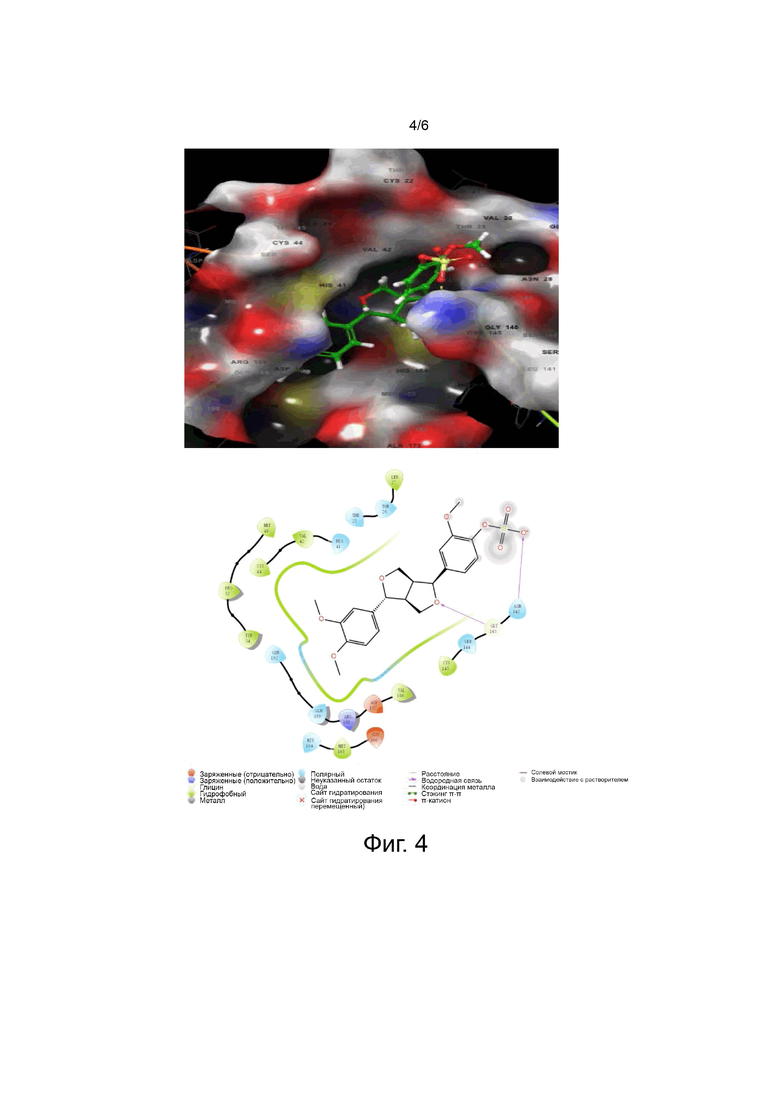
Фиг. 4 показывает моделирование связи KD-2-SO3H с белком-мишенью 3CLpro вируса COVID-19.
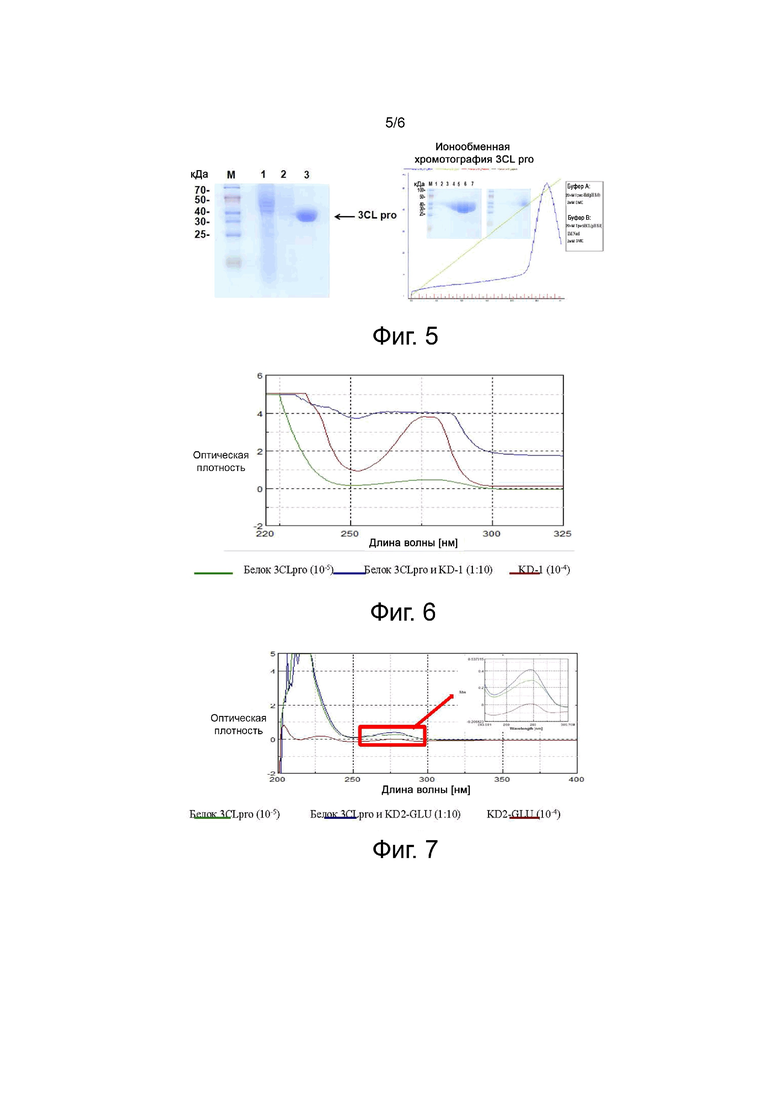
Фиг. 5 показывает результаты клонирования, экспрессии и очистки белка 3CL pro.
Фиг. 6 показывает график УФ-анализа белка 3CLpro и KD-1.
Фиг. 7 показывает график УФ-анализа белка 3CLpro и KD2-GLU.
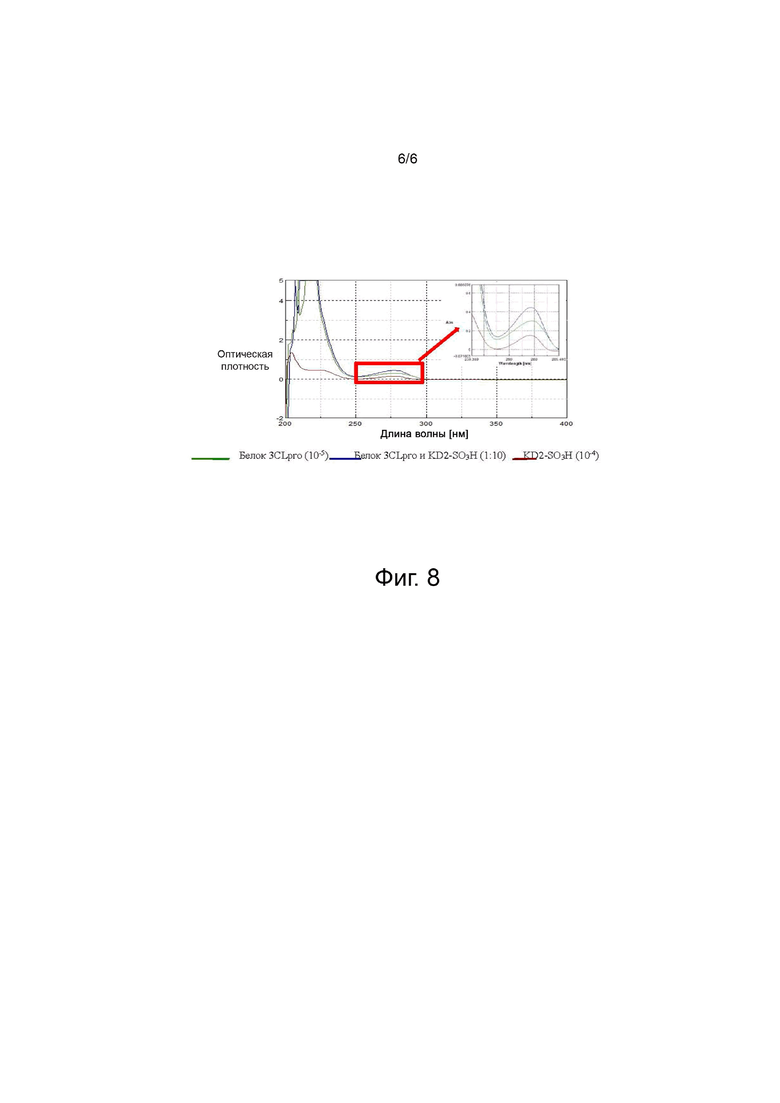
Фиг. 8 показывает график УФ-анализа белка 3CLpro и KD2-SO3H.
Подробное описание изобретения
Настоящее изобретение дополнительно иллюстрируется с помощью следующих частных вариантов осуществления. Если не указано иное, способы, используемые в частных вариантах осуществления, описаны в технической литературе из области, к которой принадлежит настоящее изобретение, и в нормативных документах органов по регулированию обращения лекарственных средств, а приборы, сырье и реагенты приобретались на открытом рынке.
Пример 1. Изучение влияния композиции филлирина/филлигенина на вирус COVID-19 in vitro
1. Испытание лекарственного средства: композиция филлирина/филлигенина, в которой весовое соотношение филлирина к филлигенину составляет 90:10 (Даляньская компания разработки натуральных лекарственных средств «Фушэн» Лтд.).
2. Клетки: клетки VeroE6 (Главная государственная лаборатория респираторных заболеваний при Гуанчжоуском институте здоровья дыхательных путей).
3. Вирус: штамм SARS-CoV-2 вируса COVID-19 (Лаборатория BSL-3 при Гуанчжоуском технологическом центре (лаборатория высокопатогенных микроорганизмов при Главной государственной лаборатории заболеваний дыхательных путей)), титр TCID50 = 10-6/100 мл.
4. План эксперимента (все процедуры эксперимента были выполнены в лаборатории BSL-3):
(1) по 100 мкл клеток VeroE6 в концентрации 2 × 105 клеток VeroE6/мл были добавлены в лунки стерильного 96-луночного культурального планшета, и культивировались в 5% CO2 при 37°C в течение 24 часов;
(2) по 100 мкл/лунку вирусного раствора 100 TCID50 добавили к тестируемой и контрольным группам на культуральном планшете, и при инкубации при 37°C в 5% CO2 в течение 2 часов обеспечили возможность присоединения вируса;
(3) через 2 часа раствор для культивирования клеток из 96-луночного планшета удалили; композицию филлирина/филлигенина разбавили до ряда концентраций, указанных в таблице 1. Раствор добавляли по 100 мкл/лунку в трех повторах для каждой концентрации;
(4) контроль по клеткам, слепая проба (контроль по растворителю) и вирусный контроль (отрицательный контроль) проводили одновременно;
(5) клетки инкубировали в 5% CO2 при 37°C в течение 3-4 дней;
(6) цитопатический эффект (CPE) наблюдали под оптическим микроскопом. Уровни CPE записывали с помощью следующих 6 оценок: «-» CPE не наблюдалось; «±» цитопатический эффект составляет менее 10%; «+» цитопатический эффект составляет около 25%; «+ +» цитопатический эффект составляет около 50%; «+ + +» цитопатический эффект составляет около 75%: «+ + + +» цитопатический эффект составляет более 75%. Половину максимально эффективной концентрации (IC50) рассчитывали с использованием метода Рида-Мюнха или GraphPad Prism 5.0.
5. Результаты эксперимента:
Как показано в таблице 1-1, композиция филлирина/филлигенина может эффективно подавлять вирус COVID-19 даже при низких концентрациях. Подсчитали, что концентрация полумаксимального ингибирования IC50 составляет 63,90 мкг/мл (в то же время, исследования показали, что для чистого филлирина величина концентрации полумаксимального ингибирования IC50 составляет 179,1 мкг/мл, а чистый филлигенин обладает еще более плохим ингибирующим эффектом). Комбинация филлирина и филлигенина в композиции обладает синергетическим эффектом, так что данная композиция, как ожидается, будет полезна для лечения COVID-19.
Таблица 1-1
Пример 2. Изучение влияния композиции филлирина/филлигенина на вирус HCoV-229E in vitro
Коронавирус HCoV-229E является менее патогенным и обычно вызывает только респираторные симптомы, похожие на простуду. Данный пример осуществления изобретения в основном основан на процессе, показанном в примере 1, с той только разницей, что используемый коронавирус представляет собой вирус HCoV-229E (Лаборатория Гуанчжоуском технологическом центре BSL-3 (лаборатория высокопатогенных микроорганизмов при Главной государственной лаборатории заболеваний дыхательных путей)), с титром TCID50 = 10-5,5/100 мкл, и титр используемого вируса был 100TCID50; а композицию филлирина/филлигенина разбавляли до ряда концентраций, указанных в таблице 2-1. Все процедуры эксперимента были выполнены в лаборатории BSL-3.
Как показано в таблице 2-1, композиция филлирина/филлигенина может эффективно ингибировать вирус HCoV-229E даже при низких концентрациях. Подсчитали, что концентрация полумаксимального ингибирования IC50 составляет 64,53 мкг/мл (в то же время, исследования показали, что чистый филлирин и чистый филлигенин обладают более плохим ингибирующим эффектом). Комбинация филлирина и филлигенина в композиции обладает синергетическим эффектом, и как ожидается, композиция будет полезна для лечения заболеваний, вызванных вирусом HCoV-229E.
Таблица 2-1
Пример 3. Исследование молекулярного механизма ингибирования вируса COVID-19 филлирином и его производными
I. Исходные данные эксперимента
Белок Spike (белок S) на поверхности вируса COVID-19 и гидролаза вируса COVID-19 (подобная химотрипсину цистеиновая протеаза 3, обозначаемая как белок 3CL pro) являются важными звеньями в жизненном цикле вируса COVID-19. Жизненный цикл COVID-19 заключается в том, что белок S на поверхности COVID-19 связывается с ангиотензин-превращающим ферментом 2 (ACE2), через эндоцитоз клетки проникает в нее с высвобождением генетического материала РНК, и с участием белка 3CL pro генетический материал РНК успешно реплицируется с образованием вируса.
Для виртуального скрининга в основном используется технология молекулярной стыковки, которая моделирует процесс скрининга лекарственного средства на компьютере. Сперва, для проведения этого скрининга необходимо узнать молекулярную структуру мишени для действия лекарственного средства, потом рассчитать связывающую способность малых молекул из библиотеки соединений с мишенью с помощью молекулярного моделирования, и спрогнозировать физиологическую активность соединений-кандидатов.
В этом эксперименте, технология молекулярной стыковки Glide используется для выполнения виртуального скрининга с целью поиска оптимального связывающего эффекта филлирина (KD-1) и его производных с белком-мишенью 3CL pro. На основании результатов скрининга изучено влияние связывания KD-1 и его производных с белком-мишенью in vitro, а также объяснено межмолекулярное взаимодействие и форма связывания и взаимосвязь структуры и активности KD-1 и его производных. Анализ активности белка-мишени с помощью KD-1 и его производных позволило выявить молекулярный механизм ингибирования вируса COVID-19 с помощью филлирина (KD-1) и его производных.
II. Методика эксперимента
1. Молекулярная стыковка KD-1 и его производных с белком-мишенью
(1) Подготовка системы: Кристаллическая структура размером 2.16Å основной протеазы SARS-CoV-2 (белка 3CL pro) получена из базы данных белков (PDB ID: 6LU7). Структура фермента предварительно обработана с помощью protein Preparation Wizard в Schrodinger, кристаллизационную воду удаляли и добавляли отсутствующие атомы водорода/атомы боковых цепей, а также кислотным и основным аминокислотным остаткам при pH 7,0 были присвоены соответствующие заряды и состояния протонирования, была проведена энергетическая минимизация структуры фермента с использованием силового поля OPLS-2005 и, наконец, активный сайт белка был предсказан с помощью Sitemap. В то же время, с помощью модуля LigPrep Schrodinger была оптимизирована пространственная структура филлирина и его производных.
(2) Молекулярная стыковка: Виртуальный скрининг, основанный на молекулярной стыковке, выполнен с помощью технологии Glide Maestro 11.5. Расчет присоединения филлирина и его производных (фиг. 1) выполнен с использованием режима «сверхточного» разрешения (XP) Glide.
(3) Оценка стыковки: Вычислено взаимодействие между малой молекулой и белком-мишенью по значению показателя функции «Glide- оценки». В данной функции учитывается взаимодействие водородной связи, гидрофобных сил, сил Ван-дер-Ваальса и т.д. Таким образом, чем больше абсолютное значение функции, тем более стабилен будет комплекс стыковки малой молекулы и белка-мишени, и тем лучше будет соответствующий эффект связывания.
(4) Анализ мишеней: Были проанализированы результаты стыковки KD-1 и его производных с ключевым белком-мишенью нового коронавируса и ключевые аминокислоты, участвующие во взаимодействии KD-1 и его производных с ключевым белком-мишенью нового коронавируса, чтобы обеспечить теоретическую базу и важным подспорьем для профилактики, диагностики и лечения новой коронавирусной инфекции в клинической практике.
2. Экспрессия и очистка белка
(1) Клонирование: полноразмерный ген, кодирующий белок 3CL pro SARS-CoV-2 (UniprotKB - P0DTD1, остатки 3264-3569), оптимизировали и синтезировали в экспрессионной системе E. coli (Уханьская биотехническая компания «Цзинькайжуй» Лтд.).
(2) Экспрессия: Выделенные плазмиды трансфицировали в клетки E. coli BL21 (DE3), и затем проводили культивирование в среде Лурия-Бертани, содержащей 100 мкг ампициллина/мл, при 37°C. Когда клетки размножились до OD600 0,6-0,8 нм, добавили 0,5 мМ изопропилтиогалактозида в клеточную культуру для индукции экспрессии при 30°С и 180 об/мин. Через 10 часов клеток были выделены центрифугированием при 3,000 g.
(3) Очистка: Осадок клеток ресуспендировали в лизирующем буфере (20 мМ трис-HCl pH 8,0, 150 мМ NaCl, 2 мМ 2-меркаптоэтанол), лизирование производили ультразвуком, а затем проводили центрифугирование при 13,000 g в течение 30 минут. Надосадочную жидкость загрузили в колонку для аффинной хроматографии Ni-NTA, с последующей промывкой ресуспендирующим буфером, содержащим 20 мМ имидазола, и затем связанный с гистидиновой меткой белок 3CL pro элюировали лизирующим буфером, содержащим 300 мМ имидазол (50 мМ Tris-HCl pH 7,0, 150 мМ NaCl). Белок 3CL pro дополнительно был очищен посредством ионообменной хроматографии. В конце, белок 3CL pro получили в виде смеси мономера и димера и хранили в растворе.
3. Спектроскопический эксперимент
В этом эксперименте структурные изменения белка исследовали с помощью спектрофотометра серии JASCO-V560, работающего в видимой и ультрафиолетовой областях света. Ультрафиолетовый спектр поглощения белка имеет два пика поглощения: большой пик поглощения при 210 нм отражает конформацию каркаса белка, которая обусловлена переходом n-π* C = O в пептидной связи. Появление слабого пика поглощения при 280 нм является результатом перехода π-π*, вызванного поглощением света ароматическими аминокислотами (Trp, Tyr и Phe).
В этом эксперименте спектры поглощения видимого и ультрафиолетового света получили при сканировании в диапазоне 200-700 nm белкового раствора и смешанного раствора филлирина и белка и использованием буферного раствора в качестве эталона. Gel Buffer 2 мл (50 мМ трис-HCl pH 7,0, 150 мМ NaCl) поместили в кварцевую кювету, добавили 10 мкл белка 3CL pro в концентрации 10-5 М, и измерили значение поглощения, и затем добавили 10 мкл филлирина и его производных в концентрации 10-4 М, и измерили изменения в значении поглощения.
III. Результаты эксперимента
Жизненный цикл COVID-19 включает связывания белка S на поверхности COVID-19 с ангиотензин-превращающим ферментом 2 (ACE2), проникновение в клетку посредством клеточного эндоцитоза с высвобождением генетического материала РНК, а затем с помощью белка 3CL pro генетический материал РНК успешно реплицируется с образованием вируса. В этом эксперименте исследовали соединения, которые могут блокировать участие белка 3CL pro в репликации генетического материала РНК, и затем разработали лекарственные средства против вируса COVID-19.
В этом эксперименте отобрали оптимальный целевой сайт на основе кристаллической структуры белка 3CL pro и выполнили виртуальный скрининг соединений KD-1 и его производных (KD-2-GLU и KD-2-SO3H). Были получены показатели связывания соединений KD-1, KD-2-GLU и KD-2-SO3H с сайтом белка 3CL pro, тем самым доказывая нацеленность соединений на белок 3CL pro.
Посредством расчета и анализа были обнаружены пять потенциально активных сайтов в трехмерной структуре белка 3CLpro, из которых сайт 1 является сайтом, в котором молекулы лекарственного средства могут легко связываться с белком 3CLpro. KD-1 успешно стыкован с 5 потенциальными активными сайтами белка 3CLpro, и все 5 активных сайтов успешно стыкованы со стыковочными баллами, показанными в таблице 3-1. Бал по Glide Score для KD-1 в активном сайте 1 белка 3CLpro значительно выше, чем в других активных сайтах белка 3CLpro, и активный сайт 1 белка 3CLpro выбрали в качестве теоретической величины молекулярного докинга. Анализ и расчет для соединений KD-2-GLU и KD-2-SO3H был такой же, как и выше.
Таблица 3-1. Стыковочные баллы KD-1 с 5 потенциальными активными сайтами белка 3CLpro
Выбрали оптимальный активный сайт, в котором KD-1, KD-2-GLU и KD-2-SO3H показали оптимальную активность по отношению к белку 3CLpro. С помощью Glide Score была оценена способность малых молекул связываться с активными сайтами белка 3CLpro. Чем выше абсолютное значение, тем стабильнее взаимное связывание, лучше соответствие. В таблице 3-2 приведены стыковочные баллы для соединений KD-1, KD-2-GLU и KD-2-SO3H в активном сайте белка-мишени вируса COVID-19.
Также в таблице 3-2 показано, что теоретические стыковочные баллы для соединений KD-1, KD-2-GLU и KD-2-SO3H по отношению к коровой структуре белка 3CL pro COVID-19, которая играет важную роль в процессе репликации РНК, являются значительными. KD-1 и KD-2-GLU имеют высокие стыковочные баллы, что свидетельствует о том, что данные соединения имеют различную степень нацеливания на белок 3CL pro.
Таблица 3-2. Сводная таблица стыковочных баллов для KD-1 и его производных по отношению к сайтам белка-мишени 3CLpro COVID-19
Посредством трехмерного моделирования и проекции на плоскость молекулярной стыковки KD-1 и белка-мишени 3CLpro было показано, что соединение KD-1 может входить в молекулярный карман белка (фиг. 2, верхняя часть). Соединение KD-1, связываясь с белком 3CL pro, образует π-π связь с аминокислотным остатком His41 активного сайта белка 3CL pro, образует три водородные связи с пептидными связями Gly143, Asn142, Glu166, и гидрофобно взаимодействует с группой Met165 (фиг. 2, нижняя часть). Эти результаты указывают на то, что различные аминокислотные группы, такие как His, Gly, Asn, Glu, Met или подобные им, могут стерически подходить к структуре KD-1, тем самым определяя конформацию комплекса. Предполагается, что соединение KD-1 может нацелиться на белок 3CL pro и таким образом предотвратить участие белка 3CL pro в репликации РНК COVID-19 при воспроизведении вируса.
Посредством трехмерного моделирования и проекции на плоскость молекулярной стыковки KD-2-GLU и белка-мишени 3CLpro было показано, что соединение KD-2-GLU может входить в молекулярный карман белка (фиг. 3, верхняя часть). Соединение KD-2-GLU связывается с белком 3CL pro путем образования трех водородных связей с пептидными связями Gly143, Thr43, Thr25 в активном сайте белка 3CL pro и гидрофобного взаимодействуя с Tyr54 (фиг. 3, нижняя часть). Эти результаты показывают, что различные аминокислотные остатки, такие как Gly, Thr, Tyr или подобные им, могут стерически подходить структуре KD-2-GLU, тем самым определяя конформацию комплекса. Предполагается, что соединение KD-2-GLU может нацеливаться на белок 3CL pro и предотвращать участие белка 3CL pro в репликации РНК COVID-19 для воспроизведения вируса.
Посредством трехмерного моделирования и проекции на плоскость молекулярной стыковки KD-2-SO3H и белка-мишени 3CLpro было показано, что соединение KD-2-GLU может входить в молекулярный карман белка (фиг. 4, верхняя часть). Соединение KD-2-SO3H взаимодействует с группами Gly143 и Asn142 путем образования водородных связей и гидрофобно взаимодействует с Tyr54, Val42, Cys44, Cys145 (фиг. 4, нижняя часть). Эти результаты демонстрируют, что различные аминокислотные остатки, такие как Gly, Asn, Val и подобные им могут стерически подходить структуре KD-2-SO3H, тем самым определяя конформацию комплекса.
Взаимодействие соединений KD-1 и его производных с активным сайтом белка 3CLpro показано в таблице 3-3. Эти результаты показывают, что взаимодействие филлирина и его двух производных с активным сайтом белка 3CLpro является не полностью гидрофобным, но также задействует водородные связи и связь конфигурации π-π. Взаимодействие посредством водородных связей и π-π связи может помочь стабилизировать комплекс. Было обнаружено, что соединения KD-1, KD-2-GLU и KD-2-SO3H взаимодействуют с белком 3CLpro с помощью водородной связи только с GLY143 с расстоянием между атомами водорода 2,22 Å, 2,22 Å и 2,06 Å соответственно. Тем не менее, гидрофобные и электростатические взаимодействия играют важную роль в связывании соединений KD-1, KD-2-GLU и KD-2-SO3H с белком 3CLpro. Различные соединения связываются с различными остатками белка 3CLpro, что и объясняет различия в результатах связывания.
Таблица 3-3. Взаимодействие KD-1 и его производных с белком 3CLpro
Фрагментированный белок был очищен на никелевой колонке и было установлено, что его молекулярная масса составляет 34 кДа, (фиг. 5, справа). Проводили ионообменную хроматографию белка, и затем был проведен ДНС-ПААГ, чтобы детектировать таким образом образец белка 3CL pro концентрации белка 65 мг/мл (фиг. 5, справа).
На основании результатов виртуального скрининга с помощью молекулярного докинга связывание соединений KD-1, KD-2-GLU и KD-2-SO3H с белком 3CLpro исследовали in vitro с помощью метода детекции поглощения в УФ и видимой областях света, что дополнительно подтвердило, что соединения могут нацеливаться на белок 3CLpro.
На фиг. 6 показано поглощение для соединения KD-1, белка 3CLpro и их смеси, детектированное с помощью спектроскопии в ультрафиолетовой и видимой областях света. Эти результаты показывают, что белку 3CL pro соответствует пик поглощения на длине волны 278 нм, а после добавления KD-1 происходит увеличение степени светопоглощения и смещение пика. KD-1 взаимодействует с белком 3CL pro и может ингибировать активность этого фермента. KD-1 может образовывать новый комплекс при взаимодействии с белком 3CL pro, и KD-1 может связываться с белком 3CL pro с помощью водородных связей или гидрофобного взаимодействия.
На фиг. 7 показано поглощение для соединения KD2-GLU, белка 3CLpro и их смеси, детектированное с помощью спектроскопии в ультрафиолетовой и видимой областях света. Эти результаты показывают, что белку 3CL pro соответствует пик поглощения на длине волны 278 нм, а после добавления KD2-GLU происходит увеличение степени светопоглощения и смещение пика. KD2-GLU взаимодействует с белком 3CL pro и может ингибировать активность этого фермента. KD2-GLU может образовывать новый комплекс при взаимодействии с белком 3CL pro, и они могут связываться с помощью водородных связей или гидрофобного взаимодействия.
На фиг. 8 показано поглощение для соединения KD2-SO3H, белка 3CLpro и их смеси, детектированное с помощью спектроскопии в ультрафиолетовой и видимой областях света. Эти результаты показывают, что после добавления KD2-SO3H происходит увеличение степени светопоглощения и смещение пика белка 3CLpro. KD2-SO3H взаимодействует с белком 3CL pro и может ингибировать активность этого фермента. KD2-SO3H может связываться с белком 3CL pro с помощью водородных связей или гидрофобного взаимодействия, и они могут образовывать новый комплекс.
IV. Выводы по эксперименту
Результаты молекулярного докинга показывают, что были значительными теоретические стыковочные баллы соединений KD-1, KD-2-GLU и KD-2-SO3H по отношению к белку 3CL pro в качестве ключевого белка COVID-19, вовлеченного в репликацию РНК, и среди них соединения KD-1 и KD-2-GLU имели высокие стыковочные баллы. Анализ показал, что соединения KD-1, KD-2-GLU и KD-2-SO3H были связаны с пептидными связями в активном сайте белка 3CL pro посредством водородной связи и гидрофобного взаимодействия, образуя π-π связь с аминокислотными остатками.
Теоретические данные смогли доказать, что эти соединения могли изменять структуру белка 3CL pro. Спектроскопические эксперименты in vitro показывают, что соединения KD-1, KD-2-GLU и KD-2-SO3H приводят к смещению и увеличению главного пика для белка 3CL pro на длине волны 278 нм, и оно было наиболее явным у соединения KD-1. Таким образом, каждое из соединений KD-1, KD-2-GLU и KD-2-SO3H оказывает может нацеливаться на белок 3CL pro, может предотвращать участие белка 3CL pro вируса COVID-19 в процессе репликации вируса, и, таким образом, может являться потенциальным таргентным ингибитором вируса COVID-19.
Пример 4. Исследование in vivo эффективности против коронавируса нового типа
I. Материалы для эксперимента
Мыши для эксперимента: мыши hACE2, возраст 6-7 недель, вес 20-40 г, всего 120 самцов, поставщик лабораторных животных - Цзянсуская биотехническая компания «Цзицуй Юаокан» Лтд., лицензия на производство лабораторных животных: SCXK(СУ) 2018-0008, номер сертификата лабораторных животных: №32072720201100243581, поставщик корма: Цзянсуская биотехническая компания «Мэйдисэнь» Лтд.
Лекарственное средство: композиция филлирина/филлигенина, в которой весовое соотношение филлирина к филлигенину составляет 90:10 (Даляньская компания разработки натуральных лекарственных средств «Фушэн» Лтд.).
II. Методика эксперимента
(1) Защитное действие лекарственного средства на прогрессирование заболевания у мышей, зараженных COVID-19
Трансгенные мыши hACE2 C57BL/6 были разделены на нормальную группу, группу мышей, зараженных SARS-CoV-2, которая в свою очередь была поделена на группы: с введением препарата 80 мг/кг, с введением препарата 40 мг/кг и группу положительного контроля (ремдесивир 50 мг/кг), причем каждая группа содержала по 8 мышей. Только мышам нормальной группы закапывали в нос ФСБ, мышам в других группах закапывали в нос вирус SARS-CoV-2 в концентрации 105 БОЕ. Через два часа после заражения, мышам в зараженной группе вводили филлирин в желудок через зонд один раз в день в течении 5 последовательных дней. Регистрацию изменения веса производили ежедневно после заражения, и подсчитывали смертность среди мышей за 5 дней.
(2) Исследование эффективности лекарственного средства при чрезмерном воспалении, вызванной у мышей инфекцией COVID-19
Трансгенные мыши ACE2 C57BL/6 были разделены на нормальную группу, зараженные группы вирусом SARS-CoV-2: группу с введением препарата 80 мг/кг, группу с введением препарата 40 мг/кг и группу положительного контроля (ремдесивир 50 мг/кг). Только мышам нормальной группы закапывали в нос ФСБ, мышам в других группах закапывали в нос вирус SARS-CoV-2 в концентрации 105 БОЕ. Через два часа после заражения, мышам в зараженной группе вводили филлирин в желудок через зонд, один раз в день в течение 5 последовательных дней. Животных вскрыли на 5-й день после заражения для получения легких для гомогенизации ткани для определения титра вируса. Суммарную РНК экстрагировали из супернатанта гомогената легочной ткани методом с Trizol, а с помощью метода ОТ-кПЦР определяли экспрессию мРНК соответствующих воспалительных факторов.
III. Результаты эксперимента
(1) Результаты исследований лекарственного препарата против нового коронавируса на предмет защиты от смерти
Результаты защиты от смерти показаны в таблице 4-1. Эти результаты показывают, что защитные эффекты двух доз препарата (80 мг/кг и 40 мг/кг) у мышей, инфицированных коронавирусом нового типа, составляли 87,5% и 42,86% соответственно; в группе мышей, инфицированной вирусом, гибель составляла 71,43%, степень защиты от гибели в группе, которой вводили препараты 80 мг/кг была сопоставима со степенью защиты в группе, принимавшей ремдесивир.
Таблица 4-1. Результаты исследования защиты мышей, инфицированных коронавирусом нового типа, от гибели (n = 3)
(2) Результаты исследования титра вируса в легочной ткани мышей, инфицированных коронавирусом нового типа, которым вводили лекарственные средства
Как показано в таблице 4-2, при введении двух доз препаратов (80 мг/кг и 40 мг/кг) титр вируса в легких у инфицированных мышей был значительно снижен, и не было статистической разницы между титром ингибированного в легких вируса в группе, получавшей 80 мг/кг, и титром в группе ремдесивира.
Таблица 4-2. Результаты исследования титра вируса в легочной ткани мышей, инфицированных коронавирусом нового типа (x̄±s, n=3)
SARS-CoV-2
Примечание: по сравнению с группой заражения вирусом, * P < 0,05, ** P < 0,01, *** P < 0,001
(3) Результаты испытания на индуцирование чрезмерного воспаления у мышей, инфицированных коронавирусом нового типа, которым вводили лекарственные средства
Результаты анализа показателей воспаления у инфицированных мышей приведены в таблице 4-3. На пятый день после инфекции экспрессия IL-1β, IFN-γ, MCP-1 и IFN-α в инфицированной вирусом группе значительно повысилась. Введение двух доз лекарств (80 мг/кг и 40 мг/кг) имело ингибирующее действие на факторы воспаления IL-1β, IFN-γ, MCP-1 и IFN-α. Группа которая получала дозу 80 мг/кг препарата показала лучшее ингибирование сверхэкспрессии медиаторов воспаления, чем при ремдесивире.
Таблица 4-3. Влияние лекарственных препаратов на экспрессию мРНК IL-1β, IFN-γ, MCP-1 и IFN-αmРНК в гомогенате легких инфицированных мышей (x̄±s, n=3)
Примечание: по сравнению с группой заражения вирусом, * P < 0,05, ** P < 0,01, *** P < 0,001
IV. Заключение
Приведенные выше результаты экспериментов показывают, что лекарственное средство согласно настоящему изобретению оказывает значительное защитное действие от гибели в отношении мышей, инфицированных коронавирусом нового типа, со 87,5% степенью защиты от гибели инфицированных мышей, что сопоставимо с эффективностью ремдесивира. Лекарственное средство заявленного изобретения может значительно ингибировать титр вируса в легочной ткани у мышей, инфицированных новой коронавирусной инфекцией. Оно также ингибирует экспрессию мРНК факторов чрезмерного воспаления IL-1β, IFN-α, MCP-1 и IFN-γ, индуцированную коронавирусом нового типа. Поэтому это лекарственное средство играет значительную роль в лечении новой коронавирусной инфекции.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ КОМПОЗИЦИИ ФИЛЛИРИНА/ФИЛЛИГЕНИНА ПРИ ПРИГОТОВЛЕНИИ МЕДИКАМЕНТА ИЛИ ПРОДУКТА МЕДИЦИНСКОГО НАЗНАЧЕНИЯ ДЛЯ ОБЛЕГЧЕНИЯ И/ИЛИ НАЗНАЧЕНИЯ ДЛЯ ЛЕЧЕНИЯ ВИРУСНЫХ ЗАБОЛЕВАНИЙ, И МЕДИКАМЕНТ ИЛИ ПРОДУКТ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ ДЛЯ ЛЕЧЕНИЯ ВИРУСНЫХ ЗАБОЛЕВАНИЙ | 2014 |
|
RU2655616C1 |
| ПРОИЗВОДНОЕ ФИЛЛИГЕНИНА И ГЛЮКУРОНОВОЙ КИСЛОТЫ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ | 2016 |
|
RU2684100C1 |
| СЛОЖНЫЙ ЭФИР ФИЛЛИГЕНИНА И ИБУПРОФЕНА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ | 2014 |
|
RU2659072C1 |
| СПОСОБЫ ХИМИЧЕСКОГО СИНТЕЗА ФИЛЛИРИНА | 2014 |
|
RU2667917C2 |
| БЕЛОК И ВАКЦИНА ПРОТИВ ИНФЕКЦИИ SARS-CoV-2 | 2020 |
|
RU2815060C1 |
| Антитело против PD-1 и его применение | 2017 |
|
RU2739610C1 |
| ГУМАНИЗОВАННОЕ АНТИТЕЛО ПРОТИВ PD-1 ИЛИ ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ИХ ПРИМЕНЕНИЕ | 2022 |
|
RU2829508C2 |
| АНТИТЕЛО ПРОТИВ КЛАУДИНА 18A2 И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2811431C2 |
| Композиции из гинзенозида Rg3 и гинзенозида Rg5 и их фармацевтическое применение, включая противоопухолевые эффекты | 2021 |
|
RU2812611C1 |
| ХИМЕРНЫЕ КОНСТРУКЦИИ АНТИТЕЛО/Т-КЛЕТОЧНЫЙ РЕЦЕПТОР И ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2767209C2 |
Группа изобретений относится к области медицины и, более конкретно, относится к применению филлирина и/или его производных, и/или композиции филлирина/филлигенина, а также к способам с использованием указанных выше активных ингредиентов. Предлагается применение филлирина и производных филлирина KD-2-GLU и KD-2-SO3H, представленных следующими формулами:
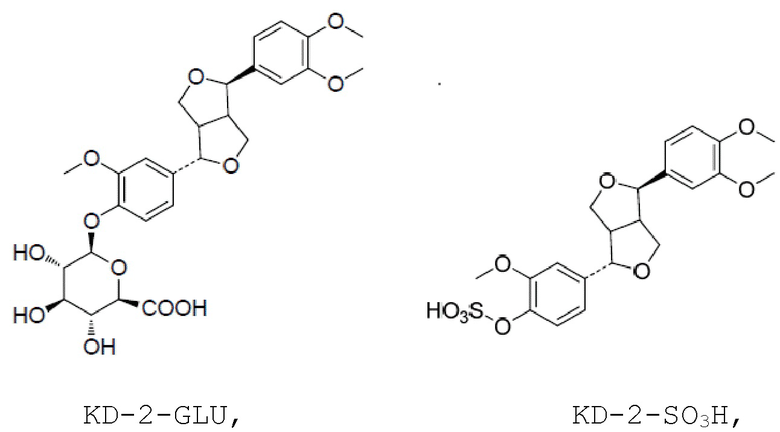
в приготовлении средства для ингибирования белка 3CLpro вируса COVID-19. Предлагаются также способы ингибирования белка 3CLpro вируса COVID-19, включающие стадию взаимодействия белка 3CLpro вируса COVID-19 с филлирином или с любым из указанных выше производных филлирина KD-2-GLU и KD-2-SO3H. Предлагается применение композиции филлирина/филлигенина с весовым отношением филлирина к филлигенину 2~98:2~98 в качестве единственного фармацевтически активного ингредиента в приготовлении лекарственного средства против вируса COVID-19 или лекарственного средства для лечения заболевания, вызываемого вирусом COVID-19, а также способы борьбы с вирусом COVID-19 или лечения заболевания, вызванного вирусом COVID-19, включающие стадию введения нуждающемуся пациенту эффективного количества указанной выше композиции филлирина/филлигенина или лекарственного средства, содержащего такую композицию филлирина/филлигенина в качестве единственного фармацевтически активного ингредиента. Филлирин и указанные выше производные филлирина обладают специфическим ингибирующим действием на белок 3CLpro вируса COVID-19, композиция филлирина/филлигенина проявляет значительное ингибирующее действие на вирус COVID-19 и сверхэкспрессию медиаторов воспаления. 7 н. и 4 з.п. ф-лы, 8 табл., 4 пр., 8 ил.
1. Применение филлирина в приготовлении средства для ингибирования белка 3CLpro вируса COVID-19.
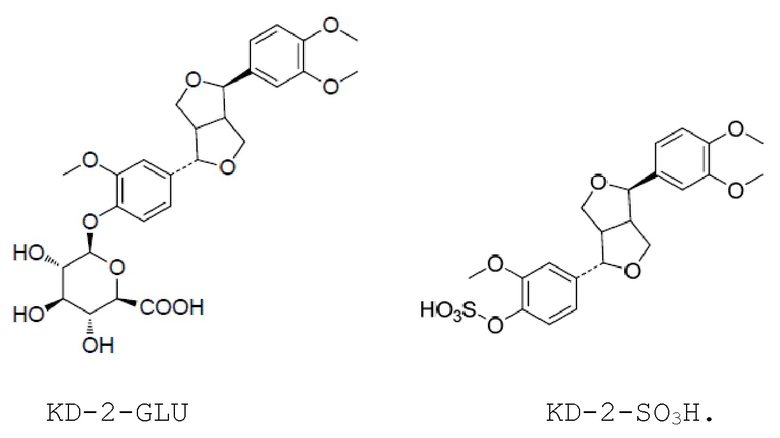
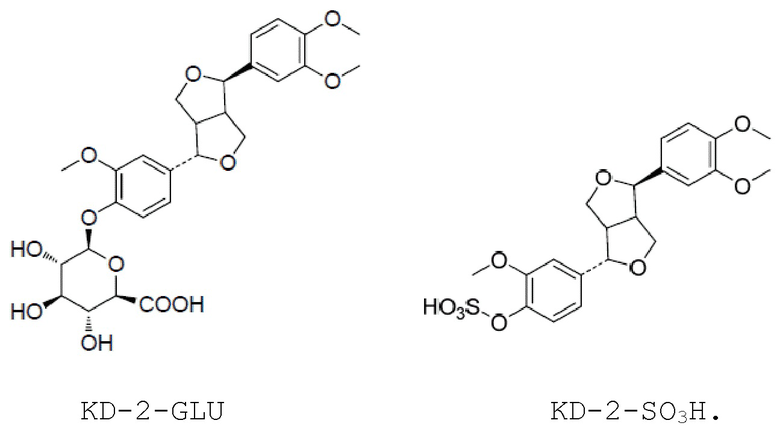
2. Применение производного филлирина в приготовлении средства для ингибирования белка 3CLpro вируса COVID-19, где производное филлирина представляет собой KD-2-GLU, представленное следующей формулой, или KD-2-SO3H, представленное следующей формулой:
3. Способ ингибирования белка 3CLpro вируса COVID-19, включающий стадию взаимодействия белка 3CLpro вируса COVID-19 с филлирином.
4. Способ ингибирования белка 3CLpro вируса COVID-19, включающий стадию взаимодействия белка 3CLpro вируса COVID-19 с производным филлирина, где производное филлирина представляет собой KD-2-GLU, представленное следующей формулой, или KD-2-SO3H, представленное следующей формулой:
5. Применение композиции филлирина/филлигенина в качестве единственного фармацевтически активного ингредиента в приготовлении лекарственного средства против вируса COVID-19 или лекарственного средства для лечения заболевания, вызываемого вирусом COVID-19, где весовое отношение филлирина к филлигенину в композиции филлирина/филлигенина составляет 2~98:2~98.
6. Применение по п. 5, отличающееся тем, что лекарственное средство находится в форме таблетки, капсулы, пилюли, порошка, гранулы, сиропа, раствора, эмульсии, инъекции, спрея, аэрозоля, геля, крема, катаплазмы, адгезивного пластыря или пластыря.
7. Применение по п. 5, отличающееся тем, что композиция филлирина/филлигенина ингибирует белок 3CLpro вируса COVID-19.
8. Способ борьбы с вирусом COVID-19 или лечения заболевания, вызванного вирусом COVID-19, включающий стадию введения нуждающемуся пациенту эффективного количества композиции филлирина/филлигенина, где весовое отношение филлирина к филлигенину в композиции филлирина/филлигенина составляет 2~98:2~98, и эта композиция филлирина/филлигенина используется в качестве единственного фармацевтически активного ингредиента.
9. Способ борьбы с вирусом COVID-19 или лечения заболевания, вызванного вирусом COVID-19, включающий стадию введения нуждающемуся пациенту эффективного количества лекарственного средства, содержащего композицию филлирина/филлигенина, где весовое отношение филлирина к филлигенину в композиции филлирина/филлигенина составляет 2~98:2~98, и эта композиция филлирина/филлигенина используется в качестве единственного фармацевтически активного ингредиента.
10. Способ по п. 8 или 9, отличающийся тем, что лекарственное средство находится в форме таблетки, капсулы, пилюли, порошка, гранулы, сиропа, раствора, эмульсии, инъекции, спрея, аэрозоля, геля, крема, катаплазмы, адгезивного пластыря или пластыря.
11. Способ по п. 8 или 9, отличающийся тем, что композиция филлирина/филлигенина ингибирует белок 3CLpro вируса COVID-19.
Авторы
Даты
2023-09-27—Публикация
2021-02-09—Подача