Область техники, к которой относится изобретение
Данная заявка относится к области биомедицинской технологии. Более конкретно, она касается гуманизованного антитела против PD-1 или его антигенсвязывающего фрагмента и их применения.
Уровень техники
Фактор запрограммированной смерти-1 (PD1) является представителем семейства CD28 и экспрессируется на активированных B-клетках, T-клетках и миелоидных клетках. PD1 человека кодируется геном Pdcd1, расположенным на участке 2q37.3, имеет общую длину 9,6 т.н., состоит из 5 экзонов и 4 интронов и содержит промотор в 663 п.н. перед ним. PD1 представляет собой трансмембранный белок I-го типа в 55 кДа. Его молекулярная структура состоит из внеклеточной области, трансмембранной области и внутриклеточной области. Внеклеточная область содержит один вариабельный домен иммуноглобулина (IgV), а внутриклеточная область содержит ингибирующий мотив иммунорецептора на основе тирозина (ITIM) и мотив переключения иммунорецептора на основе тирозина (ITSM). Аминокислотная последовательность внеклеточной области PD-1 на 24% гомологична последовательности CTLA-4 и на 28% гомологична CD28. После активации T-клеток PD-1 в основном собирает тирозиновые фосфолипазы SHP2 через ITIM, что ведет к дефосфорилированию нижележащих эффекторных молекул.
PD-1 имеет два лиганда: PD-L1 и PD-L2. Оба они являются гомологами B7. Ген PDL расположен на участке 9P24.2 хромосом человека и имеет длину в 42 т.н. И PD-L1, и PD-L2 имеют молекулярную структуру, содержащую один домен типа вариабельного домена иммуноглобулина, один домен типа константной области, одну трансмембранную область и один короткий цитоплазматический хвост.
PD-1 при связывании с PD-L1 и PD-L2 может подавлять активацию T-клеток. PD-L1 экспрессируется на поверхности различных опухолевых клеток, в том числе рака легких, рака желудка, рака печени, рака пищевода, рака почек, рака яичников, рака шейки матки, рака молочной железы, рака кожи, рака толстой кишки, рака мочевого пузыря, глиального рака, рака головы и шеи и плоскоклеточной карциномы полости рта. Кроме того, на периферии этих раковых опухолей обнаруживается большое количество T-клеток CD8+, экспрессирующих PD-L1. Статистика клинических результатов показывает, что высокий уровень экспрессии PD-L1 на опухолевых клетках связан с плохим прогнозом у больных раком.
Сущность изобретения
Техническая проблема, которую должна решить заявка, заключается в преодолении дефектов и недостатков существующих антител с низкой аффинностью связывания и низкой специфичностью к PD-1 путем получения гуманизованного антитела против PD-1 или его антигенсвязывающего фрагмента и их применения.
Целью данной заявки является получение гуманизованного антитела против PD-1 или его антигенсвязывающего фрагмента. Антитело включает область CDR легкой цепи и область CDR тяжелой цепи. Область CDR тяжелой цепи состоит из HCDR1, HCDR2 и HCDR3. Область CDR легкой цепи состоит из LCDR1, LCDR2 и LCDR3. Аминокислотные последовательности HCDR1, HCDR2 и HCDR3 представлены последовательно в SEQIDNO: 8-10, а аминокислотные последовательности LCDR1, LCDR2 и LCDR3 представлены последовательно в SEQIDNO: 11-13. Аминокислотная последовательность вариабельной области тяжелой цепи антитела представлена в любой из SEQIDNO:3-5.
Аминокислотная последовательность вариабельной области легкой цепи антитела представлена в любой из SEQIDNO:6-7.
Заявка также касается нуклеиновой кислоты, вектора, клетки или фармацевтической композиции, относящейся к антителу или его антигенсвязывающему фрагменту.
Заявка также касается применения антитела или его антигенсвязывающего фрагмента и соответствующей им нуклеиновой кислоты, вектора, клетки или фармацевтической композиции при получении лекарственного средства для лечения заболевания или состояния, опосредованных PD-1.
Заявка также касается способа лечения опосредованных PD-1 заболевания или состояния, который включает введение субъекту эффективного количества антитела или его антигенсвязывающего фрагмента, нуклеиновой кислоты, вектора, клеток или фармацевтической композиции.
Заявка также касается антитела или его антигенсвязывающего фрагмента, нуклеиновой кислоты, вектора, клеток или фармацевтической композициидля лечения.
Заявка также касается антитела или его антигенсвязывающего фрагмента, нуклеиновой кислоты, вектора, клеток или фармацевтической композициидля лечения опосредованных PD-1 заболевания или состояния.
Краткое описание фигур
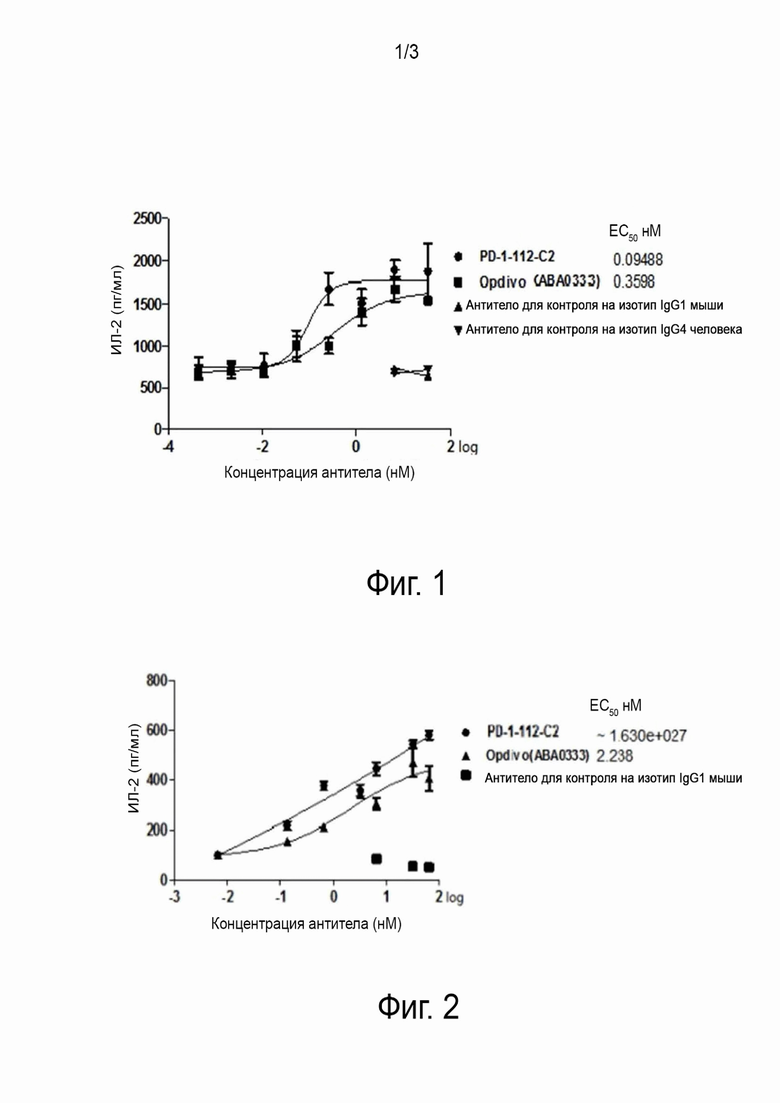
На фиг. 1 представлен график, показывающий влияние различных концентраций PD-1-112-C2 на секрецию ИЛ-2/ИНФ-γ.
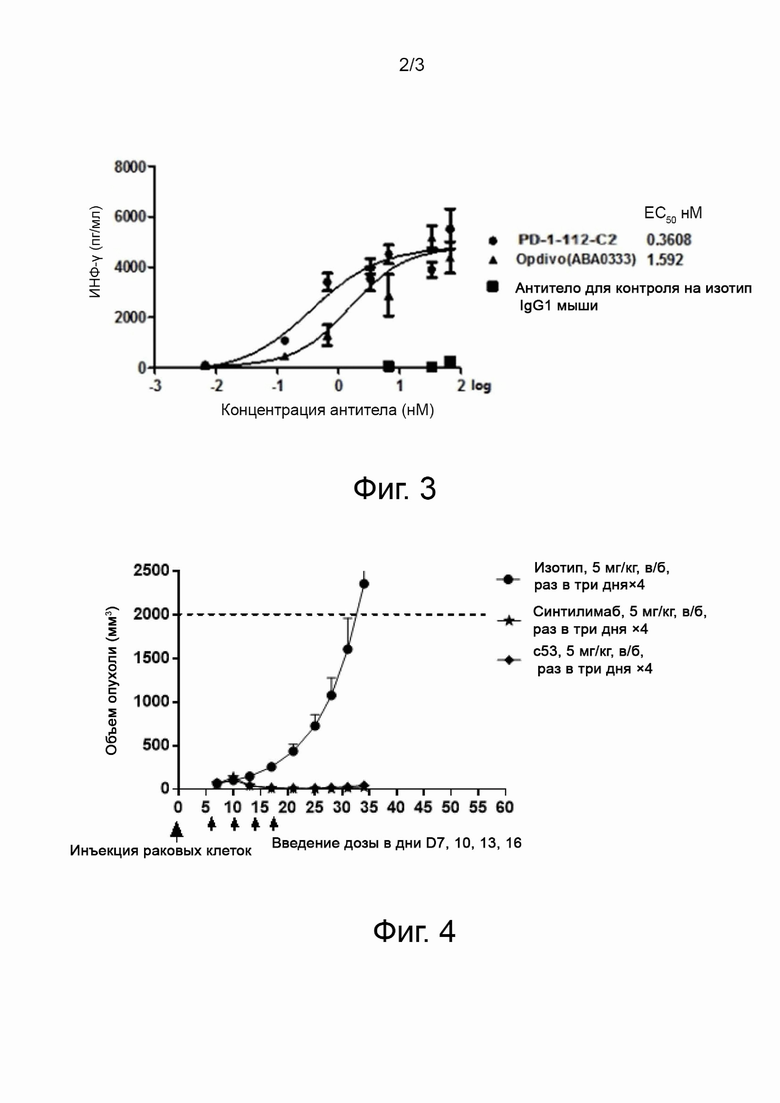
На фиг. 2 представлен график, показывающий влияние различных концентраций PD-1-112-C2 на пролиферацию T-клеток и секрецию ими цитокина ИЛ-2.
На фиг. 3 представлен график, показывающий влияние различных концентраций PD-1-112-C2 на пролиферацию T-клеток и секрецию ими цитокина ИНФ-γ.
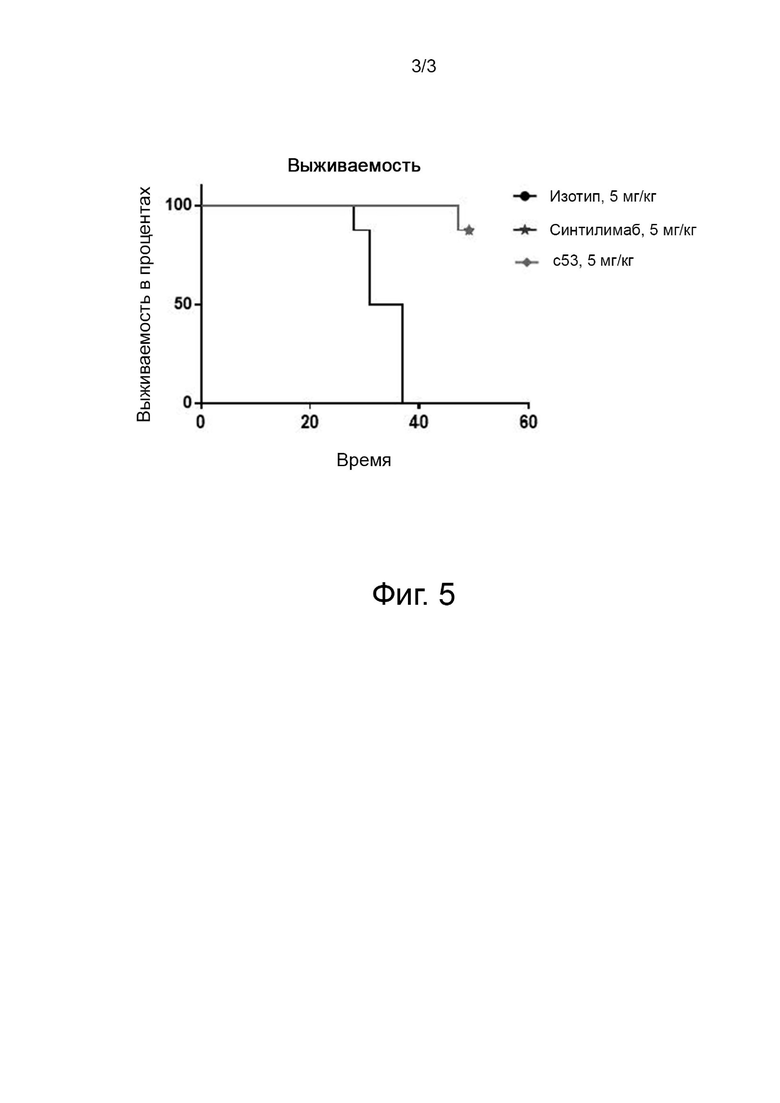
На фиг. 4 представлен график, показывающий влияние гуманизованного антитела c53 против PD-1 на объем опухолей.
На фиг. 5 представлен график, показывающий влияние гуманизованного антитела c53 против PD-1 на выживаемость мышей.
Раскрытие сущности изобретения
Далее настоящее изобретение будет объяснено на конкретных примерах, но эти примеры не ограничивают настоящее изобретение никоим образом. Если не указано иначе, реагенты, методы и устройства, используемые в заявке, представляют собой стандартные для данной области техники реагенты, методы и устройства.
Если не указано иначе, реагенты и материалы, используемые в следующих примерах, коммерчески доступны.
Данная заявка касается гуманизованного антитела против PD-1 или его антигенсвязывающего фрагмента. Антитело включает области CDR легкой цепи и области CDR тяжелой цепи. Области CDR тяжелой цепи состоят из HCDR1, HCDR2 и HCDR3. Области CDR легкой цепи состоят из LCDR1, LCDR2 и LCDR3. Аминокислотные последовательности HCDR1, HCDR2 и HCDR3 представлены последовательно в SEQIDNO:8-10, а аминокислотные последовательности LCDR1, LCDR2 и LCDR3 представлены последовательно в SEQIDNO: 11-13. Аминокислотная последовательность вариабельной области тяжелой цепи антитела представлена в любой из SEQIDNO: 3-5. Аминокислотная последовательность вариабельной области легкой цепи антитела представлена в любой из SEQIDNO: 6-7.
В данной заявке области CDR идентифицируют по системе нумерации Кабата, но области CDR, идентифицированные другими способами, также входят в заявленный объем заявки.
В некоторых воплощениях аминокислотная последовательность вариабельной области тяжелой цепи антитела представлена в SEQ ID NO: 3, а аминокислотная последовательность вариабельной области легкой цепи антитела представлена в SEQ ID NO: 6, или же аминокислотная последовательность вариабельной области тяжелой цепи антитела представлена в SEQ ID NO: 4, а аминокислотная последовательность вариабельной области легкой цепи антитела представлена в SEQ ID NO: 7, или же аминокислотная последовательность вариабельной области тяжелой цепи антитела представлена в SEQ ID NO: 5, а аминокислотная последовательность вариабельной области легкой цепи антитела представлена в SEQ ID NO: 7.
В некоторых воплощениях антитело содержит константную область тяжелой цепи и константную область легкой цепи, причем константная область тяжелой цепи представляет собой любой один или несколько из IgG1, IgG2, IgG3, IgG4, IgA, IgD, IgE или IgM; а константная область легкой цепи представляет собой κ- или λ-цепь.
В некоторых воплощениях вид источника константной области тяжелой цепи и константной области легкой цепи выбран из человека, мыши или обезьяны.
В некоторых воплощениях антитело представляет собой химерное антитело или полиспецифичное антитело (например, биспецифичное антитело).
В данной заявке термин “полиспецифичное антитело” означает такой антигенсвязывающий белок или такое антитело, которое нацелено более чем на один антиген или эпитоп.
В данной заявке термин “биспецифичное антитело” означает полиспецифичный антигенсвязывающий белок или полиспецифичное антитело, которые могут быть получены различными способами, включая, без ограничения, слияние гибридом или соединение Fab′-фрагментов. Например, см. Songsivilai and Lachmann, 1990, Clin. Exp. Immunol. 79: 315-321; Kostelny et al., 1992, J. Immunol. 148:1547-1553. Два сайта связывания биспецифичного антигенсвязывающего белка или антитела должны связываться с двумя разными эпитопами, присутствующими на одном и том же или на разных белках-мишенях.
В данной заявке термин “специфическое связывание” и подобные выражения относятся к связыванию антитела или его антигенсвязывающего фрагмента с эпитопом заданного антигена. Обычно антитело или его антигенсвязывающий фрагмент связывается с аффинностью (KD) примерно менее 10-6 М, например, примерно менее 10-7 М, 10-8 М, 10-9 М или 10-10 М либо меньше. KD означает соотношение скорости диссоциации и скорости ассоциации (koff/kon), величина которых может быть измерена методом, известным специалистам в данной области.
В некоторых воплощениях антигенсвязывающий фрагмент представляет собой любой один или несколько из F(ab′)2, Fab, scFv, Fv и однодоменных антител.
В данной заявке термин “F(ab′)2” охватывает две легкие цепи и две тяжелые цепи, которые содержат часть константной области между доменами CH1 и CH2, образуя межцепочечную дисульфидную связь между двумя тяжелыми цепями. Таким образом, фрагмент F(ab′)2 состоит из двух Fab′-фрагментов, удерживаемых вместе дисульфидной связью между двумя тяжелыми цепями.
В данной заявке термин “Fab” охватывает одну легкую цепь, участок CH1 и вариабельную область одной тяжелой цепи. Тяжелая цепь молекулы Fab не может образовывать дисульфидную связь с другой молекулой тяжелой цепи.
В данной заявке термин “scFv” означает такую молекулу Fv, в которой вариабельные области тяжелой и легкой цепи соединяются гибким линкером с образованием единой полипептидной цепи (которая образует антигенсвязывающую область) (например, см., Birdetal., Science, 242:423-426 (1988); и Hustonetal., Proc. Natl. Acad. Sci. USA, 90:5879-5883 (1988)).
В данной заявке термин “Fv” охватывает вариабельные области тяжелой и легкой цепи, но не содержит константной области.
В данной заявке термин “однодоменное антитело” охватывает только одну вариабельную область тяжелой цепи (VHH) и два обычных участка CH2 и CH3, но они не так легко связываются друг с другом, как искусственно созданное одноцепочечное антитело (scFv), и даже объединяются в блоки. Более важно то, что структура VHH, клонированная и экспрессированная отдельно, обладает структурной стабильностью и антигенсвязывающей активностью, сравнимой с исходной тяжелой цепью антитела, и представляет собой наименьшую известную единицу, способную связываться с целевым антигеном.
Заявка также касается нуклеиновой кислоты, кодирующей гуманизованное антитело против PD-1 или его антигенсвязывающий фрагмент.
В предпочтительном воплощении нуклеиновая кислота включает: первую нуклеиновую кислоту, кодирующую вариабельную область тяжелой цепи антитела или его антигенсвязывающего фрагмента, и/или вторую нуклеиновую кислоту, кодирующую вариабельную область легкой цепи антитела или его антигенсвязывающего фрагмента.
В данной заявке нуклеиновая кислота обычно представлена РНК или ДНК, причем молекула нуклеиновой кислоты может быть одноцепочечной или двухцепочечной, предпочтительно это двухцепочечная ДНК. Нуклеиновая кислота является “функционально связанной”, когда она находится в функциональной связи с другой последовательностью нуклеиновой кислоты. Например, промотор или энхансер функционально связан с кодирующей последовательностью, если промотор или энхансер влияет на транскрипцию кодирующей последовательности. ДНК предпочтительно используется тогда, когда нуклеиновая кислота лигирована в вектор. Более того, поскольку антитело является мембранным белком, то нуклеиновая кислота обычно несет последовательность сигнального пептида.
Заявка также касается вектора, несущего нуклеиновую кислоту.
В данной заявке термин “вектор” означает носитель нуклеиновой кислоты, в который может быть вставлен полинуклеотид. Если вектор может обеспечить экспрессию белка, кодируемого вставленным полинуклеотидом, такой вектор называется экспрессирующим вектором. Вектор может быть введен в клетки хозяина посредством трансформации, трансдукции или трансфекции с тем, чтобы элемент генетического материала, переносимый вектором, мог экспрессироваться в клетке-хозяине. Векторы хорошо известны специалистам в данной области, включают, без ограничения: плазмиды; фагемиды; космиды; искусственные хромосомы, к примеру, искусственные дрожжевые хромосомы (YAC), искусственные бактериальные хромосомы (BAC) или искусственные хромосомы, полученные из P1 (PAC); фаги, к примеру, фаг λ или M13, и вирусы животных и т.п. Вирусы животных, которые можно использовать в качестве вектора, включают, без ограничения, ретровирусы (в том числе и лентивирусы), аденовирусы, аденоассоциированные вирусы, герпесвирусы (например, вирус простого герпеса), поксвирусы, бакуловирусы, папилломавирусы, паповавирусы (например, SV40).
Заявка также касается клеток, несущих нуклеиновую кислоту, содержащих вектор или способных экспрессировать антитело или его антигенсвязывающий фрагмент.
Заявка также касается фармацевтической композиции, включающей указанные антитело или его антигенсвязывающий фрагмент, нуклеиновую кислоту, вектор или клетку.
В данной заявке термин “фармацевтическая композиция” означает такую форму, которая обеспечивает эффективную биологическую активность активного ингредиента и не содержит дополнительных ингредиентов, неприемлемо токсичных для субъекта, которому будет вводиться композиция.
В некоторых воплощениях фармацевтическая композиция дополнительно включает фармацевтически приемлемый носитель и/или наполнитель.
В данной заявке термин “фармацевтически приемлемый носитель” может охватывать всевозможные растворители, дисперсионные среды, покрытия, антибактериальные средства и противогрибковые средства, вещества для изотонизации и замедляющие всасывание вещества и т.п., которые физиологически совместимы и применяются для увеличения срока годности или эффективности антитела.
Кроме того, применение указанных антитела или его антигенсвязывающего фрагмента, нуклеиновой кислоты, вектора, клетки или фармацевтической композиции при получении лекарственного средства для лечения заболевания или состояния, опосредованного PD-1, также должно входить в заявленный объем этой заявки.
В некоторых воплощениях фармацевтическая композиция или лекарственное средство находится в форме, подходящей для инъекций.
В предпочтительном воплощении фармацевтическая композиция или лекарственное средство находится в форме, подходящей для введения посредством подкожной инъекции, внутрикожной инъекции, внутривенной инъекции, внутримышечной инъекции или инъекционное введение в очаг поражения.
Данная заявка имеет следующие полезные эффекты.
Гуманизованное антитело против PD-1 или его антигенсвязывающий фрагмент, представленные в заявке, могут связываться с клетками CHO-hPD1, клетками CHO-cyno и активированными РВМС с высокой аффинностью. У них значительно улучшена аффинность по сравнению с положительным контролем. Они могут эффективно и специфически связываться с PD-1 и эффективно блокировать связывание лигандов PD-L1/PD-L2 с CHO-hPD1. При MLR они могут блокировать связывание PD-1 с лигандами и ингибировать сигнальный путь PD-1, тем самым способствуя пролиферации T-клеток и секреции цитокинов ИЛ-2 и ИНФ-γ. Таким образом, антитело или его антигенсвязывающий фрагмент и соответствующая нуклеиновая кислота, вектор, клетки или фармацевтическая композиция имеют широкие перспективы для применения при получении лекарственного средства для лечения заболевания или состояния, опосредованного PD-1.
Примеры
Пример 1. Получение антител против PD-1
1. Иммуноген
Искусственно синтезировали последовательность PD-1 человека (NCBINP 005009) и использовали верхний праймер: 5′-CCGCAAGCTTGCCGCCACCATG-3′ (SEQIDNO:1) и нижний праймер: 5′-CCGGAATTCTCATTAATGGTGATGGTGATGATGCTGGAACTGGCCGGCAGGTC-3′ (SEQIDNO:2) для ПЦР-амплификации внеклеточного конца последовательности PD-1 человека. Затем внеклеточный конец отщепляли с помощью HindIII и EcoRI и клонировали в эукариотическую систему экспрессии pCDNA3.4A, получая плазмиду. Этой плазмидой трансфецировали клетки 293, собирали супернатант и проводили очистку, получая рекомбинантный белок PD-1 человека (hPD-1).
2. Иммунизация животных
Смешивали 125 мкг рекомбинантного белка hPD-1 при концентрации 1,23 мг/мл в качестве антигена с эквивалентным количеством адъюванта Фрейнда (Sigma-AldrichF5881) в качестве иммунного адъюванта, отбирали пять 6-недельных мышей BALb/C и подвергали подкожной иммунизации, при этом количество вводимого антигена составляло 25 мкг на мышь. После первичной иммунизации раз в неделю проводили повторную (бустерную) иммунизацию при той же дозе. После в совокупности 5 иммунизаций определяли иммунный ответ путем сбора хвостовой крови у мышей. Проводили слияние при помощи FACS-скрининга (как описано ниже), используя мышей с достаточными титрами иммуноглобулина против hPD-1. Через 3 дня после внутрибрюшинной бустерной иммунизации антигеном мышей забивали и извлекали селезенку для слияния клеток.
3. Отбор мышей BALb/C, вырабатывающих антитела против hPD-1
Для отбора мышей BALb/C, вырабатывающих антитела против hPD-1, тестировали сыворотки иммунизированных мышей методом FACS. Разведения сыворотки мышей, иммунизированных рекомбинантным белком hPD-1, инкубировали с трансфецированными hPD1 клетками CHO при 4°C в течение 30 минут, промывали 3 раза ФСБ, а затем добавляли 0,4 мкг/мл козьего конъюгированного с фикоэритрином (PE) антитела против IgG мыши (Biolegend 405307) и инкубировали при 4°C в течение 30 минут. После 3-кратной промывки ФСБ образцы помещали в проточный цитометр фирмы BeckmanCoulter (CytoFLEXA00-1-1102) для проверки того, могут ли они связываться с клетками CHO, трансфицированными hPD1, и отбора мышей BALb/C, вырабатывающих антитела против hPD-1, а затем проводили слияние клеток.
4. Получение гибридом, вырабатывающих мышиные моноклональные антитела против hPD-1
Спленоциты из иммунизированных мышей BALb/c сливали с клетками мышиной миеломы, а затем полученные гибридомы подвергали скринингу на наличие антигенспецифичных антител. Суспензии отдельных клеток из спленоцитов иммунизированных мышей подвергали слиянию с одной пятой клеток мышиной миеломы (SP2/0, ATCCCRL1581), не секретирующих иммуноглобулины, с помощью PEG 1500 (Roche 10783641001). Слившиеся клетки высеивали в 96-луночный планшет для культивирования клеток примерно по 1×105 клеток на лунку, помещали планшет в инкубатор (PanasonicMCO-18AIC) и проводили культивирование при 37°C и 5% CO2. Затем проводили культивирование в селективной среде HAT, то есть среде 1640, содержащей два антибиотика: пенициллин и стрептомицин (Gibco 15140122), 1×HAT (SigmaCRLP-7185) и 20% фетальной телячьей сыворотки (RoyacelRY-F11-01), в течение 1 недели. Через 1 неделю среду HAT заменяли средой HT (среда 1640, содержащая два антибиотика: пенициллин и стрептомицин (Gibco 15140122), 1×HT (Gibco 11067030) и 20% фетальной телячьей сыворотки (RoyacelRY-F11-01) для культивирования, а затем тестировали супернатанты клеточных культур из планшета со слияниями методом FACS для отбора гибридом, секретирующих антитела, способные связываться с белком hPD-1. Гибридомы, секретирующие антитела, способные связываться с белком hPD-1, пересеивали и снова подвергали скринингу. Гибридомы с положительными результатами скрининга на антитела, связывающиеся с белком hPD-1, субклонировали по меньшей мере дважды методом предельного разведения. Затем культивировали стабильные субклоны invitro и получали небольшое количество антител для дальнейшего анализа. Клон гибридомы PD1-112-C2 был выбран для дальнейшего анализа.
Пример 2. Характеристика аффинности мышиного моноклонального антитела против PD-1
Стандартными методами получали клеточную линию CHO (клетки яичников китайского хомячка) (CHO-hPD1), экспрессирующую рекомбинантный PD-1 человека на поверхности клеток, клеточную линию CHO (CHO-cynoPD1), экспрессирующую PD-1 обезьяны (Uniprot: B0LAJ2) на поверхности клеток, и клеточную линию CHO (CHO-mousePD1), экспрессирующую PD-1 мыши (Uniprot: Q02242) на поверхности клеток, по рекомбинантной технологии. Эти линии клеток будут использоваться при проточной цитометрии (FCM) для определения характеристик связывания мышиного моноклонального антитела PD-1-112C2 против PD-1.
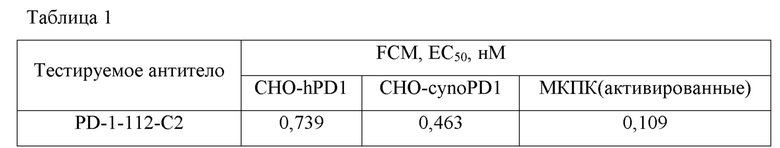
Для оценки связывания мышиного моноклонального антитела против PD-1 с клетками CHO-hPD1 в 96-луночный планшет вносили по 2×105 клеток CHO-hPD1 и добавляли серийные разведения мышиного моноклонального антитела против PD-1 (3-кратные серийные разведения при начальной концентрации 10 мкг/мл) и инкубировали при 4°C в течение 30 минут. Клетки 1 раз промывали буфером (ФСЮ, содержащим 3% БСА), а затем добавляли меченное PE флуоресцентное вторичное антитело против IgG мыши (Fc) Ab (Biolegend), инкубировали при 4°C в течение 30 минут, после чего промывали 1 раз буфером и ресуспендировали в ФСБ. После этого суспензии клеток подвергали анализу методом проточной цитометрии на CytoFlex (проточном цитометре Beckman) и измеряли количество антител, связавшихся с клетками, по средней интенсивности флуоресценции (MFI) окрашивания. Такой же метод применяли для оценки связывания мышиного моноклонального антитела против PD-1 с клетками CHO-cyno и с клетками CHO-mousePD1 (иногда в заявке они сокращенно называются “CHO-mPD1”).
Результаты представлены в таблице 1. Эти данные показывают, что каждое мышиное моноклональное антитело PD-1-112-C2 против PD-1 способно связываться с высокой аффинностью как с клетками CHO-hPD1, так и с клетками CHO-cyno; тогда как все мышиные моноклональные антитела не связывались с клетками CHO-mousePD1.
Пример 3. Связывание антитела против PD-1 с активированными РВМС
При стимуляции ФГА (Sigma) свежих мононуклеарных клеток периферической крови человека (МКПК) активировались и пролиферировали лимфоциты, достигая наибольшего уровня по экспрессии PD1 на третий день, и поэтому их можно было использовать для эксперимента по связыванию антител к PD-1 с PD1, который экспрессировался естественным образом в активированных лимфоцитах.
После получения из свежей периферической крови человека центрифугированием в градиенте среды для разделения лимфатических клеток доводили МКПК до плотности 1 ×106 клеток/мл и инокулировали в T75, а затем добавляли ФГА-L (Sigma) в конечной концентрации 1 мкг/мл для стимулирования пролиферации лимфоцитов. После инкубации при 37°C и 5% CO2 в течение 3 дней клеточную суспензию извлекали и центрифугировали. Супернатант отбрасывали, а осадок ресуспендировали в буфере (ФСБ, содержащий 3% БСА) и вносили в 96-луночный U-образный планшет по 2×105 на лунку, а затем добавляли в общей сложности 10 серийных разведений антител против PD1 при 3-кратных серийных разведениях, начиная с 30 мкг/мл, инкубировали при 4°C в течение 30 минут и центрифугировали при 300 g в течение 5 минут. Клетки промывали 1 раз буфером, добавляли меченное PE флуоресцентное козье антитело против IgG человека (Biolegend) и инкубировали при 4°C в течение 30 минут. Клетки центрифугировали и промывали один раз, а затем ресуспендировали в ФСБ и проводили анализ на проточном цитометре CytoFlex для определения количества антител, связавшихся с МКПК.
Результаты представлены в таблице 1, причем антитело против PD1 способно было связываться с активированными лимфоцитами с высокой аффинностью.
Пример 4. Специфичность связывания мышиного моноклонального антитела против PD1
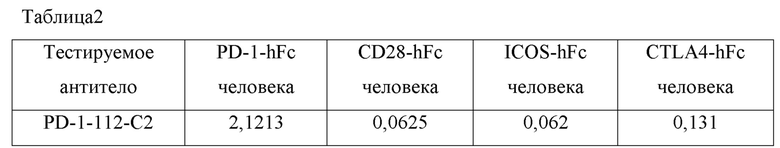
Проводили связывание мышиного моноклонального антитела против PD1 с четырьмя различными белками, представителями семейства CD28, для проверки специфичности антитела при связывании с PD-1. По стандартному методу ELISA на планшете для ELISA иммобилизировали PD-1, CD28, CTLA-4 и ICOS (ACRO) при концентрации в 1 мкг/мл и добавляли мышиное моноклональное антитело против PD-1 человека в концентрации 10 мкг/мл. В качестве вторичного антитела использовали конъюгированное с пероксидазой хрена (HRP) антитело против IgG мыши (Sigma). После проявления с помощью ТМБ и остановки реакции проводили считывание значений OD450 на считывающем устройстве.
Результаты представлены в таблице 2. Каждое мышиное моноклональное антитело PD-1-112C2 против PD-1 было способно специфически связываться с PD-1, но не с другими представителями семейства CD28.
Пример 5. Определение аффинности мышиного моноклонального антитела против PD1 человека методом биослойной интерферометрии (BLI)
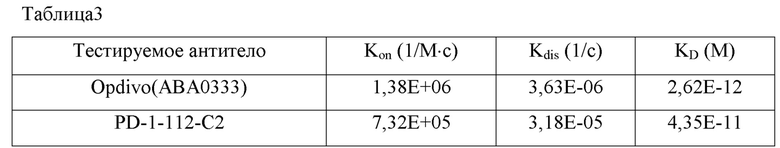
Определение аффинности на ForteBio (OctetQke). На биосенсор HISIK наносили рекомбинантный белок PD-1-his (ACRO) в концентрации 5 мкг/мл на 120 секунд, а затем заполненный сенсор уравновешивали в стандартном буфере (ФСБТ, ФСБ + 0,02% Твин 20) в течение 120 секунд, после чего переносили сенсор в одно разведение мышиного моноклонального антитела против PD-1 и оставляли на 180 секунд для измерения скорости ассоциации, а затем переносили в стандартный буфер на 20 минут для измерения скорости диссоциации. Наконец, проводили анализ с использованием кинетической модели.
Результаты обработки данных представлены в таблице 3.
Пример 6. Блокирование связывания лиганда PD-L1/PD-L2 с CHO-hPD1 мышиным моноклональным антителом против PD-1
На проточном цитометре анализировали способность мышиного моноклонального антитела против PD-1 блокировать связывание лигандов с PD-1, стабильно экспрессированным на поверхности трансфецированных клеток CHO. Белки лигандов, используемые в эксперименте, представляли собой слитые белки рекомбинантного внеклеточного сегмента PD-L1/PD-L2, соединенные с Fc-сегментом IgG человека: PD-L1-hFc (ACRO) и PD-L2-hFc (ACRO).
Клетки CHO-PD1 ресуспендировали в буфере (ФСБ, содержащем 3% БСА) и доводили до плотности 2×106 клеток/мл. Суспензию клеток вносили в 96-луночный U-образный планшет по 100 мкл на лунку и центрифугировали при 300 g в течение 5 минут, а затем отбрасывали супернатант.
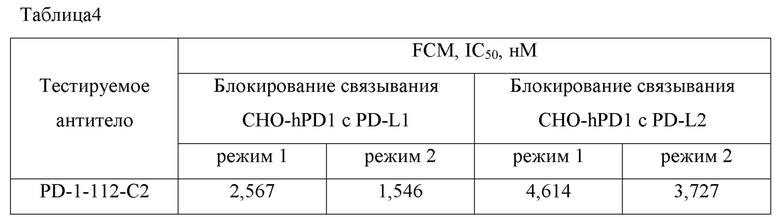
Последующий процесс можно разделить на два режима блокирования: режим 1, при котором в лунки, содержащие клетки, добавляли PD-L1-hFc/PD-L2-hFc в концентрации 3 мкг/мл, инкубировали при 4°C в течение 30 минут, а затем добавляли в общей сложности 10 серийных разведений мышиных моноклональных антител против PD-1 при 3-кратных серийных разведениях, начиная с 30 мкг/мл, и инкубировали при 4°C в течение 30 минут; и режим 2, при котором в лунки, содержащие клетки, добавляли в общей сложности 10 серийных разведений мышиных моноклональных антител против PD-1 при 3-кратных серийных разведениях, начиная с 30 мкг/мл, инкубировали при 4°C в течение 30 минут, а затем добавляли белок PD-L1-hFc/PD-L2-hFc в концентрации 3 мкг/мл и инкубировали при 4°C в течение 30 минут.
Клетки центрифугировали при 300 g в течение 5 минут, промывали 1 раз буфером, добавляли меченное PE флуоресцентное козье антитело против IgG человека (Biolegend) и инкубировали при 4°C в течение 30 минут. Клетки центрифугировали и промывали 1 раз, а затем ресуспендировали в ФСБ и проводили анализ на проточном цитометре CytoFlex для определения количества белка лиганда, связавшегося с клетками, и расчета значения IC50 антитела к PD-1 при блокировании связывания.
Результаты представлены в таблице 4. Мышиное моноклональное антитело PD-1-112-C2 против PD-1 было способно эффективно блокировать связывание PD-L1/PD-L2 с клетками CHO-PD1 в обоих режимах.
Пример 7. Влияние антитела против PD-1 на высвобождение цитокинов из стимулируемых SEB клеток МКПК
В этом примере определяли влияние на секрецию цитокинов в присутствии или в отсутствие антитела против PD-1 при стимуляции культивируемых в течение ночи мононуклеарных клеток периферической крови (МКПК) добавлением энтеротоксина BStaphylococcusaureus (SEB) в качестве суперантигена.
Свежие мононуклеарные клетки периферической крови (МКПК) ресуспендировали в среде X-VIVO 15 (LONZA), содержащей 10% БСА, а затем вносили в культуральную колбу T25 и инкубировали при 37°C и 5% CO2 в течение ночи для культивирования. На следующий день отбирали суспендированные клетки, центрифугировали, а затем ресуспендировали в свежей среде X-VIVO (содержащей 10% БСА) и добавляли SEB в качестве суперантигена (ToxinTechnology) в конечной концентрации 200 нг/мл, а затем вносили в 96-луночный планшет по 1×105 клеток на лунку и при этом добавляли различные концентрации антител против PD-1. Кроме того, ставили две лунки с антителами для контроля на изотип (одна с антителом для контроля на изотип mIgG1 (Biolegend); другая с антителом для контроля на изотип hIgG4 (Biolegend)), а также контрольные лунки без антител. Через 3 дня из лунок отбирали образцы и измеряли уровни ИЛ-2/ИНФ-γ с помощью набора IL2/ИНФ-γ HumanUncoatedELISAKit (eBioscience).
Результаты по влиянию различных концентраций PD-1-112-C2 на секрецию ИЛ-2/ИНФ-γ представлены на фиг. 1. Антитело против PD-1 улучшает секрецию ИЛ-2/ИНФ-γ в зависимости от концентрации. Эти результаты показывают, что в МКПК при стимуляции SEB в качестве суперантигена антитело PD-1-112-C2 против PD-1 было способно еще больше усиливать секрецию цитокинов T-клетками.
Пример 8. Влияние антитела против PD-1 на смешанную лимфоцитарную реакцию
При смешанной лимфоцитарной реакции (MLR) в присутствии или в отсутствие антитела против PD-1 может проявляться пролиферация T-клеток и уровень цитокинов, секретируемых T-клетками, характерный для ситуации, когда блокируется передача сигналов PD1.
Из свежих МКПК выделяли моноциты CD14+ с помощью микрошариков с CD14 человека (Miltenyi), индуцировали их в присутствии ГМ-КСФ/ИЛ-4 в течение 6 дней, затем добавляли ФНО-α и индуцировали созревание клеток ДК через 3 дня. В день эксперимента очищали T-клетки из МКПК с помощью набора для обогащения T-клеток человека EasySep™ (StemCell). Смешивали 1×105 T-клеток с 1×104 клеток ДК и проводили культивирование, а к смешанным клеткам добавляли различные серийные разведения антител против PD-1. Кроме того, ставили две лунки с антителами для контроля на изотип (одна с антителом для контроля на изотип mIgG1 (Biolegend); другая с антителом для контроля на изотип hIgG4 (Biolegend)), а также контрольные лунки без антител. Через 3 дня из смешанной культуры отбирали супернатанты и определяли ИЛ-2, а еще через 2 дня культивирования отбирали супернатанты и определяли ИНФ-γ.
Результаты по влиянию различных концентраций PD-1-112-C2 на пролиферацию T-клеток и секрецию цитокина ИЛ-2 T-клетками представлены на фиг. 2. Результаты по влиянию различных концентраций PD-1-112-C2 на пролиферацию T-клеток и секрецию цитокина ИНФ-γ T-клетками представлены на фиг. 3. Результаты на фиг. 2 и 3 показывают, что в эксперименте по MLR антитело PD-1-112-C2 против PD-1 способно было блокировать связывание PD1 с лигандом в зависимости от концентрации антитела и ингибировать сигнальный путь PD1, тем самым усиливая пролиферацию T-клеток и стимулируя секрецию цитокинов ИЛ-2 и ИНФ-γ T-клетками.
Пример 9. Гуманизация мышиного моноклонального антитела против PD-1
Мышиное моноклональное антитело PD-1-112-C2 против PD-1, полученное выше (аминокислотные последовательности его HCDR1, HCDR2 и HCDR3 представлены последовательно в SEQIDNO: 8-10, а аминокислотные последовательности его LCDR1, LCDR2 и LCDR3 представлены последовательно в SEQIDNO: 11-13, последовательность вариабельной области его тяжелой цепи представлена в SEQIDNO: 14, а последовательность вариабельной области его легкой цепи представлена в SEQIDNO: 15), подвергали гуманизации, а конкретный метод заключался в следующем.
Искусственно синтезировали последовательность PD-1 человека (NCBINP 005009) и клонировали её в эукариотическую систему экспрессии pCDNA3.4A. Этой плазмидой трансфицировали клетки 293, собирали супернатанты и проводили очистку, получая рекомбинантный белок PD-1 человека. Полученным рекомбинантным белком PD-1 человека подкожно иммунизировали самок мышей BALb/C. Спленоциты от иммунизированных мышей BALb/c сливали с клетками мышиной миеломы, а затем полученные гибридомы подвергали скринингу на наличие антигенспецифичных антител. Гибридомы с положительными результатами скрининга на антитела, связывающиеся с белком hPD-1, субклонировали по меньшей мере дважды методом предельного разведения, а затем культивировали стабильные субклоны invitro для получения небольшого количества антител, которые подвергали дальнейшему скринингу для получения клонов PD-1-112-C2.
SEQ ID NO: 14:
QVQLQQPGAELVKPGASVKLSCKASGYTFTTYYMYWVKQRPGQGLEWIGGINPSNGGTNFNEKFKSKATLTVDKSSSTAYMQLSSLTSEDSAVYYCTRRDSNYDGGFDYWGQGTTLTVSS.
SEQ ID NO: 15:
DIVLTQSPASLAVSLGQRATISCRASKSVSTSGYSYMHWYQQKPGQPPKLLIYLAYHLESGVPARFSGSGSGTDFTLNIHPVEEEDAATYYCQHSWELPITFGSGTKLEIKR.
Обращаясь к SEQIDNO: 14 и SEQIDNO: 15: гуманизованные матрицы, которые лучше всего соответствуют их участкам не, являющимися CDR, были выбраны из базы данных Germline. Матрица для тяжелой цепи антитела - IGHV1, а матрица для легкой цепи антитела - IGKV1. В соответствии с принципом повышения структурной стабильности без влияния на структурную стабильность антитела, без влияния на связывание антитела с антигеном, без введения сайтов модификации белка типа гликозилирования и фосфорилирования и без введения таких сайтов, которые легко окисляются или аминируются, гуманизованную последовательность тяжелой цепи составляли в виде VH1-5, а гуманизованную последовательность легкой цепи составляли в виде VL1-3, и, при этом, принимая IGKV7-3*01 с наибольшей гомологией в качестве другого набора гуманизованных матриц для легкой цепи, была составлена гуманизованная последовательность VL-4. Для получения гуманизованных антител форма образования пары легкой и тяжелой цепей была составлена в виде IGHV1/IGKV2 в качестве общей формы образования пар.
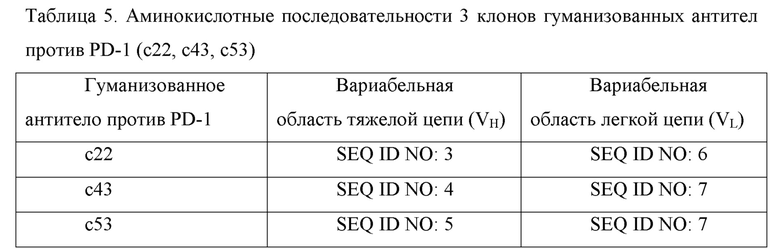
Гены синтезировали в соответствии с аминокислотной последовательностью каждой легкой и тяжелой цепи гуманизированных антител и подвергали расщеплению двумя ферментами: HindIII (NEB) и EcoRI (NEB). Затем фрагменты генов вставляли в экспрессирующий вектор pDNA3.4A (Invitrogen) по сайтам расщепления ферментами HindIII/EcoRI (NEB) с помощью ДНК-лигазы T4 (TAKARA 2011A). Экспрессирующим вектором трансфицировали клетки HEK293 (LifeTechnologies, кат. № 11625019) с помощью реагента для трансфекции полиэтиленимина (PEI) (PolyscienceInc., кат. № 23966) в соотношении 1:2, которые помещали в инкубатор с CO2 и культивировали в течение 5-7 дней. Экспрессированные антитела выделяли центрифугированием, а затем очищали стандартным методом, получая гуманизованные антитела против PD-1 (c11, c21, c31, c41, c51, c12, c22, c32, c42, c52, c43, c53, c44, c54) по настоящей заявке, причем аминокислотные последовательности 3 клонов гуманизованных антител против PD-1 (c22, c43, c53) представлены в таблице 5.
SEQ ID NO:3:
QVQLVQSGAEVKKPGASVKVSCKASGYTFTTYYMYWVRQAPGQGLEWMGGINPSNGGTNFNEKFKSRVTMTVDKSTSTAYMELSSLRSEDTAVYYCTRRDSNYDGGFDYWGQGTTVTVSS.
SEQ ID NO:4:
QVQLVQSGAEVKKPGASVKVSCKASGYTFTTYYMYWVRQAPGQGLEWIGGINPSNGGTNYAEKFKGRVTLTVDTSTSTAYMELSSLRSEDTAVYYCTRRDSNYDGGFDYWGQGTTVTVSS.
SEQ ID NO:5:
QVQLVQSGAEVKKPGASVKVSCKASGYTFTTYYMYWVRQAPGQGLEWMGGINPSNGGTNYAQKFQGRATMTVDTSTSTAYMELSSLRSEDTAVYYCTRRDSNYDGGFDYWGQGTTVTVSS.
SEQ ID NO:6:
DIQLTQSPSSLSASVGDRATITCRASKSVSTSGYSYMHWYQQKPGKAPKLLIYLAYHLESGVPSRFSGSGSGTDFTLTISSVQPEDFATYYCQHSWELPITFGQGTKLEIKR.
SEQ ID NO: 7:
DIQMTQSPSSLSASVGDRVTITCRASKSVSTSGYSYMHWYQQKPGKAPKLLIYLAYHLESGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHSWELPITFGQGTKLEIKR.
Пример 10. Характеристика аффинности гуманизованных антител против PD-1
1. Экспериментальный метод
По рекомбинантной технологии получали клеточные линии CHO (клетки яичников китайского хомячка), CHO-hPD1, способные экспрессировать рекомбинантный PD-1 человека на поверхности клеток, и клеточные линии CHO, CHO-cynoPD1, способные экспрессировать PD-1 обезьяны на поверхности клеток. Эти две линии клеток будут использоваться при проточной цитометрии (FCM) для определения характеристик связывания гуманизованных моноклональных антител-кандидатов против PD-1 (c22, c43, c53). Конкретный метод заключался в следующем.
Для оценки связывания гуманизованных антител с CHO-hPD1 в 96-луночный планшет вносили по 2×105 клеток CHO-hPD1, добавляли серийные разведения гуманизованных антител (3-кратные серийные разведения при начальной концентрации 30 мкг/мл) и инкубировали при 4°C в течение 30 минут. Клетки 1 раз промывали буфером (ФСБ, содержащим 3% БСА), а затем добавляли меченное PE флуоресцентное вторичное антитело против IgG человека (Fc) Ab (Biolegend), инкубировали при 4°C в течение 30 минут, после чего промывали 1 раз буфером и ресуспендировали в ФСБ. После этого суспензии клеток подвергали анализу методом проточной цитометрии на CytoFlex (проточном цитометре Beckman) и измеряли количество антител, связавшихся с клетками, по средней интенсивности флуоресценции (MFI) окрашивания. Такой же метод применялся для оценки связывания гуманизованных антител с клетками CHO-cyno.
2. Экспериментальные результаты
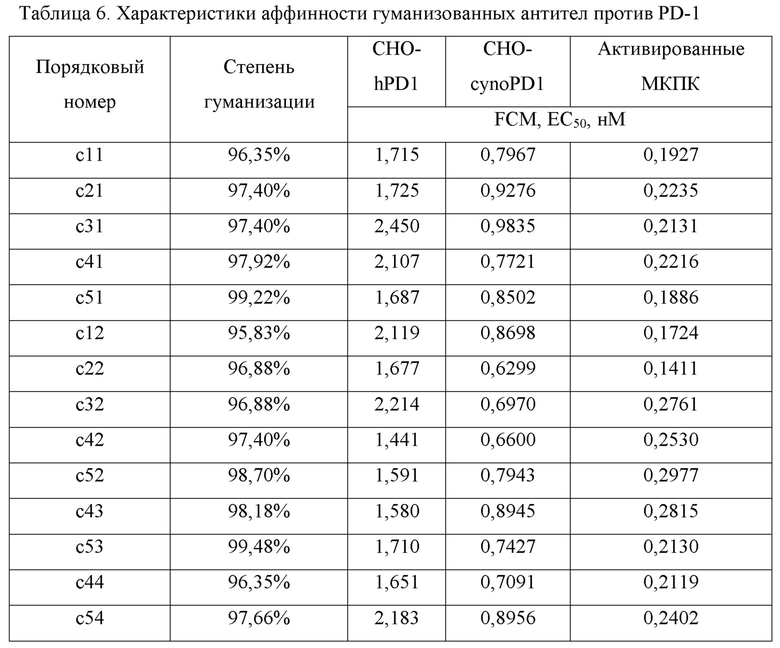
Характеристики аффинности гуманизованных антител против PD-1 представлены в таблице 6, и результаты показывают, что гуманизованные антитела против PD-1 по настоящей заявке способны связываться с высокой аффинностью как с клетками CHO-hPD1, так и с клетками CHO-cynoPD1.
Пример 11. Связывание гуманизованных антител против PD-1 с активированными МКПК
1. Экспериментальный метод
При стимуляции ФГА (Sigma) свежих мононуклеарных клеток периферической крови человека (МКПК) лимфоциты активировались и пролиферировали, достигая наибольшего уровня по экспрессии PD1 на третий день, поэтому их можно было использовать для эксперимента по связыванию гуманизованных антител против PD-1 (c22, c43, c53) с PD1, который экспрессируется естественным образом в активированных лимфоцитах. Конкретный метод заключался в следующем.
После получения из свежей периферической крови человека центрифугированием в градиенте среды для разделения лимфатических клеток доводили МКПК до плотности 1 ×106 клеток/мл и инокулировали в T75, а затем добавляли ФГА-L (Sigma) в конечной концентрации 1 мкг/мл для стимулирования пролиферации лимфоцитов. После инкубации при 37°C и 5% CO2 в течение 3 дней клеточную суспензию извлекали и центрифугировали. Супернатант отбрасывали, а осадок ресуспендировали в буфере (ФСБ, содержащий 3% БСА) и вносили в 96-луночный U-образный планшет по 2×105 на лунку, а затем добавляли различные серийные разведения гуманизованных антител, инкубировали при 4°C в течение 30 минут и центрифугировали при 300 g в течение 5 минут. Клетки промывали 1 раз буфером, добавляли меченное PE флуоресцентное козье антитело против IgG человека (Biolegend) и инкубировали при 4°C в течение 30 минут. Затем клетки центрифугировали и промывали 1 раз, а затем ресуспендировали в ФСБ и проводили анализ на проточном цитометре CytoFlex для определения количества антител, связавшихся с МКПК.
2. Экспериментальные результаты
Результаты по определению способности к связыванию гуманизированных антител против PD-1 с активированными МКПК представлены в таблице 6, причем результаты показывают, что гуманизованные антитела против PD-1 по настоящей заявке способны связываться с активированными лимфоцитами с высокой аффинностью.
По сравнению с мышиным моноклональным антителом PD1-112-C2 против PD-1 (таблица 1) из примеров 2 и 3, гуманизованные антитела против PD-1 (c22, c43, c53) по настоящей заявке обладали сравнимой способностью к связыванию с клетками CHO-hPD1, клетками CHO-cyno и активированными МКПК.
Пример 12. Специфичность связывания гуманизованных антител против PD-1
1. Экспериментальный метод
Проводили связывание гуманизованных антител против PD-1 (c22, c43, c53) по настоящей заявке с четырьмя различными белками-представителями семейства CD28 для проверки специфичности гуманизованных антител против PD-1 при связывании с PD-1. По стандартному методу ELISA на планшете для ELISA иммобилизировали PD-1 (Acro), CD28 (Acro), CTLA-4 (Acro) и ICOS (Acro), соответственно, при концентрации в 1 мкг/мл и добавляли гуманизованное антитело в концентрации 10 мкг/мл. В качестве вторичного антитела использовали конъюгированное с пероксидазой хрена (HRP) антитело против IgG человека (F). После проявления с помощью ТМБ и остановки реакции проводили считывание значений OD450 на считывающем устройстве.
2. Экспериментальные результаты
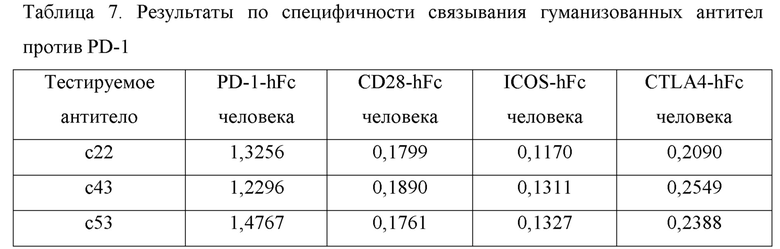
Результаты по специфичности связывания гуманизованных антител против PD-1 представлены в таблице 7, причем эти результатыпоказывают, что гуманизованные антитела против PD-1 по настоящей заявке способны были специфически связываться с PD-1, но не с другими представителями семейства CD28.
Пример 13. Определение аффинности гуманизованных антител против PD-1
1. Экспериментальный метод
Определение аффинности на ForteBio (OctetQke). На биосенсор HISIK наносили рекомбинантный белок PD-1-his в концентрации 5 мкг/мл на 120 секунд, а затем заполненный сенсор уравновешивали в стандартном буфере (ФСБТ, ФСБ + 0,02% Твин 20) в течение 120 секунд, после чего переносили сенсор в одно разведение гуманизованного антитела против PD-1 (c22, c43, c53) и оставляли на 180 секунд для измерения скорости ассоциации, а затем переносили в стандартный буфер на 20 минут для измерения скорости диссоциации. Наконец, проводили анализ с использованием кинетической модели, а также проводили обработку данных. В качестве положительного контроля использовали Opdivo (ABA0333).
2. Экспериментальные результаты
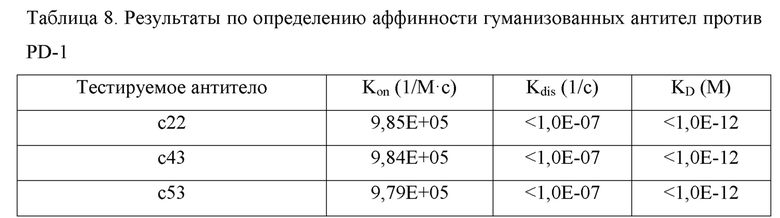
Результаты по определению аффинности гуманизованных антител против PD-1 представлены в таблице 8, и они показывают, что все гуманизованные антитела против PD-1 по настоящей заявке способны были связываться с PD-1 с высокой аффинностью.
По сравнению с мышиным моноклональным антителом PD-1-112-C2 против PD-1 (таблица 3) из примера 5, гуманизованные антитела против PD-1 по настоящей заявке обладали сравнимой аффинностью, а по сравнению с положительным контролем Opdivo (таблица 3) аффинность гуманизованных антител против PD-1 по настоящей заявке значительно улучшалась.
Пример 14. Блокирование связывания лиганда PD-L1/PD-L2 с CHO-hPD1 гуманизованными антителами против PD-1
1. Экспериментальный метод
На проточном цитометре анализировали способность гуманизированных антител против PD-1 блокировать связывание лигандов с трансфецированными клетками CHO, способными стабильно экспрессировать PD-1 на своей поверхности. Белки лигандов, используемые в эксперименте, представляли собой слитые белки рекомбинантного внеклеточного сегмента PD-L1/PD-L2, соединенные с Fc-сегментом IgG1 мыши: PD-L1-mFc и PD-L2-mFc. Белками лигандов в эксперименте служили два рекомбинантных слитых белка: PD-L1-mFc и PD-L2-mFc, которые образовались при соединении внеклеточных сегментов PD-L1/PD-L2 с Fc-сегментом IgG1 мыши.
Клетки CHO-PD1 ресуспендировали в буфере (ФСБ, содержащем 3% БСА) и доводили до плотности 2×106 клеток/мл. Суспензию клеток вносили в 96-луночный U-образный планшет по 100 мкл на лунку и центрифугировали при 300 g в течение 5 минут, а затем отбрасывали супернатант. В лунки, содержащие клетки, добавляли PD-L1-mFc/PD-L2-mFc в концентрации 0,2 мкг/мл, инкубировали при 4°C в течение 30 минут, а затем добавляли серийные разведения гуманизованных антител против PD-1 (c22, c43, c53) и инкубировали при 4°C в течение 30 минут.
Клетки центрифугировали при 300 g в течение 5 минут, промывали 1 раз буфером, добавляли меченное PE флуоресцентное козье антитело против IgG мыши (Biolegend) и инкубировали при 4°C в течение 30 минут. Клетки центрифугировали и промывали 1 раз, а затем ресуспендировали в ФСБ и проводили анализ на проточном цитометре CytoFlex для определения количества белка лиганда, связавшегося с клетками, и расчета значения IC50 антитела к PD-1 при блокировании связывания.
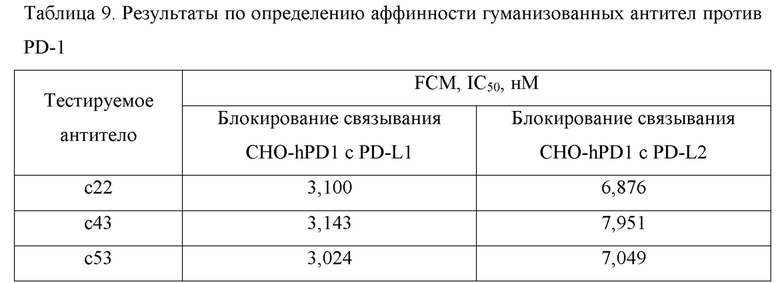
2. Экспериментальные результаты
Результаты по определению аффинности гуманизованных антител против PD-1 представлены в таблице 9, и эти результаты показывают, что все гуманизованные антитела против PD-1 по настоящей заявке способны были эффективно блокировать связывание PD-L1/PD-L2 с клетками CHO-PD1.
Пример 15. Влияние гуманизованных антител против PD-1 на смешанную лимфоцитарную реакцию
1. Экспериментальный метод
При смешанной лимфоцитарной реакции (MLR) в присутствии или в отсутствие гуманизованных антител против PD-1 может проявляться пролиферация T-клеток и уровень цитокинов, секретируемых T-клетками, характерный для ситуации, когда блокируется передача сигналов PD1. Конкретный метод заключался в следующем.
Из свежих МКПК выделяли моноциты CD14+ с помощью микрошариков с CD14 человека (Miltenyi), индуцировали их в присутствии ГМ-КСФ/ИЛ-4 в течение 6 дней, затем добавляли TNF-α и индуцировали созревание клеток ДК через 3 дня. В день эксперимента очищали T-клетки из МКПК с помощью набора для обогащения T-клеток человека EasySep™ (StemCell). Смешивали по 1×105 T-клеток с 1×104 клеток ДК на лунку и проводили культивирование, а к смешанным клеткам добавляли различные серийные разведения гуманизованных антител против PD-1 (c22, c43, c53). Кроме того, ставили одну лунку с антителом для контроля на изотип и контрольную лунку без антител. Через 3 дня из смешанной культуры отбирали супернатанты и определяли ИЛ-2, а еще через 2 дня культивирования отбирали супернатанты и определяли ИНФ-γ.
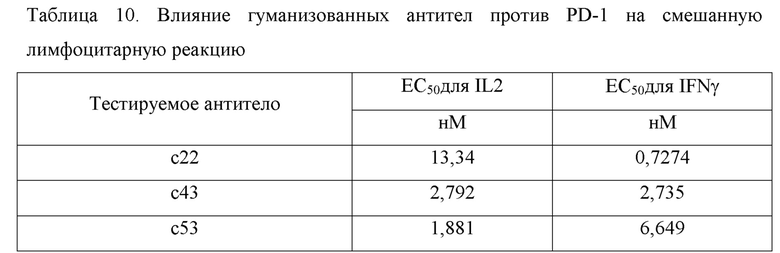
2. Экспериментальные результаты
Результаты по влиянию гуманизованных антител против PD-1 на смешанную лимфоцитарную реакцию представлены в таблице 10. Эти результаты показывают, что в эксперименте по MLR гуманизованные антитела против PD-1 по настоящей заявке способны блокировать связывание PD1 с лигандом и ингибировать сигнальный путь PD1, тем самым усиливая пролиферацию T-клеток и стимулируя секрецию цитокинов ИЛ-2 и ИНФ-γ T-клетками.
Пример 16. Оценка противоопухолевого действия гуманизованного антитела против PD-1 invivo на раковых клетках толстой кишки мыши
1. Экспериментальный метод
Цель эксперимента: определить противоопухолевое действие гуманизованного антитела против PD-1 (c53) invivo против раковых клеток толстой кишки мышей (клеток MC38), в группе контроля на изотип (Isotype) и в группе положительного контроля (Sintilimab) одновременно.
Экспериментальные материалы: 6-8-недельные самки мышей с внедренным геном hPD1 Knock-in (на фоне C57BL/6, источник: BeijingVitalstarBiotechnologyCo., Ltd.); клетки MC38 (NationalInfrastructureofCellLineResources); БСА (Gibco, 10091-148), 0,25% трипсин-ЭДТА (Gibco, 25200056), ДМСО (Sigma, D2650), фосфатно-солевой буфер Дюльбекко (Hyclone, SH30028.02), пенициллин-стрептомицин (Gibco, 15140122), среда DMEM с высоким содержанием глюкозы (Gibco, 11965084), фетальная телячья сыворотка (Gibco) и глутамин (Gibco).
Приборы и оборудование: электронные весы (ShanghaiSunnyHengpingScientificInstrumentCo., Ltd., JA12002), штангенциркуль (ShanghaiMenetIndustrialCo., Ltd., MNT-150T), микроскоп (ChongqingOptecInstrumentCo., Ltd., BDS200), медицинская центрифуга (HunanXiangyiLaboratoryInstrumentDevelopmentCo., Ltd., L530R), водяная баня с постоянной температурой и цифровым дисплеем (PrecisionMachineryCo., Ltd., HH-S), инкубатор с углекислым газом (PanasonicHealthcareCo., Ltd., Япония, MCO-18AC), двойной сверхчистый рабочий стол вертикального типа (WuxiYichunPurificationEquipmentCo., Ltd., SW-CJ-VS2).
Экспериментальные операции
Культивирование клеток: клетки MC38 культивировали в среде DMEM с высоким содержанием глюкозы, содержащей 10% фетальной телячьей сыворотки, 1% глутамина и 1% пенициллина-стрептомицина (1:1).
Инокуляция: собирали клетки MC38 в логарифмической фазе роста и доводили до концентрации 3×106 клеток/мл. Отбирали 40 самок мышей hPD1 и инокулировали им подкожно клетки MC38 в объеме 0,1 мл на мышь, т.е. 3×105 клеток на мышь.
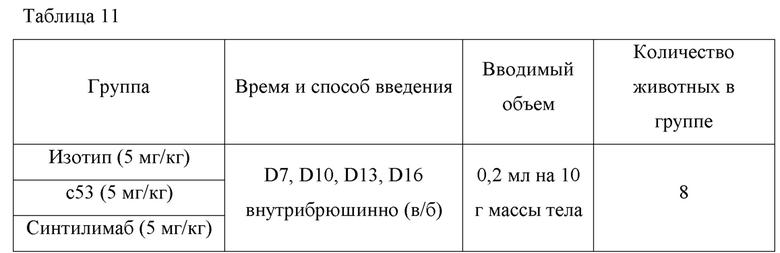
Введение: день инокуляции регистрировали как день 0 (D0). На 7-й день мышей случайным образом разбивали на 3 группы в зависимости от объема опухолей, по 8 мышей в каждой группе, и начинали введение (вводимая доза, способ и частота введения клеток модели опухоли MC38 представлены в таблице 11).
Регистрация данных: измерение и запись объема опухолей начинали в D7, а затем два раза в неделю штангенциркулем измеряли длину и ширину опухолей. Объем опухолей рассчитывали по формуле: (1/2)×длина×(ширина)2. Когда мыши достигали конечной точки эксперимента (объем опухолей превышал 2000 мм3, достигая конечной точки с точки зрения гуманности), мышей забивали путем смещения шейных позвонков и регистрировали кривую выживаемости.
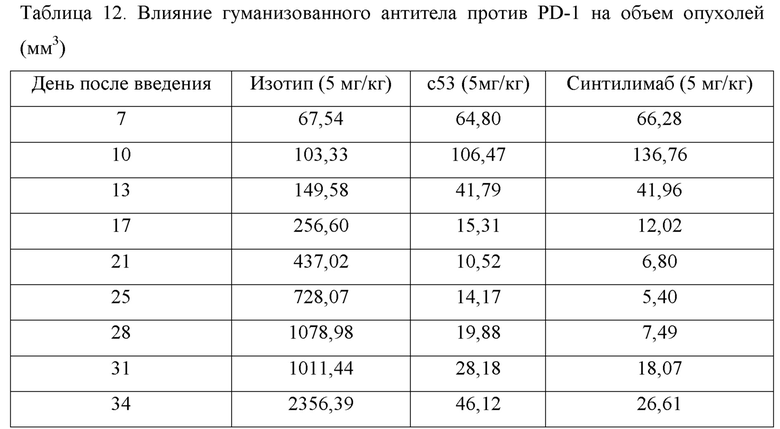
2. Экспериментальные результаты
Результаты по влиянию гуманизованного антитела против PD-1 на объем опухолей представлены в таблице 12 и на фиг. 4. Видно, что по сравнению с группой изотипа гуманизованное антитело против PD-1 (c53) оказывало значительный ингибирующий эффект на рост опухолей на модели опухолей MC38 (TGI = 104,44%, у 7 мышей было полное устранение опухолей), что сравнимо с противоопухолевым эффектом в группе синтилимаба (TGI = 105,81%, 7 мышей были полностью свободны от опухолей).
Результаты по влиянию гуманизованного антитела против PD-1 на выживаемость мышей представлены на фиг. 5. Видно, что по сравнению с группой изотипа гуманизованное антитело против PD-1 (c53) явно повышало выживаемость мышей.
Приведенные выше результаты показывают, что гуманизованное антитело против PD-1 (c53), представленное в настоящей заявке, способно значительно ингибировать рост клеток MC38, эффективно повышать выживаемость мышей и оказывать значительный лечебный эффект при лечении рака толстой кишки у мышей.
Вышеприведенные воплощения являются предпочтительными воплощениями настоящей заявки. Однако реализация настоящей заявки не ограничивается приведенными выше воплощениями. Любые другие изменения, модификации, замены, комбинации и упрощения, произведенные без отхода от духовной сущности и принципа настоящей заявки, должны быть эквивалентным способом замены, и все они включены в заявленный объем настоящей заявки.
--->
SEQUENCE LISTING
<110> Guangdong Fapon Biopharma Inc.
<120> ANTI-PD-1 HUMANIZED ANTIBODY OR ANTIGEN-BINDING FRAGMENT THEREOF
AND APPLICATION THEREOF
<130> PN214664FPSW
<150> CN202110654827.4
<151> 2021-06-11
<160> 15
<170> PatentIn version 3.5
<210> 1
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Forward primer
<400> 1
ccgcaagctt gccgccacca tg 22
<210> 2
<211> 53
<212> DNA
<213> Artificial Sequence
<220>
<223> Reverse primer
<400> 2
ccggaattct cattaatggt gatggtgatg atgctggaac tggccggcag gtc 53
<210> 3
<211> 120
<212> PRT
<213> Artificial Sequence
<220>
<223> c22 VH
<400> 3
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Thr Tyr
20 25 30
Tyr Met Tyr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Asn Pro Ser Asn Gly Gly Thr Asn Phe Asn Glu Lys Phe
50 55 60
Lys Ser Arg Val Thr Met Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Arg Asp Ser Asn Tyr Asp Gly Gly Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 4
<211> 120
<212> PRT
<213> Artificial Sequence
<220>
<223> c43 VH
<400> 4
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Thr Tyr
20 25 30
Tyr Met Tyr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gly Ile Asn Pro Ser Asn Gly Gly Thr Asn Tyr Ala Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Val Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Arg Asp Ser Asn Tyr Asp Gly Gly Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 5
<211> 120
<212> PRT
<213> Artificial Sequence
<220>
<223> c53 VH
<400> 5
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Thr Tyr
20 25 30
Tyr Met Tyr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Asn Pro Ser Asn Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Met Thr Val Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Arg Asp Ser Asn Tyr Asp Gly Gly Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 6
<211> 112
<212> PRT
<213> Artificial Sequence
<220>
<223> c22 VL
<400> 6
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Ala Thr Ile Thr Cys Arg Ala Ser Lys Ser Val Ser Thr Ser
20 25 30
Gly Tyr Ser Tyr Met His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
35 40 45
Lys Leu Leu Ile Tyr Leu Ala Tyr His Leu Glu Ser Gly Val Pro Ser
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Val Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His Ser Trp
85 90 95
Glu Leu Pro Ile Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
<210> 7
<211> 112
<212> PRT
<213> Artificial Sequence
<220>
<223> c43/c53 VL
<400> 7
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Lys Ser Val Ser Thr Ser
20 25 30
Gly Tyr Ser Tyr Met His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
35 40 45
Lys Leu Leu Ile Tyr Leu Ala Tyr His Leu Glu Ser Gly Val Pro Ser
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His Ser Trp
85 90 95
Glu Leu Pro Ile Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
<210> 8
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> HCDR1
<400> 8
Thr Tyr Tyr Met Tyr
1 5
<210> 9
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> HCDR2
<400> 9
Gly Ile Asn Pro Ser Asn Gly Gly Thr Asn Phe Asn Glu Lys Phe Lys
1 5 10 15
Ser
<210> 10
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> HCDR3
<400> 10
Arg Asp Ser Asn Tyr Asp Gly Gly Phe Asp Tyr
1 5 10
<210> 11
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> LCDR1
<400> 11
Arg Ala Ser Lys Ser Val Ser Thr Ser Gly Tyr Ser Tyr Met His
1 5 10 15
<210> 12
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> LCDR2
<400> 12
Leu Ala Tyr His Leu Glu Ser
1 5
<210> 13
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> LCDR3
<400> 13
Gln His Ser Trp Glu Leu Pro Ile Thr
1 5
<210> 14
<211> 120
<212> PRT
<213> Artificial Sequence
<220>
<223> Heavy chain variable region
<400> 14
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Thr Tyr
20 25 30
Tyr Met Tyr Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gly Ile Asn Pro Ser Asn Gly Gly Thr Asn Phe Asn Glu Lys Phe
50 55 60
Lys Ser Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Arg Asp Ser Asn Tyr Asp Gly Gly Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Leu Thr Val Ser Ser
115 120
<210> 15
<211> 112
<212> PRT
<213> Artificial Sequence
<220>
<223> Light chain variable region
<400> 15
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Arg Ala Ser Lys Ser Val Ser Thr Ser
20 25 30
Gly Tyr Ser Tyr Met His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Leu Ala Tyr His Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Asn Ile His
65 70 75 80
Pro Val Glu Glu Glu Asp Ala Ala Thr Tyr Tyr Cys Gln His Ser Trp
85 90 95
Glu Leu Pro Ile Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Антитело против PD-1 и его применение | 2017 |
|
RU2739610C1 |
| АНТИТЕЛА ПРОТИВ БЕЛКА-1 ЗАПРОГРАММИРОВАННОЙ КЛЕТОЧНОЙ СМЕРТИ (PD-1) И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2725950C1 |
| АНТИТЕЛО, НАЦЕЛЕННОЕ НА CD47, И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2832773C1 |
| НОВЫЕ КОМПОЗИЦИИ АНТИТЕЛ ДЛЯ ИММУНОТЕРАПИИ РАКА | 2019 |
|
RU2804490C2 |
| АНТИТЕЛО ПРОТИВ TNFR2 И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2793165C1 |
| АНТИ-ГАЛЕКТИН-9 АНТИТЕЛО И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2840501C1 |
| ГУМАНИЗИРОВАННОЕ АНТИТЕЛО ПРОТИВ PD-1 И ЕГО ПРИМЕНЕНИЕ | 2019 |
|
RU2803460C2 |
| АНТИТЕЛА ПРОТИВ PD-L1 И ИХ ВАРИАНТЫ | 2017 |
|
RU2770590C2 |
| АНТИТЕЛА ПРОТИВ OX40 И ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2783314C2 |
| БИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА, СПЕЦИФИЧЕСКИ СВЯЗЫВАЮЩИЕСЯ С PD1 И LAG3 | 2018 |
|
RU2778805C2 |
Изобретение относится к области биотехнологии, а именно к гуманизованному антителу против PD-1 и его антигенсвязывающему фрагменту, а также к композиции, его содержащей. Также раскрыты нуклеиновая кислота, кодирующая вышеуказанное антитело или его фрагмент, а также вектор и клетка, ее содержащие. Изобретение эффективно для лечения заболевания или состояния, опосредованного PD-1. 7 н. и 5 з.п. ф-лы, 5 ил., 12 табл., 16 пр.
1. Гуманизованное антитело против PD-1 или его антигенсвязывающий фрагмент, включающие область CDR легкой цепи и область CDR тяжелой цепи, причем область CDR тяжелой цепи состоит из HCDR1, HCDR2 и HCDR3, а область CDR легкой цепи состоит из LCDR1, LCDR2 и LCDR3, аминокислотные последовательности HCDR1 и HCDR3 представлены последовательно в SEQ ID NO: 8 и SEQ ID NO: 10, а аминокислотные последовательности LCDR1, LCDR2 и LCDR3 представлены последовательно в SEQ ID NO: 11-13, при этом аминокислотная последовательность вариабельной области тяжелой цепи антитела представлена в любой из SEQ ID NO: 3-5.
2. Антитело или его антигенсвязывающий фрагмент по п. 1, при этом аминокислотная последовательность вариабельной области легкой цепи антитела представлена в любой из SEQ ID NO: 6-7.
3. Антитело или его антигенсвязывающий фрагмент по п. 2, при этом аминокислотная последовательность вариабельной области тяжелой цепи антитела представлена в SEQ ID NO: 3, а аминокислотная последовательность вариабельной области легкой цепи антитела представлена в SEQ ID NO: 6, или
аминокислотная последовательность вариабельной области тяжелой цепи антитела представлена в SEQ ID NO: 4, а аминокислотная последовательность вариабельной области легкой цепи антитела представлена в SEQ ID NO: 7, или
аминокислотная последовательность вариабельной области тяжелой цепи антитела представлена в SEQ ID NO: 5, а аминокислотная последовательность вариабельной области легкой цепи антитела представлена в SEQ ID NO: 7.
4. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, при этом антитело содержит константную область тяжелой цепи и константную область легкой цепи, причем константная область тяжелой цепи представляет собой любой один или несколько из IgG1, IgG2, IgG3, IgG4, IgA, IgD, IgE или IgM; а константная область легкой цепи представляет собой κ- или λ-цепь.
5. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-4, при этом антитело представляет собой химерное антитело, а антигенсвязывающий фрагмент представляет собой любой один или несколько из F(ab′)2, Fab, scFv, Fv и однодоменного антитела.
6. Нуклеиновая кислота, кодирующая гуманизованное антитело против PD-1 или его антигенсвязывающий фрагмент по любому из пп. 1-5.
7. Нуклеиновая кислота по п. 6, которая включает: первую нуклеиновую кислоту, кодирующую вариабельную область тяжелой цепи антитела или его антигенсвязывающего фрагмента, и/или вторую нуклеиновую кислоту, кодирующую вариабельную область легкой цепи антитела или его антигенсвязывающего фрагмента.
8. Вектор, несущий нуклеиновую кислоту по п. 6 или 7, где вектор является экспрессирующим вектором.
9. Клетка, экспрессирующая антитело или его антигенсвязывающий фрагмент по любому из п.п. 1-5, где указанная клетка включает нуклеиновую кислоту по п. 6 или 7 или вектор по п. 8.
10. Фармацевтическая композиция для лечения заболевания или состояния, опосредованного PD-1, включающая антитело или его антигенсвязывающий фрагмент по любому из пп. 1-5, нуклеиновую кислоту по п. 6 или 7, вектор по п. 8 или клетку по п. 9 и фармацевтически приемлемый носитель и/или наполнитель.
11. Применение антитела или его антигенсвязывающего фрагмента по любому из пп. 1-5, нуклеиновой кислоты по п. 6 или 7, вектора по п. 8, клетки по п. 9 или фармацевтической композиции по п. 10 при получении лекарственного средства для лечения заболевания или состояния, опосредованного PD-1.
12. Способ лечения заболевания или состояния, опосредованного PD-1, включающий:
введение эффективного количества антитела или его антигенсвязывающего фрагмента по любому из пп. 1-5, нуклеиновой кислоты по п. 6 или 7, вектора по п. 8, клетки по п. 9 или фармацевтической композиции по п. 10.
| WO 2010029434 A1, 18.03.2010 | |||
| US 2017044259 A1, 16.02.2017 | |||
| HUI ZHOU et al., Safety and Efficacy of Anti-PD-1 Monoclonal Antibodies in Patients With Relapsed or Refractory Lymphoma: A Meta-Analysis of Prospective Clinic Trails, Front Pharmacol, 2019; 10: 387 | |||
| MINGZHU WANG et al., Identification of a monoclonal antibody that targets PD-1 in a |
Авторы
Даты
2024-10-30—Публикация
2022-06-09—Подача