Изобретение относится к машиностроению и производству медицинских изделий, а именно технологиям формирования биосовместимых покрытий на титановых внутрикостных имплантатах.
Известны танталовые конструкции медицинского назначения, например, ацетабулярные компоненты, пористые блоки, а также дентальные имплантаты [В.А. Филиппенко, В.А. Танькут, А.И. Жигун, М. Аконджом, СЕ. Бондаренко Результаты клинического применения ацетабулярных компонентов с поверхностью из пористого тантала в эндопротезах при дефектах стенок вертлужной впадины и остеопорозе // Травма. - 2016. - Т. 17. - №. 1. - С.19-23.; М. De Francesco, Е.А. Gobbato, D. Noce, F. Cavallari, A. Fioretti Clinical and radiographic evaluation of single tantalum dental implants: a prospective pilot clinical study // Oral & implantology. - 2016. - V.9. - №. Suppl. 1/2016 to N 4/2016. - P.38.]. Высокая стоимость тантала ограничивает его применение при производстве цельнометаллических имплантируемых конструкций. Поэтому интенсивно ведутся работы по исследованию биосовместимых характеристик танталовых металлических и металлокерамических покрытий, а также разработке методов их нанесения [М. Roy, V.K. Balla, S. Bose, A. Bandyopadhyay Comparison of tantalum and hydroxyapatite coatings on titanium for applications in load bearing implants // Advanced engineering materials. - 2010. - V.12. - №.11. - P. B637-B641.]. Танталовые слои формируют на металлических изделиях методами электрохимического осаждения, вакуумного напыления и др. Несмотря на широкое распространение указанных технологий, остается потребность в малозатратном способе, позволяющем получать на титановых изделиях медицинского назначения биосовместимые покрытия, отличающиеся наличием наноразмерных элементов структуры и высокими значениями микротведости.
Известен способ электролитического осаждения тантала из водного раствора электролита, заключающийся в катодном осаждении на изделии танталового покрытия при плотности постоянного тока до 50 А/дм2 с одновременным воздействием импульсного тока с амплитудой 0,05-5 А, частотой от 10 Гц до 10 кГц, длительностью импульса от 10-5 до 10-2 с из водного раствора электролита. При этом электролит заранее приготавливается, путем растворения металлического тантала в водном растворе, содержащем 100-300 г/л гидрофторида аммония, при наложении переменного тока частотой 50 Гц до достижения концентрации тантала в электролите 10-50 г/л. В качестве анода используется платина. В результате реализации способа на металлической подложке формируется равномерное танталовое покрытие [патент RU на изобретение №2352691 С2 / СЕ. Андрюшечкин, Г.О. Климова, И.В. Локтев, П.П. Сидоров, Н.С Федотова // Способ электролитического осаждения тантала из водного раствора электролита (варианты). - 2009].
Основными недостатками способа являются: использование токсичного и взрывоопасного гидрофторида аммония; длительность подготовки электролита; использование дорогостоящего платинового анода.
Более экологически безопасными являются методы вакуумного напыления. Например, известен способ нанесения биоинертных танталовых покрытий, модифицированных ионами азота, на титановые имплантаты. Способ включает электрический взрыв танталовой фольги массой 100-600 мг, формирование из продуктов взрыва импульсной многофазной плазменной струи, опыление ею поверхности имплантата при поглощаемой мощности 1,5-1,8 ГВт/м2. В результате на поверхность титана осаждаются продукты взрыва и формируется биоинертное танталовое покрытие. Затем производят операции азотирования в течение 3-5 часов при температуре 500-600°С и импульсно-периодической электронно-пучковой обработки поверхности сформированных слоев при поглощаемой плотности энергии 20-40 Дж/см2, длительности импульсов 150-200 мкс в азотной атмосфере. При использовании способа на поверхности титановых имплантируемых конструкций формируются биоинертные танталовые покрытия, модифицированные ионами азота [патент RU на изобретение №2737912 С1 / Д.А. Романов, К.В. Соснин, С.Ю. Пронин // Способ нанесения биоинертных танталовых покрытий, модифицированных ионами азота, на титановые имплантаты. - 2020.]
Основными недостатками способа являются: технологическая сложность и длительность процесса; необходимость использования дорогостоящего оборудования.
Известен также способ изготовления материала для имплантата с электретными свойствами для остеосинтеза. Нанесение электретного покрытия на имплантаты для остеосинтеза осуществляют посредством электроно-лучевого испарения мишени и последовательного осаждения двухслойного покрытия на экранированную в период геттерного испарения предварительно нагретую до 480-520°С титановую конструкцию. Первоначально, при токе луча 780-810 мА и закрытой экранирующей заслонке проводится геттерное испарение танталовой мишени в течение 40-50 с. Затем экранирующая заслонка отрывается и на имплантате формируется слой тантала заданной толщины при скорости конденсации 1,5-1,6 мкм/мин. После чего температуру поверхности титанового изделия снижают до 450-480°С. При токе электронного луча до 290-310 мА производится испарение мишени из окиси тантала и соответственно формирование электретного слоя при скорости конденсации 1,2-1,3 мкм/мин [патент RU на изобретение 2040277 С1 / Способ изготовления материала для имплантата с электретными свойствами для остеосинтеза. - 1995].
К основным недостаткам способа можно отнести высокую стоимость применяемого оборудования и необходимость использования двух мишеней для формирования слоистой «Та-ТахОу» системы.
Для формирования высококачественных металлических и керамических слоев широко применяется метод магнетронного напыления. Например, известен способ изготовления имплантата с электретными свойствами для остеосинтеза, согласно которому, титановые имплантаты помещают в вакуумную камеру, производят очистку тлеющим разрядом, затем нагревают радиационным нагревателем до 250-400°С в вакууме не хуже 10-2 Па, после чего в рабочую камеру осуществляют напуск смеси аргона с кислородом и производится магнетронное распыление танталовой мишени. В результате применения способа на поверхности титанового имплантата формируется биосовместимое покрытие из Ta2O5 [патент RU на изобретение 2142819 С1 / Способ изготовления имплантата с электретными свойствами для остеосинтеза. - 1999.].
Основным недостатками способа является необходимость использования сложного и дорогостоящего технологического оборудования.
Рассмотренные способы отличаются необходимостью использования опасных расходных материалов, дорогостоящего оборудования, длительностью и сложностью технологических процессов. Значительной части указанных недостатков лишены методы термического вакуумного напыления. При нагреве до определенной температуры и при пониженном давлении металлы испаряются в атомарном виде и конденсируются на подложках [D.L. Olson, Welding, Brazing, and Soldering, American Society for Metals. Joining Division, ASM International. Handbook Committee, vol. 6, ASM International, Metals Park, OH, 1993. ASM handbook.]. Известные технологии термического напыления не применяются для формирования покрытий из тугоплавких металлов, например тантала.
Задачей изобретения является создание, технологически простого, ресурсосберегающего и экологически безопасного способа формирования на титановых имплантируемых изделиях биосовместимых танталсодержащих слоев.
Поставленная задача решается тем, что имплантируемые конструкции предварительно очищенные от технологических загрязнений размещают внутри керамической вакуумной камеры с наружным водоохлаждаемым индуктором, затем между поверхностью имплантата и внутренней поверхностью камеры соосно имплантату размещают танталовую трубчатую мишень с толщиной стенки 0,1-1,5 мм, внутренним диаметром на 10-25 мм больше диаметра цилиндрического титанового имплантата и высотой равной длине упомянутого имплантата, производят откачку керамической вакуумной камеры до остаточного давления не более 30±10 Па и проводят последующий индукционный нагрев мишени до 2800±100°С при частоте тока индуктора 50±20 кГц, удельной потребляемой электрической мощности 100-200 кВт/кг с выдержкой в течение 60-600 с, что приводит к формированию на титановом цилиндрическом имплантате танталсодержащего биосовместимого покрытия. По завершении процесса камеру охлаждают до комнатной температуры.
Техническим результатом является формирование технологически простым, производительным и экологически безопасным способом на титановых имплантатах биосовместимых слоев системы «ТахОу-Та», характеризуемых микротвердостью Н до 48,34±8,79 ГПа (HV0,98=4930±896), а также наличием в поверхностном слое наноразмерных структурных элементов в виде зерен и пор.
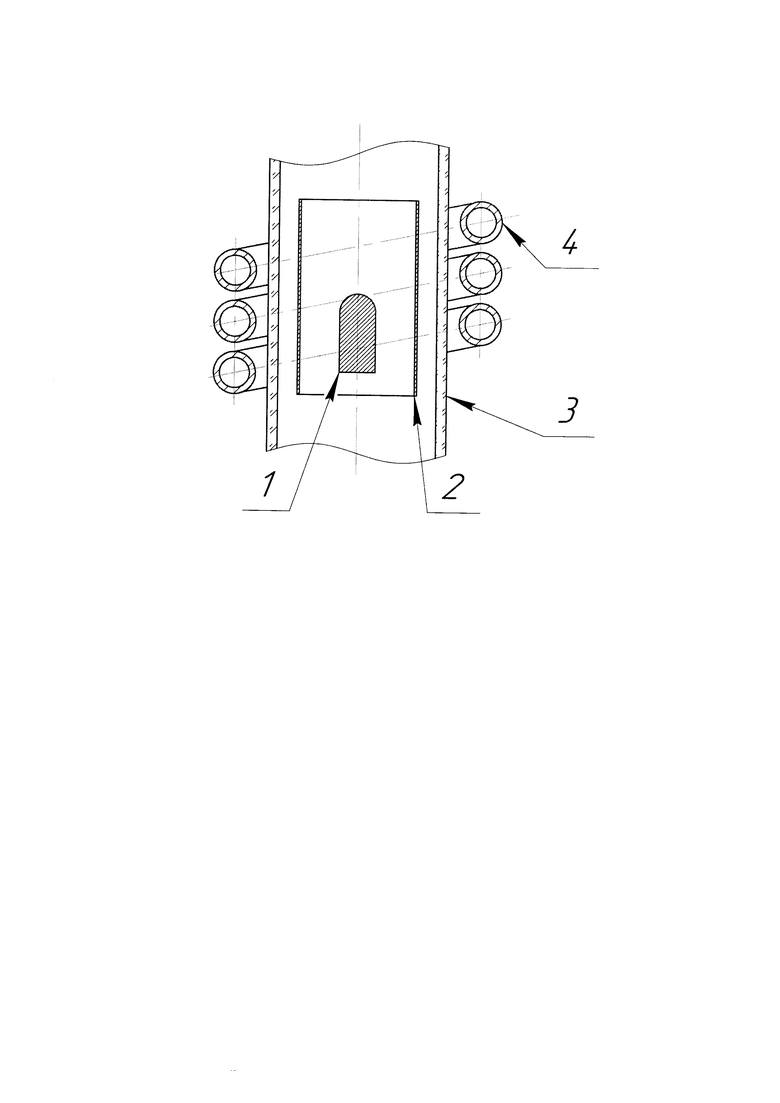
Изобретение поясняется фигурой, на которой представлен процесс формирования покрытия (Фиг.).
На Фиг. позициями 1-3 обозначены:
1 - титановый имплантат;
2 - танталовая цилиндрическая мишень;
3 - керамическая камера;
4 - водоохлаждаемый индуктор.
Предлагаемый способ осуществляют следующим образом.
Титановый имплантат 1 предварительно очищают от технологических загрязнений, например, ультразвуковой очисткой в водном 4-6% растворе поверхностно-активных веществ, последующей промывкой в дистилированной воде, водном растворе этилового спирта или ацетоне и сушкой на воздухе. Затем изделие размещают в технологическом объеме вакуумной керамической камеры 3 с наружным водоохлаждаемым индуктором 4. Затем между поверхностью имплантата 1 и внутренней поверхностью камеры 3 соосно имплантату 1 размещают танталовую трубчатую мишень 2 с толщиной стенки 0,1-1,5 мм, внутренним диаметром на 10-25 мм больше диаметра титанового имплантата 1 и высотой равной длине покрываемого цилиндрического титанового имплантата (Фиг. ). После производят откачку керамической вакуумной камеры 3 до остаточного давления не более 30±10 Па и последующий индукционный нагрев мишени до 2800±100°С при частоте тока индуктора 50±20 кГц, удельной потребляемой электрической мощности 100-200 кВт/кг с выдержкой в течение 60-600 с, что приводит к формированию на титане танталсодержащего биосовместимого покрытия. По завершении процесса камеру охлаждают до комнатной температуры.
Приведенные значения технологических режимов индукционно-термического вакуумного распыления мишени определены исследовательскими методами и обеспечивают формирование на поверхности имплантата танталсодержащих слоев заданной толщины.
Использование мишени трубчатой формы, высотой примерно равной длине имплантата или участка его поверхности на котором необходимо нанести покрытие, обеспечивает формирование на цилиндрическом титановом изделии равномерного по толщине покрытия системы «ТахОу-Та». Внутренний диаметр танталовой трубки 10-25 мм обеспечивает рациональную дистанцию напыления 5-12,5 мм), уменьшение которой приводит к перегреву титановой подложки и ее деформации. Увеличение дистанции приводит к снижению производительности процесса. Использование тантала толщиной менее 0,1 не целесообразно, поскольку увеличивается вероятность локального перегрева и нарушения целостности мишени. Применение мишеней со стенкой более 1,5 мм приводит к увеличению длительности прогрева, и как следствие процесса в целом. При остаточном давлении среды в камере более 30±10 Па значительно снижается производительность процесса, увеличивается содержание кислорода и оксидов тантала в формируемых слоя.
При подаче на индуктор тока частотой менее 30 кГц снижается электрический коэффициент полезного действия устройства индукционного нагрева и самого процесса обработки. При частоте более 70 кГц не происходит улучшение эффективности процесса обработки и наблюдается снижение коэффициента мощности. Предельные значения потребляемой удельной электрической мощности (100-200 кВт/кг) обусловлены тем, что при величине менее 100 кВт/кг будет затруднен нагрев мишени до заданной температуры (2800±100°С) из-за тепловых потерь, а при значении более 200 кВт/кг увеличивается вероятность перегрева и деформации тантала и титанового имплантата. Длительность процесса (60-600 с) обуславливает толщину формируемых слоев, а также температуру технологической оснастки и изделий. При длительности напыления менее 60 с формируются слои с содержанием тантала менее 5,5 ат.%. Процесс распыления длительностью более 600 с приводит к нагреву имплантатов до температуры более 600°С, и как следствие происходит деформация изделия или возникает риск испарения поверхностного слоя титана.
Примеры выполнения способа.
Пример 1. Стоматологический винтовой имплантат из технического титана ВТ1 с максимальным наружным диаметром 6 и длиной 10 мм предварительно очищают от технологических загрязнений путем ультразвуковой обработки в растворе моющих средств, затем последовательно промывают в дистиллированной воде, ацетоне и сушат на воздухе. После очистки изделие размещают внутри вакуумной камеры, фиксируя за внутреннее отверстие. Для формирования танталсодержащего покрытия на всей внутрикостной поверхности титанового имплантата, между изделием и внутренней поверхностью камеры соосно имплантату размещают танталовую трубку с внутренним диаметром 14 мм, толщиной стенки 1 мм и высотой 12 мм. Затем производят откачку керамической вакуумной камеры до остаточного давления 25±5 Па и последующий индукционный нагрев мишени до 2750±50°С при частоте тока индуктора 40°3 кГц, удельной потребляемой электрической мощности 150±5 кВт/кг с выдержкой в течение 180 с. После процесса распыления мишень с имплантатом охлаждают до комнатной температуры при пониженном давлении, затем изделие извлекают из технологического объема.
Пример 2. Спонгиозный винт для фиксации вертлужного компонента эндопротеза тазобедренного сустава из титана ВТ6 с наружным диаметром 7 мм, длиной резьбы 32 мм и суммарной длиной 40 мм, предварительно очищают от технологических загрязнений. Затем изделие размещают в технологическом оснастке вакуумной камеры с наружным водоохлаждаемым индуктором. Между имплантатом и боковой стенкой керамической камеры, соосно имплантату напротив внуктрикостной части размещают танталовую мишень в виде трубки диаметром 18 мм и высотой 40 мм с толщиной стенки 0,5 мм. После производят откачку вакуумной камеры до остаточного давления не более 30±5 Па. При достижении заданного давления производят индукционный нагрев мишени до 2850±50°С при частоте тока индуктора 35±3 кГц, удельной потребляемой электрической мощности 195±5 кВт/кг с выдержкой в течение 500±5 с. По завершении процесса вакуумную камеру охлаждают до комнатной температуры и извлекают спонгиозный винт.
Для подтверждения формирования на поверхности титана в результате напыления биосовместимых танталсодержащих покрытий системы «ТахОу-Та» с высокими механическими характеристиками проводились исследования элементно-фазового состава, структуры, микротвердости с использованием дисковых образцов диаметром 14±0,1 мм и высотой 2±0,1 мм из ВТ1-0. Дополнительно проводились исследования in vivo, для которых применялись титановые двухступенчатые цилиндры с диаметром внекостной части Dh=2,15±0,05 мм и длиной 0,5±0,1 мм, диаметром внутрикостной рабочей части D=2,05±0,02 мм и общей длиной L=2±0,1 мм. Предварительно образцы подвергались ультразвуковой очистке от технологических загрязнений в водном 4-6% растворе поверхностно-активных веществ, последующей промывке в водном растворе этилового спирта и сушке на воздухе. Титановые диски и цилиндры размещались в технологическом объеме вакуумной керамической камеры с использованием технологической оснастки. Между камерой и образцами фиксировалась танталовая трубчатая мишень с толщиной стенки 0,3 мм диаметром 24±0,5 мм и высотой 7 мм. Затем камера герметизировалась и производилась откачка камеры до остаточного давления 35±5 Па. Последующий индукционный нагрев мишени до 2800±100°С проводился при частоте тока индуктора 40±5 кГц, удельной потребляемой электрической мощности 100-200 кВт/кг с выдержкой в течение 60-600 с. По завершении процесса камеру охлаждали до комнатной температуры и производили извлечение титановых образцов.
Исследования структуры и элементного состава проводились методами растровой электронной микроскопии и энергодисперсионного анализа с применением детектора «INCA PentaFETx3» на микроскопе «MIRA II LMU». Фазовый состав определялся на дифрактометре «ARL XTRA». Анализ результатов проводился в программе «Match! Phase Iddentification from Powder Diffraction" (v.1.11k)» с использованием базы данных «COD-Inorganics reference database)). Размеры поверхностных структурных элементов определялись с использованием анализатора «АГПМ-6М» в программном комплексе для автоматического определения размерных характеристик микроструктуры «Metallograph» по изображениям, полученным растровой электронной микроскопией. Микротвердость образцов с покрытиями изучалась на твердомере «ПМТ-3» при нагрузке на индентор Виккерса равной 100 гс (0,98 Н).
Биологическая совместимость экспериментальных образцов титановых имплантатов изучалась in vivo. В качестве моделей использовались белые лабораторные крысы. Установка имплантатов по одной штуке в одно модельное животное проводилась в дистальный эпифиз бедренной кости. За экспериментальными животными осуществляли наблюдение до 40 суток после операции, при этом фиксировалось общее состояние животных.
Наноразмерная структура танталсодержащих слоев отличалась наличием зерен со средним размер от 85-105 нм до 133-347 нм и пор размером от 64-83 до 101-163 нм. В зависимости от удельной потребляемой мощности и длительности процесса напыления содержание тантала в покрытии увеличивалось от 5,5 до 42,1±0,5 ат.%, а кислорода с 22,9±0,5 до 65,2±0,5 ат.%, остальное титан. Согласно анализу фазового состава, первоначально при длительности процесса напыления менее 60 с, происходит поглощение остаточной атмосферы титаном с образованием оксидов Ti3O, TiO, TiO2 (анатаз и рутил).
Затем на поверхности формируются слои, состоящие из кристаллов Та2О, Ta2O5, ТаО2 и тантала.
Микротвердость образцов титана с танталсодержащими покрытиями увеличивалась с увеличением длительности процесса от 15-20 ГПа (при напылении в течение 60 с и менее) до 48,34±8,79 ГПа при максимальной продолжительности 600 с.
Исследования in vivo позволили определить биосовместимость формируемых танталсодержащих слоев. Наблюдения за лабораторными животными в послеоперационный период выявили выраженную положительную тенденцию восстановления опороспособности прооперированной конечности. Незначительная хромота и посттравматический отек в месте установки имплантата наблюдались в первые 2-3 суток после операции. В течение остального времени эксперимента никаких визуальных признаков воспаления в зоне установки имплантата не наблюдалось, пальпация прооперированной конечности у крыс не вызывала беспокойства.
Морфология скола кости в области установленного имплантата визуально характеризовала формирование контактной границы «поверхность имплантата-костная ткань». У контрольной группы крыс титановые имплантаты без покрытия не обеспечивали выраженную способность к остеоинтеграции. У животных имплантаты легко извлекались на этапе удаления мягких тканей или при раскалывании костного фрагмента. При макроанализе контрольных образцов наблюдались единичные участки с закрепленными фрагментами молодой костной ткани.
Титановые имплантаты с покрытием системы «ТахОу-Та» обеспечивали интенсивную способность к остеоинтеграции после тестового периода (до 40 сут.). На поверхности имплантата наблюдались многочисленные скопления костных структур, что характеризовало протекание процессов необходимого контактного взаимодействия с костной тканью. Анализ динамики гематологических показателей экспериментальных животных показал, что у крыс отсутствовала реакция в виде воспаления или аллергии на внедрение имплантата с танталсодержащими покрытиями на системном уровне, что выражалось стабильностью гематологических показателей на момент введения животных в эксперимент и в день окончания эксперимента. У крыс контрольной группы с титановыми имплантатами (без покрытия) динамика гематологических показателей по ряду показателей имела отличные тенденции.
Из полученных результатов следует, что предложенный способ позволяет формировать на титановых внутрикостных имплантатах танталсодержащие покрытия, характеризуемые высокой твердостью, наличием наноразмерных структурных элементов и улучшенной биосовместимостью в сравнении с титаном.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ формирования наноструктурированного оксидного покрытия на техническом титане | 2017 |
|
RU2650221C1 |
| Способ формирования металлооксидных пористых покрытий на титановых изделиях | 2022 |
|
RU2781873C1 |
| СПОСОБ ФОРМИРОВАНИЯ НАНОСТРУКТУРИРОВАННОГО БИОИНЕРТНОГО ПОКРЫТИЯ НА ТИТАНОВЫХ ИМПЛАНТАТАХ | 2015 |
|
RU2604085C1 |
| Способ формирования титановых пористых покрытий на титановых имплантатах | 2017 |
|
RU2647968C1 |
| Способ формирования оксидных покрытий на изделиях из нержавеющих хромоникелевых сталей | 2018 |
|
RU2689485C1 |
| Способ формирования на быстрорежущей стали покрытия системы титан - оксиды титана | 2022 |
|
RU2789262C1 |
| Способ азотирования малогабаритных изделий из инструментальных быстрорежущих сталей | 2022 |
|
RU2784616C1 |
| СПОСОБ ХИМИКО-ТЕРМИЧЕСКОЙ ИНДУКЦИОННОЙ ОБРАБОТКИ МАЛОГАБАРИТНЫХ ИЗДЕЛИЙ ИЗ АЛЬФА-ТИТАНОВЫХ СПЛАВОВ | 2015 |
|
RU2623979C2 |
| Способ формирования покрытия на штамповых сталях | 2020 |
|
RU2746518C1 |
| Способ химико-термического упрочнения малогабаритных изделий из технического титана | 2018 |
|
RU2690067C1 |
Изобретение относится к способу формирования танталсодержащего биосовместимого покрытия на поверхности цилиндрического титанового имплантата. Проводят очистку упомянутого имплантата от технологических загрязнений. Размещают цилиндрический титановый имплантат внутри керамической вакуумной камеры с наружным водоохлаждаемым индуктором. Затем между поверхностью упомянутого имплантата и внутренней поверхностью камеры соосно имплантату размещают танталовую трубчатую мишень с толщиной стенки 0,1-1,5 мм, внутренним диаметром на 10-25 мм больше диаметра цилиндрического титанового имплантата и высотой, равной длине упомянутого имплантата. Осуществляют откачку керамической вакуумной камеры до остаточного давления не более 30±10 Па и проводят последующий индукционный нагрев мишени до 2800±100°С при частоте тока индуктора 50±20 кГц, удельной потребляемой электрической мощности 100-200 кВт/кг с выдержкой в течение 60-600 сек с формированием на цилиндрическом титановом имплантате танталсодержащего биосовместимого покрытия. Затем камеру охлаждают до комнатной температуры. Обеспечивается формирование танталсодержащего покрытия на титановых имплантатах, обладающего высокой твердостью и улучшенной биосовместимостью по сравнению с титаном. 1 ил., 2 пр.
Способ формирования танталсодержащего биосовместимого покрытия на поверхности цилиндрического титанового имплантата, включающий очистку упомянутого имплантата от технологических загрязнений, отличающийся тем, что цилиндрический титановый имплантат размещают внутри керамической вакуумной камеры с наружным водоохлаждаемым индуктором, затем между поверхностью упомянутого имплантата и внутренней поверхностью камеры соосно имплантату размещают танталовую трубчатую мишень с толщиной стенки 0,1-1,5 мм, внутренним диаметром на 10-25 мм больше диаметра цилиндрического титанового имплантата и высотой, равной длине упомянутого имплантата, осуществляют откачку керамической вакуумной камеры до остаточного давления не более 30±10 Па и проводят последующий индукционный нагрев мишени до 2800±100°С при частоте тока индуктора 50±20 кГц, удельной потребляемой электрической мощности 100-200 кВт/кг с выдержкой в течение 60-600 с с формированием на цилиндрическом титановом имплантате танталсодержащего биосовместимого покрытия, затем камеру охлаждают до комнатной температуры.
| СПОСОБ ИЗГОТОВЛЕНИЯ ИМПЛАНТАТА С ЭЛЕКТРЕТНЫМИ СВОЙСТВАМИ ДЛЯ ОСТЕОСИНТЕЗА | 1996 |
|
RU2142819C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ИМПЛАНТАТА С ЭЛЕКТРЕТНЫМИ СВОЙСТВАМИ ДЛЯ ОСТЕОСИНТЕЗА | 1993 |
|
RU2049481C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ МАТЕРИАЛА ДЛЯ ИМПЛАНТАТА С ЭЛЕКТРЕТНЫМИ СВОЙСТВАМИ ДЛЯ ОСТЕОСИНТЕЗА | 1992 |
|
RU2040277C1 |
| US 9279178 B2, 08.03.2016 | |||
| US 10039619 B2, 07.08.2018 | |||
| US 20150209480 A1, 30.07.2015. | |||
Авторы
Даты
2023-11-02—Публикация
2023-05-22—Подача