Изобретение относится к экологии, биологии и токсикологической химии, а именно к способам количественного определения цинка в биологическом материале, и может быть использовано в практике химико-токсикологических, клинических, ветеринарных и экологических лабораторий.
Известен способ определения цинка в цельной крови путем обработки исследуемой пробы 0,5-5,0%-ным водным раствором азотной кислоты при объемном соотношении проба-кислота 1:1, последующего ее подсушивания в два этапа при температуре 110°С и 250°С, озоления при температуре 430°С, обработки полученной золы концентрированной азотной кислотой, выпаривания до состояния влажных солей, введения фонового раствора - 0,5-5,0%-ного раствора азотной кислоты - и определения содержания цинка в полученном растворе с помощью метода атомно-абсорбционной спектрофотометрии (Патент 2184973 Российская Федерация, МПК G01N 33/84 (2000.01) / Способ определения содержания тяжелых металлов в цельной крови / Зайцева Н.В., Уланова Т.С., Плахова Л.В., Суетина Г.Н., Стенно Е.В.; патентообладатель Пермский научно-исследовательский клинический институт детской экопатологии (RU) - №2001114386/14; Заяв. 24.05.2001; Опуб. 10.07.2002 // Описание изобретения к патенту. - 2002).
Недостаток данного способа заключается в том, что атомно-абсорбционная спектрометрия предполагает применение дорогостоящего оборудования и требует определенных условий для работы с открытым огнем и баллонами с горючими газами под давлением, поэтому метод не доступен большинству лабораторий.
Наиболее близкой является методика определения цинка в пробах сточных, подсточных вод и растительной биомассе путем подкисления анализируемого водного раствора объемом 25 мл до рН 2-3, помещения его в делительную воронку, добавления 5 мл ацетатного буферного раствора и 5 мл раствора тиосульфата натрия, встряхивания с малыми порциями раствора дитизона в тетрахлорметане, объединения экстрактов, промывания встряхиванием с двумя порциями по 5 мл промывного раствора, перенесения розового раствора дитизоната цинка в тетрахлорметане в мерную колбу на 25 мл, доведения до метки растворителем, перемешивания и измерения оптической плотности при 538 нм относительно растворителя с использованием спектрофотометра СПЕКС ССП 310 (Петракова, Е.А. Методики определения цинка в пробах сточных, подсточных вод и растительной биомассе / Е.А. Петракова // Вестник Брянского государственного университета. - 2014. - №4. - С. 148-151).
Недостатками данного способа являются недостаточно высокий процент обнаружения цинка, недостаточно высокая точность и чувствительность.
Техническим результатом настоящего изобретения является повышение процента обнаружения, а также увеличение точности и чувствительности определения цинка в биологическом материале при использовании общедоступного в аппаратурном и экономическом отношении способа.
Технический результат достигается тем, что биологический объект измельчают, высушивают, осуществляют минерализацию методом сухого озоления, золу обрабатывают концентрированным раствором нитрата аммония при нагревании, полученные кристаллы растворяют в 0,1М хлороводородной кислоте, фильтруют через обеззоленный фильтр «белая лента», аликвоту приготовленного раствора наносят на линию старта нормально-фазовой пластины ТСХ, процесс хроматографирования осуществляют, используя двухкомпонентную подвижную фазу, которой является смесь растворителей гексан-уксусная кислота в соотношении 7:3 по объему, сорбент с зоны абсорбции тщательно счищают, не допуская потерь сорбента, растворяют в 0,5% растворе аммиака, смесь интенсивно взбалтывают, фильтруют через обеззоленный фильтр «белая лента», к фильтрату добавляют раствор эриохрома черного Т, приготовленный в 0,5% растворе аммиака, далее проводят определение цинка в пробе спектрофотометрическим методом при длине волны 557±2 нм, соответствующей максимуму поглощения комплекса эриохром + цинк в 0,5% растворе аммиака, и толщине поглощающего слоя 1 см.
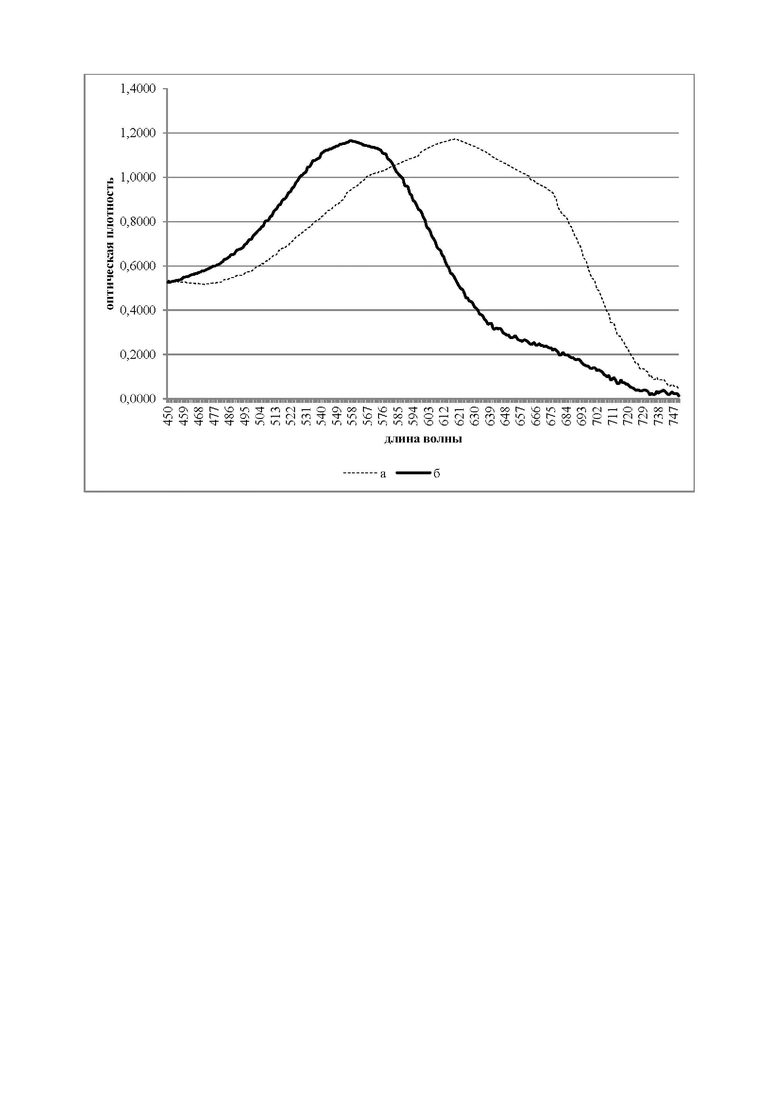
Изобретение поясняется фигурой.
На фигуре изображены спектры: а - 0,001% раствора эриохрома; б - раствора комплекса эриохром + цинк (концентрация цинка = 0,7 мкг/мл).
Способ осуществляется следующим образом: биологический объект, содержащий цинк, измельчают, высушивают, осуществляют минерализацию методом сухого озоления, золу обрабатывают концентрированным раствором нитрата аммония при нагревании, полученные кристаллы растворяют в 0,1М хлороводородной кислоте, фильтруют через обеззоленный фильтр «белая лента», аликвоту приготовленного раствора наносят на линию старта нормально-фазовой пластины ТСХ, процесс хроматографирования осуществляют, используя двухкомпонентную подвижную фазу, которой является смесь растворителей гексан-уксусная кислота в соотношении 7:3 по объему, сорбент с зоны абсорбции тщательно счищают, не допуская потерь сорбента, растворяют в 0,5% растворе аммиака, смесь интенсивно взбалтывают, фильтруют через обеззоленный фильтр «белая лента», к фильтрату добавляют раствор эриохрома черного Т, приготовленный в 0,5% растворе аммиака, далее проводят определение цинка в пробе спектрофотометрическим методом при длине волны 557±2 нм, соответствующей максимуму поглощения комплекса эриохром + цинк в 0,5% растворе аммиака, и толщине поглощающего слоя 1 см. Способ иллюстрируется следующими примерами.
Пример 1
Определение цинка в ткани печени
К 3,0 г мелкоизмельченной ткани печени прибавляют 1 мл раствора, содержащего 150 мкг цинка (соответствует 660 мкг цинка сульфата семи-водного), тщательно перемешивают биологическую ткань с раствором и оставляют на два часа при температуре 18-20°С. По истечении указанного времени биологический объект, содержащий анализируемое вещество, переносят в фарфоровый тигель вместимостью 25 мл, высушивают в сушильном шкафу при температуре 150°С, охлаждают в эксикаторе и помещают в муфельную печь. В течение 8-12 часов при постепенном нагреве температуры до 400°С осуществляют минерализацию методом сухого озоления до полного сжигания органических веществ. Полученную золу обрабатывают по каплям концентрированным раствором нитрата аммония при нагревании (в фарфоровой чашке на электрической плитке) до получения бесцветных кристаллов цинка нитрата. Кристаллы растворяют в 3 мл 0,1М хлороводородной кислоты, фильтруют через обеззоленный фильтр «белая лента» диаметром 55 мм в колбу вместимостью 5 мл, доводят объем до метки тем же растворителем.
Аликвоту приготовленного раствора в объеме 0,1 мл наносят на линию старта нормально-фазовой пластины ТСХ «Merck» 20×20 см с силикагелем 60. Процесс хроматографирования осуществляют, используя двухкомпонентную подвижную фазу, которой является смесь растворителей гексан-уксусная кислота в соотношении 7:3 по объему. При достижении фронта растворителей линии финиша сорбент с зоны абсорбции (Rf = 0,45) тщательно счищают, не допуская потерь сорбента, и растворяют в 5 мл 0,5% раствора аммиака. Смесь интенсивно взбалтывают и фильтруют через обеззоленный фильтр «белая лента» диаметром 55 мм в колбу вместимостью 10 мл. К фильтрату добавляют 1 мл 0,01% раствора эриохрома черного Т, приготовленного в 0,5% растворе аммиака, доводят объем до метки тем же растворителем и проводят определение цинка в пробе спектрофотометрическим методом.
Определение проводят, используя спектрофотометр BioRad SmartSpecPlus (США). Измеряют оптическую плотность испытуемого раствора на фоне 0,5% раствора аммиака при длине волны 557±2 нм, соответствующей максимуму поглощения комплекса эриохром + цинк в 0,5% растворе аммиака, и толщине поглощающего слоя 1 см. Количественное содержание цинка рассчитывают по оптической плотности, используя уравнение градуировочного графика с учетом навески и разведения.
Контрольный опыт проводят по предлагаемой методике без предварительного внесения в биоматериал анализируемого вещества.
Построение градуировочного графика.
Готовят 0,02% раствор эриохрома черного Т в 0,5% растворе аммиака (раствор 1). В колбу вместимостью 100 мл вносят 0,0220 г цинка сульфата семи-водного, что составляет 0,005 г в пересчете на цинк, и доводят до метки водой дистиллированной (раствор 2). В ряд мерных колб вместимостью 10 мл вносят 10; 20; 40; 80; 120; 160; 200; 240 мкл раствора 2 и 40; 80; 160; 320; 480; 640; 800; 900 мкл раствора 1, доводят объем содержимого каждой колбы до метки 0,5% раствором аммиака. Полученные растворы измеряют на спектрофотометре BioRad SmartSpecPlus (США) на фоне 0,5% раствора аммиака при длине волны 557 ± 2 нм, соответствующей максимуму поглощения комплекса эриохром + цинк в 0,5% растворе аммиака, и толщине поглощающего слоя 1 см.
По результатам измерений на спектрофотометре строят график зависимости оптической плотности от концентрации определяемого вещества. График линеен в интервале концентраций 5∙10-8-1,2∙10-6 г/мл.
Методом наименьших квадратов рассчитывают уравнение градуировочного графика, которое в данном случае имеет вид:
А = 1,6442Х - 0,000036,
где А - оптическая плотность; Х - концентрация определяемого вещества в спектрофотометрируемой пробе, мкг/мл.
Результаты количественного определения цинка в ткани печени представлены в таблице 1.
Пример 2
Определение цинка в ткани зерновок кукурузы
К 3,0 г мелкоизмельченной ткани зерновок кукурузы прибавляют 1 мл раствора, содержащего 150 мкг цинка (соответствует 660 мкг цинка сульфата семи-водного), тщательно перемешивают биологическую ткань с раствором и оставляют на два часа при температуре 18-20°С. По истечении указанного времени биологический объект, содержащий анализируемое вещество, переносят в фарфоровый тигель вместимостью 25 мл, высушивают в сушильном шкафу при температуре 150°С, охлаждают в эксикаторе и помещают в муфельную печь. В течение 8-12 часов при постепенном нагреве температуры до 400°С осуществляют минерализацию методом сухого озоления до полного сжигания органических веществ. Полученную золу обрабатывают по каплям концентрированным раствором нитрата аммония при нагревании (в фарфоровой чашке на электрической плитке) до получения бесцветных кристаллов цинка нитрата. Кристаллы растворяют в 3 мл 0,1М хлористоводородной кислоты, фильтруют через обеззоленный фильтр «белая лента» диаметром 55 мм в колбу вместимостью 5 мл, доводят объем до метки тем же растворителем.
Аликвоту приготовленного раствора в объеме 0,1 мл наносят на линию старта нормально-фазовой пластины ТСХ «Merck»20×20 см с силикагелем 60. Процесс хроматографирования осуществляют, используя двухкомпонентную подвижную фазу, которой является смесь растворителей гексан-уксусная кислота в соотношении 7:3 по объему. При достижении фронта растворителей линии финиша сорбент с зоны абсорбции (Rf = 0,45) тщательно соскребают, не допуская потерь сорбента, растворяют в 5 мл 0,5% раствора аммиака, фильтруют через обеззоленный фильтр «белая лента» диаметром 55 мм в колбу вместимостью 10 мл. К фильтрату добавляют 1 мл 0,01% раствора эриохрома черного Т, приготовленного в 0,5% растворе аммиака, доводят объем до метки тем же растворителем и проводят определение цинка в пробе спектрофотометрическим методом.
Определение проводят, используя спектрофотометр BioRad SmartSpecPlus (США). Измеряют оптическую плотность испытуемого раствора на фоне 0,5% раствора аммиака при длине волны 557±2 нм, соответствующей максимуму поглощения комплекса эриохром + цинк в 0,5% растворе аммиака, и толщине поглощающего слоя 1 см. Количественное содержание цинка рассчитывают по оптической плотности, используя уравнение градуировочного графика, с учетом навески и разведения.
Контрольный опыт проводят по предлагаемой методике без предварительного внесения в биоматериал анализируемого вещества.
Построение градуировочного графика
Построение градуировочного графика и его уравнение приводятся в примере 1.
Результаты количественного определения цинка в ткани зерновок кукурузы представлены в таблице 2.
Нижний предел обнаружения цинка в биологическом материале составляет 3 мкг/г (при увеличении объема аликвоты, вносимой на пластину ТСХ, до 0,3 мл). Нижний предел обнаружения цинка в спектрофотометрируемой пробе составляет 0,05 мкг/мл. Сравнение предлагаемого способа с методом атомно-абсорбционной спектрометрии цинка представлено в таблице 3.
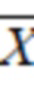 = 95,13%
= 95,13%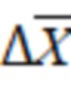
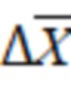 = 0,44
= 0,44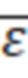
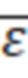 = 0,46%
= 0,46%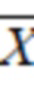
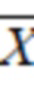 = 95,83%
= 95,83%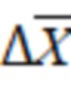
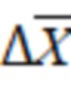 = 0,45
= 0,45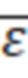
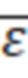 = 0,47%
= 0,47%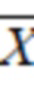
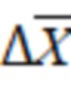
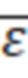
Таким образом, предлагаемый способ, основанный на образовании комплексного соединения эриохрома черного Т с цинком и спектрофотометрии этого комплекса в видимой области, по сравнению с прототипом, основанном на образовании комплексного соединения дитизона с цинком и спектрофотометрии этого комплекса в видимой области, повышает процент обнаружения цинка, улучшает точность и существенно увеличивает чувствительность определения. Аналитические характеристики предлагаемого способа - процент обнаружения, относительная погрешность среднего результата, нижний предел обнаружения - приближены к методу атомно-абсорбционной спектрометрии, при этом предлагаемый способ не требует наличия дорогостоящего, сложного в эксплуатации оборудования и является общедоступным.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения кадмия в биологическом материале | 2023 |
|
RU2810518C1 |
| Способ определения простых сахаров в тонком слое сорбента | 2016 |
|
RU2642264C2 |
| Способ количественного определения алюминия, ванадия, вольфрама, железа, кадмия, кобальта, магния, марганца, меди, никеля, свинца, стронция, титана, хрома, цинка в атмосферном воздухе методом масс-спектрометрии с индуктивно связанной плазмой | 2016 |
|
RU2627854C1 |
| СПОСОБ ИДЕНТИФИКАЦИИ И КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ГЛУТАМИНОВОЙ КИСЛОТЫ | 2014 |
|
RU2581727C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПОЛИФЕНОЛЬНЫХ СОЕДИНЕНИЙ МЕТОДОМ СТУПЕНЧАТОГО ЭЛЮИРОВАНИЯ В ТОНКОМ СЛОЕ СОРБЕНТА | 2015 |
|
RU2597661C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ Н-БУТИЛОВОГО ЭФИРА 2-[4-(5-ТРИФТОРМЕТИЛПИРИДИЛ-2-ОКСИ)ФЕНОКСИ]ПРОПИОНОВОЙ КИСЛОТЫ В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2005 |
|
RU2287812C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ МАГНИЯ В МАСЛАХ | 2005 |
|
RU2278380C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КАРМУАЗИНА В СОКАХ | 2015 |
|
RU2596796C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ КАДМИЯ, СВИНЦА, МЫШЬЯКА, ХРОМА, НИКЕЛЯ, МЕДИ, ЦИНКА, МАРГАНЦА, ВАНАДИЯ, СТРОНЦИЯ, СЕЛЕНА, ТАЛЛИЯ В КРОВИ МЕТОДОМ МАСС-СПЕКТРОМЕТРИИ С ИНДУКТИВНО СВЯЗАННОЙ ПЛАЗМОЙ | 2015 |
|
RU2585369C1 |
| Способ определения бора | 1990 |
|
SU1797022A1 |
Изобретение относится к экологии, биологии и токсикологической химии. Предложен способ определения цинка в биологическом материале, заключающийся в том, что биологический объект измельчают, высушивают, осуществляют минерализацию методом сухого озоления, золу обрабатывают концентрированным раствором нитрата аммония при нагревании, полученные кристаллы растворяют в хлороводородной кислоте, фильтруют, устраняют мешающие влияния других тяжелых металлов, получают окрашенное комплексное соединение цинка с органическим веществом и проводят определение спектрофотометрическим методом, отличающийся тем, что полученные кристаллы растворяют в 0,1М хлороводородной кислоте, фильтруют через обеззоленный фильтр «белая лента», аликвоту приготовленного раствора наносят на линию старта нормально-фазовой пластины ТСХ, процесс хроматографирования осуществляют, используя двухкомпонентную подвижную фазу, которой является смесь растворителей гексан-уксусная кислота в соотношении 7:3 по объему, сорбент с зоны абсорбции тщательно счищают, не допуская потерь сорбента, растворяют в 0,5% растворе аммиака, смесь интенсивно взбалтывают, фильтруют через обеззоленный фильтр «белая лента», к фильтрату добавляют раствор эриохрома черного Т, приготовленный в 0,5% растворе аммиака, далее проводят определение цинка в пробе спектрофотометрическим методом при длине волны 557 ± 2 нм, соответствующей максимуму поглощения комплекса эриохром + цинк в 0,5% растворе аммиака, и толщине поглощающего слоя 1 см. Технический результат - повышение процента обнаружения, а также увеличение точности и чувствительности определения цинка в биологическом материале при использовании общедоступного в аппаратурном и экономическом отношении способа. 1 ил., 3 табл., 2 пр.
Способ определения цинка в биологическом материале, заключающийся в том, что биологический объект измельчают, высушивают, осуществляют минерализацию методом сухого озоления, золу обрабатывают концентрированным раствором нитрата аммония при нагревании, полученные кристаллы растворяют в хлороводородной кислоте, фильтруют, устраняют мешающие влияния других тяжелых металлов, получают окрашенное комплексное соединение цинка с органическим веществом и проводят определение спектрофотометрическим методом, отличающийся тем, что полученные кристаллы растворяют в 0,1М хлороводородной кислоте, фильтруют через обеззоленный фильтр «белая лента», аликвоту приготовленного раствора наносят на линию старта нормально-фазовой пластины ТСХ, процесс хроматографирования осуществляют, используя двухкомпонентную подвижную фазу, которой является смесь растворителей гексан-уксусная кислота в соотношении 7:3 по объему, сорбент с зоны абсорбции тщательно счищают, не допуская потерь сорбента, растворяют в 0,5% растворе аммиака, смесь интенсивно взбалтывают, фильтруют через обеззоленный фильтр «белая лента», к фильтрату добавляют раствор эриохрома черного Т, приготовленный в 0,5% растворе аммиака, далее проводят определение цинка в пробе спектрофотометрическим методом при длине волны 557 ± 2 нм, соответствующей максимуму поглощения комплекса эриохром + цинк в 0,5% растворе аммиака, и толщине поглощающего слоя 1 см.
| Е.А.ПЕТРАКОВА "Методики определения цинка в пробах сточных, подсточных вод и растительной биомассе", Вестник Брянского государственного университета | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| стр | |||
| Раздвижной паровозный золотник с подвижными по его скалке поршнями между упорными шайбами | 1922 |
|
SU148A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ КАТИОНОВ ЦИНКА В СЫВОРОТКЕ КРОВИ С ОДНОВРЕМЕННЫМ ОПРЕДЕЛЕНИЕМ СООТНОШЕНИЯ КАТИОНОВ ЦИНКА И МЕДИ В ТОЙ ЖЕ ПРОБЕ | 2013 |
|
RU2548751C2 |
| КОЛЬЦЕВАЯ ХЛЕБОПЕКАРНАЯ ПЕЧЬ НЕПРЕРЫВНОГО ДЕЙСТВИЯ | 1927 |
|
SU21065A1 |
| Способ определения тяжелых металлов в биологических объектах | 1989 |
|
SU1735774A1 |
| DE3817907 A1 30.11.1989 | |||
| СПОСОБ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ТЯЖЕЛЫХ МЕТАЛЛОВ В ЦЕЛЬНОЙ КРОВИ | 2001 |
|
RU2184973C1 |
Авторы
Даты
2023-11-28—Публикация
2023-03-10—Подача