Область техники
[0001] Настоящее изобретение относится к нуклеиновой кислоте, кодирующей мутант капсидного белка аденоассоциированного вируса (AAV), который обладает тропизмом в отношении головного мозга; к частице AAV, содержащей вариант капсидного белка; и к способу получения клетки, трансдуцированной геном, с использованием этой частицы.
Предпосылки создания изобретения
[0002] AAV представляет собой вирус, имеющий геном линейной одноцепочечной ДНК размером 4,7 т.п.о., содержащий открытые рамки считывания двух генов rep и cap. Ген rep кодирует четыре белка, необходимых для репликации генома (Rep78, Rep68, Rep52 и Rep40). Ген cap экспрессирует три капсидных белка, которые подвергаются сборке с образованием вирусного капсида (VP1, VP2, VP3) и белка, активирующего сборку (AAP). Репликация AAV в природе зависит от присутствия вируса-помощника, такого как аденовирус или герпесвирус. В отсутствии вируса-помощника, геном AAV сохраняется в эписоме или интегрируется в хромосому хозяина, а поэтому AAV присутствует в латентном состоянии. В настоящее время идентифицировано более ста серотипов и кладотипов AAV (непатентная литература 1). В частности, продвигается разработка векторов для доставки генов на основе AAV2.
[0003] В 1989 г. впервые была разработана система векторов для доставки генов на основе AAV2. Было обнаружено, что векторы на основе AAV имеют много преимуществ. Поскольку AAV дикого типа не являются патогенными и не имеют этиологической связи с какими-либо известными заболеваниями, то векторы на основе AAV считаются довольно безопасными. Кроме того, AAV обладает высокой эффективностью в отношении трансдукции генов.
[0004] Введение частиц AAV обеспечивает длительную и стабильную трансдукцию гена в различные органы-мишени и клетки-мишени. В настоящее время уже сообщалось о трансдукции генов с высокой эффективностью в скелетные мышцы, в печень (клетки печени), в сердце (клетки сердечной мышцы), в нервные клетки, в клетки поджелудочной железы и в клетки панкреатических островков. Кроме того, AAV использовали в клинических испытаниях с участием человека. С другой стороны, была предпринята попытка изменить клеточный тропизм AAV путем модификации капсидных белков AAV и попытка избежать удаления частиц AAV нейтрализующими антителами. Так, например, были получены капсиды AAV с тропизмом в отношении конкретных органов и клеток, таких как нейроглиальные клетки, эпителиальные клетки дыхательных путей, эндотелиальные клетки сосудов коронарных артерий и легкие, и были созданы капсиды AAV с тропизмом в отношении опухолевых клеток, таких как клетки глиобластомы, клетки меланомы, клетки рака легких, и клетки рака молочной железы (непатентная литература 2).
Список цитируемой литературы
Непатентная литература
[0005] Непатентная литература 1: Gao et al., J. Virology, Vol. 78, рр. 6381-6388, 2004.
Непатентная литература 2: Adachi K. et al., Genen Ther. Regul., Vol. 5. рр. 31-55, 2010.
Сущность изобретения
Проблема, которая может быть решена с помощью настоящего изобретения
[0006] Целями настоящего изобретения являются получение мутанта капсидного белка AAV с тропизмом в отношении головного мозга и разработка способа эффективного введения гена в головной мозг.
Решение проблем
[0007] Авторами настоящего изобретения были предприняты усиленные попытки решить вышеописанные проблемы, в результате чего была создана нужная частица AAV, где указанная частица AAV включает капсидный белок, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 15-62. Таким образом было осуществлено настоящее изобретение.
[0008] В общих чертах, настоящее изобретение относится:
[1] к нуклеиновой кислоте, кодирующей мутант капсидного белка аденоассоциированного вируса (AAV), включающий пептид, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 15-62, или пептид, содержащий аминокислотную последовательность, которая отличается от аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 15-62, заменой, делецией, инсерцией и/или добавлением одной или нескольких аминокислот;
[2] к нуклеиновой кислоте согласно [1], где капсидный белок AAV происходит от AAV2;
[3] к нуклеиновой кислоте согласно [2], где пептид находится в положении между аминокислотой 588 и аминокислотой 589 в VP1 AAV2;
[4] к рекомбинантной ДНК, содержащей нуклеиновую кислоту согласно любому из [1] - [3];
[5] к клетке, содержащей нуклеиновую кислоту согласно любому из [1] - [3] или рекомбинантную ДНК согласно [4];
[6] к частице AAV, содержащей мутант капсидного белка AAV, который включает пептид, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 15-62, или пептид, содержащий аминокислотную последовательность, которая отличается от аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 15-62, заменой, делецией, инсерцией и/или добавлением одной или нескольких аминокислот;
[7] к частице AAV согласно [6], где капсидный белок AAV происходит от AAV2;
[8] к частице AAV согласно [7], где пептид находится в положении между аминокислотой 588 и аминокислотой 589 в VP1 AAV2;
[9] к способу получения клетки, трансдуцированной геном, где указанный способ включает стадию контактирования частицы AAV, содержащей мутант капсидного белка AAV, который включает пептид, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 15-62, или пептид, содержащий аминокислотную последовательность, которая отличается от аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 15-62, заменой, делецией, инсерцией и/или добавлением одной или нескольких аминокислот, с клеткой;
[10] к способу согласно [9], где капсидный белок AAV происходит от AAV2; и
[11] к способу согласно [10], где пептид находится в положении между аминокислотой 588 и аминокислотой 589 в VP1 AAV2.
Эффекты изобретения
[0009] В соответствии с этим, настоящее изобретение относится к системе трансдукции генов, подходящей для переноса генов в головной мозг. Частица AAV согласно изобретению обладает высоким клеточным тропизмом в отношении головного мозга, и ген, трансдуцированный частицей AAV, может экспрессироваться на высоком уровне.
Краткое описание чертежей
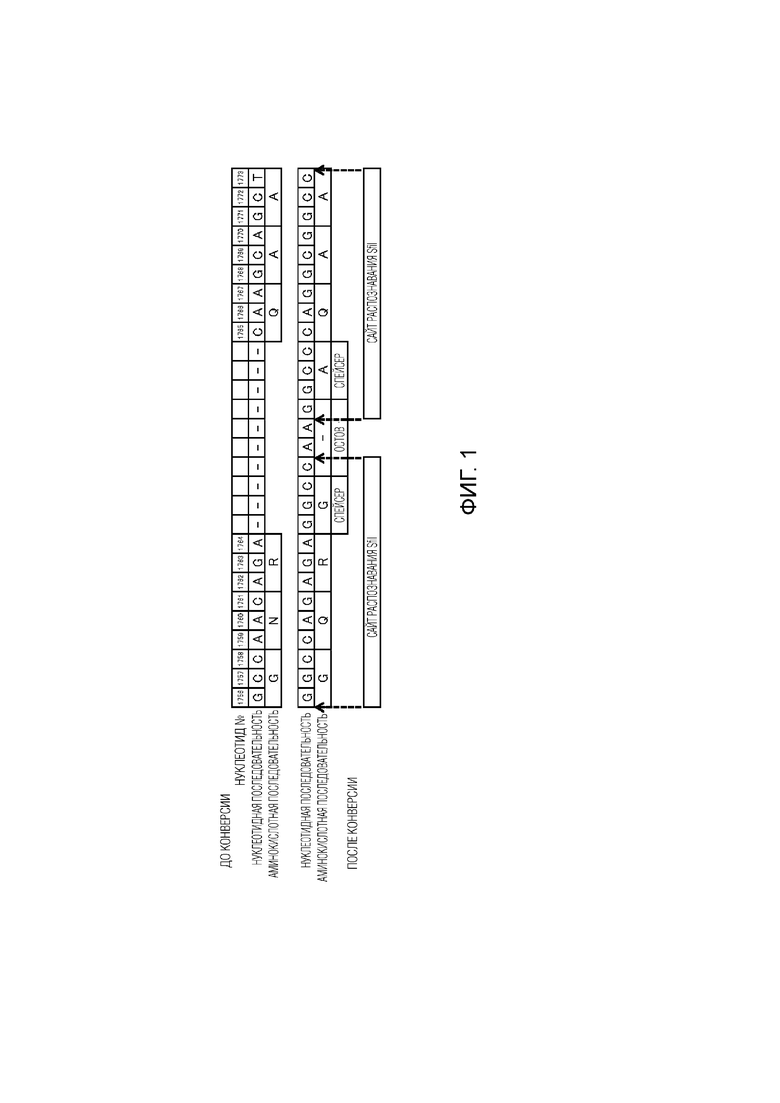
[0010] [Фиг.1] На Фигуре 1 проиллюстрирован способ получения конструкции нуклеиновой кислоты, позволяющей капсидному белку включать неспецифический пептид.
[фиг. 2] На Фигуре 2 представлены результаты оценки тропизма мутантов капсидного белка AAV согласно изобретению.
Способ осуществления изобретения
[0011] Используемый здесь термин «аденоассоциированный вирус» означает небольшой вирус, принадлежащий к роду Dependovirus, который принадлежит семейству Parvoviridae и способен инфицировать приматов, включая человека и других млекопитающих. Далее, аденоассоциированный вирус будет обозначаться AAV. AAV имеет капсулу без оболочки (капсид) в виде правильного икосаэдра и линейную одноцепочечную ДНК внутри этой капсулы. Используемый здесь термин «AAV» включает вирус дикого типа и его производные, а также все серотипы и кладотипы AAV, если это не оговорено особо.
[0012] Используемый здесь термин «вектор» означает молекулу или ассоциированную молекулу, которая используется для опосредуемой доставки полинуклеотида в клетку, и которая содержит полинуклеотид или ассоциируется с полинуклеотидом. Примерами вектора являются векторные ДНК, такие как плазмидные векторы и фаговые векторы, частицы вирусного вектора, липосомы и другие носители для доставки генов, если это не оговорено особо.
[0013] Используемый здесь термин «капсидный белок» означает белок, который кодируется геном cap, присутствующим в геноме AAV, и составляет капсид AAV. Геном AAV дикого типа кодирует три капсидных белка, а именно, VP1, VP2 и VP3. Используемый здесь термин капсидный белок включает VP1, VP2 и VP3.
[0014] Используемый здесь термин «несколько», если он относится к замене, делеции, инсерции и/или к добавлению аминокислот означает, например, 2, 3, 4, 5, 6, 7, 8 или 9 аминокислот в зависимости от длины эталонной аминокислотной последовательности.
[0015] (1) Нуклеиновая кислота, кодирующая мутантный капсидный белок AAV
Нуклеиновая кислота согласно изобретению кодирует мутант капсидного белка AAV, который включает пептид, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 15-62, или пептид, содержащий аминокислотную последовательность, которая отличается от аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 15-62, заменой, делецией, инсерцией и/или добавлением одной или нескольких аминокислот. Предпочтительно, нуклеиновая кислота согласно изобретению кодирует мутант капсидного белка AAV, который включает пептид, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 15 - SEQ ID NO: 62. Более предпочтительно, нуклеиновая кислота согласно изобретению кодирует мутант капсидного белка AAV, который включает пептид, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 15, SEQ ID NO: 16, SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19 и SEQ ID NO: 20, или пептид, содержащий аминокислотную последовательность, которая отличается от аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 15, SEQ ID NO: 16, SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19 и SEQ ID NO: 20 заменой, делецией, инсерцией и/или добавлением одной или нескольких аминокислот. Пептид, содержащий аминокислотную последовательность, которая отличается от аминокислотной последовательности, представленной вышеупомяными SEQ ID NO, заменой, делецией, инсерцией и/или добавлением одной или нескольких аминокислот, если они содержатся в капсидном белке AAV, сохраняет клеточный тропизм мутанта капсидного белка AAV, который включает пептид, содержащий аминокислотную последовательность, представленную вышеупомянутыми SEQ ID NO. Другими словами, количество аминокислот, которые должны быть заменены, делетированы, встроены и/или добавлены в аминокислотную последовательность, представленную вышеупомянутыми SEQ ID NO, не имеет конкретных ограничения, при условии, что будет сохраняться клеточный тропизм, то есть, пептид, содержащий аминокислотную последовательность, представленную вышеупомянутыми SEQ ID NO, будет передаваться мутантному капсидному белку AAV, содержащему этот пептид. Так, например, могут быть заменены, делетированы и/или встроены от 1 до 5, предпочтительно от 1 до 4, более предпочтительно 1, 2 или 3 аминокислоты. Так, например, могут быть добавлены от 1 до 9, предпочтительно от 1 до 8, более предпочтительно от 1 до 7, еще более предпочтительно от 1 до 6, еще более предпочтительно от 1 до 5, а еще более предпочтительно 1, 2, 3 или 4 аминокислоты.
[0016] Так, например, пептид, который должен быть включен в мутант капсидного белка AAV, может представлять собой пептид, содержащий аминокислотную последовательность, которая по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85% или по меньшей мере на 90% идентична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 15 - SEQ ID NO: 62. Пептид, содержащий аминокислотную последовательность, которая по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85% или по меньшей мере на 90% идентична аминокислотной последовательности, представленной вышеупомянутыми SEQ ID NO, если они содержатся в капсидном белке AAV, сохраняет клеточный тропизм мутанта капсидного белка AAV, включающего пептид, содержащий аминокислотную последовательность, представленную вышеупомянутыми SEQ ID NO.
[0017] Так, например, пептид, который должен входить в состав мутантного капсидного белка AAV, может представлять собой пептид, содержащий аминокислотную последовательность, представленную:
формулой I: X1X2GX3GWV;
формулой II: X4X5X6X7GWV;
формулой III: X8X9GX10X11WV;
формулой IV: X12X13GX14GX15V;
формулой V: X16X17GX18GWX19; или
формулой VI: X20X21GX22REX23
где каждый из X1-X23 представляет собой любой аминокислотный остаток, G представляет собой глицин, W представляет собой триптофан, V представляет собой валин, R представляет собой аргинин и E представляет собой глутаминовую кислоту. Предпочтительно, в формуле I (X1X2GX3GWV), X1 представляет собой E (глутаминовую кислоту), G (глицин) или T (треонин), а X2 представляет собой R (аргинин), T (треонин), S (серин), N (аспарагин), E (глутаминовую кислоту) или D (аспарагиновую кислоту), а X3 представляет собой V (валин), H (гистидин), R, M (метионин) или L (лейцин). Предпочтительно, в формуле II (X4X5X6X7GWV), X4 представляет собой A (аланин) или E, X5 представляет собой D, G или A, X6 представляет собой K (лизин), Q (глутамин) или N, а X7 представляет собой V или L. Предпочтительно, в формуле III (X8X9GX10X11WV), X8 представляет собой A, E или G, X9 представляет собой S, D, G или R, X10 представляет собой T, M, D или V, а X11 представляет собой R, V, S или T. Предпочтительно, в формуле IV (X12X13GX14GX15V), X12 представляет собой D, E, G или R, X13 представляет собой A, G, D или V, X14 представляет собой I, H, D, F (фенилаланин), G или L, а X15 представляет собой Y (тирозин), F, R, G или V. Предпочтительно, в формуле V (X16X17GX18GWX19), X16 представляет собой A, E или G, X17 представляет собой G, R или S, X18 представляет собой V, H или D, а X19 представляет собой T, G, K, I (изолейцин) или A. Предпочтительно, в формуле VI (X20X21GX22REX23), X20 представляет собой E или A, X21 представляет собой Y или H, X22 представляет собой F или Y, а X23 представляет собой G или P (пролин).
[0018] Примерами пептида, содержащего аминокислотную последовательность, представленную формулой I, являются, но не ограничиваются ими, пептид, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 18, 20, 21, 22, 46, 55, 59 и 60, и пептид, содержащий аминокислотную последовательность, которая отличается от аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 18, 20, 21, 22, 46, 55, 59 и 60, заменой, делецией, инсерцией и/или добавлением от 1 до 3 аминокислот. Примерами пептида, содержащего аминокислотную последовательность, представленную формулой II, являются, но не ограничиваются ими, пептид, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 25, 29 и 32, и пептид, содержащий аминокислотную последовательность, которая отличается от аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 25, 29 и 32, заменой, делецией, инсерцией и/или добавлением от 1 до 4 аминокислот. Примерами пептида, содержащего аминокислотную последовательность, представленную формулой III, являются, но не ограничиваются ими, пептид, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 15, 24, 38, 48 и 54, и пептид, содержащий аминокислотную последовательность, которая отличается от аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 15, 24, 38, 48 и 54, заменой, делецией, инсерцией и/или добавлением от 1 до 4 аминокислот. Примерами пептида, содержащего аминокислотную последовательность, представленную формулой IV, являются, но не ограничиваются ими, пептид, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 19, 31, 35, 44, 56 и 58, и пептид, содержащий аминокислотную последовательность, которая отличается от аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 19, 31, 35, 44, 56 и 58, заменой, делецией, инсерцией и/или добавлением от 1 до 4 аминокислот. Примерами пептида, содержащего аминокислотную последовательность, представленную формулой V, являются, но не ограничиваются ими, пептид, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 26, 39, 42, 43, 47 и 50, и пептид, содержащий аминокислотную последовательность, которая отличается от аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 26, 39, 42, 43, 47 и 50, заменой, делецией, инсерцией и/или добавлением от 1 до 4 аминокислот. Примерами пептида, содержащего аминокислотную последовательность, представленную формулой VI, являются, но не ограничиваются ими, пептид, содержащий аминокислотную последовательность, представленную SEQ ID NO: 16 или 17, и пептид, содержащий аминокислотную последовательность, которая отличается от аминокислотной последовательности, представленной SEQ ID NO: 16 или 17, заменой, делецией, инсерцией и/или добавлением от 1 до 4 аминокислот.
[0019] Мутантный капсидный белок AAV, кодируемый нуклеиновой кислотой согласно изобретению, может быть получен путем встраивания пептида в капсидный белок AAV любого AAV дикого типа, такого как AAV типа 1 (AAV1), AAV типа 2 (AAV2), AAV типа 3 (AAV3A, AAV3B и т.п.), AAV типа 4 (AAV4), AAV типа 5 (AAV5), AAV типа 6 (AAV6), AAV типа 7 (AAV7), AAV типа 8 (AAV8), AAV типа 9 (AAV9), AAV типа 10 (AAV10), AAV типа 11 (AAV11), птичий AAV, бычий AAV, собачий AAV, лошадиный AAV или овечий AAV, или путем замены части аминокислотной последовательности капсидного белка AAV пептидом (другими словами, путем получения капсидного белка AAV, содержащего пептид). В настоящем изобретении, предпочтительно используется капсидный белок AAV2.
[0020] Мутантный капсидный белок AAV, кодируемый нуклеиновой кислотой согласно изобретению, может представлять собой белок, содержащий замену, делецию, инсерцию и/или добавление одной или более или нескольких аминокислот, а также вышеупомянутый пептид в капсидном белке AAV дикого типа. «Белок, содержащий замену, делецию, инсерцию и/или добавление одной или более или нескольких аминокислот, а также вышеупомянутый пептид» сохраняет свойства исходного белка, например, клеточный тропизм мутантного капсидного белка AAV, сообщаемый вышеупомянутым пептидом, способность образовывать капсид, функцию капсидного белка (например, защиту вирусного генома, удаление оболочки после проникновения в клетки-хозяева) и т.п.
[0021] Кроме того, к N-концу и/или C-концу пептида, который должен входить в состав капсидного белка AAV, может быть присоеднена спейсерная последовательность. Спейсерная последовательность предпочтительно состоит из 1-5 аминокислотных остатков. Аминокислотные остатки, составляющие спейсерную последовательность, имеют конкретные ограничения. Так, например, спейсерная последовательность может содержать аминокислоту, выбранную из группы, состоящей из глицина, аланина и серина.
[0022] В качестве капсидного белка AAV для включения пептида могут быть использованы AAV VP1, VP2 или VP3. Только один из VP1, VP2 и VP3 может быть получен так, чтобы он содержал пептид, либо все VP1, VP2 и VP3 могут быть получены так, чтобы они содержали пептид. Кроме того, два капсидных белка, такие как VP1 и VP2, VP2 и VP3 или VP1 и VP3 могут быть получены так, чтобы они содержали пептид. VP1-VP3 кодируются областью гена cap в геноме AAV. В одном варианте осуществления изобретения, область, охватываемая VP1-VP3, создана так, чтобы она содержала пептид, и так, чтобы мутация могла быть введена во все VP1-VP3. В другом варианте осуществления изобретения, ген, кодирующий VP1, VP2 или VP3, получают отдельно от области гена cap AAV, и в этот ген вводят мутацию. В этом случае, может быть осуществлена обработка, которая ингибирует капсидный белок дикого типа, соответствующий капсидному белку, кодируемому геном, в который была введена мутация посредством экспрессии в области гена cap AAV.
[0023] В случае использования VP1 AAV2, мутант капсидного белка AAV, кодируемый нуклеиновой кислотой согласно изобретению, предпочтительно содержит пептид в положении между аминокислотой 588 и аминокислотой 589. Аминокислота 588 в VP1 AAV2 представляет собой аргинин. Аминокислота 589 в VP1 AAV2 представляет собой глутамин. Аминокислота 588 VP1 AAV2 соответствует аминокислоте 451 VP2 AAV2 и аминокислоте 386 VP3 AAV2. В случае, когда в качестве капсидного белка AAV используют капсидный белок AAV, серотипы и кладотипы которого отличаются от AAV2, то капсидный белок AAV получают так, чтобы он содержал пептид между аминокислотами, соответствующими аминокислотам 588 и 589 VP1 AAV2. Специалист в данной области может легко идентифицировать аминокислоту капсидного белка серотипов и кладотипов AAV, отличающихся от AAV2, которая соответствует аминокислоте 588 VP1 AAV2. Так, например, см. выравнивание аминокислотных последовательностей VP1, представленное Gao et al., Proc. Natl. Acad. Sci. USA, Vol.99, No. 18, pp. 11854-11859, 2002. Так, например, аминокислота 588 VP1 AAV2 соответствует аминокислоте 589 AAV1, аминокислоте 590 AAV7 и аминокислоте 591 AAV8.
[0024] Нуклеиновая кислота согласно изобретению может быть функционально связана с подходящей регуляторной последовательностью. Примерами регуляторной последовательности являются промоторная последовательность, сигнал полиаденилирования, последовательность терминации транскрипции, вышерасположенный регуляторный домен, ориджин репликации, внутренний сайт связывания с рибосомой (IRES) и энхансер. Примерами промоторных последовательностей являются индуцибельная промоторная последовательность и конститутивная промоторная последовательность. Регуляторная последовательность может представлять собой эндогенную или экзогенную последовательность AAV, от которой происходит капсидный белок, нативную последовательность или синтезированную последовательность. Настоящее изобретение также включает такую рекомбинантную ДНК, способную экспрессировать мутантный капсидный белок AAV.
[0025] Рекомбинантная ДНК согласно изобретению является подходящей для доставки нуклеиновой кислоты согласно изобретению в клетки in vitro, ex vivo или in vivo и сообщения клеткам способности экспрессировать мутантный капсидный белок AAV. Затем, клетка, в которую доставляется нуклеиновая кислота согласно изобретению, может быть использована для получения частиц AAV. Рекомбинантная ДНК может быть, в частности, использована для доставки или введения нуклеиновой кислоты согласно изобретению в клетки животных, а предпочтительно в клетки млекопитающих.
[0026] В настоящем изобретении, рекомбинантная ДНК согласно изобретению может быть получена путем создания ДНК, используемой в качестве вектора для сохранения нуклеиновой кислоты согласно изобретению. Так, например, могут быть использованы плазмидная ДНК, фаговая ДНК, транспозон, космидная ДНК, эписомная ДНК или вирусный геном.
[0027] (2) Клетка, содержащая нуклеиновую кислоту согласно изобретению
Настоящее изобретение также относится к клетке-хозяину, например, к выделенной клетке-хозяину, содержащей нуклеиновую кислоту согласно изобретению, а в частности, рекомбинантную ДНК, как описано выше в (1). Выделенная клетка представляет собой, например, клеточную линию, поддерживаемую in vitro. Клетка-хозяин согласно изобретению является подходящей для получения частицы AAV согласно изобретению, как объясняется ниже. Если клетка-хозяин согласно изобретению используется для продуцирования частиц AAV, то такая клетка-хозяин может называться «упаковывающей клеткой» или «клеткой-продуцентом». Клетка-хозяин согласно изобретению может содержать рекомбинантную ДНК согласно изобретению, описанную выше в (1) и интегрированную в геном, или сохранять рекомбинантную ДНК в клетке, так, чтобы она временно экспрессировала мутант капсидного белка AAV.
[0028] Введение рекомбинантной ДНК согласно изобретению в клетку-хозяина может быть осуществлено известным способом. Так, например, могут быть осуществлены электропорация, осаждение фосфатом кальция, прямая микроинъекция в клетки, опосредуемая липосомами трансфекция генов, или доставка нуклеиновой кислоты с использованием «дробовика» для высокоскоростной подачи частиц. При использовании вирусного вектора может быть выбран способ инфицирования, подходящий для этого вектора. При применении такого разработанного метода, рекомбинантную ДНК согласно изобретению стабильно вводят в хромосому клетки-хозяина или временно в цитоплазму клетки-хозяина. Для стабильной трансформации, селективный маркер, например, хорошо известный селективный маркер, такой как ген резистентности к неомицину (кодирующий неомицинфосфотрансферазу) или ген резистентности к гигромицину B (кодирующий аминогликозид-фосфотрансферазу (APH)), может быть связан с рекомбинантной ДНК согласно изобретению.
[0029] В качестве клетки-хозяина могут быть использованы различные клетки, например, клетки млекопитающих, включая клетки мышей и клетки приматов (например, человеческие клетки) или клетки насекомых. Подходящими примерами клеток млекопитающих являются, но не ограничиваются ими, первичные клетки и клеточные линии. Примерами подходящих клеточных линий являются клетки 293, клетки COS, клетки HeLa, клетки Vero, мышиные фибробласты 3T3, фибробласты C3H10T1/2, клетки CHO и клетки, полученные из этих клеток.
[0030] (3) Частица AAV, включающая капсидный белок AAV, содержащий аминокислотную последовательность, кодируемую нуклеиновой кислотой согласно изобретению.
Частица AAV согласно изобретению представляет собой частицу AAV, включающую мутант капсидного белка AAV, содержащий пептид, описанный выше в (1). Частица AAV согласно изобретению может быть получена из клетки-хозяина, описанной выше в (2). Частица AAV согласно изобретению обладает тропизмом в отношении головного мозга и может быть использована для введения гена в головной мозг. Головной мозг включает клетки головного мозга, такие как нейроны и глиальные клетки (микроглиальные клетки, олигодендроциты, астроциты). Ген, вводимый частицей AAV согласно изобретению, в высокой степени экспрессируется в вышеупомянутых тканях, органах и клетках.
[0031] Для продуцирования частиц AAV, клетка, содержащая некоторые элементы, необходимые для продуцирования частиц AAV, может быть использована в качестве упаковывающей клетки. Первый элемент представляет собой векторный геном (также называемый экспрессионным вектором) для рекомбинантного AAV, который может реплицироваться в клетке-хозяине и упаковываться в частицу AAV. Геном рекомбинантного вектора AAV содержит представляющий интерес гетерологичный полинуклеотид и последовательности инвертированных концевых повторов (ITR) AAV, расположенные на каждой стороне, то есть, на 5'- и 3'-сторонах представляющего интерес гетерологичного полинуклеотида. Представляющий интерес гетерологичный полинуклеотид может иметь последовательность регуляции экспрессии. Нуклеотидные последовательности ITR являются известными. Так, например, последовательности AAV2-ITR можно найти в публикации Human Gene Therapy, Vol.5, pp. 793-801, 1994. Что касается последовательностей ITR AAV, то могут быть использованы последовательности ITR, происходящие от AAV любых различных серотипов, включая AAV1, AAV2, AAV3, AAV4, AAV5, AAV7 и т.п. Последовательности ITR, используемые в настоящем изобретении, могут происходить от AAV дикого типа или могут быть модифицированы путем инсерции, делеции или замены нуклеотида(ов). Последовательности ITR позволяют осуществлять репликацию генома рекомбинантного вектора AAV в присутствии белка Rep и обеспечивают включение генома рекомбинантного вектора AAV в капсидную часть при продуцировании частиц AAV.
[0032] Размер представляющего интерес гетерологичного полинуклеотида, который может находиться внутри частиц AAV согласно изобретению, обычно составляет приблизительно менее, чем 5 тысяч пар оснований (т.п.о.). Представляющий интерес гетерологичный полинуклеотид может представлять собой, например, ген, кодирующий представляющий интерес белок, который у реципиента либо отсутствует, либо удаляется; ген, кодирующий белок, обладающий нужной биологической или терапевтической активностью (например, антимикробной, противовирусной или противоопухолевой активностью); нужную нуклеотидную последовательность, кодирующую РНК, которая ингибирует или снижает уровень продуцирования вредного или нежелательного белка; или нуклеотидную последовательность, кодирующую антигенный белок. Представляющий интерес гетерологичный полинуклеотид может быть соответствующим образом выбран в зависимости от целей его применения.
[0033] В одном варианте осуществления изобретения, в геноме рекомбинантного вектора AAV отсутствует область гена cap и/или область гена rep. В этом варианте осуществления изобретения, частица AAV, в которой упакован геном рекомбинантного вектора AAV, не реплицируется отдельно, и в инфицированной клетке, частица AAV повторно не образуется.
[0034] Второй элемент, необходимый для продуцирования частиц AAV, представляет собой конструкцию, которая обеспечивает белки, кодируемые AAV дикого типа. Эта конструкция кодирует гены, происходящие от AAV и обеспечивающие продукты генов AAV, необходимые для образования частиц AAV. Другими словами, эта конструкция содержит одну или две основных ОРС AAV, кодирующих области гена rep и гена cap. Для получения частиц AAV согласно изобретению, в качестве ген cap используется по меньшей мере нуклеиновая кислота, кодирующая мутант капсидного белка AAV, включающий пептид, имеющий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 15 - SEQ ID NO: 62. Клетка-хозяин согласно изобретению, описанная выше в (2) и способная экспрессировать мутант, может быть использована для продуцирования частиц AAV. Частица AAV имеет капсулу, состоящую из множества капсидных белков. Все капсидные белки могут быть мутантами, либо часть капсидных белков могут быть мутантами, а другие могут представлять собой белки капсида дикого типа. Частица AAV согласно изобретению может содержать мутант капсидных белков одного вида или мутанты капсидных белков нескольких видов.
[0035] Ген rep AAV содержится в кодирующих областях гена rep и включает гены, кодирующие белки репликации Rep78, Rep68, Rep52 и Rep40. Было показано, что эти продукты экспрессии Rep обладают многими функциями, включая распознавание, связывание и образование одноцепочесного разрыва ориджина репликации геномной ДНК AAV, ДНК-геликазную активность и модуляцию транскрипции из промоторов, происходящих от AAV.
[0036] Третий элемент, необходимый для продуцирования частиц AAV, представляет собой функциональный вирус-помощник (также называемый вспомогательным функциональным вирусом) для репликации AAV. Для сообщения хелперных функций обычно используется аденовирус. Однако, могут быть также использованы и другие вирусы, такие как вирус простого герпеса типа 1 или типа 2 и вирус осповакцины. При использовании вируса, клетку-хозяина инфицируют вирусом в качестве вируса-помощника. Так, например, поскольку экспрессия ранних генов аденовируса необходима только для упаковки частиц AAV, то может быть использован аденовирус, который не обнаруживает экспрессию поздних генов. Также может быть использован мутант аденовируса, который не экспрессирует поздние гены (например, вариант аденовируса ts100K или ts149). Конструкция нуклеиновой кислоты, которая обеспечивает функции вируса-помощника, может быть также получена с использованием нуклеиновых кислот, необходимых для функционирования вируса-помощника и выделенных из вируса-помощника, а затем она может быть введена в клетку-хозяина. Конструкция, которая обеспечивает функции вируса-помощника, содержит нуклеотидную последовательность, обеспечивающую одну или несколько функций вируса-помощника, и презентируется клетке-хозяину в форме плазмиды, фага, транспозона, космиды или других вирусов.
[0037] Для получения частиц AAV осуществляют: (а) стадию введения первого элемента, генома рекомбинантного вектора AAV в клетку-хозяина, (b) стадию введения второго элемента, то есть, конструкции, которая сообщает хелперные функции AAV клетке-хозяину, и (c) стадию введения третьего элемента, то есть, вируса-помощника в клетку-хозяина. Эти стадии могут быть осуществлены одновременно или по порядку. Порядок проведения стадий (а) - (с) может быть любым. Если в клетку-хозяина вводят элементы с первого по третий, то продукты экспрессии гена rep вырезаются и реплицируется геном рекомбинантного вектора. Экспрессированные капсидные белки образуют капсид, и геном рекомбинантного вектора упаковывается в капсид с образованием частицы AAV. Если клетка-хозяин экспрессирует мутантный капсидный белок AAV, то оболочка полученной частицы AAV включает мутантный капсидный белок AAV.
[0038] Частица AAV может быть выделена и очищена из супернатанта культуры или лизата клетки-хозяина с применением различных методов очистки, таких как центрифугирование в градиенте плотности CaCl. Если вирус используется в вышеописанной стадии (c), то, например, может быть дополнительно проведена стадия отделения частицы AAV от вируса-помощника исходя из их размера. Частица AAV также может быть отделена от вируса-помощника исходя из различий в аффинности к гепарину. Кроме того, оставшиеся вирусы-помощники могут быть инактивированы известными методами. Так, например, аденовирусы могут быть инактивированы путем нагревания приблизительно при 60ºC, например, в течение 20 минут или более. Поскольку частицы AAV очень устойчивы к нагреванию, то описанная выше обработка является эффективной для селективного удаления аденовирусов, используемых в качестве вирусов-помощников.
[0039] (4) Способ получения клетки согласно изобретению, трансдуцированной геном
Частицу AAV согласно изобретению, полученную как описано выше в (3), используют для доставки представляющего интерес гетерологичного полинуклеотида в клетку в целях проведения генотерапии или в других целях. Частицу AAV обычно вводят в клетку in vivo или in vitro. Для введения in vitro, частицу AAV подвергают контактированию с клеткой, полученной из живого организма. Затем клетка может быть также трансплантирована в живой организм. Для введения клетки в живой организм, клетка может быть получена в виде фармацевтической композиции, которая может быть введена различными методами, такими как внутримышечное, внутривенное, подкожное и внутрибрюшинное введение. Для трансдукции in vivo, частицу AAV получают в виде фармацевтической композиции и, обычно вводят парентерально (например, внутримышечно, подкожно, вовнутрь опухоли, трансдермально или интраспинально). Фармацевтическая композиция, включающая частицу AAV, может содержать фармацевтически приемлемый носитель и, при необходимости, другой агент, лекарственное средство, стабилизатор, носитель, адъювант, разбавитель и т.п.
Примеры
[0040] Настоящее изобретение более подробно описано со ссылкой на нижеследующие Примеры, которые не рассматриваются как ограничение объема изобретения.
[0041] Пример 1. Получение библиотеки плазмид неспецифических пептидов AAV2
Плазмидный вектор pAV1 (АТСС: № 37215), несущий геном AAV2, экстрагировали из широко распространенного хозяина Escherichia coli HB101. Из экстрагированной плазмиды вырезали геномную ДНК AAV2 (приблизительно 4,7 т.п.о.) под действием рестриктирующего фермента BgIII (производимого TAKARA BIO Inc.). Эту геномную ДНК встраивали в pUC118 BamHI/BAP (производимую TAKARA BIO Inc.). Полученная таким образом плазмидная ДНК была названа AAV2WG/pUC118.
[0042] AAV2WG/pUC118 расщепляли рестриктирующим ферментом ScaI (производства TAKARA BIO Inc.) с получением фрагмента размером приблизительно 0,8 т.п.о., содержащего нуклеотиды 1190-2017 гена cap. Этот фрагмент был встроен в pUC118 HincII/BAP (производства TAKARA BIO Inc.). Полученная таким образом плазмидная ДНК была названа Cap-ScaI/pUC118. Затем Cap-ScaI/pUC118 подвергали ПЦР для проведения серии модификаций, где нуклеотидную последовательность AAC(587N), состоящую из нуклеотидов 1759-1761 гена Cap в Cap-ScaI/pUC118, конвертировали в CAG (587Q), где 10 нуклеотидов, состоящих из GGC в качестве спейсера, CAAG в качестве остова и GCC в качестве спейсера, были встроены между нуклеотидом 1764 и нуклеотидом 1765, а нуклеотидная последовательность CAA(589Q)GCA(590A)GCT(591A), состоящая из нуклеотидов 1765-1773, была конвертирована в CAG(589Q GCG(590A)GCC(591A), где буквы в скобках означают номера аминокислот и кодируемые аминокислоты. Таким образом, были встроены два сайта распознавания рестриктирующего фермента SfiI, и между ними были встроены спейсер, остов и спейсер. На фигуре 1 показаны нуклеотидные последовательности до и после конверсии нуклеотидов 1756-1773 гена Cap. Нуклеотидная последовательность до конверсии представлена SEQ ID NO: 1 в списке последовательностей. Нуклеотидная последовательность после конверсии представлена SEQ ID NO: 2. Плазмидная ДНК, содержащая конвертированную нуклеотидную последовательность, была названа Cap-ScaI-S4/pUC118. Для клонирования методом слияния, часть гена Cap в Cap-ScaI-S4/pUC118 амплифицировали с помощью ПЦР с получением фрагмента размером приблизительно 0,8 т.п.о. Этот фрагмент использовали в качестве ДНК-вставки.
[0043] AAV2WG/pUC118 был подвергнут ПЦР, так, чтобы мутация была введена в сайт распознавания рестриктирующего фермента ScaI в гене резистентности к ампициллину и в сайт распознавания рестриктирующего фермента SfiI в гене Rep, так, чтобы эти сайты распознавания были конвертированы в последовательности, которые не распознаются рестриктирующими ферментами. Для сайта распознавания ScaI, нуклеотидная последовательность GAG (E), состоящая из нуклеотидов 304-306 гена резистентности к ампициллину, была конвертирована в GAA(E). Последовательность до конверсии представлена SEQ ID NO: 3, а последовательность после конверсии представлена SEQ ID NO: 4. Для сайта распознавания SfiI, нуклеотидная последовательность GCC(A), состоящая из нуклеотидов 217-219 гена Rep, была конвертирована в GCA(A). Последовательность до конверсии представлена SEQ ID NO: 5, а последовательность после конверсии представлена SEQ ID NO: 6. Полученная таким образом плазмидная ДНК была расщеплена ферментом ScaI (производства TAKARA BIO Inc.) с получением линейного вектора, не содержащего приблизительно 0,8 т.п.о., которые были частью гена Cap. Этот вектор был использован в качестве линейного вектора для клонирования методом слияния.
[0044] С использованием набора для клонирования HD методом слияния (зарегистрированный товарный знак) (производимого Clontech Laboratories, Inc.) и усилителя клонирования (производимого Сlontech Laboratories, Inc.), ДНК-вставку встраивали в линейный вектор, и тем самым осуществляли направленное клонирование. Полученная таким образом плазмидная ДНК была названа AAV2WG-Cap-ScaI-S4/pUC118Sx.
[0045] Олиго-ДНК (SEQ ID NO: 7), содержащая нуклеотидную последовательность, кодирующую неспецифический пептид из 7 аминокислот, была получена путем искусственного синтеза. Двухцепочечную ДНК получали из олиго-ДНК посредством реакции взаимодействия с праймером (SEQ ID NO: 8) и фрагментом Кленова (производимым TAKARA BIO Inc.) при 37°C в течение 3 часов. Двухцепочечную ДНК очищали с использованием набора для удаления нуклеотидов (производимого QIAGEN), а затем расщепляли рестриктирующим ферментом BglI (производимым TAKARA BIO Inc.). Эту ДНК встраивали в AAV2WG-Cap-ScaI-S4/pUC118Sx, расщепленную SfiI, с использованием набора для лигирования ДНК <Mighty Mix> (производимого TAKARA BIO Inc.). Полученная таким образом плазмида была названа AAV2WG-RPL/pUC118Sx и использовалась в качестве библиотеки плазмид неспецифических пептидов AAV2.
[0046] Пример 2: Получение вирусной библиотеки неспецифических пептидов AAV2
(1) Посев клеток AAV293
Культивируемые клетки AAV293 (производимые Stratagene Corp.) собирали, а затем суспендировали в среде DMEM (производимой Sigma), содержащей 10% FBS и 2 мМ L-глутамата натрия в концентрации 5 × 104 клеток/мл. В колбу T225 см2 для культивирования клеток (изготовленную Corning Incorporated) помещали 40 мл суспензии, содержащей клетки AAV293, а затем культивировали при 37°C в течение 72 часов в инкубаторе с CO2.
[0047] (2) Введение плазмиды в клетку AAV293.
Клетки AAV293 трансфицировали 400 нг AAV2WG-RPL/pUC118Sx, полученной как описано в Примере 1, и 40 мкг pHELP (производимого CELL BIOLABS, Inc.) обычным методом с использованием фосфата кальция. Через шесть часов после трансфекции, среду полностью удаляли. После добавления 40 мл среды DMEM, содержащей 2% FBS и 2 мМ L-глутамата натрия, клетки культивировали при 37ºC в течение 48 часов в CO2-инкубаторе.
[0048] (3) Сбор вирусной библиотеки неспецифических пептидов AAV2.
В инкубируемую колбу T225 см2 добавляли 0,5 мл 0,5 М EDTA с последующим выдерживанием в течение нескольких минут. Затем клетки AAV293 слущивали и собирали в 50 мл-пробирку с помощью пипетки и центрифугировали при 300× g в течение 10 минут. Затем удаляли супернатант. Клетки ресуспендировали в 2 мл TBS (трис-забуференного солевого раствора) на колбу, а затем трижды подвергали последовательной обработке, состоящей из замораживания смесью этанола/сухого льда в течение 15 минут, оттаивания на водяной бане при 37°C в течение 15 минут и встряхивания в течение 1 минуты для сбора клеточного лизата, содержащего библиотеку вирусов AAV-неспецифических пептидов. К этому клеточному лизату добавляли 5 мкл 1M MgCl2 на 1 мл TBS и нуклеазу Бензоназа (зарегистрированный торговый знак) (производства Merck KGaA) в конечной концентрации 200 ед./мл с последующим проведением реакции при 37ºC в течение 30 минут. Затем реакцию прекращали добавлением 6,5 мкл 0,5 М EDTA на 1 мл TBS. Клеточный лизат центрифугировали при 10000 об/мин и при 4°C в течение 10 минут, а затем собирали супернатант в виде раствора вектора AAV.
[0049] (4) Количественная оценка титра раствора вектора AAV с помощью ПЦР в реальном времени
В 2 мкл раствора вектора AAV добавляли 2 мкл 10 × буфера ДНКазы I, 15,2 мкл воды для инъекций (производства Otsuka Pharmaceutical Co., Ltd.) и 0,8 мкл ДНКазы I (производства TAKARA BIO Inc.), и смесь инкубировали при 37°C в течение 1 часа для удаления свободных геномных ДНК и плазмидных ДНК. Для инактивации ДНКазы I, смесь нагревали при 99ºC в течение 10 минут. Затем добавляли 15 мкл воды для инъекций, 4 мкл буфера 10 × ProK [0,1 M трис-HCl (pH 7,8), 0,1 M EDTA, 5% ДСН] и 1 мкл протеиназы K (производства TAKARA BIO Inc.), и смесь инкубировали при 55ºC в течение 1 часа. Затем для инактивации протеиназы K, смесь нагревали при 95ºC в течение 10 минут. Этот образец подвергали количественной оценке титра AAV с использованием SYBR (зарегистрированный торговый знак) Premix ExTaq2 (производства TAKARA BIO Inc.) и праймеров (SEQ ID NO: 9 и SEQ ID NO: 10) в соответствии с инструкциями, прилагаемыми к набору. Образец 50-кратно разводили водой для инъекций, и 2 мкл разведенного раствора использовали для количественной оценки титра. В качестве стандарта использовали линейную ДНК, полученную путем гидролиза pAV1 рестриктирующим ферментом.
[0050] Пример 3: Очистка вирусной библиотеки неспецифических пептидов AAV
(1) Очистка 1 путем центрифугирования в градиенте плотности хлорида цезия.
В пробирку 40PA для ультрацентрифугирования (производства HITACHI-KOKI Co., Ltd.) последовательно, в указанном порядке, начиная снизу слоями добавляли 4 мл раствора хлорида цезия, доведенного до плотности 1,5; 4 мл раствора хлорида цезия, доведенного до плотности 1,25; и 28 мл раствора вектора AAV, приготовленного как описано в Примере 2-(4). Пробирку центрифугировали при 25000 об/мин и при 16°C в течение 3 часов на ультрацентрифуге HIMAC (производства HITACHI-KOKI Co., Ltd.). После центрифугирования, 28 мл раствора удаляли из верхней части пробирки, а затем аликвоту 0,7 мл раствора собирали из верхней части в 1,5-мл пробирку. Таким же образом, как и в Примере 2-(4), определяли титр вектора AAV, содержащегося в каждом собранном растворе.
[0051] (2) Очистка 2 путем центрифугирования в градиенте плотности хлорида цезия.
В нескольких фракциях, которые, как было показано в Примере 3-(1), имеют высокий титр, добавляли раствор хлорида цезия, доведенный до плотности 1,39, для достижения общего объема 10,5 мл. Полученный таким образом раствор помещали в пробирку 13РА для ультрацентрифугирования (изготовленную HITACHI-KOKI Co., Ltd.), а затем центрифугировали при 38000 об/мин и при 18°C в течение 16 часов. После центрифугирования, аликвоту 0,7 мл раствора отбирали из верхней части пробирки. Таким же образом, как и в Примере 2-(4), определяли титр вектора AAV, содержащегося в каждом собранном растворе.
[0052] (3) Обессоливание путем диализа
Несколько фракций, которые, как было показано в Примере 3-(2), имели высокий титр, смешивали, а затем добавляли в кассету для диализа Slide-A-lyzer (производства Pierce). Очищенный раствор AAV дважды обессоливали путем диализа 1 л забуференного фосфатом физиологическиого раствора (PBS) при 4ºC в течение 3 часов и путем диализа 500 мл раствора PBS/5% сорбита при 4ºC в течение ночи. Затем раствор собирали, стерилизовали на 0,22 мкм-фильтре (производства Millipore) и хранили при -80°C непосредственно перед использованием. Отдельно, титр очищенных частиц AAV определяли количественно таким же образом, как и в Примере 2-(4).
[0053] Пример 4: Скрининг библиотеки неспецифических пептидов AAV2
(1) Введение в хвостовую вену мышей
Очищенные частицы AAV, полученные как описано в Примере 3-(3), вводили мышам BALB/c в хвостовую вену при 1,5 × 1014 вирусного генома (VG)/кг. Через 72 часа после введения, головной мозг собирали, и геномные ДНК экстрагировали с использованием ткани NucleoSpin (торговую марку) (производства MACHEREY-NAGEL GmbH & Co. KG) (Раунд 1).
[0054] (2) Повторное клонирование неспецифической пептидной последовательности с помощью ПЦР.
ДНК, кодирующую неспецифическую пептидную последовательность, амплифицировали с использованием геномной ДНК, экстрагированной как описано в Примере 4-(1), в качестве матрицы, и ДНК-полимеразы GXL PrimeSTAR (зарегистрированный торговый знак) (производства TAKARA BIO Inc.). В качестве праймеров использовали прямой праймер 1 (SEQ ID NO: 11) и обратный праймер 1 (SEQ ID NO: 12). ПЦР осуществляли путем повторения 30 циклов, и каждый цикл ПЦР состоял из нагревания при 98°C в течение 10 секунд, при 55°C в течение 15 секунд и при 68°C в течение 40 секунд. Затем двадцать пятую часть реакционного раствора ПЦР, прямой праймер 2 (SEQ ID NO: 13) и обратный праймер 2 (SEQ ID NO: 14) использовади для приготовления реакционной смеси в том же количестве, как и ранее. Реакционную смесь подвергали ПЦР с 30 циклами, где каждый цикл состоял из нагревания при 98°C в течение 10 секунд, при 55°C в течение 15 секунд и при 68°C в течение 15 секунд. Из полученного таким образом реакционного раствора, ДНК очищали с использованием экстракта NucleoSpin II (производства MACHEREY-NAGEL GmbH & Co. KG) и расщепляли рестриктирующим ферментом BglI. После электрофореза, расщепленный продукт очищали с использованием экстракта NucleoSpin II и повторно клонировали в AAV2WG-Cap-ScaI-S4/pUC118Sx, полученную как описано в Примере 1, с использованием набора для лигирования ДНК <Mighty Mix>.
[0055] (3) Получение и очистка вирусной библиотеки неспецифических пептидов AAV2.
Получение вирусной библиотеки неспецифических пептидов вируса AAV2 и очистку частиц AAV осуществляли с использованием плазмиды, полученной как описано в Примере 4-(2), такими же методами, которые были описаны в Примере 2 и в Примере 3.
[0056] (4) Скрининг
Таким же образом, как и в Примере 4-(1) был проведен скрининг (введение частиц AAV мышам и сбор головного мозга) и были экстрагированы геномные ДНК (раунд 2). Кроме того, с использованием экстрагированной геномной ДНК были повторно проведены клонирование, получение и очистка библиотеки, а также были экстрагированы геномные ДНК (раунд 3).
[0057] (5) Секвенирование неспецифического пептида.
На каждой стадии скрининга (от раунда 1 до раунда 3) проводили секвенирование плазмидной библиотеки неспецифических пептидов AAV. Пептидные последовательности, кодируемые клонами, которые аккумулировались в головном мозге во 2-м и 3-м раундах, и частота их появления представлены в Таблице 1 и в Таблице 2.
[0058] [Таблица 1]
[0059]
[Таблица 2]
[0060]
Как показано в Таблице 1 и Таблице 2, AAV имеет капсиды, содержащие специфические пептидные последовательности, накопленные в головном мозге. В частности, предполагается, что пептидные последовательности GSGVTWV (SEQ ID NO: 15), AHGYREP (SEQ ID NO: 16), EYGFREG (SEQ ID NO: 17) и ETGHGWV (SEQ ID NO: 18), которые наблюдались в третьем раунде, имеют тенденцию инфицировать головной мозг.
[0061] Кроме того, предполагается, что пептидные последовательности от SEQ ID NO: 63 до SEQ ID NO: 110, которые представляют собой последовательности, содержащие последовательности, наблюдаемые во втором раунде, и спейсер, имеют тенденцию инфицировать головной мозг. В частности, GGSGVTWVA (SEQ ID NO: 63), GAHGYREPA (SEQ ID NO: 64), GEYGFREGA (SEQ ID NO: 65) и GETGHGWVA (SEQ ID NO: 66), которые представляют собой последовательности, содержащие последовательности, наблюдаемые в третьем раунде 3 и спейсер, обычно инфицируют головной мозг.
[0062] Пример 5: Оценка тропизма вектора AAV, имеющего приобретенную пептидную последовательность
(1) Конструирование pRC-GDDGTRG, имеющего приобретенную пептидную последовательность.
Клоны AAV2WG-Cap-ScaI-S4/pUC118Sx, имеющие пептидные последовательности (SEQ ID NO: 15-20) и полученные как описано в Примере 4-(5), расщепляли рестриктирующими ферментами SnaBI (производства TAKARA BIO Inc.) и HindIII (производства TAKARA BIO Inc.) с получением фрагмента. Этот фрагмент лигировали с фрагментом вектора, полученным путем расщепления вектора pAAVRC2 (производства CELL BIOLABS, Inc.) ферментами SnaBI и HindIII с помощью набора для лигирования ДНК <Mighty Mix> (производства TAKARA BIO Inc.), с получением хелперных плазмид pRC-GSGVTWV, pRC-AHGYREP, pRC-EYGFREG, pRC-ETGHGWV, pRC-GGGIGYV и pRC-ERGVGWV.
[0063] (2) Получение и очистка мутанта капсида AAV2-LacZ
С использованием PEIpro (производства Polyplus Transfection), Т-клетки 293, засеянные в колбу T225 см2, трансфецировали pAAV-LacZ (произведено TAKARA BIO Inc.), pHELP и хелперной плазмидой pRC (pRC-GSGVTWV, pRC-AHGYREP, pRC-EYGFREG, pRC-ETGHGWV, pRC-GGGIGYV или pRC-ERGVGWV), полученными как описано в Примере 5-(1). В качестве контроля осуществляли трансфекцию вектором pRC2, несущим капсид дикого типа, вместо хелперной плазмиды pRC, имеющей пептидную последовательность. Трансфецированные Т-клетки 293 культивировали при 37°C в течение 72 часов в CO2-инкубаторе. Супернатант, содержащий AAV, собирали из колбы T225 см2, а затем подвергали аффинной очистке с использованием сефарозы AVB (производства GE healthcare). Затем AAV концентрировали и очищали путем ультрафильтрации с получением очищенного раствора AAV. Затем титр векторов AAV количественно определяли методом, описанным в Примере 2-(4).
[0064] (3) Введение очищенного раствора AAV мышам
Очищенный раствор AAV, полученный как описано в Примере 5-(2), фильтровали с использованием 0,22 мкм-фильтра, а и затем вводили мышам в хвостовую вену при 0,5 × 1011 VG/мышь.
[0065] (4) Получение геномной ДНК из головного мозга и других тканей и количественное определение генома AAV
Мышей, которым вводили AAV как описано в Примере 5-(3), подвергали эвтаназии через 4 недели после введения и собирали каждую ткань. Геномную ДНК экстрагировали из каждой ткани с использованием ткани NucleoSpin (производства MACHEREY-NAGEL GmbH & Co. KG). Экстрагированную геномную ДНК в качестве образца подвергали ПЦР в реальном времени для определения количества генома вектора AAV, содержащегося в каждой ткани. На фигуре 2 указано количество молекул геномной ДНК AAV на 1 мкг общей геномной ДНК в каждой ткани.
[0066] Как видно на фигуре 2, векторы AAV, содержащие капсиды с пептидными последовательностями GSGVTWV, AHGYREP, EYGFREG, ETGHGWV, GGGIGYV и ERGVGWV, имели тенденцию переноситься в головной мозг. Кроме того, некоторые из векторов AAV обладали тропизмом как в отношении легких, так и в отношении головного мозга.
[0067] Промышленное применение
В соответствии с этим, настоящее изобретение относится к мутантам капсидного белка AAV, обладающим тропизмом по отношению к головному мозгу при системном введении, и к их аминокислотным последовательностям, и, таким образом, к способу эффективного введения гена в головной мозг.
Список последовательностей в свободном формате
[0068]
SEQ ID NO: 1: Кодирующая последовательность капсида AAV2 586-591
SEQ ID NO: 2: Конвертированная кодирующая последовательность капсида AAV2
SEQ ID NO: 3: Ген резистентности к ампициллину перед конверсией
SEQ ID NO: 4: ген резистентности к ампициллину после конверсии
SEQ ID NO: 5: Ген rep AAV2 до конверсии
SEQ ID NO: 6: Ген rep AAV2 после конверсии
SEQ ID NO: 7: Последовательность ДНК, кодирующая неспецифический пептид
SEQ ID NO: 8: Праймер для синтеза двухцепочечной ДНК
SEQ ID NO: 9: Прямой праймер для количественного определения титра AAV
SEQ ID NO: 10: Обратный праймер для количественного определения титра AAV
SEQ ID NO: 11: Прямой праймер 1 для амплификации области, кодирующей неспецифический пептид
SEQ ID NO: 12: Обратный праймер 1 для амплификации области, кодирующей неспецифический пептид
SEQ ID NO: 13: Прямой праймер 2 для амплификации области, кодирующей неспецифический пептид
SEQ ID NO: 14: Обратный праймер 2 для амплификации области, кодирующей неспецифический пептид
SEQ ID NO: 15: Пептидная последовательность GSGVTWV для мутанта капсидного белка AAV
SEQ ID NO: 16: Пептидная последовательность AHGYREP для мутанта капсидного белка AAV
SEQ ID NO: 17: Пептидная последовательность EYGFREG для мутанта капсидного белка AAV
SEQ ID NO: 18: Пептидная последовательность ETGHGWV для мутанта капсидного белка AAV
SEQ ID NO: 19: Пептидная последовательность GGGIGYV для мутанта капсидного белка AAV
SEQ ID NO: 20: Пептидная последовательность ERGVGWV для мутанта капсидного белка AAV
SEQ ID NO: 21: Пептидная последовательность ENGVGWV для мутанта капсидного белка AAV
SEQ ID NO: 22: Пептидная последовательность GSGVGWV для мутанта капсидного белка AAV
SEQ ID NO: 23: Пептидная последовательность ADGITWG для мутанта капсидного белка AAV
SEQ ID NO: 24: Пептидная последовательность ADGTRWV для мутанта капсидного белка AAV
SEQ ID NO: 25: Пептидная последовательность ADKVGWV для мутанта капсидногобелка AAV
SEQ ID NO: 26: Пептидная последовательность AGGVGWT для мутанта капсидного белка AAV
SEQ ID NO: 27: Пептидная последовательность AGGVTGV для мутанта капсидного белка AAV
SEQ ID NO: 28: Пептидная последовательность AGNAGGM для мутанта капсидного белка AAV
SEQ ID NO: 29: Пептидная последовательность AGQLGWV для мутанта капсидного протеина AAV
SEQ ID NO: 30: Пептидная последовательность ARGTEWE для мутанта капсидного белка AAV
SEQ ID NO: 31: Пептидная последовательность DAGHGFV для мутанта капсидного белка AAV
SEQ ID NO: 32: Пептидная последовательность EANVGWV для мутанта капсидного белка AAV
SEQ ID NO: 33: Пептидная последовательность ECGLGEG для мутанта капсидного белка AAV
SEQ ID NO: 34: Пептидная последовательность EGEVTWL для мутанта капсидного белка AAV
SEQ ID NO: 35: Пептидная последовательность EGGDGRV для мутанта капсидного белка AAV
SEQ ID NO: 36: Пептидная последовательность EGGFGEA для мутанта капсидного белка AAV
SEQ ID NO: 37: Пептидная последовательность EGGG для мутанта капсидного белка AAV
SEQ ID NO: 38: Пептидная последовательность EGGMVWV для мутанта капсидного белка AAV
SEQ ID NO: 39: Пептидная последовательность EGGVGWT для мутанта капсидного белка AAV
SEQ ID NO: 40: Пептидная последовательность EGGVMWL для мутанта капсидного белка AAV
SEQ ID NO: 41: Пептидная последовательность EGQVTWL для мутанта капсидного белка AAV
SEQ ID NO: 42: Пептидная последовательность ERGHGWG для мутанта капсидного белка AAV
SEQ ID NO: 43: Пептидная последовательность ESGVGWK для мутанта капсидного белка AAV
SEQ ID NO: 44: Пептидная оследовательность GDGFGGV для мутантного белка цапсид AAV
SEQ ID NO: 45: Пептидная последовательность GDGVTWA для мутанта капсидного белка AAV
SEQ ID NO: 46: Пептидная последовательность GEGRGWV для мутанта капсидного белка AAV
SEQ ID NO: 47: Пептидная последовательность GGGDGWI для мутанта капсидного белка AAV
SEQ ID NO: 48: Пептидная последовательность GGGDSWV для мутанта капсидного белка AAV
SEQ ID NO: 49: Пептидная последовательность GGGIAWVAQAAL для мутанта капсидного белка AAV
SEQ ID NO: 50: Пептидная последовательность GGGVGWA для мутанта капсидного белка AAV
SEQ ID NO: 51: Пептидная последовательность GKGQVME для мутанта капсидного белка AAV
SEQ ID NO: 52: Пептидная последовательность GNGTGGG для мутанта капсидного белка AAV
SEQ ID NO: 53: Пептидная последовательность GQGGHME для мутанта капсидного белка AAV
SEQ ID NO: 54: Пептидная последовательность GRGVTWV для мутанта капсидного белка AAV
SEQ ID NO: 55: Пептидная последовательность GSGMGWV для мутантного белка капсида AAV
SEQ ID NO: 56: Пептидная последовательность GVGGGVV для мутанта капсидного белка AAV
SEQ ID NO: 57: Пептидная последовательность NDVRGRV для мутанта капсидного белка AAV
SEQ ID NO: 58: Пептидная последовательность RDGLGFV для мутанта капсидного белка AAV
SEQ ID NO: 59: Пептидная последовательность TDGLGWV для мутанта капсидного белка AAV
SEQ ID NO: 60: Пептидная последовательность TEGHGWV для мутанта капсидного белка AAV
SEQ ID NO: 61: Пептидная последовательность VAERLYG для мутанта капсидного белка AAV
SEQ ID NO: 62: Пептидная последовательность VARGAGE для мутанта капсидного белка AAV
SEQ ID NO: 63: Пептидная последовательность GGSGVTWVA для мутанта капсидного белка AAV
SEQ ID NO: 64: Пептидная последовательность GAHGYREPA для мутанта капсидного белка AAV
SEQ ID NO: 65: Пептидная последовательность GEYGFREGA для мутанта капсидного белка AAV
SEQ ID NO: 66: Пептидная последовательность GETGHGWVA для мутанта капсидного белка AAV
SEQ ID NO: 67: Пептидная последовательность GGGGIGYVA для мутанта капсидного белка AAV
SEQ ID NO: 68: Пептидная последовательность GERGVGWVA для мутанта капсидного белка AAV
SEQ ID NO: 69: Пептидная последовательность GENGVGWVA для мутанта капсидного белка AAV
SEQ ID NO: 70: Пептидная последовательность GGSGVGWVA для мутанта капсидного белка AAV
SEQ ID NO: 71: Пептидная последовательность GADGITWGA для мутанта капсидного белка AAV
SEQ ID NO: 72: Пептидная последовательность GADGTRWVA для мутанта капсидного белка AAV
SEQ ID NO: 73: Пептидная последовательность GADKVGWVA для мутанта капсидного белка AAV
SEQ ID NO: 74: Пептидная последовательность GAGGVGWTA для мутанта капсидного белка AAV
SEQ ID NO: 75: Пептидная последовательность GAGGVTGVA для мутанта капсидного белка AAV
SEQ ID NO: 76: Пептидная последовательность GAGNAGGMA для мутанта капсидного белка AAV
SEQ ID NO: 77: Пептидная последовательность GAGQLGWVA для мутанта капсидного белка AAV
SEQ ID NO: 78: Пептидная последовательность GARGTEWEA для мутанта капсидного белка AAV
SEQ ID NO: 79: Пептидная последовательность GDAGHGFVA для мутанта капсидного белка AAV
SEQ ID NO: 80: Пептидная последовательность GEANVGWVA для мутанта капсидного белка AAV
SEQ ID NO: 81: Пептидная последовательность GECGLGEGA для мутанта капсидного белка AAV
SEQ ID NO: 82: Пептидная последовательность GEGEVTWLA для мутанта капсидного белка AAV
SEQ ID NO: 83: Пептидная последовательность GEGGDGRVA для мутанта капсидного белка AAV
SEQ ID NO: 84: Пептидная последовательность GEGGFGEAA для мутантного AV капсидного белка
SEQ ID NO: 85: Пептидная последовательность GEGGGA для мутанта капсидного белка AAV
SEQ ID NO: 86: Пептидная последовательность GEGGMVWVA для мутанта капсидного белка AAV
SEQ ID NO: 87: Пептидная последовательность GEGGVGWTA для мутанта капсидного белка AAV
SEQ ID NO: 88: Пептидная последовательность GEGGVMWLA для мутанта капсидного белка AAV
SEQ ID NO: 89: Пептидная последовательность GEGQVTWLA для мутанта капсидного белка AAV
SEQ ID NO: 90: Пептидная последовательность GERGHGWGA для мутанта капсидного белка AAV
SEQ ID NO: 91: Пептидная последовательность GESGVGWKA для мутанта капсидного белка AAV
SEQ ID NO: 92: Пептидная последовательность GGDGFGGVA для мутанта капсидного белка AAV
SEQ ID NO: 93: Пептидная последовательность GGDGVTWAA для мутанта капсидного белка AAV
SEQ ID NO: 94: Пептидная последовательность GGEGRGWVA для мутанта капсидного белка AAV
SEQ ID NO: 95: Пептидная последовательность GGGGDGWIA для мутанта капсидного белка AAV
SEQ ID NO: 96: Пептидная последовательность GGGGDSWVA для мутанта капсидного белка AAV
SEQ ID NO: 97: Пептидная последовательность GGGGIAWVAQAALA для мутанта капсидного белка AAV
SEQ ID NO: 98: Пептидная последовательность GGGGVGWAA для мутанта капсидного белка AAV
SEQ ID NO: 99: Пептидная последовательность GGKGQVMEA для мутанта капсидного белка AAV
SEQ ID NO: 100: Пептидная последовательность GGNGTGGGA для мутанта капсидного белка AAV
SEQ ID NO: 101: Пептидная последовательность GGQGGHMEA для мутанта капсидного белка AAV
SEQ ID NO: 102: Пептидная последовательность GGRGVTWVA для мутанта капсидного белка AAV
SEQ ID NO: 103: Пептидная последовательность GGSGMGWVA для мутанта капсидного белка AAV
SEQ ID NO: 104: Пептидная последовательность GGVGGGVVA для мутанта капсидного белка AAV
SEQ ID NO: 105: Пептидная последовательность GNDVRGRVA для мутанта капсидного белка AAV
SEQ ID NO: 106: Пептидная последовательность GRDGLGFVA для мутанта капсидного белка AAV
SEQ ID NO: 107: Пептидная последовательность GTDGLGWVA для мутанта капсидного белка AAV
SEQ ID NO: 108: Пептидная последовательность GTEGHGWVA для мутанта капсидного белка AAV
SEQ ID NO: 109: Пептидная последовательность GVAERLYGA для мутантного белка CAPSID AAV
SEQ ID NO: 110: Пептидная последовательность GVARGAGEA для мутанта капсидного белка AAV
SEQ ID NO: 111: Пептидная последовательность, представленная формулой I
SEQ ID NO: 112: Пептидная последовательность, представленная формулой II
SEQ ID NO: 113: Пептидная последовательность, представленная формулой III
SEQ ID NO: 114: Пептидная последовательность, представленная формулой IV
SEQ ID NO: 115: Пептидная последовательность, представленная формулой V
SEQ ID NO: 116: Пептидная последовательность, представленная формулой VI.

Изобретение относится к биотехнологии. Описана нуклеиновая кислота, кодирующая мутант капсидного белка аденоассоциированного вируса (AAV), который включает пептид, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 18, 15-17 и 19-62. Также описана рекомбинантная ДНК для получения AAV частицы, обладающей тропизмом в отношении головного мозга, содержащая указанную нуклеиновую кислоту. Представлена клетка для получения AAV частицы, обладающей тропизмом в отношении головного мозга, содержащая указанную нуклеиновую кислоту или рекомбинантную ДНК. Также представлена частица AAV для введения гена в мозг, содержащая мутант капсидного белка AAV, который включает пептид, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 18, 15-17 и 19-62. Раскрыт способ получения клетки, трансдуцированной геном, где указанный способ включает стадию контактирования частицы AAV, содержащей мутант капсидного белка AAV, который включает пептид, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 18, 15-17 и 19-62, с клеткой. Представлен способ получения частицы AAV, где способ включает выделение или очистку частицы AAV из супернатанта культуры или лизата клетки. 6 н. и 6 з.п. ф-лы, 2 ил., 2 табл., 5 пр.
1. Нуклеиновая кислота, кодирующая мутант капсидного белка аденоассоциированного вируса (AAV), который включает пептид, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 18, 15-17 и 19-62.
2. Нуклеиновая кислота по п. 1, где капсидный белок AAV происходит от AAV2.
3. Нуклеиновая кислота по п. 2, где пептид находится в положении между аминокислотой 588 и аминокислотой 589 в VP1 AAV2.
4. Рекомбинантная ДНК для получения AAV частицы, обладающей тропизмом в отношении головного мозга, содержащая нуклеиновую кислоту по любому из пп. 1-3.
5. Клетка для получения AAV частицы, обладающей тропизмом в отношении головного мозга, содержащая нуклеиновую кислоту по любому из пп. 1-3 или рекомбинантную ДНК по п. 4.
6. Частица AAV для введения гена в мозг, содержащая мутант капсидного белка AAV, который включает пептид, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 18, 15-17 и 19-62.
7. Частица AAV по п. 6, где капсидный белок AAV происходит от AAV2.
8. Частица AAV по п. 7, где пептид находится в положении между аминокислотой 588 и аминокислотой 589 в VP1 AAV2.
9. Способ получения клетки, трансдуцированной геном, где указанный способ включает стадию контактирования частицы AAV, содержащей мутант капсидного белка AAV, который включает пептид, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 18, 15-17 и 19-62, с клеткой.
10. Способ по п. 9, где капсидный белок AAV происходит от AAV2.
11. Способ по п. 10, где пептид находится в положении между аминокислотой 588 и аминокислотой 589 в VP1 AAV2.
| JP 2017513486 A, 01.06.2017 | |||
| WO 2014103957 A1, 03.07.2014 | |||
| WO 2020114143 A1, 11.06.2020 | |||
| WO 2013014764 A1, 31.01.2013 | |||
| ВИРИОНЫ АДЕНОАССОЦИИРОВАННОГО ВИРУСА С ВАРИАНТНЫМ КАПСИДОМ И СПОСОБЫ ИХ ИСПОЛЬЗОВАНИЯ | 2012 |
|
RU2611202C2 |
| RU 2016104614 A, 18.08.2017 | |||
| RU 2016133623 A, 22.03.2018. | |||
Авторы
Даты
2023-12-11—Публикация
2020-04-23—Подача