Изобретение относится к электрохимическому способу получения карбида молибдена, обладающего каталитическими свойствами и имеющего нано- и субмикронную размерность частиц.
Известны способы высокотемпературного электрохимического синтеза высокодисперсных (нано-, субмикро-, микродисперсных) порошков карбида молибдена и вольфрама в хлоридно-оксидных расплавов под избыточным давлением диоксида углерода (в качестве источника углерода) и в оксидных (вольфраматно-молибдатных-карбонатных) расплавах:
Малышев В.В., Кушхов Х.Б., Успехи высокотемпературного электрохимического синтеза в ионных расплавах//Журнал общей химии. 2004. т 74, Вып.8, С-1233-1240
Шаповал В.И., Малышев В.В., Новоселова И.А., Кушхов Х.Б. Современные проблемы высокотемпературного электрохимического синтеза соединений переходных металлов IV-IV групп. //Успехи химии.1995, Т.64, Вып.2, с.133-140.
Malyshev V.V., Kushkhov Kh.B, Shapoval V.J., High-temperature electrochemical synthesis of carbides, silicides and borides of IV-group metals in ionic melts//Jornal of Applied Electrochemistry.2002, p.573-279.
Способ получения нанодисперсных порошков двойных карбидов вольфрама и молибдена//2459015.2012г.
Электрохимический способ получения карбида молибдена//2752624.2021г.
Недостатки способов. Вследствие низкой растворимости СО2 в хлоридно-оксидных, хлоридно-фторидно-оксидных расплавах данные способы позволяют реализовать сравнительно низкие плотности тока (оптимальное значение 0,1 А/см2). Вольфраматно-молибдатно-карбонатные расплавы (вольфрамат натрия служит растворителем) позволяет реализовать скорости процесса более чем на порядок выше (до 3,0 А/см2) Однако эти рабочие расплавленные электролиты (Nа2WO4 - Li2MoO4-Li2CO3) содержат значительное количество дорогостоящих соединений вольфрама и лития, как расплавленной среды, на фоне которых происходит совместное электровыделение молибдена и углерода на катоде и последующем взаимодействии на атомарном уровне с образованием высокодисперсных порошков карбида молибдена.
Задача предлагаемого технического решения заключается в упрощении и удешевлении процесса электрохимического синтеза высокодисперсных порошков карбида молибдена.
Сущность предлагаемого способа заключается в реализации совместного электровыделения молибдена и углерода в расплавленной системе KCl-K2CO3-Li2МоO4 и последующего взаимодействия на атомарном уровне на катоде с образованием нано-, субмикро- и микродисперсных порошков карбида вольфрама.
Предлагается электрохимический способ получения карбида молибдена с использованием молибдата лития, карбоната калия в качестве источника углерода и хлорида калия. Электролиз ведут в расплаве электролита при следующем соотношении компонентов, мол. %: KCl 82,0-86,0, К2СО3 4,0-6,0, Li2MoO4 10,0-12,0, при температуре в интервале 1123-1173 К и плотности тока 0,5-2,0 А/см2.
Возможность электрохимического синтеза порошков карбида молибдена электролизом расплавленной системы KCl-K2CO3-Li2МоO4 демонстрируют следующие примеры.
Пример 1.
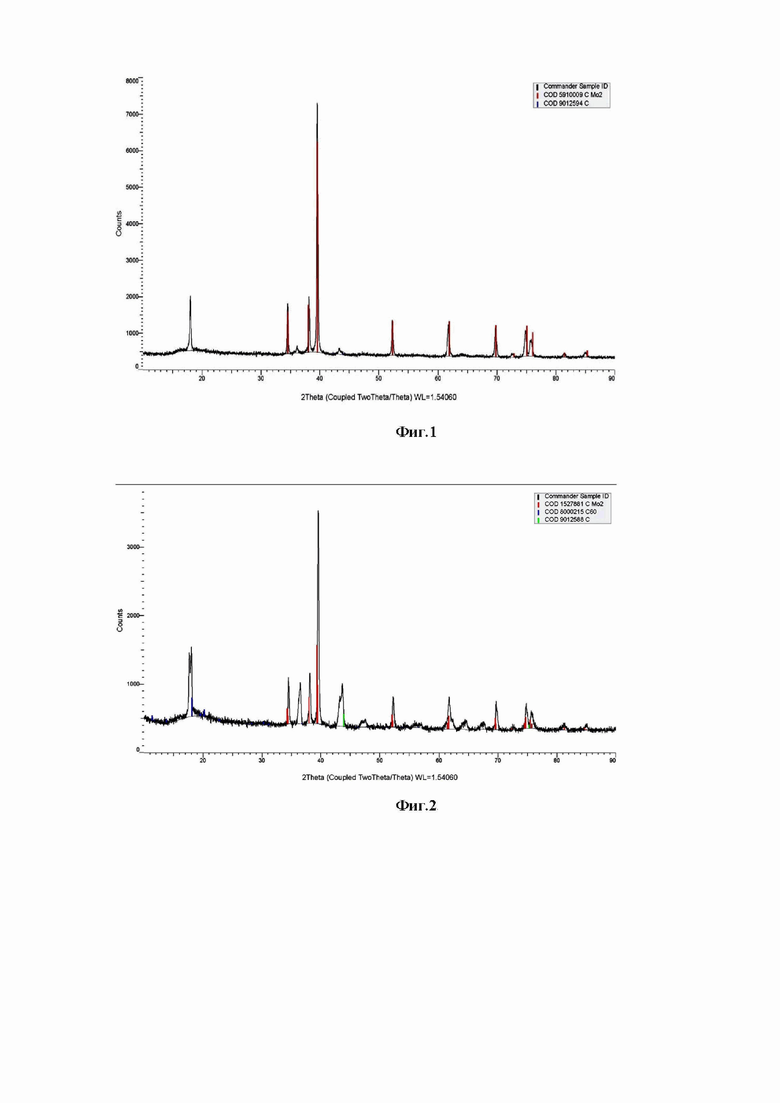
Процесс электролиза осуществлялся в расплавленной системе KCl-K2CO3-Li2MoO4, где концентрация компонентов составляла KCl (86,0 мол%), K2CO3 (4,0 мол%), Li2MoO4 (10,0 мол%). В качестве катода использовался никелевый стержень диаметром 3,0 мм площадью 2,0 см2, а анодом и одновременно контейнером для расплава являлся графитовый тигель марки МПГ-7. Плотность катодного тока 1,0 А/см2. Температура Т=1173 К. Продолжительность электролиза 30 мин. Целевой продукт карбида молибдена осаждается на никелевом электроде в виде карбидно-солевой «груши», который выщелачивали от электролита в кипящей дистиллированной воде многократной декантацией. Из-за высокой дисперсности порошок карбида молибдена отделяли от раствора центрифугированием и высушивали в сушильном шкафу при температуре 423К, затем взвешивали.
На фиг. 1 представлена рентгеновская дифрактограмма порошка карбида молибдена, полученного электролизом расплава KCl (86,0 мол %)- К2СО3 (4,0 мол %)- Li2МоO4 (10,0 мол %). Температура Т=1173 К. Плотность тока 1,0 А/см2.
Пример 2.
Процесс осуществлялся по примеру 1 в расплавленной системе KCl-K2CO3-Li2МоO4, где концентрация компонентов составляла KCl (86,0 мол%), K2CO3 (4,0 мол%), Li2МоO4 (10,0 мол%). В качестве катода использовался никелевый стержень диаметром 3,0 мм площадью 2,0 см2, а анодом и одновременно контейнером для расплава являлся графитовый тигель марки МПГ-7. Плотность катодного тока 0,5 А/см2. Температура Т=1173 К. Продолжительность электролиза 30 мин.
На фиг. 2 представлена рентгеновская дифрактограмма порошка карбида молибдена, полученного электролизом расплава KCl (86,0 мол %)- К2СО3 (4,0 мол %)- Li2МоO4 (10,0 мол %). Температура Т=1173 К. Плотность тока 0,5 А/см2.
Пример 3.
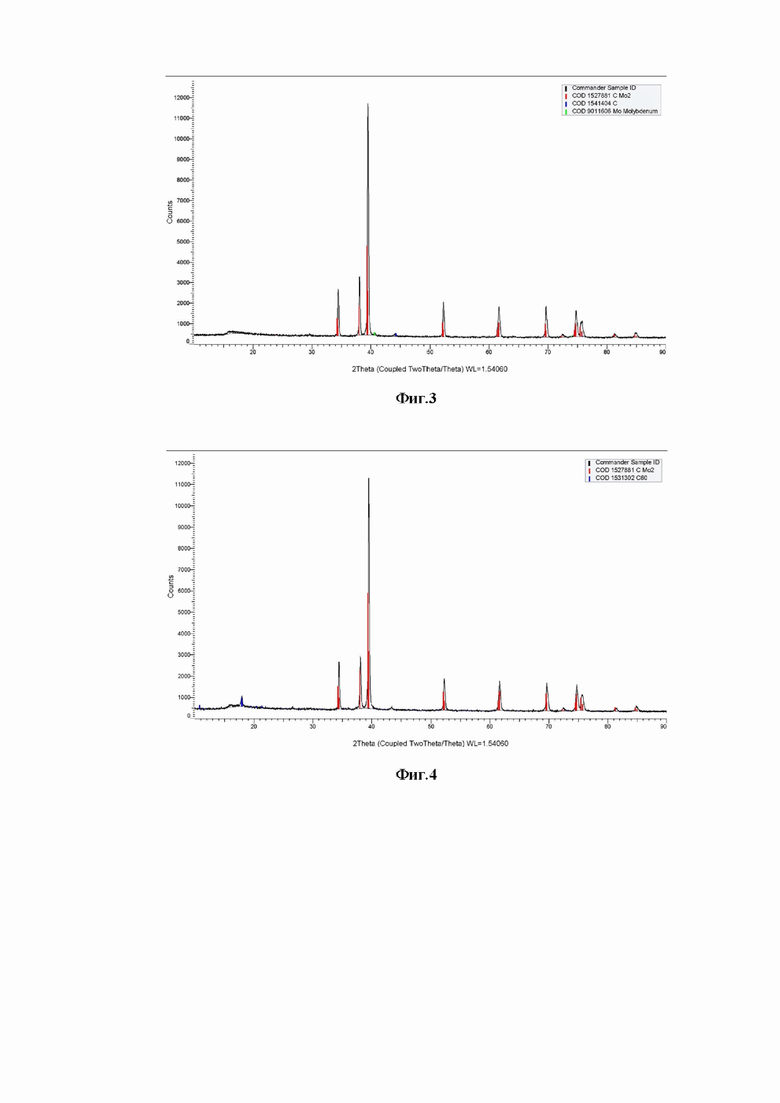
Процесс осуществлялся по примеру 1 в расплавленной системе KCl-K2CO3-Li2МоO4, где концентрация компонентов составляла KCl (84,0 мол%), K2CO3 (4,0 мол%), Li2МоO4 (12,0 мол%). В качестве катода использовался никелевый стержень диаметром 3,0 мм площадью 2,0 см2, а анодом и одновременно контейнером для расплава являлся графитовый тигель марки МПГ-7. Плотность катодного тока 1,0 А/см2. Температура Т=1173 К. Продолжительность электролиза 30 мин.
На фиг. 3 представлена рентгеновская дифрактограмма порошка карбида молибдена, полученного электролизом расплава KCl (84,0 мол %)- К2СО3 (4,0 мол %)- Li2МоO4 (12,0 мол %). Температура Т=1173 К. Плотность тока 1,0 А/см2.
Пример 4.
Процесс осуществлялся по примеру 1 в расплавленной системе KCl-K2CO3-Li2МоO4, где концентрация компонентов составляла KCl (84,0 мол%), K2CO3 (6,0 мол%), Li2МоO4 (10,0 мол%). В качестве катода использовался никелевый стержень диаметром 3,0 мм площадью 2,0 см2, а анодом и одновременно контейнером для расплава являлся графитовый тигель марки МПГ-7. Плотность катодного тока 2,0 А/см2. Температура Т=1173 К. Продолжительность электролиза 30 мин.
На фиг. 4 представлена рентгеновская дифрактограмма порошка карбида молибдена, полученного электролизом расплава KCl (84,0 мол %)- К2СО3 (6,0 мол %)- Li2МоO4 (10,0 мол %). Температура Т=1173 К. Плотность тока 2,0 А/см2.
Пример 5.
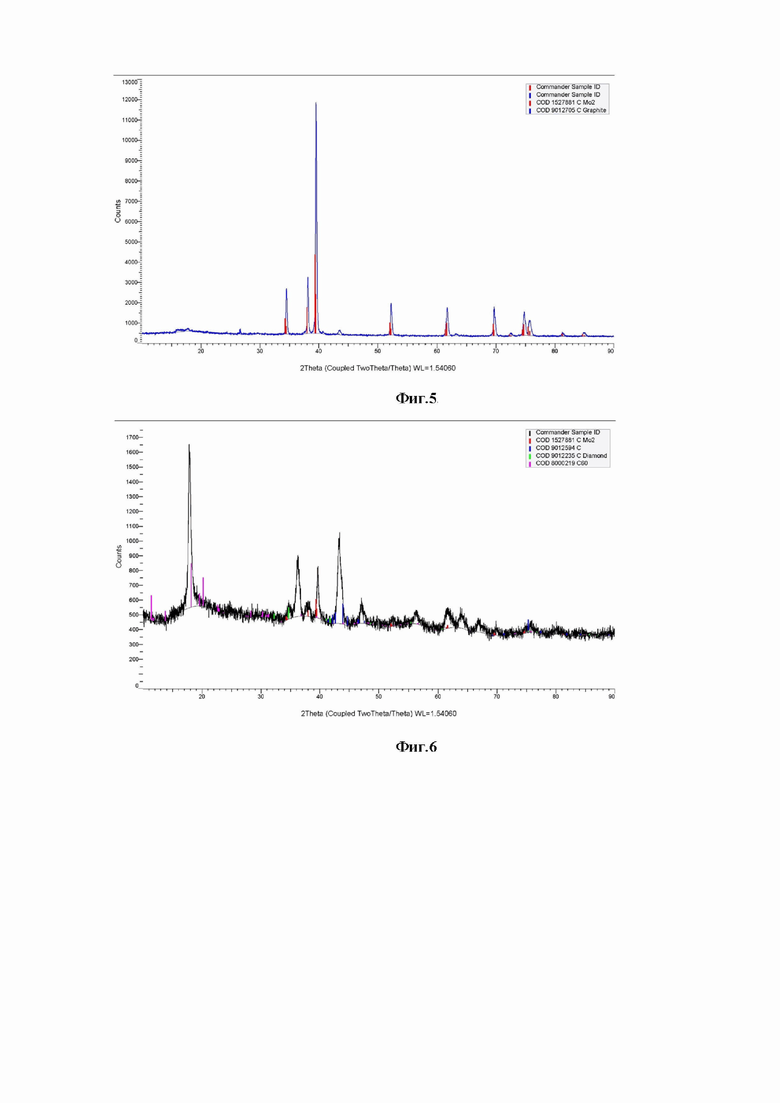
Процесс осуществлялся по примеру 1 в расплавленной системе KCl-K2CO3-Li2МоO4, где концентрация компонентов составляла KCl (86,0 мол%), K2CO3 (4,0 мол%), Li2МоO4 (10,0 мол%). В качестве катода использовался никелевый стержень диаметром 3,0 мм площадью 2,0 см2, а анодом и одновременно контейнером для расплава являлся графитовый тигель марки МПГ-7. Плотность катодного тока 1,0 А/см2. Температура Т=1123 К. Продолжительность электролиза 120 мин.
На фиг. 5 представлена рентгеновская дифрактограмма порошка карбида молибдена, полученного электролизом расплава KCl (86,0 мол %)- К2СО3 (4,0 мол %)- Li2МоO4 (10,0 мол %). Температура Т=1123 К. Плотность тока 1,0 А/см2.
Пример 6.
Процесс осуществлялся по примеру 1 в расплавленной системе KCl-K2CO3-Li2МоO4, где концентрация компонентов составляла KCl (86,0 мол%), K2CO3 (4,0 мол%), Li2МоO4 (10,0 мол%). В качестве катода использовался никелевый стержень диаметром 3,0 мм площадью 2,0 см2, а анодом и одновременно контейнером для расплава являлся графитовый тигель марки МПГ-7. Плотность катодного тока 0,5 А/см2. Температура Т=1073 К. Продолжительность электролиза 30 мин.
На фиг. 6 представлена рентгеновская дифрактограмма порошка карбида молибдена, полученного электролизом расплава KCl (86,0 мол %)- К2СО3 (4,0 мол %)- Li2МоO4 (10,0 мол %). Температура Т=1073 К. Плотность тока 0,5 А/см2.
Следует отметить, что при температурах ниже Т=1123 К содержание фазы свободного углерода в катодных осадках увеличивается.
Пример 7.
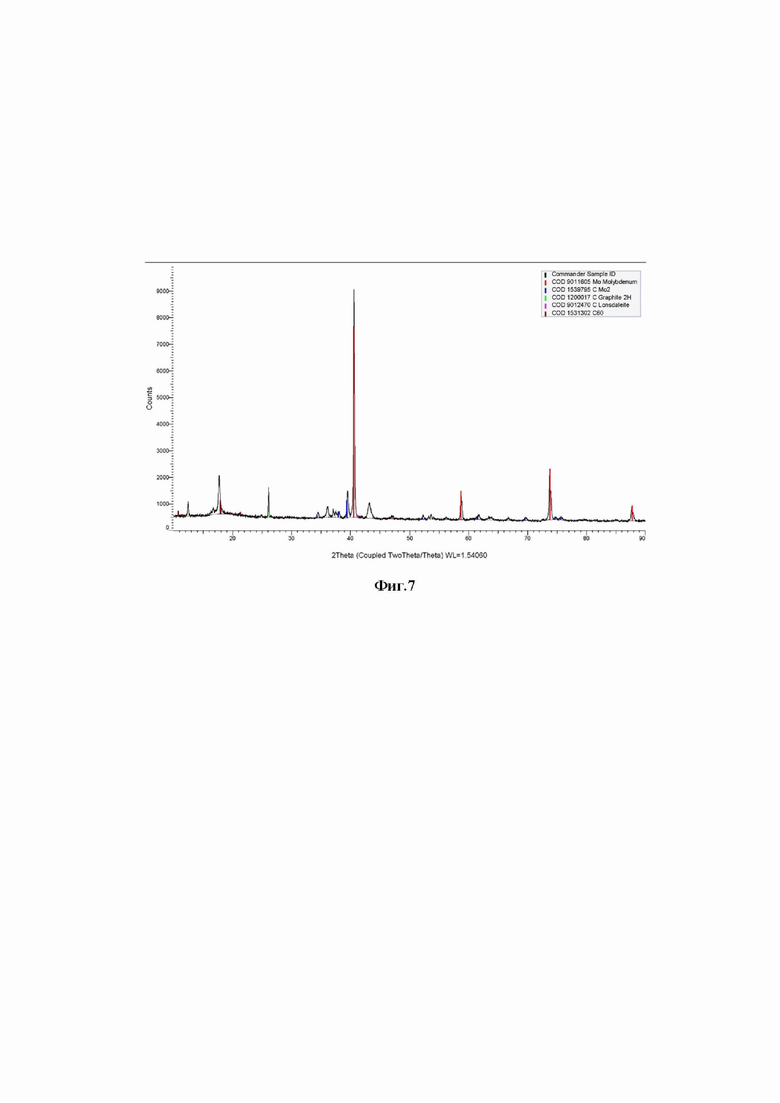
Процесс осуществлялся по примеру 1 в расплавленной системе KCl-K2CO3-Li2МоO4, где концентрация компонентов составляла KCl (82,0 мол%), K2CO3 (4,0 мол%), Li2МоO4 (14,0 мол%). В качестве катода использовался никелевый стержень диаметром 3,0 мм площадью 2,0 см2, а анодом и одновременно контейнером для расплава являлся графитовый тигель марки МПГ-7. Плотность катодного тока 1,0 А/см2. Температура Т=1173 К. Продолжительность электролиза 30 мин.
На фиг. 7 представлена рентгеновская дифрактограмма порошка карбида молибдена, полученного электролизом расплава KCl (82,0 мол %)- К2СО3 (4,0 мол %)- Li2МоO4 (14,0 мол %). Температура Т=1173 К. Плотность тока 1,0 А/см2.
При повышении концентрации молибдата лития больше 12 мол % в расплавленной системе KCl -К2СО3- Li2МоO4, наряду с фазой карбида молибдена получается фаза металлического молибдена, причем значительно превосходящее по содержанию фазу карбида молибдена.
Технический результат - реализован процесс электрохимического синтеза высокодисперсных порошков карбида молибдена в расплавленной системе KCl-K2CO3-Li2МоO4 при различных условиях.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения порошка карбида вольфрама | 2023 |
|
RU2811043C1 |
| Электрохимический способ получения карбида молибдена | 2020 |
|
RU2752624C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОДИСПЕРСНЫХ ПОРОШКОВ ДВОЙНЫХ КАРБИДОВ ВОЛЬФРАМА И МОЛИБДЕНА | 2010 |
|
RU2459015C2 |
| ЭЛЕКТРОЛИТ ДЛЯ НАНЕСЕНИЯ ПОКРЫТИЙ НА ЭЛЕКТРОПРОВОДЯЩИЕ И НЕЭЛЕКТРОПРОВОДЯЩИЕ МАТЕРИАЛЫ | 2010 |
|
RU2458189C1 |
| Электрохимический способ получения наноразмерных порошков интерметаллидов гольмия и никеля в галогенидных расплавах | 2015 |
|
RU2621508C2 |
| Способ получения порошка карбида вольфрама | 2016 |
|
RU2661298C2 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОДИСПЕРСНОГО ПОРОШКА КАРБИДА ВОЛЬФРАМА | 2008 |
|
RU2372421C1 |
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ НАНОРАЗМЕРНОГО ПОРОШКА ГЕКСАБОРИДА ЦЕРИЯ | 2013 |
|
RU2540277C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОДИСПЕРСНЫХ ТВЕРДОСПЛАВНЫХ КОМПОЗИЦИЙ НА ОСНОВЕ ДВОЙНОГО КАРБИДА ВОЛЬФРАМА И КОБАЛЬТА | 2008 |
|
RU2372420C1 |
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ ГЕКСАБОРИДА ПРАЗЕОДИМА | 2008 |
|
RU2393115C2 |
Изобретение может быть использовано при получении карбида молибдена, обладающего каталитическими свойствами. Предложен электрохимический способ получения карбида молибдена с использованием молибдата лития и карбоната калия в качестве источника углерода. Электролиз ведут в расплаве электролита, содержащего хлорид калия, при следующем соотношении компонентов, мол.%: KCl 82,0-86,0, К2СО3 4,0-6,0, Li2MoO4 10,0-12,0, при температуре в интервале 1123-1173 K и плотности тока 0,5-2,0 А/см2. Изобретение позволяет упростить получение высокодисперсных порошков карбида молибдена. 7 ил., 7 пр.
Электрохимический способ получения карбида молибдена с использованием молибдата лития и карбоната калия в качестве источника углерода, отличающийся тем, что электролиз ведут в расплаве электролита, содержащего хлорид калия, при следующем соотношении компонентов, мол.%:
при температуре в интервале 1123-1173 K и плотности тока 0,5-2,0 А/см2.
| Электрохимический способ получения карбида молибдена | 2020 |
|
RU2752624C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОКРИСТАЛЛИЧЕСКОГО КУБИЧЕСКОГО КАРБИДА МОЛИБДЕНА | 2020 |
|
RU2748929C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОЧАСТИЦ КАРБИДА МОЛИБДЕНА | 2011 |
|
RU2489351C2 |
| US 3330646 A1, 11.07.1967 | |||
| MALYSHEV V | |||
| V., Theoretical Foundations and Implementation of the High-Temperature Electrosynthesis of Molybdenum Carbide in Ionic Melts, Theoretical Foundations of Chemical Engineering, 2002, v | |||
| Коридорная многокамерная вагонеточная углевыжигательная печь | 1921 |
|
SU36A1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ЧЕРТЕЖЕЙ ДЛЯ ОДНООБРАЗНОЙ РАСКРОЙКИ ПРЕДМЕТОВ ОДЕЖДЫ | 1919 |
|
SU287A1 |
Авторы
Даты
2024-01-10—Публикация
2023-05-23—Подача