РОДСТВЕННАЯ ЗАЯВКА
Настоящая заявка испрашивает приоритет на основании заявки на патент США с порядковым номером 62/574188, поданной 18 октября 2017 года, содержание которой включено в данный документ посредством ссылки во всей своей полноте.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Настоящая заявка содержит перечень последовательностей, который был подан в электронном виде в формате ASCII и настоящим включен посредством ссылки во всей своей полноте. Указанная ASCII-копия, созданная 17 октября 2018 года, имеет название N2067-7136WO_SL.txt, и ее размер составляет 2052554 байт.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Множество терапевтических белков были разработаны в качестве важных препаратов для предупреждения или лечения заболеваний. Во время или после лечения могут наблюдаться побочные эффекты, варьирующиеся от утраты эффективности лекарственного средства до опасных токсических явлений. Требуется разработка стратегий, осуществляющих модуляцию уровня экспрессии терапевтических белков, например, модуляцию уровней терапевтических белков для увеличения эффективности и/или уменьшения побочных эффектов.
КРАТКОЕ ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
В настоящем изобретении, по крайней мере помимо прочего, представлен слитый полипептид, содержащий полипептид, связывающий соединение формулы (I) (COF1)/CRBN, полипептид, связывающий соединение формулы (II) (COF2)/CRBN, или полипептид, связывающий соединение формулы (III) (COF3)/CRBN, предназначенный для нацеливаемой инактивации белков. В некоторых вариантах осуществления слитый полипептид содержит один или несколько COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающих полипептидов и один или несколько гетерологичных полипептидов, например, представляющих интерес полипептидов. COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид может быть функционально связан с гетерологичным полипептидом, например, через линкер. В некоторых вариантах осуществления в присутствии COF1 или COF2 (такого как талидомид и его производные (например, леналидомид, помалидомид и талидомид)) или в присутствии COF3 (например, соединения, раскрытого в таблице 29) COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид изменяет уровень и/или активность слитого полипептида; например, увеличивает деградацию, например, протеасомную деградацию, слитого полипептида. В некоторых вариантах осуществления деградация слитого полипептида является убиквитин-зависимой.
Без ограничения какой-либо теорией, в некоторых вариантах осуществления в COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающем полипептиде предусмотрены аминокислотная последовательность и/или структурный мотив, которые в присутствии COF1 или COF2 (такого как талидомид и его производные (например, леналидомид, помалидомид и талидомид)) или в присутствии COF3 (например, соединения, раскрытого в таблице 29) приводят к посттрансляционной модификации (например, убиквитинированию) слитого полипептида, что приводит к модифицированному, например, убиквитинированному, слитому полипептиду. Например, одна или несколько аминокислот, например, лизин или метионин, в слитом полипептиде могут подвергаться убиквитинированию в присутствии COF1, COF2 или COF3. В некоторых вариантах осуществления убиквитинированный слитый полипептид подвергается селективной деградации. В некоторых вариантах осуществления посттрансляционная модификация слитого полипептида увеличивает деградацию (например, увеличивает уровень и/или скорость деградации) слитого полипептида. В некоторых вариантах осуществления уровень и/или скорость деградации увеличиваются в по меньшей мере 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз относительно уровня и/или скорости деградации эталонного полипептида, например, слитого полипептида в отсутствие COF1, COF2 или COF3, гетерологичного полипептида или слияния гетерологичного полипептида без COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающего полипептида или с фрагментом, отличным от COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающего полипептида.
В одном аспекте данного документа представлен слитый полипептид, содержащий полипептид, связывающий соединение формулы (I) (COF1)/CRBN, и гетерологичный полипептид, где соединение формулы (I) представляет собой:

или его фармацевтически приемлемую соль, сложный эфир, гидрат, сольват или таутомер, где:
X представляет собой O или S;
R1 представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, карбоциклил, гетероциклил, арил или гетероарил, каждый из которых независимо и необязательно замещен одним или несколькими R4;
каждый из R2a и R2b независимо представляет собой водород или C1-C6алкил; или R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу или тиокарбонильную группу;
каждый из R3 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD) или -N(RC)S(O)xRE, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или несколькими R6;
каждый R4 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, оксо, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD), -N (RC)S(O)xRE, карбоциклил, гетероциклил, арил или гетероарил, где каждый алкил, алкенил, алкинил, гетероалкил, карбоциклил, гетероциклил, арил и гетероарил независимо и необязательно замещен одним или несколькими R7;
каждый из RA, RB, RC, RD и RE независимо представляет собой водород или C1-C6алкил;
каждый R6 независимо представляет собой C1-C6алкил, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, арил или гетероарил, где каждый арил и гетероарил независимо и необязательно замещен одним или несколькими R8;
каждый R7 независимо представляет собой галоген, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
каждый R8 независимо представляет собой C1-C6алкил, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
n составляет 0, 1, 2, 3 или 4; и
x составляет 0, 1 или 2.
В некоторых вариантах осуществления гетерологичный полипептид представляет собой гетерологичный полипептид млекопитающего. В некоторых вариантах осуществления гетерологичный полипептид представляет собой гетерологичный бактериальный полипептид. В некоторых вариантах осуществления гетерологичный полипептид представляет собой гетерологичный вирусный полипептид. В некоторых вариантах осуществления гетерологичный полипептид содержит аминокислотную последовательность или получен из полипептида млекопитающего, бактериального полипептида, вирусного полипептида, полипептида растения, полипептида дрожжей, полипептида гриба, полипептида археи, полипептида рыбы, например, данио-рерио. В некоторых вариантах осуществления гетерологичный полипептид содержит полипептид из таблицы 2, например, цитоплазматический и/или ядерный полипептид или трансмембранный полипептид, описанные в таблице 2.
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид слит с гетерологичным полипептидом. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид и гетерологичный полипептид связаны с помощью пептидной связи. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид и гетерологичный полипептид связаны с помощью связи, отличной от пептидной связи. В некоторых вариантах осуществления гетерологичный полипептид связан непосредственно с COF1/CRBN-связывающим полипептидом. В некоторых вариантах осуществления гетерологичный полипептид связан опосредованно с COF1/CRBN-связывающим полипептидом. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид и гетерологичный полипептид функционально связаны через линкер, например, глицин-сериновый линкер, например, линкер, содержащий аминокислотную последовательность под SEQ ID NO: 28. В некоторых вариантах осуществления линкер содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 28, 37, 38, 39 и 99.
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид связан с C-концом гетерологичного полипептида. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид связан с N-концом гетерологичного полипептида. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид находится посередине гетерологичного полипептида.
В некоторых вариантах осуществления ассоциация COF1/CRBN-связывающего полипептида с цереблоном (CRBN) в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации COF1/CRBN-связывающего полипептида с CRBN в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид не связывается с CRBN в отсутствие COF1. В некоторых вариантах осуществления ассоциация слитого полипептида с CRBN в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации слитого полипептида с CRBN в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации. В некоторых вариантах осуществления слитый полипептид не связывается с CRBN в отсутствие COF1. В некоторых вариантах осуществления ассоциация или связывание измеряются в клетке млекопитающего, например, клетке человека.
В некоторых вариантах осуществления убиквитинирование гетерологичного полипептида в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования гетерологичного полипептида в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе. В некоторых вариантах осуществления убиквитинирование слитого полипептида в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования слитого полипептида в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе. В некоторых вариантах осуществления гетерологичный полипептид или слитый полипептид подвергается убиквитинированию по одному или нескольким остаткам лизина или метионина в присутствии COF1. В некоторых вариантах осуществления убиквитинирование измеряется в клетке млекопитающего, например, клетке человека.
В некоторых вариантах осуществления деградация слитого полипептида в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от деградации слитого полипептида в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии. В некоторых вариантах осуществления деградация слитого полипептида опосредуется убиквитинированием в присутствии COF1. В некоторых вариантах осуществления деградация слитого полипептида опосредуется лизосомой. В некоторых вариантах осуществления деградация измеряется в клетке млекопитающего, например, клетке человека.
В некоторых вариантах осуществления слитый полипептид представляет собой полипептид клеточной поверхности. В некоторых вариантах осуществления скорость рециклирования слитого полипептида с клеточной поверхности во внутриклеточный компартмент в отсутствие COF1 составляет, например, не более 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, или 90% от рециклирования слитого полипептида с клеточной поверхности во внутриклеточный компартмент в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе. В некоторых вариантах осуществления рециклирование измеряется в клетке млекопитающего, например, клетке человека.
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид составляет от 10 до 95 аминокислотных остатков в длину, от 15 до 90 аминокислотных остатков в длину, от 20 до 85 аминокислотных остатков в длину, от 25 до 80 аминокислотных остатков в длину, от 30 до 75 аминокислотных остатков в длину, от 35 до 70 аминокислотных остатков в длину, от 40 до 65 аминокислотных остатков в длину, от 45 до 65 аминокислотных остатков в длину, от 50 до 65 аминокислотных остатков в длину или от 55 до 65 аминокислотных остатков в длину.
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит бета-изгиб. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит бета-изгиб из IKZF1 или IKZF3 (например, IKZF1 или IKZF3 человека). В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит бета-шпильку. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит бета-шпильку из IKZF1 или IKZF3 (например, IKZF1 или IKZF3 человека). В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит бета-нить. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит бета-нить из IKZF1 или IKZF3 (например, IKZF1 или IKZF3 человека). В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит альфа-спираль. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит альфа-спираль из IKZF1 или IKZF3 (например, IKZF1 или IKZF3 человека). В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит в направлении от N-конца к C-концу: первую бета-нить, бета-шпильку, вторую бета-нить и первую альфа-спираль. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит в направлении от N-конца к C-концу: первую бета-нить, бета-шпильку, вторую бета-нить и первую альфа-спираль из IKZF1 или IKZF3 (например, IKZF1 или IKZF3 человека). В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит в направлении от N-конца к C-концу: первую бета-нить, бета-шпильку, вторую бета-нить, первую альфа-спираль и вторую альфа-спираль. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит в направлении от N-конца к C-концу: первую бета-нить, бета-шпильку, вторую бета-нить, первую альфа-спираль и вторую альфа-спираль из IKZF1 или IKZF3 (например, IKZF1 или IKZF3 человека). В некоторых вариантах осуществления бета-шпилька и вторая альфа-спираль разделены не более чем 60, 50, 40 или 30 аминокислотными остатками.
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит COF1/CRBN-связывающую последовательность из встречающегося в природе полипептида или его COF1/CRBN-связывающего варианта. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит COF1/CRBN-связывающую последовательность из встречающегося в природе полипептида IKZF или его COF1/CRBN-связывающего варианта. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит COF1/CRBN-связывающую последовательность из встречающегося в природе IKZF1, IKZF2, IKZF3, IKZF4 или IKZF5 или их COF1/CRBN-связывающего варианта. В некоторых вариантах осуществления COF1/CRBN-связывающая последовательность содержит две или более прерывистые последовательности из встречающегося в природе полипептида, например, встречающегося в природе полипептида IKZF, например, встречающегося в природе IKZF1, IKZF2, IKZF3, IKZF4 или IKZF5.
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит полипептид IKZF или его структурный мотив.
В некоторых вариантах осуществления полипептид IKZF представляет собой полипептид IKZF1, полипептид IKZF3, полипептид IKZF2 с заменой H141Q (пронумерованной в соответствии с SEQ ID NO: 21) или полипептид IKZF4 с заменой H188Q (пронумерованной в соответствии с SEQ ID NO: 22).
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит достаточную аминокислотную последовательность и/или структурный мотив из IKZF (например, IKZF1 или IKZF3), так что:
i) ассоциация COF1/CRBN-связывающего полипептида с CRBN в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации COF1/CRBN-связывающего полипептида с CRBN в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
ii) ассоциация слитого полипептида с CRBN в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации слитого полипептида с CRBN в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
iii) убиквитинирование гетерологичного полипептида в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования гетерологичного полипептида в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе;
iv) убиквитинирование слитого полипептида в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования слитого полипептида в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе; или
v) деградация слитого полипептида в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от деградации слитого полипептида в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В некоторых вариантах осуществления ассоциация, убиквитинирование и/или деградация измеряются в клетке млекопитающего, например, клетке человека.
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит от приблизительно 10 до приблизительно 95 аминокислотных остатков, от приблизительно 15 до приблизительно 90 аминокислотных остатков, от приблизительно 20 до приблизительно 85 аминокислотных остатков, от приблизительно 25 до приблизительно 80 аминокислотных остатков, от приблизительно 30 до приблизительно 75 аминокислотных остатков, от приблизительно 35 до приблизительно 70 аминокислотных остатков, от приблизительно 40 до приблизительно 65 аминокислотных остатков, от приблизительно 45 до приблизительно 65 аминокислотных остатков, от приблизительно 50 до приблизительно 65 аминокислотных остатков или от приблизительно 55 до приблизительно 65 аминокислотных остатков из IKZF1 или IKZF3.
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит достаточную аминокислотную последовательность и/или структурный мотив из аминокислотных остатков 136-180 из IKZF3 (пронумерованных в соответствии с SEQ ID NO: 19) (например, достаточную аминокислотную последовательность и/или структурный мотив из аминокислотных остатков 136-180 из SEQ ID NO: 19), так что:
i) ассоциация COF1/CRBN-связывающего полипептида с CRBN в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации COF1/CRBN-связывающего полипептида с CRBN в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
ii) ассоциация слитого полипептида с CRBN в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации слитого полипептида с CRBN в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
iii) убиквитинирование гетерологичного полипептида в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования гетерологичного полипептида в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе;
iv) убиквитинирование слитого полипептида в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования слитого полипептида в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе; или
v) деградация слитого полипептида в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от деградации слитого полипептида в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В некоторых вариантах осуществления ассоциация, убиквитинирование и/или деградация измеряются в клетке млекопитающего, например, клетке человека.
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотные остатки 136-180 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19) (например, COF1/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 5) или последовательность, которая отличается от аминокислотных остатков 136-180 из IKZF3 (пронумерованных в соответствии с SEQ ID NO: 19) не более чем 1, 2, 3, 4, 5, 10, 15, 20, 25, 30, 35, или 40 аминокислотными остатками (например, последовательность, которая отличается от аминокислотных остатков 136-180 из SEQ ID NO: 19 не более чем 1, 2, 3, 4, 5, 10, 15, 20, 25, 30, 35, или 40 аминокислотными остатками) (например, последовательность, имеющую не более 1, 2, 3, 4, 5, 10, 15, 20, 25, 30, 35, или 40 аминокислотных замен по сравнению с аминокислотными остатками 136-180 из SEQ ID NO: 19).
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит достаточную аминокислотную последовательность и/или структурный мотив из аминокислотных остатков 136-170 из IKZF3 (пронумерованных в соответствии с SEQ ID NO: 19) (например, достаточную аминокислотную последовательность и/или структурный мотив из аминокислотных остатков 136-170 из SEQ ID NO: 19), так что:
i) ассоциация COF1/CRBN-связывающего полипептида с CRBN в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации COF1/CRBN-связывающего полипептида с CRBN в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
ii) ассоциация слитого полипептида с CRBN в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации слитого полипептида с CRBN в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
iii) убиквитинирование гетерологичного полипептида в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования гетерологичного полипептида в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе;
iv) убиквитинирование слитого полипептида в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования слитого полипептида в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе; или
v) деградация слитого полипептида в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от деградации слитого полипептида в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В некоторых вариантах осуществления ассоциация, убиквитинирование и/или деградация измеряются в клетке млекопитающего, например, клетке человека.
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотные остатки 136-170 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19) (например, COF1/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 6) или последовательность, которая отличается от аминокислотных остатков 136-170 из IKZF3 (пронумерованных в соответствии с SEQ ID NO: 19) не более чем 1, 2, 3, 4, 5, 10, 15, 20, 25 или 30 аминокислотными остатками (например, последовательность, которая отличается от аминокислотных остатков 136-170 из SEQ ID NO: 19 не более чем 1, 2, 3, 4, 5, 10, 15, 20, 25, или 30 аминокислотными остатками) (например, последовательность, имеющую не более 1, 2, 3, 4, 5, 10, 15, 20, 25, или 30 аминокислотных замен по сравнению с аминокислотными остатками 136-170 из SEQ ID NO: 19).
В некоторых вариантах осуществления один, два, три или все из следующих аминокислотных остатков остаются неизмененными: глутамин в положении 147, цистеин в положении 148, глутамин в положении 150, глицин в положении 152, лейцин в положении 161 или лейцин в положении 162, пронумерованные в соответствии с SEQ ID NO: 19. В некоторых вариантах осуществления неизмененным остается глутамин в положении 147, пронумерованном в соответствии с SEQ ID NO: 19. В некоторых вариантах осуществления неизмененным остается цистеин в положении 148, пронумерованном в соответствии с SEQ ID NO: 19. В некоторых вариантах осуществления неизмененным остается глутамин в положении 150, пронумерованном в соответствии с SEQ ID NO: 19. В некоторых вариантах осуществления неизмененным остается глицин в положении 152, пронумерованном в соответствии с SEQ ID NO: 19. В некоторых вариантах осуществления неизмененным остается лейцин в положении 161, пронумерованном в соответствии с SEQ ID NO: 19. В некоторых вариантах осуществления неизмененным остается лейцин в положении 162, пронумерованном в соответствии с SEQ ID NO: 19.
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотные остатки 136-139 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19), например, COF1/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 40.
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотные остатки 136-180 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19). В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 5. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 77. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 5. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 5.
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотные остатки 136-170 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19). В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 6. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 78. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 6. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 78.
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит достаточную аминокислотную последовательность и/или структурный мотив из аминокислотных остатков 236-249 из IKZF3 (пронумерованных в соответствии с SEQ ID NO: 19) (например, достаточную аминокислотную последовательность и/или структурный мотив из аминокислотных остатков 236-249 из SEQ ID NO: 19), так что:
i) ассоциация COF1/CRBN-связывающего полипептида с CRBN в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации COF1/CRBN-связывающего полипептида с CRBN в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
ii) ассоциация слитого полипептида с CRBN в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации слитого полипептида с CRBN в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
iii) убиквитинирование гетерологичного полипептида в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования гетерологичного полипептида в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе;
iv) убиквитинирование слитого полипептида в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования слитого полипептида в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе; или
v) деградация слитого полипептида в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от деградации слитого полипептида в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В некоторых вариантах осуществления ассоциация, убиквитинирование и/или деградация измеряются в клетке млекопитающего, например, клетке человека.
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотные остатки 236-249 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19) (например, COF1/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 11) или последовательность, которая отличается от аминокислотных остатков 236-249 из IKZF3 (пронумерованных в соответствии с SEQ ID NO: 19) не более чем 1, 2, 3, 4, 5, 6 или 7 аминокислотными остатками (например, последовательность, которая отличается от аминокислотных остатков 236-249 из SEQ ID NO: 19 не более чем 1, 2, 3, 4, 5, 6 или 7 аминокислотными остатками) (например, последовательность, имеющую не более 1, 2, 3, 4, 5, 6 или 7 аминокислотных замен по сравнению с аминокислотными остатками 236-249 из SEQ ID NO: 19).
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотные остатки 236-249 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19). В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 11.
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 91.
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит достаточную аминокислотную последовательность и/или структурный мотив из аминокислотных остатков 136-180 и 236-249 из IKZF3 (пронумерованных в соответствии с SEQ ID NO: 19) (например, достаточную аминокислотную последовательность и/или структурный мотив из аминокислотных остатков 136-180 и 236-249 из SEQ ID NO: 19), так что:
i) ассоциация COF1/CRBN-связывающего полипептида с CRBN в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации COF1/CRBN-связывающего полипептида с CRBN в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
ii) ассоциация слитого полипептида с CRBN в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации слитого полипептида с CRBN в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
iii) убиквитинирование гетерологичного полипептида в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования гетерологичного полипептида в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе;
iv) убиквитинирование слитого полипептида в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования слитого полипептида в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе; или
v) деградация слитого полипептида в отсутствие COF1 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от деградации слитого полипептида в присутствии COF1, например, избытка COF1, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В некоторых вариантах осуществления ассоциация, убиквитинирование и/или деградация измеряются в клетке млекопитающего, например, клетке человека.
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит первую последовательность, содержащую аминокислотные остатки 136-180 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19) (например, первую последовательность, содержащую аминокислотную последовательность под SEQ ID NO: 5), или первую последовательность, которая отличается от аминокислотных остатков 136-180 из IKZF3 (пронумерованных в соответствии с SEQ ID NO: 19) не более чем 1, 2, 3, 4, 5, 10, 15, 20, 25, 30, 35, или 40 аминокислотными остатками (например, первую последовательность, которая отличается от аминокислотных остатков 136-180 из SEQ ID NO: 19 не более чем 1, 2, 3, 4, 5, 10, 15, 20, 25, 30, 35, или 40 аминокислотными остатками); и вторую последовательность, содержащую аминокислотные остатки 236-249 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19) (например, вторую последовательность, содержащую аминокислотную последовательность под SEQ ID NO: 11), или вторую последовательность, которая отличается от аминокислотных остатков 236-249 из IKZF3 (пронумерованных в соответствии с SEQ ID NO: 19) не более чем 1, 2, 3, 4, 5, 6 или 7 аминокислотными остатками (например, вторую последовательность, которая отличается от аминокислотных остатков 236-249 из SEQ ID NO: 19 не более чем 1, 2, 3, 4, 5, 6 или 7 аминокислотными остатками).
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотные остатки 136-180 и 236-249 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19). В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 1. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 3. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 1. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 3.
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит первую последовательность, содержащую аминокислотные остатки 136-180 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19), и вторую последовательность, содержащую аминокислотную последовательность MALEKMALEKMALE (SEQ ID NO: 91). В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 14. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 85. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 14. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 85.
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит первую последовательность, содержащую аминокислотные остатки 136-170 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19), и вторую последовательность, содержащую аминокислотную последовательность MALEKMALEKMALE (SEQ ID NO: 91). В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 15. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 86. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 15. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 86.
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит на по меньшей мере один лизин меньше, чем соответствующая нативная последовательность. В некоторых вариантах осуществления один или несколько остатков лизина в соответствующей нативной последовательности заменены на другую аминокислоту, например, аргинин. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит менее 1, 2, 3, 4 или 5 остатков лизина. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид не содержит остаток лизина. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид не подвергается убиквитинированию, например, в присутствии COF1, например, как измерено с помощью анализа, описанного в данном документе, необязательно, где убиквитинирование измеряется в клетке млекопитающего, например, клетке человека.
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 4, 41, 42 и 43. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 4. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 41. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 42. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 43.
В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 2. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 4. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 2. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 4.
В некоторых вариантах осуществления COF1 представляет собой иммуномодулирующее лекарственное средство на основе имида (IMiD) или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления COF1 характеризуется структурой формулы (I-a):

или ее фармацевтически приемлемой соли, сложного эфира, гидрата или таутомера, где:
кольцо A представляет собой карбоциклил, гетероциклил, арил или гетероарил, каждый из которых независимо и необязательно замещен одним или несколькими R4;
M отсутствует или представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил или C1-C6гетероалкил, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или несколькими R4;
каждый из R2a и R2b независимо представляет собой водород или C1-C6алкил; или R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу или тиокарбонильную группу;
R3a представляет собой водород, C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD) или -N(RC)S(O)xRE, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или несколькими R6;
каждый из R3 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD) или -N (RC)S(O)xRE, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или несколькими R6;
каждый R4 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, оксо, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, S(O)xRE, -S(O)xN(RC)(RD), -N (RC)S(O)xRE, карбоциклил, гетероциклил, арил или гетероарил, где каждый алкил, алкенил, алкинил, карбоциклил, гетероциклил, арил и гетероарил независимо и необязательно замещен одним или несколькими R7;
каждый из RA, RB, RC, RD и RE независимо представляет собой водород или C1-C6алкил;
каждый R6 независимо представляет собой C1-C6алкил, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, арил или гетероарил, где каждый арил и гетероарил независимо и необязательно замещен одним или несколькими R8;
каждый R7 независимо представляет собой галоген, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
каждый R8 независимо представляет собой C1-C6алкил, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
n составляет 0, 1, 2 или 3;
o составляет 0, 1, 2, 3, 4 или 5; и
x составляет 0, 1 или 2.
В некоторых вариантах осуществления формулы (I-a) X представляет собой O. В некоторых вариантах осуществления M отсутствует. В некоторых вариантах осуществления кольцо A представляет собой гетероциклил (например, азотсодержащий гетероциклил, например, 2-(2,6-диоксопиперидин-3-ил)изоиндолин-1,3-дион). В некоторых вариантах осуществления R4 представляет собой оксо или ORB (например, -OCH3 или -OCH2CH3), и o составляет 0, 1 или 2. В некоторых вариантах осуществления каждый из R2a и R2b независимо представляет собой водород, или R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу. В некоторых вариантах осуществления R3a представляет собой гетероалкил (например, -CH2NHC(O)CH2), -N(RC)(RD) (например, -NH2) или -N(RC)C(O)RA (например, -NHC(O)CH3). В некоторых вариантах осуществления n составляет 0.
В некоторых вариантах осуществления COF1 представляет собой талидомид или его аналог или фармацевтически приемлемую соль.
В некоторых вариантах осуществления COF1 выбрано из группы, состоящей из леналидомида, помалидомида, талидомида и 2-(4-(трет-бутил)фенил)-N-((2-(2,6-диоксопиперидин-3-ил)-1-оксоизоиндолин-5-ил)метил)ацетамида или их фармацевтически приемлемой соли.
В некоторых вариантах осуществления COF1 выбрано из группы, состоящей из:

или их фармацевтически приемлемой соли.
В некоторых вариантах осуществления COF1 представляет собой леналидомид или помалидомид или их фармацевтически приемлемую соль. В некоторых вариантах осуществления COF1 представляет собой леналидомид или его аналог или фармацевтически приемлемую соль. В некоторых вариантах осуществления COF1 представляет собой леналидомид или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления слитый полипептид дополнительно содержит домен деградации, где домен деградации отделен от COF1/CRBN-связывающего полипептида и гетерологичного полипептида с помощью гетерологичного сайта расщепления протеазами.
В некоторых вариантах осуществления слитый полипептид содержит в направлении от N-конца к C-концу:
i) домен деградации, гетерологичный сайт расщепления протеазами, гетерологичный полипептид и COF1/CRBN-связывающий полипептид;
ii) домен деградации, гетерологичный сайт расщепления протеазами, COF1/CRBN-связывающий полипептид и гетерологичный полипептид;
iii) COF1/CRBN-связывающий полипептид, гетерологичный полипептид, гетерологичный сайт расщепления протеазами и домен деградации; или
iv) гетерологичный полипептид и COF1/CRBN-связывающий полипептид, гетерологичный сайт расщепления протеазами и домен деградации.
В некоторых вариантах осуществления слитый полипептид содержит в направлении от N-конца к C-концу: домен деградации, гетерологичный сайт расщепления протеазами, гетерологичный полипептид и COF1/CRBN-связывающий полипептид.
В некоторых вариантах осуществления домен деградации имеет первое состояние, ассоциированное с первым уровнем экспрессии слитого полипептида, и второе состояние, ассоциированное со вторым уровнем экспрессии слитого полипептида, где второй уровень увеличивается, например, в по меньшей мере 2, 3, 4, 5, 10, 20 или 30 раз, по сравнению с первым уровнем в присутствии стабилизирующего соединения.
В некоторых вариантах осуществления в отсутствие стабилизирующего соединения слитый полипептид подвергается деградации под действием клеточного пути деградации, например, подвергается деградации по меньшей мере 50%, 60%, 70%, 80%, 90% или более слитого полипептида, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В некоторых вариантах осуществления уровень экспрессии и/или деградация измеряются в клетке млекопитающего, например, клетке человека.
В некоторых вариантах осуществления в присутствии стабилизирующего соединения:
i) домен деградации принимает конформацию, которая является более устойчивой к клеточной деградации относительно конформации в отсутствие стабилизирующего соединения; или
ii) конформация слитого полипептида более восприимчива к расщеплению в гетерологичном сайте расщепления протеазами относительно конформации в отсутствие стабилизирующего соединения.
В некоторых вариантах осуществления домен деградации выбран из домена эстрогенового рецептора (ER), домена белка FKB (FKBP) или домена дигидрофолатредуктазы (DHFR).
В некоторых вариантах осуществления домен деградации представляет собой домен эстрогенового рецептора (ER). В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность, которая на по меньшей мере 90, 95, 97, 98, 99 или 100% идентична SEQ ID NO: 46 или 48. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность под SEQ ID NO: 46. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность под SEQ ID NO: 48.
В некоторых вариантах осуществления стабилизирующее соединение представляет собой базедоксифен или 4-гидрокситамоксифен (4-OHT) или их фармацевтически приемлемую соль. В некоторых вариантах осуществления домен деградации представляет собой домен эстрогенового рецептора (ER), и стабилизирующее соединение представляет собой базедоксифен или его фармацевтически приемлемую соль. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность под SEQ ID NO: 46, и стабилизирующее соединение представляет собой базедоксифен или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления домен деградации представляет собой домен белка FKB (FKBP). В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность, которая на по меньшей мере 90, 95, 97, 98, 99 или 100% идентична SEQ ID NO: 50. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность под SEQ ID NO: 50. В некоторых вариантах осуществления стабилизирующее соединение представляет собой Shield-1 или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления домен деградации представляет собой домен дигидрофолатредуктазы (DHFR). В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность, которая на по меньшей мере 90, 95, 97, 98, 99 или 100% идентична SEQ ID NO: 51. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность под SEQ ID NO: 51. В некоторых вариантах осуществления стабилизирующее соединение представляет собой триметоприм или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами расщепляется под действием внутриклеточной протеазы млекопитающего. В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами расщепляется под действием протеазы, выбранной из группы, состоящей из фурина, PCSK1, PCSK5, PCSK6, PCSK7, катепсина B, гранзима B, фактора XA, энтерокиназы, гененазы, сортазы, протеазы precission, тромбина, протеазы TEV и эластазы-1. В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами содержит последовательность, имеющую мотив расщепления, выбранный из группы, состоящей из консенсусного мотива RX(K/R)R (X может быть любой аминокислотой; SEQ ID NO: 52), консенсусного мотива RXXX[KR]R (X может быть любой аминокислотой; SEQ ID NO: 53), консенсусного мотива RRX (SEQ ID NO: 54), консенсусного мотива I-E-P-D-X (SEQ ID NO: 55), Ile-Glu/Asp-Gly-Arg (SEQ ID NO: 56), Asp-Asp-Asp-Asp-Lys (SEQ ID NO: 57), Pro-Gly-Ala-Ala-His-Tyr (SEQ ID NO: 58), консенсусного мотива LPXTG/A (SEQ ID NO: 59), Leu-Glu-Val-Phe-Gln-Gly-Pro (SEQ ID NO: 60), Leu-Val-Pro-Arg-Gly-Ser (SEQ ID NO: 61), E-N-L-Y-F-Q-G (SEQ ID NO: 62) и [AGSV]-X (X может быть любой аминокислотой; SEQ ID NO: 63). В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами расщепляется под действием фурина. В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами содержит сайт расщепления фурином, выбранный из группы, состоящей из RTKR (SEQ ID NO: 123); GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125); GTGAEDPRPSRKRR (SEQ ID NO: 127); LQWLEQQVAKRRTKR (SEQ ID NO: 129); GTGAEDPRPSRKRRSLGG (SEQ ID NO: 131); GTGAEDPRPSRKRRSLG (SEQ ID NO: 133); SLNLTESHNSRKKR (SEQ ID NO: 135); CKINGYPKRGRKRR (SEQ ID NO: 137) и SARNRQKR (SEQ ID NO: 34). В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами не содержит аминокислотную последовательность SARNRQKR (SEQ ID NO: 34). В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами содержит сайт расщепления фурином GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125). В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами расщепляется под действием внеклеточной протеазы млекопитающего. В некоторых вариантах осуществления внеклеточная протеаза млекопитающего выбрана из группы, состоящей из фактора XA, энтерокиназы, гененазы, сортазы, протеазы precission, тромбина, протеазы TEV и эластазы-1. В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами содержит аминокислотную последовательность, выбранную из группы, состоящей из Ile-Glu/Asp-Gly-Arg (SEQ ID NO: 56), Asp-Asp-Asp-Asp-Lys (SEQ ID NO: 57), Pro-Gly-Ala-Ala-His-Tyr (SEQ ID NO: 58), консенсусного мотива LPXTG/A (SEQ ID NO: 59), Leu-Glu-Val-Phe-Gln-Gly-Pro (SEQ ID NO: 60), Leu-Val-Pro-Arg-Gly-Ser (SEQ ID NO: 61), E-N-L-Y-F-Q-G (SEQ ID NO: 62) и [AGSV]-X (X может быть любой аминокислотой; SEQ ID NO: 63).
В одном аспекте данного документе представлен слитый полипептид, содержащий первый домен и второй домен, разделенные гетерологичным сайтом расщепления протеазами, где первый домен содержит домен деградации, а второй домен содержит полипептид, связывающий соединение формулы (II) (COF2)/CRBN, и гетерологичный полипептид, например, гетерологичный полипептид млекопитающего, бактериальный или вирусный полипептид, где соединение формулы (II) представляет собой:

или его фармацевтически приемлемую соль, сложный эфир, гидрат, таутомер или пролекарство, где:
X представляет собой O или S;
R1 представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, карбоциклил, гетероциклил, арил или гетероарил, каждый из которых независимо и необязательно замещен одним или несколькими R4;
каждый из R2a и R2b независимо представляет собой водород или C1-C6алкил; или R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу или тиокарбонильную группу;
каждый из R10 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD), или -N (RC)S(O)xRE, или L-метку; где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или несколькими R11;
каждый R4 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, оксо, C(O)RA, -C(O)ORB, ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, S(O)xRE, -S(O)xN(RC)(RD), -N (RC)S(O)xRE, карбоциклил, гетероциклил, арил или гетероарил, где каждый алкил, алкенил, алкинил, гетероалкил, карбоциклил, гетероциклил, арил и гетероарил независимо и необязательно замещен одним или несколькими R7;
каждый из RA, RB, RC, RD и RE независимо представляет собой водород или C1-C6алкил;
каждый R11 независимо представляет собой C1-C6алкил, галоген, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, арил или гетероарил, где каждый арил и гетероарил независимо и необязательно замещен одним или несколькими R8;
каждый R7 независимо представляет собой галоген, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
каждый R8 независимо представляет собой C1-C6алкил, галоген, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
каждый L независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, -C(O)RA1, -C(O)ORB1, -ORB1, -N(RC1)(RD1), -C(O)N(RC1)(RD1), -N(RC1)C(O)RA1, -S(O)xRE1, -S(O)xN(RC1)(RD1) или -N (RC1)S(O)xRE1, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или несколькими R12;
каждая метка представляет собой нацеливающий фрагмент, способный к связыванию с белком-мишенью;
каждый из RA1, RB1, RC1, RD1, и RE1 независимо представляет собой водород, C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, карбоциклил, гетероциклил, арил или гетероарил, где каждый алкил, алкенил, алкинил, гетероалкил, карбоциклил, гетероциклил, арил и гетероарил независимо и необязательно замещен одним или несколькими R12;
каждый R12 независимо представляет собой C1-C6алкил, галоген, циано, карбоциклил или гетероциклил;
n составляет 0, 1, 2, 3 или 4; и
x составляет 0, 1 или 2.
В некоторых вариантах осуществления домен деградации имеет первое состояние, ассоциированное с первым уровнем экспрессии слитого полипептида, и второе состояние, ассоциированное со вторым уровнем экспрессии слитого полипептида, где второй уровень увеличивается, например, в по меньшей мере 2, 3, 4, 5, 10, 20 или 30 раз, по сравнению с первым уровнем в присутствии стабилизирующего соединения.
В некоторых вариантах осуществления в отсутствие стабилизирующего соединения слитый полипептид подвергается деградации под действием клеточного пути деградации, например, подвергается деградации по меньшей мере 50%, 60%, 70%, 80%, 90% или более слитого полипептида, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В некоторых вариантах осуществления уровень экспрессии и/или деградация измеряются в клетке млекопитающего, например, клетке человека.
В некоторых вариантах осуществления в присутствии стабилизирующего соединения:
i) домен деградации принимает конформацию, которая является более устойчивой к клеточной деградации относительно конформации в отсутствие стабилизирующего соединения; или
ii) конформация слитого полипептида более восприимчива к расщеплению в гетерологичном сайте расщепления протеазами относительно конформации в отсутствие стабилизирующего соединения.
В некоторых вариантах осуществления домен деградации выбран из домена эстрогенового рецептора (ER), домена белка FKB (FKBP) или домена дигидрофолатредуктазы (DHFR).
В некоторых вариантах осуществления домен деградации представляет собой домен эстрогенового рецептора (ER). В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность, которая на по меньшей мере 90, 95, 97, 98, 99 или 100% идентична SEQ ID NO: 46 или 48. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность под SEQ ID NO: 46. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность под SEQ ID NO: 48.
В некоторых вариантах осуществления стабилизирующее соединение представляет собой базедоксифен, или 4-гидрокситамоксифен (4-OHT), или их фармацевтически приемлемую соль. В некоторых вариантах осуществления домен деградации представляет собой домен эстрогенового рецептора (ER), и стабилизирующее соединение представляет собой базедоксифен или его фармацевтически приемлемую соль. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность под SEQ ID NO: 46, и стабилизирующее соединение представляет собой базедоксифен или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления домен деградации представляет собой домен белка FKB (FKBP). В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность, которая на по меньшей мере 90, 95, 97, 98, 99 или 100% идентична SEQ ID NO: 50. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность под SEQ ID NO: 50. В некоторых вариантах осуществления стабилизирующее соединение представляет собой Shield-1 или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления домен деградации представляет собой домен дигидрофолатредуктазы (DHFR). В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность, которая на по меньшей мере 90, 95, 97, 98, 99 или 100% идентична SEQ ID NO: 51. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность под SEQ ID NO: 51. В некоторых вариантах осуществления стабилизирующее соединение представляет собой триметоприм или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами расщепляется под действием внутриклеточной протеазы млекопитающего. В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами расщепляется под действием протеазы, выбранной из группы, состоящей из фурина, PCSK1, PCSK5, PCSK6, PCSK7, катепсина B, гранзима B, фактора XA, энтерокиназы, гененазы, сортазы, протеазы precission, тромбина, протеазы TEV и эластазы-1. В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами содержит последовательность, имеющую мотив расщепления, выбранный из группы, состоящей из консенсусного мотива RX(K/R)R (X может быть любой аминокислотой; SEQ ID NO: 52), консенсусного мотива RXXX[KR]R (X может быть любой аминокислотой; SEQ ID NO: 53), консенсусного мотива RRX (SEQ ID NO: 54), консенсусного мотива I-E-P-D-X (SEQ ID NO: 55), Ile-Glu/Asp-Gly-Arg (SEQ ID NO: 56), Asp-Asp-Asp-Asp-Lys (SEQ ID NO: 57), Pro-Gly-Ala-Ala-His-Tyr (SEQ ID NO: 58), консенсусного мотива LPXTG/A (SEQ ID NO: 59), Leu-Glu-Val-Phe-Gln-Gly-Pro (SEQ ID NO: 60), Leu-Val-Pro-Arg-Gly-Ser (SEQ ID NO: 61), E-N-L-Y-F-Q-G (SEQ ID NO: 62) и [AGSV]-X (X может быть любой аминокислотой; SEQ ID NO: 63). В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами расщепляется под действием фурина. В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами содержит сайт расщепления фурином выбранный из группы, состоящей из RTKR (SEQ ID NO: 123); GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125); GTGAEDPRPSRKRR (SEQ ID NO: 127); LQWLEQQVAKRRTKR (SEQ ID NO: 129); GTGAEDPRPSRKRRSLGG (SEQ ID NO: 131); GTGAEDPRPSRKRRSLG (SEQ ID NO: 133); SLNLTESHNSRKKR (SEQ ID NO: 135); CKINGYPKRGRKRR (SEQ ID NO: 137); и SARNRQKR (SEQ ID NO: 34). В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами не содержит аминокислотную последовательность SARNRQKR (SEQ ID NO: 34). В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами содержит сайт расщепления фурином GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125). В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами расщепляется под действием внеклеточной протеазы млекопитающего. В некоторых вариантах осуществления внеклеточная протеаза млекопитающего выбрана из группы, состоящей из фактора XA, энтерокиназы, гененазы, сортазы, протеазы precission, тромбина, протеазы TEV и эластазы-1. В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами содержит аминокислотную последовательность, выбранную из группы, состоящей из Ile-Glu/Asp-Gly-Arg (SEQ ID NO: 56), Asp-Asp-Asp-Asp-Lys (SEQ ID NO: 57), Pro-Gly-Ala-Ala-His-Tyr (SEQ ID NO: 58), консенсусного мотива LPXTG/A (SEQ ID NO: 59), Leu-Glu-Val-Phe-Gln-Gly-Pro (SEQ ID NO: 60), Leu-Val-Pro-Arg-Gly-Ser (SEQ ID NO: 61), E-N-L-Y-F-Q-G (SEQ ID NO: 62) и [AGSV]-X (X может быть любой аминокислотой; SEQ ID NO: 63).
В некоторых вариантах осуществления домен деградации слит с гетерологичным сайтом расщепления протеазами, который дополнительно слит со вторым доменом.
В некоторых вариантах осуществления слитый полипептид содержит в направлении от N-конца к C-концу:
i) домен деградации, гетерологичный сайт расщепления протеазами, гетерологичный полипептид и COF2/CRBN-связывающий полипептид;
ii) домен деградации, гетерологичный сайт расщепления протеазами, COF2/CRBN-связывающий полипептид и гетерологичный полипептид;
iii) COF2/CRBN-связывающий полипептид, гетерологичный полипептид, гетерологичный сайт расщепления протеазами и домен деградации; или
iv) гетерологичный полипептид и COF2/CRBN-связывающий полипептид, гетерологичный сайт расщепления протеазами и домен деградации.
В некоторых вариантах осуществления слитый полипептид содержит в направлении от N-конца к C-концу: домен деградации, гетерологичный сайт расщепления протеазами, гетерологичный полипептид и COF2/CRBN-связывающий полипептид. В некоторых вариантах осуществления слитый полипептид содержит в направлении от N-конца к C-концу: домен деградации, гетерологичный сайт расщепления протеазами, COF2/CRBN-связывающий полипептид и гетерологичный полипептид. В некоторых вариантах осуществления слитый полипептид содержит в направлении от N-конца к C-концу: COF2/CRBN-связывающий полипептид, гетерологичный полипептид, гетерологичный сайт расщепления протеазами и домен деградации. В некоторых вариантах осуществления слитый полипептид содержит в направлении от N-конца к C-концу: гетерологичный полипептид и COF2/CRBN-связывающий полипептид, гетерологичный сайт расщепления протеазами и домен деградации.
В некоторых вариантах осуществления ассоциация COF2/CRBN-связывающего полипептида с цереблоном (CRBN) в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации COF2/CRBN-связывающего полипептида с CRBN в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид не связывается с CRBN в отсутствие COF2. В некоторых вариантах осуществления ассоциация слитого полипептида с CRBN в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации слитого полипептида с CRBN в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации. В некоторых вариантах осуществления слитый полипептид не связывается с CRBN в отсутствие COF2. В некоторых вариантах осуществления ассоциация и/или связывание измеряются в клетке млекопитающего, например, клетке человека.
В некоторых вариантах осуществления убиквитинирование гетерологичного полипептида в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования гетерологичного полипептида в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе. В некоторых вариантах осуществления убиквитинирование слитого полипептида в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования слитого полипептида в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе. В некоторых вариантах осуществления гетерологичный полипептид или слитый полипептид подвергается убиквитинированию по одному или нескольким остаткам лизина или метионина в присутствии COF2. В некоторых вариантах осуществления убиквитинирование измеряется в клетке млекопитающего, например, клетке человека.
В некоторых вариантах осуществления деградация слитого полипептида в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от деградации слитого полипептида в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии. В некоторых вариантах осуществления деградация слитого полипептида опосредуется убиквитинированием в присутствии COF2. В некоторых вариантах осуществления деградация измеряется в клетке млекопитающего, например, клетке человека.
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид составляет от 10 до 95 аминокислотных остатков в длину, от 15 до 90 аминокислотных остатков в длину, от 20 до 85 аминокислотных остатков в длину, от 25 до 80 аминокислотных остатков в длину, от 30 до 75 аминокислотных остатков в длину, от 35 до 70 аминокислотных остатков в длину, от 40 до 65 аминокислотных остатков в длину, от 45 до 65 аминокислотных остатков в длину, от 50 до 65 аминокислотных остатков в длину или от 55 до 65 аминокислотных остатков в длину.
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит бета-изгиб. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит бета-изгиб из IKZF1 или IKZF3 (например, IKZF1 или IKZF3 человека). В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит бета-шпильку. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит бета-шпильку из IKZF1 или IKZF3 (например, IKZF1 или IKZF3 человека). В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит бета-нить. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит бета-нить из IKZF1 или IKZF3 (например, IKZF1 или IKZF3 человека). В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит альфа-спираль. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит альфа-спираль из IKZF1 или IKZF3 (например, IKZF1 или IKZF3 человека). В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит в направлении от N-конца к C-концу: первую бета-нить, бета-шпильку, вторую бета-нить и первую альфа-спираль. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит в направлении от N-конца к C-концу: первую бета-нить, бета-шпильку, вторую бета-нить и первую альфа-спираль из IKZF1 или IKZF3 (например, IKZF1 или IKZF3 человека). В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит в направлении от N-конца к C-концу: первую бета-нить, бета-шпильку, вторую бета-нить, первую альфа-спираль и вторую альфа-спираль. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит в направлении от N-конца к C-концу: первую бета-нить, бета-шпильку, вторую бета-нить, первую альфа-спираль и вторую альфа-спираль из IKZF1 или IKZF3 (например, IKZF1 или IKZF3 человека). В некоторых вариантах осуществления бета-шпилька и вторая альфа-спираль разделены не более чем 60, 50, 40 или 30 аминокислотными остатками.
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит COF2/CRBN-связывающую последовательность из встречающегося в природе полипептида или его COF2/CRBN-связывающего варианта. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит COF2/CRBN-связывающую последовательность из встречающегося в природе полипептида IKZF или его COF2/CRBN-связывающего варианта. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит COF2/CRBN-связывающую последовательность из встречающегося в природе IKZF1, IKZF2, IKZF3, IKZF4 или IKZF5 или их COF2/CRBN-связывающего варианта. В некоторых вариантах осуществления COF2/CRBN-связывающая последовательность содержит две или более прерывистые последовательности из встречающегося в природе полипептида, например, встречающегося в природе полипептида IKZF, например, встречающегося в природе IKZF1, IKZF2, IKZF3, IKZF4 или IKZF5.
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит полипептид IKZF или его структурный мотив.
В некоторых вариантах осуществления полипептид IKZF представляет собой полипептид IKZF1, полипептид IKZF3, полипептид IKZF2 с заменой H141Q (пронумерованной в соответствии с SEQ ID NO: 21) или полипептид IKZF4 с заменой H188Q (пронумерованной в соответствии с SEQ ID NO: 22).
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит достаточную аминокислотную последовательность и/или структурный мотив из IKZF (например, IKZF1 или IKZF3), так что:
i) ассоциация COF2/CRBN-связывающего полипептида с CRBN в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации COF2/CRBN-связывающего полипептида с CRBN в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
ii) ассоциация слитого полипептида с CRBN в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации слитого полипептида с CRBN в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
iii) убиквитинирование гетерологичного полипептида в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования гетерологичного полипептида в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе;
iv) убиквитинирование слитого полипептида в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования слитого полипептида в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе; или
v) деградация слитого полипептида в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от деградации слитого полипептида в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В некоторых вариантах осуществления ассоциация, убиквитинирование и/или деградация измеряются в клетке млекопитающего, например, клетке человека.
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит от приблизительно 10 до приблизительно 95 аминокислотных остатков, от приблизительно 15 до приблизительно 90 аминокислотных остатков, от приблизительно 20 до приблизительно 85 аминокислотных остатков, от приблизительно 25 до приблизительно 80 аминокислотных остатков, от приблизительно 30 до приблизительно 75 аминокислотных остатков, от приблизительно 35 до приблизительно 70 аминокислотных остатков, от приблизительно 40 до приблизительно 65 аминокислотных остатков, от приблизительно 45 до приблизительно 65 аминокислотных остатков, от приблизительно 50 до приблизительно 65 аминокислотных остатков или от приблизительно 55 до приблизительно 65 аминокислотных остатков из IKZF1 или IKZF3.
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит достаточную аминокислотную последовательность и/или структурный мотив из аминокислотных остатков 136-180 из IKZF3 (пронумерованных в соответствии с SEQ ID NO: 19) (например, достаточную аминокислотную последовательность и/или структурный мотив из аминокислотных остатков 136-180 из SEQ ID NO: 19), так что:
i) ассоциация COF2/CRBN-связывающего полипептида с CRBN в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации COF2/CRBN-связывающего полипептида с CRBN в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
ii) ассоциация слитого полипептида с CRBN в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации слитого полипептида с CRBN в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
iii) убиквитинирование гетерологичного полипептида в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования гетерологичного полипептида в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе;
iv) убиквитинирование слитого полипептида в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования слитого полипептида в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе; или
v) деградация слитого полипептида в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от деградации слитого полипептида в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В некоторых вариантах осуществления ассоциация, убиквитинирование и/или деградация измеряются в клетке млекопитающего, например, клетке человека.
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотные остатки 136-180 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19) (например, COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 5) или последовательность, которая отличается от аминокислотных остатков 136-180 из IKZF3 (пронумерованных в соответствии с SEQ ID NO: 19) не более чем 1, 2, 3, 4, 5, 10, 15, 20, 25, 30, 35, или 40 аминокислотными остатками (например, последовательность, которая отличается от аминокислотных остатков 136-180 из SEQ ID NO: 19 не более чем 1, 2, 3, 4, 5, 10, 15, 20, 25, 30, 35, или 40 аминокислотными остатками) (например, последовательность, имеющую не более 1, 2, 3, 4, 5, 10, 15, 20, 25, 30, 35, или 40 аминокислотных замен по сравнению с аминокислотными остатками 136-180 из SEQ ID NO: 19).
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит достаточную аминокислотную последовательность и/или структурный мотив из аминокислотных остатков 136-170 из IKZF3 (пронумерованных в соответствии с SEQ ID NO: 19) (например, достаточную аминокислотную последовательность и/или структурный мотив из аминокислотных остатков 136-170 из SEQ ID NO: 19), так что:
i) ассоциация COF2/CRBN-связывающего полипептида с CRBN в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации COF2/CRBN-связывающего полипептида с CRBN в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
ii) ассоциация слитого полипептида с CRBN в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации слитого полипептида с CRBN в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
iii) убиквитинирование гетерологичного полипептида в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования гетерологичного полипептида в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе;
iv) убиквитинирование слитого полипептида в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования слитого полипептида в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе; или
v) деградация слитого полипептида в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от деградации слитого полипептида в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В некоторых вариантах осуществления ассоциация, убиквитинирование и/или деградация измеряются в клетке млекопитающего, например, клетке человека.
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотные остатки 136-170 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19) (например, COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 6) или последовательность, которая отличается от аминокислотных остатков 136-170 из IKZF3 (пронумерованных в соответствии с SEQ ID NO: 19) не более чем 1, 2, 3, 4, 5, 10, 15, 20, 25, или 30 аминокислотными остатками (например, последовательность, которая отличается от аминокислотных остатков 136-170 из SEQ ID NO: 19 не более чем 1, 2, 3, 4, 5, 10, 15, 20, 25, или 30 аминокислотными остатками) (например, последовательность, имеющую не более 1, 2, 3, 4, 5, 10, 15, 20, 25, или 30 аминокислотных замен по сравнению с аминокислотными остатками 136-170 из SEQ ID NO: 19).
В некоторых вариантах осуществления один, два, три или все из следующих аминокислотных остатков остаются неизмененными: глутамин в положении 147, цистеин в положении 148, глутамин в положении 150, глицин в положении 152, лейцин в положении 161 или лейцин в положении 162, пронумерованные в соответствии с SEQ ID NO: 19. В некоторых вариантах осуществления неизмененным остается глутамин в положении 147, пронумерованном в соответствии с SEQ ID NO: 19. В некоторых вариантах осуществления неизмененным остается цистеин в положении 148, пронумерованном в соответствии с SEQ ID NO: 19. В некоторых вариантах осуществления неизмененным остается глутамин в положении 150, пронумерованном в соответствии с SEQ ID NO: 19. В некоторых вариантах осуществления неизмененным остается глицин в положении 152, пронумерованном в соответствии с SEQ ID NO: 19. В некоторых вариантах осуществления неизмененным остается лейцин в положении 161, пронумерованном в соответствии с SEQ ID NO: 19. В некоторых вариантах осуществления неизмененным остается лейцин в положении 162, пронумерованном в соответствии с SEQ ID NO: 19.
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотные остатки 136-139 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19), например, COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 40.
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотные остатки 136-180 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19). В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 5. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 77. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 5. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 5.
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотные остатки 136-170 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19). В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 6. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 78. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 6. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 78.
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит достаточную аминокислотную последовательность и/или структурный мотив из аминокислотных остатков 236-249 из IKZF3 (пронумерованных в соответствии с SEQ ID NO: 19) (например, достаточную аминокислотную последовательность и/или структурный мотив из аминокислотных остатков 236-249 из SEQ ID NO: 19), так что:
i) ассоциация COF2/CRBN-связывающего полипептида с CRBN в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации COF2/CRBN-связывающего полипептида с CRBN в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
ii) ассоциация слитого полипептида с CRBN в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации слитого полипептида с CRBN в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
iii) убиквитинирование гетерологичного полипептида в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования гетерологичного полипептида в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе;
iv) убиквитинирование слитого полипептида в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования слитого полипептида в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе; или
v) деградация слитого полипептида в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от деградации слитого полипептида в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В некоторых вариантах осуществления ассоциация, убиквитинирование и/или деградация измеряются в клетке млекопитающего, например, клетке человека.
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотные остатки 236-249 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19) (например, COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 11) или последовательность, которая отличается от аминокислотных остатков 236-249 из IKZF3 (пронумерованных в соответствии с SEQ ID NO: 19) не более чем 1, 2, 3, 4, 5, 6 или 7 аминокислотными остатками (например, последовательность, которая отличается от аминокислотных остатков 236-249 из SEQ ID NO: 19 не более чем 1, 2, 3, 4, 5, 6 или 7 аминокислотными остатками) (например, последовательность, имеющую не более 1, 2, 3, 4, 5, 6 или 7 аминокислотных замен по сравнению с аминокислотными остатками 236-249 из SEQ ID NO: 19).
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотные остатки 236-249 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19). В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 11.
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 91.
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит достаточную аминокислотную последовательность и/или структурный мотив из аминокислотных остатков 136-180 и 236-249 из IKZF3 (пронумерованных в соответствии с SEQ ID NO: 19) (например, достаточную аминокислотную последовательность и/или структурный мотив из аминокислотных остатков 136-180 и 236-249 из SEQ ID NO: 19), так что:
i) ассоциация COF2/CRBN-связывающего полипептида с CRBN в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации COF2/CRBN-связывающего полипептида с CRBN в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
ii) ассоциация слитого полипептида с CRBN в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации слитого полипептида с CRBN в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
iii) убиквитинирование гетерологичного полипептида в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования гетерологичного полипептида в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе;
iv) убиквитинирование слитого полипептида в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования слитого полипептида в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе; или
v) деградация слитого полипептида в отсутствие COF2 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от деградации слитого полипептида в присутствии COF2, например, избытка COF2, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В некоторых вариантах осуществления ассоциация, убиквитинирование и/или деградация измеряются в клетке млекопитающего, например, клетке человека.
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит первую последовательность, содержащую аминокислотные остатки 136-180 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19) (например, первую последовательность, содержащую аминокислотную последовательность под SEQ ID NO: 5), или первую последовательность, которая отличается от аминокислотных остатков 136-180 из IKZF3 (пронумерованных в соответствии с SEQ ID NO: 19) не более чем 1, 2, 3, 4, 5, 10, 15, 20, 25, 30, 35, или 40 аминокислотными остатками (например, первую последовательность, которая отличается от аминокислотных остатков 136-180 из SEQ ID NO: 19 не более чем 1, 2, 3, 4, 5, 10, 15, 20, 25, 30, 35, или 40 аминокислотными остатками); и вторую последовательность, содержащую аминокислотные остатки 236-249 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19) (например, вторую последовательность, содержащую аминокислотную последовательность под SEQ ID NO: 11), или вторую последовательность, которая отличается от аминокислотных остатков 236-249 из IKZF3 (пронумерованных в соответствии с SEQ ID NO: 19) не более чем 1, 2, 3, 4, 5, 6 или 7 аминокислотными остатками (например, вторую последовательность, которая отличается от аминокислотных остатков 236-249 из SEQ ID NO: 19 не более чем 1, 2, 3, 4, 5, 6 или 7 аминокислотными остатками).
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотные остатки 136-180 и 236-249 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19). В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 1. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 3. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 1. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 3.
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит первую последовательность, содержащую аминокислотные остатки 136-180 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19), и вторую последовательность, содержащую аминокислотную последовательность MALEKMALEKMALE (SEQ ID NO: 91). В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 14. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 85. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 14. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 85.
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит первую последовательность, содержащую аминокислотные остатки 136-170 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19), и вторую последовательность, содержащую аминокислотную последовательность MALEKMALEKMALE (SEQ ID NO: 91). В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 15. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 86. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 15. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 86.
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит на по меньшей мере один лизин меньше, чем соответствующая нативная последовательность. В некоторых вариантах осуществления один или несколько остатков лизина в соответствующей нативной последовательности заменены на другую аминокислоту, например, аргинин. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит менее 1, 2, 3, 4 или 5 остатков лизина. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид не содержит остаток лизина. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид не подвергается убиквитинированию, например, в присутствии COF2, например, как измерено с помощью анализа, описанного в данном документе, необязательно, где убиквитинирование измеряется в клетке млекопитающего, например, клетке человека.
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 4, 41, 42 и 43. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 4. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 41. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 42. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 43.
В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 2. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 4. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 2. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид состоит из аминокислотной последовательности под SEQ ID NO: 4.
В некоторых вариантах осуществления COF2 представляет собой иммуномодулирующее лекарственное средство на основе имида (IMiD) или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления COF2 характеризуется структурой формулы (I):
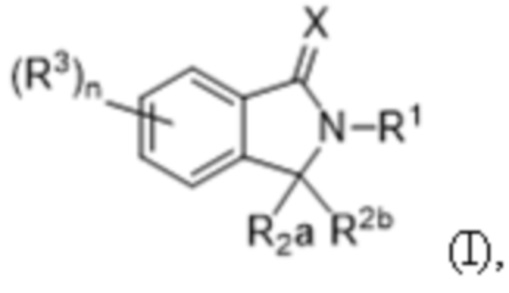
или ее фармацевтически приемлемой соли, сложного эфира, гидрата, сольвата или таутомера, где:
X представляет собой O или S;
R1 представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, карбоциклил, гетероциклил, арил или гетероарил, каждый из которых независимо и необязательно замещен одним или несколькими R4;
каждый из R2a и R2b независимо представляет собой водород или C1-C6алкил; или R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу или тиокарбонильную группу;
каждый из R3 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD) или -N(RC)S(O)xRE, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или несколькими R6;
каждый R4 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, оксо, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD), -N (RC)S(O)xRE, карбоциклил, гетероциклил, арил или гетероарил, где каждый алкил, алкенил, алкинил, гетероалкил, карбоциклил, гетероциклил, арил и гетероарил независимо и необязательно замещен одним или несколькими R7;
каждый из RA, RB, RC, RD и RE независимо представляет собой водород или C1-C6алкил;
каждый R6 независимо представляет собой C1-C6алкил, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, арил или гетероарил, где каждый арил и гетероарил независимо и необязательно замещен одним или несколькими R8;
каждый R7 независимо представляет собой галоген, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
каждый R8 независимо представляет собой C1-C6алкил, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
n составляет 0, 1, 2, 3 или 4; и
x составляет 0, 1 или 2.
В некоторых вариантах осуществления COF2 характеризуется структурой формулы (I-a):
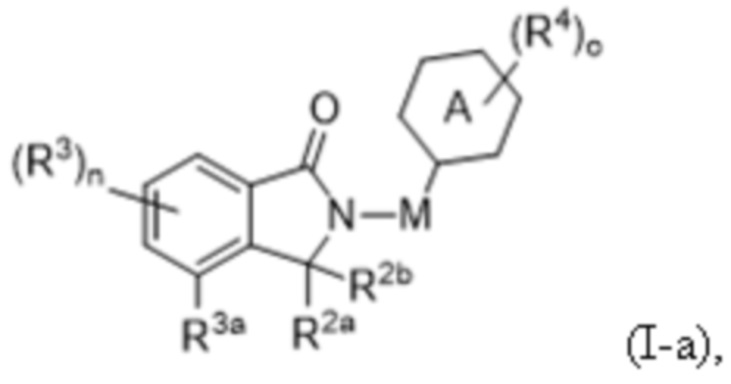
или ее фармацевтически приемлемой соли, сложного эфира, гидрата или таутомера, где:
кольцо A представляет собой карбоциклил, гетероциклил, арил или гетероарил, каждый из которых независимо и необязательно замещен одним или несколькими R4;
M отсутствует или представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил или C1-C6гетероалкил, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или несколькими R4;
каждый из R2a и R2b независимо представляет собой водород или C1-C6алкил; или R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу или тиокарбонильную группу;
R3a представляет собой водород, C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD) или -N(RC)S(O)xRE, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или несколькими R6;
каждый из R3 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD) или -N (RC)S(O)xRE, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или несколькими R6;
каждый R4 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, оксо, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, S(O)xRE, -S(O)xN(RC)(RD), -N (RC)S(O)xRE, карбоциклил, гетероциклил, арил или гетероарил, где каждый алкил, алкенил, алкинил, карбоциклил, гетероциклил, арил и гетероарил независимо и необязательно замещен одним или несколькими R7;
каждый из RA, RB, RC, RD и RE независимо представляет собой водород или C1-C6алкил;
каждый R6 независимо представляет собой C1-C6алкил, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, арил или гетероарил, где каждый арил и гетероарил независимо и необязательно замещен одним или несколькими R8;
каждый R7 независимо представляет собой галоген, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
каждый R8 независимо представляет собой C1-C6алкил, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
n составляет 0, 1, 2 или 3;
o составляет 0, 1, 2, 3, 4 или 5; и
x составляет 0, 1 или 2.
В некоторых вариантах осуществления COF2 представляет собой талидомид или его аналог или фармацевтически приемлемую соль. В некоторых вариантах осуществления COF2 выбрано из группы, состоящей из леналидомида, помалидомида, талидомида и 2-(4-(трет-бутил)фенил)-N-((2-(2,6-диоксопиперидин-3-ил)-1-оксоизоиндолин-5-ил)метил)ацетамида или их фармацевтически приемлемой соли.
В некоторых вариантах осуществления COF2 выбрано из группы, состоящей из:

или их фармацевтически приемлемой соли.
В некоторых вариантах осуществления COF2 представляет собой леналидомид или помалидомид или их фармацевтически приемлемую соль. В некоторых вариантах осуществления COF2 представляет собой леналидомид или его аналог или фармацевтически приемлемую соль. В некоторых вариантах осуществления COF2 представляет собой леналидомид или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления COF2 содержит структуру формулы (I):
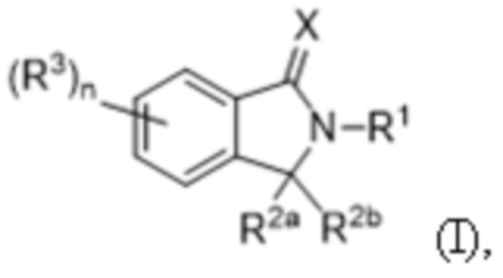
или ее фармацевтически приемлемую соль, сложный эфир, гидрат, сольват или таутомер, где:
X представляет собой O или S;
R1 представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, карбоциклил, гетероциклил, арил или гетероарил, каждый из которых независимо и необязательно замещен одним или несколькими R4;
каждый из R2a и R2b независимо представляет собой водород или C1-C6алкил; или R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу или тиокарбонильную группу;
каждый из R3 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD) или -N(RC)S(O)xRE, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или несколькими R6;
каждый R4 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, оксо, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD), -N (RC)S(O)xRE, карбоциклил, гетероциклил, арил или гетероарил, где каждый алкил, алкенил, алкинил, гетероалкил, карбоциклил, гетероциклил, арил и гетероарил независимо и необязательно замещен одним или несколькими R7;
каждый из RA, RB, RC, RD и RE независимо представляет собой водород или C1-C6алкил;
каждый R6 независимо представляет собой C1-C6алкил, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, арил или гетероарил, где каждый арил и гетероарил независимо и необязательно замещен одним или несколькими R8;
каждый R7 независимо представляет собой галоген, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
каждый R8 независимо представляет собой C1-C6алкил, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
n составляет 0, 1, 2, 3 или 4; и
x составляет 0, 1 или 2.
В некоторых вариантах осуществления COF2 содержит структуру формулы (I-a):

или ее фармацевтически приемлемую соль, сложный эфир, гидрат или таутомер, где:
кольцо A представляет собой карбоциклил, гетероциклил, арил или гетероарил, каждый из которых независимо и необязательно замещен одним или несколькими R4;
M отсутствует или представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил или C1-C6гетероалкил, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или несколькими R4;
каждый из R2a и R2b независимо представляет собой водород или C1-C6алкил; или R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу или тиокарбонильную группу;
R3a представляет собой водород, C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD) или -N(RC)S(O)xRE, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или несколькими R6;
каждый из R3 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD) или -N (RC)S(O)xRE, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или несколькими R6;
каждый R4 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, оксо, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, S(O)xRE, -S(O)xN(RC)(RD), -N (RC)S(O)xRE, карбоциклил, гетероциклил, арил или гетероарил, где каждый алкил, алкенил, алкинил, карбоциклил, гетероциклил, арил и гетероарил независимо и необязательно замещен одним или несколькими R7;
каждый из RA, RB, RC, RD и RE независимо представляет собой водород или C1-C6алкил;
каждый R6 независимо представляет собой C1-C6алкил, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, арил или гетероарил, где каждый арил и гетероарил независимо и необязательно замещен одним или несколькими R8;
каждый R7 независимо представляет собой галоген, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
каждый R8 независимо представляет собой C1-C6алкил, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
n составляет 0, 1, 2 или 3;
o составляет 0, 1, 2, 3, 4 или 5; и
x составляет 0, 1 или 2.
В некоторых вариантах осуществления COF2 содержит иммуномодулирующее лекарственное средство на основе имида (IMiD) или его фармацевтически приемлемую соль. В некоторых вариантах осуществления COF2 содержит талидомид или его аналог или фармацевтически приемлемую соль. В некоторых вариантах осуществления COF2 содержит леналидомид, помалидомид, талидомид и 2-(4-(трет-бутил)фенил)-N-((2-(2,6-диоксопиперидин-3-ил)-1-оксоизоиндолин-5-ил)метил)ацетамид или их фармацевтически приемлемую соль.
В некоторых вариантах осуществления COF2 содержит соединение, выбранное из группы, состоящей из:

или их фармацевтически приемлемой соли.
В некоторых вариантах осуществления COF2 содержит леналидомид или помалидомид или их фармацевтически приемлемую соль. В некоторых вариантах осуществления COF2 содержит леналидомид или его аналог или фармацевтически приемлемую соль. В некоторых вариантах осуществления COF2 содержит леналидомид или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления COF2 дополнительно содержит лиганд (например, где R10 в формуле (II) представляет собой L-метку). В некоторых вариантах осуществления R10 в формуле (II) представляет собой L-метку, при этом L представляет собой линкер, выбранный из линкера, раскрытого в публикации международной патентной заявки № WO2017/024318 (например, фигуры 28-31), а метка выбрана из лиганда, нацеливающегося на dTAG, раскрытого в публикации международной патентной заявки № WO2017/024318 (например, таблица T, страницы 119-129). В некоторых вариантах осуществления COF2 содержит IMiD (например, леналидомид или помалидомид или их фармацевтически приемлемую соль) и лиганд, где IMiD (например, леналидомид или помалидомид или их фармацевтически приемлемая соль) связаны с лигандом, например, через линкер. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид связывается с лигандом, и при этом связывание между COF2/CRBN-связывающим полипептидом и IMiD (например, леналидомидом или помалидомидом или их фармацевтически приемлемой солью) в отсутствие лиганда составляет не более 0,0001, 0,001, 0,01, 0,1, 1 или 10% от связывания между COF2/CRBN-связывающим полипептидом и лигандом, например, COF2/CRBN-связывающий полипептид не связывается с IMiD (например, леналидомидом или помалидомидом или их фармацевтически приемлемой солью), необязательно, где COF2/CRBN-связывающий полипептид выбран из dTAG, раскрытого в публикации международной патентной заявки № WO2017/024318 (например, страницы 36-65).
В одном аспекте данного документа представлен слитый полипептид, содержащий полипептид, связывающий соединение формулы (III) (COF3)/CRBN, и гетерологичный полипептид, где соединение формулы (III) представляет собой:
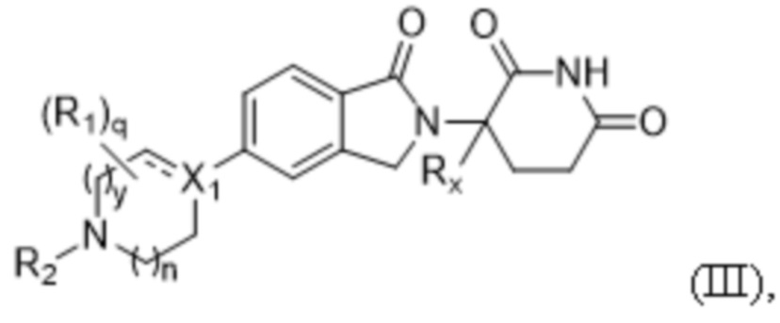
или его фармацевтически приемлемую соль, сложный эфир, гидрат, сольват или таутомер, где:
X1 представляет собой CR3;
 необязательно представляет собой двойную связь, если X1 представляет собой CR3 и R3 отсутствует;
необязательно представляет собой двойную связь, если X1 представляет собой CR3 и R3 отсутствует;
каждый R1 независимо представляет собой C1-C6алкил, C1-C6галогеналкил, C1-C6гидроксиалкил или галоген, или
два R1 вместе с атомами углерода, к которым они присоединены, образуют 5- или 6-членное гетероциклильное кольцо, или
два R1, когда они находятся при смежных атомах, вместе с атомами, к которым они присоединены, образуют C6-C10арил или 5- или 6-членное гетероарильное кольцо, содержащее 1-3 гетероатома, выбранные из O, N и S;
R2 представляет собой водород, C1-C6алкил, -C(O)C1-C6алкил, -C(O)(CH2)0-3-C6-C10арил, -C(O)O(CH2)0-3-C6-C10арил, C6-C10арил или 5- или 6-членный гетероарил, содержащий 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклил или 5-7-гетероциклил, содержащий 1-3 гетероатома, выбранные из O, N и S, где алкил необязательно замещен одним или несколькими R4; и арил, гетероарил, карбоциклил и гетероциклил необязательно замещены одним или несколькими R5, или
R1 и R2, когда они находятся при смежных атомах, вместе с атомами, к которым они присоединены, образуют 5- или 6-членное гетероциклильное кольцо;
R3 представляет собой водород, или R3 отсутствует, если  представляет собой двойную связь;
представляет собой двойную связь;
каждый R4 независимо выбран из -C(O)OR6, -C(O)NR6R6', -NR6C(O)R6', галогена, -OH, -NH2, циано, C6-C10арила, 5- или 6-членного гетероарила, содержащего 1-4 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклильного кольца, содержащего 1-3 гетероатома, выбранные из O, N и S, где арил, гетероарил, карбоциклил и гетероциклил необязательно замещены одним или несколькими R7;
каждый R5 независимо выбран из C1-C6алкила, C2-C6алкенила, C2-C6алкинила, C1-C6алкокси, C1-C6галогеналкила, C1-C6галогеналкокси, C1-C6гидроксиалкила, галогена, -OH, -NH2, циано, C3-C7карбоциклила, 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, C6-C10арила и 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, или
два R5, когда они находятся при смежных атомах, вместе с атомами, к которым они присоединены, образуют C6-C10арил или 5- или 6-членный гетероарил, содержащий 1-3 гетероатома, выбранные из O, N и S, необязательно замещенные одним или несколькими R10, или
два R5, когда они находятся при смежных атомах, вместе с атомами, к которым они присоединены, образуют C5-C7карбоциклил или 5-7-членный гетероциклил, содержащий 1-3 гетероатома, выбранные из O, N и S, необязательно замещенные одним или несколькими R10;
каждый R6 и R6' независимо представляет собой водород, C1-C6алкил или C6-C10арил;
каждый R7 независимо выбран из C1-C6алкила, C2-C6алкенила, C2-C6алкинила, C1-C6алкокси, C1-C6галогеналкила, C1-C6галогеналкокси, -C(O)R8, -(CH2)0-3C(O)OR8, -C(O)NR8R9, -NR8C(O)R9, -NR8C(O)OR9, -S(O)pNR8R9, -S(O)pR12, (C1-C6)гидроксиалкила, галогена, -OH, -O(CH2)1-3CN, -NH2, циано, -O(CH2)0-3-C6-C10арила, адамантила, -O(CH2)0-3-5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C6-C10арила, моноциклического или бициклического 5-10-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C7 карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где алкил необязательно замещен одним или несколькими R11, и арил, гетероарил и гетероциклил необязательно замещены одним или несколькими заместителями, каждый из которых независимо выбран из галогена, C1-C6алкила, C1-C6галогеналкила и C1-C6алкокси, или
два R7 вместе с атомом углерода, к которому они присоединены, образуют =(O), или
два R7, когда они находятся при смежных атомах, вместе с атомами, к которым они присоединены, образуют C6-C10арил или 5- или 6-членный гетероарил, содержащий 1-3 гетероатома, выбранные из O, N и S, необязательно замещенные одним или несколькими R10, или
два R7 вместе с атомами, к которым они присоединены, образуют C5-C7карбоциклил или 5-7-членный гетероциклил, содержащий 1-3 гетероатома, выбранные из O, N и S, необязательно замещенные одним или несколькими R10;
каждый R8 и R9 независимо представляет собой водород или C1-C6алкил;
каждый R10 независимо выбран из C1-C6алкила, C1-C6алкокси, C1-C6галогеналкила, C1-C6галогеналкокси, C1-C6гидроксиалкила, галогена, -OH, -NH2 и циано, или
два R10 вместе с атомом углерода, к которому они присоединены, образуют =(O);
каждый R11 независимо выбран из циано, C1-C6алкокси, C6-C10арила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где каждый арил и гетероциклил необязательно замещен одним или несколькими заместителями, каждый из которых независимо выбран из C1-C6алкила, C1-C6алкокси, C1-C6галогеналкила, C1-C6галогеналкокси, C1-C6гидроксиалкила, галогена, -OH, -NH2 и циано;
R12 представляет собой C1-C6алкил, C1-C6галогеналкил, C6-C10арил или 5-7-членный гетероциклил, содержащий 1-3 гетероатома, выбранные из O, N и S;
Rx представляет собой водород или дейтерий;
p составляет 0, 1 или 2;
n составляет 0, 1 или 2;
y составляет 1 или 2, где n+y≤3; и
q составляет 0, 1, 2, 3 или 4.
В одном варианте осуществления соединение формулы (III) представляет собой соединение формулы (III-b):
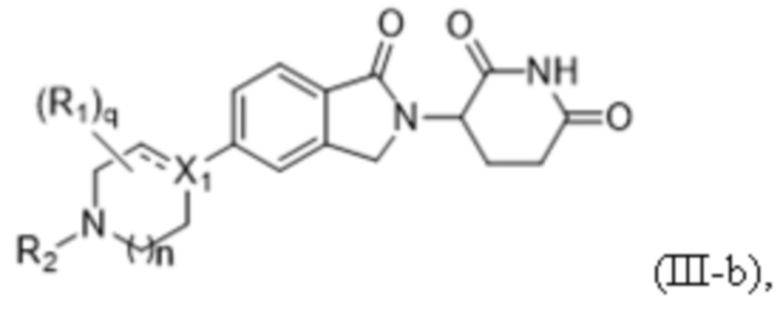
или его фармацевтически приемлемую соль, гидрат, сольват, пролекарство, стереоизомер и таутомер, где X1, R1, R2, n, q и их подпеременные определены, как описано выше для формулы (III).
В одном варианте осуществления соединение формулы (III) представляет собой соединение формулы (III-d):
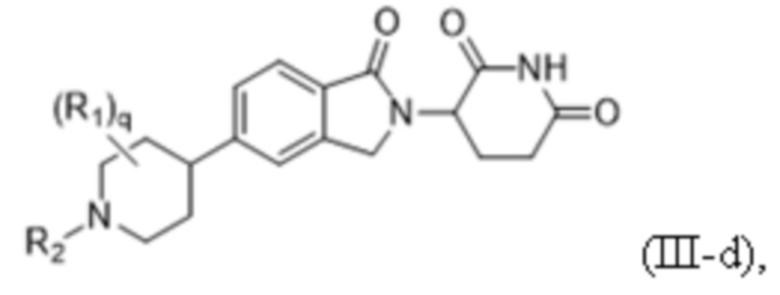
или его фармацевтически приемлемую соль, гидрат, сольват, пролекарство, стереоизомер и таутомер, где R1, R2, q, и их подпеременные определены, как описано выше для формулы (III).
В одном варианте осуществления COF3/CRBN-связывающий полипептид слит с гетерологичным полипептидом. В одном варианте осуществления COF3/CRBN-связывающий полипептид и гетерологичный полипептид связаны с помощью пептидной связи. В одном варианте осуществления COF3/CRBN-связывающий полипептид и гетерологичный полипептид связаны с помощью связи, отличной от пептидной связи. В одном варианте осуществления гетерологичный полипептид связан непосредственно с COF3/CRBN-связывающим полипептидом. В одном варианте осуществления гетерологичный полипептид связан опосредованно с COF3/CRBN-связывающим полипептидом. В одном варианте осуществления COF3/CRBN-связывающий полипептид и гетерологичный полипептид функционально связаны через линкер, например, глицин-сериновый линкер, например, линкер, содержащий аминокислотную последовательность под SEQ ID NO: 28. В одном варианте осуществления COF3/CRBN-связывающий полипептид связан с C-концом гетерологичного полипептида. В одном варианте осуществления COF3/CRBN-связывающий полипептид связан с N-концом гетерологичного полипептида.
В одном варианте осуществления ассоциация слитого полипептида с CRBN в отсутствие COF3 составляет, например, не более 0,01%, 0,1%, 1%, 5%, 10%, 15%, или 20% от ассоциации слитого полипептида с CRBN в присутствии COF3, например, избытка COF3, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации. В одном варианте осуществления слитый полипептид не связывается с CRBN в отсутствие COF3. В одном варианте осуществления убиквитинирование слитого полипептида в отсутствие COF3 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от убиквитинирования слитого полипептида в присутствии COF3, например, избытка COF3, например, как измерено с помощью анализа, описанного в данном документе. В одном варианте осуществления слитый полипептид подвергается убиквитинированию по одному или нескольким остаткам лизина или метионина в присутствии COF3. В одном варианте осуществления деградация слитого полипептида в отсутствие COF3 составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от деградации слитого полипептида в присутствии COF3, например, избытка COF3, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии. В одном варианте осуществления деградация слитого полипептида опосредуется убиквитинированием в присутствии COF3. В одном варианте осуществления ассоциация, убиквитинирование, и/или деградация измеряются в клетке млекопитающего, например, клетке человека.
В одном варианте осуществления COF3/CRBN-связывающий полипептид составляет от 10 до 95 аминокислотных остатков в длину, от 15 до 90 аминокислотных остатков в длину, от 20 до 85 аминокислотных остатков в длину, от 25 до 80 аминокислотных остатков в длину, от 30 до 75 аминокислотных остатков в длину, от 35 до 70 аминокислотных остатков в длину, от 40 до 65 аминокислотных остатков в длину, от 45 до 65 аминокислотных остатков в длину, от 50 до 65 аминокислотных остатков в длину или от 55 до 65 аминокислотных остатков в длину. В одном варианте осуществления COF3/CRBN-связывающий полипептид составляет 59 аминокислотных остатков в длину.
В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит бета-изгиб. В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит бета-шпильку. В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит бета-нить. В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит альфа-спираль. В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит в направлении от N-конца к C-концу: первую бета-нить, бета-шпильку, вторую бета-нить и первую альфа-спираль. В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит в направлении от N-конца к C-концу: первую бета-нить, бета-шпильку, вторую бета-нить, первую альфа-спираль и вторую альфа-спираль. В одном варианте осуществления бета-шпилька и вторая альфа-спираль разделены не более чем 60, 50, 40 или 30 аминокислотными остатками.
В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит COF3/CRBN-связывающую последовательность из встречающегося в природе полипептида или его COF3/CRBN-связывающего варианта. В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит COF3/CRBN-связывающую последовательность из встречающегося в природе полипептида IKZF или его COF3/CRBN-связывающего варианта. В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит COF3/CRBN-связывающую последовательность из встречающегося в природе IKZF2 или его COF3/CRBN-связывающего варианта. В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит две или более прерывистые последовательности из встречающегося в природе полипептида IKZF, например, встречающегося в природе IKZF2.
В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит аминокислотные остатки 130-174 из IKZF2 (пронумерованные в соответствии с SEQ ID NO: 21). В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 113. В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит последовательность, которая отличается от аминокислотных остатков 130-174 из IKZF2 (пронумерованных в соответствии с SEQ ID NO: 21) не более чем 1, 2, 3, 4, 5, 10, 15, 20, 25, 30, 35, или 40 аминокислотными остатками. В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит последовательность, которая отличается от аминокислотных остатков 130-174 из SEQ ID NO: 21 не более чем 1, 2, 3, 4, 5, 10, 15, 20, 25, 30, 35, или 40 аминокислотными остатками. В одном варианте осуществления COF3/CRBN-связывающий полипептид содержат последовательность, имеющую не более 1, 2, 3, 4, 5, 10, 15, 20, 25, 30, 35, или 40 аминокислотных замен по сравнению с аминокислотными остатками 130-174 из SEQ ID NO: 21.
В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит аминокислотные остатки 230-243 из IKZF2 (пронумерованные в соответствии с SEQ ID NO: 21). В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 114. В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит последовательность, которая отличается от аминокислотных остатков 230-243 из IKZF2 (пронумерованных в соответствии с SEQ ID NO: 21) не более чем 1, 2, 3, 4, 5 или 10 аминокислотными остатками. В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит последовательность, которая отличается от аминокислотных остатков 230-243 из SEQ ID NO: 21 не более чем 1, 2, 3, 4, 5 или 10 аминокислотными остатками. В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит последовательность, имеющую не более 1, 2, 3, 4, 5 или 10 аминокислотных замен по сравнению с аминокислотными остатками 230-243 из SEQ ID NO: 21.
В одном варианте осуществления неизмененным остается гистидин в положении 141, пронумерованном в соответствии с SEQ ID NO: 21.
В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит аминокислотные остатки 130-174 из IKZF2 (пронумерованные в соответствии с SEQ ID NO: 21). В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 113. В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит аминокислотные остатки 230-243 из IKZF2 (пронумерованные в соответствии с SEQ ID NO: 21). В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит аминокислотную последовательность под SEQ ID NO: 114. В одном варианте осуществления COF3/CRBN-связывающий полипептид содержит или состоит из аминокислотной последовательности под SEQ ID NO: 109.
В некоторых вариантах осуществления слитый полипептид дополнительно содержит домен деградации, где домен деградации отделен от COF3/CRBN-связывающего полипептида и гетерологичного полипептида с помощью гетерологичного сайта расщепления протеазами.
В некоторых вариантах осуществления слитый полипептид содержит в направлении от N-конца к C-концу:
i) домен деградации, гетерологичный сайт расщепления протеазами, гетерологичный полипептид и COF3/CRBN-связывающий полипептид;
ii) домен деградации, гетерологичный сайт расщепления протеазами, COF3/CRBN-связывающий полипептид и гетерологичный полипептид;
iii) COF3/CRBN-связывающий полипептид, гетерологичный полипептид, гетерологичный сайт расщепления протеазами и домен деградации; или
iv) гетерологичный полипептид и COF3/CRBN-связывающий полипептид, гетерологичный сайт расщепления протеазами и домен деградации.
В некоторых вариантах осуществления слитый полипептид содержит в направлении от N-конца к C-концу: домен деградации, гетерологичный сайт расщепления протеазами, гетерологичный полипептид и COF3/CRBN-связывающий полипептид.
В некоторых вариантах осуществления домен деградации имеет первое состояние, ассоциированное с первым уровнем экспрессии слитого полипептида, и второе состояние, ассоциированное со вторым уровнем экспрессии слитого полипептида, где второй уровень увеличивается, например, в по меньшей мере 2, 3, 4, 5, 10, 20 или 30 раз, по сравнению с первым уровнем в присутствии стабилизирующего соединения.
В некоторых вариантах осуществления в отсутствие стабилизирующего соединения слитый полипептид подвергается деградации под действием клеточного пути деградации, например, подвергается деградации по меньшей мере 50%, 60%, 70%, 80%, 90% или более слитого полипептида, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В некоторых вариантах осуществления уровень экспрессии и/или деградация измеряются в клетке млекопитающего, например, клетке человека.
В некоторых вариантах осуществления в присутствии стабилизирующего соединения:
i) домен деградации принимает конформацию, которая является более устойчивой к клеточной деградации относительно конформации в отсутствие стабилизирующего соединения; или
ii) конформация слитого полипептида более восприимчива к расщеплению в гетерологичном сайте расщепления протеазами относительно конформации в отсутствие стабилизирующего соединения.
В некоторых вариантах осуществления домен деградации выбран из домена эстрогенового рецептора (ER), домена белка FKB (FKBP) или домена дигидрофолатредуктазы (DHFR).
В некоторых вариантах осуществления домен деградации представляет собой домен эстрогенового рецептора (ER). В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность, которая на по меньшей мере 90, 95, 97, 98, 99 или 100% идентична SEQ ID NO: 46 или 48. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность под SEQ ID NO: 46. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность под SEQ ID NO: 48.
В некоторых вариантах осуществления стабилизирующее соединение представляет собой базедоксифен или 4-гидрокситамоксифен (4-OHT) или их фармацевтически приемлемую соль. В некоторых вариантах осуществления домен деградации представляет собой домен эстрогенового рецептора (ER), и стабилизирующее соединение представляет собой базедоксифен или его фармацевтически приемлемую соль. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность под SEQ ID NO: 46, и стабилизирующее соединение представляет собой базедоксифен или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления домен деградации представляет собой домен белка FKB (FKBP). В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность, которая на по меньшей мере 90, 95, 97, 98, 99 или 100% идентична SEQ ID NO: 50. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность под SEQ ID NO: 50. В некоторых вариантах осуществления стабилизирующее соединение представляет собой Shield-1 или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления домен деградации представляет собой домен дигидрофолатредуктазы (DHFR). В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность, которая на по меньшей мере 90, 95, 97, 98, 99 или 100% идентична SEQ ID NO: 51. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность под SEQ ID NO: 51. В некоторых вариантах осуществления стабилизирующее соединение представляет собой триметоприм или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами расщепляется под действием внутриклеточной протеазы млекопитающего. В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами расщепляется под действием протеазы, выбранной из группы, состоящей из фурина, PCSK1, PCSK5, PCSK6, PCSK7, катепсина B, гранзима B, фактора XA, энтерокиназы, гененазы, сортазы, протеазы precission, тромбина, протеазы TEV и эластазы-1. В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами содержит последовательность, имеющую мотив расщепления, выбранный из группы, состоящей из консенсусного мотива RX(K/R)R (X может быть любой аминокислотой; SEQ ID NO: 52), консенсусного мотива RXXX[KR]R (X может быть любой аминокислотой; SEQ ID NO: 53), консенсусного мотива RRX (SEQ ID NO: 54), консенсусного мотива I-E-P-D-X (SEQ ID NO: 55), Ile-Glu/Asp-Gly-Arg (SEQ ID NO: 56), Asp-Asp-Asp-Asp-Lys (SEQ ID NO: 57), Pro-Gly-Ala-Ala-His-Tyr (SEQ ID NO: 58), консенсусного мотива LPXTG/A (SEQ ID NO: 59), Leu-Glu-Val-Phe-Gln-Gly-Pro (SEQ ID NO: 60), Leu-Val-Pro-Arg-Gly-Ser (SEQ ID NO: 61), E-N-L-Y-F-Q-G (SEQ ID NO: 62) и [AGSV]-X (X может быть любой аминокислотой; SEQ ID NO: 63). В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами расщепляется под действием фурина. В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами содержит сайт расщепления фурином, выбранный из группы, состоящей из RTKR (SEQ ID NO: 123); GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125); GTGAEDPRPSRKRR (SEQ ID NO: 127); LQWLEQQVAKRRTKR (SEQ ID NO: 129); GTGAEDPRPSRKRRSLGG (SEQ ID NO: 131); GTGAEDPRPSRKRRSLG (SEQ ID NO: 133); SLNLTESHNSRKKR (SEQ ID NO: 135); CKINGYPKRGRKRR (SEQ ID NO: 137) и SARNRQKR (SEQ ID NO: 34). В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами не содержит аминокислотную последовательность SARNRQKR (SEQ ID NO: 34). В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами содержит сайт расщепления фурином GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125). В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами расщепляется под действием внеклеточной протеазы млекопитающего. В некоторых вариантах осуществления внеклеточная протеаза млекопитающего выбрана из группы, состоящей из фактора XA, энтерокиназы, гененазы, сортазы, протеазы precission, тромбина, протеазы TEV и эластазы-1. В некоторых вариантах осуществления гетерологичный сайт расщепления протеазами содержит аминокислотную последовательность, выбранную из группы, состоящей из Ile-Glu/Asp-Gly-Arg (SEQ ID NO: 56), Asp-Asp-Asp-Asp-Lys (SEQ ID NO: 57), Pro-Gly-Ala-Ala-His-Tyr (SEQ ID NO: 58), консенсусного мотива LPXTG/A (SEQ ID NO: 59), Leu-Glu-Val-Phe-Gln-Gly-Pro (SEQ ID NO: 60), Leu-Val-Pro-Arg-Gly-Ser (SEQ ID NO: 61), E-N-L-Y-F-Q-G (SEQ ID NO: 62) и [AGSV]-X (X может быть любой аминокислотой; SEQ ID NO: 63).
В определенных вариантах осуществления вышеуказанных аспектов гетерологичный полипептид выбран из цитоплазматического и/или ядерного полипептида или трансмембранного полипептида, например, гетерологичного полипептида из таблицы 2. В некоторых вариантах осуществления цитоплазматический и/или ядерный полипептид выбран из группы, состоящей из компонента пути апоптоза (например, каспазы 9), компонента системы CRISPR/Cas (например, Cas9), транскрипционного фактора (например, MITF, c-Myc, STAT3, STAT5, NF-каппа-B, бета-катенина, Notch, GLI или c-JUN), Tet-метилцитозиндиоксигеназы-2 (TET2), FKBP и тау-белка. В некоторых вариантах осуществления трансмембранный полипептид выбран из группы, состоящей из CD62L, CCR1, CCR2, CCR5, CCR7, CCR10, CXCR2, CXCR3, CXCR4, CXCR6, CTLA4, PD1, BTLA, VISTA, CD137L, CD80, CD86, TIGIT, CD3, CD8, CD19, CD22, CD20, BCMA и химерного антигенного рецептора (CAR). В некоторых вариантах осуществления гетерологичный полипептид выбран из группы, состоящей из химерного антигенного рецептора (CAR), компонента системы CRISPR/Cas (например, Cas9), CD8, CD19 и CD22.
В некоторых вариантах осуществления гетерологичный полипептид представляет собой химерный антигенный рецептор (CAR). В некоторых вариантах осуществления CAR содержит в направлении от N-конца к C-концу: антигенсвязывающий домен, трансмембранный домен и один или несколько внутриклеточных сигнальных доменов. В некоторых вариантах осуществления внутриклеточный сигнальный домен содержит один или несколько первичных сигнальных доменов. В некоторых вариантах осуществления внутриклеточный сигнальный домен содержит один или несколько костимулирующих сигнальных доменов. В некоторых вариантах осуществления один из одного или нескольких первичных сигнальных доменов содержит стимулирующий домен CD3-дзета. В некоторых вариантах осуществления один или несколько из костимулирующих сигнальных доменов представляют собой внутриклеточный домен из костимулирующего белка, выбранного из группы, состоящей из CD27, CD28, 4-1BB (CD137), OX40, GITR, CD30, CD40, ICOS, BAFFR, HVEM, ICAM-1, лимфоцитарного функционально-ассоциированного антигена-1 (LFA-1), CD2, CDS, CD7, CD287, LIGHT, NKG2C, NKG2D, SLAMF7, NKp80, NKp30, NKp44, NKp46, CD160, B7-H3 и лиганда, который специфически связывается с CD83. В некоторых вариантах осуществления один или несколько из указанных костимулирующих сигнальных доменов содержат костимулирующий домен 4-1BB. В некоторых вариантах осуществления один или несколько из указанных костимулирующих сигнальных доменов содержат костимулирующий домен CD28. В некоторых вариантах осуществления антигенсвязывающий домен представляет собой scFv.
В некоторых вариантах осуществления антигенсвязывающий домен связывает антиген, выбранный из группы, состоящей из CD19; CD123; CD22; CD30; CD171; CS-1; лектиноподобной молекулы-1 C-типа, CD33; варианта III рецептора эпидермального фактора роста (EGFRvIII); ганглиозида G2 (GD2); ганглиозида GD3; представителя семейства рецепторов TNF; антигена созревания B-клеток; Tn-антигена ((Tn Ag) или (GalNAcα-Ser/Thr)); простатического специфического мембранного антигена (PSMA); орфанного рецептора-1, подобного рецепторной тирозинкиназе (ROR1); Fms-подобной тирозинкиназы 3 (FLT3); опухолеассоциированного гликопротеина-72 (TAG72); CD38; CD44v6; раково-эмбрионального антигена (CEA); молекулы адгезии эпителиальных клеток (EPCAM); B7H3 (CD276); KIT (CD117); субъединицы альфа-2 рецептора интерлейкина-13; мезотелина; альфа-субъединицы рецептора интерлейкина-11 (IL-11Ra); антигена стволовых клеток предстательной железы (PSCA); сериновой протеазы-21; рецептора-2 фактора роста эндотелия сосудов (VEGFR2); антигена системы Льюис (Y); CD24; рецептора фактора роста тромбоцитов бета-типа (PDGFR-бета); стадиеспецифического эмбрионального антигена-4 (SSEA-4); CD20; рецептора фолиевой кислоты альфа-типа; рецепторной тирозинпротеинкиназы ERBB2 (Her2/neu); муцина-1, ассоциированного с клеточной поверхностью (MUC1); рецептора эпидермального фактора роста (EGFR); молекулы адгезии нейронов (NCAM); простазы; простатической кислой фосфатазы (PAP); мутантного фактора элонгации 2 (ELF2M); эфрина B2; белка активации фибробластов альфа (FAP); рецептора инсулиноподобного фактора роста-1 (рецептора IGF-I), карбоангидразы IX (CAIX); субъединицы-9 протеасомы (просомы, мультикаталитической протеазы) бета-типа (LMP2); гликопротеина 100 (gp100); онкогенного полипептида, состоящего из кластерного региона точечных разрывов (BCR) и гомолога-1 вирусного онкогена лейкоза мышей Абельсона (Abl) (bcr-abl); тирозиназы; эфринового рецептора-2 A-типа (EphA2); фукозил-GM1; молекулы адгезии, представляющей собой сиалилированный антиген системы Льюис (sLe); ганглиозида GM3; трансглютаминазы-5 (TGS5); высокомолекулярного меланома-ассоциированного антигена (HMWMAA); ганглиозида o-ацетил-GD2 (OAcGD2); рецептора фолиевой кислоты бета-типа; маркера-1 эндотелия опухоли (TEM1/CD248); белка, родственного маркеру-7 эндотелия опухоли (TEM7R); клаудина-6 (CLDN6); рецептора тиреотропного гормона (TSHR); представителя D группы 5 класса С рецепторов, сопряженных с G-белком (GPRC5D); белка, кодируемого открытой рамкой считывания 61 X-хромосомы (CXORF61); CD97; CD179a; киназы анапластической лимфомы (ALK); полисиаловой кислоты; плацентоспецифического белка-1 (PLAC1); гексасахаридной части гликоцерамида globoH (GloboH); дифференцировочного антигена молочной железы (NY-BR-1); уроплакина-2 (UPK2); клеточного рецептора-1 вируса гепатита A (HAVCR1); бета-3 адренорецептора (ADRB3); паннексина-3 (PANX3); рецептора-20, сопряженного с G-белком (GPR20); антигена локуса K9 комплекса лимфоцитарных антигенов 6 (LY6K); обонятельного рецептора 51E2 (OR51E2); белка, кодируемого альтернативной рамкой считывания гена TCR-гамма (TARP); белка опухоли Вильмса (WT1); раково-тестикулярного антигена-1 (NY-ESO-1); раково-тестикулярного антигена-2 (LAGE-1a); меланома-ассоциированного антигена-1 (MAGE-A1); белка, кодируемого транслокационным вариантом-6 гена ETS, локализованным в р-плече 12 хромосомы (ETV6-AML); белка-17 сперматозоидов (SPA17); представителя 1А семейства X-антигенов (XAGE1); ангиопоэтин-связывающего рецептора-2 клеточной поверхности 2 (Tie 2); раково-тестикулярного антигена-1 из клеток меланомы (MAD-CT-1); раково-тестикулярного антигена-2 из клеток меланомы (MAD-CT-2); Fos-родственного антигена-1; опухолевого белка p53 (p53); мутанта p53; простеина; сурвивина; теломеразы; опухолевого антигена-1 карциномы предстательной железы, антигена-1 меланомы, распознаваемого T-клетками; мутантного белка саркомы крыс (Ras); обратной транскриптазы теломеразы человека (hTERT); антигенов саркомы с точечными разрывами при транслокации; меланомного ингибитора апоптоза (ML-IAP); ERG (продукта слитого гена трансмембранной сериновой протеазы-2 (TMPRSS2) и ETS); N-ацетилглюкозаминилтрансферазы V (NA17); белка с парным box-доменом Рах-3 (PAX3); андрогенового рецептора; циклина-B1; нейробластомного гомолога вирусного онкогена миелоцитоматоза птиц v-myc (MYCN); представителя С семейства гомологов Ras (RhoC); белка-2, родственного тирозиназе (TRP-2); цитохрома P450 1B1 (CYP1B1); белка, подобного CCCTC-связывающему фактору (белку с "цинковыми пальцами"), антигена плоскоклеточной карциномы 3, распознаваемого Т-клетками (SART3); белка с парным box-доменом Рах-5 (PAX5); проакрозин-связывающего белка sp32 (OY-TES1); лимфоцит-специфической протеинтирозинкиназы (LCK); якорного белка-4 киназы A (AKAP-4); антигена 2 синовиальной саркомы с точечным разрывом в X-хромосоме (SSX2); рецептора конечных продуктов неферментативного гликозилирования (RAGE-1); почечного убиквитарного белка-1 (RU1); почечного убиквитарного белка-2 (RU2); легумаина; Е6 вируса папилломы человека (HPV E6); Е7 вируса папилломы человека (HPV E7); кишечной карбоксилэстеразы; мутантного белка теплового шока 70-2 (mut hsp70-2); CD79a; CD79b; CD72; иммуноглобулиноподобного рецептора-1, ассоциированного с лейкоцитами (LAIR1); рецептора Fc-фрагмента IgA (FCAR или CD89); представителя 2 подсемейства А иммуноглобулиноподобных рецепторов лейкоцитов (LILRA2); представителя f семейства белков, подобных молекулам CD300 (CD300LF); представителя А семейства 12 лектиновых доменов С-типа (CLEC12A); антигена-2 клеток стромы костного мозга (BST2); белка-2, подобного муциноподобному рецептору гормонов, содержащему EGF-подобный модуль (EMR2); лимфоцитарного антигена-75 (LY75); глипикана-3 (GPC3); белка-5, подобного Fc-рецептору (FCRL5); и полипептида-1, подобного лямбда-цепи иммуноглобулина (IGLL1). В некоторых вариантах осуществления антиген выбран из CD19, CD22, BCMA, CD20, CD123, EGFRvIII или мезотелина. В некоторых вариантах осуществления антиген представляет собой CD19. В некоторых вариантах осуществления антиген представляет собой CD22. В некоторых вариантах осуществления антиген представляет собой BCMA. В некоторых вариантах осуществления антиген представляет собой CD20. В некоторых вариантах осуществления антиген представляет собой CD123. В некоторых вариантах осуществления антиген представляет собой EGFRvIII.
В одном аспекте данного документа представлена молекула нуклеиновой кислоты, кодирующая слитый полипептид, раскрытый в данном документе. В другом аспекте данного документа представлен вектор, содержащий молекулу нуклеиновой кислоты. В некоторых вариантах осуществления вектор представляет собой вирусный вектор. В некоторых вариантах осуществления вектор представляет собой лентивирусный вектор. В другом аспекте данного документа представлена вирусная частица, содержащая вектор.
В другом аспекте данного документа представлена клетка, например, клетка-хозяин, содержащая слитый полипептид, раскрытый в данном документе, молекулу нуклеиновой кислоты, раскрытую в данном документе, или вектор, раскрытый в данном документе. В некоторых вариантах осуществления клетка, например, клетка-хозяин, представляет собой клетку млекопитающего, например, клетку человека, например, эффекторную клетку человека, например, T-клетку человека или NK-клетку человека.
В некоторых вариантах осуществления клетка, например, клетка-хозяин, представляет собой клетку, экспрессирующую CAR, например, CAR-T-клетку. В некоторых вариантах осуществления клетка, например, клетка-хозяин, содержит компонент системы CRISPR/Cas. В некоторых вариантах осуществления клетка, например, клетка-хозяин, представляет собой раковую клетку человека, например, опухолевую клетку человека.
В некоторых вариантах осуществления клетка, например, клетка-хозяин, содержит комплекс убиквитинлигазы, например, комплекс убиквитинлигазы E3, где комплекс убиквитинлигазы содержит CRBN.
В некоторых вариантах осуществления клетка содержит слитый полипептид, раскрытый в данном документе (например, слитый полипептид, содержащий COF1/CRBN-связывающий полипептид и гетерологичный полипептид), где при приведении клетки в контакт с COF1, например, избытком COF1:
i) ассоциация COF1/CRBN-связывающего полипептида с CRBN увеличивается, например, в по меньшей мере 10, 50, 100, 1000 или 10000 раз, по сравнению с ассоциацией COF1/CRBN-связывающего полипептида с CRBN при отсутствии приведения клетки в контакт с COF1, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
ii) ассоциация слитого полипептида с CRBN увеличивается, например, в по меньшей мере 10, 50, 100, 1000 или 10000 раз, по сравнению с ассоциацией слитого полипептида с CRBN при отсутствии приведения клетки в контакт с COF1, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
iii) убиквитинирование гетерологичного полипептида увеличивается, например, в по меньшей мере 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, по сравнению с убиквитинированием гетерологичного полипептида при отсутствии приведения клетки в контакт с COF1, например, как измерено с помощью анализа, описанного в данном документе;
iv) убиквитинирование слитого полипептида увеличивается, например, в по меньшей мере 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, по сравнению с убиквитинированием слитого полипептида при отсутствии приведения клетки в контакт с COF1, например, как измерено с помощью анализа, описанного в данном документе;
v) деградация слитого полипептида увеличивается, например, в по меньшей мере 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, по сравнению с деградацией слитого полипептида при отсутствии приведения клетки в контакт с COF1, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии; или
vi) уровень экспрессии слитого полипептида составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от уровня экспрессии слитого полипептида при отсутствии приведения клетки в контакт с COF1, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В некоторых вариантах осуществления клетка дополнительно содержит COF1, например, леналидомид или помалидомид или их фармацевтически приемлемую соль.
В некоторых вариантах осуществления клетка содержит слитый полипептид, раскрытый в данном документе (например, слитый полипептид, содержащий COF3/CRBN-связывающий полипептид и гетерологичный полипептид), где при приведении клетки в контакт с COF3, например, избытком COF3:
i) ассоциация COF3/CRBN-связывающего полипептида с CRBN увеличивается, например, в по меньшей мере 10, 50, 100, 1000 или 10000 раз, по сравнению с ассоциацией COF3/CRBN-связывающего полипептида с CRBN при отсутствии приведения клетки в контакт с COF3, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
ii) ассоциация слитого полипептида с CRBN увеличивается, например, в по меньшей мере 10, 50, 100, 1000 или 10000 раз, по сравнению с ассоциацией слитого полипептида с CRBN при отсутствии приведения клетки в контакт с COF3, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
iii) убиквитинирование гетерологичного полипептида увеличивается, например, в по меньшей мере 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, по сравнению с убиквитинированием гетерологичного полипептида при отсутствии приведения клетки в контакт с COF3, например, как измерено с помощью анализа, описанного в данном документе;
iv) убиквитинирование слитого полипептида увеличивается, например, в по меньшей мере 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, по сравнению с убиквитинированием слитого полипептида при отсутствии приведения клетки в контакт с COF3, например, как измерено с помощью анализа, описанного в данном документе;
v) деградация слитого полипептида увеличивается, например, в по меньшей мере 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, по сравнению с деградацией слитого полипептида при отсутствии приведения клетки в контакт с COF3, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии; или
vi) уровень экспрессии слитого полипептида составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от уровня экспрессии слитого полипептида при отсутствии приведения клетки в контакт с COF3, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В некоторых вариантах осуществления клетка дополнительно содержит COF3, например, соединение, раскрытое в таблице 29, или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления клетка содержит слитый полипептид, раскрытый в данном документе (например, слитый полипептид, содержащий COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид, гетерологичный полипептид и домен деградации), где в отсутствие стабилизирующего соединения слитый полипептид подвергается деградации под действием клеточного пути деградации, например, подвергается деградации по меньшей мере 50%, 60%, 70%, 80%, 90% или более слитого полипептида, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В некоторых вариантах осуществления слитый полипептид дополнительно содержит гетерологичный сайт расщепления протеазами. В некоторых вариантах осуществления клетка дополнительно содержит протеазу, способную к расщеплению гетерологичного сайта расщепления протеазами.
В некоторых вариантах осуществления клетка содержит слитый полипептид, раскрытый в данном документе (например, слитый полипептид, содержащий COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид, гетерологичный полипептид и домен деградации), где при приведении клетки в контакт со стабилизирующим соединением, например, избытком стабилизирующего соединения:
i) домен деградации принимает конформацию, которая является более устойчивой к клеточной деградации относительно конформации в отсутствие стабилизирующего соединения;
ii) конформация слитого полипептида более восприимчива к расщеплению в гетерологичном сайте расщепления протеазами относительно конформации в отсутствие стабилизирующего соединения; или
iii) уровень экспрессии слитого полипептида увеличивается, например, в по меньшей мере 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, по сравнению с уровнем экспрессии слитого полипептида при отсутствии приведения клетки в контакт со стабилизирующим соединением, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В некоторых вариантах осуществления клетка дополнительно содержит стабилизирующее соединение. В некоторых вариантах осуществления стабилизирующее соединение представляет собой базедоксифен или его фармацевтически приемлемую соль. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность под SEQ ID NO: 46.
В некоторых вариантах осуществления клетка содержит слитый полипептид, раскрытый в данном документе (например, слитый полипептид, содержащий COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид, гетерологичный полипептид и домен деградации), где при приведении клетки в контакт как со стабилизирующим соединением, например, избытком стабилизирующего соединения, так и с COF1, COF2 или COF3, например, избытком COF1, COF2 или COF3:
i) ассоциация COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающего полипептида с CRBN увеличивается, например, в по меньшей мере 10, 50, 100, 1000 или 10000 раз, по сравнению с ассоциацией COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающего полипептида с CRBN при приведении клетки в контакт только со стабилизирующим соединением, но не с COF1, COF2 или COF3, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
ii) ассоциация слитого полипептида с CRBN увеличивается, например, в по меньшей мере 10, 50, 100, 1000 или 10000 раз, по сравнению с ассоциацией слитого полипептида с CRBN при приведении клетки в контакт только со стабилизирующим соединением, но не COF1, COF2 или COF3, например, как измерено с помощью анализа, описанного в данном документе, например, иммунопреципитации;
iii) убиквитинирование гетерологичного полипептида увеличивается, например, в по меньшей мере 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, по сравнению с убиквитинированием гетерологичного полипептида при приведении клетки в контакт только со стабилизирующим соединением, но не с COF1, COF2 или COF3, например, как измерено с помощью анализа, описанного в данном документе;
iv) убиквитинирование слитого полипептида увеличивается, например, в по меньшей мере 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, по сравнению с убиквитинированием слитого полипептида при приведении клетки в контакт только со стабилизирующим соединением, но не с COF1, COF2 или COF3, например, как измерено с помощью анализа, описанного в данном документе;
v) деградация слитого полипептида увеличивается, например, в по меньшей мере 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, по сравнению с деградацией слитого полипептида при приведении клетки в контакт только со стабилизирующим соединением, но не с COF1, COF2 или COF3, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии; или
vi) уровень экспрессии слитого полипептида составляет, например, не более 0,01%, 0,1%, 1%, 10%, 20%, 30%, 40%, 50%, 60%, или 70% от уровня экспрессии слитого полипептида при приведении клетки в контакт только со стабилизирующим соединением, но не с COF1, COF2 или COF3, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В некоторых вариантах осуществления клетка дополнительно содержит COF1 (например, леналидомид или помалидомид или их фармацевтически приемлемую соль), COF2 (например, леналидомид или помалидомид или их фармацевтически приемлемую соль) или COF3 (соединение, раскрытое в таблице 29, или его фармацевтически приемлемую соль).
В некоторых вариантах осуществления гетерологичный полипептид представляет собой химерный антигенный рецептор (CAR), необязательно, где CAR содержит в направлении от N-конца к C-концу: антигенсвязывающий домен, трансмембранный домен и один или несколько внутриклеточных сигнальных доменов.
В одном аспекте, в данном документе раскрыта фармацевтическая композиция, содержащая слитый полипептид, раскрытый в данном документе, или клетку, раскрытую в данном документе, и фармацевтически приемлемый носитель, вспомогательное вещество или стабилизатор.
В одном аспекте данного документа раскрыт способ получения клетки, раскрытой в данном документе.
В одном аспекте данного документа раскрыт способ деградации слитого полипептида, раскрытого в данном документе (например, слитого полипептида, содержащего COF1/CRBN-связывающий полипептид и гетерологичный полипептид (например, CAR-полипептид)), предусматривающий приведение слитого полипептида или клетки, содержащей указанный слитый полипептид, в контакт с COF1 (например, леналидомидом или помалидомидом или их фармацевтически приемлемой солью). В некоторых вариантах осуществления в присутствии COF1 (например, леналидомида или помалидомида или их фармацевтически приемлемой соли) уровень экспрессии указанного слитого полипептида значительно уменьшается, например, на по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, или 100 процентов, относительно уровня экспрессии указанного слитого полипептида в отсутствие COF1 (например, леналидомида или помалидомида или их фармацевтически приемлемой соли), например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии. В некоторых вариантах осуществления слитый полипептид или клетку приводят в контакт с COF1 (например, леналидомидом или помалидомидом или их фармацевтически приемлемой солью) ex vivo. В некоторых вариантах осуществления слитый полипептид или клетку приводят в контакт с COF1 (например, леналидомидом или помалидомидом или их фармацевтически приемлемой солью) in vivo.
В одном аспекте данного документа раскрыт способ регуляции экспрессии слитого полипептида, раскрытого в данном документе (например, слитого полипептида, содержащего COF1/CRBN- или COF2/CRBN-связывающий полипептида, гетерологичный полипептид (например, CAR-полипептид) и домен деградации), предусматривающий:
i) приведение слитого полипептида или клетки, содержащей слитый полипептид, в контакт со стабилизирующим соединением, необязательно, где в присутствии стабилизирующего соединения:
a) домен деградации принимает конформацию, которая является более устойчивой к клеточной деградации относительно конформации в отсутствие стабилизирующего соединения;
b) конформация слитого полипептида более восприимчива к расщеплению в гетерологичном сайте расщепления протеазами относительно конформации в отсутствие стабилизирующего соединения; или
c) уровень экспрессии слитого полипептида увеличивается, например, в по меньшей мере 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, по сравнению с уровнем экспрессии слитого полипептида в отсутствие стабилизирующего соединения, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии i):
ii) приведение слитого полипептида или клетки, содержащей слитый полипептид, в контакт с COF1 (например, леналидомидом или помалидомидом или их фармацевтически приемлемой солью) или COF2 (например, леналидомидом или помалидомидом или их фармацевтически приемлемой солью), необязательно, где в присутствии COF1 или COF2 уровень экспрессии слитого полипептида значительно уменьшается, например, на по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, или 100 процентов, относительно уровня экспрессии слитого полипептида после стадии i) и перед стадией ii), например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В некоторых вариантах осуществления стабилизирующее соединение представляет собой базедоксифен или его фармацевтически приемлемую соль. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность под SEQ ID NO: 46.
В некоторых вариантах осуществления слитый полипептид или клетку приводят в контакт с COF1 или COF2 (например, леналидомидом или помалидомидом или их фармацевтически приемлемой солью) и/или стабилизирующим соединением ex vivo. В некоторых вариантах осуществления слитый полипептид или клетку приводят в контакт с COF1 или COF2 (например, леналидомидом или помалидомидом или их фармацевтически приемлемой солью) и/или стабилизирующим соединением in vivo.
В некоторых вариантах осуществления гетерологичный полипептид представляет собой химерный антигенный рецептор (CAR). В некоторых вариантах осуществления CAR содержит в направлении от N-конца к C-концу: антигенсвязывающий домен, трансмембранный домен и один или несколько внутриклеточных сигнальных доменов.
В одном аспекте данного документа раскрыт способ получения клетки, предусматривающий:
i) обеспечение клетки, содержащей молекулу нуклеиновой кислоты, кодирующую слитый полипептид, содержащий полипептид, связывающий соединение формулы 1 (COF1)/CRBN, и химерный антигенный рецептор (CAR), необязательно, где CAR содержит в направлении от N-конца к C-концу: антигенсвязывающий домен, трансмембранный домен и один или несколько внутриклеточных сигнальных доменов; и
ii) приведение клетки в контакт с COF1 ex vivo, необязательно, где:
в присутствии COF1 уровень экспрессии слитого полипептида значительно уменьшается, например, на по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, или 100 процентов, относительно уровня экспрессии слитого полипептида в отсутствие COF1, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии, где соединение формулы (I) представляет собой:

или его фармацевтически приемлемую соль, сложный эфир, гидрат, сольват или таутомер, где:
X представляет собой O или S;
R1 представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, карбоциклил, гетероциклил, арил или гетероарил, каждый из которых независимо и необязательно замещен одним или несколькими R4;
каждый из R2a и R2b независимо представляет собой водород или C1-C6алкил; или R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу или тиокарбонильную группу;
каждый из R3 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD) или -N(RC)S(O)xRE, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или несколькими R6;
каждый R4 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, оксо, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD), -N (RC)S(O)xRE, карбоциклил, гетероциклил, арил или гетероарил, где каждый алкил, алкенил, алкинил, гетероалкил, карбоциклил, гетероциклил, арил и гетероарил независимо и необязательно замещен одним или несколькими R7;
каждый из RA, RB, RC, RD и RE независимо представляет собой водород или C1-C6алкил;
каждый R6 независимо представляет собой C1-C6алкил, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, арил или гетероарил, где каждый арил и гетероарил независимо и необязательно замещен одним или несколькими R8;
каждый R7 независимо представляет собой галоген, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
каждый R8 независимо представляет собой C1-C6алкил, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
n составляет 0, 1, 2, 3 или 4; и
x составляет 0, 1 или 2.
В некоторых вариантах осуществления после приведения клетки в контакт с COF1 ex vivo пролиферация клетки увеличивается, например, в по меньшей мере 1,2, 1,5, 2, 5 или 10 раз, по сравнению с пролиферацией клетки до приведения ее в контакт с COF1. В некоторых вариантах осуществления COF1 представляет собой леналидомид или помалидомид или их фармацевтически приемлемую соль. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид содержит или состоит из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 1-6, 11-15, 40, 41-43, 77, 78, 84-86, и 100 (например, COF1/CRBN-связывающий полипептид содержит или состоит из аминокислотной последовательности под SEQ ID NO: 3).
В одном аспекте данного документа представлен способ лечения субъекта, у которого имеется заболевание, ассоциированное с экспрессией опухолевого антигена, предусматривающий:
i) приведение клетки, раскрытой в данном документе (например, клетки, содержащей слитый полипептид, содержащий COF1/CRBN-связывающий полипептид и гетерологичный полипептид (например, полипептид CAR)), в контакт с COF1 ex vivo, необязательно, где:
в присутствии COF1 уровень экспрессии слитого полипептида уменьшается, например, на по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, или 100 процентов, относительно уровня экспрессии слитого полипептида перед приведением клетки в контакт с COF1 ex vivo, и
ii) введение субъекту эффективного количества клетки, необязательно, где способ дополнительно предусматривает после стадии i) и до стадии ii):
снижение количества COF1, контактирующего с клеткой, например, внутри клетки и/или в ее окружении,
за счет чего осуществляется лечение заболевания.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии ii):
iii) введение субъекту эффективного количества COF1, необязательно, где введение COF1 уменьшает, например, на по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, или 100 процентов, уровень экспрессии слитого полипептида относительно уровня экспрессии слитого полипептида после стадии ii) и до стадии iii), необязательно, где:
a) у субъекта развилась нежелательная реакция, она развивается или ожидается ее развитие,
b) введение COF1 осуществляют в ответ на возникновение нежелательной реакции у субъекта или в ответ на ожидание возникновения нежелательной реакции у субъекта, и/или
c) введение COF1 снижает или предупреждает нежелательный эффект.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии iii):
iv) прекращение введения COF1, необязательно, где прекращение введения COF1 увеличивает, например, в по меньшей мере приблизительно 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, уровень экспрессии слитого полипептида относительно уровня экспрессии слитого полипептида после стадии iii) и до стадии iv) (например, где прекращение введения COF1 восстанавливает уровень экспрессии слитого полипептида до уровня экспрессии после стадии ii) и до стадии iii)), необязательно, где:
a) у субъекта произошел рецидив, происходит рецидив или ожидается рецидив,
b) прекращение введения COF1 осуществляют в ответ на рецидив опухоли у субъекта или в ответ на ожидание рецидива у субъекта, и/или
c) прекращение введения COF1 приводит к лечению или предупреждению рецидива.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии iv):
v) повторение стадии iii) и/или iv),
за счет чего осуществляется лечение заболевания.
В некоторых вариантах осуществления COF1 представляет собой леналидомид или помалидомид или их фармацевтически приемлемую соль, необязательно, где COF1/CRBN-связывающий полипептид, содержит или состоит из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 1-6, 11-15, 40, 41-43, 77, 78, 84-86, и 100 (например, COF1/CRBN-связывающий полипептид содержит или состоит из аминокислотной последовательности под SEQ ID NO: 3). В некоторых вариантах осуществления COF1 представляет собой леналидомид или его фармацевтически приемлемую соль, необязательно, где леналидомид или его фармацевтически приемлемую соль вводят из расчета, например, 2,5 мг, 5 мг, 10 мг, 15 мг или 25 мг в день.
В одном аспекте данного документа представлен способ лечения субъекта, у которого имеется заболевание, ассоциированное с экспрессией опухолевого антигена, предусматривающий:
i) введение субъекту эффективного количества клетки, раскрытой в данном документе (например, клетки, содержащий слитый полипептид, содержащий COF1/CRBN-связывающий полипептид и гетерологичный полипептид (например, полипептид CAR)), необязательно, где клетку приводят в контакт с COF1 ex vivo перед введением, необязательно, где:
в присутствии COF1 уровень экспрессии слитого полипептида уменьшается, например, на по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, или 100 процентов, относительно уровня экспрессии слитого полипептида перед тем, как клетка приводится в контакт с COF1 ex vivo, необязательно, где после приведения клетки в контакт с COF1 ex vivo и перед введением клетки субъекту количество COF1, контактирующего с клеткой, например, внутри клетки и/или в ее окружении, снижают,
за счет чего осуществляется лечение заболевания.
В некоторых вариантах осуществления клетку не приводят в контакт с COF1 ex vivo перед введением.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии i):
ii) введение субъекту эффективного количества COF1, необязательно, где введение COF1 уменьшает, например, на по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, или 100 процентов, уровень экспрессии слитого полипептида относительно уровня экспрессии слитого полипептида после стадии i) и до стадии ii), необязательно, где:
a) у субъекта развилась нежелательная реакция, она развивается или ожидается ее развитие,
b) введение COF1 осуществляют в ответ на возникновение нежелательной реакции у субъекта или в ответ на ожидание возникновения нежелательной реакции у субъекта, и/или
c) введение COF1 снижает или предупреждает нежелательный эффект.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии ii):
iii) прекращение введения COF1, необязательно, где прекращение введения COF1 увеличивает, например, в по меньшей мере приблизительно 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, уровень экспрессии слитого полипептида относительно уровня экспрессии слитого полипептида после стадии ii) и до стадии iii) (например, где прекращение введения COF1 восстанавливает уровень экспрессии слитого полипептида до уровня экспрессии после стадии i) и до стадии ii)), необязательно, где:
a) у субъекта произошел рецидив, происходит рецидив или ожидается рецидив,
b) прекращение введения COF1 осуществляют в ответ на рецидив опухоли у субъекта или в ответ на ожидание рецидива у субъекта, и/или
c) прекращение введения COF1 приводит к лечению или предупреждению рецидива.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии iii):
iv) повторение стадии ii) и/или iii),
за счет чего осуществляется лечение заболевания.
В некоторых вариантах осуществления COF1 представляет собой леналидомид или помалидомид или их фармацевтически приемлемую соль, необязательно, где COF1/CRBN-связывающий полипептид, содержит или состоит из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 1-6, 11-15, 40, 41-43, 77, 78, 84-86, и 100 (например, COF1/CRBN-связывающий полипептид содержит или состоит из аминокислотной последовательности под SEQ ID NO: 3). В некоторых вариантах осуществления COF1 представляет собой леналидомид или его фармацевтически приемлемую соль, необязательно, где леналидомид или его фармацевтически приемлемую соль вводят из расчета, например, 2,5 мг, 5 мг, 10 мг, 15 мг или 25 мг в день.
В одном аспекте данного документа представлен способ лечения субъекта, у которого имеется заболевание, ассоциированное с экспрессией опухолевого антигена, предусматривающий:
i) введение эффективного количества COF1 субъекту, где субъект содержит клетку, раскрытую в данном документе (например, клетку, содержащую слитый полипептид, содержащий COF1/CRBN-связывающий полипептид и гетерологичный полипептид (например, полипептид CAR)), необязательно, где введение COF1 уменьшает, например, на по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, или 100 процентов, уровень экспрессии слитого полипептида относительно уровня экспрессии слитого полипептида перед введением COF1, необязательно, где:
a) у субъекта развилась нежелательная реакция, она развивается или ожидается ее развитие,
b) введение COF1 осуществляют в ответ на возникновение нежелательной реакции у субъекта или в ответ на ожидание возникновения нежелательной реакции у субъекта, и/или
c) введение COF1 снижает или предупреждает нежелательный эффект.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии i):
ii) прекращение введения COF1, необязательно, где прекращение введения COF1 увеличивает, например, в по меньшей мере приблизительно 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, уровень экспрессии слитого полипептида относительно уровня экспрессии слитого полипептида после стадии i) и до стадии ii) (например, где прекращение введения COF1 восстанавливает уровень экспрессии слитого полипептида до уровня экспрессии перед введением COF1), необязательно, где:
a) у субъекта произошел рецидив, происходит рецидив или ожидается рецидив,
b) прекращение введения COF1 осуществляют в ответ на рецидив опухоли у субъекта или в ответ на ожидание рецидива у субъекта, и/или
c) прекращение введения COF1 приводит к лечению или предупреждению рецидива.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии ii):
iii) повторение стадии i) и/или ii),
за счет чего осуществляется лечение заболевания.
В некоторых вариантах осуществления COF1 представляет собой леналидомид или помалидомид или их фармацевтически приемлемую соль, необязательно, где COF1/CRBN-связывающий полипептид, содержит или состоит из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 1-6, 11-15, 40, 41-43, 77, 78, 84-86, и 100 (например, COF1/CRBN-связывающий полипептид содержит или состоит из аминокислотной последовательности под SEQ ID NO: 3). В некоторых вариантах осуществления COF1 представляет собой леналидомид или его фармацевтически приемлемую соль, необязательно, где леналидомид или его фармацевтически приемлемую соль вводят из расчета, например, 2,5 мг, 5 мг, 10 мг, 15 мг или 25 мг в день.
В одном аспекте данного документа представлен способ лечения субъекта, у которого имеется заболевание, ассоциированное с экспрессией опухолевого антигена, предусматривающий:
i) введение субъекту:
(1) стабилизирующего соединения и
(2) эффективного количества клетки, раскрытой в данном документе (например, клетки, содержащей слитый полипептид, содержащий COF1/CRBN- или COF2/CRBN-связывающий полипептид, гетерологичный полипептид (например, полипептид CAR) и домен деградации), необязательно, где:
уровень экспрессии слитого полипептида в присутствии стабилизирующего соединения, например, в по меньшей мере приблизительно 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз выше, чем уровень экспрессии слитого полипептида в отсутствие стабилизирующего соединения,
за счет чего осуществляется лечение заболевания.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии i):
ii) прекращение введения стабилизирующего соединения, необязательно, где прекращение введения стабилизирующего соединения снижает, например, в по меньшей мере приблизительно 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, уровень экспрессии слитого полипептида относительно экспрессии слитого полипептида после стадии i) и до стадии ii), необязательно, где:
a) у субъекта произошел ответ на лечение, осуществляемое на стадии i) (например, у субъекта имеется полный ответ на лечение, осуществляемое на стадии i), при этом у субъекта наблюдается сокращение опухолевой массы, у субъекта наблюдается уменьшение числа опухолевых клеток, или лечение, осуществляемое на стадии i), является эффективным у субъекта), и/или
b) прекращение введения стабилизирующего соединения осуществляют в ответ на ответ субъекта на лечение, осуществляемое на стадии i) (например, у субъекта имеется полный ответ на лечение, осуществляемое на стадии i), у субъекта наблюдается сокращение опухолевой массы, у субъекта наблюдается уменьшение числа опухолевых клеток, или лечение, осуществляемое на стадии i), является эффективным у субъекта).
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии i):
iii) прекращение введения стабилизирующего соединения, необязательно, где прекращение введения стабилизирующего соединения снижает, например, в по меньшей мере приблизительно 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, уровень экспрессии слитого полипептида относительно экспрессии слитого полипептида после стадии i) и до стадии ii), необязательно, где:
a) у субъекта развилась нежелательная реакция, она развивается или ожидается ее развитие,
b) прекращение введения стабилизирующего соединения в ответ на возникновение нежелательной реакции у субъекта или в ответ на ожидание возникновения нежелательной реакции у субъекта, и/или
c) прекращение введения стабилизирующего соединения снижает или предупреждает нежелательный эффект.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии i):
iv) прекращение введения стабилизирующего соединения и введение субъекту эффективного количества COF1 или COF2, необязательно, где стадия iv) снижает, например, в по меньшей мере приблизительно 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, уровень экспрессии слитого полипептида относительно экспрессии слитого полипептида после стадии i) и до стадии iv), необязательно, где:
a) у субъекта развилась нежелательная реакция, она развивается или ожидается ее развитие,
b) стадию iv) осуществляют в ответ на возникновение нежелательной реакции у субъекта или в ответ на ожидание возникновения нежелательной реакции у субъекта, и/или
c) стадия iv) снижает или предупреждает нежелательный эффект. В некоторых вариантах осуществления нежелательный эффект представляет собой острую токсичность.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии iv):
v) прекращение введения COF1 или COF2, например, после того, как число клеток, экспрессирующих слитый полипептид на поверхности, становится меньшим, чем заранее заданное значение, например, на 1 день, 5 дней, 10 дней или 15 дней.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии ii), iii), iv) или v):
vi) введение эффективного количества стабилизирующего соединения, необязательно, где введение стабилизирующего соединения увеличивает, например, в по меньшей мере приблизительно 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, уровень экспрессии слитого полипептида относительно уровня экспрессии слитого полипептида после стадии ii), iii), iv) или v) и до стадии vi), необязательно, где:
a) у субъекта произошел рецидив, происходит рецидив или ожидается рецидив,
b) введение стабилизирующего соединения осуществляют в ответ на рецидив опухоли у субъекта или в ответ на ожидание рецидива у субъекта, и/или
c) введение стабилизирующего соединения приводит к лечению или предупреждению рецидива опухоли.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии vi):
vii) повторение стадии iii), iv), v) или vi),
за счет чего осуществляется лечение заболевания.
В некоторых вариантах осуществления способ дополнительно предусматривает до стадии i):
viii) приведение клетки в контакт со стабилизирующим соединением ex vivo, необязательно, где уровень экспрессии слитого полипептида в присутствии стабилизирующего соединения, например, в по меньшей мере приблизительно 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз выше, чем уровень экспрессии слитого полипептида в отсутствие стабилизирующего соединения.
В некоторых вариантах осуществления клетку не приводят в контакт со стабилизирующим соединением ex vivo перед введением. В некоторых вариантах осуществления клетку не приводят в контакт с любым из стабилизирующего соединения, COF1 или COF2 ex vivo перед введением.
В некоторых вариантах осуществления стабилизирующее соединение представляет собой базедоксифен или его фармацевтически приемлемую соль, и необязательно, где домен деградации содержит аминокислотную последовательность под SEQ ID NO: 46.
В некоторых вариантах осуществления COF1 представляет собой леналидомид или помалидомид или их фармацевтически приемлемую соль, необязательно, где COF1/CRBN-связывающий полипептид, содержит или состоит из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 1-6, 11-15, 40, 41-43, 77, 78, 84-86, и 100 (например, COF1/CRBN-связывающий полипептид содержит или состоит из аминокислотной последовательности под SEQ ID NO: 3).
В некоторых вариантах осуществления COF2 представляет собой леналидомид или помалидомид или их фармацевтически приемлемую соль, необязательно, где COF2/CRBN-связывающий полипептид, содержит или состоит из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 1-6, 11-15, 40, 41-43, 77, 78, 84-86, и 100 (например, COF1/CRBN-связывающий полипептид содержит или состоит из аминокислотной последовательности под SEQ ID NO: 3).
В некоторых вариантах осуществления COF1 или COF2 представляет собой леналидомид или его фармацевтически приемлемую соль, необязательно, где леналидомид или его фармацевтически приемлемую соль вводят из расчета, например, 2,5 мг, 5 мг, 10 мг, 15 мг или 25 мг в день.
В одном аспекте данного документа раскрыт способ деградации слитого полипептида, раскрытого в данном документе (например, слитого полипептида, содержащего COF3/CRBN-связывающий полипептид и гетерологичный полипептид (например, полипептид CAR)), предусматривающий приведение слитого полипептида или клетки, содержащей указанный слитый полипептид, в контакт с COF3 (например, соединением, раскрытым в таблице 29, или его фармацевтически приемлемой солью). В одном варианте осуществления в присутствии COF3 уровень экспрессии указанного слитого полипептида значительно уменьшается, например, на по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, или 100 процентов, относительно уровня экспрессии указанного слитого полипептида в отсутствие COF3, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии. В одном варианте осуществления слитый полипептид или клетку приводят в контакт с COF3 ex vivo. В одном варианте осуществления слитый полипептид или клетку приводят в контакт с COF3 in vivo.
В одном аспекте данного документ раскрыт способ регулирования экспрессии слитого полипептида, раскрытого в данном документе (например, слитого полипептида, содержащего COF3/CRBN-связывающий полипептид, гетерологичный полипептид (например, полипептид CAR) и домен деградации), предусматривающий:
i) приведение слитого полипептида или клетки, содержащей слитый полипептид, в контакт со стабилизирующим соединением, необязательно, где в присутствии стабилизирующего соединения:
a) домен деградации принимает конформацию, которая является более устойчивой к клеточной деградации относительно конформации в отсутствие стабилизирующего соединения;
b) конформация слитого полипептида более восприимчива к расщеплению в гетерологичном сайте расщепления протеазами относительно конформации в отсутствие стабилизирующего соединения; или
c) уровень экспрессии слитого полипептида увеличивается, например, в по меньшей мере 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, по сравнению с уровнем экспрессии слитого полипептида в отсутствие стабилизирующего соединения, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии i):
ii) приведение слитого полипептида или клетки, содержащей слитый полипептид, в контакт с COF3 (например, соединением, раскрытым в таблице 29, или его фармацевтически приемлемой солью), необязательно, где в присутствии COF3 уровень экспрессии слитого полипептида значительно уменьшается, например, на по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, или 100 процентов, относительно уровня экспрессии слитого полипептида после стадии i) и перед стадией ii), например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В некоторых вариантах осуществления слитый полипептид или клетку приводят в контакт с COF3 ex vivo. В некоторых вариантах осуществления слитый полипептид или клетку приводят в контакт с COF3 in vivo. В некоторых вариантах осуществления стабилизирующее соединение представляет собой базедоксифен или его фармацевтически приемлемую соль. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность под SEQ ID NO: 46.
В одном аспекте данного документа раскрыт способ получения клетки, предусматривающий:
i) обеспечение клетки, содержащей молекулу нуклеиновой кислоты, кодирующую слитый полипептид, содержащий COF3/CRBN-связывающий полипептид и химерный антигенный рецептор (CAR), необязательно, где CAR содержит в направлении от N-конца к C-концу: антигенсвязывающий домен, трансмембранный домен и один или несколько внутриклеточных сигнальных доменов; и
ii) приведение клетки в контакт с COF3 ex vivo, необязательно, где:
в присутствии COF3 уровень экспрессии слитого полипептида значительно уменьшается, например, на по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, или 100 процентов, относительно уровня экспрессии слитого полипептида в отсутствие COF3, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В одном аспекте данного документа представлен способ лечения субъекта, у которого имеется заболевание, ассоциированное с экспрессией опухолевого антигена, предусматривающий:
i) приведение клетки, раскрытой в данном документе (например, клетки, содержащей слитый полипептид, содержащий COF3/CRBN-связывающий полипептид и гетерологичный полипептид (например, полипептид CAR)), в контакт с COF3 ex vivo, необязательно, где:
в присутствии COF3 уровень экспрессии слитого полипептида уменьшается, например, на по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, или 100 процентов, относительно уровня экспрессии слитого полипептида перед приведением клетки в контакт с COF3 ex vivo, и
ii) введение субъекту эффективного количества клетки, необязательно, где способ дополнительно предусматривает после стадии i) и до стадии ii):
снижение количества COF3, контактирующего с клеткой, например, внутри клетки и/или в ее окружении,
за счет чего осуществляется лечение заболевания.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии ii):
iii) введение субъекту эффективного количества COF3, необязательно, где введение COF3 уменьшает, например, на по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, или 100 процентов, уровень экспрессии слитого полипептида относительно уровня экспрессии слитого полипептида после стадии ii) и до стадии iii), необязательно, где:
a) у субъекта развилась нежелательная реакция, она развивается или ожидается ее развитие,
b) введение COF3 осуществляют в ответ на возникновение нежелательной реакции у субъекта или в ответ на ожидание возникновения нежелательной реакции у субъекта, и/или
c) введение COF3 снижает или предупреждает нежелательный эффект.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии iii):
iv) прекращение введения COF3, необязательно, где прекращение введения COF3 увеличивает, например, в по меньшей мере приблизительно 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, уровень экспрессии слитого полипептида относительно уровня экспрессии слитого полипептида после стадии iii) и до стадии iv) (например, где прекращение введения COF3 восстанавливает уровень экспрессии слитого полипептида до уровня экспрессии после стадии ii) и до стадии iii)), необязательно, где:
a) у субъекта произошел рецидив, происходит рецидив или ожидается рецидив,
b) прекращение введения COF3 осуществляют в ответ на рецидив опухоли у субъекта или в ответ на ожидание рецидива у субъекта, и/или
c) прекращение введения COF3 приводит к лечению или предупреждению рецидива.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии iv):
v) повторение стадии iii) и/или iv),
за счет чего осуществляется лечение заболевания.
В некоторых вариантах осуществления COF3 представляет собой соединение, раскрытое в таблице 29, или его фармацевтически приемлемую соль. В некоторых вариантах осуществления COF3/CRBN-связывающий полипептид содержит или состоит из аминокислотной последовательности под SEQ ID NO: 109 или аминокислотной последовательности, характеризующейся по меньшей мере 80, 85, 90 или 95% идентичностью с ней.
В одном аспекте данного документа представлен способ лечения субъекта, у которого имеется заболевание, ассоциированное с экспрессией опухолевого антигена, предусматривающий:
i) введение субъекту эффективного количества клетки, раскрытой в данном документе (например, клетки, содержащий слитый полипептид, содержащий COF3/CRBN-связывающий полипептид и гетерологичный полипептид (например, полипептид CAR)), необязательно, где клетку приводят в контакт с COF3 ex vivo перед введением, необязательно, где:
в присутствии COF3 уровень экспрессии слитого полипептида уменьшается, например, на по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, или 100 процентов, относительно уровня экспрессии слитого полипептида перед тем, как клетка приводится в контакт с COF3 ex vivo, необязательно, где после приведения клетки в контакт с COF3 ex vivo и перед введением клетки субъекту количество COF3, контактирующего с клеткой, например, внутри клетки и/или в ее окружении, снижают,
за счет чего осуществляется лечение заболевания.
В некоторых вариантах осуществления клетку не приводят в контакт с COF3 ex vivo перед введением.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии i):
ii) введение субъекту эффективного количества COF3, необязательно, где введение COF3 уменьшает, например, на по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, или 100 процентов, уровень экспрессии слитого полипептида относительно уровня экспрессии слитого полипептида после стадии i) и до стадии ii), необязательно, где:
a) у субъекта развилась нежелательная реакция, она развивается или ожидается ее развитие,
b) введение COF3 осуществляют в ответ на возникновение нежелательной реакции у субъекта или в ответ на ожидание возникновения нежелательной реакции у субъекта, и/или
c) введение COF3 снижает или предупреждает нежелательный эффект.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии ii):
iii) прекращение введения COF3, необязательно, где прекращение введения COF3 увеличивает, например, в по меньшей мере приблизительно 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, уровень экспрессии слитого полипептида относительно уровня экспрессии слитого полипептида после стадии ii) и до стадии iii) (например, где прекращение введения COF3 восстанавливает уровень экспрессии слитого полипептида до уровня экспрессии после стадии i) и до стадии ii)), необязательно, где:
a) у субъекта произошел рецидив, происходит рецидив или ожидается рецидив,
b) прекращение введения COF3 осуществляют в ответ на рецидив опухоли у субъекта или в ответ на ожидание рецидива у субъекта, и/или
c) прекращение введения COF3 приводит к лечению или предупреждению рецидива.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии iii):
iv) повторение стадии ii) и/или iii),
за счет чего осуществляется лечение заболевания.
В некоторых вариантах осуществления COF3 представляет собой соединение, раскрытое в таблице 29, или его фармацевтически приемлемую соль. В некоторых вариантах осуществления COF3/CRBN-связывающий полипептид содержит или состоит из аминокислотной последовательности под SEQ ID NO: 109 или аминокислотной последовательности, характеризующейся по меньшей мере 80, 85, 90 или 95% идентичностью с ней.
В одном аспекте данного документа представлен способ лечения субъекта, у которого имеется заболевание, ассоциированное с экспрессией опухолевого антигена, предусматривающий:
i) введение эффективного количества COF3 субъекту, где субъект содержит клетку, раскрытую в данном документе (например, клетку, содержащую слитый полипептид, содержащий COF3/CRBN-связывающий полипептид и гетерологичный полипептид (например, полипептид CAR)), необязательно, где введение COF3 уменьшает, например, на по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, или 100 процентов, уровень экспрессии слитого полипептида относительно уровня экспрессии слитого полипептида перед введением COF3, необязательно, где:
a) у субъекта развилась нежелательная реакция, она развивается или ожидается ее развитие,
b) введение COF3 осуществляют в ответ на возникновение нежелательной реакции у субъекта или в ответ на ожидание возникновения нежелательной реакции у субъекта, и/или
c) введение COF3 снижает или предупреждает нежелательный эффект.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии i):
ii) прекращение введения COF3, необязательно, где прекращение введения COF3 увеличивает, например, в по меньшей мере приблизительно 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, уровень экспрессии слитого полипептида относительно уровня экспрессии слитого полипептида после стадии i) и до стадии ii) (например, где прекращение введения COF3 восстанавливает уровень экспрессии слитого полипептида до уровня экспрессии перед введением COF3), необязательно, где:
a) у субъекта произошел рецидив, происходит рецидив или ожидается рецидив,
b) прекращение введения COF3 осуществляют в ответ на рецидив опухоли у субъекта или в ответ на ожидание рецидива у субъекта, и/или
c) прекращение введения COF3 приводит к лечению или предупреждению рецидива.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии ii):
iii) повторение стадии i) и/или ii),
за счет чего осуществляется лечение заболевания.
В некоторых вариантах осуществления COF3 представляет собой соединение, раскрытое в таблице 29, или его фармацевтически приемлемую соль. В некоторых вариантах осуществления COF3/CRBN-связывающий полипептид содержит или состоит из аминокислотной последовательности под SEQ ID NO: 109 или аминокислотной последовательности, характеризующейся по меньшей мере 80, 85, 90 или 95% идентичностью с ней.
В одном аспекте данного документа представлен способ лечения субъекта, у которого имеется заболевание, ассоциированное с экспрессией опухолевого антигена, предусматривающий:
i) введение субъекту:
(1) стабилизирующего соединения и
(2) эффективного количества клетки, раскрытой в данном документе (например, клетки, содержащей слитый полипептид, содержащий COF3/CRBN-связывающий полипептид, гетерологичный полипептид (например, полипептид CAR) и домен деградации), необязательно, где:
уровень экспрессии слитого полипептида в присутствии стабилизирующего соединения, например, в по меньшей мере приблизительно 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз выше, чем уровень экспрессии слитого полипептида в отсутствие стабилизирующего соединения,
за счет чего осуществляется лечение заболевания.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии i):
ii) прекращение введения стабилизирующего соединения, необязательно, где прекращение введения стабилизирующего соединения снижает, например, в по меньшей мере приблизительно 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, уровень экспрессии слитого полипептида относительно экспрессии слитого полипептида после стадии i) и до стадии ii), необязательно, где:
a) у субъекта произошел ответ на лечение, осуществляемое на стадии i) (например, у субъекта имеется полный ответ на лечение, осуществляемое на стадии i), при этом у субъекта наблюдается сокращение опухолевой массы, у субъекта наблюдается уменьшение числа опухолевых клеток, или лечение, осуществляемое на стадии i), является эффективным у субъекта), и/или
b) прекращение введения стабилизирующего соединения осуществляют в ответ на ответ субъекта на лечение, осуществляемое на стадии i) (например, у субъекта имеется полный ответ на лечение, осуществляемое на стадии i), у субъекта наблюдается сокращение опухолевой массы, у субъекта наблюдается уменьшение числа опухолевых клеток, или лечение, осуществляемое на стадии i), является эффективным у субъекта).
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии i):
iii) прекращение введения стабилизирующего соединения, необязательно, где прекращение введения стабилизирующего соединения снижает, например, в по меньшей мере приблизительно 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, уровень экспрессии слитого полипептида относительно экспрессии слитого полипептида после стадии i) и до стадии ii), необязательно, где:
a) у субъекта развилась нежелательная реакция, она развивается или ожидается ее развитие,
b) прекращение введения стабилизирующего соединения в ответ на возникновение нежелательной реакции у субъекта или в ответ на ожидание возникновения нежелательной реакции у субъекта, и/или
c) прекращение введения стабилизирующего соединения снижает или предупреждает нежелательный эффект.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии i):
iv) прекращение введения стабилизирующего соединения и введение субъекту эффективного количества COF3, необязательно, где стадия iv) снижает, например, в по меньшей мере приблизительно 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, уровень экспрессии слитого полипептида относительно экспрессии слитого полипептида после стадии i) и до стадии iv), необязательно, где:
a) у субъекта развилась нежелательная реакция, она развивается или ожидается ее развитие,
b) стадию iv) осуществляют в ответ на возникновение нежелательной реакции у субъекта или в ответ на ожидание возникновения нежелательной реакции у субъекта, и/или
c) стадия iv) снижает или предупреждает нежелательный эффект. В некоторых вариантах осуществления нежелательный эффект представляет собой острую токсичность.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии iv):
v) прекращение введения COF3, например, после того, как число клеток, экспрессирующих слитый полипептид на поверхности, становится меньшим, чем заранее заданное значение, например, на 1 день, 5 дней, 10 дней или 15 дней.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии ii), iii), iv) или v):
vi) введение эффективного количества стабилизирующего соединения, необязательно, где введение стабилизирующего соединения увеличивает, например, в по меньшей мере приблизительно 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, уровень экспрессии слитого полипептида относительно уровня экспрессии слитого полипептида после стадии ii), iii), iv) или v) и до стадии vi), необязательно, где:
a) у субъекта произошел рецидив, происходит рецидив или ожидается рецидив,
b) введение стабилизирующего соединения осуществляют в ответ на рецидив опухоли у субъекта или в ответ на ожидание рецидива у субъекта, и/или
c) введение стабилизирующего соединения приводит к лечению или предупреждению рецидива опухоли.
В некоторых вариантах осуществления способ дополнительно предусматривает после стадии vi):
vii) повторение стадии iii), iv), v) или vi),
за счет чего осуществляется лечение заболевания.
В некоторых вариантах осуществления способ дополнительно предусматривает до стадии i):
viii) приведение клетки в контакт со стабилизирующим соединением ex vivo, необязательно, где уровень экспрессии слитого полипептида в присутствии стабилизирующего соединения, например, в по меньшей мере приблизительно 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз выше, чем уровень экспрессии слитого полипептида в отсутствие стабилизирующего соединения.
В некоторых вариантах осуществления клетку не приводят в контакт со стабилизирующим соединением ex vivo перед введением.
В некоторых вариантах осуществления стабилизирующее соединение представляет собой базедоксифен или его фармацевтически приемлемую соль, и необязательно, где домен деградации содержит аминокислотную последовательность под SEQ ID NO: 46.
В некоторых вариантах осуществления COF3 представляет собой соединение, раскрытое в таблице 29, или его фармацевтически приемлемую соль. В некоторых вариантах осуществления COF3/CRBN-связывающий полипептид содержит или состоит из аминокислотной последовательности под SEQ ID NO: 109 или аминокислотной последовательности, характеризующейся по меньшей мере 80, 85, 90 или 95% идентичностью с ней.
В некоторых вариантах осуществления гетерологичный полипептид слитого полипептида представляет собой химерный антигенный рецептор (CAR), необязательно, где CAR содержит в направлении от N-конца к C-концу: антигенсвязывающий домен, трансмембранный домен и один или несколько внутриклеточных сигнальных доменов.
В одном аспекте настоящего изобретения также представлены слитый полипептид, молекула нуклеиновой кислоты, вектор, вирусная частица, клетка или фармацевтическая композиция, раскрытые в данном документе, для применения в качестве лекарственного препарата. В одном аспекте настоящего изобретения также представлены слитый полипептид, молекула нуклеиновой кислоты, вектор, вирусная частица, клетка или фармацевтическая композиция, раскрытые в данном документе, для применения в лечении субъекта, у которого имеется заболевание, ассоциированное с экспрессией опухолевого антигена.
В определенных вариантах осуществления вышеуказанных способов заболевание, ассоциированное с экспрессией опухолевого антигена, представляет собой рак.
В некоторых вариантах осуществления рак представляет собой мезотелиому (например, злокачественную мезотелиому плевры), например, у субъекта, у которого имеется прогрессирование на фоне по меньшей мере одной предшествующей стандартной терапии; рак легкого (например, немелкоклеточный рак легкого, мелкоклеточный рак легкого, плоскоклеточный рак легкого или крупноклеточный рак легкого); рак поджелудочной железы (например, аденокарциному протоков поджелудочной железы или метастатическую аденокарциному протоков поджелудочной железы (PDA), например, у субъекта, у которого имеется прогрессирование на фоне по меньшей мере одной предшествующей стандартной терапии); аденокарциному пищевода, рак яичника (например, серозный эпителиальный рак яичника, например, у субъекта, у которого имеется прогрессирование после по меньшей мере одной предшествующей схемы стандартной терапии), рак молочной железы, колоректальный рак, рак мочевого пузыря или любую их комбинацию.
В некоторых вариантах осуществления заболевание, ассоциированное с экспрессией опухолевого антигена, представляет собой гематологический рак, например, гематологический рак, выбранный из лейкоза или лимфомы.
В некоторых вариантах осуществления рак выбран из хронического лимфоцитарного лейкоза (CLL), лимфомы из клеток мантийной зоны (MCL), множественной миеломы, острого лимфоидного лейкоза (ALL), лимфомы Ходжкина, B-клеточного острого лимфоидного лейкоза (BALL), T-клеточного острого лимфоидного лейкоза (TALL), малого лимфоцитарного лейкоза (SLL), B-клеточного пролимфоцитарного лейкоза, новообразования из бластных плазмоцитоидных дендритных клеток, лимфомы Беркитта, диффузной В-крупноклеточной лимфомы (DLBCL), DLBCL, ассоциированной с хроническим воспалением, хронического миелоидного лейкоза, миелопролиферативных новообразований, фолликулярной лимфомы, фолликулярной лимфомы у детей, волосатоклеточного лейкоза, мелкоклеточной или крупноклеточной фолликулярной лимфомы, злокачественных лимфопролиферативных состояний, MALT-лимфомы (эстранодальной лимфомы маргинальной зоны из лимфоидной ткани слизистых оболочек), лимфомы маргинальной зоны, миелодисплазии, миелодиспластического синдрома, неходжкинской лимфомы, плазмобластной лимфомы, новообразования из плазмоцитоидных дендритных клеток, макроглобулинемии Вальденстрема, лимфомы маргинальной зоны селезенки, лимфомы/лейкоза селезенки, диффузной мелкоклеточной B-клеточной лимфомы красной пульпы селезенки, варианта волосатоклеточного лейкоза, лимфоплазмоцитарной лимфомы, болезни тяжелых цепей, плазмоклеточной миеломы, солитарной плазмоцитомы кости, внекостной плазмоцитомы, нодальной лимфомы маргинальной зоны, нодальной лимфомы маргинальной зоны у детей, первичной кожной лимфомы из клеток центра фолликула, лимфоматоидного гранулематоза, первичной медиастинальной (тимусной) крупноклеточной B-клеточной лимфомы, внутрисосудистой крупноклеточной B-клеточной лимфомы, ALK+ крупноклеточной B-клеточной лимфомы, крупноклеточной B-клеточной лимфомы, возникающей при HHV8-ассоциированной многоочаговой болезни Кастельмана, первичной выпотной лимфомы, B-клеточной лимфомы, острого миелоидного лейкоза (AML) или неклассифицируемой лимфомы.
В некоторых вариантах осуществления рак выбран из MCL, CLL, ALL, лимфомы Ходжкина, AML или множественной миеломы.
В определенных вариантах осуществления вышеуказанных способов клетка является аутологичной для указанного субъекта. В определенных вариантах осуществления вышеуказанных способов клетка является аллогенной для указанного субъекта. В некоторых вариантах осуществления клетка представляет собой клетку, экспрессирующую CAR, например CAR-T-клетку.
В некоторых вариантах осуществления субъекту вводили клетку, экспрессирующую по меньшей мере один слитый полипептид, раскрытый в данном документе, до введения COF1, COF2 или COF3.
В одном аспекте данного документа раскрыт способ идентификации генетического элемента, ассоциированного со специфическим биологическим фенотипом, например, генетического элемента, ассоциированного с развитием и/или прогрессированием рака, причем способ предусматривает стадии:
i) модулирования экспрессии слитого полипептида, раскрытого в данном документе (например, слитого полипептида, содержащего COF1/CRBN- или COF3/CRBN-связывающий полипептид и гетерологичный полипептид), в клетках посредством воздействия на указанную клетку с помощью COF1 или COF3, например, леналидомида или его фармацевтически приемлемой соли,
(ii) отбора клеток с представляющим интерес фенотипом, например, фенотипом, ассоциированным с развитием и/или прогрессированием рака, и
(iii) идентификации указанного слитого полипептида, который индуцирует указанный представляющий интерес фенотип,
где воздействие на указанную клетку с помощью COF1 или COF3, например, леналидомида или его фармацевтически приемлемой соли, уменьшает, например, на по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, или 100 процентов, уровень экспрессии указанного слитого полипептида относительно уровня экспрессии указанного слитого полипептида до воздействия с помощью COF1 или COF3, например, леналидомида или его фармацевтически приемлемой соли.
В одном аспекте данного документа раскрыт способ идентификации генетического элемента, ассоциированного со специфическим биологическим фенотипом, например, генетического элемента ассоциированного с развитием и/или прогрессированием рака, причем способ предусматривает стадии:
i) модулирования экспрессии слитого полипептида, раскрытого в данном документе (например, слитого полипептида, содержащего COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид, гетерологичный полипептид и домен деградации), в клетках посредством воздействия на указанную клетку с помощью стабилизирующего соединения, например, базедоксифена или его фармацевтически приемлемой соли, а затем COF1, COF2 или COF3, например, леналидомида, или их фармацевтически приемлемой соли,
(ii) отбора клеток с представляющим интерес фенотипом, например, фенотипом, ассоциированным с развитием и/или прогрессированием рака, и
(iii) идентификации указанного слитого полипептида, который индуцирует указанный представляющий интерес фенотип,
где воздействие на указанную клетку с помощью стабилизирующего соединения, например, базедоксифена или его фармацевтически приемлемой соли, увеличивает, например, в по меньшей мере приблизительно 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, уровень экспрессии слитого полипептида относительно уровня экспрессии слитого полипептида до воздействия с помощью стабилизирующего соединения, например, базедоксифена или его фармацевтически приемлемой соли, и где воздействие на указанную клетку с помощью COF1, COF2 или COF3, например, леналидомида или его фармацевтически приемлемой соли, уменьшает, например, на по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, или 100 процентов, уровень экспрессии указанного слитого полипептида относительно уровня экспрессии указанного слитого полипептида после воздействия с помощью стабилизирующего соединения и до воздействия с помощью COF1 или COF2 (такого как талидомид и его производные (например, леналидомид, помалидомид и талидомид)) или COF3 (например, соединения, раскрытого в таблице 29).
В определенных вариантах осуществления вышеуказанных аспектов гетерологичный полипептид представляет собой полипептид химерного антигенного рецептора (CAR). В некоторых вариантах осуществления полипептид CAR содержит аминокислотную последовательность, раскрытую в данном документе, например, аминокислотную последовательность, раскрытую в таблице 3. В некоторых вариантах осуществления полипептид CAR представляет собой полипептид CAR для CD19 и содержит аминокислотную последовательность, раскрытую в данном документе, например, аминокислотную последовательность, раскрытую в любой из таблицы 5, таблицы 6, таблицы 7 и таблицы 30. В некоторых вариантах осуществления полипептид CAR представляет собой полипептид CAR для CD123 и содержит аминокислотную последовательность, раскрытую в данном документе, например, аминокислотную последовательность, раскрытую в любой из таблицы 8, таблицы 9, таблицы 10, таблицы 11, таблицы 12, таблицы 13 и таблицы 14. В некоторых вариантах осуществления полипептид CAR представляет собой полипептид CAR для BCMA и содержит аминокислотную последовательность, раскрытую в данном документе, например, аминокислотную последовательность, раскрытую в любой из таблицы 15, таблицы 16, таблицы 17, таблицы 18 и таблицы 31. В некоторых вариантах осуществления полипептид CAR представляет собой полипептид CAR для CD22 и содержит аминокислотную последовательность, раскрытую в данном документе, например, аминокислотную последовательность, раскрытую в любой из таблицы 19 и таблицы 20. В некоторых вариантах осуществления полипептид CAR представляет собой полипептид CAR для CD20 и содержит аминокислотную последовательность, раскрытую в данном документе, например, аминокислотную последовательность, раскрытую в таблице 32. В некоторых вариантах осуществления полипептид CAR представляет собой полипептид CAR для EGFRvIII и содержит аминокислотную последовательность, раскрытую в данном документе, например, аминокислотную последовательность, раскрытую в таблице 33. В некоторых вариантах осуществления полипептид CAR представляет собой полипептид CAR для мезотелина и содержит аминокислотную последовательность, раскрытую в данном документе, например, аминокислотную последовательность, раскрытую в таблице 34.
В определенных вариантах осуществления вышеуказанных аспектов слитый полипептид содержит аминокислотную последовательность, раскрытую в данном документе, например, аминокислотную последовательность, раскрытую в таблице 4 или таблице 28.
В определенных вариантах осуществления вышеуказанных аспектов COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид содержит аминокислотную последовательность, раскрытую в данном документе, например, аминокислотную последовательность, раскрытую в таблице 1.
В определенных вариантах осуществления вышеуказанных аспектов домен деградации содержит аминокислотную последовательность, раскрытую в данном документе, например, аминокислотную последовательность, раскрытую в таблице 22.
В определенных вариантах осуществления вышеуказанных аспектов гетерологичный сайт расщепления протеазами содержит аминокислотную последовательность, раскрытую в данном документе, например, аминокислотную последовательность, раскрытую в таблице 23.
Краткое описание графических материалов
ФИГ. 1A представляет собой схему HilD-метки, представляющую собой дегрон IKZF3 136-180 и 236-249, слитый с NanoLuciferase через 16-глицин-сериновый линкер. ФИГ. 1B представляет собой диаграмму, на которой показан уровень люминесценции, измеренный у клеток HEK293T, подвергнутых обратной трансфекции с помощью 50 нг конструкции pNL1.1CMV, кодирующей NanoLuciferase, связанную с IKZF3 136-180 и 236-249. IKZF3 136-180 и 236-249 содействует снижению люминесценции у клеток, обработанных с помощью 1 мкМ, 10 мкМ или 100 мкМ леналидомида в течение 6 часов, по сравнению с клетками, обработанными только с помощью DMSO. Обработка с помощью MG132 блокировала леналидомид-зависимую деградацию NanoLuciferase.
ФИГ. 2 представляет собой вестерн-блот, на котором показано, что IKZF3 136-180 и 236-249 содействовал леналидомид-зависимой деградации NanoLuciferase (IC50=10 нМ) в клетках HEK293GT, трансфицированных с помощью конструкции pNL1.1CMV, кодирующей NanoLuciferase с меткой IKZF3 136-180 и 236-249. Леналидомид-зависимую деградацию не наблюдали к клетках HEK293GT с KO по цереблону (CRBN), которые были трансфицированы аналогичным образом. Обработка с помощью ингибитора протеасомы, MG132, блокировала способность IKZF3 136-180 и 236-249 содействовать леналидомид-зависимой деградации.
ФИГ. 3A представляет собой схему, изображающую IKZF3 136-180, который содержит два бета-листа, фланкирующие шпильку и альфа-спираль, а также IKZF3 236-249, который прогнозируется в виде дополнительной альфа-спирали. Под схемой находится диаграмма укороченных вариантов дегрона IKZF3 136-180 с удалением аминокислот на N- и C-конце (SEQ ID NO: 3, 5 и 7-10 соответственно, в представленном порядке). ФИГ. 3B представляет собой вестерн-блот, на котором показаны результаты исследования с тестированием леналидомид-зависимой деградации NanoLuciferase, слитой с различными метками деградации на основе IKZF3. Метки деградации на основе IKZF3 сливали с N-концом NanoLuciferase, клонировали в векторы pNL1.1CMV и трансфицировали в клетки HEK293T. Трансфицированные клетки обрабатывали с помощью либо DMSO, либо 10 мкМ леналидомида в течение 4 часов перед проведением вестерн-блоттинг-анализа. Два воздействия (длительное и короткое воздействие) показаны для NanoLuciferase ("Nanoluc"). Все из IKZF3 136-180 и 236-249, IKZF3 136-180 и 236-249 K245R, IKZF3 136-180 и 236-249 K245S, IKZF3 136-180 MALEK и IKZF3 136-170 MALEK содействовали леналидомид-индуцированной деградации, при этом IKZF3 140-170 MALEK, IKZF3 141-163 MALEK и IKZF3 145-155 MALEK не опосредовали леналидомид-индуцированную деградацию.
ФИГ. 4A и 4B представляют собой диаграммы вестерн-блотов, на которых показана леналидомид-зависимая деградация NanoLuciferase с меткой IKZF3 136-180 (ФИГ. 4A) или NanoLuciferase с меткой IKZF3 136-170 MALEK (ФИГ. 4B) в клетках HEK293T, при этом IC50 составляет примерно 100 нМ при 2-часовой обработке леналидомидом в обоих случаях. Слияния NanoLuciferase с меткой экспрессировали с использованием конструкций pNL1.1CMV. ФИГ. 4C представляет собой вестерн-блот, на котором показана временная динамика леналидомид-зависимой деградации NanoLuciferase с меткой IKZF3 136-180 в клетках HEK293T, при этом деградация видна уже через 1 час и почти полная деградация через 4 часа. Слияние NanoLuciferase с меткой экспрессировали с использованием конструкции pNL1.1CMV.
ФИГ. 5A представляет собой вестерн-блот, на котором показана леналидомид-зависимая деградация ассоциированного с меланогенезом транскрипционного фактора (MITF) с меткой IKZF3 136-180 и 236-249 (левая панель), а также MITF с меткой IKZF3 136-180 (правая панель). Слияния MITF с меткой трансфицировали HEK293T с применением конструкций pNL1.1CMV. Деградация MITF с меткой IKZF3 136-180 и 236-249 показана при IC50, составляющей ~100 нМ. Эта деградация была зависимой от активности протеасомы, поскольку деградация блокировалась обработкой MG132. IKZF3 136-180 также опосредовал леналидомид-зависимую деградацию, хотя и в меньшей степени, чем IKZF3 136-180 и 236-249. ФИГ. 5B представляет собой вестерн-блот, на котором показана леналидомид-зависимая деградация MITF с меткой IKZF3 136-180 и 236-249 (левая панель), а также MITF с меткой IKZF3 136-180 (правая панель) после того, как клетки, экспрессирующие такие слитые белки, обрабатывали с помощью 10 мкМ леналидомида в течение различных временных промежутков. Среди протестированных моментов времени для 4-часовой обработки показана максимальная деградация.
ФИГ. 6A и 6B представляют собой диаграммы вестерн-блотов, на которых показана леналидомид-зависимая деградация MITF с меткой IKZF3 136-180 и 236-249 (ФИГ. 6A) или IKZF3 136-180 и 236-249, в которой каждый остаток лизина в метке был мутирован в аргинин ("IKZF3 136-180 и 236-249 без лизина") (ФИГ. 6B). Клетки HEK293T, экспрессирующие слияния MITF с меткой с применением конструкций pNL1.1CMV, обрабатывали различными концентрациями леналидомида в течение 24 часов. IC50 составляет примерно 10 нМ для MITF с меткой IKZF3 136-180 и 236-249 (ФИГ. 6A) и менее 100 нМ для MITF с меткой IKZF3 136-180 и 236-249 без лизина (ФИГ. 6B). В обоих случаях леналидомид-зависимая деградация была зависимой от протеасомы, поскольку деградацию можно было блокировать за счет ингибитора протеасомы, MG132. Эти данные позволяют предполагать, что MITF, а не метка-дегрон IKZF3, подвергалась убиквитинированию. ФИГ. 6C представляет собой вестерн-блот, на котором показана леналидомид-зависимая деградация MITF с меткой IKZF3 136-180 и 236-249 без лизина. Клетки HEK293T, экспрессирующие слияние MITF с меткой с применением конструкции pNL1.1CMV, обрабатывали с помощью 10 мкМ леналидомида в течение 2 часов, 4 часов, 8 часов или 24 часов. ФИГ. 6D представляет собой вестерн-блот для MITF с меткой IKZF3 136-180 и 236-249 (левая панель), а также MITF с меткой IKZF3 136-180 и 236-249 без лизина (правая панель). Клетки HEK293T, экспрессирующие слияния MITF с меткой с применением конструкций pNL1.1CMV, обрабатывали с помощью 10 мкМ одного из леналидомида, помалидомида, талидомид, IMiD отрицательного контроля, который может связываться с CRBN, но отличен от IKZF1 или IKZF3, или DMSO в течение 24 часов перед тем, как клетки подвергали вестерн-блоттинг-анализу. Помалидомид опосредовал деградацию меченого MITF в немного большей степени, чем леналидомид, тогда как талидомид был намного менее эффективным в опосредовании такой деградации.
ФИГ. 7 представляет собой вестерн-блот, на котором показана леналидомид-зависимая деградация MITF с меткой IKZF3 136-180 Q147H. Клетки HEK293T, трансфицированные с помощью конструкций pNL1.1CMV, кодирующих слияния MITF с меткой, обрабатывали различными дозами леналидомида в течение 24 часов. Для MITF с меткой IKZF3 136-180 Q147H не показана деградация в присутствии леналидомида.
ФИГ. 8 представляет собой вестерн-блот, на котором показана леналидомид-зависимая деградация гомолога вирусного онкогена миелоцитоматоза птиц (MYC) с меткой IKZF3 136-180 и 236-249 при IC50, составляющей примерно 10 нМ. Клетки HEK293T, экспрессирующие слияния MYC с меткой с применением конструкций pNL1.1CMV, обрабатывали различными дозами леналидомида в течение 4 часов.
ФИГ. 9A представляет собой вестерн-блот, на котором показана 4-часовая леналидомид-зависимая деградация однопроходных мембранных белков CD3-дзета, химеры CD8/CD3-дзета, CD8, CD19 и CD22 с меткой-дегроном на С-конце. Клетки Jurkat инфицировали с помощью вирусной конструкции pNGX_LV_V002-CDx-IKZF3 136-180 и 236-249, проводили отбор с помощью G418 и обрабатывали с помощью 10 мкМ леналидомида или DMSO. На ФИГ. 9A показано окрашивание с применением антитела к V5 (показаны как длительное 1-минутное воздействие, так и короткое 1-секундное воздействие) и антитела к бета-актину. Все конструкции экспрессировались и подвергались деградации при обработке 10 мкМ леналидомида. В таблице на ФИГ. 9A показаны молекулярная масса (MW) белка, число цитозольных аминокислотных остатков ("цитозольные AA") и число цитозольных лизинов для каждого белка. Интересно, что деградация лучше коррелирует с суммарным числом цитоплазматических аминокислот ("AA"), чем с числом цитозольных остатков лизина. ФИГ. 9B, 9C и 9D представляют собой диаграммы вестерн-блотов, на которых показана леналидомид-зависимая деградация CD19 с меткой на C-конце (ФИГ. 9B), CD3-дзета с меткой на C-конце (ФИГ. 9C) и CD8/CD3-дзета с меткой на C-конце (ФИГ. 9D). Клетки, экспрессирующие CD19, CD3-дзета или CD8/CD3-дзета с меткой IKZF3 136-180 и 236-249 обрабатывали с помощью 10 мкМ леналидомида в течение 6 часов или различными дозами леналидомида в течение 24 часов. На ФИГ. 9B показано, что деградация CD19 с меткой IKZF3 136-180 и 236-249 характеризуется IC50, составляющей приблизительно 100 нМ, и сильную деградацию определяли через 6 часов. Деградация CD3-дзета с меткой IKZF3 136-180 и 236-249, показанная на ФИГ. 9C, является более слабой, чем деградация CD19 с меткой IKZF3 136-180 и 236-249. Деградация меченого CD3-дзета была выраженной после того, как клеток обрабатывали с помощью 10 мкМ леналидомида в течение 24 часов. Деградация CD8/CD3-дзета с меткой IKZF3 136-180 и 236-249, показанная на ФИГ. 9D, является более сильной, чем деградация CD3-дзета с меткой IKZF3 136-180 и 236-249.
ФИГ. 10A, 10B, 10C и 10D представляют собой серию гистограмм проточной цитометрии, сравнивающих экспрессию CD19 с меткой IKZF3 136-180 и 236-249 на клеточной поверхности клеток Jurkat, которые обрабатывали с помощью 1 мкМ или 10 мкМ леналидомида в течение 1 часа (ФИГ. 10A), 6 часов (ФИГ. 10B), 16 часов (ФИГ. 10C) или 24 часов (ФИГ. 10D). Некоторые клетки предварительно обрабатывали с помощью 10 мкМ MG132 до обработки с помощью 10 мкМ леналидомида. DMSO служил в качестве контроля со средой-носителем. IKZF3 136-180 и 236-249 сливали с C-концом CD19. ФИГ. 10E и 10F представляют собой столбчатые диаграммы, на которых показан % CD19-положительных клеток (ФИГ. 10E) или средняя интенсивность флуоресценции (MFI) CD19-положительных клеток (ФИГ. 10F) для всех протестированных доз леналидомида и моментов времени. Минимальную деградацию наблюдали через 1 час и незначительную деградацию через 6 часов. Деградация была намного более заметна через 16 и 24 часа в обеих группах обработки 1 мкМ и 10 мкМ, и эту деградацию можно было частично блокировать за счет ингибитора протеасомы MG132. Наблюдали примерно 50% снижение числа CD19-положительных клеток через 16 часов в обеих группах обработки 1 мкМ и 10 мкМ (ФИГ. 10E), и это снижение соответствовало снижению MFI (ФИГ. 10F).
ФИГ. 11 представляет собой схему, на которой показан иллюстративный слитый белок, содержащий домен деградации (дегрон), сайт расщепления протеазами и второй белковый домен (CAR), а также изменение деградации слитого белка в присутствии лекарственного средства, например, стабилизирующего соединения.
ФИГ. 12A, 12B и 12C представляют собой схемы, на которых показана регуляция молекулы CAR, слитой с FurON (ФИГ. 12A), HilD (ФИГ. 12B) или как с FurON, так и с HilD (ФИГ. 12C). Как показано на ФИГ. 12A, CAR, слитый с FurON, может быть "включен" при введении стабилизирующего соединения (например, низкомолекулярного лиганда, который связывается с доменом деградации и стабилизирует его, например, базедоксифена (BZA)) или "выключен" при удалении стабилизирующего соединения. Как показано на ФИГ. 12B, CAR, слитый с HilD-меткой, может быть "включен" при введении соединения IMiD (например, леналидомида или помалидомида) и вновь "выключен" при прекращении введения соединения IMiD. Как показано на ФИГ. 12C, CAR, слитый как с FurON, так и с HilD-меткой, может быть "включен" при введении стабилизирующего соединения, "выключен" при остановке введения стабилизирующего соединения и введении соединения IMiD и вновь "включен" при остановке введения соединения IMiD и введении стабилизирующего соединения. Объединение переключателя FurON и переключателя HilD добавляет дополнительные возможности регуляции экспрессии и активности молекулы CAR.
ФИГ. 13A, 13B и 13C представляют собой диаграммы вестерн-блотов, на которых показана леналидомид-зависимая деградация молекулы CAR. Клетки JNL, экспрессирующие конструкцию 765 (FurON_CAR19) (ФИГ. 13A), конструкцию 766 (FurON_CAR19_16GS_HilD-метка_V5) (ФИГ. 13B) или конструкцию 767 (FurON_CAR19_16GS_HilD-метка) (ФИГ. 13C), инкубировали в присутствии 10 мкМ леналидомида ("+") или DMSO ("-") в течение 24 часов перед проведением вестерн-блоттинг-анализа. Все образцы обрабатывали 1 мкМ базедоксифена. "A" представляет клетки, трансдуцированные с помощью 275 мкл вирусного супернатанта. "B" представляет клетки, трансдуцированные с помощью 700 мкл вирусного супернатанта.
ФИГ. 14A, 14B, 14C и 14D представляют собой диаграммы вестерн-блотов, на которых показана леналидомид-зависимая деградация молекулы CAR. Клетки JNL, экспрессирующие конструкцию 771 (CAR19_HilD-метка_V5) (ФИГ. 14A), конструкцию 769 (CAR19_16GS_HilD-метка) (ФИГ. 14B), конструкцию 768 (CAR19_16GS_HilD-метка_V5) (ФИГ. 14C) или конструкцию 770 (CAR19_16GS_HilD-метка_без K), инкубировали в присутствии 10 мкМ леналидомида ("+") или DMSO ("-") в течение 24 часов перед проведением вестерн-блоттинг-анализа. "A" представляет клетки, трансдуцированные с помощью 275 мкл вирусного супернатанта. "B" представляет клетки, трансдуцированные с помощью 700 мкл вирусного супернатанта.
ФИГ. 15A и 15B представляют собой диаграммы вестерн-блотов, на которых показана леналидомид-зависимая деградация молекулы CAR. Клетки JNL, экспрессирующие конструкцию 769 (CAR19_16GS_HilD-метка), инкубировали с 10 мкМ леналидомида или DMSO в течение 2, 4, 8, 16 или 24 часов (ФИГ. 15A) или инкубировали с различными дозами леналидомида или DMSO в течение 24 часов (ФИГ. 15B) перед проведением вестерн-блоттинг-анализа. На ФИГ. 15A показана временная динамика при обработке 10 мкМ леналидомида. На ФИГ. 15B показан дозозависимый ответ на леналидомид через 24 часа.
ФИГ. 16A, 16B, 16C, 16D, 16E, 16F и 16G представляют собой комплект гистограмм проточной цитометрии, показывающих экспрессию CAR на поверхности клеток в присутствии или в отсутствие леналидомида. Протестированные конструкции включают: конструкцию 769 (CAR19_16GS_HilD-метка) (ФИГ. 16A), конструкцию 771 (CAR19_HilD-метка_V5) (ФИГ. 16B), конструкцию 6761 (CAR19_16KGS_HilD-метка_V5) (ФИГ. 16C), конструкцию 768 (CAR19_16GS_HilD-метка_V5) (ФИГ. 16D), конструкцию 770 (CAR19_16GS_HilD-метка_без K) (ФИГ. 16E), конструкцию 773 (HilD-метка_CAR19_modSigPep) (ФИГ. 16F) b конструкцию 774 (HilD-метка_CAR19) (ФИГ. 16G). Клетки JNL, экспрессирующие указанные конструкции, инкубировали с 10 мкМ леналидомида или без него в течение 24 часов и затем подвергали анализу посредством проточной цитометрии.
ФИГ. 17A, 17B и 17C представляют собой комплект гистограмм проточной цитометрии, показывающих экспрессию CAR на клеток под контролем леналидомида и/или базедоксифена (BZA). Протестированные конструкции включали: конструкцию 765 (FurON_CAR19) (ФИГ. 17A), конструкцию 767 (FurON_CAR19_16GS_HilD-метка) (ФИГ. 17B) и конструкцию 766 (FurON_CAR19_16GS_HilD-метка_V5) (ФИГ. 17C). Клетки JNL, экспрессирующие указанные конструкции, инкубировали в присутствии или в отсутствие леналидомида и/или базедоксифена (BZA) в течение 24 часов до анализа посредством проточной цитометрии.
ФИГ. 18A, 18B, 18C и 18D представляют собой комплект гистограмм проточной цитометрии, показывающих экспрессию CAR на поверхности клеток в присутствии или в отсутствие различных концентраций леналидомида. Протестированные конструкции включали: конструкцию 769 (CAR19_16GS_HilD-метка) (ФИГ. 18A и 18C) и конструкцию 770 (CAR19_16GS_HilD-метка_без K) (ФИГ. 18B и 18D). Клетки JNL, экспрессирующие указанные конструкции, инкубировали в присутствии или в отсутствие леналидомида в течение 4 часов (ФИГ. 18A и 18B) или 20 часов (ФИГ. 18C и 18D) до анализа посредством проточной цитометрии. ФИГ. 18E и 18F представляют собой столбчатые диаграммы, на которых показаны % экспрессии CAR (ФИГ. 18E) или средняя интенсивность флуоресценции (ФИГ. 18F) для каждой клеточной линии и каждой протестированной концентрации леналидомида.
ФИГ. 19A и 19B представляют собой серию столбчатых диаграмм, на которых показаны сравнения ответов на леналидомид при разных условиях обработки линии клеток-мишеней для JNL, продолжительности времени обработки линии клеток-мишеней, времени обработки леналидомидом и количестве клеток. ФИГ. 19A представляет собой комплект диаграмм, на которых показаны сигналы люминесценции в исследовании, где клетки JNL, экспрессирующие конструкцию 769 (CAR19_16GS_HilD-метка) (9000 или 12000 клеток/лунка), обрабатывали с помощью 10 мкМ леналидомида в течение 4 часов или 24 часов и затем инкубировали с клетками Nalm6, CD19-экспрессирующими клетками K562 ("K562 +CD19"), клетками K562 или средой (без клеток) в течение 4 часов, 8 часов или 20 часов. ФИГ. 19B представляет собой комплект диаграмм, на которых показана подгруппа данных из исследования, описанного на ФИГ. 19A: Клетки JNL, экспрессирующие конструкцию 769 (CAR19_16GS_HilD-метка) (9000 клеток/лунка), обрабатывали с помощью 10 мкМ леналидомида в течение 4 часов и затем инкубировали с клетками Nalm6, CD19-экспрессирующими клетками K562 ("K562 +CD19"), клетками K562 или средой (без клеток) в течение 20 часов. По y-оси на ФИГ. 19B показаны сигналы люминесценции после вычитания фоновых сигналов (сигналов от среды образца). На обеих ФИГ. 19A и 19B два столбца на каждой диаграмме представляют образцы, обработанные с помощью DMSO ("DMSO"), и образцы, обработанные с помощью леналидомида ("леналидомид (10 мкМ μM)"), соответственно.
ФИГ. 20A и 20B представляют собой серию столбчатых диаграмм, на которых показаны сравнения ответов на леналидомид при разных условиях обработки клеток-мишеней для JNL, продолжительности времени обработки клеток-мишеней, времени обработки леналидомидом и количестве клеток. ФИГ. 20A представляет собой комплект диаграмм, на которых показаны сигналы люминесценции в исследовании, где клетки JNL, экспрессирующие конструкцию 767 (FurON_CAR19_16GS_HilD-метка) (9000 или 12000 клеток/лунка), обрабатывали с помощью 10 мкМ леналидомида в течение 4 часов или 24 часов и затем инкубировали с клетками Nalm6, CD19-экспрессирующими клетками K562 ("K562 +CD19"), клетками K562 или средой (без клеток) в течение 4 часов, 8 часов или 20 часов. ФИГ. 20B представляет собой комплект диаграмм, на которых показана подгруппа данных из исследования, описанного на ФИГ. 20A: Клетки JNL, экспрессирующие конструкцию 767 (FurON_CAR19_16GS_HilD-метка) (9000 клеток/лунка), обрабатывали с помощью 10 мкМ леналидомида в течение 4 часов и затем инкубировали с клетками Nalm6, CD19-экспрессирующими клетками K562 ("K562 +CD19"), клетками K562 или средой (без клеток) в течение 20 часов. По y-оси на ФИГ. 20B показаны сигналы люминесценции после вычитания фоновых сигналов (сигналов от среды образца). На обеих ФИГ. 20A и 20B четыре столбца на каждой диаграмме представляют образцы, не обработанные леналидомидом и базедоксифеном ("DMSO>>DMSO"), образцы, обработанные базедоксифеном, но не леналидомидом ("DMSO>>BZA (1 мкМ)"), образцы, обработанные леналидомидом, но не базедоксифеном ("леналидомид (10 мкМ)>>DMSO"), и образцы, обработанные как леналидомидом, так и базедоксифеном ("леналидомид (10 мкМ)>>BZA (1 мкМ)"), соответственно.
ФИГ. 21A, 21B, 21C и 21D представляют собой диаграммы, на которых показан дозозависимый эффект леналидомида на люциферазный репортер NFAT для трех различных моментов времени обработки. Клетки JNL, экспрессирующие конструкцию 765 (FurON_CAR19) (ФИГ. 21A), конструкцию 767 (FurON_CAR19_16GS_HilD-метка) (ФИГ. 21B), конструкцию 769 (CAR19_16GS_HilD-метка) (ФИГ. 21C) или конструкцию 770 (CAR19_16GS_HilD-метка_без K) (ФИГ. 21D), инкубировали клетками-мишенями K562 ("K562") или клетками-мишенями K562, экспрессирующими CD19 ("K562+CD19"). Леналидомид добавляли за 20 часов до добавления клеток-мишеней (44-часовая обработка леналидомидом, "20 ч до клеток-мишеней"), за 4 часа до добавления клеток-мишеней (28-часовая обработка леналидомидом, "4 ч до клеток-мишеней") или через 16 часов после добавления клеток-мишеней (8-часовая обработка леналидомидом, "16 ч после клеток-мишеней"). Клетки JNL, экспрессирующие конструкцию 765 (FurON_CAR19) (ФИГ. 21A) или конструкцию 767 (FurON_CAR19_16GS_HilD-метка) (ФИГ. 21B), также обрабатывали базедоксифеном. На каждой диаграмме исходный сигнал люминесценции нанесен на график относительно указанной концентрации леналидомида.
ФИГ. 22A, 22B, 22C и 22D представляют собой диаграммы, на которых показаны данные из исследования, описанного на ФИГ. 21A, 21B, 21C и 21D, где клетки JNL обрабатывали с помощью MG132 за 5 часов до обработки K562+CD19 клетками-мишенями и обрабатывали леналидомидом за 4 часа до обработки K562+CD19 клетками-мишенями. Протестированные клетки включали: клетки JNL, экспрессирующие конструкцию 765 (FurON_CAR19) (ФИГ. 22A), конструкцию 767 (FurON_CAR19_16GS_HilD-метка) (ФИГ. 22B), конструкцию 769 (CAR19_16GS_HilD-метка) (ФИГ. 22C) или конструкцию 770 (CAR19_16GS_HilD-метка_без K) (ФИГ. 22D). Четыре столбца на каждой диаграмме представляют образцы, обработанные с помощью базедоксифена (BZA), MG132 и леналидомида ("BZA, MG132, леналидомид"), образцы, обработанные с помощью базедоксифена (BZA) и леналидомида ("BZA, леналидомид"), образцы, обработанные с помощью базедоксифена (BZA) ("BZA"), и образцы, обработанные только с помощью DMSO("DMSO"), соответственно. По y-оси на каждой диаграмме показан исходный сигнал люминесценции.
ФИГ. 23 представляет собой комплект схем, на которых показаны конструкции слияния HilD-тау. Использовали изоформу тау-белка 0N4R, которая содержит C-концевой экзон с доменом повтора, но содержит N-концевых экзонов. Использовали лентивирусные конструкций, хотя все конструкции вводили посредством трансфекции с липофектамином или нуклеофекции. Продукты слияния с тау-белком экспрессировались ниже промотора CAG или CMV.
ФИГ. 24A и 24B представляют собой диаграммы, на которых показаны дизайн и результаты исследования, проверяющего привлечение E3-лигазы CRBN к слитым белкам HilD-тау. ФИГ. 24A. Схема эксперимента. Леналидомид привлекает E3-лигазу цереблон (CRBN) к бета-шпильке IKZF3, что приводит к убиквитинированию и деградации ассоциированного белка. Для тестирования того, что данное привлечение происходило у слияний HilD-тау, создавали слияния HilD-тау-биотинлигаза. В присутствии биотина биотинлигаза образует реакционно-способные молекулы биотина, которые ковалентно связываются с ближайшими белками. Если добавляют леналидомид, CRBN должен привлекаться к слиянию HilD-тау и должен находиться в радиусе биотинилирования, опосредованного биотинлигазой. ФИГ. 24B. Клетки HEK293T трансфицировали с помощью слияний CRBN с FLAG-меткой и HilD-тау-биотинлигазы или тау-биотинлигазы. Через 48 часов после трансфекции клетки обрабатывали в течение 21 часа с помощью 50 мкМ биотина и либо DMSO, либо 1 мкМ леналидомида. После этого клетки промывали в PBS и затем лизировали в ледяном буфере M-PER с ингибиторами протеазы. Предположительно примерно 1 миллион клеток лизировали в объеме 300 мкл. Вестерн-блоттинг-анализ клеточного лизата показан на нижнем блоте, при зондировании с антителами к тау-белку (HT7) или GAPDH. Биотинилированные белки подвергали иммунопреципитации путем инкубирования 20% клеточного лизата с 50 мкл магнитных микрогранул со стрептавидином (Dynabeads M-280) в течение 30 минут при комнатной температуре. Биотинилированные белки элюировали из микрогранул путем кипячения и затем анализировали посредством вестерн-блоттинга. При анализе в отношении сигнала FLAG на FLAG-CRBN широкие полоски наблюдали только у подвергнутого иммунопреципитации материала из клеток HEK293T, обработанных леналидомидом и содержащих HilD-метки, но не у клеток, обработанных с помощью DMSO, или у клеток, обработанных леналидомидом, но трансфицированным с помощью конструкций с тау-белком, не содержащих HilD-метку.
ФИГ. 25A, 25B и 25C представляют собой диаграммы, на которых показано снижение уровня токсичного тау-белка путем индуцируемого привлечения E3-лигазы CRBN. Клетки HEK293T трансфицировали с помощью конструкций со слиянием HilD-тау (P301S)-YFP. Тау-белок (P301S) представляет собой склонную к образованию скоплений форму тау-белка, идентифицированную у пациентов с наследственными нейродегенеративными заболеваниями. После обработки леналидомидом на протяжении ночи флуоресценция YFP снижалась дозозависимым образом под действием леналидомида, что видно на визуализации флуоресценции YFP (ФИГ. 25A). Показано по девять полей зрения для каждого условия. ФИГ. 25B. Интенсивность флуоресценции YFP количественно определяли после обработки леналидомидом в различных дозах. ФИГ. 25C. Отмечали токсичность, обусловленную сверхэкспрессией склонного к образованию скоплений тау-белка, которую оценивали количественно как число клеток, идентифицированных за счет вычленения при флуоресценции красителя Hoecht. При обработке леналидомидом гибель клеток прекращалась, и снижение уровней тау-белка указывает на то, что индуцируемая леналидомидом деградация может оказывать цитопротекторное действие при нацеленной белковой деградации токсичных белков.
ФИГ. 26A, 26B, 26C и 26D представляют собой диаграммы, на которых показано количественное определение снижения содержания тау-белка и снижение содержания специфических форм тау-белка в клетках HEK293T при индуцируемом привлечении CRBN. ФИГ. 26A. Клетки HEK293T трансфицировали конструкциями со слиянием HilD-тау (дикого типа) и обрабатывали с помощью либо леналидомида при разных дозах, либо DMSO. Верхний и нижний вестерн блоты представляют эксперименты, проводимые в трех повторностях. Интенсивность полосок тау-белка, при использовании либо поликлонального антитела к тау-белку (Dako), либо антитела к фосфорилированным формам тау-белка (AT8), оценивали количественно путем нормализации относительно интенсивности полоски с антителом к актину. Трансфекция уменьшенного количества ДНК в данном эксперименте давала большее снижение фосфорилированной формы тау-белка (1X ДНК: 0,625 микрограммов ДНК трансфицировали в 50 мкл среды Optimem с 1,5 мкл липофектамина 2000; 0,1X ДНК=0,0625 микрограммов; в 24-луночных планшетах с клетками HEK). Это позволяет предположить, что такая система может измерять мощность деградации тау-белка, опосредованной E3-лигазой. В экспериментах показано, что дозу леналидомида применяли в течение 4 часов после трансфекции (в случае трансфекции с более высокой концентрацией ДНК) или 24 часов после трансфекции (в случае трансфекции с более низкой концентрацией ДНК). ФИГ. 26B. Левые панели: уровень тау-белка без HilD-метки не снижался при обработке леналидомидом. Правые панели: отсутствует снижение уровней тау-белка при обработке леналидомидом в клетках HEK293T с нокаутом по цереблону (CRBN). ФИГ. 26C. Количественное определение дозозависимого ответа интенсивности YFP на обработку леналидомидом в клетках с нокаутом (KO) по цереблону (CRBN) в сравнении с клетками дикого типа (WT) (те же данные для клеток дикого типа, показанные на ФИГ. 26B). ФИГ. 26D. Совместная обработка с ингибитором неддилирования MLN4924 (1 мкМ), включающая 1-часовую предварительную обработку с помощью MLN4924, также предотвращала деградацию тау-белка. Совместно эти данные указывают на то, что E3-лигазная функция CRBN требуется для деградации слияния HilD-тау, индуцированного леналидомидом.
ФИГ. 27 представляет собой комплект диаграмм, на которых показана оценка склонности к образованию скоплений у слияния HilD-тау (P301S)-YFP, экспрессируемого в кортикальных нейронах грызунов. Кортикальные нейроны грызунов подвергали нуклеофекции с помощью слияния HilD-тау (P301S)-YFP, а затем последовательно инкубировали с нерастворимыми фракциями тау-белка, выделенными из мыши, трансгенной по тау-белку, полученной в лаборатории. Прижизненную флуоресценцию YFP визуализировали с применением анализатора InCell 6000. На средней и нижней панелях показано увеличенное изображение нейронов, идентифицированных на верхней панели. Скопления тау-белка, на которые указывает интенсивная точечная флуоресценция YFP, явно различимы.
ФИГ. 28 представляет собой комплект диаграмм, на которых показана опосредованная леналидомидом деградация HilD-тау (P301S)-YFP, экспрессируемого в нейронах крыс. Кортикальные нейроны грызунов подвергали нуклеофекции с помощью слияния HilD-тау (P301S)-YFP или слияния тау (P301S)-YFP. Также тестировали совместную трансфекцию с CRBN с FLAG-меткой (верхние ряды). Начиная с 9 дней in vitro, нейроны обрабатывали указанными дозами леналидомида. Нейроны визуализировали прижизненно в отношении флуоресценции YFP в указанные интервалы времени. Обработка леналидомидом с течением времени снижала интенсивность YFP относительно нейронов, экспрессирующих HilD-тау (P301S)-YFP и обработанных с помощью DMSO, или нейронов, экспрессирующих тау (P301S)-YFP и обработанных леналидомидом. Деградация происходила как при совместной трансфекции с CRBN человека, так и без нее, что указывает на то, что слияние HilD-тау может быть подвергаться деградации с леналидомидом под действием CRBN или грызуна, или человека.
ФИГ. 29 представляет собой комплект диаграмм, на которых показана опосредованная леналидомидом деградация HilD-тау (P301S)-YFP, экспрессируемого в нейронах крыс. Суспензию отдельных клеток из диссоциированных нейросфер человека возрастом 63 дня in vitro, которые были получены из эмбриональных стволовых клеток, подвергали нуклеофекции с помощью HilD - тау (P301S) - YFP. Нейросферы содержат как нейроны, так и предшественники нейронов. После 10 дней культивирования нейроны обрабатывали леналидомидом (при суммарном возрасте 73 дня in vitro). На фотографиях показана флуоресценция YFP после 20 часов обработки леналидомидом при указанной дозе. Леналидомид в значительной степени снижал интенсивность флуоресценции YFP дозозависимым образом.
ФИГ. 30A и 30B представляют собой комплект диаграмм, на которых показана опосредованная леналидомидом деградация CAR19-16GS-HilD-метка. ФИГ. 30A представляет собой комплект диаграмм вестерн-блотов для клеток Jurkat, трансдуцированных с помощью CAR19-HilD-метка, обработанных одной дозой леналидомида с течением времени. Тестировали образцы после обработки соединением или после периода отмывки. ФИГ. 30B представляет собой комплект гистограмм проточной цитометрии, анализирующих те же образцы, которые использовали в вестерн-блоттинг-анализе. Антитело к CD3-дзета использовали в вестерн-блоттинг-анализе и конъюгат CD19-PE использовали в анализе посредством проточной цитометрии.
ФИГ. 31A, 31B и 31C представляют собой комплект гистограмм проточной цитометрии, анализирующих экспрессию CAR в различных условиях. ФИГ. 31A представляет собой комплект гистограмм проточной цитометрии, на которых показана экспрессия CAR в первичных T-клетках. Эффект леналидомида на экспрессию CAR19 через 24 часа показан на ФИГ. 31B. Эффект леналидомида на экспрессию CAR19-HilD через 24 или 48 часов показан на ФИГ. 31C.
ФИГ. 32A, 32B и 32C представляют собой комплект гистограмм, на которых показан % уничтожения, опосредованного CAR-T клетками. ФИГ. 32A представляет собой диаграмму, на которой показан процент уничтожения для CD19-отрицательных клеток. ФИГ. 32B и 32C представляют собой диаграммы, на которых показан процент уничтожения CAR19-T-клетками (ФИГ. 32B) или CAR19-HilD T клетками (ФИГ. 32C) для CD19-положительный клеток в присутствии или в отсутствие 1 мкМ леналидомида.
ФИГ. 33A и 33B представляют собой диаграммы, на которых показаны соответственно уровни IFN-гамма и IL2, секретируемых из T-клеток, экспрессирующих CAR19 или CAR19-HilD, в присутствии или в отсутствие 1 мкМ леналидомида. По x-оси показана концентрация леналидомида в мкМ.
ФИГ. 34 представляет собой диаграмму, на которой показано, что леналидомид устраняет способность CART19.HilD контролировать опухолевый рост in vivo. Суммарный поток ROI нанесен на график относительно дней после имплантации Nalm6.
ФИГ. 35 представляет собой комплект графиков проточной цитометрии, показывающих утрату экспрессии CAR19-HilD после обработки леналидомидом.
ФИГ. 36 представляет собой диаграмму, на которой показаны уровни контроля опухоли в различных группах обработки. Суммарный поток ROI нанесен на график относительно дней после имплантации Nalm6. Ранняя инъекция леналидомида эффективно устраняла экспрессию CART у мышей, которых обрабатывали с помощью CART-HilD, что приводило к отсутствию контроля опухоли в данной группе. Более поздняя обработка леналидомидом (день 5 после инъекции CART) также снижала функцию CART, на что указывает утрата контроля опухоли в данной группе мышей.
ФИГ. 37A, 37B, 37C, 37D и 37E представляют собой диаграммы, анализирующие экспрессию CAR в CD3+ клетках из спленоцитов. ФИГ. 37A представляет собой диаграмму, на которой показана экспрессия CAR в CD3+ клетках из спленоцитов мышей, обработанных с помощью CART-HilD (группа 1). ФИГ. 37B, 37C и 37D представляют собой диаграммы, на которых показана экспрессия CAR в CD3+ клетках из спленоцитов мышей, обработанных с помощью CART-HilD и леналидомида (группа 2, группа 3 и группа 4 соответственно). Пики на ФИГ. 37A-37D представляют уровни экспрессии CD3 у отдельный мышей. Группа 1. CART19.HilD (5×106). Группа 2. CART19-HilD (5×106) + леналидомид qd. Группа 3. CART19-HilD (5×106) + леналидомид bid. Группа 4. CART19.HilD (5×106) + леналидомид+ 5 дней. ФИГ. 37E представляет собой диаграмму, обобщающую данные.
ФИГ. 38A, 38B и 38C представляют собой диаграммы, на которых показано воздействие соединения I-112 на экспрессию и активность CAR19-CARB-метка. ФИГ. 38A представляет собой вестерн-блот для клеток Jurkat с NFAT-люциферазой (JNL), экспрессирующих CAR19-CARB-метку, обработанных различными дозами соединения I-112 или DMSO в течение 24 часов, на которых показана дозочувстительная деградация CAR19-CARB-метки. ФИГ. 38B представляет собой комплект гистограмм, на которых показан анализ посредством проточной цитометрии экспрессии CAR19 на поверхности клеток JNL с CAR19-CARB-меткой по сравнению с клетками с немеченным CAR19 после обработки с помощью 10 мкМ соединения I-112. ФИГ. 38C представляет собой диаграмму, на которой показаны результаты JNL-анализа для клеток JNL с люциферазой, экспрессирующих CAR19-CARB-метку, обработанных разными дозами соединения I-112 в течение 15 часов с последующей совместной обработкой с помощью либо клеток K562 (CD19-), либо клеток Nalm6 (CD19+) со считыванием люциферазной активности.
ФИГ. 39 представляет собой вестерн-блот для клеток HEK293T, транзиентно трансфицированный с помощью CARB-метка-MITF-FLAG и обработанных с помощью одного из 10 мкМ, 1 мкМ, 0,1 мкМ или 0,01 мкМ соединения I-112, или леналидомида, или DMSO, что показывает I-112-специфическую деградацию MITF с CARB-меткой.
ФИГ. 40A и 40B представляют собой диаграммы, анализирующие воздействие леналидомида на экспрессию и активность CAR для BCMA-HilD-метки. ФИГ. 40A представляет собой комплект гистограмм, на которых показаны результаты анализа посредством проточной цитометрии клеток JNL, инфицированных с помощью CAR для BCMA-HilD-метки и обработанных с помощью различных доз леналидомида в течение 24 часов, что показывает деградацию CAR для BCMA, зависимую от дозы леналидомида. ФИГ. 40B представляет собой диаграмму, на которой показаны результаты JNL-анализа для клеток Jurkat с NFAT- люциферазой, экспрессирующих BCMA-CARB-метку, обработанных разными дозами леналидомида в течение 15 часов с последующей совместной обработкой с помощью клеток KMS11 со считыванием люциферазной активности.
ПОДРОБНОЕ ОПИСАНИЕ
В настоящем изобретении, по крайней мере помимо прочего, представлен слитый полипептид, содержащий полипептид, связывающий соединение формулы (I) (COF1)/CRBN, полипептид, связывающий соединение формулы (II) (COF2)/CRBN, или полипептид, связывающий соединение формулы (III) (COF3)/CRBN, предназначенный для нацеливаемой инактивации белков. В некоторых вариантах осуществления слитый полипептид содержит один или несколько COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающих полипептидов и один или несколько гетерологичных полипептидов, например, гетерологичных полипептидов млекопитающего, бактериальных или вирусных полипептидов, например, один или несколько представляющих интерес полипептидов. COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид может быть функционально связан с гетерологичным полипептидом, например, через линкер. В некоторых вариантах осуществления в присутствии COF1 или COF2 (такого как талидомид и его производные (например, леналидомид, помалидомид и талидомид)) или в присутствии COF3 (например, соединения, раскрытого в таблице 29) COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид увеличивает деградацию слитого полипептида, например, деградацию, опосредованную убиквитинированием; и/или изменяет уровень и/или активность слитого полипептида. В некоторых вариантах осуществления деградация слитого полипептида является убиквитин-зависимой.
Без ограничения какой-либо теорией, в некоторых вариантах осуществления в COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающем полипептиде предусмотрены аминокислотная последовательность и/или структурный мотив, которые в присутствии COF1 или COF2 (такого как талидомид и его производные (например, леналидомид, помалидомид и талидомид)) или в присутствии COF3 (например, соединения, раскрытого в таблице 29) приводят к посттрансляционной модификации (например, убиквитинированию) слитого полипептида, что приводит к модифицированному, например, убиквитинированному, слитому полипептиду. Например, одна или несколько аминокислот, например, лизин или метионин, в слитом полипептиде могут подвергаться убиквитинированию в присутствии COF1, COF2 или COF3. В некоторых вариантах осуществления убиквитинированный слитый полипептид подвергается селективной деградации. В некоторых вариантах осуществления посттрансляционная модификация слитого полипептида увеличивает деградацию (например, увеличивает уровень или скорость деградации) слитого полипептида (например, всего гетерологичного полипептида или его части). В некоторых вариантах осуществления увеличение уровня и/или скорости деградации составляет по меньшей мере 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 100%, 200%, 500%, 10 раз, 100 раз, 1000 раз или более относительно уровня и/или скорости деградации эталонного белка, например, слитого полипептида в отсутствие COF1, COF2 или COF3, гетерологичного полипептида, слияния гетерологичного полипептида без COF1/CRBN-, COF2/CRBN-или COF3/CRBN-связывающего полипептида или слияния гетерологичного полипептида с фрагментом, отличным от COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающего полипептида.
Без ограничения какой-либо теорией, деградация слитого полипептида может включать одну, две или все из следующих стадий: (1) связывание COF1 или COF2 (например, талидомида и его производных (например, леналидомида)) или COF3 (например, соединения, раскрытого в таблице 29) с одной или несколькими субъединицами комплекса убиквитинлигазы (например, комплекса убиквитинлигазы E3), например, связывание с CUL4, RBX1, DDBI и/или CRBN, также известным как CRL4(CRBN), как правило, с комплексом DDB1-CRBN, за счет чего образуется комплекс COF1-лигаза или COF2-лигаза;
(2) комплекс COF1-лигаза, COF2-лигаза или COF3-лигаза связывается и увеличивает убиквитинирование одной или нескольких аминокислот, например, лизина или метионина, в слитом полипептиде, за счет чего образуется убиквитинированный слитый полипептид, например, моно- или полиубиквитинированный слитый полипептид; и
(3) убиквитинированный слитый полипептид направляется на деградацию, например, слитый полипептид селективно направляется, например, к протеасоме, для деградации.
В некоторых вариантах осуществления COF1/CRBN- или COF2/CRBN-связывающий полипептид содержит от приблизительно 10 до приблизительно 95 аминокислотных остатков, от приблизительно 15 до приблизительно 90 аминокислотных остатков, от приблизительно 20 до приблизительно 85 аминокислотных остатков, от приблизительно 25 до приблизительно 80 аминокислотных остатков, от приблизительно 30 до приблизительно 75 аминокислотных остатков, от приблизительно 35 до приблизительно 70 аминокислотных остатков, от приблизительно 40 до приблизительно 65 аминокислотных остатков, от приблизительно 45 до приблизительно 65 аминокислотных остатков, от приблизительно 50 до приблизительно 65 аминокислотных остатков или от приблизительно 55 до приблизительно 65 аминокислотных остатков из IKZF1 (например, SEQ ID NO: 20) или IKZF3 (например, SEQ ID NO: 19).
В некоторых вариантах осуществления COF3/CRBN-связывающий полипептид содержит от приблизительно 10 до приблизительно 95 аминокислотных остатков, от приблизительно 15 до приблизительно 90 аминокислотных остатков, от приблизительно 20 до приблизительно 85 аминокислотных остатков, от приблизительно 25 до приблизительно 80 аминокислотных остатков, от приблизительно 30 до приблизительно 75 аминокислотных остатков, от приблизительно 35 до приблизительно 70 аминокислотных остатков, от приблизительно 40 до приблизительно 65 аминокислотных остатков, от приблизительно 45 до приблизительно 65 аминокислотных остатков, от приблизительно 50 до приблизительно 65 аминокислотных остатков или от приблизительно 55 до приблизительно 65 аминокислотных остатков из IKZF2 (например, SEQ ID NO: 21).
В некоторых вариантах осуществления COF1/CRBN- или COF2/CRBN-связывающий полипептид содержит бета-изгиб (например, бета-изгиб из IKZF3). В некоторых вариантах осуществления COF1/CRBN- или COF2/CRBN-связывающий полипептид содержит бета-изгиб (например, бета-изгиб из IKZF3) и альфа-спираль (например, альфа-спираль из IKZF3). В некоторых вариантах осуществления COF1/CRBN- или COF2/CRBN-связывающий полипептид содержит аминокислотные остатки 136-170, или 136-180, и/или 236-249 из IKZF3 (пронумерованные в соответствии с SEQ ID NO: 19) или аминокислотную последовательность, практически идентичную им (например, на по меньшей мере 85, 87, 90, 95, 97, 98, 99, или 100% идентичную им). В некоторых вариантах осуществления COF1/CRBN- или COF2/CRBN-связывающий полипептид содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1-6, 11-15, 40, 41-43, 77, 78, 84-86, и 100, или аминокислотную последовательность, практически идентичную ей (например, на по меньшей мере 85, 87, 90, 95, 97, 98, 99, или 100% идентичную ей).
В некоторых вариантах осуществления COF3/CRBN-связывающий полипептид содержит бета-изгиб (например, бета-изгиб из IKZF2). В некоторых вариантах осуществления COF3/CRBN-связывающий полипептид содержит бета-изгиб (например, бета-изгиб из IKZF2) и альфа-спираль (например, альфа-спираль из IKZF2). В некоторых вариантах осуществления COF3/CRBN-связывающий полипептид содержит аминокислотные остатки 130-174 и/или 230-243 из IKZF2 (пронумерованные в соответствии с SEQ ID NO: 21) или аминокислотную последовательность, практически идентичную им (например, на по меньшей мере 85, 87, 90, 95, 97, 98, 99, или 100% идентичную им). В некоторых вариантах осуществления COF3/CRBN-связывающий полипептид содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 109, 113 и 114, или аминокислотную последовательность, практически идентичную ей (например, на по меньшей мере 85, 87, 90, 95, 97, 98, 99, или 100% идентичную ей).
В некоторых вариантах осуществления COF1/CRBN- или COF2/CRBN-связывающий полипептид содержит бета-изгиб (например, бета-изгиб из IKZF1). В некоторых вариантах осуществления COF1/CRBN- или COF2/CRBN-связывающий полипептид содержит бета-изгиб (например, бета-изгиб из IKZF1) и альфа-спираль (например, альфа-спираль из IKZF1).
В некоторых вариантах осуществления гетерологичный полипептид слитого полипептида восприимчив к посттрансляционной модификации (например, убиквитинированию по одному или нескольким остаткам) и деградации в присутствии COF1 или COF2 (например, талидомида и его производных, например, леналидомида, помалидомида и талидомида) или в присутствии COF3 (например, соединения, раскрытого в таблице 29).
Необязательно, COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид и гетерологичный полипептид могут быть функционально связаны, например, через линкер, например, глицин-сериновый линкер (например, SEQ ID NO: 28, 37, 38, 39 или 99). Например, слитые полипептиды могут содержать три элемента: COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид, например, часть аминокислотной последовательности деградации (например, дегрон), представляющий интерес гетерологичный полипептид, подлежащий деградации, и линкер, отделяющий эти два элемента. Гетерологичный полипептид может представлять собой цитозольный белок, ядерный белок, трансмембранный белок (например, включающий один или несколько трнасмембранных доменов) или секретируемый белок. Например, представляющие интерес гетерологичные полипептиды могут содержать, например, химерный антигенный рецептор (CAR), CRISPR-ассоциированный белок, CD8, CD19, CD22, транскрипционный фактор (например, STAT3, STAT5, NF-каппа-B, бета-катенин, Notch, GLI или c-JUN), например, описанные в данном документе.
В некоторых вариантах осуществления слитый полипептид по настоящему изобретению дополнительно содержит домен деградации. В некоторых вариантах осуществления домен деградации имеет первое состояние, ассоциированное с первым уровнем экспрессии слитого полипептида, и второе состояние, ассоциированное со вторым уровнем экспрессии слитого полипептида, где второй уровень увеличивается, например, в по меньшей мере 2, 3, 4, 5, 10, 20 или 30 раз, по сравнению с первым уровнем в присутствии стабилизирующего соединения. В некоторых вариантах осуществления домен деградации отделен от COF1/CRBN-связывающего полипептида и гетерологичного полипептида с помощью гетерологичного сайта расщепления. В некоторых вариантах осуществления домен деградации отделен от COF2/CRBN-связывающего полипептида и гетерологичного полипептида с помощью гетерологичного сайта расщепления. В некоторых вариантах осуществления домен деградации отделен от COF3/CRBN-связывающего полипептида и гетерологичного полипептида с помощью гетерологичного сайта расщепления.
В некоторых вариантах осуществления слитый полипептид содержит первый домен и второй домен, где первый домен содержит домен деградации, а второй домен содержит COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид и гетерологичный полипептид. В некоторых вариантах осуществления первый домен и второй домен отделены гетерологичным сайтом расщепления. Без ограничения какой-либо теорией, уровень экспрессии слитого полипептида может контролироваться стабилизирующим соединением и COF1, COF2 или COF3. В некоторых вариантах осуществления в отсутствие стабилизирующего соединения домен деградации не может приобрести правильную конформацию и направляется на деградацию под действием внутриклеточных путей деградации вместе с остальной частью слитого полипептида. В некоторых вариантах осуществления в присутствии стабилизирующего соединения домен деградации принимает правильную конформацию и менее восприимчив в деградации под действием внутриклеточных путей деградации. В некоторых вариантах осуществления в присутствии стабилизирующего соединения правильная укладка домена деградации открывает гетерологичный сайт расщепления, что приводит к расщеплению гетерологичного сайта расщепления и удалению домена деградации из остальной части слитого полипептида. Уровень слитого полипептида может дополнительно контролироваться с помощью COF1, COF2 или COF3, как описано выше.
В некоторых вариантах осуществления домен деградации выбран из домена эстрогенового рецептора (ER), домена белка FKB (FKBP) или домена дигидрофолатредуктазы (DHFR). В некоторых вариантах осуществления домен деградации представляет собой домен эстрогенового рецептора (ER), например, домен деградации содержит аминокислотную последовательность, которая на по меньшей мере 90, 95, 97, 98, 99 или 100% идентична SEQ ID NO: 46 или 48, например, домен деградации содержит аминокислотную последовательность под SEQ ID NO: 46. В некоторых вариантах осуществления домен деградации представляет собой домен эстрогенового рецептора (ER), и стабилизирующее соединение представляет собой базедоксифен или 4-гидрокситамоксифен (4-OHT). В некоторых вариантах осуществления домен деградации представляет собой домен белка FKB (FKBP), например, домен деградации содержит аминокислотную последовательность, которая на по меньшей мере 90, 95, 97, 98, 99 или 100% идентична SEQ ID NO: 50, например, домен деградации содержит аминокислотную последовательность под SEQ ID NO: 50. В некоторых вариантах осуществления домен деградации представляет собой домен белка FKB (FKBP), и стабилизирующее соединение представляет собой Shield-1. В некоторых вариантах осуществления домен деградации представляет собой домен дигидрофолатредуктазы (DHFR), например, домен деградации содержит аминокислотную последовательность, которая на по меньшей мере 90, 95, 97, 98, 99 или 100% идентична SEQ ID NO: 51, например, домен деградации содержит аминокислотную последовательность под SEQ ID NO: 51. В некоторых вариантах осуществления домен деградации представляет собой домен дигидрофолатредуктазы (DHFR), и стабилизирующее соединение представляет собой триметоприм.
Соответственно, в данном документе раскрыты слитые полипептиды, которые содержат гетерологичный полипептид, COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид и/или домен деградации, например, представляющие интерес полипептиды для селективной деградации белка, а также молекулы нуклеиновой кислоты, кодирующие слитые полипептиды, векторы и клетки, например, клетки-хозяева, которые содержат вышеуказанные слитые полипептиды. Слитые полипептиды и связанные с ними композиции, раскрытые в данном документе, можно применять для активации или инактивации, например, деградации, разнообразных белков-мишеней для регуляции средств терапии, например, секретируемых, клеточных или трансмембранных средств терапии (например, средств терапии в виде CAR), регуляции генной экспрессии (например, путем регуляции экспрессии и/или активности компонента системы CRISPR/CAS), валидации мишени, а также скрининга библиотек. Дополнительно раскрыты способы селективной регуляции (например, деградации) указанных слитых полипептидов, например, для лечения субъекта.
В композициях и способах, раскрытых в данном документе, предложены новые и патентоспособные признаки, усовершенствованные по сравнению с известными из уровня техники системами регуляции, предусматривающие тот факт, что COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид действует на уровне белка (а не на уровне мРНК) и приводит к активной деградации существующих и новообразованных белков в клетке (а не блокировке продуцирования растущего белка). Кроме того, COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид может иметь короткую длину, и COF1, COF2 и COF3, как правило, являются низкомолекулярными.
Без ограничения какой-либо теорией, как описано в примере 16, COF1 или COF2 (например, талидомид и его производные (например, леналидомид, помалидомид и талидомид)) не приводят или фактически не приводят к деградации слитого полипептида, содержащего COF3/CRBN-связывающий полипептид, описанный в данном документе (например, слитого полипептида, содержащего CARB-метку, описанную в данном документе, например, слитого полипептида, содержащего CARB-метку, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 109, 113 и 114). В некоторых вариантах осуществления деградация слитого полипептида, содержащего COF3/CRBN-связывающий полипептид, описанный в данном документе, в присутствии COF1 или COF2 составляет не более 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, или 20% от деградации указанного слитого полипептида в присутствии COF3 при таких же условиях.
Аналогичным образом, COF3 (например, соединение, раскрытое в таблице 29) не приводит или фактически не приводит к деградации слитого полипептида, содержащего COF1/CRBN- или COF2/CRBN-связывающий полипептид, описанный в данном документе (например, слитого полипептида, содержащего HilD-метку, описанную в данном документе, например, слитого полипептида, содержащего HilD-метку, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1-6, 11-15, 40, 41-43, 77, 78, 84-86, и 100). В некоторых вариантах осуществления деградация слитого полипептида, содержащего COF1/CRBN- или COF2/CRBN-связывающий полипептид, описанный в данном документе, в присутствии COF3 составляет не более 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, или 20% от деградации указанного слитого полипептида в присутствии COF1 или COF2 при таких же условиях.
Вследствие этого, два полипептида-мишени, один, меченный с помощью COF1/CRBN- или COF2/CRBN-связывающего полипептида, (например, HilD-метки, описанной в данном документе), другой, меченный с помощью COF3/CRBN-связывающего полипептида (например, CARB-метки, описанной в данном документе), могут контролироваться независимо с применением COF1 или COF2 и COF3. Например, клеткой, экспрессирующей белок с HilD-меткой и белок с CARB-меткой, можно управлять, чтобы она экспрессировала только белок с HilD-меткой (например, путем приведения клетки в контакт с COF3), экспрессировала только белок с CARB-меткой (например, путем приведения клетки в контакт с COF1 или COF2) или не экспрессировала ни один белок (например, путем приведения клетки в контакт с COF1 или COF2 и COF3).
Определения
Если не указано иное, то все технические и научные термины, используемые в данном документе, имеют то же значение, которое обычно понятно специалисту обычной квалификации в области техники, к которой относится настоящее изобретение.
Используемый в данном документе термин "полипептид, связывающий соединение формулы (I) (COF1)/CRBN" относится к полипептиду, который связывается с COF1, полипептиду, которые связывается с комплексом COF1 и CRBN, или полипептиду, который связывается с CRBN в присутствии COF1. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид связывается с COF1 с аффинностью (KD), которая является меньшей, чем 10-3, 10-4, 10-5, 10-6, 10-7 или 10-8 M, например, как измерено с помощью способа, общепризнанного в данной области техники, например, Biacore. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид связывается с комплексом COF1 и CRBN с аффинностью (KD), которая является меньшей, чем 10-3, 10-4, 10-5, 10-6, 10-7 или 10-8 M, например, как измерено с помощью способа, общепризнанного в данной области техники, например, Biacore. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид связывается с CRBN в присутствии COF1 с аффинностью (KD), которая является меньшей, чем 10-3, 10-4, 10-5, 10-6, 10-7 или 10-8 M, например, как измерено с помощью способа, общепризнанного в данной области техники, например, Biacore. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид, когда присутствует в слитом полипептиде (например, функционально связан с гетерологичным полипептидом (например, в слитом полипептиде, описанном в данном документе)), может приводить к увеличению убиквитинирования слитого полипептида. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид, когда присутствует в слитом полипептиде (например, функционально связан с гетерологичным полипептидом (например, в слитом полипептиде, описанном в данном документе)), может приводить к увеличению деградации слитого полипептида. В некоторых вариантах осуществления COF1/CRBN-связывающий полипептид, когда присутствует в слитом полипептиде (например, функционально связан с гетерологичным полипептидом (например, в слитом полипептиде, описанном в данном документе)), может приводить к увеличению инактивации слитого полипептида. В некоторых вариантах осуществления увеличение убиквитинирования, деградации и/или инактивации происходит в присутствии COF1 и одного или нескольких компонентов комплекса убиквитинлигазы (например, CRBN). В некоторых вариантах осуществления убиквитинирование, деградация и/или инактивация увеличиваются на по меньшей мере 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 100%, 200%, 500%, в 10 раз, 100 раз, 1000 раз или более по сравнению с убиквитинированием, деградацией и/или инактивацией эталонного полипептида, например, эталонного слитого полипептида с COF1/CRBN-связывающим полипептидом в отсутствие COF1 или эталонного полипептида без COF1/CRBN-связывающего полипептида. В некоторых вариантах осуществления деградация слитого полипептида, содержащего COF1/CRBN-связывающий полипептид, является убиквитин-зависимой. Например, одна или несколько аминокислот, например, лизин или метионин, в слитом полипептид с COF1/CRBN-связывающим полипептидом, подвергаются убиквитинированию в присутствии COF1.
Используемый в данном документе термин "полипептид, связывающий соединение формулы (II) (COF2)/CRBN" относится к полипептиду, который связывается с COF2, полипептиду, которые связывается с комплексом COF2 и CRBN, или полипептиду, который связывается с CRBN в присутствии COF2. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид связывается с COF2 с аффинностью (KD), которая является меньшей, чем 10-3, 10-4, 10-5, 10-6, 10-7 или 10-8 M, например, как измерено с помощью способа, общепризнанного в данной области техники, например, Biacore. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид связывается с комплексом COF2 и CRBN с аффинностью (KD), которая является меньшей, чем 10-3, 10-4, 10-5, 10-6, 10-7 или 10-8 M, например, как измерено с помощью способа, общепризнанного в данной области техники, например, Biacore. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид связывается с CRBN в присутствии COF2 с аффинностью (KD), которая является меньшей, чем 10-3, 10-4, 10-5, 10-6, 10-7 или 10-8 M, например, как измерено с помощью способа, общепризнанного в данной области техники, например, Biacore. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид, когда присутствует в слитом полипептиде (например, функционально связан с гетерологичным полипептидом (например, в слитом полипептиде, описанном в данном документе)), может приводить к увеличению убиквитинирования слитого полипептида. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид, когда присутствует в слитом полипептиде (например, функционально связан с гетерологичным полипептидом (например, в слитом полипептиде, описанном в данном документе)), может приводить к увеличению деградации слитого полипептида. В некоторых вариантах осуществления COF2/CRBN-связывающий полипептид, когда присутствует в слитом полипептиде (например, функционально связан с гетерологичным полипептидом (например, в слитом полипептиде, описанном в данном документе)), может приводить к увеличению инактивации слитого полипептида. В некоторых вариантах осуществления увеличение убиквитинирования, деградации и/или инактивации происходит в присутствии COF2 и одного или нескольких компонентов комплекса убиквитинлигазы (например, CRBN). В некоторых вариантах осуществления убиквитинирование, деградация и/или инактивация увеличиваются на по меньшей мере 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 100%, 200%, 500%, в 10 раз, 100 раз, 1000 раз или более по сравнению с убиквитинированием, деградацией и/или инактивацией эталонного полипептида, например, эталонного слитого полипептида с COF2/CRBN-связывающим полипептидом в отсутствие COF2 или эталонного полипептида без COF2/CRBN-связывающего полипептида. В некоторых вариантах осуществления деградация слитого полипептида, содержащего COF2/CRBN-связывающий полипептид, является убиквитин-зависимой. Например, одна или несколько аминокислот, например, лизин или метионин, в слитом полипептид с COF2/CRBN-связывающим полипептидом, подвергаются убиквитинированию в присутствии COF2.
Используемый в данном документе термин "полипептид, связывающий соединение формулы (III) (COF3)/CRBN" относится к полипептиду, который связывается с COF3, полипептиду, которые связывается с комплексом COF3 и CRBN, или полипептиду, который связывается с CRBN в присутствии COF3. В некоторых вариантах осуществления COF3/CRBN-связывающий полипептид связывается с COF3 с аффинностью (KD), которая является меньшей, чем 10-3, 10-4, 10-5, 10-6, 10-7 или 10-8 M, например, как измерено с помощью способа, общепризнанного в данной области техники, например, Biacore. В некоторых вариантах осуществления COF3/CRBN-связывающий полипептид связывается с комплексом COF3 и CRBN с аффинностью (KD), которая является меньшей, чем 10-3, 10-4, 10-5, 10-6, 10-7 или 10-8 M, например, как измерено с помощью способа, общепризнанного в данной области техники, например, Biacore. В некоторых вариантах осуществления COF3/CRBN-связывающий полипептид связывается с CRBN в присутствии COF3 с аффинностью (KD), которая является меньшей, чем 10-3, 10-4, 10-5, 10-6, 10-7 или 10-8 M, например, как измерено с помощью способа, общепризнанного в данной области техники, например, Biacore. В некоторых вариантах осуществления COF3/CRBN-связывающий полипептид, когда присутствует в слитом полипептиде (например, функционально связан с гетерологичным полипептидом (например, в слитом полипептиде, описанном в данном документе)), может приводить к увеличению убиквитинирования слитого полипептида. В некоторых вариантах осуществления COF3/CRBN-связывающий полипептид, когда присутствует в слитом полипептиде (например, функционально связан с гетерологичным полипептидом (например, в слитом полипептиде, описанном в данном документе)), может приводить к увеличению деградации слитого полипептида. В некоторых вариантах осуществления COF3/CRBN-связывающий полипептид, когда присутствует в слитом полипептиде (например, функционально связан с гетерологичным полипептидом (например, в слитом полипептиде, описанном в данном документе)), может приводить к увеличению инактивации слитого полипептида. В некоторых вариантах осуществления увеличение убиквитинирования, деградации и/или инактивации происходит в присутствии COF3 и одного или нескольких компонентов комплекса убиквитинлигазы (например, CRBN). В некоторых вариантах осуществления убиквитинирование, деградация и/или инактивация увеличиваются на по меньшей мере 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 100%, 200%, 500%, в 10 раз, 100 раз, 1000 раз или более по сравнению с убиквитинированием, деградацией и/или инактивацией эталонного полипептида, например, эталонного слитого полипептида с COF3/CRBN-связывающим полипептидом в отсутствие COF3 или эталонного полипептида без COF3/CRBN-связывающего полипептида. В некоторых вариантах осуществления деградация слитого полипептида, содержащего COF3/CRBN-связывающий полипептид, является убиквитин-зависимой. Например, одна или несколько аминокислот, например, лизин или метионин, в слитом полипептид с COF3/CRBN-связывающим полипептидом, подвергаются убиквитинированию в присутствии COF3.
Используемое в данном документе "убиквитинирование" относится к добавлению молекулы убиквитина, например, одного убиквитина (моноубиквитинирование) или нескольких убиквитинов (например, цепи из молекул убиквитина или полиубиквитинирование). Убиквитинирование может осуществляться с помощью ферментного комплекса, включающего один или несколько из убиквитин-активирующего фермента (E1), убиквитин-конъюгирующего фермента (E2) и убиквитинлигазы (E3).
Используемый в данном документе термин "CRBN" относится к белку, который у человека кодируется геном CRBN, или его фрагменту, или варианту (например, с аминокислотной последовательностью, практически идентичной ему, например, на по меньшей 85, 87, 90, 95, 97, 98, 99, или 100% идентичной ему). Под номером доступа Swiss-Prot Q96SW2 представлены иллюстративные аминокислотные последовательности CRBN человека.
Используемый в данном документе "полипептид IKZF" относится к IKZF, или его фрагменту, или варианту (например, с аминокислотной последовательностью, практически идентичной ему, например, на по меньшей мере 85, 87, 90, 95, 97, 98, 99, или 100% идентичной ему).
Используемый в данном документе термин "IKZF3" относится к белку, который у человека кодируется геном IKZF3. Под номером доступа Swiss-Prot Q9UKT9 представлены иллюстративные аминокислотные последовательности IKZF3 человека. Иллюстративная аминокислотная последовательность IKZF3 человека представлена под SEQ ID NO: 19. Термин "полипептид IKZF3" относится к IKZF3, или его фрагменту, или варианту (например, с аминокислотной последовательностью, практически идентичной ему, например, на по меньшей 85, 87, 90, 95, 97, 98, 99, или 100% идентичной ему).
Используемый в данном документе термин "IKZF1" относится к белку, который у человека кодируется геном IKZF1. Под номером доступа Swiss-Prot Q13422 представлены иллюстративные аминокислотные последовательности IKZF1 человека. Иллюстративная аминокислотная последовательность IKZF1 человека представлена под SEQ ID NO: 20. Термин "полипептид IKZF1" относится к IKZF1, или его фрагменту, или варианту (например, с аминокислотной последовательностью, практически идентичной ему, например, на по меньшей 85, 87, 90, 95, 97, 98, 99, или 100% идентичной ему).
Используемый в данном документе термин "IKZF2" относится к белку, который у человека кодируется геном IKZF2. Под номером доступа Swiss-Prot Q9UKS7 представлены иллюстративные аминокислотные последовательности IKZF2 человека. Иллюстративная аминокислотная последовательность IKZF2 человека представлена под SEQ ID NO: 21. Термин "полипептид IKZF2" относится к IKZF2, или его фрагменту, или варианту (например, с аминокислотной последовательностью, практически идентичной ему, например, на по меньшей 85, 87, 90, 95, 97, 98, 99, или 100% идентичной ему).
Используемый в данном документе термин "IKZF4" относится к белку, который у человека кодируется геном IKZF4. Под номером доступа Swiss-Prot Q9H2S9 представлены иллюстративные аминокислотные последовательности IKZF4 человека. Иллюстративная аминокислотная последовательность IKZF4 человека представлена под SEQ ID NO: 22. Термин "полипептид IKZF4" относится к IKZF4, или его фрагменту, или варианту (например, с аминокислотной последовательностью, практически идентичной ему, например, на по меньшей 85, 87, 90, 95, 97, 98, 99, или 100% идентичной ему).
Используемый в данном документе термин "IKZF5" относится к белку, который у человека кодируется геном IKZF5. Под номером доступа Swiss-Prot Q9H5V7 представлены иллюстративные аминокислотные последовательности IKZF5 человека. Иллюстративная аминокислотная последовательность IKZF5 человека представлена под SEQ ID NO: 23. Термин "полипептид IKZF5" относится к IKZF5, или его фрагменту, или варианту (например, с аминокислотной последовательностью, практически идентичной ему, например, на по меньшей 85, 87, 90, 95, 97, 98, 99, или 100% идентичной ему).
Используемый в данном документе "слитый полипептид" или "химерный полипептид" относится к полипептиду, который содержит две или более гетерологичных аминокислотных последовательности и/или белковых доменов в одном непрерывном полипептиде. В некоторых вариантах осуществления два или более гетерологичных белковых домена связаны ковалентно, непосредственно или опосредованно, например, через линкер.
Используемый в данном документе термин "эстрогеновый рецептор (ER)" относится к белку, который у человека кодируется геном ESR1. Под номером доступа Swiss-Prot P03372 представлены иллюстративные аминокислотные последовательности эстрогенового рецептора (ER) человека. "Домен эстрогенового рецептора (ER)" относится к эстрогеновому рецептору, или его фрагменту, или варианту (например, с аминокислотной последовательностью, практически идентичной ему, например, на по меньшей мере 85, 87, 90, 95, 97, 98, 99, или 100% идентичной ему). Иллюстративные аминокислотные последовательности домена эстрогенового рецептора (ER) представлены под SEQ ID NO: 44, 46 и 48. Иллюстративные нуклеотидные последовательности домена эстрогенового рецептора (ER) представлены под SEQ ID NO: 45, 47 и 49.
Используемый в данном документе "домен белка FKB (FKBP)" относится к FKBP, или его фрагменту, или варианту. Иллюстративная аминокислотная последовательность домена белка FKB (FKBP) представлена под SEQ ID NO: 50.
Используемый в данном документе термин "дигидрофолатредуктаза (DHFR)" относится к белку, который у человека кодируется геном DHFR. Под номером доступа Swiss-Prot P00374 представлены иллюстративные аминокислотные последовательности дигидрофолатредуктазы (DHFR) человека. "Домен дигидрофолатредуктазы (DHFR)" относится к DHFR, или его фрагменту, или варианту. Иллюстративная аминокислотная последовательность домена дигидрофолатредуктазы (DHFR) представлена под SEQ ID NO: 51.
Используемый в данном документе термин "домен деградации" относится к домену слитого полипептида, который принимает стабильную конформацию при экспрессии в присутствии стабилизирующего соединения. В отсутствие стабильной конформации при экспрессии в представляющей интерес клетке большая часть доменов деградации (и, как правило, любой белок, с которым они слиты) будет подвергаться деградации под действием эндогенных клеточных механизмов. Следует отметить, что домен деградации представляет собой не встречающийся в природе домен белка, а сконструированный для того, чтобы быть нестабильным в отсутствие контакта со стабилизирующим соединением. Таким образом, домен деградации может быть определен по следующим характеристикам: (1) он не встречается в природе; (2) его экспрессия контролируется котрансляционно или посттрансляционно за счет увеличения или уменьшения скорости деградации; (3) скорость деградации значительно уменьшается в присутствии стабилизирующего соединение. В некоторых вариантах осуществления в отсутствие стабилизирующего соединения домен деградации или другой домен слитого полипептида фактически не выявляется в клетке или на ней. В некоторых вариантах осуществления домен деградации находится в дестабилизированном состоянии в отсутствие стабилизирующего соединения. В некоторых вариантах осуществления домен деградации не подвергается самоассоциации, например, не подвергается гомодимеризации, в отсутствие стабилизирующего соединения. В некоторых вариантах осуществления домен деградации слит с гетерологичным сайтом расщепления протеазами, где в присутствии стабилизирующего соединения расщепление гетерологичного сайта расщепления протеазами является более эффективным, чем в отсутствие стабилизирующего соединения.
Домен деградации не представляет собой домен агрегации, определенный в PCT-заявке под номером PCT/US2017/027778.
Под "стабилизирующим соединением" или "соединением стабилизации" подразумевается соединение, которое при добавлении к клетке, экспрессирующей домен деградации, стабилизирует домен деградации и любой белок, слитый с ним, и уменьшает скорость, с которой он впоследствии деградирует. Стабилизирующие соединения или соединения стабилизации могут быть встречающимися в природе или синтетическими.
Под термином "гетерологичный полипептид" подразумевается аминокислотная последовательность (например, домен белка), которая отличается от COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающего полипептида (например, на по меньшей мере одну аминокислоту) и которая не представляет собой домен активной люциферазы или обладает последовательностью люциферазы. В некоторых вариантах осуществления гетерологичный полипептид не является репортерным полипептидом, например, люциферазой, зеленым флуоресцентным белком или b-галактозидазой. В некоторых вариантах осуществления гетерологичный полипептид содержит аминокислотную последовательность из или получен из полипептида млекопитающего, полипептида бактерии, полипептида вируса, полипептида растения, полипептида дрожжей, полипептида гриба, полипептида археи или полипептида рыбы, например, данио-рерио. В некоторых вариантах осуществления гетерологичный полипептид предусматривает полипептид из таблицы 2, например, цитоплазматический и/или ядерный полипептид, секреторный полипептид или трансмембранный полипептид, описанный в таблице 2.
Кроме того, под "гетерологичным сайтом расщепления протеазами" подразумевается сайт расщепления протеазами, который имеет происхождение, отличное от одного или нескольких доменов белка, с которыми он слит (например, он слит не встречающимся в природе образом по меньшей мере с одним из других упомянутых доменов)
Под "протеазой" подразумевается белок, который расщепляет другой белок на основе присутствия сайта расщепления в белке, в котором предусматривается расщепление.
Под "внутриклеточной протеазой" подразумевается протеаза, которая нативным образом экспрессируется в представляющей интерес клетке.
Под "внеклеточной протеазой" подразумевается протеаза, которая нативным образом экспрессируется в организме (например, млекопитающем) и секретируется или выводится наружу клеток (например, в кровь или на поверхность кожи).
Используемый в данном документе термин "расщепление" относится к разрушению ковалентных связей, таких как в главной цепи молекулы нуклеиновой кислоты, или к гидролизу пептидных связей. Расщепление может инициироваться под действием различных способов, включающих без ограничения ферментативный или химический гидролиз фосфодиэфирной связи. Возможным является как расщепление одной нити, так и расщепление двух нитей. Расщепление двух нитей может происходить в результате двух различных событий расщепления одной нити.
Дополнительные термины описаны в данном документе ниже.
Форма единственного числа относится к одному или нескольким (т. e. по меньшей мере одному) грамматическим объектам настоящей заявки. В качестве примера, "элемент" означает один элемент или несколько элементов.
Подразумевается, что термин "приблизительно" в отношении измеряемого значения, такого как количество, временной промежуток и т. п., охватывает вариации на ±20%, или в некоторых случаях на ±10%, или в некоторых случаях на ±5%, или в некоторых случаях на ±1%, или в некоторых случаях на ±0,1% от указанного значения, поскольку такие вариации являются допустимыми для осуществления раскрытых способов.
Используемый в данном документе термин "антитело" относится к последовательности белка или полипептида, полученной из молекулы иммуноглобулина, который специфически связывается с антигеном. Антитела могут являться поликлональными или моноклональными, многоцепочечными или одноцепочечными или интактными иммуноглобулинами и могут быть получены из природных источников или из рекомбинантных источников. Антитела могут являться тетрамерными молекулами иммуноглобулинов.
Термин "фрагмент антитела" относится к по меньшей мере одной части антитела, которая сохраняет способность специфически взаимодействовать (например, посредством связывания, стерической изоляции, стабилизации/дестабилизации, пространственного распределения) с эпитопом антигена. Примеры фрагментов антител включают без ограничения Fab-, Fab'-, F(ab')2-, Fv-фрагменты, scFv-фрагменты антител, Fv, стабилизированные дисульфидными связями (sdFv), Fd-фрагмент, состоящий из VH- и CH1-доменов, линейные антитела, однодоменные антитела, такие как sdAb (либо VL, либо VH), VHH-домены верблюдовых, полиспецифические антитела, образованные из фрагментов антител, таких как бивалентный фрагмент, содержащий два Fab-фрагмента, связанных дисульфидным мостиком в шарнирной области, и выделенную CDR или другие эпитопсвязывающие фрагменты антитела. Антигенсвязывающий фрагмент также может быть включен в состав однодоменных антител, максиантител, миниантител, наноантител, интрател, диател, триател, тетрател, v-NAR и бис-scFv (см., например, Hollinger and Hudson, Nature Biotechnology 23:1126-1136, 2005). Антигенсвязывающие фрагменты также могут быть пересажены на каркасные структуры на основе полипептидов, таких как фибронектин III типа (Fn3) (см. патент США № 6703199, в котором описаны миниантитела на основе полипептида фибронектина).
Термин "тяжелая цепь антитела" относится к большей из двух типов полипептидных цепей, присутствующих в молекулах антител в их встречающихся в природе конформациях, и которая обычно определяет класс, к которому принадлежит антитело.
Термин "легкая цепь антитела" относится к меньшей из двух типов полипептидных цепей, присутствующих в молекулах антител в их встречающихся в природе конформациях. Легкие каппа- (κ-) и лямбда- (λ-) цепи относятся к двум основным изотипам легких цепей антител.
Термин "антиген," "Ag" или "антигенная молекула" относится к молекуле, которая вызывает иммунный ответ. Такой иммунный ответ может предусматривать либо продуцирование антител, либо активацию специфических иммунокомпетентных клеток или как то, так и другое. В некоторых вариантах осуществления антиген представляет собой любую макромолекулу, включая все белки или пептиды. В других вариантах осуществления антигены получены из рекомбинантной или геномной ДНК. Любая ДНК, которая содержит нуклеотидную последовательность или частичную нуклеотидную последовательность, кодирующую белок, который вызывает иммунный ответ, тем самым кодирует "антиген" в том смысле, в котором этот термин используется в данном документе.
Антиген не должен кодироваться исключительно полноразмерной нуклеотидной последовательностью гена. В вариантах осуществления антигены предусматривают без ограничения применение частичных нуклеотидных последовательностей из нескольких генов, и такие нуклеотидные последовательности организованы в различных комбинациях для того, чтобы кодировать полипептиды, которые вызывают требуемый иммунный ответ. В одном варианте осуществления антиген вообще не обязательно должен кодироваться "геном". В одном варианте осуществления антиген может быть получен путем синтеза, или может быть получен из биологического образца, или может представлять собой макромолекулу, отличную от полипептида. Такой биологический образец может включать без ограничения образец ткани, образец опухоли, клетку или жидкость с другими биологическими компонентами. В вариантах осуществления антигены включают, например, углеводы (например, моносахариды, дисахариды, олигосахариды и полисахариды).
Термин "антигенпрезентирующая клетка" или "APC" относится к клетке иммунной системы, такой как вспомогательная клетка (например, B-клетка, дендритная клетка и т. п.), которая представляет чужеродный антиген в комплексе с молекулами главного комплекса гистосовместимости (MHC) на своей поверхности. Т-клетки могут распознавать эти комплексы с помощью своих T-клеточных рецепторов (TCR). АРС процессируют антигены и презентируют их Т-клеткам.
Термин "химерный антигенный рецептор" или, в качестве альтернативы, "CAR" относится к совокупности полипептидов, в простейших вариантах осуществления, как правило, к двум полипептидам, которые, находясь в иммунной эффекторной клетке, наделяют клетку специфичностью в отношении клетки-мишени, как правило, раковой клетки, и способностью к генерации внутриклеточного сигнала. В некоторых вариантах осуществления CAR содержит по меньшей мере внеклеточный антигенсвязывающий домен, трансмембранный домен и цитоплазматический сигнальный домен (также обозначаемый в данном документе как "внутриклеточный сигнальный домен"), содержащий функциональный сигнальный домен, полученный из стимулирующей молекулы и/или костимулирующей молекулы, определенных ниже. В некоторых вариантах осуществления полипептиды из совокупности находятся в одной и той же полипептидной цепи (например, входят в состав химерного слитого белка). В некоторых вариантах осуществления полипептиды из совокупности не являются смежными друг с другом, например, находятся в разных полипептидных цепях. В некоторых вариантах осуществления полипептиды из совокупности не являются смежными друг с другом, например, находятся в разных полипептидных цепях. В некоторых вариантах осуществления набор полипептидов содержит переключатель димеризации, который при наличии димеризующей молекулы может связывать слитые полипептиды друг с другом, например, может связывать антигенсвязывающий домен с внутриклеточным сигнальным доменом. В одном аспекте стимулирующая молекула представляет собой дзета-цепь, ассоциированную с Т-клеточным рецепторным комплексом. В одном аспекте цитоплазматический сигнальный домен содержит первичный сигнальный домен (например, первичный сигнальный домен CD3-дзета). В одном аспекте цитоплазматический сигнальный домен дополнительно содержит один или несколько функциональных сигнальных доменов, полученных из по меньшей мере одной костимулирующей молекулы, определенной ниже. В одном аспекте костимулирующая молекула CAR выбрана из костимулирующих молекул, описанных в данном документе, например, 4-1BB (т. е. CD137), CD27, ICOS и/или CD28. В одном аспекте CAR содержит химерный слитый белок, содержащий внеклеточный антигенсвязывающий домен, трансмембранный домен и внутриклеточный сигнальный домен, содержащий функциональный сигнальный домен, полученный из стимулирующей молекулы. В одном аспекте CAR содержит химерный слитый белок, содержащий внеклеточный антигенсвязывающий домен, трансмембранный домен и внутриклеточный сигнальный домен, содержащий функциональный сигнальный домен, полученный из костимулирующей молекулы, и функциональный сигнальный домен, полученный из стимулирующей молекулы. В одном аспекте CAR содержит химерный слитый белок, содержащий внеклеточный антигенсвязывающий домен, трансмембранный домен и внутриклеточный сигнальный домен, содержащий два функциональных сигнальных домена, полученные из одной или нескольких костимулирующих молекул, и функциональный сигнальный домен, полученный из стимулирующей молекулы. В одном аспекте CAR содержит химерный слитый белок, содержащий внеклеточный антигенсвязывающий домен, трансмембранный домен и внутриклеточный сигнальный домен, содержащий по меньшей мере два функциональных сигнальных домена, полученные из одной или нескольких костимулирующих молекул, и функциональный сигнальный домен, полученный из стимулирующей молекулы. В одном аспекте CAR содержит необязательную лидерную последовательность на амино-конце (N-конце) слитого белка CAR. В одном аспекте CAR дополнительно содержит лидерную последовательность на N-конце внеклеточного антигенсвязывающего домена, где лидерная последовательность необязательно отщепляется от антигенсвязывающего домена (например, scFv) в ходе клеточного процессинга и локализации CAR в клеточной мембране.
Термин "рак" относится к заболеванию, которое характеризуется неконтролируемым ростом аберрантных клеток. Раковые клетки могут распространяться локально или через кровоток и лимфатическую систему в другие части организма. Примеры различных форм рака описаны в данном документе и включают без ограничения рак молочной железы, рак предстательной железы, рак яичника, рак шейки матки, рак кожи, рак поджелудочной железы, колоректальный рак, рак почки, рак печени, рак головного мозга, лимфому, лейкоз, рак легкого и т. п. Термины "опухоль" и "рак" используются в данном документе взаимозаменяемо, например, оба термина охватывают солидные опухоли и опухоли жидких тканей, например, диффузные или циркулирующие. Используемый в данном документе термин "рак" или "опухоль" включает предзлокачественные, а также злокачественные формы рака и опухоли.
В зависимости от контекста "молекула CAR" относится к CAR (например, полипептиду CAR), к нуклеиновой кислоте, кодирующей CAR, или к ним обоим.
CAR, который содержит антигенсвязывающий домен (например, scFv или TCR), нацеливающийся на специфический опухолевый антиген X, такой как описанные в данном документе, также называется CAR для X. Например, CAR, который содержит антигенсвязывающий домен, который нацеливается на CD19 или BCMA обозначается CAR для CD19 или CAR для BCMA соответственно.
Используемый в данном документе термин "ВСМА" относится к антигену созревания В-клеток. BCMA (также известный как TNFRSF17, BCM или CD269) является представителем семейства рецепторов некроза опухоли (TNFR) и преимущественно экспрессируется на терминально дифференцированных B-клетках, например, B-клетках памяти и плазматических клетках. Его лиганд называют B-клеточным активатором семейства TNF (BAFF) и лигандом, индуцирующим пролиферацию (APRIL). ВСМА вовлечен в опосредование выживания плазматических клеток для поддержания долгосрочного гуморального иммунитета. Ген BCMA кодируется в хромосоме 16, продуцируя первичный мРНК-транскрипт длиной 994 нуклеотида (№ доступа в NCBI NM_001192.2), который кодирует белок из 184 аминокислот (NP_001183.2). Был описан второй антисмысловой транскрипт, происходящий из локуса BCMA, который может играть роль в регуляции экспрессии BCMA. (Laabi Y. et al., Nucleic Acids Res., 1994, 22:1147-1154). Были описаны дополнительные варианты транскрипта с неизвестным значением (Smirnova AS et al. Mol Immunol., 2008, 45(4):1179-1183). Была идентифицирована вторая изоформа, также известная как TV4 (идентификатор Uniprot Q02223-2). Используемый в данном документе "BCMA" включает белки, содержащие мутации, например, точечные мутации, фрагменты, вставки, делеции и сплайс-варианты полноразмерного BCMA дикого типа.
Используемый в данном документе термин "CD19" относится к белку кластера дифференцировки 19, который представляет собой антигенную детерминанту, выявляемую на лейкозных клетках-предшественниках. Аминокислотные последовательности и последовательности нуклеиновых кислот человека и мыши можно найти в общедоступной базе данных, такой как GenBank, UniProt и Swiss-Prot. Например, аминокислотную последовательность CD19 человека можно найти под № доступа UniProt/Swiss-Prot P15391, а нуклеотидную последовательность, кодирующую CD19 человека, можно найти под № доступа NM_001178098. Используемый в данном документе "CD19" включает белки, содержащие мутации, например, точечные мутации, фрагменты, вставки, делеции и сплайс-варианты полноразмерного CD19 дикого типа.
CD19 экспрессируется на клетках большинства форм рака из B-клеточной линии дифференцировки, включая, например, острый лимфобластный лейкоз, хронический лимфоцитарный лейкоз и неходжкинскую лимфому. Другие клетки, экспрессирующие CD19, представлены ниже при определении "заболевания, ассоциированного с экспрессией CD19". Он также представляет собой ранний маркер предшественников B-клеток. См., например, Nicholson et al. Mol. Immun. 34 (16-17): 1157-1165 (1997). В одном аспекте антигенсвязывающая часть CART распознает и связывает антиген в пределах внеклеточного домена белка CD19. В одном аспекте белок CD19 экспрессируется на раковой клетке.
Используемый в данном документе термин "CD20" относится к антигенной детерминанте, которую, как известно, можно выявить на В-клетках. CD20 человека также называют представителем 1 подсемейства А белков с 4 трансмембранными доменами (MS4A1). Аминокислотные последовательности и последовательности нуклеиновых кислот человека и мыши можно найти в общедоступной базе данных, такой как GenBank, UniProt и Swiss-Prot. Например, аминокислотную последовательность CD20 человека можно найти под №№ доступа NP_690605.1 и NP_068769.2, а нуклеотидную последовательность, кодирующую варианты транскрипта 1 и 3 CD20 человека, можно найти под № доступа NM_152866.2 и NM_021950.3 соответственно. В одном аспекте антигенсвязывающая часть CAR распознает и связывает антиген в пределах внеклеточного домена белка CD20. В одном аспекте белок CD20 экспрессируется на раковой клетке. Используемый в данном документе "CD20" включает белки, содержащие мутации, например, точечные мутации, фрагменты, вставки, делеции и сплайс-варианты полноразмерного CD20 дикого типа.
Используемый в данном документе термин "CD22" относятся к антигенной детерминанте, которую, как известно, можно выявить на лейкозных клетках-предшественниках. Аминокислотные последовательности и последовательности нуклеиновых кислот человека и мыши можно найти в общедоступной базе данных, такой как GenBank, UniProt и Swiss-Prot. Например, аминокислотные последовательности изоформ 1-5 CD22 человека можно найти под №№ доступа NP 001762.2, NP 001172028.1, NP 001172029.1, NP 001172030.1 и NP 001265346.1 соответственно, и нуклеотидную последовательность, кодирующую варианты 1-5 CD22 человека, можно найти под № доступа NM 001771.3, NM 001185099.1, NM 001185100.1, NM 001185101.1 и NM 001278417.1 соответственно. В одном аспекте антигенсвязывающая часть CAR распознает и связывает антиген в пределах внеклеточного домена белка CD22. В одном аспекте белок CD22 экспрессируется на раковой клетке. Используемый в данном документе "CD22" включает белки, содержащие мутации, например, точечные мутации, фрагменты, вставки, делеции и сплайс-варианты полноразмерного CD22 дикого типа.
Используемый в данном документе термин "CD123" относится к антигенной детерминанте, которую, как известно, можно выявить на некоторых злокачественных клетках гематологического рака, например на лейкозных клетках. Аминокислотные последовательности и последовательности нуклеиновых кислот человека и мыши можно найти в общедоступной базе данных, такой как GenBank, UniProt и Swiss-Prot. Например, аминокислотные последовательности CD123 человека можно найти под №№ доступа NP_002174.1 (предшественник изоформы 1); NP_001254642.1 (предшественник изоформы 2), и последовательности мРНК, кодирующие их, можно найти под №№ доступа NM_002183.3 (вариант 1); NM_001267713.1 (вариант 2). В одном аспекте антигенсвязывающая часть CAR распознает и связывает антиген в пределах внеклеточного домена белка CD123. В одном аспекте белок CD123 экспрессируется на раковой клетке. Используемый в данном документе "CD123" включает белки, содержащие мутации, например, точечные мутации, фрагменты, вставки, делеции и сплайс-варианты полноразмерного CD123 дикого типа.
Часть CAR, содержащая антитело или фрагмент этого антитела, может существовать в различных формах, при которых антигенсвязывающий домен экспрессируется в виде части непрерывной полипептидной цепи, включая, например, фрагмент однодоменного антитела (sdAb), одноцепочечное антитело (scFv), гуманизированное антитело или биспецифическое антитело (Harlow et al., 1999, в: Using Antibodies: A Laboratory Manual, Cold Spring Harbor Laboratory Press, NY; Harlow et al., 1989, в: Antibodies: A Laboratory Manual, Cold Spring Harbor, New York; Houston et al., 1988, Proc. Natl. Acad. Sci. USA 85:5879-5883; Bird et al., 1988, Science 242:423-426). В одном аспекте антигенсвязывающий домен в составе CAR по настоящему изобретению содержит фрагмент антитела. В дополнительном аспекте CAR содержит фрагмент антитела, который содержит scFv.
Термин "когнатная антигенная молекула" относится к любому антигену, описанному в данном документе. В одном варианте осуществления он относится к антигену, который распознает, например, на который нацеливается, молекула CAR, например, любой CAR, описанный в данном документе. В другом варианте осуществления он относится к описанному в данном документе антигену, ассоциированному с раком. В одном варианте осуществления когнатная антигенная молекула представляет собой рекомбинантную молекулу.
Термин "консервативные модификации последовательности" относится к аминокислотным модификациям, которые не оказывают значительного влияния на характеристики связывания антитела или фрагмента антитела, содержащего аминокислотную последовательность, или не изменяют их в значительной степени. Такие консервативные модификации включают аминокислотные замены, добавления и делеции. Модификации могут быть введены в антитело или фрагмент антитела по настоящему изобретению с помощью стандартных методик, известных из уровня техники, таких как сайт-направленный мутагенез и ПЦР-опосредованный мутагенез. Консервативные аминокислотные замены представляют собой замены, при которых аминокислотный остаток заменяется аминокислотным остатком, имеющим аналогичную боковую цепь. Семейства аминокислотных остатков, имеющих аналогичные боковые цепи, были определены в уровне техники. Такие семейства включают аминокислоты с основными боковыми цепями (например, лизин, аргинин, гистидин), кислыми боковыми цепями (например, аспарагиновая кислота, глутаминовая кислота), незаряженными полярными боковыми цепями (например, глицин, аспарагин, глутамин, серин, треонин, тирозин, цистеин, триптофан), неполярными боковыми цепями (например, аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин), бета-разветвленными боковыми цепями (например, треонин, валин, изолейцин) и ароматическими боковыми цепями (например, тирозин, фенилаланин, триптофан, гистидин). Таким образом, один или несколько аминокислотных остатков в пределах представляющего интерес полипептида (например, CAR), описанного в данном документе, могут быть заменены другими аминокислотными остатками из семейства с такой же боковой цепью, и измененный представляющий интерес полипептид (например, CAR) может быть протестирован с применением функциональных анализов, описанных в данном документе.
Термин "костимулирующая молекула" относится к когнатному партнеру по связыванию на Т-клетке, который специфически связывается с костимулирующим лигандом, за счет чего происходит опосредование костимулируемого ответа Т-клетки, такого как, без ограничения, пролиферация. Костимулирующие молекулы представляют собой молекулы клеточной поверхности, отличные от антигенных рецепторов или их лигандов, которые необходимы для эффективного иммунного ответа. Костимулирующие молекулы включают без ограничения молекулу MHC класса I, белки рецептора TNF, иммуноглобулиноподобные белки, цитокиновые рецепторы, интегрины, молекулы сигнальной активации лимфоцитов (белки SLAM), рецепторы, активирующие NK-клетки, BTLA, лиганд Toll-подобного рецептора, OX40, CD2, CD7, CD27, CD28, CD30, CD40, CDS, ICAM-1, LFA-1 (CD11a/CD18), 4-1BB (CD137), B7-H3, CDS, ICAM-1, ICOS (CD278), GITR, BAFFR, LIGHT, HVEM (LIGHTR), KIRDS2, SLAMF7, NKp80 (KLRF1), NKp44, NKp30, NKp46, CD19, CD4, CD8-альфа, CD8-бета, IL2R-бета, IL2R-гамма, IL7R-альфа, ITGA4, VLA1, CD49a, ITGA4, IA4, CD49D, ITGA6, VLA-6, CD49f, ITGAD, CD11d, ITGAE, CD103, ITGAL, CD11a, LFA-1, ITGAM, CD11b, ITGAX, CD11c, ITGB1, CD29, ITGB2, CD18, LFA-1, ITGB7, NKG2D, NKG2C, TNFR2, TRANCE/RANKL, DNAM1 (CD226), SLAMF4 (CD244, 2B4), CD84, CD96 (Tactile), CEACAM1, CRTAM, Ly9 (CD229), CD160 (BY55), PSGL1, CD100 (SEMA4D), CD69, SLAMF6 (NTB-A, Ly108), SLAM (SLAMF1, CD150, IPO-3), BLAME (SLAMF8), SELPLG (CD162), LTBR, LAT, GADS, SLP-76, PAG/Cbp, CD19a и лиганд, который специфически связывается с CD83. Костимулирующий внутриклеточный сигнальный домен относится к внутриклеточной части костимулирующей молекулы. Внутриклеточный сигнальный домен может содержать всю внутриклеточную часть или весь нативный внутриклеточный сигнальный домен молекулы, из которого он получен, или ее функциональный фрагмент. Внутриклеточный сигнальный домен может содержать всю внутриклеточную часть или весь нативный внутриклеточный сигнальный домен молекулы, из которого он получен, или ее функциональный фрагмент.
Термин "полученный из", в том значении, в котором он используется в данном документе, указывает на взаимосвязь между первой и второй молекулой. Это обычно относится к структурному сходству между первой молекулой и второй молекулой и не имеет дополнительного значения или не включает ограничение способа или источника в отношении первой молекулы, которая получена из второй молекулы. Например, в случае внутриклеточного сигнального домена, который получен из молекулы CD3-дзета, внутриклеточный сигнальный домен сохраняет структуру CD3-дзета в достаточной степени, чтобы он характеризовался требуемой функцией, а именно, способностью генерировать сигнал в подходящих условиях. Это не имеет дополнительного значения или не включает ограничение в отношении конкретного способа получения внутриклеточного сигнального домена, например, это не означает, что для обеспечения внутриклеточного сигнального домена нужно начинать с последовательности CD3-дзета и удалять нежелательную последовательность или вводить мутации для получения внутриклеточного сигнального домена.
Описанная в данном документе фраза "заболевание, ассоциированное с экспрессией опухолевого антигена" включает без ограничения заболевание, ассоциированное с экспрессией опухолевого антигена, описанного в данном документе, или состояние, ассоциированное с клетками, которые экспрессируют опухолевый антиген, описанный в данном документе, включая, например, пролиферативные заболевания, такие как рак или злокачественное новообразование, или предраковое состояние, такое как миелодисплазия, миелодиспластический синдром или предлейкоз; или не связанное с раком показание, ассоциированное с клетками, которые экспрессируют опухолевый антиген, описанный в данном документе. В одном варианте осуществления рак, ассоциированный с экспрессией опухолевого антигена, описанного в данном документе, представляет собой гематологический рак. В одном варианте осуществления рак, ассоциированный с экспрессией опухолевого антигена, описанного в данном документе, представляет собой солидный рак. Дополнительные заболевания, ассоциированные с экспрессией опухолевого антигена, описанного в данном документе включают без ограничения, например, атипичные и/или неклассические формы рака, злокачественные опухоли, предраковые состояния или пролиферативные заболевания, ассоциированные с экспрессией опухолевого антигена, описанного в данном документе. Не связанные с раком показания, ассоциированные с экспрессией опухолевого антигена, описанного в данном документе, включают без ограничения, например, аутоиммунное заболевание (например, волчанку), воспалительные нарушения (аллергию и астму) и трансплантацию. В некоторых вариантах осуществления клетки, экспрессирующие опухолевый антиген, экспрессируют или в какой-либо момент времени экспрессировали мРНК, кодирующую опухолевый антиген. В одном варианте осуществления клетки, экспрессирующие опухолевый антиген, продуцируют белок опухолевого антигена (например, дикого типа или мутантный), и при этом белок опухолевого антигена может присутствовать на нормальных уровнях или сниженных уровнях. В одном варианте осуществления клетки, экспрессирующие опухолевый антиген, в один момент времени продуцировали белок опухолевого антигена на выявляемых уровнях, а затем фактически не продуцировали белок опухолевого антигена на выявляемых уровнях.
Фраза "заболевание, ассоциированное с экспрессией CD19" включает без ограничения заболевание, ассоциированное с клетками, которые экспрессируют CD19 (например, CD19 дикого типа или мутантный CD19), или состояние, ассоциированное с клеткой, которая экспрессирует или в какое-либо время экспрессировала CD19 (например, CD19 дикого типа или мутантный CD19), включая, например, пролиферативные заболевания, такие как рак или злокачественное новообразование, или предраковое состояние, такое как миелодисплазия, миелодиспластический синдром или предлейкоз; или не связанное с раком показание, ассоциированное с клетками, которые экспрессируют CD19. Во избежание неоднозначности толкования заболевание, ассоциированное с экспрессией CD19, может включать состояние, ассоциированное с клеткой, которая в настоящее время не экспрессирует CD19, например, вследствие того, что экспрессия CD19 была подавлена, например, вследствие обработки молекулой, нацеливающейся на CD19, например, CAR для CD19, но которая в один момент времени экспрессировала CD19. В одном аспекте рак, ассоциированный с экспрессией CD19, представляет собой гематологический рак. В одном аспекте гематологический рак представляет собой лейкоз или лимфому. В одном аспекте рак, ассоциированный с экспрессией CD19, включает формы рака и злокачественные новообразования, включающие без ограничения, например, одну или несколько форм острого лейкоза, включая без ограничения, например, острый миелоидный лейкоз (AML), B-клеточный острый лимфоидный лейкоз (BALL), T-клеточный острый лимфоидный лейкоз (TALL), острый лимфоидный лейкоз (ALL); одну или несколько форм хронического лейкоза, включая без ограничения, например, хронический миелогенный лейкоз (CML), хронический лимфоидный лейкоз (CLL). Дополнительные формы рака или гематологические состояния, ассоциированные с экспрессией CD19, предусматривают без ограничения, например, B-клеточный пролимфоцитарный лейкоз, новообразование из бластных плазмоцитоидных дендритных клеток, лимфому Беркитта, диффузную крупноклеточную B-клеточную лимфому, фолликулярную лимфому, волосатоклеточный лейкоз, мелкоклеточную или крупноклеточную фолликулярную лимфому, злокачественные лимфопролиферативные состояния, MALT-лимфому, лимфому из клеток мантийной зоны (MCL), лимфому маргинальной зоны, множественную миелому, миелодисплазию и миелодиспластический синдром, неходжкинскую лимфому, лимфому Ходжкина, плазмобластную лимфому, новообразование из плазмоцитоидных дендритных клеток, макроглобулинемию Вальденстрема, миелопролиферативное новообразование; гистиоцитарное нарушение (например, тучноклеточное нарушение или новообразование из бластных плазмоцитоидных дендритных клеток); тучноклеточное нарушение, например, системный мастоцитоз или тучноклеточный лейкоз; B-клеточный пролимфоцитарный лейкоз, плазмоклеточную миелому и "предлейкоз", который представляет собой разнородную совокупность гематологических состояний, объединенных неэффективным продуцированием (или дисплазией) миелоидных клеток крови, и т. п.
Дополнительные заболевания, ассоциированные с экспрессией CD19, включают без ограничения, например, атипичные и/или неклассические формы рака, злокачественные новообразования, предраковые состояния или пролиферативные заболевания, ассоциированные с экспрессией CD19. Не связанные с раком показания, ассоциированные с экспрессией CD19, включают без ограничения, например, аутоиммунное заболевание (например, волчанку), воспалительные нарушения (аллергию и астму) и трансплантацию. В некоторых вариантах осуществления клетки, экспрессирующие CD19, экспрессируют или в какой-либо момент времени экспрессировали мРНК, кодирующую CD19. В одном варианте осуществления клетки, экспрессирующие CD19, вырабатывают белок CD19 (например, дикого типа или мутантный), и при этом белок CD19 может присутствовать на нормальных уровнях или сниженных уровнях. В одном варианте осуществления клетки, экспрессирующие CD19, в один момент времени продуцировали белок CD19 на выявляемых уровнях, а затем фактически не продуцировали белок CD19 на выявляемых уровнях.
В некоторых вариантах осуществления клетки, экспрессирующие опухолевый антиген, экспрессируют или в какой-либо момент времени экспрессировали мРНК, кодирующую опухолевый антиген. В одном варианте осуществления клетки, экспрессирующие опухолевый антиген, продуцируют белок опухолевого антигена (например, дикого типа или мутантный), и при этом белок опухолевого антигена может присутствовать на нормальных уровнях или сниженных уровнях. В одном варианте осуществления клетки, экспрессирующие опухолевый антиген, в один момент времени продуцировали белок опухолевого антигена на выявляемых уровнях, а затем фактически не продуцировали белок опухолевого антигена на выявляемых уровнях. В других вариантах осуществления заболевание представляет собой CD19-отрицательный рак, например, CD19-отрицательный рецидивирующий рак. В некоторых вариантах осуществления клетка, экспрессирующая опухолевый антиген (например, CD19), экспрессирует или в какой-либо момент времени экспрессировала мРНК, кодирующую опухолевый антиген. В одном варианте осуществления клетка, экспрессирующая опухолевый антиген (например, CD19), продуцирует белок опухолевого антигена (например, дикого типа или мутантный), и при этом белок опухолевого антигена может присутствовать на нормальных уровнях или сниженных уровнях. В одном варианте осуществления клетка, экспрессирующая опухолевый антиген (например, CD19), в один момент времени продуцировала белок опухолевого антигена на выявляемых уровнях, а затем фактически не продуцировала белок опухолевого антигена на выявляемых уровнях.
Термин "эффекторная функция" относится к специализированной функции клетки. Например, эффекторная функция Т-клетки может представлять собой цитолитическую активность или хелперную активность, включая секрецию цитокинов. Термин "кодирование" относится к свойству, присущему специфическим последовательностям нуклеотидов в полинуклеотиде, таком как ген, кДНК или мРНК, в ходе биологических процессов служить в качестве матриц для синтеза других полимеров и макромолекул, имеющих либо заданную последовательность нуклеотидов (т. е. рРНК, тРНК и мРНК), либо заданную последовательность аминокислот и биологические свойства, обусловленные ими. Таким образом, ген, кДНК или РНК кодирует белок, если в результате транскрипции и трансляции мРНК, соответствующей этому гену, в клетке или другой биологической системе продуцируется белок. Как кодирующая нить, нуклеотидная последовательность которой идентична последовательности мРНК и обычно представлена в перечнях последовательностей, так и некодирующая нить, используемая в качестве матрицы для транскрипции гена или кДНК, могут обозначаться как кодирующие белок или другой продукт данного гена или кДНК.
Термин "эндогенный" относится к любому материалу, полученному из организма, клетки, ткани или системы или продуцируемому внутри них.
Термин "экзогенный" относится к любому материалу, введенному в организм, клетку, ткань или систему или продуцируемому вне их.
Термин "экспрессия" относится к транскрипции и/или трансляции конкретной нуклеотидной последовательности под управлением промотора.
Термин "4-1BB" относится к представителю суперсемейства TNFR с аминокислотной последовательностью, представленной под № доступа в GenBank AAA62478.2, или эквивалентным остаткам биологического вида, отличного от человека, например мыши, грызуна, обезьяны, человекообразной обезьяны и т. п.; и "костимулирующий домен 4-1BB" определен как аминокислотные остатки 214-255 из последовательности под № доступа в GenBank AAA62478.2 или эквивалентные остатки биологического вида, отличного от человека, например мыши, грызуна, обезьяны, человекообразной обезьяны и т. п. В одном аспекте "костимулирующий домен 4-1BB" представляет собой последовательность, представленную под SEQ ID NO: 158, или эквивалентные остатки биологического вида, отличного от человека, например, мыши, грызуна, обезьяны, человекообразной обезьяны и т. п.
Термин "экспрессионный вектор" относится к вектору, содержащему рекомбинантный полинуклеотид, содержащий последовательности контроля экспрессии, функционально связанные с нуклеотидной последовательностью, подлежащей экспрессии. Экспрессионный вектор содержит достаточное количество цис-действующих элементов для экспрессии; а другие элементы для экспрессии могут предоставляться клеткой-хозяином или в системе для экспрессии in vitro. Экспрессионные векторы включают все векторы, известные из уровня техники, включая космиды, плазмиды (например, "голые" или содержащиеся в липосомах) и вирусы (например, лентивирусы, ретровирусы, аденовирусы и аденоассоциированные вирусы), в состав которых включен рекомбинантный полинуклеотид.
Термин "гомологичный" или "идентичность" относится к идентичности последовательности субъединиц у двух полимерных молекул, например, двух молекул нуклеиновой кислоты, таких как две молекулы ДНК или две молекулы РНК, или двух полипептидных молекул. Если положение субъединицы в обеих из двух молекул занят одной и той же мономерной субъединицей, например, если положение в каждой из двух молекул ДНК занято аденином, то они являются гомологичными или идентичными по этому положению. Гомология между двумя последовательностями находится в прямой зависимости от числа совпадающих или гомологичных положений; например, если половина (например, пять положений в полимере длиной десять субъединиц) положений в двух последовательностях являются гомологичными, то эти две последовательности являются гомологичными на 50%; если 90% положений (например, 9 из 10) являются совпадающими или гомологичными, то эти две последовательности являются гомологичными на 90%.
Композиции и способы по настоящему изобретению охватывают полипептиды и нуклеиновые кислоты, имеющие указанные последовательности или последовательности, практически идентичные или сходные с ними, например, последовательности, идентичные на по меньшей мере 85%, 90%, 95% или больше указанной последовательности. В контексте аминокислотной последовательности термин "практически идентичная" используется в данном документе для обозначения первой аминокислотной последовательности, которая содержит достаточное или минимальное количество аминокислотных остатков, которые i) идентичны аминокислотным остаткам во второй аминокислотной последовательности после их выравнивания или ii) являются их консервативными заменами, вследствие чего первая и вторая аминокислотные последовательности могут иметь общий структурный домен и/или характеризоваться общей функциональной активностью. Например, аминокислотные последовательности, которые содержат общий структурный домен, характеризуются по меньшей мере приблизительно 85%, 90%. 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичностью с эталонной последовательностью, например, последовательностью, представленной в данном документе.
В контексте нуклеотидной последовательности термин "практически идентичная" используется в данном документе для обозначения первой последовательности нуклеиновой кислоты, которая содержит достаточное или минимальное количество нуклеотидов, которые идентичны нуклеотидам во второй последовательности нуклеиновой кислоты после их выравнивания, вследствие что первая и вторая нуклеотидные последовательности кодируют полипептид, характеризующийся общей функциональной активностью, или кодируют полипептидный домен с общей структурой или полипептид с общей функциональной активностью. Например, нуклеотидные последовательности характеризуются по меньшей мере приблизительно 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичностью с эталонной последовательностью, например, последовательностью, представленной в данном документе.
Термин "вариант" относится к полипептиду, который имеет практически идентичную аминокислотную последовательность с встречающейся в природе последовательностью или кодируется практически идентичной нуклеотидной последовательностью. В некоторых вариантах осуществления вариант представляет собой функциональный вариант.
Термин "функциональный вариант" относится к полипептиду, который имеет практически идентичную аминокислотную последовательность с встречающейся в природе последовательностью или кодируется практически идентичной нуклеотидной последовательностью и способен проявлять один или несколько видов активности встречающейся в природе последовательности.
Термин "COF1/CRBN-связывающий вариант" последовательности X относится к полипептиду, который: (1) имеет практически идентичную аминокислотную последовательность с последовательностью X, и (2) связывается с COF1, связывается с комплексом COF1 и CRBN или связывается с CRBN в присутствии COF1.
Термин "COF2/CRBN-связывающий вариант" последовательности X относится к полипептиду, который: (1) имеет практически идентичную аминокислотную последовательность с последовательностью X, и (2) связывается с COF2, связывается с комплексом COF2 и CRBN или связывается с CRBN в присутствии COF2.
Термин "COF3/CRBN-связывающий вариант" последовательности X относится к полипептиду, который: (1) имеет практически идентичную аминокислотную последовательность с последовательностью X, и (2) связывается с COF3, связывается с комплексом COF3 и CRBN или связывается с CRBN в присутствии COF3.
Используемый в данном документе термин "иммунная эффекторная клетка" относится к клетке, которая участвует в иммунном ответе, например, способствуя иммунному эффекторному ответу. Примеры иммунных эффекторных клеток включают Т-клетки, например, альфа/бета-Т-клетки и гамма/дельта-Т-клетки, В-клетки, клетки натуральные киллеры (NK), T-клетки натуральные киллеры (NKT), тучные клетки и фагоциты миелоидного происхождения.
Используемый в данном документе термин "иммунная эффекторная функция или иммунный эффекторный ответ" относится к функции или ответу, например, иммунной эффекторной клетки, которые усиливают иммунную атаку на клетку-мишень или способствуют ей. Например, иммунные эффекторные функция или ответ относятся к свойству T- или NK-клетки, которое способствует уничтожению или ингибированию роста или пролиферации клетки-мишени. В случае Т-клетки первичная стимуляция и костимуляция являются примерами иммунных эффекторных функции или ответа.
Термин "ингибирование" или "ингибитор" включает снижение определенного параметра, например, активности указанной молекулы, например, CD19, CD20, CD10, CD22, CD34, CD123, FLT-3, ROR1, CD79b, CD179b, мезотелина или CD79a. Например, данный термин включает ингибирование активности, например, активности CD20, CD10, CD19, CD22, CD34, CD123, FLT-3, ROR1, CD79b, CD179b, мезотелина или CD79a, составляющее по меньшей мере 5%, 10%, 20%, 30%, 40% или более. Таким образом, ингибирование не обязательно должно составлять 100%. Виды активности ингибиторов могут быть определены, как описано в данном документе, или с помощью анализов, известных из уровня техники.
Используемый в данном документе термин "внутриклеточный сигнальный домен" относится к внутриклеточной части молекулы. Внутриклеточный сигнальный домен может генерировать сигнал, который способствует иммунной эффекторной функции клетки, содержащей CAR, например, CAR-T-клетки. Примеры иммунной эффекторной функции, например, у CAR-T-клетки, включают цитолитическую активность и хелперную активность, в том числе секрецию цитокинов. В вариантах осуществления внутриклеточный сигнальный домен представляет собой часть белка, которая передает сигнал эффекторной функции и направляет клетку на выполнение специализированной функции. Хотя может использоваться весь внутриклеточный сигнальный домен, во многих случаях отсутствует необходимость использовать всю цепь. В том случае, если используют усеченную часть внутриклеточного сигнального домена, такую усеченную часть можно использовать вместо интактной цепи, при условии, что она передает сигнал эффекторной функции. Таким образом, подразумевается, что термин "внутриклеточный сигнальный домен" включает любую усеченную часть внутриклеточного сигнального домена, достаточную для передачи сигнала эффекторной функции.
В одном варианте осуществления внутриклеточный сигнальный домен может содержать первичный внутриклеточный сигнальный домен. Иллюстративные первичные внутриклеточные сигнальные домены включают домены, полученные из молекул, отвечающих за первичную стимуляцию или антигензависимую стимуляцию. В одном варианте осуществления внутриклеточный сигнальный домен может содержать костимулирующий внутриклеточный домен. Иллюстративные костимулирующие внутриклеточные сигнальные домены включают домены, полученные из молекул, отвечающих за костимулирующие сигналы или антигеннезависимую стимуляцию. Например, в случае с CART первичный внутриклеточный сигнальный домен может содержать цитоплазматическую последовательность Т-клеточного рецептора, и костимулирующий внутриклеточный сигнальный домен может содержать цитоплазматическую последовательность корецептора или костимулирующей молекулы.
Первичный внутриклеточный сигнальный домен может содержать сигнальный мотив, который известен как иммунорецепторный тирозиновый активирующий мотив или ITAM. Примеры первичных цитоплазматических сигнальных последовательностей, содержащих ITAM, включают без ограничения последовательности, полученные из CD3-дзета, FcR-гамма, FcR-бета, CD3-гамма, CD3-дельта, CD3-эпсилон, CD5, CD22, CD79a, CD79b, CD278 ("ICOS"), FcεRI, а также CD66d, CD32, DAP10 и DAP12.
Термин "выделенный" означает измененный относительно природного состояния или извлеченный из него. Например, нуклеиновая кислота или пептид, в природных условиях присутствующие в живом животном, не являются "выделенными", однако те же нуклеиновая кислота или пептид, частично или полностью отделенные от сопутствующих материалов в своем природном состоянии, являются "выделенными". Выделенные нуклеиновая кислота или белок могут находиться в практически чистой форме или могут находиться в ненативной среде, такой как, например, клетка-хозяин.
Используемый в данном документе термин "мезотелин" относится к белку размером 40 кДа, мезотелину, который заякорен в клеточной мембране посредством гликозилфосфатидилинозитоловой (GPI) связи и амино-концевого "слущивающегося" фрагмента размером 31 кДа, называемого потенцирующим фактором мегакариоцитов (MPF). Оба фрагмента содержат сайты N-гликозилирования. Термин также относится к растворимому сплайс-варианту карбокси-концевого фрагмента размером 40 кДа, также называемому "растворимым мезотелином/MPF-связанным". Предпочтительно данный термин относится к мезотелину человека с номером доступа в GenBank AAH03512.1 и его естественным образом расщепленным частям, например, которые экспрессируются на клеточной мембране, например, на мембране раковых клеток. Используемый в данном документе "мезотелин" включает белки, содержащие мутации, например, точечные мутации, фрагменты, вставки, делеции и сплайс-варианты полноразмерного мезотелина дикого типа.
Если не указано иное, то "нуклеотидная последовательность, кодирующая аминокислотную последовательность" включает все нуклеотидные последовательности, которые являются вырожденными вариантами друг друга и которые кодируют одну и ту же аминокислотную последовательность. Фраза "нуклеотидная последовательность, которая кодирует белок или РНК" может также включать интроны в том случае, если нуклеотидная последовательность, кодирующая белок, может в каком-либо варианте содержать интрон(-ы).
В контексте настоящего изобретения используются следующие сокращения для общераспространенных оснований нуклеиновых кислот. "А" относится к аденозину, "С" относится к цитозину, "G" относится к гуанозину, "Т" относится к тимидину, и "U" относится к уридину.
Термин "нуклеиновая кислота" или "полинуклеотид" относится к дезоксирибонуклеиновым кислотам (ДНК) или рибонуклеиновой кислоте (РНК) или комбинации на основе этих ДНК или РНК и их полимерам в однонитевой либо двухнитевой форме. Термин "нуклеиновая кислота" включает ген, кДНК или мРНК. В одном варианте осуществления молекула нуклеиновой кислоты является синтетической (например, химически синтезированной) или рекомбинантной. Если специально не ограничено, данный термин охватывает нуклеиновые кислоты, содержащие аналоги или производные природных нуклеотидов, которые характеризуются свойствами связывания, аналогичными свойствам эталонной нуклеиновой кислоты, и метаболизируются способом, аналогичным способу для встречающихся в природе нуклеотидов. Если не указано иное, конкретная последовательность нуклеиновой кислоты также неявно охватывает ее варианты с консервативными модификациями (например, с заменами вырожденными кодонами), аллели, ортологи, SNP и комплементарные последовательности, а также явно указанную последовательность. В частности, замены вырожденными кодонами можно осуществлять посредством генерирования последовательностей, в которых в третьем положении одного или нескольких выбранных (или всех) кодонов произведена замена на любое из канонических оснований и/или дезоксиинозиновые остатки (Batzer et al., Nucleic Acid Res. 19:5081 (1991); Ohtsuka et al., J. Biol. Chem. 260:2605-2608 (1985); и Rossolini et al., Mol. Cell. Probes 8:91-98 (1994)).
Термины "пептид", "полипептид" и "белок" используются взаимозаменяемо и относятся к соединению, состоящему из аминокислотных остатков, ковалентно связанных пептидными связями. Белок или пептид должен содержать по меньшей мере две аминокислоты, и не установлено ограничение на максимальное количество аминокислот, которые может содержать последовательность белка или пептида. Полипептиды включают любой пептид или белок, содержащий две или более аминокислот, соединенных друг с другом пептидными связями. Используемый в данном документе термин относится как к коротким цепям, которые также, как правило, обозначаются в уровне техники, например, как пептиды, олигопептиды и олигомеры, так и к более длинным цепям, которые обычно обозначаются в уровне техники как белки, которых существует множество типов. "Полипептиды" включают, например, среди прочих, биологически активные фрагменты, практически гомологичные полипептиды, олигопептиды, гомодимеры, гетеродимеры, варианты полипептидов, модифицированные полипептиды, производные, аналоги, слитые белки. Полипептид включает природный пептид, рекомбинантный пептид или их комбинацию.
Термин "функционально связанный" или "транскрипционный контроль" относится к функциональной связи между регуляторной последовательностью и гетерологичной последовательностью нуклеиновой кислоты, приводящей к экспрессии последней. Например, первая последовательность нуклеиновой кислоты функционально связана со второй последовательностью нуклеиновой кислоты в тех случаях, когда первая последовательность нуклеиновой кислоты размещена в функциональной взаимосвязи со второй последовательностью нуклеиновой кислоты. Например, промотор функционально связан с кодирующей последовательностью, если промотор влияет на транскрипцию или экспрессию кодирующей последовательности. Функционально связанные последовательности ДНК могут быть смежными друг с другом и, например, если необходимо соединить два участка, кодирующих белок, находятся в одной и той же рамке считывания.
Термин "парентеральное введение" иммуногенной композиции включает, например, методики подкожной (s.c.), внутривенной (i.v.), внутримышечной (i.m.) или внутригрудинной инъекции, внутриопухолевого введения или инфузии.
Термин "промотор" относится к последовательности ДНК, распознаваемой синтетическим аппаратом клетки или введенным синтетическим аппаратом, которая необходима для инициации специфической транскрипции полинуклеотидной последовательности.
Термин "промоторная/регуляторная последовательность" относится к последовательности нуклеиновой кислоты, которая необходима для экспрессии продукта гена, функционально связанного с промоторной/регуляторной последовательностью. В некоторых случаях эта последовательность может являться коровой промоторной последовательностью, а в других случаях эта последовательность может также содержать энхансерную последовательность и другие регуляторные элементы, которые необходимы для экспрессии продукта гена. Например, промоторная/регуляторная последовательность может представлять собой последовательность, которая обеспечивает экспрессию продукта гена тканеспецифическим образом.
Термин "сигнальный домен" относится к функциональной части белка, которая действует путем передачи информации в пределах клетки для регуляции клеточной активности через определенные сигнальные пути за счет образования вторичных мессенджеров или функционирует в качестве эффекторов за счет ответа на такие мессенджеры.
Термин "scFv" относится к слитому белку, который содержит по меньшей мере один фрагмент антитела, содержащий вариабельную область легкой цепи, и по меньшей мере один фрагмент антитела, содержащий вариабельную область тяжелой цепи, где вариабельные области легкой и тяжелой цепей непрерывно связаны, например, через синтетический линкер, например, короткий гибкий полипептидный линкер, и способны экспрессироваться в виде одноцепочечного полипептида, и где scFv сохраняет специфичность интактного антитела, из которого он получен. Если не указано иное, то используемый в данном документе scFv может содержать вариабельные области VL и VH в любом порядке, например, относительно N-конца и С-конца слитого полипептида, при этом scFv может содержать VL-линкер-VH или может содержать VH-линкер-VL.
Часть CAR, содержащая антитело или фрагмент этого антитела, может существовать в различных формах, в которых антигенсвязывающий домен экспрессируется в виде части непрерывной полипептидной цепи, в том числе, например, в виде фрагмента однодоменного антитела (sdAb), одноцепочечного антитела (scFv) и гуманизированного антитела (Harlow et al., 1999, в: Using Antibodies: A Laboratory Manual, Cold Spring Harbor Laboratory Press, NY; Harlow et al., 1989, в: Antibodies: A Laboratory Manual, Cold Spring Harbor, New York; Houston et al., 1988, Proc. Natl. Acad. Sci. USA 85:5879-5883; Bird et al., 1988, Science 242:423-426). В одном варианте осуществления антигенсвязывающий домен CAR содержит фрагмент антитела. В дополнительном варианте осуществления CAR содержит фрагмент антитела, который содержит scFv. Используемый в данном документе термин "связывающий домен" или "молекула антитела" относится к белку, например, к цепи иммуноглобулина или ее фрагменту, содержащему по меньшей мере последовательность одного вариабельного домена иммуноглобулина. Термин "связывающий домен" или "молекула антитела" охватывает антитела и фрагменты антител. В одном варианте осуществления молекула антитела представляет собой молекулу полиспецифического антитела, например, она содержит совокупность последовательностей вариабельных доменов иммуноглобулина, где первая последовательность вариабельного домена иммуноглобулина из совокупности характеризуется специфичностью связывания с первым эпитопом, а вторая последовательность вариабельного домена иммуноглобулина из совокупности характеризуется специфичностью связывания со вторым эпитопом. В одном варианте осуществления молекула полиспецифического антитела представляет собой молекулу биспецифического антитела. Биспецифическое антитело характеризуется специфичностью в отношении не более чем двух антигенов. Молекула биспецифического антитела отличается тем, что содержит первую последовательность вариабельного домена иммуноглобулина, которая характеризуется специфичностью связывания с первым эпитопом, и вторую последовательностью вариабельного домена иммуноглобулина, которая характеризуется специфичностью связывания со вторым эпитопом.
Термин "стимуляция" относится к первичному ответу, индуцируемому связыванием стимулирующей молекулы (например, комплекса TCR/CD3 или CAR) со своим когнатным лигандом (например, антигенной молекулой), за счет чего опосредуется событие передачи сигнала, такое как, без ограничения, передача сигнала с помощью комплекса TCR/CD3 или передача сигнала с помощью соответствующего рецептора NK или сигнальных доменов CAR. Стимуляция может опосредовать изменение экспрессии определенных молекул.
Термин "стимулирующая молекула" относится к молекуле, экспрессируемой иммунной клеткой (например, Т-клеткой, NK-клеткой, В-клеткой), которая обеспечивает цитоплазматическую(-ие) сигнальную(-ые) последовательность(-и), которая регулирует активацию иммунной клетки стимулирующим образом в по меньшей мере некоторых аспектах сигнального пути иммунной клетки. В одном аспекте сигнал представляет собой первичный сигнал, который инициируется, например, при связывании комплекса TCR/CD3 с молекулой МНС, нагруженной пептидом, и который приводит к опосредованию ответа Т-клеток, в том числе без ограничения пролиферации, активации, дифференцировки и т. п. Первичная цитоплазматическая сигнальная последовательность (также обозначаемая как "первичный сигнальный домен"), которая действует стимулирующим образом, может содержать сигнальный мотив, известный как иммунорецепторный тирозиновый активирующий мотив или ITAM. Примеры цитоплазматической сигнальной последовательности, содержащей ITAM, которая является особенно применимой в настоящем изобретении, включают без ограничения последовательности, полученные из CD3-дзета, общей гамма-цепи FcR (FCER1G), Fc-гамма-RIIa, FcR-бета (Fc-эпсилон-R1b), CD3-гамма, CD3-дельта, CD3-эпсилон, CD79a, CD79b, DAP10 и DAP12. В конкретном CAR по настоящему изобретению внутриклеточный сигнальный домен в любом одном или нескольких CAR по настоящему изобретению содержит внутриклеточную сигнальную последовательность, например, первичную сигнальную последовательность CD3-дзета. В конкретном CAR по настоящему изобретению первичная сигнальная последовательность CD3-дзета представляет собой последовательность, представленную под SEQ ID NO: 163, или эквивалентные остатки биологического вида, отличного от человека, например, мыши, грызуна, обезьяны, человекообразной обезьяны и т. п. В конкретном CAR по настоящему изобретению первичная сигнальная последовательность CD3-дзета представляет собой последовательность, представленную под SEQ ID NO: 166, или эквивалентные остатки биологического вида, отличного от человека, например, мыши, грызуна, обезьяны, человекообразной обезьяны и т. п.
Термин "вектор для переноса" относится к химическому соединению, которое содержит выделенную нуклеиновую кислоту и которое можно применять для доставки выделенной нуклеиновой кислоты внутрь клетки. Из уровня техники известны многочисленные векторы, в том числе без ограничения линейные полинуклеотиды, полинуклеотиды, ассоциированные с ионными или амфифильными соединениями, плазмиды и вирусы. Таким образом, термин "вектор для переноса" включает автономно реплицирующуюся плазмиду или вирус. Данный термин также следует толковать таким образом, что он дополнительно включает неплазмидные и невирусные соединения, которые содействуют переносу нуклеиновой кислоты в клетки, такие как, например, полилизиновое соединение, липосома и т. п. Примеры вирусных векторов для переноса включают без ограничения аденовирусные векторы, векторы на основе аденоассоциированного вируса, ретровирусные векторы, лентивирусные векторы и т. п.
Термин "дзета" или, в качестве альтернативы, "дзета-цепь", "CD3-дзета" или "TCR-дзета" определен как белок, представленный под № доступа в GenBank BAG36664.1, или эквивалентные остатки биологического вида, отличного от человека, например, мыши, грызуна, обезьяны, человекообразной обезьяны и т. п., и "стимулирующий домен дзета" или, в качестве альтернативы, "стимулирующий домен CD3-дзета" или "стимулирующий домен TCR-дзета" определен как аминокислотные остатки цитоплазматического домена дзета-цепи, которые являются достаточными для функциональной передачи исходного сигнала, необходимого для активации Т-клеток. В одном аспекте цитоплазматический домен дзета содержит остатки 52-164 из последовательности под № доступа GenBank BAG36664.1 или эквивалентные остатки биологического вида, отличного от человека, например, мыши, грызуна, обезьяны, человекообразной обезьяны и т. п., которые являются его функциональными ортологами. В одном аспекте "стимулирующий домен дзета" или "стимулирующий домен CD3-дзета" представляет собой последовательность, представленную под SEQ ID NO: 163 (мутантная CD3-дзета). В одном аспекте "стимулирующий домен дзета" или "стимулирующий домен CD3-дзета" представляет собой последовательность, представленную под SEQ ID NO: 166 (CD3-дзета человека дикого типа).
Термин "конститутивный промотор" относится к нуклеотидной последовательности, которая, находясь в функциональной связи с полинуклеотидом, который кодирует или определяет продукт гена, обуславливает продуцирование продукта гена в клетке при большинстве или всех физиологических условиях клетки.
Термин "индуцируемый промотор" относится к нуклеотидной последовательности, которая, находясь в функциональной связи с полинуклеотидом, который кодирует или определяет продукт гена, обуславливает продуцирование продукта гена в клетке практически только при присутствии в клетке индуктора, который соответствует данному промотору.
Термин "тканеспецифический промотор" относится к нуклеотидной последовательности, которая, находясь в функциональной связи с полинуклеотидом, который кодирует или определяет ген, обуславливает продуцирование продукта гена в клетке практически только в том случае, если клетка является клеткой из того типа ткани, который соответствует данному промотору.
Термины "антиген, ассоциированный с раком", "опухолевый антиген", "антиген, связанный с гиперпролиферативным нарушением" и "антиген, ассоциированный с гиперпролифративным нарушением" взаимозаменяемо относятся к антигенам, которые являются общими для специфических гиперпролиферативных нарушений. В некоторых вариантах осуществления такие термины относится к молекуле (как правило, белку, углеводу или липиду), которая экспрессируется на поверхности раковой клетки, либо полностью, либо в виде фрагмента (например, молекула MHC/пептид), и которая применима для преимущественного нацеливания фармакологического средства на раковую клетку. В некоторых вариантах осуществления опухолевый антиген представляет собой маркер, экспрессируемый как нормальными клетками, так и раковыми клетками, например, маркер линии дифференцировки, например, CD19 на В-клетках. В некоторых вариантах осуществления опухолевый антиген представляет собой молекулу клеточной поверхности, которая в раковой клетке сверхэкспрессируется по сравнению с нормальной клеткой, например, характеризуется 1-кратной сверхэкспрессией, 2-кратной сверхэкспрессией, 3-кратной или большей сверхэкспрессией по сравнению с нормальной клеткой. В некоторых вариантах осуществления опухолевый антиген представляет собой молекулу клеточной поверхности, которая синтезируется в раковой клетке ненадлежащим образом, например молекулу, которая содержит делеции, добавления или мутации по сравнению с молекулой, экспрессируемой на нормальной клетке. В некоторых вариантах осуществления опухолевый антиген будет экспрессироваться исключительно на клеточной поверхности раковой клетки, полностью или в виде фрагмента (например, молекула MHC/пептид), и не будет синтезироваться или экспрессироваться на поверхности нормальной клетки. В определенных аспектах антигены, связанные с гиперпролиферативным нарушением, по настоящему изобретению получены из форм рака, включающих без ограничения первичную или метастатическую меланому, тимому, лимфому, саркому, рак легкого, рак печени, неходжкинскую лимфому, лимфому Ходжкина, формы лейкоза, рак матки, рак шейки матки, рак мочевого пузыря, рак почки и формы аденокарциномы, такие как рак молочной железы, рак предстательной железы (например, кастрационнорезистентный или резистентный к терапии рак предстательной железы или метастатический рак предстательной железы), рак яичника, рак поджелудочной железы, и т. п., или плазмоклеточного пролиферативного нарушения, например, aсимптомaтической миеломы (вялотекущей множественной миеломы или невыраженной миеломы), моноклональной гаммапатии неустановленной этиологии (MGUS), макроглобулинемии Вальденстрема, форм плазмоцитомы (например, плазмоклеточной дискразии, солитарной миеломы, солитарной плазмоцитомы, экстрамедуллярной плазмоцитомы и множественной плазмоцитомы), системного амилоидоза с амилоидом из легких цепей и POEMS-синдрома (также известного как синдром Кроу-Фукаса, болезнь Такатцуки и PEP-синдром). В некоторых вариантах осуществления CAR по настоящему изобретению включают CAR, содержащие антигенсвязывающий домен (например, антитело или фрагмент антитела), который связывается с пептидом, презентируемым молекулой MHC. Обычно пептиды, полученные из эндогенных белков, заполняют карманы молекул главного комплекса гистосовместимости (MHC) I класса и распознаются T-клеточными рецепторами (TCR) на CD8+ T-лимфоцитах. Комплексы молекул MHC I класса конститутивно экспрессируются всеми ядросодержащими клетками. При раке комплексы вирусоспецифический и/или опухолеспецифический пептид/молекула MHC представляют собой уникальный класс мишеней клеточной поверхности для иммунотерапии. Были описаны TCR-подобные антитела, нацеливающиеся на пептиды, полученные из вирусных или опухолевых антигенов, связанные с лейкоцитарным антигеном человека (HLA)-A1 или HLA-A2 (см., например, Sastry et al., J Virol. 2011 85(5):1935-1942; Sergeeva et al., Blood, 2011 117(16):4262-4272; Verma et al., J Immunol 2010 184(4):2156-2165; Willemsen et al., Gene Ther 2001 8(21): 1601-1608; Dao et al., Sci Transl Med 2013 5(176): 176ra33; Tassev et al., Cancer Gene Ther 2012 19(2):84-100). Например, TCR-подобное антитело можно идентифицировать при скрининге библиотеки, такой как фаг-дисплейная библиотека scFv человека.
Термин "гибкий полипептидный линкер" или "линкер", используемый в отношении пептидного линкера, который содержит или состоит из аминокислот, таких как глициновые и/или сериновые остатки, применяемые отдельно или в комбинации, для связывания двух полипептидов вместе, например, COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающего полипептида и гетерологичного полипептида, или вариабельной области тяжелой цепи и вариабельной области легкой цепи. В одном варианте осуществления гибкий полипептидный линкер представляет собой Gly/Ser линкер и содержит аминокислотную последовательность (Gly-Gly-Gly-Ser)n (SEQ ID NO: 173), где n составляет положительный целое число, равное 1 или более. Например, n=1, n=2, n=3, n=4, n=5, n=6, n=7, n=8, n=9 и n=10. В одном варианте осуществления гибкие полипептидные линкеры включают без ограничения (Gly4 Ser)4 (SEQ ID NO: 141) или (Gly4 Ser)3 (SEQ ID NO: 142). В другом варианте осуществления линкеры включают множественные повторы (Gly2Ser), (GlySer) или (Gly3Ser) (SEQ ID NO: 143). В объем настоящего изобретения также включены линкеры, описанные в WO2012/138475, включенной в данный документ посредством ссылки.
Используемая в данном документе "транзиентная" относится к экспрессии неинтегрированного трансгена в течение периода нескольких часов, дней или недель, где период времени экспрессии является меньшим, чем период времени для экспрессии гена, если он интегрирован в геном или содержится в пределах стабильного плазмидного репликона в клетке. В вариантах осуществления молекула CAR транзиентно экспрессируется в клетке, например, клетке-хозяине, в течение конечного периода времени или количества репликаций клетки, например, менее 50 дней (например, менее 40, 30, 25, 20, 15, 10, 5, 4, 3, 2 или менее дней). В одном варианте осуществления транзиентная экспрессия осуществляется с применением транскрибированной in vitro РНК.
Используемая в данном документе "стабильная" относится к экспрессии трансгена, которая продолжается в течение более длительного периода, чем транзиентая экспрессия. В вариантах осуществления трансген интегрируется в геном клетки, например, клетки-хозяина, или содержится в пределах стабильного плазмидного репликона в клетке. В одном варианте осуществления трансген интегрирован в геном клетки с применением вектора для доставки гена, например, ретровирусного вектора, такого как лентивирусный вектор.
Используемые в данном документе термины "лечить", "лечение" и "осуществление лечения" относятся к снижению или ослаблению прогрессирования, тяжести и/или продолжительности пролиферативного нарушения или ослаблению одного или нескольких симптомов (например, одного или нескольких различимых симптомов) пролиферативного нарушения в результате введения одного или нескольких средств терапии (например, одного или нескольких терапевтических средств, таких как CAR по настоящему изобретению). В конкретных вариантах осуществления термины "лечить", "лечение" и "осуществление лечения" относятся к ослаблению по меньшей мере одного измеряемого физического параметра пролиферативного нарушения, такого как рост опухоли, необязательно различимого для пациента. В других вариантах осуществления термины "лечить", "лечение" и "осуществление лечения" относятся к ингибированию прогрессирования пролиферативного нарушения либо физическим путем, например, посредством стабилизации различимого симптома, физиологическим путем, например, посредством стабилизации физического параметра, либо ими обоими. В других вариантах осуществления термины "лечить", "лечение" и "осуществление лечения" относятся к снижению или стабилизации размера опухоли или числа раковых клеток. Лечение не обязательно должно быть на 100%, и в некоторых вариантах осуществления снижение или отсрочка по меньшей мере одного симптома заболевания или нарушения на по меньшей мере 50%, 60%, 70%, 80%, 90%, 95% или 99% являются достаточными, чтобы рассматриваться в рамках таких терминов.
Подразумевается, что термин "субъект" включает живые организмы, у которых можно вызвать иммунный ответ (например, млекопитающие, например, человек). Примеры субъектов включают человека, обезьян, шимпанзе, собак, кошек, мышей, крыс и их трансгенные формы. Т-клетки можно получить из ряда источников, в том числе из мононуклеарных клеток периферической крови, костного мозга, ткани лимфатических узлов, пуповинной крови, ткани тимуса, ткани из очага инфекции, асцита, плеврального выпота, ткани селезенки и опухолей.
Термин "подвергнутый трансфекции", или "подвергнутый трансформированию", или "подвергнутый трансдуцированию" относится к процессу, в ходе которого экзогенную нуклеиновую кислоту переносят или вводят в клетку-хозяина. "Трансфицированная", или "трансформированная", или "трансдуцированная" клетка представляет собой клетку, которая была подвергнута трансфекции, трансформации или трансдукции с помощью экзогенной нуклеиновой кислоты. Такая клетка включает первичную клетку субъекта и ее потомство.
Термин "специфически связывается" относится к антителу или лиганду, которые распознают когнатного белкового партнера по связыванию, присутствующего в образце, и связываются с ним, но при этом эти антитело или лиганд практически не распознают прочие молекулы в образце или не связываются с ними.
Диапазоны: на протяжении всего настоящего раскрытия различные аспекты настоящего изобретения могут быть представлены в формате диапазонов. Следует понимать, что описание в формате диапазонов служит лишь для удобства и краткости и не должно рассматриваться как жесткое ограничение объема настоящего изобретения. Соответственно, описание диапазона следует рассматривать как конкретно раскрывающее все возможные поддиапазоны, а также отдельные числовые значения в пределах этого диапазона. Например, описание такого диапазона, как от 1 до 6, следует рассматривать как конкретно раскрывающее такие поддиапазоны, как от 1 до 3, от 1 до 4, от 1 до 5, от 2 до 4, от 2 до 6, от 3 до 6 и т. д., а также отдельные числа в пределах этого диапазона, например, 1, 2, 2,7, 3, 4, 5, 5,3 и 6. В качестве другого примера, такой диапазон, как 95-99% идентичность, включает что-либо с 95%, 96%, 97%, 98% или 99% идентичностью и включает такие поддиапазоны, как 96-99%, 96-98%, 96-97%, 97-99%, 97-98% и 98-99% идентичность. Это применимо независимо от ширины диапазона.
Определения конкретных функциональных групп и химических терминов описаны более подробно ниже. Химические элементы идентифицированы в соответствии с Периодической таблицей элементов, CAS-версия, Handbook of Chemistry and Physics, 75-ое изд., форзац, и конкретные функциональные группы обычно определены, как описано там. Кроме того, общие принципы органической химии, а также конкретные функциональные фрагменты и реакционная способность, описаны в Thomas Sorrell, Organic Chemistry, University Science Books, Sausalito, 1999; Smith and March, March's Advanced Organic Chemistry, 5th Edition, John Wiley & Sons, Inc., New York, 2001; Larock, Comprehensive Organic Transformations, VCH Publishers, Inc., New York, 1989 и Carruthers, Some Modern Methods of Organic Synthesis, 3rd Edition, Cambridge University Press, Cambridge, 1987.
Используемый в данном документе термин "алкил" относится к одновалентному насыщенному углеводород с прямой или с разветвленной цепью, такому как прямая или разветвленная группа из 1-12, 1-10 или 1-6 атомов углерода, обозначаемая в данном документе как C1-C12алкил, C1-C10алкил и C1-C6алкил соответственно. Примеры алкильных групп включают без ограничения метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, втор-пентил, изопентил, трет-бутил, н-пентил, неопентил, н-гексил, втор-гексил и т. п.
Используемые в данном документе термины "алкенил" и "алкинил" относятся к ненасыщенным алифатическим группам, аналогичный по длине и возможному замещению с алкилами, описанными выше, но которые содержат по меньшей мере одну двойную или тройную связь соответственно. Иллюстративные алкенильные группы включают без ограничения -CH=CH2 и -CH2CH=CH2.
Применяемый в данном документе термин "алкокси" относится к насыщенному углеводороду с прямой или разветвленной цепью, содержащему 1-12 атомов углерода и содержащему концевой "O" в цепи, например, -O(алкил). Примеры алкокси-групп включают без ограничения метокси-, этокси-, пропокси-, бутокси-, трет-бутокси- или пентокси-группы.
Используемый в данном документе термин "арил" относится к моноциклической, бициклической или полициклической углеводородной кольцевой системе, где по меньшей мере одно кольцо является ароматическим. Иллюстративные арильные группы включают полностью ароматические кольцевые системы, такие как фенил (например, (C6)арил), нафтил (например, (C10)арил) и антраценил (например, (C14)арил), и кольцевые системы, где ароматическое углеродное кольцо слито с одним или несколькими неароматическими углеродными кольцами, такими как инданил, фталимид, нафтимидил или тетрагидронафтил и т. п.
Используемый в данном документе термин "карбоциклил" относится к моноциклической или конденсированной, спироконденсированной и/или мостиковой бициклической или полициклической углеводородной кольцевой системе, содержащей 3-18 атомов углерода, где каждое кольцо является либо полностью насыщенным, либо содержит одно или несколько ненасыщенных звеньев, но где ни одно из колец не является ароматическим. Иллюстративные карбоциклильные группы включают циклоалкильные группы (например, циклопентил, циклобутил, циклопентил, циклогексил и т. п.) и циклоалкенильные группы (например, циклопентенил, циклогексенил, циклопентадиенил и т. п.).
Используемый в данном документе термин "карбонил" относится к -C=O.
Используемый в данном документе термин "циано" относится к -CN.
Используемые в данном документе термины "галоген" или "галогенид" относятся к атому фтора (фтор, -F), атому хлора (хлор, -Cl), атому брома (бром, -Br) или атому йода (йод, -I).
Используемый в данном документе термин "галогеналкил" относится к одновалентной насыщенной прямой или разветвленной алкильной цепи, где по меньшей мере один атом углерода в цепи замещен одним или несколькими атомами галогена. В некоторых вариантах осуществления галогеналкильная группа может содержать, например, 1-12, 1-10 или 1-6 атомов углерода, и обозначается в данном документе как C1-C12галогеналкил, C1-C10галогеналкил и C1-C6галогеналкил. Примеры галогеналкильных групп включают без ограничения трифторметил, дифторметил, пентафторэтил, трихлорметил и т. д.
Термин "галогеналкокси" относится к насыщенному углеводороду с прямой или разветвленной цепью, содержащему 1-12 атомов углерода и содержащему концевой "O" в цепи, где по меньшей мере один атом углерода в цепи замещен одним или несколькими галогенами. Примеры галогеналкокси-групп включают без ограничения, трифторметокси, дифторметокси, пентафторэтокси, трихлорметокси и т. д.
Используемый в данном документе термин "гетероалкил" относится к одновалентной насыщенной прямой или разветвленной алкильной цепи, где по меньшей мере один атом углерода в цепи замещен гетероатомом, таким как O, S или N, при условии, что после замещения цепь содержит по меньшей мере один атом углерода. В некоторых вариантах осуществления гетероалкильная группа может содержать, например, 1-12, 1-10 или 1-6 атомов углерода и обозначается в данном документе как C1-C12гетероалкил, C1-C10гетероалкил и C1-C6гетероалкил. В некоторых случаях гетероалкильная группа содержит 1, 2, 3 или 4 независимо выбранных гетероатома вместо 1, 2, 3 или 4 отдельных атомов углерода в алкильной цепи. Иллюстративные гетероалкильные группы включают -CH2NHC(O)CH3, -CH2CH2OCH3, -CH2CH2NHCH3, -CH2CH2N(CH3)CH3, и т. п.
Применяемые в данном документе термины "алкилен," "алкенилен", "алкинилен" и "гетероалкилен" относятся к двухвалентному радикалу алкильной, алкенильной, алкинильной или гетероалкильной группы соответственно. Любая из одновалентной алкильной, алкенильной, алкинильной или гетероалкильной группы может стать алкиленом, алкениленом, алкиниленом или гетероалкиленом при удалении второго атома водорода из алкильной, алкенильной, алкинильной или гетероалкильной группы.
Используемый в данном документе термин "гетероарил" относится к моноциклической, бициклической или полициклической кольцевой системе, где по меньшей мере одно кольцо является ароматическим и содержит гетероатом; и где ни одно из остальных колец не является гетероциклилом (как определено ниже). Иллюстративные гетероарильные группы включают кольцевые системы, в которых (i) каждое кольцо содержит гетероатом и является ароматическим, например, представляет собой имидазолил, оксазолил, тиазолил, триазолил, пирролил, фуранил, тиофенил пиразолил, пиридинил, пиразинил, пиридазинил, пиримидинил, индолизинил, пуринил, нафтиридинил и птеридинил; (ii) каждое кольцо является ароматическим или карбоциклильным, при этом по меньшей мере одно ароматическое кольцо содержит гетероатом и по меньшей мере одно другое кольцо представляет собой углеводородное кольцо или, например, индолил, изоиндолил, бензотиенил, бензофуранил, дибензoфуранил, индазолил, бензимидазолил, бензтиазолил, хинолил, изохинолил, циннолинил, фталазинил, хиназолинил, хиноксалинил, карбазолил, акридинил, феназинил, фенотиазинил, феноксазинил, пиридо[2,3-b]-1,4-оксазин-3(4H)-он, тиазолo-[4,5-c]-пиридинил, 4,5,6,7-тетрагидротиено[2,3-c]пиридинил, 5,6-дигидро-4H-тиено[2,3-c]пирролил, 4,5,6,7,8-тетрагидрохинолинил и 5,6,7,8-тетрагидроизохинолинил; и (iii) каждое кольцо является ароматический или карбоциклильным, и по меньшей мере одно ароматическое кольцо имеет общий мостиковый гетероатом с другим ароматическим кольцом, например, представляет собой 4H-хинолизинил. В определенных вариантах осуществления гетероарил представляет собой моноциклическое или бициклическое кольцо, где каждое из указанных колец содержит 5 или 6 атомов в кольце, где 1, 2, 3 или 4 из указанных атомов в кольце представляют собой гетероатом, независимо выбранный из N, O и S.
Используемый в данном документе термин "гетероциклил" относится к моноциклической или конденсированной, спироконденсированной и/или мостиковой бициклической и полициклической кольцевым системам, где по меньшей мере одно кольцо является насыщенным или частично ненасыщенным (но не ароматическим) и содержит гетероатом. Гетероциклил может быть присоединен к своей боковой группе по любому гетероатому или атому углерода, которые приводят к стабильной структуре, и любые из атомов в кольце могут быть необязательно замещенными. Иллюстративные гетероциклилы включают кольцевые системы, в которых (i) каждое кольцо является неароматическим и по меньшей мере одно кольцо содержит гетероатом, например, представляет собой тетрагидрофуранил, тетрагидротиенил, пирролидинил, пирролидонил, пиперидинил, пирролинил, декагидрохинолинил, оксазолидинил, пиперазинил, диоксанил, диоксоланил, диазепинил, оксазепинил, тиазепинил, морфолинил и хинуклидинил; (ii) по меньшей мере одно кольцо является неароматическим и содержит гетероатом, и по меньшей мере одно другое кольцо представляет собой ароматическое углеродное кольцо, например, 1,2,3,4-тетрагидрохинолинил; и (iii) по меньшей мере одно кольцо является неароматическим и содержит гетероатом, и по меньшей мере одно другое кольцо является ароматическим и содержит гетероатом, например, представляет собой 3,4-дигидро-1H-пиранo[4,3-c]пиридинил и 1,2,3,4-тетрагидро-2,6-нафтиридинил. В определенных вариантах осуществления гетероциклил представляет собой моноциклическое или бициклическое кольцо, где каждое из указанных колец содержит 3-7 атомов в кольце, где 1, 2, 3 или 4 из указанных атомов в кольце представляют собой гетероатом, независимо выбранный из N, O и S.
Как описано в данном документе, соединения по настоящему изобретению могут содержать "необязательно замещенные" фрагменты. Обычно термин "замещенный", независимо от того, предшествует ли ему термин "необязательно" или нет, означает, что один или несколько водородов обозначенного фрагмента заменены подходящим заместителем. Если не указано иное, "необязательно замещенная" группа может иметь подходящий заместитель в каждом замещаемом положении группы, и если несколько положений в любой данной структуре может быть замещено несколькими заместителями, выбранными из указанной группы, заместитель может быть либо одним и тем же, либо различным в каждом положении. Комбинации заместителей, предусмотренных в данном изобретении, предпочтительно являются такими, которые приводят к образованию стабильных или химически возможных соединений. Используемый в данном документе термин "стабильный" относится к соединениям, которые изменяются в незначительной степени, когда их подвергают условиям, позволяющим их продуцирование, выявление и, в определенных вариантах осуществления, их извлечение, очистку и применение для одной или нескольких целей, раскрытых в данном документе.
Используемый в данном документе термин "оксо" относится к -C=O.
Используемый в данном документе термин "тиокарбонил" относится к -C=O.
Используемый в данном документе термин "фармацевтически приемлемая соль" относится к тем солям, которые с медицинской точки зрения являются подходящими для применения в контакте с тканями человека или низших животных, не вызывая чрезмерной токсичности, раздражения, аллергической реакции и т. п., и соответствуют допустимому отношению польза/риск. Фармацевтически приемлемые соли хорошо известны из уровня техники. Например, Berge et al. подробно описывают фармацевтически приемлемые соли в J. Pharmaceutical Sciences, 1977, 66: 1-19, включенной в данный документ посредством ссылки. Фармацевтически приемлемые соли соединений по настоящему изобретению включают соли, полученные из подходящих неорганических и органических кислот и оснований. Примеры фармацевтически приемлемых, нетоксичных солей присоединения кислот представляют собой соли аминогруппы, образуемые с неорганическими кислотами, такими как хлористоводородная кислота, бромистоводородная кислота, фосфорная кислота, серная кислота и перхлорная кислота, или с органическими кислотами, такими как уксусная кислота, щавелевая кислота, малеиновая кислота, винная кислота, лимонная кислота, янтарная кислота или малоновая кислота, или с применением других способов, известных из уровня техники, таких как ионный обмен. Другие фармацевтически приемлемые соли включают адипатные, альгинатые, аскорбатные, аспартатные, бензолсульфонатные, бензоатные, бисульфатные, боратные, бутиратные, камфоратные, камфорасульфонатные, цитратные, циклопентанпропионатные, диглюконатные, додецилсульфатные, этансульфонатные, формиатные, фумаратные, глюкогептонатные, глицерофосфатные, глюконатные, гемисульфатные, гептаноатные, гексанoатные, гидройодидные, 2-гидрокси-этансульфонатные, лактобионатные, лактатные, лауратные, лаурилсульфатные, малатные, малеатные, малонатные, метансульфонатные, 2-нафталинсульфонатные, никотинатные, нитратные, олеатные, оксалатные, пальмитатные, памоатные, пектинатные, персульфатные, 3-фенилпропионатные, фосфатные, пикратные, пивалатные, пропионатные, стеаратные, сукцинатные, сульфатные, тартратные, тиоцианатные, п-толуолсульфонатные, ундеканоатные, валератные соли и т. п. Соли, полученные из подходящих оснований, включают соли щелочных металлов, щелочноземельных металлов, аммония и N+(C1-4 алкила)4. Иллюстративные соли щелочных или щелочноземельных металлов включают соли натрия, лития, калия, кальция, магния и т. п. При необходимости, дополнительные фармацевтически приемлемые соли включают нетоксичные аммониевые соли, соли четвертичного аммония и катионов аминов, образованные с применением противоионов, таких как галогенид, гидроксид, карбоксилат, сульфат, фосфат, нитрат, сульфонат низшего алкила и арилсульфонат.
Термин "сольват" относится к формам соединения, которые ассоциированы с растворителем, обычно за счет реакции сольволиза. Данная физическая ассоциация может включать образование водородных связей. Традиционные растворители включают воду, метанол, этанол, уксусную кислоту, DMSO, THF, диэтиловый эфир и т. п. Соединения формулы (I), формула (I-a) и/или формулы (II) могут быть получены, например, в кристаллической форме и могут быть сольватированными. Подходящие сольваты включают фармацевтически приемлемые сольваты и дополнительно включают как стехиометрические сольваты, так и нестехиометрические сольваты. В некоторых случаях сольват может быть выделен, например, если одна или несколько молекул растворителя включены в кристаллическую решетку кристаллического твердого вещества. "Сольват" охватывает как фазу раствора, так и отделимые сольваты. Иллюстративные сольваты включают гидраты, этаноляты и метаноляты.
Термин "гидрат" относится к соединению, которое ассоциировано с водой. Как правило, количество молекул воды, содержащихся в гидрате соединения, находится в определенном отношении с количеством молекул соединения в гидрате. Следовательно, гидрат соединения может быть представлен, например, с помощью общей формулы R⋅x H2O, где R представляет собой соединение, и где x составляет число более 0. Данное соединение может образовывать несколько типов гидратов, в том числе, например, моногидраты (x составляет 1), низшие гидраты (x составляет число больше 0 и меньше 1, например, полугидраты (R⋅0,5 H2O)) и полигидраты (x составляет число более 1, например, дигидраты (R⋅2 H2O) и гексагидраты (R⋅6 H2O)).
Следует понимать, что соединения, которые имеют одинаковую молекулярную формулу, но отличаются природой или последовательностью связей своих атомов или расположением своих атомов в пространстве, называются "изомеры". Изомеры, которые отличаются расположением своих атомов в пространстве, называются "стереоизомеры".
Стереоизомеры, которые не являются зеркальными отражениями друг друга, называются "диастереомеры", а стереоизомеры, которые не представляют собой несовпадающие при наложении зеркальные отражения друг друга, называются "энантиомеры". Когда соединение имеет асимметрический центр, например, он образует связи с четырьмя различными группами, то возможна пара энантиомеров. Энантиомер может быть охарактеризован с помощью абсолютной конфигурации его асимметрического центра и описан с помощью правил последовательности Кана и Прелога для R- и S-конфигурации или по способу, которым молекула вращает плоскость поляризованного света, и обозначен как правовращающий или левовращаюший (т. е. как (+) или (-)-изомеры соответственно). Хиральное соединение может существовать либо в виде отдельного энантиомера, либо в виде их смеси. Смесь, содержащая равные доли энантиомеров, называется "рацемической смесью".
Термин "таутомеры" относится к соединениям, которые являются взаимозаменяемыми формами конкретной структуры соединения и которые отличаются перестановками атомов водорода и электронов. Таким образом, две структуры могут находиться в равновесии благодаря движению π-электронов и атома (обычно H). Например, енолы и кетоны являются таутомерами, поскольку они быстро взаимопревращаются при обработке либо кислотой, либо основанием. Другим примером таутомерии являются аци- и нитроформы фенилнитрометана, которые подобным образом образуются при обработке кислотой или основанием.
Таутомерные формы могут иметь значение для достижения оптимальной химической реакционной способности и биологической активности представляющего интерес соединения.
Если не указано иное, то подразумевается, что структуры, изображенные в данном документе, также включают все изомерные (например, энантиомерные, диастереомерные и геометрические (или конформационные)) формы данной структуры; например, R- и S-конфигурации для каждого асимметрического центра, Z- и E-изомеры с двойной связью и конформационные Z- и E-изомеры. Следовательно, в объем настоящего изобретения входят отдельные стереохимические изомеры, а также смеси из энантиомеров, диастереомеров и геометрических (или конформационных) изомеров соединений по настоящему изобретению. Если не указано иное, то в объем настоящего изобретения входят все таутомерные формы соединений по настоящему изобретению. Кроме того, если не указано иное, также подразумевается, что структуры, изображенные в данном документе, включают соединения, которые отличаются только присутствием одного или нескольких изотопно-обогащенных атомов. Например, в объем настоящего изобретения входят соединения со структурами по настоящему изобретению, включающие замену водорода на дейтерий или тритий или замену углерода на углерод, обогащенный 13C или 14C. В одном варианте осуществления атомы водорода, присутствующие в любом из соединений, раскрытых в данном документе (например, соединении формулы (I)), являются изотопно-обогащенными по дейтерию. Такие соединения применимы, например, в качестве аналитических инструментов, в качестве зондов в биологических анализах или в качестве терапевтических средств в соответствии с настоящим изобретением.
Если предпочтителен конкретный энантиомер, в некоторых вариантах осуществления его можно получать практически не содержащим соответствующего энантиомера, и он может также называться "оптически обогащенным". Используемый в данном документе "оптически обогащенный" означает, что соединение составляет значительно большая доля одного энантиомера. В определенных вариантах осуществления соединение составляет по меньшей мере приблизительно 90% по весу предпочтительного энантиомера. В других вариантах осуществления соединение составляет по меньшей мере приблизительно 95%, 98% или 99% по весу предпочтительного энантиомера. Предпочтительные энантиомеры могут быть выделены из рацемических смесей с помощью любого способа, известного специалистам в данной области техники, включая хиральную жидкостную хроматографию высокого давления (HPLC), а также образование и кристаллизация хиральных солей, или получены с помощью асимметрического синтеза. См., например, Jacques et al., Enantiomers, Racemates and Resolutions (Wiley Interscience, New York, 1981); Wilen, et al., Tetrahedron 33:2725 (1977); Eliel, E.L. Stereochemistry of Carbon Compounds (McGraw-Hill, NY, 1962); Wilen, S.H. Tables of Resolving Agents and Optical Resolutions p. 268 (E.L. Eliel, Ed., Univ. of Notre Dame Press, Notre Dame, IN 1972).
Эти и другие иллюстративные заместители описаны более подробно в разделах Подробное описание, Фигуры, Примеры и Формула изобретения. Подразумевается, что настоящее изобретение никоим образом не ограничивается вышеприведенным иллюстративным перечнем заместителей
COF1/CRBN-связывающий полипептид, COF2/CRBN-связывающий полипептид или COF3/CRBN-связывающий полипептид
В данном документе, помимо прочего, раскрыты слитые полипептиды, которые содержат полипептид, связывающий соединение формулы (I) (COF1)/CRBN, полипептид, связывающий соединение формулы (II) (COF2)/CRBN, или полипептид, связывающий соединение формулы (III) (COF3)/CRBN. В вариантах осуществления в присутствии COF1 или COF2 (например, талидомида и его производных, например, леналидомида, помалидомида и талидомид) или в присутствии COF3 (например, соединения, раскрытого в таблице 29) COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид в слитом полипептиде увеличивает посттрансляционную модификацию и/или деградацию слитого полипептида. В некоторых вариантах осуществления посттрансляционная модификация может включать убиквитинирование (например, моно- или полиубиквитинирование) одного или нескольких аминокислотных остатков, например, одного или нескольких лизинов или метионинов, в слитом полипептиде (например, одного или всех во всем гетерологичном полипептиде и/или COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающем полипептиде или их части).
В определенных вариантах осуществления один или несколько остатков лизина слитого полипептида (например, всего гетерологичного полипептида и/или COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающего полипептида или их части) подвергнуты убиквитинированию. В некоторых вариантах осуществления один или несколько остатков метионина слитого полипептида (например, всего гетерологичного полипептида и/или COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающего полипептида или их части) подвергнуты убиквитинированию (например, моно- или полиубиквитинированию).
Без ограничения какой-либо теорией, в некоторых вариантах осуществления инактивация, например, деградация, слитого полипептида, описанного в данном документе, может включать одну, две, три или все из следующих стадий, например, в клетке или реакционной смеси:
(1) ассоциация слитого полипептида, который содержит COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид, с одной или несколькими субъединицами (например, CRBN) комплекса убиквитинлигазы (например, комплекса убиквитинлигазы E3) в присутствии COF1 или COF2 (например, талидомида и его производных (например, леналидомида)) или в присутствии COF3 (например, соединения, раскрытого в таблице 29);
(2) убиквитинирование слитого полипептида (например, убиквитинирование в гетерологичном полипептиде и/или COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающей полипептиде), за счет обеспечивается подвергнутый убиквитинированию слитый полипептид; и
(3) деградация подвергнутого убиквитинированию слитого полипептида.
В некоторых вариантах осуществления любой COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид, описанный в данном документе, увеличивает посттрансляционную модификацию и/или деградацию слитого полипептида в присутствии COF1, COF2 или COF3, например, относительно модификации и/или деградации в отсутствие COF1, COF2 или COF3. В одном варианте осуществления COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид увеличивает селективное убиквитинирование слитого полипептида в присутствии COF1, COF2 или COF3, например, относительно убиквитинирования в отсутствие COF1, COF2 или COF3.
В некоторых вариантах осуществления COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид получен из аминокислотной последовательности и/или структурного мотива (например, домена), который связывается с одним или несколькими компонентами комплекса убиквитинлигазы (например, комплекса убиквитинлигазы E3) в присутствии COF1, COF2 или COF3. В некоторых вариантах осуществления COF1 или COF2 представляет собой талидомидный класс соединений (например, леналидомид, помалидомид и талидомид), например, описанный в данном документе. В некоторых вариантах осуществления COF3 представляет собой соединение, раскрытое в таблице 29. В некоторых вариантах осуществления COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид содержит домен "цинковых пальцев" (например, домен "цинковых пальцев" 2) или его часть. В некоторых вариантах осуществления COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид содержит β-изгиб. В некоторых вариантах осуществления COF1/CRBN- или COF2/CRBN-связывающий полипептид содержит β-изгиб из семейства транскрипционных факторов Ikaros, например, IKZF1 или IKZF3, или последовательность, практически идентичную ему (например, на по меньшей мере 85%, 87, 90, 95, 97, 98, 99, или 100% идентичную ему). В некоторых вариантах осуществления COF1/CRBN- или COF2/CRBN-связывающий полипептида содержит β-шпильку из семейства транскрипционных факторов Ikaros, например, IKZF1 или IKZF3, или последовательность, практически идентичную ей (например, на по меньшей мере 85%, 87, 90, 95, 97, 98, 99, или 100% идентичную β-шпильке из IKZF1 или IKZF3, например, как описано в Kronke, J. et al. (2014) Science 343(6168):301-5). В некоторых вариантах осуществления COF3/CRBN-связывающий полипептид содержит β-изгиб из IKZF2 или последовательность, практически идентичную ему (например, на по меньшей мере 85%, 87, 90, 95, 97, 98, 99, или 100% идентичную ему). В некоторых вариантах осуществления COF3/CRBN-связывающий полипептид содержит β-шпильку из IKZF2 или последовательность, практически идентичную ей (например, на по меньшей мере 85%, 87, 90, 95, 97, 98, 99, или 100% идентичную ей).
В некоторых вариантах осуществления COF1/CRBN- или COF2/CRBN-связывающий полипептид содержит от приблизительно 10 до приблизительно 95 аминокислотных остатков, от приблизительно 15 до приблизительно 90 аминокислотных остатков, от приблизительно 20 до приблизительно 85 аминокислотных остатков, от приблизительно 25 до приблизительно 80 аминокислотных остатков, от приблизительно 30 до приблизительно 75 аминокислотных остатков, от приблизительно 35 до приблизительно 70 аминокислотных остатков, от приблизительно 40 до приблизительно 65 аминокислотных остатков, от приблизительно 45 до приблизительно 65 аминокислотных остатков, от приблизительно 50 до приблизительно 65 аминокислотных остатков или от приблизительно 55 до приблизительно 65 аминокислотных остатков из IKZF1 (например, SEQ ID NO: 20) или IKZF3 (например, SEQ ID NO: 19) или последовательность, практически идентичную им (например, на по меньшей мере 85%, 87, 90, 95, 97, 98, 99, или 100% идентичную им). В некоторых вариантах осуществления COF1/CRBN- или COF2/CRBN-связывающий полипептид содержит по меньшей мере 10 аминокислот, по меньшей мере 15 аминокислот, по меньшей мере 20 аминокислот, по меньшей мере 25 аминокислот, по меньшей мере 30 аминокислот, по меньшей мере 35 аминокислот, по меньшей мере 40 аминокислот, по меньшей мере 45 аминокислот, по меньшей мере 50 аминокислот, по меньшей мере 55 аминокислот, по меньшей мере 60 аминокислот, по меньшей мере 65 аминокислот, по меньшей мере 70 аминокислот, по меньшей мере 75 аминокислот, по меньшей мере 80 аминокислот, по меньшей мере 85 аминокислот, по меньшей мере 90 аминокислот, по меньшей мере 90 аминокислот или по меньшей мере 95 аминокислот из IKZF1 (например, SEQ ID NO: 20) или IKZF3 (например, SEQ ID NO: 19) или последовательность, практически идентичную им (например, на по меньшей мере 85%, 87, 90, 95, 97, 98, 99, или 100% идентичную им). В некоторых вариантах осуществления COF1/CRBN- или COF2/CRBN-связывающий полипептид содержит или состоит из аминокислотных последовательностей, выбранных из группы, состоящей из SEQ ID NO: 1-6, 11-15, 40, 41-43, 77, 78, 84-86, и 100.
В некоторых вариантах осуществления COF3/CRBN-связывающий полипептид содержит от приблизительно 10 до приблизительно 95 аминокислотных остатков, от приблизительно 15 до приблизительно 90 аминокислотных остатков, от приблизительно 20 до приблизительно 85 аминокислотных остатков, от приблизительно 25 до приблизительно 80 аминокислотных остатков, от приблизительно 30 до приблизительно 75 аминокислотных остатков, от приблизительно 35 до приблизительно 70 аминокислотных остатков, от приблизительно 40 до приблизительно 65 аминокислотных остатков, от приблизительно 45 до приблизительно 65 аминокислотных остатков, от приблизительно 50 до приблизительно 65 аминокислотных остатков или от приблизительно 55 до приблизительно 65 аминокислотных остатков из IKZF2 (например, SEQ ID NO: 21) или последовательность, практически идентичную им (например, на по меньшей мере 85%, 87, 90, 95, 97, 98, 99, или 100% идентичную им). В некоторых вариантах осуществления COF3/CRBN-связывающий полипептид содержит по меньшей мере 10 аминокислот, по меньшей мере 15 аминокислот, по меньшей мере 20 аминокислот, по меньшей мере 25 аминокислот, по меньшей мере 30 аминокислот, по меньшей мере 35 аминокислот, по меньшей мере 40 аминокислот, по меньшей мере 45 аминокислот, по меньшей мере 50 аминокислот, по меньшей мере 55 аминокислот, по меньшей мере 60 аминокислот, по меньшей мере 65 аминокислот, по меньшей мере 70 аминокислот, по меньшей мере 75 аминокислот, по меньшей мере 80 аминокислот, по меньшей мере 85 аминокислот, по меньшей мере 90 аминокислот, по меньшей мере 90 аминокислот или по меньшей мере 95 аминокислот из IKZF2 (например, SEQ ID NO: 21) или последовательность, практически идентичную им (например, на по меньшей мере 85%, 87, 90, 95, 97, 98, 99, или 100% идентичную им). В некоторых вариантах осуществления COF3/CRBN-связывающий полипептид содержит или состоит из аминокислотных последовательностей, выбранных из группы, состоящей из SEQ ID NO: 109, 113 и 114.
В некоторых вариантах осуществления иллюстративные полноразмерные последовательности IKZF1, IKZF2, IKZF3, IKZF4 и IKZF5 или их фрагмент, представлены в таблице 1.
Соединения деградации
В данном документе, среди прочего, раскрыты соединения деградации, которые могут, например, увеличивать убиквитинирование и/или деградацию слитых белков, содержащих метку деградации.
В некоторых вариантах осуществления соединение деградации содержит представителя талидомидного класса соединений. В некоторых вариантах осуществления представители талидомидного класса соединений включают без ограничения леналидомид (CC-5013), помалидомид (CC-4047 или ACTIMID), талидомид или их соли или производные. В некоторых вариантах осуществления соединение деградации может представлять собой смесь из одного, двух, трех или более представителей талидомидного класса соединений. Аналоги талидомида и иммуномодулирующие свойства аналогов талидомида описаны в Bodera and Stankiewicz, Recent Pat Endocr Metab Immune Drug Discov. 2011 Sep;5(3):192-6, который включен в данный документ посредством ссылки во всей своей полноте. Структурный комплекс аналогов талидомида и убиквитина E3 описан в Gandhi et al., Br J Haematol. 2014 Mar;164(6):811-21, который включен в данный документ посредством ссылки во всей своей полноте. Модуляция убиквитинлигазы E3 под действием аналогов талидомида описана в Fischer et al., Nature. 2014 Aug 7;512(7512):49-53, который включен в данный документ посредством ссылки во всей своей полноте.
В некоторых вариантах осуществления соединение деградации содержит соединение формулы (I):

или его фармацевтически приемлемую соль, сложный эфир, гидрат, сольват или таутомер, где:
X представляет собой O или S;
R1 представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, карбоциклил, гетероциклил, арил или гетероарил, каждый из которых независимо и необязательно замещен одним или несколькими R4;
каждый из R2a и R2b независимо представляет собой водород или C1-C6алкил; или R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу или тиокарбонильную группу;
каждый из R3 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD) или -N(RC)S(O)xRE, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или несколькими R6;
каждый R4 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, оксо, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD), -N (RC)S(O)xRE, карбоциклил, гетероциклил, арил или гетероарил, где каждый алкил, алкенил, алкинил, гетероалкил, карбоциклил, гетероциклил, арил и гетероарил независимо и необязательно замещен одним или несколькими R7;
каждый из RA, RB, RC, RD и RE независимо представляет собой водород или C1-C6алкил;
каждый R6 независимо представляет собой C1-C6алкил, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, арил или гетероарил, где каждый арил и гетероарил независимо и необязательно замещен одним или несколькими R8;
каждый R7 независимо представляет собой галоген, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
каждый R8 независимо представляет собой C1-C6алкил, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
n составляет 0, 1, 2, 3 или 4; и
x составляет 0, 1 или 2.
В некоторых вариантах осуществления X представляет собой O.
В некоторых вариантах осуществления R1 представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, карбоциклил, гетероциклил, арил или гетероарил, каждый из которых независимо и необязательно замещен 1-12 R4 (например, 1 R4, 2 R4, 3 R4, 4 R4, 5 R4, 6 R4, 7 R4, 8 R4, 9 R4, 10 R4, 11 R4 или 12 R4). В некоторых вариантах осуществления R1 представляет собой гетероциклил. В некоторых вариантах осуществления R1 представляет собой 6-членный гетероциклил или 5-членный гетероциклил. В некоторых вариантах осуществления R1 представляет собой 6-членный гетероциклил или 5-членный гетероциклил, каждый из которых независимо и необязательно замещен 1-6 R4 (например, 1 R4, 2 R4, 3 R4, 4 R4, 5 R4 или 6 R4). В некоторых вариантах осуществления R1 представляет собой азот-содержащий гетероциклил. В некоторых вариантах осуществления R1 представляет собой пиперидинил (например, пиперидин-2,6-дионил).
В некоторых вариантах осуществления каждый из R2a и R2b независимо представляет собой водород. В некоторых вариантах осуществления R2a и R2b вместе с углеродом, к которому они присоединены, образуют карбонильную группу.
В некоторых вариантах осуществления каждый из R3 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD), или -N(RC)S(O)xRE, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен 1-12 R6 (например, 1 R6, 2 R6, 3 R6, 4 R6, 5 R6, 6 R6, 7 R6, 8 R6, 9 R6, 10 R6, 11 R6 или 12 R6). В некоторых вариантах осуществления R3 представляет собой C1-C6гетероалкил, -N(RC)(RD) или -N(RC)C(O)RA. В некоторых вариантах осуществления R3 представляет собой C1-C6гетероалкил (например, CH2NHC(O)CH2-фенил-трет-бутил), -N(RC)(RD) (например, NH2) или -N(RC)C(O)RA (например, NHC(O)CH3). В некоторых вариантах осуществления R3 представляет собой C1-C6гетероалкил, необязательно замещенный 1-6 R6 (например, 1 R6, 2 R6, 3 R6, 4 R6, 5 R6 или 6 R6).
В некоторых вариантах осуществления каждый R4 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, оксо, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD), -N (RC)S(O)xRE, карбоциклил, гетероциклил, арил или гетероарил, где каждый алкил, алкенил, алкинил, гетероалкил, карбоциклил, гетероциклил, арил и гетероарил независимо и необязательно замещен 1-12 R7 (например, 1 R7, 2 R7, 3 R7, 4 R7, 5 R7, 6 R7, 7 R7, 8 R7, 9 R7, 10 R7, 11 R7 или 12 R7).
В некоторых вариантах осуществления каждый R6 независимо представляет собой C1-C6алкил, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, арил или гетероарил, где каждый арил и гетероарил независимо и необязательно замещен 1-6 R8 (например, 1 R8, 2 R8, 3 R8, 4 R8, 5 R8 или 6 R8).
В одном варианте осуществления X представляет собой O. В одном варианте осуществления R1 представляет собой гетероциклил (например, пиперидин-2,6-дионил). В одном варианте осуществления каждый из R2a и R2b независимо представляет собой водород. В одном варианте осуществления n составляет 1. В одном варианте осуществления R3 представляет собой -N(RC)(RD) (например, -NH2). В одном варианте осуществления соединение деградации содержит леналидомид, например, 3-(4-амино-1-оксоизоиндолин-2-ил)пиперидин-2,6-дион или его фармацевтически приемлемую соль. В одном варианте осуществления соединение деградации представляет собой леналидомид, например, соответствующий следующей формулой:
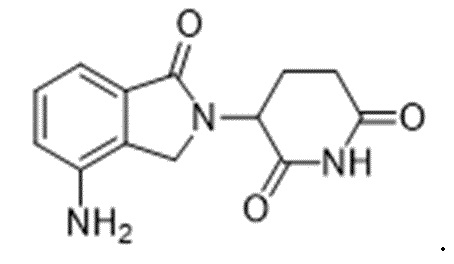
В одном варианте осуществления X представляет собой O. В одном варианте осуществления R1 представляет собой гетероциклил (например, пиперидинил-2,6-дионил). В некоторых вариантах осуществления R2a и R2b вместе с углеродом, к которому они присоединены, образуют карбонильную группу. В одном варианте осуществления n составляет 1. В одном варианте осуществления R3 представляет собой -N(RC)(RD) (например, -NH2). В одном варианте осуществления соединение деградации содержит помалидомид, например, 4-амино-2-(2,6-диоксопиперидин-3-ил)изоиндолин-1,3-дион или его фармацевтически приемлемую соль. В одном варианте осуществления соединение деградации представляет собой помалидомид, например, соответствующий следующей формуле:
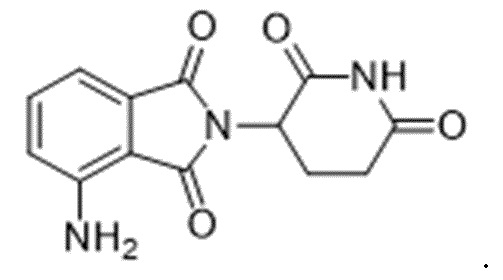
В одном варианте осуществления X представляет собой O. В одном варианте осуществления R1 представляет собой гетероциклил (например, пиперидинил-2,6-дионил). В одном варианте осуществления R2a и R2b вместе с углеродом, к которому они присоединены, образуют карбонильную группу. В одном варианте осуществления n составляет 0. В одном варианте осуществления соединение деградации содержит талидомид, например, 2-(2,6-диоксопиперидин-3-ил)изоиндолин-1,3-дион или его фармацевтически приемлемую соль. В одном варианте осуществления продукт деградации представляет собой талидомид, например, соответствующий следующей формуле:
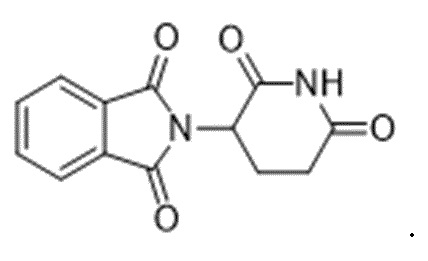
В одном варианте осуществления X представляет собой O. В одном варианте осуществления R1 представляет собой гетероциклил (например, пиперидин-2,6-дионил). В одном варианте осуществления каждый из R2a и R2b независимо представляет собой водород. В одном варианте осуществления n составляет 1. В одном варианте осуществления R3 представляет собой C1-C6гетероалкил (например, CH2NHC(O)CH2-фенил-трет-бутил). В одном варианте осуществления R3 представляет собой C1-C6гетероалкил, замещенный 1 R6 (например, CH2NHC(O)CH2-фенил-трет-бутил). В одном варианте осуществления соединение деградации содержит 2-(4-(трет-бутил)фенил)-N-((2-(2,6-диоксопиперидин-3-ил)-1-оксоизоиндолин-5-ил)метил)ацетамид или его фармацевтически приемлемую соль. В одном варианте осуществления соединение деградации характеризуется структурой, представленной следующей формулой:
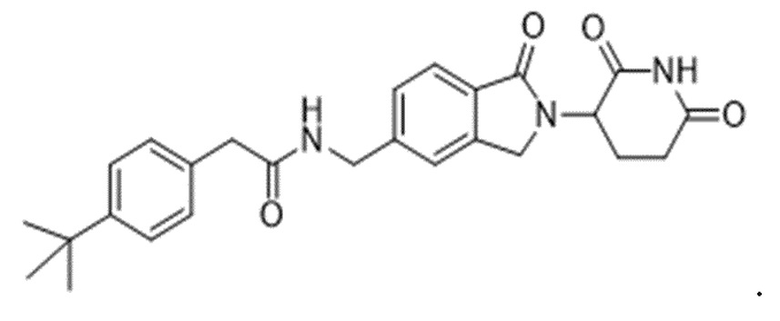
В некоторых вариантах осуществления соединение деградации представляет собой соединение формулы (I-a):
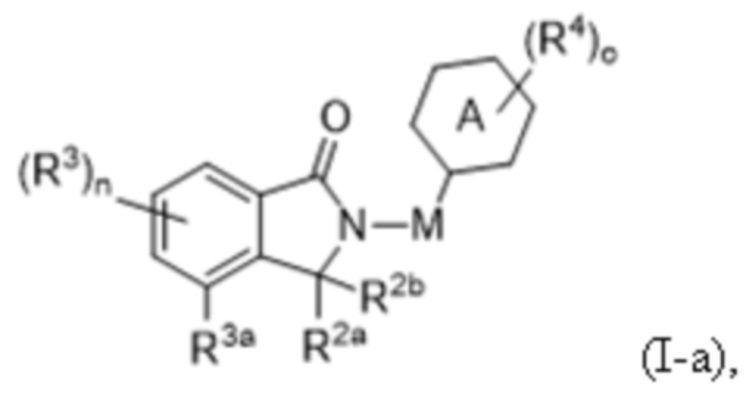
или его фармацевтически приемлемую соль, сложный эфир, гидрат или таутомер, где:
кольцо A представляет собой карбоциклил, гетероциклил, арил или гетероарил, каждый из которых независимо и необязательно замещен одним или несколькими R4;
M отсутствует или представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил или C1-C6гетероалкил, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или несколькими R4;
каждый из R2a и R2b независимо представляет собой водород или C1-C6алкил; или R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу или тиокарбонильную группу;
R3a представляет собой водород, C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD) или -N(RC)S(O)xRE, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или несколькими R6;
каждый из R3 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD) или -N (RC)S(O)xRE, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или несколькими R6;
каждый R4 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, оксо, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, S(O)xRE, -S(O)xN(RC)(RD), -N (RC)S(O)xRE, карбоциклил, гетероциклил, арил или гетероарил, где каждый алкил, алкенил, алкинил, карбоциклил, гетероциклил, арил и гетероарил независимо и необязательно замещен одним или несколькими R7;
каждый из RA, RB, RC, RD и RE независимо представляет собой водород или C1-C6алкил;
каждый R6 независимо представляет собой C1-C6алкил, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, арил или гетероарил, где каждый арил и гетероарил независимо и необязательно замещен одним или несколькими R8;
каждый R7 независимо представляет собой галоген, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
каждый R8 независимо представляет собой C1-C6алкил, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
n составляет 0, 1, 2 или 3;
o составляет 0, 1, 2, 3, 4 или 5; и
x составляет 0, 1 или 2.
В некоторых вариантах осуществления X представляет собой O.
В некоторых вариантах осуществления M представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил или C1-C6гетероалкил, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен 1-6 R4 (например, 1 R4, 2 R4, 3 R4, 4 R4, 5 R4 или 6 R4). В некоторых вариантах осуществления M отсутствует.
В некоторых вариантах осуществления кольцо A представляет собой карбоциклил, гетероциклил, арил или гетероарил, каждый из которых независимо и необязательно замещен 1-6 R4 (например, 1 R4, 2 R4, 3 R4, 4 R4, 5 R4 или 6 R4). В некоторых вариантах осуществления кольцо A представляет собой гетероциклил. В некоторых вариантах осуществления кольцо A представляет собой гетероциклил, например, 6-членный гетероциклил или 5-членный гетероциклил. В некоторых вариантах осуществления кольцо A представляет собой азот-содержащий гетероциклил. В некоторых вариантах осуществления кольцо A представляет собой пиперидинил (например, пиперидин-2,6-дионил).
В некоторых вариантах осуществления M отсутствует и кольцо A представляет собой гетероциклил (например, пиперидинил, например, пиперидин-2,6-дионил).
В некоторых вариантах осуществления каждый из R2a и R2b независимо представляет собой водород. В некоторых вариантах осуществления R2a и R2b вместе с углеродом, к которому они присоединены, образуют карбонильную группу.
В некоторых вариантах осуществления R3a представляет собой водород, C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD) или -N(RC)S(O)xRE, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен 1-12 R6 (например, 1 R6, 2 R6, 3 R6, 4 R6, 5 R6, 6 R6, 7 R6, 8 R6, 9 R6, 10 R6, 11 R6 или 12 R6). В некоторых вариантах осуществления R3a представляет собой водород, -N(RC)(RD) или -N(RC)C(O)RA. В некоторых вариантах осуществления R3a представляет собой водород. В некоторых вариантах осуществления R3a представляет собой -N(RC)(RD) (например, -NH2). В некоторых вариантах осуществления R3a представляет собой -N(RC)C(O)RA (например, NHC(O)CH3).
В некоторых вариантах осуществления каждый R3 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD) или -N (RC)S(O)xRE, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен 1-12 R6 (например, 1 R6, 2 R6, 3 R6, 4 R6, 5 R6, 6 R6, 7 R6, 8 R6, 9 R6, 10 R6, 11 R6 или 12 R6). В некоторых вариантах осуществления R3 представляет собой C1-C6гетероалкил (например, CH2NHC(O)CH2-фенил-трет-бутил).
В некоторых вариантах осуществления каждый R4 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, оксо, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, S(O)xRE, -S(O)xN(RC)(RD), -N (RC)S(O)xRE, карбоциклил, гетероциклил, арил или гетероарил, где каждый алкил, алкенил, алкинил, карбоциклил, гетероциклил, арил и гетероарил независимо и необязательно замещен 1-12 R7 (например, 1 R7, 2 R7, 3 R7, 4 R7, 5 R7, 6 R7, 7 R7, 8 R7, 9 R7, 10 R7, 11 R7 или 12 R7).
В некоторых вариантах осуществления каждый R6 независимо представляет собой C1-C6алкил, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, арил или гетероарил, где каждый арил и гетероарил независимо и необязательно замещен 1-6 R8 (например, 1 R8, 2 R8, 3 R8, 4 R8, 5 R8 или 6 R8).
В некоторых вариантах осуществления n составляет 0 или 1. В некоторых вариантах осуществления n составляет 0. В некоторых вариантах осуществления n составляет 1.
В некоторых вариантах осуществления соединение деградации представляет собой соединение формулы (III):
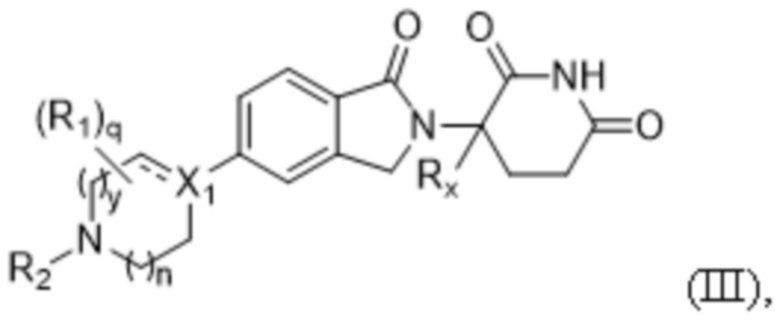
или его фармацевтически приемлемую соль, сложный эфир, гидрат или таутомер, где:
X1 представляет собой CR3;
 необязательно представляет собой двойную связь, если X1 представляет собой CR3 и R3 отсутствует;
необязательно представляет собой двойную связь, если X1 представляет собой CR3 и R3 отсутствует;
каждый R1 независимо представляет собой C1-C6алкил, C1-C6галогеналкил, C1-C6гидроксиалкил или галоген, или
два R1 вместе с атомами углерода, к которым они присоединены, образуют 5- или 6-членное гетероциклильное кольцо, или
два R1, когда они находятся при смежных атомах, вместе с атомами, к которым они присоединены, образуют C6-C10арил или 5- или 6-членное гетероарильное кольцо, содержащее 1-3 гетероатома, выбранные из O, N и S;
R2 представляет собой водород, C1-C6алкил, -C(O)C1-C6алкил, -C(O)(CH2)0-3-C6-C10арил, -C(O)O(CH2)0-3-C6-C10арил, C6-C10арил или 5- или 6-членный гетероарил, содержащий 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклил или 5-7-гетероциклил, содержащий 1-3 гетероатома, выбранные из O, N и S, где алкил необязательно замещен одним или несколькими R4; и арил, гетероарил, карбоциклил и гетероциклил необязательно замещены одним или несколькими R5, или
R1 и R2, когда они находятся при смежных атомах, вместе с атомами, к которым они присоединены, образуют 5- или 6-членное гетероциклильное кольцо;
R3 представляет собой водород, или R3 отсутствует, если  представляет собой двойную связь;
представляет собой двойную связь;
каждый R4 независимо выбран из -C(O)OR6, -C(O)NR6R6', -NR6C(O)R6', галогена, -OH, -NH2, циано, C6-C10арила, 5- или 6-членного гетероарила, содержащего 1-4 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклильного кольца, содержащего 1-3 гетероатома, выбранные из O, N и S, где арил, гетероарил, карбоциклил и гетероциклил необязательно замещены одним или несколькими R7;
каждый R5 независимо выбран из C1-C6алкила, C2-C6алкенила, C2-C6алкинила, C1-C6алкокси, C1-C6галогеналкила, C1-C6галогеналкокси, C1-C6гидроксиалкила, галогена, -OH, -NH2, циано, C3-C7карбоциклила, 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, C6-C10арила и 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, или
два R5, когда они находятся при смежных атомах, вместе с атомами, к которым они присоединены, образуют C6-C10арил или 5- или 6-членный гетероарил, содержащий 1-3 гетероатома, выбранные из O, N и S, необязательно замещенные одним или несколькими R10, или
два R5, когда они находятся при смежных атомах, вместе с атомами, к которым они присоединены, образуют C5-C7карбоциклил или 5-7-членный гетероциклил, содержащий 1-3 гетероатома, выбранные из O, N и S, необязательно замещенные одним или несколькими R10;
каждый R6 и R6' независимо представляет собой водород, C1-C6алкил или C6-C10арил;
каждый R7 независимо выбран из C1-C6алкила, C2-C6алкенила, C2-C6алкинила, C1-C6алкокси, C1-C6галогеналкила, C1-C6галогеналкокси, -C(O)R8, -(CH2)0-3C(O)OR8, -C(O)NR8R9, -NR8C(O)R9, -NR8C(O)OR9, -S(O)pNR8R9, -S(O)pR12, (C1-C6)гидроксиалкила, галогена, -OH, -O(CH2)1-3CN, -NH2, циано, -O(CH2)0-3-C6-C10арила, адамантила, -O(CH2)0-3-5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C6-C10арила, моноциклического или бициклического 5-10-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C7 карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где алкил необязательно замещен одним или несколькими R11, и арил, гетероарил и гетероциклил необязательно замещены одним или несколькими заместителями, каждый из которых независимо выбран из галогена, C1-C6алкила, C1-C6галогеналкила и C1-C6алкокси, или
два R7 вместе с атомом углерода, к которому они присоединены, образуют =(O), или
два R7, когда они находятся при смежных атомах, вместе с атомами, к которым они присоединены, образуют C6-C10арил или 5- или 6-членный гетероарил, содержащий 1-3 гетероатома, выбранные из O, N и S, необязательно замещенные одним или несколькими R10, или
два R7 вместе с атомами, к которым они присоединены, образуют C5-C7карбоциклил или 5-7-членный гетероциклил, содержащий 1-3 гетероатома, выбранные из O, N и S, необязательно замещенные одним или несколькими R10;
каждый R8 и R9 независимо представляет собой водород или C1-C6алкил;
каждый R10 независимо выбран из C1-C6алкила, C1-C6алкокси, C1-C6галогеналкила, C1-C6галогеналкокси, C1-C6гидроксиалкила, галогена, -OH, -NH2 и циано, или
два R10 вместе с атомом углерода, к которому они присоединены, образуют =(O);
каждый R11 независимо выбран из циано, C1-C6алкокси, C6-C10арила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где каждый арил и гетероциклил необязательно замещен одним или несколькими заместителями, каждый из которых независимо выбран из C1-C6алкила, C1-C6алкокси, C1-C6галогеналкила, C1-C6галогеналкокси, C1-C6гидроксиалкила, галогена, -OH, -NH2 и циано;
R12 представляет собой C1-C6алкил, C1-C6галогеналкил, C6-C10арил или 5-7-членный гетероциклил, содержащий 1-3 гетероатома, выбранные из O, N и S;
Rx представляет собой водород или дейтерий;
p составляет 0, 1 или 2;
n составляет 0, 1 или 2;
y составляет 1 или 2, где n+y≤3; и
q составляет 0, 1, 2, 3 или 4.
В некоторых вариантах осуществления соединение деградации формулы (III) представляет собой соединение формулы (III-a):

или его фармацевтически приемлемую соль, сложный эфир, гидрат или таутомер, где:
X1 представляет собой CR3;
 необязательно представляет собой двойную связь, если X1 представляет собой CR3 и R3 отсутствует;
необязательно представляет собой двойную связь, если X1 представляет собой CR3 и R3 отсутствует;
каждый R1 независимо представляет собой C1-C6алкил, C1-C6галогеналкил, C1-C6гидроксиалкил или галоген;
R2 представляет собой водород, C1-C6алкил, C6-C10арил или 5- или 6-членный гетероарил, содержащий 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклил или 5-7-членный гетероциклил, содержащий 1-3 гетероатома, выбранные из O, N и S, где алкил необязательно замещен одним или несколькими R4; и арил, гетероарил, карбоциклил и гетероциклил необязательно замещены одним или несколькими R5;
R3 представляет собой водород, или R3 отсутствует, если  представляет собой двойную связь;
представляет собой двойную связь;
каждый R4 независимо выбран из -C(O)OR6, -C(O)NR6R6', -NR6C(O)R6', C6-C10арила, 5- или 6-членного гетероарила, содержащего 1-4 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклильного кольца, содержащего 1-3 гетероатома, выбранные из O, N и S, где арил, гетероарил, карбоциклил и гетероциклил необязательно замещены одним или несколькими R7;
каждый R5 независимо выбран из C1-C6алкила, C2-C6алкенила, C2-C6алкинила, C1-C6алкокси, C1-C6галогеналкила, C1-C6галогеналкокси, C1-C6гидроксиалкила, галогена, -OH, -NH2, циано, C3-C7карбоциклила, 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, C6-C10арила и 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, или
два R5, когда они находятся при смежных атомах, вместе с атомами, к которым они присоединены, образуют C6-C10арил или 5- или 6-членный гетероарил, содержащий 1-3 гетероатома, выбранные из O, N и S, необязательно замещенные одним или несколькими R10, или
два R5, когда они находятся при смежных атомах, вместе с атомами, к которым они присоединены, образуют C5-C7карбоциклил или 5-7-членный гетероциклил, содержащий 1-3 гетероатома, выбранные из O, N и S, необязательно замещенные одним или несколькими R10;
каждый R6 и R6' независимо представляет собой водород или C1-C6алкил;
каждый R7 независимо выбран из C1-C6алкила, C2-C6алкенила, C2-C6алкинила, C1-C6алкокси, C1-C6галогеналкила, C1-C6галогеналкокси, -C(O)R8, -C(O)NR8R9, -NR8C(O)R9, -NR8C(O)OR9, (C1-C6)гидроксиалкил, галогена, -OH, -NH2, циано, C6-C10арила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C7карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, или
два R7, когда они находятся при смежных атомах, вместе с атомами, к которым они присоединены, образуют C6-C10арил или 5- или 6-членный гетероарил, содержащий 1-3 гетероатома, выбранные из O, N и S, необязательно замещенные одним или несколькими R10, или
два R7 вместе с атомами, к которым они присоединены, образуют C5-C7карбоциклил или 5-7-членный гетероциклил, содержащий 1-3 гетероатома, выбранные из O, N и S, необязательно замещенные одним или несколькими R10;
каждый R8 и R9 независимо представляет собой водород или C1-C6алкил;
каждый R10 независимо выбран из C1-C6алкила, C1-C6алкокси, C1-C6галогеналкила, C1-C6галогеналкокси, C1-C6гидроксиалкила, галогена, -OH, -NH2 и циано;
Rx представляет собой водород или дейтерий;
n составляет 1 или 2; и
q составляет 0, 1, 2, 3 или 4.
В одном варианте осуществления соединение формулы (III) представляет собой соединение формулы (III-b):
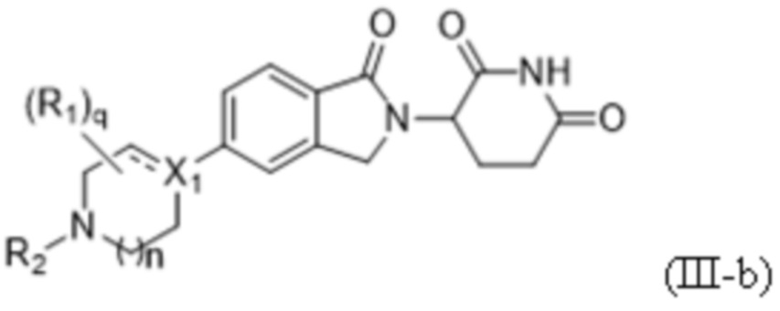 , или его фармацевтически приемлемую соль, гидрат, сольват, пролекарство, стереоизомер и таутомер, где X1, R1, R2, n, q и их подпеременные определены, как описано для формулы (III).
, или его фармацевтически приемлемую соль, гидрат, сольват, пролекарство, стереоизомер и таутомер, где X1, R1, R2, n, q и их подпеременные определены, как описано для формулы (III).
В одном варианте осуществления соединение формулы (III) представляет собой соединение формулы (III-c):
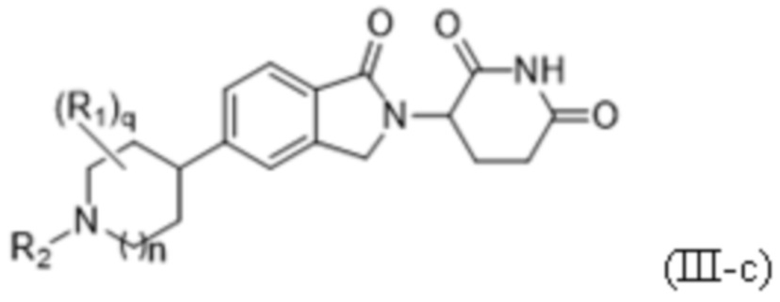 , или его фармацевтически приемлемую соль, гидрат, сольват, пролекарство, стереоизомер и таутомер, где R1, R2, n, q и их подпеременные определены, как описано для формулы (III).
, или его фармацевтически приемлемую соль, гидрат, сольват, пролекарство, стереоизомер и таутомер, где R1, R2, n, q и их подпеременные определены, как описано для формулы (III).
В одном варианте осуществления соединение формулы (III) представляет собой соединение формулы (III-d):
 , или его фармацевтически приемлемую соль, гидрат, сольват, пролекарство, стереоизомер и таутомер, где R1, R2, n, q и их подпеременные определены, как описано для формулы (III).
, или его фармацевтически приемлемую соль, гидрат, сольват, пролекарство, стереоизомер и таутомер, где R1, R2, n, q и их подпеременные определены, как описано для формулы (III).
В одном варианте осуществления соединение формулы (III) представляет собой соединение формулы (III-e):
 , или его фармацевтически приемлемую соль, гидрат, сольват, пролекарство, стереоизомер и таутомер, где R1, R2, n, q и их подпеременные определены, как описано для формулы (III).
, или его фармацевтически приемлемую соль, гидрат, сольват, пролекарство, стереоизомер и таутомер, где R1, R2, n, q и их подпеременные определены, как описано для формулы (III).
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, и n составляет 1. В другом варианте осуществления X1 представляет собой CH, n составляет 1, и q составляет 0.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, и q составляет 0 или 1. В другом варианте осуществления X1 представляет собой CH, n составляет 1, q составляет 0 или 1, и R1 представляет собой C1-C6алкил. В другом варианте осуществления X1 представляет собой CH, n составляет 1, q составляет 0 или 1, R1 представляет собой C1-C6алкил, и R2 представляет собой C1-C6алкил, необязательно замещенный одним-тремя R4. В другом варианте осуществления X1 представляет собой CH, n составляет 1, q составляет 0 или 1, R1 представляет собой C1-C6алкил, и R2 представляет собой C1-C6алкил, замещенный одним-тремя R4.
В другом варианте осуществления X1 представляет собой CH, n составляет 1, q составляет 0, и R2 представляет собой C1-C6алкил, необязательно замещенный одним-тремя R4. В другом варианте осуществления X1 представляет собой CH, n составляет 1, q составляет 0, и R2 представляет собой C1-C6алкил, замещенный одним-тремя R4.
В некоторых вариантах осуществления вышеприведенных формул X1 представляет собой CH, n составляет 1, q составляет 0 или 1, R1 представляет собой C1-C6алкил, R2 представляет собой C1-C6алкил, необязательно замещенный одним-тремя R4, и каждый R4 независимо выбран из -C(O)OR6, C6-C10арила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где арил, гетероарил, карбоциклил и гетероциклил необязательно замещен одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, q составляет 0 или 1, R1 представляет собой C1-C6алкил, R2 представляет собой C1-C6алкил, замещенный одним-тремя R4, и каждый R4 независимо выбран из -C(O)OR6, C6-C10арила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где арильная, гетероарильная, карбоциклильная и гетероциклильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, q составляет 0 или 1, R1 представляет собой C1-C6алкил, R2 представляет собой C1-C6алкил, необязательно замещенный одним-тремя R4, и каждый R4 независимо выбран из C6-C10арила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где арильная, гетероарильная, карбоциклильная и гетероциклильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, q составляет 0 или 1, R1 представляет собой C1-C6алкил, R2 представляет собой C1-C6алкил, замещенный одним-тремя R4, и каждый R4 независимо выбран из C6-C10арила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где арильная, гетероарильная, карбоциклильная и гетероциклильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, q составляет 0, и R2 представляет собой C6-C10арил, C3-C8карбоциклил или 5-7-членный гетероциклил, содержащий 1-3 гетероатома, выбранные из O, N и S, где арил, карбоциклил и гетероциклил необязательно замещены одним-тремя R5. В еще одном варианте осуществления X1 представляет собой CH, n составляет 1, q составляет 0, и R2 представляет собой C6-C10арил, C3-C8карбоциклил или 5-7-членный гетероциклил, содержащий 1-3 гетероатома, выбранные из O, N и S.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, q составляет 0, и R2 представляет собой C6-C10арил, необязательно замещенный одним-тремя R5. В другом варианте осуществления X1 представляет собой CH, n составляет 1, q составляет 0, и R2 представляет собой 5- или 6-членный гетероарил, содержащий 1-3 гетероатома, выбранные из O, N и S, необязательно замещенный одним-тремя R5. В еще одном варианте осуществления X1 представляет собой CH, n составляет 1, q составляет 0, и R2 представляет собой C3-C8карбоциклил, необязательно замещенный одним-тремя R5. В другом варианте осуществления X1 представляет собой CH, n составляет 1, q составляет 0, и R2 представляет собой 5-7-членный гетероциклил, содержащий 1-3 гетероатома, выбранные из O, N и S, необязательно замещенный одним-тремя R5.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, q составляет 0 или 1, R1 представляет собой C1-C6алкил, и R2 представляет собой C6-C10арил, C3-C8карбоциклил или 5-7-членный гетероциклил, содержащий 1-3 гетероатома, выбранные из O, N и S, где арил, карбоциклил и гетероциклил необязательно замещены одним-тремя R5. В еще одном варианте осуществления X1 представляет собой CH, n составляет 1, q составляет 0 или 1, R1 представляет собой C1-C6алкил, и R2 представляет собой C6-C10арил, C3-C8карбоциклил или 5-7-членный гетероциклил, содержащий 1-3 гетероатома, выбранные из O, N и S.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, q составляет 0 или 1, R1 представляет собой C1-C6алкил, и R2 представляет собой C6-C10арил, необязательно замещенный одним-тремя R5. В другом варианте осуществления X1 представляет собой CH, n составляет 1, q составляет 0, и R2 представляет собой 5- или 6-членный гетероарил, содержащий 1-3 гетероатома, выбранные из O, N и S, необязательно замещенный одним-тремя R5. В еще одном варианте осуществления X1 представляет собой CH, n составляет 1, q составляет 0 или 1, R1 представляет собой C1-C6алкил, и R2 представляет собой C3-C8карбоциклил, необязательно замещенный одним-тремя R5. В другом варианте осуществления X1 представляет собой CH, n составляет 1, q составляет 0 или 1, R1 представляет собой C1-C6алкил, и R2 представляет собой 5-7-членный гетероциклил, содержащий 1-3 гетероатома, выбранные из O, N и S, необязательно замещенный одним-тремя R5.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, q составляет 0, и R2 представляет собой C1-C6алкил, необязательно замещенный одним-тремя R4. В другом варианте осуществления X1 представляет собой CH, n составляет 1, q составляет 0, и R2 представляет собой C1-C6алкил, замещенный одним-тремя R4.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, необязательно замещенный одним-тремя R4, и каждый R4 независимо выбран из -C(O)OR6, C6-C10арила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где арильная, гетероарильная, карбоциклильная и гетероциклильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, замещенный одним-тремя R4, и каждый R4 независимо выбран из -C(O)OR6, C6-C10арила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где арильная, гетероарильная, карбоциклильная и гетероциклильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, необязательно замещенный одним-тремя R4, и каждый R4 независимо выбран из галогена, -OH, C6-C10арила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где арильная, гетероарильная, карбоциклильная и гетероциклильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, замещенный одним-тремя R4, и каждый R4 независимо выбран из галогена, -OH, C6-C10арила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где арильная, гетероарильная, карбоциклильная и гетероциклильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления вышеприведенных формул X1 представляет собой CH, n составляет 1, n1 составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, необязательно замещенный одним-тремя R4, и каждый R4 независимо выбран из галогена, -OH, C6-C10арила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где арильная, гетероарильная, карбоциклильная и гетероциклильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, n1 составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, замещенный одним-тремя R4, и каждый R4 независимо выбран из галогена, -OH, C6-C10арила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где арильная, гетероарильная, карбоциклильная и гетероциклильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, необязательно замещенный одним-тремя R4, и каждый R4 независимо выбран из C6-C10арила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где арильная, гетероарильная, карбоциклильная и гетероциклильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, замещенный одним-тремя R4, и каждый R4 независимо выбран из C6-C10арила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где арильная, гетероарильная, карбоциклильная и гетероциклильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, необязательно замещенный одним-тремя R4, и каждый R4 независимо выбран из галогена, -OH, фенила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где арильная, гетероарильная, карбоциклильная и гетероциклильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, замещенный одним-тремя R4, и каждый R4 независимо выбран из галогена, -OH, фенила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где арильная, гетероарильная, карбоциклильная и гетероциклильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, n1 составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, необязательно замещенный одним-тремя R4, и каждый R4 независимо выбран из галогена, -OH, фенила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где арильная, гетероарильная, карбоциклильная и гетероциклильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, n1 составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, замещенный одним-тремя R4, и каждый R4 независимо выбран из галогена, -OH, фенила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где фенильная, гетероарильная, карбоциклильная и гетероциклильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, необязательно замещенный одним-тремя R4, и каждый R4 независимо выбран из фенила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где фенильная, гетероарильная, карбоциклильная и гетероциклильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, замещенный одним-тремя R4, и каждый R4 независимо выбран из фенила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где фенильная, гетероарильная, карбоциклильная и гетероциклильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, n1 составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, необязательно замещенный одним-тремя R4, и каждый R4 независимо выбран из фенила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где фенильная, гетероарильная, карбоциклильная и гетероциклильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, n1 составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, замещенный одним-тремя R4, и каждый R4 независимо выбран из фенила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где фенильная, гетероарильная, карбоциклильная и гетероциклильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, необязательно замещенный одним-тремя R4, и каждый R4 независимо выбран из фенила и 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, где фенильная и гетероарильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, замещенный одним-тремя R4, и каждый R4 независимо выбран из фенила и 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где фенильная и гетероарильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, n1 составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, необязательно замещенный одним-тремя R4, и каждый R4 независимо выбран из фенила и 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, где фенильная и гетероарильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, n1 составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, замещенный одним-тремя R4, и каждый R4 независимо выбран из фенила и 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где фенильная и гетероарильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, необязательно замещенный одним-тремя R4, и каждый R4 представляет собой фенил, необязательно замещенный одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, замещенный одним-тремя R4, и каждый R4 представляет собой фенил, необязательно замещенный одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 1, n1 составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, необязательно замещенный одним-тремя R4, и каждый R4 представляет собой фенил, необязательно замещенный одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 м CH, n составляет 1, n1 составляет 1, q составляет 0, R2 представляет собой C1-C6алкил, замещенный одним-тремя R4, и каждый R4 представляет собой фенил, необязательно замещенный одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, и n составляет 2. В другом варианте осуществления X1 представляет собой CH, n составляет 2, и q составляет 0. В еще одном варианте осуществления X1 представляет собой CH, n составляет 2, и q составляет 0 или 1. В другом варианте осуществления X1 представляет собой CH, n составляет 2, q составляет 0 или 1, и R1 представляет собой C1-C6алкил.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 2, q составляет 0 или 1, R1 представляет собой C1-C6алкил, и R2 представляет собой C1-C6алкил, необязательно замещенный одним-тремя R4. В другом варианте осуществления X1 представляет собой CH, n составляет 2, q составляет 0 или 1, R1 представляет собой C1-C6алкил, и R2 представляет собой C1-C6алкил, замещенный одним-тремя R4.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 2, q составляет 0, и R2 представляет собой C1-C6алкил, необязательно замещенный одним-тремя R4. В другом варианте осуществления X1 представляет собой CH, n составляет 2, q составляет 0, и R2 представляет собой C1-C6алкил, замещенный одним-тремя R4.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 2, q составляет 0 или 1, R1 представляет собой C1-C6алкил, R2 представляет собой C1-C6алкил, необязательно замещенный одним-тремя R4, и каждый R4 независимо выбран из -C(O)OR6, C6-C10арила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где арильная, гетероарильная, карбоциклильная и гетероциклильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 2, q составляет 0 или 1, R1 представляет собой C1-C6алкил, R2 представляет собой C1-C6алкил, замещенный одним-тремя R4, и каждый R4 независимо выбран из -C(O)OR6, C6-C10арила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где арильная, гетероарильная, карбоциклильная и гетероциклильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 2, q составляет 0 или 1, R1 представляет собой C1-C6алкил, R2 представляет собой C1-C6алкил, необязательно замещенный одним-тремя R4, и каждый R4 независимо выбран из C6-C10арила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где арильная, гетероарильная, карбоциклильная и гетероциклильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 2, q составляет 0 или 1, R1 представляет собой C1-C6алкил, R2 представляет собой C1-C6алкил, замещенный одним-тремя R4, и каждый R4 независимо выбран из C6-C10арила, 5- или 6-членного гетероарила, содержащего 1-3 гетероатома, выбранные из O, N и S, C3-C8карбоциклила и 5-7-членного гетероциклила, содержащего 1-3 гетероатома, выбранные из O, N и S, где арильная, гетероарильная, карбоциклильная и гетероциклильная группы необязательно замещены одним-тремя R7.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 2, q составляет 0, и R2 представляет собой C6-C10арил, C3-C8карбоциклил или 5-7-членный гетероциклил, содержащий 1-3 гетероатома, выбранные из O, N и S, где арил, карбоциклил и гетероциклил необязательно замещены одним-тремя R5. В еще одном варианте осуществления X1 представляет собой CH, n составляет 2, q составляет 0, и R2 представляет собой C6-C10арил, C3-C8карбоциклил или 5-7-членный гетероциклил, содержащий 1-3 гетероатома, выбранные из O, N и S.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 2, q составляет 0, и R2 представляет собой C6-C10арил, необязательно замещенный одним-тремя R5. В другом варианте осуществления X1 представляет собой CH, n составляет 2, q составляет 0, и R2 представляет собой 5- или 6-членный гетероарил, содержащий 1-3 гетероатома, выбранные из O, N и S, необязательно замещенный одним-тремя R5. В еще одном варианте осуществления X1 представляет собой CH, n составляет 2, q составляет 0, и R2 представляет собой C3-C8карбоциклил, необязательно замещенный одним-тремя R5. В другом варианте осуществления X1 представляет собой CH, n составляет 2, q составляет 0, и R2 представляет собой 5-7-членный гетероциклил, содержащий 1-3 гетероатома, выбранные из O, N и S, необязательно замещенный одним-тремя R5.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 2, q составляет 0 или 1, R1 представляет собой C1-C6алкил, и R2 представляет собой C6-C10арил, C3-C8карбоциклил или 5-7-членный гетероциклил, содержащий 1-3 гетероатома, выбранные из O, N и S, где арил, карбоциклил и гетероциклил необязательно замещены одним-тремя R5. В еще одном варианте осуществления X1 представляет собой CH, n составляет 2, q составляет 0 или 1, R1 представляет собой C1-C6алкил, и R2 представляет собой C6-C10арил, C3-C8карбоциклил или 5-7-членный гетероциклил, содержащий 1-3 гетероатома, выбранные из O, N и S.
В некоторых вариантах осуществления формулы (III) X1 представляет собой CH, n составляет 2, q составляет 0 или 1, R1 представляет собой C1-C6алкил, и R2 представляет собой C6-C10арил, необязательно замещенный одним-тремя R5. В другом варианте осуществления X1 представляет собой CH, n составляет 2, q составляет 0, и R2 представляет собой 5- или 6-членный гетероарил, содержащий 1-3 гетероатома, выбранные из O, N и S, необязательно замещенный одним-тремя R5. В еще одном варианте осуществления X1 представляет собой CH, n составляет 2, q составляет 0 или 1, R1 представляет собой C1-C6алкил, и R2 представляет собой C3-C8карбоциклил, необязательно замещенный одним-тремя R5. В другом варианте осуществления X1 представляет собой CH, n составляет 2, q составляет 0 или 1, R1 представляет собой C1-C6алкил, и R2 представляет собой 5-7-членный гетероциклил, содержащий 1-3 гетероатома, выбранные из O, N и S, необязательно замещенный одним-тремя R5.
В некоторых вариантах осуществления формулы (III)  представляет собой
представляет собой
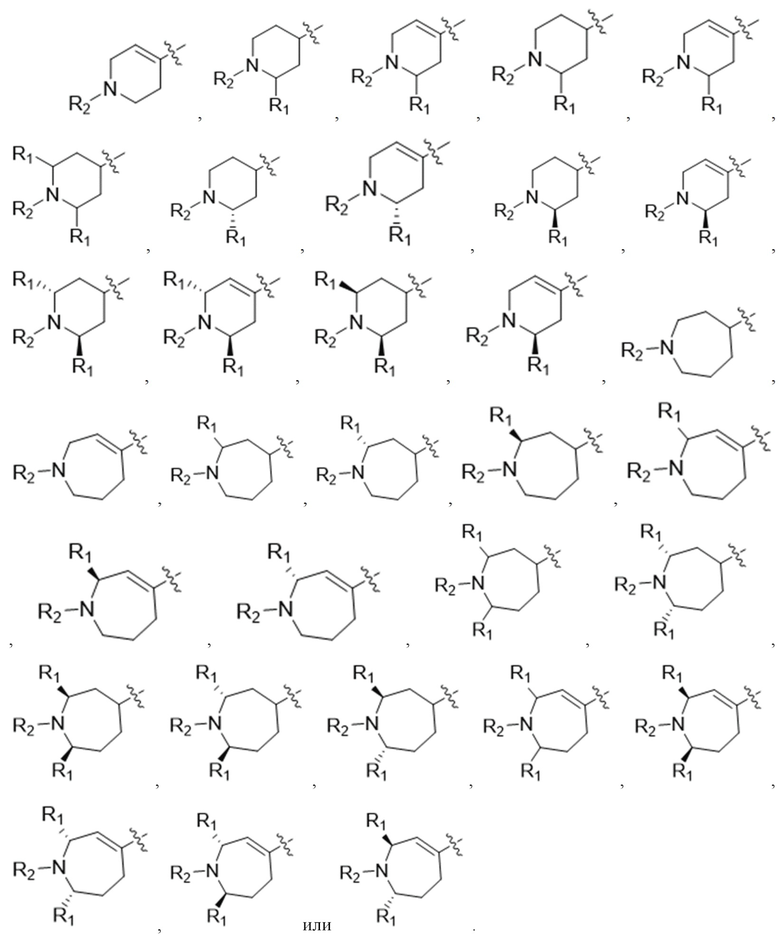
В некоторых вариантах осуществления формулы (III)  представляет собой
представляет собой
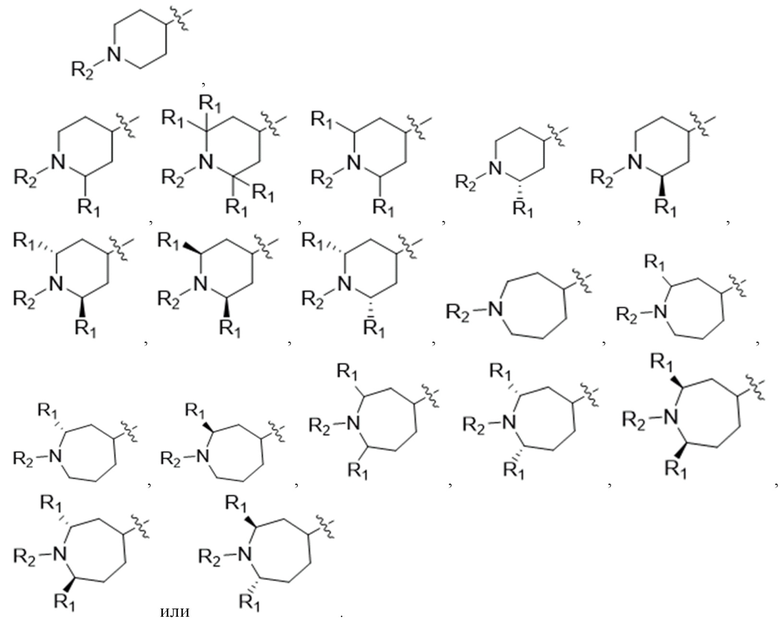
В некоторых вариантах осуществления формулы (III)  представляет собой
представляет собой

Соединение деградации может содержать один или несколько хиральных центров или существовать в виде одного или нескольких стереоизомеров. В некоторых вариантах осуществления соединение деградации содержит один хиральный центр и представляет собой смесь стереоизомеров, например, R-стереоизомера и S-стереоизомера. В некоторых вариантах осуществления смесь содержит R-стереоизомеры и S стереоизомеры при определенном соотношении, например, соотношении R-стереоизомеров и S-стереоизомеров приблизительно 1:1 (т. е. рацемическая смесь). В некоторых вариантах осуществления смесь содержит R-стереоизомеры и S-стереоизомеры при соотношении приблизительно 51:49, приблизительно 52: 48, приблизительно 53:47, приблизительно 54:46, приблизительно 55:45, приблизительно 60:40, приблизительно 65:35, приблизительно 70:30, приблизительно 75:25, приблизительно 80:20, приблизительно 85:15, приблизительно 90:10, приблизительно 95:5 или приблизительно 99:1. В некоторых вариантах осуществления смесь содержит S-стереоизомеры и R-стереоизомеры при соотношении приблизительно 51:49, приблизительно 52: 48, приблизительно 53:47, приблизительно 54:46, приблизительно 55:45, приблизительно 60:40, приблизительно 65:35, приблизительно 70:30, приблизительно 75:25, приблизительно 80:20, приблизительно 85:15, приблизительно 90:10, приблизительно 95:5 или приблизительно 99:1. В некоторых вариантах осуществления соединение деградации представляет собой один стереоизомер формулы (I) или формулы (I-a), например, один R-стереоизомер или один S-стереоизомер.
В некоторых вариантах осуществления соединение деградации (например, соединение формул (I), (I-a), (III), (III-a), (III-b), (III-c), (III-d) или (III-e)) не присоединено к линкеру или группе присоединения. В некоторых вариантах осуществления соединение деградации (например, соединение формул (I), (I-a), (III), (III-a), (III-b), (III-c), (III-d) или (III-e)) не содержит другой фрагмент, например, лиганд, нацеливающее средство или фрагмент, способный к димеризации.
В одном варианте осуществления соединение деградации представляет собой соединение формулы (I) или его фармацевтически приемлемую соль. В одном варианте осуществления соединение деградации представляет собой соединение формулы (I-a) или его фармацевтически приемлемую соль. В одном варианте осуществления соединение деградации представляет собой соединение формулы (III) или его фармацевтически приемлемую соль. В одном варианте осуществления соединение деградации представляет собой соединение формулы (III-a) или его фармацевтически приемлемую соль. В одном варианте осуществления соединение деградации представляет собой соединение формулы (III-b) или его фармацевтически приемлемую соль. В одном варианте осуществления соединение деградации представляет собой соединение формулы (III-c) или его фармацевтически приемлемую соль. В одном варианте осуществления соединение деградации представляет собой соединение формулы (III-d) или его фармацевтически приемлемую соль. В одном варианте осуществления соединение деградации представляет собой соединение формулы (III-e) или его фармацевтически приемлемую соль.
Иллюстративные соединения деградации по настоящему изобретению (например, соединение формулы (III), (III-a), (III-b), (III-c), (III-d) или (III-e) или его фармацевтически приемлемая соль) включают соединения из таблицы 29.
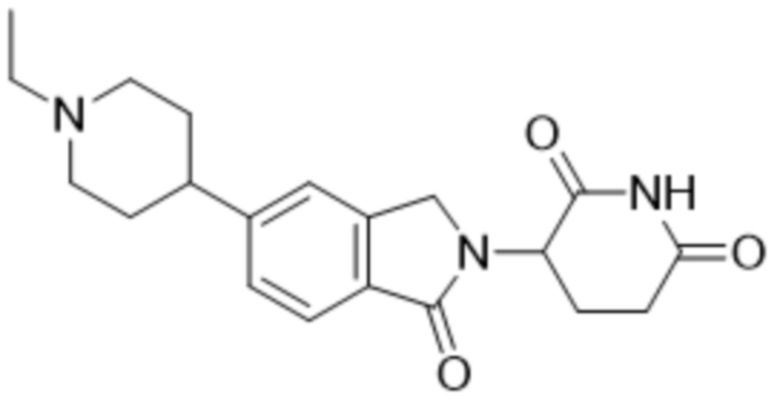

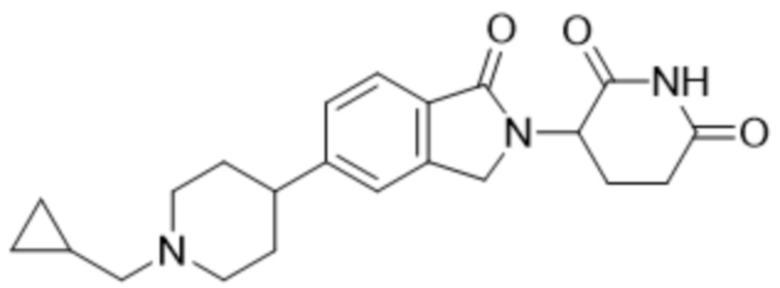
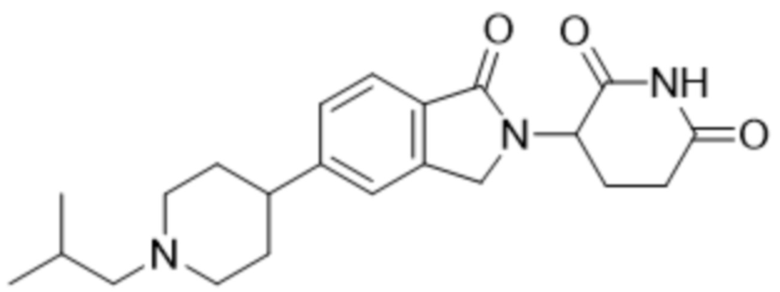
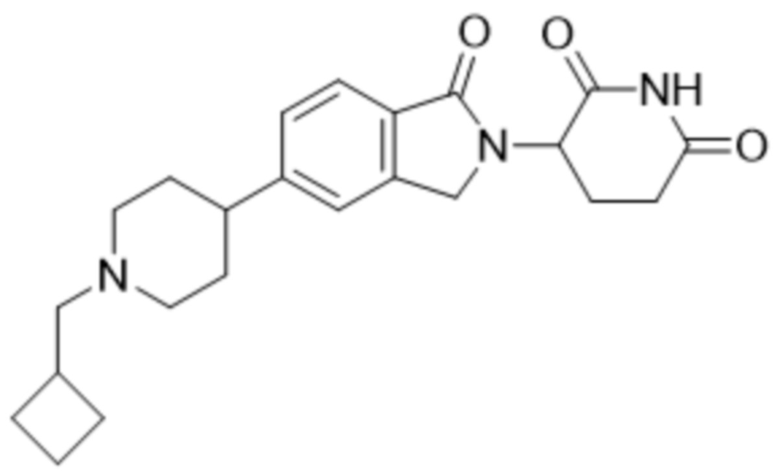
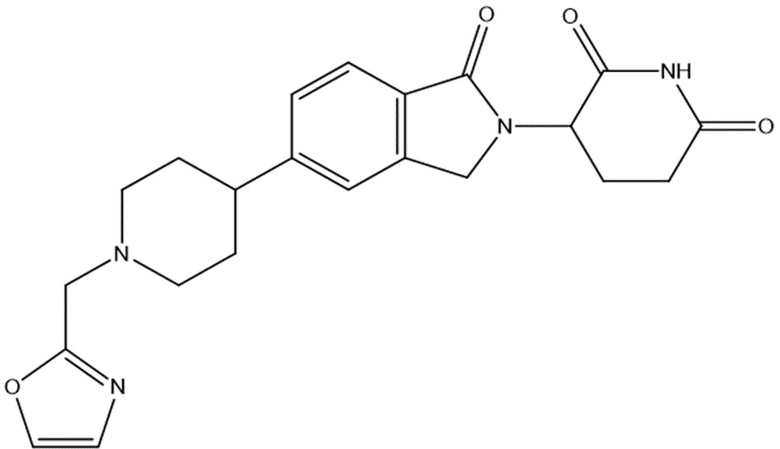
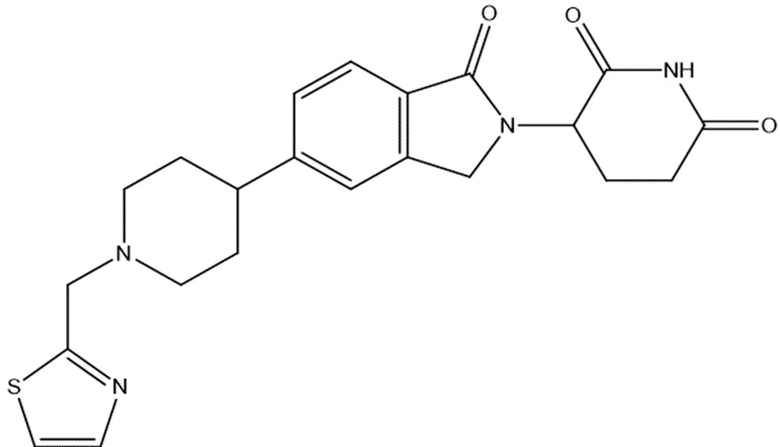
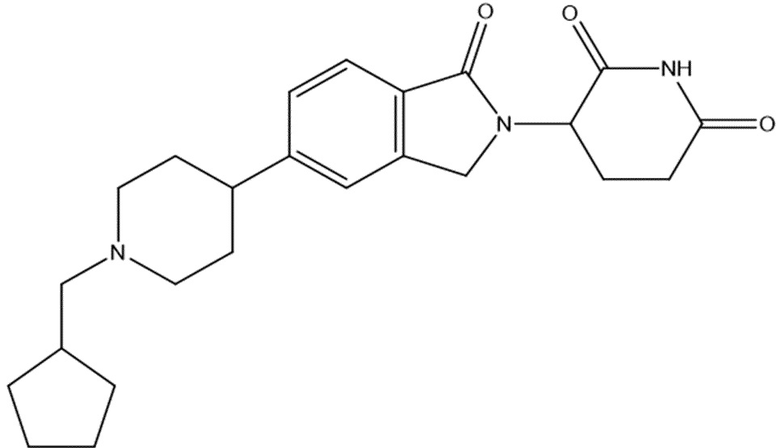

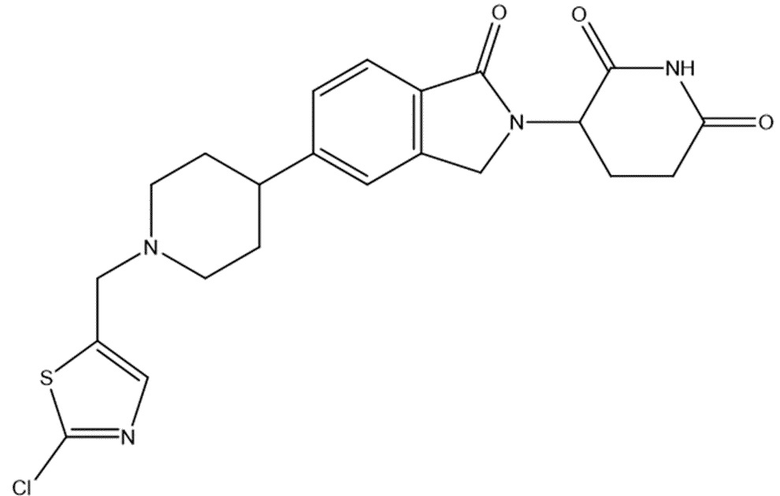
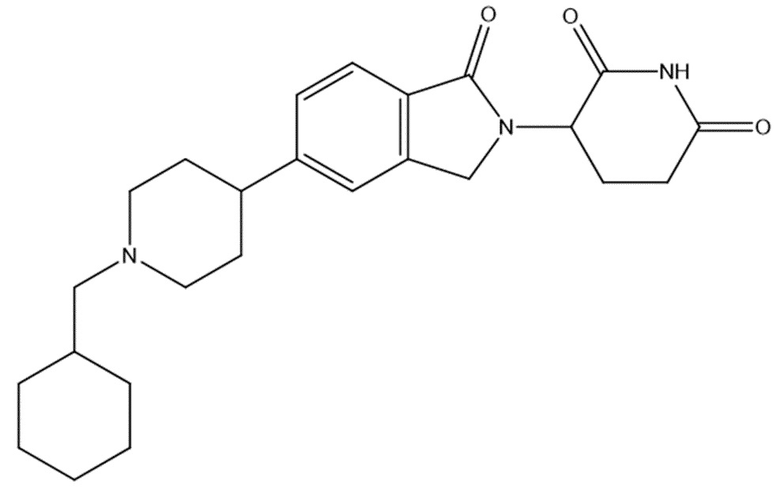

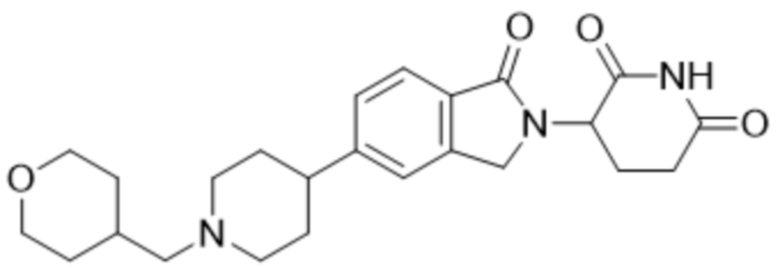
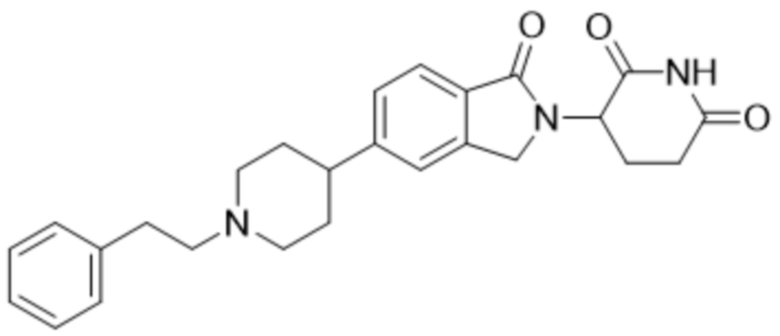



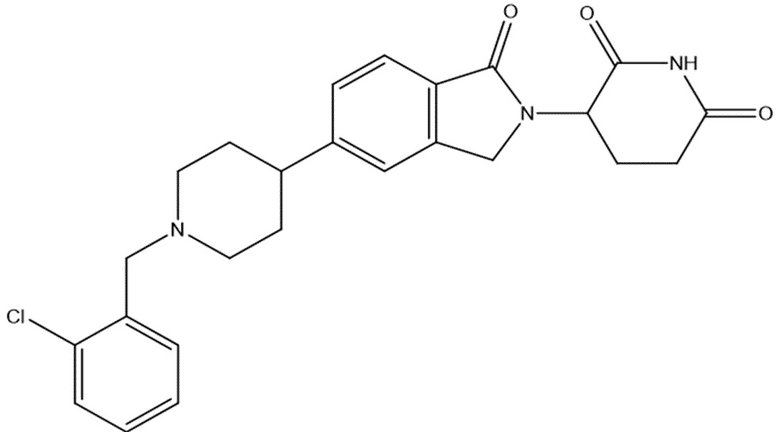
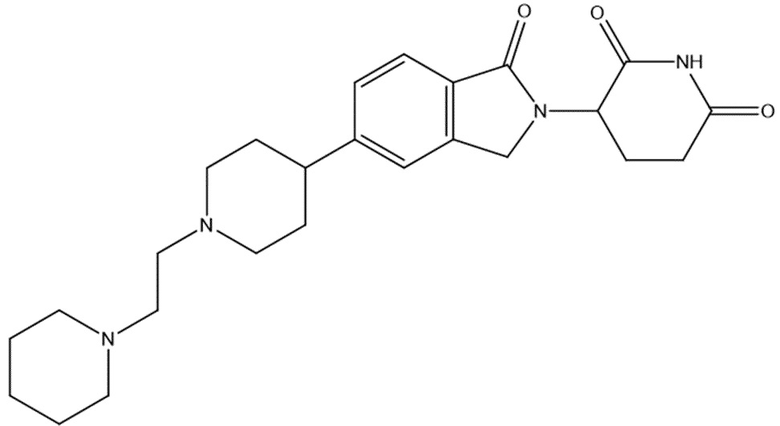
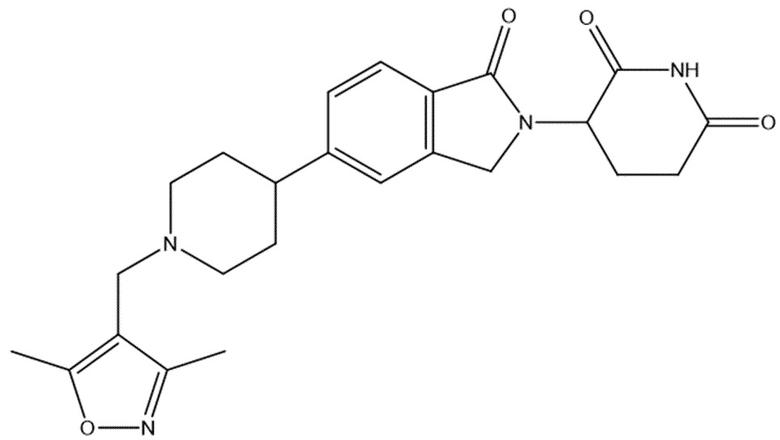
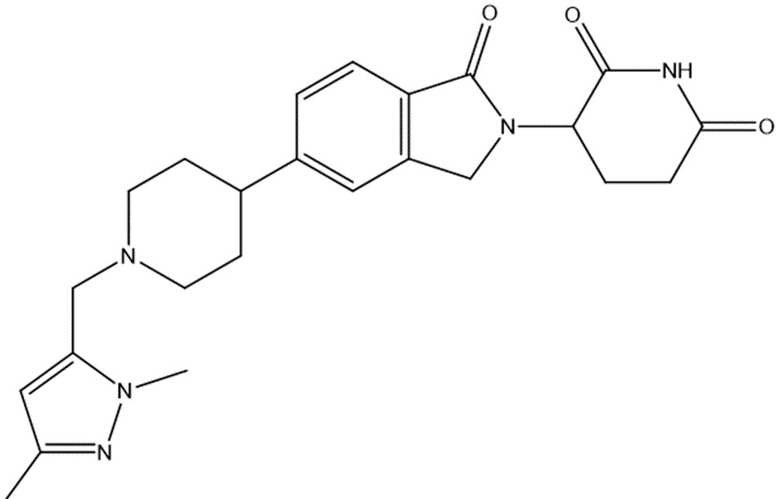
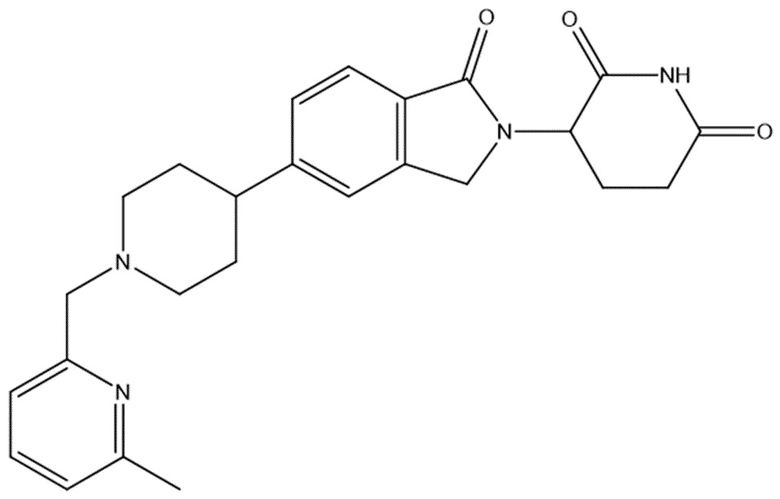
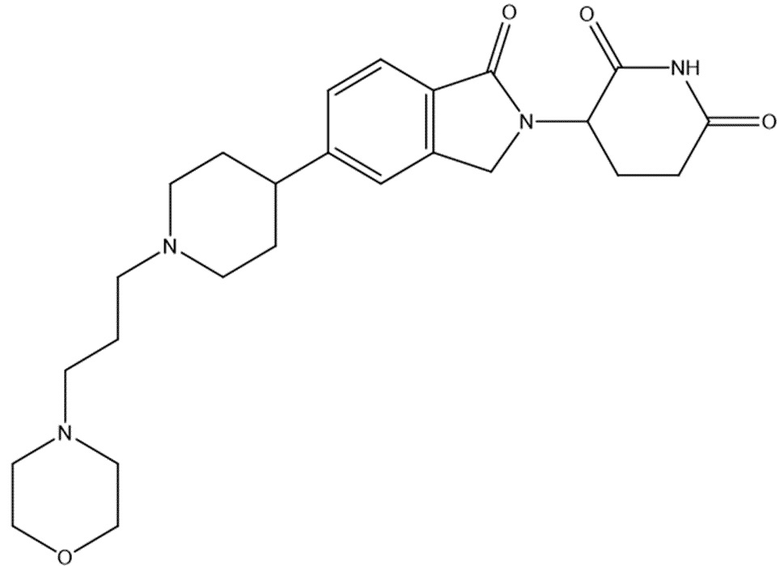



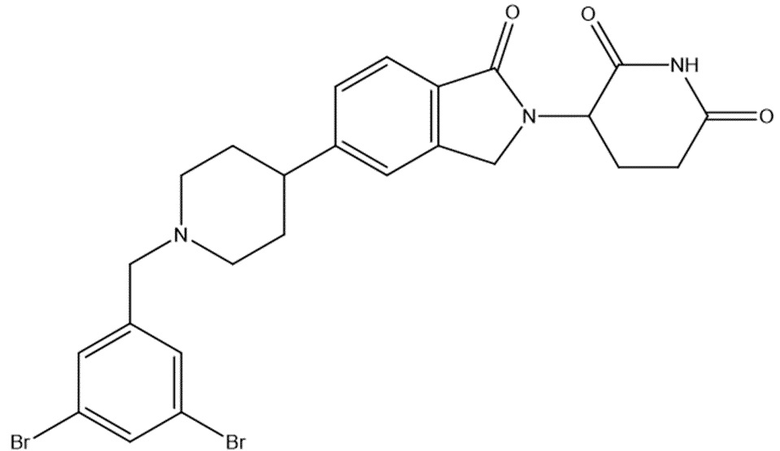

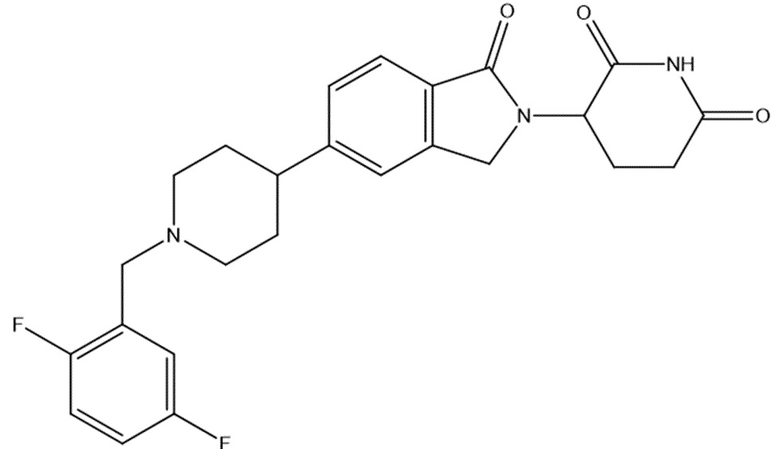
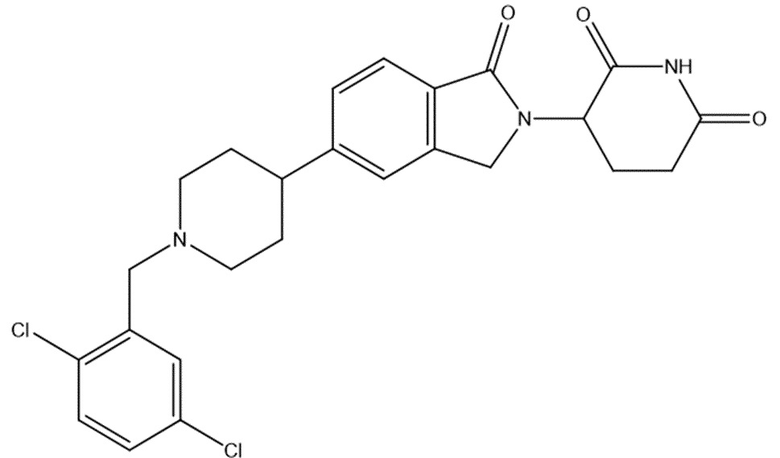

(или 3-(5-(1-(4-нитрилбензил)пиперидин-4-ил)-1-оксоизоиндолин-2-ил)пиперидин-2,6-дион)
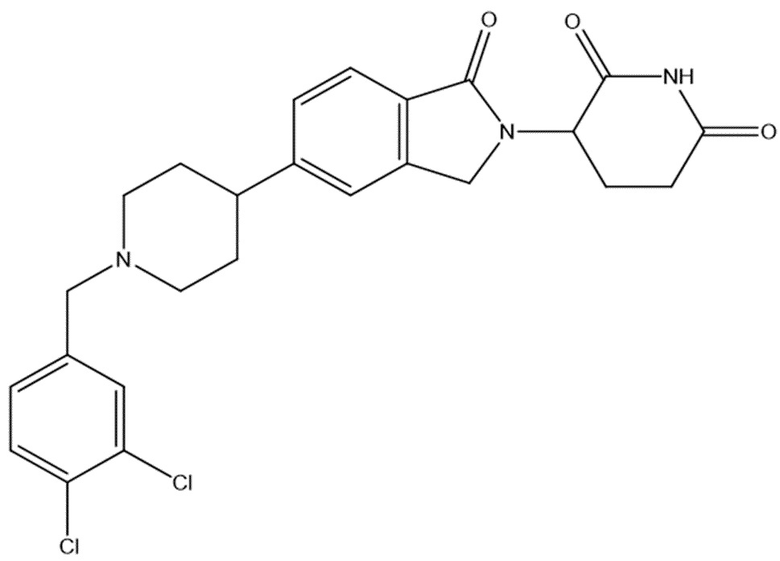
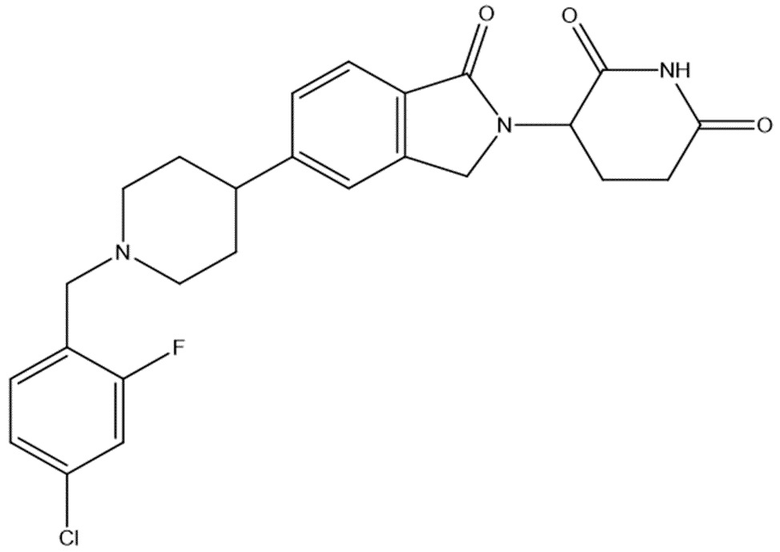
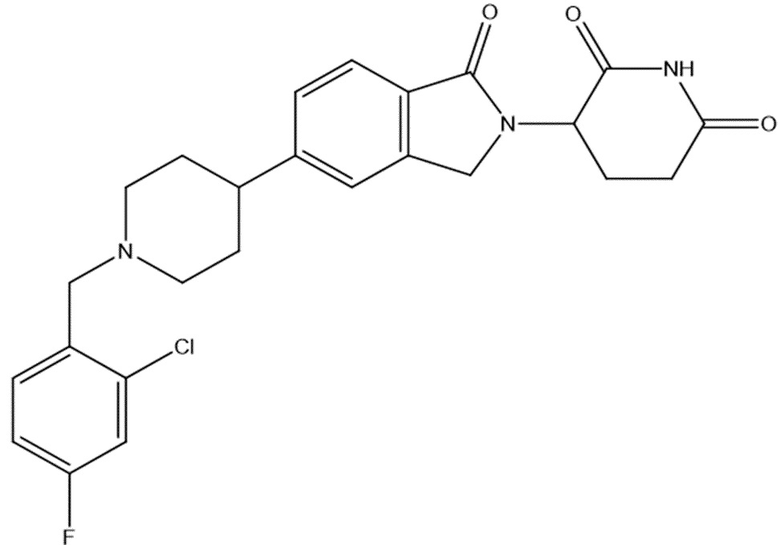

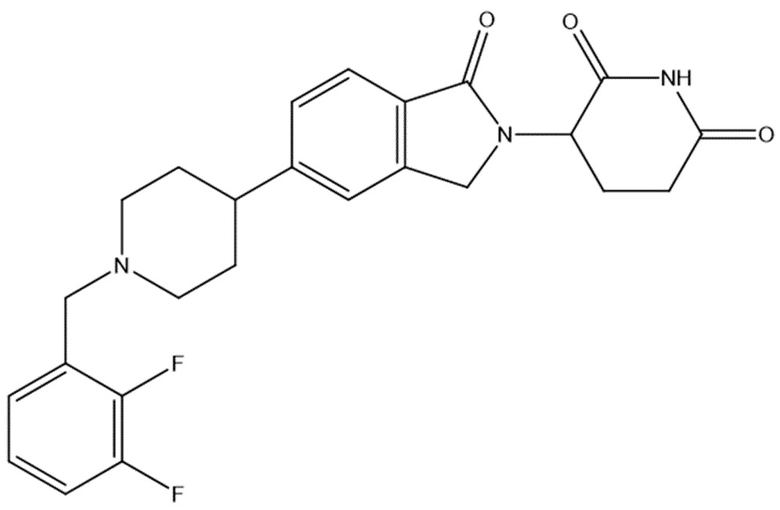
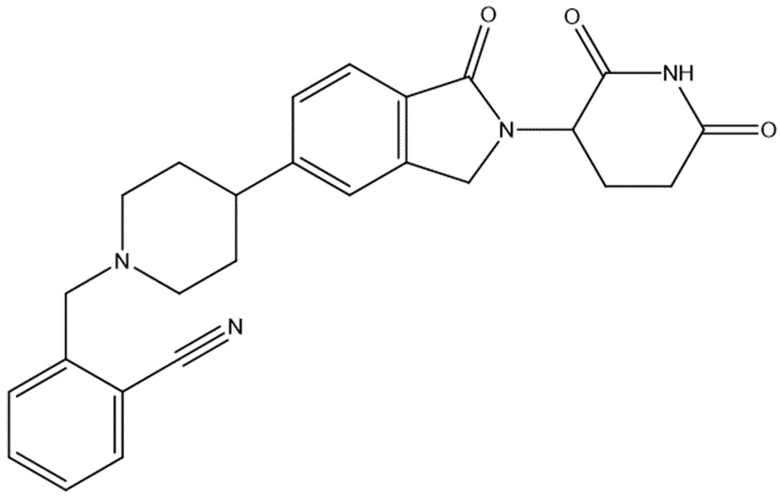
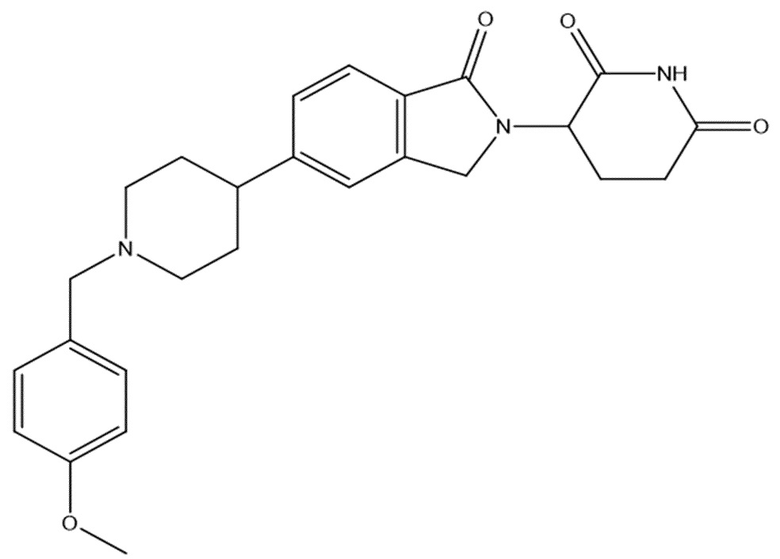



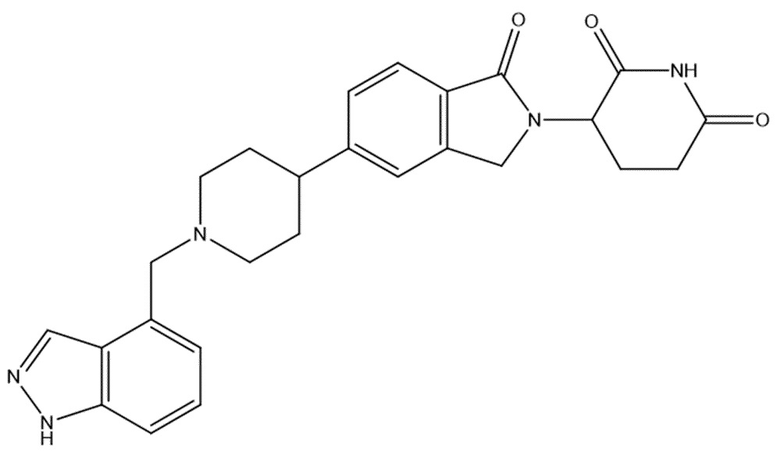
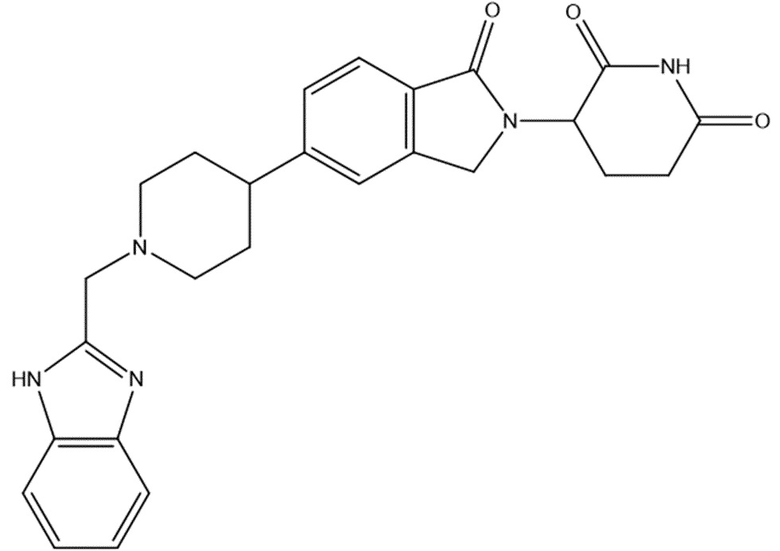

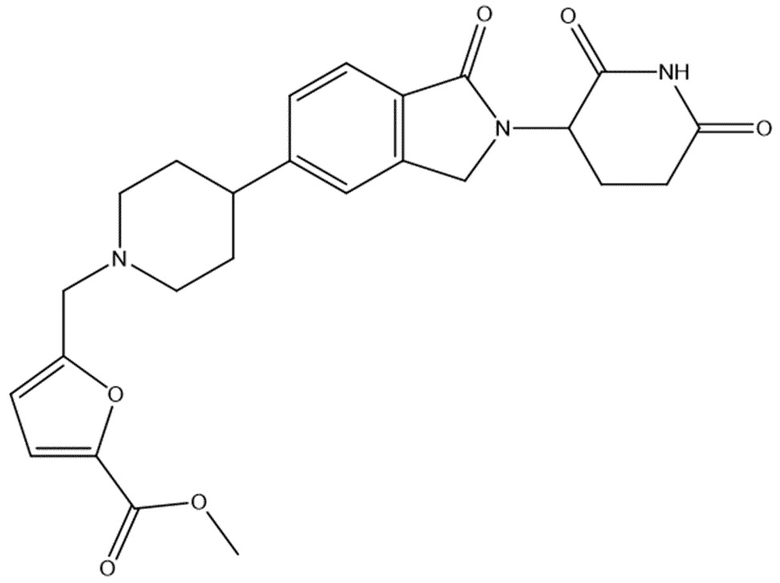
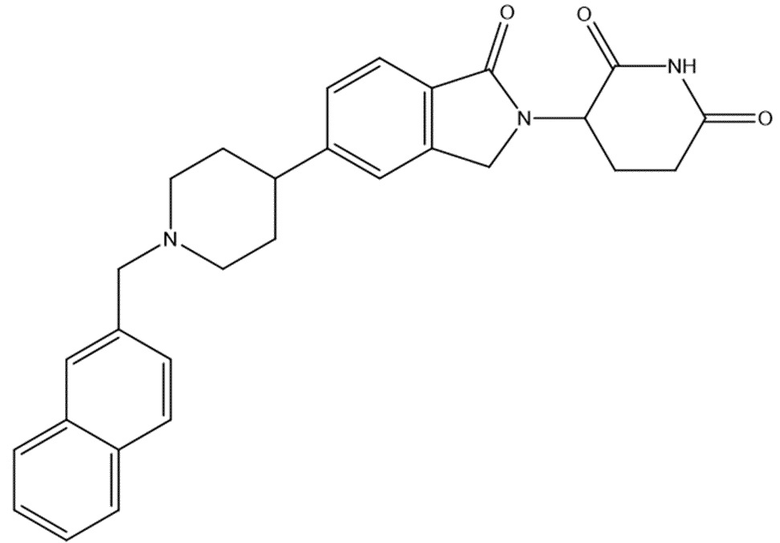
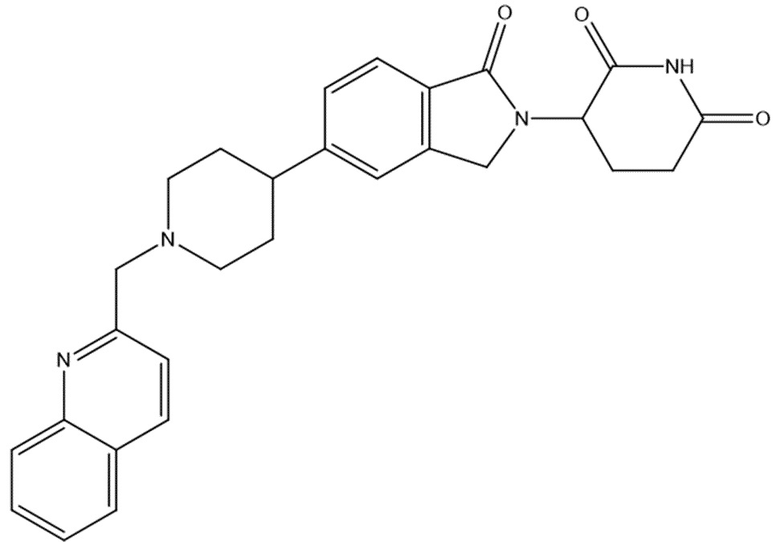
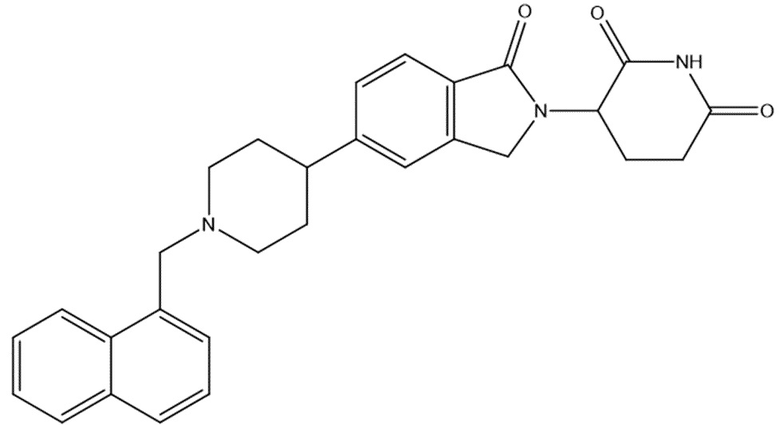

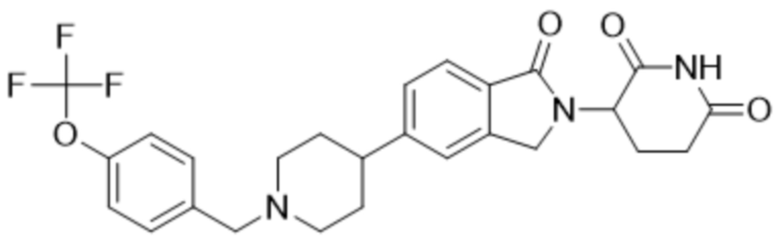
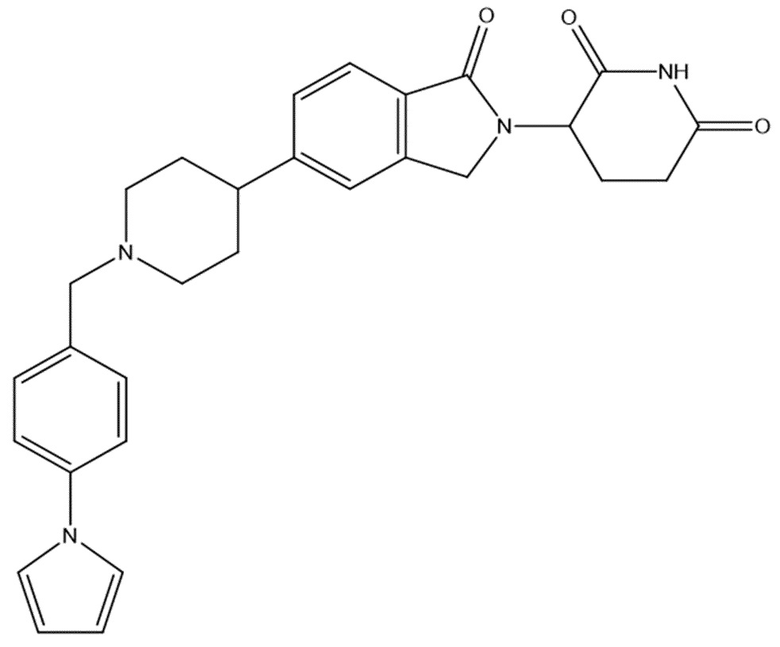

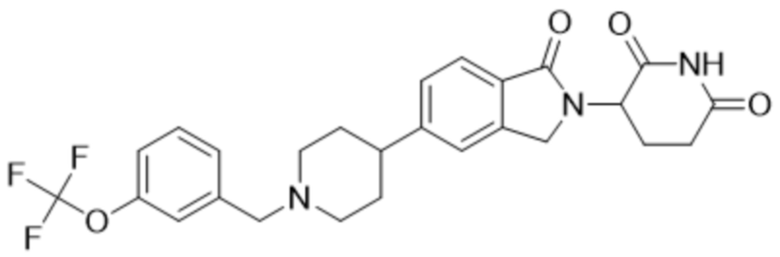

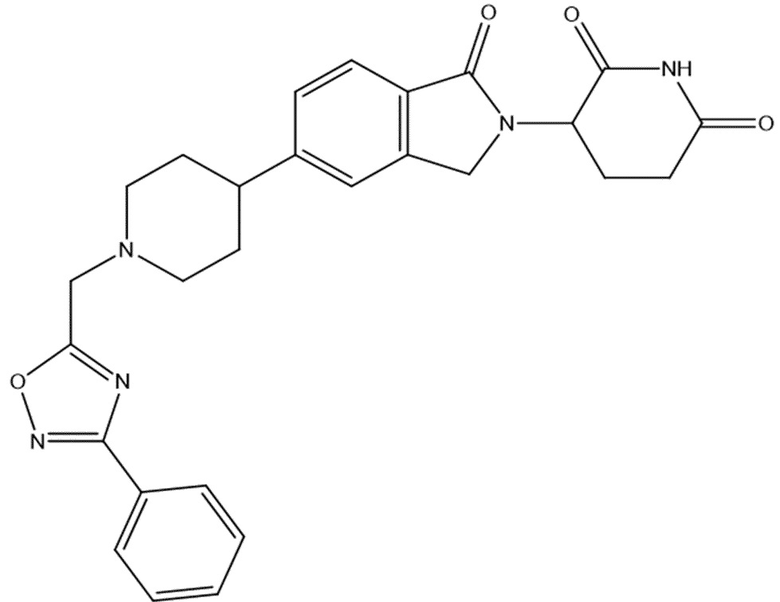

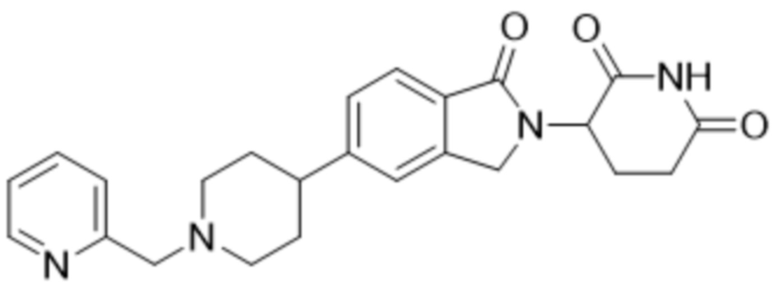

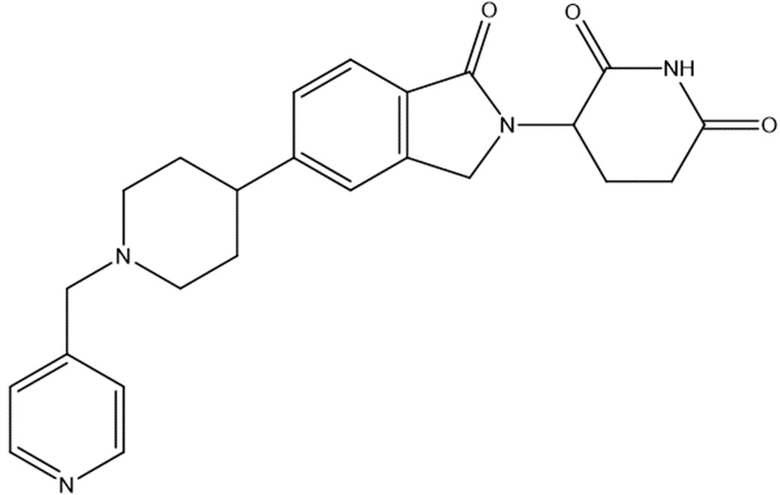


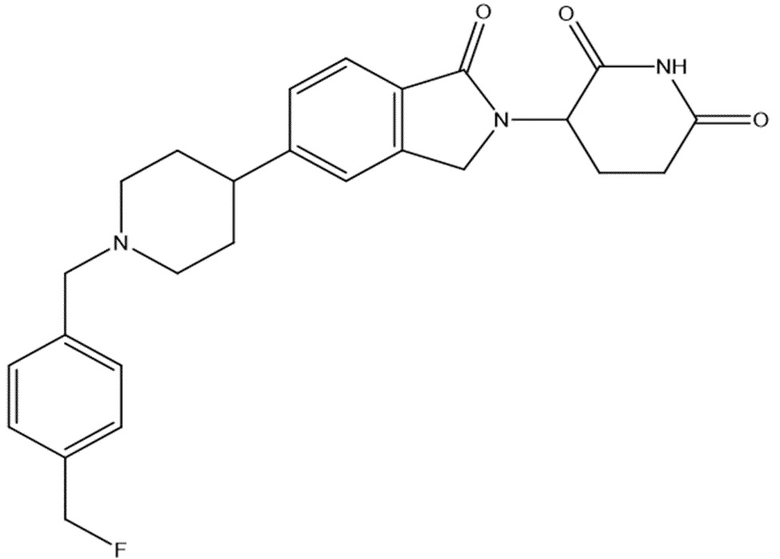
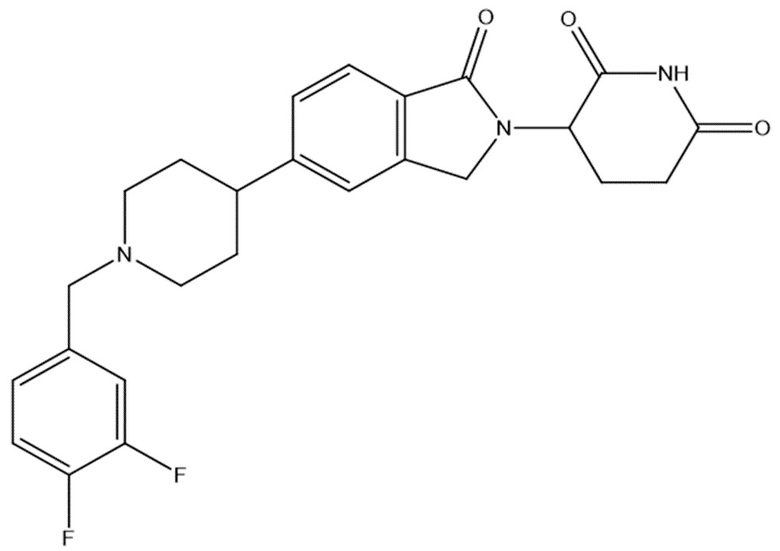

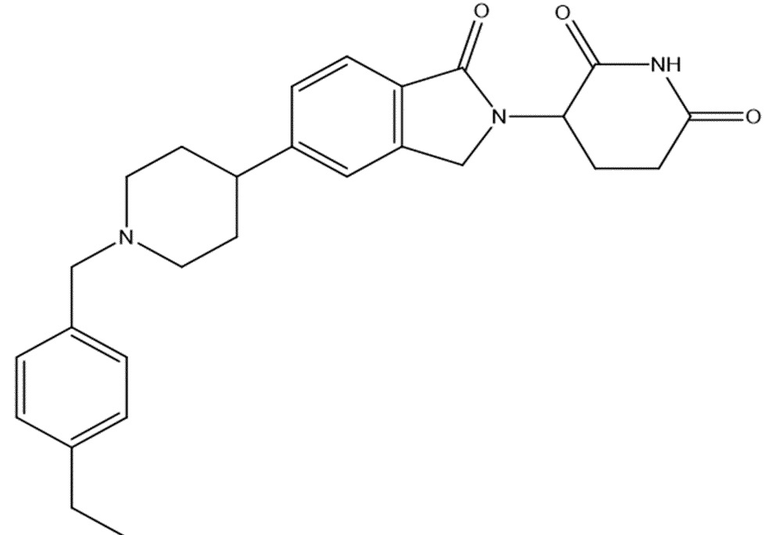
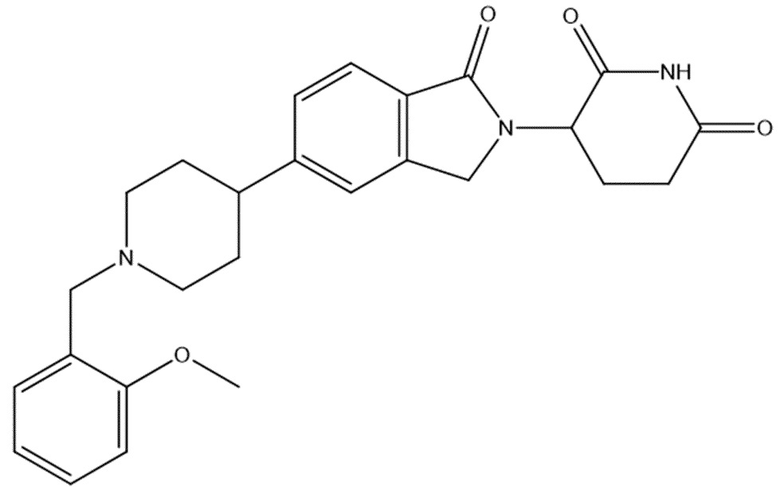




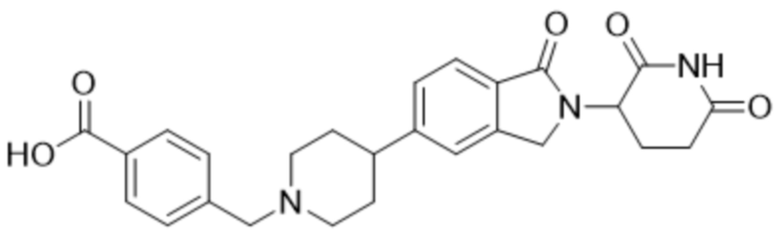
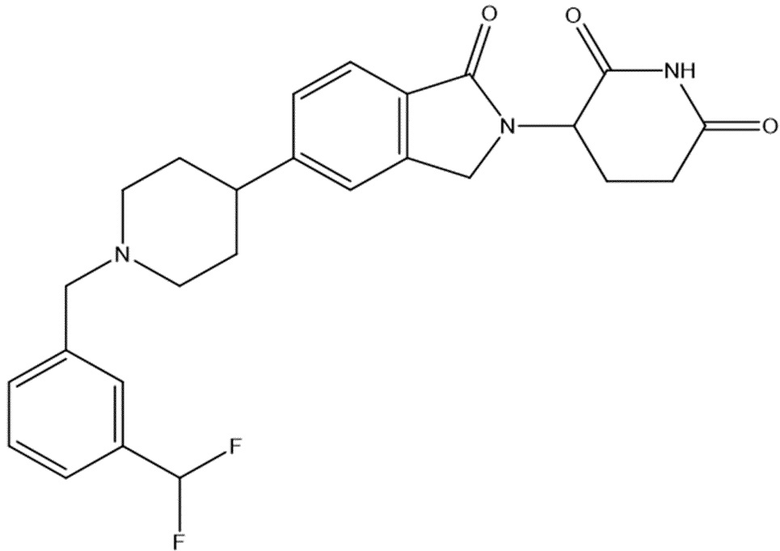
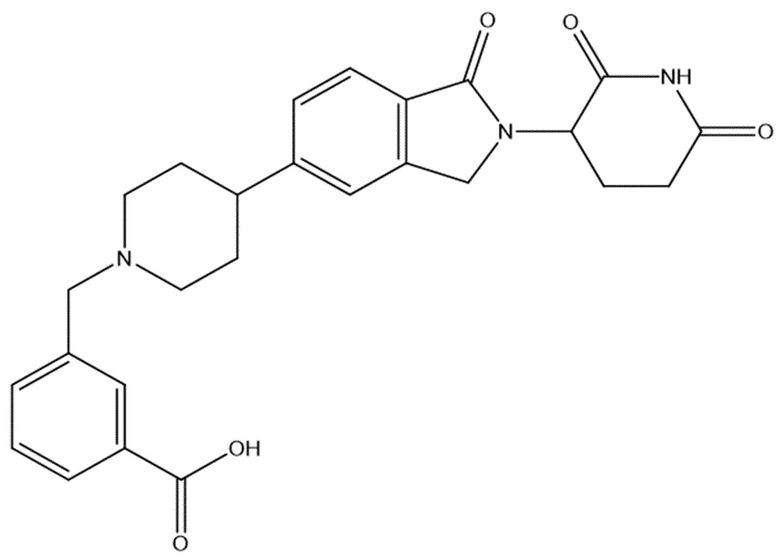

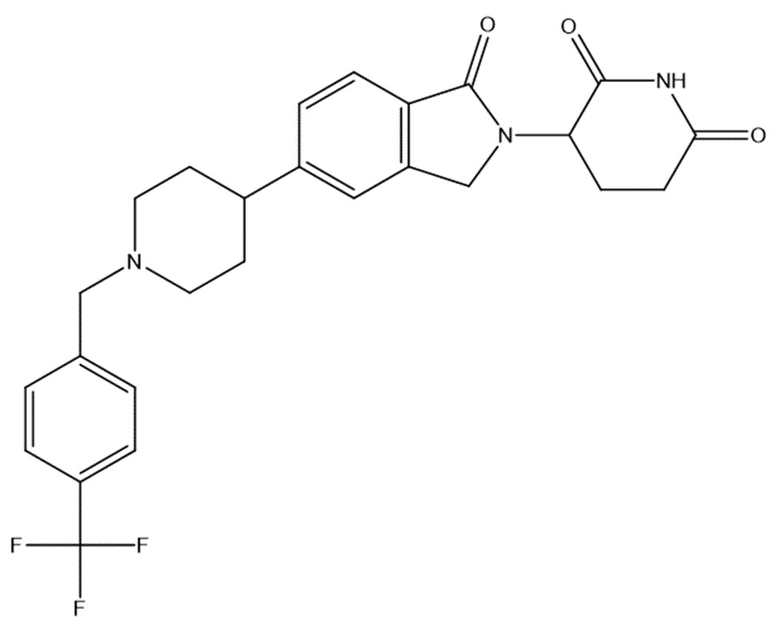

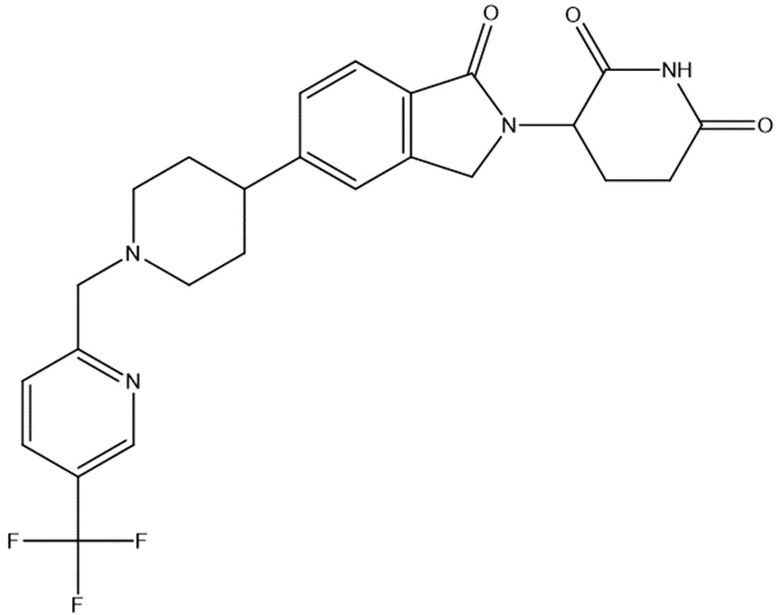

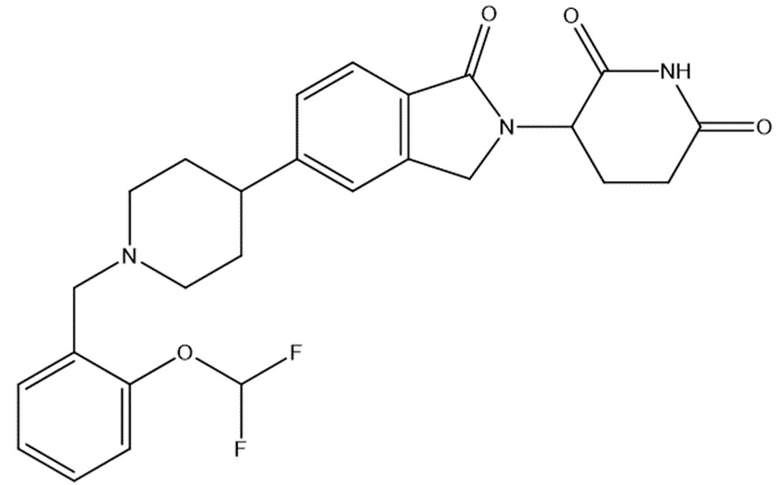


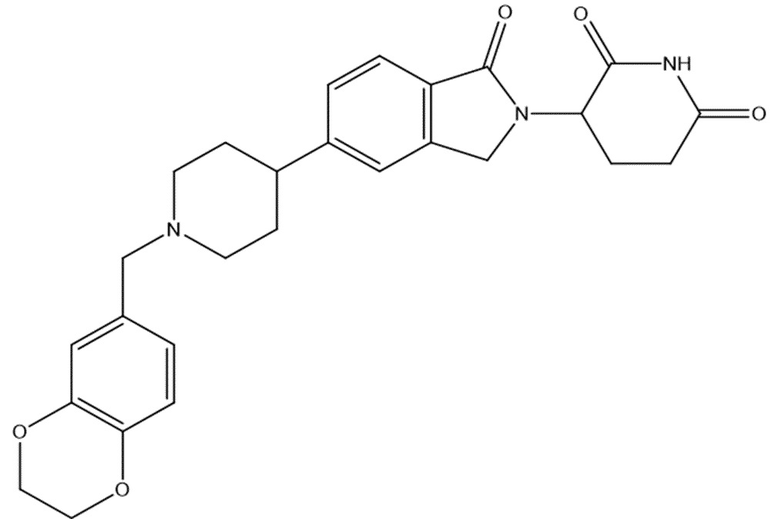


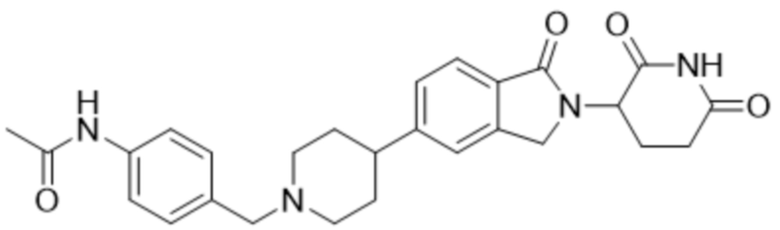
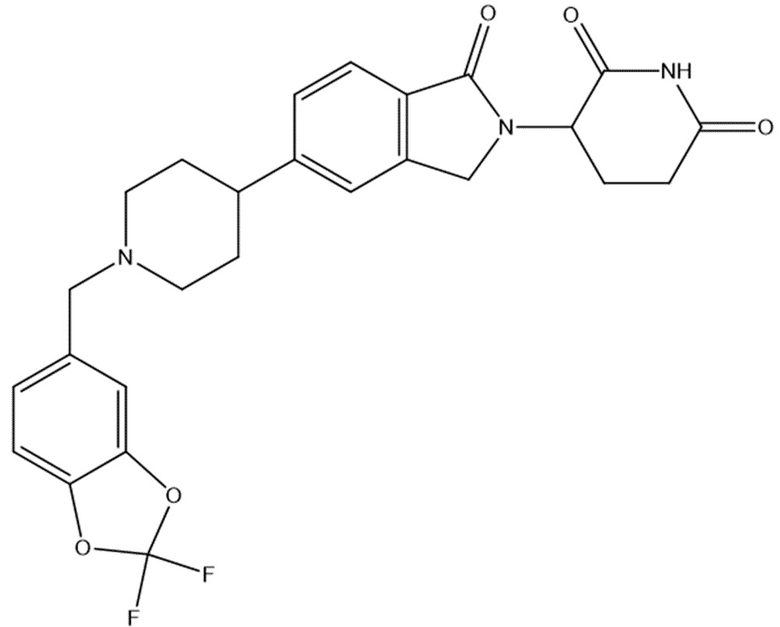
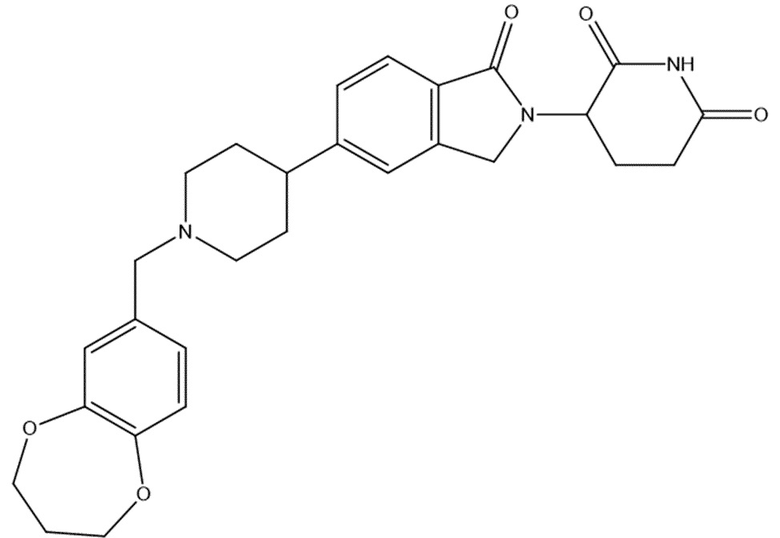
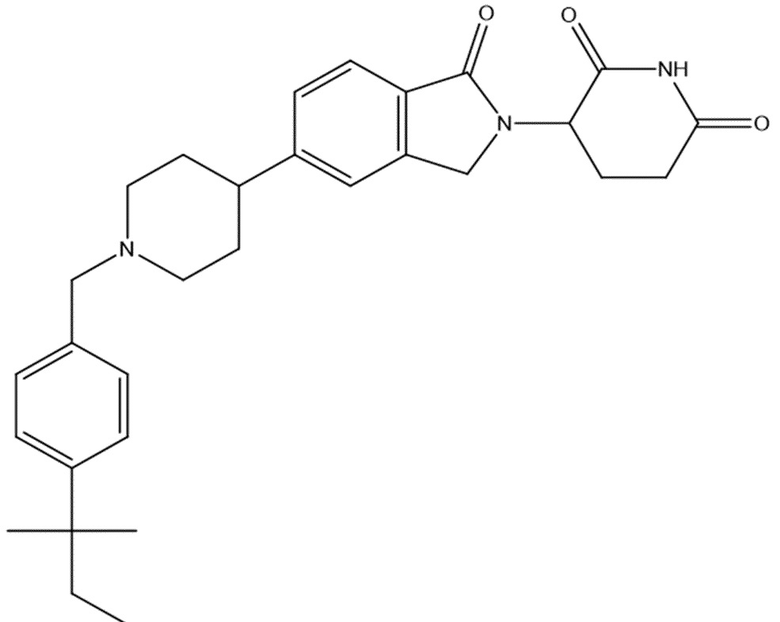

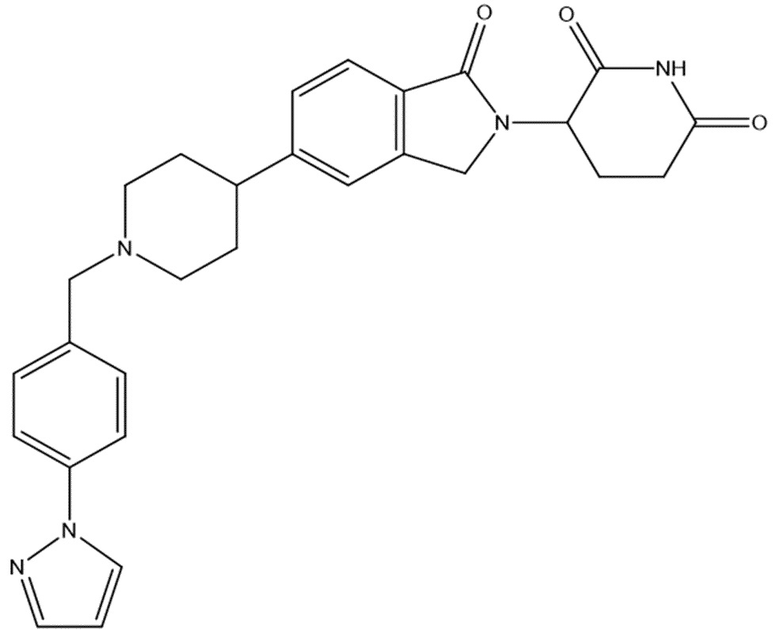
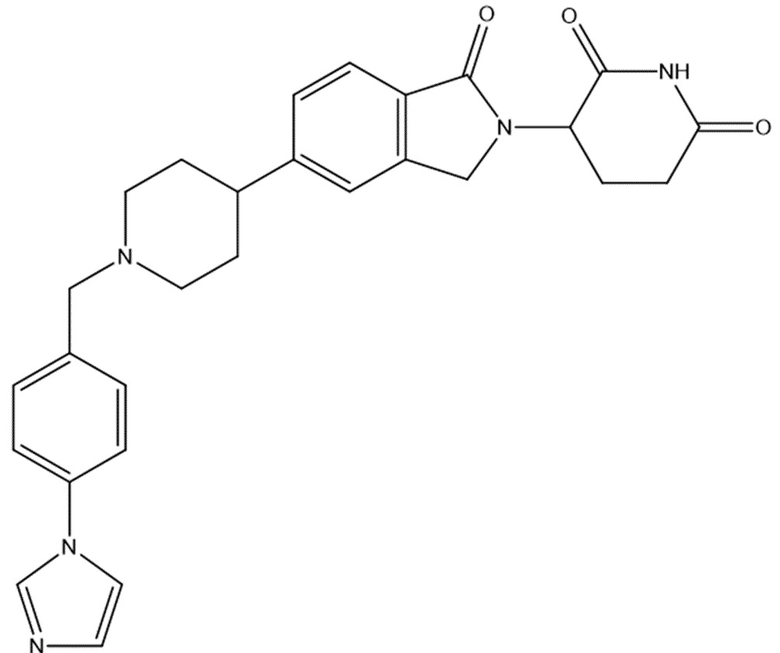
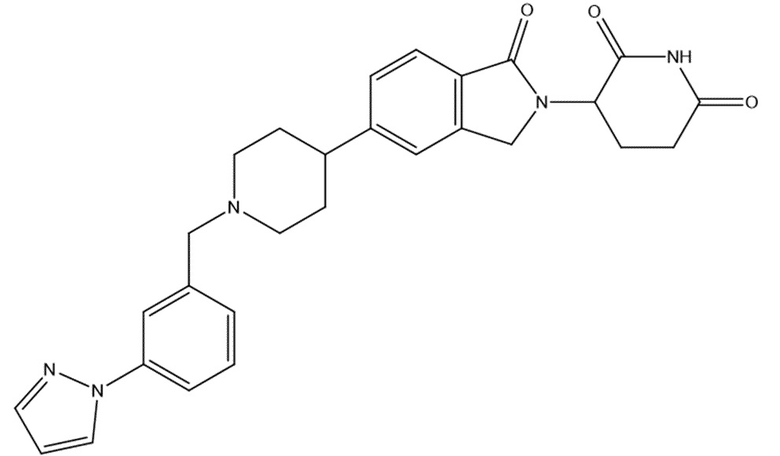
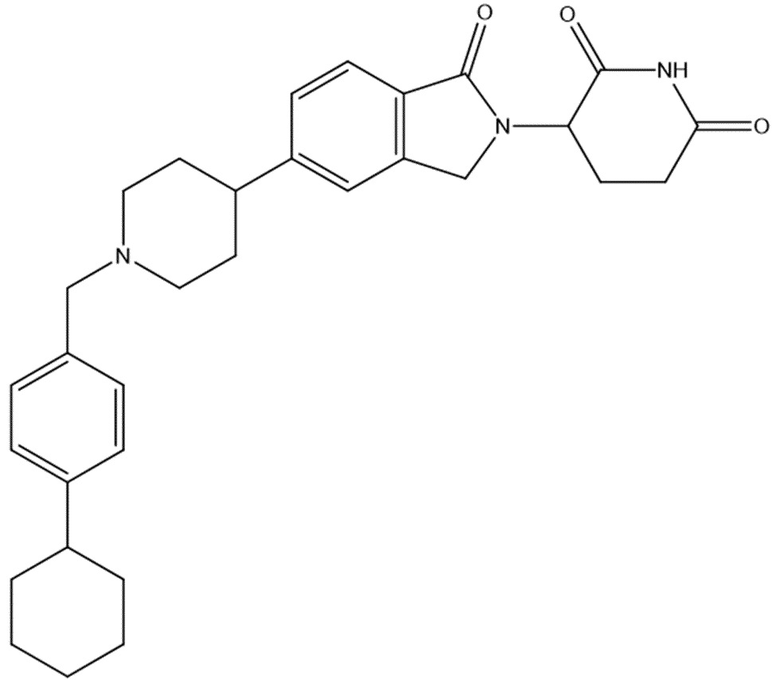

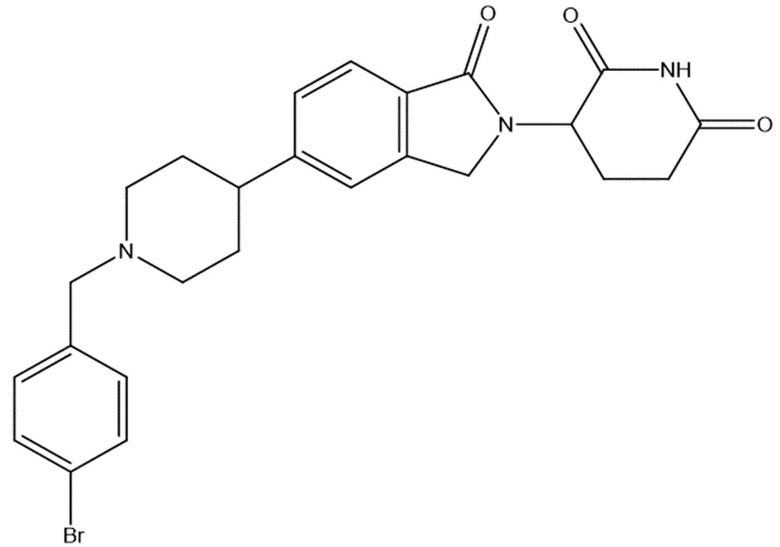
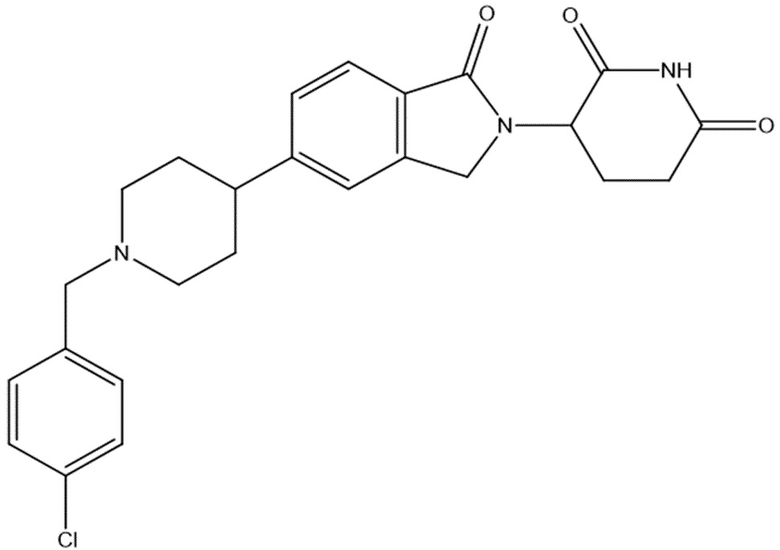


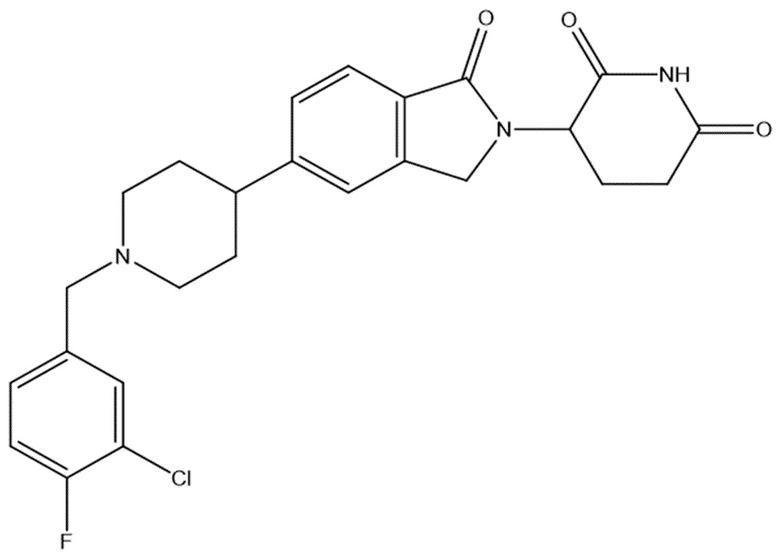
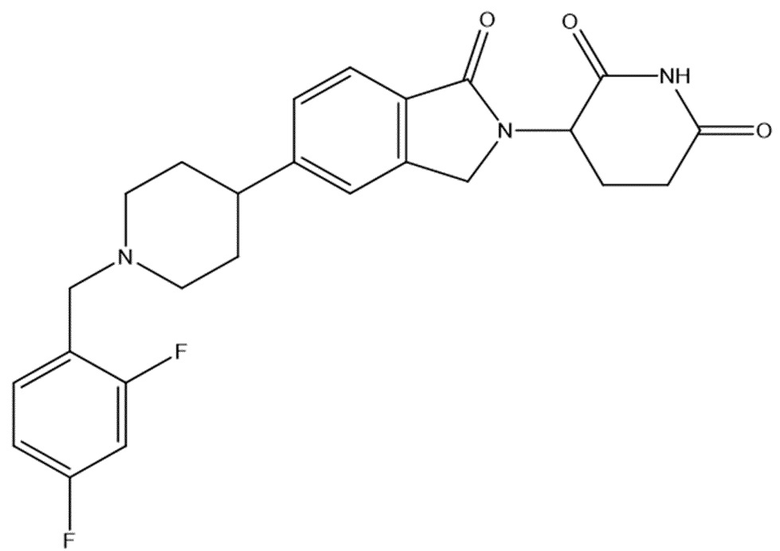

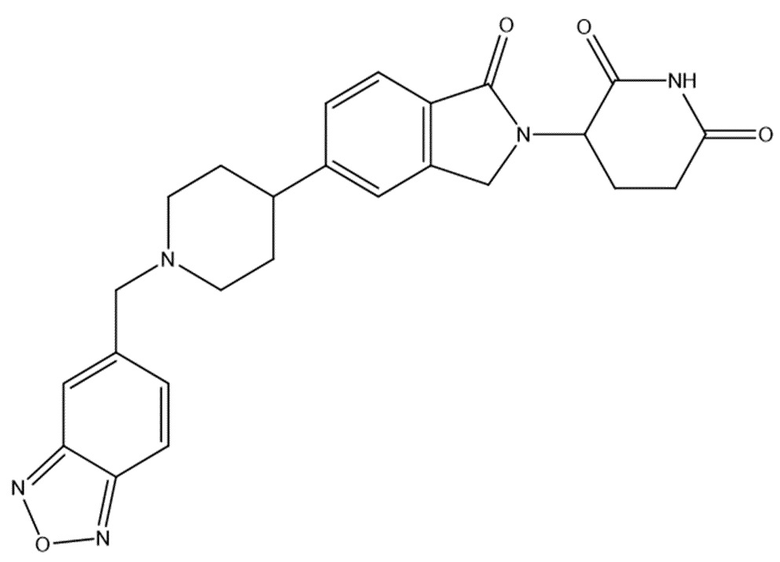


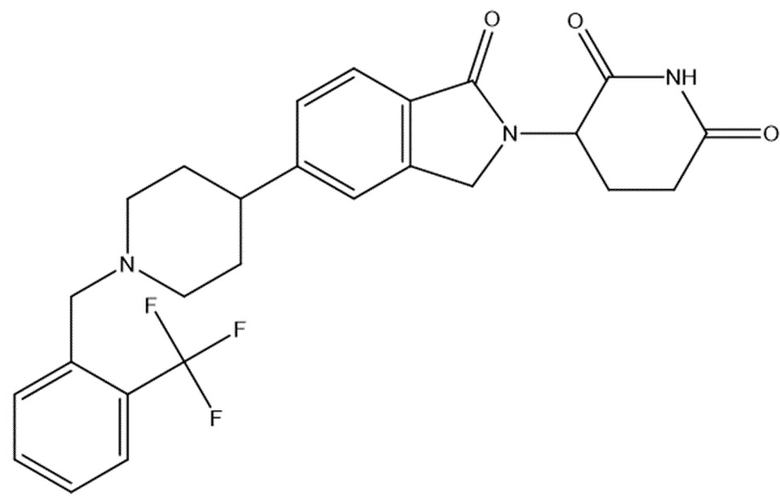
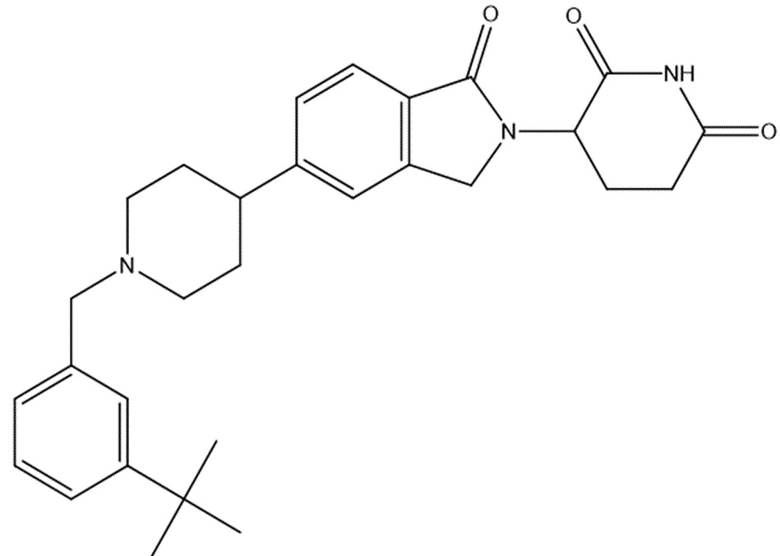
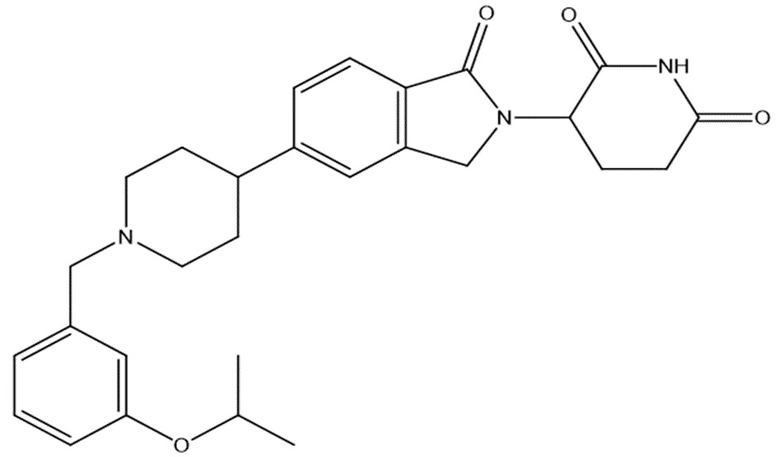



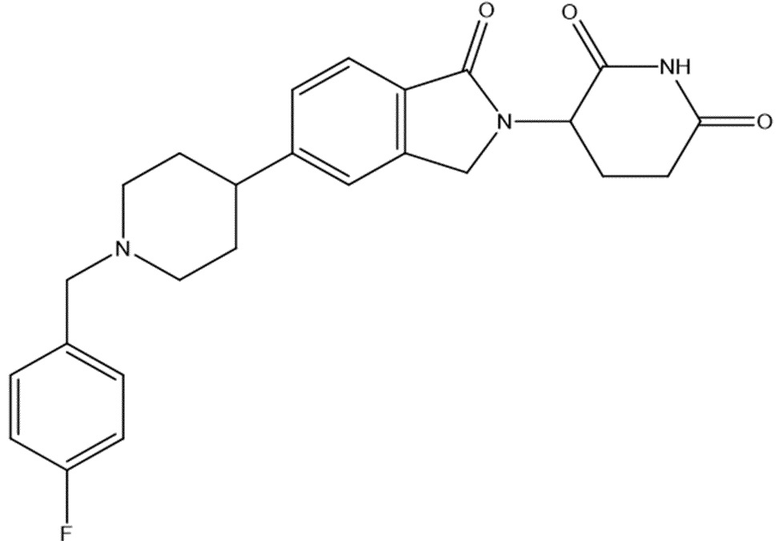
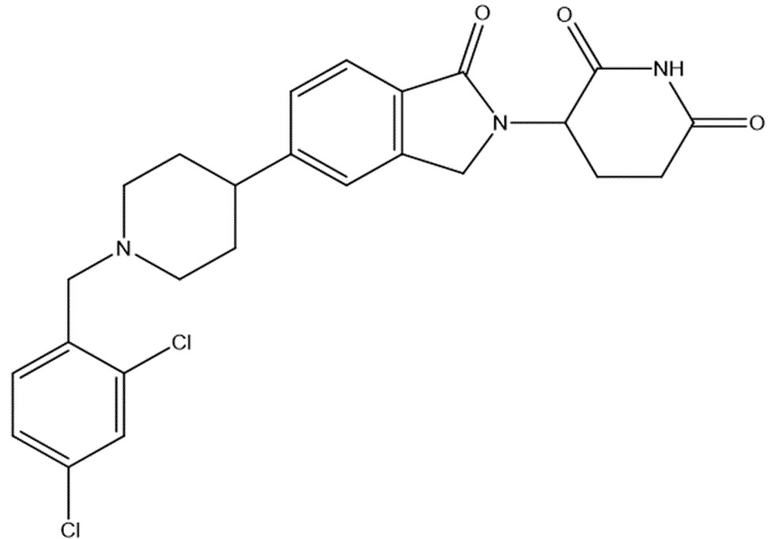

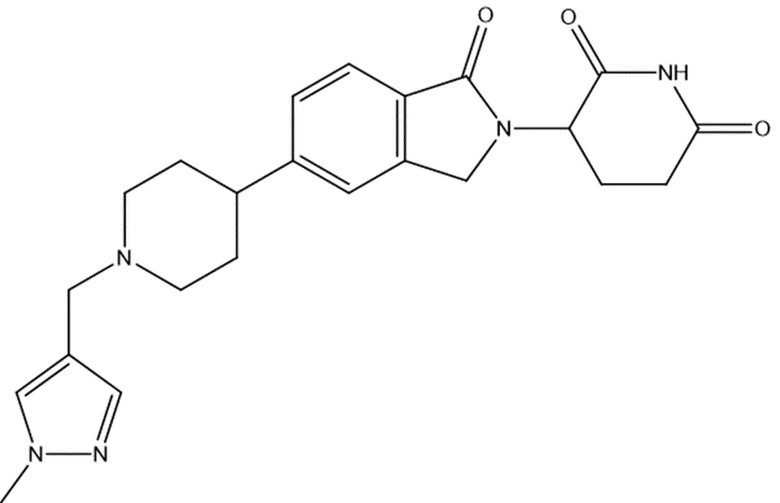

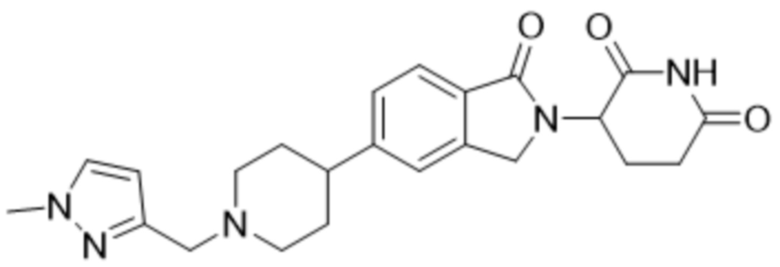
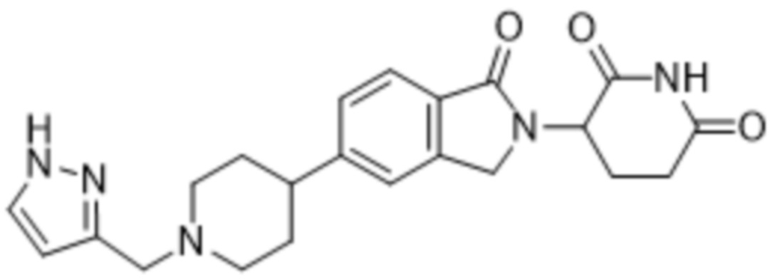
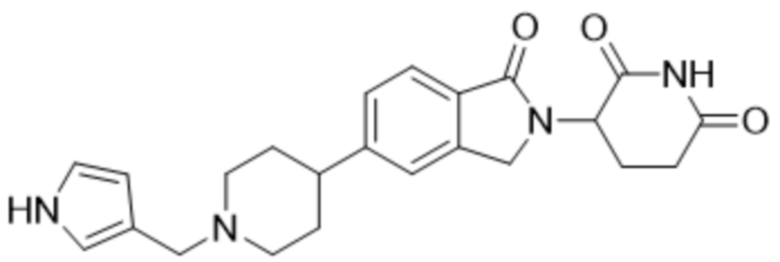
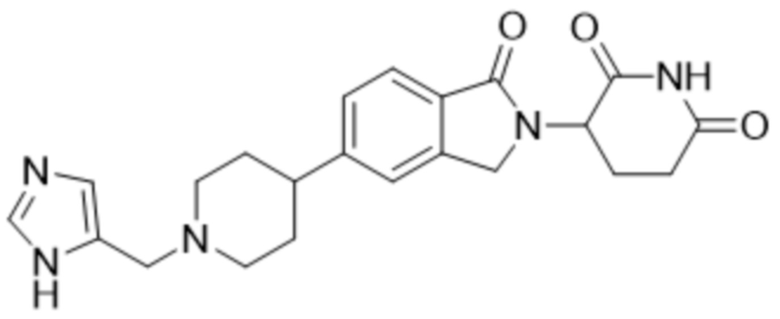


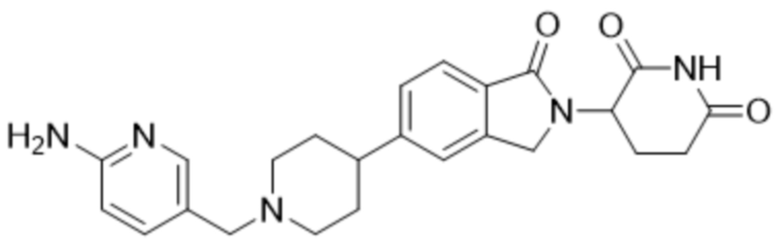
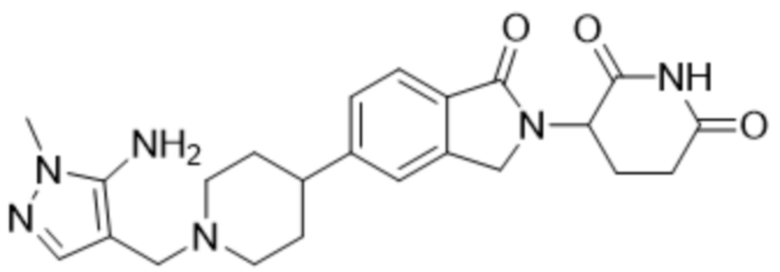
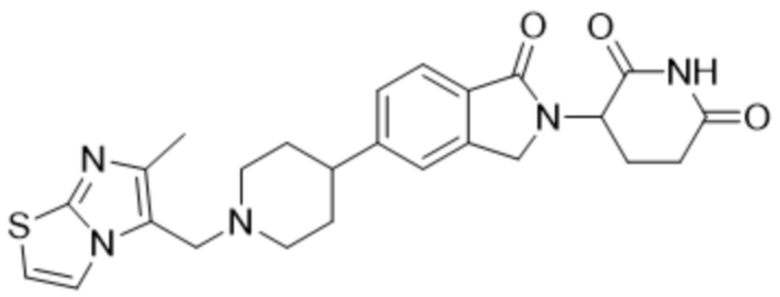







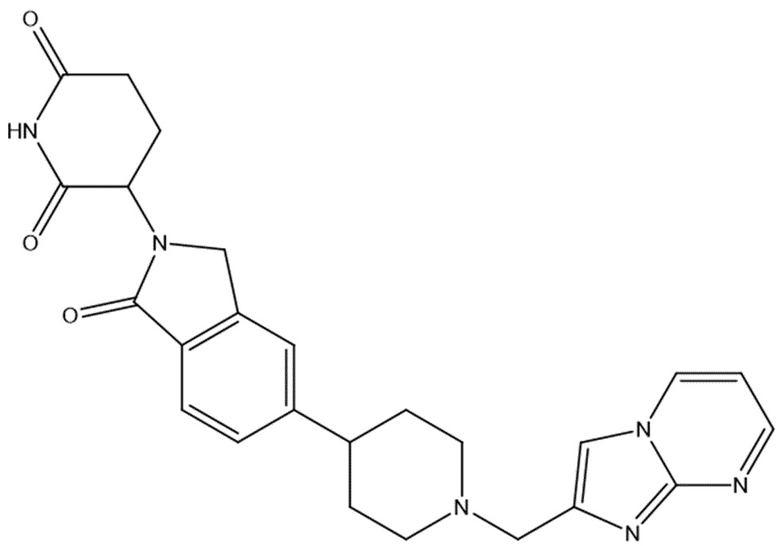

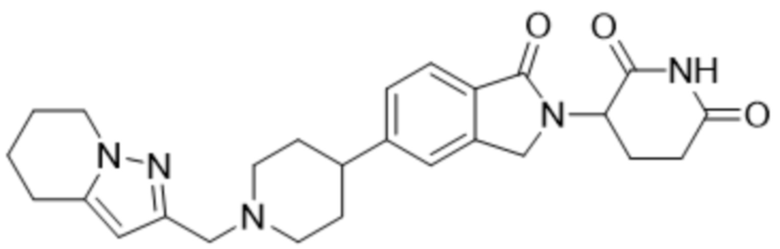
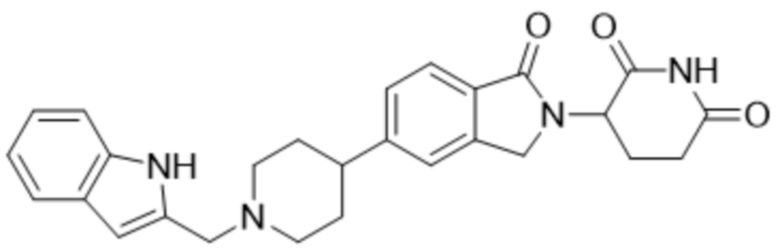
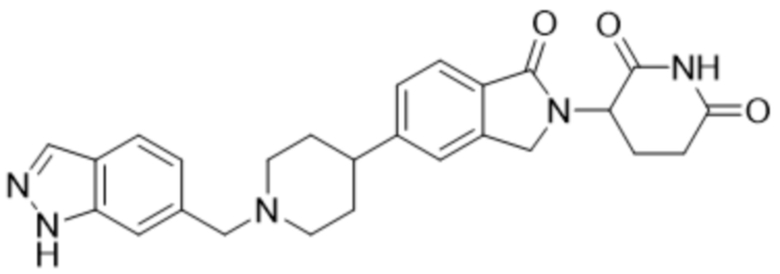


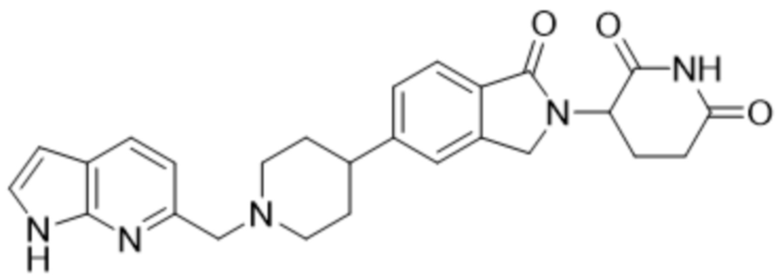


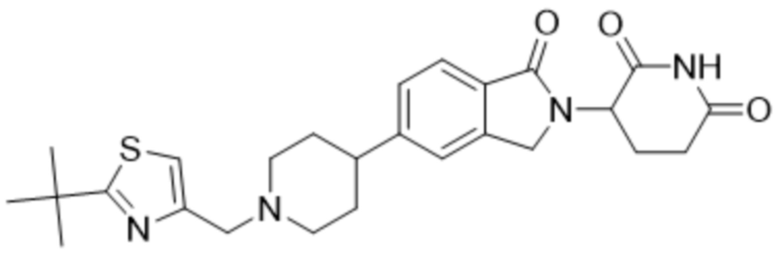
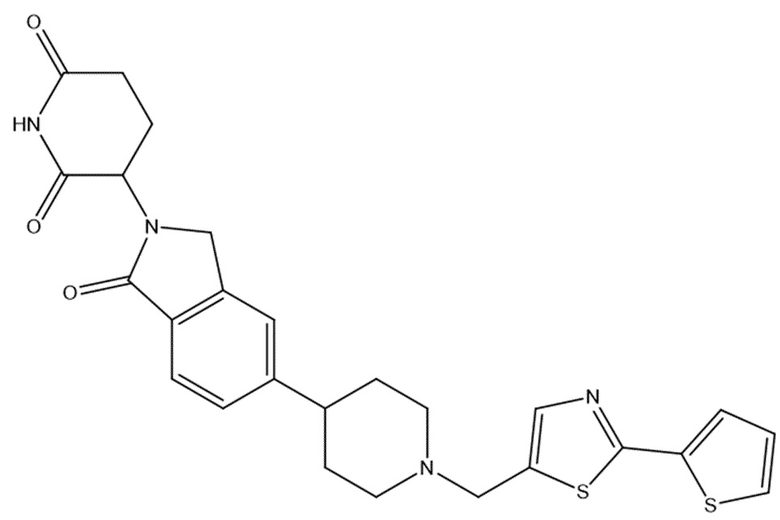
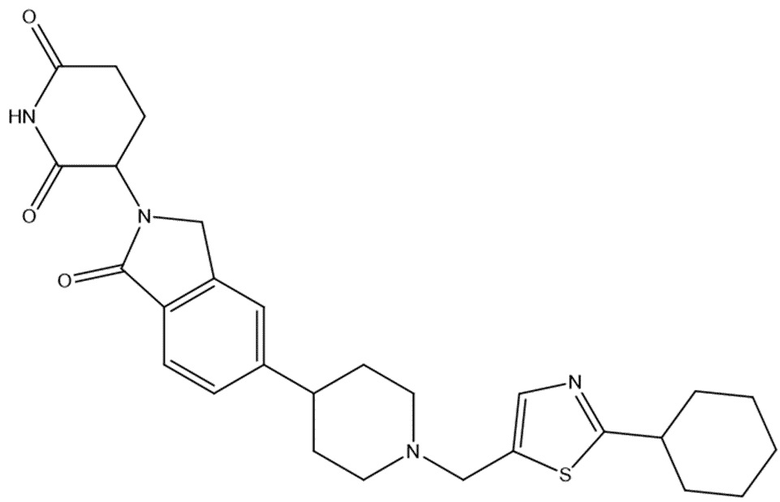
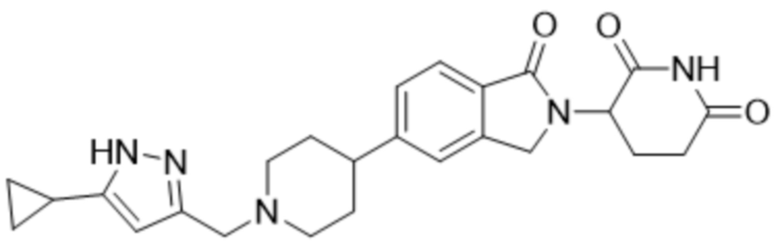
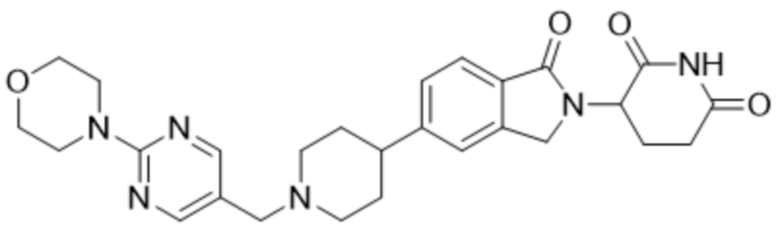


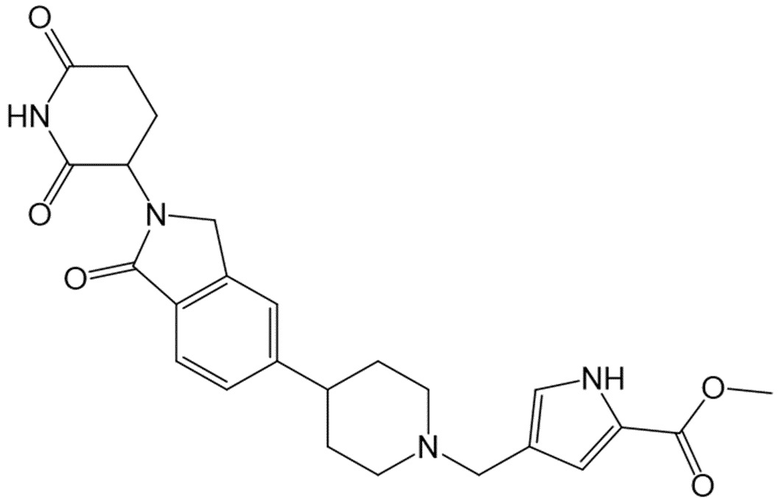
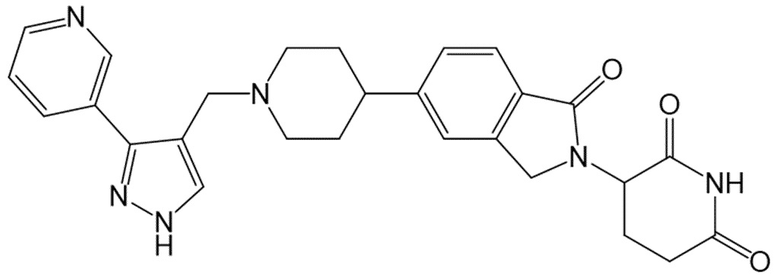

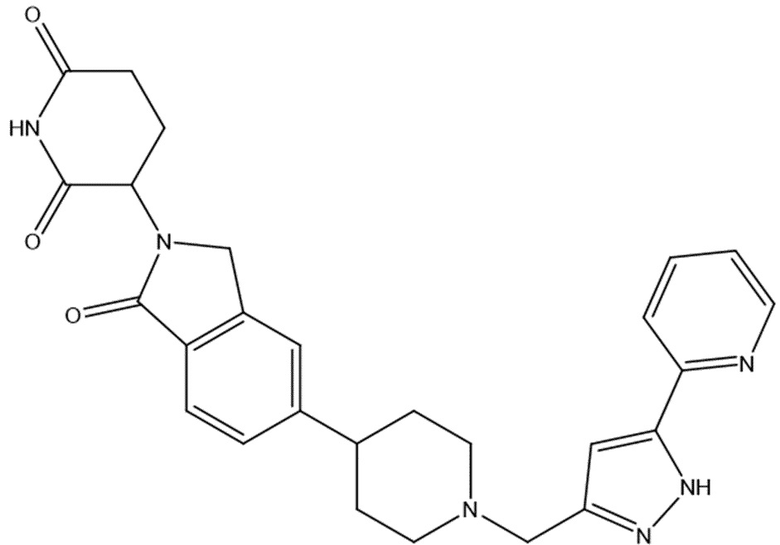
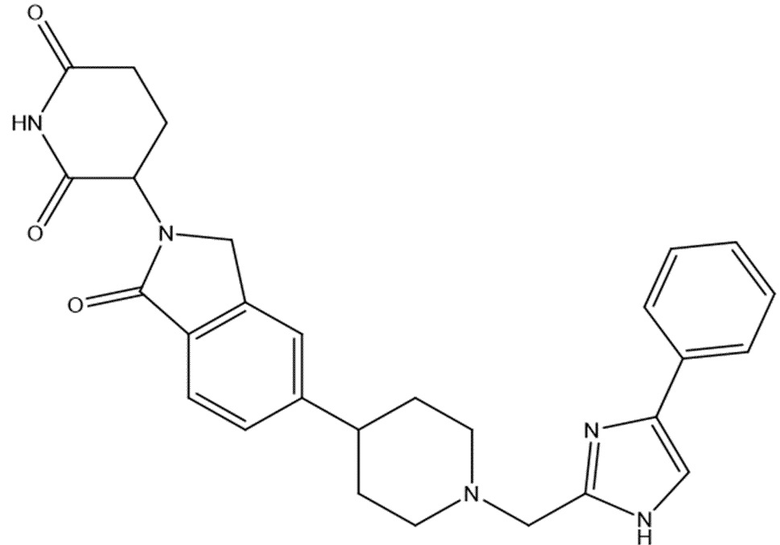


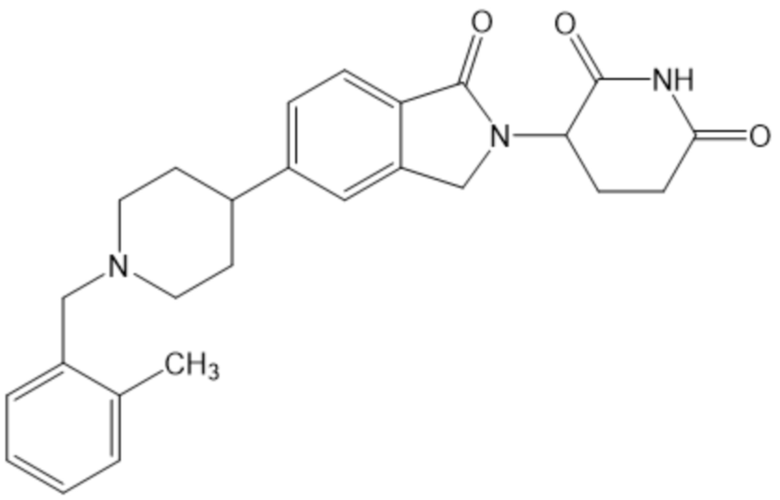
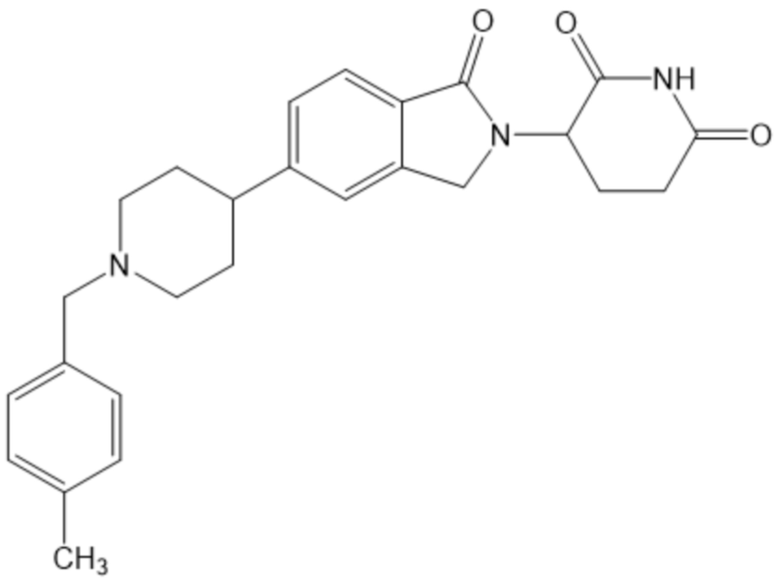
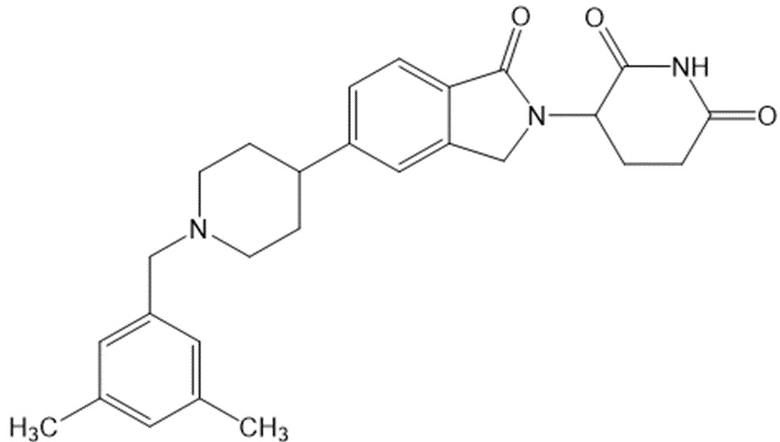

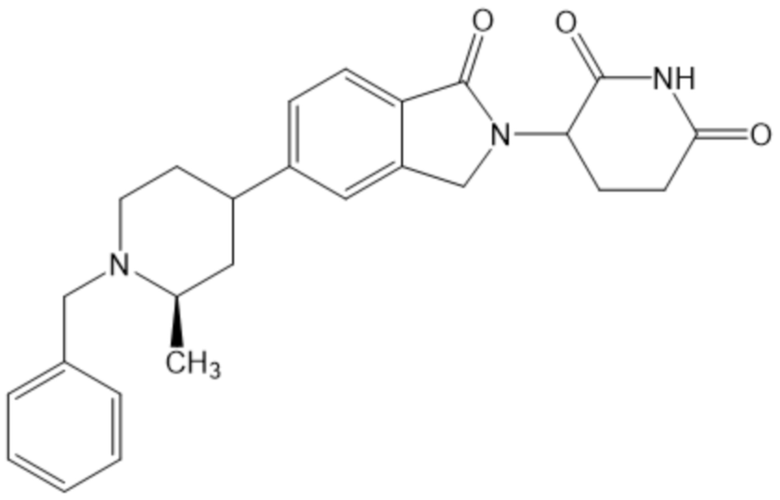
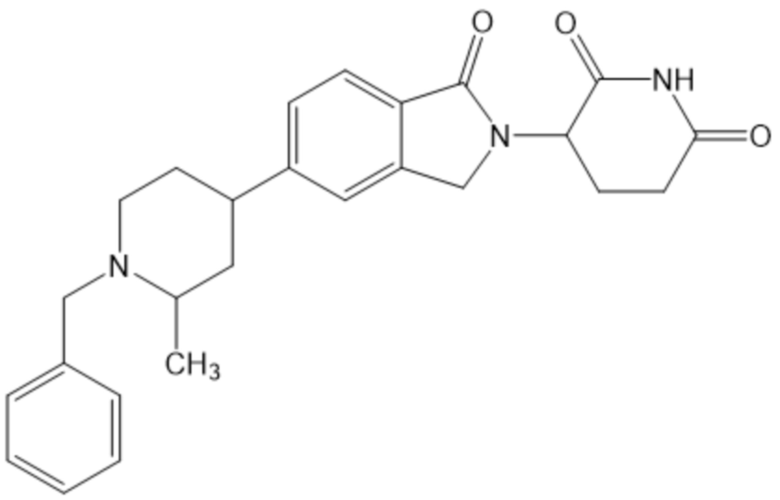
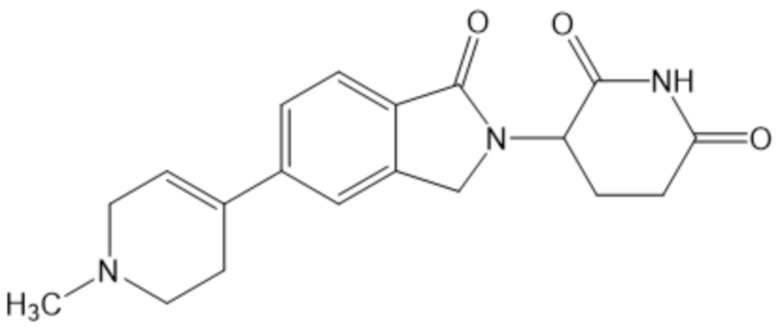


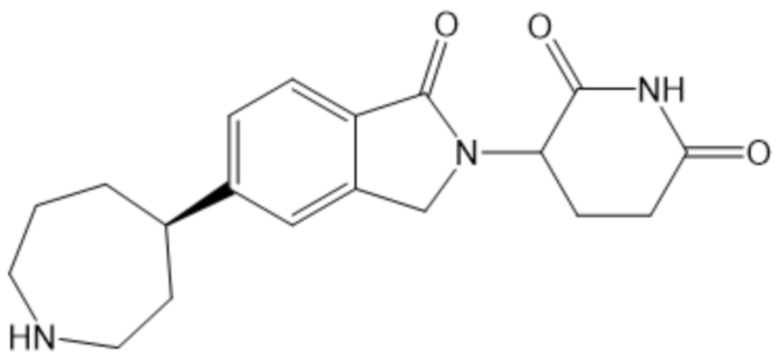




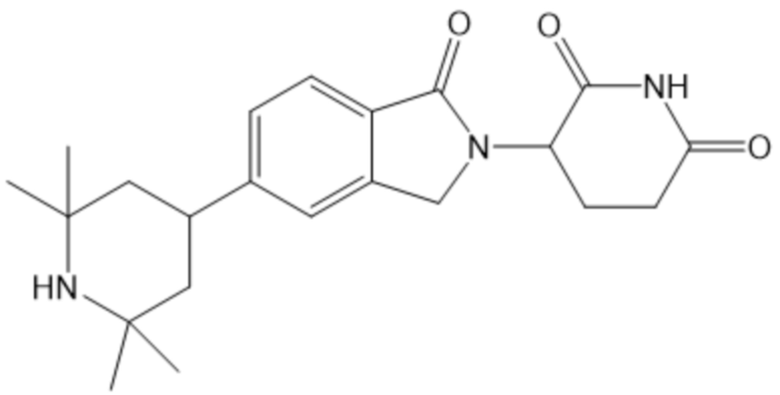

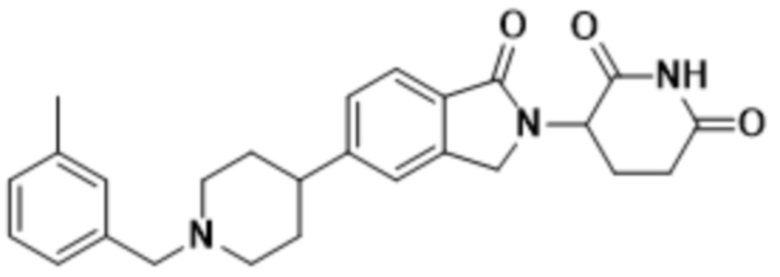
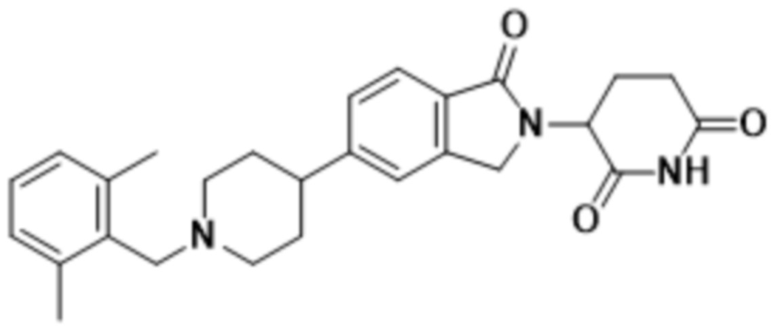
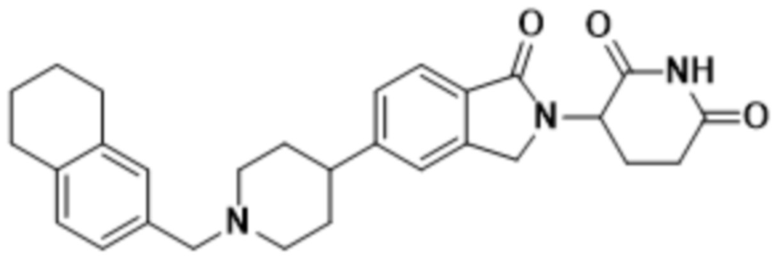
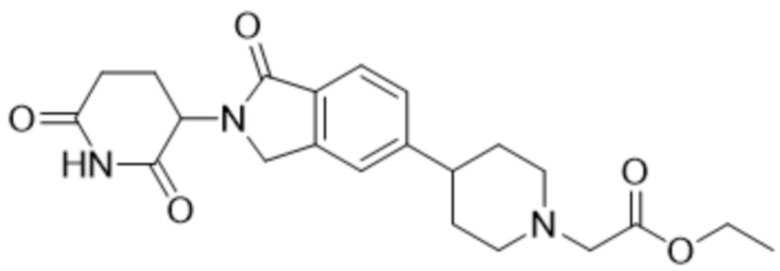




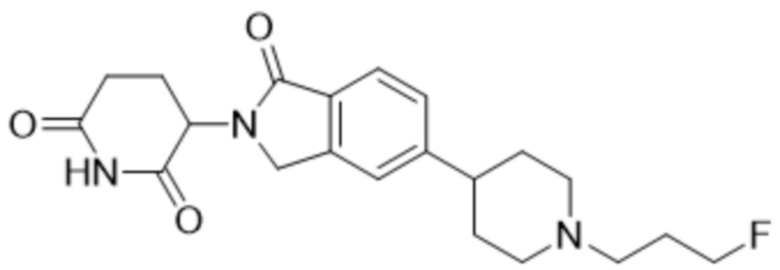


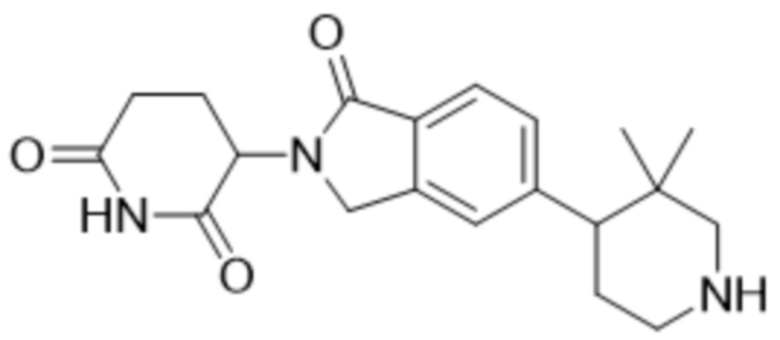

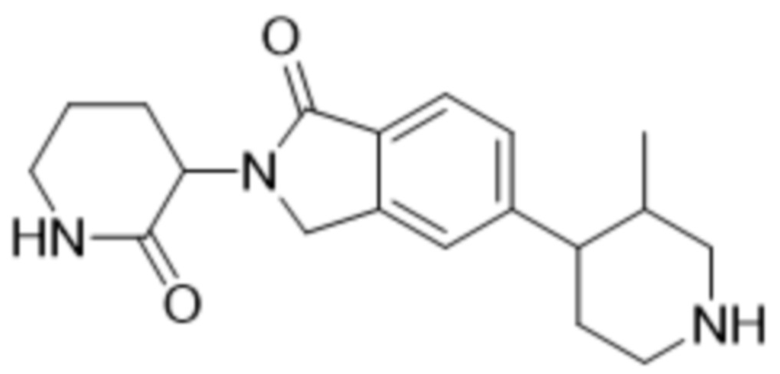

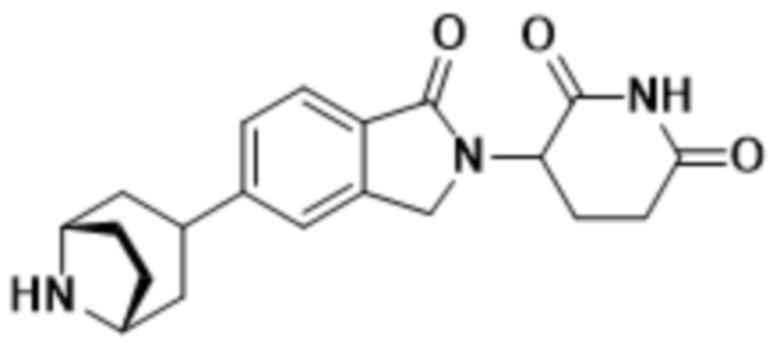
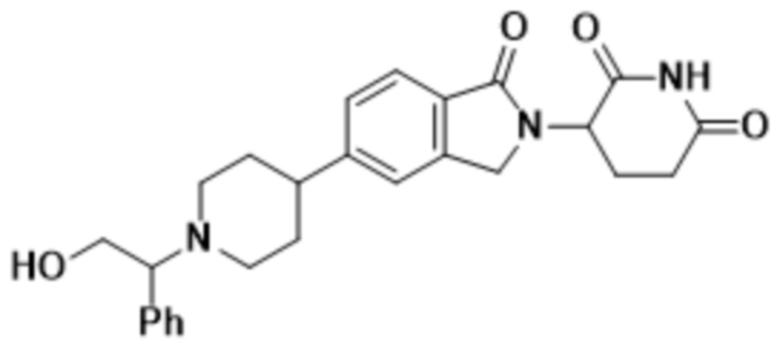
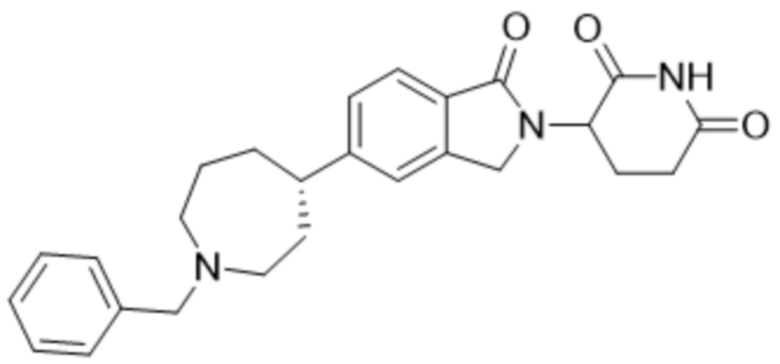

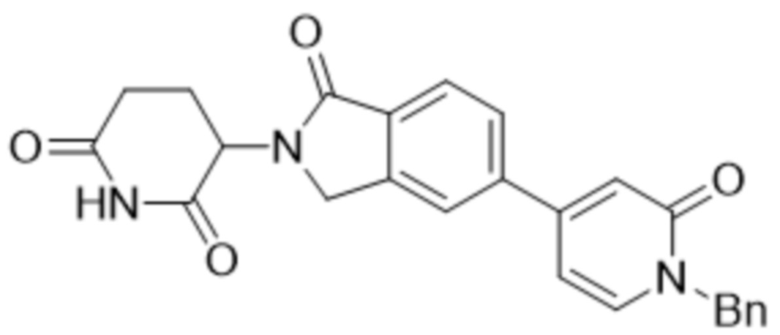
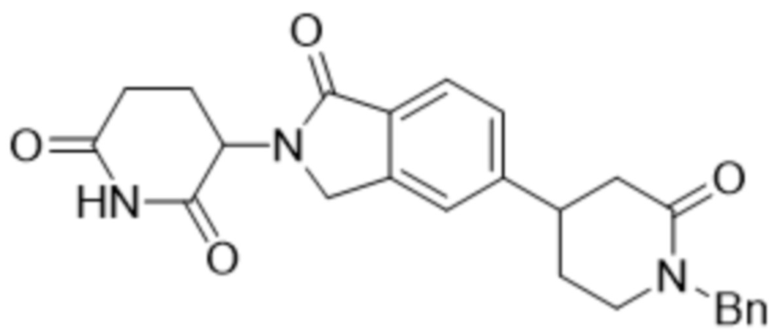
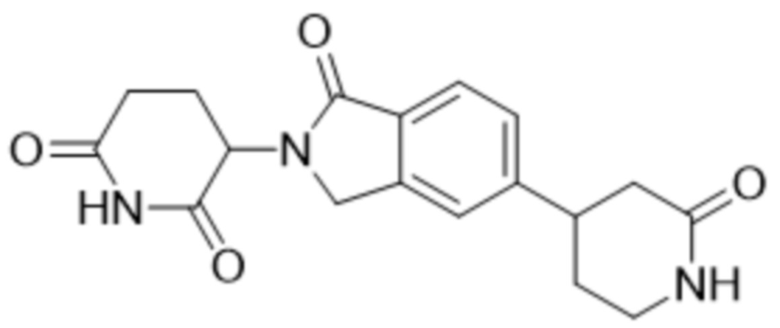

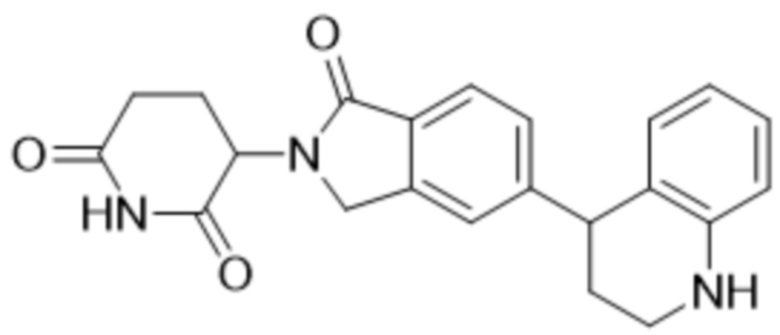


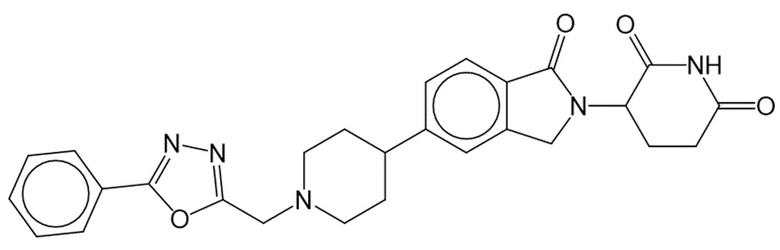
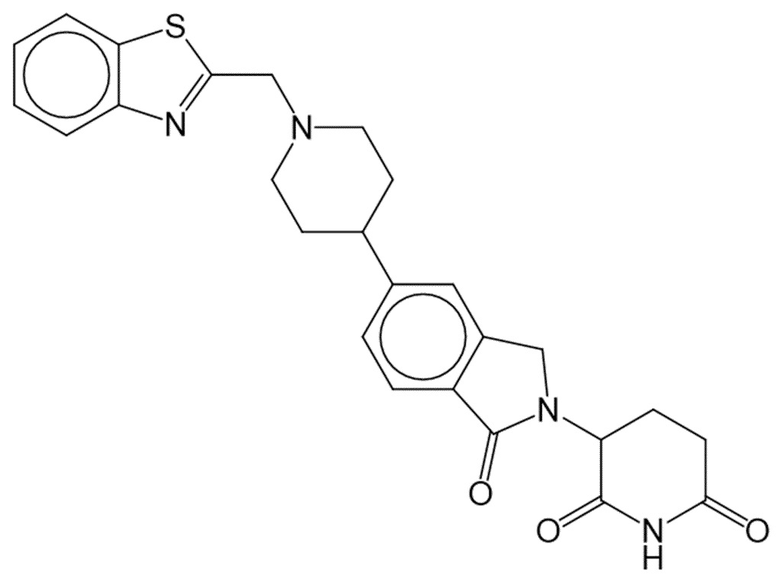


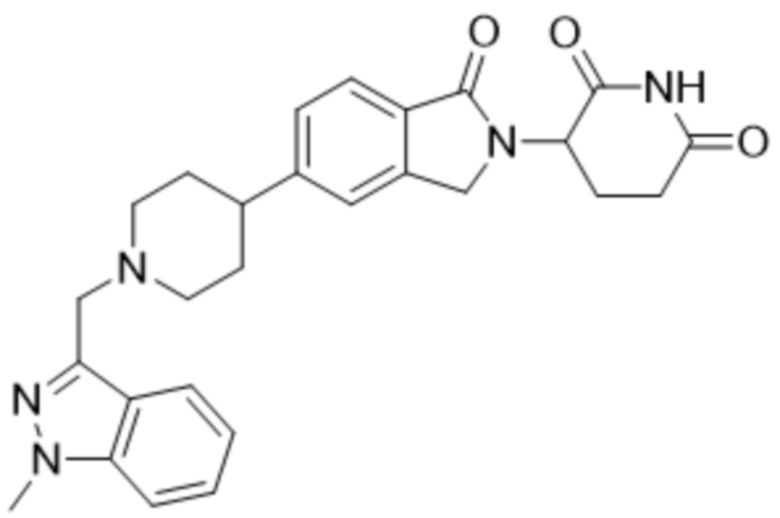
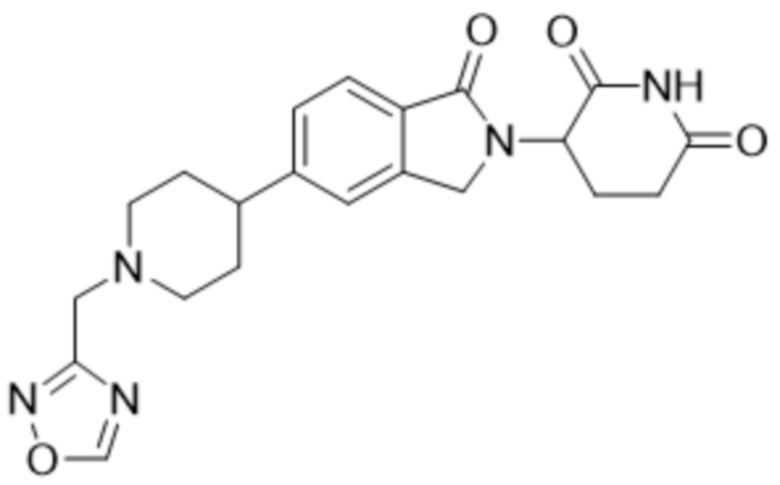
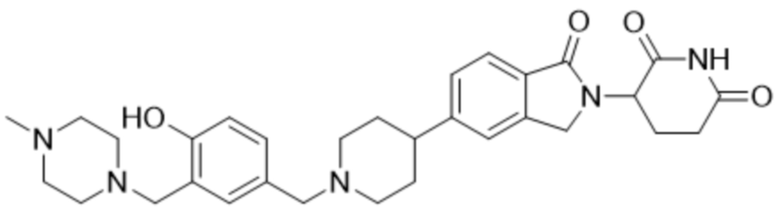

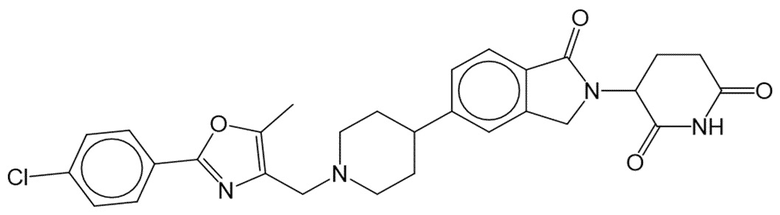

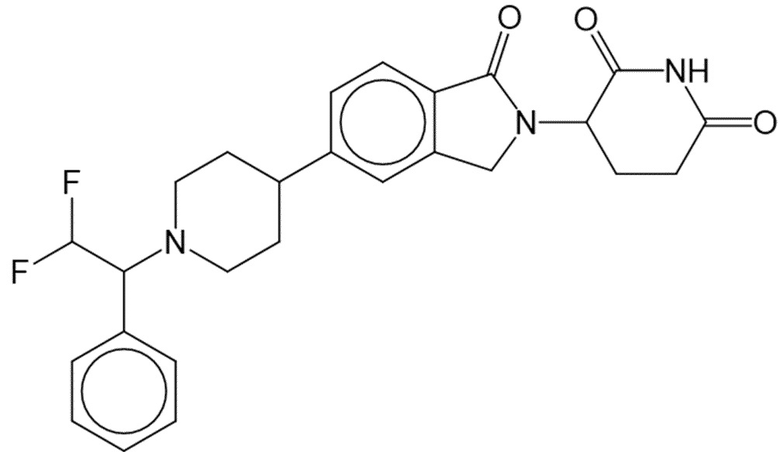

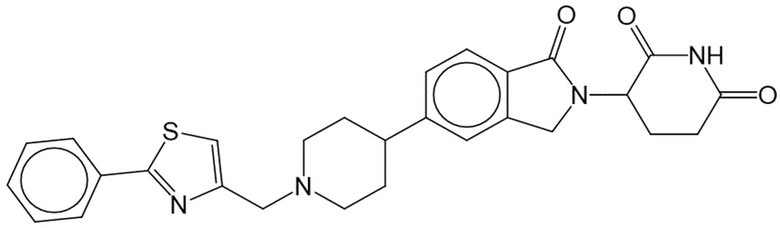
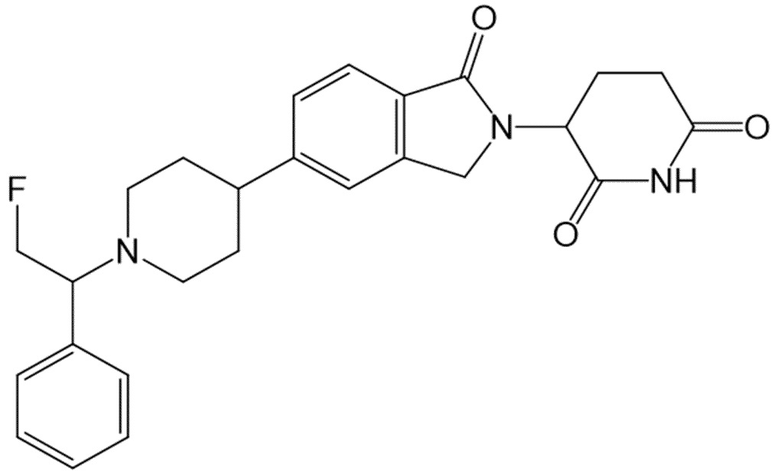

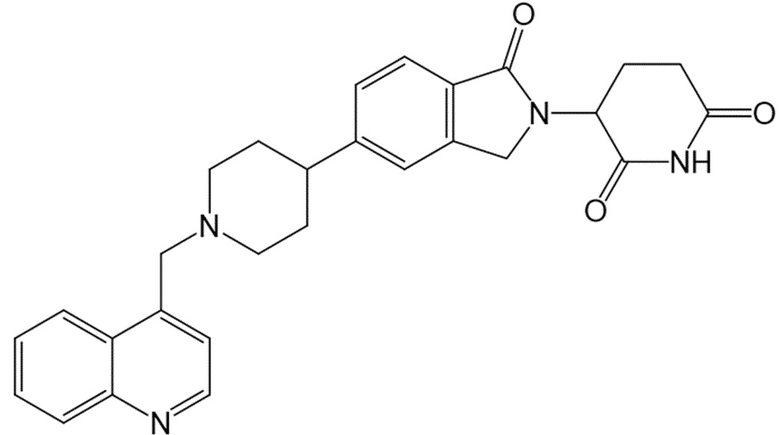


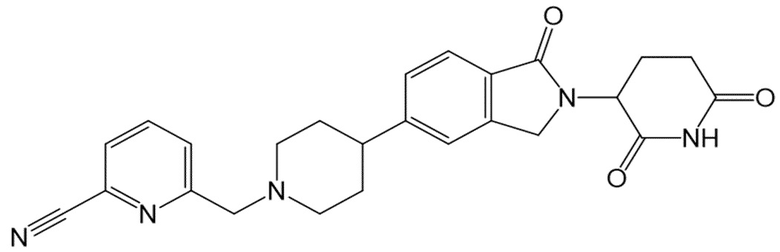

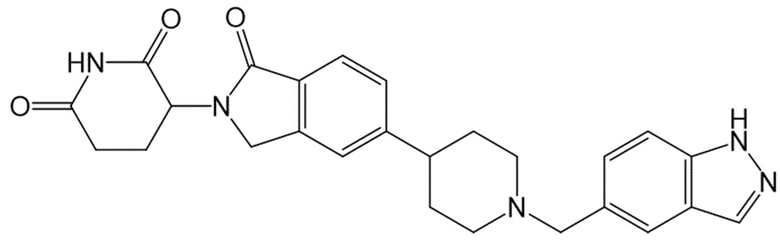
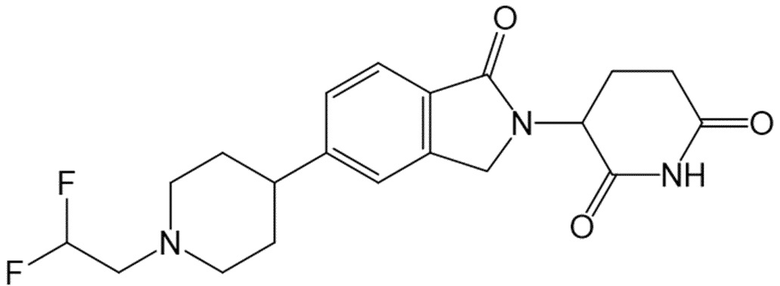
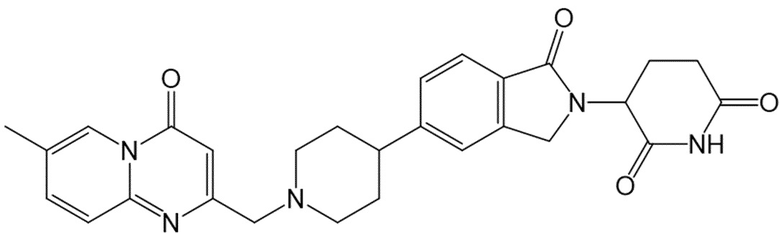
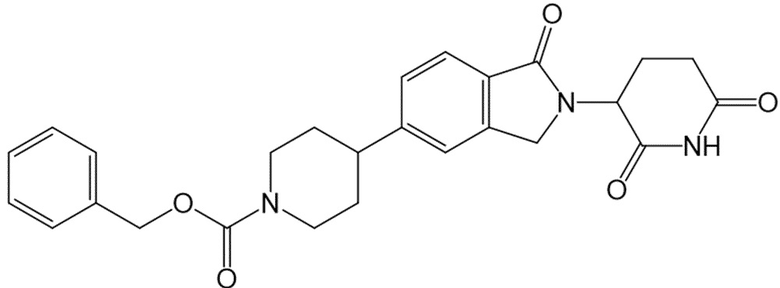
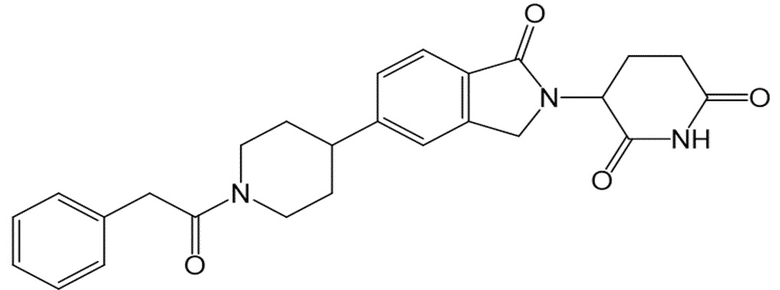
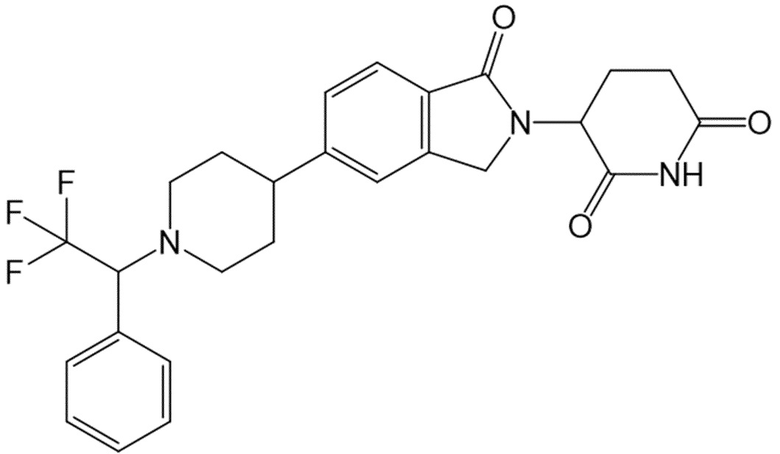
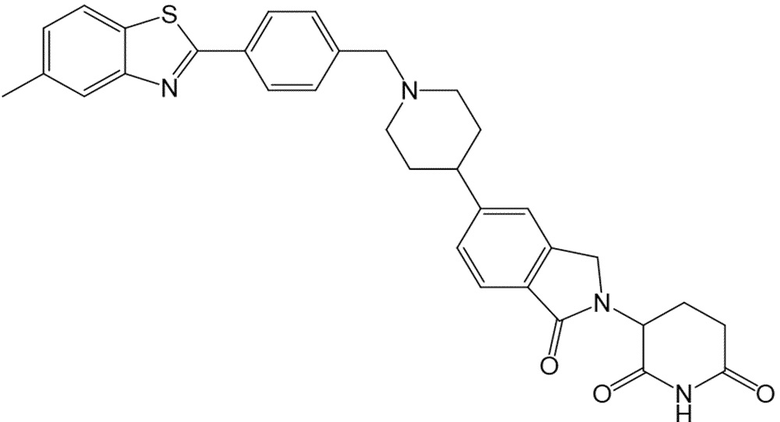
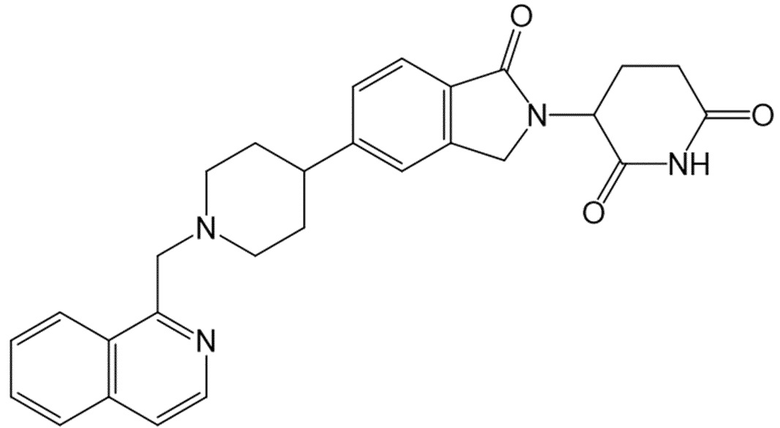
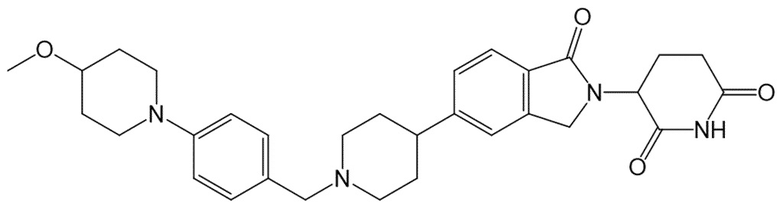
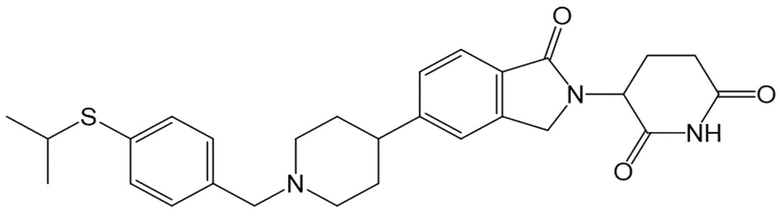
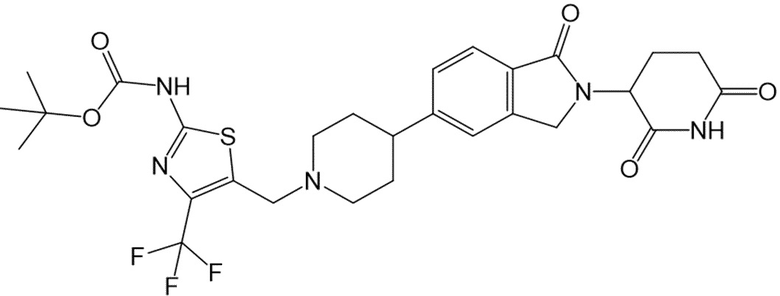
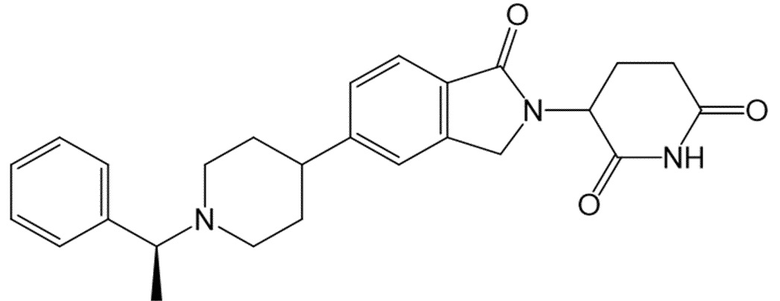


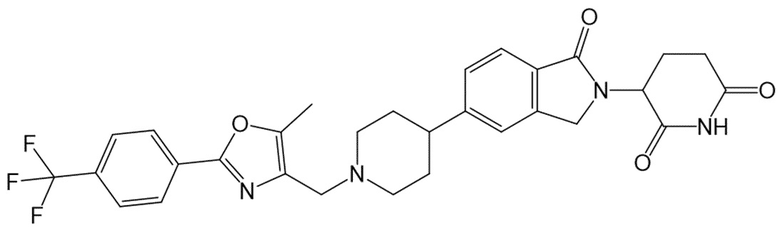

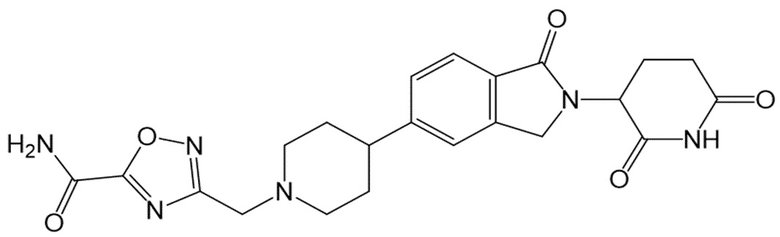


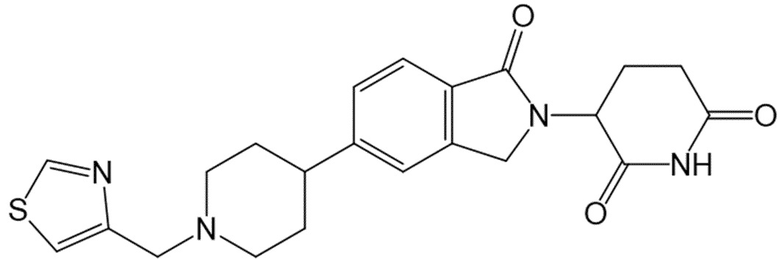
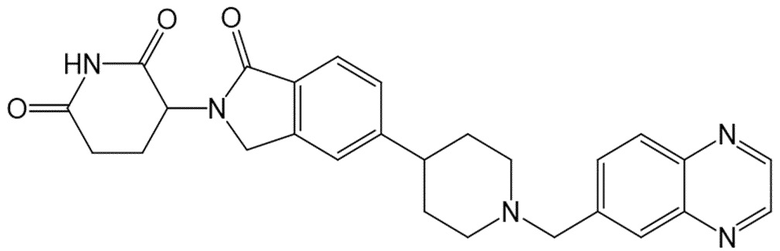


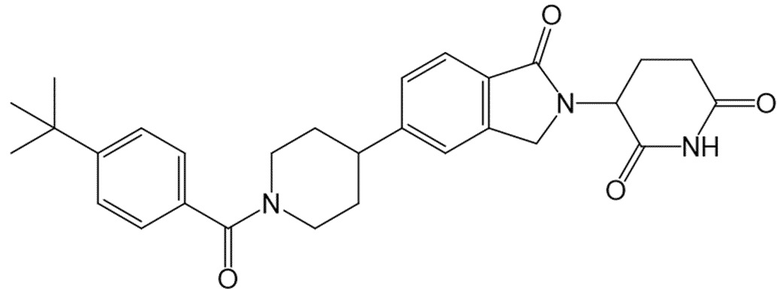


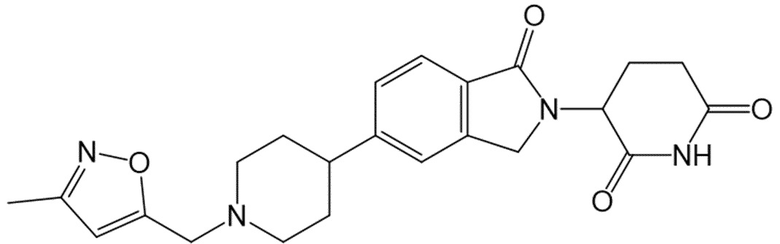
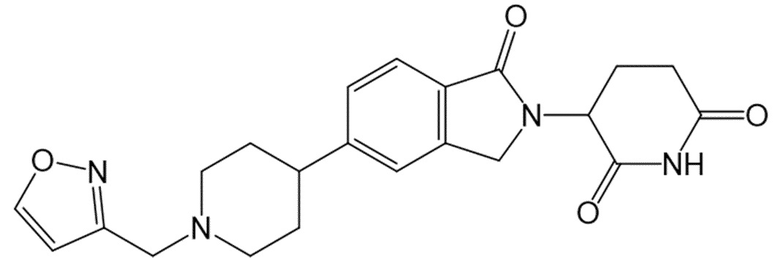



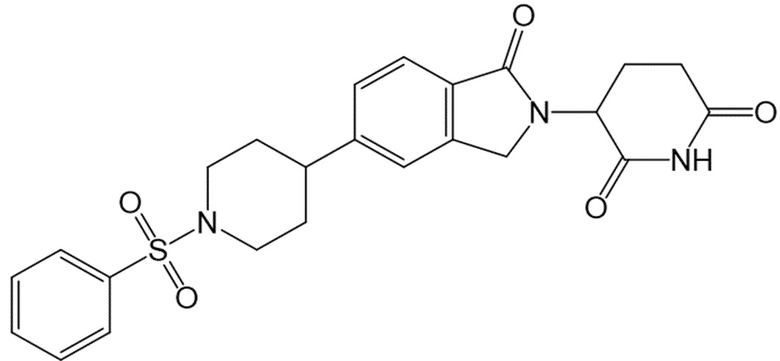
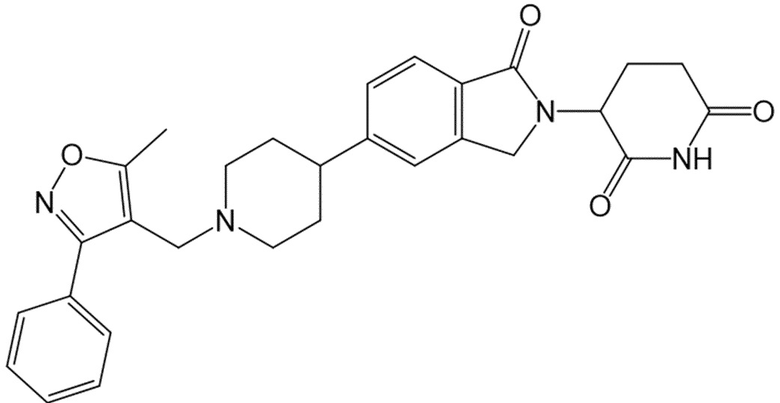
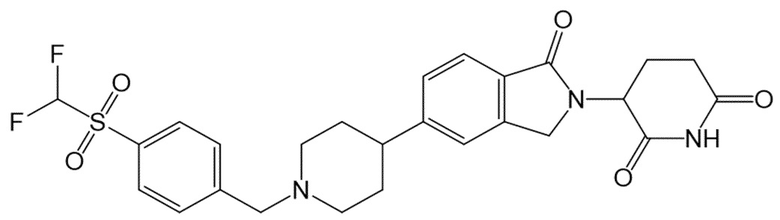

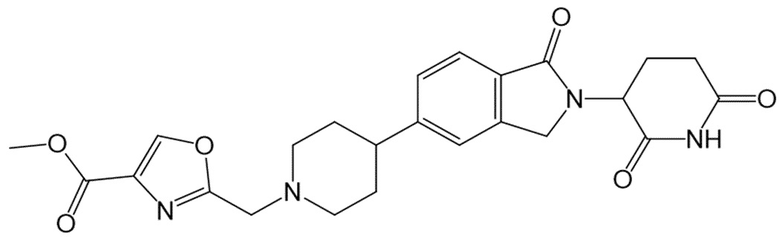
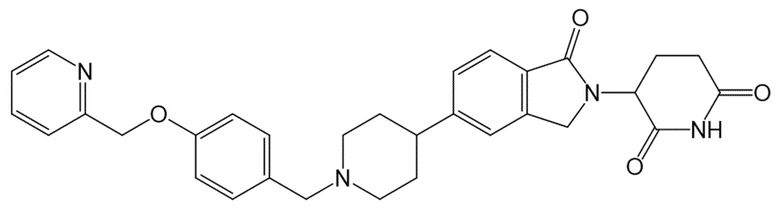
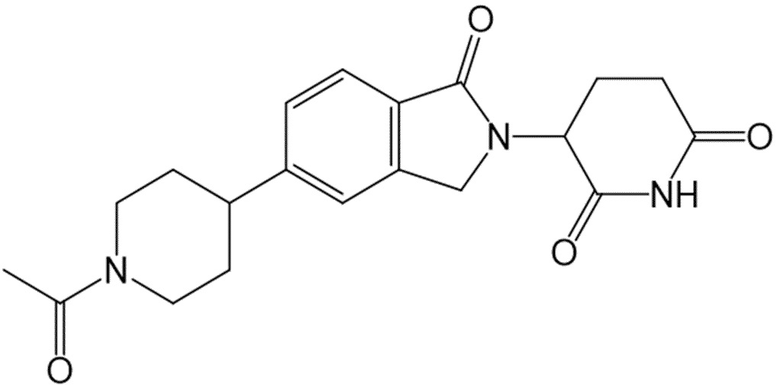
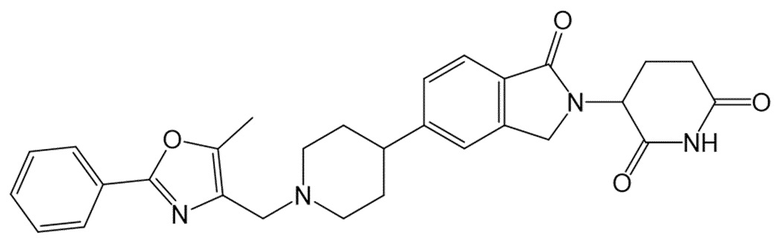
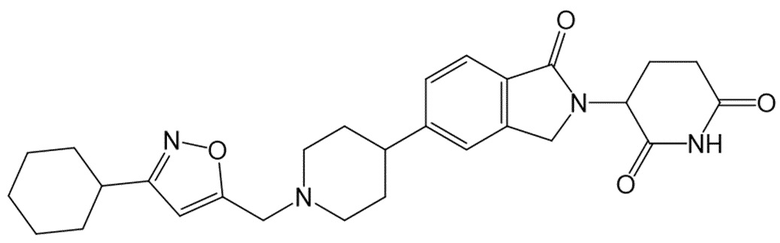
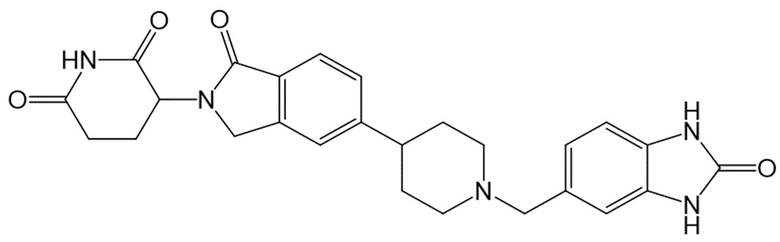


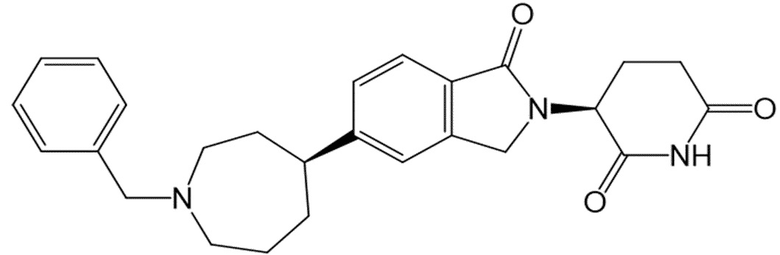
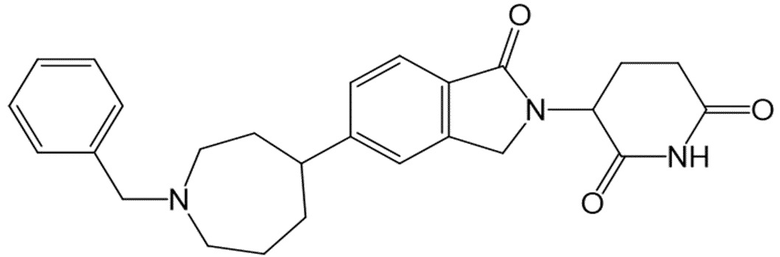
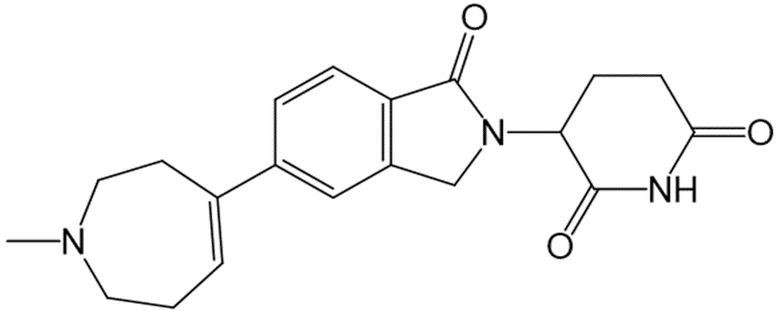
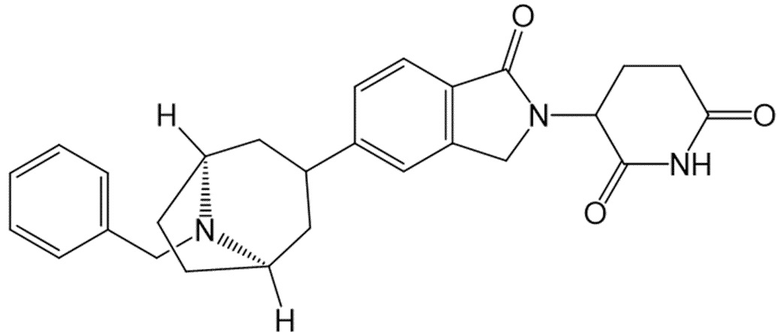

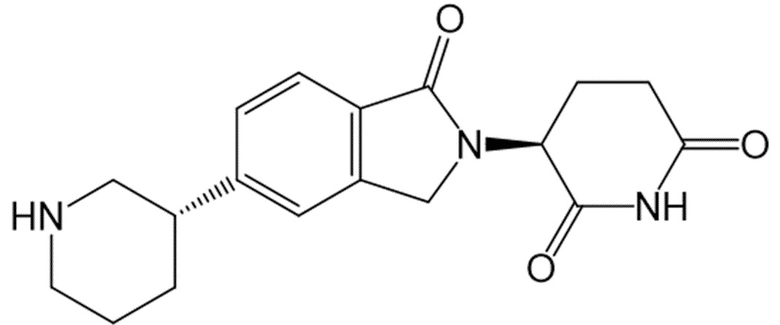

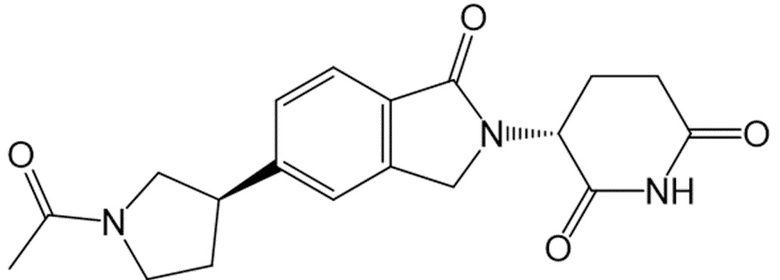
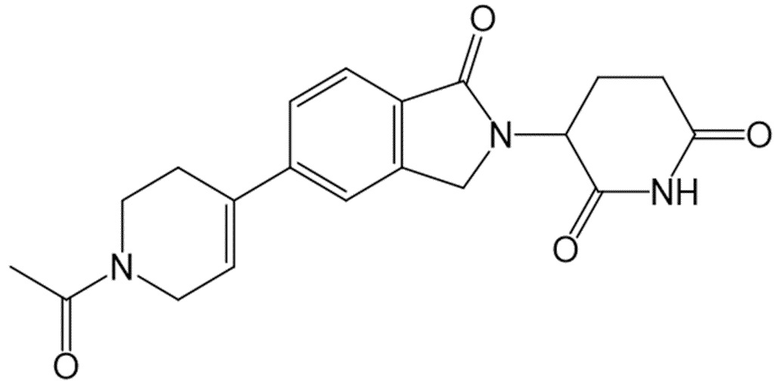
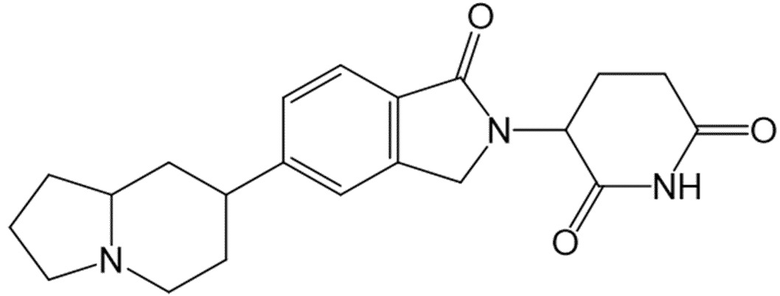
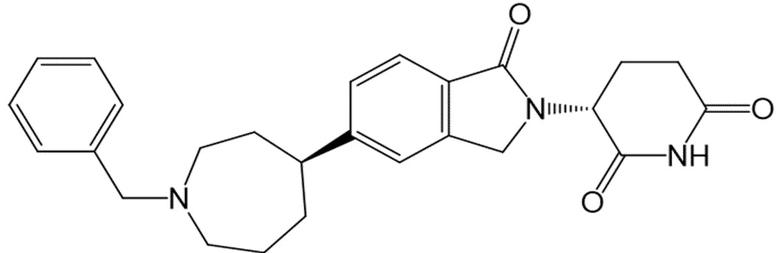



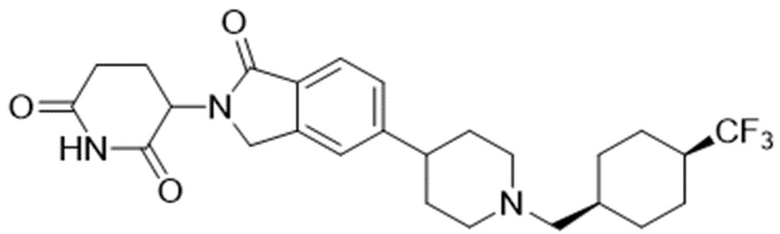

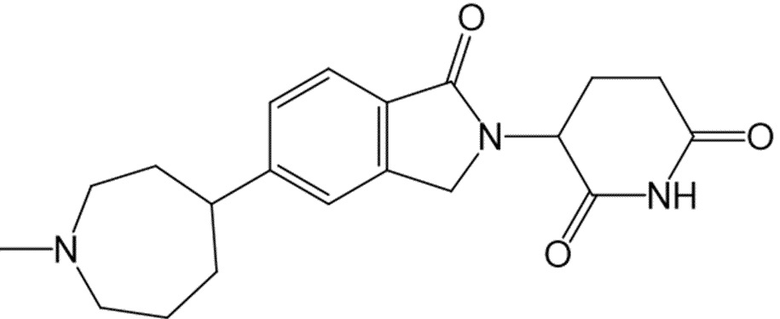
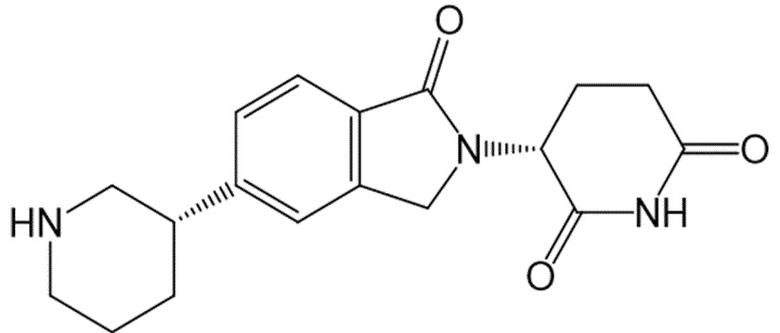
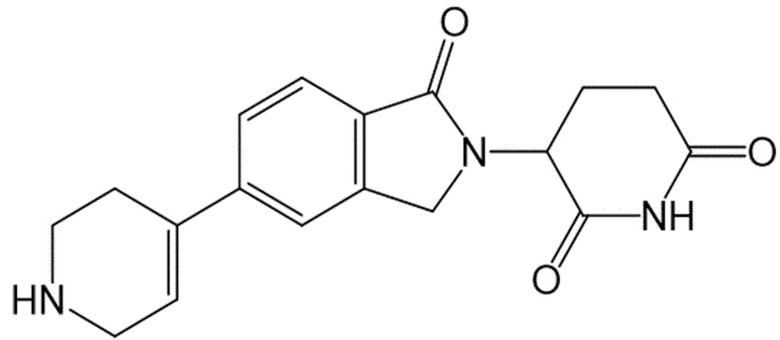


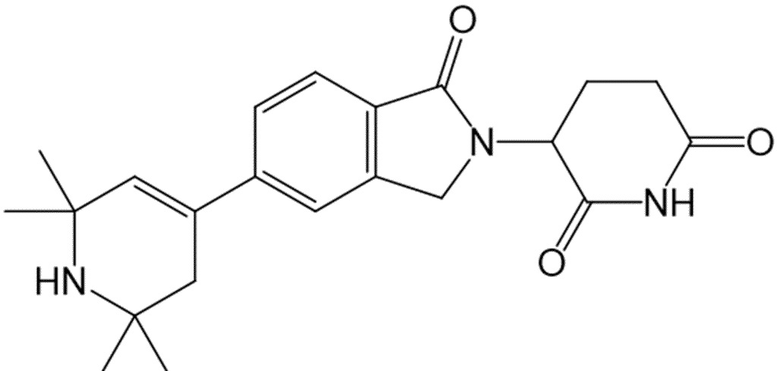

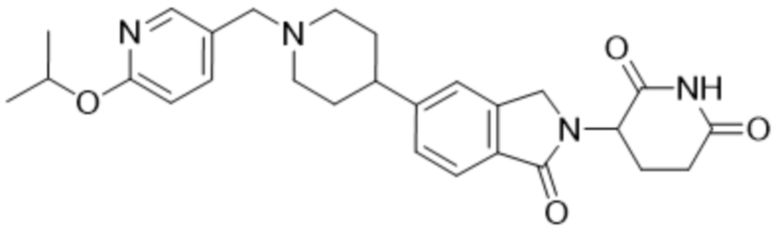
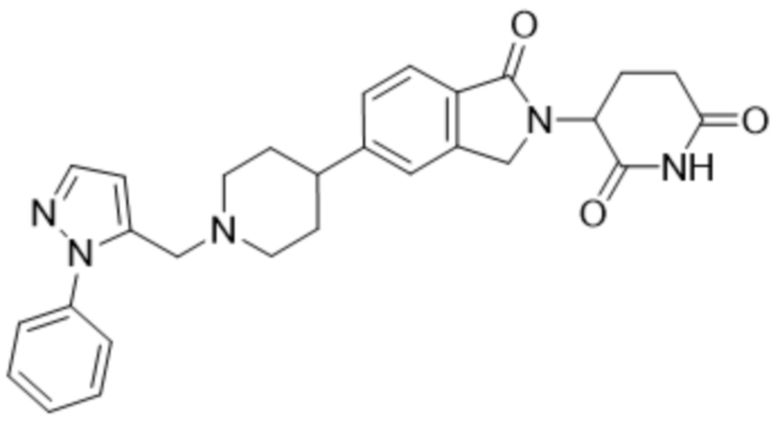
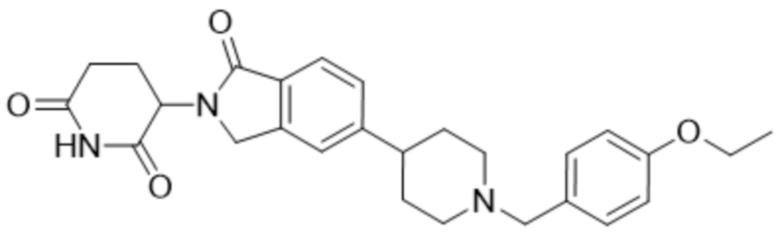



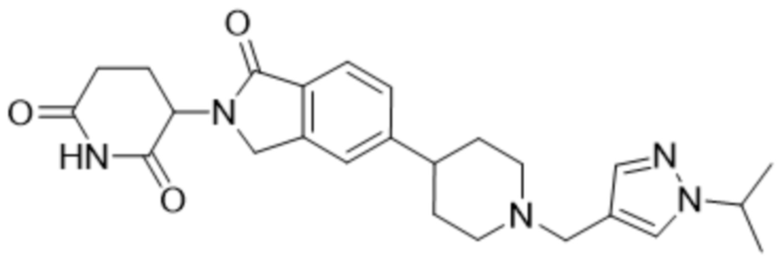
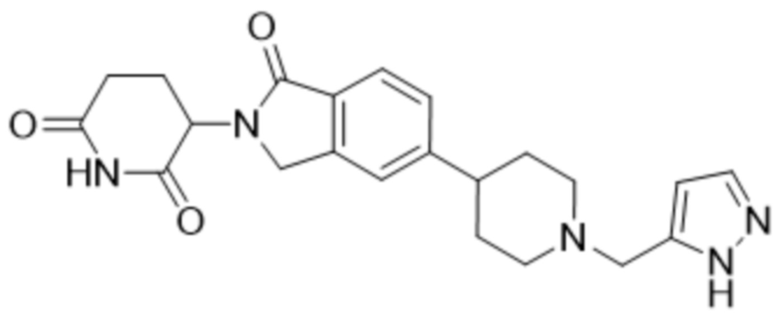
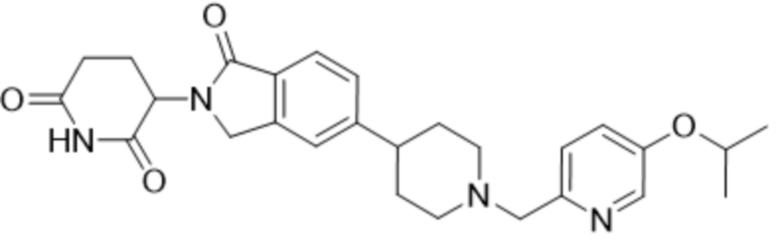

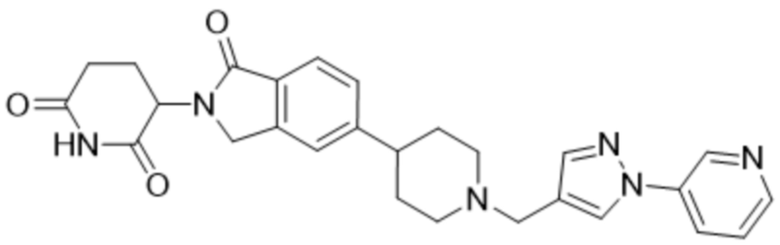

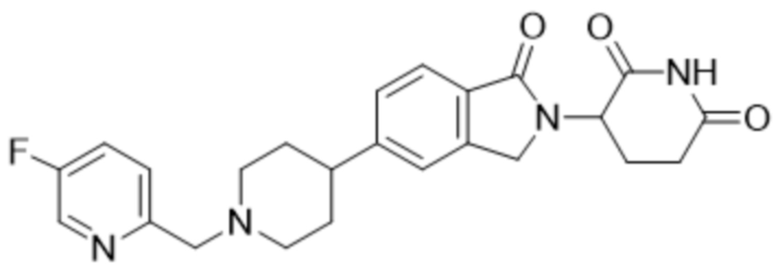

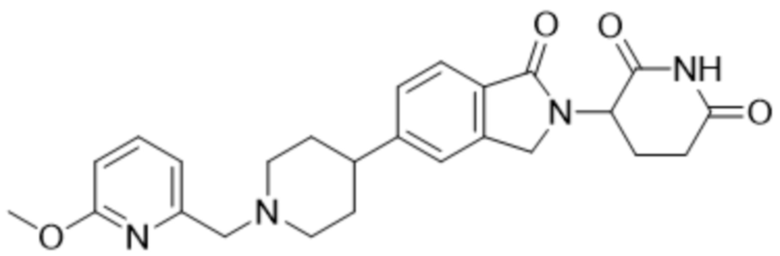

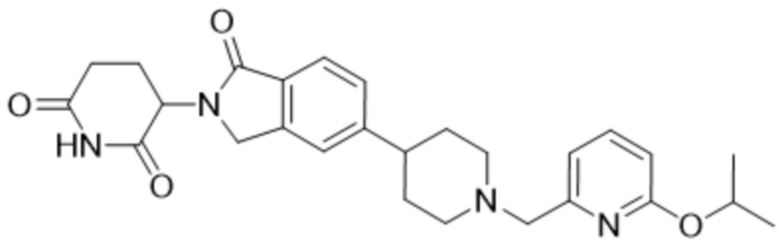
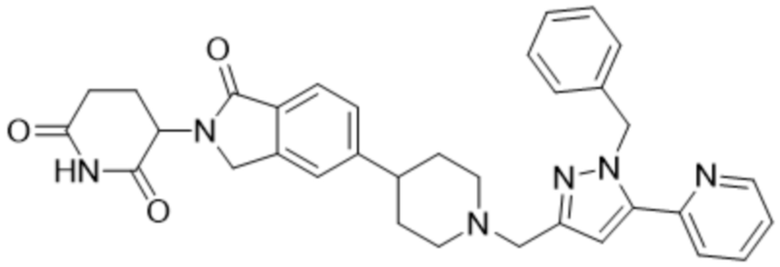
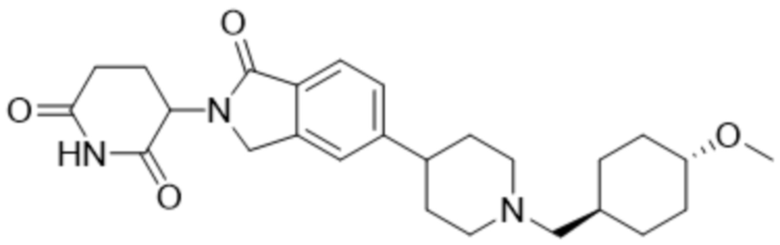
В другом аспекте, соединение деградации представляет собой соединение формулы (II):
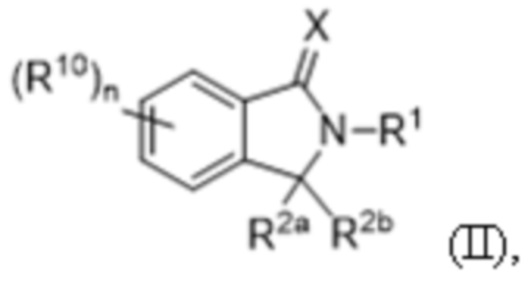
или его фармацевтически приемлемую соль, сложный эфир, гидрат, таутомер или пролекарство, где:
X представляет собой O или S;
R1 представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, карбоциклил, гетероциклил, арил или гетероарил, каждый из которых независимо и необязательно замещен одним или несколькими R4;
каждый из R2a и R2b независимо представляет собой водород или C1-C6алкил; или R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу или тиокарбонильную группу;
каждый из R10 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD), или -N (RC)S(O)xRE, или L-метку; где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или несколькими R11;
каждый R4 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, оксо, C(O)RA, -C(O)ORB, ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, S(O)xRE, -S(O)xN(RC)(RD), -N (RC)S(O)xRE, карбоциклил, гетероциклил, арил или гетероарил, где каждый алкил, алкенил, алкинил, гетероалкил, карбоциклил, гетероциклил, арил и гетероарил независимо и необязательно замещен одним или несколькими R7;
каждый из RA, RB, RC, RD и RE независимо представляет собой водород или C1-C6алкил;
каждый R11 независимо представляет собой C1-C6алкил, галоген, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, арил или гетероарил, где каждый арил и гетероарил независимо и необязательно замещен одним или несколькими R8;
каждый R7 независимо представляет собой галоген, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
каждый R8 независимо представляет собой C1-C6алкил, галоген, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
каждый L независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, -C(O)RA1, -C(O)ORB1, -ORB1, -N(RC1)(RD1), -C(O)N(RC1)(RD1), -N(RC1)C(O)RA1, -S(O)xRE1, -S(O)xN(RC1)(RD1) или -N (RC1)S(O)xRE1, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или несколькими R12;
каждая метка представляет собой нацеливающий фрагмент, способный к связыванию с белком-мишенью;
каждый из RA1, RB1, RC1, RD1, и RE1 независимо представляет собой водород, C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, карбоциклил, гетероциклил, арил или гетероарил, где каждый алкил, алкенил, алкинил, гетероалкил, карбоциклил, гетероциклил, арил и гетероарил независимо и необязательно замещен одним или несколькими R12;
каждый R12 независимо представляет собой C1-C6алкил, галоген, циано, карбоциклил или гетероциклил;
n составляет 0, 1, 2, 3 или 4; и
x составляет 0, 1 или 2.
В некоторых вариантах осуществления X представляет собой O.
В некоторых вариантах осуществления R1 представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, карбоциклил, гетероциклил, арил или гетероарил, каждый из которых независимо и необязательно замещен 1-12 R4 (например, 1 R4, 2 R4, 3 R4, 4 R4, 5 R4, 6 R4, 7 R4, 8 R4, 9 R4, 10 R4, 11 R4 или 12 R4). В некоторых вариантах осуществления R1 представляет собой C1-C6алкил или гетероциклил. В некоторых вариантах осуществления R1 представляет собой C1-C6алкил (например, метил или этил), замещенный R4. В некоторых вариантах осуществления R1 представляет собой C1-C6алкил (например, метил или этил), замещенный 1-6 R4. В некоторых вариантах осуществления R1 представляет собой гетероциклил. В некоторых вариантах осуществления R1 представляет собой 6-членный гетероциклил или 5-членный гетероциклил. В некоторых вариантах осуществления R1 представляет собой 6-членный гетероциклил или 5-членный гетероциклил, необязательно замещенный 1-6 R4 (например, 1 R4, 2 R4, 3 R4, 4 R4, 5 R4 или 6 R4). В некоторых вариантах осуществления R1 представляет собой азот-содержащий гетероциклил. В некоторых вариантах осуществления R1 представляет собой пиперидинил (например, пиперидин-2,6-дионил).
В некоторых вариантах осуществления каждый из R2a и R2b независимо представляет собой водород. В некоторых вариантах осуществления R2a и R2b вместе с углеродом, к которому они присоединены, образуют карбонильную группу.
В некоторых вариантах осуществления каждый R10 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD), или -N (RC)S(O)xRE, или L-метку; где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещены 1-12 R11 (например, 1 R11, 2 R11, 3 R11, 4 R11, 5 R11, 6 R11, 7 R11, 8 R11, 9 R11, 10 R11, 11 R11 или 12 R11). В некоторых вариантах осуществления R10 представляет собой C1-C6гетероалкил, -N(RC)(RD) или -N(RC)C(O)RA. В некоторых вариантах осуществления R10 представляет собой C1-C6гетероалкил (например, CH2NHC(O)CH2), -N(RC)(RD) (например, NH2) или -N(RC)C(O)RA (например, NHC(O)CH3).
В некоторых вариантах осуществления каждый R4 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, оксо, C(O)RA, -C(O)ORB, ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, S(O)xRE, -S(O)xN(RC)(RD), -N (RC)S(O)xRE, карбоциклил, гетероциклил, арил или гетероарил, где каждый алкил, алкенил, алкинил, гетероалкил, карбоциклил, гетероциклил, арил и гетероарил независимо и необязательно замещены 1-12 R7 (например, 1 R7, 2 R7, 3 R7, 4 R7, 5 R7, 6 R7, 7 R7, 8 R7, 9 R7, 10 R7, 11 R7 или 12 R7).
В некоторых вариантах осуществления каждый R11 независимо представляет собой C1-C6алкил, галоген, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, арил или гетероарил, где каждый арил и гетероарил независимо и необязательно замещен 1-6 R8 (например, 1 R8, 2 R8, 3 R8, 4 R8, 5 R8 или 6 R8).
В некоторых вариантах осуществления каждый L независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, -C(O)RA1, -C(O)ORB1, -ORB1, -N(RC1)(RD1), -C(O)N(RC1)(RD1), -N(RC1)C(O)RA1, -S(O)xRE1, -S(O)xN(RC1)(RD1) или -N (RC1)S(O)xRE1, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен 1-12 R12 (например, 1 R12, 2 R12, 3 R12, 4 R12, 5 R12, 6 R12, 7 R12, 8 R12, 9 R12, 10 R12, 11 R12 или 12 R12).
В некоторых вариантах осуществления каждый из RA1, RB1, RC1, RD1 и RE1 независимо представляет собой водород, C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, карбоциклил, гетероциклил, арил или гетероарил, где каждый алкил, алкенил, алкинил, гетероалкил, карбоциклил, гетероциклил, арил и гетероарил независимо и необязательно замещенный 1-12 R12 (например, 1 R12, 2 R12, 3 R12, 4 R12, 5 R12, 6 R12, 7 R12, 8 R12, 9 R12, 10 R12, 11 R12 или 12 R12).
В одном варианте осуществления X представляет собой O. В одном варианте осуществления R1 представляет собой гетероциклил (например, пиперидин-2,6-дионил). В одном варианте осуществления каждый из R2a и R2b независимо представляет собой водород. В одном варианте осуществления n составляет 1. В одном варианте осуществления R10 представляет собой -N(RC)(RD) (например, -NH2). В одном варианте осуществления соединение деградации содержит леналидомид, например, 3-(4-амино-1-оксоизоиндолин-2-ил)пиперидин-2,6-дион или его фармацевтически приемлемую соль. В одном варианте осуществления соединение деградации представляет собой леналидомид, например, соответствующий следующей формулой:
 .
.
В одном варианте осуществления X представляет собой O. В одном варианте осуществления R1 представляет собой гетероциклил (например, пиперидинил-2,6-дионил). В некоторых вариантах осуществления R2a и R2b вместе с углеродом, к которому они присоединены, образуют карбонильную группу. В одном варианте осуществления n составляет 1. В одном варианте осуществления R10 представляет собой -N(RC)(RD) (например, -NH2). В одном варианте осуществления соединение деградации содержит помалидомид, например, 4-амино-2-(2,6-диоксопиперидин-3-ил)изоиндолин-1,3-дион или его фармацевтически приемлемую соль. В одном варианте осуществления соединение деградации представляет собой помалидомид, например, соответствующий следующей формуле:
 .
.
В одном варианте осуществления X представляет собой O. В одном варианте осуществления R1 представляет собой гетероциклил (например, пиперидинил-2,6-дионил). В одном варианте осуществления R2a и R2b вместе с углеродом, к которому они присоединены, образуют карбонильную группу. В одном варианте осуществления n составляет 0. В одном варианте осуществления соединение деградации содержит талидомид, например, 2-(2,6-диоксопиперидин-3-ил)изоиндолин-1,3-дион или его фармацевтически приемлемую соль. В одном варианте осуществления продукт деградации представляет собой талидомид, например, соответствующий следующей формуле:
 .
.
В одном варианте осуществления X представляет собой O. В одном варианте осуществления R1 представляет собой гетероциклил (например, пиперидин-2,6-дионил). В одном варианте осуществления каждый из R2a и R2b независимо представляет собой водород. В одном варианте осуществления n составляет 1. В одном варианте осуществления R10 представляет собой C1-C6гетероалкил (например, CH2NHC(O)CH2-фенил-трет-бутил). В одном варианте осуществления соединение деградации содержит 2-(4-(трет-бутил)фенил)-N-((2-(2,6-диоксопиперидин-3-ил)-1-оксоизоиндолин-5-ил)метил)ацетамид или его фармацевтически приемлемую соль. В одном варианте осуществления соединение деградации характеризуется структурой, представленной следующей формулой:
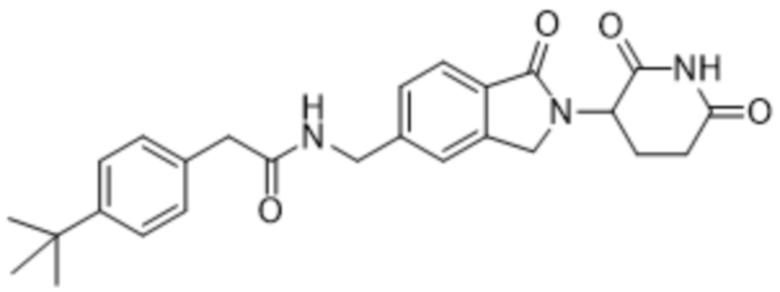 .
.
В некоторых вариантах осуществления соединение деградации (например, соединение формулы (II)) не присоединено к линкеру или группе присоединения. В некоторых вариантах осуществления соединение деградации (например, соединение формулы (II)) не содержит другой фрагмент, например, лиганд, нацеливающее средство или фрагмент, способный к димеризации. В некоторых вариантах осуществления R10 не представляет собой L-метку.
В некоторых вариантах осуществления соединение деградации (например, соединение формулы (II)) присоединено к линкеру или группе присоединения (например, по меньшей мере один R10 представляет собой L-метку). В некоторых вариантах осуществления соединение деградации (например, соединение формулы (II)) содержит другой фрагмент, например, лиганд, нацеливающее средство или фрагмент, способный к димеризации. В некоторых вариантах осуществления R10 представляет собой L-метку, и L представляет собой алкил или гетероалкил (например, PEG-цепь). В некоторых вариантах осуществления L представляет собой линкер, выбранный из линкера, раскрытого в публикации международной патентной заявки № WO2017/024318 (например, фигуры 28-31).
В некоторых вариантах осуществления R10 представляет собой L-метку, а метка представляет собой нацеливающий фрагмент, который способен к связыванию или связан с белком-мишенью. Метка может содержать низкомолекулярное соединение или аминокислотную последовательность (например, пептид или полипептид). В некоторых вариантах осуществления метка представляет собой ингибитор киназы, ингибитор бромодомен-содержащего белка, семейства BET, лиганд цитозольного сигнального белка FKBP12, ингибитор HDAC, ингибитор лизинметилтрансферазы, ингибитор ангиогенеза, иммуносупрессорное соединение или ингибитор арилуглеводородного рецептора (AHR).
В определенных вариантах осуществления метка представляет собой SERM (селективный модулятор эстрогенового рецептора) или SERD (селективный деструктор эстрогенового рецептора). Неограничивающие примеры SERM и SERD представлены в публикациях международных патентных заявок №№ WO2014/191726, WO2013/090921, WO2014/203129, WO2014/205136, WO2014/205138 и WO 2014/203132; публикациях заявок на патент США №№ US2013/0178445 и US 2015/0005286; и патентах США №№ 9078871, 8853423 и 8703810.
Дополнительные метки включают, например, любой фрагмент, который связывается с эндогенным белком (связывается с белком-мишенью). Иллюстративные метки включают, среди всего прочего, ингибиторы Hsp90, ингибиторы киназ, ингибиторы HDM2 и MDM2, соединения, нацеливающиеся на бромодомен-содержащие белки человека семейства BET, ингибиторы HDAC, ингибиторы лизинметилтрансферазы человека, ингибиторы ангиогенеза, соединения, представляющие собой ядерные рецепторы гормонов, иммуносупрессорные соединения и соединения, нацеливающиеся на арилуглеводородный рецептор (AHR). Такие низкомолекулярные метки также включают фармацевтически приемлемые соли, энантиомеры, сольваты и полиморфы таких композиций, а также другие малые молекулы, которые могут связываться с представляющим интерес белком-мишенью.
В одном варианте осуществления метка представляет собой лиганд 5F6D, нацеливающийся на Ubc9 SUMO-лигазу E2, например, описанный в Hewitt, W.M., et. al. (2016) Angew.Chem.Int.Ed.Engl.55: 5703-5707.
В одном варианте осуществления метка представляет собой лиганд, нацеливающийся на Tank1, например, описанный в Kirby, C.A. et al, (2012) Acta Crystallogr. Sect.F 68: 115-118; и Shultz, M.D., et al. (2013) J.Med.Chem.56: 7049-7059.
В одном варианте осуществления метка представляет собой SH2-домен лиганда, нацеливающегося на pp60 Src, например, описанный в Gudrun Lange, et al., (2003) J. Med. Chem. 46, 5184-5195.
В одном варианте осуществления метка представляет собой лиганд, нацеливающийся на Sec7-домен, например, описанный в Huta, B.P., et al., (2016) Chemmedchem 11: 277.
В одном варианте осуществления метка представляет собой лиганд, нацеливающийся на сапозин-B, например, описанный в I. Nemcovicova and D. M. Zajonc Acta Cryst. (2014). D70, 851-862.
В одном варианте осуществления метка представляет собой лиганд, нацеливающийся на белок S100-A7 2OWS, например, описанный в Leon, R., Murray, et al., (2009) Biochemistry 48: 10591-10600.
В одном варианте осуществления метка представляет собой лиганд, нацеливающийся на фосфолипазу A2, например, описанный в Schevitz, R.W., et al., (1995) Nat. Struct. Biol. 2, 458-465.
В одном варианте осуществления метка представляет собой лиганд, нацеливающийся на PHIP, например, описанный в Krojer, T.; et al. Chem. Sci.2016, 7, 2322-2330.
В одном варианте осуществления метка представляет собой лиганд, нацеливающийся на PDZ, например, описанный в Mangesh Joshi, et al. Angew. Chem. Int. Ed. (2006) 45, 3790-3795.
В одном варианте осуществления метка представляет собой лиганд, нацеливающийся на PARP15, например, описанный в Karlberg, T., et al., (2015) J.Biol.Chem.290: 7336-7344.
В одном варианте осуществления метка представляет собой лиганд, нацеливающийся на PARP14, например, описанный в Andersson, C.D., et al.,(2012) J.Med.Chem. 55: 7706-7718.; Wahlberg, E., et al. (2012) Nat.Biotechnol. 30: 283-288.; Andersson, C.D., et al. (2012) J.Med.Chem.55: 7706-7718.
В одном варианте осуществления метка представляет собой лиганд, нацеливающийся на MTH1, например, описанный в Helge Gad, et. al. Nature, (2014) 508, 215-221.
В одном варианте осуществления метка представляет собой лиганд, нацеливающийся на mPGES-1, например, описанный в Luz, J.G., et al., (2015) J.Med.Chem.58: 4727-4737.
В одном варианте осуществления метка представляет собой лиганд, нацеливающийся на FLAP-5-липоксигеназа-активирующий белок, например, описанный в Ferguson, A.D., et al (2007) Science 317: 510-512.
В одном варианте осуществления метка представляет собой лиганд, нацеливающийся на FA-связывающий белок, например, описанный в Kuhn, B.; et al. J. Med. Chem. (2016) 59, 4087-4102.
В одном варианте осуществления метка представляет собой лиганд, нацеливающийся на BCL2, например, описанный в Souers, A.J., et al. (2013) Nat Med 19: 202-208.
В одном варианте осуществления метка представляет собой какие-либо малую молекулу или белок, которые могут связываться с белком-мишенью, и при этом на белок-мишень воздействует убиквитинлигаза и приводит к его деградации. В некоторых вариантах осуществления метка представляет собой лиганд, нацеливающийся на dTAG, раскрытый в публикации международной патентной заявки № WO2017/024318 (например, таблица T, страницы 119-129).
Когда R10 представляет собой L-метку, метка способна к связыванию или соединению с белком-мишенью. Иллюстративные белки-мишени включают FK506-связывающий белок-12 (FKBP12), бромодомен-содержащий белок 4 (BRD4), CREB-связывающий белок (CREBBP) или транскрипционный активатор BRG1 (SMARCA4). В некоторых вариантах осуществления белок-мишень содержит рецептор гормона, например, белок эстрогенового рецептора, белок андрогенового рецептора, белок ретиноидного X рецептора (RXR) или дигидрофолатредуктазу (DHFR), в том числе бактериальную DHFR. В некоторых вариантах осуществления белок-мишень содержит аминокислотную последовательность, полученную из бактериальной дегалогеназы. В других вариантах осуществления белок-мишень содержит аминокислотные последовательности, полученные из 7,8-дигидро-8-оксогуанинтрифосфатазы, AFAD, белка, активирующего арахидонат-5-липоксигеназу, аполипобелка, ASH1L, ATAD2, белка-2, содержащего бакуловирусный IAP-повтор, BAZ1A, BAZ1B, BAZ2A, BAZ2B, Bcl-2, Bcl-xL, BRD1, BRD2, BRD3, BRD4, BRD5, BRD6, BRD7, BRD8, BRD9, BRD10, BRDT, BRPF1, BRPF3, BRWD3, CD209, CECR2, CREBBP, E3-лигаза XIAP, EP300, FALZ, белка-4, связывающего жирные кислоты, из адипоцитов (FABP4), GCN5L2, GTPазы k-RAS, HDAC6, гемопоэтической простагландин-D-синтазы, KIAA1240, лактоилглутатионлиазы, LOC93349, Mcl-1, MLL, PA2GA, PB1, PCAF, белка-1 пептидил-пролил-цис-транс изомеразы, взаимодействующего с NIMA, PHIP, поли-АДФ-рибозаполимеразы-14, поли-АДФ-рибозаполимеразы-15, PRKCBP1, просапозина, простагландин-E-синтазы, дельта-субъединицы cGMP 3','5-циклической фосфодиэстеразы, чувствительной к родопсину палочек сетчатки, S100-A7, SMARCA2, SMARCA4, SP100, SP110, SP140, Src, Sumo-конъюгирующего фермента UBC9, супероксиддисмутазы, TAF1, TAF1L, танкиразы-1, танкиразы-2, TIF1a, TRIM28, TRIM33, TRIM66, WDR9, ZMYND11 или MLL4. В других вариантах осуществления белок-мишень содержит аминокислотную последовательность, полученную из MDM2. В некоторых вариантах осуществления белок-мишень представляет собой dTAG, раскрытый в публикации международной патентной заявки № WO2017/024318 (например, страницы 112-114).
В одном варианте осуществления белок-мишень получен из BRD2, BRD3, BRD4 или BRDT. В одном варианте осуществления белок-мишень представляет собой модифицированный или мутантный белок BRD2, BRD3, BRD4 или BRDT. В определенных вариантах осуществления одна или несколько мутаций BRD2 включают мутацию триптофана (W) в аминокислотном положении 97, мутацию валина (V) в аминокислотном положении 103, мутацию лейцина (L) в аминокислотном положении 110, мутацию W в аминокислотном положении 370, мутацию V в аминокислотном положении 376 или мутацию L в аминокислотном положении 381.
В одном варианте осуществления белок-мишень получен из цитозольного сигнального белка FKBP12. В определенных вариантах осуществления белок-мишень представляет собой модифицированный или мутантный цитозольный сигнальный белок FKBP12. В определенных вариантах осуществления модифицированный или мутантный цитозольный сигнальный белок FKBP12 содержит одну или несколько мутаций, которые создают увеличенный карман связывания для лигандов FKBP12. В определенных вариантах осуществления одна или несколько мутаций включают мутацию фенилаланина (F) в аминокислотном положении 36 на валин (V) (F36V) (обозначаемую взаимозаменяемо в данном документе как FKBP12* или FKBP*).
В некоторых вариантах осуществления соединение деградации представляет собой соединение, раскрытое в патенте США № 7973057; патенте США № 8546430; патенте США № 8716315; публикации международной патентной заявки № WO2017/059062 или публикации международной патентной заявки № WO2017/024318; каждый из которых включен в данный документ посредством ссылки во всей своей полноте.
Гетерологичные полипептиды
В данном документе представлены слитые полипептиды, включающие COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид и представляющий интерес гетерологичный полипептид. В некоторых вариантах осуществления COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид и гетерологичный полипептид отделены линкером (например, глицин-сериновым линкером). В некоторых вариантах осуществления слитый полипептид, описанный в данном документе, содержит три элемента: COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид (например, часть аминокислотной последовательности дегрона, описанного в данном документе), гетерологичный полипептид и линкер, разделяющий COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид и гетерологичный полипептид. В других вариантах осуществления слитый полипептид, описанный в данном документе, содержит два элемента: COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид (например, часть аминокислотной последовательности дегрона, например, описанного в данном документе), связанный непосредственно с гетерологичным полипептидом. Такие элементы могут быть организованы таким образом, что COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид (например, часть аминокислотной последовательности дегрона, например, описанного в данном документе) расположен на N-конце представляющего интерес гетерологичного полипептида, на C-конце представляющего интерес гетерологичного полипептида или по центру представляющего интерес гетерологичного полипептида. В одном варианте осуществления гетерологичный полипептид представляет собой цитозольный и/или ядерный белок, и COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид расположен на N-конце гетерологичного полипептида. В одном варианте осуществления гетерологичный полипептид представляет собой трансмембранный белок, и COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид расположен на C-конце гетерологичного полипептида.
В некоторых вариантах осуществления слитый полипептид дополнительно содержит домен деградации. В некоторых вариантах осуществления домен деградации отделен от COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающего полипептида и гетерологичного полипептида гетерологичным сайтом расщепления протеазами.
Слитые полипептиды, раскрытые в данном документе, могут содержать любой представляющий интерес гетерологичный полипептид. В некоторых вариантах осуществления гетерологичный полипептид может представлять собой трансмембранный белок (например, трансмембранный рецептор). В определенных вариантах осуществления представляющий интерес гетерологичный полипептид может представлять собой, например, рецептор, связанный с ионными каналами, рецептор, связанный с ферментом (например, рецепторную тирозинкиназу, рецептор, ассоциированный с тирозинкиназой, рецептороподобную тирозинфосфатазу, рецепторную серин/треонинкиназу; рецепторную гуанилилциклазу и рецептор, ассоциированный с гистидинкиназой), или рецептор, сопряженный с G-белком. В некоторых вариантах осуществления трансмембранный белок представляет собой химерный антигенный рецептор, например, описанный в данном документе.
В другом варианте осуществления гетерологичный полипептид представляет собой секретируемый белок (например, малый секретируемый белок). В некоторых вариантах осуществления гетерологичный полипептид может представлять собой, например, антитело, нанотело или белок-связывающую молекулу при производстве в клетке. В некоторых вариантах осуществления гетерологичный полипептид может представлять собой терапевтический или клинический белок (например, инсулин, гормон роста, эритропоэтин или терапевтическое антитело). В определенных вариантах осуществления белок может быть токсичным для клетки при производстве (например, бактериальные токсины и протеазы).
В таблицу 2 включен перечень иллюстративных гетерологичных полипептидов для применения в слитых полипептидах, раскрытых в данном документе. Дополнительный представляющий интерес гетерологичный полипептид включает химерные антигенные T-клеточные рецепторы, описанные в разделе ниже.
(например, каспаза-9)
(например, противоопухолевый пептид или белковый гормон)
Антигенсвязывающий домен CAR
В одном аспекте CAR по настоящему изобретению, связанный с COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающим полипептидом и/или доменом деградации, содержит мишень-специфический связывающий элемент, иначе обозначаемый как антигенсвязывающий домен. В одном варианте осуществления часть CAR, содержащая антигенсвязывающий домен, содержит антигенсвязывающий домен, который нацеливается, например, специфически связывается, на антиген, например, антиген, описанный в данном документе, например, CD19. В одном варианте осуществления антигенсвязывающий домен нацеливается на CD19 человека, например, специфически связывается с ним.
В некоторых вариантах осуществления гетерологичный полипептид, связанный с COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающим полипептидом и/или доменом деградации, содержит химерный антигенный рецептор (CAR). В некоторых вариантах осуществления CAR содержит антигенсвязывающий домен (например, антитело или фрагмент антитела, TCR или фрагмент TCR), который связывается с опухолевым антигеном, трансмембранный домен и внутриклеточный сигнальный домен (например, внутриклеточный сигнальный домен, содержащий костимулирующий домен) и/или первичный сигнальный домен. Конструкции нуклеиновой кислоты для CAR, кодируемые ими белки, содержащие их векторы, клетки-хозяева, фармацевтические композиции и способы введения и лечения, связанные с настоящим изобретением раскрыты подробно в публикации международной патентной заявки № WO2015142675, которая включена посредством ссылки во всей своей полноте.
В некоторых вариантах осуществления гетерологичный полипептид представляет собой химерный антигенный рецептор (CAR), где CAR содержит антигенсвязывающий домен (например, антитело или фрагмент антитела, TCR или фрагмент TCR), который связывается с опухолеподдерживающим антигеном (например, опухолеподдерживающим антигеном, описанным в данном документе), трансмембранный домен (например, трансмембранный домен, описанный в данном документе) и внутриклеточный сигнальный домен (например, внутриклеточный сигнальный домен, описанный в данном документе) (например, внутриклеточный сигнальный домен, содержащий костимулирующий домен (например, костимулирующий домен, описанный в данном документе) и/или первичный сигнальный домен (например, первичный сигнальный домен, описанный в данном документе). В некоторых вариантах осуществления опухолеподдерживающий антиген представляет собой антиген, присутствующий на стромальной клетке или супрессорной клетке миелоидного происхождения (MDSC). В других аспектах настоящего изобретения описаны полипептиды, кодируемые такими нуклеиновыми кислотами, и клетки-хозяева, содержащие такие нуклеиновые кислоты и/или полипептиды.
В некоторых вариантах осуществления молекула CAR содержит по меньшей мере один внутриклеточный сигнальный домен, выбранный из сигнального домена CD137 (4-1BB), сигнального домена CD28, сигнального домена CD27, сигнального домена ICOS, сигнального домена CD3-дзета или любой их комбинации. В некоторых вариантах осуществления молекула CAR содержит по меньшей мере один внутриклеточный сигнальный домен, выбранный из одной или нескольких костимулирующих молекул, выбранных из CD137 (4-1BB), CD28, CD27 или ICOS.
В некоторых вариантах осуществления совокупность иммунных эффекторных клеток, например, популяция, истощенная по T-регуляторным клеткам, содержит нуклеиновую кислоту, кодирующую CAR, который содержит мишень-специфический связывающий элемент, иначе называемый антигенсвязывающим доменом. Выбор связывающего элемента зависит от типа и количества лигандов, которые определяют поверхность клетки-мишени. Например, антигенсвязывающий домен может быть выбран таким образом, чтобы он распознавал лиганд, который выступает в качестве маркера клеточной поверхности на клетках-мишенях, ассоциированных с конкретным болезненным состоянием. Таким образом, примеры маркеров клеточной поверхности, которые могут выступать в качестве лигандов для антигенсвязывающего домена в CAR, описанного в данном документе, включают маркеры, ассоциированные с вирусными, бактериальными и паразитарными инфекциями, аутоиммунным заболеванием и раковыми клетками.
Последовательности для неограничивающих примеров различных компонентов, которые могут быть частью молекулы CAR, например, CAR для TA или CAR для BCA, описанной в данном документе, перечислены в таблице 3, где "а. к." обозначает аминокислотные последовательности, а "н. к." обозначает последовательности нуклеиновых кислот, которые кодируют соответствующий пептид.
В одном аспекте иллюстративные конструкции CAR содержат необязательную лидерную последовательность (например, лидерную последовательность, описанную в данном документе), внеклеточный антигенсвязывающий домен (например, антигенсвязывающий домен, описанный в данном документе), шарнирную область (например, шарнирную область, описанную в данном документе), трансмембранный домен (например, трансмембранный домен, описанный в данном документе) и внутриклеточный стимулирующий домен (например, внутриклеточный стимулирующий домен, описанный в данном документе). В одном аспекте иллюстративная конструкция CAR содержит необязательную лидерную последовательность (например, лидерную последовательность, описанную в данном документе), внеклеточный антигенсвязывающий домен (например, антигенсвязывающий домен, описанный в данном документе), шарнирную область (например, шарнирную область, описанную в данном документе), трансмембранный домен (например, трансмембранный домен, описанный в данном документе), внутриклеточный костимулирующий сигнальный домен (например, костимулирующий сигнальный домен, описанный в данном документе) и/или внутриклеточный первичный сигнальный домен (например, первичный сигнальный домен, описанный в данном документе).
В одном аспекте CAR (например, CAR для CD19) по настоящему изобретению содержат по меньшей мере один внутриклеточный сигнальный домен, выбранный из группы сигнального домена CD137 (4-1BB), сигнального домена CD28, сигнального домена CD27, сигнального домена ICOS, сигнального домена CD3-дзета и любой их комбинации. В одном аспекте CAR содержат по меньшей мере один внутриклеточный сигнальный домен из одной или нескольких костимулирующих молекул, выбранных из CD137 (4-1BB), CD28, CD27 или ICOS.
Антигенсвязывающий домен CAR
В одном аспекте CAR по настоящему изобретению, связанный с COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающим полипептидом и/или доменом деградации, содержит мишень-специфический связывающий элемент, иначе обозначаемый как антигенсвязывающий домен. В одном варианте осуществления часть CAR, содержащая антигенсвязывающий домен, содержит антигенсвязывающий домен, который нацеливается, например, специфически связывается, на антиген, например, антиген, описанный в данном документе, например, CD19. В одном варианте осуществления антигенсвязывающий домен нацеливается на CD19 человека, например, специфически связывается с ним.
В некоторых вариантах осуществления совокупность иммунных эффекторных клеток, например, популяция, истощенная по T-регуляторным клеткам, содержит нуклеиновую кислоту, кодирующую CAR, который содержит мишень-специфический связывающий элемент, иначе называемый антигенсвязывающим доменом. Выбор связывающего элемента зависит от типа и количества лигандов, которые определяют поверхность клетки-мишени. Например, антигенсвязывающий домен может быть выбран таким образом, чтобы он распознавал лиганд, который выступает в качестве маркера клеточной поверхности на клетках-мишенях, ассоциированных с конкретным болезненным состоянием. Таким образом, примеры маркеров клеточной поверхности, которые могут выступать в качестве лигандов для антигенсвязывающего домена в CAR, описанного в данном документе, включают маркеры, ассоциированные с вирусными, бактериальными и паразитарными инфекциями, аутоиммунным заболеванием и раковыми клетками.
В одном аспекте часть CAR, содержащая антигенсвязывающий домен, содержит антигенсвязывающий домен, который нацеливается на опухолевый антиген, например, на опухолевый антиген, описанный в данном документе. В некоторых вариантах осуществления антигенсвязывающий домен выбран из: CD19; CD123; CD22; CD30; CD171; CS-1; лектиноподобной молекулы-1 C-типа, CD33; варианта III рецептора эпидермального фактора роста (EGFRvIII); ганглиозида G2 (GD2); ганглиозида GD3; представителя семейства рецепторов TNF; антигена созревания B-клеток (BCMA); Tn-антигена ((Tn Ag) или (GalNAcα-Ser/Thr)); простатического специфического мембранного антигена (PSMA); орфанного рецептора-1, подобного рецепторной тирозинкиназе (ROR1); Fms-подобной тирозинкиназы 3 (FLT3); опухолеассоциированного гликопротеина-72 (TAG72); CD38; CD44v6; раково-эмбрионального антигена (CEA); молекулы адгезии эпителиальных клеток (EPCAM); B7H3 (CD276); KIT (CD117); субъединицы альфа-2 рецептора интерлейкина-13; мезотелина; альфа-субъединицы рецептора интерлейкина-11 (IL-11Ra); антигена стволовых клеток предстательной железы (PSCA); сериновой протеазы-21; рецептора-2 фактора роста эндотелия сосудов (VEGFR2); антигена системы Льюис (Y); CD24; рецептора фактора роста тромбоцитов бета-типа (PDGFR-бета); стадиеспецифического эмбрионального антигена-4 (SSEA-4); CD20; рецептора фолиевой кислоты альфа-типа; рецепторной тирозинпротеинкиназы ERBB2 (Her2/neu); муцина-1, ассоциированного с клеточной поверхностью (MUC1); рецептора эпидермального фактора роста (EGFR); молекулы адгезии нейронов (NCAM); простазы; простатической кислой фосфатазы (PAP); мутантного фактора элонгации 2 (ELF2M); эфрина B2; белка активации фибробластов альфа (FAP); рецептора инсулиноподобного фактора роста-1 (рецептора IGF-I), карбоангидразы IX (CAIX); субъединицы-9 протеасомы (просомы, мультикаталитической протеазы) бета-типа (LMP2); гликопротеина 100 (gp100); онкогенного слитого белка, состоящего из кластерного региона точечных разрывов (BCR) и гомолога-1 вирусного онкогена лейкоза мышей Абельсона (Abl) (bcr-abl); тирозиназы; эфринового рецептора-2 A-типа (EphA2); фукозил-GM1; молекулы адгезии, представляющей собой сиалилированный антиген системы Льюис (sLe; ганглиозида GM3; трансглютаминазы-5 (TGS5); высокомолекулярного меланома-ассоциированного антигена (HMWMAA); ганглиозида o-ацетил-GD2 (OAcGD2); рецептора фолиевой кислоты бета-типа; маркера-1 эндотелия опухоли (TEM1/CD248); белка, родственного маркеру-7 эндотелия опухоли (TEM7R); клаудина-6 (CLDN6); рецептора тиреотропного гормона (TSHR); представителя D группы 5 класса С рецепторов, сопряженных с G-белком (GPRC5D); белка, кодируемого открытой рамкой считывания 61 X-хромосомы (CXORF61); CD97; CD179a; киназы анапластической лимфомы (ALK); полисиаловой кислоты; плацентоспецифического белка-1 (PLAC1); гексасахаридной части гликоцерамида globoH (GloboH); дифференцировочного антигена молочной железы (NY-BR-1); уроплакина-2 (UPK2); клеточного рецептора-1 вируса гепатита A (HAVCR1); бета-3 адренорецептора (ADRB3); паннексина-3 (PANX3); рецептора-20, сопряженного с G-белком (GPR20); антигена локуса K9 комплекса лимфоцитарных антигенов 6 (LY6K); обонятельного рецептора 51E2 (OR51E2); белка, кодируемого альтернативной рамкой считывания гена TCR-гамма (TARP); белка опухоли Вильмса (WT1); раково-тестикулярного антигена-1 (NY-ESO-1); раково-тестикулярного антигена-2 (LAGE-1a); меланома-ассоциированного антигена-1 (MAGE-A1); белка, кодируемого транслокационным вариантом-6 гена ETS, локализованным в р-плече 12 хромосомы (ETV6-AML); белка-17 сперматозоидов (SPA17); представителя 1А семейства X-антигенов (XAGE1); ангиопоэтин-связывающего рецептора-2 клеточной поверхности 2 (Tie 2); раково-тестикулярного антигена-1 из клеток меланомы (MAD-CT-1); раково-тестикулярного антигена-2 из клеток меланомы (MAD-CT-2); Fos-родственного антигена-1; опухолевого белка p53 (p53); мутанта p53; простеина; сурвивина; теломеразы; опухолевого антигена-1 карциномы предстательной железы, антигена-1 меланомы, распознаваемого T-клетками; мутантного белка саркомы крыс (Ras); обратной транскриптазы теломеразы человека (hTERT); антигенов саркомы с точечными разрывами при транслокации; меланомного ингибитора апоптоза (ML-IAP); ERG (продукта слитого гена трансмембранной сериновой протеазы-2 (TMPRSS2) и ETS); N-ацетилглюкозаминилтрансферазы V (NA17); белка с парным box-доменом Рах-3 (PAX3); андрогенового рецептора; циклина-B1; нейробластомного гомолога вирусного онкогена миелоцитоматоза птиц v-myc (MYCN); представителя С семейства гомологов Ras (RhoC); белка-2, родственного тирозиназе (TRP-2); цитохрома P450 1B1 (CYP1B1); белка, подобного CCCTC-связывающему фактору (белку с "цинковыми пальцами"), антигена плоскоклеточной карциномы 3, распознаваемого Т-клетками (SART3); белка с парным box-доменом Рах-5 (PAX5); проакрозин-связывающего белка sp32 (OY-TES1); лимфоцит-специфической протеинтирозинкиназы (LCK); якорного белка-4 киназы A (AKAP-4); антигена 2 синовиальной саркомы с точечным разрывом в X-хромосоме (SSX2); рецептора конечных продуктов неферментативного гликозилирования (RAGE-1); почечного убиквитарного белка-1 (RU1); почечного убиквитарного белка-2 (RU2); легумаина; Е6 вируса папилломы человека (HPV E6); Е7 вируса папилломы человека (HPV E7); кишечной карбоксилэстеразы; мутантного белка теплового шока 70-2 (mut hsp70-2); CD79a; CD79b; CD72; иммуноглобулиноподобного рецептора-1, ассоциированного с лейкоцитами (LAIR1); рецептора Fc-фрагмента IgA (FCAR или CD89); представителя 2 подсемейства А иммуноглобулиноподобных рецепторов лейкоцитов (LILRA2); представителя f семейства белков, подобных молекулам CD300 (CD300LF); представителя А семейства 12 лектиновых доменов С-типа (CLEC12A); антигена-2 клеток стромы костного мозга (BST2); белка-2, подобного муциноподобному рецептору гормонов, содержащему EGF-подобный модуль (EMR2); лимфоцитарного антигена-75 (LY75); глипикана-3 (GPC3); белка-5, подобного Fc-рецептору (FCRL5); и полипептида-1, подобного лямбда-цепи иммуноглобулина (IGLL1).
В одном варианте осуществления антигенсвязывающий домен связывается с CD19. В другом варианте осуществления антигенсвязывающий домен связывается с CD123. В другом варианте осуществления антигенсвязывающий домен связывается с BCMA. В другом варианте осуществления антигенсвязывающий домен связывается с CD20.
Антигенсвязывающий домен может представлять собой любой домен, который связывается с антигеном, в том числе без ограничения моноклональное антитело, поликлональное антитело, рекомбинантное антитело, антитело человека, гуманизированное антитело и их функциональный фрагмент, в том числе без ограничения однодоменное антитело, такое как вариабельный домен тяжелой цепи (VH), вариабельный домен легкой цепи (VL) и вариабельный домен (VHH) нанотела верблюдовых, а также альтернативную каркасную структуру, которая, как известно из уровня техники, функционирует в качестве антигенсвязывающего домена, такую как рекомбинантный фибронектиновый домен, T-клеточный рецептор (TCR) или его фрагмент, например, одноцепочечный TCR и т. п. В некоторых случаях целесообразно, чтобы антигенсвязывающий домен был получен от того же биологического вида, в котором в конечном итоге будут применять CAR. Например, для применения у человека может быть целесообразно, чтобы антигенсвязывающий домен CAR содержал в антигенсвязывающем домене антитела или фрагмента антитела человеческие или гуманизированные остатки.
Антигенсвязывающий домен может представлять собой любой домен, который связывается с антигеном, в том числе без ограничения моноклональное антитело, поликлональное антитело, рекомбинантное антитело, антитело человека, гуманизированное антитело и их функциональный фрагмент, в том числе без ограничения однодоменное антитело, такое как вариабельный домен тяжелой цепи (VH), вариабельный домен легкой цепи (VL) и вариабельный домен (VHH) нанотела верблюдовых, а также альтернативную каркасную структуру, которая, как известно из уровня техники, функционирует в качестве антигенсвязывающего домена, такую как рекомбинантный фибронектиновый домен, и т. п. В некоторых случаях целесообразно, чтобы антигенсвязывающий домен был получен от того же биологического вида, в котором в конечном итоге будут применять CAR. Например, для применения у человека может быть целесообразно, чтобы антигенсвязывающий домен CAR содержал в антигенсвязывающем домене антитела или фрагмента антитела человеческие или гуманизированные остатки. Таким образом, в одном аспекте антигенсвязывающий домен содержит антитело человека или фрагмент антитела.
В одном варианте осуществления антигенсвязывающий домен содержит одну, две или три (например, все три) CDR тяжелой цепи, CDR1 HC, CDR2 HC и CDR3 HC, из антитела, описанного в данном документе (например, антитела, описанного в WO2015/142675, US-2015-0283178-A1, US-2016-0046724-A1, US2014/0322212A1, US2016/0068601A1, US2016/0051651A1, US2016/0096892A1, US2014/0322275A1 или WO2015/090230, включенных в данный документ посредством ссылки), и/или одну, две или три (например, все три) CDR легкой цепи, CDR1 LC, CDR2 LC и CDR3 LC, из антитела, описанного в данном документе (например, антитела, описанного в WO2015/142675, US-2015-0283178-A1, US-2016-0046724-A1, US2014/0322212A1, US2016/0068601A1, US2016/0051651A1, US2016/0096892A1, US2014/0322275A1 или WO2015/090230, включенных в данный документ посредством ссылки). В одном варианте осуществления антигенсвязывающий домен содержит вариабельную область тяжелой цепи и/или вариабельную область легкой цепи антитела, перечисленного выше.
В вариантах осуществления антигенсвязывающий домен представляет собой антигенсвязывающий домен, описанный в WO2015/142675, US-2015-0283178-A1, US-2016-0046724-A1, US2014/0322212A1, US2016/0068601A1, US2016/0051651A1, US2016/0096892A1, US2014/0322275A1 или WO2015/090230, включенных в данный документ посредством ссылки.
Иллюстративные антигены-мишени, на которые можно нацеливаться с помощью клеток, экспрессирующих CAR, включают без ограничения, среди прочих, CD19, CD123, EGFRvIII, CD33, мезотелин, BCMA и GFR-альфа 4, описанные, например, в WO2014/153270, WO 2014/130635, WO2016/028896, WO 2014/130657, WO2016/014576, WO 2015/090230, WO2016/014565, WO2016/014535 и WO2016/025880, каждая из которых включена в данный документ посредством ссылки во всей своей полноте.
Полиспецифический CAR
В некоторых вариантах осуществления молекула CAR представляет собой молекулу полиспецифического, например биспецифического, CAR, характеризующуюся первой специфичностью связывания с первым антигеном, например, эпитопом B-клетки, и второй специфичностью связывания с тем же или другим антигеном, например, эпитопом B-клетки. В некоторых вариантах осуществления молекула биспецифического CAR характеризуется первой специфичностью связывания с CD19 (например, молекула биспецифического CAR содержит CAR для CD19, раскрытый в таблицах 5, 6, 7 и 30) и второй специфичностью связывания с CD22 (например, молекула биспецифического CAR содержит CAR для CD22, раскрытый в таблицах 19 и 20). В некоторых вариантах осуществления молекула биспецифического CAR характеризуется первой специфичностью связывания с CD19 (например, молекула биспецифического CAR содержит CAR для CD19, раскрытый в таблицах 5, 6, 7 и 30) и второй специфичностью связывания с CD20 (например, молекула биспецифического CAR содержит CAR для CD20, раскрытый в таблице 32).
В одном варианте осуществления первая и вторая специфичности связывания предусматривают молекулу антитела, например, связывающий домен антитела (например, scFv). В пределах каждой молекулы антитела (например, scFv) молекулы биспецифического CAR VH может быть вышерасположенной или нижерасположенной относительно VL.
В некоторых вариантах осуществления вышерасположенные антитело или фрагмент антитела (например, scFv) организованы так, что их VH (VH1) расположена выше их VL (VL1), а нижерасположенные антитело или фрагмент антитела (например, scFv) организованы так, что их VL (VL2) расположена выше их VH (VH2), вследствие чего вся молекула биспецифического CAR имеет такую организацию в ориентации от N- до C-конца: VH1-VL1-VL2-VH2.
В некоторых вариантах осуществления вышерасположенные антитело или фрагмент антитела (например, scFv) организованы так, что их VL (VL1) расположена выше их VH (VH1), а нижерасположенные антитело или фрагмент антитела (например, scFv) организованы так, что их VH (VH2) расположена выше их VL (VL2), вследствие чего вся молекула биспецифического CAR имеет такую организацию в ориентации от N- до C-конца: VL1-VH1-VH2-VL2.
В некоторых вариантах осуществления вышерасположенные антитело или фрагмент антитела (например, scFv) организованы так, что их VL (VL1) расположена выше их VH (VH1), а нижерасположенные антитело или фрагмент антитела (например, scFv) организованы так, что их VL (VL2) расположена выше их VH (VH2), вследствие чего вся молекула биспецифического CAR имеет такую организацию в ориентации от N- до C-конца: VL1-VH1-VL2-VH2.
В еще одних некоторых вариантах осуществления вышерасположенные антитело или фрагмент антитела (например, scFv) организованы так, что их VH (VH1) расположена выше их VL (VL1), а нижерасположенные антитело или фрагмент антитела (например, scFv) организованы так, что их VH (VH2) расположена выше их VL (VL2), вследствие чего вся молекула биспецифического CAR имеет такую организацию в ориентации от N- до C-конца: VH1-VL1-VH2-VL2.
В любой из вышеуказанных конфигураций между двумя антителами или фрагментами антител (например, scFv) необязательно расположен линкер, например, между VL1 и VL2, если конструкция организована в виде VH1-VL1-VL2-VH2; между VH1 и VH2, если конструкция организована в виде VL1-VH1-VH2-VL2; между VH1 и VL2,если конструкция организована в виде VL1-VH1-VL2-VH2; или между VL1 и VH2, если конструкция организована в виде VH1-VL1-VH2-VL2. Обычно линкер между двумя scFv должен иметь достаточную длину, чтобы предотвращать неправильное спаривание между доменами двух scFv. Линкер может представлять собой линкер, описанный в данном документе. В некоторых вариантах осуществления линкер представляет собой линкер (Gly4-Ser)n, где n составляет 1, 2, 3, 4, 5 или 6. В некоторых вариантах осуществления линкер представляет собой (Gly4-Ser)n, где n=1 (SEQ ID NO: 168), например, линкер имеет аминокислотную последовательность Gly4-Ser (SEQ ID NO: 168). В некоторых вариантах осуществления линкер представляет собой (Gly4-Ser)n, где n=3 (SEQ ID NO: 142). В некоторых вариантах осуществления линкер представляет собой (Gly4-Ser)n, где n= 4 (SEQ ID NO: 141). В некоторых вариантах осуществления линкер содержит, например, состоит из аминокислотной последовательности: LAEAAAK (SEQ ID NO: 822).
В любой из вышеуказанных конфигураций линкер необязательно располагается между VL и VH первого scFv. Линкер необязательно располагается между VL и VH второго scFv. В конструкциях, которые имеют несколько линкеров, любые два или более линкера могут быть одинаковыми или разными. Соответственно, в некоторых вариантах осуществления биспецифический CAR содержит VL, VH и необязательно один или несколько линкеров в виде организации, описанной в данном документе.
В некоторых вариантах осуществления каждая молекула антитела, например, каждый антигенсвязывающий домен (например, каждый scFv), содержит линкер между VH- и VL-областями. В некоторых вариантах осуществления линкер между VH- и VL-областями представляет собой линкер (Gly4-Ser)n, где n составляет 1, 2, 3, 4, 5 или 6. В некоторых вариантах осуществления линкер представляет собой (Gly4-Ser)n, где n=1 (SEQ ID NO: 168), например, линкер имеет аминокислотную последовательность Gly4-Ser (SEQ ID NO: 168). В некоторых вариантах осуществления линкер представляет собой (Gly4-Ser)n, где n= 3 (SEQ ID NO: 142). В некоторых вариантах осуществления линкер представляет собой (Gly4-Ser)n, где n= 4 (SEQ ID NO: 141). В некоторых вариантах осуществления VH- и VL-области соединены без линкера.
Дополнительные иллюстративные молекулы полиспецифических CAR раскрыты на страницах 26-39 в WO2018/067992, включенной в данный документ посредством ссылки.
CAR для CD19
В других вариантах осуществления клетки, экспрессирующие CAR, могут специфически связываться с CD19, например, могут содержать молекулу CAR или антигенсвязывающий домен (например, гуманизированный антигенсвязывающий домен) в соответствии с таблицей 3 из WO2014/153270, включенной в данный документ посредством ссылки.
В вариантах осуществления молекула CAR содержит антигенсвязывающий домен, который специфически связывается с CD19 (CAR для CD19). В одном варианте осуществления антигенсвязывающий домен нацеливается на CD19 человека. В одном варианте осуществления антигенсвязывающий домен CAR характеризуется такой же или аналогичной специфичностью связывания, которой характеризуется scFv-фрагмент FMC63, описанный в Nicholson et al. Mol. Immun. 34 (16-17): 1157-1165 (1997). В одном варианте осуществления антигенсвязывающий домен CAR содержит scFv-фрагмент, описанный в Nicholson et al. Mol. Immun. 34 (16-17): 1157-1165 (1997). Молекула антитела к CD19 может представлять собой, например, молекулу антитела (например, молекулу гуманизированного антитела к CD19), описанную в WO2014/153270, включенной в данный документ посредством ссылки во всей своей полноте. В WO2014/153270 также описаны способы выполнения анализа связывания и эффективности различных конструкций CAR.
В одном аспекте исходная последовательность scFv мыши представляет собой конструкцию CAR19, представленную в публикации согласно PCT WO2012/079000 (включенной в данный документ посредством ссылки). В одном варианте осуществления CD19-связывающий домен представляет собой scFv, описанный в WO2012/079000.
В одном варианте осуществления молекула CAR содержит последовательность слитого полипептида, представленную под SEQ ID NO: 12 в публикации согласно PCT WO2012/079000, и представлена в данном документе в таблице 5, в которой представлен scF-фрагмент мышиного происхождения, который специфически связывается с CD19 человека. Гуманизация этого scFv мыши может быть необходима в клинической ситуации, когда специфические для мышей остатки могут индуцировать ответ с образованием антител человека к антигену мыши (HAMA) у пациентов, которые получают лечение CART19, например, лечение с помощью T-клеток, трансдуцированных конструкцией CAR19.
В одном варианте осуществления CAR для CD19 содержит аминокислотную последовательность, представленную под SEQ ID NO: 12 в публикации согласно PCT WO2012/079000. В варианте осуществления аминокислотная последовательность представляет собой

или последовательность практически гомологичную ей. Необязательная последовательность сигнального пептида показана заглавными буквами и круглыми скобками.
В одном варианте осуществления аминокислотная последовательность представляет собой:

или последовательность практически гомологичную ей.
В одном варианте осуществления CAR для CD19 имеет обозначение согласно USAN TISAGENLECLEUCEL-T. В вариантах осуществления CTL019 получают за счет генной модификации T-клеток, опосредованной стабильной вставкой путем трансдукции с помощью самоинактивирующегося лентивирусного (LV) вектора, дефектного по репликации, содержащего трансген CTL019 под контролем промотора EF-1 альфа. CTL019 может представлять собой смесь положительных и отрицательных по трансгену Т-клеток, которые доставляют субъекту из расчета процентного количества положительных по трансгену Т-клеток.
В других вариантах осуществления CAR для CD19 содержит антигенсвязывающий домен (например, гуманизированный антигенсвязывающий домен) в соответствии с таблицей 3 из WO2014/153270, включенной в данный документ посредством ссылки.
Гуманизация мышиного антитела к CD19 необходима в клинической ситуации, когда специфические для мышей остатки могут индуцировать ответ с образованием антител человека к антигену мыши (HAMA) у пациентов, которые получают лечение CART19, т. е. лечение с помощью T-клеток, трансдуцированных конструкцией CAR19. Получение, определение характеристик и эффективность гуманизированных последовательностей CAR для CD19 описаны в международной заявке WO2014/153270, включенной в данный документ посредством ссылки во всей своей полноте, включая примеры 1-5 (стр. 115-159).
В некоторых вариантах осуществления конструкции CAR для CD19 описаны в публикации согласно PCT WO 2012/079000, включенной в данный документ посредством ссылки, и аминокислотная последовательность мышиного CAR для CD19 и конструкции scFv показаны в таблице 5 ниже, или предусматривают последовательность, практически идентичную любой из вышеуказанных последовательностей (например, на по меньшей мере 85%, 90%, 95% или больше идентичную любой из последовательностей, описанных в данном документе).
Конструкции CAR для CD19, содержащие гуманизированные scFv-домены, связывающие CD19, описаны в публикации согласно PCT WO 2014/153270, включенной в данный документ посредством ссылки.
Последовательности мышиных и гуманизированных CDR в последовательностях scFv-доменов, связывающих CD19, показаны в таблице 6 в случае вариабельных доменов тяжелой цепи и в таблице 7 в случае вариабельных доменов легкой цепи. В некоторых вариантах осуществления HCDR1 мышиного или гуманизированного CD19-связывающего домена представляет собой GVSLPDYGVS (SEQ ID NO: 230).
В соответствии с настоящим изобретением можно применять любой известный CAR для CD19, например, антигенсвязывающий домен для CD19 из любого известного из уровня техники CAR для CD19. Например, CAR для CD19, LG-740, описан в патенте США № 8399645; патенте США № 7446190; Xu et al., Leuk Lymphoma. 2013 54(2):255-260(2012); Cruz et al., Blood 122(17):2965-2973 (2013); Brentjens et al., Blood, 118(18):4817-4828 (2011); Kochenderfer et al., Blood 116(20):4099-102 (2010); Kochenderfer et al., Blood 122 (25):4129-39 (2013); и 16th Annu Meet Am Soc Gen Cell Ther (ASGCT) (May 15-18, Salt Lake City) 2013, Abst 10.
Иллюстративные CAR для CD19 включают CAR для CD19, описанные в данном документе, например, в одной или нескольких таблицах, описанных в данном документе, CAR для CD19, описанный в Xu et al. Blood 123.24(2014):3750-9; Kochenderfer et al. Blood 122.25(2013):4129-39, Cruz et al. Blood 122.17(2013):2965-73, NCT00586391, NCT01087294, NCT02456350, NCT00840853, NCT02659943, NCT02650999, NCT02640209, NCT01747486, NCT02546739, NCT02656147, NCT02772198, NCT00709033, NCT02081937, NCT00924326, NCT02735083, NCT02794246, NCT02746952, NCT01593696, NCT02134262, NCT01853631, NCT02443831, NCT02277522, NCT02348216, NCT02614066, NCT02030834, NCT02624258, NCT02625480, NCT02030847, NCT02644655, NCT02349698, NCT02813837, NCT02050347, NCT01683279, NCT02529813, NCT02537977, NCT02799550, NCT02672501, NCT02819583, NCT02028455, NCT01840566, NCT01318317, NCT01864889, NCT02706405, NCT01475058, NCT01430390, NCT02146924, NCT02051257, NCT02431988, NCT01815749, NCT02153580, NCT01865617, NCT02208362, NCT02685670, NCT02535364, NCT02631044, NCT02728882, NCT02735291, NCT01860937, NCT02822326, NCT02737085, NCT02465983, NCT02132624, NCT02782351, NCT01493453, NCT02652910, NCT02247609, NCT01029366, NCT01626495, NCT02721407, NCT01044069, NCT00422383, NCT01680991, NCT02794961 или NCT02456207, каждый из которых включен в данный документ посредством ссылки во всей своей полноте.
CAR для CD123
В других вариантах осуществления клетки, экспрессирующие CAR, могут специфически связываться с CD123, например, могут содержать молекулу CAR (например, любую из CAR1 - CAR8) или антигенсвязывающий домен в соответствии с таблицей 1-2 из WO 2014/130635, включенной в данный документ посредством ссылки. Аминокислотные последовательности молекул CAR для CD123 и антигенсвязывающих доменов (например, содержащих одну, две, три CDR VH и одну, две, три CDR VL согласно Kabat или Chothia), а также нуклеотидные последовательности, кодирующие их, указанные в WO 2014/130635, представлены в таблицах 8-14. Аминокислотные и нуклеотидная последовательности, идентичные и практически идентичные вышеуказанным последовательностям, представленные в таблицах 8-14, конкретным образом включены в настоящее описание.
CDR для CD123-связывающих доменов, представленных в таблицах 8-14, изложены в соответствии с комбинацией схемы нумерации по Kabat и Chothia.
В вариантах осуществления молекула CAR, описанная в данном документе, содержит scFv, который специфически связывается с CD123 и не содержит лидерной последовательности, например, аминокислотной последовательности под SEQ ID NO: 64. В приведенной ниже таблице 14 представлены аминокислотные и нуклеотидные последовательности для последовательностей scFv CD123, которые не содержат лидерную последовательность под SEQ ID NO: 64.
В других вариантах осуществления клетки, экспрессирующие CAR, могут специфически связываться с CD123, например, могут содержать молекулу CAR (например, любую из CAR123-1 или CAR123-4 и hzCAR123-1 - hzCAR123-32) или антигенсвязывающий домен в соответствии с таблицами 2, 6 и 9 из WO2016/028896, включенной в данный документ посредством ссылки. Аминокислотные последовательности молекул CAR для CD123 и антигенсвязывающих доменов (например, содержащих одну, две, три CDR VH и одну, две, три CDR VL согласно Kabat или Chothia), а также нуклеотидные последовательности, кодирующие их, указанные в WO2016/028896, включены в данный документ посредством ссылки во всей своей полноте.
CAR для EGFRvIII
В других вариантах осуществления клетки, экспрессирующие CAR, могут специфически связываться с EGFRvIII, например, могут содержать молекулу CAR или антигенсвязывающий домен в соответствии с таблицей 2 или SEQ ID NO: 11 из WO 2014/130657, включенной в данный документ посредством ссылки. Иллюстративные аминокислотные последовательности молекул CAR для EGFRvIII и антигенсвязывающих доменов (например, содержащих одну, две, три CDR VH и одну, две, три CDR VL согласно Kabat или Chothia) и нуклеотидные последовательности, кодирующие их, представлены в WO 2014/130657. Иллюстративные последовательности CAR, связывающих EGFRvIII, могут содержать CDR, вариабельную область, scFv или полноразмерную последовательность CAR, раскрытую в таблице 33 (или последовательность на по меньшей мере приблизительно 85%, 90%, 95%, 99% или более идентичную ей и/или имеющую одну, две, три или более замен, вставок, делеций или модификаций).
CAR для CD33
В других вариантах осуществления клетки, экспрессирующие CAR, могут специфически связываться с CD33, например, могут содержать молекулу CAR (например, любую из CAR33-1 - CAR-33-9) или антигенсвязывающий домен в соответствии с таблицей 2 или 9 из WO2016/014576, включенной в данный документ посредством ссылки. Иллюстративные аминокислотные последовательности молекул CAR для CD33 и антигенсвязывающих доменов (например, содержащих одну, две, три CDR VH и одну, две, три CDR VL согласно Kabat или Chothia) и нуклеотидные последовательности, кодирующие их, представлены в WO2016/014576.
CAR для мезотелина
В некоторых вариантах осуществления клетки, экспрессирующие CAR, могут специфически связываться с мезотелином, например, могут содержать молекулу CAR или антигенсвязывающий домен в соответствии с таблицами 2-3 из WO 2015/090230, включенной в данный документ посредством ссылки. Иллюстративные аминокислотные последовательности молекул CAR для мезотелина и антигенсвязывающих доменов (например, содержащих одну, две, три CDR VH и одну, две, три CDR VL согласно Kabat или Chothia) и нуклеотидные последовательности, кодирующие их, представлены в WO 2015/090230. Иллюстративные последовательности CAR, связывающих мезотелин, могут содержать CDR, вариабельную область, scFv или полноразмерную последовательность CAR, раскрытую в таблице 34 (или последовательность на по меньшей мере приблизительно 85%, 90%, 95%, 99% или более идентичную ей и/или имеющую одну, две, три или более замен, вставок, делеций или модификаций).
>ZA53-27BC (M1
ZA53-27BC
R001-A11
126161)
APGQGLEWMGRINPNSGGTNYAQKFQGRVTMTRDTSISTAYMELSRLRSEDTAVYYCARG
RYYGMDVWGQGTMVTVSSGGGGSGGGGSGGGGSGGGGSEIVLTQSPATLSLSPGERATIS
CRASQSVSSNFAWYQQRPGQAPRLLIYDASNRATGIPPRFSGSGSGTDFTLTISSLEPED
FAAYYCHQRSNWLYTFGQGTKVDIKTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAV
HTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQEED
GCSCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKRRGRDPE
MGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDAL
HMQALPPR
>FA56-26RC (M2
FA56-26RC
R001-A10
126162)
APGQGLEWMGWINPNSGGTNYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARD
LRRTVVTPRAYYGMDVWGQGTTVTVSSGGGGSGGGGSGGGGSGGGGSDIQLTQSPSTLSA
SVGDRVTITCQASQDISNSLNWYQQKAGKAPKLLIYDASTLETGVPSRFSGSGSGTDFSF
TISSLQPEDIATYYCQQHDNLPLTFGQGTKVEIKTTTPAPRPPTPAPTIASQPLSLRPEA
CRPAAGGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMR
PVQTTQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVL
DKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLST
ATKDTYDALHMQALPPR
>VA58-21LC (M3
VA58-21LC
R001-A1
126163)
APGQGLEWMGWINPNSGGTNYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARG
EWDGSYYYDYWGQGTLVTVSSGGGGSGGGGSGGGGSGGGGSDIVLTQTPSSLSASVGDRV
TITCRASQSINTYLNWYQHKPGKAPKLLIYAASSLQSGVPSRFSGSGSGTDFTLTISSLQ
PEDFATYYCQQSFSPLTFGGGTKLEIKTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGG
AVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQE
EDGCSCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKRRGRD
PEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYD
ALHMQALPPR
>DP37-07IC (M4
DP37-07IC
R001-C6
126164)
VPGKGLVWVSRINTDGSTTTYADSVEGRFTISRDNAKNTLYLQMNSLRDDDTAVYYCVGG
HWAVWGQGTTVTVSSGGGGSGGGGSGGGGSGGGGSDIQMTQSPSTLSASVGDRVTITCRA
SQSISDRLAWYQQKPGKAPKLLIYKASSLESGVPSRFSGSGSGTEFTLTISSLQPDDFAV
YYCQQYGHLPMYTFGQGTKVEIKTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHT
RGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQEEDGC
SCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKRRGRDPEMG
GKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHM
QALPPR
>XP31-20LC (M5
XP31-20LC
R001-B4
126165)
APGQGLEWMGWINPNSGGTNYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCASG
WDFDYWGQGTLVTVSSGGGGSGGGGSGGGGSGGGGSDIVMTQSPSSLSASVGDRVTITCR
ASQSIRYYLSWYQQKPGKAPKLLIYTASILQNGVPSRFSGSGSGTDFTLTISSLQPEDFA
TYYCLQTYTTPDFGPGTKVEIKTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTR
GLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQEEDGCS
CRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGG
KPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQ
ALPPR
>FE10-06ID (M6
46FE10-06ID
R001-A4
126166)
APGQGLEWMGIINPSGGSTSYAQKFQGRVTMTRDTSTSTVYMELSSLRSEDTAVYYCARY
RLIAVAGDYYYYGMDVWGQGTMVTVSSGGGGSGGGGSGGGGSGGGGSDIQMTQSPSSVSA
SVGDRVTITCRASQGVGRWLAWYQQKPGTAPKLLIYAASTLQSGVPSRFSGSGSGTDFTL
TINNLQPEDFATYYCQQANSFPLTFGGGTRLEIKTTTPAPRPPTPAPTIASQPLSLRPEA
CRPAAGGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMR
PVQTTQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVL
DKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLST
ATKDTYDALHMQALPPR
>VE12-01CD (M7
VE12-01CD
R001-A5
126167)
APGKGLEWVAVISYDGSNKYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARW
KVSSSSPAFDYWGQGTLVTVSSGGGGSGGGGSGGGGSGGGGSEIVLTQSPATLSLSPGER
AILSCRASQSVYTKYLGWYQQKPGQAPRLLIYDASTRATGIPDRFSGSGSGTDFTLTINR
LEPEDFAVYYCQHYGGSPLITFGQGTRLEIKTTTPAPRPPTPAPTIASQPLSLRPEACRP
AAGGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQ
TTQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKR
RGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATK
DTYDALHMQALPPR
>LE13-05XD (M8
LE13-05XD
R001-E5
126168)
APGQGLEWMGWINPNSGGTNYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARD
HYGGNSLFYWGQGTLVTVSSGGGGSGGGGSGGGGSGGGGSDIQLTQSPSSISASVGDTVS
ITCRASQDSGTWLAWYQQKPGKAPNLLMYDASTLEDGVPSRFSGSASGTEFTLTVNRLQP
EDSATYYCQQYNSYPLTFGGGTKVDIKTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGG
AVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQE
EDGCSCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKRRGRD
PEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYD
ALHMQALPPR
>BE15-00SD (M9
BE15-00SD
R001-A3
126169)
APGQGLEWMGIINPSGGSTGYAQKFQGRVTMTRDTSTSTVHMELSSLRSEDTAVYYCARG
GYSSSSDAFDIWGQGTMVTVSSGGGGSGGGGSGGGGSGGGGSDIQMTQSPPSLSASVGDR
VTITCRASQDISSALAWYQQKPGTPPKLLIYDASSLESGVPSRFSGSGSGTDFTLTISSL
QPEDFATYYCQQFSSYPLTFGGGTRLEIKTTTPAPRPPTPAPTIASQPLSLRPEACRPAA
GGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTT
QEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKRRG
RDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDT
YDALHMQALPPR
>RE16-05MD (M10
RE16-05MD
R001-D10
126170)
APGQGLEWMGWISAYNGNTNYAQKLQGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCARV
AGGIYYYYGMDVWGQGTTITVSSGGGGSGGGGSGGGGSGGGGSDIVMTQTPDSLAVSLGE
RATISCKSSHSVLYNRNNKNYLAWYQQKPGQPPKLLFYWASTRKSGVPDRFSGSGSGTDF
TLTISSLQPEDFATYFCQQTQTFPLTFGQGTRLEINTTTPAPRPPTPAPTIASQPLSLRP
EACRPAAGGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPF
MRPVQTTQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYD
VLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGL
STATKDTYDALHMQALPPR
>NE10-19WD (M11
NE10-19WD
R001-G2
126171)
APGQGLEWMGWINPNSGGTNYAQNFQGRVTMTRDTSISTAYMELRRLRSDDTAVYYCASG
WDFDYWGQGTLVTVSSGGGGSGGGGSGGGGSGGGGSDIRMTQSPSSLSASVGDRVTITCR
ASQSIRYYLSWYQQKPGKAPKLLIYTASILQNGVPSRFSGSGSGTDFTLTISSLQPEDFA
TYYCLQTYTTPDFGPGTKVEIKTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTR
GLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQEEDGCS
CRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGG
KPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQ
ALPPR
>DE12-14RD (M12
DE12-14RD
R001-G9
126172)
APGQGLEWMGRINPNSGGTNYAQKFQGRVTMTTDTSTSTAYMELRSLRSDDTAVYYCART
TTSYAFDIWGQGTMVTVSSGGGGSGGGGSGGGGSGGGGSDIQLTQSPSTLSASVGDRVTI
TCRASQSISTWLAWYQQKPGKAPNLLIYKASTLESGVPSRFSGSGSGTEFTLTISSLQPD
DFATYYCQQYNTYSPYTFGQGTKLEIKTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGG
AVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQE
EDGCSCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKRRGRD
PEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYD
ALHMQALPPR
>TE13-19LD (M13
TE13-19LD
R002-C3
126173)
APGKGLEWVSYIGRSGSSMYYADSVKGRFTFSRDNAKNSLYLQMNSLRAEDTAVYYCAAS
PVVAATEDFQHWGQGTLVTVSSGGGGSGGGGSGGGGSGGGGSDIVMTQTPATLSLSPGER
ATLSCRASQSVTSNYLAWYQQKPGQAPRLLLFGASTRATGIPDRFSGSGSGTDFTLTINR
LEPEDFAMYYCQQYGSAPVTFGQGTKLEIKTTTPAPRPPTPAPTIASQPLSLRPEACRPA
AGGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQT
TQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKRR
GRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKD
TYDALHMQALPPR
>BS83-95ID (M14
BS83-95ID
R001-E8
126174)
APGQGLEWMGIINPSGGSRAYAQKFQGRVTMTRDTSTSTVYMELSSLRSDDTAMYYCART
ASCGGDCYYLDYWGQGTLVTVSSGGGGSGGGGSGGGGSGGGGSDIQMTQSPPTLSASVGD
RVTITCRASENVNIWLAWYQQKPGKAPKLLIYKSSSLASGVPSRFSGSGSGAEFTLTISS
LQPDDFATYYCQQYQSYPLTFGGGTKVDIKTTTPAPRPPTPAPTIASQPLSLRPEACRPA
AGGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQT
TQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKRR
GRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKD
TYDALHMQALPPR
>HS86-94XD (M15
HS86-94XD
NT
127553)
APGKGLEWVSGISWNSGSIGYADSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCAKD
GSSSWSWGYFDYWGQGTLVTVSSGGGGSGGGGSGGGGSSSELTQDPAVSVALGQTVRTTC
QGDALRSYYASWYQQKPGQAPMLVIYGKNNRPSGIPDRFSGSDSGDTASLTITGAQAEDE
ADYYCNSRDSSGYPVFGTGTKVTVLTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAV
HTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQEED
GCSCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKRRGRDPE
MGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDAL
HMQALPPR
>XS87-99RD (M16
XS87-99RD
NT
127554)
APGKGLEWVSGISWNSGSTGYADSVKGRFTISRDNAKNSLYLQMNSLRAEDTALYYCAKD
SSSWYGGGSAFDIWGQGTMVTVSSGGGGSGGGGSGGGGSSSELTQEPAVSVALGQTVRIT
CQGDSLRSYYASWYQQKPGQAPVLVIFGRSRRPSGIPDRFSGSSSGNTASLIITGAQAED
EADYYCNSRDNTANHYVFGTGTKLTVLTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGG
AVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQE
EDGCSCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKRRGRD
PEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYD
ALHMQALPPR
>NS89-94MD (M17
NS89-94MD
NT
127555)
APGKGLEWVSGISWNSGSTGYADSVKGRFTISRDNAKNSLYLQMNSLRAEDTALYYCAKD
SSSWYGGGSAFDIWGQGTMVTVSSGGGGSGGGGSGGGGSSSELTQDPAVSVALGQTVRIT
CQGDSLRSYYASWYQQKPGQAPVLVIYGKNNRPSGIPDRFSGSSSGNTASLTITGAQAED
EADYYCNSRGSSGNHYVFGTGTKVTVLTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGG
AVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQE
EDGCSCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKRRGRD
PEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYD
ALHMQALPPR
>DS90-09HD (M18
DS90-09HD
R003-A05
127556)
APGKGLVWVSRINSDGSSTSYADSVKGRFTISRDNAKNTLYLQMNSLRAEDTAVYYCVRT
GWVGSYYYYMDVWGKGTTVTVSSGGGGSGGGGSGGGGSGGGGSEIVLTQSPGTLSLSPGE
RATLSCRASQSVSSNYLAWYQQKPGQPPRLLIYDVSTRATGIPARFSGGGSGTDFTLTIS
SLEPEDFAVYYCQQRSNWPPWTFGQGTKVEIKTTTPAPRPPTPAPTIASQPLSLRPEACR
PAAGGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPV
QTTQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDK
RRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTAT
KDTYDALHMQALPPR
>TS92-04BD (M19
TS92-04BD
R003-C06
127557)
APGKGLEWVAVISYDGSNKYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKG
YSRYYYYGMDVWGQGTTVTVSSGGGGSGGGGSGGGGSGGGGSEIVMTQSPATLSLSPGER
AILSCRASQSVYTKYLGWYQQKPGQAPRLLIYDASTRATGIPDRFSGSGSGTDFTLTINR
LEPEDFAVYYCQHYGGSPLITFGQGTKVDIKTTTPAPRPPTPAPTIASQPLSLRPEACRP
AAGGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQ
TTQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKR
RGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATK
DTYDALHMQALPPR
>JS93-08WD (M20
JS93-08WD
R003-E07
127558)
APGKGLEWVSAISGSGGSTYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKR
EAAAGHDWYFDLWGRGTLVTVSSGGGGSGGGGSGGGGSGGGGSDIRVTQSPSSLSASVGD
RVTITCRASQSISSYLNWYQQKPGKAPKLLIYAASSLQSGVPSRFSGSGSGTDFTLTISS
LQPEDFATYYCQQSYSIPLTFGQGTKVEIKTTTPAPRPPTPAPTIASQPLSLRPEACRPA
AGGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQT
TQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKRR
GRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKD
TYDALHMQALPPR
AGGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQT
TQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKRR
GRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKD
TYDALHMQALPPR
AGGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQT
TQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKRR
GRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKD
TYDALHMQALPPR
AGGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQT
TQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKRR
GRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKD
TYDALHMQALPPR
AGGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQT
TQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKRR
GRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKD
TYDALHMQALPPR
YNQKFRGKATLTVDKSSSTAYMDLLSLTSEDSAVYFCARGGYDGRGFDYWGQGTTVTVS
SGGGGSGGGGSGGGGSDIELTQSPAIMSASPGEKVTMTCSASSSVSYMHWYQQKSGTSP
KRWIYDTSKLASGVPGRFSGSGSGNSYSLTISSVEAEDDATYYCQQWSGYPLTFGAGTK
LEI
QSHGKSLEWIGLITPYNGASSYNQKFRGKATLTVDKSSSTAYMDLLSLTSEDSAVYFCA
RGGYDGRGFDYWGQGTTVTVSSGGGGSGGGGSGGGGSDIELTQSPAIMSASPGEKVTMT
CSASSSVSYMHWYQQKSGTSPKRWIYDTSKLASGVPGRFSGSGSGNSYSLTISSVEAED
DATYYCQQWSGYPLTFGAGTKLEITTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAV
HTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQEE
DGCSCRFPEEEEGGCELRVKFSRSADAPA
CAR для BCMA
В других вариантах осуществления клетки, экспрессирующие CAR, могут специфически связываться с BCMA, например, могут содержать молекулу CAR или антигенсвязывающий домен в соответствии с таблицей 1 или 16, SEQ ID NO: 271 или SEQ ID NO: 273 их WO2016/014565, включенной в данный документ посредством ссылки. Аминокислотные последовательности молекул CAR для BCMA и антигенсвязывающих доменов (например, содержащих одну, две, три CDR VH и одну, две, три CDR VL согласно Kabat или Chothia), а также нуклеотидные последовательности, кодирующие их, указанные в WO2016/014565, представлены в таблицах 15-18.
scFv-домен
scFv-домен
VH
VL
Полная последовательность CAR
Полная последовательность CAR
scFv-домен
Дополнительные иллюстративные последовательности, нацеливающиеся на BCMA, которые можно использовать в конструкциях CAR, связывающих BCMA, раскрыты в WO 2017/021450, WO 2017/011804, WO 2017/025038, WO 2016/090327, WO 2016/130598, WO 2016/210293, WO 2016/090320, WO 2016/014789, WO 2016/094304, WO 2016/154055, WO 2015/166073, WO 2015/188119, WO 2015/158671, US 9243058, US 8920776, US 9273141, US 7083785, US 9034324, US 2007/0049735, US 2015/0284467, US 2015/0051266, US 2015/0344844, US 2016/0131655, US 2016/0297884, US 2016/0297885, US 2017/0051308, US 2017/0051252, US 2017/0051252, WO 2016/020332, WO 2016/087531, WO 2016/079177, WO 2015/172800, WO 2017/008169, US 9340621, US 2013/0273055, US 2016/0176973, US 2015/0368351, US 2017/0051068, US 2016/0368988, US 2015/0232557, включенных в данный документ посредством ссылки во всей своей полноте.
В вариантах осуществления дополнительные иллюстративные конструкции CAR для BCMA получают с применением последовательностей VH и VL из публикации согласно PCT WO2012/0163805 (содержание которой включено в данный документ посредством ссылки во всей своей полноте). Иллюстративные конструкции CAR для BCMA и их соответствующие последовательности ДНК приведены в таблице 17.
CAR для CD22
В других вариантах осуществления клетки, экспрессирующие CAR, могут специфически связываться с CD22, например, могут содержать молекулу CAR или антигенсвязывающий домен (например, гуманизированный антигенсвязывающий домен) в соответствии с WO2016/164731, включенной в данный документ посредством ссылки.
В вариантах осуществления молекула CAR содержит антигенсвязывающий домен, который специфически связывается с CD22 (CAR для CD22). В одном варианте осуществления антигенсвязывающий домен нацеливается на CD22 человека. В одном варианте осуществления антигенсвязывающий домен содержит последовательность одноцепочечного Fv, описанного в данном документе.
Последовательности CAR для CD22 человека представлены ниже. В некоторых вариантах осуществления CAR для CD22 человека представляет собой CAR22-65.
Последовательность scFv CAR для CD22 человека (VH-(G4S)3-VL)
EVQLQQSGPGLVKPSQTLSLTCAISGDSMLSNSDTWNWIRQSPSRGLEWLGRTYHRSTWYDDYASSVRGRVSINVDTSKNQYSLQLNAVTPEDTGVYYCARVRLQDGNSWSDAFDVWGQGTMVTVSSGGGGSGGGGSGGGGSQSALTQPASASGSPGQSVTISCTGTSSDVGGYNYVSWYQQHPGKAPKLMIYDVSNRPSGVSNRFSGSKSGNTASLTISGLQAEDEADYYCSSYTSSSTLYVFGTGTQLTVL (SEQ ID NO: 811)
Вариабельная область тяжелой цепи CAR для CD22 человека
EVQLQQSGPGLVKPSQTLSLTCAISGDSMLSNSDTWNWIRQSPSRGLEWLGRTYHRSTWYDDYASSVRGRVSINVDTSKNQYSLQLNAVTPEDTGVYYCARVRLQDGNSWSDAFDVWGQGTMVTVSS (SEQ ID NO: 812)
Вариабельная область легкой цепи CAR для CD22 человека
QSALTQPASASGSPGQSVTISCTGTSSDVGGYNYVSWYQQHPGKAPKLMIYDVSNRPSGVSNRFSGSKSGNTASLTISGLQAEDEADYYCSSYTSSSTLYVFGTGTQLTVL (SEQ ID NO: 813)
В некоторых вариантах осуществления антигенсвязывающий домен содержит CDR1 HC, CDR2 HC и CDR3 HC с любыми аминокислотными последовательностями тяжелой цепи связывающего домена, перечисленными в таблице 19. В вариантах осуществления антигенсвязывающий домен дополнительно содержит CDR1 LC, CDR2 LC и CDR3 LC. В вариантах осуществления антигенсвязывающий домен содержит аминокислотные последовательности CDR1 LC, CDR2 LC и CDR3 LC, перечисленные в таблице 20.
В некоторых вариантах осуществления антигенсвязывающий домен содержит одну, две или все из CDR1 LC, CDR2 LC и CDR3 LC с любыми аминокислотными последовательностями легкой цепи связывающего домена, перечисленными в таблице 20, и одну, две или все из CDR1 HC, CDR2 HC и CDR3 HC с любыми аминокислотными последовательностями тяжелой цепи связывающего домена, перечисленными в таблице 19.
В некоторых вариантах осуществления CDR определены в соответствии со схемой нумерации по Kabat, схемой нумерации по Chothia или их комбинацией.
Дополнительные последовательности scFv, связывающего CD20, представлены ниже:
Последовательность scFv CAR для CD22 человека (VH-(G4S)-VL)
EVQLQQSGPGLVKPSQTLSLTCAISGDSMLSNSDTWNWIRQSPSRGLEWLGRTYHRSTWYDDYASSVRGRVSINVDTSKNQYSLQLNAVTPEDTGVYYCARVRLQDGNSWSDAFDVWGQGTMVTVSSGGGGSQSALTQPASASGSPGQSVTISCTGTSSDVGGYNYVSWYQQHPGKAPKLMIYDVSNRPSGVSNRFSGSKSGNTASLTISGLQAEDEADYYCSSYTSSSTLYVFGTGTQLTVL (SEQ ID NO: 1447)
Последовательность scFv CAR для CD22 человека (VL-(G4S)3-VH)
QSALTQPASASGSPGQSVTISCTGTSSDVGGYNYVSWYQQHPGKAPKLMIYDVSNRPSGVSNRFSGSKSGNTASLTISGLQAEDEADYYCSSYTSSSTLYVFGTGTQLTVLGGGGSGGGGSGGGGSEVQLQQSGPGLVKPSQTLSLTCAISGDSMLSNSDTWNWIRQSPSRGLEWLGRTYHRSTWYDDYASSVRGRVSINVDTSKNQYSLQLNAVTPEDTGVYYCARVRLQDGNSWSDAFDVWGQGTMVTVSS (SEQ ID NO: 1448)
Последовательность scFv CAR для CD22 человека (VL-(G4S)-VH)
QSALTQPASASGSPGQSVTISCTGTSSDVGGYNYVSWYQQHPGKAPKLMIYDVSNRPSGVSNRFSGSKSGNTASLTISGLQAEDEADYYCSSYTSSSTLYVFGTGTQLTVLGGGGSEVQLQQSGPGLVKPSQTLSLTCAISGDSMLSNSDTWNWIRQSPSRGLEWLGRTYHRSTWYDDYASSVRGRVSINVDTSKNQYSLQLNAVTPEDTGVYYCARVRLQDGNSWSDAFDVWGQGTMVTVSS (SEQ ID NO: 1449)
Порядок, в котором VL- и VH-домены появляются в scFv, может меняться (т. е. находятся в VL-VH или VH-VL ориентации), и при этом любое число из одной, двух, трех или четырех копий субъединиц "G4S" (SEQ ID NO: 168), где каждая субъединица содержит последовательность GGGGS (SEQ ID NO: 168) (например, (G4S)3 (SEQ ID NO: 142) или (G4S)4(SEQ ID NO: 141)), может соединять вариабельные домены для создания целого scFv-домена. В качестве альтернативы, конструкция CAR может содержать, например, линкер, содержащий последовательность GSTSGSGKPGSGEGSTKG (SEQ ID NO: 821). В качестве альтернативы, конструкция CAR может содержать, например, линкер, содержащий последовательность LAEAAAK (SEQ ID NO: 822). В одном варианте осуществления конструкция CAR не содержит линкер между VL- и VH-доменами.
Все эти клоны содержали изменение остатка Q/K в сигнальном домене костимулирующего домена, полученного из цепи CD3-дзета.
В некоторых вариантах осуществления молекула CAR, описанная в данном документе представляет собой молекулу биспецифического CAR. В одном варианте осуществления молекула биспецифического CAR содержит первую специфичность связывания с CD19, например, специфичность связывания с CD19 в виде VL1-VH1, и вторую специфичность связывания с CD22, например, специфичность связывания с CD22 в виде VL2-VH2 или VH2-VL1. В одном варианте осуществления первая и вторая специфичности связывания расположены в виде непрерывной полипептидной цепи, например, одной цепи. В некоторых вариантах осуществления первая и вторая специфичности связывания необязательно содержат линкер, описанный в данном документе. В некоторых вариантах осуществления молекула биспецифического CAR содержит CD19-связывающий домен, содержащий аминокислотную последовательность, раскрытую в таблице 5 и таблице 30.
В одном варианте осуществления молекула биспецифического CAR содержит первую специфичность связывания с CD22, например, специфичность связывания c CD22 в виде VL2-VH2 или VH2-VL1, и вторую специфичность связывания c CD19, например, специфичность связывания c CD19 в виде VL1-VH1. В одном варианте осуществления первая и вторая специфичности связывания расположены в виде непрерывной полипептидной цепи, например, одной цепи. В некоторых вариантах осуществления первая и вторая специфичности связывания необязательно содержат линкер, описанный в данном документе.
В некоторых вариантах осуществления линкер представляет собой линкер (Gly4-Ser)n, где n составляет 1, 2, 3, 4, 5 или 6. В некоторых вариантах осуществления линкер представляет собой (Gly4-Ser)n, где n=1 (SEQ ID NO: 168), например, линкер имеет аминокислотную последовательность Gly4-Ser (SEQ ID NO: 168). В некоторых вариантах осуществления линкер представляет собой (Gly4-Ser)n, где n=3 (SEQ ID NO: 142). В некоторых вариантах осуществления линкер представляет собой (Gly4-Ser)n, где n= 4 (SEQ ID NO: 141). В некоторых вариантах осуществления линкер содержит, например, состоит из аминокислотной последовательности: LAEAAAK (SEQ ID NO: 822).
CAR для CD20
В некоторых вариантах осуществления описанная в данном документе клетка, экспрессирующая CAR, представляет собой клетку, экспрессирующую CAR для CD20 (например, клетку, экспрессирующую CAR, который связывается с CD20 человека). В некоторых вариантах осуществления клетка, экспрессирующая CAR для CD20, содержит антигенсвязывающий домен в соответствии с WO2016/164731 и PCT/US2017/055627, включенными в данном документе посредством ссылки. Иллюстративные CD20-связывающие последовательности или последовательности CAR для CD20 раскрыты, например, в таблицах 1-5 из PCT/US2017/055627, включенной в данный документ посредством ссылки. В некоторых вариантах осуществления CD20-связывающие последовательности или CAR для CD20 содержит CDR, вариабельную область, scFv или полноразмерную последовательность CAR для CD20, раскрытую в PCT/US2017/055627 или WO2016/164731, включенных в данный документ посредством ссылки. Иллюстративные последовательности CAR, связывающих CD20, могут содержать CDR, вариабельную область, scFv или полноразмерную последовательность CAR, раскрытую в таблице 32 (или последовательность на по меньшей мере приблизительно 85%, 90%, 95%, 99% или более идентичную ей и/или имеющую одну, две, три или более замен, вставок, делеций или модификаций).
CAR для CLL-1
В других вариантах осуществления клетки, экспрессирующие CAR, могут специфически связываться с CLL-1, например, могут содержать молекулу CAR или антигенсвязывающий домен в соответствии с таблицей 2 из WO2016/014535, включенной в данный документ посредством ссылки. Иллюстративные аминокислотные последовательности молекул CAR для CLL-1 и антигенсвязывающих доменов (например, содержащих одну, две, три CDR VH и одну, две, три CDR VL согласно Kabat или Chothia) и нуклеотидные последовательности, кодирующие их, представлены в WO2016/014535.
GFR-альфа-4
В других вариантах осуществления клетки, экспрессирующие CAR, могут специфически связываться с GFR-альфа 4, например, могут содержать молекулу CAR или антигенсвязывающий домен в соответствии с таблицей 2 из WO2016/025880, включенной в данный документ посредством ссылки. Иллюстративные аминокислотные последовательности молекул CAR для GFR-альфа-4 и антигенсвязывающих доменов (например, содержащих одну, две, три CDR VH и одну, две, три CDR VL согласно Kabat или Chothia) и нуклеотидные последовательности, кодирующие их, представлены в WO2016/025880.
В одном варианте осуществления антигенсвязывающий домен любой из молекул CAR, описанных в данном документе (например, для любого из CD19, CD123, EGFRvIII, CD33, мезотелина, BCMA и GFR-альфа 4), содержит одну, две, три (например, все три) CDR тяжелой цепи, CDR1 HC, CDR2 HC и CDR3 HC, из антитела, перечисленного выше, и/или одну, две, три (например, все три) CDR легкой цепи, CDR1 LC, CDR2 LC и CDR3 LC, из антигенсвязывающего домена, перечисленного выше. В одном варианте осуществления антигенсвязывающий домен содержит вариабельную область тяжелой цепи и/или вариабельную область легкой цепи антитела, перечисленного или описанного выше.
В одном аспекте противоопухолевый антигенсвязывающий домен представляет собой фрагмент, например, одноцепочечный вариабельный фрагмент (scFv). В одном аспекте связывающий домен для антигена, ассоциированного с раком, описанного в данном документе, представляет собой Fv, Fab, (Fab')2 или бифункциональное (например, биспецифическое) гибридное антитело (например, Lanzavecchia et al., Eur. J. Immunol. 17, 105 (1987)). В одном аспекте антитела и их фрагменты по настоящему изобретению связываются с белком, представляющим собой антиген, ассоциированный с раком, описанный в данном документе, с аффинностью дикого типа или усиленной аффинностью.
В некоторых случаях scFv можно получить в соответствии со способом, известным из уровня техники (см., например, Bird et al., (1988) Science 242:423-426 и Huston et al., (1988) Proc. Natl. Acad. Sci. USA 85:5879-5883). Молекулы scFv можно получить путем связывания VH- и VL-областей друг с другом с помощью гибких полипептидных линкеров. Молекулы scFv содержат линкер (например, Ser-Gly линкер) с оптимизированными длиной и/или аминокислотным составом. Длина линкера может сильно влиять на укладку и взаимодействие вариабельных областей scFv. В действительности, если используют короткий полипептидный линкер (например, длиной 5-10 аминокислот), то предотвращается укладка внутри одной цепи. Межцепочечная укладка также необходима для объединения двух вариабельных областей вместе с образованием функционального эпитопсвязывающего участка. Примеры ориентации и размера линкеров см., например, в Hollinger et al. 1993 Proc Natl Acad. Sci. U.S.A. 90:6444-6448, публикациях заявок на патент США №№ 2005/0100543, 2005/0175606, 2007/0014794 и публикациях согласно PCT №№ WO2006/020258 и WO2007/024715, включенных в данный документ посредством ссылки.
В другом аспекте антигенсвязывающий домен представляет собой T-клеточный рецептор ("TCR") или его фрагмент, например, одноцепочечный TCR (scTCR). Способы получения таких TCR известны из уровня техники. См., например, Willemsen RA et al, Gene Therapy 7: 1369-1377 (2000); Zhang T et al, Cancer Gene Ther 11: 487-496 (2004); Aggen et al, Gene Ther. 19(4):365-74 (2012) (литературные источники включены в данный документ во всей своей полноте). Например, может быть сконструирован scTCR, который содержит гены Vα и Vβ из клона Т-клеток, связанные с помощью линкера (например, гибкого пептида). Данный подход является весьма применимым для мишени, ассоциированной с раком, которая сама по себе является внутриклеточной, однако фрагмент такого антигена (пептида) презентируется на поверхности раковых клеток с помощью MHC.
Дополнительные иллюстративные антигенсвязывающие домены и CAR
В одном варианте осуществления антигенсвязывающий домен для GD2 представляет собой антигенсвязывающую часть, например, CDR, антитела, описанного, например, в Mujoo et al., Cancer Res. 47(4):1098-1104 (1987); Cheung et al., Cancer Res 45(6):2642-2649 (1985), Cheung et al., J Clin Oncol 5(9):1430-1440 (1987), Cheung et al., J Clin Oncol 16(9):3053-3060 (1998), Handgretinger et al., Cancer Immunol Immunother 35(3):199-204 (1992). В некоторых вариантах осуществления антигенсвязывающий домен для GD2 представляет собой антигенсвязывающую часть антитела, выбранного из mAb 14.18, 14G2a, ch14.18, hu14.18, 3F8, hu3F8, 3G6, 8B6, 60C3, 10B8, ME36.1 и 8H9, см., например, WO2012033885, WO2013040371, WO2013192294, WO2013061273, WO2013123061, WO2013074916 и WO201385552. В некоторых вариантах осуществления антигенсвязывающий домен для GD2 представляет собой антигенсвязывающую часть антитела, описанного в публикации заявки на патент США № 20100150910 или публикации согласно PCT № WO 2011160119.
В одном варианте осуществления антигенсвязывающий домен для Tn-антигена, sTn-антигена, Tn-O-гликопептидного антигена или sTn-O-гликопептидного антигена представляет собой антигенсвязывающую часть, например, CDR, антитела, описанного, например, в US 2014/0178365, US8440798, EP 2083868 A2, Brooks et al., PNAS 107(22):10056-10061 (2010) и Stone et al., OncoImmunology 1(6):863-873 (2012).
В одном варианте осуществления антигенсвязывающий домен для PSMA, представляет собой антигенсвязывающую часть, например, CDR, антитела, описанного например, в Parker et al., Protein Expr Purif 89(2):136-145 (2013), US 20110268656 (J591 ScFv); Frigerio et al., European J. Cancer 49(9):2223-2232 (2013) (scFvD2B); WO 2006125481 (mAb 3/A12, 3/E7 и 3/F11), и одноцепочечные фрагменты антител (scFv A5 и D7).
В одном варианте осуществления антигенсвязывающий домен для CD97 представляет собой антигенсвязывающую часть, например, CDR, антитела, описанного, например, в US6846911; de Groot et al., J. Immunol. 183(6):4127-4134 (2009); или антитела от R&D: MAB3734.
В одном варианте осуществления антигенсвязывающий домен для TAG72 представляет собой антигенсвязывающую часть, например, CDR, антитела, описанного, например, в Hombach et al., Gastroenterology 113(4):1163-1170 (1997); и ab691 от Abcam.
В одном варианте осуществления антигенсвязывающий домен для CD44v6 представляет собой антигенсвязывающую часть, например, CDR, антитела, описанного, например, в Casucci et al., Blood 122(20):3461-3472 (2013).
В одном варианте осуществления антигенсвязывающий домен для СЕА представляет собой антигенсвязывающую часть, например, CDR, антитела, описанного, например, в Chmielewski et al., Gastoenterology 143(4):1095-1107 (2012).
В одном варианте осуществления антигенсвязывающий домен для EPCAM представляет собой антигенсвязывающую часть, например, CDR, антитела, выбранного из MT110, биспецифического Ab к EpCAM-CD3 (см., например, clinicaltrials.gov/ct2/show/NCT00635596); эдреколомаба; 3622W94; ING-1 и адекатумумаба (MT201).
В одном варианте осуществления антигенсвязывающий домен для KIT представляет собой антигенсвязывающую часть, например CDR, антитела, описанного, например, в US7915391, US20120288506 и нескольких коммерческих каталогах антител.
В одном варианте осуществления антигенсвязывающий домен для IL-13Ra2 представляет собой антигенсвязывающую часть, например, CDR, антитела, описанного, например, в WO2008/146911, WO2004087758, нескольких коммерческих каталогах антител и WO2004087758.
В одном варианте осуществления антигенсвязывающий домен для CD171 представляет собой антигенсвязывающую часть, например, CDR, антитела, описанного, например, в Hong et al., J Immunother 37(2):93-104 (2014).
В одном варианте осуществления антигенсвязывающий домен для PSCA представляет собой антигенсвязывающую часть, например, CDR, антитела, описанного, например, в Morgenroth et al., Prostate 67(10):1121-1131 (2007) (scFv 7F5); Nejatollahi et al., J of Oncology 2013(2013), ID статьи 839831 (scFv C5-II); и публикации патента США № 20090311181.
В одном варианте осуществления антигенсвязывающий домен для MAD-CT-2 представляет собой антигенсвязывающую часть, например, CDR, антитела, описанного, например, в PMID: 2450952; US7635753.
В одном варианте осуществления антигенсвязывающий домен для рецептора фолиевой кислоты альфа-типа представляет собой антигенсвязывающую часть, например, CDR, антитела IMGN853 или антитела, описанного в US20120009181; US4851332, LK26: US5952484.
В одном варианте осуществления антигенсвязывающий домен для ERBB2 (Her2/neu) представляет собой антигенсвязывающую часть, например, CDR, антитела трастузумаба или пертузумаба.
В одном варианте осуществления антигенсвязывающий домен для MUC1 представляет собой антигенсвязывающую часть, например, CDR, антитела SAR566658.
В одном варианте осуществления антигенсвязывающий домен для EGFR представляет собой антигенсвязывающую часть, например, CDR, антитела цетуксимаба, панитумумаба, залутумумаба, нимотузумаба или матузумаба.
В одном варианте осуществления антигенсвязывающий домен для NCAM представляет собой антигенсвязывающую часть, например, CDR, клона антитела 2-2B: MAB5324 (EMD Millipore)
В одном варианте осуществления антигенсвязывающий домен для CAIX представляет собой антигенсвязывающую часть, например, CDR, клона антитела 303123 (R&D Systems).
В одном варианте осуществления антигенсвязывающий домен для Fos-родственного антигена 1 представляет собой антигенсвязывающую часть, например, CDR, антитела 12F9 (Novus Biologicals).
В одном варианте осуществления антигенсвязывающий домен для SSEA-4 представляет собой антигенсвязывающую часть, например, CDR, антитела MC813 (Cell Signaling) или других коммерчески доступных антител.
В одном варианте осуществления антигенсвязывающий домен для PDGFR-бета представляет собой антигенсвязывающую часть, например, CDR, антитела ab32570 от Abcam.
В одном варианте осуществления антигенсвязывающий домен для ALK представляет собой антигенсвязывающую часть, например, CDR, антитела, описанного, например, в Mino-Kenudson et al., Clin Cancer Res 16(5):1561-1571 (2010).
В одном варианте осуществления антигенсвязывающий домен для полисиаловой кислоты представляет собой антигенсвязывающую часть, например CDR, антитела, описанного, например, в Nagae et al., J Biol Chem 288(47):33784-33796 (2013).
В одном варианте осуществления антигенсвязывающий домен для PLAC1 представляет собой антигенсвязывающую часть, например, CDR, антитела, описанного, например, в Ghods et al., Biotechnol Appl Biochem 2013 doi:10.1002/bab.1177.
В одном варианте осуществления антигенсвязывающий домен для GloboH представляет собой антигенсвязывающую часть антитела VK9 или антитела, описанного, например, в Kudryashov V et al., Glycoconj J.15(3):243-9 (1998), Lou et al., Proc Natl Acad Sci USA 111(7):2482-2487 (2014); MBr1: Bremer E-G et al. J Biol Chem 259:14773-14777 (1984).
В одном варианте осуществления антигенсвязывающий домен для NY-BR-1 представляет собой антигенсвязывающую часть, например, CDR, антитела, описанного, например, в Jager et al., Appl Immunohistochem Mol Morphol 15(1):77-83 (2007).
В одном варианте осуществления антигенсвязывающий домен для белка 17 сперматозоидов представляет собой антигенсвязывающую часть, например, CDR, антитела, описанного, например, в Song et al., Target Oncol 2013 Aug 14 (PMID: 23943313); Song et al., Med Oncol 29(4):2923-2931 (2012).
В одном варианте осуществления антигенсвязывающий домен для TRP-2 представляет собой антигенсвязывающую часть, например, CDR, антитела, описанного, например, в Wang et al, J Exp Med. 184(6):2207-16 (1996).
В одном варианте осуществления антигенсвязывающий домен для CYP1B1 представляет собой антигенсвязывающую часть, например, CDR, антитела, описанного, например, в Maecker et al, Blood 102 (9): 3287-3294 (2003).
В одном варианте осуществления антигенсвязывающий домен для RAGE-1 представляет собой антигенсвязывающую часть, например, CDR, антитела MAB5328 (EMD Millipore).
В одном варианте осуществления антигенсвязывающий домен для обратной транскриптазы, представляющей собой теломеразу человека, представляет собой антигенсвязывающую часть, например, CDR, антитела под кат. №: LS-B95-100 (Lifespan Biosciences)
В одном варианте осуществления антигенсвязывающий домен для кишечной карбоксилэстеразы представляет собой антигенсвязывающую часть, например, CDR, антитела 4F12 под кат. №: LS-B6190-50 (Lifespan Biosciences).
В одном варианте осуществления антигенсвязывающий домен для mut hsp70-2 представляет собой антигенсвязывающую часть, например, CDR, моноклонального антитела от Lifespan Biosciences под кат. №: LS-C133261-100 (Lifespan Biosciences).
В одном варианте осуществления антигенсвязывающий домен для MAD-CT-2 представляет собой антигенсвязывающую часть, например, CDR, антитела, описанного, например, в PMID: 2450952; US7635753.
В одном варианте осуществления антигенсвязывающий домен содержит одну, две, три (например, все три) CDR тяжелой цепи, CDR1 HC, CDR2 HC и CDR3 HC, антитела, перечисленного выше, и/или одну, две, три (например, все три) CDR легкой цепи, CDR1 LC, CDR2 LC и CDR3 LC, антитела, перечисленного выше. В одном варианте осуществления антигенсвязывающий домен содержит вариабельную область тяжелой цепи и/или вариабельную область легкой цепи антитела, перечисленного выше.
В некоторых вариантах осуществления антигенсвязывающий домен CAR нацеливается на опухолевый антиген, который представляет собой антиген, экспрессированный на миелоидной опухоли (либо поверхностный антиген, либо презентируемый с помощью молекулы MHC), и клетка, содержащая такой CAR, распознает антиген миелоидной опухоли.
В варианте осуществления антиген миелоидной опухоли представляет собой антиген, который предпочтительно или специфически экспрессируется на поверхности клетки миелоидной опухоли.
В одном варианте осуществления антигенсвязывающий домен CAR может быть выбран таким образом, чтобы он нацеливался на популяцию клеток миелоидной опухоли. В качестве альтернативы, если необходимо нацеливание на более чем один тип миелоидной опухоли, можно выбрать антигенсвязывающий домен, который нацеливается на антиген миелоидной опухоли, который экспрессируется более чем одной, например, всеми миелоидными опухолями, на которые необходимо нацеливание.
CAR может нацеливаться на следующие дополнительные опухолевые антигены: CD123, CD34, Flt3, CD33 и CLL-1. В вариантах осуществления опухолевый антиген выбран из CD123, CD33 и CLL-1. В некоторых вариантах осуществления опухолевый антиген представляет собой CD123. В некоторых вариантах осуществления опухолевый антиген представляет собой CD33. В некоторых вариантах осуществления опухолевый антиген представляет собой CD34. В некоторых вариантах осуществления опухолевый антиген представляет собой Flt3. В вариантах осуществления опухолевый антиген представляет собой CLL-1. В вариантах осуществления антигенсвязывающий домен нацеливается на антиген человека.
В одном аспекте антигенсвязывающий домен CAR связывается с CD123, например, CD123 человека. В настоящем изобретении может быть применен любой известный CD123-связывающий домен. В одном варианте осуществления антигенсвязывающий домен для CD123 представляет собой антигенсвязывающую часть, например CDR или VH и VL, антитела, антигенсвязывающего фрагмента или CAR, описанных, например, в публикации согласно РСТ WO2014/130635, включенной в данный документ посредством ссылки. В одном варианте осуществления антигенсвязывающий домен для CD123 представляет собой антигенсвязывающую часть, например, CDR или VH и VL, антитела, антигенсвязывающего фрагмента или CAR, описанных, например, в публикации согласно РСТ WO/2016/028896, включенной в данный документ посредством ссылки. В одном варианте осуществления антигенсвязывающий домен для CD123 представляет собой антигенсвязывающую часть, например, CDR, антитела, антигенсвязывающего фрагмента или CAR, описанных, например, в публикации согласно РСТ WO1997/024373, WO2008/127735 (например, CD123-связывающий домен из 26292, 32701, 37716 или 32703), WO2014/138805 (например, CD123-связывающий домен из CSL362), WO2014/138819, WO2013/173820, WO2014/144622, WO2001/66139, WO2010/126066 (например, CD123-связывающий домен из любого из Old4, Old5, Old17, Old19, New102 или Old6), WO2014/144622, WO2016/028896 или US2009/0252742, включенных в данный документ посредством ссылки. В вариантах осуществления антигенсвязывающий домен представляет собой домен мыши, связывающий CD123 человека, или получен из него. В вариантах осуществления антигенсвязывающий домен представляет собой гуманизированное антитело или фрагмент антитела, например, scFv-домен. В варианте осуществления антигенсвязывающий домен представляет собой антитело человека или фрагмент антитела, которые связываются с CD123 человека. В вариантах осуществления антигенсвязывающий домен представляет собой scFv-домен, который содержит вариабельную область легкой цепи (VL) и вариабельную область тяжелой цепи (VH). VL и VH могут присоединяться с помощью линкера, описанного в данном документе, например, содержащего последовательность GGGGSGGGGSGGGGS (SEQ ID NO: 142), и могут находиться в любой ориентации, например, VL-линкер-VH или VH-линкер-VL.
В некоторых вариантах осуществления антигенсвязывающий домен CAR нацеливается на B-клеточный антиген. В варианте осуществления B-клеточный антиген представляет собой антиген, который предпочтительно или специфически экспрессируется на поверхности В-клетки. Антиген может экспрессироваться на поверхности любого из следующих типов B-клеток: предшественники B-клеток (например, пре-B-клетки или про-B-клетки), ранние про-В-клетки, поздние про-В-клетки, крупные пре-В-клетки, малые пре-В-клетки, незрелые В-клетки, например, наивные В-клетки, зрелые В-клетки, плазматические В-клетки, плазмобласты, В-клетки памяти, В-1-клетки, В-2-клетки, В-клетки маргинальной зоны, фолликулярные В-клетки, В-клетки зародышевого центра или регуляторные В-клетки (Breg).
В настоящем изобретении предусмотрены CAR, которые могут нацеливаться на следующие антигены: CD19; CD123; CD22; CD30; CD171; CS-1; лектиноподобной молекулы-1 C-типа, CD33; варианта III рецептора эпидермального фактора роста (EGFRvIII); ганглиозида G2 (GD2); ганглиозида GD3; представителя семейства рецепторов TNF; антигена созревания B-клеток; Tn-антигена ((Tn Ag) или (GalNAcα-Ser/Thr)); простатического специфического мембранного антигена (PSMA); орфанного рецептора-1, подобного рецепторной тирозинкиназе (ROR1); Fms-подобной тирозинкиназы 3 (FLT3); опухолеассоциированного гликопротеина-72 (TAG72); CD38; CD44v6; раково-эмбрионального антигена (CEA); молекулы адгезии эпителиальных клеток (EPCAM); B7H3 (CD276); KIT (CD117); субъединицы альфа-2 рецептора интерлейкина-13; мезотелина; альфа-субъединицы рецептора интерлейкина-11 (IL-11Ra); антигена стволовых клеток предстательной железы (PSCA); сериновой протеазы-21; рецептора-2 фактора роста эндотелия сосудов (VEGFR2); антигена системы Льюис (Y); CD24; рецептора фактора роста тромбоцитов бета-типа (PDGFR-бета); стадиеспецифического эмбрионального антигена-4 (SSEA-4); CD20; рецептора фолиевой кислоты альфа-типа; рецепторной тирозинпротеинкиназы ERBB2 (Her2/neu); муцина-1, ассоциированного с клеточной поверхностью (MUC1); рецептора эпидермального фактора роста (EGFR); молекулы адгезии нейронов (NCAM); простазы; простатической кислой фосфатазы (PAP); мутантного фактора элонгации 2 (ELF2M); эфрина B2; белка активации фибробластов альфа (FAP); рецептора инсулиноподобного фактора роста-1 (рецептора IGF-I), карбоангидразы IX (CAIX); субъединицы-9 протеасомы (просомы, мультикаталитической протеазы) бета-типа (LMP2); гликопротеина 100 (gp100); онкогенного слитого белка, состоящего из кластерного региона точечных разрывов (BCR) и гомолога-1 вирусного онкогена лейкоза мышей Абельсона (Abl) (bcr-abl); тирозиназы; эфринового рецептора-2 A-типа (EphA2); фукозил-GM1; молекулы адгезии, представляющей собой сиалилированный антиген системы Льюис (sLe); ганглиозида GM3; трансглютаминазы-5 (TGS5); высокомолекулярного меланома-ассоциированного антигена (HMWMAA); ганглиозида o-ацетил-GD2 (OAcGD2); рецептора фолиевой кислоты бета-типа; маркера-1 эндотелия опухоли (TEM1/CD248); белка, родственного маркеру-7 эндотелия опухоли (TEM7R); клаудина-6 (CLDN6); рецептора тиреотропного гормона (TSHR); представителя D группы 5 класса С рецепторов, сопряженных с G-белком (GPRC5D); белка, кодируемого открытой рамкой считывания 61 X-хромосомы (CXORF61); CD97; CD179a; киназы анапластической лимфомы (ALK); полисиаловой кислоты; плацентоспецифического белка-1 (PLAC1); гексасахаридной части гликоцерамида globoH (GloboH); дифференцировочного антигена молочной железы (NY-BR-1); уроплакина-2 (UPK2); клеточного рецептора-1 вируса гепатита A (HAVCR1); бета-3 адренорецептора (ADRB3); паннексина-3 (PANX3); рецептора-20, сопряженного с G-белком (GPR20); антигена локуса K9 комплекса лимфоцитарных антигенов 6 (LY6K); обонятельного рецептора 51E2 (OR51E2); белка, кодируемого альтернативной рамкой считывания гена TCR-гамма (TARP); белка опухоли Вильмса (WT1); раково-тестикулярного антигена-1 (NY-ESO-1); раково-тестикулярного антигена-2 (LAGE-1a); меланома-ассоциированного антигена-1 (MAGE-A1); белка, кодируемого транслокационным вариантом-6 гена ETS, локализованным в р-плече 12 хромосомы (ETV6-AML); белка-17 сперматозоидов (SPA17); представителя 1А семейства X-антигенов (XAGE1); ангиопоэтин-связывающего рецептора-2 клеточной поверхности 2 (Tie 2); раково-тестикулярного антигена-1 из клеток меланомы (MAD-CT-1); раково-тестикулярного антигена-2 из клеток меланомы (MAD-CT-2); Fos-родственного антигена-1; опухолевого белка p53 (p53); мутанта p53; простеина; сурвивина; теломеразы; опухолевого антигена-1 карциномы предстательной железы, антигена-1 меланомы, распознаваемого T-клетками; мутантного белка саркомы крыс (Ras); обратной транскриптазы теломеразы человека (hTERT); антигенов саркомы с точечными разрывами при транслокации; меланомного ингибитора апоптоза (ML-IAP); ERG (продукта слитого гена трансмембранной сериновой протеазы-2 (TMPRSS2) и ETS); N-ацетилглюкозаминилтрансферазы V (NA17); белка с парным box-доменом Рах-3 (PAX3); андрогенового рецептора; циклина-B1; нейробластомного гомолога вирусного онкогена миелоцитоматоза птиц v-myc (MYCN); представителя С семейства гомологов Ras (RhoC); белка-2, родственного тирозиназе (TRP-2); цитохрома P450 1B1 (CYP1B1); белка, подобного CCCTC-связывающему фактору (белку с "цинковыми пальцами"), антигена плоскоклеточной карциномы 3, распознаваемого Т-клетками (SART3); белка с парным box-доменом Рах-5 (PAX5); проакрозин-связывающего белка sp32 (OY-TES1); лимфоцит-специфической протеинтирозинкиназы (LCK); якорного белка-4 киназы A (AKAP-4); антигена 2 синовиальной саркомы с точечным разрывом в X-хромосоме (SSX2); рецептора конечных продуктов неферментативного гликозилирования (RAGE-1); почечного убиквитарного белка-1 (RU1); почечного убиквитарного белка-2 (RU2); легумаина; Е6 вируса папилломы человека (HPV E6); Е7 вируса папилломы человека (HPV E7); кишечной карбоксилэстеразы; мутантного белка теплового шока 70-2 (mut hsp70-2); CD79a; CD79b; CD72; иммуноглобулиноподобного рецептора-1, ассоциированного с лейкоцитами (LAIR1); рецептора Fc-фрагмента IgA (FCAR или CD89); представителя 2 подсемейства А иммуноглобулиноподобных рецепторов лейкоцитов (LILRA2); представителя f семейства белков, подобных молекулам CD300 (CD300LF); представителя А семейства 12 лектиновых доменов С-типа (CLEC12A); антигена-2 клеток стромы костного мозга (BST2); белка-2, подобного муциноподобному рецептору гормонов, содержащему EGF-подобный модуль (EMR2); лимфоцитарного антигена-75 (LY75); глипикана-3 (GPC3); белка-5, подобного Fc-рецептору (FCRL5); полипептида-1, подобного лямбда-цепи иммуноглобулина (IGLL1); представителя семейства рецепторов TNF; Fms-подобной тирозинкиназы-3 (FL T3); CD10, CD19, CD20, CD21, CD22, CD23, CD24, CD25, CD37, CD38, CD53, CD72, CD73, CD74, CD75, CD77, CD79a, CD79b, CD80, CD81, CD82, CD83, CD84, CD85, ROR1, BCMA, CD86 и CD179b. Другие B-клеточные антигены, на которые может нацеливаться CAR, описанный в данном документе, включают: CD1a, CD1b, CD1c, CD1d, CD2, CD5, CD6, CD9, CD11a, CD11b, CD11c, CD17, CD18, CD26, CD27, CD29, CD30, CD31, CD32a, CD32b, CD35, CD38, CD39, CD40, CD44, CD45, CD45RA, CD45RB, CD45RC, CD45RO, CD46, CD47, CD48, CD49b, CD49c, CD49d, CD50, CD52, CD54, CD55, CD58, CD60a, CD62L, CD63, CD63, CD68 CD69, CD70, CD85E, CD85I, CD85J, CD92, CD95, CD97, CD98, CD99, CD100, CD102, CD108, CD119, CD120a, CD120b, CD121b, CD122, CD124, CD125, CD126, CD130, CD132, CD137, CD138, CD139, CD147, CD148, CD150, CD152, CD162, CD164, CD166, CD167a, CD170, CD175, CD175s, CD180, CD184, CD185, CD192, CD196, CD197, CD200, CD205, CD210a, CDw210b, CD212, CD213a1, CD213a2, CD215, CD217, CD218a, CD218b, CD220, CD221, CD224, CD225, CD226, CD227, CD229, CD230, CD232, CD252, CD253, CD257, CD258, CD261, CD262, CD263, CD264, CD267, CD268, CD269, CD270, CD272, CD274, CD275, CD277, CD279, CD283, CD289, CD290, CD295, CD298, CD300a, CD300c, CD305, CD306, CD307a, CD307b, CD307c, CD307d, CD307e, CD314, CD315, CD316, CD317, CD319, CD321, CD327, CD328, CD329, CD338, CD351, CD352, CD353, CD354, CD355, CD357, CD358, CD360, CD361, CD362 и CD363.
В другом варианте осуществления антиген, на который нацеливается CAR, выбран из CD19, BCMA, CD20, CD22, FcRn5, FcRn2, CS-1 и CD138. В варианте осуществления антиген, на который нацеливается CAR, представляет собой CD19. В варианте осуществления антиген, на который нацеливается CAR, представляет собой CD20. В варианте осуществления антиген, на который нацеливается CAR, представляет собой CD22. В варианте осуществления антиген, на который нацеливается CAR, представляет собой BCMA. В варианте осуществления антиген, на который нацеливается CAR, представляет собой FcRn5. В варианте осуществления антиген, на который нацеливается CAR, представляет собой FcRn2. В варианте осуществления антиген, на который нацеливается CAR, представляет собой CS-1. В варианте осуществления антиген, на который нацеливается CAR, представляет собой CD138.
В одном варианте осуществления антигенсвязывающий домен CAR, например, CAR, экспрессируемого клеткой по настоящему изобретению (например, клеткой, которая также экспрессирует CAR), может быть выбран таким образом, чтобы он нацеливался на предпочтительную популяцию B клеток. Например, в варианте осуществления, в котором необходимо нацеливание на регуляторные B-клетки, выбирают антигенсвязывающий домен, который нацеливается на антиген, который экспрессируется на регуляторных B-клетках, а не на других популяциях B-клеток, например, плазматических B-клетках и B-клетках памяти. Маркеры клеточной поверхности, экспрессируемые на регуляторных В-клетках, включают: CD19, CD24, CD25, CD38 или CD86 или маркеры, описанные в He et al., 2014, J Immunology Research, ID статьи 215471. Если необходимо нацеливание на более чем один тип B-клеток, можно выбрать антигенсвязывающий домен, который нацеливается на антиген, который экспрессируется всеми B-клетками, на которые необходимо нацеливание.
Трансмембранный домен CAR
Что касается трансмембранного домена, в различных вариантах осуществления CAR можно разработать таким образом, чтобы он содержал трансмембранный домен, присоединенный к внеклеточному домену CAR. Трансмембранный домен может содержать одну или несколько дополнительных аминокислот, прилегающих к трансмембранной области, например, одну или несколько аминокислот, относящихся к внеклеточной области белка, из которого получен трансмембранный домен (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 и до 15 аминокислот внеклеточной области), и/или одну или несколько дополнительных аминокислот, относящихся к внутриклеточной области белка, из которого получен трансмембранный домен (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 и до 15 аминокислот внутриклеточной области). В одном аспекте трансмембранный домен представляет собой домен, ассоциированный с одним из других доменов CAR. В некоторых случаях трансмембранный домен может быть выбран или модифицирован с помощью аминокислотной замены, чтобы избежать связывания таких доменов с трансмембранными доменами тех же или других поверхностных мембранных белков, например, чтобы свести к минимуму взаимодействия с другими элементами рецепторного комплекса. В одном аспекте трансмембранный домен способен к гомодимеризации с другим CAR на клеточной поверхности клетки, экспрессирующей CAR. В другом аспекте аминокислотную последовательность трансмембранного домена можно модифицировать или подвергнуть замене таким образом, чтобы свести к минимуму взаимодействия со связывающими доменами нативного партнера по связыванию, присутствующего в той же CART.
Трансмембранный домен может быть получен или из природного, или из рекомбинантного источника. Если источник является природным, то домен может быть получен из любого мембраносвязанного или трансмембранного белка. В одном аспекте трансмембранный домен способен передавать сигнал внутриклеточному(-ым) домену(-ам) всякий раз, когда CAR связался с мишенью. Трансмембранный домен, особенно применимый в настоящем изобретении, может включать по меньшей мере трансмембранную(-ые) область(-и), например, альфа-, бета или дзета-цепи Т-клеточного рецептора, CD28, CD27, CD3-эпсилон, CD45, CD4, CD5, CD8, CD9, CD16, CD22, CD33, CD37, CD64, CD80, CD86, CD134, CD137, CD154. В некоторых вариантах осуществления трансмембранный домен может включать по меньшей мере трансмембранную(-ые) область(-и), например, KIR2DS2, OX40, CD2, CD27, LFA-1 (CD11a, CD18), ICOS (CD278), 4-1BB (CD137), GITR, CD40, BAFFR, HVEM (LIGHTR), SLAMF7, NKp80 (KLRF1), NKp44, NKp30, NKp46, CD160, CD19, IL2R-бета, IL2R-гамма, IL7R α, ITGA1, VLA1, CD49a, ITGA4, IA4, CD49D, ITGA6, VLA-6, CD49f, ITGAD, CD11d, ITGAE, CD103, ITGAL, CD11a, LFA-1, ITGAM, CD11b, ITGAX, CD11c, ITGB1, CD29, ITGB2, CD18, LFA-1, ITGB7, TNFR2, DNAM1 (CD226), SLAMF4 (CD244, 2B4), CD84, CD96 (Tactile), CEACAM1, CRTAM, Ly9 (CD229), CD160 (BY55), PSGL1, CD100 (SEMA4D), SLAMF6 (NTB-A, Ly108), SLAM (SLAMF1, CD150, IPO-3), BLAME (SLAMF8), SELPLG (CD162), LTBR, PAG/Cbp, NKG2D, NKG2C.
В некоторых случаях трансмембранный домен может быть присоединен к внеклеточной области CAR, например, антигенсвязывающему домену CAR, через шарнирную область, например, шарнирную область из белка человека. Например, в одном варианте осуществления шарнирный участок может представлять собой шарнирную область Ig (иммуноглобулина) человека, например, шарнирную область IgG4 или шарнирную область CD8a. В одном варианте осуществления шарнирная область или спейсер содержат (например, состоят из) аминокислотную последовательность под SEQ ID NO: 147. В одном аспекте трансмембранный домен содержит (например, состоит из) трансмембранный домен под SEQ ID NO: 155.
В одном аспекте шарнирная область или спейсер содержит шарнирную область IgG4. Например, в одном варианте осуществления шарнирная область или спейсер содержат шарнирную область с аминокислотной последовательностью ESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGKM (SEQ ID NO: 149). В некоторых вариантах осуществления шарнирная область или спейсер содержат шарнирную область, кодируемую нуклеотидной последовательностью GAGAGCAAGTACGGCCCTCCCTGCCCCCCTTGCCCTGCCCCCGAGTTCCTGGGCGGACCCAGCGTGTTCCTGTTCCCCCCCAAGCCCAAGGACACCCTGATGATCAGCCGGACCCCCGAGGTGACCTGTGTGGTGGTGGACGTGTCCCAGGAGGACCCCGAGGTCCAGTTCAACTGGTACGTGGACGGCGTGGAGGTGCACAACGCCAAGACCAAGCCCCGGGAGGAGCAGTTCAATAGCACCTACCGGGTGGTGTCCGTGCTGACCGTGCTGCACCAGGACTGGCTGAACGGCAAGGAATACAAGTGTAAGGTGTCCAACAAGGGCCTGCCCAGCAGCATCGAGAAAACCATCAGCAAGGCCAAGGGCCAGCCTCGGGAGCCCCAGGTGTACACCCTGCCCCCTAGCCAAGAGGAGATGACCAAGAACCAGGTGTCCCTGACCTGCCTGGTGAAGGGCTTCTACCCCAGCGACATCGCCGTGGAGTGGGAGAGCAACGGCCAGCCCGAGAACAACTACAAGACCACCCCCCCTGTGCTGGACAGCGACGGCAGCTTCTTCCTGTACAGCCGGCTGACCGTGGACAAGAGCCGGTGGCAGGAGGGCAACGTCTTTAGCTGCTCCGTGATGCACGAGGCCCTGCACAACCACTACACCCAGAAGAGCCTGAGCCTGTCCCTGGGCAAGATG (SEQ ID NO: 150).
В одном аспекте шарнирная область или спейсер содержат шарнирную область IgD. Например, в одном варианте осуществления шарнирная область или спейсер содержат шарнирную область с аминокислотной последовательностью RWPESPKAQASSVPTAQPQAEGSLAKATTAPATTRNTGRGGEEKKKEKEKEEQEERETKTPECPSHTQPLGVYLLTPAVQDLWLRDKATFTCFVVGSDLKDAHLTWEVAGKVPTGGVEEGLLERHSNGSQSQHSRLTLPRSLWNAGTSVTCTLNHPSLPPQRLMALREPAAQAPVKLSLNLLASSDPPEAASWLLCEVSGFSPPNILLMWLEDQREVNTSGFAPARPPPQPGSTTFWAWSVLRVPAPPSPQPATYTCVVSHEDSRTLLNASRSLEVSYVTDH (SEQ ID NO: 151). В некоторых вариантах осуществления шарнирная область или спейсер содержат шарнирную область, кодируемую нуклеотидной последовательностью AGGTGGCCCGAAAGTCCCAAGGCCCAGGCATCTAGTGTTCCTACTGCACAGCCCCAGGCAGAAGGCAGCCTAGCCAAAGCTACTACTGCACCTGCCACTACGCGCAATACTGGCCGTGGCGGGGAGGAGAAGAAAAAGGAGAAAGAGAAAGAAGAACAGGAAGAGAGGGAGACCAAGACCCCTGAATGTCCATCCCATACCCAGCCGCTGGGCGTCTATCTCTTGACTCCCGCAGTACAGGACTTGTGGCTTAGAGATAAGGCCACCTTTACATGTTTCGTCGTGGGCTCTGACCTGAAGGATGCCCATTTGACTTGGGAGGTTGCCGGAAAGGTACCCACAGGGGGGGTTGAGGAAGGGTTGCTGGAGCGCCATTCCAATGGCTCTCAGAGCCAGCACTCAAGACTCACCCTTCCGAGATCCCTGTGGAACGCCGGGACCTCTGTCACATGTACTCTAAATCATCCTAGCCTGCCCCCACAGCGTCTGATGGCCCTTAGAGAGCCAGCCGCCCAGGCACCAGTTAAGCTTAGCCTGAATCTGCTCGCCAGTAGTGATCCCCCAGAGGCCGCCAGCTGGCTCTTATGCGAAGTGTCCGGCTTTAGCCCGCCCAACATCTTGCTCATGTGGCTGGAGGACCAGCGAGAAGTGAACACCAGCGGCTTCGCTCCAGCCCGGCCCCCACCCCAGCCGGGTTCTACCACATTCTGGGCCTGGAGTGTCTTAAGGGTCCCAGCACCACCTAGCCCCCAGCCAGCCACATACACCTGTGTTGTGTCCCATGAAGATAGCAGGACCCTGCTAAATGCTTCTAGGAGTCTGGAGGTTTCCTACGTGACTGACCATT (SEQ ID NO: 152).
В одном аспекте трансмембранный домен может быть рекомбинантным, и в таком случае он будет содержать в основном гидрофобные остатки, такие как лейцин и валин. В одном аспекте на каждом конце рекомбинантного трансмембранного домена может находиться триплет из фенилаланина, триптофана и валина.
Короткий олиго- или полипептидный линкер длиной от 2 до 10 аминокислот необязательно может образовывать связь между трансмембранным доменом и цитоплазматической областью CAR. Глицин-сериновый дублет представляет собой особенно подходящий линкер. Например, в одном аспекте линкер содержит аминокислотную последовательность GGGGSGGGGS (SEQ ID NO: 153). В некоторых вариантах осуществления линкер кодируется нуклеотидной последовательностью GGTGGCGGAGGTTCTGGAGGTGGAGGTTCC (SEQ ID NO: 154).
В одном аспекте шарнирная область или спейсер содержат шарнирную область KIR2DS2.
Цитоплазматический домен
Цитоплазматические домен или область CAR включают внутриклеточный сигнальный домен. Внутриклеточный сигнальный домен обычно отвечает за активацию по меньшей мере одной из нормальных эффекторных функций иммунной клетки, в которую был введен CAR.
Примеры внутриклеточных сигнальных доменов для применения в CAR, описанном в данном документе, включают цитоплазматические последовательности Т-клеточного рецептора (TCR) и корецепторов, которые действуют совместно с инициированием передачи сигнала после вступления в контакт с антигенным рецептором, а также любое производное или вариант этих последовательностей и любую рекомбинантную последовательность, которая обладает такими же функциональными способностями.
Известно, что сигналы, генерируемые при участии только TCR, являются недостаточными для полной активации Т-клетки, и что также требуется вторичный и/или костимулирующий сигнал. Таким образом, можно сказать, что активация Т-клеток опосредуется двумя различными классами цитоплазматических сигнальных последовательностей: последовательностями, которые инициируют антигензависимую первичную активацию при участии TCR (первичные внутриклеточные сигнальные домены), и последовательностями, которые действуют антигеннезависимым образом с обеспечением вторичного или костимулирующего сигнала (вторичный цитоплазматический домен, например, костимулирующий домен).
Первичный сигнальный домен регулирует первичную активацию комплекса TCR либо стимулирующим образом, либо ингибирующим образом. Первичные внутриклеточные сигнальные домены, которые действуют стимулирующим образом, могут содержать сигнальные мотивы, известные как иммунорецепторные тирозиновые активирующие мотивы или ITAM.
Примеры первичных внутриклеточных сигнальных доменов, содержащих ITAM, которые являются особенно применимыми в настоящем изобретении, включают домены из TCR-дзета, FcR-гамма, FcR-бета, CD3-гамма, CD3-дельта, CD3-эпсилон, CD5, CD22, CD79a, CD79b, CD278 (также известного как "ICOS"), FcεRI, DAP10, DAP12 и CD66d. В одном варианте осуществления CAR по настоящему изобретению содержит внутриклеточный сигнальный домен, например, первичный сигнальный домен CD3-дзета, например, последовательность CD3-дзета, описанную в данном документе.
В одном варианте осуществления первичный сигнальный домен содержит модифицированный ITAM-домен, например, мутантный ITAM-домен, который обладает измененной (например, увеличенной или уменьшенной) активностью по сравнению с нативным ITAM-доменом. В одном варианте осуществления первичный сигнальный домен содержит модифицированный ITAM-содержащий первичный внутриклеточный сигнальный домен, например, оптимизированный и/или усеченный ITAM-содержащий первичный внутриклеточный сигнальный домен. В одном варианте осуществления первичный сигнальный домен содержит один, два, три, четыре или более мотивов ITAM.
Костимулирующий сигнальный домен
Внутриклеточный сигнальный домен CAR может содержать сигнальный домен CD3-дзета сам по себе или в комбинации с любым другим необходимым внутриклеточным сигнальным доменом(-ами), применимым в контексте CAR по настоящему изобретению. Например, внутриклеточный сигнальный домен CAR может содержать часть дзета-цепи CD3 и костимулирующий сигнальный домен. Костимулирующий сигнальный домен относится к части CAR, содержащей внутриклеточный домен костимулирующей молекулы. В одном варианте осуществления внутриклеточный домен разработан таким образом, что он содержит сигнальный домен CD3-дзета и сигнальный домен CD28. В одном аспекте внутриклеточный домен разработан таким образом, что он содержит сигнальный домен CD3-дзета и сигнальный домен ICOS.
Костимулирующая молекула может быть молекулой клеточной поверхности, отличной от антигенного рецептора или его лигандов, которая требуется для эффективного ответа лимфоцитов на антиген. Примеры таких молекул включают CD27, CD28, 4-1BB (CD137), OX40, CD30, CD40, PD-1, ICOS, лимфоцитарный функционально-ассоциированный антиген-1 (LFA-1), CD2, CD7, LIGHT, NKG2C, B7-H3 и лиганд, который специфически связывается с CD83, и т. п. Например, было продемонстрировано, что костимуляция с помощью CD27 усиливает размножение, эффекторную функцию и выживание CAR-T-клеток человека in vitro и увеличивает персистенцию и противоопухолевую активность T-клеток человека in vivo (Song et al. Blood. 2012; 119(3):696-706). Дополнительные примеры таких костимулирующих молекул включают CDS, ICAM-1, GITR, BAFFR, HVEM (LIGHTR), SLAMF7, NKp80 (KLRF1), NKp30, NKp44, NKp46, CD160, CD19, CD4, CD8-альфа, CD8-бета, IL2R-бета, IL2R-гамма, IL7R-альфа, ITGA4, VLA1, CD49a, ITGA4, IA4, CD49D, ITGA6, VLA-6, CD49f, ITGAD, CD11d, ITGAE, CD103, ITGAL, CD11a, LFA-1, ITGAM, CD11b, ITGAX, CD11c, ITGB1, CD29, ITGB2, CD18, LFA-1, ITGB7, TNFR2, TRANCE/RANKL, DNAM1 (CD226), SLAMF4 (CD244, 2B4), CD84, CD96 (Tactile), CEACAM1, CRTAM, Ly9 (CD229), CD160 (BY55), PSGL1, CD100 (SEMA4D), CD69, SLAMF6 (NTB-A, Ly108), SLAM (SLAMF1, CD150, IPO-3), BLAME (SLAMF8), SELPLG (CD162), LTBR, LAT, GADS, SLP-76, NKG2D, NKG2C и PAG/Cbp.
Внутриклеточные сигнальные последовательности в пределах цитоплазматической части CAR могут быть связаны друг с другом в случайном или установленном порядке. Короткий олиго- или полипептидный линкер, например, длиной от 2 до 10 аминокислот (например, 2, 3, 4, 5, 6, 7, 8, 9 или 10 аминокислот), необязательно может образовывать связь между внутриклеточными сигнальными последовательностями. В одном варианте осуществления в качестве подходящего линкера может применяться глицин-сериновый дублет. В одном варианте осуществления в качестве подходящего линкера может применяться одна аминокислота, например, аланин, глицин.
В одном аспекте внутриклеточный сигнальный домен разработан таким образом, что он содержит два или более, например, 2, 3, 4, 5 или более, костимулирующих сигнальных доменов. В варианте осуществления два или более, например, 2, 3, 4, 5 или более, костимулирующих сигнальных доменов разделены линкерной молекулой, например, линкерной молекулой, описанной в данном документе. В одном варианте осуществления внутриклеточный сигнальный домен содержит два костимулирующих сигнальных домена. В некоторых вариантах осуществления линкерная молекула представляет собой глициновый остаток. В некоторых вариантах осуществления линкер представляет собой остаток аланина.
В одном аспекте внутриклеточный сигнальный домен разработан таким образом, что он содержит сигнальный домен CD3-дзета и сигнальный домен CD28. В одном аспекте внутриклеточный сигнальный домен разработан таким образом, что он содержит сигнальный домен CD3-дзета и сигнальный домен 4-1BB. В одном аспекте сигнальный домен 4-1BB представляет собой сигнальный домен под SEQ ID NO: 158. В одном аспекте сигнальный домен CD3-дзета представляет собой сигнальный домен под SEQ ID NO: 163.
В одном аспекте внутриклеточный сигнальный домен разработан таким образом, что он содержит сигнальный домен CD3-дзета и сигнальный домен CD27. В одном аспекте сигнальный домен CD27 содержит аминокислотную последовательность QRRKYRSNKGESPVEPAEPCRYSCPREEEGSTIPIQEDYRKPEPACSP (SEQ ID NO: 161). В одном аспекте сигнальный домен CD27 кодируется последовательностью нуклеиновой кислоты AGGAGTAAGAGGAGCAGGCTCCTGCACAGTGACTACATGAACATGACTCCCCGCCGCCCCGGGCCCACCCGCAAGCATTACCAGCCCTATGCCCCACCACGCGACTTCGCAGCCTATCGCTCC (SEQ ID NO: 162).
В одном аспекте описанная в данном документе клетка, экспрессирующая CAR, может дополнительно содержать второй CAR, например, второй CAR, который содержит другой антигенсвязывающий домен, например, для той же мишени или другой мишени (например, для мишени, отличной от антигена, ассоциированного с раком, описанного в данном документе, или другого антигена, ассоциированного с раком, описанного в данном документе, например, CD19, CD33, CLL-1, CD34, FLT3 или рецептора фолиевой кислоты бета). В одном варианте осуществления второй CAR содержит антигенсвязывающий домен для мишени, экспрессируемой на раковой клетке того же типа, что и клетка, на которой экспрессируется антиген, ассоциированный с раком. В одном варианте осуществления клетка, экспрессирующая CAR, содержит первый CAR, который нацеливается на первый антиген и содержит внутриклеточный сигнальный домен, имеющий костимулирующий сигнальный домен, а не первичный сигнальный домен, и второй CAR, который нацеливается на второй, другой, антиген и содержит внутриклеточный сигнальный домен, имеющий первичный сигнальный домен, а не костимулирующий сигнальный домен. Без ограничения какой-либо теорией, размещение костимулирующего сигнального домена, например, 4-1BB, CD28, ICOS, CD27 или OX-40, на первом CAR, и первичного сигнального домена, например, CD3-дзета, на втором CAR может ограничивать активность CAR клетками, в которых экспрессируются обе мишени. В одном варианте осуществления клетка, экспрессирующая CAR, содержит первый CAR для антигена, ассоциированного с раком, который содержит антигенсвязывающий домен, который связывает антиген-мишень, описанный в данном документе, трансмембранный домен и костимулирующий домен, и второй CAR, который нацеливается на другой антиген-мишень (например, антиген, экспрессируемый на раковой клетке того же типа, на которой экспрессируется первый антиген-мишень) и содержит антигенсвязывающий домен, трансмембранный домен и первичный сигнальный домен. В другом варианте осуществления клетка, экспрессирующая CAR, содержит первый CAR, который содержит антигенсвязывающий домен, который связывает антиген-мишень, описанный в данном документе, трансмембранный домен и первичный сигнальный домен, и второй CAR, который нацеливается на антиген, отличный от первого антигена-мишени (например, антиген, экспрессируемый на раковой клетке того же типа, на которой экспрессируется первый антиген-мишень), и содержит антигенсвязывающий домен для антигена, трансмембранный домен и костимулирующий сигнальный домен.
В другом аспекте настоящего изобретения описана популяция клеток, экспрессирующих CAR, например, CAR-T-клеток. В некоторых вариантах осуществления популяция клеток, экспрессирующих CAR, содержит смесь клеток, экспрессирующих различные CAR. Например, в одном варианте осуществления популяция CAR-T-клеток может содержать первую клетку, экспрессирующую CAR с антигенсвязывающим доменом для антигена, ассоциированного с раком, описанного в данном документе, и вторую клетку, экспрессирующую CAR с другим антигенсвязывающим доменом, например, антигенсвязывающим доменом для другого антигена, ассоциированного с раком, описанного в данном документе, например, антигенсвязывающим доменом для антигена, ассоциированного с раком, описанного в данном документе, который отличается от антигена, ассоциированного с раком, с которым связывается антигенсвязывающий домен CAR, экспрессируемого первой клеткой. В качестве другого примера, популяция клеток, экспрессирующих CAR, может содержать первую клетку, экспрессирующую CAR, который содержит антигенсвязывающий домен для антигена, ассоциированного с раком, описанного в данном документе, и вторую клетку, экспрессирующую CAR, который содержит антигенсвязывающий домен для мишени, отличной от антигена, ассоциированного с раком, описанного в данном документе. В одном варианте осуществления популяция клеток, экспрессирующих CAR, содержит, например, первую клетку, экспрессирующую CAR, который содержит первичный внутриклеточный сигнальный домен, и вторую клетку, экспрессирующую CAR, который содержит вторичный сигнальный домен.
В другом аспекте настоящего изобретения описана популяция клеток, где по меньшей мере одна клетка в популяции экспрессирует CAR, имеющий антигенсвязывающий домен для антигена, ассоциированного с раком, описанного в данном документе, а вторая клетка экспрессирует другое средство, например, средство, которое усиливает активность клетки, экспрессирующей CAR. Например, в одном варианте осуществления средство может представлять собой средство, которое ингибирует ингибирующую молекулу. Ингибирующие молекулы, например, PD-1, в некоторых вариантах осуществления могут снижать способность клеток, экспрессирующих CAR, вызывать иммунный эффекторный ответ. Примеры ингибирующих молекул включают PD-1, PD-L1, CTLA4, TIM3, CEACAM (CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4, CD80, CD86, B7-H3 (CD276), B7-H4 (VTCN1), HVEM (TNFRSF14 или CD270), KIR, A2aR, молекулу MHC I класса, молекулу MHC II класса, GAL9, аденозин и TGF (например, TGF-бета). В одном варианте осуществления средство, которое ингибирует ингибирующую молекулу, содержит первый полипептид, например ингибирующую молекулу, ассоциированный со вторым полипептидом, который передает положительный сигнал в клетку, например, с внутриклеточным сигнальным доменом, описанным в данном документе. В одном варианте осуществления средство содержит первый полипептид, например, ингибирующую молекулу, такую как PD-1, PD-L1, CTLA4, TIM3, CEACAM (CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4 и TGF-бета или фрагмент любого из них, и второй полипептид, который представляет собой внутриклеточный сигнальный домен, описанный в данном документе (например, содержащий костимулирующий домен (например, 41BB, CD27, OX40 или CD28, например, описанные в данном документе) и/или первичный сигнальный домен (например, сигнальный домен CD3-дзета, описанный в данном документе)). В одном варианте осуществления средство содержит первый полипептид, представляющий собой PD-1 или его фрагмент, и второй полипептид, представляющий собой внутриклеточный сигнальный домен, описанный в данном документе (например, сигнальный домен CD28, описанный в данном документе, и/или сигнальный домен CD3-дзета, описанный в данном документе).
Представляющие интерес регуляторные полипептиды
В некоторых вариантах осуществления представляющий интерес гетерологичный полипептид, связанный с COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающим полипептидом и/или доменом деградации, представляет собой регуляторный белок. В данном документе представлены регуляторные полипептиды и последовательности, кодирующие регуляторные полипептиды, применимые в циклах генетического контроля, клетках и способах идентификации, отбора или получения клетки или линии клеток, способный к продуцированию высоких выходов продукта, например, рекомбинантного или терапевтического полипептида. В целом, регуляторные полипептиды контролируют экспрессию продукта, например, рекомбинантного или терапевтического полипептида. В некоторых вариантах осуществления регуляторный полипептид представляет собой полипептид генного редактирования. В некоторых вариантах осуществления последовательность, кодирующая регуляторный полипептид, находится под транскрипционным контролем элемента контроля, который активирует транскрипцию последовательности, кодирующей регуляторный полипептид, в зависимости от одного или нескольких условий. В некоторых вариантах осуществления регуляторный полипептид связывается с элементом контроля, например, промоторным элементом, функционально связанным с последовательностью, кодирующей рекомбинантный или терапевтический полипептид. В некоторых вариантах осуществления связывание регуляторного полипептида с элементом контроля ингибирует транскрипцию функционально связанной последовательности, кодирующей рекомбинантный или терапевтический полипептид. В некоторых вариантах осуществления регуляторный полипептид связывается с последовательностью, кодирующей нетранслируемую область транскрипта рекомбинантного или терапевтического полипептида. В некоторых вариантах осуществления связывание регуляторного полипептида с нетранслируемой областью транскрипта рекомбинантного или терапевтического полипептида ингибирует трансляцию последовательности, кодирующей рекомбинантный или терапевтический полипептид. В некоторых вариантах осуществления регуляторный полипептид связывается с кодирующей последовательностью последовательности, кодирующей рекомбинантный или терапевтический полипептид. В некоторых вариантах осуществления связывание регуляторного полипептида с кодирующей последовательностью рекомбинантного или терапевтического полипептид ингибирует транскрипцию, трансляцию или транскрипцию и трансляцию последовательности, кодирующей рекомбинантный или терапевтический полипептид.
Подразумевается, что настоящее изобретение не ограничивается конкретным регуляторным полипептидом. Иллюстративные регуляторные полипептиды включают без ограничения: молекулы Cas9, молекулы TALE и молекулы с "цинковыми пальцами". В некоторых вариантах осуществления регуляторный полипептид представляет собой Cas-родственный белок, известный из уровня техники. В некоторых вариантах осуществления регуляторный полипептид представляет собой белок из системы CRISPR/Cas I, II, или III типа (например, описанный в K. S. Makarova et al., Nat. Rev. Microbiol. 9, 467 (2011); K. S. Makarova, N. V. Grishin, S. A. Shabalina, Y. I. Wolf, E. V. Koonin, Biol. Direct 1, 7 (2006); или K. S. Makarova, L. Aravind, Y. I. Wolf, E. V. Koonin, Biol. Direct 6, 38 (2011)).
В некоторых вариантах осуществления регуляторный полипептид представляет собой молекулу Cas9 . Регуляторным полипептидам, которые представляют собой молекулы Cas9, требуется одна или несколько (например, одна, две, три, четыре или более) подходящих gRNA для ингибирования экспрессии рекомбинантного или терапевтического полипептида.
В некоторых вариантах осуществления регуляторный полипептид представляет собой молекулу TALE.
В некоторых вариантах осуществления регуляторный полипептид представляет собой молекулу с "цинковыми пальцами".
В некоторых вариантах осуществления регуляторный полипептид является эндогенным регулятором первого элемента контроля, например, первого промоторного элемента. В одном варианте осуществления эндогенный ген, кодирующий регуляторный полипептид, является неактивным, например, был подвергнут нокауту или мутации с образованием потери функции.
Молекулы Cas9 и другие компоненты системы CRISPR/CAS
В некоторых вариантах осуществления представляющий интерес гетерологичный полипептид, связанный сCOF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающим полипептидом и/или доменом деградации, представляет собой молекулу Cas9, молекулу Cas12, молекулу Cas13 или другой компонент системы CRISPR/CAS (например, молекулу рибонуклеопротеина (RNP)). В случае видов генной терапии с применением системы CRISPR/CAS одним важным соображением является ограничение побочных эффектов, обусловленных нецелевой активностью молекулы Cas (например, молекулы Cas9). Слияние дегрона, например, COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающего полипептида, описанного в данном документе, например, HilD-метки или CARB-метки, описанных в данном документе, с компонентом системы CRISPR/CAS (например, молекулой Cas9 или молекулой RNP) содействует получению средства генной терапии, в котором активность системы CRISPR/CAS может контролироваться соединением деградации, описанным в данном документе, например, в случае побочных эффектов.
Молекулы Cas9, которые можно применять в циклах генетического контроля, клетках и способов по настоящему изобретению, могут содержать полипептиды, происходящий из различных биологических видов. Кроме того, один или несколько доменов из молекулы Cas9 одного биологического вида можно объединять с одним или несколькими доменами из молекулы Cas9 другого биологического вида, например, в слитом белке. Дополнительные биологические виды, содержащие полипептид Cas9, включают: Acidovorax avenae, Actinobacillus pleuropneumoniae, Actinobacillus succinogenes, Actinobacillus suis, Actinomyces sp., cycliphilus denitrificans, Aminomonas paucivorans, Bacillus cereus, Bacillus smithii, Bacillus thuringiensis, Bacteroides sp., Blastopirellula marina, Bradyrhizobium sp., Brevibacillus laterosporus, Campylobacter coli, Campylobacter jejuni, Campylobacter lari, Candidatus Puniceispirillum, Clostridium cellulolyticum, Clostridium perfringens, Corynebacterium accolens, Corynebacterium diphtheria, Corynebacterium matruchotii, Dinoroseobacter shibae, Eubacterium dolichum, gamma proteobacterium, Gluconacetobacter diazotrophicus, Haemophilus parainfluenzae, Haemophilus sputorum, Helicobacter canadensis, Helicobacter cinaedi, Helicobacter mustelae, Ilyobacter polytropus, Kingella kingae, Lactobacillus crispatus, Listeria ivanovii, Listeria monocytogenes, Listeriaceae bacterium, Methylocystis sp., Methylosinus trichosporium, Mobiluncus mulieris, Neisseria bacilliformis, Neisseria cinerea, Neisseria flavescens, Neisseria lactamica, Neisseria meningitidis, Neisseria sp., Neisseria wadsworthii, Nitrosomonas sp., Parvibaculum lavamentivorans, Pasteurella multocida, Phascolarctobacterium succinatutens, Ralstonia syzygii, Rhodopseudomonas palustris, Rhodovulum sp., Simonsiella muelleri, Sphingomonas sp., Sporolactobacillus vineae, Staphylococcus lugdunensis, Streptococcus sp., Subdoligranulum sp., Tistrella mobilis, Treponema sp., или Verminephrobacter eiseniae.
Молекулы Cas12 (например, Cas12a, Cas12b и Cas12c) были раскрыты, например, в Chen et al., Science. 2018 Apr 27;360(6387):436-439 и Shmakov et al., Nat Rev Microbiol. 2017 Mar;15(3):169-182, включенных в данный документ посредством ссылки во всей своей полноте. Белки CRISPR-Cas12a (Cpf1) представляют собой РНК-направляемые ферменты, которые связывают ДГК и образуют целевые, двунитевые разрывы ДНК. Аналогично CRISPR-Cas9 Cas12 также является инструментом, применимым в редактировании генома. Дополнительные молекулы Cas, которые применимы для генного редактирования включают без ограничения Cas13, например, Cas13a, Cas13b и Cas13c, раскрытые, например, в WO2017219027 и Shmakov et al., Nat Rev Microbiol. 2017 Mar;15(3):169-182, включенных в данный документ посредством ссылки во всей своей полноте. В некоторых вариантах осуществления представляющий интерес гетерологичный полипептид представляет собой Cas12. В некоторых вариантах осуществления представляющий интерес гетерологичный полипептид представляет собой Cas13.
Структура и активность Cas9
Являются доступными кристаллические структуры встречающихся в природе полипептидов Cas9 (Jinek et al., Science, 343(6176):1247997, 2014) и Cas9 S. pyogenes с направляющей РНК (например, синтетическим слиянием crRNA и tracrRNA) (Nishimasu et al., Cell, 156:935-949, 2014; и Anders et al., Nature, 2014, doi: 10.1038/nature13579).
В одном варианте осуществления молекула Cas9 или полипептид Cas9 содержат один или несколько следующих доменов: RuvC-подобный домен и HNH-подобный домен. В одном варианте осуществления молекула Cas9 или полипептид Cas9 представляют собой молекулу dCas9 или полипептид dCas9, и молекула dCas9 или полипептид dCas9 содержат RuvC-подобный домен, например, RuvC-подобный домен, у которого отсутствует нуклеазная активность, и/или HNH-подобный домен, например, HNH-подобный домен, у которого отсутствует нуклеазная активность.
В одном варианте осуществления молекула Cas9 или полипептид Cas9 могут содержать более одного RuvC-подобного домена (например, один, два, три или более RuvC-подобных доменов). В одном варианте осуществления RuvC-подобный домен содержит одну или несколько мутаций, которые изменяют его активность таким образом, что RuvC-домен не расщепляет ДНК или характеризуется сниженной активностью расщепления ДНК. В одном варианте осуществления RuvC-подобный домен составляет по меньшей мере 5, 6, 7, 8 аминокислот в длину, но не более 20, 19, 18, 17, 16 или 15 аминокислот в длину. В одном варианте осуществления молекула Cas9 или полипептид Cas9 содержат N-концевой RuvC-подобный домен длиной приблизительно 10-20 аминокислот, например, приблизительно 15 аминокислот.
В одном варианте осуществления молекула Cas9 или полипептид Cas9 могут включать более одного HNH-подобного домена (например, один, два, три или более HNH-подобных домена). В одном варианте осуществления HNH-подобный домен содержит одну или несколько мутаций, которые изменяют его активность таким образом, что HNH-подобный домен не расщепляет ДНК или характеризуется сниженной активностью расщепления ДНК. В одном варианте осуществления HNH-подобный домен составляет по меньшей мере 15, 20, 25 аминокислот в длину, но не более 40, 35 или 30 аминокислот в длину, например, 20-35 аминокислот в длину, например, 25-30 аминокислот в длину.
В вариантах осуществления молекулы Cas9 или полипептиды Cas9 обладают способностью взаимодействовать с молекулой gRNA, и в сочетании с молекулой gRNA локализоваться на коровом домене-мишени, но неспособны к расщеплению нуклеиновой кислоты-мишени, или неспособны к расщеплению с эффективными скоростями. Молекулы Cas9, не обладающие или обладающие незначительной активностью расщепления, обозначаются в данном документе как молекулы dCas9 или полипептиды dCas9. Например, у молекулы dCas9 или полипептида dCas9 может отсутствовать активность расщепления, или они характеризуются значительно меньшей, например, менее 20, 10, 5, 1 или 0,1% активностью расщепления эталонной молекулы Cas9 или полипептида Cas9, измеренной с помощью анализов, известных из уровня техники, или анализов, описанных в данном документе.
Нацеливание и PAM
Молекула Cas9 или полипептид Cas9 представляют собой полипептид, который может взаимодействовать с молекулой направляющей РНК (gRNA) и совместно с молекулой gRNA локализоваться в участке, который содержит домен-мишень и последовательность PAM.
В одном варианте осуществления способность молекулы Cas9 или полипептида Cas9 взаимодействовать с нуклеиновой кислотой-мишенью является зависимой от последовательности PAM. Последовательность PAM представляет собой последовательность в нуклеиновой кислоте-мишени. Активные молекулы Cas9 из различных видов бактерий могут распознавать различные мотивы последовательности (например, последовательности PAM). Молекулы Cas9 можно конструировать с помощью генной инженерии, чтобы изменить PAM-специфичность молекулы Cas9. Иллюстративные встречающиеся в природе молекулы Cas9 описаны в Chylinski et al., RNA Biology 2013 10:5, 727-737.
Изменения в структуре Cas9
В некоторых вариантах осуществления одна или несколько мутаций могут присутствовать, например, в одном или нескольких RuvC-подобных доменах, например, N-концевом RuvC-подобном домене; HNH-подобный домен; области за пределами RuvC-подобных доменов и HNH-подобного домена молекулы Cas9 или полипептида Cas9. В некоторых вариантах осуществления мутация(-и) присутствует(-ют) в RuvC-подобной домене, например, N-концевом RuvC-подобном домене. В некоторых вариантах осуществления мутация(-и) присутствует(-ют) в HNH-подобном домене. В некоторых вариантах осуществления мутации присутствуют как в RuvC-подобном домене, например, N-концевом RuvC-подобном домене, так и в HNH-подобном домене.
В одном варианте осуществления молекула Cas9 или полипептид Cas9, например, молекула dCas9 или полипептид dCas9, содержат аминокислотную последовательность:
характеризующуюся 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% гомологией с;
отличающуюся на не более чем 2, 5, 10, 15, 20, 30 или 40% аминокислотных остатков при сравнении с;
отличающуюся на по меньшей мере 1, 2, 5, 10 или 20 аминокислот, но не более чем 100, 80, 70, 60, 50, 40 или 30 аминокислот от; или
идентичную последовательности любой молекулы Cas9, описанной в данном документе, или последовательности встречающейся в природе молекулы Cas9, например, молекулы Cas9 от биологического вида, перечисленного в данном документе или описанного в Chylinski et al., RNA Biology 2013 10:5, 727-737; Hou et al., PNAS Early Edition 2013, 1-6;. В одном варианте осуществления молекула Cas9 или полипептид Cas9 предусматривают один или несколько из следующих видов активности: хеликазную активность или способность вместе с молекулой gRNA локализоваться на нуклеиновой кислоте-мишени. В одном варианте осуществления молекула Cas9 или полипептид Cas9 не предусматривают никазную активность или активность расщепления двух нитей (например, эндонуклеазную и/или экзонуклеазную активность).
Иллюстративные мутации, которые можно осуществить в RuvC-домене или HNH-домене с привязкой к последовательности S. pyogenes включают: D10A, E762A, H840A, N854A, N863A и/или D986A.
Иллюстративные полипептид Cas9 и последовательности домена Cas9 можно найти в таблицах 50-54 из WO2015/157070.
Полипептиды dCas9
В одном варианте осуществления представляющий интерес гетерологичный полипептид, связанный с COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающим полипептидом и/или доменом деградации, представляет собой молекулу dCas9, например, полипептид dCas9, содержащий одно или несколько отличий в RuvC-домене и/или в HNH-домене по сравнению с эталонной молекулой Cas9, и молекула dCas9 или полипептид dCas9 не расщепляют нуклеиновую кислоту или расщепляют со значительно меньшей эффективностью, чем молекула дикого типа, например, при сравнении с молекулой дикого типа в анализе расщепления, например, описанном в данном документе, разрезают менее 50, 25, 10 или 1% относительно эталонной молекулы Cas9, как измерено с помощью анализа, описанного в данном документе.
Мутирование ключевых остатков в обоих доменах расщепления ДНК белка Cas9 (например, мутации D10A и H840A) приводят к образованию каталитически неактивной молекулы Cas9 (dCas9, которая также известна как "мертвая" Cas9). Ферментативно неактивная Cas9, например, dCas9, образует комплекс с gRNA и локализуется на последовательности ДНК, которую определяет нацеливающий домен gRNA; однако она не расщепляет ДНК-мишень. Ферментативно неактивная молекула Cas9 (например, dCas9) может блокировать транскрипцию при привлечении к ранним областям в кодирующей последовательности. Дополнительная репрессия может достигаться при слиянии домена транскрипционной репрессии (например KRAB, SID или ERD) с ферментативно неактивной Cas9, например, dCas9, и привлечении ее к последовательности-мишени, например, в пределах последовательность из 1000 п. о. в направлении 3'-конца от старт-кодона или в пределах 500 п. о. от элемента контроля, например, промоторного элемента, например, в направлении 5'-конца от старт-кодон гена. Нацеливание на участки гиперчувствительности к ДНКазе I (DHS) промотора (например, путем получения gRNA, комплементарных DHS) может представлять собой дополнительную стратегию для генной репрессии, например, ингибирования последовательности, кодирующей рекомбинантный или терапевтический полипептид, поскольку такие области с большей вероятностью будут доступны для ферментативно неактивной Cas9, например, dCas9, и также, вероятно, несут участки эндогенных факторов транскрипции. Без ограничения какой-либо теорией, в данном документе предусматривается, что блокировка участка связывания эндогенного фактора транскрипции или РНК-полимеразы будет содействовать подавлению генной экспрессии, например, экспрессии последовательности, кодирующей рекомбинантный или терапевтический полипептид. В одном варианте осуществления одну или несколько ферментативно неактивных молекул Cas9, например, dCas9, можно применять для блокировки связывания одного или нескольких эндогенных факторов транскрипции. В другом варианте осуществления ферментативно неактивная молекула Cas9, например, dCas9, может быть слита с эффекторным доменом, например, доменом репрессии, доменом активации, доменом метилирования и т. д. Слияние ферментативно неактивной Cas9, например, dCas9, с эффекторным доменом делает возможным привлечение эффектора к любому участку ДНК, определенному с помощью gRNA. Изменение статуса хроматина может приводить к снижению экспрессии гена-мишени. Одну или несколько ферментативно неактивных молекул Cas9, например, dCas9, слитых с одним или несколькими белками, модифицирующими хроматин, можно применять для изменения статуса хроматина.
В одном варианте осуществления молекула gRNA может быть нацелена элемент контроля (например, промоторный элемент), например, элемент контроля, функционально связанный с последовательностью, кодирующей рекомбинантный или терапевтический полипептид. В одном варианте осуществления молекула gRNA может быть нацелена на последовательность, кодирующую рекомбинантный или терапевтический полипептид.
Молекулы TALE
В некоторых вариантах осуществления представляющий интерес гетерологичный полипептид, связанный с COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающим полипептидом и/или доменом деградации, представляет собой молекулу эффектора, подобного активатору транскрипции (TALE), или полипептид TALE. Молекула или полипептид TALE, в том значении, в котором данный термин используется в данном документе, относится к молекуле или полипептиду, содержащим несколько доменов ДНК-связывающих повторов (TALE DBD), которые могут возвращаться или локализоваться в положении нуклеиновой кислоты, определяемом с помощью TALE DBD. Молекула TALE и полипептид TALE, в том значении, в котором данные термины используются в данном документе, относятся к встречающимся в природе молекулам TALE и к сконструированным, измененным или модифицированным молекулам TALE или полипептидам TALE, которые отличаются, например, на по меньшей мере один аминокислотный остаток, от эталонной последовательности, например, наиболее сходной встречающейся в природе молекулы TALE, известной из уровня техники.
TALE DBD, в том значении, в котором данный термин используется в данном документе, относится к мотиву из 33-35 аминокислот, содержащему два гипервариабельных остатка (т. е. повтор из двух вариабельных остатков, RVD) в положениях 12 и 13 мотива. RVD в ДНК-связывающем домене (DBD) TALE определяет пару оснований или пары оснований ДНК, в отношении которых TALE DBD обладает аффинностью связывания. Когда TALE DBD объединены в массивы в пределах молекулы TALE или полипептида TALE, порядок TALE DBD (и их RVD) определяет последовательность ДНК, в отношении которой молекула TALE или полипептид TALE характеризуются аффинностью связывания. Встречающиеся в природе полипептиды TALE и TALE DBD продуцируются в бактериях Xanthomonas.
Повтор из двух вариабельных остатков (RVD), в том значении, в котором данный термин используется в данном документе, относится к двум гипервариабельным аминокислотным остаткам в положениях 12 и 13 в TALE DBD. RVD определяет аффинность TALE DBD в отношении пары оснований ДНК. Все возможные комбинации RVD и их соответствующие аффинности в отношении пар оснований известны из уровня техники. См., например, Cong L., et al. Nat Commun. 2012 Jul 24; (3):968; Juillerat A., et al. Sci Rep. 2015 Jan 30; 5():8150; Miller J. C. et al. Nat Methods 12, 465-471 (2015); Streubel J., et al. Nat Biotechnol 30, 593-595 (2012); и Yang J. et al. Cell Res 24, 628-631 (2014), включенные в данный документ посредством ссылки во всей своей полноте. Все возможные RVD предусмотрены для применения с репрессорными полипептидами, например, молекулами TALE, описанными в данном документе.
Массив TALE DBD, в том значении, в котором данный термин используется в данном документе, относится к составу и порядку TALE DBD, например, RVD в каждом TALE DBD, в пределах молекулы TALE или полипептида TALE. Массив TALE DBD определяет специфическую в отношении последовательности аффинность связывания молекулы TALE или полипептида TALE.
В некоторых вариантах осуществления репрессорный полипептид представляет собой молекулу TALE или полипептид TALE. TALE DBD и полипептид TALE из любого биологического вида Xanthomonas можно применять в циклах генетического контроля, клетках и способах идентификации, отбора или получения клетки или линия клеток, способных к продуцированию высоких выходов продукта, например, рекомбинантного или терапевтического полипептида, описанного в данном документе. В некоторых вариантах осуществления репрессорный полипептид представляет собой встречающуюся в природе молекулу TALE или полипептид TALE. В некоторых вариантах осуществления репрессорный полипептид представляет собой сконструированную молекулу TALE или полипептид TALE, т. е. молекулу TALE или полипептид TALE, которые отличаются одной или несколькими аминокислотами от встречающихся в природе молекулы TALE или полипептида TALE или от других сконструированных молекулы TALE или полипептида TALE, известных из уровня техники.
В некоторых вариантах осуществления сконструированные молекула TALE или полипептид TALE содержат аминокислотную последовательность:
характеризующуюся 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% гомологией с;
отличающуюся на не более чем 2, 5, 10, 15, 20, 30 или 40% аминокислотных остатков при сравнении с;
отличающуюся на по меньшей мере 1, 2, 5, 10 или 20 аминокислот, но не более чем 100, 80, 70, 60, 50, 40 или 30 аминокислот от; или
идентичную последовательности любой молекулы TALE, описанной в данном документе, или последовательности встречающейся в природе молекулы TALE, например, молекулы TALE из биологического вида, перечисленного в данном документе или описанного в публикации, упомянутой в данном документе.
В некоторых вариантах осуществления молекула TALE локализуется на последовательности ДНК-мишени, определяемой массивом TALE DBD таких молекул TALE. В некоторых вариантах осуществления молекула TALE может блокировать транскрипцию при ее привлечении к ранним областям в кодирующей последовательности, например, кодирующей последовательности рекомбинантного или терапевтического полипептида. В некоторых вариантах осуществления молекула TALE может блокировать транскрипцию при ее привлечении к элементу контроля, например, промоторному элементу, функционально связанному с последовательностью, кодирующей рекомбинантный или терапевтический полипептид. В некоторых вариантах осуществления дополнительная репрессия может достигаться за счет слияния домена транскрипционной репрессии (например KRAB, SID или ERD) с молекулой TALE, что делает возможным привлечение эффектора к любому участку ДНК, определяемому массивом TALE DBD.
В некоторых вариантах осуществления молекула TALE содержит два или более (например 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, или более) TALE DBD.
В некоторых вариантах осуществления массив TALE DBD репрессорного полипептида, например, молекулы TALE, определяет последовательность ДНК-мишени. В некоторых вариантах осуществления последовательность-мишень, определяемая массивом TALE DBD, содержится в пределах элемента контроля, например, промоторного элемента, функционально связанного с последовательностью, кодирующей рекомбинантный или терапевтический полипептид. В некоторых вариантах осуществления последовательность-мишень, определяемая массивом TALE DBD, содержится в пределах последовательности, кодирующей рекомбинантный или терапевтический полипептид.
Иллюстративные последовательности встречающихся в природе и сконструированных полипептидов TALE и способы разработки и тестирования полипептидов TALE для применения с циклами генетического контроля, клетками и способами идентификации, отбора или получения клетки или линии клеток, способных к продуцированию высоких выходов продукта, например, рекомбинантного или терапевтического полипептида, описанного в данном документе, можно найти в уровне техники, например, в Zhang F, et al. Nat Biotechnol. 2011; 29:149-153; Geissler R, et al. PLoS One. 2011; 6:e19509; Garg A, et al. Nucleic Acids Res. 2012; Bultmann S, et al. Nucleic Acids Res. 2012; 40:5368-5377; Cermak T, et al. Efficient design and assembly of custom TALEN and other TAL effector-based constructs for DNA targeting. Nucleic Acids Res. 2011; 39:e82; Cong L, et al. Nat Commun. 2012; 3:968; и Miller JC, et al. Nat Biotechnol. 2011; 29:143-148, включенных в данный документ посредством ссылки во всей своей полноте.
Молекулы с "цинковыми пальцами"
В некоторых вариантах осуществления представляющий интерес гетерологичный полипептид, связанный с COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающим полипептидом и/или доменом деградации, представляет собой молекулу с "цинковыми пальцами". Молекула с "цинковыми пальцами", в том значении, в котором данный термин используется в данном документе, относится к молекуле или полипептиду, содержащим несколько доменов "цинковых пальцев" (ZFD). Молекула "цинковыми пальцами" характеризуется аффинностью в отношении специфической последовательности ДНК, определяемой составом и порядком ZFD, которые содержит молекула с "цинковыми пальцами".
Домен "цинковых пальцев" (ZFD), в том значении, в котором данный термин используется в данном документе, относится к любому полипептиду из семейства полипептидов, которые связывают ДНК зависимым от последовательности образом и которым для связывания ДНК требуется лиганд, представляющий собой ион цинка. Были исследованы и охарактеризованы множество семейств ZFD (см., например, Krishna, SS., et al. Nucl. Acids Res. (2003) 31 (2): 532-550). В настоящем изобретении предусмотрены молекулы с "цинковыми пальцами", которые могут содержать ZFD любого типа или происхождения, известных специалистам в данной области техники. Не подразумевая ограничение любым конкретным типом ZFD, в настоящем раскрытии предусмотрены молекулы с "цинковыми пальцами", содержащие Cys2His2 ZFD, которые являются наиболее распространенными и хорошо изученными ZFD из уровня техники. Cys2His2 ZFD содержат две бета-нити, которые образуют антипараллельные бета-лист и альфа-спираль. Как известно, положения -1, 1, 2, 3, 5 и 6 в альфа-спирали определяют связывание, зависимое от последовательности ДНК, за счет взаимодействия с парами оснований ДНК. В одном варианте осуществления Cys2His2 ZFD может характеризоваться специфической аффинностью связывания в отношении последовательности мишени из 3 пар оснований. В одном варианте осуществления Cys2His2 ZFD может специфически взаимодействовать с дополнительной парой оснований, смежной с последовательностью-мишенью, зависящим от контекста образом, т. е. в зависимости от присутствия и состава смежных ZFD в пределах молекулы с цинковыми пальцами.
Массив доменов "цинковых пальцев" или массив ZFD, в том значении, в котором данный термин используется в данном документе, относится к составу и порядку ZFD в пределах молекулы с "цинковыми пальцами" или полипептида с "цинковыми пальцами". Массив ZFD определяет специфическую в отношении последовательности аффинность связывания молекулы с "цинковыми пальцами" или полипептид с "цинковыми пальцами".
В некоторых вариантах осуществления репрессорный полипептид представляет собой молекулу с "цинковыми пальцами" или полипептид с "цинковыми пальцами". ZFD и полипептиды с "цинковыми пальцами" из любого биологического вида (например, вида млекопитающих, например, человека) можно применять в циклах генетического контроля, клетках и способах идентификации, отбора или получения клетки или линии клеток, способных к продуцированию высоких выходов продукта, например, рекомбинантного или терапевтического полипептида, описанного в данном документе. В некоторых вариантах осуществления репрессорный полипептид представляет собой встречающуюся в природе молекулу с "цинковыми пальцами" или полипептид с "цинковыми пальцами". В некоторых вариантах осуществления репрессорный полипептид представляет собой сконструированную молекулу с "цинковыми пальцами" или полипептид с "цинковыми пальцами", т. е. молекулу с "цинковыми пальцами" или полипептид с "цинковыми пальцами", которые отличаются одной или несколькими аминокислотами от встречающихся в природе молекулы с "цинковыми пальцами" или полипептида с "цинковыми пальцами" или от других сконструированных молекулы с "цинковыми пальцами" или полипептида с "цинковыми пальцами", известных из уровня техники.
В некоторых вариантах осуществления сконструированная молекула с "цинковыми пальцами" или полипептид с "цинковыми пальцами" содержат аминокислотную последовательность:
характеризующуюся 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% гомологией с;
отличающуюся на не более 2, 5, 10, 15, 20, 30, или 40% аминокислотных остатков при сравнении с;
отличающуюся по меньшей мере 1, 2, 5, 10 или 20 аминокислотами, но не более чем 100, 80, 70, 60, 50, 40 или 30 аминокислотами от; или
идентичную последовательности любой молекулы с "цинковыми пальцами", описанной в данном документе, или последовательности встречающейся в природе молекулы с "цинковыми пальцами", например, молекулы с "цинковыми пальцами" от биологического вида, перечисленного в данном документе или описанного в публикации, упомянутой в данном документе.
В некоторых вариантах осуществления молекула с "цинковыми пальцами" локализуется на последовательности ДНК-мишени, определяемой массивом ZFD таких молекул с "цинковыми пальцами". В некоторых вариантах осуществления молекула с "цинковыми пальцами" может блокировать транскрипцию при ее привлечении к ранним областям в кодирующей последовательности, например, кодирующей последовательности рекомбинантного или терапевтического полипептида. В некоторых вариантах осуществления молекула с "цинковыми пальцами" может блокировать транскрипцию при ее привлечении к элементу контроля, например, промоторному элементу, функционально связанному с последовательностью, кодирующей рекомбинантный или терапевтический полипептид. В некоторых вариантах осуществления дополнительная репрессия может достигаться за счет слияния домена транскрипционной репрессии (например KRAB, SID или ERD) с молекулой с "цинковыми пальцами", что делает возможным привлечение эффектора к любому участку ДНК, определяемому массивом ZFD.
В некоторых вариантах осуществления молекула с "цинковыми пальцами" содержит два или более (например 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, или более) ZFD. В некоторых вариантах осуществления массив ZFD может быть сконструирован из ZFD с аффинностью в отношении известных последовательностей-мишеней для создания молекулы с "цинковыми пальцами" или полипептида с "цинковыми пальцами" с необходимой специфической последовательностью-мишенью.
В некоторых вариантах осуществления массив ZFD репрессорного полипептида, например, молекулы с "цинковыми пальцами", определяет последовательность ДНК-мишени. В некоторых вариантах осуществления последовательность-мишень, определяемая массивом ZFD, содержится в пределах элемента контроля, например, промоторного элемента, функционально связанного с последовательностью, кодирующей рекомбинантный или терапевтический полипептид. В некоторых вариантах осуществления последовательность-мишень, определяемая массивом ZFD, содержится в пределах последовательности, кодирующей рекомбинантный или терапевтический полипептид.
Иллюстративные последовательности встречающихся в природе и сконструированных полипептидов с "цинковыми пальцами" и способы разработки и тестирования полипептидов с "цинковыми пальцами" для применения с циклами генетического контроля, клетками и способами идентификации, отбора или получения клетки или линии клеток, способных к продуцированию высоких выходов продукта, например, рекомбинантного или терапевтического полипептида, описанными в данном документе, можно найти в уровне техники, например, в Wolfe SA, et al. Annu Rev Biophys Biomol Struct. 2000; 29:183-212; Pabo CO, et al. Annu Rev Biochem. 2001; 70:313-340; Greisman HA, Pabo CO. Science. 1997; 275:657-661; Isalan M, et al., Proc Natl Acad Sci U S A. 1997; 94:5617-5621; Wolfe SA, et al. J Mol Biol. 1999; 285:1917-1934, включенных в данный документ посредством ссылки во всей своей полноте.
Способы разработки ZFD и массивов ZFD для связывания специфических последовательностей ДНК-мишеней можно найти в уровне техники, например, в Maeder ML, et al. Mol Cell. 2008; 31:294-301; Sander JD, et al., Nat Methods. 2011; 8:67-69; и Meng X, et al. Nat Biotechnol. 2008; 26:695-701, включенных в данный документ посредством ссылки во всей своей полноте.
Домены деградации
В некоторых вариантах осуществления слитый полипептид по настоящему изобретению дополнительно содержит домен деградации. В некоторых вариантах осуществления домен деградации имеет первое состояние и второе состояние, например, состояния стабилизации/дестабилизации или состояния укладки/неправильной укладки. Первое состояние ассоциировано, вызывает или опосредует экспрессию слитого полипептида при первых скорости или уровне, а второе состояние ассоциировано, вызывает или опосредует экспрессию слитого полипептида при вторых скорости или уровне. В некоторых вариантах осуществления второе состояние характеризуется уровнем или скоростью, которые превышают, например, в 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, или 30 раз превышают, скорость или уровень, характерные для первого состояния. В некоторых вариантах осуществления второе состояние ассоциировано, поддерживается или обусловлено присутствием стабилизирующего соединения. В некоторых вариантах осуществления присутствие стабилизирующего соединения может быть ассоциировано, обуславливает или опосредует переход из состояния первой укладки в состояние второй укладки, например, из состояния неправильной укладки в состояние с более правильной укладкой, например, из первого состояния, восприимчивого к деградации, во второе состояние, менее восприимчивое к деградации, чем первое состояние; или из состояния первой укладки, которое характеризуется первым уровнем деградации в состояние второй укладки, которое характеризуется вторым, меньшим уровнем деградация, например, в представляющей интерес клетке.
В одном варианте осуществления добавление стабилизирующего соединения к совокупности клеток, например, клеток-хозяев или клеток, содержащих слитые полипептиды, описанные в данном документе, вызывает переход подсовокупности клеток из первого состояния во второе состояние, например, состояния стабилизации/дестабилизации или состояния укладки/неправильной укладки, описанные в данном документе. В одном варианте осуществления в отсутствие стабилизирующего соединения во втором состоянии находятся менее 10, 9, 8, 7, 6, 5, 4, 3, 2, или 1% клеток в совокупности, и в первом состоянии находятся 90, 91, 92, 93, 94, 95, 96, 97, 98, или 99% или более клеток в совокупности. В одном варианте осуществления в присутствии стабилизирующего соединения во втором состоянии находятся 20, 30, 40, 50, 60, 70, 80, 90, или 95% или более клеток в совокупности, и в первом состоянии находятся менее 20, 15, 10, 9, 8, 7, 6, 5, 4, 3, 2, или 1% клеток в совокупности. Определение процентных долей клеток в совокупности, находящихся в определенном состоянии, можно быть осуществлять с применением способов, описанных на протяжении всего описания.
В одном варианте осуществления домен деградации отделен от остальной части слитого полипептида с помощью гетерологичного сайта расщепления протеазами.
Без ограничения какой-либо теорией, в некоторых вариантах осуществления домен деградации является нестабильным и/или не может укладываться в стабильную конформацию в отсутствие стабилизирующего соединения. Данный домен деградации c неправильной укладкой/отсутствием укладки может подвергаться деградации под действием внутриклеточного пути деградации вместе с остальной частью слитого полипептида. В присутствии стабилизирующего соединения домен деградации принимает правильную конформацию и менее восприимчив к внутриклеточным путям деградации. Таким образом, уровень экспрессии слитого полипептида может контролироваться присутствием или отсутствием стабилизирующего соединения.
В некоторых вариантах осуществления правильная укладка домена деградации открывает гетерологичный сайт расщепления протеазами, что приводит к расщеплению гетерологичного сайта расщепления протеазами и удалению домена деградации из остальной части слитого полипептида.
Способы получения доменов деградации, которые являются селективно стабильными в присутствии стабилизирующего соединения, широко известны из уровня техники и дополнительно рассмотрены ниже. Несколько таких пар домен-стабилизирующих соединений были получены к настоящему времени, и они описаны в настоящем изобретении. Они включают домены деградации на основе FKBP (например, с применением "Shield" стабилизирующего соединения), описанные в: A Rapid, Reversible, and Tunable Method to Regulate Protein Function in Living Cells Using Synthetic Small Molecules." Banaszynski, L. A.; Chen, L.-C.; Maynard-Smith, L. A.; Ooi, A. G. L.; Wandless, T. J. Cell, 2006, 126, 995-1004; домены на основе DHFR (например, с применением триметоприма в качестве стабилизирующего соединения), описанные в A general chemical method to regulate protein stability in the mammalian central nervous system. Iwamoto, M.;  , T.; Lundberg, C.; Kirik, D.; Wandless, T. J. Chemistry & Biology, 2010, 17, 981-988; и домены на основе эстрогенового рецептора-альфа (например, в которых в качестве стабилизирующего соединения применяют 4OHT), описанные в Destabilizing domains derived from the human estrogen receptor Y Miyazaki, H Imoto, L-c Chen, TJ Wandless J. Am. Chem. Soc. 2012, 134, 3942-3945. Каждый из этих литературных источников включен посредством ссылки во всей своей полноте.
, T.; Lundberg, C.; Kirik, D.; Wandless, T. J. Chemistry & Biology, 2010, 17, 981-988; и домены на основе эстрогенового рецептора-альфа (например, в которых в качестве стабилизирующего соединения применяют 4OHT), описанные в Destabilizing domains derived from the human estrogen receptor Y Miyazaki, H Imoto, L-c Chen, TJ Wandless J. Am. Chem. Soc. 2012, 134, 3942-3945. Каждый из этих литературных источников включен посредством ссылки во всей своей полноте.
Настоящее изобретение охватывает домены деградации, полученные из любого встречающегося в природе белка. Предпочтительно, слитые полипептиды по настоящему изобретению будут включать домен деградации, для которого отсутствует лиганд, нативным образом экспрессируемый в представляющих интерес компартментах клетки. Например, если слитый полипептид разработан для экспрессии в T-клетках, предпочтительно выбрать домен деградации, для которого отсутствует встречающийся в природе лиганд, присутствующий в T-клетках. Таким образом, при экспрессии в представляющей интерес клетке домен деградации будет стабилизироваться только в присутствии соединения, добавляемого экзогенно. Следует отметить, что данное свойство может быть сконструировано либо путем конструирования домена деградации, который более не связывается с нативно экспрессируемым лигандом (в данном случае домен деградации будет стабильным только в присутствии синтетического соединения), либо путем экспрессии домена деградации в компартменте, в котором нативно экспрессируемый лиганд не существует (например, домен деградации может быть получен из биологического вида, отличного от биологического вида, в котором слитый полипептид будет экспрессироваться).
Пара домен деградации-стабилизирующее соединение может быть получена из любого встречающегося в природе или синтетически разработанного белка. Стабилизирующие соединения могут являться любыми встречающимися в природе или синтетическими соединениями. В определенных вариантах осуществления стабилизирующие соединения будут представлять собой существующие препараты, отпускаемые по рецепту, или безрецептурные препараты. Примеры белков, которые можно сконструировать, чтобы они обладали свойствами домена деградации, представлены в таблице 21 ниже вместе с соответствующим стабилизирующим соединением.
В некоторых вариантах осуществления домен деградации получен из белка, перечисленного в таблице 21.
В некоторых вариантах осуществления домен деградации получен из эстрогенового рецептора (ER). В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность, выбранную из SEQ ID NO: 46 или последовательность, характеризующуюся по меньшей мере 90%, 95%, 97%, 98%, или 99% идентичностью с ней, или SEQ ID NO: 48 или последовательность, характеризующуюся по меньшей мере 90%, 95%, 97%, 98%, или 99% идентичностью с ней. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность под SEQ ID NO: 46 или 48. Если домен деградации получен из эстрогенового рецептора, то стабилизирующее соединение может быть выбрано из базедоксифена или 4-гидрокситамоксифена (4-OHT). В некоторых вариантах осуществления стабилизирующее соединение представляет собой базедоксифен. Тамоксифен и базедоксифен представляют собой лекарственные средства, одобренные FDA, и, таким образом, являются безопасными для применения человеком.
В некоторых вариантах осуществления домен деградации получен из белка FKB (FKBP). В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность под SEQ ID NO: 50 или последовательность, характеризующуюся по меньшей мере 90%, 95%, 97%, 98%, или 99% идентичностью с ней. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность под SEQ ID NO: 50. Если домен деградации получен из FKBP, то стабилизирующее соединение может представлять собой Shield-1.
В некоторых вариантах осуществления домен деградации получен из дигидрофолатредуктазы (DHFR). В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность под SEQ ID NO: 51 или последовательность, характеризующуюся по меньшей мере 90%, 95%, 97%, 98%, или 99% идентичностью с ней. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность под SEQ ID NO: 51. Если домен деградации получен из DHFR, то стабилизирующее соединение может представлять собой триметоприм.
В некоторых вариантах осуществления домен деградации не получен из белка FKB, эстрогенового рецептора или DHFR.
(305aa-549aa) аминокислотная последовательность
(305aa-549aa) нуклеотидная последовательность
Домены деградации могут быть сконструированы из известных белков (например, белков, изложенных в таблице 21) с помощью любого из различных традиционных способов, известных из уровня техники. Обычно в таких способах используется, во-первых, создание представляющей интерес библиотеки, включающей белки, например, полученный из встречающегося в природе белка. Во-вторых, клетки или популяции клеток, экспрессирующих белки с отдельных конструкций библиотеки, будут отбираться на основании того, является ли экспрессия полученного белка зависимой от присутствия необходимого стабилизирующего соединения. Способ дериватизации и отбора можно повторять в виде множества циклов при необходимости идентифицировать подходящего кандидата.
Например, библиотека может быть создана с помощью рационального белкового дизайна на основании отбора образцов с различными структурами и предполагаемыми аффинностями белкового домена в отношении выбранного соединения. В качестве альтернативы, библиотеку можно создавать за счет случайного мутагенеза белка-мишени. В каждом случае, например, клетки Jurkat можно трансдуцировать с помощью лентивирусной библиотеки, созданной из конструкций. Затем клетки Jurkat можно подвергнуть раунду FACS-сортировки, чтобы исключить клетки, которые конститутивно экспрессируют представляющий интерес белок. На следующей стадии отсортированные клетки инкубируют с выбранным соединением в течение 24 часов, и положительные клетки подвергают FACS-сортировке. Эти клетки размножают путем клонирования отдельных клеток. Далее индивидуальные трансдуцированные клоны будут оценивать в отношении способности индуцировать экспрессию представляющего интерес белка зависимым от соединения образом.
В некоторых вариантах осуществления слитый полипептид по настоящему изобретению содержит домен деградации, COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид и гетерологичный полипептид. В некоторых вариантах осуществления уровень экспрессии слитого полипептида в присутствии стабилизирующего соединения увеличивается, например, в по меньшей мере 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, по сравнению с уровнем экспрессии слитого полипептида в отсутствие стабилизирующего соединения, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
Сайт расщепления
В некоторых вариантах осуществления слитый полипептид по настоящему изобретению содержит первый домен и второй домен, отделенные гетерологичным сайтом расщепления, где первый домен содержит домен деградации, и второй домен содержит COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид и гетерологичный полипептид.
Сайт расщепления может представлять собой сайт саморасщепления и/или сайт расщепления протеазами. Можно разработать сайт расщепления, который будет расщепляться под действием любой сайт-специфической протеазы, которая экспрессируется в представляющей интерес клетке (либо путем рекомбинантной экспрессии, либо эндогенной экспрессии) на уровнях, достаточных для отщепления домена деградации. В важных аспектах настоящего изобретения выбран сайт расщепления протеазами, соответствующий протеазе, которая нативным образом (или с помощью генной инженерии клетки) присутствует в клеточном компартменте, ответственном за экспрессию представляющего интерес белка. Внутриклеточная миграция протеазы должна перекрываться или частично перекрываться с внутриклеточной миграцией представляющего интерес белка, который содержит используемый домен деградации. Например, если представляющий интерес белок находится на клеточной поверхности, то фермент для его расщепления можно может добавлять в клетку экзогенным путем.
Если представляющий интерес белок постоянно находится в эндосомной/лизосомной системе, то можно применять сайт расщепления протеазами для фермента, постоянно находящегося в данных компартментах. Например, консенсусные мотивы для таких протеаз включают следующие:
фурин: консенсусный мотив RX(K/R)R (X может быть любой аминокислотой; SEQ ID NO: 52);
PCSK1: консенсусный мотив RX(K/R)R (X может быть любой аминокислотой; SEQ ID NO: 52);
PCSK5: консенсусный мотив RX(K/R)R (X может быть любой аминокислотой; SEQ ID NO: 52);
PCSK6: консенсусный мотив RX(K/R)R (X может быть любой аминокислотой; SEQ ID NO: 52);
PCSK7: консенсусный мотив RXXX[KR]R (X может быть любой аминокислотой; SEQ ID NO: 53);
катепсин B: RRX (SEQ ID NO: 54);
гранзим B: I-E-P-D-X (SEQ ID NO: 55);
фактор XA: Ile-Glu/Asp-Gly-Arg (SEQ ID NO: 56);
энтерокиназа: Asp-Asp-Asp-Asp-Lys (SEQ ID NO: 57);
гененаза: Pro-Gly-Ala-Ala-His-Tyr (SEQ ID NO: 58);
сортаза: LPXTG/A (SEQ ID NO: 59);
протеаза PreScission: Leu-Glu-Val-Phe-Gln-Gly-Pro (SEQ ID NO: 60);
тромбин: Leu-Val-Pro-Arg-Gly-Ser (SEQ ID NO: 61);
протеаза TEV: E-N-L-Y-F-Q-G (SEQ ID NO: 62);
эластаза 1: [AGSV]-X (X может быть любой аминокислотой; SEQ ID NO: 63).
В некоторых вариантах осуществления слитый полипептид, описанный в данном документе, содержит сайт расщепления фурином. В некоторых вариантах осуществления слитые полипептиды, описанные в данном документе, содержат любой из сайтов расщепления фурином, перечисленных в таблице 23.
В некоторых вариантах осуществления слитые полипептиды, описанные в данном документе, содержат сайт расщепления фурином, выбранный из RTKR (SEQ ID NO: 123) или последовательности, характеризующейся по меньшей мере 90%, 95%, 97%, 98% или 99% идентичностью с ней; GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125) или последовательности, характеризующейся по меньшей мере 90%, 95%, 97%, 98% или 99% идентичностью с ней; GTGAEDPRPSRKRR (SEQ ID NO: 127) или последовательности, характеризующейся по меньшей мере 90%, 95%, 97%, 98% или 99% идентичностью с ней; LQWLEQQVAKRRTKR (SEQ ID NO: 129) или последовательности, характеризующейся по меньшей мере 90%, 95%, 97%, 98% или 99% идентичностью с ней; GTGAEDPRPSRKRRSLGG (SEQ ID NO: 131) или последовательности, характеризующейся по меньшей мере 90%, 95%, 97%, 98% или 99% идентичностью с ней; GTGAEDPRPSRKRRSLG (SEQ ID NO: 133) или последовательности, характеризующейся по меньшей мере 90%, 95%, 97%, 98% или 99% идентичностью с ней; SLNLTESHNSRKKR (SEQ ID NO: 135) или последовательности, характеризующейся по меньшей мере 90%, 95%, 97%, 98% или 99% идентичностью с ней; или CKINGYPKRGRKRR (SEQ ID NO: 137) или последовательности, характеризующейся по меньшей мере 90%, 95%, 97%, 98% или 99% идентичностью с ней.
В некоторых вариантах осуществления слитые полипептиды, описанные в данном документе, содержат сайт расщепления фурином, выбранный из RTKR (SEQ ID NO: 123); GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125); GTGAEDPRPSRKRR (SEQ ID NO: 127); LQWLEQQVAKRRTKR (SEQ ID NO: 129); GTGAEDPRPSRKRRSLGG (SEQ ID NO: 131); GTGAEDPRPSRKRRSLG (SEQ ID NO: 133); SLNLTESHNSRKKR (SEQ ID NO: 135) или CKINGYPKRGRKRR (SEQ ID NO: 137).
В некоторых вариантах осуществления слитые полипептиды, описанные в данном документе, содержат сайт расщепления фурином, выбранный из GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125) или последовательности, характеризующейся по меньшей мере 90%, 95%, 97%, 98% или 99% идентичностью с ней, или GTGAEDPRPSRKRR (SEQ ID NO: 127) или последовательности, характеризующейся по меньшей мере 90%, 95%, 97%, 98% или 99% идентичностью с ней.
В некоторых вариантах осуществления слитые полипептиды, описанные в данном документе, содержат сайт расщепления фурином, выбранный из GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125) или GTGAEDPRPSRKRR (SEQ ID NO: 127).
В некоторых вариантах осуществления слитые полипептиды, описанные в данном документе, содержат сайт расщепления фурином GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125).
(SEQ ID NO: 129)
(SEQ ID NO: 131)
(SEQ ID NO: 133)
(SEQ ID NO: 135)
(SEQ ID NO: 137)
Сигнальный пептид
В определенных вариантах осуществления слитые полипептиды по настоящему изобретению дополнительно содержат сигнальный пептид. Сигнальные пептиды применяются, если необходимо получить белок, который следует по секреторному пути. В некоторых вариантах осуществления данный сигнальный пептид будет сконструирован таким образом, чтобы он присутствовал на самом N-конце слитого полипептида. Иллюстративные сигнальные пептиды изложены ниже:
CD8: MALPVTALLLPLALLLHAARP (SEQ ID NO: 64);
GMCSFR: MLLLVTSLLLCELPHPAFLLIP (SEQ ID NO: 65);
IL2: MYRMQLLSCIALSLALVTNS (SEQ ID NO: 66);
IgK-цепь: MAQVKLQESGTELAKPGAAVK (SEQ ID NO: 67);
NPC2: MRFLAATFLLLALSTAAQA (SEQ ID NO: 68);
LAMB1: MGLLQLLAFSFLALCRARVRA (SEQ ID NO: 69);
P3IP1: MLLAWVQAFLVSNMLLAEAYG (SEQ ID NO: 70);
DMKN: MKFQGPLACLLLALCLGSGEA (SEQ ID NO: 71);
TPA: MDAMKRGLCCVLLLCGAVFVSP (SEQ ID NO: 72);
PCSK9: MGTVSSRRSWWPLPLLLLLLLLLGPAGARAQEDED (SEQ ID NO: 73);
KDEL (SEQ ID NO: 74) или KKXX (X может быть любой аминокислотой; SEQ ID NO: 75), и производные на самом C-конце представляющего интерес белка можно сконструировать, если представляющий интерес белок является белком, постоянно находящимся в ER. Такие последовательности должны быть вставлены вместе с сигнальным пептидом.
Могут быть сконструированы представляющие интерес белки, которые содержат паттерны гликозилирования для интернализации через рецептор манноза-6-фосфата и нацеливающиеся в эндосомную/лизосомную систему. Они должны быть включены в представляющий интерес белок сам по себе, если данный белок постоянно находится в таком компартменте. Консенсусная последовательность для N-гликозилирования представляет собой Asn-X-Ser/Thr, где X представляет собой любую аминокислоту, кроме пролина (Pro), серина (Ser) и треонина (Thr) (SEQ ID NO: 76).
В вариантах осуществления, в которых необходимо получить представляющие интерес белки, нацеленные в пероксисому, может быть сконструирован слитый полипептид, содержащий C-концевой сигнал нацеливания в пероксисому (например, PTS1: -SKL).
Нуклеиновая кислота и векторы, кодирующие слитые полипептиды
В другом аспекте, настоящее изобретение относится к нуклеиновой кислоте, кодирующей любые слитые полипептиды, описанные в данном документе, или вектор, содержащий такую нуклеиновую кислоту. В одном варианте осуществления вектор выбран из ДНК-вектора, РНК-вектора, плазмиды, лентивирусного вектора, аденовирусного вектора или ретровирусного вектора. В одном варианте осуществления вектор представляет собой лентивирусный вектор.
В настоящем изобретении также представлены векторы, в которые вставлена ДНК по настоящему изобретению. Векторы, полученные из ретровирусов, таких как лентивирус, являются подходящими инструментами для достижения долгосрочного переноса генов, поскольку они обеспечивают долгосрочную стабильную интеграцию трансгена и его размножение в дочерних клетках. Лентивирусные векторы обладают дополнительным преимуществом по сравнению с векторами, полученными из онкоретровирусов, таких как вирусы лейкоза мышей, заключающемся в том, что ими можно трансдуцировать непролиферирующие клетки, такие как гепатоциты. Они также обладают дополнительным преимуществом низкой иммуногенности. Ретровирусный вектор также может представлять собой, например, гамма-ретровирусный вектор. Гамма-ретровирусный вектор может содержать, например, промотор, сигнал упаковки (ψ), сайт связывания праймера (PBS), один или несколько (например, два) длинных концевых повторов (LTR) и представляющий интерес трансген, например ген, кодирующий CAR. В гамма-ретровирусном векторе могут отсутствовать структурные гены вирусов, такие как gag, pol и env. Иллюстративные гамма-ретровирусные векторы включают вирус лейкоза мышей (MLV), вирус некроза селезенки (SFFV) и вирус миелопролиферативной саркомы (MPSV), а также векторы, полученные из них. Другие гамма-ретровирусные векторы описаны, например, в Tobias Maetzig et al., "Gammaretroviral Vectors: Biology, Technology and Application" Viruses. 2011 Jun; 3(6): 677-713, который настоящим включен в данный документ посредством ссылки.
В другом варианте осуществления вектор, содержащий нуклеиновую кислоту, кодирующую необходимый слитый полипептид по настоящему изобретению, представляет собой аденовирусный вектор (A5/35). В другом варианте осуществления экспрессию нуклеиновых кислот, кодирующих химерные молекулы, можно осуществлять с помощью транспозонов, таких как "спящая красавица", с применением инструментов генного редактирования CRISPR (например, CAS9) и с применением нуклеаз с "цинковыми пальцами". См., например, June et al. 2009, Nature Reviews Immunology 9.10: 704-716, который настоящим включен в данный документ посредством ссылки.
Нуклеиновую кислоту можно клонировать в векторы множества типов. Например, нуклеиновую кислоту можно клонировать в вектор, включающий без ограничения плазмиду, фагмиду, производное фага, вирус животных и космиду. Векторы, представляющие особый интерес, включают экспрессионные векторы, репликационные векторы, векторы для образования зондов и векторы для секвенирования.
Конструкции нуклеиновой кислоты, кодирующие слитые полипептиды, например, CAR, содержащий COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид
В настоящем изобретении также представлены молекулы нуклеиновой кислоты, кодирующие один или несколько слитых полипептидов, раскрытых в данном документе.
В одном варианте осуществления слитый полипептид содержит конструкцию CAR, которая нацеливается на опухолевый антиген и/или B-клеточный антиген, описанный в данном документе. В одном аспекте молекула нуклеиновой кислоты представлена в виде транскрипта, представляющего собой матричную РНК. В одном аспекте молекула нуклеиновой кислоты представлена в виде ДНК-конструкции.
Соответственно, в одном аспекте настоящее изобретение относится к молекуле нуклеиновой кислоты, кодирующей слитый полипептид, который содержит COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид и гетерологичный полипептид. В некоторых вариантах осуществления гетерологичный полипептид представляет собой химерный антигенный рецептор (CAR), где CAR содержит антигенсвязывающий домен, который связывается с опухолевым антигеном, описанным в данном документе, или B-клеточным антигеном, описанным в данном документе, трансмембранный домен (например, трансмембранный домен, описанный в данном документе) и внутриклеточный сигнальный домен (например, внутриклеточный сигнальный домен, описанный в данном документе), содержащий стимулирующий домен, например, костимулирующий сигнальный домен (например, костимулирующий сигнальный домен, описанный в данном документе) и/или первичный сигнальный домен (например, первичный сигнальный домен, описанный в данном документе, например, дзета-цепь описанную в данном документе). В одном варианте осуществления трансмембранный домен представляет собой трансмембранный домен белка, выбранного из группы, состоящей из альфа-, бета- или дзета-цепи Т-клеточного рецептора, CD28, CD3-эпсилон, CD45, CD4, CD5, CD8, CD9, CD16, CD22, CD33, CD37, CD64, CD80, CD86, CD134, CD137 и CD154. В некоторых вариантах осуществления трансмембранный домен может включать по меньшей мере трансмембранную(-ые) область(-и), например, KIRDS2, OX40, CD2, CD27, LFA-1 (CD11a, CD18), ICOS (CD278), 4-1BB (CD137), GITR, CD40, BAFFR, HVEM (LIGHTR), SLAMF7, NKp80 (KLRF1), NKp44, NKp30, NKp46, CD160, CD19, IL2R-бета, IL2R-гамма, IL7R α, ITGA1, VLA1, CD49a, ITGA4, IA4, CD49D, ITGA6, VLA-6, CD49f, ITGAD, CD11d, ITGAE, CD103, ITGAL, CD11a, LFA-1, ITGAM, CD11b, ITGAX, CD11c, ITGB1, CD29, ITGB2, CD18, LFA-1, ITGB7, NKG2D, NKG2C, TNFR2, DNAM1 (CD226), SLAMF4 (CD244, 2B4), CD84, CD96 (Tactile), CEACAM1, CRTAM, Ly9 (CD229), CD160 (BY55), PSGL1, CD100 (SEMA4D), SLAMF6 (NTB-A, Ly108), SLAM (SLAMF1, CD150, IPO-3), BLAME (SLAMF8), SELPLG (CD162), LTBR, PAG/Cbp, NKG2D и NKG2C.
В одном варианте осуществления трансмембранный домен содержит последовательность под SEQ ID NO: 155 или последовательность, идентичную им на с 95-99%. В одном варианте осуществления антигенсвязывающий домен соединен с трансмембранным доменом с помощью шарнирной области, например, шарнирной области, описанной в данном документе. В одном варианте осуществления шарнирная область содержит SEQ ID NO: 147, или SEQ ID NO: 149, или SEQ ID NO: 151, или SEQ ID NO: 153, или последовательность, идентичную им на 95-99%. В одном варианте осуществления выделенная молекула нуклеиновой кислоты дополнительно содержит последовательность, кодирующую костимулирующий домен. В одном варианте осуществления костимулирующий домен представляет собой функциональный сигнальный домен белка, выбранного из группы, состоящей из OX40, CD27, CD28, CDS, ICAM-1, LFA-1 (CD11a/CD18), ICOS (CD278) и 4-1BB (CD137). Дополнительные примеры таких костимулирующих молекул включают CDS, ICAM-1, GITR, BAFFR, HVEM (LIGHTR), SLAMF7, NKp80 (KLRF1), NKp44, NKp30, NKp46, CD160, CD19, CD4, CD8-альфа, CD8-бета, IL2R-бета, IL2R-гамма, IL7R-альфа, ITGA4, VLA1, CD49a, ITGA4, IA4, CD49D, ITGA6, VLA-6, CD49f, ITGAD, CD11d, ITGAE, CD103, ITGAL, CD11a, LFA-1, ITGAM, CD11b, ITGAX, CD11c, ITGB1, CD29, ITGB2, CD18, LFA-1, ITGB7, NKG2D, NKG2C, TNFR2, TRANCE/RANKL, DNAM1 (CD226), SLAMF4 (CD244, 2B4), CD84, CD96 (Tactile), CEACAM1, CRTAM, Ly9 (CD229), CD160 (BY55), PSGL1, CD100 (SEMA4D), CD69, SLAMF6 (NTB-A, Ly108), SLAM (SLAMF1, CD150, IPO-3), BLAME (SLAMF8), SELPLG (CD162), LTBR, LAT, GADS, SLP-76, PAG/Cbp, NKG2D и NKG2C. В одном варианте осуществления внутриклеточный сигнальный домен содержит функциональный сигнальный домен 4-1BB и функциональный сигнальный домен CD3-дзета. В одном варианте осуществления внутриклеточный сигнальный домен содержит последовательность под SEQ ID NO: 158, 161, 176 или 180, или последовательность, идентичную им на 95-99%, и последовательность под SEQ ID NO: 163, или SEQ ID NO: 166, или последовательность, идентичную им на 95-99%, где последовательности, содержащие внутриклеточный сигнальный домен экспрессируются в одной и той же рамке считывания и в виде одной полипептидной цепи.
В другом аспекте настоящее изобретение относится к выделенной молекуле нуклеиновой кислоты, кодирующей слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит конструкцию CAR, содержащую лидерную последовательность под SEQ ID NO: 64, scFv-домен, описанный в данном документе, шарнирную область под SEQ ID NO: 147, или SEQ ID NO: 149, или SEQ ID NO: 151, или SEQ ID NO: 153 (или последовательность, идентичную им на 95-99%), трансмембранный домен, имеющий последовательность под SEQ ID NO: 155 (или последовательность, идентичную е на 95-99%), костимулирующий домен 4-1BB, имеющий последовательность под SEQ ID NO:158, костимулирующий домен CD27, имеющий последовательность под SEQ ID NO: 161 (или последовательность, идентичную ей на 95-99%), костимулирующий домен ICOS, имеющий последовательность под SEQ ID NO: 176 (или последовательность, идентичную ей на 95-99%), или костимулирующий домен CD28, имеющий последовательность под SEQ ID NO: 180, и стимулирующий домен CD3-дзета, имеющий последовательность под SEQ ID NO: 163 или SEQ ID NO: 166 (или последовательность, идентичную им на 95-99%).
Последовательности нуклеиновой кислоты, кодирующие необходимые молекулы, можно получать с применением рекомбинантных способов, известных из уровня техники, как, например, путем скрининга библиотек из клеток, экспрессирующих ген, путем получения гена из вектора, который, как известно, включает его, или путем непосредственного выделения из клеток и тканей, содержащих его, с применением стандартных методик. В качестве альтернативы, представляющий интерес ген может быть получен синтетическим путем, а не клонирован.
В настоящем изобретении также представлены векторы, в которые встроена нуклеиновая кислота по настоящему изобретению. Векторы, полученные из ретровирусов, таких как лентивирус, являются подходящими инструментами для достижения долгосрочного переноса генов, поскольку они обеспечивают долгосрочную стабильную интеграцию трансгена и его размножение в дочерних клетках. Лентивирусные векторы обладают дополнительным преимуществом по сравнению с векторами, полученными из онкоретровирусов, таких как вирусы лейкоза мышей, заключающимся в том, что ими можно трансдуцировать непролиферирующие клетки, такие как гепатоциты. Они также обладают дополнительным преимуществом низкой иммуногенности.
Кратко обобщим, экспрессия рекомбинантных нуклеиновых кислот, кодирующих слитый полипептид по настоящему изобретению, как правило, достигается за счет функциональной связи нуклеиновой кислоты, кодирующей слитый полипептид, с промотором и введения конструкции в экспрессионный вектор. Векторы могут подходить для репликации и интеграции у эукариот. Типичные клонирующие векторы содержат терминаторы транскрипции и трансляции, последовательности инициации и промоторы, применимые для регуляции экспрессии необходимой последовательности нуклеиновой кислоты.
Экспрессионные конструкции по настоящему изобретению также можно применять для иммунизации и генной терапии нуклеиновыми кислотами с применением стандартных протоколов доставки генов. Способы доставки генов известны из уровня техники. См., например, патенты США №№ 5399346, 5580859, 5589466, включенные в данный документ посредством ссылки во всей своей полноте. В другом варианте осуществления настоящего изобретения представлен вектор для генной терапии.
Нуклеиновую кислоту можно клонировать в векторы множества типов. Например, нуклеиновую кислоту можно клонировать в вектор, включающий без ограничения плазмиду, фагмиду, производное фага, вирус животных и космиду. Векторы, представляющие особый интерес, включают экспрессионные векторы, репликационные векторы, векторы для образования зондов и векторы для секвенирования.
Кроме того, экспрессионный вектор может обеспечиваться для клетки в форме вирусного вектора. Технология вирусных векторов хорошо известна из уровня техники и описана, например, в Sambrook et al., 2012, MOLECULAR CLONING: A LABORATORY MANUAL, volumes 1-4, Cold Spring Harbor Press, NY) и в других руководствах по вирусологии и молекулярной биологии. Вирусы, применимые в качестве векторов, включают без ограничения ретровирусы, аденовирусы, аденоассоциированные вирусы, герпесвирусы и лентивирусы. Как правило, подходящий вектор содержит точку начала репликации, функционирующую в по меньшей мере одном организме, промоторную последовательность, подходящие сайты для рестрикционных эндонуклеаз и один или несколько селектируемых маркеров (например, WO 01/96584; WO 01/29058 и патент США № 6326193).
Для переноса генов в клетки млекопитающих был разработан целый ряд систем на основе вирусов. Например, ретровирусы обеспечивают удобную платформу для систем доставки генов. Выбранный ген можно вставить в вектор и упаковать в ретровирусные частицы с помощью методик, известных из уровня техники. Затем рекомбинантный вирус можно выделить и доставить в клетки субъекта либо in vivo, либо ex vivo. Из уровня техники известен целый ряд ретровирусных систем. В некоторых вариантах осуществления применяются аденовирусные векторы. Из уровня техники известен целый ряд аденовирусных векторов. В одном варианте осуществления применяются лентивирусные векторы.
Дополнительные промоторные элементы, например, энхансеры, регулируют частоту инициации транскрипции. Как правило, они расположены в области на 30-110 п. о. выше сайта начала, хотя было показано, что ряд промоторов также содержит функциональные элементы ниже сайта начала. Промежуток между промоторными элементами часто является гибким, так что промоторная функция сохраняется при инверсии элементов или их перемещении друг относительно друга. В промоторе гена тимидинкиназы (tk) промежуток между промоторными элементами можно увеличить до 50 п. о., прежде чем активность начнет снижаться. В зависимости от промотора оказывается, что отдельные элементы могут функционировать для активации транскрипции либо совместно, либо независимо. Иллюстративные промоторы включают промоторы генов IE CMV, EF-1α, убиквитина С или фосфоглицераткиназы (PGK).
В некоторых вариантах осуществления промотор представляет собой тканеспецифический промотор. В некоторых вариантах осуществления промотор активируется на конкретной стадии развития. В некоторых вариантах осуществления промотор представляет собой индуцируемый промотор. В некоторых вариантах осуществления промотор представляет собой промотор, индуцируемый тетрациклином. В некоторых вариантах осуществления промотор представляет собой промотор гена металлотионеинов. В некоторых вариантах осуществления промотор представляет собой TK-промотор HSV.
Примером промотора, который способен обеспечивать экспрессию слитого полипептида, например, описанного в данном документе, содержащего домен, который содержит молекулу нуклеиновой кислоты, кодирующую CAR, в T-клетке млекопитающего представляет собой промотор EF1a. Нативный промотор EF1a управляет экспрессией альфа-субъединицы комплекса фактора элонгации-1, который отвечает за ферментативную доставку аминоацил-тРНК к рибосоме Промотор EF1a широко применялся в экспрессионных плазмидах для клеток млекопитающих и, было показано, что он является эффективным в управлении экспрессией слитого полипептида, например, описанного в данном документе, слитого полипептида, содержащего домен, который содержит CAR, с молекулы нуклеиновой кислоты, клонированной в лентивирусный вектор. См., например, Milone et al., Mol. Ther. 17(8): 1453-1464 (2009). В одном аспекте промотор EF1a содержит последовательность, представленную под SEQ ID NO: 1.
Другим примером промотора является последовательность немедленно-раннего промотора цитомегаловируса (CMV). Эта промоторная последовательность является последовательностью сильного конститутивного промотора, способного управлять экспрессией любой полинуклеотидной последовательности, функционально связанной с ней, на высоких уровнях. Однако можно также использовать последовательности других конститутивных промоторов, в том числе без ограничения раннего промотора вируса обезьян 40 (SV40), промотора вируса опухоли молочной железы мышей (MMTV), промотора длинного концевого повтора (LTR) вируса иммунодефицита человека (HIV), промотора MoMuLV, промотора вируса лейкоза птиц, немедленно-раннего промотора вируса Эпштейна-Барр, промотора вируса саркомы Рауса, а также промоторов генов человека, таких как без ограничения промотор гена актина, промотор гена миозина, промотор гена фактора элонгации-1, промотор гена гемоглобина и промотор гена креатинкиназы. Кроме того, настоящее изобретение не должно ограничиваться использованием конститутивных промоторов. Индуцируемые промоторы также рассматриваются как часть настоящего изобретения. Использование индуцируемого промотора обеспечивает молекулярный переключатель, способный включать экспрессию полинуклеотидной последовательности, с которой он функционально связан, если такая экспрессия требуется, или отключать экспрессию, если экспрессия не требуется. Примеры индуцируемых промоторов включают без ограничения промотор гена металлотионеинов, глюкокортикоид-индуцируемый промотор, прогестерон-индуцируемый промотор и тетрациклин-индуцируемый промотор.
Другим примером промотора является промотор гена фосфоглицераткиназы (PGK). В вариантах осуществления может быть необходим усеченный промотор гена PGK (например, промотор гена PGK с одной или несколькими, например, 1, 2, 5, 10, 100, 200, 300 или 400, делециями нуклеотидов по сравнению с последовательностью промотора гена PGK дикого типа). Нуклеотидные последовательности иллюстративных промоторов гена PGK представлены ниже.
Промотор гена PGK WT
ACCCCTCTCTCCAGCCACTAAGCCAGTTGCTCCCTCGGCTGACGGCTGCACGCGAGGCCTCCGAACGTCTTACGCCTTGTGGCGCGCCCGTCCTTGTCCCGGGTGTGATGGCGGGGTGTGGGGCGGAGGGCGTGGCGGGGAAGGGCCGGCGACGAGAGCCGCGCGGGACGACTCGTCGGCGATAACCGGTGTCGGGTAGCGCCAGCCGCGCGACGGTAACGAGGGACCGCGACAGGCAGACGCTCCCATGATCACTCTGCACGCCGAAGGCAAATAGTGCAGGCCGTGCGGCGCTTGGCGTTCCTTGGAAGGGCTGAATCCCCGCCTCGTCCTTCGCAGCGGCCCCCCGGGTGTTCCCATCGCCGCTTCTAGGCCCACTGCGACGCTTGCCTGCACTTCTTACACGCTCTGGGTCCCAGCCGCGGCGACGCAAAGGGCCTTGGTGCGGGTCTCGTCGGCGCAGGGACGCGTTTGGGTCCCGACGGAACCTTTTCCGCGTTGGGGTTGGGGCACCATAAGCT (SEQ ID NO: 823)
Иллюстративные усеченные промоторы гена PGK:
PGK100:
ACCCCTCTCTCCAGCCACTAAGCCAGTTGCTCCCTCGGCTGACGGCTGCACGCGAGGCCTCCGAACGTCTTACGCCTTGTGGCGCGCCCGTCCTTGTCCCGGGTGTGATGGCGGGGTG (SEQ ID NO: 824)
PGK200:
ACCCCTCTCTCCAGCCACTAAGCCAGTTGCTCCCTCGGCTGACGGCTGCACGCGAGGCCTCCGAACGTCTTACGCCTTGTGGCGCGCCCGTCCTTGTCCCGGGTGTGATGGCGGGGTGTGGGGCGGAGGGCGTGGCGGGGAAGGGCCGGCGACGAGAGCCGCGCGGGACGACTCGTCGGCGATAACCGGTGTCGGGTAGCGCCAGCCGCGCGACGGTAACG (SEQ ID NO: 825)
PGK300:
ACCCCTCTCTCCAGCCACTAAGCCAGTTGCTCCCTCGGCTGACGGCTGCACGCGAGGCCTCCGAACGTCTTACGCCTTGTGGCGCGCCCGTCCTTGTCCCGGGTGTGATGGCGGGGTGTGGGGCGGAGGGCGTGGCGGGGAAGGGCCGGCGACGAGAGCCGCGCGGGACGACTCGTCGGCGATAACCGGTGTCGGGTAGCGCCAGCCGCGCGACGGTAACGAGGGACCGCGACAGGCAGACGCTCCCATGATCACTCTGCACGCCGAAGGCAAATAGTGCAGGCCGTGCGGCGCTTGGCGTTCCTTGGAAGGGCTGAATCCCCG (SEQ ID NO: 826)
PGK400:
ACCCCTCTCTCCAGCCACTAAGCCAGTTGCTCCCTCGGCTGACGGCTGCACGCGAGGCCTCCGAACGTCTTACGCCTTGTGGCGCGCCCGTCCTTGTCCCGGGTGTGATGGCGGGGTGTGGGGCGGAGGGCGTGGCGGGGAAGGGCCGGCGACGAGAGCCGCGCGGGACGACTCGTCGGCGATAACCGGTGTCGGGTAGCGCCAGCCGCGCGACGGTAACGAGGGACCGCGACAGGCAGACGCTCCCATGATCACTCTGCACGCCGAAGGCAAATAGTGCAGGCCGTGCGGCGCTTGGCGTTCCTTGGAAGGGCTGAATCCCCGCCTCGTCCTTCGCAGCGGCCCCCCGGGTGTTCCCATCGCCGCTTCTAGGCCCACTGCGACGCTTGCCTGCACTTCTTACACGCTCTGGGTCCCAGCCG (SEQ ID NO: 827)
Вектор также может содержать, например, сигнальную последовательность для содействия секреции, сигнал полиаденилирования и терминатор транскрипции (например, из гена бычьего гормона роста (BGH)), элемент, обеспечивающий эписомальную репликацию и репликацию у прокариот (например, точку начала репликации SV40 и ColE1 или другие, известные из уровня техники), и/или элементы для обеспечения отбора (например, ген устойчивости к ампициллину и/или маркер устойчивости к зеоцину).
Для оценки экспрессии слитого полипептида, например, описанного в данном документе, содержащего домен, который содержит полипептид CAR или его части, экспрессионный вектор, который будет вводиться в клетку, также может содержать ген селектируемого маркера или репортерный ген или их оба для содействия идентификации и отбору экспрессирующих клеток из популяции клеток, в которых стремились провести трансфекцию или инфицирование посредством вирусных векторов. В других аспектах селектируемый маркер может переноситься на отдельном фрагменте ДНК и использоваться в процедуре котрансфекции. Как селектируемые маркеры, так и репортерные гены могут быть фланкированы соответствующими регуляторными последовательностями для обеспечения экспрессии в клетках-хозяевах. Применимые селектируемые маркеры включают, например, гены устойчивости к антибиотикам, такие как neo и т. п.
Репортерные гены используют для идентификации потенциально трансфицированных клеток и для оценки функциональных свойств регуляторных последовательностей. Как правило, репортерный ген представляет собой ген, который не присутствует или не экспрессируется в организме- или ткани-реципиенте и который кодирует полипептид, экспрессия которого проявляется в виде некоторого легко выявляемого свойства, например, ферментативной активности. Экспрессию репортерного гена анализируют в подходящее время после введения ДНК в клетки-реципиенты. Подходящие репортерные гены могут включать гены, кодирующие люциферазу, бета-галактозидазу, хлорамфениколацетилтрансферазу, секретируемую щелочную фосфатазу, или ген зеленого флуоресцентного белка (например, Ui-Tei et al., 2000 FEBS Letters 479: 79-82). Подходящие системы экспрессии хорошо известны и могут быть получены с помощью известных методик или приобретены коммерческим путем. Как правило, конструкцию с минимальной 5'-фланкирующей областью, демонстрирующую наивысший уровень экспрессии репортерного гена, идентифицируют как промотор. Такие промоторные области могут быть связаны с репортерным геном и использоваться для оценки средств в отношении способности к модулированию транскрипции, управляемой промотором.
В некоторых вариантах осуществления вектор, содержащий последовательность нуклеиновой кислоты, кодирующую слитый полипептид, описанный в данном документе, например, слитый полипептид, содержащий молекулу CAR, описанную в данном документе, может дополнительно содержать вторую последовательность нуклеиновой кислоты, кодирующую полипептид, например, средство, которое увеличивает активность слитого полипептида, например, описанного в данном документе, содержащего домен, который содержит молекулу CAR. В некоторых вариантах осуществления одна молекула нуклеиновой кислоты или вектор, содержащий указанную молекулу нуклеиновой кислоты, кодирует несколько слитых полипептидов, например, описанных в данном документе, при этом каждый из них содержит домены, которые содержат CAR, описанный в данном документе. В некоторых вариантах осуществления нуклеиновая кислота, кодирующая первый слитый полипептид, находится под регуляторным контролем (например, под контролем промотора, описанного в данном документе), отдельным от нуклеиновой кислоты, кодирующей второй слитый полипептид (например, под контролем промотора, описанного в данном документе). В других вариантах осуществления две или более последовательностей нуклеиновой кислоты кодируются одной молекулой нуклеиновой кислоты в одной и той же рамке считывания и в виде одной полипептидной цепи. В этом аспекте два или более слитых полипептидов, например, описанных в данном документе, каждый из которых содержит домен, который содержит CAR, например, может быть отделен одним или несколькими сайтами расщепления пептидов (например, сайт ауторасщепления или субстрат для внутриклеточной протеазы). Примеры сайтов расщепления пептидов включают следующие, в которых остатки GSG являются необязательными:
T2A: (GSG) E G R G S L L T C G D V E E N P G P (SEQ ID NO: 828)
P2A: (GSG) A T N F S L L K Q A G D V E E N P G P (SEQ ID NO: 829)
E2A: (GSG) Q C T N Y A L L K L A G D V E S N P G P (SEQ ID NO: 830)
F2A: (GSG) V K Q T L N F D L L K L A G D V E S N P G P (SEQ ID NO: 831)
В некоторых вариантах осуществления настоящего изобретения представлена, например, молекула нуклеиновой кислоты, содержащая первую последовательность нуклеиновой кислоты, кодирующую первую молекулу и вторую последовательность нуклеиновой кислоты, кодирующую вторую молекулу. В некоторых вариантах осуществления первая молекула представляет собой первый слитый полипептид, содержащий первый COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид и первый гетерологичный полипептид (например, первую молекулу CAR), и/или вторая молекула представляет собой второй слитый полипептид, содержащий второй COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид и второй гетерологичный полипептид (например, вторую молекулу CAR). В некоторых вариантах осуществления первая и вторая последовательности нуклеиновой кислоты расположены на одной молекуле нуклеиновой кислоты. В некоторых вариантах осуществления первая и вторая последовательности нуклеиновой кислоты расположены на отдельных молекулах нуклеиновой кислоты. В некоторых вариантах осуществления первая молекула CAR связывается с CD19 (например, первая молекула CAR представляет собой CAR для CD19, раскрытый в таблицах 5, 6, 7 и 30), а вторая молекула CAR связывается с CD22 (например, вторая молекула CAR представляет собой CAR для CD22, раскрытый в таблицах 19 и 20). В некоторых вариантах осуществления первая молекула CAR связывается с CD19 (например, первая молекула CAR представляет собой CAR для CD19, раскрытый в таблицах 5, 6, 7 и 30), а вторая молекула CAR связывается с CD20 (например, вторая молекула CAR представляет собой CAR для CD20, раскрытый в таблице 32). В вариантах осуществления молекула нуклеиновой кислоты содержит РНК или ДНК. В вариантах осуществления первая и вторая последовательности нуклеиновой кислоты находятся в одинаковой ориентации, например, транскрипция первой и второй последовательностей нуклеиновой кислоты происходит в одном и том же направлении. В вариантах осуществления первая и вторая последовательности нуклеиновой кислоты находятся в различных ориентациях. В вариантах осуществления один промотор контролирует экспрессию первой и второй последовательностей нуклеиновой кислоты. В вариантах осуществления нуклеиновая кислота, кодирующая сайт расщепления протеазами (такой как сайт расщепления T2A, P2A, E2A, или F2A) находится между первой и второй последовательностями нуклеиновой кислоты. В вариантах осуществления сайт расщепления протеазами размещен так, чтобы клетка могла экспрессировать слитый белок, содержащий первую молекулу и вторую молекулу, при этом белок впоследствии процессируется на два пептида за счет протеолитического расщепления. В некоторых вариантах осуществления первая последовательность нуклеиновой кислоты расположена выше второй последовательности нуклеиновой кислоты, или вторая последовательность нуклеиновой кислоты расположена выше первой последовательности нуклеиновой кислоты. В вариантах осуществления первый промотор контролирует экспрессию первой последовательности нуклеиновой кислоты, а второй промотор контролирует экспрессию второй последовательности нуклеиновой кислоты. В вариантах осуществления молекула нуклеиновой кислоты представляет собой плазмиду. В вариантах осуществления молекула нуклеиновой кислоты содержит элемент вирусной упаковки. В некоторых аспектах настоящего изобретения представлена клетка, например, иммунная эффекторная клетка, содержащая молекулу нуклеиновой кислоты, описанную в данном документе, например, молекулу нуклеиновой кислоты, содержащую первую и вторую последовательности нуклеиновой кислоты, описанные выше. Клетка может содержать протеазу (например, эндогенную или экзогенную), которая расщепляет сайт расщепления T2A, P2A, E2A, или F2A.
Способы введения генов в клетку и обеспечения их экспрессии в ней известны из уровня техники. Что касается экспрессионного вектора, то вектор можно легко ввести в клетку-хозяина, например, клетку млекопитающего, бактерии, дрожжей или насекомого, любым способом, известным из уровня техники. Например, экспрессионный вектор можно перенести в клетку-хозяина физическим, химическим или биологическим способом.
Физические способы введения полинуклеотида в клетку-хозяина включают осаждение фосфатом кальция, липофекцию, бомбардировку частицами, микроинъекцию, электропорацию и т. п. Способы получения клеток, содержащих векторы и/или экзогенные нуклеиновые кислоты, хорошо известны из уровня техники. См., например, Sambrook et al., 2012, MOLECULAR CLONING: A LABORATORY MANUAL, volumes 1-4, Cold Spring Harbor Press, NY). Предпочтительным способом введения полинуклеотида в клетку-хозяина является трансфекция с использованием фосфата кальция или электропорация.
Биологические способы введения представляющего интерес полинуклеотида в клетку-хозяина включают использование векторов на основе ДНК и РНК. Вирусные векторы, и особенно ретровирусные векторы, стали наиболее широко применяемым способом вставки генов в клетки млекопитающего, например, человека. Другие вирусные векторы могут быть получены из лентивируса, поксвирусов, вируса простого герпеса I типа, аденовирусов и аденоассоциированных вирусов и т. п. См., например, патенты США №№ 5350674 и 5585362.
Химические средства для введения полинуклеотида в клетку-хозяина включают коллоидные дисперсные системы, такие как макромолекулярные комплексы, нанокапсулы, микросферы, микрогранулы и липидные системы, в том числе эмульсии типа "масло в воде", мицеллы, смешанные мицеллы и липосомы. Иллюстративной коллоидной системой для применения в качестве средства для доставки in vitro и in vivo является липосома (например, искусственная мембранная везикула). Из уровня техники доступны другие способы целенаправленной доставки нуклеиновых кислот, такие как доставка полинуклеотидов с помощью нацеливающихся наночастиц или другой подходящей системы доставки субмикронного размера.
В случае использования системы доставки, отличной от вирусной, иллюстративным средством для доставки является липосома. Для введения нуклеиновых кислот в клетку-хозяина (in vitro, ex vivo или in vivo) предполагается применение липидных составов. В другом аспекте нуклеиновая кислота может быть ассоциирована с липидом. Нуклеиновая кислота, ассоциированная с липидом, может быть инкапсулирована в водной внутренней части липосомы, помещена в пределах липидного бислоя липосомы, присоединена к липосоме посредством связывающей молекулы, которая ассоциирована как с липосомой, так и с олигонуклеотидом, захвачена в липосому, образует комплекс с липосомой, диспергирована в растворе, содержащем липид, смешана с липидом, объединена с липидом, содержится в виде суспензии в липиде, содержится в мицелле или образует комплекс с ней или иным образом ассоциирована с липидом. Композиции для ассоциации на основе липидов, липидов/ДНК или липидов/экспрессионного вектора не ограничиваются какой-либо конкретной структурой в растворе. Например, они могут присутствовать в двухслойной структуре, в виде мицелл или в "сжатой" структуре. Они также могут быть просто помещены в раствор, при этом по возможности образуют агрегаты, которые не являются однородными по размеру или форме. Липиды представляют собой жирные вещества, которые могут встречаться в природе или являться синтетическими липидами. Например, липиды включают жировые капли, которые в норме встречаются в цитоплазме, а также класс соединений, который содержит длинноцепочечные алифатические углеводороды и их производные, такие как жирные кислоты, спирты, амины, аминоспирты и альдегиды.
Подходящие для применения липиды можно получить из коммерческих источников. Например, димиристилфосфатидилхолин ("DMPC") можно получить от Sigma, Сент-Луис, Миссури; дицетилфосфат ("DCP") можно получить от K & K Laboratories (Плейнвью, Нью-Йорк); холестерин ("Choi") можно получить от Calbiochem-Behring; димиристилфосфатидилглицерин ("DMPG") и другие липиды можно получить от Avanti Polar Lipids, Inc. (Бирмингем, Алабама). Исходные растворы липидов в хлороформе или хлороформе/метаноле можно хранить при температуре приблизительно -20°C. Хлороформ используется в качестве единственного растворителя, поскольку он испаряется легче, чем метанол. "Липосома" является общим термином, охватывающим различные одно- и мультиламеллярные липидные носители, образованные путем формирования замкнутых липидных бислоев или агрегатов. Липосомы можно охарактеризовать как имеющие везикулярные структуры с фосфолипидной бислойной мембраной и внутренней водной средой. Мультиламеллярные липосомы имеют несколько липидных слоев, разделенных водной средой. Они образуются самопроизвольно при суспендировании фосфолипидов в избытке водного раствора. Липидные компоненты подвергаются самоперераспределению перед образованием замкнутых структур и захватывают воду и растворенные в ней вещества между липидными бислоями (Ghosh et al., 1991, Glycobiology 5: 505-10). Однако также охватываются композиции, которые в растворе имеют структуры, отличные от нормальной везикулярной структуры. Например, липиды могут принимать вид мицеллярной структуры или просто существовать в виде неоднородных агрегатов липидных молекул. Также подразумеваются комплексы липофектамин-нуклеиновая кислота.
Независимо от способа, применяемого для введения экзогенных нуклеиновых кислот в клетку-хозяина, или иного воздействия ингибитора по настоящему изобретению на клетку, можно выполнять различные анализы для подтверждения присутствия последовательности рекомбинантной ДНК в клетке-хозяине. Такие анализы включают, например, "молекулярно-биологические" анализы, хорошо известные специалистам в данной области техники, такие как Саузерн- и нозерн-блоттинг, ОТ-ПЦР и ПЦР; "биохимические" анализы, такие как выявление присутствия или отсутствия конкретного пептида, например, с помощью иммунологических способов (ELISA и вестерн-блоттинга) или с помощью описанных в данном документе анализов для идентификации средств, находящихся в пределах объема настоящего изобретения.
В настоящем изобретении дополнительно представлена молекула нуклеиновой кислоты, кодирующая вектор, содержащий слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR. В одном варианте осуществления вектор содержит молекулу нуклеиновой кислоты, кодирующую CAR, например, описанную в данном документе. В одном варианте осуществления вектор содержит две молекулы нуклеиновой кислоты, кодирующие CAR. В одном аспекте один или несколько векторов, кодирующих CAR (например, вектор, содержащий первую молекулу нуклеиновой кислоты, кодирующую CAR, и вектор содержащий вторую молекулу нуклеиновой кислоты, кодирующую CAR, или вектор, содержащий как первую, так и вторую нуклеиновые кислоты, кодирующие CAR) может быть непосредственно трансдуцирован в клетку, например, T-клетку или NK-клетку. В одном аспекте вектор представляет собой клонирующий или экспрессионный вектор, например, вектор, включающий без ограничения одну или несколько плазмид (например, экспрессионные плазмиды, клонирующие векторы, миникольца, минивекторы, двойные микрохромосомы), ретровирусные и лентивирусные векторные конструкции. В одном аспекте вектор способен экспрессировать конструкцию CAR в иммунных эффекторных клетках млекопитающего (например, T-клетках, NK-клетках).
В одном варианте осуществления, если необходима стабильная экспрессия одного или нескольких (например, одного или двух) слитых полипептидов, например, описанных в данном документе, каждый из которых содержит домен, который содержит CAR, то в иммунную эффекторную клетку трансдуцируют вектор, содержащий одну или несколько (например, одну или две) молекул нуклеиновой кислоты, кодирующих CAR. Например, иммунные эффекторные клетки со стабильной экспрессией двух слитых полипептидов, например, описанных в данном документе, каждый из которых содержит домен, который содержит CAR, могут быть получены с применением лентивирусных векторов. Клетки, которые проявляют стабильную экспрессию двух слитых полипептидов, например, описанных в данном документе, каждый из которых содержит домен, который содержит CAR, экспрессируют CAR в течение по меньшей мере 1 недели, 2 недель, 3 недель, 4 недель, 5 недель, 6 недель, 7 недель, 8 недель, 3 месяцев, 6 месяцев, 9 месяцев или 12 месяцев после трансдукции.
В одном варианте осуществления, если необходима транзиентная экспрессия одного или нескольких (например, одного или двух) слитых полипептидов, например, описанных в данном документе, содержащих домен, который содержит CAR, то в иммунную эффекторную клетку трансфицируют одну или несколько (например, одну или две) молекул нуклеиновой кислоты, кодирующих слитый полипептид. Одна или несколько (например, одна или две) молекул нуклеиновой кислоты, кодирующих слитые полипептиды, например, описанные в данном документе, содержащие домен, который содержит CAR, могут представлять собой вектор, содержащий одну или несколько (например, одну или две) молекул нуклеиновой кислоты, кодирующих CAR, или транскрибированную in vitro РНК, кодирующую один или несколько (например, один или два) CAR. Транскрибированные in vitro РНК, кодирующие CAR, и способы их трансфекции в иммунные эффекторные клетки дополнительно описаны ниже. Клетки, которые проявляют транзиентную экспрессию одного или нескольких (например, одного или двух) CAR, экспрессируют один или несколько (например, один или два) CAR в течение 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 дней после трансфекции.
Трансфекция РНК
В данном документе раскрыты способы получения транскрибированной in vitro РНК, кодирующей слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR. Настоящее изобретение также включает конструкцию РНК, кодирующую слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR, которая может быть непосредственно трансфицирована в клетку. Способ получения мРНК для применения в трансфекции может предусматривать обеспечение in vitro транскрипции (IVT) матрицы с помощью специально разработанных праймеров с последующим добавлением поли(А), чтобы получить конструкцию, содержащую 3'- и 5'-нетранслируемую последовательность ("UTR"), 5'-кэп и/или участок внутренней посадки рибосомы (IRES), нуклеиновую кислоту, которая подлежит экспрессии, и поли(A)-хвост, как правило, длиной 50-5000 оснований (SEQ ID NO: 174). С помощью РНК, полученной таким образом, можно эффективно трансфицировать различные типы клеток. В одном аспекте матрица содержит последовательности для CAR.
В одном аспекте слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR по настоящему изобретению, кодируется матричной РНК (мРНК). В одном аспекте мРНК, кодирующую CAR, описанный в данном документе, вводят в T-клетку или NK-клетку.
В одном варианте осуществления транскрибированная in vitro РНК, кодирующая слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR, может быть введена в клетку в форме, обеспечивающей транзиентную трансфекцию. РНК получают путем транскрипции in vitro с применением матрицы, полученной посредством полимеразной цепной реакции (ПЦР). Представляющая интерес ДНК из любого источника может быть непосредственно преобразована с помощью ПЦР в матрицу для синтеза мРНК in vitro с применением соответствующих праймеров и РНК-полимеразы. Источником ДНК может быть, например, геномная ДНК, плазмидная ДНК, фаговая ДНК, кДНК, синтетическая последовательность ДНК или любой другой подходящий источник ДНК. Необходимая матрица для транскрипции in vitro представляет собой слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR, описанный в данном документе. Например, матрица для РНК, кодирующей CAR, содержит внеклеточную область, содержащую одноцепочечный вариабельный домен антитела к антигену, описанному в данном документе; шарнирную область (например, шарнирную область, описанную в данном документе), трансмембранный домен (например, трансмембранный домен, описанный в данном документе, такой как трансмембранный домен CD8a) и цитоплазматическую область, которая содержит внутриклеточный сигнальный домен, например, внутриклеточный сигнальный домен, описанный в данном документе, например, содержащий сигнальный домен CD3-дзета и сигнальный домен 4-1BB.
В одном варианте осуществления ДНК, подлежащая применению в ПЦР, содержит открытую рамку считывания. ДНК может быть получена из встречающейся в природе последовательности ДНК из генома организма. В одном варианте осуществления нуклеиновая кислота может содержать некоторые или все из 5'- и/или 3'-нетранслируемых областей (UTR). Нуклеиновая кислота может содержать экзоны и интроны. В одном варианте осуществления ДНК, подлежащая применению в ПЦР, представляет собой последовательность нуклеиновой кислоты человека. В другом варианте осуществления ДНК, подлежащая применению в ПЦР, представляет собой последовательность нуклеиновой кислоты человека, содержащую 5'- и 3'-UTR. В качестве альтернативы, ДНК может представлять собой искусственную последовательность ДНК, которая обычно не экспрессируется у встречающегося в природе организма. Иллюстративная искусственная последовательность ДНК представляет собой последовательность, которая содержит части генов, лигированные друг с другом с образованием открытой рамки считывания, которая кодирует слитый полипептид. Части ДНК, лигированные друг с другом, могут быть получены из одного организма или из более чем одного организма.
ПЦР применяют для получения матрицы, предназначенной для транскрипции in vitro мРНК, которая применяется для трансфекции. Способы проведения ПЦР хорошо известны из уровня техники. Праймеры для применения в ПЦР разрабатывают таким образом, чтобы они имели области, практически комплементарные областям ДНК, подлежащей применению в качестве матрицы для ПЦР. Используемый в данном документе термин "практически комплементарные" относится к последовательностям нуклеотидов, где большинство или все основания в последовательности праймера являются комплементарными, или одно или несколько оснований являются некомплементарными или несовпадающими. Практически комплементарные последовательности способны отжигаться или гибридизироваться с предполагаемой ДНК-мишенью в условиях отжига, используемых для ПЦР. Праймеры можно разрабатывать таким образом, чтобы они были практически комплементарными любой части ДНК-матрицы. Например, праймеры можно разрабатывать таким образом, чтобы обеспечить амплификацию части нуклеиновой кислоты, которая обычно транскрибируется в клетках (открытой рамки считывания), включающей 5'- и 3'-UTR. Праймеры также можно разрабатывать таким образом, чтобы обеспечить амплификацию части нуклеиновой кислоты, которая кодирует конкретный представляющий интерес домен. В одном варианте осуществления праймеры разработаны таким образом, чтобы обеспечить амплификацию кодирующей области кДНК человека, включающей 5'- и 3'-UTR полностью или их части. Праймеры, применимые для ПЦР, могут быть получены за счет способов синтеза, которые хорошо известны из уровня техники. "Прямые праймеры" представляют собой праймеры, которые содержат область из нуклеотидов, практически комплементарных нуклеотидам в ДНК-матрице, которые расположены выше последовательности ДНК, подлежащей амплификации. "Вышерасположенное" используется в данном документе для обозначения местоположения в направлении 5'-конца последовательности ДНК, подлежащей амплификации, относительно кодирующей цепи. "Обратные праймеры" представляют собой праймеры, которые содержат области из нуклеотидов, практически комплементарных нуклеотидам в двухнитевой ДНК-матрице, которые расположены ниже последовательности ДНК, подлежащей амплификации. "Нижерасположенные" используется в данном документе для обозначения местоположения в направлении 3'-конца последовательности ДНК, подлежащей амплификации, относительно кодирующей нити.
В способах, раскрытых в данном документе, может использоваться любая ДНК-полимераза, применимая для ПЦР. Реагенты и полимераза являются коммерчески доступными из ряда источников.
Также можно использовать химические структуры, которые могут способствовать стабильности и/или эффективности трансляции. РНК предпочтительно содержит 5'- и 3'-UTR. В одном варианте осуществления длина 5'-UTR составляет от одного до 3000 нуклеотидов. Длину последовательностей 5'- и 3'-UTR, которые подлежат добавлению к кодирующей области, можно изменять с помощью различных способов, включая без ограничения разработку праймеров для ПЦР, которые отжигаются с различными областями UTR. Используя данный подход, специалист обычной квалификации в данной области техники может модифицировать длину 5'- и 3'-UTR, необходимую для достижения оптимальной эффективности трансляции после трансфекции транскрибированной РНК.
5'- и 3'-UTR могут представлять собой встречающиеся в природе эндогенные 5'- и 3'-UTR для представляющей интерес нуклеиновой кислоты. В качестве альтернативы, последовательности UTR, которые не являются эндогенными для представляющей интерес нуклеиновой кислоты, могут быть добавлены путем введения последовательностей UTR в прямой и обратный праймеры или с помощью любых других модификаций матрицы. Использование последовательностей UTR, которые не являются эндогенными для представляющей интерес нуклеиновой кислоты, может применяться для модификации стабильности и/или эффективности трансляции РНК. Например, известно, что AU-богатые элементы в последовательностях 3'-UTR могут уменьшать стабильность мРНК. Следовательно, 3'-UTR могут быть выбраны или разработаны таким образом, чтобы они увеличивали стабильность транскрибированной РНК, исходя из свойств UTR, которые хорошо известны из уровня техники.
В одном варианте осуществления 5'-UTR может содержать последовательность Козак из эндогенной нуклеиновой кислоты. В качестве альтернативы, если 5'-UTR, которая не является эндогенной для представляющей интерес нуклеиновой кислоты, добавляют с помощью ПЦР, как описано выше, консенсусная последовательность Козак может быть видоизменена путем добавления последовательности 5'-UTR. Последовательности Козак могут увеличивать эффективность трансляции некоторых РНК-транскриптов, но, по-видимому, они не являются необходимыми для обеспечения эффективной трансляции всех РНК. Требование наличия последовательностей Козак для многих мРНК известно из уровня техники. В других вариантах осуществления 5'-UTR может представлять собой 5'-UTR из РНК-содержащего вируса, РНК-геном которого является стабильным в клетках. В других вариантах осуществления можно использовать различные аналоги нуклеотидов в 3'- или 5'-UTR, чтобы воспрепятствовать разрушению мРНК под действием экзонуклеаз.
Для обеспечения синтеза РНК с ДНК-матрицы без необходимости клонирования гена, промотор транскрипции должен быть присоединен к ДНК-матрице выше последовательности, подлежащей транскрипции. Если последовательность, которая функционирует в качестве промотора для РНК-полимеразы, добавляют к 5'-концу прямого праймера, то промотор для РНК-полимеразы включается в состав продукта ПЦР выше открытой рамки считывания, которая подлежит транскрипции. В одном предпочтительном варианте осуществления промотор представляет собой промотор для полимеразы Т7, описанный в другом разделе данного документа. Другие применимые промоторы включают без ограничения промоторы для РНК-полимераз Т3 и SP6. Консенсусные нуклеотидные последовательности для промоторов T7, T3 и SP6 известны из уровня техники.
В предпочтительном варианте осуществления мРНК имеет как кэп на 5'-конце, так и 3'-поли(А) хвост, которые определяют связывание с рибосомой, инициацию трансляции и стабильность мРНК в клетке. На кольцевой ДНК-матрице, например, плазмидной ДНК, РНК-полимераза продуцирует длинный конкатемерный продукт, который не подходит для экспрессии в эукариотических клетках. Транскрипция плазмидной ДНК, линеаризованной на конце 3'-UTR, приводит к образованию мРНК нормального размера, которая не является эффективной для трансфекции эукариот, даже в случае ее полиаденилирования после транскрипции.
На линейной ДНК-матрице РНК-полимераза фага Т7 может удлинять 3'-конец транскрипта за пределами последнего основания матрицы (Schenborn and Mierendorf, Nuc Acids Res., 13:6223-36 (1985); Nacheva and Berzal-Herranz, Eur. J. Biochem., 270:1485-65 (2003).
Традиционный способ интеграции отрезков поли(А)/(Т) в ДНК-матрицу представляет собой молекулярное клонирование. Однако последовательность поли(А)/(Т), интегрированная в плазмидную ДНК, может вызывать нестабильность плазмиды, поэтому плазмидные ДНК-матрицы, полученные из бактериальных клеток, зачастую сильно засорены делециями и другими аберрациями. Это приводит к тому, что процедуры клонирования являются не только трудоемкими и времязатратными, но зачастую и ненадежными. Поэтому способ, который позволяет конструировать ДНК-матрицы с 3'-отрезком поли(А)/(Т) без клонирования, является крайне желательным.
Сегмент поли(A)/(T) в транскрипционной ДНК-матрице может быть получен в ходе ПЦР с использованием обратного праймера, содержащего поли(T)-хвост, такой как хвост из 100 T (SEQ ID NO: 832) (размер может составлять 50-5000 T (SEQ ID NO: 833)), или после ПЦР с помощью любого другого способа, в том числе без ограничения лигирования или рекомбинации ДНК in vitro. Поли(А)-хвосты также обеспечивают стабильность РНК и уменьшают их разрушение. Как правило, длина поли(А)-хвоста положительно коррелирует со стабильностью транскрибированной РНК. В одном варианте осуществления длина поли(А)-хвоста составляет от 100 до 5000 остатков аденозина (SEQ ID NO: 834).
Поли(А)-хвосты РНК могут быть дополнительно удлинены после транскрипции in vitro путем использования поли(А)-полимеразы, такой как поли(А)-полимераза Е. coli (E-PAP). В одном варианте осуществления увеличение длины поли(А)-хвоста от 100 нуклеотидов до 300-400 нуклеотидов (SEQ ID NO: 835) приводит к приблизительно двукратному увеличению эффективности трансляции РНК. Кроме того, присоединение различных химических групп к 3'-концу может увеличивать стабильность мРНК. Такое присоединение может включать присоединение модифицированных/искусственных нуклеотидов, аптамеров и других соединений. Например, в состав поли(А)-хвоста с помощью поли(А)-полимеразы могут быть аналоги АТФ. Аналоги АТФ могут дополнительно увеличивать стабильность РНК.
5'-кэпы также обеспечивают стабильность молекул РНК. В предпочтительном варианте осуществления РНК, полученные с помощью способов, раскрытых в данном документе, содержат 5'-кэп. 5'-кэп обеспечивают с применением методик, известных из уровня техники и описанных в данном документе (Cougot, et al., Trends in Biochem. Sci., 29:436-444 (2001); Stepinski, et al., RNA, 7:1468-95 (2001); Elango, et al., Biochim. Biophys. Res. Commun., 330:958-966 (2005)).
РНК, полученные с помощью способов, раскрытых в данном документе, также могут содержать последовательность участка внутренней посадки рибосомы (IRES). Последовательность IRES может быть любой вирусной, хромосомной или искусственно разработанной последовательностью, которая инициирует кэп-независимое связывание рибосомы с мРНК и содействует инициации трансляции. Могут быть включены любые растворенные вещества, подходящие для электропорации клеток, которые могут включать факторы, содействующие проникновению в клетку и жизнеспособности клеток, такие как сахара, пептиды, липиды, белки, антиоксиданты и поверхностно-активные вещества.
РНК можно вводить в клетки-мишени с помощью любого из целого ряда различных способов, например, коммерчески доступных способов, которые включают без ограничения электропорацию (Amaxa Nucleofector-II (Amaxa Biosystems, Кельн, Германия)), ECM 830 (BTX) (Harvard Instruments, Бостон, Массачусетс) или Gene Pulser II (BioRad, Денвер, Колорадо), Multiporator (Eppendorf, Гамбург, Германия)), трансфекцию, опосредованную катионными липосомами, с применением липофекции, инкапсуляцию в полимеры, трансфекцию, опосредованную пептидами, или биобаллистические системы доставки частиц, такие как "генные пушки" (см., например, Nishikawa, et al. Hum Gene Ther., 12(8):861-70 (2001).
Невирусные способы доставки
В некоторых аспектах для доставки нуклеиновой кислоты, кодирующей химерную молекулу или слитый полипептид, описанный в данном документе, в клетку, или ткань, или субъекту можно использовать невирусные способы.
В некоторых вариантах осуществления невирусный способ включает применение транспозона (также называемого мобильным генетическим элементом). В некоторых вариантах осуществления транспозон представляет собой фрагмент ДНК, который может самостоятельно вставляться в определенное местоположение в геноме, например, фрагмент ДНК, который способен к саморепликации и вставке своей копии в геном, или фрагмент ДНК, который с помощью сплайсинга может быть вырезан из более длинной нуклеиновой кислоты и вставлен в другое место в геноме. Например, транспозон содержит последовательность ДНК, состоящую из инвертированных повторов, фланкирующих гены для транспозиции.
В некоторых вариантах осуществления клетки, например, T- или NK-клетки, которые экспрессируют химерную молекулу или слитый полипептид, например, описанный в данном документе, получают с использованием комбинации вставки гена с помощью SBTS и генетического редактирования с помощью нуклеазы (например, нуклеаз с "цинковыми пальцами" (ZFN), эффекторных нуклеаз, подобных активаторам транскрипции (TALEN), системы CRISPR/Cas или сконструированной мегануклеазы на основе видоизмененных хоминг-эндонуклеаз).
В некоторых вариантах осуществления применение невирусного способа доставки делает возможным перепрограммирование клеток, например, Т- или NK-клеток, и прямую инфузию клеток в субъект. Преимущества невирусных векторов включают без ограничения простоту и относительно низкую стоимость получения достаточных количеств, необходимых для популяции пациентов, стабильность при хранении и отсутствие иммуногенности.
Клетки
Также в данном документе представлены клетки, например, иммунные эффекторные клетки (например, популяция клеток, например, популяция иммунных эффекторных клеток), содержащие молекулу нуклеиновой кислоты, молекулу слитого полипептида или вектор, например, описанный в данном документе. В некоторых вариантах осуществления предусмотренные клетки содержат слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR, молекулу нуклеиновой кислоты, кодирующую слитый полипептид, содержащий домен, который содержит CAR, или вектор, содержащий вышеуказанное.
В определенных аспектах иммунные эффекторные клетки, например, T-клетки или NK-клетки, можно получить из дозы крови, собранной у субъекта с применением всех возможных методик, известных специалисту в данной области техники, как, например, разделение с применением Ficoll™. В одном предпочтительном аспекте клетки из циркулирующей крови индивидуума получают путем афереза. Продукт афереза обычно содержит лимфоциты, в том числе Т-клетки, моноциты, гранулоциты, В-клетки, другие ядерные лейкоциты, эритроциты и тромбоциты. В одном аспекте клетки, собранные с помощью афереза, можно промыть, чтобы удалить фракцию плазмы крови и необязательно поместить клетки в соответствующий буфер или среду для последующих стадий обработки. В одном варианте осуществления клетки промывают фосфатно-солевым буферным раствором (PBS). В альтернативном варианте осуществления в растворе для промывания отсутствует кальций и может отсутствовать магний или могут отсутствовать многие, если не все, двухвалентные катионы.
Начальные стадии активации в отсутствие кальция могут приводить к усиленной активации. Как будет очевидно для специалистов обычной квалификации в данной области техники, стадию промывания можно осуществлять с помощью способов, известных специалистам в данной области техники, как, например, с помощью полуавтоматической "проточной" центрифуги (например, устройства для обработки клеток Cobe 2991, CytoMate от Baxter или Cell Saver 5 от Haemonetics) в соответствии с инструкциями производителя. После промывания клетки можно ресуспендировать в различных биосовместимых буферах, таких как, например, PBS, не содержащий Ca и не содержащий Mg, PlasmaLyte A или другой солевой раствор с буфером или без него. В качестве альтернативы, нежелательные компоненты из образца, полученного путем афереза, можно удалить, и клетки можно ресуспендировать непосредственно в культуральной среде.
Признано, что в способах применения можно использовать характеристики сред для культивирования, предусматривающие использование сыворотки крови AB человека при концентрации 5% или меньше, например, 2%, и использовать известные характеристики и составы сред для культивирования, например, описанные в Smith et al., "Ex vivo expansion of human T cells for adoptive immunotherapy using the novel Xeno-free CTS Immune Cell Serum Replacement", Clinical & Translational Immunology (2015) 4, e31; doi:10.1038/cti.2014.31.
В одном аспекте Т-клетки выделяют из лимфоцитов периферической крови путем лизиса эритроцитов и истощения популяции моноцитов, например, посредством центрифугирования в градиенте PERCOLLTM или посредством противоточного элютриационного центрифугирования.
Способы, описанные в данном документе, могут включать, например, отбор конкретной субпопуляции иммунных эффекторных клеток, например, Т-клеток, которая представляет собой популяцию, истощенную по регуляторным Т-клеткам с истощением по CD25+ клеткам, с помощью, например, методики отрицательного отбора, например, описанной в данном документе. Популяция, истощенная по регуляторным Т-клеткам, предпочтительно содержит менее 30%, 25%, 20%, 15%, 10%, 5%, 4%, 3%, 2%, 1% CD25+ клеток.
В одном варианте осуществления регуляторные T-клетки, например, CD25+ T-клетки, удаляют из популяции с помощью антитела к CD25 или его фрагмента или CD25-связывающего лиганда IL-2. В одном варианте осуществления антитело к CD25 или его фрагмент или CD25-связывающий лиганд конъюгированы с субстратом, например, микрогранулой, или, в ином случае, покрывают субстрат, например, микрогранулу. В одном варианте осуществления антитело к CD25 или его фрагмент конъюгированы с субстратом, описанным в данном документе.
В одном варианте осуществления регуляторные T-клетки, например, CD25+ T-клетки, удаляют из популяции с помощью реагента для истощения по CD25 от MiltenyiTM. В одном варианте осуществления соотношение клеток и реагента для истощения по CD25 составляет 1e7 клеток на 20 мкл, или 1e7 клеток на 15 мкл, или 1e7 клеток на 10 мкл, или 1e7 клеток на 5 мкл, или 1e7 клеток на 2,5 мкл, или 1e7 клеток на 1,25 мкл. В одном варианте осуществления, например, для истощения регуляторных Т-клеток, например, CD25+, используют более 500 миллионов клеток/мл. В дополнительном аспекте используют концентрацию клеток, составляющую 600, 700, 800 или 900 миллионов клеток/мл.
В одном варианте осуществления популяция иммунных эффекторных клеток, подлежащая истощению, содержит приблизительно 6×109 CD25+ T-клеток. В других аспектах популяция иммунных эффекторных клеток, подлежащая истощению, содержит от приблизительно 1×109 до 1×1010 CD25+ Т-клеток с включением любого целочисленного значения в данном промежутке. В одном варианте осуществления полученная популяция, истощенная по регуляторным T-клеткам, содержит 2×109 регуляторных T-клеток, например, CD25+ клеток, или меньше (например, 1×109, 5×108, 1×108, 5×107, 1×107 или меньше CD25+ клеток).
В одном варианте осуществления регуляторные Т-клетки, например, CD25+ клетки, удаляют из популяции с помощью системы CliniMACS с набором трубок для истощения, таким как, например, трубки 162-01. В одном варианте осуществления система CliniMACS работает с установленными параметрами истощения, например, такими как DEPLETION2.1.
Без ограничения какой-либо конкретной теорией, полагают, что уменьшение уровня отрицательных регуляторов иммунных клеток (например, уменьшение числа нежелательных иммунных клеток, например, TREG-клеток) у субъекта до проведения афереза или во время производства клеточного продукта, характеризующегося экспрессией слитого полипептида, например, описанного в данном документе, содержащего домен, который содержит CAR, может снижать риск рецидива у субъекта. Например, способы истощения TREG-клеток известны из уровня техники. Способы уменьшения количества TREG-клеток включают без ограничения применение циклофосфамида, антитела к GITR (антитела к GITR, описанного в данном документе), реагента для истощения по CD25 и их комбинаций.
В некоторых вариантах осуществления способы производства предусматривают снижение количества (например, истощение) TREG клеток до производства клетки, экспрессирующей слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR. Например, способы производства предусматривают приведение образца, например, образца, полученного путем афереза, в контакт с антителом к GITR и/или антителом к CD25 (или его фрагментом или CD25-связывающим лигандом), например, для истощения TREG-клеток до производства клеточного (например, T-клеточного, NK-клеточного) продукта, характеризующегося экспрессией CAR.
В одном варианте осуществления субъект подвергается предварительному лечению одним или несколькими видами терапии, которые снижают количество TREG-клеток, до сбора клеток, предназначенных для производства клеточного продукта, характеризующегося экспрессией слитого полипептида, например, описанного в данном документе, содержащего домен, который содержит CAR, за счет чего снижается риск рецидива у субъекта при лечении клетками, экспрессирующими слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR. В одном варианте осуществления способы уменьшения количества TREG-клеток включают без ограничения введение субъекту одного или нескольких из циклофосфамида, антитела к GITR, реагента для истощения по CD25 или их комбинации. Введение одного или нескольких из циклофосфамида, антитела к GITR, реагента для истощения по CD25 или их комбинации может происходить перед, во время или после инфузии клеточного продукта, характеризующегося экспрессией CAR.
В одном варианте осуществления субъект подвергается предварительному лечению циклофосфамидом до сбора клеток, предназначенных для производства клеточного продукта, характеризующегося экспрессией CAR, за счет чего снижается риск рецидива у субъекта при лечении клетками, экспрессирующими слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR. В варианте осуществления субъект подвергается предварительному лечению антителом к GITR до сбора клеток, предназначенных для производства клеточного продукта, характеризующегося экспрессией CAR, за счет чего снижается риска рецидива у субъекта при лечении клетками, экспрессирующими CAR.
В одном варианте осуществления популяция клеток, которые должны быть удалены, не представляет собой ни регуляторные Т-клетки, ни опухолевые клетки, а представляет собой клетки, которые иным способом отрицательно влияют на размножение и/или функцию CAR-T-клеток, например, клетки, экспрессирующие CD14, CD11b, CD33, CD15 или другие маркеры, экспрессируемые потенциально иммуносупрессорными клетками. В одном варианте осуществления предполагается, что такие клетки удаляют одновременно с регуляторными Т-клетками и/или опухолевыми клетками, или после указанного истощения, или в другом порядке.
Способы, описанные в данном документе, могут включать более одной стадии отбора, например, более одной стадии истощения. Обогащение популяции Т-клеток путем отрицательного отбора можно осуществлять, например, с помощью комбинации антител, нацеленных на поверхностные маркеры, уникальные для клеток, подвергаемых отрицательному отбору. Один из способов представляет собой сортировку и/или отбор клеток с помощью отрицательной магнитной иммуноадгезии или проточной цитометрии, в которых используется смесь моноклональных антител, нацеленных на маркеры клеточной поверхности, присутствующие на клетках, подвергаемых отрицательному отбору. Например, для обогащения CD4+ клетками путем отрицательного отбора смесь моноклональных антител может содержать антитела к CD14, CD20, CD11b, CD16, HLA-DR и CD8.
Способы, описанные в данном документе, могут дополнительно включать удаление из популяции клеток, которые экспрессируют опухолевый антиген, например, опухолевый антиген, который не включает CD25, например, CD19, CD30, CD38, CD123, CD20, CD14 или CD11b, за счет чего получают популяцию клеток, истощенную по регуляторным T-клеткам, например, истощенную по CD25+ клеткам, и истощенную по клеткам с опухолевым антигеном, которые подходят для экспрессии слитого полипептида, например, описанного в данном документе, содержащего домен, который содержит CAR, например, CAR, описанный в данном документе. В одном варианте осуществления клетки, экспрессирующие опухолевый антиген, удаляют одновременно с регуляторными Т-клетками, например, CD25+ клетками. Например, антитело к CD25 или его фрагмент и антитело к опухолевому антигену или его фрагмент могут быть присоединены к одному и тому же субстрату, например, микрогрануле, который можно использовать для удаления клеток, или антитело к CD25 или его фрагмент или антитело к опухолевому антигену или его фрагмент могут быть присоединены к отдельным микрогранулам, смесь которых можно использовать для удаления клеток. В других вариантах осуществления удаление регуляторных Т-клеток, например, CD25+ клеток, и удаление клеток, экспрессирующих опухолевый антиген, проводят последовательно, и, например, его можно производить в любом порядке.
Также представлены способы, которые включают удаление из популяции клеток, экспрессирующих ингибитор контрольных точек иммунного ответа, например, ингибитор контрольных точек иммунного ответа, описанный в данном документе, например, одного или нескольких из PD1+ клеток, LAG3+ клеток и TIM3+ клеток, за счет чего получают популяцию, истощенную по регуляторным Т-клеткам, например, истощенную по CD25+ клеткам и истощенную по клеткам с ингибитором контрольных точек иммунного ответа, например, истощенную по PD1+, LAG3+ и/или TIM3+ клеткам. Иллюстративные ингибиторы контрольных точек иммунного ответа включают B7-H1, B7-1, CD160, P1H, 2B4, PD1, TIM3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG3, TIGIT, CTLA-4, BTLA и LAIR1. В одном варианте осуществления клетки, экспрессирующие ингибитор контрольных точек иммунного ответа, удаляют одновременно с регуляторными Т-клетками, например, CD25+ клетками. Например, антитело к CD25 или его фрагмент и антитело к ингибитору контрольных точек иммунного ответа или его фрагмент могут быть присоединены к одной и той же микрогрануле, которую можно использовать для удаления клеток, или антитело к CD25 или его фрагмент и антитело к ингибитору контрольных точек иммунного ответа или его фрагмент могут быть присоединены к отдельным микрогранулам, смесь которых можно использовать для удаления клеток. В других вариантах осуществления удаление регуляторных Т-клеток, например, CD25+ клеток, и удаление клеток, экспрессирующих ингибитор контрольных точек иммунного ответа, проводят последовательно, и, например, его можно производить в любом порядке.
Способы, описанные в данном документе, могут включать стадию положительного отбора. Например, Т-клетки можно выделять путем инкубирования с микрогранулами, конъюгированными с антителом к CD3/антителом к CD28 (например, 3×28), такими как DYNABEADS® M-450 CD3/CD28 T, в течение периода времени, достаточного для положительного отбора требуемых Т-клеток. В одном варианте осуществления период времени составляет приблизительно 30 минут. В дополнительном варианте осуществления период времени находится в диапазоне от 30 минут до 36 часов или более и включает все целочисленные значения в данном промежутке. В дополнительном варианте осуществления период времени составляет по меньшей мере 1, 2, 3, 4, 5 или 6 часов. В еще одном варианте осуществления период времени составляет от 10 до 24 часов, например, 24 часа. Более длительное время инкубирования можно использовать для выделения Т-клеток в любой ситуации, при которой Т-клеток небольшое число по сравнению с другими типами клеток, как, например, при выделении лимфоцитов, инфильтрирующих опухоль (TIL), из опухолевой ткани или у индивидуумов с ослабленным иммунитетом. Кроме того, при использовании более длительного времени инкубирования может увеличиваться эффективность захвата CD8+ Т-клеток. Таким образом, просто сокращая или удлиняя время, в течение которого Т-клетки имеют возможность связываться с микрогранулами с антителами к CD3/CD28, и/или увеличивая или уменьшая соотношение гранул и Т-клеток (как описано дополнительно в данном документе), можно предпочтительно осуществлять положительный или отрицательный отбор субпопуляций Т-клеток в начале культивирования или в другие моменты времени в ходе процесса. Кроме того, путем увеличения или уменьшения соотношения антител к CD3 и/или антител к CD28 на микрогранулах или другой поверхности можно предпочтительно осуществлять положительный или отрицательный отбор субпопуляций Т-клеток в начале культивирования или в другие необходимые моменты времени.
В одном варианте осуществления можно выбрать популяцию Т-клеток, которые экспрессируют один или несколько из IFN-γ, TNFα, IL-17A, IL-2, IL-3, IL-4, GM-CSF, IL-10, IL-13, гранзима В и перфорина или других соответствующих молекул, например, других цитокинов. Способы скрининга в отношении клеточной экспрессии можно определить, например, с помощью способов, описанных в публикации согласно PCT № WO 2013/126712.
Для выделения необходимой популяции клеток путем положительного или отрицательного отбора можно изменять концентрацию клеток и поверхности (например, частиц, таких как микрогранулы). В определенных аспектах может потребоваться значительно уменьшить объем, в котором микрогранулы и клетки смешиваются друг с другом (например, увеличить концентрацию клеток), чтобы обеспечить максимальный контакт клеток и микрогранул. Например, в одном аспекте используют концентрацию, составляющую 10 миллиардов клеток/мл, 9 миллиардов/мл, 8 миллиардов/мл, 7 миллиардов/мл, 6 миллиардов/мл или 5 миллиардов/мл. В одном аспекте используют концентрацию, составляющую 1 миллиард клеток/мл. В еще одном аспекте используют концентрацию клеток, составляющую 75, 80, 85, 90, 95 или 100 миллионов клеток/мл. В дополнительных аспектах можно использовать концентрации, составляющие 125 или 150 миллионов клеток/мл.
Использование высоких концентраций может приводить к увеличению выхода клеток, активации клеток и размножения клеток. Кроме того, использование высоких концентраций клеток обеспечивает более эффективных захват клеток, которые могут слабо экспрессировать представляющие интерес антигены-мишени, таких как CD28-отрицательные Т-клетки, или клеток из образцов, в которых присутствует много опухолевых клеток (например, лейкозной крови, опухолевой ткани и т. д.). Такие популяции клеток могут иметь терапевтическую ценность, и может потребоваться их получение. Например, использование высокой концентрации клеток обеспечивает более эффективный отбор CD8+ Т-клеток, которые обычно характеризуются более слабой экспрессией CD28.
В родственном аспекте может потребоваться использование более низких концентраций клеток. За счет значительного разбавления смеси Т-клеток и поверхности (например, частиц, таких как микрогранулы), взаимодействие между частицами и клетками сводится к минимуму. При этом отбираются клетки, которые экспрессируют необходимые антигены, подлежащие связыванию с частицами, в высоких количествах. Например, CD4+ T-клетки экспрессируют CD28 на более высоких уровнях и улавливаются при разбавленных концентрациях более эффективно, чем CD8+ T-клетки. В одном аспекте используемая концентрация клеток составляет 5×106/мл. В других аспектах используемая концентрация может составлять от приблизительно 1×105/мл до 1×106/мл с включением любого целочисленного значения в данном промежутке.
В других аспектах клетки можно инкубировать на ротаторе в течение различных промежутков времени при различных скоростями или при 2-10°C, или при комнатной температуре.
Т-клетки для стимуляции также можно замораживать после стадии промывания. Без ограничения какой-либо теорией, полагают, что стадия замораживания и последующего размораживания обеспечивает получение более однородного продукта за счет удаления гранулоцитов и в некоторой степени моноцитов из популяции клеток. После стадии промывания, на которой удаляют плазму крови и тромбоциты, клетки можно суспендировать в замораживающем растворе. Хотя многие замораживающие растворы и параметры для замораживания известны из уровня техники и будут применимыми в данном случае, один способ предусматривает использование PBS, содержащего 20% DMSO и 8% человеческого сывороточного альбумина, или сред для культивирования, содержащих 10% декстрана-40 в 5% декстрозе, 20% человеческого сывороточного альбумина и 7,5% DMSO или 31,25% PlasmaLyte-А, 31,25% раствора с 5% декстрозой в 0,45% NaCl, 10% декстрана-40 в 5% декстрозе, 20% человеческого сывороточного альбумина и 7,5% DMSO, или других подходящих сред для замораживания клеток, содержащих, например, Hespan и PlasmaLyte A, и затем клетки замораживают до -80°C со скоростью 1° в минуту и хранят в паровой фазе резервуара для хранения жидкого азота. Можно применять другие способы контролируемого замораживания, а также неконтролируемого замораживания сразу до -20°C или в жидком азоте.
В определенных аспектах криоконсервированные клетки размораживают и промывают, как описано в данном документе, и оставляют на один час при комнатной температуре до активации с применением способов по настоящему изобретению.
В контексте настоящего изобретения также предусмотрен сбор образцов крови или продукта афереза у субъекта в период времени до того, как могут понадобится размноженные клетки, описанные в данном документе. Ввиду этого источник клеток, подлежащих размножению, можно собирать в любой необходимый момент времени, и необходимые клетки, такие как Т-клетки, можно выделять и замораживать для последующего применения в терапии с использованием иммунных эффекторных клеток для любых заболеваний или состояний, при которых будет благоприятной терапия с использованием иммунных эффекторных клеток, таких как описанные в данном документе. В одном аспекте образец крови или материал, получаемый путем афереза, отбирают у в целом здорового субъекта. В определенных аспектах образец крови или материал, получаемый путем афереза, отбирают у в целом здорового субъекта, который имеет риск развития заболевания, но у которого заболевание еще не развилось, и представляющие интерес клетки выделяют и замораживают для последующего применения. В определенных аспектах Т-клетки можно размножать, замораживать и использовать позднее. В определенных аспектах образцы собирают у пациента вскоре после диагностирования конкретного заболевания, описанного в данном документе, однако до проведения каких-либо видов лечения. В дополнительном аспекте клетки выделяют из образца крови или материала, получаемого путем афереза, у субъекта до осуществления любых соответствующих способов лечения, включая без ограничения лечение такими средствами, как натализумаб, эфализумаб, противовирусные средства, химиотерапия, лучевая терапия, иммуносупрессорные средства, такие как циклоспорин, азатиоприн, метотрексат, микофенолят и FK506, антитела или другие иммунодеструктивные средства, такие как CAMPATH, антитела к CD3, цитоксан, флударабин, циклоспорин, FK506, рапамицин, микофеноловая кислота, стероиды, FR901228 и облучение.
В дополнительном аспекте настоящего изобретения Т-клетки получают от пациента непосредственно после лечения, при котором у субъекта остаются функциональные Т-клетки. В данном отношении наблюдалось, что после определенных видов лечения рака, в частности видов лечения лекарственными средствами, которые повреждают иммунную систему, вскоре после лечения в течение периода, когда пациенты обычно восстанавливаются после лечения, качество полученных Т-клеток может быть оптимальным или улучшенным в отношении их способности размножаться ex vivo. Аналогично, после манипуляций ex vivo с применением способов, описанных в данном документе, эти клетки могут находиться в состоянии, предпочтительном для улучшенного приживления и размножения in vivo. Таким образом, в контексте настоящего изобретения предусмотрен сбор клеток крови, включая Т-клетки, дендритные клетки или другие клетки гемопоэтической линии дифференцировки, во время данной фазы восстановления. Кроме того, в определенных аспектах можно использовать мобилизацию (например, мобилизацию с помощью GM-CSF) и схемы кондиционирования для создания у субъекта состояния, благоприятного для репопуляции, рециркуляции, регенерации и/или размножения определенных типов клеток, особенно в течение определенного временного окна после терапии. Иллюстративные типы клеток включают Т-клетки, В-клетки, дендритные клетки и другие клетки иммунной системы.
В одном варианте осуществления иммунные эффекторные клетки, экспрессирующие слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит молекулу CAR, например, молекулу CAR, описанную в данном документе, получают от субъекта, который получил низкую повышающую иммунитет дозу ингибитора mTOR. В варианте осуществления популяцию иммунных эффекторных клеток, например, Т-клеток, подлежащих конструированию для экспрессии CAR, собирают спустя достаточное количество времени или после достаточного введения низкой повышающей иммунитет дозы ингибитора mTOR так, чтобы уровень PD1-отрицательных иммунных эффекторных клеток, например, Т-клеток, или соотношение PD1-отрицательных иммунных эффекторных клеток, например, Т-клеток, и PD1-положительных иммунных эффекторных клеток, например, Т-клеток, у субъекта или в клетках, собранных у субъекта, по меньшей мере временно были повышены.
В других вариантах осуществления популяция иммунных эффекторных клеток, например, Т-клеток, которые были сконструированы или будут сконструированы для экспрессии слитого белка, например, описанного в данном документе, содержащего домен, который содержит CAR, может быть обработана ex vivo путем приведения ее в контакт с таким количеством ингибитора mTOR, которое увеличивает количество PD1-отрицательных иммунных эффекторных клеток, например, Т-клеток, или увеличивает соотношение PD1-отрицательных иммунных эффекторных клеток, например, Т-клеток, и PD1-положительных иммунных эффекторных клеток, например, Т-клеток.
В одном варианте осуществления Т-клетки в популяции являются дефицитными по диацилглицеринкиназе (DGK). Клетки, дефицитные по DGK, включают клетки, которые не экспрессируют РНК или белок DGK или характеризуются сниженной или ингибированной активностью DGK. Клетки, дефицитные по DGK, можно получить с помощью генетических методов, например, путем введения средств для РНК-интерференции, например, siRNA, shRNA, miRNA, чтобы снизить или предотвратить экспрессию DGK. В качестве альтернативы, клетки, дефицитные по DGK, можно получить путем обработки ингибиторами DGK, описанными в данном документе.
В одном варианте осуществления Т-клетки в популяции являются дефицитными по Ikaros. Клетки, дефицитные по Ikaros, включают клетки, которые не экспрессируют РНК или белок Ikaros или характеризуются сниженной или ингибированной активностью Ikaros; клетки, дефицитные Ikaros можно получить с помощью генетических методов, например, путем введения средств для РНК-интерференции, например, siRNA, shRNA, miRNA, чтобы снизить или предотвратить экспрессию Ikaros. В качестве альтернативы, клетки, дефицитные по Ikaros, можно получить путем обработки ингибиторами Ikaros, например, леналидомидом.
В вариантах осуществления Т-клетки в популяции являются дефицитными по DGK и дефицитными по Ikaros, например, не экспрессируют DGK и Ikaros или характеризуются сниженной или ингибированной активностью DGK и Ikaros. Такие клетки, дефицитные по DGK и Ikaros, можно получить любым из способов, описанных в данном документе.
В одном варианте осуществления NK-клетки получают от субъекта. В другом варианте осуществления NK-клетки представляют собой линию NK-клеток, например, линию клеток NK-92 (Conkwest).
Дополнительные экспрессируемые средства
В другом варианте осуществления с помощью слитого полипептида, например, описанного в данном документе, содержащего домен, который содержит иммунная эффекторная клетка, экспрессирующая CAR, описанная в данном документе, может дополнительно экспрессироваться другое средство, например, средство, которое усиливает активность клетки, экспрессирующей CAR. Например, в одном варианте осуществления средство может представлять собой средство, которое ингибирует ингибирующую молекулу. Примеры ингибирующих молекул включают PD-1, PD-L1, CTLA-4, TIM-3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG-3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4 и TGF-бета, например, описанный в данном документе. В одном варианте осуществления средство, которое ингибирует ингибирующую молекулу, содержит первый полипептид, например, ингибирующую молекулу, ассоциированный со вторым полипептидом, передающим положительный сигнал в клетку, например, внутриклеточным сигнальным доменом, описываемым в данном документе. В одном варианте осуществления средство содержит первый полипептид, например ингибирующую молекулу, такую как PD-1, PD-L1, CTLA-4, TIM-3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG-3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4 или TGF-бета или фрагмент любого из них, и второй полипептид, который представляет собой внутриклеточный сигнальный домен, описанный в данном документе (например, содержащий костимулирующий домен (например, 41BB, CD27 или CD28, например, описанные в данном документе), и/или первичный сигнальный домен (например, сигнальный домен CD3-дзета, описанный в данном документе). В одном варианте осуществления средство содержит первый полипептид, представляющий собой PD-1 или его фрагмент, и второй полипептид, представляющий собой внутриклеточный сигнальный домен, описанный в данном документе (например, сигнальный домен CD28, CD27, OX40 или 4-IBB, описанные в данном документе, и/или сигнальный домен CD3-дзета, описанный в данном документе).
В одном варианте осуществления иммунная эффекторная клетка, экспрессирующая слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR, описанный в данном документе, может дополнительно содержать второй слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR, например, второй CAR, который содержит другой антигенсвязывающий домен, например, для той же мишени (например, мишени, описанной выше), или другой мишени. В одном варианте осуществления второй CAR содержит антигенсвязывающий домен для мишени, экспрессируемой на раковой клетке того же типа, что и мишень первого CAR. В одном варианте осуществления иммунная эффекторная клетка, экспрессирующая CAR, содержит первый CAR, который нацеливается на первый антиген и содержит внутриклеточный сигнальный домен, имеющий костимулирующий сигнальный домен, а не первичный сигнальный домен, и второй CAR, который нацеливается на второй, другой, антиген и содержит внутриклеточный сигнальный домен, имеющий первичный сигнальный домен, а не костимулирующий сигнальный домен.
Без ограничения какой-либо теорией, размещение костимулирующего сигнального домена, например, 4-1BB, CD28, CD27 или OX-40, на первом CAR, и первичного сигнального домена, например CD3-дзета, на втором CAR может ограничивать активность CAR клетками, в которых экспрессируются обе мишени. В одном варианте осуществления иммунная эффекторная клетка, экспрессирующая CAR, содержит первый CAR, который содержит антигенсвязывающий домен, например, который нацеливает на мишень, описанную выше, трансмембранный домен и костимулирующий домен, и второй CAR, который нацеливается на антиген, отличный от антигена, на который нацеливается первый CAR (например, антиген, экспрессируемый на раковой клетке того же типа, что и первая мишень) и содержит антигенсвязывающий домен, трансмембранный домен и первичный сигнальный домен. В другом варианте осуществления иммунная эффекторная клетка, экспрессирующая CAR, содержит первый CAR, который содержит антигенсвязывающий домен, например, который нацеливается на мишень, описанную выше, трансмембранный домен и первичный сигнальный домен, и второй CAR, который нацеливается на антиген, отличный от антигена, на который нацеливается первый CAR (например, антиген, экспрессируемый на раковой клетке того же типа, что и первая мишень) и содержит антигенсвязывающий домен для антигена, трансмембранный домен и костимулирующий сигнальный домен.
В одном варианте осуществления иммунная эффекторная клетка, экспрессирующая CAR, содержит CAR, описанный в данном документе, например, CAR для мишени, описанной выше, и ингибирующий CAR. В одном варианте осуществления ингибирующий CAR содержит антигенсвязывающий домен, который связывает антиген, обнаруживаемый на нормальных клетках, а не раковых клетках, например, нормальных клетках, которые также экспрессируют мишень. В одном варианте осуществления ингибирующий CAR содержит антигенсвязывающий домен, трансмембранный домен и внутриклеточный домен ингибирующей молекулы. Например, внутриклеточный домен ингибирующего CAR может представлять собой внутриклеточный домен PD1, PD-L1, CTLA-4, TIM-3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG-3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4 или TGFR-бета.
В одном варианте осуществления иммунная эффекторная клетка (например, T-клетка, NK-клетка) содержит первый CAR, содержащий антигенсвязывающий домен, который связывается с опухолевым антигеном, описанным в данном документе, и второй CAR, содержащий внеклеточный домен PD1 или его фрагмент.
В одном варианте осуществления клетка дополнительно содержит ингибирующую молекулу, описанную выше.
В одном варианте осуществления второй CAR в клетке представляет собой ингибирующий CAR, где ингибирующий CAR содержит антигенсвязывающий домен, трансмембранный домен и внутриклеточный домен ингибирующей молекулы. Ингибирующая молекула может быть выбрана из одного или нескольких из PD1, PD-L1, CTLA-4, TIM-3, LAG-3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4, TGFR-бета, CEACAM-1, CEACAM-3 и CEACAM-5. В одном варианте осуществления вторая молекула CAR содержит внеклеточный домен PD1 или его фрагмент.
В вариантах осуществления вторая молекула CAR в клетке дополнительно содержит внутриклеточный сигнальный домен, содержащий первичный сигнальный домен и/или внутриклеточный сигнальный домен.
В других вариантах осуществления внутриклеточный сигнальный домен в клетке содержит первичный сигнальный домен, содержащий функциональный домен CD3-дзета, и костимулирующий сигнальный домен, содержащий функциональный домен 4-1BB.
В определенных вариантах осуществления антигенсвязывающий домен молекулы первого CAR содержит scFv, а антигенсвязывающий домен молекулы второго CAR не содержит scFv. Например, антигенсвязывающий домен молекулы первого CAR содержит scFv, а антигенсвязывающий домен молекулы второго CAR VHH-домен верблюдовых.
Разделенный CAR
В некоторых вариантах осуществления в клетке, экспрессирующей CAR, используется разделенный CAR. Подход с разделенным CAR более подробно описан в публикациях WO2014/055442 и WO2014/055657, включенных в данный документ посредством ссылки. Вкратце, система разделенного CAR содержит клетку, экспрессирующую первый CAR, имеющий первый антигенсвязывающий домен и костимулирующий домен (например, 41BB), и эта клетка также экспрессирует второй CAR, имеющий второй антигенсвязывающий домен и внутриклеточный сигнальный домен (например, CD3-дзета). Когда клетка встречается с первым антигеном, то активируется костимулирующий домен, и клетка пролиферирует. Когда клетка встречается со вторым антигеном, то активируется внутриклеточный сигнальный домен, и запускается активность уничтожения клеток. Таким образом, клетка, экспрессирующая CAR, полностью активируется только в присутствии обоих антигенов.
Экспрессия нескольких CAR
В одном аспекте описанная в данном документе клетка, экспрессирующая слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR, может дополнительно содержать второй слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR, например, второй CAR, который содержит другой антигенсвязывающий домен, например, для той же мишени или другой мишени (например, мишени, отличной от антигена, ассоциированного с раком, описанного в данном документе, или другого антигена, ассоциированного с раком, описанного в данном документе). В одном варианте осуществления второй CAR содержит антигенсвязывающий домен для мишени, экспрессируемой на раковой клетке того же типа, что и клетка, на которой экспрессируется антиген, ассоциированный с раком. В одном варианте осуществления клетка, экспрессирующая CAR, содержит первый CAR, который нацеливается на первый антиген и содержит внутриклеточный сигнальный домен, имеющий костимулирующий сигнальный домен, а не первичный сигнальный домен, и второй CAR, который нацеливается на второй, другой, антиген и содержит внутриклеточный сигнальный домен, имеющий первичный сигнальный домен, а не костимулирующий сигнальный домен. Без ограничения какой-либо теорией, размещение костимулирующего сигнального домена, например, 4-1BB, CD28, CD27 или OX-40, на первом CAR, и первичного сигнального домена, например CD3-дзета, на втором CAR может ограничивать активность CAR клетками, в которых экспрессируются обе мишени. В одном варианте осуществления клетка, экспрессирующая CAR, содержит первый CAR для антигена, ассоциированного с раком, который содержит антигенсвязывающий домен, который связывает антиген-мишень, описанный в данном документе, трансмембранный домен и костимулирующий домен, и второй CAR, который нацеливается на другой антиген-мишень (например, антиген, экспрессируемый на раковой клетке того же типа, на которой экспрессируется первый антиген-мишень) и содержит антигенсвязывающий домен, трансмембранный домен и первичный сигнальный домен. В другом варианте осуществления клетка, экспрессирующая CAR, содержит первый CAR, который содержит антигенсвязывающий домен, который связывает антиген-мишень, описанный в данном документе, трансмембранный домен и первичный сигнальный домен, и второй CAR, который нацеливается на антиген, отличный от первого антигена-мишени (например, антиген, экспрессируемый на раковой клетке того же типа, на которой экспрессируется первый антиген-мишень), и содержит антигенсвязывающий домен для антигена, трансмембранный домен и костимулирующий сигнальный домен.
В некоторых вариантах осуществления заявляемое изобретение предусматривает первый и второй CAR, где антигенсвязывающий домен одного из указанного первого CAR и указанного второго CAR не содержит вариабельный домен легкой цепи и вариабельный домен тяжелой цепи. В некоторых вариантах осуществления антигенсвязывающий домен одного из указанного первого CAR и указанного второго CAR представляет собой scFv, а другой не является scFv. В некоторых вариантах осуществления антигенсвязывающий домен одного из указанного первого CAR и указанного второго CAR содержит один VH-домен, например, один VH-домен верблюдовых, акулы или миноги или один VH-домен, полученный из последовательности человека или мыши. В некоторых вариантах осуществления антигенсвязывающий домен одного из указанного первого CAR и указанного второго CAR содержит нанотело. В некоторых вариантах осуществления антигенсвязывающий домен одного из указанного первого CAR и указанного второго CAR содержит VHH-домен верблюдовых.
Аллогенные клетки
В вариантах осуществления, описанных в данном документе, иммунная эффекторная клетка может представлять собой аллогенную иммунную эффекторную клетку, например, Т-клетку или NK-клетку. Например, клетка может представлять собой аллогенную T-клетку, например, аллогенную T-клетку, в которой отсутствует экспрессия функционального T-клеточного рецептора (TCR) и/или лейкоцитарного антигена человека (HLA), например, HLA класса I и/или HLA класса II или бета-2-микроглобулина (B2M).
T-клетку, в которой отсутствует функциональный TCR, можно, например, сконструировать таким образом, чтобы она вообще не экспрессировала функциональный TCR на своей поверхности, сконструировать таким образом, чтобы она не экспрессировала одну или несколько субъединиц, которые составляют функциональный TCR, например, TRAC, TRBC1, TRBC2, CD3E, CD3G или CD3D, или сконструировать таким образом, чтобы она продуцировала очень небольшое количество функционального TCR на своей поверхности. В качестве альтернативы, Т-клетка может экспрессировать значительно нарушенный TCR, например, посредством экспрессии мутантных или усеченных форм одной или нескольких субъединиц TCR. Термин "значительно нарушенный TCR" означает, что этот TCR не будет вызывать нежелательную иммунную реакцию у хозяина.
Т-клетку, описанную в данном документе, можно, например, сконструировать таким образом, чтобы она не экспрессировала функциональный HLA на своей поверхности. Например, T-клетку, описанную в данном документе, можно сконструировать таким образом, чтобы экспрессия HLA, например, HLA класса 1 и/или HLA класса II, а также субъединицы или регулятора экспрессии HLA, например, B2M, на клеточной поверхности подавлялась.
Т-клетку, описанную в данном документе, например, можно, сконструировать таким образом, чтобы она не экспрессировала функциональный B2M на своей поверхности. Например, Т-клетку, описанную в данном документе, можно сконструировать таким образом, чтобы экспрессия B2M на клеточной поверхности подавлялась.
В некоторых вариантах осуществления в Т-клетке может отсутствовать функциональный TCR и функциональный HLA, например, HLA класса I и/или HLA класса II.
Модифицированные Т-клетки, в которых отсутствует экспрессия функционального TCR и/или HLA, можно получить любым подходящим способом, в том числе путем нокаута или нокдауна одной или нескольких субъединиц TCR или HLA. Например, можно предусмотреть нокдаун TCR и/или HLA в Т-клетке с помощью siRNA, shRNA, коротких палиндромных повторов, регулярно расположенных группами (CRISPR), эффекторной нуклеазы, подобной активаторам транскрипции (TALEN), или эндонуклеазы с "цинковыми пальцами" (ZFN).
В некоторых вариантах осуществления аллогенная клетка может представлять собой клетку, в которой не экспрессируется или экспрессируется на низких уровнях ингибирующая молекула, например, за счет любого способа, описанного в данном документе. Например, клетка может представлять собой клетку, в которой не экспрессируется или экспрессируется на низких уровнях ингибирующая молекула, например, молекула, которая может снижать способность клетки, экспрессирующей CAR, осуществлять иммунный эффекторный ответ. Примеры ингибирующих молекул включают PD1, PD-L1, CTLA4, TIM3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4 и TGFR-бета. Ингибирование ингибирующей молекулы, например, путем ингибирования на уровне ДНК, РНК или белка, может оптимизировать функциональные характеристики клетки, экспрессирующей CAR. В вариантах осуществления можно применять ингибирующую нуклеиновую кислоту, например, ингибирующую нуклеиновую кислоту, например, dsRNA, например, siRNA или shRNA, короткие палиндромные повторы, регулярно расположенные группами (CRISPR), эффекторную нуклеазу, подобную активаторам транскрипции (TALEN), или эндонуклеазу с "цинковыми пальцами" (ZFN), например, описанные в данном документе.
siRNA и shRNA
В некоторых вариантах осуществления экспрессия TCR и/или экспрессия HLA или B2M могут быть ингибированы с применением siRNA или shRNA которые нацеливаются на нуклеиновую кислоту, кодирующую TCR и/или HLA в T-клетке.
CRISPR
Используемые в данном документе "CRISPR", или "CRISPR для TCR и/или HLA", или "CRISPR для ингибирования TCR и/или HLA" относится к набору коротких палиндромных повторов, регулярно расположенных группами, или к системе, содержащей такой набор повторов. Используемый в данном документе "Cas" относится к CRISPR-ассоциированному белку. Система "CRISPR/Cas" относится к системе, полученной из CRISPR и Cas, которую можно использовать для сайленсинга или мутирования гена TCR и/или HLA или B2M.
Можно получить искусственные системы CRISPR/Cas, которые ингибируют TCR и/или HLA, с использованием технологии, известной из уровня техники, например, которая описана в публикации заявки на патент США № 20140068797 и Cong (2013) Science 339: 819-823, включенных в данный документ посредством ссылки во всей своей полноте. Также можно получить другие искусственные системы CRISPR/Cas, известные из уровня техники, которые ингибируют TCR и/или HLA, например, которые описаны в Tsai (2014) Nature Biotechnol., 32:6 569-576, патентах США №№ 8871445; 8865406; 8795965; 8771945 и 8697359, включенных в данный документ посредством ссылки во всей своей полноте.
TALEN
"TALEN", или "TALEN для HLA и/или TCR", или "TALEN для ингибирования HLA и/или TCR" относятся к эффекторной нуклеазе, подобной активаторам транскрипции, искусственной нуклеазе, которая может применяться для редактирования гена HLA или B2M и/или TCR.
TALEN получают искусственно путем слияния ДНК-связывающего домена эффектора TAL с доменом расщепления ДНК. Можно сконструировать эффекторы, подобные активаторам транскрипции (TALE), для связывания любой необходимой последовательности ДНК, включая часть гена HLA или TCR. Путем объединения сконструированного TALE с доменом расщепления ДНК можно получить рестрикционный фермент, который является специфичным в отношении к любой необходимой последовательности ДНК, включая последовательности HLA или TCR. Затем их можно вводить в клетку, где они могут использоваться для редактирования генома, как описано в Boch (2011) Nature Biotech. 29: 135-6; Boch et al. (2009) Science 326: 1509-12; и Moscou et al. (2009) Science 326: 3501, включенных в данный документ посредством ссылки во всей своей полноте.
TALEN, специфические в отношении последовательностей в HLA или TCR, можно сконструировать с применением любого способа, известного из уровня техники, включая различные схемы с применением модульный компонентов, описанные в Zhang et al. (2011) Nature Biotech. 29: 149-53; и Geibler et al. (2011) PLoS ONE 6: e19509, включенных в данный документе посредством ссылки во всей своей полноте.
Нуклеаза с "цинковыми пальцами" для ингибирования HLA и/или TCR
"ZFN", или "нуклеаза с цинковыми пальцами", или "ZFN для HLA и/или TCR", или "ZFN для ингибирования HLA и/или TCR" относятся к нуклеазе с "цинковыми пальцами", искусственной нуклеазе, которая может применяться для редактирования гена HLA и/или TCR или B2M.
ZFN, специфические в отношении последовательностей в HLA и/или TCR можно сконструировать с применением любого способа, известного из уровня техники, описанного в Provasi (2011) Nature Med. 18: 807-815; Torikai (2013) Blood 122: 1341-1349; Cathomen et al. (2008) Mol. Ther. 16: 1200-7; Guo et al. (2010) J. Mol. Biol. 400: 96; публикации заявки на патент США 2011/0158957 и публикации заявки на патент США 2012/0060230, включенных в данный документ посредством ссылки во всей своей полноте.
Экспрессия теломеразы
Не желая ограничиваться какой-либо конкретной теорией, полагают, что в некоторых вариантах осуществления для терапевтической Т-клетки характерна кратковременная персистенция в пациенте вследствие укороченных теломер в Т-клетке; соответственно, трансфекция гена теломеразы может приводить к удлинению теломер в Т-клетке и улучшить персистенцию Т-клетки в пациенте. См. Carl June, "Adoptive T cell therapy for cancer in the clinic", Journal of Clinical Investigation, 117:1466-1476 (2007), включенный в данный документ посредством ссылки во все своей полноте. Таким образом, в одном варианте осуществления иммунная эффекторная клетка, например, Т-клетка, характеризуется эктопической экспрессией субъединицы теломеразы, например, каталитической субъединицы теломеразы, например, TERT, например, hTERT. В некоторых аспектах настоящего изобретения представлен способ получения клетки, экспрессирующей CAR, предусматривающий приведение клетки в контакт с нуклеиновой кислотой, кодирующей субъединицу теломеразы, например, каталитическую субъединицу теломеразы, например, TERT, например, hTERT. Клетку можно приводить в контакт с нуклеиновой кислотой перед приведением в контакт с конструкцией, кодирующей CAR, одновременно с этим или после этого.
Размножение и активация
Иммунные эффекторные клетки, такие как T-клетки, как правило, можно активировать и размножать с применением способов, описанных, например, в патентах США 6352694; 6534055; 6905680; 6692964; 5858358; 6887466; 6905681; 7144575; 7067318; 7172869; 7232566; 7175843; 5883223; 6905874; 6797514; 6867041 и публикации заявки на патент США № 20060121005, каждый из которых включен посредством ссылки во всей своей полноте.
Как правило, популяцию иммунных эффекторных клеток, например, клеток, истощенных по регуляторным Т-клеткам, можно размножать путем приведения их в контакт с поверхностью, к которой присоединено средство, стимулирующее передачу сигнала, ассоциированного с комплексом CD3/TCR, и лигандом, стимулирующим костимулирующую молекулу на поверхности Т-клеток. В частности, популяции Т-клеток можно стимулировать, как описано в данном документе, например, путем приведения в контакт с антителом к CD3 или его антигенсвязывающим фрагментом или антителом к CD2, иммобилизованным на поверхности, или путем приведения в контакт с активатором протеинкиназы С (например, бриостатином) в сочетании с ионофором кальция. Для костимуляции вспомогательной молекулы на поверхности Т-клеток применяют лиганд, который связывается со вспомогательной молекулой. Например, популяцию Т-клеток можно приводить в контакт с антителом к CD3 и антителом к CD28 в условиях, подходящих для стимуляции пролиферации Т-клеток. Для стимуляции пролиферации либо CD4+ T-клеток, либо CD8+ T-клеток можно применять антитело к CD3 и антитело к CD28. Примеры антитела к CD28 включают 9.3, B-T3, XR-CD28 (Diaclone, Безансон, Франция), и их можно применять, равно как и другие способы, общеизвестные из уровня техники (Berg et al., Transplant Proc. 30(8):3975-3977, 1998; Haanen et al., J. Exp. Med. 190(9):1319-1328, 1999; Garland et al., J. Immunol Meth. 227(1-2):53-63, 1999).
В определенных аспектах первичный стимулирующий сигнал и костимулирующий сигнал для Т-клетки можно обеспечивать с помощью различных протоколов. Например, средства, обеспечивающие каждый сигнал, могут находиться в растворе или быть связаны с поверхностью. В случае, если они связаны с поверхностью, средства могут быть связаны с одной и той же поверхностью (т. е. в "цис"-расположении) или с отдельными поверхностями (т. е. в "транс"-расположении). В качестве альтернативы, одно средство может быть связано с поверхностью, а другое средство может находиться в растворе. В одном аспекте средство, обеспечивающее костимулирующий сигнал, связано с клеточной поверхностью, а средство, обеспечивающее первичный сигнал активации, находится в растворе или связано с поверхностью. В определенных аспектах оба средства могут находиться в растворе. В одном аспекте средства могут находиться в растворимой форме, а затем их сшивают с поверхностью, такой как клетка, экспрессирующая Fc-рецепторы, или антитело или другое связывающее средство, которое будет связываться с данными средствами. В связи с этим, см., например, публикации заявок на патент США №№ 20040101519 и 20060034810, включенные в данный документ посредством ссылки во всей своей полноте, касательно искусственных антигенпрезентирующих клеток (aAPC), которые предполагаются для применения в активации и размножении Т-клеток в настоящем изобретении.
В одном аспекте два средства иммобилизованы на микрогранулах, либо на одной и той же микрогрануле, т. е. в "цис"-положении, либо на отдельных микрогранулах, т. е. в "транс"-положении. В качестве примера, средство, обеспечивающее первичный сигнал активации, представляет собой антитело к CD3 или его антигенсвязывающий фрагмент, а средство, обеспечивающее костимулирующий сигнал, представляет собой антитело к CD28 или его антигенсвязывающий фрагмент; и оба средства совместно иммобилизованы на одной и той же микрогрануле в эквивалентных молекулярных количествах. В одном аспекте для размножения CD4+ T-клеток и роста T-клеток используют каждое антитело, связанное с микрогранулами, в соотношении 1:1. В определенных аспектах настоящего изобретения используют такое соотношение антител к CD3:CD28, связанных с микрогранулами, при котором наблюдается увеличение размножения Т-клеток по сравнению с размножением, наблюдаемым при использовании соотношения 1:1. В одном конкретном аспекте наблюдается увеличение от приблизительно 1 до приблизительно 3 раз по сравнению с размножением, наблюдаемым при использовании соотношения 1:1. В одном аспекте соотношение антител к CD3:CD28, связанных с микрогранулами, находится в диапазоне от 100:1 до 1:100 и включает все целочисленные значения в этом промежутке. В одном аспекте с частицами связано больше антител к CD28, чем антител к CD3, т. е. соотношение антитела к CD3:CD28 составляет меньше единицы. В определенных аспектах соотношение антитела к CD28 и антитела к CD3, связанных с микрогранулами, составляет более чем 2:1. В одном конкретном аспекте используется соотношение антител к CD3:CD28, связанных с микрогранулами, составляющее 1:100. В одном аспекте используется соотношение антител к CD3:CD28, связанных с микрогранулами, составляющее 1:75. В дополнительном аспекте используется соотношение антител к CD3:CD28, связанных с микрогранулами, составляющее 1:50. В одном аспекте используется соотношение антител к CD3:CD28, связанных с микрогранулами, составляющее 1:30. В одном предпочтительном аспекте используется соотношение антител к CD3:CD28, связанных с микрогранулами, составляющее 1:10. В одном аспекте используется соотношение антител к CD3:CD28, связанных с микрогранулами, составляющее 1:3. В еще одном аспекте используется соотношение антител к CD3:CD28, связанных с микрогранулами, составляющее 3:1.
Для стимуляции Т-клеток или других клеток-мишеней можно использовать соотношения частиц и клеток от 1:500 до 500:1 с включением любых целочисленных значений в этом промежутке. Как будет очевидно для специалистов обычной квалификации в данной области техники, соотношение частиц и клеток может зависеть от размера частиц относительно клетки-мишени. Например, микрогранулы небольшого размера могут связывать небольшое число клеток, тогда как более крупные микрогранулы могут связывать много клеток. В определенных аспектах для стимуляции Т-клеток также можно использовать соотношение клеток и частиц, находящееся в диапазоне от 1:100 до 100:1 и включающее любые целочисленные значения в этом промежутке, а в дополнительных аспектах соотношение составляет от 1:9 до 9:1 и включает любые целочисленные значения в этом промежутке. Соотношение частиц, связанных с антителами к CD3 и антителами к CD28, и Т-клеток, которое приводит к стимуляции Т-клеток, может варьироваться, как отмечено выше, однако определенные предпочтительные значения включают 1:100, 1:50, 1:40, 1:30, 1:20, 1:10, 1:9, 1:8, 1:7, 1:6, 1:5, 1:4, 1:3, 1:2, 1:1, 2:1, 3:1, 4:1, 5:1, 6:1, 7:1, 8:1, 9:1, 10:1 и 15:1, при этом одно предпочтительное соотношение составляет по меньшей мере 1:1 частиц на Т-клетку. В одном аспекте используется соотношение частиц и клеток, составляющее 1:1 или менее. В одном конкретном аспекте предпочтительное соотношение частицы:клетки составляет 1:5. В дополнительных аспектах соотношение частиц и клеток может варьироваться в зависимости от дня стимуляции. Например, в одном аспекте соотношение частиц и клеток составляет от 1:1 до 10:1 в первый день, и после этого к клеткам ежедневно или раз в два дня добавляют дополнительные частицы в течение периода до 10 дней при конечных соотношениях от 1:1 до 1:10 (в расчете на количество клеток в день добавления). В одном конкретном аспекте соотношение частиц и клеток составляет 1:1 в первый день стимуляции и доводится до 1:5 в третий и пятый дни стимуляции. В одном аспекте частицы добавляют ежедневно или раз в два дня до конечного соотношения 1:1 в первый день и 1:5 в третий и пятый дни стимуляции. В одном аспекте соотношение частиц и клеток составляет 2:1 в первый день стимуляции и доводится до 1:10 в третий и пятый дни стимуляции. В одном аспекте частицы добавляют ежедневно или раз в два дня до конечного соотношения 1:1 в первый день и 1:10 в третий и пятый дни стимуляции. Специалисту в данной области техники будет понятно, что для использования в настоящем изобретении могут подходить множество других соотношений. В частности, соотношения будут варьироваться в зависимости от размера частиц, а также от размера и типа клеток. В одном аспекте наиболее типичные соотношения для использования составляют примерно 1:1, 2:1 и 3:1 в первый день.
В дополнительных аспектах клетки, такие как Т-клетки, объединяют с микрогранулами, покрытыми средством, впоследствии микрогранулы и клетки разделяют, а затем клетки культивируют. В альтернативном аспекте микрогранулы, покрытые средством, и клетки не разделяют перед культивированием, а культивируют вместе. В дополнительном аспекте микрогранулы и клетки вначале концентрируют путем приложения силы, такой как сила магнитного поля, что приводит к увеличению лигирования маркеров клеточной поверхности, за счет чего обеспечивается индукция стимуляции клеток.
В качестве примера, белки клеточной поверхности можно лигировать, обеспечивая парамагнитным микрогранулам, к которым присоединены антитела к CD3 и антитела к CD28 (микрогранулы 3×28), контакт с Т-клетками. В одном аспекте клетки (например, от 104 до 109 T-клеток) и микрогранулы (например, парамагнитные микрогранулы DYNABEADS® M-450 CD3/CD28 T в соотношении 1:1) объединяют в буфере, например, PBS (без двухвалентных катионов, таких как кальций и магний). Специалистам обычной квалификации в данной области техники также будет легко понять, какую концентрацию клеток можно использовать. Например, клетка-мишень может очень редко встречаться в образце и составлять только 0,01% от образца, или весь образец (т. е. 100%) может составлять представляющая интерес клетка-мишень. Соответственно, любое количество клеток находится в пределах настоящего изобретения. В определенных аспектах может потребоваться значительно уменьшить объем, в котором частицы и клетки смешивают друг с другом (т. е. увеличить концентрацию клеток), чтобы гарантировать максимальный контакт клеток и частиц. Например, в одном аспекте используют концентрацию, составляющую приблизительно 10 миллиардов клеток/мл, 9 миллиардов/мл, 8 миллиардов/мл, 7 миллиардов/мл, 6 миллиардов/мл, 5 миллиардов/мл или 2 миллиарда клеток/мл. В одном аспекте используют более 100 миллионов клеток/мл. В дополнительном аспекте используют концентрацию клеток, составляющую 10, 15, 20, 25, 30, 35, 40, 45, или 50 миллионов клеток/мл. В еще одном аспекте используют концентрацию клеток от 75, 80, 85, 90, 95, или 100 миллионов клеток/мл. В дополнительных аспектах можно использовать концентрации, составляющие 125 или 150 миллионов клеток/мл. Использование высоких концентраций может приводить к увеличению выхода клеток, активации клеток и размножения клеток. Кроме того, использование высоких концентраций клеток обеспечивает более эффективный захват клеток, которые могут характеризоваться слабой экспрессией представляющих интерес антигенов-мишеней, таких как CD28-отрицательные Т-клетки. Такие популяции клеток могут иметь терапевтическую ценность, и в определенных аспектах может требоваться их получение. Например, использование высокой концентрации клеток обеспечивает более эффективный отбор CD8+ Т-клеток, которые обычно характеризуются более слабой экспрессией CD28.
В одном варианте осуществления клетки, трансдуцированные с помощью нуклеиновой кислоты, кодирующей слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR, например, CAR, описанный в данном документе, размножают, например, с помощью способа, описанного в данном документе. В одном варианте осуществления клетки размножают в культуре в течение периода от нескольких часов (например, приблизительно 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 18, 21 часов) до приблизительно 14 дней (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14 дней). В одном варианте осуществления клетки размножают в течение периода от 4 до 9 дней. В одном варианте осуществления клетки размножают в течение периода 8 дней или менее, например, 7, 6 или 5 дней. В одном варианте осуществления клетки размножают в культуре в течение 5 дней, и полученные клетки являются более активными, чем те же самые клетки, размножаемые в культуре в течение 9 дней при тех же условиях культивирования. Активность можно определить, например, по различным Т-клеточным функциям, например, пролиферации, уничтожению клеток-мишеней, продуцированию цитокинов, активации, миграции или их комбинациям. В одном варианте осуществления клетки, размножаемые в течение 5 дней, демонстрируют по меньшей мере одно-, двух-, трех- или четырехкратное увеличение скорости удвоения клеток после стимуляции антигеном по сравнению с теми же клетками, размножаемыми в культуре в течение 9 дней при тех же условиях культивирования. В одном варианте осуществления клетки размножают в культуре в течение 5 дней, и полученные клетки демонстрируют более высокие уровни продуцирования провоспалительных цитокинов, например, уровни IFN-γ и/или GM-CSF, по сравнению с теми же клетками, размножаемыми в культуре в течение 9 дней при тех же условиях культивирования. В одном варианте осуществления клетки, размножаемые в течение 5 дней, демонстрируют по меньшей мере одно-, двух-, трех-, четырех-, пяти-, десятикратное или большее увеличение продуцирования провоспалительных цитокинов в пг/мл, например, уровней IFN-γ и/или GM-CSF, по сравнению с теми же клетками, размножаемыми в культуре в течение 9 дней при тех же условиях культивирования.
Также могут потребоваться несколько циклов стимуляции, вследствие чего время культивирования Т-клеток может составлять 60 дней или больше. Условия, подходящие для культивирования Т-клеток, включают соответствующую среду (например, минимальную питательную среду, или среду RPMI 1640, или X-vivo 15 (Lonza)), которая может содержать факторы, необходимые для пролиферации и жизнеспособности, в том числе сыворотку крови (например, фетальную бычью или сыворотку крови человека), интерлейкин-2 (IL-2), инсулин, IFN-γ, IL-4, IL-7, GM-CSF, IL-10, IL-12, IL-15, TGFβ и TNF-α или любые другие добавки для роста клеток, известные специалисту в данной области техники. Другие добавки для роста клеток включают без ограничения поверхностно-активное вещество, плазманат и восстановители, такие как N-ацетилцистеин и 2-меркаптоэтанол. Среда может включать RPMI 1640, AIM-V, DMEM, MEM, α-MEM, F-12, X-Vivo 15 и X-Vivo 20, OpTmizer с добавлением аминокислот, пирувата натрия и витаминов, либо бессывороточную, либо дополненную соответствующим количеством сыворотки (или плазмы) крови или определенным набором гормонов и/или количеством цитокина(-ов), достаточным для роста и размножения Т-клеток. Антибиотики, например пенициллин и стрептомицин, включают только в экспериментальные культуры, но не в культуры клеток, которые предназначены для инфузии субъекту. Клетки-мишени содержат в условиях, необходимых для поддержания роста, например, при соответствующей температуре (например, 37°C) и атмосфере (например, воздух с 5% CO2).
В одном варианте осуществления клетки размножают в соответствующей среде (например, среде, описанной в данном документе), содержащей один или несколько интерлейкинов, что приводит к по меньшей мере 200-кратному (например, к 200-кратному, 250-кратному, 300-кратному, 350-кратному) увеличению количества клеток в течение 14-дневного периода размножения, например, как измерено с помощью способа, описанного в данном документе, такого как проточная цитометрия. В одном варианте осуществления клетки размножают в присутствии IL-15 и/или IL-7 (например, IL-15 и IL-7).
В вариантах осуществления способы, описанные в данном документе, например, способы производства клетки, экспрессирующей слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR, предусматривают удаление регуляторных T-клеток, например, CD25+ T-клеток, из популяции клеток, например, с использованием антитела к CD25, или его фрагмента, или CD25-связывающего лиганда IL-2. Способы удаления регуляторных Т-клеток, например, CD25+ Т-клеток, из популяции клеток описываются в данном документе. В вариантах осуществления способы, например, способы производства, дополнительно предусматривают приведение популяции клеток (например, популяции клеток, которая была истощена по регуляторным T-клеткам, таким как CD25+ T-клетки; или популяции клеток, которая ранее была приведена в контакт с антителом к CD25, его фрагментом или CD25-связывающим лигандом) в контакт с IL-15 и/или IL-7. Например, популяцию клеток (например, популяцию, которая ранее была приведена в контакт с антителом к CD25, его фрагментом или CD25-связывающим лигандом) размножают в присутствии IL-15 и/или IL-7.
В некоторых вариантах осуществления описанную в данном документе клетку, экспрессирующую слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR, приводят в контакт с композицией, содержащей полипептид интерлейкина-15 (IL-15), полипептид альфа-субъединицы рецептора интерлейкина-15 (IL-15Ra) или комбинацию как полипептида IL-15, так и полипептида IL-15Ra, например, hetIL-15, во время производства клетки, экспрессирующей CAR, например, ex vivo. В вариантах осуществления описанную в данном документе клетку, экспрессирующую CAR, приводят в контакт с композицией, содержащей полипептид IL-15, во время производства клетки, экспрессирующей CAR, например, ex vivo. В вариантах осуществления описанную в данном документе клетку, экспрессирующую CAR, приводят в контакт с композицией, содержащей комбинацию как полипептида IL-15, так и полипептида IL-15 Ra, во время производства клетки, экспрессирующей CAR, например, ex vivo. В вариантах осуществления описанную в данном документе клетку, экспрессирующую CAR, приводят в контакт с композицией, содержащей hetIL-15, в ходе производства клетки, экспрессирующей CAR, например, ex vivo.
В одном варианте осуществления описанную в данном документе клетку, экспрессирующую слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR, приводят в контакт с композицией, содержащей hetIL-15, во время размножения ex vivo. В одном варианте осуществления описанную в данном документе клетку, экспрессирующую CAR, приводят в контакт с композицией, содержащей полипептид IL-15, в ходе размножения ex vivo. В одном варианте осуществления описанную в данном документе клетку, экспрессирующую CAR, приводят в контакт с композицией, содержащей как полипептид IL-15, так и полипептид IL-15Ra, в ходе размножения ex vivo. В одном варианте осуществления приведение в контакт приводит к выживанию и пролиферации субпопуляции лимфоцитов, например, CD8+ T-клеток.
Т-клетки, которые подвергались стимуляции в течение разных периодов времени, могут демонстрировать разные характеристики. Например, в типичных препаратах крови или продуктах афереза мононуклеарных клеток периферической крови популяция Т-клеток-хелперов (TH, CD4+) превосходит по числу популяцию цитотоксических Т-клеток или Т-клеток-супрессоров (TC, CD8+). Размножение Т-клеток ex vivo путем стимуляции рецепторов CD3 и CD28 приводит к получению популяции Т-клеток, которая до приблизительно дней 8-9 состоит главным образом из ТН-клеток, тогда как после приблизительно дней 8-9 популяция Т-клеток содержит все более увеличивающуюся популяцию TC-клеток. Соответственно, в зависимости от цели лечения, может быть перспективной инфузия субъекту популяции Т-клеток, содержащей главным образом ТН-клетки. Аналогично, если была выделена антигенспецифическая субпопуляция TC-клеток, то может быть полезным размножение этой субпопуляции в большей степени.
Кроме того, в ходе процесса размножения клеток в дополнение к маркерам CD4 и CD8 в значительной степени, но по большей части воспроизводимо, варьируются уровни других фенотипических маркеров. Таким образом, подобная воспроизводимость дает возможность адаптировать продукт на основе активированный Т-клеток для конкретных целей.
После конструирования слитого полипептида, например, описанного в данном документе, содержащего домен, который содержит CAR, описанный в данном документе, для оценки активности молекулы можно применять различные анализы, как, например, без ограничения, способность Т-клеток размножаться после стимуляции антигеном, устойчивое размножение Т-клеток в отсутствие повторной стимуляции и формы противораковой активности на соответствующих моделях in vitro и животных моделях. Анализы для оценки эффектов CAR по настоящему изобретению описаны более подробно ниже.
Для обнаружения присутствия мономеров и димеров при экспрессии в первичных T-клетках можно использовать вестерн-блоттинг-анализ слитого полипептида, например, описанного в данном документе, содержащего домен, который содержит CAR. См., например, Milone et al., Molecular Therapy 17(8): 1453-1464 (2009). Очень коротко, T-клетки (смесь CD4+ и CD8+ T-клеток в соотношении 1:1), экспрессирующие CAR, размножают in vitro в течение более 10 дней с последующим лизисом и SDS-PAGE в восстанавливающих условиях. CAR, содержащие полноразмерный цитоплазматический домен TCR-ζ и эндогенную цепь TCR-ζ, выявляют с помощью вестерн-блоттинга с использованием антитела к цепи TCR-ζ. Те же субпопуляции T-клеток применяют для анализа посредством SDS-PAGE в невосстанавливающих условиях для обеспечения оценки образования ковалентных димеров.
В случае T-клеток, положительных+по слитому полипептиду, например, описанному в данном документе, содержащему домен, который содержит CAR, например, CAR+, их размножение in vitro после стимуляции антигеном может быть измерено с помощью проточной цитометрии. Например, смесь CD4+ и CD8+ Т-клеток стимулируют с помощью aAPC с αCD3/αCD28, а затем трансдуцируют лентивирусными векторами, экспрессирующими GFP под контролем промоторов, подлежащих анализу. Иллюстративные промоторы включают промоторы генов IE CMV, EF-1α, убиквитина С или фосфоглицераткиназы (PGK). Флуоресценцию GFP оценивают с помощью проточной цитометрии в день 6 культивирования в субпопуляциях CD4+ и/или CD8+ T-клеток. См., например, Milone et al., Molecular Therapy 17(8): 1453-1464 (2009). В качестве альтернативы, смесь CD4+ и CD8+ Т-клеток стимулируют с помощью магнитных микрогранул, покрытых αCD3/αCD28, в день 0 и трансдуцируют с помощью CAR в день 1 с использованием бицистронного лентивирусного вектора, экспрессирующего CAR вместе с eGFP с использованием последовательности 2A для "проскока" рибосомы. После промывания культуры повторно стимулируют с помощью одного из клеток K562, положительных+по антигену, ассоциированному с раком, описанному в данном документе (K562, экспрессирующих антиген, ассоциированный с раком, описанный в данном документе), клеток K562 дикого типа (K562 дикого типа) или клеток K562, экспрессирующих hCD32 и 4-1BBL в присутствии антитела к CD3 и к CD28 (K562-BBL-3/28). Экзогенный IL-2 добавляют в культуры раз в два дня из расчета 100 МЕ/мл. GFP+ Т-клетки подсчитывают с помощью проточной цитометрии с использованием подсчета по микрогранулам. См., например, Milone et al., Molecular Therapy 17(8): 1453-1464 (2009).
Также можно измерить устойчивое размножение T-клеток, положительных+ по слитому полипептиду, например, описанному в данном документе, содержащему домен, который содержит CAR, например, CAR+, в отсутствие повторной стимуляции. См., например, Milone et al., Molecular Therapy 17(8): 1453-1464 (2009). Вкратце, измеряют средний объем Т-клеток (фл) в день 8 культивирования с использованием счетчика частиц Coulter Multisizer III, Nexcelom Cellometer Vision или Millipore Scepter после стимуляции с помощью магнитных микрогранул, покрытых αCD3/αCD28, в день 0 и трансдукции с помощью указанного CAR в день 1.
Для измерения активности CART также можно использовать животные модели. Например, можно использовать ксенотрансплантатную модель с использованием CAR+ Т-клеток человека, специфических в отношении антигена, ассоциированного с раком, описанного в данном документе, для лечения первичного пре-B ALL человека у иммунодефицитных мышей. См., например, Milone et al., Molecular Therapy 17(8): 1453-1464 (2009). Очень коротко, после развития ALL мышей рандомизируют в группы лечения. Различные количества сконструированных T-клеток с CAR, специфическим в отношении антигена, ассоциированного с раком, совместно вводят инъекцией при соотношении 1:1 мышам NOD-SCID-γ−/−, несущим B-ALL. Количество копий вектора, кодирующего CAR, специфический в отношении антигена, ассоциированного с раком, в ДНК селезенки мышей оценивают в различные моменты времени после инъекции T-клеток. Животных оценивают в отношении лейкоза с интервалами в одну неделю. Количество бластных клеток B-ALL, положительных+по антигену, ассоциированному с раком, описанному в данном документе, в периферической крови измеряют у мышей, которым инъецируют ζ CAR+ T-клетки, нацеливающиеся на антиген, ассоциированный с раком, описанный в данном документе, или ложнотрансдуцированные Т-клетки. Кривые выживания для групп сравнивают с использованием логарифмического рангового критерия. Кроме того, также можно анализировать абсолютное количество CD4+ и CD8+ T-клеток в периферической крови через 4 недели после инъекции Т-клеток мышам NOD-SCID-γ−/−. Мышам инъецируют лейкозные клетки и через 3 недели инъецируют Т-клетки, сконструированные для экспрессии CAR с помощью бицистронного лентивирусного вектора, который кодирует CAR, связанный с eGFP. Перед инъекцией Т-клетки нормализуют до 45-50% вводимых GFP+ Т-клеток путем смешивания с ложнотрансдуцированными клетками и подтверждают с помощью проточной цитометрии. Животных оценивают в отношении лейкоза с интервалами в 1 неделю. Кривые выживания для групп, получавших CAR+ T-клетки, сравнивают с использованием логарифмического рангового критерия.
Можно оценить дозозависимый ответ на обработку слитым полипептидом, например, описанным в данном документе, содержащем домен, который содержит CAR. См., например, Milone et al., Molecular Therapy 17(8): 1453-1464 (2009). Например, периферическую кровь собирают через 35-70 дней после развития лейкоза у мышей, которым в день 21 инъецировали Т-клетки с CAR, эквивалентное количество ложнотрансдуцированных Т-клеток или не инъецировали Т-клетки. У мышей из каждой группы, выбранных случайным образом, собирают кровь для определения в периферической крови количества бластных клеток ALL, положительных+по антигену, ассоциированному с раком, описанному в данном документе, а затем их умерщвляют в дни 35 и 49. Остальных животных оценивают в дни 57 и 70.
Оценка клеточной пролиферации и продуцирования цитокинов была описана ранее, например, в Milone et al., Molecular Therapy 17(8): 1453-1464 (2009). Вкратце, оценку CAR-опосредованной пролиферации выполняют в микротитровальных планшетах путем смешивания промытых Т-клеток с клетками K562, экспрессирующими антиген, ассоциированный с раком, описанный в данном документе (K19), или CD32 и CD137 (KT32-BBL), с достижением конечного соотношения T-клетки:K562, составляющего 2:1. До применения клетки K562 облучают гамма-излучением. Моноклональные антитела к CD3 (клон OKT3) и к CD28 (клон 9.3) добавляют в культуры с клетками KT32-BBL, которые служат в качестве положительного контроля, для стимуляции пролиферации T-клеток, поскольку эти сигналы поддерживают долгосрочное размножение CD8+ T-клеток ex vivo. Т-клетки подсчитывают в культурах с применением флуоресцентных микрогранул CountBright ™ (Invitrogen, Carlsbad, CA) и проточной цитометрии, как описано производителем. CAR+ Т-клетки идентифицируют по экспрессии GFP, при этом используют T-клетки, которые сконструированы с помощью лентивирусных векторов, экспрессирующих CAR, связанные с eGFP-2A. В случае CAR+ Т-клеток, не экспрессирующих GFP, CAR+ Т-клетки выявляют с помощью биотинилированного рекомбинантного белка антигена, ассоциированного с раком, описанного в данном документе, и конъюгата вторичного антитела и авидина-РЕ. Экспрессию CD4+ и CD8+ на Т-клетках также одновременно выявляют с помощью специфических моноклональных антител (BD Biosciences). Измерения уровней цитокинов выполняют в надосадочных жидкостях, собранных через 24 часа после повторной стимуляции, с применением набора Cytometric Bead Array (BD Biosciences, Сан Диего, Калифорния) для определения цитокинов TH1/TH2 человека в соответствии с инструкциями производителя. Флуоресценцию оценивают с применением проточного цитометра FACScalibur и данные анализируют в соответствии с инструкциями производителя.
Цитотоксичность можно оценивать с помощью стандартного анализа высвобождения 51Cr. См., например, Milone et al., Molecular Therapy 17(8): 1453-1464 (2009). Вкратце, клетки-мишени (линии K562 и первичные клетки про-B-ALL) нагружают 51Cr (в виде NaCrO4, New England Nuclear, Бостон, Массачусетс) при 37°C в течение 2 часов при частом взбалтывании, дважды промывают в полной RPMI и высевают на микротитровальные планшеты. Эффекторные Т-клетки смешивают с клетками-мишенями в лунках в полной RPMI при варьирующихся соотношениях эффекторная клетка:клетка-мишень (E:T). Также готовят дополнительные лунки, содержащие только среду (спонтанное высвобождение, SR) или 1% раствор поверхностно-активного вещества тритон-X 100 (суммарное высвобождение, TR). После 4 часов инкубации при 37°C из каждой лунки собирают надосадочную жидкость. Затем высвобожденный 51Cr измеряют с использованием счетчика гамма-частиц (Packard Instrument Co., Уолтем, Массачусетс). Каждое из условий осуществляют по меньшей мере в трех повторностях и вычисляют процентную долю лизиса с использованием формулы: % лизиса = (ER - SR)/(TR - SR), где ER представляет собой среднее значение 51Cr, высвобожденного при каждом экспериментальном условии.
Для оценки специфической миграции и пролиферации CAR на животных моделях, несущих опухоль, можно использовать технологии визуализации. Такие анализы были описаны, например, в Barrett et al., Human Gene Therapy 22:1575-1586 (2011). Вкратце, мышам NOD/SCID/γc-/- (NSG) IV инъецируют клетки Nalm-6 с последующей инъекцией через 7 дней Т-клеток спустя 4 часа после электропорации с помощью конструкций CAR. Т-клетки стабильно трансфицируются лентивирусной конструкцией с экспрессией люциферазы светлячка, и мышей фотографируют для визуализации биолюминесценции. В качестве альтернативы, терапевтическую эффективность и специфичность однократной инъекции CAR+ Т-клеток на ксенотрансплантатной модели Nalm-6 можно измерять следующим образом. Мышам NSG инъецируют Nalm-6, трансдуцированные для обеспечения стабильной экспрессии люциферазы светлячка, а затем через 7 дней в хвостовую вену вводят однократной инъекцией Т-клетки, подвергнутые электропорации с помощью CAR по настоящему изобретению. Животных фотографируют для визуализации в разные моменты времени после инъекции. Например, можно получить тепловые карты плотности фотонов для лейкоза, положительного по люциферазе светлячка, у репрезентативных мышей в день 5 (за 2 дня до обработки) и в день 8 (через 24 часа после введения CAR+ PBL).
Другие анализы, включая анализы, описанные в данном документе в разделе "Примеры", а также анализы, которые известны из уровня техники, также можно применять для оценки CAR, описанных в данном документе.
Способы получения клеток, экспрессирующих CAR
В другом аспекте настоящее изобретение относится к способу получения клетки (например, иммунной эффекторной клетки или их популяции), предусматривающему введение (например, трансдукцию) в клетку, например, T-клетку или NK клетку, описанную в данном документе, вектора, содержащего нуклеиновую кислоту, кодирующую слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR, например, CAR, описанный в данном документе; или нуклеиновую кислоту, кодирующую молекулу CAR, например, CAR, описанного в данном документе.
Клетка в данных способах представляет собой иммунную эффекторную клетку (например, T-клетку, или NK-клетку, или их комбинацию). В некоторых вариантах осуществления клетка в данных способах является дефицитной по диаглицеринкиназе (DGK) и/или Ikaros.
В некоторых вариантах осуществления введение молекулы нуклеиновой кислоты, кодирующей CAR, предусматривает трансдукцию вектора, содержащего молекулу нуклеиновой кислоты, кодирующую слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR, или трансфекцию молекулы нуклеиновой кислоты, кодирующей CAR, где молекула нуклеиновой кислоты представляет собой транскрибированную in vitro РНК.
В некоторых вариантах осуществления способ дополнительно предусматривает:
получение популяции иммунных эффекторных клеток (например, T-клеток или NK-клеток); и
удаление регуляторных T-клеток из популяции, за счет чего получают популяцию, истощенную по регуляторным T-клеткам;
где стадии a) и b) выполняют до введения нуклеиновой кислоты, кодирующей слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR, в популяцию.
В вариантах осуществления способов регуляторные T-клетки содержат CD25+ T-клетки, и их удаляют из популяции клеток с применением антитела к CD25 или его фрагмента. Антитело к CD25 или его фрагмент могут быть конъюгированы с субстратом, например, микрогранулой.
В других вариантах осуществления популяция, истощенная по регуляторным T-клеткам, полученная на стадии (b), содержит менее 30%, 25%, 20%, 15%, 10%, 5%, 4%, 3%, 2%, 1% CD25+ клеток.
В других вариантах осуществления способ дополнительно предусматривает удаление из популяции клеток, которые экспрессируют опухолевый антиген и не содержат CD25, с получением популяции, истощенной по регуляторным T-клеткам и клеткам с опухолевым антигеном, до введения нуклеиновой кислоты, кодирующей слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR, в популяцию. Опухолевый антиген может быть выбран из CD19, CD30, CD38, CD123, CD20, CD14 или CD11b, или их комбинации.
В других вариантах осуществления способ дополнительно предусматривает удаление из популяции клеток, которые экспрессируют ингибитор контрольных точек иммунного ответа, с получением популяции, истощенной по регуляторным T-клеткам и истощенных по ингибирующей молекуле, до введения нуклеиновой кислоты, кодирующей слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR, в популяцию. Ингибитор контрольных точек иммунного ответа может быть выбран из PD-1, LAG-3, TIM3, B7-H1, CD160, P1H, 2B4, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), TIGIT, CTLA-4, BTLA и LAIR1.
Дополнительный варианты осуществления, раскрытые в данном документе, охватывают получение популяции иммунных эффекторных клеток. Получаемая популяция иммунных эффекторных клеток может быть выбрана на основании экспрессии одного или нескольких из CD3, CD28, CD4, CD8, CD45RA и/или CD45RO. В определенных вариантах осуществления получаемая популяция иммунных эффекторных клеток представляет собой CD3+ и/или CD28+ клетки.
В определенных вариантах осуществления способа способ дополнительно предусматривает размножение популяции клеток после введения молекулы нуклеиновой кислоты, кодирующей слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR.
В вариантах осуществления популяцию клеток размножают в течение периода 8 дней или менее.
В определенных вариантах осуществления популяцию клеток размножают в культуре в течение 5 дней, и полученные клетки являются более активными, чем те же самые клетки, размножаемые в культуре в течение 9 дней при тех же условиях культивирования..
В других вариантах осуществления популяция клеток, размножаемых в течение 5 дней, демонстрирует по меньшей мере одно-, двух-, трех- или четырехкратное увеличение скорости удвоения клеток после стимуляции антигеном по сравнению с теми же клетками, размножаемыми в культуре в течение 9 дней при тех же условиях культивирования.
В еще одних вариантах осуществления популяцию клеток размножают в культуре в течение 5 дней, и полученные клетки демонстрируют более высокие уровни провоспалительных IFN-γ и/или GM-CSF по сравнению с теми же клетками, размножаемыми в культуре в течение 9 дней при тех же условиях культивирования.
В других вариантах осуществления популяцию клеток размножают путем культивирования клеток в присутствии средства, которое стимулирует сигнал, ассоциированный с комплексом CD3/TCR, и/или лигандом, который стимулирует костимулирующую молекулу на поверхности клеток. Средство может представлять собой микрогранулу, конъюгированную с антителом к CD3 антитело или его фрагментом и/или антителом к CD28 или его фрагментом.
В других вариантах осуществления популяцию клеток размножают в соответствующей среде, содержащей один или несколько интерлейкинов, что приводит к по меньшей мере 200-кратному, 250-кратному, 300-кратному или 350-кратному увеличению количества клеток в течение 14-дневного периода размножения, например, как измерено с помощью проточной цитометрии.
В других вариантах осуществления популяцию клеток размножают в присутствии IL-15 и/или IL-7.
В определенных вариантах осуществления способ дополнительно включает криоконсервацию популяции клеток после соответствующего периода размножения.
В других вариантах осуществления раскрытый в данном документе способ получения дополнительно предусматривает приведение популяции иммунных эффекторных клеток в контакт с нуклеиновой кислотой, кодирующей субъединицу теломеразы, например, hТРЕТ. Нуклеиновая кислота, кодирующая субъединицу теломеразы, может представлять собой ДНК.
В настоящем изобретении также представлен способ получения популяции РНК-сконструированных клеток, например клеток, описанных в данном документе, например, иммунных эффекторных клеток (например, Т-клеток, NK клеток), транзиентно экспрессирующих экзогенную РНК. Способ предусматривает введение транскрибированной in vitro РНК или синтетической РНК в клетку, при этом РНК содержит нуклеиновую кислоту, кодирующую слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит молекулу CAR, описанную в данном документе.
В другом аспекте, настоящее изобретение относится к способу обеспечения противоопухолевого иммунитета у субъекта, предусматривающему введение субъекту эффективного количества клетки, содержащий слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит молекулу CAR, например, клетки, экспрессирующей молекулу CAR описанную в данном документе. В одном варианте осуществления клетка представляет собой аутологичную T-клетку или NK-клетку. В одном варианте осуществления клетка представляет собой аллогенную T-клетку или NK-клетку. В одном варианте осуществления субъект является человеком.
В одном аспекте, настоящее изобретение предусматривает популяцию аутологичных клеток, которые трансфицированы или трансдуцированы с помощью вектора, содержащего молекулу нуклеиновой кислоты, кодирующую слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит молекулу CAR, например, описанную в данном документе. В одном варианте осуществления вектор представляет собой ретровирусный вектор. В одном варианте осуществления вектор представляет собой самоинактивирующийся лентивирусный вектор, описанный в другом разделе в данном документе. В одном варианте осуществления вектор доставляется (например, путем трансфекции или электропорации) в клетку, например, T-клетку или NK-клетку, при этом вектор содержит молекулу нуклеиновой кислоты, кодирующей CAR по настоящему изобретению, описанный в данном документе, которая транскрибируется в виде молекулы мРНК, и CAR по настоящему изобретению транслируются с молекулы РНК и экспрессируются на поверхности клетки.
В другом аспекте настоящего изобретения представлена популяция клеток, экспрессирующих слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR, например, CAR-экспрессирующих иммунных эффекторных клеток (например, T-клеток или NK-клеток). В некоторых вариантах осуществления популяция клеток, экспрессирующих CAR, содержит смесь клеток, экспрессирующих различные CAR. Например, в одном варианте осуществления популяция CAR-экспрессирующих иммунных эффекторных клеток (например, T-клеток или NK клеток) может содержать первую клетку, экспрессирующую CAR, имеющий антиген-связывающий домен, который связывается с первым опухолевым антигеном, описанным в данном документе, и вторую клетку, экспрессирующую CAR, имеющий другой антигенсвязывающий домен, который связывается со вторым опухолевым антигеном, описанным в данном документе. В качестве другого примера, популяция клеток, экспрессирующих CAR, может содержать первую клетку, экспрессирующую CAR, который содержит антигенсвязывающий домен, который связывается с опухолевым антигеном, описанным в данном документе, и вторую клетку, экспрессирующую CAR, который содержит антигенсвязывающий домен для мишени, отличной от опухолевого антигена, описанного в данном документе. В одном варианте осуществления популяция клеток, экспрессирующих CAR, содержит, например, первую клетку, экспрессирующую CAR, который содержит первичный внутриклеточный сигнальный домен, и вторую клетку, экспрессирующую CAR, который содержит вторичный сигнальный домен, например, костимулирующий сигнальный домен.
В другом аспекте настоящего изобретения представлена популяция клеток, где по меньшей мере одна клетка в популяции экспрессирует слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR, имеющий антигенсвязывающий домен, который связывается с опухолевым антигеном, описанный в данном документе, и вторая клетка экспрессирует другое средство, например, средство, которое усиливает активность клетки, экспрессирующей CAR. Например, в одном варианте осуществления средство может представлять собой средство, которое ингибирует ингибирующую молекулу. Примеры ингибирующих молекул включают PD-1, PD-L1, CTLA-4, TIM-3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG-3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4 и TGFR-бета. В одном варианте осуществления средство, которое ингибирует ингибирующую молекулу, например, представляет собой молекулу, описанную в данном документе, например, средство, которое содержит первый полипептид, например, ингибирующую молекулу, ассоциированный со вторым полипептидом, который обеспечивает положительный сигнал для клетки, например, внутриклеточный сигнальный домен, описанный в данном документе. В одном варианте осуществления средство содержит первый полипептид, например, ингибирующую молекулу, такую как PD-1, LAG-3, CTLA-4, CD160, BTLA, LAIR1, TIM-3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), 2B4 и TIGIT или фрагмент любого из них, и второй полипептид, который представляет собой внутриклеточный сигнальный домен, описанный в данном документе (например, содержащий костимулирующий домен (например, 41BB, CD27 или CD28, например, описанные в данном документе) и/или первичный сигнальный домен (например, сигнальный домен CD3-дзета, описанный в данном документе)). В одном варианте осуществления средство содержит первый полипептид, представляющий собой PD-1 или его фрагмент, и второй полипептид, представляющий собой внутриклеточный сигнальный домен, описанный в данном документе (например, сигнальный домен CD28, CD27, OX40 или 4-IBB, описанные в данном документе, и/или сигнальный домен CD3-дзета, описанный в данном документе).
В одном варианте осуществления молекула нуклеиновой кислоты, кодирующая слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR по настоящему изобретению, например, описанный в данном документе, экспрессируется в виде молекулы мРНК. В одном варианте осуществления генетически модифицированные клетки, экспрессирующие CAR по настоящему изобретению, например, иммунные эффекторные клетки (например, T-клетки, NK-клетки), могут быть получены путем трансфекции или электропорации молекулы РНК, кодирующей необходимые CAR (например, без последовательности вектора), в клетку. В одном варианте осуществления CAR по настоящему изобретению транслируется с молекулы РНК после ее введения и экспрессируется на поверхности рекомбинантной клетки.
Способ получения мРНК для применения в трансфекции предусматривает in vitro транскрипцию (IVT) матрицы с помощью специально разработанных праймеров с последующим добавлением поли(А) с получением конструкции, содержащей 3'- и 5'-нетранслируемую последовательность ("UTR") (например, 3'- и/или 5'-UTR, описанный в данном документе), 5'-кэп (например, 5'-кэп, описанный в данном документе) и/или участок внутренней посадки рибосомы (IRES) (например, IRES, описанный в данном документе), нуклеиновую кислоту, подлежащей экспрессии, и поли(A)-хвост, обычно длиной 50-5000 оснований (SEQ ID NO: 174). С помощью РНК, полученной таким образом, можно эффективно трансфицировать различные типы клеток. В одном варианте осуществления матрица включает последовательности для слитого полипептида, например, описанного в данном документе, содержащего домен, который содержит CAR. В одном варианте осуществления РНК-вектор для слитого полипептида, например, описанного в данном документе, содержащего домен, который содержит CAR, трансдуцируют в клетку, например, T-клетку или NK-клетку, посредством электропорации.
В одном варианте осуществления слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR, вводят в иммунные эффекторные клетки (например, T-клетки, NK-клетки), например, с применением транскрипции in vitro, и субъекту (например, человеку) осуществляют первоначальное введение иммунных эффекторных клеток (например, T-клеток, NK-клеток) по настоящему изобретению, содержащих слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR, и одно или несколько последующих введений иммунных эффекторных клеток (например, T-клеток, NK-клеток) по настоящему изобретению, содержащих слитый полипептид, например, описанный в данном документе, содержащий домен, который содержит CAR, где одно или несколько последующих введений осуществляют через менее чем 15 дней, например, 14, 13, 12, 11, 10, 9, 8, 7, 6, 5, 4, 3 или 2 дня после предыдущего введения. В одном варианте осуществления субъекту (например, человеку) осуществляют более одного введения иммунных эффекторных клеток с CAR (например, T-клеток, NK-клеток) по настоящему изобретению в неделю, например, осуществляют 2, 3 или 4 введения иммунных эффекторных клеток с CAR (например, T-клеток, NK-клеток) по настоящему изобретению в неделю. В одном варианте осуществления субъекту (например, субъекту-человеку) осуществляют более одного введения иммунных эффекторных клеток с CAR (например, T-клеток, NK-клеток) в неделю (например, 2, 3 или 4 введения в неделю) (также называется в данном документе циклом) с последующим отсутствием введения иммунных эффекторных клеток с CAR (например, T-клеток, NK-клеток) в течение недели, и затем субъекту осуществляют одно или несколько дополнительных введений иммунных эффекторных клеток с CAR (например, T-клеток, NK-клеток) (например, более одного введения иммунных эффекторных клеток с CAR (например, T-клеток, NK-клеток) в неделю). В другом варианте осуществления субъекту (например, субъекту-человеку) осуществляют более одного цикла введения иммунных эффекторных клеток с CAR (например, T-клеток, NK-клеток), и период времени между каждым циклом составляет менее 10, 9, 8, 7, 6, 5, 4 или 3 дней. В одном варианте осуществления иммунные эффекторные клетки с CAR (например, T-клетки, NK-клетки) вводят раз в два дня c 3 введениями в неделю. В одном варианте осуществления иммунные эффекторные клетки с CAR (например, T-клетки, NK-клетки) по настоящему изобретению вводят в течение по меньшей мере двух, трех, четырех, пяти, шести, семи, восьми или более недель.
В одном аспекте клетки, экспрессирующие CAR, получают с применением лентивирусных вирусных векторов, таких как лентивирус. Клетки, например, CART, полученные таким способом, будут характеризоваться стабильной экспрессией CAR.
В одном аспекте клетки, экспрессирующие CAR, например, CART, получают с применением вирусного вектора, такого как гамма-ретровирусный вектор, например, гамма-ретровирусный вектор, описанный в данном документе. CART, полученные с применением таких векторов, могут характеризоваться стабильной экспрессией CAR.
В одном аспекте CART транзиентно экспрессируют векторы, кодирующие CAR, в течение 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 дней после трансдукции. Транзиентная экспрессия CAR может осуществляться с помощью доставки вектора на основе РНК CAR. В одном аспекте РНК CAR трансдуцируют в T-клетку посредством электропорации.
Потенциальная проблема, которая может возникнуть у пациентов, лечение которых осуществляют с применением иммунных эффекторных клеток (например, T-клеток, NK-клеток), транзиентно экспрессирующих CAR (в частности, CART, несущих scFv мыши), представляет собой анафилаксию после нескольких циклов лечения.
Не ограничиваясь данной теорией, полагают, что такой анафилактический ответ может быть вызван тем, что у пациента развивается гуморальный ответ против CAR, т. е. антитела к CAR, имеющие изотип IgE. Считается, что в клетках пациента, продуцирующих антитела, происходит переключение класса с изотипа IgG (который не вызывает анафилаксии) на изотип IgE, если между воздействиями антигена существует перерыв продолжительностью от десяти до четырнадцати дней. Если у пациента имеется высокий риск формирования ответа в виде антитела к CAR во время курса терапии с транзиентными CAR (такими как образуемые при трансдукциях РНК), то перерывы между инфузиями CART не должны длиться более десяти - четырнадцати дней.
Фармацевтическая композиция
Фармацевтические композиции по настоящему изобретению могут содержать любой слитый полипептид, нуклеиновую кислоту, кодирующую такой слитый полипептид, или клетки, содержащие слитый полипептид, описанный в данном документе, и один или несколько фармацевтически или физиологически приемлемых носителей, разбавителей или вспомогательных веществ. Такие композиции могут содержать буферы, такие как нейтральный буферный солевой раствор, фосфатно-солевой буферный раствор и т. п.; углеводы, такие как глюкоза, манноза, сахароза или декстраны, маннит; белки; полипептиды или аминокислоты, такие как глицин; антиоксиданты; хелатирующие средства, такие как EDTA или глутатион; адъюванты (например, гидроксид алюминия) и консерванты. В одном аспекте композиции по настоящему изобретению составляют для внутривенного введения.
Фармацевтические композиции по настоящему изобретению можно вводить с помощью способа, отвечающего требованиям к лечению (или предупреждению) данного заболевания. Количество и частота введения будут определяться такими факторами, как состояние пациента, а также тип и тяжесть заболевания пациента, хотя подходящие дозировки могут быть определены с помощью клинических испытаний.
В одном аспекте настоящего изобретения предусмотрена фармацевтическая композиция, составленная для применения в способе, описанном в данном документе, при этом композиция содержит модифицированную T-клетку, содержащую нуклеиновую кислоту, кодирующую "суицидальный" ген, и нуклеиновую кислоту, кодирующую химерный антигенный рецептор, содержащий домен, связывающий B-клетку, трансмембранный домен, костимулирующий домен и внутриклеточный сигнальный домен.
В другом аспекте настоящего изобретения предусмотрена фармацевтическая композиция, составленная для применения в способе, описанном в данном документе, при этом композиция содержит модифицированную T-клетку, содержащую нуклеиновую кислоту, кодирующую домен димеризации и химерный антигенный рецептор (CAR), содержащий домен, связывающий B-клетку, трансмембранный домен, костимулирующий домен и внутриклеточный сигнальный домен
В одном варианте осуществления фармацевтическая композиция практически не содержит, например, в ней отсутствуют выявляемые уровни загрязнителя, например, выбранного из группы, состоящей из эндотоксина, микоплазмы, способного к репликации лентивируса (RCL), p24, нуклеиновой кислоты VSV-G, gag HIV, остаточных количеств микрогранул, покрытых антителами к CD3/антителами к CD28, антител мыши, объединенной сыворотки крови человека, бычьего сывороточного альбумина, бычьей сыворотки крови, компонентов сред для культивирования, клеточных или плазмидных компонентов для упаковки векторов, бактерии и гриба. В одном варианте осуществления бактерия представляет собой по меньшей мере бактерию, выбранную из группы, состоящей из Alcaligenes faecalis, Candida albicans, Escherichia coli, Haemophilus influenzae, Neisseria meningitidis, Pseudomonas aeruginosa, Staphylococcus aureus, Streptococcus pneumoniae и Streptococcus pyogenes группы A.
В случае, если указано "иммунологически эффективное количество", "эффективное противоопухолевое количество", "количество, эффективное для ингибирования опухоли" или "терапевтическое количество", точное количество композиций по настоящему изобретению, подлежащих введению, может быть определено врачом с учетом индивидуальных различий в возрасте, массе тела, размере опухоли, степени инфекции или метастазирования и состояния пациента (субъекта). В целом, можно отметить, что фармацевтическую композицию, содержащую иммунные эффекторные клетки (например, T-клетки, NK-клетки), описанные в данном документе, можно вводить в дозе от 104 до 109 клеток/кг массы тела, в некоторых случаях от 105 до 106 клеток/кг массы тела, с включением всех целочисленных значений в пределах данных диапазонов. Композиции на основе Т-клеток можно также вводить несколько раз в этих дозах. Клетки можно вводить с помощью методик инфузии, которые являются общеизвестными в иммунотерапии (см., например, Rosenberg et al., New Eng. J. of Med. 319:1676, 1988).
В определенных аспектах субъекту может потребоваться введение активированных иммунных эффекторных клеток (например, T-клеток, NK-клеток), и тогда последовательно повторно берут кровь (или осуществляют аферез), активируют иммунные эффекторные клетки (например, T-клетки, NK-клетки) из нее в соответствии с настоящим изобретением и проводят повторную инфузию этих активированных и размноженных иммунных эффекторных клеток (например, T-клеток, NK-клеток) пациенту. Этот процесс можно осуществлять несколько раз с интервалом в несколько недель. В определенных аспектах иммунные эффекторные клетки (например, T-клетки, NK-клетки) можно активировать из образцов крови объемом от 10 куб. см до 400 куб. см. В определенных аспектах иммунные эффекторные клетки (например, T-клетки, NK-клетки) активируют из образцов крови объемом 20 куб. см, 30 куб. см, 40 куб. см, 50 куб. см, 60 куб. см, 70 куб. см, 80 куб. см, 90 куб. см или 100 куб. см.
Введение заявленных композиций можно осуществлять с помощью любого подходящего способа, в том числе аэрозольной ингаляции, инъекции, приема внутрь, трансфузии, имплантации или трансплантации. Композиции, описанные в данном документе, можно вводить пациенту трансартериально, подкожно, внутрикожно, интратуморально, интранодально, интрамедуллярно, внутримышечно, с помощью внутривенной (i.v.) инъекции или внутрибрюшинно. В одном аспекте композиции на основе клеток по настоящему изобретению вводят пациенту с помощью внутрикожной или подкожной инъекции. В одном аспекте композиции по настоящему изобретению вводят с помощью i.v. инъекции. Композиции на основе иммунных эффекторных клеток (например, T-клеток, NK-клеток) можно инъецировать непосредственно в опухоль, лимфатический узел или очаг инфекции.
В конкретном иллюстративном аспекте субъекта можно подвергать лейкаферезу, при этом лейкоциты собирают, обогащают или истощают ex vivo, чтобы отбирать и/или выделять представляющие интерес клетки, например, T-клетки. Эти изоляты Т-клеток можно размножать с помощью способов, известных из уровня техники, и обрабатывать таким образом, чтобы можно было ввести одну или несколько конструкций CAR по настоящему изобретению, за счет чего обеспечивают создание T-клеток с CAR по настоящему изобретению. Затем субъектов, нуждающихся в этом, можно подвергать стандартному лечению с помощью высокодозной химиотерапии с последующей трансплантацией стволовых клеток периферической крови. В определенных аспектах после трансплантации или параллельно с ней субъектам осуществляют инфузию размноженных T-клеток с CAR по настоящему изобретению. В дополнительном аспекте размноженные клетки вводят до или после хирургического вмешательства.
Доза вышеуказанных средств лечения, подлежащих введению пациенту, будет варьироваться в зависимости от точной природы состояния, подлежащего лечению, и реципиента средства лечения. Определение дозы для введения человеку можно осуществлять в соответствии с практикой, принятой в данной области техники.
Способы селективно регуляции экспрессии слитого полипептида
В данном документе также представлены способы селективной регуляции (например, деградации) слитого полипептида (например, слитого полипептида, содержащего COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид и гетерологичный полипептид, например, полипептид CAR). Такие способы могут включать приведение клетки, содержащей любой из слитых полипептидов, описанных в данном документе, или нуклеиновую кислоту, кодирующую такой слитый полипептид, в контакт с COF1, COF2 или COF3. В некоторых вариантах осуществления COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид увеличивает посттрансляционную модификацию и/или деградацию слитого полипептида в присутствии COF1, COF2 или COF3, например, относительно модификации и/или деградации в отсутствие COF1, COF2 или COF3. В одном варианте осуществления COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид увеличивает селективное убиквитинирование слитого полипептида в присутствии COF1, COF2 или COF3, например, относительно убиквитинирования в отсутствие COF1, COF2 или COF3. В некоторых вариантах осуществления клетку приводят в контакт с COF1, COF2 или COF3 in vivo. В некоторых вариантах осуществления клетку приводят в контакт с COF1, COF2 или COF3 ex vivo.
Используемая в данном документе "селективная деградация" слитого полипептида или полипептида-мишени и т. п. относится к увеличению деградации (например, повышению уровня и/или скорости деградации, например, на по меньшей мере 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 100%, 200%, 500%, в 10 раз, 100 раз, 1000 раз или более) слитого полипептида или полипептида мишени относительно эталонного полипептида, например, полипептида без COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающего полипептида.
Также в данном документе представлены способы селективной регуляции (например, деградации) слитого полипептида, содержащего COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид, гетерологичный полипептид и домен деградации. Такой способы предусматривают одну или несколько следующих стадий:
i) приведение слитого полипептида или клетки, содержащей слитый полипептид, в контакт со стабилизирующим соединением, необязательно, где в присутствии стабилизирующего соединения уровень экспрессии слитого полипептида увеличивается, например, в по меньшей мере 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, по сравнению с уровнем экспрессии слитого полипептида в отсутствие стабилизирующего соединения, например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии, и
ii) приведение слитого полипептида или клетки, содержащей слитый полипептид, в контакт с COF1, COF2 или COF3, необязательно, где в присутствии COF1, COF2 или COF3 уровень экспрессии слитого полипептида значительно уменьшается, например, на по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, или 100 процентов, относительно уровня экспрессии слитого полипептида после стадии i) и перед стадией ii), например, как измерено с помощью анализа, описанного в данном документе, например, вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
В другом аспекте настоящего изобретения представлены способы, предусматривающие введение слитого полипептида по настоящему изобретению в качестве средства терапии. Как правило, такое введение субъекту будет осуществляться в форме клеток (например, аутологичных или аллогенных клеток-хозяев), экспрессирующих слитый полипептид по настоящему изобретению. Соответственно, с помощью введения COF1, COF2 или COF3 (либо in vivo, либо ex vivo) можно контролировать экспрессию терапевтического средства (например, гетерологичного белка). Соответственно, с помощью введения COF1, COF2 или COF3 (либо in vivo, либо ex vivo) можно контролировать экспрессию терапевтического средства (например, гетерологичного белка). Таким образом, можно контролировать экспрессию известных синтетических терапевтических белков или трансмембранных рецепторов (например, слитого полипептида, например, описанного в данном документе, например, содержащего домен, который содержит молекулу CAR, описанную в данном документе). В одном варианте осуществления у субъекта имеется нарушение, описанное в данном документе, например, у субъекта имеется рак, например, у субъекта имеется раковые клетки, которые экспрессируют антиген-мишень, описанный в данном документе. В одном варианте осуществления субъект является человеком.
В данном документе представлены способы лечения субъекта, у которого имеется заболевание, ассоциированное с экспрессией опухолевого антигена, путем введения субъекту эффективного количества клетки, например, клетки-хозяина, содержащей любой из слитых полипептидов, описанных в данном документе, или нуклеиновую кислоту, кодирующую такой слитый полипептид. В некоторых вариантах осуществления слитый полипептид содержит химерный антигенный рецептор (CAR), который содержит, в направлении от N-конца к C-концу: антигенсвязывающий домен, который специфически связывает опухолевый антиген, трансмембранный домен и один или несколько внутриклеточных сигнальных доменов. В некоторых вариантах осуществления клетка-хозяин является аутологичной для субъекта. В некоторых вариантах осуществления клетка-хозяин является аллогенной для указанного субъекта. В некоторых вариантах осуществления клетку-хозяина приводят в контакт с COF1, COF2 или COF3.
В еще одном аспекте настоящего изобретения описан способ лечения субъекта, у которого имеется заболевание, ассоциированное с экспрессией опухолевого антигена (например, антигена, описанного в данном документе), предусматривающий введение субъекту эффективного количества клетки, например, иммунной эффекторной клетки (например, популяции иммунных эффекторных клеток), содержащей слитый полипептид, содержащий молекулу CAR, где молекула CAR содержит антигенсвязывающий домен, трансмембранный домен и внутриклеточный домен, причем указанный внутриклеточный домен содержит костимулирующий домен и/или первичный сигнальный домен, где указанный антигенсвязывающий домен связывается с опухолевым антигеном, ассоциированным с заболеванием, например опухолевым антигеном, описанным в данном документе.
В связанном аспекте настоящего изобретения описан способ лечения субъекта, у которого имеется заболевание, ассоциированного с экспрессией опухолевого антигена. Способ предусматривает введение субъекту эффективного количества клетки, например, иммунной эффекторной клетки (например, популяции иммунных эффекторных клеток), содержащих слитый полипептид, содержащий молекулу CAR, в комбинации со средством, которое увеличивает эффективность иммунной клетки, где:
средство, которое увеличивает эффективность иммунной клетки, выбрано из одного или нескольких из:
(i) ингибитора протеинфосфатазы;
(ii) ингибитора киназы;
(iii) цитокина;
(iv) ингибитора иммунной ингибирующей молекулы; или
(v) средства, которое снижает уровень или активность TREG-клетки.
В другом аспекте настоящего изобретения описана композиция, содержащая иммунную эффекторную клетку (например, популяцию иммунных эффекторных клеток), содержащую слитый полипептид, содержащий молекулу CAR (например, слитый полипептид, содержащий молекулу CAR, описанную в данном документе) для применения в лечении субъекта, у которого имеется заболевание, ассоциированное с экспрессией опухолевого антигена, например, нарушение, описанное в данном документе.
В определенных вариантах осуществления любого из вышеуказанных способов или путей применения заболевание, ассоциированное с опухолевым антигеном, например, опухолевым антигеном, описанным в данном документе, выбран из пролиферативного заболевания, такого как рак или злокачественное новообразование, или предракового состояния, такого как миелодисплазия, миелодиспластический синдром или предлейкоз, или являющееся не связанным с раком показанием, ассоциированным с экспрессией опухолевого антигена, описанного в данном документе. В одном варианте осуществления заболевание представляет собой рак, описанный в данном документе, например, рак, описанный в данном документе, являющийся ассоциированным с мишенью, описанной в данном документе. В одном варианте осуществления заболевание представляет собой гематологический рак.
В одном варианте осуществления гематологический рак представляет собой лейкоз. В одном варианте осуществления рак выбран из группы, состоящей из одной или нескольких форм острого лейкоза, включающих без ограничения B-клеточный острый лимфоидный лейкоз ("BALL"), T-клеточный острый лимфоидный лейкоз ("TALL"), острый лимфоидный лейкоз (ALL); одной или нескольких форм хронического лейкоза, включающих без ограничения хронический миелогенный лейкоз (CML), хронический лимфоцитарный лейкоз (CLL); дополнительных форм гематологического рака или гематологических состояний, включающих без ограничения B-клеточный пролимфоцитарный лейкоз, новообразование из бластных плазмоцитоидных дендритных клеток, лимфому Беркитта, диффузную В-крупноклеточную лимфому, фолликулярную лимфому, волосатоклеточный лейкоз, мелкоклеточную или крупноклеточную фолликулярную лимфому, злокачественные лимфопролиферативные состояния, MALT-лимфому, лимфому из клеток мантийной зоны, лимфому маргинальной зоны, множественную миелому, миелодисплазию и миелодиспластический синдром, неходжкинскую лимфому, лимфому Ходжкина, плазмобластную лимфому, новообразование из плазмоцитоидных дендритных клеток, макроглобулинемии Вальденстрема и "предлейкоз", который представляет собой разнородную совокупность гематологических состояний, объединенных неэффективным продуцированием (или дисплазией) миелоидных клеток крови, а также заболевания, ассоциированного с экспрессией опухолевого антигена, описанного в данном документе, включая без ограничения атипичные и/или неклассические формы рака, злокачественные опухоли, предраковые состояния или пролиферативные заболевания, экспрессирующие опухолевый антиген, описанный в данном документе; и их любой комбинации. В другом варианте осуществления заболевание, ассоциированное с опухолевым антигеном, описанным в данном документе, представляет собой солидную опухоль.
В определенных вариантах осуществления способы или пути применения проводят в комбинации со средством, которое увеличивает эффективность иммунной эффекторной клетки, например, средством, описанным в данном документе.
В любом из вышеуказанных способов или путей применения заболевание, ассоциированное с экспрессией опухолевого антигена, выбрано из группы, состоящей из пролиферативного заболевания, предракового состояния, рака и не связанного с раком показания, ассоциированного с экспрессией опухолевого антигена.
Рак может представлять собой гематологический рак, например, рак, выбранный из одного или нескольких из хронического лимфоцитарного лейкоза (CLL), форм острого лейкоза, острого лимфоидного лейкоза (ALL), B-клеточного острого лимфоидного лейкоза (B-ALL), T-клеточного острого лимфоидного лейкоза (T-ALL), хронического миелогенного лейкоза (CML), B-клеточного пролимфоцитарного лейкоза, новообразования из бластных плазмоцитоидных дендритных клеток, лимфомы Беркитта, диффузной В-крупноклеточной лимфомы, фолликулярной лимфомы, волосатоклеточного лейкоза, мелкоклеточной или крупноклеточной-фолликулярной лимфомы, злокачественных лимфопролиферативных состояний, MALT-лимфомы, лимфомы из клеток мантийной зоны, лимфомы маргинальной зоны, множественной миеломы, миелодисплазии и миелодиспластического синдрома, неходжкинской лимфомы, лимфомы Ходжкина, плазмобластной лимфомы, новообразования из плазмоцитоидных дендритных клеток, макроглобулинемии Вальденстрема или предлейкоза.
Рак также может быть выбран из группы, состоящей из рака толстой кишки, рака прямой кишки, почечно-клеточной карциномы, рака печени, немелкоклеточной карциномы легкого, рака тонкого кишечника, рака пищевода, меланомы, рака костей, рака поджелудочной железы, рака кожи, рака головы или шеи, кожной или внутриглазной злокачественной меланомы, рака матки, рака яичника, рака прямой кишки, рака анальной области, рака желудка, рака яичка, рака матки, карциномы фаллопиевых труб, карциномы эндометрия, карциномы шейки матки, карциномы влагалища, карциномы вульвы, болезни Ходжкина, неходжкинской лимфомы, рака эндокринной системы, рака щитовидной железы, рака паращитовидной железы, рака надпочечника, саркомы мягких тканей, рака уретры, рака полового члена, солидных опухолей детского возраста, рака мочевого пузыря, рака почки или мочеточника, карциномы почечной лоханки, новообразования в центральной нервной системы (ЦНС), первичной лимфомы ЦНС, ангиогенеза опухоли, опухоли спинного мозга, глиомы ствола головного мозга, аденомы гипофиза, саркомы Капоши, эпидермоидного рака, плоскоклеточного рака, T-клеточной лимфомы, форм рака, вызванных влиянием окружающей среды, комбинаций указанных форм рака и метастатических поражений при указанных формах рака.
В определенных вариантах осуществления способов или путей применения, описанных в данном документе, клетку вводят в комбинации со средством, которое увеличивает эффективность клетки, например, одним или несколькими их ингибитора протеинфосфатазы, ингибитора киназы, цитокина, ингибитора иммунной ингибирующей молекулы или средство, которое снижает уровень или активность TREG-клетки.
В определенных вариантах осуществления способов или путей применения, описанных в данном документе, ингибитор протеинфосфатазы, представляет собой ингибитор SHP-1 и/или ингибитор SHP-2.
В других вариантах осуществления способов или путей применения, описанных в данном документе, ингибитор киназы выбран из одного или нескольких из ингибитора CDK4, ингибитора CDK4/6 (например, палбоциклиба), ингибитора BTK (например, ибрутиниба или RN-486), ингибитора mTOR (например, рапамицина или эверолимуса (RAD001)), ингибитор MNK или двойного ингибитора P13K/mTOR. В одном варианте осуществления ингибитор BTK не снижает или не ингибирует киназную активность интерлейкин-2-индуцируемой киназы (ITK).
В других вариантах осуществления способов или путей применения, описанных в данном документе, средство, которое ингибирует иммунную ингибирующую молекулу, содержит антитело или фрагмент антитела, ингибирующую нуклеиновую кислоту, короткие палиндромные повторы, регулярно расположенные группами (CRISPR), эффекторную нуклеазу, подобную активаторам транскрипции (TALEN), или эндонуклеазу с "цинковыми пальцами" (ZFN), которые ингибируют экспрессию ингибирующей молекулы.
В других вариантах осуществления способов или путей применения, описанных в данном документе, средство, которое снижает уровень или активность TREG-клеток, выбрано из циклофосфамида, антитела к GITR, реагента для истощения по CD25 или их комбинации.
В определенных вариантах осуществления способов или путей применения, описанных в данном документе, иммунная ингибирующая молекула выбрана из группы, состоящей из PD1, PD-L1, CTLA-4, TIM-3, LAG-3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4, TGFR-бета, CEACAM-1, CEACAM-3 и CEACAM-5.
В других вариантах осуществления средство, которое ингибирует ингибирующую молекулу, содержит первый полипептид, содержащий ингибирующую молекулу или ее фрагмент, и второй полипептид, которые обеспечивают положительный сигнал для клетки, и где первый и второй полипептиды экспрессируются на иммунных клетках, содержащих CAR, где (i) первый полипептид содержит PD1, PD-L1, CTLA-4, TIM-3, LAG3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4, TGFR-бета, CEACAM-1, CEACAM-3 и CEACAM-5 или их фрагмент; и/или (ii) второй полипептид содержит внутриклеточный сигнальный домен, содержащий первичный сигнальный домен и/или костимулирующий сигнальный домен. В одном варианте осуществления первичный сигнальный домен содержит функциональный домен CD3-дзета; и/или костимулирующий сигнальный домен содержит функциональный домен белка, выбранного из 41BB, CD27 и CD28.
В других вариантах осуществления цитокин выбран из IL-7, IL-15, IL-18 или IL-21, или их комбинации.
В других вариантах осуществления иммунную эффекторную клетку, содержащую слитый полипептид, и второе средство, например, любой из видов комбинированной терапии, раскрытый в данном документе (например, средство, которое увеличивает эффективность иммунной эффекторной клетки), вводят практически одновременно или последовательно.
В других вариантах осуществления иммунную клетку, содержащую слитый полипептид, вводят в комбинации с молекулой, которая нацеливается на GITR и/или модулирует функцию GITR. В определенных вариантах осуществления молекулу, нацеливающуюся на GITR и/или модулирующую функцию GITR, вводят до клетки или популяции клеток, экспрессирующих CAR, или до афереза.
В одном варианте осуществления инфузию лимфоцитов, например инфузию аллогеннных лимфоцитов, применяют при лечении рака, где инфузия лимфоцитов содержит по меньшей мере одну клетку, экспрессирующую CAR по настоящему изобретению. В одном варианте осуществления инфузию аутологичных лимфоцитов применяют в лечении рака, где инфузия аутологичных лимфоцитов содержит по меньшей мере одну клетку, экспрессирующую CAR, описанный в данном документе.
В одном варианте осуществления клетка представляет собой T-клетку, и T-клетка является дефицитной по диаглицеринкиназе (DGK). В одном варианте осуществления клетка представляет собой T-клетку, T-клетка является дефицитной по Ikaros. В одном варианте осуществления клетка представляет собой T-клетку, и T-клетка является дефицитной как по DGK, так и по Ikaros.
В одном варианте осуществления способ включает введение клетки, экспрессирующей слитый полипептид, содержащий молекулу CAR, описанную в данном документе, в комбинации со средством, которое усиливает активность клетки, экспрессирующей CAR, где средство представляет собой цитокин, например, IL-7, IL-15, IL-18, IL-21 или их комбинацию. Цитокин может доставляться в комбинации с введением клетки, экспрессирующей CAR, например, одновременно или вскоре после него. В качестве альтернативы, цитокин может доставляться после продолжительного периода времени после введения клетки, экспрессирующей CAR, например, после оценки ответа субъекта на клетку, экспрессирующую CAR. В одном варианте осуществления цитокин вводят субъекту одновременно (например, вводят в тот же день) с введением клетки или популяции клеток, описанных в данном документе, или вскоре после него (например, вводят через 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней или 7 дней после введения). В других вариантах осуществления цитокин вводят субъекту после продолжительного периода времени (например, например, по меньшей мере 2 недель, 3 недель, 4 недель, 6 недель, 8 недель, 10 недель или более) после введения клетки или популяции клеток, описанных в данном документе или после оценки ответа субъекта на клетку.
В других вариантах осуществления клетки, экспрессирующие слитый полипептид, содержащий молекулу CAR, вводят в комбинации со средством, которое ослабляет один или несколько побочных эффектов, ассоциированных с введением клетки, экспрессирующей молекулу CAR. Побочные эффекты, ассоциированные с клеткой, экспрессирующей CAR, могут быть выбраны из синдрома высвобождения цитокинов (CRS) или гемофагоцитарного лимфогистиоцитоза (HLH).
В вариантах осуществления любого из вышеуказанных способов или путей применения клетки, экспрессирующие молекулу CAR, вводят в комбинации со средством, которое лечит заболевание, ассоциированное с экспрессией опухолевого антигена, например, с любым вторым или третьим видом терапии, раскрытым в данном документе.
Дополнительные иллюстративные комбинации включают одно или несколько следующего.
В другом варианте осуществления клетку, экспрессирующую молекулу CAR, например, описанную в данном документе, можно вводить в комбинации с другим средством, например, ингибитором киназы и/или ингибитором контрольных точек иммунного ответа, описанным в данном документе. В одном варианте осуществления клетка, экспрессирующая молекулу CAR, может дополнительно экспрессировать другое средство, например, средство, которое усиливает активность клетки, экспрессирующей CAR.
Например, в одном варианте осуществления средство, которое усиливает активность клетки, экспрессирующей CAR, может представлять собой средство, которое ингибирует ингибирующую молекулу (например, иммунную ингибирующую молекулу). Примеры ингибирующих молекул включают PD1, PD-L1, CTLA-4, TIM-3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG-3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4 и TGFR-бета.
В одном варианте осуществления средство, которое ингибирует ингибирующую молекулу, представляет собой ингибирующую нуклеиновую кислоту, dsRNA, siRNA или shRNA. В вариантах осуществления ингибирующая нуклеиновая кислота связана с нуклеиновой кислотой, которая кодирует компонент молекулы CAR. Например, ингибирующая молекула может экспрессироваться в клетке, экспрессирующей CAR.
В другом варианте осуществления средство, которое ингибирует ингибирующую молекулу, представляет собой молекулу, описанную в данном документе, например, средство, которое содержит первый полипептид, например, ингибирующую молекулу, ассоциированный со вторым полипептидом, который обеспечивает положительный сигнал для клетки, например, внутриклеточный сигнальный домен, описанный в данном документе. В одном варианте осуществления средство содержит первый полипептид, например, ингибирующую молекулу, такую как PD-1, PD-L1, CTLA-4, TIM-3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG-3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4 или TGFR-бета или фрагмент любой из них (например, по меньшей мере часть внеклеточного домена любой из них), и второй полипептид, который представляет собой внутриклеточный сигнальный домен, описанный в данном документе (например, содержащий костимулирующий домен (например, 41BB, CD27 или CD28, например, описанный в данном документе) и/или первичный сигнальный домен (например, сигнальный домен CD3-дзета, описанный в данном документе). В одном варианте осуществления средство содержит первый полипептид из PD1 или его фрагмент (например, по меньшей мере часть внеклеточного домена PD1) и второй полипептид из внутриклеточного сигнального домена, описанного в данном документе (например, сигнального домена CD28, описанного в данном документе, и/или сигнального домена CD3-дзета, описанного в данном документе).
В одном варианте осуществления клетку по настоящему изобретению, например, T-клетку или NK клетку, вводят субъекту, которому ранее провели трансплантацию стволовых клеток, например, трансплантацию аутологичных стволовых клеток.
В одном варианте осуществления клетку по настоящему изобретению, например, T-клетку или NK-клетку, вводят субъекту, который ранее получил дозу мелфалана.
В одном варианте осуществления клетку, экспрессирующую слитый полипептид, содержащий молекулу CAR, например, молекулу CAR, описанную в данном документе, вводят в комбинации со средством, которое увеличивает эффективность клетки, экспрессирующей молекулу CAR, например, средством, описанным в данном документе.
В одном варианте осуществления клетки, экспрессирующие слитый полипептид, содержащий молекулу CAR, например, молекулу CAR, описанную в данном документе, вводят в комбинации с низкой повышающей иммунитет дозой ингибитора mTOR. Без ограничения какой-либо теорией, полагают, что лечение с помощью низкой повышающей иммунитет дозы (например, дозы, которая является недостаточной, чтобы полностью подавить иммунную систему, но достаточной для улучшения иммунной функция) сопровождается уменьшением количества PD-1-положительных T-клеток или увеличением количества PD-1-отрицательных клеток. PD-1-положительные T-клетки, но не PD-1-отрицательные T-клетки, можно извлекать за счет взаимодействия с клетками, которые экспрессируют лиганд PD-1, например, PD-L1 или PD-L2.
В варианте осуществления данный подход может применяться у субъекта для оптимизации функциональных характеристик CAR-клеток, описанных в данном документе. Без ограничения какой-либо теорией, полагают, что в одном варианте осуществления функциональные характеристики эндогенных, немодифицированных иммунных эффекторных клеток, например Т-клеток или NK-клеток, улучшаются. Без ограничения какой-либо теорией, полагают, что, в одном варианте осуществления функциональные характеристики клетки, экспрессирующей CAR для антигена-мишени, улучшаются. В других вариантах осуществления клетки, например, T-клетки или NK-клетки, которые сконструированы или будут конструироваться для экспрессии CAR, можно обрабатывать ex vivo путем приведения в контакт с таким количеством ингибитора mTOR, которое увеличивает число PD1-отрицательных иммунных эффекторных клеток, например, T-клеток, или увеличивает соотношение PD1 отрицательных иммунных эффекторных клеток, например, T-клеток, и PD1-положительных иммунных эффекторных клеток, например, T-клеток.
В одном варианте осуществления введение низкой повышающей иммунитет дозы ингибитора mTOR, например, аллостерического ингибитора, например, RAD001, или каталитического ингибитора, начинают до введения описанной в данном документе клетки, экспрессирующей CAR, например, T-клеток или NK клеток. В одном варианте осуществления клетки с CAR вводят спустя достаточное количество времени или после достаточного введения дозы ингибитора mTOR так, чтобы уровень PD1-отрицательных иммунных эффекторных клеток, например, T-клеток или NK клеток, или соотношение PD1-отрицательных иммунных эффекторных клеток, например, T-клеток, и PD1-положительных иммунных эффекторных клеток, например, T-клеток, по меньшей мере временно были повышены.
В одном варианте осуществления клетку, например, T-клетку или NK-клетку, подлежащую конструированию для экспрессии CAR, собирают спустя достаточное количество времени или после достаточного введения низкой повышающей иммунитет дозы ингибитора mTOR так, чтобы уровень PD1-отрицательных иммунных эффекторных клеток, например, T-клеток, или соотношение PD1-отрицательных иммунных эффекторных клеток, например, T-клеток, и PD1-положительных иммунных эффекторных клеток, например, T-клеток, у субъекта или в клетках, собранных у субъекта, по меньшей мере временно были повышены.
В одном варианте осуществления клетку, экспрессирующую слитый полипептид, содержащий молекулу CAR, например, молекулу CAR, описанную в данном документе, вводят в комбинации со средством, которое ослабляет один или несколько побочных эффектов, ассоциированных с введением клетки, экспрессирующей молекулу CAR, например, средством, описанным в данном документе.
В одном варианте осуществления клетку, экспрессирующую слитый полипептид, содержащий молекулу CAR, например, молекулу CAR, описанную в данном документе, вводят в комбинации со средством, которое лечит заболевание, ассоциированное с антигеном, ассоциированным с раком, описанным в данном документе, например, средством, описанным в данном документе.
В одном варианте осуществления клетку, экспрессирующую два или более слитых полипептидов, содержащих молекулы CAR, например, описанные в данном документе, вводят субъекту, нуждающемуся в этом, для лечения рака. В одном варианте осуществления популяцию клеток, содержащих слитый полипептид содержащую клетку, экспрессирующую CAR, например, описанную в данном документе, вводят субъекту, нуждающемуся в этом, для лечения рака.
В одном варианте осуществления клетку, экспрессирующую слитый полипептид, содержащий молекулу CAR, например, молекулу CAR, описанную в данном документе, вводят в дозе и/или по схеме введения, описанных в данном документе.
В одном варианте осуществления слитый полипептид, содержащий молекулу CAR, вводят в иммунные эффекторные клетки (например, T-клетки, NK клетки), например, с применением транскрипции in vitro, и субъекту (например, человеку) осуществляют первоначальное введение клеток, содержащих слитый полипептид, содержащий молекулу CAR, и одно или несколько последующих введений клеток, содержащих слитый полипептид, содержащий молекулу CAR, где одно или несколько последующих введений осуществляют через менее чем 15 дней, например, 14, 13, 12, 11, 10, 9, 8, 7, 6, 5, 4, 3 или 2 дня после предыдущего введения. В одном варианте осуществления субъекту (например, человеку) осуществляют более одного введения клеток, содержащих слитый полипептид, содержащий молекулу CAR, в неделю, например, осуществляют 2, 3 или 4 введения клеток, содержащих слитый полипептид, содержащий молекула CAR, в неделю. В одном варианте осуществления субъект (например, субъект-человек) получает более одного введения клеток, содержащих слитый полипептид, содержащий CAR, в неделю (например, 2, 3 или 4 введения в неделю) (также называемых в данном документе циклом), за которым неделя с отсутствием введения клеток, экспрессирующих CAR, и затем субъекту осуществляют одно или несколько дополнительных введений клеток, содержащих молекулу CAR (например, более одного введения клеток, содержащих молекулу CAR, в неделю). В другом варианте осуществления субъекту (например, субъекту-человеку) осуществляют более одного цикла введения клеток, содержащих слитый полипептид, содержащий молекулу CAR, и период времени между каждым циклом составляет менее 10, 9, 8, 7, 6, 5, 4 или 3 дней. В одном варианте осуществления клетки, содержащие слитый полипептид, содержащий молекулу CAR, вводят раз в два дня с 3 введениями в неделю. В одном варианте осуществления клетки, содержащие слитый полипептид, содержащий молекулу CAR, вводят в течение по меньшей мере двух, трех, четырех, пяти, шести, семи, восьми или более недель.
В одном варианте осуществления клетки, экспрессирующие слитый полипептид, содержащий молекулу CAR, например, молекулу CAR, описанную в данном документе, вводят в качестве средства лечения первой линии для заболевания, например, рака, например, рака, описанного в данном документе. В другом варианте осуществления клетки, экспрессирующие слитый полипептид, содержащий молекулу CAR, например, молекулу CAR, описанную в данном документе, вводят в качестве средства лечения второй, третьей, четвертой линии для заболевания, например, рака, например, рака, описанного в данном документе.
В одном варианте осуществления вводят популяцию клеток, описанных в данном документе.
В другом аспекте настоящее изобретение относится к клетке, экспрессирующей слитый полипептид, содержащий молекулу CAR, описанную в данном документе, для применения в качестве лекарственного препарата в комбинации с ингибитором киназы и/или ингибитором контрольных точек иммунного ответа, описанных в данном документе. В другом аспекте настоящее изобретение относится к ингибитору киназы и/или ингибитору контрольных точек иммунного ответа, описанных в данном документе, для применения в качестве лекарственного препарата в комбинации с клеткой, экспрессирующей молекулу CAR, описанную в данном документе.
В другом аспекте настоящее изобретение относится к клетке, экспрессирующей слитый полипептид, содержащий молекулу CAR, описанную в данном документе, для применения в комбинации с цитокином, например, IL-7, IL-15 и/или IL-21, описанным в данном документе, при лечении заболевания, экспрессирующего опухолевый антиген, на который нацеливается CAR. В другом аспекте настоящее изобретение относится к цитокину, описанному в данном документе, для применения в комбинации с клеткой, экспрессирующей слитый полипептид, содержащий молекулу CAR, описанную в данном документе, при лечении заболевания, экспрессирующего опухолевый антиген, на который нацеливается CAR.
В другом аспекте настоящее изобретение относится к клетке, экспрессирующей слитый полипептид, содержащий молекулу CAR, описанную в данном документе, для применения в комбинации с ингибитором киназы и/или ингибитором контрольных точек иммунного ответа, описанными в данном документе, при лечении заболевания, экспрессирующего опухолевый антиген, на который нацеливается CAR. В другом аспекте настоящее изобретение относится к ингибитору киназы и/или ингибитору контрольных точек иммунного ответа, описанным в данном документе, для применения в комбинации с клеткой, экспрессирующей слитый полипептид, содержащий молекулу CAR, описанную в данном документе, при лечении заболевания, экспрессирующего опухолевый антиген, на который нацеливается CAR.
В другом аспекте настоящего изобретения представлен способ, предусматривающий введение слитого полипептида, содержащего молекулу CAR, например, молекулу CAR, описанную в данном документе, или клетки, содержащей нуклеиновую кислоту, кодирующую слитый полипептид, содержащий молекулу CAR, например, молекулу CAR, описанную в данном документе. В одном варианте осуществления у субъекта имеется нарушение, описанное в данном документе, например, у субъекта имеется рак, например, у субъекта имеется рак и имеются опухолеподдерживающие клетки, которые экспрессируют опухолеподдерживающий антиген, описанный в данном документе. В одном варианте осуществления субъект является человеком.
В одном варианте осуществления способов или путей применения, описанных в данном документе, слитый полипептид, содержащий молекулу CAR, вводят в комбинации с другим средством. В одном варианте осуществления средство может представлять собой ингибитор киназы, например, ингибитор CDK4/6, ингибитор BTK, ингибитор mTOR, ингибитор MNK или двойной ингибитор PI3K/mTOR и их комбинации. В одном варианте осуществления ингибитор киназы представляет собой ингибитор CDK4, например, ингибитор CDK4, описанный в данном документе, например, ингибитор CD4/6, такой как, например, 6-ацетил-8-циклопентил-5-метил-2-(5-пиперазин-1-ил-пиридин-2-иламино)-8H-пиридо[2,3-d]пиримидин-7-она гидрохлорид (также называемый палбоциклиб или PD0332991). В одном варианте осуществления ингибитор киназы представляет собой ингибитор BTK, например, ингибитор BTK, описанный в данном документе, такой как, например, ибрутиниб. В одном варианте осуществления ингибитор киназы представляет собой ингибитор mTOR, например, ингибитор mTOR, описанный в данном документе, такой как, например, рапамицин, аналог рапамицина, OSI-027. Ингибитор mTOR может представлять собой, например, ингибитор mTORC1 и/или ингибитор mTORC2, например, ингибитор mTORC1 и/или ингибитор mTORC2, описанный в данном документе. В одном варианте осуществления ингибитор киназы представляет собой ингибитор MNK, например, ингибитор MNK, описанный в данном документе, такой как, например, 4-амино-5-(4-фторанилино)-пиразолo[3,4-d]пиримидин. Ингибитор MNK может представлять собой, например, ингибитор MNK1a, MNK1b, MNK2a и/или MNK2b. Двойной ингибитор PI3K/mTOR может представлять собой, например, PF-04695102.
В одном варианте осуществления способов или путей применения, описанных в данном документе, ингибитор киназы представляет собой ингибитор CDK4, выбранный из алоизина A; флавопиридола или HMR-1275, 2-(2-хлорфенил)-5,7-дигидрокси-8-[(3S,4R)-3-гидрокси-1-метил-4-пиперидинил]-4-хроменона; кризотиниба (PF-02341066; 2-(2-хлорфенил)-5,7-дигидрокси-8-[(2R,3S)-2-(гидроксиметил)-1-метил-3-пирролидинил]- 4H-1-бензoпиран-4-она гидрохлорида (P276-00); 1-метил-5-[[2-[5-(трифторметил)-1H-имидазол-2-ил]-4-пиридинил]окси]-N-[4-(трифторметил)фенил]-1H-бензимидазол-2-амина (RAF265); индизулама (E7070); росковитина (CYC202); палбоциклиба (PD0332991); динациклиба (SCH727965); N-[5-[[(5-трет-бутилоксазол-2-ил)метил]тио]тиазол-2-ил]пиперидин-4-карбоксамида (BMS 387032); 4-[[9-хлор-7-(2,6-дифторфенил)-5H-пиримидо[5,4-d][2]бензазепин-2-ил]амино]-бензойной кислоты (MLN8054); 5-[3-(4,6-дифтор-1H-бензимидазол-2-ил)-1H-индазол-5-ил]-N-этил-4-метил-3-пиридинметанамина (AG-024322); 4-(2,6-дихлорбензоиламино)-1H-пиразол-3-карбоновой кислоты N-(пиперидин-4-ил)амида (AT7519); 4-[2-метил-1-(1-метилэтил)-1H-имидазол-5-ил]-N-[4-(метилсульфонил)фенил]-2-пиримидинамина (AZD5438) и XL281 (BMS908662).
В одном варианте осуществления способов или путей применения, описанных в данном документе, ингибитор киназы представляет собой ингибитор CDK4, например, палбоциклиб (PD0332991), и палбоциклиб вводят в дозе, составляющей приблизительно 50 мг, 60 мг, 70 мг, 75 мг, 80 мг, 90 мг, 100 мг, 105 мг, 110 мг, 115 мг, 120 мг, 125 мг, 130 мг, 135 мг (например, 75 мг, 100 мг или 125 мг) ежедневно в течение определенного периода времени, например, ежедневно в течение 14-21 дней 28-дневного цикла или ежедневно в течение 7-12 дней 21-дневного цикла. В одном варианте осуществления вводят 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 или более циклов палбоциклиба.
В одном варианте осуществления способов или путей применения, описанных в данном документе, ингибитор киназы представляет собой ингибитор BTK, выбранный из ибрутиниба (PCI-32765); GDC-0834; RN-486; CGI-560; CGI-1764; HM-71224; CC-292; ONO-4059; CNX-774 и LFM-A13. В одном варианте осуществления ингибитор BTK не снижает или не ингибирует киназную активность интерлейкин-2-индуцируемой киназы (ITK) и выбран из GDC-0834; RN-486; CGI-560; CGI-1764; HM-71224; CC-292; ONO-4059; CNX-774 и LFM-A13.
В одном варианте осуществления способов или путей применения, описанных в данном документе, ингибитор киназы представляет собой ингибитор BTK, например, ибрутиниб (PCI-32765), и ибрутиниб вводят в дозе, составляющей приблизительно 250 мг, 300 мг, 350 мг, 400 мг, 420 мг, 440 мг, 460 мг, 480 мг, 500 мг, 520 мг, 540 мг, 560 мг, 580 мг, 600 мг (например, 250 мг, 420 мг или 560 мг) ежедневно в течение определенного периода времени, например, ежедневно в течение 21-дневного цикла или ежедневно в течение 28-дневного цикла. В одном варианте осуществления вводят 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 или более циклов ибрутиниба.
В одном варианте осуществления способов или путей применения, описанных в данном документе, ингибитор киназы представляет собой ингибитор BTK, которые не ингибирует киназную активность ITK, например, RN-486, и RN-486 вводят в дозе, составляющей приблизительно 100 мг, 110 мг, 120 мг, 130 мг, 140 мг, 150 мг, 160 мг, 170 мг, 180 мг, 190 мг, 200 мг, 210 мг, 220 мг, 230 мг, 240 мг, 250 мг (например, 150 мг, 200 мг или 250 мг) ежедневно в течение определенного периода времени, например, ежедневно в течение 28-дневного цикла. В одном варианте осуществления вводят 1, 2, 3, 4, 5, 6, 7 или более циклов RN-486.
В одном варианте осуществления способов или путей применения, описанных в данном документе, ингибитор киназы представляет собой ингибитор mTOR, выбранный из темсиролимуса; ридафоролимуса (1R,2R,4S)-4-[(2R)-2 [(1R,9S,12S,15R,16E,18R,19R,21R, 23S,24E,26E,28Z,30S,32S,35R)-1,18-дигидрокси-19,30-диметокси-15,17,21,23, 29,35-гексаметил-2,3,10,14,20-пентаоксо-11,36-диокса-4-азатрицикло[30.3.1.04,9]гексатриаконта-16,24,26,28-тетраен-12-ил]пропил]-2-метоксициклогексила диметилфосфината, также известного как AP23573 и MK8669; эверолимуса (RAD001); рапамицина (AY22989); симапимода; (5-{2,4-бис[(3S)-3-метилморфолин-4-ил]пиридо[2,3-d]пиримидин-7-ил}-2-метоксифенил)метанола (AZD8055); 2-амино-8-[транс-4-(2-гидроксиэтокси)циклогексил]-6-(6-метокси-3-пиридинил)-4-метил-пиридо[2,3-d]пиримидин-7(8H)-она (PF04691502) и N2-[1,4-диоксо-4-[[4-(4-оксо-8-фенил-4H-1-бензoпиран-2-ил)морфолиний-4-ил]метокси]бутил]-L-аргинилглицил-L-α-аспартил-L-серина (SEQ ID NO: 836), внутренней соли (SF1126) и XL765.
В одном варианте осуществления способов или путей применения, описанных в данном документе, ингибитор киназы представляет собой ингибитор mTOR, например, рапамицин, и рапамицин вводят в дозе, составляющей приблизительно 3 мг, 4 мг, 5 мг, 6 мг, 7 мг, 8 мг, 9 мг, 10 мг (например, 6 мг) ежедневно в течение определенного периода времени, например, ежедневно в течение 21-дневного цикла или ежедневно в течение 28-дневного цикла. В одном варианте осуществления вводят 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 или более циклов рапамицина. В одном варианте осуществления ингибитор киназы представляет собой ингибитор mTOR, например, эверолимус, и эверолимус вводят в дозе, составляющей приблизительно 2 мг, 2,5 мг, 3 мг, 4 мг, 5 мг, 6 мг, 7 мг, 8 мг, 9 мг, 10 мг, 11 мг, 12 мг, 13 мг, 14 мг, 15 мг (например, 10 мг), ежедневно в течение определенного периода времени, например, ежедневно в течение 28-дневного цикла. В одном варианте осуществления вводят 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 или более циклов эверолимуса.
В одном варианте осуществления способов или путей применения, описанных в данном документе, ингибитор киназы представляет собой ингибитор MNK, выбранный из CGP052088; 4-амино-3-(п-фторфениламино)-пиразолo[3,4-d]пиримидина (CGP57380); церкоспорамида; ETC-1780445-2 и 4-амино-5-(4-фторанилино)-пиразолo[3,4-d]пиримидина.
В одном варианте осуществления способов или путей применения, описанных в данном документе, ингибитор киназы представляет собой двойной ингибитор фосфатидилинозитол-3-киназы (PI3K) и mTOR, выбранный из 2-амино-8-[транс-4-(2-гидроксиэтокси)циклогексил]-6-(6-метокси-3-пиридинил)-4-метил-пиридо[2,3-d]пиримидин-7(8H)-она (PF-04691502); N-[4-[[4-(диметиламино)-1-пиперидинил]карбонил]фенил]-N'-[4-(4,6-ди-4-морфолинил-1,3,5-триазин-2-ил)фенил]мочевины (PF-05212384, PKI-587); 2-метил-2-{4-[3-метил-2-оксо-8-(хинолин-3-ил)-2,3-дигидро-1H-имидазо[4,5-c]хинолин-1-ил]фенил}пропанeнитрила (BEZ-235); апитолизиба (GDC-0980, RG7422); 2,4-дифтор-N-{2-(метилокси)-5-[4-(4-пиридазинил)-6-хинолинил]-3-пиридинил}бензолсульфонамида (GSK2126458); 8-(6-метоксипиридин-3-ил)-3-метил-1-(4-(пиперазин-1-ил)-3-(трифторметил)фенил)-1H-имидазо[4,5-c]хинолин-2(3H)-она малеиновой кислоты (NVP-BGT226); 3-[4-(4-морфолинилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-2-ил]фенола (PI-103); 5-(9-изопропил-8-метил-2-морфолинo-9H-пурин-6-ил)пиримидин-2-амина (VS-5584, SB2343) и N-[2-[(3,5-диметоксифенил)амино]хиноксалин-3-ил]-4-[(4-метил-3-метоксифенил)карбонил]аминофенилсульфонамида (XL765).
В одном варианте осуществления способов или путей применения, описанных в данном документе, клетку, содержащую слитый полипептид, описанный в данном документе, вводят субъекту в комбинации с ингибитором протинтирозинфосфатазы, например, ингбитором протеинтирозинфосфатазы, описанной в данном документе. В одном варианте осуществления ингибитор протеинтирозинфосфатазы представляет собой ингибитор SHP-1, например, ингибитор SHP-1, описанный в данном документе, такой как, например, стибоглюконат натрия. В одном варианте осуществления ингибитор протеинтирозинфосфатазы представляет собой ингибитор SHP-2.
В одном варианте осуществления способов или путей применения, описанных в данном документе, клетку, содержащая слитый полипептид, описанный в данном документе, вводят в комбинацию с другим средством, и средство представляет собой цитокин. Цитокин может представлять собой, например, IL-7, IL-15, IL-21 или их комбинацию. В другом варианте осуществления клетку, содержащую слитый полипептид, описанный в данном документе, вводят в комбинации с ингибитором контрольных точек иммунного ответа, например, ингибитором контрольных точек иммунного ответа, описанным в данном документе. Например, в одном варианте осуществления ингибитор контрольных точек иммунного ответа ингибирует ингибирующую молекулу, выбранную из PD-1, PD-L1, CTLA-4, TIM-3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG-3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4 и TGFR-бета.
В одном аспекте слитый полипептид, описанный в данном документе, можно применять для устранения нормальной клетки, которая экспрессирует опухолевый антиген, описанный в данном документе, что, таким образом, применимо для использования в качестве клеточной кондиционирующей терапии перед трансплантацией клеток. В одном аспекте нормальная клетка, которая экспрессирует опухолевый антиген, описанный в данном документе, представляет собой нормальную стволовую клетку, и трансплантация клеток представляет собой трансплантацию стволовых клеток.
Ингибиторы контрольных точек иммунного ответа
В других вариантах осуществления способов или путей применения, описанных в данном документе, клетку, содержащую слитый полипептид, описанный в данном документе, вводят в комбинации с другим средством, и средство представляет собой ингибитор ингибитора контрольных точек иммунного ответа, например, ингибитор PD-1, ингибитор PD-L1, ингибитор TIM-3, ингибитор LAG-3. Иллюстративные ингибиторы раскрытый более подробно в данном документе ниже.
Ингибиторы PD-1
В определенных вариантах осуществления ингибитор ингибитора контрольных точек иммунного ответа представляет собой ингибитор PD-1. В некоторых вариантах осуществления ингибитор PD-1 выбран из PDR001 (Novartis), ниволумаба (Bristol-Myers Squibb), пембролизумаба (Merck & Co), пидилизумаба (CureTech), MEDI0680 (Medimmune), REGN2810 (Regeneron), TSR-042 (Tesaro), PF-06801591 (Pfizer), BGB-A317 (Beigene), BGB-108 (Beigene), INCSHR1210 (Incyte) или AMP-224 (Amplimmune).
Иллюстративные ингибиторы PD-1
В одном варианте осуществления ингибитор PD-1 представляет собой молекулу антитела к PD-1. В одном варианте осуществления ингибитор PD-1 представляет собой молекулу антитела к PD-1, описанную в US 2015/0210769, опубликованной 30 июля 2015 года под названием "Antibody Molecules to PD-1 and Uses Thereof", включенной посредством ссылки во всей своей полноте. Молекулы антител, описанные в данном документе, можно получать с использованием векторов, клеток-хозяев и способов, описанных в US 2015/0210769, включенной посредством ссылки во всей своей полноте.
Другие иллюстративные ингибиторы PD-1
В одном варианте осуществления молекула антитела к PD-1 представляет собой ниволумаб (Bristol-Myers Squibb), также известный как MDX-1106, MDX-1106-04, ONO-4538, BMS-936558 или OPDIVO®. Ниволумаб (клон 5C4) и другие антитела к PD-1 раскрыты в US 8008449 и WO 2006/121168, включенных посредством ссылки во всей своей полноте.
В одном варианте осуществления молекула антитела к PD-1 представляет собой пембролизумаб (Merck & Co), также известный как ламбролизумаб, MK-3475, MK03475, SCH-900475 или KEYTRUDA®. Пембролизумаб и другие антитела к PD-1 раскрыты в Hamid, O. et al. (2013) New England Journal of Medicine 369 (2): 134-44, US 8354509 и WO 2009/114335, включенных посредством ссылки во всей своей полноте.
В одном варианте осуществления молекула антитела к PD-1 представляет собой пидилизумаб (CureTech), также известный как CT-011. Пидилизумаб и другие антитела к PD-1 раскрыты в Rosenblatt, J. et al. (2011) J Immunotherapy 34(5): 409-18, US 7695715, US 7332582 и US 8686119, включенных посредством ссылки во всей своей полноте.
В одном варианте осуществления молекула антитела к PD-1 представляет собой MEDI0680 (Medimmune), также известное как AMP-514. MEDI0680 и другие антитела к PD-1 раскрыты в US 9205148 и WO 2012/145493, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи MEDI0680.
В одном варианте осуществления молекула антитела к PD-1 представляет собой REGN2810 (Regeneron). В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи REGN2810.
В одном варианте осуществления молекула антитела к PD-1 представляет собой PF-06801591 (Pfizer). В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи PF-06801591.
В одном варианте осуществления молекула антитела к PD-1 представляет собой BGB-A317 или BGB-108 (Beigene). В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи BGB-A317 или BGB-108.
В одном варианте осуществления молекула антитела к PD-1 представляет собой INCSHR1210 (Incyte), также известное как INCSHR01210 или SHR-1210. В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи INCSHR1210.
В одном варианте осуществления молекула антитела к PD-1 представляет собой TSR-042 (Tesaro), также известное как ANB011. В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи TSR-042.
Дополнительные известные антитела к PD-1 включают антитела, описанные, например, в WO 2015/112800, WO 2016/092419, WO 2015/085847, WO 2014/179664, WO 2014/194302, WO 2014/209804, WO 2015/200119, US 8735553, US 7488802, US 8927697, US 8993731 и US 9102727, включенных посредством ссылки во всей своей полноте.
В одном варианте осуществления антитело к PD-1 представляет собой антитело, которое конкурирует за связывание и/или связывается с тем же эпитопом на PD-1, что и одно из антител к PD-1, описанных в данном документе.
В одном варианте осуществления ингибитор PD-1 представляет собой пептид, который ингибирует сигнальный путь с участием PD-1, например, как описано в US 8907053, включенном посредством ссылки во всей своей полноте. В одном варианте осуществления ингибитор PD-1 представляет собой иммуноадгезин (например, иммуноадгезин, который содержит внеклеточную или PD-1-связывающую часть PD-L1 или PD-L2, слитую с константной областью (например, Fc-областью последовательности иммуноглобулина)). В одном варианте осуществления ингибитор PD-1 представляет собой AMP-224 (B7-DCIg (Amplimmune), например, раскрытый в WO 2010/027827 и WO 2011/066342, включенных посредством ссылки во всей своей полноте).
Ингибиторы PD-L1
В определенных вариантах осуществления ингибитор ингибитора контрольных точек иммунного ответа представляет собой ингибитор PD-L1. В некоторых вариантах осуществления ингибитор PD-L1 выбран из FAZ053 (Novartis), атезолизумаба (Genentech/Roche), авелумаба (Merck Serono и Pfizer), дурвалумаба (MedImmune/AstraZeneca) или BMS-936559 (Bristol-Myers Squibb).
Иллюстративные ингибиторы PD-L1
В одном варианте осуществления ингибитор PD-L1 представляет собой молекулу антитела к PD-L1. В одном варианте осуществления ингибитор PD-L1 представляет собой молекулу антитела к PD-L1, раскрытую в US 2016/0108123, опубликованной 21 апреля 2016 года под названием "Antibody Molecules to PD-L1 and Uses Thereof", включенной посредством ссылки во всей своей полноте. Молекулы антител, описанные в данном документе, можно получать с помощью векторов, клеток-хозяев и способов, описанных в US 2016/0108123, включенной посредством ссылки во всей своей полноте.
Другие иллюстративные ингибиторы PD-L1
В одном варианте осуществления молекула антитела к PD-L1 представляет собой атезолизумаб (Genentech/Roche), также известный как MPDL3280A, RG7446, RO5541267, YW243.55.S70 или TECENTRIQ™. Атезолизумаб и другие антитела к PD-L1 раскрыты в US 8217149, включенном посредством ссылки во всей своей полноте.
В одном варианте осуществления молекула антитела к PD-L1 представляет собой авелумаб (Merck Serono и Pfizer), также известный как MSB0010718C. Авелумаб и другие антитела к PD-L1 раскрыты в WO 2013/079174, включенной посредством ссылки во всей своей полноте.
В одном варианте осуществления молекула антитела к PD-L1 представляет собой дурвалумаб (MedImmune/AstraZeneca), также известный как MEDI4736. Дурвалумаб и другие антитела к PD-L1 раскрыты в US 8779108, включенном посредством ссылки во всей своей полноте.
В одном варианте осуществления молекула антитела к PD-L1 представляет собой BMS-936559 (Bristol-Myers Squibb), также известное как MDX-1105 или 12A4. BMS-936559 и другие антитела к PD-L1 раскрыты в US 7943743 и WO 2015/081158, включенных посредством ссылки во всей своей полноте.
Дополнительные известные антитела к PD-L1 включают антитела, описанные, например, в WO 2015/181342, WO 2014/100079, WO 2016/000619, WO 2014/022758, WO 2014/055897, WO 2015/061668, WO 2013/079174, WO 2012/145493, WO 2015/112805, WO 2015/109124, WO 2015/195163, US 8168179, US 8552154, US 8460927 и US 9175082, включенных посредством ссылки во всей своей полноте.
В одном варианте осуществления антитело к PD-L1 представляет собой антитело, которое конкурирует за связывание и/или связывается с тем же эпитопом на PD-L1, что и одно из антител к PD-L1, описанных в данном документе.
Ингибиторы LAG-3
В определенных вариантах осуществления ингибитор ингибитора контрольных точек иммунного ответа представляет собой ингибитор LAG-3. В некоторых вариантах осуществления ингибитор LAG-3 выбран из LAG525 (Novartis), BMS-986016 (Bristol-Myers Squibb) или TSR-033 (Tesaro).
Иллюстративные ингибиторы LAG-3
В одном варианте осуществления ингибитор LAG-3 представляет собой молекулу антитела к LAG-3. В одном варианте осуществления ингибитор LAG-3 представляет собой молекулу антитела к LAG-3, раскрытую в US 2015/0259420, опубликованной 17 сентября 2015 года под названием "Antibody Molecules to LAG-3 and Uses Thereof", включенной посредством ссылки во всей своей полноте. Молекулы антител, описанные в данном документе, можно получать с помощью векторов, клеток-хозяев и способов, описанных в US 2015/0259420, включенной посредством ссылки во всей своей полноте.
Другие иллюстративные ингибиторы LAG-3
В одном варианте осуществления молекула антитела к LAG-3 представляет собой BMS-986016 (Bristol-Myers Squibb), также известное как BMS986016. BMS-986016 и другие антитела к LAG-3 раскрыты в WO 2015/116539 и US 9505839, включенных посредством ссылки во всей своей полноте.
В одном варианте осуществления молекула антитела к LAG-3 представляет собой TSR-033 (Tesaro). В одном варианте осуществления молекула антитела к LAG-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи TSR-033.
В одном варианте осуществления молекула антитела к LAG-3 представляет собой IMP731 или GSK2831781 (GSK и Prima BioMed). IMP731 и другие антитела к LAG-3 раскрыты в WO 2008/132601 и US 9244059, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к LAG-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи IMP731. В одном варианте осуществления молекула антитела к LAG-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи GSK2831781.
В одном варианте осуществления молекула антитела к LAG-3 представляет собой IMP761 (Prima BioMed). В одном варианте осуществления молекула антитела к LAG-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи IMP761.
Дополнительные известные антитела к LAG-3 включают антитела, описанные, например, в WO 2008/132601, WO 2010/019570, WO 2014/140180, WO 2015/116539, WO 2015/200119, WO 2016/028672, US 9244059, US 9505839, включенных посредством ссылки во всей своей полноте.
В одном варианте осуществления антитело к LAG-3 представляет собой антитело, которое конкурирует за связывание и/или связывается с тем же эпитопом на LAG-3, что и одно из антител к LAG-3, описанных в данном документе.
В одном варианте осуществления ингибитор, связывающийся LAG-3, представляет собой растворимый белок LAG-3, например, IMP321 (Prima BioMed), например, раскрытый в WO 2009/044273, включенной посредством ссылки во всей своей полноте.
Ингибиторы TIM-3
В определенных вариантах осуществления ингибитор ингибитора контрольных точек иммунного ответа представляет собой ингибитор TIM-3. В некоторых вариантах осуществления ингибитор TIM-3 представляет собой MGB453 (Novartis) или TSR-022 (Tesaro).
Иллюстративные ингибиторы TIM-3
В одном варианте осуществления ингибитор TIM-3 представляет собой молекулу антитела к TIM-3. В одном варианте осуществления ингибитор TIM-3 представляет собой молекулу антитела к TIM-3, раскрытую в US 2015/0218274, опубликованной 6 августа 2015 года под названием "Antibody Molecules to TIM-3 and Uses Thereof", включенной посредством ссылки во всей своей полноте.
Молекулы антител, описанные в данном документе, можно получать с помощью векторов, клеток-хозяев и способов, описанных в US 2015/0218274, включенной посредством ссылки во всей своей полноте.
Другие иллюстративные ингибиторы TIM-3
В одном варианте осуществления молекула антитела к TIM-3 представляет собой TSR-022 (AnaptysBio/Tesaro). В одном варианте осуществления молекула антитела к TIM-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи TSR-022. В одном варианте осуществления молекула антитела к TIM-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи APE5137 или APE5121. APE5137, APE5121 и другие антитела к TIM-3 раскрыты в WO 2016/161270, включенной посредством ссылки во всей своей полноте.
В одном варианте осуществления молекула антитела к TIM-3 представляет собой клон антитела F38-2E2. В одном варианте осуществления молекула антитела к TIM-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи F38-2E2.
Дополнительные известные антитела к TIM-3 включают антитела, описанные, например, в WO 2016/111947, WO 2016/071448, WO 2016/144803, US 8552156, US 8841418 и US 9163087, включенных посредством ссылки во всей своей полноте.
В одном варианте осуществления антитело к TIM-3 представляет собой антитело, которое конкурирует за связывание и/или связывается с тем же эпитопом на TIM-3, что и одно из антител к TIM-3, описанных в данном документе.
Агонисты GITR
В определенных вариантах осуществления слитый полипептид вводят в комбинации с агонистом GITR. В некоторых вариантах осуществления агонист GITR представляет собой GWN323 (NVS), BMS-986156, MK-4166 или MK-1248 (Merck), TRX518 (Leap Therapeutics), INCAGN1876 (Incyte/Agenus), AMG 228 (Amgen) или INBRX-110 (Inhibrx).
Иллюстративные агонисты GITR
В одном варианте осуществления агонист GITR представляет собой молекулу антитела к GITR. В одном варианте осуществления агонист GITR представляет собой молекулу антитела к GITR, описанную в WO 2016/057846, опубликованной 14 апреля 2016 года под названием "Compositions and Methods of Use for Augmented Immune Response and Cancer Therapy", включенной посредством ссылки во всей своей полноте.
Молекулы антител, описанные в данном документе, можно получать с использованием векторов, клеток-хозяев и способов, описанных в WO 2016/057846, включенной посредством ссылки во всей своей полноте.
Другие иллюстративные агонисты GITR
В одном варианте осуществления молекула антитела к GITR представляет собой BMS-986156 (Bristol-Myers Squibb), также известное как BMS 986156 или BMS986156. BMS-986156 и другие антитела к GITR раскрыты, например, в US 9228016 и WO 2016/196792, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к GITR содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи BMS-986156.
В одном варианте осуществления молекула антитела к GITR представляет собой MK-4166 или MK-1248 (Merck). MK-4166, MK-1248 и другие антитела к GITR раскрыты, например, в US 8709424, WO 2011/028683, WO 2015/026684 и Mahne et al. Cancer Res. 2017; 77(5):1108-1118, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к GITR содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи MK-4166 или MK-1248.
В одном варианте осуществления молекула антитела к GITR представляет собой TRX518 (Leap Therapeutics). TRX518 и другие антитела к GITR раскрыты, например, в US 7812135, US 8388967, US 9028823, WO 2006/105021 и Ponte J et al. (2010) Clinical Immunology; 135:S96, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к GITR содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи TRX518.
В одном варианте осуществления молекула антитела к GITR представляет собой INCAGN1876 (Incyte/Agenus). INCAGN1876 и другие антитела к GITR раскрыты, например, в US 2015/0368349 и WO 2015/184099, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к GITR содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи INCAGN1876.
В одном варианте осуществления молекула антитела к GITR представляет собой AMG 228 (Amgen). AMG 228 и другие антитела к GITR раскрыты, например, в US 9464139 и WO 2015/031667, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления молекула антитела к GITR содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи AMG 228.
В одном варианте осуществления молекула антитела к GITR представляет собой INBRX-110 (Inhibrx). INBRX-110 и другие антитела к GITR раскрыты, например, в US 2017/0022284 и WO 2017/015623, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления агонист GITR содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельной области тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи INBRX-110.
В одном варианте осуществления агонист GITR (например, слитый полипептид) представляет собой MEDI 1873 (MedImmune), также известное как MEDI1873. MEDI 1873 и другие агонисты GITR раскрыты, например, в US 2017/0073386, WO 2017/025610 и Ross et al. Cancer Res 2016; 76(14 Suppl): Abstract № 561, включенных посредством ссылки во всей своей полноте. В одном варианте осуществления агонист GITR содержит один или несколько из Fc-домена IgG, функционального домена мультимеризации и домена, связывающего рецептор, из лиганда индуцируемого глюкокортикоидами рецептора TNF (GITRL) MEDI 1873.
Дополнительные известные агонисты GITR (например, антитела к GITR) включают описанные, например, в WO 2016/054638, включенной посредством ссылки во всей своей полноте.
В одном варианте осуществления антитело к GITR представляет собой антитело, которое конкурирует за связывание и/или связывается с тем же эпитопом на GITR, что и одно из антител к GITR, описанных в данном документе.
В одном варианте осуществления агонист GITR представляет собой пептид, который активирует путь передачи сигнала с участием GITR. В одном варианте осуществления агонист GITR представляет собой иммуноадгезинсвязывающий фрагмент (например, иммуноадгезинсвязывающий фрагмент, содержащий внеклеточную или GITR-связывающую часть GITRL), слитый с константной областью (например, Fc-областью последовательности иммуноглобулина).
Комплексы IL15/IL-15Ra
В определенных вариантах осуществления слитый полипептид вводят в комбинации с комплексом IL-15/IL-15Ra. В некоторых вариантах осуществления комплекс IL-15/IL-15Ra выбран из NIZ985 (Novartis), ATL-803 (Altor) или CYP0150 (Cytune).
Иллюстративные комплексы IL-15/IL-15Ra
В одном варианте осуществления комплекс IL-15/IL-15Ra содержит IL-15 человека в комплексе с растворимой формой IL-15Ra человека. Комплекс может содержать IL-15, ковалентно или нековалентно связанный с растворимой формой IL-15Ra. В конкретном варианте осуществления IL-15 человека нековалентно связан с растворимой формой IL-15Ra. В конкретном варианте осуществления IL-15 человека в композиции содержит аминокислотную последовательность, описанную в WO 2014/066527, включенной посредством ссылки во всей своей полноте. Молекулы, описанные в данном документе, можно получать с использованием векторов, клеток-хозяев и способов, описанных в WO 2007/084342, включенном посредством ссылки во всей своей полноте.
Другие иллюстративные комплексы IL-15/IL-15Ra
В одном варианте осуществления комплекс IL-15/IL-15Ra представляет собой ALT-803, слитый полипептид IL-15/IL-15Ra и Fc-области (растворимый комплекс IL-15N72D:IL-15RaSu/Fc-области). ALT-803 раскрыт в WO 2008/143794, включенной посредством ссылки во всей своей полноте.
В одном варианте осуществления комплекс IL-15/IL-15Ra содержит IL-15, слитый с доменом sushi IL-15Ra (CYP0150, Cytune). Домен sushi IL-15Ra относится к домену, который начинается с первого остатка цистеина после сигнального пептида IL-15Ra и заканчивается четвертым остатком цистеина после указанного сигнального пептида. Комплекс IL-15, слитого с доменом sushi IL-15Ra, раскрытый в WO 2007/04606 и WO 2012/175222, включенных посредством ссылки во всей своей полноте.
Способы скрининга
Настоящее изобретение включает способы идентификации генетического элемента, ассоциированного со специфическим биологическим фенотипом, например, генетического элемента, ассоциированного с развитием и/или прогрессированием нарушения, например рака Способ предусматривает стадии: (i) модулирования экспрессии слитого полипептида в клетке, например, клетке-хозяине, путем воздействия на указанную клетку с помощью COF1, COF2 или COF3, (ii) отбора клеток с представляющим интерес фенотипом, например, фенотипом, ассоциированным с развитием и/или прогрессированием нарушения, например, рака, и (iii) идентификации слитого полипептида, который индуцирует представляющий интерес фенотип, где воздействие на клетку с помощью COF1, COF2 или COF3 уменьшает, например, на по меньшей мере приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, или 100 процентов, экспрессию указанного слитого полипептида относительно уровня экспрессии указанного слитого полипептида до воздействия с помощью COF1, COF2 или COF3.
Способы лечения субъекта
В некоторых аспектах настоящего изобретения представлен способ лечения пациента, предусматривающий введение слитого полипептида (например, содержащего COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид и представляющий интерес гетерологичный полипептид) или клеток, экспрессирующих слитый полипептид (например, клеток, экспрессирующих CAR), произведенных, как описано в данном документе, необязательно в комбинации с одним или несколькими другими видами терапии. В некоторых аспектах настоящего изобретения представлен способ лечения пациента, предусматривающий введение реакционной смеси, содержащей слитый полипептид или клетки, экспрессирующие слитый полипептид (например, клетки, экспрессирующие CAR), описанный в данном документе, необязательно в комбинации с одним или несколькими другими видами терапии. В некоторых аспектах настоящего изобретения представлен способ транспортировки или приема реакционной смеси, содержащей слитый полипептид или клетки, экспрессирующие слитый полипептид (например, клетки, экспрессирующие CAR), описанные в данном документе.
В некоторых аспектах настоящего изобретения представлен способ лечения пациента, предусматривающий получение слитого полипептида (например, содержащего COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид и представляющий интерес гетерологичный полипептид) или клеток, экспрессирующих слитый полипептид (например, клеток, экспрессирующих CAR), которые были произведены, как описано в данном документе, и дополнительно предусматривающий введение слитого полипептида или клеток, экспрессирующих слитый полипептид (например, клеток, экспрессирующих CAR), пациенту, необязательно в комбинации с одним или несколькими другими видами терапии. В некоторых аспектах настоящего изобретения представлен способ лечения пациента, предусматривающий производство слитого полипептида или клеток, экспрессирующих слитый полипептид (например, клеток, экспрессирующих CAR), описанный в данном документе, и дополнительно предусматривающий введение слитого полипептида или клеток, экспрессирующих слитый полипептид (например, клеток, экспрессирующих CAR), пациенту, необязательно в комбинации с одним или несколькими другими видами терапии. Другим видом терапии может быть, например, противораковая терапия, такая как химиотерапия.
Способы, описанные в данном документе, могут дополнительно включать составление слитого полипептида (например, содержащего COF1/CRBN-, COF2/CRBN- или COF3/CRBN-связывающий полипептид и представляющий интерес гетерологичный полипептид) или клеток, экспрессирующих слитый полипептид (например, клеток, экспрессирующих CAR), в виде фармацевтической композиции. Фармацевтические композиции могут содержать слитый полипептид или клетки, экспрессирующие слитый полипептид (например, клетки, экспрессирующие CAR), например, совокупность слитых полипептидов или клеток, экспрессирующих слитый полипептид (например, клеток, экспрессирующих CAR), описанный в данном документе, в комбинации с одним или несколькими фармацевтически или физиологически приемлемыми носителями, разбавителями или вспомогательными веществами. Такие композиции могут содержать буферы, такие как нейтральный буферный солевой раствор, фосфатно-солевой буферный раствор и т. п.; углеводы, такие как глюкоза, манноза, сахароза или декстраны, маннит; белки; полипептиды или аминокислоты, такие как глицин; антиоксиданты; хелатирующие средства, такие как EDTA или глутатион; адъюванты (например, гидроксид алюминия) и консерванты. Композиции можно составлять, например, для внутривенного введения.
В одном варианте осуществления фармацевтическая композиция практически не содержит, например, в ней отсутствуют выявляемые уровни загрязнителя, например, выбранного из группы, состоящей из эндотоксина, микоплазмы, способного к репликации лентивируса (RCL), p24, нуклеиновой кислоты VSV-G, gag HIV, остаточных количеств микрогранул, покрытых антителами к CD3/антителами к CD28, антител мыши, объединенной сыворотки крови человека, бычьего сывороточного альбумина, бычьей сыворотки крови, компонентов сред для культивирования, клеточных или плазмидных компонентов для упаковки векторов, бактерии и гриба. В одном варианте осуществления бактерия представляет собой по меньшей мере бактерию, выбранную из группы, состоящей из Alcaligenes faecalis, Candida albicans, Escherichia coli, Haemophilus influenzae, Neisseria meningitidis, Pseudomonas aeruginosa, Staphylococcus aureus, Streptococcus pneumoniae и Streptococcus pyogenes группы A.
В случае, если указано "иммунологически эффективное количество", "эффективное противораковое количество", "количество, эффективное для ингибирования рака" или "терапевтическое количество", точное количество композиций по настоящему изобретению, подлежащих введению, может быть определено врачом с учетом индивидуальных различий в возрасте, массе тела, размере опухоли, степени инфекции или метастазирования и состояния пациента (субъекта). В целом, можно отметить, что фармацевтическую композицию, содержащую иммунные эффекторные клетки (например, T-клетки, NK-клетки), описанные в данном документе, можно вводить в дозе от 104 до 109 клеток/кг массы тела, в некоторых случаях от 105 до 106 клеток/кг массы тела, с включением всех целочисленных значений в пределах данных диапазонов. Композиции на основе Т-клеток можно также вводить несколько раз в этих дозах. Клетки можно вводить с помощью методик инфузии, которые являются общеизвестными в иммунотерапии (см., например, Rosenberg et al., New Eng. J. of Med. 319:1676, 1988).
В некоторых вариантах осуществления доза клеток с CAR (например, клеток с CAR для CD19) составляет приблизительно 1×106, 1,1×106, 2×106, 3,6×106, 5×106, 1×107, 1,8×107, 2×107, 5×107, 1×108, 2×108 или 5×108 клеток/кг. В некоторых вариантах осуществления доза клеток с CAR (например, клеток с CAR для CD19) составляет по меньшей мере приблизительно 1×106, 1,1×106, 2×106, 3,6×106, 5×106, 1×107, 1,8×107, 2×107, 5×107, 1×108, 2×108 или 5×108 клеток/кг. В некоторых вариантах осуществления доза клеток с CAR (например, клеток с CAR для CD19) составляет до приблизительно 1×106, 1,1×106, 2×106, 3,6×106, 5×106, 1×107, 1,8×107, 2×107, 5×107, 1×108, 2×108 или 5×108 клеток/кг. В некоторых вариантах осуществления доза клеток с CAR (например, клеток с CAR для CD19) составляет приблизительно 1,1×106-1,8×107 клеток/кг. В некоторых вариантах осуществления доза клеток с CAR (например, клеток с CAR для CD19) составляет приблизительно 1×107, 2×107, 5×107, 1×108, 2×108, 5×108, 1×109, 2×109 или 5×109 клеток. В некоторых вариантах осуществления доза клеток с CAR (например, клеток с CAR для CD19) составляет по меньшей мере приблизительно 1×107, 2×107, 5×107, 1×108, 2×108, 5×108, 1×109, 2×109 или 5×109 клеток. В некоторых вариантах осуществления доза клеток с CAR (например, клеток с CAR для CD19) составляет до приблизительно 1×107, 2×107, 5×107, 1×108, 2×108, 5×108, 1×109, 2×109 или 5×109 клеток. В определенных аспектах субъекту может потребоваться введение активированных иммунных эффекторных клеток (например, T-клеток, NK-клеток), и тогда последовательно повторно берут кровь (или осуществляют аферез), активируют иммунные эффекторные клетки (например, T-клетки, NK-клетки) из нее и проводят повторную инфузию этих активированных и размноженных иммунных эффекторных клеток (например, T-клеток, NK-клеток) пациенту. Этот процесс можно осуществлять несколько раз с интервалом в несколько недель. В определенных аспектах иммунные эффекторные клетки (например, T-клетки, NK-клетки) можно активировать из образцов крови объемом от 10 куб. см до 400 куб. см. В определенных аспектах иммунные эффекторные клетки (например, T-клетки, NK-клетки) активируют из образцов крови объемом 20 куб. см, 30 куб. см, 40 куб. см, 50 куб. см, 60 куб. см, 70 куб. см, 80 куб. см, 90 куб. см или 100 куб. см.
В вариантах осуществления клетки, экспрессирующие CAR (например, клетки, экспрессирующие CAR для CD19), вводят в виде совокупности доз, например, первой дозы, второй дозы и необязательно третьей дозы. В вариантах осуществления способ предусматривает лечение субъекта (например, взрослого субъекта), у которого имеется рак (например, острый лимфоидный лейкоз (ALL)), предусматривающий введение субъекту первой дозы, второй дозы и необязательно одной или нескольких дополнительных доз, при этом каждая доза содержит иммунные эффекторные клетки, экспрессирующие молекулу CAR, например, молекулу CAR для CD19.
В вариантах осуществления способ предусматривает введение дозы, составляющей 2-5×106 жизнеспособных клеток, экспрессирующих CAR/кг, где масса тела субъект составляет менее 50 кг; или введение дозы, составляющей 1,0-2,5×108 жизнеспособных клеток, экспрессирующих CAR, где масса тела субъекта составляет по меньшей мере 50 кг.
В вариантах осуществления субъекту, например, педиатрическому субъекту, вводят однократную дозу.
В вариантах осуществления дозы вводят в последовательные дни, например, первую дозу вводят в день 1, вторую дозу вводят в день 2 и необязательную третью дозу (если она вводится) вводят в день 3.
В вариантах осуществления вводят четвертую, пятую или шестую дозы или больше доз.
В вариантах осуществления первая доза составляет приблизительно 10% от суммарной дозы, вторая доза составляет приблизительно 30% от суммарной дозы и третья доза составляет приблизительно 60% от суммарной дозы, при этом вышеупомянутые проценты в сумме составляют 100%. В вариантах осуществления первая доза составляет приблизительно 9-11%, 8-12%, 7-13% или 5-15% от суммарной дозы. В вариантах осуществления вторая доза составляет приблизительно 29-31%, 28-32%, 27-33%, 26-34%, 25-35%, 24-36%, 23-37%, 22-38%, 21-39% или 20-40% от суммарной дозы. В вариантах осуществления третья доза составляет приблизительно 55-65%, 50-70%, 45-75% или 40-80% от суммарной дозы. В вариантах осуществления суммарная доза относится к суммарному количеству жизнеспособных клеток, экспрессирующих CAR, вводимых в течение 1 недели, 2 недель, 3 недель или 4 недель. В некоторых вариантах осуществления, в которых вводят две дозы, суммарная доза относится к сумме количества жизнеспособных клеток, экспрессирующих CAR, вводимых субъекту в первой и второй дозах. В некоторых вариантах осуществления, в которых вводят три дозы, суммарная доза относится к сумме количества жизнеспособных клеток, экспрессирующих CAR, вводимых субъекту в первой, второй и третьей дозах.
В вариантах осуществления дозу измеряют в соответствии с количеством жизнеспособных клеток, экспрессирующих в них CAR. Экспрессию CAR можно измерить, например, с помощью проточной цитометрии с использованием молекулы антитела, которая связывает молекулу CAR, и выявляемой метки. Жизнеспособность можно измерять, например, с помощью Cellometer.
В вариантах осуществления жизнеспособные клетки, экспрессирующие CAR, вводят в возрастающих дозах. В вариантах осуществления вторая доза больше, чем первая доза, например, больше на 10%, 20%, 30% или 50%. В вариантах осуществления вторая доза в два раза, в три раза, в четыре раза или в пять раз больше размера первой дозы. В вариантах осуществления третья доза больше, чем вторая доза, например, больше на 10%, 20%, 30% или 50%. В вариантах осуществления третья доза в два раза, в три раза, в четыре раза или в пять раз больше размера второй дозы.
В определенных вариантах осуществления способ включает одно, два, три, четыре, пять, шесть, семь или все из a)-h) из следующего:
a) количество жизнеспособных клеток, экспрессирующих CAR, вводимых в первой дозе, составляет не более 1/3 от количества жизнеспособных клеток, экспрессирующих CAR, вводимых во второй дозе;
b) количество жизнеспособных клеток, экспрессирующих CAR, вводимых в первой дозе, составляет не более 1/X, где X составляет 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 30, 40 или 50, от суммарного количества вводимых жизнеспособных клеток, экспрессирующих CAR;
c) количество жизнеспособных клеток, экспрессирующих CAR, вводимых в первой дозе, составляет не более 1×107, 2×107, 3×107, 4×107, 5×107, 6×107, 7×107, 8×107, 9×107, 1×108, 2×108, 3×108, 4×108 или 5×108 жизнеспособных клеток, экспрессирующих CAR, и вторая доза больше первой дозы;
d) количество жизнеспособных клеток, экспрессирующих CAR, вводимых во второй дозе, составляет не более 1/2 от количество жизнеспособных клеток, экспрессирующих CAR, вводимых в третьей дозе;
e) количество жизнеспособных клеток, экспрессирующих CAR, вводимых во второй дозе, составляет не более 1/Y, где Y составляет 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 30, 40 или 50, от суммарного количества вводимых жизнеспособных клеток, экспрессирующих CAR;
f) количество жизнеспособных клеток, экспрессирующих CAR, вводимых во второй дозе, составляет не более 1×107, 2×107, 3×107, 4×107, 5×107, 6×107, 7×107, 8×107, 9×107, 1×108, 2×108, 3×108, 4×108 или 5×108 жизнеспособных клеток, экспрессирующих CAR, и третья доза больше второй дозы;
h) дозы и периоды времени введения первой, второй и необязательно третьей доз выбирают таким образом, что субъект испытывает CRS на уровне не более 4, 3, 2 или 1.
В вариантах осуществления суммарная доза составляет приблизительно 5×108 жизнеспособных клеток, экспрессирующих CAR. В вариантах осуществления суммарная доза составляет приблизительно 5×107-5×108 жизнеспособных клеток, экспрессирующих CAR. В вариантах осуществления первая доза составляет приблизительно 5×107 (например, ± 10%, 20% или 30%) жизнеспособных клеток, экспрессирующих CAR, вторая доза составляет приблизительно 1,5×108 (например, ± 10%, 20% или 30%) жизнеспособных клеток, экспрессирующих CAR, и третья доза составляет приблизительно 3×108 (например, ± 10%, 20% или 30%) жизнеспособных клеток, экспрессирующих CAR.
В вариантах осуществления субъекта оценивают в отношении CRS после получения дозы, например, после получения первой дозы, второй дозы и/или третьей дозы.
В вариантах осуществления субъект получает средство лечения CRS, например, тоцилизумаб, кортикостероид, этанерцепт или силтуксимаб. В вариантах осуществления средство лечения CRS вводят перед или после введения первой дозы клеток, содержащих молекулу CAR. В вариантах осуществления средство лечения CRS вводят перед или после введения второй дозы клеток, содержащих молекулу CAR. В вариантах осуществления средство лечения CRS вводят перед или после введения третьей дозы клеток, содержащих молекулу CAR. В вариантах осуществления средство лечения CRS вводят между введением первой и второй доз клеток, содержащих молекулу CAR, и/или между введением второй и третьей доз клеток, содержащих молекулу CAR.
Введение рассматриваемых композиций можно осуществлять любым удобным способом. Композиции, описанные в данном документе, можно вводить пациенту трансартериально, подкожно, внутрикожно, интратуморально, интранодально, интрамедуллярно, внутримышечно, с помощью внутривенной (i.v.) инъекции или внутрибрюшинно, например, с помощью внутрикожной или подкожной инъекции. Композиции на основе иммунных эффекторных клеток (например, T-клеток, NK-клеток) можно инъецировать непосредственно в опухоль, лимфатический узел или очаг инфекции.
В одном варианте осуществления клетки, экспрессирующие CAR, описанный в данном документе, вводят субъекту в комбинации с молекулой, которая уменьшает популяцию TREG-клеток. Способы, которые уменьшают количество (например, приводят к истощению) TREG-клеток, известны из уровня техники и включают, например, истощение по CD25, введение циклофосфамида, модулирование функции GITR. Без ограничения какой-либо теорией, полагают, что снижение количества TREG-клеток у субъекта до афереза или до введения клетки, экспрессирующей CAR, описанной в данном документе, снижает количество нежелательных иммунных клеток (например, Treg) в микроокружении опухоли и снижает риск рецидива у субъекта.
В одном варианте осуществления клетки, экспрессирующие CAR, описанный в данном документе, вводят субъекту в комбинации с молекулой, нацеливающейся на GITR и/или модулирующей функции GITR, такой как агонист GITR и/или антитело к GITR, которая истощает регуляторные T-клетки (TREG). В вариантах осуществления клетки, экспрессирующие CAR, описанный в данном документе, вводят субъекту в комбинации с циклофосфамидом. В одном варианте осуществления GITR-связывающие молекулы и/или молекулы, модулирующие функции GITR (например, агонист GITR и/или антитело к GITR, приводящее к истощению Treg), вводят до введения клетки, экспрессирующей CAR. Например, в одном варианте осуществления агонист GITR можно вводить до афереза клеток. В вариантах осуществления циклофосфамид вводят субъекту до введения (например, инфузии или повторной инфузии) клетки, экспрессирующей CAR, или до афереза клеток. В вариантах осуществления циклофосфамид и антитело к GITR вводят субъекту до введения (например, инфузии или повторной инфузии) клетки, экспрессирующей CAR, или до афереза клеток. В одном варианте осуществления у субъекта имеется рак (например, солидный рак или гематологический рак, такой как ALL или CLL). В варианте осуществления у субъекта имеется CLL. В вариантах осуществления у субъекта имеется ALL. В вариантах осуществления у субъекта имеется солидный рак, например, солидный рак, описанный в данном документе. Иллюстративные агонисты GITR включают, например, слитые полипептиды на основе GITR и антитела к GITR (например, бивалентные антитела к GITR), такие как, например, слитый белок на основе GITR, описанный в патенте США № 6111090, европейском патенте № 090505B1, патенте США № 8586023, публикациях согласно PCT №№ WO 2010/003118 и 2011/090754, или антитело к GITR описанное, например, в патенте США № 7025962, европейском патенте № 1947183B1, патенте США № 7812135, патенте США № 8388967, патенте США № 8591886, европейском патенте № EP 1866339, публикации согласно PCT № WO 2011/028683, публикации согласно PCT № WO 2013/039954, публикации согласно PCT № WO2005/007190, публикации согласно PCT № WO 2007/133822, публикации согласно PCT № WO2005/055808, публикации согласно PCT №: WO 99/40196, публикации согласно PCT № WO 2001/03720, публикации согласно PCT № WO99/20758, публикации согласно PCT № WO2006/083289, публикации согласно PCT № WO 2005/115451, патенте США № 7618632 и публикация согласно PCT № WO 2011/051726.
В одном варианте осуществления описанную в данном документе клетку, экспрессирующую CAR, вводят субъекту в комбинации с агонистом GITR, например, агонистом GITR, описанным в данном документе. В одном варианте осуществления агонист GITR вводят до введения клетки, экспрессирующей CAR. Например, в одном варианте осуществления агонист GITR можно вводить до афереза клеток. В одном варианте осуществления у субъекта имеется CLL.
ПРИМЕРЫ
Настоящее изобретение дополнительно подробно описано посредством ссылки на следующие экспериментальные примеры. Эти примеры приведены лишь в целях иллюстрации и не предполагаются как ограничивающие, если не указано иное. Таким образом, настоящее изобретение никоим образом не следует истолковывать как ограниченное следующими примерами, а, наоборот, следует истолковывать как охватывающее все без исключения видоизменения, которые становятся очевидными как следствие идеи, приведенной в данном документе.
Пример 1. Оценка метки деградации на основе IKZF3 с помощью люциферазного анализа
В этом примере метку деградации на основе IKZF3 тестировали в отношении ее способности содействовать леналидомид-зависимой деградации белка-мишени. Метка деградации на основе IKZF3 содержит аминокислотные остатки 136-180 и 236-249 из IKZF3 человека и содержит аминокислотную последовательность под SEQ ID NO: 3. Эта метка в данном документе называется "IKZF3 136-180 и 236-249" или "HilD-метка". IKZF3 136-180 и 236-249 сливали с N-концом NanoLuciferase через 16GS-линкер GGGGSGGGGTGGGGSG (SEQ ID NO: 28) (ФИГ. 1A). Вектор pNL1.1CMV, кодирующий NanoLuciferase с меткой IKZF3 136-180 и 236-249, подвергали обратной трансфекции в клетки HEK293T-с применением суммарно 0 нг, 5 нг, 50 нг или 250 нг ДНК (значения для ДНК в данном примере приведены на основе трансфекции объемом 25 мкл в 384-луночном планшете, которую затем масштабировали до 6-луночной чашки).
Трансфицированные клетки подвергали 1-часовой предварительной обработке с помощью 128 нг/мл циклогексамида, 12,8 нг/мл циклогексамида или 10 мкМ MG132 до обработки с помощью 0 мкМ, 1 мкМ, 10 мкМ или 100 мкМ леналидомида в течение 2, 4 или 6 часов. DMSO включали в качестве контроля со средой-носителем. Люминесценцию измеряли посредством считывания каждого 384-луночного планшета на ViewLux® при 1-секундном и 5-секундном воздействии. Данные импортировали в Spotfire® и визуализации поучали путем проведения NC3-нормализации в соответствии со следующей формулой: 100 * ([люминесценция] / [DMSO]).
Метка деградации, содержащая аминокислотные остатки 136-180 и 236-249 из IKZF3, может содействовать леналидомид-зависимой деградации белка-мишени (ФИГ. 1B). Леналидомид-зависимую деградацию NanoLuciferase при содействии IKZF3 136-180 и 236-249 наблюдали при всех протестированных концентрациях ДНК. Большую часть деградаций (~60%) наблюдали в клетках, трансфицированных с помощью 5 нг ДНК (ФИГ. 1B). Что важно, леналидомид-зависимая деградация блокировалась при обработке MG132, что указывает на то, что леналидомид-зависимая деградация белка-мишени является зависимой от протеасомы (ФИГ. 1B). При обработке циклогексамидом не наблюдали заметного снижения леналидомид-зависимой деградации NanoLuciferase (данные не показаны).
Пример 2. Оценка метки деградации на основе IKZF3 посредством вестерн-блоттинга
Леналидомид-зависимую деградацию NanoLuciferase при содействии IKZF3 136-180 и 236-249 оценивали посредством вестерн-блоттинга. Вектор pNL1.1CMV, кодирующий NanoLuciferase с меткой IKZF3 136-180 и 236-249, описанную выше, трансфицировали в клетки 293GT и клетки 293GT с нокаутом (KO) по цереблону (CRBN). Затем трансфицированные клетки обрабатывали с помощью 100 мкМ, 10 мкМ, 1 мкМ, 0,1 мкМ, 0,01 мкМ или 0,001 мкМ леналидомида или DMSO в течение одного часа при 37°C. Образцы с предварительной обработкой обрабатывали с помощью 10 мкМ MG132 в течение одного часа при 37°C до обработки с помощью 100 мкМ леналидомида. Образцы осаждали, лизировали, прогоняли в геле для белков, переносили на мембрану, зондировали с антителом и проявляли с помощью пленки.
Данные дополнительно показывают, что IKZF3 136-180 и 236-249 могла содействовать леналидомид-зависимой деградации белка-мишени при возрастающих концентрациях леналидомида (IC50 = ~10 нМ) (ФИГ. 2). Леналидомид-зависимую деградацию NanoLuciferase не наблюдали в трансфицированных клетках 293GT CRBN KO или в клетках, предварительно обработанных с помощью MG132 (ФИГ. 2). Эти данные указывают на то, что леналидомид-зависимая деградация белка-мишени с меткой IKZF3 136-180 и 236-249 является зависимой от CRBN и протеасомы.
Пример 3. Разработка и оценка вариантов метки деградации на основе IKZF3
Чтобы определить, может ли более короткая метка деградации на основе IKZF3 содействовать леналидомид-зависимой деградации белка-мишени, разрабатывали следующие метки деградации на основе IKZF3: "IKZF3 136-180," которая содержала аминокислотные остатки 136-180 из IKZF3 (метка, содержащая аминокислотную последовательность под SEQ ID NO: 5); "IKZF3 145-170," которая содержала аминокислотные остатки 145-170 из IKZF3 (метка, содержащая аминокислотную последовательность под SEQ ID NO: 9) и "IKZF3 140-169," которая содержала аминокислотные остатки 140-169 из IKZF3 (метка, содержащая аминокислотную последовательность под SEQ ID NO: 24).
Кроме того, метки деградации на основе IKZF3 модифицировали с применением следующих стратегий:
(1) удаления N-концевых и/или C-концевых аминокислотных остатков;
(2) замены аминокислотных остатков 236-249, которые соответствуют альфа-спирали из IKZF3, аминокислотной последовательностью MALEKMALEKMALE (SEQ ID NO: 91) и/или
(3) мутирование остатка лизина в аминокислотном положении 245 в альфа-спирали из IKZF3 на аргинин или серин (т. е. путем введения мутации K245R или K245S, пронумерованной в соответствии с SEQ ID NO: 19).
Такие варианты метки деградации на основе IKZF3 сливали с N-концом NanoLuciferase и клонировали в вектор pNL1.1CMV, который имеет промотор CMV. 5 нг (в случае всех меток, которые не содержат остатки 236-249 из SEQ ID NO: 19) или 50 нг (в случае всех меток, которые содержат остатки 236-249 из SEQ ID NO: 19) каждой конструкции трансфицировали в клетки HEK293T. Трансфицированные клетки обрабатывали с помощью 100 мкМ, 10 мкМ, 1 мкМ, 0,1 мкМ, 0,01 мкМ или 0,001 мкМ леналидомида или DMSO-контроля в течение 2-4 часов при 37°C. Образцы с предварительной обработкой обрабатывали с помощью 10 мкМ MG132 в течение одного часа при 37°C до обработки с помощью 100 мкМ леналидомида. Деградацию белков измеряли с применением вестерн-блоттинга, как описано в примере 2.
Результаты двух исследований описаны ниже.
В первом исследовании IKZF3 136-180 и 236-249 (метка, содержащая аминокислотную последовательность под SEQ ID NO: 3) содействовала леналидомид-зависимой деградации NanoLuciferase (ФИГ. 3B). Мутирование остатка лизина в положении 245 (пронумерованном в соответствии с SEQ ID NO: 19) в аргинин (метка, содержащая аминокислотную последовательность под SEQ ID NO: 84) или серин (метка, содержащая аминокислотную последовательность под SEQ ID NO: 100) в незначительной степени воздействовало на способность метки опосредовать деградацию (ФИГ. 3B). Аналогичным образом, IKZF3 136-180 MALEK (метка, содержащая аминокислотную последовательность под SEQ ID NO: 85) и IKZF3 136-170 MALEK (метка, содержащая аминокислотную последовательность под SEQ ID NO: 86), в которых остатки 236-249 (пронумерованные в соответствии с SEQ ID NO: 19) были заменены на спираль MALEKMALEKMALE (SEQ ID NO: 91), также сохраняли способность содействовать леналидомид-зависимой деградации (ФИГ. 3B). В отличие от этого, IKZF3 140-170 MALEK (метка, содержащая аминокислотную последовательность под SEQ ID NO: 87), IKZF3 141-163 MALEK (метка, содержащая аминокислотную последовательность под SEQ ID NO: 88) и IKZF3 145-155 MALEK (метка, содержащая аминокислотную последовательность под SEQ ID NO: 89) не опосредовали леналидомид-индуцированную деградацию (ФИГ. 3B), что позволяет предположить, что по меньшей мере первые четыре аминокислоты HKRS (SEQ ID NO: 40) (положения 136-139, пронумерованные в соответствии с SEQ ID NO: 19) необходимы для деградации.
Во втором исследовании клетки, экспрессирующие NanoLuciferase с меткой IKZF3 136-180 или NanoLuciferase с меткой IKZF3 136-170 MALEK, обрабатывали различными дозами леналидомида в течение 2 часов и анализировали с помощью вестерн-блоттинга, как описано выше. Обе метки были способны опосредовать леналидомид-зависимую деградацию (ФИГ. 4A и 4B). Уровень деградация увеличивался по мере увеличения концентраций леналидомида (ФИГ. 4A и 4B). Кроме того, клетки, экспрессирующие NanoLuciferase с меткой IKZF3 136-180, обрабатывали с помощью 10 мкМ леналидомида в течение увеличивающихся временных промежутков перед вестерн-блоттинг-анализом. Деградация была заметна уже через 1 час и почти завершилась через 4 часа (ФИГ. 4C).
Пример 4. Оценка меток деградации на основе IKZF3, соединенных с транскрипционными факторами
Метки деградации на основе IKZF3 оценивали в отношении их способности содействовать деградации ассоциированного с меланогенезом транскрипционного фактора (MITF) или гомолога вирусного онкогена миелоцитоматоза птиц (MYC) посредством вестерн-блоттинга. В дополнение к меткам деградации на основе IKZF3 MITF и MYC также сливали с FLAG-меткой для содействия их обнаружению с применением антитела к FLAG.
В первом исследовании MITF с меткой IKZF3 136-180 и 236-249 или MITF с меткой IKZF3 136-180 проверяли в отношении их восприимчивости к леналидомид-зависимой деградации. Клетки трансфицировали с помощью конструкций pNL1.1CMV, кодирующих слияние MITF с меткой, и обрабатывали различными концентрациями леналидомида в течение 4 часов или обрабатывали с помощью 10 мкМ леналидомида в течение варьирующихся временных промежутков перед тем, как клетки подвергали вестерн-блоттинг-анализу. Некоторые клетки обрабатывали с помощью MG132 до обработки с помощью 100 мкМ леналидомида. DMSO применяли в качестве контроля со средой-носителем. Как показано на ФИГ. 5A и 5B, IKZF3 136-180 и 236-249 была более эффективной, чем IKZF3 136-180 в опосредовании леналидомид-зависимой деградации MITF. Уровень деградации коррелировал с концентрацией леналидомида (ФИГ. 5A) и продолжительностью обработки леналидомидом (ФИГ. 5B), что позволяет предположить, что уровень остаточных уровней белка-мишени можно тонко подстраивать путем изменения дозы леналидомида.
Во втором исследовании IKZF3 136-180 и 236-249 без лизина (вариант IKZF3 136-180 и 236-249, в которой каждый остаток лизина в метке был мутирован в аргинин) (метка, содержащая аминокислотную последовательность под SEQ ID NO: 4) тестировали в отношении ее способности опосредовать леналидомид-зависимую деградацию. Без ограничения какой-либо теорией, если леналидомид-зависимая деградация главным образом опосредована за счет убиквитинирования белка-мишени (в данном примере MITF), а не метки на основе IKZF самой по себе, замена всех остатков лизина в метке на аргинин может не оказывать значительного воздействия на уровень деградации. Как показано на ФИГ. 6A, 6B, 6C и 6D, замена всех остатков лизина в метке деградации IKZF3 136-180 и 236-249 не оказала значительного воздействия на способность данной метки опосредовать леналидомид-зависимую деградацию MITF, что позволяет предположить, что деградация меченого MITF преимущественно была вызвана убиквитинированием MITF, а не метки самой по себе. Как леналидомид, так и помалидомид эффективно содействовали деградации меченого MITF (ФИГ. 6D).
В третьем исследовании тестировали IKZF3 136-180 Q147H (вариант IKZF3 136-180, в который остаток глутамина в положении 147, пронумерованном на основе SEQ ID NO: 19, был заменен на гистидин) (SEQ ID NO: 27). Было показано, что глутамин в положении 147 является важным для индуцируемого IMiD связывания CRBN и деградации IKZF1 или IKZF3 ( et al., Science. 2014 Jan 17;343(6168):301-5, включенный в данный документ посредством ссылки во всей своей полноте). Как и ожидалось, замена Q147H блокировала способность IKZF3 136-180 опосредовать леналидомид-зависимую деградацию MITF (ФИГ. 7).
et al., Science. 2014 Jan 17;343(6168):301-5, включенный в данный документ посредством ссылки во всей своей полноте). Как и ожидалось, замена Q147H блокировала способность IKZF3 136-180 опосредовать леналидомид-зависимую деградацию MITF (ФИГ. 7).
В четвертом исследовании IKZF3 136-180 и 236-249 исследовали в отношении ее способности опосредовать леналидомид-зависимую деградацию другого транскрипционного фактора, гомолога вирусного онкогена миелоцитоматоза птиц (MYC). Клетки HEK293T, трансфицированные с помощью слитой молекулы, в которой IKZF3 136-180 и 236-249 был слит с N-концом MYC, обрабатывали с помощью различных концентраций леналидомида в течение 4 часов. Уровней меченого MYC, который был также слит с FLAG-меткой, оценивали посредством вестерн-блоттинга с применением антитела к FLAG. Как показано на ФИГ. 8, IKZF3 136-180 и 236-249 также опосредовала леналидомид-зависимую деградацию меченого MYC. Уровень деградации коррелировал с концентрацией леналидомида (ФИГ. 8).
Пример 5. Оценка меток деградации на основе IKZF3, соединенных с трансмембранными белками, посредством вестерн-блоттинга
Оценивали способность меток деградации на основе IKZF3 содействовать леналидомид-зависимой деградации однопроходных мембранных белков клеточной поверхности CD3-дзета, CD8, CD8/CD3-дзета, CD19 и CD22. Метку IKZF3 136-180 и 236-249 (метка, содержащая аминокислотную последовательность под SEQ ID NO: 2) сливали с C-концом однопроходных мембранных белков с применением 16GS-линкера GGGGSGGGGTGGGGSG (SEQ ID NO: 28). Вирусы создавали с использованием макси-препаратов CD3-дзета, CD8, CD8/CD3-дзета, CD19 и CD22 с меткой IKZF3 136-180 и 236-249, приобретенных в Genewiz. Стабильные линии клеток Jurkat трансдуцировали с помощью вирусов и обрабатывали с помощью 10 мкМ леналидомида в течение 4 часов до проведения анализа посредством вестерн-блоттинга. Все меченые мембранные белки дополнительно содержат V5-метку для содействия их обнаружению с применением антитела к V5.
Как показано на ФИГ. 9A, 9B, 9C и 9D, все протестированные конструкции были восприимчивы к леналидомид-зависимой деградации, хотя у разных конструкций уровень восприимчивости варьировался. Интересно отметить, что, по-видимому, существует корреляция между уровнем леналидомид-зависимой деградации и числом цитозольных аминокислот в белке-мишени (Фиг. 9A), поскольку белки-мишени с большим числом аминокислот в цитозоле подвергались деградации в большей степени.
В итоге, эти данные позволяют предположить, что метки деградации на основе IKZF3 могут быть способны опосредовать деградацию белков CD (и однопроходных мембранных белков в целом) в присутствии леналидомида.
Пример 6. Оценка меток деградации на основе IKZF3, соединенных с трансмембранными белками, посредством проточной цитометрии
Дозочувствительный эффект обработки леналидомидом на белки-мишени, слитые с метками деградации на основе IKZF3, оценивали посредством проточной цитометрии. В частности, анализ посредством проточной цитометрии проводили для определения того, было ли отличие между суммарным количеством подвергаемого деградации белка-мишени и суммарным количеством белка-мишени, экспрессируемого на клеточной поверхности.
Клетки Jurkat, экспрессирующие CD19 с меткой IKZF3 136-180 и 236-249, анализировали посредством проточной цитометрии через 0, 1, 6, 16 и 24 часа после обработки с помощью 1 мкМ или 10 мкМ леналидомида. CD19 окрашивали с помощью антитела к CD19 человека (BD Pharmingen 555413).
90% трансдуцированных клеток Jurkat экспрессировали CD19 на поверхности, при этом отсутствовала выявляемая экспрессия CD19 на исходных клетках Jurkat (ФИГ. 10E). Снижение средней интенсивности флуоресценции (MFI) и процента экспрессии CD19 наблюдали после того, как клетки обрабатывали леналидомидом в течение 16 часов или 24 часов, что может быть блокировано при обработке MG132 (ФИГ. 10C, 10D, 10E и 10F). Это отличается от того, что было видно при вестерн-блоттинг-анализе, описанном в примере 5, который показывает основное снижение уровней CD19 после 6-часовой обработки 10 мкМ леналидомида.
Эти данные показывают, что метка деградации на основе IKZF3, может использоваться для селективной деградации однопроходных трансмембранных белков.
Пример 7. Оценка химерных антигенных рецепторов (CAR), слитых с HilD-меткой и/или FurON, посредством вестерн-блоттинга
В данном примере химерный антигенный рецептор для CD19, CAR19, модифицировали с помощью HilD-метки и/или фуринового дегрона (FurON). FurON может служить в качестве переключателя, будучи слитым с молекулой CAR. FurON содержит два компонента: (1) дегрон или домен деградации, который представляет собой мутированный белковый домен, не способный принять правильную конформацию в отсутствие низкомолекулярного лиганда (например, базедоксифена), и (2) сайт расщепления фурином (ФИГ. 11). Без ограничения какой-либо теорией, в отсутствие низкомолекулярного лиганда (например, базедоксифена) домен деградации c неправильной укладкой/отсутствием укладки может подвергаться деградации под действием внутриклеточных путей деградации вместе с молекулой CAR, которая слита с доменом деградации (ФИГ. 11). В присутствии низкомолекулярного лиганда (например, базедоксифена) домен деградации принимает правильную конформацию, приводящую к экспозиции сайта расщепления фурином и удалению домена деградации (ФИГ. 11). В некоторых вариантах осуществления переключатель FurON может быть объединен с переключателем HilD (ФИГ. 12C). Объединение этих двух переключателей сможет увеличить скорость "выключения" экспрессии CAR и активности в присутствии факторов токсичности (ФИГ. 12C).
Полинуклеотидные последовательности, кодирующие CAR19 с HilD-меткой, клонировали в лентивирусный экспрессионный вектор pNGx-LV_v002. gBlock заказывали в IDT. В таблице 24 представлена информация об этих gBlock. Конструкция 765 содержит в направлении от N-конца к C-концу: сигнальный пептид, FurOn и CAR19. Конструкция 766 содержит в направлении от N-конца к C-концу: сигнальный пептид, FurON, CAR19, 16GS-линкер, HilD-метку и V5. Конструкция 767 содержит в направлении от N-конца к C-концу: сигнальный пептид, FurON, CAR19, 16GS-линкер и HilD-метку. Конструкция 768 содержит в направлении от N-конца к C-концу: сигнальный пептид, CAR19, 16GS-линкер, HilD-метку и V5. Конструкция 769 содержит в направлении от N-конца к C-концу: сигнальный пептид, CAR19, 16GS-линкер и HilD-метку. Конструкция 770 содержит в направлении от N-конца к C-концу: сигнальный пептид, CAR19, 16GS-линкер и HilD-метку без лизина. В HilD-метке без лизина (показана как "HilD-метка_без K" в таблице 24) каждый остаток лизина в метке был заменен на аргинин. Конструкция 771 содержит в направлении от N-конца к C-концу: сигнальный пептид, CAR19, HilD-метку и V5. Конструкция 6761 содержит в направлении от N-конца к C-концу: сигнальный пептид, CAR19, 16KGS-линкер, HilD-метку и V5. Конструкция 773 содержит в направлении от N-конца к C-концу: модифицированный сигнальный пептид, HilD-метку, сайт расщепления фурином и CAR19. Конструкция 774 содержит в направлении от N-конца к C-концу: сигнальный пептид, HilD-метку, сайт расщепления фурином и CAR19. Вкратце, gBlocks подвергали расщеплению, очищали с применением набора для очистки при ПЦР Qiagen MinElute (кат. № 28004) и лигировали в лентивирусных экспрессионный вектор pNGx-LV_v002. Полученные клоны подтверждали секвенированием.
Вирусы получали из макси-препаратов и использовали для трансдукции клеток JNL. Для трансдукции использовали либо 275 мкл вирусного супернатанта, либо 700 мкл. Клетки JNL представляют собой клетки Jurkat, сконструированные с геном люциферазы под контролем промотора NFAT. Трансдуцированные клетки JNL проверяли на экспрессию CAR в присутствии или в отсутствие обработки леналидомидом с применением вестерн-блоттинга.
Вкратце, клетки разводили до 0,5×106 в общем объеме 3 мл в 6-луночных чашках. Каждую клеточную линию высевали в две лунки (одну для DMSO, одну для обработки 10 мкМ леналидомида). Базедоксифен добавляли при конечной концентрации 1 мкМ в каждую лунку, которая содержала клеточную линию, экспрессирующую слияние, содержащее FurON. В случае всех клеточных линий добавляли либо конечную концентрацию 10 мкМ леналидомида, либо DMSO. Клетки инкубировали при 37°C и 5% CO2 в течение ночи.
Через 24 часа после обработки соединением, клетки осаждали, промывали с помощью PBS и лизировали с помощью 50 мкл буера RIPA буфер (Boston Bioproducts BP-115D), содержащего ингибиторы протеазы (Roche 04693124001). Лизаты центрифугировали, супернатант переносили в новые пробирки и количества белка определяли посредством анализа Лоури (BioRad 5000111). Каждый образец нормализовали до 30 мкг общего белка в объеме 20 мкл с помощью 4X буфера для образцов (Thermo Scientific NP0007) и 10X восстанавливающего средства (Thermo Scientific NP0009). Образцы подвергали вестерн-блоттинг-анализу с применением антитела мыши к V5 (Thermo Scientific MA5-15253) при разведении 1:1000, антитела мыши к актину (Sigma Aldrich A5441) при разведении 1:10000 и/или антитела мыши к CD3z (BD 551034) при разведении 1:1000.
Как и ожидалось, леналидомид не оказывал никакого воздействия на FurON-CAR19 без HilD-метки (ФИГ. 13A). В присутствии HilD-метки обработка с помощью 10 мкМ леналидомида приводила к почти полной деградации FurON-CAR19, независимо от присутствия V5-метки (ФИГ. 13B и 13C). Обработка 10 мкМ леналидомида также приводила к почти полной деградации всех конструкций CAR19-HilD, независимо от присутствия 16GS-линкера или V5-метки (ФИГ. 14A-14C). Леналидомид-зависимая деградация конструкции 770 (ФИГ. 14D), которая содержит HilD-метку без лизина (каждый остаток лизина в HilD-метке был заменен аргинином), позволяет предположить, что деградация CAR19 была опосредована в первую очередь убиквитинированием CAR19 самого по себе, а не HilD-метки.
Следующим шагом, посредством вестерн-блоттинга проверяли кинетику деградации CAR19, а также дозы леналидомида, эффективные для снижения экспрессии CAR19. Клетки JNL, экспрессирующие конструкцию 769 (CAR19_16GS_HilD-метка), разводили до 0,5×106 в общем объеме 3 мл в 6-луночных чашках. Каждую клеточную линию высевали в несколько лунок для разной обработки леналидомидом/разных моментов времени. После посева клеток образцы обрабатывали различными дозами (10 мкМ, 1 мкМ, 0,1 мкМ, 0,01 мкМ или 0,001 мкМ) леналидомида или DMSO в течение различных временных промежутков. Клетки собирали и подвергали вестерн-блоттингу, как описано выше, с применением антитела мыши к актину (Sigma Aldrich A5441) при разведении 1:10000 или антитела мыши к CD3-дзета (BD 551034) при разведении 1:1000.
10 мкМ леналидомида обеспечивали деградацию слитого белка CAR19-16GS-HilD-метка зависимым от времени образом (ФИГ. 15A). Деградация была заметна уже через 4 часа и, по-видимому, достигала максимального уровня деградации за 8 часов (ФИГ. 15A). Уровень деградации был стабильным от 8 до 24 часов, при этом отсутствовало заметное повторное возрастание белковой экспрессии (ФИГ. 15A).
Как показано на ФИГ. 15B, леналидомид обеспечивал деградацию слитого белка CAR19-16GS-HilD-метка при концентрациях уже 100 нМ. Деградация CAR19 была заметной при каждой дозе соединения, превышающей 100 нМ (ФИГ. 15B), что указывает на то, что отсутствовал эффект "высокой дозы" соединения. Титрование деградации белка, наблюдаемое при более низких концентрациях леналидомида, позволяет предположить, что деградация является подстраиваемой, и точные уровни CAR19 можно контролировать путем регулировки дозы леналидомида.
Пример 8. Оценка химерных антигенных рецепторов (CAR), слитых с HilD-меткой и/или FurON посредством проточной цитометрии
Следующим шагом, экспрессию CAR19 на поверхности стабильно трансдуцированных клеток JNL исследовали посредством проточной цитометрии. В день 1 трансдуцированные клетки JNL высевали с леналидомидом из расчета 10 мкМ или без него на 24 часа. Клетки, экспрессирующие конструкции FurON-CAR19 культивировали с леналидомидом или без него в присутствии или в отсутствие базедоксифена. В день 2 клетки собирали, окрашивали с применением биотинилированного белка L (Genscript, M00097), а затем стрептавидином, конъюгированным с PE (Jackson Lab, 016-110-084), и подвергали анализу посредством проточной цитометрии с применением устройства Fortessa.
В случае молекул, в которых HilD-метка была слита с C-концом CAR19 (конструкции 769, 771, 6761, 768 и 770), для трансдуцированных клеток показана экспрессия CAR на более 60% клеток (ФИГ. 16A, 16B, 16C, 16D и 16E). На исходных клетках JNL экспрессию CAR не выявляли (ФИГ. 16A, 16B, 16C, 16D и 16E). Обработка с помощью 10 мкМ леналидомида в течение 24 часов в значительной степени снижала экспрессию CAR на поверхности клеток (ФИГ. 16A, 16B, 16C, 16D и 16E). Следует отметить, что HilD-метка без лизина также опосредовала леналидомид-зависимое снижение экспрессии CAR на поверхности клеток (ФИГ. 16E).
В случае молекул, в которых HilD-метка была слита с сайтом расщепления фурином и затем с N-концом CAR19 (конструкции 773 и 774), для трансдуцированных клеток показана экспрессия CAR (ФИГ. 16F и 16G). Инкубирование с 10 мкМ леналидомида в течение 24 часов оказывало воздействия на экспрессию CAR на поверхности клеток (ФИГ. 16F и 16G).
Кроме того, конструкции FurON-CAR19 с HilD-меткой или без нее проверяли в отношении их экспрессии на поверхности клеток в условиях регуляции с помощью базедоксифена и/или леналидомида. Как показано на ФИГ. 17A, 17B и 17C, экспрессию CAR на поверхности клеток выявляли только в присутствии базедоксифена, а леналидомид-зависимое снижение уровней CAR на поверхности клеток наблюдали только, когда CAR19 был слит с HilD-меткой.
В таблице 25 представлено обобщение данных проточной цитометрии, показанных на ФИГ. 16A, 16B, 16C, 16D, 16E, 16F, 16G, 17A, 17B и 17C.
Следующим шагом, экспрессию CAR на поверхности клеток в присутствии протитрованной дозы леналидомида проверяли посредством проточной цитометрии. Вкратце, клетки JNL, стабильно трансдуцированные с помощью конструкции 769 (CAR19_16GS_HilD-метка) или конструкции 770 (CAR19_16GS_HilD-метка_без K), инкубировали с 8 различными концентрациями леналидомида (начиная с 2 мкМ для 4-часовой обработки или 1 мкМ для 20-часовой обработки) для определения дозозависимого эффекта. Затем клети анализировали посредством проточной цитометрии, как описано выше, с применением биотинилированного белка L (Genscript, M00097), а затем стрептавидином, конъюгированным с PE (Jackson Lab, 016-110-084).
Результаты для групп 4-часовой обработки показаны на ФИГ. 18A и 18B и в таблице 26. Результаты для групп 20-часовой обработки показаны на ФИГ. 18C, 18D, 18E и 18F и в таблице 27. После 4-часовой обработки леналидомидом определяли уменьшение MFI со слабым снижением % экспрессии CAR (% клеток, экспрессирующих CAR) (таблица 26). После 20-часовой обработки леналидомид более выражено снижал % экспрессии CAR и MFI дозозависимым образом (таблица 27, ФИГ. 18E и 18F). Отсутствовало значимое отличие между результатами для конструкции 769 (CAR19_16GS_HilD-метка) и результатами для конструкции 770 (CAR19_16GS_HilD-метка_без K), что позволяет предположить, что убиквитинирование могло происходить главным образом по остаткам лизина в белке-мишени, а не в HilD-метке самой по себе.
Пример 9. Оценка химерных антигенных рецепторов (CAR), слитых с HilD-меткой и/или FurON, с применением функциональных показателей
В данном примере проводили ряд исследований, чтобы определить, являются ли CAR19 и FurON-CAR19 функциональными, будучи мечеными с помощью HilD, и была ли деградация, индуцированная леналидомидом, достаточной для устранения функции CAR19 в клетках Jurkat.
В этом исследовании использовали линию клеток JNL, описанную выше, которая представляет собой линию клеток Jurkat, модифицированных с помощью NFAT-люциферазного репортера. Совместное культивирование клеток JNL, экспрессирующих CAR19, и B-клеток, экспрессирующих CD19, активирует передачу сигнала с помощью NFAT, что приводит к экспрессии люциферазы.
В первом исследовании высевали клетки JNL, экспрессирующие конструкцию 767 (FurON_CAR19_16GS_HilD-метка) или конструкцию 769 (CAR19_16GS_HilD-метка). Клетки JNL, экспрессирующие конструкцию 767 (FurON_CAR19_16GS_HilD-метка), инкубировали с 1 мкМ базедоксифена. Все клетки JNL обрабатывали с помощью 10 мкМ леналидомида в течение 4 часов или 24 часов. Клетки JNL, обработанные леналидомидом, инкубировали с клетками Nalm6, клетками K562 или клетками K562, экспрессирующими CD19, в течение 4 часов, 8 часов или 20 часов. Образцы обрабатывали с помощью Brightglo (Promega E2620), следуя протоколу производителя, и люминесценцию считывали на Perkin Elmer Viewlux с 5-секундным или 40-секундным воздействием.
Как и ожидалось, сигналы люминесценции наблюдали только тогда, когда клетки JNL, экспрессирующие конструкцию 769 (CAR19_16GS_HilD-метка), культивировали совместно с CD19+ клетками-мишенями (клетки Nalm6 и клетки K562, экспрессирующие CD19) (ФИГ. 19A). Обработка леналидомидом снижала сигнал люминесценции до фоновых уровней в каждом случае, за исключением 4-часовой обработки леналидомидом/4-часовой обработки клеткой-мишенью (ФИГ. 19A). Одним возможным объяснением является то, что клетки JNL, экспрессирующие конструкцию 769 (CAR19_16GS_HilD-метка), следует обрабатывать леналидомидом в течение более 8 часов, чтобы снизить сигнал люминесценции в данном анализе с NFAT-люциферазным репортером. После вычитания фоновых сигналов (сигналов от среды для образца), обработка леналидомидом снижала сигнал люминесценции на ~95% у клеток JNL, экспрессирующих CAR, культивируемых совместно с клетками K562, экспрессирующими CD19, и на ~88% у клеток JNL, экспрессирующих CAR, культивируемых совместно с клетками Nalm6. Эти данные позволяют предположить, что HilD-метка является достаточной, чтобы в значительной степени снизить функцию CAR19 в присутствии леналидомида.
Аналогичным образом, сигналы люминесценции наблюдали только тогда, когда клетки JNL, экспрессирующие конструкцию 767 (FurON_CAR19_16GS_HilD-метка), культивировали совместно с CD19+ клетками (клетки Nalm6 и клетки K562, экспрессирующие CD19) в присутствии базедоксифена (ФИГ. 20A). Обработка леналидомидом снижала сигнал люминесценции до фоновых уровней в образцах, совместно обработанных базедоксифеном (ФИГ. 20A). После вычитания фоновых сигналов (сигналов от среды для образца), обработка леналидомидом снижала сигнал люминесценции на ~90% у клеток JNL, экспрессирующих CAR, культивируемых совместно с клетками K562, экспрессирующими CD19, и на ~83% у клеток JNL, экспрессирующих CAR, культивируемых совместно с клетками Nalm6 (ФИГ. 20B). Эти данные позволили предположить, что в случае конструкции на основе CAR19, модифицированной с помощью как FurON, так и HilD-метки, функция CAR19 может увеличиваться при обработке базедоксифеном, а затем снижаться при обработке леналидомидом.
Второе исследование проводили для определения восприимчивости CAR19 с HilD-меткой или FurON-CAR19 к зависимой от леналидомида деградации. Высевали клетки JNL, экспрессирующие конструкцию 765 (FurON_CAR19), конструкцию 767 (FurON_CAR19_16GS_HilD-метка), конструкцию 769 (CAR19_16GS_HilD-метка) или конструкцию 770 (CAR19_16GS_HilD-метка_без K). Клетки JNL, экспрессирующие конструкцию 765 (FurON_CAR19) или конструкцию 767 (FurON_CAR19_16GS_HilD-метка), инкубировали с 1 мкМ базедоксифена. Было три группы обработки: "20 ч до клеток-мишеней" (суммарная 44-часовая обработка леналидомидом), "4 ч до клеток-мишеней" (суммарная 28-часовая обработка леналидомидом) и "16 ч после клеток-мишеней" (суммарная 8-часовая обработка леналидомидом). В случае группы "20 ч до клеток-мишеней" MG132 (конечная концентрация 10 мкМ) добавляли к трансдуцированным клеткам JNL через три часа после добавления базедоксифена, леналидомид добавляли через 1 час после добавления MG132, а клетки K562 или клетки-мишени K562, экспрессирующие CD19, добавляли через 20 часов после добавления леналидомида. В случае группы "4 ч до клеток-мишеней" MG132 (конечная концентрация 10 мкМ) добавляли к трансдуцированным клеткам JNL через 19 часов после добавления базедоксифена, леналидомид добавляли через 1 час после добавления MG132, а клетки K562 или клетки-мишени K562, экспрессирующие CD19, добавляли через 4 часа после добавления леналидомида. В случае группы "16 ч после клеток-мишеней" клетки K562 или клетки-мишени K562, экспрессирующие CD19, добавляли к трансдуцированным клеткам JNL через 24 часа после добавления базедоксифена, MG132 (конечная концентрация 10 мкМ) добавляли через 15 часов после добавления клеток-мишеней, а леналидомид добавляли через 1 час после добавления MG132. В случае совместного культивирования с клетками-мишенями клетки K562 или клетки K562, экспрессирующие CD19, добавляли в каждую лунку, содержащую клетки JNL, и культивировали в системе для высокопроизводительного скрининга GNF Systems Ultra в инкубаторе при 37°C и 5% CO2. Через 24 часа после добавления клеток K562 или клеток K562, экспрессирующих CD19, образцы обрабатывали с помощью Brightglo (Promega E2620), следуя протоколу производителя, и люминесценцию считывали на Perkin Elmer Viewlux с 5-секундным воздействием.
Как и ожидалось, трансдуцированные клетки JNL реагировали только на клетки K562, экспрессирующие CD19, но не на клетки K562 (ФИГ. 21A, 21B, 21C и 21D). При отсутствии HilD-метки обработка леналидомидом не оказывала воздействие на ответ с участием репортера (ФИГ. 21A). В присутствии базедоксифена в клетках JNL, экспрессирующих конструкцию 767 (FurON_CAR19_16GS_HilD-метка), показана активация репортера после совместного культивирования с клетками K562, экспрессирующими CD19, и такая активация репортера ингибировалась леналидомидом дозозависимым образом (ФИГ. 21B). IC50 находится в диапазоне ~5 мкМ - 0,1 мкМ. IC50 леналидомида демонстрируют сдвиг в сторону уменьшения активности с течением времени с самой высокой IC50 при 8-часовой обработке ("16 ч после клеток-мишеней" на ФИГ. 21B) и самой низкой IC50 при 44-часовой обработке ("20 ч до клеток-мишеней" на ФИГ. 21B). Самые высокие дозы леналидомида снижали сигнал люминесценции на 100% в группе 44-часовой обработки ("20 ч до клеток-мишеней" на ФИГ. 21B) и группе 28-часовой обработки ("4 ч до B-клеток" на ФИГ. 21B) и на 90% в группе 8-часовой обработки ("16 ч после клеток-мишеней" на ФИГ. 21B). Леналидомид также ингибировал активацию NFAT-люциферазного репортера в клетках JNL, экспрессирующих конструкцию 769 (CAR19_16GS_HilD-метка) дозозависимым образом (ФИГ. 21C). IC50 находятся в диапазоне от 1 мкМ до 0,05 мкМ, при этом наблюдается уменьшение IC50 при увеличении времени обработки леналидомидом. 2-3 самые высокие дозы леналидомида (10 мкМ, 3,16 мкМ и 1 мкМ) снижали сигнал люминесценции на почти 100% (ФИГ. 21C). Аналогичным образом, леналидомид дозозависимым способом ингибировал активацию репортера в клетках JNL, экспрессирующих конструкцию 770 (CAR19_16GS_HilD-метка_без K) (ФИГ. 21D). IC50 находятся в диапазоне от 1 мкМ до 0,05 мкМ, при этом наблюдается уменьшение IC50 при увеличении времени обработки леналидомидом. 2-3 самые высокие дозы леналидомида (10 мкМ, 3,16 мкМ и 1 мкМ) снижали сигнал на почти 100% (ФИГ. 21D). Данный ответ, наблюдаемый в случае CAR19, слитого с HilD-меткой без лизина, был аналогичен ответу, наблюдаемому в случае CAR19, слитого с HilD-меткой дикого типа, что позволяет предположить, что деградация CAR19 главным образом обусловлена убиквитинированием остатков лизина на CAR19, а не остатков лизина на HilD-метке.
28-часовая обработка 10 мкМ леналидомида вызывала снижение экспрессии CAR19 у всех клеточных линий, экспрессирующих молекулу CAR с HilD-меткой, и это снижение можно частично восстановить с помощью ингибитора протеасомы MG132 (данные не показаны). Клетки JNL, экспрессирующие различные конструкции, невозможно было сравнивать непосредственно, поскольку они имели различные уровни экспрессии CAR, что приводило к различным уровням ответов на CD19+ клетки. Вместо этого производили сравнения между обработками в одних и тех же клеточных линиях (ФИГ. 22A, 22B, 22C и 22D). В случае конструкций, содержащих FurON, обработка базедоксифеном была необходима для активации NFAT-люциферазного репортера в присутствии CD19+ клеток (ФИГ. 22A и 22B). В отсутствие HilD-метка обработка леналидомидом не оказывала воздействия на сигнал люминесценции и MG132 мог усиливать сигнал (ФИГ. 22A). В присутствии HilD-метки обработка леналидомидом снижала активацию репортера, индуцированную CD19, до почти фоновых уровней (~80%), и такое снижение могло быть почти восстановлено под действием ингибитора протеасомы MG132 (ФИГ. 22B). Конструкциям, которые не содержат FurON, не требовался базедоксифен для активации репортера (ФИГ. 22C и 22D). Клетки JNL, экспрессирующие CAR19 с HilD-меткой или CAR19 с HilD-меткой без лизина, характеризовались аналогичными ответами на леналидомид: сигнал NFAT-репортера, индуцированный CD19, в значительной степени снижался под действием леналидомида, и такое снижение могло быть частично восстановлено за счет MG132 (ФИГ. 22C и 22D).
Пример 10. Оценка тaу-белков с HilD-меткой
Способы
Конструкции
Конструкции создавали посредством синтеза из генных блоков (IDT) и введения в полученные в лаборатории плазмиды путем сборки по Гибсону. В таблице 28 перечислены последовательности из конструкций, используемых в данном примере.
Трансфекция биотинлигазы и иммнопреципитация с помощью биотина
Клетки HEK293T, выращиваемые в 6-луночных чашках для культур тканей, трансфицировали с помощью 3 микрограммов CRBN с FLAG-меткой и 2,1 микрограмма указанной конструкции слияния на основе тау-белка с применением 6 мкл липофектамина 2000 в конечном объеме 200 мкл среды Optimem. Через 48 часов после трансфекции клетки обрабатывали с помощью 50 мкМ биотина (разведенный из 100 мкМ исходного раствора, полученного в DMSO) и либо DMSO (1 к 10000), либо 1 мкмоль/л леналидомида. Клетки инкубировали в течение 21 часа, затем лизировали после промывки в ледяном PBS с помощью 300 мкл ледяного буфера M-PER (Thermo Fisher № 78501), содержащего 1X ингибиторы протеазы Halt (Thermo Fisher № 1861281). Клеточный лизат просветляли и белок определяли количественно с помощью реакции BCA и концентрацию белка нормализовали в буфере M-PER. 20% клеточного лизата (60 мкл) разводили в 4 раза в лизирующем буфере IP (15 мМ Tris, pH 7,5, 120 мМ NaCl, 25 мМ KCl, 2 мМ EGTA, 2 мМ EDTA, 0,5% Triton X-100, 1X ингибитор протеазы Halt) и инкубировали с 50 мкл магнитных Dynabeads со стрептавидином M-280 (Thermo Fisher, кат. № 11205D) в течение 30 минут при комнатной температуре. Впоследствии микрогранулы трижды промывали с помощью лизирующего буфера IP, затем окончательно растворяли в 20 мкл буфера M-PER, содержащего ингибиторы протеазы. 4X буфер NuPage LDS добавляли в этот подвергнутый иммунопреципитации материал до конечной концентрации 1X, и клеточные лизаты разводили аналогичным образом. Затем добавляли 10X восстанавливающий буфер NuPage до концентрации 1X и образцы нагревали до 95°C в течение 5 минут. Клеточный лизат или иммунопреципитированный материал прогоняли на геле 10% Bis-Tris Criterion XT (BioRad 3450111), подвергали блоттингу (TurboBlot) и инкубировали с первичными антителами, как указано. Инкубировали с вторичными антителами козы к белкам кролика, конъюгированными с LiCor RDye 800CW (№ 925-32211) или 680 RD (№ 925-68070), и сигнал измеряли на станции визуализации Li-Cor Odyssey CLx.
Анализ изображений слияний HilD-тау-YFP в клетках HEK293T
За один день до трансфекции клетки HEK 293T дикого типа или клетки HEK293T с нокаутом (KO) по CRBN высевали из расчета 22,5 тыс. клеток на лунку в 96-луночные планшеты. Затем клетки трансфицировали с помощью 0,02 микрограмма конструкции слияния HilD-тау (P301S). Через один день после трансфекции лунки обрабатывали с помощью варьирующих концентраций леналидомида. После обработки на протяжении ночи клетки фиксировали в конечном растворе, содержащем 4% PFA и 4% сахарозы, в течение 15 минут. Фиксированные клетки промывали с помощью PBS. Затем клетки инкубировали с красителями Hoechst в разведении 1:5000 и HCS в разведении 1:10000 в течение пятнадцати минут, промывали, затем визуализировали.
Планшеты визуализировали на Incell Analyzer 6000 с применением 20X объектива захвата изображения и каналов DAPI, FITC и Cy5. Данные изображений затем определяли количественно с помощью CellProfiler, при этом ядро клетки вычленяли по окрашиванию красителем Hoechst и затем тело клетки идентифицировали путем расширения ядерного объекта до краев вычлененной клетки, идентифицированный с помощью окрашивания Cell mask. Данный клеточный объект затем использовали для измерения интенсивности FITC, соответствующей HilD-тау (P301S)-YFP.
Трансфекция HEK293T и количественное определение деградации HilD-тау посредством вестерн-блоттинг-анализа
За один день до трансфекции высевали клетки HEK293T из расчета плотности 150000 на лунку в 24-луночный планшет. Затем клетки трансфицировали с помощью 0,175 микрограмма HilD-тау (дикого типа). Через четыре часа или 24 часа после трансфекции лунки обрабатывали с помощью различных доз леналидомида. Клетки инкубировали в течение ночи. Затем клетки промывали с помощью ледяного PBS и лизировали в 85 мкл буфера N-PER (Thermo Fisher № 87792), дополненного ингибиторами протеазы и фосфатазы Halt. Планшеты инкубировали на льду при периодическом встряхивании в течение 15 минут. Затем лизат просветляли центрифугированием при 15000g, 4°C в течение 15 минут. Буфер LDS и восстанавливающее средство добавляли к просветленному лизату и затем образцы нагревали при 95°C в течение 8 минут. Образцы прогоняли на геле с 10% bis-tris при 150 В в течение 70 минут. Блоты переносили с помощью Biorad turboblot (настройки для разнородной молекулярной массы). Блоты зондировали с помощью DAKO-тау (общий тау-белок) (Dako № A0024), антитела к актину (Cell signaling technologies № 3700S) и AT8 (фосфорилированный тау-белок) (Thermo Fisher #MN1020). Блоты проявляли с помощью хемилюминесцентного субстрата Supersignal west (Thermo Fisher № 34095).
Количественное определение полосок вестерн-блоттинга проводили в соответствии с Molecular Psychiatry (2017) 22, 417-429.
Иссечение и нуклеофекция нейронов крысы
Кору головного мозга крыс выделяли из эмбрионов крыс возрастом 18,5 дня. Суспензии отдельных клеток получали путем 15-минутного расщепления при 37°C под действием папаина (Brainbits № PAP), разведенного в 3 мл раствора Hibernate E (без Ca) (Brainbits № HECA); затем добавляли ДНКазу (до концентрации, составляющей 0,5 мг/мл); растирали; инкубировали 10 минут при 37°C; растирали и, в конечном итоге, фильтровали через фильтр для клеток с диаметром пор 40 мкм. Примерно 8 миллионов клеток подвергали нуклеофекции с применением раствора P3 (набор для нуклеофекции Lonza № V4XP-1024) с 2 микрограммами указанных плазмид. Использовали программу CU-133 на нуклеофекторе 4D. Затем клетки разводили в среде Neurobasal (Life Technologies № 21103), содержащей 1% сыворотки крови, и высевали при плотности 80000 клеток на лунку в 96-луночный планшет Biocoat (Corning № 356640). Следует отметить, что после нуклеофекции наблюдали значительную гибель клеток, что обусловило высокую исходную плотность посева. На следующий день среду полностью заменяли на среду, не содержащую сыворотку крови.
Среду заменяли на 50% через каждые 7 дней. В день 9 в среду добавляли соединения при указанных конечных концентрациях. Визуализацию сигнала YFP проводили в указанные интервалы с применением системы InCell 6000 (General Electric), соединенной с инкубатором Liconic Instruments IC (кат. № 391180700)/хранилищем для планшетов с помощью робота Thermo Scientific Orbitor RS.
Нуклеофекция нейронов человека
Плюрипотентные стволовые клетки человека (hPSC) поддерживали в среде E8 (Stem Cell Technologies) на планшетах для культур тканей, покрытых витронектином. Конфлюэнтные монослои hPSC переводили на нейрональный путь дифференцировки за счет замены среды на Ph I (прописи сред см. ниже). Через семь дней после индукции клетки подвергали диссоциации в суспензию отдельных клеток с помощью аккутазы, высевали из расчета 1,5 миллиона клеток на миллилитр во флаконы с перемешиванием со средой Ph II/III, дополненной 2 микромоль/л тиазовивина и 10 нг/мл FGF2 (конечная концентрация), и инкубировали при 37°C на микромешалке при 40 об/мин в течение 4 дней. Затем среду заменяли на Ph II/III и нейросферы дополнительно культивировали в течение 17 дней при 60 об/мин, заменяя среду на 50% два раза в неделю. В день 28 среду заменили на Ph IV и культуры поддерживали еще 21 день при замене среды на 50% два раза в неделю. Начиная с дня 49 культуры переключали на среду Ph V для поддержания и диссоциации с помощью набора с папином (Worthington Sciences) для распластывания нейронов на планшетах, покрытых ламинином, фибронектином и матригелем. Суспензию отдельных клеток подвергали нуклеофекции (10 миллионов клеток на реакцию), с использованием 2 микрограммов конструкции. 80000 клеток на лунку высевали в 96-луночные планшеты. Нейроны инкубировали на среде для фазы 5+бластицидин. Среду заменяли (50%) два раза в неделю.
Среда для фазы I: основа: усовершенствованная DMEM/F12; Glutamax (1X) (Life Technologies № 35050); пенициллин/стрептомицин (1x) (Life Technologies № 15140); N-ацетил-цистеин (500 микромоль/л); гепарин (2 микрограмма/мл); SB431542 (10 микромоль/л); LDN193189 (100 нМ); XAV939 (2 микромоль/л); добавка N2 (0,5% объем/объем).
Среда для фазы II/III: основа: усовершенствованная DMEM/F12; Glutamax (1X); пенициллин/стрептомицин (1X); N-ацетил-цистеин (500 микромоль/л); гепарин (2 микрограмма/мл); добавка N2 (0,5% объем/объем); добавка B27 (1% объем/объем) (Lilfe Technologies № 17504); FGF2 (10 нг/мл первые 4 дня; 2,5 нг/мл остальное время фазы II/III); LDN193189 (100 нМ); CHIR99021 (20 нМ); ретиноевая кислота (5 нМ).
Среда для фазы IV: основа: усовершенствованная DMEM/F12; GlutaMax (1x); пенициллин/стрептомицин (1x); гепарин (2 микрограмма/мл); добавка N2 (0,5% объем/объем); добавка B27 (0,4% объем/объем); форсколин (10 микромоль/л); хлорид кальция (600 микромоль/л)
Среда для фазы V: основа: усовершенствованная DMEM/F12; GlutaMax (1x); пенициллин/стрептомицин (1x); гепарин (2 микрограмма/мл); добавка N2 (0,5% объем/объем); добавка B27 (1% объем/объем); форсколин (10 микромоль/л); хлорид кальция (600 микромоль/л); BDNF (5 нг/мл); GDNF (5 нг/мл).
Получение нерастворимой фракции тау-белка
Выделение саркозил-нерастворимой фракции проводили у 6-месячных трансгенных мышей 58/4 (tg/tg), полученной в лаборатории трансгенной по тау-белку мышиной модели, которая сверхэкспрессирует полноразмерную изоформу 0N4R тау-белка человека с мутацией P301S. Вкратце, ткань головного мозга, выделенную из мышей, гомогенизировали при соотношении 9:1 (объем/вес) в высокосолевом буфере (10 мМ Tris-HCl, pH 7,4, 0,8 NaCl, 1 мМ EDTA и 2 мМ дитиотреитола) с ингибитором протеазы и фосфатазы и 0,1% саркозила. Гомогенат центрифугировали при 10000g в течение 10 минут при 4°C и супернатант собирали. Осадок повторно экстрагировали дважды с применением тех же буферных условий и все супернатанты объединяли. В супернатанты добавляли дополнительное количество саркозила для достижения конечной концентрации саркозила 1%. После 1-часового покачивания при комнатной температуре образец центрифугировали при 280000 g в течение 1 часа при 4°C. В конечном итоге, полученный осадок ресуспендировали в PBS (300 мкл/г ткани) и подвергали непродолжительному воздействию ультразвука (20% мощность при 10-секундных циклах, повторяемых 10 раз) с применением ручного зонда (QSonica). Эту конечную фракцию хранили при -80°C до использования, и она называлась саркозил-нерастворимой фракцией тау-белка.
Результаты
Получали слияния HilD-тау, содержащие мутации тау-белка, обуславливающие склонность к образованию скоплений, для создания инструментов для отслеживания деградации склонных к образованию скоплений токсичных форм тау-белка (ФИГ. 23).
В первом эксперименте тестировали, может ли слияние HilD-метки с тау-белком индуцировать привлечение E3-лигазы цереблон (CRBN) за счет обработки с помощью иммуномодулирующего лекарственного средства леналидомида,. Получали слияния HilD-тау-биотинлигаза (ФИГ. 24A). Биотинлигаза, после воздействия на нее биотином, генерирует реакционно-способную молекулу биотина, которая ковалентно связывается с ближайшими белками в радиусе десятых долей нанометра. При обработке леналидомидом, но не в контрольных условиях, HilD-тау-биотинлигаза вызывает устойчивое биотинилирование конструкции CRBN с FLAG-меткой, которую трансфицируют совместно с конструкциями HilD-тау-биотинлигаза в клетки HEK293T-(ФИГ. 24B). Это подтверждает, что HIlD-метка может привлекать CRBN к тау-белку за счет образования тройного комплекса с леналидомидом.
Следующим шагом, проверяли, может ли тау-белок подвергаться деградации при привлечении CRBN в гетерологичных клетках. Клетки HEK293T трансфицировали токсичной, склонной к образованию скоплений формой тау-белка, 0N4R тау P301S, слитой с HilD-меткой на N-конце и репортерным YFP (желтым флуоресцентным белком) на C-конце. Экспрессия этой конструкции с течением времени приводит к токсичности для клеток. Обработка с помощью леналидомида снижала экспрессию YFP (ФИГ. 25A и 25B) и улучшала жизнеспособность клеток HEK (ФИГ. 25C). Это указывает на то, что слияние HilD-тау можно использовать для оказания цитопротекторного действия в виде деградации токсичных тау-белков, обнаруживаемых при нейродегенеративных заболеваниях.
Кроме того, тестировали, будет ли тау-белок, не содержащий YFP-метку, подвергаться деградации в клетках HEK293T. Обработка леналидомидом снижала уровни тау-белка, как определяли количественно посредством вестерн-блоттинг-анализа в сравнении контролем загрузки актином (ФИГ. 26A). Интересно отметить, что уменьшение степени экспрессии тау-белка путем снижения количества трансфицированной ДНК увеличивает эффективность деградации, в частности, фосфорилированной формы тау-белка (ФИГ. 26A, нижние панели). Это позволяет предположить, что система может применяться для исследования мощности системы E3-лигазы и протеасомы для деградации различных уровней тау-белка, и, кроме того, что данная система может применяться для исследования селективной уязвимости специфических форм токсичного белка к индуцируемой деградации. Усиленное снижение содержания фосфорилированного тау-белка позволяет предположить, что либо данный конкретный подтип тау-белка является более восприимчивым к деградации, либо фрагмент тау-белка, содержащий данный эпитоп, подвергается большей деградации, чем остальные изоформы тау-белка.
В серии контрольных экспериментов, проводимых, чтобы дополнительно подтвердить, что деградация тау-белка была опосредована за счет привлечения CRBN-E3-лигазы, деградацию HilD-тау или HilD-тау (P301S)-YFP тестировали в клетках HEK293T, в которых отсутствовал CRBN, и подтверждалось, что деградация не происходила (ФИГ. 26B и 26C). Кроме того, деградация была чувствительна к ингибитору неддилирования MLN4924 (ФИГ. 26D). Неддилирование является существенно важным для активности E3-лигазы CRBN, что указывает на то, что убиквитинирующая активность CRBN необходима для нацеленной деградации тау-белка.
Следующим шагом, исследовали, может ли тау-белок подвергаться деградации в нейронах, которые представляют собой связанный с заболеванием тип клеток при нейродегенеративных заболеваниях, опосредованных тау-белком, и будет ли данный способ деградации, за счет убиквитинирования тау-белка, приводить в образованию агрегированного тау-белка в качестве побочного продукта. Во-первых, установили, что слияния HilD-тау (P301S)-YFP были способны образовывать скопления при обработке нейронов, подвергнутых нуклеофекции с помощью данной конструкции, нерастворимой фракцией из головного мозга грызунов, выделенного из трансгенной мыши, сверхэкспрессирущей мутантный тау-белок. Скопления HilD-тау (P301S)-YFP были хорошо заметны, на что указывает интенсивная точечная флуоресценция YFP внутри тела клетки и дендритов нейронов (ФИГ. 27).
Кроме того, тестировали чувствительность деградации HilD-тау (P301S)-YFP в первичных кортикальных нейронах крысы, полученных из эмбриональной ткани, а также в трансфицированных нейронах и предшественниках нейронов из нейросфер, полученных из эмбриональных стволовых клеток человека (ФИГ. 28 и 29). В первичных нейронах HilD-тау (P301S)-YFP тестировали в отношении деградации, индуцируемой леналидомидом, как отдельно, так и при совместной трансфекции с цереблоном человека с FLAG-меткой. Хотя сообщалось, что так называемые иммуномодулирующие лекарственные средства, такие как талидомид и леналидомид, проявляют различные эффекты, такие как тератогенность, у грызунов и людей, в данной системе леналидомид индуцировал деградацию HilD-тау-YFP даже тогда, когда он не трансфицировался совместно с CRBN человека (ФИГ. 28). Это указывает на то, что данная система может работать в системах грызунов, как, например, при нокине HilD-тау у трансгенных мышей для оценки воздействия деградации тау-белка на животных моделях нейродегенеративных заболеваний. Для конструкций HilD-тау-YFP продемонстрировано внутриклеточное распределение в нейронах, соответствующее физиологической локализации тау-белка в теле клетки и отростках. Деградация под действием леналидомида приводила к обширному снижению уровней тау-белка по всему телу нейрона, что указывает на то, что систему можно использовать для подтверждения того, что E3-лигаза CRBN, по-видимому, распределена по всем компартментам тела нейронов. Применение YFP-маркера в данной системе также делает возможным прямое определение кинетики деградации с применением повторной визуализации живых клеток с течением времени. Деградация была устойчивой в нейронах как грызунов, так и человека (ФИГ. 29), что служит подтверждением принципа целенаправленной деградации тау-белка в нейронах. Ни в одном случае не было каких-либо заметных признаков образования агрегированного тау-белка за счет опосредованного леналидомидом привлечения CRBN.
Поскольку система HilD-тау может быть индуцирована для образования скоплений, предполагается, что ее можно использовать для оценки ситуаций, при которых агрегированный тау-белок может подвергаться убиквитинированию и деградации под действием протеасомы или не может.
Пример 11. Оценка CAR19-HilD в клетках Jurkat
В данном исследовании проверяют кинетику влияния леналидомида на CAR19-HilD в клетках Jurkat и то, могла ли экспрессия CAR19 в клетках восстанавливаться после отмывки леналидомида.
Способы
Обработка клеток. Клетки Jurkat, трансдуцированные с помощью CAR19-16GS-HilD-метка, разводили и высевали в два флакона. После посева клеток один флакон обрабатывали с помощью DMSO, а другой с помощью 10 мкМ леналидомида для сбора с течением времени. По 3 мл клеток из каждого флакона собирали для проточной цитометрии и вестерн-блоттинга через 1, 2, 4, 6, 8, 12 и 24 часа после обработки соединением. Клеток во флаконе, обработанном леналидомидом, разделили на два флакона в момент времени 24 часа. Один пометили как "отмывка", а другой представлял собой "обработку". Леналидомид вымывали из "отмывочных" клеток путем центрифугирования при 300g, и их трижды ресуспендировали в свежей, а в другой отделенной половине был остаточный леналидомид, присутствующий в среде ранее (обработку 10 мкМ леналидомида проводили только один раз). Клетки собирали через 1, 2, 4, 6 часов после отмывки и через 36, 48, 60 и 72 часов после обработки соединением.
Вестерн-блоттинг. Клетки осаждали, промывали с помощью PBS и осадки лизировали с помощью 50 мкл буфера RIPA (Boston Bioproducts BP-115D) с ингибиторами протеазы (Roche 04693124001). Лизаты центрифугировали, супернатант переносили в новые пробирки и количества белка определяли посредством анализа Лоури (BioRad 5000111). Каждый образец нормализовали до 30 мкг общего белка в объеме 20 мкл с помощью 4X буфера для образцов (Thermo Scientific NP0007) и 10X восстанавливающего средства (Thermo Scientific NP0009). Образцы прогоняли на акриламидном геле с 4-12% Bis-Tris (Thermo Scientific WG1402BOX). Гели прогоняли в двух повторностях, одну для зондирования антителом к актину, а другую антителом к V5 или CD3Z. Гели переносили на нитроцеллюлозные мембраны и мембраны инкубировали в течение ночи в 3% молоке в TBS-0,1% Tween-20 с одним из следующих антител: антитело мыши к актину (Sigma Aldrich A5441) при разведении 1:10000 и антитело мыши к CD3z (BD 551034) при разведении 1:1000. На следующий день блоты промывали в TBS-0,1% Tween-20, помещали в 3% молоко в TBS-0,1% Tween-20 с вторичным антителом овцы к белкам мыши, конъюгированным с HRP (GE Healthcare NA931), в разведении 1:10000 при комнатной температуре в течение 1 часа, затем блоты промывали и проявляли с помощью ECL (Thermo Scientific 34076).
Проточная цитометрия. Клетки собирали в планшет с u-образным дном и промывали с применением 1X PBS. Промытые клетки окрашивали с помощью 100 мкл биотинилированного белка L (Genscript M00097) с концентрацией 1 мкг/мл в разведении 1:1000. Первичное антитело инкубировали при 4°C в течение 45 минут. После инкубации клетки промывали с применением PBS. Клетки инкубировали при 4°C со стрептавидином, конъюгированным с PE (Jackson Lab 016-110-084), в разведении 1:300 в течение 30 мин. Клетки промывали дважды с помощью PBS и суспендировали в 100 мкл буфера для фиксации (2% параформальдегид в PBS) в течение 10 минут при комнатной температуре. Фиксированные клетки промывали с помощью PBS и суспендировали в 150 мкл PBS. Затем данные об этих клетках собирали с применением анализатора клеток BD LSRF Fortessa. Мертвые клетки исключали на основании размера с использованием графика FSC и SSC. Живые клетки анализировали в отношении их экспрессии PE-CAR. Результаты FACS гейтировали с применением неокрашенных клеток JNL из исходной линии и для каждого образца регистрировали 10 тыс. событий.
Результаты
Как показано с помощью вестерн-блоттинга на ФИГ. 30A, 10 мкМ леналидомид приводили к деградации CAR19-HilD зависимым от времени образом, и после отмывки леналидомида экспрессия CAR19-HilD восстанавливалась. Это наблюдение подтверждали с применением анализа посредством проточной цитометрии. Леналидомид продолжал обеспечивать деградацию CAR19-HilD с течением времени и отмывка леналидомида увеличивала экспрессию CAR19-HilD на поверхности клеток (ФИГ. 30B).
Пример 12. Оценка CAR19-HilD в первичных T-клетках
В этом исследовании анализируют дозозависимый эффект леналидомида на экспрессию и функцию CAR в первичных T-клетках.
Во-первых, исследовали экспрессию CAR на поверхности CAR-T-клеток с CAR19-HILD при обработке леналидомидом или без нее в течение 24 и 48 часов. Во-вторых, анализировали воздействие леналидомида на уничтожение под действием CAR-T-клеток и продуцирование цитокинов в присутствии клеток, экспрессирующих CD19.
Способы
Получение вирусных векторов pELPS. Клетки LentiX-293T (Clonetech 632180) культивировали в DMEM с 10% FBS при 37°C и 5% CO2. Клетки высевали в пять 15-см планшетов для культур тканей (BD Biosciences 356451) из расчета 14×10^6 клеток на планшет в 25 мл DMEM, 10% FBS, и инкубировали в течение ночи. На следующий день 15 мкг вектора pELPs объединяли со смесью для лентивирусной упаковки (18 мкг pRSV.REV, 18 мкг pMDLg/p.RRE и 7 мкг pVSV-G), 90 мкл липофектамина 2000 (Invitrogen 11668-019) и 3 мл OptiMEM (Invitrogen 11058021) на 15-см планшет и добавляли к высеянным клеткам. На следующий день среду удаляли и заменяли 15 мл свежей среды. Клетки инкубировали в течение 30 часов и затем вирус собирали, центрифугировали при 500g в течение 10 мин и фильтровали через ацетилцеллюлозный фильтр с диаметром пор 0,45 мкм (Corning 430314). Вирусный супернатант концентрировали с применением концентратора Lenti-X (Clonetech 611232) при 4°C в течение ночи, осаждали при 1500g в течение 45 мин при 4°C, с последующей аспирацией супернатанта и ресуспендированием в DMEM, 10% FBS из расчета 1/100-ая исходного объема. Вирус делили на аликвоты и хранили при -80°C.
Титр SUPT1. 100 мкл клеток SUPT1 высевали из расчета 2E5 клеток/мл в плоскодонный 96-луночный планшет. 50 мкл разведенного вируса добавляли к клеткам. Планшет инкубировали при 37°C в CO2 в течение ночи. 100 мкл среды RPMI добавляли в каждую лунку и планшет возвращали в инкубатор. В день 4 после трансдукции клетки собирали, окрашивали в отношении белка L, и экспрессию CAR анализировали с помощью Flow Jo.
10 дней размножения CART. CAR-T-клетки получали, начиная с продукта афереза от здоровых доноров, наивные T-клетки которых получали путем отрицательного отбора в отношении T-клеток, CD3-лимфоцитов. T-клетки культивировали из расчета 0,5×106 Т-клеток в 1 мл среды на лунку 24-луночного планшета. Эти клетки активировали путем добавления микрогранул с антителом к CD3/CD28 (Dynabeads® Human T-Expander CD3/CD28) при отношении 1:3 (T-клетка на микрогранулу) в среде для T-клеток.
После 24 часов T-клетки оставляли нетрансдуцированными (UTD) или трансдуцировали при множественности заражения (MOI), составляющей 4 в случае CART19 или CART19-HilD. Рост T-клеток отслеживали путем измерения количества клеток на мл, и T-клетки разводили свежей средой раз в два дня. 1 миллион клеток переносили в день 7 в 24 луночный планшет для оценки эффекта леналидомида при трех различных концентрациях, 1 мкМ, 0,1 мкМ и 0,01 мкМ, в течение 24 часов или 48 часов. Процент трансдуцированных клеток (клеток, экспрессирующих CD19-специфический CAR на клеточной поверхности) определяли с помощью анализа посредством проточной цитометрии на FACS Fortessa (BD).
Окрашивание при FACS.
Клетки собирали и промывали с помощью PBS. Затем клетки инкубировали с 100 мкл биотинилированного белка L при 4°C в течение 45 минут. Затем клетки промывали с применением PBS и инкубировали при 4°C со стрептавидином, конъюгированным с PE, при разведении 1:300 и антителом к CD3 BV421 при разведении 1:200 в течение 30 минут. Затем клетки промывали дважды с помощью PBS и суспендировали в 100 мкл буфера для фиксации с 2% параформальдегида в течение 10 минут при комнатной температуре. Фиксированные клетки промывали с помощью PBS и суспендировали в 150 мкл PBS. Затем данные об этих клетках собирали на устройстве Fortessa и результаты анализировали с применением программного обеспечения Flow Jo.
Замороженные CAR-T-клетки размораживали в среде для T-клеток и культивировали совместно либо с CD19-отрицательными (клетки K562), либо с CD19-положительными клетками-мишенями (клетки Nalm6), при этом обе линии экспрессировали люциферазу. Как количество CAR-T-клеток, так и суммарное количество T-клеток нормализовали для всех образцов; последнее достигали путем добавления UTD-клеток. Выполняли титрование CAR-T-клеток, поддерживая число клеток-мишеней постоянным на уровне 25000 клеток. Самое высокое исследуемое соотношение эффектор:T-клетка (E:T) составляло 20:1 и использовали кривую с 8 точками разведения. Леналидомид добавляли при конечной концентрации 1 мкМ. Эксперимент с совместным культивированием проводили в черных планшетах с прозрачным дном при конечном объеме 200 мкл. После инкубации в течение 20 ч отбирали 100 мкл супернатанта и измеряли уровни цитокинов. К оставшейся части добавляли 100 мкл реагента для анализа с люфицеразой Bright-Glo (субстрат+фермент) и инкубировали в течение 10 минут при комнатной температуре. % уничтожения вычисляли с применением формулы: специфический лизис (%) = (1 - (люминесценция образца/средняя максимальная люминесценция)) * 100.
Результаты
Как показано на ФИГ. 31A, эффективность трансдукции CAR19 и CAR19-HilD была сравнимой. Кратность размножения первичных T-клеток, трансдуцированных с помощью CAR19 или CAR19-HilD, также была сравнимой. Обработка леналидомидом не оказывала влияния на экспрессию CAR19 (ФИГ. 31B). В отличие от этого, для клеток, экспрессирующих CAR19-HilD, показано дозозависимое снижение экспрессии CAR в условиях обработки леналидомидом (ФИГ. 31C). Воздействие на экспрессию CAR было более выраженным через 48 часов (ФИГ. 31C).
Низкий фоновый уровень уничтожения CD19-отрицательный клеток наблюдали у разных образцы, в независимости от добавления леналидомида (ФИГ. 32A). Способность CART19 и CART19-HilD уничтожать CD19-положительные клетки в отсутствие леналидомида была сравнимой (ФИГ. 32B и 32C). После добавления леналидомида кривая уничтожения CART19-HilD слегка сдвигалась (ФИГ. 32C).
CART19 и CART19-HilD приводили к секреции сравнимых уровней IFN-гамма (ФИГ. 33A) и IL2 (ФИГ. 33B) в ответ на CD19-положительные клетки в отсутствие леналидомида. В присутствии леналидомида уровни IFN-гамма и IL2, секретируемых клетками с CART19 HilD, снижались (ФИГ. 33A и 33B). Способность CART19 к секреции цитокинов не была восприимчивой к добавлению леналидомида (ФИГ. 33A и 33B).
Обобщая вышеизложенное, данное исследование демонстрирует, что прикрепление HilD-метки к структуре CAR19 не оказывало воздействия на способность таких CART размножаться в культуре. Леналидомид приводит к снижению экспрессии CAR на поверхности T-клеток, экспрессирующих CAR19-HilD, дозозависимым образом.
В отсутствие леналидомида активность CART19-HilD является сравнимой с CART19. Уничтожение и секреция цитокинов у клеток CART19.HilD специфичны в отношении клетки-мишени.
В анализе уничтожения, выполняемом в данном документе, леналидомид слегка нарушает способность CART19-HilD к уничтожению клеток-мишеней. В экспериментальных условиях, используемых в данном документе, клетки-мишени начинают погибать сразу после совместного добавления CART. Небольшой сдвиг в уничтожении клеток на ФИГ. 32C, по-видимому, обусловлен тем фактом, что кинетика уничтожения клеток вероятно более быстрая, чем кинетика деградации CAR19-HilD.
Леналидомид нарушает способность CART19.HilD, но CART19, секретировать цитокины.
Пример 13. Оценка CAR19-HilD in vivo
В данном исследовании проверяют in vivo активность T-клеток, экспрессирующих CAR19-HilD, и их регуляцию под действием леналидомида.
Способы
Ксенотрансплантатная мышиная модель
Самок мышей NOD.Cg-Prkdcscid Il2rgtm1Wjl/SzJ (NSG) возрастом 6-8 недель приобретали в Jackson Laboratories. Исследования на животных проводили согласно протоколам, одобренным институциональным комитетом по уходу за животными и их использованию при NIBR. Мышам NSG инокулировали 1,0×106 Nalm-6 с люциферином внутривенно. Спустя несколько дней CAR-T-клетки вводили инфузией внутривенно мышам, несущим опухоль; если не указано иное, дозу леналидомид вводили перорально в то же время. Опухолевую нагрузку измеряли с помощью IVIS и определяли количественно как светимость в представляющей интерес области (ROI), которая обычно представляла собой площадь одной мыши. Мышей подвергали эвтаназии после потери более 20% массы тела или при развитии паралича задних конечностей. Болезнь "трансплантат против хозяина" определяли у указанных животных в виде выпадения волос, изменений поведения и явного ухудшения здоровья, которое не может быть соотнесено с люциферазным сигналом в Nalm-6.
Анализ экспрессии CAR в спленоцитах
Селезенки собирали у мышей, используемых в исследовании in vivo эффективности, описанном выше, в конце исследования. Собранную селезенку гомогенизировали в суспензию отдельных клеток (селезенки или клетки, полученные из селезенки, не объединяли). Клетки промывали средой RPMI и замораживали в 1 мл среды для замораживания. В день окрашивания клетки размораживали в среде RPMI с 10% сыворотки крови. Для блокирования рецепторов CD16/CD32, клетки инкубировали с Mouse Fc block (разведение 1:100) при комнатной температуре в течение 14 мин. Клетки промывали и инкубировали при 4°C в течение 45 мин со 100 мкл биотинилированного белка с конечной концентрацией 1 мкг/мл. После промывки с помощью PBS клетки инкубировали при 4°C со стрептавидином, конъюгированным с PE, при разведении 1:300 в течение 30 мин. Затем клетки промывали дважды с помощью PBS и суспендировали в 100 мкл буфера для фиксации с 2% параформальдегида в течение 10 мин при комнатной температуре. Фиксированные клетки промывали с помощью PBS и суспендировали в 150 мкл PBS. Затем данные об этих клетках собирали на устройстве Fortessa и результаты анализировали с применением программного обеспечения Flow Jo.
Ниже приведены группы мышей, у которых собирали селезенку. В каждой группе было по три мыши:
группа 1. - CART19.HilD (5×106);
группа 2. - CART19-HilD (5×106) + леналидомид qd;
группа 3. - CART19-HilD (5×106) + леналидомид bid:
группа 4. - CART19.HilD (5×106) + леналидомид+5 дней.
Результаты
Леналидомид оказывал слабый эффект на рост Nalm6 in vivo (данные не показаны).
Для определения терапевтической эффективности CART19.HilD in vivo мышей, несущих опухоль, обрабатывали с помощью 5,0×106, 2,5×106 или 1,0×106 CART19.HilD. В то время как 5,0×106 CART19.HilD приводила к показателям регрессии опухоли, сравнимым с 2,5×106 CART19, 2,5×106 CART19.HilD могла только частично контролировать опухолевый рост (ФИГ. 34). 1,0×106 CART19.HilD показала отсутствие эффективности (ФИГ. 34). В дополнение к дозозависимой активности, которая сохранялась в течение >40 дней, обработка леналидомидом из расчета 30 мг/кг bid могла полностью устранить способность CART19.HilD контролировать опухолевый рост in vivo (ФИГ. 34). Эти результаты резко отличались от результатов, полученных in vitro, в анализе цитолиза опухоли, показанном на ФИГ. 32C. Утрата CAR-T-клеток в периферической крови после обработки леналидомидом также подтверждалась посредством проточной цитометрии (ФИГ. 35).
Контроль функции T-клеток in vivo после адоптивного переноса важен для предупреждения или преодоления потенциальной токсичности, ассоциированной с терапией с помощью CART. Таким образом, дополнительно исследовали, может ли активность CART19.HilD устраняться после того, как CART19.HilD осуществили контроль опухоли. Исследование доз леналидомида во временной динамике проводили на NSG-модели, несущей опухоль Nalm6. У мышей, которым дозу леналидомида вводили непосредственно после переноса CART19.HilD, утрачивалась способность контролировать опухолевый рост in vivo (ФИГ. 36). У мышей, которым дозу леналидомида вводили в день 5 после адоптивного переноса клеток CART19HilD, показан рецидив опухоли через несколько дней после введения дозы леналидомида (ФИГ. 36). В отсутствие леналидомида активность CART19-HilD является сравнимой с CART19.HilD (ФИГ. 36).
Анализировали экспрессию CAR в CD3+ клетках, полученных из спленоцитов мышей. Экспрессия CAR в CD3-клетках, полученных из мышей, обработанных с помощью T-клеток, экспрессирующих CAR19 или CAR19-HilD, была сравнимой (ФИГ. 37E). У всех мышей, обработанных с помощью CAR19-HilD и леналидомида, показано значительное снижение экспрессии CAR в CD3-положительных клетках, полученных из селезенки (ФИГ. 37B-37E).
Пример 14. Разработка CARB-метки
CARB-метка основана на последовательности шпильки, полученной из IKZF2, которая может использоваться в качестве метки-дегрона вместе с соединением I-112, раскрытым в таблице 29.
Соединения IMiD, такие как леналидомид, могут индуцировать деградацию IKZF1 и 3, но не IKZF2. Было установлено, что соединение I-112 приводит к специфической деградации IKZF2, но не IKZF1 или IKZF3. Поскольку HilD-метка основана на шпильке из IKZF1/IKZF3, она может подвергаться деградированию только под действием IMiD. В данном исследовании изучают, может ли шпилька на основе IKZF2 (CARB-метка) повергаться деградированию с помощью соединения I-112.
Способы
Разработка. Исходная последовательность CARB-метки происходит из IKZF2 CDS (NM_016260). N-концевая часть метки взята из H130-S174, а C-концевая взята из A230-D243. Полная аминокислотная последовательность представляет собой: HKRSHTGERPFHCNQCGASFTQKGNLLRHIKLHSGEKPFKCPFCSAGQVMSHHVPPMED (SEQ ID NO: 109)
Область, подчеркнутая выше, представляет собой C-концевую часть. Подобно HilD-метке CARB-метка прикрепляется к представляющему интерес белку с помощью 16GS-линкера (GGGGSGGGGTGGGGSG (SEQ ID NO: 28)). ДНК 16GS-CARB-метки разрабатывали с включением сайтов для рестрикционных ферментов на каждой стороне и синтезировали в виде gBlock в Integrated DNA technologies. Последовательность ДНК показана ниже:
CAGTCAGTGGGCCTCGGCGGCCAAGCTTGGCAATCCGGTACTGTTGGTgAAGCCAttCACCatgcataaaaggagtcacactggtgaacgccccttccactgtaaccagtgtggagcttcttttactcagaagggcaaccttctgagacacataaagttacactctggagagaagccgttcaaatgtcctttctgtagcgctgggcaggtcatgagtcaccatgtacctcctatggaagatggtggtggcgggagcggaggtggaggcacgggcggtggaggttcggggAacgttATGCTGGAAATGCTAGAATATAA (SEQ ID NO: 110)
Также разрабатывали и синтезировали gBlock для полного CAR19 (CTL119) с вышеуказанной последовательностью CARB-метки. Последовательность ДНК показана ниже:
ccatttcaggtgtcgtgagcggccgctctagagccGAattCGgatccatggccctccctgtcaccgccctgctgcttccgctggctcttctgctccacgccgctcggcccgaaattgtgatgacccagtcacccgccactcttagcctttcacccggtgagcgcgcaaccctgtcttgcagagcctcccaagacatctcaaaataccttaattggtatcaacagaagcccggacaggctcctcgccttctgatctaccacaccagccggctccattctggaatccctgccaggttcagcggtagcggatctgggaccgactacaccctcactatcagctcactgcagccagaggacttcgctgtctatttctgtcagcaagggaacaccctgccctacacctttggacagggcaccaagctcgagattaaaggtggaggtggcagcggaggaggtgggtccggcggtggaggaagccaggtccaactccaagaaagcggaccgggtcttgtgaagccatcagaaactctttcactgacttgtactgtgagcggagtgtctctccccgattacggggtgtcttggatcagacagccaccggggaagggtctggaatggattggagtgatttggggctcAgagactacttactaccaatcatccctcaagtcTcgcgtcaccatctcaaaggacaactctaagaatcaggtgtcactgaaactgtcatctgtgaccgcagccgacaccgccgtgtactattgcgctaagcattactattatggcgggagctacgcaatggattactggggacagggtactctggtcaccgtgtccagcaccactaccccagcaccgaggccacccaccccggctcctaccatcgcctcccagcctctgtccctgcgtccggaggcatgtagacccgcagctggtggggccgtgcatacccggggtcttgacttcgcctgcgatatctacatttgggcccctctggctggtacttgcggggtcctgctgctttcactcgtgatcactctttactgtaagcgcggtcggaagaagctgctgtacatctttaagcaacccttcatgaggcctgtgcagactactcaagaggaggacggctgttcatgccggttcccagaggaggaggaaggcggctgcgaactgcgcgtgaaattcagccgcagcgcagatgctccagcctaccagcaggggcagaaccagctctacaacgaactcaatcttggtcggagagaggagtacgacgtgctggacaagcggagaggacgggacccagaaatgggcgggaagccgcgcagaaagaatccccaagagggcctgtacaacgagctccaaaaggataagatggcagaagcctatagcgagattggtatgaaaggggaacgcagaagaggcaaaggccacgacggactgtaccagggactcagcaccgccaccaaggacacctatgacgctcttcacatgcaggccctgccgcctcggggtggtggcgggagcggaggtggaggcacgggcggtggaggttcggggcataaaaggagtcacactggtgaacgccccttccactgtaaccagtgtggagcttcttttactcagaagggcaaccttctgagacacataaagttacactctggagagaagccgttcaaatgtcctttctgtagcgctgggcaggtcatgagtcaccatgtacctcctatggaagatTAAgtcgacgcgtAACCCAGCTTTCTTGTACAAAGTGGTTGATATCCAGCACAGTGGCGGCGCGCCATTCCGCCCCTCTCCCTC (SEQ ID NO: 111). Незрелая аминокислотная последовательность CAR19-16GS-CARB-метки раскрыта под SEQ ID NO: 112.
Клонирование. gBlocks расщепляли с помощью рестрикционных ферментов, поскольку применяли вектор для экспрессии в клетках млекопитающего с промотором CMV, контролирующим либо MITF (NM_000248) с FLAG меткой, либо CD19 (NM_001770) с V5-меткой, создавая такие конечный конструкции: CD19-16GS-HilD-V5 (конструкция, описанная в примере 5), и CARB-метка-16GS-MITF-FLAG.
gBlock CTL119-16GS-CARB-метка также расщепляли с помощью рестрикционных ферментов, но клонировали в лентивирусный вектор для экспрессии в клетках млекопитающих, содержащий промотор EF1a.
Пример 15. Дозозависимый ответ CARB-метки на соединение I-112, исследуемый посредством вестерн-блоттинга, проточной цитометрии и функционального анализа JNL CAR19
Целью данного исследования является определение эффективности CARB-метки при деградации CAR19 после введения дозы соединения I-112.
Способы
Получение вирусных векторов pNGX_LV_V002. Клетки HEK293T (ATCC CRL-3216) культивировали в DMEM с 10% FBS при 37°C и 5% CO2. Клетки высевали на покрытые коллагеном 6 луночные планшеты из расчета 0,75×10^6 клеток/лунка в 2 мл DMEM, 10% FBS и инкубировали в течение ночи. На следующий день вектор pNGX_LV_V002 (0,23 мкг) и смесь ДНК для лентивирусной упаковки (0,28 мкг) (Cellecta CPC-K2A) смешивали с 1,5 мкл реагента для трансфекции TransIT (Mirus MIR2700) в 55,1 мкл OptiMEM (Invitrogen 11058021) и добавляли к высеянным клеткам, которые инкубировали в течение ночи. На следующий день из клеток удаляли среду и добавляли 1 мл свежей среды. Клетки инкубировали в течение 72 часов. Вирусный супернатант собирали из клеток и фильтровали через ацетилцеллюлозный фильтр с диаметром пор 0,45 мкм (Corning 430516), а также разделяли на аликвоты и хранили при -80°C.
Вирусный титр. Готовили восьмикратное разведение вируса, начиная с 1:3, с применением RPMI и 10% FCS. 100 мкл клеток SUPT1 высевали из расчета 2E5 клеток/мл в плоскодонный 96-луночный планшет. 50 мкл разведенного вируса добавляли к клеткам в двух повторностях. Планшет инкубировали при 37°C в CO2 в течение ночи. 100 мкл среды RPMI добавляли в каждую лунку и планшет возвращали в инкубатор. В день 4 после трансдукции клетки собирали, окрашивали в отношении белка L, и экспрессию CAR анализировали с помощью Flow Jo.
Обработка клеток Клетки Jurkat, содержащие NFAT-люциферазный репортер, инфицировали с помощью либо CAR19, либо CAR19-CARB-метка при множественности заражения (MOI), составляющей 4. Клетки размножали в течение одной недели перед применением. Клетки разводили до 0,5×10^6 в общем объеме 3 мл в 6-луночных чашках. После посева клеток образцы обрабатывали непосредственно с помощью 10 мкМ, 1 мкМ, 0,1 мкМ, 0,01 мкМ и 0,001 мкМ соединения I-112 и DMSO. Все клетки собирали через 24 часа после начала обработки соединением для вестерн-блоттинга и анализа посредством проточной цитометрии.
Вестерн-блоттинг. Клетки осаждали, промывали с помощью PBS и осадки лизировали с помощью 50 мкл буфера RIPA (Boston Bioproducts BP-115D) с ингибиторами протеазы (Roche 04693124001). Лизаты центрифугировали, супернатант переносили в новые пробирки и количества белка определяли посредством анализа Лоури (BioRad 5000111). Каждый образец нормализовали до 30 мкг общего белка в объеме 20 мкл с помощью 4X буфера для образцов (Thermo Scientific NP0007) и 10X восстанавливающего средства (Thermo Scientific NP0009). Образцы прогоняли на акриламидном геле с 4-12% Bis-Tris (Thermo Scientific WG1402BOX). Гели прогоняли в двух повторностях, одну для антитела к актину, а другую для антитела к V5 или CD3Z. Гели переносили на нитроцеллюлозные мембраны и мембраны инкубировали в течение ночи в 3% молоке в TBS-0,1% Tween-20 с одним из следующих антител: антитело мыши к актину (Sigma Aldrich A5441) при разведении 1:10000 и антитело мыши к CD3z (BD 551034) при разведении 1:1000. На следующий день блоты промывали в TBS-0,1% Tween-20, помещали в 3% молоко в TBS-0,1% Tween-20 с вторичным антителом овцы к белкам мыши, конъюгированным с HRP (GE Healthcare NA931), в разведении 1:10000 при комнатной температуре в течение 1 часа, затем блоты промывали и проявляли с помощью ECL (Thermo Scientific 34076).
Проточная цитометрия. Клетки собирали в планшет с u-образным дном и промывали с применением 1X PBS. Промытые клетки окрашивали с помощью 100 мкл биотинилированного белка L (Genscript M00097) с концентрацией 1 мкг/мл в разведении 1:1000. Первичное антитело инкубировали при 4°C в течение 45 минут. После инкубации клетки промывали с применением PBS. Клетки инкубировали при 4°C со стрептавидином, конъюгированным с PE (Jackson Lab 016-110-084), в разведении 1:300 в течение 30 мин. Клетки промывали дважды с помощью PBS и суспендировали в 100 мкл буфера для фиксации (2% параформальдегид в PBS) в течение 10 минут при комнатной температуре. Фиксированные клетки промывали с помощью PBS и суспендировали в 150 мкл PBS. Затем данные об этих клетках собирали с применением анализатора клеток BD LSRF Fortessa. Мертвые клетки исключали на основании размера с использованием графика FSC и SSC. Живые клетки анализировали в отношении их экспрессии PE-CAR. Результаты проточной цитометрии гейтировали с применением неокрашенных клеток JNL из исходной линии и для каждого образца регистрировали 10 тыс. событий.
Функциональный анализ CAR в клетках Jurkat с NFAT-люциферазой (JNL). Клетки с CAR19-CARB-меткой разводили до 0,5×10^6 в 20 мл среды RPMI 1640 (Thermo Fisher Scientific 11875-085) с 10% FBS, 1X пенициллин/стрептомицин. 20 мкл (0,5×10^6 клеток) этой клеточной линии высевали в белые 384-луночные планшеты с непрозрачным дном (Greiner789163-G). Соединение I-112 добавляли в 384 луночный планшет и расчета 8 точек концентрации при разведении со степенью  с конечной самой большой концентрацией 10 мкМ с применением акустического диспенсера Labcyte ECHO. Планшеты инкубировали в течение 15 часов при 37°C, 5% CO2. Клетки K562 и Nalm6 ресуспендировали из расчета 0,5×10^6 клеток/мл. Половину клеток, обработанных 8-точками концентрации соединения I-112, обрабатывали 20 мкл K562, а другую половину обрабатывали 20 мкл клеток Nalm6. Клетки хранили в инкубаторе при 37°C, 5% CO2 в течение восьми часов. Затем образцы обрабатывали с помощью 40 мкл (1:1) Bright Glo (Promega E2620) и люминесценцию считывали с применением Perkin Elmer Viewlux при 20-секундном воздействии.
с конечной самой большой концентрацией 10 мкМ с применением акустического диспенсера Labcyte ECHO. Планшеты инкубировали в течение 15 часов при 37°C, 5% CO2. Клетки K562 и Nalm6 ресуспендировали из расчета 0,5×10^6 клеток/мл. Половину клеток, обработанных 8-точками концентрации соединения I-112, обрабатывали 20 мкл K562, а другую половину обрабатывали 20 мкл клеток Nalm6. Клетки хранили в инкубаторе при 37°C, 5% CO2 в течение восьми часов. Затем образцы обрабатывали с помощью 40 мкл (1:1) Bright Glo (Promega E2620) и люминесценцию считывали с применением Perkin Elmer Viewlux при 20-секундном воздействии.
Результаты
Для уровней белка CAR19-CARB-метка показано дозозависимое снижение после 24 часов обработки соединением I-112 (ФИГ. 38A). Аналогичным образом, обработка соединением I-112 также снижала экспрессию CAR на поверхности клеток JNL с CAR19-CARB-меткой (ФИГ. 38B). Как показано в функциональном анализе JNL CAR, описанном выше, клетки с CAR19-CARB-меткой отвечают только на CD19+ клетки Nalm6, и этот ответ снижается дозозависимым образом при обработке возрастающими количествами соединения (ФИГ. 38C).
Пример 16. Применение CARB-метки и HilD-метки в качестве ортогональной системы для деградации белка
Целью данного исследования является определение того, могут ли белки с CARB-меткой подвергаться деградации в клетках после обработки соединением I-112. Также проверяют, что в ситуации, когда белок с HilD-меткой и белок с CARB-меткой экспрессируются совместно, может ли экспрессия каждого белка регулироваться независимо с помощью либо обработки леналидомидом (в случае белка с HilD-меткой), либо обработки соединением I-112 (в случае белка с CARB-меткой).
Способы
Экспрессия гена и обработка клеток. Клетки HEK293T (ATCC CRL-3216) культивировали в DMEM с 10% FBS и пенициллином/стрептомицином при 37°C и 5% CO2. Клетки трансфицировали с помощью либо CARB-метка-16GS-MITF-FLAG или CARB-метка-16GS-MITF-FLAG и CD19-16GS-HilD-V5 с помощью FuGene HD (Promega E2311) с применением соотношения FuGene HD и ДНК, составляющего 3:1. Трансфицированные клетки инкубировали в течение 24 часов, а затем обрабатывали либо леналидомидом, либо соединением I-112 при десятикратном разведении с 4 точками концентрации, начиная с конечного разведения 10 мкМ. Клетки обрабатывали с помощью указанного соединения в течение 24 часов и затем готовили для вестерн-блоттинга.
Вестерн-блоттинг. Через 24 часа после обработки соединением клетки осаждали, промывали с помощью PBS и осадки лизировали с помощью 50 мкл буфера RIPA (Boston Bioproducts BP-115D) с ингибиторами протеазы (Roche 04693124001). Лизаты центрифугировали, супернатант переносили в новые пробирки и количества белка определяли посредством анализа Лоури (BioRad 5000111). Каждый образец нормализовали до 30 мкг общего белка в объеме 20 мкл с помощью 4X буфера для образцов (Thermo Scientific NP0007) и 10X восстанавливающего средства (Thermo Scientific NP0009). Образцы прогоняли на акриламидном геле с 4-12% Bis-Tris (Thermo Scientific WG1402BOX). Гели прогоняли в трех повторностях (по одной для каждого антитела). Гели переносили на нитроцеллюлозные мембраны и мембраны инкубировали в течение ночи в 3% молоке в TBS-0,1% Tween-20 с одним из трех следующих антител: антитело мыши к V5 (Thermo Scientific MA5-15253) при разведении 1:1000; антитело мыши к актину (Sigma Aldrich A5441) при разведении 1:10000 и антитело мыши к FLAG M2 (Sigma F3165) при разведении 1:1000. На следующий день блоты промывали в TBS-0,1% Tween-20, затем помещали в 3% молоко в TBS-0,1% Tween-20 с вторичным антителом овцы к белкам мыши, конъюгированным с HRP (GE Healthcare NA931), в разведении 1:10000 при комнатной температуре в течение одного часа и затем блоты промывали и проявляли с помощью ECL (Thermo Scientific 34076).
Результаты
MITF с CARB-меткой эффективно подвергался деградации под действием соединения I-112, но не леналидомида (ФИГ. 39). В отличие от этого, экспрессия CD19-HilD-метки оставалась постоянной при обработке различными дозами соединения I-112 (данные не показаны).
Пример 17. Характеристика конструкции слияния CAR для BCMA-HilD-метка
Целью данного исследования является определение того, может ли HilD-метка быть использована для деградации других CAR, например, CAR для BCMA. Последовательность CAR для BCMA-16GS-линкер-HilD-метка показана ниже. HilD-метка подчеркнута одной чертой. 16GS-линкер подчеркнут двойной чертой. Сигнальный пептид показан курсивом.
MALPVTALLLPLALLLHAARPEVQLVESGGGLVQPGGSLRLSCAVSGFALSNHGMSWVRRAPGKGLEWVSGIVYSGSTYYAASVKGRFTISRDNSRNTLYLQMNSLRPEDTAIYYCSAHGGESDVWGQGTTVTVSSASGGGGSGGRASGGGGSDIQLTQSPSSLSASVGDRVTITCRASQSISSYLNWYQQKPGKAPKLLIYAASSLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQSYSTPYTFGQGTKVEIKTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPRGGGGSGGGGTGGGGSGMHKRSHTGERPFQCNQCGASFTQKGNLLRHIKLHTGEKPFKCHLCNTASAEARHIKAEMG (SEQ ID NO: 1450)
Способы
Получение вирусных векторов pELPS. Клетки LentiX-293T (Clonetech 632180) культивировали в DMEM с 10% FBS при 37°C и 5% CO2. Клетки высевали в пять 15-см планшетов для культур тканей (BD Biosciences 356451) из расчета 14×10^6 на планшет в 25 мл DMEM, 10% FBS, и инкубировали в течение ночи. На следующий день 15 мкг вектора pELPs объединяли со смесью для лентивирусной упаковки (18 мкг pRSV.REV, 18 мкг pMDLg/p.RRE и 7 мкг pVSV-G), 90 мкл липофектамина 2000 (Invitrogen 11668-019) и 3 мл OptiMEM (Invitrogen 11058021) на 15-см планшет и добавляли к высеянным клеткам. На следующий день среду удаляли и заменяли 15 мл свежей среды. Клетки инкубировали в течение 30 часов, затем вирус собирали, центрифугировали при 500g в течение 10 мин и фильтровали через ацетилцеллюлозный фильтр с диаметром пор 0,45 мкм (Corning 430314). Вирусный супернатант концентрировали с применением концентратора Lenti-X (Clonetech 611232) при 4°C в течение ночи, осаждали при 1500g в течение 45 мин при 4°C, с последующей аспирацией супернатанта и ресуспендированием в DMEM, 10% FBS из расчета 1/100ая исходного объема. Вирус делили на аликвоты и хранили при -80°C.
Вирусный титр. Готовили восьмикратное разведение вируса, начиная с 1:3, с применением RPMI и 10% FCS. 100 мкл клеток SUPT1 высевали из расчета 2E5 клеток/мл в плоскодонный 96-луночный планшет. 50 мкл разведенного вируса добавляли к клеткам в двух повторностях. Планшет инкубировали при 37°C в CO2 в течение ночи. 100 мкл среды RPMI добавляли в каждую лунку и планшет возвращали в инкубатор. В день 4 после трансдукции клетки собирали, окрашивали в отношении экспрессии CAR и анализировали с помощью Flow Jo.
Обработка клеток. Клетки Jurkat, содержащие NFAT-люциферазный репортер, инфицировали с помощью CAR для BCMA-HilD-метка при множественности инфекции (MOI), составляющей 4. Клетки размножали в течение одной недели перед применением. Клетки JNL с CAR для BCMA-HilD-меткой разводили до 0,5×10^6 в общем объеме 3 мл в 6-луночных чашках. После посева клеток образцы обрабатывали непосредственно с помощью 10 мкМ, 1 мкМ, 0,1 мкМ, 0,01 мкМ и 0,001 мкМ леналидомида и DMSO. Все клетки собирали через 24 часа после начала обработки леналидомидом для анализа посредством проточной цитометрии.
Проточная цитометрия. Клетки собирали в планшет с u-образным дном и промывали с применением 1X PBS. Промытые клетки окрашивали с помощью антитела к CAR для BCMA, конъюгированного с Alexa flour 647 (BioLegend #94581), при разведении 1:300. Первичное антитело инкубировали при 4°C в течение 45 минут. После инкубации клетки промывали дважды с помощью PBS и суспендировали в 100 мкл буфера для фиксации с 2% параформальдегида в течение 10 минут при комнатной температуре. Фиксированные клетки промывали с помощью PBS и суспендировали в 150 мкл PBS. Затем данные об этих клетках собирали с применением инструмента Fortessa. Мертвые клетки исключали на основании размера с использованием графика FSC и SSC. Живые клетки анализировали в отношении их экспрессии APC CAR. Результаты проточной цитометрии гейтировали с применением неокрашенных клеток JNL из исходной линии и для каждого образца регистрировали 10 тыс. событий.
Функциональный анализ CAR в клетках Jurkat с NFAT-люциферазой (JNL). Линию клеток с CAR для BCMA-HilD разводили до 0,5×10^6 в 20 мл среды RPMI 1640 (Thermo Fisher Scientific 11875-085) с 10% FBS и 1X пенициллина/стрептомицина. 20 мкл (0,5×10^6 клеток) этой клеточной линии высевали в белые 384-луночные планшеты с непрозрачным дном (Greiner789163-G). Леналидомид добавляли в 384 луночный планшет и расчета 8 точек концентрации при разведении со степенью  с конечной самой большой концентрацией 10 мкМ с применением акустического диспенсера Labcyte ECHO. Планшеты инкубировали в течение 15 часов при 37°C, 5% CO2. Клетки KMS11 ресуспендировали из расчета 0,5×10^6 клеток/мл. 20 мкл клеток KMS11 добавляли к клеткам JNL и хранили в инкубаторе при 37°C, 5% CO2 в течение восьми часов. Затем образцы обрабатывали с помощью 40 мкл (1:1) Bright Glo (Promega E2620) и люминесценцию считывали с применением Perkin Elmer Viewlux при 20-секундном воздействии.
с конечной самой большой концентрацией 10 мкМ с применением акустического диспенсера Labcyte ECHO. Планшеты инкубировали в течение 15 часов при 37°C, 5% CO2. Клетки KMS11 ресуспендировали из расчета 0,5×10^6 клеток/мл. 20 мкл клеток KMS11 добавляли к клеткам JNL и хранили в инкубаторе при 37°C, 5% CO2 в течение восьми часов. Затем образцы обрабатывали с помощью 40 мкл (1:1) Bright Glo (Promega E2620) и люминесценцию считывали с применением Perkin Elmer Viewlux при 20-секундном воздействии.
Результаты
Как показано на ФИГ. 40A, обработка леналидомидом приводит к дозозависимому снижению экспрессии CAR для BCMA с HilD-меткой на поверхности клеток. Клетки Jurkat с NFAT-люциферазой, экспрессирующие CAR для BCMA-HilD-метку отвечают на клетки KMS11, экспрессирующие BCMA, о чем свидетельствует увеличение люциферазной активности, что может ингибироваться дозозависимым образом при обработке возрастаюшими количествами леналидомида (ФИГ. 40B).
Пример 18. Синтез иллюстративных соединений
Соединения по настоящему изобретению можно получать множеством способов, широко известных специалистам в области органического синтеза. В качестве примера, соединения по настоящему изобретению можно синтезировать с применением способов, описанных ниже, вместе со способами синтеза, известными в области химии органического синтеза, или вариациями на их основе, как понятно специалисту в данной области техники. Предпочтительные способы включают без ограничения такие способы, описанные ниже.
Соединения по настоящему изобретению можно синтезировать с помощью следующих стадий, кратко изложенных на схеме I, которая содержит различные последовательности сборки промежуточных соединений A-1, A-2, A-3, A-4, A-5, A-5a, A-6a, A-6b и A-7. Исходные материалы являются либо коммерчески доступными, либо изготовленными с помощью известных процедур в упомянутых литературных источниках или проиллюстрированных в данном документе. Подразумевается, что на схеме 1 даны общие указания в сочетании с получением разнообразных соединений по настоящему изобретению. Специалист в данной области техники сможет понять, что стадии, показанные на схеме, могут быть модифицированы или оптимизированы с применением общих принципов органической химии для получения различных соединений по настоящему изобретению.
Схема 1:
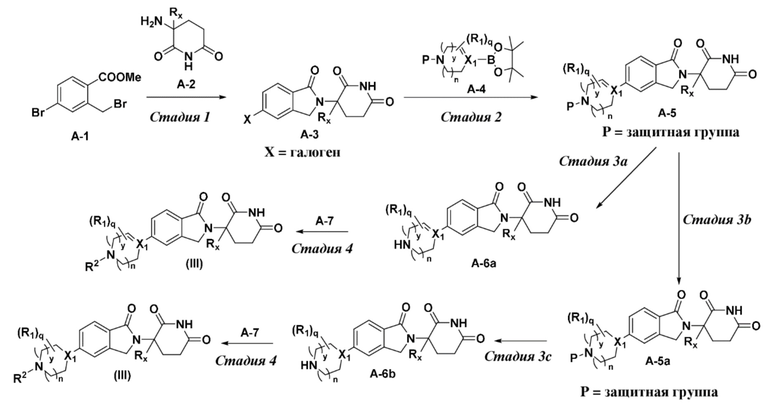
где P защитная группа амина (например, трет-бутилоксикарбонил (Boc)), и X1, R1, R2, Rx, n и y являются такими, как определено выше для формулы (III).
Общий способ получения соединений формулы (III), где  представляет собой двойную связь, а R3 отсутствует, и где
представляет собой двойную связь, а R3 отсутствует, и где  представляет собой одинарную связь, а R3 представляет собой водород, с применением промежуточных соединений A-1, A-2, A-3, A-4, A-5, A-5a, A-6a, A-6b и A-7 указан на схеме 1. A-1 может быть получено, как указано в заявке на патент США US 2009/0142297. Циклизация A-1 и 3-аминопиперидин-2,6-дион-HCl (A-2) в присутствии слабого основания (например, карбоната калия (K2CO3), карбоната цезия (Cs2CO3) и т. д.) в растворителе (например, диметилформамиде (DMF)) и необязательно при повышенной температуре дает A-3, как показано на стадии 1. Реакция сочетания A-3 со сложным эфиром бороновой кислоты A-4 с использованием катализатора (например, Pd(dppf)Cl2•DCM) и основания (например, карбоната цезия (Cs2CO3)) в растворителе (например, N, N-диметилформамиде (DMF)) при повышенной температуре дает A-5. Удаление защитной группы из A-5 с применением сильной кислоты, такой как трифторуксусная кислота (TFA) или хлористоводородная кислота (HCl), в растворителе (например, тетрагидрофуране (THF), 1,2,-дихлорэтане, диоксане или дихлорметане (DCM)) необязательно при повышенной температуре дает A-6a. Восстановительное аминирование A-6a с помощью альдегида или кетона A-7 дает соединение формулы (III), где
представляет собой одинарную связь, а R3 представляет собой водород, с применением промежуточных соединений A-1, A-2, A-3, A-4, A-5, A-5a, A-6a, A-6b и A-7 указан на схеме 1. A-1 может быть получено, как указано в заявке на патент США US 2009/0142297. Циклизация A-1 и 3-аминопиперидин-2,6-дион-HCl (A-2) в присутствии слабого основания (например, карбоната калия (K2CO3), карбоната цезия (Cs2CO3) и т. д.) в растворителе (например, диметилформамиде (DMF)) и необязательно при повышенной температуре дает A-3, как показано на стадии 1. Реакция сочетания A-3 со сложным эфиром бороновой кислоты A-4 с использованием катализатора (например, Pd(dppf)Cl2•DCM) и основания (например, карбоната цезия (Cs2CO3)) в растворителе (например, N, N-диметилформамиде (DMF)) при повышенной температуре дает A-5. Удаление защитной группы из A-5 с применением сильной кислоты, такой как трифторуксусная кислота (TFA) или хлористоводородная кислота (HCl), в растворителе (например, тетрагидрофуране (THF), 1,2,-дихлорэтане, диоксане или дихлорметане (DCM)) необязательно при повышенной температуре дает A-6a. Восстановительное аминирование A-6a с помощью альдегида или кетона A-7 дает соединение формулы (III), где  представляет собой двойную связь, а R3 отсутствует. В качестве альтернативы, соединения формулы (III), где
представляет собой двойную связь, а R3 отсутствует. В качестве альтернативы, соединения формулы (III), где  представляет собой двойную связь, а R3 отсутствует, могут быть получены путем алкилирования A-6a с помощью алкилгалогенида A-7 в присутствии основания (например, NEt3, Cs2CO3 и т. д.) в растворителе (например, DCM, DMF и т. д.) и необязательно при повышенной температуре.
представляет собой двойную связь, а R3 отсутствует, могут быть получены путем алкилирования A-6a с помощью алкилгалогенида A-7 в присутствии основания (например, NEt3, Cs2CO3 и т. д.) в растворителе (например, DCM, DMF и т. д.) и необязательно при повышенной температуре.
Гидрогенизация A-5 в присутствии подходящего катализатора (например, Pd/C или PtO2) в растворителе (например, DMF) и в атмосфере газообразного водорода дает A-5a. Удаление защитной группы из A-5a с применением сильной кислоты, такой как трифторуксусная кислота (TFA) или хлористоводородная кислота (HCl), в растворителе (например, тетрагидрофуране (THF), 1,2,-дихлорэтане, диоксане или дихлорметане (DCM)) необязательно при повышенной температуре дает A-6b. Восстановительное аминирование A-6b с помощью альдегида или кетона A-7 дает соединение формулы (III), где  представляет собой одинарную связь, а R3 отсутствует. В качестве альтернативы, соединения формулы (III), где
представляет собой одинарную связь, а R3 отсутствует. В качестве альтернативы, соединения формулы (III), где  представляет собой одинарную связь, а R3 представляет собой водород, могут быть получены путем алкилирования A-6b с помощью алкилгалогенида A-7 в присутствии основания (например, NEt3, Cs2CO3 и т. д.) в растворителе (например, DCM, DMF и т. д.) и необязательно при повышенной температуре.
представляет собой одинарную связь, а R3 представляет собой водород, могут быть получены путем алкилирования A-6b с помощью алкилгалогенида A-7 в присутствии основания (например, NEt3, Cs2CO3 и т. д.) в растворителе (например, DCM, DMF и т. д.) и необязательно при повышенной температуре.
Смесь энантиомеров, диастереомеров и цис/транс-изомеров, получаемую в способе, описанном выше, может быть разделена на ее отдельные компоненты с помощью методики хиральных солей, хроматографии с применением колонки с нормальной фазой, обращенной фазой или хиральной колонки, в зависимости от природы разделения.
Любые полученные в результате рацематы соединений по настоящему изобретению или промежуточных соединений могут быть разделены на оптические антиподы с помощью известных способов, например, посредством разделения их диастереомерных солей, полученных с помощью оптически активных кислоты или основания, и выделения оптически активных кислотного или основного соединений. В частности, основный фрагмент, таким образом, может быть использован для разделения соединений по настоящему изобретению на их оптические антиподы, например, путем фракционной кристаллизации соли, образованной с помощью оптически активной кислоты, например, винной кислоты, дибензоилвинной кислоты, диацетилвинной кислоты, ди-O, O'-п-толуоилвинной кислоты, миндальной кислоты, яблочной кислоты или камфор-10-сульфоновой кислоты. Рацемические соединения по настоящему изобретению или рацемические промежуточные соединения также могут быть разделены посредством хиральной хроматографии, например жидкостной хроматографии высокого давления (HPLC) с применением хирального адсорбента.
Любые полученные в результате смеси стереоизомеров могут быть разделены на основании физико-химических отличий составляющих на чистые или практически чистые геометрические или оптические изомеры, диастереомеры, рацематы, например, посредством хроматографии и/или фракционной кристаллизации.
Следует понимать, что в описании и формулах, показанных выше, различные группы X1, R1, R2, Rx, n и y, а также другие переменные являются такими, как определено выше, если не указано иное. Кроме того, для целей синтеза соединения из схемы 1 представлены только с выбранными радикалами для иллюстрации общей методики синтеза соединений формулы (III), определенных в данном документе.
Аналитические способы, материалы и оборудование
Если не указано иное, реагенты и растворители использовали в состоянии поставки от коммерческих поставщиков. Спектры протонного ядерного магнитного резонанса (ЯМР) получали либо на спектрометре Bruker Avance, либо на спектрометре Varian Oxford 400 MГц, если не указано иное. Спектры приведены в ppm (δ), а константы взаимодействия, J, приведены в герцах. Тетраметилсилан (TMS) применяли в качестве внутреннего стандарта. Химические сдвиги приведены в ppm относительно диметилсульфоксида (δ 2,50), метанола (δ 3,31), хлороформа (δ 7,26) или другого растворителя, указанного в данных ЯМР-спектра. Небольшое количество сухого образца (2-5 мг) растворяли в подходящем дейтерированном растворителе (1 мл). Химические названия генерировали с применением ChemBioDraw Ultra v12 от CambridgeSoft.
Масс-спектры (МС с электрораспылительной ионизацией) снимали, используя Waters System (Acquity UPLC и масс-спектрометр Micromass ZQ) или Agilent-1260 Infinity (6120 Quadrupole); все указанные массы представляют собой отношение масса/заряд протонированных исходных ионов, если не указано иное. Образец растворяли в подходящем растворителе, таком как MeCN, DMSO или MeOH, и вводили непосредственно в колонку с применением устройства для автоматической подачи образцов. Анализ проводят на системе Waters Acquity UPLC (колонка: Waters Acquity UPLC BEH C18, 1,7 мкм, 2,1×30 мм; расход: 1 мл/мин; 55°C (температура колонки); растворитель A: 0,05% муравьиной кислоты в воде, растворитель B: 0,04% муравьиной кислоты в MeOH; градиент 95% растворителя A от 0 до 0,10 мин; 95% растворителя A до 20% растворителя A от 0,10 до 0,50 мин; 20% растворителя A до 5% растворителя A от 0,50 до 0,60 мин; удержание при 5% растворителя A от 0,6 мин до 0,8 мин; 5% растворителя A до 95% растворителя A от 0,80 до 0,90 мин и удержание при 95% растворителя A от 0,90 до 1,15 мин.
Аббревиатуры, используемые в следующих примерах и в других разделах данного документа, представляют собой:
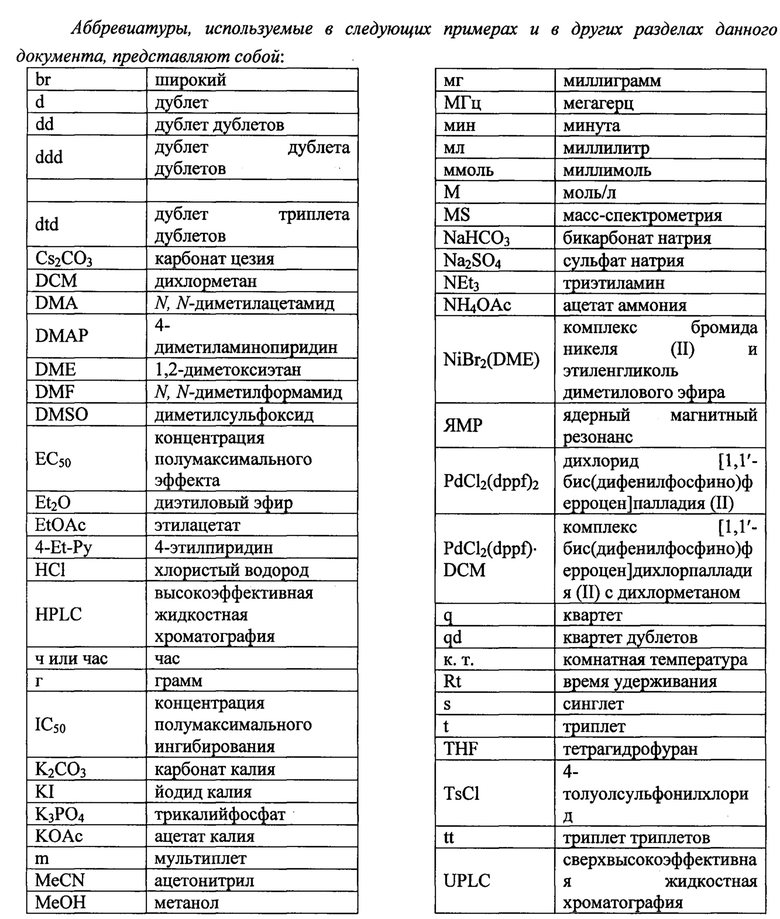
Пример 18-1. 3-(1-Оксо-5-(пиперидин-4-ил)изоиндолин-2-ил)пиперидин-2,6-дион (I-155)
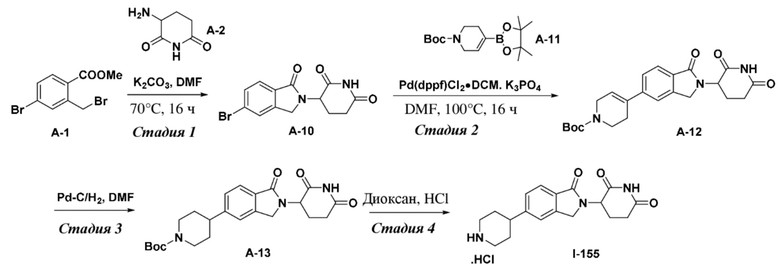
К перемешиваемому раствору метил 4-бром-2-(бромметил)бензоата (A-1, 15 г, 48,7 ммоль) в DMF (150 мл) добавляли 3-аминопиперидин-2,6-дион-HCl (A-2, 6,9 г, 53,6 ммоль) и K2CO3 (20,2 г, 146,1 ммоль). Полученную смесь нагревали при 70°C в течение 16 ч., после завершения данного периода времени реакционную смесь охлаждали до комнатной температуры и затем концентрировали до сухого состояния. Затем добавляли воду и смесь перемешивали при комнатной температуре в течение 30 мин. Полученное в результате твердое вещество фильтровали и промывали с помощью эфира и этилацетата, и высушивали посредством вакуумной фильтрации с получением A-10 (10,6 г, 32,9 ммоль, выход 67%). MS [M+H]+ = 323,0. 1H ЯМР (400 МГц, DMSO-d6) δ 10,99 (s, 1H), 7,91-7,88 (m, 1H), 7,72 (dd, J=8,1, 1,6 Гц, 1H), 7,67 (d, J=8,0 Гц, 1H), 5,11 (dd, J=13,3, 5,1 Гц, 1H), 4,47 (d, J=17,7 Гц, 1H), 4,34 (d, J=17,7 Гц, 1H), 2,98-2,83 (m, 1H), 2,65-2,55 (m, 1H), 2,45-2,29 (m, 1H), 2,01 (dtd, J=12,7, 5,3, 2,3 Гц, 1H).
Стадия 2. Трет-бутил-4-(2-(2,6-диоксопиперидин-3-ил)-1-оксоизоиндолин-5-ил)-3,6-дигидропиридин-1(2H)-карбоксилат (A-12)
Раствор A-10 (1,8 г, 5,6 ммоль) в DMF (10 мл) в герметизированной пробирке продували аргоном в течение 5 мин до добавления пинаколового сложного эфира 3,6-дигидро-2H-пиридин-1-трет-бутоксикарбонил-4-бороновой кислоты (A-11, 2,2 г, 7,2 ммоль), K3PO4 (1,42 г, 6,7 ммоль) и Pd(dppf)Cl2⋅DCM (227 мг, 0,28 ммоль). Реакционную смесь снова продували аргоном в течение 5 мин и затем нагревали при 90°C в течение 16 ч. После завершения данного периода времени реакционную смесь охлаждали до комнатной температуры и затем концентрировали при пониженном давлении. К остатку добавляли воду, затем его экстрагировали с помощью EtOAc. Органический слой промывали солевым раствором, сушили над Na2SO4, фильтровали и затем концентрировали при пониженном давлении. Неочищенное соединение очищали посредством хроматографии на силикагеле с элюированием с помощью 70-80% EtOAc в гексанах с получением A-12 в виде светло-коричневого твердого вещества (1,0 г, 2,4 ммоль, выход 42%). MS [M+H]+ = 426,3.
Стадия 3. Трет-бутил-4-(2-(2,6-диоксопиперидин-3-ил)-1-оксоизоиндолин-5-ил)пиперидин-1-карбоксилат (A-13)
К перемешиваемому раствору A-12 (1,0 г, 2,35 ммоль) в DMF (20 мл) добавляли 10% Pd/C (150 мг) и смесь перемешивали в атмосфере водорода (баллон) при к. т. в течение 6 ч. Затем реакционную смесь фильтровали через слой фильтрующей среды Celite®. Фильтрат концентрировали при пониженном давлении с получением A-12 в виде твердого вещества (0,85 г, 1,97 ммоль, выход 84%). MS [M-tBu]+ = 372,3. 1H ЯМР (400 МГц, CDCl3) δ 8,40 (s, 1H), 7,81 (d, J=7,9 Гц, 1H), 7,32 (d, J=8,0 Гц, 1H), 7,29 (s, 1H), 5,22 (dd, J=13,3, 5,1 Гц, 1H), 4,46 (d, J=16,0 Гц, 1H), 4,31 (d, J=16,1 Гц, 1H), 4,27 (d, J=16,2 Гц, 2H), 2,97-2,67 (m, 5H), 2,41-2,26 (m, 1H), 2,23-2,13 (m, 1H), 1,83 (d, J=12,6 Гц, 2H), 1,71-1,55 (m, 2H), 1,48 (s, 9H).
Стадия 4. Гидрохлорид 3-(1-оксо-5-(пиперидин-4-ил)изоиндолин-2-ил)пиперидин-2,6-диона (I-155)
К перемешиваемому раствору A-12 (0,85 г, 2,0 ммоль) в диоксане (10 мл) добавляли 4 н. HCl в диоксане (5,0 мл). Затем реакционную смесь перемешивали при комнатной температуре в течение 2 ч. Реакционную массу концентрировали при пониженном давлении с получением HCl-соли необходимого соединения I-155 в виде твердого вещества (0,65 г, 1,8 ммоль, выход 90%, гидрохлоридная соль). MS [M+H]+ = 328,3. 1H ЯМР (400 МГц, DMSO-d6): δ 10,99 (s, 1H), 9,28 (s, 1H), 7,70 (d, J=7,8 Гц, 1H), 7,46 (s, 1H), 7,39 (d, J=8,0 Гц, 1H), 5,74 (s, 1H), 5,11 (dd, J=13,3, 5,2 Гц, 1H), 4,46 (d, J=17,3 Гц, 1H), 4,32 (d, J=17,3 Гц, 1H), 3,36 (d, J=11,5 Гц, 2H), 3,10-2,86 (m, 4H), 2,61 (d, J=14,8 Гц, 1H), 2,39 (qd, J=13,2, 4,3 Гц, 1H), 2,14-1,79 (m, 5H).
Пример 18-2. 3-(1-Оксо-5-(2,2,6,6-тетраметилпиперидин-4-ил)изоиндолин-2-ил)пиперидин-2,6-дион (I-171)
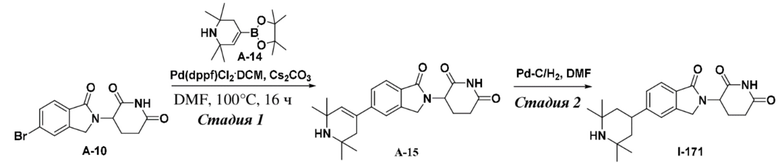
Стадия 1. 3-(1-Оксо-5-(2,2,6,6-тетраметил-1,2,3,6-тетрагидропиридин-4-ил)изоиндолин-2-ил)-пиперидин-2,6-дион (A-15)
Перемешиваемый раствор A-10 (150 мг, 0,46 ммоль) в DMF (5 мл) в герметизированной пробирке продували аргоном в течение 5 мин до добавления 2,2,6,6-тетраметил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиперидина (A-14, 185 мг, 0,69 ммоль), Cs2CO3 (300 мг, 0,92 ммоль) и Pd(dppf)Cl2⋅DCM (19 мг, 0,02 ммоль) и полученную смесь снова продували аргоном в течение 5 мин. Затем реакционную смесь нагревали при 90°C в течение 5 ч, после завершения данного периода времени реакционную смесь охлаждали до комнатной температуры, добавляли воду и смесь экстрагировали с EtOAc. Органический слой промывали солевым раствором, высушивали над Na2SO4, фильтровали и затем концентрировали при пониженном давлении. Неочищенный материал очищали посредством хроматографии на силикагеле (элюирование с помощью 15% MeOH/DCM) с получением A-15 в виде твердого вещества (35 мг, 0,092 ммоль, выход 20%). MS [M+H]+ = 382,3.
Стадия 2. 3-(1-Оксо-5-(2,2,6,6-тетраметилпиперидин-4-ил)изоиндолин-2-ил)пиперидин-2,6-дион (I-171)
К перемешиваемому раствору 3-(1-оксо-5-(2,2,6,6-тетраметил-1,2,3,6-тетрагидропиридин-4-ил)изоиндолин-2-ил)пиперидин-2,6-диона (A-15, 25 мг, 0,07 ммоль) в DMF (2 мл) добавляли Pd/C (5 мг). Полученную смесь перемешивали в атмосфере водорода (баллон) при комнатной температуре в течение 5 ч. Затем реакционную смесь фильтровали через слой фильтрующей среды Celite® и фильтрат концентрировали до сухого состояния. Неочищенный материал очищали посредством HPLC с обращенной фазой (MeCN/H2O с 0,05% муравьиной кислоты) с получением I-171 в виде твердого вещества (11 мг, 0,03 ммоль, выход 44%). MS [M+H]+ = 384,4. 1H ЯМР (600 МГц, DMSO-d6): δ 11,0 (s, 1H), 8,33-8,32 (m, 1H), 7,68 (d, J=8,0 Гц, 1H), 7,5 (s, 1H), 7,43 (d, J=8,4 Гц, 1H), 5,12 (dd, J=13,2, 4,8 Гц, 1H), 4,36 (d, J=17,4 Гц, 1H), 4,31 (d, J=17,4 Гц, 1H), 2,95-2,90 (m, 1H), 2,43-2,39 (m, 2H), 2,00-1,99 (m, 2 H), 1,54-1,50 (m, 2H), 1,52-1,50 (m, 2H), 1,26 (s, 6H), 1,23 (s, 6H).
Следующие соединения получали в соответствии с общим протоколом, представленным на схеме 1, и примеры описаны выше:

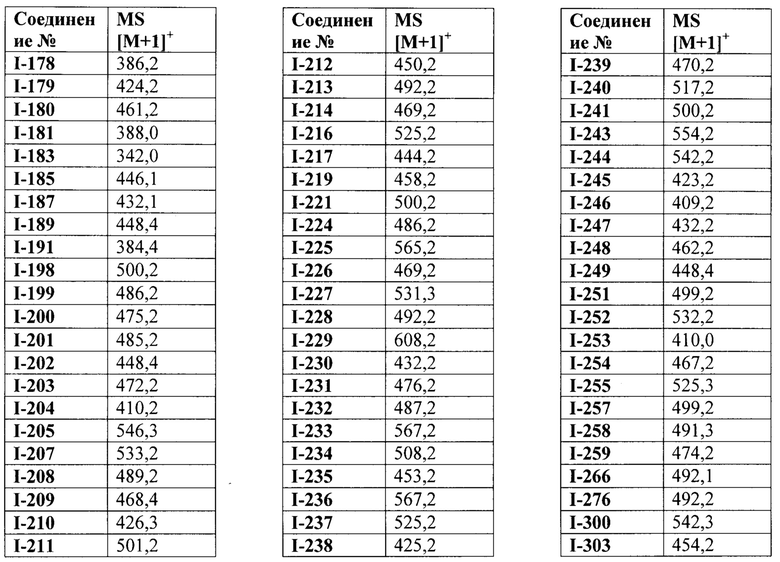
Пример 18-3. HC(O)OH-соль 3-(5-(8-Бензил-8-азабицикло[3.2.1]октан-3-ил)-1-оксоизоиндолин-2-ил)пиперидин-2,6-диона (I-265)
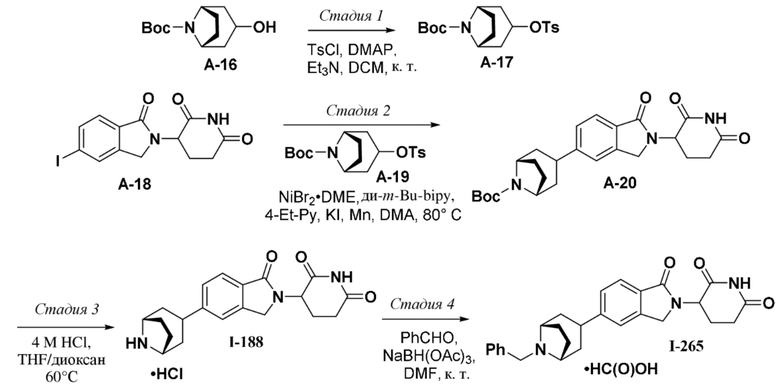
Стадия 1. Трет-бутил-3-(тозилокси)-8-азабицикло[3.2.1]октан-8-карбоксилат (A-17)
К перемешиваемому раствору 3-гидрокси-8-азабицикло[3.2.1]октан-8-карбоксилата (A-16, 570 мг, 2,51 ммоль), Et3N (0,52 мл, 3,8 ммоль) и DMAP (61 мг, 0,50 ммоль) в DCM (5 мл) добавляли TsCl (574 мг, 3,01 ммоль) и полученную смесь перемешивали в течение ночи при комнатной температуре. Затем реакционную смесь гасили с помощью нас. водн. раствора NaHCO3 и экстрагировали с помощью DCM (3x). Объединенный органические фазы сушили над Na2SO4, фильтровали и концентрировали, и неочищенный материал очищали посредством хроматографии на силикагеле с элюированием с помощью 0% - 40% EtOAc в гептане с получением A-17 (91 мг, 0,22 ммоль, выход 9%) в виде твердого вещества. 1H ЯМР (400 МГц, Хлороформ-d) δ 7,79 (d, J=8,3 Гц, 2H), 7,36 (d, J=8,5 Гц, 2H), 4,83 (t, J=5,0 Гц, 1H), 4,16 (s, 2H), 2,47 (s, 3H), 2,12- 2,02 (m, 4H), 2,00-1,90 (m, 2H), 1,84 (d, J=15,3 Гц, 2H), 1,45 (s, 9H).
Стадия 2. Трет-бутил-3-(2-(2,6-диоксопиперидин-3-ил)-1-оксоизоиндолин-5-ил)-8-азабицикло[3.2.1]-октан-8-карбоксилат (A-20)
К перемешиваемой суспензии A-18 (56 мг, 0,15 ммоль), 56b (69 мг, 0,18 ммоль), NiBr2(DME) (4,7 мг, 0,015 ммоль), 4,4'-ди-трет-бутил-2,2'-дипиридила (4,1 мг, 0,015 ммоль), KI (25 мг, 0,15 ммоль) и порошка марганца (17 мг, 0,30 ммоль) в DMA (0,7 мл) в атмосфере азота добавляли 4-этилпиридин (0,017 мл, 0,15 ммоль) и полученную смесь энергично перемешивали при 80°C в течение 4 часов. Затем реакционную смесь разбавляли с помощью MeCN и фильтровали через слой фильтрующей среды Celite® с элюированием с помощью MeCN. Фильтрат концентрировали до сухого состояния путем азеотропной перегонки с использованием гептана. Неочищенный материал очищали посредством хроматографии на силикагеле с элюированием с помощью 0% - 5% MeOH в DCM с получением A-20 (38,4 мг, 0,085 ммоль, выход 56%) в виде твердого вещества. MS [M+H]+ = 454,5. 1H ЯМР (400 МГц, Хлороформ-d) δ 8,58 (s, 1H), 7,80 (dd, J=7,9, 0,6 Гц, 1H), 7,32 (dd, J=7,9, 1,4 Гц, 1H), 7,29 (s, 1H), 5,23 (dd, J=13,3, 5,1 Гц, 1H), 4,46 (d, J=16,0 Гц, 1H), 4,39-4,24 (m, 3H), 3,20 (tt, J=11,8, 5,2 Гц, 1H), 2,94-2,74 (m, 2H), 2,34 (qd, J=12,8, 5,6 Гц, 1H), 2,23-2,13 (m, 1H), 2,09-2,02 (m, 2H), 1,90 (t, J=12,9 Гц, 2H), 1,80 (q, J=8,0, 6,6, 6,2 Гц, 2H), 1,76-1,69 (m, 2H), 1,51 (s, 9H).
Стадия 3. Гидрохлорид 3-(5-(8-азабицикло[3.2.1]октан-3-ил)-1-оксоизоиндолин-2-ил)пиперидин-2,6-диона (I-188)
К перемешиваемому раствору A-20 (38 мг, 0,084 ммоль) в THF (1 мл) добавляли 4 M HCl в диоксане (0,7 мл, 2,8 ммоль) и полученную смесь перемешивали в течение 3 часов при 60°C. Наблюдали образование белого осадка. Затем реакционную смесь разбавляли с помощью Et2O и фильтровали. Осадок промывали с помощью Et2O и затем сушили с получением гидрохлоридной соли I-188 (31,9 мг, 0,082 ммоль, 98%) в виде твердого вещества. MS [M+H]+ = 354,3. 1H ЯМР (400 МГц, DMSO-d6) δ 10,98 (s, 1H), 9,18 (s, 1H), 7,69 (dd, J=7,8, 2,3 Гц, 1H), 7,56 (s, 1H), 7,50 (d, J=7,9 Гц, 1H), 5,10 (ddd, J=13,2, 5,2, 2,1 Гц, 1H), 4,45 (d, J=18,1 Гц, 1H), 4,30 (dd, J=17,3, 2,2 Гц, 1H), 4,03 (s, 2H), 3,26-3,21 (m, 1H), 2,92 (tt, J=14,0, 5,2 Гц, 1H), 2,67-2,54 (m, 1H), 2,45-2,31 (m, 1H), 2,17 (t, J=13,1 Гц, 2H), 2,09-1,92 (m, 5H), 1,89-1,73 (m, 2H).
Стадия 4. HC(O)OH-соль 3-(5-(8-Бензил-8-азабицикло[3.2.1]октан-3-ил)-1-оксоизоиндолин-2-ил)пиперидин-2,6-диона (I-265)
К перемешиваемому раствору I-188 (20 мг, 0,051 ммоль) и бензальдегида (0,016 мл, 0,154 ммоль) в DMF (1 мл) добавляли одной порцией триацетоксиборогидрид натрия (33 мг, 0,15 ммоль) и полученную смесь энергично перемешивали при комнатной температуре в течение ночи. Затем добавляли одну каплю HCOOH и реакционную смесь концентрировали при пониженном давлении. Неочищенный материал очищали посредством HPLC с обращенной фазой (элюирование с помощью MeCN/H2O с 0,1% муравьиной кислоты) и продукт лиофилизировали с получением формиатной соли I-265 (15,0 мг, 0,031 ммоль, выход 60%) в виде твердого вещества. MS [M+H]+ = 444,3. 1H ЯМР (400 МГц, DMSO-d6) δ 10,98 (s, 1H), 8,25 (s, 1H), 7,64 (d, J=7,9 Гц, 1H), 7,52 (s, 1H), 7,42 (d, J=8,1 Гц, 3H), 7,35-7,31 (m, 2H), 7,24 (t, J=7,3 Гц, 1H), 5,10 (dd, J=13,0, 5,0 Гц, 1H), 4,42 (d, J=17,2 Гц, 1H), 4,29 (d, J=17,1 Гц, 1H), 3,61 (s, 2H), 3,25 (s, 2H), 3,13-3,01 (m, 1H), 2,91 (ddd, J=17,9, 13,2, 5,3 Гц, 1H), 2,59 (d, J=17,0 Гц, 1H), 2,46-2,31 (m, 1H), 2,14-1,94 (m, 3H), 1,85 (t, J=12,4 Гц, 2H), 1,76 (d, J=7,8 Гц, 2H), 1,63 (d, J=12,7 Гц, 2H).
Соединение I-260 синтезировали в соответствии с путем, описанным в примере 18-3 (MS [M+H]+ = 404,2).
Пример 18-4. Диастереомеры 3-(5-(1-бензилазепан-4-ил)-1-оксоизоиндолин-2-ил)пиперидин-2,6-диона (I-190) и (I-273)

Стадия 1. 3-(1-Оксо-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)изоиндолин-2-ил)пиперидин-2,6-дион (A-22a)
К перемешиваемому раствору A-10 (3,0 г, 9,28 ммоль) в DMF (20 мл) в герметизированной пробирке добавляли бис(пинаколато)дибор (A-21, 2,6 г, 10,2 ммоль), KOAc (2,37 г, 27,9 ммоль) и PdCl2(dppf)2 (0,22 г, 0,28 ммоль). Реакционную смесь продували аргоном в течение 5 мин, герметизировали и затем нагревали при 100C в течение 16 ч. В реакционную смесь добавляли воду и перемешивали при комнатной температуре в течение 15 мин. твердое вещество осаждали, фильтровали и сушили под вакуумом с получением A-22a в виде твердого вещества (2,3 г, 6,2 ммоль, выход 66%). MS [M+H]+ = 371,0.
Стадия 2. Трет-бутил-5-(2-(2,6-диоксопиперидин-3-ил)-1-оксоизоиндолин-5-ил)-2,3,4,7-тетрагидро-1H-азепин-1-карбоксилат (A-23)
Трет-бутил-5-(((трифторметил)сульфонил)окси)-2,3,4,7-тетрагидро-1H-азепин-1-карбоксилат A-22b получали, как указано в публикации заявки согласно PCT № 2007/111904.
К перемешиваемому раствору A-22a (1,0 г, 2,70 ммоль) в DMF (10,0 мл) в герметизированной пробирке добавляли трет-бутил-5-(((трифторметил)сульфонил)окси)-2,3,4,7-тетрагидро-1H-азепин-1-карбоксилат (A-22b, 1,19 г, 3,24 ммоль), Pd(PPh3)4 (0,16 г, 0,13 ммоль) и Na2CO3 (0,85 г, 8,10 ммоль). Смесь продували аргоном в течение 5 мин и затем герметизировали и нагревали при 100°C в течение 3 ч. После завершения данного периода времени реакционную смесь охлаждали и добавляли воду перед экстракцией с помощью EtOAc. Органический слой сушили над Na2SO4, фильтровали, концентрировали при пониженном давлении и очищали посредством хроматографии на силикагеле (элюирование с 60-70% EtOAc/гексанами) с получением A-23 в виде твердого вещества (350 мг, 0,796 ммоль, выход 29%). MS [M+H]+ = 440,0.
Стадия 3. Трет-бутил-4-(2-(2,6-диоксопиперидин-3-ил)-1-оксоизоиндолин-5-ил)азепан-1-карбоксилат (A-24).
К перемешиваемому раствору A-23 (0,35 г, 0,80 ммоль) в THF (10 мл) добавляли PtO2 (100 мг). Смесь перемешивали в атмосфере водорода, подаваемой из баллона, в течение 5 ч. Затем реакционную смесь фильтровали через слой фильтрующей среды Celite® и затем концентрировали при пониженном давлении. Полученный осадок очищали посредством хроматографии на силикагеле (элюирование с помощью 40-50% EtOAc/гексана) с получением A-24 в виде твердого вещества, состоящего из смеси диастереомеров (0,31 г, 0,70 ммоль, выход 88%). MS [M+H]+ = 442,0.
Стадия 4a. Хиральное разделение трет-бутил-4-(2-(2,6-диоксопиперидин-3-ил)-1-оксоизоиндолин-5-ил)азепан-1-карбоксилата (A-24)
Хиральное разделение A-24 (350 мг) проводили с применением колонки Kinetex (150 мм X 21 мм), 5,0 мкм, с использованием элюента, состоящего из подвижной фазы A=0,05% TFA в воде; подвижной фазы B=ацетонитрил, и при расходе, составляющем 20 мл/мин., при 25°C с 20-70% подвижной фазы B:подвижной фазы A в течение 20 мин. В таких условиях выделяли два соединения A-24 (пик 1), Rt=11,64 мин, и A-24 (пик 2), Rt=17,41 мин). Фракции, соответствующие пику 1 и пику 2, собирали и концентрировали при пониженном давлении, затем нейтрализовали с помощью водного насыщенного раствора NaHCO3 перед экстракцией с помощью DCM. Органические слои объединяли, сушили над Na2SO4, фильтровали и концентрировали до сухого состояния с получением соединений, соответствующих пику 1 (50 мг) и пику 2 (45 мг), в виде белых твердых веществ. MS [M+H]+ = 442,0.
Стадия 4b. 3-(5-(Азепан-4-ил)-1-оксоизоиндолин-2-ил)пиперидин-2,6-дион (I-166 и I-167)
К перемешиваемому раствору A-24 (пик 1) (50 мг, 0,113 ммоль) в диоксане (2,0 мл) при 0°C добавляли 4M HCl в диоксане (0,5 мл). Затем обеспечивали перемешивание реакционной смеси и нагревание до комнатной температуры на протяжении 2 ч. Затем реакционную смесь концентрировали при пониженном давлении с получением диастереомера A (40 мг, 0,106 ммоль, 94%, гидрохлоридная соль). MS [M+H]+ = 342,3. 1H ЯМР (CD3OD, 300 МГц): δ 7,74 (d, J=8,1 Гц, 1H), 7,49 (1H, s), 7,43 (d, J=8,4 Гц, 1H), 5,14 (dd, J=13,5, 5,1 Гц, 1H), 4,48-4,46 (m, 2H), 3,74-3,71(m, 1H), 3,68-3,63 (m, 2H), 3,59-3,55 (m, 1H), 3,44-3,37 (m, 2H), 3,02 (m, 1H), 2,90-2,78 (m, 2H), 2,51-2,47 (m, 1H), 2,16-2,08 (m, 5H), 2,00-1,80 (m, 2H).
К перемешиваемому раствору A-24 (пик 2) (40 мг, 0,091 ммоль) в диоксане (2,0 мл) при 0°C добавляли 4 M HCl в диоксане (0,5 мл). Затем обеспечивали перемешивание реакционной смеси и нагревание до к. т. на протяжении 2 ч. Затем реакционную смесь концентрировали при пониженном давлении с получением диастереомера B (30 мг, 0,079 ммоль, выход 87%, гидрохлоридная соль). MS [M+H]+ = 342,4. 1H ЯМР (CD3OD, 300 МГц): δ 7,74 (d, J=7,5 Гц, 1H), 7,49 (s, 1H), 7,42 (d, J=7,8 Гц, 1H), 5,15 (dd, J=13,5, 5,1 Гц, 1H), 4,47-4,45 (d, 2H), 3,74-3,71 (m, 1H), 3,67-3,62 (m, 3H), 3,58-3,55 (m, 1H), 3,43-3,38 (m, 2H), 3,02 (m, 1H), 2,90-2,78 (m, 2H), 2,51-2,48 (m, 1H), 2,17-2,08 (m, 5H), 2,09-1,87 (m, 1H).
Стадия 5. Диастереомеры 3-(5-(1-бензилазепан-4-ил)-1-оксоизоиндолин-2-ил)пиперидин-2,6-диона (I-190 и I-273)
Соединение I-190 получали из I-166 (80 мг, 0,21 ммоль) и бензальдегида (27 мг, 0,25 ммоль) посредством восстановительного аминирования. После полного расходования исходных материалов неочищенную реакционную смесь концентрировали при пониженном давлении и добавляли нас. водн. раствор NaHCO3. Полученную смесь экстрагировали с помощью DCM и органический слой сушили над Na2SO4, фильтровали и концентрировали до сухого состояния. Полученное твердое вещество промывали с помощью эфира (5 мл) и EtOAc (0,1 мл) с получением соединения I-190 в виде твердого вещества (55 мг, 0,13 ммоль, выход 60%). Абсолютный стереохимия неизвестна и была задана произвольным образом. MS [M+H]+ = 439,1. 1H ЯМР (CD3OD, 600 МГц) : δ 7,69 (d, J=5,2 Гц, 1H), 7,44 (s, 1H), 7,39-7,36 (m, 3H), 7,32-7,30 (m, 2H), 7,26-7,24 (m, 1H), 5,12 (dd, J=8,8, 3,2 Гц, 1H), 4,47 (d, J=11,6 Гц, 1H), 4,41 (d, J=11,2 Гц, 1H), 3,71 (2H, s), 2,98-2,97 (m, 1H), 2,92-2,86 (m, 2H), 2,80-2,74 (m, 4H), 2,47-2,45 (m, 1H), 2,16-2,14 (m, 1H), 1,94-1,84 (m, 1H), 1,80 (m, 1H).
Соединение I-273 получали из I-167 (80 мг, 0,21 ммоль) и бензальдегида (27 мг, 0,25 ммоль) аналогично тому, как описано выше для соединения I-190. I-273 выделяли в виде твердого вещества (55 мг, 0,13 ммоль, выход 60%). Абсолютная стереохимия неизвестна и была задана произвольным образом. MS [M+H]+ = 439,1. 1H ЯМР (DMSO-d6, 400 МГц): δ 11,0 (1H, s), 7,62 (d, J=5,2 Гц, 1H), 7,46 (s, 1H), 7,38-7,32 (m, 5H), 7,24-7,23 (m, 1H), 5,09 (dd, J=8,8, 3,6 Гц, 1H), 4,31 (d, J=11,6 Гц, 1H), 4,28 (d, J=11,6 Гц, 1H), 3,65 (d, J=9,1 Гц, 1H), 3,63 (d, J=9,2 Гц, 1H), 2,96-2,88 (m, 2H), 2,76-2,69 (m, 1H), 2,67-2,62 (m, 3H), 2,61- 2,50 (m, 2H), 2,46-2,36 (m, 3H), 1,99 (m, 2H), 1,82 (m, 2H).
Пример 18-5. 3-(5-(1-Бензил-2-оксо-1,2-дигидропиридин-4-ил)-1-оксоизоиндолин-2-ил)-пиперидин-2,6-дион (I-192)

К перемешиваемой суспензии A-22a (500 мг, 1,35 ммоль), A-25 (428 мг, 1,62 ммоль) и K2CO3 в DMF (5 мл) добавляли PdCl2(dppf)⋅DCM (55 мг, 0,07 ммоль), и полученную смесь барботировали аргоном в течение 10 мин и затем перемешивали при 130°C в течение 90 мин. После полного расходования исходного материала реакционную смесь гасили ледяной водой и экстрагировали с помощью EtOAc (3×50 мл). Объединенные органические экстракты промывали солевым раствором, сушили над Na2SO4 и концентрировали при пониженном давлении. Неочищенный материал очищали посредством хроматографии на силикагеле с элюированием с помощью 5% MeOH в DCM с получением I-192 в виде твердого вещества (20 мг, 0,46 ммоль, выход 35%). MS [M+H]+ = 427,8. 1H ЯМР (400 МГц, DMSO-d6): δ 10,98 (s, 1H), 7,94 (s, 1H), 7,90 (d, J=7,6 Гц, 1H), 7,80-7,76 (m, 2H), 7,33-7,25 (m, 5H), 6,76 (d, J=2,0 Гц, 1H), 6,64 (dd, J=7,2, 2,0 Гц, 1H), 5,12 (s, 2H), 5,12-5,08 (m, 1H), 4,48 (d, J=17,2 Гц, 1H), 4,36 (d, J=17,2 Гц, 1H), 2,80-2,75 (m, 1H), 2,60-2,53 (m, 1H), 2,45-2,38 (m, 1H), 2,02-1,97 (m, 1H).
Следующие соединения синтезировали в соответствии с протоколом, описанным в примере 18-5:
I-184: MS [M+H]+ = 356,1.
I-186: MS [M+H]+ = 342,1.
I-192: MS [M+H]+ = 427,8.
Пример 18-6. 3-(1-Оксо-5-(1,2,3,4-тетрагидрохинолин-4-ил)изоиндолин-2-ил)пиперидин-2,6-дион (I-196)

Стадия 1. 3-(1-Оксо-5-винилизоиндолин-2-ил)пиперидин-2,6-дион (A-26)
К раствору A-10 (1,5 г, 4,66 ммоль) и трибутил(винил)станнана (2,04 мл, 6,95 ммоль) в диоксане (15 мл) добавляли PdCl2(PPh3)2 (162 мг, 0,23 ммоль), и полученную смесь продували аргоном в течение 10 мин и затем перемешивали при 110°C в течение 1 ч при обработке микроволнами. После полного расходования исходного материала реакционную смесь гасили водой и экстрагировали с помощью EtOAc (2×50 мл). Объединенные органические экстракты промывали солевым раствором, сушили над Na2SO4 и концентрировали при пониженном давлении. Полученный неочищенный материал очищали посредством хроматографии на силикагеле с элюированием с помощью 90% EtOAc в гексане. Чистые фракции собирали и выпаривали при пониженном давлении с получением A-26 в виде твердого вещества (500 мг, 1,85 ммоль, выход 40%). MS [M+H]+ = 271,2.
Стадия 2. 3-(1-Оксо-5-(1,2,3,4-тетрагидрохинолин-4-ил)изоиндолин-2-ил)пиперидин-2,6-дион (I-196)
К раствору соединения A-26 (200 г, 0,74 ммоль) и (азидометил)бензола (118 мг, 0,89 ммоль) в DCM (4 мл) добавляли трифлатную кислоту (0,08 мл, 0,89 ммоль) и полученную смесь перемешивали при комнатной температуре в течение 2 ч. После полного расходования исходного материала реакционную смесь гасили водой и экстрагировали с помощью EtOAc (2×50 мл). Объединенные органические экстракты промывали солевым раствором, сушили над Na2SO4 и концентрировали при пониженном давлении. Полученный неочищенный материал очищали посредством HPLC с обращенной фазой (элюирование с помощью 0,01% NH4OAc в MeCN) с получением I-196 в виде твердого вещества (15 мг, 0,04 ммоль, выход 6%). MS [M+H]+ = 376,2. 1H ЯМР (400 МГц, DMSO-d6): δ 10,96 (s, 1H), 7,66 (d, J=8,0 Гц, 1H), 7,32-7,23 (m, 2H), 6,92 (t, J=7,6 Гц, 1H), 6,59-6,55 (m, 2H), 6,41 (t, J=7,2 Гц, 1H), 5,08 (dd, J=13,2, 5,2 Гц, 1H), 4,44-4,23 (m, 3H), 3,24-3,18 (m, 1H), 3,10-3,05 (m, 1H), 2,95-2,86 (m, 1H), 2,66-2,50 (m, 2H), 2,42-2,31 (m, 1H), 2,10-1,98 (m, 3H).
Соединение I-197 синтезировали тем же способом, который описан выше в примере 18-6. I-197: MS [M+H]+ = 466,2.
ЭКВИВАЛЕНТЫ
Раскрытия всех без исключения патентов, заявок на патент и публикаций, цитируемых в данном документе, настоящим включены в данный документ посредством ссылки во всей своей полноте. Несмотря на то, что настоящее изобретение было раскрыто со ссылкой на конкретные аспекты, очевидно, что другие аспекты и видоизменения настоящего изобретения могут быть разработаны другими специалистами в данной области техники без отступления от фактической сущности и объема настоящего изобретения. Предполагается, что прилагаемую формулу изобретения следует истолковывать как включающую все такие аспекты и эквивалентные видоизменения.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> NOVARTIS AG
<120> КОМПОЗИЦИИ И СПОСОБЫ СЕЛЕКТИВНОЙ ДЕГРАДАЦИИ БЕЛКА
<130> N2067-7136WO
<140>
<141>
<150> 62/574,188
<151> 2017-10-18
<160> 1560
<170> PatentIn версия 3.5
<210> 1
<211> 60
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 1
Met His Lys Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln
1. 5 10 15
Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys
20 25 30
Leu His Thr Gly Glu Lys Pro Phe Lys Cys His Leu Cys Asn Thr Ala
35 40 45
Ser Ala Glu Ala Arg His Ile Lys Ala Glu Met Gly
50 55 60
<210> 2
<211> 60
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 2
Met His Arg Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln
1. 5 10 15
Cys Gly Ala Ser Phe Thr Gln Arg Gly Asn Leu Leu Arg His Ile Arg
20 25 30
Leu His Thr Gly Glu Arg Pro Phe Arg Cys His Leu Cys Asn Thr Ala
35 40 45
Ser Ala Glu Ala Arg His Ile Arg Ala Glu Met Gly
50 55 60
<210> 3
<211> 59
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 3
His Lys Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln Cys
1. 5 10 15
Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys Leu
20 25 30
His Thr Gly Glu Lys Pro Phe Lys Cys His Leu Cys Asn Thr Ala Ser
35 40 45
Ala Glu Ala Arg His Ile Lys Ala Glu Met Gly
50 55
<210> 4
<211> 59
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 4
His Arg Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln Cys
1. 5 10 15
Gly Ala Ser Phe Thr Gln Arg Gly Asn Leu Leu Arg His Ile Arg Leu
20 25 30
His Thr Gly Glu Arg Pro Phe Arg Cys His Leu Cys Asn Thr Ala Ser
35 40 45
Ala Glu Ala Arg His Ile Arg Ala Glu Met Gly
50 55
<210> 5
<211> 45
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 5
His Lys Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln Cys
1. 5 10 15
Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys Leu
20 25 30
His Thr Gly Glu Lys Pro Phe Lys Cys His Leu Cys Asn
35 40 45
<210> 6
<211> 35
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 6
His Lys Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln Cys
1. 5 10 15
Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys Leu
20 25 30
His Thr Gly
35
<210> 7
<211> 31
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 7
His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln Cys Gly Ala Ser Phe
1. 5 10 15
Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys Leu His Thr Gly
20 25 30
<210> 8
<211> 23
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 8
Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln Cys Gly Ala Ser Phe Thr
1. 5 10 15
Gln Lys Gly Asn Leu Leu Arg
20
<210> 9
<211> 26
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 9
Pro Phe Gln Cys Asn Gln Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn
1. 5 10 15
Leu Leu Arg His Ile Lys Leu His Thr Gly
20 25
<210> 10
<211> 11
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 10
Pro Phe Gln Cys Asn Gln Cys Gly Ala Ser Phe
1. 5 10
<210> 11
<211> 14
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 11
Thr Ala Ser Ala Glu Ala Arg His Ile Lys Ala Glu Met Gly
1. 5 10
<210> 12
<211> 60
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 12
Met His Lys Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln
1. 5 10 15
Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys
20 25 30
Leu His Thr Gly Glu Lys Pro Phe Lys Cys His Leu Cys Asn Thr Ala
35 40 45
Ser Ala Glu Ala Arg His Ile Arg Ala Glu Met Gly
50 55 60
<210> 13
<211> 60
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 13
Met His Lys Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln
1. 5 10 15
Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys
20 25 30
Leu His Thr Gly Glu Lys Pro Phe Lys Cys His Leu Cys Asn Thr Ala
35 40 45
Ser Ala Glu Ala Arg His Ile Ser Ala Glu Met Gly
50 55 60
<210> 14
<211> 60
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 14
Met His Lys Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln
1. 5 10 15
Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys
20 25 30
Leu His Thr Gly Glu Lys Pro Phe Lys Cys His Leu Cys Asn Met Ala
35 40 45
Leu Glu Lys Met Ala Leu Glu Lys Met Ala Leu Glu
50 55 60
<210> 15
<211> 50
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 15
Met His Lys Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln
1. 5 10 15
Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys
20 25 30
Leu His Thr Gly Met Ala Leu Glu Lys Met Ala Leu Glu Lys Met Ala
35 40 45
Leu Glu
50
<210> 16
<211> 46
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 16
Met His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln Cys Gly Ala Ser
1. 5 10 15
Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys Leu His Thr Gly
20 25 30
Met Ala Leu Glu Lys Met Ala Leu Glu Lys Met Ala Leu Glu
35 40 45
<210> 17
<211> 38
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 17
Met Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln Cys Gly Ala Ser Phe
1. 5 10 15
Thr Gln Lys Gly Asn Leu Leu Arg Met Ala Leu Glu Lys Met Ala Leu
20 25 30
Glu Lys Met Ala Leu Glu
35
<210> 18
<211> 26
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 18
Met Pro Phe Gln Cys Asn Gln Cys Gly Ala Ser Phe Met Ala Leu Glu
1. 5 10 15
Lys Met Ala Leu Glu Lys Met Ala Leu Glu
20 25
<210> 19
<211> 509
<212> БЕЛОК
<213> Homo sapiens
<400> 19
Met Glu Asp Ile Gln Thr Asn Ala Glu Leu Lys Ser Thr Gln Glu Gln
1. 5 10 15
Ser Val Pro Ala Glu Ser Ala Ala Val Leu Asn Asp Tyr Ser Leu Thr
20 25 30
Lys Ser His Glu Met Glu Asn Val Asp Ser Gly Glu Gly Pro Ala Asn
35 40 45
Glu Asp Glu Asp Ile Gly Asp Asp Ser Met Lys Val Lys Asp Glu Tyr
50 55 60
Ser Glu Arg Asp Glu Asn Val Leu Lys Ser Glu Pro Met Gly Asn Ala
65 70 75 80
Glu Glu Pro Glu Ile Pro Tyr Ser Tyr Ser Arg Glu Tyr Asn Glu Tyr
85 90 95
Glu Asn Ile Lys Leu Glu Arg His Val Val Ser Phe Asp Ser Ser Arg
100 105 110
Pro Thr Ser Gly Lys Met Asn Cys Asp Val Cys Gly Leu Ser Cys Ile
115 120 125
Ser Phe Asn Val Leu Met Val His Lys Arg Ser His Thr Gly Glu Arg
130 135 140
Pro Phe Gln Cys Asn Gln Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn
145 150 155 160
Leu Leu Arg His Ile Lys Leu His Thr Gly Glu Lys Pro Phe Lys Cys
165 170 175
His Leu Cys Asn Tyr Ala Cys Gln Arg Arg Asp Ala Leu Thr Gly His
180 185 190
Leu Arg Thr His Ser Val Glu Lys Pro Tyr Lys Cys Glu Phe Cys Gly
195 200 205
Arg Ser Tyr Lys Gln Arg Ser Ser Leu Glu Glu His Lys Glu Arg Cys
210 215 220
Arg Thr Phe Leu Gln Ser Thr Asp Pro Gly Asp Thr Ala Ser Ala Glu
225 230 235 240
Ala Arg His Ile Lys Ala Glu Met Gly Ser Glu Arg Ala Leu Val Leu
245 250 255
Asp Arg Leu Ala Ser Asn Val Ala Lys Arg Lys Ser Ser Met Pro Gln
260 265 270
Lys Phe Ile Gly Glu Lys Arg His Cys Phe Asp Val Asn Tyr Asn Ser
275 280 285
Ser Tyr Met Tyr Glu Lys Glu Ser Glu Leu Ile Gln Thr Arg Met Met
290 295 300
Asp Gln Ala Ile Asn Asn Ala Ile Ser Tyr Leu Gly Ala Glu Ala Leu
305 310 315 320
Arg Pro Leu Val Gln Thr Pro Pro Ala Pro Thr Ser Glu Met Val Pro
325 330 335
Val Ile Ser Ser Met Tyr Pro Ile Ala Leu Thr Arg Ala Glu Met Ser
340 345 350
Asn Gly Ala Pro Gln Glu Leu Glu Lys Lys Ser Ile His Leu Pro Glu
355 360 365
Lys Ser Val Pro Ser Glu Arg Gly Leu Ser Pro Asn Asn Ser Gly His
370 375 380
Asp Ser Thr Asp Thr Asp Ser Asn His Glu Glu Arg Gln Asn His Ile
385 390 395 400
Tyr Gln Gln Asn His Met Val Leu Ser Arg Ala Arg Asn Gly Met Pro
405 410 415
Leu Leu Lys Glu Val Pro Arg Ser Tyr Glu Leu Leu Lys Pro Pro Pro
420 425 430
Ile Cys Pro Arg Asp Ser Val Lys Val Ile Asn Lys Glu Gly Glu Val
435 440 445
Met Asp Val Tyr Arg Cys Asp His Cys Arg Val Leu Phe Leu Asp Tyr
450 455 460
Val Met Phe Thr Ile His Met Gly Cys His Gly Phe Arg Asp Pro Phe
465 470 475 480
Glu Cys Asn Met Cys Gly Tyr Arg Ser His Asp Arg Tyr Glu Phe Ser
485 490 495
Ser His Ile Ala Arg Gly Glu His Arg Ala Leu Leu Lys
500 505
<210> 20
<211> 519
<212> БЕЛОК
<213> Homo sapiens
<400> 20
Met Asp Ala Asp Glu Gly Gln Asp Met Ser Gln Val Ser Gly Lys Glu
1. 5 10 15
Ser Pro Pro Val Ser Asp Thr Pro Asp Glu Gly Asp Glu Pro Met Pro
20 25 30
Ile Pro Glu Asp Leu Ser Thr Thr Ser Gly Gly Gln Gln Ser Ser Lys
35 40 45
Ser Asp Arg Val Val Ala Ser Asn Val Lys Val Glu Thr Gln Ser Asp
50 55 60
Glu Glu Asn Gly Arg Ala Cys Glu Met Asn Gly Glu Glu Cys Ala Glu
65 70 75 80
Asp Leu Arg Met Leu Asp Ala Ser Gly Glu Lys Met Asn Gly Ser His
85 90 95
Arg Asp Gln Gly Ser Ser Ala Leu Ser Gly Val Gly Gly Ile Arg Leu
100 105 110
Pro Asn Gly Lys Leu Lys Cys Asp Ile Cys Gly Ile Ile Cys Ile Gly
115 120 125
Pro Asn Val Leu Met Val His Lys Arg Ser His Thr Gly Glu Arg Pro
130 135 140
Phe Gln Cys Asn Gln Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu
145 150 155 160
Leu Arg His Ile Lys Leu His Ser Gly Glu Lys Pro Phe Lys Cys His
165 170 175
Leu Cys Asn Tyr Ala Cys Arg Arg Arg Asp Ala Leu Thr Gly His Leu
180 185 190
Arg Thr His Ser Val Gly Lys Pro His Lys Cys Gly Tyr Cys Gly Arg
195 200 205
Ser Tyr Lys Gln Arg Ser Ser Leu Glu Glu His Lys Glu Arg Cys His
210 215 220
Asn Tyr Leu Glu Ser Met Gly Leu Pro Gly Thr Leu Tyr Pro Val Ile
225 230 235 240
Lys Glu Glu Thr Asn His Ser Glu Met Ala Glu Asp Leu Cys Lys Ile
245 250 255
Gly Ser Glu Arg Ser Leu Val Leu Asp Arg Leu Ala Ser Asn Val Ala
260 265 270
Lys Arg Lys Ser Ser Met Pro Gln Lys Phe Leu Gly Asp Lys Gly Leu
275 280 285
Ser Asp Thr Pro Tyr Asp Ser Ser Ala Ser Tyr Glu Lys Glu Asn Glu
290 295 300
Met Met Lys Ser His Val Met Asp Gln Ala Ile Asn Asn Ala Ile Asn
305 310 315 320
Tyr Leu Gly Ala Glu Ser Leu Arg Pro Leu Val Gln Thr Pro Pro Gly
325 330 335
Gly Ser Glu Val Val Pro Val Ile Ser Pro Met Tyr Gln Leu His Lys
340 345 350
Pro Leu Ala Glu Gly Thr Pro Arg Ser Asn His Ser Ala Gln Asp Ser
355 360 365
Ala Val Glu Asn Leu Leu Leu Leu Ser Lys Ala Lys Leu Val Pro Ser
370 375 380
Glu Arg Glu Ala Ser Pro Ser Asn Ser Cys Gln Asp Ser Thr Asp Thr
385 390 395 400
Glu Ser Asn Asn Glu Glu Gln Arg Ser Gly Leu Ile Tyr Leu Thr Asn
405 410 415
His Ile Ala Pro His Ala Arg Asn Gly Leu Ser Leu Lys Glu Glu His
420 425 430
Arg Ala Tyr Asp Leu Leu Arg Ala Ala Ser Glu Asn Ser Gln Asp Ala
435 440 445
Leu Arg Val Val Ser Thr Ser Gly Glu Gln Met Lys Val Tyr Lys Cys
450 455 460
Glu His Cys Arg Val Leu Phe Leu Asp His Val Met Tyr Thr Ile His
465 470 475 480
Met Gly Cys His Gly Phe Arg Asp Pro Phe Glu Cys Asn Met Cys Gly
485 490 495
Tyr His Ser Gln Asp Arg Tyr Glu Phe Ser Ser His Ile Thr Arg Gly
500 505 510
Glu His Arg Phe His Met Ser
515
<210> 21
<211> 526
<212> БЕЛОК
<213> Homo sapiens
<400> 21
Met Glu Thr Glu Ala Ile Asp Gly Tyr Ile Thr Cys Asp Asn Glu Leu
1. 5 10 15
Ser Pro Glu Arg Glu His Ser Asn Met Ala Ile Asp Leu Thr Ser Ser
20 25 30
Thr Pro Asn Gly Gln His Ala Ser Pro Ser His Met Thr Ser Thr Asn
35 40 45
Ser Val Lys Leu Glu Met Gln Ser Asp Glu Glu Cys Asp Arg Lys Pro
50 55 60
Leu Ser Arg Glu Asp Glu Ile Arg Gly His Asp Glu Gly Ser Ser Leu
65 70 75 80
Glu Glu Pro Leu Ile Glu Ser Ser Glu Val Ala Asp Asn Arg Lys Val
85 90 95
Gln Glu Leu Gln Gly Glu Gly Gly Ile Arg Leu Pro Asn Gly Lys Leu
100 105 110
Lys Cys Asp Val Cys Gly Met Val Cys Ile Gly Pro Asn Val Leu Met
115 120 125
Val His Lys Arg Ser His Thr Gly Glu Arg Pro Phe His Cys Asn Gln
130 135 140
Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys
145 150 155 160
Leu His Ser Gly Glu Lys Pro Phe Lys Cys Pro Phe Cys Ser Tyr Ala
165 170 175
Cys Arg Arg Arg Asp Ala Leu Thr Gly His Leu Arg Thr His Ser Val
180 185 190
Gly Lys Pro His Lys Cys Asn Tyr Cys Gly Arg Ser Tyr Lys Gln Arg
195 200 205
Ser Ser Leu Glu Glu His Lys Glu Arg Cys His Asn Tyr Leu Gln Asn
210 215 220
Val Ser Met Glu Ala Ala Gly Gln Val Met Ser His His Val Pro Pro
225 230 235 240
Met Glu Asp Cys Lys Glu Gln Glu Pro Ile Met Asp Asn Asn Ile Ser
245 250 255
Leu Val Pro Phe Glu Arg Pro Ala Val Ile Glu Lys Leu Thr Gly Asn
260 265 270
Met Gly Lys Arg Lys Ser Ser Thr Pro Gln Lys Phe Val Gly Glu Lys
275 280 285
Leu Met Arg Phe Ser Tyr Pro Asp Ile His Phe Asp Met Asn Leu Thr
290 295 300
Tyr Glu Lys Glu Ala Glu Leu Met Gln Ser His Met Met Asp Gln Ala
305 310 315 320
Ile Asn Asn Ala Ile Thr Tyr Leu Gly Ala Glu Ala Leu His Pro Leu
325 330 335
Met Gln His Pro Pro Ser Thr Ile Ala Glu Val Ala Pro Val Ile Ser
340 345 350
Ser Ala Tyr Ser Gln Val Tyr His Pro Asn Arg Ile Glu Arg Pro Ile
355 360 365
Ser Arg Glu Thr Ala Asp Ser His Glu Asn Asn Met Asp Gly Pro Ile
370 375 380
Ser Leu Ile Arg Pro Lys Ser Arg Pro Gln Glu Arg Glu Ala Ser Pro
385 390 395 400
Ser Asn Ser Cys Leu Asp Ser Thr Asp Ser Glu Ser Ser His Asp Asp
405 410 415
His Gln Ser Tyr Gln Gly His Pro Ala Leu Asn Pro Lys Arg Lys Gln
420 425 430
Ser Pro Ala Tyr Met Lys Glu Asp Val Lys Ala Leu Asp Thr Thr Lys
435 440 445
Ala Pro Lys Gly Ser Leu Lys Asp Ile Tyr Lys Val Phe Asn Gly Glu
450 455 460
Gly Glu Gln Ile Arg Ala Phe Lys Cys Glu His Cys Arg Val Leu Phe
465 470 475 480
Leu Asp His Val Met Tyr Thr Ile His Met Gly Cys His Gly Tyr Arg
485 490 495
Asp Pro Leu Glu Cys Asn Ile Cys Gly Tyr Arg Ser Gln Asp Arg Tyr
500 505 510
Glu Phe Ser Ser His Ile Val Arg Gly Glu His Thr Phe His
515 520 525
<210> 22
<211> 585
<212> БЕЛОК
<213> Homo sapiens
<400> 22
Met His Thr Pro Pro Ala Leu Pro Arg Arg Phe Gln Gly Gly Gly Arg
1. 5 10 15
Val Arg Thr Pro Gly Ser His Arg Gln Gly Lys Asp Asn Leu Glu Arg
20 25 30
Asp Pro Ser Gly Gly Cys Val Pro Asp Phe Leu Pro Gln Ala Gln Asp
35 40 45
Ser Asn His Phe Ile Met Glu Ser Leu Phe Cys Glu Ser Ser Gly Asp
50 55 60
Ser Ser Leu Glu Lys Glu Phe Leu Gly Ala Pro Val Gly Pro Ser Val
65 70 75 80
Ser Thr Pro Asn Ser Gln His Ser Ser Pro Ser Arg Ser Leu Ser Ala
85 90 95
Asn Ser Ile Lys Val Glu Met Tyr Ser Asp Glu Glu Ser Ser Arg Leu
100 105 110
Leu Gly Pro Asp Glu Arg Leu Leu Glu Lys Asp Asp Ser Val Ile Val
115 120 125
Glu Asp Ser Leu Ser Glu Pro Leu Gly Tyr Cys Asp Gly Ser Gly Pro
130 135 140
Glu Pro His Ser Pro Gly Gly Ile Arg Leu Pro Asn Gly Lys Leu Lys
145 150 155 160
Cys Asp Val Cys Gly Met Val Cys Ile Gly Pro Asn Val Leu Met Val
165 170 175
His Lys Arg Ser His Thr Gly Glu Arg Pro Phe His Cys Asn Gln Cys
180 185 190
Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys Leu
195 200 205
His Ser Gly Glu Lys Pro Phe Lys Cys Pro Phe Cys Asn Tyr Ala Cys
210 215 220
Arg Arg Arg Asp Ala Leu Thr Gly His Leu Arg Thr His Ser Val Ser
225 230 235 240
Ser Pro Thr Val Gly Lys Pro Tyr Lys Cys Asn Tyr Cys Gly Arg Ser
245 250 255
Tyr Lys Gln Gln Ser Thr Leu Glu Glu His Lys Glu Arg Cys His Asn
260 265 270
Tyr Leu Gln Ser Leu Ser Thr Glu Ala Gln Ala Leu Ala Gly Gln Pro
275 280 285
Gly Asp Glu Ile Arg Asp Leu Glu Met Val Pro Asp Ser Met Leu His
290 295 300
Ser Ser Ser Glu Arg Pro Thr Phe Ile Asp Arg Leu Ala Asn Ser Leu
305 310 315 320
Thr Lys Arg Lys Arg Ser Thr Pro Gln Lys Phe Val Gly Glu Lys Gln
325 330 335
Met Arg Phe Ser Leu Ser Asp Leu Pro Tyr Asp Val Asn Ser Gly Gly
340 345 350
Tyr Glu Lys Asp Val Glu Leu Val Ala His His Ser Leu Glu Pro Gly
355 360 365
Phe Gly Ser Ser Leu Ala Phe Val Gly Ala Glu His Leu Arg Pro Leu
370 375 380
Arg Leu Pro Pro Thr Asn Cys Ile Ser Glu Leu Thr Pro Val Ile Ser
385 390 395 400
Ser Val Tyr Thr Gln Met Gln Pro Leu Pro Gly Arg Leu Glu Leu Pro
405 410 415
Gly Ser Arg Glu Ala Gly Glu Gly Pro Glu Asp Leu Ala Asp Gly Gly
420 425 430
Pro Leu Leu Tyr Arg Pro Arg Gly Pro Leu Thr Asp Pro Gly Ala Ser
435 440 445
Pro Ser Asn Gly Cys Gln Asp Ser Thr Asp Thr Glu Ser Asn His Glu
450 455 460
Asp Arg Val Ala Gly Val Val Ser Leu Pro Gln Gly Pro Pro Pro Gln
465 470 475 480
Pro Pro Pro Thr Ile Val Val Gly Arg His Ser Pro Ala Tyr Ala Lys
485 490 495
Glu Asp Pro Lys Pro Gln Glu Gly Leu Leu Arg Gly Thr Pro Gly Pro
500 505 510
Ser Lys Glu Val Leu Arg Val Val Gly Glu Ser Gly Glu Pro Val Lys
515 520 525
Ala Phe Lys Cys Glu His Cys Arg Ile Leu Phe Leu Asp His Val Met
530 535 540
Phe Thr Ile His Met Gly Cys His Gly Phe Arg Asp Pro Phe Glu Cys
545 550 555 560
Asn Ile Cys Gly Tyr His Ser Gln Asp Arg Tyr Glu Phe Ser Ser His
565 570 575
Ile Val Arg Gly Glu His Lys Val Gly
580 585
<210> 23
<211> 419
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF5"
<400> 23
Met Gly Glu Lys Lys Pro Glu Pro Leu Asp Phe Val Lys Asp Phe Gln
1. 5 10 15
Glu Tyr Leu Thr Gln Gln Thr His His Val Asn Met Ile Ser Gly Ser
20 25 30
Val Ser Gly Asp Lys Glu Ala Glu Ala Leu Gln Gly Ala Gly Thr Asp
35 40 45
Gly Asp Gln Asn Gly Leu Asp His Pro Ser Val Glu Val Ser Leu Asp
50 55 60
Glu Asn Ser Gly Met Leu Val Asp Gly Phe Glu Arg Thr Phe Asp Gly
65 70 75 80
Lys Leu Lys Cys Arg Tyr Cys Asn Tyr Ala Ser Lys Gly Thr Ala Arg
85 90 95
Leu Ile Glu His Ile Arg Ile His Thr Gly Glu Lys Pro His Arg Cys
100 105 110
His Leu Cys Pro Phe Ala Ser Ala Tyr Glu Arg His Leu Glu Ala His
115 120 125
Met Arg Ser His Thr Gly Glu Lys Pro Tyr Lys Cys Glu Leu Cys Ser
130 135 140
Phe Arg Cys Ser Asp Arg Ser Asn Leu Ser His His Arg Arg Arg Lys
145 150 155 160
His Lys Met Val Pro Ile Lys Gly Thr Arg Ser Ser Leu Ser Ser Lys
165 170 175
Lys Met Trp Gly Val Leu Gln Lys Lys Thr Ser Asn Leu Gly Tyr Ser
180 185 190
Arg Arg Ala Leu Ile Asn Leu Ser Pro Pro Ser Met Val Val Gln Lys
195 200 205
Pro Asp Tyr Leu Asn Asp Phe Thr His Glu Ile Pro Asn Ile Gln Thr
210 215 220
Asp Ser Tyr Glu Ser Met Ala Lys Thr Thr Pro Thr Gly Gly Leu Pro
225 230 235 240
Arg Asp Pro Gln Glu Leu Met Val Asp Asn Pro Leu Asn Gln Leu Ser
245 250 255
Thr Leu Ala Gly Gln Leu Ser Ser Leu Pro Pro Glu Asn Gln Asn Pro
260 265 270
Ala Ser Pro Asp Val Val Pro Cys Pro Asp Glu Lys Pro Phe Met Ile
275 280 285
Gln Gln Pro Ser Thr Gln Ala Val Val Ser Ala Val Ser Ala Ser Ile
290 295 300
Pro Gln Ser Ser Ser Pro Thr Ser Pro Glu Pro Arg Pro Ser His Ser
305 310 315 320
Gln Arg Asn Tyr Ser Pro Val Ala Gly Pro Ser Ser Glu Pro Ser Ala
325 330 335
His Thr Ser Thr Pro Ser Ile Gly Asn Ser Gln Pro Ser Thr Pro Ala
340 345 350
Pro Ala Leu Pro Val Gln Asp Pro Gln Leu Leu His His Cys Gln His
355 360 365
Cys Asp Met Tyr Phe Ala Asp Asn Ile Leu Tyr Thr Ile His Met Gly
370 375 380
Cys His Gly Tyr Glu Asn Pro Phe Gln Cys Asn Ile Cys Gly Cys Lys
385 390 395 400
Cys Lys Asn Lys Tyr Asp Phe Ala Cys His Phe Ala Arg Gly Gln His
405 410 415
Asn Gln His
<210> 24
<211> 30
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 24
His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln Cys Gly Ala Ser Phe
1. 5 10 15
Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys Leu His Thr
20 25 30
<210> 25
<400> 25
000
<210> 26
<400> 26
000
<210> 27
<211> 46
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 27
Met His Lys Arg Ser His Thr Gly Glu Arg Pro Phe His Cys Asn Gln
1. 5 10 15
Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys
20 25 30
Leu His Thr Gly Glu Lys Pro Phe Lys Cys His Leu Cys Asn
35 40 45
<210> 28
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 28
Gly Gly Gly Gly Ser Gly Gly Gly Gly Thr Gly Gly Gly Gly Ser Gly
1. 5 10 15
<210> 29
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 29
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
130 135 140
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
145 150 155 160
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser
195 200 205
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
210 215 220
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 30
<211> 562
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 30
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
130 135 140
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
145 150 155 160
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser
195 200 205
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
210 215 220
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Thr
485 490 495
Gly Gly Gly Gly Ser Gly Met His Lys Arg Ser His Thr Gly Glu Arg
500 505 510
Pro Phe Gln Cys Asn Gln Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn
515 520 525
Leu Leu Arg His Ile Lys Leu His Thr Gly Glu Lys Pro Phe Lys Cys
530 535 540
His Leu Cys Asn Thr Ala Ser Ala Glu Ala Arg His Ile Lys Ala Glu
545 550 555 560
Met Gly
<210> 31
<211> 562
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 31
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
130 135 140
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
145 150 155 160
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser
195 200 205
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
210 215 220
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Thr
485 490 495
Gly Gly Gly Gly Ser Gly Met His Arg Arg Ser His Thr Gly Glu Arg
500 505 510
Pro Phe Gln Cys Asn Gln Cys Gly Ala Ser Phe Thr Gln Arg Gly Asn
515 520 525
Leu Leu Arg His Ile Arg Leu His Thr Gly Glu Arg Pro Phe Arg Cys
530 535 540
His Leu Cys Asn Thr Ala Ser Ala Glu Ala Arg His Ile Arg Ala Glu
545 550 555 560
Met Gly
<210> 32
<211> 829
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 32
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly
275 280 285
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
290 295 300
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
305 310 315 320
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
325 330 335
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
340 345 350
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
355 360 365
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
370 375 380
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
385 390 395 400
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
405 410 415
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
420 425 430
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
435 440 445
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
450 455 460
Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
465 470 475 480
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
485 490 495
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
500 505 510
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
515 520 525
Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
530 535 540
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
545 550 555 560
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
565 570 575
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
580 585 590
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
595 600 605
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
610 615 620
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
625 630 635 640
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
645 650 655
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
660 665 670
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
675 680 685
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
690 695 700
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
705 710 715 720
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
725 730 735
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
740 745 750
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Thr Gly Gly Gly Gly Ser
755 760 765
Gly Met His Lys Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn
770 775 780
Gln Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile
785 790 795 800
Lys Leu His Thr Gly Glu Lys Pro Phe Lys Cys His Leu Cys Asn Thr
805 810 815
Ala Ser Ala Glu Ala Arg His Ile Lys Ala Glu Met Gly
820 825
<210> 33
<211> 829
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 33
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly
275 280 285
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
290 295 300
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
305 310 315 320
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
325 330 335
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
340 345 350
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
355 360 365
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
370 375 380
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
385 390 395 400
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
405 410 415
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
420 425 430
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
435 440 445
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
450 455 460
Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
465 470 475 480
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
485 490 495
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
500 505 510
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
515 520 525
Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
530 535 540
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
545 550 555 560
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
565 570 575
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
580 585 590
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
595 600 605
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
610 615 620
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
625 630 635 640
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
645 650 655
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
660 665 670
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
675 680 685
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
690 695 700
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
705 710 715 720
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
725 730 735
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
740 745 750
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Thr Gly Gly Gly Gly Ser
755 760 765
Gly Met His Arg Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn
770 775 780
Gln Cys Gly Ala Ser Phe Thr Gln Arg Gly Asn Leu Leu Arg His Ile
785 790 795 800
Arg Leu His Thr Gly Glu Arg Pro Phe Arg Cys His Leu Cys Asn Thr
805 810 815
Ala Ser Ala Glu Ala Arg His Ile Arg Ala Glu Met Gly
820 825
<210> 34
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 34
Ser Ala Arg Asn Arg Gln Lys Arg
1. 5
<210> 35
<211> 383
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 35
Met Ala Glu Pro Arg Gln Glu Phe Glu Val Met Glu Asp His Ala Gly
1. 5 10 15
Thr Tyr Gly Leu Gly Asp Arg Lys Asp Gln Gly Gly Tyr Thr Met His
20 25 30
Gln Asp Gln Glu Gly Asp Thr Asp Ala Gly Leu Lys Ala Glu Glu Ala
35 40 45
Gly Ile Gly Asp Thr Pro Ser Leu Glu Asp Glu Ala Ala Gly His Val
50 55 60
Thr Gln Ala Arg Met Val Ser Lys Ser Lys Asp Gly Thr Gly Ser Asp
65 70 75 80
Asp Lys Lys Ala Lys Gly Ala Asp Gly Lys Thr Lys Ile Ala Thr Pro
85 90 95
Arg Gly Ala Ala Pro Pro Gly Gln Lys Gly Gln Ala Asn Ala Thr Arg
100 105 110
Ile Pro Ala Lys Thr Pro Pro Ala Pro Lys Thr Pro Pro Ser Ser Gly
115 120 125
Glu Pro Pro Lys Ser Gly Asp Arg Ser Gly Tyr Ser Ser Pro Gly Ser
130 135 140
Pro Gly Thr Pro Gly Ser Arg Ser Arg Thr Pro Ser Leu Pro Thr Pro
145 150 155 160
Pro Thr Arg Glu Pro Lys Lys Val Ala Val Val Arg Thr Pro Pro Lys
165 170 175
Ser Pro Ser Ser Ala Lys Ser Arg Leu Gln Thr Ala Pro Val Pro Met
180 185 190
Pro Asp Leu Lys Asn Val Lys Ser Lys Ile Gly Ser Thr Glu Asn Leu
195 200 205
Lys His Gln Pro Gly Gly Gly Lys Val Gln Ile Ile Asn Lys Lys Leu
210 215 220
Asp Leu Ser Asn Val Gln Ser Lys Cys Gly Ser Lys Asp Asn Ile Lys
225 230 235 240
His Val Pro Gly Gly Gly Ser Val Gln Ile Val Tyr Lys Pro Val Asp
245 250 255
Leu Ser Lys Val Thr Ser Lys Cys Gly Ser Leu Gly Asn Ile His His
260 265 270
Lys Pro Gly Gly Gly Gln Val Glu Val Lys Ser Glu Lys Leu Asp Phe
275 280 285
Lys Asp Arg Val Gln Ser Lys Ile Gly Ser Leu Asp Asn Ile Thr His
290 295 300
Val Pro Gly Gly Gly Asn Lys Lys Ile Glu Thr His Lys Leu Thr Phe
305 310 315 320
Arg Glu Asn Ala Lys Ala Lys Thr Asp His Gly Ala Glu Ile Val Tyr
325 330 335
Lys Ser Pro Val Val Ser Gly Asp Thr Ser Pro Arg His Leu Ser Asn
340 345 350
Val Ser Ser Thr Gly Ser Ile Asp Met Val Asp Ser Pro Gln Leu Ala
355 360 365
Thr Leu Ala Asp Glu Val Ser Ala Ser Leu Ala Lys Gln Gly Leu
370 375 380
<210> 36
<211> 383
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 36
Met Ala Glu Pro Arg Gln Glu Phe Glu Val Met Glu Asp His Ala Gly
1. 5 10 15
Thr Tyr Gly Leu Gly Asp Arg Lys Asp Gln Gly Gly Tyr Thr Met His
20 25 30
Gln Asp Gln Glu Gly Asp Thr Asp Ala Gly Leu Lys Ala Glu Glu Ala
35 40 45
Gly Ile Gly Asp Thr Pro Ser Leu Glu Asp Glu Ala Ala Gly His Val
50 55 60
Thr Gln Ala Arg Met Val Ser Lys Ser Lys Asp Gly Thr Gly Ser Asp
65 70 75 80
Asp Lys Lys Ala Lys Gly Ala Asp Gly Lys Thr Lys Ile Ala Thr Pro
85 90 95
Arg Gly Ala Ala Pro Pro Gly Gln Lys Gly Gln Ala Asn Ala Thr Arg
100 105 110
Ile Pro Ala Lys Thr Pro Pro Ala Pro Lys Thr Pro Pro Ser Ser Gly
115 120 125
Glu Pro Pro Lys Ser Gly Asp Arg Ser Gly Tyr Ser Ser Pro Gly Ser
130 135 140
Pro Gly Thr Pro Gly Ser Arg Ser Arg Thr Pro Ser Leu Pro Thr Pro
145 150 155 160
Pro Thr Arg Glu Pro Lys Lys Val Ala Val Val Arg Thr Pro Pro Lys
165 170 175
Ser Pro Ser Ser Ala Lys Ser Arg Leu Gln Thr Ala Pro Val Pro Met
180 185 190
Pro Asp Leu Lys Asn Val Lys Ser Lys Ile Gly Ser Thr Glu Asn Leu
195 200 205
Lys His Gln Pro Gly Gly Gly Lys Val Gln Ile Ile Asn Lys Lys Leu
210 215 220
Asp Leu Ser Asn Val Gln Ser Lys Cys Gly Ser Lys Asp Asn Ile Lys
225 230 235 240
His Val Ser Gly Gly Gly Ser Val Gln Ile Val Tyr Lys Pro Val Asp
245 250 255
Leu Ser Lys Val Thr Ser Lys Cys Gly Ser Leu Gly Asn Ile His His
260 265 270
Lys Pro Gly Gly Gly Gln Val Glu Val Lys Ser Glu Lys Leu Asp Phe
275 280 285
Lys Asp Arg Val Gln Ser Lys Ile Gly Ser Leu Asp Asn Ile Thr His
290 295 300
Val Pro Gly Gly Gly Asn Lys Lys Ile Glu Thr His Lys Leu Thr Phe
305 310 315 320
Arg Glu Asn Ala Lys Ala Lys Thr Asp His Gly Ala Glu Ile Val Tyr
325 330 335
Lys Ser Pro Val Val Ser Gly Asp Thr Ser Pro Arg His Leu Ser Asn
340 345 350
Val Ser Ser Thr Gly Ser Ile Asp Met Val Asp Ser Pro Gln Leu Ala
355 360 365
Thr Leu Ala Asp Glu Val Ser Ala Ser Leu Ala Lys Gln Gly Leu
370 375 380
<210> 37
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 37
Ser Gly Ser Glu Thr Pro Gly Thr Ser Glu Ser Ala Thr Pro Glu Ser
1. 5 10 15
<210> 38
<211> 33
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 38
Gly Gly Gly Gly Ser Gly Gly Gly Gly Thr Gly Gly Gly Gly Gly Ser
1. 5 10 15
Gly Gly Gly Gly Thr Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Thr
20 25 30
Gly
<210> 39
<211> 33
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 39
Gly Gly Gly Gly Ser Gly Gly Gly Gly Thr Gly Gly Gly Gly Ser Gly
1. 5 10 15
Gly Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu Ala Ser Thr Gly Ser
20 25 30
Gly
<210> 40
<211> 4
<212> БЕЛОК
<213> Homo sapiens
<400> 40
His Lys Arg Ser
1
<210> 41
<211> 45
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 41
His Arg Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln Cys
1. 5 10 15
Gly Ala Ser Phe Thr Gln Arg Gly Asn Leu Leu Arg His Ile Arg Leu
20 25 30
His Thr Gly Glu Arg Pro Phe Arg Cys His Leu Cys Asn
35 40 45
<210> 42
<211> 35
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 42
His Arg Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln Cys
1. 5 10 15
Gly Ala Ser Phe Thr Gln Arg Gly Asn Leu Leu Arg His Ile Arg Leu
20 25 30
His Thr Gly
35
<210> 43
<211> 14
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 43
Thr Ala Ser Ala Glu Ala Arg His Ile Arg Ala Glu Met Gly
1. 5 10
<210> 44
<211> 245
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 44
Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln Met Val Ser Ala Leu Leu
1. 5 10 15
Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu Tyr Asp Pro Thr Arg Pro
20 25 30
Phe Ser Glu Ala Ser Met Met Gly Leu Leu Thr Asn Leu Ala Asp Arg
35 40 45
Glu Leu Val His Met Ile Asn Trp Ala Lys Arg Val Pro Gly Phe Val
50 55 60
Asp Leu Thr Leu His Asp Gln Val His Leu Leu Glu Cys Ala Trp Leu
65 70 75 80
Glu Ile Leu Met Ile Gly Leu Val Trp Arg Ser Met Glu His Pro Gly
85 90 95
Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu Asp Arg Asn Gln Gly Lys
100 105 110
Cys Val Glu Gly Met Val Glu Ile Phe Asp Met Leu Leu Ala Thr Ser
115 120 125
Ser Arg Phe Arg Met Met Asn Leu Gln Gly Glu Glu Phe Val Cys Leu
130 135 140
Lys Ser Ile Ile Leu Leu Asn Ser Gly Val Tyr Thr Phe Leu Ser Ser
145 150 155 160
Thr Leu Lys Ser Leu Glu Glu Lys Asp His Ile His Arg Val Leu Asp
165 170 175
Lys Ile Thr Asp Thr Leu Ile His Leu Met Ala Lys Ala Gly Leu Thr
180 185 190
Leu Gln Gln Gln His Gln Arg Leu Ala Gln Leu Leu Leu Ile Leu Ser
195 200 205
His Ile Arg His Met Ser Asn Lys Gly Met Glu His Leu Tyr Ser Met
210 215 220
Lys Cys Lys Asn Val Val Pro Leu Tyr Asp Leu Leu Leu Glu Met Leu
225 230 235 240
Asp Ala His Arg Leu
245
<210> 45
<211> 735
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 45
tcgttggcac tttccctgac tgccgaccag atggtgtccg cccttctgga cgccgagcct
60
ccaattctgt actcggagta cgatccgact cgcccgttct ccgaagccag catgatgggc
120
ctgttgacta acctggcgga ccgcgagttg gtgcacatga ttaactgggc taagcgggtg
180
ccgggcttcg tggacctgac tctgcacgac caagtgcacc tcctggaatg cgcctggctg
240
gaaatcctca tgatcggcct cgtgtggaga tccatggagc atcccggaaa gctcctgttt
300
gcacccaacc tcctgcttga tcgcaaccag ggaaaatgcg tggaagggat ggtcgagatt
360
ttcgacatgc tgctcgccac ctcttcccgg ttccggatga tgaatctgca gggagaagag
420
ttcgtgtgtc tgaagtcaat catcctgctg aactccgggg tctatacctt cctgagctcg
480
accctcaagt cactggagga aaaagaccac atccatcgcg tgctcgataa gatcaccgac
540
acccttatcc atctcatggc gaaggctgga ctgaccctgc aacagcagca ccagaggctg
600
gcccagttgc tgctgattct gagccacatc cggcacatgt cgaacaaggg gatggaacac
660
ctgtacagca tgaagtgcaa gaacgtcgtg cctctgtacg atctgctcct ggaaatgctg
720
gacgcgcaca gactc
735
<210> 46
<211> 245
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 46
Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln Met Val Ser Ala Leu Leu
1. 5 10 15
Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu Tyr Asp Pro Thr Arg Pro
20 25 30
Phe Ser Glu Ala Ser Met Met Gly Leu Leu Thr Asn Leu Ala Asp Arg
35 40 45
Glu Leu Val His Met Ile Asn Trp Ala Lys Arg Val Pro Gly Phe Val
50 55 60
Asp Leu Ala Leu His Asp Gln Val His Leu Leu Glu Cys Ala Trp Met
65 70 75 80
Glu Ile Leu Met Ile Gly Leu Val Trp Arg Ser Met Glu His Pro Gly
85 90 95
Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu Asp Arg Asn Gln Gly Lys
100 105 110
Cys Val Glu Gly Gly Val Glu Ile Phe Asp Met Leu Leu Ala Thr Ser
115 120 125
Ser Arg Phe Arg Met Met Asn Leu Gln Gly Glu Glu Phe Val Cys Leu
130 135 140
Lys Ser Ile Ile Leu Leu Asn Ser Gly Val Tyr Thr Phe Leu Ser Ser
145 150 155 160
Thr Leu Lys Ser Leu Glu Glu Lys Asp His Ile His Arg Val Leu Asp
165 170 175
Lys Ile Thr Asp Thr Leu Ile His Leu Met Ala Lys Ala Gly Leu Thr
180 185 190
Leu Gln Gln Gln His Gln Arg Leu Ala Gln Leu Leu Leu Ile Leu Ser
195 200 205
His Ile Arg His Met Ser Ser Lys Arg Met Glu His Leu Tyr Ser Met
210 215 220
Lys Cys Lys Asn Val Val Pro Leu Ser Asp Leu Leu Leu Glu Met Leu
225 230 235 240
Asp Ala His Arg Leu
245
<210> 47
<211> 735
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 47
tcgttggcac tttccctgac tgccgaccag atggtgtccg cccttctgga cgccgagcct
60
ccaattctgt actcggagta cgatccgact cgcccgttct ccgaagccag catgatgggc
120
ctgttgacta acctggcgga ccgcgagttg gtgcacatga ttaactgggc taagcgggtg
180
ccgggcttcg tggacctggc cctgcacgac caagtgcacc tcctggaatg cgcctggatg
240
gaaatcctca tgatcggcct cgtgtggaga tccatggagc atcccggaaa gctcctgttt
300
gcacccaacc tcctgcttga tcgcaaccag ggaaaatgcg tggaaggggg tgtcgagatt
360
ttcgacatgc tgctcgccac ctcttcccgg ttccggatga tgaatctgca gggagaagag
420
ttcgtgtgtc tgaagtcaat catcctgctg aactccgggg tctatacctt cctgagctcg
480
accctcaagt cactggagga aaaagaccac atccatcgcg tgctcgataa gatcaccgac
540
acccttatcc atctcatggc gaaggctgga ctgaccctgc aacagcagca ccagaggctg
600
gcccagttgc tgctgattct gagccacatc cggcacatgt cgtccaagag gatggaacac
660
ctgtacagca tgaagtgcaa gaacgtcgtg cctctgtccg atctgctcct ggaaatgctg
720
gacgcgcaca gactc
735
<210> 48
<211> 245
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 48
Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln Met Val Ser Ala Leu Leu
1. 5 10 15
Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu Tyr Asp Pro Thr Arg Pro
20 25 30
Phe Ser Glu Ala Ser Met Met Gly Leu Leu Thr Asn Leu Ala Asp Arg
35 40 45
Glu Leu Val His Met Ile Asn Trp Ala Lys Arg Val Pro Gly Phe Val
50 55 60
Asp Leu Thr Leu His Asp Gln Val His Leu Leu Glu Cys Ala Trp Met
65 70 75 80
Glu Ile Leu Met Ile Gly Leu Val Trp Arg Ser Met Glu His Pro Gly
85 90 95
Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu Asp Arg Asn Gln Gly Lys
100 105 110
Cys Val Glu Gly Gly Val Glu Ile Phe Asp Met Leu Leu Ala Thr Ser
115 120 125
Ser Arg Phe Arg Met Met Asn Leu Gln Gly Glu Glu Phe Val Cys Leu
130 135 140
Lys Ser Ile Ile Leu Leu Asn Ser Gly Val Tyr Thr Phe Leu Ser Ser
145 150 155 160
Thr Leu Lys Ser Leu Glu Glu Lys Asp His Ile His Arg Val Leu Asp
165 170 175
Lys Ile Thr Asp Thr Leu Ile His Leu Met Ala Lys Ala Gly Leu Thr
180 185 190
Leu Gln Gln Gln His Gln Arg Leu Ala Gln Leu Leu Leu Ile Leu Ser
195 200 205
His Ile Arg His Met Ser Asn Lys Arg Met Glu His Leu Tyr Ser Met
210 215 220
Lys Cys Lys Asn Val Val Pro Leu Ser Asp Leu Leu Leu Glu Met Leu
225 230 235 240
Asp Ala His Arg Leu
245
<210> 49
<211> 735
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 49
tcgttggcac tttccctgac tgccgaccag atggtgtccg cccttctgga cgccgagcct
60
ccaattctgt actcggagta cgatccgact cgcccgttct ccgaagccag catgatgggc
120
ctgttgacta acctggcgga ccgcgagttg gtgcacatga ttaactgggc taagcgggtg
180
ccgggcttcg tggacctgac cctgcacgac caagtgcacc tcctggaatg cgcctggatg
240
gaaatcctca tgatcggcct cgtgtggaga tccatggagc atcccggaaa gctcctgttt
300
gcacccaacc tcctgcttga tcgcaaccag ggaaaatgcg tggaaggggg tgtcgagatt
360
ttcgacatgc tgctcgccac ctcttcccgg ttccggatga tgaatctgca gggagaagag
420
ttcgtgtgtc tgaagtcaat catcctgctg aactccgggg tctatacctt cctgagctcg
480
accctcaagt cactggagga aaaagaccac atccatcgcg tgctcgataa gatcaccgac
540
acccttatcc atctcatggc gaaggctgga ctgaccctgc aacagcagca ccagaggctg
600
gcccagttgc tgctgattct gagccacatc cggcacatgt cgaacaagag gatggaacac
660
ctgtacagca tgaagtgcaa gaacgtcgtg cctctgtccg atctgctcct ggaaatgctg
720
gacgcgcaca gactc
735
<210> 50
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 50
Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg Thr Phe Pro
1. 5 10 15
Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr Gly Met Leu Glu Asp
20 25 30
Gly Lys Lys Val Asp Ser Ser Arg Asp Arg Asn Lys Pro Phe Lys Phe
35 40 45
Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu Gly Val Ala
50 55 60
Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser Pro Asp Tyr
65 70 75 80
Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro His Ala Thr
85 90 95
Leu Val Phe Asp Val Glu Leu Leu Lys Pro Glu
100 105
<210> 51
<211> 158
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 51
Ile Ser Leu Ile Ala Ala Leu Ala Val Asp Tyr Val Ile Gly Met Glu
1. 5 10 15
Asn Ala Met Pro Trp Asn Leu Pro Ala Asp Leu Ala Trp Phe Lys Arg
20 25 30
Asn Thr Leu Asn Lys Pro Val Ile Met Gly Arg His Thr Trp Glu Ser
35 40 45
Ile Gly Arg Pro Leu Pro Gly Arg Lys Asn Ile Ile Leu Ser Ser Gln
50 55 60
Pro Ser Thr Asp Asp Arg Val Thr Trp Val Lys Ser Val Asp Glu Ala
65 70 75 80
Ile Ala Ala Cys Gly Asp Val Pro Glu Ile Met Val Ile Gly Gly Gly
85 90 95
Arg Val Ile Glu Gln Phe Leu Pro Lys Ala Gln Lys Leu Tyr Leu Thr
100 105 110
His Ile Asp Ala Glu Val Glu Gly Asp Thr His Phe Pro Asp Tyr Glu
115 120 125
Pro Asp Asp Trp Glu Ser Val Phe Ser Glu Phe His Asp Ala Asp Ala
130 135 140
Gln Asn Ser His Ser Tyr Cys Phe Glu Ile Leu Glu Arg Arg
145 150 155
<210> 52
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Любая аминокислота
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Arg"
<220>
<221> Сайт
<222> (1)..(4)
<223> /примечание="вариантам остатков, указанным в
последовательности, не отдается предпочтение перед остатками в
аннотациях вариантов положений»
<400> 52
Arg Xaa Lys Arg
1
<210> 53
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> MOD_RES
<222> (2)..(4)
<223> Любая аминокислота
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Arg"
<220>
<221> Сайт
<222> (1)..(6)
<223> /примечание="вариантам остатков, указанным в
последовательности, не отдается предпочтение перед остатками в
аннотациях вариантов положений»
<400> 53
Arg Xaa Xaa Xaa Lys Arg
1. 5
<210> 54
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> MOD_RES
<222> (3)..(3)
<223> Любая аминокислота
<400> 54
Arg Arg Xaa
1
<210> 55
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> MOD_RES
<222> (5)..(5)
<223> Любая аминокислота
<400> 55
Ile Glu Pro Asp Xaa
1. 5
<210> 56
<211> 4
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: Последовательность фактора
XA"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /замена="Asp"
<220>
<221> Сайт
<222> (1)..(4)
<223> /примечание="вариантам остатков, указанным в
последовательности, не отдается предпочтение перед остатками в
аннотациях вариантов положений»
<400> 56
Ile Glu Gly Arg
1
<210> 57
<211> 5
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: Последовательность
энтерокиназы"
<400> 57
Asp Asp Asp Asp Lys
1. 5
<210> 58
<211> 6
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: Последовательность
гененазы"
<400> 58
Pro Gly Ala Ala His Tyr
1. 5
<210> 59
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> MOD_RES
<222> (3)..(3)
<223> Любая аминокислота
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Ala"
<220>
<221> Сайт
<222> (1)..(5)
<223> /примечание="вариантам остатков, указанным в
последовательности, не отдается предпочтение перед остатками в
аннотациях вариантов положений»
<400> 59
Leu Pro Xaa Thr Gly
1. 5
<210> 60
<211> 7
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: Последовательность
протеазы PreScission"
<400> 60
Leu Glu Val Phe Gln Gly Pro
1. 5
<210> 61
<211> 6
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: Последовательность
тромбина"
<400> 61
Leu Val Pro Arg Gly Ser
1. 5
<210> 62
<211> 7
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: Последовательность
протеазы TEV"
<400> 62
Glu Asn Leu Tyr Phe Gln Gly
1. 5
<210> 63
<211> 2
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: Последовательность
эластазы-1"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="Gly", или "Ser", или "Val"
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Любая аминокислота
<220>
<221> Сайт
<222> (1)..(2)
<223> /примечание="вариантам остатков, указанным в
последовательности, не отдается предпочтение перед остатками в
аннотациях вариантов положений»
<400> 63
Ala Xaa
1
<210> 64
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 64
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro
20
<210> 65
<211> 22
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 65
Met Leu Leu Leu Val Thr Ser Leu Leu Leu Cys Glu Leu Pro His Pro
1. 5 10 15
Ala Phe Leu Leu Ile Pro
20
<210> 66
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 66
Met Tyr Arg Met Gln Leu Leu Ser Cys Ile Ala Leu Ser Leu Ala Leu
1. 5 10 15
Val Thr Asn Ser
20
<210> 67
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 67
Met Ala Gln Val Lys Leu Gln Glu Ser Gly Thr Glu Leu Ala Lys Pro
1. 5 10 15
Gly Ala Ala Val Lys
20
<210> 68
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 68
Met Arg Phe Leu Ala Ala Thr Phe Leu Leu Leu Ala Leu Ser Thr Ala
1. 5 10 15
Ala Gln Ala
<210> 69
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 69
Met Gly Leu Leu Gln Leu Leu Ala Phe Ser Phe Leu Ala Leu Cys Arg
1. 5 10 15
Ala Arg Val Arg Ala
20
<210> 70
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 70
Met Leu Leu Ala Trp Val Gln Ala Phe Leu Val Ser Asn Met Leu Leu
1. 5 10 15
Ala Glu Ala Tyr Gly
20
<210> 71
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 71
Met Lys Phe Gln Gly Pro Leu Ala Cys Leu Leu Leu Ala Leu Cys Leu
1. 5 10 15
Gly Ser Gly Glu Ala
20
<210> 72
<211> 22
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 72
Met Asp Ala Met Lys Arg Gly Leu Cys Cys Val Leu Leu Leu Cys Gly
1. 5 10 15
Ala Val Phe Val Ser Pro
20
<210> 73
<211> 35
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 73
Met Gly Thr Val Ser Ser Arg Arg Ser Trp Trp Pro Leu Pro Leu Leu
1. 5 10 15
Leu Leu Leu Leu Leu Leu Leu Gly Pro Ala Gly Ala Arg Ala Gln Glu
20 25 30
Asp Glu Asp
35
<210> 74
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 74
Lys Asp Glu Leu
1
<210> 75
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> MOD_RES
<222> (3)..(4)
<223> Любая аминокислота
<400> 75
Lys Lys Xaa Xaa
1
<210> 76
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Любая аминокислота, кроме Pro, Ser или Thr
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Thr"
<220>
<221> Сайт
<222> (1)..(3)
<223> /примечание="вариантам остатков, указанным в
последовательности, не отдается предпочтение перед остатками в
аннотациях вариантов положений»
<400> 76
Asn Xaa Ser
1
<210> 77
<211> 46
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 77
Met His Lys Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln
1. 5 10 15
Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys
20 25 30
Leu His Thr Gly Glu Lys Pro Phe Lys Cys His Leu Cys Asn
35 40 45
<210> 78
<211> 36
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 78
Met His Lys Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln
1. 5 10 15
Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys
20 25 30
Leu His Thr Gly
35
<210> 79
<211> 32
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 79
Met His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln Cys Gly Ala Ser
1. 5 10 15
Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys Leu His Thr Gly
20 25 30
<210> 80
<211> 31
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 80
Met His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln Cys Gly Ala Ser
1. 5 10 15
Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys Leu His Thr
20 25 30
<210> 81
<211> 24
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 81
Met Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln Cys Gly Ala Ser Phe
1. 5 10 15
Thr Gln Lys Gly Asn Leu Leu Arg
20
<210> 82
<211> 27
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 82
Met Pro Phe Gln Cys Asn Gln Cys Gly Ala Ser Phe Thr Gln Lys Gly
1. 5 10 15
Asn Leu Leu Arg His Ile Lys Leu His Thr Gly
20 25
<210> 83
<211> 12
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 83
Met Pro Phe Gln Cys Asn Gln Cys Gly Ala Ser Phe
1. 5 10
<210> 84
<211> 59
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 84
His Lys Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln Cys
1. 5 10 15
Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys Leu
20 25 30
His Thr Gly Glu Lys Pro Phe Lys Cys His Leu Cys Asn Thr Ala Ser
35 40 45
Ala Glu Ala Arg His Ile Arg Ala Glu Met Gly
50 55
<210> 85
<211> 59
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 85
His Lys Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln Cys
1. 5 10 15
Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys Leu
20 25 30
His Thr Gly Glu Lys Pro Phe Lys Cys His Leu Cys Asn Met Ala Leu
35 40 45
Glu Lys Met Ala Leu Glu Lys Met Ala Leu Glu
50 55
<210> 86
<211> 49
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 86
His Lys Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln Cys
1. 5 10 15
Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys Leu
20 25 30
His Thr Gly Met Ala Leu Glu Lys Met Ala Leu Glu Lys Met Ala Leu
35 40 45
Glu
<210> 87
<211> 45
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 87
His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln Cys Gly Ala Ser Phe
1. 5 10 15
Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys Leu His Thr Gly Met
20 25 30
Ala Leu Glu Lys Met Ala Leu Glu Lys Met Ala Leu Glu
35 40 45
<210> 88
<211> 37
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 88
Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln Cys Gly Ala Ser Phe Thr
1. 5 10 15
Gln Lys Gly Asn Leu Leu Arg Met Ala Leu Glu Lys Met Ala Leu Glu
20 25 30
Lys Met Ala Leu Glu
35
<210> 89
<211> 25
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 89
Pro Phe Gln Cys Asn Gln Cys Gly Ala Ser Phe Met Ala Leu Glu Lys
1. 5 10 15
Met Ala Leu Glu Lys Met Ala Leu Glu
20 25
<210> 90
<211> 45
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 90
His Lys Arg Ser His Thr Gly Glu Arg Pro Phe His Cys Asn Gln Cys
1. 5 10 15
Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys Leu
20 25 30
His Thr Gly Glu Lys Pro Phe Lys Cys His Leu Cys Asn
35 40 45
<210> 91
<211> 14
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 91
Met Ala Leu Glu Lys Met Ala Leu Glu Lys Met Ala Leu Glu
1. 5 10
<210> 92
<211> 753
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 92
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly
275 280 285
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
290 295 300
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
305 310 315 320
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
325 330 335
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
340 345 350
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
355 360 365
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
370 375 380
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
385 390 395 400
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
405 410 415
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
420 425 430
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
435 440 445
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
450 455 460
Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
465 470 475 480
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
485 490 495
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
500 505 510
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
515 520 525
Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
530 535 540
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
545 550 555 560
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
565 570 575
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
580 585 590
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
595 600 605
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
610 615 620
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
625 630 635 640
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
645 650 655
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
660 665 670
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
675 680 685
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
690 695 700
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
705 710 715 720
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
725 730 735
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
740 745 750
Arg
<210> 93
<211> 843
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 93
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly
275 280 285
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
290 295 300
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
305 310 315 320
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
325 330 335
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
340 345 350
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
355 360 365
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
370 375 380
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
385 390 395 400
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
405 410 415
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
420 425 430
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
435 440 445
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
450 455 460
Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
465 470 475 480
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
485 490 495
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
500 505 510
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
515 520 525
Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
530 535 540
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
545 550 555 560
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
565 570 575
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
580 585 590
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
595 600 605
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
610 615 620
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
625 630 635 640
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
645 650 655
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
660 665 670
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
675 680 685
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
690 695 700
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
705 710 715 720
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
725 730 735
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
740 745 750
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Thr Gly Gly Gly Gly Ser
755 760 765
Gly Met His Lys Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn
770 775 780
Gln Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile
785 790 795 800
Lys Leu His Thr Gly Glu Lys Pro Phe Lys Cys His Leu Cys Asn Thr
805 810 815
Ala Ser Ala Glu Ala Arg His Ile Lys Ala Glu Met Gly Gly Lys Pro
820 825 830
Ile Pro Asn Pro Leu Leu Gly Leu Asp Ser Thr
835 840
<210> 94
<211> 576
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 94
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
130 135 140
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
145 150 155 160
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser
195 200 205
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
210 215 220
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Thr
485 490 495
Gly Gly Gly Gly Ser Gly Met His Lys Arg Ser His Thr Gly Glu Arg
500 505 510
Pro Phe Gln Cys Asn Gln Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn
515 520 525
Leu Leu Arg His Ile Lys Leu His Thr Gly Glu Lys Pro Phe Lys Cys
530 535 540
His Leu Cys Asn Thr Ala Ser Ala Glu Ala Arg His Ile Lys Ala Glu
545 550 555 560
Met Gly Gly Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu Asp Ser Thr
565 570 575
<210> 95
<211> 560
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 95
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
130 135 140
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
145 150 155 160
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser
195 200 205
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
210 215 220
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg Met His Lys Arg Ser His Thr Gly Glu Arg
485 490 495
Pro Phe Gln Cys Asn Gln Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn
500 505 510
Leu Leu Arg His Ile Lys Leu His Thr Gly Glu Lys Pro Phe Lys Cys
515 520 525
His Leu Cys Asn Thr Ala Ser Ala Glu Ala Arg His Ile Lys Ala Glu
530 535 540
Met Gly Gly Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu Asp Ser Thr
545 550 555 560
<210> 96
<211> 576
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 96
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
130 135 140
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
145 150 155 160
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser
195 200 205
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
210 215 220
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg Lys Gly Gly Gly Ser Lys Gly Gly Gly Thr
485 490 495
Lys Gly Gly Gly Ser Lys Met His Lys Arg Ser His Thr Gly Glu Arg
500 505 510
Pro Phe Gln Cys Asn Gln Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn
515 520 525
Leu Leu Arg His Ile Lys Leu His Thr Gly Glu Lys Pro Phe Lys Cys
530 535 540
His Leu Cys Asn Thr Ala Ser Ala Glu Ala Arg His Ile Lys Ala Glu
545 550 555 560
Met Gly Gly Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu Asp Ser Thr
565 570 575
<210> 97
<211> 570
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 97
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala His Lys Arg Ser His Thr
20 25 30
Gly Glu Arg Pro Phe Gln Cys Asn Gln Cys Gly Ala Ser Phe Thr Gln
35 40 45
Lys Gly Asn Leu Leu Arg His Ile Lys Leu His Thr Gly Glu Lys Pro
50 55 60
Phe Lys Cys His Leu Cys Asn Thr Ala Ser Ala Glu Ala Arg His Ile
65 70 75 80
Lys Ala Glu Met Gly Gly Thr Gly Ala Glu Asp Pro Arg Pro Ser Arg
85 90 95
Lys Arg Arg Ser Leu Gly Asp Val Gly Glu Ile Val Met Thr Gln Ser
100 105 110
Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
115 120 125
Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys
130 135 140
Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His
145 150 155 160
Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr
165 170 175
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe
180 185 190
Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys
195 200 205
Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
210 215 220
Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys
225 230 235 240
Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu
245 250 255
Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu
260 265 270
Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser
275 280 285
Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln
290 295 300
Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr
305 310 315 320
Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr
325 330 335
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala
340 345 350
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
355 360 365
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
370 375 380
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
385 390 395 400
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
405 410 415
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
420 425 430
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
435 440 445
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
450 455 460
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
465 470 475 480
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
485 490 495
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
500 505 510
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
515 520 525
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
530 535 540
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
545 550 555 560
Ala Leu His Met Gln Ala Leu Pro Pro Arg
565 570
<210> 98
<211> 565
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 98
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro His Lys Arg Ser His Thr Gly Glu Arg Pro Phe
20 25 30
Gln Cys Asn Gln Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu
35 40 45
Arg His Ile Lys Leu His Thr Gly Glu Lys Pro Phe Lys Cys His Leu
50 55 60
Cys Asn Thr Ala Ser Ala Glu Ala Arg His Ile Lys Ala Glu Met Gly
65 70 75 80
Gly Thr Gly Ala Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu
85 90 95
Gly Asp Val Gly Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser
100 105 110
Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp
115 120 125
Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
130 135 140
Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala
145 150 155 160
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser
165 170 175
Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn
180 185 190
Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly
195 200 205
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val
210 215 220
Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu
225 230 235 240
Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val
245 250 255
Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val
260 265 270
Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser Arg
275 280 285
Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu
290 295 300
Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His
305 310 315 320
Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr
325 330 335
Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
340 345 350
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
355 360 365
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
370 375 380
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
385 390 395 400
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
405 410 415
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
420 425 430
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
435 440 445
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
450 455 460
Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
465 470 475 480
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
485 490 495
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
500 505 510
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
515 520 525
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
530 535 540
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
545 550 555 560
Ala Leu Pro Pro Arg
565
<210> 99
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 99
Lys Gly Gly Gly Ser Lys Gly Gly Gly Thr Lys Gly Gly Gly Ser Lys
1. 5 10 15
<210> 100
<211> 59
<212> БЕЛОК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: последовательность IKZF3"
<400> 100
His Lys Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln Cys
1. 5 10 15
Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys Leu
20 25 30
His Thr Gly Glu Lys Pro Phe Lys Cys His Leu Cys Asn Thr Ala Ser
35 40 45
Ala Glu Ala Arg His Ile Ser Ala Glu Met Gly
50 55
<210> 101
<211> 459
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 101
Met His Lys Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln
1. 5 10 15
Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys
20 25 30
Leu His Thr Gly Glu Lys Pro Phe Lys Cys His Leu Cys Asn Thr Ala
35 40 45
Ser Ala Glu Ala Arg His Ile Lys Ala Glu Met Gly Gly Gly Gly Gly
50 55 60
Ser Gly Gly Gly Gly Thr Gly Gly Gly Gly Ser Gly Met Ala Glu Pro
65 70 75 80
Arg Gln Glu Phe Glu Val Met Glu Asp His Ala Gly Thr Tyr Gly Leu
85 90 95
Gly Asp Arg Lys Asp Gln Gly Gly Tyr Thr Met His Gln Asp Gln Glu
100 105 110
Gly Asp Thr Asp Ala Gly Leu Lys Ala Glu Glu Ala Gly Ile Gly Asp
115 120 125
Thr Pro Ser Leu Glu Asp Glu Ala Ala Gly His Val Thr Gln Ala Arg
130 135 140
Met Val Ser Lys Ser Lys Asp Gly Thr Gly Ser Asp Asp Lys Lys Ala
145 150 155 160
Lys Gly Ala Asp Gly Lys Thr Lys Ile Ala Thr Pro Arg Gly Ala Ala
165 170 175
Pro Pro Gly Gln Lys Gly Gln Ala Asn Ala Thr Arg Ile Pro Ala Lys
180 185 190
Thr Pro Pro Ala Pro Lys Thr Pro Pro Ser Ser Gly Glu Pro Pro Lys
195 200 205
Ser Gly Asp Arg Ser Gly Tyr Ser Ser Pro Gly Ser Pro Gly Thr Pro
210 215 220
Gly Ser Arg Ser Arg Thr Pro Ser Leu Pro Thr Pro Pro Thr Arg Glu
225 230 235 240
Pro Lys Lys Val Ala Val Val Arg Thr Pro Pro Lys Ser Pro Ser Ser
245 250 255
Ala Lys Ser Arg Leu Gln Thr Ala Pro Val Pro Met Pro Asp Leu Lys
260 265 270
Asn Val Lys Ser Lys Ile Gly Ser Thr Glu Asn Leu Lys His Gln Pro
275 280 285
Gly Gly Gly Lys Val Gln Ile Ile Asn Lys Lys Leu Asp Leu Ser Asn
290 295 300
Val Gln Ser Lys Cys Gly Ser Lys Asp Asn Ile Lys His Val Pro Gly
305 310 315 320
Gly Gly Ser Val Gln Ile Val Tyr Lys Pro Val Asp Leu Ser Lys Val
325 330 335
Thr Ser Lys Cys Gly Ser Leu Gly Asn Ile His His Lys Pro Gly Gly
340 345 350
Gly Gln Val Glu Val Lys Ser Glu Lys Leu Asp Phe Lys Asp Arg Val
355 360 365
Gln Ser Lys Ile Gly Ser Leu Asp Asn Ile Thr His Val Pro Gly Gly
370 375 380
Gly Asn Lys Lys Ile Glu Thr His Lys Leu Thr Phe Arg Glu Asn Ala
385 390 395 400
Lys Ala Lys Thr Asp His Gly Ala Glu Ile Val Tyr Lys Ser Pro Val
405 410 415
Val Ser Gly Asp Thr Ser Pro Arg His Leu Ser Asn Val Ser Ser Thr
420 425 430
Gly Ser Ile Asp Met Val Asp Ser Pro Gln Leu Ala Thr Leu Ala Asp
435 440 445
Glu Val Ser Ala Ser Leu Ala Lys Gln Gly Leu
450 455
<210> 102
<211> 715
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 102
Met His Lys Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln
1. 5 10 15
Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys
20 25 30
Leu His Thr Gly Glu Lys Pro Phe Lys Cys His Leu Cys Asn Thr Ala
35 40 45
Ser Ala Glu Ala Arg His Ile Lys Ala Glu Met Gly Gly Gly Gly Gly
50 55 60
Ser Gly Gly Gly Gly Thr Gly Gly Gly Gly Ser Gly Met Ala Glu Pro
65 70 75 80
Arg Gln Glu Phe Glu Val Met Glu Asp His Ala Gly Thr Tyr Gly Leu
85 90 95
Gly Asp Arg Lys Asp Gln Gly Gly Tyr Thr Met His Gln Asp Gln Glu
100 105 110
Gly Asp Thr Asp Ala Gly Leu Lys Ala Glu Glu Ala Gly Ile Gly Asp
115 120 125
Thr Pro Ser Leu Glu Asp Glu Ala Ala Gly His Val Thr Gln Ala Arg
130 135 140
Met Val Ser Lys Ser Lys Asp Gly Thr Gly Ser Asp Asp Lys Lys Ala
145 150 155 160
Lys Gly Ala Asp Gly Lys Thr Lys Ile Ala Thr Pro Arg Gly Ala Ala
165 170 175
Pro Pro Gly Gln Lys Gly Gln Ala Asn Ala Thr Arg Ile Pro Ala Lys
180 185 190
Thr Pro Pro Ala Pro Lys Thr Pro Pro Ser Ser Gly Glu Pro Pro Lys
195 200 205
Ser Gly Asp Arg Ser Gly Tyr Ser Ser Pro Gly Ser Pro Gly Thr Pro
210 215 220
Gly Ser Arg Ser Arg Thr Pro Ser Leu Pro Thr Pro Pro Thr Arg Glu
225 230 235 240
Pro Lys Lys Val Ala Val Val Arg Thr Pro Pro Lys Ser Pro Ser Ser
245 250 255
Ala Lys Ser Arg Leu Gln Thr Ala Pro Val Pro Met Pro Asp Leu Lys
260 265 270
Asn Val Lys Ser Lys Ile Gly Ser Thr Glu Asn Leu Lys His Gln Pro
275 280 285
Gly Gly Gly Lys Val Gln Ile Ile Asn Lys Lys Leu Asp Leu Ser Asn
290 295 300
Val Gln Ser Lys Cys Gly Ser Lys Asp Asn Ile Lys His Val Ser Gly
305 310 315 320
Gly Gly Ser Val Gln Ile Val Tyr Lys Pro Val Asp Leu Ser Lys Val
325 330 335
Thr Ser Lys Cys Gly Ser Leu Gly Asn Ile His His Lys Pro Gly Gly
340 345 350
Gly Gln Val Glu Val Lys Ser Glu Lys Leu Asp Phe Lys Asp Arg Val
355 360 365
Gln Ser Lys Ile Gly Ser Leu Asp Asn Ile Thr His Val Pro Gly Gly
370 375 380
Gly Asn Lys Lys Ile Glu Thr His Lys Leu Thr Phe Arg Glu Asn Ala
385 390 395 400
Lys Ala Lys Thr Asp His Gly Ala Glu Ile Val Tyr Lys Ser Pro Val
405 410 415
Val Ser Gly Asp Thr Ser Pro Arg His Leu Ser Asn Val Ser Ser Thr
420 425 430
Gly Ser Ile Asp Met Val Asp Ser Pro Gln Leu Ala Thr Leu Ala Asp
435 440 445
Glu Val Ser Ala Ser Leu Ala Lys Gln Gly Leu Gly Ser Ser Gly Ser
450 455 460
Glu Thr Pro Gly Thr Ser Glu Ser Ala Thr Pro Glu Ser Val Ser Lys
465 470 475 480
Gly Glu Glu Leu Phe Thr Gly Val Val Pro Ile Leu Val Glu Leu Asp
485 490 495
Gly Asp Val Asn Gly His Lys Phe Ser Val Ser Gly Glu Gly Glu Gly
500 505 510
Asp Ala Thr Tyr Gly Lys Leu Thr Leu Lys Phe Ile Cys Thr Thr Gly
515 520 525
Lys Leu Pro Val Pro Trp Pro Thr Leu Val Thr Thr Phe Gly Tyr Gly
530 535 540
Leu Gln Cys Phe Ala Arg Tyr Pro Asp His Met Lys Gln His Asp Phe
545 550 555 560
Phe Lys Ser Ala Met Pro Glu Gly Tyr Val Gln Glu Arg Thr Ile Phe
565 570 575
Phe Lys Asp Asp Gly Asn Tyr Lys Thr Arg Ala Glu Val Lys Phe Glu
580 585 590
Gly Asp Thr Leu Val Asn Arg Ile Glu Leu Lys Gly Ile Asp Phe Lys
595 600 605
Glu Asp Gly Asn Ile Leu Gly His Lys Leu Glu Tyr Asn Tyr Asn Ser
610 615 620
His Asn Val Tyr Ile Met Ala Asp Lys Gln Lys Asn Gly Ile Lys Val
625 630 635 640
Asn Phe Lys Ile Arg His Asn Ile Glu Asp Gly Ser Val Gln Leu Ala
645 650 655
Asp His Tyr Gln Gln Asn Thr Pro Ile Gly Asp Gly Pro Val Leu Leu
660 665 670
Pro Asp Asn His Tyr Leu Ser Tyr Gln Ser Ala Leu Ser Lys Asp Pro
675 680 685
Asn Glu Lys Arg Asp His Met Val Leu Leu Glu Phe Val Thr Ala Ala
690 695 700
Gly Ile Thr Leu Gly Met Asp Glu Leu Tyr Lys
705 710 715
<210> 103
<211> 709
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 103
Met His Lys Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln
1. 5 10 15
Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys
20 25 30
Leu His Thr Gly Glu Lys Pro Phe Lys Cys His Leu Cys Asn Thr Ala
35 40 45
Ser Ala Glu Ala Arg His Ile Lys Ala Glu Met Gly Gly Gly Gly Gly
50 55 60
Ser Gly Gly Gly Gly Thr Gly Gly Gly Gly Ser Gly Met Ala Glu Pro
65 70 75 80
Arg Gln Glu Phe Glu Val Met Glu Asp His Ala Gly Thr Tyr Gly Leu
85 90 95
Gly Asp Arg Lys Asp Gln Gly Gly Tyr Thr Met His Gln Asp Gln Glu
100 105 110
Gly Asp Thr Asp Ala Gly Leu Lys Ala Glu Glu Ala Gly Ile Gly Asp
115 120 125
Thr Pro Ser Leu Glu Asp Glu Ala Ala Gly His Val Thr Gln Ala Arg
130 135 140
Met Val Ser Lys Ser Lys Asp Gly Thr Gly Ser Asp Asp Lys Lys Ala
145 150 155 160
Lys Gly Ala Asp Gly Lys Thr Lys Ile Ala Thr Pro Arg Gly Ala Ala
165 170 175
Pro Pro Gly Gln Lys Gly Gln Ala Asn Ala Thr Arg Ile Pro Ala Lys
180 185 190
Thr Pro Pro Ala Pro Lys Thr Pro Pro Ser Ser Gly Glu Pro Pro Lys
195 200 205
Ser Gly Asp Arg Ser Gly Tyr Ser Ser Pro Gly Ser Pro Gly Thr Pro
210 215 220
Gly Ser Arg Ser Arg Thr Pro Ser Leu Pro Thr Pro Pro Thr Arg Glu
225 230 235 240
Pro Lys Lys Val Ala Val Val Arg Thr Pro Pro Lys Ser Pro Ser Ser
245 250 255
Ala Lys Ser Arg Leu Gln Thr Ala Pro Val Pro Met Pro Asp Leu Lys
260 265 270
Asn Val Lys Ser Lys Ile Gly Ser Thr Glu Asn Leu Lys His Gln Pro
275 280 285
Gly Gly Gly Lys Val Gln Ile Ile Asn Lys Lys Leu Asp Leu Ser Asn
290 295 300
Val Gln Ser Lys Cys Gly Ser Lys Asp Asn Ile Lys His Val Pro Gly
305 310 315 320
Gly Gly Ser Val Gln Ile Val Tyr Lys Pro Val Asp Leu Ser Lys Val
325 330 335
Thr Ser Lys Cys Gly Ser Leu Gly Asn Ile His His Lys Pro Gly Gly
340 345 350
Gly Gln Val Glu Val Lys Ser Glu Lys Leu Asp Phe Lys Asp Arg Val
355 360 365
Gln Ser Lys Ile Gly Ser Leu Asp Asn Ile Thr His Val Pro Gly Gly
370 375 380
Gly Asn Lys Lys Ile Glu Thr His Lys Leu Thr Phe Arg Glu Asn Ala
385 390 395 400
Lys Ala Lys Thr Asp His Gly Ala Glu Ile Val Tyr Lys Ser Pro Val
405 410 415
Val Ser Gly Asp Thr Ser Pro Arg His Leu Ser Asn Val Ser Ser Thr
420 425 430
Gly Ser Ile Asp Met Val Asp Ser Pro Gln Leu Ala Thr Leu Ala Asp
435 440 445
Glu Val Ser Ala Ser Leu Ala Lys Gln Gly Leu Gly Gly Gly Gly Ser
450 455 460
Gly Gly Gly Gly Thr Gly Gly Gly Gly Ser Gly Met Asp Phe Lys Asn
465 470 475 480
Leu Ile Trp Leu Lys Glu Val Asp Ser Thr Gln Glu Arg Leu Lys Glu
485 490 495
Trp Asn Val Ser Tyr Gly Thr Ala Leu Val Ala Asp Arg Gln Thr Lys
500 505 510
Gly Arg Gly Gly Leu Gly Arg Lys Trp Leu Ser Gln Glu Gly Gly Leu
515 520 525
Tyr Phe Ser Phe Leu Leu Asn Pro Lys Glu Phe Glu Asn Leu Leu Gln
530 535 540
Leu Pro Leu Val Leu Gly Leu Ser Val Ser Glu Ala Leu Glu Glu Ile
545 550 555 560
Thr Glu Ile Pro Phe Ser Leu Lys Trp Pro Asn Asp Val Tyr Phe Gln
565 570 575
Glu Lys Lys Val Ser Gly Val Leu Cys Glu Leu Ser Lys Asp Lys Leu
580 585 590
Ile Val Gly Ile Gly Ile Asn Val Asn Gln Arg Glu Ile Pro Glu Glu
595 600 605
Ile Lys Asp Arg Ala Thr Thr Leu Tyr Glu Ile Thr Gly Lys Asp Trp
610 615 620
Asp Arg Lys Glu Val Leu Leu Lys Val Leu Lys Arg Ile Ser Glu Asn
625 630 635 640
Leu Lys Lys Phe Lys Glu Lys Ser Phe Lys Glu Phe Lys Gly Lys Ile
645 650 655
Glu Ser Lys Met Leu Tyr Leu Gly Glu Glu Val Lys Leu Leu Gly Glu
660 665 670
Gly Lys Ile Thr Gly Lys Leu Val Gly Leu Ser Glu Lys Gly Gly Ala
675 680 685
Leu Ile Leu Thr Glu Glu Gly Ile Lys Glu Ile Leu Ser Gly Glu Phe
690 695 700
Ser Leu Arg Arg Ser
705
<210> 104
<211> 726
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 104
Met His Lys Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln
1. 5 10 15
Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys
20 25 30
Leu His Thr Gly Glu Lys Pro Phe Lys Cys His Leu Cys Asn Thr Ala
35 40 45
Ser Ala Glu Ala Arg His Ile Lys Ala Glu Met Gly Gly Gly Gly Gly
50 55 60
Ser Gly Gly Gly Gly Thr Gly Gly Gly Gly Ser Gly Met Ala Glu Pro
65 70 75 80
Arg Gln Glu Phe Glu Val Met Glu Asp His Ala Gly Thr Tyr Gly Leu
85 90 95
Gly Asp Arg Lys Asp Gln Gly Gly Tyr Thr Met His Gln Asp Gln Glu
100 105 110
Gly Asp Thr Asp Ala Gly Leu Lys Ala Glu Glu Ala Gly Ile Gly Asp
115 120 125
Thr Pro Ser Leu Glu Asp Glu Ala Ala Gly His Val Thr Gln Ala Arg
130 135 140
Met Val Ser Lys Ser Lys Asp Gly Thr Gly Ser Asp Asp Lys Lys Ala
145 150 155 160
Lys Gly Ala Asp Gly Lys Thr Lys Ile Ala Thr Pro Arg Gly Ala Ala
165 170 175
Pro Pro Gly Gln Lys Gly Gln Ala Asn Ala Thr Arg Ile Pro Ala Lys
180 185 190
Thr Pro Pro Ala Pro Lys Thr Pro Pro Ser Ser Gly Glu Pro Pro Lys
195 200 205
Ser Gly Asp Arg Ser Gly Tyr Ser Ser Pro Gly Ser Pro Gly Thr Pro
210 215 220
Gly Ser Arg Ser Arg Thr Pro Ser Leu Pro Thr Pro Pro Thr Arg Glu
225 230 235 240
Pro Lys Lys Val Ala Val Val Arg Thr Pro Pro Lys Ser Pro Ser Ser
245 250 255
Ala Lys Ser Arg Leu Gln Thr Ala Pro Val Pro Met Pro Asp Leu Lys
260 265 270
Asn Val Lys Ser Lys Ile Gly Ser Thr Glu Asn Leu Lys His Gln Pro
275 280 285
Gly Gly Gly Lys Val Gln Ile Ile Asn Lys Lys Leu Asp Leu Ser Asn
290 295 300
Val Gln Ser Lys Cys Gly Ser Lys Asp Asn Ile Lys His Val Pro Gly
305 310 315 320
Gly Gly Ser Val Gln Ile Val Tyr Lys Pro Val Asp Leu Ser Lys Val
325 330 335
Thr Ser Lys Cys Gly Ser Leu Gly Asn Ile His His Lys Pro Gly Gly
340 345 350
Gly Gln Val Glu Val Lys Ser Glu Lys Leu Asp Phe Lys Asp Arg Val
355 360 365
Gln Ser Lys Ile Gly Ser Leu Asp Asn Ile Thr His Val Pro Gly Gly
370 375 380
Gly Asn Lys Lys Ile Glu Thr His Lys Leu Thr Phe Arg Glu Asn Ala
385 390 395 400
Lys Ala Lys Thr Asp His Gly Ala Glu Ile Val Tyr Lys Ser Pro Val
405 410 415
Val Ser Gly Asp Thr Ser Pro Arg His Leu Ser Asn Val Ser Ser Thr
420 425 430
Gly Ser Ile Asp Met Val Asp Ser Pro Gln Leu Ala Thr Leu Ala Asp
435 440 445
Glu Val Ser Ala Ser Leu Ala Lys Gln Gly Leu Gly Gly Gly Gly Ser
450 455 460
Gly Gly Gly Gly Thr Gly Gly Gly Gly Ser Gly Gly Lys Pro Ile Pro
465 470 475 480
Asn Pro Leu Leu Gly Leu Asp Ser Thr Gly Ser Gly Met Asp Phe Lys
485 490 495
Asn Leu Ile Trp Leu Lys Glu Val Asp Ser Thr Gln Glu Arg Leu Lys
500 505 510
Glu Trp Asn Val Ser Tyr Gly Thr Ala Leu Val Ala Asp Arg Gln Thr
515 520 525
Lys Gly Arg Gly Gly Leu Gly Arg Lys Trp Leu Ser Gln Glu Gly Gly
530 535 540
Leu Tyr Phe Ser Phe Leu Leu Asn Pro Lys Glu Phe Glu Asn Leu Leu
545 550 555 560
Gln Leu Pro Leu Val Leu Gly Leu Ser Val Ser Glu Ala Leu Glu Glu
565 570 575
Ile Thr Glu Ile Pro Phe Ser Leu Lys Trp Pro Asn Asp Val Tyr Phe
580 585 590
Gln Glu Lys Lys Val Ser Gly Val Leu Cys Glu Leu Ser Lys Asp Lys
595 600 605
Leu Ile Val Gly Ile Gly Ile Asn Val Asn Gln Arg Glu Ile Pro Glu
610 615 620
Glu Ile Lys Asp Arg Ala Thr Thr Leu Tyr Glu Ile Thr Gly Lys Asp
625 630 635 640
Trp Asp Arg Lys Glu Val Leu Leu Lys Val Leu Lys Arg Ile Ser Glu
645 650 655
Asn Leu Lys Lys Phe Lys Glu Lys Ser Phe Lys Glu Phe Lys Gly Lys
660 665 670
Ile Glu Ser Lys Met Leu Tyr Leu Gly Glu Glu Val Lys Leu Leu Gly
675 680 685
Glu Gly Lys Ile Thr Gly Lys Leu Val Gly Leu Ser Glu Lys Gly Gly
690 695 700
Ala Leu Ile Leu Thr Glu Glu Gly Ile Lys Glu Ile Leu Ser Gly Glu
705 710 715 720
Phe Ser Leu Arg Arg Ser
725
<210> 105
<211> 726
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 105
Met His Lys Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln
1. 5 10 15
Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys
20 25 30
Leu His Thr Gly Glu Lys Pro Phe Lys Cys His Leu Cys Asn Thr Ala
35 40 45
Ser Ala Glu Ala Arg His Ile Lys Ala Glu Met Gly Gly Gly Gly Gly
50 55 60
Ser Gly Gly Gly Gly Thr Gly Gly Gly Gly Ser Gly Met Ala Glu Pro
65 70 75 80
Arg Gln Glu Phe Glu Val Met Glu Asp His Ala Gly Thr Tyr Gly Leu
85 90 95
Gly Asp Arg Lys Asp Gln Gly Gly Tyr Thr Met His Gln Asp Gln Glu
100 105 110
Gly Asp Thr Asp Ala Gly Leu Lys Ala Glu Glu Ala Gly Ile Gly Asp
115 120 125
Thr Pro Ser Leu Glu Asp Glu Ala Ala Gly His Val Thr Gln Ala Arg
130 135 140
Met Val Ser Lys Ser Lys Asp Gly Thr Gly Ser Asp Asp Lys Lys Ala
145 150 155 160
Lys Gly Ala Asp Gly Lys Thr Lys Ile Ala Thr Pro Arg Gly Ala Ala
165 170 175
Pro Pro Gly Gln Lys Gly Gln Ala Asn Ala Thr Arg Ile Pro Ala Lys
180 185 190
Thr Pro Pro Ala Pro Lys Thr Pro Pro Ser Ser Gly Glu Pro Pro Lys
195 200 205
Ser Gly Asp Arg Ser Gly Tyr Ser Ser Pro Gly Ser Pro Gly Thr Pro
210 215 220
Gly Ser Arg Ser Arg Thr Pro Ser Leu Pro Thr Pro Pro Thr Arg Glu
225 230 235 240
Pro Lys Lys Val Ala Val Val Arg Thr Pro Pro Lys Ser Pro Ser Ser
245 250 255
Ala Lys Ser Arg Leu Gln Thr Ala Pro Val Pro Met Pro Asp Leu Lys
260 265 270
Asn Val Lys Ser Lys Ile Gly Ser Thr Glu Asn Leu Lys His Gln Pro
275 280 285
Gly Gly Gly Lys Val Gln Ile Ile Asn Lys Lys Leu Asp Leu Ser Asn
290 295 300
Val Gln Ser Lys Cys Gly Ser Lys Asp Asn Ile Lys His Val Pro Gly
305 310 315 320
Gly Gly Ser Val Gln Ile Val Tyr Lys Pro Val Asp Leu Ser Lys Val
325 330 335
Thr Ser Lys Cys Gly Ser Leu Gly Asn Ile His His Lys Pro Gly Gly
340 345 350
Gly Gln Val Glu Val Lys Ser Glu Lys Leu Asp Phe Lys Asp Arg Val
355 360 365
Gln Ser Lys Ile Gly Ser Leu Asp Asn Ile Thr His Val Pro Gly Gly
370 375 380
Gly Asn Lys Lys Ile Glu Thr His Lys Leu Thr Phe Arg Glu Asn Ala
385 390 395 400
Lys Ala Lys Thr Asp His Gly Ala Glu Ile Val Tyr Lys Ser Pro Val
405 410 415
Val Ser Gly Asp Thr Ser Pro Arg His Leu Ser Asn Val Ser Ser Thr
420 425 430
Gly Ser Ile Asp Met Val Asp Ser Pro Gln Leu Ala Thr Leu Ala Asp
435 440 445
Glu Val Ser Ala Ser Leu Ala Lys Gln Gly Leu Gly Gly Gly Gly Ser
450 455 460
Gly Gly Gly Gly Thr Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Thr
465 470 475 480
Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Thr Gly Met Asp Phe Lys
485 490 495
Asn Leu Ile Trp Leu Lys Glu Val Asp Ser Thr Gln Glu Arg Leu Lys
500 505 510
Glu Trp Asn Val Ser Tyr Gly Thr Ala Leu Val Ala Asp Arg Gln Thr
515 520 525
Lys Gly Arg Gly Gly Leu Gly Arg Lys Trp Leu Ser Gln Glu Gly Gly
530 535 540
Leu Tyr Phe Ser Phe Leu Leu Asn Pro Lys Glu Phe Glu Asn Leu Leu
545 550 555 560
Gln Leu Pro Leu Val Leu Gly Leu Ser Val Ser Glu Ala Leu Glu Glu
565 570 575
Ile Thr Glu Ile Pro Phe Ser Leu Lys Trp Pro Asn Asp Val Tyr Phe
580 585 590
Gln Glu Lys Lys Val Ser Gly Val Leu Cys Glu Leu Ser Lys Asp Lys
595 600 605
Leu Ile Val Gly Ile Gly Ile Asn Val Asn Gln Arg Glu Ile Pro Glu
610 615 620
Glu Ile Lys Asp Arg Ala Thr Thr Leu Tyr Glu Ile Thr Gly Lys Asp
625 630 635 640
Trp Asp Arg Lys Glu Val Leu Leu Lys Val Leu Lys Arg Ile Ser Glu
645 650 655
Asn Leu Lys Lys Phe Lys Glu Lys Ser Phe Lys Glu Phe Lys Gly Lys
660 665 670
Ile Glu Ser Lys Met Leu Tyr Leu Gly Glu Glu Val Lys Leu Leu Gly
675 680 685
Glu Gly Lys Ile Thr Gly Lys Leu Val Gly Leu Ser Glu Lys Gly Gly
690 695 700
Ala Leu Ile Leu Thr Glu Glu Gly Ile Lys Glu Ile Leu Ser Gly Glu
705 710 715 720
Phe Ser Leu Arg Arg Ser
725
<210> 106
<211> 709
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 106
Met His Lys Arg Ser His Thr Gly Glu Arg Pro Phe Gln Cys Asn Gln
1. 5 10 15
Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys
20 25 30
Leu His Thr Gly Glu Lys Pro Phe Lys Cys His Leu Cys Asn Thr Ala
35 40 45
Ser Ala Glu Ala Arg His Ile Lys Ala Glu Met Gly Gly Gly Gly Gly
50 55 60
Ser Gly Gly Gly Gly Thr Gly Gly Gly Gly Ser Gly Met Ala Glu Pro
65 70 75 80
Arg Gln Glu Phe Glu Val Met Glu Asp His Ala Gly Thr Tyr Gly Leu
85 90 95
Gly Asp Arg Lys Asp Gln Gly Gly Tyr Thr Met His Gln Asp Gln Glu
100 105 110
Gly Asp Thr Asp Ala Gly Leu Lys Ala Glu Glu Ala Gly Ile Gly Asp
115 120 125
Thr Pro Ser Leu Glu Asp Glu Ala Ala Gly His Val Thr Gln Ala Arg
130 135 140
Met Val Ser Lys Ser Lys Asp Gly Thr Gly Ser Asp Asp Lys Lys Ala
145 150 155 160
Lys Gly Ala Asp Gly Lys Thr Lys Ile Ala Thr Pro Arg Gly Ala Ala
165 170 175
Pro Pro Gly Gln Lys Gly Gln Ala Asn Ala Thr Arg Ile Pro Ala Lys
180 185 190
Thr Pro Pro Ala Pro Lys Thr Pro Pro Ser Ser Gly Glu Pro Pro Lys
195 200 205
Ser Gly Asp Arg Ser Gly Tyr Ser Ser Pro Gly Ser Pro Gly Thr Pro
210 215 220
Gly Ser Arg Ser Arg Thr Pro Ser Leu Pro Thr Pro Pro Thr Arg Glu
225 230 235 240
Pro Lys Lys Val Ala Val Val Arg Thr Pro Pro Lys Ser Pro Ser Ser
245 250 255
Ala Lys Ser Arg Leu Gln Thr Ala Pro Val Pro Met Pro Asp Leu Lys
260 265 270
Asn Val Lys Ser Lys Ile Gly Ser Thr Glu Asn Leu Lys His Gln Pro
275 280 285
Gly Gly Gly Lys Val Gln Ile Ile Asn Lys Lys Leu Asp Leu Ser Asn
290 295 300
Val Gln Ser Lys Cys Gly Ser Lys Asp Asn Ile Lys His Val Pro Gly
305 310 315 320
Gly Gly Ser Val Gln Ile Val Tyr Lys Pro Val Asp Leu Ser Lys Val
325 330 335
Thr Ser Lys Cys Gly Ser Leu Gly Asn Ile His His Lys Pro Gly Gly
340 345 350
Gly Gln Val Glu Val Lys Ser Glu Lys Leu Asp Phe Lys Asp Arg Val
355 360 365
Gln Ser Lys Ile Gly Ser Leu Asp Asn Ile Thr His Val Pro Gly Gly
370 375 380
Gly Asn Lys Lys Ile Glu Thr His Lys Leu Thr Phe Arg Glu Asn Ala
385 390 395 400
Lys Ala Lys Thr Asp His Gly Ala Glu Ile Val Tyr Lys Ser Pro Val
405 410 415
Val Ser Gly Asp Thr Ser Pro Arg His Leu Ser Asn Val Ser Ser Thr
420 425 430
Gly Ser Ile Asp Met Val Asp Ser Pro Gln Leu Ala Thr Leu Ala Asp
435 440 445
Glu Val Ser Ala Ser Leu Ala Lys Gln Gly Leu Ser Gly Ser Glu Thr
450 455 460
Pro Gly Thr Ser Glu Ser Ala Thr Pro Glu Ser Met Asp Phe Lys Asn
465 470 475 480
Leu Ile Trp Leu Lys Glu Val Asp Ser Thr Gln Glu Arg Leu Lys Glu
485 490 495
Trp Asn Val Ser Tyr Gly Thr Ala Leu Val Ala Asp Arg Gln Thr Lys
500 505 510
Gly Arg Gly Gly Leu Gly Arg Lys Trp Leu Ser Gln Glu Gly Gly Leu
515 520 525
Tyr Phe Ser Phe Leu Leu Asn Pro Lys Glu Phe Glu Asn Leu Leu Gln
530 535 540
Leu Pro Leu Val Leu Gly Leu Ser Val Ser Glu Ala Leu Glu Glu Ile
545 550 555 560
Thr Glu Ile Pro Phe Ser Leu Lys Trp Pro Asn Asp Val Tyr Phe Gln
565 570 575
Glu Lys Lys Val Ser Gly Val Leu Cys Glu Leu Ser Lys Asp Lys Leu
580 585 590
Ile Val Gly Ile Gly Ile Asn Val Asn Gln Arg Glu Ile Pro Glu Glu
595 600 605
Ile Lys Asp Arg Ala Thr Thr Leu Tyr Glu Ile Thr Gly Lys Asp Trp
610 615 620
Asp Arg Lys Glu Val Leu Leu Lys Val Leu Lys Arg Ile Ser Glu Asn
625 630 635 640
Leu Lys Lys Phe Lys Glu Lys Ser Phe Lys Glu Phe Lys Gly Lys Ile
645 650 655
Glu Ser Lys Met Leu Tyr Leu Gly Glu Glu Val Lys Leu Leu Gly Glu
660 665 670
Gly Lys Ile Thr Gly Lys Leu Val Gly Leu Ser Glu Lys Gly Gly Ala
675 680 685
Leu Ile Leu Thr Glu Glu Gly Ile Lys Glu Ile Leu Ser Gly Glu Phe
690 695 700
Ser Leu Arg Arg Ser
705
<210> 107
<211> 633
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 107
Met Ala Glu Pro Arg Gln Glu Phe Glu Val Met Glu Asp His Ala Gly
1. 5 10 15
Thr Tyr Gly Leu Gly Asp Arg Lys Asp Gln Gly Gly Tyr Thr Met His
20 25 30
Gln Asp Gln Glu Gly Asp Thr Asp Ala Gly Leu Lys Ala Glu Glu Ala
35 40 45
Gly Ile Gly Asp Thr Pro Ser Leu Glu Asp Glu Ala Ala Gly His Val
50 55 60
Thr Gln Ala Arg Met Val Ser Lys Ser Lys Asp Gly Thr Gly Ser Asp
65 70 75 80
Asp Lys Lys Ala Lys Gly Ala Asp Gly Lys Thr Lys Ile Ala Thr Pro
85 90 95
Arg Gly Ala Ala Pro Pro Gly Gln Lys Gly Gln Ala Asn Ala Thr Arg
100 105 110
Ile Pro Ala Lys Thr Pro Pro Ala Pro Lys Thr Pro Pro Ser Ser Gly
115 120 125
Glu Pro Pro Lys Ser Gly Asp Arg Ser Gly Tyr Ser Ser Pro Gly Ser
130 135 140
Pro Gly Thr Pro Gly Ser Arg Ser Arg Thr Pro Ser Leu Pro Thr Pro
145 150 155 160
Pro Thr Arg Glu Pro Lys Lys Val Ala Val Val Arg Thr Pro Pro Lys
165 170 175
Ser Pro Ser Ser Ala Lys Ser Arg Leu Gln Thr Ala Pro Val Pro Met
180 185 190
Pro Asp Leu Lys Asn Val Lys Ser Lys Ile Gly Ser Thr Glu Asn Leu
195 200 205
Lys His Gln Pro Gly Gly Gly Lys Val Gln Ile Ile Asn Lys Lys Leu
210 215 220
Asp Leu Ser Asn Val Gln Ser Lys Cys Gly Ser Lys Asp Asn Ile Lys
225 230 235 240
His Val Pro Gly Gly Gly Ser Val Gln Ile Val Tyr Lys Pro Val Asp
245 250 255
Leu Ser Lys Val Thr Ser Lys Cys Gly Ser Leu Gly Asn Ile His His
260 265 270
Lys Pro Gly Gly Gly Gln Val Glu Val Lys Ser Glu Lys Leu Asp Phe
275 280 285
Lys Asp Arg Val Gln Ser Lys Ile Gly Ser Leu Asp Asn Ile Thr His
290 295 300
Val Pro Gly Gly Gly Asn Lys Lys Ile Glu Thr His Lys Leu Thr Phe
305 310 315 320
Arg Glu Asn Ala Lys Ala Lys Thr Asp His Gly Ala Glu Ile Val Tyr
325 330 335
Lys Ser Pro Val Val Ser Gly Asp Thr Ser Pro Arg His Leu Ser Asn
340 345 350
Val Ser Ser Thr Gly Ser Ile Asp Met Val Asp Ser Pro Gln Leu Ala
355 360 365
Thr Leu Ala Asp Glu Val Ser Ala Ser Leu Ala Lys Gln Gly Leu Gly
370 375 380
Gly Gly Gly Ser Gly Gly Gly Gly Thr Gly Gly Gly Gly Ser Gly Met
385 390 395 400
Asp Phe Lys Asn Leu Ile Trp Leu Lys Glu Val Asp Ser Thr Gln Glu
405 410 415
Arg Leu Lys Glu Trp Asn Val Ser Tyr Gly Thr Ala Leu Val Ala Asp
420 425 430
Arg Gln Thr Lys Gly Arg Gly Gly Leu Gly Arg Lys Trp Leu Ser Gln
435 440 445
Glu Gly Gly Leu Tyr Phe Ser Phe Leu Leu Asn Pro Lys Glu Phe Glu
450 455 460
Asn Leu Leu Gln Leu Pro Leu Val Leu Gly Leu Ser Val Ser Glu Ala
465 470 475 480
Leu Glu Glu Ile Thr Glu Ile Pro Phe Ser Leu Lys Trp Pro Asn Asp
485 490 495
Val Tyr Phe Gln Glu Lys Lys Val Ser Gly Val Leu Cys Glu Leu Ser
500 505 510
Lys Asp Lys Leu Ile Val Gly Ile Gly Ile Asn Val Asn Gln Arg Glu
515 520 525
Ile Pro Glu Glu Ile Lys Asp Arg Ala Thr Thr Leu Tyr Glu Ile Thr
530 535 540
Gly Lys Asp Trp Asp Arg Lys Glu Val Leu Leu Lys Val Leu Lys Arg
545 550 555 560
Ile Ser Glu Asn Leu Lys Lys Phe Lys Glu Lys Ser Phe Lys Glu Phe
565 570 575
Lys Gly Lys Ile Glu Ser Lys Met Leu Tyr Leu Gly Glu Glu Val Lys
580 585 590
Leu Leu Gly Glu Gly Lys Ile Thr Gly Lys Leu Val Gly Leu Ser Glu
595 600 605
Lys Gly Gly Ala Leu Ile Leu Thr Glu Glu Gly Ile Lys Glu Ile Leu
610 615 620
Ser Gly Glu Phe Ser Leu Arg Arg Ser
625 630
<210> 108
<211> 650
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 108
Met Ala Glu Pro Arg Gln Glu Phe Glu Val Met Glu Asp His Ala Gly
1. 5 10 15
Thr Tyr Gly Leu Gly Asp Arg Lys Asp Gln Gly Gly Tyr Thr Met His
20 25 30
Gln Asp Gln Glu Gly Asp Thr Asp Ala Gly Leu Lys Ala Glu Glu Ala
35 40 45
Gly Ile Gly Asp Thr Pro Ser Leu Glu Asp Glu Ala Ala Gly His Val
50 55 60
Thr Gln Ala Arg Met Val Ser Lys Ser Lys Asp Gly Thr Gly Ser Asp
65 70 75 80
Asp Lys Lys Ala Lys Gly Ala Asp Gly Lys Thr Lys Ile Ala Thr Pro
85 90 95
Arg Gly Ala Ala Pro Pro Gly Gln Lys Gly Gln Ala Asn Ala Thr Arg
100 105 110
Ile Pro Ala Lys Thr Pro Pro Ala Pro Lys Thr Pro Pro Ser Ser Gly
115 120 125
Glu Pro Pro Lys Ser Gly Asp Arg Ser Gly Tyr Ser Ser Pro Gly Ser
130 135 140
Pro Gly Thr Pro Gly Ser Arg Ser Arg Thr Pro Ser Leu Pro Thr Pro
145 150 155 160
Pro Thr Arg Glu Pro Lys Lys Val Ala Val Val Arg Thr Pro Pro Lys
165 170 175
Ser Pro Ser Ser Ala Lys Ser Arg Leu Gln Thr Ala Pro Val Pro Met
180 185 190
Pro Asp Leu Lys Asn Val Lys Ser Lys Ile Gly Ser Thr Glu Asn Leu
195 200 205
Lys His Gln Pro Gly Gly Gly Lys Val Gln Ile Ile Asn Lys Lys Leu
210 215 220
Asp Leu Ser Asn Val Gln Ser Lys Cys Gly Ser Lys Asp Asn Ile Lys
225 230 235 240
His Val Pro Gly Gly Gly Ser Val Gln Ile Val Tyr Lys Pro Val Asp
245 250 255
Leu Ser Lys Val Thr Ser Lys Cys Gly Ser Leu Gly Asn Ile His His
260 265 270
Lys Pro Gly Gly Gly Gln Val Glu Val Lys Ser Glu Lys Leu Asp Phe
275 280 285
Lys Asp Arg Val Gln Ser Lys Ile Gly Ser Leu Asp Asn Ile Thr His
290 295 300
Val Pro Gly Gly Gly Asn Lys Lys Ile Glu Thr His Lys Leu Thr Phe
305 310 315 320
Arg Glu Asn Ala Lys Ala Lys Thr Asp His Gly Ala Glu Ile Val Tyr
325 330 335
Lys Ser Pro Val Val Ser Gly Asp Thr Ser Pro Arg His Leu Ser Asn
340 345 350
Val Ser Ser Thr Gly Ser Ile Asp Met Val Asp Ser Pro Gln Leu Ala
355 360 365
Thr Leu Ala Asp Glu Val Ser Ala Ser Leu Ala Lys Gln Gly Leu Gly
370 375 380
Gly Gly Gly Ser Gly Gly Gly Gly Thr Gly Gly Gly Gly Ser Gly Gly
385 390 395 400
Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu Asp Ser Thr Gly Ser Gly
405 410 415
Met Asp Phe Lys Asn Leu Ile Trp Leu Lys Glu Val Asp Ser Thr Gln
420 425 430
Glu Arg Leu Lys Glu Trp Asn Val Ser Tyr Gly Thr Ala Leu Val Ala
435 440 445
Asp Arg Gln Thr Lys Gly Arg Gly Gly Leu Gly Arg Lys Trp Leu Ser
450 455 460
Gln Glu Gly Gly Leu Tyr Phe Ser Phe Leu Leu Asn Pro Lys Glu Phe
465 470 475 480
Glu Asn Leu Leu Gln Leu Pro Leu Val Leu Gly Leu Ser Val Ser Glu
485 490 495
Ala Leu Glu Glu Ile Thr Glu Ile Pro Phe Ser Leu Lys Trp Pro Asn
500 505 510
Asp Val Tyr Phe Gln Glu Lys Lys Val Ser Gly Val Leu Cys Glu Leu
515 520 525
Ser Lys Asp Lys Leu Ile Val Gly Ile Gly Ile Asn Val Asn Gln Arg
530 535 540
Glu Ile Pro Glu Glu Ile Lys Asp Arg Ala Thr Thr Leu Tyr Glu Ile
545 550 555 560
Thr Gly Lys Asp Trp Asp Arg Lys Glu Val Leu Leu Lys Val Leu Lys
565 570 575
Arg Ile Ser Glu Asn Leu Lys Lys Phe Lys Glu Lys Ser Phe Lys Glu
580 585 590
Phe Lys Gly Lys Ile Glu Ser Lys Met Leu Tyr Leu Gly Glu Glu Val
595 600 605
Lys Leu Leu Gly Glu Gly Lys Ile Thr Gly Lys Leu Val Gly Leu Ser
610 615 620
Glu Lys Gly Gly Ala Leu Ile Leu Thr Glu Glu Gly Ile Lys Glu Ile
625 630 635 640
Leu Ser Gly Glu Phe Ser Leu Arg Arg Ser
645 650
<210> 109
<211> 59
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 109
His Lys Arg Ser His Thr Gly Glu Arg Pro Phe His Cys Asn Gln Cys
1. 5 10 15
Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys Leu
20 25 30
His Ser Gly Glu Lys Pro Phe Lys Cys Pro Phe Cys Ser Ala Gly Gln
35 40 45
Val Met Ser His His Val Pro Pro Met Glu Asp
50 55
<210> 110
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 110
cagtcagtgg gcctcggcgg ccaagcttgg caatccggta ctgttggtga agccattcac
60
catgcataaa aggagtcaca ctggtgaacg ccccttccac tgtaaccagt gtggagcttc
120
ttttactcag aagggcaacc ttctgagaca cataaagtta cactctggag agaagccgtt
180
caaatgtcct ttctgtagcg ctgggcaggt catgagtcac catgtacctc ctatggaaga
240
tggtggtggc gggagcggag gtggaggcac gggcggtgga ggttcgggga acgttatgct
300
ggaaatgcta gaatataa
318
<210> 111
<211> 1814
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 111
ccatttcagg tgtcgtgagc ggccgctcta gagccgaatt cggatccatg gccctccctg
60
tcaccgccct gctgcttccg ctggctcttc tgctccacgc cgctcggccc gaaattgtga
120
tgacccagtc acccgccact cttagccttt cacccggtga gcgcgcaacc ctgtcttgca
180
gagcctccca agacatctca aaatacctta attggtatca acagaagccc ggacaggctc
240
ctcgccttct gatctaccac accagccggc tccattctgg aatccctgcc aggttcagcg
300
gtagcggatc tgggaccgac tacaccctca ctatcagctc actgcagcca gaggacttcg
360
ctgtctattt ctgtcagcaa gggaacaccc tgccctacac ctttggacag ggcaccaagc
420
tcgagattaa aggtggaggt ggcagcggag gaggtgggtc cggcggtgga ggaagccagg
480
tccaactcca agaaagcgga ccgggtcttg tgaagccatc agaaactctt tcactgactt
540
gtactgtgag cggagtgtct ctccccgatt acggggtgtc ttggatcaga cagccaccgg
600
ggaagggtct ggaatggatt ggagtgattt ggggctcaga gactacttac taccaatcat
660
ccctcaagtc tcgcgtcacc atctcaaagg acaactctaa gaatcaggtg tcactgaaac
720
tgtcatctgt gaccgcagcc gacaccgccg tgtactattg cgctaagcat tactattatg
780
gcgggagcta cgcaatggat tactggggac agggtactct ggtcaccgtg tccagcacca
840
ctaccccagc accgaggcca cccaccccgg ctcctaccat cgcctcccag cctctgtccc
900
tgcgtccgga ggcatgtaga cccgcagctg gtggggccgt gcatacccgg ggtcttgact
960
tcgcctgcga tatctacatt tgggcccctc tggctggtac ttgcggggtc ctgctgcttt
1020
cactcgtgat cactctttac tgtaagcgcg gtcggaagaa gctgctgtac atctttaagc
1080
aacccttcat gaggcctgtg cagactactc aagaggagga cggctgttca tgccggttcc
1140
cagaggagga ggaaggcggc tgcgaactgc gcgtgaaatt cagccgcagc gcagatgctc
1200
cagcctacca gcaggggcag aaccagctct acaacgaact caatcttggt cggagagagg
1260
agtacgacgt gctggacaag cggagaggac gggacccaga aatgggcggg aagccgcgca
1320
gaaagaatcc ccaagagggc ctgtacaacg agctccaaaa ggataagatg gcagaagcct
1380
atagcgagat tggtatgaaa ggggaacgca gaagaggcaa aggccacgac ggactgtacc
1440
agggactcag caccgccacc aaggacacct atgacgctct tcacatgcag gccctgccgc
1500
ctcggggtgg tggcgggagc ggaggtggag gcacgggcgg tggaggttcg gggcataaaa
1560
ggagtcacac tggtgaacgc cccttccact gtaaccagtg tggagcttct tttactcaga
1620
agggcaacct tctgagacac ataaagttac actctggaga gaagccgttc aaatgtcctt
1680
tctgtagcgc tgggcaggtc atgagtcacc atgtacctcc tatggaagat taagtcgacg
1740
cgtaacccag ctttcttgta caaagtggtt gatatccagc acagtggcgg cgcgccattc
1800
cgcccctctc cctc
1814
<210> 112
<211> 561
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 112
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
130 135 140
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
145 150 155 160
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser
195 200 205
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
210 215 220
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Thr
485 490 495
Gly Gly Gly Gly Ser Gly His Lys Arg Ser His Thr Gly Glu Arg Pro
500 505 510
Phe His Cys Asn Gln Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu
515 520 525
Leu Arg His Ile Lys Leu His Ser Gly Glu Lys Pro Phe Lys Cys Pro
530 535 540
Phe Cys Ser Ala Gly Gln Val Met Ser His His Val Pro Pro Met Glu
545 550 555 560
Asp
<210> 113
<211> 45
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 113
His Lys Arg Ser His Thr Gly Glu Arg Pro Phe His Cys Asn Gln Cys
1. 5 10 15
Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg His Ile Lys Leu
20 25 30
His Ser Gly Glu Lys Pro Phe Lys Cys Pro Phe Cys Ser
35 40 45
<210> 114
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 114
Ala Gly Gln Val Met Ser His His Val Pro Pro Met Glu Asp
1. 5 10
<210> 115
<400> 115
000
<210> 116
<400> 116
000
<210> 117
<400> 117
000
<210> 118
<400> 118
000
<210> 119
<400> 119
000
<210> 120
<400> 120
000
<210> 121
<400> 121
000
<210> 122
<400> 122
000
<210> 123
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 123
Arg Thr Lys Arg
1
<210> 124
<400> 124
000
<210> 125
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 125
Gly Thr Gly Ala Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu
1. 5 10 15
Gly Asp Val Gly
20
<210> 126
<211> 60
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 126
ggaaccggcg cggaagaccc ccggccctcc aggaagcgaa ggtccctcgg agacgtgggt
60
<210> 127
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 127
Gly Thr Gly Ala Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg
1. 5 10
<210> 128
<211> 42
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 128
ggaaccggcg cggaagaccc ccggccctcc aggaagcgaa gg
42
<210> 129
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 129
Leu Gln Trp Leu Glu Gln Gln Val Ala Lys Arg Arg Thr Lys Arg
1. 5 10 15
<210> 130
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 130
ctgcaatggc tggagcagca ggtggcgaag cggagaacta agcgg
45
<210> 131
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 131
Gly Thr Gly Ala Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu
1. 5 10 15
Gly Gly
<210> 132
<211> 54
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 132
ggcacaggtg ccgaggaccc tcggccaagc cgcaaaagga ggtcacttgg cggc
54
<210> 133
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 133
Gly Thr Gly Ala Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu
1. 5 10 15
Gly
<210> 134
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 134
ggaaccggag cagaagatcc cagaccaagc cggaaaaggc ggtccctggg t
51
<210> 135
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 135
Ser Leu Asn Leu Thr Glu Ser His Asn Ser Arg Lys Lys Arg
1. 5 10
<210> 136
<211> 42
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 136
agtctcaatt tgactgagtc acacaattcc aggaagaaaa gg
42
<210> 137
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 137
Cys Lys Ile Asn Gly Tyr Pro Lys Arg Gly Arg Lys Arg Arg
1. 5 10
<210> 138
<211> 42
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 138
tgcaagatca acggctaccc taagaggggc agaaagcggc gg
42
<210> 139
<211> 12
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 139
cgtactaaaa ga
12
<210> 140
<211> 26
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 140
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala
20 25
<210> 141
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 141
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1. 5 10 15
Gly Gly Gly Ser
20
<210> 142
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 142
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1. 5 10 15
<210> 143
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 143
Gly Gly Gly Ser
1
<210> 144
<211> 1184
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 144
cgtgaggctc cggtgcccgt cagtgggcag agcgcacatc gcccacagtc cccgagaagt
60
tggggggagg ggtcggcaat tgaaccggtg cctagagaag gtggcgcggg gtaaactggg
120
aaagtgatgt cgtgtactgg ctccgccttt ttcccgaggg tgggggagaa ccgtatataa
180
gtgcagtagt cgccgtgaac gttctttttc gcaacgggtt tgccgccaga acacaggtaa
240
gtgccgtgtg tggttcccgc gggcctggcc tctttacggg ttatggccct tgcgtgcctt
300
gaattacttc cacctggctg cagtacgtga ttcttgatcc cgagcttcgg gttggaagtg
360
ggtgggagag ttcgaggcct tgcgcttaag gagccccttc gcctcgtgct tgagttgagg
420
cctggcctgg gcgctggggc cgccgcgtgc gaatctggtg gcaccttcgc gcctgtctcg
480
ctgctttcga taagtctcta gccatttaaa atttttgatg acctgctgcg acgctttttt
540
tctggcaaga tagtcttgta aatgcgggcc aagatctgca cactggtatt tcggtttttg
600
gggccgcggg cggcgacggg gcccgtgcgt cccagcgcac atgttcggcg aggcggggcc
660
tgcgagcgcg gccaccgaga atcggacggg ggtagtctca agctggccgg cctgctctgg
720
tgcctggcct cgcgccgccg tgtatcgccc cgccctgggc ggcaaggctg gcccggtcgg
780
caccagttgc gtgagcggaa agatggccgc ttcccggccc tgctgcaggg agctcaaaat
840
ggaggacgcg gcgctcggga gagcgggcgg gtgagtcacc cacacaaagg aaaagggcct
900
ttccgtcctc agccgtcgct tcatgtgact ccacggagta ccgggcgccg tccaggcacc
960
tcgattagtt ctcgagcttt tggagtacgt cgtctttagg ttggggggag gggttttatg
1020
cgatggagtt tccccacact gagtgggtgg agactgaagt taggccagct tggcacttga
1080
tgtaattctc cttggaattt gccctttttg agtttggatc ttggttcatt ctcaagcctc
1140
agacagtggt tcaaagtttt tttcttccat ttcaggtgtc gtga
1184
<210> 145
<211> 63
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 145
atggccctgc ctgtgacagc cctgctgctg cctctggctc tgctgctgca tgccgctaga
60
ccc
63
<210> 146
<211> 63
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 146
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccc
63
<210> 147
<211> 45
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 147
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
1. 5 10 15
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
20 25 30
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
35 40 45
<210> 148
<211> 135
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 148
accacgacgc cagcgccgcg accaccaaca ccggcgccca ccatcgcgtc gcagcccctg
60
tccctgcgcc cagaggcgtg ccggccagcg gcggggggcg cagtgcacac gagggggctg
120
gacttcgcct gtgat
135
<210> 149
<211> 230
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 149
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe
1. 5 10 15
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
20 25 30
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
35 40 45
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
50 55 60
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
65 70 75 80
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
85 90 95
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
100 105 110
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
115 120 125
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
130 135 140
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
145 150 155 160
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
165 170 175
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
180 185 190
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
195 200 205
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
210 215 220
Leu Ser Leu Gly Lys Met
225 230
<210> 150
<211> 690
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 150
gagagcaagt acggccctcc ctgcccccct tgccctgccc ccgagttcct gggcggaccc
60
agcgtgttcc tgttcccccc caagcccaag gacaccctga tgatcagccg gacccccgag
120
gtgacctgtg tggtggtgga cgtgtcccag gaggaccccg aggtccagtt caactggtac
180
gtggacggcg tggaggtgca caacgccaag accaagcccc gggaggagca gttcaatagc
240
acctaccggg tggtgtccgt gctgaccgtg ctgcaccagg actggctgaa cggcaaggaa
300
tacaagtgta aggtgtccaa caagggcctg cccagcagca tcgagaaaac catcagcaag
360
gccaagggcc agcctcggga gccccaggtg tacaccctgc cccctagcca agaggagatg
420
accaagaacc aggtgtccct gacctgcctg gtgaagggct tctaccccag cgacatcgcc
480
gtggagtggg agagcaacgg ccagcccgag aacaactaca agaccacccc ccctgtgctg
540
gacagcgacg gcagcttctt cctgtacagc cggctgaccg tggacaagag ccggtggcag
600
gagggcaacg tctttagctg ctccgtgatg cacgaggccc tgcacaacca ctacacccag
660
aagagcctga gcctgtccct gggcaagatg
690
<210> 151
<211> 282
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 151
Arg Trp Pro Glu Ser Pro Lys Ala Gln Ala Ser Ser Val Pro Thr Ala
1. 5 10 15
Gln Pro Gln Ala Glu Gly Ser Leu Ala Lys Ala Thr Thr Ala Pro Ala
20 25 30
Thr Thr Arg Asn Thr Gly Arg Gly Gly Glu Glu Lys Lys Lys Glu Lys
35 40 45
Glu Lys Glu Glu Gln Glu Glu Arg Glu Thr Lys Thr Pro Glu Cys Pro
50 55 60
Ser His Thr Gln Pro Leu Gly Val Tyr Leu Leu Thr Pro Ala Val Gln
65 70 75 80
Asp Leu Trp Leu Arg Asp Lys Ala Thr Phe Thr Cys Phe Val Val Gly
85 90 95
Ser Asp Leu Lys Asp Ala His Leu Thr Trp Glu Val Ala Gly Lys Val
100 105 110
Pro Thr Gly Gly Val Glu Glu Gly Leu Leu Glu Arg His Ser Asn Gly
115 120 125
Ser Gln Ser Gln His Ser Arg Leu Thr Leu Pro Arg Ser Leu Trp Asn
130 135 140
Ala Gly Thr Ser Val Thr Cys Thr Leu Asn His Pro Ser Leu Pro Pro
145 150 155 160
Gln Arg Leu Met Ala Leu Arg Glu Pro Ala Ala Gln Ala Pro Val Lys
165 170 175
Leu Ser Leu Asn Leu Leu Ala Ser Ser Asp Pro Pro Glu Ala Ala Ser
180 185 190
Trp Leu Leu Cys Glu Val Ser Gly Phe Ser Pro Pro Asn Ile Leu Leu
195 200 205
Met Trp Leu Glu Asp Gln Arg Glu Val Asn Thr Ser Gly Phe Ala Pro
210 215 220
Ala Arg Pro Pro Pro Gln Pro Gly Ser Thr Thr Phe Trp Ala Trp Ser
225 230 235 240
Val Leu Arg Val Pro Ala Pro Pro Ser Pro Gln Pro Ala Thr Tyr Thr
245 250 255
Cys Val Val Ser His Glu Asp Ser Arg Thr Leu Leu Asn Ala Ser Arg
260 265 270
Ser Leu Glu Val Ser Tyr Val Thr Asp His
275 280
<210> 152
<211> 847
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 152
aggtggcccg aaagtcccaa ggcccaggca tctagtgttc ctactgcaca gccccaggca
60
gaaggcagcc tagccaaagc tactactgca cctgccacta cgcgcaatac tggccgtggc
120
ggggaggaga agaaaaagga gaaagagaaa gaagaacagg aagagaggga gaccaagacc
180
cctgaatgtc catcccatac ccagccgctg ggcgtctatc tcttgactcc cgcagtacag
240
gacttgtggc ttagagataa ggccaccttt acatgtttcg tcgtgggctc tgacctgaag
300
gatgcccatt tgacttggga ggttgccgga aaggtaccca cagggggggt tgaggaaggg
360
ttgctggagc gccattccaa tggctctcag agccagcact caagactcac ccttccgaga
420
tccctgtgga acgccgggac ctctgtcaca tgtactctaa atcatcctag cctgccccca
480
cagcgtctga tggcccttag agagccagcc gcccaggcac cagttaagct tagcctgaat
540
ctgctcgcca gtagtgatcc cccagaggcc gccagctggc tcttatgcga agtgtccggc
600
tttagcccgc ccaacatctt gctcatgtgg ctggaggacc agcgagaagt gaacaccagc
660
ggcttcgctc cagcccggcc cccaccccag ccgggttcta ccacattctg ggcctggagt
720
gtcttaaggg tcccagcacc acctagcccc cagccagcca catacacctg tgttgtgtcc
780
catgaagata gcaggaccct gctaaatgct tctaggagtc tggaggtttc ctacgtgact
840
gaccatt
847
<210> 153
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 153
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1. 5 10
<210> 154
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 154
ggtggcggag gttctggagg tggaggttcc
30
<210> 155
<211> 24
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 155
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
1. 5 10 15
Ser Leu Val Ile Thr Leu Tyr Cys
20
<210> 156
<211> 72
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 156
atctacatct gggcgccctt ggccgggact tgtggggtcc ttctcctgtc actggttatc
60
accctttact gc
72
<210> 157
<211> 72
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический олигонуклеотид"
<400> 157
atctacattt gggcccctct ggctggtact tgcggggtcc tgctgctttc actcgtgatc
60
actctttact gt
72
<210> 158
<211> 42
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 158
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
1. 5 10 15
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
20 25 30
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
35 40
<210> 159
<211> 126
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 159
aaacggggca gaaagaaact cctgtatata ttcaaacaac catttatgag accagtacaa
60
actactcaag aggaagatgg ctgtagctgc cgatttccag aagaagaaga aggaggatgt
120
gaactg
126
<210> 160
<211> 126
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 160
aagcgcggtc ggaagaagct gctgtacatc tttaagcaac ccttcatgag gcctgtgcag
60
actactcaag aggaggacgg ctgttcatgc cggttcccag aggaggagga aggcggctgc
120
gaactg
126
<210> 161
<211> 48
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 161
Gln Arg Arg Lys Tyr Arg Ser Asn Lys Gly Glu Ser Pro Val Glu Pro
1. 5 10 15
Ala Glu Pro Cys Arg Tyr Ser Cys Pro Arg Glu Glu Glu Gly Ser Thr
20 25 30
Ile Pro Ile Gln Glu Asp Tyr Arg Lys Pro Glu Pro Ala Cys Ser Pro
35 40 45
<210> 162
<211> 123
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 162
aggagtaaga ggagcaggct cctgcacagt gactacatga acatgactcc ccgccgcccc
60
gggcccaccc gcaagcatta ccagccctat gccccaccac gcgacttcgc agcctatcgc
120
tcc
123
<210> 163
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 163
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly
1. 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 164
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 164
agagtgaagt tcagcaggag cgcagacgcc cccgcgtaca agcagggcca gaaccagctc
60
tataacgagc tcaatctagg acgaagagag gagtacgatg ttttggacaa gagacgtggc
120
cgggaccctg agatgggggg aaagccgaga aggaagaacc ctcaggaagg cctgtacaat
180
gaactgcaga aagataagat ggcggaggcc tacagtgaga ttgggatgaa aggcgagcgc
240
cggaggggca aggggcacga tggcctttac cagggtctca gtacagccac caaggacacc
300
tacgacgccc ttcacatgca ggccctgccc cctcgc
336
<210> 165
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 165
cgcgtgaaat tcagccgcag cgcagatgct ccagcctaca agcaggggca gaaccagctc
60
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
120
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
180
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
240
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
300
tatgacgctc ttcacatgca ggccctgccg cctcgg
336
<210> 166
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 166
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
1. 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 167
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 167
agagtgaagt tcagcaggag cgcagacgcc cccgcgtacc agcagggcca gaaccagctc
60
tataacgagc tcaatctagg acgaagagag gagtacgatg ttttggacaa gagacgtggc
120
cgggaccctg agatgggggg aaagccgaga aggaagaacc ctcaggaagg cctgtacaat
180
gaactgcaga aagataagat ggcggaggcc tacagtgaga ttgggatgaa aggcgagcgc
240
cggaggggca aggggcacga tggcctttac cagggtctca gtacagccac caaggacacc
300
tacgacgccc ttcacatgca ggccctgccc cctcgc
336
<210> 168
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 168
Gly Gly Gly Gly Ser
1. 5
<210> 169
<211> 150
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 169
Pro Gly Trp Phe Leu Asp Ser Pro Asp Arg Pro Trp Asn Pro Pro Thr
1. 5 10 15
Phe Ser Pro Ala Leu Leu Val Val Thr Glu Gly Asp Asn Ala Thr Phe
20 25 30
Thr Cys Ser Phe Ser Asn Thr Ser Glu Ser Phe Val Leu Asn Trp Tyr
35 40 45
Arg Met Ser Pro Ser Asn Gln Thr Asp Lys Leu Ala Ala Phe Pro Glu
50 55 60
Asp Arg Ser Gln Pro Gly Gln Asp Cys Arg Phe Arg Val Thr Gln Leu
65 70 75 80
Pro Asn Gly Arg Asp Phe His Met Ser Val Val Arg Ala Arg Arg Asn
85 90 95
Asp Ser Gly Thr Tyr Leu Cys Gly Ala Ile Ser Leu Ala Pro Lys Ala
100 105 110
Gln Ile Lys Glu Ser Leu Arg Ala Glu Leu Arg Val Thr Glu Arg Arg
115 120 125
Ala Glu Val Pro Thr Ala His Pro Ser Pro Ser Pro Arg Pro Ala Gly
130 135 140
Gln Phe Gln Thr Leu Val
145 150
<210> 170
<211> 450
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 170
cccggatggt ttctggactc tccggatcgc ccgtggaatc ccccaacctt ctcaccggca
60
ctcttggttg tgactgaggg cgataatgcg accttcacgt gctcgttctc caacacctcc
120
gaatcattcg tgctgaactg gtaccgcatg agcccgtcaa accagaccga caagctcgcc
180
gcgtttccgg aagatcggtc gcaaccggga caggattgtc ggttccgcgt gactcaactg
240
ccgaatggca gagacttcca catgagcgtg gtccgcgcta ggcgaaacga ctccgggacc
300
tacctgtgcg gagccatctc gctggcgcct aaggcccaaa tcaaagagag cttgagggcc
360
gaactgagag tgaccgagcg cagagctgag gtgccaactg cacatccatc cccatcgcct
420
cggcctgcgg ggcagtttca gaccctggtc
450
<210> 171
<211> 394
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 171
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Pro Gly Trp Phe Leu Asp Ser Pro Asp Arg Pro
20 25 30
Trp Asn Pro Pro Thr Phe Ser Pro Ala Leu Leu Val Val Thr Glu Gly
35 40 45
Asp Asn Ala Thr Phe Thr Cys Ser Phe Ser Asn Thr Ser Glu Ser Phe
50 55 60
Val Leu Asn Trp Tyr Arg Met Ser Pro Ser Asn Gln Thr Asp Lys Leu
65 70 75 80
Ala Ala Phe Pro Glu Asp Arg Ser Gln Pro Gly Gln Asp Cys Arg Phe
85 90 95
Arg Val Thr Gln Leu Pro Asn Gly Arg Asp Phe His Met Ser Val Val
100 105 110
Arg Ala Arg Arg Asn Asp Ser Gly Thr Tyr Leu Cys Gly Ala Ile Ser
115 120 125
Leu Ala Pro Lys Ala Gln Ile Lys Glu Ser Leu Arg Ala Glu Leu Arg
130 135 140
Val Thr Glu Arg Arg Ala Glu Val Pro Thr Ala His Pro Ser Pro Ser
145 150 155 160
Pro Arg Pro Ala Gly Gln Phe Gln Thr Leu Val Thr Thr Thr Pro Ala
165 170 175
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
180 185 190
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
195 200 205
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
210 215 220
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
225 230 235 240
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
245 250 255
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
260 265 270
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
275 280 285
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
290 295 300
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
305 310 315 320
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
325 330 335
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
340 345 350
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
355 360 365
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
370 375 380
Ala Leu His Met Gln Ala Leu Pro Pro Arg
385 390
<210> 172
<211> 1182
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 172
atggccctcc ctgtcactgc cctgcttctc cccctcgcac tcctgctcca cgccgctaga
60
ccacccggat ggtttctgga ctctccggat cgcccgtgga atcccccaac cttctcaccg
120
gcactcttgg ttgtgactga gggcgataat gcgaccttca cgtgctcgtt ctccaacacc
180
tccgaatcat tcgtgctgaa ctggtaccgc atgagcccgt caaaccagac cgacaagctc
240
gccgcgtttc cggaagatcg gtcgcaaccg ggacaggatt gtcggttccg cgtgactcaa
300
ctgccgaatg gcagagactt ccacatgagc gtggtccgcg ctaggcgaaa cgactccggg
360
acctacctgt gcggagccat ctcgctggcg cctaaggccc aaatcaaaga gagcttgagg
420
gccgaactga gagtgaccga gcgcagagct gaggtgccaa ctgcacatcc atccccatcg
480
cctcggcctg cggggcagtt tcagaccctg gtcacgacca ctccggcgcc gcgcccaccg
540
actccggccc caactatcgc gagccagccc ctgtcgctga ggccggaagc atgccgccct
600
gccgccggag gtgctgtgca tacccgggga ttggacttcg catgcgacat ctacatttgg
660
gctcctctcg ccggaacttg tggcgtgctc cttctgtccc tggtcatcac cctgtactgc
720
aagcggggtc ggaaaaagct tctgtacatt ttcaagcagc ccttcatgag gcccgtgcaa
780
accacccagg aggaggacgg ttgctcctgc cggttccccg aagaggaaga aggaggttgc
840
gagctgcgcg tgaagttctc ccggagcgcc gacgcccccg cctataagca gggccagaac
900
cagctgtaca acgaactgaa cctgggacgg cgggaagagt acgatgtgct ggacaagcgg
960
cgcggccggg accccgaaat gggcgggaag cctagaagaa agaaccctca ggaaggcctg
1020
tataacgagc tgcagaagga caagatggcc gaggcctact ccgaaattgg gatgaaggga
1080
gagcggcgga ggggaaaggg gcacgacggc ctgtaccaag gactgtccac cgccaccaag
1140
gacacatacg atgccctgca catgcaggcc cttccccctc gc
1182
<210> 173
<211> 40
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<220>
<221> Сайт
<222> (1)..(40)
<223> /примечание="Эта последовательность может охватывать 1-10
повторяющихся звеньев Gly Gly Gly Ser'"
<400> 173
Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser
1. 5 10 15
Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser
20 25 30
Gly Gly Gly Ser Gly Gly Gly Ser
35 40
<210> 174
<211> 5000
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<220>
<221> другой_признак
<222> (1)..(5000)
<223> /примечание="Эта последовательность может охватывать 50-5000
нуклеотидов"
<220>
<221> источник
<223> /примечание="См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления"
<400> 174
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
60
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
120
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
180
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
240
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
300
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
360
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
420
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
480
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
540
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
600
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
660
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
720
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
780
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
840
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
900
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
960
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1020
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1080
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1140
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1200
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1260
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1320
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1380
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1440
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1500
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1560
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1620
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1680
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1740
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1800
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1860
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1920
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1980
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2040
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2100
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2160
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2220
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2280
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2340
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2400
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2460
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2520
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2580
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2640
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2700
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2760
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2820
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2880
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2940
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3000
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3060
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3120
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3180
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3240
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3300
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3360
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3420
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3480
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3540
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3600
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3660
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3720
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3780
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3840
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3900
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3960
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4020
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4080
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4140
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4200
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4260
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4320
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4380
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4440
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4500
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4560
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4620
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4680
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4740
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4800
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4860
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4920
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4980
aaaaaaaaaa aaaaaaaaaa
5000
<210> 175
<211> 373
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 175
Pro Gly Trp Phe Leu Asp Ser Pro Asp Arg Pro Trp Asn Pro Pro Thr
1. 5 10 15
Phe Ser Pro Ala Leu Leu Val Val Thr Glu Gly Asp Asn Ala Thr Phe
20 25 30
Thr Cys Ser Phe Ser Asn Thr Ser Glu Ser Phe Val Leu Asn Trp Tyr
35 40 45
Arg Met Ser Pro Ser Asn Gln Thr Asp Lys Leu Ala Ala Phe Pro Glu
50 55 60
Asp Arg Ser Gln Pro Gly Gln Asp Cys Arg Phe Arg Val Thr Gln Leu
65 70 75 80
Pro Asn Gly Arg Asp Phe His Met Ser Val Val Arg Ala Arg Arg Asn
85 90 95
Asp Ser Gly Thr Tyr Leu Cys Gly Ala Ile Ser Leu Ala Pro Lys Ala
100 105 110
Gln Ile Lys Glu Ser Leu Arg Ala Glu Leu Arg Val Thr Glu Arg Arg
115 120 125
Ala Glu Val Pro Thr Ala His Pro Ser Pro Ser Pro Arg Pro Ala Gly
130 135 140
Gln Phe Gln Thr Leu Val Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
145 150 155 160
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
165 170 175
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
180 185 190
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
195 200 205
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
210 215 220
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
225 230 235 240
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
245 250 255
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
260 265 270
Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
275 280 285
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
290 295 300
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
305 310 315 320
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
325 330 335
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
340 345 350
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
355 360 365
Ala Leu Pro Pro Arg
370
<210> 176
<211> 35
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 176
Thr Lys Lys Lys Tyr Ser Ser Ser Val His Asp Pro Asn Gly Glu Tyr
1. 5 10 15
Met Phe Met Arg Ala Val Asn Thr Ala Lys Lys Ser Arg Leu Thr Asp
20 25 30
Val Thr Leu
35
<210> 177
<211> 105
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 177
acaaaaaaga agtattcatc cagtgtgcac gaccctaacg gtgaatacat gttcatgaga
60
gcagtgaaca cagccaaaaa atccagactc acagatgtga cccta
105
<210> 178
<211> 69
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 178
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
1. 5 10 15
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
20 25 30
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Phe Trp Leu
35 40 45
Pro Ile Gly Cys Ala Ala Phe Val Val Val Cys Ile Leu Gly Cys Ile
50 55 60
Leu Ile Cys Trp Leu
65
<210> 179
<211> 207
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 179
accacgacgc cagcgccgcg accaccaaca ccggcgccca ccatcgcgtc gcagcccctg
60
tccctgcgcc cagaggcgtg ccggccagcg gcggggggcg cagtgcacac gagggggctg
120
gacttcgcct gtgatttctg gttacccata ggatgtgcag cctttgttgt agtctgcatt
180
ttgggatgca tacttatttg ttggctt
207
<210> 180
<211> 41
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 180
Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr
1. 5 10 15
Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro
20 25 30
Pro Arg Asp Phe Ala Ala Tyr Arg Ser
35 40
<210> 181
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 181
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu
20 25 30
Ser Ala Ser Leu Gly Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr
50 55 60
Val Lys Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile
85 90 95
Ser Asn Leu Glu Gln Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
130 135 140
Val Lys Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser
145 150 155 160
Leu Ser Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser
195 200 205
Arg Leu Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys
210 215 220
Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Ser Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 182
<211> 465
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 182
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1. 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Lys Leu Gln Glu
115 120 125
Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser Leu Ser Val Thr Cys
130 135 140
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
145 150 155 160
Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly Val Ile Trp Gly Ser
165 170 175
Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser Arg Leu Thr Ile Ile
180 185 190
Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys Met Asn Ser Leu Gln
195 200 205
Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
210 215 220
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser Val Thr Val
225 230 235 240
Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
245 250 255
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
260 265 270
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
275 280 285
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
290 295 300
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
305 310 315 320
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
325 330 335
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
340 345 350
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln
355 360 365
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
370 375 380
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
385 390 395 400
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
405 410 415
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
420 425 430
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
435 440 445
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
450 455 460
Arg
465
<210> 183
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 183
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu
20 25 30
Ser Ala Ser Leu Gly Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr
50 55 60
Val Lys Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile
85 90 95
Ser Asn Leu Glu Gln Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
130 135 140
Val Lys Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser
145 150 155 160
Leu Ser Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser
195 200 205
Arg Leu Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys
210 215 220
Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Ser Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 184
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 184
atggccttac cagtgaccgc cttgctcctg ccgctggcct tgctgctcca cgccgccagg
60
ccggacatcc agatgacaca gactacatcc tccctgtctg cctctctggg agacagagtc
120
accatcagtt gcagggcaag tcaggacatt agtaaatatt taaattggta tcagcagaaa
180
ccagatggaa ctgttaaact cctgatctac catacatcaa gattacactc aggagtccca
240
tcaaggttca gtggcagtgg gtctggaaca gattattctc tcaccattag caacctggag
300
caagaagata ttgccactta cttttgccaa cagggtaata cgcttccgta cacgttcgga
360
ggggggacca agctggagat cacaggtggc ggtggctcgg gcggtggtgg gtcgggtggc
420
ggcggatctg aggtgaaact gcaggagtca ggacctggcc tggtggcgcc ctcacagagc
480
ctgtccgtca catgcactgt ctcaggggtc tcattacccg actatggtgt aagctggatt
540
cgccagcctc cacgaaaggg tctggagtgg ctgggagtaa tatggggtag tgaaaccaca
600
tactataatt cagctctcaa atccagactg accatcatca aggacaactc caagagccaa
660
gttttcttaa aaatgaacag tctgcaaact gatgacacag ccatttacta ctgtgccaaa
720
cattattact acggtggtag ctatgctatg gactactggg gccaaggaac ctcagtcacc
780
gtctcctcaa ccacgacgcc agcgccgcga ccaccaacac cggcgcccac catcgcgtcg
840
cagcccctgt ccctgcgccc agaggcgtgc cggccagcgg cggggggcgc agtgcacacg
900
agggggctgg acttcgcctg tgatatctac atctgggcgc ccttggccgg gacttgtggg
960
gtccttctcc tgtcactggt tatcaccctt tactgcaaac ggggcagaaa gaaactcctg
1020
tatatattca aacaaccatt tatgagacca gtacaaacta ctcaagagga agatggctgt
1080
agctgccgat ttccagaaga agaagaagga ggatgtgaac tgagagtgaa gttcagcagg
1140
agcgcagacg cccccgcgta caagcagggc cagaaccagc tctataacga gctcaatcta
1200
ggacgaagag aggagtacga tgttttggac aagagacgtg gccgggaccc tgagatgggg
1260
ggaaagccga gaaggaagaa ccctcaggaa ggcctgtaca atgaactgca gaaagataag
1320
atggcggagg cctacagtga gattgggatg aaaggcgagc gccggagggg caaggggcac
1380
gatggccttt accagggtct cagtacagcc accaaggaca cctacgacgc ccttcacatg
1440
caggccctgc cccctcgc
1458
<210> 185
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 185
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1. 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Lys Leu Gln Glu
115 120 125
Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser Leu Ser Val Thr Cys
130 135 140
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
145 150 155 160
Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly Val Ile Trp Gly Ser
165 170 175
Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser Arg Leu Thr Ile Ile
180 185 190
Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys Met Asn Ser Leu Gln
195 200 205
Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
210 215 220
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser Val Thr Val
225 230 235 240
Ser Ser
<210> 186
<211> 244
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 186
Gln Val Gln Leu Leu Glu Ser Gly Ala Glu Leu Val Arg Pro Gly Ser
1. 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ala Phe Ser Ser Tyr
20 25 30
Trp Met Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gln Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Asn Gly Lys Phe
50 55 60
Lys Gly Gln Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Gly Leu Thr Ser Glu Asp Ser Ala Val Tyr Ser Cys
85 90 95
Ala Arg Lys Thr Ile Ser Ser Val Val Asp Phe Tyr Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Gly Gly Gly Ser Gly Gly Gly Ser Gly
115 120 125
Gly Gly Ser Gly Gly Gly Ser Glu Leu Val Leu Thr Gln Ser Pro Lys
130 135 140
Phe Met Ser Thr Ser Val Gly Asp Arg Val Ser Val Thr Cys Lys Ala
145 150 155 160
Ser Gln Asn Val Gly Thr Asn Val Ala Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Ser Pro Lys Pro Leu Ile Tyr Ser Ala Thr Tyr Arg Asn Ser Gly
180 185 190
Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
195 200 205
Thr Ile Thr Asn Val Gln Ser Lys Asp Leu Ala Asp Tyr Phe Cys Gln
210 215 220
Tyr Asn Arg Tyr Pro Tyr Thr Ser Phe Phe Phe Thr Lys Leu Glu Ile
225 230 235 240
Lys Arg Arg Ser
<210> 187
<211> 464
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 187
Gln Val Gln Leu Leu Glu Ser Gly Ala Glu Leu Val Arg Pro Gly Ser
1. 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ala Phe Ser Ser Tyr
20 25 30
Trp Met Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gln Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Asn Gly Lys Phe
50 55 60
Lys Gly Gln Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Gly Leu Thr Ser Glu Asp Ser Ala Val Tyr Ser Cys
85 90 95
Ala Arg Lys Thr Ile Ser Ser Val Val Asp Phe Tyr Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Gly Gly Gly Ser Gly Gly Gly Ser Gly
115 120 125
Gly Gly Ser Gly Gly Gly Ser Glu Leu Val Leu Thr Gln Ser Pro Lys
130 135 140
Phe Met Ser Thr Ser Val Gly Asp Arg Val Ser Val Thr Cys Lys Ala
145 150 155 160
Ser Gln Asn Val Gly Thr Asn Val Ala Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Ser Pro Lys Pro Leu Ile Tyr Ser Ala Thr Tyr Arg Asn Ser Gly
180 185 190
Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
195 200 205
Thr Ile Thr Asn Val Gln Ser Lys Asp Leu Ala Asp Tyr Phe Cys Gln
210 215 220
Tyr Asn Arg Tyr Pro Tyr Thr Ser Phe Phe Phe Thr Lys Leu Glu Ile
225 230 235 240
Lys Arg Arg Ser Lys Ile Glu Val Met Tyr Pro Pro Pro Tyr Leu Asp
245 250 255
Asn Glu Lys Ser Asn Gly Thr Ile Ile His Val Lys Gly Lys His Leu
260 265 270
Cys Pro Ser Pro Leu Phe Pro Gly Pro Ser Lys Pro Phe Trp Val Leu
275 280 285
Val Val Val Gly Gly Val Leu Ala Cys Tyr Ser Leu Leu Val Thr Val
290 295 300
Ala Phe Ile Ile Phe Trp Val Arg Ser Lys Arg Ser Arg Leu Leu His
305 310 315 320
Ser Asp Tyr Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys
325 330 335
His Tyr Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser
340 345 350
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
355 360 365
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
370 375 380
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
385 390 395 400
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
405 410 415
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
420 425 430
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
435 440 445
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
450 455 460
<210> 188
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 188
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1. 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr Gly Ser Thr Ser Gly
100 105 110
Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr Lys Gly Glu Val Lys
115 120 125
Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser Leu Ser
130 135 140
Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser
145 150 155 160
Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly Val Ile
165 170 175
Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser Arg Leu
180 185 190
Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys Met Asn
195 200 205
Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys His Tyr
210 215 220
Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser
225 230 235 240
Val Thr Val Ser Ser Glu
245
<210> 189
<211> 439
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 189
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1. 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr Gly Ser Thr Ser Gly
100 105 110
Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr Lys Gly Glu Val Lys
115 120 125
Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser Leu Ser
130 135 140
Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser
145 150 155 160
Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly Val Ile
165 170 175
Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser Arg Leu
180 185 190
Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys Met Asn
195 200 205
Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys His Tyr
210 215 220
Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser
225 230 235 240
Val Thr Val Ser Ser Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys
245 250 255
Pro Met Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr
260 265 270
Ser Leu Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val Lys Arg Gly
275 280 285
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
290 295 300
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Glu Glu Glu
305 310 315 320
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
325 330 335
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
340 345 350
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
355 360 365
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
370 375 380
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
385 390 395 400
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
405 410 415
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
420 425 430
Gln Ala Leu Pro Pro Arg Leu
435
<210> 190
<211> 819
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 190
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1. 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr Gly Ser Thr Ser Gly
100 105 110
Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr Lys Gly Glu Val Lys
115 120 125
Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser Leu Ser
130 135 140
Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser
145 150 155 160
Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly Val Ile
165 170 175
Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser Arg Leu
180 185 190
Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys Met Asn
195 200 205
Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys His Tyr
210 215 220
Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser
225 230 235 240
Val Thr Val Ser Ser Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys
245 250 255
Pro Met Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr
260 265 270
Ser Leu Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val Lys Arg Gly
275 280 285
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
290 295 300
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Glu Glu Glu
305 310 315 320
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
325 330 335
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
340 345 350
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
355 360 365
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
370 375 380
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
385 390 395 400
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
405 410 415
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
420 425 430
Gln Ala Leu Pro Pro Arg Leu Glu Gly Gly Gly Glu Gly Arg Gly Ser
435 440 445
Leu Leu Thr Cys Gly Asp Val Glu Glu Asn Pro Gly Pro Arg Met Leu
450 455 460
Leu Leu Val Thr Ser Leu Leu Leu Cys Glu Leu Pro His Pro Ala Phe
465 470 475 480
Leu Leu Ile Pro Arg Lys Val Cys Asn Gly Ile Gly Ile Gly Glu Phe
485 490 495
Lys Asp Ser Leu Ser Ile Asn Ala Thr Asn Ile Lys His Phe Lys Asn
500 505 510
Cys Thr Ser Ile Ser Gly Asp Leu His Ile Leu Pro Val Ala Phe Arg
515 520 525
Gly Asp Ser Phe Thr His Thr Pro Pro Leu Asp Pro Gln Glu Leu Asp
530 535 540
Ile Leu Lys Thr Val Lys Glu Ile Thr Gly Phe Leu Leu Ile Gln Ala
545 550 555 560
Trp Pro Glu Asn Arg Thr Asp Leu His Ala Phe Glu Asn Leu Glu Ile
565 570 575
Ile Arg Gly Arg Thr Lys Gln His Gly Gln Phe Ser Leu Ala Val Val
580 585 590
Ser Leu Asn Ile Thr Ser Leu Gly Leu Arg Ser Leu Lys Glu Ile Ser
595 600 605
Asp Gly Asp Val Ile Ile Ser Gly Asn Lys Asn Leu Cys Tyr Ala Asn
610 615 620
Thr Ile Asn Trp Lys Lys Leu Phe Gly Thr Ser Gly Gln Lys Thr Lys
625 630 635 640
Ile Ile Ser Asn Arg Gly Glu Asn Ser Cys Lys Ala Thr Gly Gln Val
645 650 655
Cys His Ala Leu Cys Ser Pro Glu Gly Cys Trp Gly Pro Glu Pro Arg
660 665 670
Asp Cys Val Ser Cys Arg Asn Val Ser Arg Gly Arg Glu Cys Val Asp
675 680 685
Lys Cys Asn Leu Leu Glu Gly Glu Pro Arg Glu Phe Val Glu Asn Ser
690 695 700
Glu Cys Ile Gln Cys His Pro Glu Cys Leu Pro Gln Ala Met Asn Ile
705 710 715 720
Thr Cys Thr Gly Arg Gly Pro Asp Asn Cys Ile Gln Cys Ala His Tyr
725 730 735
Ile Asp Gly Pro His Cys Val Lys Thr Cys Pro Ala Gly Val Met Gly
740 745 750
Glu Asn Asn Thr Leu Val Trp Lys Tyr Ala Asp Ala Gly His Val Cys
755 760 765
His Leu Cys His Pro Asn Cys Thr Tyr Gly Cys Thr Gly Pro Gly Leu
770 775 780
Glu Gly Cys Pro Thr Asn Gly Pro Lys Ile Pro Ser Ile Ala Thr Gly
785 790 795 800
Met Val Gly Ala Leu Leu Leu Leu Leu Val Val Ala Leu Gly Ile Gly
805 810 815
Leu Phe Met
<210> 191
<211> 245
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 191
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1. 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr Gly Ser Thr Ser Gly
100 105 110
Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr Lys Gly Glu Val Lys
115 120 125
Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser Leu Ser
130 135 140
Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser
145 150 155 160
Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly Val Ile
165 170 175
Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser Arg Leu
180 185 190
Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys Met Asn
195 200 205
Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys His Tyr
210 215 220
Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser
225 230 235 240
Val Thr Val Ser Ser
245
<210> 192
<211> 467
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 192
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1. 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr Gly Ser Thr Ser Gly
100 105 110
Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr Lys Gly Glu Val Lys
115 120 125
Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser Leu Ser
130 135 140
Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser
145 150 155 160
Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly Val Ile
165 170 175
Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser Arg Leu
180 185 190
Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys Met Asn
195 200 205
Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys His Tyr
210 215 220
Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser
225 230 235 240
Val Thr Val Ser Ser Ala Ala Ala Ile Glu Val Met Tyr Pro Pro Pro
245 250 255
Tyr Leu Asp Asn Glu Lys Ser Asn Gly Thr Ile Ile His Val Lys Gly
260 265 270
Lys His Leu Cys Pro Ser Pro Leu Phe Pro Gly Pro Ser Lys Pro Phe
275 280 285
Trp Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr Ser Leu Leu
290 295 300
Val Thr Val Ala Phe Ile Ile Phe Trp Val Arg Ser Lys Arg Ser Arg
305 310 315 320
Leu Leu His Ser Asp Tyr Met Asn Met Thr Pro Arg Arg Pro Gly Pro
325 330 335
Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala
340 345 350
Tyr Arg Ser Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
355 360 365
Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
370 375 380
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
385 390 395 400
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
405 410 415
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
420 425 430
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
435 440 445
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
450 455 460
Pro Pro Arg
465
<210> 193
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 193
Gln Val Gln Leu Leu Glu Ser Gly Ala Glu Leu Val Arg Pro Gly Ser
1. 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ala Phe Ser Ser Tyr
20 25 30
Trp Met Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gln Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Asn Gly Lys Phe
50 55 60
Lys Gly Gln Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Gly Leu Thr Ser Glu Asp Ser Ala Val Tyr Ser Cys
85 90 95
Ala Arg Lys Thr Ile Ser Ser Val Val Asp Phe Tyr Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr
115
<210> 194
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 194
Glu Leu Val Leu Thr Gln Ser Pro Lys Phe Met Ser Thr Ser Val Gly
1. 5 10 15
Asp Arg Val Ser Val Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Pro Leu Ile
35 40 45
Tyr Ser Ala Thr Tyr Arg Asn Ser Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Thr Asn Val Gln Ser
65 70 75 80
Lys Asp Leu Ala Asp Tyr Phe Tyr Phe Cys Gln Tyr Asn Arg Tyr Pro
85 90 95
Tyr Thr Ser Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Arg Ser
100 105 110
<210> 195
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 195
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
115 120 125
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
130 135 140
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
145 150 155 160
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
165 170 175
Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
180 185 190
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
195 200 205
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
210 215 220
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
225 230 235 240
Ser Ser
<210> 196
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 196
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
130 135 140
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
145 150 155 160
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser
195 200 205
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
210 215 220
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 197
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 197
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
115 120 125
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
130 135 140
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
145 150 155 160
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
165 170 175
Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
180 185 190
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
195 200 205
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
210 215 220
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
225 230 235 240
Ser Ser
<210> 198
<211> 813
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 198
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaaattg tgatgaccca gtcacccgcc actcttagcc tttcacccgg tgagcgcgca
120
accctgtctt gcagagcctc ccaagacatc tcaaaatacc ttaattggta tcaacagaag
180
cccggacagg ctcctcgcct tctgatctac cacaccagcc ggctccattc tggaatccct
240
gccaggttca gcggtagcgg atctgggacc gactacaccc tcactatcag ctcactgcag
300
ccagaggact tcgctgtcta tttctgtcag caagggaaca ccctgcccta cacctttgga
360
cagggcacca agctcgagat taaaggtgga ggtggcagcg gaggaggtgg gtccggcggt
420
ggaggaagcc aggtccaact ccaagaaagc ggaccgggtc ttgtgaagcc atcagaaact
480
ctttcactga cttgtactgt gagcggagtg tctctccccg attacggggt gtcttggatc
540
agacagccac cggggaaggg tctggaatgg attggagtga tttggggctc tgagactact
600
tactaccaat catccctcaa gtcacgcgtc accatctcaa aggacaactc taagaatcag
660
gtgtcactga aactgtcatc tgtgaccgca gccgacaccg ccgtgtacta ttgcgctaag
720
cattactatt atggcgggag ctacgcaatg gattactggg gacagggtac tctggtcacc
780
gtgtccagcc accaccatca tcaccatcac cat
813
<210> 199
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 199
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
130 135 140
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
145 150 155 160
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser
195 200 205
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
210 215 220
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 200
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 200
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaaattg tgatgaccca gtcacccgcc actcttagcc tttcacccgg tgagcgcgca
120
accctgtctt gcagagcctc ccaagacatc tcaaaatacc ttaattggta tcaacagaag
180
cccggacagg ctcctcgcct tctgatctac cacaccagcc ggctccattc tggaatccct
240
gccaggttca gcggtagcgg atctgggacc gactacaccc tcactatcag ctcactgcag
300
ccagaggact tcgctgtcta tttctgtcag caagggaaca ccctgcccta cacctttgga
360
cagggcacca agctcgagat taaaggtgga ggtggcagcg gaggaggtgg gtccggcggt
420
ggaggaagcc aggtccaact ccaagaaagc ggaccgggtc ttgtgaagcc atcagaaact
480
ctttcactga cttgtactgt gagcggagtg tctctccccg attacggggt gtcttggatc
540
agacagccac cggggaaggg tctggaatgg attggagtga tttggggctc tgagactact
600
tactaccaat catccctcaa gtcacgcgtc accatctcaa aggacaactc taagaatcag
660
gtgtcactga aactgtcatc tgtgaccgca gccgacaccg ccgtgtacta ttgcgctaag
720
cattactatt atggcgggag ctacgcaatg gattactggg gacagggtac tctggtcacc
780
gtgtccagca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 201
<211> 271
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 201
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
130 135 140
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
145 150 155 160
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser
195 200 205
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
210 215 220
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Leu Val Thr Val Ser Ser His His His His His His His His
260 265 270
<210> 202
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 202
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1. 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr Gln Ser Pro Ala
130 135 140
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
145 150 155 160
Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly
180 185 190
Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln
210 215 220
Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu
225 230 235 240
Ile Lys
<210> 203
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 203
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val
35 40 45
Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr
65 70 75 80
Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys
85 90 95
Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met
145 150 155 160
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
165 170 175
Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser
195 200 205
Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
225 230 235 240
Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln
245 250 255
Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 204
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 204
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1. 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr Gln Ser Pro Ala
130 135 140
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
145 150 155 160
Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly
180 185 190
Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln
210 215 220
Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu
225 230 235 240
Ile Lys
<210> 205
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 205
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val
35 40 45
Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr
65 70 75 80
Gln Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys
85 90 95
Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met
145 150 155 160
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
165 170 175
Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser
195 200 205
Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
225 230 235 240
Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln
245 250 255
Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 206
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 206
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
115 120 125
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
130 135 140
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
145 150 155 160
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
165 170 175
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser
180 185 190
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
195 200 205
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
210 215 220
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser
245
<210> 207
<211> 491
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 207
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val
145 150 155 160
Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser
165 170 175
Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly
180 185 190
Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser
195 200 205
Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn
210 215 220
Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val
225 230 235 240
Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp
245 250 255
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 208
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 208
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
115 120 125
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
130 135 140
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
145 150 155 160
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
165 170 175
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser
180 185 190
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
195 200 205
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
210 215 220
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser
245
<210> 209
<211> 491
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 209
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val
145 150 155 160
Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser
165 170 175
Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly
180 185 190
Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln
195 200 205
Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn
210 215 220
Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val
225 230 235 240
Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp
245 250 255
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 210
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 210
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1. 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met
130 135 140
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
145 150 155 160
Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser
180 185 190
Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
210 215 220
Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln
225 230 235 240
Gly Thr Lys Leu Glu Ile Lys
245
<210> 211
<211> 491
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 211
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val
35 40 45
Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr
65 70 75 80
Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys
85 90 95
Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro
165 170 175
Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys
180 185 190
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
195 200 205
Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro
245 250 255
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 212
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 212
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1. 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met
130 135 140
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
145 150 155 160
Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser
180 185 190
Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
210 215 220
Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln
225 230 235 240
Gly Thr Lys Leu Glu Ile Lys
245
<210> 213
<211> 491
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 213
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val
35 40 45
Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr
65 70 75 80
Gln Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys
85 90 95
Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro
165 170 175
Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys
180 185 190
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
195 200 205
Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro
245 250 255
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 214
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 214
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
115 120 125
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
130 135 140
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
145 150 155 160
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
165 170 175
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys Ser
180 185 190
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
195 200 205
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
210 215 220
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser
245
<210> 215
<211> 491
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 215
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val
145 150 155 160
Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser
165 170 175
Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly
180 185 190
Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn
195 200 205
Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn
210 215 220
Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val
225 230 235 240
Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp
245 250 255
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 216
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 216
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1. 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met
130 135 140
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
145 150 155 160
Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser
180 185 190
Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
210 215 220
Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln
225 230 235 240
Gly Thr Lys Leu Glu Ile Lys
245
<210> 217
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 217
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
115 120 125
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
130 135 140
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
145 150 155 160
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
165 170 175
Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
180 185 190
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
195 200 205
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
210 215 220
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
225 230 235 240
Ser Ser
<210> 218
<211> 491
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 218
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val
35 40 45
Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr
65 70 75 80
Asn Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys
85 90 95
Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro
165 170 175
Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys
180 185 190
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
195 200 205
Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro
245 250 255
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 219
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 219
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1. 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr Gln Ser Pro Ala
130 135 140
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
145 150 155 160
Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly
180 185 190
Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln
210 215 220
Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu
225 230 235 240
Ile Lys
<210> 220
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 220
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
130 135 140
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
145 150 155 160
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys Ser
195 200 205
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
210 215 220
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 221
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 221
Asp Tyr Gly Val Ser
1. 5
<210> 222
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 222
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser
1. 5 10 15
<210> 223
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 223
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr
1. 5 10
<210> 224
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 224
Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn
1. 5 10
<210> 225
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 225
His Thr Ser Arg Leu His Ser
1. 5
<210> 226
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 226
Gln Gln Gly Asn Thr Leu Pro Tyr Thr
1. 5
<210> 227
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 227
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser
1. 5 10 15
<210> 228
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 228
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser
1. 5 10 15
<210> 229
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 229
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys Ser
1. 5 10 15
<210> 230
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 230
Gly Val Ser Leu Pro Asp Tyr Gly Val Ser
1. 5 10
<210> 231
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 231
Gly Tyr Thr Phe Thr Gly Tyr Tyr Met His
1. 5 10
<210> 232
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 232
Gly Tyr Ile Phe Thr Gly Tyr Tyr Ile His
1. 5 10
<210> 233
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 233
Gly Tyr Thr Phe Thr Asp Tyr Tyr Met His
1. 5 10
<210> 234
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 234
Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln
1. 5 10 15
Gly
<210> 235
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 235
Trp Ile Asn Pro Asn Ser Gly Asp Thr Asn Tyr Ala Gln Lys Phe Gln
1. 5 10 15
Gly
<210> 236
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 236
Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile
1. 5 10
<210> 237
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 237
Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn
1. 5 10
<210> 238
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 238
Arg Ala Ser Gln Ser Ile Ser Thr Tyr Leu Asn
1. 5 10
<210> 239
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 239
Ala Ala Phe Ser Leu Gln Ser
1. 5
<210> 240
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 240
Ala Ala Ser Ser Leu Gln Ser
1. 5
<210> 241
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 241
Gln Gln Gly Asp Ser Val Pro Leu Thr
1. 5
<210> 242
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 242
Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn
1. 5 10
<210> 243
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 243
Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe Lys
1. 5 10 15
Asp
<210> 244
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 244
Gly Asn Trp Asp Asp Tyr
1. 5
<210> 245
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 245
Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala
1. 5 10
<210> 246
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 246
Ser Gly Ser Thr Leu Gln Ser
1. 5
<210> 247
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 247
Gln Gln His Asn Lys Tyr Pro Tyr Thr
1. 5
<210> 248
<211> 1461
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 248
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc aactcgtcca aagcggagcg gaagtcaaga aacccggagc gagcgtgaaa
120
gtgtcctgca aagcctccgg ctacaccttt acgggctact acatgcactg ggtgcgccag
180
gcaccaggac agggtcttga atggatggga tggatcaacc ctaattcggg cggaactaac
240
tacgcacaga agttccaggg gagagtgact ctgactcggg atacctccat ctcaactgtc
300
tacatggaac tctcccgctt gcggtcagat gatacggcag tgtactactg cgcccgcgac
360
atgaatatcc tggctaccgt gccgttcgac atctggggac aggggactat ggttactgtc
420
tcatcgggcg gtggaggttc aggaggaggc ggctcgggag gcggaggttc ggacattcag
480
atgacccagt ccccatcctc tctgtcggcc agcgtcggag atagggtgac cattacctgt
540
cgggcctcgc aaagcatctc ctcgtacctc aactggtatc agcaaaagcc gggaaaggcg
600
cctaagctgc tgatctacgc cgcttcgagc ttgcaaagcg gggtgccatc cagattctcg
660
ggatcaggct caggaaccga cttcaccctg accgtgaaca gcctccagcc ggaggacttt
720
gccacttact actgccagca gggagactcc gtgccgctta ctttcggggg gggtacccgc
780
ctggagatca agaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
840
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
900
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
960
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1020
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1080
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1140
cgcagcgcag atgctccagc ctacaagcag gggcagaacc agctctacaa cgaactcaat
1200
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
1260
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
1320
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
1380
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
1440
atgcaggccc tgccgcctcg g
1461
<210> 249
<211> 487
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 249
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Leu Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Val Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
145 150 155 160
Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
165 170 175
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala
195 200 205
Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
210 215 220
Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu Gln Pro Glu Asp Phe
225 230 235 240
Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu Thr Phe Gly
245 250 255
Gly Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
260 265 270
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
275 280 285
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
290 295 300
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
305 310 315 320
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 250
<211> 264
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 250
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Leu Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Val Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
145 150 155 160
Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
165 170 175
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala
195 200 205
Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
210 215 220
Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu Gln Pro Glu Asp Phe
225 230 235 240
Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu Thr Phe Gly
245 250 255
Gly Gly Thr Arg Leu Glu Ile Lys
260
<210> 251
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 251
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Leu Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 252
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 252
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 253
<211> 1461
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 253
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtcc aactcgttca atccggcgca gaagtcaaga agccaggagc atcagtgaaa
120
gtgtcctgca aagcctcagg ctacatcttc acgggatact acatccactg ggtgcgccag
180
gctccgggcc agggccttga gtggatgggc tggatcaacc ctaactctgg gggaaccaac
240
tacgctcaga agttccaggg gagggtcact atgactcgcg atacctccat ctccactgcg
300
tacatggaac tctcgggact gagatccgac gatcctgccg tgtactactg cgcccgggac
360
atgaacatct tggcgaccgt gccgtttgac atttggggac agggcaccct cgtcactgtg
420
tcgagcggtg gaggaggctc ggggggtggc ggatcaggag ggggaggaag cgacatccag
480
ctgactcaga gcccatcgtc gttgtccgcg tcggtggggg atagagtgac cattacttgc
540
cgcgccagcc agagcatctc atcatatctg aattggtacc agcagaagcc cggaaaggcc
600
ccaaaactgc tgatctacgc tgcaagcagc ctccaatcgg gagtgccgtc acggttctcc
660
gggtccggtt cgggaactga ctttaccctg accgtgaatt cgctgcaacc ggaggatttc
720
gccacgtact actgtcagca aggagactcc gtgccgctga ccttcggtgg aggcaccaag
780
gtcgaaatca agaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
840
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
900
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
960
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1020
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1080
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1140
cgcagcgcag atgctccagc ctacaagcag gggcagaacc agctctacaa cgaactcaat
1200
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
1260
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
1320
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
1380
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
1440
atgcaggccc tgccgcctcg g
1461
<210> 254
<211> 487
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 254
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Ile Phe Thr Gly Tyr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Ser Gly Leu Arg Ser Asp Asp Pro
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
145 150 155 160
Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
165 170 175
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala
195 200 205
Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
210 215 220
Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu Gln Pro Glu Asp Phe
225 230 235 240
Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu Thr Phe Gly
245 250 255
Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
260 265 270
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
275 280 285
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
290 295 300
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
305 310 315 320
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 255
<211> 264
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 255
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Ile Phe Thr Gly Tyr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Ser Gly Leu Arg Ser Asp Asp Pro
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
145 150 155 160
Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
165 170 175
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala
195 200 205
Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
210 215 220
Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu Gln Pro Glu Asp Phe
225 230 235 240
Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu Thr Phe Gly
245 250 255
Gly Gly Thr Lys Val Glu Ile Lys
260
<210> 256
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 256
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Gly Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Gly Leu Arg Ser Asp Asp Pro Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 257
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 257
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 258
<211> 1467
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 258
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtcc aactccaaca gtcaggcgca gaagtgaaaa agagcggtgc atcggtgaaa
120
gtgtcatgca aagcctcggg ctacaccttc actgactact atatgcactg gctgcggcag
180
gcaccgggac agggacttga gtggatggga tggatcaacc cgaattcagg ggacactaac
240
tacgcgcaga agttccaggg gagagtgacc ctgacgaggg acacctcaat ttcgaccgtc
300
tacatggaat tgtcgcgcct gagatcggac gatactgctg tgtactactg tgcccgcgac
360
atgaacatcc tcgcgactgt gccttttgat atctggggac aggggactat ggtcaccgtt
420
tcctccgctt ccggtggcgg aggctcggga ggccgggcct ccggtggagg aggcagcgac
480
atccagatga ctcagagccc ttcctcgctg agcgcctcag tgggagatcg cgtgaccatc
540
acttgccggg ccagccagtc catttcgtcc tacctcaatt ggtaccagca gaagccggga
600
aaggcgccca agctcttgat ctacgctgcg agctccctgc aaagcggggt gccgagccga
660
ttctcgggtt ccggctcggg aaccgacttc actctgacca tctcatccct gcaaccagag
720
gactttgcca cctactactg ccaacaagga gattctgtcc cactgacgtt cggcggagga
780
accaaggtcg aaatcaagac cactacccca gcaccgaggc cacccacccc ggctcctacc
840
atcgcctccc agcctctgtc cctgcgtccg gaggcatgta gacccgcagc tggtggggcc
900
gtgcataccc ggggtcttga cttcgcctgc gatatctaca tttgggcccc tctggctggt
960
acttgcgggg tcctgctgct ttcactcgtg atcactcttt actgtaagcg cggtcggaag
1020
aagctgctgt acatctttaa gcaacccttc atgaggcctg tgcagactac tcaagaggag
1080
gacggctgtt catgccggtt cccagaggag gaggaaggcg gctgcgaact gcgcgtgaaa
1140
ttcagccgca gcgcagatgc tccagcctac aagcaggggc agaaccagct ctacaacgaa
1200
ctcaatcttg gtcggagaga ggagtacgac gtgctggaca agcggagagg acgggaccca
1260
gaaatgggcg ggaagccgcg cagaaagaat ccccaagagg gcctgtacaa cgagctccaa
1320
aaggataaga tggcagaagc ctatagcgag attggtatga aaggggaacg cagaagaggc
1380
aaaggccacg acggactgta ccagggactc agcaccgcca ccaaggacac ctatgacgct
1440
cttcacatgc aggccctgcc gcctcgg
1467
<210> 259
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 259
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Ser Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Asp Tyr Tyr Met His Trp Leu Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Asp Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Leu Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Val Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu
180 185 190
Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr
195 200 205
Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
225 230 235 240
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu Thr
245 250 255
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
325 330 335
<210> 260
<211> 266
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 260
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Ser Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Asp Tyr Tyr Met His Trp Leu Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Asp Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Leu Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Val Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu
180 185 190
Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr
195 200 205
Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
225 230 235 240
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu Thr
245 250 255
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
260 265
<210> 261
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 261
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val Lys Lys Ser Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Leu Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Asp Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Leu Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 262
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 262
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 263
<211> 1461
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 263
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtcc aactcgtcca gtcaggagcg gaagtcaaga agcccggagc gtcagtcaaa
120
gtgtcatgca aagcctcggg ctacactttc actgggtact acatgcactg ggtgcgccag
180
gctccaggac agggactgga atggatggga tggatcaacc cgaactccgg tggcaccaat
240
tacgcccaga agttccaggg gagggtgacc atgactcgcg acacgtcgat cagcaccgca
300
tacatggagc tgtcaagact ccggtccgac gatactgccg tgtactactg cgcacgggac
360
atgaacattc tggccaccgt gccttttgac atctggggtc agggaactat ggttaccgtg
420
tcctctggtg gaggcggctc cggcgggggg ggaagcggag gcggtggaag cgacattcag
480
atgacccagt cgccttcatc cctttcggcg agcgtgggag atcgcgtcac tatcacttgt
540
cgggcctcgc agtccatctc cacctacctc aattggtacc agcagaagcc aggaaaagca
600
ccgaatctgc tgatctacgc cgcgttttcc ttgcaatcgg gagtgccaag cagattcagc
660
ggatcgggat caggcactga tttcaccctc accatcaact cgctgcaacc ggaggatttc
720
gctacgtact attgccaaca aggagacagc gtgccgctca ccttcggcgg agggactaag
780
ctggaaatca agaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
840
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
900
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
960
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1020
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1080
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1140
cgcagcgcag atgctccagc ctacaagcag gggcagaacc agctctacaa cgaactcaat
1200
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
1260
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
1320
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
1380
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
1440
atgcaggccc tgccgcctcg g
1461
<210> 264
<211> 487
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 264
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
145 150 155 160
Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
165 170 175
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Thr Tyr Leu Asn Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile Tyr Ala Ala
195 200 205
Phe Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
210 215 220
Gly Thr Asp Phe Thr Leu Thr Ile Asn Ser Leu Gln Pro Glu Asp Phe
225 230 235 240
Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu Thr Phe Gly
245 250 255
Gly Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
260 265 270
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
275 280 285
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
290 295 300
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
305 310 315 320
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 265
<211> 264
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 265
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
145 150 155 160
Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
165 170 175
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Thr Tyr Leu Asn Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile Tyr Ala Ala
195 200 205
Phe Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
210 215 220
Gly Thr Asp Phe Thr Leu Thr Ile Asn Ser Leu Gln Pro Glu Asp Phe
225 230 235 240
Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu Thr Phe Gly
245 250 255
Gly Gly Thr Lys Leu Glu Ile Lys
260
<210> 266
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 266
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 267
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 267
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Thr Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile
35 40 45
Tyr Ala Ala Phe Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 268
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 268
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc agctggtcca gtcgggagcc gaagtcaaga agcccggcgc tagcgtgaaa
120
gtgtcctgca aagcctccgg gtacacattc acctcctact ggatgaattg ggtcagacag
180
gcgcccggcc agggactcga gtggatggga aggattgatc cttacgactc cgaaacccat
240
tacaaccaga agttcaagga ccgcgtgacc atgactgtgg ataagtccac ttccaccgct
300
tacatggagc tgtccagcct gcgctccgag gataccgcag tgtactactg cgcccgggga
360
aactgggacg actattgggg acagggaact accgtgaccg tgtcaagcgg gggtggcggt
420
agcggaggag ggggctccgg cggcggcggc tcagggggcg gaggaagcga cgtgcagctc
480
acccagtcgc cctcatttct gtcggcctca gtgggagaca gagtgaccat tacttgtcgg
540
gcctccaaga gcatctccaa ggacctggcc tggtatcagc agaagccagg aaaggcgcct
600
aagttgctca tctactcggg gtcgaccctg caatctggcg tgccgtcccg gttctccggt
660
tcgggaagcg gtaccgaatt cacccttact atctcctccc tgcaaccgga ggacttcgcc
720
acctactact gccaacagca caacaagtac ccgtacactt tcgggggtgg cacgaaggtc
780
gaaatcaaga ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 269
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 269
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Val Thr Met Thr Val Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Gln Leu
145 150 155 160
Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly Asp Arg Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
225 230 235 240
Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 270
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 270
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Val Thr Met Thr Val Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Gln Leu
145 150 155 160
Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly Asp Arg Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
225 230 235 240
Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys
260
<210> 271
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 271
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 272
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 272
Asp Val Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 273
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 273
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc agctggtcca gtcgggagcc gaagtcaaga agcccggcgc tagcgtgaaa
120
gtgtcctgca aagcctccgg gtacacattc acctcctact ggatgaattg ggtcagacag
180
gcgcccggcc agggactcga gtggatggga aggattgatc cttacgactc cgaaacccat
240
tacaaccaga agttcaagga ccgcgtgacc atgactgtgg ataagtccac ttccaccgct
300
tacatggagc tgtccagcct gcgctccgag gataccgcag tgtactactg cgcccgggga
360
aactgggacg actattgggg acagggaact accgtgaccg tgtcaagcgg gggtggcggt
420
agcggaggag ggggctccgg cggcggcggc tcagggggcg gaggaagcga agtggtgctg
480
acccagtcgc ccgcaaccct ctctctgtcg ccgggagaac gcgccactct ttcctgtcgg
540
gcgtccaaga gcatctcaaa ggacctcgcc tggtaccagc agaagcctgg tcaagccccg
600
cggctgctga tctactccgg ctccacgctg caatcaggaa tcccagccag attttccggt
660
tcggggtcgg ggactgactt caccttgacc attagctcgc tggaacctga ggacttcgcc
720
gtgtattact gccagcagca caacaagtac ccgtacacct tcggaggcgg tactaaggtc
780
gagatcaaga ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 274
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 274
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Val Thr Met Thr Val Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Val Leu
145 150 155 160
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
165 170 175
Leu Ser Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp Phe Ala
225 230 235 240
Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 275
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 275
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Val Thr Met Thr Val Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Val Leu
145 150 155 160
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
165 170 175
Leu Ser Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp Phe Ala
225 230 235 240
Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys
260
<210> 276
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 276
Glu Val Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Ser Gly Ser Thr Leu Gln Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 277
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 277
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc agctggtcca gtcgggagcc gaagtcaaga agcccggcgc tagcgtgaaa
120
gtgtcctgca aagcctccgg gtacacattc acctcctact ggatgaattg ggtcagacag
180
gcgcccggcc agggactcga gtggatggga aggattgatc cttacgactc cgaaacccat
240
tacaaccaga agttcaagga ccgcgtgacc atgactgtgg ataagtccac ttccaccgct
300
tacatggagc tgtccagcct gcgctccgag gataccgcag tgtactactg cgcccgggga
360
aactgggacg actattgggg acagggaact accgtgaccg tgtcaagcgg gggtggcggt
420
agcggaggag ggggctccgg cggcggcggc tcagggggcg gaggaagcga cgtcgtgatg
480
acccagtcac cggcattcct gtccgtgact cccggagaaa aggtcacgat tacttgccgg
540
gcgtccaaga gcatctccaa ggacctcgcc tggtaccaac agaagccgga ccaggcccct
600
aagctgttga tctactcggg gtccaccctt caatcgggag tgccatcgcg gtttagcggt
660
tcgggttctg ggaccgactt cactttcacc atctcctcac tggaagccga ggatgccgcc
720
acttactact gtcagcagca caacaagtat ccgtacacct tcggaggcgg taccaaagtg
780
gagatcaaga ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 278
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 278
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Val Thr Met Thr Val Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met
145 150 155 160
Thr Gln Ser Pro Ala Phe Leu Ser Val Thr Pro Gly Glu Lys Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Asp Gln Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Glu Ala Glu Asp Ala Ala
225 230 235 240
Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 279
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 279
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Val Thr Met Thr Val Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met
145 150 155 160
Thr Gln Ser Pro Ala Phe Leu Ser Val Thr Pro Gly Glu Lys Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Asp Gln Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Glu Ala Glu Asp Ala Ala
225 230 235 240
Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys
260
<210> 280
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 280
Asp Val Val Met Thr Gln Ser Pro Ala Phe Leu Ser Val Thr Pro Gly
1. 5 10 15
Glu Lys Val Thr Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Asp Gln Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Glu Ala
65 70 75 80
Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 281
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 281
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc agctggtcca gtcgggagcc gaagtcaaga agcccggcgc tagcgtgaaa
120
gtgtcctgca aagcctccgg gtacacattc acctcctact ggatgaattg ggtcagacag
180
gcgcccggcc agggactcga gtggatggga aggattgatc cttacgactc cgaaacccat
240
tacaaccaga agttcaagga ccgcgtgacc atgactgtgg ataagtccac ttccaccgct
300
tacatggagc tgtccagcct gcgctccgag gataccgcag tgtactactg cgcccgggga
360
aactgggacg actattgggg acagggaact accgtgaccg tgtcaagcgg gggtggcggt
420
agcggaggag ggggctccgg cggcggcggc tcagggggcg gaggaagcga cgtggtcatg
480
actcagtccc cggactcact cgcggtgtcg cttggagaga gagcgaccat caactgtcgg
540
gcctcaaaga gcatcagcaa ggacctggcc tggtaccagc agaagccggg acagccgcca
600
aagctgctga tctactccgg gtccaccttg caatctggtg tccctgaccg gttctccggt
660
tccgggtcgg gtaccgactt cacgctcact atttcgtcgc tgcaagccga agatgtggcc
720
gtgtactatt gccaacagca caacaagtac ccctacactt ttggcggagg caccaaggtg
780
gaaatcaaga ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 282
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 282
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Val Thr Met Thr Val Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met
145 150 155 160
Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly Glu Arg Ala Thr
165 170 175
Ile Asn Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala
225 230 235 240
Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 283
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 283
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Val Thr Met Thr Val Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met
145 150 155 160
Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly Glu Arg Ala Thr
165 170 175
Ile Asn Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala
225 230 235 240
Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys
260
<210> 284
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 284
Asp Val Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1. 5 10 15
Glu Arg Ala Thr Ile Asn Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala
65 70 75 80
Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 285
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 285
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgacgtgc agctcaccca gtcgccctca tttctgtcgg cctcagtggg agacagagtg
120
accattactt gtcgggcctc caagagcatc tccaaggacc tggcctggta tcagcagaag
180
ccaggaaagg cgcctaagtt gctcatctac tcggggtcga ccctgcaatc tggcgtgccg
240
tcccggttct ccggttcggg aagcggtacc gaattcaccc ttactatctc ctccctgcaa
300
ccggaggact tcgccaccta ctactgccaa cagcacaaca agtacccgta cactttcggg
360
ggtggcacga aggtcgaaat caaggggggt ggcggtagcg gaggaggggg ctccggcggc
420
ggcggctcag ggggcggagg aagccaagtg cagctggtcc agtcgggagc cgaagtcaag
480
aagcccggcg ctagcgtgaa agtgtcctgc aaagcctccg ggtacacatt cacctcctac
540
tggatgaatt gggtcagaca ggcgcccggc cagggactcg agtggatggg aaggattgat
600
ccttacgact ccgaaaccca ttacaaccag aagttcaagg accgcgtgac catgactgtg
660
gataagtcca cttccaccgc ttacatggag ctgtccagcc tgcgctccga ggataccgca
720
gtgtactact gcgcccgggg aaactgggac gactattggg gacagggaac taccgtgacc
780
gtgtcaagca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 286
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 286
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Gln Leu Thr Gln Ser Pro Ser Phe Leu
20 25 30
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
145 150 155 160
Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Val Thr Met Thr Val Asp Lys Ser Thr
210 215 220
Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 287
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 287
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Gln Leu Thr Gln Ser Pro Ser Phe Leu
20 25 30
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
145 150 155 160
Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Val Thr Met Thr Val Asp Lys Ser Thr
210 215 220
Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser
260
<210> 288
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 288
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgg tgctgaccca gtcgcccgca accctctctc tgtcgccggg agaacgcgcc
120
actctttcct gtcgggcgtc caagagcatc tcaaaggacc tcgcctggta ccagcagaag
180
cctggtcaag ccccgcggct gctgatctac tccggctcca cgctgcaatc aggaatccca
240
gccagatttt ccggttcggg gtcggggact gacttcacct tgaccattag ctcgctggaa
300
cctgaggact tcgccgtgta ttactgccag cagcacaaca agtacccgta caccttcgga
360
ggcggtacta aggtcgagat caaggggggt ggcggtagcg gaggaggggg ctccggcggc
420
ggcggctcag ggggcggagg aagccaagtg cagctggtcc agtcgggagc cgaagtcaag
480
aagcccggcg ctagcgtgaa agtgtcctgc aaagcctccg ggtacacatt cacctcctac
540
tggatgaatt gggtcagaca ggcgcccggc cagggactcg agtggatggg aaggattgat
600
ccttacgact ccgaaaccca ttacaaccag aagttcaagg accgcgtgac catgactgtg
660
gataagtcca cttccaccgc ttacatggag ctgtccagcc tgcgctccga ggataccgca
720
gtgtactact gcgcccgggg aaactgggac gactattggg gacagggaac taccgtgacc
780
gtgtcaagca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 289
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 289
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Val Leu Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
145 150 155 160
Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Val Thr Met Thr Val Asp Lys Ser Thr
210 215 220
Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 290
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 290
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Val Leu Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
145 150 155 160
Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Val Thr Met Thr Val Asp Lys Ser Thr
210 215 220
Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser
260
<210> 291
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 291
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgacgtcg tgatgaccca gtcaccggca ttcctgtccg tgactcccgg agaaaaggtc
120
acgattactt gccgggcgtc caagagcatc tccaaggacc tcgcctggta ccaacagaag
180
ccggaccagg cccctaagct gttgatctac tcggggtcca cccttcaatc gggagtgcca
240
tcgcggttta gcggttcggg ttctgggacc gacttcactt tcaccatctc ctcactggaa
300
gccgaggatg ccgccactta ctactgtcag cagcacaaca agtatccgta caccttcgga
360
ggcggtacca aagtggagat caaggggggt ggcggtagcg gaggaggggg ctccggcggc
420
ggcggctcag ggggcggagg aagccaagtg cagctggtcc agtcgggagc cgaagtcaag
480
aagcccggcg ctagcgtgaa agtgtcctgc aaagcctccg ggtacacatt cacctcctac
540
tggatgaatt gggtcagaca ggcgcccggc cagggactcg agtggatggg aaggattgat
600
ccttacgact ccgaaaccca ttacaaccag aagttcaagg accgcgtgac catgactgtg
660
gataagtcca cttccaccgc ttacatggag ctgtccagcc tgcgctccga ggataccgca
720
gtgtactact gcgcccgggg aaactgggac gactattggg gacagggaac taccgtgacc
780
gtgtcaagca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 292
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 292
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Ala Phe Leu
20 25 30
Ser Val Thr Pro Gly Glu Lys Val Thr Ile Thr Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Asp Gln Ala
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile
85 90 95
Ser Ser Leu Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
145 150 155 160
Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Val Thr Met Thr Val Asp Lys Ser Thr
210 215 220
Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 293
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 293
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Ala Phe Leu
20 25 30
Ser Val Thr Pro Gly Glu Lys Val Thr Ile Thr Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Asp Gln Ala
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile
85 90 95
Ser Ser Leu Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
145 150 155 160
Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Val Thr Met Thr Val Asp Lys Ser Thr
210 215 220
Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser
260
<210> 294
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 294
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgacgtgg tcatgactca gtccccggac tcactcgcgg tgtcgcttgg agagagagcg
120
accatcaact gtcgggcctc aaagagcatc agcaaggacc tggcctggta ccagcagaag
180
ccgggacagc cgccaaagct gctgatctac tccgggtcca ccttgcaatc tggtgtccct
240
gaccggttct ccggttccgg gtcgggtacc gacttcacgc tcactatttc gtcgctgcaa
300
gccgaagatg tggccgtgta ctattgccaa cagcacaaca agtaccccta cacttttggc
360
ggaggcacca aggtggaaat caaggggggt ggcggtagcg gaggaggggg ctccggcggc
420
ggcggctcag ggggcggagg aagccaagtg cagctggtcc agtcgggagc cgaagtcaag
480
aagcccggcg ctagcgtgaa agtgtcctgc aaagcctccg ggtacacatt cacctcctac
540
tggatgaatt gggtcagaca ggcgcccggc cagggactcg agtggatggg aaggattgat
600
ccttacgact ccgaaaccca ttacaaccag aagttcaagg accgcgtgac catgactgtg
660
gataagtcca cttccaccgc ttacatggag ctgtccagcc tgcgctccga ggataccgca
720
gtgtactact gcgcccgggg aaactgggac gactattggg gacagggaac taccgtgacc
780
gtgtcaagca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 295
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 295
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Asp Ser Leu
20 25 30
Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
145 150 155 160
Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Val Thr Met Thr Val Asp Lys Ser Thr
210 215 220
Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 296
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 296
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Asp Ser Leu
20 25 30
Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
145 150 155 160
Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Val Thr Met Thr Val Asp Lys Ser Thr
210 215 220
Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser
260
<210> 297
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 297
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc agctggtgca gtcaggcagc gaactgaaga agcccggagc ctccgtcaaa
120
gtgtcctgca aagcctcggg atacaccttc acctcctact ggatgaactg ggtccgccag
180
gcacctggac aggggctgga gtggatggga aggatcgatc cctacgattc cgaaacccat
240
tacaatcaga agttcaagga ccggtttgtg ttctccgtgg acaagtccgt gtccaccgcc
300
tacctccaaa ttagcagcct gaaggcggag gatacagctg tctactactg cgctcgcgga
360
aactgggatg actattgggg ccagggaact accgtgactg tgtcctccgg gggtggcggt
420
agcggaggag ggggctccgg cggcggcggc tcagggggcg gaggaagcga cgtgcagctc
480
acccagtcgc cctcatttct gtcggcctca gtgggagaca gagtgaccat tacttgtcgg
540
gcctccaaga gcatctccaa ggacctggcc tggtatcagc agaagccagg aaaggcgcct
600
aagttgctca tctactcggg gtcgaccctg caatctggcg tgccgtcccg gttctccggt
660
tcgggaagcg gtaccgaatt cacccttact atctcctccc tgcaaccgga ggacttcgcc
720
acctactact gccaacagca caacaagtac ccgtacactt tcgggggtgg cacgaaggtc
780
gaaatcaaga ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 298
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 298
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Phe Val Phe Ser Val Asp Lys Ser
85 90 95
Val Ser Thr Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Gln Leu
145 150 155 160
Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly Asp Arg Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
225 230 235 240
Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 299
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 299
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Phe Val Phe Ser Val Asp Lys Ser
85 90 95
Val Ser Thr Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Gln Leu
145 150 155 160
Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly Asp Arg Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
225 230 235 240
Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys
260
<210> 300
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 300
Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Phe Val Phe Ser Val Asp Lys Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 301
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 301
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc agctggtgca gtcaggcagc gaactgaaga agcccggagc ctccgtcaaa
120
gtgtcctgca aagcctcggg atacaccttc acctcctact ggatgaactg ggtccgccag
180
gcacctggac aggggctgga gtggatggga aggatcgatc cctacgattc cgaaacccat
240
tacaatcaga agttcaagga ccggtttgtg ttctccgtgg acaagtccgt gtccaccgcc
300
tacctccaaa ttagcagcct gaaggcggag gatacagctg tctactactg cgctcgcgga
360
aactgggatg actattgggg ccagggaact accgtgactg tgtcctccgg gggtggcggt
420
agcggaggag ggggctccgg cggcggcggc tcagggggcg gaggaagcga agtggtgctg
480
acccagtcgc ccgcaaccct ctctctgtcg ccgggagaac gcgccactct ttcctgtcgg
540
gcgtccaaga gcatctcaaa ggacctcgcc tggtaccagc agaagcctgg tcaagccccg
600
cggctgctga tctactccgg ctccacgctg caatcaggaa tcccagccag attttccggt
660
tcggggtcgg ggactgactt caccttgacc attagctcgc tggaacctga ggacttcgcc
720
gtgtattact gccagcagca caacaagtac ccgtacacct tcggaggcgg tactaaggtc
780
gagatcaaga ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 302
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 302
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Phe Val Phe Ser Val Asp Lys Ser
85 90 95
Val Ser Thr Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Val Leu
145 150 155 160
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
165 170 175
Leu Ser Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp Phe Ala
225 230 235 240
Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 303
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 303
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Phe Val Phe Ser Val Asp Lys Ser
85 90 95
Val Ser Thr Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Val Leu
145 150 155 160
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
165 170 175
Leu Ser Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp Phe Ala
225 230 235 240
Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys
260
<210> 304
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 304
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc agctggtgca gtcaggcagc gaactgaaga agcccggagc ctccgtcaaa
120
gtgtcctgca aagcctcggg atacaccttc acctcctact ggatgaactg ggtccgccag
180
gcacctggac aggggctgga gtggatggga aggatcgatc cctacgattc cgaaacccat
240
tacaatcaga agttcaagga ccggtttgtg ttctccgtgg acaagtccgt gtccaccgcc
300
tacctccaaa ttagcagcct gaaggcggag gatacagctg tctactactg cgctcgcgga
360
aactgggatg actattgggg ccagggaact accgtgactg tgtcctccgg gggtggcggt
420
agcggaggag ggggctccgg cggcggcggc tcagggggcg gaggaagcga cgtcgtgatg
480
acccagtcac cggcattcct gtccgtgact cccggagaaa aggtcacgat tacttgccgg
540
gcgtccaaga gcatctccaa ggacctcgcc tggtaccaac agaagccgga ccaggcccct
600
aagctgttga tctactcggg gtccaccctt caatcgggag tgccatcgcg gtttagcggt
660
tcgggttctg ggaccgactt cactttcacc atctcctcac tggaagccga ggatgccgcc
720
acttactact gtcagcagca caacaagtat ccgtacacct tcggaggcgg taccaaagtg
780
gagatcaaga ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 305
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 305
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Phe Val Phe Ser Val Asp Lys Ser
85 90 95
Val Ser Thr Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met
145 150 155 160
Thr Gln Ser Pro Ala Phe Leu Ser Val Thr Pro Gly Glu Lys Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Asp Gln Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Glu Ala Glu Asp Ala Ala
225 230 235 240
Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 306
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 306
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Phe Val Phe Ser Val Asp Lys Ser
85 90 95
Val Ser Thr Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met
145 150 155 160
Thr Gln Ser Pro Ala Phe Leu Ser Val Thr Pro Gly Glu Lys Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Asp Gln Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Glu Ala Glu Asp Ala Ala
225 230 235 240
Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys
260
<210> 307
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 307
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc agctggtgca gtcaggcagc gaactgaaga agcccggagc ctccgtcaaa
120
gtgtcctgca aagcctcggg atacaccttc acctcctact ggatgaactg ggtccgccag
180
gcacctggac aggggctgga gtggatggga aggatcgatc cctacgattc cgaaacccat
240
tacaatcaga agttcaagga ccggtttgtg ttctccgtgg acaagtccgt gtccaccgcc
300
tacctccaaa ttagcagcct gaaggcggag gatacagctg tctactactg cgctcgcgga
360
aactgggatg actattgggg ccagggaact accgtgactg tgtcctccgg gggtggcggt
420
agcggaggag ggggctccgg cggcggcggc tcagggggcg gaggaagcga cgtggtcatg
480
actcagtccc cggactcact cgcggtgtcg cttggagaga gagcgaccat caactgtcgg
540
gcctcaaaga gcatcagcaa ggacctggcc tggtaccagc agaagccggg acagccgcca
600
aagctgctga tctactccgg gtccaccttg caatctggtg tccctgaccg gttctccggt
660
tccgggtcgg gtaccgactt cacgctcact atttcgtcgc tgcaagccga agatgtggcc
720
gtgtactatt gccaacagca caacaagtac ccctacactt ttggcggagg caccaaggtg
780
gaaatcaaga ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 308
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 308
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Phe Val Phe Ser Val Asp Lys Ser
85 90 95
Val Ser Thr Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met
145 150 155 160
Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly Glu Arg Ala Thr
165 170 175
Ile Asn Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala
225 230 235 240
Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 309
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 309
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Phe Val Phe Ser Val Asp Lys Ser
85 90 95
Val Ser Thr Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met
145 150 155 160
Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly Glu Arg Ala Thr
165 170 175
Ile Asn Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala
225 230 235 240
Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys
260
<210> 310
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 310
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgacgtgc agctcaccca gtcgccctca tttctgtcgg cctcagtggg agacagagtg
120
accattactt gtcgggcctc caagagcatc tccaaggacc tggcctggta tcagcagaag
180
ccaggaaagg cgcctaagtt gctcatctac tcggggtcga ccctgcaatc tggcgtgccg
240
tcccggttct ccggttcggg aagcggtacc gaattcaccc ttactatctc ctccctgcaa
300
ccggaggact tcgccaccta ctactgccaa cagcacaaca agtacccgta cactttcggg
360
ggtggcacga aggtcgaaat caaggggggt ggcggtagcg gaggaggggg ctccggcggc
420
ggcggctcag ggggcggagg aagccaagtg cagctggtgc agtcaggcag cgaactgaag
480
aagcccggag cctccgtcaa agtgtcctgc aaagcctcgg gatacacctt cacctcctac
540
tggatgaact gggtccgcca ggcacctgga caggggctgg agtggatggg aaggatcgat
600
ccctacgatt ccgaaaccca ttacaatcag aagttcaagg accggtttgt gttctccgtg
660
gacaagtccg tgtccaccgc ctacctccaa attagcagcc tgaaggcgga ggatacagct
720
gtctactact gcgctcgcgg aaactgggat gactattggg gccagggaac taccgtgact
780
gtgtcctcca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 311
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 311
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Gln Leu Thr Gln Ser Pro Ser Phe Leu
20 25 30
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu Lys
145 150 155 160
Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Phe Val Phe Ser Val Asp Lys Ser Val
210 215 220
Ser Thr Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 312
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 312
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Gln Leu Thr Gln Ser Pro Ser Phe Leu
20 25 30
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu Lys
145 150 155 160
Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Phe Val Phe Ser Val Asp Lys Ser Val
210 215 220
Ser Thr Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser
260
<210> 313
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 313
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgg tgctgaccca gtcgcccgca accctctctc tgtcgccggg agaacgcgcc
120
actctttcct gtcgggcgtc caagagcatc tcaaaggacc tcgcctggta ccagcagaag
180
cctggtcaag ccccgcggct gctgatctac tccggctcca cgctgcaatc aggaatccca
240
gccagatttt ccggttcggg gtcggggact gacttcacct tgaccattag ctcgctggaa
300
cctgaggact tcgccgtgta ttactgccag cagcacaaca agtacccgta caccttcgga
360
ggcggtacta aggtcgagat caaggggggt ggcggtagcg gaggaggggg ctccggcggc
420
ggcggctcag ggggcggagg aagccaagtg cagctggtgc agtcaggcag cgaactgaag
480
aagcccggag cctccgtcaa agtgtcctgc aaagcctcgg gatacacctt cacctcctac
540
tggatgaact gggtccgcca ggcacctgga caggggctgg agtggatggg aaggatcgat
600
ccctacgatt ccgaaaccca ttacaatcag aagttcaagg accggtttgt gttctccgtg
660
gacaagtccg tgtccaccgc ctacctccaa attagcagcc tgaaggcgga ggatacagct
720
gtctactact gcgctcgcgg aaactgggat gactattggg gccagggaac taccgtgact
780
gtgtcctcca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 314
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 314
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Val Leu Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu Lys
145 150 155 160
Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Phe Val Phe Ser Val Asp Lys Ser Val
210 215 220
Ser Thr Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 315
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 315
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Val Leu Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu Lys
145 150 155 160
Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Phe Val Phe Ser Val Asp Lys Ser Val
210 215 220
Ser Thr Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser
260
<210> 316
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 316
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgacgtcg tgatgaccca gtcaccggca ttcctgtccg tgactcccgg agaaaaggtc
120
acgattactt gccgggcgtc caagagcatc tccaaggacc tcgcctggta ccaacagaag
180
ccggaccagg cccctaagct gttgatctac tcggggtcca cccttcaatc gggagtgcca
240
tcgcggttta gcggttcggg ttctgggacc gacttcactt tcaccatctc ctcactggaa
300
gccgaggatg ccgccactta ctactgtcag cagcacaaca agtatccgta caccttcgga
360
ggcggtacca aagtggagat caaggggggt ggcggtagcg gaggaggggg ctccggcggc
420
ggcggctcag ggggcggagg aagccaagtg cagctggtgc agtcaggcag cgaactgaag
480
aagcccggag cctccgtcaa agtgtcctgc aaagcctcgg gatacacctt cacctcctac
540
tggatgaact gggtccgcca ggcacctgga caggggctgg agtggatggg aaggatcgat
600
ccctacgatt ccgaaaccca ttacaatcag aagttcaagg accggtttgt gttctccgtg
660
gacaagtccg tgtccaccgc ctacctccaa attagcagcc tgaaggcgga ggatacagct
720
gtctactact gcgctcgcgg aaactgggat gactattggg gccagggaac taccgtgact
780
gtgtcctcca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 317
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 317
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Ala Phe Leu
20 25 30
Ser Val Thr Pro Gly Glu Lys Val Thr Ile Thr Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Asp Gln Ala
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile
85 90 95
Ser Ser Leu Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu Lys
145 150 155 160
Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Phe Val Phe Ser Val Asp Lys Ser Val
210 215 220
Ser Thr Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 318
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 318
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Ala Phe Leu
20 25 30
Ser Val Thr Pro Gly Glu Lys Val Thr Ile Thr Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Asp Gln Ala
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile
85 90 95
Ser Ser Leu Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu Lys
145 150 155 160
Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Phe Val Phe Ser Val Asp Lys Ser Val
210 215 220
Ser Thr Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser
260
<210> 319
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 319
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgacgtgg tcatgactca gtccccggac tcactcgcgg tgtcgcttgg agagagagcg
120
accatcaact gtcgggcctc aaagagcatc agcaaggacc tggcctggta ccagcagaag
180
ccgggacagc cgccaaagct gctgatctac tccgggtcca ccttgcaatc tggtgtccct
240
gaccggttct ccggttccgg gtcgggtacc gacttcacgc tcactatttc gtcgctgcaa
300
gccgaagatg tggccgtgta ctattgccaa cagcacaaca agtaccccta cacttttggc
360
ggaggcacca aggtggaaat caaggggggt ggcggtagcg gaggaggggg ctccggcggc
420
ggcggctcag ggggcggagg aagccaagtg cagctggtgc agtcaggcag cgaactgaag
480
aagcccggag cctccgtcaa agtgtcctgc aaagcctcgg gatacacctt cacctcctac
540
tggatgaact gggtccgcca ggcacctgga caggggctgg agtggatggg aaggatcgat
600
ccctacgatt ccgaaaccca ttacaatcag aagttcaagg accggtttgt gttctccgtg
660
gacaagtccg tgtccaccgc ctacctccaa attagcagcc tgaaggcgga ggatacagct
720
gtctactact gcgctcgcgg aaactgggat gactattggg gccagggaac taccgtgact
780
gtgtcctcca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 320
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 320
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Asp Ser Leu
20 25 30
Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu Lys
145 150 155 160
Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Phe Val Phe Ser Val Asp Lys Ser Val
210 215 220
Ser Thr Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 321
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 321
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Asp Ser Leu
20 25 30
Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu Lys
145 150 155 160
Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Phe Val Phe Ser Val Asp Lys Ser Val
210 215 220
Ser Thr Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser
260
<210> 322
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 322
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaggtgc agctggtgca gagcggagcc gaggtcaaga agcctggaga atccctgagg
120
atcagctgca aaggcagcgg gtataccttc acctcctact ggatgaattg ggtccgccag
180
atgcccggaa aaggcctgga gtggatggga cggattgacc cctacgactc ggaaacccat
240
tacaaccaga agttcaagga tcacgtgacc atctccgtgg acaagtccat ttccactgcg
300
tacctccagt ggtcaagcct gaaggcctcc gacactgcta tgtactactg cgcacgcgga
360
aactgggatg attactgggg acagggaaca accgtgactg tgtcctccgg gggtggcggt
420
agcggaggag ggggctccgg cggcggcggc tcagggggcg gaggaagcga cgtgcagctc
480
acccagtcgc cctcatttct gtcggcctca gtgggagaca gagtgaccat tacttgtcgg
540
gcctccaaga gcatctccaa ggacctggcc tggtatcagc agaagccagg aaaggcgcct
600
aagttgctca tctactcggg gtcgaccctg caatctggcg tgccgtcccg gttctccggt
660
tcgggaagcg gtaccgaatt cacccttact atctcctccc tgcaaccgga ggacttcgcc
720
acctactact gccaacagca caacaagtac ccgtacactt tcgggggtgg cacgaaggtc
780
gaaatcaaga ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 323
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 323
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Met Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp His Val Thr Ile Ser Val Asp Lys Ser
85 90 95
Ile Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Gln Leu
145 150 155 160
Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly Asp Arg Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
225 230 235 240
Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 324
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 324
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Met Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp His Val Thr Ile Ser Val Asp Lys Ser
85 90 95
Ile Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Gln Leu
145 150 155 160
Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly Asp Arg Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
225 230 235 240
Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys
260
<210> 325
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 325
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1. 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp His Val Thr Ile Ser Val Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 326
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 326
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaggtgc agctggtgca gagcggagcc gaggtcaaga agcctggaga atccctgagg
120
atcagctgca aaggcagcgg gtataccttc acctcctact ggatgaattg ggtccgccag
180
atgcccggaa aaggcctgga gtggatggga cggattgacc cctacgactc ggaaacccat
240
tacaaccaga agttcaagga tcacgtgacc atctccgtgg acaagtccat ttccactgcg
300
tacctccagt ggtcaagcct gaaggcctcc gacactgcta tgtactactg cgcacgcgga
360
aactgggatg attactgggg acagggaaca accgtgactg tgtcctccgg gggtggcggt
420
agcggaggag ggggctccgg cggcggcggc tcagggggcg gaggaagcga agtggtgctg
480
acccagtcgc ccgcaaccct ctctctgtcg ccgggagaac gcgccactct ttcctgtcgg
540
gcgtccaaga gcatctcaaa ggacctcgcc tggtaccagc agaagcctgg tcaagccccg
600
cggctgctga tctactccgg ctccacgctg caatcaggaa tcccagccag attttccggt
660
tcggggtcgg ggactgactt caccttgacc attagctcgc tggaacctga ggacttcgcc
720
gtgtattact gccagcagca caacaagtac ccgtacacct tcggaggcgg tactaaggtc
780
gagatcaaga ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 327
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 327
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Met Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp His Val Thr Ile Ser Val Asp Lys Ser
85 90 95
Ile Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Val Leu
145 150 155 160
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
165 170 175
Leu Ser Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp Phe Ala
225 230 235 240
Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 328
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 328
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Met Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp His Val Thr Ile Ser Val Asp Lys Ser
85 90 95
Ile Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Val Leu
145 150 155 160
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
165 170 175
Leu Ser Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp Phe Ala
225 230 235 240
Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys
260
<210> 329
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 329
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaggtgc agctggtgca gagcggagcc gaggtcaaga agcctggaga atccctgagg
120
atcagctgca aaggcagcgg gtataccttc acctcctact ggatgaattg ggtccgccag
180
atgcccggaa aaggcctgga gtggatggga cggattgacc cctacgactc ggaaacccat
240
tacaaccaga agttcaagga tcacgtgacc atctccgtgg acaagtccat ttccactgcg
300
tacctccagt ggtcaagcct gaaggcctcc gacactgcta tgtactactg cgcacgcgga
360
aactgggatg attactgggg acagggaaca accgtgactg tgtcctccgg gggtggcggt
420
agcggaggag ggggctccgg cggcggcggc tcagggggcg gaggaagcga cgtcgtgatg
480
acccagtcac cggcattcct gtccgtgact cccggagaaa aggtcacgat tacttgccgg
540
gcgtccaaga gcatctccaa ggacctcgcc tggtaccaac agaagccgga ccaggcccct
600
aagctgttga tctactcggg gtccaccctt caatcgggag tgccatcgcg gtttagcggt
660
tcgggttctg ggaccgactt cactttcacc atctcctcac tggaagccga ggatgccgcc
720
acttactact gtcagcagca caacaagtat ccgtacacct tcggaggcgg taccaaagtg
780
gagatcaaga ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 330
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 330
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Met Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp His Val Thr Ile Ser Val Asp Lys Ser
85 90 95
Ile Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met
145 150 155 160
Thr Gln Ser Pro Ala Phe Leu Ser Val Thr Pro Gly Glu Lys Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Asp Gln Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Glu Ala Glu Asp Ala Ala
225 230 235 240
Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 331
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 331
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Met Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp His Val Thr Ile Ser Val Asp Lys Ser
85 90 95
Ile Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met
145 150 155 160
Thr Gln Ser Pro Ala Phe Leu Ser Val Thr Pro Gly Glu Lys Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Asp Gln Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Glu Ala Glu Asp Ala Ala
225 230 235 240
Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys
260
<210> 332
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 332
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaggtgc agctggtgca gagcggagcc gaggtcaaga agcctggaga atccctgagg
120
atcagctgca aaggcagcgg gtataccttc acctcctact ggatgaattg ggtccgccag
180
atgcccggaa aaggcctgga gtggatggga cggattgacc cctacgactc ggaaacccat
240
tacaaccaga agttcaagga tcacgtgacc atctccgtgg acaagtccat ttccactgcg
300
tacctccagt ggtcaagcct gaaggcctcc gacactgcta tgtactactg cgcacgcgga
360
aactgggatg attactgggg acagggaaca accgtgactg tgtcctccgg gggtggcggt
420
agcggaggag ggggctccgg cggcggcggc tcagggggcg gaggaagcga cgtggtcatg
480
actcagtccc cggactcact cgcggtgtcg cttggagaga gagcgaccat caactgtcgg
540
gcctcaaaga gcatcagcaa ggacctggcc tggtaccagc agaagccggg acagccgcca
600
aagctgctga tctactccgg gtccaccttg caatctggtg tccctgaccg gttctccggt
660
tccgggtcgg gtaccgactt cacgctcact atttcgtcgc tgcaagccga agatgtggcc
720
gtgtactatt gccaacagca caacaagtac ccctacactt ttggcggagg caccaaggtg
780
gaaatcaaga ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 333
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 333
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Met Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp His Val Thr Ile Ser Val Asp Lys Ser
85 90 95
Ile Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met
145 150 155 160
Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly Glu Arg Ala Thr
165 170 175
Ile Asn Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala
225 230 235 240
Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 334
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 334
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Met Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp His Val Thr Ile Ser Val Asp Lys Ser
85 90 95
Ile Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met
145 150 155 160
Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly Glu Arg Ala Thr
165 170 175
Ile Asn Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala
225 230 235 240
Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys
260
<210> 335
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 335
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgacgtgc agctcaccca gtcgccctca tttctgtcgg cctcagtggg agacagagtg
120
accattactt gtcgggcctc caagagcatc tccaaggacc tggcctggta tcagcagaag
180
ccaggaaagg cgcctaagtt gctcatctac tcggggtcga ccctgcaatc tggcgtgccg
240
tcccggttct ccggttcggg aagcggtacc gaattcaccc ttactatctc ctccctgcaa
300
ccggaggact tcgccaccta ctactgccaa cagcacaaca agtacccgta cactttcggg
360
ggtggcacga aggtcgaaat caaggggggt ggcggtagcg gaggaggggg ctccggcggc
420
ggcggctcag ggggcggagg aagcgaggtg cagctggtgc agagcggagc cgaggtcaag
480
aagcctggag aatccctgag gatcagctgc aaaggcagcg ggtatacctt cacctcctac
540
tggatgaatt gggtccgcca gatgcccgga aaaggcctgg agtggatggg acggattgac
600
ccctacgact cggaaaccca ttacaaccag aagttcaagg atcacgtgac catctccgtg
660
gacaagtcca tttccactgc gtacctccag tggtcaagcc tgaaggcctc cgacactgct
720
atgtactact gcgcacgcgg aaactgggat gattactggg gacagggaac aaccgtgact
780
gtgtcctcca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 336
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 336
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Gln Leu Thr Gln Ser Pro Ser Phe Leu
20 25 30
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
145 150 155 160
Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Met Pro Gly Lys Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp His Val Thr Ile Ser Val Asp Lys Ser Ile
210 215 220
Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala
225 230 235 240
Met Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 337
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 337
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Gln Leu Thr Gln Ser Pro Ser Phe Leu
20 25 30
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
145 150 155 160
Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Met Pro Gly Lys Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp His Val Thr Ile Ser Val Asp Lys Ser Ile
210 215 220
Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala
225 230 235 240
Met Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser
260
<210> 338
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 338
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgg tgctgaccca gtcgcccgca accctctctc tgtcgccggg agaacgcgcc
120
actctttcct gtcgggcgtc caagagcatc tcaaaggacc tcgcctggta ccagcagaag
180
cctggtcaag ccccgcggct gctgatctac tccggctcca cgctgcaatc aggaatccca
240
gccagatttt ccggttcggg gtcggggact gacttcacct tgaccattag ctcgctggaa
300
cctgaggact tcgccgtgta ttactgccag cagcacaaca agtacccgta caccttcgga
360
ggcggtacta aggtcgagat caaggggggt ggcggtagcg gaggaggggg ctccggcggc
420
ggcggctcag ggggcggagg aagcgaggtg cagctggtgc agagcggagc cgaggtcaag
480
aagcctggag aatccctgag gatcagctgc aaaggcagcg ggtatacctt cacctcctac
540
tggatgaatt gggtccgcca gatgcccgga aaaggcctgg agtggatggg acggattgac
600
ccctacgact cggaaaccca ttacaaccag aagttcaagg atcacgtgac catctccgtg
660
gacaagtcca tttccactgc gtacctccag tggtcaagcc tgaaggcctc cgacactgct
720
atgtactact gcgcacgcgg aaactgggat gattactggg gacagggaac aaccgtgact
780
gtgtcctcca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 339
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 339
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Val Leu Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
145 150 155 160
Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Met Pro Gly Lys Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp His Val Thr Ile Ser Val Asp Lys Ser Ile
210 215 220
Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala
225 230 235 240
Met Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 340
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 340
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Val Leu Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
145 150 155 160
Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Met Pro Gly Lys Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp His Val Thr Ile Ser Val Asp Lys Ser Ile
210 215 220
Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala
225 230 235 240
Met Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser
260
<210> 341
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 341
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgacgtcg tgatgaccca gtcaccggca ttcctgtccg tgactcccgg agaaaaggtc
120
acgattactt gccgggcgtc caagagcatc tccaaggacc tcgcctggta ccaacagaag
180
ccggaccagg cccctaagct gttgatctac tcggggtcca cccttcaatc gggagtgcca
240
tcgcggttta gcggttcggg ttctgggacc gacttcactt tcaccatctc ctcactggaa
300
gccgaggatg ccgccactta ctactgtcag cagcacaaca agtatccgta caccttcgga
360
ggcggtacca aagtggagat caaggggggt ggcggtagcg gaggaggggg ctccggcggc
420
ggcggctcag ggggcggagg aagcgaggtg cagctggtgc agagcggagc cgaggtcaag
480
aagcctggag aatccctgag gatcagctgc aaaggcagcg ggtatacctt cacctcctac
540
tggatgaatt gggtccgcca gatgcccgga aaaggcctgg agtggatggg acggattgac
600
ccctacgact cggaaaccca ttacaaccag aagttcaagg atcacgtgac catctccgtg
660
gacaagtcca tttccactgc gtacctccag tggtcaagcc tgaaggcctc cgacactgct
720
atgtactact gcgcacgcgg aaactgggat gattactggg gacagggaac aaccgtgact
780
gtgtcctcca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 342
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 342
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Ala Phe Leu
20 25 30
Ser Val Thr Pro Gly Glu Lys Val Thr Ile Thr Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Asp Gln Ala
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile
85 90 95
Ser Ser Leu Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
145 150 155 160
Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Met Pro Gly Lys Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp His Val Thr Ile Ser Val Asp Lys Ser Ile
210 215 220
Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala
225 230 235 240
Met Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 343
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 343
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Ala Phe Leu
20 25 30
Ser Val Thr Pro Gly Glu Lys Val Thr Ile Thr Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Asp Gln Ala
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile
85 90 95
Ser Ser Leu Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
145 150 155 160
Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Met Pro Gly Lys Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp His Val Thr Ile Ser Val Asp Lys Ser Ile
210 215 220
Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala
225 230 235 240
Met Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser
260
<210> 344
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 344
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgacgtgg tcatgactca gtccccggac tcactcgcgg tgtcgcttgg agagagagcg
120
accatcaact gtcgggcctc aaagagcatc agcaaggacc tggcctggta ccagcagaag
180
ccgggacagc cgccaaagct gctgatctac tccgggtcca ccttgcaatc tggtgtccct
240
gaccggttct ccggttccgg gtcgggtacc gacttcacgc tcactatttc gtcgctgcaa
300
gccgaagatg tggccgtgta ctattgccaa cagcacaaca agtaccccta cacttttggc
360
ggaggcacca aggtggaaat caaggggggt ggcggtagcg gaggaggggg ctccggcggc
420
ggcggctcag ggggcggagg aagcgaggtg cagctggtgc agagcggagc cgaggtcaag
480
aagcctggag aatccctgag gatcagctgc aaaggcagcg ggtatacctt cacctcctac
540
tggatgaatt gggtccgcca gatgcccgga aaaggcctgg agtggatggg acggattgac
600
ccctacgact cggaaaccca ttacaaccag aagttcaagg atcacgtgac catctccgtg
660
gacaagtcca tttccactgc gtacctccag tggtcaagcc tgaaggcctc cgacactgct
720
atgtactact gcgcacgcgg aaactgggat gattactggg gacagggaac aaccgtgact
780
gtgtcctcca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 345
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 345
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Asp Ser Leu
20 25 30
Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
145 150 155 160
Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Met Pro Gly Lys Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp His Val Thr Ile Ser Val Asp Lys Ser Ile
210 215 220
Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala
225 230 235 240
Met Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 346
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 346
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Asp Ser Leu
20 25 30
Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
145 150 155 160
Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Met Pro Gly Lys Gly
180 185 190
Leu Glu Trp Met Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp His Val Thr Ile Ser Val Asp Lys Ser Ile
210 215 220
Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala
225 230 235 240
Met Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser
260
<210> 347
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 347
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc agctcgtcga gagcggaggg ggactggtgc agcccggagg aagcctgagg
120
ctgtcctgcg ctgcctccgg ctacaccttc acctcctact ggatgaactg ggtcagacag
180
gcacctggaa agggactggt ctgggtgtcg cgcattgacc cctacgactc cgaaacccat
240
tacaatcaga aattcaagga ccgcttcacc atctccgtgg acaaagccaa gagcaccgcg
300
tacctccaaa tgaactccct gcgcgctgag gatacagcag tgtactattg cgcccgggga
360
aactgggatg attactgggg ccagggaact actgtgactg tgtcatccgg gggtggcggt
420
agcggaggag ggggctccgg cggcggcggc tcagggggcg gaggaagcga cgtgcagctc
480
acccagtcgc cctcatttct gtcggcctca gtgggagaca gagtgaccat tacttgtcgg
540
gcctccaaga gcatctccaa ggacctggcc tggtatcagc agaagccagg aaaggcgcct
600
aagttgctca tctactcggg gtcgaccctg caatctggcg tgccgtcccg gttctccggt
660
tcgggaagcg gtaccgaatt cacccttact atctcctccc tgcaaccgga ggacttcgcc
720
acctactact gccaacagca caacaagtac ccgtacactt tcgggggtgg cacgaaggtc
780
gaaatcaaga ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 348
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 348
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Val Trp Val Ser Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ala
85 90 95
Lys Ser Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Gln Leu
145 150 155 160
Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly Asp Arg Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
225 230 235 240
Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 349
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 349
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Val Trp Val Ser Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ala
85 90 95
Lys Ser Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Gln Leu
145 150 155 160
Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly Asp Arg Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
225 230 235 240
Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys
260
<210> 350
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 350
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Val Trp Val
35 40 45
Ser Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ala Lys Ser Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 351
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 351
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc agctcgtcga gagcggaggg ggactggtgc agcccggagg aagcctgagg
120
ctgtcctgcg ctgcctccgg ctacaccttc acctcctact ggatgaactg ggtcagacag
180
gcacctggaa agggactggt ctgggtgtcg cgcattgacc cctacgactc cgaaacccat
240
tacaatcaga aattcaagga ccgcttcacc atctccgtgg acaaagccaa gagcaccgcg
300
tacctccaaa tgaactccct gcgcgctgag gatacagcag tgtactattg cgcccgggga
360
aactgggatg attactgggg ccagggaact actgtgactg tgtcatccgg gggtggcggt
420
agcggaggag ggggctccgg cggcggcggc tcagggggcg gaggaagcga agtggtgctg
480
acccagtcgc ccgcaaccct ctctctgtcg ccgggagaac gcgccactct ttcctgtcgg
540
gcgtccaaga gcatctcaaa ggacctcgcc tggtaccagc agaagcctgg tcaagccccg
600
cggctgctga tctactccgg ctccacgctg caatcaggaa tcccagccag attttccggt
660
tcggggtcgg ggactgactt caccttgacc attagctcgc tggaacctga ggacttcgcc
720
gtgtattact gccagcagca caacaagtac ccgtacacct tcggaggcgg tactaaggtc
780
gagatcaaga ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 352
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 352
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Val Trp Val Ser Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ala
85 90 95
Lys Ser Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Val Leu
145 150 155 160
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
165 170 175
Leu Ser Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp Phe Ala
225 230 235 240
Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 353
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 353
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Val Trp Val Ser Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ala
85 90 95
Lys Ser Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Val Leu
145 150 155 160
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
165 170 175
Leu Ser Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp Phe Ala
225 230 235 240
Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys
260
<210> 354
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 354
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc agctcgtcga gagcggaggg ggactggtgc agcccggagg aagcctgagg
120
ctgtcctgcg ctgcctccgg ctacaccttc acctcctact ggatgaactg ggtcagacag
180
gcacctggaa agggactggt ctgggtgtcg cgcattgacc cctacgactc cgaaacccat
240
tacaatcaga aattcaagga ccgcttcacc atctccgtgg acaaagccaa gagcaccgcg
300
tacctccaaa tgaactccct gcgcgctgag gatacagcag tgtactattg cgcccgggga
360
aactgggatg attactgggg ccagggaact actgtgactg tgtcatccgg gggtggcggt
420
agcggaggag ggggctccgg cggcggcggc tcagggggcg gaggaagcga cgtcgtgatg
480
acccagtcac cggcattcct gtccgtgact cccggagaaa aggtcacgat tacttgccgg
540
gcgtccaaga gcatctccaa ggacctcgcc tggtaccaac agaagccgga ccaggcccct
600
aagctgttga tctactcggg gtccaccctt caatcgggag tgccatcgcg gtttagcggt
660
tcgggttctg ggaccgactt cactttcacc atctcctcac tggaagccga ggatgccgcc
720
acttactact gtcagcagca caacaagtat ccgtacacct tcggaggcgg taccaaagtg
780
gagatcaaga ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 355
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 355
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Val Trp Val Ser Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ala
85 90 95
Lys Ser Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met
145 150 155 160
Thr Gln Ser Pro Ala Phe Leu Ser Val Thr Pro Gly Glu Lys Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Asp Gln Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Glu Ala Glu Asp Ala Ala
225 230 235 240
Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 356
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 356
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Val Trp Val Ser Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ala
85 90 95
Lys Ser Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met
145 150 155 160
Thr Gln Ser Pro Ala Phe Leu Ser Val Thr Pro Gly Glu Lys Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Asp Gln Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Glu Ala Glu Asp Ala Ala
225 230 235 240
Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys
260
<210> 357
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 357
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc agctcgtcga gagcggaggg ggactggtgc agcccggagg aagcctgagg
120
ctgtcctgcg ctgcctccgg ctacaccttc acctcctact ggatgaactg ggtcagacag
180
gcacctggaa agggactggt ctgggtgtcg cgcattgacc cctacgactc cgaaacccat
240
tacaatcaga aattcaagga ccgcttcacc atctccgtgg acaaagccaa gagcaccgcg
300
tacctccaaa tgaactccct gcgcgctgag gatacagcag tgtactattg cgcccgggga
360
aactgggatg attactgggg ccagggaact actgtgactg tgtcatccgg gggtggcggt
420
agcggaggag ggggctccgg cggcggcggc tcagggggcg gaggaagcga cgtggtcatg
480
actcagtccc cggactcact cgcggtgtcg cttggagaga gagcgaccat caactgtcgg
540
gcctcaaaga gcatcagcaa ggacctggcc tggtaccagc agaagccggg acagccgcca
600
aagctgctga tctactccgg gtccaccttg caatctggtg tccctgaccg gttctccggt
660
tccgggtcgg gtaccgactt cacgctcact atttcgtcgc tgcaagccga agatgtggcc
720
gtgtactatt gccaacagca caacaagtac ccctacactt ttggcggagg caccaaggtg
780
gaaatcaaga ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 358
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 358
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Val Trp Val Ser Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ala
85 90 95
Lys Ser Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met
145 150 155 160
Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly Glu Arg Ala Thr
165 170 175
Ile Asn Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala
225 230 235 240
Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 359
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 359
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Val Trp Val Ser Arg Ile Asp Pro Tyr Asp Ser Glu Thr His
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ala
85 90 95
Lys Ser Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met
145 150 155 160
Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly Glu Arg Ala Thr
165 170 175
Ile Asn Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr Ser Gly Ser
195 200 205
Thr Leu Gln Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala
225 230 235 240
Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly
245 250 255
Gly Thr Lys Val Glu Ile Lys
260
<210> 360
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 360
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgacgtgc agctcaccca gtcgccctca tttctgtcgg cctcagtggg agacagagtg
120
accattactt gtcgggcctc caagagcatc tccaaggacc tggcctggta tcagcagaag
180
ccaggaaagg cgcctaagtt gctcatctac tcggggtcga ccctgcaatc tggcgtgccg
240
tcccggttct ccggttcggg aagcggtacc gaattcaccc ttactatctc ctccctgcaa
300
ccggaggact tcgccaccta ctactgccaa cagcacaaca agtacccgta cactttcggg
360
ggtggcacga aggtcgaaat caaggggggt ggcggtagcg gaggaggggg ctccggcggc
420
ggcggctcag ggggcggagg aagcgaagtg cagctcgtcg agagcggagg gggactggtg
480
cagcccggag gaagcctgag gctgtcctgc gctgcctccg gctacacctt cacctcctac
540
tggatgaact gggtcagaca ggcacctgga aagggactgg tctgggtgtc gcgcattgac
600
ccctacgact ccgaaaccca ttacaatcag aaattcaagg accgcttcac catctccgtg
660
gacaaagcca agagcaccgc gtacctccaa atgaactccc tgcgcgctga ggatacagca
720
gtgtactatt gcgcccgggg aaactgggat gattactggg gccagggaac tactgtgact
780
gtgtcatcca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 361
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 361
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Gln Leu Thr Gln Ser Pro Ser Phe Leu
20 25 30
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val
145 150 155 160
Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly
180 185 190
Leu Val Trp Val Ser Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ala Lys
210 215 220
Ser Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 362
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 362
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Gln Leu Thr Gln Ser Pro Ser Phe Leu
20 25 30
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val
145 150 155 160
Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly
180 185 190
Leu Val Trp Val Ser Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ala Lys
210 215 220
Ser Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser
260
<210> 363
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 363
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgg tgctgaccca gtcgcccgca accctctctc tgtcgccggg agaacgcgcc
120
actctttcct gtcgggcgtc caagagcatc tcaaaggacc tcgcctggta ccagcagaag
180
cctggtcaag ccccgcggct gctgatctac tccggctcca cgctgcaatc aggaatccca
240
gccagatttt ccggttcggg gtcggggact gacttcacct tgaccattag ctcgctggaa
300
cctgaggact tcgccgtgta ttactgccag cagcacaaca agtacccgta caccttcgga
360
ggcggtacta aggtcgagat caaggggggt ggcggtagcg gaggaggggg ctccggcggc
420
ggcggctcag ggggcggagg aagcgaagtg cagctcgtcg agagcggagg gggactggtg
480
cagcccggag gaagcctgag gctgtcctgc gctgcctccg gctacacctt cacctcctac
540
tggatgaact gggtcagaca ggcacctgga aagggactgg tctgggtgtc gcgcattgac
600
ccctacgact ccgaaaccca ttacaatcag aaattcaagg accgcttcac catctccgtg
660
gacaaagcca agagcaccgc gtacctccaa atgaactccc tgcgcgctga ggatacagca
720
gtgtactatt gcgcccgggg aaactgggat gattactggg gccagggaac tactgtgact
780
gtgtcatcca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 364
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 364
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Val Leu Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val
145 150 155 160
Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly
180 185 190
Leu Val Trp Val Ser Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ala Lys
210 215 220
Ser Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 365
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 365
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Val Leu Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val
145 150 155 160
Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly
180 185 190
Leu Val Trp Val Ser Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ala Lys
210 215 220
Ser Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser
260
<210> 366
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 366
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgacgtcg tgatgaccca gtcaccggca ttcctgtccg tgactcccgg agaaaaggtc
120
acgattactt gccgggcgtc caagagcatc tccaaggacc tcgcctggta ccaacagaag
180
ccggaccagg cccctaagct gttgatctac tcggggtcca cccttcaatc gggagtgcca
240
tcgcggttta gcggttcggg ttctgggacc gacttcactt tcaccatctc ctcactggaa
300
gccgaggatg ccgccactta ctactgtcag cagcacaaca agtatccgta caccttcgga
360
ggcggtacca aagtggagat caaggggggt ggcggtagcg gaggaggggg ctccggcggc
420
ggcggctcag ggggcggagg aagcgaagtg cagctcgtcg agagcggagg gggactggtg
480
cagcccggag gaagcctgag gctgtcctgc gctgcctccg gctacacctt cacctcctac
540
tggatgaact gggtcagaca ggcacctgga aagggactgg tctgggtgtc gcgcattgac
600
ccctacgact ccgaaaccca ttacaatcag aaattcaagg accgcttcac catctccgtg
660
gacaaagcca agagcaccgc gtacctccaa atgaactccc tgcgcgctga ggatacagca
720
gtgtactatt gcgcccgggg aaactgggat gattactggg gccagggaac tactgtgact
780
gtgtcatcca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 367
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 367
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Ala Phe Leu
20 25 30
Ser Val Thr Pro Gly Glu Lys Val Thr Ile Thr Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Asp Gln Ala
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile
85 90 95
Ser Ser Leu Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val
145 150 155 160
Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly
180 185 190
Leu Val Trp Val Ser Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ala Lys
210 215 220
Ser Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 368
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 368
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Ala Phe Leu
20 25 30
Ser Val Thr Pro Gly Glu Lys Val Thr Ile Thr Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Asp Gln Ala
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile
85 90 95
Ser Ser Leu Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val
145 150 155 160
Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly
180 185 190
Leu Val Trp Val Ser Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ala Lys
210 215 220
Ser Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser
260
<210> 369
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 369
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgacgtgg tcatgactca gtccccggac tcactcgcgg tgtcgcttgg agagagagcg
120
accatcaact gtcgggcctc aaagagcatc agcaaggacc tggcctggta ccagcagaag
180
ccgggacagc cgccaaagct gctgatctac tccgggtcca ccttgcaatc tggtgtccct
240
gaccggttct ccggttccgg gtcgggtacc gacttcacgc tcactatttc gtcgctgcaa
300
gccgaagatg tggccgtgta ctattgccaa cagcacaaca agtaccccta cacttttggc
360
ggaggcacca aggtggaaat caaggggggt ggcggtagcg gaggaggggg ctccggcggc
420
ggcggctcag ggggcggagg aagcgaagtg cagctcgtcg agagcggagg gggactggtg
480
cagcccggag gaagcctgag gctgtcctgc gctgcctccg gctacacctt cacctcctac
540
tggatgaact gggtcagaca ggcacctgga aagggactgg tctgggtgtc gcgcattgac
600
ccctacgact ccgaaaccca ttacaatcag aaattcaagg accgcttcac catctccgtg
660
gacaaagcca agagcaccgc gtacctccaa atgaactccc tgcgcgctga ggatacagca
720
gtgtactatt gcgcccgggg aaactgggat gattactggg gccagggaac tactgtgact
780
gtgtcatcca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 370
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 370
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Asp Ser Leu
20 25 30
Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val
145 150 155 160
Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly
180 185 190
Leu Val Trp Val Ser Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ala Lys
210 215 220
Ser Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 371
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 371
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Asp Ser Leu
20 25 30
Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Arg Ala Ser Lys
35 40 45
Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro
50 55 60
Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro
65 70 75 80
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln His
100 105 110
Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val
145 150 155 160
Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr
165 170 175
Phe Thr Ser Tyr Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly
180 185 190
Leu Val Trp Val Ser Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr
195 200 205
Asn Gln Lys Phe Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ala Lys
210 215 220
Ser Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Thr Val Thr Val Ser Ser
260
<210> 372
<211> 729
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 372
caagtgcaac tcgtccaaag cggagcggaa gtcaagaaac ccggagcgag cgtgaaagtg
60
tcctgcaaag cctccggcta cacctttacg ggctactaca tgcactgggt gcgccaggca
120
ccaggacagg gtcttgaatg gatgggatgg atcaacccta attcgggcgg aactaactac
180
gcacagaagt tccaggggag agtgactctg actcgggata cctccatctc aactgtctac
240
atggaactct cccgcttgcg gtcagatgat acggcagtgt actactgcgc ccgcgacatg
300
aatatcctgg ctaccgtgcc gttcgacatc tggggacagg ggactatggt tactgtctca
360
tcgggcggtg gaggttcagg aggaggcggc tcgggaggcg gaggttcgga cattcagatg
420
acccagtccc catcctctct gtcggccagc gtcggagata gggtgaccat tacctgtcgg
480
gcctcgcaaa gcatctcctc gtacctcaac tggtatcagc aaaagccggg aaaggcgcct
540
aagctgctga tctacgccgc ttcgagcttg caaagcgggg tgccatccag attctcggga
600
tcaggctcag gaaccgactt caccctgacc gtgaacagcc tccagccgga ggactttgcc
660
acttactact gccagcaggg agactccgtg ccgcttactt tcgggggggg tacccgcctg
720
gagatcaag
729
<210> 373
<211> 243
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 373
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Leu Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro
130 135 140
Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg
145 150 155 160
Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro
165 170 175
Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser
180 185 190
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
195 200 205
Leu Thr Val Asn Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys
210 215 220
Gln Gln Gly Asp Ser Val Pro Leu Thr Phe Gly Gly Gly Thr Arg Leu
225 230 235 240
Glu Ile Lys
<210> 374
<211> 1760
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 374
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc aactcgtcca aagcggagcg gaagtcaaga aacccggagc gagcgtgaaa
120
gtgtcctgca aagcctccgg ctacaccttt acgggctact acatgcactg ggtgcgccag
180
gcaccaggac agggtcttga atggatggga tggatcaacc ctaattcggg cggaactaac
240
tacgcacaga agttccaggg gagagtgact ctgactcggg atacctccat ctcaactgtc
300
tacatggaac tctcccgctt gcggtcagat gatacggcag tgtactactg cgcccgcgac
360
atgaatatcc tggctaccgt gccgttcgac atctggggac aggggactat ggttactgtc
420
tcatcgggcg gtggaggttc aggaggaggc ggctcgggag gcggaggttc ggacattcag
480
atgacccagt ccccatcctc tctgtcggcc agcgtcggag atagggtgac cattacctgt
540
cgggcctcgc aaagcatctc ctcgtacctc aactggtatc agcaaaagcc gggaaaggcg
600
cctaagctgc tgatctacgc cgcttcgagc ttgcaaagcg gggtgccatc cagattctcg
660
ggatcaggct caggaaccga cttcaccctg accgtgaaca gcctccagcc ggaggacttt
720
gccacttact actgccagca gggagactcc gtgccgctta ctttcggggg gggtacccgc
780
ctggagatca agaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
840
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
900
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
960
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1020
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1080
tgttcttgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1140
cgcagcgcag acgctccagc ctacaagcag gggcagaacc agctctacaa cgaactcaat
1200
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
1260
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
1320
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
1380
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
1440
atgcaggccc tgccgcctcg gtaagtcgac agctcgcttt cttgctgtcc aatttctatt
1500
aaaggttcct ttgttcccta agtccaacta ctaaactggg ggatattatg aagggccttg
1560
agcatctgga ttctgcctaa taaaaaacat ttattttcat tgctgcgtcg agagctcgct
1620
ttcttgctgt ccaatttcta ttaaaggttc ctttgttccc taagtccaac tactaaactg
1680
ggggatatta tgaagggcct tgagcatctg gattctgcct aataaaaaac atttattttc
1740
attgctgcct cgacgaattc
1760
<210> 375
<211> 729
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 375
caagtccaac tcgttcaatc cggcgcagaa gtcaagaagc caggagcatc agtgaaagtg
60
tcctgcaaag cctcaggcta catcttcacg ggatactaca tccactgggt gcgccaggct
120
ccgggccagg gccttgagtg gatgggctgg atcaacccta actctggggg aaccaactac
180
gctcagaagt tccaggggag ggtcactatg actcgcgata cctccatctc cactgcgtac
240
atggaactct cgggactgag atccgacgat cctgccgtgt actactgcgc ccgggacatg
300
aacatcttgg cgaccgtgcc gtttgacatt tggggacagg gcaccctcgt cactgtgtcg
360
agcggtggag gaggctcggg gggtggcgga tcaggagggg gaggaagcga catccagctg
420
actcagagcc catcgtcgtt gtccgcgtcg gtgggggata gagtgaccat tacttgccgc
480
gccagccaga gcatctcatc atatctgaat tggtaccagc agaagcccgg aaaggcccca
540
aaactgctga tctacgctgc aagcagcctc caatcgggag tgccgtcacg gttctccggg
600
tccggttcgg gaactgactt taccctgacc gtgaattcgc tgcaaccgga ggatttcgcc
660
acgtactact gtcagcaagg agactccgtg ccgctgacct tcggtggagg caccaaggtc
720
gaaatcaag
729
<210> 376
<211> 243
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 376
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Gly Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Gly Leu Arg Ser Asp Asp Pro Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro
130 135 140
Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg
145 150 155 160
Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro
165 170 175
Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser
180 185 190
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
195 200 205
Leu Thr Val Asn Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys
210 215 220
Gln Gln Gly Asp Ser Val Pro Leu Thr Phe Gly Gly Gly Thr Lys Val
225 230 235 240
Glu Ile Lys
<210> 377
<211> 735
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 377
caagtccaac tccaacagtc aggcgcagaa gtgaaaaaga gcggtgcatc ggtgaaagtg
60
tcatgcaaag cctcgggcta caccttcact gactactata tgcactggct gcggcaggca
120
ccgggacagg gacttgagtg gatgggatgg atcaacccga attcagggga cactaactac
180
gcgcagaagt tccaggggag agtgaccctg acgagggaca cctcaatttc gaccgtctac
240
atggaattgt cgcgcctgag atcggacgat actgctgtgt actactgtgc ccgcgacatg
300
aacatcctcg cgactgtgcc ttttgatatc tggggacagg ggactatggt caccgtttcc
360
tccgcttccg gtggcggagg ctcgggaggc cgggcctccg gtggaggagg cagcgacatc
420
cagatgactc agagcccttc ctcgctgagc gcctcagtgg gagatcgcgt gaccatcact
480
tgccgggcca gccagtccat ttcgtcctac ctcaattggt accagcagaa gccgggaaag
540
gcgcccaagc tcttgatcta cgctgcgagc tccctgcaaa gcggggtgcc gagccgattc
600
tcgggttccg gctcgggaac cgacttcact ctgaccatct catccctgca accagaggac
660
tttgccacct actactgcca acaaggagat tctgtcccac tgacgttcgg cggaggaacc
720
aaggtcgaaa tcaag
735
<210> 378
<211> 245
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 378
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val Lys Lys Ser Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Leu Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Asp Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Leu Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
130 135 140
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
145 150 155 160
Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln
165 170 175
Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu
180 185 190
Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
195 200 205
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
210 215 220
Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu Thr Phe Gly Gly Gly Thr
225 230 235 240
Lys Val Glu Ile Lys
245
<210> 379
<211> 243
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 379
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro
130 135 140
Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg
145 150 155 160
Ala Ser Gln Ser Ile Ser Thr Tyr Leu Asn Trp Tyr Gln Gln Lys Pro
165 170 175
Gly Lys Ala Pro Asn Leu Leu Ile Tyr Ala Ala Phe Ser Leu Gln Ser
180 185 190
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
195 200 205
Leu Thr Ile Asn Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys
210 215 220
Gln Gln Gly Asp Ser Val Pro Leu Thr Phe Gly Gly Gly Thr Lys Leu
225 230 235 240
Glu Ile Lys
<210> 380
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 380
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Asp Val Gln Leu Thr Gln Ser Pro Ser
130 135 140
Phe Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
145 150 155 160
Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Lys Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly
180 185 190
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln
210 215 220
Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu
225 230 235 240
Ile Lys
<210> 381
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 381
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Glu Val Val Leu Thr Gln Ser Pro Ala
130 135 140
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
145 150 155 160
Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Ala Pro Arg Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly
180 185 190
Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
195 200 205
Thr Ile Ser Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln
210 215 220
Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu
225 230 235 240
Ile Lys
<210> 382
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 382
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr Gln Ser Pro Ala
130 135 140
Phe Leu Ser Val Thr Pro Gly Glu Lys Val Thr Ile Thr Cys Arg Ala
145 150 155 160
Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Asp
165 170 175
Gln Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly
180 185 190
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe
195 200 205
Thr Ile Ser Ser Leu Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln
210 215 220
Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu
225 230 235 240
Ile Lys
<210> 383
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 383
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr Gln Ser Pro Asp
130 135 140
Ser Leu Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Arg Ala
145 150 155 160
Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Pro Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly
180 185 190
Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln
210 215 220
Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu
225 230 235 240
Ile Lys
<210> 384
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 384
Asp Val Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
115 120 125
Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser
130 135 140
Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp
145 150 155 160
Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly
165 170 175
Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe Lys
180 185 190
Asp Arg Val Thr Met Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr Met
195 200 205
Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
225 230 235 240
Ser Ser
<210> 385
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 385
Glu Val Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Ser Gly Ser Thr Leu Gln Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
115 120 125
Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser
130 135 140
Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp
145 150 155 160
Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly
165 170 175
Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe Lys
180 185 190
Asp Arg Val Thr Met Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr Met
195 200 205
Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
225 230 235 240
Ser Ser
<210> 386
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 386
Asp Val Val Met Thr Gln Ser Pro Ala Phe Leu Ser Val Thr Pro Gly
1. 5 10 15
Glu Lys Val Thr Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Asp Gln Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Glu Ala
65 70 75 80
Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
115 120 125
Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser
130 135 140
Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp
145 150 155 160
Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly
165 170 175
Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe Lys
180 185 190
Asp Arg Val Thr Met Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr Met
195 200 205
Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
225 230 235 240
Ser Ser
<210> 387
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 387
Asp Val Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1. 5 10 15
Glu Arg Ala Thr Ile Asn Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala
65 70 75 80
Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
115 120 125
Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser
130 135 140
Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp
145 150 155 160
Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly
165 170 175
Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe Lys
180 185 190
Asp Arg Val Thr Met Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr Met
195 200 205
Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
225 230 235 240
Ser Ser
<210> 388
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 388
Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Phe Val Phe Ser Val Asp Lys Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Asp Val Gln Leu Thr Gln Ser Pro Ser
130 135 140
Phe Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
145 150 155 160
Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Lys Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly
180 185 190
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln
210 215 220
Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu
225 230 235 240
Ile Lys
<210> 389
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 389
Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Phe Val Phe Ser Val Asp Lys Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Glu Val Val Leu Thr Gln Ser Pro Ala
130 135 140
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
145 150 155 160
Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Ala Pro Arg Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly
180 185 190
Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
195 200 205
Thr Ile Ser Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln
210 215 220
Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu
225 230 235 240
Ile Lys
<210> 390
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 390
Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Phe Val Phe Ser Val Asp Lys Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr Gln Ser Pro Ala
130 135 140
Phe Leu Ser Val Thr Pro Gly Glu Lys Val Thr Ile Thr Cys Arg Ala
145 150 155 160
Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Asp
165 170 175
Gln Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly
180 185 190
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe
195 200 205
Thr Ile Ser Ser Leu Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln
210 215 220
Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu
225 230 235 240
Ile Lys
<210> 391
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 391
Gln Val Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Phe Val Phe Ser Val Asp Lys Ser Val Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr Gln Ser Pro Asp
130 135 140
Ser Leu Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Arg Ala
145 150 155 160
Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Pro Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly
180 185 190
Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln
210 215 220
Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu
225 230 235 240
Ile Lys
<210> 392
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 392
Asp Val Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
115 120 125
Val Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala Ser
130 135 140
Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp
145 150 155 160
Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly
165 170 175
Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe Lys
180 185 190
Asp Arg Phe Val Phe Ser Val Asp Lys Ser Val Ser Thr Ala Tyr Leu
195 200 205
Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
225 230 235 240
Ser Ser
<210> 393
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 393
Glu Val Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Ser Gly Ser Thr Leu Gln Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
115 120 125
Val Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala Ser
130 135 140
Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp
145 150 155 160
Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly
165 170 175
Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe Lys
180 185 190
Asp Arg Phe Val Phe Ser Val Asp Lys Ser Val Ser Thr Ala Tyr Leu
195 200 205
Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
225 230 235 240
Ser Ser
<210> 394
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 394
Asp Val Val Met Thr Gln Ser Pro Ala Phe Leu Ser Val Thr Pro Gly
1. 5 10 15
Glu Lys Val Thr Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Asp Gln Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Glu Ala
65 70 75 80
Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
115 120 125
Val Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala Ser
130 135 140
Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp
145 150 155 160
Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly
165 170 175
Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe Lys
180 185 190
Asp Arg Phe Val Phe Ser Val Asp Lys Ser Val Ser Thr Ala Tyr Leu
195 200 205
Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
225 230 235 240
Ser Ser
<210> 395
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 395
Asp Val Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1. 5 10 15
Glu Arg Ala Thr Ile Asn Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala
65 70 75 80
Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
115 120 125
Val Gln Leu Val Gln Ser Gly Ser Glu Leu Lys Lys Pro Gly Ala Ser
130 135 140
Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp
145 150 155 160
Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly
165 170 175
Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe Lys
180 185 190
Asp Arg Phe Val Phe Ser Val Asp Lys Ser Val Ser Thr Ala Tyr Leu
195 200 205
Gln Ile Ser Ser Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
225 230 235 240
Ser Ser
<210> 396
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 396
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1. 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp His Val Thr Ile Ser Val Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Asp Val Gln Leu Thr Gln Ser Pro Ser
130 135 140
Phe Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
145 150 155 160
Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Lys Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly
180 185 190
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln
210 215 220
Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu
225 230 235 240
Ile Lys
<210> 397
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 397
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1. 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp His Val Thr Ile Ser Val Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Glu Val Val Leu Thr Gln Ser Pro Ala
130 135 140
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
145 150 155 160
Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Ala Pro Arg Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly
180 185 190
Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
195 200 205
Thr Ile Ser Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln
210 215 220
Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu
225 230 235 240
Ile Lys
<210> 398
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 398
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1. 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp His Val Thr Ile Ser Val Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr Gln Ser Pro Ala
130 135 140
Phe Leu Ser Val Thr Pro Gly Glu Lys Val Thr Ile Thr Cys Arg Ala
145 150 155 160
Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Asp
165 170 175
Gln Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly
180 185 190
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe
195 200 205
Thr Ile Ser Ser Leu Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln
210 215 220
Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu
225 230 235 240
Ile Lys
<210> 399
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 399
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1. 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp His Val Thr Ile Ser Val Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr Gln Ser Pro Asp
130 135 140
Ser Leu Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Arg Ala
145 150 155 160
Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Pro Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly
180 185 190
Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln
210 215 220
Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu
225 230 235 240
Ile Lys
<210> 400
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 400
Asp Val Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
115 120 125
Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu Ser
130 135 140
Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Thr Phe Thr Ser Tyr Trp
145 150 155 160
Met Asn Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met Gly
165 170 175
Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe Lys
180 185 190
Asp His Val Thr Ile Ser Val Asp Lys Ser Ile Ser Thr Ala Tyr Leu
195 200 205
Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys Ala
210 215 220
Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
225 230 235 240
Ser Ser
<210> 401
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 401
Glu Val Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Ser Gly Ser Thr Leu Gln Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
115 120 125
Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu Ser
130 135 140
Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Thr Phe Thr Ser Tyr Trp
145 150 155 160
Met Asn Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met Gly
165 170 175
Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe Lys
180 185 190
Asp His Val Thr Ile Ser Val Asp Lys Ser Ile Ser Thr Ala Tyr Leu
195 200 205
Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys Ala
210 215 220
Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
225 230 235 240
Ser Ser
<210> 402
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 402
Asp Val Val Met Thr Gln Ser Pro Ala Phe Leu Ser Val Thr Pro Gly
1. 5 10 15
Glu Lys Val Thr Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Asp Gln Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Glu Ala
65 70 75 80
Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
115 120 125
Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu Ser
130 135 140
Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Thr Phe Thr Ser Tyr Trp
145 150 155 160
Met Asn Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met Gly
165 170 175
Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe Lys
180 185 190
Asp His Val Thr Ile Ser Val Asp Lys Ser Ile Ser Thr Ala Tyr Leu
195 200 205
Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys Ala
210 215 220
Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
225 230 235 240
Ser Ser
<210> 403
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 403
Asp Val Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1. 5 10 15
Glu Arg Ala Thr Ile Asn Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala
65 70 75 80
Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
115 120 125
Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu Ser
130 135 140
Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Thr Phe Thr Ser Tyr Trp
145 150 155 160
Met Asn Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met Gly
165 170 175
Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe Lys
180 185 190
Asp His Val Thr Ile Ser Val Asp Lys Ser Ile Ser Thr Ala Tyr Leu
195 200 205
Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys Ala
210 215 220
Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
225 230 235 240
Ser Ser
<210> 404
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 404
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Val Trp Val
35 40 45
Ser Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ala Lys Ser Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Asp Val Gln Leu Thr Gln Ser Pro Ser
130 135 140
Phe Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
145 150 155 160
Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Lys Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly
180 185 190
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln
210 215 220
Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu
225 230 235 240
Ile Lys
<210> 405
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 405
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Val Trp Val
35 40 45
Ser Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ala Lys Ser Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Glu Val Val Leu Thr Gln Ser Pro Ala
130 135 140
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
145 150 155 160
Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Ala Pro Arg Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly
180 185 190
Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
195 200 205
Thr Ile Ser Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln
210 215 220
Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu
225 230 235 240
Ile Lys
<210> 406
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 406
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Val Trp Val
35 40 45
Ser Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ala Lys Ser Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr Gln Ser Pro Ala
130 135 140
Phe Leu Ser Val Thr Pro Gly Glu Lys Val Thr Ile Thr Cys Arg Ala
145 150 155 160
Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Asp
165 170 175
Gln Ala Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly
180 185 190
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe
195 200 205
Thr Ile Ser Ser Leu Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln
210 215 220
Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu
225 230 235 240
Ile Lys
<210> 407
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 407
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Val Trp Val
35 40 45
Ser Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Phe Thr Ile Ser Val Asp Lys Ala Lys Ser Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr Gln Ser Pro Asp
130 135 140
Ser Leu Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Arg Ala
145 150 155 160
Ser Lys Ser Ile Ser Lys Asp Leu Ala Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Pro Pro Lys Leu Leu Ile Tyr Ser Gly Ser Thr Leu Gln Ser Gly
180 185 190
Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln
210 215 220
Gln His Asn Lys Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu
225 230 235 240
Ile Lys
<210> 408
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 408
Asp Val Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp
145 150 155 160
Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Val Trp Val Ser
165 170 175
Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe Lys
180 185 190
Asp Arg Phe Thr Ile Ser Val Asp Lys Ala Lys Ser Thr Ala Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
225 230 235 240
Ser Ser
<210> 409
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 409
Glu Val Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Ser Gly Ser Thr Leu Gln Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp
145 150 155 160
Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Val Trp Val Ser
165 170 175
Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe Lys
180 185 190
Asp Arg Phe Thr Ile Ser Val Asp Lys Ala Lys Ser Thr Ala Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
225 230 235 240
Ser Ser
<210> 410
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 410
Asp Val Val Met Thr Gln Ser Pro Ala Phe Leu Ser Val Thr Pro Gly
1. 5 10 15
Glu Lys Val Thr Ile Thr Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Asp Gln Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Glu Ala
65 70 75 80
Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp
145 150 155 160
Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Val Trp Val Ser
165 170 175
Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe Lys
180 185 190
Asp Arg Phe Thr Ile Ser Val Asp Lys Ala Lys Ser Thr Ala Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
225 230 235 240
Ser Ser
<210> 411
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 411
Asp Val Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1. 5 10 15
Glu Arg Ala Thr Ile Asn Cys Arg Ala Ser Lys Ser Ile Ser Lys Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Gly Ser Thr Leu Gln Ser Gly Val Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala
65 70 75 80
Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln His Asn Lys Tyr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
115 120 125
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
130 135 140
Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp
145 150 155 160
Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Val Trp Val Ser
165 170 175
Arg Ile Asp Pro Tyr Asp Ser Glu Thr His Tyr Asn Gln Lys Phe Lys
180 185 190
Asp Arg Phe Thr Ile Ser Val Asp Lys Ala Lys Ser Thr Ala Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
210 215 220
Arg Gly Asn Trp Asp Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
225 230 235 240
Ser Ser
<210> 412
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 412
Asn His Gly Met Ser
1. 5
<210> 413
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 413
Asn Tyr Ala Met Ser
1. 5
<210> 414
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 414
Asp Tyr Ala Met His
1. 5
<210> 415
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 415
Asn Phe Gly Ile Asn
1. 5
<210> 416
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 416
Ser Asp Ala Met Thr
1. 5
<210> 417
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 417
Asn Tyr Gly Ile Thr
1. 5
<210> 418
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 418
Asp Tyr Tyr Met Ser
1. 5
<210> 419
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 419
Ser Ser Tyr Tyr Tyr Trp Gly
1. 5
<210> 420
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 420
Thr Ser Gly Met Cys Val Ser
1. 5
<210> 421
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 421
Ser Tyr Ser Met Asn
1. 5
<210> 422
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 422
Ser His Tyr Ile His
1. 5
<210> 423
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 423
Ser Gly Gly Tyr Tyr Trp Ser
1. 5
<210> 424
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 424
Ser Tyr Ala Ile Ser
1. 5
<210> 425
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 425
Ser Asn Ser Ala Ala Trp Asn
1. 5
<210> 426
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 426
Ser Tyr Ala Met Ser
1. 5
<210> 427
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 427
Arg Tyr Pro Met Ser
1. 5
<210> 428
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 428
Asn Phe Gly Met Asn
1. 5
<210> 429
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 429
Asp Tyr Ser Ile Asn
1. 5
<210> 430
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 430
His Tyr Ser Met Asn
1. 5
<210> 431
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 431
Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys Gly
1. 5 10 15
<210> 432
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 432
Gly Ile Ser Arg Ser Gly Glu Asn Thr Tyr Tyr Ala Asp Ser Val Lys
1. 5 10 15
Gly
<210> 433
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 433
Gly Ile Ser Trp Asn Ser Gly Ser Ile Gly Tyr Ala Asp Ser Val Lys
1. 5 10 15
Gly
<210> 434
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 434
Trp Ile Asn Pro Lys Asn Asn Asn Thr Asn Tyr Ala Gln Lys Phe Gln
1. 5 10 15
Gly
<210> 435
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 435
Val Ile Ser Gly Ser Gly Gly Thr Thr Tyr Tyr Ala Asp Ser Val Lys
1. 5 10 15
Gly
<210> 436
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 436
Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn Tyr Ala Gln Lys Phe Gln
1. 5 10 15
Gly
<210> 437
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 437
Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val Lys
1. 5 10 15
Gly
<210> 438
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 438
Tyr Ile Ser Ser Ser Gly Asn Thr Ile Tyr Tyr Ala Asp Ser Val Lys
1. 5 10 15
Gly
<210> 439
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 439
Ser Ile Tyr Tyr Ser Gly Ser Ala Tyr Tyr Asn Pro Ser Leu Lys Ser
1. 5 10 15
<210> 440
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 440
Arg Ile Asp Trp Asp Glu Asp Lys Phe Tyr Ser Thr Ser Leu Lys Thr
1. 5 10 15
<210> 441
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 441
Ser Ile Ser Ser Ser Ser Ser Tyr Ile Tyr Tyr Ala Asp Ser Val Lys
1. 5 10 15
Gly
<210> 442
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 442
Met Ile Asn Pro Ser Gly Gly Val Thr Ala Tyr Ser Gln Thr Leu Gln
1. 5 10 15
Gly
<210> 443
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 443
Tyr Ile Tyr Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser
1. 5 10 15
<210> 444
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 444
Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe Gln
1. 5 10 15
Gly
<210> 445
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 445
Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Ser Phe Tyr Ala Ile Ser Leu
1. 5 10 15
Lys Ser
<210> 446
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 446
Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1. 5 10 15
Gly
<210> 447
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 447
Gly Ile Ser Asp Ser Gly Val Ser Thr Tyr Tyr Ala Asp Ser Ala Lys
1. 5 10 15
Gly
<210> 448
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 448
Ser Ile Asn Trp Lys Gly Asn Ser Leu Ala Tyr Gly Asp Ser Val Lys
1. 5 10 15
Gly
<210> 449
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 449
Trp Ile Asn Thr Tyr Thr Gly Glu Ser Tyr Phe Ala Asp Asp Phe Lys
1. 5 10 15
Gly
<210> 450
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 450
Trp Ile Asn Thr Glu Thr Arg Glu Pro Ala Tyr Ala Tyr Asp Phe Arg
1. 5 10 15
Gly
<210> 451
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 451
Arg Ile Asn Thr Glu Ser Gly Val Pro Ile Tyr Ala Asp Asp Phe Lys
1. 5 10 15
Gly
<210> 452
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 452
Arg Ile Asn Thr Glu Thr Gly Glu Pro Leu Tyr Ala Asp Asp Phe Lys
1. 5 10 15
Gly
<210> 453
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 453
His Gly Gly Glu Ser Asp Val
1. 5
<210> 454
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 454
Ser Pro Ala His Tyr Tyr Gly Gly Met Asp Val
1. 5 10
<210> 455
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 455
His Ser Phe Leu Ala Tyr
1. 5
<210> 456
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 456
Gly Pro Tyr Tyr Tyr Gln Ser Tyr Met Asp Val
1. 5 10
<210> 457
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 457
Leu Asp Ser Ser Gly Tyr Tyr Tyr Ala Arg Gly Pro Arg Tyr
1. 5 10
<210> 458
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 458
Gly Pro Tyr Tyr Tyr Tyr Met Asp Val
1. 5
<210> 459
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 459
Glu Ser Gly Asp Gly Met Asp Val
1. 5
<210> 460
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 460
Ser Thr Met Val Arg Glu Asp Tyr
1. 5
<210> 461
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 461
His Trp Gln Glu Trp Pro Asp Ala Phe Asp Ile
1. 5 10
<210> 462
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 462
Ser Gly Ala Gly Gly Thr Ser Ala Thr Ala Phe Asp Ile
1. 5 10
<210> 463
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 463
Thr Ile Ala Ala Val Tyr Ala Phe Asp Ile
1. 5 10
<210> 464
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 464
Asp Leu Arg Gly Ala Phe Asp Ile
1. 5
<210> 465
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 465
Glu Gly Ser Gly Ser Gly Trp Tyr Phe Asp Phe
1. 5 10
<210> 466
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 466
Ala Gly Ile Ala Ala Arg Leu Arg Gly Ala Phe Asp Ile
1. 5 10
<210> 467
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 467
Arg Gly Gly Tyr Gln Leu Leu Arg Trp Asp Val Gly Leu Leu Arg Ser
1. 5 10 15
Ala Phe Asp Ile
20
<210> 468
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 468
Ser Ser Pro Glu Gly Leu Phe Leu Tyr Trp Phe Asp Pro
1. 5 10
<210> 469
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 469
Val Glu Gly Ser Gly Ser Leu Asp Tyr
1. 5
<210> 470
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 470
Arg Ala Gly Ser Glu Ala Ser Asp Ile
1. 5
<210> 471
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 471
Ala Thr Tyr Lys Arg Glu Leu Arg Tyr Tyr Tyr Gly Met Asp Val
1. 5 10 15
<210> 472
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 472
Val Gly Lys Ala Val Pro Asp Val
1. 5
<210> 473
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 473
His Gln Gly Val Ala Tyr Tyr Asn Tyr Ala Met Asp Val
1. 5 10
<210> 474
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 474
Val Val Arg Asp Gly Met Asp Val
1. 5
<210> 475
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 475
Ile Pro Gln Thr Gly Thr Phe Asp Tyr
1. 5
<210> 476
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 476
Ala Asn Tyr Lys Arg Glu Leu Arg Tyr Tyr Tyr Gly Met Asp Val
1. 5 10 15
<210> 477
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 477
Ala Leu Val Gly Ala Thr Gly Ala Phe Asp Ile
1. 5 10
<210> 478
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 478
Trp Phe Gly Glu Gly Phe Asp Pro
1. 5
<210> 479
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 479
Val Gly Tyr Asp Ser Ser Gly Tyr Tyr Arg Asp Tyr Tyr Gly Met Asp
1. 5 10 15
Val
<210> 480
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 480
Met Gly Trp Ser Ser Gly Tyr Leu Gly Ala Phe Asp Ile
1. 5 10
<210> 481
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 481
Gly Glu Ile Tyr Tyr Gly Tyr Asp Gly Gly Phe Ala Tyr
1. 5 10
<210> 482
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 482
Asp Tyr Ser Tyr Ala Met Asp Tyr
1. 5
<210> 483
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 483
Asp Tyr Leu Tyr Ser Leu Asp Phe
1. 5
<210> 484
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 484
Asp Tyr Leu Tyr Ser Cys Asp Tyr
1. 5
<210> 485
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 485
Arg Ala Ser Gln Ser Ile Ser Ser Ser Phe Leu Ala
1. 5 10
<210> 486
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 486
Arg Ser Ser Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr Leu Asp
1. 5 10 15
<210> 487
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 487
Lys Ser Ser Gln Ser Leu Leu Arg Asn Asp Gly Lys Thr Pro Leu Tyr
1. 5 10 15
<210> 488
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 488
Arg Ser Ser Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr Leu Asn
1. 5 10 15
<210> 489
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 489
Arg Ser Ser Gln Ser Leu Leu Tyr Ser Asn Gly Tyr Asn Tyr Val Asp
1. 5 10 15
<210> 490
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 490
Arg Ala Ser Gln Ser Val Ser Ser Asn Leu Ala
1. 5 10
<210> 491
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 491
Arg Ala Ser Gln Ser Val Ser Ser Lys Leu Ala
1. 5 10
<210> 492
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 492
Arg Ala Ser Gln Ser Val Gly Ser Thr Asn Leu Ala
1. 5 10
<210> 493
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 493
Lys Ser Ser Glu Ser Leu Val His Asn Ser Gly Lys Thr Tyr Leu Asn
1. 5 10 15
<210> 494
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 494
Gln Ala Ser Glu Asp Ile Asn Lys Phe Leu Asn
1. 5 10
<210> 495
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 495
Arg Ala Ser Gln Ser Val Gly Ser Asn Leu Ala
1. 5 10
<210> 496
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 496
Arg Ala Ser Gln Ser Ile Gly Ser Ser Ser Leu Ala
1. 5 10
<210> 497
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 497
Lys Ala Ser Gln Asp Ile Asp Asp Ala Met Asn
1. 5 10
<210> 498
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 498
Arg Ala Ser Gln Asp Ile Tyr Asn Asn Leu Ala
1. 5 10
<210> 499
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 499
Gly Gly Asn Asn Ile Gly Thr Lys Ser Val His
1. 5 10
<210> 500
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 500
Ser Gly Asp Gly Leu Ser Lys Lys Tyr Val Ser
1. 5 10
<210> 501
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 501
Arg Ala Ser Gln Gly Ile Arg Asn Trp Leu Ala
1. 5 10
<210> 502
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 502
Gly Gly Asn Asn Ile Gly Ser Lys Ser Val His
1. 5 10
<210> 503
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 503
Gln Gly Asp Ser Leu Gly Asn Tyr Tyr Ala Thr
1. 5 10
<210> 504
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 504
Arg Ala Ser Gln Ser Val Ser Ser Ala Tyr Leu Ala
1. 5 10
<210> 505
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 505
Arg Ala Ser Gln Ser Val Ser Asn Ser Leu Ala
1. 5 10
<210> 506
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 506
Arg Ala Ser Gln Ser Val Ser Ser Ser Phe Leu Ala
1. 5 10
<210> 507
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 507
Arg Ala Ser Gln Ser Val Ser Thr Thr Phe Leu Ala
1. 5 10
<210> 508
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 508
Arg Ala Thr Gln Ser Ile Gly Ser Ser Phe Leu Ala
1. 5 10
<210> 509
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 509
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1. 5 10
<210> 510
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 510
Arg Ala Ser Gln Arg Val Ala Ser Asn Tyr Leu Ala
1. 5 10
<210> 511
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 511
Arg Ala Ser Gln Ser Leu Ser Ser Asn Phe Leu Ala
1. 5 10
<210> 512
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 512
Arg Ala Ser Gln Ser Val Ala Ser Ser Phe Leu Ala
1. 5 10
<210> 513
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 513
Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ser
1. 5 10
<210> 514
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 514
Arg Ala Ser Glu Ser Val Ser Val Ile Gly Ala His Leu Ile His
1. 5 10 15
<210> 515
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 515
Arg Ala Ser Glu Ser Val Thr Ile Leu Gly Ser His Leu Ile Tyr
1. 5 10 15
<210> 516
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 516
Gly Ala Ser Arg Arg Ala Thr
1. 5
<210> 517
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 517
Leu Gly Ser Asn Arg Ala Ser
1. 5
<210> 518
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 518
Glu Val Ser Asn Arg Phe Ser
1. 5
<210> 519
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 519
Leu Gly Ser Lys Arg Ala Ser
1. 5
<210> 520
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 520
Gly Ala Ser Thr Leu Ala Ser
1. 5
<210> 521
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 521
Gly Ala Ser Thr Arg Ala Ser
1. 5
<210> 522
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 522
Gly Ala Ser Ile Arg Ala Thr
1. 5
<210> 523
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 523
Asp Ala Ser Asn Arg Ala Thr
1. 5
<210> 524
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 524
Glu Val Ser Asn Arg Asp Ser
1. 5
<210> 525
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 525
Asp Ala Ser Thr Leu Gln Thr
1. 5
<210> 526
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 526
Gly Ala Ser Thr Arg Ala Thr
1. 5
<210> 527
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 527
Gly Ala Ser Ser Arg Ala Ser
1. 5
<210> 528
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 528
Ser Ala Thr Ser Pro Val Pro
1. 5
<210> 529
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 529
Ala Ala Asn Lys Ser Gln Ser
1. 5
<210> 530
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 530
Asp Asp Ser Val Arg Pro Ser
1. 5
<210> 531
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 531
Arg Asp Lys Glu Arg Pro Ser
1. 5
<210> 532
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 532
Ala Ala Ser Asn Leu Gln Ser
1. 5
<210> 533
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 533
Gly Lys Asn Asn Arg Pro Ser
1. 5
<210> 534
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 534
Gly Thr Asn Asn Arg Pro Ser
1. 5
<210> 535
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 535
Asp Ala Ser Ser Arg Ala Thr
1. 5
<210> 536
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 536
Gly Ala Ser Ser Arg Ala Thr
1. 5
<210> 537
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 537
Gly Ser Ser Asn Arg Ala Thr
1. 5
<210> 538
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 538
Gly Ala Ser Gln Arg Ala Thr
1. 5
<210> 539
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 539
Gly Ala Ser Asn Trp Ala Thr
1. 5
<210> 540
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 540
Gly Thr Ser Ser Arg Ala Thr
1. 5
<210> 541
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 541
Gly Ala Ser Gly Arg Ala Thr
1. 5
<210> 542
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 542
Ser Ala Ser Tyr Arg Tyr Thr
1. 5
<210> 543
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 543
Leu Ala Ser Asn Leu Glu Thr
1. 5
<210> 544
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 544
Leu Ala Ser Asn Val Gln Thr
1. 5
<210> 545
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 545
Gln Gln Ser Tyr Ser Thr Pro Tyr Thr
1. 5
<210> 546
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 546
Gln Gln Tyr His Ser Ser Pro Ser Trp Thr
1. 5 10
<210> 547
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 547
Met Gln Ala Leu Gln Thr Pro Tyr Thr
1. 5
<210> 548
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 548
Met Gln Asn Ile Gln Phe Pro Ser
1. 5
<210> 549
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 549
Gln Gln Ser Tyr Lys Arg Ala Ser
1. 5
<210> 550
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 550
Met Gln Gly Arg Gln Phe Pro Tyr Ser
1. 5
<210> 551
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 551
Gln Gln Tyr Gly Ser Ser Leu Thr
1. 5
<210> 552
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 552
Gln Gln Tyr Gly Ser Ser Ser Trp Thr
1. 5
<210> 553
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 553
Gln Gln Tyr Gly Ser Ser Pro Pro Trp Thr
1. 5 10
<210> 554
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 554
Gln Gln Ser Tyr Thr Leu Ala
1. 5
<210> 555
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 555
Met Gln Gly Thr His Trp Pro Gly Thr
1. 5
<210> 556
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 556
Gln Gln Tyr Glu Ser Leu Pro Leu Thr
1. 5
<210> 557
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 557
Gln Gln Tyr Asn Asp Trp Leu Pro Val Thr
1. 5 10
<210> 558
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 558
Gln Gln Tyr Ala Gly Ser Pro Pro Phe Thr
1. 5 10
<210> 559
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 559
Leu Gln His Asp Asn Phe Pro Leu Thr
1. 5
<210> 560
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 560
Gln His Tyr Tyr Arg Phe Pro Tyr Ser
1. 5
<210> 561
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 561
Gln Val Trp Asp Ser Asp Ser Glu His Val Val
1. 5 10
<210> 562
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 562
Gln Ala Trp Asp Asp Thr Thr Val Val
1. 5
<210> 563
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 563
Gln Lys Tyr Asn Ser Ala Pro Phe Thr
1. 5
<210> 564
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 564
Ser Ser Arg Asp Ser Ser Gly Asp His Leu Arg Val
1. 5 10
<210> 565
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 565
Asn Ser Arg Asp Ser Ser Gly His His Leu Leu
1. 5 10
<210> 566
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 566
Gln His Tyr Gly Ser Ser Phe Asn Gly Ser Ser Leu Phe Thr
1. 5 10
<210> 567
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 567
Gln Gln Phe Gly Thr Ser Ser Gly Leu Thr
1. 5 10
<210> 568
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 568
Gln Gln Ser Tyr Ser Thr Pro Tyr Ser
1. 5
<210> 569
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 569
Gln His Tyr Glu Ser Ser Pro Ser Trp Thr
1. 5 10
<210> 570
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 570
Gln Gln Tyr Gly Ser Pro Pro Arg Phe Thr
1. 5 10
<210> 571
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 571
Gln His Tyr Gly Ser Ser Pro Ser Trp Thr
1. 5 10
<210> 572
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 572
Gln His Tyr Asp Ser Ser Pro Ser Trp Thr
1. 5 10
<210> 573
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 573
Gln Tyr Tyr Gly Thr Ser Pro Met Tyr Thr
1. 5 10
<210> 574
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 574
Met Gln Ala Leu Gln Thr Pro Leu Thr
1. 5
<210> 575
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 575
Gln His Tyr Gly Asn Ser Pro Pro Lys Phe Thr
1. 5 10
<210> 576
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 576
Gln His Tyr Gly Gly Ser Pro Arg Leu Thr
1. 5 10
<210> 577
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 577
Gln Gln His Tyr Ser Thr Pro Trp Thr
1. 5
<210> 578
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 578
Leu Gln Ser Arg Ile Phe Pro Arg Thr
1. 5
<210> 579
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 579
Leu Gln Ser Arg Thr Ile Pro Arg Thr
1. 5
<210> 580
<211> 239
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 580
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly
115 120 125
Gly Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser
130 135 140
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser
145 150 155 160
Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
165 170 175
Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
180 185 190
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
195 200 205
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr
210 215 220
Ser Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
225 230 235
<210> 581
<211> 717
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 581
gaagtgcaat tggtggaatc agggggagga cttgtgcagc ctggaggatc gctgagactg
60
tcatgtgccg tgtccggctt tgccctgtcc aaccacggga tgtcctgggt ccgccgcgcg
120
cctggaaagg gcctcgaatg ggtgtcgggt attgtgtaca gcggtagcac ctactatgcc
180
gcatccgtga aggggagatt caccatcagc cgggacaact ccaggaacac tctgtacctc
240
caaatgaatt cgctgaggcc agaggacact gccatctact actgctccgc gcatggcgga
300
gagtccgacg tctggggaca ggggaccacc gtgaccgtgt ctagcgcgtc cggcggaggc
360
ggcagcgggg gtcgggcatc agggggcggc ggatcggaca tccagctcac ccagtccccg
420
agctcgctgt ccgcctccgt gggagatcgg gtcaccatca cgtgccgcgc cagccagtcg
480
atttcctcct acctgaactg gtaccaacag aagcccggaa aagccccgaa gcttctcatc
540
tacgccgcct cgagcctgca gtcaggagtg ccctcacggt tctccggctc cggttccggt
600
actgatttca ccctgaccat ttcctccctg caaccggagg acttcgctac ttactactgc
660
cagcagtcgt actccacccc ctacactttc ggacaaggca ccaaggtcga aatcaag
717
<210> 582
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 582
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 583
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 583
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 584
<211> 483
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 584
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe
35 40 45
Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr
65 70 75 80
Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg
85 90 95
Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala
100 105 110
Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser
145 150 155 160
Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys
165 170 175
Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys
180 185 190
Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln
195 200 205
Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
210 215 220
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr
225 230 235 240
Cys Gln Gln Ser Tyr Ser Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys
245 250 255
Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
260 265 270
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
275 280 285
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
290 295 300
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
305 310 315 320
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
325 330 335
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
340 345 350
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
355 360 365
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
370 375 380
Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
385 390 395 400
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
405 410 415
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
420 425 430
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
435 440 445
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
450 455 460
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
465 470 475 480
Pro Pro Arg
<210> 585
<211> 1449
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 585
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc aattggtgga atcaggggga ggacttgtgc agcctggagg atcgctgaga
120
ctgtcatgtg ccgtgtccgg ctttgccctg tccaaccacg ggatgtcctg ggtccgccgc
180
gcgcctggaa agggcctcga atgggtgtcg ggtattgtgt acagcggtag cacctactat
240
gccgcatccg tgaaggggag attcaccatc agccgggaca actccaggaa cactctgtac
300
ctccaaatga attcgctgag gccagaggac actgccatct actactgctc cgcgcatggc
360
ggagagtccg acgtctgggg acaggggacc accgtgaccg tgtctagcgc gtccggcgga
420
ggcggcagcg ggggtcgggc atcagggggc ggcggatcgg acatccagct cacccagtcc
480
ccgagctcgc tgtccgcctc cgtgggagat cgggtcacca tcacgtgccg cgccagccag
540
tcgatttcct cctacctgaa ctggtaccaa cagaagcccg gaaaagcccc gaagcttctc
600
atctacgccg cctcgagcct gcagtcagga gtgccctcac ggttctccgg ctccggttcc
660
ggtactgatt tcaccctgac catttcctcc ctgcaaccgg aggacttcgc tacttactac
720
tgccagcagt cgtactccac cccctacact ttcggacaag gcaccaaggt cgaaatcaag
780
accactaccc cagcaccgag gccacccacc ccggctccta ccatcgcctc ccagcctctg
840
tccctgcgtc cggaggcatg tagacccgca gctggtgggg ccgtgcatac ccggggtctt
900
gacttcgcct gcgatatcta catttgggcc cctctggctg gtacttgcgg ggtcctgctg
960
ctttcactcg tgatcactct ttactgtaag cgcggtcgga agaagctgct gtacatcttt
1020
aagcaaccct tcatgaggcc tgtgcagact actcaagagg aggacggctg ttcatgccgg
1080
ttcccagagg aggaggaagg cggctgcgaa ctgcgcgtga aattcagccg cagcgcagat
1140
gctccagcct acaagcaggg gcagaaccag ctctacaacg aactcaatct tggtcggaga
1200
gaggagtacg acgtgctgga caagcggaga ggacgggacc cagaaatggg cgggaagccg
1260
cgcagaaaga atccccaaga gggcctgtac aacgagctcc aaaaggataa gatggcagaa
1320
gcctatagcg agattggtat gaaaggggaa cgcagaagag gcaaaggcca cgacggactg
1380
taccagggac tcagcaccgc caccaaggac acctatgacg ctcttcacat gcaggccctg
1440
ccgcctcgg
1449
<210> 586
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 586
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Gly Trp Val
35 40 45
Ser Gly Ile Ser Arg Ser Gly Glu Asn Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Pro Ala His Tyr Tyr Gly Gly Met Asp Val Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Val Leu Thr Gln Ser
130 135 140
Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
145 150 155 160
Arg Ala Ser Gln Ser Ile Ser Ser Ser Phe Leu Ala Trp Tyr Gln Gln
165 170 175
Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Arg Arg
180 185 190
Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
195 200 205
Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Ser Ala Val Tyr
210 215 220
Tyr Cys Gln Gln Tyr His Ser Ser Pro Ser Trp Thr Phe Gly Gln Gly
225 230 235 240
Thr Lys Leu Glu Ile Lys
245
<210> 587
<211> 738
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 587
caagtgcaac tcgtggaatc tggtggagga ctcgtgcaac ccggaagatc gcttagactg
60
tcgtgtgccg ccagcgggtt cactttctcg aactacgcga tgtcctgggt ccgccaggca
120
cccggaaagg gactcggttg ggtgtccggc atttcccggt ccggcgaaaa tacctactac
180
gccgactccg tgaagggccg cttcaccatc tcaagggaca acagcaaaaa caccctgtac
240
ttgcaaatga actccctgcg ggatgaagat acagccgtgt actattgcgc ccggtcgcct
300
gcccattact acggcggaat ggacgtctgg ggacagggaa ccactgtgac tgtcagcagc
360
gcgtcgggtg gcggcggctc agggggtcgg gcctccgggg ggggagggtc cgacatcgtg
420
ctgacccagt ccccgggaac cctgagcctg agcccgggag agcgcgcgac cctgtcatgc
480
cgggcatccc agagcattag ctcctccttt ctcgcctggt atcagcagaa gcccggacag
540
gccccgaggc tgctgatcta cggcgctagc agaagggcta ccggaatccc agaccggttc
600
tccggctccg gttccgggac cgatttcacc cttactatct cgcgcctgga acctgaggac
660
tccgccgtct actactgcca gcagtaccac tcatccccgt cgtggacgtt cggacagggc
720
accaagctgg agattaag
738
<210> 588
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 588
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Gly Trp Val
35 40 45
Ser Gly Ile Ser Arg Ser Gly Glu Asn Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Pro Ala His Tyr Tyr Gly Gly Met Asp Val Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 589
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 589
Asp Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Ser Ser
20 25 30
Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Arg Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Ser Ala Val Tyr Tyr Cys Gln Gln Tyr His Ser Ser Pro
85 90 95
Ser Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 590
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 590
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Asn Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Gly Trp Val Ser Gly Ile Ser Arg Ser Gly Glu Asn Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Ser Pro Ala His Tyr Tyr Gly Gly Met
115 120 125
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile
145 150 155 160
Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg
165 170 175
Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Ser Ser Phe Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
195 200 205
Gly Ala Ser Arg Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu
225 230 235 240
Asp Ser Ala Val Tyr Tyr Cys Gln Gln Tyr His Ser Ser Pro Ser Trp
245 250 255
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 591
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 591
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc aactcgtgga atctggtgga ggactcgtgc aacccggaag atcgcttaga
120
ctgtcgtgtg ccgccagcgg gttcactttc tcgaactacg cgatgtcctg ggtccgccag
180
gcacccggaa agggactcgg ttgggtgtcc ggcatttccc ggtccggcga aaatacctac
240
tacgccgact ccgtgaaggg ccgcttcacc atctcaaggg acaacagcaa aaacaccctg
300
tacttgcaaa tgaactccct gcgggatgaa gatacagccg tgtactattg cgcccggtcg
360
cctgcccatt actacggcgg aatggacgtc tggggacagg gaaccactgt gactgtcagc
420
agcgcgtcgg gtggcggcgg ctcagggggt cgggcctccg gggggggagg gtccgacatc
480
gtgctgaccc agtccccggg aaccctgagc ctgagcccgg gagagcgcgc gaccctgtca
540
tgccgggcat cccagagcat tagctcctcc tttctcgcct ggtatcagca gaagcccgga
600
caggccccga ggctgctgat ctacggcgct agcagaaggg ctaccggaat cccagaccgg
660
ttctccggct ccggttccgg gaccgatttc acccttacta tctcgcgcct ggaacctgag
720
gactccgccg tctactactg ccagcagtac cactcatccc cgtcgtggac gttcggacag
780
ggcaccaagc tggagattaa gaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 592
<211> 244
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 592
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Asn Ser Gly Ser Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ser Val His Ser Phe Leu Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly
115 120 125
Gly Gly Gly Ser Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Pro
130 135 140
Val Thr Pro Gly Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser
145 150 155 160
Leu Leu His Ser Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys
165 170 175
Pro Gly Gln Ser Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala
180 185 190
Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
195 200 205
Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr
210 215 220
Cys Met Gln Ala Leu Gln Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys
225 230 235 240
Val Glu Ile Lys
<210> 593
<211> 732
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 593
caagtgcaac tcgtcgaatc cggtggaggt ctggtccaac ctggtagaag cctgagactg
60
tcgtgtgcgg ccagcggatt cacctttgat gactatgcta tgcactgggt gcggcaggcc
120
ccaggaaagg gcctggaatg ggtgtcggga attagctgga actccgggtc cattggctac
180
gccgactccg tgaagggccg cttcaccatc tcccgcgaca acgcaaagaa ctccctgtac
240
ttgcaaatga actcgctcag ggctgaggat accgcgctgt actactgctc cgtgcattcc
300
ttcctggcct actggggaca gggaactctg gtcaccgtgt cgagcgcctc cggcggcggg
360
ggctcgggtg gacgggcctc gggcggaggg gggtccgaca tcgtgatgac ccagaccccg
420
ctgagcttgc ccgtgactcc cggagagcct gcatccatct cctgccggtc atcccagtcc
480
cttctccact ccaacggata caactacctc gactggtacc tccagaagcc gggacagagc
540
cctcagcttc tgatctacct ggggtcaaat agagcctcag gagtgccgga tcggttcagc
600
ggatctggtt cgggaactga tttcactctg aagatttccc gcgtggaagc cgaggacgtg
660
ggcgtctact actgtatgca ggcgctgcag accccctata ccttcggcca agggacgaaa
720
gtggagatca ag
732
<210> 594
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 594
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Asn Ser Gly Ser Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ser Val His Ser Phe Leu Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 595
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 595
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Pro Val Thr Pro Gly
1. 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 596
<211> 488
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 596
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Asp Asp Tyr Ala Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Ser Trp Asn Ser Gly Ser Ile Gly
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Leu Tyr Tyr Cys Ser Val His Ser Phe Leu Ala Tyr Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr Gln Thr
145 150 155 160
Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser Ile Ser Cys
165 170 175
Arg Ser Ser Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr Leu Asp
180 185 190
Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Gln Leu Leu Ile Tyr Leu
195 200 205
Gly Ser Asn Arg Ala Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly
210 215 220
Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp
225 230 235 240
Val Gly Val Tyr Tyr Cys Met Gln Ala Leu Gln Thr Pro Tyr Thr Phe
245 250 255
Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg
260 265 270
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
275 280 285
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
290 295 300
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
305 310 315 320
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg
325 330 335
Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro
340 345 350
Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu
355 360 365
Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala
370 375 380
Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
385 390 395 400
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
405 410 415
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
420 425 430
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
435 440 445
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
450 455 460
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
465 470 475 480
His Met Gln Ala Leu Pro Pro Arg
485
<210> 597
<211> 1464
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 597
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc aactcgtcga atccggtgga ggtctggtcc aacctggtag aagcctgaga
120
ctgtcgtgtg cggccagcgg attcaccttt gatgactatg ctatgcactg ggtgcggcag
180
gccccaggaa agggcctgga atgggtgtcg ggaattagct ggaactccgg gtccattggc
240
tacgccgact ccgtgaaggg ccgcttcacc atctcccgcg acaacgcaaa gaactccctg
300
tacttgcaaa tgaactcgct cagggctgag gataccgcgc tgtactactg ctccgtgcat
360
tccttcctgg cctactgggg acagggaact ctggtcaccg tgtcgagcgc ctccggcggc
420
gggggctcgg gtggacgggc ctcgggcgga ggggggtccg acatcgtgat gacccagacc
480
ccgctgagct tgcccgtgac tcccggagag cctgcatcca tctcctgccg gtcatcccag
540
tcccttctcc actccaacgg atacaactac ctcgactggt acctccagaa gccgggacag
600
agccctcagc ttctgatcta cctggggtca aatagagcct caggagtgcc ggatcggttc
660
agcggatctg gttcgggaac tgatttcact ctgaagattt cccgcgtgga agccgaggac
720
gtgggcgtct actactgtat gcaggcgctg cagaccccct ataccttcgg ccaagggacg
780
aaagtggaga tcaagaccac taccccagca ccgaggccac ccaccccggc tcctaccatc
840
gcctcccagc ctctgtccct gcgtccggag gcatgtagac ccgcagctgg tggggccgtg
900
catacccggg gtcttgactt cgcctgcgat atctacattt gggcccctct ggctggtact
960
tgcggggtcc tgctgctttc actcgtgatc actctttact gtaagcgcgg tcggaagaag
1020
ctgctgtaca tctttaagca acccttcatg aggcctgtgc agactactca agaggaggac
1080
ggctgttcat gccggttccc agaggaggag gaaggcggct gcgaactgcg cgtgaaattc
1140
agccgcagcg cagatgctcc agcctacaag caggggcaga accagctcta caacgaactc
1200
aatcttggtc ggagagagga gtacgacgtg ctggacaagc ggagaggacg ggacccagaa
1260
atgggcggga agccgcgcag aaagaatccc caagagggcc tgtacaacga gctccaaaag
1320
gataagatgg cagaagccta tagcgagatt ggtatgaaag gggaacgcag aagaggcaaa
1380
ggccacgacg gactgtacca gggactcagc accgccacca aggacaccta tgacgctctt
1440
cacatgcagg ccctgccgcc tcgg
1464
<210> 598
<211> 243
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 598
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly
115 120 125
Gly Gly Gly Ser Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser
130 135 140
Val Thr Pro Gly Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser
145 150 155 160
Leu Leu Arg Asn Asp Gly Lys Thr Pro Leu Tyr Trp Tyr Leu Gln Lys
165 170 175
Ala Gly Gln Pro Pro Gln Leu Leu Ile Tyr Glu Val Ser Asn Arg Phe
180 185 190
Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
195 200 205
Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Ala Tyr Tyr
210 215 220
Cys Met Gln Asn Ile Gln Phe Pro Ser Phe Gly Gly Gly Thr Lys Leu
225 230 235 240
Glu Ile Lys
<210> 599
<211> 729
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 599
gaagtgcaat tgttggaatc tggaggagga cttgtgcagc ctggaggatc actgagactt
60
tcgtgtgcgg tgtcaggctt cgccctgagc aaccacggca tgagctgggt gcggagagcc
120
ccggggaagg gtctggaatg ggtgtccggg atcgtctact ccggttcaac ttactacgcc
180
gcaagcgtga agggtcgctt caccatttcc cgcgataact cccggaacac cctgtacctc
240
caaatgaact ccctgcggcc cgaggacacc gccatctact actgttccgc gcatggagga
300
gagtccgatg tctggggaca gggcactacc gtgaccgtgt cgagcgcctc ggggggagga
360
ggctccggcg gtcgcgcctc cggggggggt ggcagcgaca ttgtgatgac gcagactcca
420
ctctcgctgt ccgtgacccc gggacagccc gcgtccatct cgtgcaagag ctcccagagc
480
ctgctgagga acgacggaaa gactcctctg tattggtacc tccagaaggc tggacagccc
540
ccgcaactgc tcatctacga agtgtcaaat cgcttctccg gggtgccgga tcggttttcc
600
ggctcgggat cgggcaccga cttcaccctg aaaatctcca gggtcgaggc cgaggacgtg
660
ggagcctact actgcatgca aaacatccag ttcccttcct tcggcggcgg cacaaagctg
720
gagattaag
729
<210> 600
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 600
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 601
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 601
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1. 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Leu Arg Asn
20 25 30
Asp Gly Lys Thr Pro Leu Tyr Trp Tyr Leu Gln Lys Ala Gly Gln Pro
35 40 45
Pro Gln Leu Leu Ile Tyr Glu Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Ala Tyr Tyr Cys Met Gln Asn
85 90 95
Ile Gln Phe Pro Ser Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 602
<211> 487
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 602
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe
35 40 45
Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr
65 70 75 80
Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg
85 90 95
Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala
100 105 110
Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr Gln Thr
145 150 155 160
Pro Leu Ser Leu Ser Val Thr Pro Gly Gln Pro Ala Ser Ile Ser Cys
165 170 175
Lys Ser Ser Gln Ser Leu Leu Arg Asn Asp Gly Lys Thr Pro Leu Tyr
180 185 190
Trp Tyr Leu Gln Lys Ala Gly Gln Pro Pro Gln Leu Leu Ile Tyr Glu
195 200 205
Val Ser Asn Arg Phe Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly
210 215 220
Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp
225 230 235 240
Val Gly Ala Tyr Tyr Cys Met Gln Asn Ile Gln Phe Pro Ser Phe Gly
245 250 255
Gly Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
260 265 270
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
275 280 285
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
290 295 300
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
305 310 315 320
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 603
<211> 1461
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 603
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc aattgttgga atctggagga ggacttgtgc agcctggagg atcactgaga
120
ctttcgtgtg cggtgtcagg cttcgccctg agcaaccacg gcatgagctg ggtgcggaga
180
gccccgggga agggtctgga atgggtgtcc gggatcgtct actccggttc aacttactac
240
gccgcaagcg tgaagggtcg cttcaccatt tcccgcgata actcccggaa caccctgtac
300
ctccaaatga actccctgcg gcccgaggac accgccatct actactgttc cgcgcatgga
360
ggagagtccg atgtctgggg acagggcact accgtgaccg tgtcgagcgc ctcgggggga
420
ggaggctccg gcggtcgcgc ctccgggggg ggtggcagcg acattgtgat gacgcagact
480
ccactctcgc tgtccgtgac cccgggacag cccgcgtcca tctcgtgcaa gagctcccag
540
agcctgctga ggaacgacgg aaagactcct ctgtattggt acctccagaa ggctggacag
600
cccccgcaac tgctcatcta cgaagtgtca aatcgcttct ccggggtgcc ggatcggttt
660
tccggctcgg gatcgggcac cgacttcacc ctgaaaatct ccagggtcga ggccgaggac
720
gtgggagcct actactgcat gcaaaacatc cagttccctt ccttcggcgg cggcacaaag
780
ctggagatta agaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
840
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
900
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
960
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1020
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1080
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1140
cgcagcgcag atgctccagc ctacaagcag gggcagaacc agctctacaa cgaactcaat
1200
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
1260
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
1320
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
1380
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
1440
atgcaggccc tgccgcctcg g
1461
<210> 604
<211> 249
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 604
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Arg Lys Thr Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Asp Asn Phe
20 25 30
Gly Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Lys Asn Asn Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Val Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Pro Tyr Tyr Tyr Gln Ser Tyr Met Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr Gln Thr
130 135 140
Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser Ile Ser Cys
145 150 155 160
Arg Ser Ser Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr Leu Asn
165 170 175
Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Gln Leu Leu Ile Tyr Leu
180 185 190
Gly Ser Lys Arg Ala Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Asp Phe Thr Leu His Ile Thr Arg Val Gly Ala Glu Asp
210 215 220
Val Gly Val Tyr Tyr Cys Met Gln Ala Leu Gln Thr Pro Tyr Thr Phe
225 230 235 240
Gly Gln Gly Thr Lys Leu Glu Ile Lys
245
<210> 605
<211> 747
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 605
caagtccaac tcgtccagtc cggcgcagaa gtcagaaaaa ccggtgctag cgtgaaagtg
60
tcctgcaagg cctccggcta cattttcgat aacttcggaa tcaactgggt cagacaggcc
120
ccgggccagg ggctggaatg gatgggatgg atcaacccca agaacaacaa caccaactac
180
gcacagaagt tccagggccg cgtgactatc accgccgatg aatcgaccaa taccgcctac
240
atggaggtgt cctccctgcg gtcggaggac actgccgtgt attactgcgc gaggggccca
300
tactactacc aaagctacat ggacgtctgg ggacagggaa ccatggtgac cgtgtcatcc
360
gcctccggtg gtggaggctc cggggggcgg gcttcaggag gcggaggaag cgatattgtg
420
atgacccaga ctccgcttag cctgcccgtg actcctggag aaccggcctc catttcctgc
480
cggtcctcgc aatcactcct gcattccaac ggttacaact acctgaattg gtacctccag
540
aagcctggcc agtcgcccca gttgctgatc tatctgggct cgaagcgcgc ctccggggtg
600
cctgaccggt ttagcggatc tgggagcggc acggacttca ctctccacat cacccgcgtg
660
ggagcggagg acgtgggagt gtactactgt atgcaggcgc tgcagactcc gtacacattc
720
ggacagggca ccaagctgga gatcaag
747
<210> 606
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 606
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Arg Lys Thr Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Asp Asn Phe
20 25 30
Gly Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Lys Asn Asn Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Val Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Pro Tyr Tyr Tyr Gln Ser Tyr Met Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 607
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 607
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Pro Val Thr Pro Gly
1. 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asn Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Lys Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu His Ile
65 70 75 80
Thr Arg Val Gly Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 608
<211> 493
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 608
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Arg Lys Thr Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Ile Phe Asp Asn Phe Gly Ile Asn Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Lys Asn Asn Asn Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser
85 90 95
Thr Asn Thr Ala Tyr Met Glu Val Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Pro Tyr Tyr Tyr Gln Ser Tyr Met
115 120 125
Asp Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile
145 150 155 160
Val Met Thr Gln Thr Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro
165 170 175
Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser Asn Gly
180 185 190
Tyr Asn Tyr Leu Asn Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Gln
195 200 205
Leu Leu Ile Tyr Leu Gly Ser Lys Arg Ala Ser Gly Val Pro Asp Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu His Ile Thr Arg
225 230 235 240
Val Gly Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala Leu Gln
245 250 255
Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 609
<211> 1479
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 609
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtcc aactcgtcca gtccggcgca gaagtcagaa aaaccggtgc tagcgtgaaa
120
gtgtcctgca aggcctccgg ctacattttc gataacttcg gaatcaactg ggtcagacag
180
gccccgggcc aggggctgga atggatggga tggatcaacc ccaagaacaa caacaccaac
240
tacgcacaga agttccaggg ccgcgtgact atcaccgccg atgaatcgac caataccgcc
300
tacatggagg tgtcctccct gcggtcggag gacactgccg tgtattactg cgcgaggggc
360
ccatactact accaaagcta catggacgtc tggggacagg gaaccatggt gaccgtgtca
420
tccgcctccg gtggtggagg ctccgggggg cgggcttcag gaggcggagg aagcgatatt
480
gtgatgaccc agactccgct tagcctgccc gtgactcctg gagaaccggc ctccatttcc
540
tgccggtcct cgcaatcact cctgcattcc aacggttaca actacctgaa ttggtacctc
600
cagaagcctg gccagtcgcc ccagttgctg atctatctgg gctcgaagcg cgcctccggg
660
gtgcctgacc ggtttagcgg atctgggagc ggcacggact tcactctcca catcacccgc
720
gtgggagcgg aggacgtggg agtgtactac tgtatgcagg cgctgcagac tccgtacaca
780
ttcggacagg gcaccaagct ggagatcaag accactaccc cagcaccgag gccacccacc
840
ccggctccta ccatcgcctc ccagcctctg tccctgcgtc cggaggcatg tagacccgca
900
gctggtgggg ccgtgcatac ccggggtctt gacttcgcct gcgatatcta catttgggcc
960
cctctggctg gtacttgcgg ggtcctgctg ctttcactcg tgatcactct ttactgtaag
1020
cgcggtcgga agaagctgct gtacatcttt aagcaaccct tcatgaggcc tgtgcagact
1080
actcaagagg aggacggctg ttcatgccgg ttcccagagg aggaggaagg cggctgcgaa
1140
ctgcgcgtga aattcagccg cagcgcagat gctccagcct acaagcaggg gcagaaccag
1200
ctctacaacg aactcaatct tggtcggaga gaggagtacg acgtgctgga caagcggaga
1260
ggacgggacc cagaaatggg cgggaagccg cgcagaaaga atccccaaga gggcctgtac
1320
aacgagctcc aaaaggataa gatggcagaa gcctatagcg agattggtat gaaaggggaa
1380
cgcagaagag gcaaaggcca cgacggactg taccagggac tcagcaccgc caccaaggac
1440
acctatgacg ctcttcacat gcaggccctg ccgcctcgg
1479
<210> 610
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 610
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Asp
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Val Ile Ser Gly Ser Gly Gly Thr Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Leu Asp Ser Ser Gly Tyr Tyr Tyr Ala Arg Gly Pro Arg Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Gln Leu
130 135 140
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
145 150 155 160
Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Gly Ala Ser
180 185 190
Thr Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr His Phe Thr Leu Thr Ile Asn Ser Leu Gln Ser Glu Asp Ser Ala
210 215 220
Thr Tyr Tyr Cys Gln Gln Ser Tyr Lys Arg Ala Ser Phe Gly Gln Gly
225 230 235 240
Thr Lys Val Glu Ile Lys
245
<210> 611
<211> 738
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 611
caagtgcaac ttcaagaatc aggcggagga ctcgtgcagc ccggaggatc attgcggctc
60
tcgtgcgccg cctcgggctt caccttctcg agcgacgcca tgacctgggt ccgccaggcc
120
ccggggaagg ggctggaatg ggtgtctgtg atttccggct ccgggggaac tacgtactac
180
gccgattccg tgaaaggtcg cttcactatc tcccgggaca acagcaagaa caccctttat
240
ctgcaaatga attccctccg cgccgaggac accgccgtgt actactgcgc caagctggac
300
tcctcgggct actactatgc ccggggtccg agatactggg gacagggaac cctcgtgacc
360
gtgtcctccg cgtccggcgg aggagggtcg ggagggcggg cctccggcgg cggcggttcg
420
gacatccagc tgacccagtc cccatcctca ctgagcgcaa gcgtgggcga cagagtcacc
480
attacatgca gggcgtccca gagcatcagc tcctacctga actggtacca acagaagcct
540
ggaaaggctc ctaagctgtt gatctacggg gcttcgaccc tggcatccgg ggtgcccgcg
600
aggtttagcg gaagcggtag cggcactcac ttcactctga ccattaacag cctccagtcc
660
gaggattcag ccacttacta ctgtcagcag tcctacaagc gggccagctt cggacagggc
720
actaaggtcg agatcaag
738
<210> 612
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 612
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Asp
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Val Ile Ser Gly Ser Gly Gly Thr Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Leu Asp Ser Ser Gly Tyr Tyr Tyr Ala Arg Gly Pro Arg Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 613
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 613
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Thr Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr His Phe Thr Leu Thr Ile Asn Ser Leu Gln Ser
65 70 75 80
Glu Asp Ser Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Lys Arg Ala Ser
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 614
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 614
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Asp Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Val Ile Ser Gly Ser Gly Gly Thr Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Leu Asp Ser Ser Gly Tyr Tyr Tyr Ala
115 120 125
Arg Gly Pro Arg Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
130 135 140
Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
165 170 175
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser
180 185 190
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
195 200 205
Ile Tyr Gly Ala Ser Thr Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr His Phe Thr Leu Thr Ile Asn Ser Leu Gln
225 230 235 240
Ser Glu Asp Ser Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Lys Arg Ala
245 250 255
Ser Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 615
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 615
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc aacttcaaga atcaggcgga ggactcgtgc agcccggagg atcattgcgg
120
ctctcgtgcg ccgcctcggg cttcaccttc tcgagcgacg ccatgacctg ggtccgccag
180
gccccgggga aggggctgga atgggtgtct gtgatttccg gctccggggg aactacgtac
240
tacgccgatt ccgtgaaagg tcgcttcact atctcccggg acaacagcaa gaacaccctt
300
tatctgcaaa tgaattccct ccgcgccgag gacaccgccg tgtactactg cgccaagctg
360
gactcctcgg gctactacta tgcccggggt ccgagatact ggggacaggg aaccctcgtg
420
accgtgtcct ccgcgtccgg cggaggaggg tcgggagggc gggcctccgg cggcggcggt
480
tcggacatcc agctgaccca gtccccatcc tcactgagcg caagcgtggg cgacagagtc
540
accattacat gcagggcgtc ccagagcatc agctcctacc tgaactggta ccaacagaag
600
cctggaaagg ctcctaagct gttgatctac ggggcttcga ccctggcatc cggggtgccc
660
gcgaggttta gcggaagcgg tagcggcact cacttcactc tgaccattaa cagcctccag
720
tccgaggatt cagccactta ctactgtcag cagtcctaca agcgggccag cttcggacag
780
ggcactaagg tcgagatcaa gaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 616
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 616
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Asn Tyr
20 25 30
Gly Ile Thr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asn Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Pro Tyr Tyr Tyr Tyr Met Asp Val Trp Gly Lys Gly Thr
100 105 110
Met Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg
115 120 125
Ala Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr Gln Ser Pro Leu
130 135 140
Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser Ile Ser Cys Arg Ser
145 150 155 160
Ser Gln Ser Leu Leu Tyr Ser Asn Gly Tyr Asn Tyr Val Asp Trp Tyr
165 170 175
Leu Gln Lys Pro Gly Gln Ser Pro Gln Leu Leu Ile Tyr Leu Gly Ser
180 185 190
Asn Arg Ala Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Phe Lys Leu Gln Ile Ser Arg Val Glu Ala Glu Asp Val Gly
210 215 220
Ile Tyr Tyr Cys Met Gln Gly Arg Gln Phe Pro Tyr Ser Phe Gly Gln
225 230 235 240
Gly Thr Lys Val Glu Ile Lys
245
<210> 617
<211> 741
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 617
caagtccaac tggtccagag cggtgcagaa gtgaagaagc ccggagcgag cgtgaaagtg
60
tcctgcaagg cttccgggta caccttctcc aactacggca tcacttgggt gcgccaggcc
120
ccgggacagg gcctggaatg gatggggtgg atttccgcgt acaacggcaa tacgaactac
180
gctcagaagt tccagggtag agtgaccatg actaggaaca cctccatttc caccgcctac
240
atggaactgt cctccctgcg gagcgaggac accgccgtgt actattgcgc ccggggacca
300
tactactact acatggatgt ctgggggaag gggactatgg tcaccgtgtc atccgcctcg
360
ggaggcggcg gatcaggagg acgcgcctct ggtggtggag gatcggagat cgtgatgacc
420
cagagccctc tctccttgcc cgtgactcct ggggagcccg catccatttc atgccggagc
480
tcccagtcac ttctctactc caacggctat aactacgtgg attggtacct ccaaaagccg
540
ggccagagcc cgcagctgct gatctacctg ggctcgaaca gggccagcgg agtgcctgac
600
cggttctccg ggtcgggaag cgggaccgac ttcaagctgc aaatctcgag agtggaggcc
660
gaggacgtgg gaatctacta ctgtatgcag ggccgccagt ttccgtactc gttcggacag
720
ggcaccaaag tggaaatcaa g
741
<210> 618
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 618
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Asn Tyr
20 25 30
Gly Ile Thr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asn Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Pro Tyr Tyr Tyr Tyr Met Asp Val Trp Gly Lys Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 619
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 619
Glu Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1. 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu Tyr Ser
20 25 30
Asn Gly Tyr Asn Tyr Val Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Lys Leu Gln Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Ile Tyr Tyr Cys Met Gln Gly
85 90 95
Arg Gln Phe Pro Tyr Ser Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 620
<211> 491
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 620
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Ser Asn Tyr Gly Ile Thr Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asn Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Pro Tyr Tyr Tyr Tyr Met Asp Val
115 120 125
Trp Gly Lys Gly Thr Met Val Thr Val Ser Ser Ala Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Glu Ile Val Met
145 150 155 160
Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser
165 170 175
Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu Tyr Ser Asn Gly Tyr Asn
180 185 190
Tyr Val Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Gln Leu Leu
195 200 205
Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro Asp Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Phe Lys Leu Gln Ile Ser Arg Val Glu
225 230 235 240
Ala Glu Asp Val Gly Ile Tyr Tyr Cys Met Gln Gly Arg Gln Phe Pro
245 250 255
Tyr Ser Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 621
<211> 1473
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 621
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtcc aactggtcca gagcggtgca gaagtgaaga agcccggagc gagcgtgaaa
120
gtgtcctgca aggcttccgg gtacaccttc tccaactacg gcatcacttg ggtgcgccag
180
gccccgggac agggcctgga atggatgggg tggatttccg cgtacaacgg caatacgaac
240
tacgctcaga agttccaggg tagagtgacc atgactagga acacctccat ttccaccgcc
300
tacatggaac tgtcctccct gcggagcgag gacaccgccg tgtactattg cgcccgggga
360
ccatactact actacatgga tgtctggggg aaggggacta tggtcaccgt gtcatccgcc
420
tcgggaggcg gcggatcagg aggacgcgcc tctggtggtg gaggatcgga gatcgtgatg
480
acccagagcc ctctctcctt gcccgtgact cctggggagc ccgcatccat ttcatgccgg
540
agctcccagt cacttctcta ctccaacggc tataactacg tggattggta cctccaaaag
600
ccgggccaga gcccgcagct gctgatctac ctgggctcga acagggccag cggagtgcct
660
gaccggttct ccgggtcggg aagcgggacc gacttcaagc tgcaaatctc gagagtggag
720
gccgaggacg tgggaatcta ctactgtatg cagggccgcc agtttccgta ctcgttcgga
780
cagggcacca aagtggaaat caagaccact accccagcac cgaggccacc caccccggct
840
cctaccatcg cctcccagcc tctgtccctg cgtccggagg catgtagacc cgcagctggt
900
ggggccgtgc atacccgggg tcttgacttc gcctgcgata tctacatttg ggcccctctg
960
gctggtactt gcggggtcct gctgctttca ctcgtgatca ctctttactg taagcgcggt
1020
cggaagaagc tgctgtacat ctttaagcaa cccttcatga ggcctgtgca gactactcaa
1080
gaggaggacg gctgttcatg ccggttccca gaggaggagg aaggcggctg cgaactgcgc
1140
gtgaaattca gccgcagcgc agatgctcca gcctacaagc aggggcagaa ccagctctac
1200
aacgaactca atcttggtcg gagagaggag tacgacgtgc tggacaagcg gagaggacgg
1260
gacccagaaa tgggcgggaa gccgcgcaga aagaatcccc aagagggcct gtacaacgag
1320
ctccaaaagg ataagatggc agaagcctat agcgagattg gtatgaaagg ggaacgcaga
1380
agaggcaaag gccacgacgg actgtaccag ggactcagca ccgccaccaa ggacacctat
1440
gacgctcttc acatgcaggc cctgccgcct cgg
1473
<210> 622
<211> 238
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 622
Glu Val Gln Leu Leu Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly
115 120 125
Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser
130 135 140
Val Ser Pro Gly Glu Ser Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser
145 150 155 160
Val Ser Ser Asn Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
165 170 175
Arg Leu Leu Ile Tyr Gly Ala Ser Thr Arg Ala Ser Gly Ile Pro Asp
180 185 190
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
195 200 205
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Tyr Gly
210 215 220
Ser Ser Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
225 230 235
<210> 623
<211> 714
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 623
gaagtgcaat tgctcgaaac tggaggaggt ctggtgcaac ctggaggatc acttcgcctg
60
tcctgcgccg tgtcgggctt tgccctgtcc aaccatggaa tgagctgggt ccgccgcgcg
120
ccggggaagg gcctcgaatg ggtgtccggc atcgtctact ccggctccac ctactacgcc
180
gcgtccgtga agggccggtt cacgatttca cgggacaact cgcggaacac cctgtacctc
240
caaatgaatt cccttcggcc ggaggatact gccatctact actgctccgc ccacggtggc
300
gaatccgacg tctggggcca gggaaccacc gtgaccgtgt ccagcgcgtc cgggggagga
360
ggaagcgggg gtagagcatc gggtggaggc ggatcagaga tcgtgctgac ccagtccccc
420
gccaccttga gcgtgtcacc aggagagtcc gccaccctgt catgccgcgc cagccagtcc
480
gtgtcctcca acctggcttg gtaccagcag aagccggggc aggcccctag actcctgatc
540
tatggggcgt cgacccgggc atctggaatt cccgataggt tcagcggatc gggctcgggc
600
actgacttca ctctgaccat ctcctcgctg caagccgagg acgtggctgt gtactactgt
660
cagcagtacg gaagctccct gactttcggt ggcgggacca aagtcgagat taag
714
<210> 624
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 624
Glu Val Gln Leu Leu Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 625
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 625
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1. 5 10 15
Glu Ser Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Asn
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Thr Arg Ala Ser Gly Ile Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala
65 70 75 80
Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Leu Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 626
<211> 482
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 626
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Thr Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe
35 40 45
Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr
65 70 75 80
Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg
85 90 95
Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala
100 105 110
Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Arg Ala Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser
145 150 155 160
Pro Ala Thr Leu Ser Val Ser Pro Gly Glu Ser Ala Thr Leu Ser Cys
165 170 175
Arg Ala Ser Gln Ser Val Ser Ser Asn Leu Ala Trp Tyr Gln Gln Lys
180 185 190
Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Thr Arg Ala
195 200 205
Ser Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
210 215 220
Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr
225 230 235 240
Cys Gln Gln Tyr Gly Ser Ser Leu Thr Phe Gly Gly Gly Thr Lys Val
245 250 255
Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
260 265 270
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
275 280 285
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
290 295 300
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
305 310 315 320
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
325 330 335
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
340 345 350
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
355 360 365
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys
370 375 380
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
385 390 395 400
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
405 410 415
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
420 425 430
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
435 440 445
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
450 455 460
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
465 470 475 480
Pro Arg
<210> 627
<211> 1446
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 627
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc aattgctcga aactggagga ggtctggtgc aacctggagg atcacttcgc
120
ctgtcctgcg ccgtgtcggg ctttgccctg tccaaccatg gaatgagctg ggtccgccgc
180
gcgccgggga agggcctcga atgggtgtcc ggcatcgtct actccggctc cacctactac
240
gccgcgtccg tgaagggccg gttcacgatt tcacgggaca actcgcggaa caccctgtac
300
ctccaaatga attcccttcg gccggaggat actgccatct actactgctc cgcccacggt
360
ggcgaatccg acgtctgggg ccagggaacc accgtgaccg tgtccagcgc gtccggggga
420
ggaggaagcg ggggtagagc atcgggtgga ggcggatcag agatcgtgct gacccagtcc
480
cccgccacct tgagcgtgtc accaggagag tccgccaccc tgtcatgccg cgccagccag
540
tccgtgtcct ccaacctggc ttggtaccag cagaagccgg ggcaggcccc tagactcctg
600
atctatgggg cgtcgacccg ggcatctgga attcccgata ggttcagcgg atcgggctcg
660
ggcactgact tcactctgac catctcctcg ctgcaagccg aggacgtggc tgtgtactac
720
tgtcagcagt acggaagctc cctgactttc ggtggcggga ccaaagtcga gattaagacc
780
actaccccag caccgaggcc acccaccccg gctcctacca tcgcctccca gcctctgtcc
840
ctgcgtccgg aggcatgtag acccgcagct ggtggggccg tgcatacccg gggtcttgac
900
ttcgcctgcg atatctacat ttgggcccct ctggctggta cttgcggggt cctgctgctt
960
tcactcgtga tcactcttta ctgtaagcgc ggtcggaaga agctgctgta catctttaag
1020
caacccttca tgaggcctgt gcagactact caagaggagg acggctgttc atgccggttc
1080
ccagaggagg aggaaggcgg ctgcgaactg cgcgtgaaat tcagccgcag cgcagatgct
1140
ccagcctaca agcaggggca gaaccagctc tacaacgaac tcaatcttgg tcggagagag
1200
gagtacgacg tgctggacaa gcggagagga cgggacccag aaatgggcgg gaagccgcgc
1260
agaaagaatc cccaagaggg cctgtacaac gagctccaaa aggataagat ggcagaagcc
1320
tatagcgaga ttggtatgaa aggggaacgc agaagaggca aaggccacga cggactgtac
1380
cagggactca gcaccgccac caaggacacc tatgacgctc ttcacatgca ggccctgccg
1440
cctcgg
1446
<210> 628
<211> 239
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 628
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly
115 120 125
Gly Gly Gly Ser Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser
130 135 140
Val Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser
145 150 155 160
Val Ser Ser Lys Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
165 170 175
Arg Leu Leu Met Tyr Gly Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp
180 185 190
Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser
195 200 205
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly
210 215 220
Ser Ser Ser Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
225 230 235
<210> 629
<211> 717
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 629
gaagtgcaat tggtggaaac tggaggagga cttgtgcaac ctggaggatc attgagactg
60
agctgcgcag tgtcgggatt cgccctgagc aaccatggaa tgtcctgggt cagaagggcc
120
cctggaaaag gcctcgaatg ggtgtcaggg atcgtgtact ccggttccac ttactacgcc
180
gcctccgtga aggggcgctt cactatctca cgggataact cccgcaatac cctgtacctc
240
caaatgaaca gcctgcggcc ggaggatacc gccatctact actgttccgc ccacggtgga
300
gagtctgacg tctggggcca gggaactacc gtgaccgtgt cctccgcgtc cggcggtgga
360
gggagcggcg gccgcgccag cggcggcgga ggctccgaga tcgtgatgac ccagagcccc
420
gctactctgt cggtgtcgcc cggagaaagg gcgaccctgt cctgccgggc gtcgcagtcc
480
gtgagcagca agctggcttg gtaccagcag aagccgggcc aggcaccacg cctgcttatg
540
tacggtgcct ccattcgggc caccggaatc ccggaccggt tctcggggtc ggggtccggt
600
accgagttca cactgaccat ttcctcgctc gagcccgagg actttgccgt ctattactgc
660
cagcagtacg gctcctcctc atggacgttc ggccagggga ccaaggtcga aatcaag
717
<210> 630
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 630
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 631
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 631
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Lys
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Met
35 40 45
Tyr Gly Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Ser Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 632
<211> 483
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 632
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe
35 40 45
Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr
65 70 75 80
Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg
85 90 95
Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala
100 105 110
Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Arg Ala Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr Gln Ser
145 150 155 160
Pro Ala Thr Leu Ser Val Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
165 170 175
Arg Ala Ser Gln Ser Val Ser Ser Lys Leu Ala Trp Tyr Gln Gln Lys
180 185 190
Pro Gly Gln Ala Pro Arg Leu Leu Met Tyr Gly Ala Ser Ile Arg Ala
195 200 205
Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe
210 215 220
Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr
225 230 235 240
Cys Gln Gln Tyr Gly Ser Ser Ser Trp Thr Phe Gly Gln Gly Thr Lys
245 250 255
Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
260 265 270
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
275 280 285
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
290 295 300
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
305 310 315 320
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
325 330 335
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
340 345 350
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
355 360 365
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
370 375 380
Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
385 390 395 400
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
405 410 415
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
420 425 430
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
435 440 445
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
450 455 460
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
465 470 475 480
Pro Pro Arg
<210> 633
<211> 1449
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 633
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc aattggtgga aactggagga ggacttgtgc aacctggagg atcattgaga
120
ctgagctgcg cagtgtcggg attcgccctg agcaaccatg gaatgtcctg ggtcagaagg
180
gcccctggaa aaggcctcga atgggtgtca gggatcgtgt actccggttc cacttactac
240
gccgcctccg tgaaggggcg cttcactatc tcacgggata actcccgcaa taccctgtac
300
ctccaaatga acagcctgcg gccggaggat accgccatct actactgttc cgcccacggt
360
ggagagtctg acgtctgggg ccagggaact accgtgaccg tgtcctccgc gtccggcggt
420
ggagggagcg gcggccgcgc cagcggcggc ggaggctccg agatcgtgat gacccagagc
480
cccgctactc tgtcggtgtc gcccggagaa agggcgaccc tgtcctgccg ggcgtcgcag
540
tccgtgagca gcaagctggc ttggtaccag cagaagccgg gccaggcacc acgcctgctt
600
atgtacggtg cctccattcg ggccaccgga atcccggacc ggttctcggg gtcggggtcc
660
ggtaccgagt tcacactgac catttcctcg ctcgagcccg aggactttgc cgtctattac
720
tgccagcagt acggctcctc ctcatggacg ttcggccagg ggaccaaggt cgaaatcaag
780
accactaccc cagcaccgag gccacccacc ccggctccta ccatcgcctc ccagcctctg
840
tccctgcgtc cggaggcatg tagacccgca gctggtgggg ccgtgcatac ccggggtctt
900
gacttcgcct gcgatatcta catttgggcc cctctggctg gtacttgcgg ggtcctgctg
960
ctttcactcg tgatcactct ttactgtaag cgcggtcgga agaagctgct gtacatcttt
1020
aagcaaccct tcatgaggcc tgtgcagact actcaagagg aggacggctg ttcatgccgg
1080
ttcccagagg aggaggaagg cggctgcgaa ctgcgcgtga aattcagccg cagcgcagat
1140
gctccagcct acaagcaggg gcagaaccag ctctacaacg aactcaatct tggtcggaga
1200
gaggagtacg acgtgctgga caagcggaga ggacgggacc cagaaatggg cgggaagccg
1260
cgcagaaaga atccccaaga gggcctgtac aacgagctcc aaaaggataa gatggcagaa
1320
gcctatagcg agattggtat gaaaggggaa cgcagaagag gcaaaggcca cgacggactg
1380
taccagggac tcagcaccgc caccaaggac acctatgacg ctcttcacat gcaggccctg
1440
ccgcctcgg
1449
<210> 634
<211> 241
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 634
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Val Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly
115 120 125
Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser
130 135 140
Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser
145 150 155 160
Val Gly Ser Thr Asn Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala
165 170 175
Pro Arg Leu Leu Ile Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro
180 185 190
Asp Arg Phe Ser Gly Gly Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
195 200 205
Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr
210 215 220
Gly Ser Ser Pro Pro Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile
225 230 235 240
Lys
<210> 635
<211> 723
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 635
gaagtgcaat tggtggagac tggaggagga gtggtgcaac ctggaggaag cctgagactg
60
tcatgcgcgg tgtcgggctt cgccctctcc aaccacggaa tgtcctgggt ccgccgggcc
120
cctgggaaag gacttgaatg ggtgtccggc atcgtgtact cgggttccac ctactacgcg
180
gcctcagtga agggccggtt tactattagc cgcgacaact ccagaaacac actgtacctc
240
caaatgaact cgctgcggcc ggaagatacc gctatctact actgctccgc ccatggggga
300
gagtcggacg tctggggaca gggcaccact gtcactgtgt ccagcgcttc cggcggtggt
360
ggaagcgggg gacgggcctc aggaggcggt ggcagcgaga ttgtgctgac ccagtccccc
420
gggaccctga gcctgtcccc gggagaaagg gccaccctct cctgtcgggc atcccagtcc
480
gtggggtcta ctaaccttgc atggtaccag cagaagcccg gccaggcccc tcgcctgctg
540
atctacgacg cgtccaatag agccaccggc atcccggatc gcttcagcgg aggcggatcg
600
ggcaccgact tcaccctcac catttcaagg ctggaaccgg aggacttcgc cgtgtactac
660
tgccagcagt atggttcgtc cccaccctgg acgttcggcc aggggactaa ggtcgagatc
720
aag
723
<210> 636
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 636
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Val Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 637
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 637
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Gly Ser Thr
20 25 30
Asn Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Gly Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro
85 90 95
Pro Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 638
<211> 485
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 638
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Thr Gly Gly Gly Val
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe
35 40 45
Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr
65 70 75 80
Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg
85 90 95
Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala
100 105 110
Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Arg Ala Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser
145 150 155 160
Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
165 170 175
Arg Ala Ser Gln Ser Val Gly Ser Thr Asn Leu Ala Trp Tyr Gln Gln
180 185 190
Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Asp Ala Ser Asn Arg
195 200 205
Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Gly Gly Ser Gly Thr Asp
210 215 220
Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr
225 230 235 240
Tyr Cys Gln Gln Tyr Gly Ser Ser Pro Pro Trp Thr Phe Gly Gln Gly
245 250 255
Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
260 265 270
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
275 280 285
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
290 295 300
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
305 310 315 320
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
325 330 335
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
340 345 350
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
355 360 365
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
370 375 380
Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
385 390 395 400
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
405 410 415
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
420 425 430
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
435 440 445
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
450 455 460
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
465 470 475 480
Ala Leu Pro Pro Arg
485
<210> 639
<211> 1455
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 639
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc aattggtgga gactggagga ggagtggtgc aacctggagg aagcctgaga
120
ctgtcatgcg cggtgtcggg cttcgccctc tccaaccacg gaatgtcctg ggtccgccgg
180
gcccctggga aaggacttga atgggtgtcc ggcatcgtgt actcgggttc cacctactac
240
gcggcctcag tgaagggccg gtttactatt agccgcgaca actccagaaa cacactgtac
300
ctccaaatga actcgctgcg gccggaagat accgctatct actactgctc cgcccatggg
360
ggagagtcgg acgtctgggg acagggcacc actgtcactg tgtccagcgc ttccggcggt
420
ggtggaagcg ggggacgggc ctcaggaggc ggtggcagcg agattgtgct gacccagtcc
480
cccgggaccc tgagcctgtc cccgggagaa agggccaccc tctcctgtcg ggcatcccag
540
tccgtggggt ctactaacct tgcatggtac cagcagaagc ccggccaggc ccctcgcctg
600
ctgatctacg acgcgtccaa tagagccacc ggcatcccgg atcgcttcag cggaggcgga
660
tcgggcaccg acttcaccct caccatttca aggctggaac cggaggactt cgccgtgtac
720
tactgccagc agtatggttc gtccccaccc tggacgttcg gccaggggac taaggtcgag
780
atcaagacca ctaccccagc accgaggcca cccaccccgg ctcctaccat cgcctcccag
840
cctctgtccc tgcgtccgga ggcatgtaga cccgcagctg gtggggccgt gcatacccgg
900
ggtcttgact tcgcctgcga tatctacatt tgggcccctc tggctggtac ttgcggggtc
960
ctgctgcttt cactcgtgat cactctttac tgtaagcgcg gtcggaagaa gctgctgtac
1020
atctttaagc aacccttcat gaggcctgtg cagactactc aagaggagga cggctgttca
1080
tgccggttcc cagaggagga ggaaggcggc tgcgaactgc gcgtgaaatt cagccgcagc
1140
gcagatgctc cagcctacaa gcaggggcag aaccagctct acaacgaact caatcttggt
1200
cggagagagg agtacgacgt gctggacaag cggagaggac gggacccaga aatgggcggg
1260
aagccgcgca gaaagaatcc ccaagagggc ctgtacaacg agctccaaaa ggataagatg
1320
gcagaagcct atagcgagat tggtatgaaa ggggaacgca gaagaggcaa aggccacgac
1380
ggactgtacc agggactcag caccgccacc aaggacacct atgacgctct tcacatgcag
1440
gccctgccgc ctcgg
1455
<210> 640
<211> 239
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 640
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Tyr Met Ser Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Ser Gly Asp Gly Met Asp Val Trp Gly Gln Gly Thr Thr
100 105 110
Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala
115 120 125
Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser
130 135 140
Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser
145 150 155 160
Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys
165 170 175
Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val
180 185 190
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
195 200 205
Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln
210 215 220
Ser Tyr Thr Leu Ala Phe Gly Gln Gly Thr Lys Val Asp Ile Lys
225 230 235
<210> 641
<211> 717
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 641
caagtgcaac tcgtggaatc tggtggagga ctcgtgaaac ctggaggatc attgagactg
60
tcatgcgcgg cctcgggatt cacgttctcc gattactaca tgagctggat tcgccaggct
120
ccggggaagg gactggaatg ggtgtcctac atttcctcat ccggctccac catctactac
180
gcggactccg tgaaggggag attcaccatt agccgcgata acgccaagaa cagcctgtac
240
cttcagatga actccctgcg ggctgaagat actgccgtct actactgcgc aagggagagc
300
ggagatggga tggacgtctg gggacagggt accactgtga ccgtgtcgtc ggcctccggc
360
ggagggggtt cgggtggaag ggccagcggc ggcggaggca gcgacatcca gatgacccag
420
tccccctcat cgctgtccgc ctccgtgggc gaccgcgtca ccatcacatg ccgggcctca
480
cagtcgatct cctcctacct caattggtat cagcagaagc ccggaaaggc ccctaagctt
540
ctgatctacg cagcgtcctc cctgcaatcc ggggtcccat ctcggttctc cggctcgggc
600
agcggtaccg acttcactct gaccatctcg agcctgcagc cggaggactt cgccacttac
660
tactgtcagc aaagctacac cctcgcgttt ggccagggca ccaaagtgga catcaag
717
<210> 642
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 642
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Tyr Met Ser Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Ser Gly Asp Gly Met Asp Val Trp Gly Gln Gly Thr Thr
100 105 110
Val Thr Val Ser Ser
115
<210> 643
<211> 105
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 643
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Thr Leu Ala Phe
85 90 95
Gly Gln Gly Thr Lys Val Asp Ile Lys
100 105
<210> 644
<211> 483
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 644
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Lys Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Asp Tyr Tyr Met Ser Trp Ile Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Glu Ser Gly Asp Gly Met Asp Val Trp
115 120 125
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr
145 150 155 160
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
165 170 175
Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln
180 185 190
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser
195 200 205
Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
210 215 220
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
225 230 235 240
Tyr Tyr Cys Gln Gln Ser Tyr Thr Leu Ala Phe Gly Gln Gly Thr Lys
245 250 255
Val Asp Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
260 265 270
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
275 280 285
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
290 295 300
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
305 310 315 320
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
325 330 335
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
340 345 350
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
355 360 365
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
370 375 380
Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
385 390 395 400
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
405 410 415
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
420 425 430
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
435 440 445
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
450 455 460
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
465 470 475 480
Pro Pro Arg
<210> 645
<211> 1449
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 645
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc aactcgtgga atctggtgga ggactcgtga aacctggagg atcattgaga
120
ctgtcatgcg cggcctcggg attcacgttc tccgattact acatgagctg gattcgccag
180
gctccgggga agggactgga atgggtgtcc tacatttcct catccggctc caccatctac
240
tacgcggact ccgtgaaggg gagattcacc attagccgcg ataacgccaa gaacagcctg
300
taccttcaga tgaactccct gcgggctgaa gatactgccg tctactactg cgcaagggag
360
agcggagatg ggatggacgt ctggggacag ggtaccactg tgaccgtgtc gtcggcctcc
420
ggcggagggg gttcgggtgg aagggccagc ggcggcggag gcagcgacat ccagatgacc
480
cagtccccct catcgctgtc cgcctccgtg ggcgaccgcg tcaccatcac atgccgggcc
540
tcacagtcga tctcctccta cctcaattgg tatcagcaga agcccggaaa ggcccctaag
600
cttctgatct acgcagcgtc ctccctgcaa tccggggtcc catctcggtt ctccggctcg
660
ggcagcggta ccgacttcac tctgaccatc tcgagcctgc agccggagga cttcgccact
720
tactactgtc agcaaagcta caccctcgcg tttggccagg gcaccaaagt ggacatcaag
780
accactaccc cagcaccgag gccacccacc ccggctccta ccatcgcctc ccagcctctg
840
tccctgcgtc cggaggcatg tagacccgca gctggtgggg ccgtgcatac ccggggtctt
900
gacttcgcct gcgatatcta catttgggcc cctctggctg gtacttgcgg ggtcctgctg
960
ctttcactcg tgatcactct ttactgtaag cgcggtcgga agaagctgct gtacatcttt
1020
aagcaaccct tcatgaggcc tgtgcagact actcaagagg aggacggctg ttcatgccgg
1080
ttcccagagg aggaggaagg cggctgcgaa ctgcgcgtga aattcagccg cagcgcagat
1140
gctccagcct acaagcaggg gcagaaccag ctctacaacg aactcaatct tggtcggaga
1200
gaggagtacg acgtgctgga caagcggaga ggacgggacc cagaaatggg cgggaagccg
1260
cgcagaaaga atccccaaga gggcctgtac aacgagctcc aaaaggataa gatggcagaa
1320
gcctatagcg agattggtat gaaaggggaa cgcagaagag gcaaaggcca cgacggactg
1380
taccagggac tcagcaccgc caccaaggac acctatgacg ctcttcacat gcaggccctg
1440
ccgcctcgg
1449
<210> 646
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 646
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Tyr Met Ser Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Asn Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Thr Met Val Arg Glu Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala
115 120 125
Ser Gly Gly Gly Gly Ser Asp Ile Val Leu Thr Gln Ser Pro Leu Ser
130 135 140
Leu Pro Val Thr Leu Gly Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser
145 150 155 160
Glu Ser Leu Val His Asn Ser Gly Lys Thr Tyr Leu Asn Trp Phe His
165 170 175
Gln Arg Pro Gly Gln Ser Pro Arg Arg Leu Ile Tyr Glu Val Ser Asn
180 185 190
Arg Asp Ser Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val
210 215 220
Tyr Tyr Cys Met Gln Gly Thr His Trp Pro Gly Thr Phe Gly Gln Gly
225 230 235 240
Thr Lys Leu Glu Ile Lys
245
<210> 647
<211> 738
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 647
caagtgcaac tggtgcaaag cggaggagga ttggtcaaac ccggaggaag cctgagactg
60
tcatgcgcgg cctctggatt caccttctcc gattactaca tgtcatggat cagacaggcc
120
ccggggaagg gcctcgaatg ggtgtcctac atctcgtcct ccgggaacac catctactac
180
gccgacagcg tgaagggccg ctttaccatt tcccgcgaca acgcaaagaa ctcgctgtac
240
cttcagatga attccctgcg ggctgaagat accgcggtgt actattgcgc ccggtccact
300
atggtccggg aggactactg gggacagggc acactcgtga ccgtgtccag cgcgagcggg
360
ggtggaggca gcggtggacg cgcctccggc ggcggcggtt cagacatcgt gctgactcag
420
tcgcccctgt cgctgccggt caccctgggc caaccggcct caattagctg caagtcctcg
480
gagagcctgg tgcacaactc aggaaagact tacctgaact ggttccatca gcggcctgga
540
cagtccccac ggaggctcat ctatgaagtg tccaacaggg attcgggggt gcccgaccgc
600
ttcactggct ccgggtccgg caccgacttc accttgaaaa tctccagagt ggaagccgag
660
gacgtgggcg tgtactactg tatgcagggt acccactggc ctggaacctt tggacaagga
720
actaagctcg agattaag
738
<210> 648
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 648
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Tyr Met Ser Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Asn Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Thr Met Val Arg Glu Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 649
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 649
Asp Ile Val Leu Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1. 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Glu Ser Leu Val His Asn
20 25 30
Ser Gly Lys Thr Tyr Leu Asn Trp Phe His Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Arg Leu Ile Tyr Glu Val Ser Asn Arg Asp Ser Gly Val Pro
50 55 60
Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Gly
85 90 95
Thr His Trp Pro Gly Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 650
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 650
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu
20 25 30
Val Lys Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Asp Tyr Tyr Met Ser Trp Ile Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Tyr Ile Ser Ser Ser Gly Asn Thr Ile Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Ser Thr Met Val Arg Glu Asp Tyr Trp
115 120 125
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Val Leu Thr
145 150 155 160
Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly Gln Pro Ala Ser Ile
165 170 175
Ser Cys Lys Ser Ser Glu Ser Leu Val His Asn Ser Gly Lys Thr Tyr
180 185 190
Leu Asn Trp Phe His Gln Arg Pro Gly Gln Ser Pro Arg Arg Leu Ile
195 200 205
Tyr Glu Val Ser Asn Arg Asp Ser Gly Val Pro Asp Arg Phe Thr Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
225 230 235 240
Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Gly Thr His Trp Pro Gly
245 250 255
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 651
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 651
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc aactggtgca aagcggagga ggattggtca aacccggagg aagcctgaga
120
ctgtcatgcg cggcctctgg attcaccttc tccgattact acatgtcatg gatcagacag
180
gccccgggga agggcctcga atgggtgtcc tacatctcgt cctccgggaa caccatctac
240
tacgccgaca gcgtgaaggg ccgctttacc atttcccgcg acaacgcaaa gaactcgctg
300
taccttcaga tgaattccct gcgggctgaa gataccgcgg tgtactattg cgcccggtcc
360
actatggtcc gggaggacta ctggggacag ggcacactcg tgaccgtgtc cagcgcgagc
420
gggggtggag gcagcggtgg acgcgcctcc ggcggcggcg gttcagacat cgtgctgact
480
cagtcgcccc tgtcgctgcc ggtcaccctg ggccaaccgg cctcaattag ctgcaagtcc
540
tcggagagcc tggtgcacaa ctcaggaaag acttacctga actggttcca tcagcggcct
600
ggacagtccc cacggaggct catctatgaa gtgtccaaca gggattcggg ggtgcccgac
660
cgcttcactg gctccgggtc cggcaccgac ttcaccttga aaatctccag agtggaagcc
720
gaggacgtgg gcgtgtacta ctgtatgcag ggtacccact ggcctggaac ctttggacaa
780
ggaactaagc tcgagattaa gaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 652
<211> 239
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 652
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly
115 120 125
Gly Gly Gly Ser Asp Ile Arg Leu Thr Gln Ser Pro Ser Pro Leu Ser
130 135 140
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Glu Asp
145 150 155 160
Ile Asn Lys Phe Leu Asn Trp Tyr His Gln Thr Pro Gly Lys Ala Pro
165 170 175
Lys Leu Leu Ile Tyr Asp Ala Ser Thr Leu Gln Thr Gly Val Pro Ser
180 185 190
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn
195 200 205
Ser Leu Gln Pro Glu Asp Ile Gly Thr Tyr Tyr Cys Gln Gln Tyr Glu
210 215 220
Ser Leu Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
225 230 235
<210> 653
<211> 717
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 653
caagtgcaac tcgtggaatc tggtggagga ctcgtgcaac ccggtggaag ccttaggctg
60
tcgtgcgccg tcagcgggtt tgctctgagc aaccatggaa tgtcctgggt ccgccgggca
120
ccgggaaaag ggctggaatg ggtgtccggc atcgtgtaca gcgggtcaac ctattacgcc
180
gcgtccgtga agggcagatt cactatctca agagacaaca gccggaacac cctgtacttg
240
caaatgaatt ccctgcgccc cgaggacacc gccatctact actgctccgc ccacggagga
300
gagtcggacg tgtggggcca gggaacgact gtgactgtgt ccagcgcatc aggagggggt
360
ggttcgggcg gccgggcctc ggggggagga ggttccgaca ttcggctgac ccagtccccg
420
tccccactgt cggcctccgt cggcgaccgc gtgaccatca cttgtcaggc gtccgaggac
480
attaacaagt tcctgaactg gtaccaccag acccctggaa aggcccccaa gctgctgatc
540
tacgatgcct cgacccttca aactggagtg cctagccggt tctccgggtc cggctccggc
600
actgatttca ctctgaccat caactcattg cagccggaag atatcgggac ctactattgc
660
cagcagtacg aatccctccc gctcacattc ggcgggggaa ccaaggtcga gattaag
717
<210> 654
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 654
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 655
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 655
Asp Ile Arg Leu Thr Gln Ser Pro Ser Pro Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Glu Asp Ile Asn Lys Phe
20 25 30
Leu Asn Trp Tyr His Gln Thr Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Thr Leu Gln Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Gly Thr Tyr Tyr Cys Gln Gln Tyr Glu Ser Leu Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 656
<211> 483
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 656
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe
35 40 45
Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr
65 70 75 80
Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg
85 90 95
Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala
100 105 110
Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Arg Leu Thr Gln Ser
145 150 155 160
Pro Ser Pro Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys
165 170 175
Gln Ala Ser Glu Asp Ile Asn Lys Phe Leu Asn Trp Tyr His Gln Thr
180 185 190
Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Asp Ala Ser Thr Leu Gln
195 200 205
Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
210 215 220
Thr Leu Thr Ile Asn Ser Leu Gln Pro Glu Asp Ile Gly Thr Tyr Tyr
225 230 235 240
Cys Gln Gln Tyr Glu Ser Leu Pro Leu Thr Phe Gly Gly Gly Thr Lys
245 250 255
Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
260 265 270
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
275 280 285
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
290 295 300
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
305 310 315 320
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
325 330 335
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
340 345 350
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
355 360 365
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
370 375 380
Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
385 390 395 400
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
405 410 415
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
420 425 430
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
435 440 445
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
450 455 460
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
465 470 475 480
Pro Pro Arg
<210> 657
<211> 1449
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 657
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc aactcgtgga atctggtgga ggactcgtgc aacccggtgg aagccttagg
120
ctgtcgtgcg ccgtcagcgg gtttgctctg agcaaccatg gaatgtcctg ggtccgccgg
180
gcaccgggaa aagggctgga atgggtgtcc ggcatcgtgt acagcgggtc aacctattac
240
gccgcgtccg tgaagggcag attcactatc tcaagagaca acagccggaa caccctgtac
300
ttgcaaatga attccctgcg ccccgaggac accgccatct actactgctc cgcccacgga
360
ggagagtcgg acgtgtgggg ccagggaacg actgtgactg tgtccagcgc atcaggaggg
420
ggtggttcgg gcggccgggc ctcgggggga ggaggttccg acattcggct gacccagtcc
480
ccgtccccac tgtcggcctc cgtcggcgac cgcgtgacca tcacttgtca ggcgtccgag
540
gacattaaca agttcctgaa ctggtaccac cagacccctg gaaaggcccc caagctgctg
600
atctacgatg cctcgaccct tcaaactgga gtgcctagcc ggttctccgg gtccggctcc
660
ggcactgatt tcactctgac catcaactca ttgcagccgg aagatatcgg gacctactat
720
tgccagcagt acgaatccct cccgctcaca ttcggcgggg gaaccaaggt cgagattaag
780
accactaccc cagcaccgag gccacccacc ccggctccta ccatcgcctc ccagcctctg
840
tccctgcgtc cggaggcatg tagacccgca gctggtgggg ccgtgcatac ccggggtctt
900
gacttcgcct gcgatatcta catttgggcc cctctggctg gtacttgcgg ggtcctgctg
960
ctttcactcg tgatcactct ttactgtaag cgcggtcgga agaagctgct gtacatcttt
1020
aagcaaccct tcatgaggcc tgtgcagact actcaagagg aggacggctg ttcatgccgg
1080
ttcccagagg aggaggaagg cggctgcgaa ctgcgcgtga aattcagccg cagcgcagat
1140
gctccagcct acaagcaggg gcagaaccag ctctacaacg aactcaatct tggtcggaga
1200
gaggagtacg acgtgctgga caagcggaga ggacgggacc cagaaatggg cgggaagccg
1260
cgcagaaaga atccccaaga gggcctgtac aacgagctcc aaaaggataa gatggcagaa
1320
gcctatagcg agattggtat gaaaggggaa cgcagaagag gcaaaggcca cgacggactg
1380
taccagggac tcagcaccgc caccaaggac acctatgacg ctcttcacat gcaggccctg
1440
ccgcctcgg
1449
<210> 658
<211> 240
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 658
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly
115 120 125
Gly Gly Gly Ser Glu Thr Thr Leu Thr Gln Ser Pro Ala Thr Leu Ser
130 135 140
Val Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser
145 150 155 160
Val Gly Ser Asn Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Gly Pro
165 170 175
Arg Leu Leu Ile Tyr Gly Ala Ser Thr Arg Ala Thr Gly Ile Pro Ala
180 185 190
Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser
195 200 205
Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Asn
210 215 220
Asp Trp Leu Pro Val Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
225 230 235 240
<210> 659
<211> 720
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 659
gaagtgcaat tggtggaaac tggaggagga cttgtgcaac ctggaggatc attgcggctc
60
tcatgcgctg tctccggctt cgccctgtca aatcacggga tgtcgtgggt cagacgggcc
120
ccgggaaagg gtctggaatg ggtgtcgggg attgtgtaca gcggctccac ctactacgcc
180
gcttcggtca agggccgctt cactatttca cgggacaaca gccgcaacac cctctatctg
240
caaatgaact ctctccgccc ggaggatacc gccatctact actgctccgc acacggcggc
300
gaatccgacg tgtggggaca gggaaccact gtcaccgtgt cgtccgcatc cggtggcgga
360
ggatcgggtg gccgggcctc cgggggcggc ggcagcgaga ctaccctgac ccagtcccct
420
gccactctgt ccgtgagccc gggagagaga gccaccctta gctgccgggc cagccagagc
480
gtgggctcca acctggcctg gtaccagcag aagccaggac agggtcccag gctgctgatc
540
tacggagcct ccactcgcgc gaccggcatc cccgcgaggt tctccgggtc gggttccggg
600
accgagttca ccctgaccat ctcctccctc caaccggagg acttcgcggt gtactactgt
660
cagcagtaca acgattggct gcccgtgaca tttggacagg ggacgaaggt ggaaatcaaa
720
<210> 660
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 660
Glu Thr Thr Leu Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Gly Ser Asn
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Gly Pro Arg Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Thr Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Asn Asp Trp Leu Pro
85 90 95
Val Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 661
<211> 484
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 661
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe
35 40 45
Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr
65 70 75 80
Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg
85 90 95
Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala
100 105 110
Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Arg Ala Ser Gly Gly Gly Gly Ser Glu Thr Thr Leu Thr Gln Ser
145 150 155 160
Pro Ala Thr Leu Ser Val Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
165 170 175
Arg Ala Ser Gln Ser Val Gly Ser Asn Leu Ala Trp Tyr Gln Gln Lys
180 185 190
Pro Gly Gln Gly Pro Arg Leu Leu Ile Tyr Gly Ala Ser Thr Arg Ala
195 200 205
Thr Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe
210 215 220
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Tyr
225 230 235 240
Cys Gln Gln Tyr Asn Asp Trp Leu Pro Val Thr Phe Gly Gln Gly Thr
245 250 255
Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro
260 265 270
Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys
275 280 285
Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala
290 295 300
Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu
305 310 315 320
Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys
325 330 335
Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr
340 345 350
Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly
355 360 365
Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala
370 375 380
Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg
385 390 395 400
Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu
405 410 415
Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn
420 425 430
Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met
435 440 445
Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly
450 455 460
Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala
465 470 475 480
Leu Pro Pro Arg
<210> 662
<211> 1452
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 662
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc aattggtgga aactggagga ggacttgtgc aacctggagg atcattgcgg
120
ctctcatgcg ctgtctccgg cttcgccctg tcaaatcacg ggatgtcgtg ggtcagacgg
180
gccccgggaa agggtctgga atgggtgtcg gggattgtgt acagcggctc cacctactac
240
gccgcttcgg tcaagggccg cttcactatt tcacgggaca acagccgcaa caccctctat
300
ctgcaaatga actctctccg cccggaggat accgccatct actactgctc cgcacacggc
360
ggcgaatccg acgtgtgggg acagggaacc actgtcaccg tgtcgtccgc atccggtggc
420
ggaggatcgg gtggccgggc ctccgggggc ggcggcagcg agactaccct gacccagtcc
480
cctgccactc tgtccgtgag cccgggagag agagccaccc ttagctgccg ggccagccag
540
agcgtgggct ccaacctggc ctggtaccag cagaagccag gacagggtcc caggctgctg
600
atctacggag cctccactcg cgcgaccggc atccccgcga ggttctccgg gtcgggttcc
660
gggaccgagt tcaccctgac catctcctcc ctccaaccgg aggacttcgc ggtgtactac
720
tgtcagcagt acaacgattg gctgcccgtg acatttggac aggggacgaa ggtggaaatc
780
aaaaccacta ccccagcacc gaggccaccc accccggctc ctaccatcgc ctcccagcct
840
ctgtccctgc gtccggaggc atgtagaccc gcagctggtg gggccgtgca tacccggggt
900
cttgacttcg cctgcgatat ctacatttgg gcccctctgg ctggtacttg cggggtcctg
960
ctgctttcac tcgtgatcac tctttactgt aagcgcggtc ggaagaagct gctgtacatc
1020
tttaagcaac ccttcatgag gcctgtgcag actactcaag aggaggacgg ctgttcatgc
1080
cggttcccag aggaggagga aggcggctgc gaactgcgcg tgaaattcag ccgcagcgca
1140
gatgctccag cctacaagca ggggcagaac cagctctaca acgaactcaa tcttggtcgg
1200
agagaggagt acgacgtgct ggacaagcgg agaggacggg acccagaaat gggcgggaag
1260
ccgcgcagaa agaatcccca agagggcctg tacaacgagc tccaaaagga taagatggca
1320
gaagcctata gcgagattgg tatgaaaggg gaacgcagaa gaggcaaagg ccacgacgga
1380
ctgtaccagg gactcagcac cgccaccaag gacacctatg acgctcttca catgcaggcc
1440
ctgccgcctc gg
1452
<210> 663
<211> 241
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 663
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly
115 120 125
Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser
130 135 140
Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser
145 150 155 160
Ile Gly Ser Ser Ser Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala
165 170 175
Pro Arg Leu Leu Met Tyr Gly Ala Ser Ser Arg Ala Ser Gly Ile Pro
180 185 190
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
195 200 205
Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr
210 215 220
Ala Gly Ser Pro Pro Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile
225 230 235 240
Lys
<210> 664
<211> 723
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 664
gaagtgcaat tggtggaatc tggtggagga cttgtgcaac ctggaggatc actgagactg
60
tcatgcgcgg tgtccggttt tgccctgagc aatcatggga tgtcgtgggt ccggcgcgcc
120
cccggaaagg gtctggaatg ggtgtcgggt atcgtctact ccgggagcac ttactacgcc
180
gcgagcgtga agggccgctt caccatttcc cgcgataact cccgcaacac cctgtacttg
240
caaatgaact cgctccggcc tgaggacact gccatctact actgctccgc acacggagga
300
gaatccgacg tgtggggcca gggaactacc gtgaccgtca gcagcgcctc cggcggcggg
360
ggctcaggcg gacgggctag cggcggcggt ggctccgaga tcgtgctgac ccagtcgcct
420
ggcactctct cgctgagccc cggggaaagg gcaaccctgt cctgtcgggc cagccagtcc
480
attggatcat cctccctcgc ctggtatcag cagaaaccgg gacaggctcc gcggctgctt
540
atgtatgggg ccagctcaag agcctccggc attcccgacc ggttctccgg gtccggttcc
600
ggcaccgatt tcaccctgac tatctcgagg ctggagccag aggacttcgc cgtgtactac
660
tgccagcagt acgcggggtc cccgccgttc acgttcggac agggaaccaa ggtcgagatc
720
aag
723
<210> 665
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 665
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Gly Ser Ser
20 25 30
Ser Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Gly Ala Ser Ser Arg Ala Ser Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Ala Gly Ser Pro
85 90 95
Pro Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 666
<211> 485
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 666
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe
35 40 45
Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr
65 70 75 80
Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg
85 90 95
Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala
100 105 110
Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Arg Ala Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser
145 150 155 160
Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
165 170 175
Arg Ala Ser Gln Ser Ile Gly Ser Ser Ser Leu Ala Trp Tyr Gln Gln
180 185 190
Lys Pro Gly Gln Ala Pro Arg Leu Leu Met Tyr Gly Ala Ser Ser Arg
195 200 205
Ala Ser Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
210 215 220
Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr
225 230 235 240
Tyr Cys Gln Gln Tyr Ala Gly Ser Pro Pro Phe Thr Phe Gly Gln Gly
245 250 255
Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
260 265 270
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
275 280 285
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
290 295 300
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
305 310 315 320
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
325 330 335
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
340 345 350
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
355 360 365
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
370 375 380
Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
385 390 395 400
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
405 410 415
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
420 425 430
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
435 440 445
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
450 455 460
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
465 470 475 480
Ala Leu Pro Pro Arg
485
<210> 667
<211> 1455
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 667
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc aattggtgga atctggtgga ggacttgtgc aacctggagg atcactgaga
120
ctgtcatgcg cggtgtccgg ttttgccctg agcaatcatg ggatgtcgtg ggtccggcgc
180
gcccccggaa agggtctgga atgggtgtcg ggtatcgtct actccgggag cacttactac
240
gccgcgagcg tgaagggccg cttcaccatt tcccgcgata actcccgcaa caccctgtac
300
ttgcaaatga actcgctccg gcctgaggac actgccatct actactgctc cgcacacgga
360
ggagaatccg acgtgtgggg ccagggaact accgtgaccg tcagcagcgc ctccggcggc
420
gggggctcag gcggacgggc tagcggcggc ggtggctccg agatcgtgct gacccagtcg
480
cctggcactc tctcgctgag ccccggggaa agggcaaccc tgtcctgtcg ggccagccag
540
tccattggat catcctccct cgcctggtat cagcagaaac cgggacaggc tccgcggctg
600
cttatgtatg gggccagctc aagagcctcc ggcattcccg accggttctc cgggtccggt
660
tccggcaccg atttcaccct gactatctcg aggctggagc cagaggactt cgccgtgtac
720
tactgccagc agtacgcggg gtccccgccg ttcacgttcg gacagggaac caaggtcgag
780
atcaagacca ctaccccagc accgaggcca cccaccccgg ctcctaccat cgcctcccag
840
cctctgtccc tgcgtccgga ggcatgtaga cccgcagctg gtggggccgt gcatacccgg
900
ggtcttgact tcgcctgcga tatctacatt tgggcccctc tggctggtac ttgcggggtc
960
ctgctgcttt cactcgtgat cactctttac tgtaagcgcg gtcggaagaa gctgctgtac
1020
atctttaagc aacccttcat gaggcctgtg cagactactc aagaggagga cggctgttca
1080
tgccggttcc cagaggagga ggaaggcggc tgcgaactgc gcgtgaaatt cagccgcagc
1140
gcagatgctc cagcctacaa gcaggggcag aaccagctct acaacgaact caatcttggt
1200
cggagagagg agtacgacgt gctggacaag cggagaggac gggacccaga aatgggcggg
1260
aagccgcgca gaaagaatcc ccaagagggc ctgtacaacg agctccaaaa ggataagatg
1320
gcagaagcct atagcgagat tggtatgaaa ggggaacgca gaagaggcaa aggccacgac
1380
ggactgtacc agggactcag caccgccacc aaggacacct atgacgctct tcacatgcag
1440
gccctgccgc ctcgg
1455
<210> 668
<211> 243
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 668
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1. 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Ser
20 25 30
Tyr Tyr Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Ser Ala Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg His Trp Gln Glu Trp Pro Asp Ala Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Glu Thr Thr Leu Thr Gln Ser Pro
130 135 140
Ala Phe Met Ser Ala Thr Pro Gly Asp Lys Val Ile Ile Ser Cys Lys
145 150 155 160
Ala Ser Gln Asp Ile Asp Asp Ala Met Asn Trp Tyr Gln Gln Lys Pro
165 170 175
Gly Glu Ala Pro Leu Phe Ile Ile Gln Ser Ala Thr Ser Pro Val Pro
180 185 190
Gly Ile Pro Pro Arg Phe Ser Gly Ser Gly Phe Gly Thr Asp Phe Ser
195 200 205
Leu Thr Ile Asn Asn Ile Glu Ser Glu Asp Ala Ala Tyr Tyr Phe Cys
210 215 220
Leu Gln His Asp Asn Phe Pro Leu Thr Phe Gly Gln Gly Thr Lys Leu
225 230 235 240
Glu Ile Lys
<210> 669
<211> 729
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 669
caagtgcagc ttcaggaaag cggaccgggc ctggtcaagc catccgaaac tctctccctg
60
acttgcactg tgtctggcgg ttccatctca tcgtcgtact actactgggg ctggattagg
120
cagccgcccg gaaagggact ggagtggatc ggaagcatct actattccgg ctcggcgtac
180
tacaacccta gcctcaagtc gagagtgacc atctccgtgg atacctccaa gaaccagttt
240
tccctgcgcc tgagctccgt gaccgccgct gacaccgccg tgtactactg tgctcggcat
300
tggcaggaat ggcccgatgc cttcgacatt tggggccagg gcactatggt cactgtgtca
360
tccgggggtg gaggcagcgg gggaggaggg tccggggggg gaggttcaga gacaaccttg
420
acccagtcac ccgcattcat gtccgccact ccgggagaca aggtcatcat ctcgtgcaaa
480
gcgtcccagg atatcgacga tgccatgaat tggtaccagc agaagcctgg cgaagcgccg
540
ctgttcatta tccaatccgc aacctcgccc gtgcctggaa tcccaccgcg gttcagcggc
600
agcggtttcg gaaccgactt ttccctgacc attaacaaca ttgagtccga ggacgccgcc
660
tactacttct gcctgcaaca cgacaacttc cctctcacgt tcggccaggg aaccaagctg
720
gaaatcaag
729
<210> 670
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 670
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1. 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Ser
20 25 30
Tyr Tyr Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Ser Ala Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg His Trp Gln Glu Trp Pro Asp Ala Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 671
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 671
Glu Thr Thr Leu Thr Gln Ser Pro Ala Phe Met Ser Ala Thr Pro Gly
1. 5 10 15
Asp Lys Val Ile Ile Ser Cys Lys Ala Ser Gln Asp Ile Asp Asp Ala
20 25 30
Met Asn Trp Tyr Gln Gln Lys Pro Gly Glu Ala Pro Leu Phe Ile Ile
35 40 45
Gln Ser Ala Thr Ser Pro Val Pro Gly Ile Pro Pro Arg Phe Ser Gly
50 55 60
Ser Gly Phe Gly Thr Asp Phe Ser Leu Thr Ile Asn Asn Ile Glu Ser
65 70 75 80
Glu Asp Ala Ala Tyr Tyr Phe Cys Leu Gln His Asp Asn Phe Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 672
<211> 487
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 672
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Ser Ser Tyr Tyr Tyr Trp Gly Trp Ile Arg Gln Pro Pro
50 55 60
Gly Lys Gly Leu Glu Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Ser Ala
65 70 75 80
Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr
85 90 95
Ser Lys Asn Gln Phe Ser Leu Arg Leu Ser Ser Val Thr Ala Ala Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Ala Arg His Trp Gln Glu Trp Pro Asp Ala
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Thr Thr
145 150 155 160
Leu Thr Gln Ser Pro Ala Phe Met Ser Ala Thr Pro Gly Asp Lys Val
165 170 175
Ile Ile Ser Cys Lys Ala Ser Gln Asp Ile Asp Asp Ala Met Asn Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Glu Ala Pro Leu Phe Ile Ile Gln Ser Ala
195 200 205
Thr Ser Pro Val Pro Gly Ile Pro Pro Arg Phe Ser Gly Ser Gly Phe
210 215 220
Gly Thr Asp Phe Ser Leu Thr Ile Asn Asn Ile Glu Ser Glu Asp Ala
225 230 235 240
Ala Tyr Tyr Phe Cys Leu Gln His Asp Asn Phe Pro Leu Thr Phe Gly
245 250 255
Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
260 265 270
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
275 280 285
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
290 295 300
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
305 310 315 320
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 673
<211> 1461
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 673
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc agcttcagga aagcggaccg ggcctggtca agccatccga aactctctcc
120
ctgacttgca ctgtgtctgg cggttccatc tcatcgtcgt actactactg gggctggatt
180
aggcagccgc ccggaaaggg actggagtgg atcggaagca tctactattc cggctcggcg
240
tactacaacc ctagcctcaa gtcgagagtg accatctccg tggatacctc caagaaccag
300
ttttccctgc gcctgagctc cgtgaccgcc gctgacaccg ccgtgtacta ctgtgctcgg
360
cattggcagg aatggcccga tgccttcgac atttggggcc agggcactat ggtcactgtg
420
tcatccgggg gtggaggcag cgggggagga gggtccgggg ggggaggttc agagacaacc
480
ttgacccagt cacccgcatt catgtccgcc actccgggag acaaggtcat catctcgtgc
540
aaagcgtccc aggatatcga cgatgccatg aattggtacc agcagaagcc tggcgaagcg
600
ccgctgttca ttatccaatc cgcaacctcg cccgtgcctg gaatcccacc gcggttcagc
660
ggcagcggtt tcggaaccga cttttccctg accattaaca acattgagtc cgaggacgcc
720
gcctactact tctgcctgca acacgacaac ttccctctca cgttcggcca gggaaccaag
780
ctggaaatca agaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
840
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
900
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
960
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1020
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1080
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1140
cgcagcgcag atgctccagc ctacaagcag gggcagaacc agctctacaa cgaactcaat
1200
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
1260
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
1320
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
1380
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
1440
atgcaggccc tgccgcctcg g
1461
<210> 674
<211> 244
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 674
Val Asn Leu Arg Glu Ser Gly Pro Ala Leu Val Lys Pro Thr Gln Thr
1. 5 10 15
Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Arg Thr Ser Gly
20 25 30
Met Cys Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu Trp
35 40 45
Leu Ala Arg Ile Asp Trp Asp Glu Asp Lys Phe Tyr Ser Thr Ser Leu
50 55 60
Lys Thr Arg Leu Thr Ile Ser Lys Asp Thr Ser Asp Asn Gln Val Val
65 70 75 80
Leu Arg Met Thr Asn Met Asp Pro Ala Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Arg Ser Gly Ala Gly Gly Thr Ser Ala Thr Ala Phe Asp Ile Trp
100 105 110
Gly Pro Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser
130 135 140
Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys
145 150 155 160
Arg Ala Ser Gln Asp Ile Tyr Asn Asn Leu Ala Trp Phe Gln Leu Lys
165 170 175
Pro Gly Ser Ala Pro Arg Ser Leu Met Tyr Ala Ala Asn Lys Ser Gln
180 185 190
Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Ala Ser Gly Thr Asp Phe
195 200 205
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr
210 215 220
Cys Gln His Tyr Tyr Arg Phe Pro Tyr Ser Phe Gly Gln Gly Thr Lys
225 230 235 240
Leu Glu Ile Lys
<210> 675
<211> 735
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 675
caagtcaatc tgcgcgaatc cggccccgcc ttggtcaagc ctacccagac cctcactctg
60
acctgtactt tctccggctt ctccctgcgg acttccggga tgtgcgtgtc ctggatcaga
120
cagcctccgg gaaaggccct ggagtggctc gctcgcattg actgggatga ggacaagttc
180
tactccacct cactcaagac caggctgacc atcagcaaag atacctctga caaccaagtg
240
gtgctccgca tgaccaacat ggacccagcc gacactgcca cttactactg cgcgaggagc
300
ggagcgggcg gaacctccgc caccgccttc gatatttggg gcccgggtac catggtcacc
360
gtgtcaagcg gaggaggggg gtccgggggc ggcggttccg ggggaggcgg atcggacatt
420
cagatgactc agtcaccatc gtccctgagc gctagcgtgg gcgacagagt gacaatcact
480
tgccgggcat cccaggacat ctataacaac cttgcgtggt tccagctgaa gcctggttcc
540
gcaccgcggt cacttatgta cgccgccaac aagagccagt cgggagtgcc gtcccggttt
600
tccggttcgg cctcgggaac tgacttcacc ctgacgatct ccagcctgca acccgaggat
660
ttcgccacct actactgcca gcactactac cgctttccct actcgttcgg acagggaacc
720
aagctggaaa tcaag
735
<210> 676
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 676
Gln Val Asn Leu Arg Glu Ser Gly Pro Ala Leu Val Lys Pro Thr Gln
1. 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Arg Thr Ser
20 25 30
Gly Met Cys Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu
35 40 45
Trp Leu Ala Arg Ile Asp Trp Asp Glu Asp Lys Phe Tyr Ser Thr Ser
50 55 60
Leu Lys Thr Arg Leu Thr Ile Ser Lys Asp Thr Ser Asp Asn Gln Val
65 70 75 80
Val Leu Arg Met Thr Asn Met Asp Pro Ala Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Ala Arg Ser Gly Ala Gly Gly Thr Ser Ala Thr Ala Phe Asp Ile
100 105 110
Trp Gly Pro Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 677
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 677
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Tyr Asn Asn
20 25 30
Leu Ala Trp Phe Gln Leu Lys Pro Gly Ser Ala Pro Arg Ser Leu Met
35 40 45
Tyr Ala Ala Asn Lys Ser Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Ala Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His Tyr Tyr Arg Phe Pro Tyr
85 90 95
Ser Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 678
<211> 489
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 678
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Asn Leu Arg Glu Ser Gly Pro Ala Leu
20 25 30
Val Lys Pro Thr Gln Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe
35 40 45
Ser Leu Arg Thr Ser Gly Met Cys Val Ser Trp Ile Arg Gln Pro Pro
50 55 60
Gly Lys Ala Leu Glu Trp Leu Ala Arg Ile Asp Trp Asp Glu Asp Lys
65 70 75 80
Phe Tyr Ser Thr Ser Leu Lys Thr Arg Leu Thr Ile Ser Lys Asp Thr
85 90 95
Ser Asp Asn Gln Val Val Leu Arg Met Thr Asn Met Asp Pro Ala Asp
100 105 110
Thr Ala Thr Tyr Tyr Cys Ala Arg Ser Gly Ala Gly Gly Thr Ser Ala
115 120 125
Thr Ala Phe Asp Ile Trp Gly Pro Gly Thr Met Val Thr Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Tyr Asn Asn Leu
180 185 190
Ala Trp Phe Gln Leu Lys Pro Gly Ser Ala Pro Arg Ser Leu Met Tyr
195 200 205
Ala Ala Asn Lys Ser Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Ala Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
225 230 235 240
Asp Phe Ala Thr Tyr Tyr Cys Gln His Tyr Tyr Arg Phe Pro Tyr Ser
245 250 255
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
325 330 335
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
340 345 350
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
355 360 365
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
370 375 380
Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu
385 390 395 400
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
405 410 415
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
420 425 430
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
435 440 445
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
450 455 460
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
465 470 475 480
Leu His Met Gln Ala Leu Pro Pro Arg
485
<210> 679
<211> 1467
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 679
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtca atctgcgcga atccggcccc gccttggtca agcctaccca gaccctcact
120
ctgacctgta ctttctccgg cttctccctg cggacttccg ggatgtgcgt gtcctggatc
180
agacagcctc cgggaaaggc cctggagtgg ctcgctcgca ttgactggga tgaggacaag
240
ttctactcca cctcactcaa gaccaggctg accatcagca aagatacctc tgacaaccaa
300
gtggtgctcc gcatgaccaa catggaccca gccgacactg ccacttacta ctgcgcgagg
360
agcggagcgg gcggaacctc cgccaccgcc ttcgatattt ggggcccggg taccatggtc
420
accgtgtcaa gcggaggagg ggggtccggg ggcggcggtt ccgggggagg cggatcggac
480
attcagatga ctcagtcacc atcgtccctg agcgctagcg tgggcgacag agtgacaatc
540
acttgccggg catcccagga catctataac aaccttgcgt ggttccagct gaagcctggt
600
tccgcaccgc ggtcacttat gtacgccgcc aacaagagcc agtcgggagt gccgtcccgg
660
ttttccggtt cggcctcggg aactgacttc accctgacga tctccagcct gcaacccgag
720
gatttcgcca cctactactg ccagcactac taccgctttc cctactcgtt cggacaggga
780
accaagctgg aaatcaagac cactacccca gcaccgaggc cacccacccc ggctcctacc
840
atcgcctccc agcctctgtc cctgcgtccg gaggcatgta gacccgcagc tggtggggcc
900
gtgcataccc ggggtcttga cttcgcctgc gatatctaca tttgggcccc tctggctggt
960
acttgcgggg tcctgctgct ttcactcgtg atcactcttt actgtaagcg cggtcggaag
1020
aagctgctgt acatctttaa gcaacccttc atgaggcctg tgcagactac tcaagaggag
1080
gacggctgtt catgccggtt cccagaggag gaggaaggcg gctgcgaact gcgcgtgaaa
1140
ttcagccgca gcgcagatgc tccagcctac aagcaggggc agaaccagct ctacaacgaa
1200
ctcaatcttg gtcggagaga ggagtacgac gtgctggaca agcggagagg acgggaccca
1260
gaaatgggcg ggaagccgcg cagaaagaat ccccaagagg gcctgtacaa cgagctccaa
1320
aaggataaga tggcagaagc ctatagcgag attggtatga aaggggaacg cagaagaggc
1380
aaaggccacg acggactgta ccagggactc agcaccgcca ccaaggacac ctatgacgct
1440
cttcacatgc aggccctgcc gcctcgg
1467
<210> 680
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 680
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ser Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Ser Ser Ser Ser Ser Tyr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Thr Ile Ala Ala Val Tyr Ala Phe Asp Ile Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Leu Ser
130 135 140
Leu Pro Val Thr Pro Glu Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser
145 150 155 160
Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu
165 170 175
Gln Lys Pro Gly Gln Ser Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn
180 185 190
Arg Ala Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val
210 215 220
Tyr Tyr Cys Met Gln Ala Leu Gln Thr Pro Tyr Thr Phe Gly Gln Gly
225 230 235 240
Thr Lys Leu Glu Ile Lys
245
<210> 681
<211> 738
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 681
gaagtgcagc ttgtcgaatc cgggggggga ctggtcaagc cgggcggatc actgagactg
60
tcctgcgccg cgagcggctt cacgttctcc tcctactcca tgaactgggt ccgccaagcc
120
cccgggaagg gactggaatg ggtgtcctct atctcctcgt cgtcgtccta catctactac
180
gccgactccg tgaagggaag attcaccatt tcccgcgaca acgcaaagaa ctcactgtac
240
ttgcaaatga actcactccg ggccgaagat actgctgtgt actattgcgc caagactatt
300
gccgccgtct acgctttcga catctggggc cagggaacca ccgtgactgt gtcgtccggt
360
ggtggtggct cgggcggagg aggaagcggc ggcggggggt ccgagattgt gctgacccag
420
tcgccactga gcctccctgt gacccccgag gaacccgcca gcatcagctg ccggtccagc
480
cagtccctgc tccactccaa cggatacaat tacctcgatt ggtaccttca gaagcctgga
540
caaagcccgc agctgctcat ctacttggga tcaaaccgcg cgtcaggagt gcctgaccgg
600
ttctccggct cgggcagcgg taccgatttc accctgaaaa tctccagggt ggaggcagag
660
gacgtgggag tgtattactg tatgcaggcg ctgcagactc cgtacacatt tgggcagggc
720
accaagctgg agatcaag
738
<210> 682
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 682
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ser Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Ser Ser Ser Ser Ser Tyr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Thr Ile Ala Ala Val Tyr Ala Phe Asp Ile Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 683
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 683
Glu Ile Val Leu Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Glu
1. 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 684
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 684
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Lys Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ser Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ser Ile Ser Ser Ser Ser Ser Tyr Ile Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Thr Ile Ala Ala Val Tyr Ala Phe Asp
115 120 125
Ile Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr
145 150 155 160
Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Glu Glu Pro Ala Ser Ile
165 170 175
Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr
180 185 190
Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Gln Leu Leu Ile
195 200 205
Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
225 230 235 240
Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala Leu Gln Thr Pro Tyr
245 250 255
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 685
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 685
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc agcttgtcga atccgggggg ggactggtca agccgggcgg atcactgaga
120
ctgtcctgcg ccgcgagcgg cttcacgttc tcctcctact ccatgaactg ggtccgccaa
180
gcccccggga agggactgga atgggtgtcc tctatctcct cgtcgtcgtc ctacatctac
240
tacgccgact ccgtgaaggg aagattcacc atttcccgcg acaacgcaaa gaactcactg
300
tacttgcaaa tgaactcact ccgggccgaa gatactgctg tgtactattg cgccaagact
360
attgccgccg tctacgcttt cgacatctgg ggccagggaa ccaccgtgac tgtgtcgtcc
420
ggtggtggtg gctcgggcgg aggaggaagc ggcggcgggg ggtccgagat tgtgctgacc
480
cagtcgccac tgagcctccc tgtgaccccc gaggaacccg ccagcatcag ctgccggtcc
540
agccagtccc tgctccactc caacggatac aattacctcg attggtacct tcagaagcct
600
ggacaaagcc cgcagctgct catctacttg ggatcaaacc gcgcgtcagg agtgcctgac
660
cggttctccg gctcgggcag cggtaccgat ttcaccctga aaatctccag ggtggaggca
720
gaggacgtgg gagtgtatta ctgtatgcag gcgctgcaga ctccgtacac atttgggcag
780
ggcaccaagc tggagatcaa gaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 686
<211> 240
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 686
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Tyr Met Ser Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Leu Arg Gly Ala Phe Asp Ile Trp Gly Gln Gly Thr Met
100 105 110
Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Ser Tyr Val Leu Thr Gln Ser Pro Ser Val Ser Ala
130 135 140
Ala Pro Gly Tyr Thr Ala Thr Ile Ser Cys Gly Gly Asn Asn Ile Gly
145 150 155 160
Thr Lys Ser Val His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Leu
165 170 175
Leu Val Ile Arg Asp Asp Ser Val Arg Pro Ser Lys Ile Pro Gly Arg
180 185 190
Phe Ser Gly Ser Asn Ser Gly Asn Met Ala Thr Leu Thr Ile Ser Gly
195 200 205
Val Gln Ala Gly Asp Glu Ala Asp Phe Tyr Cys Gln Val Trp Asp Ser
210 215 220
Asp Ser Glu His Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
225 230 235 240
<210> 687
<211> 720
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 687
gaagtccagc tcgtggagtc cggcggaggc cttgtgaagc ctggaggttc gctgagactg
60
tcctgcgccg cctccggctt caccttctcc gactactaca tgtcctggat cagacaggcc
120
ccgggaaagg gcctggaatg ggtgtcctac atctcgtcat cgggcagcac tatctactac
180
gcggactcag tgaaggggcg gttcaccatt tcccgggata acgcgaagaa ctcgctgtat
240
ctgcaaatga actcactgag ggccgaggac accgccgtgt actactgcgc ccgcgatctc
300
cgcggggcat ttgacatctg gggacaggga accatggtca cagtgtccag cggaggggga
360
ggatcgggtg gcggaggttc cgggggtgga ggctcctcct acgtgctgac tcagagccca
420
agcgtcagcg ctgcgcccgg ttacacggca accatctcct gtggcggaaa caacattggg
480
accaagtctg tgcactggta tcagcagaag ccgggccaag ctcccctgtt ggtgatccgc
540
gatgactccg tgcggcctag caaaattccg ggacggttct ccggctccaa cagcggcaat
600
atggccactc tcaccatctc gggagtgcag gccggagatg aagccgactt ctactgccaa
660
gtctgggact cagactccga gcatgtggtg ttcgggggcg gaaccaagct gactgtgctc
720
<210> 688
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 688
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Tyr Met Ser Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Leu Arg Gly Ala Phe Asp Ile Trp Gly Gln Gly Thr Met
100 105 110
Val Thr Val Ser Ser
115
<210> 689
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 689
Ser Tyr Val Leu Thr Gln Ser Pro Ser Val Ser Ala Ala Pro Gly Tyr
1. 5 10 15
Thr Ala Thr Ile Ser Cys Gly Gly Asn Asn Ile Gly Thr Lys Ser Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Leu Leu Val Ile Arg
35 40 45
Asp Asp Ser Val Arg Pro Ser Lys Ile Pro Gly Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Met Ala Thr Leu Thr Ile Ser Gly Val Gln Ala Gly
65 70 75 80
Asp Glu Ala Asp Phe Tyr Cys Gln Val Trp Asp Ser Asp Ser Glu His
85 90 95
Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 690
<211> 484
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 690
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Lys Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Asp Tyr Tyr Met Ser Trp Ile Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Leu Arg Gly Ala Phe Asp Ile Trp
115 120 125
Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Tyr Val Leu Thr Gln Ser
145 150 155 160
Pro Ser Val Ser Ala Ala Pro Gly Tyr Thr Ala Thr Ile Ser Cys Gly
165 170 175
Gly Asn Asn Ile Gly Thr Lys Ser Val His Trp Tyr Gln Gln Lys Pro
180 185 190
Gly Gln Ala Pro Leu Leu Val Ile Arg Asp Asp Ser Val Arg Pro Ser
195 200 205
Lys Ile Pro Gly Arg Phe Ser Gly Ser Asn Ser Gly Asn Met Ala Thr
210 215 220
Leu Thr Ile Ser Gly Val Gln Ala Gly Asp Glu Ala Asp Phe Tyr Cys
225 230 235 240
Gln Val Trp Asp Ser Asp Ser Glu His Val Val Phe Gly Gly Gly Thr
245 250 255
Lys Leu Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro
260 265 270
Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys
275 280 285
Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala
290 295 300
Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu
305 310 315 320
Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys
325 330 335
Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr
340 345 350
Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly
355 360 365
Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala
370 375 380
Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg
385 390 395 400
Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu
405 410 415
Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn
420 425 430
Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met
435 440 445
Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly
450 455 460
Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala
465 470 475 480
Leu Pro Pro Arg
<210> 691
<211> 1452
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 691
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtcc agctcgtgga gtccggcgga ggccttgtga agcctggagg ttcgctgaga
120
ctgtcctgcg ccgcctccgg cttcaccttc tccgactact acatgtcctg gatcagacag
180
gccccgggaa agggcctgga atgggtgtcc tacatctcgt catcgggcag cactatctac
240
tacgcggact cagtgaaggg gcggttcacc atttcccggg ataacgcgaa gaactcgctg
300
tatctgcaaa tgaactcact gagggccgag gacaccgccg tgtactactg cgcccgcgat
360
ctccgcgggg catttgacat ctggggacag ggaaccatgg tcacagtgtc cagcggaggg
420
ggaggatcgg gtggcggagg ttccgggggt ggaggctcct cctacgtgct gactcagagc
480
ccaagcgtca gcgctgcgcc cggttacacg gcaaccatct cctgtggcgg aaacaacatt
540
gggaccaagt ctgtgcactg gtatcagcag aagccgggcc aagctcccct gttggtgatc
600
cgcgatgact ccgtgcggcc tagcaaaatt ccgggacggt tctccggctc caacagcggc
660
aatatggcca ctctcaccat ctcgggagtg caggccggag atgaagccga cttctactgc
720
caagtctggg actcagactc cgagcatgtg gtgttcgggg gcggaaccaa gctgactgtg
780
ctcaccacta ccccagcacc gaggccaccc accccggctc ctaccatcgc ctcccagcct
840
ctgtccctgc gtccggaggc atgtagaccc gcagctggtg gggccgtgca tacccggggt
900
cttgacttcg cctgcgatat ctacatttgg gcccctctgg ctggtacttg cggggtcctg
960
ctgctttcac tcgtgatcac tctttactgt aagcgcggtc ggaagaagct gctgtacatc
1020
tttaagcaac ccttcatgag gcctgtgcag actactcaag aggaggacgg ctgttcatgc
1080
cggttcccag aggaggagga aggcggctgc gaactgcgcg tgaaattcag ccgcagcgca
1140
gatgctccag cctacaagca ggggcagaac cagctctaca acgaactcaa tcttggtcgg
1200
agagaggagt acgacgtgct ggacaagcgg agaggacggg acccagaaat gggcgggaag
1260
ccgcgcagaa agaatcccca agagggcctg tacaacgagc tccaaaagga taagatggca
1320
gaagcctata gcgagattgg tatgaaaggg gaacgcagaa gaggcaaagg ccacgacgga
1380
ctgtaccagg gactcagcac cgccaccaag gacacctatg acgctcttca catgcaggcc
1440
ctgccgcctc gg
1452
<210> 692
<211> 241
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 692
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Pro Ser Gly Tyr Thr Val Thr Ser His
20 25 30
Tyr Ile His Trp Val Arg Arg Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asn Pro Ser Gly Gly Val Thr Ala Tyr Ser Gln Thr Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Ser Asp Thr Ser Ser Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Ser Gly Ser Gly Trp Tyr Phe Asp Phe Trp Gly Arg
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Ser Tyr Val Leu Thr Gln Pro Pro Ser
130 135 140
Val Ser Val Ser Pro Gly Gln Thr Ala Ser Ile Thr Cys Ser Gly Asp
145 150 155 160
Gly Leu Ser Lys Lys Tyr Val Ser Trp Tyr Gln Gln Lys Ala Gly Gln
165 170 175
Ser Pro Val Val Leu Ile Ser Arg Asp Lys Glu Arg Pro Ser Gly Ile
180 185 190
Pro Asp Arg Phe Ser Gly Ser Asn Ser Ala Asp Thr Ala Thr Leu Thr
195 200 205
Ile Ser Gly Thr Gln Ala Met Asp Glu Ala Asp Tyr Tyr Cys Gln Ala
210 215 220
Trp Asp Asp Thr Thr Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val
225 230 235 240
Leu
<210> 693
<211> 723
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 693
caagtgcagc tggtgcagag cggggccgaa gtcaagaagc cgggagcctc cgtgaaagtg
60
tcctgcaagc cttcgggata caccgtgacc tcccactaca ttcattgggt ccgccgcgcc
120
cccggccaag gactcgagtg gatgggcatg atcaacccta gcggcggagt gaccgcgtac
180
agccagacgc tgcagggacg cgtgactatg acctcggata cctcctcctc caccgtctat
240
atggaactgt ccagcctgcg gtccgaggat accgccatgt actactgcgc ccgggaagga
300
tcaggctccg ggtggtattt cgacttctgg ggaagaggca ccctcgtgac tgtgtcatct
360
gggggagggg gttccggtgg tggcggatcg ggaggaggcg gttcatccta cgtgctgacc
420
cagccaccct ccgtgtccgt gagccccggc cagactgcat cgattacatg tagcggcgac
480
ggcctctcca agaaatacgt gtcgtggtac cagcagaagg ccggacagag cccggtggtg
540
ctgatctcaa gagataagga gcggcctagc ggaatcccgg acaggttctc gggttccaac
600
tccgcggaca ctgctactct gaccatctcg gggacccagg ctatggacga agccgattac
660
tactgccaag cctgggacga cactactgtc gtgtttggag ggggcaccaa gttgaccgtc
720
ctt
723
<210> 694
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 694
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Pro Ser Gly Tyr Thr Val Thr Ser His
20 25 30
Tyr Ile His Trp Val Arg Arg Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asn Pro Ser Gly Gly Val Thr Ala Tyr Ser Gln Thr Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Ser Asp Thr Ser Ser Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Ser Gly Ser Gly Trp Tyr Phe Asp Phe Trp Gly Arg
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 695
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 695
Ser Tyr Val Leu Thr Gln Pro Pro Ser Val Ser Val Ser Pro Gly Gln
1. 5 10 15
Thr Ala Ser Ile Thr Cys Ser Gly Asp Gly Leu Ser Lys Lys Tyr Val
20 25 30
Ser Trp Tyr Gln Gln Lys Ala Gly Gln Ser Pro Val Val Leu Ile Ser
35 40 45
Arg Asp Lys Glu Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser Gly Ser
50 55 60
Asn Ser Ala Asp Thr Ala Thr Leu Thr Ile Ser Gly Thr Gln Ala Met
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Ala Trp Asp Asp Thr Thr Val Val
85 90 95
Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 696
<211> 485
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 696
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Pro Ser Gly Tyr
35 40 45
Thr Val Thr Ser His Tyr Ile His Trp Val Arg Arg Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Met Ile Asn Pro Ser Gly Gly Val Thr Ala
65 70 75 80
Tyr Ser Gln Thr Leu Gln Gly Arg Val Thr Met Thr Ser Asp Thr Ser
85 90 95
Ser Ser Thr Val Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Arg Glu Gly Ser Gly Ser Gly Trp Tyr Phe
115 120 125
Asp Phe Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Tyr Val Leu
145 150 155 160
Thr Gln Pro Pro Ser Val Ser Val Ser Pro Gly Gln Thr Ala Ser Ile
165 170 175
Thr Cys Ser Gly Asp Gly Leu Ser Lys Lys Tyr Val Ser Trp Tyr Gln
180 185 190
Gln Lys Ala Gly Gln Ser Pro Val Val Leu Ile Ser Arg Asp Lys Glu
195 200 205
Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser Gly Ser Asn Ser Ala Asp
210 215 220
Thr Ala Thr Leu Thr Ile Ser Gly Thr Gln Ala Met Asp Glu Ala Asp
225 230 235 240
Tyr Tyr Cys Gln Ala Trp Asp Asp Thr Thr Val Val Phe Gly Gly Gly
245 250 255
Thr Lys Leu Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
260 265 270
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
275 280 285
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
290 295 300
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
305 310 315 320
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
325 330 335
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
340 345 350
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
355 360 365
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
370 375 380
Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
385 390 395 400
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
405 410 415
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
420 425 430
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
435 440 445
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
450 455 460
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
465 470 475 480
Ala Leu Pro Pro Arg
485
<210> 697
<211> 1455
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 697
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc agctggtgca gagcggggcc gaagtcaaga agccgggagc ctccgtgaaa
120
gtgtcctgca agccttcggg atacaccgtg acctcccact acattcattg ggtccgccgc
180
gcccccggcc aaggactcga gtggatgggc atgatcaacc ctagcggcgg agtgaccgcg
240
tacagccaga cgctgcaggg acgcgtgact atgacctcgg atacctcctc ctccaccgtc
300
tatatggaac tgtccagcct gcggtccgag gataccgcca tgtactactg cgcccgggaa
360
ggatcaggct ccgggtggta tttcgacttc tggggaagag gcaccctcgt gactgtgtca
420
tctgggggag ggggttccgg tggtggcgga tcgggaggag gcggttcatc ctacgtgctg
480
acccagccac cctccgtgtc cgtgagcccc ggccagactg catcgattac atgtagcggc
540
gacggcctct ccaagaaata cgtgtcgtgg taccagcaga aggccggaca gagcccggtg
600
gtgctgatct caagagataa ggagcggcct agcggaatcc cggacaggtt ctcgggttcc
660
aactccgcgg acactgctac tctgaccatc tcggggaccc aggctatgga cgaagccgat
720
tactactgcc aagcctggga cgacactact gtcgtgtttg gagggggcac caagttgacc
780
gtccttacca ctaccccagc accgaggcca cccaccccgg ctcctaccat cgcctcccag
840
cctctgtccc tgcgtccgga ggcatgtaga cccgcagctg gtggggccgt gcatacccgg
900
ggtcttgact tcgcctgcga tatctacatt tgggcccctc tggctggtac ttgcggggtc
960
ctgctgcttt cactcgtgat cactctttac tgtaagcgcg gtcggaagaa gctgctgtac
1020
atctttaagc aacccttcat gaggcctgtg cagactactc aagaggagga cggctgttca
1080
tgccggttcc cagaggagga ggaaggcggc tgcgaactgc gcgtgaaatt cagccgcagc
1140
gcagatgctc cagcctacaa gcaggggcag aaccagctct acaacgaact caatcttggt
1200
cggagagagg agtacgacgt gctggacaag cggagaggac gggacccaga aatgggcggg
1260
aagccgcgca gaaagaatcc ccaagagggc ctgtacaacg agctccaaaa ggataagatg
1320
gcagaagcct atagcgagat tggtatgaaa ggggaacgca gaagaggcaa aggccacgac
1380
ggactgtacc agggactcag caccgccacc aaggacacct atgacgctct tcacatgcag
1440
gccctgccgc ctcgg
1455
<210> 698
<211> 245
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 698
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1. 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Gly
20 25 30
Gly Tyr Tyr Trp Ser Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Tyr Ile Tyr Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Ala Gly Ile Ala Ala Arg Leu Arg Gly Ala Phe Asp Ile
100 105 110
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr Gln
130 135 140
Ser Pro Ser Ser Val Ser Ala Ser Val Gly Asp Arg Val Ile Ile Thr
145 150 155 160
Cys Arg Ala Ser Gln Gly Ile Arg Asn Trp Leu Ala Trp Tyr Gln Gln
165 170 175
Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile Tyr Ala Ala Ser Asn Leu
180 185 190
Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Ala Asp
195 200 205
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Val Ala Thr Tyr
210 215 220
Tyr Cys Gln Lys Tyr Asn Ser Ala Pro Phe Thr Phe Gly Pro Gly Thr
225 230 235 240
Lys Val Asp Ile Lys
245
<210> 699
<211> 735
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 699
caagtgcagc ttcaggagag cggcccggga ctcgtgaagc cgtcccagac cctgtccctg
60
acttgcaccg tgtcgggagg aagcatctcg agcggaggct actattggtc gtggattcgg
120
cagcaccctg gaaagggcct ggaatggatc ggctacatct actactccgg ctcgacctac
180
tacaacccat cgctgaagtc cagagtgaca atctcagtgg acacgtccaa gaatcagttc
240
agcctgaagc tctcttccgt gactgcggcc gacaccgccg tgtactactg cgcacgcgct
300
ggaattgccg cccggctgag gggtgccttc gacatttggg gacagggcac catggtcacc
360
gtgtcctccg gcggcggagg ttccgggggt ggaggctcag gaggaggggg gtccgacatc
420
gtcatgactc agtcgccctc aagcgtcagc gcgtccgtcg gggacagagt gatcatcacc
480
tgtcgggcgt cccagggaat tcgcaactgg ctggcctggt atcagcagaa gcccggaaag
540
gcccccaacc tgttgatcta cgccgcctca aacctccaat ccggggtgcc gagccgcttc
600
agcggctccg gttcgggtgc cgatttcact ctgaccatct cctccctgca acctgaagat
660
gtggctacct actactgcca aaagtacaac tccgcacctt ttactttcgg accggggacc
720
aaagtggaca ttaag
735
<210> 700
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 700
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1. 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Gly
20 25 30
Gly Tyr Tyr Trp Ser Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Tyr Ile Tyr Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Ala Gly Ile Ala Ala Arg Leu Arg Gly Ala Phe Asp Ile
100 105 110
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 701
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 701
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Ile Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Asn Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Ala Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Lys Tyr Asn Ser Ala Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 702
<211> 489
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 702
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Ser Gly Gly Tyr Tyr Trp Ser Trp Ile Arg Gln His Pro
50 55 60
Gly Lys Gly Leu Glu Trp Ile Gly Tyr Ile Tyr Tyr Ser Gly Ser Thr
65 70 75 80
Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr
85 90 95
Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Ala Arg Ala Gly Ile Ala Ala Arg Leu Arg
115 120 125
Gly Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Val Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Ile Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Trp Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile Tyr
195 200 205
Ala Ala Ser Asn Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Ala Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
225 230 235 240
Asp Val Ala Thr Tyr Tyr Cys Gln Lys Tyr Asn Ser Ala Pro Phe Thr
245 250 255
Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
325 330 335
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
340 345 350
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
355 360 365
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
370 375 380
Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu
385 390 395 400
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
405 410 415
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
420 425 430
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
435 440 445
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
450 455 460
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
465 470 475 480
Leu His Met Gln Ala Leu Pro Pro Arg
485
<210> 703
<211> 1467
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 703
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc agcttcagga gagcggcccg ggactcgtga agccgtccca gaccctgtcc
120
ctgacttgca ccgtgtcggg aggaagcatc tcgagcggag gctactattg gtcgtggatt
180
cggcagcacc ctggaaaggg cctggaatgg atcggctaca tctactactc cggctcgacc
240
tactacaacc catcgctgaa gtccagagtg acaatctcag tggacacgtc caagaatcag
300
ttcagcctga agctctcttc cgtgactgcg gccgacaccg ccgtgtacta ctgcgcacgc
360
gctggaattg ccgcccggct gaggggtgcc ttcgacattt ggggacaggg caccatggtc
420
accgtgtcct ccggcggcgg aggttccggg ggtggaggct caggaggagg ggggtccgac
480
atcgtcatga ctcagtcgcc ctcaagcgtc agcgcgtccg tcggggacag agtgatcatc
540
acctgtcggg cgtcccaggg aattcgcaac tggctggcct ggtatcagca gaagcccgga
600
aaggccccca acctgttgat ctacgccgcc tcaaacctcc aatccggggt gccgagccgc
660
ttcagcggct ccggttcggg tgccgatttc actctgacca tctcctccct gcaacctgaa
720
gatgtggcta cctactactg ccaaaagtac aactccgcac cttttacttt cggaccgggg
780
accaaagtgg acattaagac cactacccca gcaccgaggc cacccacccc ggctcctacc
840
atcgcctccc agcctctgtc cctgcgtccg gaggcatgta gacccgcagc tggtggggcc
900
gtgcataccc ggggtcttga cttcgcctgc gatatctaca tttgggcccc tctggctggt
960
acttgcgggg tcctgctgct ttcactcgtg atcactcttt actgtaagcg cggtcggaag
1020
aagctgctgt acatctttaa gcaacccttc atgaggcctg tgcagactac tcaagaggag
1080
gacggctgtt catgccggtt cccagaggag gaggaaggcg gctgcgaact gcgcgtgaaa
1140
ttcagccgca gcgcagatgc tccagcctac aagcaggggc agaaccagct ctacaacgaa
1200
ctcaatcttg gtcggagaga ggagtacgac gtgctggaca agcggagagg acgggaccca
1260
gaaatgggcg ggaagccgcg cagaaagaat ccccaagagg gcctgtacaa cgagctccaa
1320
aaggataaga tggcagaagc ctatagcgag attggtatga aaggggaacg cagaagaggc
1380
aaaggccacg acggactgta ccagggactc agcaccgcca ccaaggacac ctatgacgct
1440
cttcacatgc aggccctgcc gcctcgg
1467
<210> 704
<211> 253
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 704
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Gly Gly Tyr Gln Leu Leu Arg Trp Asp Val Gly Leu Leu
100 105 110
Arg Ser Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Ser Tyr Val Leu Thr Gln Pro Pro Ser Val Ser Val Ala Pro Gly Gln
145 150 155 160
Thr Ala Arg Ile Thr Cys Gly Gly Asn Asn Ile Gly Ser Lys Ser Val
165 170 175
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Leu Tyr
180 185 190
Gly Lys Asn Asn Arg Pro Ser Gly Val Pro Asp Arg Phe Ser Gly Ser
195 200 205
Arg Ser Gly Thr Thr Ala Ser Leu Thr Ile Thr Gly Ala Gln Ala Glu
210 215 220
Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Arg Asp Ser Ser Gly Asp His
225 230 235 240
Leu Arg Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
245 250
<210> 705
<211> 759
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 705
caagtgcagc tggtccagtc gggcgccgag gtcaagaagc ccgggagctc tgtgaaagtg
60
tcctgcaagg cctccggggg cacctttagc tcctacgcca tctcctgggt ccgccaagca
120
ccgggtcaag gcctggagtg gatgggggga attatcccta tcttcggcac tgccaactac
180
gcccagaagt tccagggacg cgtgaccatt accgcggacg aatccacctc caccgcttat
240
atggagctgt ccagcttgcg ctcggaagat accgccgtgt actactgcgc ccggaggggt
300
ggataccagc tgctgagatg ggacgtgggc ctcctgcggt cggcgttcga catctggggc
360
cagggcacta tggtcactgt gtccagcgga ggaggcggat cgggaggcgg cggatcaggg
420
ggaggcggtt ccagctacgt gcttactcaa cccccttcgg tgtccgtggc cccgggacag
480
accgccagaa tcacttgcgg aggaaacaac attgggtcca agagcgtgca ttggtaccag
540
cagaagccag gacaggcccc tgtgctggtg ctctacggga agaacaatcg gcccagcgga
600
gtgccggaca ggttctcggg ttcacgctcc ggtacaaccg cttcactgac tatcaccggg
660
gcccaggcag aggatgaagc ggactactac tgttcctccc gggattcatc cggcgaccac
720
ctccgggtgt tcggaaccgg aacgaaggtc accgtgctg
759
<210> 706
<211> 129
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 706
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Gly Gly Tyr Gln Leu Leu Arg Trp Asp Val Gly Leu Leu
100 105 110
Arg Ser Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser
115 120 125
Ser
<210> 707
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 707
Ser Tyr Val Leu Thr Gln Pro Pro Ser Val Ser Val Ala Pro Gly Gln
1. 5 10 15
Thr Ala Arg Ile Thr Cys Gly Gly Asn Asn Ile Gly Ser Lys Ser Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Leu Tyr
35 40 45
Gly Lys Asn Asn Arg Pro Ser Gly Val Pro Asp Arg Phe Ser Gly Ser
50 55 60
Arg Ser Gly Thr Thr Ala Ser Leu Thr Ile Thr Gly Ala Gln Ala Glu
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Arg Asp Ser Ser Gly Asp His
85 90 95
Leu Arg Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
100 105
<210> 708
<211> 497
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 708
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly
35 40 45
Thr Phe Ser Ser Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Arg Gly Gly Tyr Gln Leu Leu Arg Trp
115 120 125
Asp Val Gly Leu Leu Arg Ser Ala Phe Asp Ile Trp Gly Gln Gly Thr
130 135 140
Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Ser Tyr Val Leu Thr Gln Pro Pro Ser Val Ser
165 170 175
Val Ala Pro Gly Gln Thr Ala Arg Ile Thr Cys Gly Gly Asn Asn Ile
180 185 190
Gly Ser Lys Ser Val His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
195 200 205
Val Leu Val Leu Tyr Gly Lys Asn Asn Arg Pro Ser Gly Val Pro Asp
210 215 220
Arg Phe Ser Gly Ser Arg Ser Gly Thr Thr Ala Ser Leu Thr Ile Thr
225 230 235 240
Gly Ala Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Arg Asp
245 250 255
Ser Ser Gly Asp His Leu Arg Val Phe Gly Thr Gly Thr Lys Val Thr
260 265 270
Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
275 280 285
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
290 295 300
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
305 310 315 320
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
325 330 335
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
340 345 350
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
355 360 365
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
370 375 380
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln
385 390 395 400
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
405 410 415
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
420 425 430
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
435 440 445
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
450 455 460
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
465 470 475 480
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
485 490 495
Arg
<210> 709
<211> 1491
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 709
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc agctggtcca gtcgggcgcc gaggtcaaga agcccgggag ctctgtgaaa
120
gtgtcctgca aggcctccgg gggcaccttt agctcctacg ccatctcctg ggtccgccaa
180
gcaccgggtc aaggcctgga gtggatgggg ggaattatcc ctatcttcgg cactgccaac
240
tacgcccaga agttccaggg acgcgtgacc attaccgcgg acgaatccac ctccaccgct
300
tatatggagc tgtccagctt gcgctcggaa gataccgccg tgtactactg cgcccggagg
360
ggtggatacc agctgctgag atgggacgtg ggcctcctgc ggtcggcgtt cgacatctgg
420
ggccagggca ctatggtcac tgtgtccagc ggaggaggcg gatcgggagg cggcggatca
480
gggggaggcg gttccagcta cgtgcttact caaccccctt cggtgtccgt ggccccggga
540
cagaccgcca gaatcacttg cggaggaaac aacattgggt ccaagagcgt gcattggtac
600
cagcagaagc caggacaggc ccctgtgctg gtgctctacg ggaagaacaa tcggcccagc
660
ggagtgccgg acaggttctc gggttcacgc tccggtacaa ccgcttcact gactatcacc
720
ggggcccagg cagaggatga agcggactac tactgttcct cccgggattc atccggcgac
780
cacctccggg tgttcggaac cggaacgaag gtcaccgtgc tgaccactac cccagcaccg
840
aggccaccca ccccggctcc taccatcgcc tcccagcctc tgtccctgcg tccggaggca
900
tgtagacccg cagctggtgg ggccgtgcat acccggggtc ttgacttcgc ctgcgatatc
960
tacatttggg cccctctggc tggtacttgc ggggtcctgc tgctttcact cgtgatcact
1020
ctttactgta agcgcggtcg gaagaagctg ctgtacatct ttaagcaacc cttcatgagg
1080
cctgtgcaga ctactcaaga ggaggacggc tgttcatgcc ggttcccaga ggaggaggaa
1140
ggcggctgcg aactgcgcgt gaaattcagc cgcagcgcag atgctccagc ctacaagcag
1200
gggcagaacc agctctacaa cgaactcaat cttggtcgga gagaggagta cgacgtgctg
1260
gacaagcgga gaggacggga cccagaaatg ggcgggaagc cgcgcagaaa gaatccccaa
1320
gagggcctgt acaacgagct ccaaaaggat aagatggcag aagcctatag cgagattggt
1380
atgaaagggg aacgcagaag aggcaaaggc cacgacggac tgtaccaggg actcagcacc
1440
gccaccaagg acacctatga cgctcttcac atgcaggccc tgccgcctcg g
1491
<210> 710
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 710
Glu Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1. 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Ala Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Ser Phe Tyr Ala
50 55 60
Ile Ser Leu Lys Ser Arg Ile Ile Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Lys Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Arg Ser Ser Pro Glu Gly Leu Phe Leu Tyr Trp Phe
100 105 110
Asp Pro Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Asp
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Ser Glu Leu
130 135 140
Thr Gln Asp Pro Ala Val Ser Val Ala Leu Gly Gln Thr Ile Arg Ile
145 150 155 160
Thr Cys Gln Gly Asp Ser Leu Gly Asn Tyr Tyr Ala Thr Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr Gly Thr Asn Asn
180 185 190
Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser Ala Ser Ser Ser Gly Asn
195 200 205
Thr Ala Ser Leu Thr Ile Thr Gly Ala Gln Ala Glu Asp Glu Ala Asp
210 215 220
Tyr Tyr Cys Asn Ser Arg Asp Ser Ser Gly His His Leu Leu Phe Gly
225 230 235 240
Thr Gly Thr Lys Val Thr Val Leu
245
<210> 711
<211> 744
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 711
gaagtgcagc tccaacagtc aggaccgggg ctcgtgaagc catcccagac cctgtccctg
60
acttgtgcca tctcgggaga tagcgtgtca tcgaactccg ccgcctggaa ctggattcgg
120
cagagcccgt cccgcggact ggagtggctt ggaaggacct actaccggtc caagtggtac
180
tctttctacg cgatctcgct gaagtcccgc attatcatta accctgatac ctccaagaat
240
cagttctccc tccaactgaa atccgtcacc cccgaggaca cagcagtgta ttactgcgca
300
cggagcagcc ccgaaggact gttcctgtat tggtttgacc cctggggcca ggggactctt
360
gtgaccgtgt cgagcggcgg agatgggtcc ggtggcggtg gttcgggggg cggcggatca
420
tcatccgaac tgacccagga cccggctgtg tccgtggcgc tgggacaaac catccgcatt
480
acgtgccagg gagactccct gggcaactac tacgccactt ggtaccagca gaagccgggc
540
caagcccctg tgttggtcat ctacgggacc aacaacagac cttccggcat ccccgaccgg
600
ttcagcgctt cgtcctccgg caacactgcc agcctgacca tcactggagc gcaggccgaa
660
gatgaggccg actactactg caacagcaga gactcctcgg gtcatcacct cttgttcgga
720
actggaacca aggtcaccgt gctg
744
<210> 712
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 712
Glu Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1. 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Ala Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Ser Phe Tyr Ala
50 55 60
Ile Ser Leu Lys Ser Arg Ile Ile Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Lys Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Arg Ser Ser Pro Glu Gly Leu Phe Leu Tyr Trp Phe
100 105 110
Asp Pro Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 713
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 713
Ser Ser Glu Leu Thr Gln Asp Pro Ala Val Ser Val Ala Leu Gly Gln
1. 5 10 15
Thr Ile Arg Ile Thr Cys Gln Gly Asp Ser Leu Gly Asn Tyr Tyr Ala
20 25 30
Thr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Gly Thr Asn Asn Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser Ala Ser
50 55 60
Ser Ser Gly Asn Thr Ala Ser Leu Thr Ile Thr Gly Ala Gln Ala Glu
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Asn Ser Arg Asp Ser Ser Gly His His
85 90 95
Leu Leu Phe Gly Thr Gly Thr Lys Val Thr Val Leu
100 105
<210> 714
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 714
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp
35 40 45
Ser Val Ser Ser Asn Ser Ala Ala Trp Asn Trp Ile Arg Gln Ser Pro
50 55 60
Ser Arg Gly Leu Glu Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp
65 70 75 80
Tyr Ser Phe Tyr Ala Ile Ser Leu Lys Ser Arg Ile Ile Ile Asn Pro
85 90 95
Asp Thr Ser Lys Asn Gln Phe Ser Leu Gln Leu Lys Ser Val Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Ser Pro Glu Gly Leu
115 120 125
Phe Leu Tyr Trp Phe Asp Pro Trp Gly Gln Gly Thr Leu Val Thr Val
130 135 140
Ser Ser Gly Gly Asp Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Ser Ser Glu Leu Thr Gln Asp Pro Ala Val Ser Val Ala Leu Gly
165 170 175
Gln Thr Ile Arg Ile Thr Cys Gln Gly Asp Ser Leu Gly Asn Tyr Tyr
180 185 190
Ala Thr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile
195 200 205
Tyr Gly Thr Asn Asn Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser Ala
210 215 220
Ser Ser Ser Gly Asn Thr Ala Ser Leu Thr Ile Thr Gly Ala Gln Ala
225 230 235 240
Glu Asp Glu Ala Asp Tyr Tyr Cys Asn Ser Arg Asp Ser Ser Gly His
245 250 255
His Leu Leu Phe Gly Thr Gly Thr Lys Val Thr Val Leu Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 715
<211> 1476
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 715
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc agctccaaca gtcaggaccg gggctcgtga agccatccca gaccctgtcc
120
ctgacttgtg ccatctcggg agatagcgtg tcatcgaact ccgccgcctg gaactggatt
180
cggcagagcc cgtcccgcgg actggagtgg cttggaagga cctactaccg gtccaagtgg
240
tactctttct acgcgatctc gctgaagtcc cgcattatca ttaaccctga tacctccaag
300
aatcagttct ccctccaact gaaatccgtc acccccgagg acacagcagt gtattactgc
360
gcacggagca gccccgaagg actgttcctg tattggtttg acccctgggg ccaggggact
420
cttgtgaccg tgtcgagcgg cggagatggg tccggtggcg gtggttcggg gggcggcgga
480
tcatcatccg aactgaccca ggacccggct gtgtccgtgg cgctgggaca aaccatccgc
540
attacgtgcc agggagactc cctgggcaac tactacgcca cttggtacca gcagaagccg
600
ggccaagccc ctgtgttggt catctacggg accaacaaca gaccttccgg catccccgac
660
cggttcagcg cttcgtcctc cggcaacact gccagcctga ccatcactgg agcgcaggcc
720
gaagatgagg ccgactacta ctgcaacagc agagactcct cgggtcatca cctcttgttc
780
ggaactggaa ccaaggtcac cgtgctgacc actaccccag caccgaggcc acccaccccg
840
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
900
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
960
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1020
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1080
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1140
cgcgtgaaat tcagccgcag cgcagatgct ccagcctaca agcaggggca gaaccagctc
1200
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
1260
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
1320
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
1380
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
1440
tatgacgctc ttcacatgca ggccctgccg cctcgg
1476
<210> 716
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 716
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Val Glu Gly Ser Gly Ser Leu Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Glu Ile Val Met Thr Gln Ser Pro Gly Thr Leu
130 135 140
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
145 150 155 160
Ser Val Ser Ser Ala Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
165 170 175
Pro Pro Arg Leu Leu Ile Ser Gly Ala Ser Thr Arg Ala Thr Gly Ile
180 185 190
Pro Asp Arg Phe Gly Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
195 200 205
Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His
210 215 220
Tyr Gly Ser Ser Phe Asn Gly Ser Ser Leu Phe Thr Phe Gly Gln Gly
225 230 235 240
Thr Arg Leu Glu Ile Lys
245
<210> 717
<211> 738
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 717
gaagtgcagc tcgtggagtc aggaggcggc ctggtccagc cgggagggtc ccttagactg
60
tcatgcgccg caagcggatt cactttctcc tcctatgcca tgagctgggt ccgccaagcc
120
cccggaaagg gactggaatg ggtgtccgcc atctcggggt ctggaggctc aacttactac
180
gctgactccg tgaagggacg gttcaccatt agccgcgaca actccaagaa caccctctac
240
ctccaaatga actccctgcg ggccgaggat accgccgtct actactgcgc caaagtggaa
300
ggttcaggat cgctggacta ctggggacag ggtactctcg tgaccgtgtc atcgggcgga
360
ggaggttccg gcggtggcgg ctccggcggc ggagggtcgg agatcgtgat gacccagagc
420
cctggtactc tgagcctttc gccgggagaa agggccaccc tgtcctgccg cgcttcccaa
480
tccgtgtcct ccgcgtactt ggcgtggtac cagcagaagc cgggacagcc ccctcggctg
540
ctgatcagcg gggccagcac ccgggcaacc ggaatcccag acagattcgg gggttccggc
600
agcggcacag atttcaccct gactatttcg aggttggagc ccgaggactt tgcggtgtat
660
tactgtcagc actacgggtc gtcctttaat ggctccagcc tgttcacgtt cggacagggg
720
acccgcctgg aaatcaag
738
<210> 718
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 718
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Val Glu Gly Ser Gly Ser Leu Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 719
<211> 113
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 719
Glu Ile Val Met Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ala
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Arg Leu Leu
35 40 45
Ile Ser Gly Ala Ser Thr Arg Ala Thr Gly Ile Pro Asp Arg Phe Gly
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Ser Ser Phe
85 90 95
Asn Gly Ser Ser Leu Phe Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile
100 105 110
Lys
<210> 720
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 720
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Val Glu Gly Ser Gly Ser Leu Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr Gln
145 150 155 160
Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser
165 170 175
Cys Arg Ala Ser Gln Ser Val Ser Ser Ala Tyr Leu Ala Trp Tyr Gln
180 185 190
Gln Lys Pro Gly Gln Pro Pro Arg Leu Leu Ile Ser Gly Ala Ser Thr
195 200 205
Arg Ala Thr Gly Ile Pro Asp Arg Phe Gly Gly Ser Gly Ser Gly Thr
210 215 220
Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val
225 230 235 240
Tyr Tyr Cys Gln His Tyr Gly Ser Ser Phe Asn Gly Ser Ser Leu Phe
245 250 255
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 721
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 721
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc agctcgtgga gtcaggaggc ggcctggtcc agccgggagg gtcccttaga
120
ctgtcatgcg ccgcaagcgg attcactttc tcctcctatg ccatgagctg ggtccgccaa
180
gcccccggaa agggactgga atgggtgtcc gccatctcgg ggtctggagg ctcaacttac
240
tacgctgact ccgtgaaggg acggttcacc attagccgcg acaactccaa gaacaccctc
300
tacctccaaa tgaactccct gcgggccgag gataccgccg tctactactg cgccaaagtg
360
gaaggttcag gatcgctgga ctactgggga cagggtactc tcgtgaccgt gtcatcgggc
420
ggaggaggtt ccggcggtgg cggctccggc ggcggagggt cggagatcgt gatgacccag
480
agccctggta ctctgagcct ttcgccggga gaaagggcca ccctgtcctg ccgcgcttcc
540
caatccgtgt cctccgcgta cttggcgtgg taccagcaga agccgggaca gccccctcgg
600
ctgctgatca gcggggccag cacccgggca accggaatcc cagacagatt cgggggttcc
660
ggcagcggca cagatttcac cctgactatt tcgaggttgg agcccgagga ctttgcggtg
720
tattactgtc agcactacgg gtcgtccttt aatggctcca gcctgttcac gttcggacag
780
gggacccgcc tggaaatcaa gaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 722
<211> 241
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 722
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Ile Thr Phe Ser Arg Tyr
20 25 30
Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Asp Ser Gly Val Ser Thr Tyr Tyr Ala Asp Ser Ala
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Asp Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Thr Arg Ala Gly Ser Glu Ala Ser Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu
130 135 140
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
145 150 155 160
Ser Val Ser Asn Ser Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala
165 170 175
Pro Arg Leu Leu Ile Tyr Asp Ala Ser Ser Arg Ala Thr Gly Ile Pro
180 185 190
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
195 200 205
Ser Arg Leu Glu Pro Glu Asp Phe Ala Ile Tyr Tyr Cys Gln Gln Phe
210 215 220
Gly Thr Ser Ser Gly Leu Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
225 230 235 240
Lys
<210> 723
<211> 723
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 723
gaagtgcaac tggtggaaac cggtggcggc ctggtgcagc ctggaggatc attgaggctg
60
tcatgcgcgg ccagcggtat taccttctcc cggtacccca tgtcctgggt cagacaggcc
120
ccggggaaag ggcttgaatg ggtgtccggg atctcggact ccggtgtcag cacttactac
180
gccgactccg ccaagggacg cttcaccatt tcccgggaca actcgaagaa caccctgttc
240
ctccaaatga gctccctccg ggacgaggat actgcagtgt actactgcgt gacccgcgcc
300
gggtccgagg cgtctgacat ttggggacag ggcactatgg tcaccgtgtc gtccggcgga
360
gggggctcgg gaggcggtgg cagcggagga ggagggtccg agatcgtgct gacccaatcc
420
ccggccaccc tctcgctgag ccctggagaa agggcaacct tgtcctgtcg cgcgagccag
480
tccgtgagca actccctggc ctggtaccag cagaagcccg gacaggctcc gagacttctg
540
atctacgacg cttcgagccg ggccactgga atccccgacc gcttttcggg gtccggctca
600
ggaaccgatt tcaccctgac aatctcacgg ctggagccag aggatttcgc catctattac
660
tgccagcagt tcggtacttc ctccggcctg actttcggag gcggcacgaa gctcgaaatc
720
aag
723
<210> 724
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 724
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Ile Thr Phe Ser Arg Tyr
20 25 30
Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Asp Ser Gly Val Ser Thr Tyr Tyr Ala Asp Ser Ala
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Asp Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Thr Arg Ala Gly Ser Glu Ala Ser Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 725
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 725
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Asn Ser
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Ile Tyr Tyr Cys Gln Gln Phe Gly Thr Ser Ser Gly
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 726
<211> 485
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 726
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Ile
35 40 45
Thr Phe Ser Arg Tyr Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Ser Asp Ser Gly Val Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Ala Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Phe Leu Gln Met Ser Ser Leu Arg Asp Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Val Thr Arg Ala Gly Ser Glu Ala Ser Asp Ile
115 120 125
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln
145 150 155 160
Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser
165 170 175
Cys Arg Ala Ser Gln Ser Val Ser Asn Ser Leu Ala Trp Tyr Gln Gln
180 185 190
Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Asp Ala Ser Ser Arg
195 200 205
Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
210 215 220
Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Ile Tyr
225 230 235 240
Tyr Cys Gln Gln Phe Gly Thr Ser Ser Gly Leu Thr Phe Gly Gly Gly
245 250 255
Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
260 265 270
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
275 280 285
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
290 295 300
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
305 310 315 320
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
325 330 335
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
340 345 350
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
355 360 365
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
370 375 380
Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
385 390 395 400
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
405 410 415
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
420 425 430
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
435 440 445
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
450 455 460
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
465 470 475 480
Ala Leu Pro Pro Arg
485
<210> 727
<211> 1455
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 727
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc aactggtgga aaccggtggc ggcctggtgc agcctggagg atcattgagg
120
ctgtcatgcg cggccagcgg tattaccttc tcccggtacc ccatgtcctg ggtcagacag
180
gccccgggga aagggcttga atgggtgtcc gggatctcgg actccggtgt cagcacttac
240
tacgccgact ccgccaaggg acgcttcacc atttcccggg acaactcgaa gaacaccctg
300
ttcctccaaa tgagctccct ccgggacgag gatactgcag tgtactactg cgtgacccgc
360
gccgggtccg aggcgtctga catttgggga cagggcacta tggtcaccgt gtcgtccggc
420
ggagggggct cgggaggcgg tggcagcgga ggaggagggt ccgagatcgt gctgacccaa
480
tccccggcca ccctctcgct gagccctgga gaaagggcaa ccttgtcctg tcgcgcgagc
540
cagtccgtga gcaactccct ggcctggtac cagcagaagc ccggacaggc tccgagactt
600
ctgatctacg acgcttcgag ccgggccact ggaatccccg accgcttttc ggggtccggc
660
tcaggaaccg atttcaccct gacaatctca cggctggagc cagaggattt cgccatctat
720
tactgccagc agttcggtac ttcctccggc ctgactttcg gaggcggcac gaagctcgaa
780
atcaagacca ctaccccagc accgaggcca cccaccccgg ctcctaccat cgcctcccag
840
cctctgtccc tgcgtccgga ggcatgtaga cccgcagctg gtggggccgt gcatacccgg
900
ggtcttgact tcgcctgcga tatctacatt tgggcccctc tggctggtac ttgcggggtc
960
ctgctgcttt cactcgtgat cactctttac tgtaagcgcg gtcggaagaa gctgctgtac
1020
atctttaagc aacccttcat gaggcctgtg cagactactc aagaggagga cggctgttca
1080
tgccggttcc cagaggagga ggaaggcggc tgcgaactgc gcgtgaaatt cagccgcagc
1140
gcagatgctc cagcctacaa gcaggggcag aaccagctct acaacgaact caatcttggt
1200
cggagagagg agtacgacgt gctggacaag cggagaggac gggacccaga aatgggcggg
1260
aagccgcgca gaaagaatcc ccaagagggc ctgtacaacg agctccaaaa ggataagatg
1320
gcagaagcct atagcgagat tggtatgaaa ggggaacgca gaagaggcaa aggccacgac
1380
ggactgtacc agggactcag caccgccacc aaggacacct atgacgctct tcacatgcag
1440
gccctgccgc ctcgg
1455
<210> 728
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 728
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Ile Tyr Tyr Cys
85 90 95
Ala Arg Ala Thr Tyr Lys Arg Glu Leu Arg Tyr Tyr Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr
130 135 140
Gln Ser Pro Gly Thr Val Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu
145 150 155 160
Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser Phe Leu Ala Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser
180 185 190
Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Ser Ala
210 215 220
Val Tyr Tyr Cys Gln Gln Tyr His Ser Ser Pro Ser Trp Thr Phe Gly
225 230 235 240
Gln Gly Thr Arg Leu Glu Ile Lys
245
<210> 729
<211> 744
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 729
caagtgcagc tcgtggaatc gggtggcgga ctggtgcagc cggggggctc acttagactg
60
tcctgcgcgg ccagcggatt cactttctcc tcctacgcca tgtcctgggt cagacaggcc
120
cctggaaagg gcctggaatg ggtgtccgca atcagcggca gcggcggctc gacctattac
180
gcggattcag tgaagggcag attcaccatt tcccgggaca acgccaagaa ctccttgtac
240
cttcaaatga actccctccg cgcggaagat accgcaatct actactgcgc tcgggccact
300
tacaagaggg aactgcgcta ctactacggg atggacgtct ggggccaggg aaccatggtc
360
accgtgtcca gcggaggagg aggatcggga ggaggcggta gcgggggtgg agggtcggag
420
atcgtgatga cccagtcccc cggcactgtg tcgctgtccc ccggcgaacg ggccaccctg
480
tcatgtcggg ccagccagtc agtgtcgtca agcttcctcg cctggtacca gcagaaaccg
540
ggacaagctc cccgcctgct gatctacgga gccagcagcc gggccaccgg tattcctgac
600
cggttctccg gttcggggtc cgggaccgac tttactctga ctatctctcg cctcgagcca
660
gaggactccg ccgtgtatta ctgccagcag taccactcct ccccgtcctg gacgttcgga
720
cagggcacaa ggctggagat taag
744
<210> 730
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 730
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Ile Tyr Tyr Cys
85 90 95
Ala Arg Ala Thr Tyr Lys Arg Glu Leu Arg Tyr Tyr Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 731
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 731
Glu Ile Val Met Thr Gln Ser Pro Gly Thr Val Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Ser Ala Val Tyr Tyr Cys Gln Gln Tyr His Ser Ser Pro
85 90 95
Ser Trp Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 732
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 732
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Ile Tyr Tyr Cys Ala Arg Ala Thr Tyr Lys Arg Glu Leu Arg Tyr
115 120 125
Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Met Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Glu Ile Val Met Thr Gln Ser Pro Gly Thr Val Ser Leu Ser Pro Gly
165 170 175
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
180 185 190
Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
195 200 205
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
225 230 235 240
Pro Glu Asp Ser Ala Val Tyr Tyr Cys Gln Gln Tyr His Ser Ser Pro
245 250 255
Ser Trp Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 733
<211> 1476
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 733
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc agctcgtgga atcgggtggc ggactggtgc agccgggggg ctcacttaga
120
ctgtcctgcg cggccagcgg attcactttc tcctcctacg ccatgtcctg ggtcagacag
180
gcccctggaa agggcctgga atgggtgtcc gcaatcagcg gcagcggcgg ctcgacctat
240
tacgcggatt cagtgaaggg cagattcacc atttcccggg acaacgccaa gaactccttg
300
taccttcaaa tgaactccct ccgcgcggaa gataccgcaa tctactactg cgctcgggcc
360
acttacaaga gggaactgcg ctactactac gggatggacg tctggggcca gggaaccatg
420
gtcaccgtgt ccagcggagg aggaggatcg ggaggaggcg gtagcggggg tggagggtcg
480
gagatcgtga tgacccagtc ccccggcact gtgtcgctgt cccccggcga acgggccacc
540
ctgtcatgtc gggccagcca gtcagtgtcg tcaagcttcc tcgcctggta ccagcagaaa
600
ccgggacaag ctccccgcct gctgatctac ggagccagca gccgggccac cggtattcct
660
gaccggttct ccggttcggg gtccgggacc gactttactc tgactatctc tcgcctcgag
720
ccagaggact ccgccgtgta ttactgccag cagtaccact cctccccgtc ctggacgttc
780
ggacagggca caaggctgga gattaagacc actaccccag caccgaggcc acccaccccg
840
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
900
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
960
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1020
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1080
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1140
cgcgtgaaat tcagccgcag cgcagatgct ccagcctaca agcaggggca gaaccagctc
1200
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
1260
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
1320
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
1380
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
1440
tatgacgctc ttcacatgca ggccctgccg cctcgg
1476
<210> 734
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 734
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Thr Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Thr Tyr Lys Arg Glu Leu Arg Tyr Tyr Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr
130 135 140
Gln Ser Pro Ser Thr Leu Ser Leu Ser Pro Gly Glu Ser Ala Thr Leu
145 150 155 160
Ser Cys Arg Ala Ser Gln Ser Val Ser Thr Thr Phe Leu Ala Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ser Ser
180 185 190
Asn Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Phe Thr Leu Thr Ile Arg Arg Leu Glu Pro Glu Asp Phe Ala
210 215 220
Val Tyr Tyr Cys Gln Gln Tyr His Ser Ser Pro Ser Trp Thr Phe Gly
225 230 235 240
Gln Gly Thr Lys Val Glu Ile Lys
245
<210> 735
<211> 744
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 735
gaggtgcagc ttgtggaaac cggtggcgga ctggtgcagc ccggaggaag cctcaggctg
60
tcctgcgccg cgtccggctt caccttctcc tcgtacgcca tgtcctgggt ccgccaggcc
120
cccggaaagg gcctggaatg ggtgtccgcc atctctggaa gcggaggttc cacgtactac
180
gcggacagcg tcaagggaag gttcacaatc tcccgcgata attcgaagaa cactctgtac
240
cttcaaatga acaccctgaa ggccgaggac actgctgtgt actactgcgc acgggccacc
300
tacaagagag agctccggta ctactacgga atggacgtct ggggccaggg aactactgtg
360
accgtgtcct cgggaggggg tggctccggg gggggcggct ccggcggagg cggttccgag
420
attgtgctga cccagtcacc ttcaactctg tcgctgtccc cgggagagag cgctactctg
480
agctgccggg ccagccagtc cgtgtccacc accttcctcg cctggtatca gcagaagccg
540
gggcaggcac cacggctctt gatctacggg tcaagcaaca gagcgaccgg aattcctgac
600
cgcttctcgg ggagcggttc aggcaccgac ttcaccctga ctatccggcg cctggaaccc
660
gaagatttcg ccgtgtatta ctgtcaacag taccactcct cgccgtcctg gacctttggc
720
caaggaacca aagtggaaat caag
744
<210> 736
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 736
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Thr Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Thr Tyr Lys Arg Glu Leu Arg Tyr Tyr Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 737
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 737
Glu Ile Val Leu Thr Gln Ser Pro Ser Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Ser Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Thr Thr
20 25 30
Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ser Ser Asn Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Arg Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr His Ser Ser Pro
85 90 95
Ser Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 738
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 738
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Thr Leu Lys Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Ala Thr Tyr Lys Arg Glu Leu Arg Tyr
115 120 125
Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Glu Ile Val Leu Thr Gln Ser Pro Ser Thr Leu Ser Leu Ser Pro Gly
165 170 175
Glu Ser Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Thr Thr
180 185 190
Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
195 200 205
Ile Tyr Gly Ser Ser Asn Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Arg Arg Leu Glu
225 230 235 240
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr His Ser Ser Pro
245 250 255
Ser Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 739
<211> 1476
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 739
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaggtgc agcttgtgga aaccggtggc ggactggtgc agcccggagg aagcctcagg
120
ctgtcctgcg ccgcgtccgg cttcaccttc tcctcgtacg ccatgtcctg ggtccgccag
180
gcccccggaa agggcctgga atgggtgtcc gccatctctg gaagcggagg ttccacgtac
240
tacgcggaca gcgtcaaggg aaggttcaca atctcccgcg ataattcgaa gaacactctg
300
taccttcaaa tgaacaccct gaaggccgag gacactgctg tgtactactg cgcacgggcc
360
acctacaaga gagagctccg gtactactac ggaatggacg tctggggcca gggaactact
420
gtgaccgtgt cctcgggagg gggtggctcc ggggggggcg gctccggcgg aggcggttcc
480
gagattgtgc tgacccagtc accttcaact ctgtcgctgt ccccgggaga gagcgctact
540
ctgagctgcc gggccagcca gtccgtgtcc accaccttcc tcgcctggta tcagcagaag
600
ccggggcagg caccacggct cttgatctac gggtcaagca acagagcgac cggaattcct
660
gaccgcttct cggggagcgg ttcaggcacc gacttcaccc tgactatccg gcgcctggaa
720
cccgaagatt tcgccgtgta ttactgtcaa cagtaccact cctcgccgtc ctggaccttt
780
ggccaaggaa ccaaagtgga aatcaagacc actaccccag caccgaggcc acccaccccg
840
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
900
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
960
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1020
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1080
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1140
cgcgtgaaat tcagccgcag cgcagatgct ccagcctaca agcaggggca gaaccagctc
1200
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
1260
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
1320
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
1380
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
1440
tatgacgctc ttcacatgca ggccctgccg cctcgg
1476
<210> 740
<211> 239
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 740
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Arg
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Asn Ser Gly Ser Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Gly Lys Ala Val Pro Asp Val Trp Gly Gln Gly Thr Thr
100 105 110
Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Asp Ile Val Met Thr Gln Thr Pro Ser Ser Leu Ser
130 135 140
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser
145 150 155 160
Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
165 170 175
Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
180 185 190
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
195 200 205
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr
210 215 220
Ser Thr Pro Tyr Ser Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
225 230 235
<210> 741
<211> 717
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 741
gaagtgcagc tcgtggaaac tggaggtgga ctcgtgcagc ctggacggtc gctgcggctg
60
agctgcgctg catccggctt caccttcgac gattatgcca tgcactgggt cagacaggcg
120
ccagggaagg gacttgagtg ggtgtccggt atcagctgga atagcggctc aatcggatac
180
gcggactccg tgaagggaag gttcaccatt tcccgcgaca acgccaagaa ctccctgtac
240
ttgcaaatga acagcctccg ggatgaggac actgccgtgt actactgcgc ccgcgtcgga
300
aaagctgtgc ccgacgtctg gggccaggga accactgtga ccgtgtccag cggcgggggt
360
ggatcgggcg gtggagggtc cggtggaggg ggctcagata ttgtgatgac ccagaccccc
420
tcgtccctgt ccgcctcggt cggcgaccgc gtgactatca catgtagagc ctcgcagagc
480
atctccagct acctgaactg gtatcagcag aagccgggga aggccccgaa gctcctgatc
540
tacgcggcat catcactgca atcgggagtg ccgagccggt tttccgggtc cggctccggc
600
accgacttca cgctgaccat ttcttccctg caacccgagg acttcgccac ttactactgc
660
cagcagtcct actccacccc ttactccttc ggccaaggaa ccaggctgga aatcaag
717
<210> 742
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 742
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Arg
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Asn Ser Gly Ser Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Gly Lys Ala Val Pro Asp Val Trp Gly Gln Gly Thr Thr
100 105 110
Val Thr Val Ser Ser
115
<210> 743
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 743
Asp Ile Val Met Thr Gln Thr Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Tyr
85 90 95
Ser Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 744
<211> 483
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 744
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Asp Asp Tyr Ala Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Ser Trp Asn Ser Gly Ser Ile Gly
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Val Gly Lys Ala Val Pro Asp Val Trp
115 120 125
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr Gln Thr
145 150 155 160
Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys
165 170 175
Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys
180 185 190
Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln
195 200 205
Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
210 215 220
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr
225 230 235 240
Cys Gln Gln Ser Tyr Ser Thr Pro Tyr Ser Phe Gly Gln Gly Thr Arg
245 250 255
Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
260 265 270
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
275 280 285
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
290 295 300
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
305 310 315 320
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
325 330 335
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
340 345 350
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
355 360 365
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
370 375 380
Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
385 390 395 400
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
405 410 415
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
420 425 430
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
435 440 445
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
450 455 460
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
465 470 475 480
Pro Pro Arg
<210> 745
<211> 1449
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 745
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc agctcgtgga aactggaggt ggactcgtgc agcctggacg gtcgctgcgg
120
ctgagctgcg ctgcatccgg cttcaccttc gacgattatg ccatgcactg ggtcagacag
180
gcgccaggga agggacttga gtgggtgtcc ggtatcagct ggaatagcgg ctcaatcgga
240
tacgcggact ccgtgaaggg aaggttcacc atttcccgcg acaacgccaa gaactccctg
300
tacttgcaaa tgaacagcct ccgggatgag gacactgccg tgtactactg cgcccgcgtc
360
ggaaaagctg tgcccgacgt ctggggccag ggaaccactg tgaccgtgtc cagcggcggg
420
ggtggatcgg gcggtggagg gtccggtgga gggggctcag atattgtgat gacccagacc
480
ccctcgtccc tgtccgcctc ggtcggcgac cgcgtgacta tcacatgtag agcctcgcag
540
agcatctcca gctacctgaa ctggtatcag cagaagccgg ggaaggcccc gaagctcctg
600
atctacgcgg catcatcact gcaatcggga gtgccgagcc ggttttccgg gtccggctcc
660
ggcaccgact tcacgctgac catttcttcc ctgcaacccg aggacttcgc cacttactac
720
tgccagcagt cctactccac cccttactcc ttcggccaag gaaccaggct ggaaatcaag
780
accactaccc cagcaccgag gccacccacc ccggctccta ccatcgcctc ccagcctctg
840
tccctgcgtc cggaggcatg tagacccgca gctggtgggg ccgtgcatac ccggggtctt
900
gacttcgcct gcgatatcta catttgggcc cctctggctg gtacttgcgg ggtcctgctg
960
ctttcactcg tgatcactct ttactgtaag cgcggtcgga agaagctgct gtacatcttt
1020
aagcaaccct tcatgaggcc tgtgcagact actcaagagg aggacggctg ttcatgccgg
1080
ttcccagagg aggaggaagg cggctgcgaa ctgcgcgtga aattcagccg cagcgcagat
1140
gctccagcct acaagcaggg gcagaaccag ctctacaacg aactcaatct tggtcggaga
1200
gaggagtacg acgtgctgga caagcggaga ggacgggacc cagaaatggg cgggaagccg
1260
cgcagaaaga atccccaaga gggcctgtac aacgagctcc aaaaggataa gatggcagaa
1320
gcctatagcg agattggtat gaaaggggaa cgcagaagag gcaaaggcca cgacggactg
1380
taccagggac tcagcaccgc caccaaggac acctatgacg ctcttcacat gcaggccctg
1440
ccgcctcgg
1449
<210> 746
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 746
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1. 5 10 15
Ser Leu Arg Leu Ser Cys Thr Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Arg Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Asn Trp Lys Gly Asn Ser Leu Ala Tyr Gly Asp Ser Val
50 55 60
Lys Gly Arg Phe Ala Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Thr Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser His Gln Gly Val Ala Tyr Tyr Asn Tyr Ala Met Asp Val Trp
100 105 110
Gly Arg Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser
130 135 140
Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
145 150 155 160
Arg Ala Thr Gln Ser Ile Gly Ser Ser Phe Leu Ala Trp Tyr Gln Gln
165 170 175
Arg Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Gln Arg
180 185 190
Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Arg Gly Ser Gly Thr Asp
195 200 205
Phe Thr Leu Thr Ile Ser Arg Val Glu Pro Glu Asp Ser Ala Val Tyr
210 215 220
Tyr Cys Gln His Tyr Glu Ser Ser Pro Ser Trp Thr Phe Gly Gln Gly
225 230 235 240
Thr Lys Val Glu Ile Lys
245
<210> 747
<211> 738
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 747
gaagtgcagc tcgtggagag cgggggagga ttggtgcagc ccggaaggtc cctgcggctc
60
tcctgcactg cgtctggctt caccttcgac gactacgcga tgcactgggt cagacagcgc
120
ccgggaaagg gcctggaatg ggtcgcctca atcaactgga agggaaactc cctggcctat
180
ggcgacagcg tgaagggccg cttcgccatt tcgcgcgaca acgccaagaa caccgtgttt
240
ctgcaaatga attccctgcg gaccgaggat accgctgtgt actactgcgc cagccaccag
300
ggcgtggcat actataacta cgccatggac gtgtggggaa gagggacgct cgtcaccgtg
360
tcctccgggg gcggtggatc gggtggagga ggaagcggtg gcgggggcag cgaaatcgtg
420
ctgactcaga gcccgggaac tctttcactg tccccgggag aacgggccac tctctcgtgc
480
cgggccaccc agtccatcgg ctcctccttc cttgcctggt accagcagag gccaggacag
540
gcgccccgcc tgctgatcta cggtgcttcc caacgcgcca ctggcattcc tgaccggttc
600
agcggcagag ggtcgggaac cgatttcaca ctgaccattt cccgggtgga gcccgaagat
660
tcggcagtct actactgtca gcattacgag tcctcccctt catggacctt cggtcaaggg
720
accaaagtgg agatcaag
738
<210> 748
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 748
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1. 5 10 15
Ser Leu Arg Leu Ser Cys Thr Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Arg Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Asn Trp Lys Gly Asn Ser Leu Ala Tyr Gly Asp Ser Val
50 55 60
Lys Gly Arg Phe Ala Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Thr Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser His Gln Gly Val Ala Tyr Tyr Asn Tyr Ala Met Asp Val Trp
100 105 110
Gly Arg Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 749
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 749
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Thr Gln Ser Ile Gly Ser Ser
20 25 30
Phe Leu Ala Trp Tyr Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Gln Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Arg Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Val Glu
65 70 75 80
Pro Glu Asp Ser Ala Val Tyr Tyr Cys Gln His Tyr Glu Ser Ser Pro
85 90 95
Ser Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 750
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 750
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Thr Ala Ser Gly Phe
35 40 45
Thr Phe Asp Asp Tyr Ala Met His Trp Val Arg Gln Arg Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ala Ser Ile Asn Trp Lys Gly Asn Ser Leu Ala
65 70 75 80
Tyr Gly Asp Ser Val Lys Gly Arg Phe Ala Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Val Phe Leu Gln Met Asn Ser Leu Arg Thr Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Ser His Gln Gly Val Ala Tyr Tyr Asn Tyr
115 120 125
Ala Met Asp Val Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile
145 150 155 160
Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg
165 170 175
Ala Thr Leu Ser Cys Arg Ala Thr Gln Ser Ile Gly Ser Ser Phe Leu
180 185 190
Ala Trp Tyr Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
195 200 205
Gly Ala Ser Gln Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Arg
210 215 220
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Val Glu Pro Glu
225 230 235 240
Asp Ser Ala Val Tyr Tyr Cys Gln His Tyr Glu Ser Ser Pro Ser Trp
245 250 255
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 751
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 751
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc agctcgtgga gagcggggga ggattggtgc agcccggaag gtccctgcgg
120
ctctcctgca ctgcgtctgg cttcaccttc gacgactacg cgatgcactg ggtcagacag
180
cgcccgggaa agggcctgga atgggtcgcc tcaatcaact ggaagggaaa ctccctggcc
240
tatggcgaca gcgtgaaggg ccgcttcgcc atttcgcgcg acaacgccaa gaacaccgtg
300
tttctgcaaa tgaattccct gcggaccgag gataccgctg tgtactactg cgccagccac
360
cagggcgtgg catactataa ctacgccatg gacgtgtggg gaagagggac gctcgtcacc
420
gtgtcctccg ggggcggtgg atcgggtgga ggaggaagcg gtggcggggg cagcgaaatc
480
gtgctgactc agagcccggg aactctttca ctgtccccgg gagaacgggc cactctctcg
540
tgccgggcca cccagtccat cggctcctcc ttccttgcct ggtaccagca gaggccagga
600
caggcgcccc gcctgctgat ctacggtgct tcccaacgcg ccactggcat tcctgaccgg
660
ttcagcggca gagggtcggg aaccgatttc acactgacca tttcccgggt ggagcccgaa
720
gattcggcag tctactactg tcagcattac gagtcctccc cttcatggac cttcggtcaa
780
gggaccaaag tggagatcaa gaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 752
<211> 241
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 752
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Val Val Arg Asp Gly Met Asp Val Trp Gly Gln Gly Thr Thr
100 105 110
Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser
130 135 140
Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser
145 150 155 160
Val Ser Ser Ser Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala
165 170 175
Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro
180 185 190
Asp Arg Phe Ser Gly Asn Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
195 200 205
Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr
210 215 220
Gly Ser Pro Pro Arg Phe Thr Phe Gly Pro Gly Thr Lys Val Asp Ile
225 230 235 240
Lys
<210> 753
<211> 723
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 753
gaggtgcagt tggtcgaaag cgggggcggg cttgtgcagc ctggcggatc actgcggctg
60
tcctgcgcgg catcaggctt cacgttttct tcctacgcca tgtcctgggt gcgccaggcc
120
cctggaaagg gactggaatg ggtgtccgcg atttcggggt ccggcgggag cacctactac
180
gccgattccg tgaagggccg cttcactatc tcgcgggaca actccaagaa caccctctac
240
ctccaaatga atagcctgcg ggccgaggat accgccgtct actattgcgc taaggtcgtg
300
cgcgacggaa tggacgtgtg gggacagggt accaccgtga cagtgtcctc ggggggaggc
360
ggtagcggcg gaggaggaag cggtggtgga ggttccgaga ttgtgctgac tcaatcaccc
420
gcgaccctga gcctgtcccc cggcgaaagg gccactctgt cctgtcgggc cagccaatca
480
gtctcctcct cgtacctggc ctggtaccag cagaagccag gacaggctcc gagactcctt
540
atctatggcg catcctcccg cgccaccgga atcccggata ggttctcggg aaacggatcg
600
gggaccgact tcactctcac catctcccgg ctggaaccgg aggacttcgc cgtgtactac
660
tgccagcagt acggcagccc gcctagattc actttcggcc ccggcaccaa agtggacatc
720
aag
723
<210> 754
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 754
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Val Val Arg Asp Gly Met Asp Val Trp Gly Gln Gly Thr Thr
100 105 110
Val Thr Val Ser Ser
115
<210> 755
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 755
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Asn Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Pro Pro
85 90 95
Arg Phe Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 756
<211> 485
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 756
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Val Val Arg Asp Gly Met Asp Val Trp
115 120 125
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser
145 150 155 160
Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
165 170 175
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala Trp Tyr Gln Gln
180 185 190
Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ser Arg
195 200 205
Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Asn Gly Ser Gly Thr Asp
210 215 220
Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr
225 230 235 240
Tyr Cys Gln Gln Tyr Gly Ser Pro Pro Arg Phe Thr Phe Gly Pro Gly
245 250 255
Thr Lys Val Asp Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
260 265 270
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
275 280 285
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
290 295 300
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
305 310 315 320
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
325 330 335
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
340 345 350
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
355 360 365
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
370 375 380
Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
385 390 395 400
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
405 410 415
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
420 425 430
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
435 440 445
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
450 455 460
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
465 470 475 480
Ala Leu Pro Pro Arg
485
<210> 757
<211> 1455
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 757
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaggtgc agttggtcga aagcgggggc gggcttgtgc agcctggcgg atcactgcgg
120
ctgtcctgcg cggcatcagg cttcacgttt tcttcctacg ccatgtcctg ggtgcgccag
180
gcccctggaa agggactgga atgggtgtcc gcgatttcgg ggtccggcgg gagcacctac
240
tacgccgatt ccgtgaaggg ccgcttcact atctcgcggg acaactccaa gaacaccctc
300
tacctccaaa tgaatagcct gcgggccgag gataccgccg tctactattg cgctaaggtc
360
gtgcgcgacg gaatggacgt gtggggacag ggtaccaccg tgacagtgtc ctcgggggga
420
ggcggtagcg gcggaggagg aagcggtggt ggaggttccg agattgtgct gactcaatca
480
cccgcgaccc tgagcctgtc ccccggcgaa agggccactc tgtcctgtcg ggccagccaa
540
tcagtctcct cctcgtacct ggcctggtac cagcagaagc caggacaggc tccgagactc
600
cttatctatg gcgcatcctc ccgcgccacc ggaatcccgg ataggttctc gggaaacgga
660
tcggggaccg acttcactct caccatctcc cggctggaac cggaggactt cgccgtgtac
720
tactgccagc agtacggcag cccgcctaga ttcactttcg gccccggcac caaagtggac
780
atcaagacca ctaccccagc accgaggcca cccaccccgg ctcctaccat cgcctcccag
840
cctctgtccc tgcgtccgga ggcatgtaga cccgcagctg gtggggccgt gcatacccgg
900
ggtcttgact tcgcctgcga tatctacatt tgggcccctc tggctggtac ttgcggggtc
960
ctgctgcttt cactcgtgat cactctttac tgtaagcgcg gtcggaagaa gctgctgtac
1020
atctttaagc aacccttcat gaggcctgtg cagactactc aagaggagga cggctgttca
1080
tgccggttcc cagaggagga ggaaggcggc tgcgaactgc gcgtgaaatt cagccgcagc
1140
gcagatgctc cagcctacaa gcaggggcag aaccagctct acaacgaact caatcttggt
1200
cggagagagg agtacgacgt gctggacaag cggagaggac gggacccaga aatgggcggg
1260
aagccgcgca gaaagaatcc ccaagagggc ctgtacaacg agctccaaaa ggataagatg
1320
gcagaagcct atagcgagat tggtatgaaa ggggaacgca gaagaggcaa aggccacgac
1380
ggactgtacc agggactcag caccgccacc aaggacacct atgacgctct tcacatgcag
1440
gccctgccgc ctcgg
1455
<210> 758
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 758
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Ile Pro Gln Thr Gly Thr Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu
130 135 140
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
145 150 155 160
Ser Val Ser Ser Ser Tyr Leu Ala Trp Tyr Gln Gln Arg Pro Gly Gln
165 170 175
Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile
180 185 190
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
195 200 205
Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His
210 215 220
Tyr Gly Ser Ser Pro Ser Trp Thr Phe Gly Gln Gly Thr Arg Leu Glu
225 230 235 240
Ile Lys
<210> 759
<211> 726
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 759
gaagtgcagc tgctggagtc cggcggtgga ttggtgcaac cggggggatc gctcagactg
60
tcctgtgcgg cgtcaggctt caccttctcg agctacgcca tgtcatgggt cagacaggcc
120
cctggaaagg gtctggaatg ggtgtccgcc atttccggga gcgggggatc tacatactac
180
gccgatagcg tgaagggccg cttcaccatt tcccgggaca actccaagaa cactctctat
240
ctgcaaatga actccctccg cgctgaggac actgccgtgt actactgcgc caaaatccct
300
cagaccggca ccttcgacta ctggggacag gggactctgg tcaccgtcag cagcggtggc
360
ggaggttcgg ggggaggagg aagcggcggc ggagggtccg agattgtgct gacccagtca
420
cccggcactt tgtccctgtc gcctggagaa agggccaccc tttcctgccg ggcatcccaa
480
tccgtgtcct cctcgtacct ggcctggtac cagcagaggc ccggacaggc cccacggctt
540
ctgatctacg gagcaagcag ccgcgcgacc ggtatcccgg accggttttc gggctcgggc
600
tcaggaactg acttcaccct caccatctcc cgcctggaac ccgaagattt cgctgtgtat
660
tactgccagc actacggcag ctccccgtcc tggacgttcg gccagggaac tcggctggag
720
atcaag
726
<210> 760
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 760
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Ile Pro Gln Thr Gly Thr Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 761
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 761
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Ser Ser Pro
85 90 95
Ser Trp Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 762
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 762
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Ile Pro Gln Thr Gly Thr Phe Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln
145 150 155 160
Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser
165 170 175
Cys Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala Trp Tyr Gln
180 185 190
Gln Arg Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ser
195 200 205
Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
210 215 220
Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val
225 230 235 240
Tyr Tyr Cys Gln His Tyr Gly Ser Ser Pro Ser Trp Thr Phe Gly Gln
245 250 255
Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 763
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 763
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc agctgctgga gtccggcggt ggattggtgc aaccgggggg atcgctcaga
120
ctgtcctgtg cggcgtcagg cttcaccttc tcgagctacg ccatgtcatg ggtcagacag
180
gcccctggaa agggtctgga atgggtgtcc gccatttccg ggagcggggg atctacatac
240
tacgccgata gcgtgaaggg ccgcttcacc atttcccggg acaactccaa gaacactctc
300
tatctgcaaa tgaactccct ccgcgctgag gacactgccg tgtactactg cgccaaaatc
360
cctcagaccg gcaccttcga ctactgggga caggggactc tggtcaccgt cagcagcggt
420
ggcggaggtt cggggggagg aggaagcggc ggcggagggt ccgagattgt gctgacccag
480
tcacccggca ctttgtccct gtcgcctgga gaaagggcca ccctttcctg ccgggcatcc
540
caatccgtgt cctcctcgta cctggcctgg taccagcaga ggcccggaca ggccccacgg
600
cttctgatct acggagcaag cagccgcgcg accggtatcc cggaccggtt ttcgggctcg
660
ggctcaggaa ctgacttcac cctcaccatc tcccgcctgg aacccgaaga tttcgctgtg
720
tattactgcc agcactacgg cagctccccg tcctggacgt tcggccaggg aactcggctg
780
gagatcaaga ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 764
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 764
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Met Ser Arg Glu Asn Asp Lys Asn Ser Val Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Val Glu Asp Thr Gly Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Tyr Lys Arg Glu Leu Arg Tyr Tyr Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr
130 135 140
Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Ser Ala Thr Leu
145 150 155 160
Ser Cys Arg Ala Ser Gln Arg Val Ala Ser Asn Tyr Leu Ala Trp Tyr
165 170 175
Gln His Lys Pro Gly Gln Ala Pro Ser Leu Leu Ile Ser Gly Ala Ser
180 185 190
Ser Arg Ala Thr Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Phe Thr Leu Ala Ile Ser Arg Leu Glu Pro Glu Asp Ser Ala
210 215 220
Val Tyr Tyr Cys Gln His Tyr Asp Ser Ser Pro Ser Trp Thr Phe Gly
225 230 235 240
Gln Gly Thr Lys Val Glu Ile Lys
245
<210> 765
<211> 744
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 765
gaagtgcaac tggtggaaac cggtggagga ctcgtgcagc ctggcggcag cctccggctg
60
agctgcgccg cttcgggatt caccttttcc tcctacgcga tgtcttgggt cagacaggcc
120
cccggaaagg ggctggaatg ggtgtcagcc atctccggct ccggcggatc aacgtactac
180
gccgactccg tgaaaggccg gttcaccatg tcgcgcgaga atgacaagaa ctccgtgttc
240
ctgcaaatga actccctgag ggtggaggac accggagtgt actattgtgc gcgcgccaac
300
tacaagagag agctgcggta ctactacgga atggacgtct ggggacaggg aactatggtg
360
accgtgtcat ccggtggagg gggaagcggc ggtggaggca gcgggggcgg gggttcagaa
420
attgtcatga cccagtcccc gggaactctt tccctctccc ccggggaatc cgcgactttg
480
tcctgccggg ccagccagcg cgtggcctcg aactacctcg catggtacca gcataagcca
540
ggccaagccc cttccctgct gatttccggg gctagcagcc gcgccactgg cgtgccggat
600
aggttctcgg gaagcggctc gggtaccgat ttcaccctgg caatctcgcg gctggaaccg
660
gaggattcgg ccgtgtacta ctgccagcac tatgactcat ccccctcctg gacattcgga
720
cagggcacca aggtcgagat caag
744
<210> 766
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 766
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Met Ser Arg Glu Asn Asp Lys Asn Ser Val Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Val Glu Asp Thr Gly Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Tyr Lys Arg Glu Leu Arg Tyr Tyr Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 767
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 767
Glu Ile Val Met Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Ser Ala Thr Leu Ser Cys Arg Ala Ser Gln Arg Val Ala Ser Asn
20 25 30
Tyr Leu Ala Trp Tyr Gln His Lys Pro Gly Gln Ala Pro Ser Leu Leu
35 40 45
Ile Ser Gly Ala Ser Ser Arg Ala Thr Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Ala Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Ser Ala Val Tyr Tyr Cys Gln His Tyr Asp Ser Ser Pro
85 90 95
Ser Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 768
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 768
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Met Ser Arg Glu Asn Asp
85 90 95
Lys Asn Ser Val Phe Leu Gln Met Asn Ser Leu Arg Val Glu Asp Thr
100 105 110
Gly Val Tyr Tyr Cys Ala Arg Ala Asn Tyr Lys Arg Glu Leu Arg Tyr
115 120 125
Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Met Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Glu Ile Val Met Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
165 170 175
Glu Ser Ala Thr Leu Ser Cys Arg Ala Ser Gln Arg Val Ala Ser Asn
180 185 190
Tyr Leu Ala Trp Tyr Gln His Lys Pro Gly Gln Ala Pro Ser Leu Leu
195 200 205
Ile Ser Gly Ala Ser Ser Arg Ala Thr Gly Val Pro Asp Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Ala Ile Ser Arg Leu Glu
225 230 235 240
Pro Glu Asp Ser Ala Val Tyr Tyr Cys Gln His Tyr Asp Ser Ser Pro
245 250 255
Ser Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 769
<211> 1476
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 769
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc aactggtgga aaccggtgga ggactcgtgc agcctggcgg cagcctccgg
120
ctgagctgcg ccgcttcggg attcaccttt tcctcctacg cgatgtcttg ggtcagacag
180
gcccccggaa aggggctgga atgggtgtca gccatctccg gctccggcgg atcaacgtac
240
tacgccgact ccgtgaaagg ccggttcacc atgtcgcgcg agaatgacaa gaactccgtg
300
ttcctgcaaa tgaactccct gagggtggag gacaccggag tgtactattg tgcgcgcgcc
360
aactacaaga gagagctgcg gtactactac ggaatggacg tctggggaca gggaactatg
420
gtgaccgtgt catccggtgg agggggaagc ggcggtggag gcagcggggg cgggggttca
480
gaaattgtca tgacccagtc cccgggaact ctttccctct cccccgggga atccgcgact
540
ttgtcctgcc gggccagcca gcgcgtggcc tcgaactacc tcgcatggta ccagcataag
600
ccaggccaag ccccttccct gctgatttcc ggggctagca gccgcgccac tggcgtgccg
660
gataggttct cgggaagcgg ctcgggtacc gatttcaccc tggcaatctc gcggctggaa
720
ccggaggatt cggccgtgta ctactgccag cactatgact catccccctc ctggacattc
780
ggacagggca ccaaggtcga gatcaagacc actaccccag caccgaggcc acccaccccg
840
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
900
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
960
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1020
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1080
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1140
cgcgtgaaat tcagccgcag cgcagatgct ccagcctaca agcaggggca gaaccagctc
1200
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
1260
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
1320
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
1380
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
1440
tatgacgctc ttcacatgca ggccctgccg cctcgg
1476
<210> 770
<211> 244
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 770
Glu Val Gln Leu Leu Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Ala Leu Val Gly Ala Thr Gly Ala Phe Asp Ile Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly
130 135 140
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
145 150 155 160
Ser Gln Ser Leu Ser Ser Asn Phe Leu Ala Trp Tyr Gln Gln Lys Pro
165 170 175
Gly Gln Ala Pro Gly Leu Leu Ile Tyr Gly Ala Ser Asn Trp Ala Thr
180 185 190
Gly Thr Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
195 200 205
Leu Thr Ile Thr Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys
210 215 220
Gln Tyr Tyr Gly Thr Ser Pro Met Tyr Thr Phe Gly Gln Gly Thr Lys
225 230 235 240
Val Glu Ile Lys
<210> 771
<211> 732
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 771
gaagtgcagc tgctcgaaac cggtggaggg ctggtgcagc cagggggctc cctgaggctt
60
tcatgcgccg ctagcggatt ctccttctcc tcttacgcca tgtcgtgggt ccgccaagcc
120
cctggaaaag gcctggaatg ggtgtccgcg atttccggga gcggaggttc gacctattac
180
gccgactccg tgaagggccg ctttaccatc tcccgggata actccaagaa cactctgtac
240
ctccaaatga actcgctgag agccgaggac accgccgtgt attactgcgc gaaggcgctg
300
gtcggcgcga ctggggcatt cgacatctgg ggacagggaa ctcttgtgac cgtgtcgagc
360
ggaggcggcg gctccggcgg aggagggagc gggggcggtg gttccgaaat cgtgttgact
420
cagtccccgg gaaccctgag cttgtcaccc ggggagcggg ccactctctc ctgtcgcgcc
480
tcccaatcgc tctcatccaa tttcctggcc tggtaccagc agaagcccgg acaggccccg
540
ggcctgctca tctacggcgc ttcaaactgg gcaacgggaa cccctgatcg gttcagcgga
600
agcggatcgg gtactgactt taccctgacc atcaccagac tggaaccgga ggacttcgcc
660
gtgtactact gccagtacta cggcacctcc cccatgtaca cattcggaca gggtaccaag
720
gtcgagatta ag
732
<210> 772
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 772
Glu Val Gln Leu Leu Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Ala Leu Val Gly Ala Thr Gly Ala Phe Asp Ile Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 773
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 773
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Leu Ser Ser Asn
20 25 30
Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Gly Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Asn Trp Ala Thr Gly Thr Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Thr Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Tyr Tyr Gly Thr Ser Pro
85 90 95
Met Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 774
<211> 488
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 774
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Thr Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Ser Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Ala Leu Val Gly Ala Thr Gly Ala Phe
115 120 125
Asp Ile Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu
145 150 155 160
Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
165 170 175
Leu Ser Cys Arg Ala Ser Gln Ser Leu Ser Ser Asn Phe Leu Ala Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Gln Ala Pro Gly Leu Leu Ile Tyr Gly Ala
195 200 205
Ser Asn Trp Ala Thr Gly Thr Pro Asp Arg Phe Ser Gly Ser Gly Ser
210 215 220
Gly Thr Asp Phe Thr Leu Thr Ile Thr Arg Leu Glu Pro Glu Asp Phe
225 230 235 240
Ala Val Tyr Tyr Cys Gln Tyr Tyr Gly Thr Ser Pro Met Tyr Thr Phe
245 250 255
Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg
260 265 270
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
275 280 285
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
290 295 300
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
305 310 315 320
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg
325 330 335
Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro
340 345 350
Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu
355 360 365
Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala
370 375 380
Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
385 390 395 400
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
405 410 415
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
420 425 430
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
435 440 445
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
450 455 460
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
465 470 475 480
His Met Gln Ala Leu Pro Pro Arg
485
<210> 775
<211> 1464
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 775
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc agctgctcga aaccggtgga gggctggtgc agccaggggg ctccctgagg
120
ctttcatgcg ccgctagcgg attctccttc tcctcttacg ccatgtcgtg ggtccgccaa
180
gcccctggaa aaggcctgga atgggtgtcc gcgatttccg ggagcggagg ttcgacctat
240
tacgccgact ccgtgaaggg ccgctttacc atctcccggg ataactccaa gaacactctg
300
tacctccaaa tgaactcgct gagagccgag gacaccgccg tgtattactg cgcgaaggcg
360
ctggtcggcg cgactggggc attcgacatc tggggacagg gaactcttgt gaccgtgtcg
420
agcggaggcg gcggctccgg cggaggaggg agcgggggcg gtggttccga aatcgtgttg
480
actcagtccc cgggaaccct gagcttgtca cccggggagc gggccactct ctcctgtcgc
540
gcctcccaat cgctctcatc caatttcctg gcctggtacc agcagaagcc cggacaggcc
600
ccgggcctgc tcatctacgg cgcttcaaac tgggcaacgg gaacccctga tcggttcagc
660
ggaagcggat cgggtactga ctttaccctg accatcacca gactggaacc ggaggacttc
720
gccgtgtact actgccagta ctacggcacc tcccccatgt acacattcgg acagggtacc
780
aaggtcgaga ttaagaccac taccccagca ccgaggccac ccaccccggc tcctaccatc
840
gcctcccagc ctctgtccct gcgtccggag gcatgtagac ccgcagctgg tggggccgtg
900
catacccggg gtcttgactt cgcctgcgat atctacattt gggcccctct ggctggtact
960
tgcggggtcc tgctgctttc actcgtgatc actctttact gtaagcgcgg tcggaagaag
1020
ctgctgtaca tctttaagca acccttcatg aggcctgtgc agactactca agaggaggac
1080
ggctgttcat gccggttccc agaggaggag gaaggcggct gcgaactgcg cgtgaaattc
1140
agccgcagcg cagatgctcc agcctacaag caggggcaga accagctcta caacgaactc
1200
aatcttggtc ggagagagga gtacgacgtg ctggacaagc ggagaggacg ggacccagaa
1260
atgggcggga agccgcgcag aaagaatccc caagagggcc tgtacaacga gctccaaaag
1320
gataagatgg cagaagccta tagcgagatt ggtatgaaag gggaacgcag aagaggcaaa
1380
ggccacgacg gactgtacca gggactcagc accgccacca aggacaccta tgacgctctt
1440
cacatgcagg ccctgccgcc tcgg
1464
<210> 776
<211> 244
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 776
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Trp Phe Gly Glu Gly Phe Asp Pro Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Asp Ile Val Leu Thr Gln Ser Pro Leu Ser Leu Pro
130 135 140
Val Thr Pro Gly Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser
145 150 155 160
Leu Leu His Ser Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys
165 170 175
Pro Gly Gln Ser Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala
180 185 190
Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
195 200 205
Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr
210 215 220
Cys Met Gln Ala Leu Gln Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys
225 230 235 240
Val Asp Ile Lys
<210> 777
<211> 733
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 777
gaagtgcagc tgcttgagag cggtggaggt ctggtgcagc ccgggggatc actgcgcctg
60
tcctgtgccg cgtccggttt cactttctcc tcgtacgcca tgtcgtgggt cagacaggca
120
ccgggaaagg gactggaatg ggtgtcagcc atttcgggtt cggggggcag cacctactac
180
gctgactccg tgaagggccg gttcaccatt tcccgcgaca actccaagaa caccttgtac
240
ctccaaatga actccctgcg ggccgaagat accgccgtgt attactgcgt gctgtggttc
300
ggagagggat tcgacccgtg gggacaagga acactcgtga ctgtgtcatc cggcggaggc
360
ggcagcggtg gcggcggttc cggcggcggc ggatctgaca tcgtgttgac ccagtcccct
420
ctgagcctgc cggtcactcc tggcgaacca gccagcatct cctgccggtc gagccagtcc
480
ctcctgcact ccaatgggta caactacctc gattggtatc tgcaaaagcc gggccagagc
540
ccccagctgc tgatctacct tgggtcaaac cgcgcttccg gggtgcctga tagattctcc
600
gggtccggga gcggaaccga ctttaccctg aaaatctcga gggtggaggc cgaggacgtc
660
ggagtgtact actgcatgca ggcgctccag actcccctga ccttcggagg aggaacgaag
720
gtcgacatca aga
733
<210> 778
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 778
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Trp Phe Gly Glu Gly Phe Asp Pro Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 779
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 779
Asp Ile Val Leu Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1. 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Asp Ile Lys
100 105 110
<210> 780
<211> 488
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 780
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Val Leu Trp Phe Gly Glu Gly Phe Asp Pro Trp
115 120 125
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Leu Thr Gln Ser
145 150 155 160
Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser Ile Ser Cys
165 170 175
Arg Ser Ser Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr Leu Asp
180 185 190
Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Gln Leu Leu Ile Tyr Leu
195 200 205
Gly Ser Asn Arg Ala Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly
210 215 220
Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp
225 230 235 240
Val Gly Val Tyr Tyr Cys Met Gln Ala Leu Gln Thr Pro Leu Thr Phe
245 250 255
Gly Gly Gly Thr Lys Val Asp Ile Lys Thr Thr Thr Pro Ala Pro Arg
260 265 270
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
275 280 285
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
290 295 300
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
305 310 315 320
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg
325 330 335
Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro
340 345 350
Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu
355 360 365
Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala
370 375 380
Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
385 390 395 400
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
405 410 415
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
420 425 430
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
435 440 445
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
450 455 460
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
465 470 475 480
His Met Gln Ala Leu Pro Pro Arg
485
<210> 781
<211> 1464
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 781
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc agctgcttga gagcggtgga ggtctggtgc agcccggggg atcactgcgc
120
ctgtcctgtg ccgcgtccgg tttcactttc tcctcgtacg ccatgtcgtg ggtcagacag
180
gcaccgggaa agggactgga atgggtgtca gccatttcgg gttcgggggg cagcacctac
240
tacgctgact ccgtgaaggg ccggttcacc atttcccgcg acaactccaa gaacaccttg
300
tacctccaaa tgaactccct gcgggccgaa gataccgccg tgtattactg cgtgctgtgg
360
ttcggagagg gattcgaccc gtggggacaa ggaacactcg tgactgtgtc atccggcgga
420
ggcggcagcg gtggcggcgg ttccggcggc ggcggatctg acatcgtgtt gacccagtcc
480
cctctgagcc tgccggtcac tcctggcgaa ccagccagca tctcctgccg gtcgagccag
540
tccctcctgc actccaatgg gtacaactac ctcgattggt atctgcaaaa gccgggccag
600
agcccccagc tgctgatcta ccttgggtca aaccgcgctt ccggggtgcc tgatagattc
660
tccgggtccg ggagcggaac cgactttacc ctgaaaatct cgagggtgga ggccgaggac
720
gtcggagtgt actactgcat gcaggcgctc cagactcccc tgaccttcgg aggaggaacg
780
aaggtcgaca tcaagaccac taccccagca ccgaggccac ccaccccggc tcctaccatc
840
gcctcccagc ctctgtccct gcgtccggag gcatgtagac ccgcagctgg tggggccgtg
900
catacccggg gtcttgactt cgcctgcgat atctacattt gggcccctct ggctggtact
960
tgcggggtcc tgctgctttc actcgtgatc actctttact gtaagcgcgg tcggaagaag
1020
ctgctgtaca tctttaagca acccttcatg aggcctgtgc agactactca agaggaggac
1080
ggctgttcat gccggttccc agaggaggag gaaggcggct gcgaactgcg cgtgaaattc
1140
agccgcagcg cagatgctcc agcctacaag caggggcaga accagctcta caacgaactc
1200
aatcttggtc ggagagagga gtacgacgtg ctggacaagc ggagaggacg ggacccagaa
1260
atgggcggga agccgcgcag aaagaatccc caagagggcc tgtacaacga gctccaaaag
1320
gataagatgg cagaagccta tagcgagatt ggtatgaaag gggaacgcag aagaggcaaa
1380
ggccacgacg gactgtacca gggactcagc accgccacca aggacaccta tgacgctctt
1440
cacatgcagg ccctgccgcc tcgg
1464
<210> 782
<211> 251
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 782
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Val Gly Tyr Asp Ser Ser Gly Tyr Tyr Arg Asp Tyr Tyr Gly
100 105 110
Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val
130 135 140
Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala
145 150 155 160
Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly
180 185 190
Thr Ser Ser Arg Ala Thr Gly Ile Ser Asp Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp
210 215 220
Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Asn Ser Pro Pro Lys Phe
225 230 235 240
Thr Phe Gly Pro Gly Thr Lys Leu Glu Ile Lys
245 250
<210> 783
<211> 753
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 783
caagtgcagc tcgtggagtc aggcggagga ctggtgcagc ccgggggctc cctgagactt
60
tcctgcgcgg catcgggttt taccttctcc tcctatgcta tgtcctgggt gcgccaggcc
120
ccgggaaagg gactggaatg ggtgtccgca atcagcggta gcgggggctc aacatactac
180
gccgactccg tcaagggtcg cttcactatt tcccgggaca actccaagaa taccctgtac
240
ctccaaatga acagcctcag ggccgaggat actgccgtgt actactgcgc caaagtcgga
300
tacgatagct ccggttacta ccgggactac tacggaatgg acgtgtgggg acagggcacc
360
accgtgaccg tgtcaagcgg cggaggcggt tcaggagggg gaggctccgg cggtggaggg
420
tccgaaatcg tcctgactca gtcgcctggc actctgtcgt tgtccccggg ggagcgcgct
480
accctgtcgt gtcgggcgtc gcagtccgtg tcgagctcct acctcgcgtg gtaccagcag
540
aagcccggac aggcccctag acttctgatc tacggcactt cttcacgcgc caccgggatc
600
agcgacaggt tcagcggctc cggctccggg accgacttca ccctgaccat tagccggctg
660
gagcctgaag atttcgccgt gtattactgc caacactacg gaaactcgcc gccaaagttc
720
acgttcggac ccggaaccaa gctggaaatc aag
753
<210> 784
<211> 126
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 784
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Val Gly Tyr Asp Ser Ser Gly Tyr Tyr Arg Asp Tyr Tyr Gly
100 105 110
Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 785
<211> 110
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 785
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Thr Ser Ser Arg Ala Thr Gly Ile Ser Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Asn Ser Pro
85 90 95
Pro Lys Phe Thr Phe Gly Pro Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 786
<211> 495
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 786
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Val Gly Tyr Asp Ser Ser Gly Tyr Tyr
115 120 125
Arg Asp Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr
130 135 140
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser
165 170 175
Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser
180 185 190
Ser Ser Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg
195 200 205
Leu Leu Ile Tyr Gly Thr Ser Ser Arg Ala Thr Gly Ile Ser Asp Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg
225 230 235 240
Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Asn
245 250 255
Ser Pro Pro Lys Phe Thr Phe Gly Pro Gly Thr Lys Leu Glu Ile Lys
260 265 270
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
275 280 285
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
290 295 300
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
305 310 315 320
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
325 330 335
Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
340 345 350
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
355 360 365
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
370 375 380
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln
385 390 395 400
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
405 410 415
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
420 425 430
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
435 440 445
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
450 455 460
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
465 470 475 480
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 787
<211> 1485
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 787
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc agctcgtgga gtcaggcgga ggactggtgc agcccggggg ctccctgaga
120
ctttcctgcg cggcatcggg ttttaccttc tcctcctatg ctatgtcctg ggtgcgccag
180
gccccgggaa agggactgga atgggtgtcc gcaatcagcg gtagcggggg ctcaacatac
240
tacgccgact ccgtcaaggg tcgcttcact atttcccggg acaactccaa gaataccctg
300
tacctccaaa tgaacagcct cagggccgag gatactgccg tgtactactg cgccaaagtc
360
ggatacgata gctccggtta ctaccgggac tactacggaa tggacgtgtg gggacagggc
420
accaccgtga ccgtgtcaag cggcggaggc ggttcaggag ggggaggctc cggcggtgga
480
gggtccgaaa tcgtcctgac tcagtcgcct ggcactctgt cgttgtcccc gggggagcgc
540
gctaccctgt cgtgtcgggc gtcgcagtcc gtgtcgagct cctacctcgc gtggtaccag
600
cagaagcccg gacaggcccc tagacttctg atctacggca cttcttcacg cgccaccggg
660
atcagcgaca ggttcagcgg ctccggctcc gggaccgact tcaccctgac cattagccgg
720
ctggagcctg aagatttcgc cgtgtattac tgccaacact acggaaactc gccgccaaag
780
ttcacgttcg gacccggaac caagctggaa atcaagacca ctaccccagc accgaggcca
840
cccaccccgg ctcctaccat cgcctcccag cctctgtccc tgcgtccgga ggcatgtaga
900
cccgcagctg gtggggccgt gcatacccgg ggtcttgact tcgcctgcga tatctacatt
960
tgggcccctc tggctggtac ttgcggggtc ctgctgcttt cactcgtgat cactctttac
1020
tgtaagcgcg gtcggaagaa gctgctgtac atctttaagc aacccttcat gaggcctgtg
1080
cagactactc aagaggagga cggctgttca tgccggttcc cagaggagga ggaaggcggc
1140
tgcgaactgc gcgtgaaatt cagccgcagc gcagatgctc cagcctacaa gcaggggcag
1200
aaccagctct acaacgaact caatcttggt cggagagagg agtacgacgt gctggacaag
1260
cggagaggac gggacccaga aatgggcggg aagccgcgca gaaagaatcc ccaagagggc
1320
ctgtacaacg agctccaaaa ggataagatg gcagaagcct atagcgagat tggtatgaaa
1380
ggggaacgca gaagaggcaa aggccacgac ggactgtacc agggactcag caccgccacc
1440
aaggacacct atgacgctct tcacatgcag gccctgccgc ctcgg
1485
<210> 788
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 788
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Met Gly Trp Ser Ser Gly Tyr Leu Gly Ala Phe Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser
130 135 140
Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
145 150 155 160
Arg Ala Ser Gln Ser Val Ala Ser Ser Phe Leu Ala Trp Tyr Gln Gln
165 170 175
Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Gly Arg
180 185 190
Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
195 200 205
Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr
210 215 220
Tyr Cys Gln His Tyr Gly Gly Ser Pro Arg Leu Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Val Asp Ile Lys
245
<210> 789
<211> 739
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 789
gaagtccaac tggtggagtc cgggggaggg ctcgtgcagc ccggaggcag ccttcggctg
60
tcgtgcgccg cctccgggtt cacgttctca tcctacgcga tgtcgtgggt cagacaggca
120
ccaggaaagg gactggaatg ggtgtccgcc attagcggct ccggcggtag cacctactat
180
gccgactcag tgaagggaag gttcactatc tcccgcgaca acagcaagaa caccctgtac
240
ctccaaatga actctctgcg ggccgaggat accgcggtgt actattgcgc caagatgggt
300
tggtccagcg gatacttggg agccttcgac atttggggac agggcactac tgtgaccgtg
360
tcctccgggg gtggcggatc gggaggcggc ggctcgggtg gagggggttc cgaaatcgtg
420
ttgacccagt caccgggaac cctctcgctg tccccgggag aacgggctac actgtcatgt
480
agagcgtccc agtccgtggc ttcctcgttc ctggcctggt accagcagaa gccgggacag
540
gcaccccgcc tgctcatcta cggagccagc ggccgggcga ccggcatccc tgaccgcttc
600
tccggttccg gctcgggcac cgactttact ctgaccatta gcaggcttga gcccgaggat
660
tttgccgtgt actactgcca acactacggg gggagccctc gcctgacctt cggaggcgga
720
actaaggtcg atatcaaaa
739
<210> 790
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 790
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Met Gly Trp Ser Ser Gly Tyr Leu Gly Ala Phe Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 791
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 791
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ala Ser Ser
20 25 30
Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Gly Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Gly Ser Pro
85 90 95
Arg Leu Thr Phe Gly Gly Gly Thr Lys Val Asp Ile Lys
100 105
<210> 792
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 792
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Met Gly Trp Ser Ser Gly Tyr Leu Gly
115 120 125
Ala Phe Asp Ile Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile
145 150 155 160
Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg
165 170 175
Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ala Ser Ser Phe Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
195 200 205
Gly Ala Ser Gly Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu
225 230 235 240
Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Gly Ser Pro Arg Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Asp Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 793
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 793
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtcc aactggtgga gtccggggga gggctcgtgc agcccggagg cagccttcgg
120
ctgtcgtgcg ccgcctccgg gttcacgttc tcatcctacg cgatgtcgtg ggtcagacag
180
gcaccaggaa agggactgga atgggtgtcc gccattagcg gctccggcgg tagcacctac
240
tatgccgact cagtgaaggg aaggttcact atctcccgcg acaacagcaa gaacaccctg
300
tacctccaaa tgaactctct gcgggccgag gataccgcgg tgtactattg cgccaagatg
360
ggttggtcca gcggatactt gggagccttc gacatttggg gacagggcac tactgtgacc
420
gtgtcctccg ggggtggcgg atcgggaggc ggcggctcgg gtggaggggg ttccgaaatc
480
gtgttgaccc agtcaccggg aaccctctcg ctgtccccgg gagaacgggc tacactgtca
540
tgtagagcgt cccagtccgt ggcttcctcg ttcctggcct ggtaccagca gaagccggga
600
caggcacccc gcctgctcat ctacggagcc agcggccggg cgaccggcat ccctgaccgc
660
ttctccggtt ccggctcggg caccgacttt actctgacca ttagcaggct tgagcccgag
720
gattttgccg tgtactactg ccaacactac ggggggagcc ctcgcctgac cttcggaggc
780
ggaactaagg tcgatatcaa aaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 794
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 794
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Asn Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Thr Tyr Arg Gly His Ser Asp Thr Tyr Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Ile Tyr Asp Gly Tyr Asp Val Leu Asp Asn Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 795
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 795
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Ala Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Asn Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Arg Lys Leu Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg
100 105
<210> 796
<211> 451
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<220>
<221> ВАРИАНТ
<222> (451)..(451)
<223> /замена=" "
<220>
<221> Сайт
<222> (1)..(451)
<223> /примечание="вариантам остатков, указанным в
последовательности, не отдается предпочтение перед остатками в
аннотациях вариантов положений»
<400> 796
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Asn Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Thr Tyr Arg Gly His Ser Asp Thr Tyr Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Ile Tyr Asn Gly Tyr Asp Val Leu Asp Asn Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Ala Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Ala Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Cys Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
355 360 365
Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 797
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 797
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Ala Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Asn Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Arg Lys Leu Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 798
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 798
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Val Ala Pro Tyr Phe Ala Pro Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 799
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 799
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Asn Pro Pro
85 90 95
Leu Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 800
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<220>
<221> ВАРИАНТ
<222> (449)..(449)
<223> /замена=" "
<220>
<221> Сайт
<222> (1)..(449)
<223> /примечание="вариантам остатков, указанным в
последовательности, не отдается предпочтение перед остатками в
аннотациях вариантов положений»
<400> 800
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Val Ala Pro Tyr Phe Ala Pro Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr
340 345 350
Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Ser
355 360 365
Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 801
<211> 216
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 801
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Asn Pro Pro
85 90 95
Leu Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val
100 105 110
Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys
115 120 125
Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg
130 135 140
Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn
145 150 155 160
Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser
165 170 175
Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys
180 185 190
Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr
195 200 205
Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 802
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 802
Gln Ile Gln Leu Val Gln Ser Gly Pro Glu Leu Lys Lys Pro Gly Glu
1. 5 10 15
Thr Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Ser Ile Asn Trp Val Lys Arg Ala Pro Gly Lys Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Glu Thr Arg Glu Pro Ala Tyr Ala Tyr Asp Phe
50 55 60
Arg Gly Arg Phe Ala Phe Ser Leu Glu Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Asn Asn Leu Lys Tyr Glu Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Ala Leu Asp Tyr Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser
100 105 110
Val Thr Val Ser Ser
115
<210> 803
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 803
Asp Ile Val Leu Thr Gln Ser Pro Pro Ser Leu Ala Met Ser Leu Gly
1. 5 10 15
Lys Arg Ala Thr Ile Ser Cys Arg Ala Ser Glu Ser Val Thr Ile Leu
20 25 30
Gly Ser His Leu Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Thr Leu Leu Ile Gln Leu Ala Ser Asn Val Gln Thr Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Arg Thr Asp Phe Thr Leu Thr Ile Asp
65 70 75 80
Pro Val Glu Glu Asp Asp Val Ala Val Tyr Tyr Cys Leu Gln Ser Arg
85 90 95
Thr Ile Pro Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 804
<211> 447
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<220>
<221> ВАРИАНТ
<222> (447)..(447)
<223> /замена=" "
<220>
<221> Сайт
<222> (1)..(447)
<223> /примечание="вариантам остатков, указанным в
последовательности, не отдается предпочтение перед остатками в
аннотациях вариантов положений»
<400> 804
Gln Ile Gln Leu Val Gln Ser Gly Pro Glu Leu Lys Lys Pro Gly Glu
1. 5 10 15
Thr Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Ser Ile Asn Trp Val Lys Arg Ala Pro Gly Lys Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Glu Thr Arg Glu Pro Ala Tyr Ala Tyr Asp Phe
50 55 60
Arg Gly Arg Phe Ala Phe Ser Leu Glu Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Asn Asn Leu Lys Tyr Glu Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Ala Leu Asp Tyr Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser
100 105 110
Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
115 120 125
Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys
130 135 140
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
145 150 155 160
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
165 170 175
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
180 185 190
Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn
195 200 205
Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His
210 215 220
Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro
340 345 350
Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Ser Cys Ala
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 805
<211> 218
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 805
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Met Ser Leu Gly
1. 5 10 15
Lys Arg Ala Thr Ile Ser Cys Arg Ala Ser Glu Ser Val Ser Val Ile
20 25 30
Gly Ala His Leu Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Leu Ala Ser Asn Leu Glu Thr Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asp
65 70 75 80
Pro Val Glu Glu Asp Asp Val Ala Ile Tyr Ser Cys Leu Gln Ser Arg
85 90 95
Ile Phe Pro Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 806
<211> 116
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 806
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Val Leu Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 807
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 807
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Tyr Pro Pro
85 90 95
Asp Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 808
<211> 477
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<220>
<221> ВАРИАНТ
<222> (477)..(477)
<223> /замена=" "
<220>
<221> Сайт
<222> (1)..(477)
<223> /примечание="вариантам остатков, указанным в
последовательности, не отдается предпочтение перед остатками в
аннотациях вариантов положений»
<400> 808
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Val Leu Gly Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro
130 135 140
Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg
145 150 155 160
Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala Trp Tyr Gln Gln Lys
165 170 175
Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ser Arg Ala
180 185 190
Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
195 200 205
Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr
210 215 220
Cys Gln Gln Tyr Gly Tyr Pro Pro Asp Phe Thr Phe Gly Gln Gly Thr
225 230 235 240
Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Asp Lys Thr His Thr Cys
245 250 255
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
260 265 270
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
275 280 285
Val Thr Cys Val Val Val Ala Val Ser His Glu Asp Pro Glu Val Lys
290 295 300
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
305 310 315 320
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
325 330 335
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
340 345 350
Val Ser Asn Lys Ala Leu Ala Ala Pro Ile Glu Lys Thr Ile Ser Lys
355 360 365
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys
370 375 380
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys
385 390 395 400
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
405 410 415
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
420 425 430
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
435 440 445
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
450 455 460
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
465 470 475
<210> 809
<211> 215
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 809
Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1. 5 10 15
Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Glu Lys Pro Gly Gln Ala Phe Arg Gly
35 40 45
Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Thr Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Ala
65 70 75 80
Gln Pro Glu Asp Glu Ala Glu Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn
85 90 95
Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Gln Pro
100 105 110
Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu Glu Leu
115 120 125
Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe Tyr Pro
130 135 140
Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro Val Lys Ala
145 150 155 160
Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys Tyr Ala
165 170 175
Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser His Arg
180 185 190
Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu Lys Thr
195 200 205
Val Ala Pro Thr Glu Cys Ser
210 215
<210> 810
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<220>
<221> ВАРИАНТ
<222> (449)..(449)
<223> /замена=" "
<220>
<221> Сайт
<222> (1)..(449)
<223> /примечание="вариантам остатков, указанным в
последовательности, не отдается предпочтение перед остатками в
аннотациях вариантов положений»
<400> 810
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1. 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ser
20 25 30
Gly Met Ile Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly His Ile Arg Ser Lys Thr Asp Gly Gly Thr Thr Asp Tyr Ala Ala
50 55 60
Pro Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Thr Thr Gly Gly Ser Gly Ser Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr
340 345 350
Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Ser
355 360 365
Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 811
<211> 253
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 811
Glu Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1. 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Met Leu Ser Asn
20 25 30
Ser Asp Thr Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Thr Tyr His Arg Ser Thr Trp Tyr Asp Asp Tyr Ala
50 55 60
Ser Ser Val Arg Gly Arg Val Ser Ile Asn Val Asp Thr Ser Lys Asn
65 70 75 80
Gln Tyr Ser Leu Gln Leu Asn Ala Val Thr Pro Glu Asp Thr Gly Val
85 90 95
Tyr Tyr Cys Ala Arg Val Arg Leu Gln Asp Gly Asn Ser Trp Ser Asp
100 105 110
Ala Phe Asp Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ser
130 135 140
Ala Leu Thr Gln Pro Ala Ser Ala Ser Gly Ser Pro Gly Gln Ser Val
145 150 155 160
Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr Asn Tyr
165 170 175
Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu Met Ile
180 185 190
Tyr Asp Val Ser Asn Arg Pro Ser Gly Val Ser Asn Arg Phe Ser Gly
195 200 205
Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu Gln Ala
210 215 220
Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser Ser Thr
225 230 235 240
Leu Tyr Val Phe Gly Thr Gly Thr Gln Leu Thr Val Leu
245 250
<210> 812
<211> 127
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 812
Glu Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1. 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Met Leu Ser Asn
20 25 30
Ser Asp Thr Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Thr Tyr His Arg Ser Thr Trp Tyr Asp Asp Tyr Ala
50 55 60
Ser Ser Val Arg Gly Arg Val Ser Ile Asn Val Asp Thr Ser Lys Asn
65 70 75 80
Gln Tyr Ser Leu Gln Leu Asn Ala Val Thr Pro Glu Asp Thr Gly Val
85 90 95
Tyr Tyr Cys Ala Arg Val Arg Leu Gln Asp Gly Asn Ser Trp Ser Asp
100 105 110
Ala Phe Asp Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 813
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 813
Gln Ser Ala Leu Thr Gln Pro Ala Ser Ala Ser Gly Ser Pro Gly Gln
1. 5 10 15
Ser Val Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Thr Leu Tyr Val Phe Gly Thr Gly Thr Gln Leu Thr Val Leu
100 105 110
<210> 814
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 814
Gly Asp Ser Met Leu Ser Asn Ser Asp Thr Trp Asn
1. 5 10
<210> 815
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 815
Ser Asn Ser Asp Thr Trp Asn
1. 5
<210> 816
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 816
Arg Thr Tyr His Arg Ser Thr Trp Tyr Asp Asp Tyr Ala Ser Ser Val
1. 5 10 15
Arg Gly
<210> 817
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 817
Val Arg Leu Gln Asp Gly Asn Ser Trp Ser Asp Ala Phe Asp Val
1. 5 10 15
<210> 818
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 818
Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr Asn Tyr Val Ser
1. 5 10
<210> 819
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 819
Asp Val Ser Asn Arg Pro Ser
1. 5
<210> 820
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 820
Ser Ser Tyr Thr Ser Ser Ser Thr Leu Tyr Val
1. 5 10
<210> 821
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 821
Gly Ser Thr Ser Gly Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr
1. 5 10 15
Lys Gly
<210> 822
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 822
Leu Ala Glu Ala Ala Ala Lys
1. 5
<210> 823
<211> 521
<212> ДНК
<213> Неустановленное
<220>
<221> источник
<223> /примечание="Описание незивестного: Промотор PGK дикого типа"
<400> 823
acccctctct ccagccacta agccagttgc tccctcggct gacggctgca cgcgaggcct
60
ccgaacgtct tacgccttgt ggcgcgcccg tccttgtccc gggtgtgatg gcggggtgtg
120
gggcggaggg cgtggcgggg aagggccggc gacgagagcc gcgcgggacg actcgtcggc
180
gataaccggt gtcgggtagc gccagccgcg cgacggtaac gagggaccgc gacaggcaga
240
cgctcccatg atcactctgc acgccgaagg caaatagtgc aggccgtgcg gcgcttggcg
300
ttccttggaa gggctgaatc cccgcctcgt ccttcgcagc ggccccccgg gtgttcccat
360
cgccgcttct aggcccactg cgacgcttgc ctgcacttct tacacgctct gggtcccagc
420
cgcggcgacg caaagggcct tggtgcgggt ctcgtcggcg cagggacgcg tttgggtccc
480
gacggaacct tttccgcgtt ggggttgggg caccataagc t
521
<210> 824
<211> 118
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 824
acccctctct ccagccacta agccagttgc tccctcggct gacggctgca cgcgaggcct
60
ccgaacgtct tacgccttgt ggcgcgcccg tccttgtccc gggtgtgatg gcggggtg
118
<210> 825
<211> 221
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 825
acccctctct ccagccacta agccagttgc tccctcggct gacggctgca cgcgaggcct
60
ccgaacgtct tacgccttgt ggcgcgcccg tccttgtccc gggtgtgatg gcggggtgtg
120
gggcggaggg cgtggcgggg aagggccggc gacgagagcc gcgcgggacg actcgtcggc
180
gataaccggt gtcgggtagc gccagccgcg cgacggtaac g
221
<210> 826
<211> 324
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 826
acccctctct ccagccacta agccagttgc tccctcggct gacggctgca cgcgaggcct
60
ccgaacgtct tacgccttgt ggcgcgcccg tccttgtccc gggtgtgatg gcggggtgtg
120
gggcggaggg cgtggcgggg aagggccggc gacgagagcc gcgcgggacg actcgtcggc
180
gataaccggt gtcgggtagc gccagccgcg cgacggtaac gagggaccgc gacaggcaga
240
cgctcccatg atcactctgc acgccgaagg caaatagtgc aggccgtgcg gcgcttggcg
300
ttccttggaa gggctgaatc cccg
324
<210> 827
<211> 422
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 827
acccctctct ccagccacta agccagttgc tccctcggct gacggctgca cgcgaggcct
60
ccgaacgtct tacgccttgt ggcgcgcccg tccttgtccc gggtgtgatg gcggggtgtg
120
gggcggaggg cgtggcgggg aagggccggc gacgagagcc gcgcgggacg actcgtcggc
180
gataaccggt gtcgggtagc gccagccgcg cgacggtaac gagggaccgc gacaggcaga
240
cgctcccatg atcactctgc acgccgaagg caaatagtgc aggccgtgcg gcgcttggcg
300
ttccttggaa gggctgaatc cccgcctcgt ccttcgcagc ggccccccgg gtgttcccat
360
cgccgcttct aggcccactg cgacgcttgc ctgcacttct tacacgctct gggtcccagc
420
cg
422
<210> 828
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(3)
<223> /замена=" "
<220>
<221> Сайт
<222> (1)..(21)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 828
Gly Ser Gly Glu Gly Arg Gly Ser Leu Leu Thr Cys Gly Asp Val Glu
1. 5 10 15
Glu Asn Pro Gly Pro
20
<210> 829
<211> 22
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(3)
<223> /замена=" "
<220>
<221> Сайт
<222> (1)..(22)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 829
Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val
1. 5 10 15
Glu Glu Asn Pro Gly Pro
20
<210> 830
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(3)
<223> /замена=" "
<220>
<221> Сайт
<222> (1)..(23)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 830
Gly Ser Gly Gln Cys Thr Asn Tyr Ala Leu Leu Lys Leu Ala Gly Asp
1. 5 10 15
Val Glu Ser Asn Pro Gly Pro
20
<210> 831
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(3)
<223> /замена=" "
<220>
<221> Сайт
<222> (1)..(25)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 831
Gly Ser Gly Val Lys Gln Thr Leu Asn Phe Asp Leu Leu Lys Leu Ala
1. 5 10 15
Gly Asp Val Glu Ser Asn Pro Gly Pro
20 25
<210> 832
<211> 100
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 832
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
60
tttttttttt tttttttttt tttttttttt tttttttttt
100
<210> 833
<211> 5000
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<220>
<221> другой_признак
<222> (1)..(5000)
<223> /примечание="Эта последовательность может охватывать 50-5000
нуклеотидов"
<220>
<221> источник
<223> /примечание="См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления"
<400> 833
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
60
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
120
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
180
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
240
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
300
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
360
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
420
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
480
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
540
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
600
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
660
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
720
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
780
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
840
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
900
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
960
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1020
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1080
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1140
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1200
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1260
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1320
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1380
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1440
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1500
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1560
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1620
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1680
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1740
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1800
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1860
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1920
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1980
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2040
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2100
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2160
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2220
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2280
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2340
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2400
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2460
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2520
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2580
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2640
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2700
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2760
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2820
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2880
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2940
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3000
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3060
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3120
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3180
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3240
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3300
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3360
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3420
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3480
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3540
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3600
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3660
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3720
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3780
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3840
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3900
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3960
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4020
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4080
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4140
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4200
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4260
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4320
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4380
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4440
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4500
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4560
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4620
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4680
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4740
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4800
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4860
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4920
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4980
tttttttttt tttttttttt
5000
<210> 834
<211> 5000
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<220>
<221> другой_признак
<222> (1)..(5000)
<223> /примечание="Эта последовательность может охватывать 100-5000
нуклеотидов"
<220>
<221> источник
<223> /примечание="См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления"
<400> 834
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
60
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
120
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
180
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
240
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
300
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
360
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
420
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
480
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
540
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
600
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
660
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
720
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
780
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
840
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
900
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
960
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1020
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1080
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1140
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1200
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1260
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1320
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1380
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1440
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1500
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1560
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1620
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1680
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1740
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1800
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1860
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1920
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1980
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2040
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2100
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2160
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2220
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2280
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2340
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2400
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2460
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2520
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2580
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2640
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2700
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2760
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2820
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2880
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2940
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3000
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3060
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3120
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3180
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3240
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3300
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3360
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3420
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3480
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3540
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3600
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3660
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3720
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3780
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3840
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3900
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3960
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4020
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4080
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4140
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4200
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4260
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4320
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4380
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4440
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4500
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4560
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4620
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4680
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4740
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4800
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4860
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4920
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4980
aaaaaaaaaa aaaaaaaaaa
5000
<210> 835
<211> 400
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<220>
<221> другой_признак
<222> (1)..(400)
<223> /примечание="Эта последовательность может охватывать 100-400
нуклеотидов"
<220>
<221> источник
<223> /примечание="См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления"
<400> 835
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
60
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
120
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
180
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
240
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
300
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
360
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
400
<210> 836
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 836
Arg Gly Asp Ser
1
<210> 837
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 837
Met Ala Leu Glu Lys
1. 5
<210> 838
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 838
Asn Tyr Asn Leu His
1. 5
<210> 839
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 839
Ala Ile Tyr Pro Gly Asn Tyr Asp Thr Ser Tyr Asn Gln Lys Phe Lys
1. 5 10 15
Gly
<210> 840
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 840
Val Asp Phe Gly His Ser Arg Tyr Trp Tyr Phe Asp Val
1. 5 10
<210> 841
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 841
Gly Tyr Thr Phe Thr Asn Tyr
1. 5
<210> 842
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 842
Tyr Pro Gly Asn Tyr Asp
1. 5
<210> 843
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 843
Val Asp Phe Gly His Ser Arg Tyr Trp Tyr Phe Asp Val
1. 5 10
<210> 844
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 844
Gly Tyr Thr Phe Thr Asn Tyr Asn
1. 5
<210> 845
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 845
Ile Tyr Pro Gly Asn Tyr Asp Thr
1. 5
<210> 846
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 846
Ala Arg Val Asp Phe Gly His Ser Arg Tyr Trp Tyr Phe Asp Val
1. 5 10 15
<210> 847
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 847
Gly Tyr Thr Phe Thr Asn Tyr Asn Leu His
1. 5 10
<210> 848
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 848
Ala Ile Tyr Pro Gly Asn Tyr Asp Thr Ser Tyr Asn Gln Lys Phe Lys
1. 5 10 15
Gly
<210> 849
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 849
Val Asp Phe Gly His Ser Arg Tyr Trp Tyr Phe Asp Val
1. 5 10
<210> 850
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 850
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Asn Leu His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Tyr Asp Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Met Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Asp Phe Gly His Ser Arg Tyr Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 851
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 851
caagtccaac tcgtccagtc cggtgcagaa gtcaagaaac ctggagcatc cgtgaaagtg
60
tcttgcaaag cctccggcta caccttcacc aactacaacc tccattgggt cagacaggcc
120
cccggacaag gactcgaatg gatgggagcg atctacccgg gaaactacga caccagctac
180
aaccagaagt tcaagggccg cgtgactatg accgccgata agagcacctc caccgcctac
240
atggaactgt cctcgctgag gtccgaggac actgcggtgt actactgcgc ccgcgtggac
300
ttcggacact cacggtattg gtacttcgac gtctggggac agggcactac cgtgaccgtg
360
tcgagc
366
<210> 852
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 852
Arg Ala Thr Ser Ser Val Ser Ser Met Asn
1. 5 10
<210> 853
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 853
Ala Thr Ser Asn Leu Ala Ser
1. 5
<210> 854
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 854
Gln Gln Trp Thr Phe Asn Pro Pro Thr
1. 5
<210> 855
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 855
Thr Ser Ser Val Ser Ser
1. 5
<210> 856
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 856
Ala Thr Ser
1
<210> 857
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 857
Trp Thr Phe Asn Pro Pro
1. 5
<210> 858
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 858
Ser Ser Val Ser Ser
1. 5
<210> 859
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 859
Ala Thr Ser
1
<210> 860
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 860
Gln Gln Trp Thr Phe Asn Pro Pro Thr
1. 5
<210> 861
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 861
Arg Ala Thr Ser Ser Val Ser Ser Met Asn
1. 5 10
<210> 862
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 862
Ala Thr Ser Asn Leu Ala Ser
1. 5
<210> 863
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 863
Gln Gln Trp Thr Phe Asn Pro Pro Thr
1. 5
<210> 864
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 864
Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Thr Ser Ser Val Ser Ser Met
20 25 30
Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro Leu Ile His
35 40 45
Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Glu Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
65 70 75 80
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Trp Thr Phe Asn Pro Pro Thr
85 90 95
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 865
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 865
gatatccagc tgactcagtc cccgtcattc ctgtccgcct ccgtgggaga cagagtgacc
60
atcacctgtc gggccacttc ctccgtgtca agcatgaact ggtatcagca gaagcccggg
120
aaggccccaa agccgctgat tcacgcgacg tccaacctgg cttccggcgt gccgagccgg
180
ttctccggct cggggagcgg gactgagtac accctgacta tttcctcgct tcaacccgag
240
gactttgcta cctactactg ccaacagtgg accttcaatc ctccgacatt cggacagggt
300
accaagttgg aaatcaag
318
<210> 866
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 866
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1. 5 10 15
Gly Gly Gly Ser
20
<210> 867
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 867
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Asn Leu His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Tyr Asp Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Met Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Asp Phe Gly His Ser Arg Tyr Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly Asp Arg
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Thr Ser Ser Val Ser Ser Met Asn Trp
165 170 175
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro Leu Ile His Ala Thr
180 185 190
Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
195 200 205
Gly Thr Glu Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
210 215 220
Ala Thr Tyr Tyr Cys Gln Gln Trp Thr Phe Asn Pro Pro Thr Phe Gly
225 230 235 240
Gln Gly Thr Lys Leu Glu Ile Lys
245
<210> 868
<211> 744
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 868
caagtccaac tcgtccagtc cggtgcagaa gtcaagaaac ctggagcatc cgtgaaagtg
60
tcttgcaaag cctccggcta caccttcacc aactacaacc tccattgggt cagacaggcc
120
cccggacaag gactcgaatg gatgggagcg atctacccgg gaaactacga caccagctac
180
aaccagaagt tcaagggccg cgtgactatg accgccgata agagcacctc caccgcctac
240
atggaactgt cctcgctgag gtccgaggac actgcggtgt actactgcgc ccgcgtggac
300
ttcggacact cacggtattg gtacttcgac gtctggggac agggcactac cgtgaccgtg
360
tcgagcggcg gaggaggttc gggagggggc ggatcagggg gcggcggcag cggtggaggg
420
ggctcggata tccagctgac tcagtccccg tcattcctgt ccgcctccgt gggagacaga
480
gtgaccatca cctgtcgggc cacttcctcc gtgtcaagca tgaactggta tcagcagaag
540
cccgggaagg ccccaaagcc gctgattcac gcgacgtcca acctggcttc cggcgtgccg
600
agccggttct ccggctcggg gagcgggact gagtacaccc tgactatttc ctcgcttcaa
660
cccgaggact ttgctaccta ctactgccaa cagtggacct tcaatcctcc gacattcgga
720
cagggtacca agttggaaat caag
744
<210> 869
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 869
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Asn Tyr Asn Leu His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Ala Ile Tyr Pro Gly Asn Tyr Asp Thr Ser
65 70 75 80
Tyr Asn Gln Lys Phe Lys Gly Arg Val Thr Met Thr Ala Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Val Asp Phe Gly His Ser Arg Tyr Trp
115 120 125
Tyr Phe Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala
165 170 175
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Thr Ser Ser Val
180 185 190
Ser Ser Met Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro
195 200 205
Leu Ile His Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Glu Tyr Thr Leu Thr Ile Ser Ser Leu
225 230 235 240
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Trp Thr Phe Asn
245 250 255
Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 870
<211> 1476
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 870
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtcc aactcgtcca gtccggtgca gaagtcaaga aacctggagc atccgtgaaa
120
gtgtcttgca aagcctccgg ctacaccttc accaactaca acctccattg ggtcagacag
180
gcccccggac aaggactcga atggatggga gcgatctacc cgggaaacta cgacaccagc
240
tacaaccaga agttcaaggg ccgcgtgact atgaccgccg ataagagcac ctccaccgcc
300
tacatggaac tgtcctcgct gaggtccgag gacactgcgg tgtactactg cgcccgcgtg
360
gacttcggac actcacggta ttggtacttc gacgtctggg gacagggcac taccgtgacc
420
gtgtcgagcg gcggaggagg ttcgggaggg ggcggatcag ggggcggcgg cagcggtgga
480
gggggctcgg atatccagct gactcagtcc ccgtcattcc tgtccgcctc cgtgggagac
540
agagtgacca tcacctgtcg ggccacttcc tccgtgtcaa gcatgaactg gtatcagcag
600
aagcccggga aggccccaaa gccgctgatt cacgcgacgt ccaacctggc ttccggcgtg
660
ccgagccggt tctccggctc ggggagcggg actgagtaca ccctgactat ttcctcgctt
720
caacccgagg actttgctac ctactactgc caacagtgga ccttcaatcc tccgacattc
780
ggacagggta ccaagttgga aatcaagacc actaccccag caccgaggcc acccaccccg
840
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
900
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
960
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1020
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1080
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1140
cgcgtgaaat tcagccgcag cgcagatgct ccagcctacc agcaggggca gaaccagctc
1200
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
1260
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
1320
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
1380
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
1440
tatgacgctc ttcacatgca ggccctgccg cctcgg
1476
<210> 871
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 871
Ser Tyr Asn Met His
1. 5
<210> 872
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 872
Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Asn Pro Lys Phe Lys
1. 5 10 15
Gly
<210> 873
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 873
Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val
1. 5 10
<210> 874
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 874
Gly Tyr Thr Phe Thr Ser Tyr
1. 5
<210> 875
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 875
Tyr Pro Gly Asn Gly Asp
1. 5
<210> 876
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 876
Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val
1. 5 10
<210> 877
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 877
Gly Tyr Thr Phe Thr Ser Tyr Asn
1. 5
<210> 878
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 878
Ile Tyr Pro Gly Asn Gly Asp Thr
1. 5
<210> 879
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 879
Ala Arg Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val
1. 5 10 15
<210> 880
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 880
Gly Tyr Thr Phe Thr Ser Tyr Asn Met His
1. 5 10
<210> 881
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 881
Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Asn Pro Lys Phe Lys
1. 5 10 15
Gly
<210> 882
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 882
Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val
1. 5 10
<210> 883
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 883
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Asn Pro Lys Phe
50 55 60
Lys Gly Arg Val Thr Met Thr Ala Asp Lys Ser Thr Arg Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 884
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 884
caagtgcagc tcgtccagtc cggtgcagaa gtcaagaaac ccggtgcttc agtgaaagtg
60
tcctgcaagg cctccggtta caccttcacc tcctacaaca tgcactgggt ccgccaagcc
120
ccgggccagg gactcgaatg gatgggagcc atctaccctg gcaacgggga cacctcatac
180
aaccctaagt tcaagggcag agtgaccatg actgcggaca agtccactag aacagcgtac
240
atggagctga gcagcctgcg gtccgaggat actgccgtgt actactgcgc ccgctcctac
300
ttctacggaa gctcgtcgtg gtacttcgat gtctggggac agggcaccac tgtgactgtg
360
tcctcc
366
<210> 885
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 885
Arg Ala Ser Ser Ser Val Ser Ser Met His
1. 5 10
<210> 886
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 886
Ala Thr Ser Asn Leu Ala Ser
1. 5
<210> 887
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 887
Gln Gln Trp Ile Phe Asn Pro Pro Thr
1. 5
<210> 888
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 888
Ser Ser Ser Val Ser Ser
1. 5
<210> 889
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 889
Ala Thr Ser
1
<210> 890
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 890
Trp Ile Phe Asn Pro Pro
1. 5
<210> 891
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 891
Ser Ser Val Ser Ser
1. 5
<210> 892
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 892
Ala Thr Ser
1
<210> 893
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 893
Gln Gln Trp Ile Phe Asn Pro Pro Thr
1. 5
<210> 894
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 894
Arg Ala Ser Ser Ser Val Ser Ser Met His
1. 5 10
<210> 895
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 895
Ala Thr Ser Asn Leu Ala Ser
1. 5
<210> 896
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 896
Gln Gln Trp Ile Phe Asn Pro Pro Thr
1. 5
<210> 897
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 897
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Ser Ser Val Ser Ser Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Pro Leu Ile Phe
35 40 45
Ala Thr Ser Asn Leu Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu
65 70 75 80
Asp Ala Ala Val Tyr Tyr Cys Gln Gln Trp Ile Phe Asn Pro Pro Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 898
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 898
gaaattgtgc tgactcagag ccccgccacc ctgagcttgt cccccgggga aagggcaacg
60
ctgtcatgcc gcgcctcgtc atccgtgtcc tccatgcatt ggtaccagca gaagccggga
120
caggcccctc ggccgctgat cttcgccacc tccaatctcg cttccggcat tccggcccgg
180
ttctcgggaa gcgggtcggg gaccgactat accctgacca tctctagcct tgaacctgag
240
gacgccgcgg tgtactattg tcaacagtgg atctttaacc ccccaacctt cggtggaggc
300
accaaagtgg agattaag
318
<210> 899
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 899
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1. 5 10 15
Gly Gly Gly Ser
20
<210> 900
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 900
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Asn Pro Lys Phe
50 55 60
Lys Gly Arg Val Thr Met Thr Ala Asp Lys Ser Thr Arg Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile
130 135 140
Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg
145 150 155 160
Ala Thr Leu Ser Cys Arg Ala Ser Ser Ser Val Ser Ser Met His Trp
165 170 175
Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Pro Leu Ile Phe Ala Thr
180 185 190
Ser Asn Leu Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser
195 200 205
Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp Ala
210 215 220
Ala Val Tyr Tyr Cys Gln Gln Trp Ile Phe Asn Pro Pro Thr Phe Gly
225 230 235 240
Gly Gly Thr Lys Val Glu Ile Lys
245
<210> 901
<211> 744
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 901
caagtgcagc tcgtccagtc cggtgcagaa gtcaagaaac ccggtgcttc agtgaaagtg
60
tcctgcaagg cctccggtta caccttcacc tcctacaaca tgcactgggt ccgccaagcc
120
ccgggccagg gactcgaatg gatgggagcc atctaccctg gcaacgggga cacctcatac
180
aaccctaagt tcaagggcag agtgaccatg actgcggaca agtccactag aacagcgtac
240
atggagctga gcagcctgcg gtccgaggat actgccgtgt actactgcgc ccgctcctac
300
ttctacggaa gctcgtcgtg gtacttcgat gtctggggac agggcaccac tgtgactgtg
360
tcctccggtg gcggaggctc gggcggaggc ggaagcggcg gcgggggatc gggaggagga
420
gggtccgaaa ttgtgctgac tcagagcccc gccaccctga gcttgtcccc cggggaaagg
480
gcaacgctgt catgccgcgc ctcgtcatcc gtgtcctcca tgcattggta ccagcagaag
540
ccgggacagg cccctcggcc gctgatcttc gccacctcca atctcgcttc cggcattccg
600
gcccggttct cgggaagcgg gtcggggacc gactataccc tgaccatctc tagccttgaa
660
cctgaggacg ccgcggtgta ctattgtcaa cagtggatct ttaacccccc aaccttcggt
720
ggaggcacca aagtggagat taag
744
<210> 902
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 902
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Asn Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser
65 70 75 80
Tyr Asn Pro Lys Phe Lys Gly Arg Val Thr Met Thr Ala Asp Lys Ser
85 90 95
Thr Arg Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Ser Tyr Phe Tyr Gly Ser Ser Ser Trp
115 120 125
Tyr Phe Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu
165 170 175
Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Ser Ser Val
180 185 190
Ser Ser Met His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Pro
195 200 205
Leu Ile Phe Ala Thr Ser Asn Leu Ala Ser Gly Ile Pro Ala Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu
225 230 235 240
Glu Pro Glu Asp Ala Ala Val Tyr Tyr Cys Gln Gln Trp Ile Phe Asn
245 250 255
Pro Pro Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 903
<211> 1476
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 903
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc agctcgtcca gtccggtgca gaagtcaaga aacccggtgc ttcagtgaaa
120
gtgtcctgca aggcctccgg ttacaccttc acctcctaca acatgcactg ggtccgccaa
180
gccccgggcc agggactcga atggatggga gccatctacc ctggcaacgg ggacacctca
240
tacaacccta agttcaaggg cagagtgacc atgactgcgg acaagtccac tagaacagcg
300
tacatggagc tgagcagcct gcggtccgag gatactgccg tgtactactg cgcccgctcc
360
tacttctacg gaagctcgtc gtggtacttc gatgtctggg gacagggcac cactgtgact
420
gtgtcctccg gtggcggagg ctcgggcgga ggcggaagcg gcggcggggg atcgggagga
480
ggagggtccg aaattgtgct gactcagagc cccgccaccc tgagcttgtc ccccggggaa
540
agggcaacgc tgtcatgccg cgcctcgtca tccgtgtcct ccatgcattg gtaccagcag
600
aagccgggac aggcccctcg gccgctgatc ttcgccacct ccaatctcgc ttccggcatt
660
ccggcccggt tctcgggaag cgggtcgggg accgactata ccctgaccat ctctagcctt
720
gaacctgagg acgccgcggt gtactattgt caacagtgga tctttaaccc cccaaccttc
780
ggtggaggca ccaaagtgga gattaagacc actaccccag caccgaggcc acccaccccg
840
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
900
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
960
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1020
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1080
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1140
cgcgtgaaat tcagccgcag cgcagatgct ccagcctacc agcaggggca gaaccagctc
1200
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
1260
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
1320
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
1380
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
1440
tatgacgctc ttcacatgca ggccctgccg cctcgg
1476
<210> 904
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 904
Asn Tyr Trp Met His
1. 5
<210> 905
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 905
Phe Ile Thr Pro Thr Thr Gly Tyr Pro Glu Tyr Asn Gln Lys Phe Lys
1. 5 10 15
Asp
<210> 906
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 906
Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr
1. 5 10
<210> 907
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 907
Gly Tyr Thr Phe Thr Asn Tyr
1. 5
<210> 908
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 908
Thr Pro Thr Thr Gly Tyr
1. 5
<210> 909
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 909
Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr
1. 5 10
<210> 910
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 910
Gly Tyr Thr Phe Thr Asn Tyr Trp
1. 5
<210> 911
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 911
Ile Thr Pro Thr Thr Gly Tyr Pro
1. 5
<210> 912
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 912
Ala Arg Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr
1. 5 10 15
<210> 913
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 913
Gly Tyr Thr Phe Thr Asn Tyr Trp Met His
1. 5 10
<210> 914
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 914
Phe Ile Thr Pro Thr Thr Gly Tyr Pro Glu Tyr Asn Gln Lys Phe Lys
1. 5 10 15
Asp
<210> 915
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 915
Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr
1. 5 10
<210> 916
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 916
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Thr Pro Thr Thr Gly Tyr Pro Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 917
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 917
caagtgcaac tcgtccagtc cggtgcagaa gtcaagaaac caggcgcatc cgtgaaagtc
60
tcctgcaaag cctccggcta cacattcact aactattgga tgcattgggt gcgccaggcc
120
ccgggacagg ggctggagtg gatggggttc attaccccta ccaccggcta ccctgagtac
180
aaccagaagt tcaaggatag ggtcaccatg accgctgaca agtccacctc caccgcgtac
240
atggaactgt catcgctccg gtccgaggat accgcggtgt actactgcgc ccggagaaaa
300
gtcggaaagg gagtgtatta cgccttggac tactggggac aggggactac cgtgaccgtg
360
tcgagc
366
<210> 918
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 918
Arg Ala Ser Gly Asn Ile His Asn Tyr Leu Ala
1. 5 10
<210> 919
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 919
Asn Thr Lys Thr Leu Ala Asp
1. 5
<210> 920
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 920
Gln His Phe Trp Ser Ser Pro Trp Thr
1. 5
<210> 921
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 921
Ser Gly Asn Ile His Asn Tyr
1. 5
<210> 922
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 922
Asn Thr Lys
1
<210> 923
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 923
Phe Trp Ser Ser Pro Trp
1. 5
<210> 924
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 924
Gly Asn Ile His Asn Tyr
1. 5
<210> 925
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 925
Asn Thr Lys
1
<210> 926
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 926
Gln His Phe Trp Ser Ser Pro Trp Thr
1. 5
<210> 927
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 927
Arg Ala Ser Gly Asn Ile His Asn Tyr Leu Ala
1. 5 10
<210> 928
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 928
Asn Thr Lys Thr Leu Ala Asp
1. 5
<210> 929
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 929
Gln His Phe Trp Ser Ser Pro Trp Thr
1. 5
<210> 930
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 930
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gly Asn Ile His Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu Ile
35 40 45
Tyr Asn Thr Lys Thr Leu Ala Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln His Phe Trp Ser Ser Pro Trp
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 931
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 931
gacatccaga tgacccagtc cccgtcaagc cttagcgcct ccgtgggcga ccgcgtgacc
60
attacttgtc gggcgtcggg aaacatccac aactacctcg cctggtacca gcagaagccg
120
ggaaaggtcc ccaagctgct gatctacaat accaagactc tggccgacgg agtgccttcc
180
cgcttttccg gttcgggaag cgggactgac tacaccctga ctatctcctc gctgcaaccc
240
gaagatgtgg ctacgtacta ctgccagcac ttctggtcct ctccctggac cttcggcggt
300
ggcactaagg tcgagattaa g
321
<210> 932
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 932
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1. 5 10 15
Gly Gly Gly Ser
20
<210> 933
<211> 249
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 933
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Thr Pro Thr Thr Gly Tyr Pro Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Gly Asn Ile His Asn Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu Ile Tyr Asn
180 185 190
Thr Lys Thr Leu Ala Asp Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
210 215 220
Val Ala Thr Tyr Tyr Cys Gln His Phe Trp Ser Ser Pro Trp Thr Phe
225 230 235 240
Gly Gly Gly Thr Lys Val Glu Ile Lys
245
<210> 934
<211> 747
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 934
caagtgcaac tcgtccagtc cggtgcagaa gtcaagaaac caggcgcatc cgtgaaagtc
60
tcctgcaaag cctccggcta cacattcact aactattgga tgcattgggt gcgccaggcc
120
ccgggacagg ggctggagtg gatggggttc attaccccta ccaccggcta ccctgagtac
180
aaccagaagt tcaaggatag ggtcaccatg accgctgaca agtccacctc caccgcgtac
240
atggaactgt catcgctccg gtccgaggat accgcggtgt actactgcgc ccggagaaaa
300
gtcggaaagg gagtgtatta cgccttggac tactggggac aggggactac cgtgaccgtg
360
tcgagcggtg gaggcggctc cggcggagga ggaagcgggg gaggcggttc agggggcgga
420
ggaagcgaca tccagatgac ccagtccccg tcaagcctta gcgcctccgt gggcgaccgc
480
gtgaccatta cttgtcgggc gtcgggaaac atccacaact acctcgcctg gtaccagcag
540
aagccgggaa aggtccccaa gctgctgatc tacaatacca agactctggc cgacggagtg
600
ccttcccgct tttccggttc gggaagcggg actgactaca ccctgactat ctcctcgctg
660
caacccgaag atgtggctac gtactactgc cagcacttct ggtcctctcc ctggaccttc
720
ggcggtggca ctaaggtcga gattaag
747
<210> 935
<211> 493
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 935
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Asn Tyr Trp Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Phe Ile Thr Pro Thr Thr Gly Tyr Pro Glu
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Val Thr Met Thr Ala Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Arg Lys Val Gly Lys Gly Val Tyr Tyr
115 120 125
Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala
165 170 175
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gly Asn Ile
180 185 190
His Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys
195 200 205
Leu Leu Ile Tyr Asn Thr Lys Thr Leu Ala Asp Gly Val Pro Ser Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser
225 230 235 240
Leu Gln Pro Glu Asp Val Ala Thr Tyr Tyr Cys Gln His Phe Trp Ser
245 250 255
Ser Pro Trp Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 936
<211> 1479
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 936
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc aactcgtcca gtccggtgca gaagtcaaga aaccaggcgc atccgtgaaa
120
gtctcctgca aagcctccgg ctacacattc actaactatt ggatgcattg ggtgcgccag
180
gccccgggac aggggctgga gtggatgggg ttcattaccc ctaccaccgg ctaccctgag
240
tacaaccaga agttcaagga tagggtcacc atgaccgctg acaagtccac ctccaccgcg
300
tacatggaac tgtcatcgct ccggtccgag gataccgcgg tgtactactg cgcccggaga
360
aaagtcggaa agggagtgta ttacgccttg gactactggg gacaggggac taccgtgacc
420
gtgtcgagcg gtggaggcgg ctccggcgga ggaggaagcg ggggaggcgg ttcagggggc
480
ggaggaagcg acatccagat gacccagtcc ccgtcaagcc ttagcgcctc cgtgggcgac
540
cgcgtgacca ttacttgtcg ggcgtcggga aacatccaca actacctcgc ctggtaccag
600
cagaagccgg gaaaggtccc caagctgctg atctacaata ccaagactct ggccgacgga
660
gtgccttccc gcttttccgg ttcgggaagc gggactgact acaccctgac tatctcctcg
720
ctgcaacccg aagatgtggc tacgtactac tgccagcact tctggtcctc tccctggacc
780
ttcggcggtg gcactaaggt cgagattaag accactaccc cagcaccgag gccacccacc
840
ccggctccta ccatcgcctc ccagcctctg tccctgcgtc cggaggcatg tagacccgca
900
gctggtgggg ccgtgcatac ccggggtctt gacttcgcct gcgatatcta catttgggcc
960
cctctggctg gtacttgcgg ggtcctgctg ctttcactcg tgatcactct ttactgtaag
1020
cgcggtcgga agaagctgct gtacatcttt aagcaaccct tcatgaggcc tgtgcagact
1080
actcaagagg aggacggctg ttcatgccgg ttcccagagg aggaggaagg cggctgcgaa
1140
ctgcgcgtga aattcagccg cagcgcagat gctccagcct accagcaggg gcagaaccag
1200
ctctacaacg aactcaatct tggtcggaga gaggagtacg acgtgctgga caagcggaga
1260
ggacgggacc cagaaatggg cgggaagccg cgcagaaaga atccccaaga gggcctgtac
1320
aacgagctcc aaaaggataa gatggcagaa gcctatagcg agattggtat gaaaggggaa
1380
cgcagaagag gcaaaggcca cgacggactg taccagggac tcagcaccgc caccaaggac
1440
acctatgacg ctcttcacat gcaggccctg ccgcctcgg
1479
<210> 937
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 937
Asn Tyr Trp Met His
1. 5
<210> 938
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 938
Phe Ile Thr Pro Thr Thr Gly Tyr Pro Glu Tyr Asn Gln Lys Phe Lys
1. 5 10 15
Asp
<210> 939
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 939
Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr
1. 5 10
<210> 940
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 940
Gly Tyr Thr Phe Thr Asn Tyr
1. 5
<210> 941
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 941
Thr Pro Thr Thr Gly Tyr
1. 5
<210> 942
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 942
Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr
1. 5 10
<210> 943
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 943
Gly Tyr Thr Phe Thr Asn Tyr Trp
1. 5
<210> 944
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 944
Ile Thr Pro Thr Thr Gly Tyr Pro
1. 5
<210> 945
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 945
Ala Arg Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr
1. 5 10 15
<210> 946
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 946
Gly Tyr Thr Phe Thr Asn Tyr Trp Met His
1. 5 10
<210> 947
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 947
Phe Ile Thr Pro Thr Thr Gly Tyr Pro Glu Tyr Asn Gln Lys Phe Lys
1. 5 10 15
Asp
<210> 948
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 948
Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr
1. 5 10
<210> 949
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 949
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Thr Pro Thr Thr Gly Tyr Pro Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 950
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 950
caagtccaac tcgtccaatc aggagcagaa gtcaagaagc ccggaagctc tgtcaaagtg
60
tcctgcaagg cctccggtta caccttcacc aactattgga tgcactgggt cagacaggcc
120
ccgggacagg gcttggaatg gatgggtttc atcactccaa ccaccggtta cccggagtac
180
aaccagaagt ttaaggaccg cgtgaccatt actgccgaca agtccacgag caccgcttac
240
atggaactta gcagcctgcg gtccgaggac actgccgtgt attactgcgc gcggaggaag
300
gtcggaaagg gagtgtacta cgcactggac tactggggcc agggaaccac cgtgactgtg
360
tcctcc
366
<210> 951
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 951
Arg Ala Ser Gly Asn Ile His Asn Tyr Leu Ala
1. 5 10
<210> 952
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 952
Asn Thr Lys Thr Leu Ala Asp
1. 5
<210> 953
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 953
Gln His Phe Trp Ser Ser Pro Trp Thr
1. 5
<210> 954
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 954
Ser Gly Asn Ile His Asn Tyr
1. 5
<210> 955
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 955
Asn Thr Lys
1
<210> 956
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 956
Phe Trp Ser Ser Pro Trp
1. 5
<210> 957
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 957
Gly Asn Ile His Asn Tyr
1. 5
<210> 958
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 958
Asn Thr Lys
1
<210> 959
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 959
Gln His Phe Trp Ser Ser Pro Trp Thr
1. 5
<210> 960
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 960
Arg Ala Ser Gly Asn Ile His Asn Tyr Leu Ala
1. 5 10
<210> 961
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 961
Asn Thr Lys Thr Leu Ala Asp
1. 5
<210> 962
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 962
Gln His Phe Trp Ser Ser Pro Trp Thr
1. 5
<210> 963
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 963
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gly Asn Ile His Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu Ile
35 40 45
Tyr Asn Thr Lys Thr Leu Ala Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln His Phe Trp Ser Ser Pro Trp
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 964
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 964
gatattcaga tgacccagtc cccttcatcc ctgagcgcct cagtgggcga tagagtgacc
60
atcacttgtc gcgcctcggg caatatccac aactacctcg cctggtacca gcagaagccg
120
ggaaaagtgc ctaagctgct gatctacaac actaagaccc tggcggatgg agtgcccagc
180
cggttctccg gctccggcag cggcacagac tacaccctca ccatctcctc gctgcaacca
240
gaggacgtgg ctacctacta ctgccagcat ttctggtcgt ccccctggac tttcggaggg
300
gggaccaaag tggagattaa g
321
<210> 965
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 965
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1. 5 10 15
Gly Gly Gly Ser
20
<210> 966
<211> 249
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 966
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Thr Pro Thr Thr Gly Tyr Pro Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Gly Asn Ile His Asn Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu Ile Tyr Asn
180 185 190
Thr Lys Thr Leu Ala Asp Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
210 215 220
Val Ala Thr Tyr Tyr Cys Gln His Phe Trp Ser Ser Pro Trp Thr Phe
225 230 235 240
Gly Gly Gly Thr Lys Val Glu Ile Lys
245
<210> 967
<211> 747
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 967
caagtccaac tcgtccaatc aggagcagaa gtcaagaagc ccggaagctc tgtcaaagtg
60
tcctgcaagg cctccggtta caccttcacc aactattgga tgcactgggt cagacaggcc
120
ccgggacagg gcttggaatg gatgggtttc atcactccaa ccaccggtta cccggagtac
180
aaccagaagt ttaaggaccg cgtgaccatt actgccgaca agtccacgag caccgcttac
240
atggaactta gcagcctgcg gtccgaggac actgccgtgt attactgcgc gcggaggaag
300
gtcggaaagg gagtgtacta cgcactggac tactggggcc agggaaccac cgtgactgtg
360
tcctccggtg gcggagggtc gggagggggg ggctcgggag gaggagggtc cgggggcggt
420
ggctcagata ttcagatgac ccagtcccct tcatccctga gcgcctcagt gggcgataga
480
gtgaccatca cttgtcgcgc ctcgggcaat atccacaact acctcgcctg gtaccagcag
540
aagccgggaa aagtgcctaa gctgctgatc tacaacacta agaccctggc ggatggagtg
600
cccagccggt tctccggctc cggcagcggc acagactaca ccctcaccat ctcctcgctg
660
caaccagagg acgtggctac ctactactgc cagcatttct ggtcgtcccc ctggactttc
720
ggagggggga ccaaagtgga gattaag
747
<210> 968
<211> 493
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 968
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Asn Tyr Trp Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Phe Ile Thr Pro Thr Thr Gly Tyr Pro Glu
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Val Thr Ile Thr Ala Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Arg Lys Val Gly Lys Gly Val Tyr Tyr
115 120 125
Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala
165 170 175
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gly Asn Ile
180 185 190
His Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys
195 200 205
Leu Leu Ile Tyr Asn Thr Lys Thr Leu Ala Asp Gly Val Pro Ser Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser
225 230 235 240
Leu Gln Pro Glu Asp Val Ala Thr Tyr Tyr Cys Gln His Phe Trp Ser
245 250 255
Ser Pro Trp Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 969
<211> 1479
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 969
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtcc aactcgtcca atcaggagca gaagtcaaga agcccggaag ctctgtcaaa
120
gtgtcctgca aggcctccgg ttacaccttc accaactatt ggatgcactg ggtcagacag
180
gccccgggac agggcttgga atggatgggt ttcatcactc caaccaccgg ttacccggag
240
tacaaccaga agtttaagga ccgcgtgacc attactgccg acaagtccac gagcaccgct
300
tacatggaac ttagcagcct gcggtccgag gacactgccg tgtattactg cgcgcggagg
360
aaggtcggaa agggagtgta ctacgcactg gactactggg gccagggaac caccgtgact
420
gtgtcctccg gtggcggagg gtcgggaggg gggggctcgg gaggaggagg gtccgggggc
480
ggtggctcag atattcagat gacccagtcc ccttcatccc tgagcgcctc agtgggcgat
540
agagtgacca tcacttgtcg cgcctcgggc aatatccaca actacctcgc ctggtaccag
600
cagaagccgg gaaaagtgcc taagctgctg atctacaaca ctaagaccct ggcggatgga
660
gtgcccagcc ggttctccgg ctccggcagc ggcacagact acaccctcac catctcctcg
720
ctgcaaccag aggacgtggc tacctactac tgccagcatt tctggtcgtc cccctggact
780
ttcggagggg ggaccaaagt ggagattaag accactaccc cagcaccgag gccacccacc
840
ccggctccta ccatcgcctc ccagcctctg tccctgcgtc cggaggcatg tagacccgca
900
gctggtgggg ccgtgcatac ccggggtctt gacttcgcct gcgatatcta catttgggcc
960
cctctggctg gtacttgcgg ggtcctgctg ctttcactcg tgatcactct ttactgtaag
1020
cgcggtcgga agaagctgct gtacatcttt aagcaaccct tcatgaggcc tgtgcagact
1080
actcaagagg aggacggctg ttcatgccgg ttcccagagg aggaggaagg cggctgcgaa
1140
ctgcgcgtga aattcagccg cagcgcagat gctccagcct accagcaggg gcagaaccag
1200
ctctacaacg aactcaatct tggtcggaga gaggagtacg acgtgctgga caagcggaga
1260
ggacgggacc cagaaatggg cgggaagccg cgcagaaaga atccccaaga gggcctgtac
1320
aacgagctcc aaaaggataa gatggcagaa gcctatagcg agattggtat gaaaggggaa
1380
cgcagaagag gcaaaggcca cgacggactg taccagggac tcagcaccgc caccaaggac
1440
acctatgacg ctcttcacat gcaggccctg ccgcctcgg
1479
<210> 970
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 970
Asn Tyr Trp Met His
1. 5
<210> 971
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 971
Phe Ile Thr Pro Thr Thr Gly Tyr Pro Glu Tyr Asn Gln Lys Phe Lys
1. 5 10 15
Asp
<210> 972
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 972
Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr
1. 5 10
<210> 973
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 973
Gly Tyr Thr Phe Thr Asn Tyr
1. 5
<210> 974
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 974
Thr Pro Thr Thr Gly Tyr
1. 5
<210> 975
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 975
Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr
1. 5 10
<210> 976
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 976
Gly Tyr Thr Phe Thr Asn Tyr Trp
1. 5
<210> 977
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 977
Ile Thr Pro Thr Thr Gly Tyr Pro
1. 5
<210> 978
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 978
Ala Arg Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr
1. 5 10 15
<210> 979
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 979
Gly Tyr Thr Phe Thr Asn Tyr Trp Met His
1. 5 10
<210> 980
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 980
Phe Ile Thr Pro Thr Thr Gly Tyr Pro Glu Tyr Asn Gln Lys Phe Lys
1. 5 10 15
Asp
<210> 981
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 981
Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr
1. 5 10
<210> 982
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 982
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Thr Pro Thr Thr Gly Tyr Pro Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 983
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 983
caagtccaac tcgtccagtc cggtgcagaa gtcaagaaac ccggagcttc cgtgaaagtg
60
tcctgcaaag cctccggtta cacctttacg aactactgga tgcattgggt gcgccaggcc
120
ccgggacagg ggctggaatg gatgggcttc attaccccca ccaccggata ccccgagtac
180
aatcagaagt tcaaggaccg ggtcaccatg accgccgaca agtcaacctc tactgcttac
240
atggagctgt ccagcctgcg gtcggaagat accgccgtgt attactgcgc gagaaggaaa
300
gtcggaaagg gagtgtacta tgccctggac tactggggac aggggaccac tgtgactgtg
360
tcaagc
366
<210> 984
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 984
Arg Ala Ser Gly Asn Ile His Asn Tyr Leu Ala
1. 5 10
<210> 985
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 985
Asn Thr Lys Thr Leu Ala Asp
1. 5
<210> 986
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 986
Gln His Phe Trp Ser Ser Pro Trp Thr
1. 5
<210> 987
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 987
Ser Gly Asn Ile His Asn Tyr
1. 5
<210> 988
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 988
Asn Thr Lys
1
<210> 989
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 989
Phe Trp Ser Ser Pro Trp
1. 5
<210> 990
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 990
Gly Asn Ile His Asn Tyr
1. 5
<210> 991
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 991
Asn Thr Lys
1
<210> 992
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 992
Gln His Phe Trp Ser Ser Pro Trp Thr
1. 5
<210> 993
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 993
Arg Ala Ser Gly Asn Ile His Asn Tyr Leu Ala
1. 5 10
<210> 994
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 994
Asn Thr Lys Thr Leu Ala Asp
1. 5
<210> 995
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 995
Gln His Phe Trp Ser Ser Pro Trp Thr
1. 5
<210> 996
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 996
Ala Ile Arg Met Thr Gln Ser Pro Phe Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gly Asn Ile His Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Ala Lys Ala Pro Lys Leu Phe Ile
35 40 45
Tyr Asn Thr Lys Thr Leu Ala Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His Phe Trp Ser Ser Pro Trp
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 997
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 997
gcgatccgca tgacccagag cccgttctcc ctgtccgcgt ccgtggggga ccgcgtgact
60
atcacgtgtc gggcctccgg gaacatccac aactacctcg catggtacca gcagaagccg
120
gccaaggccc ctaagttgtt catctacaac accaagactc ttgccgacgg agtgccgtcc
180
cggtttagcg gaagcggttc cggcaccgac tacaccctga ctatctcgag cctgcaacca
240
gaagatttcg ccacttacta ctgccagcac ttctggtcgt ccccttggac attcggcggc
300
ggcaccaagg tcgagattaa g
321
<210> 998
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 998
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1. 5 10 15
Gly Gly Gly Ser
20
<210> 999
<211> 249
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 999
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Thr Pro Thr Thr Gly Tyr Pro Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ala Ile
130 135 140
Arg Met Thr Gln Ser Pro Phe Ser Leu Ser Ala Ser Val Gly Asp Arg
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Gly Asn Ile His Asn Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Pro Ala Lys Ala Pro Lys Leu Phe Ile Tyr Asn
180 185 190
Thr Lys Thr Leu Ala Asp Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
210 215 220
Phe Ala Thr Tyr Tyr Cys Gln His Phe Trp Ser Ser Pro Trp Thr Phe
225 230 235 240
Gly Gly Gly Thr Lys Val Glu Ile Lys
245
<210> 1000
<211> 747
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1000
caagtccaac tcgtccagtc cggtgcagaa gtcaagaaac ccggagcttc cgtgaaagtg
60
tcctgcaaag cctccggtta cacctttacg aactactgga tgcattgggt gcgccaggcc
120
ccgggacagg ggctggaatg gatgggcttc attaccccca ccaccggata ccccgagtac
180
aatcagaagt tcaaggaccg ggtcaccatg accgccgaca agtcaacctc tactgcttac
240
atggagctgt ccagcctgcg gtcggaagat accgccgtgt attactgcgc gagaaggaaa
300
gtcggaaagg gagtgtacta tgccctggac tactggggac aggggaccac tgtgactgtg
360
tcaagcggag gcggaggctc ggggggcgga ggttcgggcg gaggaggatc agggggcggc
420
ggttccgcga tccgcatgac ccagagcccg ttctccctgt ccgcgtccgt gggggaccgc
480
gtgactatca cgtgtcgggc ctccgggaac atccacaact acctcgcatg gtaccagcag
540
aagccggcca aggcccctaa gttgttcatc tacaacacca agactcttgc cgacggagtg
600
ccgtcccggt ttagcggaag cggttccggc accgactaca ccctgactat ctcgagcctg
660
caaccagaag atttcgccac ttactactgc cagcacttct ggtcgtcccc ttggacattc
720
ggcggcggca ccaaggtcga gattaag
747
<210> 1001
<211> 493
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1001
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Asn Tyr Trp Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Phe Ile Thr Pro Thr Thr Gly Tyr Pro Glu
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Val Thr Met Thr Ala Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Arg Lys Val Gly Lys Gly Val Tyr Tyr
115 120 125
Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Ala Ile Arg Met Thr Gln Ser Pro Phe Ser Leu Ser Ala
165 170 175
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gly Asn Ile
180 185 190
His Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Ala Lys Ala Pro Lys
195 200 205
Leu Phe Ile Tyr Asn Thr Lys Thr Leu Ala Asp Gly Val Pro Ser Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser
225 230 235 240
Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His Phe Trp Ser
245 250 255
Ser Pro Trp Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1002
<211> 1479
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1002
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtcc aactcgtcca gtccggtgca gaagtcaaga aacccggagc ttccgtgaaa
120
gtgtcctgca aagcctccgg ttacaccttt acgaactact ggatgcattg ggtgcgccag
180
gccccgggac aggggctgga atggatgggc ttcattaccc ccaccaccgg ataccccgag
240
tacaatcaga agttcaagga ccgggtcacc atgaccgccg acaagtcaac ctctactgct
300
tacatggagc tgtccagcct gcggtcggaa gataccgccg tgtattactg cgcgagaagg
360
aaagtcggaa agggagtgta ctatgccctg gactactggg gacaggggac cactgtgact
420
gtgtcaagcg gaggcggagg ctcggggggc ggaggttcgg gcggaggagg atcagggggc
480
ggcggttccg cgatccgcat gacccagagc ccgttctccc tgtccgcgtc cgtgggggac
540
cgcgtgacta tcacgtgtcg ggcctccggg aacatccaca actacctcgc atggtaccag
600
cagaagccgg ccaaggcccc taagttgttc atctacaaca ccaagactct tgccgacgga
660
gtgccgtccc ggtttagcgg aagcggttcc ggcaccgact acaccctgac tatctcgagc
720
ctgcaaccag aagatttcgc cacttactac tgccagcact tctggtcgtc cccttggaca
780
ttcggcggcg gcaccaaggt cgagattaag accactaccc cagcaccgag gccacccacc
840
ccggctccta ccatcgcctc ccagcctctg tccctgcgtc cggaggcatg tagacccgca
900
gctggtgggg ccgtgcatac ccggggtctt gacttcgcct gcgatatcta catttgggcc
960
cctctggctg gtacttgcgg ggtcctgctg ctttcactcg tgatcactct ttactgtaag
1020
cgcggtcgga agaagctgct gtacatcttt aagcaaccct tcatgaggcc tgtgcagact
1080
actcaagagg aggacggctg ttcatgccgg ttcccagagg aggaggaagg cggctgcgaa
1140
ctgcgcgtga aattcagccg cagcgcagat gctccagcct accagcaggg gcagaaccag
1200
ctctacaacg aactcaatct tggtcggaga gaggagtacg acgtgctgga caagcggaga
1260
ggacgggacc cagaaatggg cgggaagccg cgcagaaaga atccccaaga gggcctgtac
1320
aacgagctcc aaaaggataa gatggcagaa gcctatagcg agattggtat gaaaggggaa
1380
cgcagaagag gcaaaggcca cgacggactg taccagggac tcagcaccgc caccaaggac
1440
acctatgacg ctcttcacat gcaggccctg ccgcctcgg
1479
<210> 1003
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1003
Asn Tyr Trp Met His
1. 5
<210> 1004
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1004
Phe Ile Thr Pro Thr Thr Gly Tyr Pro Glu Tyr Asn Gln Lys Phe Lys
1. 5 10 15
Asp
<210> 1005
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1005
Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr
1. 5 10
<210> 1006
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1006
Gly Tyr Thr Phe Thr Asn Tyr
1. 5
<210> 1007
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1007
Thr Pro Thr Thr Gly Tyr
1. 5
<210> 1008
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1008
Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr
1. 5 10
<210> 1009
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1009
Gly Tyr Thr Phe Thr Asn Tyr Trp
1. 5
<210> 1010
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1010
Ile Thr Pro Thr Thr Gly Tyr Pro
1. 5
<210> 1011
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1011
Ala Arg Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr
1. 5 10 15
<210> 1012
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1012
Gly Tyr Thr Phe Thr Asn Tyr Trp Met His
1. 5 10
<210> 1013
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1013
Phe Ile Thr Pro Thr Thr Gly Tyr Pro Glu Tyr Asn Gln Lys Phe Lys
1. 5 10 15
Asp
<210> 1014
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1014
Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr
1. 5 10
<210> 1015
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1015
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Thr Pro Thr Thr Gly Tyr Pro Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 1016
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1016
caagtccaac tcgtccaaag cggtgcagaa gtcaagaagc ccggttcctc cgtgaaagtg
60
tcctgcaaag cctcgggcta caccttcact aattactgga tgcattgggt ccgccaggcg
120
cccggacagg gattggaatg gatggggttc atcacgccga ccaccggata cccggagtac
180
aaccagaagt tcaaggacag agtgaccatt accgccgata agtccacctc caccgcttac
240
atggagctct cctcactgcg gtccgaagat acagccgtgt actattgtgc tcgccggaaa
300
gtcggaaagg gagtgtacta cgccctggac tattggggcc agggcaccac cgtgaccgtg
360
tcctcg
366
<210> 1017
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1017
Arg Ala Ser Gly Asn Ile His Asn Tyr Leu Ala
1. 5 10
<210> 1018
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1018
Asn Thr Lys Thr Leu Ala Asp
1. 5
<210> 1019
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1019
Gln His Phe Trp Ser Ser Pro Trp Thr
1. 5
<210> 1020
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1020
Ser Gly Asn Ile His Asn Tyr
1. 5
<210> 1021
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1021
Asn Thr Lys
1
<210> 1022
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1022
Phe Trp Ser Ser Pro Trp
1. 5
<210> 1023
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1023
Gly Asn Ile His Asn Tyr
1. 5
<210> 1024
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1024
Asn Thr Lys
1
<210> 1025
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1025
Gln His Phe Trp Ser Ser Pro Trp Thr
1. 5
<210> 1026
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1026
Arg Ala Ser Gly Asn Ile His Asn Tyr Leu Ala
1. 5 10
<210> 1027
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1027
Asn Thr Lys Thr Leu Ala Asp
1. 5
<210> 1028
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1028
Gln His Phe Trp Ser Ser Pro Trp Thr
1. 5
<210> 1029
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1029
Ala Ile Arg Met Thr Gln Ser Pro Phe Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gly Asn Ile His Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Ala Lys Ala Pro Lys Leu Phe Ile
35 40 45
Tyr Asn Thr Lys Thr Leu Ala Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His Phe Trp Ser Ser Pro Trp
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 1030
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1030
gccattagga tgactcagtc ccctttctcc ctctccgcga gcgtgggcga ccgcgtgacg
60
atcacttgcc gggcctcggg gaacattcac aactacctgg cctggtacca gcagaagccg
120
gccaaggccc ctaagctgtt catctacaac accaagaccc ttgcggacgg agtgccatcg
180
agattttccg gctcgggctc tgggaccgat tacactctga ctatctcaag cctgcaacct
240
gaggacttcg ccacttacta ctgccagcac ttctggagca gcccctggac tttcggtggc
300
gggaccaagg tcgaaatcaa g
321
<210> 1031
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1031
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1. 5 10 15
Gly Gly Gly Ser
20
<210> 1032
<211> 249
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1032
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Thr Pro Thr Thr Gly Tyr Pro Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ala Ile
130 135 140
Arg Met Thr Gln Ser Pro Phe Ser Leu Ser Ala Ser Val Gly Asp Arg
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Gly Asn Ile His Asn Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Pro Ala Lys Ala Pro Lys Leu Phe Ile Tyr Asn
180 185 190
Thr Lys Thr Leu Ala Asp Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
210 215 220
Phe Ala Thr Tyr Tyr Cys Gln His Phe Trp Ser Ser Pro Trp Thr Phe
225 230 235 240
Gly Gly Gly Thr Lys Val Glu Ile Lys
245
<210> 1033
<211> 747
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1033
caagtccaac tcgtccaaag cggtgcagaa gtcaagaagc ccggttcctc cgtgaaagtg
60
tcctgcaaag cctcgggcta caccttcact aattactgga tgcattgggt ccgccaggcg
120
cccggacagg gattggaatg gatggggttc atcacgccga ccaccggata cccggagtac
180
aaccagaagt tcaaggacag agtgaccatt accgccgata agtccacctc caccgcttac
240
atggagctct cctcactgcg gtccgaagat acagccgtgt actattgtgc tcgccggaaa
300
gtcggaaagg gagtgtacta cgccctggac tattggggcc agggcaccac cgtgaccgtg
360
tcctcgggag gagggggttc gggcggaggc ggctccggtg gaggcggaag cggagggggc
420
ggatcagcca ttaggatgac tcagtcccct ttctccctct ccgcgagcgt gggcgaccgc
480
gtgacgatca cttgccgggc ctcggggaac attcacaact acctggcctg gtaccagcag
540
aagccggcca aggcccctaa gctgttcatc tacaacacca agacccttgc ggacggagtg
600
ccatcgagat tttccggctc gggctctggg accgattaca ctctgactat ctcaagcctg
660
caacctgagg acttcgccac ttactactgc cagcacttct ggagcagccc ctggactttc
720
ggtggcggga ccaaggtcga aatcaag
747
<210> 1034
<211> 493
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1034
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Asn Tyr Trp Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Phe Ile Thr Pro Thr Thr Gly Tyr Pro Glu
65 70 75 80
Tyr Asn Gln Lys Phe Lys Asp Arg Val Thr Ile Thr Ala Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Arg Lys Val Gly Lys Gly Val Tyr Tyr
115 120 125
Ala Leu Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Ala Ile Arg Met Thr Gln Ser Pro Phe Ser Leu Ser Ala
165 170 175
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gly Asn Ile
180 185 190
His Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Ala Lys Ala Pro Lys
195 200 205
Leu Phe Ile Tyr Asn Thr Lys Thr Leu Ala Asp Gly Val Pro Ser Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser
225 230 235 240
Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His Phe Trp Ser
245 250 255
Ser Pro Trp Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1035
<211> 1479
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1035
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtcc aactcgtcca aagcggtgca gaagtcaaga agcccggttc ctccgtgaaa
120
gtgtcctgca aagcctcggg ctacaccttc actaattact ggatgcattg ggtccgccag
180
gcgcccggac agggattgga atggatgggg ttcatcacgc cgaccaccgg atacccggag
240
tacaaccaga agttcaagga cagagtgacc attaccgccg ataagtccac ctccaccgct
300
tacatggagc tctcctcact gcggtccgaa gatacagccg tgtactattg tgctcgccgg
360
aaagtcggaa agggagtgta ctacgccctg gactattggg gccagggcac caccgtgacc
420
gtgtcctcgg gaggaggggg ttcgggcgga ggcggctccg gtggaggcgg aagcggaggg
480
ggcggatcag ccattaggat gactcagtcc cctttctccc tctccgcgag cgtgggcgac
540
cgcgtgacga tcacttgccg ggcctcgggg aacattcaca actacctggc ctggtaccag
600
cagaagccgg ccaaggcccc taagctgttc atctacaaca ccaagaccct tgcggacgga
660
gtgccatcga gattttccgg ctcgggctct gggaccgatt acactctgac tatctcaagc
720
ctgcaacctg aggacttcgc cacttactac tgccagcact tctggagcag cccctggact
780
ttcggtggcg ggaccaaggt cgaaatcaag accactaccc cagcaccgag gccacccacc
840
ccggctccta ccatcgcctc ccagcctctg tccctgcgtc cggaggcatg tagacccgca
900
gctggtgggg ccgtgcatac ccggggtctt gacttcgcct gcgatatcta catttgggcc
960
cctctggctg gtacttgcgg ggtcctgctg ctttcactcg tgatcactct ttactgtaag
1020
cgcggtcgga agaagctgct gtacatcttt aagcaaccct tcatgaggcc tgtgcagact
1080
actcaagagg aggacggctg ttcatgccgg ttcccagagg aggaggaagg cggctgcgaa
1140
ctgcgcgtga aattcagccg cagcgcagat gctccagcct accagcaggg gcagaaccag
1200
ctctacaacg aactcaatct tggtcggaga gaggagtacg acgtgctgga caagcggaga
1260
ggacgggacc cagaaatggg cgggaagccg cgcagaaaga atccccaaga gggcctgtac
1320
aacgagctcc aaaaggataa gatggcagaa gcctatagcg agattggtat gaaaggggaa
1380
cgcagaagag gcaaaggcca cgacggactg taccagggac tcagcaccgc caccaaggac
1440
acctatgacg ctcttcacat gcaggccctg ccgcctcgg
1479
<210> 1036
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1036
Asn Tyr Asn Leu His
1. 5
<210> 1037
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1037
Ala Ile Tyr Pro Gly Asn Tyr Asp Thr Ser Tyr Asn Gln Lys Phe Lys
1. 5 10 15
Gly
<210> 1038
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1038
Val Asp Phe Gly His Ser Arg Tyr Trp Tyr Phe Asp Val
1. 5 10
<210> 1039
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1039
Gly Tyr Thr Phe Thr Asn Tyr
1. 5
<210> 1040
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1040
Tyr Pro Gly Asn Tyr Asp
1. 5
<210> 1041
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1041
Val Asp Phe Gly His Ser Arg Tyr Trp Tyr Phe Asp Val
1. 5 10
<210> 1042
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1042
Gly Tyr Thr Phe Thr Asn Tyr Asn
1. 5
<210> 1043
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1043
Ile Tyr Pro Gly Asn Tyr Asp Thr
1. 5
<210> 1044
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1044
Ala Arg Val Asp Phe Gly His Ser Arg Tyr Trp Tyr Phe Asp Val
1. 5 10 15
<210> 1045
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1045
Gly Tyr Thr Phe Thr Asn Tyr Asn Leu His
1. 5 10
<210> 1046
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1046
Ala Ile Tyr Pro Gly Asn Tyr Asp Thr Ser Tyr Asn Gln Lys Phe Lys
1. 5 10 15
Gly
<210> 1047
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1047
Val Asp Phe Gly His Ser Arg Tyr Trp Tyr Phe Asp Val
1. 5 10
<210> 1048
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1048
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Asn Leu His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Tyr Asp Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Met Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Asp Phe Gly His Ser Arg Tyr Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 1049
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1049
caagtccaac tcgtccaatc cggtgcagaa gtcaagaaac ccggtgcatc cgtgaaagtg
60
tcatgcaaag cctccgggta caccttcact aactacaacc tccactgggt ccgccaggcc
120
ccgggacagg gactggagtg gatgggggcc atctacccgg gaaactacga cacttcatac
180
aaccagaagt tcaagggcag agtgaccatg actgccgaca agagcacatc gaccgcctac
240
atggaactca gctccctgcg ctccgaggat actgccgtct actactgtgc ccgggtggac
300
ttcggccact cccggtattg gtatttcgat gtctggggac agggaaccac cgtgactgtg
360
tccagc
366
<210> 1050
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1050
Arg Ala Thr Ser Ser Val Ser Ser Met Asn
1. 5 10
<210> 1051
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1051
Ala Thr Ser Asn Leu Ala Ser
1. 5
<210> 1052
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1052
Gln Gln Trp Thr Phe Asn Pro Pro Thr
1. 5
<210> 1053
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1053
Thr Ser Ser Val Ser Ser
1. 5
<210> 1054
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1054
Ala Thr Ser
1
<210> 1055
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1055
Trp Thr Phe Asn Pro Pro
1. 5
<210> 1056
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1056
Ser Ser Val Ser Ser
1. 5
<210> 1057
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1057
Ala Thr Ser
1
<210> 1058
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1058
Gln Gln Trp Thr Phe Asn Pro Pro Thr
1. 5
<210> 1059
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1059
Arg Ala Thr Ser Ser Val Ser Ser Met Asn
1. 5 10
<210> 1060
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1060
Ala Thr Ser Asn Leu Ala Ser
1. 5
<210> 1061
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1061
Gln Gln Trp Thr Phe Asn Pro Pro Thr
1. 5
<210> 1062
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1062
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Thr Ser Ser Val Ser Ser Met
20 25 30
Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Pro Leu Ile His
35 40 45
Ala Thr Ser Asn Leu Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu
65 70 75 80
Asp Ala Ala Val Tyr Tyr Cys Gln Gln Trp Thr Phe Asn Pro Pro Thr
85 90 95
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1063
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1063
gaaatcgtgc tgacccagtc ccctgcgact ctgagcctga gccctgggga acgcgccact
60
ttgtcatgcc gggccacctc ctccgtgtcc tccatgaact ggtaccagca gaagcccgga
120
caggctccgc ggccgctgat ccatgccacc tccaacctgg ccagcggcat tcccgcgagg
180
ttttccggct cgggctctgg taccgactac accctgacca tctcgagcct tgagccagaa
240
gatgctgcgg tgtactactg ccaacagtgg accttcaatc cgcctacgtt cggacagggg
300
accaagctgg agattaag
318
<210> 1064
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1064
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1. 5 10 15
Gly Gly Gly Ser
20
<210> 1065
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1065
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Asn Leu His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Tyr Asp Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Met Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Asp Phe Gly His Ser Arg Tyr Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile
130 135 140
Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg
145 150 155 160
Ala Thr Leu Ser Cys Arg Ala Thr Ser Ser Val Ser Ser Met Asn Trp
165 170 175
Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Pro Leu Ile His Ala Thr
180 185 190
Ser Asn Leu Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser
195 200 205
Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp Ala
210 215 220
Ala Val Tyr Tyr Cys Gln Gln Trp Thr Phe Asn Pro Pro Thr Phe Gly
225 230 235 240
Gln Gly Thr Lys Leu Glu Ile Lys
245
<210> 1066
<211> 744
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1066
caagtccaac tcgtccaatc cggtgcagaa gtcaagaaac ccggtgcatc cgtgaaagtg
60
tcatgcaaag cctccgggta caccttcact aactacaacc tccactgggt ccgccaggcc
120
ccgggacagg gactggagtg gatgggggcc atctacccgg gaaactacga cacttcatac
180
aaccagaagt tcaagggcag agtgaccatg actgccgaca agagcacatc gaccgcctac
240
atggaactca gctccctgcg ctccgaggat actgccgtct actactgtgc ccgggtggac
300
ttcggccact cccggtattg gtatttcgat gtctggggac agggaaccac cgtgactgtg
360
tccagcgggg gcggaggatc gggtggcgga ggttcggggg gaggaggatc aggcggcggc
420
ggatcggaaa tcgtgctgac ccagtcccct gcgactctga gcctgagccc tggggaacgc
480
gccactttgt catgccgggc cacctcctcc gtgtcctcca tgaactggta ccagcagaag
540
cccggacagg ctccgcggcc gctgatccat gccacctcca acctggccag cggcattccc
600
gcgaggtttt ccggctcggg ctctggtacc gactacaccc tgaccatctc gagccttgag
660
ccagaagatg ctgcggtgta ctactgccaa cagtggacct tcaatccgcc tacgttcgga
720
caggggacca agctggagat taag
744
<210> 1067
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1067
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Asn Tyr Asn Leu His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Ala Ile Tyr Pro Gly Asn Tyr Asp Thr Ser
65 70 75 80
Tyr Asn Gln Lys Phe Lys Gly Arg Val Thr Met Thr Ala Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Val Asp Phe Gly His Ser Arg Tyr Trp
115 120 125
Tyr Phe Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu
165 170 175
Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Thr Ser Ser Val
180 185 190
Ser Ser Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Pro
195 200 205
Leu Ile His Ala Thr Ser Asn Leu Ala Ser Gly Ile Pro Ala Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu
225 230 235 240
Glu Pro Glu Asp Ala Ala Val Tyr Tyr Cys Gln Gln Trp Thr Phe Asn
245 250 255
Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1068
<211> 1476
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1068
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtcc aactcgtcca atccggtgca gaagtcaaga aacccggtgc atccgtgaaa
120
gtgtcatgca aagcctccgg gtacaccttc actaactaca acctccactg ggtccgccag
180
gccccgggac agggactgga gtggatgggg gccatctacc cgggaaacta cgacacttca
240
tacaaccaga agttcaaggg cagagtgacc atgactgccg acaagagcac atcgaccgcc
300
tacatggaac tcagctccct gcgctccgag gatactgccg tctactactg tgcccgggtg
360
gacttcggcc actcccggta ttggtatttc gatgtctggg gacagggaac caccgtgact
420
gtgtccagcg ggggcggagg atcgggtggc ggaggttcgg ggggaggagg atcaggcggc
480
ggcggatcgg aaatcgtgct gacccagtcc cctgcgactc tgagcctgag ccctggggaa
540
cgcgccactt tgtcatgccg ggccacctcc tccgtgtcct ccatgaactg gtaccagcag
600
aagcccggac aggctccgcg gccgctgatc catgccacct ccaacctggc cagcggcatt
660
cccgcgaggt tttccggctc gggctctggt accgactaca ccctgaccat ctcgagcctt
720
gagccagaag atgctgcggt gtactactgc caacagtgga ccttcaatcc gcctacgttc
780
ggacagggga ccaagctgga gattaagacc actaccccag caccgaggcc acccaccccg
840
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
900
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
960
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1020
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1080
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1140
cgcgtgaaat tcagccgcag cgcagatgct ccagcctacc agcaggggca gaaccagctc
1200
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
1260
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
1320
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
1380
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
1440
tatgacgctc ttcacatgca ggccctgccg cctcgg
1476
<210> 1069
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1069
Asn Tyr Asn Leu His
1. 5
<210> 1070
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1070
Ala Ile Tyr Pro Gly Asn Tyr Asp Thr Ser Tyr Asn Gln Lys Phe Lys
1. 5 10 15
Gly
<210> 1071
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1071
Val Asp Phe Gly His Ser Arg Tyr Trp Tyr Phe Asp Val
1. 5 10
<210> 1072
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1072
Gly Tyr Thr Phe Thr Asn Tyr
1. 5
<210> 1073
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1073
Tyr Pro Gly Asn Tyr Asp
1. 5
<210> 1074
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1074
Val Asp Phe Gly His Ser Arg Tyr Trp Tyr Phe Asp Val
1. 5 10
<210> 1075
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1075
Gly Tyr Thr Phe Thr Asn Tyr Asn
1. 5
<210> 1076
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1076
Ile Tyr Pro Gly Asn Tyr Asp Thr
1. 5
<210> 1077
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1077
Ala Arg Val Asp Phe Gly His Ser Arg Tyr Trp Tyr Phe Asp Val
1. 5 10 15
<210> 1078
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1078
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Thr Pro Thr Thr Gly Tyr Pro Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 1079
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1079
caagtccaac tcgtccagtc gggagcagaa gtcaagaagc ccggatcatc cgtgaaagtg
60
tcctgcaaag cctcaggcta cacctttacc aactacaact tgcactgggt cagacaggcc
120
ccgggacagg gcctggagtg gatgggcgcc atctaccccg gaaactatga cacctcgtac
180
aaccagaagt tcaagggtcg cgtgactatc acggctgaca agtccactag caccgcgtac
240
atggaacttt cctcactgcg gtccgaggat actgcggtgt actactgcgc ccgggtggac
300
ttcggacact cgagatattg gtacttcgat gtctggggac aggggaccac cgtgactgtg
360
tcctcc
366
<210> 1080
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1080
Arg Ala Thr Ser Ser Val Ser Ser Met Asn
1. 5 10
<210> 1081
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1081
Ala Thr Ser Asn Leu Ala Ser
1. 5
<210> 1082
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1082
Gln Gln Trp Thr Phe Asn Pro Pro Thr
1. 5
<210> 1083
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1083
Thr Ser Ser Val Ser Ser
1. 5
<210> 1084
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1084
Ala Thr Ser
1
<210> 1085
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1085
Trp Thr Phe Asn Pro Pro
1. 5
<210> 1086
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1086
Ser Ser Val Ser Ser
1. 5
<210> 1087
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1087
Ala Thr Ser
1
<210> 1088
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1088
Gln Gln Trp Thr Phe Asn Pro Pro Thr
1. 5
<210> 1089
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1089
Arg Ala Thr Ser Ser Val Ser Ser Met Asn
1. 5 10
<210> 1090
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1090
Ala Thr Ser Asn Leu Ala Ser
1. 5
<210> 1091
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1091
Gln Gln Trp Thr Phe Asn Pro Pro Thr
1. 5
<210> 1092
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1092
Ala Ile Arg Met Thr Gln Ser Pro Phe Ser Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gly Asn Ile His Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Ala Lys Ala Pro Lys Leu Phe Ile
35 40 45
Tyr Asn Thr Lys Thr Leu Ala Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His Phe Trp Ser Ser Pro Trp
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 1093
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1093
gaaattgtgc tgacccagtc tcccgcaacc ctgtccctga gccctggaga gcgcgccacc
60
ctgtcctgcc gggccacatc ctccgtgtcg tccatgaact ggtaccagca gaagcccggc
120
caagccccga ggcctctgat tcatgctacc tcaaatctgg ccagcggaat cccggcgcgc
180
ttctccggct cgggcagcgg tactgactac actctcacca tctcgtccct cgaaccggag
240
gacgccgccg tctactactg tcagcagtgg accttcaacc cacctacttt cggacaaggg
300
accaagctgg agatcaag
318
<210> 1094
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1094
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
1. 5 10 15
Gly Gly Ser
<210> 1095
<211> 249
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1095
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Thr Pro Thr Thr Gly Tyr Pro Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ala Ile
130 135 140
Arg Met Thr Gln Ser Pro Phe Ser Leu Ser Ala Ser Val Gly Asp Arg
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Gly Asn Ile His Asn Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Pro Ala Lys Ala Pro Lys Leu Phe Ile Tyr Asn
180 185 190
Thr Lys Thr Leu Ala Asp Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
210 215 220
Phe Ala Thr Tyr Tyr Cys Gln His Phe Trp Ser Ser Pro Trp Thr Phe
225 230 235 240
Gly Gly Gly Thr Lys Val Glu Ile Lys
245
<210> 1096
<211> 744
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1096
caagtccaac tcgtccagtc gggagcagaa gtcaagaagc ccggatcatc cgtgaaagtg
60
tcctgcaaag cctcaggcta cacctttacc aactacaact tgcactgggt cagacaggcc
120
ccgggacagg gcctggagtg gatgggcgcc atctaccccg gaaactatga cacctcgtac
180
aaccagaagt tcaagggtcg cgtgactatc acggctgaca agtccactag caccgcgtac
240
atggaacttt cctcactgcg gtccgaggat actgcggtgt actactgcgc ccgggtggac
300
ttcggacact cgagatattg gtacttcgat gtctggggac aggggaccac cgtgactgtg
360
tcctccgggg gcggtggcag cgggggaggc ggaagcggcg gagggggttc cgggggtgga
420
ggaagcgaaa ttgtgctgac ccagtctccc gcaaccctgt ccctgagccc tggagagcgc
480
gccaccctgt cctgccgggc cacatcctcc gtgtcgtcca tgaactggta ccagcagaag
540
cccggccaag ccccgaggcc tctgattcat gctacctcaa atctggccag cggaatcccg
600
gcgcgcttct ccggctcggg cagcggtact gactacactc tcaccatctc gtccctcgaa
660
ccggaggacg ccgccgtcta ctactgtcag cagtggacct tcaacccacc tactttcgga
720
caagggacca agctggagat caag
744
<210> 1097
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1097
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Asn Tyr Asn Leu His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Ala Ile Tyr Pro Gly Asn Tyr Asp Thr Ser
65 70 75 80
Tyr Asn Gln Lys Phe Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Val Asp Phe Gly His Ser Arg Tyr Trp
115 120 125
Tyr Phe Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu
165 170 175
Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Thr Ser Ser Val
180 185 190
Ser Ser Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Pro
195 200 205
Leu Ile His Ala Thr Ser Asn Leu Ala Ser Gly Ile Pro Ala Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu
225 230 235 240
Glu Pro Glu Asp Ala Ala Val Tyr Tyr Cys Gln Gln Trp Thr Phe Asn
245 250 255
Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1098
<211> 1476
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1098
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtcc aactcgtcca gtcgggagca gaagtcaaga agcccggatc atccgtgaaa
120
gtgtcctgca aagcctcagg ctacaccttt accaactaca acttgcactg ggtcagacag
180
gccccgggac agggcctgga gtggatgggc gccatctacc ccggaaacta tgacacctcg
240
tacaaccaga agttcaaggg tcgcgtgact atcacggctg acaagtccac tagcaccgcg
300
tacatggaac tttcctcact gcggtccgag gatactgcgg tgtactactg cgcccgggtg
360
gacttcggac actcgagata ttggtacttc gatgtctggg gacaggggac caccgtgact
420
gtgtcctccg ggggcggtgg cagcggggga ggcggaagcg gcggaggggg ttccgggggt
480
ggaggaagcg aaattgtgct gacccagtct cccgcaaccc tgtccctgag ccctggagag
540
cgcgccaccc tgtcctgccg ggccacatcc tccgtgtcgt ccatgaactg gtaccagcag
600
aagcccggcc aagccccgag gcctctgatt catgctacct caaatctggc cagcggaatc
660
ccggcgcgct tctccggctc gggcagcggt actgactaca ctctcaccat ctcgtccctc
720
gaaccggagg acgccgccgt ctactactgt cagcagtgga ccttcaaccc acctactttc
780
ggacaaggga ccaagctgga gatcaagacc actaccccag caccgaggcc acccaccccg
840
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
900
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
960
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1020
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1080
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1140
cgcgtgaaat tcagccgcag cgcagatgct ccagcctacc agcaggggca gaaccagctc
1200
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
1260
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
1320
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
1380
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
1440
tatgacgctc ttcacatgca ggccctgccg cctcgg
1476
<210> 1099
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1099
Asn Tyr Asn Leu His
1. 5
<210> 1100
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1100
Ala Ile Tyr Pro Gly Asn Tyr Asp Thr Ser Tyr Asn Gln Lys Phe Lys
1. 5 10 15
Gly
<210> 1101
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1101
Val Asp Phe Gly His Ser Arg Tyr Trp Tyr Phe Asp Val
1. 5 10
<210> 1102
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1102
Gly Tyr Thr Phe Thr Asn Tyr
1. 5
<210> 1103
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1103
Tyr Pro Gly Asn Tyr Asp
1. 5
<210> 1104
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1104
Val Asp Phe Gly His Ser Arg Tyr Trp Tyr Phe Asp Val
1. 5 10
<210> 1105
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1105
Gly Tyr Thr Phe Thr Asn Tyr Asn
1. 5
<210> 1106
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1106
Ile Tyr Pro Gly Asn Tyr Asp Thr
1. 5
<210> 1107
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1107
Ala Arg Val Asp Phe Gly His Ser Arg Tyr Trp Tyr Phe Asp Val
1. 5 10 15
<210> 1108
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1108
Gly Tyr Thr Phe Thr Asn Tyr Asn Leu His
1. 5 10
<210> 1109
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1109
Ala Ile Tyr Pro Gly Asn Tyr Asp Thr Ser Tyr Asn Gln Lys Phe Lys
1. 5 10 15
Gly
<210> 1110
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1110
Val Asp Phe Gly His Ser Arg Tyr Trp Tyr Phe Asp Val
1. 5 10
<210> 1111
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1111
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Asn Leu His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Tyr Asp Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Asp Phe Gly His Ser Arg Tyr Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 1112
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1112
caagtccaac tcgtccagtc gggagcagaa gtcaagaagc ccggatcatc cgtgaaagtg
60
tcctgcaaag cctcaggcta cacctttacc aactacaact tgcactgggt cagacaggcc
120
ccgggacagg gcctggagtg gatgggcgcc atctaccccg gaaactatga cacctcgtac
180
aaccagaagt tcaagggtcg cgtgactatc acggctgaca agtccactag caccgcgtac
240
atggaacttt cctcactgcg gtccgaggat actgcggtgt actactgcgc ccgggtggac
300
ttcggacact cgagatattg gtacttcgat gtctggggac aggggaccac cgtgactgtg
360
tcctcc
366
<210> 1113
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1113
Arg Ala Thr Ser Ser Val Ser Ser Met Asn
1. 5 10
<210> 1114
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1114
Ala Thr Ser Asn Leu Ala Ser
1. 5
<210> 1115
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1115
Gln Gln Trp Thr Phe Asn Pro Pro Thr
1. 5
<210> 1116
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1116
Thr Ser Ser Val Ser Ser
1. 5
<210> 1117
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1117
Ala Thr Ser
1
<210> 1118
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1118
Trp Thr Phe Asn Pro Pro
1. 5
<210> 1119
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1119
Ser Ser Val Ser Ser
1. 5
<210> 1120
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1120
Ala Thr Ser
1
<210> 1121
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1121
Gln Gln Trp Thr Phe Asn Pro Pro Thr
1. 5
<210> 1122
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1122
Arg Ala Thr Ser Ser Val Ser Ser Met Asn
1. 5 10
<210> 1123
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1123
Ala Thr Ser Asn Leu Ala Ser
1. 5
<210> 1124
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1124
Gln Gln Trp Thr Phe Asn Pro Pro Thr
1. 5
<210> 1125
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1125
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Thr Ser Ser Val Ser Ser Met
20 25 30
Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Pro Leu Ile His
35 40 45
Ala Thr Ser Asn Leu Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu
65 70 75 80
Asp Ala Ala Val Tyr Tyr Cys Gln Gln Trp Thr Phe Asn Pro Pro Thr
85 90 95
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1126
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1126
gaaattgtgc tgacccagtc tcccgcaacc ctgtccctga gccctggaga gcgcgccacc
60
ctgtcctgcc gggccacatc ctccgtgtcg tccatgaact ggtaccagca gaagcccggc
120
caagccccga ggcctctgat tcatgctacc tcaaatctgg ccagcggaat cccggcgcgc
180
ttctccggct cgggcagcgg tactgactac actctcacca tctcgtccct cgaaccggag
240
gacgccgccg tctactactg tcagcagtgg accttcaacc cacctacttt cggacaaggg
300
accaagctgg agatcaag
318
<210> 1127
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1127
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1. 5 10 15
Gly Gly Gly Ser
20
<210> 1128
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1128
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Asn Leu His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Tyr Asp Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Asp Phe Gly His Ser Arg Tyr Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile
130 135 140
Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg
145 150 155 160
Ala Thr Leu Ser Cys Arg Ala Thr Ser Ser Val Ser Ser Met Asn Trp
165 170 175
Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Pro Leu Ile His Ala Thr
180 185 190
Ser Asn Leu Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser
195 200 205
Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp Ala
210 215 220
Ala Val Tyr Tyr Cys Gln Gln Trp Thr Phe Asn Pro Pro Thr Phe Gly
225 230 235 240
Gln Gly Thr Lys Leu Glu Ile Lys
245
<210> 1129
<211> 744
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1129
caagtccaac tcgtccaatc cggcgcagaa gtcaagaaac caggatcgtc cgtgaaagtg
60
tcctgcaagg cgtccgggta caccttcact aattacaacc tccactgggt cagacaggcc
120
ccaggacagg gcctggaatg gatgggcgcc atctaccctg gaaactacga tacctcgtac
180
aaccagaagt tcaagggccg cgtgactatt accgccgaca agagcacctc caccgcctat
240
atggaactgt cgtccctgcg gtccgaggac actgccgtgt actactgtgc aagggtggac
300
ttcggtcact cccggtattg gtacttcgac gtctggggac aggggaccac tgtgaccgtg
360
tcgtcgggag gcggtggaag cggcggtggc ggaagcggag gcggcggatc agggggcgga
420
ggaagcgaca ttcagcttac ccagtcaccg tccttcctga gcgcctccgt gggagatcgc
480
gtgaccatca catgccgcgc cacttcctcg gtgtcctcca tgaactggta ccagcagaag
540
cccggaaagg ctcctaagcc tctgatccat gcgacctcca acttggcttc cggggtgccg
600
tcacggttca gcggcagcgg ttcaggaact gagtacaccc tgactattag ctctctccaa
660
cccgaggact tcgccaccta ctactgccag cagtggacct tcaacccgcc cacgtttggg
720
cagggtacca agctggagat caag
744
<210> 1130
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1130
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Asn Tyr Asn Leu His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Ala Ile Tyr Pro Gly Asn Tyr Asp Thr Ser
65 70 75 80
Tyr Asn Gln Lys Phe Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Val Asp Phe Gly His Ser Arg Tyr Trp
115 120 125
Tyr Phe Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala
165 170 175
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Thr Ser Ser Val
180 185 190
Ser Ser Met Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro
195 200 205
Leu Ile His Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Glu Tyr Thr Leu Thr Ile Ser Ser Leu
225 230 235 240
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Trp Thr Phe Asn
245 250 255
Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1131
<211> 1476
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1131
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtcc aactcgtcca atccggcgca gaagtcaaga aaccaggatc gtccgtgaaa
120
gtgtcctgca aggcgtccgg gtacaccttc actaattaca acctccactg ggtcagacag
180
gccccaggac agggcctgga atggatgggc gccatctacc ctggaaacta cgatacctcg
240
tacaaccaga agttcaaggg ccgcgtgact attaccgccg acaagagcac ctccaccgcc
300
tatatggaac tgtcgtccct gcggtccgag gacactgccg tgtactactg tgcaagggtg
360
gacttcggtc actcccggta ttggtacttc gacgtctggg gacaggggac cactgtgacc
420
gtgtcgtcgg gaggcggtgg aagcggcggt ggcggaagcg gaggcggcgg atcagggggc
480
ggaggaagcg acattcagct tacccagtca ccgtccttcc tgagcgcctc cgtgggagat
540
cgcgtgacca tcacatgccg cgccacttcc tcggtgtcct ccatgaactg gtaccagcag
600
aagcccggaa aggctcctaa gcctctgatc catgcgacct ccaacttggc ttccggggtg
660
ccgtcacggt tcagcggcag cggttcagga actgagtaca ccctgactat tagctctctc
720
caacccgagg acttcgccac ctactactgc cagcagtgga ccttcaaccc gcccacgttt
780
gggcagggta ccaagctgga gatcaagacc actaccccag caccgaggcc acccaccccg
840
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
900
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
960
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1020
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1080
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1140
cgcgtgaaat tcagccgcag cgcagatgct ccagcctacc agcaggggca gaaccagctc
1200
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
1260
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
1320
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
1380
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
1440
tatgacgctc ttcacatgca ggccctgccg cctcgg
1476
<210> 1132
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1132
Ser Tyr Asn Met His
1. 5
<210> 1133
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1133
Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Asn Pro Lys Phe Lys
1. 5 10 15
Gly
<210> 1134
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1134
Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val
1. 5 10
<210> 1135
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1135
Gly Tyr Thr Phe Thr Ser Tyr
1. 5
<210> 1136
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1136
Tyr Pro Gly Asn Gly Asp
1. 5
<210> 1137
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1137
Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val
1. 5 10
<210> 1138
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1138
Gly Tyr Thr Phe Thr Ser Tyr Asn
1. 5
<210> 1139
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1139
Ile Tyr Pro Gly Asn Gly Asp Thr
1. 5
<210> 1140
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1140
Ala Arg Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val
1. 5 10 15
<210> 1141
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1141
Gly Tyr Thr Phe Thr Ser Tyr Asn Met His
1. 5 10
<210> 1142
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1142
Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Asn Pro Lys Phe Lys
1. 5 10 15
Gly
<210> 1143
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1143
Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val
1. 5 10
<210> 1144
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1144
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Asn Pro Lys Phe
50 55 60
Lys Gly Arg Val Thr Met Thr Ala Asp Lys Ser Thr Arg Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 1145
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1145
caagtccaac tcgtccagtc aggagcagaa gtcaagaaac ctggagcttc cgtgaaagtg
60
tcgtgcaagg cctccggcta caccttcacc tcttacaaca tgcactgggt cagacaggcc
120
cctggtcaag gactggaatg gatgggagcg atctacccgg gcaacggaga cacttcgtac
180
aaccccaagt tcaagggacg ggtcactatg accgccgata agagcacgcg caccgcgtac
240
atggaactga gcagcctgcg ctccgaggac actgccgtgt attactgcgc gaggagctac
300
ttctacggat catcgtcgtg gtacttcgac gtctggggcc agggcaccac cgtgaccgtg
360
tcatcc
366
<210> 1146
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1146
Arg Ala Ser Ser Ser Val Ser Ser Met His
1. 5 10
<210> 1147
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1147
Ala Thr Ser Asn Leu Ala Ser
1. 5
<210> 1148
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1148
Gln Gln Trp Ile Phe Asn Pro Pro Thr
1. 5
<210> 1149
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1149
Ser Ser Ser Val Ser Ser
1. 5
<210> 1150
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1150
Ala Thr Ser
1
<210> 1151
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1151
Trp Ile Phe Asn Pro Pro
1. 5
<210> 1152
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1152
Ser Ser Val Ser Ser
1. 5
<210> 1153
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1153
Ala Thr Ser
1
<210> 1154
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1154
Gln Gln Trp Ile Phe Asn Pro Pro Thr
1. 5
<210> 1155
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1155
Arg Ala Ser Ser Ser Val Ser Ser Met His
1. 5 10
<210> 1156
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1156
Ala Thr Ser Asn Leu Ala Ser
1. 5
<210> 1157
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1157
Gln Gln Trp Ile Phe Asn Pro Pro Thr
1. 5
<210> 1158
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1158
Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro Leu Ile Phe
35 40 45
Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Glu Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
65 70 75 80
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Trp Ile Phe Asn Pro Pro Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 1159
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1159
gatattcagc tgacccagag cccgtcattc ctgtccgcct ccgtgggaga cagagtgacc
60
atcacttgtc gggccagctc ctcggtgtcc tccatgcatt ggtatcagca gaagcctggg
120
aaggctccca agcccctcat cttcgccaca tcaaatcttg cctccggggt gccaagccgg
180
ttctccggga gcggctccgg tactgagtac actctgacca tttcctcctt gcaacccgag
240
gactttgcca cctactactg ccagcagtgg atctttaacc cgccgacctt cggaggagga
300
accaaagtgg agatcaag
318
<210> 1160
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1160
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1. 5 10 15
Gly Gly Gly Ser
20
<210> 1161
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1161
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Asn Pro Lys Phe
50 55 60
Lys Gly Arg Val Thr Met Thr Ala Asp Lys Ser Thr Arg Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly Asp Arg
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Met His Trp
165 170 175
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro Leu Ile Phe Ala Thr
180 185 190
Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
195 200 205
Gly Thr Glu Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
210 215 220
Ala Thr Tyr Tyr Cys Gln Gln Trp Ile Phe Asn Pro Pro Thr Phe Gly
225 230 235 240
Gly Gly Thr Lys Val Glu Ile Lys
245
<210> 1162
<211> 744
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1162
caagtccaac tcgtccagtc aggagcagaa gtcaagaaac ctggagcttc cgtgaaagtg
60
tcgtgcaagg cctccggcta caccttcacc tcttacaaca tgcactgggt cagacaggcc
120
cctggtcaag gactggaatg gatgggagcg atctacccgg gcaacggaga cacttcgtac
180
aaccccaagt tcaagggacg ggtcactatg accgccgata agagcacgcg caccgcgtac
240
atggaactga gcagcctgcg ctccgaggac actgccgtgt attactgcgc gaggagctac
300
ttctacggat catcgtcgtg gtacttcgac gtctggggcc agggcaccac cgtgaccgtg
360
tcatccggtg gcggaggatc ggggggcgga ggaagcggcg gggggggctc cggcggtgga
420
ggctcggata ttcagctgac ccagagcccg tcattcctgt ccgcctccgt gggagacaga
480
gtgaccatca cttgtcgggc cagctcctcg gtgtcctcca tgcattggta tcagcagaag
540
cctgggaagg ctcccaagcc cctcatcttc gccacatcaa atcttgcctc cggggtgcca
600
agccggttct ccgggagcgg ctccggtact gagtacactc tgaccatttc ctccttgcaa
660
cccgaggact ttgccaccta ctactgccag cagtggatct ttaacccgcc gaccttcgga
720
ggaggaacca aagtggagat caag
744
<210> 1163
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1163
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Asn Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser
65 70 75 80
Tyr Asn Pro Lys Phe Lys Gly Arg Val Thr Met Thr Ala Asp Lys Ser
85 90 95
Thr Arg Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Ser Tyr Phe Tyr Gly Ser Ser Ser Trp
115 120 125
Tyr Phe Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala
165 170 175
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val
180 185 190
Ser Ser Met His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro
195 200 205
Leu Ile Phe Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Glu Tyr Thr Leu Thr Ile Ser Ser Leu
225 230 235 240
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Trp Ile Phe Asn
245 250 255
Pro Pro Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1164
<211> 1476
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1164
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtcc aactcgtcca gtcaggagca gaagtcaaga aacctggagc ttccgtgaaa
120
gtgtcgtgca aggcctccgg ctacaccttc acctcttaca acatgcactg ggtcagacag
180
gcccctggtc aaggactgga atggatggga gcgatctacc cgggcaacgg agacacttcg
240
tacaacccca agttcaaggg acgggtcact atgaccgccg ataagagcac gcgcaccgcg
300
tacatggaac tgagcagcct gcgctccgag gacactgccg tgtattactg cgcgaggagc
360
tacttctacg gatcatcgtc gtggtacttc gacgtctggg gccagggcac caccgtgacc
420
gtgtcatccg gtggcggagg atcggggggc ggaggaagcg gcgggggggg ctccggcggt
480
ggaggctcgg atattcagct gacccagagc ccgtcattcc tgtccgcctc cgtgggagac
540
agagtgacca tcacttgtcg ggccagctcc tcggtgtcct ccatgcattg gtatcagcag
600
aagcctggga aggctcccaa gcccctcatc ttcgccacat caaatcttgc ctccggggtg
660
ccaagccggt tctccgggag cggctccggt actgagtaca ctctgaccat ttcctccttg
720
caacccgagg actttgccac ctactactgc cagcagtgga tctttaaccc gccgaccttc
780
ggaggaggaa ccaaagtgga gatcaagacc actaccccag caccgaggcc acccaccccg
840
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
900
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
960
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1020
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1080
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1140
cgcgtgaaat tcagccgcag cgcagatgct ccagcctacc agcaggggca gaaccagctc
1200
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
1260
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
1320
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
1380
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
1440
tatgacgctc ttcacatgca ggccctgccg cctcgg
1476
<210> 1165
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1165
Ser Tyr Asn Met His
1. 5
<210> 1166
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1166
Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Asn Pro Lys Phe Lys
1. 5 10 15
Gly
<210> 1167
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1167
Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val
1. 5 10
<210> 1168
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1168
Gly Tyr Thr Phe Thr Ser Tyr
1. 5
<210> 1169
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1169
Tyr Pro Gly Asn Gly Asp
1. 5
<210> 1170
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1170
Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val
1. 5 10
<210> 1171
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1171
Gly Tyr Thr Phe Thr Ser Tyr Asn
1. 5
<210> 1172
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1172
Ile Tyr Pro Gly Asn Gly Asp Thr
1. 5
<210> 1173
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1173
Ala Arg Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val
1. 5 10 15
<210> 1174
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1174
Gly Tyr Thr Phe Thr Ser Tyr Asn Met His
1. 5 10
<210> 1175
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1175
Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Asn Pro Lys Phe Lys
1. 5 10 15
Gly
<210> 1176
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1176
Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val
1. 5 10
<210> 1177
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1177
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Asn Pro Lys Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Arg Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 1178
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1178
caagtgcaac tcgtccagtc cggtgcagaa gtcaagaagc ctggttcatc ggtgaaagtg
60
tcctgcaaag cgtcgggcta caccttcacc tcgtacaaca tgcactgggt ccgccaggcc
120
cccggacaag gactggaatg gatgggtgct atctaccccg gaaacggaga taccagctac
180
aaccccaagt tcaagggacg cgtgaccatt actgccgaca agtccacaag aaccgcctac
240
atggaactgt ccagcctgag atccgaggac actgcggtgt actactgtgc gaggtcctac
300
ttctacgggt cctcctcttg gtacttcgac gtctggggac agggcactac tgtgaccgtg
360
tccagc
366
<210> 1179
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1179
Arg Ala Ser Ser Ser Val Ser Ser Met His
1. 5 10
<210> 1180
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1180
Ala Thr Ser Asn Leu Ala Ser
1. 5
<210> 1181
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1181
Gln Gln Trp Ile Phe Asn Pro Pro Thr
1. 5
<210> 1182
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1182
Ser Ser Ser Val Ser Ser
1. 5
<210> 1183
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1183
Ala Thr Ser
1
<210> 1184
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1184
Trp Ile Phe Asn Pro Pro
1. 5
<210> 1185
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1185
Ser Ser Val Ser Ser
1. 5
<210> 1186
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1186
Ala Thr Ser
1
<210> 1187
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1187
Gln Gln Trp Ile Phe Asn Pro Pro Thr
1. 5
<210> 1188
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1188
Arg Ala Ser Ser Ser Val Ser Ser Met His
1. 5 10
<210> 1189
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1189
Ala Thr Ser Asn Leu Ala Ser
1. 5
<210> 1190
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1190
Gln Gln Trp Ile Phe Asn Pro Pro Thr
1. 5
<210> 1191
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1191
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1. 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Ser Ser Val Ser Ser Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Pro Leu Ile Phe
35 40 45
Ala Thr Ser Asn Leu Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu
65 70 75 80
Asp Ala Ala Val Tyr Tyr Cys Gln Gln Trp Ile Phe Asn Pro Pro Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 1192
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1192
gagatcgtgc tgacgcagtc gccggccacc ctgagccttt caccgggaga acgcgccact
60
ctgtcatgcc gggccagcag ctccgtgtcc tccatgcatt ggtaccagca gaagccgggg
120
caggccccgc ggcctctcat cttcgccacc tccaatctgg cctccggcat ccctgctcgg
180
tttagcggaa gcggcagcgg aactgactat accttgacca tctcctcgct ggaaccagag
240
gatgcagccg tgtactattg ccagcagtgg atcttcaacc cgccaacctt cggcggcggc
300
accaaggtcg agattaag
318
<210> 1193
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1193
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1. 5 10 15
Gly Gly Gly Ser
20
<210> 1194
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1194
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Asn Pro Lys Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Arg Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile
130 135 140
Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg
145 150 155 160
Ala Thr Leu Ser Cys Arg Ala Ser Ser Ser Val Ser Ser Met His Trp
165 170 175
Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Pro Leu Ile Phe Ala Thr
180 185 190
Ser Asn Leu Ala Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser
195 200 205
Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp Ala
210 215 220
Ala Val Tyr Tyr Cys Gln Gln Trp Ile Phe Asn Pro Pro Thr Phe Gly
225 230 235 240
Gly Gly Thr Lys Val Glu Ile Lys
245
<210> 1195
<211> 744
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1195
caagtgcaac tcgtccagtc cggtgcagaa gtcaagaagc ctggttcatc ggtgaaagtg
60
tcctgcaaag cgtcgggcta caccttcacc tcgtacaaca tgcactgggt ccgccaggcc
120
cccggacaag gactggaatg gatgggtgct atctaccccg gaaacggaga taccagctac
180
aaccccaagt tcaagggacg cgtgaccatt actgccgaca agtccacaag aaccgcctac
240
atggaactgt ccagcctgag atccgaggac actgcggtgt actactgtgc gaggtcctac
300
ttctacgggt cctcctcttg gtacttcgac gtctggggac agggcactac tgtgaccgtg
360
tccagcgggg gaggcggtag cggggggggt ggatcgggcg gcggcggatc aggaggagga
420
gggtccgaga tcgtgctgac gcagtcgccg gccaccctga gcctttcacc gggagaacgc
480
gccactctgt catgccgggc cagcagctcc gtgtcctcca tgcattggta ccagcagaag
540
ccggggcagg ccccgcggcc tctcatcttc gccacctcca atctggcctc cggcatccct
600
gctcggttta gcggaagcgg cagcggaact gactatacct tgaccatctc ctcgctggaa
660
ccagaggatg cagccgtgta ctattgccag cagtggatct tcaacccgcc aaccttcggc
720
ggcggcacca aggtcgagat taag
744
<210> 1196
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1196
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Asn Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser
65 70 75 80
Tyr Asn Pro Lys Phe Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser
85 90 95
Thr Arg Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Ser Tyr Phe Tyr Gly Ser Ser Ser Trp
115 120 125
Tyr Phe Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu
165 170 175
Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Ser Ser Val
180 185 190
Ser Ser Met His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Pro
195 200 205
Leu Ile Phe Ala Thr Ser Asn Leu Ala Ser Gly Ile Pro Ala Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu
225 230 235 240
Glu Pro Glu Asp Ala Ala Val Tyr Tyr Cys Gln Gln Trp Ile Phe Asn
245 250 255
Pro Pro Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1197
<211> 1476
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1197
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc aactcgtcca gtccggtgca gaagtcaaga agcctggttc atcggtgaaa
120
gtgtcctgca aagcgtcggg ctacaccttc acctcgtaca acatgcactg ggtccgccag
180
gcccccggac aaggactgga atggatgggt gctatctacc ccggaaacgg agataccagc
240
tacaacccca agttcaaggg acgcgtgacc attactgccg acaagtccac aagaaccgcc
300
tacatggaac tgtccagcct gagatccgag gacactgcgg tgtactactg tgcgaggtcc
360
tacttctacg ggtcctcctc ttggtacttc gacgtctggg gacagggcac tactgtgacc
420
gtgtccagcg ggggaggcgg tagcgggggg ggtggatcgg gcggcggcgg atcaggagga
480
ggagggtccg agatcgtgct gacgcagtcg ccggccaccc tgagcctttc accgggagaa
540
cgcgccactc tgtcatgccg ggccagcagc tccgtgtcct ccatgcattg gtaccagcag
600
aagccggggc aggccccgcg gcctctcatc ttcgccacct ccaatctggc ctccggcatc
660
cctgctcggt ttagcggaag cggcagcgga actgactata ccttgaccat ctcctcgctg
720
gaaccagagg atgcagccgt gtactattgc cagcagtgga tcttcaaccc gccaaccttc
780
ggcggcggca ccaaggtcga gattaagacc actaccccag caccgaggcc acccaccccg
840
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
900
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
960
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1020
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1080
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1140
cgcgtgaaat tcagccgcag cgcagatgct ccagcctacc agcaggggca gaaccagctc
1200
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
1260
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
1320
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
1380
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
1440
tatgacgctc ttcacatgca ggccctgccg cctcgg
1476
<210> 1198
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1198
Ser Tyr Asn Met His
1. 5
<210> 1199
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1199
Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Asn Pro Lys Phe Lys
1. 5 10 15
Gly
<210> 1200
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1200
Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val
1. 5 10
<210> 1201
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1201
Gly Tyr Thr Phe Thr Ser Tyr
1. 5
<210> 1202
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1202
Tyr Pro Gly Asn Gly Asp
1. 5
<210> 1203
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1203
Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val
1. 5 10
<210> 1204
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1204
Gly Tyr Thr Phe Thr Ser Tyr Asn
1. 5
<210> 1205
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1205
Ile Tyr Pro Gly Asn Gly Asp Thr
1. 5
<210> 1206
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1206
Ala Arg Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val
1. 5 10 15
<210> 1207
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1207
Gly Tyr Thr Phe Thr Ser Tyr Asn Met His
1. 5 10
<210> 1208
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1208
Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Asn Pro Lys Phe Lys
1. 5 10 15
Gly
<210> 1209
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1209
Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val
1. 5 10
<210> 1210
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1210
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Asn Pro Lys Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Arg Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 1211
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1211
caagtgcaac tcgtccagtc cggtgcagaa gtcaagaagc caggttcctc ggtgaaagtg
60
tcctgcaaag cctcgggtta caccttcacc tcgtacaata tgcactgggt ccgccaagct
120
ccgggacaag gcctggaatg gatgggagcg atctaccccg gaaacggcga cacgtcctac
180
aacccgaagt tcaagggaag agtgaccatc accgccgaca agtccacccg caccgcgtac
240
atggagctta gcagcctgcg gagcgaggac actgccgtgt attactgcgc ccggtcctac
300
ttctatggat catcctcgtg gtacttcgat gtctggggcc aggggaccac cgtgaccgtg
360
tccagc
366
<210> 1212
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1212
Arg Ala Ser Ser Ser Val Ser Ser Met His
1. 5 10
<210> 1213
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1213
Ala Thr Ser Asn Leu Ala Ser
1. 5
<210> 1214
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1214
Gln Gln Trp Ile Phe Asn Pro Pro Thr
1. 5
<210> 1215
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1215
Ser Ser Ser Val Ser Ser
1. 5
<210> 1216
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1216
Ala Thr Ser
1
<210> 1217
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1217
Trp Ile Phe Asn Pro Pro
1. 5
<210> 1218
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1218
Ser Ser Val Ser Ser
1. 5
<210> 1219
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1219
Ala Thr Ser
1
<210> 1220
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1220
Gln Gln Trp Ile Phe Asn Pro Pro Thr
1. 5
<210> 1221
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1221
Arg Ala Ser Ser Ser Val Ser Ser Met His
1. 5 10
<210> 1222
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1222
Ala Thr Ser Asn Leu Ala Ser
1. 5
<210> 1223
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1223
Gln Gln Trp Ile Phe Asn Pro Pro Thr
1. 5
<210> 1224
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1224
Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly
1. 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro Leu Ile Phe
35 40 45
Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Glu Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
65 70 75 80
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Trp Ile Phe Asn Pro Pro Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 1225
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1225
gatatccagc tgacccagag cccttccttc ctgtccgctt ccgtgggaga cagagtcact
60
attacttgtc gggcctcctc atccgtgtca tccatgcact ggtaccagca gaagccggga
120
aaggccccaa agcccttgat ctttgccact tccaacctgg catccggcgt gccctcgagg
180
ttctccggga gcggttcagg gaccgagtac actctgacca ttagcagcct ccagcctgag
240
gactttgcca cctactactg ccagcagtgg attttcaacc cgcctacatt cggagggggc
300
actaaggtcg aaatcaag
318
<210> 1226
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1226
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1. 5 10 15
Gly Gly Gly Ser
20
<210> 1227
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1227
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Asn Pro Lys Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Arg Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly Asp Arg
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Met His Trp
165 170 175
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro Leu Ile Phe Ala Thr
180 185 190
Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
195 200 205
Gly Thr Glu Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
210 215 220
Ala Thr Tyr Tyr Cys Gln Gln Trp Ile Phe Asn Pro Pro Thr Phe Gly
225 230 235 240
Gly Gly Thr Lys Val Glu Ile Lys
245
<210> 1228
<211> 744
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1228
caagtgcaac tcgtccagtc cggtgcagaa gtcaagaagc caggttcctc ggtgaaagtg
60
tcctgcaaag cctcgggtta caccttcacc tcgtacaata tgcactgggt ccgccaagct
120
ccgggacaag gcctggaatg gatgggagcg atctaccccg gaaacggcga cacgtcctac
180
aacccgaagt tcaagggaag agtgaccatc accgccgaca agtccacccg caccgcgtac
240
atggagctta gcagcctgcg gagcgaggac actgccgtgt attactgcgc ccggtcctac
300
ttctatggat catcctcgtg gtacttcgat gtctggggcc aggggaccac cgtgaccgtg
360
tccagcggtg gcggaggcag cggcggagga gggtctggag gaggcggctc ggggggaggg
420
ggctcggata tccagctgac ccagagccct tccttcctgt ccgcttccgt gggagacaga
480
gtcactatta cttgtcgggc ctcctcatcc gtgtcatcca tgcactggta ccagcagaag
540
ccgggaaagg ccccaaagcc cttgatcttt gccacttcca acctggcatc cggcgtgccc
600
tcgaggttct ccgggagcgg ttcagggacc gagtacactc tgaccattag cagcctccag
660
cctgaggact ttgccaccta ctactgccag cagtggattt tcaacccgcc tacattcgga
720
gggggcacta aggtcgaaat caag
744
<210> 1229
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1229
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Asn Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser
65 70 75 80
Tyr Asn Pro Lys Phe Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser
85 90 95
Thr Arg Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Ser Tyr Phe Tyr Gly Ser Ser Ser Trp
115 120 125
Tyr Phe Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala
165 170 175
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val
180 185 190
Ser Ser Met His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro
195 200 205
Leu Ile Phe Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Glu Tyr Thr Leu Thr Ile Ser Ser Leu
225 230 235 240
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Trp Ile Phe Asn
245 250 255
Pro Pro Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1230
<211> 1476
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1230
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc aactcgtcca gtccggtgca gaagtcaaga agccaggttc ctcggtgaaa
120
gtgtcctgca aagcctcggg ttacaccttc acctcgtaca atatgcactg ggtccgccaa
180
gctccgggac aaggcctgga atggatggga gcgatctacc ccggaaacgg cgacacgtcc
240
tacaacccga agttcaaggg aagagtgacc atcaccgccg acaagtccac ccgcaccgcg
300
tacatggagc ttagcagcct gcggagcgag gacactgccg tgtattactg cgcccggtcc
360
tacttctatg gatcatcctc gtggtacttc gatgtctggg gccaggggac caccgtgacc
420
gtgtccagcg gtggcggagg cagcggcgga ggagggtctg gaggaggcgg ctcgggggga
480
gggggctcgg atatccagct gacccagagc ccttccttcc tgtccgcttc cgtgggagac
540
agagtcacta ttacttgtcg ggcctcctca tccgtgtcat ccatgcactg gtaccagcag
600
aagccgggaa aggccccaaa gcccttgatc tttgccactt ccaacctggc atccggcgtg
660
ccctcgaggt tctccgggag cggttcaggg accgagtaca ctctgaccat tagcagcctc
720
cagcctgagg actttgccac ctactactgc cagcagtgga ttttcaaccc gcctacattc
780
ggagggggca ctaaggtcga aatcaagacc actaccccag caccgaggcc acccaccccg
840
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
900
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
960
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1020
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1080
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1140
cgcgtgaaat tcagccgcag cgcagatgct ccagcctacc agcaggggca gaaccagctc
1200
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
1260
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
1320
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
1380
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
1440
tatgacgctc ttcacatgca ggccctgccg cctcgg
1476
<210> 1231
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1231
Arg Tyr Asn Met His
1. 5
<210> 1232
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1232
Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Ser Gln Lys Phe Lys
1. 5 10 15
Gly
<210> 1233
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1233
Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val
1. 5 10
<210> 1234
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1234
Gly Tyr Thr Phe Thr Arg Tyr
1. 5
<210> 1235
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1235
Tyr Pro Gly Asn Gly Asp
1. 5
<210> 1236
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1236
Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val
1. 5 10
<210> 1237
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1237
Gly Tyr Thr Phe Thr Arg Tyr Asn
1. 5
<210> 1238
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1238
Ile Tyr Pro Gly Asn Gly Asp Thr
1. 5
<210> 1239
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1239
Ala Arg Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val
1. 5 10 15
<210> 1240
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1240
Gly Tyr Thr Phe Thr Arg Tyr Asn Met His
1. 5 10
<210> 1241
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1241
Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Ser Gln Lys Phe Lys
1. 5 10 15
Gly
<210> 1242
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1242
Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val
1. 5 10
<210> 1243
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1243
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 1244
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1244
caagtccaac tcgtccagtc aggagcagaa gtcaagaaac caggagcatc cgtgaaagtg
60
tcgtgcaaag cctctggcta caccttcacc cggtacaaca tgcactgggt cagacaggcc
120
ccgggacagc ggctcgagtg gatgggtgcc atctaccccg gcaacgggga cacctcctac
180
tcccaaaagt tcaagggtcg cgtgaccatc acggcggata agtcggccag cactgcgtac
240
atggaattgt catccctgcg ctccgaggat accgccgtgt attactgcgc gcggtccttc
300
ttctacggct cctccgattg gtacttcgac gtctggggac agggaactac cgtgaccgtg
360
tcctcc
366
<210> 1245
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1245
Arg Ala Ser Ser Ser Val Asn Asn Met His
1. 5 10
<210> 1246
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1246
Ala Thr Ser Asn Leu Ala Ser
1. 5
<210> 1247
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1247
Gln Gln Trp Ile Phe Asn Pro Pro Thr
1. 5
<210> 1248
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1248
Ser Ser Ser Val Asn Asn
1. 5
<210> 1249
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1249
Ala Thr Ser
1
<210> 1250
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1250
Trp Ile Phe Asn Pro Pro
1. 5
<210> 1251
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1251
Ser Ser Val Asn Asn
1. 5
<210> 1252
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1252
Ala Thr Ser
1
<210> 1253
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1253
Gln Gln Trp Ile Phe Asn Pro Pro Thr
1. 5
<210> 1254
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1254
Arg Ala Ser Ser Ser Val Asn Asn Met His
1. 5 10
<210> 1255
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1255
Ala Thr Ser Asn Leu Ala Ser
1. 5
<210> 1256
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1256
Gln Gln Trp Ile Phe Asn Pro Pro Thr
1. 5
<210> 1257
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1257
Glu Ile Val Leu Thr Gln Ser Pro Asp Phe Gln Ser Val Thr Pro Lys
1. 5 10 15
Glu Lys Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Asn Asn Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Asp Gln Ser Pro Lys Pro Leu Ile Tyr
35 40 45
Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Asn Ser Leu Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ile Phe Asn Pro Pro Thr
85 90 95
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1258
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1258
gaaatcgtgc tgactcagtc gccggacttc caaagcgtga ccccaaagga gaaggtcacc
60
atcacctgta gagcctcatc gtccgtgaac aatatgcact ggtaccagca gaagccggac
120
cagtccccta agcccctgat ctacgccact tccaacctgg cctccggcgt gccgtcgagg
180
ttcagcggct cgggcagcgg gaccgactac accctgacca tcaacagcct tgaagctgag
240
gacgccgcta cctactactg ccagcagtgg attttcaacc ctcccacatt tggacagggc
300
actaagctgg agattaag
318
<210> 1259
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1259
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1. 5 10 15
Gly Gly Gly Ser
20
<210> 1260
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1260
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile
130 135 140
Val Leu Thr Gln Ser Pro Asp Phe Gln Ser Val Thr Pro Lys Glu Lys
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Asn Asn Met His Trp
165 170 175
Tyr Gln Gln Lys Pro Asp Gln Ser Pro Lys Pro Leu Ile Tyr Ala Thr
180 185 190
Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
195 200 205
Gly Thr Asp Tyr Thr Leu Thr Ile Asn Ser Leu Glu Ala Glu Asp Ala
210 215 220
Ala Thr Tyr Tyr Cys Gln Gln Trp Ile Phe Asn Pro Pro Thr Phe Gly
225 230 235 240
Gln Gly Thr Lys Leu Glu Ile Lys
245
<210> 1261
<211> 744
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1261
caagtccaac tcgtccagtc aggagcagaa gtcaagaaac caggagcatc cgtgaaagtg
60
tcgtgcaaag cctctggcta caccttcacc cggtacaaca tgcactgggt cagacaggcc
120
ccgggacagc ggctcgagtg gatgggtgcc atctaccccg gcaacgggga cacctcctac
180
tcccaaaagt tcaagggtcg cgtgaccatc acggcggata agtcggccag cactgcgtac
240
atggaattgt catccctgcg ctccgaggat accgccgtgt attactgcgc gcggtccttc
300
ttctacggct cctccgattg gtacttcgac gtctggggac agggaactac cgtgaccgtg
360
tcctccgggg gtggcgggag cggagggggc ggaagcgggg gtggaggatc aggaggcgga
420
ggctccgaaa tcgtgctgac tcagtcgccg gacttccaaa gcgtgacccc aaaggagaag
480
gtcaccatca cctgtagagc ctcatcgtcc gtgaacaata tgcactggta ccagcagaag
540
ccggaccagt cccctaagcc cctgatctac gccacttcca acctggcctc cggcgtgccg
600
tcgaggttca gcggctcggg cagcgggacc gactacaccc tgaccatcaa cagccttgaa
660
gctgaggacg ccgctaccta ctactgccag cagtggattt tcaaccctcc cacatttgga
720
cagggcacta agctggagat taag
744
<210> 1262
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1262
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1. 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Arg Tyr Asn Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Arg Leu Glu Trp Met Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser
65 70 75 80
Tyr Ser Gln Lys Phe Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser
85 90 95
Ala Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Ser Phe Phe Tyr Gly Ser Ser Asp Trp
115 120 125
Tyr Phe Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Asp Phe Gln Ser Val
165 170 175
Thr Pro Lys Glu Lys Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val
180 185 190
Asn Asn Met His Trp Tyr Gln Gln Lys Pro Asp Gln Ser Pro Lys Pro
195 200 205
Leu Ile Tyr Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Asn Ser Leu
225 230 235 240
Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ile Phe Asn
245 250 255
Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1263
<211> 1476
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1263
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtcc aactcgtcca gtcaggagca gaagtcaaga aaccaggagc atccgtgaaa
120
gtgtcgtgca aagcctctgg ctacaccttc acccggtaca acatgcactg ggtcagacag
180
gccccgggac agcggctcga gtggatgggt gccatctacc ccggcaacgg ggacacctcc
240
tactcccaaa agttcaaggg tcgcgtgacc atcacggcgg ataagtcggc cagcactgcg
300
tacatggaat tgtcatccct gcgctccgag gataccgccg tgtattactg cgcgcggtcc
360
ttcttctacg gctcctccga ttggtacttc gacgtctggg gacagggaac taccgtgacc
420
gtgtcctccg ggggtggcgg gagcggaggg ggcggaagcg ggggtggagg atcaggaggc
480
ggaggctccg aaatcgtgct gactcagtcg ccggacttcc aaagcgtgac cccaaaggag
540
aaggtcacca tcacctgtag agcctcatcg tccgtgaaca atatgcactg gtaccagcag
600
aagccggacc agtcccctaa gcccctgatc tacgccactt ccaacctggc ctccggcgtg
660
ccgtcgaggt tcagcggctc gggcagcggg accgactaca ccctgaccat caacagcctt
720
gaagctgagg acgccgctac ctactactgc cagcagtgga ttttcaaccc tcccacattt
780
ggacagggca ctaagctgga gattaagacc actaccccag caccgaggcc acccaccccg
840
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
900
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
960
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1020
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1080
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1140
cgcgtgaaat tcagccgcag cgcagatgct ccagcctacc agcaggggca gaaccagctc
1200
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
1260
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
1320
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
1380
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
1440
tatgacgctc ttcacatgca ggccctgccg cctcgg
1476
<210> 1264
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1264
Arg Tyr Asn Met His
1. 5
<210> 1265
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1265
Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Ser Gln Lys Phe Lys
1. 5 10 15
Gly
<210> 1266
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1266
Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val
1. 5 10
<210> 1267
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1267
Gly Tyr Thr Phe Thr Arg Tyr
1. 5
<210> 1268
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1268
Tyr Pro Gly Asn Gly Asp
1. 5
<210> 1269
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1269
Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val
1. 5 10
<210> 1270
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1270
Gly Tyr Thr Phe Thr Arg Tyr Asn
1. 5
<210> 1271
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1271
Ile Tyr Pro Gly Asn Gly Asp Thr
1. 5
<210> 1272
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1272
Ala Arg Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val
1. 5 10 15
<210> 1273
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1273
Gly Tyr Thr Phe Thr Arg Tyr Asn Met His
1. 5 10
<210> 1274
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1274
Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Ser Gln Lys Phe Lys
1. 5 10 15
Gly
<210> 1275
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1275
Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val
1. 5 10
<210> 1276
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1276
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1. 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 1277
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1277
caagtgcaac tcgtccaatc cggcgcggaa gtcaaaaagc ctggagcctc cgtcaaagtg
60
tcctgcaagg cctccggtta cactttcact cgctacaaca tgcattgggt gcggcaggcc
120
ccgggacagc gcctggaatg gatgggcgca atctaccccg gcaacggaga cacctcctat
180
tcccaaaagt tcaagggaag ggtcacaatc acggccgaca agagcgcctc aactgcctac
240
atggagctga gcagcctcag atccgaagat accgcggtgt actactgcgc ccggagcttc
300
ttctacggtt cgtctgattg gtactttgac gtctggggcc agggaaccac cgtgaccgtg
360
tcgtcc
366
<210> 1278
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1278
Arg Ala Ser Ser Ser Val Asn Asn Met His
1. 5 10
<210> 1279
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1279
Ala Thr Ser Asn Leu Ala Ser
1. 5
<210> 1280
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1280
Gln Gln Trp Ile Phe Asn Pro Pro Thr
1. 5
<210> 1281
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1281
Ser Ser Ser Val Asn Asn
1. 5
<210> 1282
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1282
Ala Thr Ser
1
<210> 1283
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1283
Trp Ile Phe Asn Pro Pro
5
<210> 1284
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1284
Ser Ser Val Asn Asn
5
<210> 1285
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1285
Ala Thr Ser
1
<210> 1286
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1286
Gln Gln Trp Ile Phe Asn Pro Pro Thr
5
<210> 1287
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1287
Arg Ala Ser Ser Ser Val Asn Asn Met His
5 10
<210> 1288
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1288
Ala Thr Ser Asn Leu Ala Ser
5
<210> 1289
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1289
Gln Gln Trp Ile Phe Asn Pro Pro Thr
5
<210> 1290
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1290
Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly
5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Asn Asn Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro Leu Ile Tyr
35 40 45
Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Glu Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
65 70 75 80
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Trp Ile Phe Asn Pro Pro Thr
85 90 95
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1291
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1291
gacatccagc ttacccagtc gccatcattc ctgtccgcat cagtgggtga tcgcgtgacc
60
attacctgtc gggcgtcctc ctccgtgaac aacatgcact ggtaccagca gaagccgggg
120
aaggctccca agcctctgat ctacgccact agcaatttgg ccagcggcgt gccttcgaga
180
ttctcggggt cgggctcagg aaccgagtat accctgacca tttcctccct ccaaccggag
240
gactttgcta cttactactg ccagcagtgg attttcaacc ccccgacttt cggacagggc
300
accaagctgg aaatcaag
318
<210> 1292
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1292
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
5 10 15
Gly Gly Gly Ser
20
<210> 1293
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1293
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly Asp Arg
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Asn Asn Met His Trp
165 170 175
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro Leu Ile Tyr Ala Thr
180 185 190
Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
195 200 205
Gly Thr Glu Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
210 215 220
Ala Thr Tyr Tyr Cys Gln Gln Trp Ile Phe Asn Pro Pro Thr Phe Gly
225 230 235 240
Gln Gly Thr Lys Leu Glu Ile Lys
245
<210> 1294
<211> 744
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1294
caagtgcaac tcgtccaatc cggcgcggaa gtcaaaaagc ctggagcctc cgtcaaagtg
60
tcctgcaagg cctccggtta cactttcact cgctacaaca tgcattgggt gcggcaggcc
120
ccgggacagc gcctggaatg gatgggcgca atctaccccg gcaacggaga cacctcctat
180
tcccaaaagt tcaagggaag ggtcacaatc acggccgaca agagcgcctc aactgcctac
240
atggagctga gcagcctcag atccgaagat accgcggtgt actactgcgc ccggagcttc
300
ttctacggtt cgtctgattg gtactttgac gtctggggcc agggaaccac cgtgaccgtg
360
tcgtccggtg gcggagggag cggtggagga ggctccgggg gaggaggcag cggcggggga
420
ggcagcgaca tccagcttac ccagtcgcca tcattcctgt ccgcatcagt gggtgatcgc
480
gtgaccatta cctgtcgggc gtcctcctcc gtgaacaaca tgcactggta ccagcagaag
540
ccggggaagg ctcccaagcc tctgatctac gccactagca atttggccag cggcgtgcct
600
tcgagattct cggggtcggg ctcaggaacc gagtataccc tgaccatttc ctccctccaa
660
ccggaggact ttgctactta ctactgccag cagtggattt tcaacccccc gactttcgga
720
cagggcacca agctggaaat caag
744
<210> 1295
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1295
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Arg Tyr Asn Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Arg Leu Glu Trp Met Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser
65 70 75 80
Tyr Ser Gln Lys Phe Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser
85 90 95
Ala Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Ser Phe Phe Tyr Gly Ser Ser Asp Trp
115 120 125
Tyr Phe Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala
165 170 175
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val
180 185 190
Asn Asn Met His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro
195 200 205
Leu Ile Tyr Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Glu Tyr Thr Leu Thr Ile Ser Ser Leu
225 230 235 240
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Trp Ile Phe Asn
245 250 255
Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1296
<211> 1476
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1296
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc aactcgtcca atccggcgcg gaagtcaaaa agcctggagc ctccgtcaaa
120
gtgtcctgca aggcctccgg ttacactttc actcgctaca acatgcattg ggtgcggcag
180
gccccgggac agcgcctgga atggatgggc gcaatctacc ccggcaacgg agacacctcc
240
tattcccaaa agttcaaggg aagggtcaca atcacggccg acaagagcgc ctcaactgcc
300
tacatggagc tgagcagcct cagatccgaa gataccgcgg tgtactactg cgcccggagc
360
ttcttctacg gttcgtctga ttggtacttt gacgtctggg gccagggaac caccgtgacc
420
gtgtcgtccg gtggcggagg gagcggtgga ggaggctccg ggggaggagg cagcggcggg
480
ggaggcagcg acatccagct tacccagtcg ccatcattcc tgtccgcatc agtgggtgat
540
cgcgtgacca ttacctgtcg ggcgtcctcc tccgtgaaca acatgcactg gtaccagcag
600
aagccgggga aggctcccaa gcctctgatc tacgccacta gcaatttggc cagcggcgtg
660
ccttcgagat tctcggggtc gggctcagga accgagtata ccctgaccat ttcctccctc
720
caaccggagg actttgctac ttactactgc cagcagtgga ttttcaaccc cccgactttc
780
ggacagggca ccaagctgga aatcaagacc actaccccag caccgaggcc acccaccccg
840
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
900
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
960
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1020
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1080
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1140
cgcgtgaaat tcagccgcag cgcagatgct ccagcctacc agcaggggca gaaccagctc
1200
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
1260
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
1320
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
1380
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
1440
tatgacgctc ttcacatgca ggccctgccg cctcgg
1476
<210> 1297
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1297
Arg Tyr Asn Met His
5
<210> 1298
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1298
Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Ser Gln Lys Phe Lys
5 10 15
Gly
<210> 1299
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1299
Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val
5 10
<210> 1300
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1300
Gly Tyr Thr Phe Thr Arg Tyr
5
<210> 1301
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1301
Tyr Pro Gly Asn Gly Asp
5
<210> 1302
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1302
Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val
5 10
<210> 1303
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1303
Gly Tyr Thr Phe Thr Arg Tyr Asn
5
<210> 1304
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1304
Ile Tyr Pro Gly Asn Gly Asp Thr
5
<210> 1305
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1305
Ala Arg Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val
5 10 15
<210> 1306
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1306
Gly Tyr Thr Phe Thr Arg Tyr Asn Met His
5 10
<210> 1307
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1307
Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Ser Gln Lys Phe Lys
5 10 15
Gly
<210> 1308
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1308
Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val
5 10
<210> 1309
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1309
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 1310
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1310
caagtgcaac tcgtccagtc cggtgcagaa gtcaagaagc ctggttcctc cgtgaaagtg
60
tcctgcaaag cgtctggcta caccttcacc cggtacaata tgcactgggt cagacaggcg
120
cccggacagg gcctggagtg gatgggggcc atctaccctg ggaacggcga cactagctac
180
tcccaaaagt tcaagggccg cgtgacgatt accgccgaca agtcaaccag cactgcctat
240
atggagctga gctcgcttcg gagcgaagat accgccgtgt actactgcgc tcggagcttc
300
ttctacgggt cctcggattg gtacttcgac gtctggggcc aggggactac tgtgaccgtg
360
tcctcc
366
<210> 1311
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1311
Arg Ala Ser Ser Ser Val Asn Asn Met His
5 10
<210> 1312
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1312
Ala Thr Ser Asn Leu Ala Ser
5
<210> 1313
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1313
Gln Gln Trp Ile Phe Asn Pro Pro Thr
5
<210> 1314
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1314
Ser Ser Ser Val Asn Asn
5
<210> 1315
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1315
Ala Thr Ser
1
<210> 1316
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1316
Trp Ile Phe Asn Pro Pro
5
<210> 1317
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1317
Ser Ser Val Asn Asn
5
<210> 1318
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1318
Ala Thr Ser
1
<210> 1319
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1319
Gln Gln Trp Ile Phe Asn Pro Pro Thr
5
<210> 1320
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1320
Arg Ala Ser Ser Ser Val Asn Asn Met His
5 10
<210> 1321
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1321
Ala Thr Ser Asn Leu Ala Ser
5
<210> 1322
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1322
Gln Gln Trp Ile Phe Asn Pro Pro Thr
5
<210> 1323
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1323
Glu Ile Val Leu Thr Gln Ser Pro Asp Phe Gln Ser Val Thr Pro Lys
5 10 15
Glu Lys Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Asn Asn Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Asp Gln Ser Pro Lys Pro Leu Ile Tyr
35 40 45
Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Asn Ser Leu Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ile Phe Asn Pro Pro Thr
85 90 95
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1324
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1324
gaaatcgtgc tgacccagtc cccggacttt cagtcagtga ctcccaagga gaaggtcacc
60
attacttgtc gcgcctcctc ctcggtgaac aacatgcact ggtaccagca gaagccggac
120
cagtccccga agcccctgat ctatgctacc tccaacttgg cgtccggcgt gccgtcaagg
180
ttcagcggat cgggttccgg gacagactac accctgacta ttaactcact cgaggccgag
240
gatgccgcca cctactactg ccagcagtgg atcttcaacc ctccaacctt cggacaagga
300
accaagctgg aaatcaag
318
<210> 1325
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1325
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
5 10 15
Gly Gly Gly Ser
20
<210> 1326
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1326
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile
130 135 140
Val Leu Thr Gln Ser Pro Asp Phe Gln Ser Val Thr Pro Lys Glu Lys
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Asn Asn Met His Trp
165 170 175
Tyr Gln Gln Lys Pro Asp Gln Ser Pro Lys Pro Leu Ile Tyr Ala Thr
180 185 190
Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
195 200 205
Gly Thr Asp Tyr Thr Leu Thr Ile Asn Ser Leu Glu Ala Glu Asp Ala
210 215 220
Ala Thr Tyr Tyr Cys Gln Gln Trp Ile Phe Asn Pro Pro Thr Phe Gly
225 230 235 240
Gln Gly Thr Lys Leu Glu Ile Lys
245
<210> 1327
<211> 744
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1327
caagtgcaac tcgtccagtc cggtgcagaa gtcaagaagc ctggttcctc cgtgaaagtg
60
tcctgcaaag cgtctggcta caccttcacc cggtacaata tgcactgggt cagacaggcg
120
cccggacagg gcctggagtg gatgggggcc atctaccctg ggaacggcga cactagctac
180
tcccaaaagt tcaagggccg cgtgacgatt accgccgaca agtcaaccag cactgcctat
240
atggagctga gctcgcttcg gagcgaagat accgccgtgt actactgcgc tcggagcttc
300
ttctacgggt cctcggattg gtacttcgac gtctggggcc aggggactac tgtgaccgtg
360
tcctccgggg gaggaggatc gggcggaggc ggttcgggag gcggcggaag cggaggcgga
420
ggttcagaaa tcgtgctgac ccagtccccg gactttcagt cagtgactcc caaggagaag
480
gtcaccatta cttgtcgcgc ctcctcctcg gtgaacaaca tgcactggta ccagcagaag
540
ccggaccagt ccccgaagcc cctgatctat gctacctcca acttggcgtc cggcgtgccg
600
tcaaggttca gcggatcggg ttccgggaca gactacaccc tgactattaa ctcactcgag
660
gccgaggatg ccgccaccta ctactgccag cagtggatct tcaaccctcc aaccttcgga
720
caaggaacca agctggaaat caag
744
<210> 1328
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1328
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Arg Tyr Asn Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser
65 70 75 80
Tyr Ser Gln Lys Phe Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Ser Phe Phe Tyr Gly Ser Ser Asp Trp
115 120 125
Tyr Phe Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Asp Phe Gln Ser Val
165 170 175
Thr Pro Lys Glu Lys Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val
180 185 190
Asn Asn Met His Trp Tyr Gln Gln Lys Pro Asp Gln Ser Pro Lys Pro
195 200 205
Leu Ile Tyr Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Asn Ser Leu
225 230 235 240
Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ile Phe Asn
245 250 255
Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1329
<211> 1476
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1329
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc aactcgtcca gtccggtgca gaagtcaaga agcctggttc ctccgtgaaa
120
gtgtcctgca aagcgtctgg ctacaccttc acccggtaca atatgcactg ggtcagacag
180
gcgcccggac agggcctgga gtggatgggg gccatctacc ctgggaacgg cgacactagc
240
tactcccaaa agttcaaggg ccgcgtgacg attaccgccg acaagtcaac cagcactgcc
300
tatatggagc tgagctcgct tcggagcgaa gataccgccg tgtactactg cgctcggagc
360
ttcttctacg ggtcctcgga ttggtacttc gacgtctggg gccaggggac tactgtgacc
420
gtgtcctccg ggggaggagg atcgggcgga ggcggttcgg gaggcggcgg aagcggaggc
480
ggaggttcag aaatcgtgct gacccagtcc ccggactttc agtcagtgac tcccaaggag
540
aaggtcacca ttacttgtcg cgcctcctcc tcggtgaaca acatgcactg gtaccagcag
600
aagccggacc agtccccgaa gcccctgatc tatgctacct ccaacttggc gtccggcgtg
660
ccgtcaaggt tcagcggatc gggttccggg acagactaca ccctgactat taactcactc
720
gaggccgagg atgccgccac ctactactgc cagcagtgga tcttcaaccc tccaaccttc
780
ggacaaggaa ccaagctgga aatcaagacc actaccccag caccgaggcc acccaccccg
840
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
900
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
960
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1020
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1080
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1140
cgcgtgaaat tcagccgcag cgcagatgct ccagcctacc agcaggggca gaaccagctc
1200
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
1260
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
1320
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
1380
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
1440
tatgacgctc ttcacatgca ggccctgccg cctcgg
1476
<210> 1330
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1330
Arg Tyr Asn Met His
5
<210> 1331
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1331
Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Ser Gln Lys Phe Lys
5 10 15
Gly
<210> 1332
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1332
Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val
5 10
<210> 1333
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1333
Gly Tyr Thr Phe Thr Arg Tyr
5
<210> 1334
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1334
Tyr Pro Gly Asn Gly Asp
5
<210> 1335
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1335
Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val
5 10
<210> 1336
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1336
Gly Tyr Thr Phe Thr Arg Tyr Asn
5
<210> 1337
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1337
Ile Tyr Pro Gly Asn Gly Asp Thr
5
<210> 1338
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1338
Ala Arg Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val
5 10 15
<210> 1339
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1339
Gly Tyr Thr Phe Thr Arg Tyr Asn Met His
5 10
<210> 1340
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1340
Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Ser Gln Lys Phe Lys
5 10 15
Gly
<210> 1341
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1341
Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val
5 10
<210> 1342
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1342
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 1343
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1343
caagtccaac tcgtccagtc tggcgcagaa gtcaagaagc ccggaagctc cgtgaaagtg
60
tcctgcaaag cgtcgggtta cactttcacc cggtacaaca tgcactgggt cagacaggcc
120
cctggacaag gactggagtg gatgggtgcc atctaccctg gaaacggaga tacctcctac
180
tcccaaaagt tcaaggggag agtgaccatt accgccgaca agtcaacttc caccgcttac
240
atggagctca gctccctgcg gtccgaagat actgcggtgt actattgcgc tcgctcattt
300
ttctacggct catcggattg gtacttcgac gtctggggac agggaactac cgtgaccgtg
360
tcctcg
366
<210> 1344
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1344
Arg Ala Ser Ser Ser Val Asn Asn Met His
5 10
<210> 1345
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1345
Ala Thr Ser Asn Leu Ala Ser
5
<210> 1346
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1346
Gln Gln Trp Ile Phe Asn Pro Pro Thr
5
<210> 1347
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1347
Ser Ser Ser Val Asn Asn
5
<210> 1348
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1348
Ala Thr Ser
1
<210> 1349
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1349
Trp Ile Phe Asn Pro Pro
5
<210> 1350
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1350
Ser Ser Val Asn Asn
5
<210> 1351
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1351
Ala Thr Ser
1
<210> 1352
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1352
Gln Gln Trp Ile Phe Asn Pro Pro Thr
5
<210> 1353
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1353
Arg Ala Ser Ser Ser Val Asn Asn Met His
5 10
<210> 1354
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1354
Ala Thr Ser Asn Leu Ala Ser
5
<210> 1355
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1355
Gln Gln Trp Ile Phe Asn Pro Pro Thr
5
<210> 1356
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1356
Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly
5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Asn Asn Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro Leu Ile Tyr
35 40 45
Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Glu Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
65 70 75 80
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Trp Ile Phe Asn Pro Pro Thr
85 90 95
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1357
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1357
gacatccagc tgactcagtc cccgtccttc ctgtccgcct ccgtggggga ccgcgtgacg
60
attacttgtc gggcctcctc atccgtgaac aacatgcatt ggtaccagca gaagccagga
120
aaggcaccga agccgcttat ctatgccacc tcgaatctgg ccagcggagt gccttcgagg
180
tttagcggct ccggctccgg caccgagtac actttgacca ttagcagcct ccagccggag
240
gacttcgcca catactactg ccagcagtgg atcttcaacc cccccacctt cggccaagga
300
accaagctgg aaatcaag
318
<210> 1358
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1358
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
5 10 15
Gly Gly Gly Ser
20
<210> 1359
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1359
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly Asp Arg
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val Asn Asn Met His Trp
165 170 175
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro Leu Ile Tyr Ala Thr
180 185 190
Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
195 200 205
Gly Thr Glu Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
210 215 220
Ala Thr Tyr Tyr Cys Gln Gln Trp Ile Phe Asn Pro Pro Thr Phe Gly
225 230 235 240
Gln Gly Thr Lys Leu Glu Ile Lys
245
<210> 1360
<211> 744
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1360
caagtccaac tcgtccagtc tggcgcagaa gtcaagaagc ccggaagctc cgtgaaagtg
60
tcctgcaaag cgtcgggtta cactttcacc cggtacaaca tgcactgggt cagacaggcc
120
cctggacaag gactggagtg gatgggtgcc atctaccctg gaaacggaga tacctcctac
180
tcccaaaagt tcaaggggag agtgaccatt accgccgaca agtcaacttc caccgcttac
240
atggagctca gctccctgcg gtccgaagat actgcggtgt actattgcgc tcgctcattt
300
ttctacggct catcggattg gtacttcgac gtctggggac agggaactac cgtgaccgtg
360
tcctcggggg gaggaggatc gggcggaggc ggttcgggag gcggcggaag cggaggcgga
420
ggttcagaca tccagctgac tcagtccccg tccttcctgt ccgcctccgt gggggaccgc
480
gtgacgatta cttgtcgggc ctcctcatcc gtgaacaaca tgcattggta ccagcagaag
540
ccaggaaagg caccgaagcc gcttatctat gccacctcga atctggccag cggagtgcct
600
tcgaggttta gcggctccgg ctccggcacc gagtacactt tgaccattag cagcctccag
660
ccggaggact tcgccacata ctactgccag cagtggatct tcaacccccc caccttcggc
720
caaggaacca agctggaaat caag
744
<210> 1361
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1361
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Arg Tyr Asn Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser
65 70 75 80
Tyr Ser Gln Lys Phe Lys Gly Arg Val Thr Ile Thr Ala Asp Lys Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Ser Phe Phe Tyr Gly Ser Ser Asp Trp
115 120 125
Tyr Phe Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Phe Leu Ser Ala
165 170 175
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Ser Ser Val
180 185 190
Asn Asn Met His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro
195 200 205
Leu Ile Tyr Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Glu Tyr Thr Leu Thr Ile Ser Ser Leu
225 230 235 240
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Trp Ile Phe Asn
245 250 255
Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1362
<211> 1476
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1362
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtcc aactcgtcca gtctggcgca gaagtcaaga agcccggaag ctccgtgaaa
120
gtgtcctgca aagcgtcggg ttacactttc acccggtaca acatgcactg ggtcagacag
180
gcccctggac aaggactgga gtggatgggt gccatctacc ctggaaacgg agatacctcc
240
tactcccaaa agttcaaggg gagagtgacc attaccgccg acaagtcaac ttccaccgct
300
tacatggagc tcagctccct gcggtccgaa gatactgcgg tgtactattg cgctcgctca
360
tttttctacg gctcatcgga ttggtacttc gacgtctggg gacagggaac taccgtgacc
420
gtgtcctcgg ggggaggggg gagcggcgga gggggctcgg gcggtggagg aagcggaggc
480
ggcggttcgg acatccagct gactcagtcc ccgtccttcc tgtccgcctc cgtgggggac
540
cgcgtgacga ttacttgtcg ggcctcctca tccgtgaaca acatgcattg gtaccagcag
600
aagccaggaa aggcaccgaa gccgcttatc tatgccacct cgaatctggc cagcggagtg
660
ccttcgaggt ttagcggctc cggctccggc accgagtaca ctttgaccat tagcagcctc
720
cagccggagg acttcgccac atactactgc cagcagtgga tcttcaaccc ccccaccttc
780
ggccaaggaa ccaagctgga aatcaagacc actaccccag caccgaggcc acccaccccg
840
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
900
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
960
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1020
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1080
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1140
cgcgtgaaat tcagccgcag cgcagatgct ccagcctacc agcaggggca gaaccagctc
1200
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
1260
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
1320
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
1380
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
1440
tatgacgctc ttcacatgca ggccctgccg cctcgg
1476
<210> 1363
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1363
Gln Val His Leu Gln Gln Ser Gly Ala Glu Leu Ala Lys Pro Gly Ala
5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Trp Met His Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Phe Ile Thr Pro Thr Thr Gly Tyr Pro Glu Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Lys Val Gly Lys Gly Val Tyr Tyr Ala Leu Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 1364
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1364
caagtgcatc tgcagcagtc gggggccgaa ctggcaaagc caggcgccag cgtgaagatg
60
agctgcaagg cctccgggta caccttcacc aactactgga tgcactgggt caagcagcgc
120
ccgggccagg gactcgagtg gatcgggttc atcacgccga ctaccggcta cccggagtat
180
aaccagaagt tcaaggacaa ggccactctg actgccgaca agtcctcgtc taccgcgtac
240
atgcaactgt cctcactgac ttcggaggat tccgctgtgt actactgcgc gcggaggaaa
300
gtcggaaagg gagtgtacta tgccctggac tactggggcc agggtaccag cgtcactgtg
360
tcctcc
366
<210> 1365
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1365
Asp Ile Leu Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly
5 10 15
Glu Thr Val Thr Ile Thr Cys Arg Ala Ser Gly Asn Ile His Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Gln Gly Asn Ser Pro Gln Leu Leu Val
35 40 45
Tyr Asn Thr Lys Thr Leu Ala Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Ser Leu Gln Thr
65 70 75 80
Glu Asp Phe Gly Thr Tyr Tyr Cys Gln His Phe Trp Ser Ser Pro Trp
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1366
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1366
gacattctga tgacccagtc ccctgcatca ctctccgcgt ccgtgggaga aaccgtgacc
60
atcacgtgta gagcctccgg caacatccac aactacctgg cctggtacca gcagaagcag
120
ggaaactcgc cccaactgct tgtgtacaac accaagacct tggctgacgg agtgccttcc
180
cggttctcgg gttcgggatc aggcacacag tactccctga aaatcaatag cctccagacc
240
gaagattttg gaacctacta ctgccaacac ttctggagct ccccctggac tttcggaggc
300
ggtaccaagc tcgagattaa g
321
<210> 1367
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1367
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Leu Val Lys Pro Gly Ala
5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Asn Leu His Trp Val Lys Gln Thr Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Tyr Asp Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Leu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Arg Val Asp Phe Gly His Ser Arg Tyr Trp Tyr Phe Asp Val Trp
100 105 110
Gly Ala Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 1368
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1368
caagtgcagc tgcagcagcc tggtgccgag ctcgtgaagc cgggagcgtc cgtgaagatg
60
agctgcaaag cctcgggcta caccttcacc aattacaact tgcattgggt caagcagacc
120
ccgggccagg gcctcgaatg gatcggagcg atctaccccg ggaactacga tactagctac
180
aaccagaagt tcaagggaaa ggccaccctg accgccgata agtcctcatc caccgcctac
240
atgctgctgt cctcgctgac ttccgaggac tccgctgtgt acttctgcgc ccgcgtggac
300
ttcggacaca gcagatattg gtattttgac gtctggggcg ccgggactac cgtgactgtg
360
tcgtcc
366
<210> 1369
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1369
Gln Ile Val Leu Ser Gln Ser Pro Ala Ile Leu Ser Ala Ser Pro Gly
5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Thr Ser Ser Val Ser Ser Met
20 25 30
Asn Trp Tyr Gln Gln Lys Pro Gly Ser Phe Pro Arg Pro Trp Ile His
35 40 45
Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Arg Val Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Thr Phe Asn Pro Pro Thr
85 90 95
Phe Gly Ala Gly Ala Lys Leu Glu Leu Lys
100 105
<210> 1370
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1370
caaattgtcc tgagccagag cccggctatc ctgtccgcct caccgggcga aaaggtcacc
60
atgacttgtc gggccacttc ctccgtgtca tccatgaact ggtaccagca gaagcctggc
120
agcttccctc ggccatggat tcacgccacg tcaaacctgg catcgggagt gcccgcaagg
180
ttctccgggt ccggcagcgg aacatcctac tccctcacca tctcgcgcgt ggaagcggag
240
gacgctgcca cctactactg ccaacagtgg accttcaacc cccccacctt tggagcggga
300
gccaagctgg aacttaag
318
<210> 1371
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1371
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Leu Val Lys Pro Gly Ala
5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asn Met His Trp Val Lys Gln Thr Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Asn Pro Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser Arg Thr Ala Tyr
65 70 75 80
Ile His Leu Ser Ser Leu Thr Ser Glu Asp Ser Val Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Phe Tyr Gly Ser Ser Ser Trp Tyr Phe Asp Val Trp
100 105 110
Gly Ala Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 1372
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1372
caagtgcagc tgcagcagcc gggagcagag ctcgtgaagc ctggagcctc agtgaagatg
60
agctgcaagg cctccggtta caccttcacc tcctacaaca tgcactgggt caagcagacc
120
cccggacaag gcctggaatg gatcggcgcc atctacccgg gaaacgggga cacctcctat
180
aaccccaagt tcaagggaaa agcaaccctg accgcggaca agtccagcag aactgcctac
240
atccatcttt cctcgctgac gtccgaggat tccgtggtgt actactgtgc ccgctcctac
300
ttctacgggt catcctcgtg gtacttcgat gtctggggcg ctggaaccac cgtgactgtg
360
tcctcc
366
<210> 1373
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1373
Gln Ile Ile Leu Ser Gln Ser Pro Ala Ile Leu Ser Ala Ser Pro Gly
5 10 15
Glu Lys Val Thr Leu Thr Cys Arg Ala Ser Ser Ser Val Ser Ser Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Pro Trp Ile Phe
35 40 45
Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Thr Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Arg Val Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ile Phe Asn Pro Pro Thr
85 90 95
Phe Gly Gly Gly Thr Ser Leu Glu Ile Lys
100 105
<210> 1374
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1374
cagatcattc tgagccagag cccggccatt ctgtctgcct cgcctggaga aaaagtcacc
60
ctcacttgcc gggccagctc ctccgtgtcc tcaatgcact ggtaccagca gaagcctggc
120
tcaagcccga agccctggat cttcgccacc tccaatctgg cgtcaggagt gcccgcgagg
180
ttcactggat cggggtccgg cacatcgtat tcgctcacca tttcccgggt ggaggccgag
240
gacgccgcta cttactactg ccaacagtgg atcttcaacc caccgacctt tggcggaggg
300
acttccttgg aaatcaag
318
<210> 1375
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1375
Gln Ile Gln Leu Val Gln Ser Gly Pro Glu Leu Lys Lys Pro Gly Glu
5 10 15
Thr Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Ser His
20 25 30
Gly Ile Asn Trp Val Lys Gln Ala Pro Arg Lys Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Tyr Thr Gly Glu Pro Thr Tyr Gly Asp Asp Phe
50 55 60
Lys Gly Arg Phe Ala Phe Ser Leu Glu Thr Ser Ala Arg Thr Ala Tyr
65 70 75 80
Leu Gln Ile Asn Asn Leu Lys Asn Glu Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Ala Arg Tyr Gly Asn Tyr Glu Glu Pro Tyr Ala Met Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 1376
<211> 363
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1376
caaattcagc tggtgcagtc gggacctgag ctcaagaagc ccggagaaac cgtgaagatc
60
tcctgcaaga cttccgggta cacttttact tcccacggca tcaactgggt caagcaggca
120
ccaaggaagg ggcttaagtg gatgggctgg attaacacct acaccggcga acccacctat
180
ggcgatgact tcaaaggacg gttcgcgttc tccctcgaaa cctcagcaag aaccgcgtat
240
ttgcaaatca acaacctgaa gaacgaggac accgccacct acttctgcgc ccgctacgga
300
aattacgagg aaccttacgc tatggactac tggggccagg gcacttccgt gactgtgtcg
360
tcc
363
<210> 1377
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1377
Gln Ile Val Leu Ser Gln Ser Pro Ala Ile Leu Ser Ala Ser Pro Gly
5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Thr Ser Ser Val Ser Ser Met
20 25 30
Asn Trp Tyr Gln Gln Lys Pro Gly Ser Phe Pro Arg Pro Trp Ile His
35 40 45
Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Arg Val Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Thr Phe Asn Pro Pro Thr
85 90 95
Phe Gly Ala Gly Ala Lys Leu Glu Leu Lys
100 105
<210> 1378
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1378
cagatcgtgc tgagccagag ccccgccatc ctgagcgctt ccccgggaga aaaggtcacc
60
atgacttgcc gggccactag cagcgtgtcc tccatgaact ggtaccagca gaagccgggc
120
tccttccctc gcccctggat tcatgccacc tcaaacctgg ccagcggagt gccagccaga
180
ttctcgggat ctggatcggg gacgtcctac tccctcacca tctcgcgggt ggaggccgaa
240
gatgccgcca catactactg tcaacagtgg accttcaacc cgccgacctt tggagcgggg
300
gccaagctgg agctgaaa
318
<210> 1379
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1379
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Leu Val Lys Pro Gly Ala
5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asn Ile His Trp Val Lys Gln Thr Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser Thr Thr Ala Phe
65 70 75 80
Ile His Phe Ser Ser Leu Thr Ser Glu Asp Ser Val Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Phe Tyr Gly Ser Asp Ser Trp Tyr Phe Asp Val Trp
100 105 110
Gly Ala Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 1380
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1380
caagtgcagc ttcagcagcc tggggccgaa ctcgtgaagc caggagcctc cgtgaagatg
60
tcatgcaaag cctccggcta cacttttacc tcctacaaca ttcattgggt caagcagaca
120
cctggccagg gcctggaatg gattggtgca atctacccgg gcaacggaga cacctcgtac
180
aaccagaagt ttaaggggaa ggccaccctg accgcggaca agtcaagcac taccgcgttc
240
attcacttct cgtccttgac ctccgaggat agcgtggtgt actactgcgc ccgctcctat
300
ttctacggct ccgattcgtg gtacttcgac gtctggggag ccggaactac cgtgaccgtg
360
tcctcc
366
<210> 1381
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1381
Gln Ile Ile Leu Ser Gln Ser Pro Ala Ile Leu Ser Ala Ser Pro Gly
5 10 15
Glu Lys Val Thr Leu Thr Cys Arg Ala Ser Ser Gly Val Pro Ser Leu
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Pro Trp Ile Phe
35 40 45
Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Arg Val Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ile Phe Asn Pro Pro Thr
85 90 95
Phe Gly Gly Gly Thr Ser Leu Glu Ile Lys
100 105
<210> 1382
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1382
caaatcatcc tgagccagag cccggccatc ctgtcggctt cacccgggga aaaggtcacg
60
ctgacttgcc gggcctcctc cggcgtgcca agcctccact ggtaccagca aaagcctggc
120
tcgtccccca aaccctggat tttcgccacc tccaacctgg ctagcggagt gccggccaga
180
ttctcgggtt ccgggtccgg caccagctat tctctcacca tctcccgggt cgaggcggag
240
gacgcagcga cttactactg tcaacagtgg atcttcaatc cgcccacctt cggcggagga
300
acttccctgg aaatcaag
318
<210> 1383
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1383
Gln Val Gln Leu Leu Gln Pro Gly Ala Glu Leu Val Lys Pro Gly Ala
5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Asn Met His Trp Val Lys Gln Thr Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Phe Phe Tyr Gly Ser Ser Asp Trp Tyr Phe Asp Val Trp
100 105 110
Gly Ala Gly Thr Thr Val Ser Val Ser Ser
115 120
<210> 1384
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1384
caagtgcagc tgctgcagcc cggagccgaa ctcgtgaagc cgggcgcatc cgtgaaaatg
60
agctgcaagg cgtccggtta caccttcact cgctacaaca tgcactgggt caagcagacc
120
cctggacaag gcctggagtg gattggtgct atctacccgg gaaacggaga cactagctac
180
tcgcagaaat tcaagggaaa ggccacgctg accgccgata agtcctcctc cactgcctac
240
atgcaactca gctcactgac ctcagaggac tcggccgtgt actactgcgc gaggtccttc
300
ttctacgggt cctcggattg gtacttcgac gtctggggcg ccggtaccac cgtgtccgtg
360
tcatcc
366
<210> 1385
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1385
Gln Ile Val Leu Ser Gln Ser Pro Ala Ile Leu Ser Thr Ser Pro Gly
5 10 15
Glu Lys Val Thr Leu Thr Cys Arg Ala Ser Ser Ser Val Asn Asn Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Pro Trp Ile Tyr
35 40 45
Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Arg Val Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ile Phe Asn Pro Pro Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 1386
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1386
cagatcgtgc tgagccagtc cccggcgatt ctgtccacct cgcctgggga aaaggtcacc
60
ctgacatgta gagcctcctc ctccgtgaac aatatgcatt ggtatcagca gaagccagga
120
tcaagcccca agccctggat ctatgccact tcgaaccttg cctctggagt gccctcacgg
180
ttctccggct cgggatcggg gaccagctac agcttgacta tctcccgggt ggaggctgag
240
gacgccgcaa cctactactg ccagcaatgg atcttcaacc ctccgacttt tggggccgga
300
accaagctgg aactcaag
318
<210> 1387
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1387
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Asp Tyr
20 25 30
Tyr Met Ala Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Tyr Glu Gly Asn Pro Tyr Tyr Gly Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Ser Thr Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg His Asp His Asn Asn Val Asp Trp Phe Ala Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val
115
<210> 1388
<211> 357
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1388
caagtgcagt tggtggaatc aggaggaggt gtcgtgcaac caggaagatc attgaggctc
60
tcatgcgccg ccagcggatt cacctttcgg gattactaca tggcctgggt ccgccaggcc
120
ccggggaagg gactggaatg ggtggcatcc atctcgtacg aagggaaccc ctactatggg
180
gactccgtga agggacggtt caccatctcc cgggacaacg ccaagtccac cctgtacctt
240
caaatgtcct cgctgagggc ggaggatact gctgtctact actgtgcccg ccacgaccat
300
aacaacgtgg actggttcgc ctactggggc cagggaaccc tcgtcaccgt gtcctcg
357
<210> 1389
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1389
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
5 10 15
Gln Pro Val Ser Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Tyr Ser
20 25 30
Glu Asn Lys Lys Asn Tyr Leu Ala Trp Tyr Leu Gln Lys Pro Gly Gln
35 40 45
Ser Pro Gln Leu Leu Ile Phe Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys
65 70 75 80
Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Asn Phe Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 1390
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1390
gacattgtga tgacgcagac tcccctgtcg ctctccgtga cccctggcca gcccgtgtcg
60
atgtcgtgca agagctccca gtccctgctg tattccgaga acaagaagaa ttaccttgcg
120
tggtacctcc agaagccggg gcagagcccg cagctgctga ttttctgggc gtccactaga
180
gagtctggag tgcctgaccg gtttagcgga agcggctccg gtactgattt caccctgaaa
240
atctcgcgcg tggaagctga ggacgtgggc gtgtactact gccagcagta ctacaacttc
300
cctactttcg gacaaggaac caagctggaa atcaag
336
<210> 1391
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1391
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
5 10 15
Gly Gly Gly Ser
20
<210> 1392
<211> 251
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1392
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Asp Tyr
20 25 30
Tyr Met Ala Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Tyr Glu Gly Asn Pro Tyr Tyr Gly Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Ser Thr Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg His Asp His Asn Asn Val Asp Trp Phe Ala Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr
130 135 140
Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly Gln Pro Val Ser Met
145 150 155 160
Ser Cys Lys Ser Ser Gln Ser Leu Leu Tyr Ser Glu Asn Lys Lys Asn
165 170 175
Tyr Leu Ala Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Gln Leu Leu
180 185 190
Ile Phe Trp Ala Ser Thr Arg Glu Ser Gly Val Pro Asp Arg Phe Ser
195 200 205
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu
210 215 220
Ala Glu Asp Val Gly Val Tyr Tyr Cys Gln Gln Tyr Tyr Asn Phe Pro
225 230 235 240
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
245 250
<210> 1393
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1393
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Thr Phe Arg Asp Tyr
20 25 30
Tyr Met Ala Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Ser Ile Ser Tyr Glu Gly Asn Pro Tyr Tyr Gly Asp Ser Val Lys
50 55 60
Gly Arg Val Thr Ile Thr Arg Asp Asn Ser Ala Ser Thr Leu Tyr Met
65 70 75 80
Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg His Asp His Asn Asn Val Asp Trp Phe Ala Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 1394
<211> 357
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1394
caagtccaac tcgtccagtc cggtgcagaa gtcaagaaac caggagcttc cgtgaaagtg
60
tcgtgcaaag cttcaggctt caccttccgc gactattaca tggcctgggt ccgccaagcg
120
cccggacagc ggctggagtg gatggggtcc atttcctacg aggggaaccc ctactatgga
180
gattccgtga agggcagagt gacgatcact cgggataact ccgcctccac tctctacatg
240
gaactgtcct cgcttcggag cgaagatacc gcggtgtact actgcgcccg ccacgaccat
300
aacaacgtgg actggttcgc ctactgggga caggggaccc tcgtgaccgt gtcctct
357
<210> 1395
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1395
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ser Ser Gln Ser Leu Leu Tyr Ser
20 25 30
Glu Asn Lys Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys
35 40 45
Val Pro Lys Leu Leu Ile Phe Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Pro Glu Asp Val Ala Thr Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Asn Phe Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 1396
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1396
gacattcaga tgacccagtc cccgagctcg ctgtccgcct ccgtgggaga cagagtgaca
60
atcacttgca agagcagcca gtcactgttg tactccgaga acaagaagaa ctacctcgcc
120
tggtaccagc agaagccggg aaaggtccct aagctgctga tcttctgggc cagcactagg
180
gagtcgggag tgccgtcacg gttcagcgga tcgggatcgg gtaccgactt caccctgact
240
atctcctccc tgcaacctga ggacgtggcc acctactact gtcagcagta ctacaatttt
300
cccaccttcg gccagggtac caagctggaa atcaag
336
<210> 1397
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1397
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
5 10 15
Gly Gly Gly Ser
20
<210> 1398
<211> 251
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1398
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Thr Phe Arg Asp Tyr
20 25 30
Tyr Met Ala Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Ser Ile Ser Tyr Glu Gly Asn Pro Tyr Tyr Gly Asp Ser Val Lys
50 55 60
Gly Arg Val Thr Ile Thr Arg Asp Asn Ser Ala Ser Thr Leu Tyr Met
65 70 75 80
Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg His Asp His Asn Asn Val Asp Trp Phe Ala Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr
130 135 140
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
145 150 155 160
Thr Cys Lys Ser Ser Gln Ser Leu Leu Tyr Ser Glu Asn Lys Lys Asn
165 170 175
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu
180 185 190
Ile Phe Trp Ala Ser Thr Arg Glu Ser Gly Val Pro Ser Arg Phe Ser
195 200 205
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
210 215 220
Pro Glu Asp Val Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Asn Phe Pro
225 230 235 240
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
245 250
<210> 1399
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1399
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Phe Thr Phe Arg Asp Tyr
20 25 30
Tyr Met Ala Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Ser Ile Ser Tyr Glu Gly Asn Pro Tyr Tyr Gly Asp Ser Val Lys
50 55 60
Gly Gln Val Thr Ile Ser Arg Asp Asn Ser Ile Ser Thr Leu Tyr Leu
65 70 75 80
Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg His Asp His Asn Asn Val Asp Trp Phe Ala Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 1400
<211> 357
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1400
gaagtccaac tggtgcagtc aggagcagaa gtcaaaaaac caggagaaag cctcaagatc
60
agctgcaagg gctcgggttt caccttccgg gactactata tggcctgggt cagacagatg
120
ccgggaaagg gactggaatg gatggggtca atcagctacg agggcaaccc ctactacgga
180
gactccgtga agggacaggt cacaatctcc cgggacaact cgatttccac tctgtatctg
240
caatggagct ccctcaaggc ctccgacact gcgatgtact actgtgcgcg gcatgaccac
300
aacaatgtgg attggttcgc ctactgggga cagggaaccc tcgtgaccgt gtccagc
357
<210> 1401
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1401
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ser Ser Gln Ser Leu Leu Tyr Ser
20 25 30
Glu Asn Lys Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys
35 40 45
Val Pro Lys Leu Leu Ile Phe Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Pro Glu Asp Val Ala Thr Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Asn Phe Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 1402
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1402
gatatccaaa tgacccagtc gccctcctca ctctccgcct ccgtgggaga tcgcgtgacc
60
attacttgca agagctcgca gtccctgctg tactccgaga acaagaagaa ctacttggcc
120
tggtaccagc agaagcccgg caaagtgccg aagctgctta tcttttgggc ctcgaccagg
180
gaaagcggag tgccgtcacg cttctccggc tccgggtctg gcaccgactt cactctgact
240
atttcctccc tgcaacctga ggacgtggct acctactact gccagcagta ctacaacttc
300
cctaccttcg gccaagggac gaagctggag atcaag
336
<210> 1403
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1403
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
5 10 15
Gly Gly Gly Ser
20
<210> 1404
<211> 251
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1404
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Phe Thr Phe Arg Asp Tyr
20 25 30
Tyr Met Ala Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Ser Ile Ser Tyr Glu Gly Asn Pro Tyr Tyr Gly Asp Ser Val Lys
50 55 60
Gly Gln Val Thr Ile Ser Arg Asp Asn Ser Ile Ser Thr Leu Tyr Leu
65 70 75 80
Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg His Asp His Asn Asn Val Asp Trp Phe Ala Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr
130 135 140
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
145 150 155 160
Thr Cys Lys Ser Ser Gln Ser Leu Leu Tyr Ser Glu Asn Lys Lys Asn
165 170 175
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu
180 185 190
Ile Phe Trp Ala Ser Thr Arg Glu Ser Gly Val Pro Ser Arg Phe Ser
195 200 205
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
210 215 220
Pro Glu Asp Val Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Asn Phe Pro
225 230 235 240
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
245 250
<210> 1405
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1405
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Phe Thr Phe Arg Asp Tyr
20 25 30
Tyr Met Ala Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Ser Ile Ser Tyr Glu Gly Asn Pro Tyr Tyr Gly Asp Ser Val Lys
50 55 60
Gly Gln Val Thr Ile Ser Arg Asp Asn Ser Ile Ser Thr Leu Tyr Leu
65 70 75 80
Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg His Asp His Asn Asn Val Asp Trp Phe Ala Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 1406
<211> 357
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1406
gaagtgcagt tggtccaatc aggcgcagaa gtgaagaaac ccggagaatc attgaagatt
60
tcgtgcaaag gaagcgggtt cacattccgc gattactaca tggcgtgggt cagacagatg
120
ccgggaaagg gactcgagtg gatggggtcc atcagctacg aaggaaaccc ttactacggg
180
gactccgtga agggccaggt caccatctcc cgcgacaact caatctccac tctgtatctg
240
caatggtcga gcctcaaggc ctctgatact gcgatgtact actgcgctcg gcatgaccac
300
aacaacgtgg actggttcgc ttactgggga cagggtaccc ttgtgaccgt gtcctcc
357
<210> 1407
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1407
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
5 10 15
Glu Arg Ala Thr Leu Ser Cys Lys Ser Ser Gln Ser Leu Leu Tyr Ser
20 25 30
Glu Asn Lys Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Ala Pro Arg Leu Leu Ile Phe Trp Ala Ser Thr Arg Glu Ser Gly Ile
50 55 60
Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Pro Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Asn Phe Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 1408
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1408
gagatcgtga tgactcagtc ccctgccacc ctctcgctgt cccccgggga gagggccacg
60
ctgtcctgca agagctccca gtcactgctg tattccgaaa acaagaagaa ctacctcgcc
120
tggtaccaac agaagccggg acaggccccg cggcttctga tcttctgggc ctccactcgg
180
gagtccggca ttccggcccg cttctccggc tcggggagcg gaactgactt caccctgacc
240
atcagcagcc tgcagccaga ggacctcgca gtgtactact gtcaacagta ctacaatttc
300
cccacctttg gccagggtac caagctggag attaag
336
<210> 1409
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1409
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
5 10 15
Gly Gly Gly Ser
20
<210> 1410
<211> 251
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1410
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Phe Thr Phe Arg Asp Tyr
20 25 30
Tyr Met Ala Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Ser Ile Ser Tyr Glu Gly Asn Pro Tyr Tyr Gly Asp Ser Val Lys
50 55 60
Gly Gln Val Thr Ile Ser Arg Asp Asn Ser Ile Ser Thr Leu Tyr Leu
65 70 75 80
Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg His Asp His Asn Asn Val Asp Trp Phe Ala Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr
130 135 140
Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu
145 150 155 160
Ser Cys Lys Ser Ser Gln Ser Leu Leu Tyr Ser Glu Asn Lys Lys Asn
165 170 175
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
180 185 190
Ile Phe Trp Ala Ser Thr Arg Glu Ser Gly Ile Pro Ala Arg Phe Ser
195 200 205
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
210 215 220
Pro Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln Tyr Tyr Asn Phe Pro
225 230 235 240
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
245 250
<210> 1411
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1411
Asp Tyr Ala Met His
5
<210> 1412
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1412
Thr Ile Ser Trp Asn Ser Gly Ser Ile Gly Tyr Ala Asp Ser Val Lys
5 10 15
Gly
<210> 1413
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1413
Asp Ile Gln Tyr Gly Asn Tyr Tyr Tyr Gly Met Asp Val
5 10
<210> 1414
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1414
Gly Phe Thr Phe Asn Asp Tyr
5
<210> 1415
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1415
Ser Trp Asn Ser Gly Ser
5
<210> 1416
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1416
Asp Ile Gln Tyr Gly Asn Tyr Tyr Tyr Gly Met Asp Val
5 10
<210> 1417
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1417
Gly Phe Thr Phe Asn Asp Tyr Ala
5
<210> 1418
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1418
Ile Ser Trp Asn Ser Gly Ser Ile
5
<210> 1419
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1419
Ala Lys Asp Ile Gln Tyr Gly Asn Tyr Tyr Tyr Gly Met Asp Val
5 10 15
<210> 1420
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1420
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Thr Ile Ser Trp Asn Ser Gly Ser Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Lys Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Asp Ile Gln Tyr Gly Asn Tyr Tyr Tyr Gly Met Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 1421
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1421
gaggtgcagc tggtcgagtc ggggggagga ttggtgcagc cgggcagaag cctgcggctc
60
tcatgtgccg cctccggctt cacctttaac gactacgcaa tgcactgggt cagacaggct
120
cctgggaagg gcctggaatg ggtgtccacc atttcctgga actccgggag catcggctac
180
gctgactccg tgaagggccg cttcacgatt agccgcgata acgcgaaaaa gagcctgtac
240
ctccaaatga actccctgcg ggccgaagat accgcccttt actactgcgc gaaggacatt
300
cagtatggaa actactacta cggaatggac gtctggggac aggggaccac agtgaccgtg
360
tcaagc
366
<210> 1422
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1422
Arg Ala Ser Gln Ser Val Ser Ser Tyr Leu Ala
5 10
<210> 1423
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1423
Asp Ala Ser Asn Arg Ala Thr
5
<210> 1424
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1424
Gln Gln Arg Ser Asn Trp Pro Ile Thr
5
<210> 1425
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1425
Ser Gln Ser Val Ser Ser Tyr
5
<210> 1426
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1426
Asp Ala Ser
1
<210> 1427
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1427
Arg Ser Asn Trp Pro Ile
5
<210> 1428
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1428
Gln Ser Val Ser Ser Tyr
5
<210> 1429
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1429
Asp Ala Ser
1
<210> 1430
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1430
Gln Gln Arg Ser Asn Trp Pro Ile Thr
5
<210> 1431
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1431
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Ile
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 1432
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1432
gaaatcgtgc tgacccagag cccagccact ttgtcactgt cccccggcga aagagccact
60
ctgtcctgcc gggcatcgca gtccgtgtcg tcctacctgg cctggtacca gcaaaagccc
120
ggacaagccc ctcgccttct catctacgac gcctccaatc gcgcgaccgg aatcccggcc
180
aggttctccg ggagcggttc aggcactgac ttcaccctga ccatctcgtc cctggagccg
240
gaggatttcg ccgtgtatta ctgccagcag cggtccaact ggcccatcac cttcggccaa
300
gggactcggc tcgaaatcaa g
321
<210> 1433
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1433
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
5 10 15
Gly Gly Gly Ser
20
<210> 1434
<211> 249
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1434
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Thr Ile Ser Trp Asn Ser Gly Ser Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Lys Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Asp Ile Gln Tyr Gly Asn Tyr Tyr Tyr Gly Met Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile
130 135 140
Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg
145 150 155 160
Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Asp
180 185 190
Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp
210 215 220
Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Ile Thr Phe
225 230 235 240
Gly Gln Gly Thr Arg Leu Glu Ile Lys
245
<210> 1435
<211> 747
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1435
gaggtgcagc tggtcgagtc ggggggagga ttggtgcagc cgggcagaag cctgcggctc
60
tcatgtgccg cctccggctt cacctttaac gactacgcaa tgcactgggt cagacaggct
120
cctgggaagg gcctggaatg ggtgtccacc atttcctgga actccgggag catcggctac
180
gctgactccg tgaagggccg cttcacgatt agccgcgata acgcgaaaaa gagcctgtac
240
ctccaaatga actccctgcg ggccgaagat accgcccttt actactgcgc gaaggacatt
300
cagtatggaa actactacta cggaatggac gtctggggac aggggaccac agtgaccgtg
360
tcaagcggcg gtggaggatc tggcggagga ggttccggtg gcggtggatc gggaggggga
420
ggatcggaaa tcgtgctgac ccagagccca gccactttgt cactgtcccc cggcgaaaga
480
gccactctgt cctgccgggc atcgcagtcc gtgtcgtcct acctggcctg gtaccagcaa
540
aagcccggac aagcccctcg ccttctcatc tacgacgcct ccaatcgcgc gaccggaatc
600
ccggccaggt tctccgggag cggttcaggc actgacttca ccctgaccat ctcgtccctg
660
gagccggagg atttcgccgt gtattactgc cagcagcggt ccaactggcc catcaccttc
720
ggccaaggga ctcggctcga aatcaag
747
<210> 1436
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1436
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Asp Tyr
20 25 30
Tyr Met Ala Trp Val Arg Gln Ala Pro Lys Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Tyr Glu Gly Asn Pro Tyr Tyr Gly Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asn Asn Ala Lys Ser Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ser Glu Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg His Asp His Asn Asn Val Asp Trp Phe Ala Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 1437
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1437
Asp Ile Val Met Thr Gln Thr Pro Ser Ser Gln Ala Val Ser Ala Gly
5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Tyr Ser
20 25 30
Glu Asn Lys Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Ser Pro Lys Leu Leu Ile Phe Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ile Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Asn Phe Pro Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 1438
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1438
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
5 10 15
Gly Gly Gly Ser
20
<210> 1439
<211> 251
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1439
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Asp Tyr
20 25 30
Tyr Met Ala Trp Val Arg Gln Ala Pro Lys Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Tyr Glu Gly Asn Pro Tyr Tyr Gly Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asn Asn Ala Lys Ser Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ser Glu Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg His Asp His Asn Asn Val Asp Trp Phe Ala Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr
130 135 140
Gln Thr Pro Ser Ser Gln Ala Val Ser Ala Gly Glu Lys Val Thr Met
145 150 155 160
Ser Cys Lys Ser Ser Gln Ser Leu Leu Tyr Ser Glu Asn Lys Lys Asn
165 170 175
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu
180 185 190
Ile Phe Trp Ala Ser Thr Arg Glu Ser Gly Val Pro Asp Arg Phe Ile
195 200 205
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Val Gln
210 215 220
Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln Tyr Tyr Asn Phe Pro
225 230 235 240
Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
245 250
<210> 1440
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1440
Glu Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Lys Pro Gly Ala
5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asn Met His Trp Val Lys Gln Thr Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Tyr Pro Gly Asn Gly Asp Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Asp Tyr Tyr Cys
85 90 95
Ala Arg Ser Asn Tyr Tyr Gly Ser Ser Tyr Trp Phe Phe Asp Val Trp
100 105 110
Gly Ala Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 1441
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1441
gaggtgcaac tgcagcagtc aggagcagaa ctggtcaagc cgggcgcatc cgtcaagatg
60
agctgcaagg cctcaggata caccttcact tcatacaaca tgcactgggt caagcagacg
120
cctgggcagg ggctggagtg gatcggtgcc atctaccccg gaaacggcga cacctcctac
180
aaccagaagt tcaagggaaa ggccaccctc accgctgata agtccagcag caccgcctac
240
atgcaactgt cgtccctgac ttcggaggac agcgctgact actattgcgc ccgctctaat
300
tactacggtt cctcctactg gttcttcgac gtgtggggcg cgggtaccac tgtgactgtc
360
tccagc
366
<210> 1442
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1442
Asp Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Ala Ser Pro Gly
5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Ser Ser Ser Val Asn Tyr Met
20 25 30
Asp Trp Tyr Gln Lys Lys Pro Gly Ser Ser Pro Lys Pro Trp Ile Tyr
35 40 45
Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Arg Val Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Phe Asn Pro Pro Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 1443
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1443
gacatcgtgc tcactcagtc gcccgccatt ctgagcgcta gccccggcga aaaggtcacc
60
atgacctgta gagcgtcatc ctcggtgaac tacatggact ggtaccagaa gaagccggga
120
tcgagcccta agccatggat ctacgccaca tccaatctgg cgtccggcgt gccggcccgg
180
ttcagcggga gcggctcagg cacctcctat tccctcacca tctcgagagt ggaggctgag
240
gatgcagcca cgtactactg tcagcagtgg tcgttcaacc ccccaacctt tggtggtgga
300
accaagctgg aaatcaag
318
<210> 1444
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1444
Gly Ser Thr Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Gly
5 10 15
Ser Ser
<210> 1445
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1445
Asp Ile Val Leu Thr Gln Ser Pro Ala Ile Leu Ser Ala Ser Pro Gly
5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Ser Ser Ser Val Asn Tyr Met
20 25 30
Asp Trp Tyr Gln Lys Lys Pro Gly Ser Ser Pro Lys Pro Trp Ile Tyr
35 40 45
Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Arg Val Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Phe Asn Pro Pro Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly Ser Thr Ser Gly Gly
100 105 110
Gly Ser Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Glu Val Gln Leu
115 120 125
Gln Gln Ser Gly Ala Glu Leu Val Lys Pro Gly Ala Ser Val Lys Met
130 135 140
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Asn Met His Trp
145 150 155 160
Val Lys Gln Thr Pro Gly Gln Gly Leu Glu Trp Ile Gly Ala Ile Tyr
165 170 175
Pro Gly Asn Gly Asp Thr Ser Tyr Asn Gln Lys Phe Lys Gly Lys Ala
180 185 190
Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr Met Gln Leu Ser
195 200 205
Ser Leu Thr Ser Glu Asp Ser Ala Asp Tyr Tyr Cys Ala Arg Ser Asn
210 215 220
Tyr Tyr Gly Ser Ser Tyr Trp Phe Phe Asp Val Trp Gly Ala Gly Thr
225 230 235 240
Thr Val Thr Val Ser Ser
245
<210> 1446
<211> 738
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1446
gacatcgtgc tcactcagtc gcccgccatt ctgagcgcta gccccggcga aaaggtcacc
60
atgacctgta gagcgtcatc ctcggtgaac tacatggact ggtaccagaa gaagccggga
120
tcgagcccta agccatggat ctacgccaca tccaatctgg cgtccggcgt gccggcccgg
180
ttcagcggga gcggctcagg cacctcctat tccctcacca tctcgagagt ggaggctgag
240
gatgcagcca cgtactactg tcagcagtgg tcgttcaacc ccccaacctt tggtggtgga
300
accaagctgg aaatcaaggg aagcacctcc ggcggaggtt ccggaggagg gtccggaggc
360
ggaggcagct ccgaggtgca actgcagcag tcaggagcag aactggtcaa gccgggcgca
420
tccgtcaaga tgagctgcaa ggcctcagga tacaccttca cttcatacaa catgcactgg
480
gtcaagcaga cgcctgggca ggggctggag tggatcggtg ccatctaccc cggaaacggc
540
gacacctcct acaaccagaa gttcaaggga aaggccaccc tcaccgctga taagtccagc
600
agcaccgcct acatgcaact gtcgtccctg acttcggagg acagcgctga ctactattgc
660
gcccgctcta attactacgg ttcctcctac tggttcttcg acgtgtgggg cgcgggtacc
720
actgtgactg tctccagc
738
<210> 1447
<211> 243
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1447
Glu Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Met Leu Ser Asn
20 25 30
Ser Asp Thr Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Thr Tyr His Arg Ser Thr Trp Tyr Asp Asp Tyr Ala
50 55 60
Ser Ser Val Arg Gly Arg Val Ser Ile Asn Val Asp Thr Ser Lys Asn
65 70 75 80
Gln Tyr Ser Leu Gln Leu Asn Ala Val Thr Pro Glu Asp Thr Gly Val
85 90 95
Tyr Tyr Cys Ala Arg Val Arg Leu Gln Asp Gly Asn Ser Trp Ser Asp
100 105 110
Ala Phe Asp Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly
115 120 125
Gly Gly Gly Ser Gln Ser Ala Leu Thr Gln Pro Ala Ser Ala Ser Gly
130 135 140
Ser Pro Gly Gln Ser Val Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp
145 150 155 160
Val Gly Gly Tyr Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys
165 170 175
Ala Pro Lys Leu Met Ile Tyr Asp Val Ser Asn Arg Pro Ser Gly Val
180 185 190
Ser Asn Arg Phe Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr
195 200 205
Ile Ser Gly Leu Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser
210 215 220
Tyr Thr Ser Ser Ser Thr Leu Tyr Val Phe Gly Thr Gly Thr Gln Leu
225 230 235 240
Thr Val Leu
<210> 1448
<211> 253
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1448
Gln Ser Ala Leu Thr Gln Pro Ala Ser Ala Ser Gly Ser Pro Gly Gln
5 10 15
Ser Val Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Thr Leu Tyr Val Phe Gly Thr Gly Thr Gln Leu Thr Val Leu Gly
100 105 110
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val
115 120 125
Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln Thr Leu
130 135 140
Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Met Leu Ser Asn Ser Asp
145 150 155 160
Thr Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu Trp Leu
165 170 175
Gly Arg Thr Tyr His Arg Ser Thr Trp Tyr Asp Asp Tyr Ala Ser Ser
180 185 190
Val Arg Gly Arg Val Ser Ile Asn Val Asp Thr Ser Lys Asn Gln Tyr
195 200 205
Ser Leu Gln Leu Asn Ala Val Thr Pro Glu Asp Thr Gly Val Tyr Tyr
210 215 220
Cys Ala Arg Val Arg Leu Gln Asp Gly Asn Ser Trp Ser Asp Ala Phe
225 230 235 240
Asp Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
245 250
<210> 1449
<211> 243
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1449
Gln Ser Ala Leu Thr Gln Pro Ala Ser Ala Ser Gly Ser Pro Gly Gln
5 10 15
Ser Val Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Thr Leu Tyr Val Phe Gly Thr Gly Thr Gln Leu Thr Val Leu Gly
100 105 110
Gly Gly Gly Ser Glu Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val
115 120 125
Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser
130 135 140
Met Leu Ser Asn Ser Asp Thr Trp Asn Trp Ile Arg Gln Ser Pro Ser
145 150 155 160
Arg Gly Leu Glu Trp Leu Gly Arg Thr Tyr His Arg Ser Thr Trp Tyr
165 170 175
Asp Asp Tyr Ala Ser Ser Val Arg Gly Arg Val Ser Ile Asn Val Asp
180 185 190
Thr Ser Lys Asn Gln Tyr Ser Leu Gln Leu Asn Ala Val Thr Pro Glu
195 200 205
Asp Thr Gly Val Tyr Tyr Cys Ala Arg Val Arg Leu Gln Asp Gly Asn
210 215 220
Ser Trp Ser Asp Ala Phe Asp Val Trp Gly Gln Gly Thr Met Val Thr
225 230 235 240
Val Ser Ser
<210> 1450
<211> 559
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1450
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe
35 40 45
Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr
65 70 75 80
Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg
85 90 95
Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala
100 105 110
Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser
145 150 155 160
Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys
165 170 175
Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys
180 185 190
Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln
195 200 205
Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
210 215 220
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr
225 230 235 240
Cys Gln Gln Ser Tyr Ser Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys
245 250 255
Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
260 265 270
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
275 280 285
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
290 295 300
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
305 310 315 320
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
325 330 335
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
340 345 350
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
355 360 365
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
370 375 380
Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
385 390 395 400
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
405 410 415
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
420 425 430
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
435 440 445
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
450 455 460
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
465 470 475 480
Pro Pro Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Thr Gly Gly Gly
485 490 495
Gly Ser Gly Met His Lys Arg Ser His Thr Gly Glu Arg Pro Phe Gln
500 505 510
Cys Asn Gln Cys Gly Ala Ser Phe Thr Gln Lys Gly Asn Leu Leu Arg
515 520 525
His Ile Lys Leu His Thr Gly Glu Lys Pro Phe Lys Cys His Leu Cys
530 535 540
Asn Thr Ala Ser Ala Glu Ala Arg His Ile Lys Ala Glu Met Gly
545 550 555
<210> 1451
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1451
Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
5 10 15
Thr Val Lys Ile Ser Cys Lys Gly Ser Gly Phe Asn Ile Glu Asp Tyr
20 25 30
Tyr Ile His Trp Val Gln Gln Ala Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys Tyr Gly Pro Ile Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser Thr Asn Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
100 105 110
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr Gln Ser Pro Asp Ser
130 135 140
Leu Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser
145 150 155 160
Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln
165 170 175
Gln Lys Pro Gly Gln Pro Pro Lys Arg Leu Ile Ser Leu Val Ser Lys
180 185 190
Leu Asp Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val
210 215 220
Tyr Tyr Cys Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Val Glu Ile Lys
245
<210> 1452
<211> 738
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1452
gaaatccagc tggtccaatc gggagctgag gtcaagaagc cgggagccac cgtcaagatc
60
tcatgcaagg ggtcgggatt caacatcgag gactactaca ttcactgggt gcagcaagct
120
ccgggaaaag gcctggaatg gatgggcaga atcgacccag aaaacgacga aactaagtac
180
ggaccgattt tccaaggaag agtgactatc accgccgata cttcaaccaa taccgtctac
240
atggaactga gctcgctccg gtccgaagat actgcagtgt attactgtgc ctttcgcgga
300
ggggtgtact ggggccaagg aactactgtc actgtctcgt caggaggcgg agggtcggga
360
ggaggcggga gcggaggcgg tggctcgggt ggcggaggaa gcgacgtggt gatgacccag
420
tccccggact ccctcgccgt gagcctcgga gagagggcga ctatcaattg caagtcgtcc
480
cagtcacttc tggattccga tggtaaaacg tacctcaact ggctgcagca aaagccaggg
540
cagccaccca aacggttgat ctcccttgtg tccaaactgg atagcggagt gcctgaccgc
600
ttctcgggtt ccggtagcgg gaccgacttc accctgacga tcagctcact gcaggcggag
660
gacgtggcag tgtactactg ctggcaggga acccacttcc ctggcacctt tggaggtggc
720
accaaggtgg agatcaag
738
<210> 1453
<211> 831
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1453
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaaatcc agctggtcca atcgggagct gaggtcaaga agccgggagc caccgtcaag
120
atctcatgca aggggtcggg attcaacatc gaggactact acattcactg ggtgcagcaa
180
gctccgggaa aaggcctgga atggatgggc agaatcgacc cagaaaacga cgaaactaag
240
tacggaccga ttttccaagg aagagtgact atcaccgccg atacttcaac caataccgtc
300
tacatggaac tgagctcgct ccggtccgaa gatactgcag tgtattactg tgcctttcgc
360
ggaggggtgt actggggcca aggaactact gtcactgtct cgtcaggagg cggagggtcg
420
ggaggaggcg ggagcggagg cggtggctcg ggtggcggag gaagcgacgt ggtgatgacc
480
cagtccccgg actccctcgc cgtgagcctc ggagagaggg cgactatcaa ttgcaagtcg
540
tcccagtcac ttctggattc cgatggtaaa acgtacctca actggctgca gcaaaagcca
600
gggcagccac ccaaacggtt gatctccctt gtgtccaaac tggatagcgg agtgcctgac
660
cgcttctcgg gttccggtag cgggaccgac ttcaccctga cgatcagctc actgcaggcg
720
gaggacgtgg cagtgtacta ctgctggcag ggaacccact tccctggcac ctttggaggt
780
ggcaccaagg tggagatcaa gggatcgcac caccatcacc atcatcatca c
831
<210> 1454
<211> 277
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1454
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Thr Val Lys Ile Ser Cys Lys Gly Ser Gly Phe
35 40 45
Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Gln Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys
65 70 75 80
Tyr Gly Pro Ile Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser
85 90 95
Thr Asn Thr Val Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly
115 120 125
Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr
145 150 155 160
Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly Glu Arg Ala Thr Ile
165 170 175
Asn Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr
180 185 190
Leu Asn Trp Leu Gln Gln Lys Pro Gly Gln Pro Pro Lys Arg Leu Ile
195 200 205
Ser Leu Val Ser Lys Leu Asp Ser Gly Val Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala
225 230 235 240
Glu Asp Val Ala Val Tyr Tyr Cys Trp Gln Gly Thr His Phe Pro Gly
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Ser His His His
260 265 270
His His His His His
275
<210> 1455
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1455
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgagatcc agctggtgca gtcgggagct gaagtcaaaa agcctggcgc aaccgtcaag
120
atctcgtgca aaggatcagg gttcaacatc gaggactact acatccattg ggtgcaacag
180
gcacccggaa aaggcctgga gtggatgggg aggattgacc cagaaaatga cgaaaccaag
240
tacggaccga tcttccaagg acgggtgacc atcacggctg acacttccac taacaccgtc
300
tacatggaac tctcgagcct tcgctcggaa gataccgcgg tgtactactg cgcctttaga
360
ggtggagtct actggggaca agggactacc gtcaccgtgt cgtcaggtgg cggaggatca
420
ggcggaggcg gctccggtgg aggaggaagc ggaggaggtg gctccgacgt ggtgatgacg
480
cagtcaccgg actccttggc ggtgagcctg ggtgaacgcg ccactatcaa ctgcaagagc
540
tcccagagct tgctggactc cgatggaaag acttatctca attggctgca acagaagcct
600
ggccagccgc caaagagact catctcactg gtgagcaagc tggatagcgg agtgccagat
660
cggttttcgg gatcgggctc aggcaccgac ttcaccctga ctatttcctc cctccaagcc
720
gaggatgtgg ccgtctacta ctgttggcag gggactcact tcccggggac cttcggtgga
780
ggcactaagg tggagatcaa aaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 1456
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1456
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Thr Val Lys Ile Ser Cys Lys Gly Ser Gly Phe
35 40 45
Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Gln Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys
65 70 75 80
Tyr Gly Pro Ile Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser
85 90 95
Thr Asn Thr Val Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly
115 120 125
Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr
145 150 155 160
Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly Glu Arg Ala Thr Ile
165 170 175
Asn Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr
180 185 190
Leu Asn Trp Leu Gln Gln Lys Pro Gly Gln Pro Pro Lys Arg Leu Ile
195 200 205
Ser Leu Val Ser Lys Leu Asp Ser Gly Val Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala
225 230 235 240
Glu Asp Val Ala Val Tyr Tyr Cys Trp Gln Gly Thr His Phe Pro Gly
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1457
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1457
Asp Val Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln Gln Lys Pro Gly Gln Pro
35 40 45
Pro Lys Arg Leu Ile Ser Leu Val Ser Lys Leu Asp Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Trp Gln Gly
85 90 95
Thr His Phe Pro Gly Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val Lys
130 135 140
Lys Pro Gly Ala Thr Val Lys Ile Ser Cys Lys Gly Ser Gly Phe Asn
145 150 155 160
Ile Glu Asp Tyr Tyr Ile His Trp Val Gln Gln Ala Pro Gly Lys Gly
165 170 175
Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys Tyr
180 185 190
Gly Pro Ile Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser Thr
195 200 205
Asn Thr Val Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
210 215 220
Val Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly Thr
225 230 235 240
Thr Val Thr Val Ser Ser
245
<210> 1458
<211> 738
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1458
gatgtcgtga tgacccagtc cccagactcc ctcgcagtgt ccttgggaga acgggccacc
60
atcaactgca aatcgagcca gtcactgctg gactcagacg gaaagaccta cctcaactgg
120
ctgcagcaga agcctggcca gccaccgaag cgcctgatct ccctggtgtc caagctggac
180
tcgggcgtcc cggacaggtt tagcggtagc ggctcgggaa ccgacttcac tctgaccatt
240
agctcgctcc aagctgaaga tgtggcggtc tactactgct ggcaggggac ccacttcccc
300
gggacctttg gcggaggaac taaagtcgaa atcaaaggag gaggcggatc aggtggagga
360
ggcagcggag gaggagggag cggcggtggc ggctccgaaa ttcaacttgt gcaatccggt
420
gccgaggtga agaaacctgg tgccactgtc aagatctcgt gtaagggatc gggattcaat
480
atcgaggact actacatcca ctgggtgcaa caggcgccag gaaagggatt ggagtggatg
540
ggtcgcatcg acccggaaaa cgatgagact aagtacggac cgatcttcca aggccgggtc
600
acgatcactg cggatacctc cactaatacc gtgtatatgg agctctcgtc actgagaagc
660
gaagatacgg ccgtgtacta ctgcgcattc agaggaggtg tgtactgggg ccagggaact
720
actgtgaccg tgtcgtcg
738
<210> 1459
<211> 831
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1459
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgatgtcg tgatgaccca gtccccagac tccctcgcag tgtccttggg agaacgggcc
120
accatcaact gcaaatcgag ccagtcactg ctggactcag acggaaagac ctacctcaac
180
tggctgcagc agaagcctgg ccagccaccg aagcgcctga tctccctggt gtccaagctg
240
gactcgggcg tcccggacag gtttagcggt agcggctcgg gaaccgactt cactctgacc
300
attagctcgc tccaagctga agatgtggcg gtctactact gctggcaggg gacccacttc
360
cccgggacct ttggcggagg aactaaagtc gaaatcaaag gaggaggcgg atcaggtgga
420
ggaggcagcg gaggaggagg gagcggcggt ggcggctccg aaattcaact tgtgcaatcc
480
ggtgccgagg tgaagaaacc tggtgccact gtcaagatct cgtgtaaggg atcgggattc
540
aatatcgagg actactacat ccactgggtg caacaggcgc caggaaaggg attggagtgg
600
atgggtcgca tcgacccgga aaacgatgag actaagtacg gaccgatctt ccaaggccgg
660
gtcacgatca ctgcggatac ctccactaat accgtgtata tggagctctc gtcactgaga
720
agcgaagata cggccgtgta ctactgcgca ttcagaggag gtgtgtactg gggccaggga
780
actactgtga ccgtgtcgtc ggggtcacat caccaccatc atcatcacca c
831
<210> 1460
<211> 277
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1460
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Asp Ser Leu
20 25 30
Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln
35 40 45
Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln Gln
50 55 60
Lys Pro Gly Gln Pro Pro Lys Arg Leu Ile Ser Leu Val Ser Lys Leu
65 70 75 80
Asp Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
85 90 95
Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr
100 105 110
Tyr Cys Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly Gly Gly Thr
115 120 125
Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Gln Leu Val Gln Ser
145 150 155 160
Gly Ala Glu Val Lys Lys Pro Gly Ala Thr Val Lys Ile Ser Cys Lys
165 170 175
Gly Ser Gly Phe Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Gln Gln
180 185 190
Ala Pro Gly Lys Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn
195 200 205
Asp Glu Thr Lys Tyr Gly Pro Ile Phe Gln Gly Arg Val Thr Ile Thr
210 215 220
Ala Asp Thr Ser Thr Asn Thr Val Tyr Met Glu Leu Ser Ser Leu Arg
225 230 235 240
Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr
245 250 255
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Ser His His His
260 265 270
His His His His His
275
<210> 1461
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1461
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgacgtgg tcatgactca aagcccagat tccttggctg tctcccttgg agaaagagca
120
acgatcaatt gcaaaagctc gcagtccctg ttggactccg atggaaaaac ctacctcaac
180
tggctgcagc agaagccggg acaaccacca aagcggctga tttccctcgt gtccaagctg
240
gacagcggcg tgccggatcg cttctcgggc agcggctcgg gaaccgattt tactctcact
300
atttcgtcac tgcaagcgga ggacgtggcg gtgtattact gctggcaggg cactcacttc
360
ccgggtactt ttggtggagg taccaaagtc gaaatcaagg gtggaggcgg gagcggagga
420
ggcgggtcgg gaggaggagg atcgggtggc ggaggctcag aaatccagct ggtgcagtca
480
ggtgccgaag tgaagaagcc tggggccacg gtgaagatct cgtgcaaggg gagcggattc
540
aacatcgagg attactacat ccattgggtg caacaggccc ctggcaaagg gctggaatgg
600
atgggaagga tcgaccccga gaatgacgag actaagtacg gcccgatctt ccaaggacgg
660
gtgaccatca ctgcagacac ttcaaccaac accgtctaca tggaactctc ctcgctgcgc
720
tccgaggaca ccgccgtgta ctactgtgct ttcagaggag gagtctactg gggacaggga
780
acgaccgtga ccgtcagctc aaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 1462
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1462
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Asp Ser Leu
20 25 30
Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln
35 40 45
Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln Gln
50 55 60
Lys Pro Gly Gln Pro Pro Lys Arg Leu Ile Ser Leu Val Ser Lys Leu
65 70 75 80
Asp Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
85 90 95
Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr
100 105 110
Tyr Cys Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly Gly Gly Thr
115 120 125
Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Gln Leu Val Gln Ser
145 150 155 160
Gly Ala Glu Val Lys Lys Pro Gly Ala Thr Val Lys Ile Ser Cys Lys
165 170 175
Gly Ser Gly Phe Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Gln Gln
180 185 190
Ala Pro Gly Lys Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn
195 200 205
Asp Glu Thr Lys Tyr Gly Pro Ile Phe Gln Gly Arg Val Thr Ile Thr
210 215 220
Ala Asp Thr Ser Thr Asn Thr Val Tyr Met Glu Leu Ser Ser Leu Arg
225 230 235 240
Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr
245 250 255
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1463
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1463
Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Phe Asn Ile Glu Asp Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys Tyr Gly Pro Ile Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Thr Ser Ile Asn Thr Val Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
100 105 110
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr Gln Ser Pro Leu Ser
130 135 140
Leu Pro Val Thr Leu Gly Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser
145 150 155 160
Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln
165 170 175
Gln Arg Pro Gly Gln Ser Pro Arg Arg Leu Ile Ser Leu Val Ser Lys
180 185 190
Leu Asp Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val
210 215 220
Tyr Tyr Cys Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Val Glu Ile Lys
245
<210> 1464
<211> 738
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1464
gagattcagc tggtccaaag cggcgcagaa gtgaaaaagc caggggaatc gttgcgcatc
60
agctgtaaag gttccggctt caacatcgag gactattaca tccattgggt gcggcagatg
120
ccaggaaagg ggctggaatg gatgggacgg attgacccgg agaacgacga aaccaagtac
180
ggaccgatct ttcaaggaca cgtgactatc tccgccgaca ccagcatcaa tacggtgtac
240
ctccaatggt cctcactcaa ggcctcggat accgcgatgt actactgcgc gttcagagga
300
ggcgtctact ggggacaagg gactactgtg actgtctcat caggaggtgg aggaagcgga
360
ggaggtggct cgggcggagg tggatcggga ggaggagggt ccgatgtggt gatgacccag
420
tccccactgt cgctcccggt gaccctcgga cagcctgcta gcatctcgtg caaatcctcg
480
caatccctgc tggactcgga cggaaaaacg tacctcaatt ggctgcagca gcgccctggc
540
cagagcccga gaaggcttat ctcgctggtg tcaaagctgg atagcggtgt gcccgaccgg
600
ttcagcggct cagggtcagg aaccgatttc accttgaaga tctcccgcgt ggaagccgaa
660
gatgtcggag tctactactg ctggcagggt actcacttcc cggggacctt tggtggcggc
720
actaaggtcg agattaag
738
<210> 1465
<211> 831
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1465
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgagattc agctggtcca aagcggcgca gaagtgaaaa agccagggga atcgttgcgc
120
atcagctgta aaggttccgg cttcaacatc gaggactatt acatccattg ggtgcggcag
180
atgccaggaa aggggctgga atggatggga cggattgacc cggagaacga cgaaaccaag
240
tacggaccga tctttcaagg acacgtgact atctccgccg acaccagcat caatacggtg
300
tacctccaat ggtcctcact caaggcctcg gataccgcga tgtactactg cgcgttcaga
360
ggaggcgtct actggggaca agggactact gtgactgtct catcaggagg tggaggaagc
420
ggaggaggtg gctcgggcgg aggtggatcg ggaggaggag ggtccgatgt ggtgatgacc
480
cagtccccac tgtcgctccc ggtgaccctc ggacagcctg ctagcatctc gtgcaaatcc
540
tcgcaatccc tgctggactc ggacggaaaa acgtacctca attggctgca gcagcgccct
600
ggccagagcc cgagaaggct tatctcgctg gtgtcaaagc tggatagcgg tgtgcccgac
660
cggttcagcg gctcagggtc aggaaccgat ttcaccttga agatctcccg cgtggaagcc
720
gaagatgtcg gagtctacta ctgctggcag ggtactcact tcccggggac ctttggtggc
780
ggcactaagg tcgagattaa gggctcacac catcatcacc atcaccacca c
831
<210> 1466
<211> 277
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1466
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Phe
35 40 45
Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Arg Gln Met Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys
65 70 75 80
Tyr Gly Pro Ile Phe Gln Gly His Val Thr Ile Ser Ala Asp Thr Ser
85 90 95
Ile Asn Thr Val Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly
115 120 125
Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr
145 150 155 160
Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly Gln Pro Ala Ser Ile
165 170 175
Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr
180 185 190
Leu Asn Trp Leu Gln Gln Arg Pro Gly Gln Ser Pro Arg Arg Leu Ile
195 200 205
Ser Leu Val Ser Lys Leu Asp Ser Gly Val Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
225 230 235 240
Glu Asp Val Gly Val Tyr Tyr Cys Trp Gln Gly Thr His Phe Pro Gly
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Ser His His His
260 265 270
His His His His His
275
<210> 1467
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1467
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaaatcc agctggtgca aagcggagcc gaggtgaaga agcccggaga atccctgcgc
120
atctcgtgta agggttccgg ctttaacatc gaggattact acatccactg ggtgagacag
180
atgccgggca aaggtctgga atggatgggc cgcatcgacc cggagaacga cgaaaccaaa
240
tacggaccaa tcttccaagg acatgtgact atttccgcgg atacctccat caacactgtc
300
tacttgcagt ggagctcgct caaggcgtcg gataccgcca tgtactactg cgcattcaga
360
ggaggtgtgt actggggcca gggcactacg gtcaccgtgt cctcgggagg tggagggtca
420
ggaggcggag gctcgggcgg tggaggatca ggcggaggag gaagcgatgt ggtcatgact
480
caatccccac tgtcactgcc tgtcactctg gggcaaccgg cttccatctc atgcaagtca
540
agccaatcgc tgctcgactc cgacggaaaa acctacctca attggcttca gcagcgccca
600
ggccagtcgc ctcggaggct gatctcactc gtgtcgaagc ttgactccgg ggtgccggat
660
cggtttagcg gaagcggatc ggggaccgac ttcacgttga agattagccg ggtggaagcc
720
gaggacgtgg gagtctatta ctgctggcag gggacccact tcccggggac tttcggagga
780
ggcaccaaag tcgagattaa gaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 1468
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1468
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Phe
35 40 45
Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Arg Gln Met Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys
65 70 75 80
Tyr Gly Pro Ile Phe Gln Gly His Val Thr Ile Ser Ala Asp Thr Ser
85 90 95
Ile Asn Thr Val Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly
115 120 125
Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr
145 150 155 160
Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly Gln Pro Ala Ser Ile
165 170 175
Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr
180 185 190
Leu Asn Trp Leu Gln Gln Arg Pro Gly Gln Ser Pro Arg Arg Leu Ile
195 200 205
Ser Leu Val Ser Lys Leu Asp Ser Gly Val Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
225 230 235 240
Glu Asp Val Gly Val Tyr Tyr Cys Trp Gln Gly Thr His Phe Pro Gly
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1469
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1469
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Arg Leu Ile Ser Leu Val Ser Lys Leu Asp Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Trp Gln Gly
85 90 95
Thr His Phe Pro Gly Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val Lys
130 135 140
Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Phe Asn
145 150 155 160
Ile Glu Asp Tyr Tyr Ile His Trp Val Arg Gln Met Pro Gly Lys Gly
165 170 175
Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys Tyr
180 185 190
Gly Pro Ile Phe Gln Gly His Val Thr Ile Ser Ala Asp Thr Ser Ile
195 200 205
Asn Thr Val Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala
210 215 220
Met Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly Thr
225 230 235 240
Thr Val Thr Val Ser Ser
245
<210> 1470
<211> 738
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1470
gacgtcgtca tgacccagag cccgctgtca ctgcctgtga ccctgggcca gccggcgtcc
60
attagctgca aatcctcgca atccctgctc gactcagacg gaaaaacgta cttgaactgg
120
ctccaacagc gccctgggca atccccaagg cggcttatct cactcgtcag caagctcgat
180
agcggtgtcc cagacagatt ttcgggctcg ggatcgggca ctgatttcac tctgaagatc
240
tcgcgggtgg aagccgagga tgtgggagtg tactattgct ggcagggcac tcacttcccc
300
gggacgtttg gcggaggaac taaggtcgag atcaaaggag gaggtggatc aggcggaggt
360
gggagcggag gaggaggaag cggtggtgga ggttccgaaa tccagctggt gcaatcagga
420
gccgaggtga agaagccggg agaatccctg cgcatctcgt gcaagggctc gggcttcaac
480
atcgaggatt actacatcca ctgggtgcgg cagatgccgg gaaaggggtt ggaatggatg
540
ggacgcattg acccggaaaa tgatgaaacc aaatacgggc caatcttcca aggccacgtg
600
accattagcg ctgacacttc catcaacacc gtgtaccttc agtggtcctc actgaaggcg
660
tcggacactg ccatgtacta ctgtgcattc agaggagggg tctactgggg acagggcacc
720
accgtgaccg tgagctcc
738
<210> 1471
<211> 831
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1471
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgacgtcg tcatgaccca gagcccgctg tcactgcctg tgaccctggg ccagccggcg
120
tccattagct gcaaatcctc gcaatccctg ctcgactcag acggaaaaac gtacttgaac
180
tggctccaac agcgccctgg gcaatcccca aggcggctta tctcactcgt cagcaagctc
240
gatagcggtg tcccagacag attttcgggc tcgggatcgg gcactgattt cactctgaag
300
atctcgcggg tggaagccga ggatgtggga gtgtactatt gctggcaggg cactcacttc
360
cccgggacgt ttggcggagg aactaaggtc gagatcaaag gaggaggtgg atcaggcgga
420
ggtgggagcg gaggaggagg aagcggtggt ggaggttccg aaatccagct ggtgcaatca
480
ggagccgagg tgaagaagcc gggagaatcc ctgcgcatct cgtgcaaggg ctcgggcttc
540
aacatcgagg attactacat ccactgggtg cggcagatgc cgggaaaggg gttggaatgg
600
atgggacgca ttgacccgga aaatgatgaa accaaatacg ggccaatctt ccaaggccac
660
gtgaccatta gcgctgacac ttccatcaac accgtgtacc ttcagtggtc ctcactgaag
720
gcgtcggaca ctgccatgta ctactgtgca ttcagaggag gggtctactg gggacagggc
780
accaccgtga ccgtgagctc cggctcgcat caccatcatc accaccatca c
831
<210> 1472
<211> 277
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1472
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu
20 25 30
Pro Val Thr Leu Gly Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln
35 40 45
Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln Gln
50 55 60
Arg Pro Gly Gln Ser Pro Arg Arg Leu Ile Ser Leu Val Ser Lys Leu
65 70 75 80
Asp Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
85 90 95
Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr
100 105 110
Tyr Cys Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly Gly Gly Thr
115 120 125
Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Gln Leu Val Gln Ser
145 150 155 160
Gly Ala Glu Val Lys Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys
165 170 175
Gly Ser Gly Phe Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Arg Gln
180 185 190
Met Pro Gly Lys Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn
195 200 205
Asp Glu Thr Lys Tyr Gly Pro Ile Phe Gln Gly His Val Thr Ile Ser
210 215 220
Ala Asp Thr Ser Ile Asn Thr Val Tyr Leu Gln Trp Ser Ser Leu Lys
225 230 235 240
Ala Ser Asp Thr Ala Met Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr
245 250 255
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Ser His His His
260 265 270
His His His His His
275
<210> 1473
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1473
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgacgtcg tcatgaccca atcccctctc tccctgccgg tcaccctggg tcagccggcg
120
tcgatctcat gcaaaagctc acagtccctg ctggattcgg acggaaaaac ctacttgaac
180
tggctccaac agaggccggg tcagtcccct cgcagactga tctcgctggt gagcaagctc
240
gactcgggtg tgccggatcg gttctccggg tcaggatcgg gcaccgactt tacgctcaag
300
atttcgagag tggaggccga ggatgtggga gtgtactatt gctggcaggg cacgcatttc
360
cccgggacct ttggaggcgg gactaaggtg gaaatcaagg gaggtggcgg atcaggcgga
420
ggaggcagcg gcggaggtgg atcaggaggc ggagggtcag agatccagct ggtccaaagc
480
ggagcagagg tgaagaagcc aggcgagtcc cttcgcattt cgtgcaaagg gagcggcttc
540
aacattgaag attactacat ccactgggtg cggcaaatgc caggaaaggg tctggaatgg
600
atgggacgga tcgacccaga aaatgatgaa actaagtacg gaccgatctt ccaaggacac
660
gtcactatct ccgcggacac ttcgatcaac accgtgtacc tccagtggag cagcttgaaa
720
gcctccgaca ccgctatgta ctactgtgcc ttccgcggag gagtctactg gggacagggg
780
actactgtga ccgtgtcgtc caccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 1474
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1474
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu
20 25 30
Pro Val Thr Leu Gly Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln
35 40 45
Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln Gln
50 55 60
Arg Pro Gly Gln Ser Pro Arg Arg Leu Ile Ser Leu Val Ser Lys Leu
65 70 75 80
Asp Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
85 90 95
Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr
100 105 110
Tyr Cys Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly Gly Gly Thr
115 120 125
Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Gln Leu Val Gln Ser
145 150 155 160
Gly Ala Glu Val Lys Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys
165 170 175
Gly Ser Gly Phe Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Arg Gln
180 185 190
Met Pro Gly Lys Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn
195 200 205
Asp Glu Thr Lys Tyr Gly Pro Ile Phe Gln Gly His Val Thr Ile Ser
210 215 220
Ala Asp Thr Ser Ile Asn Thr Val Tyr Leu Gln Trp Ser Ser Leu Lys
225 230 235 240
Ala Ser Asp Thr Ala Met Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr
245 250 255
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1475
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1475
Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
5 10 15
Thr Val Lys Ile Ser Cys Lys Gly Ser Gly Phe Asn Ile Glu Asp Tyr
20 25 30
Tyr Ile His Trp Val Gln Gln Ala Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys Tyr Gly Pro Ile Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser Thr Asn Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
100 105 110
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr Gln Ser Pro Leu Ser
130 135 140
Leu Pro Val Thr Leu Gly Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser
145 150 155 160
Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln
165 170 175
Gln Arg Pro Gly Gln Ser Pro Arg Arg Leu Ile Ser Leu Val Ser Lys
180 185 190
Leu Asp Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val
210 215 220
Tyr Tyr Cys Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Val Glu Ile Lys
245
<210> 1476
<211> 738
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1476
gaaatccagc tcgtgcagag cggagccgag gtcaagaaac cgggtgctac cgtgaagatt
60
tcatgcaagg gatcgggctt caacatcgag gattactaca tccactgggt gcagcaggca
120
ccaggaaaag gacttgaatg gatgggccgg atcgacccgg aaaatgacga gactaagtac
180
ggccctatct tccaaggacg ggtgacgatc accgcagaca ctagcaccaa caccgtctat
240
atggaactct cgtccctgag gtccgaagat actgccgtgt actactgtgc gtttcgcgga
300
ggtgtgtact ggggacaggg taccaccgtc accgtgtcat cgggcggtgg aggctccggt
360
ggaggagggt caggaggcgg tggaagcgga ggaggcggca gcgacgtggt catgactcaa
420
tcgccgctgt cgctgcccgt cactctggga caacccgcgt ccatcagctg caaatcctcg
480
cagtcactgc ttgactccga tggaaagacc tacctcaact ggctgcagca acgcccaggc
540
caatccccaa gacgcctgat ctcgttggtg tcaaagctgg actcaggggt gccggaccgg
600
ttctccggga gcgggtcggg cacggatttc actctcaaga tctccagagt ggaagccgag
660
gatgtgggag tctactactg ctggcaggga acccatttcc ctggaacttt tggcggagga
720
actaaggtcg agattaaa
738
<210> 1477
<211> 831
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1477
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaaatcc agctcgtgca gagcggagcc gaggtcaaga aaccgggtgc taccgtgaag
120
atttcatgca agggatcggg cttcaacatc gaggattact acatccactg ggtgcagcag
180
gcaccaggaa aaggacttga atggatgggc cggatcgacc cggaaaatga cgagactaag
240
tacggcccta tcttccaagg acgggtgacg atcaccgcag acactagcac caacaccgtc
300
tatatggaac tctcgtccct gaggtccgaa gatactgccg tgtactactg tgcgtttcgc
360
ggaggtgtgt actggggaca gggtaccacc gtcaccgtgt catcgggcgg tggaggctcc
420
ggtggaggag ggtcaggagg cggtggaagc ggaggaggcg gcagcgacgt ggtcatgact
480
caatcgccgc tgtcgctgcc cgtcactctg ggacaacccg cgtccatcag ctgcaaatcc
540
tcgcagtcac tgcttgactc cgatggaaag acctacctca actggctgca gcaacgccca
600
ggccaatccc caagacgcct gatctcgttg gtgtcaaagc tggactcagg ggtgccggac
660
cggttctccg ggagcgggtc gggcacggat ttcactctca agatctccag agtggaagcc
720
gaggatgtgg gagtctacta ctgctggcag ggaacccatt tccctggaac ttttggcgga
780
ggaactaagg tcgagattaa agggagccac catcatcatc accaccacca c
831
<210> 1478
<211> 277
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1478
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Thr Val Lys Ile Ser Cys Lys Gly Ser Gly Phe
35 40 45
Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Gln Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys
65 70 75 80
Tyr Gly Pro Ile Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser
85 90 95
Thr Asn Thr Val Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly
115 120 125
Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr
145 150 155 160
Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly Gln Pro Ala Ser Ile
165 170 175
Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr
180 185 190
Leu Asn Trp Leu Gln Gln Arg Pro Gly Gln Ser Pro Arg Arg Leu Ile
195 200 205
Ser Leu Val Ser Lys Leu Asp Ser Gly Val Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
225 230 235 240
Glu Asp Val Gly Val Tyr Tyr Cys Trp Gln Gly Thr His Phe Pro Gly
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Ser His His His
260 265 270
His His His His His
275
<210> 1479
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1479
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaaatcc agctcgtgca gagcggagcc gaggtcaaga aaccgggtgc taccgtgaag
120
atttcatgca agggatcggg cttcaacatc gaggattact acatccactg ggtgcagcag
180
gcaccaggaa aaggacttga atggatgggc cggatcgacc cggaaaatga cgagactaag
240
tacggcccta tcttccaagg acgggtgacg atcaccgcag acactagcac caacaccgtc
300
tatatggaac tctcgtccct gaggtccgaa gatactgccg tgtactactg tgcgtttcgc
360
ggaggtgtgt actggggaca gggtaccacc gtcaccgtgt catcgggcgg tggaggctcc
420
ggtggaggag ggtcaggagg cggtggaagc ggaggaggcg gcagcgacgt ggtcatgact
480
caatcgccgc tgtcgctgcc cgtcactctg ggacaacccg cgtccatcag ctgcaaatcc
540
tcgcagtcac tgcttgactc cgatggaaag acctacctca actggctgca gcaacgccca
600
ggccaatccc caagacgcct gatctcgttg gtgtcaaagc tggactcagg ggtgccggac
660
cggttctccg ggagcgggtc gggcacggat ttcactctca agatctccag agtggaagcc
720
gaggatgtgg gagtctacta ctgctggcag ggaacccatt tccctggaac ttttggcgga
780
ggaactaagg tcgagattaa aaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 1480
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1480
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Thr Val Lys Ile Ser Cys Lys Gly Ser Gly Phe
35 40 45
Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Gln Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys
65 70 75 80
Tyr Gly Pro Ile Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser
85 90 95
Thr Asn Thr Val Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly
115 120 125
Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr
145 150 155 160
Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly Gln Pro Ala Ser Ile
165 170 175
Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr
180 185 190
Leu Asn Trp Leu Gln Gln Arg Pro Gly Gln Ser Pro Arg Arg Leu Ile
195 200 205
Ser Leu Val Ser Lys Leu Asp Ser Gly Val Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
225 230 235 240
Glu Asp Val Gly Val Tyr Tyr Cys Trp Gln Gly Thr His Phe Pro Gly
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1481
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1481
Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Phe Asn Ile Glu Asp Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys Tyr Gly Pro Ile Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Thr Ser Ile Asn Thr Val Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
100 105 110
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr Gln Ser Pro Asp Ser
130 135 140
Leu Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser
145 150 155 160
Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln
165 170 175
Gln Lys Pro Gly Gln Pro Pro Lys Arg Leu Ile Ser Leu Val Ser Lys
180 185 190
Leu Asp Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val
210 215 220
Tyr Tyr Cys Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Val Glu Ile Lys
245
<210> 1482
<211> 738
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1482
gaaatccagc tggtgcagtc aggcgccgag gtcaagaagc cgggagagtc gctgagaatc
60
tcgtgcaagg gctcggggtt caacatcgag gactactaca ttcactgggt caggcagatg
120
ccgggaaagg gactggaatg gatgggccgg atcgacccag aaaatgacga aaccaaatac
180
gggccgattt ttcaaggcca cgtgactatc agcgcagaca cgagcatcaa cactgtctac
240
ctccagtggt cctcgcttaa ggccagcgat accgctatgt actactgcgc attcagaggc
300
ggggtgtact ggggacaagg aaccactgtg accgtgagca gcggaggtgg cggctcggga
360
ggaggtggga gcggaggagg aggttccggc ggtggaggat cagatgtcgt gatgacccag
420
tccccggact ccctcgctgt ctcactgggc gagcgcgcga ccatcaactg caaatcgagc
480
cagtcgctgt tggactccga tggaaagact tatctgaatt ggctgcaaca gaaaccagga
540
caacctccca agcggctcat ctcgcttgtg tcaaaactcg attcgggagt gccagaccgc
600
ttctcggggt ccgggagcgg aactgacttt actttgacca tttcctcact gcaagcggag
660
gatgtggccg tgtattactg ttggcagggc acgcatttcc ctggaacctt cggtggcgga
720
actaaggtgg aaatcaag
738
<210> 1483
<211> 834
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1483
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaaatcc agctggtgca gtcaggcgcc gaggtcaaga agccgggaga gtcgctgaga
120
atctcgtgca agggctcggg gttcaacatc gaggactact acattcactg ggtcaggcag
180
atgccgggaa agggactgga atggatgggc cggatcgacc cagaaaatga cgaaaccaaa
240
tacgggccga tttttcaagg ccacgtgact atcagcgcag acacgagcat caacactgtc
300
tacctccagt ggtcctcgct taaggccagc gataccgcta tgtactactg cgcattcaga
360
ggcggggtgt actggggaca aggaaccact gtgaccgtga gcagcggagg tggcggctcg
420
ggaggaggtg ggagcggagg aggaggttcc ggcggtggag gatcagatgt cgtgatgacc
480
cagtccccgg actccctcgc tgtctcactg ggcgagcgcg cgaccatcaa ctgcaaatcg
540
agccagtcgc tgttggactc cgatggaaag acttatctga attggctgca acagaaacca
600
ggacaacctc ccaagcggct catctcgctt gtgtcaaaac tcgattcggg agtgccagac
660
cgcttctcgg ggtccgggag cggaactgac tttactttga ccatttcctc actgcaagcg
720
gaggatgtgg ccgtgtatta ctgttggcag ggcacgcatt tccctggaac cttcggtggc
780
ggaactaagg tggaaatcaa gggatcacac caccatcatc accatcacca ccat
834
<210> 1484
<211> 278
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1484
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Phe
35 40 45
Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Arg Gln Met Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys
65 70 75 80
Tyr Gly Pro Ile Phe Gln Gly His Val Thr Ile Ser Ala Asp Thr Ser
85 90 95
Ile Asn Thr Val Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly
115 120 125
Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr
145 150 155 160
Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly Glu Arg Ala Thr Ile
165 170 175
Asn Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr
180 185 190
Leu Asn Trp Leu Gln Gln Lys Pro Gly Gln Pro Pro Lys Arg Leu Ile
195 200 205
Ser Leu Val Ser Lys Leu Asp Ser Gly Val Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala
225 230 235 240
Glu Asp Val Ala Val Tyr Tyr Cys Trp Gln Gly Thr His Phe Pro Gly
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Gly Ser His His His
260 265 270
His His His His His His
275
<210> 1485
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1485
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgagattc agctcgtgca atcgggagcg gaagtcaaga agccaggaga gtccttgcgg
120
atctcatgca agggtagcgg ctttaacatc gaggattact acatccactg ggtgaggcag
180
atgccgggga agggactcga atggatggga cggatcgacc cagaaaacga cgaaactaag
240
tacggtccga tcttccaagg ccatgtgact attagcgccg atacttcaat caataccgtg
300
tatctgcaat ggtcctcatt gaaagcctca gataccgcga tgtactactg tgctttcaga
360
ggaggggtct actggggaca gggaactacc gtgactgtct cgtccggcgg aggcgggtca
420
ggaggtggcg gcagcggagg aggagggtcc ggcggaggtg ggtccgacgt cgtgatgacc
480
cagagccctg acagcctggc agtgagcctg ggcgaaagag ctaccattaa ctgcaaatcg
540
tcgcagagcc tgctggactc ggacggaaaa acgtacctca attggctgca gcaaaagcct
600
ggccagccac cgaagcgcct tatctcactg gtgtcgaagc tggattcggg agtgcccgat
660
cgcttctccg gctcgggatc gggtactgac ttcaccctca ctatctcctc gcttcaagca
720
gaggacgtgg ccgtctacta ctgctggcag ggaacccact ttccgggaac cttcggcgga
780
gggacgaaag tggagatcaa gaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 1486
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1486
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Phe
35 40 45
Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Arg Gln Met Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys
65 70 75 80
Tyr Gly Pro Ile Phe Gln Gly His Val Thr Ile Ser Ala Asp Thr Ser
85 90 95
Ile Asn Thr Val Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly
115 120 125
Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr
145 150 155 160
Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly Glu Arg Ala Thr Ile
165 170 175
Asn Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr
180 185 190
Leu Asn Trp Leu Gln Gln Lys Pro Gly Gln Pro Pro Lys Arg Leu Ile
195 200 205
Ser Leu Val Ser Lys Leu Asp Ser Gly Val Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala
225 230 235 240
Glu Asp Val Ala Val Tyr Tyr Cys Trp Gln Gly Thr His Phe Pro Gly
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1487
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1487
Asp Val Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln Gln Lys Pro Gly Gln Pro
35 40 45
Pro Lys Arg Leu Ile Ser Leu Val Ser Lys Leu Asp Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Trp Gln Gly
85 90 95
Thr His Phe Pro Gly Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val Lys
130 135 140
Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Phe Asn
145 150 155 160
Ile Glu Asp Tyr Tyr Ile His Trp Val Arg Gln Met Pro Gly Lys Gly
165 170 175
Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys Tyr
180 185 190
Gly Pro Ile Phe Gln Gly His Val Thr Ile Ser Ala Asp Thr Ser Ile
195 200 205
Asn Thr Val Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala
210 215 220
Met Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly Thr
225 230 235 240
Thr Val Thr Val Ser Ser
245
<210> 1488
<211> 738
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1488
gacgtggtga tgacccaatc gccagattcc ctggcagtgt ccctgggcga acgcgccact
60
attaactgca aatcgtcaca gtccttgctt gattccgacg gaaagaccta cctcaattgg
120
ctccagcaga agccaggaca accgccaaag agactgatct ccctggtgtc aaagctggac
180
tcgggagtgc ctgatcggtt ctcgggtagc gggagcggca ccgacttcac tctgaccatc
240
tcgtcactcc aggctgagga cgtggccgtg tattactgtt ggcagggtac tcactttccg
300
ggcactttcg gaggcggcac caaggtggag attaaaggag gaggcggaag cggaggtgga
360
ggatcgggag gtggtgggag cggcggagga gggagcgaga tccagctcgt ccaatcggga
420
gcggaagtga agaagcccgg agagtcactt agaatctcat gcaaggggtc gggcttcaac
480
atcgaggatt actacatcca ttgggtccgc cagatgcctg gtaaaggact ggaatggatg
540
gggaggattg acccggaaaa cgacgaaact aagtacggac cgatctttca agggcacgtg
600
actatctccg ctgatacctc aatcaatact gtctacctcc agtggtcctc gctgaaagca
660
agcgacaccg cgatgtacta ctgcgccttc cggggaggag tgtactgggg ccaaggcacc
720
acggtcacgg tcagctcc
738
<210> 1489
<211> 834
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1489
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgacgtgg tgatgaccca atcgccagat tccctggcag tgtccctggg cgaacgcgcc
120
actattaact gcaaatcgtc acagtccttg cttgattccg acggaaagac ctacctcaat
180
tggctccagc agaagccagg acaaccgcca aagagactga tctccctggt gtcaaagctg
240
gactcgggag tgcctgatcg gttctcgggt agcgggagcg gcaccgactt cactctgacc
300
atctcgtcac tccaggctga ggacgtggcc gtgtattact gttggcaggg tactcacttt
360
ccgggcactt tcggaggcgg caccaaggtg gagattaaag gaggaggcgg aagcggaggt
420
ggaggatcgg gaggtggtgg gagcggcgga ggagggagcg agatccagct cgtccaatcg
480
ggagcggaag tgaagaagcc cggagagtca cttagaatct catgcaaggg gtcgggcttc
540
aacatcgagg attactacat ccattgggtc cgccagatgc ctggtaaagg actggaatgg
600
atggggagga ttgacccgga aaacgacgaa actaagtacg gaccgatctt tcaagggcac
660
gtgactatct ccgctgatac ctcaatcaat actgtctacc tccagtggtc ctcgctgaaa
720
gcaagcgaca ccgcgatgta ctactgcgcc ttccggggag gagtgtactg gggccaaggc
780
accacggtca cggtcagctc cggctcccat caccaccacc atcaccatca tcac
834
<210> 1490
<211> 278
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1490
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Asp Ser Leu
20 25 30
Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln
35 40 45
Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln Gln
50 55 60
Lys Pro Gly Gln Pro Pro Lys Arg Leu Ile Ser Leu Val Ser Lys Leu
65 70 75 80
Asp Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
85 90 95
Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr
100 105 110
Tyr Cys Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly Gly Gly Thr
115 120 125
Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Gln Leu Val Gln Ser
145 150 155 160
Gly Ala Glu Val Lys Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys
165 170 175
Gly Ser Gly Phe Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Arg Gln
180 185 190
Met Pro Gly Lys Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn
195 200 205
Asp Glu Thr Lys Tyr Gly Pro Ile Phe Gln Gly His Val Thr Ile Ser
210 215 220
Ala Asp Thr Ser Ile Asn Thr Val Tyr Leu Gln Trp Ser Ser Leu Lys
225 230 235 240
Ala Ser Asp Thr Ala Met Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr
245 250 255
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Ser His His His
260 265 270
His His His His His His
275
<210> 1491
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1491
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgacgtgg tgatgactca gtcgcctgac tcgctggctg tgtcccttgg agagcgggcc
120
actatcaatt gcaagtcatc ccagtcgctg ctggattccg acgggaaaac ctacctcaat
180
tggctgcagc aaaaaccggg acagcctcca aagcggctca tcagcctggt gtccaagttg
240
gacagcggcg tgccagaccg cttctccggt tcgggaagcg gtactgattt cacgctgacc
300
atctcatccc tccaagcgga ggatgtggca gtctactact gttggcaggg cacgcatttt
360
ccgggcactt ttggaggagg gaccaaggtc gaaatcaagg gaggaggtgg ctcgggcgga
420
ggaggctcgg gaggaggagg atcaggaggc ggtggaagcg agattcaact ggtccagagc
480
ggcgcagaag tcaagaagcc gggtgaatcg ctcagaatct cgtgcaaagg atcgggattc
540
aacatcgagg actactacat tcactgggtc agacaaatgc cgggcaaagg gctggaatgg
600
atggggagga tcgaccccga aaacgatgaa accaagtacg gaccaatctt ccaagggcac
660
gtgaccattt cggcggacac ctcaatcaac actgtgtacc tccagtggag ctcacttaag
720
gccagcgata ccgccatgta ctattgcgct ttccgcggag gggtgtactg gggacagggc
780
actactgtga ccgtgtcatc caccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 1492
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1492
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Asp Ser Leu
20 25 30
Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln
35 40 45
Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln Gln
50 55 60
Lys Pro Gly Gln Pro Pro Lys Arg Leu Ile Ser Leu Val Ser Lys Leu
65 70 75 80
Asp Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
85 90 95
Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr
100 105 110
Tyr Cys Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly Gly Gly Thr
115 120 125
Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Gln Leu Val Gln Ser
145 150 155 160
Gly Ala Glu Val Lys Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys
165 170 175
Gly Ser Gly Phe Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Arg Gln
180 185 190
Met Pro Gly Lys Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn
195 200 205
Asp Glu Thr Lys Tyr Gly Pro Ile Phe Gln Gly His Val Thr Ile Ser
210 215 220
Ala Asp Thr Ser Ile Asn Thr Val Tyr Leu Gln Trp Ser Ser Leu Lys
225 230 235 240
Ala Ser Asp Thr Ala Met Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr
245 250 255
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1493
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1493
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Arg Leu Ile Ser Leu Val Ser Lys Leu Asp Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Trp Gln Gly
85 90 95
Thr His Phe Pro Gly Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val Lys
130 135 140
Lys Pro Gly Ala Thr Val Lys Ile Ser Cys Lys Gly Ser Gly Phe Asn
145 150 155 160
Ile Glu Asp Tyr Tyr Ile His Trp Val Gln Gln Ala Pro Gly Lys Gly
165 170 175
Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys Tyr
180 185 190
Gly Pro Ile Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser Thr
195 200 205
Asn Thr Val Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
210 215 220
Val Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly Thr
225 230 235 240
Thr Val Thr Val Ser Ser
245
<210> 1494
<211> 738
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1494
gatgtggtca tgacgcagtc accactgtcc ctccccgtga cccttggaca gccagcgtcg
60
attagctgca agtcatccca atccctgctc gattcggatg gaaagaccta tctcaactgg
120
ctgcagcaaa gacccggtca gagccctagg agactcatct cgttggtgtc aaagctggac
180
agcggagtgc cggaccggtt ttccggttcg ggatcgggga cggacttcac tctgaagatt
240
tcacgggtgg aagctgagga tgtgggagtg tactactgct ggcagggaac ccatttccct
300
ggcacttttg gcggaggaac taaggtcgaa atcaagggag gaggtggctc gggaggaggc
360
ggatcgggcg gaggcgggag cggcggagga gggtccgaaa tccaacttgt ccagtcagga
420
gccgaagtga agaaaccggg agccaccgtc aaaatcagct gtaagggatc gggattcaat
480
atcgaggact actacatcca ctgggtgcag caagctccgg gcaaaggact ggagtggatg
540
gggcgcatcg acccagagaa cgacgaaacc aaatacggcc cgatcttcca agggcgggtg
600
accatcaccg cggacacctc aactaacact gtgtacatgg agctgagctc cctgcgctcc
660
gaagatactg cagtctacta ctgcgccttc cgcggtggtg tgtactgggg acagggcacc
720
actgtgactg tcagctcg
738
<210> 1495
<211> 831
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1495
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgatgtgg tcatgacgca gtcaccactg tccctccccg tgacccttgg acagccagcg
120
tcgattagct gcaagtcatc ccaatccctg ctcgattcgg atggaaagac ctatctcaac
180
tggctgcagc aaagacccgg tcagagccct aggagactca tctcgttggt gtcaaagctg
240
gacagcggag tgccggaccg gttttccggt tcgggatcgg ggacggactt cactctgaag
300
atttcacggg tggaagctga ggatgtggga gtgtactact gctggcaggg aacccatttc
360
cctggcactt ttggcggagg aactaaggtc gaaatcaagg gaggaggtgg ctcgggagga
420
ggcggatcgg gcggaggcgg gagcggcgga ggagggtccg aaatccaact tgtccagtca
480
ggagccgaag tgaagaaacc gggagccacc gtcaaaatca gctgtaaggg atcgggattc
540
aatatcgagg actactacat ccactgggtg cagcaagctc cgggcaaagg actggagtgg
600
atggggcgca tcgacccaga gaacgacgaa accaaatacg gcccgatctt ccaagggcgg
660
gtgaccatca ccgcggacac ctcaactaac actgtgtaca tggagctgag ctccctgcgc
720
tccgaagata ctgcagtcta ctactgcgcc ttccgcggtg gtgtgtactg gggacagggc
780
accactgtga ctgtcagctc ggggtcccac catcatcacc accaccatca c
831
<210> 1496
<211> 277
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1496
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu
20 25 30
Pro Val Thr Leu Gly Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln
35 40 45
Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln Gln
50 55 60
Arg Pro Gly Gln Ser Pro Arg Arg Leu Ile Ser Leu Val Ser Lys Leu
65 70 75 80
Asp Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
85 90 95
Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr
100 105 110
Tyr Cys Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly Gly Gly Thr
115 120 125
Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Gln Leu Val Gln Ser
145 150 155 160
Gly Ala Glu Val Lys Lys Pro Gly Ala Thr Val Lys Ile Ser Cys Lys
165 170 175
Gly Ser Gly Phe Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Gln Gln
180 185 190
Ala Pro Gly Lys Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn
195 200 205
Asp Glu Thr Lys Tyr Gly Pro Ile Phe Gln Gly Arg Val Thr Ile Thr
210 215 220
Ala Asp Thr Ser Thr Asn Thr Val Tyr Met Glu Leu Ser Ser Leu Arg
225 230 235 240
Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr
245 250 255
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Ser His His His
260 265 270
His His His His His
275
<210> 1497
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1497
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgatgtgg tcatgacgca gtcaccactg tccctccccg tgacccttgg acagccagcg
120
tcgattagct gcaagtcatc ccaatccctg ctcgattcgg atggaaagac ctatctcaac
180
tggctgcagc aaagacccgg tcagagccct aggagactca tctcgttggt gtcaaagctg
240
gacagcggag tgccggaccg gttttccggt tcgggatcgg ggacggactt cactctgaag
300
atttcacggg tggaagctga ggatgtggga gtgtactact gctggcaggg aacccatttc
360
cctggcactt ttggcggagg aactaaggtc gaaatcaagg gaggaggtgg ctcgggagga
420
ggcggatcgg gcggaggcgg gagcggcgga ggagggtccg aaatccaact tgtccagtca
480
ggagccgaag tgaagaaacc gggagccacc gtcaaaatca gctgtaaggg atcgggattc
540
aatatcgagg actactacat ccactgggtg cagcaagctc cgggcaaagg actggagtgg
600
atggggcgca tcgacccaga gaacgacgaa accaaatacg gcccgatctt ccaagggcgg
660
gtgaccatca ccgcggacac ctcaactaac actgtgtaca tggagctgag ctccctgcgc
720
tccgaagata ctgcagtcta ctactgcgcc ttccgcggtg gtgtgtactg gggacagggc
780
accactgtga ctgtcagctc gaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 1498
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1498
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu
20 25 30
Pro Val Thr Leu Gly Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln
35 40 45
Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln Gln
50 55 60
Arg Pro Gly Gln Ser Pro Arg Arg Leu Ile Ser Leu Val Ser Lys Leu
65 70 75 80
Asp Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
85 90 95
Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr
100 105 110
Tyr Cys Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly Gly Gly Thr
115 120 125
Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Gln Leu Val Gln Ser
145 150 155 160
Gly Ala Glu Val Lys Lys Pro Gly Ala Thr Val Lys Ile Ser Cys Lys
165 170 175
Gly Ser Gly Phe Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Gln Gln
180 185 190
Ala Pro Gly Lys Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn
195 200 205
Asp Glu Thr Lys Tyr Gly Pro Ile Phe Gln Gly Arg Val Thr Ile Thr
210 215 220
Ala Asp Thr Ser Thr Asn Thr Val Tyr Met Glu Leu Ser Ser Leu Arg
225 230 235 240
Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr
245 250 255
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1499
<211> 243
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1499
Glu Ile Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Lys Pro Gly Ala
5 10 15
Ser Val Lys Leu Ser Cys Thr Gly Ser Gly Phe Asn Ile Glu Asp Tyr
20 25 30
Tyr Ile His Trp Val Lys Gln Arg Thr Glu Gln Gly Leu Glu Trp Ile
35 40 45
Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys Tyr Gly Pro Ile Phe
50 55 60
Gln Gly Arg Ala Thr Ile Thr Ala Asp Thr Ser Ser Asn Thr Val Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Phe Arg Gly Gly Val Tyr Trp Gly Pro Gly Thr Thr Leu Thr Val
100 105 110
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser His Met Asp Val Val Met Thr Gln Ser Pro Leu Thr Leu Ser Val
130 135 140
Ala Ile Gly Gln Ser Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu
145 150 155 160
Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp Leu Leu Gln Arg Pro
165 170 175
Gly Gln Ser Pro Lys Arg Leu Ile Ser Leu Val Ser Lys Leu Asp Ser
180 185 190
Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr
195 200 205
Leu Arg Ile Ser Arg Val Glu Ala Glu Asp Leu Gly Ile Tyr Tyr Cys
210 215 220
Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly Gly Gly Thr Lys Leu
225 230 235 240
Glu Ile Lys
<210> 1500
<211> 729
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1500
gagatccagc tccaacagag cggagccgaa ctggtcaaac cgggagcgtc ggtgaagttg
60
tcatgcactg gatcgggctt caacatcgag gattactaca tccactgggt caagcaacgc
120
accgagcagg ggctggaatg gatcggacgg atcgaccccg aaaacgatga aaccaagtac
180
gggcctatct tccaaggacg ggccaccatt acggctgaca cgtcaagcaa taccgtctac
240
ctccagcttt ccagcctgac ctccgaggac actgccgtgt actactgcgc cttcagagga
300
ggcgtgtact ggggaccagg aaccactttg accgtgtcca gcggaggcgg tggatcagga
360
ggaggaggct caggcggtgg cggctcgcac atggacgtgg tcatgactca gtccccgctg
420
accctgtcgg tggcaattgg acagagcgca tccatctcgt gcaagagctc acagtcgctg
480
ctggattccg acggaaagac ttatctgaac tggctgctcc aaagaccagg gcaatcaccg
540
aaacgcctta tctccctggt gtcgaaactc gactcgggtg tgccggatcg gtttaccggt
600
agcgggtccg gcacggactt cactctccgc atttcgaggg tggaagcgga ggatctcggg
660
atctactact gttggcaggg aacccacttc cctgggactt ttggaggcgg aactaagctg
720
gaaatcaag
729
<210> 1501
<211> 822
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1501
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgagatcc agctccaaca gagcggagcc gaactggtca aaccgggagc gtcggtgaag
120
ttgtcatgca ctggatcggg cttcaacatc gaggattact acatccactg ggtcaagcaa
180
cgcaccgagc aggggctgga atggatcgga cggatcgacc ccgaaaacga tgaaaccaag
240
tacgggccta tcttccaagg acgggccacc attacggctg acacgtcaag caataccgtc
300
tacctccagc tttccagcct gacctccgag gacactgccg tgtactactg cgccttcaga
360
ggaggcgtgt actggggacc aggaaccact ttgaccgtgt ccagcggagg cggtggatca
420
ggaggaggag gctcaggcgg tggcggctcg cacatggacg tggtcatgac tcagtccccg
480
ctgaccctgt cggtggcaat tggacagagc gcatccatct cgtgcaagag ctcacagtcg
540
ctgctggatt ccgacggaaa gacttatctg aactggctgc tccaaagacc agggcaatca
600
ccgaaacgcc ttatctccct ggtgtcgaaa ctcgactcgg gtgtgccgga tcggtttacc
660
ggtagcgggt ccggcacgga cttcactctc cgcatttcga gggtggaagc ggaggatctc
720
gggatctact actgttggca gggaacccac ttccctggga cttttggagg cggaactaag
780
ctggaaatca agggtagcca tcaccatcac caccaccatc at
822
<210> 1502
<211> 274
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1502
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Glu Ile Gln Leu Gln Gln Ser Gly Ala Glu Leu
20 25 30
Val Lys Pro Gly Ala Ser Val Lys Leu Ser Cys Thr Gly Ser Gly Phe
35 40 45
Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Lys Gln Arg Thr Glu Gln
50 55 60
Gly Leu Glu Trp Ile Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys
65 70 75 80
Tyr Gly Pro Ile Phe Gln Gly Arg Ala Thr Ile Thr Ala Asp Thr Ser
85 90 95
Ser Asn Thr Val Tyr Leu Gln Leu Ser Ser Leu Thr Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr Trp Gly Pro Gly
115 120 125
Thr Thr Leu Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser His Met Asp Val Val Met Thr Gln Ser Pro
145 150 155 160
Leu Thr Leu Ser Val Ala Ile Gly Gln Ser Ala Ser Ile Ser Cys Lys
165 170 175
Ser Ser Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp
180 185 190
Leu Leu Gln Arg Pro Gly Gln Ser Pro Lys Arg Leu Ile Ser Leu Val
195 200 205
Ser Lys Leu Asp Ser Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser
210 215 220
Gly Thr Asp Phe Thr Leu Arg Ile Ser Arg Val Glu Ala Glu Asp Leu
225 230 235 240
Gly Ile Tyr Tyr Cys Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly
245 250 255
Gly Gly Thr Lys Leu Glu Ile Lys Gly Ser His His His His His His
260 265 270
His His
<210> 1503
<211> 1461
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1503
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgagatcc agctccaaca gagcggagcc gaactggtca aaccgggagc gtcggtgaag
120
ttgtcatgca ctggatcggg cttcaacatc gaggattact acatccactg ggtcaagcaa
180
cgcaccgagc aggggctgga atggatcgga cggatcgacc ccgaaaacga tgaaaccaag
240
tacgggccta tcttccaagg acgggccacc attacggctg acacgtcaag caataccgtc
300
tacctccagc tttccagcct gacctccgag gacactgccg tgtactactg cgccttcaga
360
ggaggcgtgt actggggacc aggaaccact ttgaccgtgt ccagcggagg cggtggatca
420
ggaggaggag gctcaggcgg tggcggctcg cacatggacg tggtcatgac tcagtccccg
480
ctgaccctgt cggtggcaat tggacagagc gcatccatct cgtgcaagag ctcacagtcg
540
ctgctggatt ccgacggaaa gacttatctg aactggctgc tccaaagacc agggcaatca
600
ccgaaacgcc ttatctccct ggtgtcgaaa ctcgactcgg gtgtgccgga tcggtttacc
660
ggtagcgggt ccggcacgga cttcactctc cgcatttcga gggtggaagc ggaggatctc
720
gggatctact actgttggca gggaacccac ttccctggga cttttggagg cggaactaag
780
ctggaaatca agaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
840
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
900
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
960
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1020
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1080
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1140
cgcagcgcag atgctccagc ctacaagcag gggcagaacc agctctacaa cgaactcaat
1200
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
1260
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
1320
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
1380
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
1440
atgcaggccc tgccgcctcg g
1461
<210> 1504
<211> 487
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1504
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Glu Ile Gln Leu Gln Gln Ser Gly Ala Glu Leu
20 25 30
Val Lys Pro Gly Ala Ser Val Lys Leu Ser Cys Thr Gly Ser Gly Phe
35 40 45
Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Lys Gln Arg Thr Glu Gln
50 55 60
Gly Leu Glu Trp Ile Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys
65 70 75 80
Tyr Gly Pro Ile Phe Gln Gly Arg Ala Thr Ile Thr Ala Asp Thr Ser
85 90 95
Ser Asn Thr Val Tyr Leu Gln Leu Ser Ser Leu Thr Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr Trp Gly Pro Gly
115 120 125
Thr Thr Leu Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser His Met Asp Val Val Met Thr Gln Ser Pro
145 150 155 160
Leu Thr Leu Ser Val Ala Ile Gly Gln Ser Ala Ser Ile Ser Cys Lys
165 170 175
Ser Ser Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp
180 185 190
Leu Leu Gln Arg Pro Gly Gln Ser Pro Lys Arg Leu Ile Ser Leu Val
195 200 205
Ser Lys Leu Asp Ser Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser
210 215 220
Gly Thr Asp Phe Thr Leu Arg Ile Ser Arg Val Glu Ala Glu Asp Leu
225 230 235 240
Gly Ile Tyr Tyr Cys Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly
245 250 255
Gly Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
260 265 270
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
275 280 285
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
290 295 300
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
305 310 315 320
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 1505
<211> 240
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1505
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asn
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Arg Leu Ile
35 40 45
Tyr Ala Ala Ser Asn Leu Gln Ser Gly Val Pro Ser Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Ile Val Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln His His Ser Tyr Pro Leu
85 90 95
Thr Ser Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Gly Ser Thr
100 105 110
Ser Gly Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Glu Val Gln Val
115 120 125
Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu
130 135 140
Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Ala Met Ser Trp
145 150 155 160
Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Ala Ile Ser
165 170 175
Gly Ser Gly Gly Ser Thr Asn Tyr Ala Asp Ser Val Lys Gly Arg Phe
180 185 190
Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn
195 200 205
Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Gly Ser Ser
210 215 220
Gly Trp Ser Glu Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
225 230 235 240
<210> 1506
<211> 720
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1506
gatatccaaa tgactcagag cccttcatcc ctgagcgcca gcgtcggaga cagggtgacc
60
atcacgtgcc gggcatccca aggcattaga aataacttgg cgtggtatca gcaaaaacca
120
ggaaaggccc cgaagcgcct gatctacgcg gcctccaacc ttcagtcagg agtgccctcg
180
cgcttcaccg ggagcggtag cggaactgag tttaccctta tcgtgtcgtc cctgcagcca
240
gaggacttcg cgacctacta ctgcctccag catcactcgt acccgttgac ttcgggaggc
300
ggaaccaagg tcgaaatcaa acgcactggc tcgacgtcag ggtccggtaa accgggatcg
360
ggagaaggat cggaagtcca agtgctggag agcggaggcg gactcgtgca acctggcggg
420
tcgctgcggc tcagctgtgc cgcgtcgggt tttactttca gctcgtacgc tatgtcatgg
480
gtgcggcagg ctccgggaaa ggggctggaa tgggtgtccg ctatttccgg ctcgggtgga
540
agcaccaatt acgccgactc cgtgaaggga cgcttcacca tctcacggga taactccaag
600
aatactctgt acctccagat gaactcgctg agagccgagg acaccgcagt gtactactgc
660
gcagggtcaa gcggctggtc cgaatactgg ggacagggca ccctcgtcac tgtcagctcc
720
<210> 1507
<211> 807
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1507
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgatatcc aaatgactca gagcccttca tccctgagcg ccagcgtcgg agacagggtg
120
accatcacgt gccgggcatc ccaaggcatt agaaataact tggcgtggta tcagcaaaaa
180
ccaggaaagg ccccgaagcg cctgatctac gcggcctcca accttcagtc aggagtgccc
240
tcgcgcttca ccgggagcgg tagcggaact gagtttaccc ttatcgtgtc gtccctgcag
300
ccagaggact tcgcgaccta ctactgcctc cagcatcact cgtacccgtt gacttcggga
360
ggcggaacca aggtcgaaat caaacgcact ggctcgacgt cagggtccgg taaaccggga
420
tcgggagaag gatcggaagt ccaagtgctg gagagcggag gcggactcgt gcaacctggc
480
gggtcgctgc ggctcagctg tgccgcgtcg ggttttactt tcagctcgta cgctatgtca
540
tgggtgcggc aggctccggg aaaggggctg gaatgggtgt ccgctatttc cggctcgggt
600
ggaagcacca attacgccga ctccgtgaag ggacgcttca ccatctcacg ggataactcc
660
aagaatactc tgtacctcca gatgaactcg ctgagagccg aggacaccgc agtgtactac
720
tgcgcagggt caagcggctg gtccgaatac tggggacagg gcaccctcgt cactgtcagc
780
tcccatcacc atcaccacca ccatcac
807
<210> 1508
<211> 269
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1508
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
20 25 30
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
35 40 45
Gly Ile Arg Asn Asn Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala
50 55 60
Pro Lys Arg Leu Ile Tyr Ala Ala Ser Asn Leu Gln Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Thr Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Ile Val
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln His
100 105 110
His Ser Tyr Pro Leu Thr Ser Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Arg Thr Gly Ser Thr Ser Gly Ser Gly Lys Pro Gly Ser Gly Glu Gly
130 135 140
Ser Glu Val Gln Val Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
145 150 155 160
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser
165 170 175
Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
180 185 190
Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Asn Tyr Ala Asp Ser
195 200 205
Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu
210 215 220
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
225 230 235 240
Cys Ala Gly Ser Ser Gly Trp Ser Glu Tyr Trp Gly Gln Gly Thr Leu
245 250 255
Val Thr Val Ser Ser His His His His His His His His
260 265
<210> 1509
<211> 1452
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 1509
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgatatcc aaatgactca gagcccttca tccctgagcg ccagcgtcgg agacagggtg
120
accatcacgt gccgggcatc ccaaggcatt agaaataact tggcgtggta tcagcaaaaa
180
ccaggaaagg ccccgaagcg cctgatctac gcggcctcca accttcagtc aggagtgccc
240
tcgcgcttca ccgggagcgg tagcggaact gagtttaccc ttatcgtgtc gtccctgcag
300
ccagaggact tcgcgaccta ctactgcctc cagcatcact cgtacccgtt gacttcggga
360
ggcggaacca aggtcgaaat caaacgcact ggctcgacgt cagggtccgg taaaccggga
420
tcgggagaag gatcggaagt ccaagtgctg gagagcggag gcggactcgt gcaacctggc
480
gggtcgctgc ggctcagctg tgccgcgtcg ggttttactt tcagctcgta cgctatgtca
540
tgggtgcggc aggctccggg aaaggggctg gaatgggtgt ccgctatttc cggctcgggt
600
ggaagcacca attacgccga ctccgtgaag ggacgcttca ccatctcacg ggataactcc
660
aagaatactc tgtacctcca gatgaactcg ctgagagccg aggacaccgc agtgtactac
720
tgcgcagggt caagcggctg gtccgaatac tggggacagg gcaccctcgt cactgtcagc
780
tccaccacta ccccagcacc gaggccaccc accccggctc ctaccatcgc ctcccagcct
840
ctgtccctgc gtccggaggc atgtagaccc gcagctggtg gggccgtgca tacccggggt
900
cttgacttcg cctgcgatat ctacatttgg gcccctctgg ctggtacttg cggggtcctg
960
ctgctttcac tcgtgatcac tctttactgt aagcgcggtc ggaagaagct gctgtacatc
1020
tttaagcaac ccttcatgag gcctgtgcag actactcaag aggaggacgg ctgttcatgc
1080
cggttcccag aggaggagga aggcggctgc gaactgcgcg tgaaattcag ccgcagcgca
1140
gatgctccag cctacaagca ggggcagaac cagctctaca acgaactcaa tcttggtcgg
1200
agagaggagt acgacgtgct ggacaagcgg agaggacggg acccagaaat gggcgggaag
1260
ccgcgcagaa agaatcccca agagggcctg tacaacgagc tccaaaagga taagatggca
1320
gaagcctata gcgagattgg tatgaaaggg gaacgcagaa gaggcaaagg ccacgacgga
1380
ctgtaccagg gactcagcac cgccaccaag gacacctatg acgctcttca catgcaggcc
1440
ctgccgcctc gg
1452
<210> 1510
<211> 484
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1510
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
20 25 30
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
35 40 45
Gly Ile Arg Asn Asn Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala
50 55 60
Pro Lys Arg Leu Ile Tyr Ala Ala Ser Asn Leu Gln Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Thr Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Ile Val
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln His
100 105 110
His Ser Tyr Pro Leu Thr Ser Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Arg Thr Gly Ser Thr Ser Gly Ser Gly Lys Pro Gly Ser Gly Glu Gly
130 135 140
Ser Glu Val Gln Val Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
145 150 155 160
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser
165 170 175
Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
180 185 190
Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Asn Tyr Ala Asp Ser
195 200 205
Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu
210 215 220
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
225 230 235 240
Cys Ala Gly Ser Ser Gly Trp Ser Glu Tyr Trp Gly Gln Gly Thr Leu
245 250 255
Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro
260 265 270
Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys
275 280 285
Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala
290 295 300
Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu
305 310 315 320
Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys
325 330 335
Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr
340 345 350
Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly
355 360 365
Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala
370 375 380
Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg
385 390 395 400
Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu
405 410 415
Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn
420 425 430
Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met
435 440 445
Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly
450 455 460
Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala
465 470 475 480
Leu Pro Pro Arg
<210> 1511
<211> 244
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1511
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Arg Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Met
100 105 110
Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser
130 135 140
Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Ile Ser Cys
145 150 155 160
Arg Ala Ser Gln Ser Val Ser Ser Asn Phe Ala Trp Tyr Gln Gln Arg
165 170 175
Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Asp Ala Ser Asn Arg Ala
180 185 190
Thr Gly Ile Pro Pro Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
195 200 205
Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp Phe Ala Ala Tyr Tyr
210 215 220
Cys His Gln Arg Ser Asn Trp Leu Tyr Thr Phe Gly Gln Gly Thr Lys
225 230 235 240
Val Asp Ile Lys
<210> 1512
<211> 488
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1512
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Ser Arg Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Arg Tyr Tyr Gly Met Asp Val Trp
115 120 125
Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile
145 150 155 160
Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg
165 170 175
Ala Thr Ile Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Asn Phe Ala
180 185 190
Trp Tyr Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Asp
195 200 205
Ala Ser Asn Arg Ala Thr Gly Ile Pro Pro Arg Phe Ser Gly Ser Gly
210 215 220
Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp
225 230 235 240
Phe Ala Ala Tyr Tyr Cys His Gln Arg Ser Asn Trp Leu Tyr Thr Phe
245 250 255
Gly Gln Gly Thr Lys Val Asp Ile Lys Thr Thr Thr Pro Ala Pro Arg
260 265 270
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
275 280 285
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
290 295 300
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
305 310 315 320
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg
325 330 335
Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro
340 345 350
Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu
355 360 365
Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala
370 375 380
Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
385 390 395 400
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
405 410 415
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
420 425 430
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
435 440 445
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
450 455 460
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
465 470 475 480
His Met Gln Ala Leu Pro Pro Arg
485
<210> 1513
<211> 253
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1513
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Leu Arg Arg Thr Val Val Thr Pro Arg Ala Tyr Tyr Gly
100 105 110
Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser
145 150 155 160
Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Asp Ile Ser
165 170 175
Asn Ser Leu Asn Trp Tyr Gln Gln Lys Ala Gly Lys Ala Pro Lys Leu
180 185 190
Leu Ile Tyr Asp Ala Ser Thr Leu Glu Thr Gly Val Pro Ser Arg Phe
195 200 205
Ser Gly Ser Gly Ser Gly Thr Asp Phe Ser Phe Thr Ile Ser Ser Leu
210 215 220
Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln His Asp Asn Leu
225 230 235 240
Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
245 250
<210> 1514
<211> 497
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1514
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Leu Arg Arg Thr Val Val Thr Pro
115 120 125
Arg Ala Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr
130 135 140
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser
165 170 175
Thr Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala
180 185 190
Ser Gln Asp Ile Ser Asn Ser Leu Asn Trp Tyr Gln Gln Lys Ala Gly
195 200 205
Lys Ala Pro Lys Leu Leu Ile Tyr Asp Ala Ser Thr Leu Glu Thr Gly
210 215 220
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Ser Phe
225 230 235 240
Thr Ile Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln
245 250 255
Gln His Asp Asn Leu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu
260 265 270
Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
275 280 285
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
290 295 300
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
305 310 315 320
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
325 330 335
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
340 345 350
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
355 360 365
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
370 375 380
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln
385 390 395 400
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
405 410 415
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
420 425 430
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
435 440 445
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
450 455 460
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
465 470 475 480
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
485 490 495
Arg
<210> 1515
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1515
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
5 10 15
Pro Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Glu Trp Asp Gly Ser Tyr Tyr Tyr Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Leu
130 135 140
Thr Gln Thr Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
145 150 155 160
Ile Thr Cys Arg Ala Ser Gln Ser Ile Asn Thr Tyr Leu Asn Trp Tyr
165 170 175
Gln His Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser
180 185 190
Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
210 215 220
Thr Tyr Tyr Cys Gln Gln Ser Phe Ser Pro Leu Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Leu Glu Ile Lys
245
<210> 1516
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1516
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Pro Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Glu Trp Asp Gly Ser Tyr Tyr Tyr
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Val Leu Thr Gln Thr Pro Ser Ser Leu Ser Ala Ser Val
165 170 175
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Asn Thr
180 185 190
Tyr Leu Asn Trp Tyr Gln His Lys Pro Gly Lys Ala Pro Lys Leu Leu
195 200 205
Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Phe Ser Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1517
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1517
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Val Trp Val
35 40 45
Ser Arg Ile Asn Thr Asp Gly Ser Thr Thr Thr Tyr Ala Asp Ser Val
50 55 60
Glu Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Asp Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Gly Gly His Trp Ala Val Trp Gly Gln Gly Thr Thr Val Thr Val
100 105 110
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Thr
130 135 140
Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser
145 150 155 160
Gln Ser Ile Ser Asp Arg Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys
165 170 175
Ala Pro Lys Leu Leu Ile Tyr Lys Ala Ser Ser Leu Glu Ser Gly Val
180 185 190
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr
195 200 205
Ile Ser Ser Leu Gln Pro Asp Asp Phe Ala Val Tyr Tyr Cys Gln Gln
210 215 220
Tyr Gly His Leu Pro Met Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu
225 230 235 240
Ile Lys
<210> 1518
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1518
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Trp Met His Trp Val Arg Gln Val Pro Gly Lys
50 55 60
Gly Leu Val Trp Val Ser Arg Ile Asn Thr Asp Gly Ser Thr Thr Thr
65 70 75 80
Tyr Ala Asp Ser Val Glu Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Asp Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Val Gly Gly His Trp Ala Val Trp Gly Gln Gly
115 120 125
Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr
145 150 155 160
Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
165 170 175
Thr Cys Arg Ala Ser Gln Ser Ile Ser Asp Arg Leu Ala Trp Tyr Gln
180 185 190
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Lys Ala Ser Ser
195 200 205
Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
210 215 220
Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp Asp Phe Ala Val
225 230 235 240
Tyr Tyr Cys Gln Gln Tyr Gly His Leu Pro Met Tyr Thr Phe Gly Gln
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 1519
<211> 241
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1519
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Glu Lys Pro Gly Ala
5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Gly Trp Asp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr Gln Ser Pro Ser
130 135 140
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
145 150 155 160
Ser Gln Ser Ile Arg Tyr Tyr Leu Ser Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Lys Ala Pro Lys Leu Leu Ile Tyr Thr Ala Ser Ile Leu Gln Asn Gly
180 185 190
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu
210 215 220
Gln Thr Tyr Thr Thr Pro Asp Phe Gly Pro Gly Thr Lys Val Glu Ile
225 230 235 240
Lys
<210> 1520
<211> 485
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1520
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Glu Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Asp Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Ser Gly Trp Asp Phe Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met
145 150 155 160
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Gln Ser Ile Arg Tyr Tyr Leu Ser Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Thr Ala Ser
195 200 205
Ile Leu Gln Asn Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
225 230 235 240
Thr Tyr Tyr Cys Leu Gln Thr Tyr Thr Thr Pro Asp Phe Gly Pro Gly
245 250 255
Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
260 265 270
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
275 280 285
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
290 295 300
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
305 310 315 320
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
325 330 335
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
340 345 350
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
355 360 365
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
370 375 380
Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
385 390 395 400
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
405 410 415
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
420 425 430
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
435 440 445
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
450 455 460
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
465 470 475 480
Ala Leu Pro Pro Arg
485
<210> 1521
<211> 253
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1521
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Arg Leu Ile Ala Val Ala Gly Asp Tyr Tyr Tyr Tyr Gly
100 105 110
Met Asp Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser
145 150 155 160
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Val Gly
165 170 175
Arg Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Thr Ala Pro Lys Leu
180 185 190
Leu Ile Tyr Ala Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe
195 200 205
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Asn Leu
210 215 220
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Phe
225 230 235 240
Pro Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys
245 250
<210> 1522
<211> 497
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1522
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Thr Ser Thr Val Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Tyr Arg Leu Ile Ala Val Ala Gly Asp
115 120 125
Tyr Tyr Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Met Val Thr
130 135 140
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser
165 170 175
Ser Val Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
180 185 190
Ser Gln Gly Val Gly Arg Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly
195 200 205
Thr Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Thr Leu Gln Ser Gly
210 215 220
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
225 230 235 240
Thr Ile Asn Asn Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln
245 250 255
Gln Ala Asn Ser Phe Pro Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu
260 265 270
Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
275 280 285
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
290 295 300
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
305 310 315 320
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
325 330 335
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
340 345 350
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
355 360 365
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
370 375 380
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln
385 390 395 400
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
405 410 415
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
420 425 430
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
435 440 445
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
450 455 460
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
465 470 475 480
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
485 490 495
Arg
<210> 1523
<211> 250
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1523
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Val Val Gln Pro Gly Arg
5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Trp Lys Val Ser Ser Ser Ser Pro Ala Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val
130 135 140
Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala
145 150 155 160
Ile Leu Ser Cys Arg Ala Ser Gln Ser Val Tyr Thr Lys Tyr Leu Gly
165 170 175
Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Asp
180 185 190
Ala Ser Thr Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Arg Leu Glu Pro Glu Asp
210 215 220
Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Gly Ser Pro Leu Ile Thr
225 230 235 240
Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
245 250
<210> 1524
<211> 494
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1524
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Gly Gly Val
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Trp Lys Val Ser Ser Ser Ser Pro Ala
115 120 125
Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser
165 170 175
Pro Gly Glu Arg Ala Ile Leu Ser Cys Arg Ala Ser Gln Ser Val Tyr
180 185 190
Thr Lys Tyr Leu Gly Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg
195 200 205
Leu Leu Ile Tyr Asp Ala Ser Thr Arg Ala Thr Gly Ile Pro Asp Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Arg
225 230 235 240
Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Gly
245 250 255
Ser Pro Leu Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Thr
260 265 270
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
275 280 285
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
290 295 300
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
305 310 315 320
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
325 330 335
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
340 345 350
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
355 360 365
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
370 375 380
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn
385 390 395 400
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
405 410 415
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
420 425 430
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
435 440 445
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
450 455 460
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
465 470 475 480
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1525
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1525
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
5 10 15
Ser Val Lys Val Ser Cys Lys Thr Ser Gly Tyr Pro Phe Thr Gly Tyr
20 25 30
Ser Leu His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly Gly Asn Ser Leu Phe Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Leu Thr
130 135 140
Gln Ser Pro Ser Ser Ile Ser Ala Ser Val Gly Asp Thr Val Ser Ile
145 150 155 160
Thr Cys Arg Ala Ser Gln Asp Ser Gly Thr Trp Leu Ala Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Met Tyr Asp Ala Ser Thr
180 185 190
Leu Glu Asp Gly Val Pro Ser Arg Phe Ser Gly Ser Ala Ser Gly Thr
195 200 205
Glu Phe Thr Leu Thr Val Asn Arg Leu Gln Pro Glu Asp Ser Ala Thr
210 215 220
Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Pro Leu Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Val Asp Ile Lys
245
<210> 1526
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1526
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Thr Ser Gly Tyr
35 40 45
Pro Phe Thr Gly Tyr Ser Leu His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp His Tyr Gly Gly Asn Ser Leu Phe
115 120 125
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Ile Ser Ala Ser Val Gly
165 170 175
Asp Thr Val Ser Ile Thr Cys Arg Ala Ser Gln Asp Ser Gly Thr Trp
180 185 190
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Met
195 200 205
Tyr Asp Ala Ser Thr Leu Glu Asp Gly Val Pro Ser Arg Phe Ser Gly
210 215 220
Ser Ala Ser Gly Thr Glu Phe Thr Leu Thr Val Asn Arg Leu Gln Pro
225 230 235 240
Glu Asp Ser Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Asp Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1527
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1527
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
5 10 15
Ser Val Glu Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Gly Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val His
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Tyr Ser Ser Ser Ser Asp Ala Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
130 135 140
Met Thr Gln Ser Pro Pro Ser Leu Ser Ala Ser Val Gly Asp Arg Val
145 150 155 160
Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Ser Ala Leu Ala Trp
165 170 175
Tyr Gln Gln Lys Pro Gly Thr Pro Pro Lys Leu Leu Ile Tyr Asp Ala
180 185 190
Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
195 200 205
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
210 215 220
Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Ser Tyr Pro Leu Thr Phe Gly
225 230 235 240
Gly Gly Thr Arg Leu Glu Ile Lys
245
<210> 1528
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1528
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Glu Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Gly
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Thr Ser Thr Val His Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Gly Tyr Ser Ser Ser Ser Asp Ala
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Pro Ser Leu Ser Ala Ser
165 170 175
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser
180 185 190
Ser Ala Leu Ala Trp Tyr Gln Gln Lys Pro Gly Thr Pro Pro Lys Leu
195 200 205
Leu Ile Tyr Asp Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
225 230 235 240
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Ser Tyr
245 250 255
Pro Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1529
<211> 255
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1529
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Gly Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn Tyr Ala Gln Lys Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Ala Gly Gly Ile Tyr Tyr Tyr Tyr Gly Met Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Ile Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Val Met Thr Gln Thr Pro Asp Ser Leu Ala Val Ser Leu Gly Glu Arg
145 150 155 160
Ala Thr Ile Ser Cys Lys Ser Ser His Ser Val Leu Tyr Asn Arg Asn
165 170 175
Asn Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
180 185 190
Lys Leu Leu Phe Tyr Trp Ala Ser Thr Arg Lys Ser Gly Val Pro Asp
195 200 205
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
210 215 220
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Thr Gln
225 230 235 240
Thr Phe Pro Leu Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Asn
245 250 255
<210> 1530
<211> 499
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1530
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Gly Ile Ser Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn
65 70 75 80
Tyr Ala Gln Lys Leu Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Val Ala Gly Gly Ile Tyr Tyr Tyr Tyr
115 120 125
Gly Met Asp Val Trp Gly Gln Gly Thr Thr Ile Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Val Met Thr Gln Thr Pro Asp Ser Leu Ala Val
165 170 175
Ser Leu Gly Glu Arg Ala Thr Ile Ser Cys Lys Ser Ser His Ser Val
180 185 190
Leu Tyr Asn Arg Asn Asn Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys
195 200 205
Pro Gly Gln Pro Pro Lys Leu Leu Phe Tyr Trp Ala Ser Thr Arg Lys
210 215 220
Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
225 230 235 240
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Phe
245 250 255
Cys Gln Gln Thr Gln Thr Phe Pro Leu Thr Phe Gly Gln Gly Thr Arg
260 265 270
Leu Glu Ile Asn Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
275 280 285
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
290 295 300
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
305 310 315 320
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
325 330 335
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
340 345 350
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
355 360 365
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
370 375 380
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
385 390 395 400
Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
405 410 415
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
420 425 430
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
435 440 445
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
450 455 460
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
465 470 475 480
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
485 490 495
Pro Pro Arg
<210> 1531
<211> 241
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1531
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Asn Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Gly Trp Asp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Asp Ile Arg Met Thr Gln Ser Pro Ser
130 135 140
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
145 150 155 160
Ser Gln Ser Ile Arg Tyr Tyr Leu Ser Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Lys Ala Pro Lys Leu Leu Ile Tyr Thr Ala Ser Ile Leu Gln Asn Gly
180 185 190
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu
210 215 220
Gln Thr Tyr Thr Thr Pro Asp Phe Gly Pro Gly Thr Lys Val Glu Ile
225 230 235 240
Lys
<210> 1532
<211> 485
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1532
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Asn Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Arg Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Ser Gly Trp Asp Phe Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Arg Met
145 150 155 160
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Gln Ser Ile Arg Tyr Tyr Leu Ser Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Thr Ala Ser
195 200 205
Ile Leu Gln Asn Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
225 230 235 240
Thr Tyr Tyr Cys Leu Gln Thr Tyr Thr Thr Pro Asp Phe Gly Pro Gly
245 250 255
Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
260 265 270
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
275 280 285
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
290 295 300
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
305 310 315 320
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
325 330 335
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
340 345 350
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
355 360 365
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
370 375 380
Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
385 390 395 400
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
405 410 415
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
420 425 430
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
435 440 445
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
450 455 460
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
465 470 475 480
Ala Leu Pro Pro Arg
485
<210> 1533
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1533
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Thr Thr Thr Ser Tyr Ala Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Leu Thr Gln
130 135 140
Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
145 150 155 160
Cys Arg Ala Ser Gln Ser Ile Ser Thr Trp Leu Ala Trp Tyr Gln Gln
165 170 175
Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile Tyr Lys Ala Ser Thr Leu
180 185 190
Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu
195 200 205
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp Asp Phe Ala Thr Tyr
210 215 220
Tyr Cys Gln Gln Tyr Asn Thr Tyr Ser Pro Tyr Thr Phe Gly Gln Gly
225 230 235 240
Thr Lys Leu Glu Ile Lys
245
<210> 1534
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1534
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Thr Thr Thr Ser Tyr Ala Phe Asp Ile
115 120 125
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Leu Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Thr Trp Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile Tyr
195 200 205
Lys Ala Ser Thr Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp
225 230 235 240
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Thr Tyr Ser Pro Tyr
245 250 255
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1535
<211> 249
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1535
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
5 10 15
Ser Leu Arg Leu Ser Cys Glu Ala Ser Gly Phe Ile Phe Ser Asp Tyr
20 25 30
Tyr Met Gly Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Gly Arg Ser Gly Ser Ser Met Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Phe Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ala Ser Pro Val Val Ala Ala Thr Glu Asp Phe Gln His Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val
130 135 140
Met Thr Gln Thr Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala
145 150 155 160
Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Thr Ser Asn Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Leu Phe Gly
180 185 190
Ala Ser Thr Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Arg Leu Glu Pro Glu Asp
210 215 220
Phe Ala Met Tyr Tyr Cys Gln Gln Tyr Gly Ser Ala Pro Val Thr Phe
225 230 235 240
Gly Gln Gly Thr Lys Leu Glu Ile Lys
245
<210> 1536
<211> 493
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1536
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu
20 25 30
Val Lys Pro Gly Gly Ser Leu Arg Leu Ser Cys Glu Ala Ser Gly Phe
35 40 45
Ile Phe Ser Asp Tyr Tyr Met Gly Trp Ile Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Tyr Ile Gly Arg Ser Gly Ser Ser Met Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Phe Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Ala Ser Pro Val Val Ala Ala Thr Glu Asp
115 120 125
Phe Gln His Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Asp Ile Val Met Thr Gln Thr Pro Ala Thr Leu Ser Leu Ser
165 170 175
Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Thr
180 185 190
Ser Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg
195 200 205
Leu Leu Leu Phe Gly Ala Ser Thr Arg Ala Thr Gly Ile Pro Asp Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Arg
225 230 235 240
Leu Glu Pro Glu Asp Phe Ala Met Tyr Tyr Cys Gln Gln Tyr Gly Ser
245 250 255
Ala Pro Val Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1537
<211> 249
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1537
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Arg Ala Pro Gly Ala
5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Phe Thr Phe Arg Gly Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Arg Ala Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Asp Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Thr Ala Ser Cys Gly Gly Asp Cys Tyr Tyr Leu Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Met Thr Gln Ser Pro Pro Thr Leu Ser Ala Ser Val Gly Asp Arg
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Val Asn Ile Trp Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Lys
180 185 190
Ser Ser Ser Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Ala Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp Asp
210 215 220
Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Gln Ser Tyr Pro Leu Thr Phe
225 230 235 240
Gly Gly Gly Thr Lys Val Asp Ile Lys
245
<210> 1538
<211> 493
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1538
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Arg Ala Pro Gly Ala Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Phe
35 40 45
Thr Phe Arg Gly Tyr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Ile Ile Asn Pro Ser Gly Gly Ser Arg Ala
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Thr Ser Thr Val Tyr Met Glu Leu Ser Ser Leu Arg Ser Asp Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Arg Thr Ala Ser Cys Gly Gly Asp Cys Tyr
115 120 125
Tyr Leu Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Pro Thr Leu Ser Ala
165 170 175
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Val
180 185 190
Asn Ile Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys
195 200 205
Leu Leu Ile Tyr Lys Ser Ser Ser Leu Ala Ser Gly Val Pro Ser Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Ala Glu Phe Thr Leu Thr Ile Ser Ser
225 230 235 240
Leu Gln Pro Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Gln Ser
245 250 255
Tyr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Asp Ile Lys Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1539
<211> 244
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1539
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Asn Ser Gly Ser Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Gly Ser Ser Ser Trp Ser Trp Gly Tyr Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Ser Glu Leu Thr Gln Asp
130 135 140
Pro Ala Val Ser Val Ala Leu Gly Gln Thr Val Arg Thr Thr Cys Gln
145 150 155 160
Gly Asp Ala Leu Arg Ser Tyr Tyr Ala Ser Trp Tyr Gln Gln Lys Pro
165 170 175
Gly Gln Ala Pro Met Leu Val Ile Tyr Gly Lys Asn Asn Arg Pro Ser
180 185 190
Gly Ile Pro Asp Arg Phe Ser Gly Ser Asp Ser Gly Asp Thr Ala Ser
195 200 205
Leu Thr Ile Thr Gly Ala Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys
210 215 220
Asn Ser Arg Asp Ser Ser Gly Tyr Pro Val Phe Gly Thr Gly Thr Lys
225 230 235 240
Val Thr Val Leu
<210> 1540
<211> 488
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1540
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Asp Asp Tyr Ala Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Ser Trp Asn Ser Gly Ser Ile Gly
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Asp Gly Ser Ser Ser Trp Ser Trp Gly
115 120 125
Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Ser
145 150 155 160
Glu Leu Thr Gln Asp Pro Ala Val Ser Val Ala Leu Gly Gln Thr Val
165 170 175
Arg Thr Thr Cys Gln Gly Asp Ala Leu Arg Ser Tyr Tyr Ala Ser Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Gln Ala Pro Met Leu Val Ile Tyr Gly Lys
195 200 205
Asn Asn Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser Gly Ser Asp Ser
210 215 220
Gly Asp Thr Ala Ser Leu Thr Ile Thr Gly Ala Gln Ala Glu Asp Glu
225 230 235 240
Ala Asp Tyr Tyr Cys Asn Ser Arg Asp Ser Ser Gly Tyr Pro Val Phe
245 250 255
Gly Thr Gly Thr Lys Val Thr Val Leu Thr Thr Thr Pro Ala Pro Arg
260 265 270
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
275 280 285
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
290 295 300
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
305 310 315 320
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg
325 330 335
Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro
340 345 350
Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu
355 360 365
Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala
370 375 380
Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
385 390 395 400
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
405 410 415
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
420 425 430
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
435 440 445
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
450 455 460
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
465 470 475 480
His Met Gln Ala Leu Pro Pro Arg
485
<210> 1541
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1541
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Asn Ser Gly Ser Thr Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Asp Ser Ser Ser Trp Tyr Gly Gly Gly Ser Ala Phe Asp Ile
100 105 110
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Ser Glu Leu Thr Gln
130 135 140
Glu Pro Ala Val Ser Val Ala Leu Gly Gln Thr Val Arg Ile Thr Cys
145 150 155 160
Gln Gly Asp Ser Leu Arg Ser Tyr Tyr Ala Ser Trp Tyr Gln Gln Lys
165 170 175
Pro Gly Gln Ala Pro Val Leu Val Ile Phe Gly Arg Ser Arg Arg Pro
180 185 190
Ser Gly Ile Pro Asp Arg Phe Ser Gly Ser Ser Ser Gly Asn Thr Ala
195 200 205
Ser Leu Ile Ile Thr Gly Ala Gln Ala Glu Asp Glu Ala Asp Tyr Tyr
210 215 220
Cys Asn Ser Arg Asp Asn Thr Ala Asn His Tyr Val Phe Gly Thr Gly
225 230 235 240
Thr Lys Leu Thr Val Leu
245
<210> 1542
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1542
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Asp Asp Tyr Ala Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Ser Trp Asn Ser Gly Ser Thr Gly
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Leu Tyr Tyr Cys Ala Lys Asp Ser Ser Ser Trp Tyr Gly Gly Gly
115 120 125
Ser Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser
145 150 155 160
Ser Glu Leu Thr Gln Glu Pro Ala Val Ser Val Ala Leu Gly Gln Thr
165 170 175
Val Arg Ile Thr Cys Gln Gly Asp Ser Leu Arg Ser Tyr Tyr Ala Ser
180 185 190
Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Phe Gly
195 200 205
Arg Ser Arg Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser Gly Ser Ser
210 215 220
Ser Gly Asn Thr Ala Ser Leu Ile Ile Thr Gly Ala Gln Ala Glu Asp
225 230 235 240
Glu Ala Asp Tyr Tyr Cys Asn Ser Arg Asp Asn Thr Ala Asn His Tyr
245 250 255
Val Phe Gly Thr Gly Thr Lys Leu Thr Val Leu Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1543
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1543
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Asn Ser Gly Ser Thr Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Asp Ser Ser Ser Trp Tyr Gly Gly Gly Ser Ala Phe Asp Ile
100 105 110
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Ser Glu Leu Thr Gln
130 135 140
Asp Pro Ala Val Ser Val Ala Leu Gly Gln Thr Val Arg Ile Thr Cys
145 150 155 160
Gln Gly Asp Ser Leu Arg Ser Tyr Tyr Ala Ser Trp Tyr Gln Gln Lys
165 170 175
Pro Gly Gln Ala Pro Val Leu Val Ile Tyr Gly Lys Asn Asn Arg Pro
180 185 190
Ser Gly Ile Pro Asp Arg Phe Ser Gly Ser Ser Ser Gly Asn Thr Ala
195 200 205
Ser Leu Thr Ile Thr Gly Ala Gln Ala Glu Asp Glu Ala Asp Tyr Tyr
210 215 220
Cys Asn Ser Arg Gly Ser Ser Gly Asn His Tyr Val Phe Gly Thr Gly
225 230 235 240
Thr Lys Val Thr Val Leu
245
<210> 1544
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1544
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Asp Asp Tyr Ala Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Ser Trp Asn Ser Gly Ser Thr Gly
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Leu Tyr Tyr Cys Ala Lys Asp Ser Ser Ser Trp Tyr Gly Gly Gly
115 120 125
Ser Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser
145 150 155 160
Ser Glu Leu Thr Gln Asp Pro Ala Val Ser Val Ala Leu Gly Gln Thr
165 170 175
Val Arg Ile Thr Cys Gln Gly Asp Ser Leu Arg Ser Tyr Tyr Ala Ser
180 185 190
Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr Gly
195 200 205
Lys Asn Asn Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser Gly Ser Ser
210 215 220
Ser Gly Asn Thr Ala Ser Leu Thr Ile Thr Gly Ala Gln Ala Glu Asp
225 230 235 240
Glu Ala Asp Tyr Tyr Cys Asn Ser Arg Gly Ser Ser Gly Asn His Tyr
245 250 255
Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1545
<211> 251
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1545
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Val Trp Val
35 40 45
Ser Arg Ile Asn Ser Asp Gly Ser Ser Thr Ser Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Arg Thr Gly Trp Val Gly Ser Tyr Tyr Tyr Tyr Met Asp Val Trp
100 105 110
Gly Lys Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile
130 135 140
Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg
145 150 155 160
Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Asn Tyr Leu
165 170 175
Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Arg Leu Leu Ile Tyr
180 185 190
Asp Val Ser Thr Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly Gly
195 200 205
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu
210 215 220
Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Pro Trp
225 230 235 240
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
245 250
<210> 1546
<211> 495
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1546
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Trp Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Val Trp Val Ser Arg Ile Asn Ser Asp Gly Ser Ser Thr Ser
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Val Arg Thr Gly Trp Val Gly Ser Tyr Tyr Tyr
115 120 125
Tyr Met Asp Val Trp Gly Lys Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu
165 170 175
Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val
180 185 190
Ser Ser Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
195 200 205
Arg Leu Leu Ile Tyr Asp Val Ser Thr Arg Ala Thr Gly Ile Pro Ala
210 215 220
Arg Phe Ser Gly Gly Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
225 230 235 240
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser
245 250 255
Asn Trp Pro Pro Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
260 265 270
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
275 280 285
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
290 295 300
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
305 310 315 320
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
325 330 335
Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
340 345 350
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
355 360 365
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
370 375 380
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln
385 390 395 400
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
405 410 415
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
420 425 430
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
435 440 445
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
450 455 460
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
465 470 475 480
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 1547
<211> 250
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1547
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Val Val Gln Pro Gly Arg
5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Gly Tyr Ser Arg Tyr Tyr Tyr Tyr Gly Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val
130 135 140
Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala
145 150 155 160
Ile Leu Ser Cys Arg Ala Ser Gln Ser Val Tyr Thr Lys Tyr Leu Gly
165 170 175
Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Asp
180 185 190
Ala Ser Thr Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Arg Leu Glu Pro Glu Asp
210 215 220
Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Gly Ser Pro Leu Ile Thr
225 230 235 240
Phe Gly Gln Gly Thr Lys Val Asp Ile Lys
245 250
<210> 1548
<211> 494
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1548
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Gly Gly Val
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Gly Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Gly Tyr Ser Arg Tyr Tyr Tyr Tyr Gly
115 120 125
Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser
165 170 175
Pro Gly Glu Arg Ala Ile Leu Ser Cys Arg Ala Ser Gln Ser Val Tyr
180 185 190
Thr Lys Tyr Leu Gly Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg
195 200 205
Leu Leu Ile Tyr Asp Ala Ser Thr Arg Ala Thr Gly Ile Pro Asp Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Arg
225 230 235 240
Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Gly
245 250 255
Ser Pro Leu Ile Thr Phe Gly Gln Gly Thr Lys Val Asp Ile Lys Thr
260 265 270
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
275 280 285
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
290 295 300
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
305 310 315 320
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
325 330 335
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
340 345 350
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
355 360 365
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
370 375 380
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn
385 390 395 400
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
405 410 415
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
420 425 430
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
435 440 445
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
450 455 460
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
465 470 475 480
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1549
<211> 249
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1549
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Arg Glu Ala Ala Ala Gly His Asp Trp Tyr Phe Asp Leu Trp
100 105 110
Gly Arg Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Arg Val Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn
165 170 175
Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala
180 185 190
Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
210 215 220
Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Ile Pro Leu Thr Phe
225 230 235 240
Gly Gln Gly Thr Lys Val Glu Ile Lys
245
<210> 1550
<211> 493
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1550
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Arg Glu Ala Ala Ala Gly His Asp Trp
115 120 125
Tyr Phe Asp Leu Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Arg Val Thr Gln Ser Pro Ser Ser Leu Ser Ala
165 170 175
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile
180 185 190
Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys
195 200 205
Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser
225 230 235 240
Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser
245 250 255
Ile Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1551
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1551
Gln Val Gln Leu Val Gln Ser Trp Ala Glu Val Lys Lys Pro Gly Ala
5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Asn Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Pro Arg Val Thr Thr Gly Tyr Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Leu
130 135 140
Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp Arg Val Thr
145 150 155 160
Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Lys Ala Ser
180 185 190
Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp Asp Phe Ala
210 215 220
Thr Tyr Tyr Cys Gln Gln Tyr Ser Ser Tyr Pro Leu Thr Phe Gly Gly
225 230 235 240
Gly Thr Arg Leu Glu Ile Lys
245
<210> 1552
<211> 491
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1552
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Trp Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Thr Ser Thr Val Tyr Met Glu Leu Ser Asn Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Ser Pro Arg Val Thr Thr Gly Tyr Phe
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val
165 170 175
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser
180 185 190
Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
195 200 205
Ile Tyr Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln
225 230 235 240
Pro Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Ser Ser Tyr Pro
245 250 255
Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1553
<211> 253
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1553
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Arg Arg Pro Gly Ala
5 10 15
Ser Val Lys Ile Ser Cys Arg Ala Ser Gly Asp Thr Ser Thr Arg His
20 25 30
Tyr Ile His Trp Leu Arg Gln Ala Pro Gly Gln Gly Pro Glu Trp Met
35 40 45
Gly Val Ile Asn Pro Thr Thr Gly Pro Ala Thr Gly Ser Pro Ala Tyr
50 55 60
Ala Gln Met Leu Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr
65 70 75 80
Arg Thr Val Tyr Met Glu Leu Arg Ser Leu Arg Phe Glu Asp Thr Ala
85 90 95
Val Tyr Tyr Cys Ala Arg Ser Val Val Gly Arg Ser Ala Pro Tyr Tyr
100 105 110
Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
145 150 155 160
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser
165 170 175
Asp Tyr Ser Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu
180 185 190
Leu Ile Tyr Ala Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe
195 200 205
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Tyr Leu
210 215 220
Gln Ser Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ser Tyr
225 230 235 240
Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Asp Ile Lys
245 250
<210> 1554
<211> 497
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1554
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Arg Arg Pro Gly Ala Ser Val Lys Ile Ser Cys Arg Ala Ser Gly Asp
35 40 45
Thr Ser Thr Arg His Tyr Ile His Trp Leu Arg Gln Ala Pro Gly Gln
50 55 60
Gly Pro Glu Trp Met Gly Val Ile Asn Pro Thr Thr Gly Pro Ala Thr
65 70 75 80
Gly Ser Pro Ala Tyr Ala Gln Met Leu Gln Gly Arg Val Thr Met Thr
85 90 95
Arg Asp Thr Ser Thr Arg Thr Val Tyr Met Glu Leu Arg Ser Leu Arg
100 105 110
Phe Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Val Val Gly Arg
115 120 125
Ser Ala Pro Tyr Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
130 135 140
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser
165 170 175
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
180 185 190
Ser Gln Gly Ile Ser Asp Tyr Ser Ala Trp Tyr Gln Gln Lys Pro Gly
195 200 205
Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Thr Leu Gln Ser Gly
210 215 220
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
225 230 235 240
Thr Ile Ser Tyr Leu Gln Ser Glu Asp Phe Ala Thr Tyr Tyr Cys Gln
245 250 255
Gln Tyr Tyr Ser Tyr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Asp
260 265 270
Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
275 280 285
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
290 295 300
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
305 310 315 320
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
325 330 335
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
340 345 350
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
355 360 365
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
370 375 380
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln
385 390 395 400
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
405 410 415
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
420 425 430
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
435 440 445
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
450 455 460
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
465 470 475 480
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
485 490 495
Arg
<210> 1555
<211> 249
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1555
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Tyr Thr Thr Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Leu Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ile Arg Ser Cys Gly Gly Asp Cys Tyr Tyr Phe Asp Asn Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Leu Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp Arg
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Val Asn Ile Trp Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Lys
180 185 190
Ser Ser Ser Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Ala Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp Asp
210 215 220
Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Gln Ser Tyr Pro Leu Thr Phe
225 230 235 240
Gly Gly Gly Thr Lys Val Asp Ile Lys
245
<210> 1556
<211> 493
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1556
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Asn Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Ile Ile Asn Pro Ser Gly Gly Tyr Thr Thr
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Leu Thr Met Thr Arg Asp Thr Ser
85 90 95
Thr Ser Thr Val Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Ile Arg Ser Cys Gly Gly Asp Cys Tyr
115 120 125
Tyr Phe Asp Asn Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Thr Leu Ser Ala
165 170 175
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Val
180 185 190
Asn Ile Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys
195 200 205
Leu Leu Ile Tyr Lys Ser Ser Ser Leu Ala Ser Gly Val Pro Ser Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Ala Glu Phe Thr Leu Thr Ile Ser Ser
225 230 235 240
Leu Gln Pro Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Gln Ser
245 250 255
Tyr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Asp Ile Lys Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1557
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1557
Gln Ile Thr Leu Lys Glu Ser Gly Pro Ala Leu Val Lys Pro Thr Gln
5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Ser Thr Ala
20 25 30
Gly Val His Val Gly Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu
35 40 45
Trp Leu Ala Leu Ile Ser Trp Ala Asp Asp Lys Arg Tyr Arg Pro Ser
50 55 60
Leu Arg Ser Arg Leu Asp Ile Thr Arg Val Thr Ser Lys Asp Gln Val
65 70 75 80
Val Leu Ser Met Thr Asn Met Gln Pro Glu Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Ala Leu Gln Gly Phe Asp Gly Tyr Glu Ala Asn Trp Gly Pro Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr
130 135 140
Gln Ser Pro Ser Ser Leu Ser Ala Ser Ala Gly Asp Arg Val Thr Ile
145 150 155 160
Thr Cys Arg Ala Ser Arg Gly Ile Ser Ser Ala Leu Ala Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Lys Pro Pro Lys Leu Leu Ile Tyr Asp Ala Ser Ser
180 185 190
Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Thr Ile Asp Ser Leu Glu Pro Glu Asp Phe Ala Thr
210 215 220
Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Trp Thr Phe Gly Gln Gly
225 230 235 240
Thr Lys Val Asp Ile Lys
245
<210> 1558
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1558
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Ile Thr Leu Lys Glu Ser Gly Pro Ala Leu
20 25 30
Val Lys Pro Thr Gln Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe
35 40 45
Ser Leu Ser Thr Ala Gly Val His Val Gly Trp Ile Arg Gln Pro Pro
50 55 60
Gly Lys Ala Leu Glu Trp Leu Ala Leu Ile Ser Trp Ala Asp Asp Lys
65 70 75 80
Arg Tyr Arg Pro Ser Leu Arg Ser Arg Leu Asp Ile Thr Arg Val Thr
85 90 95
Ser Lys Asp Gln Val Val Leu Ser Met Thr Asn Met Gln Pro Glu Asp
100 105 110
Thr Ala Thr Tyr Tyr Cys Ala Leu Gln Gly Phe Asp Gly Tyr Glu Ala
115 120 125
Asn Trp Gly Pro Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Ala Gly
165 170 175
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Arg Gly Ile Ser Ser Ala
180 185 190
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Pro Pro Lys Leu Leu Ile
195 200 205
Tyr Asp Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asp Ser Leu Glu Pro
225 230 235 240
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Trp
245 250 255
Thr Phe Gly Gln Gly Thr Lys Val Asp Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 1559
<211> 239
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1559
Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Glu Lys Pro Gly Ala
5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Thr Met Asn Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Leu Ile Thr Pro Tyr Asn Gly Ala Ser Ser Tyr Asn Gln Lys Phe
50 55 60
Arg Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Asp Leu Leu Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Arg Gly Gly Tyr Asp Gly Arg Gly Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Asp Ile Glu Leu Thr Gln Ser Pro Ala Ile
130 135 140
Met Ser Ala Ser Pro Gly Glu Lys Val Thr Met Thr Cys Ser Ala Ser
145 150 155 160
Ser Ser Val Ser Tyr Met His Trp Tyr Gln Gln Lys Ser Gly Thr Ser
165 170 175
Pro Lys Arg Trp Ile Tyr Asp Thr Ser Lys Leu Ala Ser Gly Val Pro
180 185 190
Gly Arg Phe Ser Gly Ser Gly Ser Gly Asn Ser Tyr Ser Leu Thr Ile
195 200 205
Ser Ser Val Glu Ala Glu Asp Asp Ala Thr Tyr Tyr Cys Gln Gln Trp
210 215 220
Ser Gly Tyr Pro Leu Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile
225 230 235
<210> 1560
<211> 383
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1560
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Leu
20 25 30
Glu Lys Pro Gly Ala Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Ser Phe Thr Gly Tyr Thr Met Asn Trp Val Lys Gln Ser His Gly Lys
50 55 60
Ser Leu Glu Trp Ile Gly Leu Ile Thr Pro Tyr Asn Gly Ala Ser Ser
65 70 75 80
Tyr Asn Gln Lys Phe Arg Gly Lys Ala Thr Leu Thr Val Asp Lys Ser
85 90 95
Ser Ser Thr Ala Tyr Met Asp Leu Leu Ser Leu Thr Ser Glu Asp Ser
100 105 110
Ala Val Tyr Phe Cys Ala Arg Gly Gly Tyr Asp Gly Arg Gly Phe Asp
115 120 125
Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Glu Leu Thr
145 150 155 160
Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly Glu Lys Val Thr Met
165 170 175
Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Met His Trp Tyr Gln Gln
180 185 190
Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr Asp Thr Ser Lys Leu
195 200 205
Ala Ser Gly Val Pro Gly Arg Phe Ser Gly Ser Gly Ser Gly Asn Ser
210 215 220
Tyr Ser Leu Thr Ile Ser Ser Val Glu Ala Glu Asp Asp Ala Thr Tyr
225 230 235 240
Tyr Cys Gln Gln Trp Ser Gly Tyr Pro Leu Thr Phe Gly Ala Gly Thr
245 250 255
Lys Leu Glu Ile Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
260 265 270
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
275 280 285
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
290 295 300
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
305 310 315 320
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
325 330 335
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
340 345 350
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
355 360 365
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala
370 375 380
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СКОНСТРУИРОВАННЫЕ PH-ЗАВИСИМЫЕ АНТИТЕЛА К CD3, А ТАКЖЕ СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2020 |
|
RU2832079C2 |
| АНТАГОНИСТЫ NGF ДЛЯ МЕДИЦИНСКОГО ИСПОЛЬЗОВАНИЯ | 2020 |
|
RU2829812C2 |
| КОНСТРУКЦИИ СЛИТОГО БЕЛКА ДЛЯ ЗАБОЛЕВАНИЯ, СВЯЗАННОГО С КОМПЛЕМЕНТОМ | 2019 |
|
RU2824402C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, НАЦЕЛЕННЫЕ НА АНТИГЕН СОЗРЕВАНИЯ В-КЛЕТОК, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2829097C2 |
| АНТИТЕЛА К РЕЦЕПТОРУ IL4 ДЛЯ ПРИМЕНЕНИЯ В ВЕТЕРИНАРИИ | 2019 |
|
RU2837141C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, НАЦЕЛЕННЫЕ НА ПОДОБНЫЙ FC-РЕЦЕПТОРУ БЕЛОК 5, И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2779747C2 |
| ВАРИАНТЫ IgG-FC ДЛЯ ПРИМЕНЕНИЯ В ВЕТЕРИНАРИИ | 2018 |
|
RU2814952C2 |
| CD47-АНТИГЕНСВЯЗЫВАЮЩАЯ ЕДИНИЦА И ЕЕ ПРИМЕНЕНИЕ | 2018 |
|
RU2780859C2 |
| СЛИТЫЙ БЕЛОК GDF15 ДЛИТЕЛЬНОГО ДЕЙСТВИЯ И СОДЕРЖАЩАЯ ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2020 |
|
RU2836280C1 |
| ПОЛИВАЛЕНТНЫЕ И ПОЛИСПЕЦИФИЧЕСКИЕ ОХ40-СВЯЗЫВАЮЩИЕ СЛИТЫЕ БЕЛКИ | 2017 |
|
RU2773052C2 |

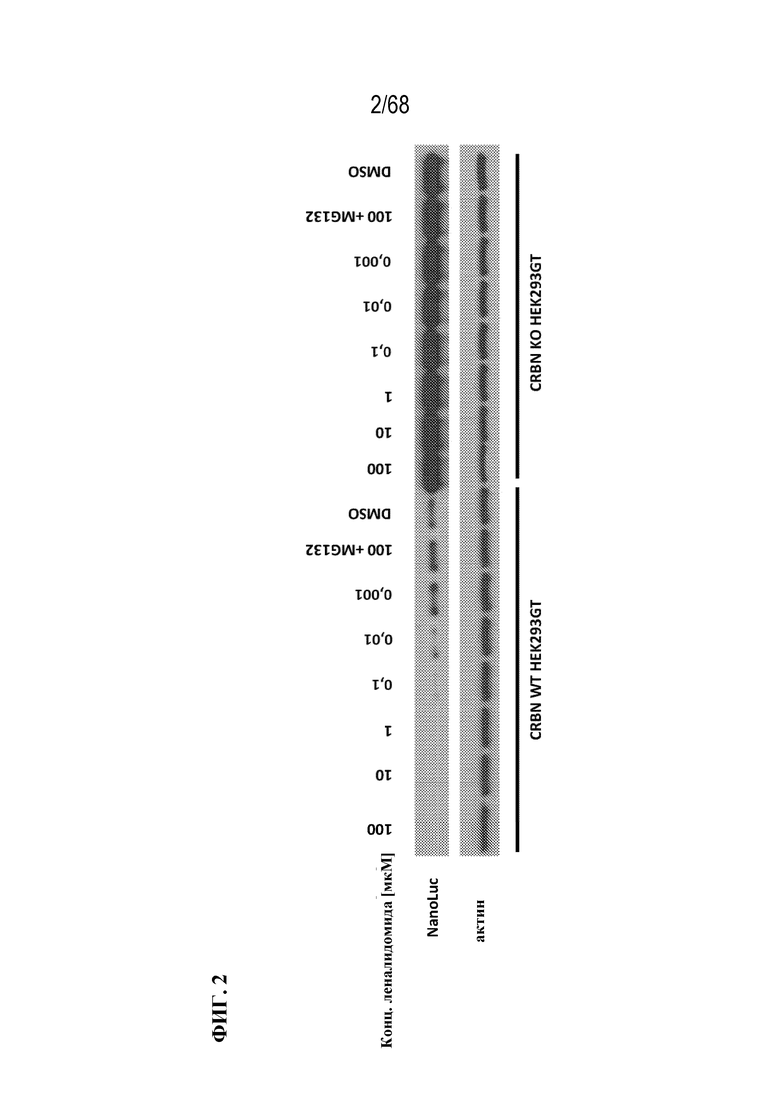
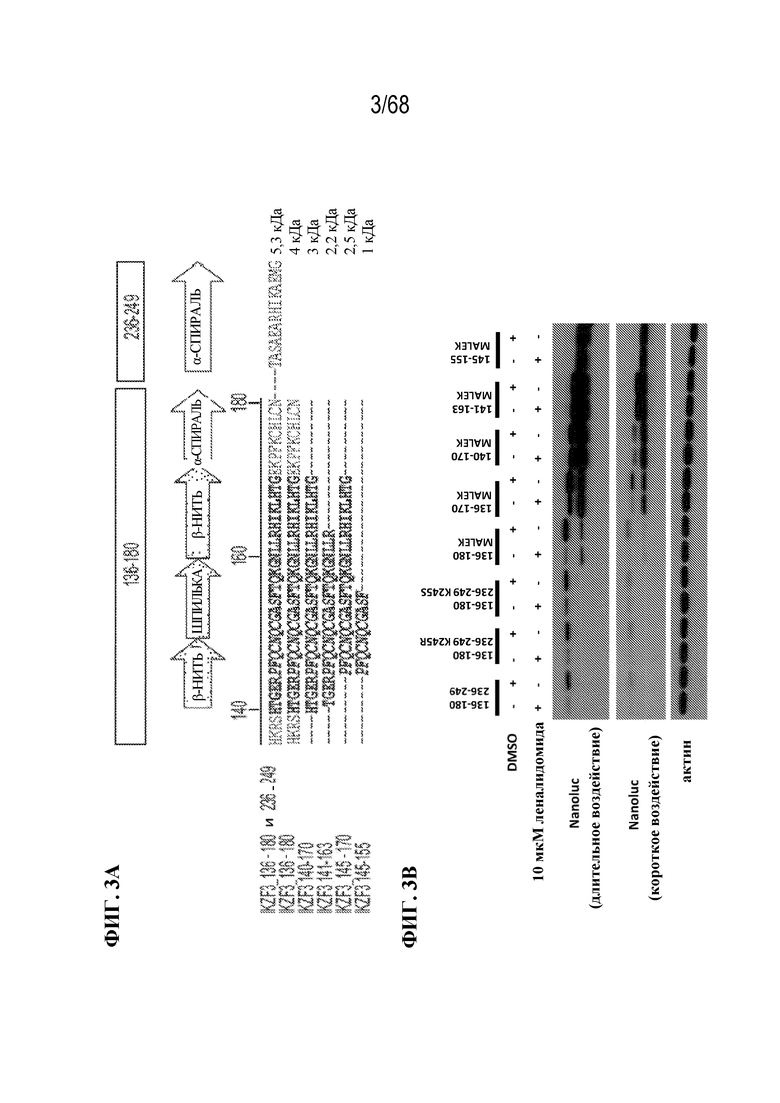

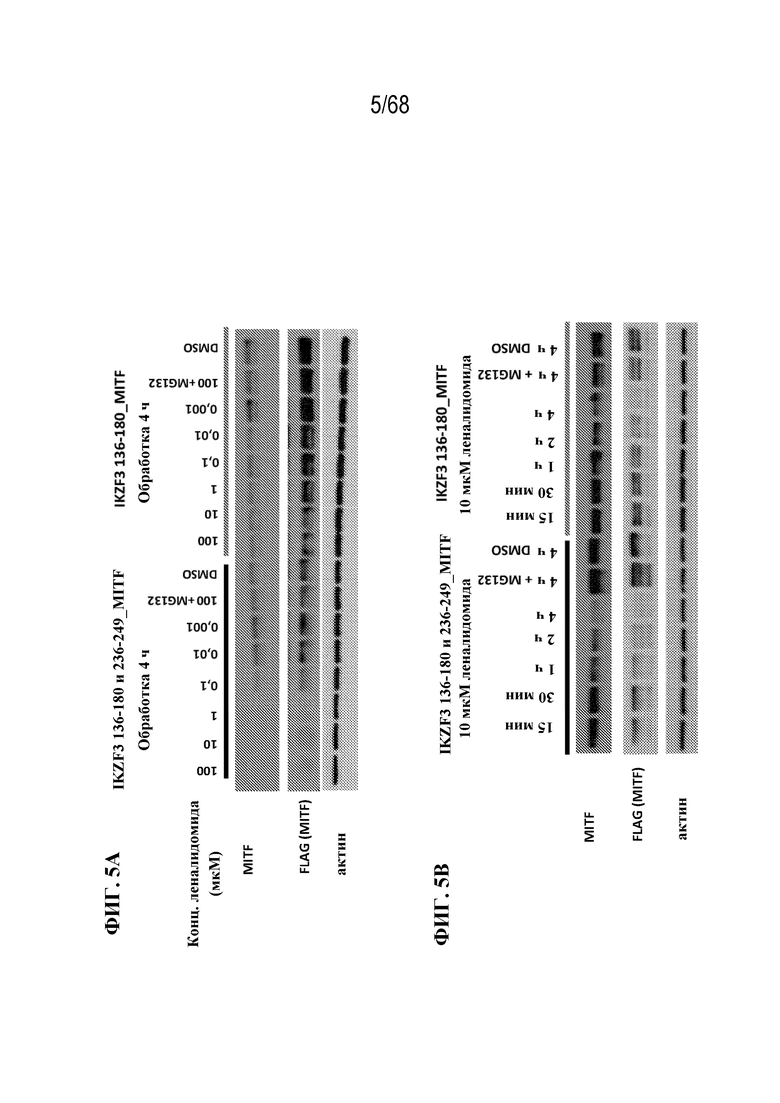
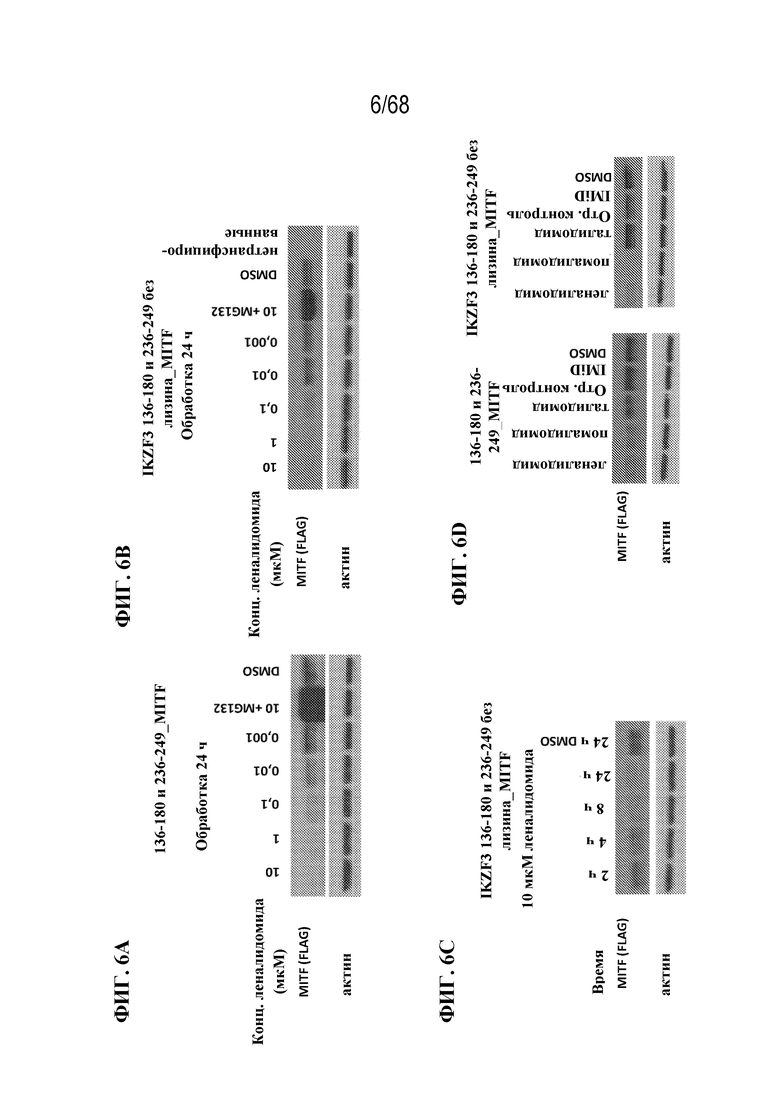

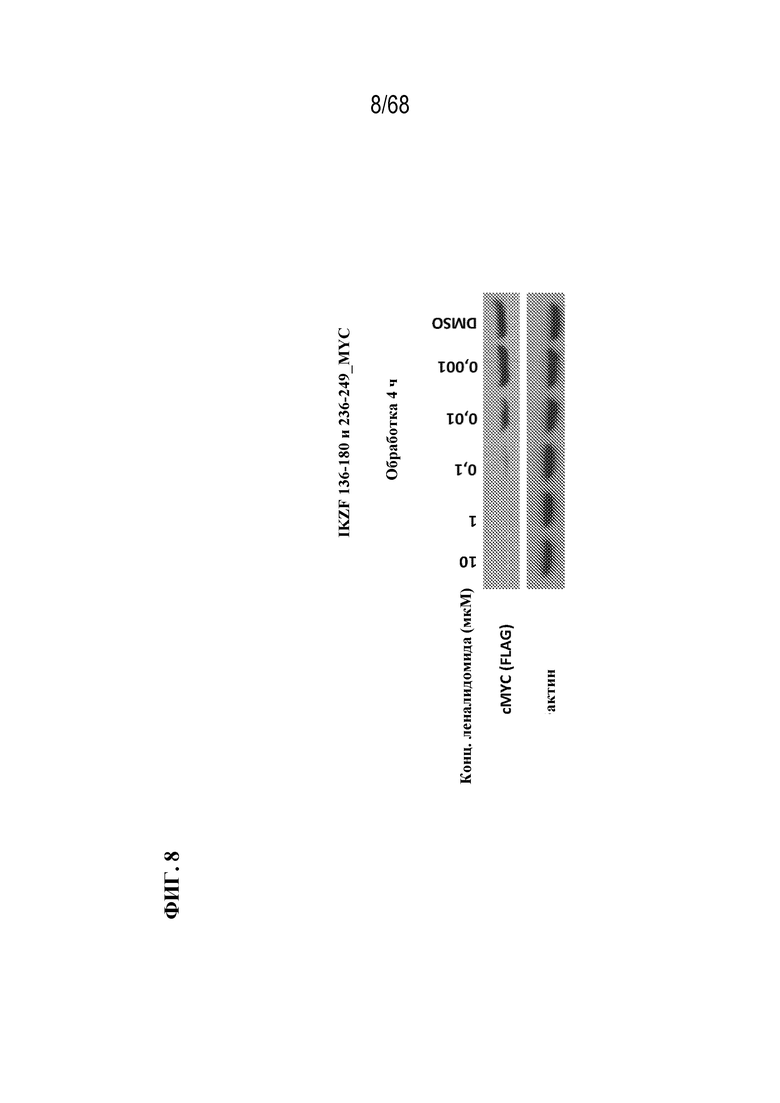

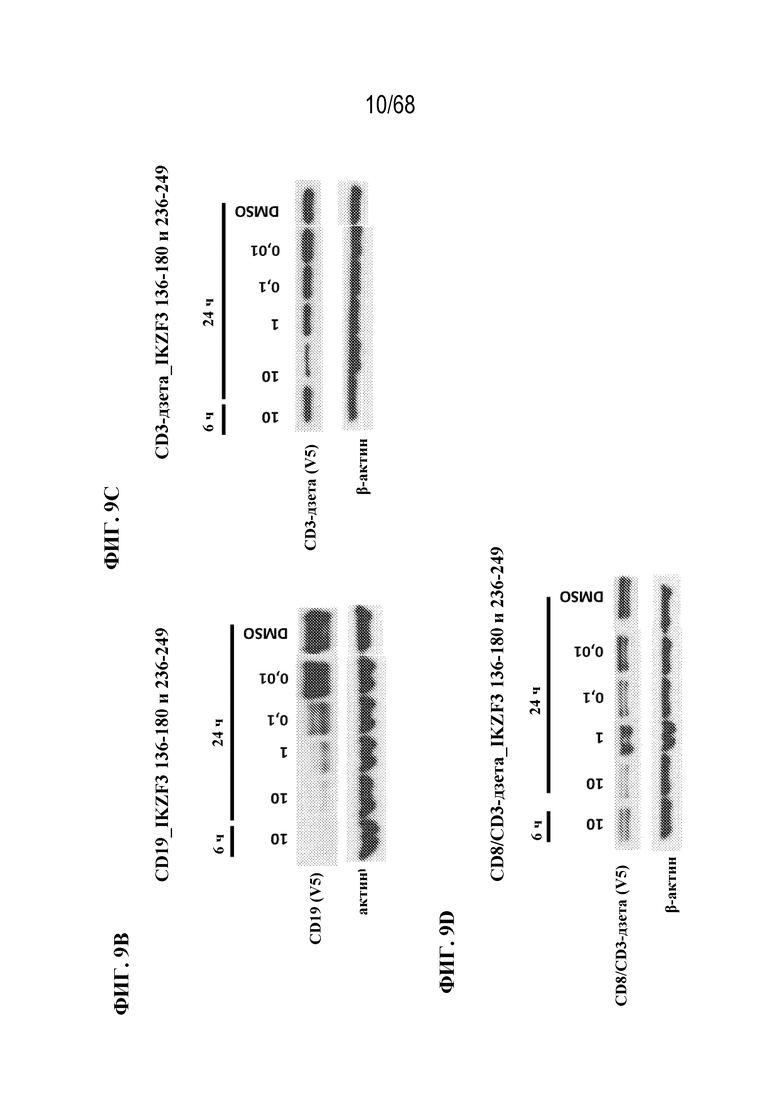
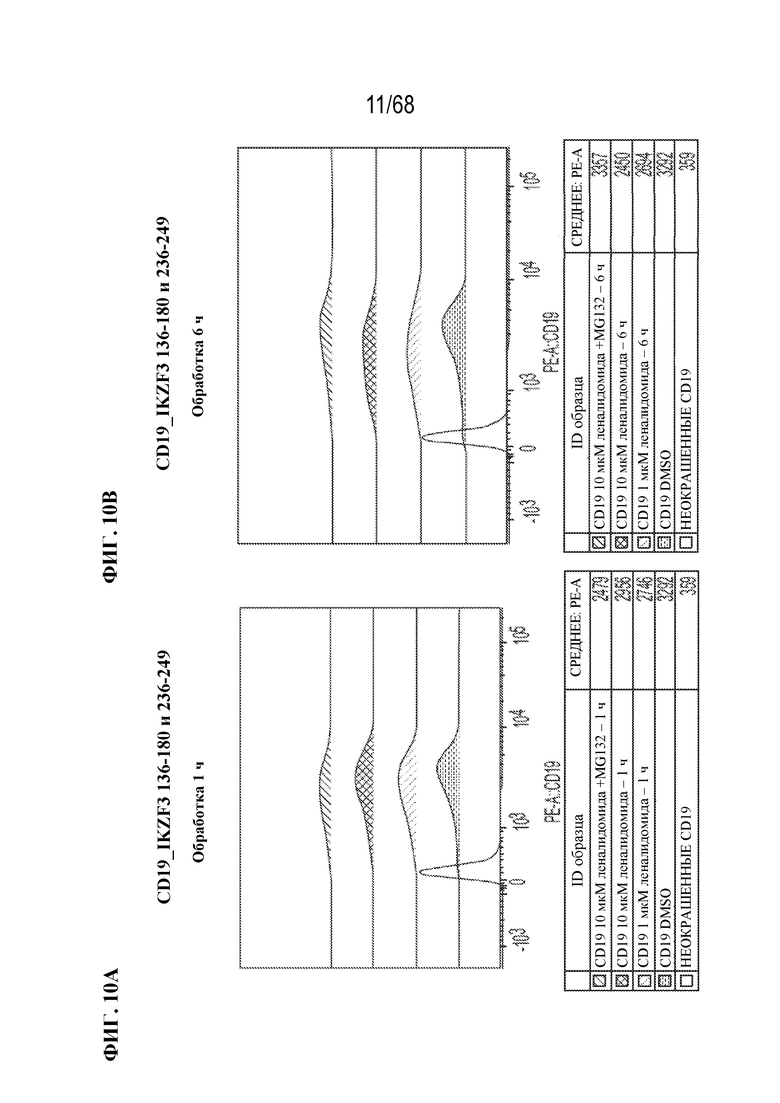


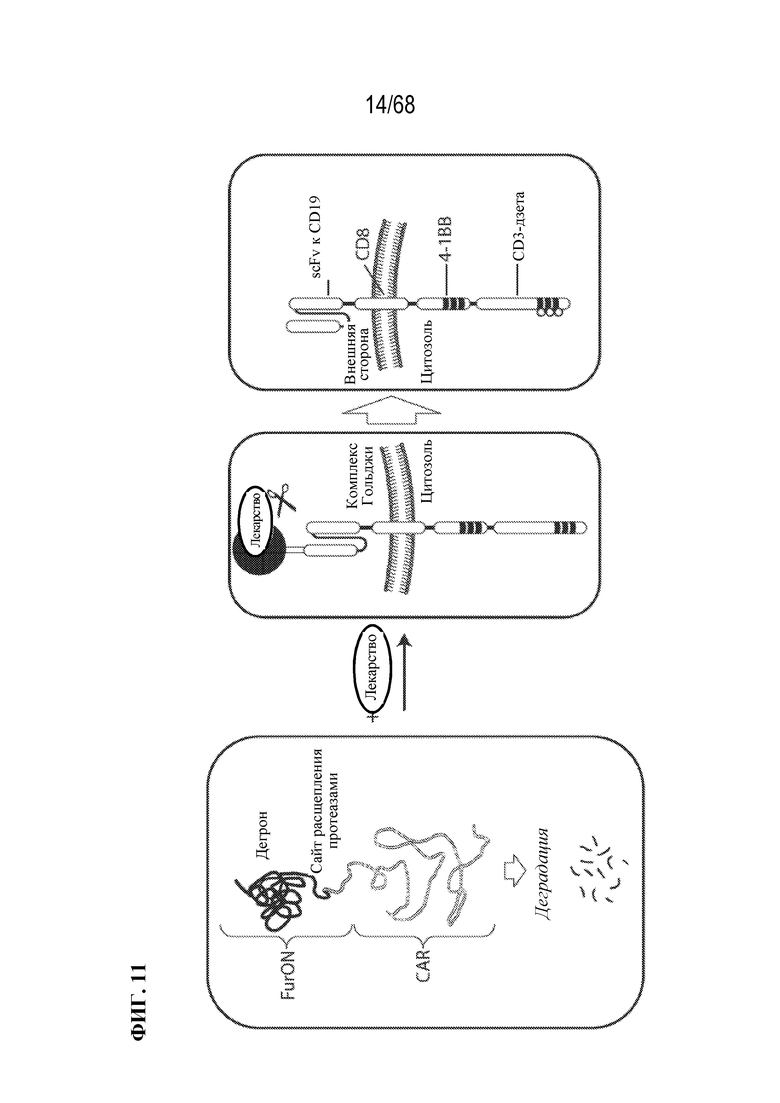
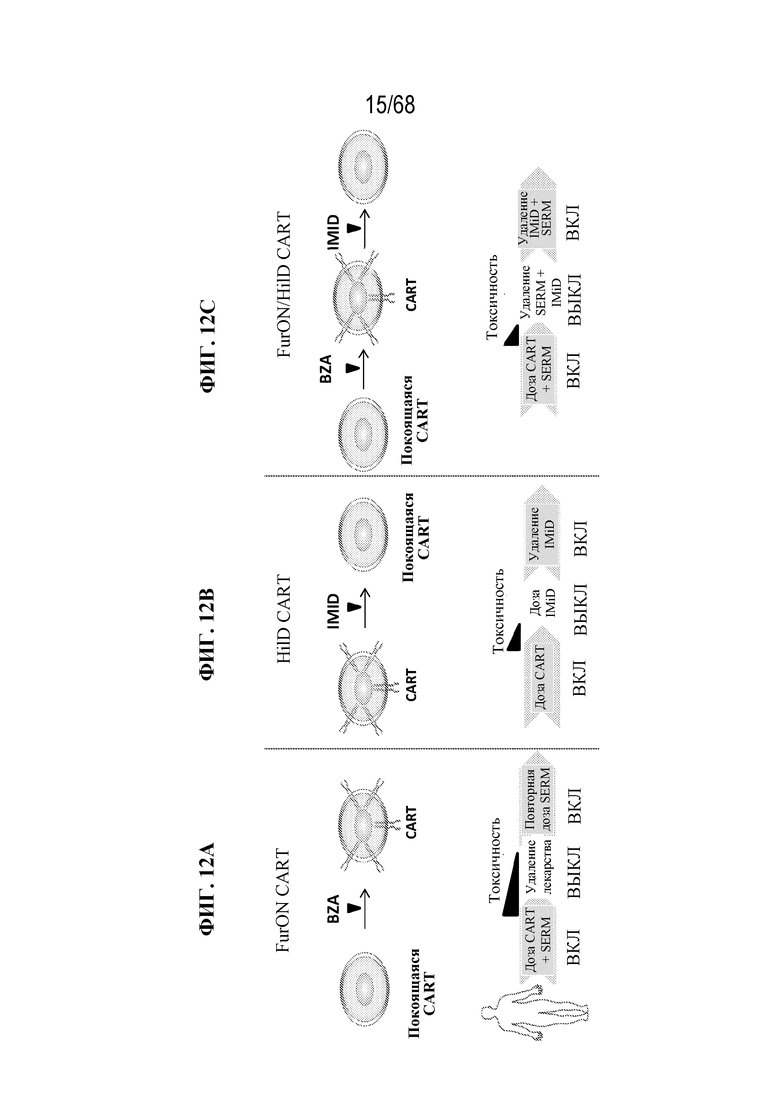
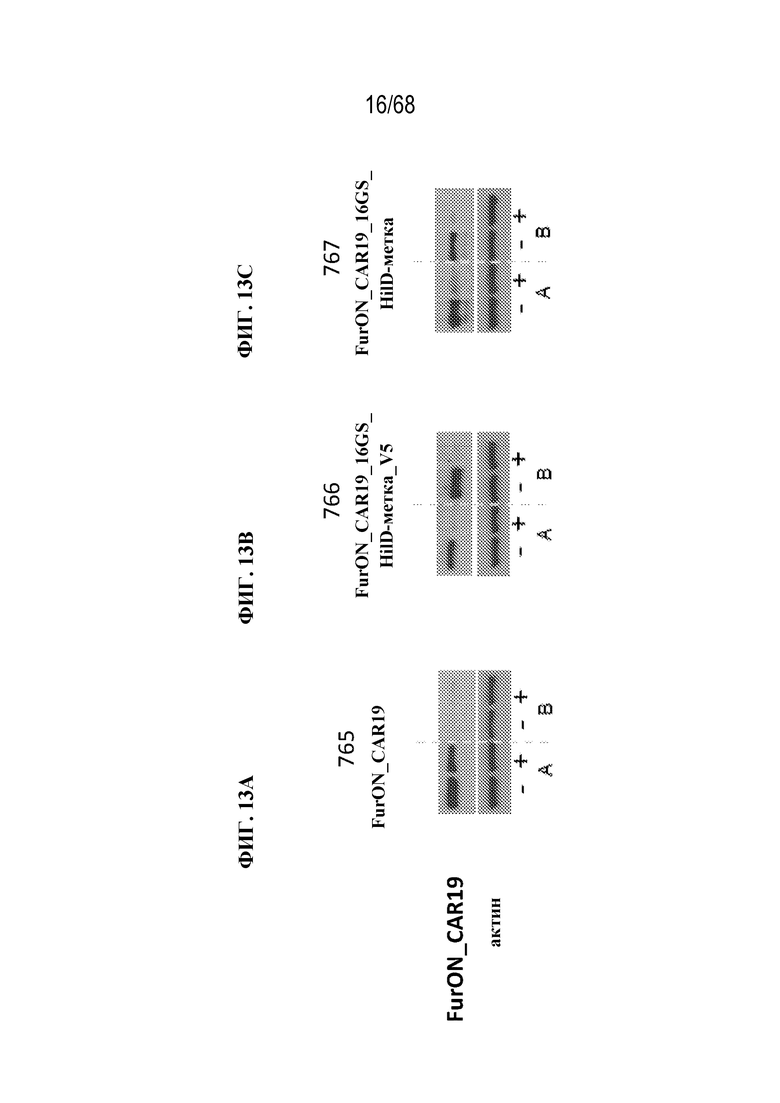
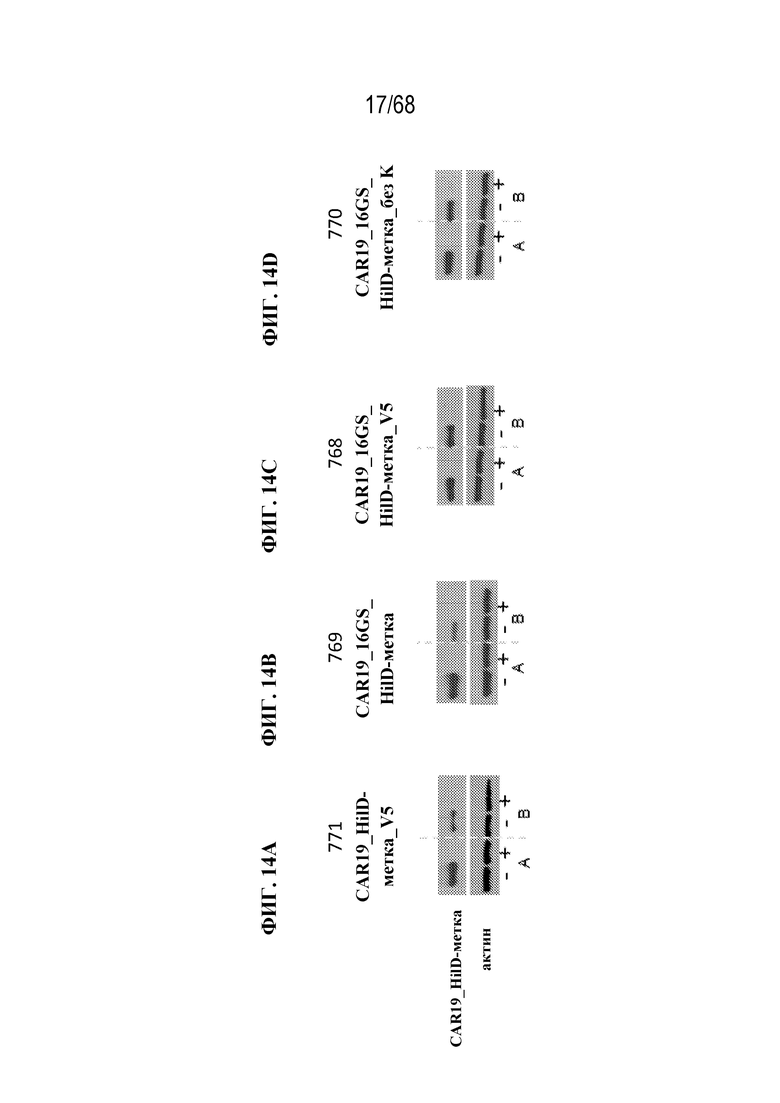




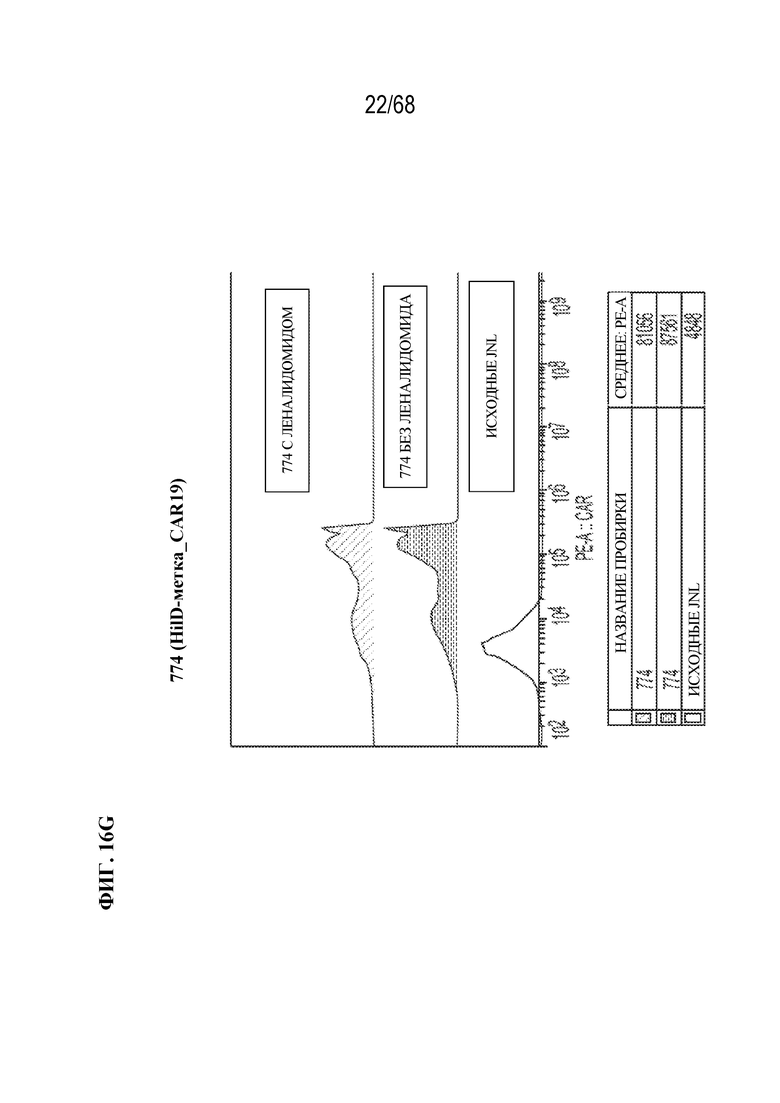


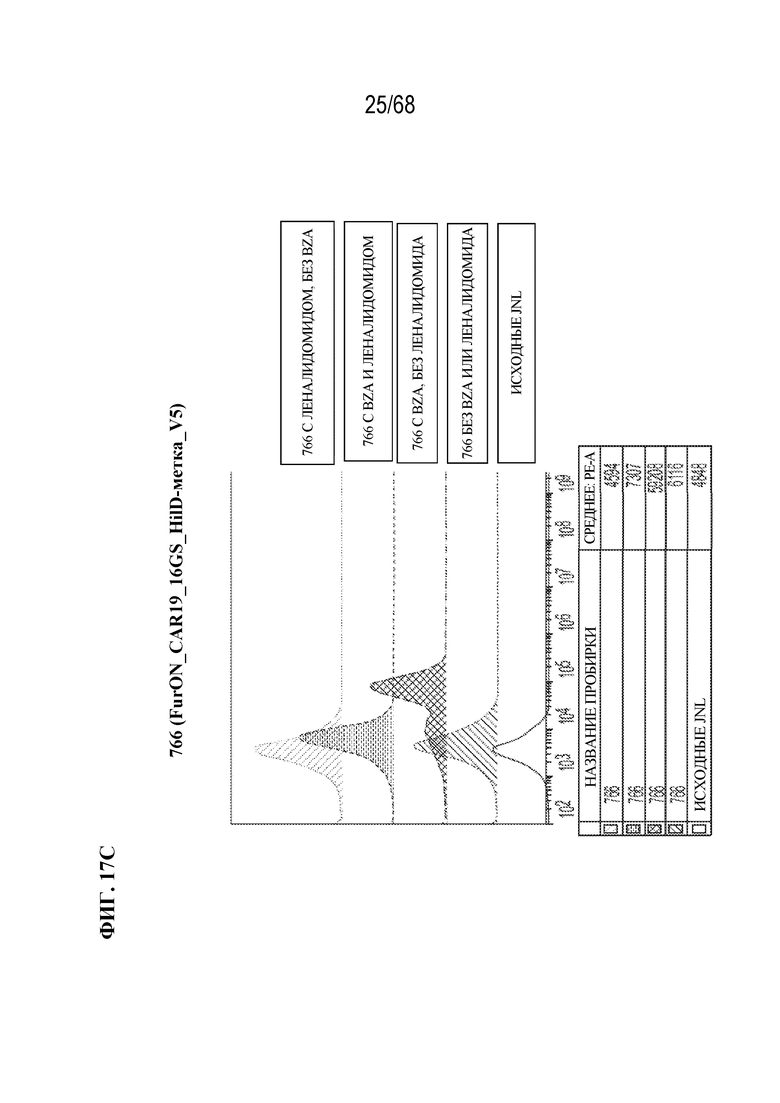
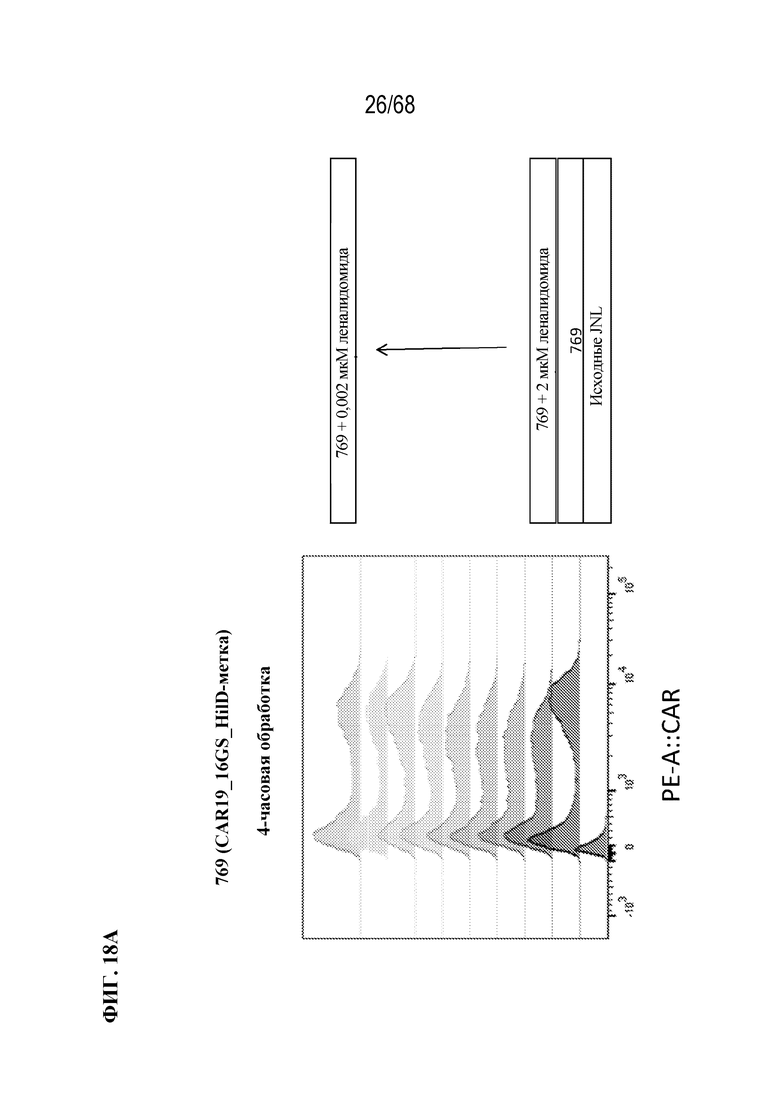
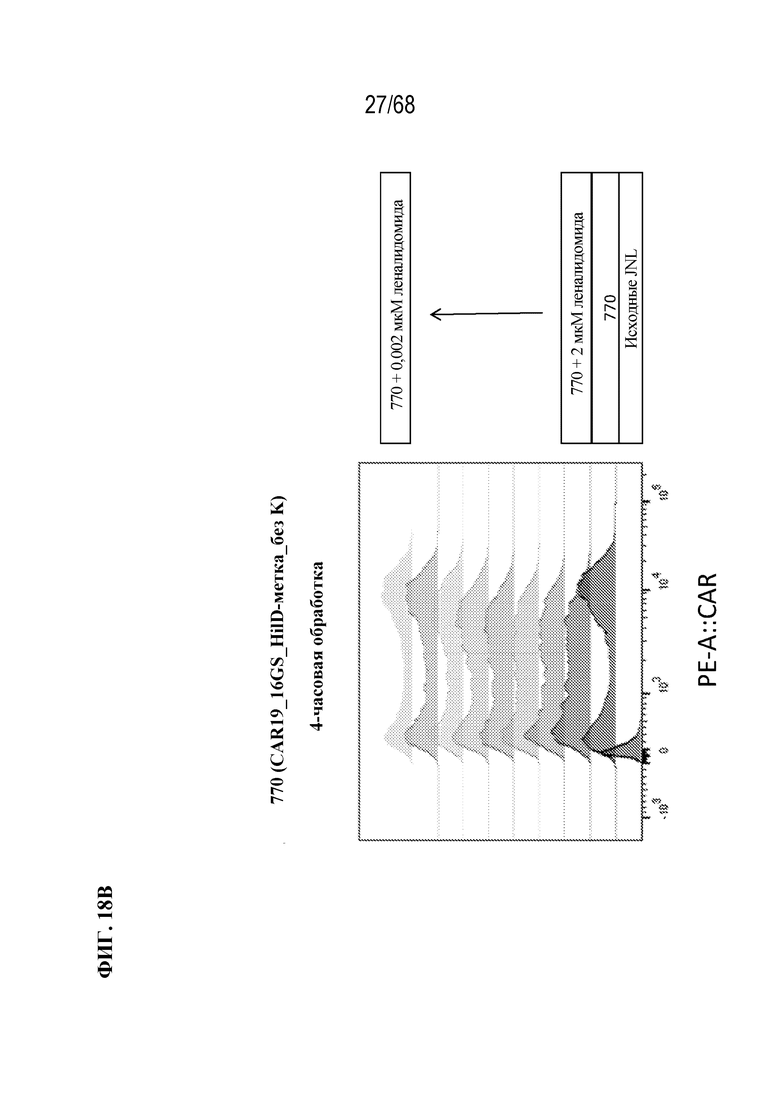
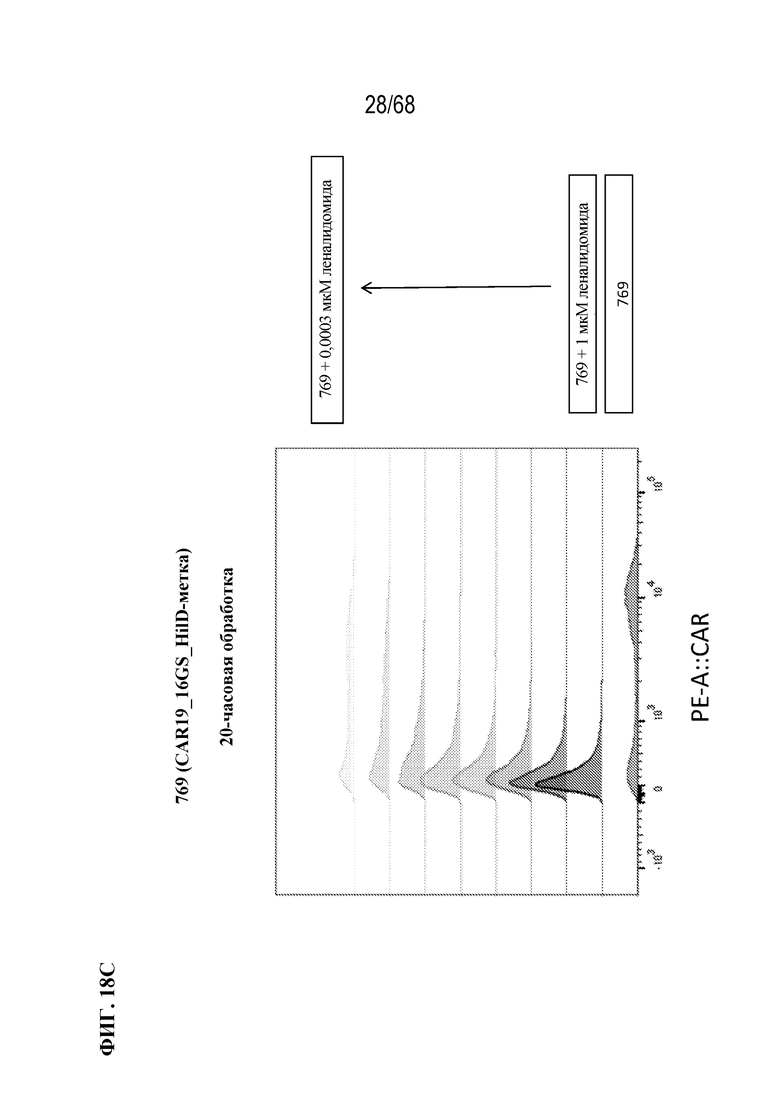

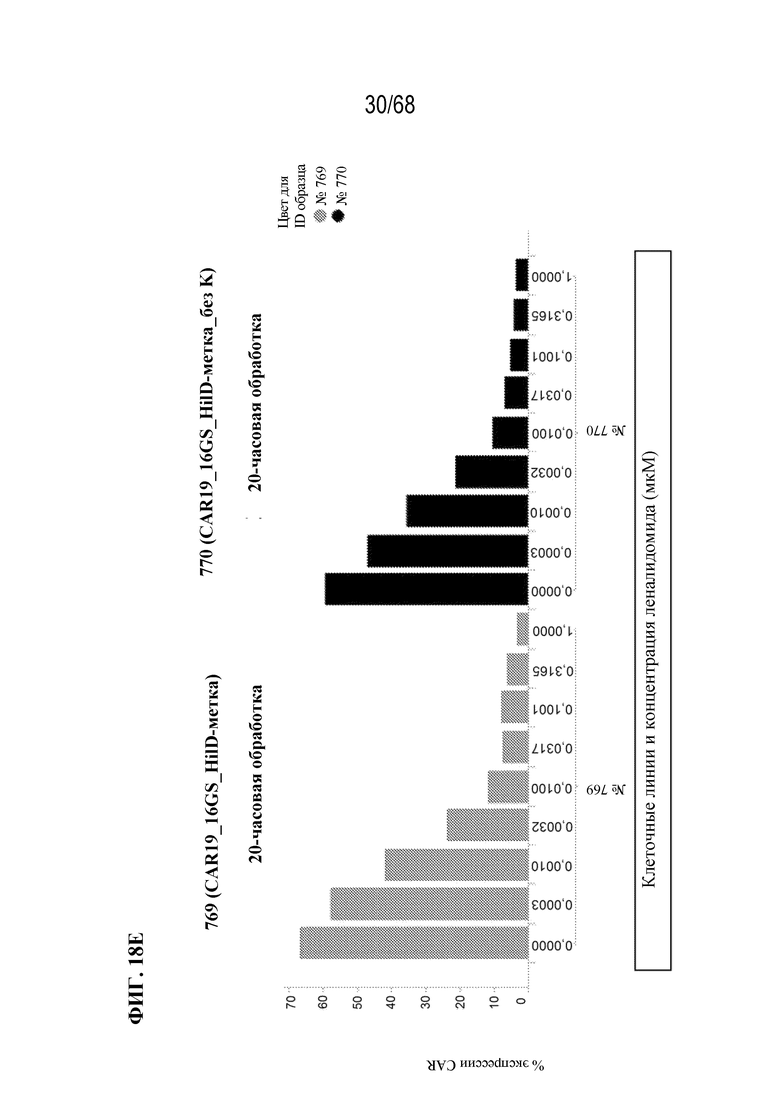
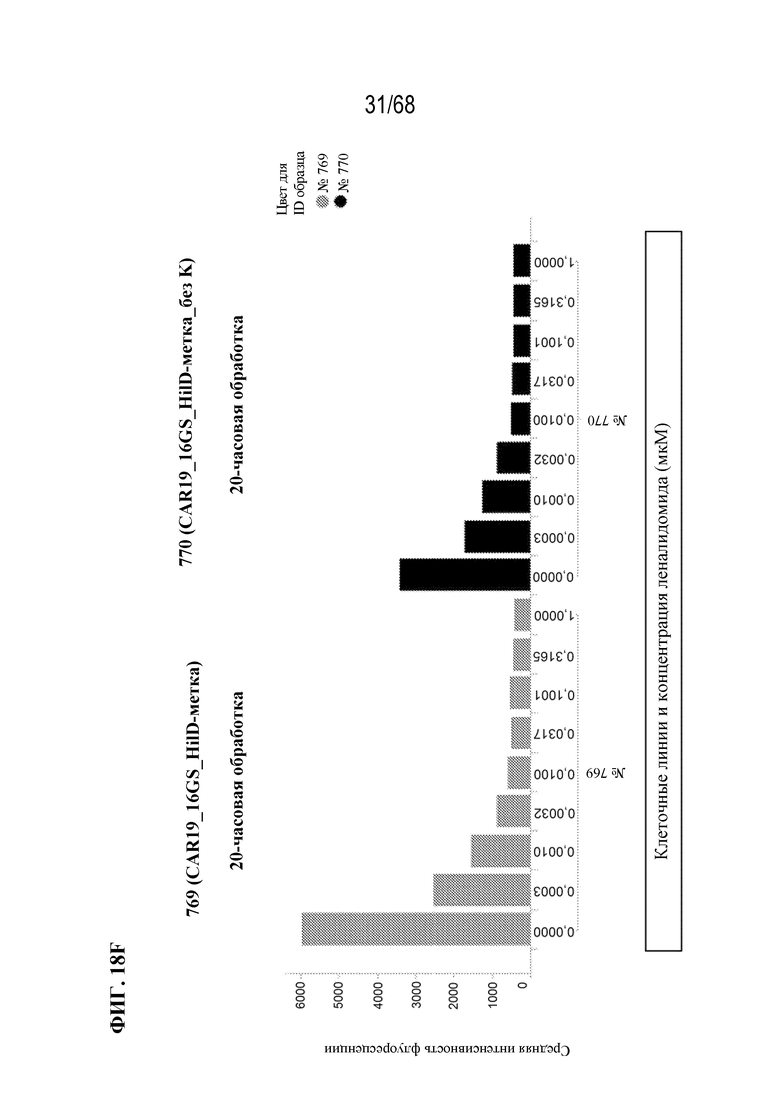
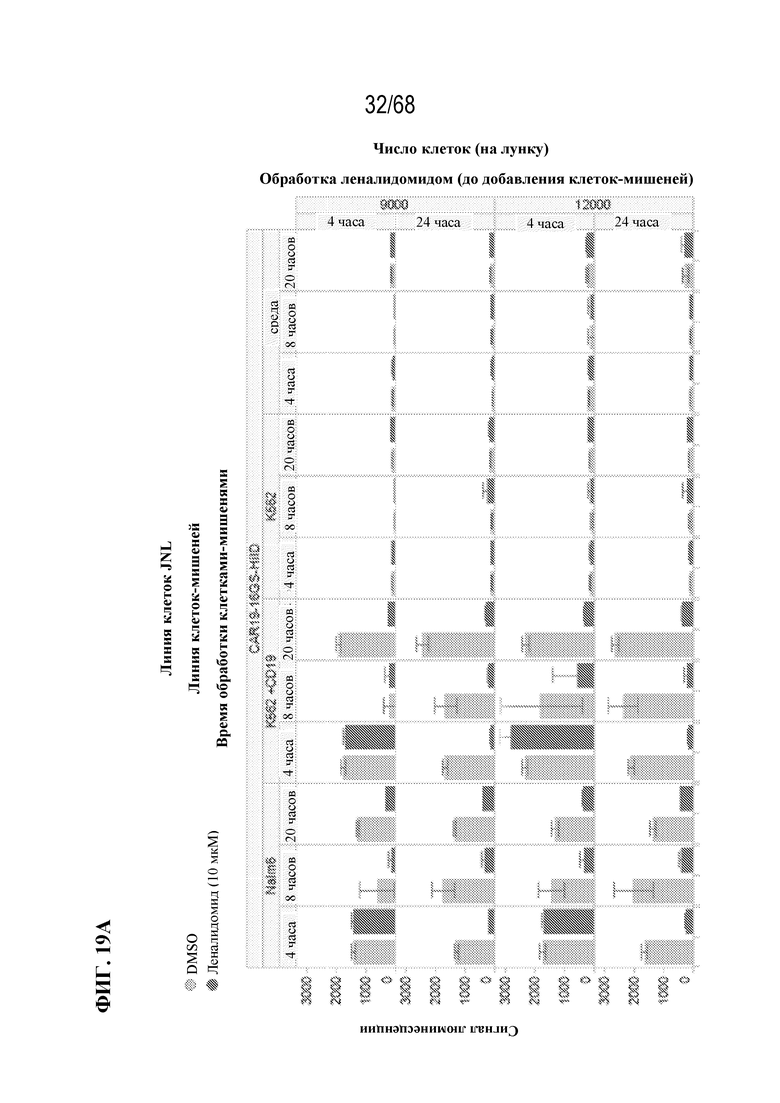




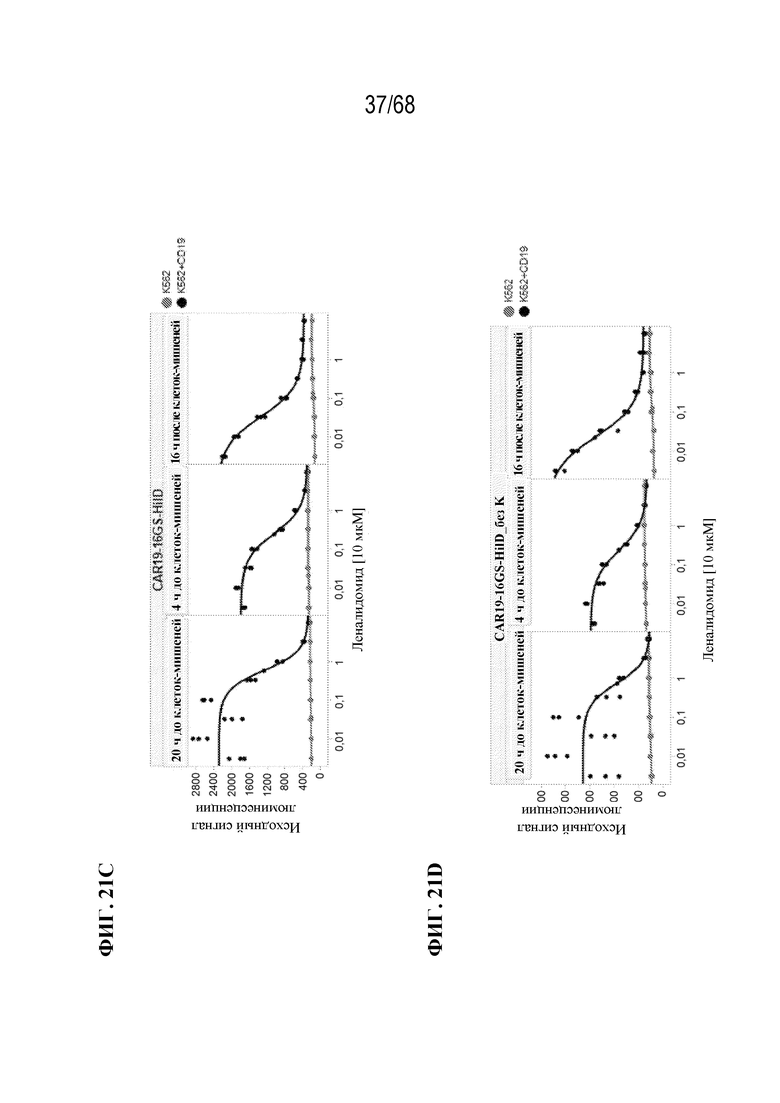
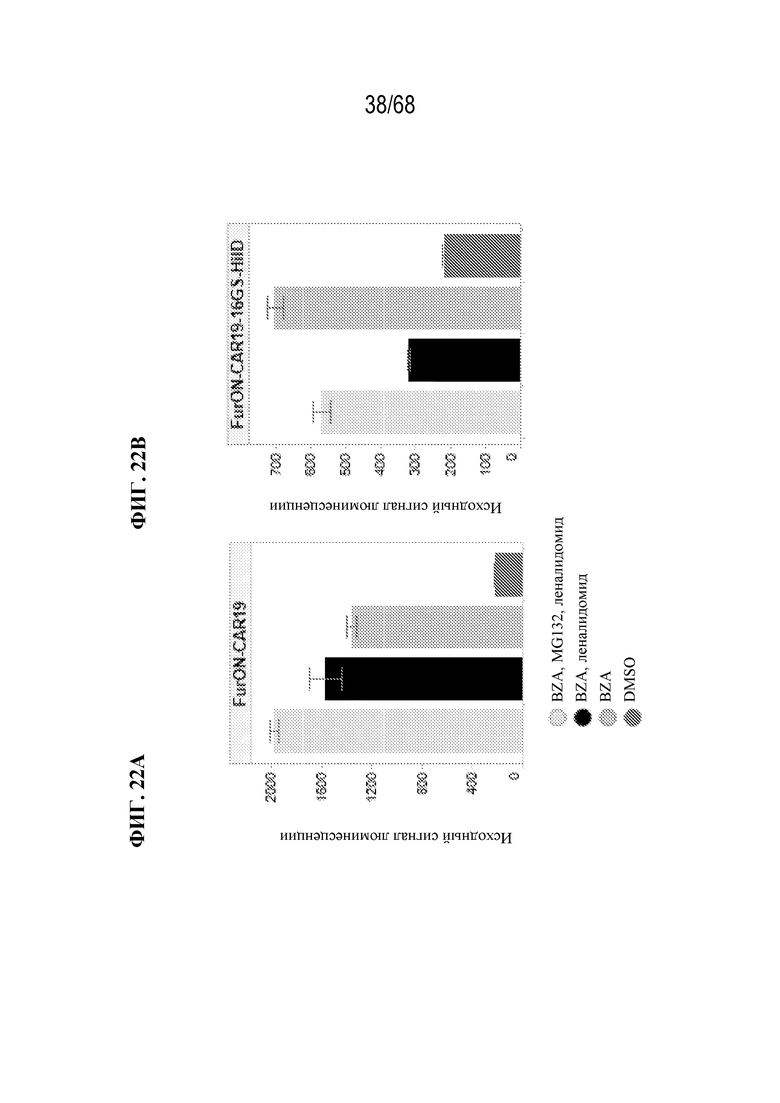




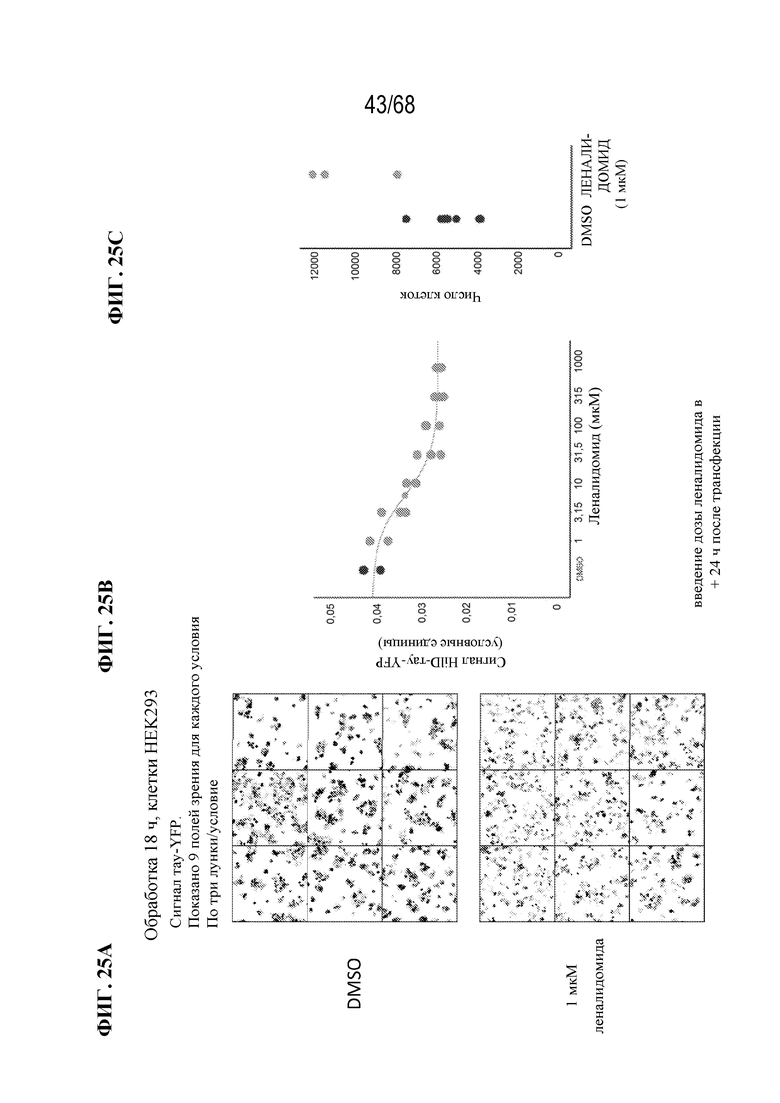
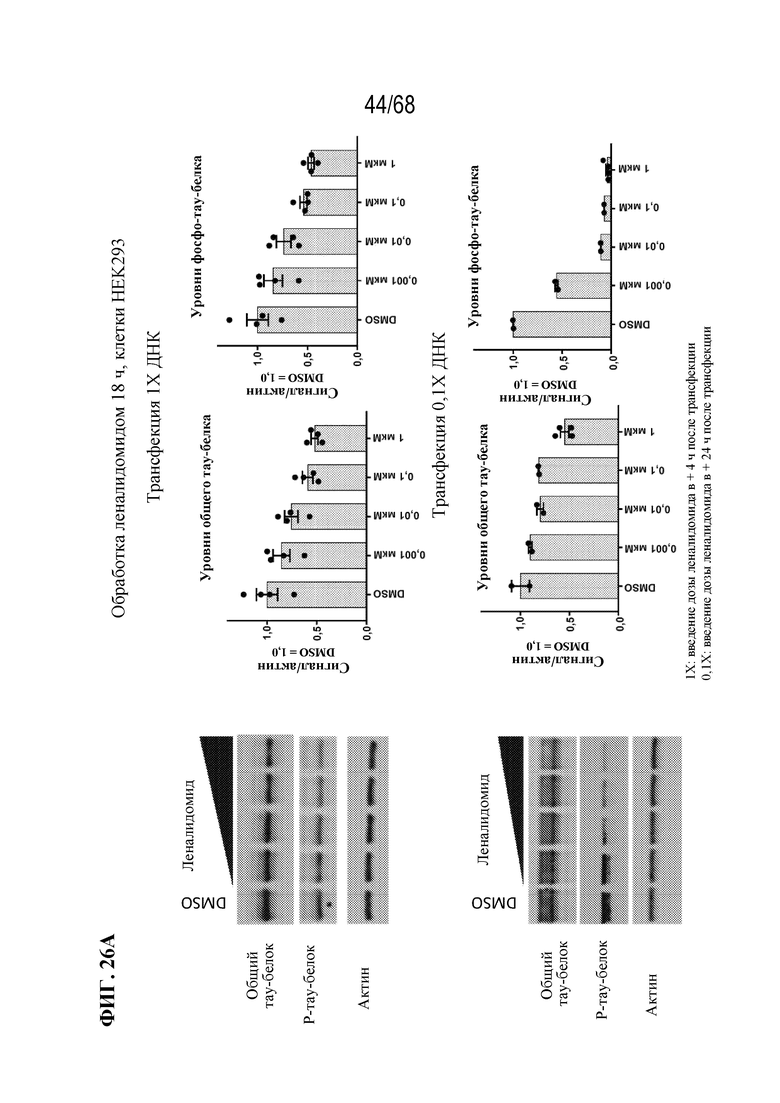


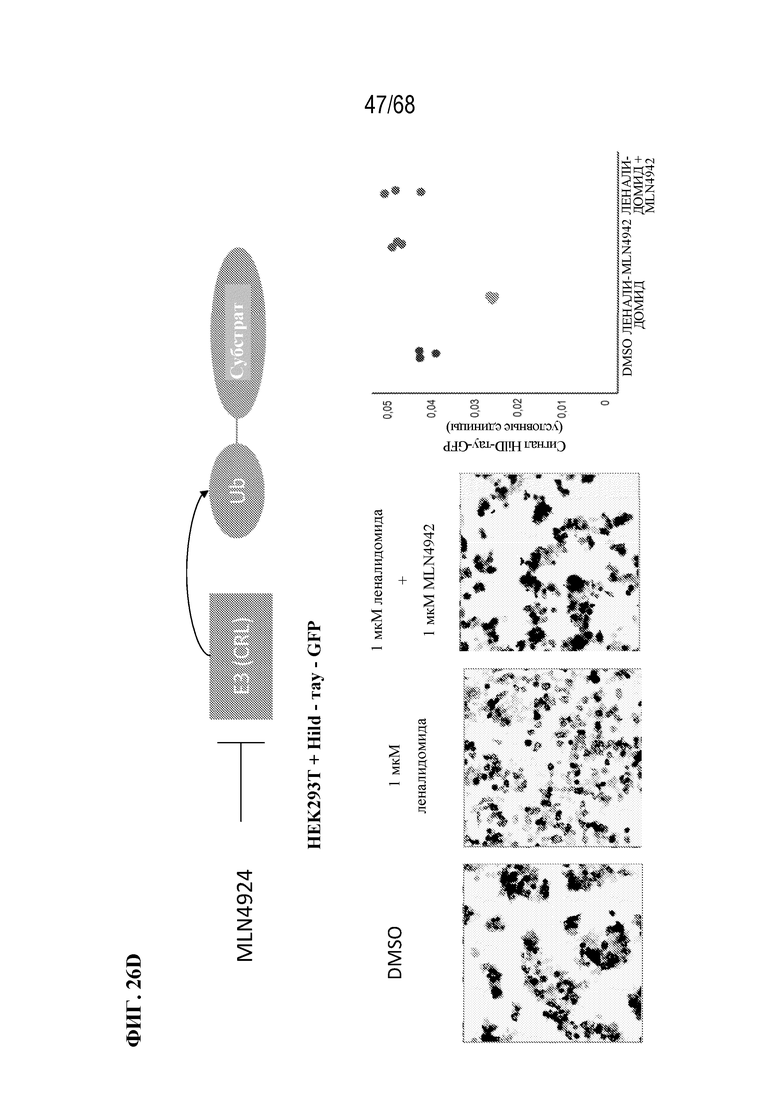
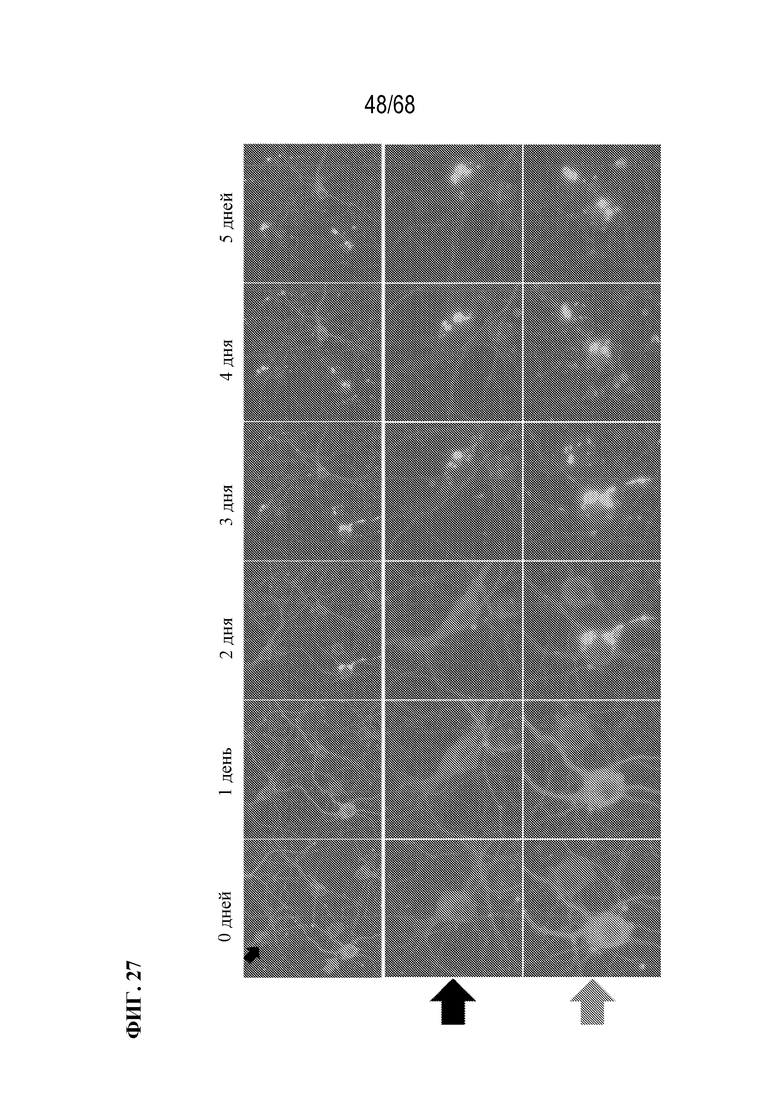
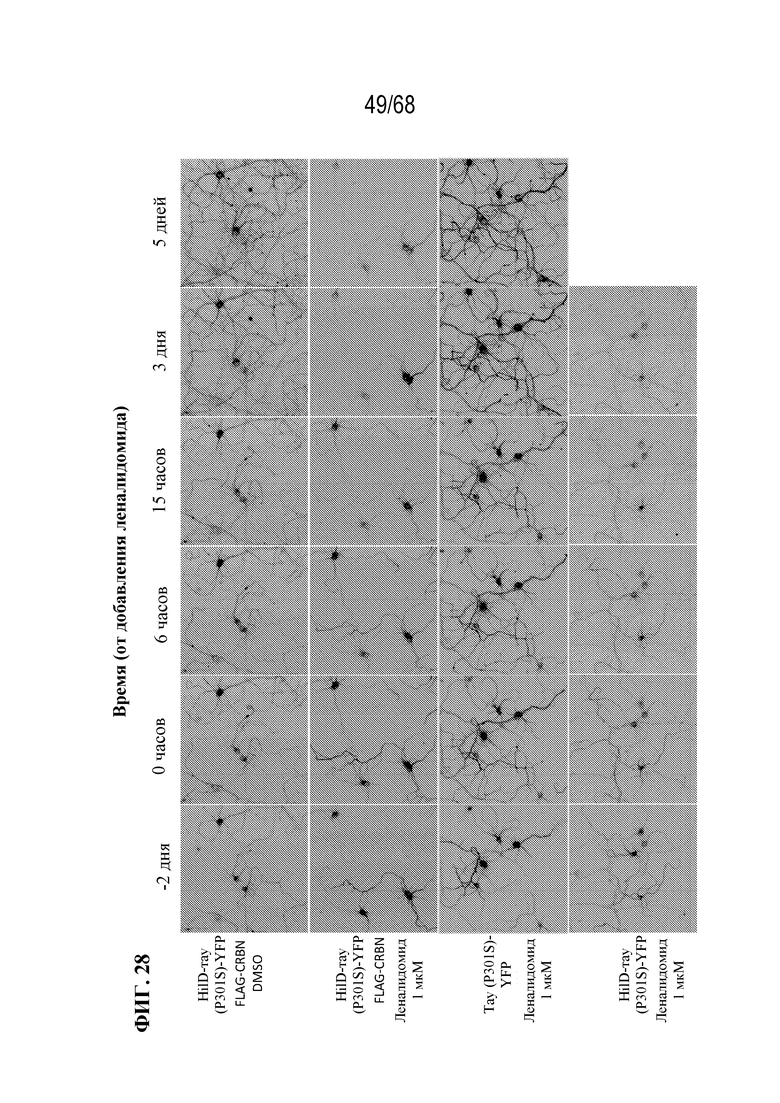
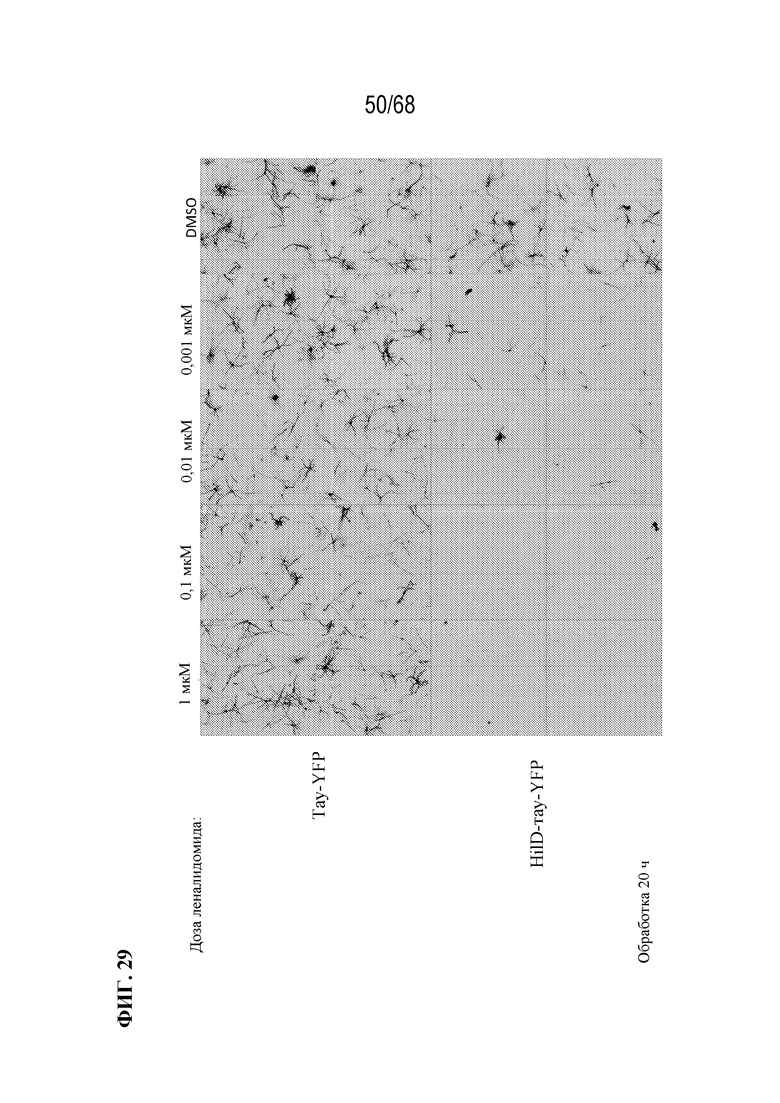

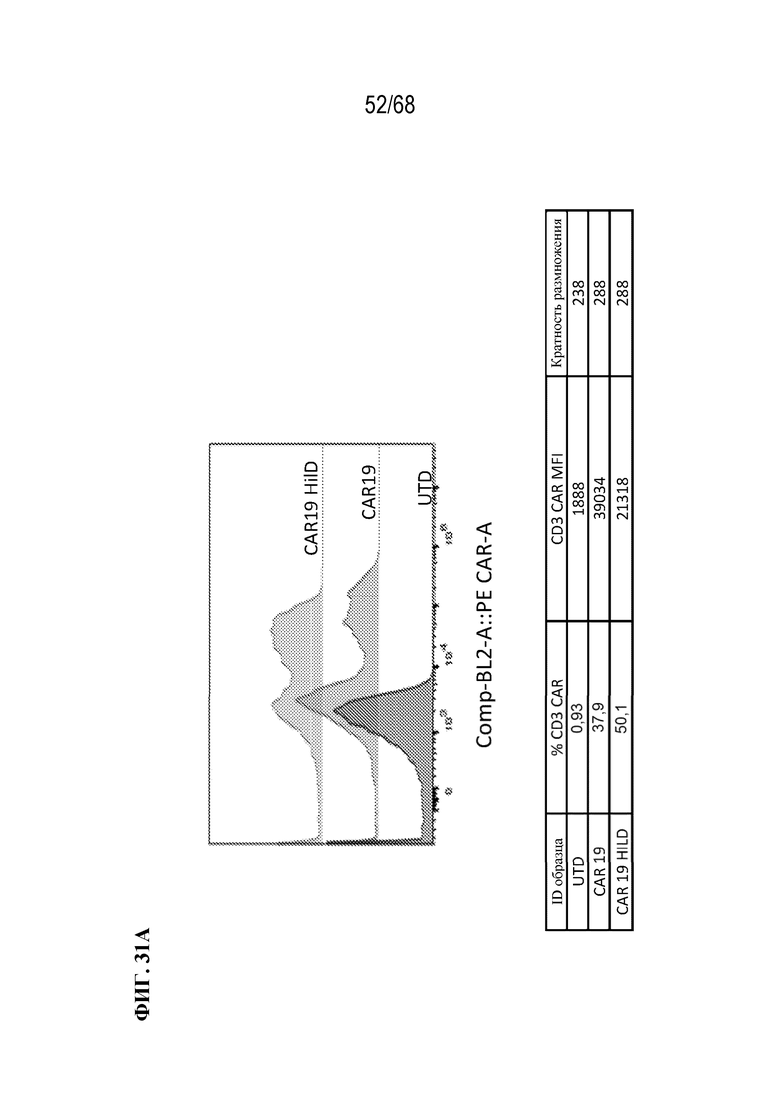



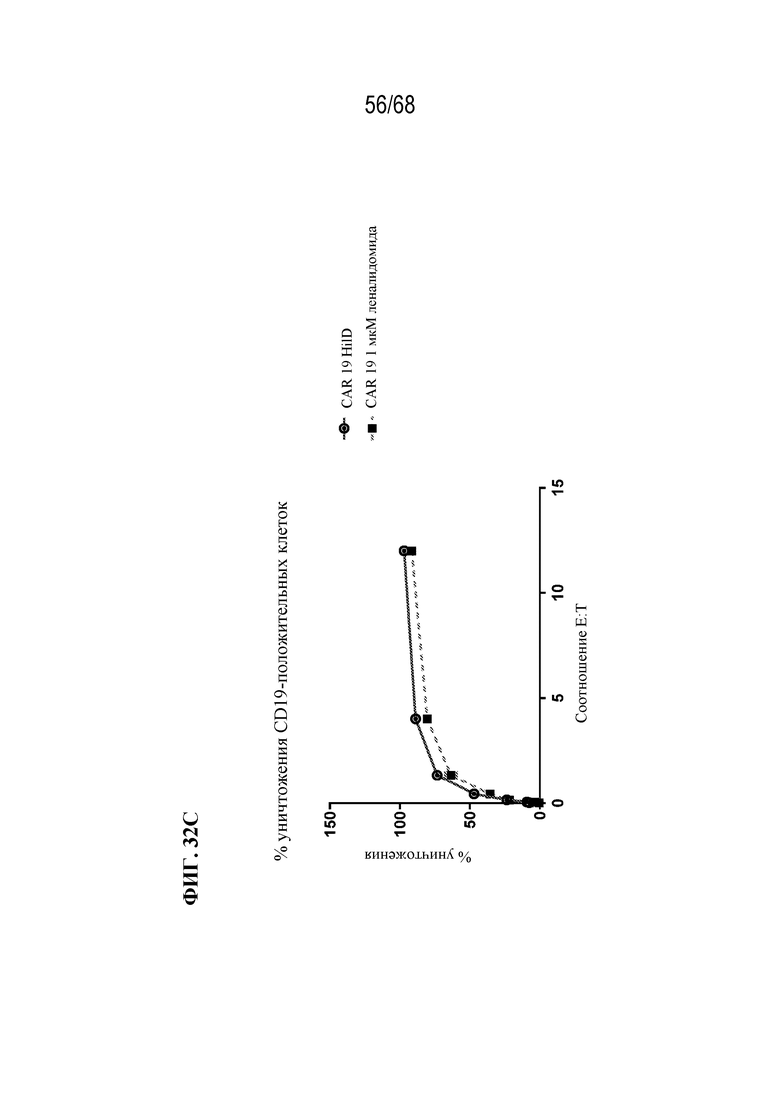

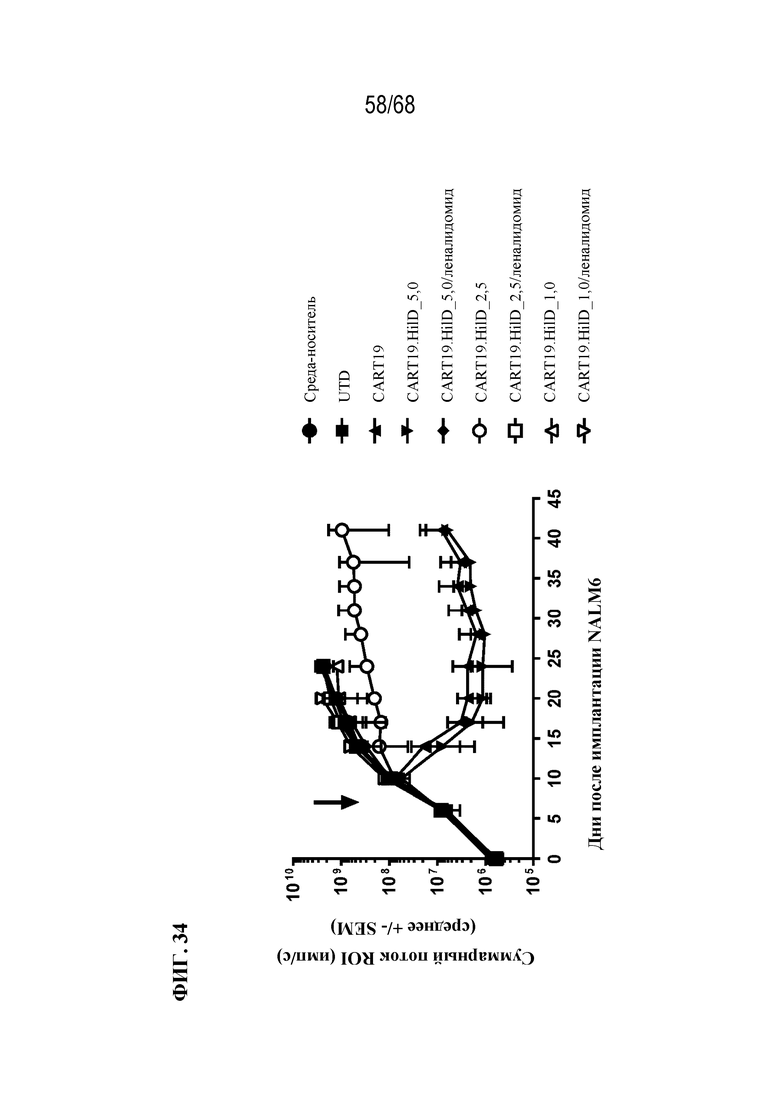
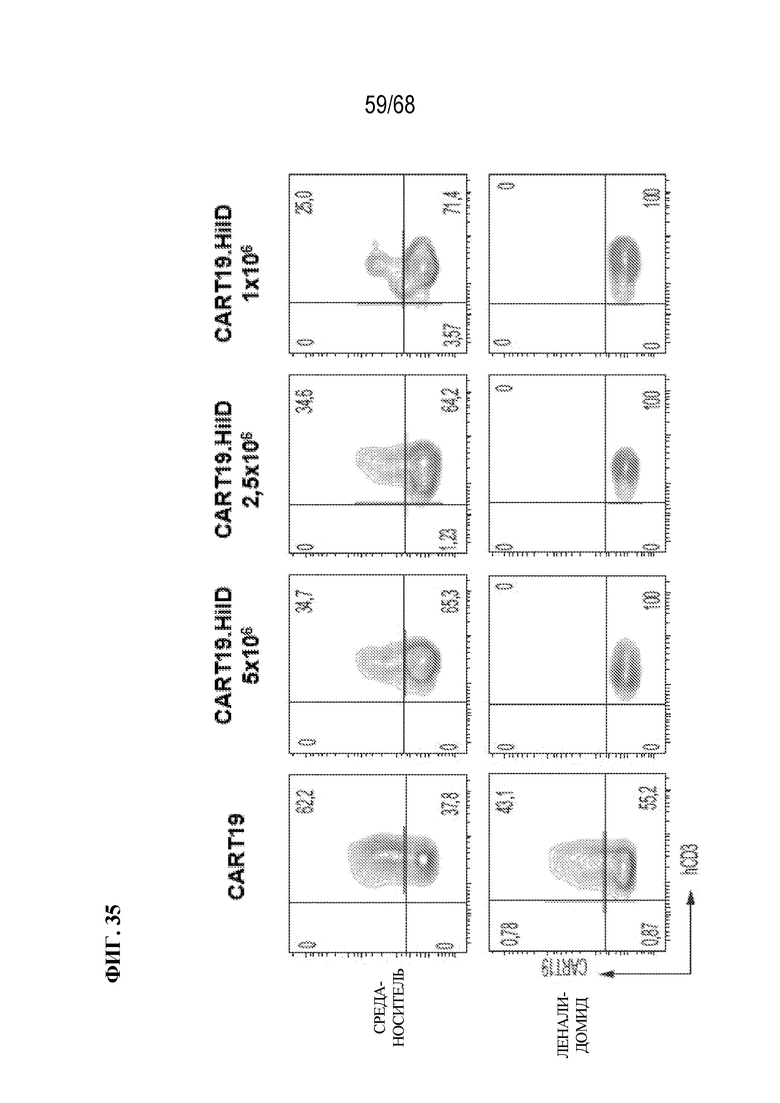
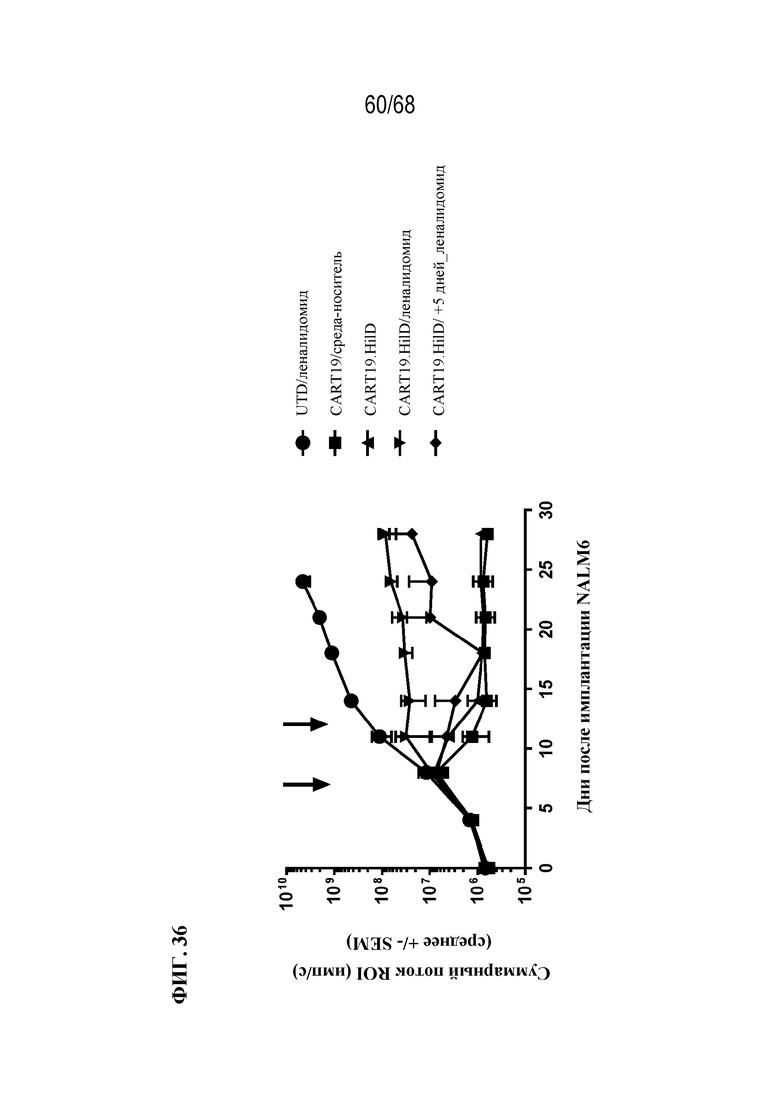
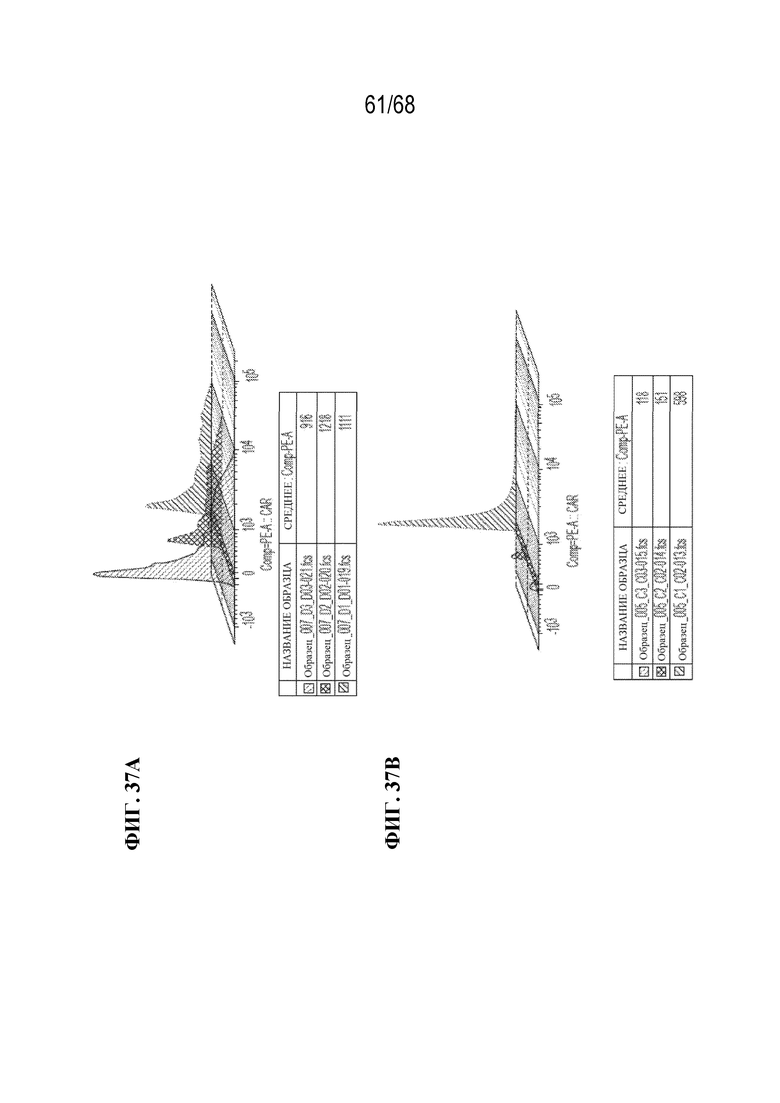
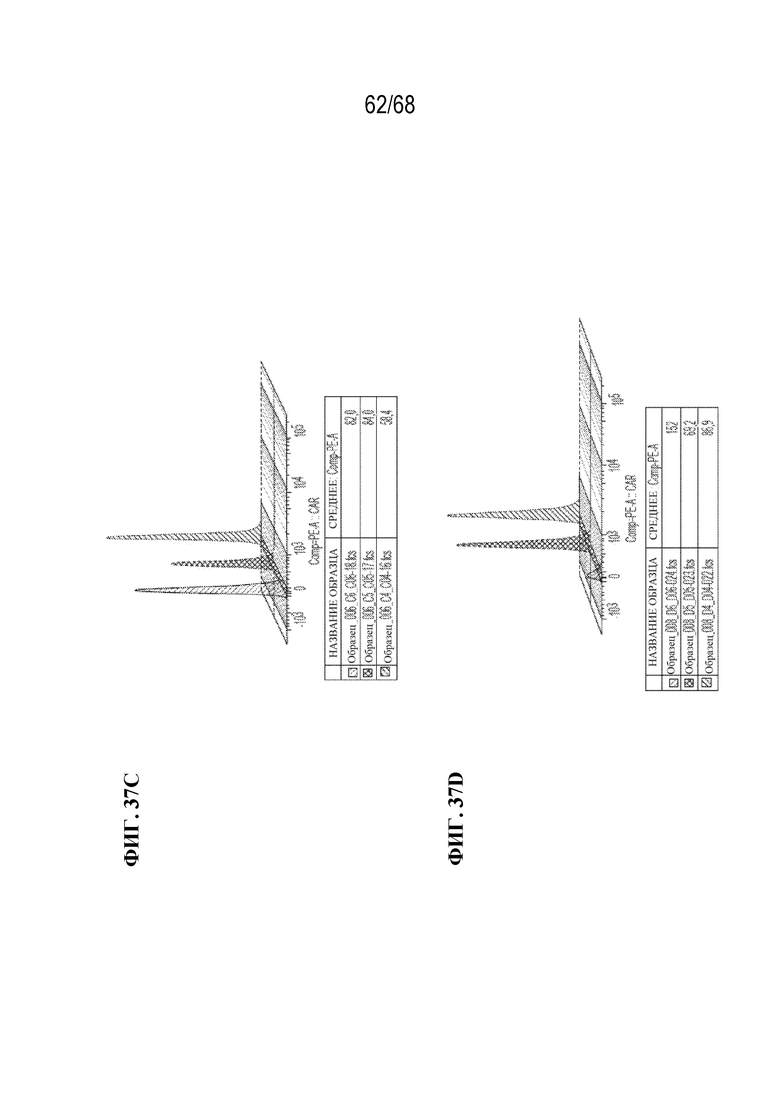
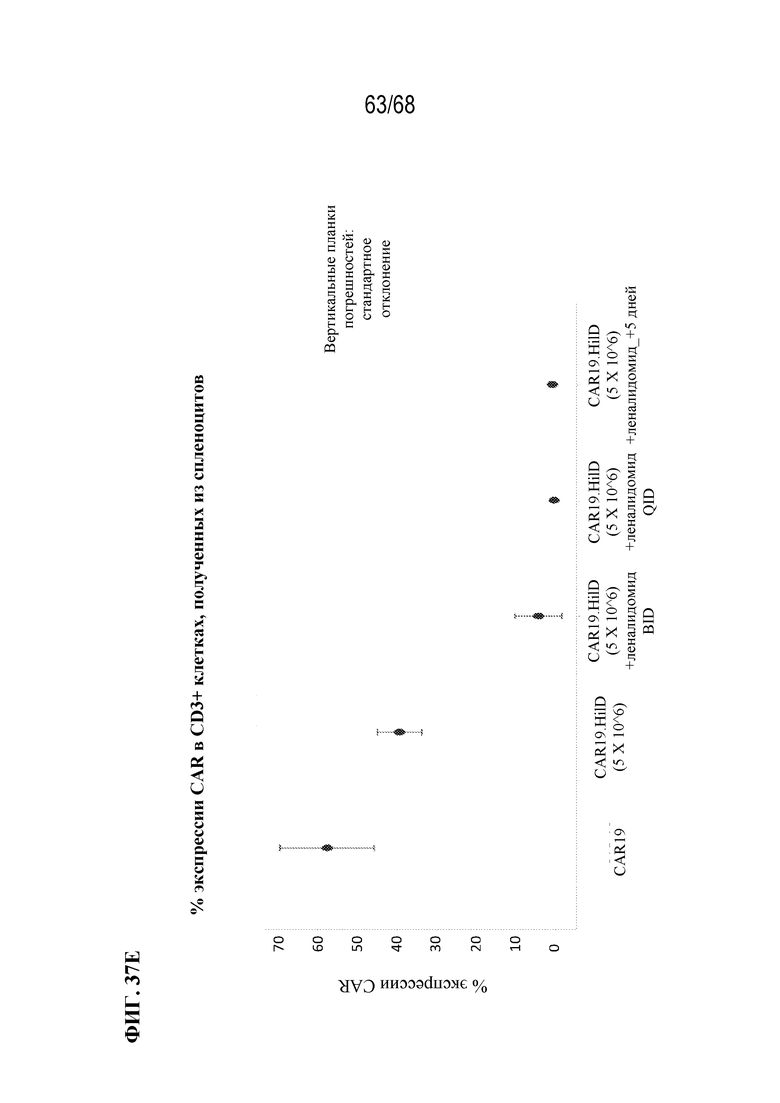
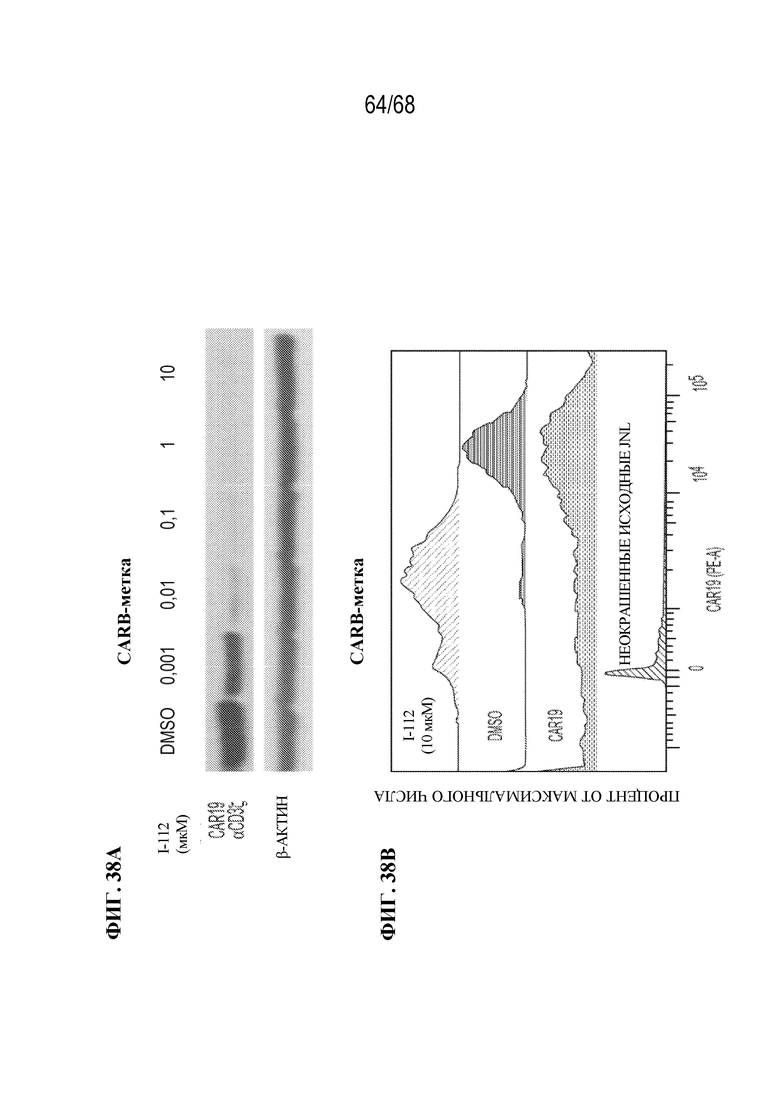




Настоящее изобретение относится к области биотехнологии и может быть применимо в медицине. Изобретение раскрывает слитый полипептид, содержащий связывающий цереблон (CRBN) фрагмент и фрагмент специфичного к опухолевому антигену химерного антигенного рецептора (CAR). Изобретение может быть использовано в медицине при лечении злокачественных опухолей в качестве модулирующего экспрессию терапевтических белков агента. Изобретение позволяет регулировать экспрессию белков путем стимулирования их протеасомной и/или убиквитинзависимой деградации. Изобретение также раскрывает способ устранения побочных эффектов, возникающих при терапии рака с использованием CAR. 13 н. и 31 з.п. ф-лы, 18 пр., 34 табл., 40 ил.
1. Слитый полипептид для применения в лечении субъекта, страдающего заболеванием, связанным с экспрессией опухолевого антигена, где слитый полипептид содержит
(i) связывающий CRBN (цереблон) полипептид и
(ii) химерный антигенный рецептор (CAR), который содержит в направлении от N-конца до C-конца антигенсвязывающий домен, трансмембранный домен и один или более внутриклеточные сигнальные домены;
где связывающий CRBN полипептид содержит от 45 до 65 аминокислотных остатков IKZF3 (SEQ ID NO: 19) и содержит аминокислотную последовательность SEQ ID NO: 5.
2. Слитый полипептид по п. 1, где:
(a) связывающий CRBN полипептид содержит от 50 до 65 аминокислотных остатков или от 55 до 65 аминокислотных остатков IKZF3 (SEQ ID NO: 19); и/или
(b) связывающий CRBN полипептид дополнительно содержит аминокислотную последовательность SEQ ID NO: 11.
3. Слитый полипептид по п. 1 или 2, где связывающий CRBN полипептид содержит или состоит из аминокислотной последовательности SEQ ID NO: 1 или 3.
4. Слитый полипептид по любому из пп. 1-3, где:
(i) ассоциация слитого полипептида с CRBN в отсутствие леналидомида или помалидомида или их фармацевтически приемлемой соли составляет не более 0,01, 0,1, 1, 5, 10, 15 или 20% от ассоциации слитого полипептида с CRBN в присутствии леналидомида или помалидомида или их фармацевтически приемлемой соли;
(ii) слитый полипептид не связывается с CRBN в отсутствие леналидомида или помалидомида или их фармацевтически приемлемой соли;
(iii) убиквитинирование слитого полипептида в отсутствие леналидомида или помалидомида или их фармацевтически приемлемой соли составляет не более 0,01, 0,1, 1, 10, 20, 30, 40, 50, 60 или 70% от убиквитинирования слитого полипептида в присутствии леналидомида или помалидомида или их фармацевтически приемлемой соли; или
(iv) деградация слитого полипептида в отсутствие леналидомида или помалидомида или их фармацевтически приемлемой соли составляет не более 0,01, 0,1, 1, 10, 20, 30, 40, 50, 60 или 70% от деградации слитого полипептида в присутствии леналидомида или помалидомида или их фармацевтически приемлемой соли.
5. Слитый полипептид по п. 4, где
(i) ассоциацию измеряют с помощью иммунопреципитации; и/или
(ii) деградацию слитого полипептида измеряют с помощью вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
6. Слитый полипептид для применения в лечении субъекта, страдающего заболеванием, связанным с экспрессией опухолевого антигена, где слитый полипептид дополнительно содержит:
(i) связывающий CRBN (цереблон) полипептид,
(ii) химерный антигенный рецептор (CAR), который содержит в направлении от N-конца до C-конца антигенсвязывающий домен, трансмембранный домен и один или более внутриклеточные сигнальные домены; и
(iii) домен деградации,
где связывающий CRBN полипептид содержит от 45 до 65 аминокислотных остатков IKZF3 (SEQ ID NO: 19) и содержит аминокислотную последовательность SEQ ID NO: 5;
где домен деградации отделен от связывающего CRBN полипептида и CAR с помощью гетерологичного сайта расщепления протеазами и
домен деградации выбран из домена эстрогенового рецептора (ER), домена белка FKB (FKBP) или домена дигидрофолатредуктазы (DHFR).
7. Слитый полипептид по п. 6, где:
(a) связывающий CRBN полипептид содержит от 50 до 65 аминокислотных остатков или от 55 до 65 аминокислотных остатков IKZF3 (SEQ ID NO: 19); и/или
(b) связывающий CRBN полипептид дополнительно содержит аминокислотную последовательность SEQ ID NO: 11.
8. Слитый полипептид по п. 6 или 7, где связывающий CRBN полипептид содержит или состоит из аминокислотной последовательности SEQ ID NO: 1 или 3.
9. Слитый полипептид по любому из пп. 6-8, где
(i) слитый полипептид содержит в направлении от N-конца к C-концу:
(a) домен деградации, гетерологичный сайт расщепления протеазами, CAR и связывающий CRBN полипептид;
(b) домен деградации, гетерологичный сайт расщепления протеазами, связывающий CRBN полипептид и CAR;
(c) связывающий CRBN полипептид, CAR, гетерологичный сайт расщепления протеазами и домен деградации; или
(d) CAR, связывающий CRBN полипептид, гетерологичный сайт расщепления протеазами и домен деградации; и/или
(ii) домен деградации имеет первое состояние, ассоциированное с первым уровнем экспрессии слитого полипептида, и второе состояние, ассоциированное со вторым уровнем экспрессии слитого полипептида, где второй уровень увеличивается по сравнению с первым уровнем в присутствии стабилизирующего соединения.
10. Слитый полипептид по п. 9, где:
(i) второй уровень экспрессии слитого полипептида увеличивается в по меньшей мере 2, 3, 4, 5, 10, 20 или 30 раз по сравнению с первым уровнем в присутствии стабилизирующего соединения; и/или
(ii) в отсутствие стабилизирующего соединения слитый полипептид подвергается деградации под действием клеточного пути деградации, например по меньшей мере 50%, 60%, 70%, 80%, 90% или более из слитого полипептида подвергается деградации.
11. Слитый полипептид по любому из пп. 6-10, где
(i) домен деградации представляет собой домен ER и содержит аминокислотную последовательность, которая на по меньшей мере 90, 95, 97, 98, 99 или 100% идентична SEQ ID NO: 46 или 48;
(ii) домен деградации представляет собой домен FKBP и содержит аминокислотную последовательность, которая на по меньшей мере 90, 95, 97, 98, 99 или 100% идентична SEQ ID NO: 50; и/или
(iii) домен деградации представляет собой домен DHFR и содержит аминокислотную последовательность, которая на по меньшей мере 90, 95, 97, 98, 99 или 100% идентична SEQ ID NO: 51.
12. Слитый полипептид по любому из пп. 9-11, где указанное стабилизирующее соединение представляет собой:
(a) базедоксифен или 4-гидрокситамоксифен (4-OHT) или их фармацевтически приемлемую соль, когда домен деградации представляет собой указанный домен ER;
(b) Shield-1 или его фармацевтически приемлемую соль, где домен деградации представляет собой указанный домен FKBP; или
(c) триметоприм или его фармацевтически приемлемую соль, когда домен деградации представляет собой указанный домен DHFR.
13. Слитый полипептид по любому из пп. 6-12, где гетерологичный сайт расщепления протеазами расщепляется под действием внутриклеточной протеазы млекопитающего.
14. Слитый полипептид по п. 13, где
(i) гетерологичный сайт расщепления протеазами расщепляется под действием протеазы, выбранной из группы, состоящей из фурина, PCSK1, PCSK5, PCSK6, PCSK7, катепсина B, гранзима B, фактора XA, энтерокиназы, гененазы, сортазы, протеазы precission, тромбина, протеазы TEV и эластазы-1; или
(ii) гетерологичный сайт расщепления протеазами содержит последовательность, имеющую мотив расщепления, выбранный из группы, состоящей из консенсусного мотива Arg-X-Lys/Arg-Arg (X может быть любой аминокислотой; SEQ ID NO: 52), консенсусного мотива Arg-X-X-X-Lys/Arg-Arg (X может быть любой аминокислотой; SEQ ID NO: 53), консенсусного мотива Arg-Arg-X (SEQ ID NO: 54), консенсусного мотива Ile-Glu-Pro-Asp-X (SEQ ID NO: 55), Ile-Glu/Asp-Gly-Arg (SEQ ID NO: 56), Asp-Asp-Asp-Asp-Lys (SEQ ID NO: 57), Pro-Gly-Ala-Ala-His-Tyr (SEQ ID NO: 58), консенсусного мотива Leu-Pro-X-Thr-Gly/Ala (SEQ ID NO: 59), Leu-Glu-Val-Phe-Gln-Gly-Pro (SEQ ID NO: 60), Leu-Val-Pro-Arg-Gly-Ser (SEQ ID NO: 61), Glu-Asn-Leu-Tyr-Phe-Gln-Gly (SEQ ID NO: 62) и [Ala-Gly-Ser-Val]-X (X может быть любой аминокислотой; SEQ ID NO: 63).
15. Слитый полипептид по п. 13, где гетерологичный сайт расщепления протеазами содержит сайт расщепления фурином, выбранный из группы, состоящей из RTKR (SEQ ID NO: 123); GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125); GTGAEDPRPSRKRR (SEQ ID NO: 127); LQWLEQQVAKRRTKR (SEQ ID NO: 129); GTGAEDPRPSRKRRSLGG (SEQ ID NO: 131); GTGAEDPRPSRKRRSLG (SEQ ID NO: 133); SLNLTESHNSRKKR (SEQ ID NO: 135); CKINGYPKRGRKRR (SEQ ID NO: 137) и SARNRQKR (SEQ ID NO: 34).
16. Слитый полипептид по любому из пп. 6-12, где гетерологичный сайт расщепления протеазами расщепляется под действием внеклеточной протеазы млекопитающего.
17. Слитый полипептид по п. 16, где
(i) гетерологичный сайт расщепления протеазами расщепляется под действием внеклеточной протеазы млекопитающего, выбранной из группы, состоящей из фактора XA, энтерокиназы, гененазы, сортазы, протеазы precission, тромбина, протеазы TEV и эластазы-1; или
(ii) гетерологичный сайт расщепления протеазами содержит аминокислотную последовательность, выбранную из группы, состоящей из Ile-Glu/Asp-Gly-Arg (SEQ ID NO: 56), Asp-Asp-Asp-Asp-Lys (SEQ ID NO: 57), Pro-Gly-Ala-Ala-His-Tyr (SEQ ID NO: 58), консенсусного мотива Leu-Pro-X-Thr-Gly/Ala (SEQ ID NO: 59), Leu-Glu-Val-Phe-Gln-Gly-Pro (SEQ ID NO: 60), Leu-Val-Pro-Arg-Gly-Ser (SEQ ID NO: 61), Glu-Asn-Leu-Tyr-Phe-Gln-Gly (SEQ ID NO: 62) и [Ala-Gly-Ser-Val]-X (X может быть любой аминокислотой; SEQ ID NO: 63).
18. Слитый полипептид по любому из пп. 1-17, где
(i) указанный внутриклеточный сигнальный домен содержит один или несколько первичных сигнальных доменов; или
(ii) указанный внутриклеточный сигнальный домен содержит один или несколько костимулирующих сигнальных доменов.
19. Слитый полипептид по любому из пп. 1-18, где указанный антигенсвязывающий домен представляет собой scFv.
20. Слитый полипептид по любому из пп. 1-19, где указанный антигенсвязывающий домен связывает антиген, выбранный из группы, состоящей из CD19; CD123; CD22; CD30; CD171; CS-1; лектиноподобной молекулы-1 C-типа, CD33; варианта III рецептора эпидермального фактора роста (EGFRvIII); ганглиозида G2 (GD2); ганглиозида GD3; представителя семейства рецепторов TNF; антигена созревания B-клеток; Tn-антигена ((Tn Ag) или (GalNAcα-Ser/Thr)); простатического специфического мембранного антигена (PSMA); орфанного рецептора-1, подобного рецепторной тирозинкиназе (ROR1); Fms-подобной тирозинкиназы 3 (FLT3); опухолеассоциированного гликопротеина-72 (TAG72); CD38; CD44v6; раково-эмбрионального антигена (CEA); молекулы адгезии эпителиальных клеток (EPCAM); B7H3 (CD276); KIT (CD117); субъединицы альфа-2 рецептора интерлейкина-13; мезотелина; альфа-субъединицы рецептора интерлейкина-11 (IL-11Ra); антигена стволовых клеток предстательной железы (PSCA); сериновой протеазы-21; рецептора-2 фактора роста эндотелия сосудов (VEGFR2); антигена системы Льюис (Y); CD24; рецептора фактора роста тромбоцитов бета-типа (PDGFR-бета); стадиеспецифического эмбрионального антигена-4 (SSEA-4); CD20; рецептора фолиевой кислоты альфа-типа; рецепторной тирозинпротеинкиназы ERBB2 (Her2/neu); муцина-1, ассоциированного с клеточной поверхностью (MUC1); рецептора эпидермального фактора роста (EGFR); молекулы адгезии нейронов (NCAM); простазы; простатической кислой фосфатазы (PAP); мутантного фактора элонгации 2 (ELF2M); эфрина B2; белка активации фибробластов альфа (FAP); рецептора инсулиноподобного фактора роста-1 (рецептора IGF-I), карбоангидразы IX (CAIX); субъединицы-9 протеасомы (просомы, мультикаталитической протеазы) бета-типа (LMP2); гликопротеина 100 (gp100); онкогенного полипептида, состоящего из кластерного региона точечных разрывов (BCR) и гомолога-1 вирусного онкогена лейкоза мышей Абельсона (Abl) (bcr-abl); тирозиназы; эфринового рецептора-2 A-типа (EphA2); фукозил-GM1; молекулы адгезии, представляющей собой сиалилированный антиген системы Льюис (sLe); ганглиозида GM3; трансглютаминазы-5 (TGS5); высокомолекулярного меланома-ассоциированного антигена (HMWMAA); ганглиозида o-ацетил-GD2 (OAcGD2); рецептора фолиевой кислоты бета-типа; маркера-1 эндотелия опухоли (TEM1/CD248); белка, родственного маркеру-7 эндотелия опухоли (TEM7R); клаудина-6 (CLDN6); рецептора тиреотропного гормона (TSHR); представителя D группы 5 класса С рецепторов, сопряженных с G-белком (GPRC5D); белка, кодируемого открытой рамкой считывания 61 X-хромосомы (CXORF61); CD97; CD179a; киназы анапластической лимфомы (ALK); полисиаловой кислоты; плацентоспецифического белка-1 (PLAC1); гексасахаридной части гликоцерамида globoH (GloboH); дифференцировочного антигена молочной железы (NY-BR-1); уроплакина-2 (UPK2); клеточного рецептора-1 вируса гепатита A (HAVCR1); бета-3 адренорецептора (ADRB3); паннексина-3 (PANX3); рецептора-20, сопряженного с G-белком (GPR20); антигена локуса K9 комплекса лимфоцитарных антигенов 6 (LY6K); обонятельного рецептора 51E2 (OR51E2); белка, кодируемого альтернативной рамкой считывания гена TCR-гамма (TARP); белка опухоли Вильмса (WT1); раково-тестикулярного антигена-1 (NY-ESO-1); раково-тестикулярного антигена-2 (LAGE-1a); меланома-ассоциированного антигена-1 (MAGE-A1); белка, кодируемого транслокационным вариантом-6 гена ETS, локализованным в р-плече 12 хромосомы (ETV6-AML); белка-17 сперматозоидов (SPA17); представителя 1А семейства X-антигенов (XAGE1); ангиопоэтин-связывающего рецептора-2 клеточной поверхности 2 (Tie 2); раково-тестикулярного антигена-1 из клеток меланомы (MAD-CT-1); раково-тестикулярного антигена-2 из клеток меланомы (MAD-CT-2); Fos-родственного антигена-1; опухолевого белка p53 (p53); мутанта p53; простеина; сурвивина; теломеразы; опухолевого антигена-1 карциномы предстательной железы, антигена-1 меланомы, распознаваемого T-клетками; мутантного белка саркомы крыс (Ras); обратной транскриптазы теломеразы человека (hTERT); антигенов саркомы с точечными разрывами при транслокации; меланомного ингибитора апоптоза (ML-IAP); ERG (продукта слитого гена трансмембранной сериновой протеазы-2 (TMPRSS2) и ETS); N-ацетилглюкозаминилтрансферазы V (NA17); белка с парным box-доменом Рах-3 (PAX3); андрогенового рецептора; циклина-B1; нейробластомного гомолога вирусного онкогена миелоцитоматоза птиц v-myc (MYCN); представителя С семейства гомологов Ras (RhoC); белка-2, родственного тирозиназе (TRP-2); цитохрома P450 1B1 (CYP1B1); белка, подобного CCCTC-связывающему фактору (белку с "цинковыми пальцами"), антигена плоскоклеточной карциномы 3, распознаваемого Т-клетками (SART3); белка с парным box-доменом Рах-5 (PAX5); проакрозин-связывающего белка sp32 (OY-TES1); лимфоцит-специфической протеинтирозинкиназы (LCK); якорного белка-4 киназы A (AKAP-4); антигена 2 синовиальной саркомы с точечным разрывом в X-хромосоме (SSX2); рецептора конечных продуктов неферментативного гликозилирования (RAGE-1); почечного убиквитарного белка-1 (RU1); почечного убиквитарного белка-2 (RU2); легумаина; Е6 вируса папилломы человека (HPV E6); Е7 вируса папилломы человека (HPV E7); кишечной карбоксилэстеразы; мутантного белка теплового шока 70-2 (mut hsp70-2); CD79a; CD79b; CD72; иммуноглобулиноподобного рецептора-1, ассоциированного с лейкоцитами (LAIR1); рецептора Fc-фрагмента IgA (FCAR или CD89); представителя 2 подсемейства А иммуноглобулиноподобных рецепторов лейкоцитов (LILRA2); представителя f семейства белков, подобных молекулам CD300 (CD300LF); представителя А семейства 12 лектиновых доменов С-типа (CLEC12A); антигена-2 клеток стромы костного мозга (BST2); белка-2, подобного муциноподобному рецептору гормонов, содержащему EGF-подобный модуль (EMR2); лимфоцитарного антигена-75 (LY75); глипикана-3 (GPC3); белка-5, подобного Fc-рецептору (FCRL5); и полипептида-1, подобного лямбда-цепи иммуноглобулина (IGLL1).
21. Слитый полипептид по п. 20, где указанный антиген выбран из CD19, CD22, BCMA, CD20, CD123, EGFRvIII или мезотелина.
22. Слитый полипептид по п. 18, где:
(a) один из указанных одного или несколько первичных сигнальных доменов содержит стимулирующий домен CD3-дзета; и/или
(b) один или более из указанных костимулирующих сигнальных доменов представляет собой внутриклеточный домен из костимулирующего белка, выбранного из группы, состоящей из CD27, CD28, 4-1BB (CD137), OX40, GITR, CD30, CD40, ICOS, BAFFR, HVEM, ICAM-1, лимфоцитарного функционально-ассоциированного антигена-1 (LFA-1), CD2, CD7, CD287, LIGHT, NKG2C, NKG2D, SLAMF7, NKp80, NKp30, NKp44, NKp46, CD160, B7-H3, и лиганда, который специфически связывается с CD83.
23. Молекула нуклеиновой кислоты для применения в лечении субъекта, страдающего заболеванием, связанным с экспрессией опухолевого антигена, где молекула нуклеиновой кислоты кодирует слитый полипептид по любому из пп. 1-22.
24. Экспрессионный вектор, содержащий молекулу нуклеиновой кислоты по п. 23.
25. Клетка для применения в лечении субъекта, страдающего заболеванием, связанным с экспрессией опухолевого антигена, где клетка содержит слитый полипептид по любому из пп. 1-22 или экспрессионный вектор по п. 23.
26. Клетка по п. 25, где клетка представляет собой T-клетку или NK-клетку.
27. Фармацевтическая композиция для применения в лечении субъекта, страдающего заболеванием, связанным с экспрессией опухолевого антигена, содержащая терапевтически эффективное количество слитого полипептида по любому из пп. 1-22 или клетки по п. 25 или 26 и фармацевтически приемлемый носитель, вспомогательное вещество или стабилизатор.
28. Способ получения клетки по п. 25 или 26, причем указанный способ предусматривает трансдукцию клетки молекулой нуклеиновой кислоты по п. 23 или экспрессионным вектором по п. 24.
29. Способ деградации слитого полипептида, предусматривающий приведение слитого полипептида по любому из пп. 1-5, 18-22 или клетки, содержащей указанный слитый полипептид, в контакт с леналидомидом или помалидомидом или их фармацевтически приемлемой солью.
30. Способ по п. 29, где в присутствии леналидомида или помалидомида или их фармацевтически приемлемой соли уровень экспрессии указанного слитого полипептида уменьшается относительно уровня экспрессии указанного слитого полипептида в отсутствие леналидомида или помалидомида или их фармацевтически приемлемой соли.
31. Способ по п. 30, где:
(i) где в присутствии леналидомида или помалидомида или их фармацевтически приемлемой соли уровень экспрессии указанного слитого полипептида уменьшается на по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90 или 100% относительно уровня экспрессии указанного слитого полипептида в отсутствие леналидомида или помалидомида или их фармацевтически приемлемой соли; и/или
(ii) уровень экспрессии измеряют с помощью вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
32. Способ повышения экспрессии слитого полипептида, где способ включает:
(i) приведение слитого полипептида по любому из пп. 6-22 или клетки, содержащей указанный слитый полипептид, в контакт со стабилизирующим соединением, где:
(a) в присутствии стабилизирующего соединения уровень экспрессии слитого полипептида увеличивается по меньшей мере в 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз по сравнению с уровнем экспрессии слитого полипептида в отсутствие стабилизирующего соединения; и/или
(b) стабилизирующее соединение представляет собой базедоксифен или его фармацевтически приемлемую соль.
33. Способ снижения экспрессии слитого полипептида, где способ включает:
(i) приведение слитого полипептида по любому из пп. 6-22 или клетки, содержащей указанный слитый полипептид, в контакт со стабилизирующим соединением;
(ii) приведение в контакт слитого полипептида или клетки в контакт с леналидомидом или помалидомидом или их фармацевтически приемлемой солью, где в присутствии леналидомида или помалидомида или их фармацевтически приемлемой соли уровень экспрессии слитого полипептида уменьшается на по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90 или 100% относительно уровня экспрессии слитого полипептида после стадии (i) и до стадии (ii).
34. Способ по п. 33, где:
(a) слитый полипептид или клетку приводят в контакт с леналидомидом или помалидомидом или их фармацевтически приемлемой солью и/или стабилизирующим соединением in vivo или ex vivo; и/или
(b) уровень экспрессии измеряют с помощью вестерн-блоттинг-анализа или анализа посредством проточной цитометрии.
35. Способ лечения субъекта, у которого имеется рак, предусматривающий введение субъекту эффективного количества слитого полипептида по любому из пп. 1-22, молекулы нуклеиновой кислоты по п. 23, экспрессионного вектора по п. 24, клетки по п. 25 или 26 или фармацевтической композиции по п. 27.
36. Способ лечения побочного эффекта терапии рака у субъекта, где терапия включает введение клетки, экспрессирующей слитый полипептид, который раскрыт в любом из пп. 1-5 или 18-22, 14 или 15, субъекту, где способ предусматривает:
(i) введение субъекту эффективного количества леналидомида или помалидомида или их фармацевтически приемлемой соли, где:
(a) введение леналидомида или помалидомида или их фармацевтически приемлемой соли снижает по меньшей мере на приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90 или 100% уровень экспрессии слитого полипептида относительно уровня экспрессии слитого полипептида до введения леналидомида или помалидомида или их фармацевтически приемлемой соли;
(b) у субъекта развилась нежелательная реакция, она развивается или ожидается ее развитие;
(c) введение леналидомида или помалидомида или их фармацевтически приемлемой соли осуществляют в ответ на возникновение нежелательной реакции у субъекта или в ответ на ожидание возникновения нежелательной реакции у субъекта;
(d) введение леналидомида или помалидомида или их фармацевтически приемлемой соли снижает или предупреждает нежелательный эффект; и/или
(e) леналидомид или его фармацевтически приемлемую соль вводят в количестве 2,5, 5, 10, 15 или 25 мг в день.
37. Способ по п. 36, дополнительно предусматривающий после стадии (i):
(ii) прекращение введения леналидомида или помалидомида или их фармацевтически приемлемой соли, где:
(a) у субъекта произошел рецидив, происходит рецидив или ожидается рецидив;
(b) прекращение введения леналидомида или помалидомида или их фармацевтически приемлемой соли осуществляют в ответ на рецидив опухоли у субъекта или в ответ на ожидание рецидива у субъекта; и/или
(c) прекращение введения леналидомида или помалидомида или их фармацевтически приемлемой соли приводит к лечению или предупреждению рецидива опухоли.
38. Способ лечения субъекта, страдающего раком, включающий (i) введение эффективного количества слитого полипептида по любому из пп. 6-22 в комбинации со стабилизирующим соединением, где стабилизирующее соединение представляет собой:
(a) базедоксифен или 4-гидрокситамоксифен (4-OHT) или их фармацевтически приемлемую соль, когда домен деградации представляет собой указанный домен ER;
(b) Shield-1 или его фармацевтически приемлемую соль, где домен деградации представляет собой указанный домен FKBP; или
(c) триметоприм или его фармацевтически приемлемую соль, когда домен деградации представляет собой указанный домен DHFR.
39. Способ по п. 38, дополнительно включающий:
(a) после стадии (i), стадию (ii) прекращения введения стабилизирующего соединения, где:
(I) субъект отвечал на лечение стадии (i) и/или
(II) введение стабилизирующего соединения прекращают при проявлении ответа субъекта на лечение стадии (i);
(b) после стадии (i) стадию (iii) прекращения введения стабилизирующего соединения, где прекращение введения стабилизирующего соединения приводит к лечению или предупреждению нежелательного эффекта; или
(c) после стадии (i) стадию (iv) прекращения введения стабилизирующего соединения и введения субъекту эффективного количества леналидомида или помалидомида или их фармацевтически приемлемой соли, где:
(I) стадия (iv) приводит к лечению или предупреждению нежелательного эффекта или острой токсичности и/или
(II) после стадии (iv) - стадию (v) прекращения введения леналидомида или помалидомида или их фармацевтически приемлемой соли.
40. Способ по п. 38 или 39, где:
(a) уровень экспрессии слитого полипептида в присутствии стабилизирующего соединения выше по меньшей мере в 1,5, 2, 3, 4, 5, 10, 20, 30, 40 или 50 раз, чем уровень экспрессии слитого полипептида в отсутствие стабилизирующего соединения;
(b) способ дополнительно включает после стадий (ii), (iii), (iv) или (v) стадию (vi) введения эффективного количества стабилизирующего соединения, где:
(I) введение стабилизирующего соединения приводит к лечению или предупреждению рецидива опухоли и/или
(II) способ дополнительно включает после стадии (vi) стадию (vii) повторения стадий (iii), (iv), (v) или (vi), таким образом осуществляя лечение рака;
(c) способ дополнительно содержит до стадии (i) стадию (viii) приведения клетки в контакт со стабилизирующим соединением ex vivo, где стабилизирующее соединение представляет собой:
(i) базедоксифен или 4-гидрокситамоксифен (4-OHT) или их фармацевтически приемлемую соль, когда домен деградации представляет собой указанный домен ER;
(ii) Shield-1 или его фармацевтически приемлемую соль, где домен деградации представляет собой указанный домен FKBP; или
(iii) триметоприм или его фармацевтически приемлемую соль, когда домен деградации представляет собой указанный домен DHFR;
(d) клетку не приводят в контакт со стабилизирующим соединением ex vivo до введения; и/или
(e) клетку не приводят в контакт с леналидомидом или помалидомидом или их фармацевтически приемлемой солью ex vivo до введения.
41. Слитый полипептид по любому из пп. 1-22, молекула нуклеиновой кислоты по п. 23, клетка по п. 25 или 26 или фармацевтическая композиция по п. 27, где заболеванием, связанным с экспрессией опухолевым антигеном, является рак.
42. Слитый полипептид, молекула нуклеиновой кислоты, клетка или фармацевтическая композиция по п. 41 или способ по любому из пп. 35-40, где:
(a) рак представляет собой мезотелиому; рак легкого; рак поджелудочной железы; аденокарциному пищевода, рак яичника, рак молочной железы, колоректальный рак, рак мочевого пузыря или любую их комбинацию; или
(b) рак представляет собой гематологический рак.
43. Слитый полипептид, молекула нуклеиновой кислоты, вектор, клетка, фармацевтическая композиция или способ по п. 42, где:
(i) гематологический рак представляет собой лейкоз или лимфома;
(ii) мезотелиома представляет собой злокачественную мезотелиому плевры или мезотелиому у субъекта, у которого имеется прогрессирование на фоне по меньшей мере одной предшествующей стандартной терапии;
(iii) рак легкого представляет собой немелкоклеточный рак легкого, мелкоклеточный рак легкого, плоскоклеточный рак легкого или крупноклеточный рак легкого;
(iv) рак поджелудочной железы представляет собой аденокарциному протоков поджелудочной железы или метастатическую аденокарциному протоков поджелудочной железы (PDA) или рак поджелудочной железы у субъекта, у которого имеется прогрессирование на фоне по меньшей мере одной предшествующей стандартной терапии; или
(v) рак яичника представляет собой серозный эпителиальный рак яичника или рак яичника у субъекта, у которого имеется прогрессирование после по меньшей мере одной предшествующей схемы стандартной терапии.
44. Слитый полипептид, молекула нуклеиновой кислоты, вектор, клетка, фармацевтическая композиция или способ по п. 41, где:
(i) рак выбран из хронического лимфоцитарного лейкоза (CLL), лимфомы из клеток мантийной зоны (MCL), множественной миеломы, острого лимфоидного лейкоза (ALL), лимфомы Ходжкина, B-клеточного острого лимфоидного лейкоза (BALL), T-клеточного острого лимфоидного лейкоза (TALL), малого лимфоцитарного лейкоза (SLL), B-клеточного пролимфоцитарного лейкоза, новообразования из бластных плазмоцитоидных дендритных клеток, лимфомы Беркитта, диффузной В-крупноклеточной лимфомы (DLBCL), DLBCL, ассоциированной с хроническим воспалением, хронического миелоидного лейкоза, миелопролиферативных новообразований, фолликулярной лимфомы, фолликулярной лимфомы у детей, волосатоклеточного лейкоза, мелкоклеточной или крупноклеточной фолликулярной лимфомы, злокачественных лимфопролиферативных состояний, MALT-лимфомы (эстранодальной лимфомы маргинальной зоны из лимфоидной ткани слизистых оболочек), лимфомы маргинальной зоны, миелодисплазии, миелодиспластического синдрома, неходжкинской лимфомы, плазмобластной лимфомы, новообразования из плазмоцитоидных дендритных клеток, макроглобулинемии Вальденстрема, лимфомы маргинальной зоны селезенки, лимфомы/лейкоза селезенки, диффузной мелкоклеточной B-клеточной лимфомы красной пульпы селезенки, варианта волосатоклеточного лейкоза, лимфоплазмоцитарной лимфомы, болезни тяжелых цепей, плазмоклеточной миеломы, солитарной плазмоцитомы кости, внекостной плазмоцитомы, нодальной лимфомы маргинальной зоны, нодальной лимфомы маргинальной зоны у детей, первичной кожной лимфомы из клеток центра фолликула, лимфоматоидного гранулематоза, первичной медиастинальной (тимусной) крупноклеточной B-клеточной лимфомы, внутрисосудистой крупноклеточной B-клеточной лимфомы, ALK+ крупноклеточной B-клеточной лимфомы, крупноклеточной B-клеточной лимфомы, возникающей при HHV8-ассоциированной многоочаговой болезни Кастельмана, первичной выпотной лимфомы, B-клеточной лимфомы, острого миелоидного лейкоза (AML) или неклассифицируемой лимфомы;
(ii) указанная клетка является аутологичной или аллогенной для указанного субъекта; или
(iii) субъекту вводили клетку, экспрессирующую по меньшей мере один слитый полипептид по любому из пп. 1-22, до введения леналидомида или помалидомида или их фармацевтически приемлемой соли.
| WO 2017044801 A2, 16.03.2017 | |||
| LU G | |||
| et al.: "The myeloma drug lenalidomide promotes the cereblon-dependent destruction of Ikaros proteins", Science, 2014, v | |||
| Питательное приспособление к трепальной машине для лубовых растений | 1923 |
|
SU343A1 |
| WO 2015127351 A1, 27.08.2015 | |||
| WO 2017024318 A1, 09.02.2017 | |||
| US 2014090111 A1, 27.04.2014 | |||
| СПОСОБ СКРИНИНГА С ИСПОЛЬЗОВАНИЕМ ФАКТОРА, ЯВЛЯЮЩЕГОСЯ МИШЕНЬЮ ДЛЯ ТАЛИДОМИДА | 2010 |
|
RU2528380C2 |
Авторы
Даты
2024-01-16—Публикация
2018-10-18—Подача