ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящая заявка испрашивает приоритет на основании предварительной заявки США №62/774209, поданной 1 декабря 2018 года; предварительной заявки США №62/816187, поданной 10 марта 2019 года; и предварительной заявки США №62/931487, поданной 6 ноября 2019 года, полное содержание всех из которых включено в настоящее описание посредством ссылки.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[0002] Настоящая заявка включает перечень последовательностей, который был подан в электронном виде в формате ASCII и полное содержание которого включено посредством ссылки. Указанная копия ASCII, созданная 7 ноября 2019 года, называется АТ-022-04WO_SL и ее размер составляет 412161 байт.
УРОВЕНЬ ТЕХНИКИ
[0003] Множественная миелома (ММ) представляет собой злокачественное новообразование, характеризующееся накоплением клональных плазматических клеток. ММ в большинстве случаев остается неизлечимой, и у большинства субъектов со временем развивается резистентность.
[0004] Антиген созревания В-клеток (ВСМА, CD269 или TNFRSF17) является членом суперсемейства рецепторов фактора некроза опухоли (TNFR) и вовлечен в передачу сигнала, способствующую выживанию. ВСМА идентифицировали в злокачественной Т-клеточной лимфоме человека, содержащей транслокацию t(4; 16). ВСМА экспрессируется на высоких уровнях на нормальных и злокачественных плазматических клетках на всех стадиях ММ и некоторых других злокачественных новообразованиях из плазматических клеток (например, диффузная В-крупноклеточная лимфома (ДВКЛ)). ВСМА также экспрессируется на большинстве или на всех клетках миеломы, а экспрессия отсутствует на не-В-клеточных линиях.
[0005] Адоптивный перенос Т-клеток, генетически модифицированных для распознавания антигенов, связанных со злокачественными новообразованиями, является новым перспективным подходом к лечению рака. Т-клетки можно генетически модифицировать для экспрессии химерных антигенных рецепторов (CAR), которые представляют собой слитые белки, состоящие из антигенраспознающего фрагмента и доменов активации Т-клеток.
[0006] В медицине существует неудовлетворенная потребность во вмешательствах, которые могут эффективно лечить ММ, в том числе рецидивирующую/рефрактерную ММ. Согласно настоящему изобретению предложены способы и композиции, которые удовлетворяют эту потребность.
КРАТКОЕ ОПИСАНИЕ
[0007] Согласно настоящему изобретению предложены химерные антигенные рецепторы (CAR), которые связываются с ВСМА; а также подходы к дозированию для применения в лечении множественной миеломы (ММ), включая рецидивирующую и/или рефрактерную ММ.
[0008] Более конкретно, в соответствии с одним из аспектов настоящего изобретения предложен способ лечения ММ у субъекта, включающий введение указанному субъекту по меньшей мере одной дозы аллогенных Т-клеток с химерными антигенными рецепторами (CAR), содержащих CAR к ВСМА человека (ВСМА CAR-T-клетки), при этом указанная по меньшей мере одна доза составляет от примерно 7 х 10∧6 клеток/доза до примерно 480 х 10∧6 клеток/доза.
[0009] В некоторых вариантах реализации масса тела субъекта составляет ≥50 кг, и указанный способ включает введение по меньшей мере одной дозы ВСМА CAR-T-клеток, при этом указанная доза находится в диапазоне от примерно 20 х 10∧6 клеток/доза до примерно 480 х 10∧6 клеток/доза. В некоторых вариантах реализации указанная по меньшей мере одна доза составляет примерно 20 х 10∧6 клеток/доза, примерно 40 х 10∧6 клеток/доза, примерно 120 х 10∧6 клеток/доза, примерно 360 х 10∧6 клеток/доза или примерно 480 х 10∧6 клеток/доза. В некоторых вариантах реализации по меньшей мере одна доза составляет от примерно 20 х 10∧6 клеток/доза до примерно 40 х 10∧6 клеток/доза, от примерно 40 х 10∧6 клеток/доза до примерно 120 х 10∧6 клеток/доза, от примерно 120 х 10∧6 клеток/доза до примерно 360 х 10∧6 клеток/доза или от примерно 360 х 10∧6 клеток/доза до примерно 480 х 10∧6 клеток/доза.
[0010] В некоторых вариантах реализации масса тела субъекта составляет >50 кг, и указанный способ включает введение по меньшей мере одной дозы ВСМА CAR-T-клеток, при этом указанная доза находится в диапазоне от примерно 20 х 10∧6 клеток/доза до примерно 480 х 10∧6 клеток/доза. В некоторых вариантах реализации указанная по меньшей мере одна доза составляет примерно 20 х 10∧6 клеток/доза, примерно 40 х 10∧6 клеток/доза, примерно 160 х 10∧6 клеток/доза, примерно 240 х 10∧6 клеток/доза, примерно 320 х 10∧6 клеток/доза или примерно 480 х 10∧6 клеток/доза. В некоторых вариантах реализации по меньшей мере одна доза составляет от примерно 20 х 10∧6 клеток/доза до примерно 40 х 10∧6 клеток/доза, от примерно 40 х 10∧6 клеток/доза до примерно 160 х 10∧6 клеток/доза, от примерно 160 х 10∧6 клеток/доза до примерно 240 х 10∧6 клеток/доза, от примерно 240 х 10∧6 клеток/доза до примерно 320 х 10∧6 клеток/доза, от примерно 160 х 10∧6 клеток/доза до примерно 320 х 10∧6 клеток/доза или от примерно 320 х 10∧6 клеток/доза до примерно 480 х 10∧6 клеток/доза.
[0011] В некоторых вариантах реализации масса тела субъекта составляет <50 кг, и указанный способ включает введение по меньшей мере одной дозы ВСМА CAR-T-клеток, при этом указанная доза находится в диапазоне от примерно 7 х 10∧6 клеток/доза до примерно 360 х 10∧6 клеток/доза. В некоторых вариантах реализации указанная по меньшей мере одна доза составляет примерно 7 х 10∧6 клеток/доза, примерно 14 х 10∧6 клеток/доза, примерно 20 х 10∧6 клеток/доза, примерно 80 х 10∧6 клеток/доза, примерно 240 х 10∧6 клеток/доза или примерно 360 х 10∧6 клеток/доза. В некоторых вариантах реализации по меньшей мере одна доза составляет от примерно 7 х 10∧6 или 14 х 10∧6 клеток/доза до примерно 20 х 10∧6 клеток/доза, от примерно 20 х 10∧6 клеток/доза до примерно 80 х 10∧6 клеток/доза, от примерно 80 х 10∧6 клеток/доза до примерно 240 х 10∧6 клеток/доза или от примерно 240 х 10∧6 клеток/доза до примерно 360 х 10∧6 клеток/доза.
[0012] В некоторых вариантах реализации масса тела субъекта составляет ≤50 кг, и указанный способ включает введение по меньшей мере одной дозы ВСМА CAR-T-клеток, при этом указанная доза находится в диапазоне от примерно 14 х 10∧6 клеток/доза до примерно 320 х 10∧6 клеток/доза. В некоторых вариантах реализации указанная по меньшей мере одна доза составляет примерно 14 х 10∧6 клеток/доза, примерно 20 х 10∧6 клеток/доза, примерно 80 х 10∧6 клеток/доза, примерно 160 х 10∧6 клеток/доза, примерно 200 х 10∧6 клеток/доза или примерно 320 х 10∧6 клеток/доза. В некоторых вариантах реализации по меньшей мере одна доза составляет от примерно 14 х 10∧6 клеток/доза до примерно 20 х 10∧6 клеток/доза, от примерно 20 х 10∧6 клеток/доза до примерно 80 х 10∧6 клеток/доза, от примерно 80 х 10∧6 клеток/доза до примерно 200 х 10∧6 клеток/доза, от примерно 80 х 10∧6 клеток/доза до примерно 160 х 10∧6 клеток/доза, от примерно 160 х 10∧6 клеток/доза до примерно 200 х 10∧6 клеток/доза или от примерно 200 х 10∧6 клеток/доза до примерно 320 х 10∧6 клеток/доза.
[0013] В некоторых вариантах реализации субъект не получал никакой предшествующей терапии множественной миеломы. В некоторых вариантах реализации субъект получил по меньшей мере один, два или три вида предшествующей терапии множественной миеломы. В некоторых вариантах реализации указанные режимы дозирования представляют собой терапию первой линии. В некоторых вариантах реализации режимы дозирования представляют собой терапию второй линии. В некоторых вариантах реализации режимы дозирования представляют собой терапию третьей линии. В некоторых вариантах реализации режимы дозирования представляют собой терапию четвертой линии.
[0014] В некоторых вариантах реализации у субъекта применяли предшествующий химиотерапевтический режим; предшествующий режим на основе биологических препаратов и/или предшествующий режим на основе терапии аутологичными клетками (например, терапия стволовыми клетками).
[0015] В некоторых вариантах реализации у субъекта рецидивирующая ММ. В некоторых вариантах реализации у субъекта рефрактерная ММ. В некоторых вариантах реализации у субъекта рефрактерная и рецидивирующая ММ.
[0016] В некоторых вариантах реализации ВСМА CAR-T-клетки содержат CAR, содержащий внеклеточный связывающий домен, содержащий одноцепочечный Fv-фрагмент (scFv), при этом указанный scFv содержит вариабельную область тяжелой цепи (VH) и вариабельную область легкой цепи (VL), причем указанная VH-область содержит определяющий комплементарность участок-1 VH (CDR1 VH), определяющий комплементарность участок-2 VH (CDR2 VH) и определяющий комплементарность участок-3 VH (CDR3 VH), и указанная VL-область содержит определяющий комплементарность участок-1 VL(CDR1 VL), определяющий комплементарность участок-2 VL (CDR2 VL) и определяющий комплементарность участок-3 VL (CDR3 VL), где: (a) CDR1 VH содержит аминокислотную последовательность SEQ ID NO: 150, 151 или 152; CDR2 VH содержит аминокислотную последовательность SEQ ID NO: 153 или 154; CDR3 VH содержит аминокислотную последовательность SEQ ID NO: 155; CDR1 VL содержит аминокислотную последовательность SEQ ID NO: 209; CDR2 VL содержит аминокислотную последовательность SEQ ID NO: 221; и CDR3 VL содержит аминокислотную последовательность SEQ ID NO: 222; (b) CDR1 VH содержит аминокислотную последовательность SEQ ID NO: 150, 151 или 152; CDR2 VH содержит аминокислотную последовательность SEQ ID NO: 187 или 188; CDR3 VH содержит аминокислотную последовательность SEQ ID NO: 155; CDR1 VL содержит аминокислотную последовательность SEQ ID NO: 249; CDR2 VL содержит аминокислотную последовательность SEQ ID NO: 221; и CDR3 VL содержит аминокислотную последовательность SEQ ID NO: 225; (c) CDR1 VH содержит аминокислотную последовательность SEQ ID NO: 150, 151 или 152; CDR2 VH содержит аминокислотную последовательность SEQ ID NO: 165 или 166; CDR3 VH содержит аминокислотную последовательность SEQ ID NO: 155; CDR1 VL содержит аминокислотную последовательность SEQ ID NO: 226; CDR2 VL содержит аминокислотную последовательность SEQ ID NO: 221; и CDR3 VL содержит аминокислотную последовательность SEQ ID NO: 227; (d) CDR1 VH содержит аминокислотную последовательность SEQ ID NO: 151, 156 или 157; CDR2 VH содержит аминокислотную последовательность SEQ ID NO: 159 или 162; CDR3 VH содержит аминокислотную последовательность SEQ ID NO: 161; CDR1 VL содержит аминокислотную последовательность SEQ ID NO: 251; CDR2 VL содержит аминокислотную последовательность SEQ ID NO: 252; и CDR3 VL содержит аминокислотную последовательность SEQ ID NO: 253; (e) CDR1 VH содержит аминокислотную последовательность SEQ ID NO: 151, 156 или 157; CDR2 VH содержит аминокислотную последовательность SEQ ID NO: 190 или 191; CDR3 VH содержит аминокислотную последовательность SEQ ID NO: 161; CDR1 VL содержит аминокислотную последовательность SEQ ID NO: 262; CDR2 VL содержит аминокислотную последовательность SEQ ID NO: 252; и CDR3 VL содержит аминокислотную последовательность SEQ ID NO: 263; (f) CDR1 VH содержит аминокислотную последовательность SEQ ID NO: 150, 151 или 152; CDR2 VH содержит аминокислотную последовательность SEQ ID NO: 154 или 169; CDR3 VH содержит аминокислотную последовательность SEQ ID NO: 155; CDR1 VL содержит аминокислотную последовательность SEQ ID NO: 271; CDR2 VL содержит аминокислотную последовательность SEQ ID NO: 221; и CDR3 VL содержит аминокислотную последовательность SEQ ID NO: 272; (g) CDR1 VH содержит аминокислотную последовательность SEQ ID NO: 129, 130 или 131; CDR2 VH содержит аминокислотную последовательность SEQ ID NO: 139 или 140; CDR3 VH содержит аминокислотную последовательность SEQ ID NO: 134; CDR1 VL содержит аминокислотную последовательность SEQ ID NO: 217; CDR2 VL содержит аминокислотную последовательность SEQ ID NO: 210; и CDR3 VL содержит аминокислотную последовательность SEQ ID NO: 216; (h) CDR1 VH содержит аминокислотную последовательность SEQ ID NO: 151, 156 или 157; CDR2 VH содержит аминокислотную последовательность SEQ ID NO: 158 или 159; CDR3 VH содержит аминокислотную последовательность SEQ ID NO: 155; CDR1 VL содержит аминокислотную последовательность SEQ ID NO: 209; CDR2 VL содержит аминокислотную последовательность SEQ ID NO: 221; и CDR3 VL содержит аминокислотную последовательность SEQ ID NO: 225; или (i) CDR1 VH содержит аминокислотную последовательность SEQ ID NO: 129, 130 или 131; CDR2 VH содержит аминокислотную последовательность SEQ ID NO: 132 или 133; CDR3 VH содержит аминокислотную последовательность SEQ ID NO: 137; CDR1 VL содержит аминокислотную последовательность SEQ ID NO: 377; CDR2 VL содержит аминокислотную последовательность SEQ ID NO: 210; и CDR3 VL содержит аминокислотную последовательность SEQ ID NO: 214.
[0017] В некоторых вариантах реализации VH-область scFv CAR-рецептора ВСМА содержит CDR1 VH, содержащий аминокислотную последовательность SEQ ID NO: 150, 151 или 152; CDR2 VH, содержащий аминокислотную последовательность SEQ ID NO: 153 или 154; и CDR3 VH, содержащий аминокислотную последовательность SEQ ID NO: 155; и VL-область scFv содержит CDR1 VL, содержащий аминокислотную последовательность SEQ ID NO: 209; CDR2 VL, содержащий аминокислотную последовательность SEQ ID NO: 221; и CDR3 VL, содержащий аминокислотную последовательность SEQ ID NO: 222.
[0018] В некоторых вариантах реализации VH-область scFv CAR-рецептора ВСМА содержит CDR1 VH, содержащий аминокислотную последовательность SEQ ID NO: 151, 156 или 157; CDR2 VH, содержащий аминокислотную последовательность SEQ ID NO: 158 или 159; и CDR3 VH, содержащий аминокислотную последовательность SEQ ID NO: 155; и VL-область scFv содержит CDR1 VL, содержащий аминокислотную последовательность SEQ ID NO: 209; CDR2 VL, содержащий аминокислотную последовательность SEQ ID NO: 221; и CDR3 VL, содержащий аминокислотную последовательность SEQ ID NO: 225.
[0019] В некоторых вариантах реализации ВСМА CAR-T-клетки содержат CAR, содержащий аминокислотную последовательность, представленную в SEQ ID NO: 344. В некоторых из этих вариантов реализации CAR дополнительно содержит эпитоп CD20. В некоторых из этих вариантов реализации указанный эпитоп CD20 содержит аминокислотную последовательность, представленную в SEQ ID NO: 397 или SEQ ID NO: 398.
[0020] В некоторых вариантах реализации ВСМА CAR-T-клетки содержат CAR, содержащий сигнальный пептид CD8α, имеющий последовательность SEQ ID NO: 318; VH-область, имеющую последовательность SEQ ID NO: 112; линкер GS, имеющий последовательность SEQ ID NO: 333; VL-область, имеющую последовательность SEQ ID NO: 38; шарнирную область CD8α, имеющую последовательность SEQ ID NO: 320; транс мембранный домен CD8α, имеющий последовательность SEQ ID NO: 322; внутриклеточный сигнальный домен 4-1ВВ, имеющий последовательность SEQ ID NO: 323; и внутриклеточный сигнальный домен CD3ζ, имеющий последовательность SEQ ID NO: 324.
[0021] В некоторых вариантах реализации ВСМА CAR-T-клетки содержат CAR, содержащий сигнальный пептид CD8α, имеющий последовательность SEQ ID NO: 318; VH-область, имеющую последовательность SEQ ID NO: 112; линкер GS, имеющий последовательность SEQ ID NO: 333; VL-область, имеющую последовательность SEQ ID NO: 38; эпитоп CD20, имеющий последовательность SEQ ID NO: 398; шарнирную область CD8α, имеющую последовательность SEQ ID NO: 320; трансмембранный домен CD8α, имеющий последовательность SEQ ID NO: 322; внутриклеточный сигнальный домен 4-1ВВ, имеющий последовательность SEQ ID NO: 323; и внутриклеточный сигнальный домен CD3ζ, имеющий последовательность SEQ ID NO: 324.
[0022] В некоторых вариантах реализации ВСМА CAR-T-клетки содержат CAR, содержащий сигнальный пептид CD8α, имеющий последовательность SEQ ID NO: 318; VH-область, имеющую последовательность SEQ ID NO: 33; линкер GS, имеющий последовательность SEQ ID NO: 333; VL-область, имеющую последовательность SEQ ID NO: 34; шарнирную область CD8α, имеющую последовательность SEQ ID NO: 320; транс мембранный домен CD8α, имеющий последовательность SEQ ID NO: 322; внутриклеточный сигнальный домен 4-1ВВ, имеющий последовательность SEQ ID NO: 323; и внутриклеточный сигнальный домен CD3ζ, имеющий последовательность SEQ ID NO: 324.
[0023] В некоторых вариантах реализации ВСМА CAR-T-клетки содержат CAR, содержащий сигнальный пептид CD8α, имеющий последовательность SEQ ID NO: 318; VH-область, имеющую последовательность SEQ ID NO: 33; линкер GS, имеющий последовательность SEQ ID NO: 333; VL-область, имеющую последовательность SEQ ID NO: 34; эпитоп CD20, имеющий последовательность SEQ ID NO: 398; шарнирную область CD8α, имеющую последовательность SEQ ID NO: 320; трансмембранный домен CD8α, имеющий последовательность SEQ ID NO: 322; внутриклеточный сигнальный домен 4-1BB, имеющий последовательность SEQ ID NO: 323; и внутриклеточный сигнальный домен CD3ζ, имеющий последовательность SEQ ID NO: 324.
[0024] В некоторых вариантах реализации ВСМА CAR-T-клетки содержат CAR, содержащий внеклеточный связывающий домен, содержащий одноцепочечный Fv-фрагмент (scFv), при этом указанный scFv содержит VH-область и VL-область, причем комбинация VH- и VL-областей выбрана из комбинаций, представленных в Таблице 1. В некоторых вариантах реализации ВСМА CAR-T-клетки содержат CAR, содержащий внеклеточный лигандсвязывающий домен, первый трансмембранный домен и внутриклеточный сигнальный домен, при этом указанный внеклеточный домен содержит scFv, содержащий вариабельную область тяжелой цепи (VH), содержащую последовательность, представленную в SEQ ID NO: 33, 72, 39, 76, 83, 92, 25, 112 или 8 в Таблице 1; и вариабельную область легкой цепи (VL), содержащую последовательность, представленную в SEQ ID NO: 34, 73, 40, 77, 84, 93, 18, 38 или 80 в Таблице 1, указанный первый трансмембранный домен содержит трансмембранный домен цепи CD8α, и указанный внутриклеточный сигнальный домен содержит сигнальный домен CD3ζ и/или сигнальный домен 4-1ВВ. В некоторых вариантах реализации VH содержит SEQ ID NO: 33, и VL содержит SEQ ID NO: 34. В некоторых вариантах реализации VH содержит SEQ ID NO: 112, и VL содержит SEQ ID NO: 38.
[0025] В некоторых вариантах реализации CAR-T-клетки дефицитны по CD52. В некоторых вариантах реализации CAR-T-клетки дефицитны по TCRα и/или TCRβ. В некоторых вариантах реализации CAR-T-клетки не экспрессируют «защитный выключатель». В некоторых вариантах реализации генотип указанных клеток представляет собой TCRαβ- и CD52+/-.
[0026] В некоторых вариантах реализации субъект получает первый режим лимфодеплеции перед введением по меньшей мере одной дозы. В некоторых вариантах реализации указанный первый режим лимфодеплеции включает введение флударабина и циклофосфамида. В некоторых вариантах реализации первый режим лимфодеплеции включает введение флударабина, циклофосфамида и антитела к CD52. В некоторых вариантах реализации первый режим лимфодеплеции включает введение антитела к CD52. В некоторых вариантах реализации первый режим лимфодеплеции включает введение только антитела к CD52. В некоторых вариантах реализации флударабин вводят в дозе примерно 30 мг/м2/день; циклофосфамид вводят в дозе примерно 300 мг/м2/день; и антитело к CD52 вводят в дозе от примерно 10 до примерно 13 мг/день, от примерно 13 до 20 мг/день, от примерно 13 до 30 мг/день или от примерно 20 до 30 мг/день. В некоторых вариантах реализации первый режим лимфодеплеции начинают примерно за 1-15 дней до введения указанной по меньшей мере одной дозы. В некоторых вариантах реализации первый режим лимфодеплеции применяют на протяжении 1, 2, 3, 4 или 5 дней. В некоторых вариантах реализации первый режим лимфодеплеции применяют за 5 дней до введения указанной по меньшей мере одной дозы на протяжении 3 дней. В некоторых вариантах реализации первый режим лимфодеплеции применяют за 7 дней до введения указанной по меньшей мере одной дозы на протяжении 3 дней.
[0027] В некоторых вариантах реализации субъект получает последующую дозу CAR-T-клеток.
[0028] В соответствии с другим аспектом настоящего изобретения предложен состав, содержащий ВСМА CAR-T-клетки. В одном из вариантов реализации указанный состав содержит раствор, содержащий примерно 5% диметилсульфоксид (ДМСО) и 14 × 10∧6 клеток/мл. В другом варианте реализации клетки получают в смеси CryoStor® Basal Solution и CryoStor® CS10 в соотношении 1:1, что позволяет получить 5% конечную концентрацию диметилсульфоксида, при этом дозировка состава составляет 14×10∧6 клеток/мл, причем генотип клеток представляет собой BCMA-CAR+_TCRαβ-_CD52+/-, и ВСМА CAR-T-клетки содержат CAR, содержащий внеклеточный лигандсвязывающий домен, два ритуксимаб-связывающих домена, первый трансмембранный домен и внутриклеточный сигнальный домен, при этом указанный внеклеточный домен содержит scFv, содержащий вариабельную область тяжелой цепи (VH), содержащую последовательность, представленную в SEQ ID NO: 33, 72, 39, 76, 83, 92, 25, 112 или 8 в Таблице 1; и вариабельную область легкой цепи (VL), содержащую последовательность, представленную в SEQ ID NO: 34, 73, 40, 77, 84, 93, 18, 38 или 80 в Таблице 1, указанный первый трансмембранный домен содержит трансмембранный домен цепи CD8α, и указанный внутриклеточный сигнальный домен содержит сигнальный домен CD3ζ и/или сигнальный домен 4-1ВВ.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0029] На Фиг. 1 показана ВСМА-содержащая CAR-T-клетка согласно настоящему изобретению. CAR содержит функциональный «выключатель», активируемый ритуксимабом и scFv к ВСМА. Указанная модифицированная Т-клетка также демонстрирует снижение экспрессии CD52 (для минимизации отторжения) и генов рецепторов Т-клеток (TCRα и/или TCRβ) (чтобы избежать БТПХ, болезни трансплантат против хозяина).
[0030] На Фиг. 2 показано, что опосредованное ритуксимабом «выключение» обеспечивает обнаружение и деплецию (антителом ритуксимабом) ВСМА-содержащих CAR-T-клеток согласно настоящему изобретению.
[0031] На фиг. 3 показано, что BCMA-scFV-содержащая CAR-T-клетка согласно настоящему изобретению (ВСМА-1) с нокдауном/нокаутом эндогенного гена CD52 не поддается лечению антителом к CD52.
[0032] На Фиг. 4 показана экспрессия ВСМА в клетках-мишенях.
[0033] На фиг. 5 показано, что BCMA-scFV-содержащие CAR-T-клетки согласно настоящему изобретению (ВСМА-1) демонстрируют зависимый от мишени рост и сохраняют активность после повторной стимуляции.
[0034] На Фиг. 6 показано, что ВСМА scFV-содержащие CAR-T-клетки согласно настоящему изобретению (ВСМА-1) проявляют специфическую цитотоксическую активность. ВСМА-1 с нередактированными генами относится к CAR-Т-клеткам, не содержащим нокдаун/нокаут CD52 и/или TCRα, и/или TCRβ.
[0035] На Фиг. 7 показано, что ВСМА scFV-содержащие CAR-T-клетки согласно настоящему изобретению (ВСМА-1) обладают дозозависимой цитотоксической активностью, которая не ингибируется растворимым ВСМА.
[0036] На Фиг. 8-11А и 11В ВСМА scFV-содержащие CAR-T-клетки согласно настоящему изобретению (ВСМА-1) демонстрируют противоопухолевую эффективность в модели ортотопической опухоли и могут быть деплецированы ритуксимабом. На Фиг. 8 показана активность ВСМА scFV-содержащих CAR-T-клеток согласно настоящему изобретению (ВСМА-1) в модели MM.1S. На Фиг. 9 показано влияние ВСМА scFV-содержащих CAR-T-клеток согласно настоящему изобретению (ВСМА-1) на уничтожение опухоли после второй дозы. На Фиг. 10 показано длительное противоопухолевое действие ВСМА scFV-содержащих CAR-T-клеток согласно настоящему изобретению (ВСМА-1) у мышей с добавлением IL-7/IL-15. Использовали модель MOLP-8 у животных. Мышам NSG (N=10) вводили либо 5×106 клеток MM.1S, либо 2×106 клеток MOLP-8. Цитокины обеспечивали посредством AAV-опосредованной доставки генов. Результаты представлены в виде среднего значения ± стандартная ошибка среднего (SEM). На Фиг. 11А - 11В показано, что ритуксимаб истощает ВСМА scFV-содержащие CAR-T-клетки согласно настоящему изобретению (ВСМА-1) в указанной модели (Фиг. 11В) и подавляет противоопухолевую активность (Фиг. 11А).
[0037] На Фиг. 12-15 представлены способы получения ВСМА CAR-T-клеток согласно настоящему изобретению - в частности, ВСМА scFV-содержащие CAR-T-клетки согласно настоящему изобретению (ВСМА-1) могут быть получены в условиях, подобных GMP, с сохранением противоопухолевой активности. На Фиг. 12 представлен типичный способ получения аллогенных CAR-T для ВСМА CAR-T-клеток согласно настоящему изобретению. На Фиг. 13 показана высокая жизнеспособность и рост ВСМА scFV-содержащих CAR-T-клеток согласно настоящему изобретению (ВСМА-1). На Фиг. 14 показано эффективное обогащение TCRαβ-отрицательных клеток. MACS: активируемая магнитным полем сортировка клеток (Miltenyi Biotec). На Фиг. 15 показано сильное противоопухолевое действие различных доз ВСМА scFV-содержащих CAR-T-клеток согласно настоящему изобретению (ВСМА-1) в модели ортотопической опухоли MM.1S.
[0038] На Фиг. 16 показано, что scFv ВСМА-1 не демонстрирует нецелевого связывания в исследованиях тканевой перекрестной реактивности, что указывает на низкий риск нецелевого связывания в клинических условиях или его отсутствие.
[0039] На Фиг. 17 описаны ограничения терапии аутологичными CAR-T.
[0040] На Фиг. 18 описаны преимущества терапии аллогенными CAR-T.
[0041] На Фиг. 19 показана схема исследования фазы 1 (дизайн А или В).
[0042] На Фиг. 20 показана схема исследования фазы 1, дизайн В.
[0043] На Фиг. 21 представлена схематическая диаграмма типичного векторного элемента/конструкции согласно настоящему изобретению.
ПОДРОБНОЕ ОПИСАНИЕ
[0044] Согласно настоящему изобретению предложены химерные антигенные рецепторы (CAR) и иммунные клетки (например, Т-клетки), содержащие CAR (CAR-T-клетки), которые специфично связываются с ВСМА, и режимы дозирования для применения в лечении ММ, включая рефрактерную/рецидивирующую ММ. Согласно настоящему изобретению также предложены полинуклеотиды, кодирующие эти CAR, композиции, содержащие эти CAR-T-клетки, и способы получения и применения этих CAR и CAR-T-клеток.
[0045] Согласно настоящему изобретению предложены CAR, которые связываются с ВСМА (например, ВСМА человека, номер доступа Uniprot: Q02223-2). ВСМА-специфичные CAR, предложенные согласно настоящему изобретению, включают одноцепочечные CAR и многоцепочечные CAR. CAR обладают способностью перенаправлять специфичность и реактивность Т-клеток на ВСМА без ограничения по главному комплексу гистосовместимости (ГКГС), используя антигенсвязывающие свойства моноклональных антител. Неограниченное по ГКГС распознавание антигена наделяет Т-клетки, экспрессирующие CAR, способностью распознавать антиген независимо от процессирования антигена, что таким образом позволяет обойти основной механизм ускользания опухоли.
I. ВСМА-специфичные CAR
[0046] В некоторых вариантах реализации CAR, предложенные согласно настоящему изобретению, содержат внеклеточный лигандсвязывающий домен (например, одноцепочечный вариабельный фрагмент (scFv)), трансмембранный домен и внутриклеточный сигнальный домен. В некоторых вариантах реализации внеклеточный лигандсвязывающий домен, трансмембранный домен и внутриклеточный сигнальный домен находятся в одном полипептиде, т.е. в одной цепи. Согласно настоящему изобретению также предложены многоцепочечные CAR и полипептиды. В некоторых вариантах реализации многоцепочечные CAR содержат: первый полипептид, содержащий транс мембранный домен и по меньшей мере один внеклеточный лигандсвязывающий домен, и второй полипептид, содержащий трансмембранный домен и по меньшей мере один внутриклеточный сигнальный домен, при этом указанные полипептиды вместе образуют многоцепочечный CAR.
[0047] В некоторых вариантах реализации ВСМА-специфичный многоцепочечный CAR основан на рецепторе для IgE с высокой аффинностью (FcsRI). FcsRI, экспрессируемый на тучных клетках и базофилах, запускает аллергические реакции. FcεRI представляет собой тетрамерный комплекс, состоящий из одной субъединицы α, одной субъединицы β и двух связанных дисульфидными связями субъединиц γ. Субъединица а содержит IgE-связывающий домен. Субъединицы β и γ содержат иммунорецепторные тирозиновые активирующие мотивы (ITAM), которые опосредуют передачу сигнала. В некоторых вариантах реализации внеклеточный домен цепи FcRα удален и заменен ВСМА-специфичным внеклеточным лигандсвязывающим доменом. В некоторых вариантах реализации многоцепочечный ВСМА-специфичный CAR содержит scFv, который специфично связывается с ВСМА, шарнирную область CD8α и ITAM цепи FcRβ. В некоторых вариантах реализации CAR может содержать или не содержать цепь FcRγ. В некоторых вариантах реализации присутствуют две копии мимотопа ритуксимаба (например, CPYSNPSLC (SEQ ID NO: 397); см. также WO 2016/120216, полное содержание которого включено в настоящий документ посредством ссылки). Типичная конструкция показана на Фиг. 21.
[0048] Согласно настоящему изобретению внеклеточный лигандсвязывающий домен CAR к ВСМА содержит scFv, содержащий вариабельную область легкой цепи (VL) и вариабельную область тяжелой цепи (VH) моноклонального антитела, специфичного в отношении антигена-мишени, соединенные гибким линкером. Одноцепочечные вариабельные фрагменты получают путем связывания вариабельных областей легкой и/или тяжелой цепи с использованием короткого связывающего пептида (Bird et al., Science 242: 423-426, 1988). Примером связывающего пептида является линкер GS, имеющий аминокислотную последовательность (GGGGS)3 (SEQ ID NO: 333), который образует приблизительно 3,5 нм мостик между карбокси-концом одной вариабельной области и амино-концом другой вариабельной области. Сконструированы и используются линкеры с другими последовательностями (Bird et al., 1988, см. выше). В целом, линкеры могут представлять собой короткие гибкие полипептиды и предпочтительно состоят из примерно 20 или меньше аминокислотных остатков. Линкеры, в свою очередь, можно модифицировать для выполнения дополнительных функций, таких как присоединение лекарственных средств или присоединение к твердым подложкам. Одноцепочечные варианты могут быть получены либо рекомбинантно, либо путем синтеза. Для получения scFv путем синтеза можно использовать автоматический синтезатор. Для рекомбинантного получения scFv подходящая плазмида, содержащая полинуклеотид, кодирующий указанный scFv, может быть введена в подходящую клетку-хозяина, либо эукариотическую, такую как клетки дрожжей, растений, насекомых или млекопитающих, либо прокариотическую, такую как Е. coli. Полинуклеотиды, кодирующие представляющий интерес scFv, можно получить посредством рутинных манипуляций, таких как лигирование полинуклеотидов. Полученный scFv можно выделить с использованием стандартных способов очистки белка, известных в данной области техники.
[0049] В некоторых вариантах реализации настоящего изобретения предложен CAR к ВСМА, при этом указанный CAR содержит внеклеточный связывающий домен, содержащий одноцепочечный Fv-фрагмент (scFv), при этом указанный scFv содержит вариабельную область тяжелой цепи (VH) и вариабельную область легкой цепи (VL), причем VH-область содержит определяющий комплементарность участок-1 VH (CDR1 VH), определяющий комплементарность участок-2 VH (CDR2 VH) и определяющий комплементарность участок-3 VH (CDR3 VH), и VL-область содержит определяющий комплементарность участок-1 VL(CDR1 VL), определяющий комплементарность участок-2 VL (CDR2 VL) и определяющий комплементарность участок-3 VL (CDR3 VL), где: (a) CDR1 VH содержит последовательность, выбранную из группы, состоящей из: SEQ ID NO.: 129, 130, 131, 150, 151, 152, 156, 157, 301, 302, 303, 381, 382, 386, 387 и 388; (b) CDR2 VH содержит последовательность, выбранную из группы, состоящей из: SEQ ID NO.: 132, 133, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 153, 154, 158, 159, 160, 162, 163, 165, 166, 167, 168, 169, 171, 172, 174, 175, 176, 177, 178, 179, 180, 181, 183, 184, 185, 186, 187, 188, 190, 191, 192, 193, 194, 195, 196, 198, 199, 200, 201, 202, 203, 204, 206, 207, 208, 304, 305, 306, 383, 384, 389 и 390; (с) CDR3 VH содержит последовательность, выбранную из группы, состоящей из: SEQ ID NO.: 134, 135, 136, 137, 148, 149, 155, 161, 164, 170, 173, 182, 189, 197, 205, 307, 308, 385 и 391; (d) CDR1 VL содержит последовательность, выбранную из группы, состоящей из: SEQ ID NO.: 209, 212, 215, 217, 218, 219, 223, 226, 228, 230, 232, 235, 238, 239, 241, 243, 245, 246, 247, 249, 250, 251, 254, 257, 260, 262, 265, 266, 267, 269, 270, 271, 273, 275, 277, 279, 283, 285, 287, 290, 292, 295, 297, 299, 309, 377, 415 и 417; (е) CDR2 VL содержит последовательность, выбранную из группы, состоящей из: SEQ ID NO.: 210, 221, 252, 310, 392 и 395; и (f) CDR3 VL содержит последовательность, выбранную из группы, состоящей из: 211, 213, 214, 216, 220, 222, 224, 225, 227, 229, 231, 233, 234, 236, 237, 240, 242, 244, 248, 253, 255, 256, 258, 259, 261, 263, 264, 268, 272, 274, 276, 278, 280, 281, 282, 284, 286, 288, 289, 291, 293, 294, 296, 298, 300, 311, 312, 393 и 416.
[0050] В некоторых вариантах реализации настоящего изобретения предложен CAR к ВСМА, при этом указанный CAR содержит внеклеточный лигандсвязывающий домен, содержащий: VH-область, содержащую CDR1 VH, CDR2 VH и CDR3 VH последовательности VH, представленной в SEQ ID NO: 2, 3, 7, 8, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 35, 37, 39, 42, 44, 46, 48, 50, 52, 54, 56, 58, 60, 62, 64, 66, 68, 70, 72, 74, 76, 78, 83, 87, 92, 95, 97, 99, 101, 104, 106, 110, 112, 114, 76, 118, 120, 122, 125, 127, 313, 314 или 413; и/или VL-область, содержащую CDR1 VL, CDR2 VL и CDR3 VL последовательности VL, представленной в SEQ ID NO: 1, 4, 5, 6, 9, 10, 11, 12, 13, 15, 16, 17, 18, 19, 20, 21, 22, 23, 34, 36, 38, 40, 41, 43, 45, 47, 49, 51, 53, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 317, 81, 82, 84, 85, 86, 88, 89, 90, 91, 93, 94, 96, 98, 100, 102, 103, 105, 107, 108, 109, 111, 113, 115, 116, 117, 119, 121, 123, 124, 126, 128, 315, 316 или 414. В некоторых вариантах реализации VH и VL связаны друг с другом гибким линкером. В некоторых вариантах реализации гибкий линкер содержит аминокислотную последовательность, представленную в SEQ ID NO: 333.
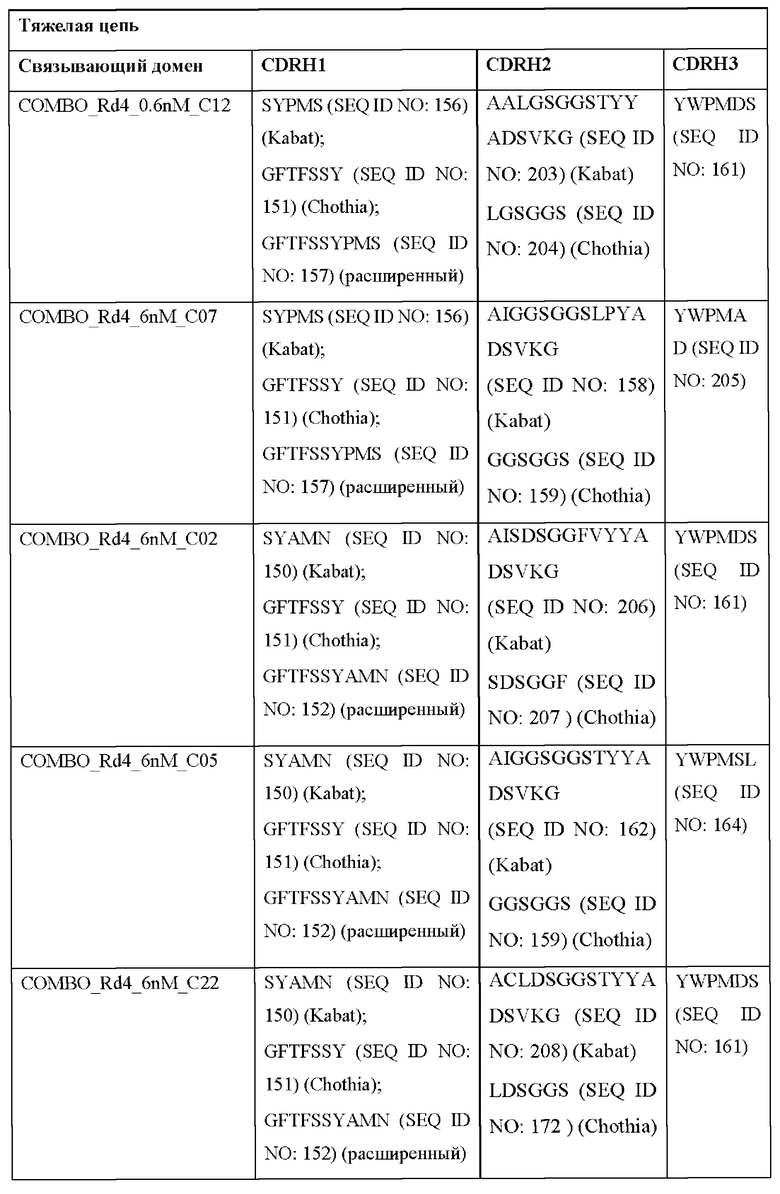
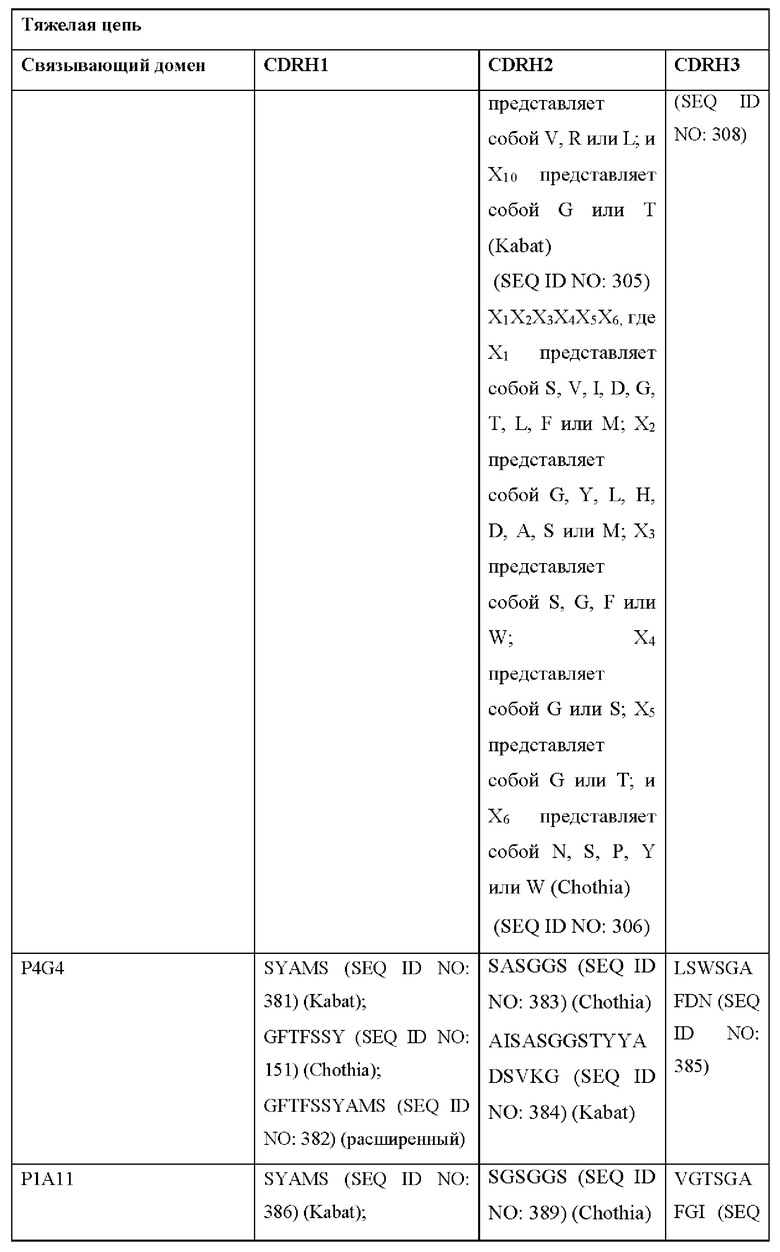
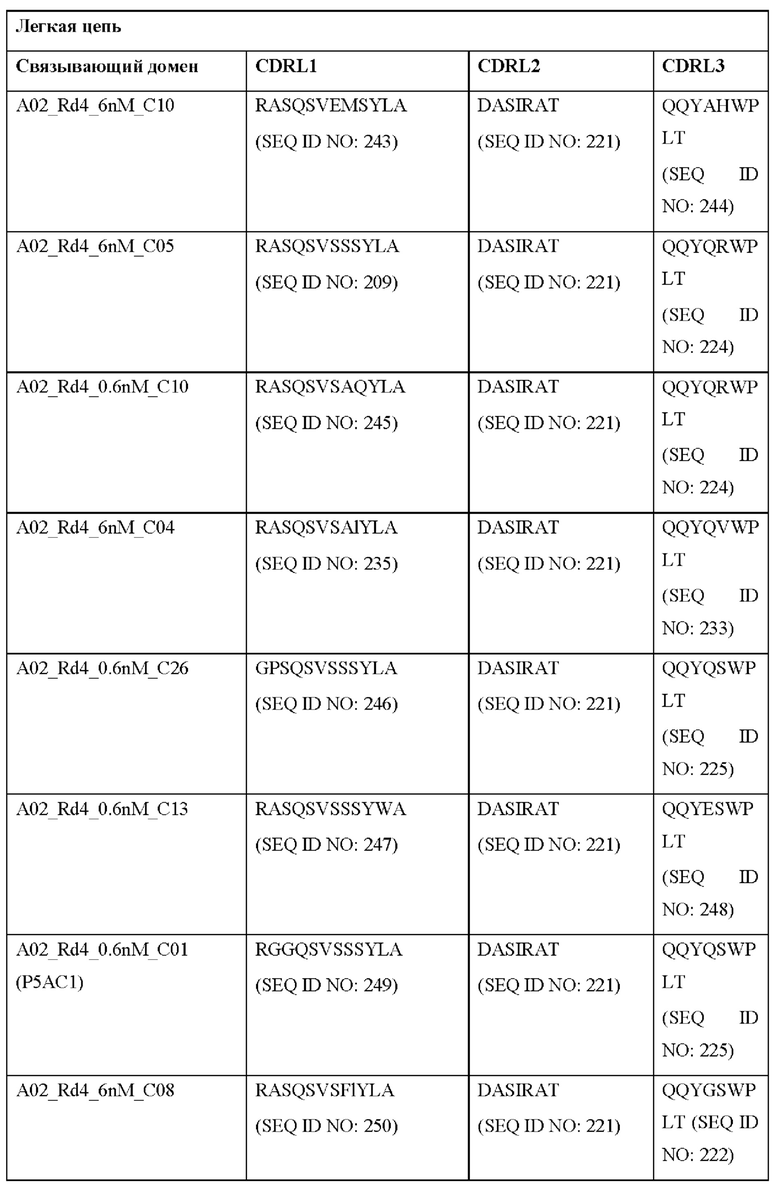
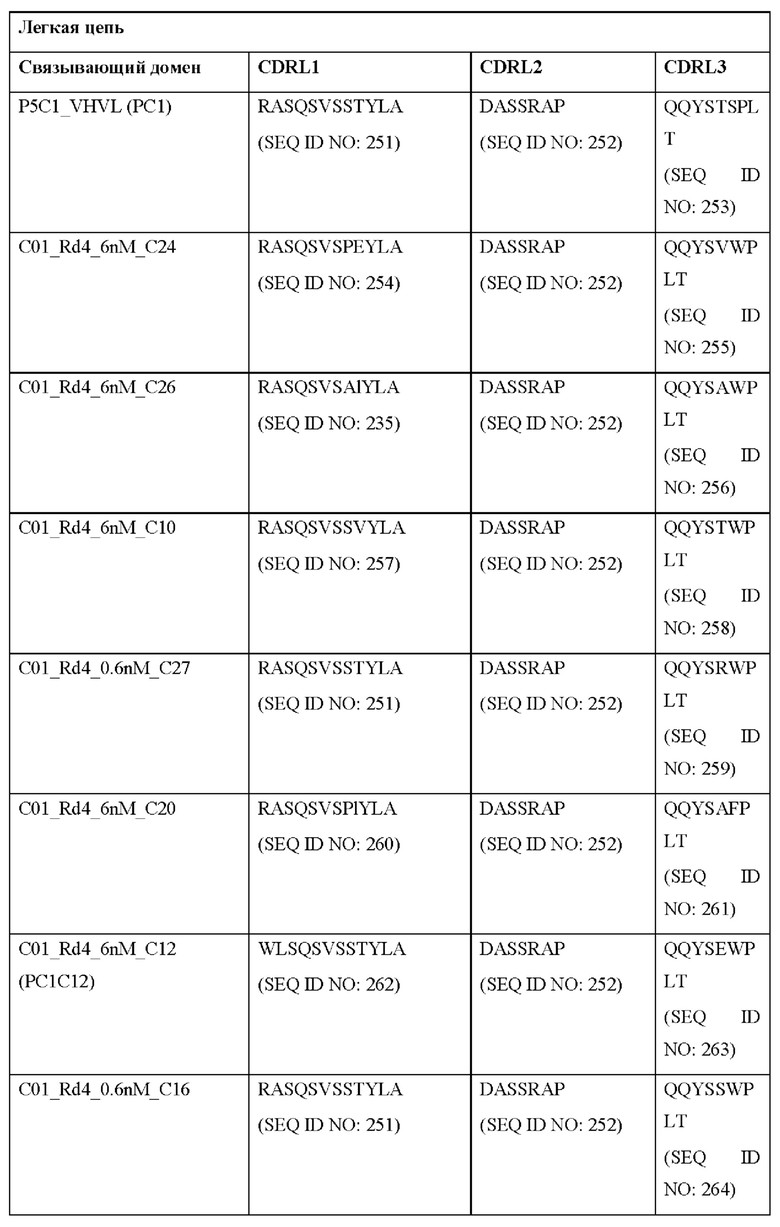
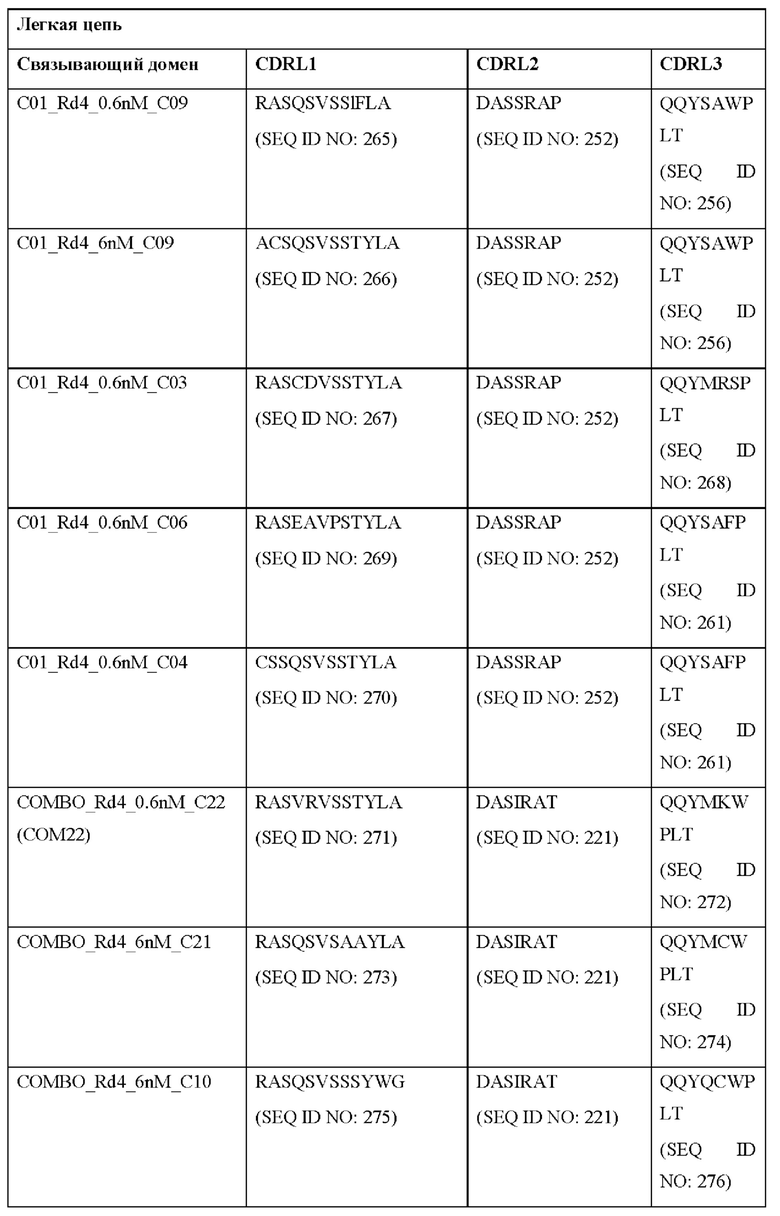
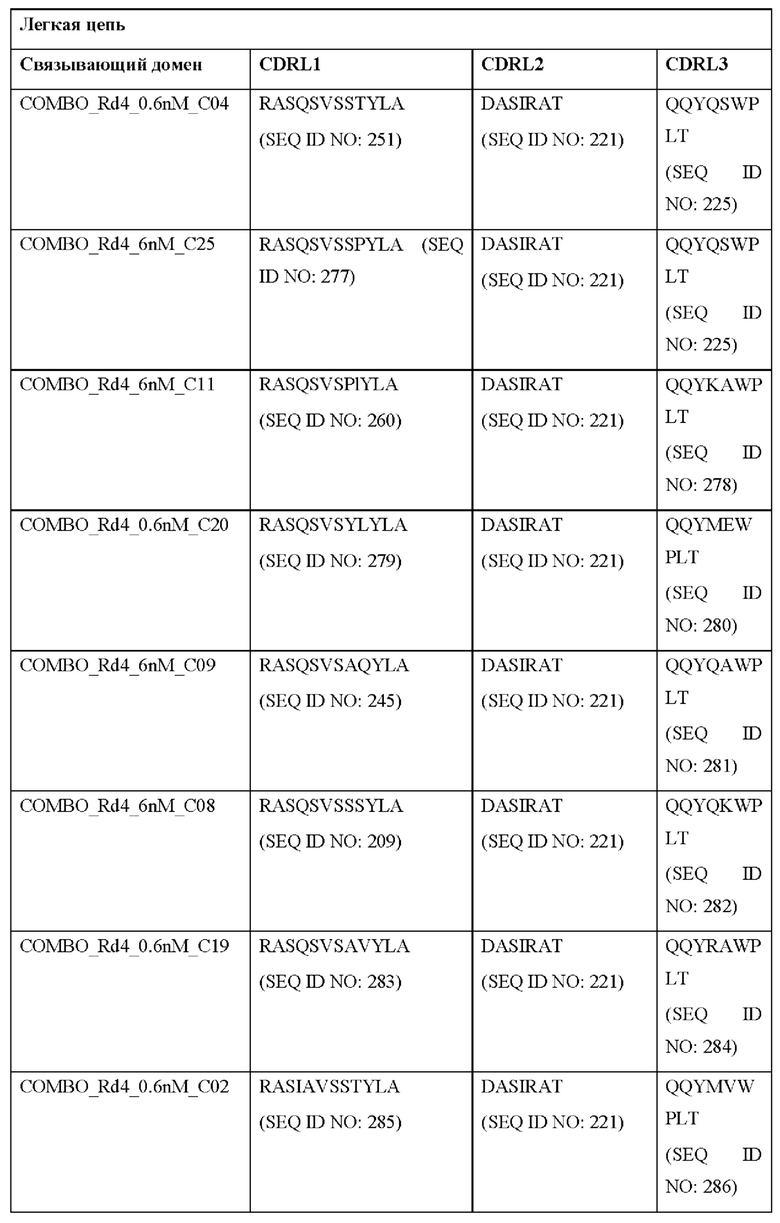
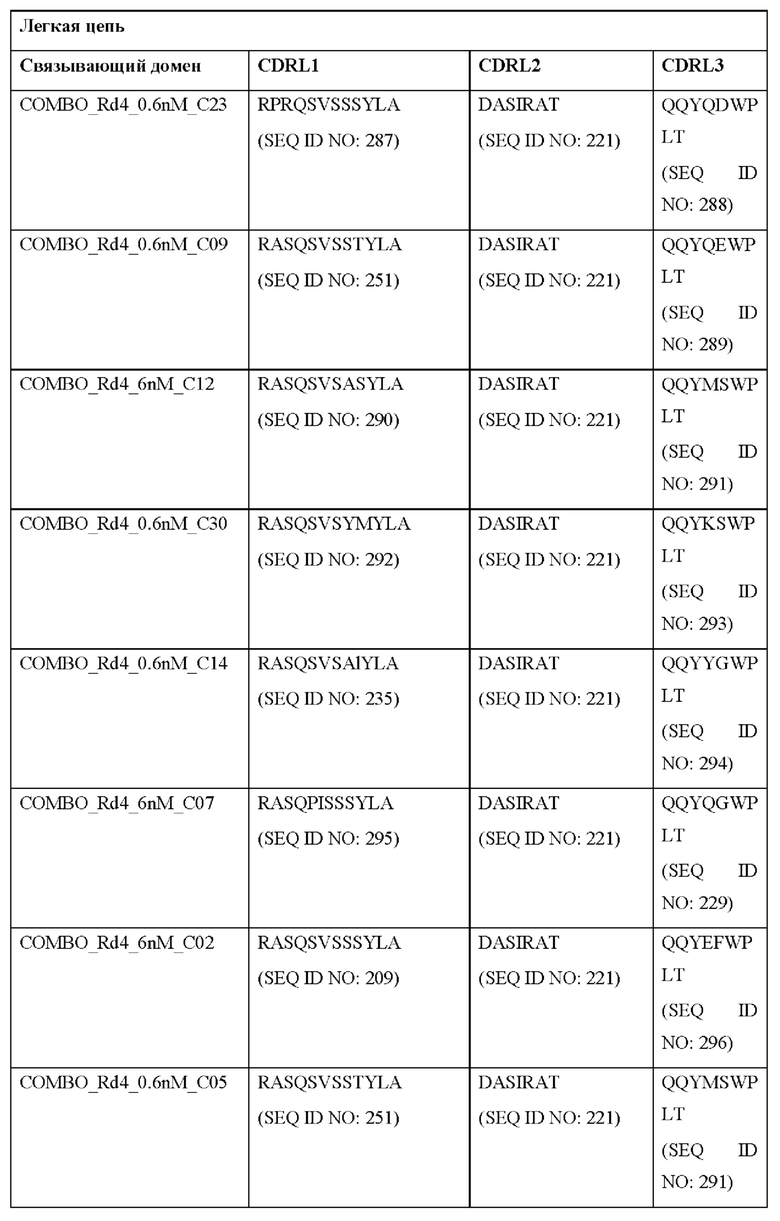
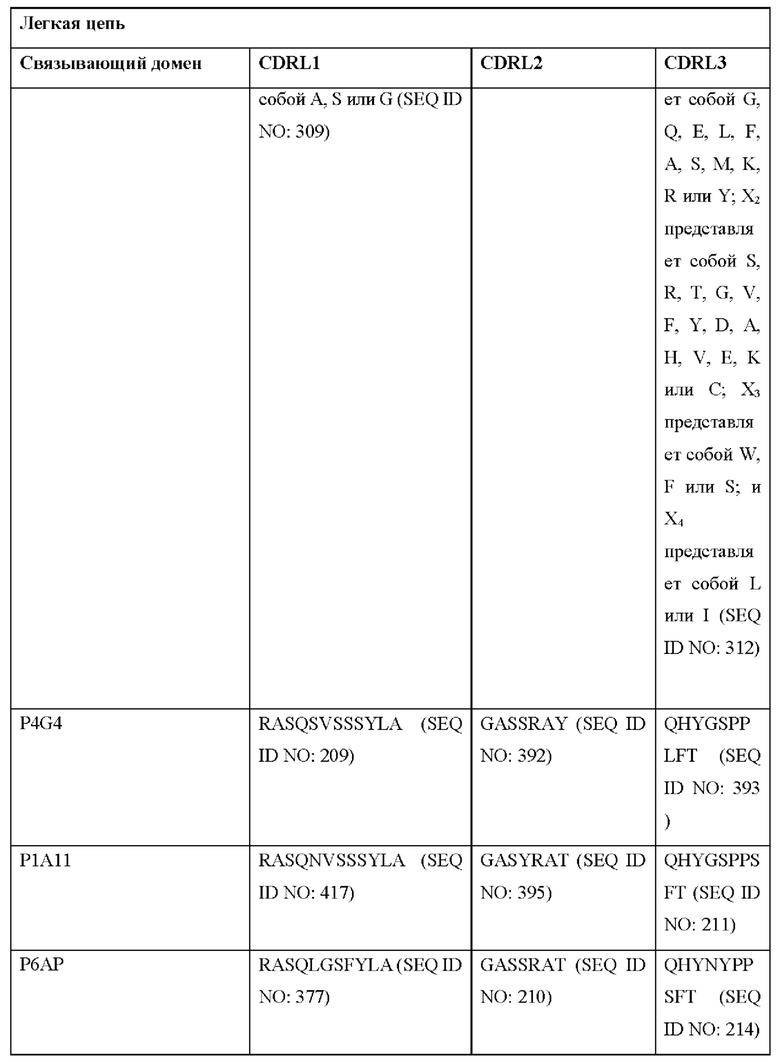
[0051] В некоторых вариантах реализации CAR согласно настоящему изобретению содержит внеклеточный лигандсвязывающий домен, содержащий любую из частичных последовательностей легкой цепи, приведенных в Таблице 1, и/или любую из частичных последовательностей тяжелой цепи, приведенных в Таблице 1. В Таблице 1 подчеркнутые последовательности представляют собой последовательности CDR согласно Kabat, а выделенные жирным шрифтом - согласно Chothia, за исключением следующих последовательностей CDR2 тяжелой цепи, в которых последовательность CDR согласно Chothia подчеркнута, а последовательность CDR согласно Kabat выделена жирным шрифтом: Р5А2_VHVL, А02_Rd4_0.6nM_С06, А02_Rd4_0.6nM_С09, А02_Rd4_6nM_С16, А02_Rd4_6nM_С03, А02_Rd4_6nM_С01, А02_Rd4_6nM_С26, А02_Rd4_6nM_С25, A02_Rd4_6nM_C22, A02_Rd4_6nM_C19, A02_Rd4_0.6nM_C03, A02_Rd4_6nM_C07, A02_Rd4_6nM_C23, A02_Rd4_0.6nM_С18, A02_Rd4_6nM_С10, А02_Rd4_6nM_С05, A02_Rd4_0.6nM_C10, A02_Rd4_6nM_C04, A02_Rd4_0.6nM_C26, A02_Rd4_0.6nM_C13, A02_Rd4_0.6nM_C01, A02_Rd4_6nM_C08, P5C1VHVL, C01_Rd4_6nM_C24, C01_Rd4_6nM_C26, C01_Rd4_6nM_С10, C01_Rd4_0.6nM_C27, C01_Rd4_6nM_C20, C01_Rd4_6nM_С12, C01_Rd4_0.6nM_С16, C01_Rd4_0.6nM_C09, C01_Rd4_6nM_C09, C01_Rd4_0.6nM_C03, C01_Rd4_0.6nM_C06, C01_Rd4_6nM_C04, COMBO_Rd4_0.6nM_C22, COMBO_Rd4_6nM_C21, COMBO_Rd4_6nM_C10, COMBO_Rd4_0.6nM_C04, COMBO_Rd4_6nM_C25, COMBO_Rd4_0.6nM_C21, COMBO_Rd4_6nM_С11, COMBO_Rd4_0.6nM_C20, COMBO_Rd4_6nM_C09, COMBO_Rd4_6nM_C08, COMBO_Rd4_0.6nM_C19, COMBO_Rd4_0.6nM_C02, COMBO_Rd4_0.6nM_C23, COMBO_Rd4_0.6nM_C29, COMBO_Rd4_0.6nM_C09, COMBO_Rd4_6nM_С12, COMBO_Rd4_0.6nM_C30, COMBO_Rd4_0.6nM_С14, COMBO_Rd4_6nM_C07, COMBO_Rd4_6nM_C02, COMBO_Rd4_0.6nM_C05, COMBO_Rd4_0.6nM_C17, COMBO_Rd4_6nM_C22 и COMBO_Rd4_0.6nM_C11.
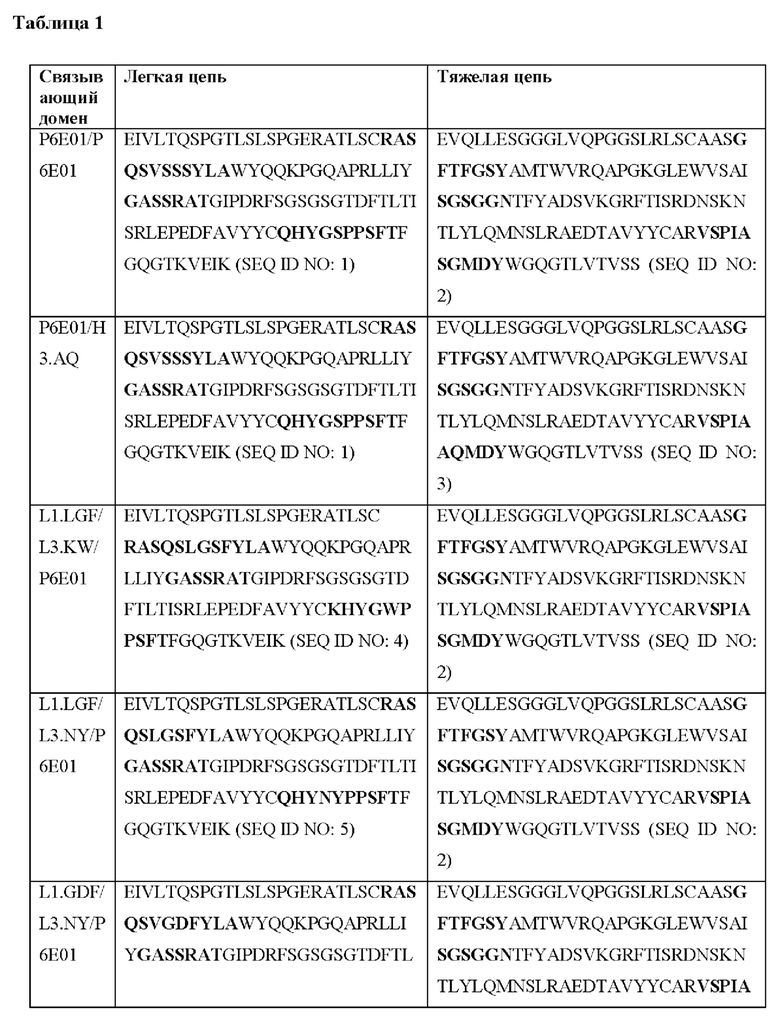
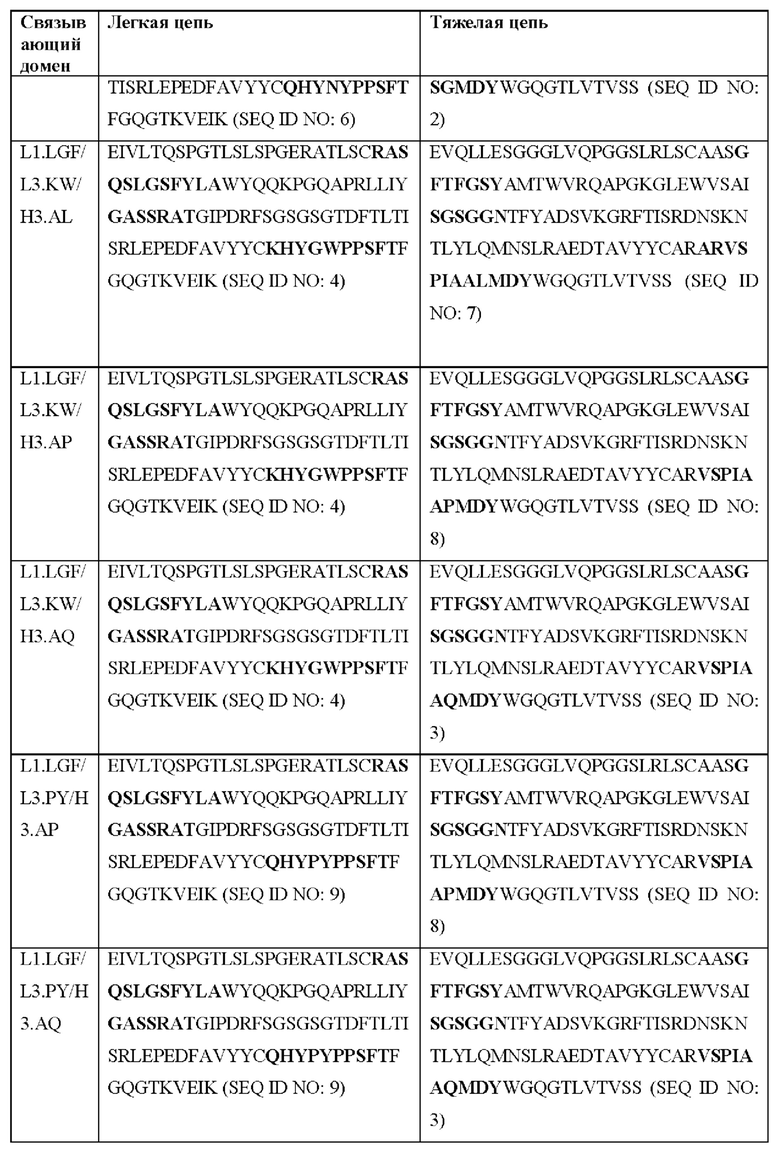
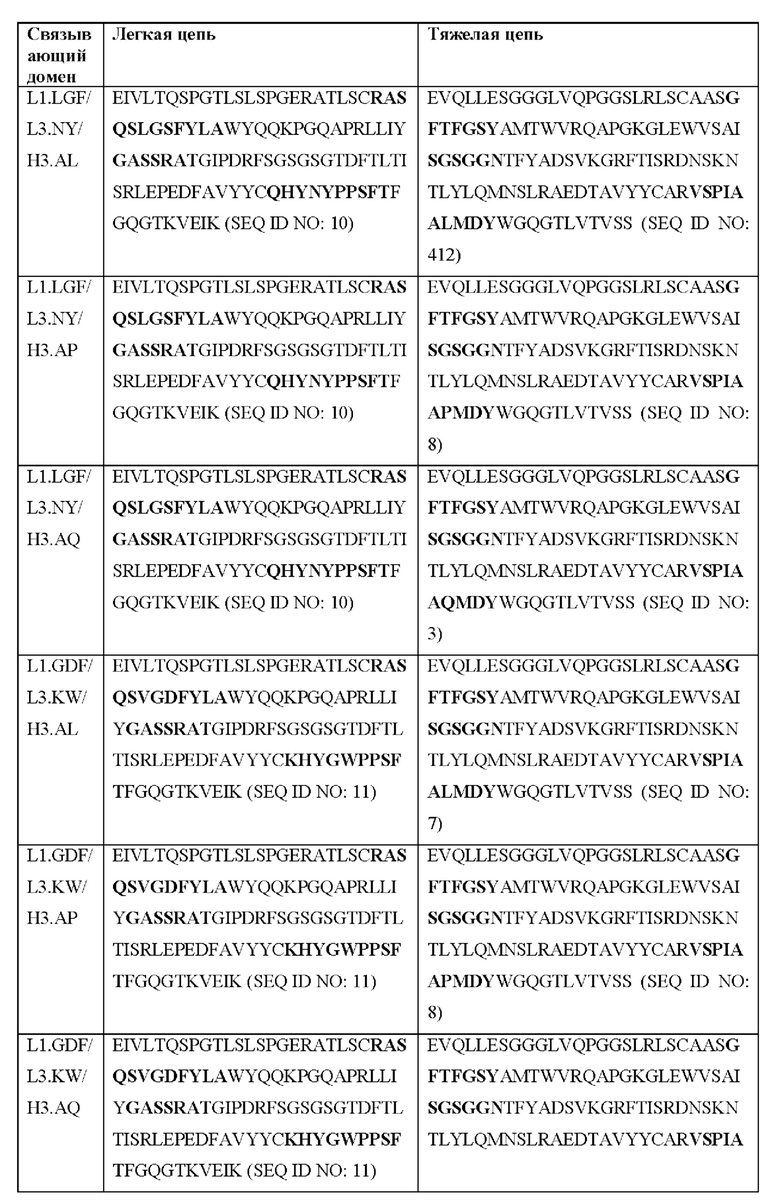
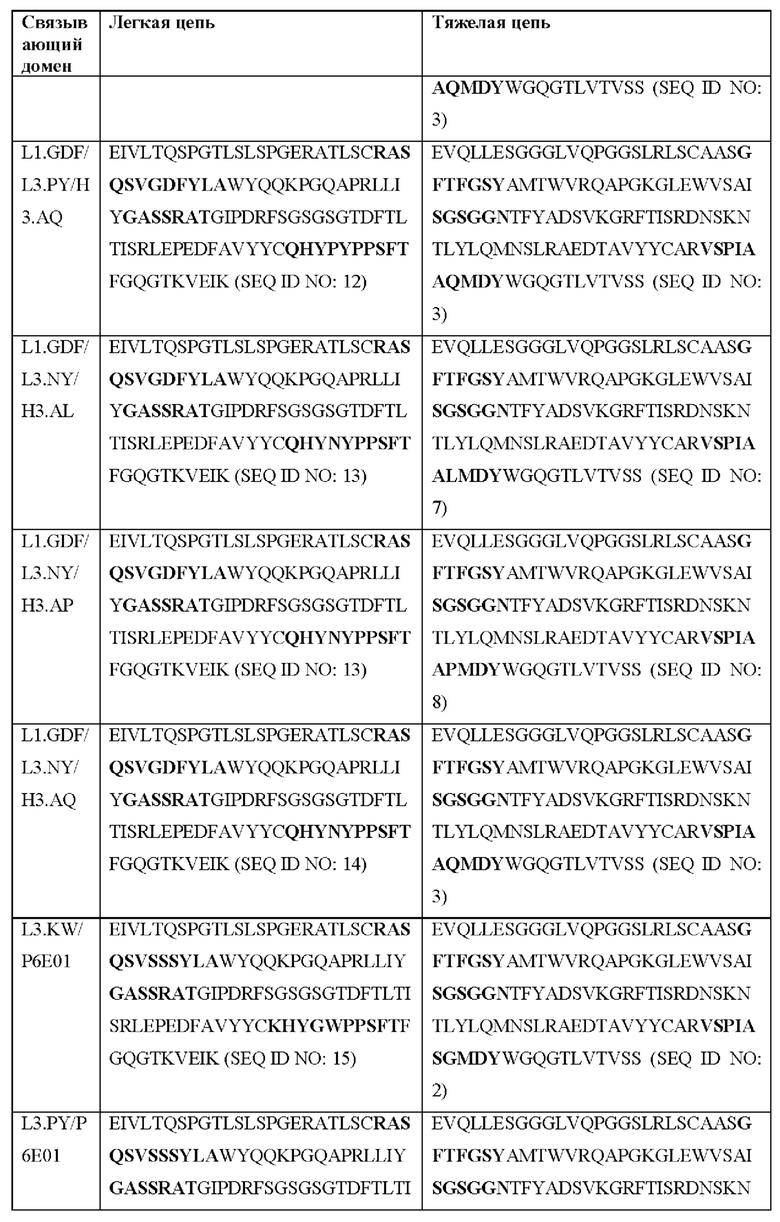
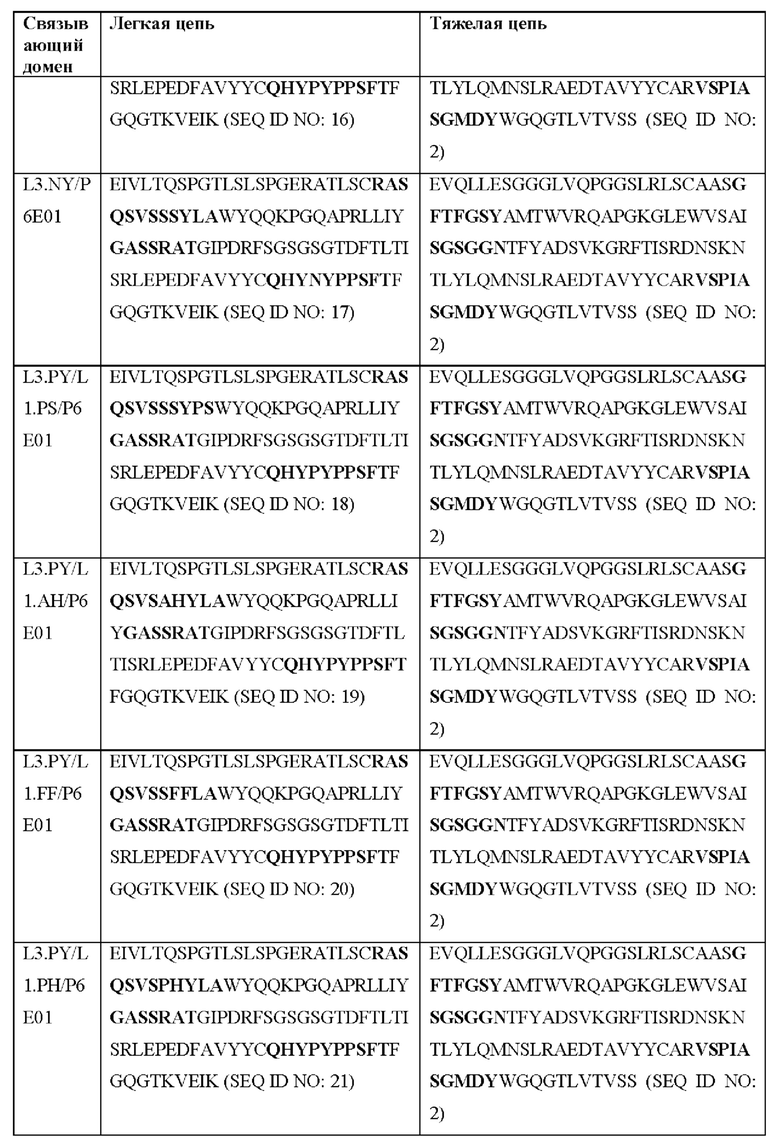

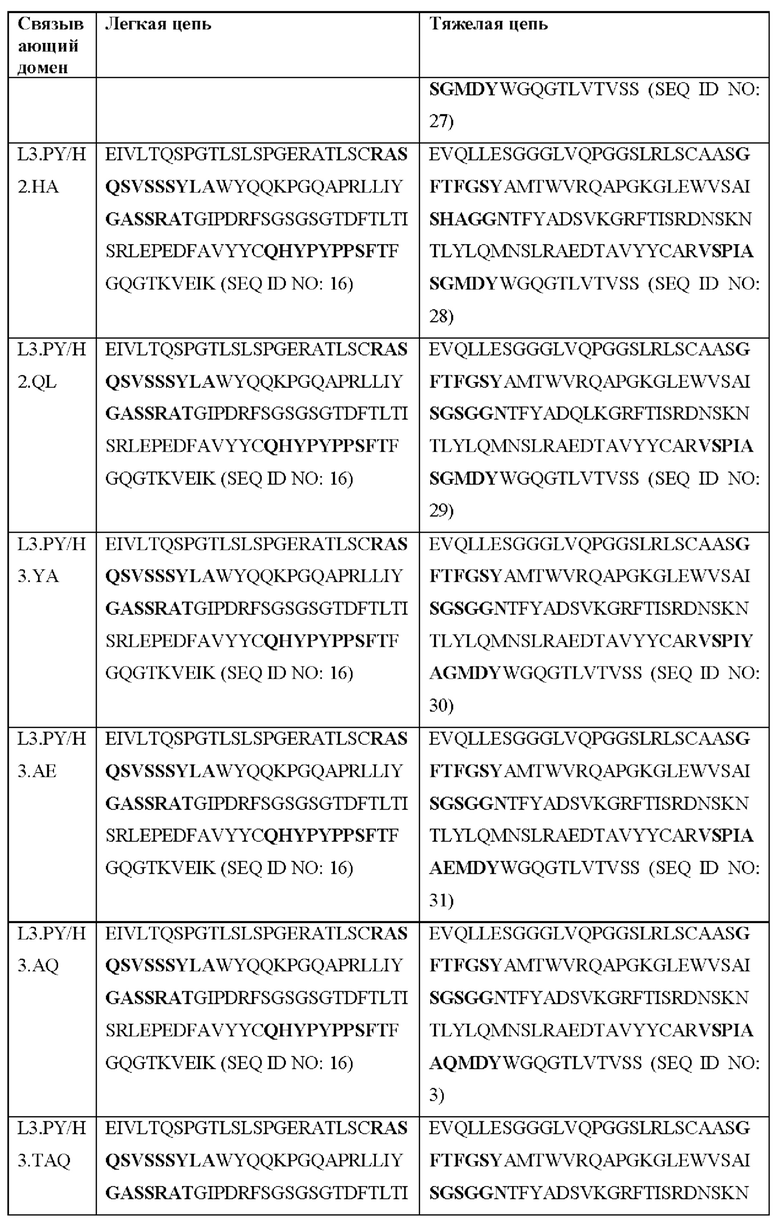
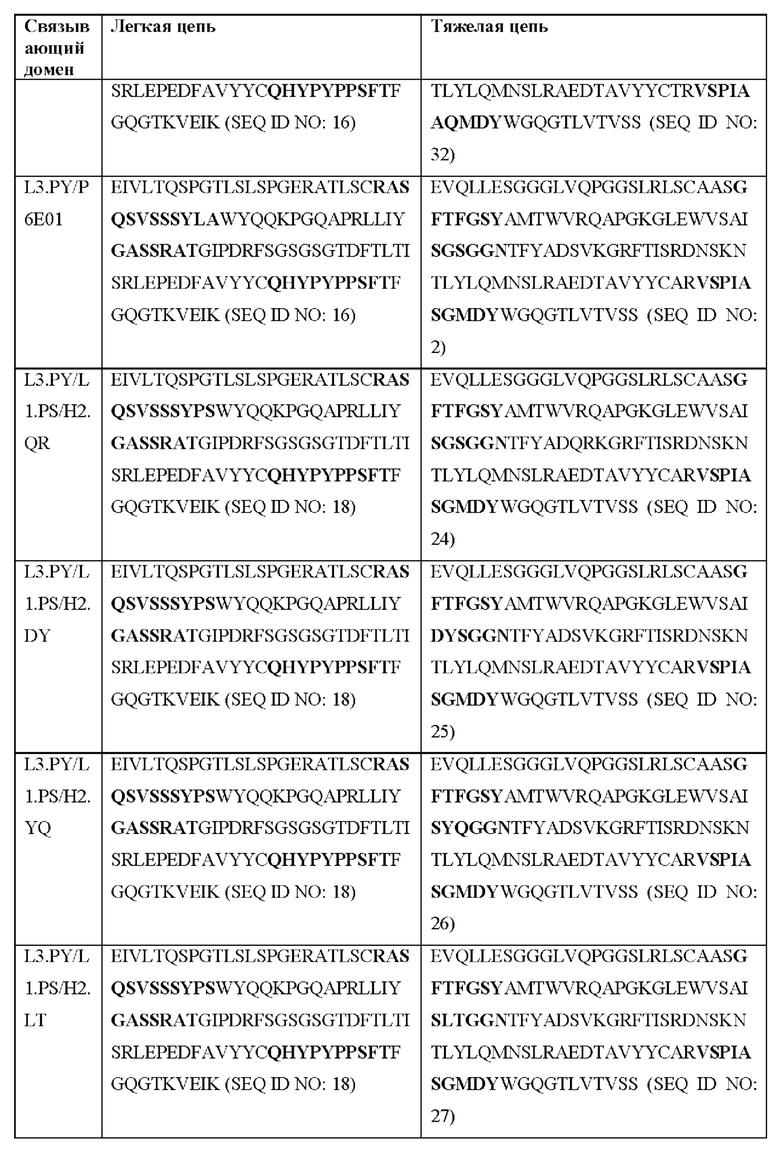
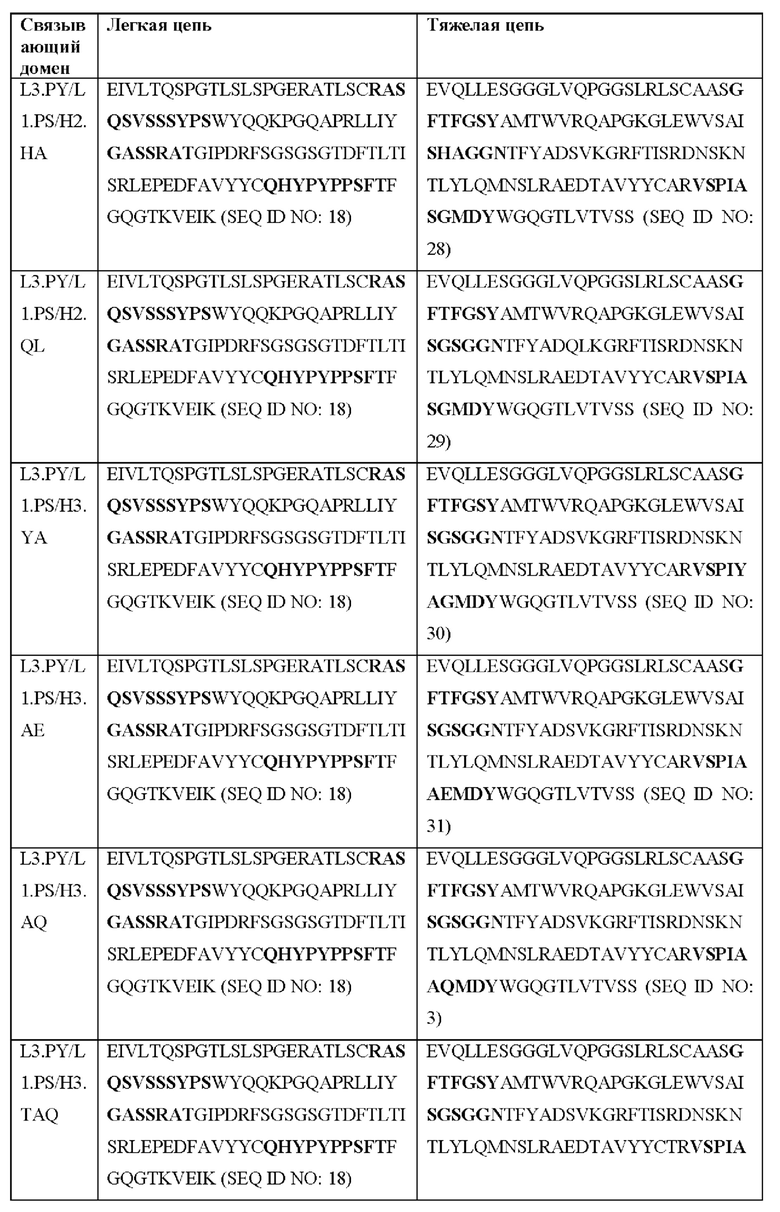
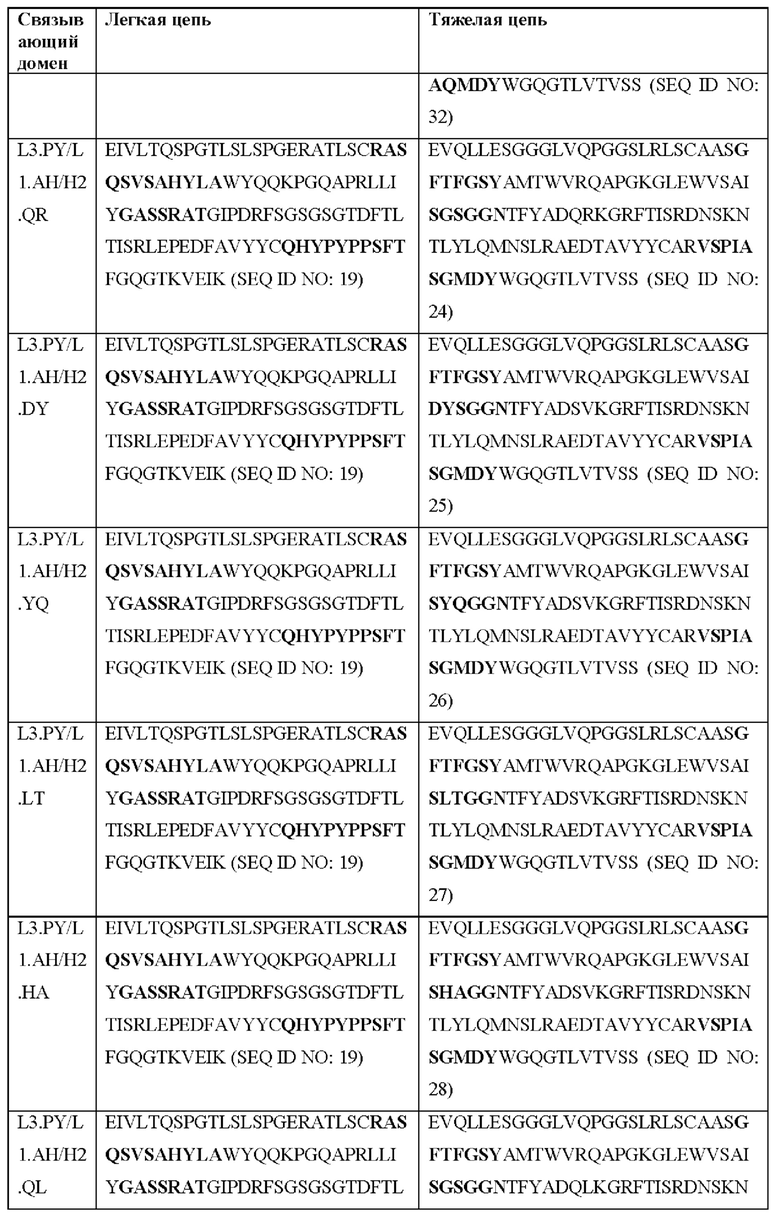
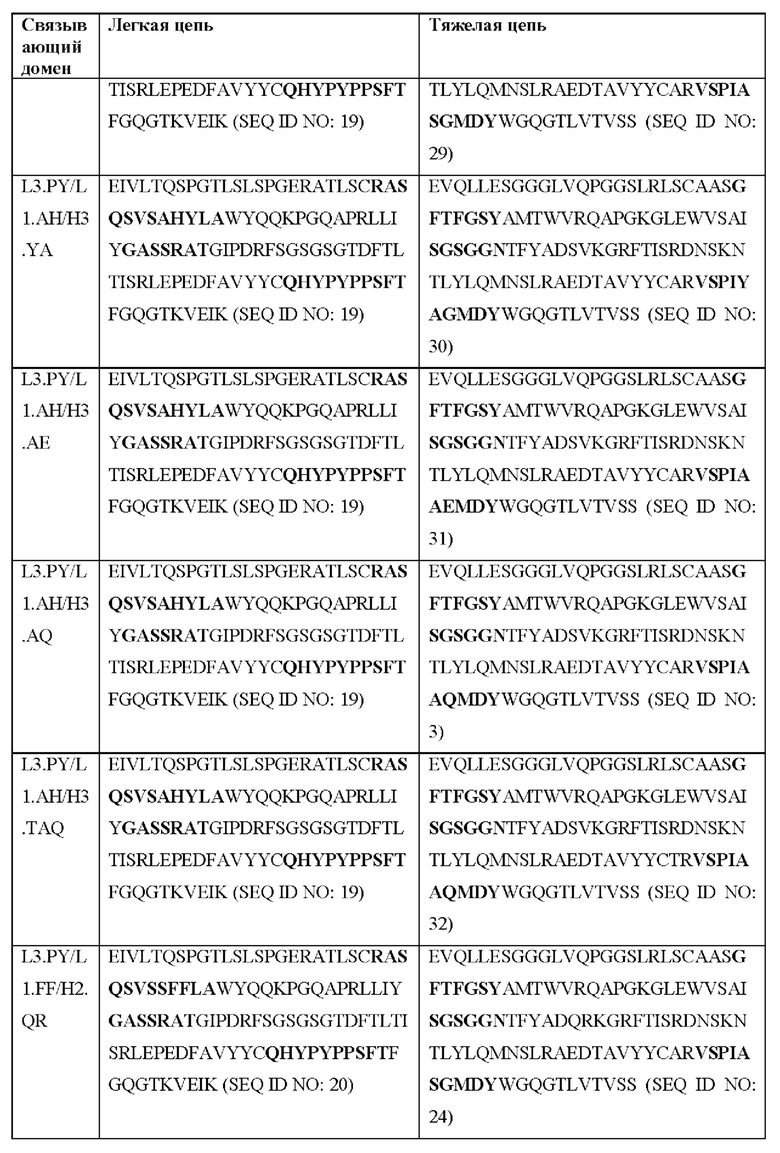
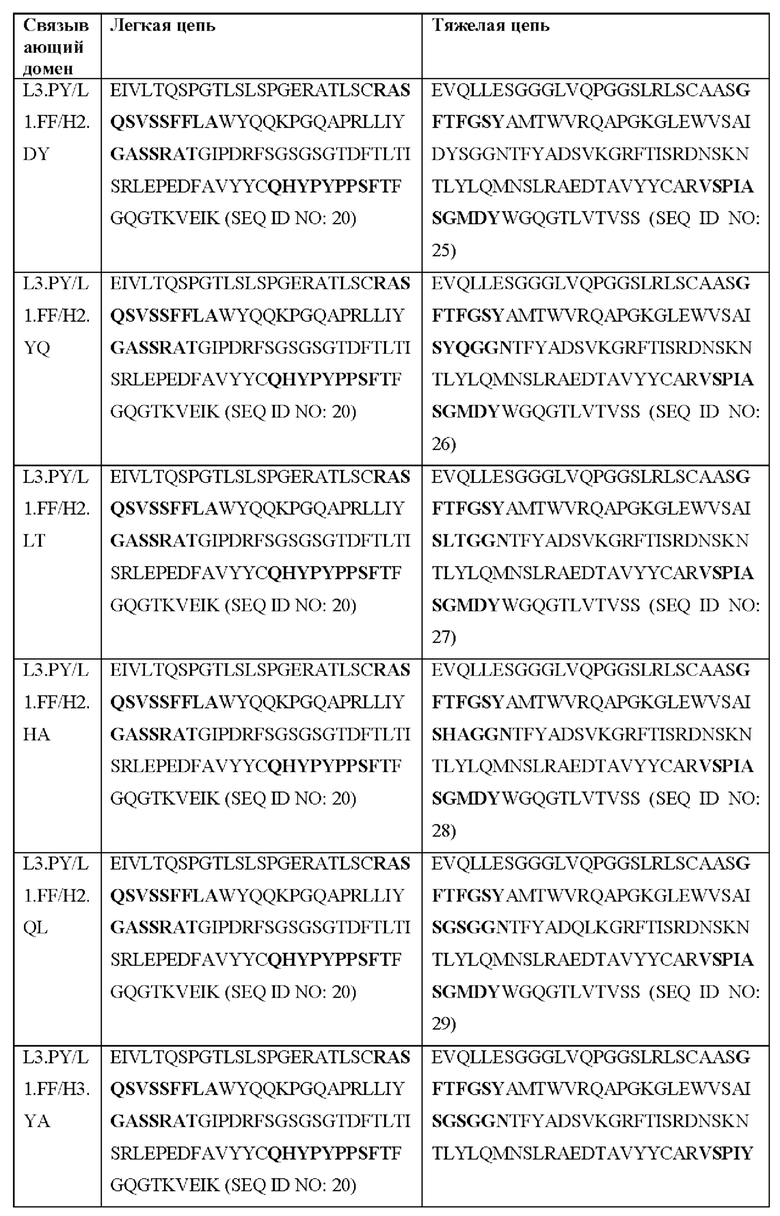
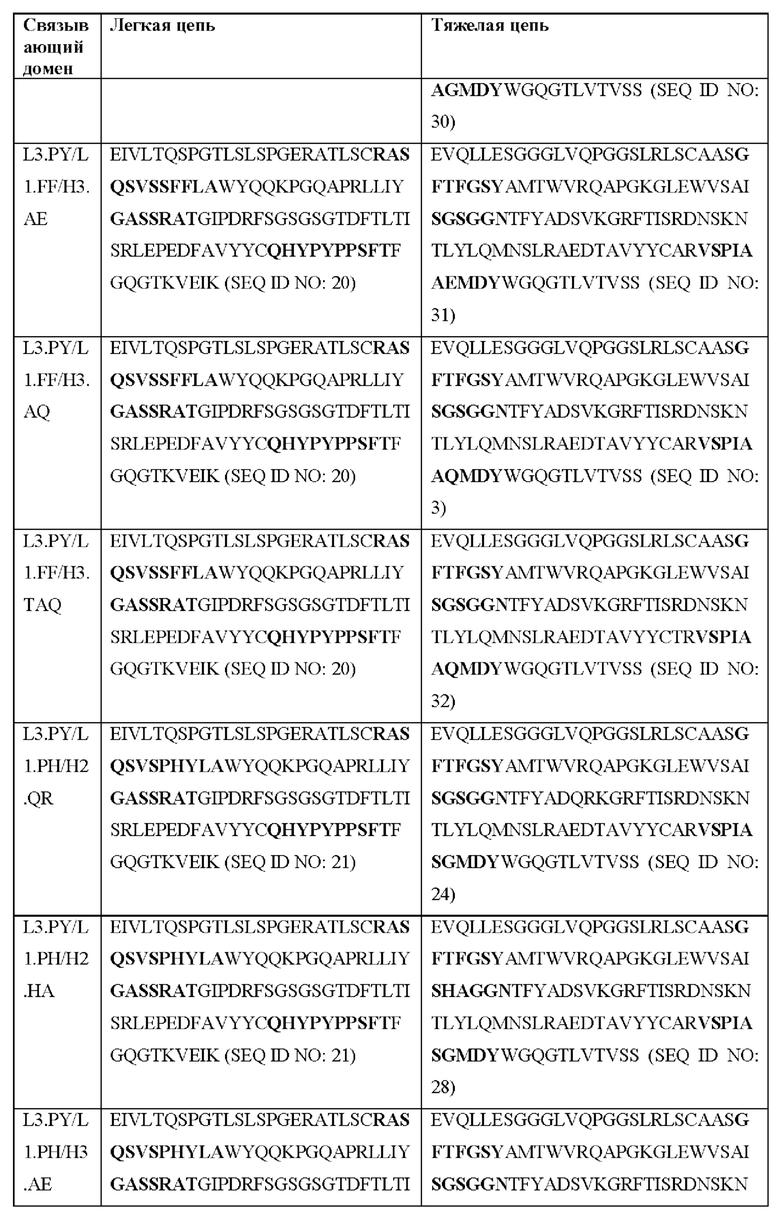
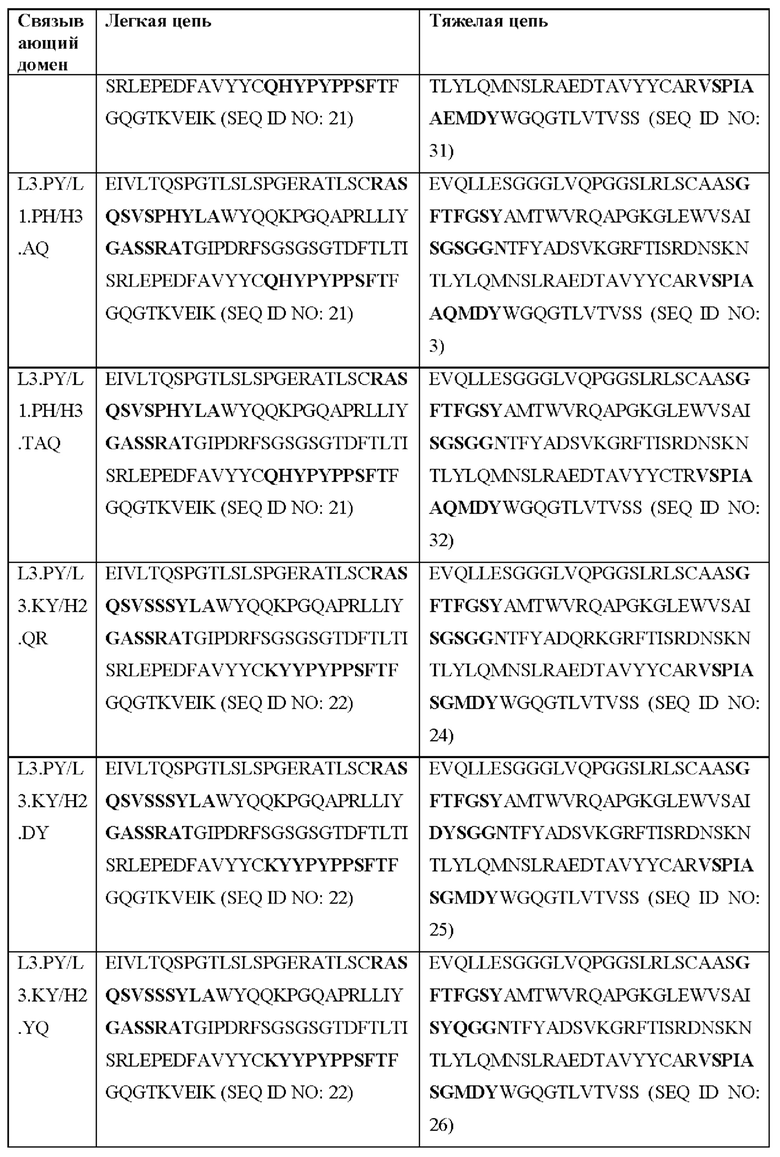
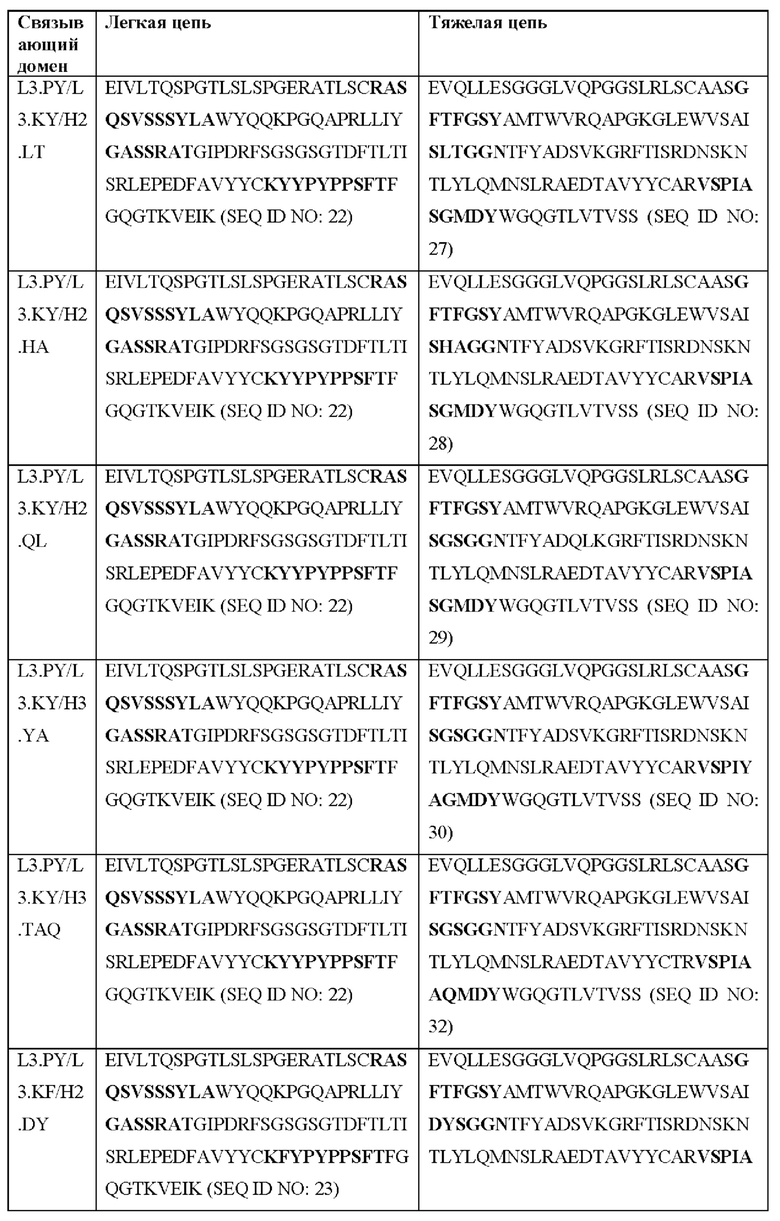
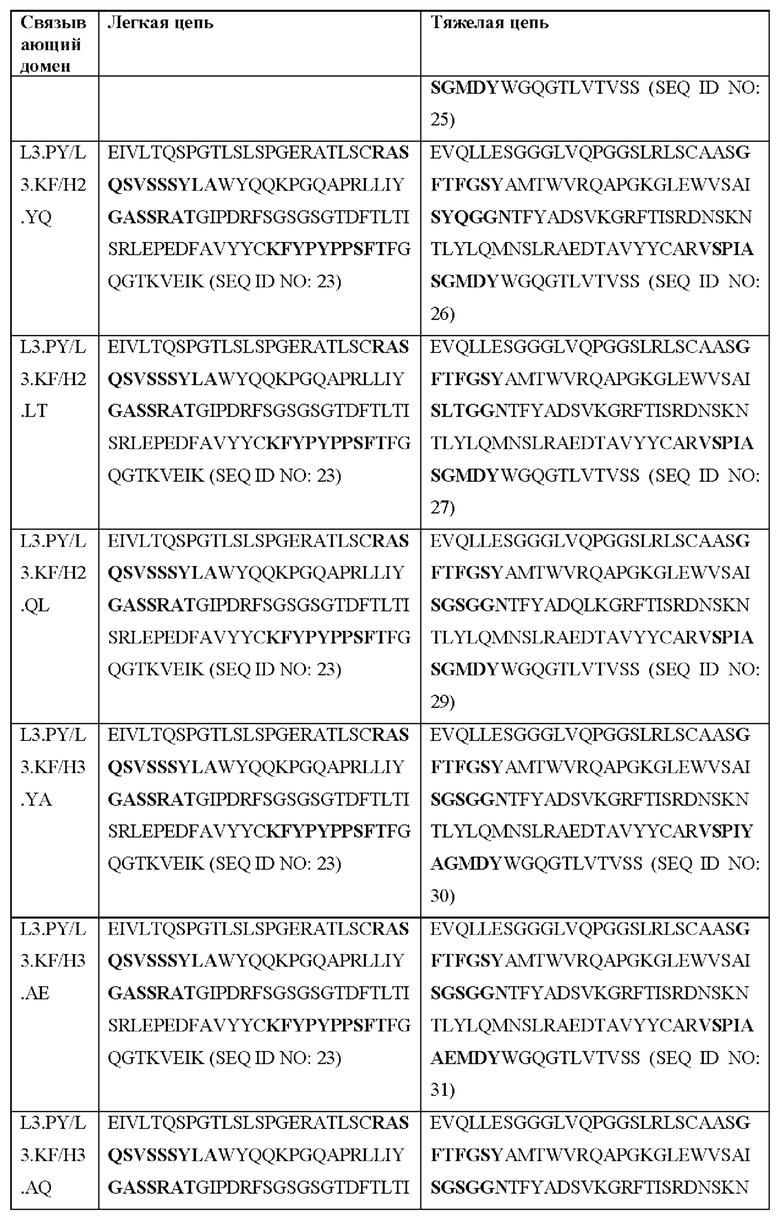
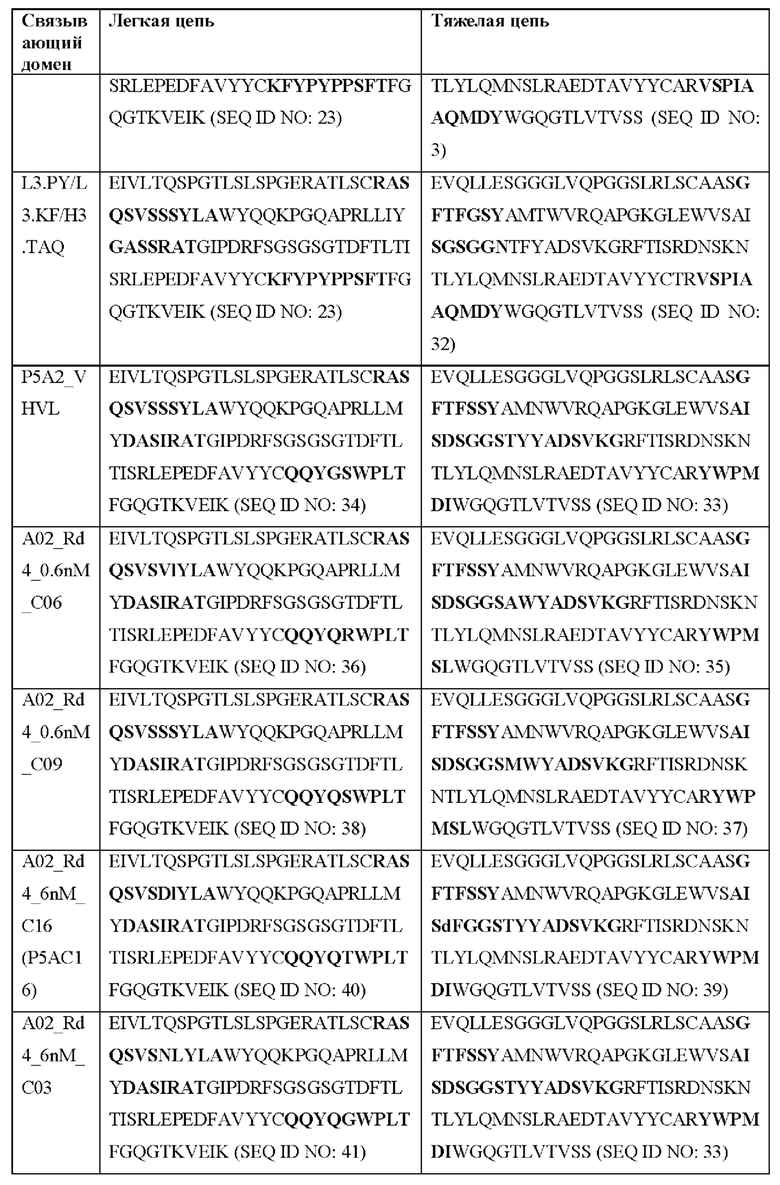
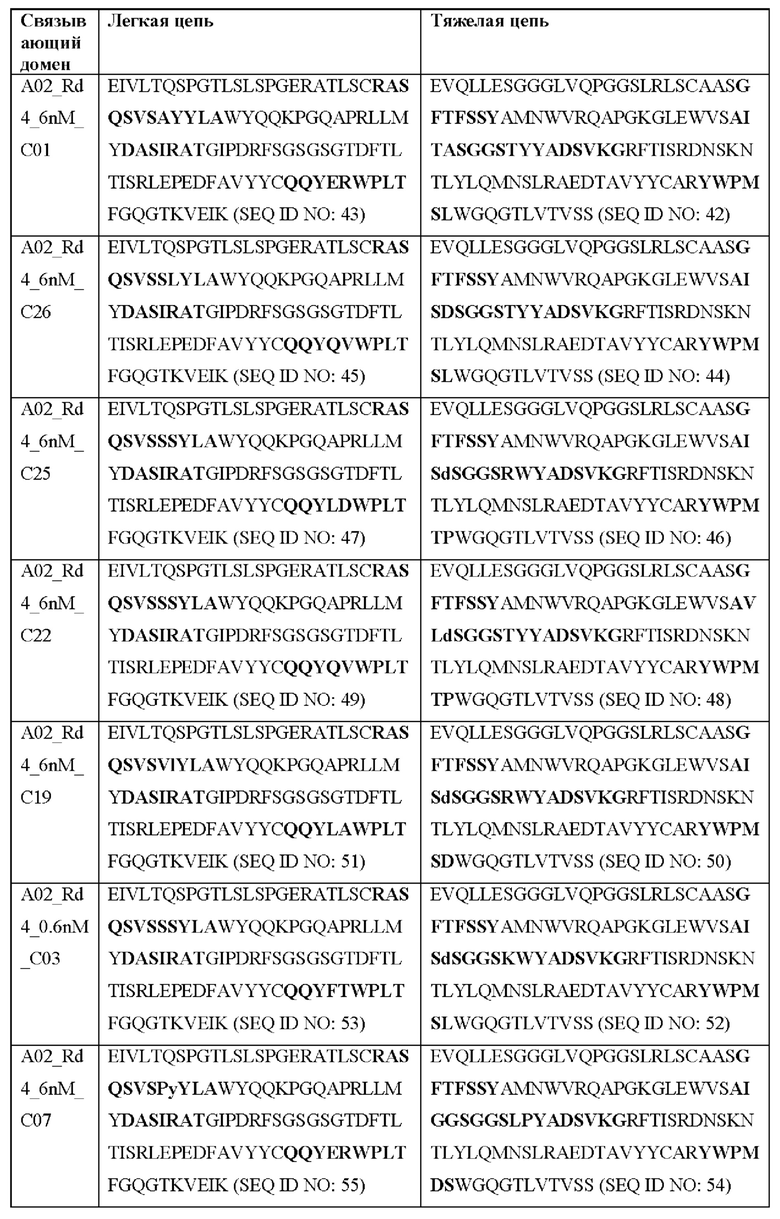
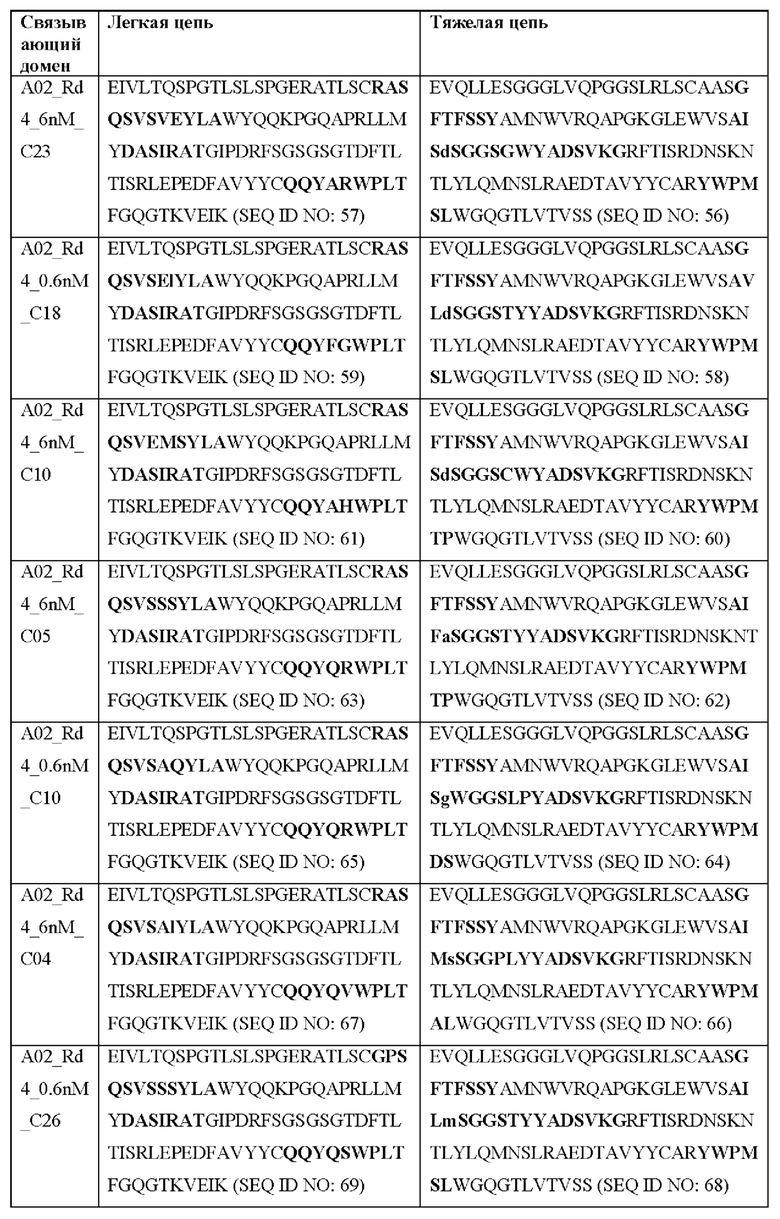
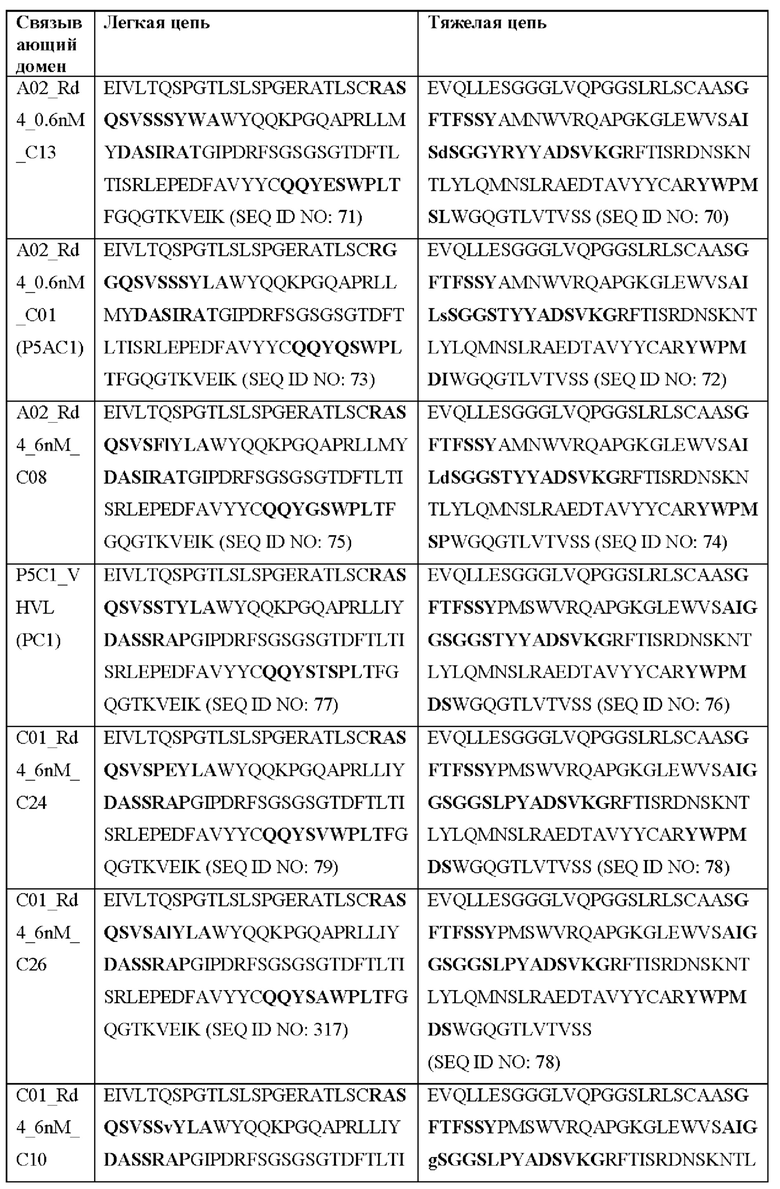
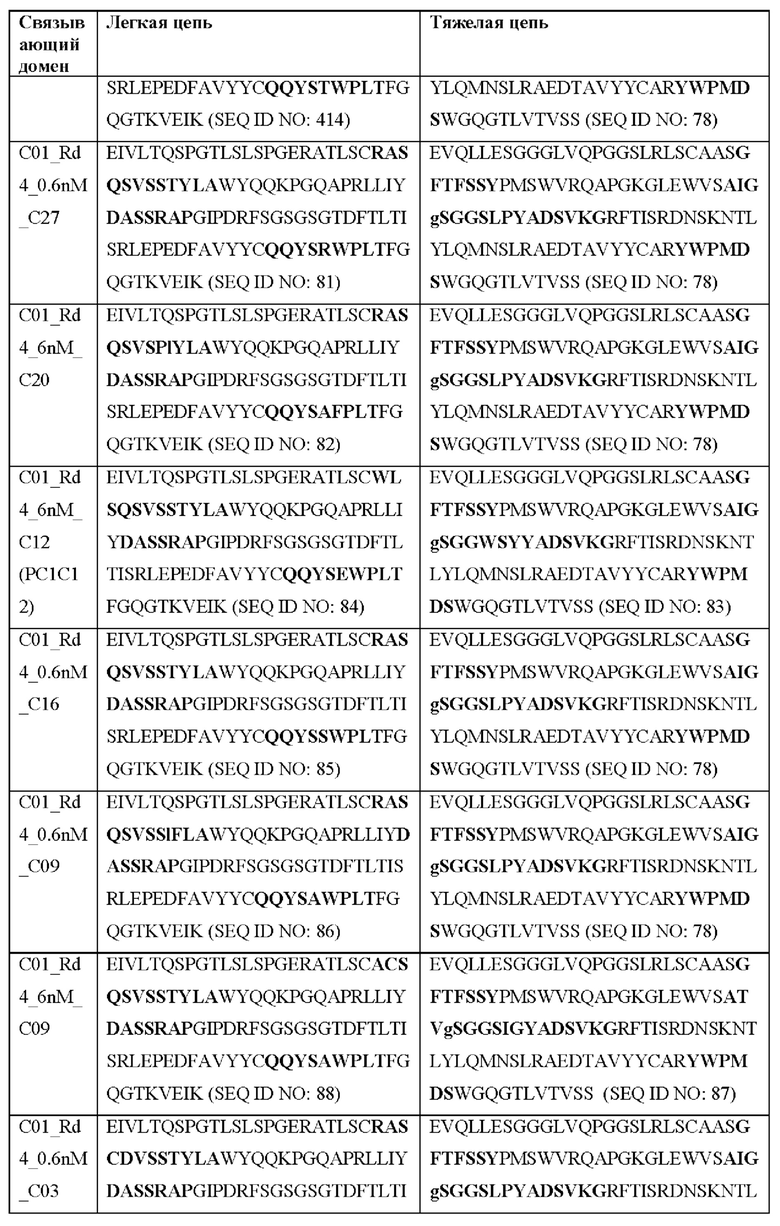
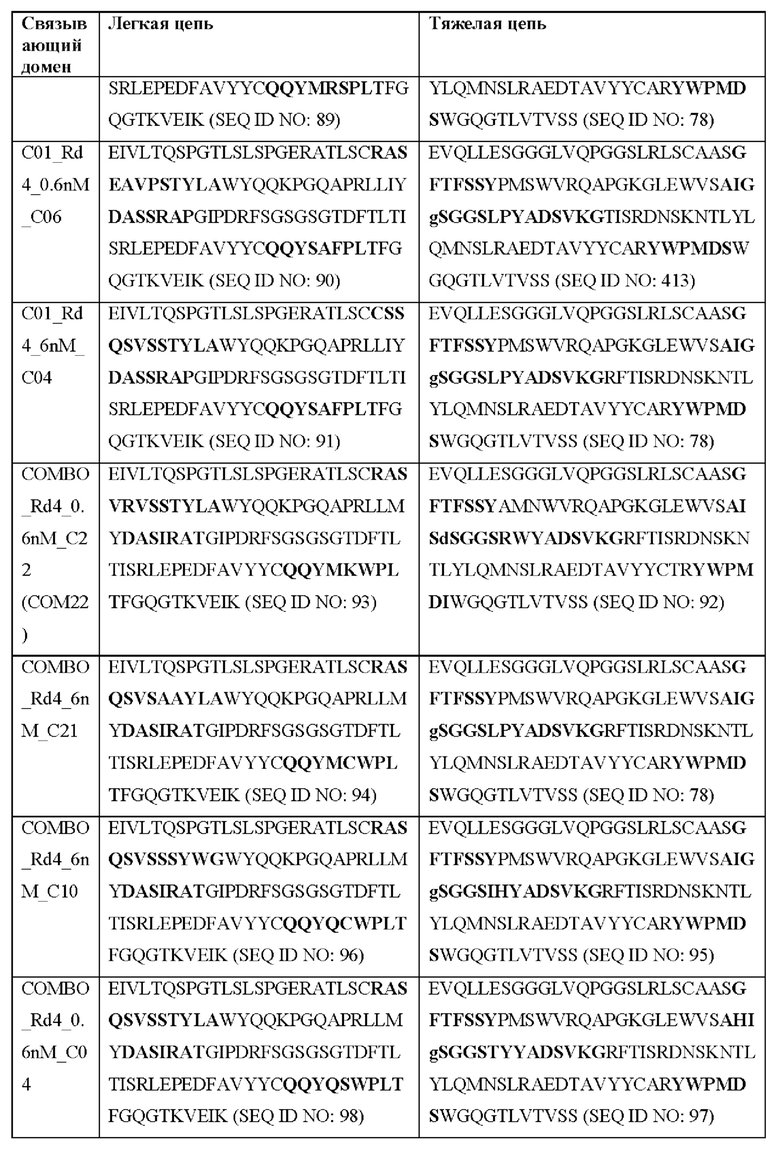
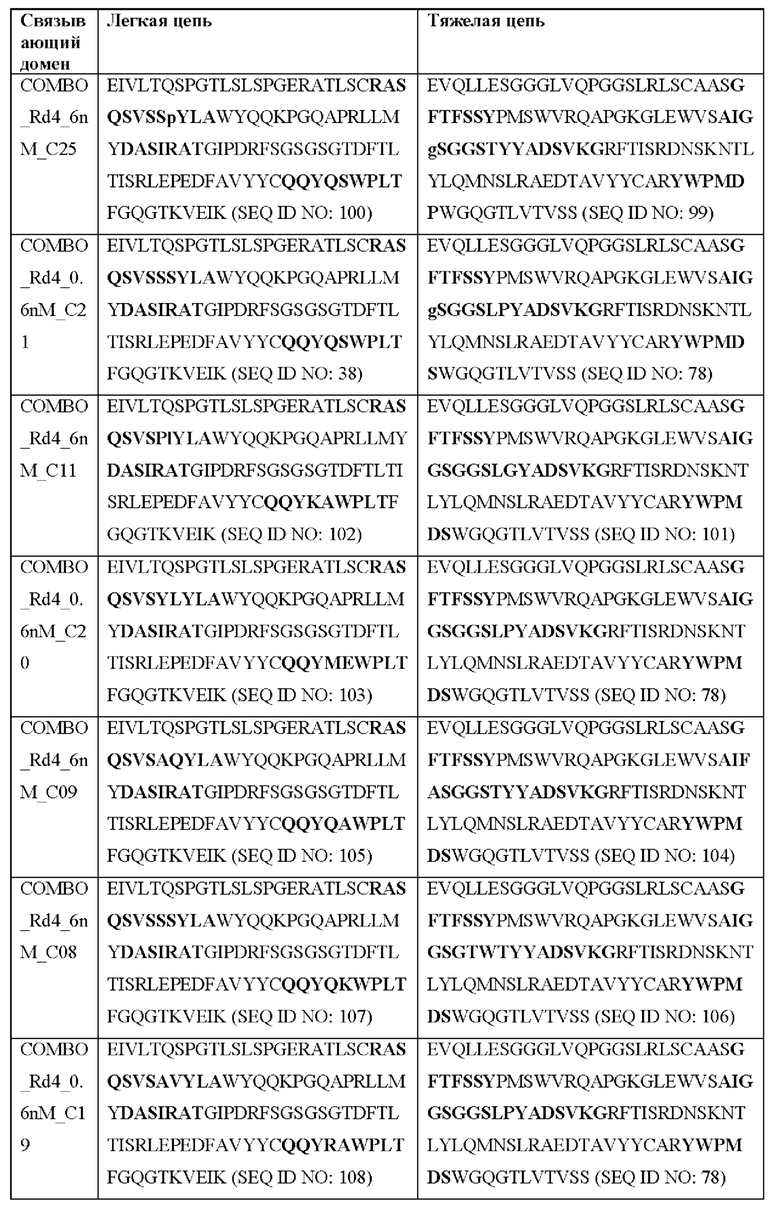
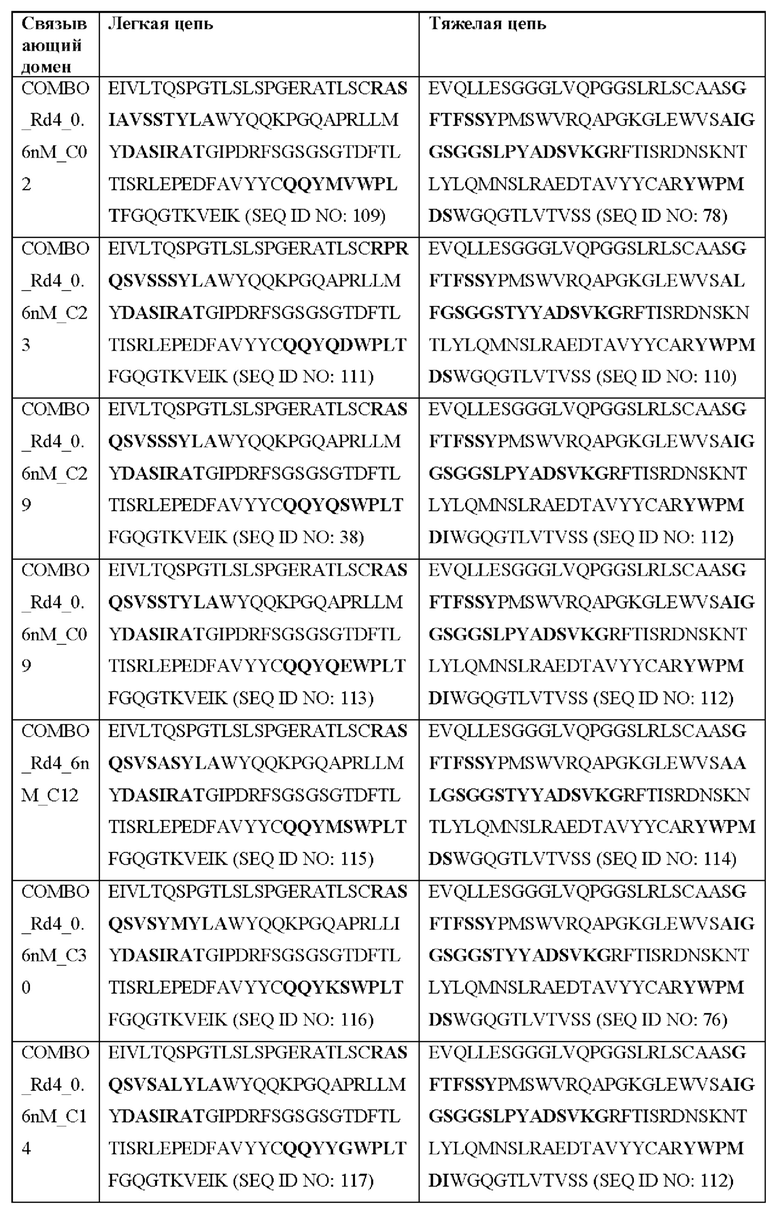
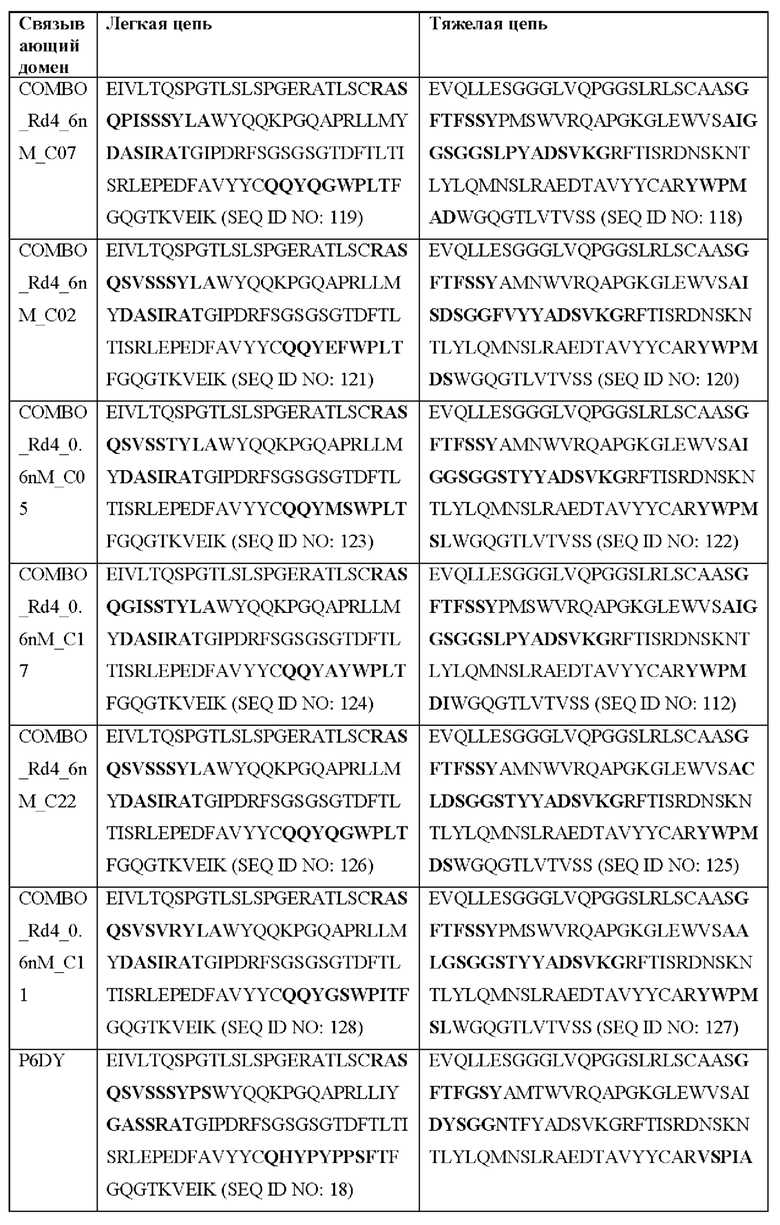



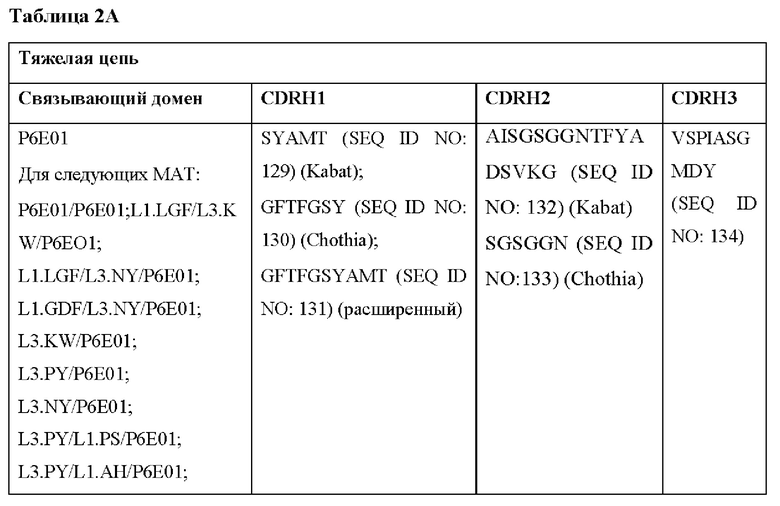
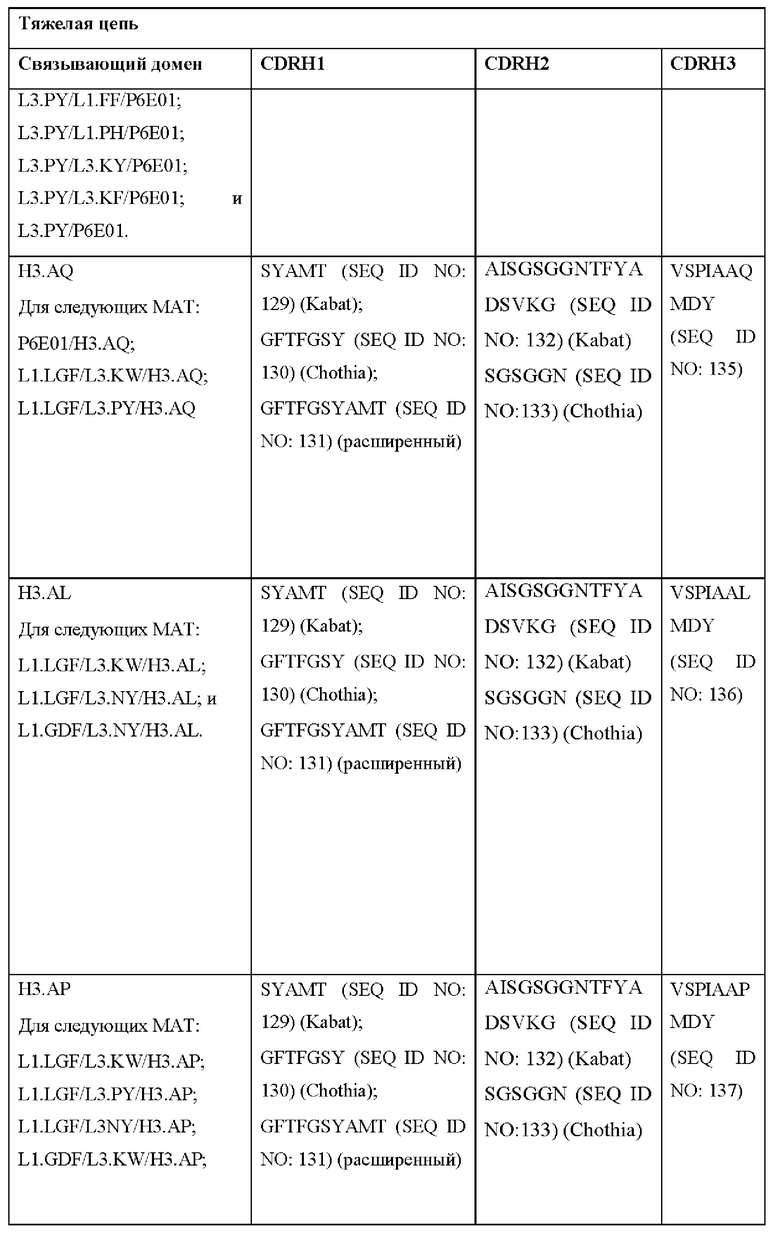
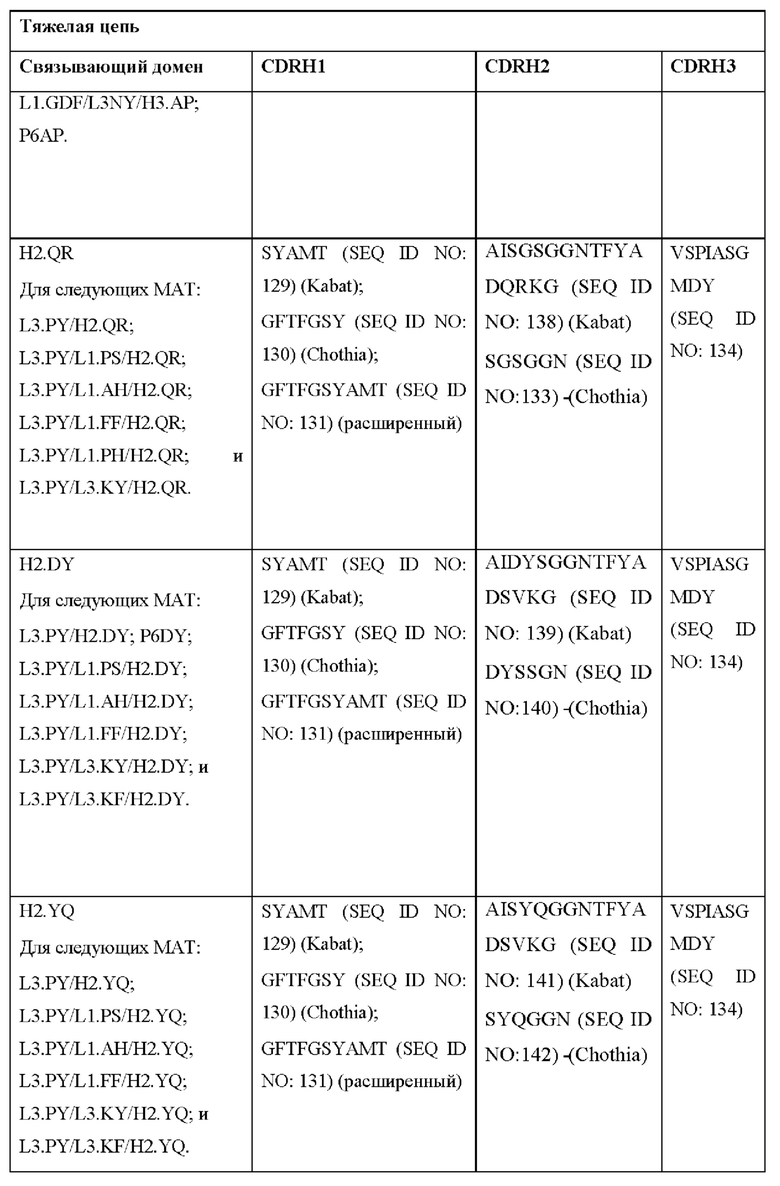
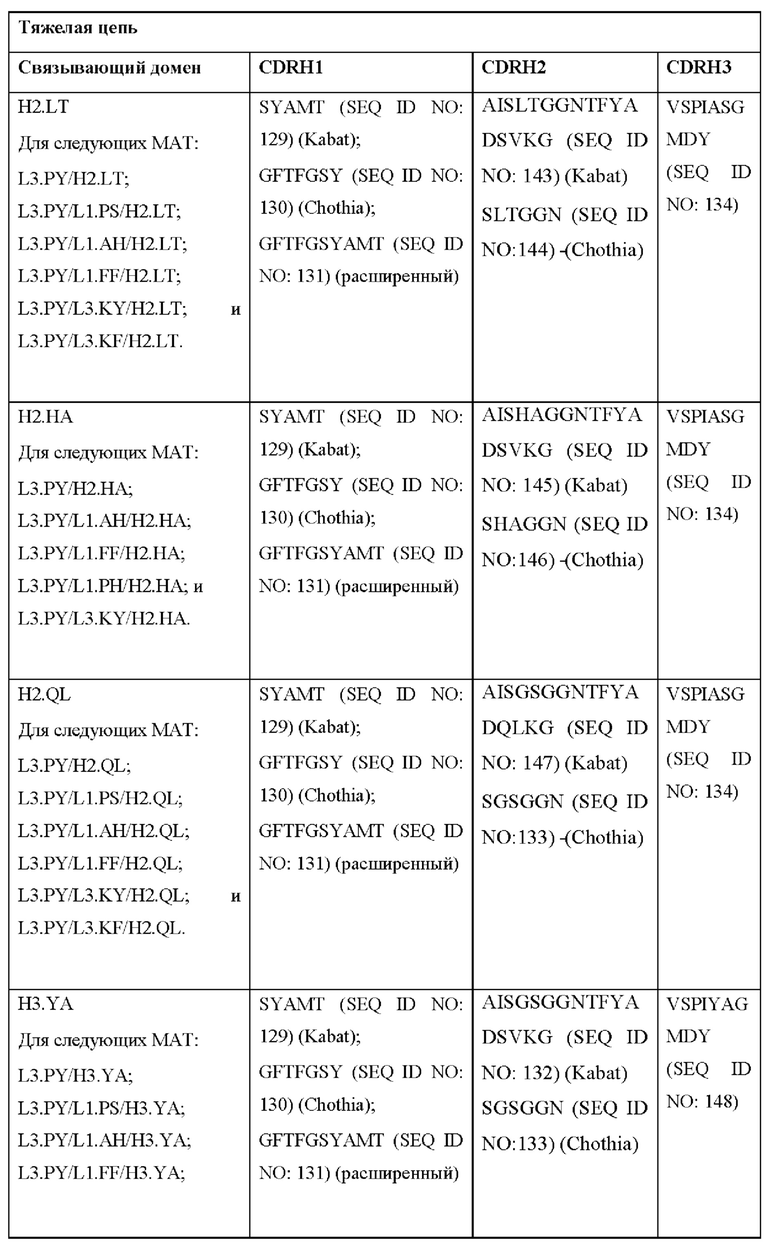
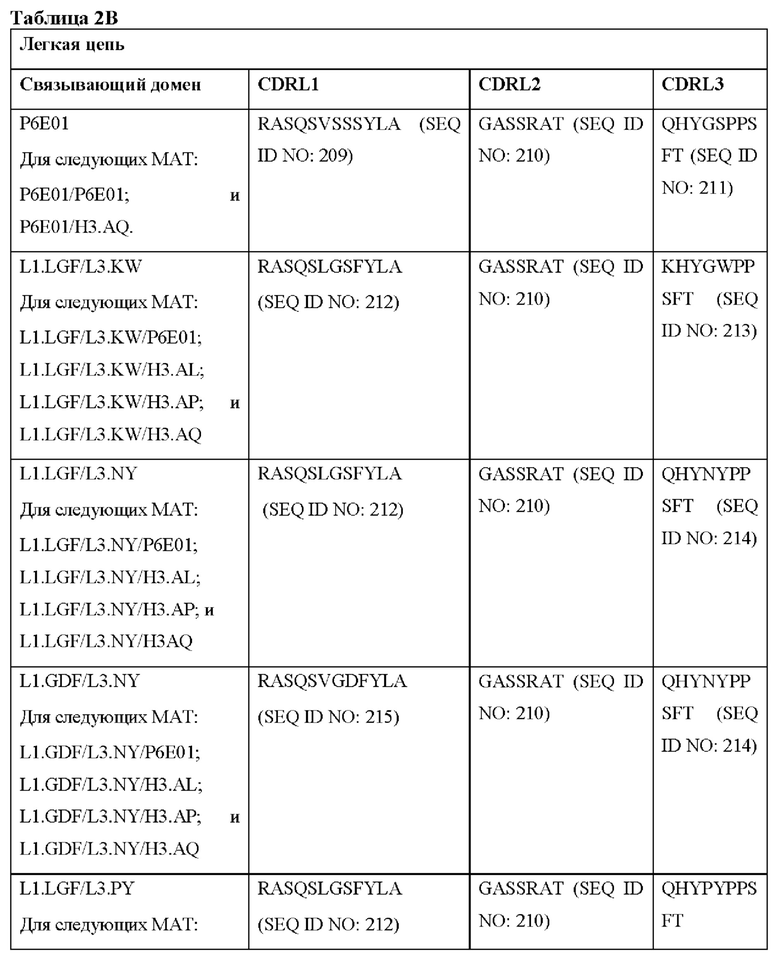
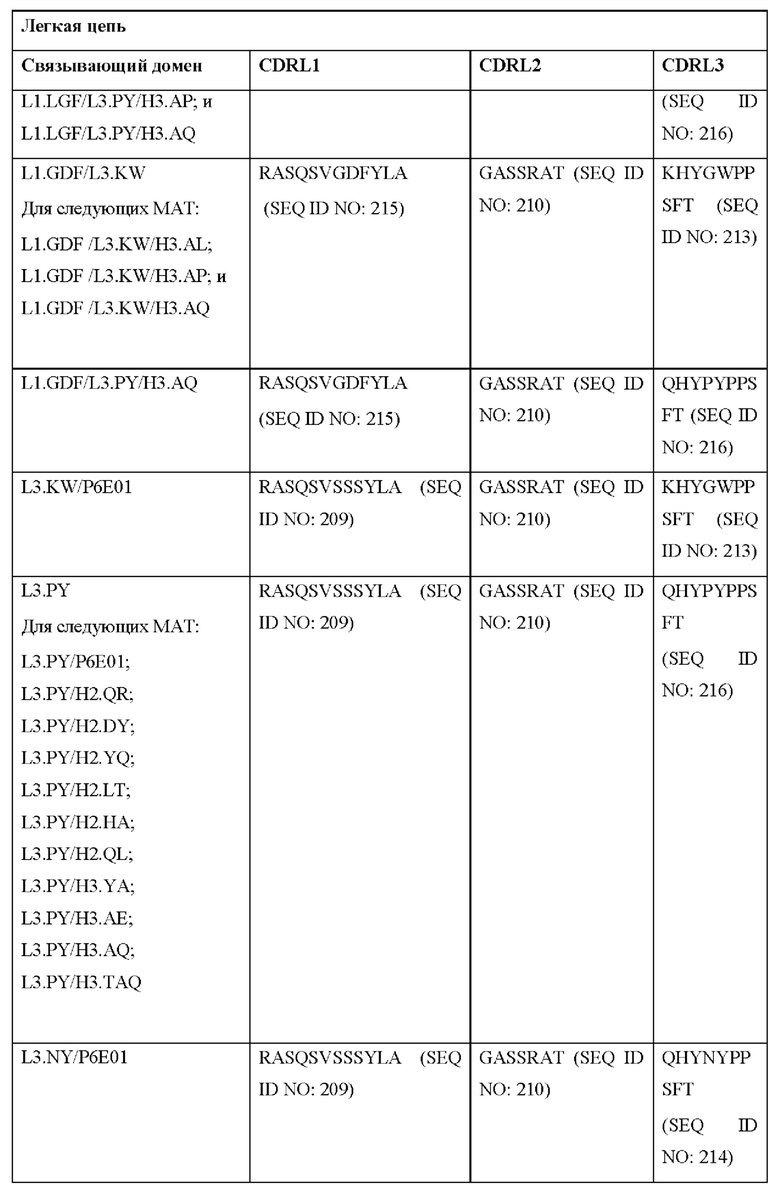
[0052] В настоящем документе также приведены участки CDR внеклеточных лигандсвязывающих доменов CAR для ВСМА (включая CDR согласно Chothia, Kabat и контактные области CDR). Определение CDR-участков известно специалисту в данной области техники. Понятно, что в некоторых вариантах реализации CDR могут представлять собой комбинацию CDR согласно Kabat и Chothia (также называемые «комбинированными CR» или «расширенными CDR»). В некоторых вариантах реализации CDR представляют собой CDR согласно Kabat. В других вариантах реализации CDR представляют собой CDR согласно Chothia. Другими словами, в вариантах реализации с более чем одной CDR эти CDR могут представлять собой любые из: CDR согласно Kabat, Chothia, комбинированных CDR или их комбинаций. В Таблице 2А и Таблице 2В приведены примеры последовательностей CDR согласно настоящему изобретению.
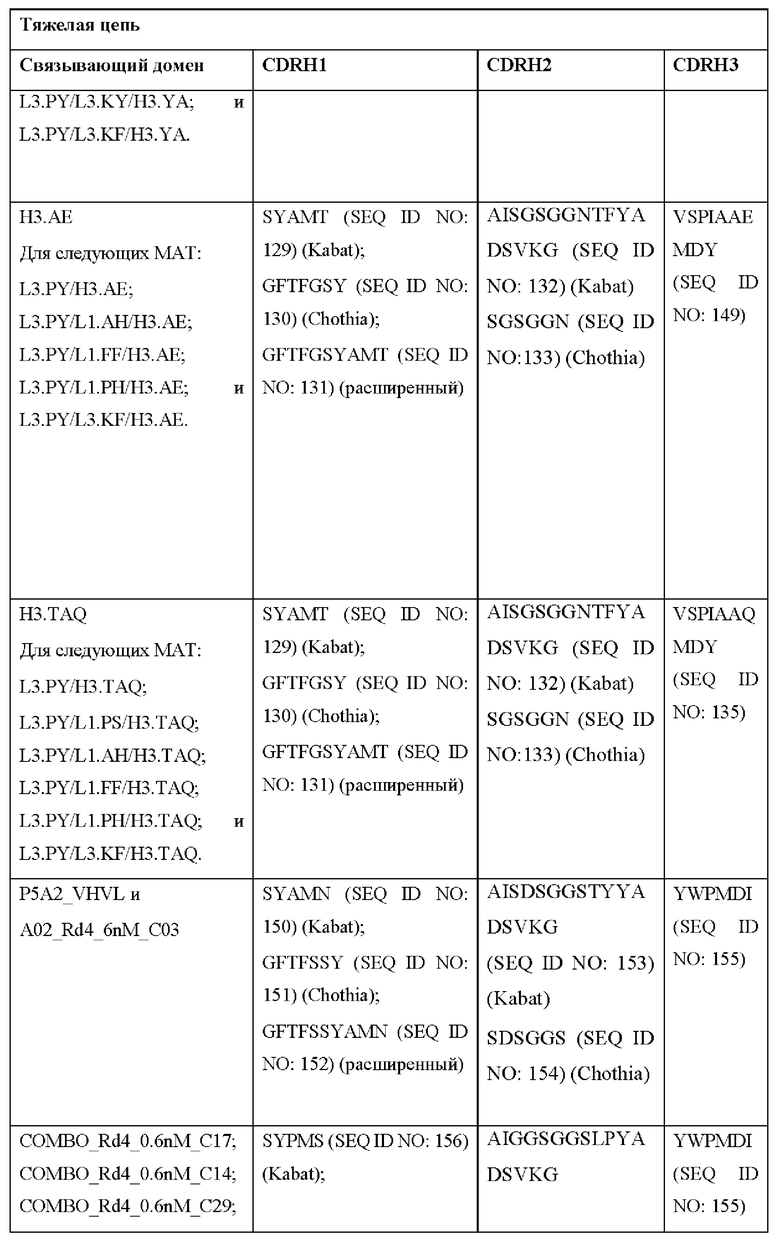
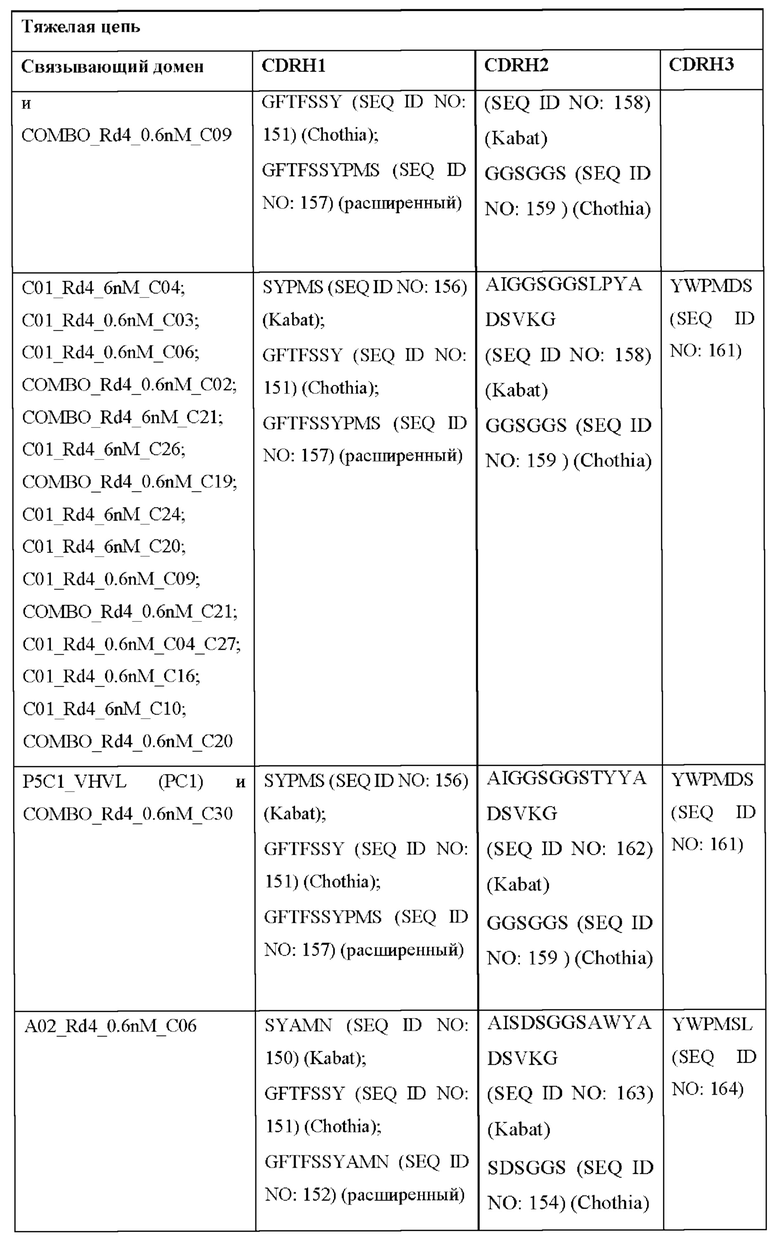
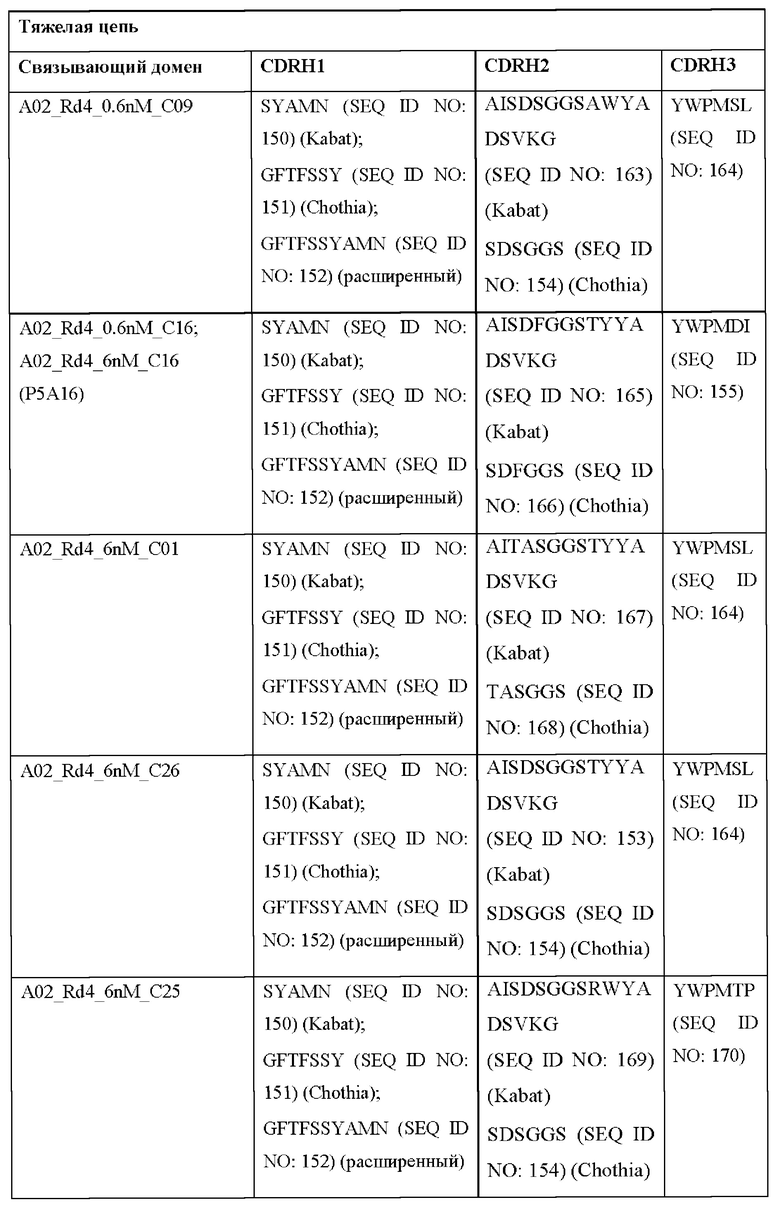
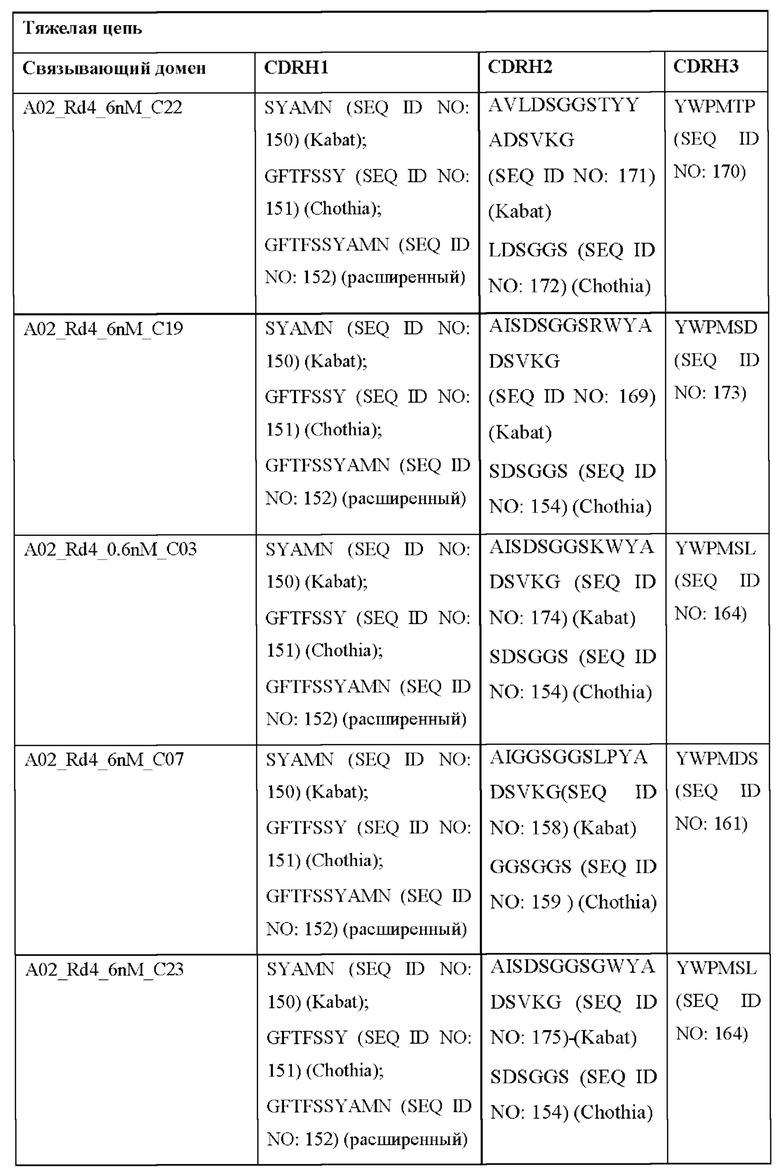
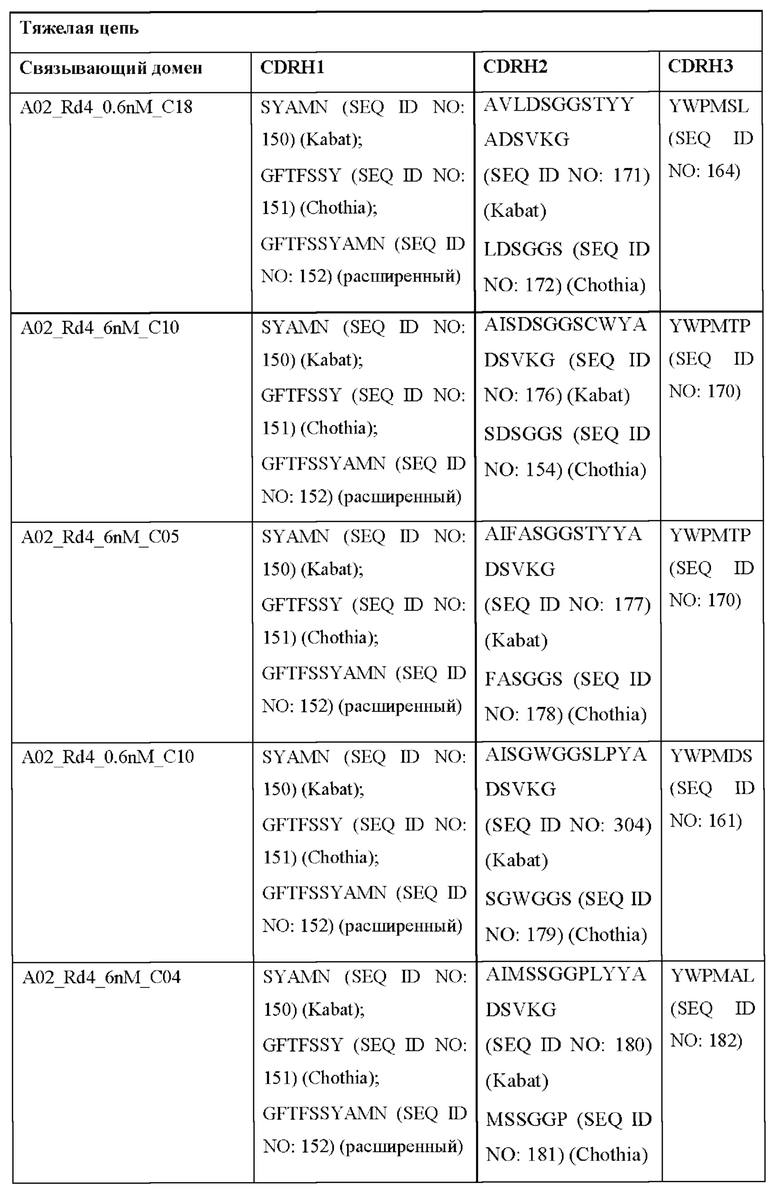
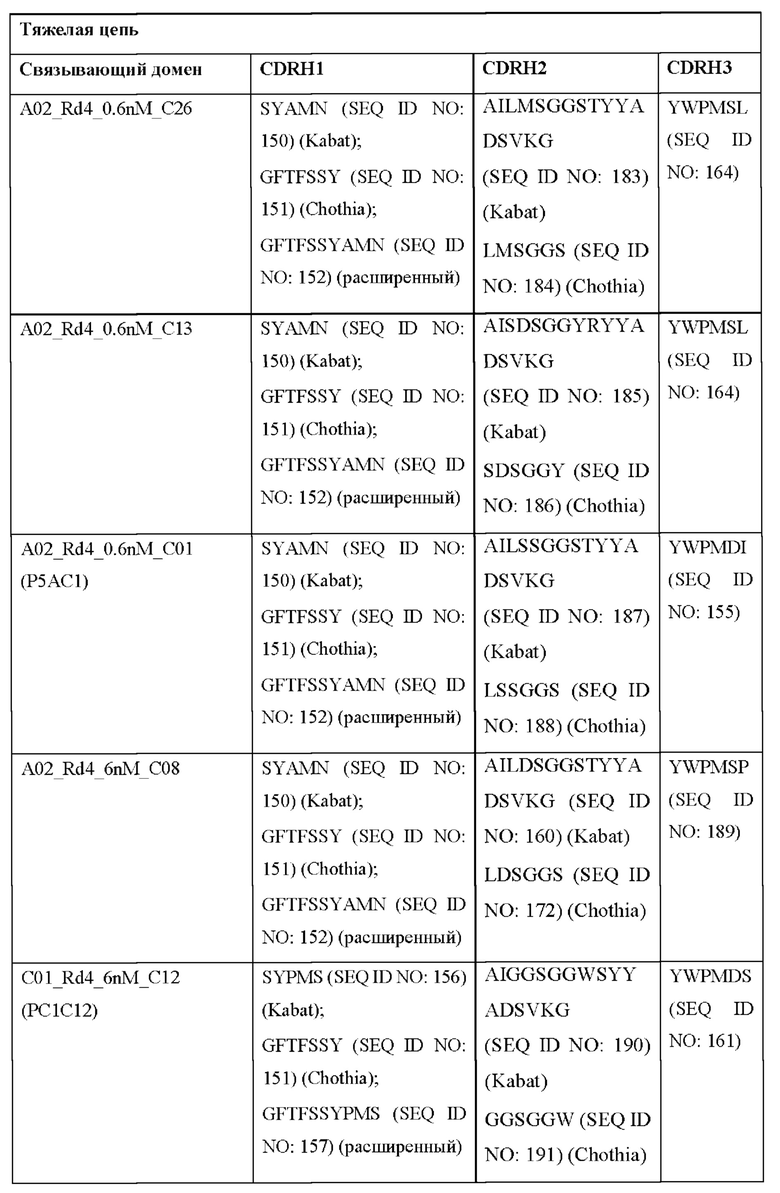
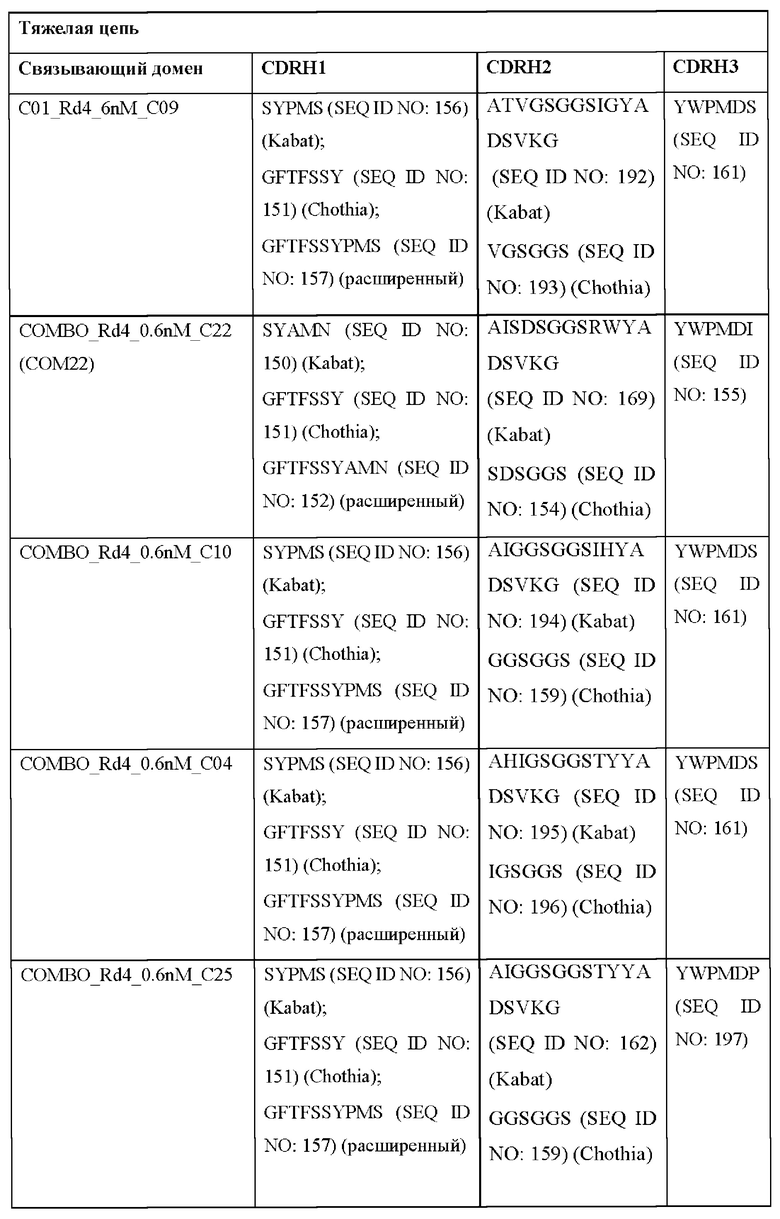
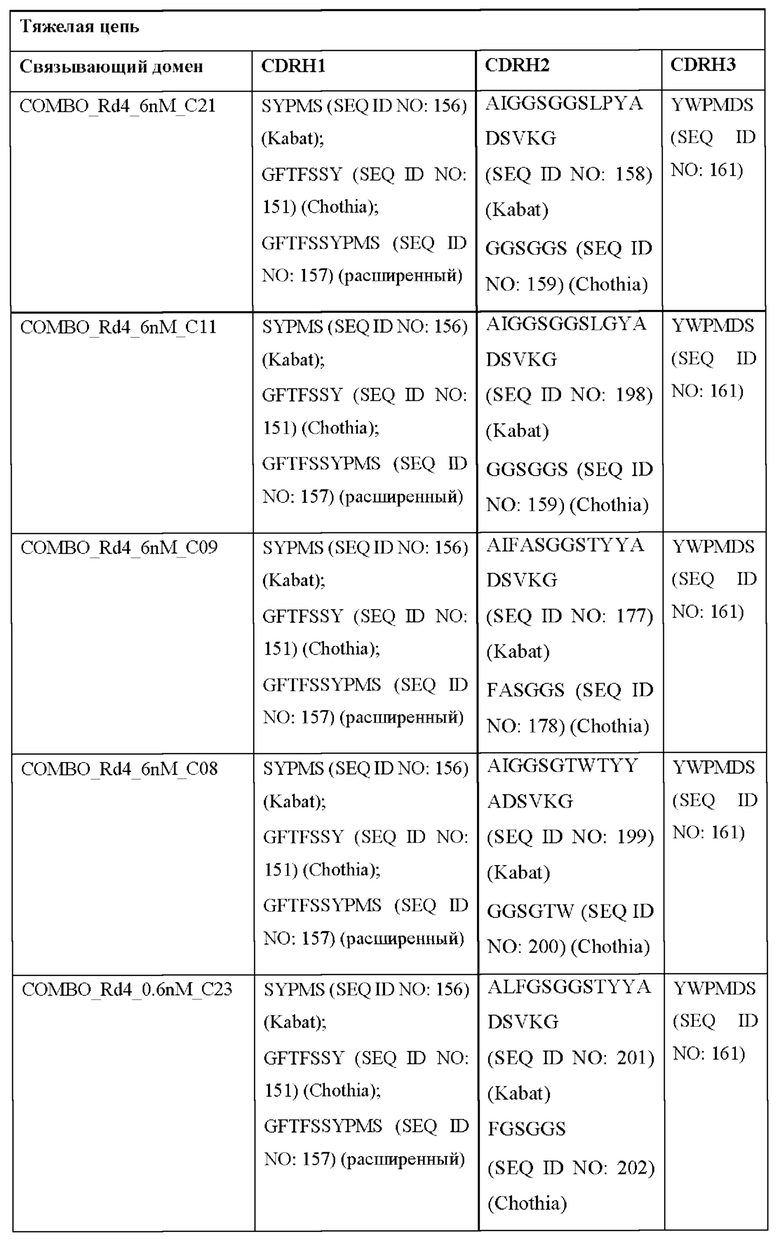


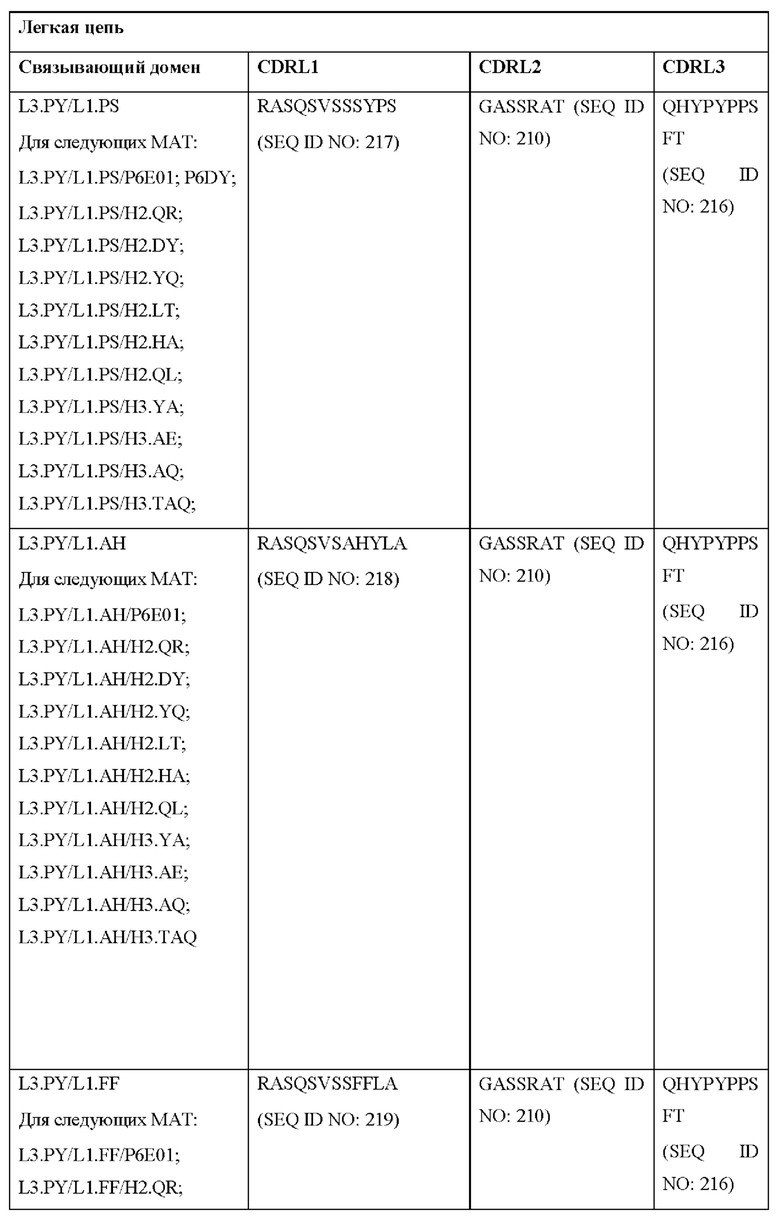
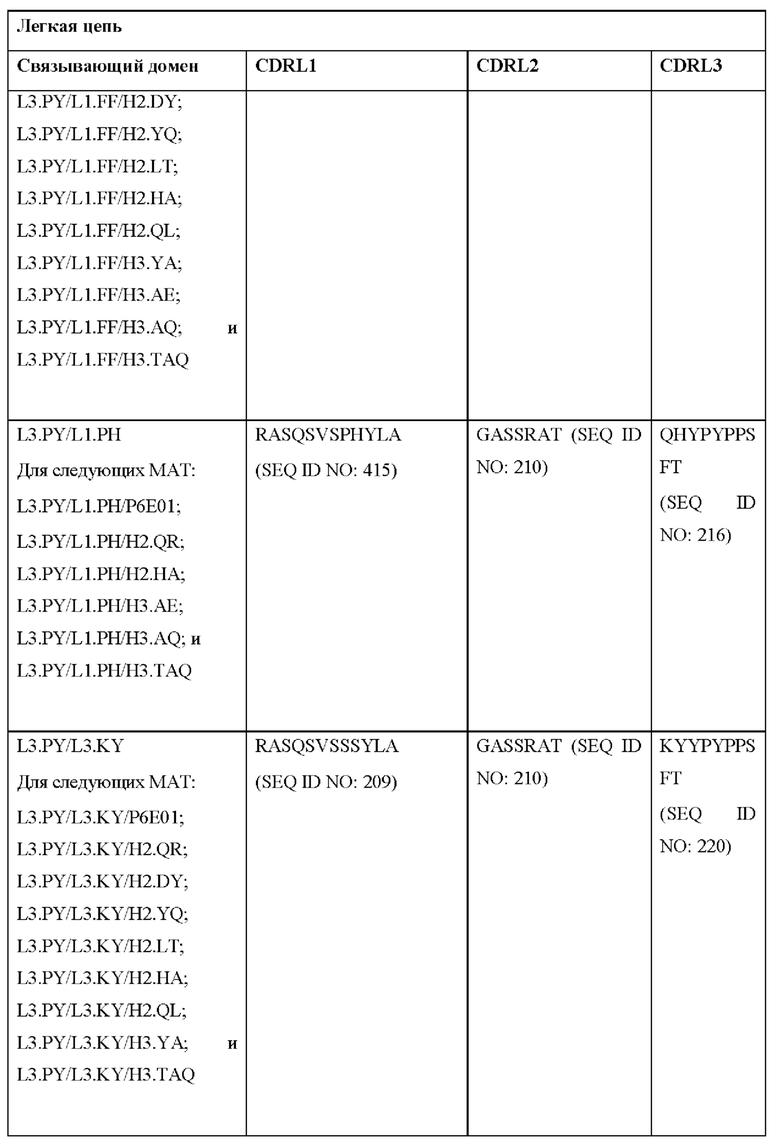
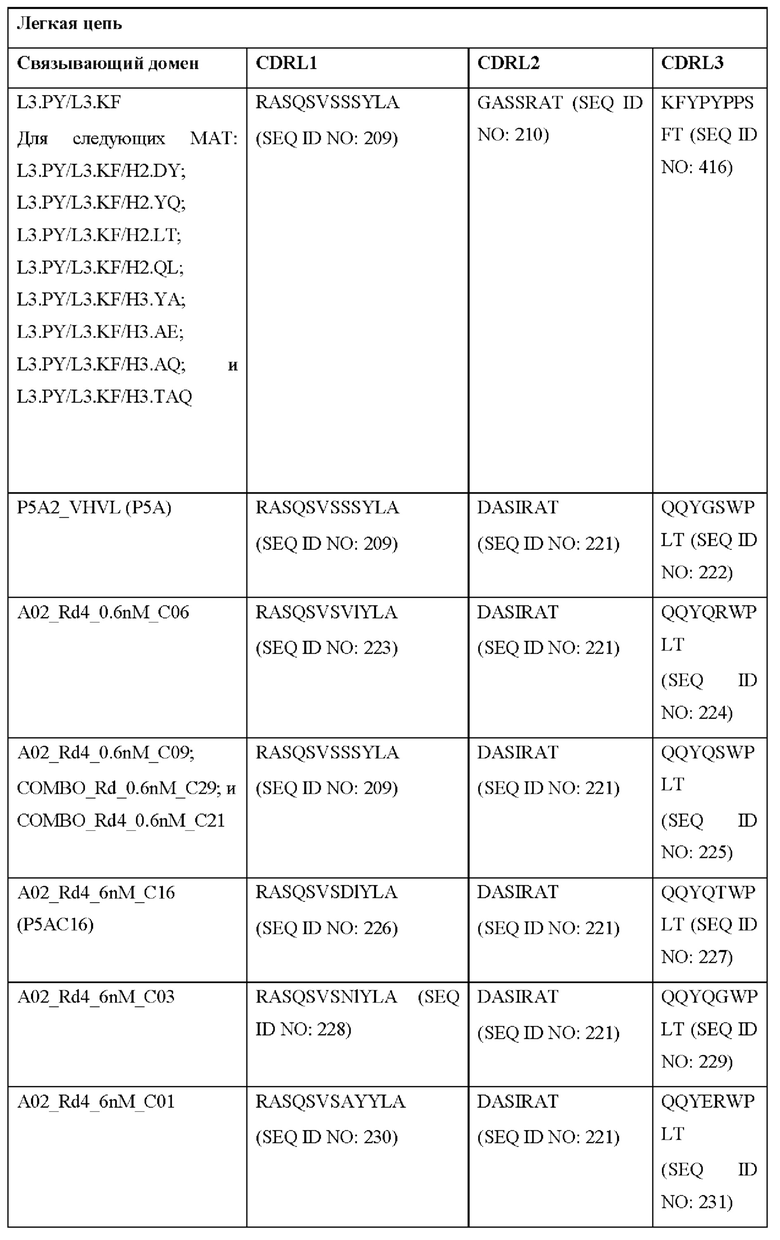
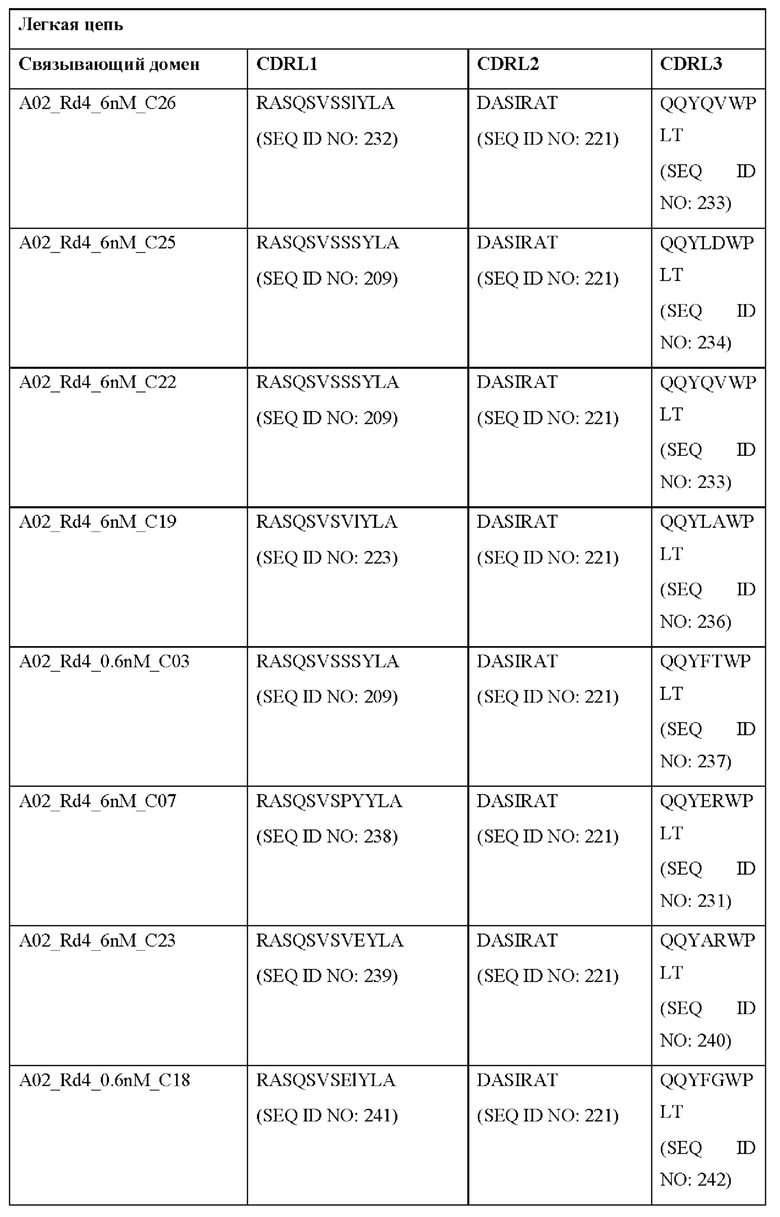

[0053] В некоторых вариантах реализации CAR к ВСМА содержит внеклеточный лигандсвязывающий домен, первый трансмембранный домен и внутриклеточный сигнальный домен, при этом указанный внеклеточный домен содержит одноцепочечный Fv-фрагмент (scFv), содержащий вариабельную область тяжелой цепи (VH), содержащую три определяющих комплементарность участка (CDR), содержащие последовательности, представленные в SEQ ID NO: 33, 72, 39, 76, 83, 92, 25, 112 или 8 в Таблице 1; и вариабельную область легкой цепи (VL), содержащую три CDR, содержащие последовательности, представленные в SEQ ID NO: 34, 73, 40, 77, 84, 93, 18, 38 или 80 в Таблице 1, указанный первый трансмембранный домен содержит трансмембранный домен цепи CD8α, и указанный внутриклеточный сигнальный домен содержит сигнальный домен CD3ζ и/или сигнальный домен 4-1ВВ.
[0054] В некоторых вариантах реализации внеклеточная связывающая область CAR к ВСМА содержит VH-область, которая содержит аминокислотную последовательность, представленную в SEQ ID NO: 112, и VL-область содержит аминокислотную последовательность, представленную в SEQ ID NO: 38.
[0055] В некоторых вариантах реализации внеклеточная связывающая область CAR к ВСМА содержит VH-область, которая содержит аминокислотную последовательность, представленную в SEQ ID NO: 33, и VL-область содержит аминокислотную последовательность, представленную в SEQ ID NO: 34.
[0056] В некоторых вариантах реализации внеклеточная связывающая область CAR к ВСМА содержит VH-область, которая содержит CDR1 VH, содержащий аминокислотную последовательность, представленную в SEQ ID NO: 150, 151 или 152; CDR2 VH, содержащий аминокислотную последовательность, представленную в SEQ ID NO: 153 или 154; и CDR3 VH, содержащий аминокислотную последовательность, представленную в SEQ ID NO: 155; и содержит VL-область, содержащую CDR1 VL, содержащий аминокислотную последовательность, представленную в SEQ ID NO: 209; CDR2 VL, содержащий аминокислотную последовательность, представленную в SEQ ID NO: 221; и CDR3 VL, содержащий аминокислотную последовательность, представленную в SEQ ID NO: 222.
[0057] В некоторых вариантах реализации внеклеточная связывающая область CAR к ВСМА содержит VH-область, которая содержит CDR1 VH, содержащий аминокислотную последовательность, представленную в SEQ ID NO: 151, 156 или 157; CDR2 VH, содержащий аминокислотную последовательность, представленную в SEQ ID NO: 158 или 159; и CDR3 VH, содержащий аминокислотную последовательность, представленную в SEQ ID NO: 155; и содержит VL-область, содержащую CDR1 VL, содержащий аминокислотную последовательность, представленную в SEQ ID NO: 209; CDR2 VL, содержащий аминокислотную последовательность, представленную в SEQ ID NO: 221; и CDR3 VL, содержащий аминокислотную последовательность, представленную в SEQ ID NO: 225.
[0058] Аффинность связывания (KD) ВСМА-специфичного CAR, описанного в настоящем документе, в отношении ВСМА (например, ВСМА человека (например, SEQ ID NO: 354)) может составлять от примерно 0,002 до примерно 6500 нМ. В некоторых вариантах реализации аффинность связывания составляет примерно любое значение из 6500 нм, 6000 нм, 5986 нм, 5567 нм, 5500 нм, 4500 нм, 4000 нм, 3500 нм, 3000 нм, 2500 нм, 2134 нм, 2000 нм, 1500 нм, 1000 нм, 750 нм, 500 нм, 400 нм, 300 нм, 250 нм, 200 нМ, 193 нМ, 100 нМ, 90 нМ, 50 нМ, 45 нМ, 40 нМ, 35 нМ, 30 нМ, 25 нМ, 20 нМ, 19 нм, 18 нм, 17 нм, 16 нм, 15 нМ, 10 нМ, 8 нМ, 7,5 нМ, 7 нМ, 6,5 нМ, 6 нМ, 5,5 нМ, 5 нМ, 4 нМ, 3 нМ, 2 нМ, 1 нМ, 0,5 нМ, 0,3 нМ, 0,1 нМ, 0,01 нМ или 0,002 нМ. В некоторых вариантах реализации аффинность связывания меньше примерно любого значения из 6500 нм, 6000 нм, 5500 нм, 5000 нм, 4000 нм, 3000 нм, 2000 нм, 1000 нм, 900 нм, 800 нм, 250 нМ, 200 нМ, 100 нМ, 50 нМ, 30 нМ, 20 нМ, 10 нМ, 7,5 нМ, 7 нМ, 6,5 нМ, 6 нМ, 5 нМ, 4,5 нМ, 4 нМ, 3,5 нМ, 3 нМ, 2,5 нМ, 2 нМ, 1,5 нМ, 1 нМ или 0,5 нМ.
[0059] Внутриклеточный сигнальный домен CAR согласно настоящему изобретению отвечает за внутриклеточную передачу сигнала после связывания внеклеточного лигандсвязывающего домена с мишенью, что приводит к активации иммунной клетки и иммунного ответа. Внутриклеточный сигнальный домен обладает способностью активировать по меньшей мере одну из нормальных эффекторных функций иммунной клетки, в которой экспрессируется CAR. Например, эффекторная функция Т-клетки может представлять собой цитолитическую активность или активность хелперов, включая секрецию цитокинов.
[0060] В некоторых вариантах реализации внутриклеточный сигнальный домен для использования в CAR может представлять собой цитоплазматические последовательности, например, но не ограничиваясь ими, Т-клеточного рецептора и корецепторов, которые действуют совместно, инициируя передачу сигнала после взаимодействия с антигенным рецептором, а также любое производное или вариант этих последовательностей и любую синтетическую последовательность, обладающую такой же функциональной способностью. Внутриклеточные сигнальные домены содержат два различных класса цитоплазматических сигнальных последовательностей: те, которые инициируют антиген-зависимую первичную активацию, и те, которые действуют антиген-независимым образом, обеспечивая вторичный или костимулирующий сигнал. Первичные цитоплазматические сигнальные последовательности могут содержать сигнальные мотивы, которые известны как иммунорецепторные тирозиновые активирующие мотивы, ITAM. ITAM представляют собой хорошо определенные сигнальные мотивы, обнаруженные во внутрицитоплазматическом хвосте различных рецепторов, которые служат сайтами связывания для тирозинкиназ класса syk/zap70. Примеры ITAM, используемых согласно настоящему изобретению, могут включать в качестве неограничивающих примеров те, которые получены из TCRζ, FcRγ, FcRβ, FcRε, CD3γ, CD3δ, CD3ε, CD5, CD22, CD79a, CD79b и CD66d. В некоторых вариантах реализации внутриклеточный сигнальный домен CAR может содержать сигнальный домен CD3ζ, который имеет аминокислотную последовательность, по меньшей мере примерно на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90%, 95%, 97% или 99% идентичную аминокислотной последовательности, представленной в SEQ. ID NO: 324. В некоторых вариантах реализации внутриклеточный сигнальный домен CAR согласно настоящему изобретению содержит домен костимулирующей молекулы.
[0061] В некоторых вариантах реализации внутриклеточный сигнальный домен CAR согласно настоящему изобретению содержит часть костимулирующей молекулы, выбранной из группы, состоящей из фрагмента 41ВВ (GenBank: ААА53133.) и CD28 (NP_006130.1). В некоторых вариантах реализации внутриклеточный сигнальный домен CAR согласно настоящему изобретению содержит аминокислотную последовательность, которая по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90%, 95%, 97% или 99% идентична аминокислотной последовательности, представленной в SEQ. ID NO: 323 и SEQ. ID NO: 327.
[0062] CAR экспрессируются на поверхностной мембране клетки. Таким образом, CAR может содержать трансмембранный домен. Подходящие транс мембранные домены для CAR, описанного в настоящем документе, обладают способностью (а) экспрессироваться на поверхности клетки, предпочтительно иммунной клетки, такой как, например, но не ограничиваясь ими, лимфоциты или естественные клетки-киллеры (NK-клетки), и (b) взаимодействовать с лигандсвязывающим доменом и внутриклеточным сигнальным доменом для направления клеточного ответа иммунной клетки на заранее определенную клетку-мишень. Трансмембранный домен может быть получен либо из природного, либо из синтетического источника. Трансмембранный домен может быть получен из любого мембраносвязанного или транс мембранного белка. В качестве неограничивающих примеров, транс мембранный полипептид может представлять собой субъединицу Т-клеточного рецептора, такую как α, β, γ или δ, полипептид, составляющий комплекс CD3, р55 (а-цепь), р75 (β-цепь) или γ-цепь рецептора IL-2, цепь субъединицы Fc-рецепторов, в частности, Fcγ-рецептора III, или белки CD. В качестве альтернативы, трансмембранный домен может быть синтетическим и может содержать преимущественно гидрофобные остатки, такие как лейцин и валин. В некоторых вариантах реализации указанный транс мембранный домен получен из цепи CD8α человека (например, NP_001139345.1). Трансмембранный домен может дополнительно содержать стеблевой домен между внеклеточным лигандсвязывающим доменом и указанным трансмембранным доменом. Стеблевой домен может содержать до 300 аминокислот, предпочтительно от 10 до 100 аминокислот и наиболее предпочтительно от 25 до 50 аминокислот. Стеблевая область может быть получена из всех или части встречающихся в природе молекул, например, из всей или части внеклеточной области CD8, CD4 или CD28, или из всей или части константной области антитела. В качестве альтернативы, стеблевой домен может представлять собой синтетическую последовательность, которая соответствует встречающейся в природе последовательности стеблевого домена, или может представлять собой полностью синтетическую последовательность стеблевого домена. В некоторых вариантах реализации указанный стеблевой домен является частью цепи CD8α человека (например, NP_001139345.1). В другом конкретном варианте реализации указанные трансмембранные и шарнирные домены содержат часть цепи CD8α человека, последовательность которой предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90%, 95%, 97% или 99% идентична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 318. В некоторых вариантах реализации CAR, описанные в настоящем документе, могут содержать внеклеточный лигандсвязывающий домен, который специфично связывает ВСМА, шарнирный и трансмембранный домены CD8α человека, сигнальный домен CD3ζ, и сигнальный домен 4-1ВВ.
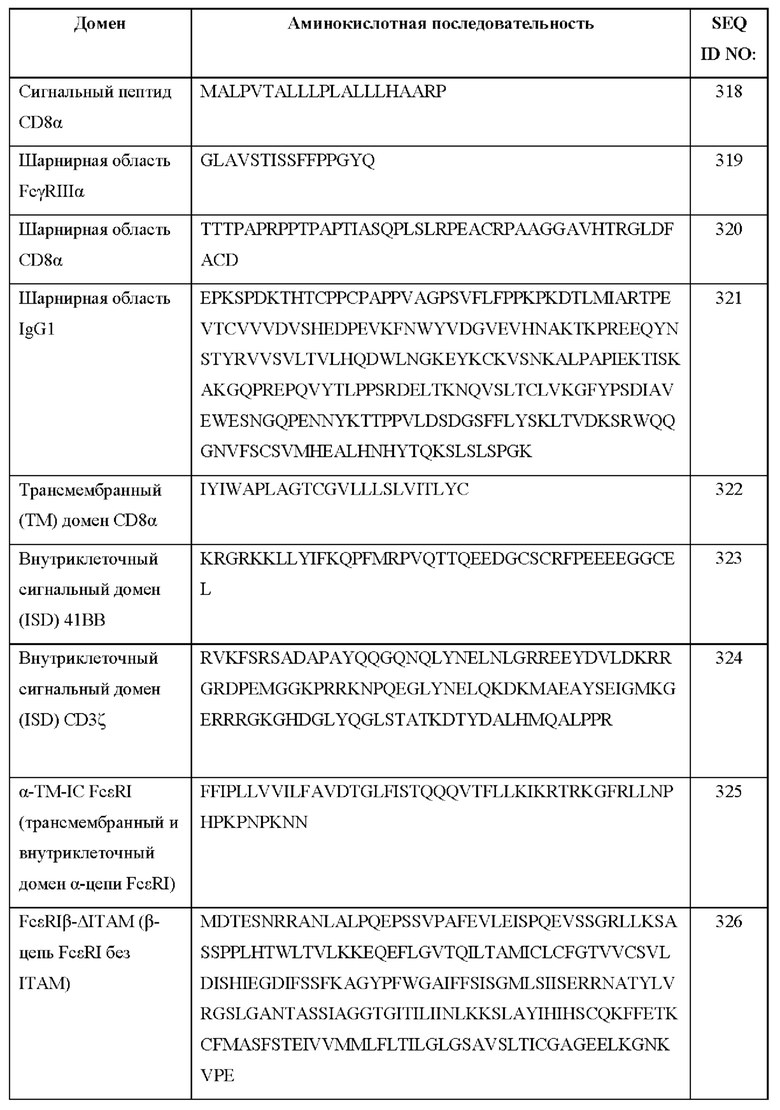
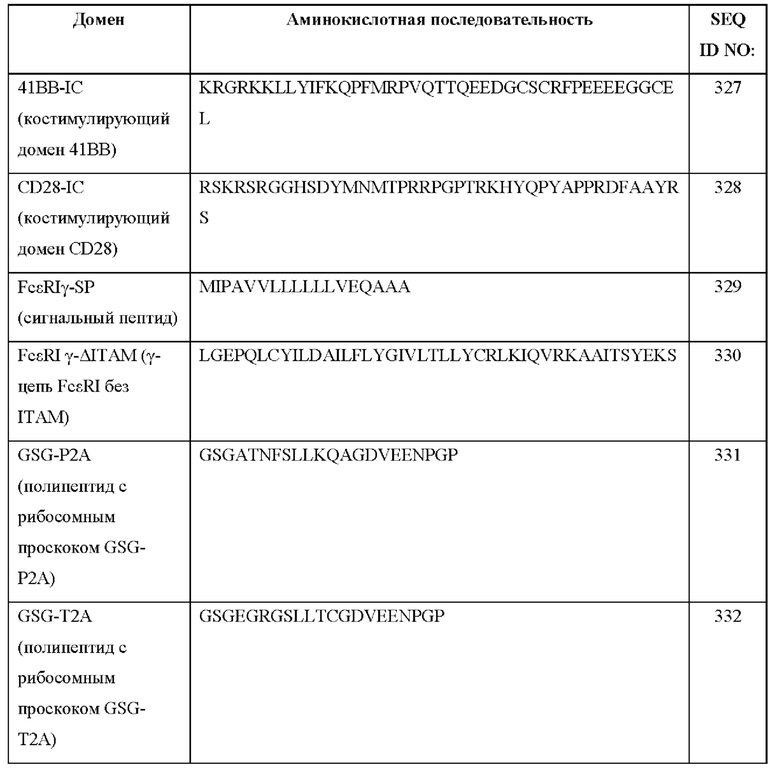
[0063] В Таблице 3 представлены примеры последовательностей доменов, которые могут быть использованы в CAR, описанных в настоящем документе.

[0064] В соответствии с другим аспектом настоящего изобретения предложены полинуклеотиды, кодирующие любой из CAR и полипептидов, описанных в настоящем документе. Полинуклеотиды можно получать и экспрессировать способами, известными в этой области техники.
[0065] В соответствии с другим аспектом настоящего изобретения предложены композиции (такие как фармацевтические композиции), содержащие любую из клеток согласно настоящему изобретению.
II. Искусственно сконструированные иммунные клетки
[0066] Согласно настоящему изобретению предложены искусственно сконструированные иммунные клетки, содержащие любой из полинуклеотидов для CAR к ВСМА, описанных в настоящем документе. В некоторых вариантах реализации CAR к ВСМА вводят в иммунную клетку с помощью лентивирусного вектора. В некоторых вариантах реализации указанный лентивирусный вектор представляет собой самоинактивирующийся лентивирусный вектор, который интегрируется в иммунную клетку реципиента. В некоторых вариантах реализации CAR к ВСМА вводят в иммунную клетку в виде трансгена с помощью плазмидного вектора. В некоторых вариантах реализации указанный плазмидный вектор может также содержать, например, селективный маркер, который обеспечивает идентификацию и/или селекцию клеток, которые получили вектор. В некоторых вариантах реализации CAR может быть введен в иммунную клетку с применением невирусных способов.
[0067] Типичная векторная конструкция показана на Фиг. 21.
[0068] Способы получения искусственно сконструированных иммунных клеток, экспрессирующих любой из CAR к ВСМА, предложенных согласно настоящему изобретению, описаны в WO/2016/166630, полное содержание которого включено в настоящее описание посредством ссылки.
[0069] Согласно настоящему изобретению предложены выделенные иммунные клетки, полученные в соответствии с любым из способов, описанных выше. Для экспрессии представляющего интерес CAR может быть использована любая иммунная клетка, способная экспрессировать гетерологичные ДНК. В некоторых вариантах реализации иммунная клетка представляет собой Т-клетку. В некоторых вариантах реализации иммунная клетка может быть получена, например, но не ограничиваясь ею, из стволовой клетки. Стволовые клетки могут представлять собой стволовые клетки взрослого, эмбриональные стволовые клетки нечеловеческого происхождения, в частности стволовые клетки нечеловеческого происхождения, стволовые клетки пуповинной крови, клетки-предшественники, стволовые клетки костного мозга, индуцированные плюрипотентные стволовые клетки, тотипотентные стволовые клетки или гемопоэтические стволовые клетки. Типичными клетками человека являются CD34+ клетки. Выделенная клетка может также представлять собой дендритную клетку, дендритную клетку-киллер, тучную клетку, NK-клетку, В-клетку или Т-клетку, выбранную из группы, состоящей из воспалительных Т-лимфоцитов, цитотоксических Т-лимфоцитов, регуляторных Т-лимфоцитов или хелперных Т-лимфоцитов. В некоторых вариантах реализации клетка может происходить из группы, состоящей из CD4+ Т-лимфоцитов и CD8+ Т-лимфоцитов.
[0070] В некоторых вариантах реализации выделенная клетка согласно настоящему изобртению содержит один инактивированный ген, выбранный из группы, состоящей из CD52, GR, PD-1, CTLA-4, LAG3, Tim3, BTLA, BY55, TIGIT, В7Н5, LAIR1, SIGLEC10, 2B4, HLA, TCRα и TCRβ, и/или экспрессирует CAR, многоцепочечный CAR и/или трансген pTα. В некоторых вариантах реализации выделенная клетка содержит полинуклеотиды, кодирующие полипептиды, содержащие многоцепочечный CAR. В некоторых вариантах реализации выделенная клетка согласно настоящему изобретению содержит два инактивированных гена, выбранных из группы, состоящей из: CD52 и GR, CD52 и TCRα, CDR52 и TCRβ, GR и TCRα, GR и TCRβ, TCRα и TCRβ, PD-1 и TCRα, PD-1 и TCRβ, CTLA-4 и TCRα, CTLA-4 и TCRβ, LAG3 и TCRα, LAG3 и TCRβ, Tim3 и TCRα, Tim3 и TCRβ, BTLA и TCRα, BTLA и TCRβ, BY55 и TCRα, BY55 и TCRβ, TIGIT и TCRα, TIGIT и TCRβ, B7H5 и TCRα, B7H5 и TCRβ, LAIR1 и TCRα, LAIR1 и TCRβ, SIGLEC10 и TCRα, SIGLEC10 и TCRβ, 2B4 и TCRα, 2B4 и TCRβ, и/или экспрессирует многоцепочечный CAR и трансген pTα.
[0071] Инактивацию гена можно осуществлять способами, применяемыми специалистом в этой области техники. Указанные способы включают, но не ограничиваются ими, инактивацию генов путем использования цинковых пальцев, TALEN® и системы на основе CRISPR/Cas.
[0072] В некоторых вариантах реализации иммунная клетка, содержащая CAR к ВСМА, содержит инактивированный ген CD52. В некоторых вариантах реализации инактивирована только одна копия гена CD52.
[0073] В некоторых вариантах реализации иммунная клетка, содержащая CAR к ВСМА, содержит инактивированный ген TCRα.
[0074] В некоторых вариантах реализации иммунная клетка, содержащая CAR к ВСМА, содержит инактивированный ген TCRβ.
[0075] В некоторых вариантах реализации для инактивации гена используют TALEN®. В таких вариантах реализации эффективность инактивации гена с помощью TALEN® не является 100%, и полученные TCRαβ-отрицательные Т-клетки обогащают путем деплеции остаточных TCRαβ-положительных Т-клеток перед криоконсервацией. Однако CD52-отрицательные клетки не очищают, что приводит к получению клеточного продукта с различной частотой CD52-отрицательных клеток, как правило, 60-80%. Соответственно, в некоторых вариантах реализации генотип ВСМА CAR-T-клеток согласно настоящему изобретению представляет собой BCMA-CAR+_TCRαβ-_CD52+/- Т-клетки.
[0076] В некоторых вариантах реализации TCR делают нефункциональным в клетках согласно настоящему изобретению путем инактивации гена TCRα и/или гена (генов) TCRβ. В некоторых вариантах реализации предложен способ получения модифицированных клеток, происходящих от индивидуума, согласно которому клетки могут пролиферировать независимо от пути передачи сигнала главного комплекса гистосовместимости (ГКГС). Модифицированные клетки, которые могут пролиферировать независимо от пути передачи ГКГС, которые могут быть получены этим способом, включены в объем настоящего изобретения. Описанные в настоящем документе модифицированные клетки можно применять для лечения нуждающихся в этом субъектов от отторжения «хозяин против трансплантата» (HvG) и болезни «трансплантат против хозяина» (GvHD); соответственно, в объем настоящего изобретения включен способ лечения нуждающихся в этом субъектов от отторжения «хозяин против трансплантата» (HvG) и болезни «трансплантат против хозяина» (GvHD), включающий лечение указанного субъекта путем введения указанному субъекту эффективного количества модифицированных клеток, содержащих инактивированные гены TCRα и/или TCRβ.
[0077] В некоторых вариантах реализации иммунные клетки искусственно конструируют таким образом, чтобы они были устойчивыми к одному или более химиотерапевтическим лекарственным средствам. Указанное химиотерапевтическое лекарственное средство может представлять собой, например, аналог пуринового нуклеотида (PNA), что таким образом делает иммунную клетку подходящей для лечения рака, комбинирующего адоптивную иммунотерапию и химиотерапию. Примеры PNA включают, например, клофарабин, флударабин и цитарабин отдельно или в комбинации. PNA метаболизируются дезоксицитидинкиназой (dCK) в моно-, ди- и трифосфатные PNA. Их трифосфатные формы конкурируют с АТФ за синтез ДНК, действуют как проапоптотические агенты и являются мощными ингибиторами рибонуклеотидредуктазы (RNR), которая вовлечена в образование тринуклеотидов. Согласно настоящему изобретению предложены ВСМА-специфичные CAR-T-клетки, содержащие инактивированный ген dCK. В некоторых вариантах реализации указанные клетки с нокаутом dCK получают путем трансфекции Т-клеток с использованием полинуклеотидов, кодирующих специфическую TAL-нуклеазу, направленную против генов dCK, например, путем электропорации мРНК. ВСМА-специфичные CAR-T-клетки с нокаутом dCK устойчивы к PNA, включая, например, клорофарабин и/или флударабин, и сохраняют цитотоксическую активность Т-клеток в отношении клеток, экспрессирующих ВСМА.
[0078] В некоторых вариантах реализации выделенные клетки или линии клеток согласно настоящему изобретению могут содержать рТα или его функциональный вариант. В некоторых вариантах реализации выделенная клетка или линия клеток может быть дополнительно генетически модифицирована путем инактивации гена TCRα.
[0079] В некоторых вариантах реализации CAR-T-клетка содержит полинуклеотид, кодирующий «защитный выключатель», такой как, например, RQR8. См., например, WO 2013153391 A, полное содержание которого включено в настоящий документ посредством ссылки. В CAR-T-клетках, содержащих указанный полинуклеотид, полипептид, представляющий собой «защитный выключатель», экспрессируется на поверхности CAR-T-клетки. В некоторых вариантах реализации полипептид, представляющий собой «защитный выключатель», содержит аминокислотную последовательность, представленную в SEQ ID NO: 342.
[0080] CPYSNPSLCSGGGGSELPTQGTFSNVSTNVSPAKPTTTACPYSNPSLCSGGGGSPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCNHRNRRRVCKCPRPVV (SEQ ID NO: 342)
[0081] Полипептид, представляющий собой «защитный выключатель», может также содержать сигнальный пептид на амино-конце. В некоторых вариантах реализации полипептид, представляющий собой «защитный выключатель», содержит аминокислотную последовательность, представленную в SEQ ID NO: 400.
[0082] MGTSLLCWMALCLLGADHADACPYSNPSLCSGGGGSELPTQGTFSNVSTNVSPAKPTTTACPYSNPSLCSGGGGSPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCNHRNRRRVCKCPRPVV (SEQ ID NO: 400)
[0083] Когда полипептид, представляющий собой «защитный выключатель», экспрессируется на поверхности CAR-T-клетки, связывание ритуксимаба с R эпитопами полипептида вызывает лизис клетки. Более чем одна молекула ритуксимаба может связываться с полипептидом, экспрессируемым на поверхности клетки. Каждый R эпитоп полипептида может связывать отдельную молекулу ритуксимаба. Удаление ВСМА-специфичных CAR-T-клеток может происходить in vivo, например, при введении субъекту ритуксимаба. Решение об удалении перенесенных клеток может быть принято при обнаружении у субъекта нежелательных эффектов, которые связывают с перенесенными клетками, например, при обнаружении неприемлемых уровней токсичности.
[0084] В некоторых вариантах реализации CAR-T-клетка содержит выбранный эпитоп в scFv, обладающий специфичностью распознаваться специфичным антителом. См., например, РСТ-заявку РСТ/ЕР 2016/051467, WO 2016/120216, "mAb-DRIVEN CHIMERIC ANTIGEN RECEPTOR SYSTEMS FOR SORTING/DEPLETING ENGINEERED IMMUNE CELLS", поданную 25 января 2016 года, полное содержание которой включено в настоящее описание посредством ссылки. Такой эпитоп облегчает сортировку и/или деплецию CAR-T-клеток. Указанный эпитоп может быть выбран из большого числа эпитопов, известных в этой области техники. В некоторых вариантах реализации эпитоп может являться мишенью моноклонального антитела, одобренного для применения в медицине, такой как например, без ограничения, эпитоп CD20, распознаваемый ритуксимабом. В некоторых вариантах реализации эпитоп содержит аминокислотную последовательность, представленную в SEQ ID NO: 397.
[0085] CPYSNPSLC (SEQ ID NO: 397)
[0086] В некоторых вариантах реализации эпитоп расположен в пределах CAR. Например, без ограничения, эпитоп может быть расположен между scFv и шарнирной областью CAR. В некоторых вариантах реализации в CAR можно использовать два «экземпляра» одного и того же эпитопа, разделенные линкерами. Например, в CAR можно использовать полипептид, содержащий аминокислотную последовательность, представленную в SEQ ID NO: 398, расположенный между вариабельной областью легкой цепи и шарнирной областью.
[0087] GSGGGGSCPYSNPSLCSGGGGSCPYSNPSLCSGGGGS (SEQ ID NO: 398)
[0088] В некоторых вариантах реализации эпитоп-специфичное антитело может быть конъюгировано с цитотоксическим лекарственным средством. Также можно усиливать комплементзависимую цитотоксичность (CDC) путем использования искусственно сконструированных антител, на которые привит компонент (компоненты) системы комплемента. В некоторых вариантах реализации активацию CAR-T-клеток можно модулировать путем деплеции клеток с применением антитела, которое распознает эпитоп.
III. Применение в терапии
[0089] Выделенные клетки, полученные описанными выше способами, или линии клеток, полученные из таких выделенных клеток, можно применять в качестве лекарственного средства. В некоторых вариантах реализации такое лекарственное средство можно применять для лечения ММ. В некоторых вариантах реализации ММ представляет собой рефрактерную ММ. В некоторых вариантах реализации ММ представляет собой рецидивирующую ММ. В некоторых вариантах реализации ММ представляет собой рефрактерную/рецидивирующую ММ.
[0090] В некоторых вариантах реализации субъект не получал никакой предшествующей терапии множественной миеломы. В некоторых вариантах реализации субъект получил по меньшей мере один, два или три вида предшествующей терапии множественной миеломы. В некоторых вариантах реализации режимы дозирования, указанные в настоящем документе, представляют собой терапию первой линии. В некоторых вариантах реализации режимы дозирования, указанные в настоящем документе, представляют собой терапию второй линии. В некоторых вариантах реализации режимы дозирования, указанные в настоящем документе, представляют собой терапию третьей линии. В некоторых вариантах реализации режимы дозирования, приведенные в настоящем документе, представляют собой терапию четвертой линии. В некоторых вариантах реализации у субъекта рецидивирующая ММ. В некоторых вариантах реализации у субъекта рефрактерная ММ. В некоторых вариантах реализации у субъекта рефрактерная и рецидивирующая ММ.
[0091] В некоторых вариантах реализации выделенные клетки согласно настоящему изобретению или линию клеток, полученную из указанных выделенных клеток, можно применять в изготовлении лекарственного средства для лечения рака у нуждающегося в этом субъекта.
[0092] Согласно настоящему изобретению также предложены способы лечения субъектов. В некоторых вариантах реализации указанный способ включает предоставление иммунных клеток согласно настоящему изобретению нуждающемуся в этом субъекту. В некоторых вариантах реализации способ включает этап введения трансформированных иммунных клеток согласно настоящему изобретению нуждающемуся в этом субъекту. Указанный субъект может представлять собой мужчину или женщину, взрослого, подростка или ребенка. В некоторых вариантах реализации субъект представляет собой человека.
[0093] В некоторых вариантах реализации может происходить рост Т-клеток согласно настоящему изобретению in vivo и они могут сохраняться в течение продолжительного периода времени.
[0094] Способы лечения согласно настоящему изобретению могут уменьшать интенсивность заболевания, излечивать или являться профилактическими. Способ согласно настоящему изобретению может являться либо частью аутологичной иммунотерапии, либо частью аллогенного иммунотерапевтического лечения. Настоящее изобретение особенно подходит для аллогенной иммунотерапии. Т-клетки от доноров можно трансформировать в неаллореактивные клетки с применением стандартных протоколов и репродуцировать при необходимости и таким образом получать CAR-T-клетки, которые можно вводить одному или нескольким субъектам. Такую терапию CAR-T-клетками можно предоставлять в виде готового к применению терапевтического продукта. На Фиг. 17 и 18 описаны ограничения терапии аутологичными CAR-T и преимущества аллогенной терапии.
[0095] Клетки, которые можно применять с описанными способами, описаны в предыдущем разделе. Лечение можно применять для лечения субъектов с диагнозом ММ. Также включены опухоли/раковые заболевания у взрослых и опухоли/раковые заболевания у детей. В некоторых вариантах реализации лечение можно осуществлять в комбинации с одним или более вариантами терапии ММ, выбранными из группы терапии антителами, химиотерапии, терапии цитокинами, терапии дендритными клетками, генной терапии, гормональной терапии, лазерной терапии и лучевой терапии.
[0096] В некоторых вариантах реализации данного изобретения лечение можно осуществлять у субъектов, проходящих иммуносупрессивное лечение. Действительно, настоящее изобретение предпочтительно основано на применении клеток или популяции клеток, которые сделали устойчивыми по меньшей мере к одному иммуносупрессивному агенту за счет инактивации гена, кодирующего рецептор для такого иммуносупрессивного агента. В соответствии с этим аспектом иммуносупрессивное лечение должно способствовать отбору и росту Т-клеток согласно настоящему изобретению в организме субъекта.
[0097] Введение клеток или популяции клеток согласно настоящему изобретению можно осуществлять любым удобным способом, в том числе путем ингаляции аэрозоля, инъекции, приема внутрь, трансфузии, имплантации или трансплантации. Композиции, описанные в настоящем документе, можно вводить субъекту подкожно, внутрикожно, внутрь опухоли, внутрь узлов, интрамедуллярно, внутримышечно, путем внутривенной или внутрилимфатической инъекции, или интраперитонеально. В некоторых вариантах реализации композиции клеток согласно настоящему изобретению предпочтительно вводят путем внутривенной инъекции.
[0098] В некоторых вариантах реализации искусственно сконструированные иммунные клетки согласно настоящему изобретению, экспрессирующие CAR к ВСМА, представлены в форме для инфузии. В некоторых вариантах реализации указанные клетки представлены в растворе, содержащем примерно 5% ДМСО. В одном из вариантов реализации 14×10∧6 BCMA-CAR-T-клеток/мл представлены в растворе, содержащем примерно 5% ДМСО. В другом варианте реализации состав содержит смесь CryoStor® Basal Solution и CryoStor® CS10 в соотношении 1:1, что позволяет получить 5% конечную концентрацию диметилсульфоксида. В некоторых вариантах реализации дозировка состава составляет 14×10∧6 BCMA-CAR-T-клеток/мл. В некоторых вариантах реализации этот лекарственный препарат поставляют в 2 мл флаконе с закрытой системой со встроенной пробкой в номинальном объеме 1 мл.
[0099] В некоторых вариантах реализации изобретения ВСМА-направленные CAR-T-клетки согласно настоящему описанию представляют собой BCMA-CAR+_TCRαβ-CD52+/- Т-клетки и представлены в форме суспензии для инфузии. В некоторых вариантах реализации BCMA-CAR+_TCRαβ-_CD52+/- Т-клетки представлены в смеси CryoStor® Basal Solution и CryoStor® CS10 в соотношении 1:1, что позволяет получить 5% конечную концентрацию диметилсульфоксида. В некоторых вариантах реализации дозировка состава составляет 14×10∧6 BCMA-CAR+_TCRαβ-CD52+/- Т-клеток/мл.
IV. Лимфодеплеции
[00100] В некоторых вариантах реализации у субъекта применяют режим лимфодеплеции (LD) перед первой и/или последующей дозой ВСМА CAR-T-клеток. В некоторых вариантах реализации у субъекта применяют режим лимфодеплеции одновременно с первой и/или последующей дозой CAR-T-клеток. В некоторых вариантах реализации режим лимфодеплеции применяют до, во время и/или после первой и/или последующей дозы ВСМА CAR-T-клеток.
[00101] Подходящие режимы LD описаны в настоящем документе и/или известны в этой области техники. В некоторых вариантах реализации LD начинают до, одновременно или после инфузии CAR-T. Дозы и время введения LD можно корректировать с учетом первого или последующего введения дозы ВСМА CAR-T. В некоторых вариантах реализации продолжительность LD составляет от 3 до 5 дней. В некоторых вариантах реализации временной интервал между завершением LD и началом введения CAR-T составляет от примерно 2 дней до примерно 2 недель. В некоторых вариантах реализации LD начинают примерно за 15-7 дней до введения дозы CAR-T-клеток. В некоторых вариантах реализации LD начинают примерно за 19-5 дней до введения дозы CAR-T-клеток. В некоторых вариантах реализации LD начинают примерно за 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 дней до введения дозы CAR-T-клеток. В некоторых вариантах реализации продолжительность режима LD составляет примерно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14 дней. В некоторых вариантах реализации дозу CAR-T-клеток вводят примерно через 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14 дней после завершения LD.
[00102] В некоторых вариантах реализации режим LD включает введение одного или более химиотерапевтических лекарственных средств.
[00103] В некоторых вариантах реализации режим LD включает введение антитела к CD52, такого как антитело, которое распознает антиген 52 кластера дифференцировки (CD) человека, гликопротеин клеточной поверхности, экспрессируемый на большинстве лимфоидных клеток. В настоящем описании моноклональное антитело к CD52 представляет собой антитело, которое направлено против гликопротеина CD52 клеточной поверхности массой 21-28 кДа. CD52 представляет собой распространенную молекулу (приблизительно 5×105 сайтов связывания антитела на клетку), присутствующую по меньшей мере на 95% всех лимфоцитов и моноцитов/макрофагов периферической крови человека. Типичные антитела к CD52 для применения в способах и композициях, описанных в настоящем документе, включают, например, алемтузумаб. В некоторых вариантах реализации антитело к CD52 содержит последовательности HCDR1, HCDR2, HCDR3, LCDR1, LCDR2 и LCDR3, представленные в Таблице 4 ниже.
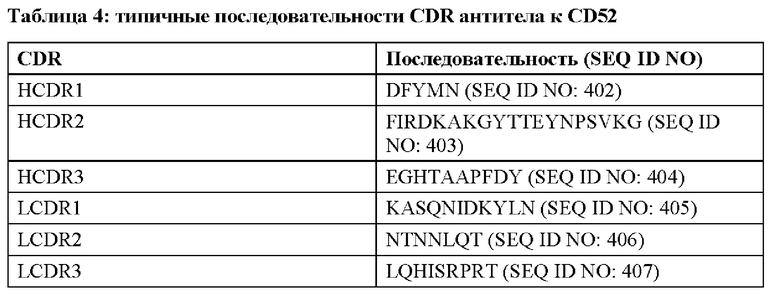
[00104] В некоторых вариантах реализации антитело к CD52 содержит VH и/или VL, содержащие последовательности, представленные в Таблице 5 ниже.


[00105] В некоторых вариантах реализации антитело к CD52 содержит VH, имеющую последовательность SEQ ID NO: 8 или последовательность, по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98% или по меньшей мере на 99% идентичную последовательности SEQ ID NO: 408. В некоторых вариантах реализации антитело к CD52 содержит VL, имеющую последовательность SEQ ID NO: 410 или последовательность, по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98% или по меньшей мере на 99% идентичную последовательности SEQ ID NO: 410. В некоторых вариантах реализации антитело к CD52 содержит VH, имеющую последовательность SEQ ID NO: 408, и VL, имеющую последовательность SEQ ID NO: 410. В некоторых вариантах реализации антитело к CD52 содержит VH, кодируемую ДНК-последовательностью SEQ ID NO: 409, и VL, кодируемую ДНК-последовательностью SEQ ID NO: 411.
[00106] В некоторых вариантах реализации антитело к CD52 представляет собой рекомбинантное гуманизированное моноклональное антитело (МАТ) IgG1-каппа. В некоторых вариантах реализации антитело к CD52 представляет собой алемтузумаб. Алемтузумаб представляет собой полученное из рекомбинантной ДНК гуманизированное моноклональное антитело, направленное против гликопротеина клеточной поверхности массой 21-28 кДа, CD52. См., например, Saif et al., Pediatr Transplant 2015 Mar; 19 (2): 211-8. В некоторых вариантах реализации антитело к CD52 содержит одну или более последовательностей CDR, выделенных или полученных из CDR алемтузумаба. В некоторых вариантах реализации антитело к CD52 содержит последовательность SEQ ID NO: 408 или последовательность, по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98% или по меньшей мере на 99% идентичную последовательности SEQ ID NO: 408. В некоторых вариантах реализации антитело к CD52 содержит последовательность SEQ ID NO: 410 или последовательность, по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98% или по меньшей мере на 99% идентичную последовательности SEQ ID NO: 410. В некоторых вариантах реализации антитело к CD52 содержит HCDR1, содержащий последовательность SEQ ID NO: 402, HCDR2, содержащий последовательность SEQ ID NO: 403, HCDR3, содержащий последовательность SEQ ID NO: 404, LCDR1, содержащий последовательность SEQ ID NO: 405, LCDR1, содержащий последовательность SEQ ID NO: 406, и/или LCDR3, содержащий последовательность SEQ ID NO: 407. В некоторых вариантах реализации антитело к CD52 содержит HCDR1, содержащий последовательность SEQ ID NO: 402, HCDR2, содержащий последовательность SEQ ID NO: 403, HCDR3, содержащий последовательность SEQ ID NO: 404, LCDR1, содержащий последовательность SEQ ID NO: 405, LCDR1, содержащий последовательность SEQ ID NO: 406, и LCDR3, содержащий последовательность SEQ ID NO: 407; при этом указанное антитело к CD52 содержит последовательность SEQ ID NO: 408 и/или SEQ ID NO: 410, или последовательность, по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98% или по меньшей мере на 99% идентичную последовательности SEQ ID NO: 408 и/или SEQ ID NO: 410.
[00107] В некоторых вариантах реализации LD включает введение только антитела к CD52.
[00108] В некоторых вариантах реализации LD включает введение комбинации вариантов терапии. В некоторых вариантах реализации указанная комбинация включает: флударабин (диапазон общей дозы от примерно 90 до 150 мг/м2) и циклофосфамид (диапазон общей дозы от примерно 1000 до 4000 мг/м2) с анти-CD52 лекарственным средством или без него (например, антитело к CD52, такое как антитело, содержащее последовательность SEQ ID NO: 408 и/или SEQ ID NO: 410) (общая доза от примерно 0,3 до примерно 1 мг/кг или постоянная доза от примерно 30 мг до примерно 40 мг, от примерно 25 до примерно 60 мг, от примерно 60 мг до примерно 90 мг или от примерно 100 мг до примерно 120 мг). В некоторых вариантах реализации комбинация включает: флударабин (примерно 30 мг/м2) и циклофосфамид (диапазон общей дозы от примерно 500 до 600 мг/м2) с анти-CD52 лекарственным средством или без него (например, антитело к CD52) (общая доза от примерно 0,3 до примерно 1 мг/кг или постоянная доза от примерно 30 мг до примерно 40 мг, от примерно 25 до примерно 60 мг, от примерно 60 мг до примерно 90 мг или от примерно 100 мг до примерно 120 мг). В некоторых вариантах реализации комбинация включает: флударабин (примерно 30 мг/м2) и циклофосфамид (примерно 300 мг/м2) с анти-CD52 лекарственным средством или без него (например, антитело к CD52) (общая доза от примерно 0,3 до примерно 1 мг/кг или постоянная доза от примерно 30 мг до примерно 40 мг, от примерно 20 мг до примерно 30 мг, от примерно 25 до примерно 60 мг, от примерно 60 мг до примерно 90 мг или от примерно 100 мг до примерно 120 мг). В некоторых вариантах реализации комбинация включает: флударабин (примерно 90 мг/м2) и циклофосфамид (примерно 900 мг/м2) с анти-CD52 лекарственным средством или без него (например, антитело к CD52) (общая доза от примерно 0,3 до примерно 1 мг/кг или постоянная доза от примерно 30 мг до примерно 40 мг, от примерно 20 мг до примерно 30 мг, от примерно 25 до примерно 60 мг, от примерно 60 мг до примерно 90 мг или от примерно 100 мг до примерно 120 мг). В некоторых вариантах реализации комбинация включает: флударабин (примерно 90 мг/м2), циклофосфамид (примерно 1500 мг/м2) и с анти-CD52 лекарственным средством или без него (например, антитело к CD52, примерно 1 мг/кг). В некоторых вариантах реализации комбинация включает: флударабин (примерно 150 г/м2) и циклофосфамид (примерно 130 мг/кг) с анти-CD52 лекарственным средством или без него (например, антитело к CD52, общая доза от примерно 0,3 до примерно 1 мг/кг или постоянная доза от примерно 30 мг до примерно 40 мг, от примерно 25 до примерно 60 мг, от примерно 60 мг до примерно 90 мг или от примерно 100 мг до примерно 120 мг). В некоторых вариантах реализации комбинация включает: флударабин (примерно 150 г/м2) и циклофосфамид (примерно 120 мг/кг или примерно 130 мг/кг) с анти-CD52 лекарственным средством или без него (например, антитело к CD52), общая доза от примерно 0,3 до примерно 1 мг/кг или постоянная доза от примерно 30 мг до примерно 40 мг, от примерно 25 до примерно 60 мг или от примерно 100 мг до примерно 120 мг). В некоторых вариантах реализации комбинация включает: флударабин (примерно 30 мг/м2/день) и циклофосфамид (примерно 300 мг/м2/день) с анти-CD52 лекарственным средством или без него (например, антитело к CD52, примерно 13 мг/день). В некоторых вариантах реализации комбинация включает: флударабин (примерно 30 мг/м2/день) и циклофосфамид (примерно 300 мг/м2/день) с анти-CD52 лекарственным средством или без него (например, антитело к CD52, примерно 10 мг/день). В некоторых вариантах реализации комбинация включает: циклофосфамид и анти-CD52 лекарственное средство (например, антитело к CD52). В некоторых вариантах реализации эти вышеуказанные дозы вводят в течение одного дня. В некоторых вариантах реализации вышеуказанные дозы вводят в течение нескольких дней.
[00109] В некоторых вариантах реализации флударабин и циклофосфамид вводят в первый день, а антитело к CD52 (например, антитело, содержащее последовательность SEQ ID NO: 408 и/или SEQ ID NO: 410) вводят во второй день. В некоторых вариантах реализации флударабин и циклофосфамид вводят в первый день перед введением CAR-T-клеток, а антитело к CD52 (например, антитело, содержащее последовательность SEQ ID NO: 408 и/или SEQ ID NO: 410) вводят во второй день; при этом второй день представляет собой тот же день, в который вводят CAR-T-клетки, или второй день наступает после введения CAR-T-клеток. В некоторых вариантах реализации флударабин и циклофосфамид вводят в первый день, CAR-T-клетки вводят во второй день и антитело к CD52 (например, антитело, содержащее последовательность SEQ ID NO: 408 и/или SEQ ID NO: 410) вводят спустя по меньшей мере примерно 1, примерно 2, примерно 3, примерно 4, примерно 5, примерно 6, примерно 7, примерно 8, примерно 9, примерно 10, примерно 11 или примерно 12 недель после второго дня. В некоторых вариантах реализации флударабин и циклофосфамид вводят перед введением CAR-T-клеток, а антитело к CD52 (например, антитело, содержащее последовательность SEQ ID NO: 408 и/или SEQ ID NO: 410) вводят спустя по меньшей мере примерно 1, примерно 2, примерно 3, примерно 4, примерно 5, примерно 6, примерно 7, примерно 8, примерно 9, примерно 10, примерно 11 или примерно 12 недель после введения CAR-T-клеток.
[00110] В некоторых вариантах реализации режим лимфодеплеции включает введение флударабина и циклофосфамида (FC). В некоторых вариантах реализации режим лимфодеплеции включает введение флударабина и антитела к CD52 (например, антитела, содержащего последовательность SEQ ID NO: 408 и/или SEQ ID NO: 410) (FA). В некоторых вариантах реализации режим лимфодеплеции включает введение циклофосфамида и антитела к CD52 (например, антитела, содержащего последовательность SEQ ID NO: 408 и/или SEQ ID NO: 410) (СА). В некоторых вариантах реализации режим лимфодеплеции включает введение флударабина, циклофосфамида и антитела к CD52 (например, антитела, содержащего последовательность SEQ ID NO: 408 и/или SEQ ID NO: 410) (FCA).
[00111] Выбор конкретных лекарственных средств и дозы для режима лимфодеплеции перед первой или второй/последующей дозой CAR-T-клеток может быть основан на гематологическом анализе и гематологическом восстановлении пациента. В случае повторного введения дозы второй режим лимфодеплеции может быть более или менее интенсивным по сравнению с первым режимом лимфодеплеции (например, исходя из восстановления лимфоцитов, нейтрофилов и вирусной реактивации после первой дозы). Например, если уровни лимфоцитов и нейтрофилов высокие на момент повторного введения дозы, можно применять интенсивный или агрессивный режим лимфодеплеции. В качестве альтернативы, если уровни лимфоцитов низкие на момент повторного введения дозы, можно применять более слабый или менее агрессивный режим лимфодеплеции. В некоторых вариантах реализации, если количество бластных клеток на момент повторного введения дозы является высоким, применяют интенсивный или агрессивный режим лимфодеплеции. В некоторых вариантах реализации, если количество бластных клеток на момент повторного введения дозы является низким, применяют более слабый или менее агрессивный режим лимфодеплеции.
[00112] В некоторых вариантах реализации можно применять режим LD повышенной интенсивности при повторном введении дозы (совместно с анти-CD52 лекарственным средством или без него). В некоторых вариантах реализации можно применять режим LD пониженной интенсивности, например, в случае лимфопении 3-4 степени на момент повторного введения дозы (совместно с анти-CD52 лекарственным средством или без него).
[00113] В некоторых вариантах реализации компоненты режима лимфодеплеции флударабин/циклофосфамид (FC) или флударабин/циклофосфамид/антитело к CD52 (FCA) вводят одновременно; в других вариантах реализации указанные компоненты вводят последовательно. В некоторых вариантах реализации компоненты режима лимфодеплеции флударабин/циклофосфамид (FC) или флударабин/циклофосфамид/антитело к CD52 (FCA) вводят одновременно в -5 день, -4 день и -3 день. В некоторых вариантах реализации компоненты режима лимфодеплеции флударабин/циклофосфамид (FC) вводят до введения антитела к CD52. В некоторых вариантах реализации флударабин/циклофосфамид (FC) вводят в -7 день, -6 день и -5 день с последующим введением антитела к CD52 (А) в -4 день и -3 день. В некоторых вариантах реализации флударабин/циклофосфамид (FC) вводят в -7 день, -6 день и -5 день с последующим введением антитела к CD52 (А) в -5 день, -4 день и -3 день. В некоторых вариантах реализации у субъекта применяют режим FC перед первой дозой терапии CAR-T-клетками; и режим FCA перед повторным введением терапии CAR-T-клетками. В некоторых вариантах реализации у субъекта применяют режим FCA перед первой дозой терапии CAR-T-клетками; и второй режим FCA перед повторным введением терапии CAR-T-клетками.
[00114] Типичные режимы LD представлены в Таблицах 6А, 6В, 6С, 6D, 6Е, 6F и 6G. В Таблицах 6A-6G время, указанное в «Графике», указано относительно времени введения дозы CAR-T-клеток (0Д) в днях. Отрицательные числа обозначают дни до введения CAR-T-клеток (в 0Д).

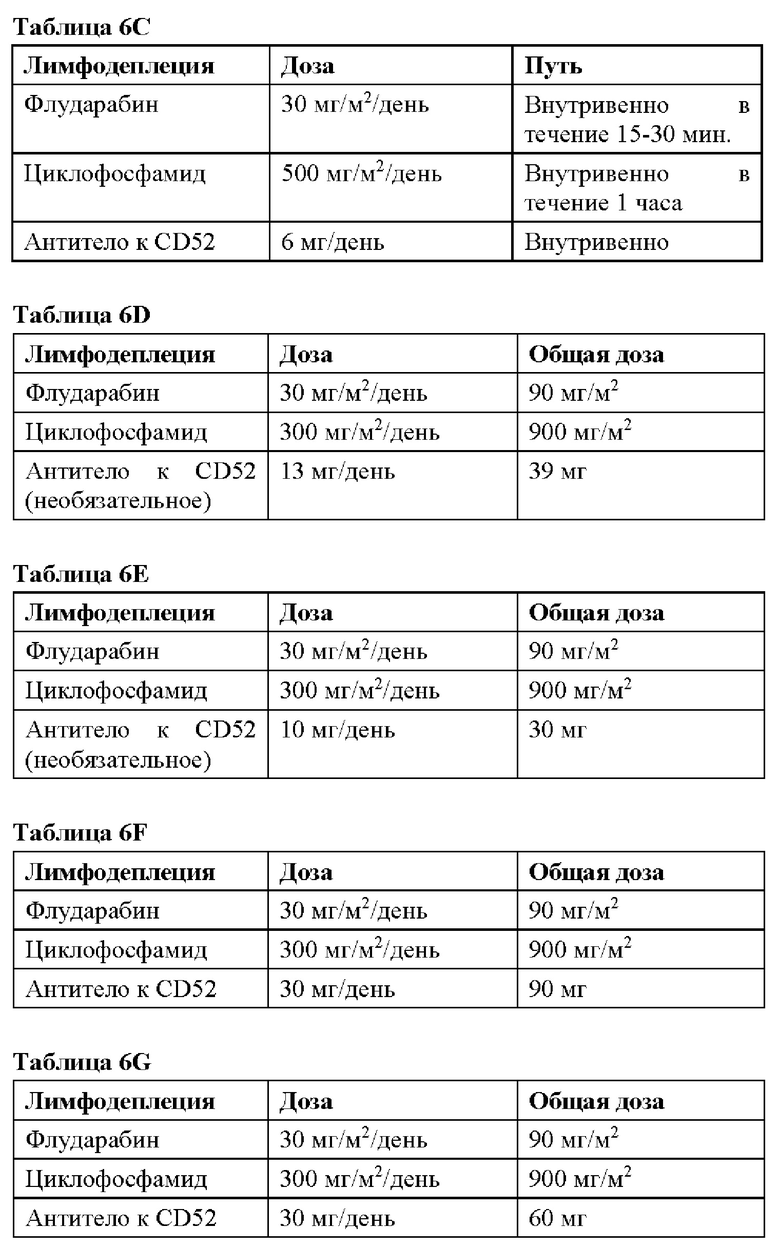
V. Режимы дозирования
[00115] В некоторых вариантах реализации аллогенные ВСМА CAR-T-клетки согласно настоящему изобретению вводят с использованием постоянной дозы. В других вариантах реализации аллогенные ВСМА CAR-T-клетки вводят с использованием привязки доз к диапазонам. Например, можно использовать привязку доз к диапазонам, чтобы избежать риска обширного воздействия CAR-T-клеток. В некоторых вариантах реализации можно использовать диапазон массы тела. Например, без ограничения, субъектам <66 кг можно вводить дозу X, а субъектам ≥66 кг можно вводить дозу примерно 1,33Х. В некоторых вариантах реализации субъектам ≥50 кг можно вводить одну дозу, а субъектам ≤50 кг можно вводить другую дозу.
[00116] Типичные уровни доз для первой дозы аллогенных ВСМА CAR-T-клеток приведены в Таблице 7А для применения у субъектов с рецидивирующей/рефрактерной ММ. Уровень дозы, обозначенный как вводят только при необходимости.
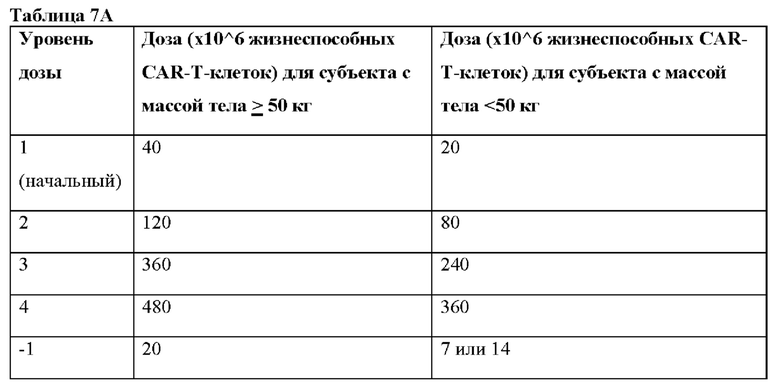
[00117] В некоторых вариантах реализации субъекту с массой тела ≥50 кг вводят дозу аллогенных ВСМА CAR-T-клеток согласно настоящему изобретению, при этом указанная доза находится в диапазоне от примерно 20 х 10∧6 клеток/доза до примерно 480 х 10∧6 клеток/доза. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой BCMA-CAR+_TCRαβ-_CD52+/- Т-клетки. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой CAR-T-клетки ВСМА-1 (описанные в Примере 1).
[00118] В некоторых вариантах реализации субъекту с массой тела ≥50 кг вводят дозу аллогенных ВСМА CAR-T-клеток согласно настоящему изобретению, при этом указанная доза находится в диапазоне от примерно 20 х 10∧6 клеток/доза до примерно 40 х 10∧6 клеток/доза, от примерно 40 х 10∧6 клеток/доза до примерно 120 х 10∧6 клеток/доза, от примерно 120 х 10∧6 клеток/доза до примерно 360 х 10∧6 клеток/доза или от примерно 360 х 10∧6 клеток/доза до примерно 480 х 10∧6 клеток/доза. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой BCMA-CAR+_TCRαβ-_CD52+/- Т-клетки. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой CAR-T-клетки ВСМА-1.
[00119] В некоторых вариантах реализации субъекту с массой тела <50 кг вводят дозу аллогенных ВСМА CAR-T-клеток согласно настоящему изобретению, при этом указанная доза находится в диапазоне от примерно 7 х 10∧6 клеток/доза до примерно 360 х 10∧6 клеток/доза. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой BCMA-CAR+_TCRαβ-_CD52+/- Т-клетки. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой CAR-T-клетки ВСМА-1.
[00120] В некоторых вариантах реализации субъекту с массой тела <50 кг вводят дозу аллогенных ВСМА CAR-T-клеток согласно настоящему изобретению, при этом указанная доза находится в диапазоне от примерно 7 х 10∧6 клеток/доза или 14 х 10∧6 клеток/доза до примерно 20 х 10∧6 клеток/доза, от примерно 20 х 10∧6 клеток/доза до примерно 80 х 10∧6 клеток/доза, от примерно 80 х 10∧6 клеток/доза до примерно 240 х 10∧6 клеток/доза или от примерно 240 х 10∧6 клеток/доза до примерно 360 х 10∧6 клеток/доза. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой BCMA-CAR+TCRαβ-_CD52+/- Т-клетки. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой CAR-T-клетки ВСМА-1.
[00121] Альтернативные типичные уровни доз для первой дозы аллогенных ВСМА CAR-T-клеток приведены в Таблице 7В для применения у субъектов с рецидивирующей/рефрактерной ММ. Средний уровень доз и уровни доз, обозначенные как «4» и «-1», вводят только при необходимости.
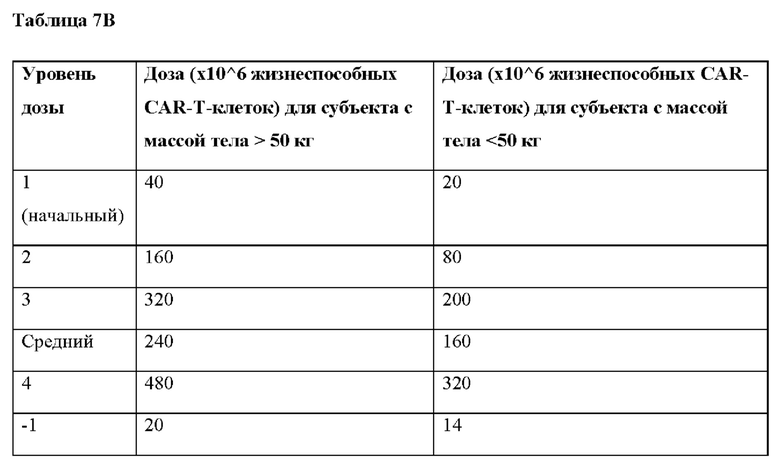
[00122] В некоторых вариантах реализации субъекту с массой тела >50 кг вводят дозу аллогенных ВСМА CAR-T-клеток согласно настоящему изобретению, при этом указанная доза находится в диапазоне от примерно 20 х 10∧6 клеток/доза до примерно 480 х 10∧6 клеток/доза. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой BCMA-CAR+TCRαβ-_CD52+/- Т-клетки. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой CAR-T-клетки ВСМА-1 (описанные в Примере 1).
[00123] В некоторых вариантах реализации субъекту с массой тела >50 кг вводят дозу аллогенных ВСМА CAR-T-клеток согласно настоящему изобретению, при этом указанная доза находится в диапазоне от примерно 20 х 10∧6 клеток/доза до примерно 40 х 10∧6 клеток/доза, от примерно 40 х 10∧6 клеток/доза до примерно 160 х 10∧6 клеток/доза, от примерно 160 х 10∧6 клеток/доза до примерно 320 х 10∧6 клеток/доза, от примерно 160 х 10∧6 клеток/доза до примерно 240 х 10∧6 клеток/доза, от примерно 240 х 10∧6 клеток/доза до примерно 320 х 10∧6 клеток/доза, от примерно 240 х 10∧6 клеток/доза до примерно 480 х 10∧6 клеток/доза или от примерно 320 х 10∧6 клеток/доза до примерно 480 х 10∧6 клеток/доза. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой CAR-T-клетки ВСМА-1. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой BCMA-CAR+TCRαβ-_CD52+/- Т-клетки.
[00124] В некоторых вариантах реализации субъекту с массой тела ≤50 кг вводят дозу аллогенных ВСМА CAR-T-клеток согласно настоящему изобретению, при этом указанная доза находится в диапазоне от примерно 14 х 10∧6 клеток/доза до примерно 320 х 10∧6 клеток/доза. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой BCMA-CAR+_TCRαβ-_CD52+/- Т-клетки. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой CAR-T-клетки ВСМА-1.
[00125] В некоторых вариантах реализации субъекту с массой тела ≤50 кг вводят дозу аллогенных ВСМА CAR-T-клеток согласно настоящему изобртению, при этом указанная доза находится в диапазоне от примерно 14 х 10∧6 клеток/доза до примерно 20 х 10∧6 клеток/доза, от примерно 20 х 10∧6 клеток/доза до примерно 80 х 10∧6 клеток/доза, от примерно 80 х 10∧6 клеток/доза до примерно 160 х 10∧6 клеток/доза, от примерно 80 х 10∧6 клеток/доза до примерно 200 х 10∧6 клеток/доза, от примерно 160 х 10∧6 клеток/доза до примерно 200 х 10∧6 клеток/доза, от примерно 200 х 10∧6 клеток/доза до примерно 320 х 10∧6 клеток/доза, от примерно 160 х 10∧6 клеток/доза до примерно 320 х 10∧6 клеток/доза или от примерно 200 х 10∧6 клеток/доза до примерно 320 х 10∧6 клеток/доза. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой ВСМА-CAR+_TCRαβ-_CD52+/- Т-клетки. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой CAR-T-клетки ВСМА-1.
[00126] В некоторых вариантах реализации субъекту с массой тела >50 кг вводят дозу аллогенных ВСМА CAR-T-клеток согласно настоящему изобретению, при этом указанная доза составляет примерно 40 х 10∧6 клеток/доза, 160 х 10∧6 клеток/доза или 320 х 10∧6 клеток/доза. В некоторых вариантах реализации вводят среднюю дозу примерно 240 х 10∧6 клеток/доза (или другой уровень дозы между уровнем дозы 1 или уровнем дозы 3), если при уровне дозы 3 наблюдают токсичность, или для определения более низкой дозы, которая является эффективной. В некоторых вариантах реализации вводят уровень дозы 480 х 10∧6 клеток/доза (уровень дозы 4), если при уровне дозы 3 наблюдают параметры недостаточной эффективности. (Фиг. 20). В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой BCMA-CAR+_TCRαβ-_CD52 Т-клетки. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой CAR-T-клетки ВСМА-1.
[00127] Клетки или популяция клеток можно вводить одной или более дозами. В некоторых вариантах реализации указанное эффективное количество клеток можно вводить в виде однократной дозы. В некоторых вариантах реализации указанное эффективное количество клеток можно вводить в виде более чем одной дозы в течение определенного периода времени. Время введения определяется лечащим врачом и зависит от клинического состояния субъекта. Клетки или популяция клеток могут быть получены из любого источника, такого как банк крови или донор. Хотя индивидуальные потребности варьируются, определение оптимальных диапазонов эффективных количеств конкретного типа клеток для конкретного заболевания или состояния находится в пределах компетенции специалиста в этой области техники. Эффективное количество означает количество, которое обеспечивает терапевтический или профилактический эффект. Вводимая доза, в целом, будет зависеть от возраста, состояния здоровья и массы реципиента, вида сопутствующего лечения, при наличии такового, частоты лечения и характера желаемого эффекта. В некоторых вариантах реализации эффективное количество клеток или композиции, содержащей эти клетки, вводят парентерально. В некоторых вариантах реализации введение может представлять собой внутривенное введение. В некоторых вариантах реализации введение можно осуществлять непосредственно путем инъекции внутрь опухоли.
[00128] В некоторых вариантах реализации настоящего изобретения клетки можно вводить субъекту в сочетании (например, до, одновременно или после) с любым количеством подходящих методов лечения, включая, но не ограничиваясь ими, лечение такими агентами, как терапия моноклональными антителами, антагонист CCR2 (например, INC-8761), противовирусная терапия, цидофовир и интерлейкин-2, лечение цитарабином (также известным как ARA-C) или натализиимабом для субъектов с рассеянным склерозом (MS) или лечение эфализтимабом для субъектов с псориазом, или другое лечение для субъектов с PML. В некоторых вариантах реализации ВСМА-специфичные CAR-T-клетки вводят субъекту в сочетании с одним или более из следующих агентов: антитела к PD-1 (например, ниволумаб, пембролизумаб или PF-06801591), антитела к PD-L1 (например, авелумаб, атезолизумаб или дурвалумаб), антитела к ОХ40 (например, PF-04518600), антитела к 4-1ВВ (например, PF-05082566), антитела к MCSF (например, PD-0360324), антитела к GITR и/или антитела к TIGIT. В некоторых вариантах реализации ВСМА-специфичный CAR согласно настоящему изобретению вводят субъекту в сочетании с антителом к PD-L1 авелумабом. В дополнительных вариантах реализации Т-клетки согласно настоящему изобретению можно применять в комбинации с химиотерапией, лучевой терапией, иммуносупрессивными агентами, такими как циклоспорин, азатиоприн, метотрексат, микофенолат и FK506, антителами или другими иммунодеструктивными агентами, такими как САМРАТН, антителами к CD3 или другими вариантами терапии антителами, цитоксином, флударибином, циклоспорином, FK506, рапамицином, микофеноловой кислотой, стероидами, FR901228, цитокинами и/или облучением. Эти лекарственные средства либо ингибируют кальцийзависимую фосфатазу кальциневрин (циклоспорин и FK506), либо ингибируют киназу p70S6, которая важна для передачи сигнала, индуцированной фактором роста (рапамицин) (Henderson, Naya et al. 1991; Liu, Albers et al. 1992; Bierer, Hollander et al. 1993). В другом варианте реализации композиции клеток согласно настоящему изобретению вводят субъекту в сочетании (например, до, одновременно или после) с трансплантацией костного мозга, терапией, разрушающей Т-клетки, с применением либо химиотерапевтических агентов, таких как флударабин, наружной дистанционной лучевой терапии (XRT), циклофосфамида, либо антител, таких как OKT3 или САМРАТН. В некоторых вариантах реализации композиции клеток согласно настоящему изобретению вводят после терапии, разрушающей В-клетки, такой как агенты, которые взаимодействуют с CD20, например, ритуксан. Например, в одном из вариантов реализации субъекты могут проходить стандартное лечение химиотерапией высокими дозами с последующей трансплантацией стволовых клеток периферической крови. В некоторых вариантах реализации после указанной трансплантации субъекты получают инфузию размноженных иммунных клеток согласно настоящему изобретению. В некоторых вариантах реализации размноженные клетки вводят до или после оперативного вмешательства.
VI. Способы повторного лечения CAR-T-клетками
[00129] Согласно настоящему изобретению также предложены способы повторного лечения (повторного введения доз) ВСМА CAR-T-клетками. В частности, указанные способы включают введение одной или более последующих доз клеток субъектам, получившим первую дозу, и/или введение первой и одной или более последующих доз. Указанные дозы обычно вводят в конкретных количествах и в соответствии с конкретными временными параметрами. В некоторых вариантах реализации способы, в целом, включают введение первой дозы клеток со снижением таким образом тяжести заболевания, с последующей дозой клеток, вводимой в течение конкретного временного интервала по отношению к первой дозе, или введение последующей дозы субъекту, получившему такую первую дозу. В некоторых вариантах реализации затем вводят дополнительные последующие дозы, например, в пределах такого же или подобного временного интервала по отношению к последующей дозе. В некоторых вариантах реализации количество вводимых клеток и время для введения нескольких доз предназначены для улучшения одного или более результатов, например, для снижения вероятности или степени токсичности для субъекта, улучшения воздействия на субъекта и/или стойкости вводимых клеток, и/или повышения терапевтической эффективности. Также предложены готовые изделия, содержащие указанные клетки и предназначенные для введения в соответствии с такими режимами дозирования.
[00130] В некоторых вариантах повторного лечения (повторного введения доз) субъекту с массой тела >50 кг вводят повторную дозу аллогенных ВСМА CAR-T-клеток согласно настоящему изобретению, при этом указанная доза находится в диапазоне от примерно 20 х 10∧6 клеток/доза до примерно 480 х 10∧6 клеток/доза. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой BCMA-CAR+_TCRαβ-_CD52+/- Т-клетки. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой CAR-T-клетки ВСМА-1 (описанные в Примере 1).
[00131] В некоторых вариантах повторного лечения (повторного введения доз) субъекту с массой тела >50 кг вводят повторную дозу аллогенных ВСМА CAR-T-клеток согласно настоящему изобретению, при этом указанная доза находится в диапазоне от примерно 20 х 10∧6 клеток/доза до примерно 40 х 10∧6 клеток/доза, от примерно 40 х 10∧6 клеток/доза до примерно 160 х 10∧6 клеток/доза, от примерно 160 х 10∧6 клеток/доза до примерно 320 х 10∧6 клеток/доза, от примерно 160 х 10∧6 клеток/доза до примерно 240 х 10∧6 клеток/доза, от примерно 240 х 10∧6 клеток/доза до примерно 320 х 10∧6 клеток/доза, от примерно 240 х 10∧6 клеток/доза до примерно 480 х 10∧6 клеток/доза или от примерно 320 х 10∧6 клеток/доза до примерно 480 х 10∧6 клеток/доза. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой CAR-T-клетки ВСМА-1. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой ВСМА-CAR+_TCRαβ-_CD52+/- Т-клетки.
[00132] В некоторых вариантах повторного лечения (повторного введения доз) субъекту с массой тела >50 кг вводят повторную дозу аллогенных ВСМА CAR-T-клеток согласно настоящему изобретению, при этом указанная доза составляет примерно 40 х 10∧6 клеток/доза, 160 х 10∧6 клеток/доза или 320 х 10∧6 клеток/доза. В некоторых вариантах реализации вводят среднюю дозу примерно 240 х 10∧6 клеток/доза (или другой уровень дозы между уровнем дозы 1 или уровнем дозы 3), если при уровне дозы 3 наблюдают токсичность, или для определения более низкой дозы, которая является эффективной. В некоторых вариантах реализации вводят уровень дозы 480 х 10∧6 клеток/доза (уровень дозы 4), если при уровне дозы 3 наблюдают параметры недостаточной эффективности. (Фиг. 20). В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой BCMA-CAR+_TCRαβ-_CD52+/- Т-клетки. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой CAR-T-клетки ВСМА-1.
[00133] В некоторых вариантах повторного лечения (повторного введения доз) субъекту с массой тела ≥50 кг вводят повторную дозу аллогенных ВСМА CAR-T-клеток согласно настоящему изобретению, при этом указанная доза находится в диапазоне от примерно 20 х 10∧6 клеток/доза до примерно 480 х 10∧6 клеток/доза. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой BCMA-CAR+TCRαβ-_CD52+/- Т-клетки. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой CAR-T-клетки ВСМА-1 (описанные в Примере 1).
[00134] В некоторых вариантах повторного лечения (повторного введения доз) субъекту с массой тела ≥50 кг вводят повторную дозу аллогенных ВСМА CAR-T-клеток согласно настоящему изобретению, при этом указанная доза находится в диапазоне от примерно 20 х 10∧6 клеток/доза до примерно 40 х 10∧6 клеток/доза, от примерно 40 х 10∧6 клеток/доза до примерно 120 х 10∧6 клеток/доза, от примерно 120 х 10∧6 клеток/доза до примерно 360 х 10∧6 клеток/доза или от примерно 360 х 10∧6 клеток/доза до примерно 480 х 10∧6 клеток/доза. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой BCMA-CAR+_TCRαβ-_CD52+/- Т-клетки. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой CAR-T-клетки ВСМА-1.
[00135] В некоторых вариантах повторного лечения (повторного введения доз) субъекту с массой тела ≤50 кг вводят повторную дозу аллогенных ВСМА CAR-T-клеток согласно настоящему изобретению, при этом указанная доза находится в диапазоне от примерно 14 х 10∧6 клеток/доза до примерно 320 х 10∧6 клеток/доза. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой BCMA-CAR+TCRαβ-_CD52+/- Т-клетки. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой CAR-T-клетки ВСМА-1.
[00136] В некоторых вариантах повторного лечения (повторного введения доз) субъекту с массой тела ≤50 кг вводят повторную дозу аллогенных ВСМА CAR-T-клеток согласно настоящему изобртению, при этом указанная доза находится в диапазоне от примерно 14 х 10∧6 клеток/доза до примерно 20 х 10∧6 клеток/доза, от примерно 20 х 10∧6 клеток/доза до примерно 80 х 10∧6 клеток/доза, от примерно 80 х 10∧6 клеток/доза до примерно 160 х 10∧6 клеток/доза, от примерно 80 х 10∧6 клеток/доза до примерно 200 х 10∧6 клеток/доза, от примерно 160 х 10∧6 клеток/доза до примерно 200 х 10∧6 клеток/доза, от примерно 200 х 10∧6 клеток/доза до примерно 320 х 10∧6 клеток/доза, от примерно 160 х 10∧6 клеток/доза до примерно 320 х 10∧6 клеток/доза или от примерно 200 х 10∧6 клеток/доза до примерно 320 х 10∧6 клеток/доза. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой BCMA-CAR+TCRαβ-_CD52+/- Т-клетки. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой CAR-T-клетки ВСМА-1.
[00137] В некоторых вариантах повторного лечения (повторного введения доз) субъекту с массой тела <50 кг вводят повторную дозу аллогенных ВСМА CAR-T-клеток согласно настоящему изобретению, при этом указанная доза находится в диапазоне от примерно 7 х 10∧6 клеток/доза до примерно 360 х 10∧6 клеток/доза. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой BCMA-CAR+TCRαβ-_CD52+/- Т-клетки. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой CAR-T-клетки ВСМА-1.
[00138] В некоторых вариантах повторного лечения (повторного введения доз) субъекту с массой тела <50 кг вводят повторную дозу аллогенных ВСМА CAR-T-клеток согласно настоящему изобретению, при этом указанная доза находится в диапазоне от примерно 7 х 10∧6 клеток/доза или 14 х 10∧6 клеток/доза до примерно 20 х 10∧6 клеток/доза, от примерно 20 х 10∧6 клеток/доза до примерно 80 х 10∧6 клеток/доза, от примерно 80 х 10∧6 клеток/доза до примерно 240 х 10∧6 клеток/доза или от примерно 240 х 10∧6 клеток/доза до примерно 360 х 10∧6 клеток/доза. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой BCMA-CAR+_TCRαβ-_CD52+/- Т-клетки. В некоторых вариантах реализации ВСМА CAR-T-клетки представляют собой CAR-T-клетки ВСМА-1.
VII. Наборы и готовые изделия
[00139] Согласно настоящему изобретению также предложены наборы и готовые изделия для применения в описанных способах. Наборы согласно настоящему изобретению содержат одну или более емкостей (например, стеклянных флаконов), содержащих полинуклеотид, кодирующий ВСМА-специфичный CAR, или искусственно сконструированные иммунные клетки, содержащие полинуклеотид, кодирующий ВСМА-специфичный CAR, описанные в настоящем документе (например, ВСМА-1 CAR-T-клетки, например, BCMA-CAR+_TCRαβ-_CD52+/- Т-клетки) и инструкции по применению в соответствии с любым из способов согласно настоящему изобретению, описанных в настоящем документе. В некоторых вариантах реализации указанные искусственно сконструированные иммунные клетки представлены в растворе, содержащем примерно 5% ДМСО. Кроме того, искусственно сконструированные иммунные клетки могут быть представлены в замороженном состоянии.
[00140] В некоторых вариантах реализации настоящего изобретения предложены дополнительные флаконы, содержащие единичные дозы антитела к CD52 (которое может быть представлено в замороженном состоянии или в форме раствора комнатной температуры, содержащего буферную среду), флударабин и/или циклофосфамид.
[00141] Эти инструкции, предложенные согласно настоящему изобретению, в целом, содержат описание введения искусственно сконструированных иммунных клеток для описанного выше терапевтического лечения. Инструкции по применению искусственно сконструированных иммунных клеток, описанных в настоящем документе, в целом, включают информацию о дозировке, схеме дозирования и пути введения для предполагаемого лечения. Емкости могут представлять собой упаковки со единичными дозами, упаковки с несколькими дозами (например, многодозовые упаковки) или упаковки с субъединичными дозами. Инструкции, поставляемые в наборах согласно настоящему изобретению, как правило, представляют собой письменные инструкции на этикетке или вкладыше в упаковке (например, на листе бумаги, включенном в набор), а также допустимы машиночитаемые инструкции (например, инструкции на магнитном или оптическом диске для хранения данных).
[00142] Наборы согласно настоящему изобретению находятся в подходящей упаковке. Подходящая упаковка включает, но не ограничивается ими, флаконы, бутыли, сосуды, гибкую упаковку (например, герметичные майларовые или пластиковые пакеты) и т.п. Также предусмотрены упаковки для использования в сочетании с конкретным устройством, таким как устройство для инфузии, такое как мининасос. Набор может иметь стерильный порт доступа (например, емкость может представлять собой пакет с раствором для внутривенного введения или флакон с пробкой, которую можно проткнуть иглой для подкожной инъекции). Емкость может также иметь стерильный порт доступа (например, емкость может представлять собой пакет с раствором для внутривенного введения или флакон с пробкой, которую можно проткнуть иглой для подкожной инъекции). По меньшей мере один активный агент в композиции представляет собой антитело к ВСМА. Емкость может дополнительно содержать второй фармацевтически активный агент.
[00143] Наборы могут необязательно включать дополнительные компоненты, такие как буферы и поясняющая информация. Обычно набор содержит емкость и этикетку или вкладыш (вкладыши) в упаковке на указанной емкости, или связанные с ней.
[00144] Следующие ниже примеры представлены только в целях иллюстрации и никоим образом не ограничивают объем настоящего изобретения. Действительно, на основании вышеприведенного описания специалисту в этой области техники будут понятны различные модификации настоящего изобретения в дополнение к тем, которые показаны и описаны в настоящем документе, и они входят в объем прилагаемой формулы изобретения.
ПРИМЕРЫ
Пример 1: получение и тестирование ВСМА-1
[00145] На Фиг. 1-16 показано получение и тестирование ВСМА-1. ВСМА-1 представляет собой аллогенную Т-клетку, содержащую интегрированный самоинактивирующийся рекомбинантный лентивирусный вектор третьего поколения, который экспрессирует CAR к ВСМА. Указанный CAR к ВСМА содержит scFv, при этом указанный scFV CAR представляет собой Р5А2 из Таблицы 1. scFV содержит VH и VL, при этом указанная VH содержит аминокислотную последовательность, представленную в SEQ ID NO: 33, и указанная VL содержит аминокислотную последовательность, представленную в SEQ ID NO: 34. Внеклеточная область CAR также содержит 2 мимотопа, которые придают свойство распознавания ритуксимабом.
[00146] Генотип ВСМА CAR-T-клеток представляет собой BCMA-CAR+_TCRαβ-_CD52+/-. Клетки могут быть представлены в растворе, содержащем 5% ДМСО. В одном из вариантов реализации клетки представлены в форме суспензии для инфузии в смеси CryoStor® Basal Solution и CryoStor® CS10 в соотношении 1:1, что позволяет получить 5% конечную концентрацию диметилсульфоксида, и полученная дозировка состава составляет 14 х 10∧6 BCMA-CAR+_TCRαβ-_CD52+/- Т-клеток/мл.
[00147] На Фиг. 2 показано, что опосредованное ритуксимабом «защитное выключение» обеспечивает обнаружение и деплецию (антителом ритуксимабом) ВСМА-содержащих CAR-T-клеток согласно настоящему изобретению. Клетки ВСМА-1 инкубировали совместно с комплементом кролика и ритуксимабом. Через 3 часа клетки окрашивали на предмет экспрессии CAR. График показывает процент живых CAR+ клеток (среднее значение +/- SEM). (Фиг. 2)
[00148] Цитотоксичность ВСМА-1 тестировали в отношении линий клеток, экспрессирующих ВСМА, оценивали in vitro путем совместной культивации эффекторных клеток ВСМА-1 с клетками-мишенями, стабильно экспрессирующими люциферазу, при увеличивающихся соотношениях Э:М, и измерения остаточной активности люциферазы через 24 часа. ВСМА-отрицательные клетки REH служили в качестве контрольной линии клеток. По сравнению с нетрансдуцированными контрольными Т-клетками (треугольники), ВСМА-1 (кружки) проявляли дозозависимую цитотоксичность в отношении ВСМА-экспрессирующих клеток, но не демонстрировали очевидного уничтожения контрольных клеток (REH). Направленная на уничтожение активность ВСМА-1 и ВСМА-1 без редактирования гена (незаштрихованные кружки) была сопоставимой. Графики показывают процент лизиса клеток относительно клеток-мишеней, культивируемых отдельно (Фиг. 6). Приведенные результаты представляют собой среднее значение +/- SEM для 3 доноров. Отрицательные значения цитотоксичности (в результате роста клеток-мишеней или усиленного сигнала люциферазы во время анализа) наносили на график как 0% лизиса.
[00149] На Фиг. 16 показано, что scFv ВСМА-1 не демонстрирует нецелевого связывания в исследованиях тканевой перекрестной реактивности, что указывает на низкий риск нецелевого связывания в клинических условиях или его отсутствие. Тестирование проводили на 13 тканях человека. Внеклеточный домен CAR подвергали слиянию с IgG2dA D265A человека (мутация для предотвращения связывания Fc). Указанный способ был разработан для оптимального окрашивания линий клеток, сверхэкспрессирующих ВСМА. Не наблюдали окрашивания в тканях человека.
[00150] Результат иммуногистохимического окрашивания в 9 тканях человека - проводили тройное усиление сигнала для увеличения сигнала. Обнаруживали ожидаемый сигнал в тканях миндалин, лимфатических узлов, селезенки. В тканях молочной железы, поджелудочной железы, фаллопиевой трубы, предстательной железы, мочевого пузыря не наблюдали эпителиального связывания. Соответственно, риск неожиданного связывания считается низким или отсутствующим.
Пример 2: исследование фазы 1, дизайн А
[00151] На Фиг. 19 представлена схема исследования фазы 1 (дизайн А) для лечения рефрактерной/рецидивирующей ММ. Схема дизайна А включает фазу лимфодеплеции: флударабином (flu), 30 мг/м2/день внутривенно; циклофосфамидом (су), 300 мг/м2/день внутривенно; и антителом к CD52, 13 мг/день внутривенно за 3-5 дней до лечения; и фазу лечения (в 0 день), которая включает повышающиеся дозы от 20-80х10∧6 клеток внутривенно (для субъектов ≥50 кг) или 7-360 х 10∧6 клеток внутривенно (для субъектов <50 кг).
[00152] Критерии включения могут включать одно или более из следующего:
• Измеримая ММ после ≥3 предшествующих режимов ММ
 Индукция +/- ASCT +/- поддержание представляет собой 1 режим
Индукция +/- ASCT +/- поддержание представляет собой 1 режим
 Получено предварительное PL IMiD и ингибирование CD38 (при отсутствии противопоказаний) по меньшей мере с 2 непрерывными циклами каждого режима, пока прогрессирование заболевания (PD) не стало лучшим ответом
Получено предварительное PL IMiD и ингибирование CD38 (при отсутствии противопоказаний) по меньшей мере с 2 непрерывными циклами каждого режима, пока прогрессирование заболевания (PD) не стало лучшим ответом
 Не поддается лечению в соответствии с самым последним предыдущим режимом
Не поддается лечению в соответствии с самым последним предыдущим режимом
• Показатель общего состояния по шкале ECOG: 0-1
• Адекватная функция органов
• 5 периодов полувыведения, вымывание до LD
 4 недели для МАТ
4 недели для МАТ
• Экспрессию ВСМА можно использовать для отбора пациентов.
[00153] Уровни с привязкой доз к диапазонам для повышения ВСМА-1 в дизайне А фазы 1 приведены в Таблице 8.
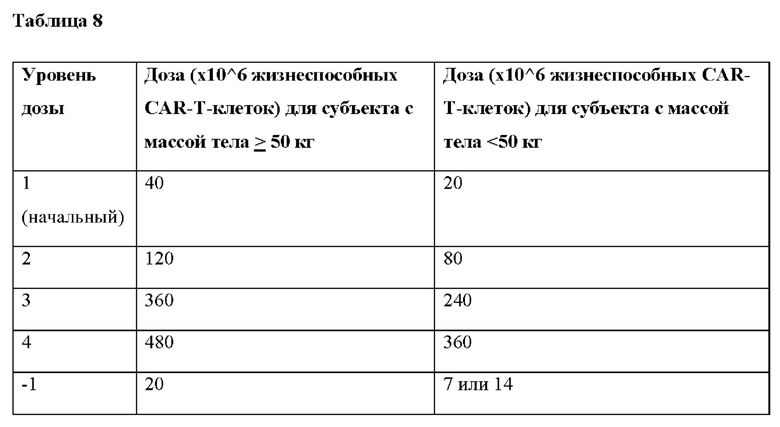
[00154] Повышение дозы обычно определяют схемой 3+3; для каждого уровня дозы могут быть получены клетки по меньшей мере от двух разных доноров; можно тестировать до пяти уровней доз. Начальная доза обозначена как уровень дозы 1 в Таблице 8, в некоторых вариантах реализации субъект может получать уровень дозы -1, при наличии показаний.
[00155] У пациента с рецидивом можно осуществлять повторное дозирование с использованием ВСМА CAR-T-клеток от другого донора с использованием кондиционирования, например, кондиционирование 20 мг антитела к CD52.
Пример 3: исследование фазы 1, дизайн В
[00156] На Фиг. 19 представлена схема исследования фазы 1, дизайн В, для лечения рефрактерной/рецидивирующей ММ. Схема дизайна В включает фазу лимфодеплеции: флударабином (flu), 30 мг/м2/день внутривенно; циклофосфамидом (су), 300 мг/м2/день внутривенно; и антителом к CD52, 13 мг/день внутривенно за 3-5 дней до лечения; и фазу лечения (в 0 день), которая включает повышающиеся дозы от 20-80х10∧6 клеток внутривенно (для субъектов ≥50 кг) или 7-360 х 10∧6 клеток внутривенно (для субъектов <50 кг).
[00157] Критерии включения могут включать одно или более из следующего:
[00158] 1. Подтвержденный диагноз рецидивирующая/рефрактерная множественная миелома (Р/Р ММ) в соответствии с едиными критериями IMWG оценки ответа и минимального остаточного заболевания при множественной миеломе.
[00159] 2. Субъекты демонстрируют измеряемые проявления заболевания, включая один или более следующих критериев:
a. Сывороточный М-белок ≥0,5 г/дл
b. М-белок в моче ≥200 мг/24 часа,
с. Уровень вовлеченных свободных легких цепей (СЛЦ) в сыворотке ≥10 мг/дл (100 мг/л) при условии, что соотношение СЛЦ в сыворотке не соответствует норме.
[00160] 3. Пациенты получили лечение ММ в соответствии с по меньшей мере ≥3 предшествующими режимами:
a. Индукция с трансплантацией гемопоэтических стволовых клеток или без нее и с поддерживающей терапией или без нее считается единым режимом.
b. Ранее получали ингибитор протеасом, иммуномодулирующее средство и антитело к CD38 (при отсутствии противопоказаний) по меньшей мере 2 последовательными циклами для каждого режима, пока прогрессирование заболевания не стало лучшим ответом на режим.
c. Не поддается лечению в соответствии с последним режимом лечения.
[00161] 4. Показатель общего состояния 0 или 1 по шкале Восточной объединенной онкологической группы (ECOG).
[00162] Цикл лечения рассматривается как комбинация 1 лимфодеплеции и 1 периода лечения.
[00163] Одной из целей этого исследования является оценка максимальной переносимой дозы (MTD) ВСМА-1 и/или установление рекомендуемой дозы фазы 2 (RP2D).
[00164] В некоторых вариантах реализации указанное исследование включает 2 части: повышение дозы и расширение когорты установленной дозы.
[00165] В части с повышением дозы последовательные когорты пациентов могут получать повышающиеся дозы ВСМА-1 по схеме 3+3. При каждом уровне дозы первого пациента можно лечить и наблюдать в течение 28 дней до лечения ВСМА-1 последующих пациентов. Как правило, за всеми пациентами внимательно наблюдают на предмет дозолимитирующей токсичности (DLT) в течение первых 28 дней после инфузии ВСМА-1. Целевая частота DLT для ВСМА-1 составляет <33%. Можно исследовать средний уровень дозы между DL1 и DL3 (Таблица 9). Может быть реализована стратегия дозирования с использованием 2 различных диапазонов массы тела на основе вариаций массы тела, наблюдаемых в общей популяции. Пациенты с массой тела ≤50 кг могут получать дозу на 33-50% ниже, чем доза, вводимая пациентам с массой тела >50 кг. Предварительные уровни доз при повышения ВСМА-1 в фазе 1, дизайн В, приведены в Таблице 9. При необходимости можно вводить средний уровень дозы, уровень дозы 4 и уровень дозы -1.
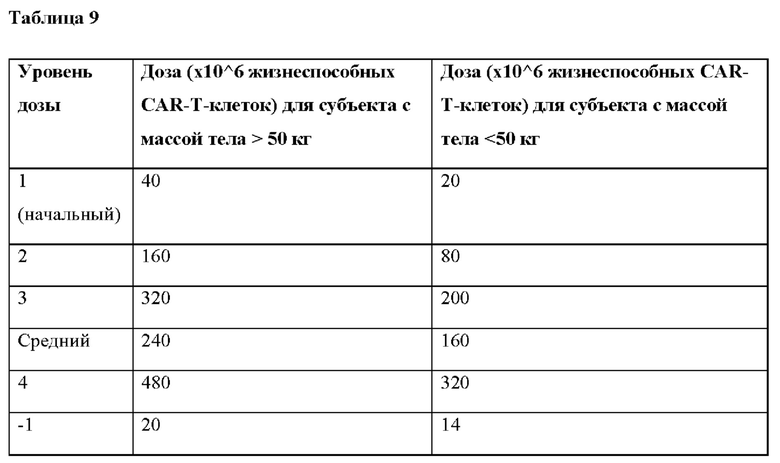
[00166] Повышение дозы обычно определяют схемой 3+3; для каждого уровня дозы могут быть получены клетки по меньшей мере от двух разных доноров; можно тестировать до пяти уровней доз. Начальная доза обозначена как уровень дозы 1 в Таблице 9, в некоторых вариантах реализации субъект может получать уровень дозы -1, уровень дозы 4 или средний уровень дозы (как показано в таблице 9), при наличии показаний.
[00167] Соответственно, в дизайне В ВСМА-1 можно вводить в 0 день путем внутривенной (в/в) инфузии в течение приблизительно 5 минут. Для пациентов с массой тела >50 кг можно исследовать повышающиеся дозы 40 х 10∧6, 160 х 10∧6 и 320 х 10∧6 аллогенных CAR-T-клеток. Соответствующие дозы для пациентов с массой тела ≤50 кг составляют 20 х 10∧6, 80 х 10∧6 и 200 х 10∧6.
[00168] Моноклональное антитело IgG1 человека к CD52, которое распознает антиген CD52 человека, можно применять как часть режима лимфодеплеции.
[00169] Указанное антитело к CD52 можно вводить в -5 день, -4 день и -3 день путем внутривенной инфузии в течение 4 часов в дозе 13 мг/день одновременно с флударабином (30 мг/мг/день) и/или циклофосфамидом (300 мг/мг/день) или как только одно антитело. В случае токсичности предполагается более низкая доза 10 мг/день. Флударабин (30 мг/м2/день) можно вводить в течение 3 дней.
[00170] Общая продолжительность этого исследования фазы 1 составляет примерно 48 месяцев от первого включенного пациента до последнего пациента, завершившего исследование.
[00171] Часть с расширением когорты установленной дозы может включать дополнительные когорты, добавленные к протоколу, для получения характеристик R2PD с соответствующими режимами кондиционирования ВСМА-1. До 3 когорт по 12 пациентов в каждой когорте можно оценить для уровней доз и режимов кондиционирования, выбранных на основе результатов повышения дозы.
[00172] Исследование можно завершать, когда всех пациентов, получавших лечение ВСМА-1, наблюдали в течение по меньшей мере 24 месяцев после первоначальной инфузии ВСМА-1, когда они отозвали согласие на дальнейший контакт, когда с ними был утрачен контакт для последующего наблюдения или когда они умирали, если исследование не было прекращено спонсором ранее.
[00173] У пациента с рецидивом можно осуществлять повторное дозирование с использованием ВСМА CAR-T-клеток от другого донора с использованием кондиционирования, например, кондиционирование 20 мг антитела к CD52.
Пример 4: исследование фазы 2
[00174] Фаза 2 может включать тестирование дополнительной когорты из 6-12 субъектов с применением самой высокой дозы с приемлемой токсичностью из Фазы 1, дизайн А или дизайн В (либо RP2D - уровень дозы, обуславливающий около 20% дозолимитирующей токсичности из фазы 1; либо уровень дозы выше дозы RP2D). Субъекты могут получать антитело к CD52 без flu/cy; указанное антитело CD52 можно вводить в дозе -40 мг (13 мг/день х 3 дня) перед лечением CAR-T-клетками и повторять в дозе 13 мг/день в 7, 14 и 21 дни после лечения CAR-T-клетками.
[00175] Хотя раскрытые в настоящем документе идеи описаны со ссылкой на различные применения, способы и композиции, понятно, что могут быть осуществлены различные изменения и модификации в пределах объема идей, описанных в настоящем документе, и приведенной ниже формулы изобретения. Примеры выше приведены для лучшей иллюстрации раскрытых в настоящем документе идей и не ограничивают объем идей, представленных в настоящем документе. Хотя идеи настоящего изобретения описаны в контексте данных иллюстративных вариантов реализации настоящего изобретения, специалисту в этой области техники понятно, что возможны многочисленные вариации и модификации этих иллюстративных вариантов реализации данного изобретения без проведения излишних экспериментов. Все такие вариации и модификации входят в объем идей настоящего изобретения.
[00176] Полное содержание всех источников, указанных в настоящем описании, включая патенты, заявки на патент, документы, учебники и т.п., и указанных в них источников, в той степени, в какой еще не включено, включено в настоящее описание посредством ссылки. В случае, если один или более включенных литературных источников и аналогичных материалов отличаются от настоящей заявки или противоречат ей, включая, но не ограничиваясь ими, определенные термины, употребление терминов, описанные методики и т.п., настоящая заявка имеет преимущественную силу.
[00177] Вышеприведенное описание и примеры подробно описывают некоторые конкретные варианты реализации настоящего изобретения и описывают лучший вариант реализации изобретения, предусмотренный авторами настоящего изобретения. Однако следует понимать, что независимо от того, насколько подробно изложенное выше может быть представлено в тексте, настоящее изобретение может быть реализовано на практике многими способами и его следует толковать в соответствии с прилагаемой формулой изобретения и любыми ее эквивалентами.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> АЛЛОДЖЕН ТЕРАПЬЮТИКС, ИНК.
<120> ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, НАЦЕЛЕННЫЕ НА АНТИГЕН СОЗРЕВАНИЯ В-КЛЕТОК, И
СПОСОБЫ ИХ ПРИМЕНЕНИЯ
<130> AT-022/04WO
<140>
<141>
<150> 62/931,487
<151> 2019-11-06
<150> 62/816,187
<151> 2019-03-10
<150> 62/774,209
<151> 2018-12-01
<160> 417
<170> PatentIn, версия 3.5
<210> 1
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 1
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Ser Pro Pro
85 90 95
Ser Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 2
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 2
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Gly Ser Tyr
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Asn Thr Phe Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Ser Pro Ile Ala Ser Gly Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 3
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 3
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Gly Ser Tyr
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Asn Thr Phe Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Ser Pro Ile Ala Ala Gln Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 4
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 4
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Leu Gly Ser Phe
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Lys His Tyr Gly Trp Pro Pro
85 90 95
Ser Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 5
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 5
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Leu Gly Ser Phe
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Asn Tyr Pro Pro
85 90 95
Ser Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 6
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 6
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Gly Asp Phe
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Asn Tyr Pro Pro
85 90 95
Ser Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 7
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 7
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Gly Ser Tyr
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Asn Thr Phe Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Arg Val Ser Pro Ile Ala Ala Leu Met Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 8
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 8
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Gly Ser Tyr
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Asn Thr Phe Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Ser Pro Ile Ala Ala Pro Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 9
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 9
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Leu Gly Ser Phe
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Pro Tyr Pro Pro
85 90 95
Ser Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 10
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 10
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Leu Gly Ser Phe
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Asn Tyr Pro Pro
85 90 95
Ser Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 11
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 11
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Gly Asp Phe
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Lys His Tyr Gly Trp Pro Pro
85 90 95
Ser Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 12
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 12
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Gly Asp Phe
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Pro Tyr Pro Pro
85 90 95
Ser Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 13
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 13
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Gly Asp Phe
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Asn Tyr Pro Pro
85 90 95
Ser Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 14
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 14
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Gly Asp Phe
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Asn Tyr Pro Pro
85 90 95
Ser Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 15
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 15
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Lys His Tyr Gly Trp Pro Pro
85 90 95
Ser Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 16
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 16
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Pro Tyr Pro Pro
85 90 95
Ser Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 17
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 17
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Asn Tyr Pro Pro
85 90 95
Ser Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 18
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 18
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Pro Ser Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Pro Tyr Pro Pro
85 90 95
Ser Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 19
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 19
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ala His
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Pro Tyr Pro Pro
85 90 95
Ser Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 20
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 20
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Phe
20 25 30
Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Pro Tyr Pro Pro
85 90 95
Ser Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 21
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 21
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Pro His
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Pro Tyr Pro Pro
85 90 95
Ser Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 22
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 22
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Lys Tyr Tyr Pro Tyr Pro Pro
85 90 95
Ser Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 23
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 23
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Lys Phe Tyr Pro Tyr Pro Pro
85 90 95
Ser Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 24
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 24
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Gly Ser Tyr
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Asn Thr Phe Tyr Ala Asp Gln Arg
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Ser Pro Ile Ala Ser Gly Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 25
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 25
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Gly Ser Tyr
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Asp Tyr Ser Gly Gly Asn Thr Phe Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Ser Pro Ile Ala Ser Gly Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 26
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 26
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Gly Ser Tyr
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Tyr Gln Gly Gly Asn Thr Phe Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Ser Pro Ile Ala Ser Gly Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 27
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 27
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Gly Ser Tyr
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Leu Thr Gly Gly Asn Thr Phe Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Ser Pro Ile Ala Ser Gly Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 28
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 28
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Gly Ser Tyr
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser His Ala Gly Gly Asn Thr Phe Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Ser Pro Ile Ala Ser Gly Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 29
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 29
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Gly Ser Tyr
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Asn Thr Phe Tyr Ala Asp Gln Leu
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Ser Pro Ile Ala Ser Gly Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 30
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 30
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Gly Ser Tyr
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Asn Thr Phe Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Ser Pro Ile Tyr Ala Gly Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 31
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 31
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Gly Ser Tyr
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Asn Thr Phe Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Ser Pro Ile Ala Ala Glu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 32
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 32
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Gly Ser Tyr
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Asn Thr Phe Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Val Ser Pro Ile Ala Ala Gln Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 33
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 33
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Asp Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Asp Ile Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 34
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 34
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 35
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 35
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Asp Ser Gly Gly Ser Ala Trp Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Ser Leu Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 36
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 36
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Val Leu
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gln Arg Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 37
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 37
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Asp Ser Gly Gly Ser Met Trp Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Ser Leu Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 38
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 38
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gln Ser Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 39
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 39
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Asp Phe Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Asp Ile Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 40
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 40
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Asp Leu
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gln Thr Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 41
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 41
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Asn Leu
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gln Gly Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 42
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 42
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Thr Ala Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Ser Leu Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 43
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 43
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ala Tyr
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Glu Arg Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 44
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 44
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Asp Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Ser Leu Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 45
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 45
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Leu
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gln Val Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 46
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 46
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Asp Ser Gly Gly Ser Arg Trp Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Thr Pro Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 47
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 47
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Leu Asp Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 48
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 48
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Val Leu Asp Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Thr Pro Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 49
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 49
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gln Val Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 50
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 50
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Asp Ser Gly Gly Ser Arg Trp Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Ser Asp Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 51
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 51
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Val Leu
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Leu Ala Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 52
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 52
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Asp Ser Gly Gly Ser Lys Trp Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Ser Leu Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 53
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 53
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Phe Thr Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 54
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 54
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Gly Gly Ser Gly Gly Ser Leu Pro Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Asp Ser Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 55
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 55
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Pro Tyr
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Glu Arg Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 56
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 56
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Asp Ser Gly Gly Ser Gly Trp Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Ser Leu Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 57
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 57
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Val Glu
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Ala Arg Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 58
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 58
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Val Leu Asp Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Ser Leu Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 59
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 59
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Glu Leu
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Phe Gly Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 60
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 60
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Asp Ser Gly Gly Ser Cys Trp Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Thr Pro Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 61
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 61
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Glu Met Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Ala His Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 62
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 62
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Phe Ala Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Thr Pro Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 63
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 63
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gln Arg Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 64
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 64
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Trp Gly Gly Ser Leu Pro Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Asp Ser Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 65
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 65
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ala Gln
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gln Arg Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 66
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 66
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Met Ser Ser Gly Gly Pro Leu Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Ala Leu Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 67
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 67
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ala Leu
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gln Val Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 68
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 68
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Leu Met Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Ser Leu Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 69
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 69
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Gly Pro Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gln Ser Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 70
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 70
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Asp Ser Gly Gly Tyr Arg Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Ser Leu Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 71
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 71
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Trp Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Glu Ser Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 72
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 72
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Leu Ser Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Asp Ile Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 73
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 73
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Gly Gly Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gln Ser Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 74
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 74
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Leu Asp Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Ser Pro Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 75
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 75
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Phe Leu
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 76
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 76
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Gly Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Asp Ser Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 77
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 77
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Thr
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Asp Ala Ser Ser Arg Ala Pro Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Ser Thr Ser Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 78
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 78
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Gly Gly Ser Gly Gly Ser Leu Pro Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Asp Ser Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 79
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 79
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Pro Glu
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Asp Ala Ser Ser Arg Ala Pro Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Ser Val Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 80
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 80
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Leu Gly Ser Phe Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Asn Tyr Pro Pro Ser
85 90 95
Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 81
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 81
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Thr
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Asp Ala Ser Ser Arg Ala Pro Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Ser Arg Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 82
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 82
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Pro Leu
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Asp Ala Ser Ser Arg Ala Pro Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Ser Ala Phe Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 83
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 83
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Gly Gly Ser Gly Gly Trp Ser Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Asp Ser Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 84
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 84
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Trp Leu Ser Gln Ser Val Ser Ser Thr
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Asp Ala Ser Ser Arg Ala Pro Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Ser Glu Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 85
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 85
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Thr
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Asp Ala Ser Ser Arg Ala Pro Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Ser Ser Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 86
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 86
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Leu
20 25 30
Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Asp Ala Ser Ser Arg Ala Pro Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Ser Ala Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 87
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 87
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Thr Val Gly Ser Gly Gly Ser Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Asp Ser Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 88
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 88
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ala Cys Ser Gln Ser Val Ser Ser Thr
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Asp Ala Ser Ser Arg Ala Pro Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Ser Ala Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 89
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 89
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Cys Asp Val Ser Ser Thr
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Asp Ala Ser Ser Arg Ala Pro Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Met Arg Ser Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 90
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 90
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Glu Ala Val Pro Ser Thr
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Asp Ala Ser Ser Arg Ala Pro Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Ser Ala Phe Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 91
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 91
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Cys Ser Ser Gln Ser Val Ser Ser Thr
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Asp Ala Ser Ser Arg Ala Pro Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Ser Ala Phe Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 92
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 92
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Asp Ser Gly Gly Ser Arg Trp Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Tyr Trp Pro Met Asp Ile Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 93
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 93
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Val Arg Val Ser Ser Thr
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Met Lys Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 94
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 94
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ala Ala
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Met Cys Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 95
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 95
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Gly Gly Ser Gly Gly Ser Ile His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Asp Ser Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 96
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 96
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Trp Gly Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gln Cys Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 97
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 97
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala His Ile Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Asp Ser Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 98
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 98
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Thr
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gln Ser Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 99
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 99
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Gly Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Asp Pro Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 100
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 100
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Pro
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gln Ser Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 101
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 101
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Gly Gly Ser Gly Gly Ser Leu Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Asp Ser Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 102
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 102
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Pro Leu
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Lys Ala Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 103
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 103
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Tyr Leu
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Met Glu Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 104
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 104
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Phe Ala Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Asp Ser Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 105
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 105
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ala Gln
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gln Ala Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 106
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 106
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Gly Gly Ser Gly Thr Trp Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Asp Ser Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 107
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 107
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gln Lys Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 108
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 108
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ala Val
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Arg Ala Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 109
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 109
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Ile Ala Val Ser Ser Thr
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Met Val Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 110
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 110
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Leu Phe Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Asp Ser Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 111
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 111
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Pro Arg Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gln Asp Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 112
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 112
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Gly Gly Ser Gly Gly Ser Leu Pro Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Asp Ile Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 113
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 113
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Thr
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gln Glu Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 114
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 114
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ala Leu Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Asp Ser Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 115
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 115
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ala Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Met Ser Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 116
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 116
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Tyr Met
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Lys Ser Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 117
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 117
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ala Leu
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Tyr Gly Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 118
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 118
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Gly Gly Ser Gly Gly Ser Leu Pro Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Ala Asp Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 119
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 119
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Pro Ile Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gln Gly Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 120
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 120
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Asp Ser Gly Gly Phe Val Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Asp Ser Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 121
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 121
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Glu Phe Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 122
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 122
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Gly Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Ser Leu Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 123
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 123
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Thr
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Met Ser Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 124
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 124
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Gly Ile Ser Ser Thr
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Ala Tyr Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 125
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 125
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Cys Leu Asp Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Asp Ser Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 126
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 126
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gln Gly Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 127
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 127
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ala Leu Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Ser Leu Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 128
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 128
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Val Arg
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Asp Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Trp Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 129
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 129
Ser Tyr Ala Met Thr
1 5
<210> 130
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 130
Gly Phe Thr Phe Gly Ser Tyr
1 5
<210> 131
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 131
Gly Phe Thr Phe Gly Ser Tyr Ala Met Thr
1 5 10
<210> 132
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 132
Ala Ile Ser Gly Ser Gly Gly Asn Thr Phe Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 133
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 133
Ser Gly Ser Gly Gly Asn
1 5
<210> 134
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 134
Val Ser Pro Ile Ala Ser Gly Met Asp Tyr
1 5 10
<210> 135
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 135
Val Ser Pro Ile Ala Ala Gln Met Asp Tyr
1 5 10
<210> 136
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 136
Val Ser Pro Ile Ala Ala Leu Met Asp Tyr
1 5 10
<210> 137
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 137
Val Ser Pro Ile Ala Ala Pro Met Asp Tyr
1 5 10
<210> 138
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 138
Ala Ile Ser Gly Ser Gly Gly Asn Thr Phe Tyr Ala Asp Gln Arg Lys
1 5 10 15
Gly
<210> 139
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 139
Ala Ile Asp Tyr Ser Gly Gly Asn Thr Phe Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 140
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 140
Asp Tyr Ser Ser Gly Asn
1 5
<210> 141
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 141
Ala Ile Ser Tyr Gln Gly Gly Asn Thr Phe Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 142
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 142
Ser Tyr Gln Gly Gly Asn
1 5
<210> 143
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 143
Ala Ile Ser Leu Thr Gly Gly Asn Thr Phe Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 144
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 144
Ser Leu Thr Gly Gly Asn
1 5
<210> 145
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 145
Ala Ile Ser His Ala Gly Gly Asn Thr Phe Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 146
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 146
Ser His Ala Gly Gly Asn
1 5
<210> 147
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 147
Ala Ile Ser Gly Ser Gly Gly Asn Thr Phe Tyr Ala Asp Gln Leu Lys
1 5 10 15
Gly
<210> 148
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 148
Val Ser Pro Ile Tyr Ala Gly Met Asp Tyr
1 5 10
<210> 149
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 149
Val Ser Pro Ile Ala Ala Glu Met Asp Tyr
1 5 10
<210> 150
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 150
Ser Tyr Ala Met Asn
1 5
<210> 151
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 151
Gly Phe Thr Phe Ser Ser Tyr
1 5
<210> 152
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 152
Gly Phe Thr Phe Ser Ser Tyr Ala Met Asn
1 5 10
<210> 153
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 153
Ala Ile Ser Asp Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 154
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 154
Ser Asp Ser Gly Gly Ser
1 5
<210> 155
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 155
Tyr Trp Pro Met Asp Ile
1 5
<210> 156
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 156
Ser Tyr Pro Met Ser
1 5
<210> 157
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 157
Gly Phe Thr Phe Ser Ser Tyr Pro Met Ser
1 5 10
<210> 158
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 158
Ala Ile Gly Gly Ser Gly Gly Ser Leu Pro Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 159
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 159
Gly Gly Ser Gly Gly Ser
1 5
<210> 160
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 160
Ala Ile Leu Asp Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 161
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 161
Tyr Trp Pro Met Asp Ser
1 5
<210> 162
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 162
Ala Ile Gly Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 163
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 163
Ala Ile Ser Asp Ser Gly Gly Ser Ala Trp Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 164
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 164
Tyr Trp Pro Met Ser Leu
1 5
<210> 165
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 165
Ala Ile Ser Asp Phe Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 166
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 166
Ser Asp Phe Gly Gly Ser
1 5
<210> 167
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 167
Ala Ile Thr Ala Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 168
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 168
Thr Ala Ser Gly Gly Ser
1 5
<210> 169
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 169
Ala Ile Ser Asp Ser Gly Gly Ser Arg Trp Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 170
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 170
Tyr Trp Pro Met Thr Pro
1 5
<210> 171
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 171
Ala Val Leu Asp Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 172
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 172
Leu Asp Ser Gly Gly Ser
1 5
<210> 173
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 173
Tyr Trp Pro Met Ser Asp
1 5
<210> 174
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 174
Ala Ile Ser Asp Ser Gly Gly Ser Lys Trp Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 175
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 175
Ala Ile Ser Asp Ser Gly Gly Ser Gly Trp Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 176
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 176
Ala Ile Ser Asp Ser Gly Gly Ser Cys Trp Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 177
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 177
Ala Ile Phe Ala Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 178
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 178
Phe Ala Ser Gly Gly Ser
1 5
<210> 179
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 179
Ser Gly Trp Gly Gly Ser
1 5
<210> 180
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 180
Ala Ile Met Ser Ser Gly Gly Pro Leu Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 181
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 181
Met Ser Ser Gly Gly Pro
1 5
<210> 182
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 182
Tyr Trp Pro Met Ala Leu
1 5
<210> 183
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 183
Ala Ile Leu Met Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 184
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 184
Leu Met Ser Gly Gly Ser
1 5
<210> 185
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 185
Ala Ile Ser Asp Ser Gly Gly Tyr Arg Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 186
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 186
Ser Asp Ser Gly Gly Tyr
1 5
<210> 187
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 187
Ala Ile Leu Ser Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 188
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 188
Leu Ser Ser Gly Gly Ser
1 5
<210> 189
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 189
Tyr Trp Pro Met Ser Pro
1 5
<210> 190
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 190
Ala Ile Gly Gly Ser Gly Gly Trp Ser Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 191
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 191
Gly Gly Ser Gly Gly Trp
1 5
<210> 192
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 192
Ala Thr Val Gly Ser Gly Gly Ser Ile Gly Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 193
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 193
Val Gly Ser Gly Gly Ser
1 5
<210> 194
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 194
Ala Ile Gly Gly Ser Gly Gly Ser Ile His Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 195
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 195
Ala His Ile Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 196
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 196
Ile Gly Ser Gly Gly Ser
1 5
<210> 197
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 197
Tyr Trp Pro Met Asp Pro
1 5
<210> 198
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 198
Ala Ile Gly Gly Ser Gly Gly Ser Leu Gly Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 199
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 199
Ala Ile Gly Gly Ser Gly Thr Trp Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 200
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 200
Gly Gly Ser Gly Thr Trp
1 5
<210> 201
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 201
Ala Leu Phe Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 202
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 202
Phe Gly Ser Gly Gly Ser
1 5
<210> 203
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 203
Ala Ala Leu Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 204
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 204
Leu Gly Ser Gly Gly Ser
1 5
<210> 205
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 205
Tyr Trp Pro Met Ala Asp
1 5
<210> 206
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 206
Ala Ile Ser Asp Ser Gly Gly Phe Val Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 207
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 207
Ser Asp Ser Gly Gly Phe
1 5
<210> 208
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 208
Ala Cys Leu Asp Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 209
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 209
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 210
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 210
Gly Ala Ser Ser Arg Ala Thr
1 5
<210> 211
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 211
Gln His Tyr Gly Ser Pro Pro Ser Phe Thr
1 5 10
<210> 212
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 212
Arg Ala Ser Gln Ser Leu Gly Ser Phe Tyr Leu Ala
1 5 10
<210> 213
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 213
Lys His Tyr Gly Trp Pro Pro Ser Phe Thr
1 5 10
<210> 214
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 214
Gln His Tyr Asn Tyr Pro Pro Ser Phe Thr
1 5 10
<210> 215
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 215
Arg Ala Ser Gln Ser Val Gly Asp Phe Tyr Leu Ala
1 5 10
<210> 216
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 216
Gln His Tyr Pro Tyr Pro Pro Ser Phe Thr
1 5 10
<210> 217
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 217
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Pro Ser
1 5 10
<210> 218
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 218
Arg Ala Ser Gln Ser Val Ser Ala His Tyr Leu Ala
1 5 10
<210> 219
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 219
Arg Ala Ser Gln Ser Val Ser Ser Phe Phe Leu Ala
1 5 10
<210> 220
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 220
Lys Tyr Tyr Pro Tyr Pro Pro Ser Phe Thr
1 5 10
<210> 221
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 221
Asp Ala Ser Ile Arg Ala Thr
1 5
<210> 222
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 222
Gln Gln Tyr Gly Ser Trp Pro Leu Thr
1 5
<210> 223
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 223
Arg Ala Ser Gln Ser Val Ser Val Leu Tyr Leu Ala
1 5 10
<210> 224
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 224
Gln Gln Tyr Gln Arg Trp Pro Leu Thr
1 5
<210> 225
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 225
Gln Gln Tyr Gln Ser Trp Pro Leu Thr
1 5
<210> 226
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 226
Arg Ala Ser Gln Ser Val Ser Asp Leu Tyr Leu Ala
1 5 10
<210> 227
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 227
Gln Gln Tyr Gln Thr Trp Pro Leu Thr
1 5
<210> 228
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 228
Arg Ala Ser Gln Ser Val Ser Asn Leu Tyr Leu Ala
1 5 10
<210> 229
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 229
Gln Gln Tyr Gln Gly Trp Pro Leu Thr
1 5
<210> 230
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 230
Arg Ala Ser Gln Ser Val Ser Ala Tyr Tyr Leu Ala
1 5 10
<210> 231
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 231
Gln Gln Tyr Glu Arg Trp Pro Leu Thr
1 5
<210> 232
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 232
Arg Ala Ser Gln Ser Val Ser Ser Leu Tyr Leu Ala
1 5 10
<210> 233
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 233
Gln Gln Tyr Gln Val Trp Pro Leu Thr
1 5
<210> 234
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 234
Gln Gln Tyr Leu Asp Trp Pro Leu Thr
1 5
<210> 235
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 235
Arg Ala Ser Gln Ser Val Ser Ala Leu Tyr Leu Ala
1 5 10
<210> 236
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 236
Gln Gln Tyr Leu Ala Trp Pro Leu Thr
1 5
<210> 237
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 237
Gln Gln Tyr Phe Thr Trp Pro Leu Thr
1 5
<210> 238
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 238
Arg Ala Ser Gln Ser Val Ser Pro Tyr Tyr Leu Ala
1 5 10
<210> 239
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 239
Arg Ala Ser Gln Ser Val Ser Val Glu Tyr Leu Ala
1 5 10
<210> 240
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 240
Gln Gln Tyr Ala Arg Trp Pro Leu Thr
1 5
<210> 241
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 241
Arg Ala Ser Gln Ser Val Ser Glu Leu Tyr Leu Ala
1 5 10
<210> 242
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 242
Gln Gln Tyr Phe Gly Trp Pro Leu Thr
1 5
<210> 243
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 243
Arg Ala Ser Gln Ser Val Glu Met Ser Tyr Leu Ala
1 5 10
<210> 244
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 244
Gln Gln Tyr Ala His Trp Pro Leu Thr
1 5
<210> 245
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 245
Arg Ala Ser Gln Ser Val Ser Ala Gln Tyr Leu Ala
1 5 10
<210> 246
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 246
Gly Pro Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 247
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 247
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Trp Ala
1 5 10
<210> 248
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 248
Gln Gln Tyr Glu Ser Trp Pro Leu Thr
1 5
<210> 249
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 249
Arg Gly Gly Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 250
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 250
Arg Ala Ser Gln Ser Val Ser Phe Leu Tyr Leu Ala
1 5 10
<210> 251
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 251
Arg Ala Ser Gln Ser Val Ser Ser Thr Tyr Leu Ala
1 5 10
<210> 252
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 252
Asp Ala Ser Ser Arg Ala Pro
1 5
<210> 253
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 253
Gln Gln Tyr Ser Thr Ser Pro Leu Thr
1 5
<210> 254
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 254
Arg Ala Ser Gln Ser Val Ser Pro Glu Tyr Leu Ala
1 5 10
<210> 255
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 255
Gln Gln Tyr Ser Val Trp Pro Leu Thr
1 5
<210> 256
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 256
Gln Gln Tyr Ser Ala Trp Pro Leu Thr
1 5
<210> 257
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 257
Arg Ala Ser Gln Ser Val Ser Ser Val Tyr Leu Ala
1 5 10
<210> 258
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 258
Gln Gln Tyr Ser Thr Trp Pro Leu Thr
1 5
<210> 259
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 259
Gln Gln Tyr Ser Arg Trp Pro Leu Thr
1 5
<210> 260
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 260
Arg Ala Ser Gln Ser Val Ser Pro Leu Tyr Leu Ala
1 5 10
<210> 261
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 261
Gln Gln Tyr Ser Ala Phe Pro Leu Thr
1 5
<210> 262
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 262
Trp Leu Ser Gln Ser Val Ser Ser Thr Tyr Leu Ala
1 5 10
<210> 263
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 263
Gln Gln Tyr Ser Glu Trp Pro Leu Thr
1 5
<210> 264
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 264
Gln Gln Tyr Ser Ser Trp Pro Leu Thr
1 5
<210> 265
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 265
Arg Ala Ser Gln Ser Val Ser Ser Leu Phe Leu Ala
1 5 10
<210> 266
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 266
Ala Cys Ser Gln Ser Val Ser Ser Thr Tyr Leu Ala
1 5 10
<210> 267
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 267
Arg Ala Ser Cys Asp Val Ser Ser Thr Tyr Leu Ala
1 5 10
<210> 268
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 268
Gln Gln Tyr Met Arg Ser Pro Leu Thr
1 5
<210> 269
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 269
Arg Ala Ser Glu Ala Val Pro Ser Thr Tyr Leu Ala
1 5 10
<210> 270
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 270
Cys Ser Ser Gln Ser Val Ser Ser Thr Tyr Leu Ala
1 5 10
<210> 271
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 271
Arg Ala Ser Val Arg Val Ser Ser Thr Tyr Leu Ala
1 5 10
<210> 272
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 272
Gln Gln Tyr Met Lys Trp Pro Leu Thr
1 5
<210> 273
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 273
Arg Ala Ser Gln Ser Val Ser Ala Ala Tyr Leu Ala
1 5 10
<210> 274
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 274
Gln Gln Tyr Met Cys Trp Pro Leu Thr
1 5
<210> 275
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 275
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Trp Gly
1 5 10
<210> 276
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 276
Gln Gln Tyr Gln Cys Trp Pro Leu Thr
1 5
<210> 277
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 277
Arg Ala Ser Gln Ser Val Ser Ser Pro Tyr Leu Ala
1 5 10
<210> 278
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 278
Gln Gln Tyr Lys Ala Trp Pro Leu Thr
1 5
<210> 279
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 279
Arg Ala Ser Gln Ser Val Ser Tyr Leu Tyr Leu Ala
1 5 10
<210> 280
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 280
Gln Gln Tyr Met Glu Trp Pro Leu Thr
1 5
<210> 281
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 281
Gln Gln Tyr Gln Ala Trp Pro Leu Thr
1 5
<210> 282
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 282
Gln Gln Tyr Gln Lys Trp Pro Leu Thr
1 5
<210> 283
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 283
Arg Ala Ser Gln Ser Val Ser Ala Val Tyr Leu Ala
1 5 10
<210> 284
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 284
Gln Gln Tyr Arg Ala Trp Pro Leu Thr
1 5
<210> 285
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 285
Arg Ala Ser Ile Ala Val Ser Ser Thr Tyr Leu Ala
1 5 10
<210> 286
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 286
Gln Gln Tyr Met Val Trp Pro Leu Thr
1 5
<210> 287
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 287
Arg Pro Arg Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 288
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 288
Gln Gln Tyr Gln Asp Trp Pro Leu Thr
1 5
<210> 289
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 289
Gln Gln Tyr Gln Glu Trp Pro Leu Thr
1 5
<210> 290
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 290
Arg Ala Ser Gln Ser Val Ser Ala Ser Tyr Leu Ala
1 5 10
<210> 291
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 291
Gln Gln Tyr Met Ser Trp Pro Leu Thr
1 5
<210> 292
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 292
Arg Ala Ser Gln Ser Val Ser Tyr Met Tyr Leu Ala
1 5 10
<210> 293
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 293
Gln Gln Tyr Lys Ser Trp Pro Leu Thr
1 5
<210> 294
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 294
Gln Gln Tyr Tyr Gly Trp Pro Leu Thr
1 5
<210> 295
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 295
Arg Ala Ser Gln Pro Ile Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 296
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 296
Gln Gln Tyr Glu Phe Trp Pro Leu Thr
1 5
<210> 297
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 297
Arg Ala Ser Gln Gly Ile Ser Ser Thr Tyr Leu Ala
1 5 10
<210> 298
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 298
Gln Gln Tyr Ala Tyr Trp Pro Leu Thr
1 5
<210> 299
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 299
Arg Ala Ser Gln Ser Val Ser Val Arg Tyr Leu Ala
1 5 10
<210> 300
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 300
Gln Gln Tyr Gly Ser Trp Pro Ile Thr
1 5
<210> 301
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена=«P»
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена=«N» или «S»
<220>
<221> САЙТ
<222> (1)..(5)
<223> /примечание=«Варианты остатков, указанные в последовательности, не имеют
предпочтений относительно тех, что в пояснениях
для положений вариантов»
<400> 301
Ser Tyr Ala Met Thr
1 5
<210> 302
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена=«S»
<220>
<221> САЙТ
<222> (1)..(7)
<223> /примечание=«Варианты остатков, указанные в последовательности, не имеют
предпочтений относительно тех, что в пояснениях
для положений вариантов»
<400> 302
Gly Phe Thr Phe Gly Ser Tyr
1 5
<210> 303
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена=«S»
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена=«P»
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /замена=«N» или «S»
<220>
<221> САЙТ
<222> (1)..(10)
<223> /примечание=«Варианты остатков, указанные в последовательности, не имеют
предпочтений относительно тех, что в пояснениях
для положений вариантов»
<400> 303
Gly Phe Thr Phe Gly Ser Tyr Ala Met Thr
1 5 10
<210> 304
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 304
Ala Ile Ser Gly Trp Gly Gly Ser Leu Pro Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 305
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /замена=«V» или «T», или «H», или «L», или «A», или «C»
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена=«D» или «G», или «T», или «I», или «L», или «F», или «M», или «V»
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена=«Y» или «L», или «H», или «D», или «A», или «S», или «M»
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена=«Q» или «T», или «A», или «F», или «W»
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена=«Т»
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена=«S» или «P», или «Y», или «W», или «F»
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /замена=«T» или «I», или «L», или «T», или «A», или «R», или «V», или «K»
, или «G», или «C»
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /замена=«Y» или «P», или «W», или «H», или «G»
<220>
<221> ВАРИАНТ
<222> (14)..(14)
<223> /замена=«R» или «L»
<220>
<221> ВАРИАНТ
<222> (15)..(15)
<223> /замена=«Т»
<220>
<221> САЙТ
<222> (1)..(17)
<223> /примечание=«Варианты остатков, указанные в последовательности, не имеют
предпочтений относительно тех, что в пояснениях
для положений вариантов»
<400> 305
Ala Ile Ser Gly Ser Gly Gly Asn Ser Phe Tyr Ala Asp Val Gly Lys
1 5 10 15
Gly
<210> 306
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена=«V» или «I», или «D», или «G, T, L, F или M
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /замена=«Y» или «L», или «H», или «D», или «A», или «S», или «M»
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена=«G» или «F», или «W»
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена=«S»
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена=«Т»
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена=«S» или «P», или «Y», или «W»
<220>
<221> САЙТ
<222> (1)..(6)
<223> /примечание=«Варианты остатков, указанные в последовательности, не имеют
предпочтений относительно тех, что в пояснениях
для положений вариантов»
<400> 306
Ser Gly Ser Gly Gly Asn
1 5
<210> 307
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена=«Y»
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена=«S»
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена=«Q» или «L», или «P», или «E»
<220>
<221> САЙТ
<222> (1)..(10)
<223> /примечание=«Варианты остатков, указанные в последовательности, не имеют
предпочтений относительно тех, что в пояснениях
для положений вариантов»
<400> 307
Val Ser Pro Ile Ala Ala Gly Met Asp Tyr
1 5 10
<210> 308
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена=«S» или «T», или «A»
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена=«S» или «L», или «P», или «D»
<220>
<221> САЙТ
<222> (1)..(6)
<223> /примечание=«Варианты остатков, указанные в последовательности, не имеют
предпочтений относительно тех, что в пояснениях
для положений вариантов»
<400> 308
Tyr Trp Pro Met Asp Ile
1 5
<210> 309
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена=«G» или «W», или «A», или «C»
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /замена=«P» или «G», или «L», или «C», или «S»
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена=«G» или «R»
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена=«C» или «E», или «V», или «I»
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена=«P» или «G», или «A», или «R», или «D»
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена=«G» или «I», или «L»
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена=«E» или «D», или «P», или «G»
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена=«P» или «F», или «A», или «M», или «E», или «V», или «N»
, или «D», или «Y»
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /замена=«T» или «V», или «E», или «F», или «S», или «A», или «M»
, или «Q», или «Y», или «H», или «R»
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /замена=«F»
<220>
<221> ВАРИАНТ
<222> (11)..(11)
<223> /замена=«W» или «P»
<220>
<221> ВАРИАНТ
<222> (12)..(12)
<223> /замена=«S» или «G»
<220>
<221> САЙТ
<222> (1)..(12)
<223> /примечание=«Варианты остатков, указанные в последовательности, не имеют
предпочтений относительно тех, что в пояснениях
для положений вариантов»
<400> 309
Arg Ala Ser Gln Ser Val Ser Ser Ile Tyr Leu Ala
1 5 10
<210> 310
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена=«D»
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена=«I»
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена=«P»
<220>
<221> САЙТ
<222> (1)..(7)
<223> /примечание=«Варианты остатков, указанные в последовательности, не имеют
предпочтений относительно тех, что в пояснениях
для положений вариантов»
<400> 310
Gly Ala Ser Ser Arg Ala Thr
1 5
<210> 311
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена=«K»
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /замена=«Y»
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена=«N» или «P»
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена=«W» или «Y»
<400> 311
Gln His Tyr Gly Ser Pro Pro Ser Phe Thr
1 5 10
<210> 312
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена=«Q» или «E», или «L», или «F», или «A», или «S», или «M»
, или «К», или «R», или «Y»
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена=«R» или «T», или «G», или «V», или «F», или «Y», или «D»
, или «А», или «Н», или «V», или «Е», или «К», или «С»
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена=«F» или «S»
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена=«I»
<220>
<221> САЙТ
<222> (1)..(9)
<223> /примечание=«Варианты остатков, указанные в последовательности, не имеют
предпочтений относительно тех, что в пояснениях
для положений вариантов»
<400> 312
Gln Gln Tyr Gly Ser Trp Pro Leu Thr
1 5
<210> 313
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<220>
<221> ВАРИАНТ
<222> (30)..(30)
<223> /замена=«S»
<220>
<221> ВАРИАНТ
<222> (33)..(33)
<223> /замена=«P»
<220>
<221> ВАРИАНТ
<222> (35)..(35)
<223> /замена=«N» или «S»
<220>
<221> ВАРИАНТ
<222> (51)..(51)
<223> /замена=«V» или «T», или «H», или «L», или «A», или «C»
<220>
<221> ВАРИАНТ
<222> (52)..(52)
<223> /замена=«D» или «G», или «T», или «I», или «L», или «F», или «M», или «V»
<220>
<221> ВАРИАНТ
<222> (53)..(53)
<223> /замена=«Y» или «L», или «H», или «D», или «A», или «S», или «M»
<220>
<221> ВАРИАНТ
<222> (54)..(54)
<223> /замена=«Q» или «T», или «A», или «F», или «W»
<220>
<221> ВАРИАНТ
<222> (56)..(56)
<223> /замена=«Т»
<220>
<221> ВАРИАНТ
<222> (57)..(57)
<223> /замена=«S» или «P», или «Y», или «W», или «F»
<220>
<221> ВАРИАНТ
<222> (58)..(58)
<223> /замена=«T» или «I», или «L», или «T», или «A», или «R», или «V», или «K»
, или «G», или «C»
<220>
<221> ВАРИАНТ
<222> (59)..(59)
<223> /замена=«Y» или «P», или «W», или «H», или «G»
<220>
<221> ВАРИАНТ
<222> (63)..(63)
<223> /замена=«R» или «L»
<220>
<221> ВАРИАНТ
<222> (64)..(64)
<223> /замена=«Т»
<220>
<221> ВАРИАНТ
<222> (103)..(103)
<223> /замена=«Y»
<220>
<221> ВАРИАНТ
<222> (104)..(104)
<223> /замена=«S»
<220>
<221> ВАРИАНТ
<222> (105)..(105)
<223> /замена=«Q» или «L», или «P», или «E»
<220>
<221> САЙТ
<222> (1)..(119)
<223> /примечание=«Варианты остатков, указанные в последовательности, не имеют
предпочтений относительно тех, что в пояснениях
для положений вариантов»
<400> 313
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Gly Ser Tyr
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Asn Ser Phe Tyr Ala Asp Val Gly
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Ser Pro Ile Ala Ala Gly Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 314
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<220>
<221> ВАРИАНТ
<222> (30)..(30)
<223> /замена=«S»
<220>
<221> ВАРИАНТ
<222> (33)..(33)
<223> /замена=«P»
<220>
<221> ВАРИАНТ
<222> (35)..(35)
<223> /замена=«N» или «S»
<220>
<221> ВАРИАНТ
<222> (51)..(51)
<223> /замена=«V» или «T», или «H», или «L», или «A», или «C»
<220>
<221> ВАРИАНТ
<222> (52)..(52)
<223> /замена=«D» или «G», или «T», или «I», или «L», или «F», или «M»
, или «V»
<220>
<221> ВАРИАНТ
<222> (53)..(53)
<223> /замена=«Y» или «L», или «H», или «D», или «A», или «S», или «M»
<220>
<221> ВАРИАНТ
<222> (54)..(54)
<223> /замена=«Q» или «T», или «A», или «F», или «W»
<220>
<221> ВАРИАНТ
<222> (56)..(56)
<223> /замена=«Т»
<220>
<221> ВАРИАНТ
<222> (57)..(57)
<223> /замена=«S» или «P», или «Y», или «W», или «F»
<220>
<221> ВАРИАНТ
<222> (58)..(58)
<223> /замена=«T» или «I», или «L», или «T», или «A», или «R», или «V»
, или «К», или «G», или «С»
<220>
<221> ВАРИАНТ
<222> (59)..(59)
<223> /замена=«Y» или «P», или «W», или «H», или «G»
<220>
<221> ВАРИАНТ
<222> (63)..(63)
<223> /замена=«R» или «L»
<220>
<221> ВАРИАНТ
<222> (64)..(64)
<223> /замена=«Т»
<220>
<221> ВАРИАНТ
<222> (103)..(103)
<223> /замена=«S» или «T», или «A»
<220>
<221> ВАРИАНТ
<222> (104)..(104)
<223> /замена=«S» или «L», или «P», или «D»
<220>
<221> САЙТ
<222> (1)..(115)
<223> /примечание=«Варианты остатков, указанные в последовательности, не имеют
предпочтений относительно тех, что в пояснениях
для положений вариантов»
<400> 314
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Gly Ser Tyr
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Asn Ser Phe Tyr Ala Asp Val Gly
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Trp Pro Met Asp Ile Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 315
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<220>
<221> ВАРИАНТ
<222> (24)..(24)
<223> /замена=«G» или «W», или «A», или «C»
<220>
<221> ВАРИАНТ
<222> (25)..(25)
<223> /замена=«P» или «G», или «L», или «C», или «S»
<220>
<221> ВАРИАНТ
<222> (26)..(26)
<223> /замена=«G» или «R»
<220>
<221> ВАРИАНТ
<222> (27)..(27)
<223> /замена=«C» или «E», или «V», или «I»
<220>
<221> ВАРИАНТ
<222> (28)..(28)
<223> /замена=«P» или «G», или «A», или «R», или «D»
<220>
<221> ВАРИАНТ
<222> (29)..(29)
<223> /замена=«G» или «I», или «L»
<220>
<221> ВАРИАНТ
<222> (30)..(30)
<223> /замена=«E» или «D», или «P», или «G»
<220>
<221> ВАРИАНТ
<222> (31)..(31)
<223> /замена=«P» или «F», или «A», или «M», или «E», или «V», или «N»
, или «D», или «Y»
<220>
<221> ВАРИАНТ
<222> (32)..(32)
<223> /замена=«T» или «V», или «E», или «S», или «A», или «M», или «Q»
, или «Y», или «H», или «R», или «F»
<220>
<221> ВАРИАНТ
<222> (33)..(33)
<223> /замена=«F»
<220>
<221> ВАРИАНТ
<222> (34)..(34)
<223> /замена=«W» или «P»
<220>
<221> ВАРИАНТ
<222> (35)..(35)
<223> /замена=«S» или «G»
<220>
<221> ВАРИАНТ
<222> (51)..(51)
<223> /замена=«D»
<220>
<221> ВАРИАНТ
<222> (54)..(54)
<223> /замена=«I»
<220>
<221> ВАРИАНТ
<222> (57)..(57)
<223> /замена=«P»
<220>
<221> ВАРИАНТ
<222> (90)..(90)
<223> /замена=«K»
<220>
<221> ВАРИАНТ
<222> (91)..(91)
<223> /замена=«Y»
<220>
<221> ВАРИАНТ
<222> (93)..(93)
<223> /замена=«N» или «P»
<220>
<221> ВАРИАНТ
<222> (94)..(94)
<223> /замена=«W» или «Y»
<220>
<221> САЙТ
<222> (1)..(109)
<223> /примечание=«Варианты остатков, указанные в последовательности, не имеют
предпочтений относительно тех, что в пояснениях
для положений вариантов»
<400> 315
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ile
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Ser Pro Pro
85 90 95
Ser Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 316
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<220>
<221> ВАРИАНТ
<222> (24)..(24)
<223> /замена=«G» или «W», или «A», или «C»
<220>
<221> ВАРИАНТ
<222> (25)..(25)
<223> /замена=«P», или «G», или «L», или «C», или «S»
<220>
<221> ВАРИАНТ
<222> (26)..(26)
<223> /замена=«G» или «R»
<220>
<221> ВАРИАНТ
<222> (27)..(27)
<223> /замена=«C» или «E», или «V», или «I»
<220>
<221> ВАРИАНТ
<222> (28)..(28)
<223> /замена=«L» или «P», или «G», или «A», или «R», или «D»
<220>
<221> ВАРИАНТ
<222> (29)..(29)
<223> /замена=«G» или «I»
<220>
<221> ВАРИАНТ
<222> (30)..(30)
<223> /замена=«E» или «D», или «P»
<220>
<221> ВАРИАНТ
<222> (31)..(31)
<223> /замена=«P» или «F», или «A», или «M», или «E», или «V», или «N»
, или «D», или «Y»
<220>
<221> ВАРИАНТ
<222> (32)..(32)
<223> /замена=«T» или «V», или «E», или «S», или «A», или «M», или «Q»
, или «Y», или «H», или «R»
<220>
<221> ВАРИАНТ
<222> (33)..(33)
<223> /замена=«F»
<220>
<221> ВАРИАНТ
<222> (34)..(34)
<223> /замена=«W» или «P»
<220>
<221> ВАРИАНТ
<222> (35)..(35)
<223> /замена=«S» или «G»
<220>
<221> ВАРИАНТ
<222> (51)..(51)
<223> /замена=«D»
<220>
<221> ВАРИАНТ
<222> (54)..(54)
<223> /замена=«I»
<220>
<221> ВАРИАНТ
<222> (57)..(57)
<223> /замена=«P»
<220>
<221> ВАРИАНТ
<222> (93)..(93)
<223> /замена=«Q» или «E», или «L», или «F», или «A», или «S», или «M»
, или «R», или «K», или «Y»
<220>
<221> ВАРИАНТ
<222> (94)..(94)
<223> /замена= «R» или «T», или «G», или «R», или «V», или «D», или «A»
, или «H», или «E», или «K», или «C», или «F», или «Y»
<220>
<221> ВАРИАНТ
<222> (95)..(95)
<223> /замена=«S» или «F»
<220>
<221> ВАРИАНТ
<222> (97)..(97)
<223> /замена=«I»
<220>
<221> САЙТ
<222> (1)..(107)
<223> /примечание=«Варианты остатков, указанные в последовательности, не имеют
предпочтений относительно тех, что в пояснениях
для положений вариантов»
<400> 316
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ile
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Trp Pro
85 90 95
Leu Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 317
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 317
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ala Leu
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Asp Ala Ser Ser Arg Ala Pro Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Ser Ala Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 318
<211> 21
<212> Белок
<213> Homo sapiens
<400> 318
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro
20
<210> 319
<211> 16
<212> Белок
<213> Homo sapiens
<400> 319
Gly Leu Ala Val Ser Thr Ile Ser Ser Phe Phe Pro Pro Gly Tyr Gln
1 5 10 15
<210> 320
<211> 45
<212> Белок
<213> Homo sapiens
<400> 320
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
1 5 10 15
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
20 25 30
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
35 40 45
<210> 321
<211> 231
<212> Белок
<213> Homo sapiens
<400> 321
Glu Pro Lys Ser Pro Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys
130 135 140
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 322
<211> 24
<212> Белок
<213> Homo sapiens
<400> 322
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
1 5 10 15
Ser Leu Val Ile Thr Leu Tyr Cys
20
<210> 323
<211> 42
<212> Белок
<213> Homo sapiens
<400> 323
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
1 5 10 15
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
20 25 30
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
35 40
<210> 324
<211> 112
<212> Белок
<213> Homo sapiens
<400> 324
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 325
<211> 52
<212> Белок
<213> Homo sapiens
<400> 325
Phe Phe Ile Pro Leu Leu Val Val Ile Leu Phe Ala Val Asp Thr Gly
1 5 10 15
Leu Phe Ile Ser Thr Gln Gln Gln Val Thr Phe Leu Leu Lys Ile Lys
20 25 30
Arg Thr Arg Lys Gly Phe Arg Leu Leu Asn Pro His Pro Lys Pro Asn
35 40 45
Pro Lys Asn Asn
50
<210> 326
<211> 215
<212> Белок
<213> Homo sapiens
<400> 326
Met Asp Thr Glu Ser Asn Arg Arg Ala Asn Leu Ala Leu Pro Gln Glu
1 5 10 15
Pro Ser Ser Val Pro Ala Phe Glu Val Leu Glu Ile Ser Pro Gln Glu
20 25 30
Val Ser Ser Gly Arg Leu Leu Lys Ser Ala Ser Ser Pro Pro Leu His
35 40 45
Thr Trp Leu Thr Val Leu Lys Lys Glu Gln Glu Phe Leu Gly Val Thr
50 55 60
Gln Ile Leu Thr Ala Met Ile Cys Leu Cys Phe Gly Thr Val Val Cys
65 70 75 80
Ser Val Leu Asp Ile Ser His Ile Glu Gly Asp Ile Phe Ser Ser Phe
85 90 95
Lys Ala Gly Tyr Pro Phe Trp Gly Ala Ile Phe Phe Ser Ile Ser Gly
100 105 110
Met Leu Ser Ile Ile Ser Glu Arg Arg Asn Ala Thr Tyr Leu Val Arg
115 120 125
Gly Ser Leu Gly Ala Asn Thr Ala Ser Ser Ile Ala Gly Gly Thr Gly
130 135 140
Ile Thr Ile Leu Ile Ile Asn Leu Lys Lys Ser Leu Ala Tyr Ile His
145 150 155 160
Ile His Ser Cys Gln Lys Phe Phe Glu Thr Lys Cys Phe Met Ala Ser
165 170 175
Phe Ser Thr Glu Ile Val Val Met Met Leu Phe Leu Thr Ile Leu Gly
180 185 190
Leu Gly Ser Ala Val Ser Leu Thr Ile Cys Gly Ala Gly Glu Glu Leu
195 200 205
Lys Gly Asn Lys Val Pro Glu
210 215
<210> 327
<211> 42
<212> Белок
<213> Homo sapiens
<400> 327
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
1 5 10 15
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
20 25 30
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
35 40
<210> 328
<211> 41
<212> Белок
<213> Homo sapiens
<400> 328
Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp Tyr Met Asn Met Thr
1 5 10 15
Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro
20 25 30
Pro Arg Asp Phe Ala Ala Tyr Arg Ser
35 40
<210> 329
<211> 18
<212> Белок
<213> Homo sapiens
<400> 329
Met Ile Pro Ala Val Val Leu Leu Leu Leu Leu Leu Val Glu Gln Ala
1 5 10 15
Ala Ala
<210> 330
<211> 43
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 330
Leu Gly Glu Pro Gln Leu Cys Tyr Ile Leu Asp Ala Ile Leu Phe Leu
1 5 10 15
Tyr Gly Ile Val Leu Thr Leu Leu Tyr Cys Arg Leu Lys Ile Gln Val
20 25 30
Arg Lys Ala Ala Ile Thr Ser Tyr Glu Lys Ser
35 40
<210> 331
<211> 22
<212> Белок
<213> Homo sapiens
<400> 331
Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val
1 5 10 15
Glu Glu Asn Pro Gly Pro
20
<210> 332
<211> 21
<212> Белок
<213> Homo sapiens
<400> 332
Gly Ser Gly Glu Gly Arg Gly Ser Leu Leu Thr Cys Gly Asp Val Glu
1 5 10 15
Glu Asn Pro Gly Pro
20
<210> 333
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 333
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 334
<211> 530
<212> Белок
<213> Homo sapiens
<400> 334
Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys
1 5 10 15
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
20 25 30
His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly
35 40 45
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
50 55 60
Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn
65 70 75 80
Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
85 90 95
Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala
100 105 110
Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu
115 120 125
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala
130 135 140
Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
145 150 155 160
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val
165 170 175
Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val
180 185 190
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu
195 200 205
Gln Val Val Ala Ile Ala Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu
210 215 220
Thr Val Gln Ala Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
225 230 235 240
Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala
245 250 255
Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly
260 265 270
Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser Asn Ile Gly Gly Lys
275 280 285
Gln Ala Leu Glu Thr Val Gln Ala Leu Leu Pro Val Leu Cys Gln Ala
290 295 300
His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly
305 310 315 320
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
325 330 335
Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser Asn
340 345 350
Ile Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Ala Leu Leu Pro Val
355 360 365
Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala
370 375 380
Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu
385 390 395 400
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala
405 410 415
Ile Ala Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Ala
420 425 430
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val
435 440 445
Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val
450 455 460
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu
465 470 475 480
Gln Val Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu
485 490 495
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
500 505 510
Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Arg Pro Ala
515 520 525
Leu Glu
530
<210> 335
<211> 530
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 335
Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly Gly Lys
1 5 10 15
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
20 25 30
His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly
35 40 45
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
50 55 60
Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His
65 70 75 80
Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
85 90 95
Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala
100 105 110
Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Ala Leu Leu
115 120 125
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala
130 135 140
Ile Ala Ser Asn Asn Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
145 150 155 160
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val
165 170 175
Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val
180 185 190
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln
195 200 205
Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu
210 215 220
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
225 230 235 240
Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys Gln Ala
245 250 255
Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly
260 265 270
Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys
275 280 285
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
290 295 300
His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly
305 310 315 320
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
325 330 335
Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser Asn
340 345 350
Ile Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Ala Leu Leu Pro Val
355 360 365
Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala
370 375 380
Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu
385 390 395 400
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala
405 410 415
Ile Ala Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Ala
420 425 430
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val
435 440 445
Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val
450 455 460
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln
465 470 475 480
Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys Gln Ala Leu Glu
485 490 495
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
500 505 510
Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Arg Pro Ala
515 520 525
Leu Glu
530
<210> 336
<211> 530
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 336
Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys
1 5 10 15
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
20 25 30
His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly
35 40 45
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
50 55 60
Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn
65 70 75 80
Asn Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
85 90 95
Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala
100 105 110
Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu
115 120 125
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala
130 135 140
Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
145 150 155 160
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val
165 170 175
Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val
180 185 190
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln
195 200 205
Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys Gln Ala Leu Glu
210 215 220
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
225 230 235 240
Pro Glu Gln Val Val Ala Ile Ala Ser Asn Ile Gly Gly Lys Gln Ala
245 250 255
Leu Glu Thr Val Gln Ala Leu Leu Pro Val Leu Cys Gln Ala His Gly
260 265 270
Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys
275 280 285
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
290 295 300
His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly
305 310 315 320
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
325 330 335
Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His
340 345 350
Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
355 360 365
Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala
370 375 380
Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Ala Leu Leu
385 390 395 400
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala
405 410 415
Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
420 425 430
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val
435 440 445
Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val
450 455 460
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu
465 470 475 480
Gln Val Val Ala Ile Ala Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu
485 490 495
Thr Val Gln Ala Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
500 505 510
Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Arg Pro Ala
515 520 525
Leu Glu
530
<210> 337
<211> 539
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 337
Asn Pro Gln Arg Ser Thr Val Trp Tyr Leu Thr Pro Gln Gln Val Val
1 5 10 15
Ala Ile Ala Ser Asn Asn Gly Gly Lys Gln Ala Leu Glu Thr Val Gln
20 25 30
Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln
35 40 45
Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr
50 55 60
Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro
65 70 75 80
Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys Gln Ala Leu
85 90 95
Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu
100 105 110
Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys Gln
115 120 125
Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His
130 135 140
Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly Gly
145 150 155 160
Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln
165 170 175
Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp
180 185 190
Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu
195 200 205
Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser
210 215 220
Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro
225 230 235 240
Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile
245 250 255
Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu
260 265 270
Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val
275 280 285
Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln
290 295 300
Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln
305 310 315 320
Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr
325 330 335
Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro
340 345 350
Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys Gln Ala Leu
355 360 365
Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu
370 375 380
Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys Gln
385 390 395 400
Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His
405 410 415
Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly
420 425 430
Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln
435 440 445
Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly
450 455 460
Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu
465 470 475 480
Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser
485 490 495
Asn Asn Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro
500 505 510
Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile
515 520 525
Ala Ser Asn Gly Gly Gly Arg Pro Ala Leu Glu
530 535
<210> 338
<211> 530
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 338
Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly Gly Lys
1 5 10 15
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
20 25 30
His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly
35 40 45
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
50 55 60
Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His
65 70 75 80
Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
85 90 95
Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala
100 105 110
Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Ala Leu Leu
115 120 125
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala
130 135 140
Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
145 150 155 160
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val
165 170 175
Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val
180 185 190
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu
195 200 205
Gln Val Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu
210 215 220
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
225 230 235 240
Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys Gln Ala
245 250 255
Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly
260 265 270
Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser Asn Ile Gly Gly Lys
275 280 285
Gln Ala Leu Glu Thr Val Gln Ala Leu Leu Pro Val Leu Cys Gln Ala
290 295 300
His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly
305 310 315 320
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
325 330 335
Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn
340 345 350
Asn Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
355 360 365
Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala
370 375 380
Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu
385 390 395 400
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala
405 410 415
Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
420 425 430
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val
435 440 445
Val Ala Ile Ala Ser Asn Asn Gly Gly Lys Gln Ala Leu Glu Thr Val
450 455 460
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu
465 470 475 480
Gln Val Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu
485 490 495
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
500 505 510
Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Arg Pro Ala
515 520 525
Leu Glu
530
<210> 339
<211> 530
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 339
Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly Gly Lys
1 5 10 15
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
20 25 30
His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly
35 40 45
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
50 55 60
Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn
65 70 75 80
Asn Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
85 90 95
Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala
100 105 110
Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Ala Leu Leu
115 120 125
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala
130 135 140
Ile Ala Ser Asn Asn Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
145 150 155 160
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val
165 170 175
Val Ala Ile Ala Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu Thr Val
180 185 190
Gln Ala Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln
195 200 205
Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu
210 215 220
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
225 230 235 240
Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala
245 250 255
Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly
260 265 270
Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys
275 280 285
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
290 295 300
His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly
305 310 315 320
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
325 330 335
Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn
340 345 350
Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
355 360 365
Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala
370 375 380
Ser Asn Asn Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu
385 390 395 400
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala
405 410 415
Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
420 425 430
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val
435 440 445
Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val
450 455 460
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln
465 470 475 480
Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu
485 490 495
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
500 505 510
Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Arg Pro Ala
515 520 525
Leu Glu
530
<210> 340
<211> 530
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 340
Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys
1 5 10 15
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
20 25 30
His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly
35 40 45
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
50 55 60
Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His
65 70 75 80
Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
85 90 95
Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala
100 105 110
Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu
115 120 125
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala
130 135 140
Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
145 150 155 160
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val
165 170 175
Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val
180 185 190
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln
195 200 205
Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu
210 215 220
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
225 230 235 240
Pro Glu Gln Val Val Ala Ile Ala Ser Asn Ile Gly Gly Lys Gln Ala
245 250 255
Leu Glu Thr Val Gln Ala Leu Leu Pro Val Leu Cys Gln Ala His Gly
260 265 270
Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly Gly Lys
275 280 285
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
290 295 300
His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly
305 310 315 320
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
325 330 335
Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His
340 345 350
Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
355 360 365
Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala
370 375 380
Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Ala Leu Leu
385 390 395 400
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala
405 410 415
Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
420 425 430
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val
435 440 445
Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val
450 455 460
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu
465 470 475 480
Gln Val Val Ala Ile Ala Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu
485 490 495
Thr Val Gln Ala Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
500 505 510
Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Arg Pro Ala
515 520 525
Leu Glu
530
<210> 341
<211> 530
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 341
Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys
1 5 10 15
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
20 25 30
His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn Asn Gly
35 40 45
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
50 55 60
Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His
65 70 75 80
Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
85 90 95
Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala
100 105 110
Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu
115 120 125
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val Val Ala
130 135 140
Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
145 150 155 160
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val
165 170 175
Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val
180 185 190
Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln
195 200 205
Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu
210 215 220
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
225 230 235 240
Pro Glu Gln Val Val Ala Ile Ala Ser Asn Ile Gly Gly Lys Gln Ala
245 250 255
Leu Glu Thr Val Gln Ala Leu Leu Pro Val Leu Cys Gln Ala His Gly
260 265 270
Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly Gly Lys
275 280 285
Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala
290 295 300
His Gly Leu Thr Pro Glu Gln Val Val Ala Ile Ala Ser His Asp Gly
305 310 315 320
Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val Leu Cys
325 330 335
Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala Ser Asn
340 345 350
Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu Pro Val
355 360 365
Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala Ile Ala
370 375 380
Ser Asn Asn Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg Leu Leu
385 390 395 400
Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Gln Gln Val Val Ala
405 410 415
Ile Ala Ser Asn Gly Gly Gly Lys Gln Ala Leu Glu Thr Val Gln Arg
420 425 430
Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu Gln Val
435 440 445
Val Ala Ile Ala Ser Asn Ile Gly Gly Lys Gln Ala Leu Glu Thr Val
450 455 460
Gln Ala Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr Pro Glu
465 470 475 480
Gln Val Val Ala Ile Ala Ser His Asp Gly Gly Lys Gln Ala Leu Glu
485 490 495
Thr Val Gln Arg Leu Leu Pro Val Leu Cys Gln Ala His Gly Leu Thr
500 505 510
Pro Gln Gln Val Val Ala Ile Ala Ser Asn Gly Gly Gly Arg Pro Ala
515 520 525
Leu Glu
530
<210> 342
<211> 136
<212> Белок
<213> Homo sapiens
<400> 342
Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser Glu
1 5 10 15
Leu Pro Thr Gln Gly Thr Phe Ser Asn Val Ser Thr Asn Val Ser Pro
20 25 30
Ala Lys Pro Thr Thr Thr Ala Cys Pro Tyr Ser Asn Pro Ser Leu Cys
35 40 45
Ser Gly Gly Gly Gly Ser Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
50 55 60
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
65 70 75 80
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
85 90 95
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
100 105 110
Ser Leu Val Ile Thr Leu Tyr Cys Asn His Arg Asn Arg Arg Arg Val
115 120 125
Cys Lys Cys Pro Arg Pro Val Val
130 135
<210> 343
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 343
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Asp Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Tyr Trp Pro Met Asp Ile Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly
145 150 155 160
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
165 170 175
Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala Trp Tyr Gln Gln Lys Pro
180 185 190
Gly Gln Ala Pro Arg Leu Leu Met Tyr Asp Ala Ser Ile Arg Ala Thr
195 200 205
Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
210 215 220
Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys
225 230 235 240
Gln Gln Tyr Gly Ser Trp Pro Leu Thr Phe Gly Gln Gly Thr Lys Val
245 250 255
Glu Ile Lys Gly Leu Ala Val Ser Thr Ile Ser Ser Phe Phe Pro Pro
260 265 270
Gly Tyr Gln Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
275 280 285
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
290 295 300
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
305 310 315 320
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
325 330 335
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
340 345 350
Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
355 360 365
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
370 375 380
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
385 390 395 400
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
405 410 415
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
420 425 430
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
435 440 445
Ala Leu Pro Pro Arg
450
<210> 344
<211> 482
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 344
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Asp Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Tyr Trp Pro Met Asp Ile Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly
145 150 155 160
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
165 170 175
Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala Trp Tyr Gln Gln Lys Pro
180 185 190
Gly Gln Ala Pro Arg Leu Leu Met Tyr Asp Ala Ser Ile Arg Ala Thr
195 200 205
Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
210 215 220
Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys
225 230 235 240
Gln Gln Tyr Gly Ser Trp Pro Leu Thr Phe Gly Gln Gly Thr Lys Val
245 250 255
Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
260 265 270
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
275 280 285
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
290 295 300
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
305 310 315 320
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
325 330 335
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
340 345 350
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
355 360 365
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
370 375 380
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
385 390 395 400
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
405 410 415
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
420 425 430
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
435 440 445
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
450 455 460
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
465 470 475 480
Pro Arg
<210> 345
<211> 668
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 345
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Asp Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Tyr Trp Pro Met Asp Ile Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly
145 150 155 160
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
165 170 175
Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala Trp Tyr Gln Gln Lys Pro
180 185 190
Gly Gln Ala Pro Arg Leu Leu Met Tyr Asp Ala Ser Ile Arg Ala Thr
195 200 205
Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
210 215 220
Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys
225 230 235 240
Gln Gln Tyr Gly Ser Trp Pro Leu Thr Phe Gly Gln Gly Thr Lys Val
245 250 255
Glu Ile Lys Glu Pro Lys Ser Pro Asp Lys Thr His Thr Cys Pro Pro
260 265 270
Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro
275 280 285
Lys Pro Lys Asp Thr Leu Met Ile Ala Arg Thr Pro Glu Val Thr Cys
290 295 300
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
305 310 315 320
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
325 330 335
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
340 345 350
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
355 360 365
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
370 375 380
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
385 390 395 400
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
405 410 415
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
420 425 430
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
435 440 445
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
450 455 460
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
465 470 475 480
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ile Tyr Ile Trp Ala Pro
485 490 495
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
500 505 510
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
515 520 525
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
530 535 540
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
545 550 555 560
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
565 570 575
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
580 585 590
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
595 600 605
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
610 615 620
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
625 630 635 640
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
645 650 655
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
660 665
<210> 346
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 346
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Leu Ser Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Tyr Trp Pro Met Asp Ile Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly
145 150 155 160
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Gly
165 170 175
Gly Gln Ser Val Ser Ser Ser Tyr Leu Ala Trp Tyr Gln Gln Lys Pro
180 185 190
Gly Gln Ala Pro Arg Leu Leu Met Tyr Asp Ala Ser Ile Arg Ala Thr
195 200 205
Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
210 215 220
Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys
225 230 235 240
Gln Gln Tyr Gln Ser Trp Pro Leu Thr Phe Gly Gln Gly Thr Lys Val
245 250 255
Glu Ile Lys Gly Leu Ala Val Ser Thr Ile Ser Ser Phe Phe Pro Pro
260 265 270
Gly Tyr Gln Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
275 280 285
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
290 295 300
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
305 310 315 320
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
325 330 335
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
340 345 350
Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
355 360 365
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
370 375 380
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
385 390 395 400
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
405 410 415
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
420 425 430
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
435 440 445
Ala Leu Pro Pro Arg
450
<210> 347
<211> 482
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 347
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Leu Ser Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Tyr Trp Pro Met Asp Ile Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly
145 150 155 160
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Gly
165 170 175
Gly Gln Ser Val Ser Ser Ser Tyr Leu Ala Trp Tyr Gln Gln Lys Pro
180 185 190
Gly Gln Ala Pro Arg Leu Leu Met Tyr Asp Ala Ser Ile Arg Ala Thr
195 200 205
Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
210 215 220
Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys
225 230 235 240
Gln Gln Tyr Gln Ser Trp Pro Leu Thr Phe Gly Gln Gly Thr Lys Val
245 250 255
Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
260 265 270
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
275 280 285
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
290 295 300
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
305 310 315 320
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
325 330 335
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
340 345 350
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
355 360 365
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
370 375 380
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
385 390 395 400
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
405 410 415
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
420 425 430
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
435 440 445
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
450 455 460
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
465 470 475 480
Pro Arg
<210> 348
<211> 668
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 348
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Leu Ser Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Tyr Trp Pro Met Asp Ile Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly
145 150 155 160
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Gly
165 170 175
Gly Gln Ser Val Ser Ser Ser Tyr Leu Ala Trp Tyr Gln Gln Lys Pro
180 185 190
Gly Gln Ala Pro Arg Leu Leu Met Tyr Asp Ala Ser Ile Arg Ala Thr
195 200 205
Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
210 215 220
Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys
225 230 235 240
Gln Gln Tyr Gln Ser Trp Pro Leu Thr Phe Gly Gln Gly Thr Lys Val
245 250 255
Glu Ile Lys Glu Pro Lys Ser Pro Asp Lys Thr His Thr Cys Pro Pro
260 265 270
Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro
275 280 285
Lys Pro Lys Asp Thr Leu Met Ile Ala Arg Thr Pro Glu Val Thr Cys
290 295 300
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
305 310 315 320
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
325 330 335
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
340 345 350
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
355 360 365
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
370 375 380
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
385 390 395 400
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
405 410 415
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
420 425 430
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
435 440 445
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
450 455 460
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
465 470 475 480
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ile Tyr Ile Trp Ala Pro
485 490 495
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
500 505 510
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
515 520 525
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
530 535 540
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
545 550 555 560
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
565 570 575
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
580 585 590
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
595 600 605
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
610 615 620
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
625 630 635 640
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
645 650 655
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
660 665
<210> 349
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 349
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Asp Phe Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Tyr Trp Pro Met Asp Ile Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly
145 150 155 160
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
165 170 175
Ser Gln Ser Val Ser Asp Leu Tyr Leu Ala Trp Tyr Gln Gln Lys Pro
180 185 190
Gly Gln Ala Pro Arg Leu Leu Met Tyr Asp Ala Ser Ile Arg Ala Thr
195 200 205
Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
210 215 220
Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys
225 230 235 240
Gln Gln Tyr Gln Thr Trp Pro Leu Thr Phe Gly Gln Gly Thr Lys Val
245 250 255
Glu Ile Lys Gly Leu Ala Val Ser Thr Ile Ser Ser Phe Phe Pro Pro
260 265 270
Gly Tyr Gln Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
275 280 285
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
290 295 300
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
305 310 315 320
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
325 330 335
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
340 345 350
Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
355 360 365
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
370 375 380
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
385 390 395 400
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
405 410 415
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
420 425 430
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
435 440 445
Ala Leu Pro Pro Arg
450
<210> 350
<211> 482
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 350
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Asp Phe Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Tyr Trp Pro Met Asp Ile Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly
145 150 155 160
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
165 170 175
Ser Gln Ser Val Ser Asp Leu Tyr Leu Ala Trp Tyr Gln Gln Lys Pro
180 185 190
Gly Gln Ala Pro Arg Leu Leu Met Tyr Asp Ala Ser Ile Arg Ala Thr
195 200 205
Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
210 215 220
Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys
225 230 235 240
Gln Gln Tyr Gln Thr Trp Pro Leu Thr Phe Gly Gln Gly Thr Lys Val
245 250 255
Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
260 265 270
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
275 280 285
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
290 295 300
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
305 310 315 320
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
325 330 335
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
340 345 350
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
355 360 365
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
370 375 380
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
385 390 395 400
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
405 410 415
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
420 425 430
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
435 440 445
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
450 455 460
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
465 470 475 480
Pro Arg
<210> 351
<211> 668
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 351
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Asp Phe Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Tyr Trp Pro Met Asp Ile Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly
145 150 155 160
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
165 170 175
Ser Gln Ser Val Ser Asp Leu Tyr Leu Ala Trp Tyr Gln Gln Lys Pro
180 185 190
Gly Gln Ala Pro Arg Leu Leu Met Tyr Asp Ala Ser Ile Arg Ala Thr
195 200 205
Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
210 215 220
Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys
225 230 235 240
Gln Gln Tyr Gln Thr Trp Pro Leu Thr Phe Gly Gln Gly Thr Lys Val
245 250 255
Glu Ile Lys Glu Pro Lys Ser Pro Asp Lys Thr His Thr Cys Pro Pro
260 265 270
Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro
275 280 285
Lys Pro Lys Asp Thr Leu Met Ile Ala Arg Thr Pro Glu Val Thr Cys
290 295 300
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
305 310 315 320
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
325 330 335
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
340 345 350
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
355 360 365
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
370 375 380
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
385 390 395 400
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
405 410 415
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
420 425 430
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
435 440 445
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
450 455 460
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
465 470 475 480
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ile Tyr Ile Trp Ala Pro
485 490 495
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
500 505 510
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
515 520 525
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
530 535 540
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
545 550 555 560
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
565 570 575
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
580 585 590
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
595 600 605
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
610 615 620
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
625 630 635 640
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
645 650 655
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
660 665
<210> 352
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 352
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Gly Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Tyr Trp Pro Met Asp Ser Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly
145 150 155 160
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
165 170 175
Ser Gln Ser Val Ser Ser Thr Tyr Leu Ala Trp Tyr Gln Gln Lys Pro
180 185 190
Gly Gln Ala Pro Arg Leu Leu Ile Tyr Asp Ala Ser Ser Arg Ala Pro
195 200 205
Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
210 215 220
Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys
225 230 235 240
Gln Gln Tyr Ser Thr Ser Pro Leu Thr Phe Gly Gln Gly Thr Lys Val
245 250 255
Glu Ile Lys Gly Leu Ala Val Ser Thr Ile Ser Ser Phe Phe Pro Pro
260 265 270
Gly Tyr Gln Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
275 280 285
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
290 295 300
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
305 310 315 320
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
325 330 335
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
340 345 350
Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
355 360 365
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
370 375 380
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
385 390 395 400
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
405 410 415
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
420 425 430
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
435 440 445
Ala Leu Pro Pro Arg
450
<210> 353
<211> 482
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 353
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Gly Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Tyr Trp Pro Met Asp Ser Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly
145 150 155 160
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
165 170 175
Ser Gln Ser Val Ser Ser Thr Tyr Leu Ala Trp Tyr Gln Gln Lys Pro
180 185 190
Gly Gln Ala Pro Arg Leu Leu Ile Tyr Asp Ala Ser Ser Arg Ala Pro
195 200 205
Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
210 215 220
Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys
225 230 235 240
Gln Gln Tyr Ser Thr Ser Pro Leu Thr Phe Gly Gln Gly Thr Lys Val
245 250 255
Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
260 265 270
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
275 280 285
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
290 295 300
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
305 310 315 320
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
325 330 335
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
340 345 350
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
355 360 365
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
370 375 380
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
385 390 395 400
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
405 410 415
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
420 425 430
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
435 440 445
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
450 455 460
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
465 470 475 480
Pro Arg
<210> 354
<211> 668
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 354
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Gly Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Tyr Trp Pro Met Asp Ser Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly
145 150 155 160
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
165 170 175
Ser Gln Ser Val Ser Ser Thr Tyr Leu Ala Trp Tyr Gln Gln Lys Pro
180 185 190
Gly Gln Ala Pro Arg Leu Leu Ile Tyr Asp Ala Ser Ser Arg Ala Pro
195 200 205
Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
210 215 220
Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys
225 230 235 240
Gln Gln Tyr Ser Thr Ser Pro Leu Thr Phe Gly Gln Gly Thr Lys Val
245 250 255
Glu Ile Lys Glu Pro Lys Ser Pro Asp Lys Thr His Thr Cys Pro Pro
260 265 270
Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro
275 280 285
Lys Pro Lys Asp Thr Leu Met Ile Ala Arg Thr Pro Glu Val Thr Cys
290 295 300
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
305 310 315 320
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
325 330 335
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
340 345 350
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
355 360 365
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
370 375 380
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
385 390 395 400
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
405 410 415
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
420 425 430
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
435 440 445
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
450 455 460
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
465 470 475 480
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ile Tyr Ile Trp Ala Pro
485 490 495
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
500 505 510
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
515 520 525
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
530 535 540
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
545 550 555 560
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
565 570 575
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
580 585 590
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
595 600 605
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
610 615 620
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
625 630 635 640
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
645 650 655
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
660 665
<210> 355
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 355
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Gly Gly Ser Gly Gly Trp Ser Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Tyr Trp Pro Met Asp Ser Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly
145 150 155 160
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Trp Leu
165 170 175
Ser Gln Ser Val Ser Ser Thr Tyr Leu Ala Trp Tyr Gln Gln Lys Pro
180 185 190
Gly Gln Ala Pro Arg Leu Leu Ile Tyr Asp Ala Ser Ser Arg Ala Pro
195 200 205
Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
210 215 220
Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys
225 230 235 240
Gln Gln Tyr Ser Glu Trp Pro Leu Thr Phe Gly Gln Gly Thr Lys Val
245 250 255
Glu Ile Lys Gly Leu Ala Val Ser Thr Ile Ser Ser Phe Phe Pro Pro
260 265 270
Gly Tyr Gln Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
275 280 285
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
290 295 300
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
305 310 315 320
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
325 330 335
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
340 345 350
Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
355 360 365
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
370 375 380
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
385 390 395 400
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
405 410 415
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
420 425 430
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
435 440 445
Ala Leu Pro Pro Arg
450
<210> 356
<211> 482
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 356
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Gly Gly Ser Gly Gly Trp Ser Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Tyr Trp Pro Met Asp Ser Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly
145 150 155 160
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Trp Leu
165 170 175
Ser Gln Ser Val Ser Ser Thr Tyr Leu Ala Trp Tyr Gln Gln Lys Pro
180 185 190
Gly Gln Ala Pro Arg Leu Leu Ile Tyr Asp Ala Ser Ser Arg Ala Pro
195 200 205
Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
210 215 220
Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys
225 230 235 240
Gln Gln Tyr Ser Glu Trp Pro Leu Thr Phe Gly Gln Gly Thr Lys Val
245 250 255
Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
260 265 270
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
275 280 285
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
290 295 300
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
305 310 315 320
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
325 330 335
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
340 345 350
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
355 360 365
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
370 375 380
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
385 390 395 400
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
405 410 415
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
420 425 430
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
435 440 445
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
450 455 460
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
465 470 475 480
Pro Arg
<210> 357
<211> 668
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 357
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Gly Gly Ser Gly Gly Trp Ser Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Tyr Trp Pro Met Asp Ser Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly
145 150 155 160
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Trp Leu
165 170 175
Ser Gln Ser Val Ser Ser Thr Tyr Leu Ala Trp Tyr Gln Gln Lys Pro
180 185 190
Gly Gln Ala Pro Arg Leu Leu Ile Tyr Asp Ala Ser Ser Arg Ala Pro
195 200 205
Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
210 215 220
Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys
225 230 235 240
Gln Gln Tyr Ser Glu Trp Pro Leu Thr Phe Gly Gln Gly Thr Lys Val
245 250 255
Glu Ile Lys Glu Pro Lys Ser Pro Asp Lys Thr His Thr Cys Pro Pro
260 265 270
Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro
275 280 285
Lys Pro Lys Asp Thr Leu Met Ile Ala Arg Thr Pro Glu Val Thr Cys
290 295 300
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
305 310 315 320
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
325 330 335
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
340 345 350
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
355 360 365
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
370 375 380
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
385 390 395 400
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
405 410 415
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
420 425 430
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
435 440 445
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
450 455 460
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
465 470 475 480
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ile Tyr Ile Trp Ala Pro
485 490 495
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
500 505 510
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
515 520 525
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
530 535 540
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
545 550 555 560
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
565 570 575
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
580 585 590
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
595 600 605
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
610 615 620
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
625 630 635 640
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
645 650 655
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
660 665
<210> 358
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 358
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Asp Ser Gly Gly Ser Arg Trp
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Thr Arg Tyr Trp Pro Met Asp Ile Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly
145 150 155 160
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
165 170 175
Ser Val Arg Val Ser Ser Thr Tyr Leu Ala Trp Tyr Gln Gln Lys Pro
180 185 190
Gly Gln Ala Pro Arg Leu Leu Met Tyr Asp Ala Ser Ile Arg Ala Thr
195 200 205
Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
210 215 220
Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys
225 230 235 240
Gln Gln Tyr Met Lys Trp Pro Leu Thr Phe Gly Gln Gly Thr Lys Val
245 250 255
Glu Ile Lys Gly Leu Ala Val Ser Thr Ile Ser Ser Phe Phe Pro Pro
260 265 270
Gly Tyr Gln Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
275 280 285
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
290 295 300
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
305 310 315 320
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
325 330 335
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
340 345 350
Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
355 360 365
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
370 375 380
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
385 390 395 400
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
405 410 415
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
420 425 430
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
435 440 445
Ala Leu Pro Pro Arg
450
<210> 359
<211> 482
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 359
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Asp Ser Gly Gly Ser Arg Trp
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Thr Arg Tyr Trp Pro Met Asp Ile Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly
145 150 155 160
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
165 170 175
Ser Val Arg Val Ser Ser Thr Tyr Leu Ala Trp Tyr Gln Gln Lys Pro
180 185 190
Gly Gln Ala Pro Arg Leu Leu Met Tyr Asp Ala Ser Ile Arg Ala Thr
195 200 205
Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
210 215 220
Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys
225 230 235 240
Gln Gln Tyr Met Lys Trp Pro Leu Thr Phe Gly Gln Gly Thr Lys Val
245 250 255
Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
260 265 270
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
275 280 285
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
290 295 300
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
305 310 315 320
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
325 330 335
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
340 345 350
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
355 360 365
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
370 375 380
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
385 390 395 400
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
405 410 415
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
420 425 430
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
435 440 445
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
450 455 460
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
465 470 475 480
Pro Arg
<210> 360
<211> 668
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 360
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Asp Ser Gly Gly Ser Arg Trp
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Thr Arg Tyr Trp Pro Met Asp Ile Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly
145 150 155 160
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
165 170 175
Ser Val Arg Val Ser Ser Thr Tyr Leu Ala Trp Tyr Gln Gln Lys Pro
180 185 190
Gly Gln Ala Pro Arg Leu Leu Met Tyr Asp Ala Ser Ile Arg Ala Thr
195 200 205
Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
210 215 220
Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys
225 230 235 240
Gln Gln Tyr Met Lys Trp Pro Leu Thr Phe Gly Gln Gly Thr Lys Val
245 250 255
Glu Ile Lys Glu Pro Lys Ser Pro Asp Lys Thr His Thr Cys Pro Pro
260 265 270
Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro
275 280 285
Lys Pro Lys Asp Thr Leu Met Ile Ala Arg Thr Pro Glu Val Thr Cys
290 295 300
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
305 310 315 320
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
325 330 335
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
340 345 350
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
355 360 365
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
370 375 380
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
385 390 395 400
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
405 410 415
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
420 425 430
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
435 440 445
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
450 455 460
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
465 470 475 480
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ile Tyr Ile Trp Ala Pro
485 490 495
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
500 505 510
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
515 520 525
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
530 535 540
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
545 550 555 560
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
565 570 575
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
580 585 590
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
595 600 605
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
610 615 620
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
625 630 635 640
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
645 650 655
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
660 665
<210> 361
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 361
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Gly Ser Tyr Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Asp Tyr Ser Gly Gly Asn Thr Phe
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Val Ser Pro Ile Ala Ser Gly Met Asp
115 120 125
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr
145 150 155 160
Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu
165 170 175
Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Pro Ser Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser
195 200 205
Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala
225 230 235 240
Val Tyr Tyr Cys Gln His Tyr Pro Tyr Pro Pro Ser Phe Thr Phe Gly
245 250 255
Gln Gly Thr Lys Val Glu Ile Lys Gly Leu Ala Val Ser Thr Ile Ser
260 265 270
Ser Phe Phe Pro Pro Gly Tyr Gln Ile Tyr Ile Trp Ala Pro Leu Ala
275 280 285
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
290 295 300
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
305 310 315 320
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
325 330 335
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
340 345 350
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
355 360 365
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
370 375 380
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
385 390 395 400
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
405 410 415
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
420 425 430
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
435 440 445
Ala Leu His Met Gln
450
<210> 362
<211> 487
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 362
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Gly Ser Tyr Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Asp Tyr Ser Gly Gly Asn Thr Phe
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Val Ser Pro Ile Ala Ser Gly Met Asp
115 120 125
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr
145 150 155 160
Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu
165 170 175
Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Pro Ser Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser
195 200 205
Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala
225 230 235 240
Val Tyr Tyr Cys Gln His Tyr Pro Tyr Pro Pro Ser Phe Thr Phe Gly
245 250 255
Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
260 265 270
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
275 280 285
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
290 295 300
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
305 310 315 320
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 363
<211> 673
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 363
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Gly Ser Tyr Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Asp Tyr Ser Gly Gly Asn Thr Phe
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Val Ser Pro Ile Ala Ser Gly Met Asp
115 120 125
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr
145 150 155 160
Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu
165 170 175
Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Pro Ser Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser
195 200 205
Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala
225 230 235 240
Val Tyr Tyr Cys Gln His Tyr Pro Tyr Pro Pro Ser Phe Thr Phe Gly
245 250 255
Gln Gly Thr Lys Val Glu Ile Lys Glu Pro Lys Ser Pro Asp Lys Thr
260 265 270
His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
275 280 285
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ala Arg Thr
290 295 300
Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu
305 310 315 320
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
325 330 335
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
340 345 350
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
355 360 365
Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile
370 375 380
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
385 390 395 400
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
405 410 415
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
420 425 430
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
435 440 445
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
450 455 460
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
465 470 475 480
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ile
485 490 495
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
500 505 510
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
515 520 525
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
530 535 540
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
545 550 555 560
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
565 570 575
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
580 585 590
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
595 600 605
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
610 615 620
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
625 630 635 640
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
645 650 655
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
660 665 670
Arg
<210> 364
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 364
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Gly Ser Tyr Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Asn Thr Phe
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Val Ser Pro Ile Ala Ala Pro Met Asp
115 120 125
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr
145 150 155 160
Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu
165 170 175
Ser Cys Arg Ala Ser Gln Leu Gly Ser Phe Tyr Leu Ala Trp Tyr Gln
180 185 190
Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ser
195 200 205
Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
210 215 220
Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val
225 230 235 240
Tyr Tyr Cys Gln His Tyr Asn Tyr Pro Pro Ser Phe Thr Phe Gly Gln
245 250 255
Gly Thr Lys Val Glu Ile Lys Gly Leu Ala Val Ser Thr Ile Ser Ser
260 265 270
Phe Phe Pro Pro Gly Tyr Gln Ile Tyr Ile Trp Ala Pro Leu Ala Gly
275 280 285
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
290 295 300
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
305 310 315 320
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
325 330 335
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
340 345 350
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
355 360 365
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
370 375 380
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
385 390 395 400
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
405 410 415
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
420 425 430
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
435 440 445
Leu His Met Gln Ala
450
<210> 365
<211> 486
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 365
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Gly Ser Tyr Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Asn Thr Phe
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Val Ser Pro Ile Ala Ala Pro Met Asp
115 120 125
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr
145 150 155 160
Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu
165 170 175
Ser Cys Arg Ala Ser Gln Leu Gly Ser Phe Tyr Leu Ala Trp Tyr Gln
180 185 190
Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ser
195 200 205
Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
210 215 220
Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val
225 230 235 240
Tyr Tyr Cys Gln His Tyr Asn Tyr Pro Pro Ser Phe Thr Phe Gly Gln
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 366
<211> 672
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 366
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Gly Ser Tyr Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Asn Thr Phe
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Val Ser Pro Ile Ala Ala Pro Met Asp
115 120 125
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr
145 150 155 160
Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu
165 170 175
Ser Cys Arg Ala Ser Gln Leu Gly Ser Phe Tyr Leu Ala Trp Tyr Gln
180 185 190
Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ser
195 200 205
Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
210 215 220
Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val
225 230 235 240
Tyr Tyr Cys Gln His Tyr Asn Tyr Pro Pro Ser Phe Thr Phe Gly Gln
245 250 255
Gly Thr Lys Val Glu Ile Lys Glu Pro Lys Ser Pro Asp Lys Thr His
260 265 270
Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe
275 280 285
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ala Arg Thr Pro
290 295 300
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
305 310 315 320
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
325 330 335
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
340 345 350
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
355 360 365
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
370 375 380
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
385 390 395 400
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
405 410 415
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
420 425 430
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
435 440 445
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
450 455 460
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
465 470 475 480
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ile Tyr
485 490 495
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
500 505 510
Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
515 520 525
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
530 535 540
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
545 550 555 560
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
565 570 575
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
580 585 590
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
595 600 605
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
610 615 620
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
625 630 635 640
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
645 650 655
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
660 665 670
<210> 367
<211> 345
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полинуклеотид»
<220>
<221> модифицированное_основание
<222> (293)..(293)
<223> a, c, t, g, неизвестно или другое
<400> 367
gaggtgcagc tgctggaatc tggcggagga ctggtgcagc ctggcggctc tctgagactg 60
tcttgtgccg ccagcggctt caccttcagc agctacgcca tgaactgggt gcgccaggcc 120
cctggcaaag gcctggaatg ggtgtccgcc atcagcgata gcggcggcag cacctactac 180
gccgatagcg tgaagggccg gttcaccatc agccgggaca acagcaagaa caccctgtac 240
ctgcagatga acagcctgcg ggccgaggac accgccgtgt actactgtgc canatactgg 300
cccatggaca tctggggcca gggaaccttg gtcaccgtct cctca 345
<210> 368
<211> 324
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 368
gagatcgtgc tgacacagag ccctggcacc ctgagcctgt ctccaggcga aagagccacc 60
ctgtcctgca aagccagcca gagcgtgtcc agcagctacc tggcctggta tcagcaaaag 120
cccggccagg ctccccggct gctgatgtac gatgccagca tcagagccac cggcatcccc 180
gacagatttt ccggctctgg cagcggcacc gacttcaccc tgaccatcag cagactggaa 240
cccgaggact tcgccgtgta ctactgccag cagtacggca gctggcccct gacatttggc 300
cagggcacaa aggtggagat caaa 324
<210> 369
<211> 345
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 369
gaggtgcagc tgctggaatc tggcggagga ctggtgcagc ctggcggctc tctgagactg 60
tcttgtgccg ccagcggctt caccttcagc agctacgcca tgaactgggt gcgccaggcc 120
cctggtaaag gtttggaatg ggtttctgct attctgtcgt ctggtggttc tacttactat 180
gccgattctg ttaagggtag attcaccatt tctagagaca actctaagaa caccttgtac 240
ttgcaaatga actccttgag agctgaagat actgctgttt attactgtgc tagatactgg 300
ccaatggata tttggggtca aggtactctg gtcaccgtct cctca 345
<210> 370
<211> 324
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 370
gagatcgtgc tgacacagag ccctggcacc ctgagcctgt ctcctggtga aagagctact 60
ttgtcttgta gagggggtca atccgtttcc tcttcttatt tggcttggta tcaacaaaaa 120
ccaggtcaag ctccaagatt attgatgtac gatgcttcta ttagagccac cggtattcca 180
gatagatttt ctggttctgg ttccggtact gatttcactt tgactatctc tagattggaa 240
ccagaagatt tcgctgttta ctactgtcaa caatatcagt cttggccatt gacttttggt 300
caaggtacaa aggttgaaat caaa 324
<210> 371
<211> 345
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 371
gaggtgcagc tgctggaatc tggcggagga ctggtgcagc ctggcggctc tctgagactg 60
tcttgtgccg ccagcggctt caccttcagc agctacccta tgagctgggt gcgccaggcc 120
cctggcaaag gactggaatg ggtgtccgcc atcggaggct ctggcggcag cacctactac 180
gccgatagcg tgaagggccg gttcaccatc agccgggaca acagcaagaa caccctgtac 240
ctgcaaatga acagcctgcg ggccgaggac accgccgtgt actactgtgc cagatactgg 300
cccatggaca gctggggcca gggaactttg gtcaccgtct cctca 345
<210> 372
<211> 324
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 372
gagatcgtgc tgacacagag ccctggcacc ctgagcctgt ctccaggcga aagagccacc 60
ctgtcctgca aagccagcca gagcgtgtcc agcacatacc tggcctggta tcagcaaaag 120
cccggccagg ctccccggct gctgatctac gatgcctctt ctagagcccc tggcatcccc 180
gacagattca gcggctctgg cagcggcacc gacttcaccc tgaccatcag cagactggaa 240
cccgaggact tcgccgtgta ctactgccag cagtacagca ccagccccct gacctttggc 300
cagggcacaa aggtggagat caaa 324
<210> 373
<211> 345
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 373
gaggtgcagc tgctggaatc tggcggagga ctggtgcagc ctggcggctc tctgagactg 60
tcttgtgccg ccagcggctt caccttcagc agctacccta tgagctgggt gcgccaggcc 120
cctggtaaag gtttggaatg ggtttctgct attggtggtt caggtggttg gagttattat 180
gccgattctg ttaagggtag attcaccatt tctagagaca actctaagaa caccttgtac 240
ttgcaaatga actccttgag agctgaagat actgctgttt attactgtgc tagatactgg 300
ccaatggatt cttggggtca aggtactctg gtcaccgtct cctca 345
<210> 374
<211> 324
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 374
gagatcgtgc tgacacagag ccctggcacc ctgagcctgt ctcctggtga aagagctact 60
ttgtcttgtt ggttgtctca atctgtttcc tctacttact tggcttggta tcaacaaaaa 120
ccaggtcaag ctccaagatt attgatctac gatgcttctt ctagagcacc aggtattcca 180
gatagatttt ctggttctgg ttccggtact gatttcactt tgactatctc tagattggaa 240
ccagaagatt tcgctgttta ctactgccaa caatactctg agtggccatt gacttttggt 300
caaggtacaa aggttgaaat caaa 324
<210> 375
<211> 345
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 375
gaggtgcagc tgctggaatc tggcggagga ctggtgcagc ctggcggctc tctgagactg 60
tcttgtgccg ccagcggctt caccttcagc agctacgcca tgaactgggt gcgccaggcc 120
cctggtaaag gtttggaatg ggtttctgct atttctgatt ctggtggttc taggtggtat 180
gccgattctg ttaagggtag attcaccatt tctagagaca actctaagaa caccttgtac 240
ttgcaaatga actccttgag agctgaagat actgctgttt attactgtac gcggtactgg 300
ccaatggata tttggggtca aggtactctg gtcaccgtct cctca 345
<210> 376
<211> 324
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 376
gagatcgtgc tgacacagag ccctggcacc ctgagcctgt ctcctggtga aagagctact 60
ttgtcttgtt ggttgtctca atctgtttcc tctacttact tggcttggta tcaacaaaaa 120
ccaggtcaag ctccaagatt attgatctac gatgcttctt ctagagcacc aggtattcca 180
gatagatttt ctggttctgg ttccggtact gatttcactt tgactatctc tagattggaa 240
ccagaagatt tcgctgttta ctactgccaa caatactctg agtggccatt gacttttggt 300
caaggtacaa aggttgaaat caaa 324
<210> 377
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 377
Arg Ala Ser Gln Leu Gly Ser Phe Tyr Leu Ala
1 5 10
<210> 378
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 378
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Ala Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Leu Ser Trp Ser Gly Ala Phe Asp Asn Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 379
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 379
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asn Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Tyr Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Ser Pro Pro
85 90 95
Ser Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 380
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 380
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Phe Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Thr Val Gly Thr Ser Gly Ala Phe Gly Ile Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 381
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 381
Ser Tyr Ala Met Ser
1 5
<210> 382
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 382
Gly Phe Thr Phe Ser Ser Tyr Ala Met Ser
1 5 10
<210> 383
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 383
Ser Ala Ser Gly Gly Ser
1 5
<210> 384
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 384
Ala Ile Ser Ala Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 385
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 385
Leu Ser Trp Ser Gly Ala Phe Asp Asn
1 5
<210> 386
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 386
Ser Tyr Ala Met Ser
1 5
<210> 387
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 387
Gly Phe Thr Phe Arg Ser Tyr
1 5
<210> 388
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 388
Gly Phe Thr Phe Arg Ser Tyr Ala Met Ser
1 5 10
<210> 389
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 389
Ser Gly Ser Gly Gly Ser
1 5
<210> 390
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 390
Ala Ile Ser Gly Ser Gly Gly Ser Thr Phe Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 391
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 391
Val Gly Thr Ser Gly Ala Phe Gly Ile
1 5
<210> 392
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 392
Gly Ala Ser Ser Arg Ala Tyr
1 5
<210> 393
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 393
Gln His Tyr Gly Ser Pro Pro Leu Phe Thr
1 5 10
<210> 394
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 394
Arg Ala Ser Gln Asn Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 395
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 395
Gly Ala Ser Tyr Arg Ala Thr
1 5
<210> 396
<211> 519
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 396
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Leu Ser Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Tyr Trp Pro Met Asp Ile Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly
145 150 155 160
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Gly
165 170 175
Gly Gln Ser Val Ser Ser Ser Tyr Leu Ala Trp Tyr Gln Gln Lys Pro
180 185 190
Gly Gln Ala Pro Arg Leu Leu Met Tyr Asp Ala Ser Ile Arg Ala Thr
195 200 205
Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
210 215 220
Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys
225 230 235 240
Gln Gln Tyr Gln Ser Trp Pro Leu Thr Phe Gly Gln Gly Thr Lys Val
245 250 255
Glu Ile Lys Gly Ser Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro
260 265 270
Ser Leu Cys Ser Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser
275 280 285
Leu Cys Ser Gly Gly Gly Gly Ser Thr Thr Thr Pro Ala Pro Arg Pro
290 295 300
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
305 310 315 320
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
325 330 335
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
340 345 350
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly
355 360 365
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
370 375 380
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
385 390 395 400
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
405 410 415
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
420 425 430
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
435 440 445
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
450 455 460
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
465 470 475 480
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
485 490 495
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
500 505 510
Met Gln Ala Leu Pro Pro Arg
515
<210> 397
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 397
Cys Pro Tyr Ser Asn Pro Ser Leu Cys
1 5
<210> 398
<211> 37
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 398
Gly Ser Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys
1 5 10 15
Ser Gly Gly Gly Gly Ser Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser
20 25 30
Gly Gly Gly Gly Ser
35
<210> 399
<211> 1497
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 399
atggcactgc ctgtgaccgc cctgctgctg ccactggccc tgctgctgca cgccgcccgg 60
ccagaggtgc agctgctgga gagcggagga ggactggtgc agccaggagg aagcctgaga 120
ctgtcctgcg ccgcctctgg cttcaccttc agctcctacg ccatgaactg ggtgaggcag 180
gcaccaggca agggactgga gtgggtgtct gccatcctgt ctagcggcgg cagcacctac 240
tatgccgatt ccgtgaaggg ccgcttcaca atcagccggg acaactccaa gaataccctg 300
tacctgcaga tgaacagcct gagagccgag gatacagccg tgtactattg cgccaggtat 360
tggcccatgg acatctgggg ccagggcaca ctggtgaccg tgtcctctgg aggaggagga 420
tccggcggag gaggctctgg cggcggcggc agcgagatcg tgctgacaca gagcccaggc 480
accctgagcc tgtcccctgg agagagagcc accctgtctt gtaggggcgg ccagagcgtg 540
agctcctctt acctggcctg gtatcagcag aagccaggcc aggcccccag actgctgatg 600
tacgacgcct ccatcagggc aacaggcatc cccgatcggt tctctggaag cggatccgga 660
accgacttta cactgaccat ctccaggctg gagcctgagg atttcgccgt gtactattgc 720
cagcagtacc agtcttggcc actgacattt ggccagggca ccaaggtgga gatcaaggga 780
tccggaggag gaggatcttg cccttattcc aacccatctc tgtgcaccac aacccctgca 840
ccaaggccac ctacaccagc acctaccatc gcctctcagc cactgagcct gagacccgag 900
gcctgtaggc ctgcagcagg aggagcagtg cacacacggg gactggactt tgcctgcgat 960
atctacatct gggcacctct ggcaggaaca tgtggcgtgc tgctgctgag cctggtcatc 1020
accctgtact gcaagagagg caggaagaag ctgctgtata tcttcaagca gccctttatg 1080
cgccctgtgc agacaaccca ggaggaggat ggctgctcct gtaggttccc agaagaggag 1140
gagggaggat gtgagctgcg cgtgaagttt tctcggagcg ccgacgcacc tgcataccag 1200
cagggacaga atcagctgta taacgagctg aatctgggcc ggagagagga gtatgacgtg 1260
ctggataaga ggaggggaag ggacccagag atgggaggca agccacggag aaagaacccc 1320
caggagggcc tgtacaatga gctgcagaag gataagatgg ccgaggccta tagcgagatc 1380
ggcatgaagg gagagaggcg ccggggcaag ggacacgacg gactgtacca gggactgtcc 1440
acagccacca aggacaccta tgatgccctg cacatgcagg ccctgccacc aaggtga 1497
<210> 400
<211> 157
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 400
Met Gly Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Asp His Ala Asp Ala Cys Pro Tyr Ser Asn Pro Ser Leu Cys Ser Gly
20 25 30
Gly Gly Gly Ser Glu Leu Pro Thr Gln Gly Thr Phe Ser Asn Val Ser
35 40 45
Thr Asn Val Ser Pro Ala Lys Pro Thr Thr Thr Ala Cys Pro Tyr Ser
50 55 60
Asn Pro Ser Leu Cys Ser Gly Gly Gly Gly Ser Pro Ala Pro Arg Pro
65 70 75 80
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
85 90 95
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
100 105 110
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
115 120 125
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Asn His Arg
130 135 140
Asn Arg Arg Arg Val Cys Lys Cys Pro Arg Pro Val Val
145 150 155
<210> 401
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 401
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Tyr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Ser Pro Pro
85 90 95
Leu Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 402
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 402
Asp Phe Tyr Met Asn
1 5
<210> 403
<211> 19
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 403
Phe Ile Arg Asp Lys Ala Lys Gly Tyr Thr Thr Glu Tyr Asn Pro Ser
1 5 10 15
Val Lys Gly
<210> 404
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 404
Glu Gly His Thr Ala Ala Pro Phe Asp Tyr
1 5 10
<210> 405
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 405
Lys Ala Ser Gln Asn Ile Asp Lys Tyr Leu Asn
1 5 10
<210> 406
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 406
Asn Thr Asn Asn Leu Gln Thr
1 5
<210> 407
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 407
Leu Gln His Ile Ser Arg Pro Arg Thr
1 5
<210> 408
<211> 451
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 408
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Arg Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Thr Phe Thr Asp Phe
20 25 30
Tyr Met Asn Trp Val Arg Gln Pro Pro Gly Arg Gly Leu Glu Trp Ile
35 40 45
Gly Phe Ile Arg Asp Lys Ala Lys Gly Tyr Thr Thr Glu Tyr Asn Pro
50 55 60
Ser Val Lys Gly Arg Val Thr Met Leu Val Asp Thr Ser Lys Asn Gln
65 70 75 80
Phe Ser Leu Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Ala Arg Glu Gly His Thr Ala Ala Pro Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Ser Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 409
<211> 1353
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 409
caagtgcagc ttcaagaatc cggccctggt ctggtccgcc cctcccaaac cctctccctg 60
acatgcaccg tgtcgggatt cacctttacc gatttctaca tgaactgggt ccggcagccg 120
cccggaagag gtctggagtg gatcggcttc attcgggaca aagccaaggg gtacaccacc 180
gagtacaacc cgtccgtgaa gggacgcgtg actatgctcg tggacacgtc caagaaccag 240
ttcagcttga ggctgagcag cgtgactgcc gcggataccg cagtgtacta ctgtgcccgg 300
gaagggcaca ctgccgctcc attcgactat tggggccagg gatcactggt cactgtgtcg 360
tccgcctcca ccaagggccc atcggtcttc cccctggcac cctcctccaa gagcacctct 420
gggggcacag cggccctggg ctgcctggtc aaggactact tccccgaacc ggtgacggtg 480
tcgtggaact caggcgccct gaccagcggc gtgcacacct tcccggctgt cctacagtcc 540
tcaggactct actccctcag cagcgtagtg accgtgccct ccagcagctt gggcacccag 600
acctacatct gcaacgtgaa tcacaagccc agcaacacca aggtggacaa gaaagttgag 660
cccaaatctt gtgacaaaac tcacacatgc ccaccgtgcc cagcacctga actcctgggg 720
ggaccgtcag tcttcctctt ccccccaaaa cccaaggaca ccctcatgat ctcccggacc 780
cctgaggtca catgcgtggt ggtggacgtg agccacgaag accctgaggt caagttcaac 840
tggtacgtgg acggcgtgga ggtgcataat gccaagacaa agccgcggga ggagcagtac 900
aacagcacgt accgtgtggt cagcgtcctc accgtcctgc accaggactg gctgaatggc 960
aaggagtaca agtgcaaggt ctccaacaaa gccctcccag cccccatcga gaaaaccatc 1020
tccaaagcca aagggcagcc ccgagaacca caggtgtaca ccctgccccc atcccgggac 1080
gagctgacca agaaccaggt cagcctgacc tgcctggtca aaggcttcta tcccagcgac 1140
atcgccgtgg agtgggagag caatgggcag ccggagaaca actacaagac cacgcctccc 1200
gtgctggact ccgacggctc cttcttcctc tatagcaagc tcaccgtgga caagagcagg 1260
tggcagcagg ggaacgtctt ctcatgctcc gtgatgcatg aggctctgca caaccactac 1320
acgcagaaga gcctctccct gtctccggga aaa 1353
<210> 410
<211> 214
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 410
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Ile Asp Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asn Thr Asn Asn Leu Gln Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Leu Gln His Ile Ser Arg Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 411
<211> 699
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 411
atgggatgga gctgtatcat cctcttcttg gtagcaacag ctacaggcgt gcactccgac 60
atccaaatga cccaatcccc atcctcactt tccgcctccg tgggcgaccg cgtgactatt 120
acctgtaaag cgtcacagaa tatcgacaag tacctgaact ggtaccagca gaagcctgga 180
aaggccccca agctcctgat ctacaacacc aacaacttgc agactggagt gccgagcaga 240
ttttccggct ccggctcggg gactgatttc accttcacca tctcgagcct gcagccggag 300
gatattgcta cctattactg cctgcaacac attagccggc ccaggacgtt cggacagggt 360
accaaggtcg aaatcaagcg tacggtggct gcaccatctg tcttcatctt cccgccatct 420
gatgagcagt tgaaatctgg aactgcctct gttgtgtgcc tgctgaataa cttctatccc 480
agagaggcca aagtacagtg gaaggtggat aacgccctcc aatcgggtaa ctcccaggag 540
agtgtcacag agcaggacag caaggacagc acctacagcc tcagcagcac cctgacgctg 600
agcaaagcag actacgagaa acacaaagtc tacgcctgcg aagtcaccca tcagggcctg 660
agctcgcccg tcacaaagag cttcaacagg ggagagtgt 699
<210> 412
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 412
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Gly Ser Tyr
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Asn Thr Phe Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Ser Pro Ile Ala Ala Leu Met Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 413
<211> 113
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 413
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Gly Gly Ser Gly Gly Ser Leu Pro Tyr Ala Asp Ser Val
50 55 60
Lys Gly Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu Gln
65 70 75 80
Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg
85 90 95
Tyr Trp Pro Met Asp Ser Trp Gly Gln Gly Thr Leu Val Thr Val Ser
100 105 110
Ser
<210> 414
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
полипептид»
<400> 414
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Val
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Asp Ala Ser Ser Arg Ala Pro Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Ser Thr Trp Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 415
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 415
Arg Ala Ser Gln Ser Val Ser Pro His Tyr Leu Ala
1 5 10
<210> 416
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 416
Lys Phe Tyr Pro Tyr Pro Pro Ser Phe Thr
1 5 10
<210> 417
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности: синтетический
пептид»
<400> 417
Arg Ala Ser Gln Asn Val Ser Ser Ser Tyr Leu Ala
1 5 10
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ И СВЯЗЫВАЮЩИЕ АГЕНТЫ, НАЦЕЛЕННЫЕ НА DLL3 | 2020 |
|
RU2822366C2 |
| CD20 ТЕРАПИЯ, CD22 ТЕРАПИЯ И КОМБИНИРОВАННАЯ ТЕРАПИЯ КЛЕТКАМИ, ЭКСПРЕССИРУЮЩИМИ ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР (CAR) K CD19 | 2016 |
|
RU2752918C2 |
| Т-КЛЕТКИ С КОСТИМУЛИРУЮЩИМ ХИМЕРНЫМ АНТИГЕННЫМ РЕЦЕПТОРОМ, НАЦЕЛЕННЫЕ НА IL13Rα2 | 2015 |
|
RU2749922C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ ДЛЯ ЛЕЧЕНИЯ РАКА | 2017 |
|
RU2826270C2 |
| Т-КЛЕТКИ С ХИМЕРНЫМИ АНТИГЕННЫМИ РЕЦЕПТОРАМИ (CAR-T) ДЛЯ ЛЕЧЕНИЯ РАКА | 2019 |
|
RU2811466C2 |
| Т-КЛЕТКИ, МОДИФИЦИРОВАННЫЕ ХИМЕРНЫМ РЕЦЕПТОРОМ АНТИГЕНА, НАЦЕЛЕННЫМ НА CS1, ДЛЯ ЛЕЧЕНИЯ АМИЛОИДОЗА AL | 2018 |
|
RU2774895C2 |
| Химерные антигенные рецепторы, нацеливающиеся на CD70 | 2019 |
|
RU2801824C2 |
| ВИДЫ КОМБИНИРОВАННОЙ ТЕРАПИИ С ИСПОЛЬЗОВАНИЕМ ХИМЕРНЫХ АНТИГЕННЫХ РЕЦЕПТОРОВ И ИНГИБИТОРОВ PD-1 | 2017 |
|
RU2809160C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ИЗБИРАТЕЛЬНОЙ ЭКСПРЕССИИ БЕЛКА | 2017 |
|
RU2795467C2 |
| ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР (CAR) ПРОТИВ CD123 ДЛЯ ИСПОЛЬЗОВАНИЯ В ЛЕЧЕНИИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ | 2015 |
|
RU2724999C2 |
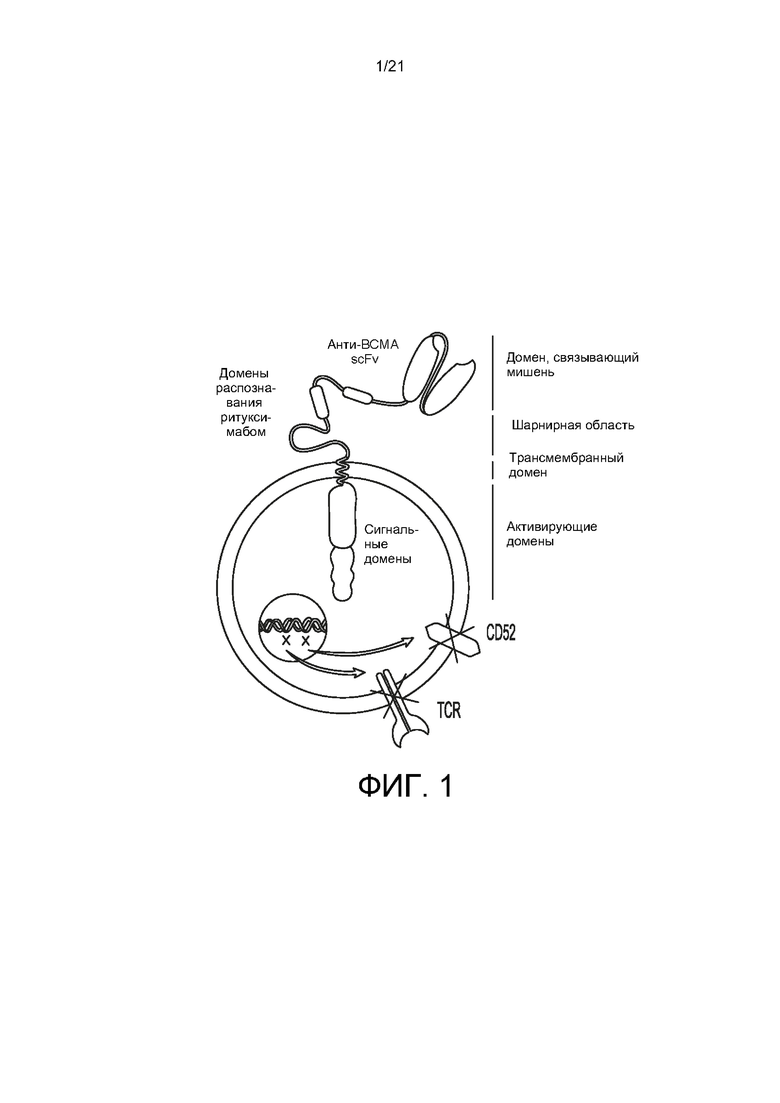
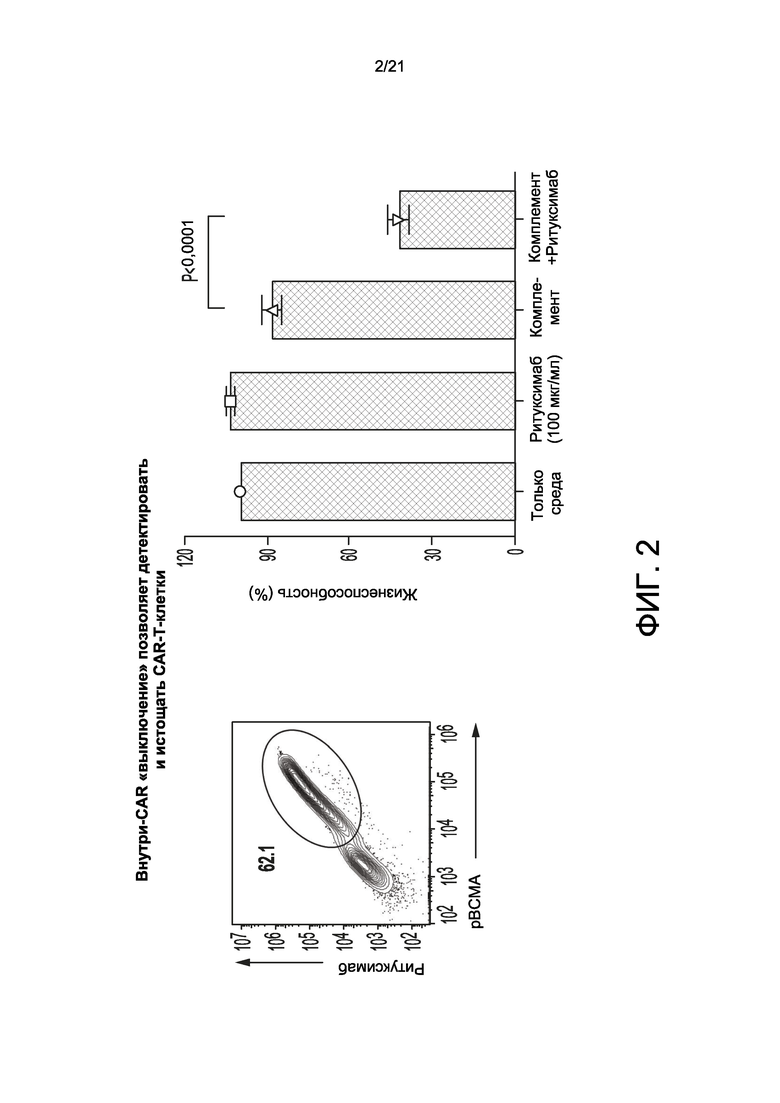
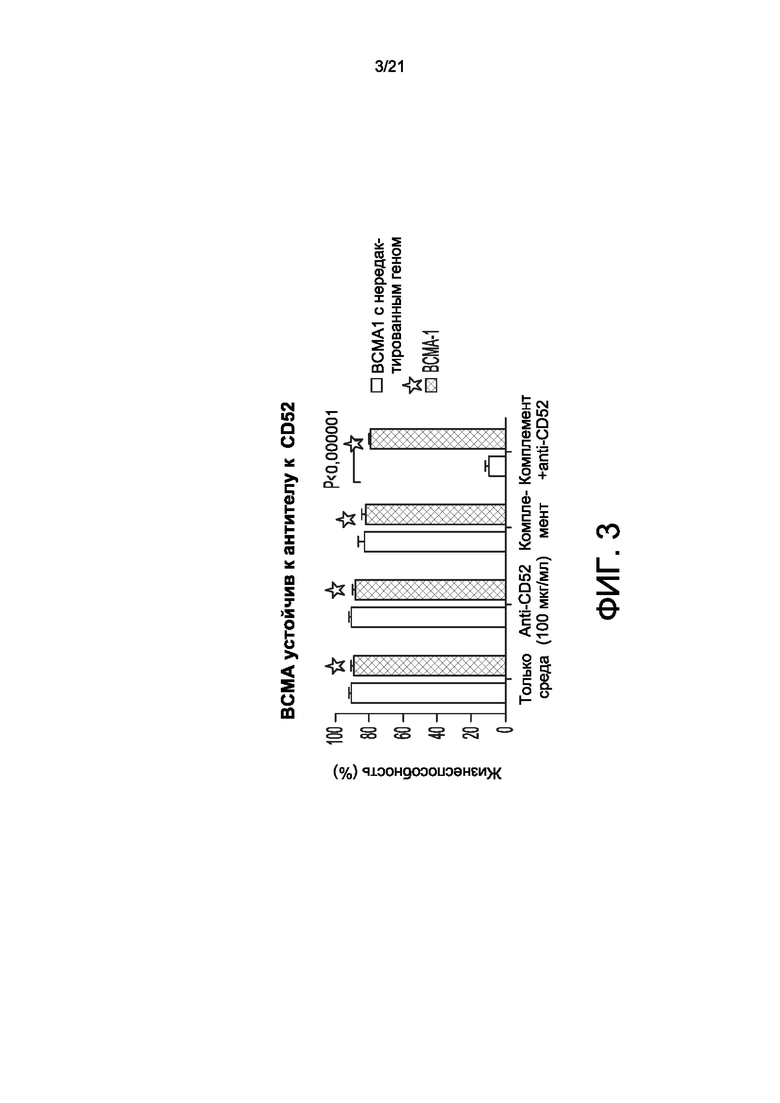
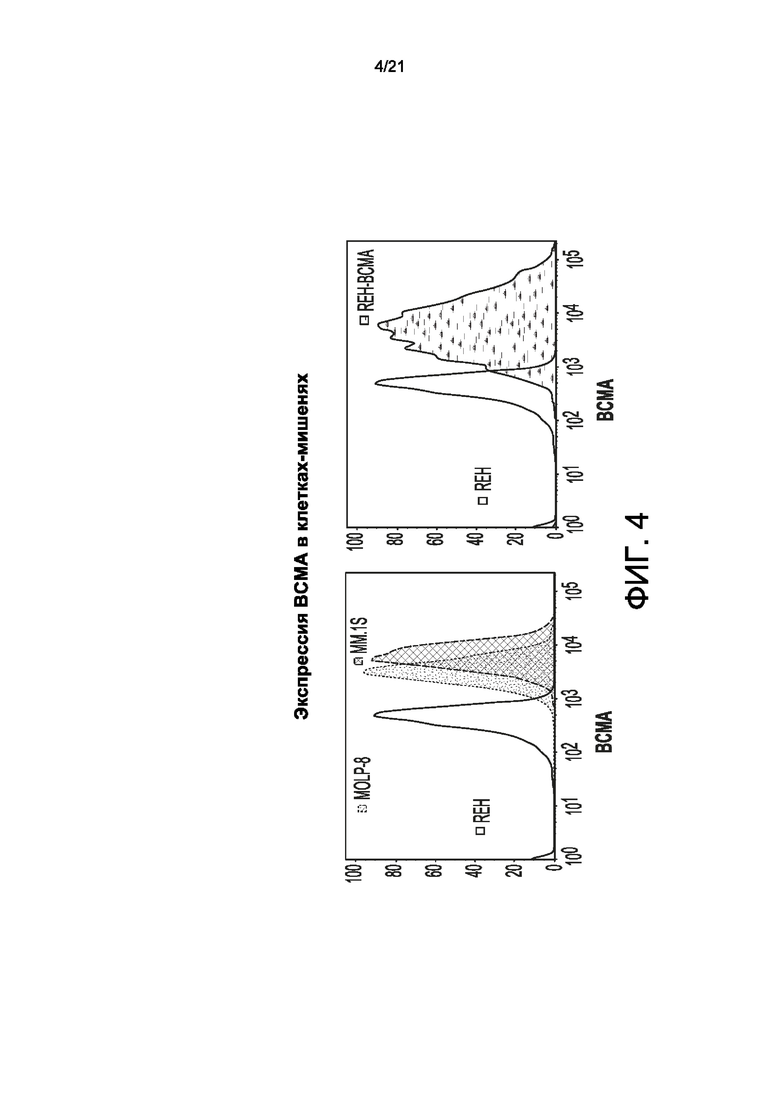
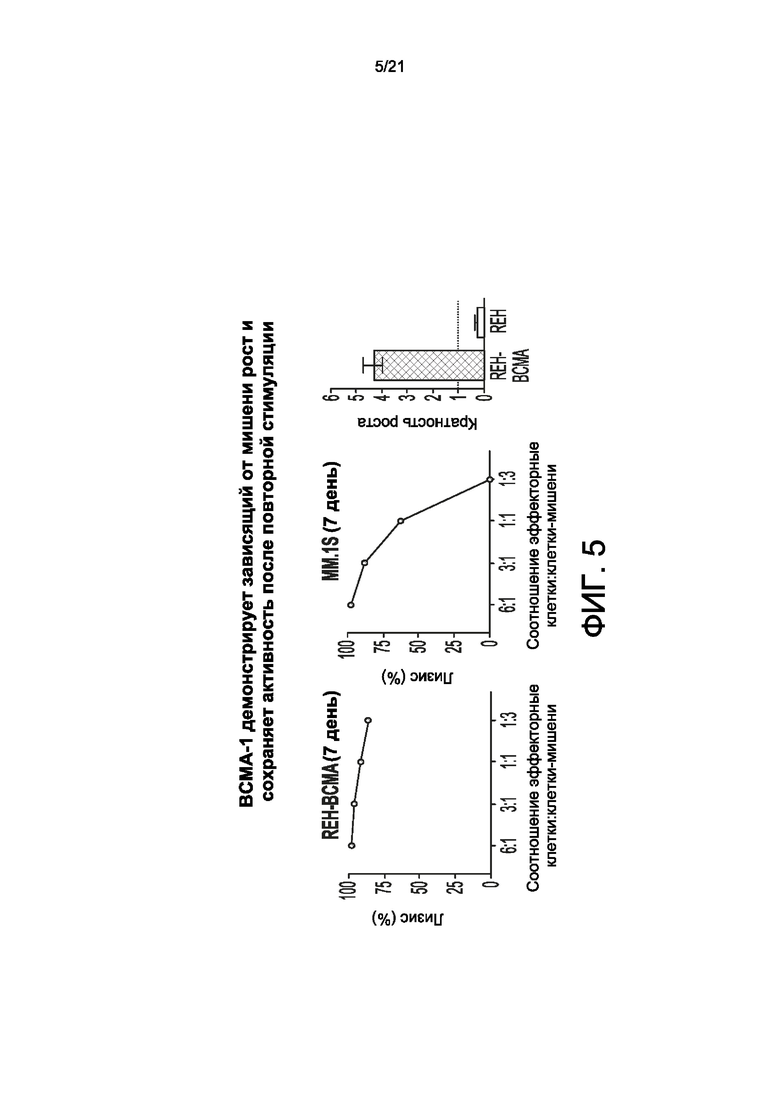

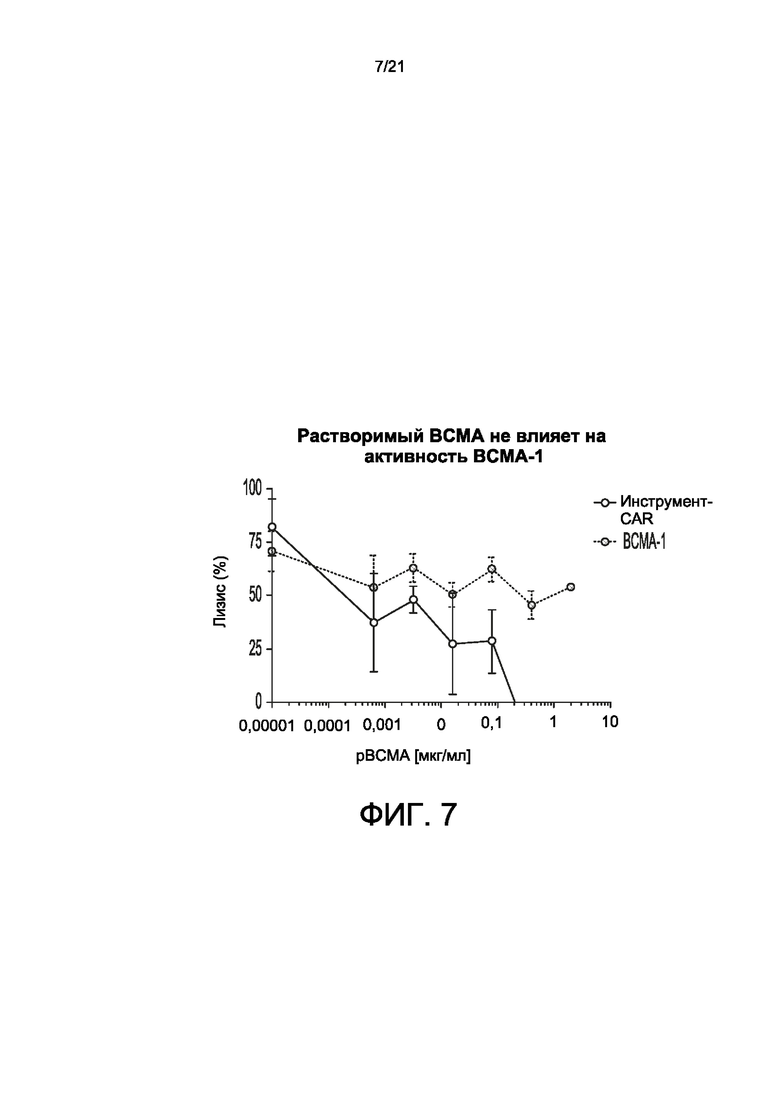
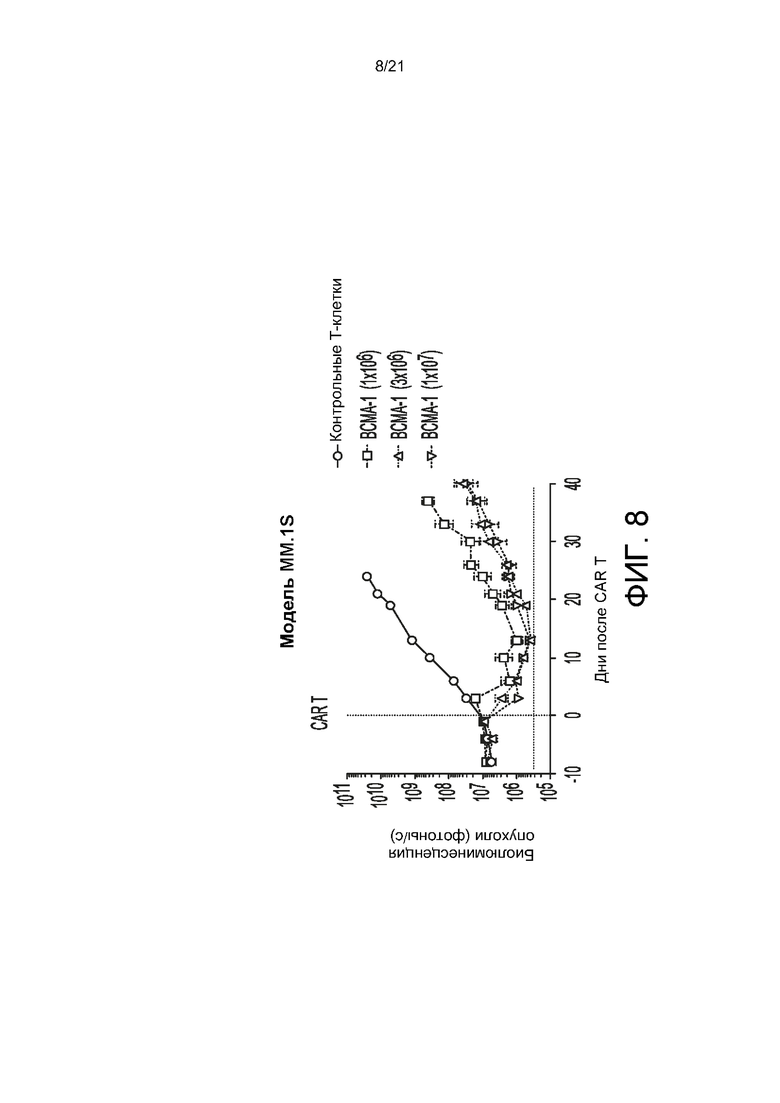
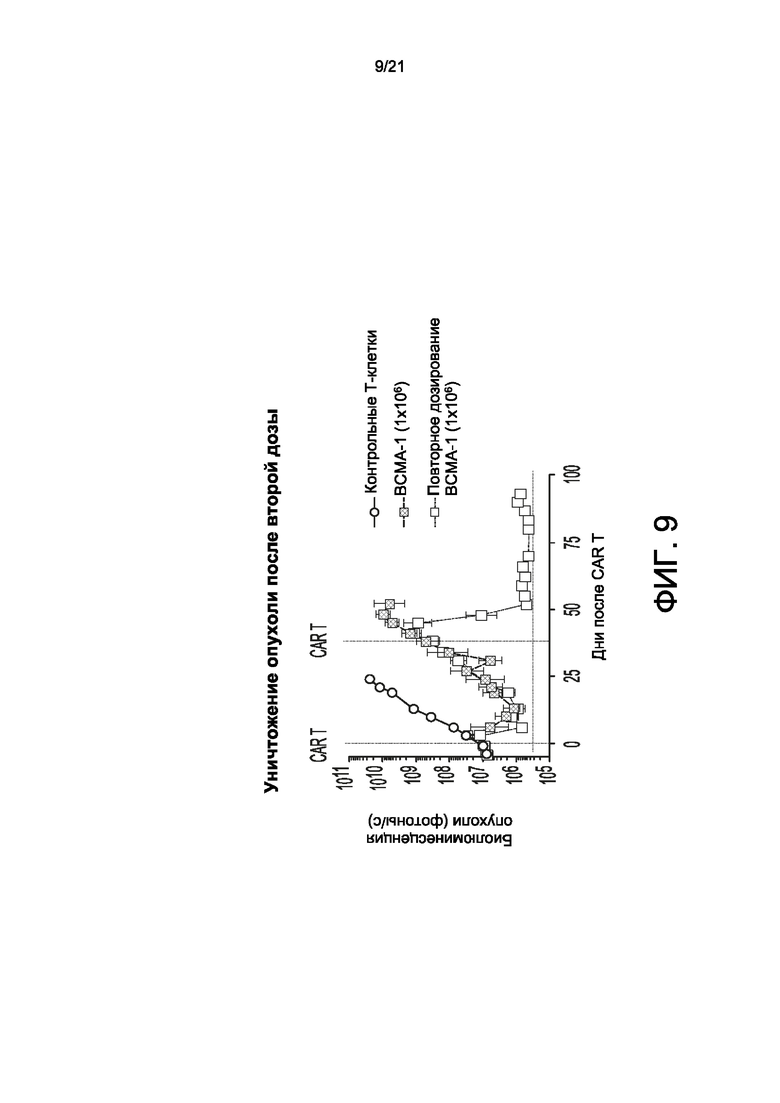
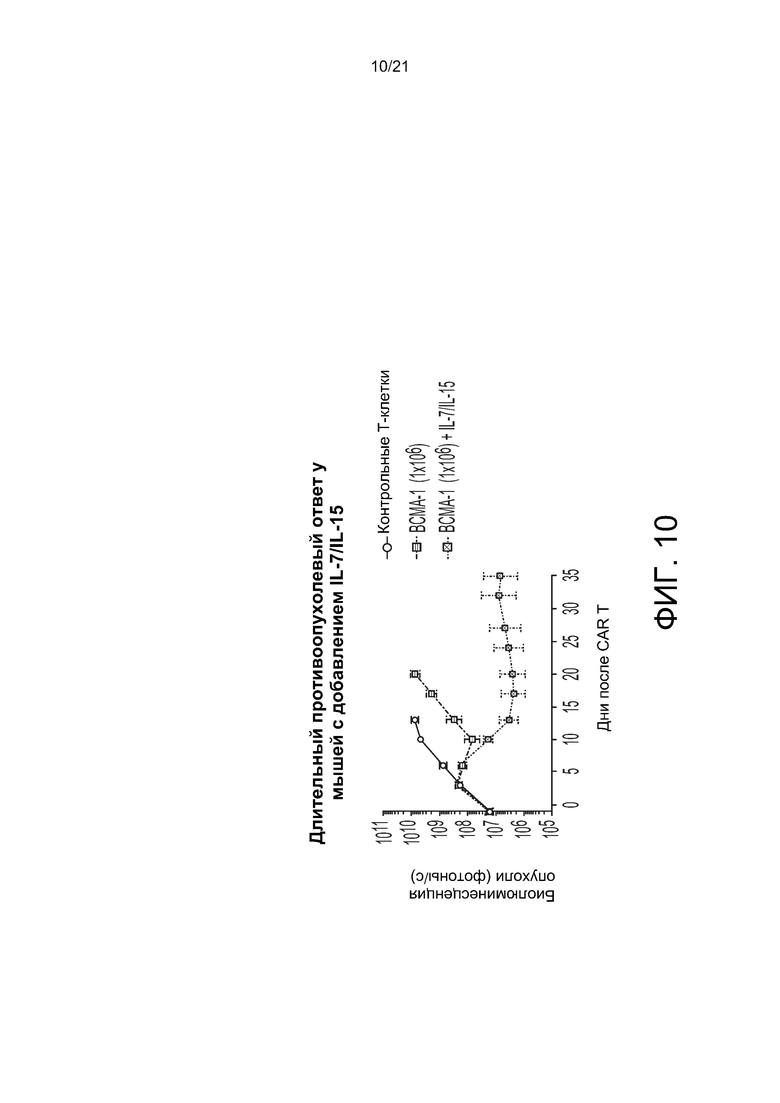
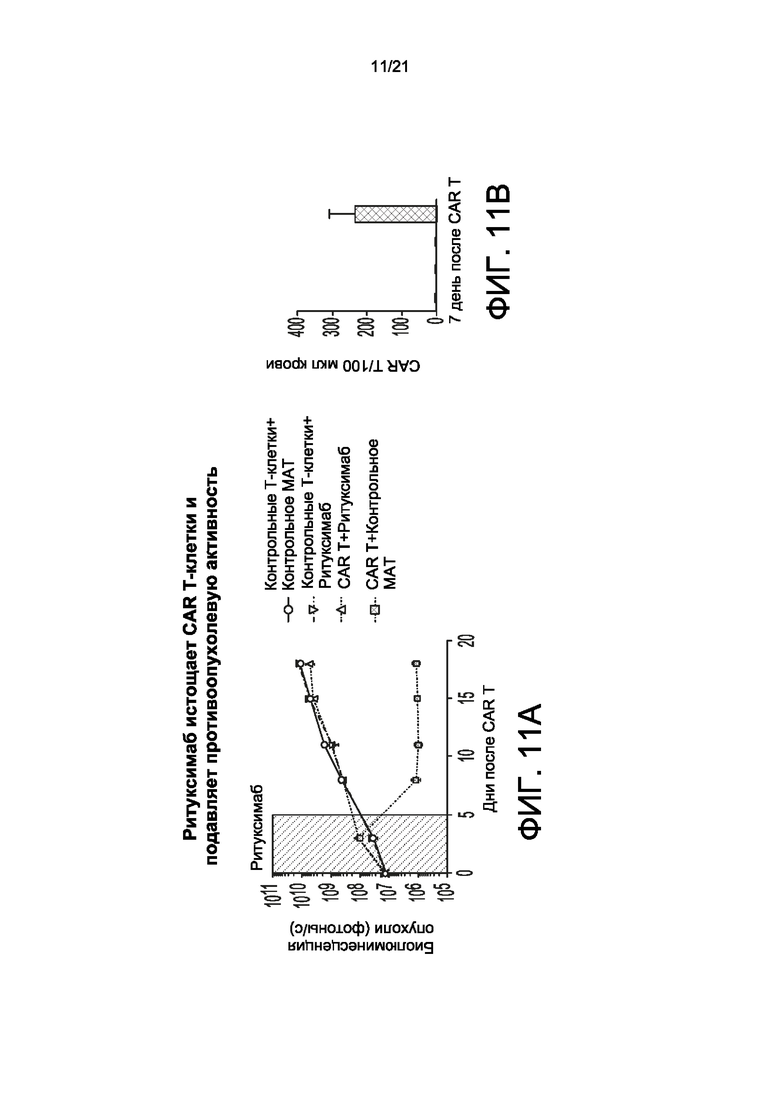
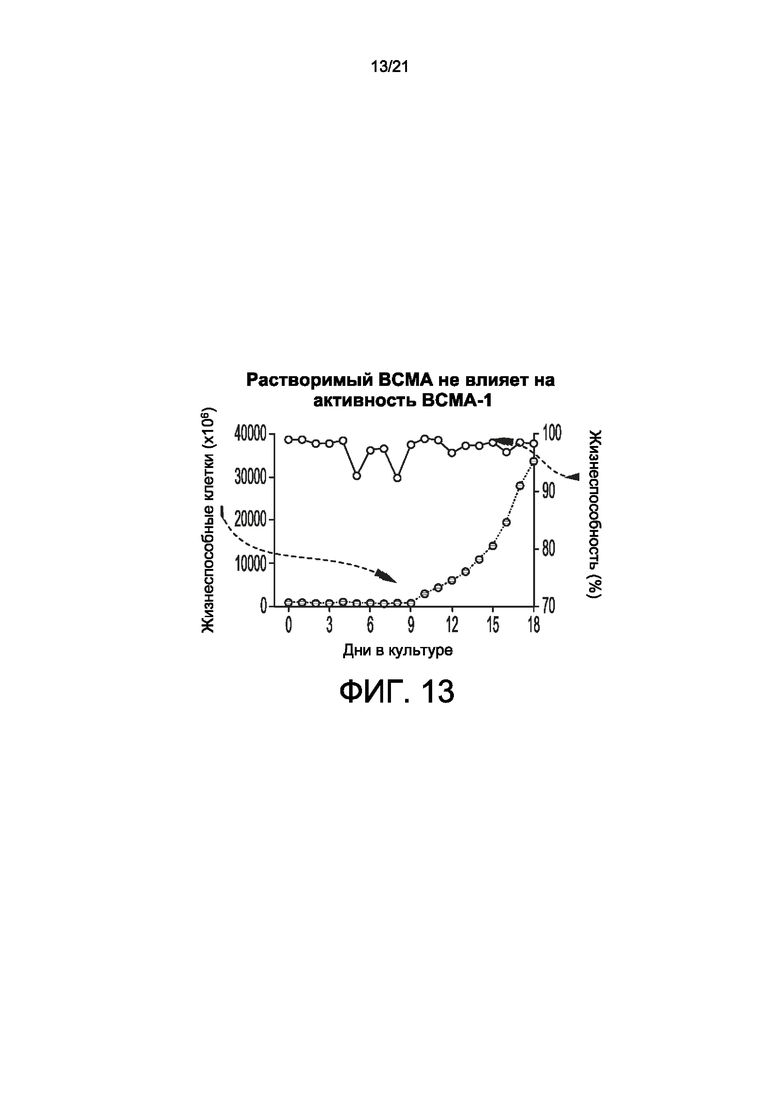
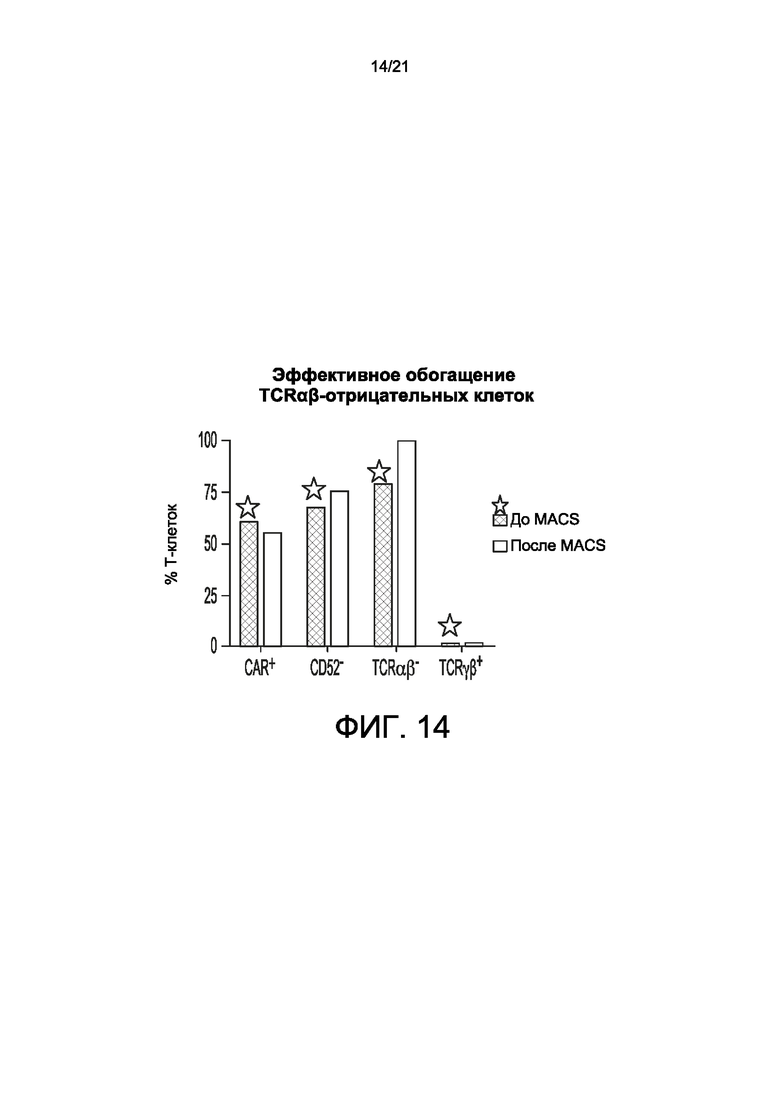
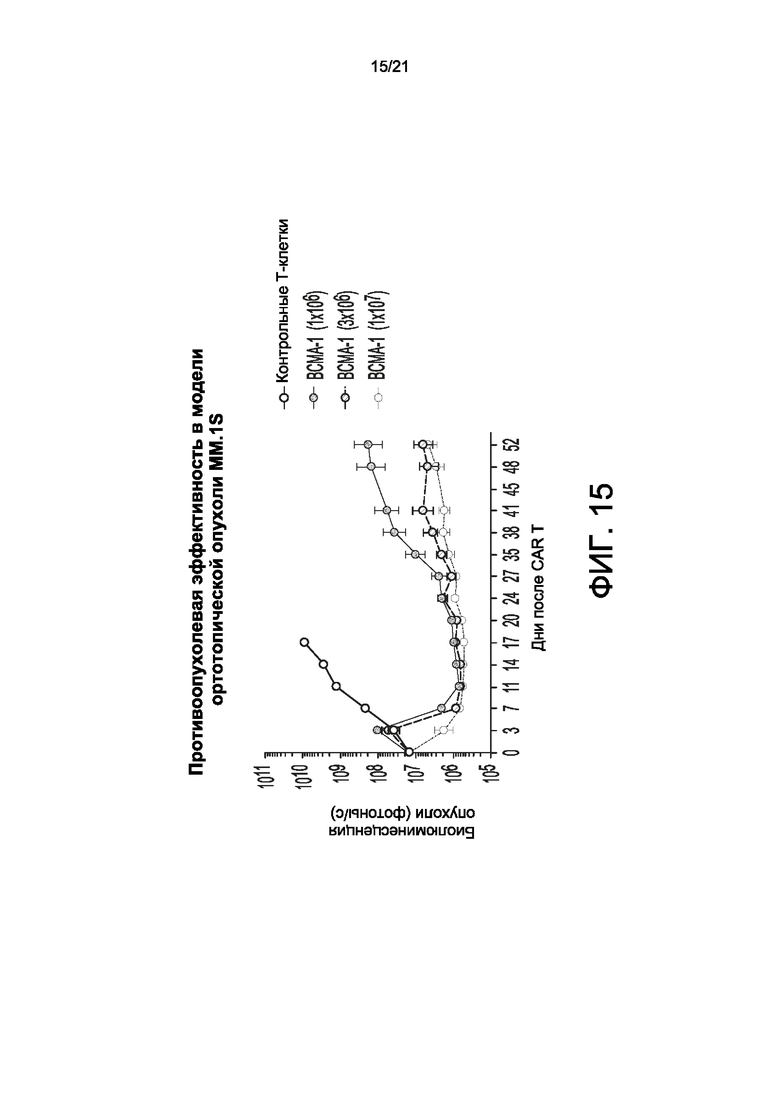
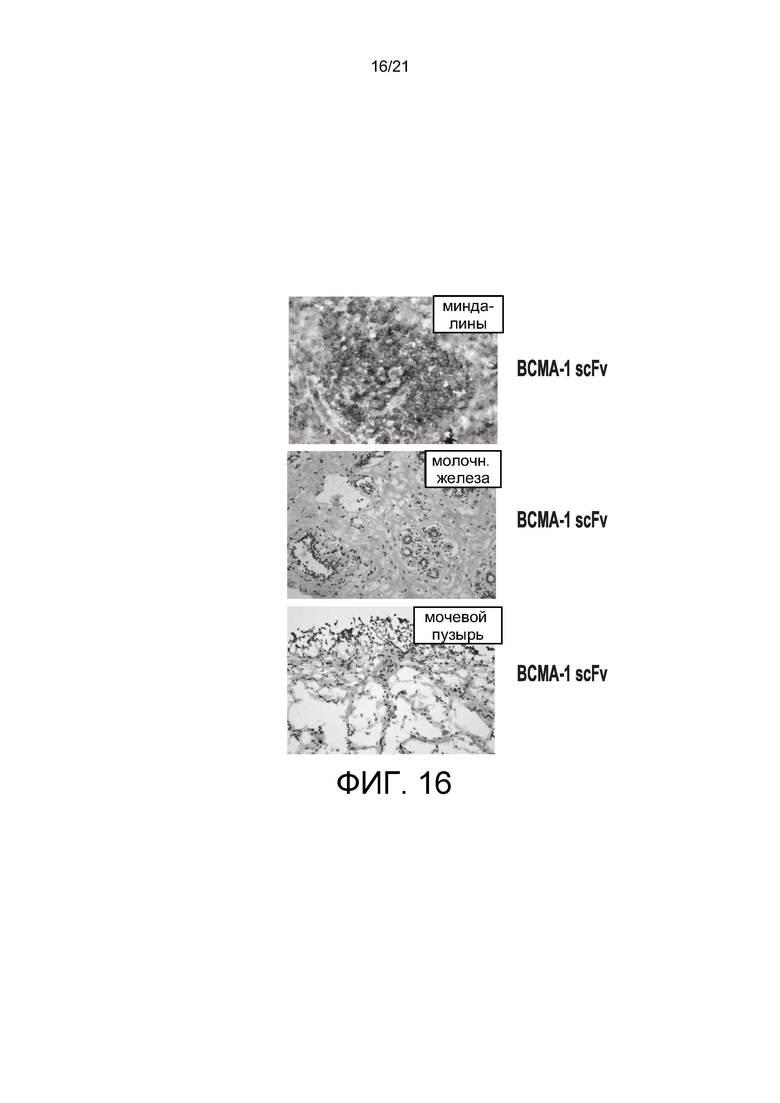

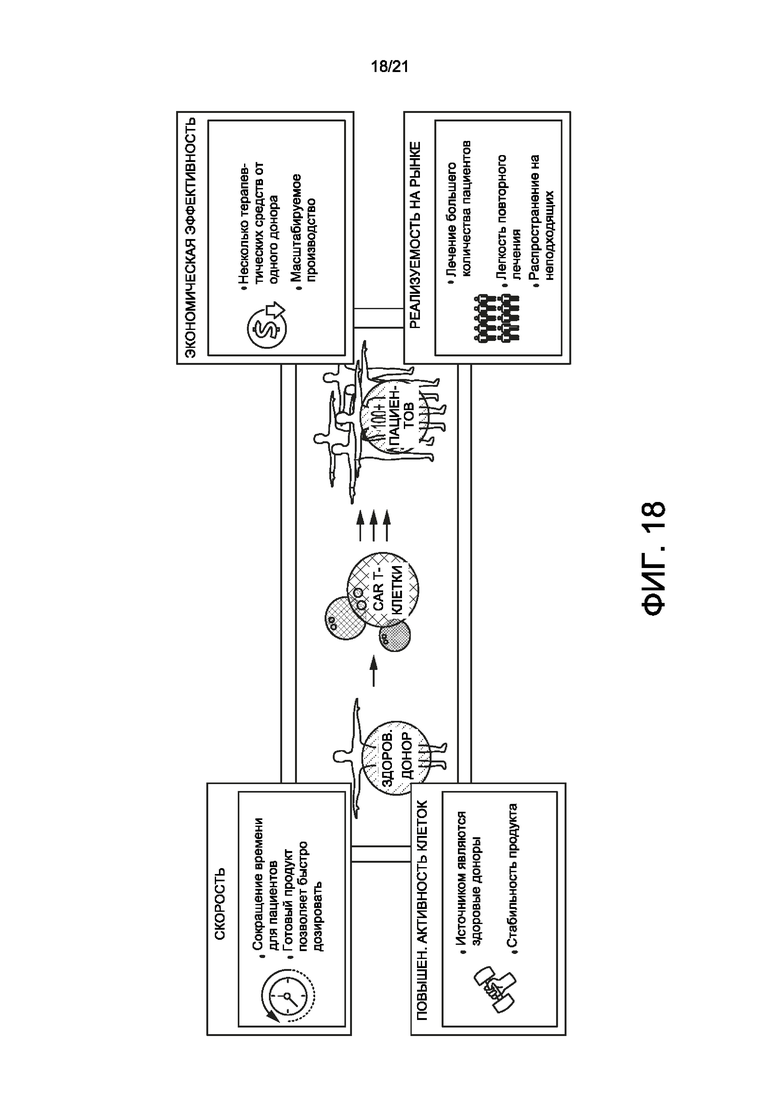
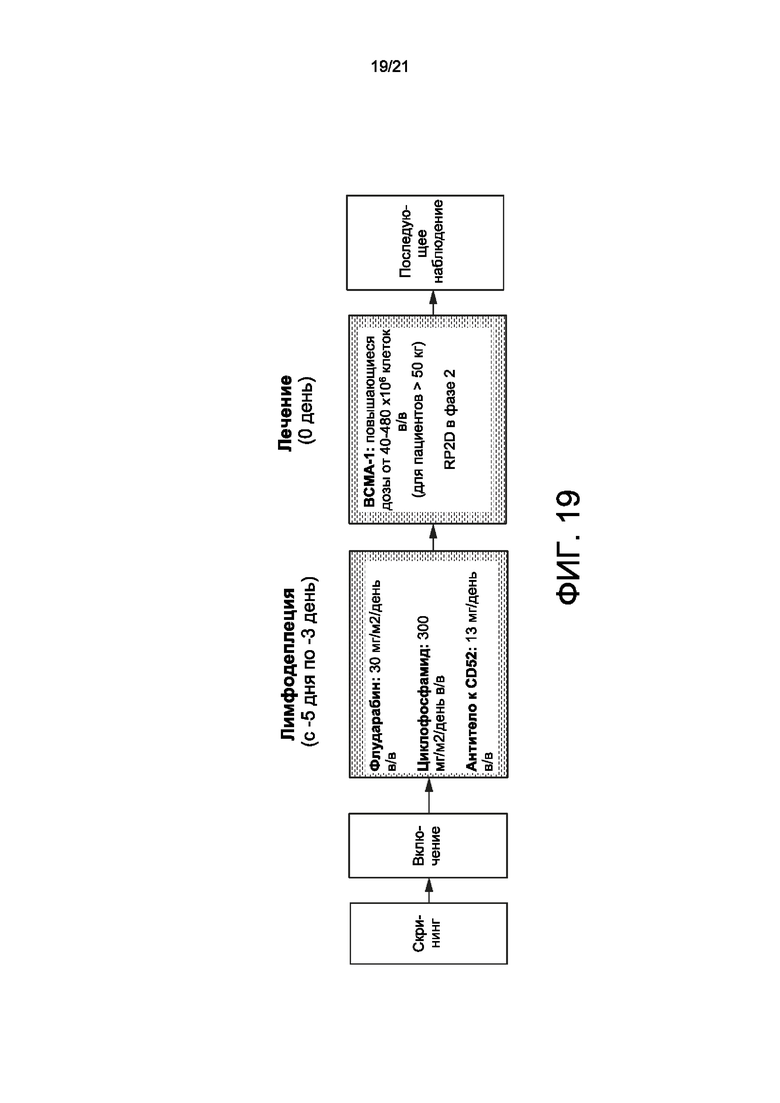

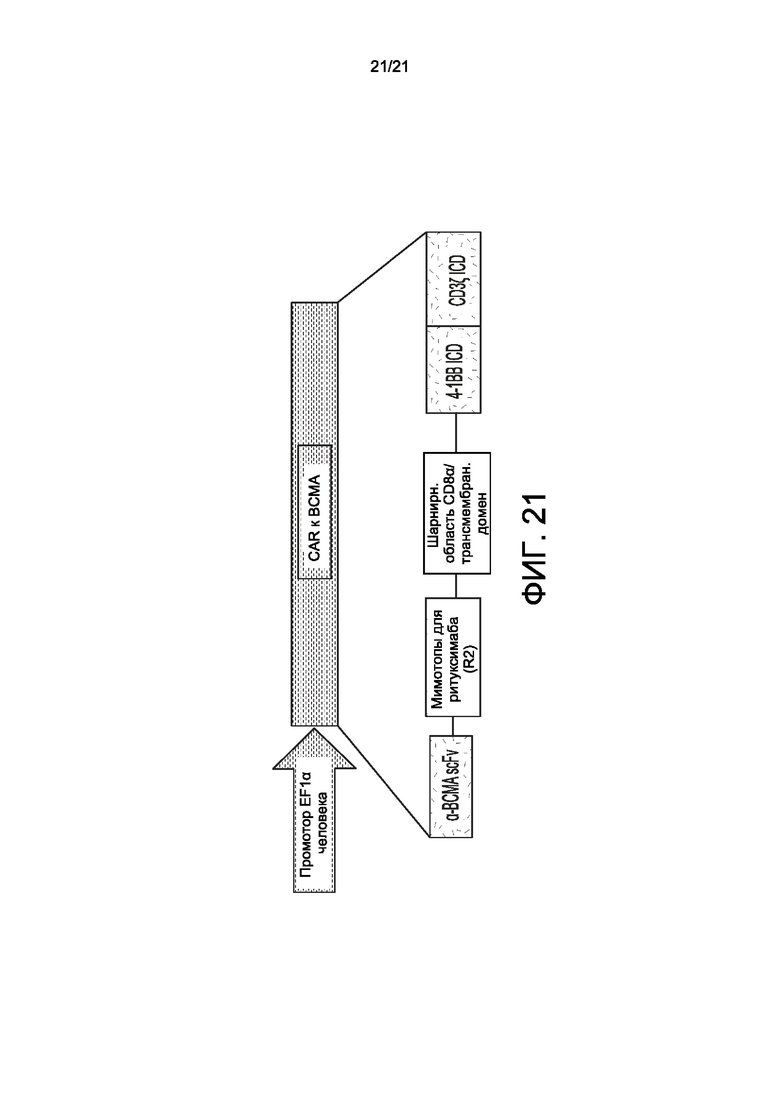
Настоящее изобретение относится к области биотехнологии, в частности к применению аллогенных Т-клеток с химерными антигенными рецепторами (CAR) к BCMA человека для терапии множественной миеломы у субъекта. В некоторых вариантах реализации предложены конкретные режимы дозирования, режимы повторного дозирования и комбинированные с лимфодеплецией режимы для терапии множественной миеломы у нуждающихся в этом субъектов. Изобретение эффективно для CAR-T-терапии множественной миеломы. 36 з.п. ф-лы, 21 ил., 9 табл., 4 пр.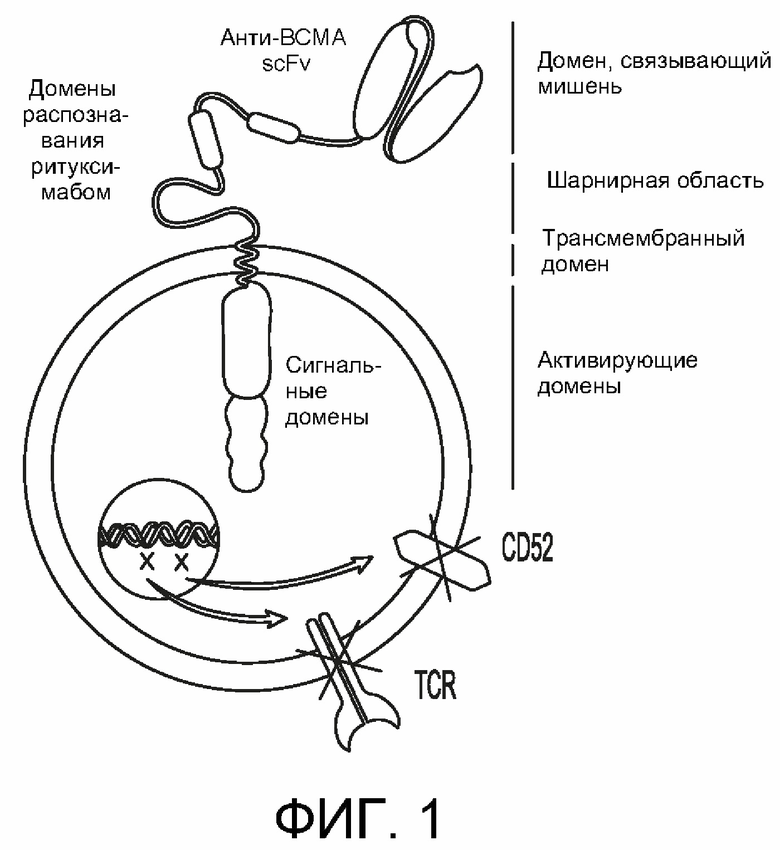
1. Применение аллогенных Т-клеток с химерными антигенными рецепторами (CAR) в по меньшей мере одной дозе, составляющей 320 × 106 клеток/доза или 480 ×106 клеток/доза, для лечения множественной миеломы у субъекта, причем аллогенные CAR-T-клетки содержат CAR к ВСМА человека (ВСМА CAR-T-клетки), причем CAR к ВСМА содержит внеклеточный связывающий домен, содержащий одноцепочечный Fv-фрагмент (scFv), при этом указанный scFv содержит вариабельную область тяжелой цепи (VH) и вариабельную область легкой цепи (VL), причем указанная VH-область содержит определяющий комплементарность участок-1 VH (CDR1 VH), определяющий комплементарность участок-2 VH (CDR2 VH) и определяющий комплементарность участок-3 VH (CDR3 VH) и указанная VL-область содержит определяющий комплементарность участок-1 VL (CDR1 VL), определяющий комплементарность участок-2 VL (CDR2 VL) и определяющий комплементарность участок-3 VL (CDR3 VL), где CDR1 VH содержит аминокислотную последовательность SEQ ID NO: 150, 151 или 152; CDR2 VH содержит аминокислотную последовательность SEQ ID NO: 153 или 154; CDR3 VH содержит аминокислотную последовательность SEQ ID NO: 155; CDR1 VL содержит аминокислотную последовательность SEQ ID NO: 209; CDR2 VL содержит аминокислотную последовательность SEQ ID NO: 221; и CDR3 VL содержит аминокислотную последовательность SEQ ID NO: 222.
2. Применение по п. 1, отличающееся тем, что по меньшей мере одна доза ВСМА CAR-Т-клеток составляет 320 × 106 клеток/доза.
3. Применение по п. 1, отличающееся тем, что по меньшей мере одна доза составляет 480 × 106 клеток/доза.
4. Применение по любому из пп. 1-3, отличающееся тем, что по меньшей мере одна доза представляет собой по меньшей мере одну постоянную дозу.
5. Применение по любому из пп. 1-4, отличающееся тем, что множественная миелома представляет собой рефрактерную множественную миелому.
6. Применение по любому из пп. 1-4, отличающееся тем, что множественная миелома представляет собой рецидивирующую множественную миелому.
7. Применение по любому из пп. 1-4, отличающееся тем, что множественная миелома представляет собой рефрактерную и рецидивирующую множественную миелому.
8. Применение по любому из пп. 1-4, отличающееся тем, что субъект не получал никакой предшествующей терапии множественной миеломы.
9. Применение по любому из пп. 1-4, отличающееся тем, что субъект получил по меньшей мере один, два или три вида предшествующей терапии множественной миеломы.
10. Применение по любому из пп. 1-9, отличающееся тем, что VH-область содержит SEQ ID NO: 33 и VL-область содержит SEQ ID NO: 34.
11. Применение по любому из пп. 1-10, отличающееся тем, что CAR к ВСМА содержит первый трансмембранный домен и внутриклеточный сигнальный домен, причем указанный первый трансмембранный домен содержит трансмембранный домен цепи CD8α и указанный внутриклеточный сигнальный домен содержит сигнальный домен CD3ζ и/или сигнальный домен 4-1ВВ.
12. Применение по любому из пп. 1-11, отличающееся тем, что CAR к ВСМА содержит аминокислотную последовательность, представленную в SEQ ID NO: 344.
13. Применение по п. 12, отличающееся тем, что внеклеточный связывающий домен содержит эпитоп CD20.
14. Применение по п. 13, отличающееся тем, что указанный эпитоп CD20 содержит аминокислотную последовательность, представленную в SEQ ID NO: 397 или SEQ ID NO: 398.
15. Применение по любому из пп. 1-14, отличающееся тем, что CAR к ВСМА содержит сигнальный пептид CD8α, имеющий последовательность SEQ ID NO: 318; причем VH-область и VL-область содержат соответственно аминокислотные последовательности SEQ ID NO: 33 и SEQ ID NO: 34, и отличающееся тем, что VH-область и VL-область соединены линкером GS, имеющим последовательность SEQ ID NO: 333.
16. Применение по любому из пп. 1-15, отличающееся тем, что CAR к ВСМА содержит шарнирную область CD8α, имеющую последовательность SEQ ID NO: 320; трансмембранный домен CD8α, имеющий последовательность SEQ ID NO: 322; внутриклеточный сигнальный домен 4-1ВВ, имеющий последовательность SEQ ID NO: 323; и внутриклеточный сигнальный домен CD3ζ, имеющий последовательность SEQ ID NO: 324.
17. Применение по п. 15 или 16, отличающееся тем, что внеклеточный связывающий домен содержит эпитоп CD20.
18. Применение по п. 17, отличающееся тем, что эпитоп CD20 содержит аминокислотную последовательность SEQ ID NO: 397.
19. Применение по п. 17, отличающееся тем, что эпитоп CD20 содержит аминокислотную последовательность SEQ ID NO: 398.
20. Применение по любому из пп. 1-19, отличающееся тем, что CAR-T-клетки дефицитны по CD52.
21. Применение по любому из пп. 1-19, отличающееся тем, что CAR-T-клетки дефицитны по TCRα и/или TCRβ.
22. Применение по любому из пп. 1-21, отличающееся тем, что генотип указанных клеток представляет собой TCRαβ- и CD52+/-.
23. Применение по любому из пп. 1-19, отличающееся тем, что CAR-T-клетки не экспрессируют «защитный выключатель».
24. Применение по любому из пп. 1-19, отличающееся тем, что CAR-T-клетки экспрессируют эпитоп для ритуксимаба.
25. Применение по любому из пп. 1-24, отличающееся тем, что субъект получает первый режим лимфодеплеции перед применением указанной по меньшей мере одной дозы.
26. Применение по п. 25, отличающееся тем, что указанный первый режим лимфодеплеции включает применение флударабина и циклофосфамида.
27. Применение по п. 25, отличающееся тем, что указанный первый режим лимфодеплеции включает применение флударабина, циклофосфамида и антитела к CD52.
28. Применение по п. 25, отличающееся тем, что указанный первый режим лимфодеплеции включает применение антитела к CD52.
29. Применение по п. 25, отличающееся тем, что указанный первый режим лимфодеплеции включает применение только антитела к CD52.
30. Применение по пп. 27-29, отличающееся тем, что флударабин применяют в дозе 30 мг/м2/день; циклофосфамид применяют в дозе 300 мг/м2/день; и антитело к CD52 применяют в дозе от 10 до 13 мг/день.
31. Применение по п. 27, отличающееся тем, что флударабин применяют в дозе 30 мг/м2/день; циклофосфамид применяют в дозе 300 мг/м2/день.
32. Применение по п. 31, причем антитело к CD52 применяют в дозе от 13 до 30 мг/день, от 13 до 20 мг/день, от 13 до 30 мг/день или от 20 до 30 мг/день.
33. Применение по п. 31, отличающееся тем, что антитело к CD52 применяют в дозе 13 мг/день, 20 мг/день или 30 мг/день.
34. Применение по любому из пп. 25-33, отличающееся тем, что указанный первый режим лимфодеплеции начинают за 1-15 дней до применения указанной по меньшей мере одной дозы.
35. Применение по любому из пп. 25-34, отличающееся тем, что указанный первый режим лимфодеплеции применяют на протяжении 1, 2, 3, 4 или 5 дней.
36. Применение по любому из пп. 25-35, отличающееся тем, что указанный первый режим лимфодеплеции применяют за 5 дней до применения указанной по меньшей мере одной дозы на протяжении 3 дней.
37. Применение по любому из пп. 1-36, отличающийся тем, что субъект получает последующую дозу CAR-T-клеток.
| WO 2016166630 A1, 20.10.2016 | |||
| WO 2018085690 A1, 11.05.2018 | |||
| WO 2016014565 A2, 28.01.2016 | |||
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, НАЦЕЛЕННЫЕ НА АНТИГЕН СОЗРЕВАНИЯ В-КЛЕТОК | 2013 |
|
RU2650805C2 |
| Парораспределительный механизм для машин прямого действия | 1931 |
|
SU28220A1 |
| ПАВЛОВА А.А., и др | |||
| Адоптивная иммунотерапия генетически модифицированными Т-лимфоцитами, экспрессирующими химерные антигенные рецепторы // ОГ | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| URL: | |||
Авторы
Даты
2024-10-23—Публикация
2019-11-26—Подача