Изобретение относится к области ветеринарной вирусологии и биотехнологии, в частности, созданию тест-системы жидкофазного блокирующего непрямого «сэндвич»-варианта ИФА для определения титра антител против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 в сыворотках крови животных.
Ящур - высококонтагиозное вирусное заболевание парнокопытных животных, которое характеризуется высокой заболеваемостью, что влечет за собой ограничения на международную торговлю скотом и его продукцией. Основными клиническими признаками заболевания являются лихорадка, хромота, афты во рту, ступнях и сосках. Молодые животные имеют более высокую смертность из-за поражения миокарда по сравнению со взрослыми особями. Вспышки ящура часто возникают в странах Ближнего Востока, Азии и Африки [1, 2].
Вирус ящура является представителем рода Aphthovirus семейства Picornaviridae и имеет 7 различных серотипов: О, А, Азия-1, С и SAT-1, SAT-2, SAT-3 [2]. Геном кодирует 4 структурных белка VP4, VP1, VP3, VP2. Петля G-H белка VP1 была идентифицирована как основной антигенный сайт (141-160 а.о.). РНК вируса ящура также несет в себе информацию о 8 неструктурных белках (L-протеаза, 2А, 2В, 2С, 3А, 3В, 3С-протеаза и 3D-РНК-зависимая РНК-полимераза). Вирус ящура имеет очень высокую частоту мутаций из-за отсутствия механизма репарации вирусной РНК-зависимой РНК-полимеразы. Антигенные варианты вызваны различными аминокислотными мутациями, приводящими к трудностям в борьбе с ящуром [1,2].
В РНК-содержащих вирусах вариациям в геноме благоприятствуют высокие частоты мутаций во время репликации вируса, а возникающие линии и сублинии обусловлены мутациями и рекомбинацией. Рекомбинация - еще один важный процесс, определяющий биологию и эволюцию вирусов. Она представляет собой обмен генетическим материалом между двумя несегментированными РНК-геномами. Было показано, что генетическая рекомбинация происходит между вирусами одного и того же серотипа [3, 4]. Внутритипическая рекомбинация происходит часто и, по-видимому, события рекомбинации при ящуре происходят легче в 3'-части генома, чем в участках, кодирующих структурные вирусные белки. Мутации в результате рекомбинации приводят к обмену генетическим материалом и образованию новых антигенных вариантов, которые могут избежать иммунного давления и привести к изменениям тропизма клеток и диапазона хозяев [2, 5, 6]. Одна или несколько аминокислотных замен на поверхности вирусных частиц могут привести к изменению распознавания и использования рецепторов. В результате один и тот же вирус будет приобретать способность проникать в клетки с использованием альтернативных рецепторов [6].
Антигенные вариации возникают из-за аминокислотных мутаций, которые изменяют распознавание вирусных белков иммунной системой организма. Поверхностно открытые структуры вируса особенно подвержены иммунной атаке. Процесс появления новых антигенных форм определяется сложным взаимодействием вирусных факторов и клеток-хозяев [6, 7]. Изменения в генах, кодирующих капсидные белки, путем мутации могут привести к антигенным изменениям и появлению новых генетических линий [6].
Наиболее вариабельным является белок VP1 вируса ящура, поскольку на него приходится не менее 90% мутаций всех структурных генов. Самыми вариабельными областями являются участки 40-60, 130-160 и 190-213 а.о. [7]. Участок поверхностного белка VP1 в регионе 130-160 а.о. отличается высокой вариабельностью, поскольку участвует в процессе связывания с рецепторами клетки-хозяина [8, 9, 10]. Изменчивость данного региона дает возможность вирусу ящура взаимодействовать с рецепторами клеток разных типов и облегчает переход от одного вида хозяина к другому [9].
В Российской Федерации вспышки ящура типа О регистрировались начиная с 2000 по 2021 гг. на территории Приморского, Хабаровского, Забайкальского краев, Амурской, Оренбургской областей, Республики Башкортостан. Вспышки болезни были вызваны вирусом ящура типа О, генотипов O/SEA/Mya-98, O/ME-SA/PanAsia, O/ME-SA/Ind-2001.
Для изготовления высокоспецифичных и высокочувствительных диагностических тест-систем для выявления вируса ящура генотипа О/МЕ-SA/PanAsia2 применяется производственный штамм «О №2047/Саудовская Аравия/2008», однако, в последние годы в странах Юго-Восточной Азии и Ближнего Востока стали возникать вспышки ящура, вызванные новым генотипом О/ME-SA/PanAsia2ANT-10. При этом известные штаммы, в том числе «О №2047/Саудовская Аравия/2008», не дают возможности создать высокоспецифичных и высокочувствительных тест-систем для проведения диагностики ящура, причиной которого являются изоляты, относящиеся к генотипу вируса О/ME-SA/PanAsia2ANT-10.
В 2018 г. на территории Исламской Республики Пакистан от крупного рогатого скота с клиническими признаками ящура был отобран патологический материал, который поступил для научных исследований в ФГБУ «ВНИИЗЖ». Изолят вируса ящура «О РК18/12», послуживший источником для получения штамма О №2356/Пакистан/2018, был выделен в культуре клеток IB-RS-2. По результатам сравнительного анализа нуклеотидных последовательностей, выделенный изолят принадлежит к вирусу ящура типа О топотипа ME-SA генетической линии PanAsia2 новой сублинии ANT-10.
В ФГБУ «ВНИИЗЖ» данный изолят был адаптирован к различным чувствительным клеточным линиям, в том числе, к монослойной и суспензионной перевиваемой клеточной линии почки новорожденного сирийского хомячка ВНК-21/2-17 и ВНК-21/SUSP/ARRIAH, соответственно, и получен штамм «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10. Штамм «О №2356/Пакистан/2018» вируса ящура депонирован во Всероссийской государственной коллекции экзотических типов вирусов ящура и других патогенов животных (ГКШМ) ФГБУ «ВНИИЗЖ» под регистрационным номером: №415 - деп / 22-49 - ГКШМ ФГБУ «ВНИИЗЖ».
Филогенетическая принадлежность штамма «О №2356/Пакистан/2018» вируса ящура представлена на фиг. 4.
Иммунизация является эффективным инструментом борьбы с болезнью. В связи с появлением представителя нового генотипа вируса ящура и необходимостью защиты животных от него в ФГБУ «ВНИИЗЖ» разработали вакцину, в состав которой входит антиген вируса ящура данного штамма.
Возникла необходимость создания высокоспецифичных и высокочувствительных диагностических тест-систем, которые позволили бы выявлять антитела против вируса ящура штамма «О №2356/Пакистан/2018» (генотип О/ME-SA/PanAsia2ANT-10), которые вырабатываются у животных после вакцинации вакциной содержащей данный штамм.
Защита от ящура после вакцинации определяется уровнем специфических антител в сыворотке крови животных [11, 12, 13, 14]. Уровень гуморального иммунитета вакцинированного поголовья определяется путем выявления антител, специфичных к капсиду или структурным белкам вируса ящура. В соответствии с рекомендациями МЭБ (OIE) [2] для определения иммунного статуса животных применяют реакцию нейтрализации и иммуноферментный анализ (ИФА). Реакция нейтрализации считается чувствительным и специфичным методом, однако проведение анализа имеет ряд следующих ограничений: 1) большая продолжительность времени постановки реакции (не менее 3 суток), 2) высокая стоимость процедуры, связанная с применением чувствительной клеточной линии, наличием СО2-инкубатора, 3) предполагает использование живого вируса ящура, который является биологическим агентом II группы опасности.
В свою очередь ИФА обладает многими преимуществами, включая экспрессность, высокую специфичность и чувствительность, пригодность для крупномасштабного скрининга полевых образцов и отсутствие требований к специальным лабораторным условиям, например, культуре клеток или среде углекислого газа [15, 16]. Исходя из этого ИФА целесообразно применять для определения титра антител у вакцинированных животных.
Выделяют прямой и непрямой варианты ИФА. Преимущества прямого варианта ИФА заключаются в быстроте анализа, поскольку используется только один вариант иммуноглобулинов G и устраняется перекрестная реактивность вторичных антител. При этом имеются и некоторые недостатки, а именно, снижение иммунной активности первичных антител в следствие отрицательного влияния ферментов или меток, отсутствие гибкости в выборе первичной метки антител в зависимости от задачи исследования, а также минимальное усиление сигнала.
Существует непрямой вариант ИФА, который имеет заметные преимущества по сравнению с прямым. К достоинствам этого варианта метода относится следующее: 1) наличие большого разнообразия меченых вторичных антител, 2) универсальность (многие первичные антитела могут быть получены у одного вида, и одно и то же меченое вторичное антитело может быть использовано для обнаружения), 3) максимальная иммунная активность основного антитела сохраняется, поскольку оно не маркировано, 4) повышение чувствительности, поскольку каждое первичное антитело содержит несколько эпитопов, которые могут быть связаны меченым вторичным антителом, что позволяет усиливать детектируемый сигнал. К ограничениям метода относится вероятность появления перекрестной активности со вторичным антителом, что может привести к появлению неспецифического сигнала, а также наличие дополнительного этапа реакции [4, 15, 17].
Большое значение в лабораторной деятельности имеет «сэндвич»-вариант ИФА, который обычно требует использования пар подобранных антител, где каждое антитело специфично для другого, неперекрывающегося эпитопа антигена. Первые антитела принято называть сенсибилизирующими и предназначены они для захвата антигена. Вторые антитела - детекторные, необходимы для обнаружения антигена. Указанный вариант ИФА имеет следующие преимущества:
- высокая специфичность анализа;
- подходит для исследования полевых образцов разной степени очистки;
- высокая чувствительность реакции.
ИФА также разделяют на твердофазные и жидкофазные варианты. В настоящее время твердофазный вариант широко распространен по причине удобства применения и быстроте проведения анализа. На первом этапе реакции для твердофазного варианта адсорбируют антитела на твердой фазе. При этом не связавшиеся с твердой фазой реагенты легко удаляются отмыванием. В сенсибилизированных лунках инкубируют исследуемый образец. При этом на поверхности твердой фазы формируются иммунные комплексы. Не связавшиеся компоненты удаляют отмыванием. При добавлении конъюгата и связывании его с иммобилизованным иммунным комплексом активный центр фермента остается доступным для последующего взаимодействия с субстратом. Инкубация субстрата в лунках с иммобилизованным конъюгатом приводит к развитию цветной реакции. Эту реакцию можно остановить на нужной стадии, выраженность окрашивания можно оценить визуально или по оптической плотности.
Жидкофазный блокирующий непрямой вариант ИФА имеет ряд следующих преимуществ: 1) анализ максимально из всех модификаций данного анализа приближен к классической реакции нейтрализации, поскольку частицы антигена не прикреплены к субстрату; 2) эпитопы антигена наиболее доступны в пространстве для специфичных антител, и это позволяет получать наиболее приближенные результаты к реакции нейтрализации в клеточной линии; 3) обладает высокими показателями аналитической и диагностической чувствительности, специфичности и общей точности.
Sharma G.K. и др. (2015) предложили способ определения антител против вируса ящура типов А, О, Азия-1 с помощью жидкофазного блокирующего непрямого «сэндвич»-варианта ИФА [18]. Данная методика позволяла идентифицировать широкий спектр противоящурных антител, но при этом специфичность по отношению к вирусу ящура генотипа О/ME-SA/PanAsia2ANT-10 не более 55%, а, следовательно, точное выявление иммуноглобулинов G не представляется возможным. Следует заметить, что данный способ предполагал применение в качестве блокирующего компонента не иммунную сыворотку лошади, которая содержит различные белковые соединения, в том числе, возможно, гомологичные участки аминокислотных последовательностей относительно антигенных детерминант. Авторы тест-системы применяли моноклональные антитела, использование которых увеличивает спектр выявления различных генетических линий вируса ящура в рамках одного серотипа, но при этом существенно снижается специфичность относительно выявления антител против изолятов/штаммов конкретного генотипа, в частности О/ME-SA/PanAsia2ANT-10. В качестве красителя использовали тетраметилбензидин (ТМВ), являющийся агрессивным канцерогеном и нестабильным компонентом для проведения цветной реакции. Для остановки реакции применяли серную кислоту, являющуюся опасным соединением.
Указанные выше тест-системы не представлены на рынке в качестве набора для детекции противоящурных антител в сыворотках крови животных и остаются недоступными для широкого потребителя в качестве диагностикумов. В свою очередь на мировом рынке в настоящее время имеются европейские наборы для детекции антител против вируса ящура типа О - IZSLER (Италия) и PrioCHECK (Нидерланды).
Тест-система в наборе IZSLER предназначена для детекции противоящурных антител с помощью твердофазного прямого «сэндвич»-варианта ИФА. Комплектующие набора IZSLER (Institute Zooprofllattico Sperimentale della Lombardia e dell'Emilia Romagna Brescia, Italy The Pirbright Institute) следующие:
1. Герметичные микропланшеты, сенсибилизированные инактивированным вирусом ящура типа О.
2. Конъюгат (моноклональные антитела против вируса ящура типа О, конъюгированные с пероксидазой).
3. Положительный контроль сыворотки против вируса ящура типа О.
4. Отрицательный контроль.
5. Буферный раствор для ИФА - фосфатно-солевой буфер с твином-20 (ФСБ-Tween).
6. Буфер для разведения сыворотки крови и конъюгата.
7. Субстрат (раствор хромогена ТМВ).
8. Раствор для остановки реакции (0,6N раствор серной кислоты).
Достоинством данного набора является применение моноклональных антител, однако они были получены ранее 2018 года (период, когда выделен штамм «О №2356/Пакистан/2018») и не могут с высокой достоверностью и точностью детектировать специфические антитела в сыворотках крови животных. Специфичность и чувствительность указанной тест-системы для выявления антител против вируса ящура генотипа О/ME-SA/PanAsia2ANT-10 ниже 50%, что подтверждают данные реакции нейтрализации в чувствительной перевиваемой монослойной клеточной линии почки свиньи IB-RS-2. Таким образом, применяемая тест-система не позволяет получать точных результатов именно в отношении изолятов и штаммов вируса ящура вновь появившегося генотипа.
Наиболее близким прототипом для разработанной нами тест-системы является тест-система PrioCHECK (Prionics Lelystad B.V., Netherlands) для выявления антител к вирусу ящура типа О.
Комплектующие для соответствующего набора представлены ниже:
Компонент 1 - Планшеты иммунологические.
Компонент 2 - Конъюгат (30х). Разбавленный конъюгат не стабилен, готовят непосредственно перед применением.
Компонент 3 - Буфер для разведения (5х).
Компонент 4 - Неиммунная сыворотка крови лошади.
Компонент 5 - Деминерализованная вода.
Компонент 6 - Промывочный буфер (200х).
Компонент 7 - Референтная сыворотка 1 (позитивная) (жидкая).
Компонент 8 - Референтная сыворотка 2 (менее позитивная) (жидкая).
Компонент 9 - Референтная сыворотка 3 (еще менее позитивная) (жидкая).
Компонент 10 - Референтная сыворотка 4 (отрицательный контроль) (жидкая).
Компонент 11 - Субстрат хромогена (ТМВ).
Компонент 12 - Стоп-раствор (1 N раствор серной кислоты). Данные отражены в инструкции производителя.
Диагностикум удобен в применении и позволяет за 5-6 ч получить результаты исследования. Данная тест-система включает в себя конъюгат, который представляет собой меченые моноклональные антитела против вируса ящура серотипа О, исходя из этого является типоспецифичной, но без более узкой дифференциации. Разработана прототипная тест-система в конце 90-гг XX в. и получены соответствующие антитела против антигенов вируса ящура различных генотипов, созданных с использованием вирусов, кроме активно циркулирующего с 2018 г. генотипа О/ME-SA/PanAsia2ANT-10. Изоляты и штаммы данной линии имеют существенные отличия от других линий серотипа О. Анализируя нуклеотидную и аминокислотную последовательность высоко вариабельного пептида вируса ящура VP1, ученые пришли к выводу о наличии достаточного количества существенных замен, позволяющих отнести вирус к иному генотипу. Исходя из выше отраженного, прототипная тест-система не является высокочувствительной и специфичной по отношению к вирусу ящура генотипа О/ME-SA/PanAsia2ANT-10. Данная тест-система выявляет антитела к данному штамму не более, чем на 55%. Исходя из этого требуется разработать высокочувствительную, специфичную тест-систему для детекции и количественного анализа уровня антител против вируса ящура представленного генотипа.
Прототипная тест-система основана на твердофазном конкурентном «сэндвич»-варианте ИФА, однако эта форма хоть и является одним из вариантов серологических реакций, но находится дальше от реакции нейтрализации относительно возможностей улавливания антигенных сайтов по сравнению с жидкофазным блокирующим непрямым «сэндвич»-вариантом ИФА.
Прототипный вариант предполагает наличие в своем составе нативных контрольных сывороток крови животных, что снижает сохранность компонентов тест-системы в течение длительного периода времени и есть риск контаминации микроорганизмами.
Прототипный вариант имеет также некоторое ограничение в применении, а именно, рабочий раствор конъюгата не стабилен и быстро разрушается. В составе набора он представлен в виде 30-кратного концентрата. В таком состоянии в отличии от лиофилизированного компонента срок хранения заметно сокращается. Следует также отметить, что данная тест-система не предусматривает контроля конъюгата, что не позволяет получать более достоверные данные по оптическим плотностям и титру антител против вируса ящура.
В прототипной тест-системе применяется прямой конъюгат, что удобно в применении, однако при этом повышается вероятность шумовых фоновых явлений, что может негативно отражаться на конечных результатах количественного исследования сывороток крови животных.
В прототипной тест-системе для проявления цветной реакции используют краситель ТМВ, который обладает канцерогенными свойствами.
Учитывая найденные ограничения в применении имеющихся тест-систем, в том числе прототипной, для проведения точного анализа гуморального иммунитета животных после вакцинации противоящурными вакцинами, содержащими инактивированный вирус ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10, актуальной является разработка серологической тест-системы жидкофазного блокирующего непрямого «сэндвич»-варианта ИФА для выявления антител в сыворотках крови животных с учетом выше приведенных недостатков.
В настоящее время ветеринарная служба Российской Федерации не располагает современной отечественной тест-системой ИФА, которая позволила бы с высокой достоверностью определять титр антител против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 в сыворотках животных.
Целью изобретения является создание тест-системы на основе жидкофазного блокирующего непрямого «сэндвич»-варианта ИФА для определения титра антител против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10.
Цель достигается благодаря тому, что метод жидкофазного блокирующего непрямого «сэндвич»-варианта ИФА наиболее приближен к классической реакции нейтрализации в естественных условиях, поскольку все антигенные сайты полных вирионов вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 находятся в свободном состоянии в жидкой фазе, открыты для связывания со специфическими сенсибилизирующими и детекторными антителами кролика и морской свинки, соответственно. Реакция основана на взаимодействии исследуемой сыворотки крови животного и инактивированного вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 в жидкой фазе в лунках круглодонного планшета с образованием иммунных комплексов. Параллельно с этим проводится сенсибилизация лунок плоскодонного планшета иммуноглобулинами G кролика против вируса ящура того же генотипа. После этого сенсибилизированные лунки блокируют с помощью фетальной сыворотки крови КРС, добавляют полученные иммунные комплексы из круглодонного планшета, инкубируют, вносят восстановленную суспензию детекторных антител. Образовавшийся сложный иммунный комплекс выявляют с помощью антител против Ig G морской свинки, конъюгированных с пероксидазой хрена и хромогенного субстрата.
Технический результат от изобретения заключается в разработке современной, высокоспецифической и чувствительной тест-системы, предназначенной для определения титра антител против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 методом жидкофазного блокирующего непрямого «сэндвич»-варианта ИФА, вследствие применения инактивированного вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 и при получении специфических компонентов реакции в жидкой фазе.
В состав разработанной тест-системы ИФА входят следующие иммуноспецифические компоненты:
1. культуральный инактивированный лиофилизированный вирус ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 -1 флакон (0,5 см3);
2. сенсибилизирующие лиофилизированные антитела - иммуноглобулины G кролика против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 - 1 флакон (0,5 см3);
3. детекторные лиофилизированные антитела - иммуноглобулины G морской свинки против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 - 1 флакон (0,5 см3);
4. контроль 1 - положительная лиофилизированная сыворотка крови крупного рогатого скота к вирусу ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10, с процентом ингибиции ≥75% - 1 флакон (0,2 см3);
5. контроль 2 - положительная лиофилизированная сыворотка крови крупного рогатого скота к вирусу ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10, с процентом ингибиции от 50% до 75% - 1 флакон (0,2 см3);
6. контроль 3 - нормальная лиофилизированная сыворотка крови крупного рогатого скота, не содержащая антител к вирусу ящура - 1 флакон (0,2 см3);
7. фетальная лиофилизированная сыворотка крови крупного рогатого скота нормальная для блокирования открытых сайтов связывания на дне лунок планшета - 2 флакона (по 2,0 см3);
8. антивидовой лиофилизированный конъюгат - иммуноглобулины кролика против IgG морской свинки, конъюгированные с пероксидазой хрена.
Предлагаемая тест-система содержит неспецифические компоненты:
9. карбонатно-бикарбонатный буферный раствор (рН 9,5-9,6) для разведения антигена;
10. 20-кратный концентрат буферного раствора;
11. хромогенный субстрат - краситель ABTS (2,2-азино-ди-(3-этилбензоаминосульфоновая кислота);
12. «стоп»-раствор - 0,5%-ный раствор додецилсульфата натрия.
В состав тест-системы также входят 4 иммунологических 96-луночных плоскодонных полистироловых планшета для проведения ИФА и 1 полимерный 96-луночный круглодонный планшет для связывания антигена и антител в жидкой фазе.
В отличии от прототипа в разработанной тест-системе применяется культуральный инактивированный вирус ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10, который представлен в виде лиофилизата. Данный факт дает возможность выявлять именно антитела против вируса ящура указанного штамма с высокими показателями чувствительности (более 99%) и специфичности (100%), что более чем на 45% выше по сравнению с наиболее близким прототипом. Кроме того, лиофилизированный компонент остается стабильным не менее 3 лет по сравнению с антигеном в нативном состоянии, что является преимуществом в использовании данной тест-системы. Активность полученного антигена вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 составляет 1:4000.
В отличии от прототипа применяются сенсибилизирующие и детекторные антитела кролика и морской свинки, соответственно, высокоспецифичные по отношению к антигену вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10, поскольку были получены с применением высокоочищенного антигена с высокой активностью. Указанные в тест-системе ИФА иммуноглобулины G кролика и морской свинки против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 представлены в виде лиофильного компонента, что позволяет антителам находится в стабильном состоянии не менее 3 лет с активностью не менее 1:9000 и 1:5000, соответственно.
В отличии от прототипа сыворотки крови КРС, контроль 1 и 2, получены против высокоочищенного инактивированного вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10, что позволяет достичь высокой специфичности и чувствительности при контроле работы тест-системы. Указанные компоненты представлены в виде лиофилизата, что позволяет хранить их не менее 3 лет с сохранением высокой активности в ИФА. Для контроля 1 активность составляет не менее 1:3000, для контроля 2 - не менее 1:3000. Данная активность высокая и удобна для получения большого количества контролей в рабочем нативном состоянии.
В отличии от прототипа для блокирования открытых сайтов связывания применяется очищенная фетальная сыворотка телят, белковые составляющие которой обеспечивают полное закрытие пустых участков на дне иммунологического планшета. Данный компонент также представлен в лиофильном виде, что позволяет хранить его в данном состоянии не менее 3 лет.
В отличии от прототипного варианта представленная тест-система предусматривает контроль антигена и конъюгата, что дает возможность учитывать фоновые значения и, тем самым, получать достоверные абсолютные данные по оптическим плотностям и значению титра антител против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10.
В отличии от прототипа в предложенной тест-системе применяется непрямой конъюгат, что позволяет снижать вероятность шумовых фоновых явлений и получать более достоверные результаты определения титра антител против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/МЕ-SA/PanAsia2ANT-10 в сыворотках крови животных. Активность конъюгата составляет 1:3500.
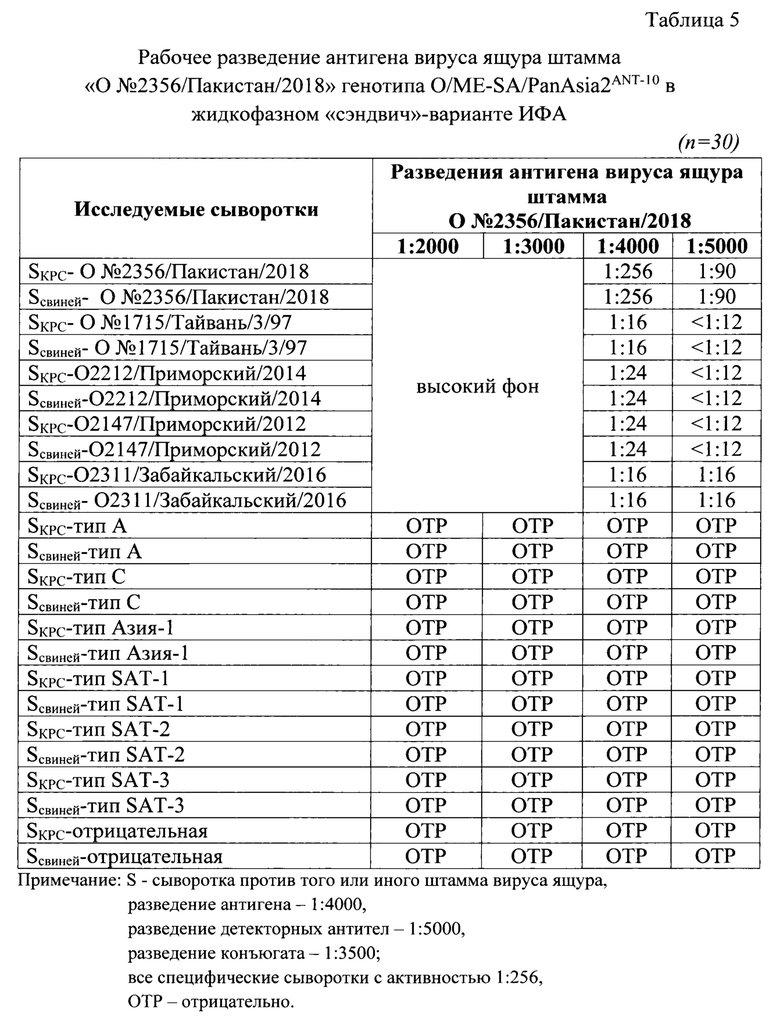
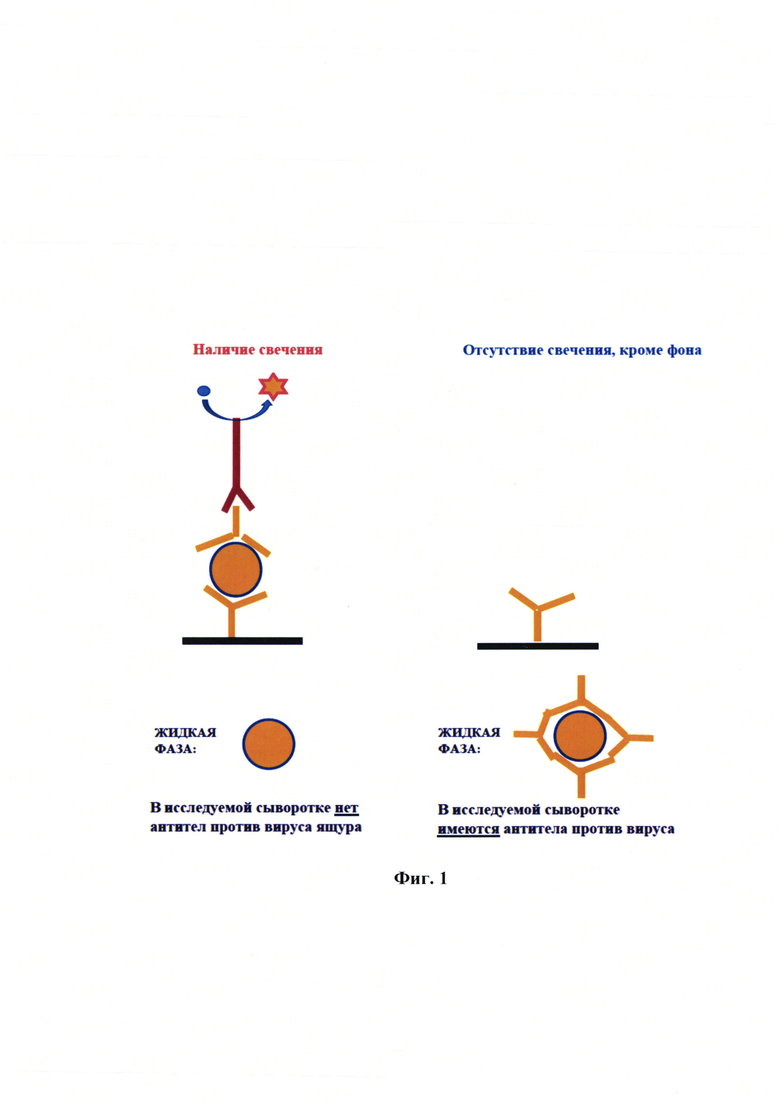
Сущность изобретения отражена на графических изображениях: Фиг. 1 - Принципиальная схема жидкофазного блокирующего непрямого «сэндвич»-варианта ИФА.
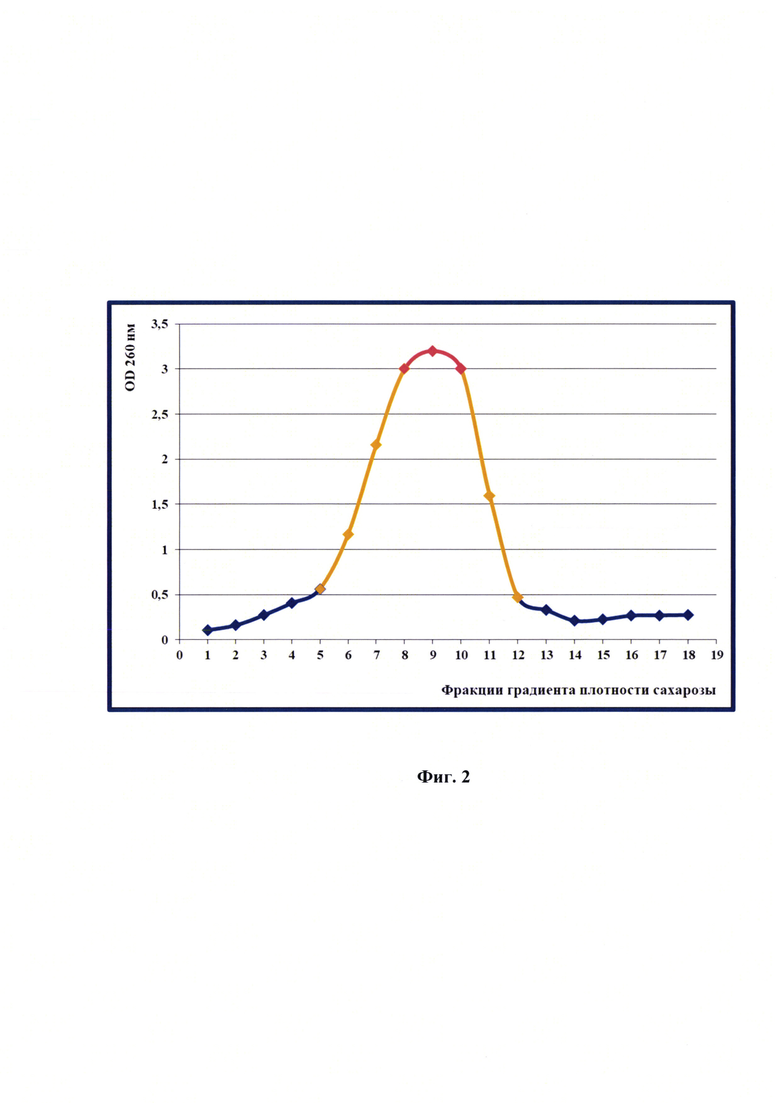
Фиг. 2 - Спектральный профиль фракций антигена вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10.
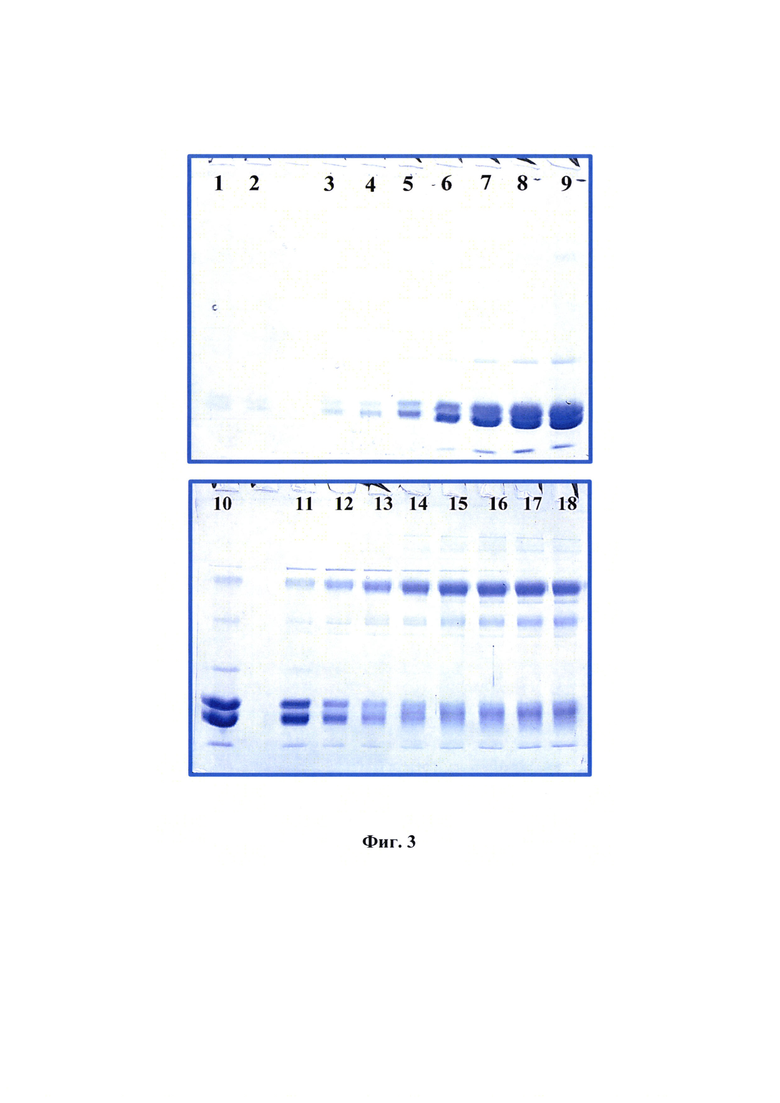
Фиг. 3 - Электрофореграмма для антигена вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 в 12% полиакриламидном геле. Примечание: 1-3: фракции с 50% сахарозы, 4-8: фракции с 40% сахарозы, 9-13: фракции с 30% сахарозы, 14-18: фракции с 20% сахарозы; целевой белок с молекулярным весом 25 кDa.
Фиг. 4 - Филогенетическая принадлежность штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 вируса ящура.
Разработанная тест-система на основе жидкофазного блокирующего непрямого «сэндвич»-варианта ИФА основана на специфическом блокировании антигена вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 антителами, содержащимися в исследуемой пробе сыворотки в жидкой фазе. Смесь «исследуемая сыворотка/антиген» переносится в лунки планшета, предварительно иммобилизованного сенсибилизирующими антителами кролика против штамма «О №2356/Пакистан/2018» генотипа О/МЕ-SA/PanAsia2ANT-10. Наличие антител к вирусу ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 в исследуемой пробе будет выражаться в формировании иммунного комплекса и уменьшении количества свободного антигена, который связывается сенсибилизирующими антителами. Фиксированный в лунках антиген взаимодействует с детекторными антителами морской свинки, которые выявляются в реакции с иммунопероксидазным конъюгатом против Ig G морской свинки и последующим окрашиванием с помощью хромогенного субстрата ABTS. Интенсивность окрашивания обратно пропорциональна концентрации специфических антител в исследуемой пробе. Интенсивность цветной реакции учитывают с помощью спектрофотометра-ридера. Принципиальная схема жидкофазного блокирующего непрямого «сэндвич»-варианта ИФА представлена на фиг. 1.
Проводят подготовку лиофилизированных компонентов тест-системы. Перед началом работы лиофилизированные препараты (антиген вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10, конъюгат, положительные и отрицательный контроли, фетальную сыворотку крови телят) восстанавливают до необходимого объема дистиллированной водой.
Проводят приготовление рабочих растворов.
Раствор №1 (карбонатно-бикарбонатный буферный раствор - КББ). Готовят по стандартной методике 100 мл КББ раствора (рН 9,5-9,7) для сенсибилизации планшетов.
Раствор №2 (промывочный раствор). Раствор используется для приготовления рабочего раствора для межэтапной промывки планшетов и подготовки проб для исследования, а так же как основа для приготовления рабочего буферного раствора для разведения детекторных антител и иммунопероксидазного конъюгата. Готовят 2 л стандартного буферного раствора TBS с добавлением 0,05% твин-20 (рН 7,4-7,6).
Раствор №3 (буфер для восстановления антител и конъюгата). Рабочий буферный раствор для разведения детекторных антител и иммунопероксидазного конъюгата (рН 7,4-7,6) готовится из раствора №2 с добавлением 10% фетальной сыворотки телят.Для этого к 36 см3 раствора №2 следует добавить 4,0 см3 фетальной сыворотки телят, восстановленной из лиофилизированного препарата путем добавления к содержимому флакона с сывороткой 4,0 см3 дистиллированной воды. Готовится непосредственно перед использованием.
Этапы проведения жидкофазного блокирующего непрямого «сэндвич»-варианта ИФА для определения титра антител против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 представлены ниже.
1. Сенсибилизация планшетов. Восстановленную суспензию сенсибилизирующих антител готовят в разведении 1:9000 в растворе №1 (карбонатно-бикарбонатный буферный раствор). Во все лунки иммунологического полистиролового 96-луночного планшета для ИФА вносят по 100 мкл суспензии сенсибилизирующих антител, накрывают крышкой и инкубируют в течение 18-20 часов при температуре (2-8)°С.
2. Промывание лунок планшета осуществляют с использованием Washer любой марки, либо вручную раствором №2. Процедуру повторяют два раза.
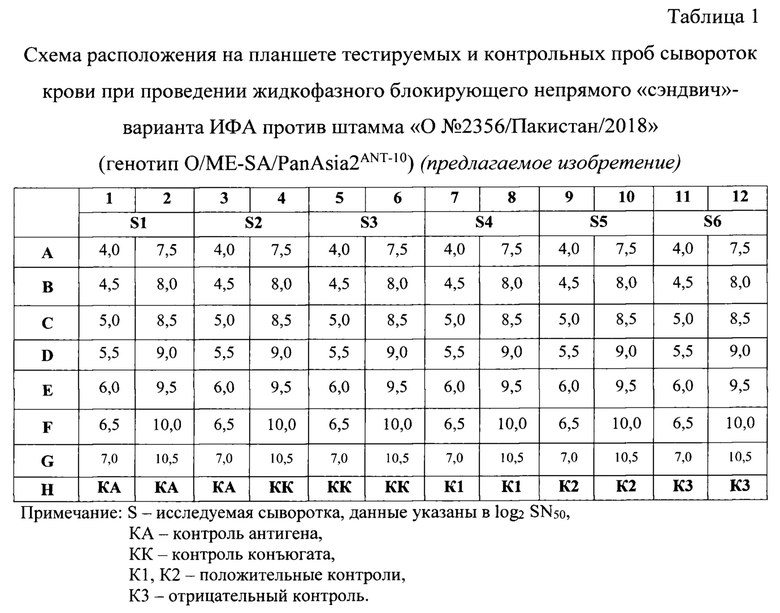
3. Серологическая реакция в жидкой фазе. Параллельно с сенсибилизацией планшета проводят иммунную реакцию связывания антигена с испытуемыми и контрольными пробами сыворотки крови. Готовят следующие разведения сывороток крови животных: 4,0; 4,5; 5,0; 5,5; 6,0; 6,5; 7,0; 7,5; 8,0; 8,5; 9,0; 9,5; 10,0; 10,5 log2 SN50 (1:16-1:1448) в растворе №2. Для этого во все лунки полимерного планшета за исключением лунок HI-6, которые оставляют для контроля антигена (КА) и контроля конъюгата (КК), вносят по 0,047 см3 (47 мкл) буферного раствора и 0,003 см3 (3 мкл) пробы. В лунки HI-6 вносят по 0,05 см3 (50 мкл) буферного раствора. Испытуемые и контрольные пробы располагают на планшете согласно таблице 1.
В качестве контроля 1 используют положительную сыворотку крови свиней против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/МЕ-SA/PanAsia2ANT-10 - процент ингибиции 75-100%, контроля 2 - положительную сыворотку крови свиней против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 - процент ингибиции 50-74%, контроля 3 - нормальную сыворотку свиней - процент ингибиции меньше 50%.
Во все лунки планшета добавляют по 0,05 см3 рабочего разведения антигена в растворе №2 в соответствии с разведением. После перемешивания содержимого лунок планшета при помощи шейкера или легким встряхиванием вручную планшет закрывают крышкой и инкубируют в течение 18-20 часов при температуре (2-8)°С.
4. Улавливание антигена. В промытые лунки сенсибилизированного планшета вносят по 0,05 см3 смеси контрольных и испытуемых проб и антигена, планшет закрывают крышкой и инкубируют в течение 60±5 мин при температуре (37±1)°С.
5. Промывание лунок планшета. Проводят, как представлено выше (п. 2). Процедуру повторяют 4 раза.
6. Внесение детекторных антител. Во все лунки планшета, за исключением лунок с КК (контроль конъюгата), куда добавляют по 0,05 см3 раствора №3, вносят по 0,05 см3 рабочего разведения детекторных антител (1:5000) в растворе №3. Планшет накрывают крышкой и инкубируют в течение 60±5 мин при температуре (37±1)°С.
7. Промывание лунок планшета. Проводят, как представлено выше (п.2). Процедуру повторяют 4 раза.
8. Внесение конъюгата. Во все лунки планшета вносят по 0,05 см3 рабочего разведения конъюгата (1:3500) в растворе №3. Планшет накрывают крышкой и инкубируют в течение 60±5 мин при температуре (37±1)°С.
9. Промывание лунок планшета. Проводят, как представлено выше (п.2). Процедуру повторяют 4 раза.
10. Проявление цветной реакции. Во все лунки планшета вносят по 0,05 см3 хромогенного субстрата ABTS, закрывают крышкой и выдерживают 15-20 минут при температуре (18-23)°С.
11. Остановка реакции. Реакцию останавливают добавлением в каждую лунку планшета 0,05 см3 0,5% раствора додецилсульфата натрия.
12. Учет результатов ИФА. Результаты анализа учитывают инструментальным способом. Сразу после остановки реакции измеряют оптическую плотность (D) продуктов реакции в каждой лунке при длине волны 410 нм, используя спектрофотометр-ридер для микропланшетов с вертикальным лучом света. Значения D контрольных и исследуемых проб переводят в значение процента ингибиции (ПИ, %) по формуле:
ПИ (%) = (1-(OD415 сыворотки - OD415 КК)/(OD415 КА - OD415 КК)) × 100%,
где, OD415 сыворотки - среднее значение оптической плотности при длине волны 415 нм для смеси сыворотки с инактивированным вирусом ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10;
OD415 КА - среднее значение оптической плотности контроля антигена при длине волны 415 нм;
OD415 КК - среднее значение оптической плотности контроля конъюгата при длине волны 415 нм.
Результаты реакции достоверны в том случае, если данные удовлетворяют следующим критериям:
- разница между значениями OD415 КА и OD415 КК не менее 0,38 оптических единиц (о.е.);
- контроль 1 имеет значение PI>75%;
- контроль 2 имеет значение PI в пределах 50-74%;
- контроль 3 имеет значение PI<50%.
Пробы, демонстрирующие значение Р1>50%, считают положительными, а животные, от которых получены данные пробы сыворотки крови, иммунными к ящуру, вызванного вирусом штамма «О №2356/Пакистан/2018» генотипа О/МЕ-SA/PanAsia2ANT-10. Значение PI<50% в сыворотке крови обследуемых животных является отрицательным, что свидетельствует об отсутствии специфических антител к ящуру, вызванного вирусом штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10. Исходя из полученных данных берут последнее разведение сыворотки, для которого процент ингибиции составляет ≥50%. Это разведение считают титром антител против ящура, вызванного вирусом штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10.
В результате проведенных экспериментов были оптимизированы условия постановки реакции. Активность детекторных антител, определенная в непрямом варианте ИФА, составила 1:5000, антивидового конъюгата - 1:3500; сенсибилизирующих антител - 1:9000, антигена вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 - 1:4000, контроля 1 - 1:3000, контроля 2 - 1:3000, контроля 3 - 1:3000. С использованием разработанной тест-системы проведено исследование образцов сывороток крови животных с определением титра антител и проведен сравнительный анализ с результатами реакции нейтрализации в чувствительной перевиваемой монослойной клеточной линии почки свиньи (IB-RS-2) [2].
Разработанный вариант ИФА позволяет тестировать одновременно в формате 96-луночного планшета 6 проб сывороток в следующих разведениях, выраженных в двоичном логарифме: 4,0; 4,5; 5,0; 5,5; 6,0; 6,5; 7,0; 7,5; 8,0; 8,5; 9,0: 9,5; 10,0; 10,5 log2 SN50 (1:16-1:1448). Срок годности предлагаемой тест-системы составляет не менее 24 месяцев со дня изготовления при температуре хранения (4-8)°С.
В качестве рабочего применяли инактивированный вирус ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10.
Контроль штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 вируса ящура на специфичность. Вирусный изолят, послуживший источником для получения штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 вируса ящура, был выделен от теленка с территории Исламской Республики Пакистан. Специфичность определена с помощью ОТ-ПЦР с последующим секвенированием 1D-гена, соответствующего белку VP1, отвечающему за изменчивость вируса ящура. По результатам исследования нуклеотидной последовательности (фиг. 4) указанного гена была выявлена принадлежность штамма «О №2356/Пакистан/2018» генотипу О/ME-SA/PanAsia2ANT-10. Расчет проводился в соответствии с Байесовской теорией вероятности. Специфичность подтверждена также в реакции связывания комплемента со штаммоспецифической сывороткой. Концентрация общего вирусного белка в исследуемом антигене вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 составила 3,42 мкг/мл, концентрация 146S компонента - 2,43 мкг/мл, 146+75S компонента - 3,27 мкг/мл.
Экспериментально подтверждена возможность использования штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 вируса ящура для контроля антигенной и иммуногенной активности, а также для изготовления биопрепаратов для диагностики и специфической профилактики ящура генотипа О/ME-SA/PanAsia2ANT-10.
Сущность изобретения пояснена примерами его использования, которые не ограничивают объем изобретения.
Пример 1. Получение инактивированного вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10.
Для получения инактивированного вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 для диагностических целей проводили суспензионное культивирование вируса в клеточной линии ВНК-21 в течение 10-12 ч с получением вирусной суспензии с титром инфекционной активности не ниже 7,00 lg ТЦД50/см3. Полученную вирусную суспензию инактивировали с помощью аминоэтилэтиленимина и осветляли за счет полигексаметиленгуанидина.
Инактивированную культуральную суспензию, содержащую антиген вирус ящура, осветляли в течение 30 мин. при 6000 об/мин и 4°С на центрифуге типа Bekman J2-21 (Beckman Coulter, USA) или аналоге. Надосадочную жидкость отбирали и добавляли в нее полиэтиленгликоль с молекулярным весом 6000 Д (ПЭГ-6000) до конечной концентрации 8% и хлорида натрия (сухой) до конечной концентрации 0,85%, интенсивно перемешивали и выдерживали при температуре (4±2)°С в течение 18-24 часов. Вирусную суспензию осаждали при 6000 об/мин в течение 60 мин., осадок растворяли в 1/15 М фосфатно-солевом буферном растворе, концентрируя в 300 раз (1/300 от первоначального объема).
К полученному преципитату добавляли 50% трихлорметана, интенсивно перемешивали и фракционировали с помощью центрифуги в течение 30 мин. при 3000 об/мин. Отбирали верхнюю водную фракцию, содержащую антиген вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10. Отбирали 100 мкл образца для последующего электрофоретического анализа в 12% полиакриламидном геле.
На следующем этапе проводили получение 146S компонента вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 (данный компонент является иммуногенным и наиболее важным в иммунизации животных, поскольку представляет собой полные вирионы).
Перед помещением в градиент сахарозы антиген вируса ящура обрабатывали нонилфеноксиполиэтоксилэтанолом в концентрации 1,5%.
Для выделения 146S компонента готовили линейный градиент сахарозы с концентрациями 10, 20, 30, 40, 50%. Обработанный с помощью ноноксинона-40 антиген вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/МЕ-SA/PanAsia2ANT-10 наливали по 15 мл в центрифужные пробирки, затем последовательно подслаивали растворы сахарозы, начиная с 10%-го и заканчивая 50%-м раствором. Пробирки помещали в металлические центрифужные стаканы и после тщательно выполненного уравновешивания центрифугировали при скорости 30000 об/мин и температуре 4±2°С в течение 4 часов. Фракционирование градиента сахарозы производили с помощью перистальтического насоса, отбирая фракции по 1 мл в отдельные пробирки. Начало и конец пика 146S компонента определяли по спектральному профилю, объединяя фракции, входящие в этот диапазон.
При использовании перистальтического насоса сначала оценивали визуально пробирку с градиентом сахарозы. Опалесцирующий слой, содержащий 146S компонент, располагается приблизительно в 30%-м слое сахарозы. В этом случае отбирали последнюю верхнюю фракцию 50%-го слоя, все фракции 30%-го слоя и нижнюю фракцию 20%-го слоя сахарозы. Общий объем составляет приблизительно 7,0 мл. Затем 146S компонент переосаждали с помощью ультрацентрифугирования в течение 4 часов при скорости 30000 об/мин. и температуре (4±2)°С и ресуспендировали осадок в 1/15 М фосфатно-солевом буферном растворе.
Результаты спектрометрического исследования полученных фракций антигена вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/МЕ-SA/PanAsia2ANT-10 в виде антигенного профиля представлены на фиг. 2. Анализ проводили для всех фракций, высокие значения оптической плотности наблюдали для 5-12 фракции с максимальными значениями для 8-10 пиков. Проведен электрофорез полученных фракций в 12% полиакриламидном геле в денатурирующих условиях для 18 фракций, в которых возможно нахождение 146S компонента вируса ящура данного штамма (фиг. 3). На фиг. 3 отражено, что слоты №№1-3 - это фракции с 50% сахарозы, №№4-8 - фракции с 40% сахарозы, №№9-13 - фракции с 30% сахарозы, №№14-18 - фракции с 20% сахарозы.
Пример 2. Получение гипериммунной сыворотки крови кроликов (сенсибилизирующие антитела) против штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10.
Для получения специфических сывороток крови против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/МЕ-SA/PanAsia2ANT-10 применяли клинически здоровых кроликов средней упитанности массой 2,5-3,0 кг.
Для гипериммунизации животных применяли концентрированный очищенный инактивированный вирус ящура штамма
«О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10, полученный как описано в примере 1, из которого готовили эмульсию с использованием масляного адъюванта Montanide ISA-61 VG (в соотношении адъювант/антиген = 60/40 по массе). Полученную вакцину вводили в мышцу задних конечностей кролика на 0, 21 и 42 дни в объеме 0,5 см3. Через 7 дней после последней иммунизации кроликов тотально обескровливали и получали сыворотку крови - содержащую сенсибилизирующие антитела, которую лиофильно высушивали и хранили при температуре (4-8)°С.
Пример 3. Получение гипериммунной сыворотки крови морских свинок (детекторные антитела) против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/МЕ-SA/PanAsia2ANT-10.
Для гипериммунизации морских свинок использовали эмульсию очищенного препарата концентрированного инактивированного вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10, полученного как описано в примере 1. Приготовление вакцины и схема иммунизации такая, как в примере 2.
Пример 4. Определение активности антигена вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10, сенсибилизирующих и детекторных антител.
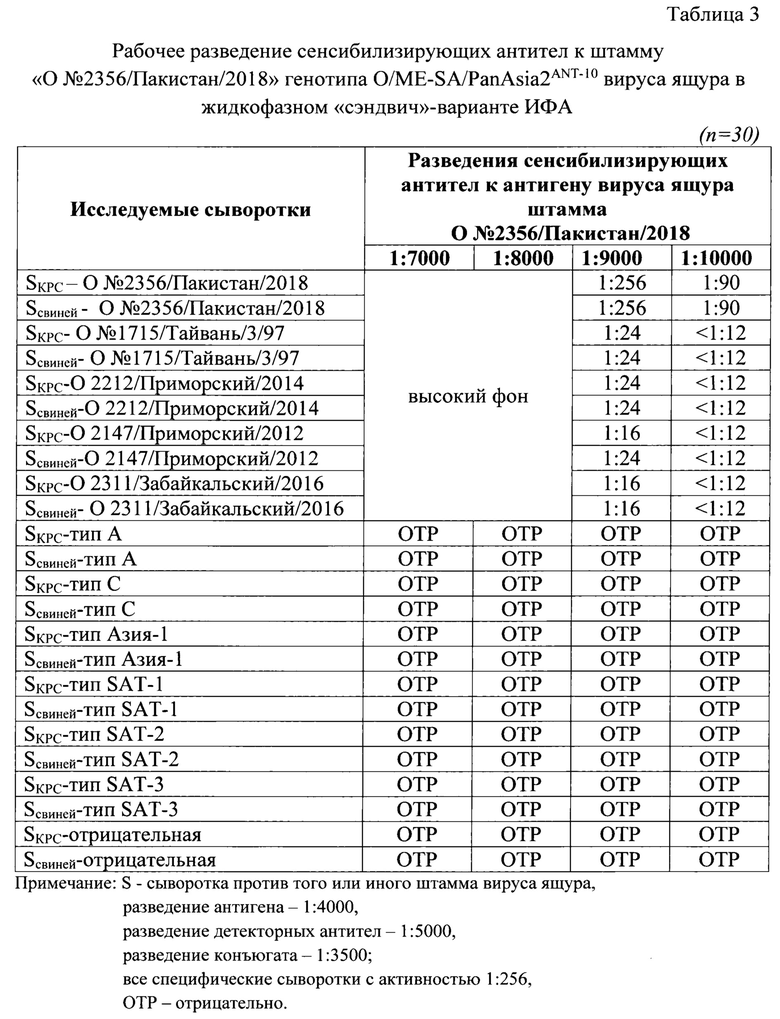
Индивидуальные пробы сывороток проверяли на активность и специфичность в жидкофазном блокирующем непрямом «сэндвич»-варианте варианте ИФА. Был проведен подбор оптимальных рабочих разведений указанных компонентов для получения достоверных результатов в ИФА. Полученные данные анализа представлены в таблицах 3, 4, 5.
Для анализа исследовали следующие разведения сенсибилизирующих антител: 1:7000, 1:8000, 1:9000, 1:10000. Разведения остальных компонентов были постоянны: для антигена - 1:4000, для детекторных антител - 1:5000, конъюгата - 1:3500. В качестве контрольных сывороток для анализа применяли сыворотки, специфичные к определенным штаммам вируса ящура с активностью 1:256. Их таблицы 3 следует, что при разведении сенсибилизирующих антител 1:9000 достигалось получение достоверного результата (1:256 или 8 log2 SN50). При меньших разведений антител наблюдали высокие фоновые значения, что не позволяло получить корректный результат. При большем разведении наблюдали снижение детектируемого значения титра антител в сыворотках крови животных. При исследовании неспецифических и отрицательных сывороток отмечали отрицательные результаты, что свидетельствовало о высокой специфичности разработанного способа.
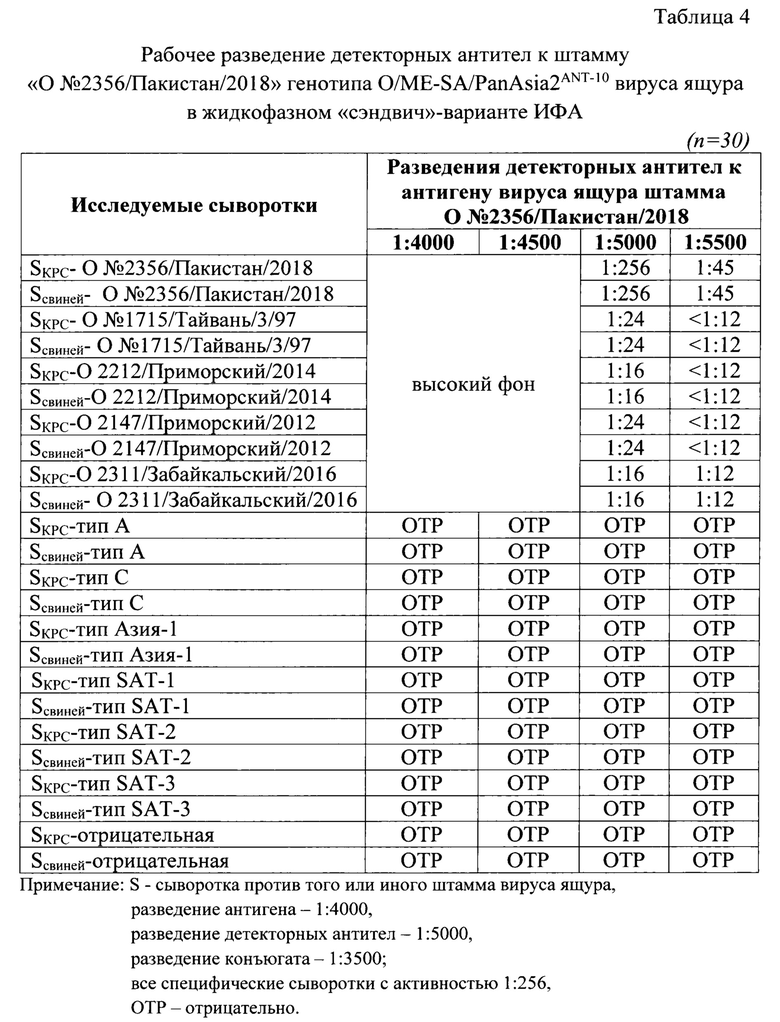
Для анализа исследовали следующие разведения детекторных антител: 1:4000, 1:4500, 1:5000, 1:5500. Разведения остальных компонентов были постоянны: для антигена - 1:4000, для сенсибилизирующих антител - 1:9000, конъюгата - 1:3500. В качестве контрольных сывороток для анализа применяли сыворотки, специфичные к определенным штаммам вируса ящура с активностью 1:256. Их таблицы 4 следует, что при разведении детекторных антител 1:5000 достигалось получение достоверного результата (1:256 или 8 log2 SN50). При меньших разведений антител наблюдали высокие фоновые значения, что не позволяло получить корректный результат. При большем разведении наблюдали снижение детектируемого значения титра антител в сыворотках крови животных. При исследовании неспецифических и отрицательных сывороток отмечали отрицательные результаты, что свидетельствовало о высокой специфичности разработанного способа.
Для анализа исследовали следующие разведения антигена: 1:2000, 1:3000, 1:4000, 1:5000. Разведения остальных компонентов были постоянны: для детекторных антител - 1:5000, для сенсибилизирующих антител - 1:9000, конъюгата - 1:3500. В качестве контрольных сывороток для анализа применяли сыворотки, специфичные к определенным штаммам вируса ящура с активностью 1:256. Их таблицы 5 следует, что при разведении антигена 1:4000 достигалось получение достоверного результата (1:256 или 8 log2 SN50). При меньших разведениях наблюдали высокие фоновые значения, что не позволяло получить корректный результат. При большем разведении наблюдали снижение детектируемого значения титра антител в сыворотках крови животных.
При исследовании неспецифических и отрицательных сывороток отмечали отрицательные результаты, что свидетельствовало о высокой специфичности разработанного способа.
Таким образом, в ходе лабораторных исследований доказано, что рабочие разведения антигена вируса ящура штамма «О №2356/Пакистан/2018» генотипа O/ME-SA/PanAsia2ANT-10, сенсибилизирующих и детекторных антител составили 1:4000, 1:9000, 1:5000, соответственно.
Пример 5. Применение тест-системы жидкофазного блокирующего непрямого «сэндвич»-варианта ИФА для определения титра антител против антигена вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/МЕ-SA/PanAsia2ANT-10.
Исследовали 12 сывороток крови животных, полученных после иммунизации инактивированными сорбированными вакцинами против ящура, содержащими антиген вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10. Определены значения титра антител с применением разработанной тест-системы ИФА, а также данные сыворотки были исследованы в реакции нейтрализации в чувствительной перевиваемой монослойной клеточной линии IB-RS-2, рекомендованной OIE [2]. Полученные результаты отражены в таблице 6, из которой следует, что степень корреляции результатов разработанной тест-системы ИФА (предлагаемое изобретение) и классического метода (РМН) высокая (приближено к 100%).
Пример 6. Определение диагностических показателей разработанной тест-системы для определения титра антител в сыворотках крови животных против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/МЕ-SA/PanAsia2ANT-10 с применением жидкофазного блокирующего непрямого «сэндвич»-варианта ИФА.
Для исследования представленной тест-системы (предлагаемое изобретение) для определения титра антител против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 исследовали стандартные диагностические показатели. Для определения чувствительности предложенной тест-системы анализировали 830 сывороток крови животных, которые являлись заведомо положительными по данным реакции микронейтрализации в чувствительной перевиваемой монослойной клеточной линии почки свиньи IB-RS-2. Титр антител для данных сывороток крови находилась в диапазоне 1:32-1:1448. Постановку ИФА проводили, как отражено выше. Разработанной тест-системой (предлагаемое изобретение) определили, что из 830 образцов сывороток крови 826 определены в качестве положительных, а 4 - в качестве отрицательных (титр 1:16-1:24). Для исследования специфичности метода тестировали 256 отрицательных сывороток крови животных. В результате исследования с помощью ИФА (предлагаемое изобретение) определили, что из 256 отрицательных проб - 256 определены в качестве отрицательных. Пользуясь представленными выше статистическими методами анализа определили, что диагностическая чувствительность (DSe) составила 99,52% (в 95%-ном доверительном интервале: 98,78-99,87%), диагностическая специфичность (DSp) - 100% (в 95%-ном доверительном интервале: 98,57-100,0%), k-критерий - 0,990; прогностичность положительного результата (PPV) - 100%, прогностичность отрицательного результата (NPV) -98,46% (в 95%-ном доверительном интервале: 96,01-99,42%), общая точность (DAc) - 99,63% (в 95%-ном доверительном интервале: 99,06-99,90%) (таблица 7).
Таким образом предлагаемая «Тест-система на основе жидкофазного блокирующего непрямого «сэндвич»-варианта ИФА для определения титра антител против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 в сыворотках крови животных» является специфичной и чувствительной, позволяющей быстро в течение 4-5 часов провести анализ сывороток крови животных с количественным определением значения титра антител против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/МЕ-SA/PanAsia2ANT-10.
Источники информации, принятые во внимание при составлении описания изобретения к заявке на выдачу патента РФ на изобретение «Тест-система на основе жидкофазного блокирующего непрямого «сэндвич»-варианта ИФА для определения титра антител против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 в сыворотках крови животных»:
1. Груздев, К.Н. Программа совместных действий по профилактике и борьбе с ящуром животных в странах СНГ / К.Н. Груздев, В.М. Захаров, A.M. Рахманов // Труды Федерального центра охраны здоровья животных. - Владимир, 2005. - Т. 3. - С. 3-13.
2. OIE. Manual of diagnostic tests and vaccines for terrestrial animals. - Paris, 2018. - Chapter 2.1.8.
3. Гуленкин, B.M. Экономическая эффективность проведения профилактической вакцинации животных против ящура на территории Российской Федерации / В.М. Гуленкин // Труды Федерального центра охраны здоровья животных. - Владимир, 2012. - Т. 10. - С. 31-41.
4. Anon Global Strategy for control of foot-and-mouth disease. - In, Bangkok, Thailand, - 2012. - P. 27-29.
5. Динамика развития противоящурного гуморального иммунитета у крупного рогатого скота, иммунизированного трехвалентной сорбированной вакциной типов А, О, Азия-1 / Д.В. Михалишин, Т.Н. Лезова // Труды Федерального центра охраны здоровья животных. - Владимир, 2007. - Т. 5. - С. 75-82.
6. Wong C.L., Yong C.Y., Ong Н.K., Но K.L., Tan W.S. Advances in the Diagnosis of Foot-and-Mouth Disease // Front Vet Sci. - 2020 Aug 21. - V.7. - P. 477.
7. Curry S., Abu-Ghazaleh R., Blakemore W., Fry E., Jackson Т., King A., Lea S., Logan D., Newman J., Stuart D. Crystallization and preliminary X-ray analysis of three serotypes of foot-and-mouth disease virus // J. Mol Biol. - 1992. - V. 228(4). - P. 1263-1268.
8. Fry E.E., Stuart D.I., Rowlands D.J. The structure of foot-and-mouth disease virus // Curr Top Microbiol Immunol - 2005. - V. 288. - P. 71-101.
9. Palmenberg A.C. Proteolytic processing of picornaviral polyprotein // Annu Rev Microbiol. - 1990. - V. 44. - P. 603-623.
10. Curry S., Fry E., Blakemore W., Abu-Ghazaleh R., Jackson Т., King A., Lea S., Newman J., Stuart D. Dissecting the roles of VP0 cleavage and RNA packaging in picornavirus capsid stabilization: the structure of empty capsids of foot-and-mouth disease virus // J. Virol. - 1997. - V. 71(12). - P. 9743-9752.
11. Curry S.R. Zunszain P.A., Leatherbarrow R.J. Foot-and-mouth disease virus 3C protease: recent structural and functional insights into an antiviral target // Int J Biochem Cell Biol. - 2007. - V. 39(1). - P. 1-6.
12. Oem J.K., Park J.H., Lee K.N., Kim Y.J., Kye S.J., Park J.Y., Song H.J. Characterization of recombinant foot-and-mouth disease virus pentamer-like structures expressed by baculovirus and their use as diagnostic antigens in a blocking ELISA // Vaccine. - 2007. - V. 25(20). - P. 4112-412.
13. Lewis S.A., Morgan D.O., Grubman M.J. Expression, processing, and assembly of foot-and-mouth disease virus capsid structures in heterologous systems: induction of a neutralizing antibody response in guinea pigs // J. Virol. - 1991. - V. 65(12). - P.6572-6580.
14. Cao Y., Lu Z., Sun J., Bai X., Sun P., Bao H., Chen Y., Guo J., Li D., Liu X., Liu Z. Synthesis of empty capsid-like particles of Asia I foot-and-mouth disease virus in insect cells and their immunogenicity in guinea pigs // Vet. Microbiol. - 2009. -V. 137(1-2).-P. 10-17.
15. Hamblin C, Barnett I.Т., Hedger R.S. A new enzyme-linked immunosorbent assay (ELISA) for the detection of antibodies against foot-and-mouth disease virus. I. Development and method of ELISA // J. Immunol. Methods. - 1986. -V. 93(1).-P. 115-121.
16. Grubman M.J., Moraes M.P., Diaz-San Segundo F., Pena L., de los Santos T. Evading the host immune response: how foot-and-mouth disease virus has become an effective pathogen // FEMS Immunol Med Microbiol. - 2008. - V. 53(1). - P. 8-17.
17. Ma L.N., Zhang J, Chen H.T., Zhou J.H., Ding Y.Z., Liu Y.S. An overview on ELISA techniques for FMD // Virol J. - 2011 Sep 4. - V. 8. - P. 419.
18. Diagnostic assays developed for the control of foot-and-mouth disease in India / Sharma G.K., Mahajan S., Matura R., Subramaniam S., Ranjan R., Biswal J., Rout M., Mohapatra J.K., Dash B.B., Sanyal A., Pattnaik B. Diagnostic assays developed for the control of foot-and-mouth disease in India // World J Virology. -2015.-V. 4(3).-P. 295-302.
| название | год | авторы | номер документа |
|---|---|---|---|
| Тест-система для определения титра антител против структурных белков вируса ящура штамма "Азия-1 N 2356/14/2018" с помощью жидкофазного блокирующего непрямого "сэндвич"-варианта ИФА | 2023 |
|
RU2812211C1 |
| Способ быстрого количественного определения уровня гуморального иммунитета животных к штамму О N2311/Забайкальский/2016 генотипа О/ME-SA/Ind-2001 вируса ящура после вакцинации с помощью жидкофазного "сэндвич"-варианта ИФА | 2022 |
|
RU2796393C1 |
| Тест-система на основе жидкофазного блокирующего непрямого "сэндвич"-варианта ИФА для определения титра антител против вируса ящура штамма О N2047/Саудовская Аравия/2008 генотипа O/ME-SA/PanAsia2 в сыворотках крови животных | 2022 |
|
RU2791614C1 |
| Штамм O N 2356/Пакистан/2018 вируса ящура Aphtae epizooticae генотипа O/ME-SA/PanAsia2 для изготовления биопрепаратов для диагностики ящура | 2023 |
|
RU2801950C1 |
| Тест-система для определения титра антител против полных вирусных частиц штамма "О/Кения/2017" вируса ящура с применением жидкофазного "сэндвич"-варианта ИФА | 2023 |
|
RU2821894C1 |
| Тест-система для определения антител к структурным белкам вируса ящура генотипа A/ASIA/Iran-05 с помощью жидкофазного блокирующего иммуноферментного анализа | 2024 |
|
RU2834234C1 |
| Тест-система для количественной детекции антител против 146S компонента вируса ящура генотипа O/EA-3 в сыворотках крови животных на основе жидкофазного иммуноферментного анализа | 2023 |
|
RU2817382C1 |
| Вакцина против ящура генотипа O/ME-SA/PanAsia2из штамма "О N2356/Пакистан/2018" культуральная инактивированная сорбированная | 2023 |
|
RU2810131C1 |
| Тест-система для детекции антител к структурным белкам штамма "SAT-2/Eritrea/1998" вируса ящура в жидкофазном варианте иммуноферментного анализа | 2023 |
|
RU2825453C1 |
| Тест-система для выявления антител к структурным белкам вируса ящура штамма "SAT-1/Кения/2017" с помощью жидкофазного блокирующего непрямого "сэндвич"-варианта ИФА | 2023 |
|
RU2821044C1 |
Настоящее изобретение относится к области биотехнологии, а именно к тест-системе жидкофазного блокирующего непрямого «сэндвич»-варианта ИФА для определения титра антител против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 в сыворотках крови животных. Изобретение эффективно для количественного определения титра антител против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 в широком диапазоне 4,0-10,5 log2 SN50 для последующего анализа иммунного статуса животных в отношении ящура. 2 з.п. ф-лы, 4 ил., 7 табл., 6 пр.
1. Тест-система на основе жидкофазного блокирующего непрямого «сэндвич»-варианта ИФА для определения титра антител против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 в сыворотках крови животных, содержащая специфические компоненты: культуральный инактивированный лиофилизированный вирус ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10; сенсибилизирующие антитела - лиофилизированные иммуноглобулины G кролика против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10; детекторные антитела - лиофилизированные иммуноглобулины G морской свинки против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/МЕ-SA/PanAsia2ANT-10; контроль 1 - лиофилизированную положительную сыворотку крови телят к антигену вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10, с процентом ингибиции ≥75%; контроль 2 - лиофилизированную положительную сыворотку крови телят к антигену вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10, с процентом ингибиции от 50 до 75%; контроль 3 - лиофилизированную сыворотку крови телят, не содержащую антитела к вирусу ящура - отрицательный контроль; лиофилизированную фетальную сыворотку крови крупного рогатого скота, нормальную для блокирования открытых сайтов связывания; антивидовой конъюгат - лиофилизированные иммуноглобулины кролика против Ig G морской свинки, конъюгированные с пероксидазой хрена; и неспецифические компоненты: карбонатно-бикарбонатный буфер рН 9,5-9,7 для разведения антигена; 20-кратный концентрат буферного раствора; хромогенный субстрат ABTS - 2,2-азино-ди-3-этилбензоаминосульфоновая кислота; «стоп»-раствор - 0,5%-ный раствор додецилсульфата натрия; при этом для определения процента ингибиции используется модифицированная формула: ПИ (%) = (1-(OD415 сыворотки - OD415 КК)/(OD415 КА - OD415 КК)) × 100%, а за титр антител принимается наибольшее разведение исследуемой сыворотки крови, для которой значение процента ингибиции составляет ≥50%.
2. Тест-система по п. 1, отличающаяся тем, что предполагает использование ноноксинона-40 для очистки антигена вируса ящура штамма «О №2356/Пакистан/2018» генотипа O/ME-SA/PanAsia2ANT-10.
3. Тест-система по п. 1, отличающаяся тем, что является специфичной и чувствительной, позволяющей быстро в течение 4-5 часов провести анализ сывороток крови животных с определением уровня антител против вируса ящура штамма «О №2356/Пакистан/2018» генотипа О/ME-SA/PanAsia2ANT-10 и определять их титр в диапазоне 4,0-10,5 log2 SN50.
| MA L | |||
| et al | |||
| An overview on ELISA techniques for FMD, Virology Journal, 2018, vol.8 | |||
| Тест-система на основе жидкофазного блокирующего непрямого "сэндвич"-варианта ИФА для определения титра антител против вируса ящура штамма О N2047/Саудовская Аравия/2008 генотипа O/ME-SA/PanAsia2 в сыворотках крови животных | 2022 |
|
RU2791614C1 |
| КАМАЛОВА Н.Е | |||
| Значение комплекса методов лабораторной диагностики в борьбе с ящуром, Ветеринарная патология, 2006, No | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Жильцова М | |||
| В | |||
| и др | |||
| Изучение чувствительности культур клеток и восприимчивых животных к изоляту вируса ящура типа | |||
Авторы
Даты
2024-01-25—Публикация
2023-04-04—Подача