Настоящее изобретение относится к сфере лечения рака, конкретнее - к иммунотерапевтическим способам. В частности, настоящее изобретение относится к различным пептидам, которые являются полезными для иммунотерапии рака.
Рак является одной из ведущих причин смертности людей по всему миру. Согласно данным Всемирной Организации Здравоохранения (ВОЗ), только в 2012 году было выявлено 14 миллионов новых случаев болезни и зарегистрировано 8,2 миллионов смертей, обусловленных раком по всему миру, причем ожидается, что в следующей второй декаде количество новых случаев увеличится приблизительно на 70%. До настоящего времени, более чем 60% новых случаев рака ежегодно возникают в Африке, Азии и странах Центральной и Южной Америки. Вклад этих регионов в общемировую смертность составляет 70%. Среди мужчин наиболее часто встречаются раковые заболевания следующих пяти локализаций: рак легких, рак предстательной железы, колоректальный рак, рак желудка и рак печени; в то время, как у женщин преобладает рак молочной железы, колоректальный рак, рак легких, рак шейки матки и рак желудка.
Для лечения рака применяется хирургическое лечение, лучевая терапия, цитотоксическая химиотерапия и эндокринные манипуляции; указанные способы обычно комбинируют последовательным образом для лучшего контроля над заболеванием. Однако основными ограничениями истинной эффективности этих стандартных способов лечения являются их нечеткая специфичность, что приводит к побочному повреждению здоровых тканей вследствие лечения, медленная скорость излечения, а также приобретенная лекарственная устойчивость.
В последние годы наблюдается колоссальный прогресс в разработке методов лечения рака, в частности, благодаря значительным достижениям в анализе профиля экспрессии опухолей и нормальных клеток, а также недавним исследованиям и первым клиническим результатам иммунотерапии или молекулярной таргетной терапии, что начинает менять наше восприятие этой болезни.
Перспективные способы противораковой иммунотерапии в настоящее время стали реальностью, а данные о том, что иммунная система хозяина может распознавать опухолевые антигены, позволили разработать противораковые лекарственные средства, которые сейчас уже одобрены регулирующими органами, такими как Управление по контролю за продуктами питания и лекарственными средствами (FDA) и Европейская организация по надзору за лекарственными средствами (ЕМА). Различные терапевтические подходы включают, среди прочих, адоптивный перенос ex vivo размноженных инфильтрирующих опухоль лимфоцитов (ТИЛ), противоопухолевые вакцины, иммуностимулирующие цитокины и их варианты, агонисты паттерн-распознающих рецепторов (PRR аббрев. от англ. Pattern Recognition Receptor), а также иммуномодулирующие моноклональные антитела, направленные против опухолевых антигенов или иммунных контрольных точек. (Galuzzi et al., Classification of current anticancer immunotherapies. Oncotarget. 2014 Dec 30;5(24):12472-508).
К сожалению, у значительного числа пациентов все же присутствует первичная резистентность к некоторым из таких иммунотерапевтических способов или развивается вторичная резистентность во время лечения. Например, было сообщено о трехлетней выживаемости при неоперабельной или метастатической меланоме при лечении анти-CTLA-4 антителом, Ипилимумабом, которая составляла приблизительно 20% (Snyder et al., Genetic basis for clinical response to CTLA-4 blockade in melanoma. N Engl J Med. 2014 Dec 4;371(23):2189-2199; Schadendorf et al., Pooled Analysis of Long-Term Survival Data from Phase II and Phase III Trials of Ipilimumab in Unresectable or Metastatic Melanoma. J Clin Oncol. 2015 Jun 10;33(17): 1889-94), причем также было сообщено о трехлетней выживаемости при использовании другого ингибитора контрольной точки, Ниволумаба, направленного против PD-1, которая составляла около 44% при почечно-клеточной карциноме (RCC) и 18% при немелкоклеточной карциноме легких (NSCLC) (Мс Dermott et al., Survival, Durable Response, and Long-Term Safety in Patients With Previously Treated Advanced Renal Cell Carcinoma Receiving Nivolumab. J Clin Oncol. 2015 Jun 20;33(18):2013-20; Gettinger et al., Overall Survival and Long-Term Safety of Nivolumab (Anti-Programmed Death 1 Antibody, BMS-936558, ONO-4538) in Patients with Previously Treated Advanced Non-Small-Cell Lung Cancer. J Clin Oncol. 2015 Jun 20;33(18):2004-12). Таким образом, фундаментальная устойчивость к лекарственному средству представляет собой существенный барьер для эффективности указанных иммунотерапевтических средств. Очевидно, что для того, чтобы преодолеть этот барьер требуются новые различные подходы.
Отсутствие ответа у большого количества субъектов, получавших лечение при помощи указанных иммунотерапевтических способов, может быть связано с недостаточным противоопухолевым иммунным ответом (например, дефектом в презентации антигена антигенпрезентирующими клетками (АПК) или в распознавании антигена Т-клетками). Другими словами, положительный ответ на иммунотерапию коррелирует со способностью иммунной системы продуцировать специфические субпопуляции лимфоцитов, способных распознавать антигены, рестриктированные по первому классу основного комплекса гистосовместимости (МНС I класса) и экспрессируемые раковыми клетками человека (Kvistborg et al., Human cancer regression antigens. Curr Opin Immunol. 2013 Apr; 25(2):284-90). Эта гипотеза убедительно подтверждается данными, демонстрирующими, что ответ на адоптивный перенос инфильтрирующих опухоль лимфоцитов (ТИЛ) напрямую коррелирует с количеством CD8+Т-клеток, перенесенных пациенту (Besser et al., Adoptive transfer of tumor-infiltrating lymphocytes in patients with metastatic melanoma: intent-to-treat analysis and efficacy after failure to prior immunotherapies. Clin Cancer Res. 2013 Sep 1; 19(17):4792-800). Сильный противоопухолевый ответ, таким образом, будет зависеть от презентации иммунореактивных пептидов и присутствия достаточного количества реактивных клеток, "натренированных" на распознавание этих антигенов.
Вакцинация препаратами на основе опухолевых антигенов представляет собой уникальный подход к терапии рака, который вызывает большой интерес, поскольку позволяет задействовать собственную иммунную систему пациента для распознавания, нападения и разрушения опухолей, специфическим и надежным образом. Действительно, известно, что опухолевые клетки экспрессируют большое количество пептидных антигенов, которые распознаются иммунной системой. Вакцины на основе таких антигенов, таким образом, предлагают большие возможности не только для улучшения общей выживаемости пациентов, но и для мониторинга иммунных ответов и получения одобренных GMP продуктов благодаря их низкой токсичности и небольшому молекулярному весу опухолевых антигенов. Примерами опухолевых антигенов являются, среди прочих, побочные продукты белков, транскрибируемых с молчащих в норме генов или гиперэкспрессируемых генов, а также белков, экспрессируемых онковирусами (Kvistborg et al., Human cancer regression antigens. Curr Opin Immunol. 2013 Apr; 25(2):284-90), а также неоантигены, полученные в результате точечных мутаций клеточных белков. Последние представляют особый интерес, поскольку было показано, что они напрямую связаны с увеличением общей выживаемости пациентов, получавших лечение CTLA-4 ингибиторами (Snyder et al., Genetic basis for clinical response to CTLA-4 blockade in melanoma. N Engl J Med. 2014 Dec 4; 371(23):2189-2199; Brown et al., Neo-antigens predicted by tumor genome meta-analysis correlate with increased patient survival. Genome Res. 2014 May; 24(5):743-50).
Тем не менее количество опухолевых антигенов человека, на основе которых могут быть разработаны противораковые вакцины, ограничено. В частности, антигены, полученные из мутировавших или модифицированных собственных белков, могут индуцировать иммунную толерантность и/или нежелательные побочные эффекты, связанные с аутоиммунными реакциями.
Таким образом, в данной области существует потребность в поиске альтернативных способов лечения рака, которые позволят преодолеть существующие ограничения.
Цель изобретения заключается в удовлетворении вышеупомянутых потребностей. Эта цель достигается посредством изложенной ниже сущности изобретения, в частности вариантов осуществления настоящего изобретения и прилагаемой формулы изобретения.
ОБЪЕКТЫ ИЗОБРЕТЕНИЯ
Настоящее изобретение конкретно предлагает следующие объекты:
1. Антигенный пептид, включающий аминокислотную последовательность, как указано в любой из SEQ ID NOs 1-580 и 861-887.
2. Антигенный пептид по п. 1, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 1-580.
3. Антигенный пептид по п. 1, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 861 887.
4. Антигенный пептид по п. 1 или п. 2, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 1-160, 162-253 и 255-580.
5. Антигенный пептид по п. 2 или п. 4, причем указанный антигенный пептид состоит из или включает в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 31, 32, 87, 97, 145, 193, 194, 220, 221, 255, 521 и 524.
6. Антигенный пептид по любому из п.п. 1-5, причем указанный антигенный пептид состоит из или включает в себя аминокислотную последовательность, как указано любой из SEQ ID NOs 30, 31, 32, 87, 97, 193, 194, 220, 255, 521 и 524.
7. Антигенный пептид по любому из п.п. 1-6, причем указанный антигенный пептид состоит из или включает в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 31, 32, 87, 97, 194, 220, 255, 521 и 524.
8. Антигенный пептид по любому из п.п. 1-7, причем указанный антигенный пептид состоит из или включает в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 32, 87, 97, и 194.
9. Антигенный пептид по любому из п.п. 1-2, причем указанный антигенный пептид состоит из или включает в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 32, 194, 220, 254 или 255.
10. Иммуногенное соединение, включающее антигенный пептид по любому из п.п. 1-9.
11. Иммуногенное соединение по п. 10, причем антигенный пептид соединен с молекулой носителя.
12. Иммуногенное соединение по п. 11, причем молекула носителя представляет собой белок-носитель или пептид-носитель.
13. Иммуногенное соединение по любому из п.п. 10-12, состоящее из полипептида формулы (I) или включающее его
PepNt- CORE-PepCt (I)
где:
-"PepNt" состоит из полипептида длиной от 0 до 500 аминокислотных остатков и расположенного на N-конце полипептида формулы (I);
-CORE состоит из антигенного пептида, как определено в любом из п.п. 1-6; и
- "PepCt" состоит из полипептида длиной от 0 до 500 аминокислотных остатков и расположенного на С-конце полипептида формулы (I).
14. Наночастица, нагруженная
- по меньшей мере одним антигенным пептидом по любому из п.п. 1-9, или
- по меньшей мере одним иммуногенным соединением по любому из п.п. 10-13;
и необязательно адъювантом.
15. Клетка, нагруженная антигенным пептидом по любому из п.п. 1-9, или иммуногенным соединением по любому из п.п. 10-13.
16. Клетка по п. 15, причем указанная клетка представляет собой антигенпрезентирующую клетку (АПК), предпочтительно дендритную клетку.
17. Нуклеиновая кислота, кодирующая антигенный пептид по любому из п.п. 1-9, полипептид формулы (I), как определено в пункте 13, или иммуногенное соединение по любому из п.п. 10-13, причем указанное иммуногенное соединение представляет собой пептид или белок.
18. Нуклеиновая кислоты по п. 17, причем нуклеиновая кислота представляет собой молекулу ДНК или молекулу РНК; предпочтительно, выбранную из геномной ДНК; кДНК; миРНК; рРНК; иРНК; антисмысловой ДНК; антисмысловой РНК; рибозима; комплементарных РНК и/или ДНК последовательностей; РНК и/или ДНК последовательностей с элементами экспрессии, регуляторными элементами и/или промоторами или без них; вектор; а также их комбинации.
19. Клетка-хозяин, содержащая нуклеиновую кислоту по п. 17 или п. 18.
20. Клетка-хозяин по п. 19, причем нуклеиновая кислота представляет собой вектор.
21. Клетка-хозяин по любому из п.п. 19-20, причем указанная клетка хозяин представляет собой бактериальную клетку, предпочтительно бактериальную клетку кишечной микрофлоры
22. Фармацевтическая композиция, включающая:
- антигенный пептид по любому из п.п. 1-9,
- иммуногенное соединение по любому из п.п. 10-13,
- наночастицу по п. 14,
- клетку по п. 15 или п. 16,
- нуклеиновую кислоту по п. 17 или п. 18, и/или
- клетку-хозяина по любому из п.п. 19-21,
и возможно один или более фармацевтически доступный эксципиент или носитель.
23. Фармацевтическая композиция по п. 22, дополнительно включающая один или более иммуностимулирующий агент.
24. Фармацевтическая композиция по п. 23, причем иммуностимулирующий агент выбран из группы, включающей иммуноадъюванты и антигенпрезентирующие клетки.
25. Фармацевтическая композиция по п. 24, причем антигенпрезентирующая клетка представляет собой дендритную клетку.
26. Фармацевтическая композиция по любому из п.п. 22-25, причем композиция включает:
(а) по меньшей мере два различных антигенных пептида по любому из п.п. 1-9;
(б) по меньшей мере два различных иммуногенных соединения по любому из п.п. 10-13;
(в) по меньшей мере, две различные наночастицы по п. 14; и/или
(г) по меньшей мере две различные нуклеиновые кислоты по п. 17 или п. 18.
27. Набор, включающий
- антигенный пептид по любому из п.п. 1-9,
- иммуногенное соединение по любому из п.п. 10-13,
- наночастицу по п. 14,
- клетку по п. 15 или п. 16,
- нуклеиновую кислоту по п. 17 или п. 18,
- клетку-хозяина по любому из п.п. 19-21, и/или
- фармацевтическую композицию по любому из п.п. 22-26.
28. Набор по п. 27 дополнительно включающий листок-вкладыш или инструкцию по применению с рекомендациями по профилактике и лечению рака путем применения антигенного пептида, иммуногенного соединения, наночастицы, клетки, нуклеиновой кислоты, клетки-хозяина и/или фармацевтической композиции.
29. Набор по п. 27 или п. 28, причем набор содержит по меньшей мере два различных антигенных пептида по любому из п.п. 1-9.
30. Набор по п. 27 или п. 28, причем набор содержит по меньшей мере два различных иммуногенных соединения по любому из п.п. 10-13.
31. Набор по п. 27 или п. 28, причем набор содержит по меньшей мере две различные наночастицы по п. 14.
32. Набор по п. 27 или п. 28, причем набор содержит по меньшей мере две различные нуклеиновые кислоты по п. 15 или 16.
33. Антигенный пептид по любому из п.п. 1-9,
- иммуногенное соединение по любому из п.п. 10-13,
- наночастица по п. 14,
- клетка по п. 15 или 16,
- нуклеиновая кислота по п. 17 или 18,
- клетка хозяин по п. 19-21,
- фармацевтическая композиция по любому из п.п. 22-26 или
- набор по любому из п.п. 27-32
для применения в профилактике и/или лечении рака.
34. Антигенный пептид, иммуногенное соединение, наночастица, клетка, нуклеиновая кислота, клетка хозяин, фармацевтическая композиция или набор для применения по п. 33, причем рак выбран из глиомы, рака почки, рака кожи, конкретнее - меланомы, рака легких, рака яичников, рака молочной железы, колоректального рака, рака печени, рака поджелудочной железы, рака головы и шеи, рака уротелия и рака предстательной железы.
35. Комбинация по меньшей мере двух различных антигенных пептидов по любому из п.п. 1-9 для применения в профилактике и/или лечении рака.
36. Комбинация по меньшей мере двух различных иммуногенных соединений по любому из п.п. 10-13 для применения в профилактике и/или лечении рака.
37. Комбинация по меньшей мере двух различных наночастиц по любому из п.п. 14 для применения в профилактике и/или лечении рака.
38. Комбинация по меньшей мере двух различных нуклеиновых кислот по п. 17 или п. 18 для применения в профилактике и/или лечении рака.
39. Комбинация для применения по любому из п.п. 35-38, причем по меньшей мере два различных компонента находятся в составе разных композиций.
40. Комбинация для применения по любому из п.п. 35-38, причем по меньшей мере два различных компонента находятся в составе одной композиции.
41. Комбинация для применения по любому из п.п. 35-39, причем по меньшей мере два различных компонента вводятся разными способами.
42. Комбинация для применения по любому из п.п. 35-40, причем по меньшей мере два различных компонента вводятся одним способом.
43. Комбинация для применения по любому из п.п. 35-39, 41 и 42, причем по меньшей мере два различных компонента вводятся последовательно.
43. Комбинация для применения по любому из п.п. 35-42, причем по меньшей мере два различных компонента вводятся приблизительно в одно и то же время.
44. Способ профилактики и/или лечения рака, или инициации, усиления или пролонгирования противоопухолевого ответа у субъекта, нуждающегося в этом, включающий введение субъекту
- антигенного пептида по любому из п.п. 1-9,
- иммуногенного соединения по любому из п.п. 10-13,
- наночастицы по п. 14,
- клетки по п. 15 или п. 16,
- нуклеиновой кислоты по п. 17 или п. 18,
- клетки-хозяина по любому из п.п. 19-21,
- фармацевтической композиции по любому из п.п. 22-26, и/или
- комбинации, как определено в любом из п.п. 35-44.
45. Способ по п. 45, где рак выбран из глиомы, рака почки, рака кожи, конкретнее - меланомы, рака легких, рака яичников, рака молочной железы, колоректального рака, рака печени, рака поджелудочной железы, рака головы и шеи, рака уротелия и рака предстательной железы.
46. Мультимер пептид-МНС (рМНС), включающий антигенный пептид по любому из п.п. 1-9.
Изобретение и в частности объекты, перечисленные выше, подробно описываются в тексте заявки ниже.
ОПРЕДЕЛЕНИЯ
Если дополнительно не оговаривается иное, научные и технические термины, используемые в настоящем описании, будут иметь значения, которые обычно хорошо известны специалистам в данной области. Кроме того, если иное не предусмотрено требованиями, используемые в описании условные обозначения, а также методики культивирования клеток и тканей хорошо известны специалистам в данной области.
Такие методики подробно описаны в литературе, например у Owen и соавт. (Kuby Immunology, 7th, edition, 2013 - W. H. Freeman) и Sambrook и соавт. (Molecular cloning: A laboratory manual 4th edition, Cold Spring Harbor Laboratory Press - Cold Spring Harbor, NY, USA, 2012).
Тем не менее, при использовании различных терминов в настоящем описании более применимыми являются следующие конкретные определения.
Термины "пептид", "полипептид", "белок" и также различные варианты указанных терминов относятся к пептидам, олигопептидам, полипептидам или белкам, включающим по меньшей мере две аминокислоты, соединенные между собой предпочтительно обычной пептидной связью или, альтернативно, модифицированной пептидной связью, как, например в случае изостерических пептидов. Термин "(поли)пептид" относится к пептиду и/или полипептиду. В частности, термины "пептид", "полипептид" и "белок" относятся к последовательной цепи аминокислот любой длины, причем аминокислоты соединены между собой пептидными связями (-NHCO-). Пептиды, полипептиды и белки могут играть структурную и/или функциональную роль в клетке in vitro и/или in vivo. Термины "пептид", "полипептид", "белок", предпочтительно объединяют аминокислотные цепи, длина которых составляет от 2-х до, приблизительно по меньшей мере 1000 аминокислотных остатков. Термин "пептид", предпочтительно объединяет аминокислотные цепи, длина которых составляет приблизительно менее 30 аминокислот, причем термины "полипептид" и "белок" предпочтительно объединяют аминокислотные цепи длиной по меньшей мере 30 аминокислот. Термины "полипептид" и "белок" используются в настоящем описании взаимозаменяемо. Согласно предпочтительному варианту осуществления изобретения, термины "пептид", "полипептид" и "белок" также включают "пептидомиметики", которые обозначаются, как пептидные аналоги, содержащие непептидные структурные элементы, причем такие пептиды способны имитировать биологическую активность натурального исходного пептида или наоборот противодействовать ей. Пептидомиметики не обладают свойствами классических белков, такими, как пептидные связи, расщепляемые ферментами. В частности, пептид, полипептид или белок может помимо основных аминокислот включать аминокислоты, которые отличаются от 20 аминокислот, зашифрованных генетическим кодом, либо он может полностью состоять из аминокислот, отличающихся от тех 20, что зашифрованы в генетическом коде. В частности, пептид, полипептид или белок в контексте настоящего изобретения могут в равной степени состоять из аминокислот, модифицированных естественными способами, такими как посттрансляционные процессы созревания или химические процессы, которые хорошо известны специалистам в данной области. Такие модификации подробно описываются в литературе. Такие модификации могут располагаться в любом месте полипептида: в пептидном остове, в аминокислотной цепи или даже на карбокси- или амино-концевых участках. В частности, пептид или полипептид может быть разветвленным после убиквитинирования или быть циклическим, с разветвлением или без. Такой тип модификации может быть результатом естественных или синтетических посттрансляционных процессов, которые хорошо известны специалистам в данной области. Термины "пептид", "полипептид", "белок" в контексте настоящего изобретения, в частности, также включают модифицированные пептиды, полипептиды и белки. Например модификации пептида, полипептида или белка могут включать ацетилирование, ацилирование, АДФ-рибозилирование, амидирование, ковалентное присоединение нуклеотида или нуклеотидного производного, ковалентное присоединение липида или липидного производного, ковалентное присоединение фосфатидилинозитола, ковалентное или нековалентное перекрестное связывание, циклизация, образование дисульфидных связей, деметилирование, гликозилирование, включая пегилирование, гидроксилирование, иодирование, метилирование, миристоилирование, окисление, протеолитические процессы, фосфорилирование, пренилирование, рацемизацию, сенелоилирование, сульфатирование, добавление аминокислот, такое, как аргинилирование или убиквитинирование. Такие модификации детально описаны в литературе (Proteins Structure and Molecular Properties (1993) 2nd Ed., Т. E. Creighton, New York; Post-translational Covalent Modifications of Proteins (1983) В. C. Johnson, Ed., Academic Press, New York; Seifter et al. (1990) Analysis for protein modifications and nonprotein cofactors, Meth. Enzymol. 182: 626-646 and Rattan et al., (1992) Protein Synthesis: Post-translational Modifications and Aging, Ann NY Acad Sci, 663: 48-62). Соответственно, термины "пептид", "полипептид", "белок" предпочтительно также включают, например липопептиды, липопротеины, гликопептиды, гликопротеины и подобные соединения.
Согласно предпочтительному варианту осуществления изобретения, (поли)пептид или белок представляет собой "классический" (поли)пептид или белок, причем "классический" (поли)пептид или белок обычно состоит из аминокислот, выбранных из 20 аминокислот, зашифрованных в генетическом коде, соединенных между собой обычной пептидной связью.
Как хорошо известно из области техники, пептиды, полипептиды и белки могут кодироваться нуклеиновыми кислотами. Термины "нуклеиновая кислота", "молекула нуклеиновой кислоты", "последовательность нуклеиновой кислоты", "полинуклеотид", "нуклеотидная последовательность" используются в настоящем описании взаимозаменяемо и обозначают точную последовательность натуральных нуклеотидов (например, А, Т, G, С и U) или синтетических нуклеотидов, то есть цепь, состоящую по меньшей мере из двух нуклеотидов. В частности, термины "нуклеиновая кислота", "молекула нуклеиновой кислоты", "последовательность нуклеиновой кислоты", "полинуклеотид", "нуклеотидная последовательность" относятся к ДНК или РНК. Нуклеиновые кислоты, предпочтительно включают одноцепочечные, двуцепочечные или частично двуцепочечные ДНК или РНК, предпочтительно, выбранные из геномной ДНК (гДНК), комплементарной ДНК (кДНК), рибосомальной ДНК (рДНК), а также продукта транскрипции указанной ДНК, такого как РНК. Предпочтительными примерами нуклеиновых кислот являются рибосомальная РНК (рРНК), информационная РНК (иРНК); антисмысловая ДНК, антисмысловая РНК; комплементарные РНК и/или ДНК последовательности, рибозимы, (комплементарные) последовательности РНК/ДНК с элементами экспрессии и без них, вектор; мини-ген, фрагменты генов, регуляторные элементы, промоторы, а также их комбинации. Дополнительными предпочтительными примерами нуклеиновых кислот (молекул) и/или полинуклеотидов являются, например рекомбинантный полинуклеотид, вектор, олигонуклеотид, молекула РНК, такая как рРНК, иРНК или транспортная РНК (тРНК), или молекула ДНК, как описано выше. Таким образом, предпочтительно, чтобы нуклеиновая кислота (молекула) представляла собой молекулу ДНК или молекулу РНК; предпочтительно, выбранную из группы гДНК; кДНК; рРНК; иРНК; антисмысловая ДНК; антисмысловая РНК; комплементарные РНК и/или ДНК последовательности; РНК и/или ДНК последовательности с элементами экспрессии или без них, регуляторные элементы, и/или промоторы; вектор; а также их комбинации. Специалисту в данной области не составляет труда определить нуклеотидную последовательность, которая может кодировать специфическую аминокислотную последовательность.
Полипептиды и/или нуклеиновые кислоты в соответствии с настоящим изобретением могут быть получены при помощи любого способа, известного из области техники, включая без ограничений указанными, любой рекомбинантный метод, любой метод синтеза ex vivo и подобные методы, а также любые их комбинации. Такие методики подробно описаны в литературе, как уже упоминалось выше.
Термин "антигенный пептид", используемый в настоящем изобретении, относится к пептиду, который способен вызывать/индуцировать, усиливать, пролонгировать или поддерживать иммунный ответ у субъекта, которому он вводится. Конкретнее, антигенный пептид представляет собой вариант последовательности (фрагмент/эпитоп) опухолевого антигена (человека). Другими словами, антигенный пептид, предпочтительно отличается от (фрагмента/эпитопа) опухолевого антигена (человека), но, предпочтительно имеет аминокислотное сходство с (фрагментом/эпитопом) опухолевого антигена (человека). Предпочтительно, иммунный ответ, индуцированный/вызванный, усиленный, пролонгированный или поддерживаемый антигенным пептидом, (также) нацелен на соответствующий (фрагмент/эпитоп) опухолевого антигена (человека).
Используемый в настоящем описании термин "опухолевый антиген" относится к опухолеспецифическим антигенам и опухолеассоциированным антигенам. В целом, термин "опухолевый антиген" в настоящем описании обозначает антигенное вещество, продуцируемое опухолевыми клетками, а иногда и здоровыми клетками, которое может инициировать иммунный ответ при введении субъекту. У людей антигены классифицируются в соответствии с их паттерном экспрессии, функцией или генетической природой, и включают, без ограничений указанными, гиперэкспрессируемые аутоантигены (такие как HER2/neu и его вариант dHER2, р53, опухоль Вильмса 1, рецептор Эфрина, Протеиназа-3, муцин-1, мезотелин, EGFR, CD20); антигены рака яичек (такие как MAGE-1, BAGE, GAGE, NY-ESO-1); мутационные антигены также известные, как неоантигены (такие как мутанты MUM-1, bcr-abl, ras, b-raf, р53, CDK-4, CDC27, бета-катенин, альфа-актенин-4); тканеспецифические дифференцировочные антигены (такие как антигены меланомы Melan A/MART-1, тирозиназа, TRP1/pg75, TRP2, gp100 и ганглиозиды GM3, GM2, GD2 и GD3; антигены рака простаты PSMA, PSA и РАР); вирусные антигены, экспрессируемые онковирусами (такими как HPV, EBV); онкофетальные антигены (такие как альфа-фетопротеин AFP и карциноэмбриональный антиген СЕА); а также универсальные антигены (теломераза, hTERT, сурвивин, mdm-2, CYP-1B1) (Srinivasan and Wolchok, Tumor antigens for cancer immunotherapy: therapeutic potential of xenogeneic DNA vaccines. J Transl Med. 2004 Apr 16;2(1):12). Соответственно, опухолевые антигены человека хорошо известны специалистам в данной области. В частности, субъединица альфа интерлейкина -13 (IL-13Rα2 или IL13RA2) представляет собой мембранносвязанный белок, который у человека кодируется геном IL13RA2. Сообщается, что IL13RA2 является потенциальной мишенью для иммунотерапии (см., Beard et at; Clin Cancer Res; 72(11); 2012). Высокая экспрессия IL13RA2 также ассоциировалась с инвазией, метастазированием в печень и плохим прогнозом колоректального рака (Barderas et al.; Cancer Res; 72(11); 2012). В частности, антигенные пептиды в соответствии с настоящим изобретением, предпочтительно, являются вариантами последовательности (эпитопа/фрагмента) опухолевых антигенов, представленных в Таблице 1 В, и могут применяться, в частности, при заболеваниях, соответствующих конкретному опухолевому антигену из Таблицы 1 В.
Термин "микробиота", используемый в настоящем описании, относится к симбиотическим микроорганизмам, которые можно обнаружить во всех многоклеточных организмах, изученных на сегодняшний день, как растительных, так и животных. В частности, было установлено, что микробиота необходима для иммуногенного, гормонального и метаболического гомеостаза организма хозяина. Микробиота включает бактерии, археи, простейшие, грибы и вирусы. Соответственно, термин "вариант последовательности микробиоты" представляет собой вариант референсной последовательности (конкретно, эпитоп/фрагмент опухолевого антигена человека), который существует у микробиоты (например, содержится в микробиотическом белке). "Вариант последовательности", в частности по всей длине последовательности обычно по меньшей мере на 50% идентичен референсной последовательности, конкретно фрагменту/эпитопу (референсного) опухолевого антигена. Предпочтительно, вариант последовательности по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 75%, более предпочтительно по меньшей мере на 80%, еще более предпочтительно по меньшей мере на 85%, еще более предпочтительно по меньшей мере на 90%, особенно предпочтительно по меньшей мере на 95% и наиболее предпочтительно по меньшей мере на 99% идентичен референсной последовательности конкретно фрагменту/эпитопу (референсного) опухолевого антигена. Идентичность последовательностей может быть рассчитана с помощью методов, хорошо известных из области техники, в частности, как описано ниже. Предпочтительно вариант последовательности сохраняет специфическую функцию референсной последовательности, например, функцию опухолевого эпитопа и/или способность вызывать или поддерживать иммунный ответ. Вариант последовательности микробиоты, предпочтительно выбран из группы, включающей варианты последовательностей бактерий, варианты последовательностей археев, варианты последовательностей простейших, варианты последовательностей грибов и варианты последовательностей вирусов. Более предпочтительно вариант последовательности микробиоты представляет собой вариант последовательности бактерий.
Анатомически микробиота располагается на поверхности или внутри целого ряда тканей и биологических жидкостей, включая кожу, конъюнктиву, молочные железы, влагалище, плаценту, семенную жидкость, матку, фолликулы яичников, легкие, слюну, ротовую полость (в частности, слизистую оболочку ротовой полости) и желудочно-кишечный тракт, в частности, кишечник. В контексте настоящего изобретения вариант последовательности микробиоты, предпочтительно представляет собой вариант последовательности микробиоты желудочно-кишечного тракта (микроорганизмов, населяющих желудочно-кишечный тракт), более предпочтительно, вариант последовательности микробиоты кишечника (микроорганизмов, населяющих кишечник). Соответственно, более предпочтительно, чтобы вариант последовательности микробиоты представлял собой вариант последовательности бактерий кишечника (человека) (то есть вариант последовательности бактерий, населяющих кишечник (человека)).
Хотя микробиоту можно обнаружить во многих многоклеточных организмах (во всех многоклеточных организмах, изученных на сегодняшний день от растений до животных), в контексте настоящего изобретения предпочтительной считается микробиота, обнаруженная в организме человека и на его поверхности. Такая микробиота упоминается в настоящем документе, как "микробиота человека" (причем термин "человек" относится конкретно к локализации / месту проживания микробиоты). В контексте настоящего изобретения вариант последовательности микробиоты представляет собой вариант последовательности микробиоты человека.
Термин "иммуногенное соединение" относится к соединению, содержащему антигенный пептид, заявленный в соответствии с настоящим изобретением. "Иммуногенное соединение" способно индуцировать/вызывать, усиливать, пролонгировать или поддерживать иммунный ответ против указанного антигенного пептида у субъекта, которому оно вводится. Согласно некоторым вариантам осуществления изобретения, иммуногенные соединения содержат по меньшей мере один антигенный пептид, или альтернативно по меньшей мере одно соединение, содержащее такой антигенный пептид, соединенный с белком, таким как белок-носитель.
"Белок-носитель" обычно представляет собой белок, который способен переносить грузы, такие как антигенный пептид, заявленный в соответствии с настоящим изобретением. Например, белок-носитель может переносить свой груз через мембрану. В контексте настоящего изобретения, белок-носитель, в частности (также) относится к белку или полипептиду, который обладает способностью вызывать иммунный ответ против антигенного пептида, с которым он связан. Белки носители хорошо известны из данной области техники.
Альтернативно, такой белок носитель или полипептид может вводиться совместно в форме иммунного адъюванта.
Предпочтительно, антигенный пептид, описанный в настоящем документе, может вводиться одновременно или быть связанным, например, посредством ковалентной или нековалентной связи с белком/пептидом, обладающим иммуноадъювантными свойствами, такими как обеспечение стимуляции CD4+ Th1-клеток. Принимая во внимание, что описанный в настоящем документе антигенный пептид предпочтительно связывается с МНС I класса, CD4+ хэлперные эпитопы могут дополнительно применяться для стимуляции эффективного иммунного ответа. Th1 хэлперные клетки способны поддерживать эффективную активацию дендритных клеток (ДК) и специфическую активацию CTL за счет секреции интерферона гамма (IFN-γ), фактора некроза опухолей альфа (TNF-α) и интерлейкина-2 (IL-2) и усиления экспрессии костимулирующего сигнала на дендритных клетках и Т-клетках (Galaine et al., Interest of Tumor-Specific CD4 T Helper 1 Cells for Therapeutic Anticancer Vaccine. Vaccines (Basel). 2015 Jun 30;3(3):490-502).
Например, адъювантный пептид/белок предпочтительно может отличаться от антигенного пептида, заявленного в соответствии с настоящим изобретением. Предпочтительно, адъювантный пептид/белок способен вызывать иммунную память или оказывать неспецифическую помощь, или представлять собой специфический хэлперный белок. В литературе описано несколько хэлперных пептидов для оказания помощи неспецифическим Т-клеткам, такие как хэлперный белок столбняка, пептид гемоцианин лимфы улитки или PADRE пептид (Adotevi et al., Targeting antitumor CD4 helper T cells with universal tumor-reactive helper peptides derived from telomerase for cancer vaccine. Hum Vaccin Immunother. 2013 May; 9(5): 1073-7, Slingluff CL, The present and future of peptide vaccines for cancer: single or multiple, long or short, alone or in combination? Cancer J. 2011 Sep-Oct; 17(5):343-50). Соответственно, хэлперный белок столбняка, пептид гемоцианина лимфы улитки и PADRE пептид являются предпочтительными примерами таких адъювантных белков/пептидов. В частности, антигенный пептид, как описано в настоящем документе, или полипептид, содержащий указанный антигенный пептид, могут быть связаны, например, ковалентной или нековалентной связью с HHD-DR3 пептидом с последовательностью MAKTIAYDEEARRGLERGLN (SEQ ID NO: 856). Этот пептид является другим примером хэлперного пептида (обладающего иммуноадъювантными свойствами), который является предпочтительным в контексте настоящего изобретения. Другим предпочтительным примером является h-pAg T13L (последовательность: TPPAYRPPNAPIL; SEQ ID NO: 860; Bhasin М, Singh Н, Raghava GP (2003) MHCBN: a comprehensive database of MHC binding and non-binding peptides. Bioinformatics 19: 665 666). Другими примерами предпочтительных хэлперных белков являются UCP2 пептид (например, описанный в WO 2013/135553 А1 или у Dosset М, Godet Y, Vauchy С, Beziaud L, Lone YC, Sedlik C, Liard C, Levionnois E, Clerc B, Sandoval F, Daguindau E, Wain-Hobson S, Tartour E, Langlade-Demoyen P, Borg C, Adotévi O: Universal cancer peptide-based therapeutic vaccine breaks tolerance against telomerase and eradicates established tumor. Clin Cancer Res. 2012 Nov 15;18(22):6284-95. doi: 10.1158/1078-0432. CCR-12-0896. Epub 2012 Oct 2) и пептид BIRC5 (например, как описано в ЕР 2119726 А1 или у Widenmeyer М, Griesemann Н, Stevanovic S, Feyerabend S, Klein R, Attig S, Hennenlotter J, Wernet D, Kuprash DV, Sazykin AY, Pascolo S, Stenzl A, Gouttefangeas C, Rammensee HG: Promiscuous survivin peptide induces robust CD4+ T-cell responses in the majority of vaccinated cancer patients. Int J Cancer. 2012 Jul 1; 131(1): 140-9. doi: 10.1002/ijc.26365. Epub 2011 Sep 14). Наиболее предпочтительным хэлперным пептидом является пептид UCP2 (аминокислотная последовательность: KSVWSKLQSIGIRQH; SEQ ID NO: 859, например, как описано в WO 2013/135553 А1 или у Dosset et al., Clin Cancer Res. 2012 Nov 15;18(22):6284-95).
Используемый в настоящем изобретении термин "иммуногенная композиция" относится к композиции, которая обладает способностью вызывать, индуцировать, усиливать, пролонгировать или поддерживать иммунный ответ, в частности к композиции, которая вызывает, индуцирует, усиливает, пролонгирует или поддерживает иммунный ответ при введении млекопитающему, в первую очередь при введении человеку. Предпочтительно, иммуногенная композиция дополнительно содержит одно или более иммуноадъювантное соединение.
Под термином "фармацевтически доступный эксципиент или носитель" в настоящем описании понимается соединение фармацевтического профиля, которое улучшает доставку, стабильность или биодоступность активного ингредиента, и может метаболизироваться в организме субъекта, которому вводится, не оказывая при этом токсического действия. Предпочтительными наполнителями или носителями в соответствии с настоящим изобретением являются любые эксципиенты или носители, обычно используемые в фармацевтических продуктах, такие как, например, вода, солевой раствор, фосфатно-буферный солевой раствор, декстроза, глицерин, этанол и подобные вещества, а также их комбинации. Во многих случаях будет предпочтительно использовать в композиции изотонические агенты, например, сахара, полиспирты, такие как маннитол, сорбитол или хлорид натрия. Фармацевтически доступные эксципиенты или носители могут дополнительно содержать минимальные количества вспомогательных соединений, таких как увлажняющие или эмульгирующие агенты, или консерванты.
Термин "вакцина" относится к композиции, способной стимулировать иммунную систему живого организма таким образом, чтобы обеспечить защиту против вредоносного антигена, либо посредством профилактики, либо посредством терапии. Профилактические вакцины являются предпочтительными. Предпочтительно, вакцина или вакцинная композиция дополнительно содержит одно или более иммуноадъювантное соединение.
Согласно различным аспектам и вариантам осуществления изобретения, описанным в настоящем документе, термин "субъект" или "хозяин", предпочтительно, относится к млекопитающему и, наиболее предпочтительно к человеку. Указанный субъект может уже иметь раковое заболевание, обследоваться с подозрением на него или иметь риск развития такого заболевания.
Термин "рак" в контексте настоящего описания относится к злокачественному новообразованию. В частности, термин "рак" относится в данном документе к любому состоянию из класса заболеваний или расстройств, которые характеризуются неконтролируемым делением клеток и способностью этих клеток вторгаться в другие ткани либо путем прямого роста в соседнюю ткань посредством инвазии, либо путем имплантации в отдаленные участки путем метастазирования. Метастазирование определяется, как стадия болезни, на которой раковые клетки переносятся посредством кровеносной или лимфатической системы. Термин объединяет, среди прочих, рак пищевода, рак желудка, рак двенадцатиперстной кишки, рак тонкой кишки, рак аппендикса, рак толстого кишечника, рак толстой кишки, рак прямой кишки, колоректальный рак, рак анального канала, рак поджелудочной железы, рак печени, рак желчного пузыря, рак селезенки, рак почек, рак мочевого пузыря, рак простаты, рак яичек, рак матки, рак эндометрия, рак яичников, рак влагалища, рак вульвы, рак груди, рак легких, рак щитовидной железы, рак тимуса, рак мозга, рак нервной системы, глиомы, полость рта рак, рак кожи, рак крови, лимфомы, рак глаз, рак костей, рак костного мозга, рак мышц и т.д. В контексте настоящего изобретения меланома, рак головы и шеи, груди, колоректальный рак или рак почек (например, светлоклеточная почечно-клеточная карцинома) являются предпочтительными типами рака.
Используемый в настоящем изобретении термин "профилактика", "предотвращение" или "предотвращать", "предупреждать" в целом означает действия, позволяющие избежать или свести к минимуму вероятность возникновения заболевания и/или развития состояния до ее возникновения, в то время как термин "лечение" или "лечить" означает уменьшение, облегчение или излечение заболевания или состояния (или симптомов заболевания или состояния) после его начала. Термин "профилактика" относится к "уменьшению вероятности возникновения" или к "уменьшению вероятности рецидива" заболевания.
Термин "эффективное количество" или "эффективная доза", используемый в настоящем описании, обозначает количество, которое обеспечивает достижение желаемого эффекта. Для терапевтических целей эффективное количество представляет собой количество, достаточное для того чтобы достичь благоприятного или желаемого клинического результата. Предпочтительное эффективное количество для данного применения может быть легко определено специалистом в данной области с учетом, например, размера, веса и возраста субъекта, типа заболевания/патологического состояния, которое подлежит профилактике или лечению, а также времени, которое прошло с начала заболевания/патологического состояния. В контексте настоящего изобретения, что касается профилактики и лечения, эффективное количество композиции представляет собой количество, достаточное для того чтобы индуцировать гуморальный/или клеточно-опосредованный иммунный ответ, направленный против заболевания/патологического состояния.
Во всем настоящем описании и в представленной ниже формуле изобретения, если контекст не подразумевает другого, термин "включает" и его производные "включающий" и "включая" следует понимать, как определяющие включение обозначенных компонентов, целых чисел и этапов, но не исключение других необозначенных компонентов, целых чисел и стадий. Термин "состоять" относится к частному случаю термина "содержать", когда другие необозначенные компоненты, целые числа и этапы исключены. В контексте настоящего изобретения, термин "содержит" включает термин "состоит". Термин "содержащий", таким образом, относится и к термину "включающий" так же как и к термину "состоящий", например, композиция, содержащая X, может состоять исключительно из X, а может включать какой-либо дополнительный элемент, например, X+Y.
Артикли "a", "an" и "the" и сходные обозначения, используемые в настоящем писании (особенно в контексте формулы изобретения), относятся, как к единственному, так и к множественному числу, если специальным образом не указано иное или иное явным образом не следует из контекста изобретения. Описание диапазона значений в настоящем документе призвано выступать в качестве упрощенного метода обращения к каждому индивидуальному значению в пределах данного диапазона. За исключением случаев, когда иное указано в настоящем описании, каждое индивидуальное значение включено в спецификацию таким образом, как если бы оно было указано в настоящем описании в индивидуальном порядке. Ни какие формулировки в данной спецификации не должны рассматриваться, как указывающие на какой-либо незаявленный элемент, имеющий важное значение для практического применения данного изобретения.
Словосочетание "практически" не исключает термина "полностью" то есть композиция, которая "практически полностью" свободна от соединения Y, может быть полностью очищена от соединения Y. Там, где это необходимо словосочетание "практически" может быть исключено из описания изобретения.
Термин "около" используемый по отношению к численной величине х означает х±10%.
Для большей ясности и удобства чтения, далее в описании представлены определения.
Любые технические характеристики, упомянутые в данных определениях, могут рассматриваться в контексте практически каждого варианта осуществления изобретения. Сущность настоящего изобретения может быть без труда понята, благодаря ссылкам на следующее детальное описание, предпочтительные варианты осуществления изобретения и включенные в него примеры. Дополнительные определения предоставлены в описании.
ДЕТАЛЬНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Несмотря на то, что настоящее изобретение подробно описано ниже, должно быть понятно, что настоящее изобретение не ограничивается конкретными методологиями, протоколами и реагентами, описанными в настоящем документе, поскольку они могут меняться. Кроме того, должно быть понятно, что вся используемая терминология не предназначена для ограничения объема настоящего изобретения, который ограничивается лишь прилагаемой формулой изобретения. Если дополнительно не оговаривается иное, технические и научные термины, используемые в настоящем описании, имеют общепринятые значения, понятные любому специалисту в данной области.
Ниже представлено описание элементов настоящего изобретения. Указанные элементы перечислены в рамках конкретных вариантов осуществления изобретения, однако должно быть понятно, что они могут комбинироваться между собой любым образом и в любых количествах с получением дополнительных вариантов осуществления изобретения. Разнообразные описанные ниже примеры и предпочтительные варианты осуществления изобретения не должны толковаться, как ограничивающие сущность настоящего изобретения только непосредственно описанными в вариантах осуществления изобретения. Следует понимать, что описание предоставляет и охватывает варианты осуществления изобретения, которые объединяют конкретно изложенные варианты с любым количеством раскрытых и/или предпочтительных элементов. Кроме того, любые перестановки и комбинации всех описанных в настоящей заявке элементов изобретения должны рассматриваться, как входящие в объем настоящего изобретения и раскрытые в настоящей заявке, если дополнительно не оговаривается иное.
Авторы настоящего изобретения идентифицировали набор антигенных пептидов, которые могут применяться для стимуляции специфического иммунного ответа против опухолевых клеток. Такие антигенные пептиды отличаются от (фрагментов) опухолевых антигенов человека, представленных в Таблицах 1А и 1В, однако имеют с ними схожую аминокислотную последовательность.
Конкретнее, антигенные пептиды, заявленные в соответствии с настоящим изобретением, содержатся в полипептидах и белках, продуцируемых комменсальными бактериями из кишечника человека. Соответственно, антигенные пептиды, заявленные в соответствии с настоящим изобретением, не являются последовательностями человека, а представляют собой бактериальные последовательности. Не желая быть связанными какой-либо теорией, авторы изобретения считают, что иммунный репертуар человека включает клоны Т-клеток, которые обладают реактивностью по отношению к бактериальным пептидам (содержащимся в белках, продуцируемых комменсальными бактериями кишечника), которые имеют аминокислотную идентичность с фрагментами опухолевых антигенов человека.
Конкретнее, антигенные пептиды, заявленные в соответствии с настоящим изобретением, могут вызывать более сильный иммунный ответ, чем соответствующие пептиды человека, поскольку Т клетки, обладающее способностью распознавать только человеческие пептиды, были истощены при распознавании аутоантигенов в процессе созревания, и это не относится к антигенным пептидам, заявленным в соответствии с настоящим изобретением. Это может объяснить, почему описанные в настоящем документе антигенные пептиды способны индуцировать иммунный ответ, особенно Т-клеточный ответ, при введении в организм индивидуума (человека).
Соответственно, авторы настоящего изобретения считают, что белки, продуцируемые комменсальными бактериями кишечника, обладают способностью "имитировать" опухолевые антигены и могут применяться для стимуляции специфического иммунного ответа против опухолевых клеток. Эти данные являются дополнительным доказательством того, что комменсальные бактерии могут способствовать уничтожению опухолевых клеток.
Антигенные пептиды, описанные в настоящей заявке, могут быть получены при помощи широко известных методик. Например, пептиды могут быть получены синтетическим путем, при помощи рекомбинантных ДНК технологий или с помощью химического синтеза. Пептиды, раскрытые в настоящем изобретении, могут синтезироваться индивидуально или в форме более длинных полипептидов, содержащих два и более пептида (например, два или более пептида или пептид и не-пептид). Антигенные пептиды могут быть выделены, то есть практически полностью очищены от других естественных белков и фрагментов клеток-хозяев, например, по меньшей мере на 70%, 80% или 90%. Предпочтительно, антигенные пептиды, заявленные в соответствии с настоящим изобретением, представляют собой выделенные антигенные пептиды.
Антигенные пептиды, заявленные в соответствии с настоящим изобретением
Согласно первому аспекту настоящее изобретение относится к антигенному пептиду, состоящему из или включающему в себя аминокислотную последовательность, как указанно в любой из SEQ ID NOs 1-580 и 861-887. Предпочтительно, антигенный пептид состоит из или включает в себя аминокислотную последовательность, как указанно в любой из SEQ ID Nos 1-580. Также предпочтительно, антигенный пептид состоит из или включает в себя аминокислотную последовательность, как указанно в любой из SEQ ID NOs 861 887.
Соответственно, настоящее изобретение относится к антигенным пептидам сходным по аминокислотному составу с опухолевым антигеном. Выражение "сходный по аминокислотному составу с опухолевым антигеном", используемое в настоящем описании, относится конкретно к варианту последовательности фрагментов исходного (референсного) опухолевого антигена человека, такого как IL13RA2 или других опухолевых антигенов человека в соответствии с примерами настоящего описания, представленными в Таблицах 1А и 1В. "Вариант последовательности" обычно имеет, в частности, по всей длине последовательности по меньшей мере 50% идентичности с референсной последовательностью, а именно, с фрагментом (референсного) опухолевого антигена. Предпочтительно, вариант последовательности по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, предпочтительно по меньшей мере на 75%, более предпочтительно по меньшей мере на 80%, еще более предпочтительно по меньшей мере на 85%, более предпочтительно по меньшей мере на 90%, наиболее предпочтительно по меньшей мере, на 95% идентичен референсной последовательности, а именно, фрагменту (референсного) опухолевого антигена. Идентичность последовательностей может быть рассчитана при помощи способов, известных из области техники, в частности, как описано ниже. Предпочтительно, варианты последовательностей сохраняют специфическую функцию референсной последовательности, например, функцию опухолевого эпитопа и/или его способность вызывать или поддерживать иммунный ответ. Конкретно, вариант аминокислотной последовательности имеет измененную последовательность, в которой одна или более аминокислота референсной последовательности подвергается мутации, например, делеции или замене, или одна или более аминокислота встроена в референсную последовательность. Например, вариант последовательности, который по меньшей мере на 90% идентичен референсной последовательности, включает не более 10 изменений, то есть делеций, вставок или замен в любых сочетаниях, на 100 аминокислот последовательности.
Способы определения идентичности (схожести) двух и более последовательностей хорошо известны из области техники. Процент идентичности двух последовательностей можно определить при помощи математического алгоритма. Предпочтительным, но не ограничивающим примером подходящего математического алгоритма, который может использоваться для этих целей является алгоритм Karlin et al. (1993), PNAS USA, 90:5873-5877. Такой алгоритм интегрирован в пакет программ BLAST, например, программу BLAST или NBLAST (см также Altschul et at, 1990, J. Mol. Biol. 215, 403-410 or Altschul et al. (1997), Nucleic Acids Res, 25:3389-3402), которые доступны на домашней странице NCBI в мировой сети интернет ncbi.nlm.nih.gov) и FASTA (Pearson (1990), Methods Enzymol. 183, 63-98; Pearson and Lipman (1988), Proc. Natl. Acad. Sci. U. S. A 85, 2444-2448). Последовательности, которые идентичны другим последовательностям на определенном протяжении, могут быть идентифицированы с помощью этих программ. Кроме того, для определения % идентичности между двумя полинуклеотидами и % между двумя (поли)пептидными последовательностями могут применяться программы, доступные в пакете для анализа последовательностей Висконсин, версия 9.1 (Devereux et al., 1984, Nucleic Acids Res., 387-395), например, программы BESTFIT и GAP. BESTFIT использует алгоритм "локальной гомологии" Смита и Уотермана (1981), J. Mol. Biol. 147, 195-197 и находит единственный участок с наилучшим сходством двух последовательностей.
"Фрагмент" (референсного) опухолевого антигена, который обычно выполняет функцию исходной последовательности, предпочтительно содержит по меньшей мере семь, более предпочтительно по меньшей мере восемь и более предпочтительно (по меньшей мере) девять или десять аминокислот. Понятно, что "фрагмент" (референсного) опухолевого антигена (белка) не является полноразмерным опухолевым антигеном (белком). Соответственно, "фрагмент" (референсного) опухолевого антигена может иметь максимальную длину, которая составляет 95%, 90%, 85%, 80%, 75%, 70%, 65%, 60%, 55%, 50%, 45%, 40%, 35%, 30%, 25%, 20%, 19%, 18%, 17%, 16%, 15%, 14%, 13%, 12%, 11%, 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от длины полноразмерного (референсного) опухолевого антигена. Согласно некоторым вариантам осуществления изобретения длина фрагмента (референсного) опухолевого антигена не превышает 50% от длины (полноразмерного) (референсного) опухолевого антигена. Согласно другим вариантам осуществления изобретения, длина фрагмента (референсного) опухолевого антигена не превышает 20% или 10% от длины (полноразмерного) (референсного) опухолевого антигена.
В целом, антигенный пептид, заявленный в соответствии с настоящим изобретением, может иметь любую длину. Предпочтительно, длина антигенного пептида, заявленного в соответствии с настоящим изобретением, не превышает 350 аминокислот. Например, максимальная длина антигенного пептида, заявленного в соответствии с настоящим изобретением, может составлять от 300 до 250 аминокислот. Более предпочтительно, максимальная длина антигенного пептида, заявленного в соответствии с настоящим изобретением, не превышает 200 аминокислот, например, не превышает 190, 180, 170, 160, 150, 140, 130, 120, 110, 100, 95, 90, 85, 80, 75, 70, 65, 60, 55, 50, 45, 40, 35, 30, 29, 28, 27, 26, 25, 24, 23, 22, 21, 20, 19, 18, 17, 16, 15, 14 или 13 аминокислот. Конкретнее, длина антигенных пептидов, заявленных в соответствии с настоящим изобретением, предпочтительно, составляет максимум 30 или 25 аминокислот, более предпочтительно максимум 20 или 15 аминокислот, причем наименьшие молекулы длиной 10 или 9 аминокислоты являются наиболее предпочтительными. Конкретнее, антигенные пептиды не являются полноразмерными белками, продуцируемыми комменсальными бактериями кишечника, из которых они получены.
В целом, настоящее изобретение относится к антигенному пептиду, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека. Опухолевый антиген человека может быть выбран из группы, включающей АСРР, ANKRD30A, AREG, ASCL1, ASCL2, BIRC5, СА9, CCNA1, CCND1, CDH17, CDH6, CDKN2A, СЕАСАМ5, CHI3L1, CHI3L2, COL11A1, CT83, CTCFL, DCT, DMRTA2, EGFR, ERBB2, ERG, ESR1, EZH2, FAP, FLT1, FOXM1, FSIP1, GAL3ST1, GPR143, HES6, FL13RA2, KISS1R, KLHDC8A, KLHL14, KLK4, KRT81, LEMD1, LRRC15, MAGEA1, MAGEA10, MAGEA11, MAGEA12, MAGEA4, MLANA, NKX2-1, NPTX2, PAGE3, PAX2, PCDHB16, PIWFL1, PMEL, PRAME, PTHLH, SEMG1, SERHL2, SLC45A3, SLC6A3, SNX31, SOX11, SPINK1, STEAP1, TBL1Y, TDRD1, TOP2A, TPTE, TRPM8, TYMS, TYR, UPK2, VCAM1, WFDC2, WT1, ZEB1, ZNF165 и ZNF280A.
Конкретнее, настоящее изобретение относится к антигенному пептиду, который представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена человека, причем указанный фрагмент опухолевого антигена может включать в себя или состоять из любой последовательности SEQ ID NOs 580-858 и 888-895. В Таблице 1А ниже представлен обзор антигенных пептидов, заявленных в соответствии с настоящим изобретением, и с их аминокислотными последовательностями и SEQ ID Nos, а также соответствующий фрагмент/эпитоп опухолевого антигена человека (также называемый в настоящем описании, как "референсный пептид человека"). В Таблице 1А также представлена информация о том, к какому опухолевому антигену относится каждый антигенный пептид по настоящему изобретению. SEQ ID NOs с 1 по 580 и с 861 по 887 относятся к антигенным пептидам, заявленным в соответствии с настоящим изобретением.










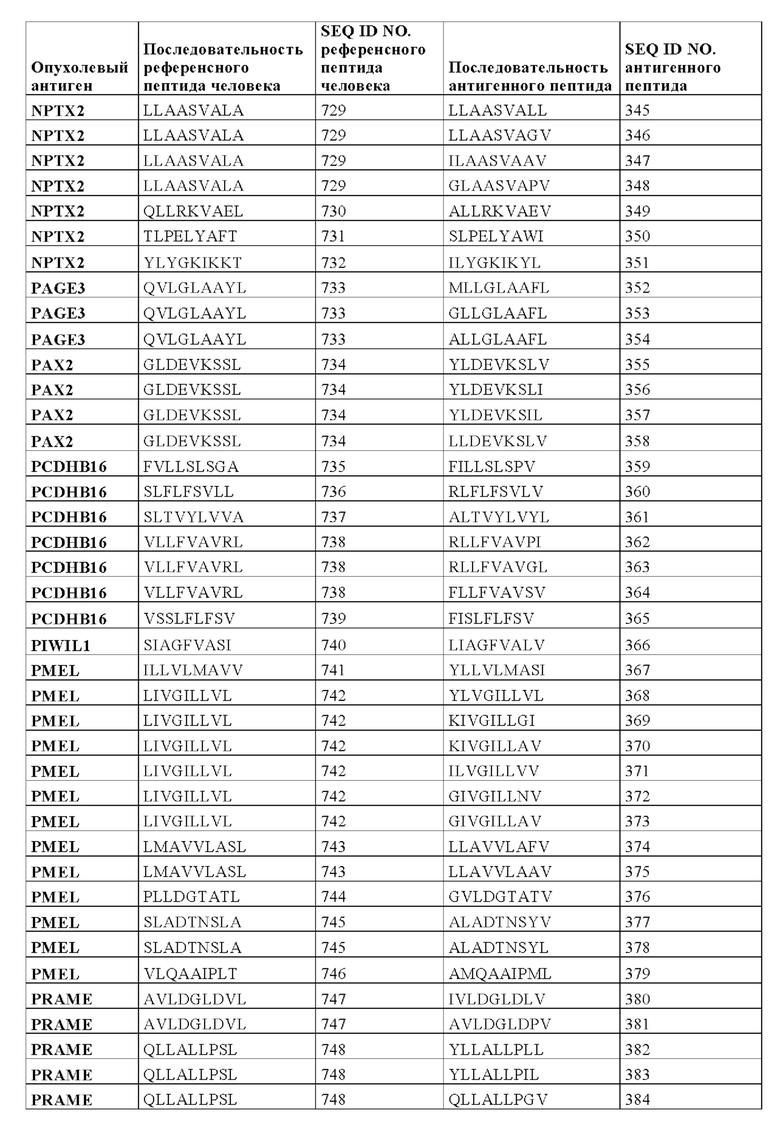


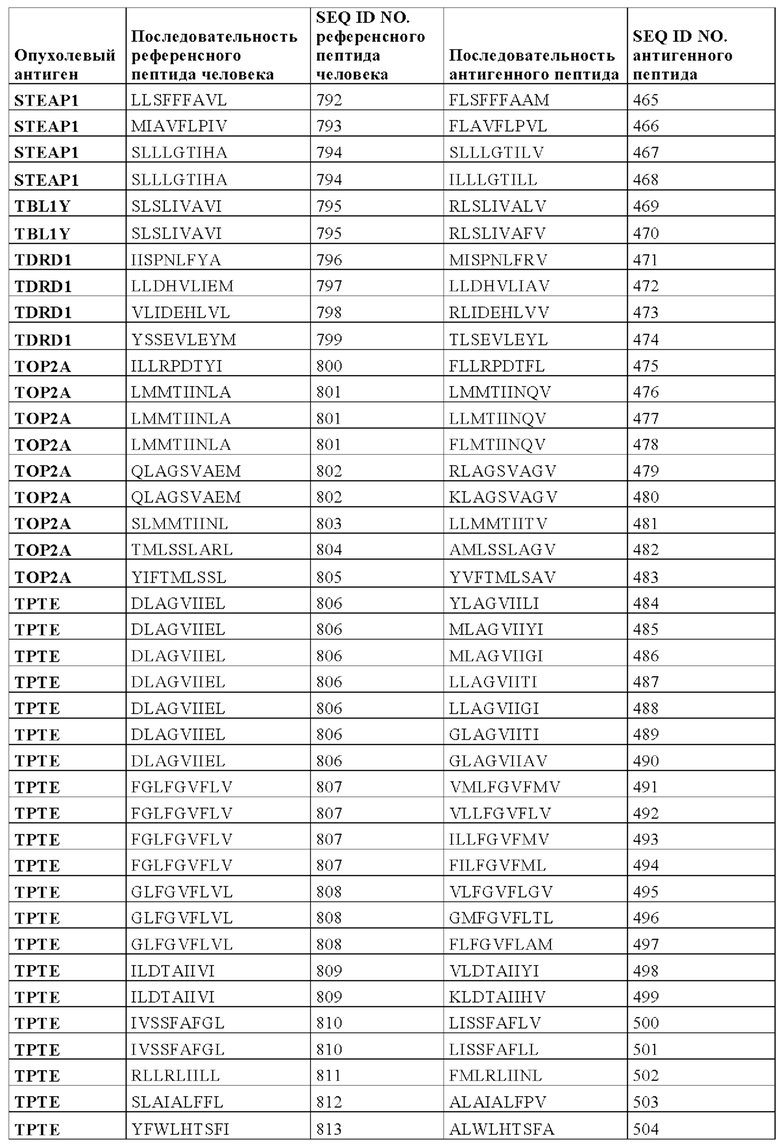
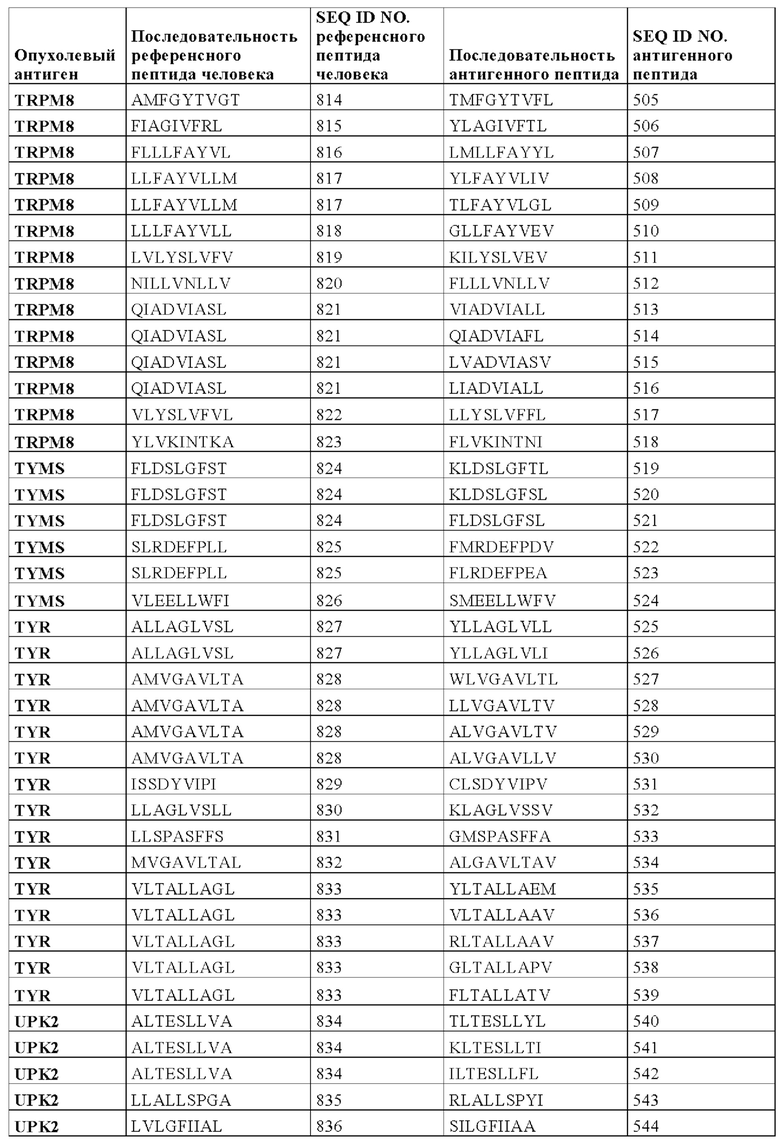

Как видно из Таблицы 1А, антигенные пептиды, заявленные в соответствии с настоящим изобретением, могут быть классифицированы в соответствии с соответствующим "референсным белком человека", а также в соответствии с соответствующим опухолевым антигеном.
Согласно одному варианту осуществления изобретения, антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена АСРР (референсный пептид человека), такой как "FLFLLFFWL" (SEQ ID NO: 581), "SLSLGFLFL" (SEQ ID NO: 582) или "LSLGFLFLL" (SEQ ID NO: 583). Согласно предпочтительному варианту осуществления изобретения, антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента опухолевого антигена АСРР, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 1-4. Более предпочтительно, антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента АСРР (референсный пептид человека) "FLFLLFFWL" (SEQ ID NO: 581), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO 1. Кроме того, более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента АСРР (человеческий референсный пептид) "SLSLGFLFL" (SEQ ID NO: 582), например, антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 2 или 3. Кроме того, более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента АСРР (человеческий референсный пептид) "LSLGFLFLL" (SEQ ID NO: 583), например, антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 4.
Согласно другому варианту осуществления изобретения, антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена ANKRD30A (референсный пептид человека), такой как "YTSNDSYIV" (SEQ ID NO: 584), "ILIDSGADI" (SEQ ID NO: 585), "SLFESSAKI" (SEQ ID NO: 586) или "SLTPLLLSI" (SEQ ID NO: 587). Согласно другому предпочтительному варианту осуществления изобретения, антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента опухолевого антигена ANKRD30A, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 5-15. Более предпочтительно, антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента ANKRD30A (референсный пептид человека) "YTSNDSYIV" (SEQ ID NO: 584), например, антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 5. Кроме того, более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента ANKRD30A (референсный пептид человека) "ILIDSGADI" (SEQ ID NO: 585), например, антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 6, 7 или 8. Кроме того, более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента ANKRD30A (референсный пептид человека) "SLFESSAKI" (SEQ ID NO: 586), например, антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 9 или 10. Кроме того, более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента ANKRD30A (референсный пептид человека) "SLTPLLLSI" (SEQ ID NO: 587), например, антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 11, 12, 13, 14 или 15.
Согласно другому варианту осуществления изобретения, антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена AREG (референсный пептид человека), такой как "MSAVILTAV" (SEQ ID NO: 588) или "ALAAIAAFM" (SEQ ID NO: 589). Согласно другому предпочтительному варианту осуществления изобретения, антигенный пептид по изобретению представляет собой вариант последовательности опухолевого антигена AREG, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 16-24. Более предпочтительно, антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента AREG (референсный пептид человека) "MSAVILTAV" (SEQ ID NO: 588), например, антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 16 или 17. Кроме того, более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента AREG (референсный пептид человека) "ALAAIAAFM" (SEQ ID NO: 589), например, антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 18, 19, 20, 21, 22, 23 или 24.
Согласно другому варианту осуществления изобретения, антигенный пептид по настоящему изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена ASCL1 (референсный пептид человека), такой как "VSAAFQAGV" (SEQ ID NO: 590). Согласно другому предпочтительному варианту осуществления изобретения, антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена ASCL1, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 25. Более конкретно, антигенный пептид по настоящему изобретению, который состоит из или включает в себя аминокислотную последовательность, как указано в SEQ ID NO: 25 представляет собой вариант последовательности фрагмента ASCL1 (референсный пептид человека) "VSAAFQAGV" (SEQ ID NO: 590).
Согласно другому варианту осуществления изобретения, антигенный пептид по настоящему изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена ASCL2 (референсный пептид человека), такой как "KLVNLGFQA" (SEQ ID NO: 591) или "ELLDFSSWL" (SEQ ID NO: 592). Согласно другому предпочтительному варианту осуществления изобретения, антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена ASCL2, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 26-29. Более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента ASCL2 (референсный пептид человека) "KLVNLGFQA" (SEQ ID NO: 591), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 26 или 27. Также более предпочтительно, антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента ASCL2 (референсный пептид человека) "ELLDFSSWL" (SEQ ID NO: 592), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID Nos 28 или 29.
Согласно другому варианту осуществления изобретения, антигенный пептид по настоящему изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена BIRC5 (референсный пептид человека), такой как "LTLGEFLKL" (SEQ ID NO: 593). Согласно другому предпочтительному варианту осуществления изобретения, антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена BIRC5, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30-32. Более предпочтительно, антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента BIRC5 (референсный пептид человека) "LTLGEFLKL" (SEQ ID NO: 593), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 30, 31 или 32. Еще более предпочтительно, антигенный пептид состоит из или включает в себя последовательность SEQ ID NO: 32.
Согласно другому варианту осуществления изобретения, антигенный пептид по настоящему изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена СА9 (референсный пептид человека), такой как "AAGDILALV" (SEQ ID NO: 594), "ALVFGLLFA" (SEQ ID NO: 595), "FQYEGSLTT" (SEQ ID NO: 596), "HLSTAFARV" (SEQ ID NO: 597), "LSLLLLVPV" (SEQ ID NO: 598), "QLLLSLLLL" (SEQ ID NO: 599) или "VQLLLSLLL" (SEQ ID NO: 600). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена СА9, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 33-50. Более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента СА9 (референсный пептид человека) "AAGDILALV" (SEQ ID NO: 594), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 33 или 34. Также более предпочтительно, антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента СА9 (референсный пептид человека) "ALVFGLLFA" (SEQ ID NO: 595), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 35, 36 или 37. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента СА9 (референсный пептид человека) "FQYEGSLTT" (SEQ ID NO: 596), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 38. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента СА9 (референсный человеческий пептид) "HLSTAFARV" (SEQ ID NO: 597), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 39, 40 или 41. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента СА9 (референсный человеческий пептид) "LSLLLLVPV" (SEQ ID NO: 598), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 42, 43 или 44. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента СА9 (референсный человеческий пептид) "QLLLSLLLL" (SEQ ID NO: 599), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 45, 46 или 47. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента СА9 (референсный человеческий пептид) "VQLLLSLLL" (SEQ ID NO: 600), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 48, 49 или 50.
Согласно другому варианту осуществления изобретения, антигенный пептид по настоящему изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена CCNA1 (референсный пептид человека), такой как "NLAKYVAEL" (SEQ ID NO: 601) или "LIAAAAFCL" (SEQ ID NO: 602). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена CCNA1, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 51-55. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента CCNA1 (референсный пептид человека) "NLAKYVAEL" (SEQ ID NO: 601), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 51. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента CCNA1 (референсный пептид человека) "LIAAAAFCL" (SEQ ID NO: 602), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 52, 53, 54 или 55.
Согласно другому варианту осуществления изобретения, антигенный пептид по настоящему изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена CCND1 (референсный пептид человека), такой как "LLNDRVLRA" (SEQ ID NO: 603). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена CCND1, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NO: 56. Конкретнее, антигенный пептид, заявленный в SEQ ID NO: 56, представляет собой вариант последовательности фрагмента CCND1 (референсный пептид человека) "LLNDRVLRA" (SEQ ID NO: 603).
Согласно другому варианту осуществления изобретения, антигенный пептид по настоящему изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена CDH17 (референсный пептид человека), такой как "GILLTTLLV" (SEQ ID NO: 604), "ILAVVFIRI" (SEQ ID NO: 605), "ILLTTLLVI" (SEQ ID NO: 606) или "LVIGIILAV" (SEQ ID NO: 607). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена CDH17, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 57-63. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента CDH17 (референсный пептид человека) "GILLTTLLV" (SEQ ID NO: 604), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 57. Согласно другому предпочтительному варианту осуществления изобретения, антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента опухолевого антигена CDH17 (референсный пептид человека) "ILAVVFIRI" (SEQ ID NO: 605), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 58 or 59. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента CDH17 (референсный пептид человека) "ILLTTLLVI" (SEQ ID NO: 606), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 60, 61 или 62. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента CDH17 (референсный пептид человека) "LVIGIILAV" (SEQ ID NO: 607), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 63.
Согласно другому варианту осуществления изобретения, антигенный пептид по настоящему изобретению, представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена CDH6 (референсный пептид человека), такой как "ALVAILLCI" (SEQ ID NO: 608), "EMSDVGTFV" (SEQ ID NO: 609), "EMSTYLLPV" (SEQ ID NO: 610), "FLLEEYTGS" (SEQ ID NO: 611), "ILLCIVILL" (SEQ ID NO: 612), или "LLVTVVLFA" (SEQ ID NO: 613). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента опухолевого антигена CDH6, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 64-81. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента CDH6 (референсный пептид человека) "ALVAILLCI" (SEQ ID NO: 608), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 64, 65, 66, 67, 68, 69 или 70. Также более предпочтительно, антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента CDH6 (референсный пептид человека) "EMSDVGTFV" (SEQ ID NO: 609), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 71. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента CDH6 (референсный пептид человека) "EMSTYLLPV" (SEQ ID NO: 610), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 72. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента CDH6 (референсный пептид человека) "FLLEEYTGS" (SEQ ID NO: 611), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 73. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента CDH6 (референсный пептид человека) "ILLCIVILL" (SEQ ID NO: 612), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 74 или 75. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента CDH6 (референсный пептид человека) "LLVTVVLFA" (SEQ ID NO: 613), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 76, 77, 78, 79, 80 или 81.
Согласно другому варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена CDKN2A (референсный пептид человека), такой как "AVALVLMLL" (SEQ ID NO: 614). Согласно другому предпочтительному варианту осуществления изобретения, антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента опухолевого антигена CDKN2A, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NO: 82. Конкретнее антигенный пептид по настоящему изобретению, который состоит из или включает в себя аминокислотную последовательность, как указано в SEQ ID NO: 82, представляет собой вариант последовательности фрагмента CDKN2A (референсный пептид человека) "AVALVLMLL" (SEQ ID NO: 614).
Согласно другому варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена СЕАСАМ5 (референсный пептид человека), такой как "LLTFWNPPT" (SEQ ID NO: 615). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента опухолевого антигена СЕАСАМ5, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 83. Конкретнее антигенный пептид по настоящему изобретению, который состоит из или включает в себя аминокислотную последовательность, как указано в SEQ ID NO: 83, представляет собой вариант последовательности фрагмента СЕАСАМ5 (референсный пептид человека) "LLTFWNPPT" (SEQ ID NO: 615).
Согласно другому варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена CHI3L1 (референсный пептид человека), такой как "KQLLLSAAL" (SEQ ID NO: 616), "LLLSAALSA" (SEQ ID NO: 617), "QLAGAMVWA" (SEQ ID NO: 618), "SQTGFVVLV" (SEQ ID NO: 619) или "TLASSETGV" (SEQ ID NO: 620). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента опухолевого антигена CHI3L1, такой как состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NOs 84-114. Более предпочтительно, антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента CHI3L1 (референсный пептид человека) "KQLLLSAAL" (SEQ ID NO: 616), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 84 или 85. Также более предпочтительно, антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента CHI3L1 (референсный пептид человека) "LLLSAALSA" (SEQ ID NO: 617), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, или 109. Также более предпочтительно, антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента CHI3L1 (референсный пептид человека) "QLAGAMVWA" (SEQ ID NO: 618), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 110, 111 или 112. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента CHI3L1 (референсный пептид человека) "SQTGFVVLV" (SEQ ID NO: 619), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 113. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента CHI3L1 (референсный пептид человека) "TLASSETGV" (SEQ ID NO: 620), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 114.
Согласно другому варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена CHI3L2 (референсный пептид человека), такой как "ILLSIGGYL" (SEQ ID NO: 621), "HLIYSFASI" (SEQ ID NO: 622), "VLIHELAEA" (SEQ ID NO: 623), "SLWAGVVVL" (SEQ ID NO: 624). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента опухолевого антигена CHI3L2, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NOs 115-119. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента CHI3L2 (референсный пептид человека) "ILLSIGGYL" (SEQ ID NO: 621), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 115. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента CHI3L2 (референсный пептид человека) "HLIYSFASI" (SEQ ID NO: 622), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 116. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента CHI3L2 (референсный пептид человека) "VLIHELAEA" (SEQ ID NO: 623), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 117 или 118. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента CHI3L2 (референсный пептид человека) "SLWAGVVVL" (SEQ ID NO: 624), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 119.
Согласно другому варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена COL11A1 (референсный пептид человека), такой как "WLWDFTVTT" (SEQ ID NO: 625). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента опухолевого антигена COL11A1, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 120. Конкретнее - антигенный пептид по настоящему изобретению, который состоит из или включает в себя аминокислотную последовательность, как указано в SEQ ID NO: 120, представляет собой вариант последовательности фрагмента COL11A1 (референсный пептид человека) "WLWDFTVTT" (SEQ ID NO: 625).
Согласно другому варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена СТ83 (референсный пептид человека), такой как "LLASSILCA" (SEQ ID NO: 626). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента опухолевого антигена СТ83, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NOs 121-123. Более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента СТ83 (референсный пептид человека) "LLASSILCA" (SEQ ID NO: 626), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 121, 122 или 123.
Согласно другому варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена CTCFL (референсный пептид человека), такой как "KLAVSLAET" (SEQ ID NO: 627). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента опухолевого антигена CTCFL, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 124. Конкретнее - антигенный пептид по настоящему изобретению, который состоит из или включает в себя аминокислотную последовательность, как указано в SEQ ID NO: 124, представляет собой вариант последовательности фрагмента CTCFL (референсный пептид человека) "KLAVSLAET" (SEQ ID NO: 627).
Согласно другому варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена DCT (референсный пептид человека), такой как "ALVGLFVLL" (SEQ ID NO: 628), "GLFVLLAFL" (SEQ ID NO: 629), "SVYDFFVWL" (SEQ ID NO: 630) или "VVMGTLVAL" (SEQ ID NO: 631). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента опухолевого антигена DCT, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NOs 125-132. Более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента DCT (референсный пептид человека) "ALVGLFVLL" (SEQ ID NO: 628), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 125 или 126. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента DCT (референсный пептид человека) "GLFVLLAFL" (SEQ ID NO: 629), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 127, 128 или 129. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента DCT (референсный пептид человека) "SVYDFFVWL"(SEQ ID NO: 630), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 130. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента DCT (референсный пептид человека) "VVMGTLVAL" (SEQ ID NO: 631), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 131 или 132.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена DMRTA2 (референсный пептид человека), такой как, "GTAEGLALA" (SEQ ID NO: 632) или "GLAAGLGPA" (SEQ ID NO: 633). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента опухолевого антигена DMRTA2, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NOs 133-134. Более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента DMRTA2 (референсный пептид человека) "GTAEGLALA" (SEQ ID NO: 632), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 133. Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента опухолевого антигена DMRTA2 (референсный пептид человека) "GLAAGLGPA"(SEQ ID NO: 633), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 134.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена EGFR (референсный пептид человека), такой как "ALESILHRI" (SEQ ID NO: 634), "ALLAALCPA" (SEQ ID NO: 635), "ALLALLAAL" (SEQ ID NO: 636), "ILDEAYVMA" (SEQ ID NO: 637), "LLLLLVVAL" (SEQ ID NO: 638), "MVGALLLLL" (SEQ ID NO: 639), "NLQEILHGA" (SEQ ID NO: 640) или "SLAVVSLNI" (SEQ ID NO: 641. Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента опухолевого антигена EGFR, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NOs 135-150. Более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента EGFR (референсный пептид человека) "ALESILHRI" (SEQ ID NO: 634), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 135 или 136. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента EGFR (референсный пептид человека) "ALLAALCPA" (SEQ ID NO: 635), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 137. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента EGFR (референсный пептид человека) "ALLALLAAL" (SEQ ID NO: 636), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 138, 139, 140, 141, 142, 143 или 144. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента EGFR (референсный пептид человека) "ILDEAYVMA" (SEQ ID NO: 637), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 145. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента EGFR (референсный пептид человека) "LLLLLVVAL" (SEQ ID NO: 638), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 146. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента EGFR (референсный пептид человека) "MVGALLLLL" (SEQ ID NO: 639), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 147. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента EGFR (референсный пептид человека) "NLQEILHGA" (SEQ ID NO: 640), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 148. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента EGFR (референсный пептид человека) "SLAVVSLNI" (SEQ ID NO: 641), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 149 или 150.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена ERBB2 (референсный пептид человека), такой как "AVVGILLVV" (SEQ ID NO: 642), "ILDEAYVMA" (SEQ ID NO: 643), "LLALLPPGA" (SEQ ID NO: 644), "SIISAVVGI" (SEQ ID NO: 645) или "VVLGVVFGI" (SEQ ID NO: 646). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента опухолевого антигена ERBB2, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NOs 151-162. Более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента ERBB2 (референсный пептид человека) "AVVGILLVV" (SEQ ID NO: 642), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 151, 152, 153 или 154. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента ERBB2 (референсный пептид человека) "ILDEAYVMA" (SEQ ID NO: 643), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 155. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента ERBB2 (референсный пептид человека) "LLALLPPGA" (SEQ ID NO: 644), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 156, 157, 158 или 159. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента ERBB2 (референсный пептид человека) "SIISAVVGI" (SEQ ID NO: 645), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 160. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента ERBB2 (референсный пептид человека) "VVLGVVFGI" (SEQ ID NO: 646), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 161 или 162, конкретнее - антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 162.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена ERG (референсный пептид человека), такой как "FLLELLSDS" (SEQ ID NO: 647) или "QLWQFLLEL" (SEQ ID NO: 857). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента опухолевого антигена ERG, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NOs 163-164. Более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента ERG (референсный пептид человека) "FLLELLSDS" (SEQ ID NO: 647), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 163. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента ERG (референсный пептид человека) "QLWQFLLEL" (SEQ ID NO: 857), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 164.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена ESR1, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NOs 165-192. Более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента ESR1 (референсный пептид человека) "ALLDAEPPI" (SEQ ID NO: 648), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 165. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента ESR1 (референсный пептид человека) "KITDTLIHL" (SEQ ID NO: 649), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 166 или 167. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента ESR1 (референсный пептид человека) "KLLFAPNLL" (SEQ ID NO: 650), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 168 или 169. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента ESR1 (референсный пептид человека) "LLDAEPPIL" (SEQ ID NO: 651), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 170. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента ESR1 (референсный пептид человека) "LLNSGVYTF" (SEQ ID NO: 652), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 171 или 172. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента ESR1 (референсный пептид человека) "LMIGLVWRS" (SEQ ID NO: 653), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 173. Также более предпочтительно, антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента ESR1 (референсный пептид человека) "PLYDLLLEM" (SEQ ID NO: 654), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 174, 175, 176, 177, 178, 179, 180 или 181. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента ESR1 (референсный пептид человека) "QLLLILSHI" (SEQ ID NO: 655), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 182, 183, 184, 185, 186, 187 или 188. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента ESR1 (референсный пептид человека) "RLAQLLLIL" (SEQ ID NO: 656 такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 189 или 190. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента ESR1 (референсный пептид человека) "TLIHLMAKA" (SEQ ID NO: 657), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 191. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента ESR1 (референсный пептид человека) "VLDKITDTL" (SEQ ID NO: 658), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 192.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена EZH2, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NOs 193-194. Более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента EZH2 (референсный пептид человека) "FMVEDETVL" (SEQ ID NO: 659), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 193. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента EZH2 (референсный пептид человека) "SMFRVLIGT" (SEQ ID NO: 660), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 194.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена FAP, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NOs 195-201. Более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента FAP (референсный пептид человека) "ATSAVLALL" (SEQ ID NO: 661), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 195, 196 или 197. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента FAP (референсный пептид человека) "TGWAGGFFV" (SEQ ID NO: 662), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 198. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента FAP (референсный пептид человека) "VLALLVMCI" (SEQ ID NO: 663), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 199, 200 или 201.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена FLT1, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NOs 202-216. Более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента FLT1 (референсный пептид человека) "ALLSCLLLT" (SEQ ID NO: 664), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 202, 203, 204, 205, 206, 207 или 208. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента FLT1 (референсный пептид человека) "CVAATLFWL" (SEQ ID NO: 665), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 209. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента FLT1 (референсный пептид человека) "EMYSEIPEI" (SEQ ID NO: 666), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 210. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента FLT1 (референсный пептид человека) "KMASTLVVA" (SEQ ID NO: 667), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 211 или 212. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента FLT1 (референсный пептид человека) "SIFDKIYST" (SEQ ID NO: 668), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 213. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента FLT1 (референсный пептид человека) "TLFWLLLTL" (SEQ ID NO: 669), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 214. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента FLT1 (референсный пептид человека) "VLLWEIFSL" (SEQ ID NO: 670), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 215. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента FLT1 (референсный пептид человека) "WLKDGLPAT" (SEQ ID NO: 671), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 216.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена FOXM1, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NOs 217-227 и 861-877, например, как указано в любой из SEQ ID NOs 217-227. Более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента FOXM1 (референсный пептид человека) "ILLDISFPG" (SEQ ID NO: 672), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 217 или 218. Дополнительными примерами антигенных пептидов, заявленных в соответствии с настоящим изобретением, которые являются вариантами последовательности фрагмента FOXM1 (референсный пептид человека) "ILLDISFPG" (SEQ ID NO: 672), являются антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NO: 861, 862, 863, 864, 865 или 866. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента FOXM1 (референсный пептид человека) "LLDISFPGL" (SEQ ID NO: 673), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 219. Другим примером антигенного пептида, заявленного в соответствии с настоящим изобретением, который представляет собой вариант последовательности фрагмента FOXM1 (референсный пептид человека) "LLDISFPGL" (SEQ ID NO: 673), является антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 867. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента FOXM1 (референсный пептид человека) "LMDLSTTPL" (SEQ ID NO: 674), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 220. Другим примером антигенного пептида, заявленного в соответствии с настоящим изобретением, который представляет собой вариант последовательности фрагмента FOXM1 (референсный пептид человека) "LMDLSTTPL" (SEQ ID NO: 674), является антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 868.
Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой микробиотический вариант последовательности фрагмента FOXM1 (референсный пептид человека) "RVSSYLVPI" (SEQ ID NO: 675), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 221, 222 или 223. Дополнительными примерами антигенных пептидов, заявленных в соответствии с настоящим изобретением, которые являются вариантами последовательности фрагмента FOXM1 (референсный пептид человека) "RVSSYLVPI" (SEQ ID NO: 675), являются антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NO: 869, 870 или 871. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента FOXM1 (референсный пептид человека) "SLSKILLDI" (SEQ ID NO: 676), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 224. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента FOXM1 (референсный пептид человека) "SQLSYSQEV" (SEQ ID NO: 677), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 225 или 226. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента FOXM1 (референсный пептид человека) "WAAELPFPA" (SEQ ID NO: 678), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 227. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента FOXM1 (референсный пептид человека) "NLSLHDMFV" (SEQ ID NO: 888), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 872. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента FOXM1 (референсный пептид человека) "KMKPLLPRV" (SEQ ID NO: 889), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 873 или 874. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента FOXM1 (референсный пептид человека) "YLVPIQFPV" (SEQ ID NO: 890), FOXM1 (референсный пептид человека) "KMKPLLPRV" (SEQ ID NO: 889), такой SEQ ID NO: 875 или 876. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента FOXM1 (референсный пептид человека) "YMAMIQFAI" (SEQ ID NO: 891), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 877. Еще более предпочтительно антигенный пептид состоит из или включает в себя SEQ ID NO: 32.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена FSIP1, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NOs 228-231. Более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента FSIP1 (референсный пептид человека) "LLNESETKV" (SEQ ID NO: 679), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 228. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента FSIP1 (референсный пептид человека) "RLVELLKDL" (SEQ ID NO: 680), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 229, 230 или 231.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена GAL3ST1 (референсный пептид человека), такой как "GLASTTPEA" (SEQ ID NO: 681) или "RMAREVAAL" (SEQ ID NO: 682). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена GAL3ST1, такой как антигенные пептиды, состоящий из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NOs 232-234. Более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента GAL3ST1 (референсный пептид человека) "GLASTTPEA" (SEQ ID NO: 681), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 232. Также более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента GAL3ST1 (референсный пептид человека) "RMAREVAAL" (SEQ ID NO: 682), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 233 или 234.
Согласно другому варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена GPR143 (референсный пептид человека), такой как "FLLSLAFYG" (SEQ ID NO: 683), "ILNPAQGFL" (SEQ ID NO: 684), "MAWGLATLL" (SEQ ID NO: 685) или "RLALGLLQL" (SEQ ID NO: 686). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена GPR143, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 235-247. Более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена GPR143 (референсный пептид человека) "FLLSLAFYG" (SEQ ID NO: 683), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 235, 236 или 237. Также более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена GPR143 (референсный пептид человека) "ILNPAQGFL" (SEQ ID NO: 684), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 238. Также более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена GPR143 (референсный пептид человека) "MAWGLATLL" (SEQ ID NO: 685), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 239. Также более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена GPR143 (референсный пептид человека) "RLALGLLQL" (SEQ ID NO: 686), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 240, 241, 242, 243, 245, 246 или 247.
Согласно другому варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена HES6 (референсный пептид человека), такой как "RLLLAGAEV" (SEQ ID NO: 687). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена HES6, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 248. Конкретнее - антигенный пептид, заявленный в соответствии с настоящим изобретением, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 248, представляет собой вариант последовательности фрагмента HES6 (референсный пептид человека) "RLLLAGAEV" (SEQ ID NO: 687).
Согласно предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности опухолевого антигена IL13RA2, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 249-255. Более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена IL13RA2 (референсный пептид человека) "CLYTFLIST" (SEQ ID NO: 688), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 249, 250 или 251. Также более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена IL13RA2 (референсный пептид человека)"FLISTTFGC" (SEQ ID NO: 689), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 252. Более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена IL13RA2 (референсный пептид человека) "VLLDTNYNL" (SEQ ID NO: 690), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 253. Также более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена IL13RA2 (референсный пептид человека) "WLPFGFILI" (SEQ ID NO: 691) или "WLPFGFILIL" (SEQ ID NO: 692), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 254 или 255, конкретнее - антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 255. Дополнительные примеры антигенных пептидов по настоящему изобретению, которые представляют собой варианты последовательностей фрагмента IL13RA2 (референсный пептид человека) "WLPFGFILIL" (SEQ ID NO: 692), включают антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NO: 878 или 879. Также более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена IL13RA2 (референсный пептид человека) "FLISTTFGCT" (SEQ ID NO: 892), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 880, 881 или 882. Также более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена IL13RA2 (референсный пептид человека) "YLYLQWQPPL" (SEQ ID NO: 893), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 883. Также более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена IL13RA2 (референсный пептид человека) "GVLLDTNYNL" (SEQ ID NO: 894), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 884 или 885. Также более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена IL13RA2 (референсный пептид человека) "FQLQNIVKPL" (SEQ ID NO: 895), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 886 или 887. Еще более предпочтительно антигенный пептид включает в себя или состоит из SEQ ID NO: 255.
Согласно другому варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена KISS1R (референсный пептид человека), такой как "ALYLLPLLA" (SEQ ID NO: 693), "FALYNLLAL" (SEQ ID NO: 694), "QLFLVLQAL" (SEQ ID NO: 695), "RLVAAVVLL" (SEQ ID NO: 696), "VLAERAGAV" (SEQ ID NO: 697), "WLVPLFFAA" (SEQ ID NO: 698) или "YLLPLLATC" (SEQ ID NO: 699). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена KISS1R, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 256-287. Более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена KISS1R (референсный пептид человека) "ALYLLPLLA" (SEQ ID NO: 693), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 256, 257 или 258. Также более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена KISS1R (референсный пептид человека) "FALYNLLAL" (SEQ ID NO: 694), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 259, 260 или 261. Также более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена KISS1R (референсный пептид человека) "QLFLVLQAL" (SEQ ID NO: 695), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 262. Также более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена KISS1R (референсный пептид человека) "RLVAAVVLL" (SEQ ID NO: 696), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 263. Также более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена KISS1R (референсный пептид человека) "VLAERAGAV" (SEQ ID NO: 697), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 264. Также более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена KISS1R (референсный пептид человека) "WLVPLFFAA" (SEQ ID NO: 698), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 266, 267, 268 или 269. Также более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена KISS1R (референсный пептид человека) "YLLPLLATC" (SEQ ID NO: 699), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 283, 284, 285, 286 или 287.
Согласно другому варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена KLHDC8A (референсный пептид человека), такой как "GLSDAVEAL" (SEQ ID NO: 700) или "MLREAAMGI" (SEQ ID NO: 701). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена KLHDC8A, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 288-289. Более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена KLHDC8A (референсный пептид человека) "GLSDAVEAL" (SEQ ID NO: 700), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 288. Также более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена KLHDC8A (референсный пептид человека) "MLREAAMGI" (SEQ ID NO: 701), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 289.
Согласно другому варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена KLHL14 (референсный пептид человека), такой как "ALIPAPELV" (SEQ ID NO: 702), "NLLHGLNLL" (SEQ ID NO: 703) или "YVSSLPQPL" (SEQ ID NO: 704). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена KLHL14, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 290-292. Более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена KLHL14 (референсный пептид человека) "ALIPAPELV" (SEQ ID NO: 702), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 290. Также более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена KLHL14 (референсный пептид человека) "NLLHGLNLL" (SEQ ID NO: 703), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 291. Также более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена KLHL14 (референсный пептид человека) "YVSSLPQPL" (SEQ ID NO: 704), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 292.
Согласно другому варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена KLK4 (референсный пептид человека), такой как "YLILGVAGS" (SEQ ID NO: 705). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена KLK4, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 293-296. Более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента KLK4 (референсный пептид человека), "YLILGVAGS" (SEQ ID NO: 705), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 293, 294, 295 или 296.
Согласно другому варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена KRT81 (референсный пептид человека), такой как "NMDCIIAEI" (SEQ ID NO: 706). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена KRT81, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NO: 297. Конкретнее - антигенный пептид, заявленный в соответствии с настоящим изобретением, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 297, представляет собой вариант последовательности фрагмента KRT81 (референсный пептид человека) "NMDCIIAEI" (SEQ ID NO: 706).
Согласно другому варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена LEMD1 (референсный пептид человека), такой как "AVLGIFIIV" (SEQ ID NO: 707) или "KLAVLGIFI" (SEQ ID NO: 708). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена LEMD1, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 298-299. Более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента LEMD1 (референсный пептид человека) "AVLGIFIIV" (SEQ ID NO: 707), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 298. Также более предпочтительно антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена LEMD1 (референсный пептид человека) "KLAVLGIFI" (SEQ ID NO: 708), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 299.
Согласно другому варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена LRRC15 (референсный пептид человека), такой как "AIAAIVIGI" (SEQ ID NO: 709), ALACSLAAC" (SEQ ID NO: 710), "IVIGIVALA" (SEQ ID NO: 711), "RIVAVPTPL" (SEQ ID NO: 712) или "SLKELSPGI" (SEQ ID NO: 713). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена LRRC15, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 300-307. Более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента LRRC15 (референсный пептид человека), "AIAAIVIGI" (SEQ ID NO: 709), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 300. Также более предпочтительно, антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента LRRC15 (референсный пептид человека), "ALACSLAAC" (SEQ ID NO: 710), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 301. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента LRRC15 (референсный пептид человека), "IVIGIVALA" (SEQ ID NO: 711), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 302. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента LRRC15 (референсный пептид человека), "RIVAVPTPL" (SEQ ID NO: 712), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 303, 304 или 305. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента LRRC15 (референсный пептид человека), "SLKELSPGI" (SEQ ID NO: 713), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 306 или 307.
Согласно другому варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена MAGEA1 (референсный пептид человека), такой как "KVADLVGFL" (SEQ ID NO: 714) или "LVLGTLEEV" (SEQ ID NO: 858). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена MAGEA1, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 308-309. Более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента MAGEA1 (референсный пептид человека) "KVADLVGFL" (SEQ ID NO: 714), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 308. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента MAGEA1 (референсный пептид человека) "LVLGTLEEV" (SEQ ID NO: 858), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 309.
Согласно другому варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена MAGEA4 (референсный пептид человека), такой как "AVSSSSPLV" (SEQ ID NO: 722), "KVDELAHFL" (SEQ ID NO: 723) или "KVLEHVVRV" (SEQ ID NO: 724. Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена MAGEA4, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 320-322. Более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента MAGEA4 (референсный пептид человека) "AVSSSSPLV" (SEQ ID NO: 722), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 320. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента MAGEA4 (референсный пептид человека) "KVDELAHFL" (SEQ ID NO: 723), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 321. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента MAGEA4 (референсный пептид человека) "KVLEHVVRV" (SEQ ID NO: 724), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 322.
Согласно другому варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена MAGEA10 (референсный пептид человека), такой как "GMLSDVQSM" (SEQ ID NO: 715) или "ILILILSIV" (SEQ ID NO: 716). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена MAGEA10, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 310-313. Более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента MAGEA10 (референсный пептид человека) "GMLSDVQSM" (SEQ ID NO: 715), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 310 или 311. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента MAGEA10 (референсный пептид человека) "ILILILSIV" (SEQ ID NO: 716), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 312 или 313.
Согласно другому варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена MAGEA11 (референсный пептид человека), такой как "AMDAIFGSL" (SEQ ID NO: 717), "GLITKAEML" (SEQ ID NO: 718), "GTLEELPAA" (SEQ ID NO: 719) или "KVLEYIANA" (SEQ ID NO: 720). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена MAGEA11, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 314-318. Более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента MAGEA11 (референсный пептид человека) "AMDAIFGSL" (SEQ ID NO: 717), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 314. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента MAGEA11 (референсный пептид человека) "GLITKAEML" (SEQ ID NO: 718), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 315. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента MAGEA11 (референсный пептид человека) "GTLEELPAA" (SEQ ID NO: 719), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 316 или 317. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента MAGEA11 (референсный пептид человека) "KVLEYIANA" (SEQ ID NO: 720), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 318.
Согласно другому варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена MAGEA12 (референсный пептид человека), такой как "QLVFGIEVV" (SEQ ID NO: 721). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена MAGEA12, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 319. Конкретнее - антигенный пептид, заявленный в соответствии с настоящим изобретением, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 319, представляет собой вариант последовательности фрагмента MAGEA12 (референсный пептид человека) "QLVFGIEVV" (SEQ ID NO: 721).
Согласно другому варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена MLANA (референсный пептид человека), такой как "VILGVLLEI" (SEQ ID NO: 725). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена MLANA, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NOs 323-334. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента MLANA (референсный пептид человека) "VILGVLLLI" (SEQ ID NO: 725), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO:323, 324, 325, 326, 327, 328, 329. 330, 331, 332, 333 или 334.
Согласно другому варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена NKX2-1 (референсный пептид человека), такой как "MTAAGVPQL" (SEQ ID NO: 726) или "SVSDILSPL" (SEQ ID NO: 727). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена NKX2-1, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NOs 335-340. Более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента NKX2-1 (референсный пептид человека) "MTAAGVPQL" (SEQ ID NO: 726), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 335. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента NKX2-1 (референсный пептид человека) "SVSDILSPL" (SEQ ID NO: 727), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 336, 337, 338, 339 или 340.
Согласно другому варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена NPTX2 (референсный пептид человека), такой как ALLAASVAL" (SEQ ID NO: 728), "LLAASVALA" (SEQ ID NO: 729), "QLLRKVAEL" (SEQ ID NO: 730), "TLPELYAFT" (SEQ ID NO: 731) или "YLYGKIKKT" (SEQ ID NO: 732). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена NPTX2, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NOs 341-351. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента NPTX2 (референсный пептид человека) "ALLAASVAL" (SEQ ID NO: 728), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 341, 342, 343 или 344. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента NPTX2 (референсный пептид человека) "LLAASVALA" (SEQ ID NO: 729), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 345, 346, 347 или 348. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента NPTX2 (референсный пептид человека) "QLLRKVAEL" (SEQ ID NO: 730), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 349. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента NPTX2 (референсный пептид человека) "TLPELYAFT" (SEQ ID NO: 731), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 350. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента NPTX2 (референсный пептид человека) "YLYGKIKKT" (SEQ ID NO: 732), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 351.
Согласно другому варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена PAGE3, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NOs 352-354. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента PAGE3 (референсный пептид человека) "QVLGLAAYL "(SEQ ID NO: 733), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 352, 353 или 354.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена РАХ2, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 355-358. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента РАХ2 (референсный пептид человека) "GLDEVKSSL" (SEQ ID NO: 734), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 355, 356, 357 или 358.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена PCDHB16, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NOs 359-365. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента PCDHB16 (референсный пептид человека) "FVLLSLSGA" (SEQ ID NO: 735), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 359. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента PCDHB16 (референсный пептид человека) "SLFLFSVLL" (SEQ ID NO: 736), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 360. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента PCDHB16 (референсный пептид человека) "SETVYLVVA" (SEQ ID NO: 737), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 361. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента PCDHB16 (референсный пептид человека) "VLLFVAVRE" (SEQ ID NO: 738), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 362, 363 или 364. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента PCDHB16 (референсный пептид человека) "VSSLFLFSV" (SEQ ID NO: 739), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 365.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена PIWIL1 (референсный пептид человека), такой как "SIAGFVASI" (SEQ ID NO: 740). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена PIWIL1, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 366. Конкретнее - антигенный пептид, заявленный в соответствии с настоящим изобретением, который состоит из или включает в себя аминокислотную последовательность, как указано в SEQ ID NO: 366, представляет собой вариант последовательности фрагмента PIWIL1 (референсный пептид человека) "SIAGFVASI" (SEQ ID NO: 740).
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена PMEL (референсный пептид человека), такой как "ILLVLMAVV" (SEQ ID NO: 741), "LIVGILLVL" (SEQ ID NO: 742), "LMAVVLASL" (SEQ ID NO: 743), "PLLDGTATL" (SEQ ID NO: 744), "SLADTNSLA" (SEQ ID NO: 745) или "VLQAAIPLT" (SEQ ID NO: 746). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена PMEL, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 367-379. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента PMEL (референсный пептид человека) "ILLVLMAVV" (SEQ ID NO: 741), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 367. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента PMEL (референсный пептид человека) "LIVGILLVL" (SEQ ID NO: 742), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 368, 369, 370, 371, 372 или 373. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента PMEL (референсный пептид человека) "LMAVVLASL" (SEQ ID NO: 743), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 374 или 375.
Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента PMEL (референсный пептид человека) "PLLDGTATL" (SEQ ID NO: 744), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 376. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента PMEL (референсный пептид человека) "SLADTNSLA" (SEQ ID NO: 745), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 377 или 378. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента PMEL (референсный пептид человека) "VLQAAIPLT" (SEQ ID NO: 746), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 379.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена PRAME ((референсный пептид человека) такой как "AVLDGLDVL" (SEQ ID NO: 747), "QLLALLPSL" (SEQ ID NO: 748), "RLRELLCEL" (SEQ ID NO: 749) или "VLYPVPLES" (SEQ ID NO: 750). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена PRAME, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NOs 380-387. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента PRAME (референсный пептид человека) "AVLDGLDVL" (SEQ ID NO: 747), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 380 или 381. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента PRAME (референсный пептид человека) "QLLALLPSL" (SEQ ID NO: 748), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 382, 383, 384 или 385. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента PRAME (референсный пептид человека) "RLRELLCEL" (SEQ ID NO: 749), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 386. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента PRAME (референсный пептид человека) "VLYPVPLES" (SEQ ID NO: 750), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 387.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена PTHLH (референсный пептид человека), такой как AVFLLSYAV" (SEQ ID NO: 751). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена PTHLH, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 388. Конкретнее - антигенный пептид, заявленный в соответствии с настоящим изобретением, который состоит из или включает в себя аминокислотную последовательность, как указано в SEQ ID NO: 388 представляет собой вариант последовательности PTHLH (референсный пептид человека) "AVFLLSYAV" (SEQ ID NO: 751).
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена SEMG1 (референсный пептид человека), такой как "FVLSLLLIL" (SEQ ID NO: 752), "IIFVLSLLL" (SEQ ID NO: 753) или "LILEKQAAV" (SEQ ID NO: 754). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена SEMG1, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 389-400. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента SEMG1 (референсный пептид человека) "FVLSLLLIL" (SEQ ID NO: 752), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 389, 390, 391, 392, 393, 394, 395, 396 или 397. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SEMG1 (референсный пептид человека) "IIFVLSLLL" (SEQ ID NO: 753), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 398 или 399. Также более предпочтительно, антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SEMG1 (референсный пептид человека) "LILEKQAAV" (SEQ ID NO: 754), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 400.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена SERHL2 (референсный пептид человека), такой как "LISELKLAV" (SEQ ID NO: 755), "RAIEHVLQV" (SEQ ID NO: 756), "SSFDRLIPL" (SEQ ID NO: 757) или "TLKEQFQFV" (SEQ ID NO: 758). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена SERHL2, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 401-405. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента SERHL2 (референсный пептид человека) "LISELKLAV" (SEQ ID NO: 755), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 401. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SERHL2 (референсный пептид человека) "RAIEHVLQV" (SEQ ID NO: 756), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 402. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SERHL2 (референсный пептид человека) "SSFDRLIPL" (SEQ ID NO: 757), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 403 или 404. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SERHL2 (референсный пептид человека) "TLKEQFQFV" (SEQ ID NO: 758), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 405.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена SLC45A3 (референсный пептид человека), такой как "AILDSAFLL" (SEQ ID NO: 759), "AISLVFSLV" (SEQ ID NO: 760), "ALQILPYTL" (SEQ ID NO: 761), "ALTGFTFSA" (SEQ ID NO: 762), "AQLLLVNLL" (SEQ ID NO: 763), "CLFGLLTLI" (SEQ ID NO: 764), "GILLSLFLI" (SEQ ID NO: 765), "GLLPPPPAL" (SEQ ID NO: 766), "GLLTLIFLT" (SEQ ID NO: 767), "GLVAIYFAT" (SEQ ID NO: 768), "NLGALLPRL" (SEQ ID NO: 769) или "SVAAFPVAA" (SEQ ID NO: 770). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена SLC45A3, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 406-427. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента SLC45A3 (референсный пептид человека) "AILDSAFLL" (SEQ ID NO: 759), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 406. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SLC45A3 (референсный пептид человека) "AISLVFSLV" (SEQ ID NO: 760), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 407 или 408. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SLC45A3 (референсный пептид человека) "ALQILPYTL" (SEQ ID NO: 761), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 409. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SLC45A3 (референсный пептид человека) "ALTGFTFSA" (SEQ ID NO: 762), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 410. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SLC45A3 (референсный пептид человека) "AQLLLVNLL" (SEQ ID NO: 763), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 411. Также более предпочтительно, антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SLC45A3 (референсный пептид человека) "CLFGLLTLI" (SEQ ID NO: 764), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 412, 413, 414 или 415. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SLC45A3 (референсный пептид человека) "GILLSLFLI" (SEQ ID NO: 765), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 416 или 417. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SLC45A3 (референсный пептид человека) "GLLPPPPAL" (SEQ ID NO: 766), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 418. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SLC45A3 (референсный пептид человека) "GLLTLIFLT" (SEQ ID NO: 767), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 419, 420, 421, 422 или 423. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SLC45A3 (референсный пептид человека) "GLVAIYFAT" (SEQ ID NO: 768), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 424. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SLC45A3 (референсный пептид человека) "NLGALLPRL" (SEQ ID NO: 769), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 425 или 426. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SLC45A3 (референсный пептид человека) "SVAAFPVAA" (SEQ ID NO: 770), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 427.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена SLC6A3 (референсный пептид человека), такой как "FLLSLFCVT" (SEQ ID NO: 771), "FSLGVGFGV" (SEQ ID NO: 772), "GLIDEFQLL" (SEQ ID NO: 773), "GMESVITGL" (SEQ ID NO: 774), "ILFGVLIEA" (SEQ ID NO: 775), "KIDFLLSVI" (SEQ ID NO: 776), "LLFMVIAGM" (SEQ ID NO: 777), "LVPYLLFMV" (SEQ ID NO: 778) или "QLTACLVLV" (SEQ ID NO: 779). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена SLC6A3, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NOs 428-441. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента SLC6A3 (референсный пептид человека) "FLLSLFCVT" (SEQ ID NO: 771), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 428, 429 или 430. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SLC6A3 (референсный пептид человека) "FSLGVGFGV" (SEQ ID NO: 772), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 431 или 432. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SLC6A3 (референсный пептид человека) GLIDEFQLL" (SEQ ID NO: 773), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 433. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SLC6A3 (референсный пептид человека) "GMESVITGL" (SEQ ID NO: 774), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 434. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SLC6A3 (референсный пептид человека) "ILFGVLIEA" (SEQ ID NO: 775), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 435 или 436. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SLC6A3 (референсный пептид человека) "KIDFLLSVI" (SEQ ID NO: 776), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 437. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SLC6A3 (референсный пептид человека) "LLFMVIAGM" (SEQ ID NO: 777), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 438 или 439. Также более предпочтительно, антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SLC6A3 (референсный пептид человека) "LVPYLLFMV" (SEQ ID NO: 778), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 440. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SLC6A3 (референсный пептид человека) "QLTACLVLV" (SEQ ID NO: 779), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 441.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена SNX31 (референсный пептид человека), такой как "MISEKMVKL" (SEQ ID NO: 780). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена SNX31, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 442. Конкретнее - антигенный пептид, заявленный в соответствии с настоящим изобретением, который состоит из или включает в себя аминокислотную последовательность, как указано в SEQ ID NO: 442, представляет собой вариант последовательности SNX31 (референсный пептид человека) "MISEKMVKL" (SEQ ID NO: 780).
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена SOX11 (референсный пептид человека), такой как "LMFDLSLNF" (SEQ ID NO: 781). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена SOX11, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 443-445. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента SOX11 (референсный пептид человека) "LMFDLSLNF" (SEQ ID NO: 781); такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 443, 444 или 445.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена SOX17 (референсный пептид человека), такой как "ALPAVMAGL" (SEQ ID NO: 782) или "GLAEPQAAA" (SEQ ID NO: 783). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена SOX17, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 446-449. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента SOX17 (референсный пептид человека) "ALPAVMAGL" (SEQ ID NO: 782), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 446. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента SOX17 (референсный пептид человека) "GLAEPQAAA" (SEQ ID NO: 783), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 447, 448 или 449.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена SPINK1 (референсный пептид человека), такой как "GIFLLSALA" (SEQ ID NO: 784). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена SPINK1, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 450. Конкретнее - антигенный пептид, заявленный в соответствии с настоящим изобретением, который состоит из или включает в себя аминокислотную последовательность, как указано в SEQ ID NO: 450, представляет собой вариант последовательности фрагмента SPINK1 (референсный пептид человека) "GIFLLSALA" (SEQ ID NO: 784).
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена STEAP1 (референсный пептид человека), такой как "ASLTFLYTL" (SEQ ID NO: 785), "AVLHAIYSL" (SEQ ID NO: 786), "FFFAVLHAI" (SEQ ID NO: 787), "GVIAAIVQL" (SEQ ID NO: 788), "KIAAIIASL" (SEQ ID NO: 789), "LIFKSILFL" (SEQ ID NO: 790), "LLLGTIHAL" (SEQ ID NO: 791), "LLSFFFAVL" (SEQ ID NO: 792), "MIAVFLPIV" (SEQ ID NO: 793) или "SLLLGTIHA" (SEQ ID NO: 794). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена STEAP1, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 451 468. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента STEAP1 (референсный пептид человека) "ASLTFLYTL" (SEQ ID NO: 785), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 451. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента STEAP1 (референсный пептид человека) "AVLHAIYSL" (SEQ ID NO: 786), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 452. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента STEAP1 (референсный пептид человека) "FFFAVLHAI" (SEQ ID NO: 787), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 453. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента STEAP1 (референсный пептид человека) "GVIAAIVQL" (SEQ ID NO: 788), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 454, 455, 456 или 457. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента STEAP1 (референсный пептид человека) "KIAAIIASL" (SEQ ID NO: 789), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 458, 459 или 460. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента STEAP1 (референсный пептид человека) "LIFKSILFL" (SEQ ID NO: 790), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 461. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента STEAP1 (референсный пептид человека) "LLLGTIHAL" (SEQ ID NO: 791), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 462. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента STEAP1 (референсный пептид человека) "LLSFFFAVL" (SEQ ID NO: 792), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 463, 464 или 465. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента STEAP1 (референсный пептид человека) "MIAVFLPIV" (SEQ ID NO: 793), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 466. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента STEAP1 (референсный пептид человека) "SLLLGTIHA" (SEQ ID NO: 794), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 467 или 468.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена TBL1Y (референсный пептид человека), такой как "SLSLIVAVI" (SEQ ID NO: 795). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена TBL1Y, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 469-470. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента TBL1Y (референсный пептид человека) "SLSLIVAVI" (SEQ ID NO: 795), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 469 или 470.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена TDRD1 (референсный пептид человека), такой как "IISPNLFYA" (SEQ ID NO: 796), "LLDHVLIEM" (SEQ ID NO: 797), "VLIDEHLVL" (SEQ ID NO: 798), "YSSEVLEYM" (SEQ ID NO: 799). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена TDRD1, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 471-474. Более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента TDRD1 (референсный пептид человека) "IISPNLFYA" (SEQ ID NO: 796), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 471. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента TDRD1 (референсный пептид человека) "LLDHVLIEM" (SEQ ID NO: 797), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 472. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента опухолевого антигена TDRD1 (референсный пептид человека) "VLIDEHLVL" (SEQ ID NO: 798), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 473. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента TDRD1 (референсный пептид человека) "YSSEVLEYM" (SEQ ID NO: 799), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 474.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена ТОР2А (референсный пептид человека) такой как "ILLRPDTYI" (SEQ ID NO: 800), "LMMTIINLA" (SEQ ID NO: 801), "QLAGSVAEM" (SEQ ID NO: 802), "SLMMTIINL" (SEQ ID NO: 803), "TMLSSLARL" (SEQ ID NO: 804) или "YIFTMLSSL" (SEQ ID NO: 805). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена ТОР2А, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 475-483. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента ТОР2А (референсный пептид человека) "ILLRPDTYI" (SEQ ID NO: 800), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 475. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента ТОР2А (референсный пептид человека) "LMMTIINLA" (SEQ ID NO: 801), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 476, 477 или 478. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента ТОР2А (референсный пептид человека) "QLAGSVAEM" (SEQ ID NO: 802), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 479 или 480. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента ТОР2А (референсный пептид человека) "SLMMTIINL" (SEQ ID NO: 803), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 481. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента ТОР2А (референсный пептид человека) "TMLSSLARL" (SEQ ID NO: 804), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 482. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента ТОР2А (референсный пептид человека) "YIFTMLSSL" (SEQ ID NO: 805), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 483.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена ТРТЕ (референсный пептид человека), такой как DLAGVIIEL" (SEQ ID NO: 806), "FGLFGVFLV" (SEQ ID NO: 807), "GLFGVFLVL" (SEQ ID NO: 808), "ILDTAIIVI" (SEQ ID NO: 809), "IVSSFAFGL" (SEQ ID NO: 810), "RLLRLIILL" (SEQ ID NO: 811), "SLAIALFFL" (SEQ ID NO: 812) или "YFWLHTSFI" (SEQ ID NO: 813). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена ТРТЕ, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 484-504. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента ТРТЕ (референсный пептид человека) "DLAGVIIEL" (SEQ ID NO: 806), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 484, 485, 486, 487, 488, 489 или 490. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента ТРТЕ "FGLFGVFLV" (SEQ ID NO: 807), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 491, 492, 493 или 494. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента ТРТЕ (референсный пептид человека) "GLFGVFLVL" (SEQ ID NO: 808), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 495, 496 или 497. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента ТРТЕ (референсный пептид человека) "ILDTAIIVI" (SEQ ID NO: 809), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 498 или 499. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента ТРТЕ (референсный пептид человека) "IVSSFAFGL" (SEQ ID NO: 810), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 500 или 501. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента ТРТЕ (референсный пептид человека) "RLLRLIILL" (SEQ ID NO: 811), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 502. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента ТРТЕ (референсный пептид человека) "SLAIALFFL" (SEQ ID NO: 812), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 503. Также более предпочтительно, антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента ТРТЕ (референсный пептид человека) "YFWLHTSFI" (SEQ ID NO: 813), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 504.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена TRPM8 (референсный пептид человека), такой как "AMFGYTVGT" (SEQ ID NO: 814), "FIAGIVFRL" (SEQ ID NO: 815), "FLLLFAYVL" (SEQ ID NO: 816), "LLFAYVLLM" (SEQ ID NO: 817), "LLLFAYVLL" (SEQ ID NO: 818), "LVLYSLVFV" (SEQ ID NO: 819), "NILLVNLLV" (SEQ ID NO: 820), "QIADVIASL" (SEQ ID NO: 821), "VLYSLVFVL" (SEQ ID NO: 822) или "YLVKINTKA" (SEQ ID NO: 823). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена TRPM8, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NOs 505-518. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента TRPM8 (референсный пептид человека) "AMFGYTVGT" (SEQ ID NO: 814), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 505. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента TRPM8 (референсный пептид человека) "FIAGIVFRL" (SEQ ID NO: 815), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 506. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента TRPM8 (референсный пептид человека) "FLLLFAYVL" (SEQ ID NO: 816), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 507. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента TRPM8 (референсный пептид человека) "LLFAYVLLM" (SEQ ID NO: 817), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 508 или 509. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента TRPM8 (референсный пептид человека) "LLLFAYVLL" (SEQ ID NO: 818), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 510. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента TRPM8 (референсный пептид человека) "LVLYSLVFV" (SEQ ID NO: 819), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 511. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента TRPM8 (референсный пептид человека) "NILLVNLLV" (SEQ ID NO: 820), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 512. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента TRPM8 (референсный пептид человека) "QIADVIASL" (SEQ ID NO: 821), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 513, 514, 515 или 516. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента TRPM8 (референсный пептид человека) "VLYSLVFVL" (SEQ ID NO: 822), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 517. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента TRPM8 (референсный пептид человека) "YLVKINTKA" (SEQ ID NO: 823), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 518.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена TYMS (референсный пептид человека), такой как "FLDSLGFST" (SEQ ID NO: 824), "SLRDEFPLL" (SEQ ID NO: 825) или "VLEELLWFI" (SEQ ID NO: 826). Согласно другому предпочтительному варианту осуществления изобретения, антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена TYMS, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 519-524. Более предпочтительно, антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента TYMS (референсный пептид человека) "FLDSLGFST" (SEQ ID NO: 824), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 519, 520 или 521.
Также более предпочтительно, антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента TYMS (референсный пептид человека) "SLRDEFPLL" (SEQ ID NO: 825), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 522 или 523. Также более предпочтительно, антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента TYMS (референсный пептид человека) "VEEELLWFI" (SEQ ID NO: 826), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 524.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена TYR (референсный пептид человека)), такой как "ALLAGLVSL" (SEQ ID NO: 827), "AMVGAVLTA" (SEQ ID NO: 828), "ISSDYVIPI" (SEQ ID NO: 829), "LLAGLVSLL" (SEQ ID NO: 830), "LLSPASFFS" (SEQ ID NO: 831), "MVGAVLTAL" (SEQ ID NO: 832) или "VLTALLAGL" (SEQ ID NO: 833). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена TYR, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 525-539. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента TYR (референсный пептид человека) "ALLAGLVSL" (SEQ ID NO: 827), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 525 или 526. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента TYR (референсный пептид человека) "AMVGAVLTA" (SEQ ID NO: 828), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 527, 528, 529 или 530.
Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента TYR (референсный пептид человека) "ISSDYVIPI" (SEQ ID NO: 829), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 531. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента TYR (референсный пептид человека) "LLAGLVSLL" (SEQ ID NO: 830), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 532. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента TYR (референсный пептид человека) "LLSPASFFS" (SEQ ID NO: 831), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 533. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента TYR (референсный пептид человека) "MVGAVLTAL" (SEQ ID NO: 832), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 534. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента TYR (референсный пептид человека) "VLTALLAGL" (SEQ ID NO: 833), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 535, 536, 537, 538 или 539.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена UPK2 (референсный пептид человека), такой как "ALTESLLVA" (SEQ ID NO: 834), "LLALLSPGA" (SEQ ID NO: 835), "LVLGFIIAL" (SEQ ID NO: 836), "SLSGLLSPA" (SEQ ID NO: 837), "TLPLILILL" (SEQ ID NO: 838), "VLGFIIALA" (SEQ ID NO: 839) или "VVITVLLSV" (SEQ ID NO: 840). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена UPK2, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 540-556. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента UPK2 (референсный пептид человека) "ALTESLLVA" (SEQ ID NO: 834), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 540, 541 или 542. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента UPK2 (референсный пептид человека) "LLALLSPGA" (SEQ ID NO: 835), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 543. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента UPK2 (референсный пептид человека) "LVLGFIIAL" (SEQ ID NO: 836), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 544, 545, 546 или 547. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента UPK2 (референсный пептид человека) "SLSGLLSPA" (SEQ ID NO: 837), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 548 или 549. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента UPK2 (референсный пептид человека) "TLPLILILL" (SEQ ID NO: 838), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 550. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента UPK2 (референсный пептид человека) "VLGFIIALA" (SEQ ID NO: 839), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 551, 552, 553 или 554. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента UPK2 (референсный пептид человека) "VVITVELSV" (SEQ ID NO: 840), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 555 или 556.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена VCAM1 (референсный пептид человека), такой как "AQIGDSVML" (SEQ ID NO: 841), "FASSLIIPA" (SEQ ID NO: 842), "KSIDGAYTI" (SEQ ID NO: 843) или "SILEEGSSV" (SEQ ID NO: 844). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена VCAM1, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в SEQ ID NOs 557-560. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента VCAM1 (референсный пептид человека) "AQIGDSVML" (SEQ ID NO: 841), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 557. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента VCAM1 (референсный пептид человека) "FASSLIIPA" (SEQ ID NO: 842), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 558. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента VCAM1 (референсный пептид человека) "KSIDGAYTI" (SEQ ID NO: 843), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 559. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента VCAM1 (референсный пептид человека) "SILEEGSSV" (SEQ ID NO: 844), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 560.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена WFDC2 (референсный пептид человека), такой как "LLFGFTLVS" (SEQ ID NO: 845), "LLLFGFTLV" (SEQ ID NO: 846) или "RLGPLAAAL" (SEQ ID NO: 847). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена WFDC2, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 561-568. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента WFDC2 (референсный пептид человека) "LLFGFTLVS" (SEQ ID NO: 845), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 561, 562, 563, 564 или 565. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента WFDC2 (референсный пептид человека) "LLLFGFTLV" (SEQ ID NO: 846), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 566. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента WFDC2 (референсный пептид человека) "RLGPLAAAL" (SEQ ID NO: 847), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 567 или 568.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена WT1 (референсный пептид человека), такой как "DLNALLPAV" (SEQ ID NO: 848). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена WT1, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 569. Конкретнее - антигенный пептид, заявленный в соответствии с настоящим изобретением, который состоит из или включает в себя аминокислотную последовательность, как указано в SEQ ID NO: 569 представляет собой вариант последовательности фрагмента WT1 (референсный пептид человека) "DLNALLPAV" (SEQ ID NO: 848).
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена ZEB1 (референсный пептид человека), такой как "ILIPQVAYT" (SEQ ID NO: 849), "NLSDIQNVL" (SEQ ID NO: 850) или "VQAVVLPTV" (SEQ ID NO: 851). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена ZEB1, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 570-574. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента ZEB1 (референсный пептид человека) "ILIPQVAYT" (SEQ ID NO: 849), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 570 или 571. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента ZEB1 (референсный пептид человека) "NLSDIQNVL" (SEQ ID NO: 850), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 572 или 573. Также более предпочтительно, антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента ZEB1 (референсный пептид человека) "VQAWLPTV" (SEQ ID NO: 851), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 574.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена ZNF165 (референсный пептид человека), такой как "LVLEQFLTI" (SEQ ID NO: 852) или "RISGYISEA" (SEQ ID NO: 853). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена ZNF165, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 575-578. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента ZNF165 (референсный пептид человека) "LVLEQFLTI" (SEQ ID NO: 852), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 575, 576 или 577. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента ZNF165 (референсный пептид человека) "RISGYISEA" (SEQ ID NO: 853), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 578.
Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой микробиотический вариант последовательности фрагмента опухолевого антигена ZNF280A (референсный пептид человека), такой как "AMTDISSLA" (SEQ ID NO: 854) или "VLLSNFYYG" (SEQ ID NO: 855). Согласно другому предпочтительному варианту осуществления изобретения антигенный пептид по изобретению представляет собой вариант последовательности фрагмента опухолевого антигена ZNF280A, такой как антигенные пептиды, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 579-580. Более предпочтительно антигенный пептид, заявленный в соответствии с настоящим изобретением, представляет собой вариант последовательности фрагмента ZNF280A (референсный пептид человека) "AMTDISSLA" (SEQ ID NO: 854), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 579. Также более предпочтительно антигенный пептид по настоящему изобретению представляет собой вариант последовательности фрагмента ZNF280A (референсный пептид человека) "VLLSNFYYG" (SEQ ID NO: 855), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 580.
Предпочтительно антигенный пептид по настоящему изобретению состоит из или включает в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 1-160, 162-253 и 255-580. Более предпочтительно антигенный пептид по настоящему изобретению состоит из или включает в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 31, 32, 87, 97, 145, 193, 194, 220, 221, 255, 521 и 524. Еще более предпочтительно состоит из или включает в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 31, 32, 87, 97, 193, 194, 220, 255, 521 и 524. Еще более предпочтительно состоит из или включает в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 31, 32, 87, 97, 194, 220, 255, 521 и 524. Более предпочтительно антигенный пептид по настоящему изобретению состоит из или включает в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 32, 87, 97, и 194.
Кроме того, антигенный пептид по настоящему изобретению, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 32, 194, 220, 254 или 255, является наиболее предпочтительным. Более предпочтительно антигенный пептид по настоящему изобретению состоит из или включает в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 30 или 32. Более предпочтительно антигенный пептид по настоящему изобретению состоит из или включает в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 194 или 220. Более предпочтительно антигенный пептид по настоящему изобретению состоит из или включает в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 254 или 255.
Как показано в примерах, раскрытых в настоящем описании, специфические антигенные пептиды по настоящему изобретению позволяют создать сильный иммунный ответ против самих себя, а также, что наиболее важно, создать сильный иммунный ответ против пептидов, имеющих аминокислотное сходство с пептидами в составе опухолевого антигена, даже в том случае, если человеческие референсные пептиды в составе опухолевого антигена вызывают иммунную толерантность.
Преимущественно антигенные пептиды по настоящему изобретению могут быть в форме иммуногенных соединений, в частности; предназначенных для применения для профилактики и лечения рака.
Иммуногенные соединения, включающие антигенный пептид по настоящему изобретению
Согласно дополнительному аспекту настоящее изобретение также относится к иммуногенному соединению, включающему антигенный пептид по настоящему изобретению, как раскрыто выше. Конкретнее - предпочтительные варианты антигенного пептида, как раскрыто выше, также применимы в качестве иммуногенного соединения по настоящему изобретению. Например, антигенный пептид в составе иммуногенного соединения, предпочтительно, состоит из или включает в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 1-580 и 861-887, такой как антигенный пептид, состоящий из и включающий в себя в аминокислотную последовательность, как указано в любой из SEQ ID NOs 1-580. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 1-160, 162-253 и 255-580, являются более предпочтительными.
Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 31, 32, 87, 97, 145, 193, 194, 220, 221, 255, 521 и 524, являются еще более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 31, 32, 87, 97, 193, 194, 220, 255, 521 и 524, являются еще более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 31, 32, 87, 97, 194, 220, 255, 521 и 524, являются еще более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 32, 87, 97, и 194, являются наиболее предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 32, 194, 220, 254 или 255, являются особенно предпочтительными. Также предпочтительными являются их комбинации, конкретнее - иммуногенное соединение, включающее отдельные антигенные пептиды по настоящему изобретению.
Используемый в настоящем изобретении термин "иммуногенное соединение" относится к соединению, которое обладает способностью индуцировать, усиливать, пролонгировать или поддерживать иммунный ответ, конкретнее - индуцировать, усиливать, пролонгировать или поддерживать иммунный ответ при введении млекопитающему, в особенности при введении человеку.
В целом, термин "иммуногенное соединение" относится ко всем типам соединений, включающим антигенный пептид по настоящему изобретению. Например, антигенный пептид по настоящему изобретению может быть связан с молекулой носителя или антигенный пептид по настоящему изобретению может быть включен в состав полипептида или белка (причем такой полипептид или белок может существовать "отдельно", то есть не быть связанным с каким-либо другим соединением, или такой полипептид или белок, включающий антигенный пептид, может быть связан с молекулой носителя).
Предпочтительно иммуногенное соединение по настоящему изобретению включает антигенный пептид и молекулу носителя, в частности, причем антигенный пептид (или полипептид или белок, включающий антигенный пептид) связан с молекулой носителя. Предпочтительной молекулой носителя является белок носитель или пептид носитель. Согласно предпочтительному варианту осуществления изобретения антигенный пептид, как раскрыто выше, или полипептид/белок, включающий указанный антигенный пептид, соединен с белком носителем или пептидом носителем, например, при помощи ковалентной или нековалентной связи. Альтернативно такой белок носитель или пептид носитель, как раскрыто в настоящем документе, может вводиться (отдельно) совместно в форме иммуностимулятора (то есть не как самостоятельный "иммуногенное соединение", но в составе комбинированной терапии, как раскрыто ниже).
Молекула носителя также может представлять собой липид или липидоподобную молекулу. В этом случае иммуногенное соединение может представлять собой липопептид. Используемый в настоящем изобретении термин "липопептид" относится к молекуле, которая включает липид или липидоподобную молекулу ковалентно связанную с молекулой пептида. В целом "липид" растворим в неполярных растворителях, обычно "липид" не растворим (или плохо растворим) в воде. Примеры липидной или липидоподобной молекулы включают, без ограничений указанными, жирные кислоты, воски, стерины, моноглицериды, диглицериды, триглицериды и фосфолипиды. Липид может представлять собой жирную кислоту, глицеролипид, глицерофосфолипид, сфинголипид, стероловый липид, преноловый липид, сахаролипид или поликетид. Предпочтительно липид представляет собой жирную кислоту или ее производное (включая моноглицериды, диглицериды, триглицериды и фосфолипиды). Жирные кислоты обычно включают углеводную цепь, которая заканчивается карбоксильной группой. Жирные кислоты могут быть насыщенными или ненасыщенными. Жирные кислоты могут прикрепляться к функциональным группам, например, включающим оксигены, галогены, азот или сера. Предпочтительные жирные кислоты представляют собой насыщенные или ненасыщенные длинноцепочечные жирные кислоты, такие как миристиновая кислота с 14 атомами углерода (СН3(СН2)12СООН) или пальмитиновая кислота с 16 атомами углерода (СН3(СН2)14СООН), а также фосфолипиды, такие как фосфатидилглицерол (PG).
Предпочтительно антигенный пептид, как раскрыто в настоящем описании, или полипептид/белок, включающий антигенный пептид, может вводиться совместно или быть связанным, например, с помощью ковалентной или нековалентной связи, с белком/пептидом, обладающим иммуностимулирующими свойствами, такими как обеспечение стимуляции CD4+ Th1 клеток. Хотя антигенный пептид, как раскрыто в настоящем документе, предпочтительно, связывается с МНС класса I, CD4+ хелперные эпитопы могут дополнительно использоваться для обеспечения эффективного иммунного ответа. Th1 хелперные клетки обладают способностью поддерживать эффективную активацию дендритных клеток (ДК) и специфическую CTL активацию за счет секреции интерферона-гамма (IFN-γ), фактора некроза опухолей-альфа (TNF-α) и интерлейкина-2 (IL-2), а также усиления экспрессии костимулирующего сигнала на DCs и Т клетках (Galaine et al., Interest of Tumor-Specific CD4 Т Helper 1 Cells for Therapeutic Anticancer Vaccine. Vaccines (Basel). 2015 Jun 30; 3(3):490-502).
Например, адъювантный пептид/белок может, предпочтительно, представлять собой неопухолевый антиген, который оживляет иммунную память или оказывает неспецифическую помощь, либо представляет собой специфический хелперный белок опухолевого происхождения. В литературе описано несколько хелперных белков для обеспечения неспецифической помощи Т-клеткам, например, столбнячный хелперный белок, гемоцианин лимфы улитки или пептид PADRE ( et al., Targeting antitumor CD4 helper Т cells with universal tumor-reactive helper peptides derived from telomerase for cancer vaccine. Hum Vaccin Immunother. 2013 May; 9(5): 1073-7, Slingluff CL, The present and future of peptide vaccines for cancer: single or multiple, long or short, alone or in combination? Cancer J. 2011 Sep-Oct; 17(5):343-50). Таким образом, столбнячный хелперный пептид, гемоцианин лимфы улитки и пептид PADRE являются предпочтительными примерами таких адъювантных пептидов/белков. Кроме того, специфические хелперные белки опухолевого происхождения являются предпочтительными. Специфические хелперные белки опухолевого происхождения обычно презентируются МНС класса II, в частности, с помощью HLA-DR, HLA-DP или HLA-DQ.
et al., Targeting antitumor CD4 helper Т cells with universal tumor-reactive helper peptides derived from telomerase for cancer vaccine. Hum Vaccin Immunother. 2013 May; 9(5): 1073-7, Slingluff CL, The present and future of peptide vaccines for cancer: single or multiple, long or short, alone or in combination? Cancer J. 2011 Sep-Oct; 17(5):343-50). Таким образом, столбнячный хелперный пептид, гемоцианин лимфы улитки и пептид PADRE являются предпочтительными примерами таких адъювантных пептидов/белков. Кроме того, специфические хелперные белки опухолевого происхождения являются предпочтительными. Специфические хелперные белки опухолевого происхождения обычно презентируются МНС класса II, в частности, с помощью HLA-DR, HLA-DP или HLA-DQ.
Специфические хелперные белки опухолевого происхождения могут представлять собой фрагменты последовательностей родственных гиперэкспрессируемых опухолевых антигенов, таких как HER2, NY-ESO-1, hTERT или IL13RA2. Такие фрагменты имеют длину по меньшей мере 10 аминокислот, более предпочтительно по меньшей мере 11 аминокислот, еще более предпочтительно по меньшей мере 12 аминокислот и еще более предпочтительно по меньшей мере 13 аминокислот. В частности, фрагменты родственных гиперэкпрессируемых опухолевых антигенов, такие как HER2, NY-ESO-1, hTERT или IL13RA2, имеющие длину от 13 до 24 аминокислот, являются предпочтительными. Предпочтительные фрагменты связываются с МНС класса II и могут, таким образом, быть идентифицированы с применением, например, средств прогнозирования IEDB (база данных иммунных эпитопов; Supported by a contract from the National Institute of Allergy and Infectious Diseases, a component of the National Institutes of Health in the Department of Health and Human Services; URL: http://www.iedb.org/; http://tools.iedb.org/mhcii/) для связывания с МНС класса II. Предпочтительно адъювантный пептид/белок может представлять собой пептид HHD-DR3 с последовательностью MAKTIAYDEEARRGLERGLN (SEQ ID NO: 856). Другим предпочтительным примером является h-pAg T13L (последовательность: TPPAYRPPNAPIL; SEQ ID NO: 860; Bhasin M, Singh H, Raghava GP (2003) MHCBN: a comprehensive database of МНС binding and non-binding peptides. Bioinformatics 19: 665-666). Другие примеры предпочтительных адъювантных пептидов/белков, в частности хелперных пептидов, включают UCP2 пептид (например, как раскрыто в WO 2013/135553 А1 или у Dosset и соавт. Clin Cancer Res. 2012 Nov 15; 18(22):6284-95) и BIRC5 пептид (например, как описано в ЕР2119726 А1 или у Widenmeyer et al. Int J Cancer. 2012 Jul 1; 131(1):140-9). Наиболее предпочтительным хелперным пептидом является UCP2 пептид (аминокислотная последовательность: KSVWSKLQSIGIRQH; SEQ ID NO: 859, например, как раскрыто в WO 2013/135553 А1 или у Dosset et al., Clin Cancer Res. 2012 Nov 15; 18(22):6284-95).
Также является предпочтительным, чтобы иммуногенное соединение по настоящему изобретению представляло собой полипептид или белок, включающий антигенный пептид по настоящему изобретению. Предпочтительно, такой белок или полипептид представляет собой рекомбинантный белок или полипептид, например, слитый белок. Термин "рекомбинантный" означает, что он не существует в природе.
Согласно предпочтительному варианту осуществления изобретения, иммуногенное соединение по настоящему изобретению состоит из или включает в себя полипептид формулы (I)
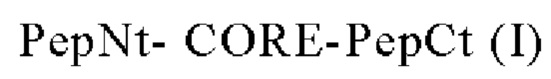
где:
-"PepNt" состоит из полипептида, имеющего длину, от 0 до 500 аминокислотных остатков, и расположенного на N-конце полипептида формулы (I);
-"CORE" состоит из антигенного пептида по настоящему изобретению, как определено выше; и
-"PepCt" состоит из полипептида, имеющего длину от 0 до 500 аминокислотных остатков и расположенного на С-конце полипептида формулы (I).
Например, иммуногенное соединение может состоять из или включать в себя полипептид формулы (1а) или (1б):
 или
или

где "PepNt" и "PepCt" и "CORE" определены выше.
Предпочтительно полипептид формулы (I), (Ia) или (Iб) представляет собой слитый пептид или белок, конкретнее - рекомбинантный слитый пептид или белок.
Также является предпочтительным, что полипептид или иммуногенное соединение, как определено выше, содержит от 9 до 1000 аминокислот; что включает 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67? 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 110, 120, 130, 140, 150, 160, 170, 180, 190, 200, 250, 300, 350, 400, 450, 500, 600, 700, 800, 900 и 1000 аминокислот. Соответственно, длина "PepNt" и "PepCt", если необходимо, может быть определена соответствующим образом.
Таким образом, "PepNt" и "PepCt", как определено выше, могут содержать от 0 до 500 аминокислотных остатков; что включает 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 110, 120, 130, 140, 150, 160, 170, 180, 190, 200, 250, 300, 350, 400, 450, и 500 аминокислотных остатков.
Типы молекул носителей, которые используются для создания иммуногенного соединения по изобретению, такого как иммуногенное соединение, состоящее из или включающее в себя полипептид формулы (I), связанный с молекулой носителя, хорошо известны специалисту в данной области. В частности функция молекулы носителя заключается в обеспечении цитокиновой помощи (или Т-клеточной помощи), для того чтобы усилить иммунный ответ против опухолевого антигена.
Предпочтительно антигенный пептид соединен с молекулой носителем, конкретнее - с белком носителем, предпочтительно, посредством ковалентной или нековалентной связи. Молекула носитель, с которой необязательно связан пептид, может быть выбрана из большого разнообразия известных носителей. Примерами молекул носителей, которые могут применяться для создания вакцин, являются белки, такие как человеческий или бычий сывороточный альбумин и гемоцианин лимфы улитки (KLH), а также жирные кислоты. Другие варианты молекул носителей, с которыми может быть ковалентно связан антигенный пептид формулы (I), включают бактериальные токсины или анатоксины, такие как дифтерийный, холерный анатоксины, термолабильный Е. coli или столбнячный анатоксины, белок наружной мембраны N. Meningitidis (Европейская патентная заявка n° EP0372501), синтетические пептиды (Европейские патентные заявки n° EP0378881 и n° ЕР0427347), белки теплового шока (заявка РСТ n° W093/17712), коклюшные белки (заявка РСТ n° W098/58668), белок D из Н. influenzae (заявка РСТ n° WO00/56360.) и токсин А или В из С.difficile (Международная патентная заявка WO00/61761).
Более предпочтительно белок носитель или пептид носитель представляет собой белок/пептид, обладающий иммуностимулирующими свойствами, такими как обеспечение стимуляции CD4+ Th1 клеток, как раскрыто в настоящем описании. Предпочтительным примером таких молекул является неопухолевый антиген, который вызывает иммунную память или оказывает неспецифическую помощь, или представляет собой специфический хелперный пептид опухолевого происхождения, такой как столбнячный хелперный пептид, пептид из гомоцианина лимфы улитки или пептид PADRE. Другим предпочтительным примером является специфический, выделенный из опухоли, специфический пептид, который может презентироваться МНС II, конкретнее - HLA-DR, HLA-DP или HLA-DQ, такой как фрагменты родственных гиперэкспрессируемых опухолевых антигенов, например, HER2, NY-ESO-1, hTERT или IL13RA2, как описано выше. Согласно предпочтительному варианту осуществления изобретения белок носитель или пептид носитель может представлять собой белок/пептид, обладающий иммуностимулирующими свойствами, например, HHD-DR3 пептид носитель MAKTIAYDEEARRGLERGLN (SEQ ID NO: 856). В частности "PepNt" и/или "PepCt" могут соответствовать белку носителю или пептиду носителю, такому как HHD-DR3 белок носитель MAKTIAYDEEARRGLERGLN (SEQ ID NO: 856). Другим предпочтительным примером является h-pAg T13L (последовательность: TPPAYRPPNAPIL; SEQ ID NO: 860; Bhasin М, Singh Н, Raghava GP (2003) MHCBN: обширная база пептидов, связывающихся и не связывающихся с МНС. Bioinformatics 19: 665 666). Другими примерами предпочтительных белков/пептидов носителей, в частности, хелперных пептидов являются UCP2 пептид (например, как раскрыто в WO 2013/135553 А1 или у Dosset и соавт., Clin Cancer Res. 2012 Nov 15; 18(22):6284-95) и BIRC5 пептид (например, как раскрыто в ЕР 2119726 А1 или у Widenmeyer и соавт., Int J Cancer. 2012 Jul 1; 131(1):140-9). Наиболее предпочтительным хелперным пептидом является UCP2 пептид (аминокислотная последовательность: KSVWSKLQSIGIRQH; SEQ ID NO: 859).
Кроме того, в полипептиде формулы (I), (Ia) или (Iб), "PepNt" и/или "PepCt" могут предпочтительно соответствовать такому белку/протеину, обладающему иммуностимулирующими свойствами, который обеспечивает стимуляцию CD4+ Th1 клеток, как раскрыто в настоящем описании.
Кроме того, иммуногенное соединение может состоять из или включать в себя такой белок/пептид с иммуностимулирующими свойствами, такими как обеспечение стимуляции CD4+ Th1 cells, как раскрыто в настоящем описании, который ковалентно связан с N-концом антигенного пептида по настоящему изобретению или N-концом полипептида/белка, включающего указанный антигенный пептид.
Предпочтительно антигенный пептид по настоящему изобретению (или полипептид/белок, включающий указанный антигенный пептид) ковалентно связан с молекулой носителя посредством линкерной молекулы.
Предпочтительные линкерные агенты включают линкерные агенты, обозначаемые GMBS, сульфо-GMBS, SMPB и сульфо-SMPB.
Согласно некоторым вариантам воплощения иммуногенного соединения, как определено в настоящем описании, линкерный агент выбран из группы, включающей GMBS эфир (N-[γ-малеимидобутурил-окси]сукцинимида), сульфо-GMBS эфир (N-[γ-малеимидобутурил-окси]сульфосукцинимида), SMPB (сукцинимидил 4-[p-малеимидофенил]бутират) и сульфо-SMPB (сульфосукцинимидил 4-[р-малеимидофенил] бутират).
Способы конъюгации двух белков с линкерным агентом в целом и конкретнее - с линкерным агентом, выбранным из группы, включающей GMBS, сульфо-GMBS, SMPB и сульфо-SMPB, хорошо известны специалисту в данной области. Например, такие протоколы раскрыты в листовках, которые публикуются компанией Pierce (Иллинойс, США). GMBS, сульфо-GMBS, SMPB и сульфо-SMPB состоит из гетеробифункциональных линкерных агентов, которые включают, как эфирную группу N-гидроксисукцинимида (NHS) так и малеимидную группу. Конъюгация с использованием GMBS, сульфо-GMBS, SMPB или сульфо-SMPB обычно происходит в два этапа. На первом этапе аминсодержащий белок вступает в реакцию с линкерным агентом, молярное количество которого в несколько раз превышает количество белка при рН 7-9 с формированием амидных связей с последующим удалением избытка, не вступившего в реакцию линкерного агента, обычно при помощи обессоливания или диализа. На втором этапе добавляют молекулу, содержащую сульфгидрильную группу (например, пептид формулы (I)), для осуществления реакции с малеимидной группой уже присоединенной к первому белку при рН 6,5-7,5 для формирования стабильных тиоэфирных связей.
Применение SMPB или сульфо-SMPB в качестве линкерных агентов для ковалентного связывания антигенного пептида по настоящему изобретению (или полипептида/белка, включающего указанный антигенный пептид, такого как полипептид формулы (I)) с аминосодержащим белком носителем приводит к образованию конъюгата формулы (II) ниже:

где:
-R1 включает одну реакционноспособную группу аминосодержащего белка носителя, причем присоединенная к ней NH группа происходит из (а) альфа аминогруппы, расположенной на N-конце аминосодержащего белка носителя или (б) аминокислотного остатка лизина (К) аминогруппы боковой цепи аминосодержащего белка носителя; и
-R2 включает антигенный пептид по настоящему изобретению (или полипептид/белок, включающий указанный антигенный пептид, такой как полипептид формулы (I)), причем прикрепленный к нему атом серы (S) происходит из сульфгидрильной группы (SH) цистеинового остатка, расположенного на N-конце или С-конце пептида формулы (I). Согласно некоторым вариантам осуществления изобретения сульфгидрильная молекула может быть частью аминокислоты не природного происхождения, или любой другой молекулы, находящейся на конце пептида формулы (I).
Применение GMBS или сульфо-GMBS в качестве линкерных агентов для ковалентного связывания антигенного пептида по настоящему изобретению (или полипептида/белка, включающего указанный антигенный пептид, такого как полипептид формулы (I)) с аминосодержащим белком носителем, в частности, с носителем CRM 197, приводит к образованию конъюгата формулы (III) ниже:

где:
- R1 включает одну реакционноспособную группу аминосодержащего белка носителя, причем прикрепленная к ней NH группа происходит из (а) альфа аминогруппы, расположенной на N-конце аминосодержащего белка носителя или (б) аминокислотного остатка лизина (К) аминогруппы боковой цепи аминосодержащего белка носителя; и
-R2 включает антигенный пептид по настоящему изобретению (или полипептид/белок, включающий указанный антигенный пептид, такой как полипептид формулы (I)), причем прикрепленный к нему атом серы (S) происходит из сульфгидрильной группы (SH) цистеинового остатка, расположенного на N-конце или С-конце пептида формулы (I).
Согласно некоторым вариантам осуществления изобретения сульфгидрильная молекула может быть частью аминокислоты не природного происхождения или любой другой молекулы, находящейся на конце пептида формулы (I).
Мультимеры пептид МНС (рМНС), включающие антигенный пептид
Согласно дополнительному аспекту настоящее изобретение также относится к мультимеру пептид-МНС (рМНС), включающему антигенный пептид по настоящему изобретению.
Используемый в настоящем изобретении термин "мультимер пептид-МНС" (рМНС) относится к стабильному мультимерному комплексу, состоящему из белковых субъединиц основного комплекса гистосовместимости (МНС аббрев. от англ. Major Histocompatibility Complex), "нагруженных" антигенным пептидом по изобретению. В целом, "мультимеры МНС" представляют собой олигомерные формы МНС молекул. Основной функцией МНС молекулы является связывание антигена. Согласно настоящему изобретению указанным антигеном является антигенный пептид по настоящему изобретению. Соответственно, комплекс белков МНС, "нагруженный" антигенным пептидом по изобретению, обычно означает, что антигенный пептид по изобретению связан с одним или более МНС белком. "Мультимеры пептид-МНС" (рМНС) по изобретению включают, без ограничений указанными, пептид-МНС димер, тример, тетрамер, пентамер, гексамер, гептамер или октамер. МНС тетрамеры и пентамеры являются предпочтительными. Термин "Основной комплекс гистосовместимости (МНС)» - это общепринятое обозначение системы антигенов гистосовместимости, описанной для разных видов, включая антигены лейкоцитов человека (HLA). У людей существует три основных различных генетических локуса, которые кодируют молекулы МНС I класса: HLA-A, HLA-В, и HLA-C. HLA-A*01, HLA-A*02, и HLA-А*11, они являются примерами аллелей различных МНС I класса, которые могут экспрессироваться с этих локусов.
Согласно одному варианту осуществления изобретения рМНС мультимер представляет собой мультимер пептида/молекулы МНС I класса. Согласно другому определенному варианту осуществления изобретения рМНС представляет собой HLA, соответствующий мультимеру МНС I класса/пептид. Соответственно, рМНС мультимер может представлять собой мультимер HLA-пептид, выбранный из группы, включающей мультимер HLA-A-пептид, мультимер HLA-B-пептид, мультимер HLA-C-пептид, мультимер HLA-E-пептид, мультимер MICA-пептид и мультимер MICB-пептид.
Способы получения рМНС мультимеров хорошо известны из области техники и описаны, например, в WO 96/26962 и WO 01/18053, которые включены в настоящее описание в качестве ссылок.
Помимо молекулы МНС и антигенного пептида по изобретению, рМНС может включать другие компоненты, такие как агент для мультимеризации и/или метка (например, для визуализации). Примеры меток включают, без ограничений указанными, флуоресцентные метки, например, флуоресцентно-меченые белки, такие как стрептавидин. Флуоресцентные метки включают аллофикоцианин (АРС), фикоэритрин (РЕ), R-фикоэритрин (R-PE) и флуоресцинизотиоцианат (FITC). Предпочтительной меткой является биотин.
Согласно одному варианту осуществления изобретения указанный рМНС мультимер может применяться для визуализации популяции Т клеток, которые являются специфичными для МНС I класса пептидного комплекса или HLA, соответствующего МНС I класса/пептидному комплексу, как описано выше. Например, рМНС мультимер может представлять собой мультимер, в котором тяжелая цепь МНС является биотинилированной, что позволяет создавать тетрамерную комбинацию со стрептавидином. Такой рМНС тетрамер обладает повышенной авидностью по отношению к соответствующим TCR-несущим Т лимфоцитам и, таким образом, может применяться для визуализации реактивных популяций с помощью иммунофлуоресценции. Согласно другому варианту осуществления изобретения указанный рМНС мультимер может применяться для детекции и/или выделения в скрининге (в проточной флуометрии или в иммуномагнитном скрининге) Т-клеточных популяций, специфичных для рМНС комплекса, как раскрыто в настоящем описании выше.
Клетки, нагруженные антигенным пептидом или иммуногенным соединением
Согласно дополнительному аспекту настоящее изобретение также относится к клеткам, нагруженным антигенным пептидом по настоящему изобретению или иммуногенным пептидом, включающим антигенный пептид по настоящему изобретению, как описано выше. В частности, предпочтительные варианты воплощения антигенного пептида, как описано выше, также применимы к таким клеткам по настоящему изобретению. Например, антигенный пептид, загруженный в клетку или включенный в иммуногенное соединение, загруженное в клетку, предпочтительно состоит из или включает в себя аминокислотную последовательность, как указано в SEQ ID NOs от 1 до 580 и от 861 до 887, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID Nos от 1 до 580. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 1-160, 162-253 и 255-580, являются более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID Nos 30, 31, 32, 87, 97, 145, 193, 194, 220, 221, 255, 521 и 524, являются еще более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID Nos 30, 31, 32, 87, 97, 193, 194, 220, 255, 521 и 524, являются более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID Nos 30, 31, 32, 87, 97, 194, 220, 255, 521 и 524, являются наиболее предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 32, 87, 97, и 194, являются наиболее предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID Nos 30, 32, 194, 220, 254 или 255 являются наиболее предпочтительными. Также предпочтительными являются их комбинации, конкретнее - клетки, нагруженные разными антигенными пептидами по настоящему изобретению (или соответствующими иммуногенными соединениями)).
Предпочтительные клетки, нагруженные антигенным пептидом по настоящему изобретению или иммуногенным соединением по настоящему изобретению, представляют собой антигенпрезентирующие клетки (АПК), более предпочтительно дендритные клетки (ДК).
АРС представляют наибольший интерес, поскольку их основная функция заключается в процессинге антигенов и презентации их на своей клеточной поверхности Т клеткам иммунной системы таким образом, чтобы инициировать и модулировать Т-клеточные ответы in vivo. В контексте настоящего изобретения является предпочтительным, чтобы APCs были нагружены антигенным пептидом(ми) и/или иммунногенным соединением(ми) по настоящему изобретению. Это можно осуществить путем экспонирования APCs in vitro указанным антигенным пептидом(ми) и/или иммуногенным соединением(ми) (как описано у Rizzo MM, Alaniz L, Mazzolini G. Ex vivo loading of autologous dendritic cells with tumor antigens. Methods Mol Biol. 2014; 1139:41-4; Rolinski J, Hus I. Breaking immunotolerance of tumors: anew perspective for dendritic cell therapy. J Immunotoxicol. 2014 Oct; 11(4):311-8).
Предпочтительные АПК в соответствии с настоящим изобретением представляют собой дендритные клетки (ДК). В действительности может быть преимущественным комбинировать по меньшей мере один антигенный пептид или иммуногенное соединение по настоящему изобретению с ДК, поскольку они являются наиболее эффективными АПК и, как сообщалось, часто бывают функционально неполноценными у пациентов с раком. ДК могут быть легко выделены специалистом в данной области, как из организма здоровых совместимых доноров (то есть ДК являются HLA-ассоциированными), так и из организма самого пациента с условием, что они являются функциональными (то есть ДК являются аутологичными), например, либо путем простого выделения из периферической крови, либо путем выведения из клеток периферической крови, таких как CD14+ моноциты или CD34+ кроветворные клетки-предшественники (Figdor CG, de Vries IJ, Lesterhuis WJ, Melief CJ. Dendritic cell immunotherapy: mapping the way. Nat Med. 2004 May; 10(5):475-80). ДК действительно можно отличить от других клеток периферической крови по их поверхностным маркерам, таким как S100, р55, CD83 и/или ОХ62, и, таким образом, их можно выделить и очистить с помощью указанных маркеров с использованием методов культур клеток, хорошо известных в данной области.
Нуклеиновые кислоты, кодирующие антигенные пептиды, и клетки-хозяева, содержащие нуклеиновые кислоты
Согласно дополнительному аспекту настоящее изобретение также относится к нуклеиновой кислоте, кодирующей антигенный пептид по настоящему изобретению, полипептид формулы (I), как раскрыто выше, или иммуногенное соединение по настоящему изобретению, причем иммуногенное соединение представляет собой пептид или белок. В частности, предпочтительные варианты воплощения антигенного пептида, как описано выше, также применимы к нуклеиновым кислотам по настоящему изобретению. Например, антигенный пептид, кодируемый нуклеиновой кислотой, предпочтительно состоит из или включает в себя аминокислотную последовательность, как указано в любой из SEQ ID Nos от 1 до 580. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 1-160, 162-253 и 255-580, являются более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 31, 32, 87, 97, 145, 193, 194, 220, 221, 255, 521 и 524, являются еще более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 31, 32, 87, 97, 193, 194, 220, 255, 521 и 524, являются еще более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 31, 32, 87, 97, 194, 220, 255, 521 и 524, являются более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 32, 87, 97, и 194, являются более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 32, 194, 220, 254 или 255, являются особенно предпочтительными. Также предпочтительными являются и комбинации, а именно, комбинации нуклеиновых кислот, кодирующих разные антигенные пептиды по изобретению.
Нуклеиновые кислоты, предпочтительно, представляют собой одноцепочечные, двухцепочечные или частично двухцепочечные нуклеиновые кислоты, предпочтительно, выбранные из геномной ДНК, кДНК, РНК, антисмысловой ДНК, антисмысловой РНК, комплементарных РНК/ДНК последовательностей, как с элементами экспрессии, так и без, мини-генов, генных фрагментов, регуляторных элементов, промоторов, а также их комбинаций.
Возможность доставки нуклеиновой кислоты, например, рибонуклеиновой кислоты (РНК) внутрь клетки, как in vitro, in vivo, in situ так и ex vivo, с целью последующей внутриклеточной трансляции нуклеиновой кислоты и синтеза интересующего кодируемого белка, представляет огромный интерес в сфере терапии, диагностики и биологических исследований. Особое значение имеют доставка и функционирование неинтегративного полинуклеотида. Соответственно, предпочтительными являются нуклеиновые кислоты, которые не встраиваются в хромосомы хозяина, такие как иРНК. В целом нуклеиновые кислоты, такие как иРНК, могут быть оптимизированы для экспрессии антигенного пептида по изобретению, например, с помощью методов известных из области техники, таких как оптимизация кодонов. Дополнительно может быть модифицирована нуклеиновая кислота, например, с целью увеличения стабильности, увеличения продолжительности службы и/или усиления экспрессии антигенного пептида по изобретению. Соответственно, оптимизированная или модифицированная иРНК (ммРНК), которая кодирует антигенный пептид по настоящему изобретению, является предпочтительной. ммРНК отличаются от иРНК дикого типа своими функциональными и/или структурными характеристиками, касающимися оптимальной доставки иРНК и/или оптимальной экспрессии антигенного пептида по изобретению (например, как раскрыто в WO 2013/151672 А2, WO 2013/101690 A1, WO 2013/052523 А, которые включены в настоящее описание в качестве ссылок). В общем нуклеиновые кислоты могут доставляться "выделенными" или вместе с носителем, например, катионным носителем. Катионные носители (положительно заряженные) обычно легко соединяются с нуклеиновыми кислотами, которые заряжены отрицательно. Носитель может быть любого типа, включая, например, полимеры, белки, липиды и наночастицы. Катионные липиды и наночастицы (в частности, липидные наночастицы, LNPs) являются предпочтительными для доставки нуклеиновых кислот. Таким образом, настоящее изобретение также относится к нуклеиновым кислотам, как раскрыто в настоящем описании, связанным с носителем (например, липидом, конкретнее - с катионным липидом или LNP).
Согласно некоторым вариантам осуществления изобретения, молекула нуклеиновой кислоты может представлять собой вектор. Термин "вектор", используемый в контексте настоящего изобретения, относится к молекуле нуклеиновой кислоты, предпочтительно, к искусственной молекуле нуклеиновой кислоты, то есть к молекуле нуклеиновой кислоты, которой не существует в природе. Вектор в контексте настоящего изобретения подходит для встраивания и сохранения последовательности нуклеиновой кислоты. Такие векторы могут представлять собой векторы хранения, векторы экспрессии, клонирующие векторы, трансферные векторы и т.д. Вектор хранения представляет собой вектор, который обеспечивает надлежащее хранение молекулы нуклеиновой кислоты. Таким образом, вектор может включать последовательность соответствующую, например, желаемому антигенному пептиду по настоящему изобретению. Вектор экспрессии может применяться для получения продуктов экспрессии, таких как РНК, например, иРНК или пептидов, полипептидов или белков. Например, вектор экспрессии может включать последовательности, необходимые для транскрипции участка последовательности вектора, например, последовательность промотора. Клонирующий вектор обычно представляет собой вектор, который включает сайт клонирования, который может применяться для встраивания последовательностей нуклеиновых кислот в вектор. Клонирующий вектор может представлять собой, например, плазмидный вектор или бактериофаговый вектор. Трансферный вектор может представлять собой вектор, подходящий для переноса молекул нуклеиновых кислот в клетки или организмы, например, вирусный вектор. Вектор в контексте настоящего изобретения может представлять собой, например, РНК вектор или ДНК вектор. Предпочтительно вектор представляет собой молекулу ДНК. Например, вектор в рамках настоящей заявки включает сайт клонирования, селекционный маркер, такой как фактор устойчивости к антибиотикам, а также последовательность, обеспечивающую размножение вектора, такую как точка начала репликации. Предпочтительно, вектор в контексте настоящей заявки представляет собой плазмидный вектор. Предпочтительный вектор представляет собой вектор для экспрессии в бактериальных клетках. Более предпочтительно вектор полезен для экспрессии в так называемых "живых бактериальных вакцинных векторах", в которых живые бактериальные клетки (такие как бактерии или их споры, например, эндоспоры, экзоспоры или микробные цисты) могут выполнять функцию вакцин. Предпочтительные примеры таких векторов описаны у a Silva et al., Live bacterial vaccine vectors: an overview; Braz J Microbiol. 2015 Mar 4;45(4):1117-29.
Нуклеиновые кислоты, кодирующие антигенные пептиды по настоящему изобретению, могут быть в форме выделенных нуклеиновых кислот или нуклеиновых кислот клонированных в плазмиды или вирусные векторы (Tregoning and Kinnear, Using Plasmids as DNA Vaccines for Infectious Diseases. Microbiol Spectr. 2014 Dec; 2(6). doi: 10.1128/microbiolspec.PLAS-0028-2014), последние являются особенно предпочтительными. Примеры подходящих вирусных векторов по настоящему изобретению включают, без ограничений указанными, ретровирусные, аденовирусные, аденоассоциированные вирусные векторы (AAV), герпес вирусные и поксвирусные векторы. В компетенции специалиста в данной области является клонирование нуклеиновой кислоты в плазмидном или вирусном векторе с применением стандартных рекомбинантных технологий.
Согласно дополнительному аспекту, настоящее изобретение также относится к клетке-хозяину, включающей нуклеиновую кислоту по настоящему изобретению. Также предпочтительными являются их комбинации, конкретнее - клетки-хозяева, включающие различные нуклеиновые кислоты по настоящему изобретению, например, кодирующие различные антигенные пептиды по настоящему изобретению.
Предпочтительно, нуклеиновые кислоты, заключенные в клетке-хозяине, представляют собой вектор. Предпочтительно, клетка-хозяин представляет собой бактериальную клетку. Такая клетка хозяин может, предпочтительно, применяться для получения антигенного пептида по настоящему изобретению или иммуногенного пептида по настоящему изобретению. Более того такая клетка хозяин также может быть активным компонентом вакцины.
Предпочтительно клетка-хозяин представляет собой бактериальную клетку, более предпочтительно бактериальную клетку микрофлоры кишечника. Термин "бактериальная клетка микрофлоры кишечника" относится к бактериям, живущим в кишечнике (человека).
Такая бактериальная клетка хозяин может выполнять роль "живого бактериального вакцинного вектора", причем живые бактериальные клетки (такие как бактерии или бактериальные споры, например, эндоспоры, экзоспоры или микробные цисты) выступают в качестве вакцин. Предпочтительные примеры таких клеток описаны у da Silva et al., Live bacterial vaccine vectors: an overview; Braz J Microbiol. 2015 Mar 4; 45(4):1117-29.
Бактериальные клетки (такие как бактерии или бактериальные споры, например, эндоспоры, экзоспоры или микробные цисты), конкретнее - виды бактерий, живущие в кишечнике (в целом), имеют преимущество, поскольку обладают способностью индуцировать более сильный иммунный ответ, чем (поли)пептиды или нуклеиновые кислоты, которые они содержат.
Альтернативно бактериальные клетки, в частности, клетки кишечных бактерий по настоящему изобретению могут находиться в форме пробиотиков, то есть в форме живых кишечных бактерий, которые, таким образом, могут применяться в качестве пищевой добавки благодаря благоприятному влиянию на здоровье. Они могут быть, например, лиофилизированы в гранулы, пилюли или капсулы, или непосредственно смешиваться с молочными продуктами перед употреблением.
Наночастицы, включающие антигенный пептид или иммуногенное соединение
Согласно дополнительному аспекту настоящее изобретение также относится к наночастице, включающей, в частности, наночастицу, нагруженную по меньшей мере одним антигенным пептидом по настоящему изобретению, или по меньшей мере одним иммуногенным соединением по настоящему изобретению;
и необязательно адъювантом.
В частности предпочтительные варианты антигенного пептида, как раскрыто в настоящем документе, также применимы для таких наночастиц по настоящему изобретению. Например, антигенный пептид, нагруженный на наночастицу или включенный в иммуногенное соединение, нагруженное на наночастицу, предпочтительно состоит из или включает в себя аминокислотную последовательность, как указано в любой из SEQ ID Nos от 1 до 580 и от 861 до 887, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID Nos от 1 до 580. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 1-160, 162-253 и 255-580, являются более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 31, 32, 87, 97, 145, 193, 194, 220, 221, 255, 521 и 524, являются еще более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 31, 32, 87, 97, 193, 194, 220, 255, 521 и 524, являются еще более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 31, 32, 87, 97, 194, 220, 255, 521 и 524, являются более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 32, 87, 97, и 194, являются более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 32, 194, 220, 254 или 255, являются особенно предпочтительными. Также предпочтительными являются их комбинации, конкретнее - наночастицы, нагруженные различными антигенными пептидами по настоящему изобретению (или соответствующими иммуногенными соединениями).
Наночастицы, в частности, предназначенные для применения в качестве вакцин, известны из области техники и описаны, например у Shao et al., Nanoparticle-based immunotherapy for cancer, ACS Nano 2015, 9(1):16-30; Zhao et al., Nanoparticle vaccines, Vaccine 2014, 32(3):327-37; and Gregory et al., Vaccine delivery using nanoparticles, Front Cell Infect Microbiol. 2013, 3:13, doi: 10.3389/fcimb.2013.00013. eCollection 2013, Review. В частности наночастица применяется для доставки антигенного пептида (или иммуногенного соединения/полипептида/белка/нуклеиновой кислоты, включающей антигенный пептид) и может, необязательно, выполнять роль адъюванта. Антигенный пептид (иммуногенное соединение/полипептид/белок/нуклеиновая кислота, включающая антигенный пептид) обычно либо инкапсулирован в наночастицу, либо связан,/присоединен (decorated onto) к поверхности наночастицы ("покрытие"). По сравнению с традиционными подходами, наночастицы могут защищать загруженное вещество (антиген/адъювант) от биологического окружения, увеличивают продолжительность жизни, минимизируют системное токсическое действие, усиливают доставку к АПК или даже напрямую запускают активацию ТАА-специфических Т-клеток. Предпочтительно наночастицы имеют размер (диаметр) не более 300 нм, более предпочтительно не менее 200 нм и более предпочтительно не более 200 нм, и еще более предпочтительно не более 100 нм. Такие наночастицы адекватным образом защищены от поглощения фагоцитами, обладают хорошей структурной целостностью в кровотоке и длительным временем циркуляции, способны накапливаться в местах роста опухоли и способны проникать глубоко в опухолевую ткань.
Примерами наночастиц являются полимерные наночастицы, такие как поли(этиленгликоль) (PEG) и поли(D,L-лактид-ко-гликолевая кислота)(PLGA); неорганические наночастицы, такие как золотые наночастицы, железооксидные бусины, железоксидные и цинкоксидные наночастицы, карбоновые нанотрубки и мезопористые кремневые наночастицы; липосомы; такие как катионные липосомы; иммуностимулирующие комплексы (ISCOM); вирусподобные частицы (VLP); и самоорганизующиеся белки.
Полимерные наночастицы представляют собой наночастицы на основе полимеров/или содержащие их, такие как поли(D,L-лактид-ко-гликолид) (PLG), поли(D,L-лактид-ко-гликолевая кислота)(PLGA), поли(γ-глутаминовая кислота) (γ-PGA), поли(этиленгликоль) (PEG), и полистирол. Полимерные наночастицы могут захватывать антиген (например, антигенный пептид или (поли)пептид, включающий его) или связываться с антигеном или конъюгировать с ним (например, антигенный пептид или (поли)пептид, включающий его).
Полимерные наночастицы могут применяться для доставки, например, в определенные клетки или для замедленного высвобождения антигена благодаря медленной скорости их биодеградации. Например, g-PGA наночастицы могут применяться для инкапсулирования гидрофобных антигенов. Полистироловые наночастицы могут образовывать конъюгаты с разнообразными антигенами, поскольку могут быть поверхностно-модифицированными при помощи различных функциональных групп. Полимеры, такие как поли(L-молочная кислота)(PLA), PLGA, PEG и природные полимеры, такие как полисахариды также могут применяться для синтеза гидрогелевых наночастиц, которые представляют собой тип гидрофильных трехмерных полимерных наночастиц. Наногели имеют благоприятные свойства, включая гибкий размер ячеек, большую поверхность для многовалентной конъюгации, высокое содержание воды и также высокая нагрузочная способность для антигенов. Соответственно, предпочтительной наночастицей является наногель, такой как хитозановый наногель. Предпочтительными полимерными наночастицами являются наночастицы на основе PEG и PLGA или содержащие их.
Неорганические наночастицы представляют собой наночастицы на основе неорганических соединений или включающие их; примерами таких наночастиц являются золотые наночастицы, железооксидные наночастицы, железооксидные циноксидные наночастицы, карбоновые наноастицы (например, углеродные нанотрубки) и мезопористые кремниевые наночастицы. Неорганические наночастицы обеспечивают ригидную структуру и контролируемый синтез. Например, золотые наночастицы могут быть синтезированы различных форм, таких как сферы, палочки, кубы. Неорганические наночастицы могут быть поверхностно-модифицированными, например, с помощью углеводородов. Карбоновые наночастицы обеспечивают хорошую биосовместимость и могут быть получены, например, в виде нанотрубок или (микроспорических) сфер. Например, множественные копии антигенного пептида по настоящему изобретению (или (поли(пептид), включающий его) могут быть конъюгированы с карбоновыми наночастицами, например, углеродными нанотрубками. Мезопористые карбоновые наночастицы являются предпочтительными для перорального введения. Наночастицы на основе кремния (SiNPs) также являются предпочтительными. SiNPs являются биосовместимыми и показывают прекрасные свойства в отношении селективного опухолевого таргетинга и доставки вакцин. Большое количество силанольных групп на поверхности SiNPs может быть добавлено для дополнительной модификации и придания частице дополнительной функциональности, такой как способность распознавать клетки, абсорбция специфических биомолекул, улучшение взаимодействия с клетками, а также усиление клеточного захвата. Микроспорические наночастицы являются наиболее предпочтительными.
Липосомы обычно образованы фосфолипидами, такими как 1,2-диолеоил-3-триметиламмоний пропан (DOTAP). В целом катионные липосомы являются предпочтительными. Липосомы самостоятельно собираются из фосфолипидной двухслойной оболочки и водного ядра. Липосомы могут быть получены в форме униламеллярных везикул (имеющих один фосфолипидный бислой) или в форме мультиламеллярных везикул (имеющих несколько концентрических фосфолипидных слоев, разделенных слоями воды). Соответственно, антигены могут быть инкапсулированы в ядро или заключены между различными слоями/оболочками. Предпочтительные липосомные системы, одобренные для применения у человека, включают системы Inflexal® V и Epaxal®.
Иммуностимулирующие комплексы (ISCOM) представляют собой частицы, напоминающие корзину, приблизительно 40 нм (в диаметре), представляющие собой коллоидные содержащие сапонин мицеллы, например, сформированные из сапонинового адъюванта Quil-A, холестерина, фосфолипидов и (поли)пептидного антигена (такого как антигенный пептид или полипептид, включающий его). Такие сферические частицы могут захватывать антигены за счет полярных взаимодействий. Описано два типа ISCOMs, оба из которых включают холестерин, фосфолипид (обычно или фосфатидилэтаноламин, или фосфатидилхолин) и сапонин (такой как Quil-A).
Вирусоподобные частицы (VLP аббрев. от англ. Virus-like particles) представляют собой самособираемые наночастицы, формирующиеся в процессе самосборки биосовместимых капсидных белков. Благодаря тому оптимизированному естественным образом размеру частиц и повторяющемуся структурному порядку, вирусоподобные частицы могут вызывать сильный иммунный ответ.Вирусоподобные частицы могут быть получены на основе различных вирусов, размер которых варьирует от 20 нм до 800 нм и обычно находится в пределах 20-150 нм. Вирусоподобные частицы могут быть сконструированы для экспрессии дополнительных пептидов или белков либо путем слияния этих пептидов / белков с частицей, либо путем экспрессии нескольких антигенов. Более этому, антигены могут быть химически связаны с вирусной поверхностью с образованием биоконъюгата VLPs.
Примерами самособираемых белков являются ферритин и основной белок хранилища (MVP абррев. От англ. Main Vault Protein). Ферритин представляет собой белок, который может самостоятельно собираться в напоминающую сферу структуру размером 10 нм. Девяносто шесть единиц MVP могут самостоятельно собираться в бочкообразную сводчатую наночастицу размером приблизительно 40 нм в ширину и 70 нм в длину. Антигены, генетически слитые с доменом минимального взаимодействия, могут быть упакованы в сводчатые наночастицы посредством процесса самосборки при смешивании с MVP. Соответственно, антиген (такой как антигенный пептид по-настоящему изобретению или полипептид, содержащий его) может быть слит с самособирающимся белком или его фрагментом/доменом, таким как домен минимального взаимодействия MVP. Соответственно, настоящее изобретение относится к слитому белку, включающему самособирающийся белок (или его фрагмент/домен) и антигенный пептид по настоящему изобретению.
В целом предпочтительными примерами наночастиц (НЧ) являются железооксидные частицы, полистироловые микросферы, наночастицы на основе поли (γ-глутаминовой кислоты) (γ-PGA), железоксидные-цинкоксидные наночастицы, катионизированные желатиновые наночастицы, стабилизированные плюроником наночастицы на основе поли(пропиленсульфида) (PPS), PLGA NPs, (катионные) липосомы, (рН-зависимые) полимерные мицеллы, PLGA, PLGA с покрытием из мембраны раковых клеток, липидно-кальциево-фосфатные наночастицы (LCP), липосомальные наночастицы на основе протамина и гиалуроновой кислоты (LPN), полистироловые латексные бусины, магнитные бусины, железо-декстрановые частицы и нанокристаллы -квантовые точки.
Предпочтительно наночастицы дополнительно включают адъювант, например, агонист толл-подобного рецептора (TLR). Таким образом, антигенный пептид (или иммуногенное соединение/полипептид/белок/нуклеиновая кислота, включающие антигенный пептид) могут доставляться к антигенпрезентирующим клеткам (АПК), таким как дендритные клетки (ДК) вместе с адъювантом. Адъювант может быть инкапсулирован в наночастицу или связан/конъюгирован с ее поверхностью, предпочтительно, аналогичным образом, что и антигенный пептид.
Наиболее предпочтительными адъювантами являются полинозиновая:полицитидиловая кислота (также обозначаемая, как "поли I:С") и/или ее производное поли-ICLC. Поли I:С представляет собой несопряженную двуцепочечную РНК, в которой одна цепь представляет собой полимер инозиновой кислоты, а другая - полимер цитидиловой кислоты. Поли I:С представляет собой иммуностимулирующий агент, который, как известно, взаимодействует с толл-подобным рецептором (TLR3). Поли I:С структурно схожа с двуцепочечной РНК, которая является "естественным" стимулятором TLR3. Соответственно, поли I:С может считаться синтетическим аналогом двуцепочечной РНК. Поли-ICLC представляет собой синтетический комплекс карбоксиметилцеллюлозы, полиинозиновой-полицитидиловой кислоты и поли-L-лизин двуцепочечная РНК. Аналогично поли I:С, поли: ICLC представляет собой лиганд для TLR3. Поли I:С и поли-ICLC обычно стимулируют высвобождение цитотоксических цитокинов. Предпочтительным примером поли-ICLC является Hiltonol®.
Фармацевтические композиции
Согласно дополнительному аспекту настоящее изобретение также относится к фармацевтической композиции, включающей по меньшей мере одно из следующих:
- антигенный пептид по настоящему изобретению, как раскрыто в настоящем описании,
- иммуногенное соединение по настоящему изобретению, как раскрыто в настоящем описании,
- наночастицы по настоящему изобретению, как раскрыто в настоящем описании,
- клетки по настоящему изобретению, как раскрыто в настоящем описании,
- нуклеиновая кислота по настоящему изобретению, как раскрыто в настоящем описании, и/или
- клетка-хозяин по настоящему изобретению, как раскрыто в настоящем описании,
и необязательно один или более фармацевтически доступный эксципиент или носитель.
В частности предпочтительные варианты воплощения антигенного пептида, как описано выше, также применимы к таким фармацевтическим композициям по настоящему изобретению. Например, антигенный пептид, в составе фармацевтической композиции или антигенный пептид, в составе иммуногенного соединения, наночастицы или клетки, или нуклеиновой кислоты, или клетки-хозяина, включенной в фармацевтическую композицию, предпочтительно, состоит из или включает в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 1 от до 580 и от 861 до 887, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID Nos от 1 до 580. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 1-160, 162-253 и 255-580, являются более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 31, 32, 87, 97, 145, 193, 194, 220, 221, 255, 521 и 524, являются еще более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 31, 32, 87, 97, 193, 194, 220, 255, 521 и 524, являются еще более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 31, 32, 87, 97, 194, 220, 255, 521 и 524, являются более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 32, 87, 97, и 194, являются более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 32, 194, 220, 254 или 255, являются особенно предпочтительными.
Кроме того, предпочтительными являются их комбинации, конкретнее -фармацевтические композиции, содержащие различные антигенные пептиды по настоящему изобретению. Например, фармацевтическая композиция может содержать
(а) по меньшей мере два различных антигенных пептида по настоящему изобретению;
(б) по меньшей мере два различных иммуногенных соединения по настоящему изобретению;
(в) по меньшей мере две различные наночастицы по настоящему изобретению; и/или
(г) по меньшей мере две различные нуклеиновые кислоты по настоящему изобретению.
Соответственно, настоящее изобретение относится к фармацевтической композиции, включающей (по меньшей мере) один антигенный пептид по настоящему изобретению, как раскрыто в настоящем документе. Кроме того, настоящее изобретение также относится к фармацевтической композиции, содержащей (по меньшей мере) одно иммуногенное соединение по настоящему изобретению, как раскрыто в настоящем описании. Кроме того, настоящее изобретение также относится к фармацевтической композиции, содержащей (по меньшей мере) одну наночастицу по настоящему изобретению, как раскрыто в настоящем описании. Кроме того, настоящее изобретение также относится к фармацевтической композиции, содержащей (по меньшей мере) одну клетку по настоящему изобретению, как раскрыто в настоящем описании. Кроме того, настоящее изобретение также относится к фармацевтической композиции, содержащей (по меньшей мере) одну нуклеиновую кислоту по настоящему изобретению, как раскрыто в настоящем описании. Кроме того, настоящее изобретение также относится к фармацевтической композиции, содержащей (по меньшей мере) одну клетку-хозяин по настоящему изобретению, как описано в настоящем документе.
Предпочтительно, фармацевтическая композиция содержит по меньшей мере два различных антигенных пептида по настоящему изобретению.
В частности, настоящее изобретение относится к фармацевтической композиции, содержащей первый антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека BIRC5; а также второй антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека FOXM1. Предпочтительно первый антигенный пептид состоит из или включает в себя микробиотический вариант последовательности фрагмента BIRC5 (референсный пептид человека) "LTLGEFLKL" (SEQ ID NO: 593), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 30, 31 или 32, а второй антигенный пептид состоит из или включает в себя микробиотический вариант последовательности фрагмента FOXM1 (референсный пептид человека) "LMDLSTTPL" (SEQ ID NO: 674), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 220 или 868. Еще более предпочтительно, фармацевтическая композиция содержит антигенный пептид, состоящий из или включающий в себя SEQ ID NO: 32, и антигенный пептид, состоящий из или включающий в себя SEQ ID NO: 220.
В частности, настоящее изобретение также относится к фармацевтической композиции, содержащей первый антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека BIRC5, а второй антигенный пептид по настоящему изобретению, который состоит из или включает вариант последовательности фрагмента опухолевого антигена человека IL13RA2. Предпочтительно, первый антигенный пептид по настоящему изобретению, состоит из или включает в себя микробиотический вариант последовательности фрагмента BIRC5 (референсный пептид человека) "LTLGEFLKL" (SEQ ID NO: 593), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 30, 31 или 32, а второй антигенный пептид состоит из или включает в себя микробиотический вариант последовательности фрагмента IL13RA2 (референсный пептид человека) "WLPFGFILI" (SEQ ID NO: 691) или "WLPFGFILIL" (SEQ ID NO: 692), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 254, 255, 878 или 879. Еще более предпочтительно, фармацевтическая композиция содержит антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 32, а также антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 225.
В частности, настоящее изобретение также относится к фармацевтической композиции, содержащей первый антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека FOXM1, а также второй антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека IL13RA2. Предпочтительно, первый антигенный пептид по настоящему изобретению, состоит из или включает в себя микробиотический вариант последовательности фрагмента FOXM1 (референсный пептид человека) "LMDLSTTPL" (SEQ ID NO: 674), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 220 или 868, а второй антигенный пептид состоит из или включает в себя микробиотический вариант последовательности фрагмента IL13RA2 (референсный пептид человека) "WLPFGFILI" (SEQ ID NO: 691) или "WLPFGFILIL" (SEQ ID NO: 692), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 254, 255, 878 или 879. Еще более предпочтительно, фармацевтическая композиция содержит антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 32, а также антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 255.
Предпочтительно, фармацевтическая композиция включает по меньшей мере три различных антигенных пептида по настоящему изобретению.
В частности, настоящее изобретение также относится к фармацевтической композиции, содержащей первый антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека BIRC5, а также второй антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека FOXM1, и третий антигенный пептид по- настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека IL13RA2. Предпочтительно, первый антигенный пептид по настоящему изобретению, состоит из или включает в себя микробиотический вариант последовательности фрагмента BIRC5 (референсный пептид человека) "LTLGEFLKL" (SEQ ID NO: 593), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 30, 31 или 32; второй антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека FOXM1 (референсный пептид человека) "LMDLSTTPL" (SEQ ID NO: 674), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой SEQ ID NO: 220 или 868; а также третий антигенный пептид, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека IL13RA2 (референсный пептид человека) "WLPFGFILI" (SEQ ID NO: 691) или "WLPFGFILIL" (SEQ ID NO: 692), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой SEQ ID NO: 254, 255, 878 или 879. Еще более предпочтительно, фармацевтическая композиция содержит антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 30, также антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 220, а также антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 255.
Должно быть понятно, что фармацевтическая композиция также может содержать - вместо указанных выше предпочтительных комбинаций антигенных пептидов - соответствующую комбинацию иммуногенных соединений по настоящему изобретению, соответствующую комбинацию наночастиц по настоящему изобретению или соответствующую комбинацию нуклеиновых кислот по изобретению.
Предпочтительно, фармацевтическая композиция дополнительно содержит один или более фармацевтически доступный эксципиент или наполнитель.
Фармацевтическая композиция по изобретению может находиться в любой форме, подходящей для осуществления целей настоящего изобретения. Например, указанная композиция может находиться в форме, подходящей для парентерального, энтерального или местного введения, такой как жидкая суспензия, твердая лекарственная форма (гранулы, пилюли, капсулы или таблетки), или же паста или гель. Выбор подходящей формы композиции в зависимости от предполагаемой области применения находится в компетенции специалиста в данной области.
Композиция, заявленная в соответствии с настоящим изобретением, может дополнительно содержать другие активные агенты, например, такие, которые могут усиливать эффекты антигенного пептида или иммуногенного соединения. Альтернативно, композиция может не содержать других активных ингредиентов (то есть, отличных от антигенного пептида по настоящему изобретению, иммуногенного соединения по настоящему изобретению, наночастицы по настоящему изобретению, клетки по настоящему изобретению, и/или клетки-хозяина по настоящему изобретению).
Фармацевтическая композиция, как определено в настоящем описании, предпочтительно представляет собой иммуногенную композицию, то есть композицию, которая способна индуцировать, усиливать, пролонгировать и поддерживать иммунный ответ. Это может достигаться за счет антигенного пептида по настоящему изобретению или за счет иммуногенного соединения по настоящему изобретению, находящихся в составе указанной композиции. Предпочтительно, фармацевтическая композиция дополнительно содержит одно или более иммуностимулирущее соединение. Фармацевтическая композиция, конкретно, иммуногенная композиция, могут в тексте настоящего описания обозначаться термином "вакцинная композиция".
Предпочтительно, фармацевтическая композиция также содержит по меньшей мере один иммуностимулирующий агент, конкретнее - способный усиливать, потенциировать, пролонгировать и поддерживать иммунный ответ, опосредованный антигенным пептидом. К предпочтительным иммуностимулирующим агентам по настоящему изобретению относятся, без ограничений указанными, иммуностимулирующие агенты, антигенпрезентирующие клетки, а также их комбинации. Предпочтительно, иммуностимулирующий агент представляет собой иммунный адъювант или антигенпрезентирующую клетку (АПК).
Предпочтительно, иммуностимулирующий агент представляет собой иммунный адъювант. Некоторые иммунные адъюванты обладают способностью помогать и пролонгировать взаимодействие между антигеном и иммунной системой, в то время как другие способны к рекрутингу или активации клеток естественного иммунитета и таким образом индуцируют адаптивный иммунный ответ. Адъюванты, принадлежащие к первой категории, включают, без ограничений указанными, минеральные соединения, такие как алюминий, гидроксид алюминия, фосфат алюминия, кальций фосфат гидроксид; и масляные эмульсии, такие как парафиновое масло, растительное масло, полный/неполный адъювант Фрейнда (FCA/FIA), сапонины (например, из таких растений, как Quillaja, соя, Polygala senega). Адъюванты, принадлежащие к последней категории, включают, без ограничений указанными, иммуностимулирующие комплексы (ISCOMs), такие как цитокины (например, GM-CSF; интерлейкины, такие как IL-1, IL-2, IL6, IL8, или IL12; фактор некроза опухолей (TNFs), такой как TNFα или TNFβ; интерфероны IFNS, такие как IFNα, IFNβ, IFNγ или IFNδ, etc); лиганды толл-подобных рецепторов (TLRs), такие как имиквимод, резикмивод или MPL; экзосомы, такие как экзосомы, выделенные из дендритных клеток (ДК) или из опухолевых клеток; бактериальные продукты, такие как белки теплового шока (БТШ), такие как gp96, hsp90, hsp70, кальретикулин, hsp110, hsp170), патоген-ассоциированные молекулярные паттерны (PAMPs), димиколат трегалозы, (TDM), мурамилдипептид (MDP), полисахариды (PLS), такие как полисахарид-К.
Более предпочтительно, иммунный адъювант представляет собой белок/пептид, обладающий иммуностимулирующими свойствами, такими как обеспечение стимуляции CD4+ Th1 клеток, как раскрыто в настоящем документе. Предпочтительным примером таких соединений являются неопухолевый антиген, который вызывает иммунную память или оказывает неспецифическую помощь, или представляет собой специфический хелперный белок опухолевого происхождения, такой как столбнячный хелперный белок, гемоцианин лимфы улитки и PADRE пептид, как раскрыто в настоящем описании. Другим предпочтительным примером является специфический хелперный пептид опухолевого происхождения, который может презентироваться МНС II, в частности HLA-DR, HLA-DP или HLA-DQ, такой как фрагменты последовательностей родственных гиперэкспрессируемых опухолевых антигенов, таких как HER2, NY-ESO-1, hTERT или IL13RA2, как раскрыто в настоящем описании выше. В частности, иммунный адъювант может представлять собой HHD-DR3 пептид с последовательностью MAKTIAYDEEARRGLERGLN (SEQ ID NO: 856). Этот пептид является другим примером хелперного пептида (обладающего иммуностимулирующими свойствами), который является предпочтительным в контексте настоящего изобретения. Другим предпочтительным примером является h-pAg T13L (последовательность: TPPAYRPPNAPIL; SEQ ID NO: 860; Bhasin М, Singh Н, Raghava GP (2003) MHCBN: всеобъемлющая база данных пептидов, которые связываются или не связываются с МНС. Bioinformatics 19: 665-666). Другими примерами предпочтительных адъювантов, в частности хелперных пептидов, является UCP2 пептид (например, как раскрыто в WO 2013/135553 А1 или у Dosset и соавт.,. Clin Cancer Res. 2012 Nov 15; 18(22):6284-95) и BIRC5 пептид (например, как раскрыто в ЕР 2119726 А1 или у Widenmeyer и соавт., Int J Cancer. 2012 Jul 1; 131(1):140-9). Наиболее предпочтительным хелперным пептидом является UCP2 (аминокислотная последовательность: KSVWSKLQSIGIRQH; SEQ ID NO: 859).
Предпочтительно, фармацевтическая композиция содержит по меньшей мере два различных антигенных пептида по настоящему изобретению и хелперный пептид, предпочтительно, UCP2 пептид (SEQ ID NO: 859).
Предпочтительно, фармацевтическая композиция содержит первый антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека BIRC5, второй антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека FOXM1 и хелперный пептид, предпочтительно UCP2 (SEQ ID NO: 859). Более предпочтительно, фармацевтическая композиция содержит первый антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека BIRC5 (референсный пептид человека) "LTLGEFLKL" (SEQ ID NO: 593), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 30, 31 или 32; второй антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека FOXM1 (референсный пептид человека) "LMDLSTTPL" (SEQ ID NO: 674), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 220 или 868; и хелперный пептид, предпочтительно UCP2 пептид (SEQ ID NO: 859). Еще более предпочтительно фармацевтическая композиция содержит антигенный пептид, состоящий из или включающий в себя SEQ ID NO: 32; антигенный пептид, состоящий из или включающий в себя SEQ ID NO: 220; и UCP2 хелперный пептид (SEQ ID NO: 859).
Также предпочтительно, фармацевтическая композиция содержит первый антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека BIRC5, второй антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека IL13RA2, и хелперный пептид, предпочтительно, пептид UCP2 (SEQ ID NO: 859). Более предпочтительно, фармацевтическая композиция содержит первый антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека BIRC5 (референсный пептид человека) "LTLGEFLKL" (SEQ ID NO: 593), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 30, 31 или 32; второй антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека IL13RA2 (второй антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека) "WLPFGFILI" (SEQ ID NO: 691) или "WLPFGFILIL" (SEQ ID NO: 692), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 254, 255, 878 или 879; и хелперный пептид, предпочтительно, пептид UCP2 (SEQ ID NO: 859). Еще более предпочтительно, фармацевтическая композиция содержит антигенный пептид, состоящий из или включающий в себя SEQ ID NO: 32; антигенный пептид, состоящий из или включающий в себя SEQ ID NO: 225; и UCP2 хелперный пептид (SEQ ID NO: 859).
Также предпочтительно, фармацевтическая композиция содержит первый антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека FOXM1; второй антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека IL13RA2; и хелперный пептид, предпочтительно, пептид UCP2 (SEQ ID NO: 859). Более предпочтительно, фармацевтическая композиция содержит первый антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека FOXM1 (референсный пептид человека) "LMDLSTTPL" (SEQ ID NO: 674), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 220 или 868; второй антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека IL13RA2 (референсный пептид человека) "WLPFGFILI" (SEQ ID NO: 691) или "WLPFGFILIL" (SEQ ID NO: 692), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 254, 255, 878 или 879; и хелперный пептид, предпочтительно, пептид UCP2 (SEQ ID NO: 859). Еще более предпочтительно, фармацевтическая композиция содержит антигенный пептид, состоящий из или включающий в себя SEQ ID NO: 220; антигенный пептид, состоящий из или включающий в себя SEQ ID NO: 225; и UCP2 хелперный пептид (SEQ ID NO: 859).
Более предпочтительно, фармацевтическая композиция содержит по меньшей мере три различных антигенных пептида по настоящему изобретению и хелперный пептид, предпочтительно, пептид UCP2 (SEQ ID NO: 859).
В частности, фармацевтическая композиция может содержать первый антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека BIRC5, второй антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека FOXM1, третий антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека IL13RA2 и хелперный пептид, предпочтительно, пептид UCP2 (SEQ ID NO: 859). Еще более предпочтительно, фармацевтическая композиция содержит первый антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека BIRC5 (референсный пептид человека) "LTLGEFLKL" (SEQ ID NO: 593), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 30, 31 или 32; второй антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека FOXM1 (референсный пептид человека) "LMDLSTTPL" (SEQ ID NO: 674), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 220 или 868; и третий антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека IL13RA2 (референсный пептид человека) "WLPFGFILI" (SEQ ID NO: 691) или "WLPFGFILIL" (SEQ ID NO: 692), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 254, 255, 878 или 879; и хелперный пептид, предпочтительно, пептид UCP2 (SEQ ID NO: 859). Еще более предпочтительно, фармацевтическая композиция содержит антигенный пептид, состоящий из или включающий в себя SEQ ID NO: 30; антигенный пептид, состоящий из или включающий в себя SEQ ID NO: 220; антигенный пептид, состоящий из или включающий в себя SEQ ID NO: 225 и хелперный пептид, предпочтительно, UCP2 пептид (SEQ ID NO: 859).
Наиболее предпочтительными иммунными адъювантами являются полинозиновая:полицитидиловая кислота (также обозначаемая, как "поли I:С") и/или ее производное поли-ICLC. Поли I:С представляет собой несопряженную двуцепочечную РНК, в которой одна цепь представляет собой полимер инозиновой кислоты, а другая полимер цитидиловой кислоты. Поли I:С представляет собой иммуностимулирующий агент, который, как известно, взаимодействует с толл-подобным рецептором 3 (TLR3). Поли I:С структурно схожа с двуцепочечной РНК, которая является "естественным" стимулятором TLR3. Соответственно, поли I:С может считаться синтетическим аналогом двуцепочечной РНК. Поли-ICLC представляет собой синтетический комплекс карбоксиметилцеллюлозы, полиинозиновой-полицитидиловой кислоты и поли-L-лизин двуцепочечной РНК. Аналогично поли I:С, поли: ICLC представляет собой лиганд для TLR3. Поли I:С и поли-ICLC обычно стимулируют высвобождение цитотоксических цитокинов. Предпочтительным примером поли-ICLC является Hiltonol®.
Более предпочтительно, адъювант представляет собой Монтанид, такой как Монтанид ISA VG и/или Монтанид ISA 720 VG. Такие адъюванты образуют стандартные эмульсии вода-в-масле при смешивании с антигенной средой на водной основе. Монтанид ISA 51 VG основан на смеси сурфактанта моноолеата маннида и минерального масла, тогда как в Монтаниде ISA 720 VG используется неминеральное масло (Aucouturier J, Dupuis L, Deville S, Ascarateil S, Ganne V. Montanide ISA 720 and 51: a new generation of water in oil emulsions as adjuvants for human vaccines. Expert Rev Vaccines. 2002 Jun; 1(1):111-8; Ascarateil S, Puget A, Koziol M-E. Safety data of Montanide ISA 51 VG and Montanide ISA 720 VG, two adjuvants dedicated to human therapeutic vaccines. Journal for Immunotherapy of Cancer. 2015; 3(Suppl 2): P428. doi:10.1186/2051-1426-3-S2-P428).
Также предпочтительно, чтобы иммуностимулирующий агент представлял собой антигенпрезентирующую клетку (АПК). АПК вызывают особый интерес поскольку их основной функцией является процессинг антигенов и презентация их на клеточной поверхности Т-клеток иммунной системы, чтобы инициировать и модулировать Т-клеточные ответы in vivo. В композиции, заявленной в соответствии с настоящим изобретением, предпочтительно, чтобы АПК были нагружены антигенным пептидом(ами) и/или иммуногенным соединением(ми) по настоящему изобретению, что может осуществляться путем взаимодействия АПК in vitro с указанным антигенным пептидом(ами) и/или иммуногенным соединением(ми) (Rizzo et al., Methods Mol Biol. 2014; 1139:41-4; Rolinski and Hus, J Immunotoxicol. 2014 Oct; 11(4):311-8).
Предпочтительно, АПК представляет собой дендритную клетку (ДК). ДК являются наиболее эффективными АПК и, как сообщается, часто являются функционально неполноценными у пациентов с раком. ДК могут быть легко выделены специалистом в данной области, как из организма здоровых совместимых доноров (то есть ДК являются HLA-ассоциированными), так и из организма самого пациента с условием, что они являются функциональными (то есть ДК являются аутологичными), например, либо путем простого выделения из периферической крови, либо путем выведения из клеток периферической крови, таких как CD14+ моноциты или CD34+ кроветворные клетки-предшественники (Emens et al., 2008). ДК действительно можно отличить от других клеток периферической крови по их поверхностным маркерам, таким как S100, р55, CD83 и/или ОХ62, и, таким образом, их можно выделить и очистить с помощью указанных маркеров с использованием методов культур клеток, хорошо известных в данной области.
Согласно предпочтительному варианту осуществления изобретения, фармацевтическая композиция может дополнительно содержать по меньшей мере противораковый лекарственный агент. Указанный лекарственный агент, таким образом, предпочтительно, способен предотвращать и/или лечить тот же тип рака, что и антигенный пептид по настоящему изобретению. Предпочтительно, противораковый лекарственный агент выбран из группы, включающей антитела, лизаты опухолевых клеток, химиотерапевтические агенты, радиотерапевтический агент, модуляторы контрольных иммунных точек и их комбинации.
Антитела являются особенно предпочтительными для лечения рака, поскольку они могут, как связываться со специфическими антигенами на поверхности раковых клеток, тем самым "направляя" терапию непосредственно в опухоль (такие антитела обозначаются, как противоопухолевые таргетные антитела), так и блокировать иммунные контрольные точки, регуляция которых нарушена при раке (такие антитела обозначаются, как иммуномодулирующие антитела). Целью последнего типа антител является подавление иммунной резистентности к раковым клеткам, которая может наблюдаться против Т клеток, которые являются специфическими по отношению к опухолевым антигенам. Действительно, из области техники хорошо известно, что в естественных физиологических условиях иммунные контрольные точки играют ключевую роль в поддержании аутотолерантности (то есть предотвращают аутоиммунные реакции) и защите тканей от повреждений в тех случаях, когда иммунная система борется с патогенной инфекцией. Однако, при раковых заболеваниях, регуляция экспрессии иммунных контрольных точек может нарушаться, что является важным механизмом в развитии иммунной резистентности. Такая резистентность наблюдается при меланоме, раке яичников, легких, глиобластоме, раке молочной железы и раке поджелудочной железы и связана с контрольной точкой PD-L1 (Konishi et al., В7-Н1 expression on non-small cell lung cancer cells and its relationship with tumor-infiltrating lymphocytes and their PD-1 expression. Clin Cancer Res. 2004 Aug 1; 10(15):5094-100; Ghebeh et al., The B7-H1 (PD-L1) T lymphocyte-inhibitory molecule is expressed in breast cancer patients with infiltrating ductal carcinoma: correlation with important high-risk prognostic factors. Neoplasia. 2006 Mar; 8(3): 190-8; Hino et al., Tumor cell expression of programmed cell death-1 ligand 1 is a prognostic factor for malignant melanoma. Cancer. 2010 Apr 1; 116(7): 1757-66). Другими примерами иммунных контрольных точек являются, без ограничений указанными, PD-L2, PD-1, CD80, CD86, CTLA-4, В7Н3, В7Н4, PVR, TIGIT, GAL9, LAG-3, GITR, CD137, TIM3, VISTA, VISTA-R (Pico de  et al., Checkpoint blockade for cancer therapy: revitalizing a suppressed immune system. Trends Mol Med. 2015 Aug; 21(8):482-91; Pardoll DM. The blockade of immune checkpoints in cancer immunotherapy. Nat Rev Cancer. 2012 Mar 22; 12(4):252-64).
et al., Checkpoint blockade for cancer therapy: revitalizing a suppressed immune system. Trends Mol Med. 2015 Aug; 21(8):482-91; Pardoll DM. The blockade of immune checkpoints in cancer immunotherapy. Nat Rev Cancer. 2012 Mar 22; 12(4):252-64).
Для описанных выше целей антитела применяются, как в форме выделенных моноклональных антител (то есть, неконъюгированных), так и в форме антител, конъюгированных с другими молекулами, которые могут являться радиоактивными или токсичными.
Примерами хорошо известных моноклональных противоопухолевых таргетных антител, которые применяются в иммунотерапии рака, являются, без ограничений указанными, алемтузумаб (хронический лимфоцитарный лейкоз), бевацизумаб (колоректальный рак, мультиформная глиобластома, рак шейки матки, рак легких, рак почек), брентуксимаб / ведотин (лимфомы), блинатумумаб (острый лимфобластный лейкоз), катумаксомаб (злокачественный асцит при ЕРСАМ+ опухолях), цетуксимаб (рак головы и шеи, колоректальный рак), деносумаб (рак молочной железы, простаты и костей), Гемтузумаб / озогамицин (острый миелолейкоз), ибритумомаб / тиуксетан (неходжкинская лимфома), панитумумаб (колоректальный рак), пертузумаб (рак молочной железы) обинутузумаб (хронический лимфоцитарный лейкоз), офатумумаб (хронический лимфоцитарный лейкоз), опилимумаб (меланома), рамуцирумаб (рак желудка и гастроэзофагеальный рак), ритуксимаб (хронический лимфоцитарный лейкоз и неходжкинская лимфома), силтуксимаб (многоочаговая болезнь Кастлемана), тозитумомаб (неходжкинская лимфома) и трастузумаб (рак молочной железы, желудка и пищевода); в то время как примеры иммуномодулирующих антител включают, без ограничений указанными, ипилимумаб (меланома), который блокирует CTLA4-зависимую иммунную контрольную точку, ниволумаб (меланома, рак легкого) и прембролизубмаб (меланома), которые оба блокируют PDCD1-зависимую иммунную контрольную точку, а также MPDL3280A, MEDI4736, MEDI0680 и MSB0010718C, которые все блокируют PD-L1-зависимую иммунную контрольную точку (Sharma and Allison, The future of immune checkpoint therapy. Science. 2015 Apr 3; 348(6230):56-61).
Другие антитела для иммунотерапии рака был описаны  и соавт., Trial Watch: Immunomodulatory monoclonal antibodies for oncological indications. Oncoimmunology. 2015 Mar 2; 4(4):e1008814. eCollection 2015 Apr; Redman и соавт., Mechanisms of action of therapeutic antibodies for cancer. Mol Immunol. 2015 Oct; 67(2 Pt A):28-45; Simpson and Caballero, Monoclonal antibodies for the therapy of cancer MC Proc. 2014; 8 (Suppl 4), а также на веб-сайте, где представлена вся совокупность антител (список терапевтических моноклональных антител, одобренных или находящихся на рассмотрении в Европейском Союзе или США, доступен по веб-ссылке http://www.antibodysociety.org/news/approved_mabs.php).
и соавт., Trial Watch: Immunomodulatory monoclonal antibodies for oncological indications. Oncoimmunology. 2015 Mar 2; 4(4):e1008814. eCollection 2015 Apr; Redman и соавт., Mechanisms of action of therapeutic antibodies for cancer. Mol Immunol. 2015 Oct; 67(2 Pt A):28-45; Simpson and Caballero, Monoclonal antibodies for the therapy of cancer MC Proc. 2014; 8 (Suppl 4), а также на веб-сайте, где представлена вся совокупность антител (список терапевтических моноклональных антител, одобренных или находящихся на рассмотрении в Европейском Союзе или США, доступен по веб-ссылке http://www.antibodysociety.org/news/approved_mabs.php).
Лизаты опухолевых клеток также могут комбинироваться с антигенным пептидом(ами) по настоящему изобретению. Опухолевые клетки действительно способны инициировать иммунный ответ за счет презентации эндогенных МНС-пептидных комплексов, а также посредством дендритных клеток (ДК) хозяина, которые могут процессировать и презентировать антиген, доставляемый такими лизатами. Таким образом, увеличивается спектр антигенов, против которых может быть индуцирован иммунный ответ.Лизаты опухолевых клеток могут быть легко получены при обработке опухолевых клеток тепловым шоком/или с помощью химической обработки, кроме того, они могут быть аутологичными (то есть выделенными из организма пациента) или аллогенными (то есть выделенными из организма другого субъекта).
Стандартные химиотерапевтические препараты и радиотерапевтические агенты не нуждаются в дополнительном описании здесь, поскольку они подробно описаны в литературе, а именно у Baskar и соавт. (Baskar et al., Cancer and radiation therapy: current advances and future directions. Int J Med Sci. 2012; 9(3):193-9), Paci et al., (Paci et al., Review of therapeutic drug monitoring of anticancer drugs part 1--cytotoxics. Eur J Cancer. 2014 Aug; 50(12):2010-9) и Widmer и соавт. (Widmer et al., Review of therapeutic drug monitoring of anticancer drugs part two-targeted therapies. Eur J Cancer. 2014 Aug; 50(12):2020-36). Список таких лекарств и агентов также доступен на сайте cancer.gov (http://www.cancer.gov/about-cancer/treatment/drugs).
Предпочтительно, модулятор иммунных контрольных точек, который может применяться в комбинации с антигенным пептидом, как раскрыто в настоящем описании, представляет собой активатор или ингибитор одной или более иммунной молекулы контрольной точки, выбранной из группы, включающей CD27, CD28, CD40, CD122, CD137, ОХ40, GITR, ICOS, A2AR, В7-Н3, В7-Н4, BTLA, CD40, CTLA-4, IDO, KIR, LAG3, PD-1, TIM-3, VISTA, СЕАСАМ1, GARP, PS, CSF1R, CD94/NKG2A, TDO, GITR, TNFR и/или FasR/DcR3; или активатор или ингибитор одного и более их лигандов.
Более предпочтительно, модулятор иммунной контрольной точки представляет собой активатор (ко)стимулирующей контрольной молекулы или ингибитор тормозящей молекулы контрольной точки, или их комбинацию. Соответственно, модулятор иммунной контрольной точки более предпочтительно представляет собой (а) активатор CD27, CD28, CD40, CD122, CD137, ОХ40, GITR и/или ICOS или (б) ингибитор A2AR, В7-Н3, В7-Н4, BTLA, CD40, CTLA-4, IDO, KIR, LAG3, PD-1, PDL-1, PD-L2, TIM-3, VISTA, СЕАСАМ1, GARP, PS, CSF1R, CD94/NKG2A, TDO, TNFR и/или FasR/DcR3.
Еще более предпочтительно, модулятор иммунной контрольной точки представляет собой ингибитор тормозящей молекулы контрольной точки (но, предпочтительно, не является ингибитором стимулирующей молекулы контрольной точки). Соответственно, модулятор иммунной контрольной точки более предпочтительно представляет собой ингибитор A2AR, В7-Н3, В7-Н4, BTLA, CTLA-4, IDO, KIR, LAG3, PD-1, PDL-1, PD-L2, TIM-3, VISTA, CEACAM1, GARP, PS, CSF1R, CD94/NKG2A, TDO, TNFR и/или DcR3 или одного и более их лигандов.
Также предпочтительно, модулятор иммунной контрольной точки представляет собой активатор стимулирующей или костимулирующей молекулы контрольной точки (но, предпочтительно, не является активатором тормозящей молекулы контрольной точки). Соответственно, модулятор иммунной контрольной точки более предпочтительно представляет собой активатор CD27, CD28, CD40, CD122, CD137, ОХ40, GITR и/или ICOS или одного и более ее лиганда.
Еще более предпочтительно, модулятор иммунной контрольной точки представляет собой модулятор CD40 каскада, или IDO каскада, или LAG3 каскада, или CTLA-4 каскада и/или PD-1 каскада. Конкретнее, модулятор иммунной контрольной точки представляет собой модулятор CD40, LAG3, CTLA-4, PD-L1, PD-L2, PD-1 и/или IDO, более предпочтительно, модулятор иммунной контрольной точки представляет собой ингибитор CTLA-4, PD-L1, PD-L2, PD-1, LAG3, и/или IDO или активатор CD40, еще более предпочтительно, модулятор иммунной контрольной точки представляет собой ингибитор LAG3, CTLA-4 и/или PD-1, и еще более предпочтительно, модулятор иммунной контрольной точки представляет собой ингибитор CTLA-4 и/или PD-1.
Таким образом, модулятор контрольной точки, для комбинации с антигенным пептидом может быть выбран из известных модуляторов CTLA-4 каскада или PD-1 каскада. Предпочтительно, модулятор контрольной точки для комбинации с антигенным пептидом, как раскрыто в настоящем описании, может быть выбран из известных модуляторов CTLA-4 каскада или PD-1 каскада. Особенно предпочтительно, модулятор иммунной контрольной точки представляет собой ингибитор PD-1. Предпочтительные ингибиторы CTLA-4 каскада или PD-1 каскада включают моноклональные антитела Yervoy® (Ипилимумаб; Bristol Myers Squibb) и Тремелимумаб (Pfizer/MedImmune) а также Opdivo® (Ниволумаб; Bristol Myers Squibb), Keytruda® (Пембролизумаб, также известный, как Ламбролизумаб или МК-3475; Merck), Imfinzi® (Дурвалумаб, также известный, как MEDI4736; MedImmune/AstraZeneca), Tecentriq® (Атезолизумаб также известный, как MPDL3280A; Roche/Genentech), Пидилизумаб (СТ-011; CureTech), MEDI0680 (АМР-514; AstraZeneca), Bavencio® (Авелумаб; Merck KGaA/Pfizer, также известный, как MSB-0010718C), MIH1 (Affymetrix), LY3300054 (Eli Lilly) и Спартализумаб (также известный, как PDR001; Novartis). Более предпочтительными ингибиторами контрольных точек являются ингибиторы CTLA-4, такие как Yervoy® (Ипилимумаб; Bristol Myers Squibb) и Тремелимумаб (Pfizer/MedImmune), а также ингибиторы PD-1 Opdivo® (Ниволумаб; Bristol Myers Squibb), Keytruda® (Пембролизумаб; Merck), Пидилизумаб (CT-011; CureTech), MEDI0680 (АМР-514; AstraZeneca), АМР-224 (PD-L2 Fc слитый белок; MedImmune).
Также предпочтительно, модулятор контрольной точки, для комбинации с антигенным пептидом, как раскрыто в настоящем описании выбран из группы, включающей Пембролизумаб, Ипилимумаб, Ниволумаб, Атезолизумаб, Дурвалумаб, Тремелимумаб, Авелумаб, Спартализумаб, LAG525 (анти-LAG-3 моноклональное антитело), Эпакадостат (также известный, как INCB24360; ингибитор IDO), Варлилумаб (анти-CD27 моноклональное антитело), Урелумаб (анти-CD137 моноклональное антитело), АМР-224 и СМ-24 (анти-СЕАСАМ1 моноклональное антитело).
Выбор подходящего иммунного противоракового лекарственного агента для целей настоящего изобретения находится в компетенции специалиста в данной области. Например, если целью является профилактика или лечение меланомы, предпочтительно использовать лизат клеток меланомы и/или антитело ипилимумаб вместе с подходящим антигенным пептидом. Подходящие антигенные пептиды могут быть выбраны путем (а) подбора подходящего опухолевого антигена для определенного типа рака, как известно из области техники и/или, как раскрыто в настоящем описании в Таблице 1В, и (б) подбора подходящего антигенного пептида по изобретению для выбранного опухолевого антигена, как описано ранее, например в таблице 1А.
Противораковый лекарственный агент также может вводиться в комбинации с композицией по настоящему изобретению, как одновременно, так раздельно или последовательно. Если композиция и лекарственный агент вводятся раздельно или последовательно, их можно вводить в различных лекарственных формах.
Таким образом согласно другому аспекту, изобретение относится к композиции по изобретению и по меньшей мере одному противораковому лекарственному агенту, как описано выше, как к комбинированной лекарственной форме для одновременного, раздельного или последовательного введения. Другими словами, изобретение предлагает комбинированное применение композиции по изобретению и по меньшей мере одного противоракового лекарственного агента, как описано выше, для одновременного, раздельного или последовательного введения.
Набор из частей
Согласно дополнительному аспекту, настоящее изобретение также относится к набору частей (который также обозначается в настоящем описании, как "набор"), который содержит, по меньшей мере, один их следующих элементов:
- антигенный пептид по настоящему изобретению, как раскрыто в настоящем описании,
- иммуногенное соединение по настоящему изобретению, как раскрыто в настоящем описании,
- наночастицы по настоящему изобретению, как раскрыто в настоящем описании,
- клетка по настоящему изобретению, как раскрыто в настоящем описании,
- нуклеиновая кислота по настоящему изобретению, как раскрыто в настоящем описании,
- клетка-хозяин по настоящему изобретению, как раскрыто в настоящем описании, и/или
- фармацевтическая композиция по настоящему изобретению, как раскрыто в настоящем описании.
В частности, предпочтительные варианты воплощения антигенного пептида, как описано выше, также применимы к такому набору по настоящему изобретению. Например, антигенный пептид, включенный в набор, или антигенный пептид в составе иммуногенного соединения, наночастицы, или клетки, или нуклеиновой кислоты, или клетки-хозяина или фармацевтической композиции, включенной в набор предпочтительно состоит из или включает в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 1 от до 580 и от 861 до 887, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID Nos от 1 до 580. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 1-160, 162-253 и 255-580, являются более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 31, 32, 87, 97, 145, 193, 194, 220, 221, 255, 521 и 524, являются еще более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 31, 32, 87, 97, 193, 194, 220, 255, 521 и 524, являются еще более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 31, 32, 87, 97, 194, 220, 255, 521 и 524, являются более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 32, 87, 97, и 194, являются более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 32, 194, 220, 254 или 255, являются особенно предпочтительными.
Также предпочтительными являются их комбинации, а именно, набор, содержащий различные антигенные пептиды по настоящему изобретению. В частности, набор частей по настоящему изобретению может содержать более чем один описанный выше компонент, например, 2, 3, 4, 5, 6, 7, 8, 9, или 10 различных компонентов. Например, набор частей по настоящему изобретению может содержать по меньшей мере два (например, 2, 3, 4, 5, 6, 7, 8, 9, или 10) различных иммуногенных соединения, по меньшей мере два (например, 2, 3, 4, 5, 6, 7, 8, 9, или 10) антигенных пептида, по меньшей мере две (например, 2, 3, 4, 5, 6, 7, 8, 9, или 10) различные наночастицы, по меньшей мере две (например, 2, 3, 4, 5, 6, 7, 8, 9, или 10) различные клетки, по меньшей мере две (например, 2, 3, 4, 5, 6, 7, 8, 9, или 10) различные нуклеиновые кислоты, по меньшей мере две (например, 2, 3, 4, 5, 6, 7, 8, 9, или 10) различные клетки-хозяева, и/или по меньшей мере две (например, 2, 3, 4, 5, 6, 7, 8, 9, или 10) различные фармацевтические композиции. Предпочтительно, такие различные компоненты в составе набора частей, как описано выше, различаются по антигенным пептидам, заявленным в соответствии с настоящим изобретением, например, один компонент относится к первому антигенному пептиду, а другой компонент относится ко второму антигенному пептиду (отличному от первого антигенного пептида). Например, набор может содержать по меньшей мере два различных иммуногенных соединения по настоящему изобретению. Например, набор может содержать по меньшей мере два различных антигенных пептида по настоящему изобретению. Например, набор может содержать по меньшей мере две различных наночастицы по настоящему изобретению. Например, набор может содержать, по меньшей мере, две различные нуклеиновые кислоты по настоящему изобретению.
Предпочтительные комбинации антигенных пептидов по настоящему изобретению в составе набора соответствуют предпочтительным комбинациям антигенных пептидов по настоящему изобретению в составе фармацевтической композиции, как описано выше.
Таким образом, настоящее изобретение относится набору, содержащему (по меньшей мере один) антигенный пептид по настоящему изобретению, как раскрыто в настоящем описании. Кроме того, настоящее изобретение также относится к набору, содержащему (по меньшей мере, одно) иммуногенное соединение по настоящему изобретению, как раскрыто в настоящем описании. Кроме того, настоящее изобретение также относится к набору, содержащему (по меньшей мере, одну) наночастицу по настоящему изобретению, как раскрыто в настоящем описании. Кроме того, настоящее изобретение также относится к набору, содержащему (по меньшей мере, одну) клетку по настоящему изобретению, как раскрыто в настоящем описании. Кроме того, настоящее изобретение также относится к набору, содержащему (по меньшей мере, одну) нуклеиновую кислоту по настоящему изобретению, как раскрыто в настоящем описании. Кроме того, настоящее изобретение также относится к набору, содержащему (по меньшей мере, одну) клетку-хозяин по настоящему изобретению, как раскрыто в настоящем описании.
Различные компоненты набора частей могут быть упакованы, как в один, так и в несколько контейнеров. Описанные выше компоненты могут быть представлены в лиофилизированной или сухой форме, или быть растворены в подходящем буфере. Набор также может содержать дополнительные реагенты, включая, например, консерванты, питательную среду и/или буферы для хранения и/или восстановления описанных выше компонентов, промывающие растворы и подобные вещества.
Таким образом, настоящее изобретение относится к набору, содержащему по меньшей мере два, предпочтительно, три различных антигенных пептида по настоящему изобретению, как раскрыто в настоящем описании (или иммуногенных соединения, наночастицы, нуклеиновых кислоты, клетки и т.д., как описано выше, которые отличаются по антигенному пептиду), и, необязательно, хелперный пептид, такой как UCP2 пептид, и/или адъювант, такой как MONTANIDE ISA 51. Различные антигенные пептиды (или иммуногенных соединения, наночастицы, нуклеиновых кислоты, клетки и т.д., как описано выше, которые отличаются по антигенному пептиду) могут быть упакованы, как в один, так и в несколько контейнеров. Например, набор может включать (один) контейнер, содержащий первый антигенный пептид, как раскрыто в настоящем описании, и второй антигенный пептид, как раскрыто в настоящем описании. Указанный (один) контейнер может также дополнительно содержать хелперный пептид, такой как UCP2 пептид. Необязательно, первый и второй антигенные пептиды (и необязательно хелперный пептид) в составе (одного) контейнера могут находиться в составе одной лекарственной формы, например, быть растворенными в воде для инъекций и/или диметилсульфоксида (DMSO). Дополнительно, набор может содержать дополнительный контейнер (отличный от контейнера, содержащего антигенные пептиды), который включает адъювант, например MONTANIDE ISA 51.
Таким образом, предпочтительно, контейнер содержит
(а) первый флакон, содержащий один или более антигенный пептид по настоящему изобретению (например по меньшей мере 200 или 300 мкг каждого антигенного пептида) и, необязательно, хелперный пептид, такой как UCP2 (например по меньшей мере 200 или 300 мкг каждого антигенного пептида) необязательно в составе воды для инъекций и диметилсульфоксида (DMSO); и
(б) второй флакон, содержащий MONTANIDE ISA 51 (например по меньшей мере 0.4 или 0.5 мл).
Кроме того, набор может содержать один или несколько (например 2 или 3) шприцев, например, шприцев, не содержащих силикона и латекса. Набор также может содержать коннектор, такой как 1-коннектор.
Неограничивающими примерами таких коннекторов являются:
I-коннектор, разработанный компанией Green Peptide (Japan), коннектор контрольный DIDRACDLLFT от Didanorm (France),
I-коннектор (контр.: ODG0015ST) от Promepla (Monaco), и
I-connector (контр.: МХ494) от Smiths medical (US).
Шприцы, предпочтительно являются предпочтительными для введения MONTANIDE, то есть не содержат латекса и резины (то есть не содержат латексного колпачка на кончике поршня) и, предпочтительно, также не содержат латекса. Неограничивающими примерами таких шприцев являются:
2 мл INKJET (Ref: 4606701V от B-Braun, Germany),
5 мл INKJET (Ref: 4606710V от B-Braun, Germany),
2 мл Norm-Ject (Ref: 4020.000V0 от Henke Sass Wolf GMBH, Germany), и
5 мл Norm-Ject (Ref: 4050.000V0 от Henke Sass Wolf GMBH, Germany).
Например, набор может содержать (а) первый флакон, включающий по меньшей мере 300 мкг антигенного пептида по изобретению (или два или три антигенных пептида по меньшей мере 300 мкг каждого) и, необязательно по меньшей мере 300 мкг UCP2, растворенного в воде для инъекций и диметилсульфоксиде (DMSO), (б) второй флакон, включающий по меньшей мере 0,5 мл MONTANIDE ISA 51, (в) два не содержащих силикон и латекс шприца, и (г) 1-коннектор.
Необязательно, набор также может включать флакон воды для инъекций и/или адаптер для флакона. Также может прилагаться стерильная игла, например, для вакцинации пациента после получения эмульсии. Объем шприцев в составе набора может составлять, например, 2 мл.
Согласно одному определенному варианту осуществления изобретения, набор содержит три различных антигенных пептида по настоящему изобретению, UCP2 пептид, и MONTANIDE ISA 51, причем указанный набор включает (i) первый флакон, включающий по меньшей мере 300 мкг каждого антигенного пептида по изобретению по меньшей мере 300 мкг UCP2 (SEQ ID NO: 859), растворенного в воде для инъекций и DMSO, (ii) второй флакон, включающий по меньшей мере 0,5 мл MONTANIDE ISA 51, (ii) два не содержащих силикон и латекс шприца, и (г) 1-коннектор.
Три антигенных пептида по настоящему изобретению в составе набора предпочтительно, антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 32, антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 220 и антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано SEQ ID NO: 255.
Кроме того, набор из частей по настоящему изобретению может необязательно содержать инструкцию по применению. Соответственно, предпочтительно набор содержит листок-вкладыш или инструкцию по применению для профилактики и лечения рака путем применения иммуногенного соединения по настоящему изобретению, антигенного пептида по настоящему изобретению, наночастицы по настоящему изобретению, клетки по настоящему изобретению, нуклеиновой кислоты по настоящему изобретению, клетки-хозяина по настоящему изобретению или фармацевтической композиции по настоящему изобретению.
Также предпочтительно, в дополнение к любому из компонентов, описанных выше, набор содержит противораковый лекарственный агент, как раскрыто в настоящем описании.
Кроме того, настоящее изобретение также относится к вакцинному набору для лечения, профилактики и/или стабилизации рака? включающему фармацевтическую композицию или вакцину, как раскрыто в настоящем документе, а также инструкции по применению указанной фармацевтической композиции или указанной вакцины для профилактики и/или лечения рака.
Медицинское применение и лечение
Как раскрыто выше, композиция по настоящему изобретению может быть особенно полезна для терапевтических целей, главным образом, для запуска специфического иммунного ответа против определенного опухолевого антигена/белка, например, для профилактики или лечения рака у пациента, нуждающегося в таком лечении.
С учетом этого, настоящее изобретение предлагает:
- антигенный пептид по настоящему изобретению, как раскрыто в настоящем описании,
- иммуногенное соединение по настоящему изобретению, как раскрыто в настоящем описании,
- наночастицу по настоящему изобретению, как раскрыто в настоящем описании,
- клетку по настоящему изобретению, как раскрыто в настоящем описании,
- нуклеиновую кислоту по настоящему изобретению, как раскрыто в настоящем описании,
- клетку-хозяин по настоящему изобретению, как раскрыто в настоящем описании, и/или
- фармацевтическую композицию по настоящему изобретению, как раскрыто в настоящем описании, или
- набор по настоящему изобретению, как раскрыто в настоящем описании предназначенные для применения в профилактике и/или лечения рака. В частности, предпочтительные варианты воплощения антигенного пептида, как описано выше, также применимы к использованию в профилактике и/или лечении рака по настоящему изобретению. Например, антигенный пептид, применяемый для профилактики и/или лечения рака, или антигенный пептид в составе иммуногенного соединения, наночастицы, или клетки, или нуклеиновой кислоты, или клетки-хозяина или фармацевтической композиции, применяемых для профилактики и/или лечения рака, предпочтительно, состоит из или включает в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 1 от до 580 и от 861 до 887, такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в любой из SEQ ID Nos от 1 до 580. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 1-160, 162 253 и 255 580, являются более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 31, 32, 87, 97, 145, 193, 194, 220, 221, 255, 521 и 524, являются еще более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 31, 32, 87, 97, 193, 194, 220, 255, 521 и 524, являются еще более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 31, 32, 87, 97, 194, 220, 255, 521 и 524, являются более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 32, 87, 97, и 194, являются более предпочтительными. Например, антигенные пептиды по настоящему изобретению, состоящие из или включающие в себя аминокислотную последовательность, как указано в любой из SEQ ID NOs 30, 32, 194, 220, 254 или 255 являются особенно предпочтительными.
Также предпочтительными являются их комбинации, а именно, применение различных антигенных пептидов по настоящему изобретению для профилактики и/или лечения рака. В частности, более чем один из описанных выше компонентов может применяться для профилактики и/или лечения рака. Например, по меньшей мере два различных антигенных пептида, по меньшей мере два различных иммуногенных соединения, по меньшей мере две различные наночастицы, по меньшей мере две различных нуклеиновых кислоты, по меньшей мере две различные клетки-хозяина и/или две различные фармацевтические композиции могут применяться для профилактики и/или лечения рака. Предпочтительно, такие различные компоненты, применяемые для профилактики и/или лечения рака, как раскрыто выше, отличаются по антигенным пептидам по настоящему изобретению, например, один компонент относится к первому антигенному пептиду, а другой компонент относится ко второму антигенному пептиду (отличному от первого антигенного пептида). Например, по меньшей мере два различных иммуногенных соединения по настоящему изобретению могут применяться для профилактики и/или лечения рака. Например, по меньшей мере две различные наночастицы по настоящему изобретению могут применяться для профилактики и/или лечения рака. Например, по меньшей мере две различные нуклеиновые кислоты по настоящему изобретению могут применяться для профилактики и/или лечения рака.
Таким образом, настоящее изобретение относится (по меньшей мере, к одному) антигенному пептиду по настоящему изобретению, как раскрыто в настоящем описании, предназначенному для профилактики и/или лечения рака. Кроме того, настоящее изобретение относится (по меньшей мере к одному) иммуногенному соединению по настоящему изобретению, как раскрыто в настоящем описании, предназначенному для профилактики и/или лечения рака. Кроме того, настоящее изобретение относится (по меньшей мере к одной) наночастице по настоящему изобретению, как раскрыто в настоящем описании, предназначенной для профилактики и/или лечения рака. Кроме того, настоящее изобретение относится (по меньшей мере к одной) клетке по настоящему изобретению, как раскрыто в настоящем описании, предназначенной для профилактики и/или лечения рака. Кроме того, настоящее изобретение относится (по меньшей мере к одной) нуклеиновой кислоте по настоящему изобретению, как раскрыто в настоящем описании, предназначенной для профилактики и/или лечения рака. Кроме того, настоящее изобретение относится (по меньшей мере к одной) клетке-хозяину по настоящему изобретению, как раскрыто в настоящем описании, предназначенной для профилактики и/или лечения рака. Кроме того, настоящее изобретение относится (по меньшей мере к одной) фармацевтической композиции по настоящему изобретению, как раскрыто в настоящем описании, предназначенной для профилактики и/или лечения рака. Кроме того, настоящее изобретение относится (по меньшей мере к одному) набору по настоящему изобретению, как раскрыто в настоящем описании, предназначенному для профилактики и/или лечения рака.
Таким образом, настоящее изобретение также относится к способу профилактики и/или лечения рака или способу индукции, усиления или пролонгирования противоопухолевого ответа у субъекта, нуждающегося в этом, включающий введение субъекту
- антигенного пептида по настоящему изобретению, -иммуногенного соединения по настоящему изобретению,
- наночастицы по настоящему изобретению, -клетки по настоящему изобретению, -нуклеиновой кислоты по настоящему изобретению, -клетки-хозяина по настоящему изобретению, -набор по настоящему изобретению; или
- фармацевтической композиции по настоящему изобретению, или -комбинации по настоящему изобретению, как раскрыто в настоящем описании.
Предпочтительно, рак, подлежащий профилактике и/или лечению, выбран из глиомы, рака почек, рака кожи, конкретнее - меланомы, рака легких, рака яичников, рака молочной железы, колоректального рака, рака печени, рака поджелудочной железы, рака головы и шеи, рака уротелия и рака предстательной железы.
Кроме того, настоящее изобретение относится к способу запуска или улучшения у субъекта иммунного ответа против одного или нескольких эпитопов, зависящих от CD8+ цитотоксических Т-клеток, причем указанный способ включает введение указанному субъекту любого из следующих компонентов:
- антигенного пептида по настоящему изобретению,
- иммуногенного соединения по настоящему изобретению,
- наночастицы по настоящему изобретению, -клетки по настоящему изобретению,
- нуклеиновой кислоты по настоящему изобретению, -клетки-хозяина по настоящему изобретению,
- фармацевтической композиции по настоящему изобретению,
- набора по настоящему изобретению или
- комбинации по настоящему изобретению, как раскрыто в настоящем описании.
Иммунный ответ, который зависит от CD8+ответа, можно определить путем оценки воспалительного ответа, провоспалительного цитокинового ответа, включая увеличение экспрессии одного или более IFN-γ, TNF-α и IL-2 иРНК или белка относительно уровня до введения соединений по настоящему изобретению. Он также может быть оценен путем измерения числа или абсолютного количества антигенспецифических Т-клеток после введения соединений по настоящему изобретению, осуществленного с помощью HLA-пептидного мультимерного окрашивания, анализа ELISPOT и тестов на отложенную гиперчувствительность замедленного типа.
Настоящее изобретение также относится к способу запуска или улучшения у субъекта иммунного ответа против одного или нескольких эпитопов, рестриктированных множественными молекулами МНС класса I, причем указанный способ включает введение указанному субъекту любого из следующих компонентов:
- антигенного пептида по настоящему изобретению,
- иммуногенного соединения по настоящему изобретению,
- наночастицы по настоящему изобретению,
- клетки по настоящему изобретению,
- нуклеиновой кислоты по настоящему изобретению,
- клетки-хозяина по настоящему изобретению,
- фармацевтической композиции по настоящему изобретению,
- набора по настоящему изобретению, или
- комбинации по настоящему изобретению, как раскрыто в настоящем описании.
Способ индукции или улучшения у субъекта иммунного ответа против множественных эпитопов, как раскрыто в настоящем описании, которые ограничены множественными молекулами МНС класса I может оцениваться путем измерения цитокинового ответа, включая усиление экспрессии одного или более IFN-γ, TNF-α и IL-2 иРНК или белка по сравнению с исходным уровнем до введения соединений по настоящему изобретению после стимуляции Т-клеток in vitro индивидуальными пептидами, связывающимися с различными молекулами МНС класса I на поверхности антигенпрезентирующих клеток. Рестрикция молекулами МНС класса I может быть подтверждена за счет использования антигенпрезентирующих клеток, экспрессирующих молекулы МНС I класса, или за счет использования антител, блокирующих МНС I класса. Ее также можно измерить по увеличению числа или абсолютного количества антиген-специфических Т-клеток после введения соединений по изобретению, которое измеряют при помощи окрашивания HLA-пептидных мультимеров с применением мультимеров, объединенных с молекулами МНС I класса.
Таким образом, согласно другому аспекту, настоящее изобретение также относится к:
- антигенному пептиду по настоящему изобретению,
- иммуногенному соединению по настоящему изобретению,
- наночастице по настоящему изобретению,
- клетке по настоящему изобретению,
- нуклеиновой кислоте по настоящему изобретению,
- клетке-хозяину по настоящему изобретению,
- фармацевтической композиции по настоящему изобретению,
- набору по настоящему изобретению, или
-комбинации по настоящему изобретению, как раскрыто в настоящем описании,
предназначенных для применения в качестве лекарственного средства.
Настоящее изобретение более конкретно относится к композиции, как раскрыто выше, предназначенной для применения в качестве вакцины для иммунотерапии. Кроме того,
- антигенный пептид по настоящему изобретению,
- иммуногенное соединение по настоящему изобретению,
- наночастица по настоящему изобретению,
- клетка по настоящему изобретению,
- нуклеиновая кислота по настоящему изобретению,
- клетка-хозяин по настоящему изобретению,
- фармацевтическая композиция по настоящему изобретению,
- набор по настоящему изобретению, или
- комбинация по настоящему изобретению, как раскрыто в настоящем описании, могут применяться в качестве вакцины, конкретнее - для иммунотерапии (рака).
Используемый в контексте настоящего изобретения термин "вакцина" относится к (биологическому) препарату, который создает естественный и/или адаптивный иммунитет к определенному заболеванию, предпочтительно, раку. Таким образом, вакцина конкретнее поддерживает естественный и/или адаптивный иммунный ответ иммунной системы у субъекта, который лечится. Например, антигенный пептид по настоящему изобретению обычно приводит к появлению адаптивного иммунного ответа у пациента, подлежащего лечению, или поддерживает такой иммунный ответ.
В контексте настоящего изобретения вакцина (композиция) может индуцировать специфический иммунный ответ против опухолевого антигена и, таким образом, предпочтительно применяется для профилактики и лечения рака. Вакцина для профилактики и лечения рака также может обозначаться, как "противораковая вакцина".
Таким образом, согласно предпочтительному варианту своего осуществления настоящее изобретение относится к композиции, как раскрыто выше, предназначенной для применения для профилактики и/или лечения рака у субъекта, нуждающегося в этом. Более предпочтительно настоящее изобретение относится к применению композиции по настоящему изобретению для производства лекарственного средства, предназначенного для профилактики или лечения рака у субъекта, нуждающегося в этом. Другими словами, настоящее изобретение относится к способу профилактики и лечения рака у субъекта, нуждающегося в этом, который заключается во введении эффективного количества композиции по изобретению указанному субъекту.
Предпочтительно, рак, профилактика и/или лечение которого проводится
- антигенным пептидом по настоящему изобретению,
- иммуногенным соединением по настоящему изобретению,
- наночастицей по настоящему изобретению,
- клеткой по настоящему изобретению,
- нуклеиновой кислотой по настоящему изобретению,
- клеткой-хозяином по настоящему изобретению,
- фармацевтической композицией по настоящему изобретению,
- набором по настоящему изобретению или
- комбинацией по настоящему изобретению, как раскрыто в настоящем описании,
имеет отношение к (референсному) опухолевому антигену, как раскрыто в настоящем описании. Конкретно- подходящие антигенные пептиды могут быть выбраны (а) путем подбора подходящего опухолевого антигена для определенного типа рака, как известно из области техники и/или раскрыто в Таблице 1В (ниже) и (б) подбора подходящего антигенного пептида по настоящему изобретению для отобранного опухолевого антигена, как описано выше, например, в Таблице 1А. Специалисту в данной области будет очевидно, что антигенный пептид по настоящему изобретению может быть выбран, исходя из природы рака, профилактика и/или лечение которого проводится, и/или на основании человеческого гена/опухолевого антигена, участвующего в патогенезе этого типа рака.
Таким образом, предпочтительные примеры рака представлены в Таблице 1В ниже. В частности, антигенные пептиды по настоящему изобретению представляют собой варианты последовательностей фрагментов опухолевых антигенов человека, представленных в Таблице 1 В, и могут применяться, в частности для лечения заболеваний, перечисленных рядом с соответствующим опухолевым антигеном в Таблице 1В.






В целом, антигенные пептиды по настоящему изобретению могут вводиться "выделенными" или в форме иммуногенных соединений по настоящему изобретению, клеток, нагруженных такими пептидами по настоящему изобретению, наночастиц по настоящему изобретению, нуклеиновых кислот по настоящему изобретению, клеток-хозяев по настоящему изобретению и/или фармацевтических композиций по настоящему изобретению.
Согласно предпочтительному варианту осуществления изобретения они также могут вводиться в составе микроорганизма, такого как бактерия микрофлоры кишечника. Полноценные бактерии микрофлоры кишечника могут также иметь преимущество, поскольку обладают способностью инициировать более мощный иммунный ответ чем (поли)пептиды или нуклеиновые кислоты, которые они содержат. Альтернативно бактерии микрофлоры кишечника по настоящему изобретению могут находиться в форме пробиотиков, то есть живых бактерий микрофлоры кишечника, которые, соответственно, могут применяться, как пищевые добавки благодаря благоприятному влиянию на здоровье, которые они оказывают. Они могут быть, например, лиофилизированы в гранулы, пилюли или капсулы или непосредственно смешиваться с молочными продуктами перед употреблением.
Способы введения хорошо известны специалисту в данной области. В зависимости от типа композиции по настоящему изобретению, она может вводиться напрямую субъекту, в пораженный орган (то есть путем местного введения) или системно (то есть путем энтерального или парентерального введения), или даже применяться ex vivo на клетках, полученных от субъекта, или человеческой клеточной линии, которая затем вновь вводится субъекту, или даже применяется in vitro для отбора субпопуляции иммунных клеток, выделенных от субъекта, которые затем повторно вводятся этому субъекту.
Энтеральные способы введения включают пероральное и ректальное введение, а также введение посредством гастральных зондов, дуоденальных зондов или гастростомы, в то время, как парентеральные способы введения включают среди прочих, подкожные, внутривенные, внутримышечные, внутриартериальные, внутрикожные, внутрикостные, внутримозговые и интратекальные инъекции. Способ введения чаще всего будет зависеть от антигенного пептида(ов) и/или иммуногенных соединения(ий) в составе композиции, а также типа рака, лечение которого проводится, а также присутствия других активных ингредиентов в составе композиции. Например, введение предпочтительно осуществляется посредством внутримышечной или внутрикожной инъекции, в том случае, если иммуногенное соединение представляет собой нуклеиновую кислоту, как раскрыто выше, пероральное/назальное введение является наиболее предпочтительным, особенно в том случае, если указанная нуклеиновая кислота клонирована в вирусном векторе. Альтернативно в том случае, если антигенный пептид и/или иммуногенное соединение представляет собой (поли)пептид, как раскрыто ранее, или если он нагружен в/на наночастицу, как раскрыто ранее, предпочтительным является внутримышечное, внутрикожное или пероральное введение. Также альтернативно, в том случае если антигенный пептид и/или иммуногенное соединение доставляется в форме бактерий микрофлоры кишечника, как раскрыто выше, особенно если бактерии микрофлоры кишечника находятся в составе пробиотиков, предпочтительным является пероральное введение.
Антигенные пептиды, иммуногенные соединения и нуклеиновые кислоты по настоящему изобретению могут быть дополнительно инкапсулированы, чтобы облегчить их введение субъекту, нуждающемуся в этом. Например, они могут быть инкапсулированы в пептидные наноносители (предпочтительно, в том случае если иммуногенное представляет собой нуклеиновую кислоту или (поли)пептид), в виросомы (предпочтительно, если иммуногенное соединение представляет собой нуклеиновую кислоту или (поли)пептид), или систему-носитель на липидной основе, такую как липосомный-поликатионный-ДНК комплекс (предпочтительно, если иммуноген представляет собой нуклеиновую кислоту или (поли)пептид) (Trovato М, De Berardinis P. Novel antigen delivery systems. World J Virol. 2015 Aug 12;4(3): 156-68; Saade F, Petrovsky N. Technologies for enhanced efficacy of DNA vaccines. Expert Rev Vaccines. 2012 Feb; 11(2): 189-209; Li et al., Peptide Vaccine: Progress and Challenges. Vaccines (Basel). 2014 Jul 2;2(3):515-36).
Композиция также может вводиться более чем один раз для достижения желаемого эффекта. Согласно предпочтительному варианту осуществления изобретения указанная композиция вводится неоднократно по меньшей мере дважды, предпочтительно более чем дважды. Введение может осуществляться в течение продолжительного периода времени, например, еженедельно, каждые две недели, каждый месяц, каждый год или даже каждые несколько лет после самого первого введения для обеспечения правильной иммунизации субъекта.
Комбинированная терапия
Введение антигенного пептида по настоящему изобретению, иммуногенного соединения по настоящему изобретению, наночастицы по настоящему изобретению, клетки по настоящему изобретению, нуклеиновой кислоты по настоящему изобретению, клетки-хозяина по настоящему изобретению, фармацевтической композиции по настоящему изобретению, в частности согласно способам и применениям по настоящему изобретению, может осуществляться отдельно или в комбинации с другим с агентом для совместного применения, полезным для лечения и/или профилактики рака, таким как противораковый лекарственный агент.
Такой лекарственный агент, таким образом, предпочтительно обладает способностью предупреждать и/или лечить тот же тип рака, что и антигенный пептид по настоящему изобретению. Наиболее предпочтительные противораковые лекарственные агенты согласно настоящему изобретению, без ограничений указанными, антитела, лизаты опухолевых клеток, химиотерапевтические агенты, радиотерапевтические агенты, модуляторы контрольных иммунных точек, а также их комбинации.
Антитела являются особенно предпочтительными для терапии рака поскольку они могут связываться, как со специфическими антигенами на поверхности раковых клеток, тем самым "направляя" терапию непосредственно в опухоль (такие антитела обозначаются, как противоопухолевые таргетные антитела), либо блокировать иммунные контрольные точки, регуляция которых нарушена при раке (такие антитела обозначаются, как иммуномодулирующие антитела). Целью последнего типа антител является подавление иммунной резистентности к раковым клеткам, которая может наблюдаться против Т клеток, которые являются специфическими по отношению к опухолевым антигенам. Действительно, из области техники хорошо известно, что в естественных физиологических условиях иммунные контрольные точки играют ключевую роль в поддержании аутотолерантности (то есть предотвращают аутоиммунные реакции) и защите тканей от повреждений в тех случаях, когда иммунная система борется с патогенной инфекцией. Однако при раковых заболеваниях регуляция экспрессии иммунных контрольных точек может нарушаться, что является важным механизмом в развитии иммунной резистентности. Такая резистентность наблюдается при меланоме, раке яичников, раке легких, глиобластоме, раке молочной железы и раке поджелудочной железы и связана с PD-L1 контрольной точкой (Konishi et al., В7-Н1 expression on non-small cell lung cancer cells and its relationship with tumor-infiltrating lymphocytes and their PD-1 expression. Clin Cancer Res. 2004 Aug 1;10(15):5094-100; Ghebeh et al., The B7-H1 (PD-L1) T lymphocyte-inhibitory molecule is expressed in breast cancer patients with infiltrating ductal carcinoma: correlation with important high-risk prognostic factors. Neoplasia. 2006 Mar; 8(3): 190-8; Hino et al., Tumor cell expression of programmed cell death-1 ligand 1 is a prognostic factor for malignant melanoma. Cancer. 2010 Apr 1; 116(7): 1757-66). Другие примеры иммунных контрольных точек включают, без ограничений указанными, PD-L2, PD-1, CD80, CD86, CTLA4, В7Н3, В7Н4, PVR, TIGIT, GAL9, LAG-3, GITR, CD137, TIM3, VISTA, VISTA-R (Pico de  et al., Checkpoint blockade for cancer therapy: revitalizing a suppressed immune system. Trends Mol Med. 2015 Aug;21(8):482-91; Pardoll DM1. The blockade of immune checkpoints in cancer immunotherapy. Nat Rev Cancer. 2012 Mar 22; 12(4):252-64).
et al., Checkpoint blockade for cancer therapy: revitalizing a suppressed immune system. Trends Mol Med. 2015 Aug;21(8):482-91; Pardoll DM1. The blockade of immune checkpoints in cancer immunotherapy. Nat Rev Cancer. 2012 Mar 22; 12(4):252-64).
Для описанных выше целей антитела применяются, как в форме выделенных моноклональных антител (то есть, неконъюгированных), так и в форме антител, конъюгированных с другими молекулами, которые могут являться радиоактивными или токсичными для клеток.
Примерами хорошо известных моноклональных противоопухолевых таргетных антител, которые применяются в иммунотерапии рака, являются, без ограничений указанными, алемтузумаб (хронический лимфоцитарный лейкоз), бевацизумаб (колоректальный рак, мультиформная глиобластома, рак шейки матки, рак легких, рак почек), брентуксимаб / ведотин (лимфомы), блинатумумаб (острый лимфобластный лейкоз), катумаксомаб (злокачественный асцит при ЕРСАМ+опухолях), цетуксимаб (рак головы и шеи, колоректальный рак), деносумаб (рак молочной железы, простаты и костей), Гемтузумаб / озогамицин (острый миелолейкоз), ибритумомаб / тиуксетан (неходжкинская лимфома), панитумумаб (колоректальный рак), пертузумаб (рак молочной железы) обинутузумаб (хронический лимфоцитарный лейкоз), офатумумаб (хронический лимфоцитарный лейкоз), опилимумаб (меланома), рамуцирумаб (рак желудка и гастроэзофагеальный рак), ритуксимаб (хронический лимфоцитарный лейкоз и неходжкинская лимфома), силтуксимаб (многоочаговая болезнь Кастлемана), тозитумомаб (неходжкинская лимфома) и трастузумаб (рак молочной железы, желудка и пищевода); в то время, как примеры иммуномодулирующих антител включают, без ограничений указанными, ипилимумаб (меланома), который блокирует CTLA4-зависимую иммунную контрольную точку, ниволумаб (меланома, рак легкого) и прембролизубмаб (меланома), которые оба блокируют PDCD1-зависимую иммунную контрольную точку, а также MPDL3280A, MEDI4736, MEDI0680, и MSB0010718C, которые все блокируют PD-L1-зависимую иммунную контрольную точку (Sharma and Allison, The future of immune checkpoint therapy. Science. 2015 Apr 3; 348(6230):56-61).
Другие антитела для иммунотерапии рака были описаны Buque и соавт., Trial Watch: Immunomodulatory monoclonal antibodies for oncological indications. Oncoimmunology. 2015 Mar 2;4(4):el008814. eCollection 2015 Apr; Redman и соавт., Mechanisms of action of therapeutic antibodies for cancer. Mol Immunol. 2015 Oct;67(2 Pt A):28-45; Simpson and Caballero, Monoclonal antibodies for the therapy of cancer MC Proc. 2014; 8(Suppl 4)Об, а также на веб-сайте, где представлена совокупность антител (список терапевтических моноклональных антител, одобренных или находящихся на рассмотрении в Европейском Союзе или США, доступен по веб-ссылке http://www.antibodysociety.org/news/approved_mabs.php).
Лизаты опухолевых клеток также могут комбинироваться с антигенным пептидом(ами) по настоящему изобретению. Опухолевые клетки действительно способны инициировать иммунный ответ за счет презентации эндогенных МНС-пептидных комплексов, а также посредством дендритных клеток (ДК) хозяина, которые могут процессировать и презентировать антиген, доставляемый такими лизатами. Таким образом, увеличивается спектр антигенов, против которых может быть индуцирован иммунный ответ. Лизаты опухолевых клеток могут быть легко получены при обработке опухолевых клеток тепловым шоком/или с помощью химической обработки, кроме того, они могут быть аутологичными (то есть выделенными из организма пациента) или аллогенными (то есть выделенными из организма другого субъекта).
Стандартные химиотерапевтические препараты и радиотерапевтические агенты не нуждаются в дополнительном описании здесь, поскольку они подробно описаны в литературе, а именно у Baskar и соавт.(Baskar et al., Cancer and radiation therapy: current advances and future directions. Int J Med Sci. 2012;9(3): 193-9), Paci et al., (Paci et al., Review of therapeutic drug monitoring of anticancer drugs part 1--cytotoxics. Eur J Cancer. 2014 Aug;50(12):2010-9) и Widmer и соавт.(Widmer et al., Review of therapeutic drug monitoring of anticancer drugs part two-targeted therapies. Eur J Cancer. 2014 Aug;50(12):2020-36). Список таких лекарств и агентов также доступен на сайте cancer.gov (http://www.cancer.gov/about-cancer/treatment/drugs).
Предпочтительно, модулятор иммунной контрольной точки, который может применяться в комбинации с антигенным пептидом, как раскрыто в настоящем описании, представляет собой активатор или ингибитор одной или более иммунной молекулы контрольной точки, выбранной из группы, включающей CD27, CD28, CD40, CD122, CD137, ОХ40, GITR, ICOS, A2AR, В7-Н3, В7-Н4, BTLA, CD40, CTLA-4, IDO, KIR, LAG3, PD-1, TIM-3, VISTA, СЕАСАМ1, GARP, PS, CSF1R, CD94/NKG2A, TDO, GITR, TNFR и/или FasR/DcR3; или активатор, или ингибитор одного и более их лигандов.
Более предпочтительно модулятор иммунной контрольной точки представляет собой активатор (ко)стимулирующей контрольной молекулы или ингибитор тормозящей молекулы контрольной точки, или их комбинацию. Соответственно, модулятор иммунной контрольной точки более предпочтительно представляет собой (i) активатор CD27, CD28, CD40, CD 122, CD137, ОХ40, GITR и/или ICOS или (ii) ингибитор A2AR, В7-Н3, В7-Н4, BTLA, CD40, CTLA-4, IDO, KIR, LAG3, PD-1, PDL-1, PD-L2, TIM-3, VISTA, CEACAM1, GARP, PS, CSF1R, CD94/NKG2A, TDO, TNFR и/или FasR/DcR3.
Еще более предпочтительно, модулятор иммунной контрольной точки представляет собой ингибитор тормозящей молекулы контрольной точки (но, предпочтительно, не является ингибитором стимулирующей молекулы контрольной точки). Соответственно, модулятор иммунной контрольной точки более предпочтительно представляет собой ингибитор A2AR, В7-Н3, В7-Н4, BTLA, CTLA-4, IDO, KIR, LAG3, PD-1, PDL-1, PD-L2, TIM-3, VISTA, СЕАСАМ1, GARP, PS, CSF1R, CD94/NKG2A, TDO, TNFR и/или DcR3 или одного и более ее лиганда.
Еще более предпочтительно модулятор иммунной контрольной точки представляет собой модулятор CD40 каскада или IDO каскада, или LAG3 каскада, или CTLA-4 каскада и/или PD-1 каскада. Конкретнее - модулятор иммунной контрольной точки представляет собой модулятор CD40, LAG3, CTLA-4, PD-L1, PD-L2, PD-1 и/или IDO, более предпочтительно модулятор иммунной контрольной точки представляет собой ингибитор CTLA-4, PD-L1, PD-L2, PD-1, LAG3, и/или IDO или активатор CD40, еще более предпочтительно модулятор иммунной контрольной точки представляет собой ингибитор LAG3, CTLA-4 и/или PD-1, и еще более предпочтительно модулятор иммунной контрольной точки представляет собой ингибитор CTLA-4 и/или PD-1.
Таким образом, модулятор контрольной точки для комбинации с антигенным пептидом может быть выбран из известных модуляторов CTLA-4 каскада или PD-1 каскада. Предпочтительно модулятор контрольной точки для комбинации с антигенным пептидом, как раскрыто в настоящем описании, может быть выбран из известных модуляторов CTLA-4 каскада или PD-1 каскада. Особенно предпочтительно модулятор иммунной контрольной точки представляет собой ингибитор PD-1. Предпочтительные ингибиторы CTLA-4 каскада или PD-1 каскада включают моноклональные антитела Yervoy (Ипилимумаб; Bristol Myers Squibb) и Тремелимумаб (Pfizer/Medlmmune) а также Opdivo® (Ниволумаб; Bristol Myers Squibb), Keytrudaf (Пембролизумаб, также известный, как Ламбролизумаб или МК-3475; Merck), Imfinzi® (Дурвалумаб, также известный, как MEDI4736; Medlmmune/AstraZeneca), Tecentriq® (Атезолизумаб также известный, как MPDL3280A; Roche/Genentech), Пидилизумаб (СТ-011; CureTech), MEDI0680 (АМР-514; AstraZeneca), Bavencio® (Авелумаб; Merck KGaA/Pfizer, также известный, как MSB-0010718C), MIH1 (Affymetrix), LY3300054 (Eli Lilly) и Спартализумаб (также известный, как PDR001; Novartis). Более предпочтительными ингибиторами контрольных точек являются ингибиторы CTLA-4,такие как Yervoy (Ипилимумаб; Bristol Myers Squibb) и Тремелимумаб (Pfizer/Medlmmune) а также ингибиторы PD-1 Opdivo® (Ниволумаб; Bristol Myers Squibb), Keytruda® (Пембролизумаб; Merck), Пидилизумаб (CT-011; CureTech), MEDI0680 (AMP-514; AstraZeneca), AMP-224 (PD-L2 Fc слитый белок; Medlmmune).
Также предпочтительно, что модулятор контрольной точки для комбинации с антигенным пептидом, как определено здесь выбирается из группы состоящей из Пембролизумаб, Ипилимумаб, Ниволумаб, Атезолизумаб, Дурвалумаб, Тремелимумаб, Авелумаб, Спартализумаб, LAG525 (анти-AG-3 моноклональное антитело), Епакадостат (также известный, как INCB24360; ингибитор IDO), Варлилумаб (анти-С027 моноклональное антитело), Юрелумаб (анти-CD137 моноклональное антитело), АМР-224 и СМ-24 (анти-CEACAM1 моноклональное антитело).
Выбор подходящего иммунного противоракового лекарственного агента для целей настоящего изобретения находится в компетенции специалиста в данной области. Например, если целью является профилактика или лечение меланомы, предпочтительно использовать лизат клеток меланомы и/или антитело ипилимумаб вместе с подходящим антигенным пептидом, как раскрыто в настоящем описании.
Противораковый лекарственный агент также может вводиться вместе с антигенным пептидом по настоящему изобретению, иммуногенным соединением по настоящему изобретению, наночастицей по настоящему изобретению, клеткой по настоящему изобретению, нуклеиновой кислотой по настоящему изобретению, клеткой-хозяином по настоящему изобретению или фармацевтической композицией по настоящему изобретению, как в одно и то же время, так и последовательно, как раскрыто в настоящем документе, а также в составе, как одной, так и нескольких разных фармацевтических форм. Таким образом, изобретение предлагает комбинированное применение заявленной композиции и по меньшей мере одного противоракового лекарственного агента, как раскрыто выше, для одновременного, отдельного или последовательного введения, как раскрыто в настоящем описании.
Кроме того, настоящее изобретение также относится к комбинации по меньшей мере двух различных антигенных пептидов по изобретению, например, для применения с целью профилактики и лечения рака. Кроме того, настоящее изобретение также относится к комбинации по меньшей мере двух различных иммуногенных соединений по изобретению, например, для применения с целью профилактики и лечения рака. Кроме того, настоящее изобретение также относится к комбинации по меньшей мере двух различных наночастиц по изобретению, например, для применения с целью профилактики и лечения рака. Кроме того, настоящее изобретение также относится к комбинации по меньшей мере двух различных нуклеиновых кислот по изобретению, например, для применения с целью профилактики и лечения рака.
Таким образом, согласно предпочтительному варианту осуществления изобретения по меньшей мере два различных антигенных пептида по изобретению могут вводиться в комбинации, например, в составе одной фармацевтической композиции. Например, по меньшей мере 3 антигенных пептида, по меньшей мере 4 антигенных пептида, по меньшей мере 5 антигенных пептидов, по меньшей мере 6 антигенных пептидов, по меньшей мере 7 антигенных пептидов, по меньшей мере 8 антигенных пептидов, по меньшей мере 9 антигенных пептидов, по меньшей мере 10 антигенных пептидов, по меньшей мере 11 антигенных пептидов, по меньшей мере 12 антигенных пептидов, по меньшей мере 13 антигенных пептидов, по меньшей мере 14 антигенных пептидов, по меньшей мере 15 антигенных пептидов, по меньшей мере 20 антигенных пептидов, по меньшей мере 25 антигенных пептидов, по меньшей мере 50 антигенных пептидов, по меньшей мере 100 антигенных пептидов, по меньшей мере 500 антигенных пептидов, по меньшей мере, 1000 антигенных пептидов или по меньшей мере 1500 антигенных пептидов могут вводиться в комбинации, например, в составе одной фармацевтической композиции. В рамках компетенции специалиста в данной области находится выбор комбинации антигенных пептидов и/или иммуногенных соединений, которая является подходящей для предусмотренной цели. Например, в том случае, если целью является профилактика или лечение меланомы, в патогенезе которой участвует опухолевый антиген, кодируемый геном согласно Таблице 1В, специалист может подобрать любую комбинацию антигенных пептидов, как описано в Таблице 1А.
Согласно особенно предпочтительному варианту осуществления изобретения два различных антигенных пептида по настоящему изобретению (например, имеющих отношение к одному и тому же типу рака и/или одному и тому же референсному антигену) применяются в комбинации. Например,
(а) по меньшей мере два различных иммуногенных соединения по настоящему изобретению;
(б) по меньшей мере два различных антигенных пептида по настоящему изобретению;
(в) по меньшей мере два различных наночастицы по настоящему изобретению; или
(г) по меньшей мере, две различных нуклеиновых кислоты по настоящему изобретению могут применяться в комбинации.
Например, настоящее изобретение относится к комбинации
(а) первого антигенного пептида по настоящему изобретению, и
(б) второго антигенного пептида по настоящему изобретению (отличного oi первого), предпочтительно для применения с целью профилактики и/или лечения рака.
Например, настоящее изобретение относится к комбинации
(а) иммуногенного соединения по настоящему изобретению, включающего первый антигенный пептид по настоящему изобретению, и
(б) иммуногенного соединения по настоящему изобретению, включающего второй антигенный пептид по настоящему изобретению (отличный от первого), предпочтительно для применения с целью профилактики и/или лечения рака.
Например, настоящее изобретение относится к комбинации
(а) наночастицы по настоящему изобретению, включающей первый антигенный пептид по настоящему изобретению, и
(б) наночастицы по настоящему изобретению, включающей второй антигенный пептид по настоящему изобретению (отличный от первого), предпочтительно для применения с целью профилактики и/или лечения рака.
Например, настоящее изобретение относится к комбинации
(а) нуклеиновой кислоты по настоящему изобретению, включающей полинуклеотид, кодирующей первый антигенный пептид по настоящему изобретению, и
(б) нуклеиновой кислоты по настоящему изобретению, включающей полинуклеотид, кодирующий второй антигенный пептид по настоящему изобретению (отличный от первого), предпочтительно для применения с целью профилактики и/или лечения рака.
Кроме того, антигенный пептид по настоящему изобретению также может комбинироваться с соответствующим эпитопом (человеческого) опухолевого антигена (как описано выше в отношении пептидных "семейств"). Таким образом, осуществляется/поддерживается отбор клонов Т-клеток, которые являются высокоэффективными против опухоли. Конкретнее - антигенный пептид по настоящему изобретению и соответствующий эпитоп (человеческого) опухолевого антигена могут вводиться совместно. Такое совместное введение может осуществляться в одно и то же время (одновременно) или последовательно, причем последовательное введение является предпочтительным, поскольку антигенный пептид по изобретению вводится первым, а соответствующий эпитоп (человеческого) опухолевого антигена вводится следом. В частности, антигенный пептид по настоящему изобретению может вводиться первым, а затем в качестве (ре)бустера вводится соответствующий эпитоп (человеческого) опухолевого эпитопа. Например, антигенный пептид согласно последовательности SEQ ID NO: 30, 31 или 32 может комбинироваться с референсным пептидом согласно последовательности SEQ ID NO: 593. В другом примере антигенный пептид согласно последовательности SEQ ID NO: 87 или 97 может комбинироваться с референсным пептидом согласно последовательности SEQ ID NO: 617. В другом примере антигенный пептид согласно последовательности SEQ ID NO: 145 может комбинироваться с референсным пептидом согласно последовательности SEQ ID NO: 637. В другом примере антигенный пептид согласно последовательности SEQ ID NO: 193 может комбинироваться с референсным пептидом согласно последовательности SEQ ID NO: 659. В другом примере антигенный пептид согласно последовательности SEQ ID NO: 194 может комбинироваться с референсным пептидом согласно последовательности SEQ ID NO: 660. В другом примере антигенный пептид согласно последовательности SEQ ID NO: 221 может комбинироваться с референсным пептидом согласно последовательности SEQ ID NO: 675. В другом примере антигенный пептид согласно последовательности SEQ ID NO: 220 может комбинироваться с референсным пептидом согласно последовательности SEQ ID NO: 674. В другом примере антигенный пептид согласно последовательности SEQ ID NO: 225 может комбинироваться с референсным пептидом согласно последовательности SEQ ID NO: 691. В другом примере антигенный пептид согласно последовательности SEQ ID NO: 524 может комбинироваться с референсным пептидом согласно последовательности SEQ ID NO: 826. В другом примере антигенный пептид согласно последовательности SEQ ID NO: 521 может комбинироваться с референсным пептидом согласно последовательности SEQ ID NO: 824.
Пептиды, которые могут комбинироваться между собой, такие как (а) антигенный пептид по настоящему изобретению и соответствующий эпитоп (человеческого) опухолевого антигена или (b) два различных антигенных пептида по настоящему изобретению, могут вводиться
- в одном иммуногенном соединении по настоящему изобретению или в различных иммуногенных соединениях по настоящему изобретению,
- (нагруженными) на одну наночастицу по настоящему изобретению или на различные наночастицы по настоящему изобретению,
- (нагруженными) в одну клетку по настоящему изобретению или в различные клетки по настоящему изобретению,
- (закодированными) в одной молекуле нуклеиновой кислоты по настоящему изобретению или в различных молекулах нуклеиновой кислоты по настоящему изобретению,
- (экспрессируемыми) одной клеткой-хозяином по настоящему изобретению или различными клетками-хозяевами по настоящему изобретению, или
- (включенными) в одну фармацевтическую композицию по настоящему изобретению или в различные фармацевтические композиции по настоящему изобретению.
В дальнейшем описании изобретения это обозначается, как "два различных компонента" (или комбинация, предназначенная для применения согласно изобретению). В целом, термин экспрессия "двух различных компонентов" в отношении комбинации, например, предназначенной для применения согласно настоящему изобретению (в комбинированной терапии), относится к
(1) первому компоненту, такому как антигенный пептид по настоящему изобретению, как раскрыто в описании, наночастице по настоящему изобретению, как раскрыто в описании, клетке по настоящему изобретению, как раскрыто в описании, нуклеиновой кислоте по настоящему изобретению, как раскрыто в описании, клетке-хозяину по настоящему изобретению, как раскрыто в описании, или к фармацевтической композиции по настоящему изобретению, как раскрыто в описании; и
(2) второму компоненту (который отличается от первого компонента), такому как противораковый лекарственный агент, как раскрыто в настоящем описании, другой антигенный пептид по настоящему изобретению, как раскрыто в описании, другое иммуногенное соединение по настоящему изобретению, как раскрыто в описании, другая наночастица по настоящему изобретению, как раскрыто в описании, другая клетка по настоящему изобретению, как раскрыто в описании, другая молекула нуклеиновой кислоты по настоящему изобретению, как раскрыто в описании, другая клетка-хозяин по настоящему изобретению, как раскрыто в описании, другая фармацевтическая композиция по настоящему изобретению, как раскрыто в описании, или один или более (фрагмент) опухолевого человеческого антигена в любой форме ("голой", как иммуногенное соединение, раскрытое в описании, наночастица, раскрытая в описании, клетка (хозяин), раскрытая в описании, нуклеиновая кислота, раскрытая в описании, или фармацевтическая композиция, раскрытая в описании).
Таким образом, "два различных компонента" в отношении комбинации, предназначенной для применения по настоящему изобретению (в комбинированной терапии), предпочтительно представляют собой активные компоненты для лечения и/или профилактики рака. Другими словами, каждый из указанных по меньшей мере двух различных компонентов также может быть полезным для профилактики и/или лечения указанного типа рака, если вводится отдельно (не в комбинации друг с другом, как раскрыто в описании) хотя их совместное применение (то есть комбинированное введение) обычно усиливает профилактический и/или терапевтический эффект (такой как иммунный ответ) каждого из них синергетическим образом.
Таким образом, настоящее изобретение также относится к комбинации (по меньшей мере) двух различных антигенных пептидов по изобретению, как раскрыто в настоящем описании. В этом контексте (по меньшей мере) два различных антигенных пептида могут находиться в любой форме, например, "голой" форме или в составе иммунногенных соединений, наночастиц и (фармацевтических) композиций, быть нагруженными на наночастицы или закодированными в нуклеиновых кислотах (например, векторах). Соответственно, (по меньшей мере) два различных антигенных пептида могут быть включены в состав (по меньшей мере) двух различных компонентов (которые затем комбинируют). Согласно предпочтительному варианту осуществления изобретения по меньшей мере два различных компонента комбинации по настоящему изобретению представляют собой по меньшей мере два различных антигенных пептида по изобретению (в любой форме, например, в составе иммуногенных соединений, наночастиц, клеток, фармацевтических композиций, закодированных нуклеиновыми кислотами и т.д.).
Предпочтительно по меньшей мере два различных компонента комбинации, предназначенной для применения согласно настоящему изобретению, имеют отношение к одному типу рака, например, к одному и тому же или различным антигенам, ассоциированным с этим типом рака, и/или к одному и тому же или различным (референсным) эпитопам антигена, ассоциированного с данным типом рака. Более предпочтительно по меньшей мере два различных компонента относятся к одному опухолевому антигену.
Согласно определенным вариантам осуществления изобретения по меньшей мере два различных компонента комбинации, предназначенной для применения по настоящему изобретению, содержатся в одной или в различных композициях. Согласно определенным вариантам осуществления изобретения по меньшей мере два различных компонента комбинации, предназначенной для применения по настоящему изобретению, вводятся одинаковым или различными способами. Согласно определенным вариантам осуществления изобретения по меньшей мере два различных компонента комбинации, предназначенной для применения по настоящему изобретению, вводятся приблизительно в одно и то же время (одновременно) или последовательно.
Предпочтительно по меньшей мере два различных компонента комбинации, предназначенной для применения по настоящему изобретению, вводятся приблизительно в одно и то же время. В более общих чертах является предпочтительным, чтобы первый компонент вводился приблизительно в то же самое время, что и второй компонент, причем по меньшей мере два различных компонента комбинации, предназначенной для применения по настоящему изобретению, предпочтительно вводятся в одной и той же форме (то есть в составе композиции одного типа, например, в составе наночастиц, фармацевтической композиции и т.п.).
Фраза "приблизительно в одно и то же время", используемая в настоящем описании, означает, в сущности, одновременное введение компонентов, либо то, что второй компонент вводится сразу после введения первого компонента, либо то, что первый компонент вводится сразу после введения второго компонента. Специалист в данной области понимает, что "сразу после" включает время, необходимое для подготовки к второму введению, - конкретнее, время, необходимое для освобождения и дезинфекции места второго введения, а также правильной подготовки "устройства для введения" (например, шприца, помпы и т.д.). Одновременное введение также подразумевает и те ситуации, когда периоды введения первого компонента и второго компонента перекрываются, а также когда, например, один компонент вводится в течение более продолжительного периода времени, такого как 30 минут, 1 час, 2 часа или даже больше, например, посредством инфузии, а другой компонент вводится в определенный момент в течение указанного длительного временного промежутка. Введение первого компонента и второго компонента приблизительно в одно и то же время является особенно предпочтительным в том случае если применяются различные способы и/или места введения.
Также предпочтительно, чтобы по меньшей мере два различных компонента композиции, предназначенной для применения согласно настоящему изобретению, вводились последовательно. В общих чертах является предпочтительным, чтобы первый и второй компоненты вводились последовательно, причем указанные два различных компонента комбинации, предназначенной для применения согласно настоящему изобретению, предпочтительно вводились бы в одной и той же форме (то есть в составе композиции одного типа, например, в составе наночастиц, фармацевтической композиции и т.п.).
Это означает, что первый компонент вводится до или после введения второго компонента. При последовательном введении время между введением первого компонента и введением второго компонента, предпочтительно не превышает одну неделю, более предпочтительно не превышает 3-х дней, еще более предпочтительно не превышает 2-х дней и еще более предпочтительно не превышает 24 дня. Особенно предпочтительно, чтобы первый компонент и второй компонент вводились в один и тот же день, а временной интервал между введением первого и второго компонента, предпочтительно не превышал 6 часов, более предпочтительно 3 часа, еще более предпочтительно 2 часа и наиболее предпочтительно 1 час.
Предпочтительно, первый и второй компоненты вводятся одним и тем же способом. В более общих чертах является предпочтительным, чтобы первый компонент и второй компонент вводились одним и тем же способом, но причем по меньшей мере два различных компонента комбинации, предназначенной для применения согласно настоящему изобретению, предпочтительно вводились бы в одной и той же форме (то есть в составе композиции одного типа, например, в составе наночастиц, фармацевтической композиции и т.п.).
Также является предпочтительным, чтобы по меньшей мере два различных компонента комбинации, предназначенной для применения согласно настоящему изобретению, вводились различными способами. В более общих чертах является предпочтительным, чтобы первый компонент и второй компонент вводились разными способами, но причем по меньшей мере два различных компонента комбинации, предназначенной для применения согласно настоящему изобретению, предпочтительно вводились бы в одной и той же форме (то есть в составе композиции одного типа, например, в составе наночастиц, фармацевтической композиции и т.п.).
Предпочтительно по меньшей мере два различных компонента комбинации, предназначенной для применения согласно настоящему изобретению, находятся в составе одной композиции. В более общих чертах является предпочтительным, чтобы первый компонент и второй компонент находились в составе одной композиции, причем по меньшей мере два различных компонента комбинации, предназначенной для применения согласно настоящему изобретению, предпочтительно, вводились бы в одной и той же форме (то есть в составе композиции одного типа, например, в составе наночастиц, фармацевтической композиции и т.п.).
Также является предпочтительным, чтобы по меньшей мере два различных компонента комбинации, предназначенной для применения согласно настоящему изобретению, находились в составе разных композиций. В более общих чертах является предпочтительным, чтобы первый компонент и второй компонент находились в составе одной композиции, причем по меньшей мере два различных компонента комбинации, предназначенной для применения согласно настоящему изобретению, предпочтительно вводились бы в одной и той же форме (то есть в составе композиции одного типа, например, в составе наночастиц, фармацевтической композиции и т.п.).
В частности, настоящее изобретение относится к комбинации, например, предназначенной для применения в профилактике и/или лечения рака, включающей первый антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека BIRC5, а также второй антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека FOXM1. Предпочтительно первый антигенный пептид состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена BIRC5 (референсный пептид человека) "LTLGEFLKL" (SEQ ID NO: 593), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 30, 31 или 32, а второй антигенный пептид состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена FOXM1 (референсный пептид человека) "LMDLSTTPL" (SEQ ID NO: 674), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 220 или 868. Еще более предпочтительно комбинация, предназначенная, например, для применения в профилактике и/или лечении рака, включает антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 32, а также антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 220.
В частности, настоящее изобретение относится к комбинации, например, предназначенной для применения в профилактике и/или лечения рака, включающей первый антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека BIRC5, а также второй антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека IL13RA2. Предпочтительно первый антигенный пептид состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена BIRC5 (референсный пептид человека) "LTLGEFLKL" (SEQ ID NO: 593), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 30, 31 или 32, а второй антигенный пептид состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена IL13RA2 (референсный пептид человека) "WLPFGFILI" (SEQ ID NO: 691) или "WLPFGFILIL" (SEQ ID NO: 692), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 254, 255, 878 или 879. Еще более предпочтительно комбинация, предназначенная, например, для применения в профилактике и/или лечении рака, включает антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 32, а также антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 255.
В частности, настоящее изобретение относится к комбинации, например, предназначенной для применения в профилактике и/или лечения рака, включающей первый антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека FOXM1, а также второй антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека IL13RA2. Предпочтительно первый антигенный пептид состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена FOXM1 (референсный пептид человека) "LMDLSTTPL" (SEQ ID NO: 674), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 220 или 868, а второй антигенный пептид состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена IL13RA2 (референсный пептид человека) "WLPFGFILI" (SEQ ID NO: 691) или "WLPFGFILIL" (SEQ ID NO: 692), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 254, 255, 878 или 879. Еще более предпочтительно, комбинация, предназначенная, например, для применения в профилактике и/или лечении рака, включает антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 220, а также антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 255.
Более предпочтительно комбинация по настоящему изобретению (например, предназначенная для применения в профилактике и/или лечении рака) включает по меньшей мере три различных компонента, как описано выше, конкретнее - по меньшей мере три различных антигенных пептида по настоящему изобретению. Представленное выше описание, касающееся комбинации двух различных компонентов также применимо и для комбинации трех различных компонентов.
Таким образом, настоящее изобретение также относится к комбинации для применения в профилактике и/или лечении рака, включающей первый антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека BIRC5, второй антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека FOXM1, а также третий антигенный пептид по настоящему изобретению, который состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена человека IL13RA2. Предпочтительно первый антигенный пептид состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена BIRC5 (референсный пептид человека) "LTLGEFLKL" (SEQ ID NO: 593), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 30, 31 или 32; второй антигенный пептид состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена FOXM1 (референсный пептид человека) "LMDLSTTPL" (SEQ ID NO: 674), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 220 или 868; а третий антигенный пептид состоит из или включает в себя микробиотический вариант последовательности фрагмента опухолевого антигена IL13RA2 (референсный пептид человека) "WLPFGFILI" (SEQ ID NO: 691) или "WLPFGFILIL" (SEQ ID NO: 692), такой как антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 254, 255, 878 или 879. Еще более предпочтительно, комбинация, предназначенная, например, для применения в профилактике и/или лечении рака, включает антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 30, антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 220, а также антигенный пептид, состоящий из или включающий в себя аминокислотную последовательность, как указано в SEQ ID NO: 255.
Понятно, что комбинация, предназначенная для применения в профилактике и/или лечении рака, также может включать - вместо описанных выше предпочтительных комбинаций антигенных пептидов соответствующую комбинацию иммуногенных соединений по изобретению, соответствующую комбинацию наночастиц по изобретению или соответствующую комбинацию нуклеиновых кислот по изобретению.
КРАТКОЕ ОПИСАНИЕ ФИГУР
Далее представлено краткое описание прилагаемых к заявке фигур. Фигуры предназначены для более детальной иллюстрации настоящего изобретения. Однако они ни коим образом не ограничивают сущность изобретения.
Фигура 1: демонстрирует аффинность in vitro для антигенных пептидов IL13RA2-B и IL13RA2-L по сравнению с соответствующим эпитопом IL13RA2-H, полученным из IL13RA2 человека, как описано в Примере 2.
Фигура 2: демонстрирует аффинность in vitro для антигенных пептидов BIRC5-B1, BIRC5-B2 и BIRC5-B3 по сравнению с соответствующим эпитопом BIRC5-H, полученным из BIRC5 человека, как описано в Примере 2.
Фигура 3: демонстрирует аффинность in vitro для (А) антигенного пептида EZH2-B по сравнению с соответствующим эпитопом EZH2-H, полученным из EZH2 человека и (В) антигенного пептида EZH2-B2 по сравнению с соответствующим эпитопом EZH2-H2, полученным из EZH2 человека, как описано в Примере 2.
Фигура 4: демонстрирует аффинность in vitro для (А) антигенного пептида TYMS-B по сравнению с соответствующим эпитопом TYMS-H, полученным из TYMS человека, и (В) антигенного пептида TYMS-В2 по сравнению с соответствующим эпитопом TYMS-H2, полученным из TYMS человека, как описано в Примере 2.
Фигура 5: демонстрирует аффинность in vitro для (А) антигенного пептида FOXM1-B по сравнению с соответствующим эпитопом FOXM1-H, полученным из FOXM1 человека и (В) антигенного пептида FOXM1-B2 по сравнению с соответствующим эпитопом FOXM1-H2, полученным из FOXM1 человека, как описано в Примере 2.
Фигура 6: демонстрирует аффинность in vitro для антигенных пептидов CHI3L1-B и CHI3L1-B3 по сравнению с соответствующим эпитопом CHI3L1-H, полученным из CHI3L1 человека, как описано в Примере 2.
Фигура 7: демонстрирует схематическую схему иммунизации, которая использовалась в Примере 3. д: день.
Фигура 8: демонстрирует для Примера 3 результаты ELISPOT у мышей, вакцинированных антигенными пептидами, как указано на фигуре (BIRC5-H, BIRC5-B1, BIRC5-B2, BIRC5-B3, FOXM1-H2, FOXM1-В2, EZH2-H2, EZH2-B2, IL13RA2-H, IL13RA2-B. Для каждой группы показано нормализованное число формирующих пятна клеток (SFC). Каждая точка соответствует средней величине для каждого индивидуального животного/мыши.
Фигура 9: демонстрирует для Примера 4 результаты ELISPOT у HLA-A2-трансгенных мышей, вакцинированных антигенным IL13R2A-L, как указано на фигуре, а также перекрестную реактивность с соответствующим пептидом IL13RA2-H человека. Для каждой группы показано нормализованное число формирующих пятна клеток (SFC).
Фигура 10: демонстрирует для Примера 5 результаты ELISPOT для HLA-A2 трансгенных мышей, вакцинированных антигенным пептидом BIRC5-B1, как показано на фигуре, и перекрестную реактивность с соответствующим пептидом BIRC5-H человека. Для каждой группы показано нормализованное число формирующих пятна клеток (SFC).
Фигура 11: демонстрирует для Примера 6 результаты ELISPOT для HLA-трансгенных мышей, вакцинированных антигенным пептидом FOXM1-B2, как показано на фигуре, и перекрестную реактивность с соответствующим пептидом FOXM1-H2 человека. Для каждой группы показано нормализованное число формирующих пятна клеток (SFC).
Фигура 12: демонстрирует аффинность in vitro для антигенных пептидов IL13RA2-B и IL13RA2-L по сравнению с соответствующим эпитопом IL13RA2-H, полученным из IL13RA2 человека, сравнительным пептидом 1A9V и позитивным контролем HIV, как описано в Примере 8.
Фигура 13: демонстрирует аффинность in vitro для антигенных пептидов BIRC5-B1 по сравнению с соответствующим эпитопом BIRC5-H, полученным из BIRC5 человека, сравнительным пептидом 2М и позитивным контролем HIV, как описано в Примере 9.
ПРИМЕРЫ
Далее приведены практические примеры, иллюстрирующие различные воплощения и аспекты изобретения. Однако настоящее изобретение не ограничивается в своем объеме специфическими воплощениями, описанными ниже. Приведенные ниже примеры и способы приведены, для того чтобы специалист в данной области техники смог более точно понять изобретение и осуществить его. Настоящее изобретение, однако, не ограничивается в своем объеме раскрытыми в примерах воплощениями, которые служат только иллюстрацией определенных аспектов изобретения, и в объем изобретения также входят способы, функционально эквивалентные раскрытым. В действительности, различные модификации изобретения, дополнительные по отношению к раскрытым в настоящем описании, будут легко понятны специалисту в данной области, исходя из приведенного ниже описания, сопровождаемого фигурами и примерами. Все такие модификации входят в объем прилагаемой формулы.
ПРИМЕР 1: Антигенные пептиды, имеющие превосходящую аффинность связывания по сравнению с пептидами человека.
Аффинность связывания раскрытых в примерах антигенных пептидов, полученных согласно настоящему изобретению, и соответствующих фрагментов опухолевых антигенов человека (референсные пептиды человека) по отношению к МНС класса I предсказывали in silico. Такую предполагаемую аффинность определяли с использованием Сервера NetMHC 4.0 (http://www.cbs.dtu.dk/services/NetMHC/) согласно описанию Andreatta М, Nielsen М, «Выравнивание последовательности с учетом пробелов с помощью искусственных нейронных сетей: применение к системе МНС класса I. Bioinformatics (2016) Feb 15; 32(4):511-7. Данный метод обеспечивает высокоточные предположения связывания пептидов с главным комплексом гистосовместимости (МНС), в частности, для пептидов, имеющих в длину 8-11 аминокислот.
В Таблице 2 ниже приведены результаты, т.е. информация о предполагаемом связывании пептида с МНС класса I.



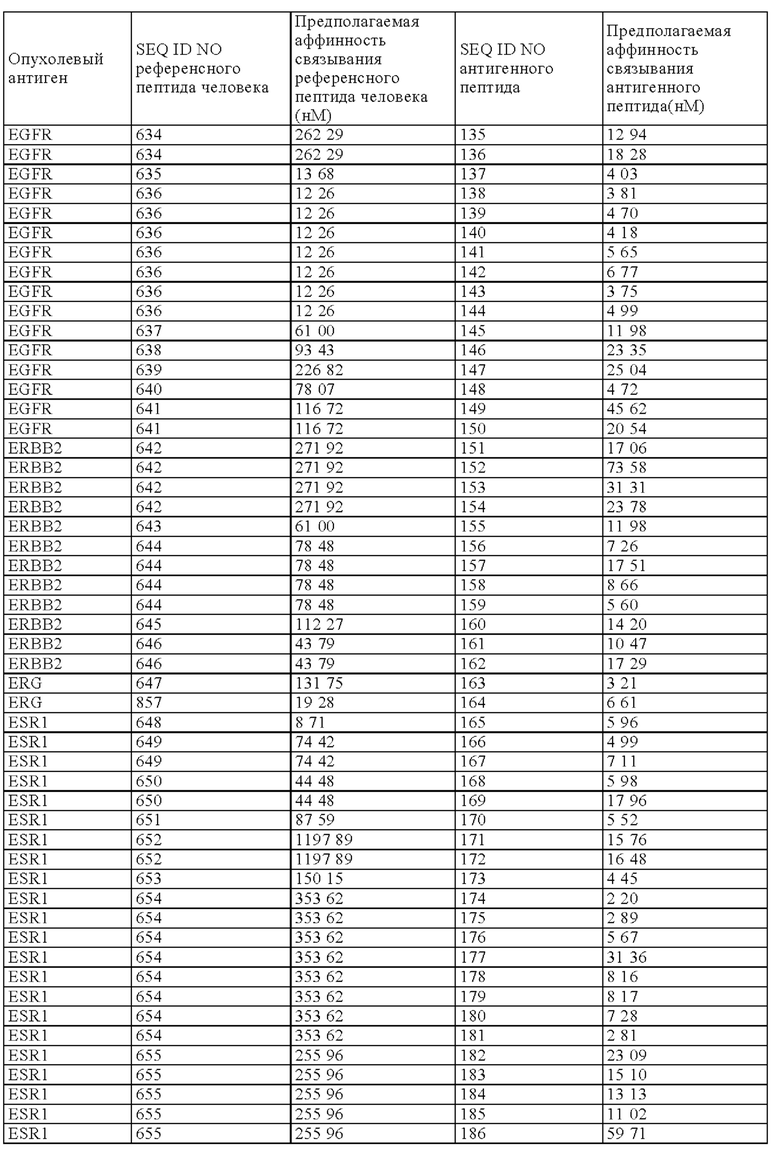

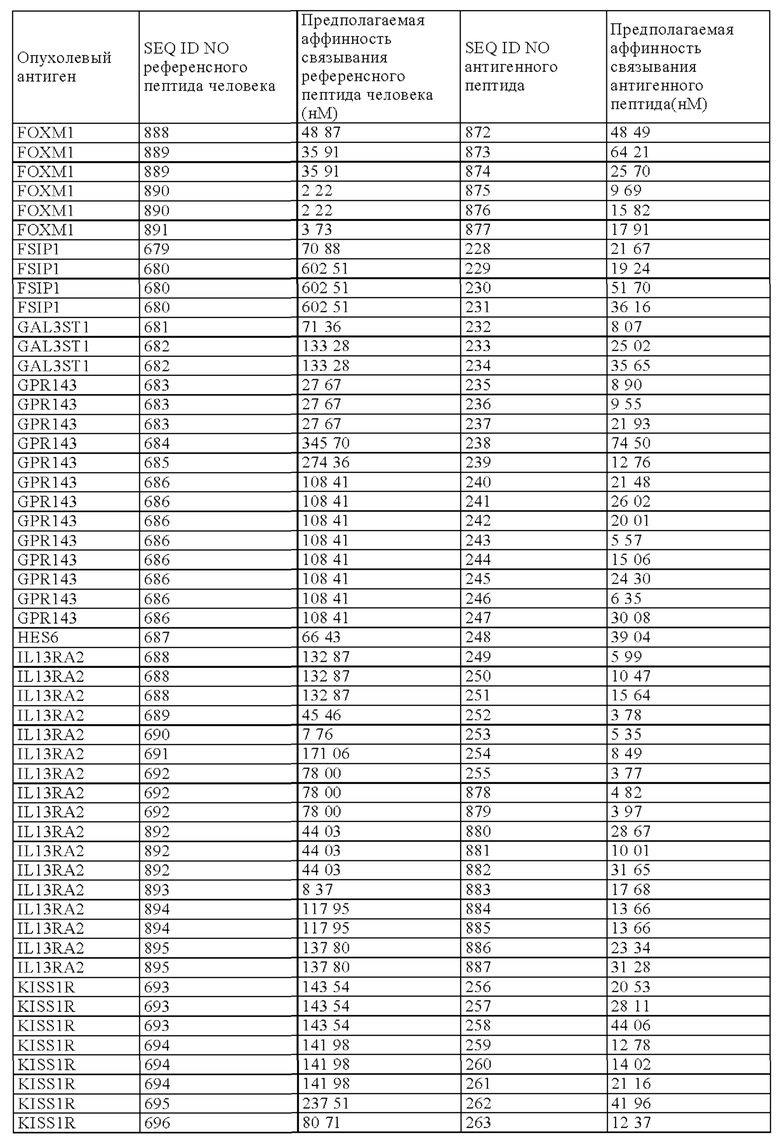



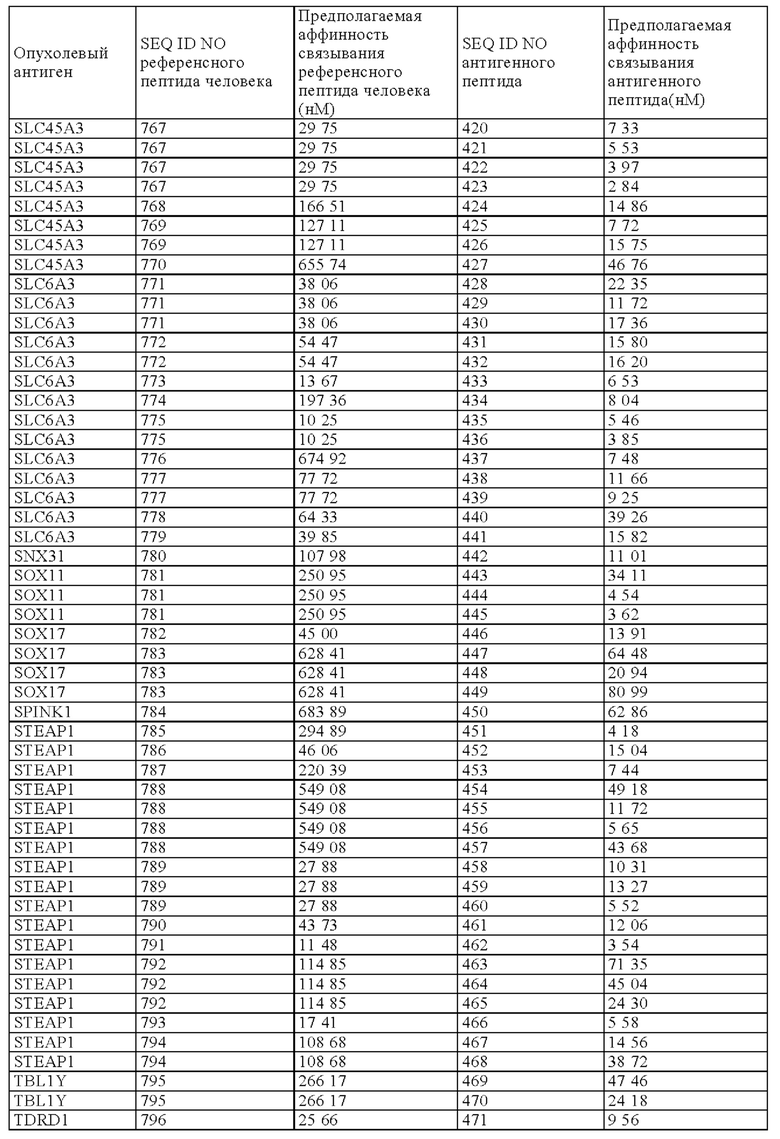



Таблица 2 - предполагаемое связывание пептида МНС класса 1 in silico. Сравнение предполагаемой аффинности каждого антигенного пептида по изобретению и референсного пептида человека показывает преимущество связывающей аффинности антигенного пептида по настоящему изобретению.
Пример 2: Антигенные пептиды, имеющие превосходящую аффинность к аллелю HLA-A*0201.
Далее, аффинность связывания различных отобранных антигенных пептидов и соответствующих фрагментов опухолевых антигенов человека (референсные пептиды человека) по отношению к аллелю HLA-A*0201 подтверждали in vitro. А именно, антигенные пептиды с последовательностью SEQ ID NO:32 ("FMLGEFLKL", также называемый здесь BIRC5-B1); с последовательностью SEQ ID NO:32 ("YTLGEFLYI", также называемый здесь BIRC5-B2) и с последовательностью SEQ ID NO:31 ("GLLGEFLQI", также называемый здесь BIRC5-B3) сравнивали с соответствующим референсным пептидом человека, происходящим из BIRC5 ("LTLGEFLKL", SEQ ID NO:593, также называемым здесь BIRC5-H). Более того, антигенные пептиды с последовательностью SEQ ID NO:97 ("LLLSAALSV", также называемый здесь CHI3L1 В) и с последовательностью SEQ ID NO:87 ("YLLSAALTI", также называемый здесь CHI3L1 В3) сравнивали с соответствующим референсным пептидом человека, происходящим из CHI3L1 ("LLLSAAALSA", SEQ ID NO:617, также называемым здесь CHI3L1 Н). Кроме того, антигенный пептид с последовательностью SEQ ID NO:145 ("ILDEAYVRV", также называемый здесь EGFR-B) сравнивали с соответствующим референсным пептидом человека, происходящим из EGFR ("ILDEAYVMA", SEQ ID NO:637, также называемым здесь EGFR-H). Более того, антигенные пептиды с последовательностью SEQ ID NO:193 ("FLVEDETVI", также называемый здесь EZH2-B) и с последовательностью SEQ ID NO:194 ("AVFRVLIPV", также называемый здесь EZH2-B 2) сравнивали с соответствующими референсными пептидами человека, происходящими из EZH2 ("FMVEDETVL", SEQ ID NO:659, также называемым здесь EZH2-H2, и "SMFRVLIGT", SEQ ID NO:660, также называемым здесь EZH2-H2, соответственно). Более того, антигенные пептиды с последовательностью SEQ ID NO:221 ("RLSSYLVEI", также называемый здесь FOXM1-B) и с последовательностью SEQ ID NO:220 ("LMDLSTTEV", также называемый здесь FOXM1-B2) сравнивали с соответствующими референсными пептидами человека, происходящими из FOXM1 ("RVSSYLVPI", SEQ ID NO:675, также называемым здесь FOXM1-Н, и "LMDLSTTPL", SEQ ID NO:674, также называемым здесь FOXM1-Н2, соответственно). Более того, антигенные пептиды с последовательностью SEQ ID NO:254 ("FLPFGFILV", также называемый здесь IL13RA2-B) и с последовательностью SEQ ID NO:255 ("FLPFGILPV", также называемый здесь IL13RA2-L) сравнивали с соответствующим референсным пептидом человека, происходящим из IL13RA2 ("WLPFGFILI", SEQ ID NO:691, также называемым здесь IL13RA2-H). Кроме того, антигенные пептиды с последовательностью SEQ ID NO:524 ("SMEELLWFV", также называемый здесь TYMS-B) и с последовательностью SEQ ID NO:521 ("FLDSLGFSL", также называемый здесь TYMS-B2) сравнивали с соответствующими референсными пептидами человека, происходящими из TYMS ("VLEELLWFI", SEQ ID NO:826, также называемым здесь TYMS -Н, и "FLDSLGFST", SEQ ID NO:824, также называемым здесь TYMS-Н2, соответственно).
А. Материалы и методы
А1. Измерение аффинности пептида с Т2-клеточной линией. Экспериментальный протокол является сходным с одним из протоколов, утвержденных для пептидов, презентируемых HLA-A*0201 (Tourdot et al., «Генеральная стратегия для усиления иммуногенности низко-аффинных, ассоциированных с HLA-A2.1 пептидов: применение в идентификации критических опухолевых эпитопов». Eur. J. Immunol. 2000 Dec; 30(12):3411-21). Измерение аффинности пептидов осуществляли с помощью линии опухолевых клеток человека Т2, экспрессирующей молекулы HLA-A*0201, но которая негативна по ТАР 1/2 и неспособна презентировать эндогенные пептиды.
Клетки Т2 (2х105 клеток на лунку) инкубировали с уменьшающимися концентрациями пептидов от 100 мкМ до 1, 5625 мкМ в среде AIMV с добавлением 100 нг/мкл β2m человека при 37°С в течение 16 ч. Затем клетки дважды промывали и маркировали антителами к HLA-A2, связанными с РЕ (клон ВВ7.2, BD Pharmagen).
Измерение проводили методом FACS (Guava Easy Cyte).
Для каждой концентрации пептида геометрическое значение мечения, ассоциированное с пептидом, представляющим интерес, вычитали из величины фонового шума и выражали в процентах геометрического значения мечения для HLA-A*0201, полученного для референсного пептида HIV ро1 589-597 при концентрации 100 мкМ. Относительную аффинность далее вычисляли следующим образом:
Относительная аффинность - концентрации каждого пептида, индуцирующей 20% экспрессии HLA-А*0201/концентрации референсного пептида, индуцирующей 20% экспрессии HLA-A*0201.
А2. Солюбилизация пептидов
Каждый пептид солюбилизировали с учетом его аминокислотного состава. Для пептидов, которые не содержат цистеина, метионина или триптофана, возможно добавление ДМСО до концентрации 10% от общего объема. Другие пептиды ресуспендировали в воде или PBS, рН. 7,4.
В. Результаты
Значения величин относительной интенсивности флуоресценции (данные нормализованы к величине флуоресценции HIV пептида, т.е. величина 100 является эквивалентной наилучшему связыванию, наблюдаемому для HIV пептида) клеток Т2, определенные для различных концентраций каждого пептида, приведены ниже в Таблице 3:
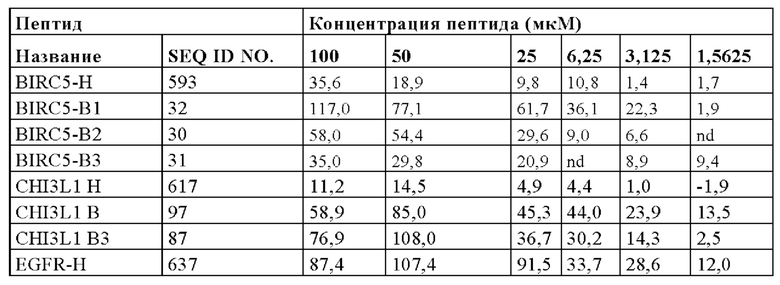

Ниже в Таблице 4 для каждого тестируемого пептида суммированы концентрации, требуемые для индуцирования 20% экспрессии HIV HLA-A*0201, и величины связывающей активности in vitro.


В дополнение. Фигуры 1-6 иллюстрируют результаты для выбранных примеров, а именно для антигенных пептидов IL13RA2-B и IL13RA2-L в сравнении с соответствующим фрагментом IL13RA-H, полученным из IL13RA человека (Фиг. 1), для антигенных пептидов BIRC5-B1, BIRC5-B2 и BIRC5-B3 в сравнении с соответствующим фрагментом BIRC5-H, полученным из BIRC5 человека (Фиг. 2), для антигенного пептида EZH2-B в сравнении с соответствующим фрагментом EZH2-H, полученным из EZH2 человека (Фиг. 3А) и для антигенного пептида EZH2-B2 в сравнении с соответствующим фрагментом EZH2-H2, полученным из EZH2 человека (Фиг. 3В),), для антигенного пептида TYMS-B в сравнении с соответствующим фрагментом TYMS-H, полученным из TYMS человека (Фиг. 4А) и для антигенного пептида TYMS-B2 в сравнении с соответствующим фрагментом TYMS-H2, полученным из TYMS человека (Фиг. 4В), для антигенного пептида FOXM1-B в сравнении с соответствующим фрагментом FOXM1-Н, полученным из FOXM1 человека (Фиг. 5А) и для антигенного пептида FOXM1-В2 в сравнении с соответствующим фрагментом FOXM1-Н2, полученным из FOXM1 человека (Фиг. 5В) и для антигенных пептидов CHI3L1-B и CHI3L1-B3 в сравнении с соответствующим фрагментом CHI3L1, полученным из CHI3L1-H человека (Фиг. 6).
В сумме, приведенные результаты показывают, что антигенные пептиды, полученные в соответствии с настоящим изобретением, показывают по меньшей мере сходную аффинность связывания по отношению к HLA-A*0201 с аффинностью соответствующих фрагментов опухолевых антигенов человека. В большинстве случаев, связывающая аффинность, выявленная для антигенных пептидов, полученных в соответствии с настоящим изобретением, является более сильной, чем таковая для соответствующих эпитопов человека. Без связи с какой-либо теорией предполагается, такая сильная связывающая аффинность антигенных пептидов, полученных в соответствии с настоящим изобретением, отражает их способность усиливать иммунный ответ (т.е. их иммуногенность).
ПРИМЕР 3: Вакцинация мышей антигенными пептидами, полученными в соответствии с настоящим изобретением, индуцирует улучшенный Т-клеточный эффект в исследовании ELISPOT-IFNγ.
А. Материалы и методы
A.1. Мышиная модель
Схема иммунизации приведена на Фигуре 7. Коротко говоря, мыши, иммунизированные HLA-A2 (HLA-A2(CB6F1-Tg(HLA-A*0201/H2-Kb)A*0201), были выборочно (на основании пола и возраста) разбиты на экспериментальные группы, причем каждую группу иммунизировали специфическим вакцинным пептидом (vacc-pAg), объединенным с обычным хелперным пептидом (h-pAg T13L; последовательность TPPAYRPPNAPIL; SEQ ID NO:860; Bhasin M. Singh Н, Raghava GP (2003) MHCBN: "Комплексная база данных связывающих и не связывающих МНС пептидов". Biomformatics 19:665-666) (как показано в Таблице 5 ниже). Vacc-pAg сравнивали попарно (группа 1 против группы 2; группа 1 против группы 3; группа 1 против группы 4; группа 5 против группы 6; группа 7 против группы 8; группа 9 против группы 10). Тем самым, как нативная, так и оптимизированная версии определенного пептида сравнивались в каждом отдельном случае.
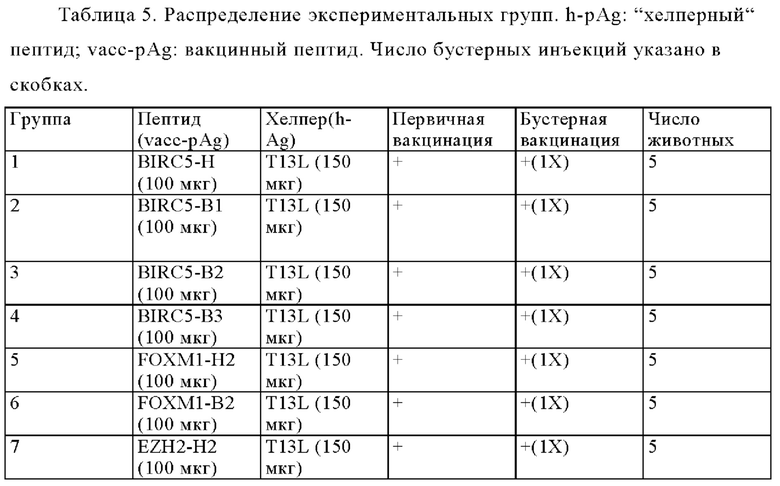

Пептиды были представлены следующим образом:
- vacc-pAg: BIRC5-H, BIRC5-B1, BIRC5-B2, BIRC5-B3, FOXM1-H2, FOXM1-B2, EZH2-H2, EZH2-B2, IL13RA2-H и IL13RA2-B; все пептиды получали и использовали в концентрации 4 мг/мл (4 мМ);
- h-pAg: T13L; партию Eurogentec 1713334 ресуспендировали в чистой дистиллированной воде при концентрации 10 мг/мл.
Животных иммунизировали в день 0 (д0) первичной инъекцией и в день 14 (д14 бустерной инъекцией. Каждую мышь инъецировали подкожно в основание хвоста 100 мкл масляной эмульсией, которая содержала:
- 100 мкг vacc-pAg (25 мкл стокового раствора с концентрацией 4 мг/мл на мышь);
- 150 мкг h-pAg (15 мкл стокового раствора с концентрацией 10 мг/мл на мышь);
- 10 мкл PBS до достижения общего объема 50 мкл (на мышь);
- неполный адъювант Фрейнда (IFA), добавляемый при соотношении 1:1 (объем/объем) (50 мкл на мышь).
Отдельную эмульсию готовили для каждого vacc-pAg следующим образом:
реагент IFA добавляли к смеси vacc-pA/h-pAg/PBS в 15-мл пробирке и перемешивали на вортексе с повторными циклами в 1 мин для формирования густой эмульсии.
А.2. Анализ
Через 7 дней после бустерной инъекции (интраперитонеально в d21) животных подвергали эвтаназии и забирали селезенку. Спленоциты получали механическим разрушением органа с последующим фильтрованием через мембрану с размером пор 70 мкм и очисткой в градиенте плотности Фиколла.
Спленоциты сразу же использовали в анализе ELISPOT-IFNγ (Таблица 6). Эксперименты повторяли трижды с применением 2х105 спленоцитов на лунку, которые культивировали в присутствии vacc-pAg (10 мкМ), иономицина (0,1 мкМ) с добавлением РМА (1 мкМ) или только среды для достижения ими способности секретировать IFNγ. Коммерческий набор ELISPOT-IFNγ (Diaclone Kit Mujrine IFNγ ELISpot) использовали согласно инструкциям производителя и анализ выполняли примерно через 19 часов инкубации.

Пятна реакции обсчитывали на ридере CTL ELISpot. Построение графика данных и статистический анализ осуществляли с помощью программного обеспечения Prism-5 (GraphPad Software Inc.).
В. Результаты
Для данного эксперимента использовали мышей в общем количестве 50 HLA-A2 (CB6F1-rTg(HLA-A*020Vm-Kb)A*0201). На дату эксперимента все мыши имели возраст от 6 до 9 недель. Для эксперимента использовали как самцов, так и самок. Животных разделяли на группы, максимально по пять животных на клетку. Во время умерщвления популяцию Т-клеток селезенки анализировали проточной цитометрией, которая показала, что основная часть этих клеток принадлежит к субпопуляции CD4+ Т-клеток.
После высева в планшеты и инкубирования с соответствующими стимулами выявляли и подсчитывали число клеток, продуцирующих IFNγ. Затем данные нормализовали, как количество специфических пятен (средний счет, полученный «только в среде», вычитался) в расчете на общее число 50х103 Т-клеток.
Индивидуальные средние значения (полученные при троекратном дублировании) далее использовали для построения графиков групповых средних значений. Поскольку функциональная способность Т-клеток способна варьировать от индивидуума к индивидууму, данные также выражали, как процент ответа в случае «РМА + лономицин» в расчете на индивидуума (см. Фигуру 8).
В целом, вакцинация антигенными пептидами, полученными в соответствии с настоящим изобретением (BIRC5-B1, BIRC5-B2 BIRC5-B, FOXM1-B2, EZH2-B и IL13RA2-B) индуцирует улучшенные ответы Т-клеток в анализе ELISPOT-IFNγ по сравнению с соответствующими референсными эпитопами человека (BIRC5-H, FOXM1-H2, EZH2-H2 и IL13RA2-H).
ПРИМЕР 4: Иммуногенность IL13RA2-L в организме HLA-A2 трансгенных мышей и перекрестная реактивность с соответствующим пептидом человека.
А. Материалы и методы
Антигенный пептид IL13RA2- L (SEQ ID NO:255), полученный согласно настоящему изобретению, и соответствующий референсный пептид человека IL13RA2- Н (SEQ ID NO:691) тестировали в отдельных группах самцов и самок мышей HHD DR3, экспрессирующих HLA-A2 и HLA-DR3 МНС и утративших мышиные антигены МНС Н-2 класса I и класса II. Животных в группах из пяти мышей (самцы и самки) подкожно инъецировали в дни 0 и 14 100 мкг IL13RA2-L (SEQ ID NO:255) или IL13RA2- Н (SEQ ID NO:691), 150 мкг хелперного пептида (DR3) и IFA. В день 21 мышей подвергали эвтаназии, забирали спленоциты и стимулировали их in vitro IL13RA2- L или соответствующим референсным пептидом человека IL13RA2- Н для достижения ими способности секретировать IFN, что определяли с помощью ELISpot. В качестве положительного контроля использовали Конканавалин А (ConA).
В. Результаты
Количество клеток, образующих пятна (SFC, от англ. spot forming cells) (нормализованное к числу CDS-клеток) представлено на Фигуре 9. Результаты приведены для мышей, иммунизированных IL13RA2- L. Приведенные результаты показывают, что иммунизация мышей IL13RA2- L обеспечивает индукцию Т-клеток, которые способны к сильному реагированию после введения IL13RA2- L или соответствующего пептида человека. Таким образом, IL13RA2- L является сильным иммуногеном и способен вызывать эффективный иммунный ответ против соответствующего пептида человека., как и ожидалось, иммунизация мышей соответствующим пептидом человека IL13RA2-H не индуцирует иммунный ответ после введения IL13RA2- L или соответствующего пептида человека IL13RA2-H (данные не представлены).
Эти результаты подтверждаются на мышах HHD DR1, экспрессирующих МНС HLA-A2 и HLA-DR1 и утративших мышиные антигены МНС Н-2 класса I и класса II (группы из 5 мышей).
ПРИМЕР 5: Иммуногенность BIRC5-B1 в организме HLA-A2 трансгенных мышей и перекрестная реактивность с соответствующим пептидом человека.
А. Материалы и методы
Антигенный пептид BIRC5-B1 (SEQ ID NO:32), полученный согласно настоящему изобретению, и соответствующий референсный пептид человека BIRC5-H (SEQ ID NO:593) тестировали в отдельных группах самцов и самок мышей HHD DR3, экспрессирующих HLA-A2 и HLA-DR3 МНС и утративших мышиные антигены МНС Н-2 класса I и класса II. Животных в группах из пяти мышей (самцы и самки) подкожно инъецировали в дни 0 и 14 100 мкг BIRC5-B1 или BIRC5-H, 150 мкг хелперного пептида (DR3) и IFA. В день 21 мышей подвергали эвтаназии, забирали спленоциты и стимулировали их in vitro BIRC5-В1 или пептидом человека BIRC5-H для достижения ими способности секретировать IFN, что определяли с помощью ELISpot. В качестве положительного контроля использовали Конканавалин А (ConA).
В. Результаты
Количество клеток, образующих пятна (SFC, от англ. spot forming cells) (нормализованное к числу CDS-клеток) представлено на Фигуре 10. Результаты приведены для мышей, иммунизированных BIRC5-B1. Приведенные результаты показывают, что иммунизация мышей BIRC5-B1 обеспечивает индукцию Т-клеток, которые способны к сильному реагированию после введения BIRC5-B1, или BIRC5-H соответствующего пептида человека. Таким образом, BIRC5-B1 является сильным иммуногеном и способен вызывать эффективный иммунный ответ против соответствующего пептида человека. Иммунизация мышей соответствующим пептидом человека BIRC5-H не индуцирует иммунный ответ против BIRC5-B1 или соответствующего пептида человека (данные не представлены).
Эти результаты подтверждаются на мышах HHD DR1, экспрессирующих МНС HLA-A2 и HLA-DR1 и утративших мышиные антигены МНС Н-2 класса I и класса II (группы из 5 мышей).
ПРИМЕР 6: Иммуногенность FOXM1-B2 в организме HLA-A2 трансгенных мышей и перекрестная реактивность с соответствующим пептидом человека.
А. Материалы и методы
Антигенный пептид FOXM1-B2 (SEQ ID NO:220), полученный согласно настоящему изобретению, и соответствующий пептид человека FOXM1-H2 (SEQ ID NO:674) тестировали в отдельных группах самцов и самок мышей HHD DR3, экспрессирующих HLA-A2 и HLA-DR3 МНС и утративших мышиные антигены МНС Н-2 класса I и класса II. Животных в группах из пяти мышей (самцы и самки) подкожно инъецировали в дни 0 и 14 100 мкг FOXM1-B2 или FOXM1-H2, 150 мкг хелперного пептида (DR3) и IFA. В день 21 мышей подвергали эвтаназии, забирали спленоциты и стимулировали их in vitro FOXM1-B2 или соответствующим пептидом человека FOXM1-H2 для достижения ими способности секретировать IFN, что определяли с помощью ELISpot. В качестве положительного контроля использовали Конканавалин А (ConA).
В. Результаты
Количество клеток, образующих пятна (SFC, от англ. spot forming cells) (нормализованное к числу CDS-клеток) представлено на Фигуре 11. Результаты приведены для мышей, иммунизированных FOXM1-B2. Приведенные результаты показывают, что иммунизация мышей FOXM1-B2 обеспечивает индукцию Т-клеток, которые способны к сильному реагированию после введения FOXM1-B2 или соответствующего пептида человека. Таким образом, FOXM1-B2 является сильным иммуногеном и способен вызывать эффективный иммунный ответ против соответствующего пептида человека FOXM1-H2. Иммунизация мышей соответствующим пептидом человека FOXM1-H2 не индуцирует иммунный ответ против FOXM1-B2 или соответствующего пептида человека (данные не представлены).
Эти результаты подтверждаются на мышах HHD DR1, экспрессирующих MHC HLA-A2 и HLA-DR1 и утративших мышиные антигены MHC Н-2 класса I и класса II (группы из 5 мышей).
Взятые все вместе, исследования иммуногенности, описанные в Примерах 5 и 6, которые были осуществлены на мышах HHD DR3 и HHD DR1, показывают, что три антигенных пептида, полученных согласно изобретению, IL13RA2- L, BIRC5-B1 и FOXM1-B2, индуцируют сильный иммунный ответ. Перекрестная реактивность Т-клеток, генерированных против IL13RA2- L, BIRC5-B1 и FOXM1-B2 для соответствующих пептидов человека, показана на мышах HHD DR3 и HHD DR1. Соответственно, эти результаты обеспечивают экспериментальное доказательство, что основанная на антигенах иммунотерапия способна усилить Т-клеточный ответ in vivo и антигенные пептиды, полученные согласно настоящему изобретению, являются чрезвычайно эффективными для данной цели.
ПРИМЕР 7: IL13RA2-B имеет превосходящую аффинность к HLA-A*0201 аллелю.
Этот пример предоставляет доказательство того, что антигенный пептид, полученный согласно изобретению, с последовательностью, представленной как SEQ ID NO:254 (FLPFGFILV, также обозначенный здесь, как IL13RA2- В), имеет более высокую аффинность к HLA-A*0201 аллелю по сравнению с другими вариантами последовательностей соответствующего референсного пептида человека, происходящего из IL13RA2 (IL13RA2-H, WLPFGFILI, SEQ ID NO:691). В данном эксперименте антигенный пептид с последовательностью SEQ ID NO:254 (IL13RA2- В) сравнивали со следующими пептидами:
- сравнительный пептид "1A9V" (SEQ ID NO:896), описанный Eguchi Junichi et al., 2006, "Идентификация пептидных аналогов рецептора интерлейкин 13 альфа-2, способных улучшать антиглиомные CTL ответы. Cancer Research 66(11): 5883-5891, в котором триптофан в положении 1 SEQ ID NO:691 замещен аланином (1А) и изолейцин в положении 9 SEQ ID NO:691 замещен валином (9V);
- пептид "1IA9A" (SEQ ID NO:897), в котором триптофан в положении 1 SEQ ID NO:691 замещен изолейцином (II) и изолейцин в положении 9 SEQ ID NO:691 замещен аланином (9А); и
- пептид "1F9M" (SEQ ID NO:898), в котором триптофан в положении 1 SEQ ID NO:691 замещен фенилаланином (IF) и изолейцин в положении 9 SEQ ID NO:691 замещен метинином (9М).
А. Материалы и методы
Экспериментальный протокол, материалы и методы соответствуют таковым, приведенным выше в Примере 2, с тем лишь различием, что используются указанные выше (поли)пептиды.
В. Результаты
Были определены следующие величины аффинности связывания in vitro:
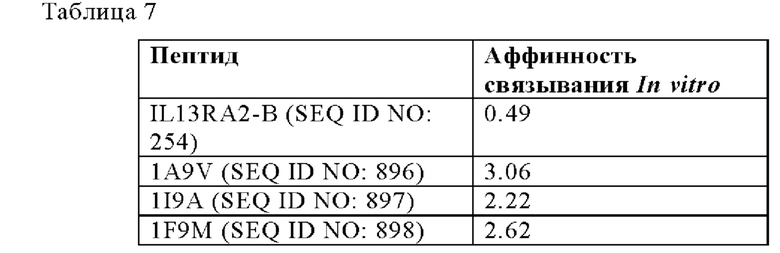
Соответственно, антигенный пептид, полученный согласно настоящему изобретению (IL13RA2-B; SEQ ID NO:254), обладает значительно более высокой связывающей аффинностью с HLA-A*0201, чем все остальные тестируемые пептиды, причем пептид "1A9V", описанный Eguchi Junichi et al., 2006, "Идентификация пептидных аналогов рецептора интерлейкин 13 альфа-2, способных улучшать антиглиомные CTL ответы. Cancer Research 66(11): 5883-5891, обнаруживает наиболее низкую аффинность среди всех протестированных пептидов.
ПРИМЕР 8: IL13RA2-L имеет превосходящую аффинность к HLA-A*0201 аллелю.
Этот пример предоставляет доказательство того, что антигенный пептид, полученный согласно изобретению, с последовательностью; представленной, как SEQ ID NO:255 (также обозначенный здесь, как IL13RA2- L), имеет сходную высокую аффинность по отношению HLA-A*0201 аллелю, что и антигенный пептид, полученный согласно изобретению, представленный, как SEQ ID NO:254 (FLPFGFILV, также обозначенный здесь, как IL13RA2-B), и более высокую аффинность по сравнению с соответствующим референсным пептидом человека, происходящим из IL13RA2 (IL13RA2-H, WLPFGFILI, SEQ ID NO:691) и другими вариантами последовательностей указанного пептида. В данном эксперименте антигенный пептид с последовательностью SEQ ID NO:255 (IL13RA2-L) сравнивали со следующими пептидами:
- сравнительный пептид "1A9V" (SEQ ID NO:896), описанный Eguchi Junichi et al., 2006, "Идентификация пептидных аналогов рецептора интерлейкин 13 альфа-2, способных улучшать антиглиомные CTL ответы. Cancer Research 66(11):5883-5891, в котором триптофан в положении 1 SEQ ID NO:691 замещен аланином (1А) и изолейцин в положении 9 SEQ ID NO:691 замещен валином (9V);
- антигенный пептид, полученный в соответствии с изобретением, с последовательностью, представленной, как SEQ ID NO:254 (как IL13RA2-B);
- соответствующий референсный пептид человека IL13RA2-H (SEQ ID NO:691; и
- положительный контроль (HIV).
А. Материалы и методы
Экспериментальный протокол, материалы и методы соответствуют таковым, приведенным выше в Примере 2, с тем лишь различием, что используются указанные выше (поли)пептиды.
В. Результаты
Были определены следующие величины аффинности связывания in vitro:


Соответственно, антигенные пептиды, полученные согласно настоящему изобретению (IL13RA2-B; SEQ ID NO:254 и IL13RA2-L; SEQ ID NO:255), обладают значительно более высокой аффинностью связывания с HLA-А*0201, чем соответствующий эпитоп человека (IL13RA2-H) и сравнительный пептид "1A9V", описанный Eguchi Junichi et al., 2006, "Идентификация пептидных аналогов рецептора интерлейкин 13 альфа-2, способных улучшать антиглиомные CTL ответы. Cancer Research 66(11):5883-5891. В частности, антигенный пептид IL13RA2-L (SEQ ID NO:255) проявляет сильную аффинность связывания по отношению к HLA-A*0201, а именно 69% от максимальной ВИЧ ро1 589-597 связывающей активности при 100 мкМ; 96% при 25 мкМ и 43% при 6, 25 мкМ. Результаты исследований также показаны на Фигуре 12.
ПРИМЕР 9:BIRC5-B1 имеет превосходящую аффинность к HLA-A*0201 аллелю.
Этот пример обеспечивает доказательство того, что антигенный пептид, полученный согласно изобретению, с последовательностью, представленной, как SEQ ID NO:32 (также обозначенный здесь, как BIRC5-B1), имеет более высокую аффинность, чем соответствующий референсный пептид человека, происходящий из BIRC5 (BIRC5-H; SEQ ID NO:593), и сравнительные варианты последовательностей указанного пептида ("2М"; SEQ ID NO:899). В данном эксперименте антигенный пептид с последовательностью SEQ ID NO:32 (BIRC5-B1) сравнивали со следующими пептидами:
- пептид "2М" (LMLGEFLKL; SEQ ID NO:899), в котором треонин в положении 2 SEQ ID NO:593 замещен метионином (2М);
- соответствующий референсный пептид человека BIRC5-H (SEQ ID NO:593); и
- положительный контроль (HIV).
А. Материалы и методы
Экспериментальный протокол, материалы и методы соответствуют таковым, приведенным выше в Примере 2, с тем лишь различием, что используются указанные выше (поли)пептиды.
В. Результаты
Были определены следующие величины связывающие аффинности in vitro:


В целом, антигенный пептид, полученный согласно настоящему изобретению (BIRC5-B1; SEQ ID NO:32), обладает in vitro значительно более высокой аффинностью связывания по отношению к HLA-A*0201, чем соответствующий эпитоп человека (BIRC5-H) и сравнительный пептид "2М". Результаты исследований также показаны на Фигуре 13.
--->
Перечень Последовательностей
<110> Энтером С.А.
<120> АНТИГЕННЫЕ ПЕПТИДЫ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ РАКА
<130> EB01P011WO1
<150> EP18305444
<151> 2018-04-11
<150> PCT/EP2018/077512
<151> 2018-10-09
<160> 899
<170> PatentIn version 3.5
<210> 1
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 1
Val Leu Phe Leu Leu Phe Phe Pro Val
1 5
<210> 2
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 2
Ser Met Ser Leu Gly Phe Leu Ser Val
1 5
<210> 3
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 3
Phe Leu Ser Leu Gly Phe Leu Ala Val
1 5
<210> 4
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 4
Leu Leu Leu Gly Phe Leu Phe Leu Ile
1 5
<210> 5
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 5
Tyr Leu Ser Asn Asp Ser Tyr Arg Val
1 5
<210> 6
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 6
Gly Leu Ile Asp Ser Gly Ala Phe Leu
1 5
<210> 7
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 7
Leu Leu Ile Asp Ser Gly Ala Leu Val
1 5
<210> 8
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 8
Arg Leu Ile Asp Ser Gly Ala Thr Val
1 5
<210> 9
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 9
Lys Leu Phe Glu Ser Ser Ala Ala Leu
1 5
<210> 10
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 10
Thr Leu Phe Glu Ser Ser Ala Phe Ala
1 5
<210> 11
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 11
Met Leu Thr Pro Leu Leu Leu Gly Leu
1 5
<210> 12
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 12
Tyr Leu Thr Pro Leu Leu Leu Ile Leu
1 5
<210> 13
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 13
Ile Met Thr Pro Leu Leu Leu Pro Val
1 5
<210> 14
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 14
Phe Met Thr Pro Leu Leu Leu Cys Leu
1 5
<210> 15
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 15
Phe Leu Thr Pro Leu Leu Leu Trp Leu
1 5
<210> 16
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 16
Trp Met Ala Val Ile Leu Thr Ala Leu
1 5
<210> 17
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 17
Val Leu Ala Val Ile Leu Thr Ala Val
1 5
<210> 18
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 18
Val Leu Ala Ala Ile Ala Ala Gly Val
1 5
<210> 19
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 19
Leu Leu Ala Ala Ile Ala Ala Phe Leu
1 5
<210> 20
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 20
Lys Leu Ala Ala Ile Ala Ala Ala Val
1 5
<210> 21
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 21
Ile Leu Ala Ala Ile Ala Ala Ala Val
1 5
<210> 22
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 22
Gly Met Ala Ala Ile Ala Ala Phe Leu
1 5
<210> 23
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 23
Phe Leu Ala Ala Ile Ala Ala Val Leu
1 5
<210> 24
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 24
Ala Leu Ala Ala Ile Ala Ala Leu Val
1 5
<210> 25
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 25
Ala Leu Ala Ala Phe Gln Ala Gly Leu
1 5
<210> 26
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 26
Ser Leu Val Asn Leu Gly Phe Ser Leu
1 5
<210> 27
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 27
Gly Leu Val Asn Leu Gly Phe Ala Leu
1 5
<210> 28
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 28
Gln Leu Leu Asp Phe Ser Ser Ser Leu
1 5
<210> 29
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 29
Ile Leu Leu Asp Phe Ser Ser Val Val
1 5
<210> 30
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 30
Tyr Thr Leu Gly Glu Phe Leu Tyr Ile
1 5
<210> 31
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 31
Gly Leu Leu Gly Glu Phe Leu Gln Ile
1 5
<210> 32
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 32
Phe Met Leu Gly Glu Phe Leu Lys Leu
1 5
<210> 33
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 33
Val Leu Gly Asp Ile Leu Ala Leu Leu
1 5
<210> 34
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 34
Lys Val Gly Asp Ile Leu Ala Leu Val
1 5
<210> 35
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 35
Asn Leu Val Phe Gly Leu Leu Pro Val
1 5
<210> 36
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 36
Phe Leu Val Phe Gly Leu Leu Gly Leu
1 5
<210> 37
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 37
Ala Leu Val Phe Gly Leu Leu Arg Val
1 5
<210> 38
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 38
Gly Val Tyr Glu Gly Ser Leu Thr Val
1 5
<210> 39
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 39
Val Leu Ser Thr Ala Phe Ala Leu Val
1 5
<210> 40
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 40
Gly Leu Ser Thr Ala Phe Ala Ala Val
1 5
<210> 41
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 41
Ala Leu Ser Thr Ala Phe Ala Val Val
1 5
<210> 42
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 42
Met Leu Leu Leu Leu Leu Val Pro Val
1 5
<210> 43
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 43
Leu Leu Leu Leu Leu Leu Val Pro Val
1 5
<210> 44
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 44
Ala Ile Leu Leu Leu Leu Val Pro Val
1 5
<210> 45
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 45
Tyr Leu Leu Leu Ser Leu Leu Arg Leu
1 5
<210> 46
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 46
Phe Leu Leu Leu Ser Leu Leu Thr Leu
1 5
<210> 47
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 47
Ala Leu Leu Leu Ser Leu Leu Pro Leu
1 5
<210> 48
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 48
Arg Leu Leu Leu Leu Ser Leu Leu Val
1 5
<210> 49
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 49
Lys Leu Leu Leu Leu Ser Leu Leu Leu
1 5
<210> 50
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 50
Phe Leu Leu Leu Leu Ser Leu Leu Ile
1 5
<210> 51
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 51
Arg Leu Ala Lys Tyr Val Ala Leu Val
1 5
<210> 52
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 52
Leu Ile Ala Ala Ala Ala Phe Thr Val
1 5
<210> 53
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 53
Gly Met Ala Ala Ala Ala Phe Cys Leu
1 5
<210> 54
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 54
Gly Leu Ala Ala Ala Ala Phe Cys Ile
1 5
<210> 55
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 55
Phe Leu Ala Ala Ala Ala Phe Cys Leu
1 5
<210> 56
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 56
Trp Leu Asn Asp Arg Val Leu Gln Leu
1 5
<210> 57
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 57
Lys Leu Leu Leu Thr Thr Leu Leu Val
1 5
<210> 58
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 58
Gly Met Ala Val Val Phe Ile Asn Val
1 5
<210> 59
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 59
Gly Met Ala Val Val Phe Ile Glu Val
1 5
<210> 60
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 60
Leu Leu Leu Thr Thr Leu Leu Ala Val
1 5
<210> 61
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 61
Ala Leu Leu Thr Thr Leu Leu Leu Val
1 5
<210> 62
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 62
Ala Leu Leu Thr Thr Leu Leu Gly Leu
1 5
<210> 63
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 63
Lys Ile Ile Gly Ile Ile Leu Ala Val
1 5
<210> 64
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 64
Tyr Leu Val Ala Ile Leu Leu Leu Val
1 5
<210> 65
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 65
Thr Leu Val Ala Ile Leu Leu Asn Val
1 5
<210> 66
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 66
Met Leu Val Ala Ile Leu Leu Ala Val
1 5
<210> 67
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 67
Leu Leu Val Ala Ile Leu Leu Ser Val
1 5
<210> 68
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 68
Phe Leu Val Ala Ile Leu Leu Asn Leu
1 5
<210> 69
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 69
Ala Met Val Ala Ile Leu Leu Asn Ile
1 5
<210> 70
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 70
Ala Leu Val Ala Ile Leu Leu Ala Ile
1 5
<210> 71
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 71
Leu Leu Ser Asp Val Gly Thr Leu Leu
1 5
<210> 72
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 72
Phe Leu Ser Thr Tyr Leu Leu Pro Met
1 5
<210> 73
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 73
Ala Leu Leu Glu Glu Tyr Thr Gly Ile
1 5
<210> 74
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 74
Ser Leu Leu Cys Ile Val Ile Gly Leu
1 5
<210> 75
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 75
Ile Leu Leu Cys Ile Val Ile Gly Leu
1 5
<210> 76
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 76
Met Leu Val Thr Val Val Leu Thr Val
1 5
<210> 77
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 77
Met Leu Val Thr Val Val Leu Leu Val
1 5
<210> 78
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 78
Leu Leu Val Thr Val Val Leu Pro Val
1 5
<210> 79
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 79
Leu Leu Val Thr Val Val Leu Ala Val
1 5
<210> 80
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 80
Lys Leu Val Thr Val Val Leu Ala Val
1 5
<210> 81
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 81
Ile Leu Val Thr Val Val Leu Gly Ile
1 5
<210> 82
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 82
Leu Met Ala Leu Val Leu Met Leu Val
1 5
<210> 83
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 83
Gly Leu Thr Phe Trp Asn Pro Asn Val
1 5
<210> 84
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 84
Phe Met Leu Leu Leu Ser Ala Ala Ala
1 5
<210> 85
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 85
Phe Leu Leu Leu Leu Ser Ala Ala Leu
1 5
<210> 86
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 86
Tyr Leu Leu Ser Ala Ala Leu Thr Leu
1 5
<210> 87
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 87
Tyr Leu Leu Ser Ala Ala Leu Thr Ile
1 5
<210> 88
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 88
Val Leu Leu Ser Ala Ala Leu Leu Leu
1 5
<210> 89
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 89
Val Leu Leu Ser Ala Ala Leu Phe Leu
1 5
<210> 90
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 90
Ser Leu Leu Ser Ala Ala Leu Thr Val
1 5
<210> 91
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 91
Arg Leu Leu Ser Ala Ala Leu Ala Leu
1 5
<210> 92
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 92
Leu Met Leu Ser Ala Ala Leu Leu Leu
1 5
<210> 93
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 93
Leu Met Leu Ser Ala Ala Leu Cys Val
1 5
<210> 94
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 94
Leu Met Leu Ser Ala Ala Leu Ala Val
1 5
<210> 95
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 95
Leu Leu Leu Ser Ala Ala Leu Trp Val
1 5
<210> 96
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 96
Leu Leu Leu Ser Ala Ala Leu Thr Val
1 5
<210> 97
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 97
Leu Leu Leu Ser Ala Ala Leu Ser Val
1 5
<210> 98
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 98
Leu Leu Leu Ser Ala Ala Leu Met Ile
1 5
<210> 99
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 99
Leu Leu Leu Ser Ala Ala Leu Leu Leu
1 5
<210> 100
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 100
Leu Leu Leu Ser Ala Ala Leu Cys Val
1 5
<210> 101
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 101
Leu Leu Leu Ser Ala Ala Leu Ala Leu
1 5
<210> 102
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 102
Lys Leu Leu Ser Ala Ala Leu Ser Val
1 5
<210> 103
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 103
Ile Leu Leu Ser Ala Ala Leu Leu Leu
1 5
<210> 104
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 104
Ile Leu Leu Ser Ala Ala Leu Gly Ile
1 5
<210> 105
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 105
Phe Leu Leu Ser Ala Ala Leu Val Val
1 5
<210> 106
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 106
Phe Leu Leu Ser Ala Ala Leu Ile Leu
1 5
<210> 107
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 107
Ala Leu Leu Ser Ala Ala Leu Met Leu
1 5
<210> 108
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 108
Ala Leu Leu Ser Ala Ala Leu Leu Val
1 5
<210> 109
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 109
Ala Leu Leu Ser Ala Ala Leu Leu Leu
1 5
<210> 110
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 110
Tyr Met Ala Gly Ala Met Val Gln Leu
1 5
<210> 111
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 111
Arg Met Ala Gly Ala Met Val Pro Val
1 5
<210> 112
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 112
Arg Leu Ala Gly Ala Met Val Asp Val
1 5
<210> 113
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 113
Met Met Thr Gly Phe Val Val Leu Met
1 5
<210> 114
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 114
Tyr Leu Ala Ser Ser Glu Thr His Val
1 5
<210> 115
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 115
Ser Met Leu Ser Ile Gly Gly Tyr Val
1 5
<210> 116
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 116
Leu Leu Ile Tyr Ser Phe Ala Arg Val
1 5
<210> 117
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 117
Lys Leu Ile His Glu Leu Ala Glu Val
1 5
<210> 118
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 118
Ile Leu Ile His Glu Leu Ala His Ile
1 5
<210> 119
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 119
His Leu Trp Ala Gly Val Val Leu Val
1 5
<210> 120
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 120
Arg Leu Trp Asp Phe Thr Val Gly Val
1 5
<210> 121
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 121
Val Leu Ala Ser Ser Ile Leu Tyr Ile
1 5
<210> 122
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 122
Ser Leu Ala Ser Ser Ile Leu Gln Leu
1 5
<210> 123
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 123
Ala Leu Ala Ser Ser Ile Leu Gln Leu
1 5
<210> 124
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 124
Phe Leu Ala Val Ser Leu Ala Pro Leu
1 5
<210> 125
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 125
Ile Leu Val Gly Leu Phe Val Pro Val
1 5
<210> 126
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 126
Ile Leu Val Gly Leu Phe Val Ala Val
1 5
<210> 127
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 127
Tyr Leu Phe Val Leu Leu Ala Gly Ile
1 5
<210> 128
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 128
Ser Leu Phe Val Leu Leu Ala Ala Val
1 5
<210> 129
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 129
Lys Leu Phe Val Leu Leu Ala Leu Val
1 5
<210> 130
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 130
Gly Ile Tyr Asp Phe Phe Val Lys Val
1 5
<210> 131
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 131
Thr Ile Met Gly Thr Leu Val Ser Val
1 5
<210> 132
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 132
Arg Val Met Gly Thr Leu Val Gly Ile
1 5
<210> 133
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 133
Thr Leu Ala Glu Gly Leu Ala Leu Ala
1 5
<210> 134
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 134
Phe Leu Ala Ala Gly Leu Gly Gln Val
1 5
<210> 135
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 135
Val Leu Glu Ser Ile Leu His Pro Val
1 5
<210> 136
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 136
Arg Met Glu Ser Ile Leu His Glu Val
1 5
<210> 137
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 137
Ala Leu Leu Ala Ala Leu Cys Tyr Val
1 5
<210> 138
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 138
Tyr Leu Leu Ala Leu Leu Ala Trp Leu
1 5
<210> 139
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 139
Val Leu Leu Ala Leu Leu Ala Glu Val
1 5
<210> 140
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 140
Ser Leu Leu Ala Leu Leu Ala Phe Val
1 5
<210> 141
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 141
Arg Leu Leu Ala Leu Leu Ala Ser Val
1 5
<210> 142
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 142
Arg Leu Leu Ala Leu Leu Ala Ala Val
1 5
<210> 143
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 143
Leu Leu Leu Ala Leu Leu Ala Pro Val
1 5
<210> 144
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 144
Ala Leu Leu Ala Leu Leu Ala Ser Val
1 5
<210> 145
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 145
Ile Leu Asp Glu Ala Tyr Val Arg Val
1 5
<210> 146
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 146
Ala Leu Leu Leu Leu Val Val Gly Val
1 5
<210> 147
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 147
Gly Leu Gly Ala Leu Leu Leu Leu Val
1 5
<210> 148
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 148
Tyr Met Gln Glu Ile Leu His Arg Leu
1 5
<210> 149
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 149
Thr Leu Ala Val Val Ser Leu Ala Val
1 5
<210> 150
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 150
Leu Leu Ala Val Val Ser Leu Phe Val
1 5
<210> 151
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 151
Tyr Leu Val Gly Ile Leu Leu Val Leu
1 5
<210> 152
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 152
Lys Val Val Gly Ile Leu Leu Pro Ile
1 5
<210> 153
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 153
Ile Leu Val Gly Ile Leu Leu Val Val
1 5
<210> 154
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 154
Phe Val Val Gly Ile Leu Leu Gln Val
1 5
<210> 155
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 155
Ile Leu Asp Glu Ala Tyr Val Arg Val
1 5
<210> 156
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 156
Leu Leu Ala Leu Leu Pro Pro Glu Val
1 5
<210> 157
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 157
Leu Leu Ala Leu Leu Pro Pro Glu Leu
1 5
<210> 158
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 158
Ala Met Ala Leu Leu Pro Pro Glu Val
1 5
<210> 159
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 159
Ala Leu Ala Leu Leu Pro Pro Pro Val
1 5
<210> 160
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 160
Ile Leu Ile Ser Ala Val Val Gly Leu
1 5
<210> 161
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 161
Ile Val Leu Gly Val Val Phe Gly Val
1 5
<210> 162
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 162
Ile Ile Leu Gly Val Val Phe Gly Leu
1 5
<210> 163
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 163
Tyr Leu Leu Glu Leu Leu Ser Ala Leu
1 5
<210> 164
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 164
Ile Met Trp Gln Phe Leu Leu Glu Leu
1 5
<210> 165
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 165
Tyr Leu Leu Asp Ala Glu Pro Gln Leu
1 5
<210> 166
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 166
Lys Leu Thr Asp Thr Leu Ile Pro Leu
1 5
<210> 167
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 167
Lys Leu Thr Asp Thr Leu Ile Glu Leu
1 5
<210> 168
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 168
Tyr Leu Leu Phe Ala Pro Asn Ala Val
1 5
<210> 169
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 169
Phe Leu Leu Phe Ala Pro Asn Ser Ala
1 5
<210> 170
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 170
Tyr Leu Asp Ala Glu Pro Pro Ala Val
1 5
<210> 171
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 171
Thr Leu Asn Ser Gly Val Tyr Leu Ile
1 5
<210> 172
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 172
Lys Met Asn Ser Gly Val Tyr Val Ile
1 5
<210> 173
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 173
Leu Leu Ile Gly Leu Val Trp Ser Leu
1 5
<210> 174
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 174
Tyr Leu Tyr Asp Leu Leu Leu Thr Val
1 5
<210> 175
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 175
Val Leu Tyr Asp Leu Leu Leu Glu Val
1 5
<210> 176
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 176
Thr Leu Tyr Asp Leu Leu Leu Ser Leu
1 5
<210> 177
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 177
Gln Leu Tyr Asp Leu Leu Leu Val Ala
1 5
<210> 178
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 178
Gln Leu Tyr Asp Leu Leu Leu Ser Leu
1 5
<210> 179
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 179
Gly Leu Tyr Asp Leu Leu Leu Arg Ile
1 5
<210> 180
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 180
Ala Val Tyr Asp Leu Leu Leu Glu Val
1 5
<210> 181
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 181
Ala Leu Tyr Asp Leu Leu Leu Glu Val
1 5
<210> 182
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 182
Val Leu Leu Leu Ile Leu Ser Gly Val
1 5
<210> 183
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 183
Val Leu Leu Leu Ile Leu Ser Glu Val
1 5
<210> 184
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 184
Ser Leu Leu Leu Ile Leu Ser Phe Val
1 5
<210> 185
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 185
Met Leu Leu Leu Ile Leu Ser Tyr Leu
1 5
<210> 186
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 186
Ile Leu Leu Leu Ile Leu Ser Gly Ile
1 5
<210> 187
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 187
Phe Leu Leu Leu Ile Leu Ser Leu Leu
1 5
<210> 188
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 188
Phe Leu Leu Leu Ile Leu Ser Phe Leu
1 5
<210> 189
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 189
Ser Leu Ala Gln Leu Leu Leu Ala Ile
1 5
<210> 190
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 190
Met Leu Ala Gln Leu Leu Leu Thr Val
1 5
<210> 191
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 191
Lys Leu Ile His Leu Met Ala Ala Val
1 5
<210> 192
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 192
Phe Leu Asp Lys Ile Thr Asp Leu Val
1 5
<210> 193
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 193
Phe Leu Val Glu Asp Glu Thr Val Ile
1 5
<210> 194
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 194
Ala Val Phe Arg Val Leu Ile Pro Val
1 5
<210> 195
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 195
Leu Leu Ser Ala Val Leu Ala Leu Val
1 5
<210> 196
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 196
Leu Leu Ser Ala Val Leu Ala Leu Ala
1 5
<210> 197
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 197
Gly Ile Ser Ala Val Leu Ala Leu Val
1 5
<210> 198
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 198
Asn Leu Trp Ala Gly Gly Phe Phe Leu
1 5
<210> 199
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 199
Tyr Leu Ala Leu Leu Val Met Leu Leu
1 5
<210> 200
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 200
Leu Leu Ala Leu Leu Val Met Ala Val
1 5
<210> 201
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 201
Ala Leu Ala Leu Leu Val Met Ala Val
1 5
<210> 202
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 202
Thr Met Leu Ser Cys Leu Leu His Leu
1 5
<210> 203
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 203
Met Leu Leu Ser Cys Leu Leu Phe Met
1 5
<210> 204
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 204
Leu Leu Leu Ser Cys Leu Leu Pro Leu
1 5
<210> 205
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 205
Leu Leu Leu Ser Cys Leu Leu His Leu
1 5
<210> 206
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 206
Ile Leu Leu Ser Cys Leu Leu Leu Leu
1 5
<210> 207
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 207
Phe Leu Leu Ser Cys Leu Leu Cys Leu
1 5
<210> 208
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 208
Ala Leu Leu Ser Cys Leu Leu Met Leu
1 5
<210> 209
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 209
Tyr Val Ala Ala Thr Leu Phe Ala Leu
1 5
<210> 210
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 210
Tyr Leu Tyr Ser Glu Ile Pro Asp Ile
1 5
<210> 211
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 211
Tyr Met Ala Ser Thr Leu Val His Leu
1 5
<210> 212
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 212
Gln Met Ala Ser Thr Leu Val Tyr Leu
1 5
<210> 213
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 213
Tyr Gln Phe Asp Lys Ile Tyr Ser Ile
1 5
<210> 214
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 214
Met Met Phe Trp Leu Leu Leu Val Val
1 5
<210> 215
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 215
Gly Met Leu Trp Glu Ile Phe Gly Val
1 5
<210> 216
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 216
Ala Met Lys Asp Gly Leu Pro Glu Val
1 5
<210> 217
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 217
Thr Leu Leu Asp Ile Ser Phe Ala Ala
1 5
<210> 218
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 218
Asn Met Leu Asp Ile Ser Phe Tyr Leu
1 5
<210> 219
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 219
Ile Leu Asp Ile Ser Phe Pro Leu Val
1 5
<210> 220
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 220
Leu Met Asp Leu Ser Thr Thr Glu Val
1 5
<210> 221
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 221
Arg Leu Ser Ser Tyr Leu Val Glu Ile
1 5
<210> 222
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 222
Met Val Ser Ser Tyr Leu Val Glu Val
1 5
<210> 223
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 223
Lys Val Ser Ser Tyr Leu Val Glu Val
1 5
<210> 224
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 224
Ile Leu Ser Lys Ile Leu Leu Phe Ala
1 5
<210> 225
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 225
Tyr Gln Leu Ser Tyr Ser Gln Met Val
1 5
<210> 226
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 226
Lys Leu Leu Ser Tyr Ser Gln Glu Leu
1 5
<210> 227
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 227
Lys Ile Ala Glu Leu Pro Phe Pro Leu
1 5
<210> 228
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 228
Tyr Leu Asn Glu Ser Glu Thr Val Leu
1 5
<210> 229
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 229
Met Leu Val Glu Leu Leu Lys Lys Val
1 5
<210> 230
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 230
Lys Leu Val Glu Leu Leu Lys Leu Leu
1 5
<210> 231
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 231
Ala Leu Val Glu Leu Leu Lys Pro Leu
1 5
<210> 232
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 232
Phe Leu Ala Ser Thr Thr Pro Thr Ala
1 5
<210> 233
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 233
Ser Leu Ala Arg Glu Val Ala Ala Val
1 5
<210> 234
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 234
Gly Met Ala Arg Glu Val Ala Ala Val
1 5
<210> 235
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 235
Trp Leu Leu Ser Leu Ala Phe Leu Leu
1 5
<210> 236
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 236
Ser Leu Leu Ser Leu Ala Phe Ser Ala
1 5
<210> 237
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 237
Leu Leu Leu Ser Leu Ala Phe Ile Leu
1 5
<210> 238
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 238
Lys Leu Asn Pro Ala Gln Gly Tyr Val
1 5
<210> 239
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 239
Lys Leu Trp Gly Leu Ala Thr Leu Ile
1 5
<210> 240
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 240
Val Leu Ala Leu Gly Leu Leu Ala Val
1 5
<210> 241
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 241
Ser Leu Ala Leu Gly Leu Leu Gln Val
1 5
<210> 242
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 242
Ser Leu Ala Leu Gly Leu Leu Leu Val
1 5
<210> 243
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 243
Met Leu Ala Leu Gly Leu Leu Glu Val
1 5
<210> 244
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 244
Gly Leu Ala Leu Gly Leu Leu Phe Val
1 5
<210> 245
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 245
Gly Leu Ala Leu Gly Leu Leu Ala Val
1 5
<210> 246
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 246
Phe Leu Ala Leu Gly Leu Leu Phe Leu
1 5
<210> 247
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 247
Ala Leu Ala Leu Gly Leu Leu Met Val
1 5
<210> 248
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 248
Val Leu Leu Leu Ala Gly Ala Tyr Val
1 5
<210> 249
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 249
Tyr Leu Tyr Thr Phe Leu Ile Val Leu
1 5
<210> 250
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 250
Gly Met Tyr Thr Phe Leu Ile Pro Met
1 5
<210> 251
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 251
Gly Leu Tyr Thr Phe Leu Ile Pro Met
1 5
<210> 252
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 252
Phe Leu Ile Ser Thr Thr Phe Ala Ala
1 5
<210> 253
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 253
Ile Leu Leu Asp Thr Asn Tyr Glu Ile
1 5
<210> 254
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 254
Phe Leu Pro Phe Gly Phe Ile Leu Val
1 5
<210> 255
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 255
Phe Leu Pro Phe Gly Phe Ile Leu Pro Val
1 5 10
<210> 256
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 256
Met Leu Tyr Leu Leu Pro Leu Ser Leu
1 5
<210> 257
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 257
Met Leu Tyr Leu Leu Pro Leu Ala Leu
1 5
<210> 258
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 258
Leu Leu Tyr Leu Leu Pro Leu Phe Leu
1 5
<210> 259
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 259
Ser Met Leu Tyr Asn Leu Leu Ala Leu
1 5
<210> 260
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 260
Ala Met Leu Tyr Asn Leu Leu Ala Leu
1 5
<210> 261
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 261
Ala Leu Leu Tyr Asn Leu Leu Ala Leu
1 5
<210> 262
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 262
Ile Leu Phe Leu Val Leu Gln Arg Val
1 5
<210> 263
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 263
Tyr Leu Val Ala Ala Val Val Leu Leu
1 5
<210> 264
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 264
Tyr Leu Ala Glu Arg Ala Gly His Val
1 5
<210> 265
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 265
Ile Leu Val Pro Leu Phe Phe Thr Leu
1 5
<210> 266
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 266
Gly Leu Val Pro Leu Phe Phe Ala Leu
1 5
<210> 267
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 267
Phe Leu Val Pro Leu Phe Phe Val Val
1 5
<210> 268
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 268
Phe Leu Val Pro Leu Phe Phe Leu Leu
1 5
<210> 269
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 269
Ala Leu Val Pro Leu Phe Phe Ala Leu
1 5
<210> 270
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 270
Tyr Met Leu Pro Leu Leu Ala Gly Ala
1 5
<210> 271
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 271
Tyr Leu Leu Pro Leu Leu Ala Leu Ala
1 5
<210> 272
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 272
Trp Leu Leu Pro Leu Leu Ala Val Val
1 5
<210> 273
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 273
Trp Leu Leu Pro Leu Leu Ala Cys Leu
1 5
<210> 274
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 274
Trp Leu Leu Pro Leu Leu Ala Ala Leu
1 5
<210> 275
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 275
Thr Leu Leu Pro Leu Leu Ala Ala Val
1 5
<210> 276
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 276
Thr Leu Leu Pro Leu Leu Ala Ala Ala
1 5
<210> 277
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 277
Ser Leu Leu Pro Leu Leu Ala Gly Val
1 5
<210> 278
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 278
Arg Leu Leu Pro Leu Leu Ala Val Leu
1 5
<210> 279
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 279
Arg Leu Leu Pro Leu Leu Ala Ala Ile
1 5
<210> 280
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 280
Gln Leu Leu Pro Leu Leu Ala Tyr Val
1 5
<210> 281
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 281
Leu Leu Leu Pro Leu Leu Ala Gly Leu
1 5
<210> 282
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 282
Leu Leu Leu Pro Leu Leu Ala Asp Leu
1 5
<210> 283
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 283
Leu Leu Leu Pro Leu Leu Ala Ala Ala
1 5
<210> 284
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 284
His Val Leu Pro Leu Leu Ala Thr Val
1 5
<210> 285
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 285
His Leu Leu Pro Leu Leu Ala Glu Val
1 5
<210> 286
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 286
Gly Leu Leu Pro Leu Leu Ala Lys Ile
1 5
<210> 287
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 287
Gly Ile Leu Pro Leu Leu Ala Thr Val
1 5
<210> 288
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 288
Tyr Leu Ser Asp Ala Val Glu Ala Val
1 5
<210> 289
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 289
Ile Leu Arg Glu Ala Ala Met Pro Val
1 5
<210> 290
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 290
Phe Leu Ile Pro Ala Pro Glu Ser Leu
1 5
<210> 291
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 291
Phe Leu Leu His Gly Leu Asn Leu Met
1 5
<210> 292
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 292
Tyr Met Ser Ser Leu Pro Gln Gly Leu
1 5
<210> 293
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 293
Tyr Met Ile Leu Gly Val Ala Met Ile
1 5
<210> 294
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 294
Val Leu Ile Leu Gly Val Ala Ala Val
1 5
<210> 295
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 295
Ser Leu Ile Leu Gly Val Ala Ala Val
1 5
<210> 296
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 296
Ile Leu Ile Leu Gly Val Ala Gly Ile
1 5
<210> 297
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 297
Leu Leu Asp Cys Ile Ile Ala Phe Leu
1 5
<210> 298
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 298
Leu Ile Leu Gly Ile Phe Ile Ser Val
1 5
<210> 299
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 299
Tyr Leu Ala Val Leu Gly Ile Ser Leu
1 5
<210> 300
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 300
Val Leu Ala Ala Ile Val Ile Gly Val
1 5
<210> 301
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 301
Leu Leu Ala Cys Ser Leu Ala Met Leu
1 5
<210> 302
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 302
Phe Val Ile Gly Ile Val Ala Leu Val
1 5
<210> 303
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 303
Tyr Val Val Ala Val Pro Thr Pro Val
1 5
<210> 304
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 304
Tyr Ile Val Ala Val Pro Thr Pro Val
1 5
<210> 305
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 305
Phe Ile Val Ala Val Pro Thr Pro Ile
1 5
<210> 306
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 306
Met Leu Lys Glu Leu Ser Pro Glu Leu
1 5
<210> 307
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 307
Phe Leu Lys Glu Leu Ser Pro Gly Leu
1 5
<210> 308
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 308
Phe Val Ala Asp Leu Val Gly His Val
1 5
<210> 309
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 309
Ser Leu Leu Gly Thr Leu Glu Glu Leu
1 5
<210> 310
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 310
Val Met Leu Ser Asp Val Gln Ser Val
1 5
<210> 311
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 311
Arg Leu Leu Ser Asp Val Gln Gly Leu
1 5
<210> 312
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 312
Ser Leu Ile Leu Ile Leu Ser Ser Val
1 5
<210> 313
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 313
Lys Leu Ile Leu Ile Leu Ser Tyr Leu
1 5
<210> 314
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 314
Ala Leu Asp Ala Ile Phe Gly Gly Val
1 5
<210> 315
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 315
Phe Leu Ile Thr Lys Ala Glu Glu Leu
1 5
<210> 316
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 316
Ser Leu Leu Glu Glu Leu Pro Ala Leu
1 5
<210> 317
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 317
Met Thr Leu Glu Glu Leu Pro Phe Leu
1 5
<210> 318
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 318
Ile Ile Leu Glu Tyr Ile Ala Leu Leu
1 5
<210> 319
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 319
Tyr Met Val Phe Gly Ile Glu Gly Ile
1 5
<210> 320
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 320
Ser Leu Ser Ser Ser Ser Pro Leu Val
1 5
<210> 321
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 321
Lys Leu Asp Glu Leu Ala His Phe Leu
1 5
<210> 322
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 322
Phe Val Leu Glu His Val Val Pro Leu
1 5
<210> 323
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 323
Tyr Leu Leu Gly Val Leu Leu Leu Leu
1 5
<210> 324
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 324
Tyr Ile Leu Gly Val Leu Leu Thr Ala
1 5
<210> 325
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 325
Met Leu Leu Gly Val Leu Leu Leu Leu
1 5
<210> 326
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 326
Met Ile Leu Gly Val Leu Leu Phe Leu
1 5
<210> 327
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 327
Leu Met Leu Gly Val Leu Leu Leu Ala
1 5
<210> 328
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 328
Leu Leu Leu Gly Val Leu Leu Leu Leu
1 5
<210> 329
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 329
Lys Leu Leu Gly Val Leu Leu Leu Val
1 5
<210> 330
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 330
Ile Ile Leu Gly Val Leu Leu Ala Val
1 5
<210> 331
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 331
Phe Ile Leu Gly Val Leu Leu Ser Leu
1 5
<210> 332
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 332
Ala Leu Leu Gly Val Leu Leu Leu Leu
1 5
<210> 333
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 333
Ala Leu Leu Gly Val Leu Leu Leu Ala
1 5
<210> 334
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 334
Ala Ile Leu Gly Val Leu Leu Leu Val
1 5
<210> 335
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 335
Ile Leu Ala Ala Gly Val Pro Glu Leu
1 5
<210> 336
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 336
Tyr Val Ser Asp Ile Leu Ser Tyr Val
1 5
<210> 337
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 337
Tyr Ile Ser Asp Ile Leu Ser Tyr Val
1 5
<210> 338
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 338
Val Ile Ser Asp Ile Leu Ser Phe Leu
1 5
<210> 339
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 339
Ser Met Ser Asp Ile Leu Ser Arg Leu
1 5
<210> 340
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 340
Phe Val Ser Asp Ile Leu Ser Ala Ala
1 5
<210> 341
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 341
Trp Leu Leu Ala Ala Ser Val Thr Val
1 5
<210> 342
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 342
Ile Leu Leu Ala Ala Ser Val Leu Val
1 5
<210> 343
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 343
Phe Leu Leu Ala Ala Ser Val Met Met
1 5
<210> 344
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 344
Ala Leu Leu Ala Ala Ser Val Leu Val
1 5
<210> 345
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 345
Leu Leu Ala Ala Ser Val Ala Leu Leu
1 5
<210> 346
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 346
Leu Leu Ala Ala Ser Val Ala Gly Val
1 5
<210> 347
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 347
Ile Leu Ala Ala Ser Val Ala Ala Val
1 5
<210> 348
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 348
Gly Leu Ala Ala Ser Val Ala Pro Val
1 5
<210> 349
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 349
Ala Leu Leu Arg Lys Val Ala Glu Val
1 5
<210> 350
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 350
Ser Leu Pro Glu Leu Tyr Ala Trp Ile
1 5
<210> 351
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 351
Ile Leu Tyr Gly Lys Ile Lys Tyr Leu
1 5
<210> 352
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 352
Met Leu Leu Gly Leu Ala Ala Phe Leu
1 5
<210> 353
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 353
Gly Leu Leu Gly Leu Ala Ala Phe Leu
1 5
<210> 354
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 354
Ala Leu Leu Gly Leu Ala Ala Phe Leu
1 5
<210> 355
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 355
Tyr Leu Asp Glu Val Lys Ser Leu Val
1 5
<210> 356
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 356
Tyr Leu Asp Glu Val Lys Ser Leu Ile
1 5
<210> 357
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 357
Tyr Leu Asp Glu Val Lys Ser Ile Leu
1 5
<210> 358
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 358
Leu Leu Asp Glu Val Lys Ser Leu Val
1 5
<210> 359
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 359
Phe Ile Leu Leu Ser Leu Ser Pro Val
1 5
<210> 360
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 360
Arg Leu Phe Leu Phe Ser Val Leu Val
1 5
<210> 361
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 361
Ala Leu Thr Val Tyr Leu Val Tyr Leu
1 5
<210> 362
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 362
Arg Leu Leu Phe Val Ala Val Pro Ile
1 5
<210> 363
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 363
Arg Leu Leu Phe Val Ala Val Gly Leu
1 5
<210> 364
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 364
Phe Leu Leu Phe Val Ala Val Ser Val
1 5
<210> 365
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 365
Phe Ile Ser Leu Phe Leu Phe Ser Val
1 5
<210> 366
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 366
Leu Ile Ala Gly Phe Val Ala Leu Val
1 5
<210> 367
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 367
Tyr Leu Leu Val Leu Met Ala Ser Ile
1 5
<210> 368
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 368
Tyr Leu Val Gly Ile Leu Leu Val Leu
1 5
<210> 369
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 369
Lys Ile Val Gly Ile Leu Leu Gly Ile
1 5
<210> 370
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 370
Lys Ile Val Gly Ile Leu Leu Ala Val
1 5
<210> 371
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 371
Ile Leu Val Gly Ile Leu Leu Val Val
1 5
<210> 372
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 372
Gly Ile Val Gly Ile Leu Leu Asn Val
1 5
<210> 373
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 373
Gly Ile Val Gly Ile Leu Leu Ala Val
1 5
<210> 374
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 374
Leu Leu Ala Val Val Leu Ala Phe Val
1 5
<210> 375
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 375
Leu Leu Ala Val Val Leu Ala Ala Val
1 5
<210> 376
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 376
Gly Val Leu Asp Gly Thr Ala Thr Val
1 5
<210> 377
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 377
Ala Leu Ala Asp Thr Asn Ser Tyr Val
1 5
<210> 378
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 378
Ala Leu Ala Asp Thr Asn Ser Tyr Leu
1 5
<210> 379
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 379
Ala Met Gln Ala Ala Ile Pro Met Leu
1 5
<210> 380
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 380
Ile Val Leu Asp Gly Leu Asp Leu Val
1 5
<210> 381
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 381
Ala Val Leu Asp Gly Leu Asp Pro Val
1 5
<210> 382
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 382
Tyr Leu Leu Ala Leu Leu Pro Leu Leu
1 5
<210> 383
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 383
Tyr Leu Leu Ala Leu Leu Pro Ile Leu
1 5
<210> 384
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 384
Gln Leu Leu Ala Leu Leu Pro Gly Val
1 5
<210> 385
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 385
Leu Leu Leu Ala Leu Leu Pro Thr Val
1 5
<210> 386
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 386
Phe Leu Arg Glu Leu Leu Cys Gln Leu
1 5
<210> 387
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 387
Leu Leu Tyr Pro Val Pro Leu Gly Val
1 5
<210> 388
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 388
Ala Leu Phe Leu Leu Ser Tyr Thr Val
1 5
<210> 389
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 389
Tyr Val Leu Ser Leu Leu Leu Thr Leu
1 5
<210> 390
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 390
Val Leu Leu Ser Leu Leu Leu Ile Val
1 5
<210> 391
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 391
Ser Leu Leu Ser Leu Leu Leu Ile Leu
1 5
<210> 392
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 392
Arg Leu Leu Ser Leu Leu Leu Val Leu
1 5
<210> 393
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 393
Leu Val Leu Ser Leu Leu Leu Leu Val
1 5
<210> 394
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 394
Lys Leu Leu Ser Leu Leu Leu Val Leu
1 5
<210> 395
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 395
Ile Leu Leu Ser Leu Leu Leu Val Leu
1 5
<210> 396
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 396
Phe Thr Leu Ser Leu Leu Leu Thr Leu
1 5
<210> 397
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 397
Ala Leu Leu Ser Leu Leu Leu Ile Leu
1 5
<210> 398
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 398
Val Leu Phe Val Leu Ser Leu Phe Leu
1 5
<210> 399
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 399
Ile Leu Phe Val Leu Ser Leu Gln Leu
1 5
<210> 400
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 400
Leu Leu Leu Glu Lys Gln Ala Glu Val
1 5
<210> 401
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 401
Val Leu Ser Glu Leu Lys Leu Ala Val
1 5
<210> 402
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 402
Arg Met Ile Glu His Val Leu Thr Val
1 5
<210> 403
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 403
Gln Ile Phe Asp Arg Leu Ile Pro Ile
1 5
<210> 404
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 404
Gly Val Phe Asp Arg Leu Ile Pro Ile
1 5
<210> 405
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 405
Tyr Leu Lys Glu Gln Phe Gln Thr Leu
1 5
<210> 406
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 406
Ser Leu Leu Asp Ser Ala Phe Leu Leu
1 5
<210> 407
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 407
Met Leu Ser Leu Val Phe Ser Leu Ile
1 5
<210> 408
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 408
Leu Met Ser Leu Val Phe Ser Leu Val
1 5
<210> 409
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 409
Trp Met Gln Ile Leu Pro Tyr Gln Val
1 5
<210> 410
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 410
Met Met Thr Gly Phe Thr Phe Gly Val
1 5
<210> 411
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 411
Met Leu Leu Leu Leu Val Asn Leu Val
1 5
<210> 412
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 412
Val Leu Phe Gly Leu Leu Thr Phe Leu
1 5
<210> 413
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 413
Gln Leu Phe Gly Leu Leu Thr Asp Val
1 5
<210> 414
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 414
Phe Leu Phe Gly Leu Leu Thr Met Ile
1 5
<210> 415
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 415
Phe Leu Phe Gly Leu Leu Thr Asp Ala
1 5
<210> 416
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 416
Thr Leu Leu Leu Ser Leu Phe Leu Leu
1 5
<210> 417
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 417
Phe Ile Leu Leu Ser Leu Phe Met Leu
1 5
<210> 418
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 418
Ile Leu Leu Pro Pro Pro Pro Val Val
1 5
<210> 419
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 419
Val Leu Leu Thr Leu Ile Phe Ala Leu
1 5
<210> 420
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 420
Arg Leu Leu Thr Leu Ile Phe Thr Leu
1 5
<210> 421
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 421
Gln Leu Leu Thr Leu Ile Phe Tyr Leu
1 5
<210> 422
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 422
Leu Leu Leu Thr Leu Ile Phe Pro Ile
1 5
<210> 423
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 423
Phe Leu Leu Thr Leu Ile Phe Ser Leu
1 5
<210> 424
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 424
Val Met Val Ala Ile Tyr Phe Thr Leu
1 5
<210> 425
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 425
Leu Leu Gly Ala Leu Leu Pro Ala Val
1 5
<210> 426
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 426
Ile Leu Gly Ala Leu Leu Pro Leu Leu
1 5
<210> 427
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 427
Ser Val Ala Ala Phe Pro Val Thr Val
1 5
<210> 428
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 428
Leu Leu Leu Ser Leu Phe Cys Leu Ile
1 5
<210> 429
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 429
Lys Leu Leu Ser Leu Phe Cys Thr Leu
1 5
<210> 430
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 430
Phe Leu Leu Ser Leu Phe Cys Ile Ala
1 5
<210> 431
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 431
Ile Leu Leu Gly Val Gly Phe Gly Ile
1 5
<210> 432
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 432
Ala Leu Leu Gly Val Gly Phe Gly Ile
1 5
<210> 433
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 433
Arg Leu Ile Asp Glu Phe Gln Ser Val
1 5
<210> 434
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 434
Phe Leu Glu Ser Val Ile Thr Thr Val
1 5
<210> 435
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 435
Gly Leu Phe Gly Val Leu Ile Gly Val
1 5
<210> 436
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 436
Ala Met Phe Gly Val Leu Ile Ser Val
1 5
<210> 437
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 437
Phe Ile Asp Phe Leu Leu Ser Glu Val
1 5
<210> 438
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 438
Gly Leu Phe Met Val Ile Ala Gly Val
1 5
<210> 439
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 439
Phe Leu Phe Met Val Ile Ala Phe Ala
1 5
<210> 440
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 440
His Leu Pro Tyr Leu Leu Phe Leu Leu
1 5
<210> 441
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 441
Thr Leu Thr Ala Cys Leu Val Gly Val
1 5
<210> 442
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 442
Met Leu Ser Glu Lys Met Val Gln Leu
1 5
<210> 443
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 443
Asn Leu Phe Asp Leu Ser Leu Val Ala
1 5
<210> 444
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 444
Gly Leu Phe Asp Leu Ser Leu Arg Val
1 5
<210> 445
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 445
Ala Leu Phe Asp Leu Ser Leu Pro Ile
1 5
<210> 446
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 446
Thr Leu Pro Ala Val Met Ala Glu Val
1 5
<210> 447
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 447
Leu Leu Ala Glu Pro Gln Ala Ser Leu
1 5
<210> 448
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 448
Ile Leu Ala Glu Pro Gln Ala Leu Val
1 5
<210> 449
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 449
Phe Ile Ala Glu Pro Gln Ala Ala Leu
1 5
<210> 450
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 450
Leu Leu Phe Leu Leu Ser Ala Leu Leu
1 5
<210> 451
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 451
Lys Met Leu Thr Phe Leu Tyr Thr Ala
1 5
<210> 452
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 452
Ala Val Leu His Ala Ile Tyr Gly Val
1 5
<210> 453
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 453
His Leu Phe Ala Val Leu His Ala Val
1 5
<210> 454
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 454
Ser Val Ile Ala Ala Ile Val Leu Val
1 5
<210> 455
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 455
Phe Val Ile Ala Ala Ile Val Cys Val
1 5
<210> 456
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 456
Phe Ile Ile Ala Ala Ile Val Ala Val
1 5
<210> 457
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 457
Ala Val Ile Ala Ala Ile Val Gly Val
1 5
<210> 458
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 458
Tyr Ile Ala Ala Ile Ile Ala Glu Ala
1 5
<210> 459
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 459
Phe Val Ala Ala Ile Ile Ala Ser Leu
1 5
<210> 460
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 460
Phe Ile Ala Ala Ile Ile Ala Pro Ile
1 5
<210> 461
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 461
Gly Leu Phe Lys Ser Ile Leu Phe Leu
1 5
<210> 462
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 462
Met Leu Leu Gly Thr Ile His Gly Val
1 5
<210> 463
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 463
Leu Leu Ser Phe Phe Phe Ala Met Leu
1 5
<210> 464
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 464
Leu Leu Ser Phe Phe Phe Ala Ala Leu
1 5
<210> 465
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 465
Phe Leu Ser Phe Phe Phe Ala Ala Met
1 5
<210> 466
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 466
Phe Leu Ala Val Phe Leu Pro Val Leu
1 5
<210> 467
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 467
Ser Leu Leu Leu Gly Thr Ile Leu Val
1 5
<210> 468
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 468
Ile Leu Leu Leu Gly Thr Ile Leu Leu
1 5
<210> 469
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 469
Arg Leu Ser Leu Ile Val Ala Leu Val
1 5
<210> 470
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 470
Arg Leu Ser Leu Ile Val Ala Phe Val
1 5
<210> 471
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 471
Met Ile Ser Pro Asn Leu Phe Arg Val
1 5
<210> 472
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 472
Leu Leu Asp His Val Leu Ile Ala Val
1 5
<210> 473
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 473
Arg Leu Ile Asp Glu His Leu Val Val
1 5
<210> 474
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 474
Thr Leu Ser Glu Val Leu Glu Tyr Leu
1 5
<210> 475
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 475
Phe Leu Leu Arg Pro Asp Thr Phe Leu
1 5
<210> 476
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 476
Leu Met Met Thr Ile Ile Asn Gln Val
1 5
<210> 477
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 477
Leu Leu Met Thr Ile Ile Asn Gln Val
1 5
<210> 478
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 478
Phe Leu Met Thr Ile Ile Asn Gln Val
1 5
<210> 479
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 479
Arg Leu Ala Gly Ser Val Ala Gly Val
1 5
<210> 480
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 480
Lys Leu Ala Gly Ser Val Ala Gly Val
1 5
<210> 481
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 481
Leu Leu Met Met Thr Ile Ile Thr Val
1 5
<210> 482
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 482
Ala Met Leu Ser Ser Leu Ala Gly Val
1 5
<210> 483
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 483
Tyr Val Phe Thr Met Leu Ser Ala Val
1 5
<210> 484
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 484
Tyr Leu Ala Gly Val Ile Ile Leu Ile
1 5
<210> 485
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 485
Met Leu Ala Gly Val Ile Ile Tyr Ile
1 5
<210> 486
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 486
Met Leu Ala Gly Val Ile Ile Gly Ile
1 5
<210> 487
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 487
Leu Leu Ala Gly Val Ile Ile Thr Ile
1 5
<210> 488
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 488
Leu Leu Ala Gly Val Ile Ile Gly Ile
1 5
<210> 489
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 489
Gly Leu Ala Gly Val Ile Ile Thr Ile
1 5
<210> 490
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 490
Gly Leu Ala Gly Val Ile Ile Ala Val
1 5
<210> 491
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 491
Val Met Leu Phe Gly Val Phe Met Val
1 5
<210> 492
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 492
Val Leu Leu Phe Gly Val Phe Leu Val
1 5
<210> 493
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 493
Ile Leu Leu Phe Gly Val Phe Met Val
1 5
<210> 494
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 494
Phe Ile Leu Phe Gly Val Phe Met Leu
1 5
<210> 495
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 495
Val Leu Phe Gly Val Phe Leu Gly Val
1 5
<210> 496
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 496
Gly Met Phe Gly Val Phe Leu Thr Leu
1 5
<210> 497
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 497
Phe Leu Phe Gly Val Phe Leu Ala Met
1 5
<210> 498
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 498
Val Leu Asp Thr Ala Ile Ile Tyr Ile
1 5
<210> 499
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 499
Lys Leu Asp Thr Ala Ile Ile His Val
1 5
<210> 500
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 500
Leu Ile Ser Ser Phe Ala Phe Leu Val
1 5
<210> 501
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 501
Leu Ile Ser Ser Phe Ala Phe Leu Leu
1 5
<210> 502
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 502
Phe Met Leu Arg Leu Ile Ile Asn Leu
1 5
<210> 503
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 503
Ala Leu Ala Ile Ala Leu Phe Pro Val
1 5
<210> 504
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 504
Ala Leu Trp Leu His Thr Ser Phe Ala
1 5
<210> 505
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 505
Thr Met Phe Gly Tyr Thr Val Phe Leu
1 5
<210> 506
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 506
Tyr Leu Ala Gly Ile Val Phe Thr Leu
1 5
<210> 507
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 507
Leu Met Leu Leu Phe Ala Tyr Tyr Leu
1 5
<210> 508
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 508
Tyr Leu Phe Ala Tyr Val Leu Ile Val
1 5
<210> 509
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 509
Thr Leu Phe Ala Tyr Val Leu Gly Leu
1 5
<210> 510
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 510
Gly Leu Leu Phe Ala Tyr Val Glu Val
1 5
<210> 511
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 511
Lys Ile Leu Tyr Ser Leu Val Glu Val
1 5
<210> 512
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 512
Phe Leu Leu Leu Val Asn Leu Leu Val
1 5
<210> 513
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 513
Val Ile Ala Asp Val Ile Ala Leu Leu
1 5
<210> 514
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 514
Gln Ile Ala Asp Val Ile Ala Phe Leu
1 5
<210> 515
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 515
Leu Val Ala Asp Val Ile Ala Ser Val
1 5
<210> 516
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 516
Leu Ile Ala Asp Val Ile Ala Leu Leu
1 5
<210> 517
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 517
Leu Leu Tyr Ser Leu Val Phe Phe Leu
1 5
<210> 518
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 518
Phe Leu Val Lys Ile Asn Thr Asn Ile
1 5
<210> 519
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 519
Lys Leu Asp Ser Leu Gly Phe Thr Leu
1 5
<210> 520
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 520
Lys Leu Asp Ser Leu Gly Phe Ser Leu
1 5
<210> 521
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 521
Phe Leu Asp Ser Leu Gly Phe Ser Leu
1 5
<210> 522
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 522
Phe Met Arg Asp Glu Phe Pro Asp Val
1 5
<210> 523
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 523
Phe Leu Arg Asp Glu Phe Pro Glu Ala
1 5
<210> 524
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 524
Ser Met Glu Glu Leu Leu Trp Phe Val
1 5
<210> 525
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 525
Tyr Leu Leu Ala Gly Leu Val Leu Leu
1 5
<210> 526
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 526
Tyr Leu Leu Ala Gly Leu Val Leu Ile
1 5
<210> 527
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 527
Trp Leu Val Gly Ala Val Leu Thr Leu
1 5
<210> 528
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 528
Leu Leu Val Gly Ala Val Leu Thr Val
1 5
<210> 529
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 529
Ala Leu Val Gly Ala Val Leu Thr Val
1 5
<210> 530
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 530
Ala Leu Val Gly Ala Val Leu Leu Val
1 5
<210> 531
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 531
Cys Leu Ser Asp Tyr Val Ile Pro Val
1 5
<210> 532
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 532
Lys Leu Ala Gly Leu Val Ser Ser Val
1 5
<210> 533
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 533
Gly Met Ser Pro Ala Ser Phe Phe Ala
1 5
<210> 534
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 534
Ala Leu Gly Ala Val Leu Thr Ala Val
1 5
<210> 535
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 535
Tyr Leu Thr Ala Leu Leu Ala Glu Met
1 5
<210> 536
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 536
Val Leu Thr Ala Leu Leu Ala Ala Val
1 5
<210> 537
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 537
Arg Leu Thr Ala Leu Leu Ala Ala Val
1 5
<210> 538
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 538
Gly Leu Thr Ala Leu Leu Ala Pro Val
1 5
<210> 539
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 539
Phe Leu Thr Ala Leu Leu Ala Thr Val
1 5
<210> 540
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 540
Thr Leu Thr Glu Ser Leu Leu Tyr Leu
1 5
<210> 541
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 541
Lys Leu Thr Glu Ser Leu Leu Thr Ile
1 5
<210> 542
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 542
Ile Leu Thr Glu Ser Leu Leu Phe Leu
1 5
<210> 543
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 543
Arg Leu Ala Leu Leu Ser Pro Tyr Ile
1 5
<210> 544
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 544
Ser Ile Leu Gly Phe Ile Ile Ala Ala
1 5
<210> 545
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 545
Leu Ile Leu Gly Phe Ile Ile Ala Val
1 5
<210> 546
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 546
Phe Val Leu Gly Phe Ile Ile Thr Ile
1 5
<210> 547
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 547
Phe Ile Leu Gly Phe Ile Ile Thr Ile
1 5
<210> 548
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 548
Ser Leu Ser Gly Leu Leu Ser Gly Val
1 5
<210> 549
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 549
Phe Leu Ser Gly Leu Leu Ser Ala Leu
1 5
<210> 550
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 550
Ile Leu Pro Leu Ile Leu Ile Thr Val
1 5
<210> 551
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 551
Met Leu Gly Phe Ile Ile Ala Phe Leu
1 5
<210> 552
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 552
Leu Leu Gly Phe Ile Ile Ala Glu Val
1 5
<210> 553
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 553
Ile Leu Gly Phe Ile Ile Ala Ala Val
1 5
<210> 554
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 554
Phe Leu Gly Phe Ile Ile Ala Asp Val
1 5
<210> 555
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 555
Met Ile Ile Thr Val Leu Leu Leu Val
1 5
<210> 556
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 556
Phe Ile Ile Thr Val Leu Leu Gly Leu
1 5
<210> 557
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 557
Tyr Gln Ile Gly Asp Ser Val Leu Leu
1 5
<210> 558
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 558
Met Leu Ser Ser Leu Ile Ile Pro Leu
1 5
<210> 559
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 559
Ile Leu Ile Asp Gly Ala Tyr Thr Val
1 5
<210> 560
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 560
Tyr Leu Leu Glu Glu Gly Ser Ser Val
1 5
<210> 561
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 561
Tyr Met Phe Gly Phe Thr Leu Thr Met
1 5
<210> 562
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 562
Tyr Leu Phe Gly Phe Thr Leu Gly Met
1 5
<210> 563
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 563
Val Leu Phe Gly Phe Thr Leu Ser Ile
1 5
<210> 564
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 564
Arg Met Phe Gly Phe Thr Leu Met Leu
1 5
<210> 565
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 565
Leu Met Phe Gly Phe Thr Leu Arg Thr
1 5
<210> 566
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 566
Tyr Leu Leu Phe Gly Phe Thr Arg Val
1 5
<210> 567
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 567
Val Leu Gly Pro Leu Ala Ala Leu Val
1 5
<210> 568
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 568
Ile Leu Gly Pro Leu Ala Ala Trp Leu
1 5
<210> 569
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 569
Ser Leu Asn Ala Leu Leu Pro Tyr Val
1 5
<210> 570
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 570
Met Met Ile Pro Gln Val Ala Thr Leu
1 5
<210> 571
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 571
Met Met Ile Pro Gln Val Ala Thr Ile
1 5
<210> 572
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 572
Tyr Leu Ser Asp Ile Gln Asn Ala Ile
1 5
<210> 573
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 573
Val Met Ser Asp Ile Gln Asn Arg Val
1 5
<210> 574
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 574
Tyr Gln Ala Val Val Leu Pro Gly Leu
1 5
<210> 575
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 575
Leu Leu Leu Glu Gln Phe Leu Ser Val
1 5
<210> 576
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 576
Leu Leu Leu Glu Gln Phe Leu Ala Ile
1 5
<210> 577
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 577
Ala Leu Leu Glu Gln Phe Leu Thr Ala
1 5
<210> 578
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 578
Gly Val Ser Gly Tyr Ile Ser Pro Val
1 5
<210> 579
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 579
Lys Leu Thr Asp Ile Ser Ser Leu Val
1 5
<210> 580
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 580
Tyr Leu Leu Ser Asn Phe Tyr Thr Val
1 5
<210> 581
<211> 9
<212> PRT
<213> Homo sapiens
<400> 581
Phe Leu Phe Leu Leu Phe Phe Trp Leu
1 5
<210> 582
<211> 9
<212> PRT
<213> Homo sapiens
<400> 582
Ser Leu Ser Leu Gly Phe Leu Phe Leu
1 5
<210> 583
<211> 9
<212> PRT
<213> Homo sapiens
<400> 583
Leu Ser Leu Gly Phe Leu Phe Leu Leu
1 5
<210> 584
<211> 9
<212> PRT
<213> Homo sapiens
<400> 584
Tyr Thr Ser Asn Asp Ser Tyr Ile Val
1 5
<210> 585
<211> 9
<212> PRT
<213> Homo sapiens
<400> 585
Ile Leu Ile Asp Ser Gly Ala Asp Ile
1 5
<210> 586
<211> 9
<212> PRT
<213> Homo sapiens
<400> 586
Ser Leu Phe Glu Ser Ser Ala Lys Ile
1 5
<210> 587
<211> 9
<212> PRT
<213> Homo sapiens
<400> 587
Ser Leu Thr Pro Leu Leu Leu Ser Ile
1 5
<210> 588
<211> 9
<212> PRT
<213> Homo sapiens
<400> 588
Met Ser Ala Val Ile Leu Thr Ala Val
1 5
<210> 589
<211> 9
<212> PRT
<213> Homo sapiens
<400> 589
Ala Leu Ala Ala Ile Ala Ala Phe Met
1 5
<210> 590
<211> 9
<212> PRT
<213> Homo sapiens
<400> 590
Val Ser Ala Ala Phe Gln Ala Gly Val
1 5
<210> 591
<211> 9
<212> PRT
<213> Homo sapiens
<400> 591
Lys Leu Val Asn Leu Gly Phe Gln Ala
1 5
<210> 592
<211> 9
<212> PRT
<213> Homo sapiens
<400> 592
Glu Leu Leu Asp Phe Ser Ser Trp Leu
1 5
<210> 593
<211> 9
<212> PRT
<213> Homo sapiens
<400> 593
Leu Thr Leu Gly Glu Phe Leu Lys Leu
1 5
<210> 594
<211> 9
<212> PRT
<213> Homo sapiens
<400> 594
Ala Ala Gly Asp Ile Leu Ala Leu Val
1 5
<210> 595
<211> 9
<212> PRT
<213> Homo sapiens
<400> 595
Ala Leu Val Phe Gly Leu Leu Phe Ala
1 5
<210> 596
<211> 9
<212> PRT
<213> Homo sapiens
<400> 596
Phe Gln Tyr Glu Gly Ser Leu Thr Thr
1 5
<210> 597
<211> 9
<212> PRT
<213> Homo sapiens
<400> 597
His Leu Ser Thr Ala Phe Ala Arg Val
1 5
<210> 598
<211> 9
<212> PRT
<213> Homo sapiens
<400> 598
Leu Ser Leu Leu Leu Leu Val Pro Val
1 5
<210> 599
<211> 9
<212> PRT
<213> Homo sapiens
<400> 599
Gln Leu Leu Leu Ser Leu Leu Leu Leu
1 5
<210> 600
<211> 9
<212> PRT
<213> Homo sapiens
<400> 600
Val Gln Leu Leu Leu Ser Leu Leu Leu
1 5
<210> 601
<211> 9
<212> PRT
<213> Homo sapiens
<400> 601
Asn Leu Ala Lys Tyr Val Ala Glu Leu
1 5
<210> 602
<211> 9
<212> PRT
<213> Homo sapiens
<400> 602
Leu Ile Ala Ala Ala Ala Phe Cys Leu
1 5
<210> 603
<211> 9
<212> PRT
<213> Homo sapiens
<400> 603
Leu Leu Asn Asp Arg Val Leu Arg Ala
1 5
<210> 604
<211> 9
<212> PRT
<213> Homo sapiens
<400> 604
Gly Ile Leu Leu Thr Thr Leu Leu Val
1 5
<210> 605
<211> 9
<212> PRT
<213> Homo sapiens
<400> 605
Ile Leu Ala Val Val Phe Ile Arg Ile
1 5
<210> 606
<211> 9
<212> PRT
<213> Homo sapiens
<400> 606
Ile Leu Leu Thr Thr Leu Leu Val Ile
1 5
<210> 607
<211> 9
<212> PRT
<213> Homo sapiens
<400> 607
Leu Val Ile Gly Ile Ile Leu Ala Val
1 5
<210> 608
<211> 9
<212> PRT
<213> Homo sapiens
<400> 608
Ala Leu Val Ala Ile Leu Leu Cys Ile
1 5
<210> 609
<211> 9
<212> PRT
<213> Homo sapiens
<400> 609
Glu Met Ser Asp Val Gly Thr Phe Val
1 5
<210> 610
<211> 9
<212> PRT
<213> Homo sapiens
<400> 610
Glu Met Ser Thr Tyr Leu Leu Pro Val
1 5
<210> 611
<211> 9
<212> PRT
<213> Homo sapiens
<400> 611
Phe Leu Leu Glu Glu Tyr Thr Gly Ser
1 5
<210> 612
<211> 9
<212> PRT
<213> Homo sapiens
<400> 612
Ile Leu Leu Cys Ile Val Ile Leu Leu
1 5
<210> 613
<211> 9
<212> PRT
<213> Homo sapiens
<400> 613
Leu Leu Val Thr Val Val Leu Phe Ala
1 5
<210> 614
<211> 9
<212> PRT
<213> Homo sapiens
<400> 614
Ala Val Ala Leu Val Leu Met Leu Leu
1 5
<210> 615
<211> 9
<212> PRT
<213> Homo sapiens
<400> 615
Leu Leu Thr Phe Trp Asn Pro Pro Thr
1 5
<210> 616
<211> 9
<212> PRT
<213> Homo sapiens
<400> 616
Lys Gln Leu Leu Leu Ser Ala Ala Leu
1 5
<210> 617
<211> 9
<212> PRT
<213> Homo sapiens
<400> 617
Leu Leu Leu Ser Ala Ala Leu Ser Ala
1 5
<210> 618
<211> 9
<212> PRT
<213> Homo sapiens
<400> 618
Gln Leu Ala Gly Ala Met Val Trp Ala
1 5
<210> 619
<211> 9
<212> PRT
<213> Homo sapiens
<400> 619
Ser Gln Thr Gly Phe Val Val Leu Val
1 5
<210> 620
<211> 9
<212> PRT
<213> Homo sapiens
<400> 620
Thr Leu Ala Ser Ser Glu Thr Gly Val
1 5
<210> 621
<211> 9
<212> PRT
<213> Homo sapiens
<400> 621
Ile Leu Leu Ser Ile Gly Gly Tyr Leu
1 5
<210> 622
<211> 9
<212> PRT
<213> Homo sapiens
<400> 622
His Leu Ile Tyr Ser Phe Ala Ser Ile
1 5
<210> 623
<211> 9
<212> PRT
<213> Homo sapiens
<400> 623
Val Leu Ile His Glu Leu Ala Glu Ala
1 5
<210> 624
<211> 9
<212> PRT
<213> Homo sapiens
<400> 624
Ser Leu Trp Ala Gly Val Val Val Leu
1 5
<210> 625
<211> 9
<212> PRT
<213> Homo sapiens
<400> 625
Trp Leu Trp Asp Phe Thr Val Thr Thr
1 5
<210> 626
<211> 9
<212> PRT
<213> Homo sapiens
<400> 626
Leu Leu Ala Ser Ser Ile Leu Cys Ala
1 5
<210> 627
<211> 9
<212> PRT
<213> Homo sapiens
<400> 627
Lys Leu Ala Val Ser Leu Ala Glu Thr
1 5
<210> 628
<211> 9
<212> PRT
<213> Homo sapiens
<400> 628
Ala Leu Val Gly Leu Phe Val Leu Leu
1 5
<210> 629
<211> 9
<212> PRT
<213> Homo sapiens
<400> 629
Gly Leu Phe Val Leu Leu Ala Phe Leu
1 5
<210> 630
<211> 9
<212> PRT
<213> Homo sapiens
<400> 630
Ser Val Tyr Asp Phe Phe Val Trp Leu
1 5
<210> 631
<211> 9
<212> PRT
<213> Homo sapiens
<400> 631
Val Val Met Gly Thr Leu Val Ala Leu
1 5
<210> 632
<211> 9
<212> PRT
<213> Homo sapiens
<400> 632
Gly Thr Ala Glu Gly Leu Ala Leu Ala
1 5
<210> 633
<211> 9
<212> PRT
<213> Homo sapiens
<400> 633
Gly Leu Ala Ala Gly Leu Gly Pro Ala
1 5
<210> 634
<211> 9
<212> PRT
<213> Homo sapiens
<400> 634
Ala Leu Glu Ser Ile Leu His Arg Ile
1 5
<210> 635
<211> 9
<212> PRT
<213> Homo sapiens
<400> 635
Ala Leu Leu Ala Ala Leu Cys Pro Ala
1 5
<210> 636
<211> 9
<212> PRT
<213> Homo sapiens
<400> 636
Ala Leu Leu Ala Leu Leu Ala Ala Leu
1 5
<210> 637
<211> 9
<212> PRT
<213> Homo sapiens
<400> 637
Ile Leu Asp Glu Ala Tyr Val Met Ala
1 5
<210> 638
<211> 9
<212> PRT
<213> Homo sapiens
<400> 638
Leu Leu Leu Leu Leu Val Val Ala Leu
1 5
<210> 639
<211> 9
<212> PRT
<213> Homo sapiens
<400> 639
Met Val Gly Ala Leu Leu Leu Leu Leu
1 5
<210> 640
<211> 9
<212> PRT
<213> Homo sapiens
<400> 640
Asn Leu Gln Glu Ile Leu His Gly Ala
1 5
<210> 641
<211> 9
<212> PRT
<213> Homo sapiens
<400> 641
Ser Leu Ala Val Val Ser Leu Asn Ile
1 5
<210> 642
<211> 9
<212> PRT
<213> Homo sapiens
<400> 642
Ala Val Val Gly Ile Leu Leu Val Val
1 5
<210> 643
<211> 9
<212> PRT
<213> Homo sapiens
<400> 643
Ile Leu Asp Glu Ala Tyr Val Met Ala
1 5
<210> 644
<211> 9
<212> PRT
<213> Homo sapiens
<400> 644
Leu Leu Ala Leu Leu Pro Pro Gly Ala
1 5
<210> 645
<211> 9
<212> PRT
<213> Homo sapiens
<400> 645
Ser Ile Ile Ser Ala Val Val Gly Ile
1 5
<210> 646
<211> 9
<212> PRT
<213> Homo sapiens
<400> 646
Val Val Leu Gly Val Val Phe Gly Ile
1 5
<210> 647
<211> 9
<212> PRT
<213> Homo sapiens
<400> 647
Phe Leu Leu Glu Leu Leu Ser Asp Ser
1 5
<210> 648
<211> 9
<212> PRT
<213> Homo sapiens
<400> 648
Ala Leu Leu Asp Ala Glu Pro Pro Ile
1 5
<210> 649
<211> 9
<212> PRT
<213> Homo sapiens
<400> 649
Lys Ile Thr Asp Thr Leu Ile His Leu
1 5
<210> 650
<211> 9
<212> PRT
<213> Homo sapiens
<400> 650
Lys Leu Leu Phe Ala Pro Asn Leu Leu
1 5
<210> 651
<211> 9
<212> PRT
<213> Homo sapiens
<400> 651
Leu Leu Asp Ala Glu Pro Pro Ile Leu
1 5
<210> 652
<211> 9
<212> PRT
<213> Homo sapiens
<400> 652
Leu Leu Asn Ser Gly Val Tyr Thr Phe
1 5
<210> 653
<211> 9
<212> PRT
<213> Homo sapiens
<400> 653
Leu Met Ile Gly Leu Val Trp Arg Ser
1 5
<210> 654
<211> 9
<212> PRT
<213> Homo sapiens
<400> 654
Pro Leu Tyr Asp Leu Leu Leu Glu Met
1 5
<210> 655
<211> 9
<212> PRT
<213> Homo sapiens
<400> 655
Gln Leu Leu Leu Ile Leu Ser His Ile
1 5
<210> 656
<211> 9
<212> PRT
<213> Homo sapiens
<400> 656
Arg Leu Ala Gln Leu Leu Leu Ile Leu
1 5
<210> 657
<211> 9
<212> PRT
<213> Homo sapiens
<400> 657
Thr Leu Ile His Leu Met Ala Lys Ala
1 5
<210> 658
<211> 9
<212> PRT
<213> Homo sapiens
<400> 658
Val Leu Asp Lys Ile Thr Asp Thr Leu
1 5
<210> 659
<211> 9
<212> PRT
<213> Homo sapiens
<400> 659
Phe Met Val Glu Asp Glu Thr Val Leu
1 5
<210> 660
<211> 9
<212> PRT
<213> Homo sapiens
<400> 660
Ser Met Phe Arg Val Leu Ile Gly Thr
1 5
<210> 661
<211> 9
<212> PRT
<213> Homo sapiens
<400> 661
Ala Thr Ser Ala Val Leu Ala Leu Leu
1 5
<210> 662
<211> 9
<212> PRT
<213> Homo sapiens
<400> 662
Thr Gly Trp Ala Gly Gly Phe Phe Val
1 5
<210> 663
<211> 9
<212> PRT
<213> Homo sapiens
<400> 663
Val Leu Ala Leu Leu Val Met Cys Ile
1 5
<210> 664
<211> 9
<212> PRT
<213> Homo sapiens
<400> 664
Ala Leu Leu Ser Cys Leu Leu Leu Thr
1 5
<210> 665
<211> 9
<212> PRT
<213> Homo sapiens
<400> 665
Cys Val Ala Ala Thr Leu Phe Trp Leu
1 5
<210> 666
<211> 9
<212> PRT
<213> Homo sapiens
<400> 666
Glu Met Tyr Ser Glu Ile Pro Glu Ile
1 5
<210> 667
<211> 9
<212> PRT
<213> Homo sapiens
<400> 667
Lys Met Ala Ser Thr Leu Val Val Ala
1 5
<210> 668
<211> 9
<212> PRT
<213> Homo sapiens
<400> 668
Ser Ile Phe Asp Lys Ile Tyr Ser Thr
1 5
<210> 669
<211> 9
<212> PRT
<213> Homo sapiens
<400> 669
Thr Leu Phe Trp Leu Leu Leu Thr Leu
1 5
<210> 670
<211> 9
<212> PRT
<213> Homo sapiens
<400> 670
Val Leu Leu Trp Glu Ile Phe Ser Leu
1 5
<210> 671
<211> 9
<212> PRT
<213> Homo sapiens
<400> 671
Trp Leu Lys Asp Gly Leu Pro Ala Thr
1 5
<210> 672
<211> 9
<212> PRT
<213> Homo sapiens
<400> 672
Ile Leu Leu Asp Ile Ser Phe Pro Gly
1 5
<210> 673
<211> 9
<212> PRT
<213> Homo sapiens
<400> 673
Leu Leu Asp Ile Ser Phe Pro Gly Leu
1 5
<210> 674
<211> 9
<212> PRT
<213> Homo sapiens
<400> 674
Leu Met Asp Leu Ser Thr Thr Pro Leu
1 5
<210> 675
<211> 9
<212> PRT
<213> Homo sapiens
<400> 675
Arg Val Ser Ser Tyr Leu Val Pro Ile
1 5
<210> 676
<211> 9
<212> PRT
<213> Homo sapiens
<400> 676
Ser Leu Ser Lys Ile Leu Leu Asp Ile
1 5
<210> 677
<211> 9
<212> PRT
<213> Homo sapiens
<400> 677
Ser Gln Leu Ser Tyr Ser Gln Glu Val
1 5
<210> 678
<211> 9
<212> PRT
<213> Homo sapiens
<400> 678
Trp Ala Ala Glu Leu Pro Phe Pro Ala
1 5
<210> 679
<211> 9
<212> PRT
<213> Homo sapiens
<400> 679
Leu Leu Asn Glu Ser Glu Thr Lys Val
1 5
<210> 680
<211> 9
<212> PRT
<213> Homo sapiens
<400> 680
Arg Leu Val Glu Leu Leu Lys Asp Leu
1 5
<210> 681
<211> 9
<212> PRT
<213> Homo sapiens
<400> 681
Gly Leu Ala Ser Thr Thr Pro Glu Ala
1 5
<210> 682
<211> 9
<212> PRT
<213> Homo sapiens
<400> 682
Arg Met Ala Arg Glu Val Ala Ala Leu
1 5
<210> 683
<211> 9
<212> PRT
<213> Homo sapiens
<400> 683
Phe Leu Leu Ser Leu Ala Phe Tyr Gly
1 5
<210> 684
<211> 9
<212> PRT
<213> Homo sapiens
<400> 684
Ile Leu Asn Pro Ala Gln Gly Phe Leu
1 5
<210> 685
<211> 9
<212> PRT
<213> Homo sapiens
<400> 685
Met Ala Trp Gly Leu Ala Thr Leu Leu
1 5
<210> 686
<211> 9
<212> PRT
<213> Homo sapiens
<400> 686
Arg Leu Ala Leu Gly Leu Leu Gln Leu
1 5
<210> 687
<211> 9
<212> PRT
<213> Homo sapiens
<400> 687
Arg Leu Leu Leu Ala Gly Ala Glu Val
1 5
<210> 688
<211> 9
<212> PRT
<213> Homo sapiens
<400> 688
Cys Leu Tyr Thr Phe Leu Ile Ser Thr
1 5
<210> 689
<211> 9
<212> PRT
<213> Homo sapiens
<400> 689
Phe Leu Ile Ser Thr Thr Phe Gly Cys
1 5
<210> 690
<211> 9
<212> PRT
<213> Homo sapiens
<400> 690
Val Leu Leu Asp Thr Asn Tyr Asn Leu
1 5
<210> 691
<211> 9
<212> PRT
<213> Homo sapiens
<400> 691
Trp Leu Pro Phe Gly Phe Ile Leu Ile
1 5
<210> 692
<211> 10
<212> PRT
<213> Homo sapiens
<400> 692
Trp Leu Pro Phe Gly Phe Ile Leu Ile Leu
1 5 10
<210> 693
<211> 9
<212> PRT
<213> Homo sapiens
<400> 693
Ala Leu Tyr Leu Leu Pro Leu Leu Ala
1 5
<210> 694
<211> 9
<212> PRT
<213> Homo sapiens
<400> 694
Phe Ala Leu Tyr Asn Leu Leu Ala Leu
1 5
<210> 695
<211> 9
<212> PRT
<213> Homo sapiens
<400> 695
Gln Leu Phe Leu Val Leu Gln Ala Leu
1 5
<210> 696
<211> 9
<212> PRT
<213> Homo sapiens
<400> 696
Arg Leu Val Ala Ala Val Val Leu Leu
1 5
<210> 697
<211> 9
<212> PRT
<213> Homo sapiens
<400> 697
Val Leu Ala Glu Arg Ala Gly Ala Val
1 5
<210> 698
<211> 9
<212> PRT
<213> Homo sapiens
<400> 698
Trp Leu Val Pro Leu Phe Phe Ala Ala
1 5
<210> 699
<211> 9
<212> PRT
<213> Homo sapiens
<400> 699
Tyr Leu Leu Pro Leu Leu Ala Thr Cys
1 5
<210> 700
<211> 9
<212> PRT
<213> Homo sapiens
<400> 700
Gly Leu Ser Asp Ala Val Glu Ala Leu
1 5
<210> 701
<211> 9
<212> PRT
<213> Homo sapiens
<400> 701
Met Leu Arg Glu Ala Ala Met Gly Ile
1 5
<210> 702
<211> 9
<212> PRT
<213> Homo sapiens
<400> 702
Ala Leu Ile Pro Ala Pro Glu Leu Val
1 5
<210> 703
<211> 9
<212> PRT
<213> Homo sapiens
<400> 703
Asn Leu Leu His Gly Leu Asn Leu Leu
1 5
<210> 704
<211> 9
<212> PRT
<213> Homo sapiens
<400> 704
Tyr Val Ser Ser Leu Pro Gln Pro Leu
1 5
<210> 705
<211> 9
<212> PRT
<213> Homo sapiens
<400> 705
Tyr Leu Ile Leu Gly Val Ala Gly Ser
1 5
<210> 706
<211> 9
<212> PRT
<213> Homo sapiens
<400> 706
Asn Met Asp Cys Ile Ile Ala Glu Ile
1 5
<210> 707
<211> 9
<212> PRT
<213> Homo sapiens
<400> 707
Ala Val Leu Gly Ile Phe Ile Ile Val
1 5
<210> 708
<211> 9
<212> PRT
<213> Homo sapiens
<400> 708
Lys Leu Ala Val Leu Gly Ile Phe Ile
1 5
<210> 709
<211> 9
<212> PRT
<213> Homo sapiens
<400> 709
Ala Ile Ala Ala Ile Val Ile Gly Ile
1 5
<210> 710
<211> 9
<212> PRT
<213> Homo sapiens
<400> 710
Ala Leu Ala Cys Ser Leu Ala Ala Cys
1 5
<210> 711
<211> 9
<212> PRT
<213> Homo sapiens
<400> 711
Ile Val Ile Gly Ile Val Ala Leu Ala
1 5
<210> 712
<211> 9
<212> PRT
<213> Homo sapiens
<400> 712
Arg Ile Val Ala Val Pro Thr Pro Leu
1 5
<210> 713
<211> 9
<212> PRT
<213> Homo sapiens
<400> 713
Ser Leu Lys Glu Leu Ser Pro Gly Ile
1 5
<210> 714
<211> 9
<212> PRT
<213> Homo sapiens
<400> 714
Lys Val Ala Asp Leu Val Gly Phe Leu
1 5
<210> 715
<211> 9
<212> PRT
<213> Homo sapiens
<400> 715
Gly Met Leu Ser Asp Val Gln Ser Met
1 5
<210> 716
<211> 9
<212> PRT
<213> Homo sapiens
<400> 716
Ile Leu Ile Leu Ile Leu Ser Ile Val
1 5
<210> 717
<211> 9
<212> PRT
<213> Homo sapiens
<400> 717
Ala Met Asp Ala Ile Phe Gly Ser Leu
1 5
<210> 718
<211> 9
<212> PRT
<213> Homo sapiens
<400> 718
Gly Leu Ile Thr Lys Ala Glu Met Leu
1 5
<210> 719
<211> 9
<212> PRT
<213> Homo sapiens
<400> 719
Gly Thr Leu Glu Glu Leu Pro Ala Ala
1 5
<210> 720
<211> 9
<212> PRT
<213> Homo sapiens
<400> 720
Lys Val Leu Glu Tyr Ile Ala Asn Ala
1 5
<210> 721
<211> 9
<212> PRT
<213> Homo sapiens
<400> 721
Gln Leu Val Phe Gly Ile Glu Val Val
1 5
<210> 722
<211> 9
<212> PRT
<213> Homo sapiens
<400> 722
Ala Val Ser Ser Ser Ser Pro Leu Val
1 5
<210> 723
<211> 9
<212> PRT
<213> Homo sapiens
<400> 723
Lys Val Asp Glu Leu Ala His Phe Leu
1 5
<210> 724
<211> 9
<212> PRT
<213> Homo sapiens
<400> 724
Lys Val Leu Glu His Val Val Arg Val
1 5
<210> 725
<211> 9
<212> PRT
<213> Homo sapiens
<400> 725
Val Ile Leu Gly Val Leu Leu Leu Ile
1 5
<210> 726
<211> 9
<212> PRT
<213> Homo sapiens
<400> 726
Met Thr Ala Ala Gly Val Pro Gln Leu
1 5
<210> 727
<211> 9
<212> PRT
<213> Homo sapiens
<400> 727
Ser Val Ser Asp Ile Leu Ser Pro Leu
1 5
<210> 728
<211> 9
<212> PRT
<213> Homo sapiens
<400> 728
Ala Leu Leu Ala Ala Ser Val Ala Leu
1 5
<210> 729
<211> 9
<212> PRT
<213> Homo sapiens
<400> 729
Leu Leu Ala Ala Ser Val Ala Leu Ala
1 5
<210> 730
<211> 9
<212> PRT
<213> Homo sapiens
<400> 730
Gln Leu Leu Arg Lys Val Ala Glu Leu
1 5
<210> 731
<211> 9
<212> PRT
<213> Homo sapiens
<400> 731
Thr Leu Pro Glu Leu Tyr Ala Phe Thr
1 5
<210> 732
<211> 9
<212> PRT
<213> Homo sapiens
<400> 732
Tyr Leu Tyr Gly Lys Ile Lys Lys Thr
1 5
<210> 733
<211> 9
<212> PRT
<213> Homo sapiens
<400> 733
Gln Val Leu Gly Leu Ala Ala Tyr Leu
1 5
<210> 734
<211> 9
<212> PRT
<213> Homo sapiens
<400> 734
Gly Leu Asp Glu Val Lys Ser Ser Leu
1 5
<210> 735
<211> 9
<212> PRT
<213> Homo sapiens
<400> 735
Phe Val Leu Leu Ser Leu Ser Gly Ala
1 5
<210> 736
<211> 9
<212> PRT
<213> Homo sapiens
<400> 736
Ser Leu Phe Leu Phe Ser Val Leu Leu
1 5
<210> 737
<211> 9
<212> PRT
<213> Homo sapiens
<400> 737
Ser Leu Thr Val Tyr Leu Val Val Ala
1 5
<210> 738
<211> 9
<212> PRT
<213> Homo sapiens
<400> 738
Val Leu Leu Phe Val Ala Val Arg Leu
1 5
<210> 739
<211> 9
<212> PRT
<213> Homo sapiens
<400> 739
Val Ser Ser Leu Phe Leu Phe Ser Val
1 5
<210> 740
<211> 9
<212> PRT
<213> Homo sapiens
<400> 740
Ser Ile Ala Gly Phe Val Ala Ser Ile
1 5
<210> 741
<211> 9
<212> PRT
<213> Homo sapiens
<400> 741
Ile Leu Leu Val Leu Met Ala Val Val
1 5
<210> 742
<211> 9
<212> PRT
<213> Homo sapiens
<400> 742
Leu Ile Val Gly Ile Leu Leu Val Leu
1 5
<210> 743
<211> 9
<212> PRT
<213> Homo sapiens
<400> 743
Leu Met Ala Val Val Leu Ala Ser Leu
1 5
<210> 744
<211> 9
<212> PRT
<213> Homo sapiens
<400> 744
Pro Leu Leu Asp Gly Thr Ala Thr Leu
1 5
<210> 745
<211> 9
<212> PRT
<213> Homo sapiens
<400> 745
Ser Leu Ala Asp Thr Asn Ser Leu Ala
1 5
<210> 746
<211> 9
<212> PRT
<213> Homo sapiens
<400> 746
Val Leu Gln Ala Ala Ile Pro Leu Thr
1 5
<210> 747
<211> 9
<212> PRT
<213> Homo sapiens
<400> 747
Ala Val Leu Asp Gly Leu Asp Val Leu
1 5
<210> 748
<211> 9
<212> PRT
<213> Homo sapiens
<400> 748
Gln Leu Leu Ala Leu Leu Pro Ser Leu
1 5
<210> 749
<211> 9
<212> PRT
<213> Homo sapiens
<400> 749
Arg Leu Arg Glu Leu Leu Cys Glu Leu
1 5
<210> 750
<211> 9
<212> PRT
<213> Homo sapiens
<400> 750
Val Leu Tyr Pro Val Pro Leu Glu Ser
1 5
<210> 751
<211> 9
<212> PRT
<213> Homo sapiens
<400> 751
Ala Val Phe Leu Leu Ser Tyr Ala Val
1 5
<210> 752
<211> 9
<212> PRT
<213> Homo sapiens
<400> 752
Phe Val Leu Ser Leu Leu Leu Ile Leu
1 5
<210> 753
<211> 9
<212> PRT
<213> Homo sapiens
<400> 753
Ile Ile Phe Val Leu Ser Leu Leu Leu
1 5
<210> 754
<211> 9
<212> PRT
<213> Homo sapiens
<400> 754
Leu Ile Leu Glu Lys Gln Ala Ala Val
1 5
<210> 755
<211> 9
<212> PRT
<213> Homo sapiens
<400> 755
Leu Ile Ser Glu Leu Lys Leu Ala Val
1 5
<210> 756
<211> 9
<212> PRT
<213> Homo sapiens
<400> 756
Arg Ala Ile Glu His Val Leu Gln Val
1 5
<210> 757
<211> 9
<212> PRT
<213> Homo sapiens
<400> 757
Ser Ser Phe Asp Arg Leu Ile Pro Leu
1 5
<210> 758
<211> 9
<212> PRT
<213> Homo sapiens
<400> 758
Thr Leu Lys Glu Gln Phe Gln Phe Val
1 5
<210> 759
<211> 9
<212> PRT
<213> Homo sapiens
<400> 759
Ala Ile Leu Asp Ser Ala Phe Leu Leu
1 5
<210> 760
<211> 9
<212> PRT
<213> Homo sapiens
<400> 760
Ala Ile Ser Leu Val Phe Ser Leu Val
1 5
<210> 761
<211> 9
<212> PRT
<213> Homo sapiens
<400> 761
Ala Leu Gln Ile Leu Pro Tyr Thr Leu
1 5
<210> 762
<211> 9
<212> PRT
<213> Homo sapiens
<400> 762
Ala Leu Thr Gly Phe Thr Phe Ser Ala
1 5
<210> 763
<211> 9
<212> PRT
<213> Homo sapiens
<400> 763
Ala Gln Leu Leu Leu Val Asn Leu Leu
1 5
<210> 764
<211> 9
<212> PRT
<213> Homo sapiens
<400> 764
Cys Leu Phe Gly Leu Leu Thr Leu Ile
1 5
<210> 765
<211> 9
<212> PRT
<213> Homo sapiens
<400> 765
Gly Ile Leu Leu Ser Leu Phe Leu Ile
1 5
<210> 766
<211> 9
<212> PRT
<213> Homo sapiens
<400> 766
Gly Leu Leu Pro Pro Pro Pro Ala Leu
1 5
<210> 767
<211> 9
<212> PRT
<213> Homo sapiens
<400> 767
Gly Leu Leu Thr Leu Ile Phe Leu Thr
1 5
<210> 768
<211> 9
<212> PRT
<213> Homo sapiens
<400> 768
Gly Leu Val Ala Ile Tyr Phe Ala Thr
1 5
<210> 769
<211> 9
<212> PRT
<213> Homo sapiens
<400> 769
Asn Leu Gly Ala Leu Leu Pro Arg Leu
1 5
<210> 770
<211> 9
<212> PRT
<213> Homo sapiens
<400> 770
Ser Val Ala Ala Phe Pro Val Ala Ala
1 5
<210> 771
<211> 9
<212> PRT
<213> Homo sapiens
<400> 771
Phe Leu Leu Ser Leu Phe Cys Val Thr
1 5
<210> 772
<211> 9
<212> PRT
<213> Homo sapiens
<400> 772
Phe Ser Leu Gly Val Gly Phe Gly Val
1 5
<210> 773
<211> 9
<212> PRT
<213> Homo sapiens
<400> 773
Gly Leu Ile Asp Glu Phe Gln Leu Leu
1 5
<210> 774
<211> 9
<212> PRT
<213> Homo sapiens
<400> 774
Gly Met Glu Ser Val Ile Thr Gly Leu
1 5
<210> 775
<211> 9
<212> PRT
<213> Homo sapiens
<400> 775
Ile Leu Phe Gly Val Leu Ile Glu Ala
1 5
<210> 776
<211> 9
<212> PRT
<213> Homo sapiens
<400> 776
Lys Ile Asp Phe Leu Leu Ser Val Ile
1 5
<210> 777
<211> 9
<212> PRT
<213> Homo sapiens
<400> 777
Leu Leu Phe Met Val Ile Ala Gly Met
1 5
<210> 778
<211> 9
<212> PRT
<213> Homo sapiens
<400> 778
Leu Val Pro Tyr Leu Leu Phe Met Val
1 5
<210> 779
<211> 9
<212> PRT
<213> Homo sapiens
<400> 779
Gln Leu Thr Ala Cys Leu Val Leu Val
1 5
<210> 780
<211> 9
<212> PRT
<213> Homo sapiens
<400> 780
Met Ile Ser Glu Lys Met Val Lys Leu
1 5
<210> 781
<211> 9
<212> PRT
<213> Homo sapiens
<400> 781
Leu Met Phe Asp Leu Ser Leu Asn Phe
1 5
<210> 782
<211> 9
<212> PRT
<213> Homo sapiens
<400> 782
Ala Leu Pro Ala Val Met Ala Gly Leu
1 5
<210> 783
<211> 9
<212> PRT
<213> Homo sapiens
<400> 783
Gly Leu Ala Glu Pro Gln Ala Ala Ala
1 5
<210> 784
<211> 9
<212> PRT
<213> Homo sapiens
<400> 784
Gly Ile Phe Leu Leu Ser Ala Leu Ala
1 5
<210> 785
<211> 9
<212> PRT
<213> Homo sapiens
<400> 785
Ala Ser Leu Thr Phe Leu Tyr Thr Leu
1 5
<210> 786
<211> 9
<212> PRT
<213> Homo sapiens
<400> 786
Ala Val Leu His Ala Ile Tyr Ser Leu
1 5
<210> 787
<211> 9
<212> PRT
<213> Homo sapiens
<400> 787
Phe Phe Phe Ala Val Leu His Ala Ile
1 5
<210> 788
<211> 9
<212> PRT
<213> Homo sapiens
<400> 788
Gly Val Ile Ala Ala Ile Val Gln Leu
1 5
<210> 789
<211> 9
<212> PRT
<213> Homo sapiens
<400> 789
Lys Ile Ala Ala Ile Ile Ala Ser Leu
1 5
<210> 790
<211> 9
<212> PRT
<213> Homo sapiens
<400> 790
Leu Ile Phe Lys Ser Ile Leu Phe Leu
1 5
<210> 791
<211> 9
<212> PRT
<213> Homo sapiens
<400> 791
Leu Leu Leu Gly Thr Ile His Ala Leu
1 5
<210> 792
<211> 9
<212> PRT
<213> Homo sapiens
<400> 792
Leu Leu Ser Phe Phe Phe Ala Val Leu
1 5
<210> 793
<211> 9
<212> PRT
<213> Homo sapiens
<400> 793
Met Ile Ala Val Phe Leu Pro Ile Val
1 5
<210> 794
<211> 9
<212> PRT
<213> Homo sapiens
<400> 794
Ser Leu Leu Leu Gly Thr Ile His Ala
1 5
<210> 795
<211> 9
<212> PRT
<213> Homo sapiens
<400> 795
Ser Leu Ser Leu Ile Val Ala Val Ile
1 5
<210> 796
<211> 9
<212> PRT
<213> Homo sapiens
<400> 796
Ile Ile Ser Pro Asn Leu Phe Tyr Ala
1 5
<210> 797
<211> 9
<212> PRT
<213> Homo sapiens
<400> 797
Leu Leu Asp His Val Leu Ile Glu Met
1 5
<210> 798
<211> 9
<212> PRT
<213> Homo sapiens
<400> 798
Val Leu Ile Asp Glu His Leu Val Leu
1 5
<210> 799
<211> 9
<212> PRT
<213> Homo sapiens
<400> 799
Tyr Ser Ser Glu Val Leu Glu Tyr Met
1 5
<210> 800
<211> 9
<212> PRT
<213> Homo sapiens
<400> 800
Ile Leu Leu Arg Pro Asp Thr Tyr Ile
1 5
<210> 801
<211> 9
<212> PRT
<213> Homo sapiens
<400> 801
Leu Met Met Thr Ile Ile Asn Leu Ala
1 5
<210> 802
<211> 9
<212> PRT
<213> Homo sapiens
<400> 802
Gln Leu Ala Gly Ser Val Ala Glu Met
1 5
<210> 803
<211> 9
<212> PRT
<213> Homo sapiens
<400> 803
Ser Leu Met Met Thr Ile Ile Asn Leu
1 5
<210> 804
<211> 9
<212> PRT
<213> Homo sapiens
<400> 804
Thr Met Leu Ser Ser Leu Ala Arg Leu
1 5
<210> 805
<211> 9
<212> PRT
<213> Homo sapiens
<400> 805
Tyr Ile Phe Thr Met Leu Ser Ser Leu
1 5
<210> 806
<211> 9
<212> PRT
<213> Homo sapiens
<400> 806
Asp Leu Ala Gly Val Ile Ile Glu Leu
1 5
<210> 807
<211> 9
<212> PRT
<213> Homo sapiens
<400> 807
Phe Gly Leu Phe Gly Val Phe Leu Val
1 5
<210> 808
<211> 9
<212> PRT
<213> Homo sapiens
<400> 808
Gly Leu Phe Gly Val Phe Leu Val Leu
1 5
<210> 809
<211> 9
<212> PRT
<213> Homo sapiens
<400> 809
Ile Leu Asp Thr Ala Ile Ile Val Ile
1 5
<210> 810
<211> 9
<212> PRT
<213> Homo sapiens
<400> 810
Ile Val Ser Ser Phe Ala Phe Gly Leu
1 5
<210> 811
<211> 9
<212> PRT
<213> Homo sapiens
<400> 811
Arg Leu Leu Arg Leu Ile Ile Leu Leu
1 5
<210> 812
<211> 9
<212> PRT
<213> Homo sapiens
<400> 812
Ser Leu Ala Ile Ala Leu Phe Phe Leu
1 5
<210> 813
<211> 9
<212> PRT
<213> Homo sapiens
<400> 813
Tyr Phe Trp Leu His Thr Ser Phe Ile
1 5
<210> 814
<211> 9
<212> PRT
<213> Homo sapiens
<400> 814
Ala Met Phe Gly Tyr Thr Val Gly Thr
1 5
<210> 815
<211> 9
<212> PRT
<213> Homo sapiens
<400> 815
Phe Ile Ala Gly Ile Val Phe Arg Leu
1 5
<210> 816
<211> 9
<212> PRT
<213> Homo sapiens
<400> 816
Phe Leu Leu Leu Phe Ala Tyr Val Leu
1 5
<210> 817
<211> 9
<212> PRT
<213> Homo sapiens
<400> 817
Leu Leu Phe Ala Tyr Val Leu Leu Met
1 5
<210> 818
<211> 9
<212> PRT
<213> Homo sapiens
<400> 818
Leu Leu Leu Phe Ala Tyr Val Leu Leu
1 5
<210> 819
<211> 9
<212> PRT
<213> Homo sapiens
<400> 819
Leu Val Leu Tyr Ser Leu Val Phe Val
1 5
<210> 820
<211> 9
<212> PRT
<213> Homo sapiens
<400> 820
Asn Ile Leu Leu Val Asn Leu Leu Val
1 5
<210> 821
<211> 9
<212> PRT
<213> Homo sapiens
<400> 821
Gln Ile Ala Asp Val Ile Ala Ser Leu
1 5
<210> 822
<211> 9
<212> PRT
<213> Homo sapiens
<400> 822
Val Leu Tyr Ser Leu Val Phe Val Leu
1 5
<210> 823
<211> 9
<212> PRT
<213> Homo sapiens
<400> 823
Tyr Leu Val Lys Ile Asn Thr Lys Ala
1 5
<210> 824
<211> 9
<212> PRT
<213> Homo sapiens
<400> 824
Phe Leu Asp Ser Leu Gly Phe Ser Thr
1 5
<210> 825
<211> 9
<212> PRT
<213> Homo sapiens
<400> 825
Ser Leu Arg Asp Glu Phe Pro Leu Leu
1 5
<210> 826
<211> 9
<212> PRT
<213> Homo sapiens
<400> 826
Val Leu Glu Glu Leu Leu Trp Phe Ile
1 5
<210> 827
<211> 9
<212> PRT
<213> Homo sapiens
<400> 827
Ala Leu Leu Ala Gly Leu Val Ser Leu
1 5
<210> 828
<211> 9
<212> PRT
<213> Homo sapiens
<400> 828
Ala Met Val Gly Ala Val Leu Thr Ala
1 5
<210> 829
<211> 9
<212> PRT
<213> Homo sapiens
<400> 829
Ile Ser Ser Asp Tyr Val Ile Pro Ile
1 5
<210> 830
<211> 9
<212> PRT
<213> Homo sapiens
<400> 830
Leu Leu Ala Gly Leu Val Ser Leu Leu
1 5
<210> 831
<211> 9
<212> PRT
<213> Homo sapiens
<400> 831
Leu Leu Ser Pro Ala Ser Phe Phe Ser
1 5
<210> 832
<211> 9
<212> PRT
<213> Homo sapiens
<400> 832
Met Val Gly Ala Val Leu Thr Ala Leu
1 5
<210> 833
<211> 9
<212> PRT
<213> Homo sapiens
<400> 833
Val Leu Thr Ala Leu Leu Ala Gly Leu
1 5
<210> 834
<211> 9
<212> PRT
<213> Homo sapiens
<400> 834
Ala Leu Thr Glu Ser Leu Leu Val Ala
1 5
<210> 835
<211> 9
<212> PRT
<213> Homo sapiens
<400> 835
Leu Leu Ala Leu Leu Ser Pro Gly Ala
1 5
<210> 836
<211> 9
<212> PRT
<213> Homo sapiens
<400> 836
Leu Val Leu Gly Phe Ile Ile Ala Leu
1 5
<210> 837
<211> 9
<212> PRT
<213> Homo sapiens
<400> 837
Ser Leu Ser Gly Leu Leu Ser Pro Ala
1 5
<210> 838
<211> 9
<212> PRT
<213> Homo sapiens
<400> 838
Thr Leu Pro Leu Ile Leu Ile Leu Leu
1 5
<210> 839
<211> 9
<212> PRT
<213> Homo sapiens
<400> 839
Val Leu Gly Phe Ile Ile Ala Leu Ala
1 5
<210> 840
<211> 9
<212> PRT
<213> Homo sapiens
<400> 840
Val Val Ile Thr Val Leu Leu Ser Val
1 5
<210> 841
<211> 9
<212> PRT
<213> Homo sapiens
<400> 841
Ala Gln Ile Gly Asp Ser Val Met Leu
1 5
<210> 842
<211> 9
<212> PRT
<213> Homo sapiens
<400> 842
Phe Ala Ser Ser Leu Ile Ile Pro Ala
1 5
<210> 843
<211> 9
<212> PRT
<213> Homo sapiens
<400> 843
Lys Ser Ile Asp Gly Ala Tyr Thr Ile
1 5
<210> 844
<211> 9
<212> PRT
<213> Homo sapiens
<400> 844
Ser Ile Leu Glu Glu Gly Ser Ser Val
1 5
<210> 845
<211> 9
<212> PRT
<213> Homo sapiens
<400> 845
Leu Leu Phe Gly Phe Thr Leu Val Ser
1 5
<210> 846
<211> 9
<212> PRT
<213> Homo sapiens
<400> 846
Leu Leu Leu Phe Gly Phe Thr Leu Val
1 5
<210> 847
<211> 9
<212> PRT
<213> Homo sapiens
<400> 847
Arg Leu Gly Pro Leu Ala Ala Ala Leu
1 5
<210> 848
<211> 9
<212> PRT
<213> Homo sapiens
<400> 848
Asp Leu Asn Ala Leu Leu Pro Ala Val
1 5
<210> 849
<211> 9
<212> PRT
<213> Homo sapiens
<400> 849
Ile Leu Ile Pro Gln Val Ala Tyr Thr
1 5
<210> 850
<211> 9
<212> PRT
<213> Homo sapiens
<400> 850
Asn Leu Ser Asp Ile Gln Asn Val Leu
1 5
<210> 851
<211> 9
<212> PRT
<213> Homo sapiens
<400> 851
Val Gln Ala Val Val Leu Pro Thr Val
1 5
<210> 852
<211> 9
<212> PRT
<213> Homo sapiens
<400> 852
Leu Val Leu Glu Gln Phe Leu Thr Ile
1 5
<210> 853
<211> 9
<212> PRT
<213> Homo sapiens
<400> 853
Arg Ile Ser Gly Tyr Ile Ser Glu Ala
1 5
<210> 854
<211> 9
<212> PRT
<213> Homo sapiens
<400> 854
Ala Met Thr Asp Ile Ser Ser Leu Ala
1 5
<210> 855
<211> 9
<212> PRT
<213> Homo sapiens
<400> 855
Val Leu Leu Ser Asn Phe Tyr Tyr Gly
1 5
<210> 856
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 856
Met Ala Lys Thr Ile Ala Tyr Asp Glu Glu Ala Arg Arg Gly Leu Glu
1 5 10 15
Arg Gly Leu Asn
20
<210> 857
<211> 9
<212> PRT
<213> Homo sapiens
<400> 857
Gln Leu Trp Gln Phe Leu Leu Glu Leu
1 5
<210> 858
<211> 9
<212> PRT
<213> Homo sapiens
<400> 858
Leu Val Leu Gly Thr Leu Glu Glu Val
1 5
<210> 859
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 859
Lys Ser Val Trp Ser Lys Leu Gln Ser Ile Gly Ile Arg Gln His
1 5 10 15
<210> 860
<211> 13
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 860
Thr Pro Pro Ala Tyr Arg Pro Pro Asn Ala Pro Ile Leu
1 5 10
<210> 861
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 861
Trp Leu Leu Asp Ile Ser Phe Pro Leu
1 5
<210> 862
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 862
His Leu Leu Asp Ile Ser Phe Pro Ala
1 5
<210> 863
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 863
Glu Leu Leu Asp Ile Ser Phe Pro Ala
1 5
<210> 864
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 864
Val Leu Leu Asp Ile Ser Phe Glu Leu
1 5
<210> 865
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 865
Val Leu Leu Asp Ile Ser Phe Lys Val
1 5
<210> 866
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 866
Ile Met Leu Asp Ile Ser Phe Leu Leu
1 5
<210> 867
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 867
Leu Leu Asp Ile Ser Phe Pro Ser Leu
1 5
<210> 868
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 868
Leu Met Asp Leu Ser Thr Thr Asn Val
1 5
<210> 869
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 869
Met Leu Ser Ser Tyr Leu Val Pro Ile
1 5
<210> 870
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 870
Leu Leu Ser Ser Tyr Leu Val Pro Ile
1 5
<210> 871
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 871
Phe Val Ser Ser Tyr Leu Val Pro Thr
1 5
<210> 872
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 872
Ser Leu Ser Leu His Asp Met Phe Leu
1 5
<210> 873
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 873
Lys Leu Lys Pro Leu Leu Pro Trp Ile
1 5
<210> 874
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 874
Lys Leu Lys Pro Leu Leu Pro Phe Leu
1 5
<210> 875
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 875
Lys Val Val Pro Ile Gln Phe Pro Val
1 5
<210> 876
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 876
Lys Ile Val Pro Ile Gln Phe Pro Ile
1 5
<210> 877
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 877
Tyr Gln Ala Met Ile Gln Phe Leu Ile
1 5
<210> 878
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 878
Phe Met Pro Phe Gly Phe Ile Leu Pro Ile
1 5 10
<210> 879
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 879
Phe Met Pro Phe Gly Phe Ile Leu Gly Val
1 5 10
<210> 880
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 880
Phe Leu Ile Ser Thr Thr Phe Thr Ile Asn
1 5 10
<210> 881
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 881
Phe Met Ile Ser Thr Thr Phe Met Arg Leu
1 5 10
<210> 882
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 882
Gln Met Ile Ser Thr Thr Phe Gly Asn Val
1 5 10
<210> 883
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 883
Trp Leu Tyr Leu Gln Trp Gln Pro Ser Val
1 5 10
<210> 884
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 884
Phe Val Leu Leu Asp Thr Asn Tyr Glu Ile
1 5 10
<210> 885
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 885
Phe Ile Leu Leu Asp Thr Asn Tyr Glu Ile
1 5 10
<210> 886
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 886
Tyr Glu Leu Gln Asn Ile Val Leu Pro Ile
1 5 10
<210> 887
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 887
Phe Met Leu Gln Asn Ile Val Lys Asn Leu
1 5 10
<210> 888
<211> 9
<212> PRT
<213> Homo sapiens
<400> 888
Asn Leu Ser Leu His Asp Met Phe Val
1 5
<210> 889
<211> 9
<212> PRT
<213> Homo sapiens
<400> 889
Lys Met Lys Pro Leu Leu Pro Arg Val
1 5
<210> 890
<211> 9
<212> PRT
<213> Homo sapiens
<400> 890
Tyr Leu Val Pro Ile Gln Phe Pro Val
1 5
<210> 891
<211> 9
<212> PRT
<213> Homo sapiens
<400> 891
Tyr Met Ala Met Ile Gln Phe Ala Ile
1 5
<210> 892
<211> 10
<212> PRT
<213> Homo sapiens
<400> 892
Phe Leu Ile Ser Thr Thr Phe Gly Cys Thr
1 5 10
<210> 893
<211> 10
<212> PRT
<213> Homo sapiens
<400> 893
Tyr Leu Tyr Leu Gln Trp Gln Pro Pro Leu
1 5 10
<210> 894
<211> 10
<212> PRT
<213> Homo sapiens
<400> 894
Gly Val Leu Leu Asp Thr Asn Tyr Asn Leu
1 5 10
<210> 895
<211> 10
<212> PRT
<213> Homo sapiens
<400> 895
Phe Gln Leu Gln Asn Ile Val Lys Pro Leu
1 5 10
<210> 896
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> comparative peptide
<400> 896
Ala Leu Pro Phe Gly Phe Ile Leu Val
1 5
<210> 897
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> comparative peptide
<400> 897
Ile Leu Pro Phe Gly Phe Ile Leu Ala
1 5
<210> 898
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> comparative peptide
<400> 898
Phe Leu Pro Phe Gly Phe Ile Leu Met
1 5
<210> 899
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> comparative peptide
<400> 899
Leu Met Leu Gly Glu Phe Leu Lys Leu
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ПЕПТИДЫ И ИХ ПРИМЕНЕНИЕ В ЛЕЧЕНИИ ЗАБОЛЕВАНИЙ, НАРУШЕНИЙ ИЛИ СОСТОЯНИЙ, АССОЦИИРОВАННЫХ С МУТАНТНЫМ р53 | 2017 |
|
RU2762089C2 |
| АНТИТЕЛА ПРОТИВ ПРЕДСТАВИТЕЛЯ А5 СЕМЕЙСТВА 19 СО СХОДСТВОМ ПОСЛЕДОВАТЕЛЬНОСТЕЙ И СПОСОБ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2785436C2 |
| ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР (CAR) С АНТИГЕНСВЯЗЫВАЮЩИМИ ДОМЕНАМИ К КОНСТАНТНОЙ ОБЛАСТИ β Т-КЛЕТОЧНОГО РЕЦЕПТОРА | 2015 |
|
RU2830064C2 |
| НЕГЕНЕТИЧЕСКАЯ МОДИФИКАЦИЯ ОБОЛОЧЕЧНЫХ ВИРУСОВ | 2017 |
|
RU2760521C2 |
| Антитела против CXCR2 и их применение | 2019 |
|
RU2807067C2 |
| АНТИТЕЛА К C10ORF54 И ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2819627C1 |
| АНТИТЕЛА ПРОТИВ PD-L1 И ИХ ВАРИАНТЫ | 2017 |
|
RU2770590C2 |
| ПОЛИПЕПТИД, ВКЛЮЧАЮЩИЙ АНТИГЕНСВЯЗЫВАЮЩИЙ ДОМЕН И ТРАНСПОРТИРУЮЩИЙ СЕГМЕНТ | 2018 |
|
RU2815452C2 |
| АНТИ-PVRIG АНТИТЕЛА И СПОСОБЫ ПРИМЕНЕНИЯ | 2016 |
|
RU2732042C2 |
| АНТИТЕЛЬНЫЕ АГЕНТЫ, СПЕЦИФИЧНЫЕ К CD19 ЧЕЛОВЕКА, И ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2773317C2 |




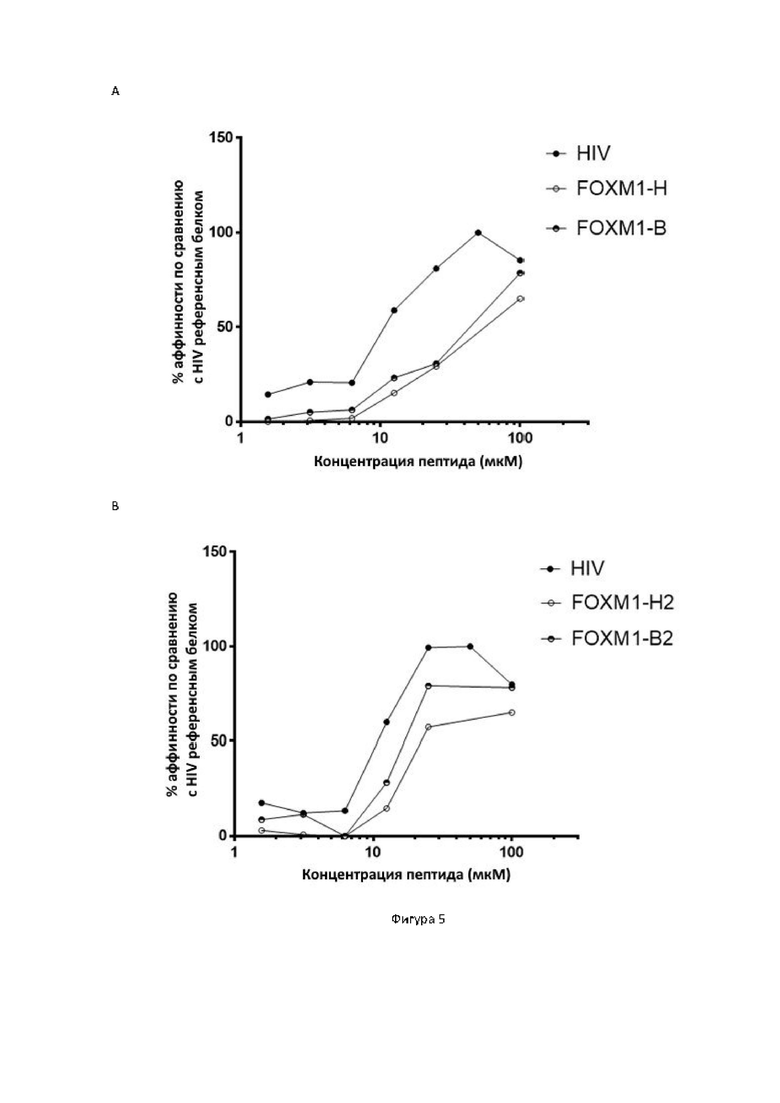


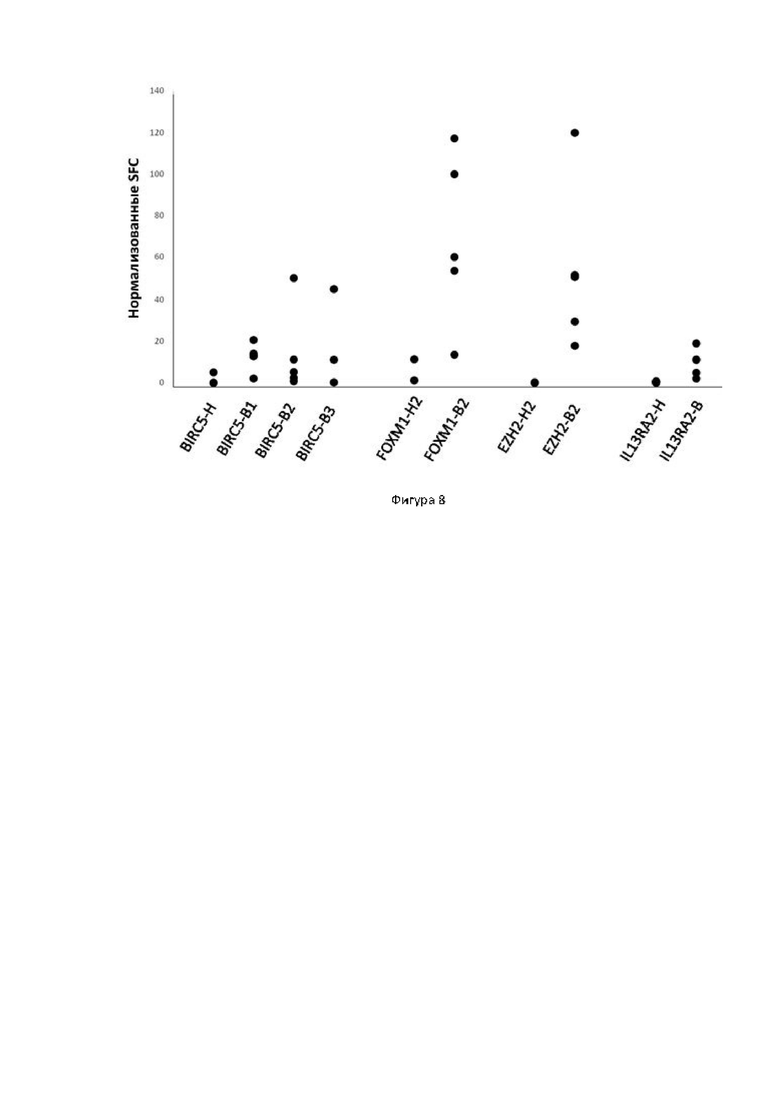
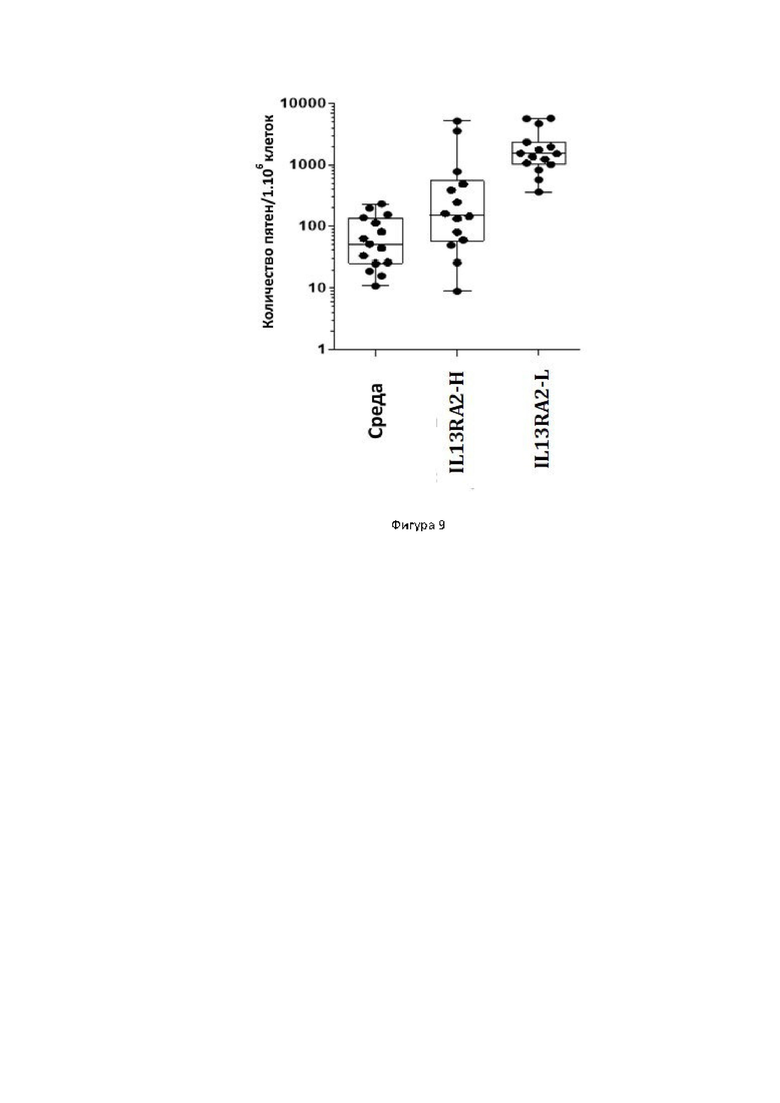



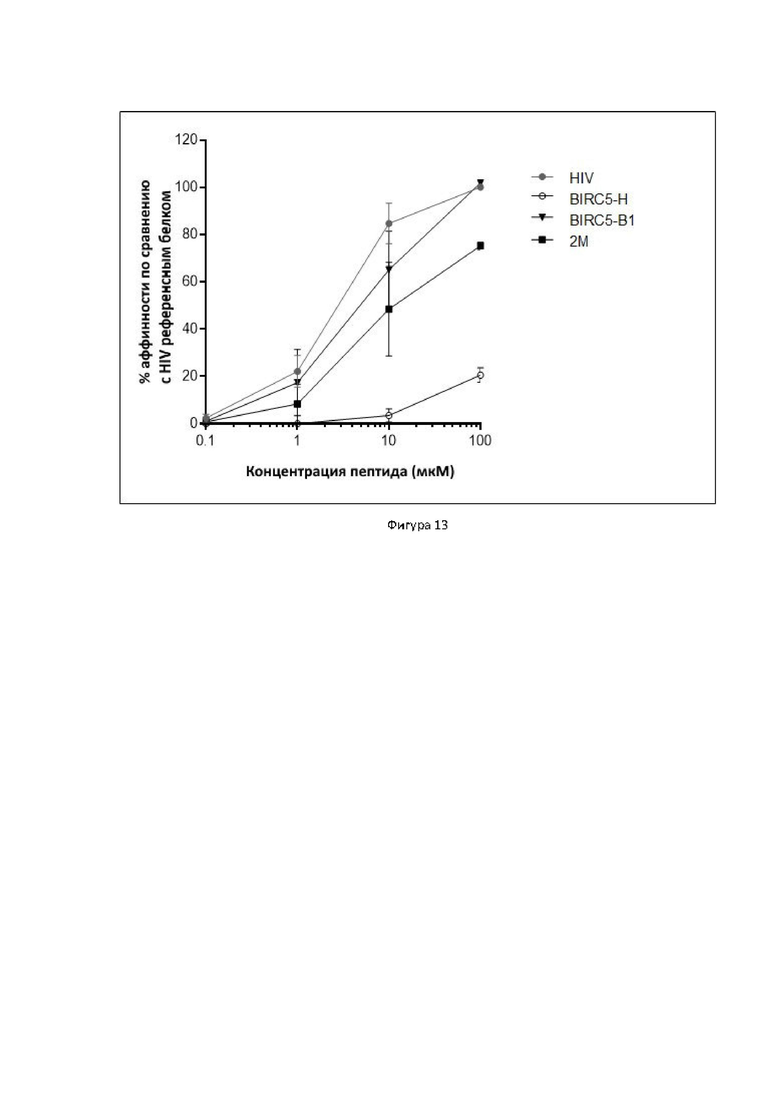
Настоящее изобретение относится к иммунотерапии, основанной на применении антигенов, конкретнее - к иммунотерапии рака. В частности, настоящее изобретение относится к антигенным пептидам, сходным по аминокислотному составу с фрагментами опухолевых антигенов человека, но отличающимся от них. Настоящее изобретение также относится к иммуногенным соединениям, клеткам и фармацевтическим композициям, содержащим такие антигенные пептиды и нуклеиновые кислоты, кодирующие такие антигенные пептиды. Изобретение предоставляет альтернативные способы лечения рака, которые позволят преодолеть существующие ограничения. 13 н. и 40 з.п. ф-лы, 13 ил., 10 табл., 9 пр.
1. Антигенный пептид для лечения рака, который состоит из или включает в себя аминокислотную последовательность, как указано в любой из SEQ ID NO: 32, 220, 1 – 31, 33 – 219, 221 – 580 и 861 – 887.
2. Антигенный пептид по п. 1, причем антигенный пептид состоит из или включает в себя аминокислотную последовательность, как указано в SEQ ID NO: 32.
3. Антигенный пептид по п. 1, причем антигенный пептид состоит из или включает в себя аминокислотную последовательность, как указано в SEQ ID NO: 220.
4. Антигенный пептид по п. 1, причем антигенный пептид состоит из или включает в себя аминокислотную последовательность, как указано в SEQ ID NO: 255.
5. Антигенный пептид по любому из пп. 1-4, причем длина антигенного пептида не превышает 30 аминокислот.
6. Антигенный пептид по любому из пп. 1-4, причем длина антигенного пептида не превышает 25 аминокислот.
7. Антигенный пептид по любому из пп. 1-4, причем длина антигенного пептида не превышает 20 аминокислот.
8. Антигенный пептид по любому из пп. 1-4, причем длина антигенного пептида не превышает 15 аминокислот.
9. Антигенный пептид по любому из пп. 1-8, причем антигенный пептид не является полноразмерным (микробиотическим) белком.
10. Иммуногенное соединение для лечения рака, которое включает антигенный пептид по любому из пп. 1-9.
11. Иммуногенное соединение по п. 10, причем антигенный пептид связан с молекулой носителя.
12. Иммуногенное соединение по п. 11, причем молекула носителя представляет собой белок-носитель или пептид-носитель.
13. Иммуногенное соединение по любому из пп. 10-12, состоящее из или включающее в себя полипептид формулы (I)
PepNt-CORE-PepCt (I)
где:
-"PepNt" состоит из полипептида, имеющего длину от 0 до 500 аминокислотных остатков и расположенного на N-конце полипептида формулы (I);
-"CORE" состоит из антигенного пептида по настоящему изобретению, как определено в любом из пп. 1-9; и
-"PepCt" состоит из полипептида, имеющего длину от 0 до 500 аминокислотных остатков и расположенного на С-конце полипептида формулы (I).
14. Антигенпрезентирующая клетка для лечения рака, которая нагружена антигенным пептидом по любому из пп. 1-9 или иммуногенным соединением по любому из пп. 10-13.
15. Антигенпрезентирующая клетка по п. 14, где указанная клетка представляет собой дендритную клетку.
16. Нуклеиновая кислота для лечения рака, кодирующая антигенный пептид по любому из пп. 1-9 или иммуногенное соединение по любому из пп. 10-13, причем указанное иммуногенное соединение представляет собой пептид или белок.
17. Нуклеиновая кислота по п. 16, причем нуклеиновая кислота представляет собой молекулу ДНК или молекулу РНК; предпочтительно, выбранную из геномной ДНК; кДНК; иРНК; антисмысловой ДНК; антисмысловой РНК; комплементарных РНК и/или ДНК последовательностей; а также их комбинации.
18. Фармацевтическая композиция для лечения рака, которая включает эффективное количество
- антигенного пептида по любому из пп. 1-9,
- иммуногенного соединения по любому из пп. 10-13,
- антигенпрезентирующей клетки по п. 14 или 15, и/или
- нуклеиновой кислоты по п. 16 или 17.
19. Фармацевтическая композиция по п. 18, дополнительно включающая один или более иммуностимулирующий агент.
20. Фармацевтическая композиция по п. 19, причем иммуностимулирующий агент выбран из группы, включающей иммуноадъюванты и антигенпрезентирующие клетки.
21. Фармацевтическая композиция по п. 20, причем антигенпрезентирующая клетка представляет собой дендритную клетку.
22. Фармацевтическая композиция по любому из пп. 18-21, причем указанная фармацевтическая композиция включает
(а) по меньшей мере два различных антигенных пептида по любому из пп. 1-9;
(б) по меньшей мере два различных иммуногенных соединения по любому из пп. 10-13; и/или
(в) по меньшей мере две различные нуклеиновые кислоты по п. 16 или 17.
23. Применение антигенного пептида по любому из пп. 1-9,
иммуногенного соединения по любому из пп. 10-13,
антигенпрезентирующей клетки по п. 14 или 15,
нуклеиновой кислоты по п. 16 или 17, или
фармацевтической композиции по любому из пп. 18-22,
в лечении рака.
24. Применение по п. 23, причем рак выбран из глиомы, рака почки, рака кожи, предпочтительно меланомы, рака легких, рака яичников, рака молочной железы, колоректального рака, рака печени, рака поджелудочной железы, рака головы и шеи, уротелиального рака и рака предстательной железы.
25. Комбинация для лечения рака, которая содержит по меньшей мере два различных антигенных пептида по любому из пп. 1-9.
26. Комбинация для лечения рака, которая содержит по меньшей мере две различные нуклеиновые кислоты по п. 16 или 17.
27. Комбинация по п. 25 или 26, причем по меньшей мере два различных компонента находятся в составе различных композиций.
28. Комбинация по п. 25 или 26, причем по меньшей мере два различных компонента находятся в составе одной композиции.
29. Применение комбинации по п. 25 или 26 в лечении рака.
30. Применение по п. 29, причем по меньшей мере два различных компонента вводятся разными способами введения.
31. Применение по п. 29, причем по меньшей мере два различных компонента вводятся одним и тем же способом введения.
32. Применение по любому из пп. 29-31, причем по меньшей мере два различных компонента вводятся последовательно.
33. Применение по любому из пп. 29-31, причем по меньшей мере два различных компонента вводятся приблизительно в одно и то же время.
34. Способ лечения рака у субъекта, нуждающегося в этом, включающий введение субъекту
- антигенного пептида по любому из пп. 1-9,
- иммуногенного соединения по любому из пп. 10-13,
- антигенпрезентирующей клетки по п. 14 или 15,
-нуклеиновой кислоты по п. 16 или 17,
- фармацевтической композиции по любому из пп. 18-22, и/или
- комбинации, как определено в любом из пп. 25-26.
35. Способ по п. 34, где рак выбран из глиомы, рака почек, рака кожи, в частности, меланомы, рака легких, рака яичников, рака молочной железы, колоректального рака, рака печени, рака поджелудочной железы, рака головы и шеи, рака уротелия и рака предстательной железы.
36. Способ усиления противоопухолевого ответа у субъекта, нуждающегося в этом, включающий введение субъекту
- антигенного пептида по любому из пп. 1-9,
- иммуногенного соединения по любому из пп. 10-13,
- антигенпрезентирующей клетки по п. 14 или 15,
- нуклеиновой кислоты по п.16 или 17,
- фармацевтической композиции по любому из пп. 18-22, и/или
- комбинации по любому из пп. 25-26.
37. Способ по п. 36, где рак выбран из глиомы, рака почек, рака кожи, в частности, меланомы, рака легких, рака яичников, рака молочной железы, колоректального рака, рака печени, рака поджелудочной железы, рака головы и шеи, рака уротелия и рака предстательной железы.
38. Способ продления противоопухолевого ответа у субъекта, нуждающегося в этом, включающий введение субъекту
- антигенного пептида по любому из пп. 1-9,
- иммуногенного соединения по любому из пп. 10-13,
- антигенпрезентирующей клетки по п. 14 или 15,
- нуклеиновой кислоты по п. 16 или 17,
- фармацевтической композиции по любому из пп. 18-22, и/или
- комбинации по любому из пп. 25-26.
39. Способ по п. 38, причем рак выбран из глиомы, рака почек, рака кожи, в частности, меланомы, рака легких, рака яичников, рака молочной железы, колоректального рака, рака печени, рака поджелудочной железы, рака головы и шеи, рака уротелия и рака предстательной железы.
40. Мультимер пептид-MHC (pMHC) для обнаружения антигенспецифических Т-клеток, включающий антигенный пептид по любому из пп. 1-9.
| УСТРОЙСТВО ДЛЯ ОГРАНИЧЕНИЯ УГЛА ПОВОРОТА СТВОРКИ С ОПОРНЫМ ОТВЕРСТИЕМ В ЛЕВОЙ КРЫШКЕ И ПРАВЫМ ПОЛЗУНКОМ | 2015 |
|
RU2600898C1 |
| XIAO Y.F | |||
| et al., Peptide-Based Treatment: A Promising Cancer Therapy, J Immunol Res., 2015, vol | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| DHANIK A | |||
| et al., In-silico discovery of cancer-specific peptide-HLA complexes for targeted therapy, BMC Bioinformatics, 2016, vol | |||
| Печь для сжигания твердых и жидких нечистот | 1920 |
|
SU17A1 |
| Устройство для определения усилий в статически неопределенных системах | 1931 |
|
SU25758A1 |
Авторы
Даты
2024-02-05—Публикация
2019-04-11—Подача