[0001] Настоящая заявка заявляет приоритет предварительной заявки на патент США № 62/831415, поданной 9 апреля 2019 г., и заявки на европейский патент № EP19306312.0, поданной 8 октября 2019 г., раскрытия которых включены в данный документ посредством ссылки в их полном объеме.
ПРЕДСТАВЛЕНИЕ ПЕРЕЧНЯ ПОСЛЕДОВАТЕЛЬНОСТЕЙ В ТЕКСТОВОМ ФАЙЛЕ ASCII
[0002] Содержание нижеследующего представленного текстового файла ASCII включено в данный документ посредством ссылки в его полном объеме: машиночитаемая форма (CRF) перечня последовательностей (название файла: 183952031940SEQLIST.TXT, дата составления: 25 марта 2020 г., размер: 580 КБ).
Область техники изобретения
[0003] Настоящее изобретение относится к триспецифическим и/или тривалентным связывающим белкам, содержащим четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, специфически связывающие один или несколько целевых белков HIV, где первая пара полипептидов, образующих связывающий белок, содержит два вариабельных домена, характеризующихся кроссоверной ориентацией. Настоящее изобретение также относится к способам получения триспецифических и/или тривалентных связывающих белков и вариантам применения таких связывающих белков для лечения и/или предупреждения инфекции HIV/СПИД.
Предпосылки изобретения
[0004] Антиретровирусная терапия (ART) в последние десятилетия является стандартом лечения пациентов с инфекцией HIV/СПИД. Лекарственные средства для ART нацелены на внутренние белки, такие как обратная транскриптаза (RT), интеграза (IN) и вирусная протеаза (PI), путем ингибирования обратной транскрипции генома HIV-1, встраивания генома HIV-1 и протеолитического расщепления необходимых белков-предшественников для продуцирования инфекционных вирусных частиц. Лечение с применением ART или комбинации различных классов ART приводит в результате к ингибированию репликации HIV-1 и последующему снижению виремии, зачастую до невыявляемого уровня (авиремического статуса). Хотя ART очень помогает пациентам с HIV контролировать прогрессирование своего заболевания и сдерживать глобальную эпидемию HIV, она на самом деле требует от пациентов ежедневного приема лекарственных препаратов зачастую согласно строгой схеме. Приблизительно 10% пациентов каждый год не могут пройти терапию из-за токсичности лекарственных средств, недостаточного соблюдения режима лечения и возникающей устойчивости к лекарственным средствам. Поскольку все больше пациентов с HIV могут прожить до нормального предельного возраста (более 80 лет), особую озабоченность вызывают хронические осложнения, такие как старение и взаимодействие лекарственных средств, а также токсичность со стороны сердечно-сосудистой системы/почек/костей. Экономическое бремя от лечения от инфекции HIV/СПИД до сих пор не ослабло.
[0005] HIV в латентной форме инфицирует долгоживущие, находящиеся в состоянии покоя CD4+ Т-клетки памяти и другие клетки в форме провирусной ДНК, встроенной в геном хозяина. Клетки, инфицированные в латентной форме, выживают десятилетиями и самовозобновляются по типу ст
[0006] воловых клеток посредством гомеостатической пролиферации, которая рассматривается как резервуар HIV-1. Резервуары HIV-1 не подвергаются воздействию ни со стороны ART, ни со стороны иммунной системы хозяина, поскольку они не экспрессируют вирусные белки. Тем не менее, небольшая доля клеток среди резервуаров случайным образом реактивируются благодаря неизвестному(-ым) механизму(-ам), который(-е) отвечает(-ют) за рецидив виремии после прекращения ART.
[0007] Следовательно, существует потребность в разработке средств лечения инфекции, вызываемой HIV/СПИД, которые нацелены на резервуар(-ы) HIV-1 и, в конечном итоге, его(их) полного устранения, достижения излечения или долговременной ремиссии HIV без какого-либо дополнительного лечения. При любой терапевтической стратегии по устранению резервуара HIV-1 сначала необходимо активировать резервуар с последующим устранением активированных клеток резервуара HIV-1.
[0008] Все цитируемые в данном документе ссылочные материалы, в том числе заявки на патенты, патентные публикации и номера доступа в UniProtKB/Swiss-Prot, включены в данный документ посредством ссылки в их полном объеме, как если бы специально и индивидуально было указано, что каждый отдельный ссылочный материал включен посредством ссылки.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0009] Для удовлетворения этих и других потребностей в данном документе предусмотрены мультиспецифические связывающие белки (например, антитела), которые образуют три антигенсвязывающих участка. В некоторых вариантах осуществления связывающие белки связывают один или несколько целевых белков HIV и полипептид CD3. В некоторых вариантах осуществления связывающие белки связывают целевой белок HIV, полипептид CD28 и полипептид CD3. Считается, что раскрытая в данном документе концепция триспецифического антитела-активатора Т-клеток к HIV/CD28xCD3 (TCE) позволит создать эффективное средство для устранения резервуара HIV-1 посредством активации антител к CD3, совместной активации антител к CD28 и последующего уничтожения активированных клеток резервуара HIV-1 посредством антител к HIV/к CD28 путем вовлечения активированных CD8 Т-клеток, что обеспечивает потенциальную стратегию для осуществления атаки на резервуар HIV-1. Кроме того, описаны участки связывания антител к CD3 с высокой аффинностью связывания с полипептидами CD3 человека и устранены потенциальные недостатки при изготовлении (например, участки дезамидирования).
[0010] В некоторых вариантах осуществления в данном документе предусмотрены связывающие белки, содержащие четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит структуру, представленную формулой
VL2-L1-VL1-L2-CL [I];
и вторая полипептидная цепь содержит структуру, представленную формулой
VH1-L3-VH2-L4-CH1-шарнир-CH2-CH3 [II];
и третья полипептидная цепь содержит структуру, представленную формулой
VH3-CH1-шарнир-CH2-CH3 [III];
и четвертая полипептидная цепь содержит структуру, представленную формулой
VL3-CL [IV];
где:
VL1 представляет собой первый вариабельный домен легкой цепи иммуноглобулина;
VL2 представляет собой второй вариабельный домен легкой цепи иммуноглобулина;
VL3 представляет собой третий вариабельный домен легкой цепи иммуноглобулина;
VH1 представляет собой первый вариабельный домен тяжелой цепи иммуноглобулина;
VH2 представляет собой второй вариабельный домен тяжелой цепи иммуноглобулина;
VH3 представляет собой третий вариабельный домен тяжелой цепи иммуноглобулина;
CL представляет собой константный домен легкой цепи иммуноглобулина;
CH1 представляет собой константный домен CH1 тяжелой цепи иммуноглобулина;
CH2 представляет собой константный домен CH2 тяжелой цепи иммуноглобулина;
CH3 представляет собой константный домен CH3 тяжелой цепи иммуноглобулина;
шарнир представляет собой шарнирную область иммуноглобулина, соединяющую домены CH1 и CH2; и
L1, L2, L3 и L4 представляют собой аминокислотные линкеры;
где полипептид формулы I и полипептид формулы II образуют кроссоверную пару легкая цепь-тяжелая цепь;
где VH1 и VL1 образуют первый антигенсвязывающий участок;
где VH2 и VL2 образуют второй антигенсвязывающий участок, который связывает полипептид CD3, где домен VH2 содержит последовательность CDR-H1, содержащую аминокислотную последовательность GFTFTKAW (SEQ ID NO:20), последовательность CDR-H2, содержащую аминокислотную последовательность IKDKSNSYAT (SEQ ID NO:21), и последовательность CDR-H3, содержащую аминокислотную последовательность RGVYYALSPFDY (SEQ ID NO:22), и домен VL2 содержит последовательность CDR-L1, содержащую аминокислотную последовательность QSLVHX1NX2X3TY, где X1 представляет собой E или Q, X2 представляет собой A или L, и X3 представляет собой Q, R или F (SEQ ID NO:293), последовательность CDR-L2, содержащую аминокислотную последовательность KVS (SEQ ID NO:29), и последовательность CDR-L3, содержащую аминокислотную последовательность gqgtqypft (SEQ ID NO:30); и
где VH3 и VL3 образуют третий антигенсвязывающий участок, который связывает целевой белок HIV.
[0011] В некоторых вариантах осуществления первый связывающий участок связывает полипептид CD28 (например, полипептид CD28 человека). В некоторых вариантах осуществления домен VH1 содержит последовательность CDR-H1, содержащую аминокислотную последовательность GYTFTSYY (SEQ ID NO:31), последовательность CDR-H2, содержащую аминокислотную последовательность IYPGNVNT (SEQ ID NO:32), и последовательность CDR-H3, содержащую аминокислотную последовательность TRSHYGLDWNFDV (SEQ ID NO:33), и домен VL1 содержит последовательность CDR-L1, содержащую аминокислотную последовательность QNIYVW (SEQ ID NO:34), последовательность CDR-L2, содержащую аминокислотную последовательность KAS (SEQ ID NO:35), и последовательность CDR-L3, содержащую аминокислотную последовательность QQGQTYPY (SEQ ID NO:36). В некоторых вариантах осуществления домен VH1 содержит аминокислотную последовательность QVQLVQSGAEVVKPGASVKVSCKASGYTFTSYYIHWVRQAPGQGLEWIGSIYPGNVNTNYAQKFQGRATLTVDTSISTAYMELSRLRSDDTAVYYCTRSHYGLDWNFDVWGKGTTVTVSS (SEQ ID NO:59), и/или домен VL1 содержит аминокислотную последовательность DIQMTQSPSSLSASVGDRVTITCQASQNIYVWLNWYQQKPGKAPKLLIYKASNLHTGVPSRFSGSGSGTDFTLTISSLQPEDIATYYCQQGQTYPYTFGQGTKLEIK (SEQ ID NO:60).
[0012] В некоторых вариантах осуществления последовательность CDR-L1 домена VL2 содержит аминокислотную последовательность, выбранную из группы, состоящей из QSLVHQNAQTY (SEQ ID NO:24), QSLVHENLQTY (SEQ ID NO:25), QSLVHENLFTY (SEQ ID NO:26) и QSLVHENLRTY (SEQ ID NO:27). В некоторых вариантах осуществления домен VH2 содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий последовательность CDR-H1, содержащую аминокислотную последовательность GFTFTKAW (SEQ ID NO:20), последовательность CDR-H2, содержащую аминокислотную последовательность IKDKSNSYAT (SEQ ID NO:21), и последовательность CDR-H3, содержащую аминокислотную последовательность RGVYYALSPFDY (SEQ ID NO:22), и домен VL2 содержит последовательность CDR-L1, содержащую аминокислотную последовательность QSLVHQNAQTY (SEQ ID NO:24), последовательность CDR-L2, содержащую аминокислотную последовательность KVS (SEQ ID NO:29), и последовательность CDR-L3, содержащую аминокислотную последовательность GQGTQYPFT (SEQ ID NO:30). В некоторых вариантах осуществления домен VH2 содержит последовательность CDR-H1, содержащую аминокислотную последовательность GFTFTKAW (SEQ ID NO:20), последовательность CDR-H2, содержащую аминокислотную последовательность IKDKSNSYAT (SEQ ID NO:21), и последовательность CDR-H3, содержащую аминокислотную последовательность RGVYYALSPFDY (SEQ ID NO:22), и домен VL2 содержит последовательность CDR-L1, содержащую аминокислотную последовательность QSLVHENLQTY (SEQ ID NO:25), последовательность CDR-L2, содержащую аминокислотную последовательность KVS (SEQ ID NO:29), и последовательность CDR-L3, содержащую аминокислотную последовательность GQGTQYPFT (SEQ ID NO:30). В некоторых вариантах осуществления домен VH2 содержит последовательность CDR-H1, содержащую аминокислотную последовательность GFTFTKAW (SEQ ID NO:20), последовательность CDR-H2, содержащую аминокислотную последовательность IKDKSNSYAT (SEQ ID NO:21), и последовательность CDR-H3, содержащую аминокислотную последовательность RGVYYALSPFDY (SEQ ID NO:22), и домен VL2 содержит последовательность CDR-L1, содержащую аминокислотную последовательность QSLVHENLFTY (SEQ ID NO:26), последовательность CDR-L2, содержащую аминокислотную последовательность KVS (SEQ ID NO:29), и последовательность CDR-L3, содержащую аминокислотную последовательность GQGTQYPFT (SEQ ID NO:30). В некоторых вариантах осуществления домен VH2 содержит последовательность CDR-H1, содержащую аминокислотную последовательность GFTFTKAW (SEQ ID NO:20), последовательность CDR-H2, содержащую аминокислотную последовательность IKDKSNSYAT (SEQ ID NO:21), и последовательность CDR-H3, содержащую аминокислотную последовательность RGVYYALSPFDY (SEQ ID NO:22), и домен VL2 содержит последовательность CDR-L1, содержащую аминокислотную последовательность QSLVHENLRTY (SEQ ID NO:27), последовательность CDR-L2, содержащую аминокислотную последовательность KVS (SEQ ID NO:29), и последовательность CDR-L3, содержащую аминокислотную последовательность GQGTQYPFT (SEQ ID NO:30). В некоторых вариантах осуществления домен VH2 содержит аминокислотную последовательность QVQLVESGGGVVQPGRSLRLSCAASGFTFTKAWMHWVRQAPGKQLEWVAQIKDKSNSYATYYADSVKGRFTISRDDSKNTLYLQMNSLRAEDTAVYYCRGVYYALSPFDYWGQGTLVTVSS (SEQ ID NO:52), и/или домен VL2 содержит аминокислотную последовательность, выбранную из группы, состоящей из DIVMTQTPLSLSVTPGQPASISCKSSQSLVHQNAQTYLSWYLQKPGQSPQSLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCGQGTQYPFTFGSGTKVEIK (SEQ ID NO:54), DIVMTQTPLSLSVTPGQPASISCKSSQSLVHENLQTYLSWYLQKPGQSPQSLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCGQGTQYPFTFGSGTKVEIK (SEQ ID NO:55), DIVMTQTPLSLSVTPGQPASISCKSSQSLVHENLFTYLSWYLQKPGQSPQSLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCGQGTQYPFTFGSGTKVEIK (SEQ ID NO:56) и DIVMTQTPLSLSVTPGQPASISCKSSQSLVHENLRTYLSWYLQKPGQSPQSLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCGQGTQYPFTFGSGTKVEIK (SEQ ID NO:57). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:52, и/или вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:54. В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:52, и/или вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:55. В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:52, и/или вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:56. В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:52, и/или вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:57.
[0013] В некоторых вариантах осуществления третий антигенсвязывающий участок связывает целевой белок HIV, выбранный из группы, состоящей из гликопротеина 120, гликопротеина 41 и гликопротеина 160. В некоторых вариантах осуществления домен VH3 содержит последовательность CDR-H1, содержащую аминокислотную последовательность NCPIN (SEQ ID NO:1), последовательность CDR-H2, содержащую аминокислотную последовательность WMKPRHGAVSYARQLQG (SEQ ID NO:2), и последовательность CDR-H3, содержащую аминокислотную последовательность GKYCTARDYYNWDFEH (SEQ ID NO:3), и домен VL3 содержит последовательность CDR-L1, содержащую аминокислотную последовательность RTSQYGSLA (SEQ ID NO:4), последовательность CDR-L2, содержащую аминокислотную последовательность SGSTRAA (SEQ ID NO:5), и последовательность CDR-L3, содержащую аминокислотную последовательность QQYEF (SEQ ID NO:6). В некоторых вариантах осуществления домен VH3 содержит последовательность CDR-H1, содержащую аминокислотную последовательность GYTFTAHI (SEQ ID NO:7), последовательность CDR-H2, содержащую аминокислотную последовательность IKPQYGAV (SEQ ID NO:8) или IKPQYGAT (SEQ ID NO:9), и последовательность CDR-H3, содержащую аминокислотную последовательность DRSYGDSSWALDA (SEQ ID NO:10), и домен VL3 содержит последовательность CDR-L1, содержащую аминокислотную последовательность QGVGSD (SEQ ID NO:11), последовательность CDR-L2, содержащую аминокислотную последовательность HTS (SEQ ID NO:12), и последовательность CDR-L3, содержащую аминокислотную последовательность CQVLQF (SEQ ID NO:13). В некоторых вариантах осуществления домен VH3 содержит последовательность CDR-H1, содержащую аминокислотную последовательность DCTLN (SEQ ID NO:14), последовательность CDR-H2, содержащую аминокислотную последовательность WLKPRWGAVNYARPLQG (SEQ ID NO:15), и последовательность CDR-H3, содержащую аминокислотную последовательность GKNCDYNWDFEH (SEQ ID NO:16), и домен VL3 содержит последовательность CDR-L1, содержащую аминокислотную последовательность RTSQYGSLA (SEQ ID NO:17), последовательность CDR-L2, содержащую аминокислотную последовательность SGSTRAA (SEQ ID NO:18), и последовательность CDR-L3, содержащую аминокислотную последовательность QQYEF (SEQ ID NO:19). В некоторых вариантах осуществления домен VH3 содержит аминокислотную последовательность QVRLSQSGGQMKKPGDSMRISCRASGYEFINCPINWIRLAPGKRPEWMGWMKPRHGAVSYARQLQGRVTMTRDMYSETAFLELRSLTSDDTAVYFCTRGKYCTARDYYNWDFEHWGQGTPVTVSS (SEQ ID NO:43), и/или домен VL3 содержит аминокислотную последовательность SLTQSPGTLSLSPGETAIISCRTSQYGSLAWYQQRPGQAPRLVIYSGSTRAAGIPDRFSGSRWGPDYNLTISNLESGDFGVYYCQQYEFFGQGTKVQVDIK (SEQ ID NO:45). В некоторых вариантах осуществления домен VH3 содержит аминокислотную последовательность QVRLSQSGGQMKKPGDSMRISCRASGYEFINCPINWIRLAPGKRPEWMGWMKPRHGAVSYARQLQGRVTMTRQLSQDPDDPDWGTAFLELRSLTSDDTAVYFCTRGKYCTARDYYNWDFEHWGQGTPVTVSS (SEQ ID NO:44), и/или домен VL3 содержит аминокислотную последовательность SLTQSPGTLSLSPGETAIISCRTSQYGSLAWYQQRPGQAPRLVIYSGSTRAAGIPDRFSGSRWGPDYNLTISNLESGDFGVYYCQQYEFFGQGTKVQVDIK (SEQ ID NO:45). В некоторых вариантах осуществления домен VH3 содержит аминокислотную последовательность RAHLVQSGTAMKKPGASVRVSCQTSGYTFTAHILFWFRQAPGRGLEWVGWIKPQYGAVNFGGGFRDRVTLTRDVYREIAYMDIRGLKPDDTAVYYCARDRSYGDSSWALDAWGQGTTVVVSA (SEQ ID NO:46), и/или домен VL3 содержит аминокислотную последовательность YIHVTQSPSSLSVSIGDRVTINCQTSQGVGSDLHWYQHKPGRAPKLLIHHTSSVEDGVPSRFSGSGFHTSFNLTISDLQADDIATYYCQVLQFFGRGSRLHIK (SEQ ID NO:49). В некоторых вариантах осуществления домен VH3 содержит аминокислотную последовательность RAHLVQSGTAMKKPGASVRVSCQTSGYTFTAHILFWFRQAPGRGLEWVGWIKPQYGATNFGGGFRDRVTLTRDVYREIAYMDIRGLKPDDTAVYYCARDRSYGDSSWALDAWGQGTTVVVSA (SEQ ID NO:47), и/или домен VL3 содержит аминокислотную последовательность YIHVTQSPSSLSVSIGDRVTINCQTSQGVGSDLHWYQHKPGRAPKLLIHHTSSVEDGVPSRFSGSGFHTSFNLTISDLQADDIATYYCQVLQFFGRGSRLHIK (SEQ ID NO:49). В некоторых вариантах осуществления домен VH3 содержит аминокислотную последовательность RAHLVQSGTAMKKPGASVRVSCQTSGYTFTAHILFWFRQAPGRGLEWVGWIKPQYGAVNFGGGFRDRVTLTRQLSQDPDDPDWGIAYMDIRGLKPDDTAVYYCARDRSYGDSSWALDAWGQGTTVVVSA (SEQ ID NO:48), и/или домен VL3 содержит аминокислотную последовательность YIHVTQSPSSLSVSIGDRVTINCQTSQGVGSDLHWYQHKPGRAPKLLIHHTSSVEDGVPSRFSGSGFHTSFNLTISDLQADDIATYYCQVLQFFGRGSRLHIK (SEQ ID NO:49). В некоторых вариантах осуществления домен VH3 содержит аминокислотную последовательность QVQLVQSGGQMKKPGESMRISCRASGYEFIDCTLNWIRLAPGKRPEWMGWLKPRWGAVNYARPLQGRVTMTRQLSQDPDDPDWGTAFLELRSLTVDDTAVYFCTRGKNCDYNWDFEHWGRGTPVIVSS (SEQ ID NO:50), и/или домен VL3 содержит аминокислотную последовательность LTQSPGTLSLSPGETAIISCRTSQYGSLAWYQQRPGQAPRLVIYSGSTRAAGIPDRFSGSRWGPDYNLTISNLESGDFGVYYCQQYEFFGQGTKVQVDIK (SEQ ID NO:51).
[0014] В некоторых вариантах осуществления, которые могут представлять собой объединение любых других вариантов осуществления, описанных в данном документе, по меньшей мере один из L1, L2, L3 или L4 независимо имеет длину, составляющую 0 аминокислот. В некоторых вариантах осуществления каждый из L1, L2, L3 и L4 независимо имеет длину, составляющую ноль аминокислот, или содержит последовательность, выбранную из группы, состоящей из GGGGSGGGGS (SEQ ID NO:40), GGGGSGGGGSGGGGS (SEQ ID NO:41), S, RT, TKGPS (SEQ ID NO:39), GQPKAAP (SEQ ID NO:38) и GGSGSSGSGG (SEQ ID NO:42). В некоторых вариантах осуществления каждый из L1, L2, L3 и L4 независимо содержит последовательность, выбранную из группы, состоящей из GGGGSGGGGS (SEQ ID NO:40), GGGGSGGGGSGGGGS (SEQ ID NO:41), S, RT, TKGPS (SEQ ID NO:39), GQPKAAP (SEQ ID NO:38) и GGSGSSGSGG (SEQ ID NO:42). В некоторых вариантах осуществления L1 содержит последовательность GQPKAAP (SEQ ID NO:38), L2 содержит последовательность TKGPS (SEQ ID NO:39), L3 содержит последовательность S, и L4 содержит последовательность RT. В некоторых вариантах осуществления по меньшей мере один из L1, L2, L3 или L4 содержит последовательность DKTHT (SEQ ID NO:37). В некоторых вариантах осуществления L1, L2, L3 и L4 содержат последовательность DKTHT (SEQ ID NO:37).
[0015] В некоторых вариантах осуществления, которые могут представлять собой объединение любых других вариантов осуществления, описанных в данном документе, домены шарнир-CH2-CH3 второй и третьей полипептидных цепей представляют собой домены шарнир_IgG4-CH2-CH3 человека, и при этом каждый из доменов шарнир-CH2-CH3 содержит аминокислотные замены в положениях, соответствующих положениям 234 и 235 IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой F234A и L235A. В некоторых вариантах осуществления домены шарнир-CH2-CH3 второй и третьей полипептидных цепей представляют собой домены шарнир_IgG4-CH2-CH3 человека, и при этом каждый из доменов шарнир-CH2-CH3 содержит аминокислотные замены в положениях, соответствующих положениям 233-236 IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой E233P, F234V, L235A, и делецию в положении 236. В некоторых вариантах осуществления домены шарнир-CH2-CH3 второй и третьей полипептидных цепей представляют собой домены шарнир_IgG4-CH2-CH3 человека, и при этом каждый из доменов шарнир-CH2-CH3 содержит аминокислотные замены в положениях, соответствующих положениям 228 и 409 IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой S228P и R409K. В некоторых вариантах осуществления домены шарнир-CH2-CH3 второй и третьей полипептидных цепей представляют собой домены шарнир_IgG1-CH2-CH3 человека, и при этом каждый из доменов шарнир-CH2-CH3 содержит аминокислотные замены в положениях, соответствующих положениям 234, 235 и 329 IgG1 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой L234A, L235A и P329A. В некоторых вариантах осуществления домены шарнир-CH2-CH3 второй и третьей полипептидных цепей представляют собой домены шарнир_IgG1-CH2-CH3 человека, и при этом каждый из доменов шарнир-CH2-CH3 содержит аминокислотные замены в положениях, соответствующих положениям 298, 299 и 300 IgG1 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой S298N, T299A и Y300S. В некоторых вариантах осуществления домен шарнир-CH2-CH3 второй полипептидной цепи содержит аминокислотные замены в положениях, соответствующих положениям 349, 366, 368 и 407 IgG1 или IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой Y349C, T366S, L368A и Y407V; и где домен шарнир-CH2-CH3 третьей полипептидной цепи содержит аминокислотные замены в положениях, соответствующих положениям 354 и 366 IgG1 или IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой S354C и T366W. В некоторых вариантах осуществления домен шарнир-CH2-CH3 второй полипептидной цепи содержит аминокислотные замены в положениях, соответствующих положениям 354 и 366 IgG1 или IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой S354C и T366W; и где домен шарнир-CH2-CH3 третьей полипептидной цепи содержит аминокислотные замены в положениях, соответствующих положениям 349, 366, 368 и 407 IgG1 или IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой Y349C, T366S, L368A и Y407V.
[0016] В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:61 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:61; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:62 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:62; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:63 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:63; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:64 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:64. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:65 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:65; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:66 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:66; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:67 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:67; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:68 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:68. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:69 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:69; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:70 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:70; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:71 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:71; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:72 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:72. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:73 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:73; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:74 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:74; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:75 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:75; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:76 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:76. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:77 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:77; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:78 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:78; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:79 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:79; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:80 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:80. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:81 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:81; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:82 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:82; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:83 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:83; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:84 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:84. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:85 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:85; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:86 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:86; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:87 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:87; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:88 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:88. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:89 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:89; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:90 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:90; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:91 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:91; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:92 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:92. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:93 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:93; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:94 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:94; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:95 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:95; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:96 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:96. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:97 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:97; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:98 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:98; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:99 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:99; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:100 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:100. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:101 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:101; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:102 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:102; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:103 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:103; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:104 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:104. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:105 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:105; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:106 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:106; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:107 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:107; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:108 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:108. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:109 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:109; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:110 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:110; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:111 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:111; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:112 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:112. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:113 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:113; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:114 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:114; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:115 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:115; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:116 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:116. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:117 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:117; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:118 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:118; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:119 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:119; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:120 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:120. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:121 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:121; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:122 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:122; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:123 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:123; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:124 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:124. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:129 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:129; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:130 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:130; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:131 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:131; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:132 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:132. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:133 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:133; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:134 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:134; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:135 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:135; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:136 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:136. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:137 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:137; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:138 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:138; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:139 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:139; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:140 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:140. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:141 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:141; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:142 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:142; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:143 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:143; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:144 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:144. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:145 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:145; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:146 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:146; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:147 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:147; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:148 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:148. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:149 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:149; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:150 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:150; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:151 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:151; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:152 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:152. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:153 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:153; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:154 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:154; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:155 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:155; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:156 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:156. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:157 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:157; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:158 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:158; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:159 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:159; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:160 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:160. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:161 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:161; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:162 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:162; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:163 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:163; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:164 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:164. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:165 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:165; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:166 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:166; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:167 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:167; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:168 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:168. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:169 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:169; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:170 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:170; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:171 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:171; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:172 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:172. В некоторых вариантах осуществления первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:173 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:173; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:174 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:174; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:175 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:175; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:176 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:176.
[0017] В некоторых вариантах осуществления в данном документе предусмотрены выделенные молекулы нуклеиновой кислоты, содержащие нуклеотидную последовательность, кодирующую связывающий белок согласно любому из вышеуказанных вариантов осуществления. В некоторых вариантах осуществления в данном документе предусмотрены векторы экспрессии, содержащие молекулу нуклеиновой кислоты согласно любому из вышеуказанных вариантов осуществления. В некоторых вариантах осуществления в данном документе предусмотрены выделенные клетки-хозяева, содержащие молекулу нуклеиновой кислоты согласно любому из вышеуказанных вариантов осуществления или вектор экспрессии согласно любому из вышеуказанных вариантов осуществления. В некоторых вариантах осуществления клетка-хозяин представляет собой клетку млекопитающего или насекомого.
[0018] В некоторых вариантах осуществления в данном документе предусмотрены фармацевтические композиции, содержащие связывающий белок в соответствии с любым из вышеуказанных вариантов осуществления и фармацевтически приемлемый носитель.
[0019] В некоторых вариантах осуществления в данном документе предусмотрены способы предупреждения и/или лечения инфекции, вызванной HIV, у пациента, включающие введение пациенту терапевтически эффективного количества по меньшей мере одного связывающего белка в соответствии с любым из вышеуказанных вариантов осуществления или фармацевтической композиции в соответствии с любым из вышеуказанных вариантов осуществления. В некоторых вариантах осуществления связывающий белок вводят совместно со стандартным средством для антиретровирусной терапии. В некоторых вариантах осуществления введение по меньшей мере одного связывающего белка приводит в результате к устранению у пациента одной или нескольких клеток, инфицированных HIV в латентной и/или хронической форме. В некоторых вариантах осуществления пациентом является человек.
[0020] В некоторых вариантах осуществления связывающий белок или фармацевтическая композиция согласно любому из вышеуказанных вариантов осуществления предусмотрены для предупреждения и/или лечения инфекции, вызванной HIV, у пациента. В некоторых вариантах осуществления связывающий белок подлежит совместному введению со стандартным средством для антиретровирусной терапии. В некоторых вариантах осуществления связывающий белок обеспечивает устранение у пациента одной или нескольких клеток, инфицированных HIV в латентной и/или хронической форме. В некоторых вариантах осуществления пациентом является человек.
[0021] В некоторых вариантах осуществления связывающий белок или фармацевтическая композиция согласно любому из вышеуказанных вариантов осуществления предусмотрены для применения в изготовлении лекарственного препарата для предупреждения и/или лечения инфекции, вызванной HIV, у пациента. В некоторых вариантах осуществления связывающий белок подлежит совместному введению со стандартным средством для антиретровирусной терапии. В некоторых вариантах осуществления связывающий белок обеспечивает устранение у пациента одной или нескольких клеток, инфицированных HIV в латентной и/или хронической форме. В некоторых вариантах осуществления пациентом является человек.
[0022] В некоторых вариантах осуществления в данном документе предусмотрена векторная система, содержащая один или несколько векторов, кодирующих первую, вторую, третью и четвертую полипептидные цепи связывающего белка согласно любому из вышеуказанных вариантов осуществления. В некоторых вариантах осуществления векторная система содержит первый вектор, кодирующий первую полипептидную цепь связывающего белка, второй вектор, кодирующий вторую полипептидную цепь связывающего белка, третий вектор, кодирующий третью полипептидную цепь связывающего белка, и четвертый вектор, кодирующий четвертую полипептидную цепь связывающего белка.
[0023] В некоторых вариантах осуществления в данном документе предусмотрены наборы, содержащие одну, две, три или четыре полипептидные цепи связывающего белка в соответствии с любым из вышеуказанных вариантов осуществления. В некоторых вариантах осуществления наборы дополнительно содержат инструкции по применению полипептидной цепи или связывающего белка в соответствии с любым из способов или вариантов применения, описанных в данном документе, например, выше.
[0024] В некоторых вариантах осуществления в данном документе предусмотрены наборы, содержащие один, два, три или четыре полинуклеотида в соответствии с любым из вышеуказанных вариантов осуществления. В некоторых вариантах осуществления в данном документе предусмотрены наборы полинуклеотидов, содержащие один, два, три или четыре полинуклеотида из набора полинуклеотидов, который содержит: (a) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:177, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:178, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:179, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:180; (b) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:181, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:182, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:183, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:184; (c) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:185, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:186, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:187, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:188; (d) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:189, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:190, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:191, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:192; (e) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:193, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:194, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:195, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:196; (f) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:197, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:198, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:199, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:200; (g) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:201, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:202, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:203, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:204; (h) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:205, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:206, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:207, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:208; (i) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:209, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:210, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:211, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:212; (j) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:213, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:214, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:215, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:216; (k) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:217, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:218, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:219, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:220; (l) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:221, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:222, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:223, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:224; (m) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:225, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:226, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:227, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:228; (n) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:229, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:230, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:231, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:232; (o) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:233, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:234, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:235, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:236; (p) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:237, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:238, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:239, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:240; (q) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:241, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:242, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:243, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:244; (r) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:245, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:246, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:247, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:248; (s) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:249, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:250, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:251, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:252; (t) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:253, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:254, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:255, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:256; (u) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:257, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:258, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:259, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:260; (v) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:261, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:262, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:263, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:264; (w) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:265, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:266, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:267, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:268; (x) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:269, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:270, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:271, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:272; (y) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:273, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:274, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:275, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:276; (z) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:277, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:278, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:279, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:280; (aa) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:281, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:282, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:283, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:284; (bb) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:285, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:286, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:287, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:288; или (cc) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:289, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:290, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:291, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:292. В некоторых вариантах осуществления первый, второй, третий и четвертый полинуклеотиды присутствуют в одном или нескольких векторах экспрессии, например, одном, двух, трех или четырех векторах экспрессии.
[0025] Следует понимать, что один, несколько или все признаки различных вариантов осуществления, описанных в данном документе, можно комбинировать с получением других вариантов осуществления настоящего изобретения. Эти и другие аспекты настоящего изобретения будут очевидны специалисту в данной области техники.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[0026] На ФИГ. 1 изображено схематическое представление триспецифического связывающего белка, содержащего четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые связывают три целевых белка CD28, CD3 и Env HIV. Первая пара полипептидов обладает двойными вариабельными доменами, имеющими кроссоверную ориентацию (VH1-VH2 и VL2-VL1), с образованием двух антигенсвязывающих участков (VH1 и VL1; VH2 и VL2), которые распознают CD28 и CD3 соответственно, а вторая пара полипептидов обладает одним вариабельным доменом (VH3 и VL3), образующим один антигенсвязывающий участок, который распознает Env HIV. В триспецифическом связывающем белке, изображенном на ФИГ. 1, используется константная область с мутацией по типу "выступы-во-впадины", где выступ находится на второй паре полипептидов с одним вариабельным доменом.
[0027] На ФИГ. 2 изображено схематическое представление стратегии с использованием триспецифического антитела-активатора Т-клеток (TCE) для применения триспецифического белка, связывающего HIV, изображенного на ФИГ. 1, для целенаправленного воздействия на резервуар HIV.
ПОДРОБНОЕ ОПИСАНИЕ
[0028] В настоящем изобретении предусмотрены триспецифические и/или тривалентные связывающие белки, содержащие четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, специфически связывающиеся с одним или несколькими целевыми белками вируса иммунодефицита человека (HIV) и/или одним или несколькими целевыми белками Т-клеточного рецептора, где первая пара полипептидов, образующих связывающий белок, содержит два вариабельных домена, характеризующихся кроссоверной ориентацией, и где вторая пара полипептидов содержит один вариабельный домен.
[0029] В нижеследующем описании изложены иллюстративные способы, параметры и т. п. Однако следует понимать, что такое описание не предусмотрено в качестве ограничения объема настоящего изобретения, а наоборот - предусмотрено в качестве описания иллюстративных вариантов осуществления.
Определения
[0030] Следующие термины, используемые в соответствии с настоящим изобретением, если не указано иное, следует понимать как имеющие следующие значения. Если контекстом не требуется иное, то термины в единственном числе будут включать формы множественного числа, и термины во множественном числе будут включать форму единственного числа.
[0031] Понятно, что аспекты и варианты осуществления настоящего изобретения, описанные в данном документе, включают аспекты и варианты осуществления "содержащие", "состоящие из" и "фактически состоящие из".
[0032] Используемый в данном документе термин "полинуклеотид" относится к полимерам в виде однонитевой или двухнитевой нуклеиновой кислоты, имеющих длину по меньшей мере 10 нуклеотидов. В определенных вариантах осуществления нуклеотиды, составляющие полинуклеотид, могут представлять собой рибонуклеотиды, или дезоксирибонуклеотиды, или модифицированную форму любого типа нуклеотида. Такие модификации включают модификации оснований, как например, бромуридин, модификации рибозы, как например, арабинозид и 2',3'-дидезоксирибоза, и модификации межнуклеотидных связей, как например, фосфотиоат, фосфодитиоат, фосфоселеноат, фосфодиселеноат, фосфоанилотиоат, фосфоаниладат и фосфоамидат. Термин "полинуклеотид" конкретно подразумевает однонитевые и двухнитевые формы ДНК.
[0033] "Выделенный полинуклеотид" представляет собой полинуклеотид, имеющий геномное, cDNA или синтетическое происхождение или характеризующийся некоторой их комбинацией, который: (1) не ассоциирован со всем полинуклеотидом, в котором выделенный полинуклеотид обнаружен в природе, или его частью, (2) связан с полинуклеотидом, с которым он не связан в природе, или (3) не встречается в природе в виде части более крупной последовательности.
[0034] "Выделенный полипептид" представляет собой полипептид, который: (1) не содержит по меньшей мере некоторых других полипептидов, с которыми он обычно обнаруживается, (2) фактически не содержит других полипептидов из одного и того же источника, например, из одного и того же вида, (3) экспрессируется клеткой из другого вида, (4) был отделен от по меньшей мере приблизительно 50 процентов полинуклеотидов, липидов, углеводов или других веществ, с которыми он связан в природе, (5) не связан (посредством ковалентного или нековалентного взаимодействия) с частями полипептида, с которыми "выделенный полипептид" связан в природе, (6) функционально связан (посредством ковалентного или нековалентного взаимодействия) с полипептидом, с которым он не связан в природе, или (7) не встречается в природе. Такой выделенный полипептид может кодироваться геномной ДНК, cDNA, mRNA или другой РНК синтетического происхождения или любой их комбинацией. Предпочтительно, выделенный полипептид по сути не содержит полипептидов или других контаминантов, которые встречаются в его природном окружении, которые вызывали бы затруднения при его применении (терапевтическом, диагностическом, профилактическом, исследовательском или ином).
[0035] Встречающиеся в природе антитела обычно представляют собой тетрамер. Каждый такой тетрамер обычно состоит из двух идентичных пар полипептидных цепей, при этом каждая пара имеет одну полноразмерную "легкую" цепь (обычно имеющую молекулярную массу приблизительно 25 кДа) и одну полноразмерную "тяжелую" цепь (обычно имеющую молекулярную массу приблизительно 50-70 кДа). Используемые в данном документе термины "тяжелая цепь" и "легкая цепь" обозначают любой полипептид иммуноглобулина, содержащий последовательность вариабельного домена, достаточную для придания специфичности в отношении антигена-мишени. Аминоконцевая часть каждой легкой и тяжелой цепей обычно содержит вариабельный домен из приблизительно 100-110 аминокислот или больше, который обычно отвечает за распознавание антигена. Карбоксиконцевая часть каждой цепи обычно определяет константный домен, ответственный за эффекторную функцию. Таким образом, во встречающемся в природе антителе полноразмерный полипептид, представляющий собой тяжелую цепь иммуноглобулина, содержит вариабельный домен (VH) и три константных домена (CH1, CH2 и CH3), где домен VH находится на аминоконце полипептида, а домен CH3 находится на карбоксильном конце, и полноразмерный полипептид, представляющий собой легкую цепь иммуноглобулина, содержит вариабельный домен (VL) и константный домен (CL), где домен VL находится на аминоконце полипептида, а домен CL находится на карбоксильном конце.
[0036] Легкие цепи человека обычно классифицируют как легкие каппа- и лямбда-цепи, и тяжелые цепи человека обычно классифицируют как мю, дельта, гамма, альфа или эпсилон, и они определяют изотип антитела IgM, IgD, IgG, IgA и IgE соответственно. IgG имеет несколько подклассов, в том числе без ограничения IgG1, IgG2, IgG3 и IgG4. IgM имеет подклассы, в том числе без ограничения IgM1 и IgM2. IgA аналогичным образом подразделяют на подклассы, в том числе без ограничения IgA1 и IgA2. В полноразмерных легких и тяжелых цепях вариабельные и константные домены обычно соединены с помощью "J"-области из приблизительно 12 или больше аминокислот, при этом тяжелая цепь также содержит "D"-область из приблизительно 10 или больше аминокислот. См., например, Fundamental Immunology (Paul, W., ed., Raven Press, 2nd ed., 1989), которая включена посредством ссылки в ее полном объеме для всех целей. Вариабельные области каждой пары легкая/тяжелая цепь обычно образуют антигенсвязывающий участок. Вариабельные домены встречающихся в природе антител обычно характеризуются одинаковой общей структурой относительно консервативных каркасных областей (FR), соединенных с помощью трех гипервариабельных областей, также называемых определяющими комплементарность областями или CDR. CDR из двух цепей каждой пары обычно выровнены с помощью каркасных областей, что может обеспечивать возможность связывания со специфическим эпитопом. От аминоконца к карбоксильному концу вариабельные домены как легкой, так и тяжелой цепей обычно содержат домены FR1, CDR1, FR2, CDR2, FR3, CDR3 и FR4.
[0037] Термин "совокупность CDR" обозначает группу из трех CDR, которые содержатся в одной вариабельной области, способной связывать антиген. Точные границы этих CDR определяли по-разному в соответствии с различными системами. Система, описанная Kabat (Kabat et al., Sequences of Proteins of Immunological Interest (Национальные институты здравоохранения, Бетесда, Мэриленд. (1987) и (1991)), не только предусматривает однозначную систему нумерации остатков, применимую к любой вариабельной области антитела, но также предусматривает точные границы остатков, определяющие три CDR. Эти CDR могут называться CDR в соответствии с Kabat. Chothia и соавторы (Chothia and Lesk, 1987, J. Mol. Biol. 196: 901-17; Chothia et al., 1989, Nature 342: 877-83) обнаружили, что определенные субфрагменты в пределах CDR в соответствии с Kabat принимают почти идентичные конформации пептидного каркаса, несмотря на наличие большого различия на уровне аминокислотной последовательности. Эти субфрагменты были обозначены как L1, L2 и L3 или H1, H2 и H3, где "L" и "H" обозначают области легкой цепи и тяжелой цепи соответственно. Эти области могут называться CDR в соответствии с Chothia, границы которых совпадают с CDR в соответствии с Kabat. Другие границы, определяющие CDR, которые совпадают с CDR в соответствии с Kabat, были описаны Padlan, 1995, FASEB J. 9: 133-39; MacCallum, 1996, J. Mol. Biol. 262(5): 732-45; и Lefranc, 2003, Dev. Comp. Immunol. 27: 55-77. Еще одни определения границ CDR могут не строго соответствовать одной из систем, приведенных в данном документе, но тем не менее будут совпадать с CDR в соответствии с Kabat, несмотря на то, что они могут быть укорочены или удлинены с учетом прогностических или экспериментальных выводов о том, что конкретные остатки или группы остатков или даже все CDR не влияют в значительной степени на связывание антигена. В способах, используемых в данном документе, можно использовать CDR, определенные в соответствии с любой из этих систем, несмотря на то, что в определенных вариантах осуществления применяют CDR, определенные в соответствии с Kabat или Chothia. Идентификация прогнозируемых CDR с помощью аминокислотной последовательности хорошо известна в данной области техники, например, в Martin, A.C. "Protein sequence and structure analysis of antibody variable domains" в Antibody Engineering, Vol. 2. Kontermann R., Dübel S., eds. Springer-Verlag, Berlin, p. 33-51 (2010). Аминокислотную последовательность вариабельного домена тяжелой и/или легкой цепи можно также исследовать с целью идентификации последовательностей CDR с помощью других традиционных способов, например, путем сравнения с известными аминокислотными последовательностями других вариабельных областей тяжелой и легкой цепей с определением участков гипервариабельности в последовательности. Пронумерованные последовательности можно выравнивать вручную или путем использования программы выравнивания, такой как одна из пакета программ CLUSTAL, как описано в Thompson, 1994, Nucleic Acids Res. 22: 4673-80. Молекулярные модели традиционно используют для того, чтобы правильно определить каркасные и CDR-области и таким образом скорректировать основанные на последовательности выравнивания.
[0038] Используемый в данном документе термин "Fc" обозначает молекулу, будь то в мономерной или мультимерной форме, содержащую последовательность, не являющуюся частью антигенсвязывающего фрагмента, которая получена в результате расщепления антитела или получена другими способами, и при этом она может содержать шарнирную область. Исходный иммуноглобулиновый источник нативного Fc предпочтительно происходит от человека и может представлять собой любой из иммуноглобулинов, тем не менее предпочтительными являются IgG1 и IgG2. Молекулы Fc составлены из мономерных полипептидов, которые могут быть связаны в димерные или мультимерные формы посредством ковалентной (т. е. дисульфидных связей) и нековалентной связи. Число межмолекулярных дисульфидных связей между мономерными субъединицами нативных молекул Fc варьирует от 1 до 4, в зависимости от класса (например, IgG, IgA и IgE) или подкласса (например, IgG1, IgG2, IgG3, IgA1 и IgGA2). Одним примером Fc является димер с дисульфидной связью, полученный в результате расщепления IgG папаином. Используемый в данном документе термин "Fc" является общим для мономерных, димерных и мультимерных форм.
[0039] F(ab)-фрагмент обычно содержит одну легкую цепь и домены VH и CH1 одной тяжелой цепи, где часть VH-CH1 тяжелой цепи F(ab)-фрагмента не может образовывать дисульфидную связь с другим полипептидом тяжелой цепи. Как используется в данном документе, F(ab)-фрагмент также может содержать одну легкую цепь, содержащую два вариабельных домена, разделенных аминокислотным линкером, и одну тяжелую цепь, содержащую два вариабельных домена, разделенных аминокислотным линкером, и домен CH1.
[0040] F(ab')-фрагмент обычно содержит одну легкую цепь и часть одной тяжелой цепи, которая содержит большую часть константной области (между доменами CH1 и CH2), вследствие чего межцепочечная дисульфидная связь может быть образована между двумя тяжелыми цепями с образованием молекулы F(ab')2.
[0041] Используемый в данном документе термин "связывающий белок" относится к не встречающейся в природе (или рекомбинантной, или сконструированной) молекуле, которая специфически связывается с по меньшей мере одним антигеном-мишенью. Триспецифический связывающий белок по настоящему изобретению, если не указано иное, содержит четыре полипептидные цепи, которые образуют по меньшей мере три антигенсвязывающих участка, где первая полипептидная цепь имеет структуру, представленную формулой
VL2- L1-VL1- L2-CL [I];
и вторая полипептидная цепь имеет структуру, представленную формулой
VH1-L3-VH2-L4-CH1-шарнир-CH2-CH3 [II];
и третья полипептидная цепь имеет структуру, представленную формулой
VH3-CH1 [III];
и четвертая полипептидная цепь имеет структуру, представленную формулой
VL3-CL [IV];
где:
VL1 представляет собой первый вариабельный домен легкой цепи иммуноглобулина;
VL2 представляет собой второй вариабельный домен легкой цепи иммуноглобулина;
VL3 представляет собой третий вариабельный домен легкой цепи иммуноглобулина;
VH1 представляет собой первый вариабельный домен тяжелой цепи иммуноглобулина;
VH2 представляет собой второй вариабельный домен тяжелой цепи иммуноглобулина;
VH3 представляет собой третий вариабельный домен тяжелой цепи иммуноглобулина;
CL представляет собой константный домен легкой цепи иммуноглобулина;
CH1 представляет собой константный домен CH1 тяжелой цепи иммуноглобулина; и
шарнир представляет собой шарнирную область иммуноглобулина, соединяющую домены CH1 и CH2;
L1, L2, L3 и L4 представляют собой аминокислотные линкеры;
и где полипептид формулы I и полипептид формулы II образуют кроссоверную пару легкая цепь-тяжелая цепь.
[0042] "Рекомбинантная" молекула представляет собой молекулу, которая была получена, экспрессирована, создана или выделена рекомбинантными способами.
[0043] В одном варианте осуществления настоящего изобретения представлены связывающие белки, характеризующиеся биологической и иммунологической специфичностью в отношении одного-трех антигенов-мишеней. В другом варианте осуществления настоящего изобретения представлены молекулы нуклеиновой кислоты, содержащие нуклеотидные последовательности, кодирующие полипептидные цепи, которые образуют такие связывающие белки. В другом варианте осуществления настоящего изобретения представлены векторы экспрессии, содержащие молекулы нуклеиновой кислоты, содержащие нуклеотидные последовательности, кодирующие полипептидные цепи, которые образуют такие связывающие белки. В еще одном варианте осуществления настоящего изобретения представлены клетки-хозяева, которые экспрессируют такие связывающие белки (т. е. содержащие молекулы нуклеиновой кислоты или векторы, кодирующие полипептидные цепи, которые образуют такие связывающие белки).
[0044] Используемый в данном документе термин "способность к обмену" обозначает способность к взаимозамене вариабельных доменов в формате связывающего белка, при этом с сохранением укладки и наивысшей аффинности связывания. "Способность к полному обмену" относится к способности менять порядок доменов как VH1, так и VH2 и, следовательно, порядок доменов VL1 и VL2 в полипептидной цепи формулы I или полипептидной цепи формулы II (т. е. обращать порядок), поддерживая при этом полную функциональность связывающего белка, о чем свидетельствует сохранение аффинности связывания. Кроме того, следует отметить, что обозначения VH и VL относятся лишь к положению домена в конкретной белковой цепи в конечном формате. Например, VH1 и VH2 могут быть получены из доменов VL1 и VL2 исходных антител и введены в положения, соответствующие VH1 и VH2 связывающего белка. Аналогично, VL1 и VL2 могут быть получены из доменов VH1 и VH2 исходных антител и помещены в положения, соответствующие VH1 и VH2 связывающего белка. Таким образом, обозначения VH и VL относятся к существующему в данный момент положению, а не к первоначальному положению в исходном антителе. Следовательно, домены VH и VL являются "способными к обмену".
[0045] Используемые в данном документе термины "антиген", или "антиген-мишень", или "целевой антиген" обозначают молекулу или часть молекулы, которая может связываться связывающим белком и дополнительно может использоваться у животного для получения антител, способных связываться с эпитопом этого антигена. Антиген-мишень может иметь один или несколько эпитопов. С учетом того, что каждый антиген-мишень распознается связывающим белком, связывающий белок способен конкурировать с интактным антителом, которое распознает антиген-мишень.
[0046] Используемый в данном документе термин "HIV" означает вирус иммунодефицита человека. Используемый в данном документе термин "инфекция, вызванная HIV" в целом охватывает инфекцию у хозяина, в частности хозяина-человека, вызываемую вирусом иммунодефицита человека (HIV) из семейства ретровирусов, в том числе без ограничения HIV I, HIV II, HIV III (также известные как HTLV-II, LAV-1, LAV-2). HIV может использоваться в данном документе для обозначения любых штаммов, форм, подтипов, клад и вариаций семейства HIV. Таким образом, лечение инфекции, вызванной HIV, будет охватывать лечение индивидуума, который является носителем любого HIV из семейства ретровирусов, или индивидуума, у которого диагностировали активную стадию СПИД, а также лечение или профилактику связанных со СПИД состояний у таких индивидуумов.
[0047] Используемый в данном документе термин "СПИД" означает синдром приобретенного иммунодефицита. СПИД вызывается HIV.
[0048] Термины "CD4bs" или "CD4-связывающий участок" обозначают связывающий участок для CD4 (кластера дифференцировки 4), который представляет собой гликопротеин, обнаруживаемый на поверхности иммунных клеток, таких как T-хелперные клетки, моноциты, макрофаги и дендритные клетки.
[0049] Термин "CD3" означает полипептид кластера дифференцировки 3, и он представляет собой поверхностный белок T-клетки, который обычно является частью Т-клеточного рецепторного (TCR) комплекса.
[0050] "CD28" означает полипептид 28 кластера дифференцировки и представляет собой поверхностный белок T-клеток, передающий костимулирующие сигналы для активации и выживания Т-клеток.
[0051] Термины "гликопротеин 160" или "белок gp160" обозначают гликопротеиновый комплекс оболочки HIV и представляет собой гомотример, который расщепляется на субъединицы gp120 и gp41.
[0052] Термин "MPER" обозначает мембранно-проксимальную наружную область гликопротеина 41 (gp41), которая является субъединицей белкового комплекса оболочки ретровирусов, в том числе HIV.
[0053] Термин "гликан" обозначает углеводную часть гликоконъюгата, такого как гликопротеин, гликолипид или протеогликан. В раскрытых связывающих белках гликан обозначает гликопротеин gp120 оболочки HIV-1.
[0054] Термин "активатор T-клеток" обозначает связывающие белки, направленные на иммунную систему хозяина, более конкретно на цитотоксическую активность T-клеток, а также направленные на целевой белок HIV.
[0055] Термин "верхняя часть тримера" обозначает верхнюю часть гликопротеина gp120 оболочки HIV-1.
[0056] Термин "моноспецифический связывающий белок" обозначает связывающий белок, который специфически связывается с одним антигеном-мишенью.
[0057] Термин "моновалентный связывающий белок" обозначает связывающий белок, который имеет один антигенсвязывающий участок.
[0058] Термин "биспецифический связывающий белок" обозначает связывающий белок, который специфически связывается с двумя различными антигенами-мишенями.
[0059] Термин "бивалентный связывающий белок" обозначает связывающий белок, который имеет два связывающих участка.
[0060] Термин "триспецифический связывающий белок" обозначает связывающий белок, который специфически связывается с тремя различными антигенами-мишенями.
[0061] Термин "тривалентный связывающий белок" обозначает связывающий белок, который имеет три связывающих участка. В конкретных вариантах осуществления тривалентный связывающий белок может связываться с одним антигеном-мишенью. В других вариантах осуществления тривалентный связывающий белок может связываться с двумя антигенами-мишенями. В других вариантах осуществления тривалентный связывающий белок может связываться с тремя антигенами-мишенями.
[0062] "Выделенный" связывающий белок представляет собой связывающий белок, который был идентифицирован и отделен и/или извлечен из компонента своего природного окружения. Компоненты-контаминанты из его природного окружения представляют собой вещества, которые бы вызывали затруднения при диагностических или терапевтических применениях связывающего белка, и могут включать ферменты, гормоны и другие растворенные вещества белковой или небелковой природы. В некоторых вариантах осуществления связывающий белок будет очищенным: (1) до более чем 95% по весу антитела, как определяется способом Лоури, и наиболее предпочтительно до более чем 99% по весу, (2) до степени, достаточной для получения по меньшей мере 15 остатков N-концевой или внутренней аминокислотной последовательности с применением секвенатора с вращающимся стаканом, или (3) до гомогенности с помощью SDS-PAGE в восстанавливающих или невосстанавливающих условиях с применением кумасси голубого или предпочтительно серебряного красителя. Выделенные связывающие белки включают связывающий белок in situ в рекомбинантных клетках, поскольку по меньшей мере один компонент природного окружения связывающего белка не будет присутствовать.
[0063] Используемые в данном документе термины "в значительной степени чистый" или "в значительной степени очищенный" обозначают соединение или структуру, которая является преобладающей присутствующей структурой (т. е. в расчете на моль она более многочисленна, чем любая другая отдельная структура в композиции). В некоторых вариантах осуществления в значительной степени очищенная фракция представляет собой композицию, где структура составляет по меньшей мере приблизительно 50% (в расчете на моль) от всех присутствующих макромолекулярных структур. В других вариантах осуществления в значительной степени чистая композиция будет содержать более чем приблизительно 80%, 85%, 90%, 95% или 99% от всех макромолекулярных структур, присутствующих в композиции. В еще одних вариантах осуществления структура является очищенной до необходимой гомогенности (загрязняющие структуры не могут быть выявлены в композиции с помощью традиционных способов выявления), где композиция состоит фактически из одной макромолекулярной структуры.
[0064] Используемый в данном документе термин "нейтрализующий" связывающий белок обозначает молекулу, которая способна блокировать или в значительной степени снижать эффекторную функцию антигена-мишени, с которым она связывается. Используемый в данном документе термин "в значительной степени снижать" означает по меньшей мере 60%, предпочтительно по меньшей мере 70%, более предпочтительно по меньшей мере 75%, еще более предпочтительно по меньшей мере 80%, еще более предпочтительно по меньшей мере 85%, наиболее предпочтительно по меньшей мере 90% снижение эффекторной функции антигена-мишени.
[0065] Термин "эпитоп" подразумевает любую детерминанту, предпочтительно полипептидную детерминанту, способную специфически связываться с иммуноглобулином или T-клеточным рецептором. В определенных вариантах осуществления эпитопные детерминанты включают химически активные поверхностные группы молекул, такие как аминокислоты, боковые цепи сахаров, фосфорильные группы или сульфонильные группы, и в определенных вариантах осуществления могут иметь специфические характеристики трехмерной структуры и/или специфические характеристики заряда. Эпитоп представляет собой область антигена, которая связывается антителом или связывающим белком. В определенных вариантах осуществления считается, что связывающий белок специфически связывает антиген, если он предпочтительно распознает свой антиген-мишень в сложной смеси белков и/или макромолекул. В некоторых вариантах осуществления считается, что связывающий белок специфически связывает антиген, если равновесная константа диссоциации составляет ≤ 10-8 M, более предпочтительно если равновесная константа диссоциации составляет ≤ 10-9 M и наиболее предпочтительно если константа диссоциации составляет ≤ 10-10 M.
[0066] Константу диссоциации (KD) связывающего белка можно определить, например, с помощью поверхностного плазмонного резонанса. В целом в анализе поверхностного плазмонного резонанса измеряют связывающие взаимодействия между лигандом (антигеном-мишенью на биосенсорной матрице) и аналитом (связывающим белком в растворе) в реальном времени с помощью поверхностного плазмонного резонанса (SPR) с применением системы BIAcore (Pharmacia Biosensor; Пискатауэй, Нью-Джерси). Анализ поверхностного плазмонного резонанса можно также выполнять посредством иммобилизации аналита (связывающего белка на биосенсорной матрице) и представления лиганда (антигена-мишени). Используемый в данном документе термин "KD" обозначает константу диссоциации взаимодействия между конкретным связывающим белком и антигеном-мишенью.
[0067] Используемый в данном документе термин "специфически связывается" обозначает способность связывающего белка или его антигенсвязывающего фрагмента связываться с антигеном, содержащим эпитоп, с Kd, составляющей по меньшей мере приблизительно 1×10-6 M, 1×10-7 M, 1×10-8 M, 1×10-9 M, 1×10-10 M, 1×10-11 M, 1×10-12 M или больше, и/или связываться с эпитопом с аффинностью, которая в по меньшей мере два раза превышает его аффинность в отношении неспецифического антигена.
[0068] Используемый в данном документе термин "линкер" обозначает один или несколько аминокислотных остатков, вставленных между доменами иммуноглобулина для обеспечения подвижности, достаточной для того, чтобы домены легкой и тяжелой цепей сворачивались в иммуноглобулины с кроссоверными двумя вариабельными областями. Линкер вставляют в переходный участок между вариабельными доменами или между вариабельным и константным доменами, соответственно, на уровне последовательности. Переходный участок между доменами можно идентифицировать, поскольку приблизительный размер доменов иммуноглобулина хорошо известен. Точное местоположение переходного участка между доменами можно определить путем определения положения пептидных отрезков, которые не образуют элементов со вторичной структурой, такой как бета-слои или альфа-спирали, что показано с помощью экспериментальных данных или что можно прогнозировать с помощью методик моделирования или прогнозирования вторичной структуры. Линкеры, описанные в данном документе, обозначены как L1, который расположен на легкой цепи между C-концом домена VL2 и N-концом домена VL1; и L2, который расположен на легкой цепи между C-концом домена VL1 и N-концом домена CL. Линкеры тяжелой цепи называют как L3, который расположен между C-концом домена VH1 и N-концом домена VH2; и L4, который расположен между C-концом домена VH2 и N-концом домена CH1.
[0069] Используемый в данном документе термин "вектор" относится к любой молекуле (например, нуклеиновой кислоте, плазмиде или вирусу), используемой для переноса закодированной информации в клетку-хозяина. Термин "вектор" подразумевает молекулу нуклеиновой кислоты, которая способна транспортировать другую нуклеиновую кислоту, с которой ее связали. Одним типом вектора является "плазмида", которая обозначает кольцевую двухнитевую молекулу ДНК, в которую могут быть вставлены дополнительные сегменты ДНК. Другим типом вектора является вирусный вектор, при этом в геном вируса могут быть вставлены дополнительные сегменты ДНК. Определенные векторы способны к автономной репликации в клетке-хозяине, в которую их вводят (например, бактериальные векторы, имеющие бактериальную точку начала репликации, и эписомные векторы для млекопитающих). Другие векторы (например, неэписомные векторы для млекопитающих) могут быть интегрированы в геном клетки-хозяина после введения в клетку-хозяина, и за счет этого они реплицируются вместе с геномом хозяина. Кроме того, определенные векторы способны управлять экспрессией генов, с которыми они функционально связаны. Такие векторы называются в данном документе "рекомбинантными векторами экспрессии" (или просто "векторами экспрессии"). Как правило, векторы экспрессии, полезные в технологиях рекомбинантных ДНК, часто находятся в форме плазмид. Термины "плазмида" и "вектор" могут использоваться взаимозаменяемо в данном документе, поскольку плазмида является наиболее широко используемой формой вектора. Однако подразумевается, что в настоящее изобретение включены и другие формы векторов экспрессии, такие как вирусные векторы (например, ретровирусы, аденовирусы и аденоассоциированные вирусы с дефектной репликацией), которые выполняют эквивалентные функции.
[0070] Используемая в данном документе фраза "рекомбинантная клетка-хозяин" (или "клетка-хозяин") обозначает клетку, в которую был введен рекомбинантный вектор экспрессии. Подразумевается, что рекомбинантная клетка-хозяин или клетка-хозяин обозначают не только конкретную рассматриваемую клетку, но также и потомство такой клетки. Поскольку в последующих поколениях могут возникать определенные модификации вследствие мутации либо влияний окружающей среды, такое потомство в действительности может не быть идентичным родительской клетке, однако такие клетки по-прежнему включены в объем используемого в данном документе термина "клетка-хозяин". Широкое разнообразие систем экспрессии в клетке-хозяине можно применять для экспрессии связывающих белков, в том числе системы экспрессии на основе бактерий, дрожжей, бакуловирусов и клеток млекопитающих (а также системы экспрессии на основе фагового дисплея). Примером подходящего бактериального вектора экспрессии является pUC19. Для рекомбинантной экспрессии связывающего белка клетку-хозяина трансформируют или трансфицируют одним или несколькими рекомбинантными векторами экспрессии, несущими фрагменты ДНК, кодирующие полипептидные цепи связывающего белка, вследствие чего полипептидные цепи экспрессируются в клетке-хозяине и предпочтительно секретируются в среду, в которой клетки-хозяева культивируются, при этом из данной среды можно извлечь связывающий белок.
[0071] Используемый в данном документе термин "трансформация" обозначает изменение генетических характеристик клетки, и при этом клетка была трансформирована, если ее модифицировали с тем, чтобы она содержала новую ДНК. Например, клетка является трансформированной, если она генетически модифицирована по сравнению с ее нативным состоянием. После трансформации трансформирующая ДНК может подвергаться рекомбинации с ДНК клетки путем физической интеграции в хромосому клетки, или может временно сохраняться в виде эписомального элемента без репликации, или может реплицироваться независимо как плазмида. Считается, что клетка является стабильно трансформированной, если ДНК реплицируется при делении клетки. Используемый в данном документе термин "трансфекция" обозначает захват чужеродной или экзогенной ДНК клеткой, и при этом клетка была "трансфицирована", если экзогенную ДНК ввели внутрь от клеточной мембраны. Ряд методик трансфекции хорошо известен из уровня техники. Такие методики можно применять для введения одной или нескольких экзогенных молекул ДНК в подходящие клетки-хозяева.
[0072] Используемый в данном документе термин "встречающийся в природе", и используемый при этом в отношении объекта, обозначает тот факт, что объект может обнаруживаться в природе и не был подвергнут манипуляциям со стороны человека. Например, полинуклеотид или полипептид, присутствующий в организме (включая вирусы), который может быть выделен из природного источника и который не был преднамеренно модифицирован человеком, является встречающимся в природе. Аналогично используемый в данном документе термин "не встречающийся в природе" обозначает объект, который не обнаружен в природе или который был структурно модифицирован или синтезирован человеком.
[0073] Как используется в данном документе, двадцать стандартных аминокислот и их аббревиатуры соответствуют общепринятой практике. Стереоизомеры (например, d-аминокислоты) двадцати стандартных аминокислот; не встречающиеся в природе аминокислоты и аналоги, такие как α-,α-двузамещенные аминокислоты, N-алкиламинокислоты, молочная кислота и другие нестандартные аминокислоты также могут быть подходящими компонентами полипептидных цепей связывающих белков. Примеры нестандартных аминокислот включают 4-гидроксипролин, γ-карбоксиглутамат, ε-N,N,N-триметиллизин, ε-N-ацетиллизин, O-фосфосерин, N-ацетилсерин, N-формилметионин, 3-метилгистидин, 5-гидроксилизин, σ-N-метиларгинин и другие подобные аминокислоты и иминокислоты (например, 4-гидроксипролин). В системе обозначений полипептидов, используемой в данном документе, левое направление представляет собой направление в сторону аминоконца, а правое направление представляет собой направление в сторону карбоксильного конца в соответствии со стандартной практикой и правилами.
[0074] Встречающиеся в природе остатки можно разделить на классы на основании общих свойств боковой цепи:
(1) гидрофобные: Met, Ala, Val, Leu, Ile, Phe, Trp, Tyr, Pro;
(2) полярные гидрофильные: Arg, Asn, Asp, Gln, Glu, His, Lys, Ser, Thr;
(3) алифатические: Ala, Gly, Ile, Leu, Val, Pro;
(4) алифатические гидрофобные: Ala, Ile, Leu, Val, Pro;
(5) нейтральные гидрофильные: Cys, Ser, Thr, Asn, Gln;
(6) кислые: Asp, Glu;
(7) основные: His, Lys, Arg;
(8) остатки, которые влияют на ориентацию цепи: Gly, Pro;
(9) ароматические: His, Trp, Tyr, Phe; и
(10) ароматические гидрофобные: Phe, Trp, Tyr.
[0075] Консервативные аминокислотные замены могут включать обмен представителя одного из этих классов на другого представителя того же класса. Неконсервативные замены могут включать обмен представителя одного из этих классов на представителя другого класса.
[0076] Специалист в данной области техники сможет определить подходящие варианты полипептидных цепей связывающих белков с помощью общеизвестных методик. Например, специалист в данной области техники может идентифицировать подходящие участки в полипептидной цепи, которые можно изменить без нарушения активности, путем нацеливания на области, которые, как предполагается, не являются важными с точки зрения активности. Альтернативно специалист в данной области техники может идентифицировать остатки и части молекул, которые являются консервативными среди схожих полипептидов. Кроме того, даже участки, которые могут быть важными с точки зрения биологической активности или с точки зрения структуры, могут подвергаться консервативным аминокислотным заменам без нарушения биологической активности или без неблагоприятного воздействия на структуру полипептида.
[0077] Используемый в данном документе термин "пациент" подразумевает субъектов-людей и субъектов-животных.
[0078] Используемые в данном документе термины "лечение" или "лечить" обозначают как терапевтическое лечение, так и профилактические или превентивные меры. Нуждающиеся в лечении включают тех, у которых имеется нарушение, а также тех, которые предрасположены к нарушению, или тех, у которых нужно предотвратить нарушение. В конкретных вариантах осуществления связывающие белки можно применять для лечения людей, инфицированных HIV, или людей, предрасположенных к инфекции, вызванной HIV, или для уменьшения тяжести инфекции, вызванной HIV, у субъекта-человека, инфицированного HIV. Связывающие белки также можно применять для предупреждения инфекции HIV у пациента-человека.
[0079] Следует понимать, что лечение людей, инфицированных HIV, подразумевает тех субъектов, у которых имеется любая из нескольких стадий прогрессирования инфекции, вызванной HIV, которые, например, включают синдром острой первичной инфекции (который может быть бессимптомным или ассоциированным с гриппоподобным заболеванием с лихорадкой, недомоганием, диареей и неврологическими симптомами, такими как головная боль), бессимптомную инфекцию (которая представляет собой длительный латентный период с постепенным снижением числа циркулирующих CD4+ T-клеток) и СПИД (который определяется более серьезным СПИД-индикаторным заболеванием и/или снижением содержания CD4-клеток ниже уровня, который соответствует эффективной иммунной функции). Кроме того, лечение или предупреждение инфекции, вызванной HIV, также будет охватывать лечение предположительной инфекции, вызванной HIV, после предположительного воздействия HIV, например, посредством контакта с зараженной HIV кровью, переливания крови, обмена биологических жидкостей, "незащищенного" полового контакта с инфицированным индивидуумом, случайного укола иглой, выполнения татуировки или иглоукалывания зараженными инструментами или переноса вируса от матери к ребенку во время беременности, родов или вскоре после этого.
[0080] Используемые в данном документе термины "фармацевтическая композиция" или "терапевтическая композиция" обозначают соединение или композицию, способные индуцировать необходимый терапевтический эффект при введении пациенту должным образом.
[0081] Используемый в данном документе термин "фармацевтически приемлемый носитель" или "физиологически приемлемый носитель" обозначает одно или несколько веществ состава, подходящие для осуществления или улучшения доставки связывающего белка.
[0082] Термины "эффективное количество" и "терапевтически эффективное количество" при использовании в отношении фармацевтической композиции, содержащей один или несколько связывающих белков, обозначают количество или дозу, достаточные для получения необходимого терапевтического результата. Более конкретно, терапевтически эффективное количество представляет собой количество связывающего белка, достаточное для ингибирования, на некоторый период времени, одного или нескольких клинически определенных патологических процессов, ассоциированных с состоянием, подлежащим лечению. Эффективное количество может меняться в зависимости от конкретного связывающего белка, подлежащего применению, а также зависит от ряда факторов и состояний, связанных с пациентом, подлежащим лечению, и тяжестью нарушения. Например, если связывающий белок подлежит введению in vivo, то факторы, такие как возраст, масса тела и состояние здоровья пациента, а также кривые зависимости "доза-эффект" и данные о токсичности, полученные в доклиническом исследовании на животных, будут входить в число таковых учитываемых факторов. Определение эффективного количества или терапевтически эффективного количества указанной фармацевтической композиции находится в пределах компетенции специалистов в данной области техники.
[0083] В одном варианте осуществления настоящего изобретения представлена фармацевтическая композиция, содержащая фармацевтически приемлемый носитель и терапевтически эффективное количество связывающего белка.
Триспецифические и/или тривалентные связывающие белки
[0084] Определенные аспекты настоящего изобретения относятся к триспецифическим и/или тривалентным связывающим белкам. Любые из CDR или вариабельных доменов любого из антигенсвязывающих белков, описанных в данном документе, могут найти применение в получении триспецифического связывающего белка по настоящему изобретению. Предусмотрены триспецифические связывающие белки различных форматов. В некоторых вариантах осуществления связывающий белок по настоящему изобретению представляет собой триспецифический и/или тривалентный связывающий белок, содержащий четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит структуру, представленную формулой
VL2- L1-VL1- L2-CL [I];
и вторая полипептидная цепь содержит структуру, представленную формулой
VH1- L3-VH2- L4-CH1-шарнир-CH2-CH3 [II];
и третья полипептидная цепь содержит структуру, представленную формулой
VH3-CH1-шарнир-CH2-CH3 [III];
и четвертая полипептидная цепь содержит структуру, представленную формулой
VL3-CL [IV];
где:
VL1 представляет собой первый вариабельный домен легкой цепи иммуноглобулина;
VL2 представляет собой второй вариабельный домен легкой цепи иммуноглобулина;
VL3 представляет собой третий вариабельный домен легкой цепи иммуноглобулина;
VH1 представляет собой первый вариабельный домен тяжелой цепи иммуноглобулина;
VH2 представляет собой второй вариабельный домен тяжелой цепи иммуноглобулина;
VH3 представляет собой третий вариабельный домен тяжелой цепи иммуноглобулина;
CL представляет собой константный домен легкой цепи иммуноглобулина;
CH1 представляет собой константный домен CH1 тяжелой цепи иммуноглобулина;
CH2 представляет собой константный домен CH2 тяжелой цепи иммуноглобулина;
CH3 представляет собой константный домен CH3 тяжелой цепи иммуноглобулина;
шарнир представляет собой шарнирную область иммуноглобулина, соединяющую домены CH1 и CH2; и
L1, L2, L3 и L4 представляют собой аминокислотные линкеры;
и где полипептид формулы I и полипептид формулы II образуют кроссоверную пару легкая цепь-тяжелая цепь.
[0085] В некоторых вариантах осуществления первая полипептидная цепь и вторая полипептидная цепь характеризуются кроссоверной ориентацией, при этом они образуют два разных антигенсвязывающих участка. В некоторых вариантах осуществления VH1 и VL1 образуют связывающую пару и образуют первый антигенсвязывающий участок. В некоторых вариантах осуществления VH2 и VL2 образуют связывающую пару и образуют второй антигенсвязывающий участок. В некоторых вариантах осуществления третий полипептид и четвертый полипептид образуют третий антигенсвязывающий участок. В некоторых вариантах осуществления VH3 и VL3 образуют связывающую пару и образуют третий антигенсвязывающий участок.
[0086] В некоторых вариантах осуществления один или несколько антигенсвязывающих участков связывают целевой белок HIV. В некоторых вариантах осуществления VH3 и VL3 образуют третий антигенсвязывающий участок, который связывает целевой белок HIV. В некоторых вариантах осуществления VH1 и VL1 образуют первый антигенсвязывающий участок, который связывает целевой белок Т-клеток, VH2 и VL2 образуют второй антигенсвязывающий участок, который связывает целевой белок Т-клеток, и VH3 и VL3 образуют третий антигенсвязывающий участок, который связывает целевой белок HIV. В некоторых вариантах осуществления VH1 и VL1 образуют первый антигенсвязывающий участок, который связывает целевой белок Т-клеток, VH2 и VL2 образуют второй антигенсвязывающий участок, который связывает полипептид CD3, и VH3 и VL3 образуют третий антигенсвязывающий участок, который связывает целевой белок HIV. В некоторых вариантах осуществления VH1 и VL1 образуют первый антигенсвязывающий участок, который связывает полипептид CD28, VH2 и VL2 образуют второй антигенсвязывающий участок, который связывает полипептид CD3, и VH3 и VL3 образуют третий антигенсвязывающий участок, который связывает целевой белок HIV.
[0087] В некоторых вариантах осуществления связывающие белки специфически связываются с одним или несколькими целевыми белками HIV (например, как описано выше) и одним или несколькими целевыми белками на T-клетке, в том числе Т-клеточным рецепторным комплексом. Эти связывающие белки, являющиеся активаторами T-клеток, способны временно рекрутировать T-клетки к целевым клеткам с одновременной активацией цитолитической активности T-клеток. Триспецифические антитела, являющиеся активаторами T-клеток, можно применять для активации резервуаров HIV-1 и перенаправления/активации T-клеток с целью осуществления лизиса инфицированных в латентной форме HIV-1+ T-клеток. Примеры целевых белков на T-клетках включают без ограничения, среди прочего, CD3 и CD28. В некоторых вариантах осуществления триспецифические связывающие белки можно получить путем объединения антигенсвязывающих доменов двух или более моноспецифических антител (исходных антител) в одно антитело. См. международные публикации №№ WO 2011/038290 A2, WO 2013/086533 A1, WO 2013/070776 A1, WO 2012/154312 A1 и WO 2013/163427 A1. Связывающие белки согласно настоящему изобретению можно получить с использованием доменов или последовательностей, полученных или происходящих из любого антитела человека или антитела нечеловеческого происхождения, в том числе, например, из антител человека, мыши или гуманизированных антител.
[0088] В некоторых вариантах осуществления настоящего изобретения тривалентный связывающий белок способен связывать три различных антигена-мишени. В одном варианте осуществления связывающий белок является триспецифическим, и одна пара легкая цепь-тяжелая цепь способна связывать два различных антигена-мишени или эпитопа, и одна пара легкая цепь-тяжелая цепь способна связывать один антиген-мишень или эпитоп.
[0089] В некоторых вариантах осуществления связывающий белок по настоящему изобретению связывает один или несколько целевых белков HIV и один или несколько целевых белков Т-клетки. В некоторых вариантах осуществления связывающий белок способен специфически связывать один целевой белок HIV и два различных эпитопа на одном целевом белке Т-клетки. В некоторых вариантах осуществления связывающий белок способен специфически связывать один целевой белок HIV и два различных целевых белка Т-клетки (например, CD28 и CD3). В некоторых вариантах осуществления первая и вторая полипептидные цепи связывающего белка образуют два антигенсвязывающих участка, которые специфически нацеливаются на два целевых белка Т-клетки, а третья и четвертая полипептидные цепи связывающего белка образуют антигенсвязывающий участок, который специфически связывает целевой белок HIV. В некоторых вариантах осуществления один или несколько целевых белков HIV представляют собой один или несколько из гликопротеина 120, гликопротеина 41 и гликопротеина 160. В некоторых вариантах осуществления один или несколько целевых белков T-клеток представляют собой один или несколько из CD3 и CD28.
[0090] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:61 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:61; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:62 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:62; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:63 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:63; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:64 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:64.
[0091] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:65 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:65; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:66 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:66; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:67 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:67; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:68 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:68.
[0092] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:69 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:69; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:70 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:70; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:71 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:71; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:72 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:72.
[0093] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:73 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:73; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:74 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:74; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:75 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:75; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:76 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:76.
[0094] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:77 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:77; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:78 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:78; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:79 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:79; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:80 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:80.
[0095] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:81 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:81; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:82 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:82; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:83 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:83; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:84 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:84.
[0096] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:85 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:85; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:86 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:86; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:87 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:87; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:88 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:88.
[0097] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:89 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:89; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:90 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:90; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:91 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:91; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:92 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:92.
[0098] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:93 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:93; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:94 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:94; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:95 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:95; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:96 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:96.
[0099] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:97 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:97; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:98 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:98; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:99 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:99; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:100 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:100.
[00100] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:101 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:101; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:102 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:102; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:103 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:103; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:104 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:104.
[0100] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:105 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:105; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:106 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:106; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:107 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:107; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:108 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:108.
[0101] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:109 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:109; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:110 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:110; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:111 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:111; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:112 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:112.
[0102] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:113 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:113; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:114 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:114; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:115 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:115; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:116 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:116.
[0103] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:117 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:117; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:118 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:118; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:119 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:119; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:120 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:120.
[0104] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:121 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:121; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:122 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:122; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:123 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:123; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:124 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:124.
[0105] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:129 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:129; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:130 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:130; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:131 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:131; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:132 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:132.
[0106] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:133 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:133; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:134 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:134; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:135 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:135; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:136 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:136.
[0107] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:137 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:137; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:138 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:138; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:139 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:139; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:140 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:140.
[0108] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:141 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:141; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:142 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:142; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:143 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:143; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:144 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:144.
[0109] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:145 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:145; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:146 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:146; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:147 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:147; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:148 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:148.
[0110] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:149 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:149; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:150 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:150; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:151 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:151; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:152 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:152.
[0111] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:153 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:153; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:154 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:154; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:155 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:155; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:156 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:156.
[0112] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:157 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:157; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:158 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:158; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:159 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:159; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:160 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:160.
[0113] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:161 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:161; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:162 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:162; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:163 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:163; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:164 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:164.
[0114] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:165 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:165; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:166 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:166; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:167 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:167; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:168 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:168.
[0115] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:169 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:169; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:170 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:170; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:171 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:171; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:172 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:172.
[0116] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, которые специфически связывают один или несколько целевых белков HIV, где первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:173 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:173; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:174 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:174; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:175 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:175; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:176 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:176.
В таблице 4 представлены иллюстративные и неограничивающие полипептиды, которые могут найти применение в любом из триспецифических связывающих белков, описанных в данном документе.
Связывающие участки антител к HIV
[0117] Определенные аспекты настоящего изобретения относятся к связывающим белкам, которые содержат антигенсвязывающий участок, который связывает целевой белок или полипептид HIV.
[0118] В некоторых вариантах осуществления целевой белок HIV представляет собой гликопротеин 120, гликопротеин 41 и гликопротеин 160. В некоторых вариантах осуществления связывающий белок связывает один или несколько из гликопротеина 120, гликопротеина 41 и гликопротеина 160. К иллюстративным белкам HIV относятся без ограничения MPER белка gp41 HIV-1, CD4-связывающий участок белка gp120 HIV-1, гликан в петле V3 белка gp120 HIV-1 или верхняя часть тримера, представляющего собой белок gp120 или gp160 HIV-1. Например, в некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который связывает CD4-связывающий участок белка gp120 HIV-1. К иллюстративным антигенсвязывающим участкам, которые связывают целевые белки HIV, предусмотренные для применения в данном документе, относятся без ограничения участки, описанные в международной публикации № WO2017/074878, такие как участки из антител CD4BS "a", CD4BS "b", MPER, MPER_100W, V1/V2 "a", V1/V2 "b" или V3.
[0119] В некоторых вариантах осуществления связывающий белок, содержащий антигенсвязывающий участок, который связывает целевой белок HIV, является моноспецифическим и/или моновалентным, биспецифическим и/или бивалентным, триспецифическим и/или тривалентным или полиспецифическим и/или поливалентным. В некоторых вариантах осуществления связывающий белок, который содержит антигенсвязывающий участок, связывающий целевой белок HIV, представляет собой триспецифический связывающий белок, содержащий четыре полипептида, которые образуют три антигенсвязывающих участка.
[0120] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, содержащий вариабельный домен тяжелой цепи (VH) антитела, который содержит последовательность CDR-H1, содержащую аминокислотную последовательность NCPIN (SEQ ID NO:1), последовательность CDR-H2, содержащую аминокислотную последовательность WMKPRHGAVSYARQLQG (SEQ ID NO:2), и последовательность CDR-H3, содержащую аминокислотную последовательность GKYCTARDYYNWDFEH (SEQ ID NO:3); и/или вариабельный домен легкой цепи (VL) антитела, который содержит последовательность CDR-L1, содержащую аминокислотную последовательность RTSQYGSLA (SEQ ID NO:4), последовательность CDR-L2, содержащую аминокислотную последовательность SGSTRAA (SEQ ID NO:5), и последовательность CDR-L3, содержащую аминокислотную последовательность QQYEF (SEQ ID NO:6). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, содержащий вариабельный домен тяжелой цепи (VH) антитела, который содержит последовательность CDR-H1, содержащую аминокислотную последовательность NCPIN (SEQ ID NO:1), последовательность CDR-H2, содержащую аминокислотную последовательность WMKPRHGAVSYARQLQG (SEQ ID NO:2), и последовательность CDR-H3, содержащую аминокислотную последовательность GKYCTARDYYNWDFEH (SEQ ID NO:3); и вариабельный домен легкой цепи (VL) антитела, который содержит последовательность CDR-L1, содержащую аминокислотную последовательность RTSQYGSLA (SEQ ID NO:4), последовательность CDR-L2, содержащую аминокислотную последовательность SGSTRAA (SEQ ID NO:5), и последовательность CDR-L3, содержащую аминокислотную последовательность QQYEF (SEQ ID NO:6).
[0121] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, содержащий вариабельный домен тяжелой цепи (VH) антитела, который содержит последовательность CDR-H1, содержащую аминокислотную последовательность GYTFTAHI (SEQ ID NO:7), последовательность CDR-H2, содержащую аминокислотную последовательность IKPQYGAV (SEQ ID NO:8) или IKPQYGAT (SEQ ID NO:9); и/или вариабельный домен легкой цепи (VL) антитела, который содержит последовательность CDR-L1, содержащую аминокислотную последовательность QGVGSD (SEQ ID NO:11), последовательность CDR-L2, содержащую аминокислотную последовательность HTS (SEQ ID NO:12), и последовательность CDR-L3, содержащую аминокислотную последовательность CQVLQF (SEQ ID NO:13). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, содержащий вариабельный домен (VH) тяжелой цепи антитела, который содержит последовательность CDR-H1, содержащую аминокислотную последовательность GYTFTAHI (SEQ ID NO:7), последовательность CDR-H2, содержащую аминокислотную последовательность IKPQYGAV (SEQ ID NO:8) или IKPQYGAT (SEQ ID NO:9); и вариабельный домен легкой цепи (VL) антитела, который содержит последовательность CDR-L1, содержащую аминокислотную последовательность QGVGSD (SEQ ID NO:11), последовательность CDR-L2, содержащую аминокислотную последовательность HTS (SEQ ID NO:12), и последовательность CDR-L3, содержащую аминокислотную последовательность CQVLQF (SEQ ID NO:13). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, содержащий вариабельный домен тяжелой цепи (VH) антитела, который содержит последовательность CDR-H1, содержащую аминокислотную последовательность GYTFTAHI (SEQ ID NO:7), последовательность CDR-H2, содержащую аминокислотную последовательность IKPQYGAV (SEQ ID NO:8); и/или вариабельный домен легкой цепи (VL) антитела, который содержит последовательность CDR-L1, содержащую аминокислотную последовательность QGVGSD (SEQ ID NO:11), последовательность CDR-L2, содержащую аминокислотную последовательность HTS (SEQ ID NO:12), и последовательность CDR-L3, содержащую аминокислотную последовательность CQVLQF (SEQ ID NO:13). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, содержащий вариабельный домен тяжелой цепи (VH) антитела, который содержит последовательность CDR-H1, содержащую аминокислотную последовательность GYTFTAHI (SEQ ID NO:7), последовательность CDR-H2, содержащую аминокислотную последовательность IKPQYGAV (SEQ ID NO:8); и вариабельный домен легкой цепи (VL) антитела, который содержит последовательность CDR-L1, содержащую аминокислотную последовательность QGVGSD (SEQ ID NO:11), последовательность CDR-L2, содержащую аминокислотную последовательность HTS (SEQ ID NO:12), и последовательность CDR-L3, содержащую аминокислотную последовательность CQVLQF (SEQ ID NO:13). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, содержащий вариабельный домен тяжелой цепи (VH) антитела, который содержит последовательность CDR-H1, содержащую аминокислотную последовательность GYTFTAHI (SEQ ID NO:7), последовательность CDR-H2, содержащую аминокислотную последовательность IKPQYGAT (SEQ ID NO:9); и/или вариабельный домен легкой цепи (VL) антитела, который содержит последовательность CDR-L1, содержащую аминокислотную последовательность QGVGSD (SEQ ID NO:11), последовательность CDR-L2, содержащую аминокислотную последовательность HTS (SEQ ID NO:12), и последовательность CDR-L3, содержащую аминокислотную последовательность CQVLQF (SEQ ID NO:13). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, содержащий вариабельный домен тяжелой цепи (VH) антитела, который содержит последовательность CDR-H1, содержащую аминокислотную последовательность GYTFTAHI (SEQ ID NO:7), последовательность CDR-H2, содержащую аминокислотную последовательность IKPQYGAT (SEQ ID NO:9); и вариабельный домен легкой цепи (VL) антитела, который содержит последовательность CDR-L1, содержащую аминокислотную последовательность QGVGSD (SEQ ID NO:11), последовательность CDR-L2, содержащую аминокислотную последовательность HTS (SEQ ID NO:12), и последовательность CDR-L3, содержащую аминокислотную последовательность CQVLQF (SEQ ID NO:13).
[0122] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, содержащий вариабельный домен тяжелой цепи (VH) антитела, который содержит последовательность CDR-H1, содержащую аминокислотную последовательность DCTLN (SEQ ID NO:14), последовательность CDR-H2, содержащую аминокислотную последовательность WLKPRWGAVNYARPLQG (SEQ ID NO:15), и последовательность CDR-H3, содержащую аминокислотную последовательность GKNCDYNWDFEH (SEQ ID NO:16); и/или вариабельный домен легкой цепи (VL) антитела, который содержит последовательность CDR-L1, содержащую аминокислотную последовательность RTSQYGSLA (SEQ ID NO:17), последовательность CDR-L2, содержащую аминокислотную последовательность SGSTRAA (SEQ ID NO:18), и последовательность CDR-L3, содержащую аминокислотную последовательность QQYEF (SEQ ID NO:19). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, содержащий вариабельный домен тяжелой цепи (VH) антитела, который содержит последовательность CDR-H1, содержащую аминокислотную последовательность DCTLN (SEQ ID NO:14), последовательность CDR-H2, содержащую аминокислотную последовательность WLKPRWGAVNYARPLQG (SEQ ID NO:15), и последовательность CDR-H3, содержащую аминокислотную последовательность GKNCDYNWDFEH (SEQ ID NO:16); и вариабельный домен легкой цепи (VL) антитела, который содержит последовательность CDR-L1, содержащую аминокислотную последовательность RTSQYGSLA (SEQ ID NO:17), последовательность CDR-L2, содержащую аминокислотную последовательность SGSTRAA (SEQ ID NO:18), и последовательность CDR-L3, содержащую аминокислотную последовательность QQYEF (SEQ ID NO:19).
[0123] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок с доменом VH, содержащим увеличенную петлю FR3 тяжелой цепи антитела VRC03, например, как описано в Liu, Q. et al. (2019) Nat. Commun. 10:721.
[0124] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности QVRLSQSGGQMKKPGDSMRISCRASGYEFINCPINWIRLAPGKRPEWMGWMKPRHGAVSYARQLQGRVTMTRDMYSETAFLELRSLTSDDTAVYFCTRGKYCTARDYYNWDFEHWGQGTPVTVSS (SEQ ID NO:43), и/или вариабельный домен легкой цепи (VL) антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности SLTQSPGTLSLSPGETAIISCRTSQYGSLAWYQQRPGQAPRLVIYSGSTRAAGIPDRFSGSRWGPDYNLTISNLESGDFGVYYCQQYEFFGQGTKVQVDIK (SEQ ID NO:45). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:43, и/или вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:45. В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:43, и вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:45.
[0125] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности QVRLSQSGGQMKKPGDSMRISCRASGYEFINCPINWIRLAPGKRPEWMGWMKPRHGAVSYARQLQGRVTMTRQLSQDPDDPDWGTAFLELRSLTSDDTAVYFCTRGKYCTARDYYNWDFEHWGQGTPVTVSS (SEQ ID NO:44), и/или вариабельный домен легкой цепи (VL) антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности SLTQSPGTLSLSPGETAIISCRTSQYGSLAWYQQRPGQAPRLVIYSGSTRAAGIPDRFSGSRWGPDYNLTISNLESGDFGVYYCQQYEFFGQGTKVQVDIK (SEQ ID NO:45). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:44, и/или вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:45. В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:44, и вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:45.
[0126] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности RAHLVQSGTAMKKPGASVRVSCQTSGYTFTAHILFWFRQAPGRGLEWVGWIKPQYGAVNFGGGFRDRVTLTRDVYREIAYMDIRGLKPDDTAVYYCARDRSYGDSSWALDAWGQGTTVVVSA (SEQ ID NO:46), и/или вариабельный домен легкой цепи (VL) антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности YIHVTQSPSSLSVSIGDRVTINCQTSQGVGSDLHWYQHKPGRAPKLLIHHTSSVEDGVPSRFSGSGFHTSFNLTISDLQADDIATYYCQVLQFFGRGSRLHIK (SEQ ID NO:49). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:46, и/или вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:49. В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:46, и вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:49.
[0127] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности RAHLVQSGTAMKKPGASVRVSCQTSGYTFTAHILFWFRQAPGRGLEWVGWIKPQYGATNFGGGFRDRVTLTRDVYREIAYMDIRGLKPDDTAVYYCARDRSYGDSSWALDAWGQGTTVVVSA (SEQ ID NO:47), и/или вариабельный домен легкой цепи (VL) антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности YIHVTQSPSSLSVSIGDRVTINCQTSQGVGSDLHWYQHKPGRAPKLLIHHTSSVEDGVPSRFSGSGFHTSFNLTISDLQADDIATYYCQVLQFFGRGSRLHIK (SEQ ID NO:49). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:47, и/или вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:49. В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:47, и вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:49.
[0128] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности RAHLVQSGTAMKKPGASVRVSCQTSGYTFTAHILFWFRQAPGRGLEWVGWIKPQYGAVNFGGGFRDRVTLTRQLSQDPDDPDWGIAYMDIRGLKPDDTAVYYCARDRSYGDSSWALDAWGQGTTVVVSA (SEQ ID NO:48), и/или вариабельный домен легкой цепи (VL) антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности YIHVTQSPSSLSVSIGDRVTINCQTSQGVGSDLHWYQHKPGRAPKLLIHHTSSVEDGVPSRFSGSGFHTSFNLTISDLQADDIATYYCQVLQFFGRGSRLHIK (SEQ ID NO:49). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:48, и/или вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:49. В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:48, и вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:49.
[0129] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности QVQLVQSGGQMKKPGESMRISCRASGYEFIDCTLNWIRLAPGKRPEWMGWLKPRWGAVNYARPLQGRVTMTRQLSQDPDDPDWGTAFLELRSLTVDDTAVYFCTRGKNCDYNWDFEHWGRGTPVIVSS (SEQ ID NO:50), и/или вариабельный домен легкой цепи (VL) антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности LTQSPGTLSLSPGETAIISCRTSQYGSLAWYQQRPGQAPRLVIYSGSTRAAGIPDRFSGSRWGPDYNLTISNLESGDFGVYYCQQYEFFGQGTKVQVDIK (SEQ ID NO:51). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:50, и/или вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:51. В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:50, и вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:51.
[0130] В некоторых вариантах осуществления любого из приведенных выше вариантов осуществления связывающий белок представляет собой триспецифический связывающий белок. В некоторых вариантах осуществления триспецифический связывающий белок содержит антигенсвязывающий участок, который связывает целевой белок HIV, антигенсвязывающий участок, который связывает полипептид CD28, и антигенсвязывающий участок, который связывает полипептид CD3. В некоторых вариантах осуществления связывающий белок представляет собой триспецифический белок, содержащий четыре полипептида, которые содержат три антигенсвязывающих участка, где полипептид формулы I и полипептид формулы II образуют кроссоверную пару легкая цепь-тяжелая цепь (например, как описано в данном документе). В некоторых вариантах осуществления домены VH и VL любого из антигенсвязывающих участков антитела к CD38, описанных выше, представляют собой VH3 и VL3 и образуют третий антигенсвязывающий участок, который связывает целевой белок HIV. В некоторых вариантах осуществления VH1 и VL1 образуют первый антигенсвязывающий участок, который связывает полипептид CD28, VH2 и VL2 образуют второй антигенсвязывающий участок, который связывает полипептид CD3, и домены VH и VL любого из антигенсвязывающих участков антитела к HIV, описанных выше и/или в таблице 1, представляют собой VH3 и VL3 и образуют третий антигенсвязывающий участок, который связывает целевой белок HIV.
[0131] Последовательности иллюстративных антигенсвязывающих участков антитела к HIV представлены в таблице 1. В некоторых вариантах осуществления связывающий белок, содержащий антигенсвязывающий участок антитела к HIV по настоящему изобретению, содержит 1, 2, 3, 4, 5 или все 6 последовательностей CDR антитела к HIV, описанного в таблице 1. В некоторых вариантах осуществления связывающий белок, содержащий антигенсвязывающий участок антитела к HIV по настоящему изобретению, содержит последовательность домена VH и/или последовательность домена VL антитела к HIV, описанного в таблице 1.
Таблица 1. Последовательности белка, связывающего HIV.
(CD4bs, связывающий gp120 Env)
(CD4bs, связывающий gp120 Env)
Исходная
Участки, связывающие CD28
[0132] Определенные аспекты настоящего изобретения относятся к связывающим белкам, которые содержат антигенсвязывающий участок, который связывает полипептид CD28. В некоторых вариантах осуществления полипептид CD28 представляет собой полипептид CD28 человека, также известный как Tp44. Полипептиды CD28 человека известны из уровня техники, и к ним относятся без ограничения полипептиды, представленные под номерами доступа NCBI XP_011510499.1, XP_011510497.1, XP_011510496.1, NP_001230007.1, NP_001230006.1 или NP_006130.1, или полипептид, полученный из гена под номером ID NCBI 940. В некоторых вариантах осуществления связывающий белок, содержащий антигенсвязывающий участок, который связывает полипептид CD28, является моноспецифическим и/или моновалентным, биспецифическим и/или бивалентным, триспецифическим и/или тривалентным или полиспецифическим и/или поливалентным. В некоторых вариантах осуществления связывающий белок, который содержит антигенсвязывающий участок, который связывает полипептид CD28, представляет собой триспецифический связывающий белок, содержащий четыре полипептида, которые образуют три антигенсвязывающих участка. В некоторых вариантах осуществления связывающий белок, который содержит антигенсвязывающий участок, который связывает полипептид CD28, представляет собой триспецифический связывающий белок, содержащий четыре полипептида, которые образуют три антигенсвязывающих участка, один из которых связывает полипептид CD28, и один из которых связывает полипептид CD3. В некоторых вариантах осуществления связывающий белок, содержащий антигенсвязывающий участок, который связывает полипептид CD28, представляет собой триспецифический связывающий белок, содержащий четыре полипептида, которые образуют три антигенсвязывающих участка, один из которых связывает полипептид CD28, один из которых связывает полипептид CD3, и один из которых связывает целевой белок HIV.
[0133] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, содержащий вариабельный домен тяжелой цепи (VH) антитела, который содержит последовательность CDR-H1, содержащую аминокислотную последовательность GYTFTSYY (SEQ ID NO:31), последовательность CDR-H2, содержащую аминокислотную последовательность IYPGNVNT (SEQ ID NO:32), и последовательность CDR-H3, содержащую аминокислотную последовательность TRSHYGLDWNFDV (SEQ ID NO:33); и/или вариабельный домен легкой цепи (VL) антитела, который содержит последовательность CDR-L1, содержащую аминокислотную последовательность QNIYVW (SEQ ID NO:34), последовательность CDR-L2, содержащую аминокислотную последовательность KAS (SEQ ID NO:35), и последовательность CDR-L3, содержащую аминокислотную последовательность QQGQTYPY (SEQ ID NO:36). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, содержащий вариабельный домен тяжелой цепи (VH) антитела, который содержит последовательность CDR-H1, содержащую аминокислотную последовательность GYTFTSYY (SEQ ID NO:31), последовательность CDR-H2, содержащую аминокислотную последовательность IYPGNVNT (SEQ ID NO:32), и последовательность CDR-H3, содержащую аминокислотную последовательность TRSHYGLDWNFDV (SEQ ID NO:33); и вариабельный домен легкой цепи (VL) антитела, который содержит последовательность CDR-L1, содержащую аминокислотную последовательность QNIYVW (SEQ ID NO:34), последовательность CDR-L2, содержащую аминокислотную последовательность KAS (SEQ ID NO:35), и последовательность CDR-L3, содержащую аминокислотную последовательность QQGQTYPY (SEQ ID NO:36).
[0134] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности QVQLVQSGAEVVKPGASVKVSCKASGYTFTSYYIHWVRQAPGQGLEWIGSIYPGNVNTNYAQKFQGRATLTVDTSISTAYMELSRLRSDDTAVYYCTRSHYGLDWNFDVWGKGTTVTVSS (SEQ ID NO:59), и/или вариабельный домен легкой цепи (VL) антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности DIQMTQSPSSLSASVGDRVTITCQASQNIYVWLNWYQQKPGKAPKLLIYKASNLHTGVPSRFSGSGSGTDFTLTISSLQPEDIATYYCQQGQTYPYTFGQGTKLEIK (SEQ ID NO:60). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:59, и/или вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:60. В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:59, и вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:60.
[0135] В некоторых вариантах осуществления любого из приведенных выше вариантов осуществления связывающий белок представляет собой триспецифический связывающий белок. В некоторых вариантах осуществления триспецифический связывающий белок содержит антигенсвязывающий участок, который связывает целевой белок HIV, антигенсвязывающий участок, который связывает полипептид CD28, и антигенсвязывающий участок, который связывает полипептид CD3. В некоторых вариантах осуществления связывающий белок представляет собой триспецифический белок, содержащий четыре полипептида, которые содержат три антигенсвязывающих участка, где полипептид формулы I и полипептид формулы II образуют кроссоверную пару легкая цепь-тяжелая цепь (например, как описано в данном документе). В некоторых вариантах осуществления домены VH и VL любого из антигенсвязывающих участков антитела к CD28, описанных выше, представляют собой VH1 и VL1 и образуют первый антигенсвязывающий участок, который связывает полипептид CD28. В некоторых вариантах осуществления домены VH и VL любого из антигенсвязывающих участков антитела к CD28, описанных выше, представляют собой VH1 и VL1 и образуют первый антигенсвязывающий участок, который связывает полипептид CD28, VH2 и VL2 образуют второй антигенсвязывающий участок, который связывает полипептид CD3, и VH3 и VL3 образуют третий антигенсвязывающий участок, который связывает целевой белок HIV.
[0136] Последовательности иллюстративных антигенсвязывающих участков антитела к CD28 представлены в таблице 2. В некоторых вариантах осуществления связывающий белок, содержащий антигенсвязывающий участок антитела к CD28 по настоящему изобретению, содержит 1, 2, 3, 4, 5 или все 6 последовательностей CDR антитела к CD28, описанного в таблице 2. В некоторых вариантах осуществления связывающий белок, содержащий антигенсвязывающий участок антитела к CD28 по настоящему изобретению, содержит последовательность домена VH и/или последовательность домена VL антитела к CD28, описанного в таблице 2.
Таблица 2. Последовательности белка, связывающего CD28.
Связывающие участки антитела к CD3
[0137] Определенные аспекты настоящего изобретения относятся к связывающим белкам, которые содержат антигенсвязывающий участок, который связывает полипептид CD3. В некоторых вариантах осуществления полипептид CD3 представляет собой полипептид CD3 человека, в том числе CD3-дельта (также известный как T3D, IMD19 и CD3-DELTA), CD3-эпсилон (также известный как T3E, IMD18 и TCRE) и CD3-гамма (также известный как T3G, IMD17 и CD3-GAMMA). Полипептиды CD3 человека известны из уровня техники, и к ним относятся без ограничения полипептиды, представленные под номерами доступа NCBI XP_006510029.1 или NP_031674.1, или полипептид, полученный из гена под номерами ID NCBI 915, 916 или 917. В некоторых вариантах осуществления связывающий белок, содержащий антигенсвязывающий участок, который связывает полипептид CD3, является моноспецифическим и/или моновалентным, биспецифическим и/или бивалентным, триспецифическим и/или тривалентным или полиспецифическим и/или поливалентным. В некоторых вариантах осуществления связывающий белок, который содержит антигенсвязывающий участок, который связывает полипептид CD3, представляет собой триспецифический связывающий белок, содержащий четыре полипептида, которые образуют три антигенсвязывающих участка. В некоторых вариантах осуществления связывающий белок, который содержит антигенсвязывающий участок, который связывает полипептид CD3, представляет собой триспецифический связывающий белок, содержащий четыре полипептида, которые образуют три антигенсвязывающих участка, один из которых связывает полипептид CD28, и один из которых связывает полипептид CD3. В некоторых вариантах осуществления связывающий белок, содержащий антигенсвязывающий участок, который связывает полипептид CD3, представляет собой триспецифический связывающий белок, содержащий четыре полипептида, которые образуют три антигенсвязывающих участка, один из которых связывает полипептид CD28, один из которых связывает полипептид CD3, и один из которых связывает целевой белок HIV.
[0138] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, содержащий вариабельный домен (VH) тяжелой цепи антитела, который содержит последовательность CDR-H1, содержащую аминокислотную последовательность GFTFTKAW (SEQ ID NO:20), последовательность CDR-H2, содержащую аминокислотную последовательность IKDKSNSYAT (SEQ ID NO:21), и последовательность CDR-H3, содержащую аминокислотную последовательность RGVYYALSPFDY (SEQ ID NO:22); и/или вариабельный домен легкой цепи (VL) антитела, который содержит последовательность CDR-L1, содержащую аминокислотную последовательность QSLVHX1NX2X3TY, где X1 представляет собой E или Q, X2 представляет собой A или L, и X3 представляет собой Q, R или F (SEQ ID NO:293), последовательность CDR-L2, содержащую аминокислотную последовательность KVS (SEQ ID NO:29), и последовательность CDR-L3, содержащую аминокислотную последовательность GQGTQYPFT (SEQ ID NO:30). В некоторых вариантах осуществления последовательность CDR-L1 домена VL2 содержит аминокислотную последовательность, выбранную из группы, состоящей из QSLVHQNAQTY (SEQ ID NO:24), QSLVHENLQTY (SEQ ID NO:25), QSLVHENLFTY (SEQ ID NO:26) и QSLVHENLRTY (SEQ ID NO:27).
[0139] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, содержащий вариабельный домен (VH) тяжелой цепи антитела, который содержит последовательность CDR-H1, содержащую аминокислотную последовательность GFTFTKAW (SEQ ID NO:20), последовательность CDR-H2, содержащую аминокислотную последовательность IKDKSNSYAT (SEQ ID NO:21), и последовательность CDR-H3, содержащую аминокислотную последовательность RGVYYALSPFDY (SEQ ID NO:22); и/или вариабельный домен легкой цепи (VL) антитела, который содержит последовательность CDR-L1, содержащую аминокислотную последовательность QSLVHQNAQTY (SEQ ID NO:24), последовательность CDR-L2, содержащую аминокислотную последовательность KVS (SEQ ID NO:29), и последовательность CDR-L3, содержащую аминокислотную последовательность GQGTQYPFT (SEQ ID NO:30). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, содержащий вариабельный домен (VH) тяжелой цепи антитела, который содержит последовательность CDR-H1, содержащую аминокислотную последовательность GFTFTKAW (SEQ ID NO:20), последовательность CDR-H2, содержащую аминокислотную последовательность IKDKSNSYAT (SEQ ID NO:21), и последовательность CDR-H3, содержащую аминокислотную последовательность RGVYYALSPFDY (SEQ ID NO:22); и вариабельный домен легкой цепи (VL) антитела, который содержит последовательность CDR-L1, содержащую аминокислотную последовательность QSLVHQNAQTY (SEQ ID NO:24), последовательность CDR-L2, содержащую аминокислотную последовательность KVS (SEQ ID NO:29), и последовательность CDR-L3, содержащую аминокислотную последовательность GQGTQYPFT (SEQ ID NO:30).
[0140] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, содержащий вариабельный домен (VH) тяжелой цепи антитела, который содержит последовательность CDR-H1, содержащую аминокислотную последовательность GFTFTKAW (SEQ ID NO:20), последовательность CDR-H2, содержащую аминокислотную последовательность IKDKSNSYAT (SEQ ID NO:21), и последовательность CDR-H3, содержащую аминокислотную последовательность RGVYYALSPFDY (SEQ ID NO:22); и/или вариабельный домен легкой цепи (VL) антитела, который содержит последовательность CDR-L1, содержащую аминокислотную последовательность QSLVHENLQTY (SEQ ID NO:25), последовательность CDR-L2, содержащую аминокислотную последовательность KVS (SEQ ID NO:29), и последовательность CDR-L3, содержащую аминокислотную последовательность GQGTQYPFT (SEQ ID NO:30). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, содержащий вариабельный домен (VH) тяжелой цепи антитела, который содержит последовательность CDR-H1, содержащую аминокислотную последовательность GFTFTKAW (SEQ ID NO:20), последовательность CDR-H2, содержащую аминокислотную последовательность IKDKSNSYAT (SEQ ID NO:21), и последовательность CDR-H3, содержащую аминокислотную последовательность RGVYYALSPFDY (SEQ ID NO:22); и вариабельный домен легкой цепи (VL) антитела, который содержит последовательность CDR-L1, содержащую аминокислотную последовательность QSLVHENLQTY (SEQ ID NO:25), последовательность CDR-L2, содержащую аминокислотную последовательность KVS (SEQ ID NO:29), и последовательность CDR-L3, содержащую аминокислотную последовательность GQGTQYPFT (SEQ ID NO:30).
[0141] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, содержащий вариабельный домен (VH) тяжелой цепи антитела, который содержит последовательность CDR-H1, содержащую аминокислотную последовательность GFTFTKAW (SEQ ID NO:20), последовательность CDR-H2, содержащую аминокислотную последовательность IKDKSNSYAT (SEQ ID NO:21), и последовательность CDR-H3, содержащую аминокислотную последовательность RGVYYALSPFDY (SEQ ID NO:22); и/или вариабельный домен легкой цепи (VL) антитела, который содержит последовательность CDR-L1, содержащую аминокислотную последовательность QSLVHENLFTY (SEQ ID NO:26), последовательность CDR-L2, содержащую аминокислотную последовательность KVS (SEQ ID NO:29), и последовательность CDR-L3, содержащую аминокислотную последовательность GQGTQYPFT (SEQ ID NO:30). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, содержащий вариабельный домен (VH) тяжелой цепи антитела, который содержит последовательность CDR-H1, содержащую аминокислотную последовательность GFTFTKAW (SEQ ID NO:20), последовательность CDR-H2, содержащую аминокислотную последовательность IKDKSNSYAT (SEQ ID NO:21), и последовательность CDR-H3, содержащую аминокислотную последовательность RGVYYALSPFDY (SEQ ID NO:22); и вариабельный домен легкой цепи (VL) антитела, который содержит последовательность CDR-L1, содержащую аминокислотную последовательность QSLVHENLFTY (SEQ ID NO:26), последовательность CDR-L2, содержащую аминокислотную последовательность KVS (SEQ ID NO:29), и последовательность CDR-L3, содержащую аминокислотную последовательность GQGTQYPFT (SEQ ID NO:30).
[0142] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, содержащий вариабельный домен (VH) тяжелой цепи антитела, который содержит последовательность CDR-H1, содержащую аминокислотную последовательность GFTFTKAW (SEQ ID NO:20), последовательность CDR-H2, содержащую аминокислотную последовательность IKDKSNSYAT (SEQ ID NO:21), и последовательность CDR-H3, содержащую аминокислотную последовательность RGVYYALSPFDY (SEQ ID NO:22); и/или вариабельный домен легкой цепи (VL) антитела, который содержит последовательность CDR-L1, содержащую аминокислотную последовательность QSLVHENLRTY (SEQ ID NO:27), последовательность CDR-L2, содержащую аминокислотную последовательность KVS (SEQ ID NO:29), и последовательность CDR-L3, содержащую аминокислотную последовательность GQGTQYPFT (SEQ ID NO:30). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, содержащий вариабельный домен (VH) тяжелой цепи антитела, который содержит последовательность CDR-H1, содержащую аминокислотную последовательность GFTFTKAW (SEQ ID NO:20), последовательность CDR-H2, содержащую аминокислотную последовательность IKDKSNSYAT (SEQ ID NO:21), и последовательность CDR-H3, содержащую аминокислотную последовательность RGVYYALSPFDY (SEQ ID NO:22); и вариабельный домен легкой цепи (VL) антитела, который содержит последовательность CDR-L1, содержащую аминокислотную последовательность QSLVHENLRTY (SEQ ID NO:27), последовательность CDR-L2, содержащую аминокислотную последовательность KVS (SEQ ID NO:29), и последовательность CDR-L3, содержащую аминокислотную последовательность GQGTQYPFT (SEQ ID NO:30).
[0143] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности QVQLVESGGGVVQPGRSLRLSCAASGFTFTKAWMHWVRQAPGKQLEWVAQIKDKSNSYATYYADSVKGRFTISRDDSKNTLYLQMNSLRAEDTAVYYCRGVYYALSPFDYWGQGTLVTVSS (SEQ ID NO:52), и/или вариабельный домен легкой цепи (VL) антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности, выбранной из группы, состоящей из DIVMTQTPLSLSVTPGQPASISCKSSQSLVHQNAQTYLSWYLQKPGQSPQSLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCGQGTQYPFTFGSGTKVEIK (SEQ ID NO:54), DIVMTQTPLSLSVTPGQPASISCKSSQSLVHENLQTYLSWYLQKPGQSPQSLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCGQGTQYPFTFGSGTKVEIK (SEQ ID NO:55), DIVMTQTPLSLSVTPGQPASISCKSSQSLVHENLFTYLSWYLQKPGQSPQSLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCGQGTQYPFTFGSGTKVEIK (SEQ ID NO:56) и DIVMTQTPLSLSVTPGQPASISCKSSQSLVHENLRTYLSWYLQKPGQSPQSLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCGQGTQYPFTFGSGTKVEIK (SEQ ID NO:57). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:52, и/или вариабельный домен легкой цепи (VL) антитела, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO:54, SEQ ID NO:55, SEQ ID NO:56 и SEQ ID NO:57. В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:52, и вариабельный домен легкой цепи (VL) антитела, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO:54, SEQ ID NO:55, SEQ ID NO:56 и SEQ ID NO:57.
[0144] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности QVQLVESGGGVVQPGRSLRLSCAASGFTFTKAWMHWVRQAPGKQLEWVAQIKDKSNSYATYYADSVKGRFTISRDDSKNTLYLQMNSLRAEDTAVYYCRGVYYALSPFDYWGQGTLVTVSS (SEQ ID NO:52), и/или вариабельный домен легкой цепи (VL) антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности DIVMTQTPLSLSVTPGQPASISCKSSQSLVHQNAQTYLSWYLQKPGQSPQSLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCGQGTQYPFTFGSGTKVEIK (SEQ ID NO:54). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:52, и/или вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:54. В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:52, и вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:54.
[0145] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности QVQLVESGGGVVQPGRSLRLSCAASGFTFTKAWMHWVRQAPGKQLEWVAQIKDKSNSYATYYADSVKGRFTISRDDSKNTLYLQMNSLRAEDTAVYYCRGVYYALSPFDYWGQGTLVTVSS (SEQ ID NO:52), и/или вариабельный домен легкой цепи (VL) антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности DIVMTQTPLSLSVTPGQPASISCKSSQSLVHENLQTYLSWYLQKPGQSPQSLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCGQGTQYPFTFGSGTKVEIK (SEQ ID NO:55). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:52, и/или вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:55. В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:52, и вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:55.
[0146] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности QVQLVESGGGVVQPGRSLRLSCAASGFTFTKAWMHWVRQAPGKQLEWVAQIKDKSNSYATYYADSVKGRFTISRDDSKNTLYLQMNSLRAEDTAVYYCRGVYYALSPFDYWGQGTLVTVSS (SEQ ID NO:52), и/или вариабельный домен легкой цепи (VL) антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности DIVMTQTPLSLSVTPGQPASISCKSSQSLVHENLFTYLSWYLQKPGQSPQSLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCGQGTQYPFTFGSGTKVEIK (SEQ ID NO:56). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:52, и/или вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:56. В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:52, и вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:56.
[0147] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности QVQLVESGGGVVQPGRSLRLSCAASGFTFTKAWMHWVRQAPGKQLEWVAQIKDKSNSYATYYADSVKGRFTISRDDSKNTLYLQMNSLRAEDTAVYYCRGVYYALSPFDYWGQGTLVTVSS (SEQ ID NO:52), и/или вариабельный домен легкой цепи (VL) антитела, содержащий аминокислотную последовательность, которая на по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или на 100% идентична аминокислотной последовательности DIVMTQTPLSLSVTPGQPASISCKSSQSLVHENLRTYLSWYLQKPGQSPQSLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCGQGTQYPFTFGSGTKVEIK (SEQ ID NO:57). В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:52, и/или вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:57. В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит антигенсвязывающий участок, который содержит вариабельный домен (VH) тяжелой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:52, и вариабельный домен (VL) легкой цепи антитела, содержащий аминокислотную последовательность под SEQ ID NO:57.
[0148] Преимущественно, в данном документе описаны участки связывания антител к CD3 с высокой аффинностью связывания с полипептидами CD3 человека и устранены потенциальные недостатки при изготовлении (например, участки дезамидирования).
[0149] В некоторых вариантах осуществления любого из приведенных выше вариантов осуществления связывающий белок представляет собой триспецифический связывающий белок. В некоторых вариантах осуществления триспецифический связывающий белок содержит антигенсвязывающий участок, который связывает целевой белок HIV, антигенсвязывающий участок, который связывает полипептид CD28, и антигенсвязывающий участок, который связывает полипептид CD3. В некоторых вариантах осуществления связывающий белок представляет собой триспецифический белок, содержащий четыре полипептида, которые содержат три антигенсвязывающих участка, где полипептид формулы I и полипептид формулы II образуют кроссоверную пару легкая цепь-тяжелая цепь (например, как описано в данном документе). В некоторых вариантах осуществления домены VH и VL любого из антигенсвязывающих участков антитела к CD3, описанных выше, представляют собой VH2 и VL2 и образуют второй антигенсвязывающий участок, который связывает полипептид CD3. В некоторых вариантах осуществления VH1 и VL1 образуют первый антигенсвязывающий участок, который связывает полипептид CD28, домены VH и VL любого из антигенсвязывающих участков антител к CD3, описанных выше и/или в таблице 3, представляют собой VH2 и VL2 и образуют второй антигенсвязывающий участок, который связывает полипептид CD3, а VH3 и VL3 образуют третий антигенсвязывающий участок, который связывает целевой белок HIV.
[0150] Последовательности иллюстративных антигенсвязывающих участков антитела к CD3 представлены в таблице 3. В некоторых вариантах осуществления связывающий белок, содержащий антигенсвязывающий участок антитела к CD3 по настоящему изобретению, содержит 1, 2, 3, 4, 5 или все 6 последовательностей CDR антитела к CD3, описанного в таблице 3. В некоторых вариантах осуществления связывающий белок, содержащий антигенсвязывающий участок антитела к CD3 по настоящему изобретению, содержит последовательность домена VH и/или последовательность домена VL антитела к CD3, описанного в таблице 3.
Таблица 3. Последовательности белка, связывающего антитело к CD3.
Исходная
Исходная
Исходная
Исходная
Исходная
Исходная
где X1 представляет собой E или Q, X2 представляет собой A или L, и X3 представляет собой Q, R или F
Исходная
32/35 QQ
ENLQ
ENLF
ENLR
DNAQ
Линкеры
[0151] В некоторых вариантах осуществления длина линкеров L1, L2, L3 и L4 варьирует от нуля аминокислот (длина=0) до приблизительно 100 аминокислот или менее чем 100, 50, 40, 30, 20 или 15 аминокислот или меньше. Длина линкеров также может составлять 10, 9, 8, 7, 6, 5, 4, 3, 2 или 1 аминокислоту. Все из L1, L2, L3 и L4 в одном связывающем белке могут иметь одинаковую аминокислотную последовательность или все могут иметь различные аминокислотные последовательности.
[0152] Примеры подходящих линкеров включают, например, GGGGSGGGGS (SEQ ID NO:40), GGGGSGGGGSGGGGS (SEQ ID NO:41), S, RT, TKGPS (SEQ ID NO:39), GQPKAAP (SEQ ID NO:38), GGSGSSGSGG (SEQ ID NO:42) и DKTHT (SEQ ID NO:37), а также раскрытые в международных публикациях №№ WO2017/074878 и WO2017/180913. Вышеперечисленные примеры не предназначены для какого-либо ограничения объема настоящего изобретения, и при этом было показано, что линкеры, содержащие выбранные случайным образом аминокислоты, выбранные из группы, состоящей из валина, лейцина, изолейцина, серина, треонина, лизина, аргинина, гистидина, аспартата, глутамата, аспарагина, глутамина, глицина и пролина, подходят для связывающих белков.
[0153] Состав и последовательность аминокислотных остатков в линкере может меняться в зависимости от типа элемента вторичной структуры, который необходимо достигнуть при помощи линкера. Например, глицин, серин и аланин являются наиболее подходящими для линкеров, характеризующихся максимальной гибкостью. Некоторые комбинации глицина, пролина, треонина и серина применимы, если необходим более жесткий и удлиненный линкер. При необходимости любой аминокислотный остаток может рассматриваться как линкер в комбинации с другими аминокислотными остатками для конструирования более длинных пептидных линкеров в зависимости от требуемых свойств.
[0154] В некоторых вариантах осуществления длина L1 в по меньшей два раза превышает длину L3. В некоторых вариантах осуществления длина L2 в по меньшей два раза превышает длину L4. В некоторых вариантах осуществления длина L1 в по меньшей мере два раза превышает длину L3, а длина L2 в по меньшей мере два раза превышает длину L4. В некоторых вариантах осуществления длина L1 составляет 3-12 аминокислотных остатков, длина L2 составляет 3-14 аминокислотных остатков, длина L3 составляет 1-8 аминокислотных остатков, и длина L4 составляет 1-3 аминокислотных остатка. В некоторых вариантах осуществления длина L1 составляет 5-10 аминокислотных остатков, длина L2 составляет 5-8 аминокислотных остатков, длина L3 составляет 1-5 аминокислотных остатков, и длина L4 составляет 1-2 аминокислотных остатка. В некоторых вариантах осуществления длина L1 составляет 7 аминокислотных остатков, длина L2 составляет 5 аминокислотных остатков, длина L3 составляет 1 аминокислотный остаток, и длина L4 составляет 2 аминокислотных остатка.
[0155] В некоторых вариантах осуществления каждый из L1, L2, L3 и L4 независимо имеет длину, составляющую ноль аминокислот, или содержит последовательность, выбранную из группы, состоящей из GGGGSGGGGS (SEQ ID NO:40), GGGGSGGGGSGGGGS (SEQ ID NO:41), S, RT, TKGPS (SEQ ID NO:39), GQPKAAP (SEQ ID NO:38) и GGSGSSGSGG (SEQ ID NO:42). В некоторых вариантах осуществления каждый из L1, L2, L3 и L4 независимо содержит последовательность, выбранную из группы, состоящей из GGGGSGGGGS (SEQ ID NO:40), GGGGSGGGGSGGGGS (SEQ ID NO:41), S, RT, TKGPS (SEQ ID NO:39), GQPKAAP (SEQ ID NO:38) и GGSGSSGSGG (SEQ ID NO:42). В некоторых вариантах осуществления L1 содержит последовательность GQPKAAP (SEQ ID NO:38), L2 содержит последовательность TKGPS (SEQ ID NO:39), L3 содержит последовательность S, и L4 содержит последовательность RT.
[0156] В некоторых вариантах осуществления по меньшей мере один из L1, L2, L3 или L4 содержит последовательность DKTHT (SEQ ID NO:37). В некоторых вариантах осуществления L1, L2, L3 и L4 содержат последовательность DKTHT (SEQ ID NO:37).
Fc-области и константные домены
[0157] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит вторую полипептидную цепь, дополнительно содержащую Fc-область, связанную с CH1, при этом Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина. В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит третью полипептидную цепь, дополнительно содержащую Fc-область, связанную с CH1, при этом Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина. В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит вторую полипептидную цепь, дополнительно содержащую Fc-область, связанную с CH1, при этом Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, и третью полипептидную цепь, дополнительно содержащую Fc-область, связанную с CH1, при этом Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина.
[0158] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит полноразмерную тяжелую цепь антитела или полипептидную цепь, содержащую Fc-область. В некоторых вариантах осуществления Fc-область представляет собой Fc-область человека, например, Fc-область IgG1, IgG2, IgG3 или IgG4 человека. В некоторых вариантах осуществления Fc-область включает шарнир, CH1, CH2, CH3 и необязательно домены CH4. В некоторых вариантах осуществления Fc-область представляет собой Fc-область IgG1 человека. В некоторых вариантах осуществления Fc-область представляет собой Fc-область IgG4 человека. В некоторых вариантах осуществления Fc-область содержит одну или несколько мутаций, описанных ниже. В некоторых вариантах осуществления Fc-область представляет собой Fc-область одного из полипептидов тяжелой цепи (например, полипептида 2 или 3) связывающего белка, представленного в таблице 4. В некоторых вариантах осуществления константная область тяжелой цепи представляет собой константную область одного из полипептидов тяжелой цепи (например, полипептида 2 или 3) связывающего белка, представленного в таблице 4. В некоторых вариантах осуществления константная область легкой цепи представляет собой константную область одного из полипептидов легкой цепи (например, полипептида 1 или 4) связывающего белка, представленного в таблице 4.
[0159] В некоторых вариантах осуществления связывающий белок согласно настоящему изобретению содержит один или два варианта Fc. Термин "вариант Fc", используемый в данном документе, обозначает молекулу или последовательность, которая модифицирована по сравнению с нативным Fc, но все еще содержит участок связывания для рецептора реутилизации FcRn (неонатального Fc-рецептора). Иллюстративные варианты Fc и их взаимодействие с рецептором реутилизации известны из уровня техники. Таким образом, термин "вариант Fc" может предусматривать молекулу или последовательность, полученную в результате гуманизации нативного Fc отличного от человеческого происхождения. Кроме того, нативный Fc содержит области, которые можно удалить, поскольку они обеспечивают структурные признаки или биологическую активность, которые не требуются для антителоподобных связывающих белков по настоящему изобретению. Таким образом, термин "вариант Fc" предусматривает молекулу или последовательность, в которой отсутствует один или несколько участков или остатков нативного Fc или в которой были модифицированы один или несколько участков или остатков Fc, воздействующих на или вовлеченных в: (1) образование дисульфидной связи, (2) несовместимость с выбранной клеткой-хозяином, (3) гетерогенность N-концов при экспрессии в выбранной клетке-хозяине, (4) гликозилирование, (5) взаимодействие с системой комплемента, (6) связывание с Fc-рецептором, отличным от рецептора реутилизации, или (7) антителозависимую клеточную цитотоксичность (ADCC).
[0160] В некоторых вариантах осуществления связывающий белок по настоящему изобретению (например, триспецифический связывающий белок) содержит мутацию по типу "выступа" на второй полипептидной цепи и мутацию по типу "впадины" на третьей полипептидной цепи. В некоторых вариантах осуществления связывающий белок согласно настоящему изобретению содержит мутацию по типу "выступа" на третьей полипептидной цепи и мутацию по типу "впадины" на второй полипептидной цепи. В некоторых вариантах осуществления мутация по типу "выступа" предусматривает замену (замены) в положениях, соответствующих положениям 354 и/или 366 IgG1 или IgG4 человека в соответствии с EU-индексом. В некоторых вариантах осуществления аминокислотные замены представляют собой S354C, T366W, T366Y, S354C и T366W или S354C и T366Y. В некоторых вариантах осуществления мутация по типу "выступа" предусматривает замены в положениях, соответствующих положениям 354 и 366 IgG1 или IgG4 человека в соответствии с EU-индексом. В некоторых вариантах осуществления аминокислотные замены представляют собой S354C и T366W. В некоторых вариантах осуществления мутация по типу "впадины" предусматривает замену(замены) в положениях, соответствующих положениям 407 и необязательно 349, 366 и/или 368 IgG1 или IgG4 человека в соответствии с EU-индексом. В некоторых вариантах осуществления аминокислотные замены представляют собой Y407V или Y407T и необязательно Y349C, T366S и/или L368A. В некоторых вариантах осуществления мутация по типу "впадины" предусматривает замены в положениях, соответствующих положениям 349, 366, 368 и 407 IgG1 или IgG4 человека в соответствии с EU-индексом. В некоторых вариантах осуществления аминокислотные замены представляют собой Y349C, T366S, L368A и Y407V.
[0161] В некоторых вариантах осуществления вторая полипептидная цепь дополнительно содержит первую Fc-область, связанную с CH1, при этом первая Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где первая Fc-область содержит аминокислотную(-ые) замену(-ы) в положениях, соответствующих положениям 366 и необязательно 354 IgG1 или IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой T366W или T366Y и необязательно S354C; и где третья полипептидная цепь дополнительно содержит вторую Fc-область, связанную с CH1, при этом вторая Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где вторая Fc-область содержит аминокислотную(-ые) замену(-ы) в положениях, соответствующих положениям 407 и необязательно 349, 366 и/или 368 IgG1 или IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой Y407V или Y407T и необязательно Y349C, T366S и/или L368A.
[0162] В некоторых вариантах осуществления вторая полипептидная цепь дополнительно содержит первую Fc-область, связанную с CH1, при этом первая Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где первая Fc-область содержит аминокислотную(-ые) замену(-ы) в положениях, соответствующих положениям 407 и необязательно 349, 366 и/или 368 IgG1 или IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой Y407V или Y407T и необязательно Y349C, T366S и/или L368A; и где третья полипептидная цепь дополнительно содержит вторую Fc-область, связанную с CH1, при этом вторая Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где вторая Fc-область содержит аминокислотную(-ые) замену(-ы) в положениях, соответствующих положениям 366 и необязательно 354 IgG1 или IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой T366W или T366Y и необязательно S354C.
[0163] В некоторых вариантах осуществления вторая полипептидная цепь дополнительно содержит первую Fc-область, связанную с CH1, при этом первая Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где первая Fc-область содержит аминокислотную замену в положении, соответствующем положению 366 IgG1 или IgG4 человека в соответствии с EU-индексом, где аминокислотная замена представляет собой T366W; и где третья полипептидная цепь дополнительно содержит вторую Fc-область, связанную с CH1, при этом вторая Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где вторая Fc-область содержит аминокислотную(-ые) замену(-ы) в положениях, соответствующих положениям 366, 368 и/или 407 IgG1 или IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой T366S, L368A и/или Y407V.
[0164] В некоторых вариантах осуществления вторая полипептидная цепь дополнительно содержит первую Fc-область, связанную с CH1, при этом первая Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где первая Fc-область содержит аминокислотную(-ые) замену(-ы) в положениях, соответствующих положениям 366, 368 и/или 407 IgG1 или IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой T366S, L368A и/или Y407V; и где третья полипептидная цепь дополнительно содержит вторую Fc-область, связанную с CH1, при этом вторая Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где вторая Fc-область содержит аминокислотную замену в положении, соответствующем положению 366 IgG1 или IgG4 человека в соответствии с EU-индексом, где аминокислотная замена представляет собой T366W.
[0165] В некоторых вариантах осуществления вторая полипептидная цепь дополнительно содержит первую Fc-область, связанную с CH1, при этом первая Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где первая Fc-область содержит аминокислотные замены в положениях, соответствующих положениям 354 и 366 IgG1 или IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой S354C и T366W; и где третья полипептидная цепь дополнительно содержит вторую Fc-область, связанную с CH1, при этом вторая Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где вторая Fc-область содержит аминокислотные замены в положениях, соответствующих положениям 349, 366, 368 и 407 IgG1 или IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой Y349C, T366S, L368A и Y407V. В некоторых вариантах осуществления вторая полипептидная цепь дополнительно содержит первую Fc-область, связанную с CH1, при этом первая Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где первая Fc-область содержит аминокислотные замены в положениях, соответствующих положениям 349, 366, 368 и 407 IgG1 или IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой Y349C, T366S, L368A и Y407V; и где третья полипептидная цепь дополнительно содержит вторую Fc-область, связанную с CH1, при этом вторая Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где вторая Fc-область содержит аминокислотные замены в положениях, соответствующих положениям 354 и 366 IgG1 или IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой S354C и T366W. В некоторых вариантах осуществления первый и/или второй Fc-области представляют собой Fc-области IgG1 человека. В некоторых вариантах осуществления первый и/или второй Fc-области представляют собой Fc-области IgG4 человека.
[0166] В некоторых вариантах осуществления вторая полипептидная цепь дополнительно содержит первую Fc-область, связанную с CH1, где первая Fc-область представляет собой Fc-область IgG4 человека, содержащую шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где первая Fc-область содержит аминокислотные замены в положениях, соответствующих положениям 228, 354, 366 и 409 IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой S228P, S354C, T366W и R409K; и где третья полипептидная цепь дополнительно содержит вторую Fc-область, связанную с CH1, где вторая Fc-область представляет собой Fc-область IgG4 человека, содержащую шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где вторая Fc-область содержит аминокислотные замены в положениях, соответствующих положениям 228, 349, 366, 368, 407 и 409 IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой S228P, Y349C, T366S, L368A, Y407V и R409K. В некоторых вариантах осуществления вторая полипептидная цепь дополнительно содержит первую Fc-область, связанную с CH1, где первая Fc-область представляет собой Fc-область IgG4 человека, содержащую шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где первая Fc-область содержит аминокислотные замены в положениях, соответствующих положениям 228, 349, 366, 368, 407 и 409 IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой S228P, Y349C, T366S, L368A, Y407V и R409K; и где третья полипептидная цепь дополнительно содержит вторую Fc-область, связанную с CH1, где вторая Fc-область представляет собой Fc-область IgG4 человека, содержащую шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где вторая Fc-область содержит аминокислотные замены в положениях, соответствующих положениям 228, 354, 366 и 409 IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой S228P, S354C, T366W и R409K.
[0167] В некоторых вариантах осуществления вторая полипептидная цепь дополнительно содержит первую Fc-область, связанную с CH1, где первая Fc-область представляет собой Fc-область IgG4 человека, содержащую шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где первая Fc-область содержит аминокислотные замены в положениях, соответствующих положениям 234, 235, 354 и 366 IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой F234A, L235A, S354C и T366W; и где третья полипептидная цепь дополнительно содержит вторую Fc-область, связанную с CH1, где вторая Fc-область представляет собой Fc-область IgG4 человека, содержащую шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где вторая Fc-область содержит аминокислотные замены в положениях, соответствующих положениям 234, 235, 349, 366, 368 и 407 IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой F234A, L235A, Y349C, T366S, L368A и Y407V. В некоторых вариантах осуществления вторая полипептидная цепь дополнительно содержит первую Fc-область, связанную с CH1, где первая Fc-область представляет собой Fc-область IgG4 человека, содержащую шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где первая Fc-область содержит аминокислотные замены в положениях, соответствующих положениям 234, 235, 349, 366, 368 и 407 IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой F234A, L235A, Y349C, T366S, L368A и Y407V; и где третья полипептидная цепь дополнительно содержит вторую Fc-область, связанную с CH1, где вторая Fc-область представляет собой Fc-область IgG4 человека, содержащую шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где вторая Fc-область содержит аминокислотные замены в положениях, соответствующих положениям 234, 235, 354 и 366 IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой F234A, L235A, S354C и T366W.
[0168] В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит одну или несколько мутаций для снижения эффекторной функции, например, антителозависимого клеточного фагоцитоза, опосредованного Fc-рецепторами (ADCP), комплементзависимой цитотоксичности (CDC) и/или антителозависимой клеточной цитотоксичности (ADCC). В некоторых вариантах осуществления вторая полипептидная цепь дополнительно содержит первую Fc-область, связанную с CH1, при этом первая Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина; где третья полипептидная цепь дополнительно содержит вторую Fc-область, связанную с CH1, при этом вторая Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина; где первая и вторая Fc-области представляют собой Fc-области IgG1 человека; и где каждая из первой и второй Fc-областей содержит аминокислотные замены в положениях, соответствующих положениям 234 и 235 IgG1 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой L234A и L235A. В некоторых вариантах осуществления Fc-области второй и третьей полипептидных цепей представляют собой Fc-области IgG1 человека, и при этом каждая из Fc-областей содержит аминокислотные замены в положениях, соответствующих положениям 234 и 235 IgG1 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой L234A и L235A. В некоторых вариантах осуществления вторая полипептидная цепь дополнительно содержит первую Fc-область, связанную с CH1, при этом первая Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина; где третья полипептидная цепь дополнительно содержит вторую Fc-область, связанную с CH1, при этом вторая Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина; где первая и вторая Fc-области представляют собой Fc-области IgG1 человека; и где каждая из первой и второй Fc-областей содержит аминокислотные замены в положениях, соответствующих положениям 234, 235 и 329 IgG1 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой L234A, L235A и P329A. В некоторых вариантах осуществления Fc-области второй и третьей полипептидных цепей представляют собой Fc-области IgG1 человека, и где каждая из Fc-областей содержит аминокислотные замены в положениях, соответствующих положениям 234, 235 и 329 IgG1 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой L234A, L235A и P329A. В некоторых вариантах осуществления Fc-области второй и третьей полипептидных цепей представляют собой Fc-области IgG4 человека, и каждая из Fc-областей содержит аминокислотные замены в положениях, соответствующих положениям 234 и 235 IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой F234A и L235A. В некоторых вариантах осуществления связывающий белок содержит вторую полипептидную цепь, дополнительно содержащую первую Fc-область, связанную с CH1, при этом первая Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, и при этом третья полипептидная цепь дополнительно содержит вторую Fc-область, связанную с CH1, при этом вторая Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина; и где каждая из первой и второй Fc-областей содержит аминокислотные замены в положениях, соответствующих положениям 234 и 235 IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой F234A и L235A.
[0169] В некоторых вариантах осуществления вторая полипептидная цепь дополнительно содержит первую Fc-область, связанную с CH1, где первая Fc-область представляет собой Fc-область IgG4 человека, содержащую шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где первая Fc-область содержит аминокислотные замены в положениях, соответствующих положениям 228, 234, 235, 354, 366 и 409 IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой S228P, F234A, L235A, S354C, T366W и R409K; и где третья полипептидная цепь дополнительно содержит вторую Fc-область, связанную с CH1, где вторая Fc-область представляет собой Fc-область IgG4 человека, содержащую шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где вторая Fc-область содержит аминокислотные замены в положениях, соответствующих положениям 228, 234, 235, 349, 366, 368, 407 и 409 IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой S228P, F234A, L235A, Y349C, T366S, L368A, Y407V и R409K. В некоторых вариантах осуществления вторая полипептидная цепь дополнительно содержит первую Fc-область, связанную с CH1, где первая Fc-область представляет собой Fc-область IgG4 человека, содержащую шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где первая Fc-область содержит аминокислотные замены в положениях, соответствующих положениям 228, 234, 235, 349, 366, 368, 407 и 409 IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой S228P, F234A, L235A, Y349C, T366S, L368A, Y407V и R409K; и где третья полипептидная цепь дополнительно содержит вторую Fc-область, связанную с CH1, где вторая Fc-область представляет собой Fc-область IgG4 человека, содержащую шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, где вторая Fc-область содержит аминокислотные замены в положениях, соответствующих положениям 228, 234, 235, 354, 366 и 409 IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой S228P, F234A, L235A, S354C, T366W и R409K.
[0170] В некоторых вариантах осуществления Fc-область представляет собой Fc-область IgG4 человека, содержащую одну или несколько мутаций, которые ослабляют или устраняют связывание FcγI и/или FcγII. В некоторых вариантах осуществления Fc-область представляет собой Fc-область IgG4 человека, содержащую одну или несколько мутаций, которые ослабляют или устраняют связывание FcγI и/или FcγII, но не влияют на связывание FcRn. В некоторых вариантах осуществления Fc-область представляет собой Fc-область IgG4 человека, содержащую аминокислотные замены в положениях, соответствующих положениям 228 и/или 409 IgG4 человека в соответствии с EU-индексом. В некоторых вариантах осуществления аминокислотные замены представляют собой S228P и/или R409K. В некоторых вариантах осуществления Fc-область представляет собой Fc-область IgG4 человека, содержащую аминокислотные замены в положениях, соответствующих положениям 234 и/или 235 IgG4 человека в соответствии с EU-индексом. В некоторых вариантах осуществления аминокислотные замены представляют собой F234A и/или L235A. В некоторых вариантах осуществления Fc-область представляет собой Fc-область IgG4 человека, содержащую аминокислотные замены в положениях, соответствующих положениям 228, 234, 235 и/или 409 IgG4 человека в соответствии с EU-индексом. В некоторых вариантах осуществления аминокислотные замены представляют собой S228P, F234A, L235A и/или R409K. В некоторых вариантах осуществления Fc-область представляет собой Fc-область IgG4 человека, содержащую аминокислотные замены в положениях, соответствующих положениям 233-236 IgG4 человека в соответствии с EU-индексом. В некоторых вариантах осуществления аминокислотные замены представляют собой E233P, F234V, L235A, и делецию в положении 236. В некоторых вариантах осуществления Fc-область представляет собой Fc-область IgG4 человека, содержащую аминокислотные мутации в положениях, соответствующих положениям 228, 233-236 и/или 409 IgG4 человека в соответствии с EU-индексом. В некоторых вариантах осуществления аминокислотные мутации представляют собой S228P; E233P, F234V, L235A, и делецию в положении 236; и/или R409K.
[0171] В некоторых вариантах осуществления Fc-область содержит одну или несколько мутаций, которые уменьшают или устраняют связывание Fc-рецептора и/или эффекторную функцию Fc-области (например, антителозависимый клеточный фагоцитоз, опосредованный Fc-рецепторами (ADCP), комплементзависимую цитотоксичность (CDC) и/или антителозависимую клеточную цитотоксичность (ADCC)).
[0172] В некоторых вариантах осуществления Fc-область представляет собой Fc-область IgG1 человека, содержащую одну или несколько аминокислотных замен в положениях, соответствующих положениям 234, 235 и/или 329 IgG1 человека в соответствии с EU-индексом. В некоторых вариантах осуществления аминокислотные замены представляют собой L234A, L235A и/или P329A. В некоторых вариантах осуществления Fc-область представляет собой Fc-область IgG1 человека, содержащую аминокислотные замены в положениях, соответствующих положениям 298, 299 и/или 300 IgG1 человека в соответствии с EU-индексом. В некоторых вариантах осуществления аминокислотные замены представляют собой S298N, T299A и/или Y300S.
[0173] В некоторых вариантах осуществления связывающий белок согласно настоящему изобретению содержит одну или несколько мутаций для улучшения стабильности, например, шарнирной области и/или поверхности контакта димера IgG4 (см., например, Spiess, C. et al. (2013) J. Biol. Chem. 288:26583-26593). В некоторых вариантах осуществления мутация предусматривает замены в положениях, соответствующих положениям 228 и 409 IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой S228P и R409K. В некоторых вариантах осуществления связывающий белок содержит вторую полипептидную цепь, дополнительно содержащую первую Fc-область, связанную с CH1, при этом первая Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина, и при этом третья полипептидная цепь дополнительно содержит вторую Fc-область, связанную с CH1, при этом вторая Fc-область содержит шарнирную область иммуноглобулина и константные домены CH2 и CH3 тяжелой цепи иммуноглобулина; где первая и вторая Fc-области представляют собой Fc-области IgG4 человека; и где каждая из первой и второй Fc-областей содержит аминокислотные замены в положениях, соответствующих положениям 228 и 409 IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой S228P и R409K. В некоторых вариантах осуществления связывающий белок по настоящему изобретению содержит мутации по типу выступа и впадины и одну или несколько мутаций для улучшения стабильности. В некоторых вариантах осуществления первый и/или второй Fc-области представляют собой Fc-области IgG4 человека.
[0174] В некоторых вариантах осуществления Fc-область представляет собой Fc-область IgG1 человека, содержащую одну или несколько аминокислотных замен в положениях, соответствующих положениям 234, 235 и/или 329 IgG1 человека в соответствии с EU-индексом. В некоторых вариантах осуществления аминокислотные замены представляют собой L234A, L235A и/или P329A. В некоторых вариантах осуществления Fc-область представляет собой Fc-область IgG1 человека, содержащую аминокислотные замены в положениях, соответствующих положениям 298, 299 и/или 300 IgG1 человека в соответствии с EU-индексом. В некоторых вариантах осуществления аминокислотные замены представляют собой S298N, T299A и/или Y300S.
Нуклеиновые кислоты
[0175] Другие аспекты настоящего изобретения относятся к выделенным молекулам нуклеиновой кислоты, содержащим нуклеотидную последовательность, кодирующую любой из связывающих белков, описанных в данном документе. Иллюстративные и неограничивающие последовательности нуклеиновых кислот представлены в таблице 5.
[0176] Другие аспекты настоящего изобретения связаны с наборами полинуклеотидов, например, которые кодируют один или несколько полипептидов связывающего белка, описанного в данном документе. В некоторых вариантах осуществления набор полинуклеотидов по настоящему изобретению содержит один, два, три или четыре полинуклеотида из набора полинуклеотидов, который содержит: (a) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:177, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:178, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:179, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:180; (b) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:181, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:182, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:183, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:184; (c) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:185, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:186, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:187, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:188; (d) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:189, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:190, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:191, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:192; (e) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:193, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:194, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:195, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:196; (f) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:197, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:198, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:199, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:200; (g) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:201, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:202, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:203, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:204; (h) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:205, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:206, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:207, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:208; (i) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:209, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:210, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:211, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:212; (j) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:213, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:214, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:215, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:216; (k) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:217, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:218, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:219, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:220; (l) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:221, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:222, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:223, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:224; (m) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:225, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:226, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:227, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:228; (n) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:229, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:230, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:231, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:232; (o) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:233, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:234, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:235, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:236; (p) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:237, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:238, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:239, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:240; (q) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:241, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:242, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:243, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:244; (r) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:245, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:246, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:247, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:248; (s) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:249, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:250, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:251, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:252; (t) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:253, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:254, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:255, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:256; (u) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:257, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:258, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:259, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:260; (v) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:261, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:262, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:263, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:264; (w) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:265, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:266, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:267, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:268; (x) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:269, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:270, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:271, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:272; (y) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:273, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:274, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:275, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:276; (z) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:277, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:278, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:279, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:280; (aa) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:281, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:282, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:283, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:284; (bb) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:285, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:286, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:287, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:288; или (cc) первый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:289, второй полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:290, третий полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:291, и четвертый полинуклеотид, содержащий полинуклеотидную последовательность под SEQ ID NO:292.
[0177] Другие аспекты настоящего изобретения относятся к векторной системе, содержащей один или несколько векторов, кодирующих первую, вторую, третью и четвертую полипептидные цепи любого из связывающих белков, описанных в данном документе. В некоторых вариантах осуществления векторная система содержит первый вектор, кодирующий первую полипептидную цепь связывающего белка, второй вектор, кодирующий вторую полипептидную цепь связывающего белка, третий вектор, кодирующий третью полипептидную цепь связывающего белка, и четвертый вектор, кодирующий четвертую полипептидную цепь связывающего белка, например, которые показаны в полинуклеотидах таблицы 5. В некоторых вариантах осуществления векторная система содержит первый вектор, кодирующий первую и вторую полипептидные цепи связывающего белка, и второй вектор, кодирующий третью и четвертую полипептидные цепи связывающего белка. В некоторых вариантах осуществления векторная система содержит первый вектор, кодирующий первую и третью полипептидные цепи связывающего белка, и второй вектор, кодирующий вторую и четвертую полипептидные цепи связывающего белка. В некоторых вариантах осуществления векторная система содержит первый вектор, кодирующий первую и четвертую полипептидные цепи связывающего белка, и второй вектор, кодирующий вторую и третью полипептидные цепи связывающего белка. В некоторых вариантах осуществления векторная система содержит первый вектор, кодирующий первую, вторую, третью и четвертую полипептидные цепи связывающего белка. Один или несколько векторов векторной системы могут представлять собой любые из векторов, описанных в данном документе. В некоторых вариантах осуществления один или несколько векторов представляют собой векторы экспрессии. В некоторых вариантах осуществления первый, второй, третий и четвертый полинуклеотиды присутствуют в одном или нескольких векторах экспрессии, например, одном, двух, трех или четырех векторах экспрессии.
[0178] Стандартные технологии рекомбинантной ДНК применяют для конструирования полинуклеотидов, которые кодируют полипептиды, образующие связывающие белки, встраивания этих полинуклеотидов в рекомбинантные векторы экспрессии и введения таких векторов в клетки-хозяева. См., например, Sambrook et al., 2001, Molecular Cloning: A Laboratory Manual (Cold Spring Harbor Laboratory Press, 3rd ed.). Ферментативные реакции и методики очистки можно проводить в соответствии со спецификациями производителей, которые обычно выполняют в данной области техники или как описано в данном документе. Если не предусмотрены конкретные определения, то терминология, используемая в контексте аналитической химии, синтетической органической химии и медицинской и фармацевтической химии, а также лабораторные процедуры и их методики, описанные в данном документе, являются общеизвестными и широко используемыми в данной области техники. Аналогично традиционные методики можно использовать для вариантов химического синтеза, вариантов химического анализа, фармацевтического получения, составления, доставки и лечения пациентов.
[0179] В некоторых вариантах осуществления выделенная нуклеиновая кислота функционально связана с гетерологичным промотором для управления транскрипцией последовательности нуклеиновой кислоты, кодирующей связывающий белок. Промотор может относиться к контролирующим последовательностям нуклеиновой кислоты, которые управляют транскрипцией нуклеиновой кислоты. Первая последовательность нуклеиновой кислоты функционально связана со второй последовательностью нуклеиновой кислоты, где первая последовательность нуклеиновой кислоты находится в функциональной связи со второй последовательностью нуклеиновой кислоты. Например, промотор функционально связан с последовательностью, кодирующей связывающий белок, если промотор влияет на транскрипцию или экспрессию кодирующей последовательности. Примеры промоторов могут включать без ограничения промоторы, полученные из геномов вирусов (таких как вирус полиомы, вирус оспы кур, аденовирус (такой как аденовирус 2), вирус папилломы крупного рогатого скота, вирус саркомы птиц, цитомегаловирус, ретровирус, вирус гепатита B, вирус обезьян 40 (SV40) и т. п.), гетерологичные промоторы эукариот (такие как промотор гена актина, промотор гена иммуноглобулина, промоторы генов белков теплового шока и т. п.), CAG-промотор (Niwa et al., Gene 108(2):193-9, 1991), промотор гена фосфоглицераткиназы (PGK), индуцируемый тетрациклином промотор (Masui et al., Nucleic Acids Res. 33:e43, 2005), lac-систему, trp-систему, tac-систему, trc-систему, основные операторные и промоторные области лямбда-фага, промотор гена 3-фосфоглицераткиназы, промоторы гена кислой фосфатазы дрожжей и промотор гена альфа-фактора спаривания дрожжей. Полинуклеотиды, кодирующие по белки согласно настоящему изобретению, могут находиться под контролем конститутивного промотора, индуцируемого промотора или любого другого подходящего промотора, описанного в данном документе, или другого подходящего промотора, который легко распознает специалист в данной области техники.
[0180] В некоторых вариантах осуществления выделенную нуклеиновую кислоту встраивают в вектор. В некоторых вариантах осуществления вектор представляет собой вектор экспрессии. Векторы экспрессии могут содержать одну или несколько регуляторных последовательностей, функционально связанных с полинуклеотидом, подлежащим экспрессии. Термин "регуляторная последовательность" включает промоторы, энхансеры и другие элементы, контролирующие экспрессию (например, сигналы полиаденилирования). Примеры подходящих энхансеров могут включать без ограничения энхансерные последовательности из генов млекопитающих (таких как гены глобина, эластазы, альбумина, α-фетопротеина, инсулина и т. п.) и энхансерные последовательности из вируса эукариотических клеток (такие как энхансер SV40 на участке позднего начала репликации (100-270 п. о.), ранний промотор/энхансер цитомегаловируса, энхансер полиомы на участке позднего начала репликации, энхансеры аденовирусов и т. п.). Примеры подходящих векторов могут включать, например, плазмиды, космиды, эписомы, транспозоны и вирусные векторы (например, векторы на основе аденовируса, вируса осповакцины, вируса Синдбис, вируса кори, вируса герпеса, лентивируса, ретровируса, аденоассоциированного вируса и т. д.). Векторы экспрессии можно применять для трансфекции клеток-хозяев, таких как, например, клетки бактерий, клетки дрожжей, клетки насекомых и клетки млекопитающих. Биологически функциональные векторы на основе ДНК вируса и плазмидной ДНК, способные экспрессироваться и реплицироваться в хозяине, известны в данной области техники и могут применяться для трансфекции любой клетки, представляющей интерес.
Клетки-хозяева
[0181] Другие аспекты настоящего изобретения связаны с клеткой-хозяином (например, выделенной клеткой-хозяином), содержащей один или несколько выделенных полинуклеотидов, векторов и/или векторных систем, описанных в данном документе. В некоторых вариантах осуществления выделенную клетку-хозяина по настоящему изобретению культивируют in vitro. В некоторых вариантах осуществления клетка-хозяин представляет собой клетку бактерии (например, клетку E. coli). В некоторых вариантах осуществления клетка-хозяин представляет собой клетку дрожжей (например, клетку S. cerevisiae). В некоторых вариантах осуществления клетка-хозяин представляет собой клетку насекомого. Примеры клеток-хозяев насекомого могут включать, например, клетки Drosophila (например, клетки S2), клетки Trichoplusia ni (например, клетки High Five™) и клетки Spodoptera frugiperda (например, клетки Sf21 или Sf9). В некоторых вариантах осуществления клетка-хозяин представляет собой клетку млекопитающего. Примеры клеток-хозяев млекопитающего могут включать, например, клетки почки эмбриона человека (например, клетки 293 или клетки 293, субклонированные для роста в суспензионной культуре), клетки Expi293™, клетки CHO, клетки почки новорожденного хомяка (например, BHK, ATCC CCL 10), клетки Сертоли мыши (например, клетки TM4), клетки почки обезьяны (например, CV1 ATCC CCL 70), клетки почки африканской зеленой мартышки (например, VERO-76, ATCC CRL-1587), клетки карциномы шейки матки человека (например, HELA, ATCC CCL 2), клетки почки собаки (например, MDCK, ATCC CCL 34), клетки печени крысы линии Buffalo (например, BRL 3A, ATCC CRL 1442), клетки легкого человека (например, W138, ATCC CCL 75), клетки печени человека (например, Hep G2, HB 8065), клетки опухоли молочной железы мыши (например, MMT 060562, ATCC CCL51), клетки TRI, клетки MRC 5, клетки FS4, линию клеток гепатомы человека (например, Hep G2) и клетки миеломы (например, клетки NS0 и Sp2/0).
[0182] Другие аспекты настоящего изобретения связаны со способом получения любого из связывающих белков, описанных в данном документе. В некоторых вариантах осуществления способ предусматривает: a) культивирование клетки-хозяина (например, любой из клеток-хозяев, описанных в данном документе), содержащей выделенную нуклеиновую кислоту, вектор и/или векторную систему (например, любое из выделенных нуклеиновых кислот, векторов и/или векторных систем, описанных в данном документе), в условиях, при которых клетка-хозяин экспрессирует связывающий белок; и b) выделение связывающего белка из клетки-хозяина. Способы культивирования клеток-хозяев в условиях, обеспечивающих экспрессию белка, хорошо известны специалисту средней квалификации в данной области. Способы выделения белков из культивируемых клеток-хозяев хорошо известны специалисту средней квалификации в данной области, в том числе, например, с помощью аффинной хроматографии (например, двухстадийной аффинной хроматографии, включающей аффинную хроматографию с использованием белка A с последующей эксклюзионной хроматографией).
Фармацевтические композиции
[0183] Терапевтические или фармацевтические композиции, содержащие связывающие белки, находятся в пределах объема настоящего изобретения. Такие терапевтические или фармацевтические композиции могут содержать терапевтически эффективное количество связывающего белка или конъюгата связывающий белок-лекарственное средство в смеси с фармацевтически или физиологически приемлемым средством для составления, выбранным в соответствии со способом введения.
[0184] Приемлемые вещества для составления являются нетоксичными для реципиентов при используемых дозировках и концентрациях.
[0185] Фармацевтическая композиция может содержать вещества для составления, предназначенные для модификации, поддержания или сохранения, например, pH, осмолярности, вязкости, прозрачности, цвета, изотоничности, запаха, стерильности, стабильности, скорости растворения или высвобождения, всасывания или проникновения композиции. Подходящие вещества для составления включают без ограничения аминокислоты (такие как глицин, глутамин, аспарагин, аргинин или лизин), противомикробные средства, антиоксиданты (такие как аскорбиновая кислота, сульфит натрия или гидросульфит натрия), буферы (такие как борат, бикарбонат, Tris-HCl, цитраты, фосфаты или другие органические кислоты), объемообразующие средства (такие как маннит или глицин), хелатирующие средства (такие как этилендиаминтетрауксусная кислота (EDTA)), комплексообразующие средства (такие как кофеин, поливинилпирролидон, бета-циклодестрин или гидроксипропил-бета-циклодекстрин), наполнители, моносахариды, дисахариды и другие углеводы (такие как глюкоза, манноза или декстрины), белки (такие как сывороточный альбумин, желатин или иммуноглобулины), красители, ароматизаторы и разбавители, эмульгаторы, гидрофильные полимеры (такие как поливинилпирролидон), низкомолекулярные полипептиды, солеобразующие противоионы (такие как натрий), консерванты (такие как хлорид бензалкония, бензойная кислота, салициловая кислота, тимеросал, фенетиловый спирт, метилпарабен, пропилпарабен, хлоргексидин, сорбиновая кислота или пероксид водорода), растворители (такие как глицерин, пропиленгликоль или полиэтиленгликоль), сахароспирты (такие как маннит или сорбит), суспендирующие средства, поверхностно-активные вещества или смачивающие средства (такие как разновидности плюроника; PEG; сложные эфиры сорбитана; полисорбаты, такие как полисорбат 20 или полисорбат 80; тритон; трометамин; лецитин; холестерин или тилоксапoл), средства, повышающие стабильность (такие как сахароза и сорбит), средства, повышающие тоничность (такие как галогениды щелочных металлов, например, хлорид натрия или калия или маннит, сорбит), среды для доставки, разбавители, вспомогательные вещества и/или фармацевтические адъюванты (см., например, Remington's Pharmaceutical Sciences (18th Ed., A.R. Gennaro, ed., Mack Publishing Company 1990) и его последующие издания, которые включены в данный документ посредством ссылки для любой цели).
[0186] Оптимальную фармацевтическую композицию будет определять специалист в данной области техники в зависимости, например, от предполагаемого пути введения, формата доставки и требуемой дозы. На такие композиции могут оказывать влияние физическое состояние, стабильность, скорость высвобождения in vivo и скорость выведения in vivo связывающего белка.
[0187] Основная среда или носитель в фармацевтической композиции могут быть водными либо неводными по своей природе. Например, подходящей средой или носителем для инъекции может быть вода, физиологический солевой раствор или искусственная спинномозговая жидкость, возможно, с добавкой других веществ, общепринятых для композиций для парентерального введения. Нейтральный забуференный солевой раствор или солевой раствор, смешанный с сывороточным альбумином, представляют собой дополнительные иллюстративные среды. Другие иллюстративные фармацевтические композиции содержат буфер Tris со значением pH, составляющим приблизительно 7,0-8,5, или ацетатный буфер со значением pH, составляющим приблизительно 4,0-5,5, который может дополнительно включать сорбит или подходящий заменитель. В одном варианте осуществления настоящего изобретения композиции на основе связывающего белка могут быть получены для хранения в форме лиофилизированной массы или водного раствора путем смешивания выбранной композиции с требуемой степенью чистоты с необязательными средствами для составления. Кроме того, связывающий белок может быть составлен в форме лиофилизата с применением подходящих вспомогательных веществ, таких как сахароза.
[0188] Фармацевтические композиции согласно настоящему изобретению могут предназначаться для парентеральной или подкожной доставки. Альтернативно композиции могут предназначаться для ингаляции или для доставки через пищеварительный тракт, например, перорально. Получение таких фармацевтически приемлемых композиций находится в пределах компетенции специалиста в данной области техники.
[0189] Компоненты состава присутствуют в концентрациях, которые являются приемлемыми для места введения. Например, буферы используют для поддержания значения pH композиции на физиологическом уровне или при немного меньшем значении pH, обычно в диапазоне значений pH от приблизительно 5 до приблизительно 8.
[0190] Если предусмотрено парентеральное введение, то терапевтические композиции, предназначенные для применения, могут быть в форме апирогенного приемлемого для парентерального введения водного раствора, содержащего требуемый связывающий белок в фармацевтически приемлемой среде. Особенно подходящей средой для парентеральной инъекции является стерильная дистиллированная вода, с помощью которой связывающий белок составляют в виде стерильного изотонического раствора с подходящими консервантами. Еще один препарат может предусматривать состав на основе требуемой молекулы со средством, таким как инъецируемые микросферы, биоразлагаемые частицы, полимерные соединения (такие как полимолочная кислота или полигликолевая кислота), гранулы или липосомы, которое обеспечивает контролируемое или замедленное высвобождение продукта, который затем может быть доставлен посредством депо-инъекции. Можно также использовать гиалуроновую кислоту, и она может оказывать эффект обеспечения длительного пребывания в кровотоке. Другие подходящие средства для введения требуемой молекулы включают имплантируемые устройства для доставки лекарственных средств.
[0191] В одном варианте осуществления фармацевтическая композиция может быть составлена для ингаляции. Например, связывающий белок может быть составлен в виде сухого порошка для ингаляции. Растворы для ингаляций на основе связывающего белка можно также составлять с пропеллентом для аэрозольной доставки. В еще одном варианте осуществления растворы можно распылять.
[0192] Также предусматривается, что определенные составы можно вводить перорально. В одном варианте осуществления настоящего изобретения связывающие белки, которые вводят таким способом, можно составлять с такими носителями, которые обычно используют при составлении твердых лекарственных форм, таких как таблетки и капсулы, или без них. Например, капсула может быть предназначена для высвобождения активной части состава в таком месте пищеварительного тракта, где биодоступность повышается до максимума, а пресистемный распад сводится к минимуму. Можно включать дополнительные средства для облегчения всасывания связывающего белка. Также можно использовать разбавители, ароматизаторы, легкоплавкие воски, растительные масла, смазывающие вещества, суспендирующие средства, средства для улучшения распадаемости таблеток и связующие средства.
[0193] Другая фармацевтическая композиция может включать эффективное количество связывающих белков в смеси с нетоксичными вспомогательными веществами, которые являются подходящими для изготовления таблеток. Путем растворения таблеток в стерильной воде или другой подходящей среде можно получить растворы в форме со стандартной дозой. Подходящие вспомогательные вещества включают без ограничения инертные разбавители, такие как карбонат кальция, карбонат или бикарбонат натрия, лактоза или фосфат кальция; или связующие средства, такие как крахмал, желатин или аравийская камедь; или смазывающие вещества, такие как стеарат магния, стеариновая кислота или тальк.
[0194] Дополнительные фармацевтические композиции согласно настоящему изобретению будут очевидны специалистам в данной области техники, в том числе составы, включающие связывающие белки, в форме с замедленной или контролируемой доставкой. Методики составления ряда других средств с замедленной или контролируемой доставкой, таких как липосомные носители, биоразлагаемые микрочастицы или пористые гранулы и формы для депо-инъекций, также известны специалистам в данной области техники. Дополнительные примеры препаратов с замедленным высвобождением включают полупроницаемые полимерные матрицы в форме изделий определенной формы, например, пленок или микрокапсул. Матрицы с замедленным высвобождением могут включать сложные полиэфиры, гидрогели, полилактиды, сополимеры L-глутаминовой кислоты и гамма-этил-L-глутамата, поли(2-гидроксиэтилметакрилат), этиленвинилацетат или поли-D(-)-3-гидроксимасляную кислоту. Композиции с замедленным высвобождением также могут включать липосомы, которые можно получить любым из нескольких известных из уровня техники способов.
[0195] Фармацевтические композиции, подлежащие применению для введения in vivo, обычно должны быть стерильными. Этого можно достичь путем фильтрации через стерильные фильтрационные мембраны. Если композиция является лиофилизированной, то стерилизация с помощью этого способа может быть проведена либо до, либо после лиофилизации и восстановления. Композиция для парентерального введения может храниться в лиофилизированной форме или в форме раствора. Кроме того, композиции для парентерального введения, как правило, помещают в контейнер, имеющий стерильное входное отверстие, например, мешок с раствором для внутривенной инъекции или флакон с пробкой, которую можно проколоть гиподермической иглой для инъекций.
[0196] После того как фармацевтическая композиция составлена, ее можно хранить в стерильных флаконах в виде раствора, суспензии, геля, эмульсии, твердого вещества или в виде обезвоженного или лиофилизированного порошка. Такие составы можно хранить либо в готовой к применению форме, либо в форме (например, лиофилизированной), требующей восстановления перед введением.
[0197] Настоящее изобретение также охватывает наборы для получения единицы для однократного введения дозы. Каждый из наборов может содержать как первый контейнер с высушенным белком, так и второй контейнер с водным составом. В объем настоящего изобретения также включены наборы, содержащие одно- и многокамерные предварительно заполненные шприцы (например, шприцы с жидкостью и шприцы с лиофилизатом).
[0198] Эффективное количество фармацевтической композиции на основе связывающего белка, подлежащей терапевтическому применению, будет зависеть, например, от терапевтического случая и целей. Специалисту в данной области техники будет понятно, что подходящие уровни доз для лечения будут, таким образом, меняться отчасти в зависимости от доставляемой молекулы, показания, в соответствии с которым будут применять связывающий белок, пути введения и метрических характеристик (массы тела, поверхности тела или размера органа) и состояния (возраста и общего состояния здоровья) пациента. Соответственно врач может подобрать дозу и видоизменить путь введения для получения оптимального терапевтического эффекта.
[0199] Частота дозирования будет зависеть от фармакокинетических параметров связывающего белка в составе, подлежащем применению. Обычно врач будет вводить композицию до тех пор, пока доза не достигнет такого уровня, при котором достигается необходимый эффект. Следовательно, композицию можно вводить в виде однократной дозы, в виде двух или более доз (которые могут содержать одинаковое количество требуемой молекулы или могут не содержать его) в течение определенного периода времени или в виде непрерывной инфузии посредством имплантируемого устройства или катетера. Дополнительное уточнение подходящей дозировки выполняется стандартным способом специалистами средней квалификации в данной области и находится в диапазоне задач, которые они обычно выполняют. Подходящие дозировки можно определять с помощью соответствующих данных о дозозависимом ответе.
[0200] Путь введения фармацевтической композиции соответствует известным способам, например, перорально; посредством инъекции с помощью внутривенного, интраперитонеального, интрацеребрального (интрапаренхиматозного), интрацеребровентрикулярного, внутримышечного, внутриглазного, внутриартериального, интрапортального или внутриочагового путей; с помощью систем с замедленным высвобождением или с помощью имплантируемых устройств. При необходимости композиции можно вводить в виде болюсной инъекции или непрерывно путем инфузии или с помощью имплантируемого устройства.
[0201] Композицию также можно вводить местно посредством имплантации мембраны, губки или другого подходящего материала, в который необходимая молекула была поглощена или инкапсулирована. Если применяют имплантируемое устройство, то устройство можно имплантировать в любую подходящую ткань или орган, и доставка требуемой молекулы может осуществляться посредством диффузии, болюсного введения с регулируемым во времени высвобождением или непрерывного введения.
[0202] Фармацевтические композиции можно применять для предупреждения и/или лечения инфекции, вызванной HIV. Фармацевтические композиции можно применять в виде отдельного средства для терапии или в комбинации со стандартным средством для антиретровирусной терапии.
[0203] Настоящее изобретение также относится к набору, содержащему связывающий белок и другие реагенты, применимые для выявления уровней целевых антигенов в биологических образцах. Такие реагенты могут включать выявляемую метку, блокирующую сыворотку крови, образцы положительного и отрицательного контроля и реагенты для выявления. В некоторых вариантах осуществления набор содержит композицию, содержащую любой связывающий белок, полинуклеотид, вектор, векторную систему и/или клетку-хозяина, описанные в данном документе. В некоторых вариантах осуществления набор содержит контейнер и этикетку или листовку-вкладыш на контейнере или вместе с ним. Подходящие контейнеры включают, например, бутылки, флаконы, шприцы, мешки с раствором для в/в инъекции и т. д. Контейнеры могут быть изготовлены из ряда материалов, таких как стекло или пластик. Контейнер содержит композицию, которая сама по себе или в комбинации с другой композицией является эффективной для лечения, предупреждения и/или диагностирования состояния (например, инфекции, вызванной HIV), и он может иметь стерильное входное отверстие (например, контейнер может представлять собой пакет с раствором для внутривенной инъекции или флакон с пробкой, которую можно проколоть иглой для подкожных инъекций). В некоторых вариантах осуществления на этикетке или листовке-вкладыше указывается, что композиция применяется для предупреждения, диагностирования и/или лечения предпочтительного состояния. Альтернативно или дополнительно изделие или набор может дополнительно содержать второй (или третий) контейнер, содержащий фармацевтически приемлемый буфер, такой как бактериостатическая вода для инъекций (BWFI), фосфатно-буферный раствор солевой раствор Рингера и раствор декстрозы. Он может дополнительно включать другие вещества, необходимые с коммерческой точки зрения и с точки зрения потребителя, в том числе другие буферы, разбавители, наполнители, иглы и шприцы.
Способы и варианты применения связывающих белков
[0204] Определенные аспекты настоящего изобретения связаны со способами предупреждения инфекции, вызванной HIV, у пациента, лечения инфекции, вызванной HIV, у пациента, предупреждения СПИД у пациента и лечения СПИД у пациента с использованием любого из связывающих белков или фармацевтических композиций, раскрытых в данном документе. Любое из связывающих белков или фармацевтических композиций, раскрытых в данном документе, может найти применение в способе по настоящему изобретению, например, в способах предупреждения инфекции, вызванной HIV, у пациента, лечения инфекции, вызванной HIV, у пациента, предупреждения СПИД у пациента и лечения СПИД у пациента.
[0205] На ФИГ. 1 представлен иллюстративный и неограничивающий формат для триспецифического связывающего белка, который можно использовать в способах и вариантах применения, описанных в данном документе. Как показано на ФИГ. 2, предусмотренный механизм, с помощью которого связывающий белок, показанный на ФИГ. 1, может привести к устранению клеток резервуара HIV у пациента, включает: (1) активацию инфицированных в латентной форме CD4+ Т-клеток посредством плечей к CD28 и к CD3 триспецифического связывающего белка; (2) рекрутинг CD8+ T-клеток к активированным, инфицированным в латентной форме CD4+ T-клеткам посредством плечей к Env и к CD3; (3) активацию задействованных CD8+ Т-клеток посредством плечей к CD28 и к CD3; и (4) уничтожение инфицированных в латентной форме CD4+ T-клеток посредством перфорин-гранзимного механизма. Преимущественно, считается, что этот механизм активирует и впоследствии уничтожает клетки резервуара HIV-1, что обеспечивает новую стратегию для осуществления атаки на резервуар HIV-1 у пациента.
[0206] В некоторых вариантах осуществления способы по настоящему изобретению предусматривают введение пациенту терапевтически эффективного количества по меньшей мере одного из связывающих белков или фармацевтических композиций, описанных в данном документе.
[0207] В некоторых вариантах осуществления по меньшей мере один связывающий белок вводят в комбинации со средством для антиретровирусной терапии (например, средством для терапии против HIV). В некоторых вариантах осуществления по меньшей мере один связывающий белок вводят перед средством для антиретровирусной терапии. В некоторых вариантах осуществления по меньшей мере один связывающий белок вводят совместно со средством для антиретровирусной терапии. В некоторых вариантах осуществления по меньшей мере один связывающий белок вводят после средства для антиретровирусной терапии. В некоторых вариантах осуществления по меньшей мере один связывающий белок вводят совместно с любым стандартным средством для антиретровирусной терапии, известным из уровня техники.
[0208] В некоторых вариантах осуществления введение по меньшей мере одного связывающего белка или фармацевтической композиции приводит в результате к устранению у пациента одной или нескольких клеток, инфицированных HIV в латентной и/или хронической форме. В некоторых вариантах осуществления введение по меньшей мере одного связывающего белка приводит к нейтрализации одного или нескольких вирионов HIV и приводит в результате к устранению у пациента одной или нескольких клеток, инфицированных HIV в латентной и/или хронической форме. В некоторых вариантах осуществления пациентом является человек.
Таблица 4. Полипептидные последовательности триспецифического связывающего белка
VRC07_523/CD28sup x CD3mid IgG1 LALA/P329A
VRC07_523/CD28sup x CD3mid IgG1 NNAS
VRC07_523/CD28sup x CD3mid IgG4 FALA/409K
VRC07_523/CD28sup x CD3mid_QQ IgG4 FALA/409K
VRC07_523/CD28sup x линкер CD3mid_QQ IgG4 FALA/409K_DKTHT
VRC07_523/CD28sup x линкер CD3mid_QQ IgG1_NNAS/409K_DKTHT
VRC07_523_FR3-03/CD28sup x линкер CD3mid_ENLQ IgG4 FALA/409K_DKTHT
VRC07_523_FR3-03/CD28sup x линкер CD3mid_ENLF IgG4 FALA/409K_DKTHT
VRC07_523_FR3-03/CD28sup x линкер CD3mid_ENLQ IgG1_NNAS_DKTHT
VRC07_523_FR3-03/CD28sup x линкер CD3mid_ENLF IgG1_NNAS_DKTHT
N6/CD28sup x CD3mid IgG4
N6/CD28sup x CD3mid IgG4
N6/CD28sup x CD3mid_QQ IgG4 FALA/409K
N6/CD28sup x линкер CD3mid_QQ IgG4 FALA/409K_DKTHT
N6/CD28sup x линкер CD3mid IgG4 FALA/409K_DKTHT
N6/CD28sup x линкер CD3mid_QQ IgG1_NNAS_DKTHT
N6/CD28sup x линкер CD3mid_DNAQ IgG4 FALA/409K_DKTHT
N6/CD28sup x линкер CD3mid_ENLQ IgG4 FALA/409K_DKTHT
N6/CD28sup x линкер CD3mid_ENLR IgG4 FALA/409K_DKTHT
N6/CD28sup x линкер CD3mid_ENLF IgG4 FALA/409K_DKTHT
N6_rw52/CD28sup x линкер CD3mid_ENLQ IgG4 FALA/409K_DKTHT
N6_rw52/CD28sup x линкер CD3mid_ENLF IgG4 FALA/409K_DKTHT
N6_rw52/CD28sup x линкер CD3mid_ENLF IgG1_NNAS_DKTHT
N6_FR3-03/CD28sup x линкер CD3mid_ENLQ IgG4 FALA/409K_DKTHT
N6_FR3-03/CD28sup x линкер CD3mid_ENLF IgG4 FALA/409K_DKTHT
N6_FR3-03/CD28sup x линкер CD3mid_ENLQIgG1_NNAS_DKTHT
N6_FR3-03/CD28sup x линкер CD3mid_ENLF IgG1_NNAS_DKTHT
VRC01.23/CD28sup x линкер CD3mid_ENLQ IgG4 FALA/409K_DKTHT
VRC01.23/CD28sup x линкер CD3mid_ENLF IgG4 FALA/409K_DKTHT
Таблица 5. Полинуклеотидные последовательности триспецифического связывающего белка
VRC07_523/CD28sup x CD3mid IgG1 LALA/P329A
VRC07_523/CD28sup x CD3mid IgG1 NNAS
VRC07_523/CD28sup x CD3mid IgG4 FALA/409K
VRC07_523/CD28sup x CD3mid_QQ IgG4 FALA/409K
VRC07_523/CD28sup x линкер CD3mid_QQ IgG4 FALA/409K_DKTHT
VRC07_523/CD28sup x линкер CD3mid_QQ IgG1_NNAS/409K_DKTHT
VRC07_523_FR3-03/CD28sup x линкер CD3mid_ENLQ IgG4 FALA/409K_DKTHT
VRC07_523_FR3-03/CD28sup x линкер CD3mid_ENLF IgG4 FALA/409K_DKTHT
VRC07_523_FR3-03/CD28sup x линкер CD3mid_ENLQ IgG1_NNAS_DKTHT
VRC07_523_FR3-03/CD28sup x линкер CD3mid_ENLF IgG1_NNAS_DKTHT
N6/CD28sup x CD3mid IgG4
N6/CD28sup x CD3mid IgG4
N6/CD28sup x CD3mid_QQ IgG4 FALA/409K
N6/CD28sup x линкер CD3mid_QQ IgG4 FALA/409K_DKTHT
N6/CD28sup x линкер CD3mid IgG4 FALA/409K_DKTHT
N6/CD28sup x линкер CD3mid_QQ IgG1_NNAS_DKTHT
N6/CD28sup x линкер CD3mid_DNAQ IgG4 FALA/409K_DKTHT
N6/CD28sup x линкер CD3mid_ENLQ IgG4 FALA/409K_DKTHT
N6/CD28sup x линкер CD3mid_ENLR IgG4 FALA/409K_DKTHT
N6/CD28sup x линкер CD3mid_ENLF IgG4 FALA/409K_DKTHT
N6_rw52/CD28sup x линкер CD3mid_ENLQ IgG4 FALA/409K_DKTHT
N6_rw52/CD28sup x линкер CD3mid_ENLF IgG4 FALA/409K_DKTHT
N6_rw52/CD28sup x линкер CD3mid_ENLF IgG1_NNAS_DKTHT
N6_FR3-03/CD28sup x линкер CD3mid_ENLQ IgG4 FALA/409K_DKTHT
N6_FR3-03/CD28sup x линкер CD3mid_ENLF IgG4 FALA/409K_DKTHT
N6_FR3-03/CD28sup x линкер CD3mid_EN LQIgG1_NNAS_DKTHT
N6_FR3-03/CD28sup x линкер CD3mid_ENLF IgG1_NNAS_DKTHT
VRC01.23/CD28sup x линкер CD3mid_ENLQ IgG4 FALA/409K_DKTHT
VRC01.23/CD28sup x линкер CD3mid_ENLF IgG4 FALA/409K_DKTHT
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Sanofi
Министерство здравоохранения и социального обеспечения Соединенных
Штатов Америки в лице министра
<120> ТРИСПЕЦИФИЧЕСКИЕ И/ИЛИ ТРИВАЛЕНТНЫЕ СВЯЗЫВАЮЩИЕ БЕЛКИ ДЛЯ ЛЕЧЕНИЯ
ИНФЕКЦИИ HIV
<130> 18395-20319.40
<140> Пока еще не назначен
<141> Одновременно с этим
<150> EP 19306312.0
<151> 2019-10-08
<150> US 62/831,415
<151> 2019-04-09
<160> 293
<170> FastSEQ для Windows версии 4.0
<210> 1
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 1
Asn Cys Pro Ile Asn
1 5
<210> 2
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 2
Trp Met Lys Pro Arg His Gly Ala Val Ser Tyr Ala Arg Gln Leu Gln
1 5 10 15
Gly
<210> 3
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 3
Gly Lys Tyr Cys Thr Ala Arg Asp Tyr Tyr Asn Trp Asp Phe Glu His
1 5 10 15
<210> 4
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 4
Arg Thr Ser Gln Tyr Gly Ser Leu Ala
1 5
<210> 5
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 5
Ser Gly Ser Thr Arg Ala Ala
1 5
<210> 6
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 6
Gln Gln Tyr Glu Phe
1 5
<210> 7
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 7
Gly Tyr Thr Phe Thr Ala His Ile
1 5
<210> 8
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 8
Ile Lys Pro Gln Tyr Gly Ala Val
1 5
<210> 9
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 9
Ile Lys Pro Gln Tyr Gly Ala Thr
1 5
<210> 10
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 10
Asp Arg Ser Tyr Gly Asp Ser Ser Trp Ala Leu Asp Ala
1 5 10
<210> 11
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 11
Gln Gly Val Gly Ser Asp
1 5
<210> 12
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 12
His Thr Ser
1
<210> 13
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 13
Cys Gln Val Leu Gln Phe
1 5
<210> 14
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 14
Asp Cys Thr Leu Asn
1 5
<210> 15
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 15
Trp Leu Lys Pro Arg Trp Gly Ala Val Asn Tyr Ala Arg Pro Leu Gln
1 5 10 15
Gly
<210> 16
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 16
Gly Lys Asn Cys Asp Tyr Asn Trp Asp Phe Glu His
1 5 10
<210> 17
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 17
Arg Thr Ser Gln Tyr Gly Ser Leu Ala
1 5
<210> 18
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 18
Ser Gly Ser Thr Arg Ala Ala
1 5
<210> 19
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 19
Gln Gln Tyr Glu Phe
1 5
<210> 20
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 20
Gly Phe Thr Phe Thr Lys Ala Trp
1 5
<210> 21
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 21
Ile Lys Asp Lys Ser Asn Ser Tyr Ala Thr
1 5 10
<210> 22
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 22
Arg Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr
1 5 10
<210> 23
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 23
Gln Ser Leu Val His Asn Asn Ala Asn Thr Tyr
1 5 10
<210> 24
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 24
Gln Ser Leu Val His Gln Asn Ala Gln Thr Tyr
1 5 10
<210> 25
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 25
Gln Ser Leu Val His Glu Asn Leu Gln Thr Tyr
1 5 10
<210> 26
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 26
Gln Ser Leu Val His Glu Asn Leu Phe Thr Tyr
1 5 10
<210> 27
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 27
Gln Ser Leu Val His Glu Asn Leu Arg Thr Tyr
1 5 10
<210> 28
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 28
Gln Ser Leu Val His Asp Asn Ala Gln Thr Tyr
1 5 10
<210> 29
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 29
Lys Val Ser
1
<210> 30
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 30
Gly Gln Gly Thr Gln Tyr Pro Phe Thr
1 5
<210> 31
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 31
Gly Tyr Thr Phe Thr Ser Tyr Tyr
1 5
<210> 32
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 32
Ile Tyr Pro Gly Asn Val Asn Thr
1 5
<210> 33
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 33
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val
1 5 10
<210> 34
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 34
Gln Asn Ile Tyr Val Trp
1 5
<210> 35
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 35
Lys Ala Ser
1
<210> 36
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 36
Gln Gln Gly Gln Thr Tyr Pro Tyr
1 5
<210> 37
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 37
Asp Lys Thr His Thr
1 5
<210> 38
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 38
Gly Gln Pro Lys Ala Ala Pro
1 5
<210> 39
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 39
Thr Lys Gly Pro Ser
1 5
<210> 40
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 40
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10
<210> 41
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 41
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 42
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 42
Gly Gly Ser Gly Ser Ser Gly Ser Gly Gly
1 5 10
<210> 43
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 43
Gln Val Arg Leu Ser Gln Ser Gly Gly Gln Met Lys Lys Pro Gly Asp
1 5 10 15
Ser Met Arg Ile Ser Cys Arg Ala Ser Gly Tyr Glu Phe Ile Asn Cys
20 25 30
Pro Ile Asn Trp Ile Arg Leu Ala Pro Gly Lys Arg Pro Glu Trp Met
35 40 45
Gly Trp Met Lys Pro Arg His Gly Ala Val Ser Tyr Ala Arg Gln Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Met Tyr Ser Glu Thr Ala Phe
65 70 75 80
Leu Glu Leu Arg Ser Leu Thr Ser Asp Asp Thr Ala Val Tyr Phe Cys
85 90 95
Thr Arg Gly Lys Tyr Cys Thr Ala Arg Asp Tyr Tyr Asn Trp Asp Phe
100 105 110
Glu His Trp Gly Gln Gly Thr Pro Val Thr Val Ser Ser
115 120 125
<210> 44
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 44
Gln Val Arg Leu Ser Gln Ser Gly Gly Gln Met Lys Lys Pro Gly Asp
1 5 10 15
Ser Met Arg Ile Ser Cys Arg Ala Ser Gly Tyr Glu Phe Ile Asn Cys
20 25 30
Pro Ile Asn Trp Ile Arg Leu Ala Pro Gly Lys Arg Pro Glu Trp Met
35 40 45
Gly Trp Met Lys Pro Arg His Gly Ala Val Ser Tyr Ala Arg Gln Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Gln Leu Ser Gln Asp Pro Asp Asp
65 70 75 80
Pro Asp Trp Gly Thr Ala Phe Leu Glu Leu Arg Ser Leu Thr Ser Asp
85 90 95
Asp Thr Ala Val Tyr Phe Cys Thr Arg Gly Lys Tyr Cys Thr Ala Arg
100 105 110
Asp Tyr Tyr Asn Trp Asp Phe Glu His Trp Gly Gln Gly Thr Pro Val
115 120 125
Thr Val Ser Ser
130
<210> 45
<211> 101
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 45
Ser Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Thr
1 5 10 15
Ala Ile Ile Ser Cys Arg Thr Ser Gln Tyr Gly Ser Leu Ala Trp Tyr
20 25 30
Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Val Ile Tyr Ser Gly Ser
35 40 45
Thr Arg Ala Ala Gly Ile Pro Asp Arg Phe Ser Gly Ser Arg Trp Gly
50 55 60
Pro Asp Tyr Asn Leu Thr Ile Ser Asn Leu Glu Ser Gly Asp Phe Gly
65 70 75 80
Val Tyr Tyr Cys Gln Gln Tyr Glu Phe Phe Gly Gln Gly Thr Lys Val
85 90 95
Gln Val Asp Ile Lys
100
<210> 46
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 46
Arg Ala His Leu Val Gln Ser Gly Thr Ala Met Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Val Ser Cys Gln Thr Ser Gly Tyr Thr Phe Thr Ala His
20 25 30
Ile Leu Phe Trp Phe Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Lys Pro Gln Tyr Gly Ala Val Asn Phe Gly Gly Gly Phe
50 55 60
Arg Asp Arg Val Thr Leu Thr Arg Asp Val Tyr Arg Glu Ile Ala Tyr
65 70 75 80
Met Asp Ile Arg Gly Leu Lys Pro Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Ser Tyr Gly Asp Ser Ser Trp Ala Leu Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Val Val Ser Ala
115 120
<210> 47
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 47
Arg Ala His Leu Val Gln Ser Gly Thr Ala Met Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Val Ser Cys Gln Thr Ser Gly Tyr Thr Phe Thr Ala His
20 25 30
Ile Leu Phe Trp Phe Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Lys Pro Gln Tyr Gly Ala Thr Asn Phe Gly Gly Gly Phe
50 55 60
Arg Asp Arg Val Thr Leu Thr Arg Asp Val Tyr Arg Glu Ile Ala Tyr
65 70 75 80
Met Asp Ile Arg Gly Leu Lys Pro Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Ser Tyr Gly Asp Ser Ser Trp Ala Leu Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Val Val Ser Ala
115 120
<210> 48
<211> 129
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 48
Arg Ala His Leu Val Gln Ser Gly Thr Ala Met Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Val Ser Cys Gln Thr Ser Gly Tyr Thr Phe Thr Ala His
20 25 30
Ile Leu Phe Trp Phe Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Lys Pro Gln Tyr Gly Ala Val Asn Phe Gly Gly Gly Phe
50 55 60
Arg Asp Arg Val Thr Leu Thr Arg Gln Leu Ser Gln Asp Pro Asp Asp
65 70 75 80
Pro Asp Trp Gly Ile Ala Tyr Met Asp Ile Arg Gly Leu Lys Pro Asp
85 90 95
Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Arg Ser Tyr Gly Asp Ser
100 105 110
Ser Trp Ala Leu Asp Ala Trp Gly Gln Gly Thr Thr Val Val Val Ser
115 120 125
Ala
<210> 49
<211> 103
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 49
Tyr Ile His Val Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Ile Gly
1 5 10 15
Asp Arg Val Thr Ile Asn Cys Gln Thr Ser Gln Gly Val Gly Ser Asp
20 25 30
Leu His Trp Tyr Gln His Lys Pro Gly Arg Ala Pro Lys Leu Leu Ile
35 40 45
His His Thr Ser Ser Val Glu Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Phe His Thr Ser Phe Asn Leu Thr Ile Ser Asp Leu Gln Ala
65 70 75 80
Asp Asp Ile Ala Thr Tyr Tyr Cys Gln Val Leu Gln Phe Phe Gly Arg
85 90 95
Gly Ser Arg Leu His Ile Lys
100
<210> 50
<211> 128
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 50
Gln Val Gln Leu Val Gln Ser Gly Gly Gln Met Lys Lys Pro Gly Glu
1 5 10 15
Ser Met Arg Ile Ser Cys Arg Ala Ser Gly Tyr Glu Phe Ile Asp Cys
20 25 30
Thr Leu Asn Trp Ile Arg Leu Ala Pro Gly Lys Arg Pro Glu Trp Met
35 40 45
Gly Trp Leu Lys Pro Arg Trp Gly Ala Val Asn Tyr Ala Arg Pro Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Gln Leu Ser Gln Asp Pro Asp Asp
65 70 75 80
Pro Asp Trp Gly Thr Ala Phe Leu Glu Leu Arg Ser Leu Thr Val Asp
85 90 95
Asp Thr Ala Val Tyr Phe Cys Thr Arg Gly Lys Asn Cys Asp Tyr Asn
100 105 110
Trp Asp Phe Glu His Trp Gly Arg Gly Thr Pro Val Ile Val Ser Ser
115 120 125
<210> 51
<211> 100
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 51
Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Thr Ala
1 5 10 15
Ile Ile Ser Cys Arg Thr Ser Gln Tyr Gly Ser Leu Ala Trp Tyr Gln
20 25 30
Gln Arg Pro Gly Gln Ala Pro Arg Leu Val Ile Tyr Ser Gly Ser Thr
35 40 45
Arg Ala Ala Gly Ile Pro Asp Arg Phe Ser Gly Ser Arg Trp Gly Pro
50 55 60
Asp Tyr Asn Leu Thr Ile Ser Asn Leu Glu Ser Gly Asp Phe Gly Val
65 70 75 80
Tyr Tyr Cys Gln Gln Tyr Glu Phe Phe Gly Gln Gly Thr Lys Val Gln
85 90 95
Val Asp Ile Lys
100
<210> 52
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 52
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 53
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 53
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Asn
20 25 30
Asn Ala Asn Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 54
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 54
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Gln
20 25 30
Asn Ala Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 55
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 55
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 56
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 56
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Phe Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 57
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 57
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Arg Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 58
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 58
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Asp
20 25 30
Asn Ala Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 59
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 59
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 60
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 60
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Asn Ile Tyr Val Trp
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly Gln Thr Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 61
<211> 338
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 61
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Asn
20 25 30
Asn Ala Asn Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Gly Gln Pro Lys Ala Ala Pro Asp Ile Gln Met Thr Gln Ser Pro Ser
115 120 125
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala
130 135 140
Ser Gln Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly
145 150 155 160
Lys Ala Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly
165 170 175
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
180 185 190
Thr Ile Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln
195 200 205
Gln Gly Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu
210 215 220
Ile Lys Thr Lys Gly Pro Ser Arg Thr Val Ala Ala Pro Ser Val Phe
225 230 235 240
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
245 250 255
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
260 265 270
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
275 280 285
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
290 295 300
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
305 310 315 320
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
325 330 335
Glu Cys
<210> 62
<211> 573
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 62
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ser Gln Val Gln Leu Val Glu Ser
115 120 125
Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala
130 135 140
Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His Trp Val Arg Gln
145 150 155 160
Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile Lys Asp Lys Ser
165 170 175
Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr
180 185 190
Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser
195 200 205
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg Gly Val Tyr Tyr
210 215 220
Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
225 230 235 240
Ser Ser Arg Thr Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
245 250 255
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
260 265 270
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
275 280 285
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
290 295 300
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
305 310 315 320
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
325 330 335
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
340 345 350
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
355 360 365
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
370 375 380
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
385 390 395 400
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
405 410 415
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
420 425 430
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
435 440 445
Lys Val Ser Asn Lys Ala Leu Ala Ala Pro Ile Glu Lys Thr Ile Ser
450 455 460
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro
465 470 475 480
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val
485 490 495
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
500 505 510
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
515 520 525
Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
530 535 540
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
545 550 555 560
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
565 570
<210> 63
<211> 454
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 63
Gln Val Arg Leu Ser Gln Ser Gly Gly Gln Met Lys Lys Pro Gly Asp
1 5 10 15
Ser Met Arg Ile Ser Cys Arg Ala Ser Gly Tyr Glu Phe Ile Asn Cys
20 25 30
Pro Ile Asn Trp Ile Arg Leu Ala Pro Gly Lys Arg Pro Glu Trp Met
35 40 45
Gly Trp Met Lys Pro Arg His Gly Ala Val Ser Tyr Ala Arg Gln Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Met Tyr Ser Glu Thr Ala Phe
65 70 75 80
Leu Glu Leu Arg Ser Leu Thr Ser Asp Asp Thr Ala Val Tyr Phe Cys
85 90 95
Thr Arg Gly Lys Tyr Cys Thr Ala Arg Asp Tyr Tyr Asn Trp Asp Phe
100 105 110
Glu His Trp Gly Gln Gly Thr Pro Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu
210 215 220
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
225 230 235 240
Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
275 280 285
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
290 295 300
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
305 310 315 320
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
325 330 335
Ala Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
340 345 350
Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys
355 360 365
Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
370 375 380
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
385 390 395 400
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
405 410 415
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
420 425 430
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
435 440 445
Leu Ser Leu Ser Pro Gly
450
<210> 64
<211> 208
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 64
Ser Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Thr
1 5 10 15
Ala Ile Ile Ser Cys Arg Thr Ser Gln Tyr Gly Ser Leu Ala Trp Tyr
20 25 30
Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Val Ile Tyr Ser Gly Ser
35 40 45
Thr Arg Ala Ala Gly Ile Pro Asp Arg Phe Ser Gly Ser Arg Trp Gly
50 55 60
Pro Asp Tyr Asn Leu Thr Ile Ser Asn Leu Glu Ser Gly Asp Phe Gly
65 70 75 80
Val Tyr Tyr Cys Gln Gln Tyr Glu Phe Phe Gly Gln Gly Thr Lys Val
85 90 95
Gln Val Asp Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
100 105 110
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
115 120 125
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
130 135 140
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
145 150 155 160
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
165 170 175
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
180 185 190
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
195 200 205
<210> 65
<211> 338
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 65
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Asn
20 25 30
Asn Ala Asn Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Gly Gln Pro Lys Ala Ala Pro Asp Ile Gln Met Thr Gln Ser Pro Ser
115 120 125
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala
130 135 140
Ser Gln Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly
145 150 155 160
Lys Ala Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly
165 170 175
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
180 185 190
Thr Ile Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln
195 200 205
Gln Gly Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu
210 215 220
Ile Lys Thr Lys Gly Pro Ser Arg Thr Val Ala Ala Pro Ser Val Phe
225 230 235 240
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
245 250 255
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
260 265 270
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
275 280 285
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
290 295 300
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
305 310 315 320
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
325 330 335
Glu Cys
<210> 66
<211> 573
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 66
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ser Gln Val Gln Leu Val Glu Ser
115 120 125
Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala
130 135 140
Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His Trp Val Arg Gln
145 150 155 160
Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile Lys Asp Lys Ser
165 170 175
Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr
180 185 190
Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser
195 200 205
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg Gly Val Tyr Tyr
210 215 220
Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
225 230 235 240
Ser Ser Arg Thr Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
245 250 255
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
260 265 270
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
275 280 285
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
290 295 300
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
305 310 315 320
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
325 330 335
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
340 345 350
Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe
355 360 365
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
370 375 380
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
385 390 395 400
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
405 410 415
Lys Pro Arg Glu Glu Gln Tyr Asn Asn Ala Ser Arg Val Val Ser Val
420 425 430
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
435 440 445
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
450 455 460
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro
465 470 475 480
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val
485 490 495
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
500 505 510
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
515 520 525
Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
530 535 540
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
545 550 555 560
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
565 570
<210> 67
<211> 454
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 67
Gln Val Arg Leu Ser Gln Ser Gly Gly Gln Met Lys Lys Pro Gly Asp
1 5 10 15
Ser Met Arg Ile Ser Cys Arg Ala Ser Gly Tyr Glu Phe Ile Asn Cys
20 25 30
Pro Ile Asn Trp Ile Arg Leu Ala Pro Gly Lys Arg Pro Glu Trp Met
35 40 45
Gly Trp Met Lys Pro Arg His Gly Ala Val Ser Tyr Ala Arg Gln Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Met Tyr Ser Glu Thr Ala Phe
65 70 75 80
Leu Glu Leu Arg Ser Leu Thr Ser Asp Asp Thr Ala Val Tyr Phe Cys
85 90 95
Thr Arg Gly Lys Tyr Cys Thr Ala Arg Asp Tyr Tyr Asn Trp Asp Phe
100 105 110
Glu His Trp Gly Gln Gly Thr Pro Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu
210 215 220
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
225 230 235 240
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
275 280 285
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
290 295 300
Asn Asn Ala Ser Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
305 310 315 320
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
325 330 335
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
340 345 350
Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys
355 360 365
Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
370 375 380
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
385 390 395 400
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
405 410 415
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
420 425 430
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
435 440 445
Leu Ser Leu Ser Pro Gly
450
<210> 68
<211> 208
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 68
Ser Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Thr
1 5 10 15
Ala Ile Ile Ser Cys Arg Thr Ser Gln Tyr Gly Ser Leu Ala Trp Tyr
20 25 30
Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Val Ile Tyr Ser Gly Ser
35 40 45
Thr Arg Ala Ala Gly Ile Pro Asp Arg Phe Ser Gly Ser Arg Trp Gly
50 55 60
Pro Asp Tyr Asn Leu Thr Ile Ser Asn Leu Glu Ser Gly Asp Phe Gly
65 70 75 80
Val Tyr Tyr Cys Gln Gln Tyr Glu Phe Phe Gly Gln Gly Thr Lys Val
85 90 95
Gln Val Asp Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
100 105 110
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
115 120 125
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
130 135 140
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
145 150 155 160
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
165 170 175
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
180 185 190
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
195 200 205
<210> 69
<211> 338
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 69
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Asn
20 25 30
Asn Ala Asn Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Gly Gln Pro Lys Ala Ala Pro Asp Ile Gln Met Thr Gln Ser Pro Ser
115 120 125
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala
130 135 140
Ser Gln Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly
145 150 155 160
Lys Ala Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly
165 170 175
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
180 185 190
Thr Ile Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln
195 200 205
Gln Gly Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu
210 215 220
Ile Lys Thr Lys Gly Pro Ser Arg Thr Val Ala Ala Pro Ser Val Phe
225 230 235 240
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
245 250 255
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
260 265 270
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
275 280 285
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
290 295 300
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
305 310 315 320
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
325 330 335
Glu Cys
<210> 70
<211> 570
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 70
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ser Gln Val Gln Leu Val Glu Ser
115 120 125
Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala
130 135 140
Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His Trp Val Arg Gln
145 150 155 160
Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile Lys Asp Lys Ser
165 170 175
Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr
180 185 190
Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser
195 200 205
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg Gly Val Tyr Tyr
210 215 220
Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
225 230 235 240
Ser Ser Arg Thr Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
245 250 255
Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu
260 265 270
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
275 280 285
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
290 295 300
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
305 310 315 320
Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr
325 330 335
Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro
340 345 350
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
355 360 365
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
370 375 380
Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn
385 390 395 400
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
405 410 415
Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
420 425 430
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
435 440 445
Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys
450 455 460
Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Gln Glu
465 470 475 480
Glu Met Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe
485 490 495
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
500 505 510
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
515 520 525
Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly
530 535 540
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
545 550 555 560
Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
565 570
<210> 71
<211> 451
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 71
Gln Val Arg Leu Ser Gln Ser Gly Gly Gln Met Lys Lys Pro Gly Asp
1 5 10 15
Ser Met Arg Ile Ser Cys Arg Ala Ser Gly Tyr Glu Phe Ile Asn Cys
20 25 30
Pro Ile Asn Trp Ile Arg Leu Ala Pro Gly Lys Arg Pro Glu Trp Met
35 40 45
Gly Trp Met Lys Pro Arg His Gly Ala Val Ser Tyr Ala Arg Gln Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Met Tyr Ser Glu Thr Ala Phe
65 70 75 80
Leu Glu Leu Arg Ser Leu Thr Ser Asp Asp Thr Ala Val Tyr Phe Cys
85 90 95
Thr Arg Gly Lys Tyr Cys Thr Ala Arg Asp Tyr Tyr Asn Trp Asp Phe
100 105 110
Glu His Trp Gly Gln Gly Thr Pro Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser
130 135 140
Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys
195 200 205
Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala
225 230 235 240
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
260 265 270
Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Cys Gln Glu Glu Met Thr Lys Asn Gln Val
355 360 365
Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Leu Gly
450
<210> 72
<211> 208
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 72
Ser Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Thr
1 5 10 15
Ala Ile Ile Ser Cys Arg Thr Ser Gln Tyr Gly Ser Leu Ala Trp Tyr
20 25 30
Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Val Ile Tyr Ser Gly Ser
35 40 45
Thr Arg Ala Ala Gly Ile Pro Asp Arg Phe Ser Gly Ser Arg Trp Gly
50 55 60
Pro Asp Tyr Asn Leu Thr Ile Ser Asn Leu Glu Ser Gly Asp Phe Gly
65 70 75 80
Val Tyr Tyr Cys Gln Gln Tyr Glu Phe Phe Gly Gln Gly Thr Lys Val
85 90 95
Gln Val Asp Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
100 105 110
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
115 120 125
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
130 135 140
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
145 150 155 160
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
165 170 175
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
180 185 190
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
195 200 205
<210> 73
<211> 338
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 73
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Gln
20 25 30
Asn Ala Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Gly Gln Pro Lys Ala Ala Pro Asp Ile Gln Met Thr Gln Ser Pro Ser
115 120 125
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala
130 135 140
Ser Gln Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly
145 150 155 160
Lys Ala Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly
165 170 175
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
180 185 190
Thr Ile Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln
195 200 205
Gln Gly Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu
210 215 220
Ile Lys Thr Lys Gly Pro Ser Arg Thr Val Ala Ala Pro Ser Val Phe
225 230 235 240
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
245 250 255
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
260 265 270
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
275 280 285
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
290 295 300
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
305 310 315 320
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
325 330 335
Glu Cys
<210> 74
<211> 570
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 74
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ser Gln Val Gln Leu Val Glu Ser
115 120 125
Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala
130 135 140
Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His Trp Val Arg Gln
145 150 155 160
Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile Lys Asp Lys Ser
165 170 175
Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr
180 185 190
Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser
195 200 205
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg Gly Val Tyr Tyr
210 215 220
Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
225 230 235 240
Ser Ser Arg Thr Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
245 250 255
Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu
260 265 270
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
275 280 285
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
290 295 300
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
305 310 315 320
Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr
325 330 335
Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro
340 345 350
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
355 360 365
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
370 375 380
Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn
385 390 395 400
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
405 410 415
Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
420 425 430
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
435 440 445
Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys
450 455 460
Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Gln Glu
465 470 475 480
Glu Met Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe
485 490 495
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
500 505 510
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
515 520 525
Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly
530 535 540
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
545 550 555 560
Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
565 570
<210> 75
<211> 451
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 75
Gln Val Arg Leu Ser Gln Ser Gly Gly Gln Met Lys Lys Pro Gly Asp
1 5 10 15
Ser Met Arg Ile Ser Cys Arg Ala Ser Gly Tyr Glu Phe Ile Asn Cys
20 25 30
Pro Ile Asn Trp Ile Arg Leu Ala Pro Gly Lys Arg Pro Glu Trp Met
35 40 45
Gly Trp Met Lys Pro Arg His Gly Ala Val Ser Tyr Ala Arg Gln Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Met Tyr Ser Glu Thr Ala Phe
65 70 75 80
Leu Glu Leu Arg Ser Leu Thr Ser Asp Asp Thr Ala Val Tyr Phe Cys
85 90 95
Thr Arg Gly Lys Tyr Cys Thr Ala Arg Asp Tyr Tyr Asn Trp Asp Phe
100 105 110
Glu His Trp Gly Gln Gly Thr Pro Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser
130 135 140
Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys
195 200 205
Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala
225 230 235 240
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
260 265 270
Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Cys Gln Glu Glu Met Thr Lys Asn Gln Val
355 360 365
Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Leu Gly
450
<210> 76
<211> 208
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 76
Ser Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Thr
1 5 10 15
Ala Ile Ile Ser Cys Arg Thr Ser Gln Tyr Gly Ser Leu Ala Trp Tyr
20 25 30
Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Val Ile Tyr Ser Gly Ser
35 40 45
Thr Arg Ala Ala Gly Ile Pro Asp Arg Phe Ser Gly Ser Arg Trp Gly
50 55 60
Pro Asp Tyr Asn Leu Thr Ile Ser Asn Leu Glu Ser Gly Asp Phe Gly
65 70 75 80
Val Tyr Tyr Cys Gln Gln Tyr Glu Phe Phe Gly Gln Gly Thr Lys Val
85 90 95
Gln Val Asp Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
100 105 110
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
115 120 125
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
130 135 140
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
145 150 155 160
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
165 170 175
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
180 185 190
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
195 200 205
<210> 77
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 77
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Gln
20 25 30
Asn Ala Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Asp Lys Thr His Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln
130 135 140
Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly
195 200 205
Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
210 215 220
Asp Lys Thr His Thr Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
225 230 235 240
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
245 250 255
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
260 265 270
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
275 280 285
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
290 295 300
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
305 310 315 320
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330 335
<210> 78
<211> 570
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 78
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ser Gln Val Gln Leu Val Glu Ser
115 120 125
Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala
130 135 140
Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His Trp Val Arg Gln
145 150 155 160
Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile Lys Asp Lys Ser
165 170 175
Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr
180 185 190
Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser
195 200 205
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg Gly Val Tyr Tyr
210 215 220
Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
225 230 235 240
Ser Ser Arg Thr Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
245 250 255
Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu
260 265 270
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
275 280 285
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
290 295 300
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
305 310 315 320
Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr
325 330 335
Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro
340 345 350
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
355 360 365
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
370 375 380
Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn
385 390 395 400
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
405 410 415
Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
420 425 430
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
435 440 445
Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys
450 455 460
Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Gln Glu
465 470 475 480
Glu Met Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe
485 490 495
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
500 505 510
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
515 520 525
Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly
530 535 540
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
545 550 555 560
Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
565 570
<210> 79
<211> 451
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 79
Gln Val Arg Leu Ser Gln Ser Gly Gly Gln Met Lys Lys Pro Gly Asp
1 5 10 15
Ser Met Arg Ile Ser Cys Arg Ala Ser Gly Tyr Glu Phe Ile Asn Cys
20 25 30
Pro Ile Asn Trp Ile Arg Leu Ala Pro Gly Lys Arg Pro Glu Trp Met
35 40 45
Gly Trp Met Lys Pro Arg His Gly Ala Val Ser Tyr Ala Arg Gln Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Met Tyr Ser Glu Thr Ala Phe
65 70 75 80
Leu Glu Leu Arg Ser Leu Thr Ser Asp Asp Thr Ala Val Tyr Phe Cys
85 90 95
Thr Arg Gly Lys Tyr Cys Thr Ala Arg Asp Tyr Tyr Asn Trp Asp Phe
100 105 110
Glu His Trp Gly Gln Gly Thr Pro Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser
130 135 140
Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys
195 200 205
Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
210 215 220
Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala
225 230 235 240
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
260 265 270
Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Cys Gln Glu Glu Met Thr Lys Asn Gln Val
355 360 365
Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Leu Gly
450
<210> 80
<211> 208
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 80
Ser Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Thr
1 5 10 15
Ala Ile Ile Ser Cys Arg Thr Ser Gln Tyr Gly Ser Leu Ala Trp Tyr
20 25 30
Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Val Ile Tyr Ser Gly Ser
35 40 45
Thr Arg Ala Ala Gly Ile Pro Asp Arg Phe Ser Gly Ser Arg Trp Gly
50 55 60
Pro Asp Tyr Asn Leu Thr Ile Ser Asn Leu Glu Ser Gly Asp Phe Gly
65 70 75 80
Val Tyr Tyr Cys Gln Gln Tyr Glu Phe Phe Gly Gln Gly Thr Lys Val
85 90 95
Gln Val Asp Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
100 105 110
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
115 120 125
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
130 135 140
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
145 150 155 160
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
165 170 175
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
180 185 190
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
195 200 205
<210> 81
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 81
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Gln
20 25 30
Asn Ala Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Asp Lys Thr His Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln
130 135 140
Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly
195 200 205
Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
210 215 220
Asp Lys Thr His Thr Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
225 230 235 240
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
245 250 255
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
260 265 270
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
275 280 285
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
290 295 300
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
305 310 315 320
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330 335
<210> 82
<211> 580
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 82
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Asp Lys Thr His Thr Gln Val Gln
115 120 125
Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg
130 135 140
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His
145 150 155 160
Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile
165 170 175
Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg
210 215 220
Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Ala Ser Thr Lys Gly
245 250 255
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
260 265 270
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
275 280 285
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
290 295 300
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
305 310 315 320
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
325 330 335
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
340 345 350
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
355 360 365
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
370 375 380
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
385 390 395 400
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
405 410 415
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Asn
420 425 430
Ala Ser Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
435 440 445
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
450 455 460
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
465 470 475 480
Gln Val Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
485 490 495
Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
500 505 510
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
515 520 525
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu
530 535 540
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
545 550 555 560
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
565 570 575
Leu Ser Pro Gly
580
<210> 83
<211> 454
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 83
Gln Val Arg Leu Ser Gln Ser Gly Gly Gln Met Lys Lys Pro Gly Asp
1 5 10 15
Ser Met Arg Ile Ser Cys Arg Ala Ser Gly Tyr Glu Phe Ile Asn Cys
20 25 30
Pro Ile Asn Trp Ile Arg Leu Ala Pro Gly Lys Arg Pro Glu Trp Met
35 40 45
Gly Trp Met Lys Pro Arg His Gly Ala Val Ser Tyr Ala Arg Gln Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Met Tyr Ser Glu Thr Ala Phe
65 70 75 80
Leu Glu Leu Arg Ser Leu Thr Ser Asp Asp Thr Ala Val Tyr Phe Cys
85 90 95
Thr Arg Gly Lys Tyr Cys Thr Ala Arg Asp Tyr Tyr Asn Trp Asp Phe
100 105 110
Glu His Trp Gly Gln Gly Thr Pro Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu
210 215 220
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
225 230 235 240
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
275 280 285
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
290 295 300
Asn Asn Ala Ser Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
305 310 315 320
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
325 330 335
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
340 345 350
Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys
355 360 365
Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
370 375 380
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
385 390 395 400
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
405 410 415
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
420 425 430
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
435 440 445
Leu Ser Leu Ser Pro Gly
450
<210> 84
<211> 208
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 84
Ser Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Thr
1 5 10 15
Ala Ile Ile Ser Cys Arg Thr Ser Gln Tyr Gly Ser Leu Ala Trp Tyr
20 25 30
Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Val Ile Tyr Ser Gly Ser
35 40 45
Thr Arg Ala Ala Gly Ile Pro Asp Arg Phe Ser Gly Ser Arg Trp Gly
50 55 60
Pro Asp Tyr Asn Leu Thr Ile Ser Asn Leu Glu Ser Gly Asp Phe Gly
65 70 75 80
Val Tyr Tyr Cys Gln Gln Tyr Glu Phe Phe Gly Gln Gly Thr Lys Val
85 90 95
Gln Val Asp Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
100 105 110
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
115 120 125
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
130 135 140
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
145 150 155 160
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
165 170 175
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
180 185 190
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
195 200 205
<210> 85
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 85
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Asp Lys Thr His Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln
130 135 140
Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly
195 200 205
Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
210 215 220
Asp Lys Thr His Thr Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
225 230 235 240
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
245 250 255
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
260 265 270
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
275 280 285
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
290 295 300
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
305 310 315 320
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330 335
<210> 86
<211> 570
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 86
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ser Gln Val Gln Leu Val Glu Ser
115 120 125
Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala
130 135 140
Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His Trp Val Arg Gln
145 150 155 160
Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile Lys Asp Lys Ser
165 170 175
Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr
180 185 190
Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser
195 200 205
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg Gly Val Tyr Tyr
210 215 220
Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
225 230 235 240
Ser Ser Arg Thr Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
245 250 255
Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu
260 265 270
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
275 280 285
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
290 295 300
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
305 310 315 320
Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr
325 330 335
Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro
340 345 350
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
355 360 365
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
370 375 380
Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn
385 390 395 400
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
405 410 415
Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
420 425 430
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
435 440 445
Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys
450 455 460
Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Gln Glu
465 470 475 480
Glu Met Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe
485 490 495
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
500 505 510
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
515 520 525
Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly
530 535 540
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
545 550 555 560
Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
565 570
<210> 87
<211> 458
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 87
Gln Val Arg Leu Ser Gln Ser Gly Gly Gln Met Lys Lys Pro Gly Asp
1 5 10 15
Ser Met Arg Ile Ser Cys Arg Ala Ser Gly Tyr Glu Phe Ile Asn Cys
20 25 30
Pro Ile Asn Trp Ile Arg Leu Ala Pro Gly Lys Arg Pro Glu Trp Met
35 40 45
Gly Trp Met Lys Pro Arg His Gly Ala Val Ser Tyr Ala Arg Gln Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Gln Leu Ser Gln Asp Pro Asp Asp
65 70 75 80
Pro Asp Trp Gly Thr Ala Phe Leu Glu Leu Arg Ser Leu Thr Ser Asp
85 90 95
Asp Thr Ala Val Tyr Phe Cys Thr Arg Gly Lys Tyr Cys Thr Ala Arg
100 105 110
Asp Tyr Tyr Asn Trp Asp Phe Glu His Trp Gly Gln Gly Thr Pro Val
115 120 125
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
130 135 140
Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu
145 150 155 160
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
165 170 175
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
180 185 190
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
195 200 205
Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr
210 215 220
Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro
225 230 235 240
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
245 250 255
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
260 265 270
Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn
275 280 285
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
290 295 300
Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
305 310 315 320
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
325 330 335
Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys
340 345 350
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Gln Glu
355 360 365
Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
370 375 380
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
385 390 395 400
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
405 410 415
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly
420 425 430
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
435 440 445
Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
450 455
<210> 88
<211> 208
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 88
Ser Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Thr
1 5 10 15
Ala Ile Ile Ser Cys Arg Thr Ser Gln Tyr Gly Ser Leu Ala Trp Tyr
20 25 30
Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Val Ile Tyr Ser Gly Ser
35 40 45
Thr Arg Ala Ala Gly Ile Pro Asp Arg Phe Ser Gly Ser Arg Trp Gly
50 55 60
Pro Asp Tyr Asn Leu Thr Ile Ser Asn Leu Glu Ser Gly Asp Phe Gly
65 70 75 80
Val Tyr Tyr Cys Gln Gln Tyr Glu Phe Phe Gly Gln Gly Thr Lys Val
85 90 95
Gln Val Asp Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
100 105 110
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
115 120 125
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
130 135 140
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
145 150 155 160
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
165 170 175
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
180 185 190
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
195 200 205
<210> 89
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 89
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Phe Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Asp Lys Thr His Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln
130 135 140
Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly
195 200 205
Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
210 215 220
Asp Lys Thr His Thr Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
225 230 235 240
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
245 250 255
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
260 265 270
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
275 280 285
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
290 295 300
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
305 310 315 320
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330 335
<210> 90
<211> 570
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 90
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ser Gln Val Gln Leu Val Glu Ser
115 120 125
Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala
130 135 140
Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His Trp Val Arg Gln
145 150 155 160
Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile Lys Asp Lys Ser
165 170 175
Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr
180 185 190
Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser
195 200 205
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg Gly Val Tyr Tyr
210 215 220
Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
225 230 235 240
Ser Ser Arg Thr Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
245 250 255
Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu
260 265 270
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
275 280 285
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
290 295 300
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
305 310 315 320
Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr
325 330 335
Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro
340 345 350
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
355 360 365
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
370 375 380
Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn
385 390 395 400
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
405 410 415
Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
420 425 430
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
435 440 445
Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys
450 455 460
Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Gln Glu
465 470 475 480
Glu Met Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe
485 490 495
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
500 505 510
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
515 520 525
Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly
530 535 540
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
545 550 555 560
Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
565 570
<210> 91
<211> 458
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 91
Gln Val Arg Leu Ser Gln Ser Gly Gly Gln Met Lys Lys Pro Gly Asp
1 5 10 15
Ser Met Arg Ile Ser Cys Arg Ala Ser Gly Tyr Glu Phe Ile Asn Cys
20 25 30
Pro Ile Asn Trp Ile Arg Leu Ala Pro Gly Lys Arg Pro Glu Trp Met
35 40 45
Gly Trp Met Lys Pro Arg His Gly Ala Val Ser Tyr Ala Arg Gln Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Gln Leu Ser Gln Asp Pro Asp Asp
65 70 75 80
Pro Asp Trp Gly Thr Ala Phe Leu Glu Leu Arg Ser Leu Thr Ser Asp
85 90 95
Asp Thr Ala Val Tyr Phe Cys Thr Arg Gly Lys Tyr Cys Thr Ala Arg
100 105 110
Asp Tyr Tyr Asn Trp Asp Phe Glu His Trp Gly Gln Gly Thr Pro Val
115 120 125
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
130 135 140
Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu
145 150 155 160
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
165 170 175
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
180 185 190
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
195 200 205
Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr
210 215 220
Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro
225 230 235 240
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
245 250 255
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
260 265 270
Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn
275 280 285
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
290 295 300
Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
305 310 315 320
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
325 330 335
Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys
340 345 350
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Gln Glu
355 360 365
Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
370 375 380
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
385 390 395 400
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
405 410 415
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly
420 425 430
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
435 440 445
Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
450 455
<210> 92
<211> 208
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 92
Ser Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Thr
1 5 10 15
Ala Ile Ile Ser Cys Arg Thr Ser Gln Tyr Gly Ser Leu Ala Trp Tyr
20 25 30
Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Val Ile Tyr Ser Gly Ser
35 40 45
Thr Arg Ala Ala Gly Ile Pro Asp Arg Phe Ser Gly Ser Arg Trp Gly
50 55 60
Pro Asp Tyr Asn Leu Thr Ile Ser Asn Leu Glu Ser Gly Asp Phe Gly
65 70 75 80
Val Tyr Tyr Cys Gln Gln Tyr Glu Phe Phe Gly Gln Gly Thr Lys Val
85 90 95
Gln Val Asp Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
100 105 110
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
115 120 125
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
130 135 140
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
145 150 155 160
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
165 170 175
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
180 185 190
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
195 200 205
<210> 93
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 93
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Asp Lys Thr His Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln
130 135 140
Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly
195 200 205
Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
210 215 220
Asp Lys Thr His Thr Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
225 230 235 240
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
245 250 255
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
260 265 270
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
275 280 285
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
290 295 300
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
305 310 315 320
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330 335
<210> 94
<211> 580
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 94
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Asp Lys Thr His Thr Gln Val Gln
115 120 125
Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg
130 135 140
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His
145 150 155 160
Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile
165 170 175
Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg
210 215 220
Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Ala Ser Thr Lys Gly
245 250 255
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
260 265 270
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
275 280 285
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
290 295 300
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
305 310 315 320
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
325 330 335
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
340 345 350
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
355 360 365
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
370 375 380
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
385 390 395 400
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
405 410 415
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Asn
420 425 430
Ala Ser Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
435 440 445
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
450 455 460
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
465 470 475 480
Gln Val Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
485 490 495
Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
500 505 510
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
515 520 525
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu
530 535 540
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
545 550 555 560
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
565 570 575
Leu Ser Pro Gly
580
<210> 95
<211> 461
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 95
Gln Val Arg Leu Ser Gln Ser Gly Gly Gln Met Lys Lys Pro Gly Asp
1 5 10 15
Ser Met Arg Ile Ser Cys Arg Ala Ser Gly Tyr Glu Phe Ile Asn Cys
20 25 30
Pro Ile Asn Trp Ile Arg Leu Ala Pro Gly Lys Arg Pro Glu Trp Met
35 40 45
Gly Trp Met Lys Pro Arg His Gly Ala Val Ser Tyr Ala Arg Gln Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Gln Leu Ser Gln Asp Pro Asp Asp
65 70 75 80
Pro Asp Trp Gly Thr Ala Phe Leu Glu Leu Arg Ser Leu Thr Ser Asp
85 90 95
Asp Thr Ala Val Tyr Phe Cys Thr Arg Gly Lys Tyr Cys Thr Ala Arg
100 105 110
Asp Tyr Tyr Asn Trp Asp Phe Glu His Trp Gly Gln Gly Thr Pro Val
115 120 125
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
130 135 140
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
145 150 155 160
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
165 170 175
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
180 185 190
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
195 200 205
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
210 215 220
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
225 230 235 240
Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe
245 250 255
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
260 265 270
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
275 280 285
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
290 295 300
Lys Pro Arg Glu Glu Gln Tyr Asn Asn Ala Ser Arg Val Val Ser Val
305 310 315 320
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
325 330 335
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
340 345 350
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
355 360 365
Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val
370 375 380
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
385 390 395 400
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
405 410 415
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
420 425 430
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
435 440 445
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
450 455 460
<210> 96
<211> 208
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 96
Ser Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Thr
1 5 10 15
Ala Ile Ile Ser Cys Arg Thr Ser Gln Tyr Gly Ser Leu Ala Trp Tyr
20 25 30
Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Val Ile Tyr Ser Gly Ser
35 40 45
Thr Arg Ala Ala Gly Ile Pro Asp Arg Phe Ser Gly Ser Arg Trp Gly
50 55 60
Pro Asp Tyr Asn Leu Thr Ile Ser Asn Leu Glu Ser Gly Asp Phe Gly
65 70 75 80
Val Tyr Tyr Cys Gln Gln Tyr Glu Phe Phe Gly Gln Gly Thr Lys Val
85 90 95
Gln Val Asp Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
100 105 110
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
115 120 125
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
130 135 140
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
145 150 155 160
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
165 170 175
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
180 185 190
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
195 200 205
<210> 97
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 97
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Phe Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Asp Lys Thr His Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln
130 135 140
Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly
195 200 205
Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
210 215 220
Asp Lys Thr His Thr Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
225 230 235 240
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
245 250 255
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
260 265 270
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
275 280 285
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
290 295 300
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
305 310 315 320
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330 335
<210> 98
<211> 580
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 98
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Asp Lys Thr His Thr Gln Val Gln
115 120 125
Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg
130 135 140
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His
145 150 155 160
Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile
165 170 175
Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg
210 215 220
Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Ala Ser Thr Lys Gly
245 250 255
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
260 265 270
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
275 280 285
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
290 295 300
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
305 310 315 320
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
325 330 335
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
340 345 350
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
355 360 365
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
370 375 380
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
385 390 395 400
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
405 410 415
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Asn
420 425 430
Ala Ser Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
435 440 445
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
450 455 460
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
465 470 475 480
Gln Val Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
485 490 495
Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
500 505 510
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
515 520 525
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu
530 535 540
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
545 550 555 560
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
565 570 575
Leu Ser Pro Gly
580
<210> 99
<211> 461
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 99
Gln Val Arg Leu Ser Gln Ser Gly Gly Gln Met Lys Lys Pro Gly Asp
1 5 10 15
Ser Met Arg Ile Ser Cys Arg Ala Ser Gly Tyr Glu Phe Ile Asn Cys
20 25 30
Pro Ile Asn Trp Ile Arg Leu Ala Pro Gly Lys Arg Pro Glu Trp Met
35 40 45
Gly Trp Met Lys Pro Arg His Gly Ala Val Ser Tyr Ala Arg Gln Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Gln Leu Ser Gln Asp Pro Asp Asp
65 70 75 80
Pro Asp Trp Gly Thr Ala Phe Leu Glu Leu Arg Ser Leu Thr Ser Asp
85 90 95
Asp Thr Ala Val Tyr Phe Cys Thr Arg Gly Lys Tyr Cys Thr Ala Arg
100 105 110
Asp Tyr Tyr Asn Trp Asp Phe Glu His Trp Gly Gln Gly Thr Pro Val
115 120 125
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
130 135 140
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
145 150 155 160
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
165 170 175
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
180 185 190
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
195 200 205
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
210 215 220
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
225 230 235 240
Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe
245 250 255
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
260 265 270
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
275 280 285
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
290 295 300
Lys Pro Arg Glu Glu Gln Tyr Asn Asn Ala Ser Arg Val Val Ser Val
305 310 315 320
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
325 330 335
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
340 345 350
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
355 360 365
Cys Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val
370 375 380
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
385 390 395 400
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
405 410 415
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
420 425 430
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
435 440 445
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
450 455 460
<210> 100
<211> 208
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 100
Ser Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Thr
1 5 10 15
Ala Ile Ile Ser Cys Arg Thr Ser Gln Tyr Gly Ser Leu Ala Trp Tyr
20 25 30
Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Val Ile Tyr Ser Gly Ser
35 40 45
Thr Arg Ala Ala Gly Ile Pro Asp Arg Phe Ser Gly Ser Arg Trp Gly
50 55 60
Pro Asp Tyr Asn Leu Thr Ile Ser Asn Leu Glu Ser Gly Asp Phe Gly
65 70 75 80
Val Tyr Tyr Cys Gln Gln Tyr Glu Phe Phe Gly Gln Gly Thr Lys Val
85 90 95
Gln Val Asp Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
100 105 110
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
115 120 125
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
130 135 140
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
145 150 155 160
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
165 170 175
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
180 185 190
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
195 200 205
<210> 101
<211> 338
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 101
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Asn
20 25 30
Asn Ala Asn Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Gly Gln Pro Lys Ala Ala Pro Asp Ile Gln Met Thr Gln Ser Pro Ser
115 120 125
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala
130 135 140
Ser Gln Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly
145 150 155 160
Lys Ala Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly
165 170 175
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
180 185 190
Thr Ile Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln
195 200 205
Gln Gly Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu
210 215 220
Ile Lys Thr Lys Gly Pro Ser Arg Thr Val Ala Ala Pro Ser Val Phe
225 230 235 240
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
245 250 255
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
260 265 270
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
275 280 285
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
290 295 300
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
305 310 315 320
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
325 330 335
Glu Cys
<210> 102
<211> 569
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 102
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ser Gln Val Gln Leu Val Glu Ser
115 120 125
Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala
130 135 140
Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His Trp Val Arg Gln
145 150 155 160
Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile Lys Asp Lys Ser
165 170 175
Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr
180 185 190
Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser
195 200 205
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg Gly Val Tyr Tyr
210 215 220
Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
225 230 235 240
Ser Ser Arg Thr Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
245 250 255
Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu
260 265 270
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
275 280 285
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
290 295 300
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
305 310 315 320
Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr
325 330 335
Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro
340 345 350
Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro
355 360 365
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
370 375 380
Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp
385 390 395 400
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
405 410 415
Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
420 425 430
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
435 440 445
Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
450 455 460
Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Gln Glu Glu
465 470 475 480
Met Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr
485 490 495
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
500 505 510
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
515 520 525
Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn
530 535 540
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
545 550 555 560
Gln Lys Ser Leu Ser Leu Ser Leu Gly
565
<210> 103
<211> 447
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 103
Arg Ala His Leu Val Gln Ser Gly Thr Ala Met Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Val Ser Cys Gln Thr Ser Gly Tyr Thr Phe Thr Ala His
20 25 30
Ile Leu Phe Trp Phe Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Lys Pro Gln Tyr Gly Ala Val Asn Phe Gly Gly Gly Phe
50 55 60
Arg Asp Arg Val Thr Leu Thr Arg Asp Val Tyr Arg Glu Ile Ala Tyr
65 70 75 80
Met Asp Ile Arg Gly Leu Lys Pro Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Ser Tyr Gly Asp Ser Ser Trp Ala Leu Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Val Val Ser Ala Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro
260 265 270
Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Cys Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
405 410 415
Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440 445
<210> 104
<211> 210
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 104
Tyr Ile His Val Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Ile Gly
1 5 10 15
Asp Arg Val Thr Ile Asn Cys Gln Thr Ser Gln Gly Val Gly Ser Asp
20 25 30
Leu His Trp Tyr Gln His Lys Pro Gly Arg Ala Pro Lys Leu Leu Ile
35 40 45
His His Thr Ser Ser Val Glu Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Phe His Thr Ser Phe Asn Leu Thr Ile Ser Asp Leu Gln Ala
65 70 75 80
Asp Asp Ile Ala Thr Tyr Tyr Cys Gln Val Leu Gln Phe Phe Gly Arg
85 90 95
Gly Ser Arg Leu His Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe
100 105 110
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
115 120 125
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
130 135 140
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
145 150 155 160
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
165 170 175
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
180 185 190
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
195 200 205
Glu Cys
210
<210> 105
<211> 338
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 105
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Asn
20 25 30
Asn Ala Asn Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Gly Gln Pro Lys Ala Ala Pro Asp Ile Gln Met Thr Gln Ser Pro Ser
115 120 125
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala
130 135 140
Ser Gln Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly
145 150 155 160
Lys Ala Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly
165 170 175
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
180 185 190
Thr Ile Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln
195 200 205
Gln Gly Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu
210 215 220
Ile Lys Thr Lys Gly Pro Ser Arg Thr Val Ala Ala Pro Ser Val Phe
225 230 235 240
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
245 250 255
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
260 265 270
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
275 280 285
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
290 295 300
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
305 310 315 320
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
325 330 335
Glu Cys
<210> 106
<211> 570
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 106
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ser Gln Val Gln Leu Val Glu Ser
115 120 125
Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala
130 135 140
Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His Trp Val Arg Gln
145 150 155 160
Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile Lys Asp Lys Ser
165 170 175
Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr
180 185 190
Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser
195 200 205
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg Gly Val Tyr Tyr
210 215 220
Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
225 230 235 240
Ser Ser Arg Thr Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
245 250 255
Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu
260 265 270
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
275 280 285
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
290 295 300
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
305 310 315 320
Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr
325 330 335
Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro
340 345 350
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
355 360 365
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
370 375 380
Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn
385 390 395 400
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
405 410 415
Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
420 425 430
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
435 440 445
Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys
450 455 460
Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Gln Glu
465 470 475 480
Glu Met Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe
485 490 495
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
500 505 510
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
515 520 525
Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly
530 535 540
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
545 550 555 560
Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
565 570
<210> 107
<211> 448
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 107
Arg Ala His Leu Val Gln Ser Gly Thr Ala Met Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Val Ser Cys Gln Thr Ser Gly Tyr Thr Phe Thr Ala His
20 25 30
Ile Leu Phe Trp Phe Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Lys Pro Gln Tyr Gly Ala Val Asn Phe Gly Gly Gly Phe
50 55 60
Arg Asp Arg Val Thr Leu Thr Arg Asp Val Tyr Arg Glu Ile Ala Tyr
65 70 75 80
Met Asp Ile Arg Gly Leu Lys Pro Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Ser Tyr Gly Asp Ser Ser Trp Ala Leu Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Val Val Ser Ala Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
260 265 270
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Cys Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440 445
<210> 108
<211> 210
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 108
Tyr Ile His Val Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Ile Gly
1 5 10 15
Asp Arg Val Thr Ile Asn Cys Gln Thr Ser Gln Gly Val Gly Ser Asp
20 25 30
Leu His Trp Tyr Gln His Lys Pro Gly Arg Ala Pro Lys Leu Leu Ile
35 40 45
His His Thr Ser Ser Val Glu Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Phe His Thr Ser Phe Asn Leu Thr Ile Ser Asp Leu Gln Ala
65 70 75 80
Asp Asp Ile Ala Thr Tyr Tyr Cys Gln Val Leu Gln Phe Phe Gly Arg
85 90 95
Gly Ser Arg Leu His Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe
100 105 110
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
115 120 125
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
130 135 140
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
145 150 155 160
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
165 170 175
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
180 185 190
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
195 200 205
Glu Cys
210
<210> 109
<211> 338
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 109
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Gln
20 25 30
Asn Ala Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Gly Gln Pro Lys Ala Ala Pro Asp Ile Gln Met Thr Gln Ser Pro Ser
115 120 125
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala
130 135 140
Ser Gln Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly
145 150 155 160
Lys Ala Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly
165 170 175
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
180 185 190
Thr Ile Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln
195 200 205
Gln Gly Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu
210 215 220
Ile Lys Thr Lys Gly Pro Ser Arg Thr Val Ala Ala Pro Ser Val Phe
225 230 235 240
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
245 250 255
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
260 265 270
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
275 280 285
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
290 295 300
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
305 310 315 320
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
325 330 335
Glu Cys
<210> 110
<211> 570
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 110
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ser Gln Val Gln Leu Val Glu Ser
115 120 125
Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala
130 135 140
Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His Trp Val Arg Gln
145 150 155 160
Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile Lys Asp Lys Ser
165 170 175
Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr
180 185 190
Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser
195 200 205
Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg Gly Val Tyr Tyr
210 215 220
Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
225 230 235 240
Ser Ser Arg Thr Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
245 250 255
Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu
260 265 270
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
275 280 285
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
290 295 300
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
305 310 315 320
Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr
325 330 335
Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro
340 345 350
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
355 360 365
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
370 375 380
Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn
385 390 395 400
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
405 410 415
Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
420 425 430
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
435 440 445
Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys
450 455 460
Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Gln Glu
465 470 475 480
Glu Met Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe
485 490 495
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
500 505 510
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
515 520 525
Phe Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly
530 535 540
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
545 550 555 560
Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
565 570
<210> 111
<211> 448
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 111
Arg Ala His Leu Val Gln Ser Gly Thr Ala Met Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Val Ser Cys Gln Thr Ser Gly Tyr Thr Phe Thr Ala His
20 25 30
Ile Leu Phe Trp Phe Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Lys Pro Gln Tyr Gly Ala Val Asn Phe Gly Gly Gly Phe
50 55 60
Arg Asp Arg Val Thr Leu Thr Arg Asp Val Tyr Arg Glu Ile Ala Tyr
65 70 75 80
Met Asp Ile Arg Gly Leu Lys Pro Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Ser Tyr Gly Asp Ser Ser Trp Ala Leu Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Val Val Ser Ala Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
260 265 270
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Cys Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440 445
<210> 112
<211> 210
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 112
Tyr Ile His Val Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Ile Gly
1 5 10 15
Asp Arg Val Thr Ile Asn Cys Gln Thr Ser Gln Gly Val Gly Ser Asp
20 25 30
Leu His Trp Tyr Gln His Lys Pro Gly Arg Ala Pro Lys Leu Leu Ile
35 40 45
His His Thr Ser Ser Val Glu Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Phe His Thr Ser Phe Asn Leu Thr Ile Ser Asp Leu Gln Ala
65 70 75 80
Asp Asp Ile Ala Thr Tyr Tyr Cys Gln Val Leu Gln Phe Phe Gly Arg
85 90 95
Gly Ser Arg Leu His Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe
100 105 110
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
115 120 125
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
130 135 140
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
145 150 155 160
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
165 170 175
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
180 185 190
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
195 200 205
Glu Cys
210
<210> 113
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 113
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Gln
20 25 30
Asn Ala Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Asp Lys Thr His Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln
130 135 140
Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly
195 200 205
Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
210 215 220
Asp Lys Thr His Thr Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
225 230 235 240
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
245 250 255
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
260 265 270
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
275 280 285
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
290 295 300
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
305 310 315 320
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330 335
<210> 114
<211> 577
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 114
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Asp Lys Thr His Thr Gln Val Gln
115 120 125
Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg
130 135 140
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His
145 150 155 160
Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile
165 170 175
Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg
210 215 220
Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Ala Ser Thr Lys Gly
245 250 255
Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser
260 265 270
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
275 280 285
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
290 295 300
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
305 310 315 320
Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val
325 330 335
Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys
340 345 350
Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
355 360 365
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
370 375 380
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu
385 390 395 400
Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
405 410 415
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg
420 425 430
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
435 440 445
Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu
450 455 460
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys
465 470 475 480
Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu
485 490 495
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
500 505 510
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
515 520 525
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
530 535 540
Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His
545 550 555 560
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu
565 570 575
Gly
<210> 115
<211> 448
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 115
Arg Ala His Leu Val Gln Ser Gly Thr Ala Met Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Val Ser Cys Gln Thr Ser Gly Tyr Thr Phe Thr Ala His
20 25 30
Ile Leu Phe Trp Phe Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Lys Pro Gln Tyr Gly Ala Val Asn Phe Gly Gly Gly Phe
50 55 60
Arg Asp Arg Val Thr Leu Thr Arg Asp Val Tyr Arg Glu Ile Ala Tyr
65 70 75 80
Met Asp Ile Arg Gly Leu Lys Pro Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Ser Tyr Gly Asp Ser Ser Trp Ala Leu Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Val Val Ser Ala Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
260 265 270
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Cys Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440 445
<210> 116
<211> 210
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 116
Tyr Ile His Val Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Ile Gly
1 5 10 15
Asp Arg Val Thr Ile Asn Cys Gln Thr Ser Gln Gly Val Gly Ser Asp
20 25 30
Leu His Trp Tyr Gln His Lys Pro Gly Arg Ala Pro Lys Leu Leu Ile
35 40 45
His His Thr Ser Ser Val Glu Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Phe His Thr Ser Phe Asn Leu Thr Ile Ser Asp Leu Gln Ala
65 70 75 80
Asp Asp Ile Ala Thr Tyr Tyr Cys Gln Val Leu Gln Phe Phe Gly Arg
85 90 95
Gly Ser Arg Leu His Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe
100 105 110
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
115 120 125
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
130 135 140
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
145 150 155 160
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
165 170 175
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
180 185 190
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
195 200 205
Glu Cys
210
<210> 117
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 117
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Asn
20 25 30
Asn Ala Asn Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Asp Lys Thr His Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln
130 135 140
Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly
195 200 205
Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
210 215 220
Asp Lys Thr His Thr Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
225 230 235 240
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
245 250 255
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
260 265 270
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
275 280 285
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
290 295 300
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
305 310 315 320
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330 335
<210> 118
<211> 577
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 118
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Asp Lys Thr His Thr Gln Val Gln
115 120 125
Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg
130 135 140
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His
145 150 155 160
Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile
165 170 175
Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg
210 215 220
Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Ala Ser Thr Lys Gly
245 250 255
Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser
260 265 270
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
275 280 285
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
290 295 300
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
305 310 315 320
Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val
325 330 335
Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys
340 345 350
Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
355 360 365
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
370 375 380
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu
385 390 395 400
Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
405 410 415
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg
420 425 430
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
435 440 445
Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu
450 455 460
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys
465 470 475 480
Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu
485 490 495
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
500 505 510
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
515 520 525
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
530 535 540
Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His
545 550 555 560
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu
565 570 575
Gly
<210> 119
<211> 448
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 119
Arg Ala His Leu Val Gln Ser Gly Thr Ala Met Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Val Ser Cys Gln Thr Ser Gly Tyr Thr Phe Thr Ala His
20 25 30
Ile Leu Phe Trp Phe Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Lys Pro Gln Tyr Gly Ala Val Asn Phe Gly Gly Gly Phe
50 55 60
Arg Asp Arg Val Thr Leu Thr Arg Asp Val Tyr Arg Glu Ile Ala Tyr
65 70 75 80
Met Asp Ile Arg Gly Leu Lys Pro Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Ser Tyr Gly Asp Ser Ser Trp Ala Leu Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Val Val Ser Ala Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
260 265 270
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Cys Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440 445
<210> 120
<211> 210
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 120
Tyr Ile His Val Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Ile Gly
1 5 10 15
Asp Arg Val Thr Ile Asn Cys Gln Thr Ser Gln Gly Val Gly Ser Asp
20 25 30
Leu His Trp Tyr Gln His Lys Pro Gly Arg Ala Pro Lys Leu Leu Ile
35 40 45
His His Thr Ser Ser Val Glu Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Phe His Thr Ser Phe Asn Leu Thr Ile Ser Asp Leu Gln Ala
65 70 75 80
Asp Asp Ile Ala Thr Tyr Tyr Cys Gln Val Leu Gln Phe Phe Gly Arg
85 90 95
Gly Ser Arg Leu His Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe
100 105 110
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
115 120 125
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
130 135 140
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
145 150 155 160
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
165 170 175
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
180 185 190
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
195 200 205
Glu Cys
210
<210> 121
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 121
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Gln
20 25 30
Asn Ala Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Asp Lys Thr His Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln
130 135 140
Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly
195 200 205
Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
210 215 220
Asp Lys Thr His Thr Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
225 230 235 240
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
245 250 255
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
260 265 270
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
275 280 285
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
290 295 300
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
305 310 315 320
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330 335
<210> 122
<211> 580
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 122
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Asp Lys Thr His Thr Gln Val Gln
115 120 125
Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg
130 135 140
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His
145 150 155 160
Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile
165 170 175
Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg
210 215 220
Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Ala Ser Thr Lys Gly
245 250 255
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
260 265 270
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
275 280 285
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
290 295 300
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
305 310 315 320
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
325 330 335
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
340 345 350
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
355 360 365
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
370 375 380
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
385 390 395 400
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
405 410 415
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Asn
420 425 430
Ala Ser Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
435 440 445
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
450 455 460
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
465 470 475 480
Gln Val Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
485 490 495
Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
500 505 510
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
515 520 525
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu
530 535 540
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
545 550 555 560
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
565 570 575
Leu Ser Pro Gly
580
<210> 123
<211> 451
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 123
Arg Ala His Leu Val Gln Ser Gly Thr Ala Met Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Val Ser Cys Gln Thr Ser Gly Tyr Thr Phe Thr Ala His
20 25 30
Ile Leu Phe Trp Phe Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Lys Pro Gln Tyr Gly Ala Val Asn Phe Gly Gly Gly Phe
50 55 60
Arg Asp Arg Val Thr Leu Thr Arg Asp Val Tyr Arg Glu Ile Ala Tyr
65 70 75 80
Met Asp Ile Arg Gly Leu Lys Pro Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Ser Tyr Gly Asp Ser Ser Trp Ala Leu Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Val Val Ser Ala Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
210 215 220
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
225 230 235 240
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
260 265 270
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Asn Ala
290 295 300
Ser Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val
355 360 365
Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Pro Gly
450
<210> 124
<211> 210
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 124
Tyr Ile His Val Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Ile Gly
1 5 10 15
Asp Arg Val Thr Ile Asn Cys Gln Thr Ser Gln Gly Val Gly Ser Asp
20 25 30
Leu His Trp Tyr Gln His Lys Pro Gly Arg Ala Pro Lys Leu Leu Ile
35 40 45
His His Thr Ser Ser Val Glu Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Phe His Thr Ser Phe Asn Leu Thr Ile Ser Asp Leu Gln Ala
65 70 75 80
Asp Asp Ile Ala Thr Tyr Tyr Cys Gln Val Leu Gln Phe Phe Gly Arg
85 90 95
Gly Ser Arg Leu His Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe
100 105 110
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
115 120 125
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
130 135 140
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
145 150 155 160
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
165 170 175
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
180 185 190
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
195 200 205
Glu Cys
210
<210> 125
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 125
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Asp
20 25 30
Asn Ala Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Asp Lys Thr His Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln
130 135 140
Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly
195 200 205
Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
210 215 220
Asp Lys Thr His Thr Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
225 230 235 240
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
245 250 255
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
260 265 270
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
275 280 285
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
290 295 300
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
305 310 315 320
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330 335
<210> 126
<211> 577
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 126
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Asp Lys Thr His Thr Gln Val Gln
115 120 125
Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg
130 135 140
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His
145 150 155 160
Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile
165 170 175
Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg
210 215 220
Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Ala Ser Thr Lys Gly
245 250 255
Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser
260 265 270
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
275 280 285
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
290 295 300
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
305 310 315 320
Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val
325 330 335
Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys
340 345 350
Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
355 360 365
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
370 375 380
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu
385 390 395 400
Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
405 410 415
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg
420 425 430
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
435 440 445
Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu
450 455 460
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys
465 470 475 480
Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu
485 490 495
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
500 505 510
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
515 520 525
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
530 535 540
Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His
545 550 555 560
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu
565 570 575
Gly
<210> 127
<211> 448
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 127
Arg Ala His Leu Val Gln Ser Gly Thr Ala Met Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Val Ser Cys Gln Thr Ser Gly Tyr Thr Phe Thr Ala His
20 25 30
Ile Leu Phe Trp Phe Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Lys Pro Gln Tyr Gly Ala Val Asn Phe Gly Gly Gly Phe
50 55 60
Arg Asp Arg Val Thr Leu Thr Arg Asp Val Tyr Arg Glu Ile Ala Tyr
65 70 75 80
Met Asp Ile Arg Gly Leu Lys Pro Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Ser Tyr Gly Asp Ser Ser Trp Ala Leu Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Val Val Ser Ala Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
260 265 270
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Cys Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440 445
<210> 128
<211> 210
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 128
Tyr Ile His Val Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Ile Gly
1 5 10 15
Asp Arg Val Thr Ile Asn Cys Gln Thr Ser Gln Gly Val Gly Ser Asp
20 25 30
Leu His Trp Tyr Gln His Lys Pro Gly Arg Ala Pro Lys Leu Leu Ile
35 40 45
His His Thr Ser Ser Val Glu Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Phe His Thr Ser Phe Asn Leu Thr Ile Ser Asp Leu Gln Ala
65 70 75 80
Asp Asp Ile Ala Thr Tyr Tyr Cys Gln Val Leu Gln Phe Phe Gly Arg
85 90 95
Gly Ser Arg Leu His Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe
100 105 110
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
115 120 125
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
130 135 140
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
145 150 155 160
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
165 170 175
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
180 185 190
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
195 200 205
Glu Cys
210
<210> 129
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 129
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Asp Lys Thr His Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln
130 135 140
Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly
195 200 205
Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
210 215 220
Asp Lys Thr His Thr Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
225 230 235 240
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
245 250 255
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
260 265 270
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
275 280 285
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
290 295 300
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
305 310 315 320
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330 335
<210> 130
<211> 577
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 130
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Asp Lys Thr His Thr Gln Val Gln
115 120 125
Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg
130 135 140
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His
145 150 155 160
Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile
165 170 175
Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg
210 215 220
Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Ala Ser Thr Lys Gly
245 250 255
Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser
260 265 270
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
275 280 285
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
290 295 300
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
305 310 315 320
Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val
325 330 335
Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys
340 345 350
Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
355 360 365
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
370 375 380
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu
385 390 395 400
Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
405 410 415
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg
420 425 430
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
435 440 445
Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu
450 455 460
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys
465 470 475 480
Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu
485 490 495
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
500 505 510
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
515 520 525
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
530 535 540
Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His
545 550 555 560
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu
565 570 575
Gly
<210> 131
<211> 448
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 131
Arg Ala His Leu Val Gln Ser Gly Thr Ala Met Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Val Ser Cys Gln Thr Ser Gly Tyr Thr Phe Thr Ala His
20 25 30
Ile Leu Phe Trp Phe Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Lys Pro Gln Tyr Gly Ala Val Asn Phe Gly Gly Gly Phe
50 55 60
Arg Asp Arg Val Thr Leu Thr Arg Asp Val Tyr Arg Glu Ile Ala Tyr
65 70 75 80
Met Asp Ile Arg Gly Leu Lys Pro Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Ser Tyr Gly Asp Ser Ser Trp Ala Leu Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Val Val Ser Ala Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
260 265 270
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Cys Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440 445
<210> 132
<211> 210
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 132
Tyr Ile His Val Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Ile Gly
1 5 10 15
Asp Arg Val Thr Ile Asn Cys Gln Thr Ser Gln Gly Val Gly Ser Asp
20 25 30
Leu His Trp Tyr Gln His Lys Pro Gly Arg Ala Pro Lys Leu Leu Ile
35 40 45
His His Thr Ser Ser Val Glu Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Phe His Thr Ser Phe Asn Leu Thr Ile Ser Asp Leu Gln Ala
65 70 75 80
Asp Asp Ile Ala Thr Tyr Tyr Cys Gln Val Leu Gln Phe Phe Gly Arg
85 90 95
Gly Ser Arg Leu His Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe
100 105 110
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
115 120 125
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
130 135 140
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
145 150 155 160
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
165 170 175
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
180 185 190
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
195 200 205
Glu Cys
210
<210> 133
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 133
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Arg Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Asp Lys Thr His Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln
130 135 140
Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly
195 200 205
Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
210 215 220
Asp Lys Thr His Thr Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
225 230 235 240
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
245 250 255
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
260 265 270
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
275 280 285
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
290 295 300
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
305 310 315 320
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330 335
<210> 134
<211> 577
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 134
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Asp Lys Thr His Thr Gln Val Gln
115 120 125
Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg
130 135 140
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His
145 150 155 160
Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile
165 170 175
Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg
210 215 220
Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Ala Ser Thr Lys Gly
245 250 255
Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser
260 265 270
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
275 280 285
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
290 295 300
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
305 310 315 320
Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val
325 330 335
Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys
340 345 350
Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
355 360 365
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
370 375 380
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu
385 390 395 400
Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
405 410 415
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg
420 425 430
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
435 440 445
Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu
450 455 460
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys
465 470 475 480
Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu
485 490 495
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
500 505 510
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
515 520 525
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
530 535 540
Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His
545 550 555 560
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu
565 570 575
Gly
<210> 135
<211> 448
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 135
Arg Ala His Leu Val Gln Ser Gly Thr Ala Met Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Val Ser Cys Gln Thr Ser Gly Tyr Thr Phe Thr Ala His
20 25 30
Ile Leu Phe Trp Phe Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Lys Pro Gln Tyr Gly Ala Val Asn Phe Gly Gly Gly Phe
50 55 60
Arg Asp Arg Val Thr Leu Thr Arg Asp Val Tyr Arg Glu Ile Ala Tyr
65 70 75 80
Met Asp Ile Arg Gly Leu Lys Pro Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Ser Tyr Gly Asp Ser Ser Trp Ala Leu Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Val Val Ser Ala Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
260 265 270
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Cys Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440 445
<210> 136
<211> 210
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 136
Tyr Ile His Val Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Ile Gly
1 5 10 15
Asp Arg Val Thr Ile Asn Cys Gln Thr Ser Gln Gly Val Gly Ser Asp
20 25 30
Leu His Trp Tyr Gln His Lys Pro Gly Arg Ala Pro Lys Leu Leu Ile
35 40 45
His His Thr Ser Ser Val Glu Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Phe His Thr Ser Phe Asn Leu Thr Ile Ser Asp Leu Gln Ala
65 70 75 80
Asp Asp Ile Ala Thr Tyr Tyr Cys Gln Val Leu Gln Phe Phe Gly Arg
85 90 95
Gly Ser Arg Leu His Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe
100 105 110
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
115 120 125
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
130 135 140
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
145 150 155 160
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
165 170 175
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
180 185 190
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
195 200 205
Glu Cys
210
<210> 137
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 137
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Phe Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Asp Lys Thr His Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln
130 135 140
Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly
195 200 205
Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
210 215 220
Asp Lys Thr His Thr Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
225 230 235 240
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
245 250 255
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
260 265 270
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
275 280 285
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
290 295 300
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
305 310 315 320
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330 335
<210> 138
<211> 577
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 138
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Asp Lys Thr His Thr Gln Val Gln
115 120 125
Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg
130 135 140
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His
145 150 155 160
Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile
165 170 175
Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg
210 215 220
Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Ala Ser Thr Lys Gly
245 250 255
Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser
260 265 270
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
275 280 285
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
290 295 300
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
305 310 315 320
Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val
325 330 335
Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys
340 345 350
Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
355 360 365
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
370 375 380
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu
385 390 395 400
Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
405 410 415
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg
420 425 430
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
435 440 445
Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu
450 455 460
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys
465 470 475 480
Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu
485 490 495
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
500 505 510
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
515 520 525
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
530 535 540
Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His
545 550 555 560
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu
565 570 575
Gly
<210> 139
<211> 448
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 139
Arg Ala His Leu Val Gln Ser Gly Thr Ala Met Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Val Ser Cys Gln Thr Ser Gly Tyr Thr Phe Thr Ala His
20 25 30
Ile Leu Phe Trp Phe Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Lys Pro Gln Tyr Gly Ala Val Asn Phe Gly Gly Gly Phe
50 55 60
Arg Asp Arg Val Thr Leu Thr Arg Asp Val Tyr Arg Glu Ile Ala Tyr
65 70 75 80
Met Asp Ile Arg Gly Leu Lys Pro Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Ser Tyr Gly Asp Ser Ser Trp Ala Leu Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Val Val Ser Ala Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
260 265 270
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Cys Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440 445
<210> 140
<211> 210
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 140
Tyr Ile His Val Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Ile Gly
1 5 10 15
Asp Arg Val Thr Ile Asn Cys Gln Thr Ser Gln Gly Val Gly Ser Asp
20 25 30
Leu His Trp Tyr Gln His Lys Pro Gly Arg Ala Pro Lys Leu Leu Ile
35 40 45
His His Thr Ser Ser Val Glu Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Phe His Thr Ser Phe Asn Leu Thr Ile Ser Asp Leu Gln Ala
65 70 75 80
Asp Asp Ile Ala Thr Tyr Tyr Cys Gln Val Leu Gln Phe Phe Gly Arg
85 90 95
Gly Ser Arg Leu His Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe
100 105 110
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
115 120 125
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
130 135 140
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
145 150 155 160
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
165 170 175
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
180 185 190
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
195 200 205
Glu Cys
210
<210> 141
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 141
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Asp Lys Thr His Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln
130 135 140
Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly
195 200 205
Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
210 215 220
Asp Lys Thr His Thr Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
225 230 235 240
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
245 250 255
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
260 265 270
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
275 280 285
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
290 295 300
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
305 310 315 320
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330 335
<210> 142
<211> 577
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 142
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Asp Lys Thr His Thr Gln Val Gln
115 120 125
Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg
130 135 140
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His
145 150 155 160
Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile
165 170 175
Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg
210 215 220
Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Ala Ser Thr Lys Gly
245 250 255
Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser
260 265 270
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
275 280 285
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
290 295 300
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
305 310 315 320
Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val
325 330 335
Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys
340 345 350
Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
355 360 365
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
370 375 380
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu
385 390 395 400
Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
405 410 415
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg
420 425 430
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
435 440 445
Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu
450 455 460
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys
465 470 475 480
Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu
485 490 495
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
500 505 510
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
515 520 525
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
530 535 540
Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His
545 550 555 560
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu
565 570 575
Gly
<210> 143
<211> 448
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 143
Arg Ala His Leu Val Gln Ser Gly Thr Ala Met Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Val Ser Cys Gln Thr Ser Gly Tyr Thr Phe Thr Ala His
20 25 30
Ile Leu Phe Trp Phe Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Lys Pro Gln Tyr Gly Ala Thr Asn Phe Gly Gly Gly Phe
50 55 60
Arg Asp Arg Val Thr Leu Thr Arg Asp Val Tyr Arg Glu Ile Ala Tyr
65 70 75 80
Met Asp Ile Arg Gly Leu Lys Pro Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Ser Tyr Gly Asp Ser Ser Trp Ala Leu Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Val Val Ser Ala Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
260 265 270
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Cys Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440 445
<210> 144
<211> 210
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 144
Tyr Ile His Val Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Ile Gly
1 5 10 15
Asp Arg Val Thr Ile Asn Cys Gln Thr Ser Gln Gly Val Gly Ser Asp
20 25 30
Leu His Trp Tyr Gln His Lys Pro Gly Arg Ala Pro Lys Leu Leu Ile
35 40 45
His His Thr Ser Ser Ser Glu Glu Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Phe His Thr Ser Phe Asn Leu Thr Ile Ser Asp Leu Gln Ala
65 70 75 80
Asp Asp Ile Ala Thr Tyr Tyr Cys Gln Val Leu Gln Phe Phe Gly Arg
85 90 95
Gly Ser Arg Leu His Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe
100 105 110
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
115 120 125
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
130 135 140
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
145 150 155 160
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
165 170 175
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
180 185 190
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
195 200 205
Glu Cys
210
<210> 145
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 145
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Phe Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Asp Lys Thr His Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln
130 135 140
Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly
195 200 205
Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
210 215 220
Asp Lys Thr His Thr Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
225 230 235 240
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
245 250 255
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
260 265 270
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
275 280 285
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
290 295 300
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
305 310 315 320
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330 335
<210> 146
<211> 577
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 146
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Asp Lys Thr His Thr Gln Val Gln
115 120 125
Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg
130 135 140
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His
145 150 155 160
Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile
165 170 175
Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg
210 215 220
Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Ala Ser Thr Lys Gly
245 250 255
Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser
260 265 270
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
275 280 285
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
290 295 300
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
305 310 315 320
Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val
325 330 335
Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys
340 345 350
Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
355 360 365
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
370 375 380
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu
385 390 395 400
Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
405 410 415
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg
420 425 430
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
435 440 445
Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu
450 455 460
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys
465 470 475 480
Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu
485 490 495
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
500 505 510
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
515 520 525
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
530 535 540
Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His
545 550 555 560
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu
565 570 575
Gly
<210> 147
<211> 448
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 147
Arg Ala His Leu Val Gln Ser Gly Thr Ala Met Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Val Ser Cys Gln Thr Ser Gly Tyr Thr Phe Thr Ala His
20 25 30
Ile Leu Phe Trp Phe Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Lys Pro Gln Tyr Gly Ala Thr Asn Phe Gly Gly Gly Phe
50 55 60
Arg Asp Arg Val Thr Leu Thr Arg Asp Val Tyr Arg Glu Ile Ala Tyr
65 70 75 80
Met Asp Ile Arg Gly Leu Lys Pro Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Ser Tyr Gly Asp Ser Ser Trp Ala Leu Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Val Val Ser Ala Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
260 265 270
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Cys Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Trp
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440 445
<210> 148
<211> 210
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 148
Tyr Ile His Val Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Ile Gly
1 5 10 15
Asp Arg Val Thr Ile Asn Cys Gln Thr Ser Gln Gly Val Gly Ser Asp
20 25 30
Leu His Trp Tyr Gln His Lys Pro Gly Arg Ala Pro Lys Leu Leu Ile
35 40 45
His His Thr Ser Ser Ser Glu Glu Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Phe His Thr Ser Phe Asn Leu Thr Ile Ser Asp Leu Gln Ala
65 70 75 80
Asp Asp Ile Ala Thr Tyr Tyr Cys Gln Val Leu Gln Phe Phe Gly Arg
85 90 95
Gly Ser Arg Leu His Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe
100 105 110
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
115 120 125
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
130 135 140
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
145 150 155 160
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
165 170 175
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
180 185 190
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
195 200 205
Glu Cys
210
<210> 149
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 149
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Phe Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Asp Lys Thr His Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln
130 135 140
Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly
195 200 205
Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
210 215 220
Asp Lys Thr His Thr Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
225 230 235 240
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
245 250 255
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
260 265 270
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
275 280 285
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
290 295 300
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
305 310 315 320
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330 335
<210> 150
<211> 580
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 150
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Asp Lys Thr His Thr Gln Val Gln
115 120 125
Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg
130 135 140
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His
145 150 155 160
Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile
165 170 175
Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg
210 215 220
Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Ala Ser Thr Lys Gly
245 250 255
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
260 265 270
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
275 280 285
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
290 295 300
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
305 310 315 320
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
325 330 335
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
340 345 350
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
355 360 365
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
370 375 380
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
385 390 395 400
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
405 410 415
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Asn
420 425 430
Ala Ser Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
435 440 445
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
450 455 460
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
465 470 475 480
Gln Val Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
485 490 495
Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
500 505 510
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
515 520 525
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu
530 535 540
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
545 550 555 560
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
565 570 575
Leu Ser Pro Gly
580
<210> 151
<211> 451
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 151
Arg Ala His Leu Val Gln Ser Gly Thr Ala Met Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Val Ser Cys Gln Thr Ser Gly Tyr Thr Phe Thr Ala His
20 25 30
Ile Leu Phe Trp Phe Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Lys Pro Gln Tyr Gly Ala Thr Asn Phe Gly Gly Gly Phe
50 55 60
Arg Asp Arg Val Thr Leu Thr Arg Asp Val Tyr Arg Glu Ile Ala Tyr
65 70 75 80
Met Asp Ile Arg Gly Leu Lys Pro Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Ser Tyr Gly Asp Ser Ser Trp Ala Leu Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Val Val Ser Ala Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
210 215 220
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
225 230 235 240
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
260 265 270
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Asn Ala
290 295 300
Ser Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Cys Arg Asp Glu Leu Thr Lys Asn Gln Val
355 360 365
Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Pro Gly
450
<210> 152
<211> 210
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 152
Tyr Ile His Val Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Ile Gly
1 5 10 15
Asp Arg Val Thr Ile Asn Cys Gln Thr Ser Gln Gly Val Gly Ser Asp
20 25 30
Leu His Trp Tyr Gln His Lys Pro Gly Arg Ala Pro Lys Leu Leu Ile
35 40 45
His His Thr Ser Ser Ser Glu Glu Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Phe His Thr Ser Phe Asn Leu Thr Ile Ser Asp Leu Gln Ala
65 70 75 80
Asp Asp Ile Ala Thr Tyr Tyr Cys Gln Val Leu Gln Phe Phe Gly Arg
85 90 95
Gly Ser Arg Leu His Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe
100 105 110
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
115 120 125
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
130 135 140
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
145 150 155 160
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
165 170 175
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
180 185 190
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
195 200 205
Glu Cys
210
<210> 153
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 153
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Asp Lys Thr His Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln
130 135 140
Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly
195 200 205
Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
210 215 220
Asp Lys Thr His Thr Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
225 230 235 240
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
245 250 255
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
260 265 270
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
275 280 285
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
290 295 300
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
305 310 315 320
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330 335
<210> 154
<211> 577
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 154
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Asp Lys Thr His Thr Gln Val Gln
115 120 125
Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg
130 135 140
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His
145 150 155 160
Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile
165 170 175
Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg
210 215 220
Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Ala Ser Thr Lys Gly
245 250 255
Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser
260 265 270
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
275 280 285
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
290 295 300
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
305 310 315 320
Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val
325 330 335
Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys
340 345 350
Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
355 360 365
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
370 375 380
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu
385 390 395 400
Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
405 410 415
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg
420 425 430
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
435 440 445
Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu
450 455 460
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys
465 470 475 480
Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu
485 490 495
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
500 505 510
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
515 520 525
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
530 535 540
Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His
545 550 555 560
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu
565 570 575
Gly
<210> 155
<211> 455
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 155
Arg Ala His Leu Val Gln Ser Gly Thr Ala Met Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Val Ser Cys Gln Thr Ser Gly Tyr Thr Phe Thr Ala His
20 25 30
Ile Leu Phe Trp Phe Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Lys Pro Gln Tyr Gly Ala Val Asn Phe Gly Gly Gly Phe
50 55 60
Arg Asp Arg Val Thr Leu Thr Arg Gln Leu Ser Gln Asp Pro Asp Asp
65 70 75 80
Pro Asp Trp Gly Ile Ala Tyr Met Asp Ile Arg Gly Leu Lys Pro Asp
85 90 95
Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Arg Ser Tyr Gly Asp Ser
100 105 110
Ser Trp Ala Leu Asp Ala Trp Gly Gln Gly Thr Thr Val Val Val Ser
115 120 125
Ala Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser
130 135 140
Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
145 150 155 160
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
165 170 175
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
180 185 190
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys
195 200 205
Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp
210 215 220
Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly
325 330 335
Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Gln Glu Glu Met Thr
355 360 365
Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Leu Gly
450 455
<210> 156
<211> 210
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 156
Tyr Ile His Val Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Ile Gly
1 5 10 15
Asp Arg Val Thr Ile Asn Cys Gln Thr Ser Gln Gly Val Gly Ser Asp
20 25 30
Leu His Trp Tyr Gln His Lys Pro Gly Arg Ala Pro Lys Leu Leu Ile
35 40 45
His His Thr Ser Ser Val Glu Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Phe His Thr Ser Phe Asn Leu Thr Ile Ser Asp Leu Gln Ala
65 70 75 80
Asp Asp Ile Ala Thr Tyr Tyr Cys Gln Val Leu Gln Phe Phe Gly Arg
85 90 95
Gly Ser Arg Leu His Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe
100 105 110
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
115 120 125
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
130 135 140
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
145 150 155 160
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
165 170 175
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
180 185 190
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
195 200 205
Glu Cys
210
<210> 157
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 157
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Phe Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Asp Lys Thr His Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln
130 135 140
Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly
195 200 205
Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
210 215 220
Asp Lys Thr His Thr Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
225 230 235 240
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
245 250 255
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
260 265 270
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
275 280 285
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
290 295 300
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
305 310 315 320
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330 335
<210> 158
<211> 577
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 158
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Asp Lys Thr His Thr Gln Val Gln
115 120 125
Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg
130 135 140
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His
145 150 155 160
Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile
165 170 175
Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg
210 215 220
Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Ala Ser Thr Lys Gly
245 250 255
Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser
260 265 270
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
275 280 285
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
290 295 300
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
305 310 315 320
Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val
325 330 335
Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys
340 345 350
Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
355 360 365
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
370 375 380
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu
385 390 395 400
Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
405 410 415
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg
420 425 430
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
435 440 445
Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu
450 455 460
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys
465 470 475 480
Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu
485 490 495
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
500 505 510
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
515 520 525
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
530 535 540
Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His
545 550 555 560
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu
565 570 575
Gly
<210> 159
<211> 455
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 159
Arg Ala His Leu Val Gln Ser Gly Thr Ala Met Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Val Ser Cys Gln Thr Ser Gly Tyr Thr Phe Thr Ala His
20 25 30
Ile Leu Phe Trp Phe Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Lys Pro Gln Tyr Gly Ala Val Asn Phe Gly Gly Gly Phe
50 55 60
Arg Asp Arg Val Thr Leu Thr Arg Gln Leu Ser Gln Asp Pro Asp Asp
65 70 75 80
Pro Asp Trp Gly Ile Ala Tyr Met Asp Ile Arg Gly Leu Lys Pro Asp
85 90 95
Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Arg Ser Tyr Gly Asp Ser
100 105 110
Ser Trp Ala Leu Asp Ala Trp Gly Gln Gly Thr Thr Val Val Val Ser
115 120 125
Ala Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser
130 135 140
Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
145 150 155 160
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
165 170 175
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
180 185 190
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys
195 200 205
Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp
210 215 220
Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly
325 330 335
Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Gln Glu Glu Met Thr
355 360 365
Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Leu Gly
450 455
<210> 160
<211> 210
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 160
Tyr Ile His Val Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Ile Gly
1 5 10 15
Asp Arg Val Thr Ile Asn Cys Gln Thr Ser Gln Gly Val Gly Ser Asp
20 25 30
Leu His Trp Tyr Gln His Lys Pro Gly Arg Ala Pro Lys Leu Leu Ile
35 40 45
His His Thr Ser Ser Val Glu Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Phe His Thr Ser Phe Asn Leu Thr Ile Ser Asp Leu Gln Ala
65 70 75 80
Asp Asp Ile Ala Thr Tyr Tyr Cys Gln Val Leu Gln Phe Phe Gly Arg
85 90 95
Gly Ser Arg Leu His Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe
100 105 110
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
115 120 125
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
130 135 140
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
145 150 155 160
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
165 170 175
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
180 185 190
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
195 200 205
Glu Cys
210
<210> 161
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 161
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Asp Lys Thr His Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln
130 135 140
Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly
195 200 205
Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
210 215 220
Asp Lys Thr His Thr Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
225 230 235 240
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
245 250 255
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
260 265 270
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
275 280 285
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
290 295 300
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
305 310 315 320
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330 335
<210> 162
<211> 580
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 162
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Asp Lys Thr His Thr Gln Val Gln
115 120 125
Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg
130 135 140
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His
145 150 155 160
Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile
165 170 175
Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg
210 215 220
Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Ala Ser Thr Lys Gly
245 250 255
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
260 265 270
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
275 280 285
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
290 295 300
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
305 310 315 320
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
325 330 335
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
340 345 350
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
355 360 365
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
370 375 380
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
385 390 395 400
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
405 410 415
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Asn
420 425 430
Ala Ser Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
435 440 445
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
450 455 460
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
465 470 475 480
Gln Val Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
485 490 495
Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
500 505 510
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
515 520 525
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu
530 535 540
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
545 550 555 560
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
565 570 575
Leu Ser Pro Gly
580
<210> 163
<211> 458
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 163
Arg Ala His Leu Val Gln Ser Gly Thr Ala Met Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Val Ser Cys Gln Thr Ser Gly Tyr Thr Phe Thr Ala His
20 25 30
Ile Leu Phe Trp Phe Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Lys Pro Gln Tyr Gly Ala Val Asn Phe Gly Gly Gly Phe
50 55 60
Arg Asp Arg Val Thr Leu Thr Arg Gln Leu Ser Gln Asp Pro Asp Asp
65 70 75 80
Pro Asp Trp Gly Ile Ala Tyr Met Asp Ile Arg Gly Leu Lys Pro Asp
85 90 95
Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Arg Ser Tyr Gly Asp Ser
100 105 110
Ser Trp Ala Leu Asp Ala Trp Gly Gln Gly Thr Thr Val Val Val Ser
115 120 125
Ala Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
130 135 140
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
145 150 155 160
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
165 170 175
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
180 185 190
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
195 200 205
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
210 215 220
Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
225 230 235 240
Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
245 250 255
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
260 265 270
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
275 280 285
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
290 295 300
Glu Glu Gln Tyr Asn Asn Ala Ser Arg Val Val Ser Val Leu Thr Val
305 310 315 320
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
325 330 335
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
340 345 350
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp
355 360 365
Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
370 375 380
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
385 390 395 400
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
405 410 415
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
420 425 430
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
435 440 445
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
450 455
<210> 164
<211> 210
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 164
Tyr Ile His Val Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Ile Gly
1 5 10 15
Asp Arg Val Thr Ile Asn Cys Gln Thr Ser Gln Gly Val Gly Ser Asp
20 25 30
Leu His Trp Tyr Gln His Lys Pro Gly Arg Ala Pro Lys Leu Leu Ile
35 40 45
His His Thr Ser Ser Val Glu Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Phe His Thr Ser Phe Asn Leu Thr Ile Ser Asp Leu Gln Ala
65 70 75 80
Asp Asp Ile Ala Thr Tyr Tyr Cys Gln Val Leu Gln Phe Phe Gly Arg
85 90 95
Gly Ser Arg Leu His Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe
100 105 110
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
115 120 125
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
130 135 140
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
145 150 155 160
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
165 170 175
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
180 185 190
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
195 200 205
Glu Cys
210
<210> 165
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 165
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Phe Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Asp Lys Thr His Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln
130 135 140
Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly
195 200 205
Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
210 215 220
Asp Lys Thr His Thr Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
225 230 235 240
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
245 250 255
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
260 265 270
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
275 280 285
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
290 295 300
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
305 310 315 320
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330 335
<210> 166
<211> 580
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 166
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Asp Lys Thr His Thr Gln Val Gln
115 120 125
Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg
130 135 140
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His
145 150 155 160
Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile
165 170 175
Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg
210 215 220
Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Ala Ser Thr Lys Gly
245 250 255
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
260 265 270
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
275 280 285
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
290 295 300
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
305 310 315 320
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
325 330 335
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
340 345 350
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
355 360 365
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
370 375 380
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
385 390 395 400
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
405 410 415
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Asn
420 425 430
Ala Ser Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
435 440 445
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
450 455 460
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
465 470 475 480
Gln Val Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
485 490 495
Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
500 505 510
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
515 520 525
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu
530 535 540
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
545 550 555 560
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
565 570 575
Leu Ser Pro Gly
580
<210> 167
<211> 458
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 167
Arg Ala His Leu Val Gln Ser Gly Thr Ala Met Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Val Ser Cys Gln Thr Ser Gly Tyr Thr Phe Thr Ala His
20 25 30
Ile Leu Phe Trp Phe Arg Gln Ala Pro Gly Arg Gly Leu Glu Trp Val
35 40 45
Gly Trp Ile Lys Pro Gln Tyr Gly Ala Val Asn Phe Gly Gly Gly Phe
50 55 60
Arg Asp Arg Val Thr Leu Thr Arg Gln Leu Ser Gln Asp Pro Asp Asp
65 70 75 80
Pro Asp Trp Gly Ile Ala Tyr Met Asp Ile Arg Gly Leu Lys Pro Asp
85 90 95
Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Arg Ser Tyr Gly Asp Ser
100 105 110
Ser Trp Ala Leu Asp Ala Trp Gly Gln Gly Thr Thr Val Val Val Ser
115 120 125
Ala Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
130 135 140
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
145 150 155 160
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
165 170 175
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
180 185 190
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
195 200 205
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
210 215 220
Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
225 230 235 240
Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
245 250 255
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
260 265 270
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
275 280 285
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
290 295 300
Glu Glu Gln Tyr Asn Asn Ala Ser Arg Val Val Ser Val Leu Thr Val
305 310 315 320
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
325 330 335
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
340 345 350
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Asp
355 360 365
Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
370 375 380
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
385 390 395 400
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
405 410 415
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
420 425 430
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
435 440 445
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
450 455
<210> 168
<211> 210
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 168
Tyr Ile His Val Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Ile Gly
1 5 10 15
Asp Arg Val Thr Ile Asn Cys Gln Thr Ser Gln Gly Val Gly Ser Asp
20 25 30
Leu His Trp Tyr Gln His Lys Pro Gly Arg Ala Pro Lys Leu Leu Ile
35 40 45
His His Thr Ser Ser Val Glu Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Phe His Thr Ser Phe Asn Leu Thr Ile Ser Asp Leu Gln Ala
65 70 75 80
Asp Asp Ile Ala Thr Tyr Tyr Cys Gln Val Leu Gln Phe Phe Gly Arg
85 90 95
Gly Ser Arg Leu His Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe
100 105 110
Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val
115 120 125
Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp
130 135 140
Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr
145 150 155 160
Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr
165 170 175
Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val
180 185 190
Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly
195 200 205
Glu Cys
210
<210> 169
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 169
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Gln Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Asp Lys Thr His Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln
130 135 140
Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly
195 200 205
Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
210 215 220
Asp Lys Thr His Thr Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
225 230 235 240
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
245 250 255
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
260 265 270
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
275 280 285
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
290 295 300
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
305 310 315 320
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330 335
<210> 170
<211> 577
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 170
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Asp Lys Thr His Thr Gln Val Gln
115 120 125
Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg
130 135 140
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His
145 150 155 160
Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile
165 170 175
Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg
210 215 220
Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Ala Ser Thr Lys Gly
245 250 255
Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser
260 265 270
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
275 280 285
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
290 295 300
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
305 310 315 320
Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val
325 330 335
Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys
340 345 350
Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
355 360 365
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
370 375 380
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu
385 390 395 400
Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
405 410 415
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg
420 425 430
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
435 440 445
Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu
450 455 460
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys
465 470 475 480
Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu
485 490 495
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
500 505 510
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
515 520 525
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
530 535 540
Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His
545 550 555 560
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu
565 570 575
Gly
<210> 171
<211> 454
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 171
Gln Val Gln Leu Val Gln Ser Gly Gly Gln Met Lys Lys Pro Gly Glu
1 5 10 15
Ser Met Arg Ile Ser Cys Arg Ala Ser Gly Tyr Glu Phe Ile Asp Cys
20 25 30
Thr Leu Asn Trp Ile Arg Leu Ala Pro Gly Lys Arg Pro Glu Trp Met
35 40 45
Gly Trp Leu Lys Pro Arg Trp Gly Ala Val Asn Tyr Ala Arg Pro Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Gln Leu Ser Gln Asp Pro Asp Asp
65 70 75 80
Pro Asp Trp Gly Thr Ala Phe Leu Glu Leu Arg Ser Leu Thr Val Asp
85 90 95
Asp Thr Ala Val Tyr Phe Cys Thr Arg Gly Lys Asn Cys Asp Tyr Asn
100 105 110
Trp Asp Phe Glu His Trp Gly Arg Gly Thr Pro Val Ile Val Ser Ser
115 120 125
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
130 135 140
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
145 150 155 160
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
165 170 175
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
180 185 190
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
195 200 205
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
210 215 220
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro
225 230 235 240
Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
275 280 285
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
290 295 300
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
305 310 315 320
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
325 330 335
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
340 345 350
Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Gln Glu Glu Met Thr Lys
355 360 365
Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
370 375 380
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
385 390 395 400
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
405 410 415
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
420 425 430
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
435 440 445
Leu Ser Leu Ser Leu Gly
450
<210> 172
<211> 207
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 172
Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Thr Ala
1 5 10 15
Ile Ile Ser Cys Arg Thr Ser Gln Tyr Gly Ser Leu Ala Trp Tyr Gln
20 25 30
Gln Arg Pro Gly Gln Ala Pro Arg Leu Val Ile Tyr Ser Gly Ser Thr
35 40 45
Arg Ala Ala Gly Ile Pro Asp Arg Phe Ser Gly Ser Arg Trp Gly Pro
50 55 60
Asp Tyr Asn Leu Thr Ile Ser Asn Leu Glu Ser Gly Asp Phe Gly Val
65 70 75 80
Tyr Tyr Cys Gln Gln Tyr Glu Phe Phe Gly Gln Gly Thr Lys Val Gln
85 90 95
Val Asp Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro
100 105 110
Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu
115 120 125
Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp
130 135 140
Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp
145 150 155 160
Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys
165 170 175
Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln
180 185 190
Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
195 200 205
<210> 173
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 173
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Val His Glu
20 25 30
Asn Leu Phe Thr Tyr Leu Ser Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ser Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Val Glu Ile Lys
100 105 110
Asp Lys Thr His Thr Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
115 120 125
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln
130 135 140
Asn Ile Tyr Val Trp Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
145 150 155 160
Pro Lys Leu Leu Ile Tyr Lys Ala Ser Asn Leu His Thr Gly Val Pro
165 170 175
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
180 185 190
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly
195 200 205
Gln Thr Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
210 215 220
Asp Lys Thr His Thr Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
225 230 235 240
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
245 250 255
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
260 265 270
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
275 280 285
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
290 295 300
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
305 310 315 320
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
325 330 335
<210> 174
<211> 577
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 174
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ser Ile Tyr Pro Gly Asn Val Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser His Tyr Gly Leu Asp Trp Asn Phe Asp Val Trp Gly Lys
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Asp Lys Thr His Thr Gln Val Gln
115 120 125
Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu Arg
130 135 140
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Lys Ala Trp Met His
145 150 155 160
Trp Val Arg Gln Ala Pro Gly Lys Gln Leu Glu Trp Val Ala Gln Ile
165 170 175
Lys Asp Lys Ser Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
195 200 205
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Arg
210 215 220
Gly Val Tyr Tyr Ala Leu Ser Pro Phe Asp Tyr Trp Gly Gln Gly Thr
225 230 235 240
Leu Val Thr Val Ser Ser Asp Lys Thr His Thr Ala Ser Thr Lys Gly
245 250 255
Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser
260 265 270
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
275 280 285
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
290 295 300
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
305 310 315 320
Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val
325 330 335
Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys
340 345 350
Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
355 360 365
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
370 375 380
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu
385 390 395 400
Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
405 410 415
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg
420 425 430
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
435 440 445
Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu
450 455 460
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys
465 470 475 480
Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu
485 490 495
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
500 505 510
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
515 520 525
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
530 535 540
Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His
545 550 555 560
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu
565 570 575
Gly
<210> 175
<211> 454
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 175
Gln Val Gln Leu Val Gln Ser Gly Gly Gln Met Lys Lys Pro Gly Glu
1 5 10 15
Ser Met Arg Ile Ser Cys Arg Ala Ser Gly Tyr Glu Phe Ile Asp Cys
20 25 30
Thr Leu Asn Trp Ile Arg Leu Ala Pro Gly Lys Arg Pro Glu Trp Met
35 40 45
Gly Trp Leu Lys Pro Arg Trp Gly Ala Val Asn Tyr Ala Arg Pro Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Gln Leu Ser Gln Asp Pro Asp Asp
65 70 75 80
Pro Asp Trp Gly Thr Ala Phe Leu Glu Leu Arg Ser Leu Thr Val Asp
85 90 95
Asp Thr Ala Val Tyr Phe Cys Thr Arg Gly Lys Asn Cys Asp Tyr Asn
100 105 110
Trp Asp Phe Glu His Trp Gly Arg Gly Thr Pro Val Ile Val Ser Ser
115 120 125
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
130 135 140
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
145 150 155 160
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
165 170 175
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
180 185 190
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
195 200 205
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
210 215 220
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro
225 230 235 240
Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
275 280 285
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
290 295 300
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
305 310 315 320
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
325 330 335
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
340 345 350
Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys Gln Glu Glu Met Thr Lys
355 360 365
Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
370 375 380
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
385 390 395 400
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
405 410 415
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
420 425 430
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
435 440 445
Leu Ser Leu Ser Leu Gly
450
<210> 176
<211> 207
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 176
Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Thr Ala
1 5 10 15
Ile Ile Ser Cys Arg Thr Ser Gln Tyr Gly Ser Leu Ala Trp Tyr Gln
20 25 30
Gln Arg Pro Gly Gln Ala Pro Arg Leu Val Ile Tyr Ser Gly Ser Thr
35 40 45
Arg Ala Ala Gly Ile Pro Asp Arg Phe Ser Gly Ser Arg Trp Gly Pro
50 55 60
Asp Tyr Asn Leu Thr Ile Ser Asn Leu Glu Ser Gly Asp Phe Gly Val
65 70 75 80
Tyr Tyr Cys Gln Gln Tyr Glu Phe Phe Gly Gln Gly Thr Lys Val Gln
85 90 95
Val Asp Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro
100 105 110
Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu
115 120 125
Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp
130 135 140
Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp
145 150 155 160
Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys
165 170 175
Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln
180 185 190
Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
195 200 205
<210> 177
<211> 1014
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 177
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacaacaacg ccaacaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaagggcc agcccaaggc cgcccccgac 360
atccagatga cccagagccc cagcagcctg tctgccagcg tgggcgacag agtgaccatc 420
acctgtcagg ccagccagaa catctacgtg tggctgaact ggtatcagca gaagcccggc 480
aaggccccca agctgctgat ctacaaggcc agcaacctgc acaccggcgt gcccagcaga 540
ttttctggca gcggctccgg caccgacttc accctgacaa tcagctccct gcagcccgag 600
gacattgcca cctactactg ccagcagggc cagacctacc cctacacctt tggccagggc 660
accaagctgg aaatcaagac caagggcccc agccgtacgg tggccgctcc cagcgtgttc 720
atcttcccac ctagcgacga gcagctgaag tccggcacag cctctgtcgt gtgcctgctg 780
aacaacttct acccccgcga ggccaaagtg cagtggaagg tggacaacgc cctgcagagc 840
ggcaacagcc aggaaagcgt gaccgagcag gacagcaagg actccaccta cagcctgagc 900
agcaccctga cactgagcaa ggccgactac gagaagcaca aggtgtacgc ctgcgaagtg 960
acccaccagg gcctgtctag ccccgtgacc aagagcttca accggggcga gtgt 1014
<210> 178
<211> 1725
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 178
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
agccaggtgc agctggtgga atctggcggc ggagtggtgc agcctggcag aagcctgaga 420
ctgagctgtg ccgccagcgg cttcaccttc accaaggcct ggatgcactg ggtgcgccag 480
gcccctggaa agcagctgga atgggtggcc cagatcaagg acaagagcaa cagctacgcc 540
acctactacg ccgacagcgt gaagggccgg ttcaccatca gccgggacga cagcaagaac 600
accctgtacc tgcagatgaa cagcctgcgg gccgaggaca ccgccgtgta ctactgtcgg 660
ggcgtgtact atgccctgag ccccttcgat tactggggcc agggaaccct cgtgaccgtg 720
tctagtcgga ccgccagcac aaagggcccc agcgtgttcc ctctggcccc tagcagcaag 780
agcacatctg gcggaacagc cgccctgggc tgcctcgtga aggactactt tcccgagccc 840
gtgaccgtgt cctggaattc tggcgccctg accagcggcg tgcacacctt tccagctgtg 900
ctgcagtcca gcggcctgta cagcctgagc agcgtcgtga cagtgcccag cagctctctg 960
ggcacccaga cctacatctg caacgtgaac cacaagccca gcaacaccaa ggtggacaag 1020
aaggtggaac ccaagagctg cgacaagacc cacacctgtc ccccttgtcc tgcccccgaa 1080
gccgccggag gcccttccgt gttcctgttc cccccaaagc ccaaggacac cctgatgatc 1140
agccggaccc ccgaagtgac ctgcgtggtg gtggatgtgt cccacgagga ccctgaagtg 1200
aagttcaatt ggtacgtgga cggcgtggaa gtgcacaacg ccaagaccaa gccaagagag 1260
gaacagtaca acagcaccta ccgggtggtg tccgtgctga ccgtgctgca ccaggactgg 1320
ctgaacggca aagagtacaa gtgcaaggtg tccaacaagg ccctggccgc ccccatcgag 1380
aaaaccatca gcaaggccaa gggccagccc cgcgaacccc aggtgtgcac actgccccca 1440
agcagggacg agctgaccaa gaaccaggtg tccctgagct gtgccgtgaa aggcttctac 1500
ccctccgata tcgccgtgga atgggagagc aacggccagc ccgagaacaa ctacaagacc 1560
accccccctg tgctggacag cgacggctca ttcttcctgg tgtccaagct gacagtggac 1620
aagtcccggt ggcagcaggg caacgtgttc agctgctccg tgatgcacga ggccctgcac 1680
aaccactaca cccagaagtc cctgagcctg agccccggct agtga 1725
<210> 179
<211> 1362
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 179
caagtgcggc tgtctcagtc tggcggccag atgaagaaac ccggcgacag catgcggatc 60
agctgcagag ccagcggcta cgagttcatc aactgcccca tcaactggat cagactggcc 120
cctggcaagc ggcctgagtg gatgggatgg atgaagccca gacacggggc cgtgtcctac 180
gccagacagc tgcagggcag agtgaccatg acccgggaca tgtacagcga gacagccttc 240
ctggaactgc ggagcctgac cagcgacgat accgccgtgt acttctgcac ccggggcaag 300
tactgcaccg ccagagacta ctacaactgg gacttcgagc actggggcca gggcacacct 360
gtgacagtgt ctagcgcttc gaccaagggc cccagcgtgt tccctctggc ccctagcagc 420
aagagcacat ctggcggaac agccgccctg ggctgcctcg tgaaggacta ctttcccgag 480
cccgtgaccg tgtcctggaa ttctggcgcc ctgaccagcg gcgtgcacac ctttccagct 540
gtgctgcagt ccagcggcct gtacagcctg agcagcgtcg tgacagtgcc cagcagctct 600
ctgggcaccc agacctacat ctgcaacgtg aaccacaagc ccagcaacac caaggtggac 660
aagaaggtgg aacccaagag ctgcgacaag acccacacct gtcccccttg tcctgccccc 720
gaagccgccg gaggcccttc cgtgttcctg ttccccccaa agcccaagga caccctgatg 780
atcagccgga cccccgaagt gacctgcgtg gtggtggatg tgtcccacga ggaccctgaa 840
gtgaagttca attggtacgt ggacggcgtg gaagtgcaca acgccaagac caagccaaga 900
gaggaacagt acaacagcac ctaccgggtg gtgtccgtgc tgaccgtgct gcaccaggac 960
tggctgaacg gcaaagagta caagtgcaag gtgtccaaca aggccctggc cgcccccatc 1020
gagaaaacca tcagcaaggc caagggccag ccccgcgaac cccaggtgta cacactgccc 1080
ccatgcaggg acgagctgac caagaaccag gtgtccctgt ggtgtctggt gaaaggcttc 1140
tacccctccg atatcgccgt ggaatgggag agcaacggcc agcccgagaa caactacaag 1200
accacccccc ctgtgctgga cagcgacggc tcattcttcc tgtactccaa gctgacagtg 1260
gacaagtccc ggtggcagca gggcaacgtg ttcagctgct ccgtgatgca cgaggccctg 1320
cacaaccact acacccagaa gtccctgagc ctgagccccg gc 1362
<210> 180
<211> 624
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 180
agcctgacac agagccctgg caccctgtca ctgagcccag gcgagacagc catcatcagc 60
tgccggacaa gccagtacgg cagcctggcc tggtatcagc agaggcctgg acaggccccc 120
agactcgtga tctacagcgg cagcacaaga gccgccggaa tccccgatag attcagcggc 180
tccagatggg gacccgacta caacctgacc atcagcaacc tggaaagcgg cgacttcggc 240
gtgtactact gccagcagta cgagttcttc ggccagggca ccaaggtgca ggtggacatc 300
aagcgtacgg tggccgctcc cagcgtgttc atcttcccac ctagcgacga gcagctgaag 360
tccggcacag cctctgtcgt gtgcctgctg aacaacttct acccccgcga ggccaaagtg 420
cagtggaagg tggacaacgc cctgcagagc ggcaacagcc aggaaagcgt gaccgagcag 480
gacagcaagg actccaccta cagcctgagc agcaccctga cactgagcaa ggccgactac 540
gagaagcaca aggtgtacgc ctgcgaagtg acccaccagg gcctgtctag ccccgtgacc 600
aagagcttca accggggcga gtgt 624
<210> 181
<211> 1014
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 181
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacaacaacg ccaacaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaagggcc agcccaaggc cgcccccgac 360
atccagatga cccagagccc cagcagcctg tctgccagcg tgggcgacag agtgaccatc 420
acctgtcagg ccagccagaa catctacgtg tggctgaact ggtatcagca gaagcccggc 480
aaggccccca agctgctgat ctacaaggcc agcaacctgc acaccggcgt gcccagcaga 540
ttttctggca gcggctccgg caccgacttc accctgacaa tcagctccct gcagcccgag 600
gacattgcca cctactactg ccagcagggc cagacctacc cctacacctt tggccagggc 660
accaagctgg aaatcaagac caagggcccc agccgtacgg tggccgctcc cagcgtgttc 720
atcttcccac ctagcgacga gcagctgaag tccggcacag cctctgtcgt gtgcctgctg 780
aacaacttct acccccgcga ggccaaagtg cagtggaagg tggacaacgc cctgcagagc 840
ggcaacagcc aggaaagcgt gaccgagcag gacagcaagg actccaccta cagcctgagc 900
agcaccctga cactgagcaa ggccgactac gagaagcaca aggtgtacgc ctgcgaagtg 960
acccaccagg gcctgtctag ccccgtgacc aagagcttca accggggcga gtgt 1014
<210> 182
<211> 1719
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 182
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
agccaggtgc agctggtgga atctggcggc ggagtggtgc agcctggcag aagcctgaga 420
ctgagctgtg ccgccagcgg cttcaccttc accaaggcct ggatgcactg ggtgcgccag 480
gcccctggaa agcagctgga atgggtggcc cagatcaagg acaagagcaa cagctacgcc 540
acctactacg ccgacagcgt gaagggccgg ttcaccatca gccgggacga cagcaagaac 600
accctgtacc tgcagatgaa cagcctgcgg gccgaggaca ccgccgtgta ctactgtcgg 660
ggcgtgtact atgccctgag ccccttcgat tactggggcc agggaaccct cgtgaccgtg 720
tctagtcgga ccgccagcac aaagggcccc agcgtgttcc ctctggcccc tagcagcaag 780
agcacatctg gcggaacagc cgccctgggc tgcctcgtga aggactactt tcccgagccc 840
gtgaccgtgt cctggaattc tggcgccctg accagcggcg tgcacacctt tccagctgtg 900
ctgcagtcca gcggcctgta cagcctgagc agcgtcgtga cagtgcccag cagctctctg 960
ggcacccaga cctacatctg caacgtgaac cacaagccca gcaacaccaa ggtggacaag 1020
aaggtggaac ccaagagctg cgacaagacc cacacctgtc ccccttgtcc tgcccccgaa 1080
ctgctgggag gcccttccgt gttcctgttc cccccaaagc ccaaggacac cctgatgatc 1140
agccggaccc ccgaagtgac ctgcgtggtg gtggatgtgt cccacgagga ccctgaagtg 1200
aagttcaatt ggtacgtgga cggcgtggaa gtgcacaacg ccaagaccaa gccaagagag 1260
gaacagtaca acaatgcctc ccgggtggtg tccgtgctga ccgtgctgca ccaggactgg 1320
ctgaacggca aagagtacaa gtgcaaggtg tccaacaagg ccctgcctgc ccccatcgag 1380
aaaaccatca gcaaggccaa gggccagccc cgcgaacccc aggtgtgcac actgccccca 1440
agcagggacg agctgaccaa gaaccaggtg tccctgagct gtgccgtgaa aggcttctac 1500
ccctccgata tcgccgtgga atgggagagc aacggccagc ccgagaacaa ctacaagacc 1560
accccccctg tgctggacag cgacggctca ttcttcctgg tgtccaagct gacagtggac 1620
aagtcccggt ggcagcaggg caacgtgttc agctgctccg tgatgcacga ggccctgcac 1680
aaccactaca cccagaagtc cctgagcctg agccccggc 1719
<210> 183
<211> 1362
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 183
caagtgcggc tgtctcagtc tggcggccag atgaagaaac ccggcgacag catgcggatc 60
agctgcagag ccagcggcta cgagttcatc aactgcccca tcaactggat cagactggcc 120
cctggcaagc ggcctgagtg gatgggatgg atgaagccca gacacggggc cgtgtcctac 180
gccagacagc tgcagggcag agtgaccatg acccgggaca tgtacagcga gacagccttc 240
ctggaactgc ggagcctgac cagcgacgat accgccgtgt acttctgcac ccggggcaag 300
tactgcaccg ccagagacta ctacaactgg gacttcgagc actggggcca gggcacacct 360
gtgacagtgt ctagcgcttc gaccaagggc ccatcggtct tccccctggc accctcctcc 420
aagagcacct ctgggggcac agcggccctg ggctgcctgg tcaaggacta cttccccgaa 480
ccggtgacgg tgtcgtggaa ctcaggcgcc ctgaccagcg gcgtgcacac cttcccggct 540
gtcctacagt cctcaggact ctactccctc agcagcgtgg tgaccgtgcc ctccagcagc 600
ttgggcaccc agacctacat ctgcaacgtg aatcacaagc ccagcaacac caaggtggac 660
aagaaagttg agcccaaatc ttgtgacaaa actcacacat gcccaccgtg cccagcacct 720
gaactcctgg ggggaccgtc agtcttcctc ttccccccaa aacccaagga caccctcatg 780
atctcccgga cccctgaggt cacatgcgtg gtggtggacg tgagccacga agaccctgag 840
gtcaagttca actggtatgt tgacggcgtg gaggtgcata atgccaagac aaagccgcgg 900
gaggagcagt acaacaatgc ctcccgtgtg gtcagcgtcc tcaccgtcct gcaccaggac 960
tggctgaatg gcaaggagta caagtgcaag gtctccaaca aagccctccc agcccccatc 1020
gagaaaacca tctccaaagc caaagggcag ccccgagaac cacaggtgta caccctgccc 1080
ccatgccggg atgagctgac caagaatcaa gtcagcctgt ggtgcctggt aaaaggcttc 1140
tatcccagcg acatcgccgt ggagtgggag agcaatgggc agccggagaa caactacaag 1200
accacgcctc ccgtgctgga ctccgacggc tccttcttcc tctattcaaa actcaccgtg 1260
gacaagagca ggtggcagca ggggaacgtc ttctcatgct ccgtgctgca tgaggctctg 1320
cacagccact acacgcagaa gagcctctcc ctgtctccgg gt 1362
<210> 184
<211> 624
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 184
agcctgacac agagccctgg caccctgtca ctgagcccag gcgagacagc catcatcagc 60
tgccggacaa gccagtacgg cagcctggcc tggtatcagc agaggcctgg acaggccccc 120
agactcgtga tctacagcgg cagcacaaga gccgccggaa tccccgatag attcagcggc 180
tccagatggg gacccgacta caacctgacc atcagcaacc tggaaagcgg cgacttcggc 240
gtgtactact gccagcagta cgagttcttc ggccagggca ccaaggtgca ggtggacatc 300
aagcgtacgg tggccgctcc cagcgtgttc atcttcccac ctagcgacga gcagctgaag 360
tccggcacag cctctgtcgt gtgcctgctg aacaacttct acccccgcga ggccaaagtg 420
cagtggaagg tggacaacgc cctgcagagc ggcaacagcc aggaaagcgt gaccgagcag 480
gacagcaagg actccaccta cagcctgagc agcaccctga cactgagcaa ggccgactac 540
gagaagcaca aggtgtacgc ctgcgaagtg acccaccagg gcctgtctag ccccgtgacc 600
aagagcttca accggggcga gtgt 624
<210> 185
<211> 1014
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 185
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacaacaacg ccaacaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaagggcc agcccaaggc cgcccccgac 360
atccagatga cccagagccc cagcagcctg tctgccagcg tgggcgacag agtgaccatc 420
acctgtcagg ccagccagaa catctacgtg tggctgaact ggtatcagca gaagcccggc 480
aaggccccca agctgctgat ctacaaggcc agcaacctgc acaccggcgt gcccagcaga 540
ttttctggca gcggctccgg caccgacttc accctgacaa tcagctccct gcagcccgag 600
gacattgcca cctactactg ccagcagggc cagacctacc cctacacctt tggccagggc 660
accaagctgg aaatcaagac caagggcccc agccgtacgg tggccgctcc cagcgtgttc 720
atcttcccac ctagcgacga gcagctgaag tccggcacag cctctgtcgt gtgcctgctg 780
aacaacttct acccccgcga ggccaaagtg cagtggaagg tggacaacgc cctgcagagc 840
ggcaacagcc aggaaagcgt gaccgagcag gacagcaagg actccaccta cagcctgagc 900
agcaccctga cactgagcaa ggccgactac gagaagcaca aggtgtacgc ctgcgaagtg 960
acccaccagg gcctgtctag ccccgtgacc aagagcttca accggggcga gtgt 1014
<210> 186
<211> 1710
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 186
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
agccaggtgc agctggtgga atctggcggc ggagtggtgc agcctggcag aagcctgaga 420
ctgagctgtg ccgccagcgg cttcaccttc accaaggcct ggatgcactg ggtgcgccag 480
gcccctggaa agcagctgga atgggtggcc cagatcaagg acaagagcaa cagctacgcc 540
acctactacg ccgacagcgt gaagggccgg ttcaccatca gccgggacga cagcaagaac 600
accctgtacc tgcagatgaa cagcctgcgg gccgaggaca ccgccgtgta ctactgtcgg 660
ggcgtgtact atgccctgag ccccttcgat tactggggcc agggaaccct cgtgaccgtg 720
tctagtcgga ccgccagcac aaagggccca tcggtgttcc ctctggcccc ttgcagcaga 780
agcaccagcg aatctacagc cgccctgggc tgcctcgtga aggactactt tcccgagccc 840
gtgaccgtgt cctggaactc tggcgctctg acaagcggcg tgcacacctt tccagccgtg 900
ctccagagca gcggcctgta ctctctgagc agcgtcgtga cagtgcccag cagcagcctg 960
ggcaccaaga cctacacctg taacgtggac cacaagccca gcaacaccaa ggtggacaag 1020
cgggtggaat ctaagtacgg ccctccctgc cctccttgcc cagcccctga agctgccggc 1080
ggaccctccg tgttcctgtt ccccccaaag cccaaggaca ccctgatgat cagccggacc 1140
cccgaagtga cctgcgtggt ggtggatgtg tcccaggaag atcccgaggt gcagttcaat 1200
tggtacgtgg acggcgtgga agtgcacaac gccaagacca agcccagaga ggaacagttc 1260
aacagcacct accgggtggt gtccgtgctg accgtgctgc accaggactg gctgaacggc 1320
aaagagtaca agtgcaaggt gtccaacaag ggcctgccca gctccatcga gaaaaccatc 1380
agcaaggcca agggccagcc ccgcgagcct caagtgtgta ccctgccccc tagccaggaa 1440
gagatgacca agaaccaggt gtccctgagc tgtgccgtga aaggcttcta ccccagcgac 1500
attgccgtgg aatgggagag caacggccag cccgagaaca actacaagac caccccccct 1560
gtgctggaca gcgacggctc attcttcctg gtgtccaagc tgaccgtgga caagagccgg 1620
tggcaggaag gcaacgtgtt cagctgctcc gtgatgcacg aggccctgca caaccactac 1680
acccagaagt ccctgtctct gtccctgggc 1710
<210> 187
<211> 1353
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 187
caagtgcggc tgtctcagtc tggcggccag atgaagaaac ccggcgacag catgcggatc 60
agctgcagag ccagcggcta cgagttcatc aactgcccca tcaactggat cagactggcc 120
cctggcaagc ggcctgagtg gatgggatgg atgaagccca gacacggggc cgtgtcctac 180
gccagacagc tgcagggcag agtgaccatg acccgggaca tgtacagcga gacagccttc 240
ctggaactgc ggagcctgac cagcgacgat accgccgtgt acttctgcac ccggggcaag 300
tactgcaccg ccagagacta ctacaactgg gacttcgagc actggggcca gggcacacct 360
gtgacagtgt ctagcgcttc gaccaagggc ccatcggtgt tccctctggc cccttgcagc 420
agaagcacca gcgaatctac agccgccctg ggctgcctcg tgaaggacta ctttcccgag 480
cccgtgaccg tgtcctggaa ctctggcgct ctgacaagcg gcgtgcacac ctttccagcc 540
gtgctccaga gcagcggcct gtactctctg agcagcgtcg tgacagtgcc cagcagcagc 600
ctgggcacca agacctacac ctgtaacgtg gaccacaagc ccagcaacac caaggtggac 660
aagcgggtgg aatctaagta cggccctccc tgccctcctt gcccagcccc tgaagctgcc 720
ggcggaccct ccgtgttcct gttcccccca aagcccaagg acaccctgat gatcagccgg 780
acccccgaag tgacctgcgt ggtggtggat gtgtcccagg aagatcccga ggtgcagttc 840
aattggtacg tggacggcgt ggaagtgcac aacgccaaga ccaagcccag agaggaacag 900
ttcaacagca cctaccgggt ggtgtccgtg ctgaccgtgc tgcaccagga ctggctgaac 960
ggcaaagagt acaagtgcaa ggtgtccaac aagggcctgc ccagctccat cgagaaaacc 1020
atcagcaagg ccaagggcca gccccgcgag cctcaagtgt ataccctgcc cccttgccag 1080
gaagagatga ccaagaacca ggtgtccctg tggtgtctcg tgaaaggctt ctaccccagc 1140
gacattgccg tggaatggga gagcaacggc cagcccgaga acaactacaa gaccaccccc 1200
cctgtgctgg acagcgacgg ctcattcttc ctgtactcca agctgaccgt ggacaagagc 1260
cggtggcagg aaggcaacgt gttcagctgc tccgtgatgc acgaggccct gcacaaccac 1320
tacacccaga agtccctgtc tctgtccctg ggc 1353
<210> 188
<211> 624
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 188
agcctgacac agagccctgg caccctgtca ctgagcccag gcgagacagc catcatcagc 60
tgccggacaa gccagtacgg cagcctggcc tggtatcagc agaggcctgg acaggccccc 120
agactcgtga tctacagcgg cagcacaaga gccgccggaa tccccgatag attcagcggc 180
tccagatggg gacccgacta caacctgacc atcagcaacc tggaaagcgg cgacttcggc 240
gtgtactact gccagcagta cgagttcttc ggccagggca ccaaggtgca ggtggacatc 300
aagcgtacgg tggccgctcc cagcgtgttc atcttcccac ctagcgacga gcagctgaag 360
tccggcacag cctctgtcgt gtgcctgctg aacaacttct acccccgcga ggccaaagtg 420
cagtggaagg tggacaacgc cctgcagagc ggcaacagcc aggaaagcgt gaccgagcag 480
gacagcaagg actccaccta cagcctgagc agcaccctga cactgagcaa ggccgactac 540
gagaagcaca aggtgtacgc ctgcgaagtg acccaccagg gcctgtctag ccccgtgacc 600
aagagcttca accggggcga gtgt 624
<210> 189
<211> 1014
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 189
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg caccagaacg cccagaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaagggcc agcccaaggc cgcccccgac 360
atccagatga cccagagccc cagcagcctg tctgccagcg tgggcgacag agtgaccatc 420
acctgtcagg ccagccagaa catctacgtg tggctgaact ggtatcagca gaagcccggc 480
aaggccccca agctgctgat ctacaaggcc agcaacctgc acaccggcgt gcccagcaga 540
ttttctggca gcggctccgg caccgacttc accctgacaa tcagctccct gcagcccgag 600
gacattgcca cctactactg ccagcagggc cagacctacc cctacacctt tggccagggc 660
accaagctgg aaatcaagac caagggcccc agccgtacgg tggccgctcc cagcgtgttc 720
atcttcccac ctagcgacga gcagctgaag tccggcacag cctctgtcgt gtgcctgctg 780
aacaacttct acccccgcga ggccaaagtg cagtggaagg tggacaacgc cctgcagagc 840
ggcaacagcc aggaaagcgt gaccgagcag gacagcaagg actccaccta cagcctgagc 900
agcaccctga cactgagcaa ggccgactac gagaagcaca aggtgtacgc ctgcgaagtg 960
acccaccagg gcctgtctag ccccgtgacc aagagcttca accggggcga gtgt 1014
<210> 190
<211> 1710
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 190
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
agccaggtgc agctggtgga atctggcggc ggagtggtgc agcctggcag aagcctgaga 420
ctgagctgtg ccgccagcgg cttcaccttc accaaggcct ggatgcactg ggtgcgccag 480
gcccctggaa agcagctgga atgggtggcc cagatcaagg acaagagcaa cagctacgcc 540
acctactacg ccgacagcgt gaagggccgg ttcaccatca gccgggacga cagcaagaac 600
accctgtacc tgcagatgaa cagcctgcgg gccgaggaca ccgccgtgta ctactgtcgg 660
ggcgtgtact atgccctgag ccccttcgat tactggggcc agggaaccct cgtgaccgtg 720
tctagtcgga ccgccagcac aaagggccca tcggtgttcc ctctggcccc ttgcagcaga 780
agcaccagcg aatctacagc cgccctgggc tgcctcgtga aggactactt tcccgagccc 840
gtgaccgtgt cctggaactc tggcgctctg acaagcggcg tgcacacctt tccagccgtg 900
ctccagagca gcggcctgta ctctctgagc agcgtcgtga cagtgcccag cagcagcctg 960
ggcaccaaga cctacacctg taacgtggac cacaagccca gcaacaccaa ggtggacaag 1020
cgggtggaat ctaagtacgg ccctccctgc cctccttgcc cagcccctga agctgccggc 1080
ggaccctccg tgttcctgtt ccccccaaag cccaaggaca ccctgatgat cagccggacc 1140
cccgaagtga cctgcgtggt ggtggatgtg tcccaggaag atcccgaggt gcagttcaat 1200
tggtacgtgg acggcgtgga agtgcacaac gccaagacca agcccagaga ggaacagttc 1260
aacagcacct accgggtggt gtccgtgctg accgtgctgc accaggactg gctgaacggc 1320
aaagagtaca agtgcaaggt gtccaacaag ggcctgccca gctccatcga gaaaaccatc 1380
agcaaggcca agggccagcc ccgcgagcct caagtgtgta ccctgccccc tagccaggaa 1440
gagatgacca agaaccaggt gtccctgagc tgtgccgtga aaggcttcta ccccagcgac 1500
attgccgtgg aatgggagag caacggccag cccgagaaca actacaagac caccccccct 1560
gtgctggaca gcgacggctc attcttcctg gtgtccaagc tgaccgtgga caagagccgg 1620
tggcaggaag gcaacgtgtt cagctgctcc gtgatgcacg aggccctgca caaccactac 1680
acccagaagt ccctgtctct gtccctgggc 1710
<210> 191
<211> 1353
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 191
caagtgcggc tgtctcagtc tggcggccag atgaagaaac ccggcgacag catgcggatc 60
agctgcagag ccagcggcta cgagttcatc aactgcccca tcaactggat cagactggcc 120
cctggcaagc ggcctgagtg gatgggatgg atgaagccca gacacggggc cgtgtcctac 180
gccagacagc tgcagggcag agtgaccatg acccgggaca tgtacagcga gacagccttc 240
ctggaactgc ggagcctgac cagcgacgat accgccgtgt acttctgcac ccggggcaag 300
tactgcaccg ccagagacta ctacaactgg gacttcgagc actggggcca gggcacacct 360
gtgacagtgt ctagcgcttc gaccaagggc ccatcggtgt tccctctggc cccttgcagc 420
agaagcacca gcgaatctac agccgccctg ggctgcctcg tgaaggacta ctttcccgag 480
cccgtgaccg tgtcctggaa ctctggcgct ctgacaagcg gcgtgcacac ctttccagcc 540
gtgctccaga gcagcggcct gtactctctg agcagcgtcg tgacagtgcc cagcagcagc 600
ctgggcacca agacctacac ctgtaacgtg gaccacaagc ccagcaacac caaggtggac 660
aagcgggtgg aatctaagta cggccctccc tgccctcctt gcccagcccc tgaagctgcc 720
ggcggaccct ccgtgttcct gttcccccca aagcccaagg acaccctgat gatcagccgg 780
acccccgaag tgacctgcgt ggtggtggat gtgtcccagg aagatcccga ggtgcagttc 840
aattggtacg tggacggcgt ggaagtgcac aacgccaaga ccaagcccag agaggaacag 900
ttcaacagca cctaccgggt ggtgtccgtg ctgaccgtgc tgcaccagga ctggctgaac 960
ggcaaagagt acaagtgcaa ggtgtccaac aagggcctgc ccagctccat cgagaaaacc 1020
atcagcaagg ccaagggcca gccccgcgag cctcaagtgt ataccctgcc cccttgccag 1080
gaagagatga ccaagaacca ggtgtccctg tggtgtctcg tgaaaggctt ctaccccagc 1140
gacattgccg tggaatggga gagcaacggc cagcccgaga acaactacaa gaccaccccc 1200
cctgtgctgg acagcgacgg ctcattcttc ctgtactcca agctgaccgt ggacaagagc 1260
cggtggcagg aaggcaacgt gttcagctgc tccgtgatgc acgaggccct gcacaaccac 1320
tacacccaga agtccctgtc tctgtccctg ggc 1353
<210> 192
<211> 624
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 192
agcctgacac agagccctgg caccctgtca ctgagcccag gcgagacagc catcatcagc 60
tgccggacaa gccagtacgg cagcctggcc tggtatcagc agaggcctgg acaggccccc 120
agactcgtga tctacagcgg cagcacaaga gccgccggaa tccccgatag attcagcggc 180
tccagatggg gacccgacta caacctgacc atcagcaacc tggaaagcgg cgacttcggc 240
gtgtactact gccagcagta cgagttcttc ggccagggca ccaaggtgca ggtggacatc 300
aagcgtacgg tggccgctcc cagcgtgttc atcttcccac ctagcgacga gcagctgaag 360
tccggcacag cctctgtcgt gtgcctgctg aacaacttct acccccgcga ggccaaagtg 420
cagtggaagg tggacaacgc cctgcagagc ggcaacagcc aggaaagcgt gaccgagcag 480
gacagcaagg actccaccta cagcctgagc agcaccctga cactgagcaa ggccgactac 540
gagaagcaca aggtgtacgc ctgcgaagtg acccaccagg gcctgtctag ccccgtgacc 600
aagagcttca accggggcga gtgt 624
<210> 193
<211> 1008
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 193
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg caccagaacg cccagaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaaggaca aaacccatac cgacatccag 360
atgacccaga gccccagcag cctgtctgcc agcgtgggcg acagagtgac catcacctgt 420
caggccagcc agaacatcta cgtgtggctg aactggtatc agcagaagcc cggcaaggcc 480
cccaagctgc tgatctacaa ggccagcaac ctgcacaccg gcgtgcccag cagattttct 540
ggcagcggct ccggcaccga cttcaccctg acaatcagct ccctgcagcc cgaggacatt 600
gccacctact actgccagca gggccagacc tacccctaca cctttggcca gggcaccaag 660
ctggaaatca aggataagac ccacacccgt acggtggccg ctcccagcgt gttcatcttc 720
ccacctagcg acgagcagct gaagtccggc acagcctctg tcgtgtgcct gctgaacaac 780
ttctaccccc gcgaggccaa agtgcagtgg aaggtggaca acgccctgca gagcggcaac 840
agccaggaaa gcgtgaccga gcaggacagc aaggactcca cctacagcct gagcagcacc 900
ctgacactga gcaaggccga ctacgagaag cacaaggtgt acgcctgcga agtgacccac 960
cagggcctgt ctagccccgt gaccaagagc ttcaaccggg gcgagtgt 1008
<210> 194
<211> 1731
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 194
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
gacaaaaccc atacccaggt gcagctggtg gaatctggcg gcggagtggt gcagcctggc 420
agaagcctga gactgagctg tgccgccagc ggcttcacct tcaccaaggc ctggatgcac 480
tgggtgcgcc aggcccctgg aaagcagctg gaatgggtgg cccagatcaa ggacaagagc 540
aacagctacg ccacctacta cgccgacagc gtgaagggcc ggttcaccat cagccgggac 600
gacagcaaga acaccctgta cctgcagatg aacagcctgc gggccgagga caccgccgtg 660
tactactgtc ggggcgtgta ctatgccctg agccccttcg attactgggg ccagggaacc 720
ctcgtgaccg tgtctagtga taagacccac accgccagca caaagggccc atcggtgttc 780
cctctggccc cttgcagcag aagcaccagc gaatctacag ccgccctggg ctgcctcgtg 840
aaggactact ttcccgagcc cgtgaccgtg tcctggaact ctggcgctct gacaagcggc 900
gtgcacacct ttccagccgt gctccagagc agcggcctgt actctctgag cagcgtcgtg 960
acagtgccca gcagcagcct gggcaccaag acctacacct gtaacgtgga ccacaagccc 1020
agcaacacca aggtggacaa gcgggtggaa tctaagtacg gccctccctg ccctccttgc 1080
ccagcccctg aagctgccgg cggaccctcc gtgttcctgt tccccccaaa gcccaaggac 1140
accctgatga tcagccggac ccccgaagtg acctgcgtgg tggtggatgt gtcccaggaa 1200
gatcccgagg tgcagttcaa ttggtacgtg gacggcgtgg aagtgcacaa cgccaagacc 1260
aagcccagag aggaacagtt caacagcacc taccgggtgg tgtccgtgct gaccgtgctg 1320
caccaggact ggctgaacgg caaagagtac aagtgcaagg tgtccaacaa gggcctgccc 1380
agctccatcg agaaaaccat cagcaaggcc aagggccagc cccgcgagcc tcaagtgtgt 1440
accctgcccc ctagccagga agagatgacc aagaaccagg tgtccctgag ctgtgccgtg 1500
aaaggcttct accccagcga cattgccgtg gaatgggaga gcaacggcca gcccgagaac 1560
aactacaaga ccaccccccc tgtgctggac agcgacggct cattcttcct ggtgtccaag 1620
ctgaccgtgg acaagagccg gtggcaggaa ggcaacgtgt tcagctgctc cgtgatgcac 1680
gaggccctgc acaaccacta cacccagaag tccctgtctc tgtccctggg c 1731
<210> 195
<211> 1353
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 195
caagtgcggc tgtctcagtc tggcggccag atgaagaaac ccggcgacag catgcggatc 60
agctgcagag ccagcggcta cgagttcatc aactgcccca tcaactggat cagactggcc 120
cctggcaagc ggcctgagtg gatgggatgg atgaagccca gacacggggc cgtgtcctac 180
gccagacagc tgcagggcag agtgaccatg acccgggaca tgtacagcga gacagccttc 240
ctggaactgc ggagcctgac cagcgacgat accgccgtgt acttctgcac ccggggcaag 300
tactgcaccg ccagagacta ctacaactgg gacttcgagc actggggcca gggcacacct 360
gtgacagtgt ctagcgcttc gaccaagggc ccatcggtgt tccctctggc cccttgcagc 420
agaagcacca gcgaatctac agccgccctg ggctgcctcg tgaaggacta ctttcccgag 480
cccgtgaccg tgtcctggaa ctctggcgct ctgacaagcg gcgtgcacac ctttccagcc 540
gtgctccaga gcagcggcct gtactctctg agcagcgtcg tgacagtgcc cagcagcagc 600
ctgggcacca agacctacac ctgtaacgtg gaccacaagc ccagcaacac caaggtggac 660
aagcgggtgg aatctaagta cggccctccc tgccctcctt gcccagcccc tgaagctgcc 720
ggcggaccct ccgtgttcct gttcccccca aagcccaagg acaccctgat gatcagccgg 780
acccccgaag tgacctgcgt ggtggtggat gtgtcccagg aagatcccga ggtgcagttc 840
aattggtacg tggacggcgt ggaagtgcac aacgccaaga ccaagcccag agaggaacag 900
ttcaacagca cctaccgggt ggtgtccgtg ctgaccgtgc tgcaccagga ctggctgaac 960
ggcaaagagt acaagtgcaa ggtgtccaac aagggcctgc ccagctccat cgagaaaacc 1020
atcagcaagg ccaagggcca gccccgcgag cctcaagtgt ataccctgcc cccttgccag 1080
gaagagatga ccaagaacca ggtgtccctg tggtgtctcg tgaaaggctt ctaccccagc 1140
gacattgccg tggaatggga gagcaacggc cagcccgaga acaactacaa gaccaccccc 1200
cctgtgctgg acagcgacgg ctcattcttc ctgtactcca agctgaccgt ggacaagagc 1260
cggtggcagg aaggcaacgt gttcagctgc tccgtgatgc acgaggccct gcacaaccac 1320
tacacccaga agtccctgtc tctgtccctg ggc 1353
<210> 196
<211> 624
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 196
agcctgacac agagccctgg caccctgtca ctgagcccag gcgagacagc catcatcagc 60
tgccggacaa gccagtacgg cagcctggcc tggtatcagc agaggcctgg acaggccccc 120
agactcgtga tctacagcgg cagcacaaga gccgccggaa tccccgatag attcagcggc 180
tccagatggg gacccgacta caacctgacc atcagcaacc tggaaagcgg cgacttcggc 240
gtgtactact gccagcagta cgagttcttc ggccagggca ccaaggtgca ggtggacatc 300
aagcgtacgg tggccgctcc cagcgtgttc atcttcccac ctagcgacga gcagctgaag 360
tccggcacag cctctgtcgt gtgcctgctg aacaacttct acccccgcga ggccaaagtg 420
cagtggaagg tggacaacgc cctgcagagc ggcaacagcc aggaaagcgt gaccgagcag 480
gacagcaagg actccaccta cagcctgagc agcaccctga cactgagcaa ggccgactac 540
gagaagcaca aggtgtacgc ctgcgaagtg acccaccagg gcctgtctag ccccgtgacc 600
aagagcttca accggggcga gtgt 624
<210> 197
<211> 1008
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 197
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg caccagaacg cccagaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaaggaca aaacccatac cgacatccag 360
atgacccaga gccccagcag cctgtctgcc agcgtgggcg acagagtgac catcacctgt 420
caggccagcc agaacatcta cgtgtggctg aactggtatc agcagaagcc cggcaaggcc 480
cccaagctgc tgatctacaa ggccagcaac ctgcacaccg gcgtgcccag cagattttct 540
ggcagcggct ccggcaccga cttcaccctg acaatcagct ccctgcagcc cgaggacatt 600
gccacctact actgccagca gggccagacc tacccctaca cctttggcca gggcaccaag 660
ctggaaatca aggataagac ccacacccgt acggtggccg ctcccagcgt gttcatcttc 720
ccacctagcg acgagcagct gaagtccggc acagcctctg tcgtgtgcct gctgaacaac 780
ttctaccccc gcgaggccaa agtgcagtgg aaggtggaca acgccctgca gagcggcaac 840
agccaggaaa gcgtgaccga gcaggacagc aaggactcca cctacagcct gagcagcacc 900
ctgacactga gcaaggccga ctacgagaag cacaaggtgt acgcctgcga agtgacccac 960
cagggcctgt ctagccccgt gaccaagagc ttcaaccggg gcgagtgt 1008
<210> 198
<211> 1740
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 198
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
gacaaaaccc atacccaggt gcagctggtg gaatctggcg gcggagtggt gcagcctggc 420
agaagcctga gactgagctg tgccgccagc ggcttcacct tcaccaaggc ctggatgcac 480
tgggtgcgcc aggcccctgg aaagcagctg gaatgggtgg cccagatcaa ggacaagagc 540
aacagctacg ccacctacta cgccgacagc gtgaagggcc ggttcaccat cagccgggac 600
gacagcaaga acaccctgta cctgcagatg aacagcctgc gggccgagga caccgccgtg 660
tactactgtc ggggcgtgta ctatgccctg agccccttcg attactgggg ccagggaacc 720
ctcgtgaccg tgtctagtga taagacccac accgccagca caaagggccc cagcgtgttc 780
cctctggccc ctagcagcaa gagcacatct ggcggaacag ccgccctggg ctgcctcgtg 840
aaggactact ttcccgagcc cgtgaccgtg tcctggaatt ctggcgccct gaccagcggc 900
gtgcacacct ttccagctgt gctgcagtcc agcggcctgt acagcctgag cagcgtcgtg 960
acagtgccca gcagctctct gggcacccag acctacatct gcaacgtgaa ccacaagccc 1020
agcaacacca aggtggacaa gaaggtggaa cccaagagct gcgacaagac ccacacctgt 1080
cccccttgtc ctgcccccga actgctggga ggcccttccg tgttcctgtt ccccccaaag 1140
cccaaggaca ccctgatgat cagccggacc cccgaagtga cctgcgtggt ggtggatgtg 1200
tcccacgagg accctgaagt gaagttcaat tggtacgtgg acggcgtgga agtgcacaac 1260
gccaagacca agccaagaga ggaacagtac aacaatgcct cccgggtggt gtccgtgctg 1320
accgtgctgc accaggactg gctgaacggc aaagagtaca agtgcaaggt gtccaacaag 1380
gccctgcctg cccccatcga gaaaaccatc agcaaggcca agggccagcc ccgcgaaccc 1440
caggtgtgca cactgccccc aagcagggac gagctgacca agaaccaggt gtccctgagc 1500
tgtgccgtga aaggcttcta cccctccgat atcgccgtgg aatgggagag caacggccag 1560
cccgagaaca actacaagac caccccccct gtgctggaca gcgacggctc attcttcctg 1620
gtgtccaagc tgacagtgga caagtcccgg tggcagcagg gcaacgtgtt cagctgctcc 1680
gtgatgcacg aggccctgca caaccactac acccagaagt ccctgagcct gagccccggc 1740
<210> 199
<211> 1362
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 199
caagtgcggc tgtctcagtc tggcggccag atgaagaaac ccggcgacag catgcggatc 60
agctgcagag ccagcggcta cgagttcatc aactgcccca tcaactggat cagactggcc 120
cctggcaagc ggcctgagtg gatgggatgg atgaagccca gacacggggc cgtgtcctac 180
gccagacagc tgcagggcag agtgaccatg acccgggaca tgtacagcga gacagccttc 240
ctggaactgc ggagcctgac cagcgacgat accgccgtgt acttctgcac ccggggcaag 300
tactgcaccg ccagagacta ctacaactgg gacttcgagc actggggcca gggcacacct 360
gtgacagtgt ctagcgcttc gaccaagggc ccatcggtct tccccctggc accctcctcc 420
aagagcacct ctgggggcac agcggccctg ggctgcctgg tcaaggacta cttccccgaa 480
ccggtgacgg tgtcgtggaa ctcaggcgcc ctgaccagcg gcgtgcacac cttcccggct 540
gtcctacagt cctcaggact ctactccctc agcagcgtgg tgaccgtgcc ctccagcagc 600
ttgggcaccc agacctacat ctgcaacgtg aatcacaagc ccagcaacac caaggtggac 660
aagaaagttg agcccaaatc ttgtgacaaa actcacacat gcccaccgtg cccagcacct 720
gaactcctgg ggggaccgtc agtcttcctc ttccccccaa aacccaagga caccctcatg 780
atctcccgga cccctgaggt cacatgcgtg gtggtggacg tgagccacga agaccctgag 840
gtcaagttca actggtatgt tgacggcgtg gaggtgcata atgccaagac aaagccgcgg 900
gaggagcagt acaacaatgc ctcccgtgtg gtcagcgtcc tcaccgtcct gcaccaggac 960
tggctgaatg gcaaggagta caagtgcaag gtctccaaca aagccctccc agcccccatc 1020
gagaaaacca tctccaaagc caaagggcag ccccgagaac cacaggtgta caccctgccc 1080
ccatgccggg atgagctgac caagaatcaa gtcagcctgt ggtgcctggt aaaaggcttc 1140
tatcccagcg acatcgccgt ggagtgggag agcaatgggc agccggagaa caactacaag 1200
accacgcctc ccgtgctgga ctccgacggc tccttcttcc tctattcaaa actcaccgtg 1260
gacaagagca ggtggcagca ggggaacgtc ttctcatgct ccgtgctgca tgaggctctg 1320
cacagccact acacgcagaa gagcctctcc ctgtctccgg gt 1362
<210> 200
<211> 624
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 200
agcctgacac agagccctgg caccctgtca ctgagcccag gcgagacagc catcatcagc 60
tgccggacaa gccagtacgg cagcctggcc tggtatcagc agaggcctgg acaggccccc 120
agactcgtga tctacagcgg cagcacaaga gccgccggaa tccccgatag attcagcggc 180
tccagatggg gacccgacta caacctgacc atcagcaacc tggaaagcgg cgacttcggc 240
gtgtactact gccagcagta cgagttcttc ggccagggca ccaaggtgca ggtggacatc 300
aagcgtacgg tggccgctcc cagcgtgttc atcttcccac ctagcgacga gcagctgaag 360
tccggcacag cctctgtcgt gtgcctgctg aacaacttct acccccgcga ggccaaagtg 420
cagtggaagg tggacaacgc cctgcagagc ggcaacagcc aggaaagcgt gaccgagcag 480
gacagcaagg actccaccta cagcctgagc agcaccctga cactgagcaa ggccgactac 540
gagaagcaca aggtgtacgc ctgcgaagtg acccaccagg gcctgtctag ccccgtgacc 600
aagagcttca accggggcga gtgt 624
<210> 201
<211> 1008
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 201
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacgagaacc tgcagaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaaggaca aaacccatac cgacatccag 360
atgacccaga gccccagcag cctgtctgcc agcgtgggcg acagagtgac catcacctgt 420
caggccagcc agaacatcta cgtgtggctg aactggtatc agcagaagcc cggcaaggcc 480
cccaagctgc tgatctacaa ggccagcaac ctgcacaccg gcgtgcccag cagattttct 540
ggcagcggct ccggcaccga cttcaccctg acaatcagct ccctgcagcc cgaggacatt 600
gccacctact actgccagca gggccagacc tacccctaca cctttggcca gggcaccaag 660
ctggaaatca aggataagac ccacacccgt acggtggccg ctcccagcgt gttcatcttc 720
ccacctagcg acgagcagct gaagtccggc acagcctctg tcgtgtgcct gctgaacaac 780
ttctaccccc gcgaggccaa agtgcagtgg aaggtggaca acgccctgca gagcggcaac 840
agccaggaaa gcgtgaccga gcaggacagc aaggactcca cctacagcct gagcagcacc 900
ctgacactga gcaaggccga ctacgagaag cacaaggtgt acgcctgcga agtgacccac 960
cagggcctgt ctagccccgt gaccaagagc ttcaaccggg gcgagtgt 1008
<210> 202
<211> 1731
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 202
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
gacaaaaccc atacccaggt gcagctggtg gaatctggcg gcggagtggt gcagcctggc 420
agaagcctga gactgagctg tgccgccagc ggcttcacct tcaccaaggc ctggatgcac 480
tgggtgcgcc aggcccctgg aaagcagctg gaatgggtgg cccagatcaa ggacaagagc 540
aacagctacg ccacctacta cgccgacagc gtgaagggcc ggttcaccat cagccgggac 600
gacagcaaga acaccctgta cctgcagatg aacagcctgc gggccgagga caccgccgtg 660
tactactgtc ggggcgtgta ctatgccctg agccccttcg attactgggg ccagggaacc 720
ctcgtgaccg tgtctagtga taagacccac accgccagca caaagggccc atcggtgttc 780
cctctggccc cttgcagcag aagcaccagc gaatctacag ccgccctggg ctgcctcgtg 840
aaggactact ttcccgagcc cgtgaccgtg tcctggaact ctggcgctct gacaagcggc 900
gtgcacacct ttccagccgt gctccagagc agcggcctgt actctctgag cagcgtcgtg 960
acagtgccca gcagcagcct gggcaccaag acctacacct gtaacgtgga ccacaagccc 1020
agcaacacca aggtggacaa gcgggtggaa tctaagtacg gccctccctg ccctccttgc 1080
ccagcccctg aagctgccgg cggaccctcc gtgttcctgt tccccccaaa gcccaaggac 1140
accctgatga tcagccggac ccccgaagtg acctgcgtgg tggtggatgt gtcccaggaa 1200
gatcccgagg tgcagttcaa ttggtacgtg gacggcgtgg aagtgcacaa cgccaagacc 1260
aagcccagag aggaacagtt caacagcacc taccgggtgg tgtccgtgct gaccgtgctg 1320
caccaggact ggctgaacgg caaagagtac aagtgcaagg tgtccaacaa gggcctgccc 1380
agctccatcg agaaaaccat cagcaaggcc aagggccagc cccgcgagcc tcaagtgtgt 1440
accctgcccc ctagccagga agagatgacc aagaaccagg tgtccctgag ctgtgccgtg 1500
aaaggcttct accccagcga cattgccgtg gaatgggaga gcaacggcca gcccgagaac 1560
aactacaaga ccaccccccc tgtgctggac agcgacggct cattcttcct ggtgtccaag 1620
ctgaccgtgg acaagagccg gtggcaggaa ggcaacgtgt tcagctgctc cgtgatgcac 1680
gaggccctgc acaaccacta cacccagaag tccctgtctc tgtccctggg c 1731
<210> 203
<211> 1374
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 203
caagtgcggc tgtctcagtc tggcggccag atgaagaaac ccggcgacag catgcggatc 60
agctgcagag ccagcggcta cgagttcatc aactgcccca tcaactggat cagactggcc 120
cctggcaagc ggcctgagtg gatgggatgg atgaagccca gacacggggc cgtgtcctac 180
gccagacagc tgcagggcag agtgaccatg acccggcagc tgagccagga ccctgatgat 240
ccggattggg gcacagcctt cctggaactg cggagcctga ccagcgacga taccgccgtg 300
tacttctgca cccggggcaa gtactgcacc gccagagact actacaactg ggacttcgag 360
cactggggcc agggcacacc tgtgacagtg tctagcgctt cgaccaaggg cccatcggtg 420
ttccctctgg ccccttgcag cagaagcacc agcgaatcta cagccgccct gggctgcctc 480
gtgaaggact actttcccga gcccgtgacc gtgtcctgga actctggcgc tctgacaagc 540
ggcgtgcaca cctttccagc cgtgctccag agcagcggcc tgtactctct gagcagcgtc 600
gtgacagtgc ccagcagcag cctgggcacc aagacctaca cctgtaacgt ggaccacaag 660
cccagcaaca ccaaggtgga caagcgggtg gaatctaagt acggccctcc ctgccctcct 720
tgcccagccc ctgaagctgc cggcggaccc tccgtgttcc tgttcccccc aaagcccaag 780
gacaccctga tgatcagccg gacccccgaa gtgacctgcg tggtggtgga tgtgtcccag 840
gaagatcccg aggtgcagtt caattggtac gtggacggcg tggaagtgca caacgccaag 900
accaagccca gagaggaaca gttcaacagc acctaccggg tggtgtccgt gctgaccgtg 960
ctgcaccagg actggctgaa cggcaaagag tacaagtgca aggtgtccaa caagggcctg 1020
cccagctcca tcgagaaaac catcagcaag gccaagggcc agccccgcga gcctcaagtg 1080
tataccctgc ccccttgcca ggaagagatg accaagaacc aggtgtccct gtggtgtctc 1140
gtgaaaggct tctaccccag cgacattgcc gtggaatggg agagcaacgg ccagcccgag 1200
aacaactaca agaccacccc ccctgtgctg gacagcgacg gctcattctt cctgtactcc 1260
aagctgaccg tggacaagag ccggtggcag gaaggcaacg tgttcagctg ctccgtgatg 1320
cacgaggccc tgcacaacca ctacacccag aagtccctgt ctctgtccct gggc 1374
<210> 204
<211> 624
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 204
agcctgacac agagccctgg caccctgtca ctgagcccag gcgagacagc catcatcagc 60
tgccggacaa gccagtacgg cagcctggcc tggtatcagc agaggcctgg acaggccccc 120
agactcgtga tctacagcgg cagcacaaga gccgccggaa tccccgatag attcagcggc 180
tccagatggg gacccgacta caacctgacc atcagcaacc tggaaagcgg cgacttcggc 240
gtgtactact gccagcagta cgagttcttc ggccagggca ccaaggtgca ggtggacatc 300
aagcgtacgg tggccgctcc cagcgtgttc atcttcccac ctagcgacga gcagctgaag 360
tccggcacag cctctgtcgt gtgcctgctg aacaacttct acccccgcga ggccaaagtg 420
cagtggaagg tggacaacgc cctgcagagc ggcaacagcc aggaaagcgt gaccgagcag 480
gacagcaagg actccaccta cagcctgagc agcaccctga cactgagcaa ggccgactac 540
gagaagcaca aggtgtacgc ctgcgaagtg acccaccagg gcctgtctag ccccgtgacc 600
aagagcttca accggggcga gtgt 624
<210> 205
<211> 1008
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 205
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacgagaacc tgttcaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaaggaca aaacccatac cgacatccag 360
atgacccaga gccccagcag cctgtctgcc agcgtgggcg acagagtgac catcacctgt 420
caggccagcc agaacatcta cgtgtggctg aactggtatc agcagaagcc cggcaaggcc 480
cccaagctgc tgatctacaa ggccagcaac ctgcacaccg gcgtgcccag cagattttct 540
ggcagcggct ccggcaccga cttcaccctg acaatcagct ccctgcagcc cgaggacatt 600
gccacctact actgccagca gggccagacc tacccctaca cctttggcca gggcaccaag 660
ctggaaatca aggataagac ccacacccgt acggtggccg ctcccagcgt gttcatcttc 720
ccacctagcg acgagcagct gaagtccggc acagcctctg tcgtgtgcct gctgaacaac 780
ttctaccccc gcgaggccaa agtgcagtgg aaggtggaca acgccctgca gagcggcaac 840
agccaggaaa gcgtgaccga gcaggacagc aaggactcca cctacagcct gagcagcacc 900
ctgacactga gcaaggccga ctacgagaag cacaaggtgt acgcctgcga agtgacccac 960
cagggcctgt ctagccccgt gaccaagagc ttcaaccggg gcgagtgt 1008
<210> 206
<211> 1731
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 206
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
gacaaaaccc atacccaggt gcagctggtg gaatctggcg gcggagtggt gcagcctggc 420
agaagcctga gactgagctg tgccgccagc ggcttcacct tcaccaaggc ctggatgcac 480
tgggtgcgcc aggcccctgg aaagcagctg gaatgggtgg cccagatcaa ggacaagagc 540
aacagctacg ccacctacta cgccgacagc gtgaagggcc ggttcaccat cagccgggac 600
gacagcaaga acaccctgta cctgcagatg aacagcctgc gggccgagga caccgccgtg 660
tactactgtc ggggcgtgta ctatgccctg agccccttcg attactgggg ccagggaacc 720
ctcgtgaccg tgtctagtga taagacccac accgccagca caaagggccc atcggtgttc 780
cctctggccc cttgcagcag aagcaccagc gaatctacag ccgccctggg ctgcctcgtg 840
aaggactact ttcccgagcc cgtgaccgtg tcctggaact ctggcgctct gacaagcggc 900
gtgcacacct ttccagccgt gctccagagc agcggcctgt actctctgag cagcgtcgtg 960
acagtgccca gcagcagcct gggcaccaag acctacacct gtaacgtgga ccacaagccc 1020
agcaacacca aggtggacaa gcgggtggaa tctaagtacg gccctccctg ccctccttgc 1080
ccagcccctg aagctgccgg cggaccctcc gtgttcctgt tccccccaaa gcccaaggac 1140
accctgatga tcagccggac ccccgaagtg acctgcgtgg tggtggatgt gtcccaggaa 1200
gatcccgagg tgcagttcaa ttggtacgtg gacggcgtgg aagtgcacaa cgccaagacc 1260
aagcccagag aggaacagtt caacagcacc taccgggtgg tgtccgtgct gaccgtgctg 1320
caccaggact ggctgaacgg caaagagtac aagtgcaagg tgtccaacaa gggcctgccc 1380
agctccatcg agaaaaccat cagcaaggcc aagggccagc cccgcgagcc tcaagtgtgt 1440
accctgcccc ctagccagga agagatgacc aagaaccagg tgtccctgag ctgtgccgtg 1500
aaaggcttct accccagcga cattgccgtg gaatgggaga gcaacggcca gcccgagaac 1560
aactacaaga ccaccccccc tgtgctggac agcgacggct cattcttcct ggtgtccaag 1620
ctgaccgtgg acaagagccg gtggcaggaa ggcaacgtgt tcagctgctc cgtgatgcac 1680
gaggccctgc acaaccacta cacccagaag tccctgtctc tgtccctggg c 1731
<210> 207
<211> 1374
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 207
caagtgcggc tgtctcagtc tggcggccag atgaagaaac ccggcgacag catgcggatc 60
agctgcagag ccagcggcta cgagttcatc aactgcccca tcaactggat cagactggcc 120
cctggcaagc ggcctgagtg gatgggatgg atgaagccca gacacggggc cgtgtcctac 180
gccagacagc tgcagggcag agtgaccatg acccggcagc tgagccagga ccctgatgat 240
ccggattggg gcacagcctt cctggaactg cggagcctga ccagcgacga taccgccgtg 300
tacttctgca cccggggcaa gtactgcacc gccagagact actacaactg ggacttcgag 360
cactggggcc agggcacacc tgtgacagtg tctagcgctt cgaccaaggg cccatcggtg 420
ttccctctgg ccccttgcag cagaagcacc agcgaatcta cagccgccct gggctgcctc 480
gtgaaggact actttcccga gcccgtgacc gtgtcctgga actctggcgc tctgacaagc 540
ggcgtgcaca cctttccagc cgtgctccag agcagcggcc tgtactctct gagcagcgtc 600
gtgacagtgc ccagcagcag cctgggcacc aagacctaca cctgtaacgt ggaccacaag 660
cccagcaaca ccaaggtgga caagcgggtg gaatctaagt acggccctcc ctgccctcct 720
tgcccagccc ctgaagctgc cggcggaccc tccgtgttcc tgttcccccc aaagcccaag 780
gacaccctga tgatcagccg gacccccgaa gtgacctgcg tggtggtgga tgtgtcccag 840
gaagatcccg aggtgcagtt caattggtac gtggacggcg tggaagtgca caacgccaag 900
accaagccca gagaggaaca gttcaacagc acctaccggg tggtgtccgt gctgaccgtg 960
ctgcaccagg actggctgaa cggcaaagag tacaagtgca aggtgtccaa caagggcctg 1020
cccagctcca tcgagaaaac catcagcaag gccaagggcc agccccgcga gcctcaagtg 1080
tataccctgc ccccttgcca ggaagagatg accaagaacc aggtgtccct gtggtgtctc 1140
gtgaaaggct tctaccccag cgacattgcc gtggaatggg agagcaacgg ccagcccgag 1200
aacaactaca agaccacccc ccctgtgctg gacagcgacg gctcattctt cctgtactcc 1260
aagctgaccg tggacaagag ccggtggcag gaaggcaacg tgttcagctg ctccgtgatg 1320
cacgaggccc tgcacaacca ctacacccag aagtccctgt ctctgtccct gggc 1374
<210> 208
<211> 624
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 208
agcctgacac agagccctgg caccctgtca ctgagcccag gcgagacagc catcatcagc 60
tgccggacaa gccagtacgg cagcctggcc tggtatcagc agaggcctgg acaggccccc 120
agactcgtga tctacagcgg cagcacaaga gccgccggaa tccccgatag attcagcggc 180
tccagatggg gacccgacta caacctgacc atcagcaacc tggaaagcgg cgacttcggc 240
gtgtactact gccagcagta cgagttcttc ggccagggca ccaaggtgca ggtggacatc 300
aagcgtacgg tggccgctcc cagcgtgttc atcttcccac ctagcgacga gcagctgaag 360
tccggcacag cctctgtcgt gtgcctgctg aacaacttct acccccgcga ggccaaagtg 420
cagtggaagg tggacaacgc cctgcagagc ggcaacagcc aggaaagcgt gaccgagcag 480
gacagcaagg actccaccta cagcctgagc agcaccctga cactgagcaa ggccgactac 540
gagaagcaca aggtgtacgc ctgcgaagtg acccaccagg gcctgtctag ccccgtgacc 600
aagagcttca accggggcga gtgt 624
<210> 209
<211> 1008
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 209
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacgagaacc tgcagaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaaggaca aaacccatac cgacatccag 360
atgacccaga gccccagcag cctgtctgcc agcgtgggcg acagagtgac catcacctgt 420
caggccagcc agaacatcta cgtgtggctg aactggtatc agcagaagcc cggcaaggcc 480
cccaagctgc tgatctacaa ggccagcaac ctgcacaccg gcgtgcccag cagattttct 540
ggcagcggct ccggcaccga cttcaccctg acaatcagct ccctgcagcc cgaggacatt 600
gccacctact actgccagca gggccagacc tacccctaca cctttggcca gggcaccaag 660
ctggaaatca aggataagac ccacacccgt acggtggccg ctcccagcgt gttcatcttc 720
ccacctagcg acgagcagct gaagtccggc acagcctctg tcgtgtgcct gctgaacaac 780
ttctaccccc gcgaggccaa agtgcagtgg aaggtggaca acgccctgca gagcggcaac 840
agccaggaaa gcgtgaccga gcaggacagc aaggactcca cctacagcct gagcagcacc 900
ctgacactga gcaaggccga ctacgagaag cacaaggtgt acgcctgcga agtgacccac 960
cagggcctgt ctagccccgt gaccaagagc ttcaaccggg gcgagtgt 1008
<210> 210
<211> 1740
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 210
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
gacaaaaccc atacccaggt gcagctggtg gaatctggcg gcggagtggt gcagcctggc 420
agaagcctga gactgagctg tgccgccagc ggcttcacct tcaccaaggc ctggatgcac 480
tgggtgcgcc aggcccctgg aaagcagctg gaatgggtgg cccagatcaa ggacaagagc 540
aacagctacg ccacctacta cgccgacagc gtgaagggcc ggttcaccat cagccgggac 600
gacagcaaga acaccctgta cctgcagatg aacagcctgc gggccgagga caccgccgtg 660
tactactgtc ggggcgtgta ctatgccctg agccccttcg attactgggg ccagggaacc 720
ctcgtgaccg tgtctagtga taagacccac accgccagca caaagggccc cagcgtgttc 780
cctctggccc ctagcagcaa gagcacatct ggcggaacag ccgccctggg ctgcctcgtg 840
aaggactact ttcccgagcc cgtgaccgtg tcctggaatt ctggcgccct gaccagcggc 900
gtgcacacct ttccagctgt gctgcagtcc agcggcctgt acagcctgag cagcgtcgtg 960
acagtgccca gcagctctct gggcacccag acctacatct gcaacgtgaa ccacaagccc 1020
agcaacacca aggtggacaa gaaggtggaa cccaagagct gcgacaagac ccacacctgt 1080
cccccttgtc ctgcccccga actgctggga ggcccttccg tgttcctgtt ccccccaaag 1140
cccaaggaca ccctgatgat cagccggacc cccgaagtga cctgcgtggt ggtggatgtg 1200
tcccacgagg accctgaagt gaagttcaat tggtacgtgg acggcgtgga agtgcacaac 1260
gccaagacca agccaagaga ggaacagtac aacaatgcct cccgggtggt gtccgtgctg 1320
accgtgctgc accaggactg gctgaacggc aaagagtaca agtgcaaggt gtccaacaag 1380
gccctgcctg cccccatcga gaaaaccatc agcaaggcca agggccagcc ccgcgaaccc 1440
caggtgtgca cactgccccc aagcagggac gagctgacca agaaccaggt gtccctgagc 1500
tgtgccgtga aaggcttcta cccctccgat atcgccgtgg aatgggagag caacggccag 1560
cccgagaaca actacaagac caccccccct gtgctggaca gcgacggctc attcttcctg 1620
gtgtccaagc tgacagtgga caagtcccgg tggcagcagg gcaacgtgtt cagctgctcc 1680
gtgatgcacg aggccctgca caaccactac acccagaagt ccctgagcct gagccccggc 1740
<210> 211
<211> 1383
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 211
caagtgcggc tgtctcagtc tggcggccag atgaagaaac ccggcgacag catgcggatc 60
agctgcagag ccagcggcta cgagttcatc aactgcccca tcaactggat cagactggcc 120
cctggcaagc ggcctgagtg gatgggatgg atgaagccca gacacggggc cgtgtcctac 180
gccagacagc tgcagggcag agtgaccatg acccggcagc tgagccagga ccctgatgat 240
ccggattggg gcacagcctt cctggaactg cggagcctga ccagcgacga taccgccgtg 300
tacttctgca cccggggcaa gtactgcacc gccagagact actacaactg ggacttcgag 360
cactggggcc agggcacacc tgtgacagtg tctagcgctt cgaccaaggg cccatcggtc 420
ttccccctgg caccctcctc caagagcacc tctgggggca cagcggccct gggctgcctg 480
gtcaaggact acttccccga accggtgacg gtgtcgtgga actcaggcgc cctgaccagc 540
ggcgtgcaca ccttcccggc tgtcctacag tcctcaggac tctactccct cagcagcgtg 600
gtgaccgtgc cctccagcag cttgggcacc cagacctaca tctgcaacgt gaatcacaag 660
cccagcaaca ccaaggtgga caagaaagtt gagcccaaat cttgtgacaa aactcacaca 720
tgcccaccgt gcccagcacc tgaactcctg gggggaccgt cagtcttcct cttcccccca 780
aaacccaagg acaccctcat gatctcccgg acccctgagg tcacatgcgt ggtggtggac 840
gtgagccacg aagaccctga ggtcaagttc aactggtatg ttgacggcgt ggaggtgcat 900
aatgccaaga caaagccgcg ggaggagcag tacaacaatg cctcccgtgt ggtcagcgtc 960
ctcaccgtcc tgcaccagga ctggctgaat ggcaaggagt acaagtgcaa ggtctccaac 1020
aaagccctcc cagcccccat cgagaaaacc atctccaaag ccaaagggca gccccgagaa 1080
ccacaggtgt acaccctgcc cccatgccgg gatgagctga ccaagaatca agtcagcctg 1140
tggtgcctgg taaaaggctt ctatcccagc gacatcgccg tggagtggga gagcaatggg 1200
cagccggaga acaactacaa gaccacgcct cccgtgctgg actccgacgg ctccttcttc 1260
ctctactcaa aactcaccgt ggacaagagc aggtggcagc aggggaacgt cttctcatgc 1320
tccgtgatgc atgaggctct gcacaaccac tacacgcaga agagcctctc cctgtctccg 1380
ggt 1383
<210> 212
<211> 624
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 212
agcctgacac agagccctgg caccctgtca ctgagcccag gcgagacagc catcatcagc 60
tgccggacaa gccagtacgg cagcctggcc tggtatcagc agaggcctgg acaggccccc 120
agactcgtga tctacagcgg cagcacaaga gccgccggaa tccccgatag attcagcggc 180
tccagatggg gacccgacta caacctgacc atcagcaacc tggaaagcgg cgacttcggc 240
gtgtactact gccagcagta cgagttcttc ggccagggca ccaaggtgca ggtggacatc 300
aagcgtacgg tggccgctcc cagcgtgttc atcttcccac ctagcgacga gcagctgaag 360
tccggcacag cctctgtcgt gtgcctgctg aacaacttct acccccgcga ggccaaagtg 420
cagtggaagg tggacaacgc cctgcagagc ggcaacagcc aggaaagcgt gaccgagcag 480
gacagcaagg actccaccta cagcctgagc agcaccctga cactgagcaa ggccgactac 540
gagaagcaca aggtgtacgc ctgcgaagtg acccaccagg gcctgtctag ccccgtgacc 600
aagagcttca accggggcga gtgt 624
<210> 213
<211> 1008
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 213
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacgagaacc tgttcaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaaggaca aaacccatac cgacatccag 360
atgacccaga gccccagcag cctgtctgcc agcgtgggcg acagagtgac catcacctgt 420
caggccagcc agaacatcta cgtgtggctg aactggtatc agcagaagcc cggcaaggcc 480
cccaagctgc tgatctacaa ggccagcaac ctgcacaccg gcgtgcccag cagattttct 540
ggcagcggct ccggcaccga cttcaccctg acaatcagct ccctgcagcc cgaggacatt 600
gccacctact actgccagca gggccagacc tacccctaca cctttggcca gggcaccaag 660
ctggaaatca aggataagac ccacacccgt acggtggccg ctcccagcgt gttcatcttc 720
ccacctagcg acgagcagct gaagtccggc acagcctctg tcgtgtgcct gctgaacaac 780
ttctaccccc gcgaggccaa agtgcagtgg aaggtggaca acgccctgca gagcggcaac 840
agccaggaaa gcgtgaccga gcaggacagc aaggactcca cctacagcct gagcagcacc 900
ctgacactga gcaaggccga ctacgagaag cacaaggtgt acgcctgcga agtgacccac 960
cagggcctgt ctagccccgt gaccaagagc ttcaaccggg gcgagtgt 1008
<210> 214
<211> 1740
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 214
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
gacaaaaccc atacccaggt gcagctggtg gaatctggcg gcggagtggt gcagcctggc 420
agaagcctga gactgagctg tgccgccagc ggcttcacct tcaccaaggc ctggatgcac 480
tgggtgcgcc aggcccctgg aaagcagctg gaatgggtgg cccagatcaa ggacaagagc 540
aacagctacg ccacctacta cgccgacagc gtgaagggcc ggttcaccat cagccgggac 600
gacagcaaga acaccctgta cctgcagatg aacagcctgc gggccgagga caccgccgtg 660
tactactgtc ggggcgtgta ctatgccctg agccccttcg attactgggg ccagggaacc 720
ctcgtgaccg tgtctagtga taagacccac accgccagca caaagggccc cagcgtgttc 780
cctctggccc ctagcagcaa gagcacatct ggcggaacag ccgccctggg ctgcctcgtg 840
aaggactact ttcccgagcc cgtgaccgtg tcctggaatt ctggcgccct gaccagcggc 900
gtgcacacct ttccagctgt gctgcagtcc agcggcctgt acagcctgag cagcgtcgtg 960
acagtgccca gcagctctct gggcacccag acctacatct gcaacgtgaa ccacaagccc 1020
agcaacacca aggtggacaa gaaggtggaa cccaagagct gcgacaagac ccacacctgt 1080
cccccttgtc ctgcccccga actgctggga ggcccttccg tgttcctgtt ccccccaaag 1140
cccaaggaca ccctgatgat cagccggacc cccgaagtga cctgcgtggt ggtggatgtg 1200
tcccacgagg accctgaagt gaagttcaat tggtacgtgg acggcgtgga agtgcacaac 1260
gccaagacca agccaagaga ggaacagtac aacaatgcct cccgggtggt gtccgtgctg 1320
accgtgctgc accaggactg gctgaacggc aaagagtaca agtgcaaggt gtccaacaag 1380
gccctgcctg cccccatcga gaaaaccatc agcaaggcca agggccagcc ccgcgaaccc 1440
caggtgtgca cactgccccc aagcagggac gagctgacca agaaccaggt gtccctgagc 1500
tgtgccgtga aaggcttcta cccctccgat atcgccgtgg aatgggagag caacggccag 1560
cccgagaaca actacaagac caccccccct gtgctggaca gcgacggctc attcttcctg 1620
gtgtccaagc tgacagtgga caagtcccgg tggcagcagg gcaacgtgtt cagctgctcc 1680
gtgatgcacg aggccctgca caaccactac acccagaagt ccctgagcct gagccccggc 1740
<210> 215
<211> 1383
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 215
caagtgcggc tgtctcagtc tggcggccag atgaagaaac ccggcgacag catgcggatc 60
agctgcagag ccagcggcta cgagttcatc aactgcccca tcaactggat cagactggcc 120
cctggcaagc ggcctgagtg gatgggatgg atgaagccca gacacggggc cgtgtcctac 180
gccagacagc tgcagggcag agtgaccatg acccggcagc tgagccagga ccctgatgat 240
ccggattggg gcacagcctt cctggaactg cggagcctga ccagcgacga taccgccgtg 300
tacttctgca cccggggcaa gtactgcacc gccagagact actacaactg ggacttcgag 360
cactggggcc agggcacacc tgtgacagtg tctagcgctt cgaccaaggg cccatcggtc 420
ttccccctgg caccctcctc caagagcacc tctgggggca cagcggccct gggctgcctg 480
gtcaaggact acttccccga accggtgacg gtgtcgtgga actcaggcgc cctgaccagc 540
ggcgtgcaca ccttcccggc tgtcctacag tcctcaggac tctactccct cagcagcgtg 600
gtgaccgtgc cctccagcag cttgggcacc cagacctaca tctgcaacgt gaatcacaag 660
cccagcaaca ccaaggtgga caagaaagtt gagcccaaat cttgtgacaa aactcacaca 720
tgcccaccgt gcccagcacc tgaactcctg gggggaccgt cagtcttcct cttcccccca 780
aaacccaagg acaccctcat gatctcccgg acccctgagg tcacatgcgt ggtggtggac 840
gtgagccacg aagaccctga ggtcaagttc aactggtatg ttgacggcgt ggaggtgcat 900
aatgccaaga caaagccgcg ggaggagcag tacaacaatg cctcccgtgt ggtcagcgtc 960
ctcaccgtcc tgcaccagga ctggctgaat ggcaaggagt acaagtgcaa ggtctccaac 1020
aaagccctcc cagcccccat cgagaaaacc atctccaaag ccaaagggca gccccgagaa 1080
ccacaggtgt acaccctgcc cccatgccgg gatgagctga ccaagaatca agtcagcctg 1140
tggtgcctgg taaaaggctt ctatcccagc gacatcgccg tggagtggga gagcaatggg 1200
cagccggaga acaactacaa gaccacgcct cccgtgctgg actccgacgg ctccttcttc 1260
ctctactcaa aactcaccgt ggacaagagc aggtggcagc aggggaacgt cttctcatgc 1320
tccgtgatgc atgaggctct gcacaaccac tacacgcaga agagcctctc cctgtctccg 1380
ggt 1383
<210> 216
<211> 624
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 216
agcctgacac agagccctgg caccctgtca ctgagcccag gcgagacagc catcatcagc 60
tgccggacaa gccagtacgg cagcctggcc tggtatcagc agaggcctgg acaggccccc 120
agactcgtga tctacagcgg cagcacaaga gccgccggaa tccccgatag attcagcggc 180
tccagatggg gacccgacta caacctgacc atcagcaacc tggaaagcgg cgacttcggc 240
gtgtactact gccagcagta cgagttcttc ggccagggca ccaaggtgca ggtggacatc 300
aagcgtacgg tggccgctcc cagcgtgttc atcttcccac ctagcgacga gcagctgaag 360
tccggcacag cctctgtcgt gtgcctgctg aacaacttct acccccgcga ggccaaagtg 420
cagtggaagg tggacaacgc cctgcagagc ggcaacagcc aggaaagcgt gaccgagcag 480
gacagcaagg actccaccta cagcctgagc agcaccctga cactgagcaa ggccgactac 540
gagaagcaca aggtgtacgc ctgcgaagtg acccaccagg gcctgtctag ccccgtgacc 600
aagagcttca accggggcga gtgt 624
<210> 217
<211> 1014
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 217
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacaacaacg ccaacaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaagggcc agcccaaggc cgcccccgac 360
atccagatga cccagagccc cagcagcctg tctgccagcg tgggcgacag agtgaccatc 420
acctgtcagg ccagccagaa catctacgtg tggctgaact ggtatcagca gaagcccggc 480
aaggccccca agctgctgat ctacaaggcc agcaacctgc acaccggcgt gcccagcaga 540
ttttctggca gcggctccgg caccgacttc accctgacaa tcagctccct gcagcccgag 600
gacattgcca cctactactg ccagcagggc cagacctacc cctacacctt tggccagggc 660
accaagctgg aaatcaagac caagggcccc agccgtacgg tggccgctcc cagcgtgttc 720
atcttcccac ctagcgacga gcagctgaag tccggcacag cctctgtcgt gtgcctgctg 780
aacaacttct acccccgcga ggccaaagtg cagtggaagg tggacaacgc cctgcagagc 840
ggcaacagcc aggaaagcgt gaccgagcag gacagcaagg actccaccta cagcctgagc 900
agcaccctga cactgagcaa ggccgactac gagaagcaca aggtgtacgc ctgcgaagtg 960
acccaccagg gcctgtctag ccccgtgacc aagagcttca accggggcga gtgt 1014
<210> 218
<211> 1707
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 218
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
agccaggtgc agctggtgga atctggcggc ggagtggtgc agcctggcag aagcctgaga 420
ctgagctgtg ccgccagcgg cttcaccttc accaaggcct ggatgcactg ggtgcgccag 480
gcccctggaa agcagctgga atgggtggcc cagatcaagg acaagagcaa cagctacgcc 540
acctactacg ccgacagcgt gaagggccgg ttcaccatca gccgggacga cagcaagaac 600
accctgtacc tgcagatgaa cagcctgcgg gccgaggaca ccgccgtgta ctactgtcgg 660
ggcgtgtact atgccctgag ccccttcgat tactggggcc agggaaccct cgtgaccgtg 720
tctagtcgga ccgccagcac aaagggccca tcggtgttcc ctctggcccc ttgcagcaga 780
agcaccagcg aatctacagc cgccctgggc tgcctcgtga aggactactt tcccgagccc 840
gtgaccgtgt cctggaactc tggcgctctg acaagcggcg tgcacacctt tccagccgtg 900
ctccagagca gcggcctgta ctctctgagc agcgtcgtga cagtgcccag cagcagcctg 960
ggcaccaaga cctacacctg taacgtggac cacaagccca gcaacaccaa ggtggacaag 1020
cgggtggaat ctaagtacgg ccctccctgc cctccttgcc cagcccctcc tgtggctgga 1080
ccctccgtgt tcctgttccc cccaaagccc aaggacaccc tgatgatcag ccggaccccc 1140
gaagtgacct gcgtggtggt ggatgtgtcc caggaagatc ccgaggtgca gttcaattgg 1200
tacgtggacg gcgtggaagt gcacaacgcc aagaccaagc ccagagagga acagttcaac 1260
agcacctacc gggtggtgtc cgtgctgacc gtgctgcacc aggactggct gaacggcaaa 1320
gagtacaagt gcaaggtgtc caacaagggc ctgcccagct ccatcgagaa aaccatcagc 1380
aaggccaagg gccagccccg cgagcctcaa gtgtgtaccc tgccccctag ccaggaagag 1440
atgaccaaga accaggtgtc cctgagctgt gccgtgaaag gcttctaccc cagcgacatt 1500
gccgtggaat gggagagcaa cggccagccc gagaacaact acaagaccac cccccctgtg 1560
ctggacagcg acggctcatt cttcctggtg tccaagctga ccgtggacaa gagccggtgg 1620
caggaaggca acgtgttcag ctgctccgtg atgcacgagg ccctgcacaa ccactacacc 1680
cagaagtccc tgtctctgtc cctgggc 1707
<210> 219
<211> 1341
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 219
agagcccacc tggtgcagtc tggcaccgcc atgaagaaac caggcgcctc tgtgcgggtg 60
tcctgtcaga caagcggcta caccttcacc gcccacatcc tgttctggtt ccggcaggcc 120
cctggcagag gactggaatg ggtgggatgg atcaagcccc agtatggcgc cgtgaacttc 180
ggcggaggct tccgggatag agtgaccctg acccgggacg tgtaccgcga gatcgcctac 240
atggacatcc ggggcctgaa gcccgatgac accgccgtgt actactgcgc cagagacaga 300
agctacggcg acagcagctg ggctctggat gcttggggcc agggcacaac cgtggtggtg 360
tctgccgcct ctacaaaggg cccatcggtg ttccctctgg ccccttgcag cagaagcacc 420
agcgaatcta cagccgccct gggctgcctc gtgaaggact actttcccga gcccgtgacc 480
gtgtcctgga actctggcgc tctgacaagc ggcgtgcaca cctttccagc cgtgctccag 540
agcagcggcc tgtactctct gagcagcgtc gtgacagtgc ccagcagcag cctgggcacc 600
aagacctaca cctgtaacgt ggaccacaag cccagcaaca ccaaggtgga caagcgggtg 660
gaatctaagt acggccctcc ctgccctcct tgcccagccc ctcctgtggc tggaccctcc 720
gtgttcctgt tccccccaaa gcccaaggac accctgatga tcagccggac ccccgaagtg 780
acctgcgtgg tggtggatgt gtcccaggaa gatcccgagg tgcagttcaa ttggtacgtg 840
gacggcgtgg aagtgcacaa cgccaagacc aagcccagag aggaacagtt caacagcacc 900
taccgggtgg tgtccgtgct gaccgtgctg caccaggact ggctgaacgg caaagagtac 960
aagtgcaagg tgtccaacaa gggcctgccc agctccatcg agaaaaccat cagcaaggcc 1020
aagggccagc cccgcgagcc tcaagtgtat accctgcccc cttgccagga agagatgacc 1080
aagaaccagg tgtccctgtg gtgtctcgtg aaaggcttct accccagcga cattgccgtg 1140
gaatgggaga gcaacggcca gcccgagaac aactacaaga ccaccccccc tgtgctggac 1200
agcgacggct cattcttcct gtactccaag ctgaccgtgg acaagagccg gtggcaggaa 1260
ggcaacgtgt tcagctgctc cgtgatgcac gaggccctgc acaaccacta cacccagaag 1320
tccctgtctc tgtccctggg c 1341
<210> 220
<211> 630
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 220
tacatccacg tgacccagag ccccagcagc ctgtccgtgt ccatcggcga cagagtgacc 60
atcaactgcc agacctctca gggcgtgggc agcgacctgc actggtatca gcacaagcct 120
ggcagagccc ccaagctgct gatccaccac acaagcagcg tggaagatgg cgtgcccagc 180
agattttccg gcagcggctt ccacaccagc ttcaacctga ccatcagcga tctgcaggcc 240
gacgacattg ccacctacta ttgtcaggtg ctgcagttct tcggcagagg cagcagactg 300
cacatcaagc gtacggtggc cgctcccagc gtgttcatct tcccacctag cgacgagcag 360
ctgaagtccg gcacagcctc tgtcgtgtgc ctgctgaaca acttctaccc ccgcgaggcc 420
aaagtgcagt ggaaggtgga caacgccctg cagagcggca acagccagga aagcgtgacc 480
gagcaggaca gcaaggactc cacctacagc ctgagcagca ccctgacact gagcaaggcc 540
gactacgaga agcacaaggt gtacgcctgc gaagtgaccc accagggcct gtctagcccc 600
gtgaccaaga gcttcaaccg gggcgagtgt 630
<210> 221
<211> 1014
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 221
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacaacaacg ccaacaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaagggcc agcccaaggc cgcccccgac 360
atccagatga cccagagccc cagcagcctg tctgccagcg tgggcgacag agtgaccatc 420
acctgtcagg ccagccagaa catctacgtg tggctgaact ggtatcagca gaagcccggc 480
aaggccccca agctgctgat ctacaaggcc agcaacctgc acaccggcgt gcccagcaga 540
ttttctggca gcggctccgg caccgacttc accctgacaa tcagctccct gcagcccgag 600
gacattgcca cctactactg ccagcagggc cagacctacc cctacacctt tggccagggc 660
accaagctgg aaatcaagac caagggcccc agccgtacgg tggccgctcc cagcgtgttc 720
atcttcccac ctagcgacga gcagctgaag tccggcacag cctctgtcgt gtgcctgctg 780
aacaacttct acccccgcga ggccaaagtg cagtggaagg tggacaacgc cctgcagagc 840
ggcaacagcc aggaaagcgt gaccgagcag gacagcaagg actccaccta cagcctgagc 900
agcaccctga cactgagcaa ggccgactac gagaagcaca aggtgtacgc ctgcgaagtg 960
acccaccagg gcctgtctag ccccgtgacc aagagcttca accggggcga gtgt 1014
<210> 222
<211> 1710
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 222
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
agccaggtgc agctggtgga atctggcggc ggagtggtgc agcctggcag aagcctgaga 420
ctgagctgtg ccgccagcgg cttcaccttc accaaggcct ggatgcactg ggtgcgccag 480
gcccctggaa agcagctgga atgggtggcc cagatcaagg acaagagcaa cagctacgcc 540
acctactacg ccgacagcgt gaagggccgg ttcaccatca gccgggacga cagcaagaac 600
accctgtacc tgcagatgaa cagcctgcgg gccgaggaca ccgccgtgta ctactgtcgg 660
ggcgtgtact atgccctgag ccccttcgat tactggggcc agggaaccct cgtgaccgtg 720
tctagtcgga ccgccagcac aaagggccca tcggtgttcc ctctggcccc ttgcagcaga 780
agcaccagcg aatctacagc cgccctgggc tgcctcgtga aggactactt tcccgagccc 840
gtgaccgtgt cctggaactc tggcgctctg acaagcggcg tgcacacctt tccagccgtg 900
ctccagagca gcggcctgta ctctctgagc agcgtcgtga cagtgcccag cagcagcctg 960
ggcaccaaga cctacacctg taacgtggac cacaagccca gcaacaccaa ggtggacaag 1020
cgggtggaat ctaagtacgg ccctccctgc cctccttgcc cagcccctga agctgccggc 1080
ggaccctccg tgttcctgtt ccccccaaag cccaaggaca ccctgatgat cagccggacc 1140
cccgaagtga cctgcgtggt ggtggatgtg tcccaggaag atcccgaggt gcagttcaat 1200
tggtacgtgg acggcgtgga agtgcacaac gccaagacca agcccagaga ggaacagttc 1260
aacagcacct accgggtggt gtccgtgctg accgtgctgc accaggactg gctgaacggc 1320
aaagagtaca agtgcaaggt gtccaacaag ggcctgccca gctccatcga gaaaaccatc 1380
agcaaggcca agggccagcc ccgcgagcct caagtgtgta ccctgccccc tagccaggaa 1440
gagatgacca agaaccaggt gtccctgagc tgtgccgtga aaggcttcta ccccagcgac 1500
attgccgtgg aatgggagag caacggccag cccgagaaca actacaagac caccccccct 1560
gtgctggaca gcgacggctc attcttcctg gtgtccaagc tgaccgtgga caagagccgg 1620
tggcaggaag gcaacgtgtt cagctgctcc gtgatgcacg aggccctgca caaccactac 1680
acccagaagt ccctgtctct gtccctgggc 1710
<210> 223
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<220>
<221> другой_признак
<222> 439
<223> n = A,T,C или G
<400> 223
agagcccacc tggtgcagtc tggcaccgcc atgaagaaac caggcgcctc tgtgcgggtg 60
tcctgtcaga caagcggcta caccttcacc gcccacatcc tgttctggtt ccggcaggcc 120
cctggcagag gactggaatg ggtgggatgg atcaagcccc agtatggcgc cgtgaacttc 180
ggcggaggct tccgggatag agtgaccctg acccgggacg tgtaccgcga gatcgcctac 240
atggacatcc ggggcctgaa gcccgatgac accgccgtgt actactgcgc cagagacaga 300
agctacggcg acagcagctg ggctctggat gcttggggcc agggcacaac cgtggtggtg 360
tctgccgcct ctacaaaggg cccatcggtg ttccctctgg ccccttgcag cagaagcacc 420
agcgaatcta cagccgccnt gggctgcctc gtgaaggact actttcccga gcccgtgacc 480
gtgtcctgga actctggcgc tctgacaagc ggcgtgcaca cctttccagc cgtgctccag 540
agcagcggcc tgtactctct gagcagcgtc gtgacagtgc ccagcagcag cctgggcacc 600
aagacctaca cctgtaacgt ggaccacaag cccagcaaca ccaaggtgga caagcgggtg 660
gaatctaagt acggccctcc ctgccctcct tgcccagccc ctgaagctgc cggcggaccc 720
tccgtgttcc tgttcccccc aaagcccaag gacaccctga tgatcagccg gacccccgaa 780
gtgacctgcg tggtggtgga tgtgtcccag gaagatcccg aggtgcagtt caattggtac 840
gtggacggcg tggaagtgca caacgccaag accaagccca gagaggaaca gttcaacagc 900
acctaccggg tggtgtccgt gctgaccgtg ctgcaccagg actggctgaa cggcaaagag 960
tacaagtgca aggtgtccaa caagggcctg cccagctcca tcgagaaaac catcagcaag 1020
gccaagggcc agccccgcga gcctcaagtg tataccctgc ccccttgcca ggaagagatg 1080
accaagaacc aggtgtccct gtggtgtctc gtgaaaggct tctaccccag cgacattgcc 1140
gtggaatggg agagcaacgg ccagcccgag aacaactaca agaccacccc ccctgtgctg 1200
gacagcgacg gctcattctt cctgtactcc aagctgaccg tggacaagag ccggtggcag 1260
gaaggcaacg tgttcagctg ctccgtgatg cacgaggccc tgcacaacca ctacacccag 1320
aagtccctgt ctctgtccct gggc 1344
<210> 224
<211> 630
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 224
tacatccacg tgacccagag ccccagcagc ctgtccgtgt ccatcggcga cagagtgacc 60
atcaactgcc agacctctca gggcgtgggc agcgacctgc actggtatca gcacaagcct 120
ggcagagccc ccaagctgct gatccaccac acaagcagcg tggaagatgg cgtgcccagc 180
agattttccg gcagcggctt ccacaccagc ttcaacctga ccatcagcga tctgcaggcc 240
gacgacattg ccacctacta ttgtcaggtg ctgcagttct tcggcagagg cagcagactg 300
cacatcaagc gtacggtggc cgctcccagc gtgttcatct tcccacctag cgacgagcag 360
ctgaagtccg gcacagcctc tgtcgtgtgc ctgctgaaca acttctaccc ccgcgaggcc 420
aaagtgcagt ggaaggtgga caacgccctg cagagcggca acagccagga aagcgtgacc 480
gagcaggaca gcaaggactc cacctacagc ctgagcagca ccctgacact gagcaaggcc 540
gactacgaga agcacaaggt gtacgcctgc gaagtgaccc accagggcct gtctagcccc 600
gtgaccaaga gcttcaaccg gggcgagtgt 630
<210> 225
<211> 1014
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 225
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacaacaacg ccaacaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaagggcc agcccaaggc cgcccccgac 360
atccagatga cccagagccc cagcagcctg tctgccagcg tgggcgacag agtgaccatc 420
acctgtcagg ccagccagaa catctacgtg tggctgaact ggtatcagca gaagcccggc 480
aaggccccca agctgctgat ctacaaggcc agcaacctgc acaccggcgt gcccagcaga 540
ttttctggca gcggctccgg caccgacttc accctgacaa tcagctccct gcagcccgag 600
gacattgcca cctactactg ccagcagggc cagacctacc cctacacctt tggccagggc 660
accaagctgg aaatcaagac caagggcccc agccgtacgg tggccgctcc cagcgtgttc 720
atcttcccac ctagcgacga gcagctgaag tccggcacag cctctgtcgt gtgcctgctg 780
aacaacttct acccccgcga ggccaaagtg cagtggaagg tggacaacgc cctgcagagc 840
ggcaacagcc aggaaagcgt gaccgagcag gacagcaagg actccaccta cagcctgagc 900
agcaccctga cactgagcaa ggccgactac gagaagcaca aggtgtacgc ctgcgaagtg 960
acccaccagg gcctgtctag ccccgtgacc aagagcttca accggggcga gtgt 1014
<210> 226
<211> 1710
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 226
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
agccaggtgc agctggtgga atctggcggc ggagtggtgc agcctggcag aagcctgaga 420
ctgagctgtg ccgccagcgg cttcaccttc accaaggcct ggatgcactg ggtgcgccag 480
gcccctggaa agcagctgga atgggtggcc cagatcaagg acaagagcaa cagctacgcc 540
acctactacg ccgacagcgt gaagggccgg ttcaccatca gccgggacga cagcaagaac 600
accctgtacc tgcagatgaa cagcctgcgg gccgaggaca ccgccgtgta ctactgtcgg 660
ggcgtgtact atgccctgag ccccttcgat tactggggcc agggaaccct cgtgaccgtg 720
tctagtcgga ccgccagcac aaagggccca tcggtgttcc ctctggcccc ttgcagcaga 780
agcaccagcg aatctacagc cgccctgggc tgcctcgtga aggactactt tcccgagccc 840
gtgaccgtgt cctggaactc tggcgctctg acaagcggcg tgcacacctt tccagccgtg 900
ctccagagca gcggcctgta ctctctgagc agcgtcgtga cagtgcccag cagcagcctg 960
ggcaccaaga cctacacctg taacgtggac cacaagccca gcaacaccaa ggtggacaag 1020
cgggtggaat ctaagtacgg ccctccctgc cctccttgcc cagcccctga agctgccggc 1080
ggaccctccg tgttcctgtt ccccccaaag cccaaggaca ccctgatgat cagccggacc 1140
cccgaagtga cctgcgtggt ggtggatgtg tcccaggaag atcccgaggt gcagttcaat 1200
tggtacgtgg acggcgtgga agtgcacaac gccaagacca agcccagaga ggaacagttc 1260
aacagcacct accgggtggt gtccgtgctg accgtgctgc accaggactg gctgaacggc 1320
aaagagtaca agtgcaaggt gtccaacaag ggcctgccca gctccatcga gaaaaccatc 1380
agcaaggcca agggccagcc ccgcgagcct caagtgtgta ccctgccccc tagccaggaa 1440
gagatgacca agaaccaggt gtccctgagc tgtgccgtga aaggcttcta ccccagcgac 1500
attgccgtgg aatgggagag caacggccag cccgagaaca actacaagac caccccccct 1560
gtgctggaca gcgacggctc attcttcctg gtgtccaagc tgaccgtgga caagagccgg 1620
tggcaggaag gcaacgtgtt cagctgctcc gtgatgcacg aggccctgca caaccactac 1680
acccagaagt ccctgtctct gtccctgggc 1710
<210> 227
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<220>
<221> другой_признак
<222> 439
<223> n = A,T,C или G
<400> 227
agagcccacc tggtgcagtc tggcaccgcc atgaagaaac caggcgcctc tgtgcgggtg 60
tcctgtcaga caagcggcta caccttcacc gcccacatcc tgttctggtt ccggcaggcc 120
cctggcagag gactggaatg ggtgggatgg atcaagcccc agtatggcgc cgtgaacttc 180
ggcggaggct tccgggatag agtgaccctg acccgggacg tgtaccgcga gatcgcctac 240
atggacatcc ggggcctgaa gcccgatgac accgccgtgt actactgcgc cagagacaga 300
agctacggcg acagcagctg ggctctggat gcttggggcc agggcacaac cgtggtggtg 360
tctgccgcct ctacaaaggg cccatcggtg ttccctctgg ccccttgcag cagaagcacc 420
agcgaatcta cagccgccnt gggctgcctc gtgaaggact actttcccga gcccgtgacc 480
gtgtcctgga actctggcgc tctgacaagc ggcgtgcaca cctttccagc cgtgctccag 540
agcagcggcc tgtactctct gagcagcgtc gtgacagtgc ccagcagcag cctgggcacc 600
aagacctaca cctgtaacgt ggaccacaag cccagcaaca ccaaggtgga caagcgggtg 660
gaatctaagt acggccctcc ctgccctcct tgcccagccc ctgaagctgc cggcggaccc 720
tccgtgttcc tgttcccccc aaagcccaag gacaccctga tgatcagccg gacccccgaa 780
gtgacctgcg tggtggtgga tgtgtcccag gaagatcccg aggtgcagtt caattggtac 840
gtggacggcg tggaagtgca caacgccaag accaagccca gagaggaaca gttcaacagc 900
acctaccggg tggtgtccgt gctgaccgtg ctgcaccagg actggctgaa cggcaaagag 960
tacaagtgca aggtgtccaa caagggcctg cccagctcca tcgagaaaac catcagcaag 1020
gccaagggcc agccccgcga gcctcaagtg tataccctgc ccccttgcca ggaagagatg 1080
accaagaacc aggtgtccct gtggtgtctc gtgaaaggct tctaccccag cgacattgcc 1140
gtggaatggg agagcaacgg ccagcccgag aacaactaca agaccacccc ccctgtgctg 1200
gacagcgacg gctcattctt cctgtactcc aagctgaccg tggacaagag ccggtggcag 1260
gaaggcaacg tgttcagctg ctccgtgatg cacgaggccc tgcacaacca ctacacccag 1320
aagtccctgt ctctgtccct gggc 1344
<210> 228
<211> 630
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 228
tacatccacg tgacccagag ccccagcagc ctgtccgtgt ccatcggcga cagagtgacc 60
atcaactgcc agacctctca gggcgtgggc agcgacctgc actggtatca gcacaagcct 120
ggcagagccc ccaagctgct gatccaccac acaagcagcg tggaagatgg cgtgcccagc 180
agattttccg gcagcggctt ccacaccagc ttcaacctga ccatcagcga tctgcaggcc 240
gacgacattg ccacctacta ttgtcaggtg ctgcagttct tcggcagagg cagcagactg 300
cacatcaagc gtacggtggc cgctcccagc gtgttcatct tcccacctag cgacgagcag 360
ctgaagtccg gcacagcctc tgtcgtgtgc ctgctgaaca acttctaccc ccgcgaggcc 420
aaagtgcagt ggaaggtgga caacgccctg cagagcggca acagccagga aagcgtgacc 480
gagcaggaca gcaaggactc cacctacagc ctgagcagca ccctgacact gagcaaggcc 540
gactacgaga agcacaaggt gtacgcctgc gaagtgaccc accagggcct gtctagcccc 600
gtgaccaaga gcttcaaccg gggcgagtgt 630
<210> 229
<211> 1008
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 229
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg caccagaacg cccagaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaaggaca aaacccatac cgacatccag 360
atgacccaga gccccagcag cctgtctgcc agcgtgggcg acagagtgac catcacctgt 420
caggccagcc agaacatcta cgtgtggctg aactggtatc agcagaagcc cggcaaggcc 480
cccaagctgc tgatctacaa ggccagcaac ctgcacaccg gcgtgcccag cagattttct 540
ggcagcggct ccggcaccga cttcaccctg acaatcagct ccctgcagcc cgaggacatt 600
gccacctact actgccagca gggccagacc tacccctaca cctttggcca gggcaccaag 660
ctggaaatca aggataagac ccacacccgt acggtggccg ctcccagcgt gttcatcttc 720
ccacctagcg acgagcagct gaagtccggc acagcctctg tcgtgtgcct gctgaacaac 780
ttctaccccc gcgaggccaa agtgcagtgg aaggtggaca acgccctgca gagcggcaac 840
agccaggaaa gcgtgaccga gcaggacagc aaggactcca cctacagcct gagcagcacc 900
ctgacactga gcaaggccga ctacgagaag cacaaggtgt acgcctgcga agtgacccac 960
cagggcctgt ctagccccgt gaccaagagc ttcaaccggg gcgagtgt 1008
<210> 230
<211> 1731
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 230
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
gacaaaaccc atacccaggt gcagctggtg gaatctggcg gcggagtggt gcagcctggc 420
agaagcctga gactgagctg tgccgccagc ggcttcacct tcaccaaggc ctggatgcac 480
tgggtgcgcc aggcccctgg aaagcagctg gaatgggtgg cccagatcaa ggacaagagc 540
aacagctacg ccacctacta cgccgacagc gtgaagggcc ggttcaccat cagccgggac 600
gacagcaaga acaccctgta cctgcagatg aacagcctgc gggccgagga caccgccgtg 660
tactactgtc ggggcgtgta ctatgccctg agccccttcg attactgggg ccagggaacc 720
ctcgtgaccg tgtctagtga taagacccac accgccagca caaagggccc atcggtgttc 780
cctctggccc cttgcagcag aagcaccagc gaatctacag ccgccctggg ctgcctcgtg 840
aaggactact ttcccgagcc cgtgaccgtg tcctggaact ctggcgctct gacaagcggc 900
gtgcacacct ttccagccgt gctccagagc agcggcctgt actctctgag cagcgtcgtg 960
acagtgccca gcagcagcct gggcaccaag acctacacct gtaacgtgga ccacaagccc 1020
agcaacacca aggtggacaa gcgggtggaa tctaagtacg gccctccctg ccctccttgc 1080
ccagcccctg aagctgccgg cggaccctcc gtgttcctgt tccccccaaa gcccaaggac 1140
accctgatga tcagccggac ccccgaagtg acctgcgtgg tggtggatgt gtcccaggaa 1200
gatcccgagg tgcagttcaa ttggtacgtg gacggcgtgg aagtgcacaa cgccaagacc 1260
aagcccagag aggaacagtt caacagcacc taccgggtgg tgtccgtgct gaccgtgctg 1320
caccaggact ggctgaacgg caaagagtac aagtgcaagg tgtccaacaa gggcctgccc 1380
agctccatcg agaaaaccat cagcaaggcc aagggccagc cccgcgagcc tcaagtgtgt 1440
accctgcccc ctagccagga agagatgacc aagaaccagg tgtccctgag ctgtgccgtg 1500
aaaggcttct accccagcga cattgccgtg gaatgggaga gcaacggcca gcccgagaac 1560
aactacaaga ccaccccccc tgtgctggac agcgacggct cattcttcct ggtgtccaag 1620
ctgaccgtgg acaagagccg gtggcaggaa ggcaacgtgt tcagctgctc cgtgatgcac 1680
gaggccctgc acaaccacta cacccagaag tccctgtctc tgtccctggg c 1731
<210> 231
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<220>
<221> другой_признак
<222> 439
<223> n = A,T,C или G
<400> 231
agagcccacc tggtgcagtc tggcaccgcc atgaagaaac caggcgcctc tgtgcgggtg 60
tcctgtcaga caagcggcta caccttcacc gcccacatcc tgttctggtt ccggcaggcc 120
cctggcagag gactggaatg ggtgggatgg atcaagcccc agtatggcgc cgtgaacttc 180
ggcggaggct tccgggatag agtgaccctg acccgggacg tgtaccgcga gatcgcctac 240
atggacatcc ggggcctgaa gcccgatgac accgccgtgt actactgcgc cagagacaga 300
agctacggcg acagcagctg ggctctggat gcttggggcc agggcacaac cgtggtggtg 360
tctgccgcct ctacaaaggg cccatcggtg ttccctctgg ccccttgcag cagaagcacc 420
agcgaatcta cagccgccnt gggctgcctc gtgaaggact actttcccga gcccgtgacc 480
gtgtcctgga actctggcgc tctgacaagc ggcgtgcaca cctttccagc cgtgctccag 540
agcagcggcc tgtactctct gagcagcgtc gtgacagtgc ccagcagcag cctgggcacc 600
aagacctaca cctgtaacgt ggaccacaag cccagcaaca ccaaggtgga caagcgggtg 660
gaatctaagt acggccctcc ctgccctcct tgcccagccc ctgaagctgc cggcggaccc 720
tccgtgttcc tgttcccccc aaagcccaag gacaccctga tgatcagccg gacccccgaa 780
gtgacctgcg tggtggtgga tgtgtcccag gaagatcccg aggtgcagtt caattggtac 840
gtggacggcg tggaagtgca caacgccaag accaagccca gagaggaaca gttcaacagc 900
acctaccggg tggtgtccgt gctgaccgtg ctgcaccagg actggctgaa cggcaaagag 960
tacaagtgca aggtgtccaa caagggcctg cccagctcca tcgagaaaac catcagcaag 1020
gccaagggcc agccccgcga gcctcaagtg tataccctgc ccccttgcca ggaagagatg 1080
accaagaacc aggtgtccct gtggtgtctc gtgaaaggct tctaccccag cgacattgcc 1140
gtggaatggg agagcaacgg ccagcccgag aacaactaca agaccacccc ccctgtgctg 1200
gacagcgacg gctcattctt cctgtactcc aagctgaccg tggacaagag ccggtggcag 1260
gaaggcaacg tgttcagctg ctccgtgatg cacgaggccc tgcacaacca ctacacccag 1320
aagtccctgt ctctgtccct gggc 1344
<210> 232
<211> 630
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 232
tacatccacg tgacccagag ccccagcagc ctgtccgtgt ccatcggcga cagagtgacc 60
atcaactgcc agacctctca gggcgtgggc agcgacctgc actggtatca gcacaagcct 120
ggcagagccc ccaagctgct gatccaccac acaagcagcg tggaagatgg cgtgcccagc 180
agattttccg gcagcggctt ccacaccagc ttcaacctga ccatcagcga tctgcaggcc 240
gacgacattg ccacctacta ttgtcaggtg ctgcagttct tcggcagagg cagcagactg 300
cacatcaagc gtacggtggc cgctcccagc gtgttcatct tcccacctag cgacgagcag 360
ctgaagtccg gcacagcctc tgtcgtgtgc ctgctgaaca acttctaccc ccgcgaggcc 420
aaagtgcagt ggaaggtgga caacgccctg cagagcggca acagccagga aagcgtgacc 480
gagcaggaca gcaaggactc cacctacagc ctgagcagca ccctgacact gagcaaggcc 540
gactacgaga agcacaaggt gtacgcctgc gaagtgaccc accagggcct gtctagcccc 600
gtgaccaaga gcttcaaccg gggcgagtgt 630
<210> 233
<211> 1002
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 233
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacaacaacg ccaacaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaaggaca aaacccatac cgacatccag 360
atgacccaga gccccagcag cctgtctgcc agcgtgggcg acagagtgac catcacctgt 420
caggccagcc agaacatcta cgtgtggctg aactggtatc agcagaagcc cggcaaggcc 480
cccaagctgc tgatctacaa ggccagcaac ctgcacaccg gcgtgcccag cagattttct 540
ggcagcggct ccggcaccga cttcaccctg acaatcagct ccctgcagcc cgaggacatt 600
gccacctact actgccagca gggccagacc tacccctaca cctttggcca gggcaccaag 660
ctggaaatca aggataagac ccacaccagt cagcccaagg ctgccccctc ggtcactctg 720
ttcccgccct cgagtgagga gcttcaagcc aacaaggcca cactggtgtg tctcataagt 780
gacttctacc cgggagccgt gacagtggcc tggaaggcag atagcagccc cgtcaaggcg 840
ggagtggaga ccaccacacc ctccaaacaa agcaacaaca agtacgcggc cagcagctac 900
ctgagcctga cgcctgagca gtggaagtcc cacagaagct acagctgcca ggtcacgcat 960
gaagggagca ccgtggagaa gacagtggcc cctacagaat gt 1002
<210> 234
<211> 1731
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 234
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
gacaaaaccc atacccaggt gcagctggtg gaatctggcg gcggagtggt gcagcctggc 420
agaagcctga gactgagctg tgccgccagc ggcttcacct tcaccaaggc ctggatgcac 480
tgggtgcgcc aggcccctgg aaagcagctg gaatgggtgg cccagatcaa ggacaagagc 540
aacagctacg ccacctacta cgccgacagc gtgaagggcc ggttcaccat cagccgggac 600
gacagcaaga acaccctgta cctgcagatg aacagcctgc gggccgagga caccgccgtg 660
tactactgtc ggggcgtgta ctatgccctg agccccttcg attactgggg ccagggaacc 720
ctcgtgaccg tgtctagtga taagacccac accgccagca caaagggccc atcggtgttc 780
cctctggccc cttgcagcag aagcaccagc gaatctacag ccgccctggg ctgcctcgtg 840
aaggactact ttcccgagcc cgtgaccgtg tcctggaact ctggcgctct gacaagcggc 900
gtgcacacct ttccagccgt gctccagagc agcggcctgt actctctgag cagcgtcgtg 960
acagtgccca gcagcagcct gggcaccaag acctacacct gtaacgtgga ccacaagccc 1020
agcaacacca aggtggacaa gcgggtggaa tctaagtacg gccctccctg ccctccttgc 1080
ccagcccctg aagctgccgg cggaccctcc gtgttcctgt tccccccaaa gcccaaggac 1140
accctgatga tcagccggac ccccgaagtg acctgcgtgg tggtggatgt gtcccaggaa 1200
gatcccgagg tgcagttcaa ttggtacgtg gacggcgtgg aagtgcacaa cgccaagacc 1260
aagcccagag aggaacagtt caacagcacc taccgggtgg tgtccgtgct gaccgtgctg 1320
caccaggact ggctgaacgg caaagagtac aagtgcaagg tgtccaacaa gggcctgccc 1380
agctccatcg agaaaaccat cagcaaggcc aagggccagc cccgcgagcc tcaagtgtgt 1440
accctgcccc ctagccagga agagatgacc aagaaccagg tgtccctgag ctgtgccgtg 1500
aaaggcttct accccagcga cattgccgtg gaatgggaga gcaacggcca gcccgagaac 1560
aactacaaga ccaccccccc tgtgctggac agcgacggct cattcttcct ggtgtccaag 1620
ctgaccgtgg acaagagccg gtggcaggaa ggcaacgtgt tcagctgctc cgtgatgcac 1680
gaggccctgc acaaccacta cacccagaag tccctgtctc tgtccctggg c 1731
<210> 235
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<220>
<221> другой_признак
<222> 439
<223> n = A,T,C или G
<400> 235
agagcccacc tggtgcagtc tggcaccgcc atgaagaaac caggcgcctc tgtgcgggtg 60
tcctgtcaga caagcggcta caccttcacc gcccacatcc tgttctggtt ccggcaggcc 120
cctggcagag gactggaatg ggtgggatgg atcaagcccc agtatggcgc cgtgaacttc 180
ggcggaggct tccgggatag agtgaccctg acccgggacg tgtaccgcga gatcgcctac 240
atggacatcc ggggcctgaa gcccgatgac accgccgtgt actactgcgc cagagacaga 300
agctacggcg acagcagctg ggctctggat gcttggggcc agggcacaac cgtggtggtg 360
tctgccgcct ctacaaaggg cccatcggtg ttccctctgg ccccttgcag cagaagcacc 420
agcgaatcta cagccgccnt gggctgcctc gtgaaggact actttcccga gcccgtgacc 480
gtgtcctgga actctggcgc tctgacaagc ggcgtgcaca cctttccagc cgtgctccag 540
agcagcggcc tgtactctct gagcagcgtc gtgacagtgc ccagcagcag cctgggcacc 600
aagacctaca cctgtaacgt ggaccacaag cccagcaaca ccaaggtgga caagcgggtg 660
gaatctaagt acggccctcc ctgccctcct tgcccagccc ctgaagctgc cggcggaccc 720
tccgtgttcc tgttcccccc aaagcccaag gacaccctga tgatcagccg gacccccgaa 780
gtgacctgcg tggtggtgga tgtgtcccag gaagatcccg aggtgcagtt caattggtac 840
gtggacggcg tggaagtgca caacgccaag accaagccca gagaggaaca gttcaacagc 900
acctaccggg tggtgtccgt gctgaccgtg ctgcaccagg actggctgaa cggcaaagag 960
tacaagtgca aggtgtccaa caagggcctg cccagctcca tcgagaaaac catcagcaag 1020
gccaagggcc agccccgcga gcctcaagtg tataccctgc ccccttgcca ggaagagatg 1080
accaagaacc aggtgtccct gtggtgtctc gtgaaaggct tctaccccag cgacattgcc 1140
gtggaatggg agagcaacgg ccagcccgag aacaactaca agaccacccc ccctgtgctg 1200
gacagcgacg gctcattctt cctgtactcc aagctgaccg tggacaagag ccggtggcag 1260
gaaggcaacg tgttcagctg ctccgtgatg cacgaggccc tgcacaacca ctacacccag 1320
aagtccctgt ctctgtccct gggc 1344
<210> 236
<211> 630
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 236
tacatccacg tgacccagag ccccagcagc ctgtccgtgt ccatcggcga cagagtgacc 60
atcaactgcc agacctctca gggcgtgggc agcgacctgc actggtatca gcacaagcct 120
ggcagagccc ccaagctgct gatccaccac acaagcagcg tggaagatgg cgtgcccagc 180
agattttccg gcagcggctt ccacaccagc ttcaacctga ccatcagcga tctgcaggcc 240
gacgacattg ccacctacta ttgtcaggtg ctgcagttct tcggcagagg cagcagactg 300
cacatcaagc gtacggtggc cgctcccagc gtgttcatct tcccacctag cgacgagcag 360
ctgaagtccg gcacagcctc tgtcgtgtgc ctgctgaaca acttctaccc ccgcgaggcc 420
aaagtgcagt ggaaggtgga caacgccctg cagagcggca acagccagga aagcgtgacc 480
gagcaggaca gcaaggactc cacctacagc ctgagcagca ccctgacact gagcaaggcc 540
gactacgaga agcacaaggt gtacgcctgc gaagtgaccc accagggcct gtctagcccc 600
gtgaccaaga gcttcaaccg gggcgagtgt 630
<210> 237
<211> 1008
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 237
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg caccagaacg cccagaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaaggaca aaacccatac cgacatccag 360
atgacccaga gccccagcag cctgtctgcc agcgtgggcg acagagtgac catcacctgt 420
caggccagcc agaacatcta cgtgtggctg aactggtatc agcagaagcc cggcaaggcc 480
cccaagctgc tgatctacaa ggccagcaac ctgcacaccg gcgtgcccag cagattttct 540
ggcagcggct ccggcaccga cttcaccctg acaatcagct ccctgcagcc cgaggacatt 600
gccacctact actgccagca gggccagacc tacccctaca cctttggcca gggcaccaag 660
ctggaaatca aggataagac ccacacccgt acggtggccg ctcccagcgt gttcatcttc 720
ccacctagcg acgagcagct gaagtccggc acagcctctg tcgtgtgcct gctgaacaac 780
ttctaccccc gcgaggccaa agtgcagtgg aaggtggaca acgccctgca gagcggcaac 840
agccaggaaa gcgtgaccga gcaggacagc aaggactcca cctacagcct gagcagcacc 900
ctgacactga gcaaggccga ctacgagaag cacaaggtgt acgcctgcga agtgacccac 960
cagggcctgt ctagccccgt gaccaagagc ttcaaccggg gcgagtgt 1008
<210> 238
<211> 1740
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 238
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
gacaaaaccc atacccaggt gcagctggtg gaatctggcg gcggagtggt gcagcctggc 420
agaagcctga gactgagctg tgccgccagc ggcttcacct tcaccaaggc ctggatgcac 480
tgggtgcgcc aggcccctgg aaagcagctg gaatgggtgg cccagatcaa ggacaagagc 540
aacagctacg ccacctacta cgccgacagc gtgaagggcc ggttcaccat cagccgggac 600
gacagcaaga acaccctgta cctgcagatg aacagcctgc gggccgagga caccgccgtg 660
tactactgtc ggggcgtgta ctatgccctg agccccttcg attactgggg ccagggaacc 720
ctcgtgaccg tgtctagtga taagacccac accgccagca caaagggccc cagcgtgttc 780
cctctggccc ctagcagcaa gagcacatct ggcggaacag ccgccctggg ctgcctcgtg 840
aaggactact ttcccgagcc cgtgaccgtg tcctggaatt ctggcgccct gaccagcggc 900
gtgcacacct ttccagctgt gctgcagtcc agcggcctgt acagcctgag cagcgtcgtg 960
acagtgccca gcagctctct gggcacccag acctacatct gcaacgtgaa ccacaagccc 1020
agcaacacca aggtggacaa gaaggtggaa cccaagagct gcgacaagac ccacacctgt 1080
cccccttgtc ctgcccccga actgctggga ggcccttccg tgttcctgtt ccccccaaag 1140
cccaaggaca ccctgatgat cagccggacc cccgaagtga cctgcgtggt ggtggatgtg 1200
tcccacgagg accctgaagt gaagttcaat tggtacgtgg acggcgtgga agtgcacaac 1260
gccaagacca agccaagaga ggaacagtac aacaatgcct cccgggtggt gtccgtgctg 1320
accgtgctgc accaggactg gctgaacggc aaagagtaca agtgcaaggt gtccaacaag 1380
gccctgcctg cccccatcga gaaaaccatc agcaaggcca agggccagcc ccgcgaaccc 1440
caggtgtgca cactgccccc aagcagggac gagctgacca agaaccaggt gtccctgagc 1500
tgtgccgtga aaggcttcta cccctccgat atcgccgtgg aatgggagag caacggccag 1560
cccgagaaca actacaagac caccccccct gtgctggaca gcgacggctc attcttcctg 1620
gtgtccaagc tgacagtgga caagtcccgg tggcagcagg gcaacgtgtt cagctgctcc 1680
gtgatgcacg aggccctgca caaccactac acccagaagt ccctgagcct gagccccggc 1740
<210> 239
<211> 1353
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 239
agagcccacc tggtgcagtc tggcaccgcc atgaagaaac caggcgcctc tgtgcgggtg 60
tcctgtcaga caagcggcta caccttcacc gcccacatcc tgttctggtt ccggcaggcc 120
cctggcagag gactggaatg ggtgggatgg atcaagcccc agtatggcgc cgtgaacttc 180
ggcggaggct tccgggatag agtgaccctg acccgggacg tgtaccgcga gatcgcctac 240
atggacatcc ggggcctgaa gcccgatgac accgccgtgt actactgcgc cagagacaga 300
agctacggcg acagcagctg ggctctggat gcttggggcc agggcacaac cgtggtggtg 360
tctgccgcct ctacaaaggg cccatcggtc ttccccctgg caccctcctc caagagcacc 420
tctgggggca cagcggccct gggctgcctg gtcaaggact acttccccga accggtgacg 480
gtgtcgtgga actcaggcgc cctgaccagc ggcgtgcaca ccttcccggc tgtcctacag 540
tcctcaggac tctactccct cagcagcgtg gtgaccgtgc cctccagcag cttgggcacc 600
cagacctaca tctgcaacgt gaatcacaag cccagcaaca ccaaggtgga caagaaagtt 660
gagcccaaat cttgtgacaa aactcacaca tgcccaccgt gcccagcacc tgaactcctg 720
gggggaccgt cagtcttcct cttcccccca aaacccaagg acaccctcat gatctcccgg 780
acccctgagg tcacatgcgt ggtggtggac gtgagccacg aagaccctga ggtcaagttc 840
aactggtatg ttgacggcgt ggaggtgcat aatgccaaga caaagccgcg ggaggagcag 900
tacaacaatg cctcccgtgt ggtcagcgtc ctcaccgtcc tgcaccagga ctggctgaat 960
ggcaaggagt acaagtgcaa ggtctccaac aaagccctcc cagcccccat cgagaaaacc 1020
atctccaaag ccaaagggca gccccgagaa ccacaggtgt acaccctgcc cccatgccgg 1080
gatgagctga ccaagaatca agtcagcctg tggtgcctgg taaaaggctt ctatcccagc 1140
gacatcgccg tggagtggga gagcaatggg cagccggaga acaactacaa gaccacgcct 1200
cccgtgctgg actccgacgg ctccttcttc ctctactcaa aactcaccgt ggacaagagc 1260
aggtggcagc aggggaacgt cttctcatgc tccgtgatgc atgaggctct gcacaaccac 1320
tacacgcaga agagcctctc cctgtctccg ggt 1353
<210> 240
<211> 630
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 240
tacatccacg tgacccagag ccccagcagc ctgtccgtgt ccatcggcga cagagtgacc 60
atcaactgcc agacctctca gggcgtgggc agcgacctgc actggtatca gcacaagcct 120
ggcagagccc ccaagctgct gatccaccac acaagcagcg tggaagatgg cgtgcccagc 180
agattttccg gcagcggctt ccacaccagc ttcaacctga ccatcagcga tctgcaggcc 240
gacgacattg ccacctacta ttgtcaggtg ctgcagttct tcggcagagg cagcagactg 300
cacatcaagc gtacggtggc cgctcccagc gtgttcatct tcccacctag cgacgagcag 360
ctgaagtccg gcacagcctc tgtcgtgtgc ctgctgaaca acttctaccc ccgcgaggcc 420
aaagtgcagt ggaaggtgga caacgccctg cagagcggca acagccagga aagcgtgacc 480
gagcaggaca gcaaggactc cacctacagc ctgagcagca ccctgacact gagcaaggcc 540
gactacgaga agcacaaggt gtacgcctgc gaagtgaccc accagggcct gtctagcccc 600
gtgaccaaga gcttcaaccg gggcgagtgt 630
<210> 241
<211> 1002
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 241
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacgacaacg cccagaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaaggaca aaacccatac cgacatccag 360
atgacccaga gccccagcag cctgtctgcc agcgtgggcg acagagtgac catcacctgt 420
caggccagcc agaacatcta cgtgtggctg aactggtatc agcagaagcc cggcaaggcc 480
cccaagctgc tgatctacaa ggccagcaac ctgcacaccg gcgtgcccag cagattttct 540
ggcagcggct ccggcaccga cttcaccctg acaatcagct ccctgcagcc cgaggacatt 600
gccacctact actgccagca gggccagacc tacccctaca cctttggcca gggcaccaag 660
ctggaaatca aggataagac ccacaccagt cagcccaagg ctgccccctc ggtcactctg 720
ttcccgccct cgagtgagga gcttcaagcc aacaaggcca cactggtgtg tctcataagt 780
gacttctacc cgggagccgt gacagtggcc tggaaggcag atagcagccc cgtcaaggcg 840
ggagtggaga ccaccacacc ctccaaacaa agcaacaaca agtacgcggc cagcagctac 900
ctgagcctga cgcctgagca gtggaagtcc cacagaagct acagctgcca ggtcacgcat 960
gaagggagca ccgtggagaa gacagtggcc cctacagaat gt 1002
<210> 242
<211> 1731
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 242
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
gacaaaaccc atacccaggt gcagctggtg gaatctggcg gcggagtggt gcagcctggc 420
agaagcctga gactgagctg tgccgccagc ggcttcacct tcaccaaggc ctggatgcac 480
tgggtgcgcc aggcccctgg aaagcagctg gaatgggtgg cccagatcaa ggacaagagc 540
aacagctacg ccacctacta cgccgacagc gtgaagggcc ggttcaccat cagccgggac 600
gacagcaaga acaccctgta cctgcagatg aacagcctgc gggccgagga caccgccgtg 660
tactactgtc ggggcgtgta ctatgccctg agccccttcg attactgggg ccagggaacc 720
ctcgtgaccg tgtctagtga taagacccac accgccagca caaagggccc atcggtgttc 780
cctctggccc cttgcagcag aagcaccagc gaatctacag ccgccctggg ctgcctcgtg 840
aaggactact ttcccgagcc cgtgaccgtg tcctggaact ctggcgctct gacaagcggc 900
gtgcacacct ttccagccgt gctccagagc agcggcctgt actctctgag cagcgtcgtg 960
acagtgccca gcagcagcct gggcaccaag acctacacct gtaacgtgga ccacaagccc 1020
agcaacacca aggtggacaa gcgggtggaa tctaagtacg gccctccctg ccctccttgc 1080
ccagcccctg aagctgccgg cggaccctcc gtgttcctgt tccccccaaa gcccaaggac 1140
accctgatga tcagccggac ccccgaagtg acctgcgtgg tggtggatgt gtcccaggaa 1200
gatcccgagg tgcagttcaa ttggtacgtg gacggcgtgg aagtgcacaa cgccaagacc 1260
aagcccagag aggaacagtt caacagcacc taccgggtgg tgtccgtgct gaccgtgctg 1320
caccaggact ggctgaacgg caaagagtac aagtgcaagg tgtccaacaa gggcctgccc 1380
agctccatcg agaaaaccat cagcaaggcc aagggccagc cccgcgagcc tcaagtgtgt 1440
accctgcccc ctagccagga agagatgacc aagaaccagg tgtccctgag ctgtgccgtg 1500
aaaggcttct accccagcga cattgccgtg gaatgggaga gcaacggcca gcccgagaac 1560
aactacaaga ccaccccccc tgtgctggac agcgacggct cattcttcct ggtgtccaag 1620
ctgaccgtgg acaagagccg gtggcaggaa ggcaacgtgt tcagctgctc cgtgatgcac 1680
gaggccctgc acaaccacta cacccagaag tccctgtctc tgtccctggg c 1731
<210> 243
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<220>
<221> другой_признак
<222> 439
<223> n = A,T,C или G
<400> 243
agagcccacc tggtgcagtc tggcaccgcc atgaagaaac caggcgcctc tgtgcgggtg 60
tcctgtcaga caagcggcta caccttcacc gcccacatcc tgttctggtt ccggcaggcc 120
cctggcagag gactggaatg ggtgggatgg atcaagcccc agtatggcgc cgtgaacttc 180
ggcggaggct tccgggatag agtgaccctg acccgggacg tgtaccgcga gatcgcctac 240
atggacatcc ggggcctgaa gcccgatgac accgccgtgt actactgcgc cagagacaga 300
agctacggcg acagcagctg ggctctggat gcttggggcc agggcacaac cgtggtggtg 360
tctgccgcct ctacaaaggg cccatcggtg ttccctctgg ccccttgcag cagaagcacc 420
agcgaatcta cagccgccnt gggctgcctc gtgaaggact actttcccga gcccgtgacc 480
gtgtcctgga actctggcgc tctgacaagc ggcgtgcaca cctttccagc cgtgctccag 540
agcagcggcc tgtactctct gagcagcgtc gtgacagtgc ccagcagcag cctgggcacc 600
aagacctaca cctgtaacgt ggaccacaag cccagcaaca ccaaggtgga caagcgggtg 660
gaatctaagt acggccctcc ctgccctcct tgcccagccc ctgaagctgc cggcggaccc 720
tccgtgttcc tgttcccccc aaagcccaag gacaccctga tgatcagccg gacccccgaa 780
gtgacctgcg tggtggtgga tgtgtcccag gaagatcccg aggtgcagtt caattggtac 840
gtggacggcg tggaagtgca caacgccaag accaagccca gagaggaaca gttcaacagc 900
acctaccggg tggtgtccgt gctgaccgtg ctgcaccagg actggctgaa cggcaaagag 960
tacaagtgca aggtgtccaa caagggcctg cccagctcca tcgagaaaac catcagcaag 1020
gccaagggcc agccccgcga gcctcaagtg tataccctgc ccccttgcca ggaagagatg 1080
accaagaacc aggtgtccct gtggtgtctc gtgaaaggct tctaccccag cgacattgcc 1140
gtggaatggg agagcaacgg ccagcccgag aacaactaca agaccacccc ccctgtgctg 1200
gacagcgacg gctcattctt cctgtactcc aagctgaccg tggacaagag ccggtggcag 1260
gaaggcaacg tgttcagctg ctccgtgatg cacgaggccc tgcacaacca ctacacccag 1320
aagtccctgt ctctgtccct gggc 1344
<210> 244
<211> 630
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 244
tacatccacg tgacccagag ccccagcagc ctgtccgtgt ccatcggcga cagagtgacc 60
atcaactgcc agacctctca gggcgtgggc agcgacctgc actggtatca gcacaagcct 120
ggcagagccc ccaagctgct gatccaccac acaagcagcg tggaagatgg cgtgcccagc 180
agattttccg gcagcggctt ccacaccagc ttcaacctga ccatcagcga tctgcaggcc 240
gacgacattg ccacctacta ttgtcaggtg ctgcagttct tcggcagagg cagcagactg 300
cacatcaagc gtacggtggc cgctcccagc gtgttcatct tcccacctag cgacgagcag 360
ctgaagtccg gcacagcctc tgtcgtgtgc ctgctgaaca acttctaccc ccgcgaggcc 420
aaagtgcagt ggaaggtgga caacgccctg cagagcggca acagccagga aagcgtgacc 480
gagcaggaca gcaaggactc cacctacagc ctgagcagca ccctgacact gagcaaggcc 540
gactacgaga agcacaaggt gtacgcctgc gaagtgaccc accagggcct gtctagcccc 600
gtgaccaaga gcttcaaccg gggcgagtgt 630
<210> 245
<211> 1008
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 245
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacgagaacc tgcagaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaaggaca aaacccatac cgacatccag 360
atgacccaga gccccagcag cctgtctgcc agcgtgggcg acagagtgac catcacctgt 420
caggccagcc agaacatcta cgtgtggctg aactggtatc agcagaagcc cggcaaggcc 480
cccaagctgc tgatctacaa ggccagcaac ctgcacaccg gcgtgcccag cagattttct 540
ggcagcggct ccggcaccga cttcaccctg acaatcagct ccctgcagcc cgaggacatt 600
gccacctact actgccagca gggccagacc tacccctaca cctttggcca gggcaccaag 660
ctggaaatca aggataagac ccacacccgt acggtggccg ctcccagcgt gttcatcttc 720
ccacctagcg acgagcagct gaagtccggc acagcctctg tcgtgtgcct gctgaacaac 780
ttctaccccc gcgaggccaa agtgcagtgg aaggtggaca acgccctgca gagcggcaac 840
agccaggaaa gcgtgaccga gcaggacagc aaggactcca cctacagcct gagcagcacc 900
ctgacactga gcaaggccga ctacgagaag cacaaggtgt acgcctgcga agtgacccac 960
cagggcctgt ctagccccgt gaccaagagc ttcaaccggg gcgagtgt 1008
<210> 246
<211> 1731
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 246
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
gacaaaaccc atacccaggt gcagctggtg gaatctggcg gcggagtggt gcagcctggc 420
agaagcctga gactgagctg tgccgccagc ggcttcacct tcaccaaggc ctggatgcac 480
tgggtgcgcc aggcccctgg aaagcagctg gaatgggtgg cccagatcaa ggacaagagc 540
aacagctacg ccacctacta cgccgacagc gtgaagggcc ggttcaccat cagccgggac 600
gacagcaaga acaccctgta cctgcagatg aacagcctgc gggccgagga caccgccgtg 660
tactactgtc ggggcgtgta ctatgccctg agccccttcg attactgggg ccagggaacc 720
ctcgtgaccg tgtctagtga taagacccac accgccagca caaagggccc atcggtgttc 780
cctctggccc cttgcagcag aagcaccagc gaatctacag ccgccctggg ctgcctcgtg 840
aaggactact ttcccgagcc cgtgaccgtg tcctggaact ctggcgctct gacaagcggc 900
gtgcacacct ttccagccgt gctccagagc agcggcctgt actctctgag cagcgtcgtg 960
acagtgccca gcagcagcct gggcaccaag acctacacct gtaacgtgga ccacaagccc 1020
agcaacacca aggtggacaa gcgggtggaa tctaagtacg gccctccctg ccctccttgc 1080
ccagcccctg aagctgccgg cggaccctcc gtgttcctgt tccccccaaa gcccaaggac 1140
accctgatga tcagccggac ccccgaagtg acctgcgtgg tggtggatgt gtcccaggaa 1200
gatcccgagg tgcagttcaa ttggtacgtg gacggcgtgg aagtgcacaa cgccaagacc 1260
aagcccagag aggaacagtt caacagcacc taccgggtgg tgtccgtgct gaccgtgctg 1320
caccaggact ggctgaacgg caaagagtac aagtgcaagg tgtccaacaa gggcctgccc 1380
agctccatcg agaaaaccat cagcaaggcc aagggccagc cccgcgagcc tcaagtgtgt 1440
accctgcccc ctagccagga agagatgacc aagaaccagg tgtccctgag ctgtgccgtg 1500
aaaggcttct accccagcga cattgccgtg gaatgggaga gcaacggcca gcccgagaac 1560
aactacaaga ccaccccccc tgtgctggac agcgacggct cattcttcct ggtgtccaag 1620
ctgaccgtgg acaagagccg gtggcaggaa ggcaacgtgt tcagctgctc cgtgatgcac 1680
gaggccctgc acaaccacta cacccagaag tccctgtctc tgtccctggg c 1731
<210> 247
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<220>
<221> другой_признак
<222> 439
<223> n = A,T,C или G
<400> 247
agagcccacc tggtgcagtc tggcaccgcc atgaagaaac caggcgcctc tgtgcgggtg 60
tcctgtcaga caagcggcta caccttcacc gcccacatcc tgttctggtt ccggcaggcc 120
cctggcagag gactggaatg ggtgggatgg atcaagcccc agtatggcgc cgtgaacttc 180
ggcggaggct tccgggatag agtgaccctg acccgggacg tgtaccgcga gatcgcctac 240
atggacatcc ggggcctgaa gcccgatgac accgccgtgt actactgcgc cagagacaga 300
agctacggcg acagcagctg ggctctggat gcttggggcc agggcacaac cgtggtggtg 360
tctgccgcct ctacaaaggg cccatcggtg ttccctctgg ccccttgcag cagaagcacc 420
agcgaatcta cagccgccnt gggctgcctc gtgaaggact actttcccga gcccgtgacc 480
gtgtcctgga actctggcgc tctgacaagc ggcgtgcaca cctttccagc cgtgctccag 540
agcagcggcc tgtactctct gagcagcgtc gtgacagtgc ccagcagcag cctgggcacc 600
aagacctaca cctgtaacgt ggaccacaag cccagcaaca ccaaggtgga caagcgggtg 660
gaatctaagt acggccctcc ctgccctcct tgcccagccc ctgaagctgc cggcggaccc 720
tccgtgttcc tgttcccccc aaagcccaag gacaccctga tgatcagccg gacccccgaa 780
gtgacctgcg tggtggtgga tgtgtcccag gaagatcccg aggtgcagtt caattggtac 840
gtggacggcg tggaagtgca caacgccaag accaagccca gagaggaaca gttcaacagc 900
acctaccggg tggtgtccgt gctgaccgtg ctgcaccagg actggctgaa cggcaaagag 960
tacaagtgca aggtgtccaa caagggcctg cccagctcca tcgagaaaac catcagcaag 1020
gccaagggcc agccccgcga gcctcaagtg tataccctgc ccccttgcca ggaagagatg 1080
accaagaacc aggtgtccct gtggtgtctc gtgaaaggct tctaccccag cgacattgcc 1140
gtggaatggg agagcaacgg ccagcccgag aacaactaca agaccacccc ccctgtgctg 1200
gacagcgacg gctcattctt cctgtactcc aagctgaccg tggacaagag ccggtggcag 1260
gaaggcaacg tgttcagctg ctccgtgatg cacgaggccc tgcacaacca ctacacccag 1320
aagtccctgt ctctgtccct gggc 1344
<210> 248
<211> 630
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 248
tacatccacg tgacccagag ccccagcagc ctgtccgtgt ccatcggcga cagagtgacc 60
atcaactgcc agacctctca gggcgtgggc agcgacctgc actggtatca gcacaagcct 120
ggcagagccc ccaagctgct gatccaccac acaagcagcg tggaagatgg cgtgcccagc 180
agattttccg gcagcggctt ccacaccagc ttcaacctga ccatcagcga tctgcaggcc 240
gacgacattg ccacctacta ttgtcaggtg ctgcagttct tcggcagagg cagcagactg 300
cacatcaagc gtacggtggc cgctcccagc gtgttcatct tcccacctag cgacgagcag 360
ctgaagtccg gcacagcctc tgtcgtgtgc ctgctgaaca acttctaccc ccgcgaggcc 420
aaagtgcagt ggaaggtgga caacgccctg cagagcggca acagccagga aagcgtgacc 480
gagcaggaca gcaaggactc cacctacagc ctgagcagca ccctgacact gagcaaggcc 540
gactacgaga agcacaaggt gtacgcctgc gaagtgaccc accagggcct gtctagcccc 600
gtgaccaaga gcttcaaccg gggcgagtgt 630
<210> 249
<211> 1008
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 249
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacgagaacc tgcgtaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaaggaca aaacccatac cgacatccag 360
atgacccaga gccccagcag cctgtctgcc agcgtgggcg acagagtgac catcacctgt 420
caggccagcc agaacatcta cgtgtggctg aactggtatc agcagaagcc cggcaaggcc 480
cccaagctgc tgatctacaa ggccagcaac ctgcacaccg gcgtgcccag cagattttct 540
ggcagcggct ccggcaccga cttcaccctg acaatcagct ccctgcagcc cgaggacatt 600
gccacctact actgccagca gggccagacc tacccctaca cctttggcca gggcaccaag 660
ctggaaatca aggataagac ccacacccgt acggtggccg ctcccagcgt gttcatcttc 720
ccacctagcg acgagcagct gaagtccggc acagcctctg tcgtgtgcct gctgaacaac 780
ttctaccccc gcgaggccaa agtgcagtgg aaggtggaca acgccctgca gagcggcaac 840
agccaggaaa gcgtgaccga gcaggacagc aaggactcca cctacagcct gagcagcacc 900
ctgacactga gcaaggccga ctacgagaag cacaaggtgt acgcctgcga agtgacccac 960
cagggcctgt ctagccccgt gaccaagagc ttcaaccggg gcgagtgt 1008
<210> 250
<211> 1731
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 250
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
gacaaaaccc atacccaggt gcagctggtg gaatctggcg gcggagtggt gcagcctggc 420
agaagcctga gactgagctg tgccgccagc ggcttcacct tcaccaaggc ctggatgcac 480
tgggtgcgcc aggcccctgg aaagcagctg gaatgggtgg cccagatcaa ggacaagagc 540
aacagctacg ccacctacta cgccgacagc gtgaagggcc ggttcaccat cagccgggac 600
gacagcaaga acaccctgta cctgcagatg aacagcctgc gggccgagga caccgccgtg 660
tactactgtc ggggcgtgta ctatgccctg agccccttcg attactgggg ccagggaacc 720
ctcgtgaccg tgtctagtga taagacccac accgccagca caaagggccc atcggtgttc 780
cctctggccc cttgcagcag aagcaccagc gaatctacag ccgccctggg ctgcctcgtg 840
aaggactact ttcccgagcc cgtgaccgtg tcctggaact ctggcgctct gacaagcggc 900
gtgcacacct ttccagccgt gctccagagc agcggcctgt actctctgag cagcgtcgtg 960
acagtgccca gcagcagcct gggcaccaag acctacacct gtaacgtgga ccacaagccc 1020
agcaacacca aggtggacaa gcgggtggaa tctaagtacg gccctccctg ccctccttgc 1080
ccagcccctg aagctgccgg cggaccctcc gtgttcctgt tccccccaaa gcccaaggac 1140
accctgatga tcagccggac ccccgaagtg acctgcgtgg tggtggatgt gtcccaggaa 1200
gatcccgagg tgcagttcaa ttggtacgtg gacggcgtgg aagtgcacaa cgccaagacc 1260
aagcccagag aggaacagtt caacagcacc taccgggtgg tgtccgtgct gaccgtgctg 1320
caccaggact ggctgaacgg caaagagtac aagtgcaagg tgtccaacaa gggcctgccc 1380
agctccatcg agaaaaccat cagcaaggcc aagggccagc cccgcgagcc tcaagtgtgt 1440
accctgcccc ctagccagga agagatgacc aagaaccagg tgtccctgag ctgtgccgtg 1500
aaaggcttct accccagcga cattgccgtg gaatgggaga gcaacggcca gcccgagaac 1560
aactacaaga ccaccccccc tgtgctggac agcgacggct cattcttcct ggtgtccaag 1620
ctgaccgtgg acaagagccg gtggcaggaa ggcaacgtgt tcagctgctc cgtgatgcac 1680
gaggccctgc acaaccacta cacccagaag tccctgtctc tgtccctggg c 1731
<210> 251
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<220>
<221> другой_признак
<222> 439
<223> n = A,T,C или G
<400> 251
agagcccacc tggtgcagtc tggcaccgcc atgaagaaac caggcgcctc tgtgcgggtg 60
tcctgtcaga caagcggcta caccttcacc gcccacatcc tgttctggtt ccggcaggcc 120
cctggcagag gactggaatg ggtgggatgg atcaagcccc agtatggcgc cgtgaacttc 180
ggcggaggct tccgggatag agtgaccctg acccgggacg tgtaccgcga gatcgcctac 240
atggacatcc ggggcctgaa gcccgatgac accgccgtgt actactgcgc cagagacaga 300
agctacggcg acagcagctg ggctctggat gcttggggcc agggcacaac cgtggtggtg 360
tctgccgcct ctacaaaggg cccatcggtg ttccctctgg ccccttgcag cagaagcacc 420
agcgaatcta cagccgccnt gggctgcctc gtgaaggact actttcccga gcccgtgacc 480
gtgtcctgga actctggcgc tctgacaagc ggcgtgcaca cctttccagc cgtgctccag 540
agcagcggcc tgtactctct gagcagcgtc gtgacagtgc ccagcagcag cctgggcacc 600
aagacctaca cctgtaacgt ggaccacaag cccagcaaca ccaaggtgga caagcgggtg 660
gaatctaagt acggccctcc ctgccctcct tgcccagccc ctgaagctgc cggcggaccc 720
tccgtgttcc tgttcccccc aaagcccaag gacaccctga tgatcagccg gacccccgaa 780
gtgacctgcg tggtggtgga tgtgtcccag gaagatcccg aggtgcagtt caattggtac 840
gtggacggcg tggaagtgca caacgccaag accaagccca gagaggaaca gttcaacagc 900
acctaccggg tggtgtccgt gctgaccgtg ctgcaccagg actggctgaa cggcaaagag 960
tacaagtgca aggtgtccaa caagggcctg cccagctcca tcgagaaaac catcagcaag 1020
gccaagggcc agccccgcga gcctcaagtg tataccctgc ccccttgcca ggaagagatg 1080
accaagaacc aggtgtccct gtggtgtctc gtgaaaggct tctaccccag cgacattgcc 1140
gtggaatggg agagcaacgg ccagcccgag aacaactaca agaccacccc ccctgtgctg 1200
gacagcgacg gctcattctt cctgtactcc aagctgaccg tggacaagag ccggtggcag 1260
gaaggcaacg tgttcagctg ctccgtgatg cacgaggccc tgcacaacca ctacacccag 1320
aagtccctgt ctctgtccct gggc 1344
<210> 252
<211> 630
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 252
tacatccacg tgacccagag ccccagcagc ctgtccgtgt ccatcggcga cagagtgacc 60
atcaactgcc agacctctca gggcgtgggc agcgacctgc actggtatca gcacaagcct 120
ggcagagccc ccaagctgct gatccaccac acaagcagcg tggaagatgg cgtgcccagc 180
agattttccg gcagcggctt ccacaccagc ttcaacctga ccatcagcga tctgcaggcc 240
gacgacattg ccacctacta ttgtcaggtg ctgcagttct tcggcagagg cagcagactg 300
cacatcaagc gtacggtggc cgctcccagc gtgttcatct tcccacctag cgacgagcag 360
ctgaagtccg gcacagcctc tgtcgtgtgc ctgctgaaca acttctaccc ccgcgaggcc 420
aaagtgcagt ggaaggtgga caacgccctg cagagcggca acagccagga aagcgtgacc 480
gagcaggaca gcaaggactc cacctacagc ctgagcagca ccctgacact gagcaaggcc 540
gactacgaga agcacaaggt gtacgcctgc gaagtgaccc accagggcct gtctagcccc 600
gtgaccaaga gcttcaaccg gggcgagtgt 630
<210> 253
<211> 1008
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 253
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacgagaacc tgttcaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaaggaca aaacccatac cgacatccag 360
atgacccaga gccccagcag cctgtctgcc agcgtgggcg acagagtgac catcacctgt 420
caggccagcc agaacatcta cgtgtggctg aactggtatc agcagaagcc cggcaaggcc 480
cccaagctgc tgatctacaa ggccagcaac ctgcacaccg gcgtgcccag cagattttct 540
ggcagcggct ccggcaccga cttcaccctg acaatcagct ccctgcagcc cgaggacatt 600
gccacctact actgccagca gggccagacc tacccctaca cctttggcca gggcaccaag 660
ctggaaatca aggataagac ccacacccgt acggtggccg ctcccagcgt gttcatcttc 720
ccacctagcg acgagcagct gaagtccggc acagcctctg tcgtgtgcct gctgaacaac 780
ttctaccccc gcgaggccaa agtgcagtgg aaggtggaca acgccctgca gagcggcaac 840
agccaggaaa gcgtgaccga gcaggacagc aaggactcca cctacagcct gagcagcacc 900
ctgacactga gcaaggccga ctacgagaag cacaaggtgt acgcctgcga agtgacccac 960
cagggcctgt ctagccccgt gaccaagagc ttcaaccggg gcgagtgt 1008
<210> 254
<211> 1731
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 254
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
gacaaaaccc atacccaggt gcagctggtg gaatctggcg gcggagtggt gcagcctggc 420
agaagcctga gactgagctg tgccgccagc ggcttcacct tcaccaaggc ctggatgcac 480
tgggtgcgcc aggcccctgg aaagcagctg gaatgggtgg cccagatcaa ggacaagagc 540
aacagctacg ccacctacta cgccgacagc gtgaagggcc ggttcaccat cagccgggac 600
gacagcaaga acaccctgta cctgcagatg aacagcctgc gggccgagga caccgccgtg 660
tactactgtc ggggcgtgta ctatgccctg agccccttcg attactgggg ccagggaacc 720
ctcgtgaccg tgtctagtga taagacccac accgccagca caaagggccc atcggtgttc 780
cctctggccc cttgcagcag aagcaccagc gaatctacag ccgccctggg ctgcctcgtg 840
aaggactact ttcccgagcc cgtgaccgtg tcctggaact ctggcgctct gacaagcggc 900
gtgcacacct ttccagccgt gctccagagc agcggcctgt actctctgag cagcgtcgtg 960
acagtgccca gcagcagcct gggcaccaag acctacacct gtaacgtgga ccacaagccc 1020
agcaacacca aggtggacaa gcgggtggaa tctaagtacg gccctccctg ccctccttgc 1080
ccagcccctg aagctgccgg cggaccctcc gtgttcctgt tccccccaaa gcccaaggac 1140
accctgatga tcagccggac ccccgaagtg acctgcgtgg tggtggatgt gtcccaggaa 1200
gatcccgagg tgcagttcaa ttggtacgtg gacggcgtgg aagtgcacaa cgccaagacc 1260
aagcccagag aggaacagtt caacagcacc taccgggtgg tgtccgtgct gaccgtgctg 1320
caccaggact ggctgaacgg caaagagtac aagtgcaagg tgtccaacaa gggcctgccc 1380
agctccatcg agaaaaccat cagcaaggcc aagggccagc cccgcgagcc tcaagtgtgt 1440
accctgcccc ctagccagga agagatgacc aagaaccagg tgtccctgag ctgtgccgtg 1500
aaaggcttct accccagcga cattgccgtg gaatgggaga gcaacggcca gcccgagaac 1560
aactacaaga ccaccccccc tgtgctggac agcgacggct cattcttcct ggtgtccaag 1620
ctgaccgtgg acaagagccg gtggcaggaa ggcaacgtgt tcagctgctc cgtgatgcac 1680
gaggccctgc acaaccacta cacccagaag tccctgtctc tgtccctggg c 1731
<210> 255
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<220>
<221> другой_признак
<222> 439
<223> n = A,T,C или G
<400> 255
agagcccacc tggtgcagtc tggcaccgcc atgaagaaac caggcgcctc tgtgcgggtg 60
tcctgtcaga caagcggcta caccttcacc gcccacatcc tgttctggtt ccggcaggcc 120
cctggcagag gactggaatg ggtgggatgg atcaagcccc agtatggcgc cgtgaacttc 180
ggcggaggct tccgggatag agtgaccctg acccgggacg tgtaccgcga gatcgcctac 240
atggacatcc ggggcctgaa gcccgatgac accgccgtgt actactgcgc cagagacaga 300
agctacggcg acagcagctg ggctctggat gcttggggcc agggcacaac cgtggtggtg 360
tctgccgcct ctacaaaggg cccatcggtg ttccctctgg ccccttgcag cagaagcacc 420
agcgaatcta cagccgccnt gggctgcctc gtgaaggact actttcccga gcccgtgacc 480
gtgtcctgga actctggcgc tctgacaagc ggcgtgcaca cctttccagc cgtgctccag 540
agcagcggcc tgtactctct gagcagcgtc gtgacagtgc ccagcagcag cctgggcacc 600
aagacctaca cctgtaacgt ggaccacaag cccagcaaca ccaaggtgga caagcgggtg 660
gaatctaagt acggccctcc ctgccctcct tgcccagccc ctgaagctgc cggcggaccc 720
tccgtgttcc tgttcccccc aaagcccaag gacaccctga tgatcagccg gacccccgaa 780
gtgacctgcg tggtggtgga tgtgtcccag gaagatcccg aggtgcagtt caattggtac 840
gtggacggcg tggaagtgca caacgccaag accaagccca gagaggaaca gttcaacagc 900
acctaccggg tggtgtccgt gctgaccgtg ctgcaccagg actggctgaa cggcaaagag 960
tacaagtgca aggtgtccaa caagggcctg cccagctcca tcgagaaaac catcagcaag 1020
gccaagggcc agccccgcga gcctcaagtg tataccctgc ccccttgcca ggaagagatg 1080
accaagaacc aggtgtccct gtggtgtctc gtgaaaggct tctaccccag cgacattgcc 1140
gtggaatggg agagcaacgg ccagcccgag aacaactaca agaccacccc ccctgtgctg 1200
gacagcgacg gctcattctt cctgtactcc aagctgaccg tggacaagag ccggtggcag 1260
gaaggcaacg tgttcagctg ctccgtgatg cacgaggccc tgcacaacca ctacacccag 1320
aagtccctgt ctctgtccct gggc 1344
<210> 256
<211> 630
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 256
tacatccacg tgacccagag ccccagcagc ctgtccgtgt ccatcggcga cagagtgacc 60
atcaactgcc agacctctca gggcgtgggc agcgacctgc actggtatca gcacaagcct 120
ggcagagccc ccaagctgct gatccaccac acaagcagcg tggaagatgg cgtgcccagc 180
agattttccg gcagcggctt ccacaccagc ttcaacctga ccatcagcga tctgcaggcc 240
gacgacattg ccacctacta ttgtcaggtg ctgcagttct tcggcagagg cagcagactg 300
cacatcaagc gtacggtggc cgctcccagc gtgttcatct tcccacctag cgacgagcag 360
ctgaagtccg gcacagcctc tgtcgtgtgc ctgctgaaca acttctaccc ccgcgaggcc 420
aaagtgcagt ggaaggtgga caacgccctg cagagcggca acagccagga aagcgtgacc 480
gagcaggaca gcaaggactc cacctacagc ctgagcagca ccctgacact gagcaaggcc 540
gactacgaga agcacaaggt gtacgcctgc gaagtgaccc accagggcct gtctagcccc 600
gtgaccaaga gcttcaaccg gggcgagtgt 630
<210> 257
<211> 1008
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 257
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacgagaacc tgcagaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaaggaca aaacccatac cgacatccag 360
atgacccaga gccccagcag cctgtctgcc agcgtgggcg acagagtgac catcacctgt 420
caggccagcc agaacatcta cgtgtggctg aactggtatc agcagaagcc cggcaaggcc 480
cccaagctgc tgatctacaa ggccagcaac ctgcacaccg gcgtgcccag cagattttct 540
ggcagcggct ccggcaccga cttcaccctg acaatcagct ccctgcagcc cgaggacatt 600
gccacctact actgccagca gggccagacc tacccctaca cctttggcca gggcaccaag 660
ctggaaatca aggataagac ccacacccgt acggtggccg ctcccagcgt gttcatcttc 720
ccacctagcg acgagcagct gaagtccggc acagcctctg tcgtgtgcct gctgaacaac 780
ttctaccccc gcgaggccaa agtgcagtgg aaggtggaca acgccctgca gagcggcaac 840
agccaggaaa gcgtgaccga gcaggacagc aaggactcca cctacagcct gagcagcacc 900
ctgacactga gcaaggccga ctacgagaag cacaaggtgt acgcctgcga agtgacccac 960
cagggcctgt ctagccccgt gaccaagagc ttcaaccggg gcgagtgt 1008
<210> 258
<211> 1731
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 258
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
gacaaaaccc atacccaggt gcagctggtg gaatctggcg gcggagtggt gcagcctggc 420
agaagcctga gactgagctg tgccgccagc ggcttcacct tcaccaaggc ctggatgcac 480
tgggtgcgcc aggcccctgg aaagcagctg gaatgggtgg cccagatcaa ggacaagagc 540
aacagctacg ccacctacta cgccgacagc gtgaagggcc ggttcaccat cagccgggac 600
gacagcaaga acaccctgta cctgcagatg aacagcctgc gggccgagga caccgccgtg 660
tactactgtc ggggcgtgta ctatgccctg agccccttcg attactgggg ccagggaacc 720
ctcgtgaccg tgtctagtga taagacccac accgccagca caaagggccc atcggtgttc 780
cctctggccc cttgcagcag aagcaccagc gaatctacag ccgccctggg ctgcctcgtg 840
aaggactact ttcccgagcc cgtgaccgtg tcctggaact ctggcgctct gacaagcggc 900
gtgcacacct ttccagccgt gctccagagc agcggcctgt actctctgag cagcgtcgtg 960
acagtgccca gcagcagcct gggcaccaag acctacacct gtaacgtgga ccacaagccc 1020
agcaacacca aggtggacaa gcgggtggaa tctaagtacg gccctccctg ccctccttgc 1080
ccagcccctg aagctgccgg cggaccctcc gtgttcctgt tccccccaaa gcccaaggac 1140
accctgatga tcagccggac ccccgaagtg acctgcgtgg tggtggatgt gtcccaggaa 1200
gatcccgagg tgcagttcaa ttggtacgtg gacggcgtgg aagtgcacaa cgccaagacc 1260
aagcccagag aggaacagtt caacagcacc taccgggtgg tgtccgtgct gaccgtgctg 1320
caccaggact ggctgaacgg caaagagtac aagtgcaagg tgtccaacaa gggcctgccc 1380
agctccatcg agaaaaccat cagcaaggcc aagggccagc cccgcgagcc tcaagtgtgt 1440
accctgcccc ctagccagga agagatgacc aagaaccagg tgtccctgag ctgtgccgtg 1500
aaaggcttct accccagcga cattgccgtg gaatgggaga gcaacggcca gcccgagaac 1560
aactacaaga ccaccccccc tgtgctggac agcgacggct cattcttcct ggtgtccaag 1620
ctgaccgtgg acaagagccg gtggcaggaa ggcaacgtgt tcagctgctc cgtgatgcac 1680
gaggccctgc acaaccacta cacccagaag tccctgtctc tgtccctggg c 1731
<210> 259
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 259
agagcccacc tggtgcagtc tggcaccgcc atgaagaaac caggcgcctc tgtgcgggtg 60
tcctgtcaga caagcggcta caccttcacc gcccacatcc tgttctggtt ccggcaggcc 120
cctggcagag gactggaatg ggtgggatgg atcaagcccc agtatggcgc caccaacttc 180
ggcggaggct tccgggatag agtgaccctg acccgggacg tgtaccgcga gatcgcctac 240
atggacatcc ggggcctgaa gcccgatgac accgccgtgt actactgcgc cagagacaga 300
agctacggcg acagcagctg ggctctggat gcttggggcc agggcacaac cgtggtggtg 360
tctgccgcct ctacaaaggg cccatcggtg ttccctctgg ccccttgcag cagaagcacc 420
agcgaatcta cagccgccct gggctgcctc gtgaaggact actttcccga gcccgtgacc 480
gtgtcctgga actctggcgc tctgacaagc ggcgtgcaca cctttccagc cgtgctccag 540
agcagcggcc tgtactctct gagcagcgtc gtgacagtgc ccagcagcag cctgggcacc 600
aagacctaca cctgtaacgt ggaccacaag cccagcaaca ccaaggtgga caagcgggtg 660
gaatctaagt acggccctcc ctgccctcct tgcccagccc ctgaagctgc cggcggaccc 720
tccgtgttcc tgttcccccc aaagcccaag gacaccctga tgatcagccg gacccccgaa 780
gtgacctgcg tggtggtgga tgtgtcccag gaagatcccg aggtgcagtt caattggtac 840
gtggacggcg tggaagtgca caacgccaag accaagccca gagaggaaca gttcaacagc 900
acctaccggg tggtgtccgt gctgaccgtg ctgcaccagg actggctgaa cggcaaagag 960
tacaagtgca aggtgtccaa caagggcctg cccagctcca tcgagaaaac catcagcaag 1020
gccaagggcc agccccgcga gcctcaagtg tataccctgc ccccttgcca ggaagagatg 1080
accaagaacc aggtgtccct gtggtgtctc gtgaaaggct tctaccccag cgacattgcc 1140
gtggaatggg agagcaacgg ccagcccgag aacaactaca agaccacccc ccctgtgctg 1200
gacagcgacg gctcattctt cctgtactcc aagctgaccg tggacaagag ccggtggcag 1260
gaaggcaacg tgttcagctg ctccgtgatg cacgaggccc tgcacaacca ctacacccag 1320
aagtccctgt ctctgtccct gggc 1344
<210> 260
<211> 630
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 260
tacatccacg tgacccagag ccccagcagc ctgtccgtgt ccatcggcga cagagtgacc 60
atcaactgcc agacctctca gggcgtgggc agcgacctgc actggtatca gcacaagcct 120
ggcagagccc ccaagctgct gatccaccac acaagcagct ccgaagaggg cgtgcccagc 180
agattttccg gcagcggctt ccacaccagc ttcaacctga ccatcagcga tctgcaggcc 240
gacgacattg ccacctacta ttgtcaggtg ctgcagttct tcggcagagg cagcagactg 300
cacatcaagc gtacggtggc cgctcccagc gtgttcatct tcccacctag cgacgagcag 360
ctgaagtccg gcacagcctc tgtcgtgtgc ctgctgaaca acttctaccc ccgcgaggcc 420
aaagtgcagt ggaaggtgga caacgccctg cagagcggca acagccagga aagcgtgacc 480
gagcaggaca gcaaggactc cacctacagc ctgagcagca ccctgacact gagcaaggcc 540
gactacgaga agcacaaggt gtacgcctgc gaagtgaccc accagggcct gtctagcccc 600
gtgaccaaga gcttcaaccg gggcgagtgt 630
<210> 261
<211> 1008
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 261
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacgagaacc tgttcaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaaggaca aaacccatac cgacatccag 360
atgacccaga gccccagcag cctgtctgcc agcgtgggcg acagagtgac catcacctgt 420
caggccagcc agaacatcta cgtgtggctg aactggtatc agcagaagcc cggcaaggcc 480
cccaagctgc tgatctacaa ggccagcaac ctgcacaccg gcgtgcccag cagattttct 540
ggcagcggct ccggcaccga cttcaccctg acaatcagct ccctgcagcc cgaggacatt 600
gccacctact actgccagca gggccagacc tacccctaca cctttggcca gggcaccaag 660
ctggaaatca aggataagac ccacacccgt acggtggccg ctcccagcgt gttcatcttc 720
ccacctagcg acgagcagct gaagtccggc acagcctctg tcgtgtgcct gctgaacaac 780
ttctaccccc gcgaggccaa agtgcagtgg aaggtggaca acgccctgca gagcggcaac 840
agccaggaaa gcgtgaccga gcaggacagc aaggactcca cctacagcct gagcagcacc 900
ctgacactga gcaaggccga ctacgagaag cacaaggtgt acgcctgcga agtgacccac 960
cagggcctgt ctagccccgt gaccaagagc ttcaaccggg gcgagtgt 1008
<210> 262
<211> 1731
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 262
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
gacaaaaccc atacccaggt gcagctggtg gaatctggcg gcggagtggt gcagcctggc 420
agaagcctga gactgagctg tgccgccagc ggcttcacct tcaccaaggc ctggatgcac 480
tgggtgcgcc aggcccctgg aaagcagctg gaatgggtgg cccagatcaa ggacaagagc 540
aacagctacg ccacctacta cgccgacagc gtgaagggcc ggttcaccat cagccgggac 600
gacagcaaga acaccctgta cctgcagatg aacagcctgc gggccgagga caccgccgtg 660
tactactgtc ggggcgtgta ctatgccctg agccccttcg attactgggg ccagggaacc 720
ctcgtgaccg tgtctagtga taagacccac accgccagca caaagggccc atcggtgttc 780
cctctggccc cttgcagcag aagcaccagc gaatctacag ccgccctggg ctgcctcgtg 840
aaggactact ttcccgagcc cgtgaccgtg tcctggaact ctggcgctct gacaagcggc 900
gtgcacacct ttccagccgt gctccagagc agcggcctgt actctctgag cagcgtcgtg 960
acagtgccca gcagcagcct gggcaccaag acctacacct gtaacgtgga ccacaagccc 1020
agcaacacca aggtggacaa gcgggtggaa tctaagtacg gccctccctg ccctccttgc 1080
ccagcccctg aagctgccgg cggaccctcc gtgttcctgt tccccccaaa gcccaaggac 1140
accctgatga tcagccggac ccccgaagtg acctgcgtgg tggtggatgt gtcccaggaa 1200
gatcccgagg tgcagttcaa ttggtacgtg gacggcgtgg aagtgcacaa cgccaagacc 1260
aagcccagag aggaacagtt caacagcacc taccgggtgg tgtccgtgct gaccgtgctg 1320
caccaggact ggctgaacgg caaagagtac aagtgcaagg tgtccaacaa gggcctgccc 1380
agctccatcg agaaaaccat cagcaaggcc aagggccagc cccgcgagcc tcaagtgtgt 1440
accctgcccc ctagccagga agagatgacc aagaaccagg tgtccctgag ctgtgccgtg 1500
aaaggcttct accccagcga cattgccgtg gaatgggaga gcaacggcca gcccgagaac 1560
aactacaaga ccaccccccc tgtgctggac agcgacggct cattcttcct ggtgtccaag 1620
ctgaccgtgg acaagagccg gtggcaggaa ggcaacgtgt tcagctgctc cgtgatgcac 1680
gaggccctgc acaaccacta cacccagaag tccctgtctc tgtccctggg c 1731
<210> 263
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 263
agagcccacc tggtgcagtc tggcaccgcc atgaagaaac caggcgcctc tgtgcgggtg 60
tcctgtcaga caagcggcta caccttcacc gcccacatcc tgttctggtt ccggcaggcc 120
cctggcagag gactggaatg ggtgggatgg atcaagcccc agtatggcgc caccaacttc 180
ggcggaggct tccgggatag agtgaccctg acccgggacg tgtaccgcga gatcgcctac 240
atggacatcc ggggcctgaa gcccgatgac accgccgtgt actactgcgc cagagacaga 300
agctacggcg acagcagctg ggctctggat gcttggggcc agggcacaac cgtggtggtg 360
tctgccgcct ctacaaaggg cccatcggtg ttccctctgg ccccttgcag cagaagcacc 420
agcgaatcta cagccgccct gggctgcctc gtgaaggact actttcccga gcccgtgacc 480
gtgtcctgga actctggcgc tctgacaagc ggcgtgcaca cctttccagc cgtgctccag 540
agcagcggcc tgtactctct gagcagcgtc gtgacagtgc ccagcagcag cctgggcacc 600
aagacctaca cctgtaacgt ggaccacaag cccagcaaca ccaaggtgga caagcgggtg 660
gaatctaagt acggccctcc ctgccctcct tgcccagccc ctgaagctgc cggcggaccc 720
tccgtgttcc tgttcccccc aaagcccaag gacaccctga tgatcagccg gacccccgaa 780
gtgacctgcg tggtggtgga tgtgtcccag gaagatcccg aggtgcagtt caattggtac 840
gtggacggcg tggaagtgca caacgccaag accaagccca gagaggaaca gttcaacagc 900
acctaccggg tggtgtccgt gctgaccgtg ctgcaccagg actggctgaa cggcaaagag 960
tacaagtgca aggtgtccaa caagggcctg cccagctcca tcgagaaaac catcagcaag 1020
gccaagggcc agccccgcga gcctcaagtg tataccctgc ccccttgcca ggaagagatg 1080
accaagaacc aggtgtccct gtggtgtctc gtgaaaggct tctaccccag cgacattgcc 1140
gtggaatggg agagcaacgg ccagcccgag aacaactaca agaccacccc ccctgtgctg 1200
gacagcgacg gctcattctt cctgtactcc aagctgaccg tggacaagag ccggtggcag 1260
gaaggcaacg tgttcagctg ctccgtgatg cacgaggccc tgcacaacca ctacacccag 1320
aagtccctgt ctctgtccct gggc 1344
<210> 264
<211> 630
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 264
tacatccacg tgacccagag ccccagcagc ctgtccgtgt ccatcggcga cagagtgacc 60
atcaactgcc agacctctca gggcgtgggc agcgacctgc actggtatca gcacaagcct 120
ggcagagccc ccaagctgct gatccaccac acaagcagct ccgaagaggg cgtgcccagc 180
agattttccg gcagcggctt ccacaccagc ttcaacctga ccatcagcga tctgcaggcc 240
gacgacattg ccacctacta ttgtcaggtg ctgcagttct tcggcagagg cagcagactg 300
cacatcaagc gtacggtggc cgctcccagc gtgttcatct tcccacctag cgacgagcag 360
ctgaagtccg gcacagcctc tgtcgtgtgc ctgctgaaca acttctaccc ccgcgaggcc 420
aaagtgcagt ggaaggtgga caacgccctg cagagcggca acagccagga aagcgtgacc 480
gagcaggaca gcaaggactc cacctacagc ctgagcagca ccctgacact gagcaaggcc 540
gactacgaga agcacaaggt gtacgcctgc gaagtgaccc accagggcct gtctagcccc 600
gtgaccaaga gcttcaaccg gggcgagtgt 630
<210> 265
<211> 1008
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 265
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacgagaacc tgttcaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaaggaca aaacccatac cgacatccag 360
atgacccaga gccccagcag cctgtctgcc agcgtgggcg acagagtgac catcacctgt 420
caggccagcc agaacatcta cgtgtggctg aactggtatc agcagaagcc cggcaaggcc 480
cccaagctgc tgatctacaa ggccagcaac ctgcacaccg gcgtgcccag cagattttct 540
ggcagcggct ccggcaccga cttcaccctg acaatcagct ccctgcagcc cgaggacatt 600
gccacctact actgccagca gggccagacc tacccctaca cctttggcca gggcaccaag 660
ctggaaatca aggataagac ccacacccgt acggtggccg ctcccagcgt gttcatcttc 720
ccacctagcg acgagcagct gaagtccggc acagcctctg tcgtgtgcct gctgaacaac 780
ttctaccccc gcgaggccaa agtgcagtgg aaggtggaca acgccctgca gagcggcaac 840
agccaggaaa gcgtgaccga gcaggacagc aaggactcca cctacagcct gagcagcacc 900
ctgacactga gcaaggccga ctacgagaag cacaaggtgt acgcctgcga agtgacccac 960
cagggcctgt ctagccccgt gaccaagagc ttcaaccggg gcgagtgt 1008
<210> 266
<211> 1740
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 266
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
gacaaaaccc atacccaggt gcagctggtg gaatctggcg gcggagtggt gcagcctggc 420
agaagcctga gactgagctg tgccgccagc ggcttcacct tcaccaaggc ctggatgcac 480
tgggtgcgcc aggcccctgg aaagcagctg gaatgggtgg cccagatcaa ggacaagagc 540
aacagctacg ccacctacta cgccgacagc gtgaagggcc ggttcaccat cagccgggac 600
gacagcaaga acaccctgta cctgcagatg aacagcctgc gggccgagga caccgccgtg 660
tactactgtc ggggcgtgta ctatgccctg agccccttcg attactgggg ccagggaacc 720
ctcgtgaccg tgtctagtga taagacccac accgccagca caaagggccc cagcgtgttc 780
cctctggccc ctagcagcaa gagcacatct ggcggaacag ccgccctggg ctgcctcgtg 840
aaggactact ttcccgagcc cgtgaccgtg tcctggaatt ctggcgccct gaccagcggc 900
gtgcacacct ttccagctgt gctgcagtcc agcggcctgt acagcctgag cagcgtcgtg 960
acagtgccca gcagctctct gggcacccag acctacatct gcaacgtgaa ccacaagccc 1020
agcaacacca aggtggacaa gaaggtggaa cccaagagct gcgacaagac ccacacctgt 1080
cccccttgtc ctgcccccga actgctggga ggcccttccg tgttcctgtt ccccccaaag 1140
cccaaggaca ccctgatgat cagccggacc cccgaagtga cctgcgtggt ggtggatgtg 1200
tcccacgagg accctgaagt gaagttcaat tggtacgtgg acggcgtgga agtgcacaac 1260
gccaagacca agccaagaga ggaacagtac aacaatgcct cccgggtggt gtccgtgctg 1320
accgtgctgc accaggactg gctgaacggc aaagagtaca agtgcaaggt gtccaacaag 1380
gccctgcctg cccccatcga gaaaaccatc agcaaggcca agggccagcc ccgcgaaccc 1440
caggtgtgca cactgccccc aagcagggac gagctgacca agaaccaggt gtccctgagc 1500
tgtgccgtga aaggcttcta cccctccgat atcgccgtgg aatgggagag caacggccag 1560
cccgagaaca actacaagac caccccccct gtgctggaca gcgacggctc attcttcctg 1620
gtgtccaagc tgacagtgga caagtcccgg tggcagcagg gcaacgtgtt cagctgctcc 1680
gtgatgcacg aggccctgca caaccactac acccagaagt ccctgagcct gagccccggc 1740
<210> 267
<211> 1353
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 267
agagcccacc tggtgcagtc tggcaccgcc atgaagaaac caggcgcctc tgtgcgggtg 60
tcctgtcaga caagcggcta caccttcacc gcccacatcc tgttctggtt ccggcaggcc 120
cctggcagag gactggaatg ggtgggatgg atcaagcccc agtatggcgc caccaacttc 180
ggcggaggct tccgggatag agtgaccctg acccgggacg tgtaccgcga gatcgcctac 240
atggacatcc ggggcctgaa gcccgatgac accgccgtgt actactgcgc cagagacaga 300
agctacggcg acagcagctg ggctctggat gcttggggcc agggcacaac cgtggtggtg 360
tctgccgcct ctacaaaggg cccatcggtc ttccccctgg caccctcctc caagagcacc 420
tctgggggca cagcggccct gggctgcctg gtcaaggact acttccccga accggtgacg 480
gtgtcgtgga actcaggcgc cctgaccagc ggcgtgcaca ccttcccggc tgtcctacag 540
tcctcaggac tctactccct cagcagcgtg gtgaccgtgc cctccagcag cttgggcacc 600
cagacctaca tctgcaacgt gaatcacaag cccagcaaca ccaaggtgga caagaaagtt 660
gagcccaaat cttgtgacaa aactcacaca tgcccaccgt gcccagcacc tgaactcctg 720
gggggaccgt cagtcttcct cttcccccca aaacccaagg acaccctcat gatctcccgg 780
acccctgagg tcacatgcgt ggtggtggac gtgagccacg aagaccctga ggtcaagttc 840
aactggtatg ttgacggcgt ggaggtgcat aatgccaaga caaagccgcg ggaggagcag 900
tacaacaatg cctcccgtgt ggtcagcgtc ctcaccgtcc tgcaccagga ctggctgaat 960
ggcaaggagt acaagtgcaa ggtctccaac aaagccctcc cagcccccat cgagaaaacc 1020
atctccaaag ccaaagggca gccccgagaa ccacaggtgt acaccctgcc cccatgccgg 1080
gatgagctga ccaagaatca agtcagcctg tggtgcctgg taaaaggctt ctatcccagc 1140
gacatcgccg tggagtggga gagcaatggg cagccggaga acaactacaa gaccacgcct 1200
cccgtgctgg actccgacgg ctccttcttc ctctactcaa aactcaccgt ggacaagagc 1260
aggtggcagc aggggaacgt cttctcatgc tccgtgatgc atgaggctct gcacaaccac 1320
tacacgcaga agagcctctc cctgtctccg ggt 1353
<210> 268
<211> 630
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 268
tacatccacg tgacccagag ccccagcagc ctgtccgtgt ccatcggcga cagagtgacc 60
atcaactgcc agacctctca gggcgtgggc agcgacctgc actggtatca gcacaagcct 120
ggcagagccc ccaagctgct gatccaccac acaagcagct ccgaagaggg cgtgcccagc 180
agattttccg gcagcggctt ccacaccagc ttcaacctga ccatcagcga tctgcaggcc 240
gacgacattg ccacctacta ttgtcaggtg ctgcagttct tcggcagagg cagcagactg 300
cacatcaagc gtacggtggc cgctcccagc gtgttcatct tcccacctag cgacgagcag 360
ctgaagtccg gcacagcctc tgtcgtgtgc ctgctgaaca acttctaccc ccgcgaggcc 420
aaagtgcagt ggaaggtgga caacgccctg cagagcggca acagccagga aagcgtgacc 480
gagcaggaca gcaaggactc cacctacagc ctgagcagca ccctgacact gagcaaggcc 540
gactacgaga agcacaaggt gtacgcctgc gaagtgaccc accagggcct gtctagcccc 600
gtgaccaaga gcttcaaccg gggcgagtgt 630
<210> 269
<211> 1008
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 269
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacgagaacc tgcagaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaaggaca aaacccatac cgacatccag 360
atgacccaga gccccagcag cctgtctgcc agcgtgggcg acagagtgac catcacctgt 420
caggccagcc agaacatcta cgtgtggctg aactggtatc agcagaagcc cggcaaggcc 480
cccaagctgc tgatctacaa ggccagcaac ctgcacaccg gcgtgcccag cagattttct 540
ggcagcggct ccggcaccga cttcaccctg acaatcagct ccctgcagcc cgaggacatt 600
gccacctact actgccagca gggccagacc tacccctaca cctttggcca gggcaccaag 660
ctggaaatca aggataagac ccacacccgt acggtggccg ctcccagcgt gttcatcttc 720
ccacctagcg acgagcagct gaagtccggc acagcctctg tcgtgtgcct gctgaacaac 780
ttctaccccc gcgaggccaa agtgcagtgg aaggtggaca acgccctgca gagcggcaac 840
agccaggaaa gcgtgaccga gcaggacagc aaggactcca cctacagcct gagcagcacc 900
ctgacactga gcaaggccga ctacgagaag cacaaggtgt acgcctgcga agtgacccac 960
cagggcctgt ctagccccgt gaccaagagc ttcaaccggg gcgagtgt 1008
<210> 270
<211> 1731
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 270
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
gacaaaaccc atacccaggt gcagctggtg gaatctggcg gcggagtggt gcagcctggc 420
agaagcctga gactgagctg tgccgccagc ggcttcacct tcaccaaggc ctggatgcac 480
tgggtgcgcc aggcccctgg aaagcagctg gaatgggtgg cccagatcaa ggacaagagc 540
aacagctacg ccacctacta cgccgacagc gtgaagggcc ggttcaccat cagccgggac 600
gacagcaaga acaccctgta cctgcagatg aacagcctgc gggccgagga caccgccgtg 660
tactactgtc ggggcgtgta ctatgccctg agccccttcg attactgggg ccagggaacc 720
ctcgtgaccg tgtctagtga taagacccac accgccagca caaagggccc atcggtgttc 780
cctctggccc cttgcagcag aagcaccagc gaatctacag ccgccctggg ctgcctcgtg 840
aaggactact ttcccgagcc cgtgaccgtg tcctggaact ctggcgctct gacaagcggc 900
gtgcacacct ttccagccgt gctccagagc agcggcctgt actctctgag cagcgtcgtg 960
acagtgccca gcagcagcct gggcaccaag acctacacct gtaacgtgga ccacaagccc 1020
agcaacacca aggtggacaa gcgggtggaa tctaagtacg gccctccctg ccctccttgc 1080
ccagcccctg aagctgccgg cggaccctcc gtgttcctgt tccccccaaa gcccaaggac 1140
accctgatga tcagccggac ccccgaagtg acctgcgtgg tggtggatgt gtcccaggaa 1200
gatcccgagg tgcagttcaa ttggtacgtg gacggcgtgg aagtgcacaa cgccaagacc 1260
aagcccagag aggaacagtt caacagcacc taccgggtgg tgtccgtgct gaccgtgctg 1320
caccaggact ggctgaacgg caaagagtac aagtgcaagg tgtccaacaa gggcctgccc 1380
agctccatcg agaaaaccat cagcaaggcc aagggccagc cccgcgagcc tcaagtgtgt 1440
accctgcccc ctagccagga agagatgacc aagaaccagg tgtccctgag ctgtgccgtg 1500
aaaggcttct accccagcga cattgccgtg gaatgggaga gcaacggcca gcccgagaac 1560
aactacaaga ccaccccccc tgtgctggac agcgacggct cattcttcct ggtgtccaag 1620
ctgaccgtgg acaagagccg gtggcaggaa ggcaacgtgt tcagctgctc cgtgatgcac 1680
gaggccctgc acaaccacta cacccagaag tccctgtctc tgtccctggg c 1731
<210> 271
<211> 1365
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<220>
<221> другой_признак
<222> 460
<223> n = A,T,C или G
<400> 271
agagcccacc tggtgcagtc tggcaccgcc atgaagaaac caggcgcctc tgtgcgggtg 60
tcctgtcaga caagcggcta caccttcacc gcccacatcc tgttctggtt ccggcaggcc 120
cctggcagag gactggaatg ggtgggatgg atcaagcccc agtatggcgc cgtgaacttc 180
ggcggaggct tccgggatag agtgaccctg acccggcagc tgagccagga ccctgatgat 240
ccggattggg gcatcgccta catggacatc cggggcctga agcccgatga caccgccgtg 300
tactactgcg ccagagacag aagctacggc gacagcagct gggctctgga tgcttggggc 360
cagggcacaa ccgtggtggt gtctgccgcc tctacaaagg gcccatcggt gttccctctg 420
gccccttgca gcagaagcac cagcgaatct acagccgccn tgggctgcct cgtgaaggac 480
tactttcccg agcccgtgac cgtgtcctgg aactctggcg ctctgacaag cggcgtgcac 540
acctttccag ccgtgctcca gagcagcggc ctgtactctc tgagcagcgt cgtgacagtg 600
cccagcagca gcctgggcac caagacctac acctgtaacg tggaccacaa gcccagcaac 660
accaaggtgg acaagcgggt ggaatctaag tacggccctc cctgccctcc ttgcccagcc 720
cctgaagctg ccggcggacc ctccgtgttc ctgttccccc caaagcccaa ggacaccctg 780
atgatcagcc ggacccccga agtgacctgc gtggtggtgg atgtgtccca ggaagatccc 840
gaggtgcagt tcaattggta cgtggacggc gtggaagtgc acaacgccaa gaccaagccc 900
agagaggaac agttcaacag cacctaccgg gtggtgtccg tgctgaccgt gctgcaccag 960
gactggctga acggcaaaga gtacaagtgc aaggtgtcca acaagggcct gcccagctcc 1020
atcgagaaaa ccatcagcaa ggccaagggc cagccccgcg agcctcaagt gtataccctg 1080
cccccttgcc aggaagagat gaccaagaac caggtgtccc tgtggtgtct cgtgaaaggc 1140
ttctacccca gcgacattgc cgtggaatgg gagagcaacg gccagcccga gaacaactac 1200
aagaccaccc cccctgtgct ggacagcgac ggctcattct tcctgtactc caagctgacc 1260
gtggacaaga gccggtggca ggaaggcaac gtgttcagct gctccgtgat gcacgaggcc 1320
ctgcacaacc actacaccca gaagtccctg tctctgtccc tgggc 1365
<210> 272
<211> 630
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 272
tacatccacg tgacccagag ccccagcagc ctgtccgtgt ccatcggcga cagagtgacc 60
atcaactgcc agacctctca gggcgtgggc agcgacctgc actggtatca gcacaagcct 120
ggcagagccc ccaagctgct gatccaccac acaagcagcg tggaagatgg cgtgcccagc 180
agattttccg gcagcggctt ccacaccagc ttcaacctga ccatcagcga tctgcaggcc 240
gacgacattg ccacctacta ttgtcaggtg ctgcagttct tcggcagagg cagcagactg 300
cacatcaagc gtacggtggc cgctcccagc gtgttcatct tcccacctag cgacgagcag 360
ctgaagtccg gcacagcctc tgtcgtgtgc ctgctgaaca acttctaccc ccgcgaggcc 420
aaagtgcagt ggaaggtgga caacgccctg cagagcggca acagccagga aagcgtgacc 480
gagcaggaca gcaaggactc cacctacagc ctgagcagca ccctgacact gagcaaggcc 540
gactacgaga agcacaaggt gtacgcctgc gaagtgaccc accagggcct gtctagcccc 600
gtgaccaaga gcttcaaccg gggcgagtgt 630
<210> 273
<211> 1008
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 273
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacgagaacc tgttcaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaaggaca aaacccatac cgacatccag 360
atgacccaga gccccagcag cctgtctgcc agcgtgggcg acagagtgac catcacctgt 420
caggccagcc agaacatcta cgtgtggctg aactggtatc agcagaagcc cggcaaggcc 480
cccaagctgc tgatctacaa ggccagcaac ctgcacaccg gcgtgcccag cagattttct 540
ggcagcggct ccggcaccga cttcaccctg acaatcagct ccctgcagcc cgaggacatt 600
gccacctact actgccagca gggccagacc tacccctaca cctttggcca gggcaccaag 660
ctggaaatca aggataagac ccacacccgt acggtggccg ctcccagcgt gttcatcttc 720
ccacctagcg acgagcagct gaagtccggc acagcctctg tcgtgtgcct gctgaacaac 780
ttctaccccc gcgaggccaa agtgcagtgg aaggtggaca acgccctgca gagcggcaac 840
agccaggaaa gcgtgaccga gcaggacagc aaggactcca cctacagcct gagcagcacc 900
ctgacactga gcaaggccga ctacgagaag cacaaggtgt acgcctgcga agtgacccac 960
cagggcctgt ctagccccgt gaccaagagc ttcaaccggg gcgagtgt 1008
<210> 274
<211> 1731
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 274
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
gacaaaaccc atacccaggt gcagctggtg gaatctggcg gcggagtggt gcagcctggc 420
agaagcctga gactgagctg tgccgccagc ggcttcacct tcaccaaggc ctggatgcac 480
tgggtgcgcc aggcccctgg aaagcagctg gaatgggtgg cccagatcaa ggacaagagc 540
aacagctacg ccacctacta cgccgacagc gtgaagggcc ggttcaccat cagccgggac 600
gacagcaaga acaccctgta cctgcagatg aacagcctgc gggccgagga caccgccgtg 660
tactactgtc ggggcgtgta ctatgccctg agccccttcg attactgggg ccagggaacc 720
ctcgtgaccg tgtctagtga taagacccac accgccagca caaagggccc atcggtgttc 780
cctctggccc cttgcagcag aagcaccagc gaatctacag ccgccctggg ctgcctcgtg 840
aaggactact ttcccgagcc cgtgaccgtg tcctggaact ctggcgctct gacaagcggc 900
gtgcacacct ttccagccgt gctccagagc agcggcctgt actctctgag cagcgtcgtg 960
acagtgccca gcagcagcct gggcaccaag acctacacct gtaacgtgga ccacaagccc 1020
agcaacacca aggtggacaa gcgggtggaa tctaagtacg gccctccctg ccctccttgc 1080
ccagcccctg aagctgccgg cggaccctcc gtgttcctgt tccccccaaa gcccaaggac 1140
accctgatga tcagccggac ccccgaagtg acctgcgtgg tggtggatgt gtcccaggaa 1200
gatcccgagg tgcagttcaa ttggtacgtg gacggcgtgg aagtgcacaa cgccaagacc 1260
aagcccagag aggaacagtt caacagcacc taccgggtgg tgtccgtgct gaccgtgctg 1320
caccaggact ggctgaacgg caaagagtac aagtgcaagg tgtccaacaa gggcctgccc 1380
agctccatcg agaaaaccat cagcaaggcc aagggccagc cccgcgagcc tcaagtgtgt 1440
accctgcccc ctagccagga agagatgacc aagaaccagg tgtccctgag ctgtgccgtg 1500
aaaggcttct accccagcga cattgccgtg gaatgggaga gcaacggcca gcccgagaac 1560
aactacaaga ccaccccccc tgtgctggac agcgacggct cattcttcct ggtgtccaag 1620
ctgaccgtgg acaagagccg gtggcaggaa ggcaacgtgt tcagctgctc cgtgatgcac 1680
gaggccctgc acaaccacta cacccagaag tccctgtctc tgtccctggg c 1731
<210> 275
<211> 1365
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<220>
<221> другой_признак
<222> 460
<223> n = A,T,C или G
<400> 275
agagcccacc tggtgcagtc tggcaccgcc atgaagaaac caggcgcctc tgtgcgggtg 60
tcctgtcaga caagcggcta caccttcacc gcccacatcc tgttctggtt ccggcaggcc 120
cctggcagag gactggaatg ggtgggatgg atcaagcccc agtatggcgc cgtgaacttc 180
ggcggaggct tccgggatag agtgaccctg acccggcagc tgagccagga ccctgatgat 240
ccggattggg gcatcgccta catggacatc cggggcctga agcccgatga caccgccgtg 300
tactactgcg ccagagacag aagctacggc gacagcagct gggctctgga tgcttggggc 360
cagggcacaa ccgtggtggt gtctgccgcc tctacaaagg gcccatcggt gttccctctg 420
gccccttgca gcagaagcac cagcgaatct acagccgccn tgggctgcct cgtgaaggac 480
tactttcccg agcccgtgac cgtgtcctgg aactctggcg ctctgacaag cggcgtgcac 540
acctttccag ccgtgctcca gagcagcggc ctgtactctc tgagcagcgt cgtgacagtg 600
cccagcagca gcctgggcac caagacctac acctgtaacg tggaccacaa gcccagcaac 660
accaaggtgg acaagcgggt ggaatctaag tacggccctc cctgccctcc ttgcccagcc 720
cctgaagctg ccggcggacc ctccgtgttc ctgttccccc caaagcccaa ggacaccctg 780
atgatcagcc ggacccccga agtgacctgc gtggtggtgg atgtgtccca ggaagatccc 840
gaggtgcagt tcaattggta cgtggacggc gtggaagtgc acaacgccaa gaccaagccc 900
agagaggaac agttcaacag cacctaccgg gtggtgtccg tgctgaccgt gctgcaccag 960
gactggctga acggcaaaga gtacaagtgc aaggtgtcca acaagggcct gcccagctcc 1020
atcgagaaaa ccatcagcaa ggccaagggc cagccccgcg agcctcaagt gtataccctg 1080
cccccttgcc aggaagagat gaccaagaac caggtgtccc tgtggtgtct cgtgaaaggc 1140
ttctacccca gcgacattgc cgtggaatgg gagagcaacg gccagcccga gaacaactac 1200
aagaccaccc cccctgtgct ggacagcgac ggctcattct tcctgtactc caagctgacc 1260
gtggacaaga gccggtggca ggaaggcaac gtgttcagct gctccgtgat gcacgaggcc 1320
ctgcacaacc actacaccca gaagtccctg tctctgtccc tgggc 1365
<210> 276
<211> 630
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 276
tacatccacg tgacccagag ccccagcagc ctgtccgtgt ccatcggcga cagagtgacc 60
atcaactgcc agacctctca gggcgtgggc agcgacctgc actggtatca gcacaagcct 120
ggcagagccc ccaagctgct gatccaccac acaagcagcg tggaagatgg cgtgcccagc 180
agattttccg gcagcggctt ccacaccagc ttcaacctga ccatcagcga tctgcaggcc 240
gacgacattg ccacctacta ttgtcaggtg ctgcagttct tcggcagagg cagcagactg 300
cacatcaagc gtacggtggc cgctcccagc gtgttcatct tcccacctag cgacgagcag 360
ctgaagtccg gcacagcctc tgtcgtgtgc ctgctgaaca acttctaccc ccgcgaggcc 420
aaagtgcagt ggaaggtgga caacgccctg cagagcggca acagccagga aagcgtgacc 480
gagcaggaca gcaaggactc cacctacagc ctgagcagca ccctgacact gagcaaggcc 540
gactacgaga agcacaaggt gtacgcctgc gaagtgaccc accagggcct gtctagcccc 600
gtgaccaaga gcttcaaccg gggcgagtgt 630
<210> 277
<211> 1008
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 277
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacgagaacc tgcagaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaaggaca aaacccatac cgacatccag 360
atgacccaga gccccagcag cctgtctgcc agcgtgggcg acagagtgac catcacctgt 420
caggccagcc agaacatcta cgtgtggctg aactggtatc agcagaagcc cggcaaggcc 480
cccaagctgc tgatctacaa ggccagcaac ctgcacaccg gcgtgcccag cagattttct 540
ggcagcggct ccggcaccga cttcaccctg acaatcagct ccctgcagcc cgaggacatt 600
gccacctact actgccagca gggccagacc tacccctaca cctttggcca gggcaccaag 660
ctggaaatca aggataagac ccacacccgt acggtggccg ctcccagcgt gttcatcttc 720
ccacctagcg acgagcagct gaagtccggc acagcctctg tcgtgtgcct gctgaacaac 780
ttctaccccc gcgaggccaa agtgcagtgg aaggtggaca acgccctgca gagcggcaac 840
agccaggaaa gcgtgaccga gcaggacagc aaggactcca cctacagcct gagcagcacc 900
ctgacactga gcaaggccga ctacgagaag cacaaggtgt acgcctgcga agtgacccac 960
cagggcctgt ctagccccgt gaccaagagc ttcaaccggg gcgagtgt 1008
<210> 278
<211> 1740
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 278
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
gacaaaaccc atacccaggt gcagctggtg gaatctggcg gcggagtggt gcagcctggc 420
agaagcctga gactgagctg tgccgccagc ggcttcacct tcaccaaggc ctggatgcac 480
tgggtgcgcc aggcccctgg aaagcagctg gaatgggtgg cccagatcaa ggacaagagc 540
aacagctacg ccacctacta cgccgacagc gtgaagggcc ggttcaccat cagccgggac 600
gacagcaaga acaccctgta cctgcagatg aacagcctgc gggccgagga caccgccgtg 660
tactactgtc ggggcgtgta ctatgccctg agccccttcg attactgggg ccagggaacc 720
ctcgtgaccg tgtctagtga taagacccac accgccagca caaagggccc cagcgtgttc 780
cctctggccc ctagcagcaa gagcacatct ggcggaacag ccgccctggg ctgcctcgtg 840
aaggactact ttcccgagcc cgtgaccgtg tcctggaatt ctggcgccct gaccagcggc 900
gtgcacacct ttccagctgt gctgcagtcc agcggcctgt acagcctgag cagcgtcgtg 960
acagtgccca gcagctctct gggcacccag acctacatct gcaacgtgaa ccacaagccc 1020
agcaacacca aggtggacaa gaaggtggaa cccaagagct gcgacaagac ccacacctgt 1080
cccccttgtc ctgcccccga actgctggga ggcccttccg tgttcctgtt ccccccaaag 1140
cccaaggaca ccctgatgat cagccggacc cccgaagtga cctgcgtggt ggtggatgtg 1200
tcccacgagg accctgaagt gaagttcaat tggtacgtgg acggcgtgga agtgcacaac 1260
gccaagacca agccaagaga ggaacagtac aacaatgcct cccgggtggt gtccgtgctg 1320
accgtgctgc accaggactg gctgaacggc aaagagtaca agtgcaaggt gtccaacaag 1380
gccctgcctg cccccatcga gaaaaccatc agcaaggcca agggccagcc ccgcgaaccc 1440
caggtgtgca cactgccccc aagcagggac gagctgacca agaaccaggt gtccctgagc 1500
tgtgccgtga aaggcttcta cccctccgat atcgccgtgg aatgggagag caacggccag 1560
cccgagaaca actacaagac caccccccct gtgctggaca gcgacggctc attcttcctg 1620
gtgtccaagc tgacagtgga caagtcccgg tggcagcagg gcaacgtgtt cagctgctcc 1680
gtgatgcacg aggccctgca caaccactac acccagaagt ccctgagcct gagccccggc 1740
<210> 279
<211> 1374
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 279
agagcccacc tggtgcagtc tggcaccgcc atgaagaaac caggcgcctc tgtgcgggtg 60
tcctgtcaga caagcggcta caccttcacc gcccacatcc tgttctggtt ccggcaggcc 120
cctggcagag gactggaatg ggtgggatgg atcaagcccc agtatggcgc cgtgaacttc 180
ggcggaggct tccgggatag agtgaccctg acccggcagc tgagccagga ccctgatgat 240
ccggattggg gcatcgccta catggacatc cggggcctga agcccgatga caccgccgtg 300
tactactgcg ccagagacag aagctacggc gacagcagct gggctctgga tgcttggggc 360
cagggcacaa ccgtggtggt gtctgccgcc tctacaaagg gcccatcggt cttccccctg 420
gcaccctcct ccaagagcac ctctgggggc acagcggccc tgggctgcct ggtcaaggac 480
tacttccccg aaccggtgac ggtgtcgtgg aactcaggcg ccctgaccag cggcgtgcac 540
accttcccgg ctgtcctaca gtcctcagga ctctactccc tcagcagcgt ggtgaccgtg 600
ccctccagca gcttgggcac ccagacctac atctgcaacg tgaatcacaa gcccagcaac 660
accaaggtgg acaagaaagt tgagcccaaa tcttgtgaca aaactcacac atgcccaccg 720
tgcccagcac ctgaactcct ggggggaccg tcagtcttcc tcttcccccc aaaacccaag 780
gacaccctca tgatctcccg gacccctgag gtcacatgcg tggtggtgga cgtgagccac 840
gaagaccctg aggtcaagtt caactggtat gttgacggcg tggaggtgca taatgccaag 900
acaaagccgc gggaggagca gtacaacaat gcctcccgtg tggtcagcgt cctcaccgtc 960
ctgcaccagg actggctgaa tggcaaggag tacaagtgca aggtctccaa caaagccctc 1020
ccagccccca tcgagaaaac catctccaaa gccaaagggc agccccgaga accacaggtg 1080
tacaccctgc ccccatgccg ggatgagctg accaagaatc aagtcagcct gtggtgcctg 1140
gtaaaaggct tctatcccag cgacatcgcc gtggagtggg agagcaatgg gcagccggag 1200
aacaactaca agaccacgcc tcccgtgctg gactccgacg gctccttctt cctctactca 1260
aaactcaccg tggacaagag caggtggcag caggggaacg tcttctcatg ctccgtgatg 1320
catgaggctc tgcacaacca ctacacgcag aagagcctct ccctgtctcc gggt 1374
<210> 280
<211> 630
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 280
tacatccacg tgacccagag ccccagcagc ctgtccgtgt ccatcggcga cagagtgacc 60
atcaactgcc agacctctca gggcgtgggc agcgacctgc actggtatca gcacaagcct 120
ggcagagccc ccaagctgct gatccaccac acaagcagcg tggaagatgg cgtgcccagc 180
agattttccg gcagcggctt ccacaccagc ttcaacctga ccatcagcga tctgcaggcc 240
gacgacattg ccacctacta ttgtcaggtg ctgcagttct tcggcagagg cagcagactg 300
cacatcaagc gtacggtggc cgctcccagc gtgttcatct tcccacctag cgacgagcag 360
ctgaagtccg gcacagcctc tgtcgtgtgc ctgctgaaca acttctaccc ccgcgaggcc 420
aaagtgcagt ggaaggtgga caacgccctg cagagcggca acagccagga aagcgtgacc 480
gagcaggaca gcaaggactc cacctacagc ctgagcagca ccctgacact gagcaaggcc 540
gactacgaga agcacaaggt gtacgcctgc gaagtgaccc accagggcct gtctagcccc 600
gtgaccaaga gcttcaaccg gggcgagtgt 630
<210> 281
<211> 1008
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 281
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacgagaacc tgttcaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaaggaca aaacccatac cgacatccag 360
atgacccaga gccccagcag cctgtctgcc agcgtgggcg acagagtgac catcacctgt 420
caggccagcc agaacatcta cgtgtggctg aactggtatc agcagaagcc cggcaaggcc 480
cccaagctgc tgatctacaa ggccagcaac ctgcacaccg gcgtgcccag cagattttct 540
ggcagcggct ccggcaccga cttcaccctg acaatcagct ccctgcagcc cgaggacatt 600
gccacctact actgccagca gggccagacc tacccctaca cctttggcca gggcaccaag 660
ctggaaatca aggataagac ccacacccgt acggtggccg ctcccagcgt gttcatcttc 720
ccacctagcg acgagcagct gaagtccggc acagcctctg tcgtgtgcct gctgaacaac 780
ttctaccccc gcgaggccaa agtgcagtgg aaggtggaca acgccctgca gagcggcaac 840
agccaggaaa gcgtgaccga gcaggacagc aaggactcca cctacagcct gagcagcacc 900
ctgacactga gcaaggccga ctacgagaag cacaaggtgt acgcctgcga agtgacccac 960
cagggcctgt ctagccccgt gaccaagagc ttcaaccggg gcgagtgt 1008
<210> 282
<211> 1740
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 282
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
gacaaaaccc atacccaggt gcagctggtg gaatctggcg gcggagtggt gcagcctggc 420
agaagcctga gactgagctg tgccgccagc ggcttcacct tcaccaaggc ctggatgcac 480
tgggtgcgcc aggcccctgg aaagcagctg gaatgggtgg cccagatcaa ggacaagagc 540
aacagctacg ccacctacta cgccgacagc gtgaagggcc ggttcaccat cagccgggac 600
gacagcaaga acaccctgta cctgcagatg aacagcctgc gggccgagga caccgccgtg 660
tactactgtc ggggcgtgta ctatgccctg agccccttcg attactgggg ccagggaacc 720
ctcgtgaccg tgtctagtga taagacccac accgccagca caaagggccc cagcgtgttc 780
cctctggccc ctagcagcaa gagcacatct ggcggaacag ccgccctggg ctgcctcgtg 840
aaggactact ttcccgagcc cgtgaccgtg tcctggaatt ctggcgccct gaccagcggc 900
gtgcacacct ttccagctgt gctgcagtcc agcggcctgt acagcctgag cagcgtcgtg 960
acagtgccca gcagctctct gggcacccag acctacatct gcaacgtgaa ccacaagccc 1020
agcaacacca aggtggacaa gaaggtggaa cccaagagct gcgacaagac ccacacctgt 1080
cccccttgtc ctgcccccga actgctggga ggcccttccg tgttcctgtt ccccccaaag 1140
cccaaggaca ccctgatgat cagccggacc cccgaagtga cctgcgtggt ggtggatgtg 1200
tcccacgagg accctgaagt gaagttcaat tggtacgtgg acggcgtgga agtgcacaac 1260
gccaagacca agccaagaga ggaacagtac aacaatgcct cccgggtggt gtccgtgctg 1320
accgtgctgc accaggactg gctgaacggc aaagagtaca agtgcaaggt gtccaacaag 1380
gccctgcctg cccccatcga gaaaaccatc agcaaggcca agggccagcc ccgcgaaccc 1440
caggtgtgca cactgccccc aagcagggac gagctgacca agaaccaggt gtccctgagc 1500
tgtgccgtga aaggcttcta cccctccgat atcgccgtgg aatgggagag caacggccag 1560
cccgagaaca actacaagac caccccccct gtgctggaca gcgacggctc attcttcctg 1620
gtgtccaagc tgacagtgga caagtcccgg tggcagcagg gcaacgtgtt cagctgctcc 1680
gtgatgcacg aggccctgca caaccactac acccagaagt ccctgagcct gagccccggc 1740
<210> 283
<211> 1374
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 283
agagcccacc tggtgcagtc tggcaccgcc atgaagaaac caggcgcctc tgtgcgggtg 60
tcctgtcaga caagcggcta caccttcacc gcccacatcc tgttctggtt ccggcaggcc 120
cctggcagag gactggaatg ggtgggatgg atcaagcccc agtatggcgc cgtgaacttc 180
ggcggaggct tccgggatag agtgaccctg acccggcagc tgagccagga ccctgatgat 240
ccggattggg gcatcgccta catggacatc cggggcctga agcccgatga caccgccgtg 300
tactactgcg ccagagacag aagctacggc gacagcagct gggctctgga tgcttggggc 360
cagggcacaa ccgtggtggt gtctgccgcc tctacaaagg gcccatcggt cttccccctg 420
gcaccctcct ccaagagcac ctctgggggc acagcggccc tgggctgcct ggtcaaggac 480
tacttccccg aaccggtgac ggtgtcgtgg aactcaggcg ccctgaccag cggcgtgcac 540
accttcccgg ctgtcctaca gtcctcagga ctctactccc tcagcagcgt ggtgaccgtg 600
ccctccagca gcttgggcac ccagacctac atctgcaacg tgaatcacaa gcccagcaac 660
accaaggtgg acaagaaagt tgagcccaaa tcttgtgaca aaactcacac atgcccaccg 720
tgcccagcac ctgaactcct ggggggaccg tcagtcttcc tcttcccccc aaaacccaag 780
gacaccctca tgatctcccg gacccctgag gtcacatgcg tggtggtgga cgtgagccac 840
gaagaccctg aggtcaagtt caactggtat gttgacggcg tggaggtgca taatgccaag 900
acaaagccgc gggaggagca gtacaacaat gcctcccgtg tggtcagcgt cctcaccgtc 960
ctgcaccagg actggctgaa tggcaaggag tacaagtgca aggtctccaa caaagccctc 1020
ccagccccca tcgagaaaac catctccaaa gccaaagggc agccccgaga accacaggtg 1080
tacaccctgc ccccatgccg ggatgagctg accaagaatc aagtcagcct gtggtgcctg 1140
gtaaaaggct tctatcccag cgacatcgcc gtggagtggg agagcaatgg gcagccggag 1200
aacaactaca agaccacgcc tcccgtgctg gactccgacg gctccttctt cctctactca 1260
aaactcaccg tggacaagag caggtggcag caggggaacg tcttctcatg ctccgtgatg 1320
catgaggctc tgcacaacca ctacacgcag aagagcctct ccctgtctcc gggt 1374
<210> 284
<211> 630
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 284
tacatccacg tgacccagag ccccagcagc ctgtccgtgt ccatcggcga cagagtgacc 60
atcaactgcc agacctctca gggcgtgggc agcgacctgc actggtatca gcacaagcct 120
ggcagagccc ccaagctgct gatccaccac acaagcagcg tggaagatgg cgtgcccagc 180
agattttccg gcagcggctt ccacaccagc ttcaacctga ccatcagcga tctgcaggcc 240
gacgacattg ccacctacta ttgtcaggtg ctgcagttct tcggcagagg cagcagactg 300
cacatcaagc gtacggtggc cgctcccagc gtgttcatct tcccacctag cgacgagcag 360
ctgaagtccg gcacagcctc tgtcgtgtgc ctgctgaaca acttctaccc ccgcgaggcc 420
aaagtgcagt ggaaggtgga caacgccctg cagagcggca acagccagga aagcgtgacc 480
gagcaggaca gcaaggactc cacctacagc ctgagcagca ccctgacact gagcaaggcc 540
gactacgaga agcacaaggt gtacgcctgc gaagtgaccc accagggcct gtctagcccc 600
gtgaccaaga gcttcaaccg gggcgagtgt 630
<210> 285
<211> 1008
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 285
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacgagaacc tgcagaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaaggaca aaacccatac cgacatccag 360
atgacccaga gccccagcag cctgtctgcc agcgtgggcg acagagtgac catcacctgt 420
caggccagcc agaacatcta cgtgtggctg aactggtatc agcagaagcc cggcaaggcc 480
cccaagctgc tgatctacaa ggccagcaac ctgcacaccg gcgtgcccag cagattttct 540
ggcagcggct ccggcaccga cttcaccctg acaatcagct ccctgcagcc cgaggacatt 600
gccacctact actgccagca gggccagacc tacccctaca cctttggcca gggcaccaag 660
ctggaaatca aggataagac ccacacccgt acggtggccg ctcccagcgt gttcatcttc 720
ccacctagcg acgagcagct gaagtccggc acagcctctg tcgtgtgcct gctgaacaac 780
ttctaccccc gcgaggccaa agtgcagtgg aaggtggaca acgccctgca gagcggcaac 840
agccaggaaa gcgtgaccga gcaggacagc aaggactcca cctacagcct gagcagcacc 900
ctgacactga gcaaggccga ctacgagaag cacaaggtgt acgcctgcga agtgacccac 960
cagggcctgt ctagccccgt gaccaagagc ttcaaccggg gcgagtgt 1008
<210> 286
<211> 1731
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 286
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
gacaaaaccc atacccaggt gcagctggtg gaatctggcg gcggagtggt gcagcctggc 420
agaagcctga gactgagctg tgccgccagc ggcttcacct tcaccaaggc ctggatgcac 480
tgggtgcgcc aggcccctgg aaagcagctg gaatgggtgg cccagatcaa ggacaagagc 540
aacagctacg ccacctacta cgccgacagc gtgaagggcc ggttcaccat cagccgggac 600
gacagcaaga acaccctgta cctgcagatg aacagcctgc gggccgagga caccgccgtg 660
tactactgtc ggggcgtgta ctatgccctg agccccttcg attactgggg ccagggaacc 720
ctcgtgaccg tgtctagtga taagacccac accgccagca caaagggccc atcggtgttc 780
cctctggccc cttgcagcag aagcaccagc gaatctacag ccgccctggg ctgcctcgtg 840
aaggactact ttcccgagcc cgtgaccgtg tcctggaact ctggcgctct gacaagcggc 900
gtgcacacct ttccagccgt gctccagagc agcggcctgt actctctgag cagcgtcgtg 960
acagtgccca gcagcagcct gggcaccaag acctacacct gtaacgtgga ccacaagccc 1020
agcaacacca aggtggacaa gcgggtggaa tctaagtacg gccctccctg ccctccttgc 1080
ccagcccctg aagctgccgg cggaccctcc gtgttcctgt tccccccaaa gcccaaggac 1140
accctgatga tcagccggac ccccgaagtg acctgcgtgg tggtggatgt gtcccaggaa 1200
gatcccgagg tgcagttcaa ttggtacgtg gacggcgtgg aagtgcacaa cgccaagacc 1260
aagcccagag aggaacagtt caacagcacc taccgggtgg tgtccgtgct gaccgtgctg 1320
caccaggact ggctgaacgg caaagagtac aagtgcaagg tgtccaacaa gggcctgccc 1380
agctccatcg agaaaaccat cagcaaggcc aagggccagc cccgcgagcc tcaagtgtgt 1440
accctgcccc ctagccagga agagatgacc aagaaccagg tgtccctgag ctgtgccgtg 1500
aaaggcttct accccagcga cattgccgtg gaatgggaga gcaacggcca gcccgagaac 1560
aactacaaga ccaccccccc tgtgctggac agcgacggct cattcttcct ggtgtccaag 1620
ctgaccgtgg acaagagccg gtggcaggaa ggcaacgtgt tcagctgctc cgtgatgcac 1680
gaggccctgc acaaccacta cacccagaag tccctgtctc tgtccctggg c 1731
<210> 287
<211> 1362
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<220>
<221> другой_признак
<222> 457, 518, 520
<223> n = A,T,C или G
<400> 287
caggtgcagc tggtgcagtc tggcggccag atgaagaaac ccggcgagag catgcggatc 60
agctgcagag ccagcggcta cgagttcatc gactgcaccc tgaactggat cagactggcc 120
cctggcaagc ggcctgagtg gatgggatgg ctgaagccta gatggggagc cgtgaactac 180
gccagacctc tgcagggcag agtgaccatg acccggcagc tgagccagga ccctgatgat 240
ccggattggg gcaccgcctt cctggaactg cggagcctga ccgtggatga taccgccgtg 300
tacttctgca cccggggcaa gaactgcgac tacaactggg acttcgagca ctggggcaga 360
ggcacccctg tgatcgtgtc aagcgcgtcg accaagggcc catcggtgtt ccctctggcc 420
ccttgcagca gaagcaccag cgaatctaca gccgccntgg gctgcctcgt gaaggactac 480
tttcccgagc ccgtgaccgt gtcctggaac tctggcgntn tgacaagcgg cgtgcacacc 540
tttccagccg tgctccagag cagcggcctg tactctctga gcagcgtcgt gacagtgccc 600
agcagcagcc tgggcaccaa gacctacacc tgtaacgtgg accacaagcc cagcaacacc 660
aaggtggaca agcgggtgga atctaagtac ggccctccct gccctccttg cccagcccct 720
gaagctgccg gcggaccctc cgtgttcctg ttccccccaa agcccaagga caccctgatg 780
atcagccgga cccccgaagt gacctgcgtg gtggtggatg tgtcccagga agatcccgag 840
gtgcagttca attggtacgt ggacggcgtg gaagtgcaca acgccaagac caagcccaga 900
gaggaacagt tcaacagcac ctaccgggtg gtgtccgtgc tgaccgtgct gcaccaggac 960
tggctgaacg gcaaagagta caagtgcaag gtgtccaaca agggcctgcc cagctccatc 1020
gagaaaacca tcagcaaggc caagggccag ccccgcgagc ctcaagtgta taccctgccc 1080
ccttgccagg aagagatgac caagaaccag gtgtccctgt ggtgtctcgt gaaaggcttc 1140
taccccagcg acattgccgt ggaatgggag agcaacggcc agcccgagaa caactacaag 1200
accacccccc ctgtgctgga cagcgacggc tcattcttcc tgtactccaa gctgaccgtg 1260
gacaagagcc ggtggcagga aggcaacgtg ttcagctgct ccgtgatgca cgaggccctg 1320
cacaaccact acacccagaa gtccctgtct ctgtccctgg gc 1362
<210> 288
<211> 621
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 288
ctgacacaga gccctggcac cctgtcactg agcccaggcg agacagccat catcagctgc 60
cggacaagcc agtacggcag cctggcctgg tatcagcaga ggcctggaca ggcccccaga 120
ctcgtgatct acagcggcag cacaagagcc gccggaatcc ccgatagatt cagcggctcc 180
agatggggac ccgactacaa cctgaccatc agcaacctgg aaagcggcga cttcggcgtg 240
tactactgcc agcagtacga gttcttcggc cagggcacca aggtgcaggt ggacatcaag 300
cgtacggtgg ccgctcccag cgtgttcatc ttcccaccta gcgacgagca gctgaagtcc 360
ggcacagcct ctgtcgtgtg cctgctgaac aacttctacc cccgcgaggc caaagtgcag 420
tggaaggtgg acaacgccct gcagagcggc aacagccagg aaagcgtgac cgagcaggac 480
agcaaggact ccacctacag cctgagcagc accctgacac tgagcaaggc cgactacgag 540
aagcacaagg tgtacgcctg cgaagtgacc caccagggcc tgtctagccc cgtgaccaag 600
agcttcaacc ggggcgagtg t 621
<210> 289
<211> 1008
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 289
gacatcgtga tgacccagac ccccctgagc ctgagcgtga cacctggaca gcctgccagc 60
atcagctgca agagcagcca gagcctggtg cacgagaacc tgttcaccta cctgagctgg 120
tatctgcaga agcccggcca gagcccccag tccctgatct acaaggtgtc caacagattc 180
agcggcgtgc ccgacagatt ctccggcagc ggctctggca ccgacttcac cctgaagatc 240
agccgggtgg aagccgagga cgtgggcgtg tactattgtg gccagggcac ccagtacccc 300
ttcacctttg gcagcggcac caaggtggaa atcaaggaca aaacccatac cgacatccag 360
atgacccaga gccccagcag cctgtctgcc agcgtgggcg acagagtgac catcacctgt 420
caggccagcc agaacatcta cgtgtggctg aactggtatc agcagaagcc cggcaaggcc 480
cccaagctgc tgatctacaa ggccagcaac ctgcacaccg gcgtgcccag cagattttct 540
ggcagcggct ccggcaccga cttcaccctg acaatcagct ccctgcagcc cgaggacatt 600
gccacctact actgccagca gggccagacc tacccctaca cctttggcca gggcaccaag 660
ctggaaatca aggataagac ccacacccgt acggtggccg ctcccagcgt gttcatcttc 720
ccacctagcg acgagcagct gaagtccggc acagcctctg tcgtgtgcct gctgaacaac 780
ttctaccccc gcgaggccaa agtgcagtgg aaggtggaca acgccctgca gagcggcaac 840
agccaggaaa gcgtgaccga gcaggacagc aaggactcca cctacagcct gagcagcacc 900
ctgacactga gcaaggccga ctacgagaag cacaaggtgt acgcctgcga agtgacccac 960
cagggcctgt ctagccccgt gaccaagagc ttcaaccggg gcgagtgt 1008
<210> 290
<211> 1731
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 290
caggtgcagc tggtgcagtc tggcgccgag gtcgtgaaac ctggcgcctc tgtgaaggtg 60
tcctgcaagg ccagcggcta cacctttacc agctactaca tccactgggt gcgccaggcc 120
cctggacagg gactggaatg gatcggcagc atctaccccg gcaacgtgaa caccaactac 180
gcccagaagt tccagggcag agccaccctg accgtggaca ccagcatcag caccgcctac 240
atggaactga gccggctgag aagcgacgac accgccgtgt actactgcac ccggtcccac 300
tacggcctgg attggaactt cgacgtgtgg ggcaagggca ccaccgtgac agtgtctagc 360
gacaaaaccc atacccaggt gcagctggtg gaatctggcg gcggagtggt gcagcctggc 420
agaagcctga gactgagctg tgccgccagc ggcttcacct tcaccaaggc ctggatgcac 480
tgggtgcgcc aggcccctgg aaagcagctg gaatgggtgg cccagatcaa ggacaagagc 540
aacagctacg ccacctacta cgccgacagc gtgaagggcc ggttcaccat cagccgggac 600
gacagcaaga acaccctgta cctgcagatg aacagcctgc gggccgagga caccgccgtg 660
tactactgtc ggggcgtgta ctatgccctg agccccttcg attactgggg ccagggaacc 720
ctcgtgaccg tgtctagtga taagacccac accgccagca caaagggccc atcggtgttc 780
cctctggccc cttgcagcag aagcaccagc gaatctacag ccgccctggg ctgcctcgtg 840
aaggactact ttcccgagcc cgtgaccgtg tcctggaact ctggcgctct gacaagcggc 900
gtgcacacct ttccagccgt gctccagagc agcggcctgt actctctgag cagcgtcgtg 960
acagtgccca gcagcagcct gggcaccaag acctacacct gtaacgtgga ccacaagccc 1020
agcaacacca aggtggacaa gcgggtggaa tctaagtacg gccctccctg ccctccttgc 1080
ccagcccctg aagctgccgg cggaccctcc gtgttcctgt tccccccaaa gcccaaggac 1140
accctgatga tcagccggac ccccgaagtg acctgcgtgg tggtggatgt gtcccaggaa 1200
gatcccgagg tgcagttcaa ttggtacgtg gacggcgtgg aagtgcacaa cgccaagacc 1260
aagcccagag aggaacagtt caacagcacc taccgggtgg tgtccgtgct gaccgtgctg 1320
caccaggact ggctgaacgg caaagagtac aagtgcaagg tgtccaacaa gggcctgccc 1380
agctccatcg agaaaaccat cagcaaggcc aagggccagc cccgcgagcc tcaagtgtgt 1440
accctgcccc ctagccagga agagatgacc aagaaccagg tgtccctgag ctgtgccgtg 1500
aaaggcttct accccagcga cattgccgtg gaatgggaga gcaacggcca gcccgagaac 1560
aactacaaga ccaccccccc tgtgctggac agcgacggct cattcttcct ggtgtccaag 1620
ctgaccgtgg acaagagccg gtggcaggaa ggcaacgtgt tcagctgctc cgtgatgcac 1680
gaggccctgc acaaccacta cacccagaag tccctgtctc tgtccctggg c 1731
<210> 291
<211> 1362
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<220>
<221> другой_признак
<222> 457, 518, 520
<223> n = A,T,C или G
<400> 291
caggtgcagc tggtgcagtc tggcggccag atgaagaaac ccggcgagag catgcggatc 60
agctgcagag ccagcggcta cgagttcatc gactgcaccc tgaactggat cagactggcc 120
cctggcaagc ggcctgagtg gatgggatgg ctgaagccta gatggggagc cgtgaactac 180
gccagacctc tgcagggcag agtgaccatg acccggcagc tgagccagga ccctgatgat 240
ccggattggg gcaccgcctt cctggaactg cggagcctga ccgtggatga taccgccgtg 300
tacttctgca cccggggcaa gaactgcgac tacaactggg acttcgagca ctggggcaga 360
ggcacccctg tgatcgtgtc aagcgcgtcg accaagggcc catcggtgtt ccctctggcc 420
ccttgcagca gaagcaccag cgaatctaca gccgccntgg gctgcctcgt gaaggactac 480
tttcccgagc ccgtgaccgt gtcctggaac tctggcgntn tgacaagcgg cgtgcacacc 540
tttccagccg tgctccagag cagcggcctg tactctctga gcagcgtcgt gacagtgccc 600
agcagcagcc tgggcaccaa gacctacacc tgtaacgtgg accacaagcc cagcaacacc 660
aaggtggaca agcgggtgga atctaagtac ggccctccct gccctccttg cccagcccct 720
gaagctgccg gcggaccctc cgtgttcctg ttccccccaa agcccaagga caccctgatg 780
atcagccgga cccccgaagt gacctgcgtg gtggtggatg tgtcccagga agatcccgag 840
gtgcagttca attggtacgt ggacggcgtg gaagtgcaca acgccaagac caagcccaga 900
gaggaacagt tcaacagcac ctaccgggtg gtgtccgtgc tgaccgtgct gcaccaggac 960
tggctgaacg gcaaagagta caagtgcaag gtgtccaaca agggcctgcc cagctccatc 1020
gagaaaacca tcagcaaggc caagggccag ccccgcgagc ctcaagtgta taccctgccc 1080
ccttgccagg aagagatgac caagaaccag gtgtccctgt ggtgtctcgt gaaaggcttc 1140
taccccagcg acattgccgt ggaatgggag agcaacggcc agcccgagaa caactacaag 1200
accacccccc ctgtgctgga cagcgacggc tcattcttcc tgtactccaa gctgaccgtg 1260
gacaagagcc ggtggcagga aggcaacgtg ttcagctgct ccgtgatgca cgaggccctg 1320
cacaaccact acacccagaa gtccctgtct ctgtccctgg gc 1362
<210> 292
<211> 621
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 292
ctgacacaga gccctggcac cctgtcactg agcccaggcg agacagccat catcagctgc 60
cggacaagcc agtacggcag cctggcctgg tatcagcaga ggcctggaca ggcccccaga 120
ctcgtgatct acagcggcag cacaagagcc gccggaatcc ccgatagatt cagcggctcc 180
agatggggac ccgactacaa cctgaccatc agcaacctgg aaagcggcga cttcggcgtg 240
tactactgcc agcagtacga gttcttcggc cagggcacca aggtgcaggt ggacatcaag 300
cgtacggtgg ccgctcccag cgtgttcatc ttcccaccta gcgacgagca gctgaagtcc 360
ggcacagcct ctgtcgtgtg cctgctgaac aacttctacc cccgcgaggc caaagtgcag 420
tggaaggtgg acaacgccct gcagagcggc aacagccagg aaagcgtgac cgagcaggac 480
agcaaggact ccacctacag cctgagcagc accctgacac tgagcaaggc cgactacgag 540
aagcacaagg tgtacgcctg cgaagtgacc caccagggcc tgtctagccc cgtgaccaag 600
agcttcaacc ggggcgagtg t 621
<210> 293
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<220>
<221> ВАРИАНТ
<222> 6
<223> Xaa = Glu или Gln
<220>
<221> ВАРИАНТ
<222> 8
<223> Xaa = Ala или Leu
<220>
<221> ВАРИАНТ
<222> 9
<223> Xaa = Gln, Arg или Phe
<400> 293
Gln Ser Leu Val His Xaa Asn Xaa Xaa Thr Tyr
1 5 10
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИИ И СПОСОБЫ РЕДАКТИРОВАНИЯ ГЕНОВ | 2019 |
|
RU2804665C2 |
| T-КЛЕТОЧНЫЕ РЕЦЕПТОРЫ, РАСПОЗНАЮЩИЕ МУТАЦИЮ R175H ИЛИ Y220C В P53 | 2020 |
|
RU2830061C2 |
| КОНСТРУКЦИИ ДНК-АНТИТЕЛ ДЛЯ ПРИМЕНЕНИЯ ПРОТИВ БОЛЕЗНИ ЛАЙМА | 2017 |
|
RU2813829C2 |
| ЛЕЧЕНИЕ РАКА С ИСПОЛЬЗОВАНИЕМ ХИМЕРНОГО АНТИГЕНСПЕЦИФИЧЕСКОГО РЕЦЕПТОРА НА ОСНОВЕ ГУМАНИЗИРОВАННОГО АНТИТЕЛА ПРОТИВ EGFRvIII | 2014 |
|
RU2831418C2 |
| ГЛИКАНЗАВИСИМЫЕ ИММУНОТЕРАПЕВТИЧЕСКИЕ МОЛЕКУЛЫ | 2016 |
|
RU2754661C2 |
| НЕ ВСТРЕЧАЮЩИЙСЯ В ПРИРОДЕ ВИРУС РЕПРОДУКТИВНО-РЕСПИРАТОРНОГО СИНДРОМА СВИНЕЙ (BPPCC) И СПОСОБЫ ПРИМЕНЕНИЯ | 2015 |
|
RU2687150C2 |
| ТЕРАПЕВТИЧЕСКИЕ СРЕДСТВА И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ TLR2-ОПОСРЕДОВАННЫХ ЗАБОЛЕВАНИЙ И НАРУШЕНИЙ | 2019 |
|
RU2791022C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ИЗБИРАТЕЛЬНОЙ ЭКСПРЕССИИ БЕЛКА | 2017 |
|
RU2795467C2 |
| ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР (CAR) ПРОТИВ CD123 ДЛЯ ИСПОЛЬЗОВАНИЯ В ЛЕЧЕНИИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ | 2015 |
|
RU2724999C2 |
| ЛЕЧЕНИЕ ЗЛОКАЧЕСТВЕННОГО НОВООБРАЗОВАНИЯ С ИСПОЛЬЗОВАНИЕМ ГУМАНИЗИРОВАННОГО ХИМЕРНОГО АНТИГЕННОГО РЕЦЕПТОРА ПРОТИВ ВСМА | 2015 |
|
RU2751660C2 |
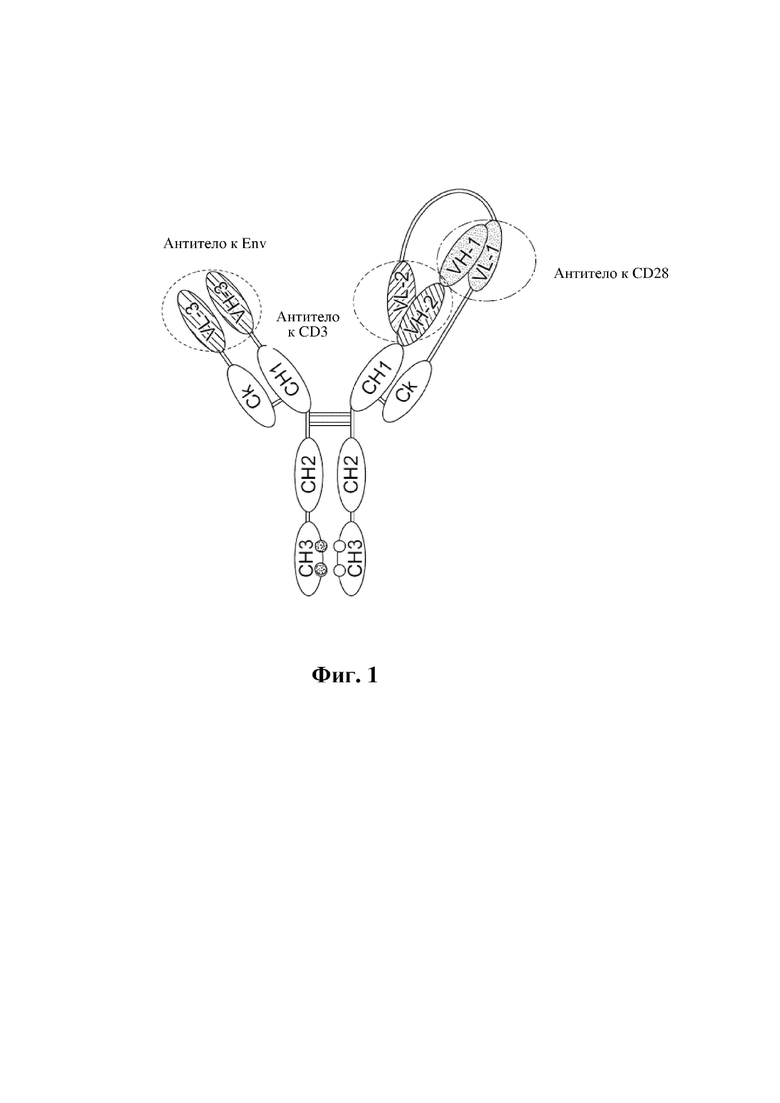
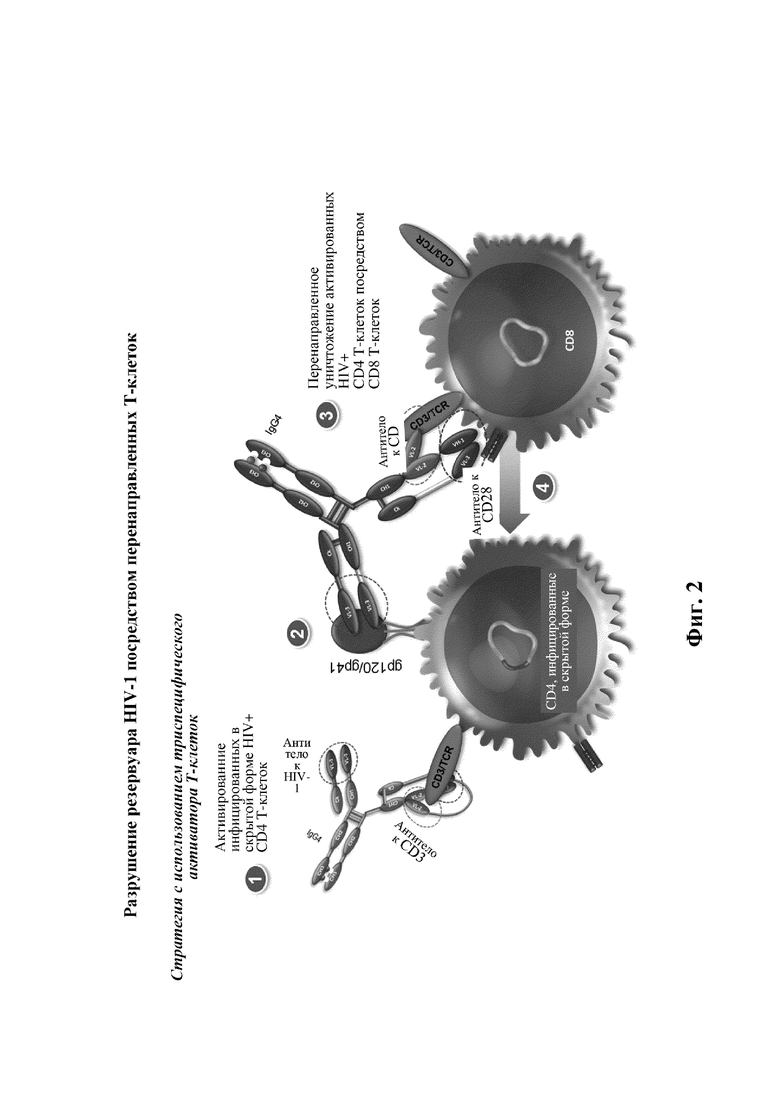
Изобретение относится к области биотехнологии, конкретно к получению триспецифических связывающих белков, связывающих целевой белок HIV, и может быть использовано в медицине для профилактики или лечения инфекции HIV. Изобретение обеспечивает получение средства для устранения резервуара HIV-1 посредством активации антител к CD3, совместной активации антител к Т-клеточному белку-мишени, например, к CD28 и последующего уничтожения активированных клеток резервуара HIV-1 посредством антител к HIV/к CD28 путем вовлечения активированных CD8 Т-клеток, что обеспечивает потенциальную стратегию для осуществления атаки на резервуар HIV-1. 5 н. и 28 з.п. ф-лы, 2 ил., 5 табл.
1. Связывающий белок для профилактики или лечения инфекции HIV, содержащий четыре полипептидные цепи, которые образуют три антигенсвязывающих участка, где первая полипептидная цепь содержит структуру, представленную формулой
VL2-L1-VL1-L2-CL [I];
и вторая полипептидная цепь содержит структуру, представленную формулой
VH1-L3-VH2-L4-CH1-шарнир-CH2-CH3 [II];
и третья полипептидная цепь содержит структуру, представленную формулой
VH3-CH1-шарнир-CH2-CH3 [III];
и четвертая полипептидная цепь содержит структуру, представленную формулой
VL3-CL [IV];
где:
VL1 представляет собой первый вариабельный домен легкой цепи иммуноглобулина;
VL2 представляет собой второй вариабельный домен легкой цепи иммуноглобулина;
VL3 представляет собой третий вариабельный домен легкой цепи иммуноглобулина;
VH1 представляет собой первый вариабельный домен тяжелой цепи иммуноглобулина;
VH2 представляет собой второй вариабельный домен тяжелой цепи иммуноглобулина;
VH3 представляет собой третий вариабельный домен тяжелой цепи иммуноглобулина;
CL представляет собой константный домен легкой цепи иммуноглобулина;
CH1 представляет собой константный домен CH1 тяжелой цепи иммуноглобулина;
CH2 представляет собой константный домен CH2 тяжелой цепи иммуноглобулина;
CH3 представляет собой константный домен CH3 тяжелой цепи иммуноглобулина;
шарнир представляет собой шарнирную область иммуноглобулина, соединяющую домены CH1 и CH2; и
L1, L2, L3 и L4 представляют собой аминокислотные линкеры;
где полипептид формулы I и полипептид формулы II образуют кроссоверную пару легкая цепь-тяжелая цепь, и
где VH1 и VL1 образуют первый антигенсвязывающий участок, который связывает Т-клеточный белок-мишень;
где VH2 и VL2 образуют второй антигенсвязывающий участок, который связывает полипептид CD3, где домен VH2 содержит последовательность CDR-H1, содержащую аминокислотную последовательность GFTFTKAW (SEQ ID NO:20), последовательность CDR-H2, содержащую аминокислотную последовательность IKDKSNSYAT (SEQ ID NO:21), и последовательность CDR-H3, содержащую аминокислотную последовательность RGVYYALSPFDY (SEQ ID NO:22), и домен VL2 содержит последовательность CDR-L1, содержащую аминокислотную последовательность QSLVHX1NX2X3TY, где X1 представляет собой E или Q, X2 представляет собой A или L, и X3 представляет собой Q, R или F (SEQ ID NO:293), последовательность CDR-L2, содержащую аминокислотную последовательность KVS (SEQ ID NO:29), и последовательность CDR-L3, содержащую аминокислотную последовательность GQGTQYPFT (SEQ ID NO:30); и
где VH3 и VL3 образуют третий антигенсвязывающий участок, который связывает целевой белок HIV.
2. Связывающий белок по п. 1, где первый связывающий участок связывает полипептид CD28.
3. Связывающий белок по п. 2, где домен VH1 содержит последовательность CDR-H1, содержащую аминокислотную последовательность GYTFTSYY (SEQ ID NO:31), последовательность CDR-H2, содержащую аминокислотную последовательность IYPGNVNT (SEQ ID NO:32), и последовательность CDR-H3, содержащую аминокислотную последовательность TRSHYGLDWNFDV (SEQ ID NO:33), и домен VL1 содержит последовательность CDR-L1, содержащую аминокислотную последовательность QNIYVW (SEQ ID NO:34), последовательность CDR-L2, содержащую аминокислотную последовательность KAS (SEQ ID NO:35), и последовательность CDR-L3, содержащую аминокислотную последовательность QQGQTYPY (SEQ ID NO:36).
4. Связывающий белок по п. 3, где домен VH1 содержит аминокислотную последовательность QVQLVQSGAEVVKPGASVKVSCKASGYTFTSYYIHWVRQAPGQGLEWIGSIYPGNVNTNYAQKFQGRATLTVDTSISTAYMELSRLRSDDTAVYYCTRSHYGLDWNFDVWGKGTTVTVSS (SEQ ID NO:59), и/или домен VL1 содержит аминокислотную последовательность DIQMTQSPSSLSASVGDRVTITCQASQNIYVWLNWYQQKPGKAPKLLIYKASNLHTGVPSRFSGSGSGTDFTLTISSLQPEDIATYYCQQGQTYPYTFGQGTKLEIK (SEQ ID NO:60).
5. Связывающий белок по любому из пп. 1-4, где последовательность CDR-L1 домена VL2 содержит аминокислотную последовательность, выбранную из группы, состоящей из QSLVHQNAQTY (SEQ ID NO:24), QSLVHENLQTY (SEQ ID NO:25), QSLVHENLFTY (SEQ ID NO:26) и QSLVHENLRTY (SEQ ID NO:27).
6. Связывающий белок по п. 5, где домен VH2 содержит аминокислотную последовательность QVQLVESGGGVVQPGRSLRLSCAASGFTFTKAWMHWVRQAPGKQLEWVAQIKDKSNSYATYYADSVKGRFTISRDDSKNTLYLQMNSLRAEDTAVYYCRGVYYALSPFDYWGQGTLVTVSS (SEQ ID NO:52), и/или домен VL2 содержит аминокислотную последовательность, выбранную из группы, состоящей из DIVMTQTPLSLSVTPGQPASISCKSSQSLVHQNAQTYLSWYLQKPGQSPQSLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCGQGTQYPFTFGSGTKVEIK (SEQ ID NO:54), DIVMTQTPLSLSVTPGQPASISCKSSQSLVHENLQTYLSWYLQKPGQSPQSLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCGQGTQYPFTFGSGTKVEIK (SEQ ID NO:55), DIVMTQTPLSLSVTPGQPASISCKSSQSLVHENLFTYLSWYLQKPGQSPQSLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCGQGTQYPFTFGSGTKVEIK (SEQ ID NO:56) и DIVMTQTPLSLSVTPGQPASISCKSSQSLVHENLRTYLSWYLQKPGQSPQSLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCGQGTQYPFTFGSGTKVEIK (SEQ ID NO:57).
7. Связывающий белок по любому из пп. 1-6, где третий антигенсвязывающий участок связывает целевой белок HIV, выбранный из группы, состоящей из гликопротеина 120, гликопротеина 41 и гликопротеина 160.
8. Связывающий белок по п. 7, где:
(a) домен VH3 содержит последовательность CDR-H1, содержащую аминокислотную последовательность NCPIN (SEQ ID NO:1), последовательность CDR-H2, содержащую аминокислотную последовательность WMKPRHGAVSYARQLQG (SEQ ID NO:2), и последовательность CDR-H3, содержащую аминокислотную последовательность GKYCTARDYYNWDFEH (SEQ ID NO:3), и домен VL3 содержит последовательность CDR-L1, содержащую аминокислотную последовательность RTSQYGSLA (SEQ ID NO:4), последовательность CDR-L2, содержащую аминокислотную последовательность SGSTRAA (SEQ ID NO:5), и последовательность CDR-L3, содержащую аминокислотную последовательность QQYEF (SEQ ID NO:6);
(b) домен VH3 содержит последовательность CDR-H1, содержащую аминокислотную последовательность GYTFTAHI (SEQ ID NO:7), последовательность CDR-H2, содержащую аминокислотную последовательность IKPQYGAV (SEQ ID NO:8) или IKPQYGAT (SEQ ID NO:9), и последовательность CDR-H3, содержащую аминокислотную последовательность DRSYGDSSWALDA (SEQ ID NO:10), и домен VL3 содержит последовательность CDR-L1, содержащую аминокислотную последовательность QGVGSD (SEQ ID NO:11), последовательность CDR-L2, содержащую аминокислотную последовательность HTS (SEQ ID NO:12), и последовательность CDR-L3, содержащую аминокислотную последовательность CQVLQF (SEQ ID NO:13); или
(c) домен VH3 содержит последовательность CDR-H1, содержащую аминокислотную последовательность DCTLN (SEQ ID NO:14), последовательность CDR-H2, содержащую аминокислотную последовательность WLKPRWGAVNYARPLQG (SEQ ID NO:15), и последовательность CDR-H3, содержащую аминокислотную последовательность GKNCDYNWDFEH (SEQ ID NO:16), и домен VL3 содержит последовательность CDR-L1, содержащую аминокислотную последовательность RTSQYGSLA (SEQ ID NO:17), последовательность CDR-L2, содержащую аминокислотную последовательность SGSTRAA (SEQ ID NO:18), и последовательность CDR-L3, содержащую аминокислотную последовательность QQYEF (SEQ ID NO:19).
9. Связывающий белок по п. 8, где:
(a) домен VH3 содержит аминокислотную последовательность QVRLSQSGGQMKKPGDSMRISCRASGYEFINCPINWIRLAPGKRPEWMGWMKPRHGAVSYARQLQGRVTMTRDMYSETAFLELRSLTSDDTAVYFCTRGKYCTARDYYNWDFEHWGQGTPVTVSS (SEQ ID NO:43), и/или домен VL3 содержит аминокислотную последовательность SLTQSPGTLSLSPGETAIISCRTSQYGSLAWYQQRPGQAPRLVIYSGSTRAAGIPDRFSGSRWGPDYNLTISNLESGDFGVYYCQQYEFFGQGTKVQVDIK (SEQ ID NO:45);
(b) домен VH3 содержит аминокислотную последовательность QVRLSQSGGQMKKPGDSMRISCRASGYEFINCPINWIRLAPGKRPEWMGWMKPRHGAVSYARQLQGRVTMTRQLSQDPDDPDWGTAFLELRSLTSDDTAVYFCTRGKYCTARDYYNWDFEHWGQGTPVTVSS (SEQ ID NO:44), и/или домен VL3 содержит аминокислотную последовательность SLTQSPGTLSLSPGETAIISCRTSQYGSLAWYQQRPGQAPRLVIYSGSTRAAGIPDRFSGSRWGPDYNLTISNLESGDFGVYYCQQYEFFGQGTKVQVDIK (SEQ ID NO:45);
(c) домен VH3 содержит аминокислотную последовательность RAHLVQSGTAMKKPGASVRVSCQTSGYTFTAHILFWFRQAPGRGLEWVGWIKPQYGAVNFGGGFRDRVTLTRDVYREIAYMDIRGLKPDDTAVYYCARDRSYGDSSWALDAWGQGTTVVVSA (SEQ ID NO:46), и/или домен VL3 содержит аминокислотную последовательность YIHVTQSPSSLSVSIGDRVTINCQTSQGVGSDLHWYQHKPGRAPKLLIHHTSSVEDGVPSRFSGSGFHTSFNLTISDLQADDIATYYCQVLQFFGRGSRLHIK (SEQ ID NO:49);
(d) домен VH3 содержит аминокислотную последовательность RAHLVQSGTAMKKPGASVRVSCQTSGYTFTAHILFWFRQAPGRGLEWVGWIKPQYGATNFGGGFRDRVTLTRDVYREIAYMDIRGLKPDDTAVYYCARDRSYGDSSWALDAWGQGTTVVVSA (SEQ ID NO:47), и/или домен VL3 содержит аминокислотную последовательность YIHVTQSPSSLSVSIGDRVTINCQTSQGVGSDLHWYQHKPGRAPKLLIHHTSSVEDGVPSRFSGSGFHTSFNLTISDLQADDIATYYCQVLQFFGRGSRLHIK (SEQ ID NO:49);
(e) домен VH3 содержит аминокислотную последовательность RAHLVQSGTAMKKPGASVRVSCQTSGYTFTAHILFWFRQAPGRGLEWVGWIKPQYGAVNFGGGFRDRVTLTRQLSQDPDDPDWGIAYMDIRGLKPDDTAVYYCARDRSYGDSSWALDAWGQGTTVVVSA (SEQ ID NO:48), и/или домен VL3 содержит аминокислотную последовательность YIHVTQSPSSLSVSIGDRVTINCQTSQGVGSDLHWYQHKPGRAPKLLIHHTSSVEDGVPSRFSGSGFHTSFNLTISDLQADDIATYYCQVLQFFGRGSRLHIK (SEQ ID NO:49); или
(f) домен VH3 содержит аминокислотную последовательность QVQLVQSGGQMKKPGESMRISCRASGYEFIDCTLNWIRLAPGKRPEWMGWLKPRWGAVNYARPLQGRVTMTRQLSQDPDDPDWGTAFLELRSLTVDDTAVYFCTRGKNCDYNWDFEHWGRGTPVIVSS (SEQ ID NO:50), и/или домен VL3 содержит аминокислотную последовательность LTQSPGTLSLSPGETAIISCRTSQYGSLAWYQQRPGQAPRLVIYSGSTRAAGIPDRFSGSRWGPDYNLTISNLESGDFGVYYCQQYEFFGQGTKVQVDIK (SEQ ID NO:51).
10. Связывающий белок по любому из пп. 1-9, где длина по меньшей мере одного из L1, L2, L3 или L4 независимо составляет 0 аминокислот.
11. Связывающий белок по любому из пп. 1-9, где (a) каждый из L1, L2, L3 и L4 независимо имеет длину, составляющую ноль аминокислот, или содержит последовательность, выбранную из группы, состоящей из GGGGSGGGGS (SEQ ID NO:40), GGGGSGGGGSGGGGS (SEQ ID NO:41), S, RT, TKGPS (SEQ ID NO:39), GQPKAAP (SEQ ID NO:38) и GGSGSSGSGG (SEQ ID NO:42); или (b) каждый из L1, L2, L3 и L4 независимо содержит последовательность, выбранную из группы, состоящей из GGGGSGGGGS (SEQ ID NO:40), GGGGSGGGGSGGGGS (SEQ ID NO:41), S, RT, TKGPS (SEQ ID NO:39), GQPKAAP (SEQ ID NO:38) и GGSGSSGSGG (SEQ ID NO:42).
12. Связывающий белок по любому из пп. 1-9, где L1 содержит последовательность GQPKAAP (SEQ ID NO:38), L2 содержит последовательность TKGPS (SEQ ID NO:39), L3 содержит последовательность S, и L4 содержит последовательность RT.
13. Связывающий белок по любому из пп. 1-9, где по меньшей мере один из L1, L2, L3 или L4 содержит последовательность DKTHT (SEQ ID NO:37).
14. Связывающий белок по п. 13, где L1, L2, L3 и L4 содержат последовательность DKTHT (SEQ ID NO:37).
15. Связывающий белок по любому из пп. 1-14, где домены шарнир-CH2-CH3 второй и третьей полипептидных цепей представляют собой домены шарнир-CH2-CH3 IgG4 человека, и где каждый из доменов шарнир-CH2-CH3 содержит аминокислотные замены в положениях, соответствующих положениям 234 и 235 IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой F234A и L235A.
16. Связывающий белок по любому из пп. 1-14, где домены шарнир-CH2-CH3 второй и третьей полипептидных цепей представляют собой домены шарнир-CH2-CH3 IgG4 человека, и где каждый из доменов шарнир-CH2-CH3 содержит аминокислотные замены в положениях, соответствующих положениям 233-236 IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой E233P, F234V, L235A, и делецию в положении 236.
17. Связывающий белок по любому из пп. 1-16, где домены шарнир-CH2-CH3 второй и третьей полипептидных цепей представляют собой домены шарнир-CH2-CH3 IgG4 человека, и где каждый из доменов шарнир-CH2-CH3 содержит аминокислотные замены в положениях, соответствующих положениям 228 и 409 IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой S228P и R409K.
18. Связывающий белок по любому из пп. 1-14, где домены шарнир-CH2-CH3 второй и третьей полипептидных цепей представляют собой домены шарнир-CH2-CH3 IgG1 человека, и где каждый из доменов шарнир-CH2-CH3 содержит аминокислотные замены в положениях, соответствующих положениям 234, 235 и 329 IgG1 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой L234A, L235A и P329A.
19. Связывающий белок по любому из пп. 1-14, где домены шарнир-CH2-CH3 второй и третьей полипептидных цепей представляют собой домены шарнир-CH2-CH3 IgG1 человека, и где каждый из доменов шарнир-CH2-CH3 содержит аминокислотные замены в положениях, соответствующих положениям 298, 299 и 300 IgG1 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой S298N, T299A и Y300S.
20. Связывающий белок по любому из пп. 1-19, где домен шарнир-CH2-CH3 второй полипептидной цепи содержит аминокислотные замены в положениях, соответствующих положениям 349, 366, 368 и 407 IgG1 или IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой Y349C, T366S, L368A и Y407V; и где домен шарнир-CH2-CH3 третьей полипептидной цепи содержит аминокислотные замены в положениях, соответствующих положениям 354 и 366 IgG1 или IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой S354C и T366W.
21. Связывающий белок по любому из пп. 1-19, где домен шарнир-CH2-CH3 второй полипептидной цепи содержит аминокислотные замены в положениях, соответствующих положениям 354 и 366 IgG1 или IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой S354C и T366W; и где домен шарнир-CH2-CH3 третьей полипептидной цепи содержит аминокислотные замены в положениях, соответствующих положениям 349, 366, 368 и 407 IgG1 или IgG4 человека в соответствии с EU-индексом, где аминокислотные замены представляют собой Y349C, T366S, L368A и Y407V.
22. Связывающий белок по п. 1, где:
(a) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:61 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:61; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:62 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:62; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:63 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:63; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:64 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:64;
(b) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:65 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:65; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:66 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:66; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:67 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:67; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:68 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:68;
(c) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:69 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:69; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:70 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:70; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:71 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:71; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:72 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:72;
(d) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:73 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:73; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:74 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:74; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:75 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:75; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:76 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:76;
(e) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:77 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:77; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:78 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:78; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:79 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:79; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:80 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:80;
(f) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:81 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:81; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:82 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:82; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:83 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:83; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:84 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:84;
(g) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:85 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:85; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:86 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:86; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:87 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:87; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:88 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:88;
(h) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:89 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:89; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:90 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:90; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:91 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:91; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:92 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:92;
(i) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:93 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:93; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:94 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:94; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:95 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:95; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:96 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:96;
(j) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:97 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:97; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:98 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:98; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:99 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:99; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:100 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:100;
(k) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:101 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:101; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:102 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:102; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:103 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:103; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:104 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:104;
(l) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:105 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:105; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:106 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:106; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:107 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:107; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:108 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:108;
(m) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:109 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:109; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:110 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:110; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:111 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:111; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:112 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:112;
(n) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:113 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:113; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:114 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:114; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:115 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:115; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:116 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:116;
(o) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:117 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:117; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:118 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:118; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:119 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:119; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:120 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:120;
(p) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:121 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:121; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:122 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:122; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:123 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:123; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:124 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:124;
(q) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:129 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:129; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:130 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:130; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:131 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:131; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:132 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:132;
(r) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:133 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:133; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:134 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:134; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:135 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:135; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:136 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:136;
(s) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:137 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:137; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:138 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:138; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:139 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:139; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:140 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:140;
(t) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:141 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:141; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:142 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:142; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:143 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:143; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:144 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:144;
(u) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:145 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:145; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:146 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:146; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:147 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:147; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:148 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:148;
(v) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:149 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:149; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:150 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:150; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:151 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:151; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:152 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:152;
(x) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:153 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:153; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:154 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:154; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:155 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:155; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:156 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:156;
(y) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:157 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:157; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:158 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:158; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:159 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:159; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:160 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:160;
(z) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:161 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:161; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:162 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:162; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:163 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:163; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:164 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:164;
(aa) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:165 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:165; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:166 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:166; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:167 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:167; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:168 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:168;
(bb) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:169 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:169; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:170 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:170; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:171 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:171; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:172 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:172;
(cc) первая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:173 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:173; вторая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:174 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:174; третья полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:175 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:175; и четвертая полипептидная цепь содержит аминокислотную последовательность под SEQ ID NO:176 или аминокислотную последовательность, которая на по меньшей мере 95% идентична аминокислотной последовательности под SEQ ID NO:176.
23. Выделенная клетка-хозяин для экспрессии связывающего белка по любому из пп. 1-22, содержащая вектор экспрессии, содержащий молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, кодирующую связывающий белок.
24. Выделенная клетка-хозяин по п. 23, где клетка-хозяин представляет собой клетку млекопитающего или насекомого, причем клетка не является эмбриональной человеческой клеткой.
25. Фармацевтическая композиция для профилактики или лечения инфекции HIV, содержащая эффективное количество связывающего белка по любому из пп. 1-22 и фармацевтически приемлемый носитель.
26. Способ профилактики или лечения инфекции HIV у пациента, включающий введение пациенту терапевтически эффективного количества связывающего белка по любому из пп. 1-22 или фармацевтической композиции по п. 25.
27. Способ по п. 26, где связывающий белок вводят совместно со средством для антиретровирусной терапии.
28. Способ по п. 26 или 27, где введение связывающего белка приводит в результате к устранению у пациента одной или нескольких клеток, инфицированных HIV в латентной и/или хронической форме.
29. Способ по любому из пп. 26-28, где пациентом является человек.
30. Применение связывающего белка по любому из пп. 1-22 или фармацевтической композиции по п. 25 для профилактики или лечения инфекции HIV у пациента.
31. Применение по п. 30, где связывающий белок подлежит совместному введению со средством для антиретровирусной терапии.
32. Применение по п. 30 или 31, где связывающий белок обеспечивает устранение у пациента одной или нескольких клеток, инфицированных HIV в латентной и/или хронической форме.
33. Применение по любому из пп. 30-32, где пациентом является человек.
| EA 201891028 A1, 28.02.2019 | |||
| EA 201791666 A1, 30.11.2017 | |||
| WO 2017011414 А1, 19.01.2017 | |||
| WO 2018015340 A1, 25.01.2018 | |||
| KONTERMANN R | |||
| E | |||
| et al | |||
| Bispecific antibodies, Drug Discovery Today, 2015, v.7, n.20, p.838-847 | |||
| ЯРИЛИН А.А | |||
| Основы иммунологии, М.: Медицина, 1999, 608с., с.172-174 | |||
| СИНГЕР М | |||
| и др | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2024-05-30—Публикация
2020-04-08—Подача