РОДСТВЕННЫЕ ЗАЯВКИ
[01] Настоящая заявка испрашивает преимущества предварительных заявок USSN 62/608,571, поданной 20 декабря 2017 года, и USSN 62/608,894, поданной 21 декабря 2017 года, содержание каждой из которых включено в настоящий документ посредством отсылок во всей своей полноте.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[02] Изобретение направлено на молекулярную биологию и, в частности, на химерные антигенные рецепторы, и на транспозоны, содержащие один или более VCAR-рецепторов, а также способы их получения и применения.
ВКЛЮЧЕНИЕ СПИСКА ПОСЛЕДОВАТЕЛЬНОСТЕЙ ПОСРЕДСТВОМ ОТСЫЛКИ
[03] Содержание файла под именем "POTH-034_001WO_SeqListing_ST25_R.txt", который был создан 19 декабря 2018 года и имеет размер 54,4 МБ, настоящим включено посредством отсылки во всей своей полноте.
УРОВЕНЬ ТЕХНИКИ
[04] В уровне техники существует давняя, но неудовлетворенная потребность в способе определения специфичности иммунной клетки без применения традиционных последовательностей антител или их фрагментов. В изобретении предложен превосходный химерный антигенный рецептор.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[05] В изобретении предложен химерный антигенный рецептор (CAR), включающий: (a) эктодомен, включающий область распознавания антигена, где область распознавания антигена включает по меньшей мере одно однодоменное антитело; (b) трансмембранный домен и (c) эндодомен, включающий по меньшей мере один костимулирующий домен. В некоторых вариантах осуществления однодоменное антитело включает человеческую или гуманизированную последовательность. В некоторых вариантах осуществления однодоменное антитело включает не встречающуюся в природе последовательность. В некоторых вариантах осуществления однодоменное антитело включает рекомбинантную или химерную последовательность. В некоторых вариантах осуществления однодоменное антитело включает VHH или последовательность, кодирующую VHH. В некоторых вариантах осуществления однодоменное антитело включает VH или последовательность, кодирующую VH. В некоторых вариантах осуществления однодоменное антитело включает VH согласно изобретению или последовательность, кодирующую VH согласно изобретению.
[06] В изобретении предложен химерный антигенный рецептор (CAR), включающий: (a) эктодомен, включающий область распознавания антигена, где область распознавания антигена включает по меньшей мере один VHH; (b) трансмембранный домен и (c) эндодомен, включающий по меньшей мере один костимулирующий домен. При использовании в тексте настоящего описания, CAR, включающий VHH, именуется VCAR. В некоторых вариантах осуществления область распознавания антигена может включать два VHH с получением биспецифичного или тандемного VCAR. В некоторых вариантах осуществления область распознавания антигена может включать три VHH с получением триспецифичного VCAR.
[07] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению эктодомен может дополнительно включать сигнальный пептид. В альтернативе или дополнительно, в некоторых вариантах осуществления, эктодомен может дополнительно включать шарнирную область между областью распознавания антигена и трансмембранным доменом. В некоторых вариантах осуществления эктодомен может дополнительно включать сигнальный пептид. В альтернативе или дополнительно, в некоторых вариантах осуществления, эктодомен может дополнительно включать шарнирную область между областью распознавания антигена и трансмембранным доменом.
[08] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, VHH включает или состоит из аминокислотной последовательности:
malpvtalllplalllhaarpevqllesggglvqpggslrlscaasgftfssyamnwvrqapgkglewvagiigsggstyyadsvkgrfsisrdnskntldlqmnslraedtavyycvkdwnttmitergqgtlvtvsstttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (VH-A; SEQ ID NO:18000)
или VHH включает или состоит из последовательности нуклеиновой кислоты:
atggctctgcctgtgacagctctgctgctgcctctggctctgcttcttcatgcggcgcgccctgaagttcagctgcttgaatctggcggaggcctggttcaacctggcggatctctgagactgagctgtgccgccagcggcttcacctttagcagctacgccatgaactgggtccgacaggcccctggcaaaggactggaatgggtggccggaatcatcggcagcggcggcagcacatattacgccgattctgtgaagggccgcttcagcatcagccgggacaacagcaagaacaccctggacctgcagatgaacagcctgagagccgaggataccgccgtgtactactgcgtgaaggattggaacaccaccatgatcaccgagagaggccagggcacactggtcaccgtgtcctctacaacaacaccggcgcctcggcctccaacaccagctcctacaatcgcgagtcagcccctgtctctcagacccgaagcctgtagacctgctgctggcggagctgtgcataccagaggactggatttcgcctgcgacatctacatctgggctcctctggctggcacatgcggagttttgctgctgagcctggtcatcaccctgtactgtaagagaggcaggaagaagctgctgtatatcttcaagcagcccttcatgagacccgtgcagaccacacaggaggaggacggctgctcttgtaggttcccagaggaggaggagggaggatgcgagctgcgcgtgaagtttagccggtccgccgatgcacctgcatacaagcagggacagaaccagctgtataacgagctgaatctgggccggagagaggagtacgacgtgctggataagaggcggggccgggaccccgagatgggaggcaagcctcggagaaagaacccacaggagggcctgtacaatgagctgcaaaaggacaagatggccgaggcctattctgagatcggcatgaagggagagaggcgccggggcaagggacacgatggcctgtaccagggcctgagcaccgccacaaaggacacctatgatgccctgcacatgcaggccctgccccctagatga (VH-A; SEQ ID NO:18001).
[09] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению VHH включает или состоит из аминокислотной последовательности:
malpvtalllplalllhaarpevqllesggglvqpggsltlscaasgftfsnyamnwvrqapgkglewvsgiigsgattyyadsvkgrftisrdnskntlnlqmnslraedtaiyycvkdwnttmitergqgtlvtvsstttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (VH-B; SEQ ID NO:18002)
или VHH включает или состоит из последовательности нуклеиновой кислоты:
atggctctgcctgtgacagctctgctgctgcctctggctctgcttcttcatgcggcgcgccctgaagttcagctgcttgaatctggcggaggcctggttcaacctggcggatctctgacactgagctgtgccgccagcggcttcaccttcagcaactacgccatgaactgggtccgacaggcccctggcaaaggccttgaatgggtgtccggcatcattggctctggcgccaccacctactacgccgattctgtgaagggcagattcaccatcagccgggacaacagcaagaacaccctgaacctgcagatgaacagcctgagagccgaggacaccgccatctactactgcgtgaaggactggaacaccaccatgatcaccgagagaggccagggcacactggtcaccgtgtcctctacaacaacaccggcgcctcggcctccaacaccagctcctacaatcgcgagtcagcccctgtctctcagacccgaagcctgtagacctgctgctggcggagctgtgcataccagaggactggatttcgcctgcgacatctacatctgggctcctctggctggcacatgcggagttttgctgctgagcctggtcatcaccctgtactgtaagagaggcaggaagaagctgctgtatatcttcaagcagcccttcatgagacccgtgcagaccacacaggaggaggacggctgctcttgtaggttcccagaggaggaggagggaggatgcgagctgcgcgtgaagtttagccggtccgccgatgcacctgcatacaagcagggacagaaccagctgtataacgagctgaatctgggccggagagaggagtacgacgtgctggataagaggcggggccgggaccccgagatgggaggcaagcctcggagaaagaacccacaggagggcctgtacaatgagctgcaaaaggacaagatggccgaggcctattctgagatcggcatgaagggagagaggcgccggggcaagggacacgatggcctgtaccagggcctgagcaccgccacaaaggacacctatgatgccctgcacatgcaggccctgccccctagatga (VH-B; SEQ ID NO:18003).
[010] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению VHH включает или состоит из аминокислотной последовательности:
malpvtalllplalllhaarpevqllesggglvqpgeslrlscaasgftfsnyamnwvrqapgkglewvsgivggggtsyyadsvrgrftisrdnskntlylqmnslraedtavyycvkdwnttmitergqgtlvtvsstttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (VH-C; SEQ ID NO:18004)
или VHH включает или состоит из последовательности нуклеиновой кислоты:
atggctctgcctgtgacagctctgctgctgcctctggctctgcttcttcatgcggcgcgccctgaagttcagctgcttgaatctggcggaggcctggttcagcctggcgaatctctgagactgagctgtgccgccagcggcttcaccttcagcaactacgccatgaactgggtccgacaggcccctggcaaaggccttgaatgggtgtccggaatcgttggcggcggaggcacaagctactacgccgattctgtgcggggcagattcaccatcagccgggacaacagcaagaacaccctgtacctgcagatgaacagcctgagagccgaggacaccgccgtgtactactgcgtgaaggactggaacaccaccatgatcaccgagagaggccagggcacactggtcaccgtgtcctctacaacaacaccggcgcctcggcctccaacaccagctcctacaatcgcgagtcagcccctgtctctcagacccgaagcctgtagacctgctgctggcggagctgtgcataccagaggactggatttcgcctgcgacatctacatctgggctcctctggctggcacatgcggagttttgctgctgagcctggtcatcaccctgtactgtaagagaggcaggaagaagctgctgtatatcttcaagcagcccttcatgagacccgtgcagaccacacaggaggaggacggctgctcttgtaggttcccagaggaggaggagggaggatgcgagctgcgcgtgaagtttagccggtccgccgatgcacctgcatacaagcagggacagaaccagctgtataacgagctgaatctgggccggagagaggagtacgacgtgctggataagaggcggggccgggaccccgagatgggaggcaagcctcggagaaagaacccacaggagggcctgtacaatgagctgcaaaaggacaagatggccgaggcctattctgagatcggcatgaagggagagaggcgccggggcaagggacacgatggcctgtaccagggcctgagcaccgccacaaaggacacctatgatgccctgcacatgcaggccctgccccctagatga (VH-C; SEQ ID NO:18005).
[011] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению VHH включает или состоит из аминокислотной последовательности:
malpvtalllplalllhaarpevqllesggglvqpggslrlscaasgftfsnyamtwirqapgkglewvsgitgdggstfyadsvkgrftisrdnskntlylqmnslraedtavyycvkdwnttmitergqgtlvtvsstttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (VH-D; SEQ ID NO:18006)
или VHH включает или состоит из последовательности нуклеиновой кислоты:
atggctctgcctgtgacagctctgctgctgcctctggctctgcttcttcatgcggcgcgccctgaagttcagctgcttgaatctggcggaggcctggttcaacctggcggatctctgagactgagctgtgccgccagcggcttcaccttcagcaattacgccatgacctggatcagacaggcccctggcaaaggcctggaatgggtgtccggaattacaggcgacggcggcagcaccttttacgccgattctgtgaagggcagattcaccatcagccgggacaacagcaagaacaccctgtacctgcagatgaacagcctgagagccgaggacaccgccgtgtactactgcgtgaaggactggaacaccaccatgatcaccgagagaggccagggcacactggtcaccgtgtcctctacaacaacaccggcgcctcggcctccaacaccagctcctacaatcgcgagtcagcccctgtctctcagacccgaagcctgtagacctgctgctggcggagctgtgcataccagaggactggatttcgcctgcgacatctacatctgggctcctctggctggcacatgcggagttttgctgctgagcctggtcatcaccctgtactgtaagagaggcaggaagaagctgctgtatatcttcaagcagcccttcatgagacccgtgcagaccacacaggaggaggacggctgctcttgtaggttcccagaggaggaggagggaggatgcgagctgcgcgtgaagtttagccggtccgccgatgcacctgcatacaagcagggacagaaccagctgtataacgagctgaatctgggccggagagaggagtacgacgtgctggataagaggcggggccgggaccccgagatgggaggcaagcctcggagaaagaacccacaggagggcctgtacaatgagctgcaaaaggacaagatggccgaggcctattctgagatcggcatgaagggagagaggcgccggggcaagggacacgatggcctgtaccagggcctgagcaccgccacaaaggacacctatgatgccctgcacatgcaggccctgccccctagatga (VH-D; SEQ ID NO:18007).
[012] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению VHH включает или состоит из аминокислотной последовательности:
malpvtalllplalllhaarpevqllesggglaqpggslrlscaasgftfssyamnwirqapgkglewvsgisgsggstyyadsvkgrftisrdnskntvylqmnslraedtavyycvkdwnttmitergqgtlvtvsstttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (VH-E; SEQ ID NO:18008)
или VHH включает или состоит из последовательности нуклеиновой кислоты:
atggcactgcctgtgacagccctgctgctgcctctggccctgctgctgcacgcagcacggcccgaggtgcagctgctggagtccggaggaggcctggcccagcctggcggcagcctgaggctgtcctgcgccgcctctggcttcacctttagctcctacgccatgaactggatcagacaggcccctggcaagggcctggagtgggtgtccggcatctccggctctggaggctctacatactatgccgacagcgtgaagggccggttcaccatcagcagagataactccaagaataccgtgtacctccagatgaactctctgcgggccgaggacaccgccgtgtactattgcgtgaaggattggaataccacaatgatcacagagaggggccagggcaccctggtgacagtgtctagcaccacaacccctgcccccagacctcccacacccgcccctaccatcgcgagtcagccactgtccctgcggcctgaggcctgccggcccgccgccggcggagcagtgcacacacggggcctggactttgcctgtgacatctacatatgggcaccactggcaggaacctgcggcgtgctgctgctgagcctggtcatcaccctgtactgtaagagaggcaggaagaagctgctgtatatcttcaagcagcccttcatgagacccgtgcagaccacacaggaggaggacggctgctcttgtaggttcccagaggaggaggagggaggatgcgagctgcgcgtgaagtttagccggtccgccgatgcacctgcatacaagcagggacagaaccagctgtataacgagctgaatctgggccggagagaggagtacgacgtgctggataagaggcggggccgggaccccgagatgggaggcaagcctcggagaaagaacccacaggagggcctgtacaatgagctgcaaaaggacaagatggccgaggcctattctgagatcggcatgaagggagagaggcgccggggcaagggacacgatggcctgtaccagggcctgagcaccgccacaaaggacacctatgatgccctgcacatgcaggccctgccccctagatga (VH-E; SEQ ID NO:18009).
[013] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению VHH включает или состоит из аминокислотной последовательности:
malpvtalllplalllhaarpevqllesggglvqpgrslrlscaasgftftnyamnwvrqapgkglewvsgisggggstyyadsvkgrftisrdnskntlylqmnslraedtavyycvkdwnttmitergqgtlvtvsstttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (VH-F; SEQ ID NO:18010)
или VHH включает или состоит из последовательности нуклеиновой кислоты:
atggcactgcctgtgacagccctgctgctgcctctggccctgctgctgcacgcagcacggcccgaggtgcagctgctggagtctggaggaggcctggtgcagcccggccggtccctgagactgtcttgcgccgccagcggcttcacctttacaaactacgccatgaattgggtgcggcaggcccctggcaagggcctggagtgggtgtctggcatcagcggaggaggaggcagcacctactatgcagactccgtgaagggcaggttcaccatctcccgcgataactctaagaatacactgtacctccagatgaacagcctgagggcagaggacaccgccgtgtactattgcgtgaaggattggaataccacaatgatcacagagaggggacagggcaccctggtgaccgtgagcagcaccacaacccctgcccccagacctcccacacccgcccctaccatcgcgagtcagccactgtccctgcggcctgaggcctgccggcccgccgccggcggagcagtgcacacacggggcctggactttgcctgtgacatctacatatgggcaccactggcaggaacctgcggcgtgctgctgctgagcctggtcatcaccctgtactgtaagagaggcaggaagaagctgctgtatatcttcaagcagcccttcatgagacccgtgcagaccacacaggaggaggacggctgctcttgtaggttcccagaggaggaggagggaggatgcgagctgcgcgtgaagtttagccggtccgccgatgcacctgcatacaagcagggacagaaccagctgtataacgagctgaatctgggccggagagaggagtacgacgtgctggataagaggcggggccgggaccccgagatgggaggcaagcctcggagaaagaacccacaggagggcctgtacaatgagctgcaaaaggacaagatggccgaggcctattctgagatcggcatgaagggagagaggcgccggggcaagggacacgatggcctgtaccagggcctgagcaccgccacaaaggacacctatgatgccctgcacatgcaggccctgccccctagatga (VH-F; SEQ ID NO:18011).
[014] В изобретении предложен химерный антигенный рецептор (CAR), включающий: (a) эктодомен, включающий область распознавания антигена, где область распознавания антигена включает по меньшей мере один VH; (b) трансмембранный домен и (c) эндодомен, включающий по меньшей мере один костимулирующий домен. При использовании в тексте настоящего описания, CAR, включающий VH, именуется VCAR. В некоторых вариантах осуществления область распознавания антигена может включать две VH с получением биспецифичного или тандемного VCAR. В некоторых вариантах осуществления область распознавания антигена может включать три VH с получением триспецифичного VCAR. В некоторых вариантах осуществления эктодомен может дополнительно включать сигнальный пептид. В альтернативе или дополнительно, в некоторых вариантах осуществления, эктодомен может дополнительно включать шарнирную область между областью распознавания антигена и трансмембранным доменом. В некоторых вариантах осуществления эктодомен может дополнительно включать сигнальный пептид. В альтернативе или дополнительно, в некоторых вариантах осуществления, эктодомен может дополнительно включать шарнирную область между областью распознавания антигена и трансмембранным доменом.
[015] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, включая тех, которые включают эктодомен, включающий область распознавания антигена, где область распознавания антигена включает по меньшей мере один VH, VH включает человеческую или гуманизированную последовательность.
[016] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, включая тех, которые включают эктодомен, включающий область распознавания антигена, где, область распознавания антигена включает по меньшей мере один VH, VH включает не встречающуюся в природе последовательность.
[017] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, включая тех, которые включают эктодомен, включающий область распознавания антигена, где область распознавания антигена включает по меньшей мере один VH, VH не встречается в природе.
[018] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, включая тех, которые включают эктодомен, включающий область распознавания антигена, где область распознавания антигена включает по меньшей мере один VH, VH включает рекомбинантную или химерную последовательность.
[019] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, включая тех, которые включают эктодомен, включающий область распознавания антигена, где область распознавания антигена включает по меньшей мере один VH, VH получена с помощью in vitro процедуры отбора аффинности и рекомбинации.
[020] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, VH включает или состоит из аминокислотной последовательности:
malpvtalllplalllhaarpevqllesggglvqpggslrlscaasgftfssyamnwvrqapgkglewvagiigsggstyyadsvkgrfsisrdnskntldlqmnslraedtavyycvkdwnttmitergqgtlvtvsstttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (VH-A; SEQ ID NO:18000)
или VH включает или состоит из последовательности нуклеиновой кислоты:
atggctctgcctgtgacagctctgctgctgcctctggctctgcttcttcatgcggcgcgccctgaagttcagctgcttgaatctggcggaggcctggttcaacctggcggatctctgagactgagctgtgccgccagcggcttcacctttagcagctacgccatgaactgggtccgacaggcccctggcaaaggactggaatgggtggccggaatcatcggcagcggcggcagcacatattacgccgattctgtgaagggccgcttcagcatcagccgggacaacagcaagaacaccctggacctgcagatgaacagcctgagagccgaggataccgccgtgtactactgcgtgaaggattggaacaccaccatgatcaccgagagaggccagggcacactggtcaccgtgtcctctacaacaacaccggcgcctcggcctccaacaccagctcctacaatcgcgagtcagcccctgtctctcagacccgaagcctgtagacctgctgctggcggagctgtgcataccagaggactggatttcgcctgcgacatctacatctgggctcctctggctggcacatgcggagttttgctgctgagcctggtcatcaccctgtactgtaagagaggcaggaagaagctgctgtatatcttcaagcagcccttcatgagacccgtgcagaccacacaggaggaggacggctgctcttgtaggttcccagaggaggaggagggaggatgcgagctgcgcgtgaagtttagccggtccgccgatgcacctgcatacaagcagggacagaaccagctgtataacgagctgaatctgggccggagagaggagtacgacgtgctggataagaggcggggccgggaccccgagatgggaggcaagcctcggagaaagaacccacaggagggcctgtacaatgagctgcaaaaggacaagatggccgaggcctattctgagatcggcatgaagggagagaggcgccggggcaagggacacgatggcctgtaccagggcctgagcaccgccacaaaggacacctatgatgccctgcacatgcaggccctgccccctagatga (VH-A; SEQ ID NO:18001).
[021] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, VH включает или состоит из аминокислотной последовательности:
malpvtalllplalllhaarpevqllesggglvqpggsltlscaasgftfsnyamnwvrqapgkglewvsgiigsgattyyadsvkgrftisrdnskntlnlqmnslraedtaiyycvkdwnttmitergqgtlvtvsstttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (VH-B; SEQ ID NO:18002)
или VH включает или состоит из последовательности нуклеиновой кислоты:
atggctctgcctgtgacagctctgctgctgcctctggctctgcttcttcatgcggcgcgccctgaagttcagctgcttgaatctggcggaggcctggttcaacctggcggatctctgacactgagctgtgccgccagcggcttcaccttcagcaactacgccatgaactgggtccgacaggcccctggcaaaggccttgaatgggtgtccggcatcattggctctggcgccaccacctactacgccgattctgtgaagggcagattcaccatcagccgggacaacagcaagaacaccctgaacctgcagatgaacagcctgagagccgaggacaccgccatctactactgcgtgaaggactggaacaccaccatgatcaccgagagaggccagggcacactggtcaccgtgtcctctacaacaacaccggcgcctcggcctccaacaccagctcctacaatcgcgagtcagcccctgtctctcagacccgaagcctgtagacctgctgctggcggagctgtgcataccagaggactggatttcgcctgcgacatctacatctgggctcctctggctggcacatgcggagttttgctgctgagcctggtcatcaccctgtactgtaagagaggcaggaagaagctgctgtatatcttcaagcagcccttcatgagacccgtgcagaccacacaggaggaggacggctgctcttgtaggttcccagaggaggaggagggaggatgcgagctgcgcgtgaagtttagccggtccgccgatgcacctgcatacaagcagggacagaaccagctgtataacgagctgaatctgggccggagagaggagtacgacgtgctggataagaggcggggccgggaccccgagatgggaggcaagcctcggagaaagaacccacaggagggcctgtacaatgagctgcaaaaggacaagatggccgaggcctattctgagatcggcatgaagggagagaggcgccggggcaagggacacgatggcctgtaccagggcctgagcaccgccacaaaggacacctatgatgccctgcacatgcaggccctgccccctagatga (VH-B; SEQ ID NO:18003).
[022] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, VH включает или состоит из аминокислотной последовательности:
malpvtalllplalllhaarpevqllesggglvqpgeslrlscaasgftfsnyamnwvrqapgkglewvsgivggggtsyyadsvrgrftisrdnskntlylqmnslraedtavyycvkdwnttmitergqgtlvtvsstttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (VH-C; SEQ ID NO:18004)
или VH включает или состоит из последовательности нуклеиновой кислоты:
atggctctgcctgtgacagctctgctgctgcctctggctctgcttcttcatgcggcgcgccctgaagttcagctgcttgaatctggcggaggcctggttcagcctggcgaatctctgagactgagctgtgccgccagcggcttcaccttcagcaactacgccatgaactgggtccgacaggcccctggcaaaggccttgaatgggtgtccggaatcgttggcggcggaggcacaagctactacgccgattctgtgcggggcagattcaccatcagccgggacaacagcaagaacaccctgtacctgcagatgaacagcctgagagccgaggacaccgccgtgtactactgcgtgaaggactggaacaccaccatgatcaccgagagaggccagggcacactggtcaccgtgtcctctacaacaacaccggcgcctcggcctccaacaccagctcctacaatcgcgagtcagcccctgtctctcagacccgaagcctgtagacctgctgctggcggagctgtgcataccagaggactggatttcgcctgcgacatctacatctgggctcctctggctggcacatgcggagttttgctgctgagcctggtcatcaccctgtactgtaagagaggcaggaagaagctgctgtatatcttcaagcagcccttcatgagacccgtgcagaccacacaggaggaggacggctgctcttgtaggttcccagaggaggaggagggaggatgcgagctgcgcgtgaagtttagccggtccgccgatgcacctgcatacaagcagggacagaaccagctgtataacgagctgaatctgggccggagagaggagtacgacgtgctggataagaggcggggccgggaccccgagatgggaggcaagcctcggagaaagaacccacaggagggcctgtacaatgagctgcaaaaggacaagatggccgaggcctattctgagatcggcatgaagggagagaggcgccggggcaagggacacgatggcctgtaccagggcctgagcaccgccacaaaggacacctatgatgccctgcacatgcaggccctgccccctagatga (VH-C; SEQ ID NO:18005).
[023] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, VH включает или состоит из аминокислотной последовательности:
malpvtalllplalllhaarpevqllesggglvqpggslrlscaasgftfsnyamtwirqapgkglewvsgitgdggstfyadsvkgrftisrdnskntlylqmnslraedtavyycvkdwnttmitergqgtlvtvsstttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (VH-D; SEQ ID NO:18006)
или VH включает или состоит из последовательности нуклеиновой кислоты:
atggctctgcctgtgacagctctgctgctgcctctggctctgcttcttcatgcggcgcgccctgaagttcagctgcttgaatctggcggaggcctggttcaacctggcggatctctgagactgagctgtgccgccagcggcttcaccttcagcaattacgccatgacctggatcagacaggcccctggcaaaggcctggaatgggtgtccggaattacaggcgacggcggcagcaccttttacgccgattctgtgaagggcagattcaccatcagccgggacaacagcaagaacaccctgtacctgcagatgaacagcctgagagccgaggacaccgccgtgtactactgcgtgaaggactggaacaccaccatgatcaccgagagaggccagggcacactggtcaccgtgtcctctacaacaacaccggcgcctcggcctccaacaccagctcctacaatcgcgagtcagcccctgtctctcagacccgaagcctgtagacctgctgctggcggagctgtgcataccagaggactggatttcgcctgcgacatctacatctgggctcctctggctggcacatgcggagttttgctgctgagcctggtcatcaccctgtactgtaagagaggcaggaagaagctgctgtatatcttcaagcagcccttcatgagacccgtgcagaccacacaggaggaggacggctgctcttgtaggttcccagaggaggaggagggaggatgcgagctgcgcgtgaagtttagccggtccgccgatgcacctgcatacaagcagggacagaaccagctgtataacgagctgaatctgggccggagagaggagtacgacgtgctggataagaggcggggccgggaccccgagatgggaggcaagcctcggagaaagaacccacaggagggcctgtacaatgagctgcaaaaggacaagatggccgaggcctattctgagatcggcatgaagggagagaggcgccggggcaagggacacgatggcctgtaccagggcctgagcaccgccacaaaggacacctatgatgccctgcacatgcaggccctgccccctagatga (VH-D; SEQ ID NO:18007).
[024] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, VH включает или состоит из аминокислотной последовательности:
malpvtalllplalllhaarpevqllesggglaqpggslrlscaasgftfssyamnwirqapgkglewvsgisgsggstyyadsvkgrftisrdnskntvylqmnslraedtavyycvkdwnttmitergqgtlvtvsstttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (VH-E; SEQ ID NO:18008)
или VH включает или состоит из последовательности нуклеиновой кислоты:
atggcactgcctgtgacagccctgctgctgcctctggccctgctgctgcacgcagcacggcccgaggtgcagctgctggagtccggaggaggcctggcccagcctggcggcagcctgaggctgtcctgcgccgcctctggcttcacctttagctcctacgccatgaactggatcagacaggcccctggcaagggcctggagtgggtgtccggcatctccggctctggaggctctacatactatgccgacagcgtgaagggccggttcaccatcagcagagataactccaagaataccgtgtacctccagatgaactctctgcgggccgaggacaccgccgtgtactattgcgtgaaggattggaataccacaatgatcacagagaggggccagggcaccctggtgacagtgtctagcaccacaacccctgcccccagacctcccacacccgcccctaccatcgcgagtcagccactgtccctgcggcctgaggcctgccggcccgccgccggcggagcagtgcacacacggggcctggactttgcctgtgacatctacatatgggcaccactggcaggaacctgcggcgtgctgctgctgagcctggtcatcaccctgtactgtaagagaggcaggaagaagctgctgtatatcttcaagcagcccttcatgagacccgtgcagaccacacaggaggaggacggctgctcttgtaggttcccagaggaggaggagggaggatgcgagctgcgcgtgaagtttagccggtccgccgatgcacctgcatacaagcagggacagaaccagctgtataacgagctgaatctgggccggagagaggagtacgacgtgctggataagaggcggggccgggaccccgagatgggaggcaagcctcggagaaagaacccacaggagggcctgtacaatgagctgcaaaaggacaagatggccgaggcctattctgagatcggcatgaagggagagaggcgccggggcaagggacacgatggcctgtaccagggcctgagcaccgccacaaaggacacctatgatgccctgcacatgcaggccctgccccctagatga (VH-E; SEQ ID NO:18009).
[025] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, VH включает или состоит из аминокислотной последовательности:
malpvtalllplalllhaarpevqllesggglvqpgrslrlscaasgftftnyamnwvrqapgkglewvsgisggggstyyadsvkgrftisrdnskntlylqmnslraedtavyycvkdwnttmitergqgtlvtvsstttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (VH-F; SEQ ID NO:18010)
или VH включает или состоит из последовательности нуклеиновой кислоты:
atggcactgcctgtgacagccctgctgctgcctctggccctgctgctgcacgcagcacggcccgaggtgcagctgctggagtctggaggaggcctggtgcagcccggccggtccctgagactgtcttgcgccgccagcggcttcacctttacaaactacgccatgaattgggtgcggcaggcccctggcaagggcctggagtgggtgtctggcatcagcggaggaggaggcagcacctactatgcagactccgtgaagggcaggttcaccatctcccgcgataactctaagaatacactgtacctccagatgaacagcctgagggcagaggacaccgccgtgtactattgcgtgaaggattggaataccacaatgatcacagagaggggacagggcaccctggtgaccgtgagcagcaccacaacccctgcccccagacctcccacacccgcccctaccatcgcgagtcagccactgtccctgcggcctgaggcctgccggcccgccgccggcggagcagtgcacacacggggcctggactttgcctgtgacatctacatatgggcaccactggcaggaacctgcggcgtgctgctgctgagcctggtcatcaccctgtactgtaagagaggcaggaagaagctgctgtatatcttcaagcagcccttcatgagacccgtgcagaccacacaggaggaggacggctgctcttgtaggttcccagaggaggaggagggaggatgcgagctgcgcgtgaagtttagccggtccgccgatgcacctgcatacaagcagggacagaaccagctgtataacgagctgaatctgggccggagagaggagtacgacgtgctggataagaggcggggccgggaccccgagatgggaggcaagcctcggagaaagaacccacaggagggcctgtacaatgagctgcaaaaggacaagatggccgaggcctattctgagatcggcatgaagggagagaggcgccggggcaagggacacgatggcctgtaccagggcctgagcaccgccacaaaggacacctatgatgccctgcacatgcaggccctgccccctagatga (VH-F; SEQ ID NO:18011).
[026] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, VCAR включает однодоменное антитело, VHH, VH или их комбинацию. В некоторых вариантах осуществления однодоменное антитело, VHH или VH включает или состоит из рекомбинантной последовательности и/или химерной последовательности. В некоторых вариантах осуществления однодоменное антитело, VHH или VH включает или состоит из человеческой последовательности и/или гуманизированной последовательности.
[027] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, VCAR включает однодоменное антитело. В некоторых вариантах осуществления однодоменное антитело является VHH или VH антителом. В некоторых вариантах осуществления VH антитело является антителом UniDab. В некоторых вариантах осуществления VH антитело не является фрагментом природного моноклонального антитела.
[028] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению сигнальный пептид может включать последовательность, кодирующую сигнальный пептид CD2, CD3δ, CD3ε, CD3γ, CD3ζ, CD4, CD8α, CD19, CD28, 4-1BB или GM-CSFR человека. В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению сигнальный пептид может включать последовательность, кодирующую сигнальный пептид CD8α человека. Сигнальный пептид CD8α человека может включать аминокислотную последовательность, включающую MALPVTALLLPLALLLHAARP (SEQ ID NO:18012). Сигнальный пептид CD8α человека может включать аминокислотную последовательность, включающую MALPVTALLLPLALLLHAARP (SEQ ID NO:18012), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей MALPVTALLLPLALLLHAARP (SEQ ID NO:18012). Сигнальный пептид CD8α человека может кодироваться последовательностью нуклеиновой кислоты, включающей gatggcactgccagtcaccgccctgctgctgcctctggctctgctgctgcacgcagctagacca (SEQ ID NO:18013).
[029] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению трансмембранный домен может включать последовательность, кодирующую трансмембранный домен CD2, CD3δ, CD3ε, CD3γ, CD3ζ, CD4, CD8α, CD19, CD28, 4-1BB или GM-CSFR человека. В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению трансмембранный домен может включать последовательность, кодирующую трансмембранный домен CD8α человека. Трансмембранный домен CD8α может включать аминокислотную последовательность, включающую IYIWAPLAGTCGVLLLSLVITLYC (SEQ ID NO:18014), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей IYIWAPLAGTCGVLLLSLVITLYC (SEQ ID NO:18014). Трансмембранный домен CD8α может кодироваться последовательностью нуклеиновой кислоты, включающей atctacatttgggcaccactggccgggacctgtggagtgctgctgctgagcctggtcatcacactgtactgc (SEQ ID NO:18015).
[030] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению эндодомен может включать эндодомен CD3ζ человека.
[031] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению по меньшей мере один костимулирующий домен может включать внутриклеточный сегмент 4-1BB, CD28, CD40, ICOS, MyD88, OX-40 человека или их любую комбинацию. В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению по меньшей мере один костимулирующий домен может включать костимулирующий домен CD28 и/или 4-1BB. Костимулирующий домен CD3-дзета может включать аминокислотную последовательность, включающую RVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR (SEQ ID NO:18016), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей RVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR (SEQ ID NO:18016). Костимулирующий домен CD3-дзета может кодироваться последовательностью нуклеиновой кислоты, включающей cgcgtgaagtttagtcgatcagcagatgccccagcttacaaacagggacagaaccagctgtataacgagctgaatctgggccgccgagaggaatatgacgtgctggataagcggagaggacgcgaccccgaaatgggaggcaagcccaggcgcaaaaaccctcaggaaggcctgtataacgagctgcagaaggacaaaatggcagaagcctattctgagatcggcatgaagggggagcgacggagaggcaaagggcacgatgggctgtaccagggactgagcaccgccacaaaggacacctatgatgctctgcatatgcaggcactgcctccaagg (SEQ ID NO:18017). Костимулирующий домен 4-1BB может включать аминокислотную последовательность, включающую KRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCEL (SEQ ID NO:18018), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей KRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCEL (SEQ ID NO:18018). Костимулирующий домен 4-1BB может кодироваться последовательностью нуклеиновой кислоты, включающей aagagaggcaggaagaaactgctgtatattttcaaacagcccttcatgcgccccgtgcagactacccaggaggaagacgggtgctcctgtcgattccctgaggaagaggaaggcgggtgtgagctg (SEQ ID NO:18019). Костимулирующий домен 4-1BB может быть расположен между трансмембранным доменом и костимулирующим доменом CD28.
[032] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению шарнирная область может включать последовательность, полученную из последовательности CD8α, IgG4 и/или CD4 человека. В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению шарнирная область может включать последовательность, полученную из последовательности CD8α человека. Шарнирная область может включать аминокислотную последовательность CD8α человека, включающую TTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACD (SEQ ID NO:18020), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей TTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACD (SEQ ID NO:18020). Аминокислотная последовательность шарнирной области CD8α человека может кодироваться последовательностью нуклеиновой кислоты, включающей actaccacaccagcacctagaccaccaactccagctccaaccatcgcgagtcagcccctgagtctgagacctgaggcctgcaggccagctgcaggaggagctgtgcacaccaggggcctggacttcgcctgcgac (SEQ ID NO:18021).
[033] VHH и/или VCAR-рецепторы согласно изобретению могут связывать антиген по меньшей мере с одной аффинностью, выбранной из KD меньше или равной 10-9 M, меньше чем или равной 10-10 M, меньше или равной 10-11 M, меньше или равной 10-12 M, меньше или равной 10-13 M, меньше или равной 10-14 M и меньше или равной 10-15 M. KD может быть определена с помощью поверхностного плазмонного резонанса.
[034] В изобретении предложен VCAR против BCMA. В изобретении предложена композиция, включающая VCAR согласно изобретению и по меньшей мере один фармацевтически приемлемый носитель.
[035] В изобретении предложен транспозон, включающий VCAR согласно изобретению.
[036] Транспозоны согласно изобретению могут включать селективный ген для идентификации, обогащения и/или выделения клеток, экспрессирующих транспозон. Примерные селективные гены кодируют любой продукт гена (например, транскрипт, белок, фермент), важный для жизнеспособности и выживания клетки. Примерные селективные гены кодируют любой продукт гена (например, транскрипт, белок, фермент), важный для придания устойчивости к лекарственному средству, к которому клетка чувствительна (или которое может быть летальным для клетки) в отсутствие продукта гена, кодируемого селективным геном. Примерные селективные гены кодируют любой продукт гена (например, транскрипт, белок, фермент), важный для жизнеспособности и/или выживания в клеточной среде, не содержащей одно или более питательных веществах, важных для жизнеспособности и/или выживания клетки в отсутствие селективного гена. Примерные селективные гены включают, без ограничения перечисленным, neo (придающий устойчивость к неомицину), DHFR (кодирующий дигидрофолатредуктазу и придающий устойчивость к метотрексату), TYMS (кодирующий тимидилатсинтетазу), MGMT (кодирующий O(6)-метилгуанин-ДНК-метилтрансферазу), ген множественной лекарственной устойчивости (MDR1), ALDH1 (кодирующий член A1 семейства альдегиддегидрогеназы 1), FRANCF, RAD51C (кодирующий паралог C RAD51), GCS (кодирующий глюкозилцерамидсинтазу) и NKX2.2 (кодирующий NK2 гомеобокс 2).
[037] Транспозоны согласно изобретению могут включать индуцируемый проапоптотический полипептид, включающий: (a) лигандсвязывающую область, (b) линкер и (c) проапоптотический полипептид, где индуцируемый проапоптотический полипептид не включает нечеловеческую последовательность. В некоторых вариантах осуществления нечеловеческая последовательность включает сайт рестрикции. В некоторых вариантах осуществления лигандсвязывающая область может быть мультимерной лигандсвязывающей областью. Индуцируемые проапоптотические полипептиды согласно изобретению также могут именоваться "iC9 выключателем безопасности". В некоторых вариантах осуществления транспозоны согласно изобретению могут включать индуцируемый полипептид каспазы, включающий: (a) лигандсвязывающую область, (b) линкер и (c) полипептид каспазы, где индуцируемый проапоптотический полипептид не включает нечеловеческую последовательность. В некоторых вариантах осуществления транспозоны согласно изобретению могут включать индуцируемый полипептид каспазы, включающий: (a) лигандсвязывающую область, (b) линкер и (c) полипептид каспазы, где индуцируемый проапоптотический полипептид не включает нечеловеческую последовательность. В некоторых вариантах осуществления транспозоны согласно изобретению могут включать индуцируемый полипептид каспазы, включающий: (a) лигандсвязывающую область, (b) линкер и (c) усеченный полипептид каспазы 9, где индуцируемый проапоптотический полипептид не включает нечеловеческую последовательность. В некоторых вариантах осуществления индуцируемых проапоптотических полипептидов, индуцируемых полипептидов каспазы или усеченных полипептидов каспазы 9 согласно изобретению, лигандсвязывающая область может включать полипептид FK506 связывающего белка 12 (FKBP12). В некоторых вариантах осуществления аминокислотная последовательность лигандсвязывающей области, которая включает полипептид FK506 связывающего белка 12 (FKBP12), может включать модификацию в положении 36 последовательности. Модификация может быть заменой валина (V) на фенилаланин (F) в положении 36 (F36V). В некоторых вариантах осуществления полипептид FKBP12 кодируется аминокислотной последовательностью, включающей GVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKVDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLE (SEQ ID NO:18022). В некоторых вариантах осуществления полипептид FKBP12 кодируется последовательностью нуклеиновой кислоты, включающей GGGGTCCAGGTCGAGACTATTTCACCAGGGGATGGGCGAACATTTCCAAAAAGGGGCCAGACTTGCGTCGTGCATTACACCGGGATGCTGGAGGACGGGAAGAAAGTGGACAGCTCCAGGGATCGCAACAAGCCCTTCAAGTTCATGCTGGGAAAGCAGGAAGTGATCCGAGGATGGGAGGAAGGCGTGGCACAGATGTCAGTCGGCCAGCGGGCCAAACTGACCATTAGCCCTGACTACGCTTATGGAGCAACAGGCCACCCAGGGATCATTCCCCCTCATGCCACCCTGGTCTTCGATGTGGAACTGCTGAAGCTGGAG (SEQ ID NO:18023). В некоторых вариантах осуществления индуцирующее средство, специфичное к лигандсвязывающей области, может включать полипептид FK506 связывающего белка 12 (FKBP12), содержащий замену валина (V) на фенилаланин (F) в положении 36 (F36V), который включает AP20187 и/или AP1903, которые являются синтетическими лекарственными средствами.
[038] В некоторых вариантах осуществления индуцируемых проапоптотических полипептидов, индуцируемых полипептидов каспазы или усеченных полипептидов каспазы 9 согласно изобретению, линкерная область кодируется аминокислотной последовательностью, включающей GGGGS (SEQ ID NO:18024), или последовательностью нуклеиновой кислоты, включающей GGAGGAGGAGGATCC (SEQ ID NO:18025). В некоторых вариантах осуществления последовательность нуклеиновой кислоты, кодирующая линкер, не включает сайт рестрикции.
[039] В некоторых вариантах осуществления усеченных полипептидов каспазы 9 согласно изобретению, усеченные полипептиды каспазы 9 кодируются аминокислотной последовательностью, не включающей аргинин (R) в положении 87 последовательности. В альтернативе или дополнительно, в некоторых вариантах осуществления индуцируемых проапоптотических полипептидов, индуцируемых полипептидов каспазы или усеченных полипептидов каспазы 9 согласно изобретению, усеченные полипептиды каспазы 9 кодируются аминокислотной последовательностью, не включающей аланин (A) в положении 282 последовательности. В некоторых вариантах осуществления индуцируемых проапоптотических полипептидов, индуцируемых полипептидов каспазы или усеченных полипептидов каспазы 9 согласно изобретению, усеченные полипептиды каспазы 9 кодируются аминокислотной последовательностью, включающей GFGDVGALESLRGNADLAYILSMEPCGHCLIINNVNFCRESGLRTRTGSNIDCEKLRRRFSSLHFMVEVKGDLTAKKMVLALLELAQQDHGALDCCVVVILSHGCQASHLQFPGAVYGTDGCPVSVEKIVNIFNGTSCPSLGGKPKLFFIQACGGEQKDHGFEVASTSPEDESPGSNPEPDATPFQEGLRTFDQLDAISSLPTPSDIFVSYSTFPGFVSWRDPKSGSWYVETLDDIFEQWAHSEDLQSLLLRVANAVSVKGIYKQMPGCFNFLRKKLFFKTS (SEQ ID NO:18026), или последовательностью нуклеиновой кислоты, включающей TTTGGGGACGTGGGGGCCCTGGAGTCTCTGCGAGGAAATGCCGATCTGGCTTACATCCTGAGCATGGAACCCTGCGGCCACTGTCTGATCATTAACAATGTGAACTTCTGCAGAGAAAGCGGACTGCGAACACGGACTGGCTCCAATATTGACTGTGAGAAGCTGCGGAGAAGGTTCTCTAGTCTGCACTTTATGGTCGAAGTGAAAGGGGATCTGACCGCCAAGAAAATGGTGCTGGCCCTGCTGGAGCTGGCTCAGCAGGACCATGGAGCTCTGGATTGCTGCGTGGTCGTGATCCTGTCCCACGGGTGCCAGGCTTCTCATCTGCAGTTCCCCGGAGCAGTGTACGGAACAGACGGCTGTCCTGTCAGCGTGGAGAAGATCGTCAACATCTTCAACGGCACTTCTTGCCCTAGTCTGGGGGGAAAGCCAAAACTGTTCTTTATCCAGGCCTGTGGCGGGGAACAGAAAGATCACGGCTTCGAGGTGGCCAGCACCAGCCCTGAGGACGAATCACCAGGGAGCAACCCTGAACCAGATGCAACTCCATTCCAGGAGGGACTGAGGACCTTTGACCAGCTGGATGCTATCTCAAGCCTGCCCACTCCTAGTGACATTTTCGTGTCTTACAGTACCTTCCCAGGCTTTGTCTCATGGCGCGATCCCAAGTCAGGGAGCTGGTACGTGGAGACACTGGACGACATCTTTGAACAGTGGGCCCATTCAGAGGACCTGCAGAGCCTGCTGCTGCGAGTGGCAAACGCTGTCTCTGTGAAGGGCATCTACAAACAGATGCCCGGGTGCTTCAATTTTCTGAGAAAGAAACTGTTCTTTAAGACTTCC (SEQ ID NO:18027).
[040] В некоторых вариантах осуществления индуцируемых проапоптотических полипептидов, где полипептид включает усеченные полипептиды каспазы 9, индуцируемый проапоптотический полипептид кодируется аминокислотной последовательностью, включающей GVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKVDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLEGGGGSGFGDVGALESLRGNADLAYILSMEPCGHCLIINNVNFCRESGLRTRTGSNIDCEKLRRRFSSLHFMVEVKGDLTAKKMVLALLELAQQDHGALDCCVVVILSHGCQASHLQFPGAVYGTDGCPVSVEKIVNIFNGTSCPSLGGKPKLFFIQACGGEQKDHGFEVASTSPEDESPGSNPEPDATPFQEGLRTFDQLDAISSLPTPSDIFVSYSTFPGFVSWRDPKSGSWYVETLDDIFEQWAHSEDLQSLLLRVANAVSVKGIYKQMPGCFNFLRKKLFFKTS (SEQ ID NO:18028), или последовательностью нуклеиновой кислоты, включающей ggggtccaggtcgagactatttcaccaggggatgggcgaacatttccaaaaaggggccagacttgcgtcgtgcattacaccgggatgctggaggacgggaagaaagtggacagctccagggatcgcaacaagcccttcaagttcatgctgggaaagcaggaagtgatccgaggatgggaggaaggcgtggcacagatgtcagtcggccagcgggccaaactgaccattagccctgactacgcttatggagcaacaggccacccagggatcattccccctcatgccaccctggtcttcgatgtggaactgctgaagctggagggaggaggaggatccggatttggggacgtgggggccctggagtctctgcgaggaaatgccgatctggcttacatcctgagcatggaaccctgcggccactgtctgatcattaacaatgtgaacttctgcagagaaagcggactgcgaacacggactggctccaatattgactgtgagaagctgcggagaaggttctctagtctgcactttatggtcgaagtgaaaggggatctgaccgccaagaaaatggtgctggccctgctggagctggctcagcaggaccatggagctctggattgctgcgtggtcgtgatcctgtcccacgggtgccaggcttctcatctgcagttccccggagcagtgtacggaacagacggctgtcctgtcagcgtggagaagatcgtcaacatcttcaacggcacttcttgccctagtctggggggaaagccaaaactgttctttatccaggcctgtggcggggaacagaaagatcacggcttcgaggtggccagcaccagccctgaggacgaatcaccagggagcaaccctgaaccagatgcaactccattccaggagggactgaggacctttgaccagctggatgctatctcaagcctgcccactcctagtgacattttcgtgtcttacagtaccttcccaggctttgtctcatggcgcgatcccaagtcagggagctggtacgtggagacactggacgacatctttgaacagtgggcccattcagaggacctgcagagcctgctgctgcgagtggcaaacgctgtctctgtgaagggcatctacaaacagatgcccgggtgcttcaattttctgagaaagaaactgttctttaagacttcc (SEQ ID NO:18029).
[041] Транспозоны согласно изобретению могут включать по меньшей мере один саморасщепляющийся пептид(ы), расположенный, например, между одним или более VHH или VCAR согласно изобретению и селективным геном согласно изобретению. Транспозоны согласно изобретению могут включать по меньшей мере один саморасщепляющийся пептид(ы), расположенный, например, между одним или более VHH или VCAR согласно изобретению и индуцируемым проапоптотическим полипептидом согласно изобретению. Транспозоны согласно изобретению могут включать по меньшей мере два саморасщепляющихся пептида, причем первый саморасщепляющийся пептид расположен, например, перед или непосредственно перед индуцируемым проапоптотическим полипептидом согласно изобретению, а второй первый саморасщепляющийся пептид расположен, например, после или непосредственно перед индуцируемым проапоптотическим полипептидом согласно изобретению.
[042] По меньшей мере один саморасщепляющийся пептид может включать, например, пептид T2A, пептид GSG-T2A, пептид E2A, пептид GSG-E2A, пептид F2A, пептид GSG-F2A, пептид P2A или пептид GSG-P2A. Пептид T2A может включать аминокислотную последовательность, включающую EGRGSLLTCGDVEENPGP (SEQ ID NO:18030), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей EGRGSLLTCGDVEENPGP (SEQ ID NO:18030). Пептид GSG-T2A может включать аминокислотную последовательность, включающую GSGEGRGSLLTCGDVEENPGP (SEQ ID NO:18031), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей GSGEGRGSLLTCGDVEENPGP (SEQ ID NO:18031). Пептид AGSG-T2A может включать последовательность нуклеиновой кислоты, включающую ggatctggagagggaaggggaagcctgctgacctgtggagacgtggaggaaaacccaggacca (SEQ ID NO:18032). Пептид E2A может включать аминокислотную последовательность, включающую QCTNYALLKLAGDVESNPGP (SEQ ID NO:18033), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей QCTNYALLKLAGDVESNPGP (SEQ ID NO:18033). Пептид GSG-E2A может включать аминокислотную последовательность, включающую GSGQCTNYALLKLAGDVESNPGP (SEQ ID NO:18034), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей GSGQCTNYALLKLAGDVESNPGP (SEQ ID NO:18034). Пептид F2A может включать аминокислотную последовательность, включающую VKQTLNFDLLKLAGDVESNPGP (SEQ ID NO:18035), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей VKQTLNFDLLKLAGDVESNPGP (SEQ ID NO:18035). Пептид GSG-F2A может включать аминокислотную последовательность, включающую GSGVKQTLNFDLLKLAGDVESNPGP (SEQ ID NO:18036), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей GSGVKQTLNFDLLKLAGDVESNPGP (SEQ ID NO:18036). Пептид P2A может включать аминокислотную последовательность, включающую ATNFSLLKQAGDVEENPGP (SEQ ID NO:18037), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей ATNFSLLKQAGDVEENPGP (SEQ ID NO:18037). Пептид GSG-P2A может включать аминокислотную последовательность, включающую GSGATNFSLLKQAGDVEENPGP (SEQ ID NO:18038), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей GSGATNFSLLKQAGDVEENPGP (SEQ ID NO:18038).
[043] Транспозоны согласно изобретению могут включать первый и второй саморасщепляющийся пептид, причем первый саморасщепляющийся пептид расположен, например, перед одим или более VHH или VCAR согласно изобретению, а второй саморасщепляющийся пептид расположен, например, после одного или более VHH или VCAR согласно изобретению. Первый и/или второй саморасщепляющийся пептид могут включать, например, пептид T2A, пептид GSG-T2A, пептид E2A, пептид GSG-E2A, пептид F2A, пептид GSG-F2A, пептид P2A или пептид GSG-P2A. Пептид T2A может включать аминокислотную последовательность, включающую EGRGSLLTCGDVEENPGP (SEQ ID NO:18030), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей EGRGSLLTCGDVEENPGP (SEQ ID NO:18030). Пептид GSG-T2A может включать аминокислотную последовательность, включающую GSGEGRGSLLTCGDVEENPGP (SEQ ID NO:18031), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей GSGEGRGSLLTCGDVEENPGP (SEQ ID NO:18031). Пептид GSG-T2A может включать последовательность нуклеиновой кислоты, включающую ggatctggagagggaaggggaagcctgctgacctgtggagacgtggaggaaaacccaggacca (SEQ ID NO:18032). Пептид E2A может включать аминокислотную последовательность, включающую QCTNYALLKLAGDVESNPGP (SEQ ID NO:18033), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей QCTNYALLKLAGDVESNPGP (SEQ ID NO:18033). Пептид GSG-E2A может включать аминокислотную последовательность, включающую GSGQCTNYALLKLAGDVESNPGP (SEQ ID NO:18034), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей GSGQCTNYALLKLAGDVESNPGP (SEQ ID NO:18034). Пептид F2A может включать аминокислотную последовательность, включающую VKQTLNFDLLKLAGDVESNPGP (SEQ ID NO:18035), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей VKQTLNFDLLKLAGDVESNPGP (SEQ ID NO:18035). Пептид GSG-F2A может включать аминокислотную последовательность, включающую GSGVKQTLNFDLLKLAGDVESNPGP (SEQ ID NO:18036), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей GSGVKQTLNFDLLKLAGDVESNPGP (SEQ ID NO:18036). Пептид P2A может включать аминокислотную последовательность, включающую ATNFSLLKQAGDVEENPGP (SEQ ID NO:18037), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей ATNFSLLKQAGDVEENPGP (SEQ ID NO:18037). Пептид GSG-P2A может включать аминокислотную последовательность, включающую GSGATNFSLLKQAGDVEENPGP (SEQ ID NO:18038), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей GSGATNFSLLKQAGDVEENPGP (SEQ ID NO:18038).
[044] В изобретении предложена композиция, включающая транспозон согласно изобретению. В некоторых вариантах осуществления композиция может дополнительно включать плазмиду, включающую последовательность, кодирующую фермент транспозазу. Последовательность, кодирующая фермент транспозазу, может быть последовательностью мРНК.
[045] Транспозоны согласно изобретению могут включать транспозоны piggyBac. В некоторых вариантах осуществления данного способа транспозон является транспозоном ДНК плазмиды с последовательностью, кодирующей химерный антигенный рецептор, между двумя цис-регуляторными инсуляторными элементами. В некоторых вариантах осуществления транспозон является транспозоном piggyBac. Ферменты транспозазы согласно изобретению могут включать транспозазы piggyBac или совместимые ферменты. В некоторых вариантах осуществления и, в частности, таких вариантах осуществления, в которых транспозон является транспозоном piggyBac, транспозаза является транспозазой piggyBac или Super piggyBac (SPB). В некоторых вариантах осуществления и, в частности, таких вариантах осуществления, в которых транспозаза является транспозазой Super piggyBac (SPB), последовательность, кодирующая транспозазу, является последовательностью мРНК.
[046] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза является ферментом транспозазой piggyBac (PB). Фермент транспозаза piggyBac (PB) может включать или состоять из аминокислотной последовательности, которая по меньшей мере на 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент идентична:
1 MGSSLDDEHI LSALLQSDDE LVGEDSDSEI SDHVSEDDVQ SDTEEAFIDE VHEVQPTSSG
61 SEILDEQNVI EQPGSSLASN RILTLPQRTI RGKNKHCWST SKSTRRSRVS ALNIVRSQRG
121 PTRMCRNIYD PLLCFKLFFT DEIISEIVKW TNAEISLKRR ESMTGATFRD TNEDEIYAFF
181 GILVMTAVRK DNHMSTDDLF DRSLSMVYVS VMSRDRFDFL IRCLRMDDKS IRPTLRENDV
241 FTPVRKIWDL FIHQCIQNYT PGAHLTIDEQ LLGFRGRCPF RMYIPNKPSK YGIKILMMCD
301 SGTKYMINGM PYLGRGTQTN GVPLGEYYVK ELSKPVHGSC RNITCDNWFT SIPLAKNLLQ
361 EPYKLTIVGT VRSNKREIPE VLKNSRSRPV GTSMFCFDGP LTLVSYKPKP AKMVYLLSSC
421 DEDASINEST GKPQMVMYYN QTKGGVDTLD QMCSVMTCSR KTNRWPMALL YGMINIACIN
481 SFIIYSHNVS SKGEKVQSRK KFMRNLYMSL TSSFMRKRLE APTLKRYLRD NISNILPNEV
541 PGTSDDSTEE PVMKKRTYCT YCPSKIRRKA NASCKKCKKV ICREHNIDMC QSCF
(SEQ ID NO:14487).
[047] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза является ферментом транспозазой piggyBac (PB), включающим или состоящим из аминокислотной последовательности, содержащей аминокислотную замену в одном или более из положений 30, 165, 282 или 538 последовательности:
61 SEILDEQNVI EQPGSSLASN RILTLPQRTI RGKNKHCWST SKSTRRSRVS ALNIVRSQRG
121 PTRMCRNIYD PLLCFKLFFT DEIISEIVKW TNAEISLKRR ESMTGATFRD TNEDEIYAFF
181 GILVMTAVRK DNHMSTDDLF DRSLSMVYVS VMSRDRFDFL IRCLRMDDKS IRPTLRENDV
241 FTPVRKIWDL FIHQCIQNYT PGAHLTIDEQ LLGFRGRCPF RMYIPNKPSK YGIKILMMCD
301 SGTKYMINGM PYLGRGTQTN GVPLGEYYVK ELSKPVHGSC RNITCDNWFT SIPLAKNLLQ
361 EPYKLTIVGT VRSNKREIPE VLKNSRSRPV GTSMFCFDGP LTLVSYKPKP AKMVYLLSSC
421 DEDASINEST GKPQMVMYYN QTKGGVDTLD QMCSVMTCSR KTNRWPMALL YGMINIACIN
481 SFIIYSHNVS SKGEKVQSRK KFMRNLYMSL TSSFMRKRLE APTLKRYLRD NISNILPNEV
541 PGTSDDSTEE PVMKKRTYCT YCPSKIRRKA NASCKKCKKV ICREHNIDMC QSCF
(SEQ ID NO:14487).
[048] В некоторых вариантах осуществления фермент транспозаза является ферментом транспозазой piggyBac (PB), включающим или состоящим из аминокислотной последовательности, имеющей аминокислотную замену в двух или более из положений 30, 165, 282 или 538 последовательности SEQ ID NO:14487. В некоторых вариантах осуществления фермент транспозаза является ферментом транспозазой piggyBac (PB), включающим или состоящим из аминокислотной последовательности, имеющей аминокислотную замену в трех или более из положений 30, 165, 282 или 538 последовательности SEQ ID NO:14487. В некоторых вариантах осуществления фермент транспозаза является ферментом транспозазой piggyBac (PB), включающим или состоящим из аминокислотной последовательности, имеющей аминокислотную замену в каждом из следующих положений 30, 165, 282 и 538 последовательности SEQ ID NO:14487. В некоторых вариантах осуществления аминокислотная замена в положении 30 последовательности SEQ ID NO:14487 является заменой валина (V) на изолейцин (I). В некоторых вариантах осуществления аминокислотная замена в положении 165 последовательности SEQ ID NO:14487 является заменой серина (S) на глицин (G). В некоторых вариантах осуществления аминокислотная замена в положении 282 последовательности SEQ ID NO:14487 является заменой валина (V) на метионин (M). В некоторых вариантах осуществления аминокислотная замена в положении 538 последовательности SEQ ID NO:14487 является заменой лизина (K) на аспарагин (N).
[049] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза является ферментом транспозазой Super piggyBac (SPB). В некоторых вариантах осуществления фермент транспозаза Super piggyBac (SPB) согласно изобретению может включать или состоять из аминокислотной последовательности последовательности SEQ ID NO:14487, где аминокислотная замена в положении 30 является заменой валина (V) на изолейцин (I), аминокислотная замена в положении 165 является заменой серина (S) на глицин (G), аминокислотная замена в положении 282 является заменой валина (V) на метионин (M), и аминокислотная замена в положении 538 является заменой лизина (K) на аспарагин (N). В некоторых вариантах осуществления фермент транспозаза Super piggyBac (SPB) может включать или состоять из аминокислотной последовательности, которая по меньшей мере на 75%, 80%, 85%, 90%, 95%, 99% или любого промежуточный процент идентична:
61 SEILDEQNVI EQPGSSLASN RILTLPQRTI RGKNKHCWST SKSTRRSRVS ALNIVRSQRG
121 PTRMCRNIYD PLLCFKLFFT DEIISEIVKW TNAEISLKRR ESMTSATFRD TNEDEIYAFF
181 GILVMTAVRK DNHMSTDDLF DRSLSMVYVS VMSRDRFDFL IRCLRMDDKS IRPTLRENDV
241 FTPVRKIWDL FIHQCIQNYT PGAHLTIDEQ LLGFRGRCPF RVYIPNKPSK YGIKILMMCD
301 SGTKYMINGM PYLGRGTQTN GVPLGEYYVK ELSKPVHGSC RNITCDNWFT SIPLAKNLLQ
361 EPYKLTIVGT VRSNKREIPE VLKNSRSRPV GTSMFCFDGP LTLVSYKPKP AKMVYLLSSC
421 DEDASINEST GKPQMVMYYN QTKGGVDTLD QMCSVMTCSR KTNRWPMALL YGMINIACIN
481 SFIIYSHNVS SKGEKVQSRK KFMRNLYMSL TSSFMRKRLE APTLKRYLRD NISNILPKEV
541 PGTSDDSTEE PVMKKRTYCT YCPSKIRRKA NASCKKCKKV ICREHNIDMC QSCF
(SEQ ID NO:14484).
[050] В изобретении предложен вектор, включающий VCAR согласно изобретению. В некоторых вариантах осуществления вектор является вирусным вектором. Вектор может быть рекомбинантным вектором.
[051] Вирусные векторы согласно изобретению могут включать последовательность, выделенную или полученную из ретровируса, лентивируса, аденовируса, аденоассоциированного вируса или их любой комбинации. Вирусный вектор может включать последовательность, выделенную или полученную из аденоассоциированного вируса (AAV). Вирусный вектор может включать рекомбинантный AAV (rAAV). Примерные аденоассоциированные вирусы и рекомбинантные аденоассоциированные вирусы согласно изобретению включают две или более последовательностей инвертированных концевых повторов (ITR), расположенных в цис-положении рядом с последовательностью, кодирующей VHH или VCAR согласно изобретению. Примерные аденоассоциированные вирусы и рекомбинантные аденоассоциированные вирусы согласно изобретению включают, без ограничения перечисленными, все серотипы (например, AAV1, AAV2, AAV3, AAV4, AAV5, AAV6, AAV7, AAV8 и AAV9). Примерные аденоассоциированные вирусы и рекомбинантные аденоассоциированные вирусы согласно изобретению включают, без ограничения перечисленными, самокомплементарный AAV (scAAV) и AAV гибриды, содержащие геном одного серотипа и капсид другого серотипа (например, AAV2/5, AAV-DJ и AAV-DJ8). Примерные аденоассоциированные вирусы и рекомбинантные аденоассоциированные вирусы согласно изобретению включают, без ограничения, rAAV-LK03.
[052] Вирусные векторы согласно изобретению могут включать селективный ген. Селективный ген может кодировать продукт гена, важный для жизнеспособности и выживания клетки. Селективный ген может кодировать продукт гена, важный для жизнеспособности и выживания клетки при воздействии селективных условий клеточной культуры. Селективные условия клеточной культуры могут включать соединение, опасное для жизнеспособности или выживания клетки, и где продукт гена придает устойчивость к соединению. Примерные селективные гены согласно изобретению могут включать, без ограничения перечисленными, neo (придающий устойчивость к неомицину), DHFR (кодирующий дигидрофолатредуктазу и придающий устойчивость к метотрексату), TYMS (кодирующий тимидилатсинтетазу), MGMT (кодирующий O(6)-метилгуанин-ДНК-метилтрансферазу), ген множественной лекарственной устойчивости (MDR1), ALDH1 (кодирующий члена A1 семейства альдегиддегидрогеназы 1), FRANCF, RAD51C (кодирующий паралог C RAD51), GCS (кодирующий глюкозилцерамидсинтазу), NKX2.2 (кодирующий NK2 гомеобокс 2) или их любую комбинацию.
[053] Вирусные векторы согласно изобретению могут включать индуцируемый проапоптотический полипептид, включающий: (a) лигандсвязывающую область, (b) линкер и (c) проапоптотический полипептид, где индуцируемый проапоптотический полипептид не включает нечеловеческую последовательность. В некоторых вариантах осуществления нечеловеческая последовательность включает сайт рестрикции. В некоторых вариантах осуществления лигандсвязывающая область может быть мультимерной лигандсвязывающей областью. Индуцируемые проапоптотические полипептиды согласно изобретению могут также именоваться "iC9 выключателем безопасности". В некоторых вариантах осуществления вирусные векторы согласно изобретению могут включать индуцируемый полипептид каспазы, включающий: (a) лигандсвязывающую область, (b) линкер и (c) полипептид каспазы, где индуцируемый проапоптотический полипептид не включает нечеловеческую последовательность. В некоторых вариантах осуществления вирусные векторы согласно изобретению могут включать индуцируемый полипептид каспазы, включающий: (a) лигандсвязывающую область, (b) линкер и (c) полипептид каспазы, где индуцируемый проапоптотический полипептид не включает нечеловеческую последовательность. В некоторых вариантах осуществления вирусные векторы согласно изобретению могут включать индуцируемый полипептид каспазы, включающий: (a) лигандсвязывающую область, (b) линкер и (c) усеченный полипептид каспазы 9, где индуцируемый проапоптотический полипептид не включает нечеловеческую последовательность. В некоторых вариантах осуществления индуцируемых проапоптотических полипептидов, индуцируемых полипептидов каспазы или усеченных полипептидов каспазы 9 согласно изобретению, лигандсвязывающая область может включать полипептид FK506 связывающего белка 12 (FKBP12). В некоторых вариантах осуществления аминокислотная последовательность лигандсвязывающей области, которая включает полипептид FK506 связывающего белка 12 (FKBP12), может включать модификацию в положении 36 последовательности. Модификация может быть заменой валина (V) на фенилаланин (F) в положении 36 (F36V). В некоторых вариантах осуществления полипептид FKBP12 кодируется аминокислотной последовательностью, включающей GVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKVDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLE (SEQ ID NO:18022). В некоторых вариантах осуществления полипептид FKBP12 кодируется последовательностью нуклеиновой кислоты, включающей GGGGTCCAGGTCGAGACTATTTCACCAGGGGATGGGCGAACATTTCCAAAAAGGGGCCAGACTTGCGTCGTGCATTACACCGGGATGCTGGAGGACGGGAAGAAAGTGGACAGCTCCAGGGATCGCAACAAGCCCTTCAAGTTCATGCTGGGAAAGCAGGAAGTGATCCGAGGATGGGAGGAAGGCGTGGCACAGATGTCAGTCGGCCAGCGGGCCAAACTGACCATTAGCCCTGACTACGCTTATGGAGCAACAGGCCACCCAGGGATCATTCCCCCTCATGCCACCCTGGTCTTCGATGTGGAACTGCTGAAGCTGGAG (SEQ ID NO:18023). В некоторых вариантах осуществления индуцирующее средство, спецфичное к лигандсвязывающей области, может включать полипептид FK506 связывающего белка 12 (FKBP12), содержащий замену валина (V) на фенилаланин (F) в положении 36 (F36V), которое включает AP20187 и/или AP1903, которые являются синтетическими лекарственными средствами.
[054] В некоторых вариантах осуществления индуцируемых проапоптотических полипептидов, индуцируемых полипептидов каспазы или усеченных полипептидов каспазы 9 согласно изобретению, линкерная область кодируется аминокислотной последовательностью, включающей GGGGS (SEQ ID NO:18024), или последовательностью нуклеиновой кислоты, включающей GGAGGAGGAGGATCC (SEQ ID NO:18025). В некоторых вариантах осуществления последовательность нуклеиновой кислоты, кодирующая линкер, не включает сайт рестрикции.
[055] В некоторых вариантах осуществления усеченных полипептидов каспазы 9 согласно изобретению усеченные полипептиды каспазы 9 кодируются аминокислотной последовательностью, не включающей аргинин (R) в положении 87 последовательности. В альтернативе или дополнительно, в некоторых вариантах осуществления индуцируемых проапоптотических полипептидов, индуцируемых полипептидов каспазы или усеченных полипептидов каспазы 9 согласно изобретению, усеченные полипептиды каспазы 9 кодируются аминокислотной последовательностью, не включающей аланин (A) в положении 282 последовательности. В некоторых вариантах осуществления индуцируемых проапоптотических полипептидов, индуцируемых полипептидов каспазы или усеченных полипептидов каспазы 9 согласно изобретению, усеченные полипептиды каспазы 9 кодируются аминокислотной последовательностью, включающей GFGDVGALESLRGNADLAYILSMEPCGHCLIINNVNFCRESGLRTRTGSNIDCEKLRRRFSSLHFMVEVKGDLTAKKMVLALLELAQQDHGALDCCVVVILSHGCQASHLQFPGAVYGTDGCPVSVEKIVNIFNGTSCPSLGGKPKLFFIQACGGEQKDHGFEVASTSPEDESPGSNPEPDATPFQEGLRTFDQLDAISSLPTPSDIFVSYSTFPGFVSWRDPKSGSWYVETLDDIFEQWAHSEDLQSLLLRVANAVSVKGIYKQMPGCFNFLRKKLFFKTS (SEQ ID NO:18026), или последовательностью нуклеиновой кислоты, включающей TTTGGGGACGTGGGGGCCCTGGAGTCTCTGCGAGGAAATGCCGATCTGGCTTACATCCTGAGCATGGAACCCTGCGGCCACTGTCTGATCATTAACAATGTGAACTTCTGCAGAGAAAGCGGACTGCGAACACGGACTGGCTCCAATATTGACTGTGAGAAGCTGCGGAGAAGGTTCTCTAGTCTGCACTTTATGGTCGAAGTGAAAGGGGATCTGACCGCCAAGAAAATGGTGCTGGCCCTGCTGGAGCTGGCTCAGCAGGACCATGGAGCTCTGGATTGCTGCGTGGTCGTGATCCTGTCCCACGGGTGCCAGGCTTCTCATCTGCAGTTCCCCGGAGCAGTGTACGGAACAGACGGCTGTCCTGTCAGCGTGGAGAAGATCGTCAACATCTTCAACGGCACTTCTTGCCCTAGTCTGGGGGGAAAGCCAAAACTGTTCTTTATCCAGGCCTGTGGCGGGGAACAGAAAGATCACGGCTTCGAGGTGGCCAGCACCAGCCCTGAGGACGAATCACCAGGGAGCAACCCTGAACCAGATGCAACTCCATTCCAGGAGGGACTGAGGACCTTTGACCAGCTGGATGCTATCTCAAGCCTGCCCACTCCTAGTGACATTTTCGTGTCTTACAGTACCTTCCCAGGCTTTGTCTCATGGCGCGATCCCAAGTCAGGGAGCTGGTACGTGGAGACACTGGACGACATCTTTGAACAGTGGGCCCATTCAGAGGACCTGCAGAGCCTGCTGCTGCGAGTGGCAAACGCTGTCTCTGTGAAGGGCATCTACAAACAGATGCCCGGGTGCTTCAATTTTCTGAGAAAGAAACTGTTCTTTAAGACTTCC (SEQ ID NO:18027).
[056] В некоторых вариантах осуществления индуцируемых проапоптотических полипептидов, где полипептид включает усеченный полипептид каспазы 9, индуцируемый проапоптотический полипептид кодируется аминокислотной последовательностью, включающей GVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKVDSSRDRNKPFKFMLGK QEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLEGGGGSGFGDVGALESLRGNADLAYILSMEPCGHCLIINNVNFCRESGLRTRTGSNIDCEKLRRRFSSLHFMVEVKGDLTAKKMVLALLELAQQDHGALDCCVVVILSHGCQASHLQFPGAVYGTDGCPVSVEKIVNIFNGTSCPSLGGKPKLFFIQACGGEQKDHGFEVASTSPEDESPGSNPEPDATPFQEGLRTFDQLDAISSLPTPSDIFVSYSTFPGFVSWRDPKSGSWYVETLDDIFEQWAHSEDLQSLLLRVANAVSVKGIYKQMPGCFNFLRKKLFFKTS (SEQ ID NO:18028), или последовательностью нуклеиновой кислоты, включающей ggggtccaggtcgagactatttcaccaggggatgggcgaacatttccaaaaaggggccagacttgcgtcgtgcattacaccgggatgctggaggacgggaagaaagtggacagctccagggatcgcaacaagcccttcaagttcatgctgggaaagcaggaagtgatccgaggatgggaggaaggcgtggcacagatgtcagtcggccagcgggccaaactgaccattagccctgactacgcttatggagcaacaggccacccagggatcattccccctcatgccaccctggtcttcgatgtggaactgctgaagctggagggaggaggaggatccggatttggggacgtgggggccctggagtctctgcgaggaaatgccgatctggcttacatcctgagcatggaaccctgcggccactgtctgatcattaacaatgtgaacttctgcagagaaagcggactgcgaacacggactggctccaatattgactgtgagaagctgcggagaaggttctctagtctgcactttatggtcgaagtgaaaggggatctgaccgccaagaaaatggtgctggccctgctggagctggctcagcaggaccatggagctctggattgctgcgtggtcgtgatcctgtcccacgggtgccaggcttctcatctgcagttccccggagcagtgtacggaacagacggctgtcctgtcagcgtggagaagatcgtcaacatcttcaacggcacttcttgccctagtctggggggaaagccaaaactgttctttatccaggcctgtggcggggaacagaaagatcacggcttcgaggtggccagcaccagccctgaggacgaatcaccagggagcaaccctgaaccagatgcaactccattccaggagggactgaggacctttgaccagctggatgctatctcaagcctgcccactcctagtgacattttcgtgtcttacagtaccttcccaggctttgtctcatggcgcgatcccaagtcagggagctggtacgtggagacactggacgacatctttgaacagtgggcccattcagaggacctgcagagcctgctgctgcgagtggcaaacgctgtctctgtgaagggcatctacaaacagatgcccgggtgcttcaattttctgagaaagaaactgttctttaagacttcc (SEQ ID NO:18029).
[057] Вирусные векторы согласно изобретению могут включать по меньшей мере один саморасщепляющийся пептид. В некоторых вариантах осуществления вектор может включать по меньшей мере один саморасщепляющийся пептид, и где саморасщепляющийся пептид расположен между CAR и селективным геном. В некоторых вариантах осуществления вектор может включать по меньшей мере один саморасщепляющийся пептид, и где первый саморасщепляющийся пептид расположен перед CAR, а второй саморасщепляющийся пептид расположен после CAR. Вирусные векторы согласно изобретению могут включать по меньшей мере один саморасщепляющийся пептид(ы), расположенный, например, между одним или более VCAR, VCAR или VCAR согласно изобретению и индуцируемым проапоптотическим полипептидом согласно изобретению. Вирусные векторы согласно изобретению могут включать по меньшей мере два саморасщепляющихся пептида, причем первый саморасщепляющийся пептид расположен, например, перед или непосредственно перед индуцируемым проапоптотическим полипептидом согласно изобретению, а второй первый саморасщепляющийся пептид расположен, например, после или непосредственно перед индуцируемым проапоптотическим полипептидом согласно изобретению. Саморасщепляющийся пептид может включать, например, пептид T2A, пептид GSG-T2A, пептид E2A, пептид GSG-E2A, пептид F2A, пептид GSG-F2A, пептид P2A или пептид GSG-P2A. Пептид T2A может включать аминокислотную последовательность, включающую EGRGSLLTCGDVEENPGP (SEQ ID NO:18030), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей EGRGSLLTCGDVEENPGP (SEQ ID NO:18030). Пептид GSG-T2A может включать аминокислотную последовательность, включающую GSGEGRGSLLTCGDVEENPGP (SEQ ID NO:18031), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей GSGEGRGSLLTCGDVEENPGP (SEQ ID NO:18031). Пептид GSG-T2A может включать последовательность нуклеиновой кислоты, включающую ggatctggagagggaaggggaagcctgctgacctgtggagacgtggaggaa aacccaggacca (SEQ ID NO:18032). Пептид E2A может включать аминокислотную последовательность, включающую QCTNYALLKLAGDVESNPGP (SEQ ID NO:18033), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей QCTNYALLKLAGDVESNPGP (SEQ ID NO:18033). Пептид GSG-E2A может включать аминокислотную последовательность, включающую GSGQCTNYALLKLAGDVESNPGP (SEQ ID NO:18034), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей GSGQCTNYALLKLAGDVESNPGP (SEQ ID NO:18034). Пептид F2A может включать аминокислотную последовательность, включающую VKQTLNFDLLKLAGDVESNPGP (SEQ ID NO:18035), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей VKQTLNFDLLKLAGDVESNPGP (SEQ ID NO:18035). Пептид GSG-F2A может включать аминокислотную последовательность, включающую GSGVKQTLNFDLLKLAGDVESNPGP (SEQ ID NO:18036), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей GSGVKQTLNFDLLKLAGDVESNPGP (SEQ ID NO:18036). Пептид P2A может включать аминокислотную последовательность, включающую ATNFSLLKQAGDVEENPGP (SEQ ID NO:18037), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей ATNFSLLKQAGDVEENPGP (SEQ ID NO:18037). Пептид GSG-P2A может включать аминокислотную последовательность, включающую GSGATNFSLLKQAGDVEENPGP (SEQ ID NO:18038), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей GSGATNFSLLKQAGDVEENPGP (SEQ ID NO:18038).
[058] В изобретении предложен вектор, включающий VCAR согласно изобретению. В некоторых вариантах осуществления вектор является наночастицей. Примерные векторы в форме наночастиц согласно изобретению включают, без ограничения перечисленным, нуклеиновые кислоты (например, РНК, ДНК, синтетические нуклеотиды, модифицированные нуклеотиды или их любую комбинацию), аминокислоты (L-аминокислоты, D-аминокислоты, синтетические аминокислоты, модифицированные аминокислоты или их любую комбинацию), полимеры (например, полимерсомы), мицеллы, липиды (например, липосомы), органические молекулы (например, атомы углерода, листы, волокна, трубки), неорганические молекулы (например, фосфат кальция или золото) или их любую комбинацию. Вектор в форме наночастицы может подвергаться пассивному или активному транспорту через клеточную мембрану.
[059] Векторы в форме наночастиц согласно изобретению могут включать селективный ген. Селективный ген может кодировать продукт гена, важный для жизнеспособности и выживания клетки. Селективный ген может кодировать продукт гена, важный для жизнеспособности и выживания клетки при воздействии селективных условий клеточной культуры. Селективные условия клеточной культуры могут включать соединение, опасное для жизнеспособности или выживания клетки, и где продукт гена придает устойчивость к соединению. Примерные селективные гены согласно изобретению могут включать, без ограничения перечисленными, neo (придающий устойчивость к неомицину), DHFR (кодирующий дигидрофолатаредуктазу и придающий устойчивость к метотрексату), TYMS (кодирующий тимидилатсинтетазу), MGMT (кодирующий O(6)-метилгуанин-ДНК-метилтрансферазу), ген множественной лекарственной устойчивости (MDR1), ALDH1 (кодирующий члена A1 семейства альдегиддегидрогеназы 1), FRANCF, RAD51C (кодирующий паралог C RAD51), GCS (кодирующий глюкозилцерамидсинтазу), NKX2.2 (кодирующий NK2 гомеобокс 2) или их любую комбинацию.
[060] Векторы в форме наночастиц согласно изобретению могут включать индуцируемый проапоптотический полипептид, включающий: (a) лигандсвязывающую область, (b) линкер и (c) проапоптотический полипептид, где индуцируемый проапоптотический полипептид не включает нечеловеческую последовательность. В некоторых вариантах осуществления нечеловеческая последовательность включает сайт рестрикции. В некоторых вариантах осуществления лигандсвязывающая область может быть мультимерной лигандсвязывающей областью. Индуцируемые проапоптотические полипептиды согласно изобретению также могут именоваться "iC9 выключателем безопасности". В некоторых вариантах осуществления векторы в форме наночастиц согласно изобретению могут включать индуцируемый полипептид каспазы, включающий: (a) лигандсвязывающую область, (b) линкер и (c) полипептид каспазы, где индуцируемый проапоптотический полипептид не включает нечеловеческую последовательность. В некоторых вариантах осуществления векторы в форме наночастиц согласно изобретению могут включать индуцируемый полипептид каспазы, включающий: (a) лигандсвязывающую область, (b) линкер и (c) полипептид каспазы, где индуцируемый проапоптотический полипептид не включает нечеловеческую последовательность. В некоторых вариантах осуществления векторы в форме наночастиц согласно изобретению могут включать индуцируемый полипептид каспазы, включающий: (a) лигандсвязывающую область, (b) линкер и (c) усеченный полипептид каспазы 9, где индуцируемый проапоптотический полипептид не включает нечеловеческую последовательность. В некоторых вариантах осуществления индуцируемых проапоптотических полипептидов, индуцируемых полипептидов каспазы или усеченных полипептидов каспазы 9 согласно изобретению, лигандсвязывающая область может включать полипептиды FK506 связывающего белка 12 (FKBP12). В некоторых вариантах осуществления аминокислотная последовательность лигандсвязывающей области, которая включает полипептид FK506 связывающего белка 12 (FKBP12), может включать модификацию в положении 36 последовательности. Модификация может быть заменой валина (V) на фенилаланин (F) в положении 36 (F36V). В некоторых вариантах осуществления полипептид FKBP12 кодируется аминокислотной последовательностью, включающей GVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKVDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLE (SEQ ID NO:18022). В некоторых вариантах осуществления полипептид FKBP12 кодируется последовательностью нуклеиновой кислоты, включающей GGGGTCCAGGTCGAGACTATTTCACCAGGGGATGGGCGAACATTTCCAAAAAGGGGCCAGACTTGCGTCGTGCATTACACCGGGATGCTGGAGGACGGGAAGAAAGTGGACAGCTCCAGGGATCGCAACAAGCCCTTCAAGTTCATGCTGGGAAAGCAGGAAGTGATCCGAGGATGGGAGGAAGGCGTGGCACAGATGTCAGTCGGCCAGCGGGCCAAACTGACCATTAGCCCTGACTACGCTTATGGAGCAACAGGCCACCCAGGGATCATTCCCCCTCATGCCACCCTGGTCTTCGATGTGGAACTGCTGAAGCTGGAG (SEQ ID NO:18023). В некоторых вариантах осуществления индуцирующее средство, специфичное к лигандсвязывающей области, может включать полипептид FK506 связывающего белка 12 (FKBP12), содержащий замену валина (V) на фенилаланин (F) в положении 36 (F36V), которое включает AP20187 и/или AP1903, которые являются синтетическими лекарственными средствами.
[061] В некоторых вариантах осуществления индуцируемых проапоптотических полипептидов, индуцируемых полипептидов каспазы или усеченных полипептидов каспазы 9 согласно изобретению, линкерная область кодируется аминокислотной последовательностью, включающей GGGGS (SEQ ID NO:18024), или последовательностью нуклеиновой кислоты, включающей GGAGGAGGAGGATCC (SEQ ID NO:18025). В некоторых вариантах осуществления последовательность нуклеиновой кислоты, кодирующая линкер, не включает сайт рестрикции.
[062] В некоторых вариантах осуществления усеченных полипептидов каспазы 9 согласно изобретению усеченные полипептиды каспазы 9 кодируются аминокислотной последовательностью, не включающей аргинин (R) в положении 87 последовательности. В альтернативе или дополнительно, в некоторых вариантах осуществления индуцируемых проапоптотических полипептидов, индуцируемых полипептидов каспазы или усеченных полипептидов каспазы 9 согласно изобретению, усеченные полипептиды каспазы 9 кодируются аминокислотной последовательностью, не включающей аланин (A) в положении 282 последовательности. В некоторых вариантах осуществления индуцируемых проапоптотических полипептидов, индуцируемых полипептидов каспазы или усеченных полипептидов каспазы 9 согласно изобретению, усеченные полипептиды каспазы 9 кодируются аминокислотной последовательностью, включающей GFGDVGALESLRGNADLAYILSMEPCGHCLIINNVNFCRESGLRTRTGSNIDCEKLRRRFSSLHFMVEVKGDLTAKKMVLALLELAQQDHGALDCCVVVILSHGCQASHLQFPGAVYGTDGCPVSVEKIVNIFNGTSCPSLGGKPKLFFIQACGGEQKDHGFEVASTSPEDESPGSNPEPDATPFQEGLRTFDQLDAISSLPTPSDIFVSYSTFPGFVSWRDPKSGSWYVETLDDIFEQWAHSEDLQSLLLRVANAVSVKGIYKQMPGCFNFLRKKLFFKTS (SEQ ID NO:18026), или последовательностью нуклеиновой кислоты, включающей TTTGGGGACGTGGGGGCCCTGGAGTCTCTGCGAGGAAATGCCGATCTGGCTTACATCCTGAGCATGGAACCCTGCGGCCACTGTCTGATCATTAACAATGTGAACTTCTGCAGAGAAAGCGGACTGCGAACACGGACTGGCTCCAATATTGACTGTGAGAAGCTGCGGAGAAGGTTCTCTAGTCTGCACTTTATGGTCGAAGTGAAAGGGGATCTGACCGCCAAGAAAATGGTGCTGGCCCTGCTGGAGCTGGCTCAGCAGGACCATGGAGCTCTGGATTGCTGCGTGGTCGTGATCCTGTCCCACGGGTGCCAGGCTTCTCATCTGCAGTTCCCCGGAGCAGTGTACGGAACAGACGGCTGTCCTGTCAGCGTGGAGAAGATCGTCAACATCTTCAACGGCACTTCTTGCCCTAGTCTGGGGGGAAAGCCAAAACTGTTCTTTATCCAGGCCTGTGGCGGGGAACAGAAAGATCACGGCTTCGAGGTGGCCAGCACCAGCCCTGAGGACGAATCACCAGGGAGCAACCCTGAACCAGATGCAACTCCATTCCAGGAGGGACTGAGGACCTTTGACCAGCTGGATGCTATCTCAAGCCTGCCCACTCCTAGTGACATTTTCGTGTCTTACAGTACCTTCCCAGGCTTTGTCTCATGGCGCGATCCCAAGTCAGGGAGCTGGTACGTGGAGACACTGGACGACATCTTTGAACAGTGGGCCCATTCAGAGGACCTGCAGAGCCTGCTGCTGCGAGTGGCAAACGCTGTCTCTGTGAAGGGCATCTACAAACAGATGCCCGGGTGCTTCAATTTTCTGAGAAAGAAACTGTTCTTTAAGACTTCC (SEQ ID NO:18027).
[063] В некоторых вариантах осуществления индуцируемых проапоптотических полипептидов, где полипептид включает усеченный полипептид каспазы 9, индуцируемый проапоптотический полипептид кодируется аминокислотной последовательностью, включающей GVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKVDSSRDRNKPFKFMLG KQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLEGGGGSGFGDVGALESLRGNADLAYILSMEPCGHCLIINNVNFCRESGLRTRTGSNIDCEKLRRRFSSLHFMVEVKGDLTAKKMVLALLELAQQDHGALDCCVVVILSHGCQASHLQFPGAVYGTDGCPVSVEKIVNIFNGTSCPSLGGKPKLFFIQACGGEQKDHGFEVASTSPEDESPGSNPEPDATPFQEGLRTFDQLDAISSLPTPSDIFVSYSTFPGFVSWRDPKSGSWYVETLDDIFEQWAHSEDLQSLLLRVANAVSVKGIYKQMPGCFNFLRKKLFFKTS (SEQ ID NO:18028), или последовательностью нуклеиновой кислоты, включающей ggggtccaggtcgagactatttcaccaggggatgggcgaacatttccaaaaaggggccagacttgcgtcgtgcattacaccgggatgctggaggacgggaagaaagtggacagctccagggatcgcaacaagcccttcaagttcatgctgggaaagcaggaagtgatccgaggatgggaggaaggcgtggcacagatgtcagtcggccagcgggccaaactgaccattagccctgactacgcttatggagcaacaggccacccagggatcattccccctcatgccaccctggtcttcgatgtggaactgctgaagctggagggaggaggaggatccggatttggggacgtgggggccctggagtctctgcgaggaaatgccgatctggcttacatcctgagcatggaaccctgcggccactgtctgatcattaacaatgtgaacttctgcagagaaagcggactgcgaacacggactggctccaatattgactgtgagaagctgcggagaaggttctctagtctgcactttatggtcgaagtgaaaggggatctgaccgccaagaaaatggtgctggccctgctggagctggctcagcaggaccatggagctctggattgctgcgtggtcgtgatcctgtcccacgggtgccaggcttctcatctgcagttccccggagcagtgtacggaacagacggctgtcctgtcagcgtggagaagatcgtcaacatcttcaacggcacttcttgccctagtctggggggaaagccaaaactgttctttatccaggcctgtggcggggaacagaaagatcacggcttcgaggtggccagcaccagccctgaggacgaatcaccagggagcaaccctgaaccagatgcaactccattccaggagggactgaggacctttgaccagctggatgctatctcaagcctgcccactcctagtgacattttcgtgtcttacagtaccttcccaggctttgtctcatggcgcgatcccaagtcagggagctggtacgtggagacactggacgacatctttgaacagtgggcccattcagaggacctgcagagcctgctgctgcgagtggcaaacgctgtctctgtgaagggcatctacaaacagatgcccgggtgcttcaattttctgagaaagaaactgttctttaagacttcc (SEQ ID NO:18029).
[064] Векторы в форме наночастиц согласно изобретению могут включать по меньшей мере один саморасщепляющийся пептид. В некоторых вариантах осуществления вектор в форме наночастицы может включать по меньшей мере один саморасщепляющийся пептид, и где саморасщепляющийся пептид расположен между VCAR и наночастицей. В некоторых вариантах осуществления вектор в форме наночастицы может включать по меньшей мере один саморасщепляющийся пептид, и где первый саморасщепляющийся пептид расположен перед VCAR, а второй саморасщепляющийся пептид расположен после VCAR. В некоторых вариантах осуществления вектор в форме наночастицы может включать по меньшей мере один саморасщепляющийся пептид, и где первый саморасщепляющийся пептид расположен между VCAR и наночастицей, а второй саморасщепляющийся пептид расположен после VCAR. В некоторых вариантах осуществления вектор в форме наночастицы может включать по меньшей мере один саморасщепляющийся пептид, и где первый саморасщепляющийся пептид расположен между VCAR и наночастицей, а второй саморасщепляющийся пептид расположен после VCAR, например, между VCAR и селективным геном.
[065] Векторы в форме наночастиц согласно изобретению могут включать по меньшей мере один саморасщепляющийся пептид(ы), расположенный, например, между одним или более VHH или VCAR согласно изобретению и индуцируемым проапоптотическим полипептидом согласно изобретению. Векторы в форме наночастиц согласно изобретению могут включать по меньшей мере два саморасщепляющихся пептида, причем первый саморасщепляющийся пептид расположен, например, перед или непосредственно перед индуцируемым проапоптотическим полипептидом согласно изобретению, а второй первый саморасщепляющийся пептид расположен, например, после или непосредственно перед индуцируемым проапоптотическим полипептидом согласно изобретению. Саморасщепляющийся пептид может включать, например, пептид T2A, пептид GSG-T2A, пептид E2A, пептид GSG-E2A, пептид F2A, пептид GSG-F2A, пептид P2A или пептид GSG-P2A. Пептид T2A может включать аминокислотную последовательность, включающую EGRGSLLTCGDVEENPGP (SEQ ID NO:18030), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей EGRGSLLTCGDVEENPGP (SEQ ID NO:18030). Пептид GSG-T2A может включать аминокислотную последовательность, включающую GSGEGRGSLLTCGDVEENPGP (SEQ ID NO:18031), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей GSGEGRGSLLTCGDVEENPGP (SEQ ID NO:18031). Пептид GSG-T2A может включать последовательность нуклеиновой кислоты, включающую ggatctggagagggaaggggaagcctgctgacctgtggagacgtggaggaaaa cccaggacca (SEQ ID NO:18032). Пептид E2A может включать аминокислотную последовательность, включающую QCTNYALLKLAGDVESNPGP (SEQ ID NO:18033), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей QCTNYALLKLAGDVESNPGP (SEQ ID NO:18033). Пептид GSG-E2A может включать аминокислотную последовательность, включающую GSGQCTNYALLKLAGDVESNPGP (SEQ ID NO:18034), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей GSGQCTNYALLKLAGDVESNPGP (SEQ ID NO:18034). Пептид F2A может включать аминокислотную последовательность, включающую VKQTLNFDLLKLAGDVESNPGP (SEQ ID NO:18035), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей VKQTLNFDLLKLAGDVESNPGP (SEQ ID NO:18035). Пептид GSG-F2A может включать аминокислотную последовательность, включающую GSGVKQTLNFDLLKLAGDVESNPGP (SEQ ID NO:18036), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей GSGVKQTLNFDLLKLAGDVESNPGP (SEQ ID NO:18036). Пептид P2A может включать аминокислотную последовательность, включающую ATNFSLLKQAGDVEENPGP (SEQ ID NO:18037), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей ATNFSLLKQAGDVEENPGP (SEQ ID NO:18037). Пептид GSG-P2A может включать аминокислотную последовательность, включающую GSGATNFSLLKQAGDVEENPGP (SEQ ID NO:18038), или последовательность, обладающую по меньшей мере 70%, 80%, 90%, 95% или 99% идентичностью с аминокислотной последовательностью, включающей GSGATNFSLLKQAGDVEENPGP (SEQ ID NO:18038).
[066] В изобретении предложена композиция, включающая вектор согласно изобретению.
[067] В изобретении предложена клетка, включающая VCAR согласно изобретению. В изобретении предложена клетка, включающая транспозон согласно изобретению. В некоторых вариантах осуществления клетка, включающая VCAR, транспозон или вектор согласно изобретению, может экспрессировать VCAR на поверхности клетки. Клетка может быть клеткой любого типа. Предпочтительно клетка является иммунной клеткой. Иммунная клетка может быть T-клеткой, естественной киллерной клеткой (NK), подобной естественным киллерам (NK) клеткой, клетка цитокин-индуцированной киллерной (CIK) клеткой, гемопоэтической клеткой-предшественником, T-клеткой из периферической крови (PB) или T-клеткой из пуповинной крови (UCB). Предпочтительно иммунная клетка является T-клеткой. T-клетка может быть ранней клеткой памяти, T-клеткой, подобной стволовым клеткам, TSCM-подобной клеткой, TSCM или TCM. T-клеткой может быть TSCM. Клетка может быть клеткой, презентирующей искусственный антиген, которая необязательно может применяться для стимуляции и размножения модифицированной иммуной клеткой или T-клеткой согласно изобретению. Клетка может быть опухолевой клеткой, которая необязательно может применяться в качестве клетки, презентирующей искусственный или модифицированный антиген.
[068] Модифицированные клетки согласно изобретению, которые могут применяться для адоптивной терапии, могут быть аутологичными или аллогенными.
[069] В изобретении предложен способ экспрессии VCAR на поверхности клетки, включающий: (a) получение популяции клеток; (b) контакт популяции клеток с композицией, включающей VCAR согласно изобретению или последовательность, кодирующую VCAR, при условиях, достаточных для переноса VCAR через клеточную мембрану по меньшей мере одной клетки в популяции клеток, с получением, таким образом, модифицированной популяции клеток; (c) культивирование модифицированной популяции клеток при условиях, подходящих для интеграции транспозона; и (d) размножение и/или отбор по меньшей мере одной клетки из популяции модифицированных клеток, которые экспрессируют VCAR на поверхности клеток.
[070] В некоторых вариантах осуществления данного способа экспрессии VCAR, популяция клеток может включать лейкоциты и/или CD4+ и CD8+ лейкоциты. Популяция клеток может включать CD4+ и CD8+ лейкоциты в оптимизированном соотношении. Оптимизированное соотношение CD4+ к CD8+ лейкоцитам не встречается в природе in vivo. Популяция клеток может включать опухолевую клетку.
[071] В некоторых вариантах осуществления данного способа экспрессии VCAR, транспозон или вектор включает VCAR или последовательность, кодирующую VCAR.
[072] В некоторых вариантах осуществления данного способа экспрессии VCAR, условия, достаточные для переноса последовательности, кодирующей VCAR, через клеточную мембрану по меньшей мере одной клетки в популяции клеток, включают нуклеофекцию.
[073] В некоторых вариантах осуществления данного способа экспрессии VCAR, где условия, достаточные для переноса последовательности, кодирующей VCAR, через клеточную мембрану по меньшей мере одной клетки в популяции клеток, включают по меньшей мере одно из применения одного или более импульсов электрического тока при указанном напряжении, буфера и одного или более дополнительных факторов. В некоторых вариантах осуществления буфер может включать PBS, HBSS, OptiMEM, BTXpress, Amaxa Nucleofector, буфер для нуклеофекции человеческих T-клеток или их любую комбинацию. В некоторых вариантах осуществления один или более дополнительных факторов могут включать: (a) рекомбинантный человеческий цитокин, хемокин, интерлейкин или их любую комбинацию; (b) соль, минеральное вещество, метаболит или их любую комбинацию; (c) клеточную среду; (d) ингибитор обнаружения клеточной ДНК, метаболизма, дифференцировки, сигнальной трансдукции, одного или более апоптотических путей или их комбинации; и (e) реагент, который модифицирует или стабилизирует одну или более нуклеиновых кислот. Рекомбинантный человеческий цитокин, хемокин, интерлейкин или их любая комбинация могут включать IL2, IL7, IL12, IL15, IL21, IL1, IL3, IL4, IL5, IL6, IL8, CXCL8, IL9, IL10, IL11, IL13, IL14, IL16, IL17, IL18, IL19, IL20, IL22, IL23, IL25, IL26, IL27, IL28, IL29, IL30, IL31, IL32, IL33, IL35, IL36, ГМ-КСФ, IFN-гамма, IL-1 альфа/IL-1F1, IL-1 бета/IL-1F2, IL-12 p70, IL-12/IL-35 p35, IL-13, IL-17/IL-17A, гетеродимер IL-17A/F, IL-17F, IL-18/IL-1F4, IL-23, IL-24, IL-32, IL-32 бета, IL-32 гамма, IL-33, LAP (TGF-бета 1), лимфотоксин-альфа/TNF-бета, TGF-бета, ФНО-альфа, TRANCE/TNFSF11/RANK L или их любую комбинацию. Соль, минеральное вещество, метаболит или их любая комбинация могут включать HEPES, никотинамид, гепарин, пируват натрия, L-глутамин, MEM раствор заменимых аминокислот, аскорбиновую кислоту, нуклеозиды, FBS/FCS, человеческую сыворотку, заменитель сыворотки, антибиотики, регуляторы pH, соли эрла, 2-меркаптоэтанол, человеческий трансферрин, рекомбинантный человеческий инсулин, человеческий сывороточный альбумин, добавку Nucleofector PLUS, KCL, MgCl2, Na2HPO4, NAH2PO4, лактобионат натрия, маннит, сукцинат натрия, хлорид натрия, CINa, глюкозу, Ca(NO3)2, Tris/HCl, K2HPO4, KH2PO4, полиэтиленимин, полиэтиленгликоль, полоксамер 188, полоксамер 181, полоксамер 407, поливинилпирролидон, Pop313, Краун-5 или их любую комбинацию. Клеточная среда может включать PBS, HBSS, OptiMEM, DMEM, RPMI 1640, AIM-V, X-VIVO 15, среду CellGro DC, среду CTS OpTimizer T Cell Expansion SFM, среду TexMACS, среду PRIME-XV T Cell Expansion Medium, среду ImmunoCult-XF T Cell Expansion Medium или их любую комбинацию. Ингибитор обнаружения клеточной ДНК, метаболизма, дифференцировки, сигнальной трансдукции, одного или более апоптотических путей или их комбинаций включает ингибиторы TLR9, MyD88, IRAK, TRAF6, TRAF3, IRF-7, NF-KB, интерфероны типа 1, провоспалительные цитокины, cGAS, STING, Sec5, TBK1, IRF-3, RNA pol III, RIG-1, IPS-1, FADD, RIP1, TRAF3, AIM2, ASC, Caspase1, Pro-IL1B, PI3K, Akt, Wnt3A, ингибиторы киназы гликогенсинтазы 3β (GSK-3β) (например, TWS119), бафиломицин, хлорохин, хинакрин, AC-YVAD-CMK, Z-VAD-FMK, Z-IETD-FMK или их любую комбинацию. Реагент, который модифицирует или стабилизирует одну или более нуклеиновых кислот, включает модификатор pH, ДНК-связывающий белок, липид, фосфолипид, CaPO4, пептид, связывающий ДНК с суммарным нейтральным зарядом, с или без последовательности NLS, фермент TREX1 или их любую комбинацию.
[074] В некоторых вариантах осуществления данного способа экспрессии VCAR условия, подходящие для интеграции VCAR или последовательности, кодирующей VCAR согласно изобретению, включают по меньшей мере одно из буфера и одного или более дополнительных факторов. В некоторых вариантах осуществления транспозон или вектор согласно изобретению включают VCAR или последовательность, кодирующую VCAR согласно изобретению. В некоторых вариантах осуществления буфер может включать PBS, HBSS, OptiMEM, BTXpress, Amaxa Nucleofector, буфер для нуклеофекции человеческих T-клеток или их любую комбинацию. В некоторых вариантах осуществления один или более дополнительных факторов могут включать: (a) рекомбинантный человеческий цитокин, хемокин, интерлейкин или их любую комбинацию; (b) соль, минеральное вещество, метаболит или их любую комбинацию; (c) клеточную среду; (d) ингибитор обнаружения клеточной ДНК, метаболизма, дифференцировки, сигнальной трансдукции, одного или более апоптотических путей или их комбинации; и (e) реагент, который модифицирует или стабилизирует одну или более нуклеиновых кислот. Рекомбинантный человеческий цитокин, хемокин, интерлейкин или их любая комбинация могут включать IL2, IL7, IL12, IL15, IL21, IL1, IL3, IL4, IL5, IL6, IL8, CXCL8, IL9, IL10, IL11, IL13, IL14, IL16, IL17, IL18, IL19, IL20, IL22, IL23, IL25, IL26, IL27, IL28, IL29, IL30, IL31, IL32, IL33, IL35, IL36, ГМ-КСФ, IFN-гамма, IL-1 альфа/IL-1F1, IL-1 бета/IL-1F2, IL-12 p70, IL-12/IL-35 p35, IL-13, IL-17/IL-17A, гетеродимер IL-17A/F, IL-17F, IL-18/IL-1F4, IL-23, IL-24, IL-32, IL-32 бета, IL-32 гамма, IL-33, LAP (TGF-бета 1), лимфотоксин-альфа/TNF-бета, TGF-бета, ФНО-альфа, TRANCE/TNFSF11/RANK L или их любую комбинацию. Соль, минеральное вещество, метаболит или их любая комбинация могут включать HEPES, никотинамид, гепарин, пируват натрия, L-глутамин, MEM раствор заменимых аминокислот, аскорбиновую кислоту, нуклеозиды, FBS/FCS, человеческую сыворотку, заменитель сыворотки, антибиотики, регуляторы pH, соли Эрла, 2-меркаптоэтанол, человеческий трансферрин, рекомбинантный человеческий инсулин, человеческий сывороточный альбумин, добавку Nucleofector PLUS, KCL, MgCl2, Na2HPO4, NAH2PO4, лактобионат натрия, маннит, сукцинат натрия, хлорид натрия, CINa, глюкозу, Ca(NO3)2, Tris/HCl, K2HPO4, KH2PO4, полиэтиленимин, полиэтиленгликоль, полоксамер 188, полоксамер 181, полоксамер 407, Поливинилпирролидон, Pop313, Краун-5 или их любую комбинацию. Клеточная среда может включать PBS, HBSS, OptiMEM, DMEM, RPMI 1640, AIM-V, X-VIVO 15, среду CellGro DC, среду CTS OpTimizer T Cell Expansion SFM, среду TexMACS, среду PRIME-XV T Cell Expansion Medium, среду ImmunoCult-XF T Cell Expansion Medium или их любую комбинацию. Ингибитор обнаружения клеточной ДНК, метаболизма, дифференцировки, сигнальной трансдукции, одного или более апоптотических путей или их комбинации включают ингибиторы TLR9, MyD88, IRAK, TRAF6, TRAF3, IRF-7, NF-KB, интерферон типа 1, провоспалительные цитокины, cGAS, STING, Sec5, TBK1, IRF-3, RNA pol III, RIG-1, IPS-1, FADD, RIP1, TRAF3, AIM2, ASC, каспазу 1, Pro-IL1B, PI3K, Akt, Wnt3A, ингибиторы киназы гликогенасинтазы 3β (GSK-3β) (например, TWS119), бафиломицин, хлорохин, хинакрин, AC-YVAD-CMK, Z-VAD-FMK, Z-IETD-FMK или их любую комбинацию. Реагент, который модифицирует или стабилизирует одну или более нуклеиновых кислот, включает модификатор pH, ДНК-связывающий белок, липид, фосфолипид, CaPO4, пептид, связывающий ДНК с суммарным нейтральным зарядом, с или без последовательности NLS, фермент TREX1 или их любую комбинацию.
[075] В некоторых вариантах осуществления данного способа экспрессии VCAR этапы экспансии и отбора проходят последовательно. Экспансия может проходить до отбора. Экспансия может проходить после отбора и, необязательно, дополнительный (т.е. второй) отбор может проходить после экспансии.
[076] В некоторых вариантах осуществления данного способа экспрессии VCAR этапы экспансии и отбора могут проходить одновременно.
[077] В некоторых вариантах осуществления данного способа экспрессии VCAR экспансия может включать контакт по меньшей мере одной клетки популяции модифицированных клеток с антигеном для стимуляции по меньшей мере одной клетки посредством VCAR, с получением, таким образом, популяции размноженных клеток. Антиген может быть презентирован на поверхности субстрата. Субстрат может иметь любую форму, в том числе, без ограничения перечисленным, поверхность, лунку, сферу или их множество и матрицу. Субстрат может дополнительно включать парамагнитный или магнитный компонент. В некоторых вариантах осуществления данного способа экспрессии VCAR антиген может быть презентирован на поверхности субстрата, где субстрат является магнитной сферой, и где магнит может использоваться для удаления или отделения магнитных сфер от популяции модифицированных и размноженных клеток. Антиген может быть презентирован на поверхности клетки или клетки, презентирующей искусственный антиген. Клетки, презентирующие искусственный антиген согласно изобретению, могут включать, без ограничения перечисленными, опухолевые клетки и стволовые клетки.
[078] В некоторых вариантах осуществления данного способа экспрессии VCAR, где транспозон или вектор включают селективный ген, и где этап отбора включает контакт по меньшей мере одной клетки популяции модифицированных клеток с соединением, устойчивость к которому придает селективный ген, что позволяет идентифицировать клетку, экспрессирующую селективный ген, как выживающую при отборе и идентифицировать клетку, не способную экспрессировать селективный ген, как не способную выжить в этапе отбора.
[079] В некоторых вариантах осуществления данного способа экспрессии VCAR этапы экспансии и/или отбора могут проходить в течение периода длительностью 10-14 дней, включая конечные точки.
[080] В изобретении предложена композиция, включающая популяцию модифицированных, размноженных и отобранных клеток согласно способам изобретения.
[081] В изобретении предложен способ лечения рака у пациента, включающий введение индивиду композиции согласно изобретению, где VCAR специфично связывается с антигеном на опухолевой клетке. В некоторых вариантах осуществления опухолевая клетка может быть клеткой злокачественной опухоли. В некоторых вариантах осуществления, включающих введение индивиду композиции, включающей модифицированную клетку или популяцию клеток согласно изобретению, клетка или популяция клеток может быть аутологичной. В некоторых вариантах осуществления, включающих введение индивиду композиции, включающей модифицированную клетку или популяцию клеток согласно изобретению, клетка или популяция клеток может быть аллогенной.
[082] В изобретении предложен способ лечения аутоиммунного состояния у пациента, включающий введение индивиду композиции согласно изобретению, где VCAR специфично связывается с антигеном на аутоиммунной клетке индивида. В некоторых вариантах осуществления аутоиммунная клетка может быть лимфоцитом, который специфично связывается с аутоантигеном на клетке-мишени индивида. В некоторых вариантах осуществления аутоиммунная клетка может быть B-лимфоцитом (т.е. B-клеткой). В некоторых вариантах осуществления аутоиммуння клетка может быть T-лимфоцитом (т.е. T-клеткой). В некоторых вариантах осуществления, включающих введение индивиду композиции, включающей модифицированную клетку или популяцию клеток согласно изобретению, клетка или популяция клеток может быть аутологичной. В некоторых вариантах осуществления, включающих введение индивиду композиции, включающей модифицированную клетку или популяцию клеток согласно изобретению, клетка или популяция клеток может быть аллогенной.
[083] В изобретении предложен способ лечения инфекции у пациента, включающий введение индивиду композиции согласно изобретению, где VCAR специфично связывается с антигеном на клетке, включающей возбудитель инфекции, клетку в контакте с возбудителем инфекции или клетку, которая подвергается воздействию возбудителя инфекции. В некоторых вариантах осуществления клетка в контакте с возбудителем инфекции может быть в воздушном контакте (например, возбудитель инфекции передается воздушно-капельным путем или вдыхается) или жидкостном контакте (например, возбудитель инфекции переносится в водной или биологической жидкости) с возбудителем инфекции. Возбудитель инфекции, вызывающий инфекцию клетки-хозяина, может быть бактерией, вирусом, дрожжами или микроорганизмом. Возбудитель инфекции может вызывать в клетке или организме-хозяине клетки (у индивида) примерные состояния, включающие, без ограничения перечисленными, вирусную инфекцию, состояние иммуннодефицита, воспалительное заболевание и пролиферативное нарушение. В некоторых вариантах осуществления инфекция вызывает туберкулез, микроэнцефалию, нейродегенерацию или малярию. В некоторых вариантах осуществления инфекция вызывает микроэнцефалию в плоде индивида. В некоторых вариантах осуществления, включая те, в которых инфекция вызывает микроэнцефалию в плоде индивида, возбудитель инфекции является вирусом, и где вирус является вирусом Зика. В некоторых вариантах осуществления состоянием иммуннодефицита является синдром приобретенного иммунодефицита (СПИД). В некоторых вариантах осуществления пролиферативное нарушение представляет собой рак. В некоторых вариантах осуществления рак является раком шейки матки, и где возбудитель инфекции является вирусом папилломы человека (ВПЧ). В некоторых вариантах осуществления, включающих введение индивиду композиции, включающей модифицированную клетку или популяция клеток согласно изобретению, клетка или популяция клеток может быть аутологичной. В некоторых вариантах осуществления, включающих введение индивиду композиции, включающей модифицированную клетку или популяцию клеток согласно изобретению, клетка или популяция клеток может быть аллогенной.
[084] В изобретении предложен способ лечения мастоцитоза у пациента, включающий введение индивиду композиции согласно изобретению, где VCAR специфично связывается с антигеном на тучной клетке. В некоторых вариантах осуществления VCAR специфично связывает с антигеном на тучной клетке индивида. В некоторых вариантах осуществления мастоцитоз может включать, без ограничения перечисленными, нарушения, связанные с избыточной пролиферацией тучных клеток, нарушения, связанные с тучными клетками, обладающими патологической активностью, и нарушения, связанные как с патологическим количеством тучных клеток, так и с патологической активностью тучных клеток. Примерные нарушения, связанные с избыточной пролиферацией тучных клеток, включают, без ограничения перечисленными, мастоцитоз, кожный мастоцитоз (например, пигментная крапивница или макулопапулезный кожный мастоцитоз), системный мастоцитоз (включая тучноклеточный лейкоз), и локализованные пролиферации тучных клеток. Примерные нарушения, связанные с тучными клетками, обладающими патологической активностью, включают, без ограничения перечисленными, синдром активации тучных клеток (MCAS) или нарушение активации тучных клеток (MCAD), аллергическое заболевание (включая анафилаксию), астму, воспалительное заболевание (включая связанное с аутоиммунным заболеванием воспаление, например, суставных тканей, артрит и т.д.) или их любую комбинацию. В некоторых вариантах осуществления, включающих введение индивиду композиции, включающей модифицированную клетку или популяцию клеток согласно изобретению, клетка или популяция клеток может быть аутологичной. В некоторых вариантах осуществления, включающих введение индивиду композиции, включающей модифицированную клетку или популяцию клеток согласно изобретению, клетка или популяция клеток может быть аллогенной. В изобретении предложен способ лечения дегенеративного заболевания у пациента, включающий введение индивиду композиции согласно изобретению, где VCAR специфично связывается с антигеном на патогенной клетке или состарившейся клетке. В некоторых вариантах осуществления VCAR специфично связывается с антигеном на патогенной клетке или состарившейся клетке индивида. В некоторых вариантах осуществления дегенеративное заболевание может включать, без ограничения перечисленными, нейродегенеративное нарушение, нарушение обмена веществ, сосудистое нарушение и старение. Примерные нейродегенеративные нарушения включают, без ограничения перечисленными, нарушения, связанные с потерей функции или эффективности одного или более нейронов, глиальных клеток или микроглии. Примерные нейродегенеративные нарушения включают, без ограничения перечисленными, нарушения, связались с накоплением одной или более из сигнальной молекулы, белка или приона, которые нарушают функцию или уменьшают эффективность одного или более нейронов, глиальных клеток или микроглии. Примерные нарушения обмена веществ включают, без ограничения перечисленными, нарушения, связанные с митохондриальными нарушениями, разрывами цепи переноса электронов, нарушениями клеточного синтеза АТФ, потерей функции или снижением эффективности одной или более митохондрий одного или более нейронов, глиальных клеток или микроглии. Примерные нарушения обмена веществ включают, без ограничения перечисленными, нарушения, связанные с нарушением кровообращения или снижением притока крови к нейрону, глиальной клетке или микроглии (например, инсульт); кратковременное или стойкое состояние гипоксии в нейроне, глиальной клетке или микроглии (например, достаточное для высвобождения свободных радикалов в клетке); нарушение циркуляции ЦНС или снижение тока ЦНС к нейрону, глиальной клетке или микроглии во время состояния сна у индивида, достаточное для уменьшения эффективности удаления продуктов обмена из нейрона, глиальной клетки или микроглии во время такого состояния сна. Примерные нарушения, связанные со старением, включают, без ограничения перечисленными, нарушения, связанные с увеличением укорачивания или укороченных теломер на одной или более хромосомах нейрона, глиальной клетки или микроглии; потерю функции или снижение эффективности теломеразы в нейроне, глиальной клетке или микроглии; или потерю функции или снижение эффективности механизма репарации ДНК в нейроне, глиальной клетке или микроглии. В некоторых вариантах осуществления патогенная клетка или состарившаяся клетка нарушает функцию или уменьшает эффективность другой клетки в сети, включающей патогенную клетку или состарившуюся клетку, при этом направленное удаление патогенной клетки или состарившейся клетки улучшает или восстанавливает функцию или увеличивает эффективность сети. В некоторых вариантах осуществления патогенная клетка или состарившаяся клетка может трансформировать функцию или эффективность второй клетки, при этом направленное удаление патогенной клетки или состарившейся клетки предотвращает трансформацию второй клетки. В некоторых вариантах осуществления дегенеративное заболевание является нейродегенеративным нарушением, и патогенная клетка или состарившаяся клетка является стволовой клеткой, иммунной клеткой, нейроном, глией или микроглией. В некоторых вариантах осуществления дегенеративное заболевание является нарушением обмена веществ, и патогенная клетка или состарившаяся клетка является стволовой клеткой, соматической клеткой, нейроном, глией или микроглией. В некоторых вариантах осуществления дегенеративное заболевание является сосудистым нарушением, и патогенная клетка или состарившаяся клетка является стволовой клеткой, соматической клеткой, иммунной клеткой, эндотелиальной клеткой, нейроном, глией или микроглией. В некоторых вариантах осуществления дегенеративное заболевание является старением, а патогенная клетка или состарившаяся клетка является ооцитом, сперматозоидом, стволовой клеткой, соматической клеткой, иммунной клеткой, эндотелиальной клеткой, нейроном, глией или микроглией. В некоторых вариантах осуществления, включающих введение индивиду композиции, включающей модифицированную клетку или популяцию клеток согласно изобретению, клетка или популяция клеток может быть аутологичной. В некоторых вариантах осуществления, включающих введение индивиду композиции, включающей модифицированную клетку или популяцию клеток согласно изобретению, клетка или популяция клеток может быть аллогенной.
[085] В изобретении предложен способ модификации клеточной терапии у пациента, включающий введение индивиду композиции, включающей клетку, включающую транспозон или вектор, композиции, включающей индуцируемый проапоптотический полипептид, где апоптоз может быть селективно индуцирован в клетке путем контакта с клеткой с индуцирующим средством. В некоторых вариантах осуществления клетка является аутологичной. В некоторых вариантах осуществления клетка является аллогенной. В некоторых вариантах осуществления данного способа клеточная терапия является адоптивной клеточной терапией. В некоторых вариантах осуществления данного способа модификация клеточной терапии включает завершение клеточной терапии. В некоторых вариантах осуществления данного способа модификация клеточной терапии включает элиминирование части клеток, представленных в клеточной терапии. В некоторых вариантах осуществления способ дополнительно включает этап введения ингибитора индуцирующего средства для ингибирования модификации клеточной терапии, приводящего, таким образом, к восстановлению функции и/или эффективности клеточной терапии.
[086] Способы модификации клеточной терапии согласно изобретению могут применяться для завершения или ослабления терапии, например, в ответ на признак восстановления или признак уменьшения тяжести/прогрессирования заболевания, признак ремиссии/прекращения заболевания и/или возникновение нежелательного явления. Клеточная терапия согласно изобретению может быть возобновлена путем ингибирования индуцирующего средства в случае повторного появления признака или симптома заболевания или увеличения степени тяжести и/или устранения нежелательного явления.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[087] Фигура 1 является графиком, на котором показано изменение веса в зависимости от количества дней, прошедших после лечения, для VCAR-рецепторов согласно изобретению.
[088] Фигура 2 является графиком, на котором показана опухолевая нагрузка в зависимости от количества дней, прошедших после лечения, для VCAR-рецепторов согласно изобретению.
[089] Фигура 3 является графиком, на котором показана процентная выживаемость в зависимости от количества дней, прошедших после лечения, для VCAR-рецепторов согласно изобретению.
[090] Фигура 4 является графиком, на котором показана опухолевая нагрузка, показанная сигналом биолюминесценции в зависимости от количества дней, прошедших после лечения VH-A (треугольники), нерелевантным CAR (квадраты) или без опухоли/без CAR-T (круги).
[091] Фигура 5 является графиком, на котором показана опухолевая нагрузка, показанная сигналом биолюминесценции в зависимости от количества дней, прошедших после лечения VH-B (треугольники), нерелевантным CAR (квадраты) или без опухоли/без CAR-T (круги).
[092] Фигура 6 является графиком, на котором показана опухолевая нагрузка, показанная сигналом биолюминесценции в зависимости от количества дней, прошедших после лечения VH-C (треугольники), нерелевантным CAR (квадраты) или без опухоли/без CAR-T (круги).
[093] Фигура 7 является графиком, на котором показана опухолевая нагрузка, показанная сигналом биолюминесценции в зависимости от количества дней, прошедших после лечения VH-D (треугольники), нерелевантным CAR (квадраты) или без опухоли/без CAR-T (круги).
[094] Фигура 8 - график, на котором показана опухолевая нагрузка, показанная сигналом биолюминесценции в зависимости от количества дней, прошедших после лечения VH-E (треугольники), нерелевантным CAR (квадраты) или без опухоли/без CAR-T (круги).
[095] Фигура 9 - график, на котором показана опухолевая нагрузка, показанная сигналом биолюминесценции в зависимости от количества дней, прошедших после лечения VH-F (треугольники), нерелевантным CAR (квадраты) или без опухоли/без CAR-T (круги).
[096] Фигура 10A является таблицей, в которой приведены консенсусные последовательности каркасных и CDR последовательностей для примерных VH согласно изобретению.
[097] Фигура 10B является выравниванием примерных VH согласно изобретению. Сверху вниз, последовательности соответствуют консенсусным последовательностям каркасных областей VH-B (SEQ ID NO:18050), VH-D (SEQ ID NO:18051), VH-A (SEQ ID NO:18052), VH-E (SEQ ID NO:18053), VH-F (SEQ ID NO:18054) и VH-C (SEQ ID NO:18055).
[098] Фигура 11 является гистограммой, на которой показана эффективность нокаута сигнальных белков контрольных точек на "бронированных" T-клетках. Первичные человеческие T-клетки обычно находятся в состоянии покоя при выделении у нормальных здоровых доноров. Cas-CLOVER использовали для нокаута рецепторов контрольных точек, PD-1, TGFBR2, LAG-3, TIM-3 и CTLA-4. Процент нокаута показан на оси Y. Редактирование генов приводило к 30-70% потере экспрессии белка на клеточной поверхности, как измеряли с помощью проточной цитометрии.
[099] Фигура 12 представляет собой схематические диаграммы рецепторов дикого типа, нулевых и переключаемых рецепторов и их эффектов в отношении внутриклеточной сигнализации, ингибирующей или стимулирующей, в первичных T-клетках. Связывание ингибирующего рецептора дикого типа, эндогенно экспрессируемого на T-клетке, с его эндогенным лигандом, приводит к передаче ингибирующего сигнала, который частично снижает эффекторную функцию T-клетки. Однако мутация (Мутантный нулевой) или делеция (Усеченный нулевой) внутриклеточного домена (ICD) белка рецептора контрольной точки, такого как PD-1 (верхняя панель) или TGFBRII (нижняя панель), снижает или устраняет его сигнальную способность при связывании когнатного лиганда(ов). Таким образом, экспрессия сконструированных мутантных или усеченных нулевых рецепторов на поверхности модифицированных T-клеток приводит к конкуренции с эндогенно экспрессируемыми рецепторами дикого типа за связывание свободного эндогенного лиганда(ов), эффективно уменьшая или устраняя доставку ингибирующих сигналов эндогенно экспрессируемыми рецепторами дикого типа. В частности, любое связывание с мутантным или нулевым рецептором блокирует связывание эндогенного лиганда(ов) с рецептором дикого типа и приводит к разбавлению общего уровня сигнализации контрольной точки, эффективно доставляемого в модифицированную T-клетку, что уменьшает или блокирует ингибирование контрольной точки и функциональное истощение модифицированных T-клеток. Переключаемый рецептор создают путем замены ICD дикого типа на ICD из костимулирующей молекулы (такой как CD3z, CD28, 4-1BB) или другой ингибирующей молекулы (такой как CTLA4, PD-1, Lag3). В первом случае связывание эндогенного лиганда(ов) модифицированным переключаемым рецептором приводит к доставке положительного сигнала в T-клетки, что способствует усилению стимуляции модифицированных T-клеток и потенциально усиливает уничтожение клеток-мишеней. В последнем случае связывание эндогенного лиганда(ов) модифицированным переключаемым рецептором приводит к доставке отрицательного сигнала в T-клетки, что устраняет стимуляцию модифицированных T-клеток и потенциально уменьшает гибель опухолевых клеток-мишеней. Сигнальный пептид (фиолетовая стрелка), внеклеточный домен (ECD) (ярко-зеленый), трансмембранный домен (желтый), внутриклеточный сигнальный домен (ICD) (оранжевый) и заменяющий ICD (зеленый) показаны на диаграммах рецепторов. "*" обозначает мутировавший ICD. "+" указывает на присутствие сигнала контрольной точки. "-" указывает на отсутствие сигнала контрольной точки.
[0100] Фигура 13 является схематической диаграммой, на которой показана конструкция нулевых рецепторов PD-1 и TGFBRII. Показаны сигнальный пептидный домен (SP), трансмембранный домен (ТМ) и внеклеточный домен (ECD) усеченных нулевых рецепторов PD-1 (верхняя панель) и TGFBRII (нижняя панель). Первой из лучших четырех молекул является рецептор PD-1 дикого типа, который кодирует SP и ТМ PD-1 дикого типа. Для нулевого рецептора PD-1 показана замена SP или ТМ домена PD-1 дикого типа (зеленый; светло-зеленый) доменом SP или ТМ человеческого T-клеточного CD8a рецептора (красный). Вторая молекула кодирует SP CD8a вместе с нативным ТМ PD-1, третья кодирует SP PD-1 дикого типа и альтернативный ТМ CD8a, и четвертая кодирует альтернативные SP и ТМ CD8a. Аналогичным образом, для нулевого рецептора TGFβRII, замена SP TGFBRII дикого типа (розовый) доменом SP человеческого T-клеточного CD8a рецептора (красный). Названия конструкций и длины аминокислотных последовательностей (ак) белка каждой конструкции перечислены слева от диаграммы.
[0101] Фигура 14 представляет собой серию гистограмм, на которых показана экспрессия нулевых рецепторов PD-1 и TGFBRII на поверхности первичных человеческих T-клеток, определенная с помощью проточной цитометрии. Каждая из шести усеченных нулевых конструкций на Фигуре 13 была экспрессирована на поверхности первичных человеческих T-клеток. T-клетки окрашивали либо антителом к PD-1 (вверху; синие гистограммы), либо антителом к TGFβRII (внизу; синие гистограммы), либо изотипическим контрольным или только вторичным антителом (серые гистограммы). Клетки, положительно окрашенные на экспрессию PD-1 или TGFβRII, подвергали гейтированию (частота показана над гейтом) и значение средней интенсивности флуоресценции (MFI) показано над каждой положительной гистограммой. Названия конструкций с нулевым рецептором показаны над каждым графиком. Обе стратегии генов с нулевым рецептором, замена SP дикого типа на альтернативный CD8a были успешно экспрессированы. 02.8aSP-PD-1 и 02.8aSP-TGFβRII приводили к наибольшему уровню экспрессии на поверхности T-клеток. Нулевой рецептор 02.8aSP-PD-1 показал MFI 43680, что в 177 раз выше, чем экспрессия эндогенного PD-1 T-клеток, и в 2,8 раза выше, чем нулевой рецептор PD-1 дикого типа. Нулевой рецептор 02.8aSP-TGFβRII показал MFI 13809, что в 102 раза выше, чем экспрессия эндогенного TGFβRII T-клеток, и в 1,8 раза выше, чем нулевой рецептор TGFβRII дикого типа. Замена SP дикого типа альтернативным SP CD8a, как для PD-1, так и для TGRBRII, приводит к усилению поверхностной экспрессии нулевого или переключаемого рецептора, что способствует максимальному повышению ингибирования или костимуляции контрольной точки, соответственно, при связывании эндогенного лиганда(ов).
[0102] Фигура 15А-В представляет собой пару схематических изображений, на которых показаны индуцируемые векторы NF-KB для экспрессии в T-клетках. Были разработаны два индуцируемых вектора NF-KB активации T-клеток: один с системой экспрессии генов (GES) в прямой ориентации (A), а другой в комплементарном направлении (B), оба предшествуют конститутивному промотору EF1a. Эти векторы также направляют экспрессию молекулы CAR и селективного гена DHFR, разделенных T2A последовательностью. Как кондиционно индуцируемая система NF-KB, так и EF1a направленные гены являются частью транспозона piggyBac, который можно постоянно интегрировать в T-клетки с помощью электропорации (ЭП). После интеграции в геном, T-клетки будут конститутивно экспрессировать CAR на поверхности мембраны и DHFR в клетке, при этом экспрессия индуцируемого NF-KB гена, GFP, будет экспрессироваться до наиболее высокого уровня только после активации T-клеток.
[0103] Фигура 16 является парой графиков, на которых показана индуцируемая NF-KB экспрессия GFP в активированных T-клетках. T-клетки подвергали нуклеофекции с использованием вектора piggyBac, экспрессирующего CAR против BCMA и ген мутеина DHFR под контролем EF1a промотора, наряду с отсутствием (без контроля GES) или присутствием индуцируемой системы экспрессии NF-KB, направляющей экспрессию GFP в прямой (pNFKB-GFP forward) или в обратной ориентации (pNFKB-GFP reverse). Клетки культивировали в присутствии селекции метотрексатом, пока клетки почти полностью не перешли в состояние покоя (день 19), и экспрессию GFP оценивали в день 5 и день 19. В день 5 все T-клетки пролиферировали и подвергались сильной стимуляции, при этом клетки, несущие NF-KB индуцируемую кассету экспрессии, продуцировали высокие уровни GFP из-за высокой активности NFκB. Контрольные клетки без GES не экспрессировали обнаружимые уровни GFP. В день 19 GES T-клетки почти полностью перешли в состояние покоя, и экспрессия GFP становилась значительно ниже, чем в день 5 (~1/8 MFI), поскольку активность NFκB снизилась. Экспрессия GFP все еще наблюдалась в день 19, что может быть связано с длительным полупериодом существования белка GFP (~30 часов) или с базальным уровнем активности NFκB, например, посредством сигнала TCR, CAR, цитокинового рецептора или рецептора фактора роста.
[0104] Фигура 17 является серией графиков, на которых показана опосредованная CAR против ВСМА активация NF-KB индуцируемой экспрессии GFP в присутствии ВСМА+ опухолевых клеток. T-клетки были либо немодифицированными (ложно трансфицированными T-клетками), либо были подвергнуты нуклеофекции вектором piggyBac, экспрессирующим CAR против BCMA и ген мутеина DHFR под контролем EF1a промотора наряду с отсутствием (без контроля GES) или присутствием NF-KB индуцируемой системы экспрессии, направляющей экспрессию GFP в прямой (pNFKB-GFP forward) или обратной ориентации (pNFKB-GFP reverse). Все клетки культивировали в течение 22 дней, с или без селекции метотрексатом (ложно трансфицированные T-клетки), пока клетки почти полностью не переходили в состояние покоя. Затем клетки стимулировали в течение 3 дней в отсутствие (без стимуляции) или в присутствии BCMA- (K562), BMCA+ (RPMI 8226) или активирующего реагента против CD3 и против CD28 (стимуляция CD3/28) в качестве положительного контроля. Экспрессию GFP не обнаруживали ни при каких условиях с контролем без GES или с ложно трансфицированными T-клетками. Впрочем, хотя pNFKB-GFP forward и reverse-транспонированные клетки демонстрировали небольшую экспрессию GFP по сравнению с контролем без стимуляции при культивировании с клетками BCMA-K562, они демонстрировали существенное усиление экспрессии генов либо в присутствии опухолевых клеток BCMA+, либо в условиях положительного контроля. Небольшое различие в экспрессии GFP наблюдалось между pNFKB-GFP forward и reverse-транспонированными клетками, которые совместно культивировали с BCMA+ опухолевыми клетками.
[0105] Фигура 18 является серией графиков, на которых показано, что уровень экспрессии индуцируемого гена может регулироваться количеством элементов ответа, предшествующих промотору. T-клетки подвергали нуклеофекции вектором piggyBac, кодирующим CARTирин против BCMA, за которым следует селективный ген, при этом оба из них находятся под контролем промотора EF1a человека. Кроме того, векторы либо дополнительно кодировали кондиционно NF-KB индуцируемую систему экспрессии генов, направляющую экспрессию усеченного белка CD19 (dCD19), и вводили ряд элементов ответа NFKB (RE), варьирующих от 0 до 5, без GES (Без GES), либо делали электропорацию, но без нуклеиновой кислоты piggyBac (ложно трансфицированные). Данные показаны только для GES в обратном (противоположном) направлении/ориентации. Все клетки культивировали в течение 18 дней и включали отбор T-клеток, модифицированных piggyBac, при использовании добавления метотрексата. Затем клетки стимулировали в течение 3 дней с использованием гранул активирующего реагента против CD3 против CD28 и оценивали поверхностную экспрессию dCD19 с помощью FACS в дни 0, 3 и 18, данные представлены в виде гистограмм FACS и значений MFI при окрашивании белка-мишени. Поверхностную экспрессию dCD19 детектировали на низких уровнях в день 0 во всех T-клетках, транспонированных векторами, кодирующими GES. Через 3 дня после стимуляции наблюдали существенное повышение экспрессии dCD19 для всех T-клеток, экспрессирующих GES, с более высоким кратным увеличением поверхностной экспрессии у клеток с более высоким количеством RE. Таким образом, поверхностная экспрессия dCD19 была прямо пропорциональна количеству RE, кодируемых в GES. DCD19 не был обнаружен на поверхности T-клеток, которые не несут GES: контроль GES и ложно трансфицированный контроль.
[0106] Фигура 19 является схематическим изображением карты конструкции Csy4-T2A-Clo051-G4Sлинкер-dCas9 (Вариант осуществления 2).
[0107] Фигура 20 является схематическим изображением карты конструкции pRT1-Clo051-dCas9 Двойной NLS (Вариант осуществления 1).
[0108] Фигура 21 является парой графиков, на которых сравнивается эффективность нокаута экспрессии B2M в пан-T-клетках (слева) или α-цепи T-клеточного рецептора в клетках Jurkat (справа) либо для Варианта осуществления 1 (pRT1-Clo051-dCas9 Двойной NLS, как показано в Фигуре 20), либо для Варианта осуществления 2 (Csy4-T2A-Clo051-G4Sлинкер-dCas9, как показано на Фигуре 19) слитого белка Cas-Clover согласно изобретению. На графика справа слитый белок представлен в количестве 10 мкг или 20 мкг, как указано.
[0109] Фигура 22 является фотографией гель-электрофореза мРНК в присутствии каждого из Варианта осуществления 1 (pRT1-Clo051-dCas9 Двойной NLS, как показано на Фигуре 20) и Варианта осуществления 2 (Csy4-T2A-Clo051-G4Sлинкер-dCas9, как показано на Фигуре 19). Как показано, оба эффективно вызывают нокдаун экспрессии мРНК.
[0110] Фигура 23 является диаграммой платформы получения человеческих антител из тяжелой цепи UniRatTM.
[0111] Фигура 24 является диаграммой процесса иммунизации, выделения B-клеток, очистки мРНК, секвенирования следующего поколения (NGS), биоинформационного анализа, высокопроизводительной сборки векторов и высокопроизводительной экспрессии и скрининга, используемых для идентификации полного антигенспецифического репертуара антител из тяжелой цепи, полученных с применением UniRatTM после иммунизации. Уникальные способы сборки генов позволяют преобразовывать информацию о последовательности репертуара антител в большие коллекции полностью человеческих антител из тяжелой цепи, которые можно подвергнуть скринингу на различные функции.
[0112] Фигура 25 является парой тепловых карт, на которых показано, как анализ методом секвенирования следующего поколения (NGS) позволяет обнаружить расширенные линии последовательностей VH. Степень красного (высокий) или синего (низкий) цветов на тепловой карте указывает на расширенные семейства последовательностей VH в результате иммунизации. Некоторые последовательности VH с высоким рейтингом уникальны для одного животного. Другие последовательности VH с высоким рейтингом появляются больше чем у одного животного, что указывает на конвергентный отбор таких семейств последовательностей.
[0113] Фигура 26 представляет собой серию диаграмм проточной цитометрии, на которых показано, что популяция CAR-T, экспрессирующая P-PSMA-101 и содержащая смесь TSCM/TCM, дает CAR+ TCM, TEM и Teff для атаки солидной опухоли. После элиминации солидной опухоли популяция CAR-T+ TSCM персистирует. Хотя это продемонстрировано с CARTирином, данный принцип, показанный здесь, применим к популяциям VCAR+ TSCM и VCAR+ TCM, описанным в изобретении. В частности, ксенотрансплантатную модель на мышах с использованием экспрессирующей люциферазу клеточной линии LNCaP (LNCaP.luc) получали при подкожной (п/к) инъеции мышам NSG и использовали для оценки in vivo противоопухолевой эффективности CAR (P-PSMA5-101 и P-PSMA8-101) при 'стрессовой' дозе (4×106) суммарных CAR-T клеток. Для этих исследований in vivo все клетки CAR-T были получены с использованием PB доставки плазмиды P-PSMA5-101 или P-PSMA8-101 с использованием процесса производства Poseida. Мышам делали инъекции LNCaP в подмышечную впадину и обрабатывали при развитии опухолей (100-300 мм3 при измерении штангенциркулем). Мышам вводили 'стрессовую' дозу (4×106) P-PSMA-101 путем внутривенной инъекции, чтобы выявить любые возможные различия в эффективности между CAR-рецепторами PSMA5 и PSMA8. Противоопухолевую активность оценивали по выживаемости, экспансии и обнаружению CD8+ T-клеток в крови, по оценке объема опухоли путем измерения штангенциркулем и по биолюминесценции LNCaP опухоли. P-PSMA5-101 и P-PSMA8-101 в 'стрессовой' дозе продемонстрировали значимо повышенную противоопухолевую эффективность и выживаемость по сравнению с мышами, получавшими контрольные T-клетки (без CAR), против развившихся п/к солидных опухолей LNCaP.luc у мышей NSG. В частности, отсутствовала выживаемость у животных, получавших контрольные T-клетки (без CAR), присутствовала выживаемость 25% в группе, получавшей P-BCMA-101, выживаемость 75% в группе, получавшей P-PSMA5-101, и 100% выживаемость у животных, получавших 'стрессовую' дозу P-PSMA8-101. В периферической крови P-PSMA5-101 и P-PSMA8-101 размножались и давали дифференцированные эффекторные CARTирин+ T-клетки, что сопровождалось снижением опухолевой нагрузки ниже пределов, определяемых с помощью штангенциркуля и визуалиации биолюминесценции. Затем количество этих клеток снижалось, но сохранялось их персистирование в периферической крови.
ПОДРОБНОЕ ОПИСАНИЕ
[0114] В изобретении предложены химерные антигенные рецепторы (CAR-рецепторы), включающие по меньшей мере один VHH (VCAR). Химерные антигенные рецепторы согласно изобретению могут включать больше одного VHH. Например, биспецифичный VCAR может включать два VHH, которые специфично связывают два разных антигена.
[0115] Белки VHH согласно изобретению специфично связываются с антигеном. Химерные антигенные рецепторы согласно изобретению, включающие один или более VHH, которые специфично связывают антиген, могут применяться для направления специфичности клетки (например, цитотоксической иммуной клетки) против специфического антигена.
[0116] В изобретении предложены химерные антигенные рецепторы (CAR-рецепторы), область распознавания антигена которых включает однодоменное антитело (VCAR-рецепторы). В некоторых вариантах осуществления однодоменное антитело является VHH антителом. В некоторых вариантах осуществления однодоменное антитело является VH антителом.
[0117] Химерные антигенные рецепторы согласно изобретению могут включать сигнальный пептид человеческого CD2, CD3δ, CD3ε, CD3γ, CD3ζ, CD4, CD8α, CD19, CD28, 4-1BB или GM-CSFR. Шарнирный/спейсерный домен согласно изобретению может включать шарнир/спейсер/стебель человеческого CD8α, IgG4 и/или CD4. Внутриклеточный домен или эндодомен согласно изобретению могут включать внутриклеточный сигнальный домен человеческого CD3ζ и могут дополнительно включать внутриклеточный сегмент человеческого 4-1BB, CD28, CD40, ICOS, MyD88, OX-40 или их любую комбинацию. Примерные трансмембранные домены включают, без ограничения перечисленными, трансмембранный домен человеческого CD2, CD3δ, CD3ε, CD3γ, CD3ζ, CD4, CD8α, CD19, CD28, 4-1BB или GM-CSFR.
[0118] В изобретении предложены генетически модифицированные клетки, такие как T-клетки, NK-клетки, гемопоэтические клетки-предшественники, T-клетки из периферической крови (PB) (включая T-клетки или Г-КСФ-мобилизованной периферической крови), T-клетки из пуповинной крови (UCB), сделанные специфичными к одному или более антигенам путем введения в эти клетки VCAR согласно изобретению. Клетки согласно изобретению могут быть модифицированы путем электропереноса транспозона, кодирующего VCAR согласно изобретению, и плазмиды, включающей последовательность, кодирующую транспозазу согласно изобретению (предпочтительно, последовательность, кодирующая транспозазу согласно изобретению, является последовательностью мРНК).
VH согласно изобретению
[0119] В изобретении предложены химерные антигенные рецепторы (CAR-рецепторы), включающие однодоменное антитело (VCAR-рецепторы). В некоторых вариантах осуществления однодоменное антитело включает VH. В некоторых вариантах осуществления VH выделен или получен из человеческой последовательности. В некоторых вариантах осуществления VH включает человеческую CDR-последовательность и/или человеческую каркасную последовательность, и нечеловеческую или гуманизированную последовательность (например, крысиный Fc-домен). В некоторых вариантах осуществления VH является полностью гуманизированным VH. В некоторых вариантах осуществления VH не является ни природным антителом, ни фрагментом природного антитела. В некоторых вариантах осуществления VH не является фрагментом моноклонального антитела. В некоторых вариантах осуществления VH является антителом UniDabTM (TeneoBio).
[0120] В некоторых вариантах осуществления VH полностью сконструирован при использовании системы UniRatTM (TeneoBio) и "открытие, основанном на NGS", с получением VH. При использовании этого метода, специфические VH не встречаются в природе и созданы с помощью полностью сконструированных систем. VH не получены из природных моноклональных антител (мАт), которые были либо выделены непосредственно у хозяина (например, мыши, крысы или человека), либо непосредственно из одиночного клона клеток или линии клеток (гибридомы). Такие VH не были затем клонированы из указанных клеточных линий. Вместо этого последовательности VH полностью сконструированы при ипользовании системы UniRatTM в качестве трансгенов, которые включают человеческие вариабельные области (VH-домены) с крысиным Fc-доменом и являются, таким образом, химерными человеческими/крысиными конструкциями без легкой цепи и не похожи на стандартный формат мАт. Нативные крысиные гены подвергнуты нокауту, и единственные антитела, экспрессирующиеся у крысы, получены с трансгенов с доменами VH, соединенными с крысиным Fc (UniAbs). Это единственные Ат, экспрессирующиеся в UniRat. Секвенирование следующего поколения (NGS) и биоинформатику используют для идентификации полного антигенспецифического репертуара антител из тяжелых цепей, получаемых с помощью UniRatTM после иммунизации. Затем используют уникальный способ сборки генов для преобразования информации о последовательности репертуара антитела в большие коллекции полностью человеческих антител из тяжелых цепей, которые можно подвергать скринингу in vitro на различные функции. В некоторых вариантах осуществления полностью гуманизированный VH получают путем слияния человеческих VH-доменов с человеческими Fc in vitro (с получением не встречающегося в природе рекомбинантного VH антитела). В некоторых вариантах осуществления VH полностью гуманизированы, но они экспрессируются in vivo в виде человеческой/крысиной химерной конструкции (VH человека, крысиный Fc) без легкой цепи. Полностью гуманизированные VH, которые экспрессируются in vivo в виде человеческой/крысиной химерной конструкции (VH человека, Fc крысы) без легкой цепи, имеют размер 80 кДа (а не 150 кДа).
[0121] VCAR-рецепторы согласно изобретению могут включать по меньшей мере один VH согласно изобретению. В некоторых вариантах осуществления VH согласно изобретению может быть модифицирован с удалением Fc-домена или его части. В некоторых вариантах осуществления каркасная последовательность VH согласно изобретению может быть модифицирована, например, для улучшения экспрессии, снижения иммуногенности или улучшения функции.
Примерные VCAR-рецепторы согласно изобретению
[0122] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, VCAR включает по меньшей мере одну аминокислотную последовательность, обладающую по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентичностью с аминокислотной последовательностью:
VH-A:
malpvtalllplalllhaarpevqllesggglvqpggslrlscaasgftfssyamnwvrqapgkglewvagiigsggstyyadsvkgrfsisrdnskntldlqmnslraedtavyycvkdwnttmitergqgtlvtvsstttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (SEQ ID NO:18000).
[0123] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению аминокислотная последовательность VCAR кодируется нуклеотидной последовательностью, включающей последовательность, обладающую по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентичностью с нуклеотидной последовательностью:
VH-A:
atggctctgcctgtgacagctctgctgctgcctctggctctgcttcttcatgcggcgcgccctgaagttcagctgcttgaatctggcggaggcctggttcaacctggcggatctctgagactgagctgtgccgccagcggcttcacctttagcagctacgccatgaactgggtccgacaggcccctggcaaaggactggaatgggtggccggaatcatcggcagcggcggcagcacatattacgccgattctgtgaagggccgcttcagcatcagccgggacaacagcaagaacaccctggacctgcagatgaacagcctgagagccgaggataccgccgtgtactactgcgtgaaggattggaacaccaccatgatcaccgagagaggccagggcacactggtcaccgtgtcctctacaacaacaccggcgcctcggcctccaacaccagctcctacaatcgcgagtcagcccctgtctctcagacccgaagcctgtagacctgctgctggcggagctgtgcataccagaggactggatttcgcctgcgacatctacatctgggctcctctggctggcacatgcggagttttgctgctgagcctggtcatcaccctgtactgtaagagaggcaggaagaagctgctgtatatcttcaagcagcccttcatgagacccgtgcagaccacacaggaggaggacggctgctcttgtaggttcccagaggaggaggagggaggatgcgagctgcgcgtgaagtttagccggtccgccgatgcacctgcatacaagcagggacagaaccagctgtataacgagctgaatctgggccggagagaggagtacgacgtgctggataagaggcggggccgggaccccgagatgggaggcaagcctcggagaaagaacccacaggagggcctgtacaatgagctgcaaaaggacaagatggccgaggcctattctgagatcggcatgaagggagagaggcgccggggcaagggacacgatggcctgtaccagggcctgagcaccgccacaaaggacacctatgatgccctgcacatgcaggccctgccccctagatga(SEQ ID NO:18001).
[0124] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, VCAR включает по меньшей мере одну аминокислотную последовательность, обладающую по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентичностью с аминокислотной последовательностью:
VH-B:
malpvtalllplalllhaarpevqllesggglvqpggsltlscaasgftfsnyamnwvrqapgkglewvsgiigsgattyyadsvkgrftisrdnskntlnlqmnslraedtaiyycvkdwnttmitergqgtlvtvsstttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (SEQ ID NO:18002).
[0125] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, аминокислотная последовательность VCAR кодируется нуклеотидной последовательностью, включающей последовательность, обладающую по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентичностью с нуклеотидной последовательностью:
VH-B
atggctctgcctgtgacagctctgctgctgcctctggctctgcttcttcatgcggcgcgccctgaagttcagctgcttgaatctggcggaggcctggttcaacctggcggatctctgacactgagctgtgccgccagcggcttcaccttcagcaactacgccatgaactgggtccgacaggcccctggcaaaggccttgaatgggtgtccggcatcattggctctggcgccaccacctactacgccgattctgtgaagggcagattcaccatcagccgggacaacagcaagaacaccctgaacctgcagatgaacagcctgagagccgaggacaccgccatctactactgcgtgaaggactggaacaccaccatgatcaccgagagaggccagggcacactggtcaccgtgtcctctacaacaacaccggcgcctcggcctccaacaccagctcctacaatcgcgagtcagcccctgtctctcagacccgaagcctgtagacctgctgctggcggagctgtgcataccagaggactggatttcgcctgcgacatctacatctgggctcctctggctggcacatgcggagttttgctgctgagcctggtcatcaccctgtactgtaagagaggcaggaagaagctgctgtatatcttcaagcagcccttcatgagacccgtgcagaccacacaggaggaggacggctgctcttgtaggttcccagaggaggaggagggaggatgcgagctgcgcgtgaagtttagccggtccgccgatgcacctgcatacaagcagggacagaaccagctgtataacgagctgaatctgggccggagagaggagtacgacgtgctggataagaggcggggccgggaccccgagatgggaggcaagcctcggagaaagaacccacaggagggcctgtacaatgagctgcaaaaggacaagatggccgaggcctattctgagatcggcatgaagggagagaggcgccggggcaagggacacgatggcctgtaccagggcctgagcaccgccacaaaggacacctatgatgccctgcacatgcaggccctgccccctagatgac (SEQ ID NO:18003).
[0126] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, VCAR включает по меньшей мере одну аминокислотную последовательность, обладающую по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентичностью с аминокислотной последовательностью:
VH-C:
malpvtalllplalllhaarpevqllesggglvqpgeslrlscaasgftfsnyamnwvrqapgkglewvsgivggggtsyyadsvrgrftisrdnskntlylqmnslraedtavyycvkdwnttmitergqgtlvtvsstttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (SEQ ID NO:18004).
[0127] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, аминокислотная последовательность VCAR кодируется нуклеотидной последовательностью, включающей последовательность, обладающую по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентичностью с нуклеотидной последовательностью VH-C:
atggctctgcctgtgacagctctgctgctgcctctggctctgcttcttcatgcggcgcgccctgaagttcagctgcttgaatctggcggaggcctggttcagcctggcgaatctctgagactgagctgtgccgccagcggcttcaccttcagcaactacgccatgaactgggtccgacaggcccctggcaaaggccttgaatgggtgtccggaatcgttggcggcggaggcacaagctactacgccgattctgtgcggggcagattcaccatcagccgggacaacagcaagaacaccctgtacctgcagatgaacagcctgagagccgaggacaccgccgtgtactactgcgtgaaggactggaacaccaccatgatcaccgagagaggccagggcacactggtcaccgtgtcctctacaacaacaccggcgcctcggcctccaacaccagctcctacaatcgcgagtcagcccctgtctctcagacccgaagcctgtagacctgctgctggcggagctgtgcataccagaggactggatttcgcctgcgacatctacatctgggctcctctggctggcacatgcggagttttgctgctgagcctggtcatcaccctgtactgtaagagaggcaggaagaagctgctgtatatcttcaagcagcccttcatgagacccgtgcagaccacacaggaggaggacggctgctcttgtaggttcccagaggaggaggagggaggatgcgagctgcgcgtgaagtttagccggtccgccgatgcacctgcatacaagcagggacagaaccagctgtataacgagctgaatctgggccggagagaggagtacgacgtgctggataagaggcggggccgggaccccgagatgggaggcaagcctcggagaaagaacccacaggagggcctgtacaatgagctgcaaaaggacaagatggccgaggcctattctgagatcggcatgaagggagagaggcgccggggcaagggacacgatggcctgtaccagggcctgagcaccgccacaaaggacacctatgatgccctgcacatgcaggccctgccccctagatga (SEQ ID NO:18005).
[0128] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, VCAR включает по меньшей мере одну аминокислотную последовательность, обладающую по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентичностью с аминокислотной последовательностью:
VH-D:
malpvtalllplalllhaarpevqllesggglvqpggslrlscaasgftfsnyamtwirqapgkglewvsgitgdggstfyadsvkgrftisrdnskntlylqmnslraedtavyycvkdwnttmitergqgtlvtvsstttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (SEQ ID NO:18006).
[0129] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, аминокислотная последовательность VCAR кодируется нуклеотидной последовательностью, включающей последовательность, обладающую по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентичностью с нуклеотидной последовательностью:
VH-D
atggctctgcctgtgacagctctgctgctgcctctggctctgcttcttcatgcggcgcgccctgaagttcagctgcttgaatctggcggaggcctggttcaacctggcggatctctgagactgagctgtgccgccagcggcttcaccttcagcaattacgccatgacctggatcagacaggcccctggcaaaggcctggaatgggtgtccggaattacaggcgacggcggcagcaccttttacgccgattctgtgaagggcagattcaccatcagccgggacaacagcaagaacaccctgtacctgcagatgaacagcctgagagccgaggacaccgccgtgtactactgcgtgaaggactggaacaccaccatgatcaccgagagaggccagggcacactggtcaccgtgtcctctacaacaacaccggcgcctcggcctccaacaccagctcctacaatcgcgagtcagcccctgtctctcagacccgaagcctgtagacctgctgctggcggagctgtgcataccagaggactggatttcgcctgcgacatctacatctgggctcctctggctggcacatgcggagttttgctgctgagcctggtcatcaccctgtactgtaagagaggcaggaagaagctgctgtatatcttcaagcagcccttcatgagacccgtgcagaccacacaggaggaggacggctgctcttgtaggttcccagaggaggaggagggaggatgcgagctgcgcgtgaagtttagccggtccgccgatgcacctgcatacaagcagggacagaaccagctgtataacgagctgaatctgggccggagagaggagtacgacgtgctggataagaggcggggccgggaccccgagatgggaggcaagcctcggagaaagaacccacaggagggcctgtacaatgagctgcaaaaggacaagatggccgaggcctattctgagatcggcatgaagggagagaggcgccggggcaagggacacgatggcctgtaccagggcctgagcaccgccacaaaggacacctatgatgccctgcacatgcaggccctgccccctagatga (SEQ ID NO:18007).
[0130] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, VCAR включает по меньшей мере одну аминокислотную последовательность, обладающую по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентичностью с аминокислотной последовательностью:
VH-E:
malpvtalllplalllhaarpevqllesggglaqpggslrlscaasgftfssyamnwirqapgkglewvsgisgsggstyyadsvkgrftisrdnskntvylqmnslraedtavyycvkdwnttmitergqgtlvtvsstttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (SEQ ID NO:18008).
[0131] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, аминокислотная последовательность VCAR кодируется нуклеотидной последовательностью, включающей последовательность, обладающую по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентичностью с нуклеотидной последовательностью:
VH-E
atggcactgcctgtgacagccctgctgctgcctctggccctgctgctgcacgcagcacggcccgaggtgcagctgctggagtccggaggaggcctggcccagcctggcggcagcctgaggctgtcctgcgccgcctctggcttcacctttagctcctacgccatgaactggatcagacaggcccctggcaagggcctggagtgggtgtccggcatctccggctctggaggctctacatactatgccgacagcgtgaagggccggttcaccatcagcagagataactccaagaataccgtgtacctccagatgaactctctgcgggccgaggacaccgccgtgtactattgcgtgaaggattggaataccacaatgatcacagagaggggccagggcaccctggtgacagtgtctagcaccacaacccctgcccccagacctcccacacccgcccctaccatcgcgagtcagccactgtccctgcggcctgaggcctgccggcccgccgccggcggagcagtgcacacacggggcctggactttgcctgtgacatctacatatgggcaccactggcaggaacctgcggcgtgctgctgctgagcctggtcatcaccctgtactgtaagagaggcaggaagaagctgctgtatatcttcaagcagcccttcatgagacccgtgcagaccacacaggaggaggacggctgctcttgtaggttcccagaggaggaggagggaggatgcgagctgcgcgtgaagtttagccggtccgccgatgcacctgcatacaagcagggacagaaccagctgtataacgagctgaatctgggccggagagaggagtacgacgtgctggataagaggcggggccgggaccccgagatgggaggcaagcctcggagaaagaacccacaggagggcctgtacaatgagctgcaaaaggacaagatggccgaggcctattctgagatcggcatgaagggagagaggcgccggggcaagggacacgatggcctgtaccagggcctgagcaccgccacaaaggacacctatgatgccctgcacatgcaggccctgccccctagatga (SEQ ID NO:18009).
[0132] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, VCAR включает по меньшей мере одну аминокислотную последовательность, обладающую по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентичностью с аминокислотной последовательностью:
VH-F:
malpvtalllplalllhaarpevqllesggglvqpgrslrlscaasgftftnyamnwvrqapgkglewvsgisggggstyyadsvkgrftisrdnskntlylqmnslraedtavyycvkdwnttmitergqgtlvtvsstttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (SEQ ID NO:18010).
[0133] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, аминокислотная последовательность VCAR кодируется нуклеотидной последовательностью, включающей последовательность, обладающую по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентичностью с нуклеотидной последовательностью:
VH-F
atggcactgcctgtgacagccctgctgctgcctctggccctgctgctgcacgcagcacggcccgaggtgcagctgctggagtctggaggaggcctggtgcagcccggccggtccctgagactgtcttgcgccgccagcggcttcacctttacaaactacgccatgaattgggtgcggcaggcccctggcaagggcctggagtgggtgtctggcatcagcggaggaggaggcagcacctactatgcagactccgtgaagggcaggttcaccatctcccgcgataactctaagaatacactgtacctccagatgaacagcctgagggcagaggacaccgccgtgtactattgcgtgaaggattggaataccacaatgatcacagagaggggacagggcaccctggtgaccgtgagcagcaccacaacccctgcccccagacctcccacacccgcccctaccatcgcgagtcagccactgtccctgcggcctgaggcctgccggcccgccgccggcggagcagtgcacacacggggcctggactttgcctgtgacatctacatatgggcaccactggcaggaacctgcggcgtgctgctgctgagcctggtcatcaccctgtactgtaagagaggcaggaagaagctgctgtatatcttcaagcagcccttcatgagacccgtgcagaccacacaggaggaggacggctgctcttgtaggttcccagaggaggaggagggaggatgcgagctgcgcgtgaagtttagccggtccgccgatgcacctgcatacaagcagggacagaaccagctgtataacgagctgaatctgggccggagagaggagtacgacgtgctggataagaggcggggccgggaccccgagatgggaggcaagcctcggagaaagaacccacaggagggcctgtacaatgagctgcaaaaggacaagatggccgaggcctattctgagatcggcatgaagggagagaggcgccggggcaagggacacgatggcctgtaccagggcctgagcaccgccacaaaggacacctatgatgccctgcacatgcaggccctgccccctagatga (SEQ ID NO:18011).
[0134] В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, VCAR включает последовательность, кодирующую VH-A VH-B, VH-C, VH-D, VH-E или VH-F. В некоторых вариантах осуществления VCAR-рецепторов согласно изобретению, VCAR включает две последовательности, кодирующие VH-A, VH-B, VH-C, VH-D, VH-E или VH-F.
Иммунные клетки и иммунные клетки-предшественники
[0135] В некоторых вариантах осуществления изобретения иммунные клетки согласно изобретению включают лимфоидные клетки-предшественники, естественные киллерные клетки (NK), T-лимфоциты (T-клетки), T-клетки стволовой памяти (TSCM-клетки), T-клетки центральной памяти (TCM), подобные стволовым клеткам T-клетки, B-лимфоциты (B-клетки), миелоидные клетки-предшественники, нейтрофилы, базофилы, эозинофилы, моноциты, макрофаги, тромбоциты, эритроциты, мегакариоциты или остеокласты.
[0136] В некоторых вариантах осуществления иммунные клетки-предшественники включают любые клетки, которые могут дифференцироваться в иммуные клетки одного или нескольких типов. В некоторых вариантах осуществления иммунные клетки-предшественники включают мультипотентные стволовые клетки, которые могут самообновляться и развиваться в иммуные клетки. В некоторых вариантах осуществления иммунные клетки-предшественники включают гемопоэтические стволовые клетки (HSC) или их потомство. В некоторых вариантах осуществления иммунные клетки-предшественники включают клетки-предшественники, которые могут развиваться в иммуные клетки. В некоторых вариантах осуществления иммунные клетки-предшественники включают гемопоэтические клетки-предшественники (HPC).
Гемопоэтические стволовые клетки (HSC)
[0137] Гемопоэтические стволовые клетки (HSC) являются мультипотентными, самообновляющимися клетками. Все дифференцируемые клетки крови из лимфоидных и миелоидных линий дифференцировки образуются из HSC. HSC могут быть обнаружены в зрелом костном мозге, периферической крови, мобилизованной периферической крови, сливаемом растворе перитонеального диализа и пуповинной крови.
[0138] HSC согласно изобретению могут быть выделены или получены из первичной или культивируемой стволовой клетки. HSC согласно изобретению могут быть выделены или получены из эмбриональной стволовой клетки, мультипотентной стволовой клетки, плюрипотентной стволовой клетки, зрелой стволовой клетки или индуцированной плюрипотентной стволовой клетки (иПСК).
[0139] Иммунные клетки-предшественники согласно изобретению могут включать HSC или клетку, происходящую из HSC. Примерные происходящие из HSC клетки согласно изобретению включают, без ограничения перечисленными, мультипотентные стволовые клетки, лимфоидные клетки-предшественники, естественные киллерные клетки (NK), T-лимфоциты (T-клетки), B-лимфоциты (B-клетки), миелоидные клетки-предшественники, нейтрофилы, базофилы, эозинофилы, моноциты и макрофаги.
[0140] HSC, полученные способами согласно изобретению, могут сохранять свойства "примитивных" стволовых клеток, которые, будучи выделенными или полученными из зрелой стволовой клетки и при этом относящимися к одной линии, обладают общими свойствами эмбриональных стволовых клеток. Например, "примитивные" HSC, полученные способами согласно изобретению, сохраняют свою "стволовость" после деления и не дифференцируются. Следовательно, в качестве адоптивной клеточной терапии, "примитивные" HSC, полученные способами согласно изобретению, не только восполняют свое количество, но и размножаются in vivo. "Примитивные" HSC, полученные способами согласно изобретению, могут быть терапевтически эффективными при введении в виде однократной дозы. В некоторых вариантах осуществления примитивные HSC согласно изобретению являются CD34+. В некоторых вариантах осуществления изобретения примитивные HSC являются CD34+ и CD38-. В некоторых вариантах осуществления изобретения примитивные HSC представляют собой CD34+, CD38- и CD90+. В некоторых вариантах осуществления изобретения примитивные HSC являются CD34+, CD38-, CD90+ и CD45RA-. В некоторых вариантах осуществления изобретения примитивные HSC являются CD34+, CD38-, CD90+, CD45RA- и CD49f+. В некоторых вариантах осуществления большинство примитивных HSC согласно изобретению являются CD34+, CD38-, CD90+, CD45RA- и CD49f+.
[0141] В некоторых вариантах осуществления согласно изобретению примитивные HSC, HSC и/или клетки, происходящие из HSC, могут быть модифицированы согласно способам изобретения для экспрессии экзогенной последовательности (например, химерного антигенного рецептора или терапевтического белка). В некоторых вариантах осуществления согласно изобретению модифицированные примитивные HSC, модифицированные HSC и/или модифицированные клетки, происходящие из HSC, могут быть подвергнуты дифференцировке с получением модифицированной иммуной клетки, включающей, без ограничения перечисленными, модифицированную T-клетку, модифицированную NK-клетку и/или модифицированную B-клетку согласно изобретению.
T-клетки
[0142] Модифицированные T-клетки согласно изобретению могут быть получены из модифицированных гемопоэтических стволовых клеток и клеток-предшественников (HSPC) или модифицированных HSC.
[0143] В отличие от традиционных биологических и химиотерапевтических средств, модифицированные T-клетки согласно изобретению обладают способностью быстро размножаться при распознавании антигена, что потенциально исключает необходимость в повторных обработках. Для достижения этого в некоторых вариантах осуществления модифицированные T-клетки согласно изобретению не только направляют первичный ответ, но также персистируют у пациента в виде стабильной популяции жизнеспособных T-клеток памяти для предотвращения возможных рецидивов. В альтернативе, в некоторых вариантах осуществления, когда это нежелательно, модифицированные T-клетки согласно изобретению не персистируют у пациента.
[0144] Интенсивные усилия были сосредоточены на разработке молекул антигенных рецепторов, которые не вызывают истощения T-клеток в результате антиген-независимой (тонической) передачи сигналов, а также на получении модифицированных T-клеток, содержащих ранние T-клетки памяти, в особенности стволовые клетки памяти (TSCM) или подобные стволовым клеткам T-клетки. Подобные стволовым клеткам модифицированные T-клетки согласно изобретению демонстрируют наибольшую способность к самообновлению и мультипотентную способность давать T-клетки центральной памяти (TCM) или TCM-подобные клетки, эффекторные T-клетки памяти (TEM) и эффекторные T-клетки (TE), что обеспечивает лучшее удаление опухоли и устойчивое приживление модифицированных T-клеток. Линейный путь дифференцировки может отвечать за образование следующих клеток: наивные T-клетки (TN)>TSCM>TCM>TEM>TE>TTE, где TN является исходной клеткой-предшественником, из которой непосредственно образуется TSCM, которая затем, в свою очередь, непосредственно дает TCM и т.д. Композиции T-клеток согласно изобретению могут содержать одну или несколько каждых исходных субпопуляций T-клеток, в которых наиболее распространенными являются TSCM или TCM (например, TSCM>TCM>TEM>TE>TTE).
[0145] В некоторых вариантах осуществления способов согласно изобретению иммуная клетка-предшественник дифференцируется в или способна к дифференцировке в раннюю T-клетку памяти, подобную стволовой клетке T-клетку, наивные T-клетки (TN), TSCM, TCM, TEM, TE или TTE. В некоторых вариантах осуществления иммуная клетка-предшественник является примитивной HSC, HSC или клеткой, происходящей из HSC согласно изобретению.
[0146] В некоторых вариантах осуществления способов согласно изобретению иммунная клетка является ранней T-клеткой памяти, подобной стволовой клетке T-клеткой, наивными T-клетками (TN), TSCM, TCM, TEM, TE или TTE.
[0147] В некоторых вариантах осуществления способов согласно изобретению иммунная клетка является ранней T-клеткой памяти.
[0148] В некоторых вариантах осуществления способов согласно изобретению иммуная клетка является подобной стволовой клетке T-клеткой.
[0149] В некоторых вариантах осуществления способов согласно изобретению иммуной клеткой является TSCM.
[0150] В некоторых вариантах осуществления способов согласно изобретению иммуной клеткой является TCM.
[0151] В некоторых вариантах осуществления способов согласно изобретению способы позволяют модифицировать и/или способы позволяют получать множество модифицированных T-клеток, где по меньшей мере 2%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент из множества модифицированных T-клеток экспрессируют один или более маркеров клеточной поверхности ранней T-клетки памяти. В некоторых вариантах осуществления множество модифицированных ранних T-клеток памяти включает по меньшей мере одну модифицированную подобную стволовой клетке T-клетку. В некоторых вариантах осуществления множество модифицированных ранних T-лимфоцитов памяти включает по меньшей мере одну модифицированную TSCM. В некоторых вариантах осуществления множество модифицированных ранних T-клеток памяти включает по меньшей мере одну модифицированную TCM.
[0152] В некоторых вариантах осуществления способов согласно изобретению способы позволяют модифицировать и/или способы позволяют получать множество модифицированных T-клеток, где по меньшей мере 2%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент из множества модифицированных T-клеток экспрессируют один или более маркеров клеточной поверхности подобной стволовой клетке T-клетки. В некоторых вариантах осуществления множество модифицированных подобных стволовым клеткам T-клеток включает по меньшей мере одну модифицированную TSCM. В некоторых вариантах осуществления множество модифицированных подобных стволовым клеткам T-клеток включает по меньшей мере одну модифицированную TCM.
[0153] В некоторых вариантах осуществления способов согласно изобретению способы позволяют модифицировать и/или способы позволяют получать множество модифицированных T-клеток, где по меньшей мере 2%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент из множества модифицированных T-клеток экспрессируют один или более маркеров клеточной поверхности стволовой T-клетки памяти (TSCM). В некоторых вариантах осуществления маркеры клеточной поверхности включают CD62L и CD45RA. В некоторых вариантах осуществления маркеры клеточной поверхности включают один или более из CD62L, CD45RA, CD28, CCR7, CD127, CD45RO, CD95, CD95 и IL-2Rβ. В некоторых вариантах осуществления маркеры клеточной поверхности включают один или более из CD45RA, CD95, IL-2Rβ, CCR7 и CD62L.
[0154] В некоторых вариантах осуществления способов согласно изобретению способы позволяют модифицировать и/или способы позволяют получать множество модифицированных T-клеток, где по меньшей мере 2%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент из множества модифицированных T-клеток экспрессируют один или более маркеров клеточной поверхности T-клетки центральной памяти (TCM). В некоторых вариантах осуществления маркеры клеточной поверхности включают один или более из CD45RO, CD95, IL-2Rβ, CCR7 и CD62L.
[0155] В некоторых вариантах осуществления способов согласно изобретению способы позволяют модифицировать и/или способы позволяют получать множество модифицированных T-клеток, где по меньшей мере 2%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент из множества модифицированных T-клеток экспрессируют один или более маркеров клеточной поверхности наивной T-клетки (TN). В некоторых вариантах осуществления маркеры клеточной поверхности включают один или более из CD45RA, CCR7 и CD62L.
[0156] В некоторых вариантах осуществления способов согласно изобретению способы позволяют модифицировать и/или способы позволяют получать множество модифицированных T-клеток, где по меньшей мере 2%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент из множества модифицированных T-клеток экспрессируют один или более маркеров клеточной поверхности эффекторной T-клетки (модифицированной TEFF). В некоторых вариантах осуществления маркеры клеточной поверхности включают один или более из CD45RA, CD95 и IL-2Rβ.
[0157] В некоторых вариантах осуществления способов согласно изобретению способы позволяют модифицировать и/или способы позволяют получать множество модифицированных T-клеток, где по меньшей мере 2%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент из множества модифицированных T-клеток экспрессируют один или более маркеров клеточной поверхности подобной стволовой клетке T-клетки, стволовой T-клетки памяти (TSCM) или T-клетки центральной памяти (TCM).
[0158] В некоторых вариантах осуществления способов согласно изобретению буфер содержит иммунную клетку или ее предшественник. Буфер поддерживает или повышает уровень жизнеспособности клеток и/или подобный стволовому фенотип иммунной клетки или ее предшественника, включая T-клетки. В некоторых вариантах осуществления буфер поддерживает или повышает уровень жизнеспособности клеток и/или подобный стволовому фенотип первичных T-клеток человека до нуклеофекции. В некоторых вариантах осуществления буфер поддерживает или повышает уровень жизнеспособности клеток и/или подобный стволовому фенотип первичных T-клеток человека во время нуклеофекции. В некоторых вариантах осуществления буфер поддерживает или повышает уровень жизнеспособности клеток и/или подобный стволовому фенотип первичных T-клеток человека после нуклеофекции. В некоторых вариантах осуществления буфер содержит одно или более из KCl, MgCl2, ClNa, глюкозы и Ca(NO3)2 в любой абсолютной или относительной представленности или концентрации, и, необязательно, буфер дополнительно содержит добавку, выбранную из группы, состоящей из HEPES, Трис/HCl и фосфатного буфера. В некоторых вариантах осуществления буфер содержит 5 мМ KCl, 15 мМ MgCl2, 90 мМ ClNa, 10 мМ глюкозы и 0,4 мМ Ca(NO3)2. В некоторых вариантах осуществления буфер содержит 5 мМ KCl, 15 мМ MgCl2, 90 мМ ClNa, 10 мМ глюкозы и 0,4 мМ Ca(NO3)2 и добавку, содержащую 20 мМ HEPES и 75 мМ Трис/HCl. В некоторых вариантах осуществления буфер содержит 5 мМ KCl, 15 мМ MgCl2, 90 мМ ClNa, 10 мМ глюкозы и 0,4 мМ Ca(NO3)2 и добавку, содержащую 40 мМ Na2HPO4/NaH2PO4 при pH 7,2. В некоторых вариантах осуществления композиция, содержащая первичные T-клетки человека, содержит 100 мкл буфера и от 5×106 до 25×106 клеток. В некоторых вариантах осуществления композиция содержит масштабируемое соотношение 250×106 первичных человеческих T-клеток на миллилитр буфера или другой среды во время стадии введения.
[0159] В некоторых вариантах осуществления способов согласно изобретению способы включают контакт иммунной клетки согласно изобретению, включая T-клетку согласно изобретению, и композиции для экспансии T-клеток. В некоторых вариантах осуществления способов согласно изобретению этап введения транспозона и/или транспозазы согласно изобретению в иммунную клетку согласно изобретению может дополнительно включать контакт иммунной клетки и композиции для экспансии T-клеток. В некоторых вариантах осуществления, включая варианты осуществления, в которых этап введения способов включает этап электропорации или этап нуклеофекции, этап электропорации или нуклеофекции могут выполнять с композицией для экспансии T-клеток в контакте с иммунными клетками согласно изобретению.
[0160] В некоторых вариантах осуществления способов согласно изобретению композиция для экспансии T-клеток включает, состоит по существу из или состоит из фосфора; одной или более из октановой кислоты, пальмитиновой кислоты, линолевой кислоты и олеиновой кислоты; стерина; и алкана.
[0161] В некоторых вариантах осуществления способов получения модифицированной T-клетки согласно изобретению, добавка для экспансии включает один или более цитокинов. Один или более цитокинов могут включать любой цитокин, в том числе, но не ограничения, лимфокины. Примерные лимфокины включают, без ограничения перечисленным, интерлейкин-2 (IL-2), интерлейкин-3 (IL-3), интерлейкин-4 (IL-4), интерлейкин-5 (IL-5), интерлейкин-6 (IL-6), интерлейкин-7 (IL-7), интерлейкин-15 (IL-15), интерлейкин-21 (IL-21), гранулоцитарно-макрофагальный колониестимулирующий фактор (ГМ-КСФ) и интерферон (INFγ). Один или более цитокинов могут включать IL-2.
[0162] В некоторых вариантах осуществления способов согласно изобретению композиция для экспансии T-клеток включает человеческий сывороточный альбумин, рекомбинантный человеческий инсулин, человеческий трансферрин, 2-меркаптоэтанол и добавку для экспансии. В некоторых вариантах осуществления данного способа композиция для экспансии T-клеток дополнительно включает одно или более из октановой кислоты, никотинамида, 2,4,7,9-тетраметил-5-децин-4,7-диола (TMDD), диизопропиладипата (DIPA), н-бутилбензолсульфонамида, 1,2-бензолдикарбоновой кислоты, бис(2-метилпропилового) сложного эфира, пальмитиновой кислоты, линолевой кислоты, олеиновой кислоты, гидразида стеариновой кислоты, олеамида, стерина и алкана. В некоторых вариантах осуществления данного способа композиция для экспансии T-клеток дополнительно включает одно или более из октановой кислоты, пальмитиновой кислоты, линолевой кислоты, олеиновой кислоты и стерина. В некоторых вариантах осуществления данного способа композиция для экспансии T-клеток дополнительно включает одно или более из октановой кислоты в концентрации от 0,9 до 90 мг/кг, включая конечные значения; пальмитиновой кислота в концентрации от 0,2 до 20 мг/кг, включая конечные точки; линолевая кислота в концентрации от 0,2 мг/кг до 20 мг/кг, включая конечные значения; олеиновой кислоты в концентрации от 0,2 до 20 мг/кг, включая конечные значения; и стерин в концентрации от приблизительно 0,1 мг/кг до 10 мг/кг, включая конечные значения. В некоторых вариантах осуществления данного способа композиция для экспансии T-клеток дополнительно включает одно или более из октановой кислоты в концентрации приблизительно 9 мг/кг, пальмитиновой кислоты в концентрации приблизительно 2 мг/кг, линолевой кислоты в концентрации приблизительно 2 мг/кг, олеиновой кислоты в концентрации приблизительно 2 мг/кг и стерин в концентрации приблизительно 1 мг/кг. В некоторых вариантах осуществления данного способа композиция для экспансии T-клеток дополнительно включает одно или более из октановой кислоты в концентрации от 6,4 мкмоль/кг до 640 мкмоль/кг, включая конечные значения; пальмитиновой кислоты в концентрации от 0,7 мкмоль/кг до 70 мкмоль/кг, включая конечные значения; линолевой кислоты в концентрации от 0,75 мкмоль/кг до 75 мкмоль/кг, включая конечные значения; олеиновой кислоты в концентрации от 0,75 мкмоль/кг до 75 мкмоль/кг, включая конечные значения; и стерина в концентрации от 0,25 мкмоль/кг до 25 мкмоль/кг, включая конечные значения. В некоторых вариантах осуществления данного способа композиция для экспансии T-клеток дополнительно включает одно или более из октановой кислоты в концентрации приблизительно 64 мкмоль/кг, пальмитиновой кислоты в концентрации приблизительно 7 мкмоль/кг, линолевой кислоты в концентрации приблизительно 7,5 мкмоль/кг, олеиновой кислоты в концентрации приблизительно 7,5 мкмоль/кг и стерина в концентрации приблизительно 2,5 мкмоль/кг.
[0163] В некоторых вариантах осуществления композиция для экспансии T-клеток включает одно или более из человеческого сывороточного альбумина, рекомбинантного человеческого инсулина, человеческого трансферрина, 2-меркаптоэтанола и добавки для экспансии для получения множества размноженных модифицированных T-клеток, где по меньшей мере 2% из множества модифицированных T-клеток экспрессируют один или более маркеров клеточной поверхности ранней T-клетки памяти, подобной стволовой клетке T-клетки, стволовой T-клетки памяти (TSCM) и/или T-клетки центральной памяти (TCM). В некоторых вариантах осуществления композиция для экспансии T-клеток включает или дополнительно включает одно или более из октановой кислоты, никотинамида, 2,4,7,9-тетраметил-5-децин-4,7-диола (TMDD), диизопропиладипата (DIPA), н-бутил-бензолсульфонамида, 1,2-бензолдикарбоновой кислоты, бис(2-метилпропилового) сложного эфира, пальмитиновой кислоты, линолевой кислоты, олеиновой кислоты, гидразида стеариновой кислоты, олеамида, стерина и алкана. В некоторых вариантах осуществления композиция для экспансии T-клеток включает одно или более из октановой кислоты, пальмитиновой кислоты, линолевой кислоты, олеиновой кислоты и стерина (например, холестерина). В некоторых вариантах осуществления композиция для экспансии T-клеток включает одно или более из октановой кислоты в концентрации от 0,9 мг/кг до 90 мг/кг, включая конечные значения; пальмитиновой кислоты в концентрации от 0,2 мг/кг до 20 мг/кг, включая конечные значения; линолевой кислоты в концентрации от 0,2 мг/кг до 20 мг/кг, включая конечные значения; олеиновой кислоты в концентрации от 0,2 мг/кг до 20 мг/кг, включая конечные значения; и стерина в концентрации от приблизительно 0,1 мг/кг до 10 мг/кг, включая конечные значения (где мг/кг=миллионные доли). В некоторых вариантах осуществления композиция для экспансии T-клеток включает одно или более из октановой кислоты в концентрации приблизительно 9 мг/кг, пальмитиновой кислоты в концентрации приблизительно 2 мг/кг, линолевой кислоты в концентрации приблизительно 2 мг/кг, олеиновой кислоты в концентрации приблизительно 2 мг/кг и стерина в концентрации приблизительно 1 мг/кг (где мг/кг=миллионные доли). В некоторых вариантах осуществления композиция для экспансии T-клеток включает одно или более из октановой кислоты в концентрации 9,19 мг/кг, пальмитиновой кислоты в концентрации 1,86 мг/кг, линолевой кислоты в концентрации приблизительно 2,12 мг/кг, олеиновой кислоты в концентрации приблизительно 2,13 мг/кг и стерина в концентрации приблизительно 1,01 мг/кг (где мг/кг=миллионные доли). В некоторых вариантах осуществления композиция для экспансии T-клеток включает октановую кислоту в концентрации 9,19 мг/кг, пальмитиновую кислоту в концентрации 1,86 мг/кг, линолевую кислоту в концентрации 2,12 мг/кг, олеиновую кислоту в концентрации приблизительно 2,13 мг/кг и стерин в концентрации 1,01 мг/кг (где мг/кг=миллионные доли). В некоторых вариантах осуществления композиция для экспансии T-клеток включает одно или более из октановой кислоты в концентрации от 6,4 мкмоль/кг и 640 мкмоль/кг, включая конечные значения; пальмитиновой кислоты в концентрации от 0,7 мкмоль/кг до 70 мкмоль/кг, включая конечные значения; линолевой кислоты в концентрации от 0,75 мкмоль/кг до 75 мкмоль/кг, включая конечные значения; олеиновой кислоты в концентрации от 0,75 мкмоль/кг до 75 мкмоль/кг, включая конечные значения; и стерина в концентрации от 0,25 мкмоль/кг до 25 мкмоль/кг, включая конечные значения. В некоторых вариантах осуществления композиция для экспансии T-клеток включает одно или более из октановой кислоты в концентрации приблизительно 64 мкмоль/кг, пальмитиновой кислоты в концентрации приблизительно 7 мкмоль/кг, линолевой кислоты в концентрации приблизительно 7,5 мкмоль/кг, олеиновой кислоты в концентрации приблизительно 7,5 мкмоль/кг и стерина в концентрации приблизительно 2,5 мкмоль/кг. В некоторых вариантах осуществления композиция для экспансии T-клеток включает одно или более из октановой кислоты в концентрации приблизительно 63,75 мкмоль/кг, пальмитиновой кислоты в концентрации приблизительно 7,27 мкмоль/кг, линолевой кислоты в концентрации приблизительно 7,57 мкмоль/кг, олеиновой кислоты в концентрации приблизительно 7,56 мкмоль/кг и стерина в концентрации приблизительно 2,61 мкмоль/кг. В некоторых вариантах осуществления композиция для экспансии T-клеток включает октановую кислоту в концентрации приблизительно 63,75 мкмоль/кг, пальмитиновую кислоту в концентрации приблизительно 7,27 мкмоль/кг, линолевую кислоту в концентрации приблизительно 7,57 мкмоль/кг, олеиновую кислоту в концентрации 7,56 мкмоль/кг и стерин в концентрации 2,61 мкмоль/кг.
[0164] При использовании в настоящем документе термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей одно или более из человеческого сывороточного альбумина, рекомбинантного человеческого инсулина, человеческого трансферрина, 2-меркаптоэтанола и добавки для экспансии при 37°C. В альтернативе или дополнительно, термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей одно или более из фосфора, октановой жирной кислоты, пальмитиновой жирной кислоты, линолевой жирной кислоты и олеиновой кислоты. В некоторых вариантах осуществления среда включает некоторое количество фосфора, которое в 10 раз выше, чем можно найти, например, в средк Дульбекко в модификации Искоува ((IMDM); доступна в каталоге ThermoFisher Scientific под номером 12440053).
[0165] При использовании в настоящем документе термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей одно или более из человеческого сывороточного альбумина, рекомбинантного человеческого инсулина, человеческого трансферрина, 2-меркаптоэтанола, MDM в модификации Искоува и добавки для экспансии при 37°C. В альтернативе или дополнительно, термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей одно или более из следующих элементов: бор, натрий, магний, фосфор, калий и кальций. В некоторых вариантах осуществления термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей одно или более из следующих элементов, присутствующих в соответствующих средних концентрациях: бор в концентрации 3,7 мг/л, натрий в концентрации 3000 мг/л, магний в концентрации 18 мг/л, фосфор в концентрации 29 мг/л, калий в концентрации 15 мг/л и кальций в концентрации 4 мг/л.
[0166] При использовании в настоящем документе термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей одно или более из человеческого сывороточного альбумина, рекомбинантного человеческого инсулина, человеческого трансферрина, 2-меркаптоэтанола и добавки для экспансии при 37°C. В альтернативе или дополнительно, термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей один или более из следующих компонентов: октановая кислота (номер CAS 124-07-2), никотинамид (номер CAS 98-92-0), 2,4,7,9-тетраметил-5-децин-4,7-диол (TMDD) (номер CAS 126-86-3), диизопропиладипат (DIPA) (номер CAS 6938-94-9), н-бутил-бензолсульфонамид (номер CAS 3622-84-2), 1,2-бензолдикарбоновая кислота, бис(2-метилпропиловый) сложный эфир (номер CAS 84-69-5), пальмитиновая кислота (номер CAS 57-10-3), линолевая кислота (номер CAS 60-33-3), олеиновая кислота (номер CAS 112-80-1), гидразид стеариновой кислоты (номер CAS 4130-54-5), олеамид (номер CAS 3322-62-1), стерин (например, холестерин) (номер CAS 57-88-5) и алканы (например, нонадекан) (номер CAS 629-92-5). В некоторых вариантах осуществления термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей один или более из следующих компонентов: октановая кислота (номер CAS 124-07-2), никотинамид (номер CAS 98-92-0), 2,4,7,9-тетраметил-5-децин-4,7-диол (TMDD) (номер CAS 126-86-3), диизопропиладипат (DIPA) (номер CAS 6938-94-9), н-бутил-бензолсульфонамид (номер CAS 3622-84-2), 1,2-бензолдикарбоновая кислота, бис(2-метилпропиловый) сложный эфир (номер CAS 84-69-5), пальмитиновая кислота (номер CAS 57-10-3), линолевая кислота (номер CAS 60-33-3), олеиновая кислота (номер CAS 112-80-1), гидразид стеариновой кислоты (номер CAS 4130-54-5), олеамид (номер CAS 3322-62-1), стерин (например, холестерин) (номер CAS 57-88-5), алканы (например, нонадекан) (номер CAS 629-92-5) и феноловый красный (номер CAS 143-74-8). В некоторых вариантах осуществления термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей один или более из следующих компонентов: октановая кислота (номер CAS 124-07-2), никотинамид (номер CAS 98-92-0), 2,4,7,9-тетраметил-5-децин-4,7-диол (TMDD) (номер CAS 126-86-3), диизопропиладипат (DIPA) (номер CAS 6938-94-9), н-бутил-бензолсульфонамид (номер CAS 3622-84-2), 1,2-бензолдикарбоновая кислота, бис(2-метилпропиловый) сложный эфир (номер CAS 84-69-5), пальмитиновая кислота (номер CAS 57-10-3), линолевая кислота (номер CAS 60-33-3), олеиновая кислота (номер CAS 112-80-1), гидразид стеариновой кислоты (номер CAS 4130-54-5), олеамид (номер CAS 3322-62-1), феноловый красный (номер CAS 143-74-8) и ланолиновый спирт.
[0167] В некоторых вариантах осуществления термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей одно или более из человеческого сывороточного альбумина, рекомбинантного человеческого инсулина, человеческого трансферрина, 2-меркаптоэтанола и добавки для экспансии при 37°C. В альтернативе или дополнительно, термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей один или более из следующих ионов: натрий, аммоний, калий, магний, кальций, хлорид, сульфат и фосфат.
[0168] При использовании в настоящем документе термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей одно или более из человеческого сывороточного альбумина, рекомбинантного человеческого инсулина, человеческого трансферрина, 2-меркаптоэтанола и добавки для экспансии при 37°C. В альтернативе или дополнительно, термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей одну или более из следующих свободных аминокислот: гистидин, аспарагин, серин, глутамат, аргинин, глицин, аспарагиновая кислота, глутаминовая кислота, треонин, аланин, пролин, цистеин, лизин, тирозин, метионин, валин, изолейцин, лейцин, фенилаланин и триптофан. В некоторых вариантах осуществления термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей одну или более из следующих свободных аминокислот в соответствующих средних молярных концентрациях: гистидин (приблизительно 1%), аспарагин (приблизительно 0,5%), серин (приблизительно 1,5%), глутамин (приблизительно 67%), аргинин (приблизительно 1,5%), глицин (приблизительно 1,5%), аспарагиновая кислота (приблизительно 1%), глутаминовая кислота (приблизительно 2%), треонин (приблизительно 2%), аланин (приблизительно 1%), пролин (приблизительно 1,5%), цистеин (приблизительно 1,5%), лизин (приблизительно 3%), тирозин (приблизительно 1,5%), метионин (приблизительно 1%), валин (приблизительно 3,5%), изолейцин (приблизительно 3%), лейцин (приблизительно 3,5%), фенилаланин (приблизительно 1,5%) и триптофан (приблизительно 0,5%). В некоторых вариантах осуществления термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей одну или более из следующих свободных аминокислот в соответствующих средних молярных концентрациях: гистидин (приблизительно 0,78%), аспарагин (приблизительно 0,4%), серин (приблизительно 1,6%), глутамин (приблизительно 67,01%), аргинин (приблизительно 1,67%), глицин (приблизительно 1,72%), аспарагиновая кислота (приблизительно 1,00%), глутаминовая кислота (приблизительно 1,93%), треонин (приблизительно 2,38%), аланин (приблизительно 1,11%), пролин (приблизительно 1,49%), цистеин (приблизительно 1,65%), лизин (приблизительно 2,84%), тирозин (приблизительно 1,62%), метионин (приблизительно 0,85%), валин (приблизительно 3,45%), изолейцин (приблизительно 3,14%), лейцин (приблизительно 3,3%), фенилаланин (приблизительно 1,64%) и триптофан (приблизительно 0,37%).
[0169] При использовании в настоящем документе термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей одно или более из человеческого сывороточного альбумина, рекомбинантного человеческого инсулина, человеческого трансферрина, 2-меркаптоэтанола, MDM в модификации Искоува и добавки для экспансии при 37°C. В альтернативе или дополнительно, термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей одно или более из фосфора, октановой жирной кислоты, пальмитиновой жирной кислоты, линолевой жирной кислоты и олеиновой кислоты. В некоторых вариантах осуществления среда включает некоторое количество фосфора, которое в 10 раз выше, чем можно найти, например, в среде Дульбекко в модификации Искоува ((IMDM); доступна в катологе ThermoFisher Scientific под номером 12440053).
[0170] В некоторых вариантах осуществления термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей одно или более из октановой кислоты, пальмитиновой кислоты, линолевой кислоты, олеиновой кислоты и стерина (например, холестерина). В некоторых вариантах осуществления термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей одно или более из октановой кислоты в концентрации от 0,9 мг/кг до 90 мг/кг, включая конечные значения; пальмитиновой кислоты в концентрации от 0,2 мг/кг до 20 мг/кг, включая конечные значения; линолевой кислоты в концентрации от 0,2 мг/кг до 20 мг/кг, включая конечные значения; олеиновой кислоты в концентрации 0,2 мг/кг до 20 мг/кг, включая конечные значения; и стерина в концентрации от приблизительно 0,1 мг/кг до 10 мг/кг, включая конечные значения (где мг/кг=миллионные доли). В некоторых вариантах осуществления термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей одно или более из октановой кислоты в концентрации приблизительно 9 мг/кг, пальмитиновой кислоты в концентрации приблизительно 2 мг/кг, линолевой кислоты в концентрации приблизительно 2 мг/кг, олеиновой кислоты в концентрации приблизительно 2 мг/кг и стерина в концентрации приблизительно 1 мг/кг (где мг/кг=миллионные доли). В некоторых вариантах осуществления термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей одно или более из октановой кислоты в концентрации 9,19 мг/кг, пальмитиновой кислоты в концентрации 1,86 мг/кг, линолевой кислоты в концентрации приблизительно 2,12 мг/кг, олеиновой кислоты в концентрации приблизительно 2,13 мг/кг и стерина в концентрации приблизительно 1,01 мг/кг (где мг/кг=миллионные доли). В некоторых вариантах осуществления термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей одно или более из октановой кислоты в концентрации 9,19 мг/кг, пальмитиновой кислоты в концентрации 1,86 мг/кг, линолевой кислоты в концентрации 2,12 мг/кг, олеиновой кислоты в концентрации приблизительно 2,13 мг/кг и стерина в концентрации 1,01 мг/кг (где мг/кг=миллионные доли). В некоторых вариантах осуществления термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей одно или более из октановой кислоты в концентрации от 6,4 мкмоль/кг до 640 мкмоль/кг, включая конечные значения; пальмитиновой кислоты в концентрации от 0,7 мкмоль/кг до 70 мкмоль/кг, включая конечные значения; линолевой кислоты в концентрации от 0,75 мкмоль/кг до 75 мкмоль/кг, включая конечные значения; олеиновой кислоты в концентрации от 0,75 мкмоль/кг до 75 мкмоль/кг, включая конечные значения; и стерина в концентрации от 0,25 мкмоль/кг до 25 мкмоль/кг, включая конечные значения. В некоторых вариантах осуществления термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей одно или более из октановой кислоты в концентрации приблизительно 64 мкмоль/кг, пальмитиновой кислоты в концентрации приблизительно 7 мкмоль/кг, линолевой кислоты в концентрации приблизительно 7,5 мкмоль/кг, олеиновой кислоты в концентрации приблизительно 7,5 мкмоль/кг и стерина в концентрации приблизительно 2,5 мкмоль/кг.
[0171] В некоторых вариантах осуществления термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей одно или более из октановой кислоты в концентрации приблизительно 63,75 мкмоль/кг, пальмитиновой кислоты в концентрации приблизительно 7,27 мкмоль/кг, линолевой кислоты в концентрации приблизительно 7,57 мкмоль/кг, олеиновой кислоты в концентрации приблизительно 7,56 мкмоль/кг и стерина в концентрации приблизительно 2,61 мкмоль/кг. В некоторых вариантах осуществления термины "содержащая добавку композиция для экспансии T-клеток" или "композиция для экспансии T-клеток" могут использоваться попеременно со средой, включающей одно или более из октановой кислоты в концентрации приблизительно 63,75 мкмоль/кг, пальмитиновой кислоты в концентрации приблизительно 7,27 мкмоль/кг, линолевой кислоты в концентрации приблизительно 7,57 мкмоль/кг, олеиновой кислоты в концентрации 7,56 мкмоль/кг и стерина в концентрации 2,61 мкмоль/кг.
[0172] В некоторых вариантах осуществления способов получения модифицированной T-клетки (например, подобной стволовой клетке T-клетки, TSCM и/или TCM) согласно изобретению, способ включает контакт модифицированной T-клетки и ингибитора пути P13K-Akt-mTOR. Модифицированные T-клетки согласно изобретению, включая модифицированные подобные стволовой клетке T-клетки, TSCM и/или TCM согласно изобретению, могут инкубировать, культивировать, выращиваться, хранить или иным образом комбинировать на любом этапе в способах процедуры со средой для выращивания, включающей один или более ингибиторов компонента пути PI3K. Примерные ингибиторы компонента пути PI3K включают, без ограничения перечисленными, ингибитор GSK3β, такой как TWS119 (также известный как ингибитор XII GSK 3B; номер CAS 601514-19-6, имеющий химическую формулу C18H14N4O2). Примерные ингибиторы компонента пути PI3K включают, без ограничения перечисленными, bb007 (BLUEBIRDBIOTM). Дополнительные примерные ингибиторы компонента пути PI3K включают, без ограничения перечисленными, аллостерический ингибитор VIII Akt (также называемый как Akti-1/2, имеющий номер соединения 10196499), конкурентные ингибиторы АТФ (ортостерические ингибиторы, направленно воздействующие на АТФ-связывающий карман протеинкиназы B (Akt)), изохинолин-5-сульфонамиды (H-8, H-89 и NL-71-101), производные азепана (A серия структур, полученных из (-)-баланола), аминофуразаны (GSK690693), гетероциклические кольца (7-азаиндол, производные 6-фенилпурина, производные пирроло[2,3-d]пиримидина, CCT128930, 3-аминопирролидин, производные анилинотриазола, производные спироиндолина, AZD5363, ипатасертиб (GDC-0068, RG7440), A-674563 и A-443654), производные Фенилпиразола (AT7867 и AT13148), производные тиофенкарбоксамида (афуресертиб (GSK2110183), производное 2-пиримидил-5-амидотиофена (DC120), упросертиб (GSK2141795)), аллостерические ингибиторы (превосходящие ортостерические ингибиторы и обеспечивающие более высокую специфичность, снижение побочных эффектов и менее выраженное токсическое действие), аналоги 2,3-дифенилхиноксалина (производные 2,3-дифенилхиноксалина, производное триазоло[3,4-f][1,6]нафтиридин-3(2H)-она (MK-2206)), алкилфосфолипиды (эдельфозин (1-O-октадецил-2O-метил-рац-глицеро-3-фосфохолин, ET-18-OCH3), илмофозин (BM 41.440), милтефозин (гексадецилфосфохолин, HePC), перифозин (D-21266), эруцилфосфохолин (ErPC), эруфозин (ErPC3, эруцилфосфогомохолин), аналоги индол-3-карбинола (индол-3-карбинол, 3-хлорацетилиндол, дииндолилметан, диэтил-6-метокси-5,7-дигидроиндоло[2,3-b]карбазол-2,10-дикарбоксилат (SR13668), OSU-A9), производные сульфонамида (ТЕЛ. 316 и PHT-427), производные тиомочевины (PIT-1, PIT-2, DM-PIT-1, N-[(1-метил-1H-пиразол-4-ил)карбонил]-N'-(3-бромфенил)-тиомочевину), производные пурина (трицирибин (TCN, NSC 154020), активный аналог трицирибина монофосфата (TCN-P), производное 4-амино-пиридо[2,3-d]пиримидина API-1, производные 3-фенил-3H-имидазо[4,5-b]пиридина, ARQ 092), BAY 1125976, 3-метилксантин, хинолин-4-карбоксамид и 2-[4-(циклогекса-1,3-диен-1-ил)-1H-пиразол-3-ил]фенол, 3-оксо-тирукалловую кислоту, 3α- и 3β-ацетокси-тирукалловые кислоты, ацетокси-тирукалловую кислоту и необратимые ингибиторы (антибиотики, лактохиномицин, френолицин B, калафунгин, медермицин, Boc-Phe-винилкетон, 4-гидроксиноненаль (4-HNE), производные 1,6-нафтиридинона и производные имидазо-1,2-пиридина).
[0173] В некоторых вариантах осуществления способов получения модифицированной T-клетки (например, подобной стволовой клетке T-клетки, TSCM и/или TCM) согласно изобретению, способ включает контакт модифицированной T-клетки и ингибитора дифференцировки эффекторных T-клеток. Примерные ингибиторы дифференцировки эффекторных T-клеток включают, без ограничения перечисленными, ингибитор BET (например, JQ1, тиенотриазолодиазепин) и/или ингибитор семейства белков BET (например, BRD2, BRD3, BRD4 и BRDT).
[0174] В некоторых вариантах осуществления способов получения модифицированной T-клетки (например, подобной стволовой клетке T-клетки, TSCM и/или TCM) согласно изобретению, способ включает контакт модифицированной T-клетки и средства, понижающие ядерно-цитоплазматический ацетил-КоА. Примерные средства, которые снижают ядерно-цитоплазматический ацетил-КоА, включают, без ограничения перечисленным, 2-гидрокси-цитрат (2-HC), а также средства, повышающие экспрессию Acss1.
[0175] В некоторых вариантах осуществления способов получения модифицированной T-клетки (например, подобной стволовой клетке T-клетки, TSCM и/или TCM) согласно изобретению, способ включает контакт модифицированной T-клетки и композиции, включающей ингибитор гистондеацетилазы (HDAC). В некоторых вариантах осуществления композиция, включающая ингибитор HDAC, включает или состоит из вальпроевой кислоты, натрия фенилбутирата (NaPB) или их комбинации. В некоторых вариантах осуществления композиция, включающая ингибитор HDAC, включает или состоит из вальпроевой кислоты. В некоторых вариантах осуществления композиция, включающая ингибитор HDAC, включает или состоит из натрия фенилбутирата (NaPB).
[0176] В некоторых вариантах осуществления способов получения модифицированной T-клетки (например, подобной стволовой клетке T-клетки, TSCM и/или TCM) согласно изобретению, активирующая добавка может включать один или более цитокинов. Один или более цитокинов могут включать любой цитокин, включающий, без ограничения, лимфокины. Примерные лимфокины включают, без ограничения перечисленными, интерлейкин-2 (IL-2), интерлейкин-3 (IL-3), интерлейкин-4 (IL-4), интерлейкин-5 (IL-5), интерлейкин-6 (IL-6), интерлейкин-7 (IL-7), интерлейкин-15 (IL-15), интерлейкин-21 (IL-21), гранулоцитарно-макрофагальный колониестимулирующий фактор (ГМ-КСФ) и интерферон (INFγ). Один или более цитокинов могут включать IL-2.
[0177] В некоторых вариантах осуществления способов получения модифицированной T-клетки (например, подобной стволовой клетке T-клетки, TSCM и/или TCM) согласно изобретению, активирующая добавка может включать один или более активаторных комплексов. Примерные и неограничивающие активаторные комплексы могут включать комплекс мономерного, димерного, тримерного или тетрамерного антитела, который связывает один или более из CD3, CD28 и CD2. В некоторых вариантах осуществления активирующая добавка включает или состоит из активаторного комплекса, включающего человеческое, гуманизированное или рекомбинантное или химерное антитело. В некоторых вариантах осуществления активирующая добавка включает или состоит из активаторного комплекса, который связывает CD3 и CD28. В некоторых вариантах осуществления активирующая добавка включает или состоит из активаторного комплекса, который связывает CD3, CD28 и CD2.
Естественные киллерные клетки (NK)
[0178] В некоторых вариантах осуществления модифицированные иммунные клетки или иммунные клетки-предшественники согласно изобретению являются естественными киллерными клетками (NK). В некоторых вариантах осуществления NK-клетки являются цитотоксическими лимфоцитами, которые дифференцируются из лимфоидных клеток-предшественников.
[0179] Модифицированные NK-клетки согласно изобретению могут быть получены из модифицированных гемопоэтических стволовых клеток и клеток-предшественников (HSPC) или модифицированных HSC.
[0180] В некоторых вариантах осуществления неактивированные NK-клетки получены из CD3-элиминированного образца лейкофереза (содержащего CD14/CD19/CD56+ клетки).
[0181] В некоторых вариантах осуществления NK-клетки электропорируют при использовании нуклеофектора Lonza 4D или BTX ECM 830 (500 В, длительность импульса 700 мксек, зазор между электродами 0,2 мм, один импульс). Все программы нуклеофектора Lonza 4D рассматриваются как включенные в рамки способов согласно изобретению.
[0182] В некоторых вариантах осуществления 5×106 клеток электропорировали за электропорацию в 100 мкл буфера P3 в кюветах. Впрочем, такое отношение клеток на объем можно масштабировать для коммерческих способов производства.
[0183] В некоторых вариантах осуществления NK-клетки были стимулированы при совместном культивировании с дополнительной клеточной линией. В некоторых вариантах осуществления дополнительная клеточная линия включает искусственные антигенпрезентирующие клетки (иАПК). В некоторых вариантах осуществления стимуляция происходит в день 1, 2, 3, 4, 5, 6 или 7 после электропорации. В некоторых вариантах осуществления стимуляция происходит в день 2 после электропорации.
[0184] В некоторых вариантах осуществления NK-клетки экспрессируют CD56.
B-клетки
[0185] В некоторых вариантах осуществления модифицированные иммунные клетки или иммунные клетки-предшественники согласно изобретению являются B-клетками. B-клетки представляют собой тип лимфоцитов, которые экспрессируют B-клеточные рецепторы на своей поверхности. B-клеточные рецепторы связываются со специфическими антигенами.
[0186] Модифицированные B-клетки согласно изобретению могут быть получены из модифицированных гемопоэтических стволовых клеток и клеток-предшественников (HSPC) или модифицированных HSC.
[0187] В некоторых вариантах осуществления HSPC модифицированы с применением способов согласно изобретению, и затем примированы для B-клеточной дифференцировки в присутствии человеческого IL-3, Flt3L, TPO, SCF и Г-КСФ в течение по меньшей мере 3 дней, по меньшей мере 4 дней, по меньшей мере 5 дней, по меньшей мере 6 дней или по меньшей мере 7 дней. В некоторых вариантах осуществления HSPC модифицированы с применением способов согласно изобретению, и затем примированы для B-клеточной дифференцировки в присутствии человеческого IL-3, Flt3L, TPO, SCF и Г-КСФ в течение 5 дней.
[0188] В некоторых вариантах осуществления, после примирования, модифицированные клетки HSPC переносят в слой питающих клеток и подпитывают раз в две недели, вместе с переносом в свежий слой фидеров один раз в неделю. В некоторых вариантах осуществления питающие клетки представляют собой питающие клетки MS-5.
[0189] В некоторых вариантах осуществления модифицированные клетки HSPC культивируют с питающими клетками MS-5 в течение по меньшей мере 7, 14, 21, 28, 30, 33, 35, 42 или 48 дней. В некоторых вариантах осуществления модифицированные клетки HSPC культивировали с питающими клетками MS-5 в течение 33 дней.
Системы транспозиции
[0190] Примерные системы транспозона/транспозазы согласно изобретению включают, без ограничения перечисленными, транспозоны и транспозазы piggyBac, подобные piggyBac транспозоны и транспозазы, транспозоны и транспозазы Sleeping Beauty, транспозоны и транспозазы Helraiser и транспозоны и транспозазы Tol2.
[0191] Транспозаза piggyBac распознает транспозон-специфические последовательности инвертированных концевых повторов (ITR) на концах транспозона и перемещает содержимое между ITR в хромосомные сайты TTAA. Система транспозона piggyBac не имеет ограничения по полезной нагрузке представляющих интерес генов, которые могут быть встроены между ITR. В некоторых вариантах осуществления и, в частности, в тех вариантах осуществления, в которых транспозон представляет собой транспозон piggyBac, транспозаза является транспозазой piggyBac или Super piggyBac (SPB). В некоторых вариантах осуществления и, в частности, в тех вариантах осуществления, в которых транспозаза представляет собой транспозазу Super piggyBac (SPB), последовательность, кодирующая транспозазу, является последовательностью мРНК.
[0192] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза является ферментом транспозазой piggyBac (PB). Фермент транспозаза piggyBac (PB) может включать или состоять из аминокислотной последовательности, которая по меньшей мере на 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент идентична последовательности:
61 SEILDEQNVI EQPGSSLASN RILTLPQRTI RGKNKHCWST SKSTRRSRVS ALNIVRSQRG
121 PTRMCRNIYD PLLCFKLFFT DEIISEIVKW TNAEISLKRR ESMTGATFRD TNEDEIYAFF
181 GILVMTAVRK DNHMSTDDLF DRSLSMVYVS VMSRDRFDFL IRCLRMDDKS IRPTLRENDV
241 FTPVRKIWDL FIHQCIQNYT PGAHLTIDEQ LLGFRGRCPF RMYIPNKPSK YGIKILMMCD
301 SGTKYMINGM PYLGRGTQTN GVPLGEYYVK ELSKPVHGSC RNITCDNWFT SIPLAKNLLQ
361 EPYKLTIVGT VRSNKREIPE VLKNSRSRPV GTSMFCFDGP LTLVSYKPKP AKMVYLLSSC
421 DEDASINEST GKPQMVMYYN QTKGGVDTLD QMCSVMTCSR KTNRWPMALL YGMINIACIN
481 SFIIYSHNVS SKGEKVQSRK KFMRNLYMSL TSSFMRKRLE APTLKRYLRD NISNILPNEV
541 PGTSDDSTEE PVMKKRTYCT YCPSKIRRKA NASCKKCKKV ICREHNIDMC QSCF
(SEQ ID NO:14487).
[0193] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза является ферментом транспозазой piggyBac (PB), включающим или состоящим из аминокислотной последовательности, содержащей аминокислотную замену в одном или более из положений 30, 165, 282 или 538 последовательности последовательности:
61 SEILDEQNVI EQPGSSLASN RILTLPQRTI RGKNKHCWST SKSTRRSRVS ALNIVRSQRG
121 PTRMCRNIYD PLLCFKLFFT DEIISEIVKW TNAEISLKRR ESMTGATFRD TNEDEIYAFF
181 GILVMTAVRK DNHMSTDDLF DRSLSMVYVS VMSRDRFDFL IRCLRMDDKS IRPTLRENDV
241 FTPVRKIWDL FIHQCIQNYT PGAHLTIDEQ LLGFRGRCPF RMYIPNKPSK YGIKILMMCD
301 SGTKYMINGM PYLGRGTQTN GVPLGEYYVK ELSKPVHGSC RNITCDNWFT SIPLAKNLLQ
361 EPYKLTIVGT VRSNKREIPE VLKNSRSRPV GTSMFCFDGP LTLVSYKPKP AKMVYLLSSC
421 DEDASINEST GKPQMVMYYN QTKGGVDTLD QMCSVMTCSR KTNRWPMALL YGMINIACIN
481 SFIIYSHNVS SKGEKVQSRK KFMRNLYMSL TSSFMRKRLE APTLKRYLRD NISNILPNEV
541 PGTSDDSTEE PVMKKRTYCT YCPSKIRRKA NASCKKCKKV ICREHNIDMC QSCF
(SEQ ID NO:14487).
[0194] В некоторых вариантах осуществления фермент транспозаза является ферментом транспозазой piggyBac (PB), включающим или состоящим из аминокислотной последовательности, содержащей аминокислотную замену в двух или более положениях 30, 165, 282 или 538 последовательности SEQ ID NO:14487. В некоторых вариантах осуществления фермент транспозаза является ферментом транспозазой piggyBac (PB), включающим или состоящим из аминокислотной последовательности, содержащей аминокислотную замену в трех или более положениях 30, 165, 282 или 538 последовательности SEQ ID NO:14487. В некоторых вариантах осуществления фермент транспозаза является ферментом транспозазой piggyBac (PB), включающим или состоящим из аминокислотной последовательности, содержащей аминокислотную замену в каждом из следующих положений 30, 165, 282 и 538 последовательности SEQ ID NO:14487. В некоторых вариантах осуществления аминокислотная замена в положении 30 последовательности SEQ ID NO:14487 является заменой валина (V) на изолейцин (I). В некоторых вариантах осуществления аминокислотная замена в положении 165 последовательности SEQ ID NO:14487 является заменой серина (S) на глицин (G). В некоторых вариантах осуществления аминокислотная замена в положении 282 последовательности SEQ ID NO:14487 является заменой валина (V) на метионин (M). В некоторых вариантах осуществления аминокислотная замена в положении 538 последовательности SEQ ID NO:14487 является заменой лизина (K) на аспарагин (N).
[0195] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза является ферментом транспозазой Super piggyBac (SPB). В некоторых вариантах осуществления фермент транспозаза Super piggyBac (SPB) согласно изобретению может включать или состоять из аминокислотной последовательности SEQ ID NO:14487, в которой аминокислотная замена в положении 30 является заменой валина (V) на изолейцин (I), аминокислотная замена в положении 165 является заменой серина (S) на глицин (G), аминокислотная замена в положении 282 является заменой валина (V) на метионин (M), и аминокислотная замена в положении 538 является заменой лизина (K) на аспарагин (N). В некоторых вариантах осуществления фермент транспозаза Super piggyBac (SPB) может включать или состоять из аминокислотной последовательности, которая по меньшей мере на 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент идентична последовательности:
61 SEILDEQNVI EQPGSSLASN RILTLPQRTI RGKNKHCWST SKSTRRSRVS ALNIVRSQRG
121 PTRMCRNIYD PLLCFKLFFT DEIISEIVKW TNAEISLKRR ESMTSATFRD TNEDEIYAFF
181 GILVMTAVRK DNHMSTDDLF DRSLSMVYVS VMSRDRFDFL IRCLRMDDKS IRPTLRENDV
241 FTPVRKIWDL FIHQCIQNYT PGAHLTIDEQ LLGFRGRCPF RVYIPNKPSK YGIKILMMCD
301 SGTKYMINGM PYLGRGTQTN GVPLGEYYVK ELSKPVHGSC RNITCDNWFT SIPLAKNLLQ
361 EPYKLTIVGT VRSNKREIPE VLKNSRSRPV GTSMFCFDGP LTLVSYKPKP AKMVYLLSSC
421 DEDASINEST GKPQMVMYYN QTKGGVDTLD QMCSVMTCSR KTNRWPMALL YGMINIACIN
481 SFIIYSHNVS SKGEKVQSRK KFMRNLYMSL TSSFMRKRLE APTLKRYLRD NISNILPKEV
541 PGTSDDSTEE PVMKKRTYCT YCPSKIRRKA NASCKKCKKV ICREHNIDMC QSCF
(SEQ ID NO:14484).
[0196] В некоторых вариантах осуществления способов согласно изобретению, включающих такие варианты осуществления, где транспозаза включает вышеописанные мутации в положениях 30, 165, 282 и/или 538, фермент транспозаза piggyBac или Super piggyBac может дополнительно включать аминокислотную замену в одном или более из положений 3, 46, 82, 103, 119, 125, 177, 180, 185, 187, 200, 207, 209, 226, 235, 240, 241, 243, 258, 296, 298, 311, 315, 319, 327, 328, 340, 421, 436, 456, 470, 486, 503, 552, 570 и 591 последовательности SEQ ID NO:14487 или SEQ ID NO:14484. В некоторых вариантах осуществления, включающих такие варианты осуществления, где транспозаза включает вышеописанные мутации в положениях 30, 165, 282 и/или 538, фермент транспозаза piggyBac или Super piggyBac может дополнительно включать аминокислотную замену в одном или более из положений 46, 119, 125, 177, 180, 185, 187, 200, 207, 209, 226, 235, 240, 241, 243, 296, 298, 311, 315, 319, 327, 328, 340, 421, 436, 456, 470, 485, 503, 552 и 570. В некоторых вариантах осуществления аминокислотная замена в положении 3 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой аспарагина (N) на серин (S). В некоторых вариантах осуществления аминокислотная замена в положении 46 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой серина (S) на аланин (A). В некоторых вариантах осуществления аминокислотная замена в положении 46 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой треонина (T) на аланин (A). В некоторых вариантах осуществления аминокислотная замена в положении 82 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой триптофана (W) на изолейцин (I). В некоторых вариантах осуществления аминокислотная замена в положении 103 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой пролина (P) на серин (S). В некоторых вариантах осуществления аминокислотная замена в положении 119 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой пролина (P) на аргинин (R). В некоторых вариантах осуществления аминокислотная замена в положении 125 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой аланина (A) на цистеин (C). В некоторых вариантах осуществления аминокислотная замена в положении 125 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лейцина (L) на цистеин (C). В некоторых вариантах осуществления аминокислотная замена в положении 177 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лизина (K) на тирозин (Y). В некоторых вариантах осуществления аминокислотная замена в положении 177 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой гистидина (H) на тирозин (Y). В некоторых вариантах осуществления аминокислотная замена в положении 180 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лейцина (L) на фенилаланин (F). В некоторых вариантах осуществления аминокислотная замена в положении 180 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой изолейцина (I) на фенилаланин (F). В некоторых вариантах осуществления аминокислотная замена в положении 180 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой валина (V) на фенилаланин (F). В некоторых вариантах осуществления аминокислотная замена в положении 185 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лейцина (L) на метионин (M). В некоторых вариантах осуществления аминокислотная замена в положении 187 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой глицина (G) на аланин (A). В некоторых вариантах осуществления аминокислотная замена в положении 200 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой триптофана (W) на фенилаланин (F). В некоторых вариантах осуществления аминокислотная замена в положении 207 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой пролина (P) на валин (V). В некоторых вариантах осуществления аминокислотная замена в положении 209 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой фенилаланина (F) на валин (V). В некоторых вариантах осуществления аминокислотная замена в положении 226 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой фенилаланина (F) на метионин (M). В некоторых вариантах осуществления аминокислотная замена в положении 235 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой аргинина (R) на лейцин (L). В некоторых вариантах осуществления аминокислотная замена в положении 240 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лизина (K) на валин (V). В некоторых вариантах осуществления аминокислотная замена в положении 241 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лейцина (L) на фенилаланин (F). В некоторых вариантах осуществления аминокислотная замена в положении 243 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лизина (K) на пролин (P). В некоторых вариантах осуществления аминокислотная замена в положении 258 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой серина (S) на аспарагин (N). В некоторых вариантах осуществления аминокислотная замена в положении 296 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой триптофана (W) на лейцин (L). В некоторых вариантах осуществления аминокислотная замена в положении 296 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой тирозина (Y) на лейцин (L). В некоторых вариантах осуществления аминокислотная замена в положении 296 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой фенилаланина (F) на лейцин (L). В некоторых вариантах осуществления аминокислотная замена в положении 298 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лейцина (L) на метионин (M). В некоторых вариантах осуществления аминокислотная замена в положении 298 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой аланина (A) на метионин (M). В некоторых вариантах осуществления аминокислотная замена в положении 298 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой валина (V) на метионин (M). В некоторых вариантах осуществления аминокислотная замена в положении 311 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой изолейцина (I) на пролин (P). В некоторых вариантах осуществления аминокислотная замена в положении 311 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой валина на пролин (P). В некоторых вариантах осуществления аминокислотная замена в положении 315 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лизина (K) на аргинин (R). В некоторых вариантах осуществления аминокислотная замена в положении 319 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой глицина (G) на треонин (T). В некоторых вариантах осуществления аминокислотная замена в положении 327 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой аргинина (R) на тирозин (Y). В некоторых вариантах осуществления аминокислотная замена в положении 328 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой валина (V) на тирозин (Y). В некоторых вариантах осуществления аминокислотная замена в положении 340 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой глицина (G) на цистеин (C). В некоторых вариантах осуществления аминокислотная замена в положении 340 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лейцина (L) на цистеин (C). В некоторых вариантах осуществления аминокислотная замена в положении 421 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой гистидина (H) на аспарагиновую кислоту (D). В некоторых вариантах осуществления аминокислотная замена в положении 436 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой изолейцина (I) на валин (V). В некоторых вариантах осуществления аминокислотная замена в положении 456 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой тирозина (Y) на метионин (M). В некоторых вариантах осуществления аминокислотная замена в положении 470 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой фенилаланина (F) на лейцин (L). В некоторых вариантах осуществления аминокислотная замена в положении 485 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лизина (K) на серин (S). В некоторых вариантах осуществления аминокислотная замена в положении 503 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лейцина (L) на метионин (M). В некоторых вариантах осуществления аминокислотная замена в положении 503 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой изолейцина (I) на метионин (M). В некоторых вариантах осуществления аминокислотная замена в положении 552 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лизина (K) на валин (V). В некоторых вариантах осуществления аминокислотная замена в положении 570 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой треонина (T) на аланин (A). В некоторых вариантах осуществления аминокислотная замена в положении 591 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой пролина (P) на глутамин (Q). В некоторых вариантах осуществления аминокислотная замена в положении 591 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой аргинина (R) на глутамин (Q).
[0197] В некоторых вариантах осуществления способов согласно изобретению, включающих такие варианты осуществления, где транспозаза включает вышеописанные мутации в положениях 30, 165, 282 и/или 538, фермент транспозаза piggyBac может включать или фермент транспозаза Super piggyBac может дополнительно включать аминокислотную замену в одном или более из положений 103, 194, 372, 375, 450, 509 и 570 последовательности SEQ ID NO:14487 или SEQ ID NO:14484. В некоторых вариантах осуществления способов согласно изобретению, включающих такие варианты осуществления, где транспозаза включает вышеописанные мутации в положениях 30, 165, 282 и/или 538, фермент транспозаза piggyBac может включать или фермент транспозаза Super piggyBac может дополнительно включать аминокислотную замену в двух, трех, четырех, пяти, шести или более из положений 103, 194, 372, 375, 450, 509 и 570 последовательности SEQ ID NO:14487 или SEQ ID NO:14484. В некоторых вариантах осуществления, включающих такие варианты осуществления, где транспозаза включает вышеописанные мутации в положениях 30, 165, 282 и/или 538, фермент транспозаза piggyBac может включать или фермент транспозаза Super piggyBac может дополнительно включать аминокислотную замену в положениях 103, 194, 372, 375, 450, 509 и 570 последовательности SEQ ID NO:14487 или SEQ ID NO:14484. В некоторых вариантах осуществления аминокислотная замена в положении 103 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой пролина (P) на серин (S). В некоторых вариантах осуществления аминокислотная замена в положении 194 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой валина (V) на метионин (M). В некоторых вариантах осуществления аминокислотная замена в положении 372 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой аланина (A) на аргинин (R). В некоторых вариантах осуществления аминокислотная замена в положении 375 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой аланина (A) на лизин (K). В некоторых вариантах осуществления аминокислотная замена в положении 450 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой аспарагина (N) на аспарагиновую кислоту (D). В некоторых вариантах осуществления аминокислотная замена в положении 509 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой глицина (G) на серин (S). В некоторых вариантах осуществления аминокислотная замена в положении 570 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой серина (S) на аспарагин (N). В некоторых вариантах осуществления фермент транспозаза piggyBac может включать замену валина (V) на метионин (M) в положении 194 SEQ ID NO:14487. В некоторых вариантах осуществления, включающих такие варианты осуществления, где фермент транспозаза piggyBac может включать замену валина (V) на метионин (M) в положении 194 SEQ ID NO:14487, фермент транспозаза piggyBac может дополнительно включать аминокислотную замену в положениях 372, 375 и 450 последовательности SEQ ID NO:14487 или SEQ ID NO:14484. В некоторых вариантах осуществления фермент транспозаза piggyBac может включать замену валина (V) на метионин (M) в положении 194 SEQ ID NO:14487, замену аланина (A) на аргинин (R) в положении 372 SEQ ID NO:14487 и замену аланина (A) на лизин (K) в положении 375 SEQ ID NO:14487. В некоторых вариантах осуществления фермент транспозаза piggyBac может включать замену валина (V) на метионин (M) в положении 194 SEQ ID NO:14487, замену аланина (A) на аргинин (R) в положении 372 SEQ ID NO:14487, замену аланина (A) на лизин (K) в положении 375 SEQ ID NO:14487 и замену аспарагина (N) на аспарагиновую кислоту (D) в положении 450 SEQ ID NO:14487.
[0198] Транспозон Sleeping beauty перемещается в целевой геном транспозазы Sleeping beauty, которая распознает ITR-повторы и перемещает содержимое между повторами ITR в хромосомные сайты TA. В различных вариантах осуществления опосредованный транспозоном SB перенос генов или перенос генов с использованием любого из многих подобных транспозонов, может применяться в композициях и способах согласно изобретению.
[0199] В некоторых вариантах осуществления и, в частности, в тех вариантах осуществления, где транспозон является транспозоном Sleeping beauty, транспозаза является транспозазой Sleeping beauty или гиперактивной транспозазой Sleeping beauty (SB100X).
[0200] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза Sleeping beauty включает аминокислотную последовательность, которая по меньшей мере 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент идентична последовательности:
61 RRVLSPRDER TLVRKVQINP RTTAKDLVKM LEETGTKVSI STVKRVLYRH NLKGRSARKK
121 PLLQNRHKKA RLRFATAHGD KDRTFWRNVL WSDETKIELF GHNDHRYVWR KKGEACKPKN
181 TIPTVKHGGG SIMLWGCFAA GGTGALHKID GIMRKENYVD ILKQHLKTSV RKLKLGRKWV
241 FQMDNDPKHT SKVVAKWLKD NKVKVLEWPS QSPDLNPIEN LWAELKKRVR ARRPTNLTQL
301 HQLCQEEWAK IHPTYCGKLV EGYPKRLTQV KQFKGNATKY (SEQ ID NO:14485).
[0201] В некоторых вариантах осуществления способов согласно изобретению гиперактивный фермент транспозаза Sleeping beauty (SB100X) включает аминокислотную последовательность, которая по меньшей мере на 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент идентична последовательности:
61 RRVLSPRDER TLVRKVQINP RTTAKDLVKM LEETGTKVSI STVKRVLYRH NLKGHSARKK
121 PLLQNRHKKA RLRFATAHGD KDRTFWRNVL WSDETKIELF GHNDHRYVWR KKGEACKPKN
181 TIPTVKHGGG SIMLWGCFAA GGTGALHKID GIMDAVQYVD ILKQHLKTSV RKLKLGRKWV
241 FQHDNDPKHT SKVVAKWLKD NKVKVLEWPS QSPDLNPIEN LWAELKKRVR ARRPTNLTQL
301 HQLCQEEWAK IHPNYCGKLV EGYPKRLTQV KQFKGNATKY (SEQ ID NO:14486).
[0202] Транспозон Helraiser перемещается транспозазой Helitron. Транспозаза Helitron мобилизует транспозон Helraiser, древний элемент из генома летучей мыши, который был активен приблизительно 30-36 миллионов лет назад. Примерный транспозон Helraiser согласно изобретению включает Helibat1, включающий последовательность нуклеиновой кислоты, включающую:
61 CCCACCAGCC AATCAGAAGT GACTATGCAA ATTAACCCAA CAAAGATGGC AGTTAAATTT
121 GCATACGCAG GTGTCAAGCG CCCCAGGAGG CAACGGCGGC CGCGGGCTCC CAGGACCTTC
181 GCTGGCCCCG GGAGGCGAGG CCGGCCGCGC CTAGCCACAC CCGCGGGCTC CCGGGACCTT
241 CGCCAGCAGA GAGCAGAGCG GGAGAGCGGG CGGAGAGCGG GAGGTTTGGA GGACTTGGCA
301 GAGCAGGAGG CCGCTGGACA TAGAGCAGAG CGAGAGAGAG GGTGGCTTGG AGGGCGTGGC
361 TCCCTCTGTC ACCCCAGCTT CCTCATCACA GCTGTGGAAA CTGACAGCAG GGAGGAGGAA
421 GTCCCACCCC CACAGAATCA GCCAGAATCA GCCGTTGGTC AGACAGCTCT CAGCGGCCTG
481 ACAGCCAGGA CTCTCATTCA CCTGCATCTC AGACCGTGAC AGTAGAGAGG TGGGACTATG
541 TCTAAAGAAC AACTGTTGAT ACAACGTAGC TCTGCAGCCG AAAGATGCCG GCGTTATCGA
601 CAGAAAATGT CTGCAGAGCA ACGTGCGTCT GATCTTGAAA GAAGGCGGCG CCTGCAACAG
661 AATGTATCTG AAGAGCAGCT ACTGGAAAAA CGTCGCTCTG AAGCCGAAAA ACAGCGGCGT
721 CATCGACAGA AAATGTCTAA AGACCAACGT GCCTTTGAAG TTGAAAGAAG GCGGTGGCGA
781 CGACAGAATA TGTCTAGAGA ACAGTCATCA ACAAGTACTA CCAATACCGG TAGGAACTGC
841 CTTCTCAGCA AAAATGGAGT ACATGAGGAT GCAATTCTCG AACATAGTTG TGGTGGAATG
901 ACTGTTCGAT GTGAATTTTG CCTATCACTA AATTTCTCTG ATGAAAAACC ATCCGATGGG
961 AAATTTACTC GATGTTGTAG CAAAGGGAAA GTCTGTCCAA ATGATATACA TTTTCCAGAT
1021 TACCCGGCAT ATTTAAAAAG ATTAATGACA AACGAAGATT CTGACAGTAA AAATTTCATG
1081 GAAAATATTC GTTCCATAAA TAGTTCTTTT GCTTTTGCTT CCATGGGTGC AAATATTGCA
1141 TCGCCATCAG GATATGGGCC ATACTGTTTT AGAATACACG GACAAGTTTA TCACCGTACT
1201 GGAACTTTAC ATCCTTCGGA TGGTGTTTCT CGGAAGTTTG CTCAACTCTA TATTTTGGAT
1261 ACAGCCGAAG CTACAAGTAA AAGATTAGCA ATGCCAGAAA ACCAGGGCTG CTCAGAAAGA
1321 CTCATGATCA ACATCAACAA CCTCATGCAT GAAATAAATG AATTAACAAA ATCGTACAAG
1381 ATGCTACATG AGGTAGAAAA GGAAGCCCAA TCTGAAGCAG CAGCAAAAGG TATTGCTCCC
1441 ACAGAAGTAA CAATGGCGAT TAAATACGAT CGTAACAGTG ACCCAGGTAG ATATAATTCT
1501 CCCCGTGTAA CCGAGGTTGC TGTCATATTC AGAAACGAAG ATGGAGAACC TCCTTTTGAA
1561 AGGGACTTGC TCATTCATTG TAAACCAGAT CCCAATAATC CAAATGCCAC TAAAATGAAA
1621 CAAATCAGTA TCCTGTTTCC TACATTAGAT GCAATGACAT ATCCTATTCT TTTTCCACAT
1681 GGTGAAAAAG GCTGGGGAAC AGATATTGCA TTAAGACTCA GAGACAACAG TGTAATCGAC
1741 AATAATACTA GACAAAATGT AAGGACACGA GTCACACAAA TGCAGTATTA TGGATTTCAT
1801 CTCTCTGTGC GGGACACGTT CAATCCTATT TTAAATGCAG GAAAATTAAC TCAACAGTTT
1861 ATTGTGGATT CATATTCAAA AATGGAGGCC AATCGGATAA ATTTCATCAA AGCAAACCAA
1921 TCTAAGTTGA GAGTTGAAAA ATATAGTGGT TTGATGGATT ATCTCAAATC TAGATCTGAA
1981 AATGACAATG TGCCGATTGG TAAAATGATA ATACTTCCAT CATCTTTTGA GGGTAGTCCC
2041 AGAAATATGC AGCAGCGATA TCAGGATGCT ATGGCAATTG TAACGAAGTA TGGCAAGCCC
2101 GATTTATTCA TAACCATGAC ATGCAACCCC AAATGGGCAG ATATTACAAA CAATTTACAA
2161 CGCTGGCAAA AAGTTGAAAA CAGACCTGAC TTGGTAGCCA GAGTTTTTAA TATTAAGCTG
2221 AATGCTCTTT TAAATGATAT ATGTAAATTC CATTTATTTG GCAAAGTAAT AGCTAAAATT
2281 CATGTCATTG AATTTCAGAA ACGCGGACTG CCTCACGCTC ACATATTATT GATATTAGAT
2341 AGTGAGTCCA AATTACGTTC AGAAGATGAC ATTGACCGTA TAGTTAAGGC AGAAATTCCA
2401 GATGAAGACC AGTGTCCTCG ACTTTTTCAA ATTGTAAAAT CAAATATGGT ACATGGACCA
2461 TGTGGAATAC AAAATCCAAA TAGTCCATGT ATGGAAAATG GAAAATGTTC AAAGGGATAT
2521 CCAAAAGAAT TTCAAAATGC GACCATTGGA AATATTGATG GATATCCCAA ATACAAACGA
2581 AGATCTGGTA GCACCATGTC TATTGGAAAT AAAGTTGTCG ATAACACTTG GATTGTCCCT
2641 TATAACCCGT ATTTGTGCCT TAAATATAAC TGTCATATAA ATGTTGAAGT CTGTGCATCA
2701 ATTAAAAGTG TCAAATATTT ATTTAAATAC ATCTATAAAG GGCACGATTG TGCAAATATT
2761 CAAATTTCTG AAAAAAATAT TATCAATCAT GACGAAGTAC AGGACTTCAT TGACTCCAGG
2821 TATGTGAGCG CTCCTGAGGC TGTTTGGAGA CTTTTTGCAA TGCGAATGCA TGACCAATCT
2881 CATGCAATCA CAAGATTAGC TATTCATTTG CCAAATGATC AGAATTTGTA TTTTCATACC
2941 GATGATTTTG CTGAAGTTTT AGATAGGGCT AAAAGGCATA ACTCGACTTT GATGGCTTGG
3001 TTCTTATTGA ATAGAGAAGA TTCTGATGCA CGTAATTATT ATTATTGGGA GATTCCACAG
3061 CATTATGTGT TTAATAATTC TTTGTGGACA AAACGCCGAA AGGGTGGGAA TAAAGTATTA
3121 GGTAGACTGT TCACTGTGAG CTTTAGAGAA CCAGAACGAT ATTACCTTAG ACTTTTGCTT
3181 CTGCATGTAA AAGGTGCGAT AAGTTTTGAG GATCTGCGAA CTGTAGGAGG TGTAACTTAT
3241 GATACATTTC ATGAAGCTGC TAAACACCGA GGATTATTAC TTGATGACAC TATCTGGAAA
3301 GATACGATTG ACGATGCAAT CATCCTTAAT ATGCCCAAAC AACTACGGCA ACTTTTTGCA
3361 TATATATGTG TGTTTGGATG TCCTTCTGCT GCAGACAAAT TATGGGATGA GAATAAATCT
3421 CATTTTATTG AAGATTTCTG TTGGAAATTA CACCGAAGAG AAGGTGCCTG TGTGAACTGT
3481 GAAATGCATG CCCTTAACGA AATTCAGGAG GTATTCACAT TGCATGGAAT GAAATGTTCA
3541 CATTTCAAAC TTCCGGACTA TCCTTTATTA ATGAATGCAA ATACATGTGA TCAATTGTAC
3601 GAGCAACAAC AGGCAGAGGT TTTGATAAAT TCTCTGAATG ATGAACAGTT GGCAGCCTTT
3661 CAGACTATAA CTTCAGCCAT CGAAGATCAA ACTGTACACC CCAAATGCTT TTTCTTGGAT
3721 GGTCCAGGTG GTAGTGGAAA AACATATCTG TATAAAGTTT TAACACATTA TATTAGAGGT
3781 CGTGGTGGTA CTGTTTTACC CACAGCATCT ACAGGAATTG CTGCAAATTT ACTTCTTGGT
3841 GGAAGAACCT TTCATTCCCA ATATAAATTA CCAATTCCAT TAAATGAAAC TTCAATTTCT
3901 AGACTCGATA TAAAGAGTGA AGTTGCTAAA ACCATTAAAA AGGCCCAACT TCTCATTATT
3961 GATGAATGCA CCATGGCATC CAGTCATGCT ATAAACGCCA TAGATAGATT ACTAAGAGAA
4021 ATTATGAATT TGAATGTTGC ATTTGGTGGG AAAGTTCTCC TTCTCGGAGG GGATTTTCGA
4081 CAATGTCTCA GTATTGTACC ACATGCTATG CGATCGGCCA TAGTACAAAC GAGTTTAAAG
4141 TACTGTAATG TTTGGGGATG TTTCAGAAAG TTGTCTCTTA AAACAAATAT GAGATCAGAG
4201 GATTCTGCTT ATAGTGAATG GTTAGTAAAA CTTGGAGATG GCAAACTTGA TAGCAGTTTT
4261 CATTTAGGAA TGGATATTAT TGAAATCCCC CATGAAATGA TTTGTAACGG ATCTATTATT
4321 GAAGCTACCT TTGGAAATAG TATATCTATA GATAATATTA AAAATATATC TAAACGTGCA
4381 ATTCTTTGTC CAAAAAATGA GCATGTTCAA AAATTAAATG AAGAAATTTT GGATATACTT
4441 GATGGAGATT TTCACACATA TTTGAGTGAT GATTCCATTG ATTCAACAGA TGATGCTGAA
4501 AAGGAAAATT TTCCCATCGA ATTTCTTAAT AGTATTACTC CTTCGGGAAT GCCGTGTCAT
4561 AAATTAAAAT TGAAAGTGGG TGCAATCATC ATGCTATTGA GAAATCTTAA TAGTAAATGG
4621 GGTCTTTGTA ATGGTACTAG ATTTATTATC AAAAGATTAC GACCTAACAT TATCGAAGCT
4681 GAAGTATTAA CAGGATCTGC AGAGGGAGAG GTTGTTCTGA TTCCAAGAAT TGATTTGTCC
4741 CCATCTGACA CTGGCCTCCC ATTTAAATTA ATTCGAAGAC AGTTTCCCGT GATGCCAGCA
4801 TTTGCGATGA CTATTAATAA ATCACAAGGA CAAACTCTAG ACAGAGTAGG AATATTCCTA
4861 CCTGAACCCG TTTTCGCACA TGGTCAGTTA TATGTTGCTT TCTCTCGAGT TCGAAGAGCA
4921 TGTGACGTTA AAGTTAAAGT TGTAAATACT TCATCACAAG GGAAATTAGT CAAGCACTCT
4981 GAAAGTGTTT TTACTCTTAA TGTGGTATAC AGGGAGATAT TAGAATAAGT TTAATCACTT
5041 TATCAGTCAT TGTTTGCATC AATGTTGTTT TTATATCATG TTTTTGTTGT TTTTATATCA
5101 TGTCTTTGTT GTTGTTATAT CATGTTGTTA TTGTTTATTT ATTAATAAAT TTATGTATTA
5161 TTTTCATATA CATTTTACTC ATTTCCTTTC ATCTCTCACA CTTCTATTAT AGAGAAAGGG
5221 CAAATAGCAA TATTAAAATA TTTCCTCTAA TTAATTCCCT TTCAATGTGC ACGAATTTCG
5281 TGCACCGGGC CACTAG (SEQ ID NO:17006).
[0203] В отличие от других транспозаз транспозаза Helitron не содержит РНКаза-H-подобный каталитический домен, а включает вместо этого мотив RepHel, состоящий из домена-инициатора репликации (Rep) и домена ДНК-хеликазы. Rep домен является доменом нуклеазы из суперсемейства HUH нуклеаз.
[0204] Примерная транспозаза Helitron согласно изобретению включает аминокислотную последовательность, включающую:
61 RHRQKMSKDQ RAFEVERRRW RRQNMSREQS STSTTNTGRN CLLSKNGVHE DAILEHSCGG
121 MTVRCEFCLS LNFSDEKPSD GKFTRCCSKG KVCPNDIHFP DYPAYLKRLM TNEDSDSKNF
181 MENIRSINSS FAFASMGANI ASPSGYGPYC FRIHGQVYHR TGTLHPSDGV SRKFAQLYIL
241 DTAEATSKRL AMPENQGCSE RLMININNLM HEINELTKSY KMLHEVEKEA QSEAAAKGIA
301 PTEVTMAIKY DRNSDPGRYN SPRVTEVAVI FRNEDGEPPF ERDLLIHCKP DPNNPNATKM
361 KQISILFPTL DAMTYPILFP HGEKGWGTDI ALRLRDNSVI DNNTRQNVRT RVTQMQYYGF
421 HLSVRDTFNP ILNAGKLTQQ FIVDSYSKME ANRINFIKAN QSKLRVEKYS GLMDYLKSRS
481 ENDNVPIGKM IILPSSFEGS PRNMQQRYQD AMAIVTKYGK PDLFITMTCN PKWADITNNL
541 QRWQKVENRP DLVARVFNIK LNALLNDICK FHLFGKVIAK IHVIEFQKRG LPHAHILLIL
601 DSESKLRSED DIDRIVKAEI PDEDQCPRLF QIVKSNMVHG PCGIQNPNSP CMENGKCSKG
661 YPKEFQNATI GNIDGYPKYK RRSGSTMSIG NKVVDNTWIV PYNPYLCLKY NCHINVEVCA
721 SIKSVKYLFK YIYKGHDCAN IQISEKNIIN HDEVQDFIDS RYVSAPEAVW RLFAMRMHDQ
781 SHAITRLAIH LPNDQNLYFH TDDFAEVLDR AKRHNSTLMA WFLLNREDSD ARNYYYWEIP
841 QHYVFNNSLW TKRRKGGNKV LGRLFTVSFR EPERYYLRLL LLHVKGAISF EDLRTVGGVT
901 YDTFHEAAKH RGLLLDDTIW KDTIDDAIIL NMPKQLRQLF AYICVFGCPS AADKLWDENK
961 SHFIEDFCWK LHRREGACVN CEMHALNEIQ EVFTLHGMKC SHFKLPDYPL LMNANTCDQL
1021 YEQQQAEVLI NSLNDEQLAA FQTITSAIED QTVHPKCFFL DGPGGSGKTY LYKVLTHYIR
1081 GRGGTVLPTA STGIAANLLL GGRTFHSQYK LPIPLNETSI SRLDIKSEVA KTIKKAQLLI
1141 IDECTMASSH AINAIDRLLR EIMNLNVAFG GKVLLLGGDF RQCLSIVPHA MRSAIVQTSL
1201 KYCNVWGCFR KLSLKTNMRS EDSAYSEWLV KLGDGKLDSS FHLGMDIIEI PHEMICNGSI
1261 IEATFGNSIS IDNIKNISKR AILCPKNEHV QKLNEEILDI LDGDFHTYLS DDSIDSTDDA
1321 EKENFPIEFL NSITPSGMPC HKLKLKVGAI IMLLRNLNSK WGLCNGTRFI IKRLRPNIIE
1381 AEVLTGSAEG EVVLIPRIDL SPSDTGLPFK LIRRQFPVMP AFAMTINKSQ GQTLDRVGIF
1441 LPEPVFAHGQ LYVAFSRVRR ACDVKVKVVN TSSQGKLVKH SESVFTLNVV YREILE
(SEQ ID NO:14501).
[0205] При транспозициях Helitron шпилька вблизи от 3'-конца транспозона функционирует как терминатор. Однако транспозаза может обойти эту шпильку, что приводит к трансдукции фланкирующих последовательностей. Кроме того, транспозиция Helraiser создает ковалентно замкнутые кольцевые интермедиаты. Помимо этого, транспозиции Helitron могут не иметь дупликации целевых сайтов. В последовательности Helraiser транспозаза фланкирована между левой и правой концевыми последовательностями, называемыми LTS (5'-концевая последовательность) и RTS (3'-концевая последовательность). Эти последовательности заканчиваются консервативным мотивом 5'-TC/CTAG-3'. Палиндромная последовательность длиной 19 пн, способная формировать шпилечную концевую структуру, расположена через 11 нуклеотидов перед RTS и состоит из последовательности GTGCACGAATTTCGTGCACCGGGCCACTAG (SEQ ID NO:14500).
[0206] Транспозоны Tol2 могут быть выделены или получены из генома оризии и могут быть подобны транспозонам семейства hAT. Примерные транспозоны Tol2 согласно изобретению кодируются последовательностью, включающей приблизительно 4,7 тпн, и содержат ген, кодирующий транспозазу Tol2, содержащий четыре экзона. Примерная транспозаза Tol2 согласно изобретению включает аминокислотную последовательность, включающую следующее:
61 KSSPSNLRKH IERMHPNYLK NYSKLTAQKR KIGTSTHASS SKQLKVDSVF PVKHVSPVTV
121 NKAILRYIIQ GLHPFSTVDL PSFKELISTL QPGISVITRP TLRSKIAEAA LIMKQKVTAA
181 MSEVEWIATT TDCWTARRKS FIGVTAHWIN PGSLERHSAA LACKRLMGSH TFEVLASAMN
241 DIHSEYEIRD KVVCTTTDSG SNFMKAFRVF GVENNDIETE ARRCESDDTD SEGCGEGSDG
301 VEFQDASRVL DQDDGFEFQL PKHQKCACHL LNLVSSVDAQ KALSNEHYKK LYRSVFGKCQ
361 ALWNKSSRSA LAAEAVESES RLQLLRPNQT RWNSTFMAVD RILQICKEAG EGALRNICTS
421 LEVPMFNPAE MLFLTEWANT MRPVAKVLDI LQAETNTQLG WLLPSVHQLS LKLQRLHHSL
481 RYCDPLVDAL QQGIQTRFKH MFEDPEIIAA AILLPKFRTS WTNDETIIKR GMDYIRVHLE
541 PLDHKKELAN SSSDDEDFFA SLKPTTHEAS KELDGYLACV SDTRESLLTF PAICSLSIKT
601 NTPLPASAAC ERLFSTAGLL FSPKRARLDT NNFENQLLLK LNLRFYNFE
(SEQ ID NO:14502).
[0207] Примерный транспозон Tol2 согласно изобретению, включающий инвертированные повторы, субконцевые последовательности и транспозазу Tol2, кодируется последовательностью нуклеиновой кислоты, включающей следующее:
61 GGATTTTTAC TTTACTTGAG TACAATTAAA AATCAATACT TTTACTTTTA CTTAATTACA
121 TTTTTTTAGA AAAAAAAGTA CTTTTTACTC CTTACAATTT TATTTACAGT CAAAAAGTAC
181 TTATTTTTTG GAGATCACTT CATTCTATTT TCCCTTGCTA TTACCAAACC AATTGAATTG
241 CGCTGATGCC CAGTTTAATT TAAATGTTAT TTATTCTGCC TATGAAAATC GTTTTCACAT
301 TATATGAAAT TGGTCAGACA TGTTCATTGG TCCTTTGGAA GTGACGTCAT GTCACATCTA
361 TTACCACAAT GCACAGCACC TTGACCTGGA AATTAGGGAA ATTATAACAG TCAATCAGTG
421 GAAGAAAATG GAGGAAGTAT GTGATTCATC AGCAGCTGCG AGCAGCACAG TCCAAAATCA
481 GCCACAGGAT CAAGAGCACC CGTGGCCGTA TCTTCGCGAA TTCTTTTCTT TAAGTGGTGT
541 AAATAAAGAT TCATTCAAGA TGAAATGTGT CCTCTGTCTC CCGCTTAATA AAGAAATATC
601 GGCCTTCAAA AGTTCGCCAT CAAACCTAAG GAAGCATATT GAGGTAAGTA CATTAAGTAT
661 TTTGTTTTAC TGATAGTTTT TTTTTTTTTT TTTTTTTTTT TTTTTGGGTG TGCATGTTTT
721 GACGTTGATG GCGCGCCTTT TATATGTGTA GTAGGCCTAT TTTCACTAAT GCATGCGATT
781 GACAATATAA GGCTCACGTA ATAAAATGCT AAAATGCATT TGTAATTGGT AACGTTAGGT
841 CCACGGGAAA TTTGGCGCCT ATTGCAGCTT TGAATAATCA TTATCATTCC GTGCTCTCAT
901 TGTGTTTGAA TTCATGCAAA ACACAAGAAA ACCAAGCGAG AAATTTTTTT CCAAACATGT
961 TGTATTGTCA AAACGGTAAC ACTTTACAAT GAGGTTGATT AGTTCATGTA TTAACTAACA
1021 TTAAATAACC ATGAGCAATA CATTTGTTAC TGTATCTGTT AATCTTTGTT AACGTTAGTT
1081 AATAGAAATA CAGATGTTCA TTGTTTGTTC ATGTTAGTTC ACAGTGCATT AACTAATGTT
1141 AACAAGATAT AAAGTATTAG TAAATGTTGA AATTAACATG TATACGTGCA GTTCATTATT
1201 AGTTCATGTT AACTAATGTA GTTAACTAAC GAACCTTATT GTAAAAGTGT TACCATCAAA
1261 ACTAATGTAA TGAAATCAAT TCACCCTGTC ATGTCAGCCT TACAGTCCTG TGTTTTTGTC
1321 AATATAATCA GAAATAAAAT TAATGTTTGA TTGTCACTAA ATGCTACTGT ATTTCTAAAA
1381 TCAACAAGTA TTTAACATTA TAAAGTGTGC AATTGGCTGC AAATGTCAGT TTTATTAAAG
1441 GGTTAGTTCA CCCAAAAATG AAAATAATGT CATTAATGAC TCGCCCTCAT GTCGTTCCAA
1501 GCCCGTAAGA CCTCCGTTCA TCTTCAGAAC ACAGTTTAAG ATATTTTAGA TTTAGTCCGA
1561 GAGCTTTCTG TGCCTCCATT GAGAATGTAT GTACGGTATA CTGTCCATGT CCAGAAAGGT
1621 AATAAAAACA TCAAAGTAGT CCATGTGACA TCAGTGGGTT AGTTAGAATT TTTTGAAGCA
1681 TCGAATACAT TTTGGTCCAA AAATAACAAA ACCTACGACT TTATTCGGCA TTGTATTCTC
1741 TTCCGGGTCT GTTGTCAATC CGCGTTCACG ACTTCGCAGT GACGCTACAA TGCTGAATAA
1801 AGTCGTAGGT TTTGTTATTT TTGGACCAAA ATGTATTTTC GATGCTTCAA ATAATTCTAC
1861 CTAACCCACT GATGTCACAT GGACTACTTT GATGTTTTTA TTACCTTTCT GGACATGGAC
1921 AGTATACCGT ACATACATTT TCAGTGGAGG GACAGAAAGC TCTCGGACTA AATCTAAAAT
1981 ATCTTAAACT GTGTTCCGAA GATGAACGGA GGTGTTACGG GCTTGGAACG ACATGAGGGT
2041 GAGTCATTAA TGACATCTTT TCATTTTTGG GTGAACTAAC CCTTTAATGC TGTAATCAGA
2101 GAGTGTATGT GTAATTGTTA CATTTATTGC ATACAATATA AATATTTATT TGTTGTTTTT
2161 ACAGAGAATG CACCCAAATT ACCTCAAAAA CTACTCTAAA TTGACAGCAC AGAAGAGAAA
2221 GATCGGGACC TCCACCCATG CTTCCAGCAG TAAGCAACTG AAAGTTGACT CAGTTTTCCC
2281 AGTCAAACAT GTGTCTCCAG TCACTGTGAA CAAAGCTATA TTAAGGTACA TCATTCAAGG
2341 ACTTCATCCT TTCAGCACTG TTGATCTGCC ATCATTTAAA GAGCTGATTA GTACACTGCA
2401 GCCTGGCATT TCTGTCATTA CAAGGCCTAC TTTACGCTCC AAGATAGCTG AAGCTGCTCT
2461 GATCATGAAA CAGAAAGTGA CTGCTGCCAT GAGTGAAGTT GAATGGATTG CAACCACAAC
2521 GGATTGTTGG ACTGCACGTA GAAAGTCATT CATTGGTGTA ACTGCTCACT GGATCAACCC
2581 TGGAAGTCTT GAAAGACATT CCGCTGCACT TGCCTGCAAA AGATTAATGG GCTCTCATAC
2641 TTTTGAGGTA CTGGCCAGTG CCATGAATGA TATCCACTCA GAGTATGAAA TACGTGACAA
2701 GGTTGTTTGC ACAACCACAG ACAGTGGTTC CAACTTTATG AAGGCTTTCA GAGTTTTTGG
2761 TGTGGAAAAC AATGATATCG AGACTGAGGC AAGAAGGTGT GAAAGTGATG ACACTGATTC
2821 TGAAGGCTGT GGTGAGGGAA GTGATGGTGT GGAATTCCAA GATGCCTCAC GAGTCCTGGA
2881 CCAAGACGAT GGCTTCGAAT TCCAGCTACC AAAACATCAA AAGTGTGCCT GTCACTTACT
2941 TAACCTAGTC TCAAGCGTTG ATGCCCAAAA AGCTCTCTCA AATGAACACT ACAAGAAACT
3001 CTACAGATCT GTCTTTGGCA AATGCCAAGC TTTATGGAAT AAAAGCAGCC GATCGGCTCT
3061 AGCAGCTGAA GCTGTTGAAT CAGAAAGCCG GCTTCAGCTT TTAAGGCCAA ACCAAACGCG
3121 GTGGAATTCA ACTTTTATGG CTGTTGACAG AATTCTTCAA ATTTGCAAAG AAGCAGGAGA
3181 AGGCGCACTT CGGAATATAT GCACCTCTCT TGAGGTTCCA ATGTAAGTGT TTTTCCCCTC
3241 TATCGATGTA AACAAATGTG GGTTGTTTTT GTTTAATACT CTTTGATTAT GCTGATTTCT
3301 CCTGTAGGTT TAATCCAGCA GAAATGCTGT TCTTGACAGA GTGGGCCAAC ACAATGCGTC
3361 CAGTTGCAAA AGTACTCGAC ATCTTGCAAG CGGAAACGAA TACACAGCTG GGGTGGCTGC
3421 TGCCTAGTGT CCATCAGTTA AGCTTGAAAC TTCAGCGACT CCACCATTCT CTCAGGTACT
3481 GTGACCCACT TGTGGATGCC CTACAACAAG GAATCCAAAC ACGATTCAAG CATATGTTTG
3541 AAGATCCTGA GATCATAGCA GCTGCCATCC TTCTCCCTAA ATTTCGGACC TCTTGGACAA
3601 ATGATGAAAC CATCATAAAA CGAGGTAAAT GAATGCAAGC AACATACACT TGACGAATTC
3661 TAATCTGGGC AACCTTTGAG CCATACCAAA ATTATTCTTT TATTTATTTA TTTTTGCACT
3721 TTTTAGGAAT GTTATATCCC ATCTTTGGCT GTGATCTCAA TATGAATATT GATGTAAAGT
3781 ATTCTTGCAG CAGGTTGTAG TTATCCCTCA GTGTTTCTTG AAACCAAACT CATATGTATC
3841 ATATGTGGTT TGGAAATGCA GTTAGATTTT ATGCTAAAAT AAGGGATTTG CATGATTTTA
3901 GATGTAGATG ACTGCACGTA AATGTAGTTA ATGACAAAAT CCATAAAATT TGTTCCCAGT
3961 CAGAAGCCCC TCAACCAAAC TTTTCTTTGT GTCTGCTCAC TGTGCTTGTA GGCATGGACT
4021 ACATCAGAGT GCATCTGGAG CCTTTGGACC ACAAGAAGGA ATTGGCCAAC AGTTCATCTG
4081 ATGATGAAGA TTTTTTCGCT TCTTTGAAAC CGACAACACA TGAAGCCAGC AAAGAGTTGG
4141 ATGGATATCT GGCCTGTGTT TCAGACACCA GGGAGTCTCT GCTCACGTTT CCTGCTATTT
4201 GCAGCCTCTC TATCAAGACT AATACACCTC TTCCCGCATC GGCTGCCTGT GAGAGGCTTT
4261 TCAGCACTGC AGGATTGCTT TTCAGCCCCA AAAGAGCTAG GCTTGACACT AACAATTTTG
4321 AGAATCAGCT TCTACTGAAG TTAAATCTGA GGTTTTACAA CTTTGAGTAG CGTGTACTGG
4381 CATTAGATTG TCTGTCTTAT AGTTTGATAA TTAAATACAA ACAGTTCTAA AGCAGGATAA
4441 AACCTTGTAT GCATTTCATT TAATGTTTTT TGAGATTAAA AGCTTAAACA AGAATCTCTA
4501 GTTTTCTTTC TTGCTTTTAC TTTTACTTCC TTAATACTCA AGTACAATTT TAATGGAGTA
4561 CTTTTTTACT TTTACTCAAG TAAGATTCTA GCCAGATACT TTTACTTTTA ATTGAGTAAA
4621 ATTTTCCCTA AGTACTTGTA CTTTCACTTG AGTAAAATTT TTGAGTACTT TTTACACCTC
4681 TG (SEQ ID NO:17007).
[0208] Примерные системы транспозона/транспозазы согласно изобретению включают, без ограничения перечисленными, piggyBac и подобные piggyBac транспозоны и транспозазы.
[0209] PiggyBac и подобные piggyBac транспозазы распознают транспозон-специфические последовательности инвертированных концевых повторов (ITR) на концах транспозона и перемещают содержимое между ITR-повторами в хромосомные сайты TTAA или TTAT. Система транспозона piggyBac или подобная piggyBac не имеют никакого ограничения по полезной нагрузке представляющих интерес генов, которые могут быть встроены между ITR-повторами.
[0210] В некоторых вариантах осуществления и, в частности, таких вариантах осуществления, где транспозон является транспозоном piggyBac, транспозаза является транспозазой piggyBac, Super piggyBac (SPB). В некоторых вариантах осуществления и, в частности, таких вариантах осуществления, где транспозаза является piggyBac, Super piggyBac (SPB), последовательность, кодирующая транспозазу, является последовательностью мРНК.
[0211] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза является ферментом транспозазой piggyBac или piggyBac-подобной транспозазой.
[0212] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза является ферментом транспозазой piggyBac или piggyBac-подобной транспозазой. Фермент транспозаза piggyBac (PB) или подобная piggyBac может включать или состоять из аминокислотной последовательности, которая по меньшей мере на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент идентична последовательности:
61 SEILDEQNVI EQPGSSLASN RILTLPQRTI RGKNKHCWST SKSTRRSRVS ALNIVRSQRG
121 PTRMCRNIYD PLLCFKLFFT DEIISEIVKW TNAEISLKRR ESMTGATFRD TNEDEIYAFF
181 GILVMTAVRK DNHMSTDDLF DRSLSMVYVS VMSRDRFDFL IRCLRMDDKS IRPTLRENDV
241 FTPVRKIWDL FIHQCIQNYT PGAHLTIDEQ LLGFRGRCPF RMYIPNKPSK YGIKILMMCD
301 SGTKYMINGM PYLGRGTQTN GVPLGEYYVK ELSKPVHGSC RNITCDNWFT SIPLAKNLLQ
361 EPYKLTIVGT VRSNKREIPE VLKNSRSRPV GTSMFCFDGP LTLVSYKPKP AKMVYLLSSC
421 DEDASINEST GKPQMVMYYN QTKGGVDTLD QMCSVMTCSR KTNRWPMALL YGMINIACIN
481 SFIIYSHNVS SKGEKVQSRK KFMRNLYMSL TSSFMRKRLE APTLKRYLRD NISNILPNEV
541 PGTSDDSTEE PVMKKRTYCT YCPSKIRRKA NASCKKCKKV ICREHNIDMC QSCF
(SEQ ID NO:14487).
[0213] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза является ферментом транспозазой piggyBac или piggyBac-подобной транспозазой, включающим или состоящим из аминокислотной последовательности, содержащей аминокислотную замену в одном или более из положений 30, 165, 282 или 538 последовательности:
61 SEILDEQNVI EQPGSSLASN RILTLPQRTI RGKNKHCWST SKSTRRSRVS ALNIVRSQRG
121 PTRMCRNIYD PLLCFKLFFT DEIISEIVKW TNAEISLKRR ESMTGATFRD TNEDEIYAFF
181 GILVMTAVRK DNHMSTDDLF DRSLSMVYVS VMSRDRFDFL IRCLRMDDKS IRPTLRENDV
241 FTPVRKIWDL FIHQCIQNYT PGAHLTIDEQ LLGFRGRCPF RMYIPNKPSK YGIKILMMCD
301 SGTKYMINGM PYLGRGTQTN GVPLGEYYVK ELSKPVHGSC RNITCDNWFT SIPLAKNLLQ
361 EPYKLTIVGT VRSNKREIPE VLKNSRSRPV GTSMFCFDGP LTLVSYKPKP AKMVYLLSSC
421 DEDASINEST GKPQMVMYYN QTKGGVDTLD QMCSVMTCSR KTNRWPMALL YGMINIACIN
481 SFIIYSHNVS SKGEKVQSRK KFMRNLYMSL TSSFMRKRLE APTLKRYLRD NISNILPNEV
541 PGTSDDSTEE PVMKKRTYCT YCPSKIRRKA NASCKKCKKV ICREHNIDMC QSCF
(SEQ ID NO:14487).
[0214] В некоторых вариантах осуществления фермент транспозаза является ферментом транспозазой piggyBac или piggyBac-подобной транспозазой, включающим или состоящим из аминокислотной последовательности, содержащей аминокислотную замену в двух или более из положений 30, 165, 282 или 538 последовательности SEQ ID NO:14487. В некоторых вариантах осуществления фермент транспозаза является ферментом транспозазой piggyBac или piggyBac-подобной транспозазой, включающим или состоящим из аминокислотной последовательности, содержащей аминокислотную замену в трех или более из положений 30, 165, 282 или 538 последовательности SEQ ID NO:14487. В некоторых вариантах осуществления фермент транспозаза является ферментом транспозазой piggyBac или piggyBac-подобной транспозазой, включающим или состоящим из аминокислотной последовательности, содержащей аминокислотную замену в каждом из следующих положений 30, 165, 282 и 538 последовательности SEQ ID NO:14487. В некоторых вариантах осуществления аминокислотная замена в положении 30 последовательности SEQ ID NO:14487 является заменой валина (V) на изолейцин (I). В некоторых вариантах осуществления аминокислотная замена в положении 165 последовательности SEQ ID NO:14487 является заменой серина (S) на глицин (G). В некоторых вариантах осуществления аминокислотная замена в положении 282 последовательности SEQ ID NO:14487 является заменой валина (V) на метионин (M). В некоторых вариантах осуществления аминокислотная замена в положении 538 последовательности SEQ ID NO:14487 является заменой лизина (K) на аспарагин (N).
[0215] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза является ферментом транспозазой Super piggyBac (SPB) или подобной piggyBac. В некоторых вариантах осуществления фермент транспозаза Super piggyBac (SPB) или подобная piggyBac согласно изобретению могут включать или состоять из аминокислотной последовательности последовательности SEQ ID NO:14487, где аминокислотная замена в положении 30 является заменой валина (V) на изолейцин (I), аминокислотная замена в положении 165 является заменой серина (S) на глицин (G), аминокислотная замена в положении 282 является заменой валина (V) на метионин (M), и аминокислотная замена в положении 538 является заменой лизина (K) на аспарагин (N). В некоторых вариантах осуществления фермент транспозаза Super piggyBac (SPB) или подобная piggyBac могут включать или состоять из аминокислотной последовательности, которая по меньшей мере на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент идентична последовательности:
61 SEILDEQNVI EQPGSSLASN RILTLPQRTI RGKNKHCWST SKSTRRSRVS ALNIVRSQRG
121 PTRMCRNIYD PLLCFKLFFT DEIISEIVKW TNAEISLKRR ESMTSATFRD TNEDEIYAFF
181 GILVMTAVRK DNHMSTDDLF DRSLSMVYVS VMSRDRFDFL IRCLRMDDKS IRPTLRENDV
241 FTPVRKIWDL FIHQCIQNYT PGAHLTIDEQ LLGFRGRCPF RVYIPNKPSK YGIKILMMCD
301 SGTKYMINGM PYLGRGTQTN GVPLGEYYVK ELSKPVHGSC RNITCDNWFT SIPLAKNLLQ
361 EPYKLTIVGT VRSNKREIPE VLKNSRSRPV GTSMFCFDGP LTLVSYKPKP AKMVYLLSSC
421 DEDASINEST GKPQMVMYYN QTKGGVDTLD QMCSVMTCSR KTNRWPMALL YGMINIACIN
481 SFIIYSHNVS SKGEKVQSRK KFMRNLYMSL TSSFMRKRLE APTLKRYLRD NISNILPKEV
541 PGTSDDSTEE PVMKKRTYCT YCPSKIRRKA NASCKKCKKV ICREHNIDMC QSCF
(SEQ ID NO:14484).
[0216] В некоторых вариантах осуществления способов согласно изобретению, включающих такие варианты осуществления, где транспозаза включает вышеописанные мутации в положениях 30, 165, 282 и/или 538, фермент транспозаза piggyBac, Super piggyBac или подобная piggyBac могут дополнительно включать аминокислотную замену в одном или более из положений 3, 46, 82, 103, 119, 125, 177, 180, 185, 187, 200, 207, 209, 226, 235, 240, 241, 243, 258, 296, 298, 311, 315, 319, 327, 328, 340, 421, 436, 456, 470, 486, 503, 552, 570 и 591 последовательности SEQ ID NO:14487 или SEQ ID NO:14484. В некоторых вариантах осуществления, включающих такие варианты осуществления, где транспозаза включает вышеописанные мутации в положениях 30, 165, 282 и/или 538, фермент транспозаза piggyBac, Super piggyBac или подобная piggyBac могут дополнительно включать аминокислотную замену в одном или более из положений 46, 119, 125, 177, 180, 185, 187, 200, 207, 209, 226, 235, 240, 241, 243, 296, 298, 311, 315, 319, 327, 328, 340, 421, 436, 456, 470, 485, 503, 552 и 570. В некоторых вариантах осуществления аминокислотная замена в положении 3 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой аспарагина (N) на серин (S). В некоторых вариантах осуществления аминокислотная замена в положении 46 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой серина (S) на аланин (A). В некоторых вариантах осуществления аминокислотная замена в положении 46 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой треонина (T) на аланин (A). В некоторых вариантах осуществления аминокислотная замена в положении 82 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой триптофана (W) на изолейцин (I). В некоторых вариантах осуществления аминокислотная замена в положении 103 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой пролина (P) на серин (S). В некоторых вариантах осуществления аминокислотная замена в положении 119 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой пролина (P) на аргинин (R). В некоторых вариантах осуществления аминокислотная замена в положении 125 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой аланина (A) на цистеин (C). В некоторых вариантах осуществления аминокислотная замена в положении 125 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лейцина (L) на цистеин (C). В некоторых вариантах осуществления аминокислотная замена в положении 177 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лизина (K) на тирозин (Y). В некоторых вариантах осуществления аминокислотная замена в положении 177 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой гистидина (H) на тирозин (Y). В некоторых вариантах осуществления аминокислотная замена в положении 180 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лейцина (L) на фенилаланин (F). В некоторых вариантах осуществления аминокислотная замена в положении 180 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой изолейцина (I) на фенилаланин (F). В некоторых вариантах осуществления аминокислотная замена в положении 180 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой валина (V) на фенилаланин (F). В некоторых вариантах осуществления аминокислотная замена в положении 185 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лейцина (L) на метионин (M). В некоторых вариантах осуществления аминокислотная замена в положении 187 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой глицина (G) на аланин (A). В некоторых вариантах осуществления аминокислотная замена в положении 200 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой триптофана (W) на фенилаланин (F). В некоторых вариантах осуществления аминокислотная замена в положении 207 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой пролина (P) на валин (V). В некоторых вариантах осуществления аминокислотная замена в положении 209 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой фенилаланина (F) на валин (V). В некоторых вариантах осуществления аминокислотная замена в положении 226 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой фенилаланина (F) на метионин (M). В некоторых вариантах осуществления аминокислотная замена в положении 235 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой аргинина (R) на лейцин (L). В некоторых вариантах осуществления аминокислотная замена в положении 240 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лизина (K) на валин (V). В некоторых вариантах осуществления аминокислотная замена в положении 241 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лейцина (L) на фенилаланин (F). В некоторых вариантах осуществления аминокислотная замена в положении 243 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лизина (K) на пролин (P). В некоторых вариантах осуществления аминокислотная замена в положении 258 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой серина (S) на аспарагин (N). В некоторых вариантах осуществления аминокислотная замена в положении 296 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой триптофана (W) на лейцин (L). В некоторых вариантах осуществления аминокислотная замена в положении 296 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой тирозина (Y) на лейцин (L). В некоторых вариантах осуществления аминокислотная замена в положении 296 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой фенилаланина (F) на лейцин (L). В некоторых вариантах осуществления аминокислотная замена в положении 298 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лейцина (L) на метионин (M). В некоторых вариантах осуществления аминокислотная замена в положении 298 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой аланина (A) на метионин (M). В некоторых вариантах осуществления аминокислотная замена в положении 298 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой валина (V) на метионин (M). В некоторых вариантах осуществления аминокислотная замена в положении 311 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой изолейцина (I) на пролин (P). В некоторых вариантах осуществления аминокислотная замена в положении 311 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой валина на пролин (P). В некоторых вариантах осуществления аминокислотная замена в положении 315 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лизина (K) на аргинин (R). В некоторых вариантах осуществления аминокислотная замена в положении 319 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой глицина (G) на треонин (T). В некоторых вариантах осуществления аминокислотная замена в положении 327 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой аргинина (R) на тирозин (Y). В некоторых вариантах осуществления аминокислотная замена в положении 328 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой валина (V) на тирозин (Y). В некоторых вариантах осуществления аминокислотная замена в положении 340 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой глицина (G) на цистеин (C). В некоторых вариантах осуществления аминокислотная замена в положении 340 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лейцина (L) на цистеин (C). В некоторых вариантах осуществления аминокислотная замена в положении 421 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой гистидина (H) на аспарагиновую кислоту (D). В некоторых вариантах осуществления аминокислотная замена в положении 436 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой изолейцина (I) на валин (V). В некоторых вариантах осуществления аминокислотная замена в положении 456 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой тирозина (Y) на метионин (M). В некоторых вариантах осуществления аминокислотная замена в положении 470 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой фенилаланина (F) на лейцин (L). В некоторых вариантах осуществления аминокислотная замена в положении 485 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лизина (K) на серин (S). В некоторых вариантах осуществления аминокислотная замена в положении 503 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лейцина (L) на метионин (M). В некоторых вариантах осуществления аминокислотная замена в положении 503 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой изолейцина (I) на метионин (M). В некоторых вариантах осуществления аминокислотная замена в положении 552 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой лизина (K) на валин (V). В некоторых вариантах осуществления аминокислотная замена в положении 570 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой треонина (T) на аланин (A). В некоторых вариантах осуществления аминокислотная замена в положении 591 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой пролина (P) на глутамин (Q). В некоторых вариантах осуществления аминокислотная замена в положении 591 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой аргинина (R) на глутамин (Q).
[0217] В некоторых вариантах осуществления способов согласно изобретению, включающих такие варианты осуществления, где транспозаза включает вышеописанные мутации в положениях 30, 165, 282 и/или 538, фермент транспозаза piggyBac или piggyBac-подобная транспозаза может включать или фермент транспозаза Super piggyBac может дополнительно включать аминокислотную замену в одном или более из положений 103, 194, 372, 375, 450, 509 и 570 последовательности SEQ ID NO:14487 или SEQ ID NO:14484. В некоторых вариантах осуществления способов согласно изобретению, включающих такие варианты осуществления, где транспозаза включает вышеописанные мутации в положениях 30, 165, 282 и/или 538, фермент транспозаза piggyBac или piggyBac-подобная транспозаза может включать или фермент транспозаза Super piggyBac может дополнительно включать аминокислотную замену в двух, трех, четырех, пяти, шести или более из положений 103, 194, 372, 375, 450, 509 и 570 последовательности SEQ ID NO:14487 или SEQ ID NO:14484. В некоторых вариантах осуществления, включающих такие варианты осуществления, где транспозаза включает вышеописанные мутации в положениях 30, 165, 282 и/или 538, фермент транспозаза piggyBac или подобный piggyBac может включать или фермент транспозаза Super piggyBac может дополнительно включать аминокислотную замену в положениях 103, 194, 372, 375, 450, 509 и 570 последовательности SEQ ID NO:14487 или SEQ ID NO:14484. В некоторых вариантах осуществления аминокислотная замена в положении 103 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой пролина (P) на серин (S). В некоторых вариантах осуществления аминокислотная замена в положении 194 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой валина (V) на метионин (M). В некоторых вариантах осуществления аминокислотная замена в положении 372 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой аланина (A) на аргинин (R). В некоторых вариантах осуществления аминокислотная замена в положении 375 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой аланина (A) на лизин (K). В некоторых вариантах осуществления аминокислотная замена в положении 450 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой аспарагина (N) на аспарагиновую кислоту (D). В некоторых вариантах осуществления аминокислотная замена в положении 509 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой глицина (G) на серин (S). В некоторых вариантах осуществления аминокислотная замена в положении 570 SEQ ID NO:14487 или SEQ ID NO:14484 является заменой серина (S) на аспарагин (N). В некоторых вариантах осуществления фермент транспозаза piggyBac или piggyBac-подобная транспозаза может включать замену валина (V) на метионин (M) в положении 194 SEQ ID NO:14487. В некоторых вариантах осуществления, включающих такие варианты осуществления, где фермент транспозаза piggyBac или piggyBac-подобная транспозаза может включать замену валина (V) на метионин (M) в положении 194 SEQ ID NO:14487, фермент транспозаза piggyBac или piggyBac-подобная транспозаза может дополнительно включать аминокислотную замену в положениях 372, 375 и 450 последовательности SEQ ID NO:14487 или SEQ ID NO:14484. В некоторых вариантах осуществления фермент транспозаза piggyBac или piggyBac-подобная транспозаза может включать замену валина (V) на метионин (M) в положении 194 SEQ ID NO:14487, замену аланина (A) на аргинин (R) в положении 372 SEQ ID NO:14487 и замену аланина (A) на лизин (K) в положении 375 SEQ ID NO:14487. В некоторых вариантах осуществления фермент транспозаза piggyBac или piggyBac-подобная транспозаза может включать замену валина (V) на метионин (M) в положении 194 SEQ ID NO:14487, замену аланина (A) на аргинин (R) в положении 372 SEQ ID NO:14487, замену аланина (A) на лизин (K) в положении 375 SEQ ID NO:14487 и замену аспарагина (N) на аспарагиновую кислоту (D) в положении 450 SEQ ID NO:14487.
[0218] В некоторых вариантах осуществления фермент транспозаза piggyBac или piggyBac-подобная транспозаза выделена или получена из насекомого. В некоторых вариантах осуществления насекомым является Trichoplusia ni (рег. номер GenBank AAA87375; SEQ ID NO:16796), Argyrogramma agnata (рег. номер GenBank GU477713; SEQ ID NO:14534, SEQ ID NO:16797), Anopheles gambiae (рег. номер GenBank XP_312615 (SEQ ID NO:16798); рег. номер GenBank XP_320414 (SEQ ID NO:16799); рег. номер GenBank XP_310729 (SEQ ID NO:16800)), Aphis gossypii (рег. номер GenBank GU329918; SEQ ID NO:16801, SEQ ID NO:16802), Acyrthosiphon pisum (рег. номер GenBank XP_001948139; SEQ ID NO:16803), Agrotis ipsilon (рег. номер GenBank GU477714; SEQ ID NO:14537, SEQ ID NO:16804), Bombyx mori (рег. номер GenBank BAD11135; SEQ ID NO:14505), Chilo suppressalis (рег. номер GenBank JX294476; SEQ ID NO:16805, SEQ ID NO:16806), Drosophila melanogaster (рег. номер GenBank AAL39784; SEQ ID NO:16807), Helicoverpa armigera (рег. номер GenBank ABS18391; SEQ ID NO:14525), Heliothis virescens (рег. номер GenBank ABD76335; SEQ ID NO:16808), Macdunnoughia crassisigna (рег. номер GenBank EU287451; SEQ ID NO:16809, SEQ ID NO:16810), Pectinophora gossypiella (рег. номер GenBank GU270322; SEQ ID NO:14530, SEQ ID NO:16811), Tribolium castaneum (рег. номер GenBank XP_001814566; SEQ ID NO:16812), Ctenoplusia agnata (также называется Argyrogramma agnata), Messour bouvieri, Megachile rotundata, Bombus impatiens, Mamestra brassicae, Mayetiola destructor или Apis mellifera.
[0219] В некоторых вариантах осуществления фермент транспозаза piggyBac или piggyBac-подобная транспозаза выделена или получена из насекомого. В некоторых вариантах осуществления насекомым является Trichoplusia ni (AAA87375).
[0220] В некоторых вариантах осуществления фермент транспозаза piggyBac или piggyBac-подобная транспозаза выделена или получена из насекомого. В некоторых вариантах осуществления насекомым является Bombyx mori (BAD11135).
[0221] В некоторых вариантах осуществления фермент транспозаза piggyBac или piggyBac-подобная транспозаза выделена или получена из ракообразного. В некоторых вариантах осуществления ракообразным является Daphnia pulicaria (AAM76342, SEQ ID NO:16813).
[0222] В некоторых вариантах осуществления фермент транспозаза piggyBac или piggyBac-подобная транспозаза выделена или получена из позвоночного. В некоторых вариантах осуществления позвоночным является Xenopus tropicalis (рег. номер GenBank BAF82026; SEQ ID NO:14518), Homo sapiens (рег. номер GenBank NP_689808; SEQ ID NO:16814), Mus musculus (рег. номер GenBank NP_741958; SEQ ID NO:16815), Macaca fascicularis (рег. номер GenBank AB179012; SEQ ID NO:16816, SEQ ID NO:16817), Rattus norvegicus (рег. номер GenBank XP_220453; SEQ ID NO:16818) или Myotis lucifugus.
[0223] В некоторых вариантах осуществления фермент транспозаза piggyBac или piggyBac-подобная транспозаза выделена или получена из личиночнохордового. В некоторых вариантах осуществления личиночнохордовым является Ciona intestinalis (рег. номер GenBank XP_002123602; SEQ ID NO:16819).
[0224] В некоторых вариантах осуществления транспозаза piggyBac или piggyBac-подобная транспозаза вставляет транспозон в последовательность 5'-TTAT-3' в хромосомном сайте (последовательность-мишень TTAT).
[0225] В некоторых вариантах осуществления транспозаза piggyBac или piggyBac-подобная транспозаза вставляет транспозон в последовательность 5'-TTAA-3' в хромосомном сайте (последовательность-мишень TTAA).
[0226] В некоторых вариантах осуществления последовательность-мишень транспозона piggyBac или piggyBac-подобного транспозона включает или состоит из 5'-CTAA-3', 5'-TTAG-3', 5'-ATAA-3', 5'-TCAA-3', 5'AGTT-3', 5'-ATTA-3', 5'-GTTA-3', 5'-TTGA-3', 5'-TTTA-3', 5'-TTAC-3', 5'-ACTA-3', 5'-AGGG-3', 5'-CTAG-3', 5'-TGAA-3', 5'-AGGT-3', 5'-ATCA-3', 5'-CTCC-3', 5'-TAAA-3', 5'-TCTC-3', 5'TGAA-3', 5'-AAAT-3', 5'-AATC-3', 5'-ACAA-3', 5'-ACAT-3', 5'-ACTC-3', 5'-AGTG-3', 5'-ATAG-3', 5'-CAAA-3', 5'-CACA-3', 5'-CATA-3', 5'-CCAG-3', 5'-CCCA-3', 5'-CGTA-3', 5'-GTCC-3', 5'-TAAG-3', 5'-TCTA-3', 5'-TGAG-3', 5'-TGTT-3', 5'-TTCA-3', 5'-TTCT-3' и 5'-TTTT-3'.
[0227] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза является ферментом транспозазой piggyBac или piggyBac-подобной транспозазой. В некоторых вариантах осуществления фермент транспозаза piggyBac или piggyBac-подобная транспозаза выделена или получена из Bombyx mori. Фермент транспозаза piggyBac или piggyBac-подобная транспозаза может включать или состоять из аминокислотной последовательности, которая по меньшей мере на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент идентична последовательности:
61 EANAIIANES DSDPDDDLPL SLVRQRASAS RQVSGPFYTS KDGTKWYKNC QRPNVRLRSE
121 NIVTEQAQVK NIARDASTEY ECWNIFVTSD MLQEILTHTN SSIRHRQTKT AAENSSAETS
181 FYMQETTLCE LKALIALLYL AGLIKSNRQS LKDLWRTDGT GVDIFRTTMS LQRFQFLQNN
241 IRFDDKSTRD ERKQTDNMAA FRSIFDQFVQ CCQNAYSPSE FLTIDEMLLS FRGRCLFRVY
301 IPNKPAKYGI KILALVDAKN FDVVNLEVYA GKQPSGPYAV SNRPFEVVER LIQPVARSHR
361 NVTFDNWFTG YELMLHLLNE YRLTSVGTVR KNKRQIPESF IRTDRQPNSS VFGFQKDITL
421 VSYAPKKNKV VVVMSTMHHD NSIDESTGEK QKPEMITFYN STKAGVDVVD ELSANYNVSR
481 NSKRWPMTLF YGVLNMAAIN ACIIYRANKN VTIKRTEFIR SLGLSMIYEH LHSRNKKKNI
541 PTYLRQRIEK QLGEPSPRHV NVPGRYVRCQ DCPYKKDRKT KHSCNACAKP ICMEHAKFLC
601 ENCAELDSSL (SEQ ID NO:14504).
[0228] Фермент транспозаза piggyBac (PB) или подобная piggyBac может включать или состоять из аминокислотной последовательности, которая по меньшей мере на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент идентична последовательности:
61 EANAIIANES DSDPDDDLPL SLVRQRASAS RQVSGPFYTS KDGTKWYKNC QRPNVRLRSE
121 NIVTEQAQVK NIARDASTEY ECWNIFVTSD MLQEILTHTN SSIRHRQTKT AAENSSAETS
181 FYMQETTLCE LKALIALLYL AGLIKSNRQS LKDLWRTDGT GVDIFRTTMS LQRFQFLQNN
241 IRFDDKSTRD ERKQTDNMAA FRSIFDQFVQ CCQNAYSPSE FLTIDEMLLS FRGRCLFRVY
301 IPNKPAKYGI KILALVDAKN FYVVNLEVYA GKQPSGPYAV SNRPFEVVER LIQPVARSHR
361 NVTFDNWFTG YELMLHLLNE YRLTSVGTVR KNKRQIPESF IRTDRQPNSS VFGFQKDITL
421 VSYAPKKNKV VVVMSTMHHD NSIDESTGEK QKPEMITFYN STKAGVDVVD ELCANYNVSR
481 NSKRWPMTLF YGVLNMAAIN ACIIYRTNKN VTIKRTEFIR SLGLSMIYEH LHSRNKKKNI
541 PTYLRQRIEK QLGEPSPRHV NVPGRYVRCQ DCPYKKDRKT KRSCNACAKP ICMEHAKFLC
601 ENCAELDSSL (SEQ ID NO:14505).
[0229] В некоторых вариантах осуществления транспозаза piggyBac (PB) или подобная piggyBac слита с сигналом ядерной локализации. В некоторых вариантах осуществления аминокислотная последовательность транспозазы piggyBac или подобная piggyBac, слитая с сигналом ядерной локализации, кодируется полинуклеотидной последовательностью, включающей:
61 gcgatgctcg aagaagaact gagcgactac tccgacgaat cgtcatcaga ggatgaaacc
121 gaccactgta gcgagcatga ggttaactac gacaccgagg aggagagaat cgactctgtg
181 gatgtgccct ccaactcacg ccaagaagag gccaatgcaa ttatcgcaaa cgaatcggac
241 agcgatccag acgatgatct gccactgtcc ctcgtgcgcc agcgggccag cgcttcgaga
301 caagtgtcag gtccattcta cacttcgaag gacggcacta agtggtacaa gaattgccag
361 cgacctaacg tcagactccg ctccgagaat atcgtgaccg aacaggctca ggtcaagaat
421 atcgcccgcg acgcctcgac tgagtacgag tgttggaata tcttcgtgac ttcggacatg
481 ctgcaagaaa ttctgacgca caccaacagc tcgattaggc atcgccagac caagactgca
541 gcggagaact catcggccga aacctccttc tatatgcaag agactactct gtgcgaactg
601 aaggcgctga ttgcactgct gtacttggcc ggcctcatca aatcaaatag gcagagcctc
661 aaagatctct ggagaacgga tggaactgga gtggatatct ttcggacgac tatgagcttg
721 cagcggttcc agtttctgca aaacaatatc agattcgacg acaagtccac ccgggacgaa
781 aggaaacaga ctgacaacat ggctgcgttc cggtcaatat tcgatcagtt tgtgcagtgc
841 tgccaaaacg cttatagccc atcggaattc ctgaccatcg acgaaatgct tctctccttc
901 cgggggcgct gcctgttccg agtgtacatc ccgaacaagc cggctaaata cggaatcaaa
961 atcctggccc tggtggacgc caagaatttc tacgtcgtga atctcgaagt gtacgcagga
1021 aagcaaccgt cgggaccgta cgctgtttcg aaccgcccgt ttgaagtcgt cgagcggctt
1081 attcagccgg tggccagatc ccaccgcaat gttaccttcg acaattggtt caccggctac
1141 gagctgatgc ttcaccttct gaacgagtac cggctcacta gcgtggggac tgtcaggaag
1201 aacaagcggc agatcccaga atccttcatc cgcaccgacc gccagcctaa ctcgtccgtg
1261 ttcggatttc aaaaggatat cacgcttgtc tcgtacgccc ccaagaaaaa caaggtcgtg
1321 gtcgtgatga gcaccatgca tcacgacaac agcatcgacg agtcaaccgg agaaaagcaa
1381 aagcccgaga tgatcacctt ctacaattca actaaggccg gcgtcgacgt cgtggatgaa
1441 ctgtgcgcga actataacgt gtcccggaac tctaagcggt ggcctatgac tctcttctac
1501 ggagtgctga atatggccgc aatcaacgcg tgcatcatct accgcaccaa caagaacgtg
1561 accatcaagc gcaccgagtt catcagatcg ctgggtttga gcatgatcta cgagcacctc
1621 cattcacgga acaagaagaa gaatatccct acttacctga ggcagcgtat cgagaagcag
1681 ttgggagaac caagcccgcg ccacgtgaac gtgccggggc gctacgtgcg gtgccaagat
1741 tgcccgtaca aaaaggaccg caaaaccaaa agatcgtgta acgcgtgcgc caaacctatc
1801 tgcatggagc atgccaaatt tctgtgtgaa aattgtgctg aactcgattc ctccctg
(SEQ ID NO:14629).
[0230] В некоторых вариантах осуществления транспозаза piggyBac (PB) или подобная piggyBac является гиперактивной. Гиперактивная транспозаза piggyBac или piggyBac-подобная транспозаза является транспозазой, которая более активна, чем природный вариант, из которого она получена. В некоторых вариантах осуществления гиперактивный фермент транспозаза piggyBac или piggyBac-подобная транспозаза выделена или получена из Bombyx mori. В некоторых вариантах осуществления транспозаза piggyBac (PB) или подобная piggyBac представляет собой гиперактивный вариант SEQ ID NO:14505. В некоторых вариантах осуществления гиперактивная транспозаза piggyBac (PB) или подобная piggyBac включает последовательность, которая по меньшей мере на 90% идентична последовательности:
61 EANAIIANES DSDPDDDLPL SLVRQRASAS RQMSGPHYTS KDGTKWYKNC QRPNVRLRSE
121 NIVTEQAQVK NIARDASTEY ECWNIFVTSD MLQEILTHTN SSIRWRQTKT AAENSSASTS
181 FYMQETTLCE LKALIGLLYI AGLIKSNRQS LKDLWRTDGT GVDIFRTTMS LQRFQFLQNN
241 IRFDDKSTRD ERKQTDNMAA FRSIFDQFVQ SCQNAYSPSE FLTIDEMLLS FRGRCLFRVY
301 IPNKPAKYGI KILALVDAKN FYVKNLEVYA GKQPSGPYAV SNRPFEVVER LIQPVARSHR
361 NVTFDNWFTG YELMLHLLNE YRLTSVGTVR KNKRQIPESF IRTDRQPNSS VFGFQKDITL
421 VSYAPKKNKV VVVMSTMHHD NSIDESTGEK QKPEMITFYN STKAGVDVVD ELCANYNVSR
481 NSKRWPMTLF YGVLNMAAIN ACIIYRTNKN VTIKRTEFIR SLGLSMIYEH LHSRNKKKNI
541 PTYLRQRIEK QLGEPSPRHV NVPGRYVRCQ DCPYKKDRKT KRSCNACAKP ICMEHAKFLC
601 ENCAELDSHL (SEQ ID NO:14576).
[0231] В некоторых вариантах осуществления гиперактивная транспозаза piggyBac (PB) или подобная piggyBac включает SEQ ID NO:14576. В некоторых вариантах осуществления гиперактивная транспозаза piggyBac (PB) или подобная piggyBac включает последовательность:
61 EANAIIANES DSDPDDDLPL SLVRQRASAS RQVSGPFYTS KDGTKWYKNC QRPNVRLRSE
121 NIVTEQAQVK NIARDASTEY ECWNIFVTSD MLQEILTHTN SSIRWRQTKT AAENSSAETS
181 FYMQETTLCE LKALIGLLYI AGLIKSNRQS LKDLWRTDGT GVDIFRTTMS LQRFQFLLNN
241 IRFDDKSTRD ERKQTDNMAA FRSIFDQFVQ SCQNAYSPSE FLTIDEMLLS FRGRCLFRVY
301 IPNKPAKYGI KILALVDAKN FYVHNLEVYA GKQPSGPYAV SNRPFEVVER LIQPVARSHR
361 NVTFDNWFTG YEVMLHLLNE YRLTSVGTVR KNKRQIPESF IRTDRQPNSS VFGFQKDITL
421 VSYAPKKNKV VVVMSTMHHD NSIDESTGEK QKPEMITFYN STKAGVDVVD ELCANYNVSR
481 NSKRWPMTLF YGVLNMAAIN ACIIYRTNKN VTIKRTEFIR SLGLSMIYEH LHSRNKKKNI
541 PTYLRQRIEK QLGEPSPRHV NVPGRYVRCQ DCPYKKDRKT KRSCNACAKP ICMEHAKFLC
601 ENCAHLDS (SEQ ID NO:14630).
[0232] В некоторых вариантах осуществления гиперактивная транспозаза piggyBac (PB) или подобная piggyBac включает последовательность:
61 EANAIIANES DSDPDDDLPL SLVRQRASAS RQVSGPFYTS KDGTKWYKNC QRPNVRLRSE
121 NIVTEQAQVK NIARDASTEY ECWNIFVTSD MLQEILTHTN SSIRWRQTKT AAENSSASTS
181 FYMQETTLCE LKALIGLLYI AGLIKSNRQS LKDLWRTDGT GVDIFRTTMS LQRFQFLLNN
241 IRFDDKSTRD ERKQTDNMAA FRSIFDQFVQ SCQNAYSPSE FLTIDEMLLS FRGRCLFRVY
301 IPNKPAKYGI KILALVDAKN FYVKNLEVYA GKQPSGPYAV SNRPFEVVER LIQPVARSHR
361 NVTFDNWFTG YELMLHLLNE YRLTSVGTVR KNKRQIPESF IRTDRQPNSS VFGFQKDITL
421 VSYAPKKNKV VVVMSTMHHD NSIDESTGEK QKPEMITFYN STKAGVDVVD ELCANYNVSR
481 NSKRWPMTLF YGVLNMAAIN ACIIYRTNKN VTIKRTEFIR SLGLSMIYEH LHSRNKKKNI
541 PTYLRQRIAM QLGEPSPRHV NVPGRYVRCQ DCPYKKDRKT KRSCNACAKP ICMEHAKFLC
601 ENCAELDSSL (SEQ ID NO:14631).
[0233] В некоторых вариантах осуществления гиперактивная транспозаза piggyBac (PB) или подобная piggyBac включает последовательность:
61 EANAIIANES DSDPDDDLPL SLVRQRASAS RQVSGPFYTS KDGTKWYKNC QRPNVRLRSE
121 NIVTEQAQVK NIARDASTEY ECWNIFVTSD MLQEILTHTN SSIRWRQTKT AAENSSAETS
181 FYMQETTLCE LKALIGLLYI AGLIKSNRQS LKDLWRTDGT GVDIFRTTMS LQRFQFLLNN
241 IRFDDKSTRD ERKQTDNMAA FRSIFDQFVQ SCQNAYSPSE FLTIDEMLLS FRGRCLFRVY
301 IPNKPAKYGI KILALVDAKN FYVKNLEVYA GKQPSGPYAV SNRPFEVVER LIQPVARSHR
361 NVTFDNWFTG YELMLHLLNE YRLTSVGTVR KNKTQIPENF IRTDRQPNSS VFGFQKDITL
421 VSYAPKKNKV VVVMSTMHHD NSIDESTGEK QKPEMITFYN STKAGVDVVD ELQANYNVSR
481 NSKRWPMTLF YGVLNMAAIN ACIIYRTNKN VTIKRTEFIR SLGLSMIYEH LHSRNKKKNI
541 PTYLRQRIEK QLGEPSPRHV NVPGRYVRCQ DCPYKKDRKT KRSCNACAKP ICMEHAKFLC
601 ENCAELDSSL (SEQ ID NO:14632).
[0234] В некоторых вариантах осуществления гиперактивная транспозаза piggyBac (PB) или подобная piggyBac включает последовательность:
61 EANAIIANES DSDPDDDLPL SLVRQRASAS RQVSGPFYTS KDGTKWYKNC QRPNVRLRSE
121 NIVTEQAQVK NIARDASTEY ECWNIFVTSD MLQEILTHTN SSIRWRQTKT AAENSSAETS
181 FYMQETTLCE LKALIGLLYI AGLIKSNRQS LKDLWRTDGT GVDIFRTTMS LQRFQFLQNN
241 IRFDDKSTRD ERKQTDNMAA FRSIFDQFVQ SCQNAYSPSE FLTIDEMLLS FRGRCLFRVY
301 IPNKPAKYGI KILALVDAKN FYVKNLEVYA GKQPSGPYAV SNRPFEVVER LIQPVARSHR
361 NVTFDNWFTG YELMLHLLNE YRLTSVGTVR KNKRQIPESF IRTDRQPNSS VFGFQKDITL
421 VSYAPKKNKV VVVMSTMHHD NSIDESTGEK QKPEMITFYN STKAGVDVVD ELCANYNVSR
481 NSKRWPMTLF YGVLNMAAIN ACIIYRTNKN VTIKRTEFIR SLGLSMIYEH LHSRNKKKNI
541 PTYLRQRIEK QLGEPSPRHV NVPGRYVRCQ DCPYKKDRKT KRSCNACAKP ICMEHAKFLC
601 ENCAELDSSL (SEQ ID NO:14633).
[0235] В некоторых вариантах осуществления гиперактивная транспозаза piggyBac (PB) или подобная piggyBac включает последовательность:
61 EANAIIANES DSDPDDDLPL SLVRQRASAS RQVSGPFYTS KDGTKWYKNC QRPNVRLRSE
121 NIVTEQAQVK NIARDASTEY ECWNIFVTSD MLQEILTHTN SSIRHRQTKT AAENSSAETS
181 FYMQETTLCE LKALIALLYL AGLIKSNRQS LKDLWRTDGT GVDIFRTTMS LQRFQFLQNN
241 IRFDDKSTRD ERKQTDNMAA FRSIFDQFVQ CCQNAYSPSE FLTIDEMLLS FRGRCLFRVY
301 IPNKPAKYGI KILALVDAKN DYVVNLEVYA GKQPSGPYAV SNRPFEVVER LIQPVARSHR
361 NVTFDNWFTG YELMLHLLNE YRLTSVGTVR KNKRQIPESF IRTDRQPNSS VFGFQKDITL
421 VSYAPKKNKV VVVMSTMHHD NSIDESTGEK QKPEMITFYN STKAGVDVVD ELCANYNVSR
481 NSKRWPMTLF YGVLNMAAIN ACIIYRTNKN VTIKRTEFIR SLGLSMIYEH LHSRNKKKNI
541 PTYLRQRIEK QLGEPSSRHV NVKGRYVRCQ DCPYKKDRKT KRSCNACAKP ICMEHAKFLC
601 ENCAELDSSL (SEQ ID NO:14634).
[0236] В некоторых вариантах осуществления гиперактивная транспозаза piggyBac (PB) или подобная piggyBac более активна, чем транспозаза SEQ ID NO:14505. В некоторых вариантах осуществления гиперактивная транспозаза piggyBac (PB) или подобная piggyBac по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98% или по меньшей мере на 99% или любой промежуточный процент идентична SEQ ID NO:14505.
[0237] В некоторых вариантах осуществления гиперактивная транспозаза piggyBac (PB) или подобная piggyBac включает аминокислотную замену в положении, выбранном из 92, 93, 96, 97, 165, 178, 189, 196, 200, 201, 211, 215, 235, 238, 246, 253, 258, 261, 263, 271, 303, 321, 324, 330, 373, 389, 399, 402, 403, 404, 448, 473, 484, 507, 523, 527, 528, 543, 549, 550, 557, 601, 605, 607, 609, 610 или их комбинации (относительно SEQ ID NO:14505). В некоторых вариантах осуществления гиперактивная транспозаза piggyBac (PB) или подобная piggyBac включает аминокислотную замену Q92A, V93L, V93M, P96G, F97H, F97C, H165E, H165W, E178S, E178H, C189P, A196G, L200I, A201Q, L211A, W215Y, G219S, Q235Y, Q235G, Q238L, K246I, K253V, M258V, F261L, S263K, C271S, N303R, F321W, F321D, V324K, V324H, A330V, L373C, L373V, V389L, S399N, R402K, T403L, D404Q, D404S, D404M, N441R, G448W, E449A, V469T, C473Q, R484K T507C, G523A, I527M, Y528K, Y543I, E549A, K550M, P557S, E601V, E605H, E605W, D607H, S609H, L610I или любой комбинации этого. В некоторых вариантах осуществления гиперактивная транспозаза piggyBac (PB) или подобная piggyBac включает аминокислотную замену Q92A, V93L, V93M, P96G, F97H, F97C, H165E, H165W, E178S, E178H, C189P, A196G, L200I, A201Q, L211A, W215Y, G219S, Q235Y, Q235G, Q238L, K246I, K253V, M258V, F261L, S263K, C271S, N303R, F321W, F321D, V324K, V324H, A330V, L373C, L373V, V389L, S399N, R402K, T403L, D404Q, D404S, D404M, N441R, G448W, E449A, V469T, C473Q, R484K T507C, G523A, I527M, Y528K, Y543I, E549A, K550M, P557S, E601V, E605H, E605W, D607H, S609H и L610I.
[0238] В некоторых вариантах осуществления гиперактивная транспозаза piggyBac (PB) или подобная piggyBac включает одну или более замен аминокислоты, которая не относится к дикому типу, где одна или более замен аминокислоты дикого типа включают замену E4X, A12X, M13X, L14X, E15X, D20X, E24X, S25X, S26X, S27X, D32X, H33X, E36X, E44X, E45X, E46X, I48X, D49X, R58X, A62X, N63X, A64X, I65X, I66X, N68X, E69X, D71X, S72X, D76X, P79X, R84X, Q85X, A87X, S88X, Q92X, V93X, S94X, G95X, P96X, F97X, Y98X, T99X, I145X, S149X, D150X, L152X, E154X, T157X, N160X, S161X, S162X, H165X, R166X, T168X, K169X, T170X, A171X, E173X, S175X, S176X, E178X, T179X, M183X, Q184X, T186X, T187X, L188X, C189X, L194X, I195X, A196X, L198X, L200X, A201X, L203X, I204X, K205X, A206X, N207X, Q209X, S210X, L211X, K212X, D213X, L214X, W215X, R216X, T217X, G219X, V222X, D223X, I224X, T227X, M229X, Q235X, L237X, Q238X, N239X, N240X, P302X, N303X, P305X, A306X, K307X, Y308X, I310X, K311X, I312X, L313X, A314X, L315X, V316X, D317X, A318X, K319X, N320X, F321X, Y322X, V323X, V324X, L326X, E327X, V328X, A330X, Q333X, P334X, S335X, G336X, P337X, A339X, V340X, S341X, N342X, R343X, P344X, F345X, E346X, V347X, E349X, I352X, Q353X, V355X, A356X, R357X, N361X, D365X, W367X, T369X, G370X, L373X, M374X, L375X, H376X, N379X, E380X, R382X, V386X, V389X, N392X, R394X, Q395X, S399X, F400X, I401X, R402X, T403X, D404X, R405X, Q406X, P407X, N408X, S409X, S410X, V411X, F412X, F414X, Q415X, I418X, T419X, L420X, N428XV432X, M434X, D440X, N441X, S442X, I443X, D444X, E445X, G448X, E449X, Q451X, K452X, M455X, I456X, T457X, F458X, S461X, A464X, V466X, Q468X, V469X, E471X, L472X, C473X, A474X, K483X, W485X, T488X, L489X, Y491X, G492X, V493X, M496X, I499X, C502X, I503X, T507X, K509X, N510X, V511X, T512X, I513X, R515X, E517X, S521X, G523X, L524X, S525X, I527X, Y528X, E529X, H532X, S533X, N535X, K536X, K537X, N539X, I540X, T542X, Y543X, Q546X, E549X, K550X, Q551X, G553X, E554X, P555X, S556X, P557X, R558X, H559X, V560X, N561X, V562X, P563X, G564X, R565X, Y566X, V567X, Q570X, D571X, P573X, Y574X, K576X, K581X, S583X, A586X, A588X, E594X, F598X, L599X, E601X, N602X, C603X, A604X, E605X, L606X, D607X, S608X, S609X или L610X (относительно SEQ ID NO:14505). Список гиперактивных аминокислотных замен можно найти в патенте США 10,041,077, содержание которого включено в настоящий документ посредством отсылки во всей своей полноте.
[0239] В некоторых вариантах осуществления транспозаза piggyBac (PB) или подобная piggyBac не способна к интеграции. В некоторых вариантах осуществления неспособная к интеграции транспозаза piggyBac или piggyBac-подобная транспозаза является транспозазой, которая может вырезать свой соответствующий транспозон, но при этом интегрирует вырезанный транспозон с более низкой частотой, чем соответствующая транспозаза дикого типа. В некоторых вариантах осуществления транспозаза piggyBac (PB) или подобная piggyBac представляет собой неспособный к интеграции вариант SEQ ID NO:14505.
[0240] В некоторых вариантах осуществления способная к вырезанию, неспособная к интеграции транспозаза piggyBac или piggyBac-подобная транспозаза включают одну или более замен аминокислоты, которая не относится к дикому типу, где одна или более замен аминокислоты дикого типа включают замену R9X, A12X, M13X, D20X, 21 тысяча иен, D23X, E24X, S25X, S26X, S27X, E28X, E30X, D32X, H33X, E36X, H37X, A39X, Y41X, D42X, T43X, E44X, E45X, E46X, R47X, D49X, S50X, S55X, A62X, N63X, A64X, I66X, A67X, N68X, E69X, D70X, D71X, S72X, D73X, P74X, D75X, D76X, D77X, I78X, S81X, V83X, R84X, Q85X, A87X, S88X, A89X, S90X, R91X, Q92X, V93X, S94X, G95X, P96X, F97X, Y98X, T99X, W012X, G103X, Y107X, K108X, L117X, I122X, Q128X, I312X, D135X, S137X, E139X, Y140X, I145X, S149X, D150X, Q153X, E154X, T157X, S161X, S162X, R164X, H165X, R166X, Q167X, T168X, K169X, T170X, A171X, A172X, E173X, R174X, S175X, S176X, A177X, E178X, T179X, S180X, Y182X, Q184X, E185X, T187X, L188X, C189X, L194X, I195X, A196X, L198X, L200X, A201X, L203X, I204X, K205X, N207X, Q209X, L211X, D213X, L214X, W215X, R216X, T217X, G219X, T220X, V222X, D223X, I224X, T227X, T228X, F234X, Q235X, L237X, Q238X, N239X, N240X, N303X, K304X, I310X, I312X, L313X, A314X, L315X, V316X, D317X, A318X, K319X, N320X, F321X, Y322X, V323X, V324X, N325X, L326X, E327X, V328X, A330X, G331X, K332X, Q333X, S335X, P337X, P344X, F345X, E349X, H359X, N361X, V362X, D365X, F368X, Y371X, E372X, L373X, H376X, E380X, R382X, R382X, V386X, G387X, T388X, V389X, K391X, N392X, R394X, Q395X, E398X, S399X, F400X, I401X, R402X, T403X, D404X, R405X, Q406X, P407X, N408X, S409X, S410X, Q415X, K416X, A424X, K426X, N428X, V430X, V432X, V433X, M434X, D436X, D440X, N441X, S442X, I443X, D444X, E445X, S446X, T447X, G448X, E449X, K450X, Q451X, E454X, M455X, I456X, T457X, F458X, S461X, A464X, V466X, Q468X, V469X, C473X, A474X, N475X, N477X, K483X, R484X, P486X, T488X, L489X, G492X, V493X, M496X, I499X, I503X, Y505X, T507X, N510X, V511X, T512X, I513X, K514X, T516X, E517X, S521X, G523X, L524X, S525X, I527X, Y528X, L531X, H532X, S533X, N535X, I540X, T542X, Y543X, R545X, Q546X, E549X, L552X, G553X, E554X, P555X, S556X, P557X, R558X, H559X, V560X, N561X, V562X, P563X, G564X, V567X, Q570X, D571X, P573X, Y574X, K575X, K576X, N585X, A586X, M593X, K596X, E601X, N602X, A604X, E605X, L606X, D607X, S608X, S609X или L610X (относительно SEQ ID NO:14505). Список дефицитных по интеграции аминокислотных замен можно найти в патенте США 10,041,077, содержание которого включено посредством отсылки во всей своей полноте.
[0241] В некоторых вариантах осуществления неспособная к интеграции транспозаза piggyBac или piggyBac-подобная транспозаза включает последовательность:
61 EANAIIANES DSDPDDDLPL SLVRQRASAS RQVSGPFYTS KDGTKWYKNC QRPNVRLRSE
121 NIVTEQAQVK NIARDASTEY ECWNIFVTSD MLQEILTHTN SSIRHRQTKT AAENSSAETS
181 FYMQETTLCE LKALIALLYL AGLIKSNRQS LKDLWRKDGT GVDIFRTTMS LQRFQFLLNN
241 IRFDDISTRD ERKQTDNMAA FRSIFDQFVQ CCQNAYSPSE FLTIDEMLLS FRGRCLFRVY
301 IPNKPAKYGI KILALVDAKN FYVVNLEVYA GKQPSGPYAV SNRPFEVVER LIQPVARSHR
361 NVTFDNWFTG YELMLHLLNE YRLTSVGTVR KNKRQIPESF IRTDRQPNSS VFGFQKDITL
421 VSYAPKKNKV VVVMSTMHHD NSIDESTGEK QKPEMITFYN STKAGVDVVD ELCANYNVSR
481 NSKKWPMTLF YGVLNMAAIN ACIIYRTNKN VTIKRTEFIR SLGLSMMYEH LHSRNKKKNI
541 PTYLRQRIEK QLGEPVPRHV NVPGRYVRCQ DCPYKKDRKT KRSCNACAKP ICMEHAKFLC
601 ENCAELDSSL (SEQ ID NO:14606).
В некоторых вариантах осуществления неспособная к интеграции транспозаза piggyBac или piggyBac-подобная транспозаза включает последовательность:
61 EANAIIANES DSDPDDDLPL SLVRQRASAS RQVSGPFYTS KDGTKWYKNC QRPNVRLRSE
121 NIVTEQAQVK NIARDASTEY ECWNIFVTSD MLQEILTHTN SSIRHRQTKT AAENSSAETS
181 FYMQETTLCE LKALIGLLYL AGLIKSNRQS LKDLWRTDGT GVDIFRTTMS LQRFYFLQNN
241 IRFDDKSTLD ERKQTDNMAA FRSIFDQFVQ SCQNAYSPSE FLTIDEMLLS FRGRCLFRVY
301 IPNKPAKYGI KILALVDAKN FYVVNLEVYA GKQPSGPYAV SNRPFEVVER LIQPVARSHR
361 NVTFDNWFTG YELMLHLLNE YRLTSVGTVR KNKRQIPESF IRTDRQPNSS VFGFQKDITL
421 VSYAPKKNKV VVVMSTMHHD NSIDESTGEK QKPEMITFYN STKAGVDVVD ELCANYNVSR
481 NSKRWPMTLF YGVLNMAAIN ACIIYRTNKN VTIKRTEFIR SLGLSMIYEH LHSRNKKKNI
541 PTYLRQRIEK QLGEPSPRHV NYPGRYVRCQ DCPYKKDRKT KRSCNACAKP ICMEHAKFLC
601 VNCAELDSSL (SEQ ID NO:14607).
В некоторых вариантах осуществления транспозаза piggyBac (PB) или подобная piggyBac, которая не способна к интеграции, включает последовательность:
61 EANAIIANES DSDPDDDLPL SLVRQRASAS RQVSGPFYTS KDGTKWYKNC QRPNVRLRSE
121 NIVTEQAQVK NIARDASTEY ECWNIFVTSD MLQEILTHTN SSIRHRQTKT AAENSSAETS
181 FYMQETTLCE LKALIALLYL AGLIKSNRQS LKDLWRKDGT GVDIFRTTMS LQRFQFLLNN
241 IRFDDKSTRD ERKQTDNMAA FRSIFDQFVQ CCQNAYSPSE FLTIDEMLLS FRGRCLFRVY
301 IPNKPAKYGI KILALVDAKN DYVVNLEVYA GKQPSGPYAV SNRPFEVVER LIQPVARSHR
361 NVTFDNWFTG YECMLHLLNE YRLTSVGTVR KNKRQIPESF IRTDRQPNSS VFGFQKDITL
421 VSYAPKKNKV VVVMSTMHHD NSIDESTGEK QKPEMITFYN STKAGVDVVD ELCANYNVSR
481 NSKKWPMTLF YGVLNMAAIN ACIIYRTNKN VTIKRTEFIR SLGLSMIKEH LHSRNKKKNI
541 PTYLRQRIEK QLGEPSPRHV NVPGRYVRCQ DCPYKKDRKT KRSCNACAKP ICMEHAKFLC
601 ENCAELDSSL (SEQ ID NO:14608).
В некоторых вариантах осуществления неспособная к интеграции транспозаза включает последовательность, которая по меньшей мере на 90% идентична SEQ ID NO:14608.
[0242] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон выделен или получен из Bombyx mori. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ttttataaaa ttttcgtctg acaacactag cgcgctcagt agctggaggc aggagcgtgc
121 gggaggggat agtggcgtga tcgcagtgtg gcacgggaca ccggcgagat attcgtgtgc
181 aaacctgttt cgggtatgtt ataccctgcc tcattgttga cgtatttttt ttatgtaatt
241 tttccgatta ttaatttcaa ctgttttatt ggtattttta tgttatccat tgttcttttt
301 ttatgattta ctgtatcggt tgtctttcgt tcctttagtt gagttttttt ttattatttt
361 cagtttttga tcaaa (SEQ ID NO:14506).
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ttcagtatta ggttgattta tattccaaag aataatattt ttgttaaatt gttgattttt
121 gtaaacctct aaatgtttgt tgctaaaatt actgtgttta agaaaaagat taataaataa
181 taataatttc ataattaaaa acttctttca ttgaatgcca ttaaataaac cattatttta
241 caaaataaga tcaacataat tgagtaaata ataataagaa caatattata gtacaacaaa
301 atatgggtat gtcataccct gccacattct tgatgtaact ttttttcacc tcatgctcgc
361 cgggttat (SEQ ID NO:14507).
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ttttataaaa ttttcgtctg acaacactag cgcgctcagt agctggaggc aggagcgtgc
121 gggaggggat agtggcgtga tcgcagtgtg gcacgggaca ccggcgagat attcgtgtgc
181 aaacctgttt cgggtatgtt ataccctgcc tcat (SEQ ID NO:14508).
В некоторых вариантах осуществления транспозон piggyBac (PB) или подобный piggyBac включает последовательность:
61 tattttacaa aataagatca acataattga gtaaataata ataagaacaa tattatagta
121 caacaaaata tgggtatgtc ataccctgcc acattcttga tgtaactttt tttcacctca
181 tgctcgccgg gttat (SEQ ID NO:14509).
[0243] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает 5'-последовательность, соответствующую SEQ ID NO:14506, и 3'-последовательность, соответствующую SEQ ID NO:14507. В некоторых вариантах осуществления один конец транспозона piggyBac или piggyBac-подобного транспозона по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или любой промежуточный процент идентичен SEQ ID NO:14506, и другой конец транспозона piggyBac или piggyBac-подобного транспозона по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или любой промежуточный процент идентичен SEQ ID NO:14507. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает SEQ ID NO:14506 и SEQ ID NO:14507 или SEQ ID NO:14509. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает SEQ ID NO:14508 и SEQ ID NO:14507 или SEQ ID NO:14509. В некоторых вариантах осуществления 5' и 3'-конец транспозона имеет общую повторяющуюся последовательность длиной 16 пн CCCGGCGAGCATGAGG (SEQ ID NO:14510) на своих концах, непосредственно примыкающую к целевому сайту вставки 5'-TTAT-3, которая инвертирована по ориентации на двух концах. В некоторых вариантах осуществления 5'-конец транспозона начинается с последовательности, включающей 5'-TTATCCCGGCGAGCATGAGG-3 (SEQ ID NO:14511), и 3'-конец транспозона заканчивается последовательностью, включающей обратный комплемент этой последовательности: 5'-CCTCATGCTCGCCGGGTTAT-3' (SEQ ID NO:14512).
[0244] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает один конец, включающий по меньшей мере 14, 16, 18, 20, 30 или 40 последовательных нуклеотидов SEQ ID NO:14506 или SEQ ID NO:14508. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает один конец, включающий по меньшей мере 14, 16, 18, 20, 30 или 40 последовательных нуклеотидов SEQ ID NO:14507 или SEQ ID NO:14509. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает один конец, обладающий по меньшей мере 90% идентичностью с SEQ ID NO:14506 или SEQ ID NO:14508. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает один конец, обладающий по меньшей мере 90% идентичностью с SEQ ID NO:14507 или SEQ ID NO:14509.
[0245] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ttttataaaa ttttcgtctg acaacactag cgcgctcagt agctggaggc aggagcgtgc
121 gggaggggat agtggcgtga tcgcagtgtg gcacgggaca ccggcgagat attcgtgtgc
181 aaacctgttt cgggtatgtt ataccctgcc tcattgttga cgtatttttt ttatgtaatt
241 tttccgatta ttaatttcaa ctgttttatt ggtattttta tgttatccat tgttcttttt
301 ttatgattta ctgtatcggt tgtctttcgt tcctttagtt gagttttttt ttattatttt
361 cagtttttga tcaaa (SEQ ID NO:14515).
[0246] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ttcagtatta ggttgattta tattccaaag aataatattt ttgttaaatt gttgattttt
121 gtaaacctct aaatgtttgt tgctaaaatt actgtgttta agaaaaagat taataaataa
181 taataatttc ataattaaaa acttctttca ttgaatgcca ttaaataatt cattatttta
241 caaaataaga tcaacataat tgagtaaata ataataagaa caatattata gtacaacaaa
301 atatgggtat gtcataccct tttttttttt tttttttttt ttttttcggg tagagggccg
361 aacctcctac gaggtccccg cgcaaaaggg gcgcgcgggg tatgtgagac tcaacgatct
421 gcatggtgtt gtgagcagac cgcgggccca aggattttag agcccaccca ctaaacgact
481 cctctgcact cttacacccg acgtccgatc ccctccgagg tcagaacccg gatgaggtag
541 gggggctacc gcggtcaaca ctacaaccag acggcgcggc tcaccccaag gacgcccagc
601 cgacggagcc ttcgaggcga atcgaaggct ctgaaacgtc ggccgtctcg gtacggcagc
661 ccgtcgggcc gcccagacgg tgccgctggt gtcccggaat accccgctgg accagaacca
721 gcctgccggg tcgggacgcg atacaccgtc gaccggtcgc tctaatcact ccacggcagc
781 gcgctagagt gctggta (SEQ ID NO:14516).
[0247] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность CCCGGCGAGCATGAGG (SEQ ID NO:14510). В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность ITR SEQ ID NO:14510. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность TTATCCCGGCGAGCATGAGG (SEQ ID NO:14511). В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает по меньшей мере 16 последовательных нуклеотидов из SEQ ID NO:14511. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность CCTCATGCTCGCCGGGTTAT (SEQ ID NO:14512). В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает по меньшей мере 16 последовательных нуклеотидов из SEQ ID NO:14512. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает один конец, включающий по меньшей мере 16 последовательных нуклеотидов из SEQ ID NO:14511, и один конец, включающий по меньшей мере 16 последовательных нуклеотидов из SEQ ID NO:14512. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает SEQ ID NO:14511 и SEQ ID NO:14512. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность TTAACCCGGCGAGCATGAGG (SEQ ID NO:14513). В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность CCTCATGCTCGCCGGGTTAA (SEQ ID NO:14514).
[0248] В некоторых вариантах осуществления транспозон piggyBac или piggyBack-подобный транспозон может иметь концы, включающие SEQ ID NO:14506 и SEQ ID NO:14507, или вариант одного или обоих из них, обладающий по меньшей мере 90% идентичностью последовательности с SEQ ID NO:14506 или SEQ ID NO:14507, и транспозаза piggyBac или piggyBac-подобная транспозаза имеет последовательность SEQ ID NO:14504 или SEQ ID NO:14505, или последовательность, обладающую по меньшей мере 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любым промежуточным процентом идентичности с SEQ ID NO:14504 или SEQ ID NO:14505. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает гетерологичный полинуклеотид, встроенный между парой инвертированных повторов, где транспозон способен к перемещению транспозазой piggyBac или piggyBac-подобной транспозазой, обладающей по меньшей мере 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любым промежуточным процентом идентичности с SEQ ID NO:14504 или SEQ ID NO:14505. В некоторых вариантах осуществления транспозон включает два конца транспозона, каждый из которых включает SEQ ID NO:14510 в инвертированных ориентациях на двух концах транспозона. В некоторых вариантах осуществления каждый инвертированный концевой повтор (ITR) по меньшей мере на 90% идентичен SEQ ID NO:14510.
[0249] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон способен к вставке транспозазой piggyBac или piggyBac-подобной транспозазой в последовательность 5'-TTAT-3 в нуклеиновой кислоте-мишени. В некоторых вариантах осуществления один конец транспозона piggyBac или piggyBac-подобного транспозона включает по меньшей мере 16 последовательных нуклеотидов из SEQ ID NO:14506, и другой конец транспозона включает по меньшей мере 16 последовательных нуклеотидов из SEQ ID NO:14507. В некоторых вариантах осуществления один конец транспозона piggyBac или piggyBac-подобного транспозона включает по меньшей мере 17, по меньшей мере 18, по меньшей мере 19, по меньшей мере 20, по меньшей мере 22, по меньшей мере 25, по меньшей мере 30 последовательных нуклеотидов из SEQ ID NO:14506, и другой конец транспозона включает по меньшей мере 17, по меньшей мере 18, по меньшей мере 19, по меньшей мере 20, по меньшей мере 22, по меньшей мере 25, по меньшей мере 30 последовательных нуклеотидов из SEQ ID NO:14507.
[0250] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает концы транспозона (каждый конец включает ITR), соответствующие SEQ ID NO:14506 и SEQ ID NO:14507, и имеет последовательность-мишень, соответствующую 5'-TTAT3'. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон также включает последовательность, кодирующую транспозазу (например, SEQ ID NO:14505). В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает один конец транспозона, соответствующий SEQ ID NO:14506, и второй конец транспозона, соответствующий SEQ ID NO:14516. Последовательность SEQ ID NO:14516 очень похожа на SEQ ID NO:14507, но имеет большую вставку на небольшом расстоянии перед ITR. Несмотря на то, что последовательности ITR для двух концов транспозона идентичны (они обе идентичны SEQ ID NO:14510), они имеют разные последовательности-мишени: второй транспозон имеет последовательность-мишень, соответствующую 5'-TTAA-3', что подтверждает то, что никакое изменение в последовательности ITR не требуется для изменения специфичности по отношению к последовательности-мишени. Транспозаза piggyBac или piggyBac-подобная транспозаза (SEQ ID NO:14504), которая ассоциирована с сайтом-мишенью 5'-TTAA-3', отличается от 5'-TTAT-3'-ассоциированной транспозазы (SEQ ID NO:14505) только изменением 4 аминокислот (D322Y, S473C, A507T, H582R). В некоторых вариантах осуществления транспозаза piggyBac (PB) или подобная piggyBac (SEQ ID NO:14504), которая ассоциирована с сайтом-мишенью 5'-TTAA-3', менее активна, чем 5'-TTAT-3'-ассоциированная транспозаза piggyBac или piggyBac-подобная транспозаза (SEQ ID NO:14505) в отношении транспозона с концами 5'-TTAT-3'. В некоторых вариантах осуществления транспозоны piggyBac или подобные piggyBac с сайтами-мишенями 5'-TTAA-3' могут быть превращены в транспозазы piggyBac или подобные piggyBac с сайтами-мишенями 5'-TTAT-3 путем замены сайтов-мишеней 5'-TTAA-3' на 5'-TTAT-3'. Такие транспозоны могут использоваться либо с транспозазой piggyBac или piggyBac-подобной транспозазой, такой как SEQ ID NO:14504, которая распознает последовательность-мишень 5'-TTAT-3', или с вариантом транспозазы, первоначально ассоциированной с транспозоном 5'-TTAA-3'. В некоторых вариантах осуществления высокое подобие между 5'-TTAA-3' и 5'-TTAT-3' транспозазами piggyBac или подобными piggyBac демонстрирует, что очень небольшие изменения аминокислотной последовательности транспозазы piggyBac или подобной piggyBac приводят к изменению специфичности в отношении последовательности-мишени. В некоторых вариантах осуществления модификации любой системы переноса генов на основе транспозона-транспозазы piggyBac или подобных piggyBac, в которой последовательности-мишени 5'-TTAA-3' заменены последовательностями-мишенями 5'-TTAT-3', ITR-повторы остаются такими же, а транспозаза является исходной транспозазой piggyBac или piggyBac-подобной транспозазой или ее вариантом, полученным в результате применения низко уровня мутагенеза для введения мутаций в транспозазу. В некоторых вариантах осуществления системы переноса на основе транспозона-транспозазы piggyBac или подобных piggyBac могут быть получены в результате модификации 5'-TTAT-3' активных систем переноса генов на основе транспозона-транспозазы piggyBac или подобных piggyBac, в которых 5'-TTAT-3' последовательности-мишени заменяют последовательностями-мишенями 5'-TTAA-3', ITR-повторы остаются такими же, а транспозаза piggyBac или piggyBac-подобная транспозаза являются исходной транспозазой или ее вариантом.
[0251] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон выделен или получен из Bombyx mori. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ataaaatttt cgtctgacaa cactagcgcg ctcagtagct ggaggcagga gcgtgcggga
121 ggggatagtg gcgtgatcgc agtgtggcac gggacaccgg cgagatattc gtgtgcaaac
181 ctgtttcggg tatgttatac cctgcctcat tgttgacgta t (SEQ ID NO:14577).
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 gccattaaat aaaccattat tttacaaaat aagatcaaca taattgagta aataataata
121 agaacaatat tatagtacaa caaaatatgg gtatgtcata ccctgccaca ttcttgatgt
181 aacttttttt cacctcatgc tcgccggg (SEQ ID NO:14578).
В некоторых вариантах осуществления транспозон включает по меньшей мере 16 последовательных оснований из SEQ ID NO:14577 и по меньшей мере 16 последовательных оснований из SEQ ID NO:14578, и инвертированные концевые повторы, которые по меньшей мере на 87% идентичны CCCGGCGAGCATGAGG (SEQ ID NO:14510).
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ataaaatttt cgtctgacaa cactagcgcg ctcagtagct ggaggcagga gcgtgcggga
121 ggggatagtg gcgtgatcgc agtgtggcac gggacaccgg cgagatattc gtgtgcaaac
181 ctgtttcggg tatgttatac cctgcctcat tgttgacgta ttttttttat gtaatttttc
241 cgattattaa tttcaactgt tttattggta tttttatgtt atccattgtt ctttttttat
301 gatttactgt atcggttgtc tttcgttcct ttagttgagt ttttttttat tattttcagt
361 ttttgatcaa (SEQ ID NO:14595).
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ttcagtatta ggttgattta tattccaaag aataatattt ttgttaaatt gttgattttt
121 gtaaacctct aaatgtttgt tgctaaaatt actgtgttta agaaaaagat taataaataa
181 taataatttc ataattaaaa acttctttca ttgaatgcca ttaaataaac cattatttta
241 caaaataaga tcaacataat tgagtaaata ataataagaa caatattata gtacaacaaa
301 atatgggtat gtcataccct gccacattct tgatgtaact ttttttcacc tcatgctcgc
361 cggg (SEQ ID NO:14596).
[0252] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает SEQ ID NO:14595 и SEQ ID NO:14596, и перемещается транспозазой piggyBac или piggyBac-подобной транспозазой SEQ ID NO:14505. В некоторых вариантах осуществления ITR-повторы SEQ ID NO:14595 и SEQ ID NO:14596 не фланкированы последовательностью 5'-TTAA-3'. В некоторых вариантах осуществления ITR-повторы SEQ ID NO:14595 и SEQ ID NO:14596 фланкированы последовательностью 5'-TTAT-3'.
[0253] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ataaaatttt cgtctgacaa cactagcgcg ctcagtagct ggaggcagga gcgtgcggga
121 ggggatagtg gcgtgatcgc agtgtggcac gggacaccgg cgagatattc gtgtgcaaac
181 ctgtttcggg tatgttatac cctgcctcat tgttgacgta ttttttttat gtaatttttc
241 cgattattaa tttcaactgt tttattggta tttttatgtt atccattgtt ctttttttat
301 g (SEQ ID NO:14597).
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 acaacactag cgcgctcagt agctggaggc aggagcgtgc gggaggggat agtggcgtga
121 tcgcagtgtg gcacgggaca ccggcgagat attcgtgtgc aaacctgttt cgggtatgtt
181 ataccctgcc tcattgttga cgtatttttt ttatgtaatt tttccgatta ttaatttcaa
241 ctgttttatt ggtattttta tgttatccat tgttcttttt ttatg
(SEQ ID NO:14598).
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 acaacactag cgcgctcagt agctggaggc aggagcgtgc gggaggggat agtggcgtga
121 tcgcagtgtg gcacgggaca ccggcgagat attcgtgtgc aaacctgttt cgggtatgtt
181 ataccctgcc tcattgttga cgtat (SEQ ID NO:14599).
В некоторых вариантах осуществления 5'-конец транспозона piggyBac или piggyBac-подобного транспозона включают последовательность SEQ ID NO:14577, SEQ ID NO:14595, или SEQ ID NO:14597-14599. В некоторых вариантах осуществления перед 5'-концом транспозона piggyBac или piggyBac-подобного транспозона расположена 5'-последовательность-мишень.
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ttcagtatta ggttgattta tattccaaag aataatattt ttgttaaatt gttgattttt
121 gtaaacctct aaatgtttgt tgctaaaatt actgtgttta agaaaaagat taataaataa
181 taataatttc ataattaaaa acttctttca ttgaatgcca ttaaataaac cattatttta
241 caaaataaga tcaacataat tgagtaaata ataataagaa caatattata gtacaacaaa
301 atatgggtat gtcataccct gccacattct tgatgtaact ttttttcacc tcatgctcgc
361 cggg (SEQ ID NO:14600).
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 gccattaaat aaaccattat tttacaaaat aagatcaaca taattgagta aataataata
121 agaacaatat tatagtacaa caaaatatgg gtatgtcata ccctgccaca ttcttgatgt
181 aacttttttt ca (SEQ ID NO:14601).
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ataaaatttt cgtctgacaa cactagcgcg ctcagtagct ggaggcagga gcgtgcggga
121 ggggatagtg gcgtgatcgc agtgtggcac gggacaccgg cgagatattc gtgtgcaaac
181 ctgtttcggg tatgttatac cctgcctcat tgttgacgta ttttttttat gtaatttttc
241 cgattattaa tttcaactgt tttattggta tttttatgtt atccattgtt ctttttttat
301 gatttactgt atcggttgtc tttcgttcct ttagttgagt ttttttttat tattttcagt
361 ttttgatcaa (SEQ ID NO:14602).
[0254] В некоторых вариантах осуществления 3'-конец транспозона piggyBac или piggyBac-подобного транспозона включают последовательность SEQ ID NO:14578, SEQ ID NO:14596 или SEQ ID NO:14600-14601. В некоторых вариантах осуществления после 3'-конца транспозона piggyBac или piggyBac-подобного транспозона расположена 3'-последовательность-мишень. В некоторых вариантах осуществления транспозон перемещается транспозазой SEQ ID NO:14505. В некоторых вариантах осуществления 5' и 3' концы транспозона piggyBac или piggyBac-подобного транспозона имеют общую повторяющуюся последовательность длиной 16 пн SEQ ID NO:14510 в инвертированной ориентации и непосредственно примыкающую к последовательности-мишени. В некоторых вариантах осуществления 5'-конец транспозона начинается с SEQ ID NO:14510, и 3'-конец транспозона заканчивается обратным комплементом SEQ ID NO:14510, 5'-CCTCATGCTCGCCGGG-3' (SEQ ID NO:14603). В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает ITR, обладающий по меньшей мере 93%, по меньшей мере 87% или по меньшей мере 81% или любым промежуточным процентом идентичности с SEQ ID NO:14510 или SEQ ID NO:14603. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность-мишень, после которой расположен 5'-конец транспозона, включающий последовательность, выбранную из SEQ ID NO:88, 105 или 107, и 3'-конец транспозона, включающий SEQ ID NO:14578 или 106, после которого расположена последовательность-мишень. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает один конец, включающий последовательность, которая по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 99% или любой промежуточный процент идентична SEQ ID NO:14577, и один конец, включающий последовательность, которая по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 99% или любой промежуточный процент идентична SEQ ID NO:14578. В некоторых вариантах осуществления один конец транспозона включает по меньшей мере 14, по меньшей мере 16, по меньшей мере 18 или по меньшей мере 20 последовательных оснований из SEQ ID NO:14577, и один конец транспозона включает по меньшей мере 14, по меньшей мере 16, по меньшей мере 18 или по меньшей мере 20 последовательных оснований из SEQ ID NO:14578.
[0255] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает два конца транспозона, где каждый из концов транспозона включают последовательность, которая по меньшей мере на 81% идентична, по меньшей мере на 87% идентична или по меньшей мере на 93% идентична или на любой промежуточный процент идентична SEQ ID NO:14510 в инвертированной ориентации на двух концах транспозона. Один конец может дополнительно включать по меньшей мере 14, по меньшей мере 16, по меньшей мере 18 или по меньшей мере 20 последовательных оснований из SEQ ID NO:14599, а другой конец может дополнительно включать по меньшей мере 14, по меньшей мере 16, по меньшей мере 18 или по меньшей мере 20 последовательных оснований из SEQ ID NO:14601. Транспозон piggyBac или piggyBac-подобный транспозон могут быть перемещены транспозазой SEQ ID NO:14505, при этом транспозаза может быть необязательно слита с сигналом ядерной локализации.
[0256] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает SEQ ID NO:14595 и SEQ ID NO:14596, и транспозаза piggyBac или piggyBac-подобная транспозаза включает SEQ ID NO:14504 или SEQ ID NO:14505. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает SEQ ID NO:14597 и SEQ ID NO:14596, и транспозаза piggyBac или piggyBac-подобная транспозаза включает SEQ ID NO:14504 или SEQ ID NO:14505. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает SEQ ID NO:14595 и SEQ ID NO:14578, и транспозаза piggyBac или piggyBac-подобная транспозаза включает SEQ ID NO:14504 или SEQ ID NO:14505. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает SEQ ID NO:14602 и SEQ ID NO:14600, и транспозаза piggyBac или piggyBac-подобная транспозаза включает SEQ ID NO:14504 или SEQ ID NO:14505.
[0257] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает 5'-конец, включающий 1, 2, 3, 4, 5, 6 или 7 последовательностей, выбранных из ATGAGGCAGGGTAT (SEQ ID NO:14614), ATACCCTGCCTCAT (SEQ ID NO:14615), GGCAGGGTAT (SEQ ID NO:14616), ATACCCTGCC (SEQ ID NO:14617), TAAAATTTTA (SEQ ID NO:14618), ATTTTATAAAAT (SEQ ID NO:14619), TCATACCCTG (SEQ ID NO:14620) и TAAATAATAATAA (SEQ ID NO:14621). В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает 3'-конец, включающий 1, 2 или 3 последовательности, выбранные из SEQ ID NO:14617, SEQ ID NO:14620 и SEQ ID NO:14621.
[0258] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза является ферментом транспозазой piggyBac или piggyBac-подобной транспозазой. В некоторых вариантах осуществления фермент транспозаза piggyBac или piggyBac-подобная транспозаза выделена или получена из Xenopus tropicalis. Фермент транспозаза piggyBac или piggyBac-подобная транспозаза может включать или состоять из аминокислотной последовательности, которая по меньшей мере на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент идентична последовательности:
61 DEDVDDLEDQ EAGDRADAAA GGEPAWGPPC NFPPEIPPFT TVPGVKVDTS NFEPINFFQL
121 FMTEAILQDM VLYTNVYAEQ YLTQNPLPRY ARAHAWHPTD IAEMKRFVGL TLAMGLIKAN
181 SLESYWDTTT VLSIPVFSAT MSRNRYQLLL RFLHFNNNAT AVPPDQPGHD RLHKLRPLID
241 SLSERFAAVY TPCQNICIDE SLLLFKGRLQ FRQYIPSKRA RYGIKFYKLC ESSSGYTSYF
301 LIYEGKDSKL DPPGCPPDLT VSGKIVWELI SPLLGQGFHL YVDNFYSSIP LFTALYCLDT
361 PACGTINRNR KGLPRALLDK KLNRGETYAL RKNELLAIKF FDKKNVFMLT SIHDESVIRE
421 QRVGRPPKNK PLCSKEYSKY MGGVDRTDQL QHYYNATRKT RAWYKKVGIY LIQMALRNSY
481 IVYKAAVPGP KLSYYKYQLQ ILPALLFGGV EEQTVPEMPP SDNVARLIGK HFIDTLPPTP
541 GKQRPQKGCK VCRKRGIRRD TRYYCPKCPR NPGLCFKPCF EIYHTQLHY
(SEQ ID NO:14517).
[0259] В некоторых вариантах осуществления транспозаза piggyBac или piggyBac-подобная транспозаза представляет собой гиперактивный вариант SEQ ID NO:14517. В некоторых вариантах осуществления транспозаза piggyBac или piggyBac-подобная транспозаза представляет собой не способный к интеграции вариант SEQ ID NO:14517. Фермент транспозаза piggyBac или piggyBac-подобная транспозаза может включать или состоять из аминокислотной последовательности, которая по меньшей мере на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент идентична последовательности:
61 DEDVDDLEDQ EAGDRADAAA GGEPAWGPPC NFPPEIPPFT TVPGVKVDTS NFEPINFFQL
121 FMTEAILQDM VLYTNVYAEQ YLTQNPLPRY ARAHAWHPTD IAEMKRFVGL TLAMGLIKAN
181 SLESYWNTTT VLSIPVFSAT MSRNRYQLLL RFLHFNNNAT AVPPDQPDHD RLHKLRPLID
241 SLSERFAAVY TPCQNICIDE SLLLFKGRLR FRQYIPSKRA RYGIKFYKLC ESSSGYTSYF
301 LIYEGKDSKL DPPGCPPDLT VSGKIVWELI SPLLGQGFHL YVDNFYSSIP LFTALYCLDT
361 PACGTINRTR KGLPRALLDK KLNRGETYAL RKNELLAIKF FDKKNVFMLT SIHDESVIRE
421 QRVGRPPKNK PLCSKEYSKY MGGVDRTDQL QHYYNATRKT SAWYKKVGIY LIQMALRNSY
481 IVYKAAVPGP KLSYYKYQLQ ILPALLFGGV EEQTVPEMLP SDNVARLIGK HFIDTLPPTP
541 GKQRPQKGCK VCRKRGIRRD TRYYCPKCPR NPGLCFKPCF EIYHTQLHY
(SEQ ID NO:14518).
[0260] В некоторых вариантах осуществления транспозаза piggyBac или piggyBac-подобная транспозаза выделена или получена из Xenopus tropicalis. В некоторых вариантах осуществления транспозаза piggyBac или piggyBac-подобная транспозаза представляет собой гиперактивную транспозазу piggyBac или подобную piggyBac. В некоторых вариантах осуществления гиперактивная транспозаза piggyBac или piggyBac-подобная транспозаза включает последовательность, которая по меньшей мере на 90% идентична последовательности:
61 DEDVDDLEDQ EAGDRADAAA GGEPAWGPPC NFPPEIPPFT TVPGVKVDTS NFEPINFFQL
121 FMTEAILQDM VLYTNVYAEQ YLTQNPLTRG ARAHAWHPTD IAEMKRFVGL TLAMGLIKAN
181 SIESYWDTTT VLSIPVFGAT MSRNRYQLLL RFLHFNNNAT AVPPDQPGHD RLHKLRPLID
241 SLSERFANVY TPCQNICIDE SLMLFKGRLQ FRQYIPSKRA RYGIKFYKLC ESSTGYTSYF
301 LIYEGKDSKL DPPGCPPDLT VSGKIVWELI SPLLGQGFHL YVDNFYSSIP LFTALYCLNT
361 PACGTINRNR KGLPRALLDK KLNRGETYAL RKNELLAIKF FDKKNVFMLT SIHDESVIRE
421 QRVGRPPKNK PLCSKEYSKY MGGVDRTDQL QHYYNATRKT RHWYKKVGIY LIQMALRNSY
481 IVYKAAVPGP KLSYYKYQLQ ILPALLFGGV EEQTVPEMPD SDNVARLIGK HFIDTLPPTP
541 GKQRPQKGCK VCRKRGIRRD TRYYCPKCPR NPGLCRKPCF EIYHTQLHY
(SEQ ID NO:14572).
[0261] В некоторых вариантах осуществления транспозаза piggyBac или piggyBac-подобная транспозаза представляет собой гиперактивную транспозазу piggyBac или подобную piggyBac. Гиперактивная транспозаза piggyBac или piggyBac-подобная транспозаза является транспозазой, которая более активна, чем природный вариант, из которого она получена. В некоторых вариантах осуществления гиперактивная транспозаза piggyBac или piggyBac-подобная транспозаза более активна, чем транспозаза SEQ ID NO:14517. В некоторых вариантах осуществления гиперактивная транспозаза piggyBac или piggyBac-подобная транспозаза включает последовательность:
61 DEDVDDLEDQ EAGDRADAAA GGEPAWGPPC NFPPEIPPFT TVPGVKVDTS NFEPINFFQL
121 FMTEAILQDM VLYTNVYAEQ YLTQNPLTRG ARAHAWHPTD IAEMKRFVGL TLAMGLIKAN
181 SIESYWDTTT VLSIPVFGAT MSRNRYQLLL RFLHFNNNAT AVPPDQPGHD RLHKLRPLID
241 SLSERFANVY TPCQNICIDE SLMLFKGRLQ FRQYIPSKRA RYGIKFYKLC ESSTGYTSYF
301 LIYEGKDSKL DPPGCPPDLT VSGKIVWELI SPLLGQGFHL YVDNFYSSIP LFTALYCLNT
361 PACGTINRNR KGLPRALLDK KLNRGETYAL RKNELLAIKF FDKKNVFMLT SIHDESVIRE
421 QRVGRPPKNK PLCSKEYSKY MGGVDRTDQL QHYYNATRKT RHWYKKVGIY LIQMALRNSY
481 IVYKAAVPGP KLSYYKYQLQ ILPALLFGGV EEQTVPEMPD SDNVARLIGK HFIDTLPPTP
541 GKQRPQKGCK VCRKRGIRRD TRYYCPKCPR NPGLCRKPCF EIYHTQLHY
(SEQ ID NO:14572).
[0262] В некоторых вариантах осуществления гиперактивная транспозаза piggyBac или piggyBac-подобная транспозаза включает последовательность:
61 DEDVDDLEDQ EAGDRADAAA GGEPAWGPPC NFPPEIPPFT TVPGVKVDTS NFEPINFFQL
121 FMTEAILQDM VLYTNVYAEQ YLTQNPLTRY ARAHAWHPTD IAEMKRFVGL TLAMGLIKAN
181 SLESYWDTTT VLSIPVFSAT MSRNRYQLLL RFLHFNNNAT AVPPDQPGHD RLHKLRPLID
241 SLSERFAAVY TPCQNICIDE SLLLFKGRLQ FRQYIPSKRA RYGIKFYKLC ESSSGYTSYF
301 LIYEGKDSKL DPPGCPPDLT VSGKIVWELI SPLLGQGFHL YVDNFYSSIP LFTALYCLNT
361 PACGTINRNR KGLPRALLDK KLNRGETYAL RKNELLAIKF FDKKNVFMLT SIHDESVIRE
421 QRVGRPPKNK PLCSKEYSKY MGGVDRTDQL QHYYNATRKT RHWYKKVGIY LIQMALRNSY
481 IVYKAAVPGP KLSYYKYQLQ ILPALLFGGV EEQTVPEMPP SDNVARLIGK HFIDTLPPTP
541 GKQRPQKGCK VCRKRGIRRD TRYYCPKCPR NPGLCRKPCF EIYHTQLHY
(SEQ ID NO:14624).
[0263] В некоторых вариантах осуществления гиперактивная транспозаза piggyBac или piggyBac-подобная транспозаза включает последовательность:
61 DEDVDDLEDQ EAGDRADAAA GGEPAWGPPC NFPPEIPPFT TVPGVKVDTS NFEPINFFQL
121 FMTEAILQDM VLYTNVYAEQ YLTQNPLPRY ARAHAWHPTD IAEMKRFVGL TLAMGLIKAN
181 SLESYWDTTT VLKIPVFSAT MSRNRYQLLL RFLHFNNNAT AVPPDQPGHD RLHKLRPLID
241 SLSERFAAVY TPCQNICIDE SLLLFKGRLQ FRQYIPSKRA RYGIKFYKLC ESSSGYTSYF
301 LIYEGKDSKL DPPGCPPDLT VSGKIVWELI SPLLGQGFHL YVDNFYSSIP LFTALYCLNT
361 PACGTINRNR KGLPRALLDK KLNRGETYAL RKNELLAIKF FDKKNVFMLT SIHDESVIRE
421 QRVGRPPKNK PLCSKEYSKY MGGVDRTDQL QHYYNATRKT RHWYKKVGIY LIQMALRNSY
481 IVYKAAVPGP KLSYYKYQLQ ILPALLFGGV EEQTVPEMPP SDNVARLIGK HFIDTLPPTP
541 GKQRPQKGCK VCRKRGIRRD TRYYCPKCPR NPGLCFKPCF EIYHTQLHY
(SEQ ID NO:14625).
[0264] В некоторых вариантах осуществления гиперактивная транспозаза piggyBac или piggyBac-подобная транспозаза включает последовательность:
61 DEDVDDLEDQ EAGDRADAAA GGEPAWGPPC NFPPEIPPFT TVPGVKVDTS NFEPINFFQL
121 FMTEAILQDM VLYTNVYAEQ YLTQNPLTRY ARAHAWHPTD IAEMKRFVGL TLAMGLIKAN
181 SIESYWDTTT VLSIPVFGAT MSRNRYQLLL RFLHFNNNAT AVPPDQPGHD RLHKLRPLID
241 SLSERFANVY TPCQNICIDE SLLLFKGRLQ FRQYIPSKRA RYGIKFYKLC ESSSGYTSYF
301 LIYEGKDSKL DPPGCPPDLT VSGKIVWELI SPLLGQGFHL YVDNFYSSIP LFTALYCLNT
361 PACGTINRNR KGLPRALLDK KLNRGETYAL RKNELLAIKF FDKKNVFMLT SIHDESVIRE
421 QRVGRKPKNK PLCSKEYSKY MGGVDRTDQL QHYYNATRKT RHWYKKVGIY LIQMALRNSY
481 IVYKAAVPGP KLSYYKYQLQ ILPALLFGGV EEQTVPEMPP SDNVARLIGK HFIDTLPPTP
541 GKQRPQKGCK VCRKRGIRRD TRYYCPKCPR NPGLCRKPCF EIYHTQLHY
(SEQ ID NO:14627).
[0265] В некоторых вариантах осуществления гиперактивная транспозаза piggyBac или piggyBac-подобная транспозаза включает последовательность:
61 DEDVDDLEDQ EAGDRADAAA GGEPAWGPPC NFPPEIPPFT TVPGVKVDTS NFEPINFFQL
121 FMTEAILQDM VLYTNVYAEQ YLTQNPLTRG ARAHAWHPTD IAEMKRFVGL TLAMGLIKAN
181 SLESYWDTTT VLSIPVFGAT MSRNRYQLLL RFLHFNNNAT AVPPDQPGHD RLHKLRPLID
241 SLSERFANVY TPCQNICIDE SLMLFKGRLQ FRQYIPSKRA RYGIKFYKLC ESSTGYTSYF
301 LIYEGKDSKL DPPGCPPDLT VSGKIVWELI SPLLGQGFHL YVDNFYSSIP LFTALYCLNT
361 PACGTINRNR KGLPRALLDK KLNRGETYAL RKNELLAIKF FDKKNVFMLT SIHDESVIRE
421 QRVGRPPKNK PLCSKEYSKY MGGVDRTDQL QHYYNATRKT RHWYKKVGIY LIQMALRNSY
481 IVYKAAVPGP KLSYYKYQLQ ILPALLFGGV EEQTVPEMPP SDNVARLIGK HFIDTLPPTP
541 GKQRPQKGCK VCRKRGIRRD TRYYCPKCPR NPGLCRKPCF EIYHTQLHY
(SEQ ID NO:14628).
[0266] В некоторых вариантах осуществления гиперактивная транспозаза piggyBac или piggyBac-подобная транспозаза включает последовательность:
61 DEDVDDLEDQ EAGDRADAAA GGEPAWGPPC NFPPEIPPFT TVPGVKVDTS NFEPINFFQL
121 FMTEAILQDM VLYTNVYAEQ YLTQNPLTRY ARAHAWHPTD IAEMKRFVGL TLAMGLIKAN
181 SLESYWDTTT VLSIPVFGAT MSRNRYQLLL RFLHFNNNAT AVPPDQPGHD RLHKLRPLID
241 SLSERFANVY TPCQNICIDE SLLLFKGRLQ FRQYIPSKRA RYGIKFYKLC ESSSGYTSYF
301 LIYEGKDSKL DPPGCPPDLT VSGKIVWELI SPLLGQGFHL YVDNFYSSIP LFTALYCLNT
361 PACGTINRNR KGLPRALLDK KLNRGETYAL RKNELLAIKF FDKKNVFMLT SIHDESVIRE
421 QRVGRPPKNK PLCSKEYSKY MGGVDRTDQL QHYYNATRKT RHWYKKVGIY LIQMALRNSY
481 IVYKAAVPGP KLSYYKYQLQ ILPALLFGGV EEQTVPEMPP SDNVARLIGK HFIDTLPPTP
541 GKQRPQKGCK VCRKRGIRRD TRYYCPKCPR NPGLCRKPCF EIYHTQLHY
(SEQ ID NO:16820).
[0267] В некоторых вариантах осуществления гиперактивная транспозаза piggyBac или piggyBac-подобная транспозаза включает аминокислотную замену в положении, выбранном из аминокислоты 6, 7, 16, 19, 20, 21, 22, 23, 24, 26, 28, 31, 34, 67, 73, 76, 77, 88, 91, 141, 145, 146, 148, 150, 157, 162, 179, 182, 189, 192, 193, 196, 198, 200, 210, 212, 218, 248, 263, 270, 294, 297, 308, 310, 333, 336, 354, 357, 358, 359, 377, 423, 426, 428, 438, 447, 450, 462, 469, 472, 498, 502, 517, 520, 523, 533, 534, 576, 577, 582, 583 или 587 (относительно SEQ ID NO:14517). В некоторых вариантах осуществления гиперактивная транспозаза piggyBac или piggyBac-подобная транспозаза включает аминокислотную замену Y6C, S7G, M16S, S19G, S20Q, S20G, S20D, E21D, E22Q, F23T, F23P, S24Y, S26V, S28Q, V31K, A34E, L67A, G73H, A76V, D77N, P88A, N91D, Yl41Q, Y141A, N145E, N145V, P146T, P146V, P146K, P148T, P148H, Y150G, Y150S, Y150C, H157Y, A162C, A179K, L182I, L182V, T189G, L192H, S193N, S193K, V196I, S198G, T200W, L210H, F212N, N218E, A248N, L263M, Q270L, S294T, T297M, S308R, L310R, L333M, Q336M, A354H, C357V, L358F, D359N, L377I, V 423H, P426K, K428R, S438A, T447G, T447A, L450V, A462H, A462Q, I469V, I472L, Q498M, L502V, E5171, P520D, P520G, N523S, I533E, D534A, F576R, F576E, K577I, I582R, Y583F, L587Y или L587W, или их любую комбинацию, включающую по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или все указанные мутации (относительно SEQ ID NO:14517).
[0268] В некоторых вариантах осуществления гиперактивная транспозаза piggyBac или piggyBac-подобная транспозаза включает одну или более замен аминокислоты, которая не относится к дикому типу, где одна или более замен аминокислоты дикого типа включают замену A2X, K3X, R4X, F5X, Y6X, S7X, A11X, A13X, C15X, M16X, A17X, S18X, S19X, S20X, E21X, E22X, F23X, S24X, G25X, 26X, D27X, S28X, E29X, E42X, E43X, S44X, C46X, S47X, S48X, S49X, T50X, V51X, S52X, A53X, L54X, E55X, E56X, P57X, M58X, E59X, E62X, D63X, V64X, D65X, D66X, L67X, E68X, D69X, Q70X, E71X, A72X, G73X, D74X, R75X, A76X, D77X, A78X, A79X, A80X, G81X, G82X, E83X, P84X, A85X, W86X, G87X, P88X, P89X, C90X, N91X, F92X, P93X, E95X, I96X, P97X, P98X, F99X, T100X, T101X, P103X, G104X, V105X, K106X, V107X, D108X, T109X, N111X, P114X, I115X, N116X, F117X, F118X, Q119X, M122X, T123X, E124X, A125X, I126X, L127X, Q128X, D129X, M130X, L132X, Y133X, V126X, Y127X, A138X, E139X, Q140X, Y141X, L142X, Q144X, N145X, P146X, L147X, P148X, Y150X, A151X, A155X, H157X, P158X, I161X, A162X, V168X, T171X, L172X, A173X, M174X, I177X, A179X, L182X, D187X, T188X, T189X, T190X, L192X, S193X, I194X, P195X, V196X, S198X, A199X, T200X, S202X, L208X, L209X, L210X, R211X, F212X, F215X, N217X, N218X, A219X, T220X, A221X, V222X, P224X, D225X, Q226X, P227X, H229X, R231X, H233X, L235X, P237X, I239X, D240X, L242X, S243X, E244X, R244X, F246X, A247X, A248X, V249X, Y250X, T251X, P252X, C253X, Q254X, I256X, C257X, I258X, D259X, E260X, S261X, L262X, L263X, L264X, F265X, K266X, G267X, R268X, L269X, Q270X, F271X, R272X, Q273X, Y274X, I275X, P276X, S277X, K278X, R279X, A280X, R281X, Y282X, G283X, I284X, K285X, F286X, Y287X, K288X, L289X, C290X, E291X, S292X, S293XS294X, G295X, Y296X, T297X, S298X, Y299X, F300X, E304X, L310X, P313X, G314X, P316X, P317X, D318X, L319X, T320X, V321X, K324X, E328X, I330X, S331X, P332X, L333X, L334X, G335X, Q336X, F338X, L340X, D343X, N344X, F345X, Y346X, S347X, L351X, F352X, A354X, L355X, Y356X, C357X, L358X, D359X, T360X, R422X, Y423X, G424X, P426X, K428X, N429X, K430X, P431X, L432X, S434X, K435X, E436X, S438X, K439X, Y440X, G443X, R446X, T447X, L450X, Q451X, N455X, T460X, R461X, A462X, K465X, V467X, G468X, I469X, Y470X, L471X, I472X, M474X, A475X, L476X, R477X, S479X, Y480X, V482XY483X, K484X, A485X, A486X, V487X, P488X, P490X, K491X, S493X, Y494X, Y495X, K496X, Y497T, Q498X, L499X, Q500X, I501X, L502X, P503X, A504X, L505X, L506X, F507X, G508X, G509X, V510X, E511X, E512X, Q513X, T514X, V515X, E517X, M518X, P519X, P520X, S521X, D522X, N523X, V524X, A525X, L527X, I528X, K530X, H531X, F532X, I533X, D534X, T535X, L536X, T539X, P540X, Q546X, K550X, R553X, K554X, R555X, G556X, I557X, R558X, R559X, D560X, T561X, Y564X, P566X, K567X, P569X, R570X, N571X, L574X, C575X, F576X, K577X, P578X, F580X, E581X, I582X, Y583X, T585X, Q586X, L587X, H588X или Y589X (относительно SEQ ID NO:14517). Список гиперактивных аминокислотных замен можно найти в патенте США 10,041,077, содержание которого включено посредством отсылки во всей своей полноте.
[0269] В некоторых вариантах осуществления транспозаза piggyBac или piggyBac-подобная транспозаза не способна к интеграции. В некоторых вариантах осуществления неспособная к интеграции транспозаза piggyBac или piggyBac-подобная транспозаза являются транспозазой, которая может вырезать свой соответствующий транспозон, но которая интегрирует вырезанный транспозон с более низкой частотой, чем соответствующая природная транспозаза. В некоторых вариантах осуществления транспозаза piggyBac или piggyBac-подобная транспозаза представляет собой неспособный к интеграции вариант SEQ ID NO:14517. В некоторых вариантах осуществления неспособная к интеграции транспозаза piggyBac или piggyBac-подобная транспозаза являются дефицитными относительно SEQ ID NO:14517.
[0270] В некоторых вариантах осуществления транспозаза piggyBac или piggyBac-подобная транспозаза является активной для вырезания, но не способна к интеграции. В некоторых вариантах осуществления неспособная к интеграции транспозаза piggyBac или piggyBac-подобная транспозаза включают последовательность, которая по меньшей мере на 90% идентична последовательности:
61 DEDVDDLEDQ EAGDRVDAAA GGEPAWGPPC NFPPEIPPFT TVPGVKVDTS NFEPINFFQL
121 FMTEAILQDM VLYTNVYAEQ YLTQNPLPRY ARAHAWHPTD IAEMKRFVGL TLAMGLIKAN
181 SLESYWDTTT VLSIPVFSAT MSRNRYQLLL KFLHFNNEAT AVPPDQPGHD RLHKLRPLID
241 SLSERFAAVY TPCQNICIDE SLLLFKGRLQ FRQYIPSKRA RYGIKFYKLC ESSSGYTSYF
301 LIYEGKDSKL DPPGCPPDLT VSGKIVWELI SPLLGQGFHL YVDNFYSSIP LFTALYCLDT
361 PACGTINRNR KGLPRALLDK KLNRGETYAL RKNELLAIKF FDKKNVFMLT SIHDESVIRE
421 QRVGRPPKNK PLCSKEYSKY MGGVDRTDQL QHYYNATRKT RAWYKKVGIY LIQMALRNSY
481 IVYKAAVPGP KLSYYKYQLQ ILPALLFGGV EEQTVPEMPP SDNVARLIGK HFIDTLPPTP
541 GKQRPQKGCK VCRKRGIRRD TRYYCPKCPR NPGLCFKPCF EIYHTQLHYG RR
(SEQ ID NO:14605).
[0271] В некоторых вариантах осуществления неспособная к интеграции транспозаза piggyBac или piggyBac-подобная транспозаза включает последовательность, которая по меньшей мере на 90% идентична последовательности:
61 DEDVDDLEDQ EAGDRADAAA GGEPAWGPPC NFPPEIPPFT TVPGVKVDTS NFEPINFFQL
121 FMTEAILQDM VLYTNVYAEQ YLTQVPLPRY ARAHAWHPTD IAEMKRFVGL TLAMGLIKAN
181 SLESYWDTTT VLNIPVFSAT MSRNRYQLLL RFLEFNNEAT AVPPDQPGHD RLHKLRPLID
241 SLSERFAAVY TPCQNICIDE SLLLFKGRLQ FRQYIPSKRA RYGIKFYKLC ESSSGYTSYF
301 LIYEGKDSKL DPPGCPPDLT VSGKIVWELI SPLLGQGFHL YVDNFYSSIP LFTALYCLDT
361 PACGTINRNR KGLPRALLDK KLNRGETYAL RKNELLAIKF FDKKNVFMLT SIHDESVIRE
421 QRVGRPPKNK PLCSKEYSKY MGGVDRTDQL QHYYNATRKT RAWYKKVGIY LIQMALRNSY
481 IVYKAAVPGP KLSYYKYQLQ ILPALLFGGV EEQTVPEMPP SDNVARLIGK HFIDTLPPTP
541 GKQRPQKGCK VCRKRGIRRD TRYYCPKCPR NPGLCFKPCF EIYHTQLHY
(SEQ ID NO:14604).
[0272] В некоторых вариантах осуществления неспособная к интеграции транспозаза piggyBac или piggyBac-подобная транспозаза включают последовательность, которая по меньшей мере на 90% идентична последовательности:
61 DEDVDDLEDQ EAGDRADAAA GGEPAWGPPC NFPPEIPPFT TVPGVKVDTS NFEPINFFQL
121 FMTEAILQDM VLYTNVYAEQ YLTQNVLPRY ARAHAWHPTD IAEMKRFVGL TLAMGLIKAN
181 SLESYWDTTT VLSIPVFSAT MSRNRYQLLL RFLHFNNDAT AVPPDQPGHD RLHKLRPLID
241 SLTERFAAVY TPCQNICIDE SLLLFKGRLQ FRQYIPSKRA RYGIKFYKLC ESSSGYTSYF
301 LIYEGKDSKL DPPGCPPDLT VSGKIVWELI SPLLGQGFHL YVDNFYSSIP LFTALYCLDT
361 PACGTINRNR KGLPRALLDK KLNRGETYAL RKNELLAIKF FDKKNVFMLT SIHDESVIRE
421 QRVGRPPKNK PLCSKEYSKY MGGVDRTDQL QHYYNATRKT RAWYKKVGIY LIQMALRNSY
481 IVYKAAVPGP KLSYYKYQLQ ILPALLFGGV EEQTVPEMPP SDNVARLIGK HFIDTLPPTP
541 GKQRPQKGCK VCRKRGIRRD TRYYCPKCPR NPGLCFKPCF EIYHTQLHYG RR
(SEQ ID NO:14611).
[0273] В некоторых вариантах осуществления неспособная к интеграции транспозаза piggyBac или piggyBac-подобная транспозаза включают SEQ ID NO:14611. В некоторых вариантах осуществления неспособная к интеграции транспозаза piggyBac или piggyBac-подобная транспозаза включают последовательность, которая по меньшей мере на 90% идентична последовательности:
61 DEDVDDLEDQ EAGDRADAAP GGEPAWGPPC NFPPEIPPFT TVPGVKVDTS NFEPINFFQL
121 FMTEAILQDM VLYTNVYAEQ YLTQVPLPRY ARAHAWHPTD IAEMKRFVGL TLAMGLIKAN
181 SLESYWDTTT VLSIPVFSAT MSRNRYQLLL RFLHFNNEAT AVPPDQPGHD RLHKLRPLID
241 SLSERFAAVY TPCQNICIDE SLLLFKGRLQ FRQYIPSKRA RYGIKFYKLC ESSSGYTSYF
301 LIYEGKDSKL DPPGCPPDLT VSGKIVWELI SPLLGQGFHL YVDNFYSSIP LFTALYCLDT
361 PACGTINRNR KGLPRALLDK KLNRGETYAL RKNELLAIKF FDKKNVFMLT SIHDESVIRE
421 QRVGRPPKNK PLCSKEYSKY MGGVDRTDQL QHYYNATRKT RAWYKKVGIY LIQMALRNSY
481 IVYKAAVPGP KLSYYKYQLQ ILPALLFGGV EEQTVPEMPP SDNVARLIGK HFIDTLPPTP
541 GKQRPQKGCK VCRKRGIRRD TRYYCPKCPR NPGLCFKPCF EIYHTQLHYG RR
(SEQ ID NO:14612).
[0274] В некоторых вариантах осуществления неспособная к интеграции транспозаза piggyBac или piggyBac-подобная транспозаза включает SEQ ID NO:14612. В некоторых вариантах осуществления неспособная к интеграции транспозаза piggyBac или piggyBac-подобная транспозаза включает последовательность, которая по меньшей мере на 90% идентична последовательности:
61 DEDVDDLEDQ EAGDRADAAA GGEPAWGPPC NFPPEIPPFT TVPGVKVDTS NFEPINFFQL
121 FMTEAILQDM VLYTNVYAEQ YLTQVPLPRY ARAHAWHPTD IAEMKRFVGL TLAMGLIKAN
181 SLESYWDTTT VLNIPVFSAT MSRNRYQLLL RFLEFNNNAT AVPPDQPGHD RLHKLRPLID
241 SLSERFAAVY TPCQNICIDE SLLLFKGRLQ FRQYIPSKRA RYGIKFYKLC ESSSGYTSYF
301 LIYEGKDSKL DPPGCPPDLT VSGKIVWELI SPLLGQGFHL YVDNFYSSIP LFTALYCLDT
361 PACGTINRNR KGLPRALLDK KLNRGETYAL RKNELLAIKF FDKKNVFMLT SIHDESVIRE
421 QRVGRPPKNK PLCSKEYSKY MGGVDRTDQL QHYYNATRKT RAWYKKVGIY LIQMALRNSY
481 IVYKAAVPGP KLSYYKYQLQ ILPALLFGGV EEQTVPEMPP SDNVARLIGK HFIDTLPPTP
541 GKQRPQKGCK VCRKRGIRRD TRYYCPKCPR NPGLCFKPCF EIYHTQLHYG RR
(SEQ ID NO:14613).
[0275] В некоторых вариантах осуществления неспособная к интеграции транспозаза piggyBac или piggyBac-подобная транспозаза включает SEQ ID NO:14613. В некоторых вариантах осуществления неспособная к интеграции транспозаза piggyBac или piggyBac-подобная транспозаза включает аминокислотную замену, где Asn в положении 218 заменен Glu или Asp (N218D или N218E) (относительно SEQ ID NO:14517).
[0276] В некоторых вариантах осуществления способная к вырезанию, неспособная к интеграции транспозаза piggyBac или piggyBac-подобная транспозаза включает одну или более замен аминокислоты, которая не относится к дикому типу, где одна или более замен аминокислоты дикого типа включают замену A2X, K3X, R4X, F5X, Y6X, S7X, A8X, E9X, E10X, A11X, A12X, A13X, H14X, C15X, M16X, A17X, S18X, S19X, S20X, E21X, E22X, F23X, S24X, G25X, 26X, D27X, S28X, E29X, V31X, P32X, P33X, A34X, S35X, E36X, S37X, D38X, S39X, S40X, T41X, E42X, E43X, S44X, W45X, C46X, S47X, S48X, S49X, T50X, V51X, S52X, A53X, L54X, E55X, E56X, P57X, M58X, E59X, V60X, M122X, T123X, E124X, A125X, L127X, Q128X, D129X, L132X, Y133X, V126X, Y127X, E139X, Q140X, Y141X, L142X, T143X, Q144X, N145X, P146X, L147X, P148X, R149X, Y150X, A151X, H154X, H157X, P158X, T159X, D160X, I161X, A162X, E163X, M164X, K165X, R166X, F167X, V168X, G169X, L170X, T171X, L172X, A173X, M174X, G175X, L176X, I177X, K178X, A179X, N180X, S181X, L182X, S184X, Y185X, D187X, T188X, T189X, T190X, V191X, L192X, S193X, I194X, P195X, V196X, F197X, S198X, A199X, T200X, M201X, S202X, R203X, N204X, R205X, Y206X, Q207X, L208X, L209X, L210X, R211X, F212X, L213X, H241X, F215X, N216X, N217X, N218X, A219X, T220X, A221X, V222X, P223X, P224X, D225X, Q226X, P227X, G228X, H229X, D230X, R231X, H233X, K234X, L235X, R236X, L238X, I239X, D240X, L242X, S243X, E244X, R244X, F246X, A247X, A248X, V249X, Y250X, T251X, P252X, C253X, Q254X, N255X, I256X, C257X, I258X, D259X, E260X, S261X, L262X, L263X, L264X, F265X, K266X, G267X, R268X, L269X, Q270X, F271X, R272X, Q273X, Y274X, I275X, P276X, S277X, K278X, R279X, A280X, R281X, Y282X, G283X, I284X, K285X, F286X, Y287X, K288X, L289X, C290X, E291X, S292X, S293X, S294X, G295X, Y296X, T297X, S298X, Y299X, F300X, I302X, E304X, G305X, K306X, D307X, S308X, K309X, L310X, D311X, P312X, P313X, G314X, C315X, P316X, P317X, D318X, L319X, T320X, V321X, S322X, G323X, K324X, I325X, V326X, W327X, E328X, L329X, I330X, S331X, P332X, L333X, L334X, G335X, Q336X, F338X, H339X, L340X, V342X, N344X, F345X, Y346X, S347X, S348X, I349X, L351X, T353X, A354X, Y356X, C357X, L358X, D359X, T360X, P361X, A362X, C363X, G364X, I366X, N367X, R368X, D369X, K371X, G372X, L373X, R375X, A376X, L377X, L378X, D379X, K380X, K381X, L382X, N383X, R384X, G385X, T387X, Y388X, A389X, L390X, K392X, N393X, E394X, A397X, K399X, F400X, F401X, D402X, N405X, L406X, L409X, R422X, Y423X, G424X, E425X, P426X, K428X, N429X, K430X, P431X, L432X, S434X, K435X, E436X, S438X, K439X, Y440X, G442X, G443X, V444X, R446X, T447X, L450X, Q451X, H452X, N455X, T457X, R458X, T460X, R461X, A462X, Y464X, K465X, V467X, G468X, I469X, L471X, I472X, Q473X, M474X, L476X, R477X, N478X, S479X, Y480X, V482X, Y483X, K484X, A485X, A486X, V487X, P488X, G489X, P490X, K491X, L492X, S493X, Y494X, Y495X, K496X, Q498X, L499X, Q500X, I501X, L502X, P503X, A504X, L505X, L506X, F507X, G508X, G509X, V510X, E511X, E512X, Q513X, T514X, V515X, E517X, M518X, P519X, P520X, S521X, D522X, N523X, V524X, A525X, L527X, I528X, G529X, K530X, F532X, I533X, D534X, T535X, L536X, P537X, P538X, T539X, P540X, G541X, F542X, Q543X, R544X, P545X, Q546X, K547X, G548X, C549X, K550X, V551X, C552X, R553X, K554X, R555X, G556X, I557X, R558X, R559X, D560X, T561X, R562X, Y563X, Y564X, C565X, P566X, K567X, C568X, P569X, R570X, N571X, P572X, G573X, L574X, C575X, F576X, K577X, P578X, C579X, F580X, E581X, I582X, Y583X, H584X, T585X, Q586X, L587X, H588X или Y589X (относительно SEQ ID NO:14517). Список способных к вырезанию, неспособных к интеграции аминокислотных замен можно найти в патенте США 10,041,077, содержание которого включено посредством отсылки во всей своей полноте.
[0277] В некоторых вариантах осуществления транспозаза piggyBac или piggyBac-подобная транспозаза слита с сигналом ядерной локализации. В некоторых вариантах осуществления SEQ ID NO:14517 или SEQ ID NO:14518 слита с сигналом ядерной локализации. В некоторых вариантах осуществления аминокислотная последовательность транспозазы piggyBac или подобной piggyBac, слитая с сигналом ядерной локализации, кодируется полинуклеотидной последовательностью, включающей:
61 gcagcacatt gcatggcatc gtcatccgaa gaattctcgg ggagcgattc cgaatatgtc
121 ccaccggcct cggaaagcga ttcgagcact gaggagtcgt ggtgttcctc ctcaactgtc
181 tcggctcttg aggagccgat ggaagtggat gaggatgtgg acgacttgga ggaccaggaa
241 gccggagaca gggccgacgc tgccgcggga ggggagccgg cgtggggacc tccatgcaat
301 tttcctcccg aaatcccacc gttcactact gtgccgggag tgaaggtcga cacgtccaac
361 ttcgaaccga tcaatttctt tcaactcttc atgactgaag cgatcctgca agatatggtg
421 ctctacacta atgtgtacgc cgagcagtac ctgactcaaa acccgctgcc tcgctacgcg
481 agagcgcatg cgtggcaccc gaccgatatc gcggagatga agcggttcgt gggactgacc
541 ctcgcaatgg gcctgatcaa ggccaacagc ctcgagtcat actgggatac cacgactgtg
601 cttagcattc cggtgttctc cgctaccatg tcccgtaacc gctaccaact cctgctgcgg
661 ttcctccact tcaacaacaa tgcgaccgct gtgccacctg accagccagg acacgacaga
721 ctccacaagc tgcggccatt gatcgactcg ctgagcgagc gattcgccgc ggtgtacacc
781 ccttgccaaa acatttgcat cgacgagtcg cttctgctgt ttaaaggccg gcttcagttc
841 cgccagtaca tcccatcgaa gcgcgctcgc tatggtatca aattctacaa actctgcgag
901 tcgtccagcg gctacacgtc atacttcttg atctacgagg ggaaggactc taagctggac
961 ccaccggggt gtccaccgga tcttactgtc tccggaaaaa tcgtgtggga actcatctca
1021 cctctcctcg gacaaggctt tcatctctac gtcgacaatt tctactcatc gatccctctg
1081 ttcaccgccc tctactgcct ggatactcca gcctgtggga ccattaacag aaaccggaag
1141 ggtctgccga gagcactgct ggataagaag ttgaacaggg gagagactta cgcgctgaga
1201 aagaacgaac tcctcgccat caaattcttc gacaagaaaa atgtgtttat gctcacctcc
1261 atccacgacg aatccgtcat ccgggagcag cgcgtgggca ggccgccgaa aaacaagccg
1321 ctgtgctcta aggaatactc caagtacatg gggggtgtcg accggaccga tcagctgcag
1381 cattactaca acgccactag aaagacccgg gcctggtaca agaaagtcgg catctacctg
1441 atccaaatgg cactgaggaa ttcgtatatt gtctacaagg ctgccgttcc gggcccgaaa
1501 ctgtcatact acaagtacca gcttcaaatc ctgccggcgc tgctgttcgg tggagtggaa
1561 gaacagactg tgcccgagat gccgccatcc gacaacgtgg cccggttgat cggaaagcac
1621 ttcattgata ccctgcctcc gacgcctgga aagcagcggc cacagaaggg atgcaaagtt
1681 tgccgcaagc gcggaatacg gcgcgatacc cgctactatt gcccgaagtg cccccgcaat
1741 cccggactgt gtttcaagcc ctgttttgaa atctaccaca cccagttgca ttac
(SEQ ID NO:14626).
[0278] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон выделен или получен из Xenopus tropicalis. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ccaacgacgc gtcccatacg ttgttggcat tttaagtctt ctctctgcag cggcagcatg
121 tgccgccgct gcagagagtt tctagcgatg acagcccctc tgggcaacga gccggggggg
181 ctgtc (SEQ ID NO:14519).
[0279] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ttctaccata ttttgaaagc ttaggttgtt ctgaaaaaaa caatatattg ttttcctggg
121 taaactaaaa gtcccctcga ggaaaggccc ctaaagtgaa acagtgcaaa acgttcaaaa
181 actgtctggc aatacaagtt ccactttgac caaaacggct ggcagtaaaa gggttaa
(SEQ ID NO:14520).
[0280] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает SEQ ID NO:14519 и SEQ ID NO:14520. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ccaacgacgc gtcccatacg ttgttggcat tttaagtctt ctctctgcag cggcagcatg
121 tgccgccgct gcagagagtt tctagcgatg acagcccctc tgggcaacga gccggggggg
181 ctgtc (SEQ ID NO:14521).
[0281] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ttctaccata ttttgaaagc ttaggttgtt ctgaaaaaaa caatatattg ttttcctggg
121 taaactaaaa gtcccctcga ggaaaggccc ctaaagtgaa acagtgcaaa acgttcaaaa
181 actgtctggc aatacaagtt ccactttggg acaaatcggc tggcagtgaa agggttaa
(SEQ ID NO:14522).
[0282] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ccaacgacgc gtcccatacg ttgttggcat tttaattctt ctctctgcag cggcagcatg
121 tgccgccgct gcagagagtt tctagcgatg acagcccctc tgggcaacga gccggggggg
181 ctgtc (SEQ ID NO:14523).
[0283] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает SEQ ID NO:14520 и SEQ ID NO:14519, SEQ ID NO:14521 или SEQ ID NO:14523. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает SEQ ID NO:14522 и SEQ ID NO:14519, SEQ ID NO:14521 или SEQ ID NO:14523. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает один конец, включающий по меньшей мере 14, 16, 18, 20, 30 или 40 последовательных нуклеотидов из SEQ ID NO:14519, SEQ ID NO:14521 или SEQ ID NO:14523. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает один конец, включающий по меньшей мере 14, 16, 18, 20, 30 или 40 последовательных нуклеотидов из SEQ ID NO:14520 или SEQ ID NO:14522. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает один конец, обладающий по меньшей мере 90% идентичностью с SEQ ID NO:14519, SEQ ID NO:14521 или SEQ ID NO:14523. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает один конец, обладающий по меньшей мере 90% идентичностью с SEQ ID NO:14520 или SEQ ID NO:14522. В одном варианте осуществления один конец транспозона по меньшей мере на 90% идентичен SEQ ID NO:14519, а другой конец транспозона по меньшей мере на 90% идентичен SEQ ID NO:14520.
[0284] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность TTAACCTTTTTACTGCCA (SEQ ID NO:14524). В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность TTAACCCTTTGCCTGCCA (SEQ ID NO:14526). В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность TTAACCYTTTTACTGCCA (SEQ ID NO:14527). В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность TGGCAGTAAAAGGGTTAA (SEQ ID NO:14529). В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность TGGCAGTGAAAGGGTTAA (SEQ ID NO:14531). В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность TTAACCYTTTKMCTGCCA (SEQ ID NO:14533). В некоторых вариантах осуществления один конец транспозона piggyBac или piggyBac-подобного транспозона включает последовательность, выбранную из SEQ ID NO:14524, SEQ ID NO:14526 и SEQ ID NO:14527. В некоторых вариантах осуществления один конец транспозона piggyBac (PB) или piggyBac-подобного транспозона включает последовательность, выбранную из SEQ ID NO:14529 и SEQ ID NO:14531. В некоторых вариантах осуществления каждый инвертированный концевой повтор транспозона piggyBac или piggyBac-подобного транспозона включает последовательность ITR-последовательности CCYTTTKMCTGCCA (SEQ ID NO:14563). В некоторых вариантах осуществления каждый конец транспозона piggyBac (PB) или piggyBac-подобного транспозона включает SEQ ID NO:14563 в обратных ориентациях. В некоторых вариантах осуществления один ITR транспозона piggyBac или piggyBac-подобного транспозона включает последовательность, выбранную из SEQ ID NO:14524, SEQ ID NO:14526 и SEQ ID NO:14527. В некоторых вариантах осуществления один ITR транспозона piggyBac или piggyBac-подобного транспозона включает последовательность, выбранную из SEQ ID NO:14529 и SEQ ID NO:14531. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает SEQ ID NO:14533 в обратной ориентации на двух концах транспозона.
[0285] В некоторых вариантах осуществления транспозон piggyBac или piggyBack-подобный транспозон может иметь концы, включающие SEQ ID NO:14519 и SEQ ID NO:14520 или вариант одного или обоих из них, обладающий по меньшей мере 90% идентичностью последовательности с SEQ ID NO:14519 или SEQ ID NO:14520, и транспозаза piggyBac или piggyBac-подобная транспозаза имеет последовательность SEQ ID NO:14517 или вариант, демонстрирующий по меньшей мере %, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент идентичности последовательности с SEQ ID NO:14517 или SEQ ID NO:14518. В некоторых вариантах осуществления один конец транспозона piggyBac или piggyBac-подобного транспозона включает по меньшей мере 14 последовательных нуклеотидов из SEQ ID NO:14519, SEQ ID NO:14521 или SEQ ID NO:14523, а другой конец транспозона включает по меньшей мере 14 последовательных нуклеотидов из SEQ ID NO:14520 или SEQ ID NO:14522. В некоторых вариантах осуществления один конец транспозона включает по меньшей мере 15, по меньшей мере 16, по меньшей мере 17, по меньшей мере 18, по меньшей мере 19, по меньшей мере 20, по меньшей мере 22, по меньшей мере 25, по меньшей мере 30 последовательных нуклеотидов из SEQ ID NO:14519, SEQ ID NO:14521 или SEQ ID NO:14523, а другой конец транспозона включает по меньшей мере 15, по меньшей мере 16, по меньшей мере 17, по меньшей мере 18, по меньшей мере 19, по меньшей мере 20, по меньшей мере 22, по меньшей мере 25 или по меньшей мере 30 последовательных нуклеотидов из SEQ ID NO:14520 или SEQ ID NO:14522.
[0286] В некоторых вариантах осуществления транспозаза piggyBac или piggyBac-подобная транспозаза распознает конец транспозона 5'-последовательностью, соответствующей SEQ ID NO:14519, и 3'-последовательностью, соответствующей SEQ ID NO:14520. Она вырезает транспозон из одной молекулы ДНК, разрезая ДНК по последовательности 5'-TTAA-3' на 5'-конце одного конца транспозона до 5'-TTAA-3' на 3' конце второго конца транспозона, включая любую гетерологичную ДНК, которая расположена между ними, и вставляет вырезанную последовательность во вторую молекулу ДНК. В некоторых вариантах осуществления усеченные и модифицированные варианты 5' и 3'-концов транспозона также будут функционировать как часть транспозона, который может быть перемещен транспозазой piggyBac или piggyBac-подобной транспозазой. Например, 5'-конец транспозона может быть заменен последовательностью, соответствующей SEQ ID NO:14521 или SEQ ID NO:14523, 3'-конец транспозона может быть заменен более короткой последовательностью, соответствующей SEQ ID NO:14522. В некоторых вариантах осуществления 5' и 3'-концы транспозона имеют общую, почти полностью повторяющуюся последовательность длиной 18 пн на своих концах (5'-TTAACCYTTTKMCTGCCA: SEQ ID NO:14533), которая включает сайт вставки 5'-TTAA-3' и которая инвертирована по ориентации на двух концах. То есть в (SEQ ID NO:14519) и SEQ ID NO:14523 5'-конец транспозона начинается с последовательности 5'-TTAACCTTTTTACTGCCA-3' (SEQ ID NO:14524), или в (SEQ ID NO:14521) 5'-конец транспозона начинается с последовательности 5'-TTAACCCTTTGCCTGCCA-3' (SEQ ID NO:14526); 3' транспозона заканчивается приблизительно обратным комплементом этой последовательности: в SEQ ID NO:14520 он заканчивается 5'-TGGCAGTAAAAGGGTTAA-3' (SEQ ID NO:14529), в (SEQ ID NO:14522) он заканчивается 5'-TGGCAGTGAAAGGGTTAA-3' (SEQ ID NO:14531.) Один вариант осуществления изобретения является транспозоном, включающим гетерологичный полинуклеотид, встроенный между двумя концами транспозона, каждый из которых включает SEQ ID NO:14533 в обратных ориентациях на двух концах транспозона. В некоторых вариантах осуществления один конец транспозона включает последовательность, выбранную из SEQ ID NO:14524, SEQ ID NO:14526 и SEQ ID NO:14527. В некоторых вариантах осуществления один конец транспозона включает последовательность, выбранную из SEQ ID NO:14529 и SEQ ID NO:14531.
[0287] В некоторых вариантах осуществления транспозон piggyBac (PB) или piggyBac-подобный транспозон выделен или получен из Xenopus tropicalis. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 cgacgcgtcc catacgtt (SEQ ID NO:14573).
[0288] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 tcaaaaactg tctggcaata caagttccac tttgggacaa atcggctggc agtgaaaggg
(SEQ ID NO:14574).
[0289] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает по меньшей мере 16 последовательных оснований из SEQ ID NO:14573 или SEQ ID NO:14574, и инвертированный концевой повтор CCYTTTBMCTGCCA (SEQ ID NO:14575).
[0290] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 cgacgcgtcc catacgttgt tggcatttta agtcttctct ctgcagcggc agcatgtgcc
121 gccgctgcag agagtttcta gcgatgacag cccctctggg caacgagccg ggggggctgt
181 c (SEQ ID NO:14579).
[0291] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 cgacgcgtcc catacgttgt tggcatttta attcttctct ctgcagcggc agcatgtgcc
121 gccgctgcag agagtttcta gcgatgacag cccctctggg caacgagccg ggggggctgt
181 c (SEQ ID NO:14580).
[0292] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 cgacgcgtcc catacgttgt tggcatttta agtcttctct ctgcagcggc agcatgtgcc
121 gccgctgcag agagtttcta gcgatgacag cccctctggg caacgagccg ggggggctgt
181 c (SEQ ID NO:14581).
[0293] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 cgacgcgtcc catacgttgt tggcatttta agtcttctct ctgcagcggc agcatgtgcc
121 gccgctgcag agag (SEQ ID NO:14582).
[0294] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 cgacgcgtcc catacgttgt tggcatttta agtctt (SEQ ID NO:14583).
[0295] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 cgacgcgtcc catacgttgt tggcatttta agtctt (SEQ ID NO:14584).
[0296] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ccaacgacgc gtcccatacg ttgttggcat tttaagtctt ctctctgcag cggcagcatg
121 tgccgccgct gcagagagtt tctagcgatg acagcccctc tgggcaacga gccggggggg
181 ctgtc (SEQ ID NO:14585).
[0297] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ttctaccata ttttgaaagc ttaggttgtt ctgaaaaaaa caatatattg ttttcctggg
121 taaactaaaa gtcccctcga ggaaaggccc ctaaagtgaa acagtgcaaa acgttcaaaa
181 actgtctggc aatacaagtt ccactttggg acaaatcggc tggcagtgaa aggg
(SEQ ID NO:14586).
[0298] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность 5'-конца транспозона, выбранную из SEQ ID NO:14573 и SEQ ID NO:14579-14585. В некоторых вариантах осуществления последовательность 5'-конца транспозона расположена перед 5'-последовательностью-мишенью. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ttctaccata ttttgaaagc ttaggttgtt ctgaaaaaaa caatatattg ttttcctggg
121 taaactaaaa gtcccctcga ggaaaggccc ctaaagtgaa acagtgcaaa acgttcaaaa
181 actgtctggc aatacaagtt ccactttgac caaaacggct ggcagtaaaa ggg
(SEQ ID NO:14587).
[0299] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ggcccctaaa gtgaaacagt gcaaaacgtt caaaaactgt ctggcaatac aagttccact
121 ttgaccaaaa cggctggcag taaaaggg (SEQ ID NO:14588).
[0300] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ttctaccata ttttgaaagc ttaggttgtt ctgaaaaaaa caatatattg ttttcctggg
121 taaactaaaa gtcccctcga ggaaaggccc ctaaagtgaa acagtgcaaa acgttcaaaa
181 actgtctggc aatacaagtt ccactttgac caaaacggct ggcagtaaaa gggttat
(SEQ ID NO:14589).
[0301] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ggcccctaaa gtgaaacagt gcaaaacgtt caaaaactgt ctggcaatac aagttccact
121 ttgggacaaa tcggctggca gtgaaaggg (SEQ ID NO:14590).
[0302] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность 3'-конца транспозона, выбранную из SEQ ID NO:14574 и SEQ ID NO:14587-14590. В некоторых вариантах осуществления после последовательности 3'-конца транспозона расположена 3'-последовательность-мишень. В некоторых вариантах осуществления 5' и 3'-концы транспозона имеют общую повторяющуюся последовательность длиной 14, инвертированную по ориентации на двух концах (SEQ ID NO:14575), примыкающую к последовательности-мишени. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает 5'-конец транспозона, включающий последовательность-мишень и последовательность, выбранную из SEQ ID NO:14582-14584 и 14573, и 3'-конец транспозона, включающий последовательность, выбранную из SEQ ID NO:14588-14590 и 14574, после которой расположена 3'-последовательность-мишень.
[0303] В некоторых вариантах осуществления 5'-конец транспозона piggyBac или piggyBac-подобного транспозона включает:
61 cgtt
(SEQ ID NO:14591) и ITR. В некоторых вариантах осуществления 5'-конец транспозона включает:
61 cgttgttggc attttaagtc tt
(SEQ ID NO:14592) и ITR. В некоторых вариантах осуществления 3'-конец транспозона piggyBac или piggyBac-подобного транспозона включает:
61 tcaaaaactg tctggcaata caagttccac tttgggacaa atcggc
(SEQ ID NO:14593) и ITR. В некоторых вариантах осуществления 3'-конец транспозона включает:
61 ggcccctaaa gtgaaacagt gcaaaacgtt caaaaactgt ctggcaatac aagttccact
121 ttgaccaaaa cggc
(SEQ ID NO:14594) и ITR.
[0304] В некоторых вариантах осуществления один конец транспозона включает последовательность, которая по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 99% или любой промежуточный процент идентична SEQ ID NO:14573, и другой конец транспозона включает последовательность, которая по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 99% или любой промежуточный процент идентична SEQ ID NO:14574. В некоторых вариантах осуществления один конец транспозона включает по меньшей мере 14, по меньшей мере 16, по меньшей мере 18, по меньшей мере 20 или по меньшей мере 25 последовательных нуклеотидов из SEQ ID NO:14573, и один конец транспозона включает по меньшей мере 14, по меньшей мере 16, по меньшей мере 18, по меньшей мере 20 или по меньшей мере 25 последовательных нуклеотидов из SEQ ID NO:14574. В некоторых вариантах осуществления один конец транспозона включает по меньшей мере 14, по меньшей мере 16, по меньшей мере 18, по меньшей мере 20 из SEQ ID NO:14591, и другой конец включает по меньшей мере 14, по меньшей мере 16, по меньшей мере 18, по меньшей мере 20 из SEQ ID NO:14593. В некоторых вариантах осуществления каждый конец транспозона включает SEQ ID NO:14575 в обратных ориентациях.
[0305] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность, выбранную из SEQ ID NO:14573, SEQ ID NO:14579, SEQ ID NO:14581, SEQ ID NO:14582, SEQ ID NO:14583 и SEQ ID NO:14588, и последовательность, выбранную из SEQ ID NO:14587, SEQ ID NO:14588, SEQ ID NO:14589 и SEQ ID NO:14586, и транспозаза piggyBac или piggyBac-подобная транспозаза включает SEQ ID NO:14517 или SEQ ID NO:14518.
[0306] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает ITR-повторы CCCTTTGCCTGCCA (SEQ ID NO:14622) (5'-ITR) и TGGCAGTGAAAGGG (SEQ ID NO:14623) (3'-ITR), граничащие с последовательностями-мишенями.
[0307] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза является ферментом транспозазой piggyBac или piggyBac-подобной транспозазой. В некоторых вариантах осуществления фермент транспозаза piggyBac или piggyBac-подобная транспозаза выделена или получена из Helicoverpa armigera. Фермент транспозаза piggyBac или piggyBac-подобная транспозаза может включать или состоять из аминокислотной последовательности, которая по меньшей мере на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент идентична последовательности:
61 PDNNIASRES PNLEVTSLTS HRIITLPQRS IRGKNNHVWS TTKGRTTGRT SAINIIRTNR
121 GPTRMCRNIV DPLLCFQLFI TDEIIHEIVK WTNVEIIVKR QNLKDISASY RDTNTMEIWA
181 LVGILTLTAV MKDNHLSTDE LFDATFSGTR YVSVMSRERF EFLIRCIRMD DKTLRPTLRS
241 DDAFLPVRKI WEIFINQCRQ NHVPGSNLTV DEQLLGFRGR CPFRMYIPNK PDKYGIKFPM
301 MCAAATKYMI DAIPYLGKST KTNGLPLGEF YVKDLTKTVH GTNRNITCDN WFTSIPLAKN
361 MLQAPYNLTI VGTIRSNKRE MPEEIKNSRS RPVGSSMFCF DGPLTLVSYK PKPSKMVFLL
421 SSCDENAVIN ESNGKPDMIL FYNQTKGGVD SFDQMCKSMS ANRKTNRWPM AVFYGMLNMA
481 FVNSYIIYCH NKINKQEKPI SRKEFMKKLS IQLTTPWMQE RLQAPTLKRT LRDNITNVLK
541 NVVPASSENI SNEPEPKKRR YCGVCSYKKR RMTKAQCCKC KKAICGEHNI DVCQDCI
(SEQ ID NO:14525).
[0308] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон выделен или получен из Helicoverpa armigera. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 tctttcatgt ttaccgtcgg atcgccgcta acttctgaac caactcagta gccattggga
121 cctcgcagga cacagttgcg tcatctcggt aagtgccgcc attttgttgt actctctatt
181 acaacacacg tcacgtcacg tcgttgcacg tcattttgac gtataattgg gctttgtgta
241 acttttgaat ttgtttcaaa ttttttatgt ttgtgattta tttgagttaa tcgtattgtt
301 tcgttacatt tttcatataa taataatatt ttcaggttga gtacaaa
(SEQ ID NO:14570). В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 aacatttaaa actagttgat tttttttata attacataat tttaagaaaa agtgttagag
121 gcttgatttt tttgttgatt ttttctaaga tttgattaaa gtgccataat agtattaata
181 aagagtattt tttaacttaa aatgtatttt atttattaat taaaacttca attatgataa
241 ctcatgcaaa aatatagttc attaacagaa aaaaatagga aaactttgaa gttttgtttt
301 tacacgtcat ttttacgtat gattgggctt tatagctagt taaatatgat tgggcttcta
361 gggttaa (SEQ ID NO:14528).
[0309] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза является ферментом транспозазой piggyBac или piggyBac-подобной транспозазой. В некоторых вариантах осуществления фермент транспозаза piggyBac или piggyBac-подобная транспозаза выделена или получена из Pectinophora gossypiella. Фермент транспозаза piggyBac или piggyBac-подобная транспозаза может включать или состоять из аминокислотной последовательности, которая по меньшей мере на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент идентична последовательности:
61 CPSKRQRTQI IESEESDNSE SIRPSRRQTS RVIDSDETDE DVMSSTPQNI PRNPNVIQPS
121 SRFLYGKNKH KWSSAAKPSS VRTSRRNIIH FIPGPKERAR EVSEPIDIFS LFISEDMLQQ
181 VVTFTNAEML IRKNKYKTET FTVSPTNLEE IRALLGLLFN AAAMKSNHLP TRMLFNTHRS
241 GTIFKACMSA ERLNFLIKCL RFDDKLTRNV RQRDDRFAPI RDLWQALISN FQKWYTPGSY
301 ITVDEQLVGF RGRCSFRMYI PNKPNKYGIK LVMAADVNSK YIVNAIPYLG KGTDPQNQPL
361 ATFFIKEITS TLHGTNRNIT MDNWFTSVPL ANELLMAPYN LTLVGTLRSN KREIPEKLKN
421 SKSRAIGTSM FCYDGDKTLV SYKAKSNKVV FILSTIHDQP DINQETGKPE MIHFYNSTKG
481 AVDTVDQMCS SISTNRKTQR WPLCVFYNML NLSIINAYVV YVYNNVRNNK KPMSRRDFVI
541 KLGDQLMEPW LRQRLQTVTL RRDIKVMIQD ILGESSDLEA PVPSVSNVRK IYYLCPSKAR
601 RMTKHRCIKC KQAICGPHNI DICSRCIE (SEQ ID NO:14530).
[0310] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон выделен или получен из Pectinophora gossypiella. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 tttacctatt attccgcgtc ccccgccccc gccgcttttt ctagcttcct gatttgcaaa
121 atagtgcatc gcgtgacacg ctcgaggtca cacgacaatt aggtcgaaag ttacaggaat
181 ttcgtcgtcc gctcgacgaa agtttagtaa ttacgtaagt ttggcaaagg taagtgaatg
241 aagtattttt ttataattat tttttaattc tttatagtga taacgtaagg tttatttaaa
301 tttattactt ttatagttat ttagccaatt gttataaatt ccttgttatt gctgaaaaat
361 ttgcctgttt tagtcaaaat ttattaactt ttcgatcgtt ttttag
(SEQ ID NO:14532). В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 caaaacttaa gaggtttaat aaataataat aaaaaaaaaa tggtttttat ttcgtagtct
121 gctcgacgaa tgtttagtta ttacgtaacc gtgaatatag tttagtagtc tagggttaa
(SEQ ID NO:14571).
[0311] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза является ферментом транспозазой piggyBac или piggyBac-подобной транспозазой. В некоторых вариантах осуществления фермент транспозаза piggyBac или piggyBac-подобная транспозаза выделена или получена из Ctenoplusia agnata. Фермент транспозаза piggyBac или piggyBac-подобная транспозаза может включать или состоять из аминокислотной последовательности, которая по меньшей мере на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент идентична последовательности:
61 RHEDPETPDP SSEASNLEVT LSSHRIIILP QRSIREKNNH IWSTTKGQSS GRTAAINIVR
121 TNRGPTRMCR NIVDPLLCFQ LFIKEEIVEE IVKWTNVEMV QKRVNLKDIS ASYRDTNEME
181 IWAIISMLTL SAVMKDNHLS TDELFNVSYG TRYVSVMSRE RFEFLLRLLR MGDKLLRPNL
241 RQEDAFTPVR KIWEIFINQC RLNYVPGTNL TVDEQLLGFR GRCPFRMYIP NKPDKYGIKF
301 PMVCDAATKY MVDAIPYLGK STKTQGLPLG EFYVKELTQT VHGTNRNVTC DNWFTSVPLA
361 KSLLNSPYNL TLVGTIRSNK REIPEEVKNS RSRQVGSSMF CFDGPLTLVS YKPKPSKMVF
421 LLSSCNEDAV VNQSNGKPDM ILFYNQTKGG VDSFDQMCSS MSTNRKTNRW PMAVFYGMLN
481 MAFVNSYIIY CHNMLAKKEK PLSRKDFMKK LSTDLTTPSM QKRLEAPTLK RSLRDNITNV
541 LKIVPQAAID TSFDEPEPKK RRYCGFCSYK KKRMTKTQCF KCKKPVCGEH NIDVCQDCI
(SEQ ID NO:14534).
[0312] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон выделен или получен из Ctenoplusia agnata. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 tctttctcct gcacgatcgg attgccgcga acgctcgatt caacccagtt ggcgccgaga
121 tctattggag gactgcggcg ttgattcggt aagtcccgcc attttgtcat agtaacagta
181 ttgcacgtca gcttgacgta tatttgggct ttgtgttatt tttgtaaatt ttcaacgtta
241 gtttattatt gcatcttttt gttacattac tggtttattt gcatgtatta ctcaaatatt
301 atttttattt tagcgtagaa aataca (SEQ ID NO:14535).
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 aaaacattaa aataagtttc tttttgtaaa atttaattaa ttataagaaa aagtttaagt
121 tgatctcatt ttttataaaa atttgcaatg tttccaaagt tattattgta aaagaataaa
181 taaaagtaaa ctgagtttta attgatgttt tattatatca ttatactata tattacttaa
241 ataaaacaat aactgaatgt atttctaaaa ggaatcacta gaaaatatag tgatcaaaaa
301 tttacacgtc atttttgcgt atgattgggc tttataggtt ctaaaaatat gattgggcct
361 ctagggttaa (SEQ ID NO:14536).
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает ITR-последовательность CCCTAGAAGCCCAATC (SEQ ID NO:14564).
[0313] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза является ферментом транспозазой piggyBac или piggyBac-подобной транспозазой. В некоторых вариантах осуществления фермент транспозаза piggyBac или piggyBac-подобная транспозаза выделена или получена из Agrotis ipsilon. фермент транспозаза piggyBac или piggyBac-подобная транспозаза может включать или состоять из аминокислотной последовательности, которая по меньшей мере на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент идентична последовательности:
61 PDNNIASQES ANLEVTSLTS HRIISLPQRS ICGKNNHVWS TTKGRTTGRT SAINIIRTNR
121 GPTRMCRNIV DPLLCFQLFI TDEIIHEIVK WTNVEMIVKR QNLIDISASY RDTNTMEMWA
181 LVGILTLTAV MKDNHLSTDE LFDATFSGTR YVSVMSRERF EFLIRCMRMD DKTLRPTLRS
241 DDAFIPVRKL WEIFINQCRL NYVPGGNLTV DEQLLGFRGR CPFRMYIPNK PDKYGIRFPM
301 MCDAATKYMI DAIPYLGKST KTNGLPLGEF YVKELTKTVH GTNRNVTCDN WFTSIPLAKN
361 MLQAPYNLTI VGTIRSNKRE IPEEIKNSRS RPVGSSMFCF DGPLTLVSYK PKPSRMVFLL
421 SSCDENAVIN ESNGKPDMIL FYNQTKGGVD SFDQMCKSMS ANRKTNRWPM AVFYGMLNMA
481 FVNSYIIYCH NKINKQKKPI NRKEFMKNLS TDLTTPWMQE RLKAPTLKRT LRDNITNVLK
541 NVVPPSPANN SEEPGPKKRS YCGFCSYKKR RMTKTQFYKC KKAICGEHNI DVCQDCV
(SEQ ID NO:14537).
[0314] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон выделен или получен из Agrotis ipsilon. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 tctttcacgt ttaccgtcgg attcccgcta acttcggaac caactcagta gccattgaga
121 actcccagga cacagttgcg tcatctcggt aagtgccgcc attttgttgt aatagacagg
181 ttgcacgtca ttttgacgta taattgggct ttgtgtaact tttgaaatta tttataattt
241 ttattgatgt gatttatttg agttaatcgt attgtttcgt tacatttttc atatgatatt
301 aatattttca gattgaatat aaa (SEQ ID NO:14538).
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 atatttaaaa ccagttgatt tttttaataa ttacctaatt ttaagaaaaa atgttagaag
121 cttgatattt ttgttgattt ttttctaaga tttgattaaa aggccataat tgtattaata
181 aagagtattt ttaacttcaa atttatttta tttattaatt aaaacttcaa ttatgataat
241 acatgcaaaa atatagttca tcaacagaaa aatataggaa aactctaata gttttatttt
301 tacacgtcat ttttacgtat gattgggctt tatagctagt caaatatgat tgggcttcta
361 gggttaa (SEQ ID NO:14539).
[0315] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза является ферментом транспозазой piggyBac или piggyBac-подобной транспозазой. В некоторых вариантах осуществления фермент транспозаза piggyBac или piggyBac-подобная транспозаза выделена или получена из Megachile rotundata. Фермент транспозаза piggyBac или piggyBac-подобная транспозаза может включать или состоять из аминокислотной последовательности, которая по меньшей мере на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент идентична последовательности:
61 EDNNHFVKES NRYHYQIVEK YKITSKTKKW KDVTVTEMKK FLGLIILMGQ VKKDVLYDYW
121 STDPSIETPF FSKVMSRNRF LQIMQSWHFY NNNDISPNSH RLVKIQPVID YFKEKFNNVY
181 KSDQQLSLDE CLIPWRGRLS IKTYNPAKIT KYGILVRVLS EARTGYVSNF CVYAADGKKI
241 EETVLSVIGP YKNMWHHVYQ DNYYNSVNIA KIFLKNKLRV CGTIRKNRSL PQILQTVKLS
301 RGQHQFLRNG HTLLEVWNNG KRNVNMISTI HSAQMAESRN RSRTSDCPIQ KPISIIDYNK
361 YMKGVDRADQ YLSYYSIFRK TKKWTKRVVM FFINCALFNS FKVYTTLNGQ KITYKNFLHK
421 AALSLIEDCG TEEQGTDLPN SEPTTTRTTS RVDHPGRLEN FGKHKLVNIV TSGQCKKPLR
481 QCRVCASKKK LSRTGFACKY CNVPLHKGDC FERYHSLKKY (SEQ ID NO:14540).
[0316] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон выделен или получен из Megachile rotundata. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 cgtttgctcc ccagcgctta ccgaccggcc atcgattatt cgacgtttgc ttcccagcgc
121 ttaccgaccg gtcatcgact tttgatcttt ccgttagatt tggttaggtc agattgacaa
181 gtagcaagca tttcgcattc tttattcaaa taatcggtgc ttttttctaa gctttagccc
241 ttagaa (SEQ ID NO:14541).
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 gtatatttta tgtttattta tttatggtta ttatggtata ttttatgtaa ataataaact
121 gaaaacgatt gtaatagatg aaataaatat tgttttaaca ctaatataat taaagtaaaa
181 gattttaata aatttcgtta ccctacaata acacgaagcg tacaatttta ccagagttta
241 ttaa (SEQ ID NO:14542).
[0317] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза является ферментом транспозазой piggyBac или piggyBac-подобной транспозазой. В некоторых вариантах осуществления фермент транспозаза piggyBac или piggyBac-подобная транспозаза выделена или получена из Bombus impatiens. Фермент транспозаза piggyBac или piggyBac-подобная транспозаза может включать или состоять из аминокислотной последовательности, которая по меньшей мере на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент идентична последовательности:
61 EDNANNVENN DDIWSTNDEA IILEPFEGSP GLKIMPSSAE SVTDNVNLFF GDDFFEHLVR
121 ESNRYHYQVM EKYKIPSKAK KWTDITVPEM KKFLGLIVLM GQIKKDVLYD YWSTDPSIET
181 PFFSQVMSRN RFVQIMQSWH FCNNDNIPHD SHRLAKIQPV IDYFRRKFND VYKPCQQLSL
241 DESIIPWRGR LSIKTYNPAK ITKYGILVRV LSEAVTGYVC NFDVYAADGK KLEDTAVIEP
301 YKNIWHQIYQ DNYYNSVKMA RILLKNKVRV CGTIRKNRGL PRSLKTIQLS RGQYEFRRNH
361 QILLEVWNNG RRNVNMISTI HSAQLMESRS KSKRSDVPIQ KPNSIIDYNK YMKGVDRADQ
421 YLAYYSIFRK TKKWTKRVVM FFINCALFNS FRVYTILNGK NITYKNFLHK VAVSWIEDGE
481 TNCTEQDDNL PNSEPTRRAP RLDHPGRLSN YGKHKLINIV TSGRSLKPQR QCRVCAVQKK
541 RSRTCFVCKF CNVPLHKGDC FERYHTLKKY (SEQ ID NO:14543).
[0318] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон выделен или получен из Bombus impatiens. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 taccgaccga taacctatta atcggctttt tgtcgtcgaa gcttaccaac ctatagccta
121 cctatagtta atcggttgcc atggcgataa acaatctttc tcattatatg agcagtaatt
181 tgttatttag tactaaggta ccttgctcag ttgcgtcagt tgcgttgctt tgtaagctcc
241 cacagtttta taccaattcg aaaaacttac cgttcgcg (SEQ ID NO:14544).
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 aatattatgg aaacaaaaga ttttattcaa tttaattatc ctatagtaac aaaaagcggc
121 caattttatc tgagcatacg aaaagcacag atactcccgc ccgacagtct aaaccgaaac
181 agagccggcg ccagggagaa tctgcgcctg agcagccggt cggacgtgcg tttgctgttg
241 aaccgctagt ggtcagtaaa ccagaaccag tcagtaagcc agtaactgat cagttaacta
301 gattgtatag ttcaaattga acttaatcta gtttttaagc gtttgaatgt tgtctaactt
361 cgttatatat tatattcttt ttaa (SEQ ID NO:14545).
[0319] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза является ферментом транспозазой piggyBac или piggyBac-подобной транспозазой. В некоторых вариантах осуществления фермент транспозаза piggyBac или piggyBac-подобная транспозаза выделена или получена из Mamestra brassicae. Фермент транспозаза piggyBac или piggyBac-подобная транспозаза может включать или состоять из аминокислотной последовательности, которая по меньшей мере на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент идентична последовательности:
61 DDKEHGKPPK RYEDAELQAL LDEDDAQTQK QLAEQLEVSQ QAVSNRLREG GKIQKVGRWV
121 PHELNERQRE RRKNTCEILL SRYKRKSFLH RIVTGEEKWI FFVNPKRKKS YVDPGQPATS
181 TARPNRFGKK TRLCVWWDQS GVIYYELLKP GETVNTARYQ QQLINLNRAL QRKRPEYQKR
241 QHRVIFLHDN APSHTARAVR DTLETLNWEV LPHAAYSPDL APSDYHLFAS MGHALAEQRF
301 DSYESVEEWL DEWFAAKDDE FYWRGIHKLP ERWDNCVASD GKYFE
(SEQ ID NO:14546).
[0320] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон выделен или получен из Mamestra brassicae. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 tagggatcga actcagtaaa actttgacct tgtgaaataa caaacttgac tgtccaacca
121 ccatagtttg gcgcgaattg agcgtcataa ttgttttgac tttttgcagt caac
(SEQ ID NO:14547).
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 tttttgggca acccaataa (SEQ ID NO:14548).
[0321] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза является ферментом транспозазой piggyBac или piggyBac-подобной транспозазой. В некоторых вариантах осуществления фермент транспозаза piggyBac или piggyBac-подобная транспозаза выделена или получена из Mayetiola destructor. Фермент транспозаза piggyBac или piggyBac-подобная транспозаза может включать или состоять из аминокислотной последовательности, которая по меньшей мере на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент идентична последовательности:
61 DTEDKERPGQ PKKFEDEELE ALLDEDCCQT QEELAKSLGV TQQAISKRLK AAGYIQKQGN
121 WVPHELKPRD VERRFCMSEM LLQRHKKKSF LSRIITGDEK WIHYDNSKRK KSYVKRGGRA
181 KSTPKSNLHG AKVMLCIWWD QRGVLYYELL EPGQTITGDL YRTQLIRLKQ ALAEKRPEYA
241 KRHGAVIFHH DNARPHVALP VKNYLENSGW EVLPHPPYSP DLAPSDYHLF RSMQNDLAGK
301 RFTSEQGIRK WLDSFLAAKP AKFFEKGIHE LSERWEKVIA SDGQYFE
(SEQ ID NO:14549).
[0322] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон выделен или получен из Mayetiola destructor. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 accctctgat ccctggtatt gttgtcgagc acgatttata ttgggtgtac aacttaaaaa
121 ccggaattgg acgctagatg tccacactaa cgaatagtgt aaaagcacaa atttcatata
181 tacgtcattt tgaaggtaca tttgacagct atcaaaatca gtcaataaaa ctattctatc
241 tgtgtgcatc atattttttt attaact (SEQ ID NO:14550).
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ttaagttgta cacccaatat catccttagt gacaattttc aaatggcttt cccattgagc
121 tgaaaccgtg gctctagtaa gaaaaacgcc caacccgtca tcatatgcct tttttttctc
181 aacatccg (SEQ ID NO:14551).
[0323] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза является ферментом транспозазой piggyBac или piggyBac-подобной транспозазой. В некоторых вариантах осуществления фермент транспозаза piggyBac или piggyBac-подобная транспозаза выделена или получена из Apis mellifera. Фермент транспозаза piggyBac или piggyBac-подобная транспозаза может включать или состоять из аминокислотной последовательности, которая по меньшей мере на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент идентична последовательности:
61 KRSGRPVEVD DDLIKAIIDS DRHSTTREIA EKLHVSHTCI ENHLKQLGYV QKLDTWVPHE
121 LKEKHLTQRI NSCDLLKKRN ENDPFLKRLI TGDEKWVVYN NIKRKRSWSR PREPAQTTSK
181 AGIHRKKVLL SVWWDYKGIV YFELLPPNRT INSVVYIEQL TKLNNAVEEK RPELTNRKGV
241 VFHHDNARPH TSLVTRQKLL ELGWDVLPHP PYSPDLAPSD YFLFRSLQNS LNGKNFNNDD
301 DIKSYLIQFF ANKNQKFYER GIMMLPERWQ KVIDQNGQHI TE (SEQ ID NO:14552).
[0324] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон выделен или получен из Apis mellifera. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ggtttgctgg cgtagtccaa atgtaaaaca cattttgtta tttgatagtt ggcaattcag
121 ctgtcaatca gtaaaaaaag ttttttgatc ggttgcgtag ttttcgtttg gcgttcgttg
181 aaaa (SEQ ID NO:14553).
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 agttgccaat ccaa (SEQ ID NO:14554).
[0325] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза является ферментом транспозазой piggyBac или piggyBac-подобной транспозазой. В некоторых вариантах осуществления фермент транспозаза piggyBac или piggyBac-подобная транспозаза выделена или получена из Messor bouvieri. Фермент транспозаза piggyBac или piggyBac-подобная транспозаза может включать или состоять из аминокислотной последовательности, которая по меньшей мере на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент идентична последовательности:
61 QDKERPGRPK TFEDAELQEL LDEDSTQTQK QLAEKLNVSR VAICERLQAM GKIQKMGRWV
121 PHELNDRQME NRKIVSEMLL QRYERKSFLH RIVTGDEKWI YFENPKRKKS WLSPGEAGPS
181 TARPNRFGRK TMLCVWWDQI GVVYYELLKP GETVNTDRYR QQMINLNCAL IEKRPQYAQR
241 HDKVILQHDN APSHTAKPVK EMLKSLGWEV LSHPPYSPDL APSDYHLFAS MGHALAEQHF
301 ADFEEVKKWL DEWFSSKEKL FFWNGIHKLS ERWTKCIESN GQYFE
(SEQ ID NO:14555).
[0326] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон выделен или получен из Messor bouvieri. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 caacatgtta ccaggtgtgt cggtaattcc tttccggttt ttccggcaga tgtcactagc
121 cataagtatg aaatgttatg atttgataca tatgtcattt tattctactg acattaacct
181 taaaactaca caagttacgt tccgccaaaa taacagcgtt atagatttat aattttttga
241 aa (SEQ ID NO:14556).
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 attaccgaca ctcctggtat gtcaacatgt tattttcgac attgaatcgc gtcgattcga
121 agtcgatcga ggtgtcattt ctgact (SEQ ID NO:14557).
[0327] В некоторых вариантах осуществления способов согласно изобретению фермент транспозаза является ферментом транспозазой piggyBac или piggyBac-подобной транспозазой. В некоторых вариантах осуществления, фермент транспозаза piggyBac или piggyBac-подобная транспозаза выделена или получена из Trichoplusia ni. Фермент транспозаза piggyBac или piggyBac-подобная транспозаза может включать или состоять из аминокислотной последовательности, которая по меньшей мере на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или любой промежуточный процент идентична последовательности:
61 SEILDEQNVI EQPGSSLASN RILTLPQRTI RGKNKHCWST SKSTRRSRVS ALNIVRSQRG
121 PTRMCRNIYD PLLCFKLFFT DEIISEIVKW TNAEISLKRR ESMTSATFRD TNEDEIYAFF
181 GILVMTAVRK DNHMSTDDLF DRSLSMVYVS VMSRDRFDFL IRCLRMDDKS IRPTLRENDV
241 FTPVRKIWDL FIHQCIQNYT PGAHLTIDEQ LLGFRGRCPF RVYIPNKPSK YGIKILMMCD
301 SGTKYMINGM PYLGRGTQTN GVPLGEYYVK ELSKPVHGSC RNITCDNWFT SIPLAKNLLQ
361 EPYKLTIVGT VRSNKREIPE VLKNSRSRPV GTSMFCFDGP LTLVSYKPKP AKMVYLLSSC
421 DEDASINEST GKPQMVMYYN QTKGGVDTLD QMCSVMTCSR KTNRWPMALL YGMINIACIN
481 SFIIYSHNVS SKGEKVQSRK KFMRNLYMSL TSSFMRKRLE APTLKRYLRD NISNILPKEV
541 PGTSDDSTEE PVMKKRTYCT YCPSKIRRKA NASCKKCKKV ICREHNIDMC QSCF
(SEQ ID NO:14558).
[0328] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон выделен или получен из Trichoplusia ni. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 tctttctaaa tagcgcgaat ccgtcgctgt gcatttagga catctcagtc gccgcttgga
121 gctcccgtga ggcgtgcttg tcaatgcggt aagtgtcact gattttgaac tataacgacc
181 gcgtgagtca aaatgacgca tgattatctt ttacgtgact tttaagattt aactcatacg
241 ataattatat tgttatttca tgttctactt acgtgataac ttattatata tatattttct
301 tgttatagat atc (SEQ ID NO:14559).
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 aaataaattg tttgttgaat ttattattag tatgtaagtg taaatataat aaaacttaat
121 atctattcaa attaataaat aaacctcgat atacagaccg ataaaacaca tgcgtcaatt
181 ttacgcatga ttatctttaa cgtacgtcac aatatgatta tctttctagg gttaa
(SEQ ID NO:14560).
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 tctaaatagc gcgaatccgt cgctgtgcat ttaggacatc tcagtcgccg cttggagctc
121 ccgtgaggcg tgcttgtcaa tgcggtaagt gtcactgatt ttgaactata acgaccgcgt
181 gagtcaaaat gacgcatgat tatcttttac gtgactttta agatttaact catacgataa
241 ttatattgtt atttcatgtt ctacttacgt gataacttat tatatatata ttttcttgtt
301 atagatatc (SEQ ID NO:14561).
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 aaataaattg tttgttgaat ttattattag tatgtaagtg taaatataat aaaacttaat
121 atctattcaa attaataaat aaacctcgat atacagaccg ataaaacaca tgcgtcaatt
181 ttacgcatga ttatctttaa cgtacgtcac aatatgatta tctttctagg g
(SEQ ID NO:14562).
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 ccgtgaggcg tgcttgtcaa tgcggtaagt gtcactgatt ttgaactata acgaccgcgt
121 gagtcaaaat gacgcatgat tatcttttac gtgactttta agatttaact catacgataa
181 ttatattgtt atttcatgtt ctacttacgt gataacttat tatatatata ttttcttgtt
241 atagatatc (SEQ ID NO:14609).
В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает последовательность:
61 aaataaattg tttgttgaat ttattattag tatgtaagtg taaatataat aaaacttaat
121 atctattcaa attaataaat aaacctcgat atacagaccg ataaaacaca tgcgtcaatt
181 ttacgcatga ttatctttaa cgtacgtcac aatatgatta tctttctagg g
(SEQ ID NO:14610).
[0329] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает SEQ ID NO:14561 и SEQ ID NO:14562, и транспозаза piggyBac или piggyBac-подобная транспозаза включает SEQ ID NO:14558. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает SEQ ID NO:14609 и SEQ ID NO:14610, и транспозаза piggyBac или piggyBac-подобная транспозаза включает SEQ ID NO:14558.
[0330] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон выделен или получен из Aphis gossypii. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает ITR-последовательность CCTTCCAGCGGGCGCGC (SEQ ID NO:14565).
[0331] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон выделен или получен из Chilo suppressalis. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает ITR-последовательность CCCAGATTAGCCT (SEQ ID NO:14566).
[0332] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон выделен или получен из Heliothis virescens. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает ITR-последовательность CCCTTAATTACTCGCG (SEQ ID NO:14567).
[0333] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон выделен или получен из Pectinophora gossypiella. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает ITR-последовательность CCCTAGATAACTAAAC (SEQ ID NO:14568).
[0334] В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон выделен или получен из Anopheles stephensi. В некоторых вариантах осуществления транспозон piggyBac или piggyBac-подобный транспозон включает ITR-последовательность CCCTAGAAAGATA (SEQ ID NO:14569).
Способы генетической модификации не на основе транспозиции
[0335] В некоторых вариантах осуществления способов согласно изобретению модифицированная HSC или клетка, происходящая из модифицированной HSC согласно изобретению, может быть получена путем введения трансгена в HSC или происходящую из HSC клетку согласно изобретению. Этап введения может включать доставку последовательности нуклеиновой кислоты и/или редактирующей геном конструкции с помощью системы доставки не на основе транспозиции.
[0336] В некоторых вариантах осуществления способов согласно изобретению введение последовательности нуклеиновой кислоты и/или редактирующей геном конструкции в HSC или происходящую из HSC клетку ex vivo, in vivo, in vitro или in situ включает одно или более из наружной доставки, адсорбции, абсорбции, электропорации, спинфекции, совместного культивирования, трансфекции, механической доставки, звуковой доставки, вибрационной доставки, магнитофекции или опосредованной наночастицами доставки. В некоторых вариантах осуществления способов согласно изобретению введение последовательности нуклеиновой кислоты и/или редактирующей геном конструкции в HSC или происходящую из HSC клетку ex vivo, in vivo, in vitro или in situ включает липосомную трансфекцию, трансфекцию с фосфатом кальция, трансфекцию фугеном и дендример-опосредованную трансфекцию. В некоторых вариантах осуществления способов согласно изобретению введение последовательности нуклеиновой кислоты и/или редактирующей геном конструкции в HSC или происходящую из HSC клетку ex vivo, in vivo, in vitro или in situ путем механической трансфекции включает методики сжатия клеток, бомбардировки клеток или с использованием генной пушки. В некоторых вариантах осуществления способов согласно изобретению введение последовательности нуклеиновой кислоты и/или редактирующей геном конструкции в HSC или происходящую из HSC клетку ex vivo, in vivo, in vitro или in situ с помощью опосредованной наночастицами трансфекции включает липосомную доставку, доставку мицеллами и доставку полимерсомами.
[0337] В некоторых вариантах осуществления способов согласно изобретению введение последовательности нуклеиновой кислоты и/или редактирующей геном конструкции в HSC или происходящую из HSC клетку ex vivo, in vivo, in vitro или in situ включает невирусный вектор. В некоторых вариантах осуществления невирусный вектор включает нуклеиновую кислоту. В некоторых вариантах осуществления невирусный вектор включает плазмидную ДНК, линейную двухцепочечную ДНК (дцДНК), линейную одноцепочечную ДНК (оцДНК), ДНК DoggyBoneTM, наноплазмиды, миникольцевую ДНК, одноцепочечные олигодезоксинуклеотиды (оцОДН), DDNA олигонуклеотиды, одноцепочечную мРНК (оцРНК) и двухцепочечную мРНК (дцРНК). В некоторых вариантах осуществления невирусный вектор включает транспозон согласно изобретению.
[0338] В некоторых вариантах осуществления способов согласно изобретению введение последовательности нуклеиновой кислоты и/или редактирующей геном конструкции в HSC или происходящую из HSC клетку ex vivo, in vivo, in vitro или in situ включает вирусный вектор. В некоторых вариантах осуществления вирусный вектор является неинтегрирующимся внехромосомным вектором. Примерные неинтегрирующиеся внехромосомные векторы включают, без ограничения перечисленными, аденоассоциированный вирус (AAV), аденовирус и вирусы герпеса. В некоторых вариантах осуществления вирусный вектор является интегрирующимся хромосомным вектором. Интегрирующиеся хромосомные векторы включают, без ограничения перечисленными, аденоассоциированные векторы (AAV), лентивирусы и гаммаретровирусы.
[0339] В некоторых вариантах осуществления способов согласно изобретению введение последовательности нуклеиновой кислоты и/или редактирующей геном конструкции в HSC или происходящую из HSC клетку ex vivo, in vivo, in vitro или in situ включает комбинацию векторов. Примерные неограничивающие комбинации векторов включают: вирусные и невирусные векторы, множество невирусных векторов или множество вирусных векторов. Примерные, но не ограничивающие комбинации векторов включают: комбинацию вектора на основе ДНК и вектора на основе РНК, комбинацию РНК и обратной транскриптазы, комбинацию транспозона и транспозазы, комбинацию невирусного вектора и эндонуклеазы и комбинацию вирусного вектора и эндонуклеазы.
[0340] В некоторых вариантах осуществления способов согласно изобретению модификация генома, включающая введение последовательности нуклеиновой кислоты и/или редактирующей геном конструкции в HSC или происходящую из HSC клетку ex vivo, in vivo, in vitro или in situ приводит к стабильной интеграции последовательности нуклеиновой кислоты, транзиентной интеграции последовательности нуклеиновой кислоты, сайт-специфической интеграции последовательности нуклеиновой кислоты или смещенной интеграции последовательности нуклеиновой кислоты. В некоторых вариантах осуществления последовательность нуклеиновой кислоты является трансгеном.
[0341] В некоторых вариантах осуществления способов согласно изобретению модификация генома, включающая введение последовательности нуклеиновой кислоты и/или редактирующей геном конструкции в HSC или происходящую из HSC клетку ex vivo, in vivo, in vitro или in situ приводит к стабильной интеграции последовательности нуклеиновой кислоты. В некоторых вариантах осуществления стабильная хромосомная интеграция может быть случайной интеграцией, сайт-специфической интеграцией или смещенной интеграцией. В некоторых вариантах осуществления сайт-специфическая интеграция может быть самостоятельной или ассистированной. В некоторых вариантах осуществления ассистированная сайт-специфическая интеграция доставляется совместно с сайт-направленной нуклеазой. В некоторых вариантах осуществления сайт-направленная нуклеаза содержит трансген с 5'- и 3'-выступающими нуклеотидными последовательностями, которые содержат некоторый процент гомологии с участками, расположенными до и после сайта геномной интеграции. В некоторых вариантах осуществления трансген с гомологичными нуклеотидными выступающими концами обеспечивает геномную интеграцию посредством гомологичной рекомбинации, опосредованного микрогомологией соединения концов или негомологичного соединения концов. В некоторых вариантах осуществления сайт-специфическая интеграция происходит в сайте "безопасной гавани". Геномные сайты "безопасные гавани" обеспечивают интеграцию нового генетического материала таким образом, чтобы гарантировать, что новые введенные генетические элементы будут надежно функционировать (например, экспрессироваться на терапевтически эффективном уровне экспрессии) и не вызывать нежелательных изменений в хозяйском геноме, представляющих риск для организма хозяина. Потенциально геномные безопасные гавани включают, без ограничения перечисленными, интронные последовательности гена человеческого альбумина, сайт 1 аденоассоциированного вируса (AAVS1), природный сайт интеграции вируса AAV в хромосому 19, сайт гена хемокинового (CC-мотив) рецептора 5 (CCR5) и сайт человеческого ортолога локуса Rosa26 мыши.
[0342] В некоторых вариантах осуществления сайт-специфическая интеграция трансгена происходит в сайте, который прерывает экспрессию гена-мишени. В некоторых вариантах осуществления прерывание экспрессии гена-мишени происходит в результате сайт-специфической интеграции в интронах, экзонах, промоторах, генетических элементах, энхансерах, супрессорах, старт-кодонах, стоп-кодонах и элементах ответа. В некоторых вариантах осуществления примерные гены-мишени, служащие мишенями при сайт-специфической интеграции, включают, без ограничения перечисленным, TRAC, TRAB, PDI, любой иммуносупрессорный ген и гены, участвующие в аллоотторжении.
[0343] В некоторых вариантах осуществления сайт-специфическая интеграция трансгена происходит в сайте, который приводит к повышенной экспрессии гена-мишени. В некоторых вариантах осуществления повышение экспрессии гена-мишени происходит в результате сайт-специфической интеграции в интроны, экзоны, промоторы, генетические элементы, энхансеры, супрессоры, старт-кодоны, стоп-кодоны и элементы ответа.
[0344] В некоторых вариантах осуществления способов согласно изобретению ферменты могут использоваться для создания разрывов цепи в геноме хозяина для облегчения доставки или интеграции трансгена. В некоторых вариантах осуществления ферменты создают одноцепочечные разрывы. В некоторых вариантах осуществления ферменты создают двухцепочечные разрывы. В некоторых вариантах осуществления примеры ферментов, вызывающих образование разрывов, включают, без ограничения перечисленными: транспозазы, интегразы, эндонуклеазы, CRISPR-Cas9, эффекторные нуклеазы, подобные активаторам транскрипции (TALEN), цинк-пальцевые нуклеазы (ZFN), Cas-CLOVERTM и Cpf1. В некоторых вариантах осуществления ферменты, вызывающие образование разрывов, могут быть доставлены в клетку в виде кодирующей ДНК, кодирующей мРНК, в виде белка, в виде нуклеопротеинового комплекса с гидовой РНК (гРНК).
[0345] В некоторых вариантах осуществления способов согласно изобретению сайт-специфическую интеграцию трансгена регулирует вектор-опосредованное смещение сайта интеграции. В некоторых вариантах осуществления вектор-опосредованное смещение сайта интеграции регулируется выбранным лентивирусным вектором. В некоторых вариантах осуществления вектор-опосредованное смещение сайта интеграции регулируется выбранным гаммаретровирусным вектором.
[0346] В некоторых вариантах осуществления способов согласно изобретению сайт сайт-специфической интеграции трансгена является нестабильной хромосомной вставкой. В некоторых вариантах осуществления интегрированный трансген может подвергаться сайленсингу, удалению, вырезанию или другой модификации.
[0347] В некоторых вариантах осуществления способов согласно изобретению модификация генома является нестабильной интеграцией трансгена. В некоторых вариантах осуществления нестабильная интеграция может быть транзиентной внехромосомной интеграцией, полустабильной внехромосомной интеграцией, полупостоянной внехромосомной вставкой или нестабильной хромосомной вставкой. В некоторых вариантах осуществления транзиентная внехромосомная вставка может быть эпихромосомной или цитоплазматической.
[0348] В некоторых вариантах осуществления транзиентная внехромосомная вставка трансгена не интегрируется в хромосому, при этом модифицированный генетический материал не реплицируется во время деления клетки.
[0349] В некоторых вариантах осуществления способов согласно изобретению модификация генома является полустабильной или постоянной внехромосомной интеграцией трансгена. В некоторых вариантах осуществления ДНК вектор кодирует модуль скаффолд/матрикс-ассоциированной области (S-MAR), который связывается с ядерными матриксными белками для эписомного удержания невирусного вектора, что обеспечивает автономную репликацию в ядре делящихся клеток.
[0350] В некоторых вариантах осуществления способов согласно изобретению модификация генома является нестабильной хромосомной интеграцией трансгена. В некоторых вариантах осуществления интегрированный трансген может подвергаться сайленсингу, удалению, вырезанию или другой модификации.
[0351] В некоторых вариантах осуществления способов согласно изобретению модификация генома в результате вставки трансгена может происходить посредством направленной клеткой-хозяином репарации двухцепочечных разрывов (направляемой гомологией репарации) путем гомологичной рекомбинации (HR), опосредованного микрогомологией соединения концов (MMEJ), негомологичного соединения концов (NHEJ), опосредованной ферментом транспозазой модификации, опосредованной ферментом интегразой модификации, опосредованной ферментом эндонуклеазой модификации или опосредованной рекомбинантным ферментом модификации. В некоторых вариантах осуществления модификация генома в результате вставки трансгена может происходить при посредстве CRISPR-Cas9, TALEN, ZFN-нуклеаз, Cas-CLOVER и Cpf1.
[0352] В системах редактирования генов, которые включают в себя вставку новых или существующих нуклеотидов/нуклеиновых кислот, инструменты инсерции (например, ДНК-матричные векторы, мобильные элементы (транспозоны или ретротранспозоны) должны доставляться в клетку в дополнение к разрезающему ферменту (например, нуклеазе, рекомбиназе, интегразе или транспозазе). Примеры таких инструментов инсерции для рекомбиназы могут включать ДНК вектор. Другие системы редактирования генов требуют доставки интегразы вместе с вектором вставки, транспозазы вместе с транспозоном/ретротранспозоном и т.д. В некоторых вариантах осуществления примерная рекомбиназа, которая может использоваться в качестве разрезающего фермента, является CRE рекомбиназой. В различных вариантах осуществления примерные интегразы, которые могут использоваться в инструментах инсерции, включают ферменты на основе вирусов, полученные из различных вирусов, включающих, без ограничения, AAV, гаммаретровирус и лентивирус. Например, транспозоны/ретротранспозоны, которые могут использоваться в инструментах инсерции, включают, без ограничения, транспозон piggyBac, транспозон Sleeping Beauty и ретротранспозон L1.
[0353] В некоторых вариантах осуществления способов согласно изобретению трансген доставляется in vivo. В некоторых вариантах осуществления способов согласно изобретению доставка трансгена in vivo может происходить путем: наружной доставки, адсорбции, абсорбции, электропорации, спин-фекции, совместного культивирования, трансфекции, механической доставки, звуковой доставки, вибрационной доставки, магнитофекции или опосредованной наночастицами доставки. В некоторых вариантах осуществления способов согласно изобретению доставка трансгена in vivo путем трансфекции может осуществляться путем липосомной трансфекции, трансфекции с фосфатом кальция, трансфекции фугеном и дендример-опосредованной трансфекции. В некоторых вариантах осуществления способов согласно изобретению механическая доставка трансгена in vivo может осуществляться путем сжатия клеток, бомбардировки и генной пушки. В некоторых вариантах осуществления способов согласно изобретению доставка трансгена, опосредованная наночастицами in vivo, может осуществляться путем липосомной доставки, доставки мицеллами и доставки полимеросомами. В различных вариантах осуществления нуклеазы, которые могут использоваться в качестве разрезающих ферментов, включают, без ограничения перечисленными, Cas9, эффекторные нуклеазы, подобные активаторам транскрипции (TALEN), и цинк-пальцевые нуклеазы.
[0354] В некоторых вариантах осуществления способов согласно изобретению для доставки трансгена используются невирусные векторы. В некоторых вариантах осуществления невирусный вектор представляет собой нуклеиновую кислоту. В некоторых вариантах осуществления невирусный вектор на основе нуклеиновой кислоты представляет собой плазмидную ДНК, линейную двухцепочечную ДНК (дцДНК), линейную одноцепочечную ДНК (оцДНК), ДНК DoggyBoneTM, наноплазмиды, миникольцевую ДНК, одноцепочечные олигодезоксинуклеотиды (оцОДН), DDNA олигонуклеотиды, одноцепочечную мРНК (оцРНК) и двухцепочечную мРНК (дцРНК). В некоторых вариантах осуществления невирусный вектор является транспозоном. В некоторых вариантах осуществления транспозоном является piggyBac.
[0355] В некоторых вариантах осуществления способов согласно изобретению доставка трансгена может осуществляться с помощью вирусного вектора. В некоторых вариантах осуществления вирусный вектор является неинтегрирующимся внехромосомным вектором. Неинтегрирующиеся внехромосомные векторы могут включать аденоассоциированный вирус (AAV), аденовирус и вирусы герпеса. В некоторых вариантах осуществления вирусный вектор является интегрирующимся хромосомным вектором. Интегрирующиеся хромосомные векторы могут включать аденоассоциированные векторы (AAV), лентивирусы и гаммаретровирусы.
[0356] В некоторых вариантах осуществления способов согласно изобретению доставка трансгена может осуществляться с помощью комбинации векторов. Типичные, но не ограничивающие комбинации векторов могут включать: вирусные плюс невирусные векторы, больше одного невирусного вектора или больше одного вирусного вектора. Типичные, но не ограничивающие комбинации векторов могут включать: векторы на основе ДНК плюс векторы на основе РНК, РНК плюс обратную транскриптазу, транспозон и транспозазу, невирусные векторы плюс эндонуклеазу и вирусный вектор плюс эндонуклеазу.
[0357] В некоторых вариантах осуществления способов согласно изобретению модификация генома может быть стабильной интеграцией трансгена, транзиентной интеграцией трансгена, сайт-специфической интеграцией трансгена или смещенной интеграцией трансгена.
[0358] В некоторых вариантах осуществления способов согласно изобретению модификация генома может быть стабильной хромосомной интеграцией трансгена. В некоторых вариантах осуществления стабильная хромосомная интеграция может быть случайной интеграцией, сайт-специфической интеграцией или смещенной интеграцией. В некоторых вариантах осуществления сайт-специфическая интеграция может быть самостоятельной или ассистированной. В некоторых вариантах осуществления ассистированная сайт-специфическая интеграция включает совместную доставку с сайт-направленной нуклеазой. В некоторых вариантах осуществления сайт-направленная нуклеаза включает трансген с 5' и 3' выступающими концами нуклеотидной последовательности, которые содержат гомологию в областях, расположенных до и после сайта геномной интеграции. В некоторых вариантах осуществления трансген с гомологичными нуклеотидными выступающими концами обеспечивает геномную интеграцию путем гомологичной рекомбинации, опосредованного микрогомологией соединения концов или негомологичного соединения концов. В некоторых вариантах осуществления сайт-специфическая интеграция происходит в сайте "безопасной гавани". Геномные сайты безопасные гавани обеспечивают интеграцию нового генетического материала таким образом, который гарантирует, что новые вставленные генетические элементы будут надежно функционировать (например, экспрессироватся на терапевтически эффективном уровне экспрессии) и не будут вызывать нежелательных изменений в геноме хозяина, представляющих риск для организма-хозяина. Потенциальные геномные безопасные гавани включают, без ограничения перечисленными, интронные последовательности человеческого гена альбумина, сайт 1 аденоассоциированного вируса (AAVS1), природный сайт интеграции вируса AAV на хромосоме 19, сайт гена хемокинового (C-C мотив) рецептора 5 (CCR5) и сайт человеческого ортолога локуса Rosa26 мыши.
[0359] В некоторых вариантах осуществления сайт-специфическая интеграция трансгена происходит в сайте, который прерывает экспрессию гена-мишени. В некоторых вариантах осуществления прерывание экспрессии гена-мишени происходит в результате сайт-специфической интеграции в интронах, экзонах, промоторах, генетических элементах, энхансерах, супрессорах, старт-кодонах, стоп-кодонах и элементах ответа. В некоторых вариантах осуществления примерные гены-мишени, служащие мишенью при сайт-специфической интеграции, включают, без ограничения перечисленными, TRAC, TRAB, PDI, любой иммуносупрессорный ген и гены, участвующие в аллоотторжении.
[0360] В некоторых вариантах осуществления сайт-специфическая интеграция трансгена происходит в сайте, который приводит к повышению экспрессии гена-мишени. В некоторых вариантах осуществления повышение экспрессии гена-мишени происходит в результате сайт-специфической интеграции в интроны, экзоны, промоторы, генетические элементы, энхансеры, супрессоры, старт-кодоны, стоп-кодоны и элементы ответа.
[0361] В некоторых вариантах осуществления способов согласно изобретению ферменты могут использоваться для создания разрывов цепи в геноме организма для облегчения доставки или интеграции трансгена. В некоторых вариантах осуществления ферменты создают одноцепочечные разрывы. В некоторых вариантах осуществления ферменты создают двухцепочечные разрывы. В некоторых вариантах осуществления примеры вызывающих образование разрывов ферментов включают, без ограничения перечисленными: транспозазы, интегразы, эндонуклеазы, CRISPR-Cas9, подобные активаторам транскрипции эффекторные нуклеазы (TALEN), цинк-пальцевые нуклеазы (ZFN), Cas-CLOVERTM и Cpf1. В некоторых вариантах осуществления вызывающие образование разрывов ферменты могут быть доставлены в клетку в виде кодирующей ДНК, кодирующей мРНК, в виде белка, в виде нуклеопротеинового комплекса с гидовой РНК (гРНК).
[0362] В некоторых вариантах осуществления способов согласно изобретению сайт-специфическую интеграцию трансгена регулирует вектор-опосредованное смещение сайта интеграции. В некоторых вариантах осуществления вектор-опосредованное смещение сайта интеграции регулирует выбранный лентивирусный вектор. В некоторых вариантах осуществления вектор-опосредованное смещение сайта интеграции регулирует выбранный гаммаретровирусный вектор.
[0363] В некоторых вариантах осуществления способов согласно изобретению сайт сайт-специфической интеграции трансгена является нестабильной хромосомной вставкой. В некоторых вариантах осуществления интегрированный трансген может подвергаться сайленсингу, удалению, вырезанию или другой модификации. В некоторых вариантах осуществления способов согласно изобретению модификация генома является нестабильной интеграцией трансгена. В некоторых вариантах осуществления нестабильная интеграция может быть транзиентной внехромосомной интеграцией, полустабильной внехромосомной интеграцией, полупостоянной внехромосомной вставкой или нестабильной хромосомной вставкой. В некоторых вариантах осуществления транзиентная внехромосомная вставка может быть эпихромосомной или цитоплазматической. В некоторых вариантах осуществления транзиентная внехромосомная вставка трансгена не интегрируется в хромосому, при этом модифицированный генетический материал не реплицируется во время деления клетки.
[0364] В некоторых вариантах осуществления способов согласно изобретению модификация генома является полустабильной или постоянной внехромосомной интеграцией трансгена. В некоторых вариантах осуществления ДНК вектор кодирует модуль скаффолд/матрикс-ассоциированной области (S-MAR), который связывается с ядерными матриксными белками для эписомного удержания невирусного вектора, что обеспечивает автономную репликацию в ядре делящихся клеток.
[0365] В некоторых вариантах осуществления способов согласно изобретению модификация генома является нестабильной хромосомной интеграцией трансгена. В некоторых вариантах осуществления интегрированный трансгенное может подвергаться сайленсингу, удалению, вырезанию или другой модификации.
[0366] В некоторых вариантах осуществления способов согласно изобретению модификация генома в результате вставки трансгена может осуществляться посредством направленной клеткой-хозяином репарации двухцепочечных разрывов (направляемой гомологией репарации) путем гомологичной рекомбинации (HR), опосредованного микрогомологией соединения концов (MMEJ), негомологичного соединения концов (NHEJ), опосредованной ферментом транспозазой модификации, опосредованной ферментом интегразой модификации, опосредованной ферментом эндонуклеазой модификации или опосредованной рекомбинантным ферментом модификации. В некоторых вариантах осуществления модификация генома в результате вставки трансгена может происходить при посредстве CRISPR-Cas9, TALEN, ZFN-нуклеаз, Cas-CLOVER и Cpf1.
[0367] В некоторых вариантах осуществления способов согласно изобретению клетка с in vivo или ex vivo геномной модификацией может быть клеткой зародышевой линии или соматической клеткой. В некоторых вариантах осуществления модифицированная клетка может быть клеткой человека, не человека, млекопитающего, крысы, мыши или собаки. В некоторых вариантах осуществления модифицированная клетка может быть дифференцированной, недифференцированной или иммортализованной. В некоторых вариантах осуществления модифицированная недифференцированная клетка может быть стволовой клеткой. В некоторых вариантах осуществления модифицированная клетка может быть дифференцированной, недифференцированной или иммортализованной. В некоторых вариантах осуществления модифицированная недифференцированная клетка может быть индуцированной плюрипотентной стволовой клеткой. В некоторых вариантах осуществления модифицированная клетка может быть T-клеткой, гемопоэтической стволовой клеткой, естественной киллерной клеткой, макрофагом, дендритной клеткой, моноцитом, мегакариоцитом или остеокластом. В некоторых вариантах осуществления модифицированная клетка может быть модифицирована, когда клетка находится в состоянии покоя, в активированном состоянии, покоящейся, в интерфазе, в профазе, в метафазе, в анафазе или в телофазе. В некоторых вариантах осуществления модифицированная клетка может быть свежей, криоконсервированной, в клеточной массе, сортированной на субпопуляции, из цельной крови, из образца лейкафереза или из иммортализованной клеточной линии.
Получение и создание VCAR-рецепторов
[0368] По меньшей мере один белок VHH или VCAR согласно изобретению необязательно может быть получен с использованием клеточной линии, смешанной клеточной линии, иммортализованной клетки или клональной популяции иммортализованных клеток, как известно в уровне техники. См., например, Ausubel, et al., ed., Current Protocols in Molecular Biology, John Wiley & Sons, Inc., NY, N.Y. (1987-2001); Sambrook, et al., Molecular Cloning: A Laboratory Manual, 2nd Edition, Cold Spring Harbor, N.Y. (1989); Harlow and Lane, Antibodies, a Laboratory Manual, Cold Spring Harbor, N.Y. (1989); Colligan, et al., eds., Current Protocols in Immunology, John Wiley & Sons, Inc., NY (1994-2001); Colligan et al., Current Protocols in Protein Science, John Wiley & Sons, NY, N.Y., (1997-2001).
[0369] Аминокислоты из белка VHH могут быть изменены, добавлены и/или удалены для уменьшения иммуногенности или уменьшения, улучшения или изменения связывания, аффинности, скорость ассоциации, скорость диссоциации, авидности, специфичности, периода полувыведения, стабильности, растворимости или любой другой подходящей характеристики, как известно в уровне техники.
[0370] Необязательно белки VHH могут быть сконструированы с сохранением высокой аффинности к антигену, а также других желательных биологических свойств. Для достижения этой цели белки VHH необязательно могут быть получены в процессе анализа исходных последовательностей и различных концептуальных сконструированных продуктов с использованием трехмерных моделей исходных и сконструированных последовательностей. Трехмерные модели общедоступны и известны специалистам в данной области. Доступны компьютерные программы, которые иллюстрируют и отображают возможные трехмерные конформационные структуры выбранных кандидатных последовательностей и могут измерять возможную иммуногенность (например, программа Immunofilter, разработанная Xencor, Inc. of Monrovia, Calif.). Изучение этих отображаемых результатов позволяет проводить анализ вероятной роли остатков в функции кандидатной последовательности, то есть анализ остатков, которые влияют на способность кандидатного белка VHH связывать свой антиген. Таким образом, остатки могут быть отобраны и скомбинированы из исходной и референсной последовательностей, в результате чего достигается требуемая характеристика, такая как аффинность к антигену(ам)-мишени(ям). В альтернативе или в дополнение к вышеуказанным процедурам могут использоваться другие подходящие методы конструирования.
Скрининг белков VHH
[0371] Скрининг VHH на специфичное связывание с подобными белками или фрагментами может быть удобно осуществлен с использованием библиотек нуклеотидного (ДНК или РНК-дисплея) или пептидного дисплея, например, in vitro. Этот способ включает скрининг больших коллекций пептидов для выявления отдельных членов, обладающих требуемой функцией или структурой. Экспонируемые нуклеотидные или пептидные последовательности могут иметь длину от 3 до 5000 или более нуклеотидов или аминокислот, часто от 5 до 100 аминокислот в длину и часто от 8 до 25 аминокислот. В дополнение к методам прямого химического синтеза для получения пептидных библиотек было описано несколько методов рекомбинантных ДНК. Один тип включает экспонирование пептидной последовательности на поверхности бактериофага или клетки. Каждый бактериофаг или клетка содержит нуклеотидную последовательность, кодирующую конкретную экспонируемую пептидную последовательность. Белки VHH согласно изобретению могут связывать белки человека или других млекопитающих с широким диапазоном аффинностей (KD). В предпочтительном варианте осуществления по меньшей мере один VHH согласно изобретению может необязательно связываться с белком-мишенью с высокой аффинностью, например, с KD, равной или меньше чем приблизительно 10-7 М, такой как, без ограничения, 0,1-9,9 (или любой диапазон или значение в нем) ×10−8, 10−9, 10−10, 10−11, 10−12, 10−13, 10−14, 10−15 или любой диапазон или значение в нем, как определено с помощью поверхностного плазмонного резонанса или метода KinExA, применяемых на практике специалистами в данной области.
[0372] Аффинность или авидность VHH или VCAR в отношении антигена можно определить экспериментально при использовании любого подходящего метода (см., например, Berzofsky, et al., “Antibody-Antigen Interactions,” In Fundamental Immunology, Paul, W. E., Ed., Raven Press: New York, N.Y. (1984); Kuby, Janis Immunology, W.H. Freeman and Company: New York, N.Y. (1992); и способы, описанные в настоящем документе). Измеренная аффинность взаимодействия конкретного VHH-антигена или VCAR-антигена может изменяться в случае измерения в разных условиях (например, концентрации солей, pH). Таким образом, измерения аффинности и других антигенсвязывающих параметров (например, KD, Kon, Koff) предпочтительно проводят с помощью стандартных растворов VHH или VCAR и антигена, а также стандартного буфера, такого как буфер, описанный в настоящем документе.
[0373] Конкурентные анализы могут быть выполнены с VHH или VCAR согласно изобретению для определения, какие белки, антитела и другие антагонисты конкурируют за связывание белка-мишени с VHH или VCAR согласно изобретению и/или имеют общую область эпитопа. Эти анализы, которые хорошо известны специалистам в данной области, позволяют оценить конкуренцию между антагонистами или лигандами за ограниченное количество сайтов связывания на белке. Белок и/или антитело иммобилизируют или инсолюбилизируют до или после конкуренции, и образец, связанный с белком-мишенью, отделяют от несвязанного образца, например, путем декантирования (где белок/антитело были предварительно инсолюбилизированы) или путем центрифугирования (где белок/антитело были осаждены после конкурентной реакции). Кроме того, конкурентное связывание может быть определено путем определения, какая функция изменяется при связывании или отсутствии связывания VHH или VCAR с белком-мишенью, например, ингибирует ли или потенцирует ли молекула VCAR ферментную активность, например, метки. Могут использовать ИФА и другие функциональные анализы, хорошо известные в данной области.
Молекулы нуклеиновых кислот
[0374] Молекулы нуклеиновых кислот согласно изобретению, кодирующие белки VHH или VCAR-рецепторы, могут находиться в форме РНК, такой как мРНК, шРНК, тРНК или любой другой форме, или в форме ДНК, включающей, без ограничения перечисленными, кДНК и геномную ДНК, полученную путем клонирования или синтеза, или их любые комбинации. ДНК может быть трехцепочечной, двухцепочечной или одноцепочечной, или их любой комбинацией. Любая часть по меньшей мере одной цепи ДНК или РНК может быть кодирующей цепью, также известной как смысловая цепь, или она может быть некодирующей цепью, также называемой антисмысловой цепью.
[0375] Выделенные молекулы нуклеиновых кислот согласно изобретению могут включать молекулы нуклеиновых кислот, содержащие открытую рамку считывания (ORF), необязательно с одним или более интронами, например, без ограничения перечисленными, по меньшей мере одной указанной частью по меньшей мере одного VCAR; молекулы нуклеиновых кислот, содержащие последовательность, кодирующую VCAR; и молекулы нуклеиновых кислот, которые содержат нуклеотидную последовательность, существенно отличающуюся от описанной выше, но которые, вследствие вырожденности генетического кода, все же кодируют VCAR, как описано в настоящее документе и/или как известно в уровне техники. Конечно, генетический код хорошо известен в уровне техники. Таким образом, для специалиста в данной области техники будет стандартным получение таких вырожденных вариантов нуклеиновых кислот, которые кодируют конкретные VCAR согласно изобретению. См., например, Ausubel et al., выше, при этом такие варианты нуклеиновых кислот включены в настоящее изобретение.
[0376] Как указано в настоящем документе, молекулы нуклеиновых кислот согласно изобретению, которые содержат нуклеиновую кислоту, кодирующую VCAR, могут включать, без ограничения перечисленными, молекулы, кодирующие аминокислотную последовательность фрагмента VHH, сами по себе; кодирующую последовательность всего VCAR или его части; кодирующую последовательность VHH, фрагмента или части, а также дополнительные последовательности, такие как кодирующую последовательность по меньшей мере одного сигнального лидерного или слитого пептида, с или без вышеуказанных дополнительных кодирующих последовательностей, таких как по меньшей мере один интрон, вместе с дополнительными некодирующими последовательностями, включающими, без ограничения перечисленными, некодирующие 5' и 3'-последовательности, такие как транскрибированные нетранслируемые последовательности, которые играют роль в транскрипции, процессинге мРНК, включая сигналы сплайсинга и полиаденилирования (например, связывание рибосомы и стабильность мРНК); дополнительную кодирующую последовательность, которая кодирует дополнительные аминокислоты, такие как аминокислоты, которые обеспечивают дополнительные функциональности. Таким образом, последовательность, кодирующая VCAR, может быть слита с маркерной последовательностью, такой как последовательностью, кодирующей пептид, который облегчает очистку слитого VCAR, содержащего фрагмент или часть VHH.
Полинуклеотиды, селективно гибридизующиеся с полинуклеотидом, как описано в настоящем документе
[0377] В изобретении предложены выделенные нуклеиновые кислоты, гибридизующиеся при селективных условиях гибридизации с полинуклеотидом, раскрытым в настоящем документе. Таким образом, полинуклеотиды данного варианта осуществления могут применяться для выделения, обнаружения и/или количественного определения нуклеиновых кислот, включающих такие полинуклеотиды. Например, полинуклеотиды согласно настоящему изобретению могут применяться для идентификации, выделения или амплификации неполных или полноразмерных клонов в депонированной библиотеке. В некоторых вариантах осуществления полинуклеотиды представляют собой последовательности геномной или кДНК, выделенные или, в других случаях, комплементарные кДНК из библиотеки нуклеиновых кислот человека или млекопитающего.
[0378] Предпочтительно библиотека кДНК включает по меньшей мере 80% полноразмерных последовательностей, предпочтительно по меньшей мере 85% или 90% полноразмерных последовательностей, и более предпочтительно по меньшей мере 95% полноразмерных последовательностей. Библиотеки кДНК могут быть нормализованы для увеличения представленности редких последовательностей. Условия гибридизации низкой или умеренной строгости, как правило, но не исключительно, используются с последовательностями, имеющими сниженную идентичность последовательности по сравнению с комплементарными последовательностями. Условия умеренной и высокой строгости необязательно могут использоваться для последовательностей с более высокой идентичностью. Условия низкой строгости позволяют селективную гибридизацию последовательностей, обладающих приблизительно 70% идентичностью последовательности, и могут использоваться для идентификации ортологических или паралогических последовательностей.
[0379] Необязательно полинуклеотиды настоящего изобретения кодируют по меньшей мере часть VCAR, кодируемого полинуклеотидами, описанными в настоящем документе. Полинуклеотиды настоящего изобретения охватывают последовательности нуклеиновых кислот, которые могут использоваться для селективной гибридизации с полинуклеотидом, кодирующим VCAR настоящего изобретения. См., например, публикации Ausubel, выше; Colligan, выше, которые полностью включены в настоящий документ посредством отсылки.
Конструирование нуклеиновых кислот
[0380] Выделенные нуклеиновые кислоты согласно изобретению могут быть получены с помощью: (a) рекомбинантных методов, (b) методик синтеза, (c) методик очистки и/или (d) их комбинаций, как известно в уровне техники.
[0381] Нуклеиновые кислоты предпочтительно могут включать последовательности в дополнение к полинуклеотиду согласно настоящему изобретению. Например, сайт множественного клонирования, содержащий один или более сайтов рестрикции, может быть встроен в нуклеиновую кислоту для удобства выделения полинуклеотида. Кроме того, транслируемые последовательности могут быть встроены для удобства выделения транслированного полинуклеотида согласно изобретению. Например, последовательность гексагистидиновой метки обеспечивает удобное средство для очистки белков согласно изобретению. Нуклеиновая кислота согласно изобретению, за исключением кодирующей последовательности, необязательно является вектором, адаптером или линкером для клонирования и/или экспрессии полинуклеотида согласно изобретению.
[0382] Дополнительные последовательности могут быть добавлены к таким клонирующим и/или экспрессирующим последовательностям для оптимизации их функции при клонировании и/или экспрессии для удобства при выделении полинуклеотида или для улучшения введения полинуклеотида в клетку. Применение векторов клонирования, векторов экспрессии, адаптеров и линкеров хорошо известно в данной области (см., например, Ausubel, выше; или Sambrook, выше).
Рекомбинантные методы конструирования нуклеиновых кислот
[0383] Выделенные композиции нуклеиновых кислот согласно настоящему изобретению, такие как РНК, кДНК, геномная ДНК или их любая комбинация, могут быть получены из биологических источников с помощью любого количества методик клонирования, известных специалистам в данной области. В некоторых вариантах осуществления олигонуклеотидные зонды, селективно гибридизующиеся при строгих условиях с полинуклеотидами настоящего изобретения, применяются для идентификации нужной последовательности в библиотеке кДНК или геномной ДНК. Выделение РНК и получение кДНК и геномных библиотек известны средним специалистам в данной области (см., например, Ausubel, выше; или Sambrook, выше).
Методы скрининга и выделения нуклеиновых кислот
[0384] Библиотека кДНК или геномной ДНК может быть подвергнута скринингу с использованием зонда на основе последовательности полинуклеотида согласно изобретению. Зонды могут использоваться для гибридизации с последовательностями геномной ДНК или кДНК для выделения гомологичных генов в одном и или в разных организмах. Специалистам в данной области будет очевидно, что в анализе могут использоваться различные степени жесткости гибридизации; при этом гибридизация или промывочная среда могут быть жесткими. Если условия гибридизации становятся более строгими, между зондом и мишенью должна присутствовать более высокая степень комплементарности для формирования дуплекса. Степень жесткости можно регулировать одним или более из температуры, ионной силы, рН и присутствия частично денатурирующего растворителя, такого как формамид. Например, жесткость гибридизации удобно менять путем изменения полярности раствора реагентов, например, путем изменения концентрации формамида в пределах от 0% до 50%. Степень комплементарности (идентичность последовательности), требуемая для детектируемого связывания, будет изменяться в зависимости от жесткости среды гибридизации и/или промывочной среды. Степень комплементарности оптимально будет составлять 100% или 70-100%, или находиться в любом диапазоне или значении в нем. Однако следует понимать, что незначительные вариации последовательности зондов и праймеровх можно компенсировать путем снижения жесткости гибридизации и/или промывочной среды.
[0385] Способы амплификации РНК или ДНК известны в уровне техники и могут применяться в соответствии с изобретением без излишних экспериментов, на основе принципов и руководства, представленного в настоящем документе.
[0386] Известные способы амплификации ДНК или РНК включают, без ограничения перечисленными, полимеразную цепную реакцию (ПЦР) и подобные процессы амплификации (см., например, патенты США 4,683,195, 4,683,202, 4,800,159, 4,965,188 (Mullis, et al.); 4,795,699 и 4,921,794 (Tabor, et al.); 5,142,033 (Innis); 5,122,464 (Wilson, et al.); 5,091,310 (Innis); 5,066,584 (Gyllensten, et al.); 4,889,818 (Gelfand, et al.); 4,994,370 (Silver, et al.); 4,766,067 (Biswas); 4,656,134 (Ringold)), а также РНК-опосредованую амплификацию, в которой используется антисмысловая РНК к последовательности-мишени в качестве матрицы для синтеза двухцепочечной ДНК (патент США 5,130,238 (Malek, et al.), с торговым наименованием NASBA), все содержание которых включено в настоящий документ посредством отсылки (см., например, Ausubel, выше; или Sambrook, выше.)
[0387] Например, технология полимеразной цепной реакции (ПЦР) может использоваться для амплификации последовательностей полинуклеотидов согласно изобретению и родственных генов непосредственно из библиотек геномной ДНК или кДНК. ПЦР и другие методы амплификации in vitro также могут применяться, например, для клонирования последовательностей нуклеиновых кислот, кодирующих экспрессируемые белки, с получением нуклеиновых кислот для использования в качестве зондов для обнаружения присутствия нужной мРНК в образцах, для секвенирования нуклеиновых кислот или для других целей. Примеры методов, достаточных для направления специалистов в отношении методов амплификации, можно найти в публикациях Berger, выше, Sambrook, выше и Ausubel, выше, а также в Mullis, et al., патенте США 4,683,202 (1987); и Innis, et al., PCR Protocols A Guide to Methods and Applications, Eds., Academic Press Inc., San Diego, Calif. (1990). Доступные в продаже наборы для геномной ПЦР-амплификации известны в данной области. См., например, набор Advantage-GC Genomic PCR Kit (Clontech). Кроме того, например, ген белка 32 T4 (Boehringer Mannheim) может использоваться для повышения выхода длинных ПЦР-продуктов.
Способы синтеза для конструирования нуклеиновых кислот
[0388] Выделенные нуклеиновые кислоты согласно изобретению также могут быть получены путем прямого химического синтеза известными способами (см., например, Ausubel, et al., выше). Химический синтез обычно дает одноцепочечный олигонуклеотид, который может быть превращен в двухцепочечную ДНК при гибридизации с комплементарной последовательностью или при полимеризации ДНК-полимеразой с использованием одной цепи в качестве матрицы. Специалисту в данной области будет известно, что, хотя химический синтез ДНК может быть ограничен последовательностями длиной приблизительно 100 или более оснований, более длинные последовательности могут быть получены при лигировании более коротких последовательностей.
Рекомбинантные кассеты экспрессии
[0389] В изобретении также предложены рекомбинантные кассеты экспрессии, содержащие нуклеиновую кислоту согласно изобретению. Последовательность нуклеиновой кислоты согласно изобретению, например, кДНК или геномная последовательность, кодирующая VCAR согласно изобретению, может использоваться для конструирования рекомбинантной кассеты экспрессии, которая может быть введена по меньшей мере в одну требуемую клетку-хозяина. Рекомбинантная кассета экспрессии обычно содержит полинуклеотид согласно изобретению, функционально связанный с регуляторными последовательностями инициации транскрипции, которые будут направлять транскрипцию полинуклеотида в предполагаемой клетке-хозяине. Как гетерологичные, так и негетерологичные (то есть эндогенные) промоторы могут использоваться для прямой экспрессии нуклеиновых кислот согласно изобретению.
[0390] В некоторых вариантах осуществления выделенные нуклеиновые кислоты, которые служат в качестве промотора, энхансера или других элементов, могут быть введены в соответствующем положении (до, после или в интрон) негетерологичной формы полинуклеотида согласно изобретению с целью повышения или снижения экспрессии полинуклеотида согласно изобретению. Например, эндогенные промоторы могут быть изменены путем мутации, делеции и/или замены in vivo или in vitro.
Нанотранспозоны
[0391] В изобретении предложен нанотранспозон, включающий: (a) последовательность, кодирующую вставку транспозона, включающую последовательность, кодирующую первый инвертированный концевой повтор (ITR), последовательность, кодирующую второй инвертированный концевой повтор (ITR), и интра-ITR-последовательность; (b) последовательность, кодирующую скелет, где последовательность, кодирующая скелет, включает последовательность, кодирующую точку начала репликации, содержащую 1-450 нуклеотидов, включая конечные значения, и последовательность, кодирующую селективный маркер, содержащий 1-200 нуклеотидов, включая конечные значения, и (c) интер-ITR-последовательность. В некоторых вариантах осуществления интер-ITR-последовательность (c) включает последовательность (b). В некоторых вариантах осуществления интра-ITR-последовательность (a) включает последовательность (b).
[0392] В некоторых вариантах осуществления нанотранспозонов согласно изобретению последовательность, кодирующая скелет, включает 1-600 нуклеотидов, включая конечные значения. В некоторых вариантах осуществления последовательность, кодирующая скелет, состоит из 1-50 нуклеотидов, 50-100 нуклеотидов, 100-150 нуклеотидов, 150-200 нуклеотидов, 200-250 нуклеотидов, 250-300 нуклеотидов, 300-350 нуклеотидов, 350-400 нуклеотидов, 400-450 нуклеотидов, 450-500 нуклеотидов, 500-550 нуклеотидов, 550-600 нуклеотидов, где каждый диапазон включает конечные значения.
[0393] В некоторых вариантах осуществления нанотранспозонов согласно изобретению интер-ITR-последовательность включает 1-1000 нуклеотидов, включая конечные значения. В некоторых вариантах осуществления интер-ITR-последовательность состоит из 1-50 нуклеотидов, 50-100 нуклеотидов, 100-150 нуклеотидов, 150-200 нуклеотидов, 200-250 нуклеотидов, 250-300 нуклеотидов, 300-350 нуклеотидов, 350-400 нуклеотидов, 400-450 нуклеотидов, 450-500 нуклеотидов, 500-550 нуклеотидов, 550-600 нуклеотидов, 600-650 нуклеотидов, 650-700 нуклеотидов, 700-750 нуклеотидов, 750-800 нуклеотидов, 800-850 нуклеотидов, 850-900 нуклеотидов, 900-950 нуклеотидов или 950-1000 нуклеотидов, где каждый диапазон включает конечные значения.
[0394] В некоторых вариантах осуществления нанотранспозонов согласно изобретению, включая короткие нанотранспозоны (SNT) согласно изобретению, интер-ITR-последовательность включает 1-200 нуклеотидов, включая конечные значения. В некоторых вариантах осуществления интер-ITR-последовательность состоит из 1-10 нуклеотидов, 10-20 нуклеотидов, 20-30 нуклеотидов, 30-40 нуклеотидов, 40-50 нуклеотидов, 50-60 нуклеотидов, 60-70 нуклеотидов, 70-80 нуклеотидов, 80-90 нуклеотидов или 90-100 нуклеотидов, где каждый диапазон включает конечные значения.
[0395] В некоторых вариантах осуществления нанотранспозонов согласно изобретению селективный маркер, содержащий 1-200 нуклеотидов, включая конечные значения, включает последовательность, кодирующую сахароза-селективный маркер. В некоторых вариантах осуществления последовательность, кодирующая сахароза-селективный маркер, включает последовательность, кодирующую последовательность RNA-OUT. В некоторых вариантах осуществления последовательность, кодирующая последовательность RNA-OUT, включает или состоит из 137 пар оснований (пн). В некоторых вариантах осуществления селективный маркер, содержащий 1-200 нуклеотидов, включая конечные значения, включает последовательность, кодирующую флуоресцентный маркер. В некоторых вариантах осуществления селективный маркер, содержащий 1-200 нуклеотидов, включая конечные значения, включает последовательность, кодирующую маркер клеточной поверхности.
[0396] В некоторых вариантах осуществления нанотранспозонов согласно изобретению последовательность, кодирующая точку начала репликации, содержащая 1-450 нуклеотидов, включая конечные значения, содержит последовательность, кодирующую мини-начало репликации. В некоторых вариантах осуществления последовательность, кодирующая начало репликации, содержащая 1-450 нуклеотидов, включая конечные точки, содержит последовательность, кодирующую начало репликации R6K. В некоторых вариантах осуществления начало репликации R6K содержит начало репликации R6K гамма. В некоторых вариантах осуществления начало репликации R6K содержит мини-начало репликации R6K. В некоторых вариантах осуществления начало репликации R6K содержит мини-начало репликации R6K гамма. В некоторых вариантах осуществления мини-начало репликации R6K гамма содержит или состоит из 281 пары оснований (пн).
[0397] В некоторых вариантах осуществления нанотранспозонов согласно изобретению последовательность, кодирующая скелет, не содержит сайт рекомбинации, сайт вырезания, сайт лигирования или их комбинацию. В некоторых вариантах осуществления ни нанотранспозон, ни последовательность, кодирующая скелет, не содержат продукт сайта рекомбинации, сайта вырезания, сайта лигирования или их комбинации. В некоторых вариантах осуществления ни нанотранспозон, ни последовательность, кодирующая скелет, не получены из сайта рекомбинации, сайта вырезания, сайта лигирования или их комбинации.
[0398] В некоторых вариантах осуществления нанотранспозонов согласно изобретению сайт рекомбинации включает последовательность, полученную в результате события рекомбинации. В некоторых вариантах осуществления сайт рекомбинации включает последовательность, которая является продуктом события рекомбинации. В некоторых вариантах осуществления событие рекомбинации включает активность рекомбиназы (например, сайт рекомбиназы).
[0399] В некоторых вариантах осуществления нанотранспозонов согласно изобретению последовательность, кодирующая скелет, также не включает последовательность, кодирующую чужеродную ДНК.
[0400] В некоторых вариантах осуществления нанотранспозонов согласно изобретению интер-ITR-последовательность не включает сайт рекомбинации, сайт вырезания, сайт лигирования или их комбинацию. В некоторых вариантах осуществления интер-ITR-последовательность не включает продукт события рекомбинации, события вырезания, события лигирования или их комбинации. В некоторых вариантах осуществления интер-ITR-последовательность не получена из события рекомбинации, события вырезания, события лигирования или их комбинации.
[0401] В некоторых вариантах осуществления нанотранспозонов согласно изобретению интер-ITR-последовательность включает последовательность, кодирующую чужеродную ДНК.
[0402] В некоторых вариантах осуществления нанотранспозонов согласно изобретению интра-ITR-последовательность включает по меньшей мере одну последовательность, кодирующую инсулятор, и последовательность, кодирующую промотор, способный к экспрессии экзогенной последовательности в клетке млекопитающего. В некоторых вариантах осуществления клетка млекопитающего является клеткой человека.
[0403] В некоторых вариантах осуществления нанотранспозонов согласно изобретению интра-ITR-последовательность включает первую последовательность, кодирующую инсулятор, последовательность, кодирующую промотор, способный к экспрессии экзогенной последовательности в клетке млекопитающего, и вторую последовательность, кодирующую инсулятор.
[0404] В некоторых вариантах осуществления нанотранспозонов согласно изобретению интра-ITR-последовательность включает первую последовательность, кодирующую инсулятор, последовательность, кодирующую промотор, способный к экспрессии экзогенной последовательности в клетке млекопитающего, последовательность полиаденозина (поли(A)) и вторую последовательность, кодирующую инсулятор.
[0405] В некоторых вариантах осуществления нанотранспозонов согласно изобретению интра-ITR-последовательность включает первую последовательность, кодирующую инсулятор, последовательность, кодирующую промотор, способный к экспрессии экзогенной последовательности в клетке млекопитающего, по меньшей мере одну экзогенную последовательность, последовательность полиаденозина (поли(A)) и вторую последовательность, кодирующую инсулятор.
[0406] В некоторых вариантах осуществления нанотранспозонов согласно изобретению последовательность, кодирующая промотор, способный к экспрессии экзогенной последовательности в клетке млекопитающего, способна к экспрессии экзогенной последовательности в клетке человека. В некоторых вариантах осуществления последовательность, кодирующая промотор, способный к экспрессии экзогенной последовательности в клетке млекопитающего, включает последовательность, кодирующую конститутивный промотор. В некоторых вариантах осуществления последовательность, кодирующая промотор, способный к экспрессии экзогенной последовательности в клетке млекопитающего, включает последовательность, кодирующую индуцируемый промотор. В некоторых вариантах осуществления интра-ITR-последовательность включает первую последовательность, кодирующую первый промотор, способный к экспрессии экзогенной последовательности в клетке млекопитающего, и вторую последовательность, кодирующую второй промотор, способный к экспрессии экзогенной последовательности в клетке млекопитающего, где первый промотор является конститутивным промотором, где второй промотор является индуцируемым промотором, и где первая последовательность, кодирующая первый промотор, и вторая последовательность, кодирующая второй промотор, ориентированы в противоположных направлениях. В некоторых вариантах осуществления последовательность, кодирующая промотор, способный к экспрессии экзогенной последовательности в клетке млекопитающего, включает последовательность, кодирующую промотор, специфический для определенного типа клеток или типа ткани. В некоторых вариантах осуществления последовательность, кодирующая промотор, способный к экспрессии экзогенной последовательности в клетке млекопитающего, включает последовательность, кодирующую промотор EF1a, последовательность, кодирующую промотор ЦМВ, последовательность, кодирующую промотор MND, последовательность, кодирующую промотор SV40, последовательность, кодирующую промотор PGK1, последовательность, кодирующую промотор Ubc, последовательность, кодирующую промотор CAG, последовательность, кодирующую промотор H1, или последовательность, кодирующую промотор U6.
[0407] В некоторых вариантах осуществления нанотранспозонов согласно изобретению последовательность полиаденозина (поли(A)) выделена или получена из вирусной последовательности поли(A). В некоторых вариантах осуществления последовательность полиаденозина (поли(A)) выделена или получена из последовательности поли(A) (SV40).
[0408] В некоторых вариантах осуществления нанотранспозонов согласно изобретению по меньшей мере одна экзогенная последовательность включает индуцируемый проапоптотический полипептид. В некоторых вариантах осуществления индуцируемый полипептид каспазы включает: (a) лигандсвязывающую область, (b) линкер и (c) полипептид каспазы, где индуцируемый проапоптотический полипептид не включает нечеловеческую последовательность. В некоторых вариантах осуществления индуцируемый полипептид каспазы включает: (a) лигандсвязывающую область, (b) линкер и (c) усеченный полипептид каспазы 9, где индуцируемый проапоптотический полипептид не включает нечеловеческую последовательность.
[0409] В некоторых вариантах осуществления нанотранспозонов согласно изобретению, включая те, в которых по меньшей мере одна экзогенная последовательность содержит индуцируемый проапоптотический полипептид, лигандсвязывающая область содержит полипептид FK506-связывающего белка 12 (FKBP12). В некоторых вариантах осуществления аминокислотная последовательность лигандсвязывающей области содержит полипептид FK506-связывающего белка 12 (FKBP12). В некоторых вариантах осуществления полипептид FK506-связывающего белка 12 (FKBP12) содержит модификацию в положении 36 последовательности. В некоторых вариантах осуществления модификация включает замену валина (V) на фенилаланин (F) в положении 36 (F36V). В некоторых вариантах осуществления полипептид FKBP12 кодируется аминокислотной последовательностью, включающей GVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKVDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLE (SEQ ID NO:14635). В некоторых вариантах осуществления полипептид FKBP12 кодируется последовательностью нуклеиновой кислоты, включающей GGGGTCCAGGTCGAGACTATTTCACCAGGGGATGGGCGAACATTTCCAAAAAGGGGCCAGACTTGCGTCGTGCATTACACCGGGATGCTGGAGGACGGGAAGAAAGTGGACAGCTCCAGGGATCGCAACAAGCCCTTCAAGTTCATGCTGGGAAAGCAGGAAGTGATCCGAGGATGGGAGGAAGGCGTGGCACAGATGTCAGTCGGCCAGCGGGCCAAACTGACCATTAGCCCTGACTACGCTTATGGAGCAACAGGCCACCCAGGGATCATTCCCCCTCATGCCACCCTGGTCTTCGATGTGGAACTGCTGAAGCTGGAG (SEQ ID NO:14636).
[0410] В некоторых вариантах осуществления нанотранспозонов согласно изобретению, включая те, в которых по меньшей мере одна экзогенная последовательность включает индуцируемый проапоптотический полипептид, линкерная область кодируется аминокислотной последовательностью, включающей GGGGS (SEQ ID NO:14637), или последовательностью нуклеиновой кислоты, включающей GGAGGAGGAGGATCC (SEQ ID NO:14638). В некоторых вариантах осуществления последовательность нуклеиновой кислоты, кодирующая линкер, не включает сайт рестрикции.
[0411] В некоторых вариантах осуществления нанотранспозонов согласно изобретению, включая те, в которых по меньшей мере одна экзогенная последовательность включает индуцируемый проапоптотический полипептид, усеченный полипептид каспазы 9 кодируется аминокислотной последовательностью, которая не включает аргинин (R) в положении 87 последовательности. В некоторых вариантах осуществления усеченный полипептид каспазы 9 кодируется аминокислотной последовательностью, которая не включает аланин (A) в положении 282 последовательности. В некоторых вариантах осуществления усеченный полипептид каспазы 9 кодируется аминокислотной последовательностью, включающей GFGDVGALESLRGNADLAYILSMEPCGHCLIINNVNFCRESGLRTRTGSNIDCEKLRRRFSSLHFMVEVKGDLTAKKMVLALLELAQQDHGALDCCVVVILSHGCQASHLQFPGAVYGTDGCPVSVEKIVNIFNGTSCPSLGGKPKLFFIQACGGEQKDHGFEVASTSPEDESPGSNPEPDATPFQEGLRTFDQLDAISSLPTPSDIFVSYSTFPGFVSWRDPKSGSWYVETLDDIFEQWAHSEDLQSLLLRVANAVSVKGIYKQMPGCFNFLRKKLFFKTS (SEQ ID NO:14639). В некоторых вариантах осуществления усеченный полипептид каспазы 9 кодируется последовательностью нуклеиновой кислоты, включающей GGATTTGGGGACGTGGGGGCCCTGGAGTCTCTGCGAGGAAATGCCGATCTGGCTTACATCCTGAGCATGGAACCCTGCGGCCACTGTCTGATCATTAACAATGTGAACTTCTGCAGAGAAAGCGGACTGCGAACACGGACTGGCTCCAATATTGACTGTGAGAAGCTGCGGAGAAGGTTCTCTAGTCTGCACTTTATGGTCGAAGTGAAAGGGGATCTGACCGCCAAGAAAATGGTGCTGGCCCTGCTGGAGCTGGCTCAGCAGGACCATGGAGCTCTGGATTGCTGCGTGGTCGTGATCCTGTCCCACGGGTGCCAGGCTTCTCATCTGCAGTTCCCCGGAGCAGTGTACGGAACAGACGGCTGTCCTGTCAGCGTGGAGAAGATCGTCAACATCTTCAACGGCACTTCTTGCCCTAGTCTGGGGGGAAAGCCAAAACTGTTCTTTATCCAGGCCTGTGGCGGGGAACAGAAAGATCACGGCTTCGAGGTGGCCAGCACCAGCCCTGAGGACGAATCACCAGGGAGCAACCCTGAACCAGATGCAACTCCATTCCAGGAGGGACTGAGGACCTTTGACCAGCTGGATGCTATCTCAAGCCTGCCCACTCCTAGTGACATTTTCGTGTCTTACAGTACCTTCCCAGGCTTTGTCTCATGGCGCGATCCCAAGTCAGGGAGCTGGTACGTGGAGACACTGGACGACATCTTTGAACAGTGGGCCCATTCAGAGGACCTGCAGAGCCTGCTGCTGCGAGTGGCAAACGCTGTCTCTGTGAAGGGCATCTACAAACAGATGCCCGGGTGCTTCAATTTTCTGAGAAAGAAACTGTTCTTTAAGACTTCC (SEQ ID NO:14640).
[0412] В некоторых вариантах осуществления нанотранспозонов согласно изобретению, включая те, в которых по меньшей мере одна экзогенная последовательность включает индуцируемый проапоптотический полипептид, индуцируемый проапоптотический полипептид кодируется аминокислотной последовательностью, включающей GVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKVDSSRDRNKPFKFMLGKQ EVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLEGGGGSGFGDVGALESLRGNADLAYILSMEPCGHCLIINNVNFCRESGLRTRTGSNIDCEKLRRRFSSLHFMVEVKGDLTAKKMVLALLELAQQDHGALDCCVVVILSHGCQASHLQFPGAVYGTDGCPVSVEKIVNIFNGTSCPSLGGKPKLFFIQACGGEQKDHGFEVASTSPEDESPGSNPEPDATPFQEGLRTFDQLDAISSLPTPSDIFVSYSTFPGFVSWRDPKSGSWYVETLDDIFEQWAHSEDLQSLLLRVANAVSVKGIYKQMPGCFNFLRKKLFFKTS (SEQ ID NO:14641). В некоторых вариантах осуществления индуцируемый проапоптотический полипептид кодируется последовательностью нуклеиновой кислоты, включающей ggggtccaggtcgagactatttcaccaggggatgggcgaacatttccaaaaaggggccagacttgcgtcgtgcattacaccgggatgctggaggacgggaagaaagtggacagctccagggatcgcaacaagcccttcaagttcatgctgggaaagcaggaagtgatccgaggatgggaggaaggcgtggcacagatgtcagtcggccagcgggccaaactgaccattagccctgactacgcttatggagcaacaggccacccagggatcattccccctcatgccaccctggtcttcgatgtggaactgctgaagctggagggaggaggaggatccggatttggggacgtgggggccctggagtctctgcgaggaaatgccgatctggcttacatcctgagcatggaaccctgcggccactgtctgatcattaacaatgtgaacttctgcagagaaagcggactgcgaacacggactggctccaatattgactgtgagaagctgcggagaaggttctctagtctgcactttatggtcgaagtgaaaggggatctgaccgccaagaaaatggtgctggccctgctggagctggctcagcaggaccatggagctctggattgctgcgtggtcgtgatcctgtcccacgggtgccaggcttctcatctgcagttccccggagcagtgtacggaacagacggctgtcctgtcagcgtggagaagatcgtcaacatcttcaacggcacttcttgccctagtctggggggaaagccaaaactgttctttatccaggcctgtggcggggaacagaaagatcacggcttcgaggtggccagcaccagccctgaggacgaatcaccagggagcaaccctgaaccagatgcaactccattccaggagggactgaggacctttgaccagctggatgctatctcaagcctgcccactcctagtgacattttcgtgtcttacagtaccttcccaggctttgtctcatggcgcgatcccaagtcagggagctggtacgtggagacactggacgacatctttgaacagtgggcccattcagaggacctgcagagcctgctgctgcgagtggcaaacgctgtctctgtgaagggcatctacaaacagatgcccgggtgcttcaattttctgagaaagaaactgttctttaagacttcc (SEQ ID NO:14642).
[0413] В некоторых вариантах осуществления нанотранспозонов согласно изобретению, включая те, в которых по меньшей мере одна экзогенная последовательность включает индуцируемый проапоптотический полипептид, экзогенная последовательность дополнительно включает последовательность, кодирующую селективный маркер. В некоторых вариантах осуществления последовательность, кодирующая селективный маркер, включает последовательность, кодирующую детектируемый маркер. В некоторых вариантах осуществления детектируемый маркер включает флуоресцентный маркер или маркер клеточной поверхности. В некоторых вариантах осуществления последовательность, кодирующая селективный маркер, включает последовательность, кодирующую белок, который активен в делящихся клетках и не активен в неделящихся клетках. В некоторых вариантах осуществления последовательность, кодирующая селективный маркер, включает последовательность, кодирующую метаболический маркер. В некоторых вариантах осуществления последовательность, кодирующая селективный маркер, включает последовательность, кодирующую мутеин фермента дигидрофолатредуктазы (DHFR). В некоторых вариантах осуществления мутеин фермента DHFR включает или состоит из аминокислотной последовательности:
1 MVGSLNCIVA VSQNMGIGKN GDFPWPPLRN ESRYFQRMTT TSSVEGKQNL
61 VIMGKKTWFS IPEKNRPLKG RINLVLSREL KEPPQGAHFL SRSLDDALKL
121 TEQPELANKV DMVWIVGGSS VYKEAMNHPG HLKLFVTRIM QDFESDTFFP
181 EIDLEKYKLL PEYPGVLSDV QEEKGIKYKF EVYEKND (SEQ ID NO:17012).
В некоторых вариантах осуществления мутеин фермента DHFR кодируется последовательностью нуклеиновой кислоты, включающей или состоящей из ofatggtcgggtctctgaattgtatcgtcgccgtgagtcagaacatgggcattgggaagaatggcgatttcccatggccacctctgcgcaacgagtcccgatactttcagcggatgacaactacctcctctgtggaagggaaacagaatctggtcatcatgggaaagaaaacttggttcagcattccagagaagaaccggcccctgaaaggcagaatcaatctggtgctgtcccgagaactgaaggagccaccacagggagctcactttctgagccggtccctggacgatgcactgaagctgacagaacagcctgagctggccaacaaagtcgatatggtgtggatcgtcgggggaagttcagtgtataaggaggccatgaatcaccccggccatctgaaactgttcgtcacacggatcatgcaggactttgagagcgatactttctttcctgaaattgacctggagaagtacaaactgctgcccgaatatcctggcgtgctgtccgatgtccaggaagagaaaggcatcaaatacaagttcgaggtctatgagaagaatgac (SEQ ID NO:17095). В некоторых вариантах осуществления аминокислотная последовательность мутеина фермента DHFR дополнительно включает мутацию в одном или более положениях из 80, 113 или 153. В некоторых вариантах осуществления аминокислотная последовательность мутеина фермента DHFR включает одну или более из замены фенилаланина (F) или лейцина (L) в положении 80, замены лейцина (L) или валина (V) в положении 113 и замены валина (V) или аспарагиновой кислоты (D) в положении 153.
[0414] В некоторых вариантах осуществления нанотранспозонов согласно изобретению, включая те, в которых по меньшей мере одна экзогенная последовательность включает индуцируемый проапоптотический полипептид, и/или экзогенная последовательность включает последовательность, кодирующую селективный маркер, экзогенная последовательность дополнительно включает последовательность, кодирующую не встречающийся в природе антигенный рецептор и/или последовательность, кодирующую терапевтический полипептид. В некоторых вариантах осуществления не встречающийся в природе антигенный рецептор включает T-клеточный рецептор (TCR). В некоторых вариантах осуществления последовательность, кодирующая TCR, включает одно или более из вставки, делеции, замены, инверсии, транспозиции или сдвига рамки считывания по сравнению с соответствующей последовательностью дикого типа. В некоторых вариантах осуществления последовательность, кодирующая TCR, включает химерную или рекомбинантную последовательность. В некоторых вариантах осуществления не встречающийся в природе антигенный рецептор включает химерный антигенный рецептор (CAR). В некоторых вариантах осуществления CAR включает: (a) эктодомен, включающий область распознавания антигена, (b) трансмембранный домен и (c) эндодомен, включающий по меньшей мере один костимулирующий домен. В некоторых вариантах осуществления эктодомен (a) CAR дополнительно включает сигнальный пептид. В некоторых вариантах осуществления эктодомен (a) CAR дополнительно включает шарнирную область между областью распознавания антигена и трансмембранным доменом. В некоторых вариантах осуществления эндодомен включает эндодомен человеческого CD3ζ. В некоторых вариантах осуществления по меньшей мере один костимулирующий домен включает внутриклеточный сегмент 4-1BB, CD28, CD40, ICOS, MyD88, OX-40 человека или их любую комбинацию. В некоторых вариантах осуществления по меньшей мере один костимулирующий домен включает костимулирующий домен CD28 и/или 4-1BB человека. В некоторых вариантах осуществления область распознавания антигена включает одно или более из scFv, VHH, VH и Центирин.
[0415] В некоторых вариантах осуществления нанотранспозонов согласно изобретению, включая те, в которых по меньшей мере одна экзогенная последовательность включает индуцируемый проапоптотический полипептид, и/или экзогенная последовательность включает последовательность, кодирующую селективный маркер, экзогенная последовательность дополнительно включает последовательность, кодирующую транспозазу.
[0416] В некоторых вариантах осуществления нанотранспозонов согласно изобретению интра-ITR-последовательность включает последовательность, кодирующую селективный маркер, экзогенную последовательность, последовательность, кодирующую индуцируемый полипептид каспазы, и по меньшей мере одну последовательность, кодирующую саморасщепляющийся пептид. В некоторых вариантах осуществления по меньшей мере одна последовательность, кодирующая саморасщепляющийся пептид, расположена между одним или более из: (a) последовательности, кодирующей селективный маркер, и экзогенной последовательности, (b) последовательности, кодирующей селективный маркер, и индуцируемого полипептида каспазы, и (c) экзогенной последовательности и индуцируемого полипептида каспазы. В некоторых вариантах осуществления первая последовательность, кодирующая саморасщепляющийся пептид, расположена между последовательностью, кодирующей селективный маркер, и экзогенной последовательностью, и вторая последовательность, кодирующая саморасщепляющийся пептид, расположена между экзогенной последовательностью и индуцируемым полипептидом каспазы.
[0417] В некоторых вариантах осуществления нанотранспозонов согласно изобретению, включая те, в которых по меньшей мере одна экзогенная последовательность включает одно или более из индуцируемого проапоптотического полипептида, последовательности, кодирующей селективный маркер, и экзогенной последовательности, последовательность, кодирующая первое инвертированный концевой повтор (ITR) или последовательность, кодирующая второй инвертированный концевой повтор (ITR), распознается транспозазой piggyBac или piggyBack-подобной транспозазой. В некоторых вариантах осуществления последовательность, кодирующая первый инвертированный концевой повтор (ITR), или последовательность, кодирующая второй инвертированный концевой повтор (ITR), распознается транспозазой piggyBac. В некоторых вариантах осуществления последовательность, кодирующая первый инвертированный концевой повтор (ITR), или последовательность, кодирующая второй инвертированный концевой повтор (ITR), распознается piggyBac-подобной транспозазой. В некоторых вариантах осуществления последовательность, кодирующая первый инвертированный концевой повтор (ITR), или последовательность, кодирующая второй инвертированный концевой повтор (ITR), включает последовательность распознавания TTAA, TTAT или TTAX. В некоторых вариантах осуществления последовательность, кодирующая первый инвертированный концевой повтор (ITR), или последовательность, кодирующая второй инвертированный концевой повтор (ITR), включает последовательность распознавания TTAA, TTAT или TTAX и последовательность, обладающую по меньшей мере 50% идентичностью с последовательностью, выделенной или полученной из транспозазы piggyBac или piggyBac-подобной транспозазы. В некоторых вариантах осуществления последовательность, кодирующая первый инвертированный концевой повтор (ITR), или последовательность, кодирующая второй инвертированный концевой повтор (ITR), включает по меньшей мере 2 нуклеотида (нт), 3 нт, 4 нт, 5 нт, 6 нт, 7 нт, 8 нт, 9 нт, 10 нт, 11 нт, 12 нт, 13 нт, 14 нт, 15 нт, 16 нт, 17 нт, 18 нт, 19 нт или 20 нт.
[0418] В некоторых вариантах осуществления нанотранспозонов согласно изобретению, включая те, в которых по меньшей мере одна экзогенная последовательность включает одно или более из индуцируемого проапоптотического полипептида, последовательности, кодирующей селективный маркер, и экзогенной последовательности, последовательность, кодирующая первый инвертированный концевой повтор (ITR) или последовательность, кодирующая второй инвертированный концевой повтор (ITR), распознается piggyBac-транспозазой или piggyBac-подобной транспозазой. В некоторых вариантах осуществления последовательность, кодирующая первый инвертированный концевой повтор (ITR), или последовательность, кодирующая второй инвертированный концевой повтор (ITR), включает последовательность CCCTAGAAAGATAGTCTGCGTAAAATTGACGCATG (SEQ ID NO:17096) или последовательность, обладающую по меньшей мере 70% идентичностью с последовательностью CCCTAGAAAGATAGTCTGCGTAAAATTGACGCATG (SEQ ID NO:17096). В некоторых вариантах осуществления последовательность, кодирующая первый инвертированный концевой повтор (ITR), или последовательность, кодирующая второй инвертированный концевой повтор (ITR), включает последовательность CCCTAGAAAGATAATCATATTGTGACGTACGTTAAAGATAATCATGCGTAAAATTGACGCATG (SEQ ID NO:17097). В некоторых вариантах осуществления последовательность, кодирующая первый инвертированный концевой повтор (ITR), или последовательность, кодирующая второй инвертированный концевой повтор (ITR), включает последовательность CCCTAGAAAGATAGTCTGCGTAAAATTGACGCATG (SEQ ID NO:17096), и включает последовательность CCCTAGAAAGATAATCATATTGTGACGTACGTTAAAGATAATCATGCGTAAAATTGACGCATG (SEQ ID NO:17097). В некоторых вариантах осуществления последовательность, кодирующая первый инвертированный концевой повтор (ITR), или последовательность, кодирующая второй инвертированный концевой повтор (ITR), включает последовательность CCCTAGAAAGATAGTCTGCGTAAAATTGACGCATG (SEQ ID NO:17096), и включает последовательность CCCTAGAAAGATAATCATATTGTGACGTACGTTAAAGATAATCATGTGTAAAATTGACGCATG (SEQ ID NO:17098). В некоторых вариантах осуществления последовательность, кодирующая первый инвертированный концевой повтор (ITR), или последовательность, кодирующая второй инвертированный концевой повтор (ITR), включает последовательность CCCTAGAAAGATAGTCTGCGTAAAATTGACGCATG (SEQ ID NO:17096), и включает последовательность TTAACCCTAGAAAGATAATCATATTGTGACGTACGTTAAAGATAATCATGTGTAAAATTGACGCATGTGTTTTATCGGTCTGTATATCGAGGTTTATTTATTAATTTGAATAGATATTAAGTTTTATTATATTTACACTTACATACTAATAATAAATTCAACAAACAATTTATTTATGTTTATTTATTTATTAAAAAAAACAAAAACTCAAAATTTCTTCTATAAAGTAACAAAACTTTTA (SEQ ID NO:17099).
[0419] В некоторых вариантах осуществления нанотранспозонов согласно изобретению, включая те, в которых по меньшей мере одна экзогенная последовательность включает одно или более из индуцируемого проапоптотического полипептида, последовательности, кодирующей селективный маркер, и экзогенной последовательности, последовательность, кодирующая первый инвертированный концевой повтор (ITR), или последовательность, кодирующая второй инвертированный концевой повтор (ITR), распознается транспозазой piggyBac или piggyBac-подобной транспозазой. В некоторых вариантах осуществления последовательность, кодирующая первый инвертированный концевой повтор (ITR), или последовательность, кодирующая второй инвертированный концевой повтор (ITR), распознается транспозазой piggyBac, имеющей аминокислотную последовательность, которая обладает по меньшей мере 20% идентичностью с аминокислотной последовательностью
61 SEILDEQNVI EQPGSSLASN RILTLPQRTI RGKNKHCWST SKSTRRSRVS ALNIVRSQRG
121 PTRMCRNIYD PLLCFKLFFT DEIISEIVKW TNAEISLKRR ESMTGATFRD TNEDEIYAFF
181 GILVMTAVRK DNHMSTDDLF DRSLSMVYVS VMSRDRFDFL IRCLRMDDKS IRPTLRENDV
241 FTPVRKIWDL FIHQCIQNYT PGAHLTIDEQ LLGFRGRCPF RMYIPNKPSK YGIKILMMCD
301 SGTKYMINGM PYLGRGTQTN GVPLGEYYVK ELSKPVHGSC RNITCDNWFT SIPLAKNLLQ
361 EPYKLTIVGT VRSNKREIPE VLKNSRSRPV GTSMFCFDGP LTLVSYKPKP AKMVYLLSSC
421 DEDASINEST GKPQMVMYYN QTKGGVDTLD QMCSVMTCSR KTNRWPMALL YGMINIACIN
481 SFIIYSHNVS SKGEKVQSRK KFMRNLYMSL TSSFMRKRLE APTLKRYLRD NISNILPNEV
541 PGTSDDSTEE PVMKKRTYCT YCPSKIRRKA NASCKKCKKV ICREHNIDMC QSCF
(SEQ ID NO:14487).
В некоторых вариантах осуществления последовательность, кодирующая первый инвертированный концевой повтор (ITR), или последовательность, кодирующая второй инвертированный концевой повтор (ITR), распознается транспозазой piggyBac, имеющей аминокислотную последовательность
61 SEILDEQNVI EQPGSSLASN RILTLPQRTI RGKNKHCWST SKSTRRSRVS ALNIVRSQRG
121 PTRMCRNIYD PLLCFKLFFT DEIISEIVKW TNAEISLKRR ESMTGATFRD TNEDEIYAFF
181 GILVMTAVRK DNHMSTDDLF DRSLSMVYVS VMSRDRFDFL IRCLRMDDKS IRPTLRENDV
241 FTPVRKIWDL FIHQCIQNYT PGAHLTIDEQ LLGFRGRCPF RMYIPNKPSK YGIKILMMCD
301 SGTKYMINGM PYLGRGTQTN GVPLGEYYVK ELSKPVHGSC RNITCDNWFT SIPLAKNLLQ
361 EPYKLTIVGT VRSNKREIPE VLKNSRSRPV GTSMFCFDGP LTLVSYKPKP AKMVYLLSSC
421 DEDASINEST GKPQMVMYYN QTKGGVDTLD QMCSVMTCSR KTNRWPMALL YGMINIACIN
481 SFIIYSHNVS SKGEKVQSRK KFMRNLYMSL TSSFMRKRLE APTLKRYLRD NISNILPNEV
541 PGTSDDSTEE PVMKKRTYCT YCPSKIRRKA NASCKKCKKV ICREHNIDMC QSCF
(SEQ ID NO:14487).
В некоторых вариантах осуществления последовательность, кодирующая первый инвертированный концевой повтор (ITR), или последовательность, кодирующая второй инвертированный концевой повтор (ITR), распознается транспозазой piggyBac, имеющей аминокислотную последовательность, которая обладает по меньшей мере 20% идентичностью с аминокислотной последовательностью
61 SEILDEQNVI EQPGSSLASN RILTLPQRTI RGKNKHCWST SKSTRRSRVS ALNIVRSQRG
121 PTRMCRNIYD PLLCFKLFFT DEIISEIVKW TNAEISLKRR ESMTSATFRD TNEDEIYAFF
181 GILVMTAVRK DNHMSTDDLF DRSLSMVYVS VMSRDRFDFL IRCLRMDDKS IRPTLRENDV
241 FTPVRKIWDL FIHQCIQNYT PGAHLTIDEQ LLGFRGRCPF RVYIPNKPSK YGIKILMMCD
301 SGTKYMINGM PYLGRGTQTN GVPLGEYYVK ELSKPVHGSC RNITCDNWFT SIPLAKNLLQ
361 EPYKLTIVGT VRSNKREIPE VLKNSRSRPV GTSMFCFDGP LTLVSYKPKP AKMVYLLSSC
421 DEDASINEST GKPQMVMYYN QTKGGVDTLD QMCSVMTCSR KTNRWPMALL YGMINIACIN
481 SFIIYSHNVS SKGEKVQSRK KFMRNLYMSL TSSFMRKRLE APTLKRYLRD NISNILPKEV
541 PGTSDDSTEE PVMKKRTYCT YCPSKIRRKA NASCKKCKKV ICREHNIDMC QSCF
(SEQ ID NO:14484).
В некоторых вариантах осуществления последовательность, кодирующая первый инвертированный концевой повтор (ITR), или последовательность, кодирующая второй инвертированный концевой повтор (ITR), распознается транспозазой piggyBac, имеющей аминокислотную последовательность
61 SEILDEQNVI EQPGSSLASN RILTLPQRTI RGKNKHCWST SKSTRRSRVS ALNIVRSQRG
121 PTRMCRNIYD PLLCFKLFFT DEIISEIVKW TNAEISLKRR ESMTSATFRD TNEDEIYAFF
181 GILVMTAVRK DNHMSTDDLF DRSLSMVYVS VMSRDRFDFL IRCLRMDDKS IRPTLRENDV
241 FTPVRKIWDL FIHQCIQNYT PGAHLTIDEQ LLGFRGRCPF RVYIPNKPSK YGIKILMMCD
301 SGTKYMINGM PYLGRGTQTN GVPLGEYYVK ELSKPVHGSC RNITCDNWFT SIPLAKNLLQ
361 EPYKLTIVGT VRSNKREIPE VLKNSRSRPV GTSMFCFDGP LTLVSYKPKP AKMVYLLSSC
421 DEDASINEST GKPQMVMYYN QTKGGVDTLD QMCSVMTCSR KTNRWPMALL YGMINIACIN
481 SFIIYSHNVS SKGEKVQSRK KFMRNLYMSL TSSFMRKRLE APTLKRYLRD NISNILPKEV
541 PGTSDDSTEE PVMKKRTYCT YCPSKIRRKA NASCKKCKKV ICREHNIDMC QSCF
(SEQ ID NO:14484).
[0420] В некоторых вариантах осуществления нанотранспозонов согласно изобретению, включая те, в которых по меньшей мере одна экзогенная последовательность включает одно или более из индуцируемого проапоптотического полипептида, последовательности, кодирующей селективный маркер, и экзогенной последовательности, последовательность, кодирующая первый инвертированный концевой повтор (ITR), или последовательность, кодирующая второй инвертированный концевой повтор (ITR), распознается транспозаза Sleeping beauty. В некоторых вариантах осуществления транспозаза Sleeping beauty является гиперактивной транспозазой Sleeping beauty (SB100X).
[0421] В некоторых вариантах осуществления нанотранспозонов согласно изобретению, включая те, в которых по меньшей мере одна экзогенная последовательность включает одно или более из индуцируемого проапоптотического полипептида, последовательности, кодирующей селективный маркер, и экзогенной последовательности, последовательность, кодирующая первый инвертированный концевой повтор (ITR), или последовательность, кодирующая второй инвертированный концевой повтор (ITR), распознается транспозазой Helitron.
[0422] В некоторых вариантах осуществления нанотранспозонов согласно изобретению, включая те, в которых по меньшей мере одна экзогенная последовательность включает одно или более из индуцируемого проапоптотического полипептида, последовательности, кодирующей селективный маркер, и экзогенной последовательности, последовательность, кодирующая первый инвертированный концевой повтор (ITR), или последовательность, кодирующая второй инвертированный концевой повтор (ITR), распознается транспозазой Tol2.
[0423] В изобретении предложена клетка, включающая нанотранспозон согласно изобретению. В некоторых вариантах осуществления клетка дополнительно включает композицию транспозазы. В некоторых вариантах осуществления композиция транспозазы включает транспозазу или последовательность, кодирующую транспозазу, которая способна распознавать первый ITR или второй ITR нанотранспозона. В некоторых вариантах осуществления композиция транспозазы включает нанотранспозон, включающий последовательность, кодирующую транспозазу. В некоторых вариантах осуществления клетка включает первый нанотранспозон, включающий экзогенную последовательность, и второй нанотранспозон, включающий последовательность, кодирующую транспозазу. В некоторых вариантах осуществления клетка является аллогенной клеткой.
[0424] В изобретении предложена композиция, включающая нанотранспозон согласно изобретению.
[0425] В изобретении предложена композиция, включающая клетку согласно изобретению. В некоторых вариантах осуществления клетка включает нанотранспозон согласно изобретению. В некоторых вариантах осуществления клетка не модифицирована дополнительно. В некоторых вариантах осуществления клетка является аллогенной.
[0426] В изобретении предложена композиция, включающая клетку согласно изобретению. В некоторых вариантах осуществления клетка включает нанотранспозон согласно изобретению. В некоторых вариантах осуществления клетка не модифицирована дополнительно. В некоторых вариантах осуществления клетка является аутологичной.
[0427] В изобретении предложена композиция, включающая множество клеток согласно изобретению. В некоторых вариантах осуществления по меньшей мере одна клетка множества клеток включает нанотранспозон согласно изобретению. В некоторых вариантах осуществления часть множества клеток включает нанотранспозон согласно изобретению. В некоторых вариантах осуществления часть включает по меньшей мере 1%, 2%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 97%, 99% или любой промежуточный процент из множества клеток. В некоторых вариантах осуществления каждая клетка множества клеток включает нанотранспозон согласно изобретению. В некоторых вариантах осуществления множество клеток не включает модифицированную клетку согласно изобретению. В некоторых вариантах осуществления по меньшей мере одна клетка множества клеток не модифицирована дополнительно. В некоторых вариантах осуществления ни одна из множества клеток не модифицирована дополнительно. В некоторых вариантах осуществления множество клеток является аллогенным. В некоторых вариантах осуществления аллогенное множество клеток получают в соответствии со способами согласно изобретению. В некоторых вариантах осуществления множество клеток является аутологичным. В некоторых вариантах осуществления аутологичное множество клеток получают в соответствии со способами согласно изобретению.
[0428] В изобретении предложена модифицированная клетка, включающая: (a) нанотранспозон согласно изобретению; (b) последовательность, кодирующую индуцируемый проапоптотический полипептид; и где клеткой является T-клетка, (c) модификацию эндогенной последовательности, кодирующей T-клеточный рецептор (TCR), где модификация уменьшает уровень или устраняет экспрессию или активность TCR. В некоторых вариантах осуществления клетка дополнительно включает: (d) не встречающуюся в природе последовательность, включающую альфа-цепь E HLA-антигена гистосовместимости класса I (HLA-E) и (e) модификацию эндогенной последовательности, кодирующей бета-2-микроглобулин (B2M), где модификация уменьшает уровень или устраняет экспрессию или активность главного комплекса гистосовместимости (MHC) класса I (MHC-I).
[0429] В изобретении предложена модифицированная клетка, включающая: (a) нанотранспозон согласно изобретению; (b) последовательность, кодирующую индуцируемый проапоптотический полипептид; (c) не встречающуюся в природе последовательность, включающую альфа-цепь E HLA-антигена гистосовместимости класса I (HLA-E) и (e) модификацию эндогенной последовательности, кодирующей бета-2-микроглобулин (B2M), где модификация уменьшает уровень или устраняет экспрессию или активность главного комплекса гистосовместимости (MHC) класса I (MHC-I).
[0430] В некоторых вариантах осуществления модифицированных клеток согласно изобретению не встречающаяся в природе последовательность, включающая HLA-E, дополнительно включает последовательность, кодирующую сигнальный пептид B2M. В некоторых вариантах осуществления не встречающаяся в природе последовательность, включающая HLA-E, дополнительно включает линкер, где линкер расположен между последовательностью, кодирующей последовательность, кодирующую полипептид B2M, и последовательностью, кодирующей HLA-E. В некоторых вариантах осуществления не встречающаяся в природе последовательность, включающая HLA-E, дополнительно включает последовательность, кодирующую пептид, и последовательность, кодирующую полипептид B2M. В некоторых вариантах осуществления не встречающаяся в природе последовательность, включающая HLA-E, дополнительно включает первый линкер, расположенный между последовательностью, кодирующей сигнальный пептид B2M, и последовательностью, кодирующей пептид, и второй линкер, расположенный между последовательностью, кодирующей полипептид B2M, и последовательностью, кодирующей HLA-E.
[0431] В некоторых вариантах осуществления клеток, немодифицированных клеток и модифицированных клеток согласно изобретению, клетка является клеткой млекопитающего.
[0432] В некоторых вариантах осуществления клеток, немодифицированных клеток и модифицированных клеток согласно изобретению, клетка является клеткой человека.
[0433] В некоторых вариантах осуществления клеток, немодифицированных клеток и модифицированных клеток согласно изобретению, клетка является стволовой клеткой.
[0434] В некоторых вариантах осуществления клеток, немодифицированных клеток и модифицированных клеток согласно изобретению, клетка является дифференцированной клеткой.
[0435] В некоторых вариантах осуществления клеток, немодифицированных клеток и модифицированных клеток согласно изобретению, клетка является соматической клеткой.
[0436] В некоторых вариантах осуществления клеток, немодифицированных клеток и модифицированных клеток согласно изобретению, клетка является иммунной клеткой или иммуной клеткой-предшественником. В некоторых вариантах осуществления иммуная клетка является лимфоидной клеткой-предшественником, естественной киллерной клеткой (NK), цитокин-индуцированной киллерной клеткой (CIK), T-лимфоцитом (T-клеткой), B-лимфоцитом (B-клеткой) или антигенпрезентирующей клеткой (АПК). В некоторых вариантах осуществления иммунная клетка является T-клеткой, ранней T-клеткой памяти, подобной стволовой клетке T-клеткой, стволовой T-клеткой памяти (Tscm) или T-клеткой центральной памяти (Tcm). В некоторых вариантах осуществления иммуная клетка-предшественник является гемопоэтической стволовой клеткой (HSC). В некоторых вариантах осуществления клетка является антигенпрезентирующей клеткой (АПК).
[0437] В некоторых вариантах осуществления клеток, немодифицированных клеток и модифицированных клеток согласно изобретению, клетка дополнительно включает композицию редактирования гена. В некоторых вариантах осуществления композиция редактирования гена включает последовательность, кодирующую ДНК-связывающий домен, и последовательность, кодирующую белок нуклеазу или соответствующий домен нуклеазы. В некоторых вариантах осуществления композиция редактирования гена включает последовательность, кодирующую белок нуклеазы или последовательность, кодирующую соответствующий домен нуклеазы. В некоторых вариантах осуществления последовательность, кодирующая белок нуклеазу, или последовательность, кодирующая соответствующий домен нуклеазы, включает последовательность ДНК, последовательность РНК или их комбинацию. В некоторых вариантах осуществления, нуклеаза или соответствующий домен нуклеазы включает одно или более из белка CRISPR/Cas, подобной активатору транскрипции эффекторной нуклеазы (TALEN), цинк-пальцевой нуклеазы (ZFN) и эндонуклеазы. В некоторых вариантах осуществления белок CRISPR/Cas включает нуклеаза-инактивированный белок Cas (dCas).
[0438] В некоторых вариантах осуществления клеток, немодифицированных клеток и модифицированных клеток согласно изобретению клетка дополнительно включает композицию редактирования гена. В некоторых вариантах осуществления композиция редактирования гена включает последовательность, кодирующую ДНК-связывающий домен и последовательность, кодирующую белок нуклеазу или соответствующий домен нуклеазы. В некоторых вариантах осуществления нуклеаза или соответствующий домен нуклеазы включает нуклеаза-инактивированный белок Cas (dCas) и эндонуклеазу. В некоторых вариантах осуществления эндонуклеаза включает нуклеазу Clo051 или соответствующий домен нуклеазы. В некоторых вариантах осуществления композиция редактирования гена включает слитый белок. В некоторых вариантах осуществления слитый белок включает нуклеаза-инактивированный белок Cas9 (dCas9) и нуклеазу Clo051 или домен нуклеазы Clo051. В некоторых вариантах осуществления композиция редактирования гена дополнительно включает гидовую последовательность. В некоторых вариантах осуществления гидовая последовательность включает последовательность РНК. В некоторых вариантах осуществления слитый белок включает или состоит из аминокислотной последовательности:
MAPKKKRKVEGIKSNISLLKDELRGQISHISHEYLSLIDLAFDSKQNRLFEMKVLELLVNEYGFKGRHLGGSRKPDGIVYSTTLEDNFGIIVDTKAYSEGYSLPISQADEMERYVRENSNRDEEVNPNKWWENFSEEVKKYYFVFISGSFKGKFEEQLRRLSMTTGVNGSAVNVVNLLLGAEKIRSGEMTIEELERAMFNNSEFILKYGGGGSDKKYSIGLAIGTNSVGWAVITDEYKVPSKKFKVLGNTDRHSIKKNLIGALLFDSGETAEATRLKRTARRRYTRRKNRICYLQEIFSNEMAKVDDSFFHRLEESFLVEEDKKHERHPIFGNIVDEVAYHEKYPTIYHLRKKLVDSTDKADLRLIYLALAHMIKFRGHFLIEGDLNPDNSDVDKLFIQLVQTYNQLFEENPINASGVDAKAILSARLSKSRRLENLIAQLPGEKKNGLFGNLIALSLGLTPNFKSNFDLAEDAKLQLSKDTYDDDLDNLLAQIGDQYADLFLAAKNLSDAILLSDILRVNTEITKAPLSASMIKRYDEHHQDLTLLKALVRQQLPEKYKEIFFDQSKNGYAGYIDGGASQEEFYKFIKPILEKMDGTEELLVKLNREDLLRKQRTFDNGSIPHQIHLGELHAILRRQEDFYPFLKDNREKIEKILTFRIPYYVGPLARGNSRFAWMTRKSEETITPWNFEEVVDKGASAQSFIERMTNFDKNLPNEKVLPKHSLLYEYFTVYNELTKVKYVTEGMRKPAFLSGEQKKAIVDLLFKTNRKVTVKQLKEDYFKKIECFDSVEISGVEDRFNASLGTYHDLLKIIKDKDFLDNEENEDILEDIVLTLTLFEDREMIEERLKTYAHLFDDKVMKQLKRRRYTGWGRLSRKLINGIRDKQSGKTILDFLKSDGFANRNFMQLIHDDSLTFKEDIQKAQVSGQGDSLHEHIANLAGSPAIKKGILQTVKVVDELVKVMGRHKPENIVIEMARENQTTQKGQKNSRERMKRIEEGIKELGSQILKEHPVENTQLQNEKLYLYYLQNGRDMYVDQELDINRLSDYDVDAIVPQSFLKDDSIDNKVLTRSDKNRGKSDNVPSEEVVKKMKNYWRQLLNAKLITQRKFDNLTKAERGGLSELDKAGFIKRQLVETRQITKHVAQILDSRMNTKYDENDKLIREVKVITLKSKLVSDFRKDFQFYKVREINNYHHAHDAYLNAVVGTALIKKYPKLESEFVYGDYKVYDVRKMIAKSEQEIGKATAKYFFYSNIMNFFKTEITLANGEIRKRPLIETNGETGEIVWDKGRDFATVRKVLSMPQVNIVKKTEVQTGGFSKESILPKRNSDKLIARKKDWDPKKYGGFDSPTVAYSVLVVAKVEKGKSKKLKSVKELLGITIMERSSFEKNPIDFLEAKGYKEVKKDLIIKLPKYSLFELENGRKRMLASAGELQKGNELALPSKYVNFLYLASHYEKLKGSPEDNEQKQLFVEQHKHYLDEIIEQISEFSKRVILADANLDKVLSAYNKHRDKPIREQAENIIHLFTLTNLGAPAAFKYFDTTIDRKRYTSTKEVLDATLIHQSITGLYETRIDLSQLGGDGSPKKKRKVSS (SEQ ID NO:17013) или нуклеиновой кислоты, включающей или состоящей из последовательности:
61 gacgaactgc ggggacagat tagtcacatc agtcacgagt acctgtcact gattgatctg
121 gccttcgaca gcaagcagaa tagactgttt gagatgaaag tgctggaact gctggtcaac
181 gagtatggct tcaagggcag acatctgggc gggtctagga aacctgacgg catcgtgtac
241 agtaccacac tggaagacaa cttcggaatc attgtcgata ccaaggctta ttccgagggc
301 tactctctgc caattagtca ggcagatgag atggaaaggt acgtgcgcga aaactcaaat
361 agggacgagg aagtcaaccc caataagtgg tgggagaatt tcagcgagga agtgaagaaa
421 tactacttcg tctttatctc aggcagcttc aaagggaagt ttgaggaaca gctgcggaga
481 ctgtccatga ctaccggggt gaacggatct gctgtcaacg tggtcaatct gctgctgggc
541 gcagaaaaga tcaggtccgg ggagatgaca attgaggaac tggaacgcgc catgttcaac
601 aattctgagt ttatcctgaa gtatggaggc gggggaagcg ataagaaata ctccatcgga
661 ctggccattg gcaccaattc cgtgggctgg gctgtcatca cagacgagta caaggtgcca
721 agcaagaagt tcaaggtcct ggggaacacc gatcgccaca gtatcaagaa aaatctgatt
781 ggagccctgc tgttcgactc aggcgagact gctgaagcaa cccgactgaa gcggactgct
841 aggcgccgat atacccggag aaaaaatcgg atctgctacc tgcaggaaat tttcagcaac
901 gagatggcca aggtggacga tagtttcttt caccgcctgg aggaatcatt cctggtggag
961 gaagataaga aacacgagcg gcatcccatc tttggcaaca ttgtggacga agtcgcttat
1021 cacgagaagt accctactat ctatcatctg aggaagaaac tggtggactc caccgataag
1081 gcagacctgc gcctgatcta tctggccctg gctcacatga tcaagttccg ggggcatttt
1141 ctgatcgagg gagatctgaa ccctgacaat tctgatgtgg acaagctgtt catccagctg
1201 gtccagacat acaatcagct gtttgaggaa aacccaatta atgcctcagg cgtggacgca
1261 aaggccatcc tgagcgccag actgtccaaa tctaggcgcc tggaaaacct gatcgctcag
1321 ctgccaggag agaagaaaaa cggcctgttt gggaatctga ttgcactgtc cctgggcctg
1381 acacccaact tcaagtctaa ttttgatctg gccgaggacg ctaagctgca gctgtccaaa
1441 gacacttatg acgatgacct ggataacctg ctggctcaga tcggcgatca gtacgcagac
1501 ctgttcctgg ccgctaagaa tctgagtgac gccatcctgc tgtcagatat tctgcgcgtg
1561 aacacagaga ttactaaggc cccactgagt gcttcaatga tcaaaagata tgacgagcac
1621 catcaggatc tgaccctgct gaaggctctg gtgaggcagc agctgcccga gaaatacaag
1681 gaaatcttct ttgatcagag caagaatgga tacgccggct atattgacgg cggggcttcc
1741 caggaggagt tctacaagtt catcaagccc attctggaaa agatggacgg caccgaggaa
1801 ctgctggtga agctgaatcg ggaggacctg ctgagaaaac agaggacatt tgataacgga
1861 agcatccctc accagattca tctgggcgaa ctgcacgcca tcctgcgacg gcaggaggac
1921 ttctacccat ttctgaagga taaccgcgag aaaatcgaaa agatcctgac cttcagaatc
1981 ccctactatg tggggcctct ggcacgggga aatagtagat ttgcctggat gacaagaaag
2041 tcagaggaaa ctatcacccc ctggaacttc gaggaagtgg tcgataaagg cgctagcgca
2101 cagtccttca ttgaaaggat gacaaatttt gacaagaacc tgccaaatga gaaggtgctg
2161 cccaaacaca gcctgctgta cgaatatttc acagtgtata acgagctgac taaagtgaag
2221 tacgtcaccg aagggatgcg caagcccgca ttcctgtccg gagagcagaa gaaagccatc
2281 gtggacctgc tgtttaagac aaatcggaaa gtgactgtca aacagctgaa ggaagactat
2341 ttcaagaaaa ttgagtgttt cgattcagtg gaaatcagcg gcgtcgagga caggtttaac
2401 gcctccctgg ggacctacca cgatctgctg aagatcatca aggataagga cttcctggac
2461 aacgaggaaa atgaggacat cctggaggac attgtgctga cactgactct gtttgaggat
2521 cgcgaaatga tcgaggaacg actgaagact tatgcccatc tgttcgatga caaagtgatg
2581 aagcagctga aaagaaggcg ctacaccgga tggggacgcc tgagccgaaa actgatcaat
2641 gggattagag acaagcagag cggaaaaact atcctggact ttctgaagtc cgatggcttc
2701 gccaacagga acttcatgca gctgattcac gatgactctc tgaccttcaa ggaggacatc
2761 cagaaagcac aggtgtctgg ccagggggac agtctgcacg agcatatcgc aaacctggcc
2821 ggcagccccg ccatcaagaa agggattctg cagaccgtga aggtggtgga cgaactggtc
2881 aaggtcatgg gacgacacaa acctgagaac atcgtgattg agatggcccg cgaaaatcag
2941 acaactcaga agggccagaa aaacagtcga gaacggatga agagaatcga ggaaggcatc
3001 aaggagctgg ggtcacagat cctgaaggag catcctgtgg aaaacactca gctgcagaat
3061 gagaaactgt atctgtacta tctgcagaat ggacgggata tgtacgtgga ccaggagctg
3121 gatattaaca gactgagtga ttatgacgtg gatgccatcg tccctcagag cttcctgaag
3181 gatgactcca ttgacaacaa ggtgctgacc aggtccgaca agaaccgcgg caaatcagat
3241 aatgtgccaa gcgaggaagt ggtcaagaaa atgaagaact actggaggca gctgctgaat
3301 gccaagctga tcacacagcg gaaatttgat aacctgacta aggcagaaag aggaggcctg
3361 tctgagctgg acaaggccgg cttcatcaag cggcagctgg tggagacaag acagatcact
3421 aagcacgtcg ctcagattct ggatagcaga atgaacacaa agtacgatga aaacgacaag
3481 ctgatcaggg aggtgaaagt cattactctg aaatccaagc tggtgtctga ctttagaaag
3541 gatttccagt tttataaagt cagggagatc aacaactacc accatgctca tgacgcatac
3601 ctgaacgcag tggtcgggac cgccctgatt aagaaatacc ccaagctgga gtccgagttc
3661 gtgtacggag actataaagt gtacgatgtc cggaagatga tcgccaaatc tgagcaggaa
3721 attggcaagg ccaccgctaa gtatttcttt tacagtaaca tcatgaattt ctttaagacc
3781 gaaatcacac tggcaaatgg ggagatcaga aaaaggcctc tgattgagac caacggggag
3841 acaggagaaa tcgtgtggga caagggaagg gattttgcta ccgtgcgcaa agtcctgtcc
3901 atgccccaag tgaatattgt caagaaaact gaagtgcaga ccgggggatt ctctaaggag
3961 agtattctgc ctaagcgaaa ctctgataaa ctgatcgccc ggaagaaaga ctgggacccc
4021 aagaagtatg gcgggttcga ctctccaaca gtggcttaca gtgtcctggt ggtcgcaaag
4081 gtggaaaagg ggaagtccaa gaaactgaag tctgtcaaag agctgctggg aatcactatt
4141 atggaacgca gctccttcga gaagaatcct atcgattttc tggaagccaa gggctataaa
4201 gaggtgaaga aagacctgat cattaagctg ccaaaatact cactgtttga gctggaaaac
4261 ggacgaaagc gaatgctggc aagcgccgga gaactgcaga agggcaatga gctggccctg
4321 ccctccaaat acgtgaactt cctgtatctg gctagccact acgagaaact gaaggggtcc
4381 cctgaggata acgaacagaa gcagctgttt gtggagcagc acaaacatta tctggacgag
4441 atcattgaac agatttcaga gttcagcaag agagtgatcc tggctgacgc aaatctggat
4501 aaagtcctga gcgcatacaa caagcaccga gacaaaccaa tccgggagca ggccgaaaat
4561 atcattcatc tgttcaccct gacaaacctg ggcgcccctg cagccttcaa gtattttgac
4621 accacaatcg atcggaagag atacacttct accaaagagg tgctggatgc taccctgatc
4681 caccagagta ttaccggcct gtatgagaca cgcatcgacc tgtcacagct gggaggcgat
4741 gggagcccca agaaaaagcg gaaggtgtct agttaa (SEQ ID NO:17014).
В некоторых вариантах осуществления слитый белок включает или состоит из аминокислотной последовательности:
61 YGFKGRHLGG SRKPDGIVYS TTLEDNFGII VDTKAYSEGY SLPISQADEM ERYVRENSNR
121 DEEVNPNKWW ENFSEEVKKY YFVFISGSFK GKFEEQLRRL SMTTGVNGSA VNVVNLLLGA
181 EKIRSGEMTI EELERAMFNN SEFILKYGGG GSDKKYSIGL AIGTNSVGWA VITDEYKVPS
241 KKFKVLGNTD RHSIKKNLIG ALLFDSGETA EATRLKRTAR RRYTRRKNRI CYLQEIFSNE
301 MAKVDDSFFH RLEESFLVEE DKKHERHPIF GNIVDEVAYH EKYPTIYHLR KKLVDSTDKA
361 DLRLIYLALA HMIKFRGHFL IEGDLNPDNS DVDKLFIQLV QTYNQLFEEN PINASGVDAK
421 AILSARLSKS RRLENLIAQL PGEKKNGLFG NLIALSLGLT PNFKSNFDLA EDAKLQLSKD
481 TYDDDLDNLL AQIGDQYADL FLAAKNLSDA ILLSDILRVN TEITKAPLSA SMIKRYDEHH
541 QDLTLLKALV RQQLPEKYKE IFFDQSKNGY AGYIDGGASQ EEFYKFIKPI LEKMDGTEEL
601 LVKLNREDLL RKQRTFDNGS IPHQIHLGEL HAILRRQEDF YPFLKDNREK IEKILTFRIP
661 YYVGPLARGN SRFAWMTRKS EETITPWNFE EVVDKGASAQ SFIERMTNFD KNLPNEKVLP
721 KHSLLYEYFT VYNELTKVKY VTEGMRKPAF LSGEQKKAIV DLLFKTNRKV TVKQLKEDYF
781 KKIECFDSVE ISGVEDRFNA SLGTYHDLLK IIKDKDFLDN EENEDILEDI VLTLTLFEDR
841 EMIEERLKTY AHLFDDKVMK QLKRRRYTGW GRLSRKLING IRDKQSGKTI LDFLKSDGFA
901 NRNFMQLIHD DSLTFKEDIQ KAQVSGQGDS LHEHIANLAG SPAIKKGILQ TVKVVDELVK
961 VMGRHKPENI VIEMARENQT TQKGQKNSRE RMKRIEEGIK ELGSQILKEH PVENTQLQNE
1021 KLYLYYLQNG RDMYVDQELD INRLSDYDVD AIVPQSFLKD DSIDNKVLTR SDKNRGKSDN
1081 VPSEEVVKKM KNYWRQLLNA KLITQRKFDN LTKAERGGLS ELDKAGFIKR QLVETRQITK
1141 HVAQILDSRM NTKYDENDKL IREVKVITLK SKLVSDFRKD FQFYKVREIN NYHHAHDAYL
1201 NAVVGTALIK KYPKLESEFV YGDYKVYDVR KMIAKSEQEI GKATAKYFFY SNIMNFFKTE
1261 ITLANGEIRK RPLIETNGET GEIVWDKGRD FATVRKVLSM PQVNIVKKTE VQTGGFSKES
1321 ILPKRNSDKL IARKKDWDPK KYGGFDSPTV AYSVLVVAKV EKGKSKKLKS VKELLGITIM
1381 ERSSFEKNPI DFLEAKGYKE VKKDLIIKLP KYSLFELENG RKRMLASAGE LQKGNELALP
1441 SKYVNFLYLA SHYEKLKGSP EDNEQKQLFV EQHKHYLDEI IEQISEFSKR VILADANLDK
1501 VLSAYNKHRD KPIREQAENI IHLFTLTNLG APAAFKYFDT TIDRKRYTST KEVLDATLIH
1561 QSITGLYETR IDLSQLGGDG SPKKKRKV (SEQ ID NO:17058)
или нуклеиновой кислоты, включающей или состоящей из последовательности:
61 gaactccggg ggcagattag ccacattagt cacgaatacc tctccctcat cgacctggct
121 ttcgatagca agcagaacag gctctttgag atgaaagtgc tggaactgct cgtcaatgag
181 tacgggttca agggtcgaca cctcggcgga tctaggaaac cagacggcat cgtgtatagt
241 accacactgg aagacaactt tgggatcatt gtggatacca aggcatactc tgagggttat
301 agtctgccca tttcacaggc cgacgagatg gaacggtacg tgcgcgagaa ctcaaataga
361 gatgaggaag tcaaccctaa caagtggtgg gagaacttct ctgaggaagt gaagaaatac
421 tacttcgtct ttatcagcgg gtccttcaag ggtaaatttg aggaacagct caggagactg
481 agcatgacta ccggcgtgaa tggcagcgcc gtcaacgtgg tcaatctgct cctgggcgct
541 gaaaagattc ggagcggaga gatgaccatc gaagagctgg agagggcaat gtttaataat
601 agcgagttta tcctgaaata cggtggcggt ggatccgata aaaagtattc tattggttta
661 gccatcggca ctaattccgt tggatgggct gtcataaccg atgaatacaa agtaccttca
721 aagaaattta aggtgttggg gaacacagac cgtcattcga ttaaaaagaa tcttatcggt
781 gccctcctat tcgatagtgg cgaaacggca gaggcgactc gcctgaaacg aaccgctcgg
841 agaaggtata cacgtcgcaa gaaccgaata tgttacttac aagaaatttt tagcaatgag
901 atggccaaag ttgacgattc tttctttcac cgtttggaag agtccttcct tgtcgaagag
961 gacaagaaac atgaacggca ccccatcttt ggaaacatag tagatgaggt ggcatatcat
1021 gaaaagtacc caacgattta tcacctcaga aaaaagctag ttgactcaac tgataaagcg
1081 gacctgaggt taatctactt ggctcttgcc catatgataa agttccgtgg gcactttctc
1141 attgagggtg atctaaatcc ggacaactcg gatgtcgaca aactgttcat ccagttagta
1201 caaacctata atcagttgtt tgaagagaac cctataaatg caagtggcgt ggatgcgaag
1261 gctattctta gcgcccgcct ctctaaatcc cgacggctag aaaacctgat cgcacaatta
1321 cccggagaga agaaaaatgg gttgttcggt aaccttatag cgctctcact aggcctgaca
1381 ccaaatttta agtcgaactt cgacttagct gaagatgcca aattgcagct tagtaaggac
1441 acgtacgatg acgatctcga caatctactg gcacaaattg gagatcagta tgcggactta
1501 tttttggctg ccaaaaacct tagcgatgca atcctcctat ctgacatact gagagttaat
1561 actgagatta ccaaggcgcc gttatccgct tcaatgatca aaaggtacga tgaacatcac
1621 caagacttga cacttctcaa ggccctagtc cgtcagcaac tgcctgagaa atataaggaa
1681 atattctttg atcagtcgaa aaacgggtac gcaggttata ttgacggcgg agcgagtcaa
1741 gaggaattct acaagtttat caaacccata ttagagaaga tggatgggac ggaagagttg
1801 cttgtaaaac tcaatcgcga agatctactg cgaaagcagc ggactttcga caacggtagc
1861 attccacatc aaatccactt aggcgaattg catgctatac ttagaaggca ggaggatttt
1921 tatccgttcc tcaaagacaa tcgtgaaaag attgagaaaa tcctaacctt tcgcatacct
1981 tactatgtgg gacccctggc ccgagggaac tctcggttcg catggatgac aagaaagtcc
2041 gaagaaacga ttactccatg gaattttgag gaagttgtcg ataaaggtgc gtcagctcaa
2101 tcgttcatcg agaggatgac caactttgac aagaatttac cgaacgaaaa agtattgcct
2161 aagcacagtt tactttacga gtatttcaca gtgtacaatg aactcacgaa agttaagtat
2221 gtcactgagg gcatgcgtaa acccgccttt ctaagcggag aacagaagaa agcaatagta
2281 gatctgttat tcaagaccaa ccgcaaagtg acagttaagc aattgaaaga ggactacttt
2341 aagaaaattg aatgcttcga ttctgtcgag atctccgggg tagaagatcg atttaatgcg
2401 tcacttggta cgtatcatga cctcctaaag ataattaaag ataaggactt cctggataac
2461 gaagagaatg aagatatctt agaagatata gtgttgactc ttaccctctt tgaagatcgg
2521 gaaatgattg aggaaagact aaaaacatac gctcacctgt tcgacgataa ggttatgaaa
2581 cagttaaaga ggcgtcgcta tacgggctgg ggacgattgt cgcggaaact tatcaacggg
2641 ataagagaca agcaaagtgg taaaactatt ctcgattttc taaagagcga cggcttcgcc
2701 aataggaact ttatgcagct gatccatgat gactctttaa ccttcaaaga ggatatacaa
2761 aaggcacagg tttccggaca aggggactca ttgcacgaac atattgcgaa tcttgctggt
2821 tcgccagcca tcaaaaaggg catactccag acagtcaaag tagtggatga gctagttaag
2881 gtcatgggac gtcacaaacc ggaaaacatt gtaatcgaga tggcacgcga aaatcaaacg
2941 actcagaagg ggcaaaaaaa cagtcgagag cggatgaaga gaatagaaga gggtattaaa
3001 gaactgggca gccagatctt aaaggagcat cctgtggaaa atacccaatt gcagaacgag
3061 aaactttacc tctattacct acaaaatgga agggacatgt atgttgatca ggaactggac
3121 ataaaccgtt tatctgatta cgacgtcgat gccattgtac cccaatcctt tttgaaggac
3181 gattcaatcg acaataaagt gcttacacgc tcggataaga accgagggaa aagtgacaat
3241 gttccaagcg aggaagtcgt aaagaaaatg aagaactatt ggcggcagct cctaaatgcg
3301 aaactgataa cgcaaagaaa gttcgataac ttaactaaag ctgagagggg tggcttgtct
3361 gaacttgaca aggccggatt tattaaacgt cagctcgtgg aaacccgcca aatcacaaag
3421 catgttgcac agatactaga ttcccgaatg aatacgaaat acgacgagaa cgataagctg
3481 attcgggaag tcaaagtaat cactttaaag tcaaaattgg tgtcggactt cagaaaggat
3541 tttcaattct ataaagttag ggagataaat aactaccacc atgcgcacga cgcttatctt
3601 aatgccgtcg tagggaccgc actcattaag aaatacccga agctagaaag tgagtttgtg
3661 tatggtgatt acaaagttta tgacgtccgt aagatgatcg cgaaaagcga acaggagata
3721 ggcaaggcta cagccaaata cttcttttat tctaacatta tgaatttctt taagacggaa
3781 atcactctgg caaacggaga gatacgcaaa cgacctttaa ttgaaaccaa tggggagaca
3841 ggtgaaatcg tatgggataa gggccgggac ttcgcgacgg tgagaaaagt tttgtccatg
3901 ccccaagtca acatagtaaa gaaaactgag gtgcagaccg gagggttttc aaaggaatcg
3961 attcttccaa aaaggaatag tgataagctc atcgctcgta aaaaggactg ggacccgaaa
4021 aagtacggtg gcttcgatag ccctacagtt gcctattctg tcctagtagt ggcaaaagtt
4081 gagaagggaa aatccaagaa actgaagtca gtcaaagaat tattggggat aacgattatg
4141 gagcgctcgt cttttgaaaa gaaccccatc gacttccttg aggcgaaagg ttacaaggaa
4201 gtaaaaaagg atctcataat taaactacca aagtatagtc tgtttgagtt agaaaatggc
4261 cgaaaacgga tgttggctag cgccggagag cttcaaaagg ggaacgaact cgcactaccg
4321 tctaaatacg tgaatttcct gtatttagcg tcccattacg agaagttgaa aggttcacct
4381 gaagataacg aacagaagca actttttgtt gagcagcaca aacattatct cgacgaaatc
4441 atagagcaaa tttcggaatt cagtaagaga gtcatcctag ctgatgccaa tctggacaaa
4501 gtattaagcg catacaacaa gcacagggat aaacccatac gtgagcaggc ggaaaatatt
4561 atccatttgt ttactcttac caacctcggc gctccagccg cattcaagta ttttgacaca
4621 acgatagatc gcaaacgata cacttctacc aaggaggtgc tagacgcgac actgattcac
4681 caatccatca cgggattata tgaaactcgg atagatttgt cacagcttgg gggtgacgga
4741 tcccccaaga agaagaggaa agtctga (SEQ ID NO:17059).
[0439] В некоторых вариантах осуществления клеток, немодифицированных клеток и модифицированных клеток согласно изобретению нанотранспозон включает композицию редактирования гена, включающую гидовую последовательность и последовательность, кодирующую слитый белок, включающий последовательность, кодирующую инактивированную Cas9 (dCas9), и последовательность, кодирующую нуклеазу Clo051 или соответствующий домен нуклеазы.
[0440] В некоторых вариантах осуществления клеток, немодифицированных клеток и модифицированных клеток согласно изобретению клетка экспрессирует композицию редактирования гена транзиентно.
[0441] В некоторых вариантах осуществления клеток, немодифицированных клеток и модифицированных клеток согласно изобретению клетка является T-клеткой, и гидовая РНК включает последовательность, комплементарную последовательности-мишени, кодирующей эндогенный TCR. В некоторых вариантах осуществления гидовая РНК включает последовательность, комплементарную последовательности-мишени, кодирующей полипептид B2M.
[0442] В некоторых вариантах осуществления клеток, немодифицированных клеток и модифицированных клеток согласно изобретению гидовая РНК включает последовательность, комплементарную последовательности-мишени в сайте безопасной гавани последовательности геномной ДНК.
[0443] В некоторых вариантах осуществления клеток, немодифицированных клеток и модифицированных клеток согласно изобретению нуклеаза Clo051 или соответствующий домена нуклеазы вызывает образование одно или двухцепочечного разрыва в последовательности-мишени. В некоторых вариантах осуществления донорная последовательность, донорная плазмида или интра-ITR-последовательность донорного нанотранспозона интегрирована в положение одно или двухцепочечного разрыва и/или в положении клеточной репарации в последовательности-мишени.
[0444] В изобретении предложена композиция, включающая модифицированную клетку согласно изобретению. В некоторых вариантах осуществления композиция дополнительно включает фармацевтически приемлемый носитель.
[0445] В изобретении предложена композиция, включающая множество модифицированных клеток согласно изобретению. В некоторых вариантах осуществления композиция дополнительно включает фармацевтически приемлемый носитель.
[0446] В изобретении предложена композиция согласно изобретению для применения при лечении заболевания или нарушения.
[0447] В изобретении предложено применение композиции согласно изобретению для лечения заболевания или нарушения.
[0448] В изобретении предложен способ лечения заболевания или нарушения, включающий введение нуждающемуся в этом индивиду терапевтически эффективное количество композиции согласно изобретению. В некоторых вариантах осуществления у индивида не развивается реакция трансплантат против хозяина (GvH) и/или хозяин против трансплантата (HvG) после введения композиции. В некоторых вариантах осуществления введение является системным. В некоторых вариантах осуществления композицию вводят внутривенным путем. В некоторых вариантах осуществления композицию вводят путем внутривенной инъекции или внутривенной инфузии.
[0449] В изобретении предложен способ лечения заболевания или нарушения, включающий введение нуждающемуся в этом индивиду терапевтически эффективного количества композиции согласно изобретению. В некоторых вариантах осуществления у индивида не развивается реакция трансплантат против хозяина (GvH) и/или хозяин против трансплантата (HvG) после введения композиции. В некоторых вариантах осуществления введение является местным. В некоторых вариантах осуществления композицию вводят интратуморальным путем, интраспинальным путем, интрацеребровентрикулярным путем, внутриглазным путем или внутрикостным путем. В некоторых вариантах осуществления композицию вводят путем интратуморальной инъекции или инфузии, интраспинальной инъекции или инфузии, интрацеребровентрикулярной инъекции или инфузии, внутриглазной инъекции или инфузии или внутрикостной инъекции или инфузии.
[0450] В некоторых вариантах осуществления способов лечения заболевания или нарушения согласно изобретению, терапевтически эффективная доза является однократной дозой, и где аллогенные клетки композиции приживаются и/или персистируют в течение достаточного количества времени для лечения заболевания или нарушения. В некоторых вариантах осуществления однократная доза является одной из по меньшей мере 2, 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100 или любого промежуточного количества доз, которые производят одновременно.
[0451] В некоторых вариантах осуществления способов лечения заболевания или нарушения согласно изобретению, терапевтически эффективная доза является однократной дозой, и где аутологичные клетки композиции приживаются и/или персистируют в течение достаточного количества времени для лечения заболевания или нарушения. В некоторых вариантах осуществления однократная доза является одной из по меньшей мере 2, 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100 или любого промежуточного количества доз, которые производят одновременно.
[0452] В некоторых вариантах осуществления композиции и способов согласно изобретению, аллогенные клетки являются стволовыми клетками. В некоторых вариантах осуществления аллогенные клетки получены из стволовых клеток. Примерные стволовые клетки включают, без ограничения перечисленными, эмбриональные стволовые клетки, зрелые стволовые клетки, индуцированные плюрипотентные стволовые клетки (иПСК), мультипотентные стволовые клетки, плюрипотентные стволовые клетки и гемопоэтические стволовые клетки (HSC).
[0453] В некоторых вариантах осуществления композиции и способов согласно изобретению, аллогенные клетки являются дифференцированными соматическими клетками.
[0454] В некоторых вариантах осуществления композиции и способов согласно изобретению, аллогенные клетки являются иммуными клетками. В некоторых вариантах осуществления аллогенные клетки являются T-лимфоцитами (T-клетками). В некоторых вариантах осуществления аллогенные клетки являются T-клетками, которые не экспрессируют один или более компонентов природного T-клеточного рецептора (TCR). В некоторых вариантах осуществления аллогенные клетки являются T-клетками, которые экспрессируют не встречающийся в природе антигенный рецептор. В альтернативе или дополнительно, в некоторых вариантах осуществления, аллогенные клетки являются T-клетками, которые экспрессируют не встречающийся в природе химерный стимулирующий рецептор (CSR). В некоторых вариантах осуществления не встречающийся в природе CSR включает или состоит из переключаемого рецептора. В некоторых вариантах осуществления переключаемый рецептор включает внеклеточный домен, трансмембранный домен и внутриклеточный домен. В некоторых вариантах осуществления внеклеточный домен переключаемого рецептора связывается с костимулирующей молекулой TCR и передает сигнал во внутриклеточное пространство аллогенной клетки, которая воспроизводит сигнализацию TCR или костимулирующую сигнализацию TCR.
Химерные стимулирующие рецепторы (CSR)
[0455] Адоптивные композиции клеток, которые "универсально" безопасны для введения любому пациенту, требуют значительного снижения или устранения аллореактивности.
[0456] Для этой цели аллогенные клетки согласно изобретению модифицируют, чтобы прервать экспрессию или функцию T-клеточного рецептора (TCR) и/или класса главного комплекса гистосовместимости (MHC). TCR опосредует реакции трансплантат против хозяина (GvH), тогда как MHC опосредует реакции хозяин против трансплантата (HvG). В предпочтительных вариантах осуществления любая экспрессия и/или функция TCR устраняется в аллогенных клетках согласно изобретению для предотвращения опосредованной T-клетками GvH, которая может повлечь смерть индивида. Таким образом, в особенно предпочтительных вариантах осуществления настоящего изобретения предложена чистая композиция TCR-отрицательных аллогенных T-клеток (например, каждая клетка композиции экспрессирует на таком низком уровне, который либо не обнаруживается, либо отсутствует).
[0457] В предпочтительных вариантах осуществления экспрессия и/или функция MHC класса I (MHC-I, в частности, HLA-A, HLA-B и HLA-C) снижена или устранена в аллогенных клетках согласно изобретению для предотвращения HvG и, следовательно, улучшения приживления аллогенных клеток согласно изобретению у индивида. Улучшенное приживление аллогенных клеток согласно изобретению приводит к более длительному персистированию клеток и, следовательно, к более широкому терапевтическому окну для индивида. В частности, в аллогенных клетках согласно изобретению экспрессия и/или функция структурного элемента MHC-I, бета-2-микроглобулина (B2M), снижена или устранена в аллогенных клетках согласно изобретению.
[0458] Вышеуказанные стратегии создания аллогенной клетки согласно изобретению представляют другие сложности. Нокаут (KO) T-клеточного рецептора (TCR) в T-клетках приводит к потере экспрессии CD3-дзэта (CD3z или CD3ζ), который является частью комплекса TCR. Потеря CD3ζ в TCR-KO T-клетках существенно снижает возможность оптимальной активации и экспансии этих клеток с помощью стандартных реактивов стимуляции/активации, включающих, без ограничения, агонистическое мАт против CD3. При блокировании экспрессии или функции какого-либо компонента комплекса TCR будут потеряны все компоненты комплекса, включая TCR-альфа (TCRα), TCR-бета (TCRβ), CD3-гамма (CD3γ), CD3-эпсилон (CD3ε), CD3-дельта (CD3δ) и CD3-дзэта (CD3ζ). Для активации и экспансии T-клеток требуются CD3ε и CD3ζ. Агонистические мАт против CD3, как правило, распознают CD3ε и, возможно, другой белок в комплексе, что, в свою очередь, передает сигнал CD3ζ. CD3ζ дает основной стимул для активации T-клеток (вместе со вторичным костимулирующим сигналом) для оптимальной активации и экспансии. При нормальных условиях полная активация T-клеток зависит от захвата TCR в сочетании со вторым сигналом, опосредуемым одним или более костимулирующими рецепторами (например, CD28, CD2, 4-1BBL и т.д.), что усиливает иммунный ответ. Впрочем, в случае отсутствия TCR, экспансия T-клеток сильно снижается при стимуляции стандартными реагентами для активации/стимуляции, включая агонистическое мАт против CD3. Фактически экспансия T-клеток снижается только до 20-40% от нормального уровня экспансии при стимуляции с использованием стандартных реагентов для активации/стимуляции, включая агонистическое мАт против CD3.
[0459] В изобретении предложен химерный стимулирующий рецептор (CSR) для обеспечения первичной CD3z стимуляции аллогенных T-клеток в отсутствие эндогенного TCR (и, следовательно, эндогенного CD3ζ) при стимуляции с использованием стандартных реагентов для активации/стимуляции, включая агонистическое мАт против CD3.
[0460] В отсутствие эндогенного TCR химерные стимулирующие рецепторы (CSR-рецепторы) согласно изобретению обеспечивают CD3ζ стимул для улучшения активации и экспансии аллогенных T-клеток. Другими словами, в отсутствие эндогенного TCR, химерные стимулирующие рецепторы (CSR-рецепторы) согласно изобретению устраняют недостаток, связанный с активацией аллогенной клетки по сравнению с неаллогенными T-клетками, экспрессирующими эндогенный TCR. В некоторых вариантах осуществления CSR-рецепторы согласно изобретению включают внеклеточный эпитоп агонистического мАт и внутриклеточный стимулирующий домен CD3ζ, и функционально преобразуют событие связывания против CD28 или против CD2 на поверхности в CD3z сигнальное событие в аллогенной T-клетке, модифицированной для экспрессии CSR. В некоторых вариантах осуществления CSR включает белок CD28 или CD2 дикого типа и внутриклеточный стимулирующий домен CD3z, с получением CD28z CSR и CD2z CSR, соответственно. В предпочтительных вариантах осуществления CD28z CSR и/или CD2z CSR дополнительно экспрессируют не встречающийся в природе антигенный рецептор и/или терапевтический белок. В предпочтительных вариантах осуществления не встречающийся в природе антигенный рецептор включает химерный антигенный рецептор.
[0461] Данные, представленные в настоящем документе, демонстрируют, что модифицированные аллогенные T-клетки согласно изобретению, включающие/экспрессирующие CSR согласно изобретению, улучшают или сохраняют экспансию аллогенных T-клеток, которые больше не экспрессируют эндогенный TCR, по сравнению с такими клетками, которые не включают/экспрессируют CSR согласно изобретению.
Нокаут эндогенного TCR
[0462] Композиции редактирования гена согласно изобретению, включающие, без ограничения, РНК-направляемые слитые белки, включающие dCas9-Clo051, могут применяться для направленного воздействия и снижения или устранения экспрессии эндогенного T-клеточного рецептора аллогенной клетки согласно изобретению. В предпочтительных вариантах осуществления композиции редактирования гена согласно изобретению направленно воздействуют и удаляют ген, часть гена или регуляторный элемент гена (такой как промотор), кодирующего эндогенный T-клеточный рецептор аллогенной клетки согласно изобретению.
[0463] Неограничивающие примеры праймеров (включая T7 промотор, геномную последовательность-мишень и каркас гРНК) для создания матриц гидовой РНК (гРНК) для направленного воздействия и удаления TCR-альфа (TCR-α), представлены в Таблице 10.
[0464] Таблица 10. Последовательности-мишени подчеркнуты
[0465] Неограничивающие примеры праймеров для создания матриц гидовой РНК (гРНК) для направленного воздействия и удаления TCR-бета (TCR-β) представлены в Таблице 11.
[0466] Таблица 11. Последовательности-мишени подчеркнуты
[0467] Неограничивающие примеры праймеров для создания матриц гидовой РНК (гРНК) для направленного воздействия и удаления бета-2-микроглобулина (β2M), представлены в Таблице 12.
[0468] Таблица 12. Последовательности-мишени подчеркнуты
Нокаут эндогенного MHC
[0469] Композиции редактирования гена согласно изобретению, включающие, без ограничения, РНК-направляемые слитые белки, включающие dCas9-Clo051, могут применяться для направленного воздействия и уменьшения или устранения экспрессии эндогенного MHCI, MHCII или MHC активатора аллогенной клетки согласно изобретению. В предпочтительных вариантах осуществления композиции редактирования гена согласно изобретению направленно воздействуют и удаляют ген, часть гена или регуляторный элемент гена (такой как промотор), кодирующего один или более компонентов эндогенного MHCI, MHCII или MHC активатора аллогенной клетки согласно изобретению.
[0470] Неограничивающие примеры гидовых РНК (гРНК) для направленного воздействия и удаления MHC активаторов представлены в Таблицах 13 и 14.
[0471] Таблица 13.
тип
[0472] Таблица 14.
(если WT crispr)
Композиции сконструированного HLA-E
[0473] Нокаут (KO) MHCI делает клетки устойчивыми к киллингу T-клетками, но также делает их восприимчивыми к опосредованной естественными киллерами (NK-клетками) цитотоксическому действию ("Гипотеза потери своего") (см. Фигуру 23). Предполагают, что отторжение NK-клетками может снижать in vivo эффективность и/или персистирование этих KO клеток в терапевтических условиях, таких как терапия аллогенными (алло) CAR-T-клетками. Сохранение MHCI на поверхности всех CAR-T-клеток делает их восприимчивыми к уничтожению хозяйскими T-клетками, как это наблюдается в классическом эксперименте реакции смешанной культуры лимфоцитов (MLR). По некоторым оценкам до 10% T-клеток человека специфичны к чужеродным МНС, что будет вызывать отторжение чужих клеток и тканей. Направленный КО MHCI, в частности HLA-A, B и C, который может быть достигнут направленным КО B2M, приводит к потере дополнительных молекул HLA, включая HLA-E. Например, потеря HLA-E делает KO клетки более восприимчивыми к цитотоксичности, опосредованной NK-клетками, согласно "гипотезе потери своего". NK-опосредованная цитотоксичность против клеток с потерей своего является механизмом защиты от патогенов, которые подавляют MHC на поверхности инфицированных клеток, чтобы избежать обнаружения и уничтожения клетками адаптивной иммунной системы.
[0474] В описании предусмотрены две стратегии создания алло (MHCI-отр) T-клеток (включая CAR-T-клетки), более устойчивых к опосредованному NK-клетками цитотоксическому действию. В некоторых вариантах осуществления последовательность, кодирующая молекулу (такую как одноцепочечный HLA-E), которая уменьшает или предотвращает NK-киллинг, вводят или доставляют в аллогенную клетку. В альтернативе или дополнительно, способы редактирования гена согласно изобретению позволяют сохранить некоторые эндогенные молекулы HLA (такие как эндогенный HLA-E). Например, первый подход включает piggyBac (PB) доставку одноцепочечной (sc) молекулы HLA-E в B2M KO T-клетки.
[0475] Во втором методе используется композиция редактирования гена с гидовыми РНК, селективными в отношении HLA-A, HLA-B и HLA-C, но не в отношении, например, HLA-E или других молекул, которые обеспечивают защиту от опосредованого NK-клетками цитотоксического действия в отношении MHCI КО клеток.
[0476] Альтернативные или дополнительные молекулы к HLA-E, которые являются защитными против опосредованого NK-клетками цитотоксического действия, включают, без ограничения перечисленными, рецептор интерферона альфа/бета 1 (IFNAR1), IFNAR1 человека, рецептор интерферона альфа/бета 2 (IFNAR2), IFNAR2 человека, HLA-G1, HLA-G2, HLA-G3, HLA-G4, HLA-G5, HLA-G6, HLA-G7, родственную раково-эмбриональному антигену человека молекулу клеточной адгезии 1 (CEACAM1), вирусные гемагглютинины, CD48, LLT1 (также называемый членом D семейства белков с лектиновым доменом C-типа 2 (CLC2D)), ULBP2, ULBP3 и sMICA или их вариант.
[0477] Примерный белок INFAR1 согласно изобретению включает или состоит из аминокислотной последовательности (Сигнальный пептид, Внеклеточный, ТМ, Цитоплазматический):
FSFDYQKTGMDNWIKLSGCQNITSTKCNFSSLKLNVYEEIKLRIRAEKENTSSWYEVDSF
TPFRKAQIGPPEVHLEAEDKAIVIHISPGTKDSVMWALDGLSFTYSLVIWKNSSGVEERI
ENIYSRHKIYKLSPETTYCLKVKAALLTSWKIGVYSPVHCIKTTVENELPPPENIEVSVQ
NQNYVLKWDYTYANMTFQVQWLHAFLKRNPGNHLYKWKQIPDCENVKTTQCVFPQNVFQK
GIYLLRVQASDGNNTSFWSEEIKFDTEIQAFLLPPVFNIRSLSDSFHIYIGAPKQSGNTP
VIQDYPLIYEIIFWENTSNAERKIIEKKTDVTVPNLKPLTVYCVKARAHTMDEKLNKSSV
FSDAVCEKTKPGNTSKIWLIVGICIALFALPFVIYAAKVFLRCINYVFFPSLKPSSSIDE
YFSEQPLKNLLLSTSEEQIEKCFIIENISTIATVEETNQTDEDHKKYSSQTSQDSGNYSN
EDESESKTSEELQQDFV (SEQ ID NO:17017).
[0478] Примерный белок INFAR2 согласно изобретению включает или состоит из аминокислотной последовательности (Сигнальный пептид, Внеклеточный, ТМ, Цитоплазматический):
IVPTHYTLLYTIMSKPEDLKVVKNCANTTRSFCDLTDEWRSTHEAYVTVLEGFSGNTTLF
SCSHNFWLAIDMSFEPPEFEIVGFTNHINVMVKFPSIVEEELQFDLSLVIEEQSEGIVKK
HKPEIKGNMSGNFTYIIDKLIPNTNYCVSVYLEHSDEQAVIKSPLKCTLLPPGQESESAE
SAKIGGIITVFLIALVLTSTIVTLKWIGYICLRNSLPKVLNFHNFLAWPFPNLPPLEAMD
MVEVIYINRKKKVWDYNYDDESDSDTEAAPRTSGGGYTMHGLTVRPLGQASATSTESQLI
DPESEEEPDLPEVDVELPTMPKDSPQQLELLSGPCERRKSPLQDPFPEEDYSSTEGSGGR
ITFNVDLNSVFLRVLDDEDSDDLEAPLMLSSHLEEMVDPEDPDNVQSNHLLASGEGTQPT
FPSPSSEGLWSEDAPSDQSDTSESDVDLGDGYIMR (SEQ ID NO:17018).
[0479] Примерный белок HLA-G1 согласно изобретению включает или состоит из аминокислотной последовательности (Альфа-цепь 1, Альфа-цепь 2, Альфа-цепь 3):
MVVMAPRTLFLLLSGALTLTETWAGSHSMRYFSAAVSRPGRGEPRFIAMGYVDDTQFVRFDSDSACPRMEPRAPWVEQEGPEYWEEETRNTKAHAQTDRMNLQTLRGYYNQSEASSHTLQWMIGCDLGSDGRLLRGYEQYAYDGKDYLALNEDLRSWTAADTAAQISKRKCEAANVAEQRRAYLEGTCVEWLHRYLENGKEMLQRADPPKTHVTHHPVFDYEATLRCWALGFYPAEIILTWQRDGEDQTQDVELVETRPAGDGTFQKWAAVVVPSGEEQRYTCHVQHEGLPEPLMLRWKQSSLPTIPIMGIVAGLVVLAAVVTGAAVAAVLWRKKSSD (SEQ ID NO:17019).
[0480] Примерный белок HLA-G2 согласно изобретению включает или состоит из аминокислотной последовательности (Альфа-цепь 1, Альфа-цепь 2, Альфа-цепь 3):
MVVMAPRTLFLLLSGALTLTETWAGSHSMRYFSAAVSRPGRGEPRFIAMGYVDDTQFVRFDSDSACPRMEPRAPWVEQEGPEYWEEETRNTKAHAQTDRMNLQTLRGYYNQSEADPPKTHVTHHPVFDYEATLRCWALGFYPAEIILTWQRDGEDQTQDVELVETRPAGDGTFQKWAAVVVPSGEEQRYTCHVQHEGLPEPLMLRWKQSSLPTIPIMGIVAGLVVLAAVVTGAAVAAVLWRKKSSD (SEQ ID NO:17020).
[0481] Примерный белок HLA-G3 согласно изобретению включает или состоит из аминокислотной последовательности (Альфа-цепь 1, Альфа-цепь 2, Альфа-цепь 3):
MVVMAPRTLFLLLSGALTLTETWAGSHSMRYFSAAVSRPGRGEPRFIAMGYVDDTQFVRFDSDSACPRMEPRAPWVEQEGPEYWEEETRNTKAHAQTDRMNLQTLRGYYNQSEAKQSSLPTIPIMGIVAGLVVLAAVVTGAAVAAVLWRKKSSD (SEQ ID NO:17021).
[0482] Примерный белок HLA-G4 согласно изобретению включает или состоит из аминокислотной последовательности (Альфа-цепь 1, Альфа-цепь 2, Альфа-цепь 3):
MVVMAPRTLFLLLSGALTLTETWAGSHSMRYFSAAVSRPGRGEPRFIAMGYVDDTQFVRFDSDSACPRMEPRAPWVEQEGPEYWEEETRNTKAHAQTDRMNLQTLRGYYNQSEASSHTLQWMIGCDLGSDGRLLRGYEQYAYDGKDYLALNEDLRSWTAADTAAQISKRKCEAANVAEQRRAYLEGTCVEWLHRYLENGKEMLQRAKQSSLPTIPIMGIVAGLVVLAAVVTGAAVAAVLWRKKSSD (SEQ ID NO:17022).
[0483] Примерный белок HLA-G5 согласно изобретению включает или состоит из аминокислотной последовательности (Альфа-цепь 1, Альфа-цепь 2, Альфа-цепь 3, интрон 4):
MVVMAPRTLFLLLSGALTLTETWAGSHSMRYFSAAVSRPGRGEPRFIAMGYVDDTQFVRFDSDSACPRMEPRAPWVEQEGPEYWEEETRNTKAHAQTDRMNLQTLRGYYNQSEASSHTLQWMIGCDLGSDGRLLRGYEQYAYDGKDYLALNEDLRSWTAADTAAQISKRKCEAANVAEQRRAYLEGTCVEWLHRYLENGKEMLQRADPPKTHVTHHPVFDYEATLRCWALGFYPAEIILTWQRDGEDQTQDVELVETRPAGDGTFQKWAAVVVPSGEEQRYTCHVQHEGLPEPLMLRWSKEGDGGIMSVRESRSLSEDL (SEQ ID NO:17023).
[0484] Примерный белок HLA-G5 согласно изобретению включает или состоит из аминокислотной последовательности (Альфа-цепь 1, Альфа-цепь 2, Альфа-цепь 3, интрон 4):
MVVMAPRTLFLLLSGALTLTETWAGSHSMRYFSAAVSRPGRGEPRFIAMGYVDDTQFVRFDSDSACPRMEPRAPWVEQEGPEYWEEETRNTKAHAQTDRMNLQTLRGYYNQSEADPPKTHVTHHPVFDYEATLRCWALGFYPAEIILTWQRDGEDQTQDVELVETRPAGDGTFQKWAAVVVPSGEEQRYTCHVQHEGLPEPLMLRWSKEGDGGIMSVRESRSLSEDL (SEQ ID NO:17024).
[0485] Примерный белок HLA-G5 согласно изобретению включает или состоит из аминокислотной последовательности (Альфа-цепь 1, Альфа-цепь 2, Альфа-цепь 3, интрон 2):
MVVMAPRTLFLLLSGALTLTETWAGSHSMRYFSAAVSRPGRGEPRFIAMGYVDDTQFVRFDSDSACPRMEPRAPWVEQEGPEYWEEETRNTKAHAQTDRMNLQTLRGYYNQSEASE (SEQ ID NO:17025).
[0486] Примерный белок CEACAM1 согласно изобретению включает или состоит из аминокислотной последовательности (Внеклеточный, ТМ, Цитоплазматический):
MGHLSAPLHRVRVPWQGLLLTASLLTFWNPPTTAQLTTESMPFNVAEGKEVLLLVHNLPQ
QLFGYSWYKGERVDGNRQIVGYAIGTQQATPGPANSGRETIYPNASLLIQNVTQNDTGFY
TLQVIKSDLVNEEATGQFHVYPELPKPSISSNNSNPVEDKDAVAFTCEPETQDTTYLWWI
NNQSLPVSPRLQLSNGNRTLTLLSVTRNDTGPYECEIQNPVSANRSDPVTLNVTYGPDTP
TISPSDTYYRPGANLSLSCYAASNPPAQYSWLINGTFQQSTQELFIPNITVNNSGSYTCH
ANNSVTGCNRTTVKTIIVTELSPVVAKPQIKASKTTVTGDKDSVNLTCSTNDTGISIRWF
FKNQSLPSSERMKLSQGNTTLSINPVKREDAGTYWCEVFNPISKNQSDPIMLNVNYNALP
QENGLSPG AIAGIVIGVVALVALIAVALACFL HFGKTGRASDQRDLTEHKPSVSNHTQDH
SNDPPNKMNEVTYSTLNFEAQQPTQPTSASPSLTATEIIYSEVKKQ (SEQ ID NO:17026).
[0487] Примерный вирусный белок гемагглютинин согласно изобретению включает или состоит из аминокислотной последовательности (HA вируса гриппа A (A/NewCaledonia/20/1999(H1N1); ТМ):
MKAKLLVLLCTFTATYADTICIGYHANNSTDTVDTVLEKNVTVTHSVNLLEDSHNGKLCL
LKGIAPLQLGNCSVAGWILGNPECELLISKESWSYIVETPNPENGTCYPGYFADYEELRE
QLSSVSSFERFEIFPKESSWPNHTVTGVSASCSHNGKSSFYRNLLWLTGKNGLYPNLSKS
YVNNKEKEVLVLWGVHHPPNIGNQRALYHTENAYVSVVSSHYSRRFTPEIAKRPKVRDQE
GRINYYWTLLEPGDTIIFEANGNLIAPWYAFALSRGFGSGIITSNAPMDECDAKCQTPQG
AINSSLPFQNVHPVTIGECPKYVRSAKLRMVTGLRNIPSIQSRGLFGAIAGFIEGGWTGM
VDGWYGYHHQNEQGSGYAADQKSTQNAINGITNKVNSVIEKMNTQFTAVGKEFNKLERRM
ENLNKKVDDGFLDIWTYNAELLVLLENERTLDFHDSNVKNLYEKVKSQLKNNAKEIGNGC
FEFYHKCNNECMESVKNGTYDYPKYSEESKLNREKIDGVKLESMGVYQILAIYSTVASSL
VLLVSLGAISFWMCSNGSLQCRICI (SEQ ID NO:17027).
[0488] Примерный белок CD48 согласно изобретению включает или состоит из аминокислотной последовательности (Сигнальный пептид, Цепь, Пропептид, удаленный в зрелой форме):
MCSRGWDSCLALELLLLPLSLLVTSI QGHLVHMTVVSGSNVTLNISESLP
ENYKQLTWFYTFDQKIVEWDSRKSKYFESKFKGRVRLDPQSGALYISKVQ
KEDNSTYIMRVLKKTGNEQEWKIKLQVLDPVPKPVIKIEKIEDMDDNCYL
KLSCVIPGESVNYTWYGDKRPFPKELQNSVLETTLMPHNYSRCYTCQVSN
SVSSKNGTVCLSPPCTLARS FGVEWIASWLVVTVPTILGLLLT (SEQ ID NO:17028).
[0489] Примерный белок LLT1 согласно изобретению включает или состоит из аминокислотной последовательности (Цитоплазматический, ТМ, Внеклеточный):
MHDSNNVEKDITPSELPANPGCLHSKEHSIKATLIWRL FFLIMFLTIIVCGMVAALSAIR
ANCHQEPSVCLQAACPESWIGFQRKCFYFSDDTKNWTSSQRFCDSQDADLAQVESFQELN
FLLRYKGPSDHWIGLSREQGQPWKWINGTEWTRQFPILGAGECAYLNDKGASSARHYTER
KWICSKSDIHV (SEQ ID NO:17029)
[0490] Примерный белок ULBP2 согласно изобретению включает или состоит из аминокислотной последовательности (также известный как лиганд NKG2D; Рег. номер GenBank AAQ89028):
61 flhydcgnkt vtpvsplgkk lnvttawkaq npvlrevvdi lteqlrdiql enytpkeplt
121 lqarmsceqk aeghssgswq fsfdgqifll fdsekrmwtt vhpgarkmke kwendkvvam
181 sfhyfsmgdc igwledflmg mdstlepsag aplamssgtt qlratattli lcclliilpc
241 filpgi (SEQ ID NO:17030).
[0491] Примерный белок ULBP3 согласно изобретению включает или состоит из аминокислотной последовательности (также известный как лиганд NKG2D; Рег. номер GenBank NP_078794):
61 nflsydcgsd kvlsmghlee qlyatdawgk qlemlrevgq rlrleladte ledftpsgpl
121 tlqvrmscec eadgyirgsw qfsfdgrkfl lfdsnnrkwt vvhagarrmk ekwekdsglt
181 tffkmvsmrd ckswlrdflm hrkkrlepta pptmapglaq pkaiattlsp wsfliilcfi
241 lpgi (SEQ ID NO:17031).
[0492] Примерный белок sMICA согласно изобретению включает или состоит из аминокислотной последовательности (Сигнальный Пептид, Часть Внеклеточного домена, ТМ и цитоплазматический домен) (рег. номер GenBank Q29983):
61 rqkcrakpqg qwaedvlgnk twdretrdlt gngkdlrmtl ahikdqkegl hslqeirvce
121 ihednstrss qhfyydgelf lsqnletkew tmpqssraqt lamnvrnflk edamktkthy
181 hamhadclqe lrrylksgvv lrrtvppmvn vtrseasegn itvtcrasgf ypwnitlswr
241 qdgvslshdt qqwgdvlpdg ngtyqtwvat ricqgeeqrf tcymehsgnh sthpvpsgkv
301 lvlqshwqtf hvsavaaaai fviiifyvrc ckkktsaaeg pelvslqvld qhpvgtsdhr
361 datqlgfqpl msdlgstgst ega(SEQ ID NO:17032).
[0493] Примерный белок sMICA согласно изобретению включает или состоит из аминокислотной последовательности (Альфа-1, Альфа-2, Альфа-3):
61 rqkcrakpqg qwaedvlgnk twdretrdlt gngkdlrmtl ahikdqkegl hslqeirvce
121 ihednstrss qhfyydgelf lsqnletkew tmpqssraqt lamnvrnflk edamktkthy
181 hamhadclqe lrrylksgvv lrrtvppmvn vtrseasegn itvtcrasgf ypwnitlswr
241 qdgvslshdt qqwgdvlpdg ngtyqtwvat ricqgeeqrf tcymehsgnh sthpvpsgkv
301 lvlqshwqtf hvsavaaaai fviiifyvrc ckkktsaaeg pelvslqvld qhpvgtsdhr
361 datqlgfqpl msdlgstgst ega (SEQ ID NO:17033).
[0494] Примерный белок sMICA согласно изобретению включает или состоит из аминокислотной последовательности (Сигнальный пептид; Альфа-1, Альфа-2, Альфа-3):
61 rqkcrakpqg qwaedvlgnk twdretrdlt gngkdlrmtl ahikdqkegl hslqeirvce
121 ihednstrss qhfyydgelf lsqnletkew tmpqssraqt l thy
181 hamhadclqe lrrylksgvv lrrtvppmvn vtrseasegn itvtcrasgf ypwnitlswr
241 qdgvslshdt qqwgdvlpdg ngtyqtwvat ricqgeeqrf tcymehsgnh sthpvpsgkv
301 lvlqshw (SEQ ID NO:17034).
[0495] Примерный белок sMICA согласно изобретению включает или состоит из аминокислотной последовательности (Сигнальный пептид):
MGGVLLTQRTLLSLVLALLFPSMASM EPHSLRYNLTVLSWDGSVQSGFLTEVHLDGQPFLRCDRQKCRAKPQGQWAEDVLGNKTWDRETRDLTGNGKLDLRMTLAHIKLDQKEGLHSLQEIRVCEIHEDNSTRSSQHFYYNGELFLSQNLETKEWTMPQSSRAQTLTHYHAMHADCLQELRRYLKSGVVLRRTVPPMVDVTRSEASEGNITVTCRASGFYPWNITLSWRQDGVSLSHDTQQWGDVLPDGNGTYQTWVATRICQGEEQRFTCYMEHSGNHSTHPVPSGKVLVLQSHW (SEQ ID NO:17035).
[0496] Примерный тримерный белок bGBE (270G и 484S) согласно изобретению включает или состоит из аминокислотной последовательности:
MSRSVALAVLALLSLSGLEAVMAPRTLILGGGGSGGGGSGGGGSIQRTPKIQVYSRHPAENGKSNFLNCYVSGFHPSDIEVDLLKNGERIEKVEHSDLSFSKDWSFYLLYYTEFTPTEKDEYACRVNHVTLSQPKIVKWDRDMGGGGSGGGGSGGGGSGGGGSGSHSLKYFHTSVSRPGRGEPRFISVGYVDDTQFVRFDNDAASPRMVPRAPWMEQEGSEYWDRETRSARDTAQIFRVNLRTLRGYYNQSEAGSHTLQWMHGCELGPDGRFLRGYEQFAYDGKDYLTLNEDLRSWTAVDTAAQISEQKSNDASEAEHQRAYLEDTCVEWLHKYLEKGKETLLHLEPPKTHVTHHPISDHEATLRCWALGFYPAEITLTWQQDGEGHTQDTELVETRPAGDGTFQKWAAVVVPSGEEQRYTCHVQHEGLPEPVTLRWKPASQPTIPIVGIIAGLVLLGSVVSGAVVAAVIWRKKSSGGKGGSYSKAEWSDSAQGSESHSL* (SEQ ID NO:16972).
[0497] Примерный тримерный белок bGBE (270G и 484S) согласно изобретению включает или состоит из последовательности нуклеиновой кислоты:
atgtctcgcagcgtggccctggccgtgctggccctgctgtccctgtctggcctggaggccgtgatggccccccggaccctgatcctgggaggaggaggcagcggcggaggaggctccggaggcggcggctctatccagcgcacacctaagatccaggtgtattctcggcacccagccgagaacggcaagagcaacttcctgaattgctacgtgagcggctttcacccttccgacatcgaggtggatctgctgaagaatggcgagagaatcgagaaggtggagcactccgacctgagcttctccaaggattggtctttttatctgctgtactataccgagtttacccctacagagaaggacgagtacgcctgtcgcgtgaaccacgtgacactgtcccagccaaagatcgtgaagtgggaccgggatatgggcggcggcggctctggcggcggcggcagcggcggcggcggctccggaggaggcggctctggcagccactccctgaagtatttccacacctctgtgagccggccaggcagaggagagccacggttcatctctgtgggctacgtggacgatacacagttcgtgaggtttgacaatgatgccgccagcccaagaatggtgcctagggccccatggatggagcaggagggcagcgagtattgggacagggagacccggagcgccagagacacagcacagattttccgggtgaacctgagaaccctgaggggctactataatcagtccgaggccggctctcacacactccagtggatgcacggatgcgagctgggaccagatggccgcttcctgcggggctacgagcagtttgcctatgacggcaaggattacctgaccctgaacgaggacctgagatcctggaccgccgtggatacagccgcccagatcagcgagcagaagtccaatgacgcatctgaggcagagcaccagagggcatatctggaggatacctgcgtggagtggctgcacaagtacctggagaagggcaaggagacactgctgcacctggagccccctaagacccacgtgacacaccacccaatcagcgaccacgaggccaccctgaggtgttgggcactgggcttctatcccgccgagatcaccctgacatggcagcaggacggagagggacacacccaggatacagagctggtggagaccaggcccgccggcgatggcacatttcagaagtgggccgccgtggtggtgccttccggagaggagcagagatacacctgtcacgtgcagcacgagggactgccagagccagtgaccctgaggtggaagcctgccagccagcccacaatccctatcgtgggaatcatcgcaggcctggtgctgctgggctctgtggtgagcggagcagtggtggccgccgtgatctggcggaagaagagcagcggaggcaagggaggctcctactccaaggcagagtggagcgactccgcccagggctctgagagccactccctgtga (SEQ ID NO:16973).
[0498] Примерный тримерный белок bGBE (270G и 484S) согласно изобретению включает или состоит из аминокислотной последовательности:
MSRSVALAVLALLSLSGLEAVMAPRTLILGGGGSGGGGSGGGGSIQRTPKIQVYSRHPAENGKSNFLNCYVSGFHPSDIEVDLLKNGERIEKVEHSDLSFSKDWSFYLLYYTEFTPTEKDEYACRVNHVTLSQPKIVKWDRDMGGGGSGGGGSGGGGSGGGGSGSHSLKYFHTSVSRPGRGEPRFISVGYVDDTQFVRFDNDAASPRMVPRAPWMEQEGSEYWDRETRSARDTAQIFRVNLRTLRGYYNQSEAGSHTLQWMHGCELGPDRRFLRGYEQFAYDGKDYLTLNEDLRSWTAVDTAAQISEQKSNDASEAEHQRAYLEDTCVEWLHKYLEKGKETLLHLEPPKTHVTHHPISDHEATLRCWALGFYPAEITLTWQQDGEGHTQDTELVETRPAGDGTFQKWAAVVVPSGEEQRYTCHVQHEGLPEPVTLRWKPASQPTIPIVGIIAGLVLLGSVVSGAVVAAVIWRKKSSGGKGGSYSKAEWSDSAQGSESHSL* (SEQ ID NO:16974).
[0499] Примерный тримерный белок bGBE (270G и 484S) согласно изобретению включает или состоит из последовательности нуклеиновой кислоты:
atgtctcgcagcgtggccctggccgtgctggccctgctgtccctgtctggcctggaggccgtgtggccccccggaccctgatcctgggaggaggaggcagcggcggaggaggctccggaggcggcggctctatccagcgcacacctaagatccaggtgtattctcggcacccagccgagaacggcaagagcaacttcctgaattgctacgtgagcggctttcacccttccgacatcgaggtggatctgctgaagaatggcgagagaatcgagaaggtggagcactccgacctgagcttctccaaggattggtctttttatctgctgtactataccgagtttacccctacagagaaggacgagtacgcctgtcgcgtgaaccacgtgacactgtcccagccaaagatcgtgaagtgggaccgggatatgggcggcggcggctctggcggcggcggcagcggcggcggcggctccggaggaggcggctctggcagccactccctgaagtatttccacacctctgtgagccggccaggcagaggagagccacggttcatctctgtgggctacgtggacgatacacagttcgtgaggtttgacaatgatgccgccagcccaagaatggtgcctagggccccatggatggagcaggagggcagcgagtattgggacagggagacccggagcgccagagacacagcacagattttccgggtgaacctgagaaccctgaggggctactataatcagtccgaggccggctctcacacactccagtggatgcacggatgcgagctgggaccagatcgccgcttcctgcggggctacgagcagtttgcctatgacggcaaggattacctgaccctgaacgaggacctgagatcctggaccgccgtggatacagccgcccagatcagcgagcagaagtccaatgacgcatctgaggcagagcaccagagggcatatctggaggatacctgcgtggagtggctgcacaagtacctggagaagggcaaggagacactgctgcacctggagccccctaagacccacgtgacacaccacccaatcagcgaccacgaggccaccctgaggtgttgggcactgggcttctatcccgccgagatcaccctgacatggcagcaggacggagagggacacacccaggatacagagctggtggagaccaggcccgccggcgatggcacatttcagaagtgggccgccgtggtggtgccttccggagaggagcagagatacacctgtcacgtgcagcacgagggactgccagagccagtgaccctgaggtggaagcctgccagccagcccacaatccctatcgtgggaatcatcgcaggcctggtgctgctgggctctgtggtgagcggagcagtggtggccgccgtgatctggcggaagaagagcagcggaggcaagggaggctcctactccaaggcagagtggagcgactccgcccagggctctgagagccactccctgtga (SEQ ID NO:16975).
[0500] Примерный димерный белок gBE (R и S) согласно изобретению включает или состоит из аминокислотной последовательности:
MSRSVALAVLALLSLSGLEAIQRTPKIQVYSRHPAENGKSNFLNCYVSGFHPSDIEV
DLLKNGERIEKVEHSDLSFSKDWSFYLLYYTEFTPTEKDEYACRVNHVTLSQPKIVKWDR
DMGGGGSGGGGSGGGGSGGGGSGSHSLKYFHTSVSRPGRGEPRFISVGYVDDTQFVRFDN
DAASPRMVPRAPWMEQEGSEYWDRETRSARDTAQIFRVNLRTLRGYYNQSEAGSHTLQWM
HGCELGPDRRFLRGYEQFAYDGKDYLTLNEDLRSWTAVDTAAQISEQKSNDASEAEHQRA
YLEDTCVEWLHKYLEKGKETLLHLEPPKTHVTHHPISDHEATLRCWALGFYPAEITLTWQ
QDGEGHTQDTELVETRPAGDGTFQKWAAVVVPSGEEQRYTCHVQHEGLPEPVTLRWKPAS
QPTIPIVGIIAGLVLLGSVVSGAVVAAVIWRKKSSGGKGGSYSKAEWSDSAQGSESHSL (SEQ ID NO:16976).
[0501] Примерный димерный белок gBE (R и S) согласно изобретению включает или состоит из последовательности нуклеиновой кислоты:
ATGAGCAGATCTGTGGCCCTGGCTGTTCTGGCTCTGCTGTCTCTGTCTGGCCTGGAAGCCATCCAGCGGACCCCTAAGATCCAGGTGTACAGCAGACACCCCGCCGAGAACGGCAAGAGCAACTTCCTGAACTGCTACGTGTCCGGCTTTCACCCCAGCGACATTGAGGTGGACCTGCTGAAGAACGGCGAGCGGATCGAGAAGGTGGAACACAGCGATCTGAGCTTCAGCAAGGACTGGTCCTTCTACCTGCTGTACTACACCGAGTTCACCCCTACCGAGAAGGACGAGTACGCCTGCAGAGTGAACCACGTGACACTGAGCCAGCCTAAGATCGTGAAGTGGGACAGAGATATGGGCGGAGGCGGATCTGGTGGCGGAGGAAGTGGCGGCGGAGGATCTGGCGGTGGTGGTTCTGGATCTCACAGCCTGAAGTACTTTCACACCTCCGTGTCCAGACCTGGCAGAGGCGAGCCTAGATTCATCAGCGTGGGCTACGTGGACGACACCCAGTTCGTCAGATTCGACAACGACGCCGCCTCTCCTCGGATGGTTCCTAGAGCACCCTGGATGGAACAAGAGGGCAGCGAGTACTGGGATCGCGAGACAAGAAGCGCCAGAGACACAGCCCAGATCTTCCGCGTGAACCTGAGAACCCTGCGGGGCTACTACAATCAGTCTGAGGCCGGCTCTCACACCCTGCAGTGGATGCATGGATGTGAACTGGGCCCCGACAGACGGTTCCTGAGAGGCTATGAGCAGTTCGCCTACGACGGCAAGGACTACCTGACACTGAACGAGGACCTGAGAAGCTGGACCGCCGTGGATACAGCCGCTCAGATCAGCGAGCAGAAGTCTAACGACGCCAGCGAGGCCGAACACCAGAGAGCCTATCTGGAAGATACCTGCGTGGAATGGCTGCACAAGTACCTGGAAAAGGGCAAAGAGACACTGCTGCACCTGGAACCTCCAAAGACACATGTGACCCACCATCCTATCAGCGACCACGAGGCCACACTGAGATGTTGGGCCCTGGGCTTTTACCCTGCCGAGATCACACTGACATGGCAGCAGGATGGCGAGGGCCACACACAGGATACAGAGCTGGTGGAAACAAGACCTGCCGGCGACGGCACCTTCCAGAAATGGGCTGCTGTGGTTGTGCCCAGCGGCGAGGAACAGAGATACACCTGTCACGTGCAGCACGAGGGACTGCCTGAACCTGTGACTCTGAGATGGAAGCCTGCCAGCCAGCCAACAATCCCCATCGTGGGAATCATTGCCGGCCTGGTGCTGCTGGGATCTGTGGTTTCTGGTGCTGTGGTGGCCGCCGTGATTTGGAGAAAGAAGTCCTCTGGCGGCAAAGGCGGCTCCTACTCTAAGGCCGAGTGGAGCGATTCTGCCCAGGGCTCTGAAAGCCACAGCCTGTAGATAA (SEQ ID NO:16977).
[0502] Примерный димерный белок gBE (G и S) согласно изобретению включает или состоит из аминокислотной последовательности:
DLLKNGERIEKVEHSDLSFSKDWSFYLLYYTEFTPTEKDEYACRVNHVTLSQPKIVKWDR
DMGGGGSGGGGSGGGGSGGGGSGSHSLKYFHTSVSRPGRGEPRFISVGYVDDTQFVRFDN
DAASPRMVPRAPWMEQEGSEYWDRETRSARDTAQIFRVNLRTLRGYYNQSEAGSHTLQWM
HGCELGPDGRFLRGYEQFAYDGKDYLTLNEDLRSWTAVDTAAQISEQKSNDASEAEHQRA
YLEDTCVEWLHKYLEKGKETLLHLEPPKTHVTHHPISDHEATLRCWALGFYPAEITLTWQ
QDGEGHTQDTELVETRPAGDGTFQKWAAVVVPSGEEQRYTCHVQHEGLPEPVTLRWKPAS
QPTIPIVGIIAGLVLLGSVVSGAVVAAVIWRKKSSGGKGGSYSKAEWSDSAQGSESHSL
(SEQ ID NO:16978)
[0503] Примерный димерный белок gBE (G и S) согласно изобретению включает или состоит из аминокислотной последовательности:
ATGAGCAGATCTGTGGCCCTGGCTGTTCTGGCTCTGCTGTCTCTGTCTGGCCTGGAAGCCATCCAGCGGACCCCTAAGATCCAGGTGTACAGCAGACACCCCGCCGAGAACGGCAAGAGCAACTTCCTGAACTGCTACGTGTCCGGCTTTCACCCCAGCGACATTGAGGTGGACCTGCTGAAGAACGGCGAGCGGATCGAGAAGGTGGAACACAGCGATCTGAGCTTCAGCAAGGACTGGTCCTTCTACCTGCTGTACTACACCGAGTTCACCCCTACCGAGAAGGACGAGTACGCCTGCAGAGTGAACCACGTGACACTGAGCCAGCCTAAGATCGTGAAGTGGGACAGAGATATGGGCGGAGGCGGATCTGGTGGCGGAGGAAGTGGCGGCGGAGGATCTGGCGGTGGTGGTTCTGGATCTCACAGCCTGAAGTACTTTCACACCTCCGTGTCCAGACCTGGCAGAGGCGAGCCTAGATTCATCAGCGTGGGCTACGTGGACGACACCCAGTTCGTCAGATTCGACAACGACGCCGCCTCTCCTCGGATGGTTCCTAGAGCACCCTGGATGGAACAAGAGGGCAGCGAGTACTGGGATCGCGAGACAAGAAGCGCCAGAGACACAGCCCAGATCTTCCGCGTGAACCTGAGAACCCTGCGGGGCTACTACAATCAGTCTGAGGCCGGCTCTCACACCCTGCAGTGGATGCATGGATGTGAACTGGGCCCCGACAGACAGTTCCTGAGAGGCTATGAGCAGTTCGCCTACGACGGCAAGGACTACCTGACACTGAACGAGGACCTGAGAAGCTGGACCGCCGTGGATACAGCCGCTCAGATCAGCGAGCAGAAGTCTAACGACGCCAGCGAGGCCGAACACCAGAGAGCCTATCTGGAAGATACCTGCGTGGAATGGCTGCACAAGTACCTGGAAAAGGGCAAAGAGACACTGCTGCACCTGGAACCTCCAAAGACACATGTGACCCACCATCCTATCAGCGACCACGAGGCCACACTGAGATGTTGGGCCCTGGGCTTTTACCCTGCCGAGATCACACTGACATGGCAGCAGGATGGCGAGGGCCACACACAGGATACAGAGCTGGTGGAAACAAGACCTGCCGGCGACGGCACCTTCCAGAAATGGGCTGCTGTGGTTGTGCCCAGCGGCGAGGAACAGAGATACACCTGTCACGTGCAGCACGAGGGACTGCCTGAACCTGTGACTCTGAGATGGAAGCCTGCCAGCCAGCCAACAATCCCCATCGTGGGAATCATTGCCGGCCTGGTGCTGCTGGGATCTGTGGTTTCTGGTGCTGTGGTGGCCGCCGTGATTTGGAGAAAGAAGTCCTCTGGCGGCAAAGGCGGCTCCTACTCTAAGGCCGAGTGGAGCGATTCTGCCCAGGGCTCTGAAAGCCACAGCCTGTAGATAA (SEQ ID NO:16979)
[0504] Примерный мономерный белок WT HLA-E (R и S) согласно изобретению включает или состоит из аминокислотной последовательности:
MSRSVALAVLALLSLSGLEAGSHSLKYFHTSVSRPGRGEPRFISVGYVDDTQFVRF
DNDAASPRMVPRAPWMEQEGSEYWDRETRSARDTAQIFRVNLRTLRGYYNQSEAGSHTLQ
WMHGCELGPDRRFLRGYEQFAYDGKDYLTLNEDLRSWTAVDTAAQISEQKSNDASEAEHQ
RAYLEDTCVEWLHKYLEKGKETLLHLEPPKTHVTHHPISDHEATLRCWALGFYPAEITLT
WQQDGEGHTQDTELVETRPAGDGTFQKWAAVVVPSGEEQRYTCHVQHEGLPEPVTLRWKP
ASQPTIPIVGIIAGLVLLGSVVSGAVVAAVIWRKKSSGGKGGSYSKAEWSDSAQGSESHS
L (SEQ ID NO:16980)
[0505] Примерный мономерный белок WT HLA-E (R и S) согласно изобретению включает или состоит из последовательности нуклеиновой кислоты:
ATGAGCAGATCTGTGGCCCTGGCTGTTCTGGCTCTGCTGTCTCTGTCTGGACTGGAAGCCGGCAGCCACAGCCTGAAGTACTTTCACACCAGCGTGTCCAGACCTGGCAGAGGCGAGCCTAGATTCATCAGCGTGGGCTACGTGGACGACACCCAGTTCGTCAGATTCGACAACGACGCCGCCTCTCCTCGGATGGTTCCTAGAGCACCCTGGATGGAACAAGAGGGCAGCGAGTACTGGGACAGAGAGACAAGAAGCGCCAGAGACACAGCCCAGATCTTCAGAGTGAACCTGCGGACCCTGCGGGGCTACTACAATCAGTCTGAAGCCGGCTCTCACACCCTGCAGTGGATGCACGGATGTGAACTGGGCCCCGACAGAAGATTCCTGAGAGGCTACGAGCAGTTCGCCTACGACGGCAAGGACTACCTGACACTGAACGAGGACCTGAGAAGCTGGACCGCCGTGGATACAGCCGCTCAGATCAGCGAGCAGAAGTCTAACGACGCCTCTGAGGCCGAACACCAGAGAGCCTACCTGGAAGATACCTGCGTGGAATGGCTGCACAAGTACCTGGAAAAGGGCAAAGAGACACTGCTGCACCTGGAACCTCCAAAGACACACGTGACCCACCATCCTATCAGCGACCACGAGGCCACACTGAGATGTTGGGCCCTGGGCTTTTACCCCGCCGAGATCACACTGACATGGCAGCAGGATGGCGAGGGCCACACACAGGATACAGAGCTGGTGGAAACAAGACCTGCCGGCGACGGCACCTTCCAGAAATGGGCTGCTGTGGTGGTTCCCAGCGGCGAGGAACAGAGATACACCTGTCACGTGCAGCACGAGGGACTGCCTGAACCTGTGACACTGAGGTGGAAGCCTGCCAGCCAGCCTACAATCCCCATCGTGGGAATCATTGCCGGCCTGGTGCTGCTGGGATCTGTGGTTTCTGGTGCAGTGGTGGCCGCCGTGATCTGGCGGAAAAAAAGCTCAGGCGGCAAAGGCGGCTCCTACTCCAAAGCCGAGTGGAGCGATTCTGCCCAGGGCTCTGAAAGCCACTCTCTGTAGATAA (SEQ ID NO:16981).
[0506] Примерный мономерный белок WT HLA-E (G и S) согласно изобретению включает или состоит из последовательности нуклеиновой кислоты:
MSRSVALAVLALLSLSGLEAGSHSLKYFHTSVSRPGRGEPRFISVGYVDDTQFVRF
DNDAASPRMVPRAPWMEQEGSEYWDRETRSARDTAQIFRVNLRTLRGYYNQSEAGSHTLQ
WMHGCELGPDGRFLRGYEQFAYDGKDYLTLNEDLRSWTAVDTAAQISEQKSNDASEAEHQ
RAYLEDTCVEWLHKYLEKGKETLLHLEPPKTHVTHHPISDHEATLRCWALGFYPAEITLT
WQQDGEGHTQDTELVETRPAGDGTFQKWAAVVVPSGEEQRYTCHVQHEGLPEPVTLRWKP
ASQPTIPIVGIIAGLVLLGSVVSGAVVAAVIWRKKSSGGKGGSYSKAEWSDSAQGSESHS
L (SEQ ID NO:16982).
[0507] Примерный мономерный белок WT HLA-E (G и S) согласно изобретению включает или состоит из последовательности нуклеиновой кислоты:
ATGAGCAGATCTGTGGCCCTGGCTGTTCTGGCTCTGCTGTCTCTGTCTGGACTGGAAGCCGGCAGCCACAGCCTGAAGTACTTTCACACCAGCGTGTCCAGACCTGGCAGAGGCGAGCCTAGATTCATCAGCGTGGGCTACGTGGACGACACCCAGTTCGTCAGATTCGACAACGACGCCGCCTCTCCTCGGATGGTTCCTAGAGCACCCTGGATGGAACAAGAGGGCAGCGAGTACTGGGACAGAGAGACAAGAAGCGCCAGAGACACAGCCCAGATCTTCAGAGTGAACCTGCGGACCCTGCGGGGCTACTACAATCAGTCTGAAGCCGGCTCTCACACCCTGCAGTGGATGCACGGATGTGAACTGGGCCCCGACGGAAGATTCCTGAGAGGCTACGAGCAGTTCGCCTACGACGGCAAGGACTACCTGACACTGAACGAGGACCTGAGAAGCTGGACCGCCGTGGATACAGCCGCTCAGATCAGCGAGCAGAAGTCTAACGACGCCTCTGAGGCCGAACACCAGAGAGCCTACCTGGAAGATACCTGCGTGGAATGGCTGCACAAGTACCTGGAAAAGGGCAAAGAGACACTGCTGCACCTGGAACCTCCAAAGACACACGTGACCCACCATCCTATCAGCGACCACGAGGCCACACTGAGATGTTGGGCCCTGGGCTTTTACCCCGCCGAGATCACACTGACATGGCAGCAGGATGGCGAGGGCCACACACAGGATACAGAGCTGGTGGAAACAAGACCTGCCGGCGACGGCACCTTCCAGAAATGGGCTGCTGTGGTGGTTCCCAGCGGCGAGGAACAGAGATACACCTGTCACGTGCAGCACGAGGGACTGCCTGAACCTGTGACACTGAGGTGGAAGCCTGCCAGCCAGCCTACAATCCCCATCGTGGGAATCATTGCCGGCCTGGTGCTGCTGGGATCTGTGGTTTCTGGTGCAGTGGTGGCCGCCGTGATCTGGCGGAAAAAAAGCTCAGGCGGCAAAGGCGGCTCCTACTCCAAAGCCGAGTGGAGCGATTCTGCCCAGGGCTCTGAAAGCCACTCTCTGTAGATAA (SEQ ID NO:16983).
[0508]
Векторы и клетки-хозяева
[0509] Изобретение также относится к векторам, которые включают выделенные молекулы нуклеиновых кислот согласно изобретению, клетки-хозяева, которые были генетически модифицированы рекомбинантными векторами, и к получению по меньшей мере одного VHH или VCAR с помощью рекомбинантных технологий, хорошо известных в уровне техники. См., например, Sambrook et al., выше; Ausubel, et al., выше, которые полностью включены в настоящее описание посредством отсылки.
[0510] Например, может использоваться вектор PB-EF1a. Вектор включает следующую нуклеотидную последовательность:
tgtacatagattaaccctagaaagataatcatattgtgacgtacgttaaagataatcatgcgtaaaattgacgcatgtgttttatcggtctgtatatcgaggtttatttattaatttgaatagatattaagttttattatatttacacttacatactaataataaattcaacaaacaatttatttatgtttatttatttattaaaaaaaaacaaaaactcaaaatttcttctataaagtaacaaaacttttatcgaatacctgcagcccgggggatgcagagggacagcccccccccaaagcccccagggatgtaattacgtccctcccccgctagggggcagcagcgagccgcccggggctccgctccggtccggcgctccccccgcatccccgagccggcagcgtgcggggacagcccgggcacggggaaggtggcacgggatcgctttcctctgaacgcttctcgctgctctttgagcctgcagacacctggggggatacggggaaaagttgactgtgcctttcgatcgaaccatggacagttagctttgcaaagatggataaagttttaaacagagaggaatctttgcagctaatggaccttctaggtcttgaaaggagtgggaattggctccggtgcccgtcagtgggcagagcgcacatcgcccacagtccccgagaagttggggggaggggtcggcaattgaaccggtgcctagagaaggtggcgcggggtaaactgggaaagtgatgtcgtgtactggctccgcctttttcccgagggtgggggagaaccgtatataagtgcagtagtcgccgtgaacgttctttttcgcaacgggtttgccgccagaacacaggtaagtgccgtgtgtggttcccgcgggcctggcctctttacgggttatggcccttgcgtgccttgaattacttccacctggctgcagtacgtgattcttgatcccgagcttcgggttggaagtgggtgggagagttcgaggccttgcgcttaaggagccccttcgcctcgtgcttgagttgaggcctggcctgggcgctggggccgccgcgtgcgaatctggtggcaccttcgcgcctgtctcgctgctttcgataagtctctagccatttaaaatttttgatgacctgctgcgacgctttttttctggcaagatagtcttgtaaatgcgggccaagatctgcacactggtatttcggtttttggggccgcgggcggcgacggggcccgtgcgtcccagcgcacatgttcggcgaggcggggcctgcgagcgcggccaccgagaatcggacgggggtagtctcaagctggccggcctgctctggtgcctggcctcgcgccgccgtgtatcgccccgccctgggcggcaaggctggcccggtcggcaccagttgcgtgagcggaaagatggccgcttcccggccctgctgcagggagctcaaaatggaggacgcggcgctcgggagagcgggcgggtgagtcacccacacaaaggaaaagggcctttccgtcctcagccgtcgcttcatgtgactccacggagtaccgggcgccgtccaggcacctcgattagttctcgagcttttggagtacgtcgtctttaggttggggggaggggttttatgcgatggagtttccccacactgagtgggtggagactgaagttaggccagcttggcacttgatgtaattctccttggaatttgccctttttgagtttggatcttggttcattctcaagcctcagacagtggttcaaagtttttttcttccatttcaggtgtcgtgagaattctaatacgactcactatagggtgtgctgtctcatcattttggcaaagattggccaccaagcttgtcctgcaggagggtcgacgcctctagacgggcggccgctccggatccacgggtaccgatcacatatgcctttaattaaacactagttctatagtgtcacctaaattccctttagtgagggttaatggccgtaggccgccagaattgggtccagacatgataagatacattgatgagtttggacaaaccacaactagaatgcagtgaaaaaaatgctttatttgtgaaatttgtgatgctattgctttatttgtaaccattataagctgcaataaacaagttaacaacaacaattgcattcattttatgtttcaggttcagggggaggtgtgggaggttttttcggactctaggacctgcgcatgcgcttggcgtaatcatggtcatagctgtttcctgttttccccgtatccccccaggtgtctgcaggctcaaagagcagcgagaagcgttcagaggaaagcgatcccgtgccaccttccccgtgcccgggctgtccccgcacgctgccggctcggggatgcggggggagcgccggaccggagcggagccccgggcggctcgctgctgccccctagcgggggagggacgtaattacatccctgggggctttgggggggggctgtccctctcaccgcggtggagctccagcttttgttcgaattggggccccccctcgagggtatcgatgatatctataacaagaaaatatatatataataagttatcacgtaagtagaacatgaaataacaatataattatcgtatgagttaaatcttaaaagtcacgtaaaagataatcatgcgtcattttgactcacgcggtcgttatagttcaaaatcagtgacacttaccgcattgacaagcacgcctcacgggagctccaagcggcgactgagatgtcctaaatgcacagcgacggattcgcgctatttagaaagagagagcaatatttcaagaatgcatgcgtcaattttacgcagactatctttctagggttaatctagctagccttaagggcgcctattgcgttgcgctcactgcccgctttccagtcgggaaacctgtcgtgccagctgcattaatgaatcggccaacgcgcggggagaggcggtttgcgtattgggcgctcttccgcttcctcgctcactgactcgctgcgctcggtcgttcggctgcggcgagcggtatcagctcactcaaaggcggtaatacggttatccacagaatcaggggataacgcaggaaagaacatgaccaaaatcccttaacgtgagttttcgttccactgagcgtcagaccccgtagaaaagatcaaaggatcttcttgagatcctttttttctgcgcgtaatctgctgcttgcaaacaaaaaaaccaccgctaccagcggtggtttgtttgccggatcaagagctaccaactctttttccgaaggtaactggcttcagcagagcgcagataccaaatactgttcttctagtgtagccgtagttaggccaccacttcaagaactctgtagcaccgcctacatacctcgctctgctaatcctgttaccagtggctgctgccagtggcgataagtcgtgtcttaccgggttggactcaagacgatagttaccggataaggcgcagcggtcgggctgaacggggggttcgtgcacacagcccagcttggagcgaacgacctacaccgaactgagatacctacagcgtgagctatgagaaagcgccacgcttcccgaagggagaaaggcggacaggtatccggtaagcggcagggtcggaacaggagagcgcacgagggagcttccagggggaaacgcctggtatctttatagtcctgtcgggtttcgccacctctgacttgagcgtcgatttttgtgatgctcgtcaggggggcggagcctatggaaaaacgccagcaacgcggcctttttacggttcctggccttttgctggccttttgctcacatgagattatcaaaaaggatcttcacctagatccttttaaattaaaaatgaagttttaaatcaatctaaagtatatatgagtaaacttggtctgacagtcagaagaactcgtcaagaaggcgatagaaggcgatgcgctgcgaatcgggagcggcgataccgtaaagcacgaggaagcggtcagcccattcgccgccaagctcttcagcaatatcacgggtagccaacgctatgtcctgatagcggtccgccacacccagccggccacagtcgatgaatccagaaaagcggccattttccaccatgatattcggcaagcaggcatcgccatgggtcacgacgagatcctcgccgtcgggcatgctcgccttgagcctggcgaacagttcggctggcgcgagcccctgatgctcttcgtccagatcatcctgatcgacaagaccggcttccatccgagtacgtgctcgctcgatgcgatgtttcgcttggtggtcgaatgggcaggtagccggatcaagcgtatgcagccgccgcattgcatcagccatgatggatactttctcggcaggagcaaggtgagatgacaggagatcctgccccggcacttcgcccaatagcagccagtcccttcccgcttcagtgacaacgtcgagcacagctgcgcaaggaacgcccgtcgtggccagccacgatagccgcgctgcctcgtcttgcagttcattcagggcaccggacaggtcggtcttgacaaaaagaaccgggcgcccctgcgctgacagccggaacacggcggcatcagagcagccgattgtctgttgtgcccagtcatagccgaatagcctctccacccaagcggccggagaacctgcgtgcaatccatcttgttcaatcataatattattgaagcatttatcagggttcgtctcgtcccggtctcctcccaatgcatgtcaatattggccattagccatattattcattggttatatagcataaatcaatattggctattggccattgcatacgttgtatctatatcataata (SEQ ID NO:17502)
[0511] Полинуклеотиды необязательно могут быть соединены с вектором, содержащим селективный маркер для размножение в хозяине. Обычно плазмидный вектор вводят в осадке, таком как осадок фосфата кальция, или в комплексе с заряженным липидом. Если вектор является вирусом, он может быть упакован in vitro с использованием подходящей упаковывающей клеточной линии и затем трансдуцирован в клетки-хозяева.
[0512] Вставка ДНК должна быть функционально связана с подходящим промотором. Экспрессионные конструкции также содержат сайты инициации и терминации транскрипции и, в транскрибированной области, сайт связывания рибосомы для трансляции. Кодирующая часть зрелых транскриптов, экспрессируемых конструкциями, предпочтительно включает инициацию трансляции в начале и терминирующий кодон (например, UAA, UGA или UAG), соответственно расположенный на конце транслируемой мРНК, причем UAA и UAG предпочтительны для экспрессии в клетках млекопитающих или эукариотических клетках.
[0513] Векторы экспрессии предпочтительно, но не обязательно, включают по меньшей мере один селективный маркер. Такие маркеры включают, например, без ограничения перечисленными, ампициллин, зеоцин (ген Sh bla), пуромицин (ген pac), гигромицин B (ген hygB), G418/генетицин (ген neo), микофеноловую кислоту или глутаминсинтетазу (GS, патенты США 5,122,464; 5,770,359; 5,827,739), бластицидин (ген bsd), гены устойчивости культуры эукариотических клеток, а также гены устойчивости к ампициллину, зеоцину (ген Sh bla), пуромицину (ген pac), гигромицину B (ген hygB), G418/генетицину (ген neo), канамицину, спектиномицину, стрептомицину, карбенициллину, блеомицину, эритомицину, полимиксину B или тетрациклину для культивирования в E. coli и других бактериях или прокариотах (вышеуказанные патенты настоящим полностью включены посредством отсылки). Подходящие культуральные среды и условия культивирования вышеописанных клеток-хозяев известны в уровне техники. Подходящие векторы будут известны специалисту. Введение векторной конструкции в клетку-хозяина может быть выполнено путем трансфекции с фосфатом кальция, DEAE-декстран-опосредованной трансфекции, опосредованной катионным липидом трансфекции, электропорации, трансдукции, инфицирования или других известных способов. Такие способы описаны в уровне техники, например, в Sambrook, выше, Главы 1-4 и 16-18; Ausubel, выше, Главы 1, 9, 13, 15, 16.
[0514] Векторы экспрессии предпочтительно, но не обязательно, включают по меньшей мере один селективный маркер клеточной поверхности для выделения клеток, модифицированных с применением композиций и способов согласно изобретению. Селективные маркеры клеточной поверхности согласно изобретению включают поверхностные белки, гликопротеины или группу белков, которые позволяют отличить клетку или субпопуляцию клеток от другой определенной субпопуляции клеток. Предпочтительно селективный маркер клеточной поверхности позволяет отличить клетки, модифицированные с применением композиции или способа согласно изобретению, от тех клеток, которые не модифицированы с применением композиции или способа согласно изобретению. Такие маркеры клеточной поверхности включают, например, без ограничения перечисленными, "кластеры обозначения" или "детерминирующие классификацию" белки (часто сокращенно обозначаемые как "CD"), такие как усеченную или полноразмерную форму CD19, CD271, CD34, CD22, CD20, CD33, CD52 или их любую комбинацию. Маркеры клеточной поверхности дополнительно включают маркер суицидального гена RQR8 (Philip B et al.Blood. 2014 Aug 21; 124(8):1277-87).
[0515] Векторы экспрессии предпочтительно, но не обязательно, включают по меньшей мере один селективный маркер устойчивости к лекарственному средству для выделения клеток, модифицированных с применением композиций и способов согласно изобретению. Селективные маркеры устойчивости к лекарственному средству согласно изобретению могут включать дикий тип или мутантный Neo, DHFR, TYMS, FRANCF, RAD51C, GCS, MDR1, ALDH1, NKX2.2 или их любую комбинацию.
[0516] По меньшей мере один VHH или VCAR согласно изобретению может экспрессироваться в модифицированной форме, такой как слитый белок, и может включать не только сигналы секреции, но также дополнительные гетерологичные функциональные области. Например, область дополнительных аминокислот, в частности, заряженных аминокислот, может быть добавлена на N-конец VHH или VCAR для повышения стабильности и устойчивости в клетке-хозяине, во время очистки или во время последующей обработки и хранения. Также пептидные фрагменты могут быть добавлены в VHH или VCAR согласно изобретению для облегчения очистки. Такие области могут быть удалены до окончательного получения VHH или VCAR или по меньшей мере одного их фрагмента. Такие способы описаны во многих стандартных лабораторных руководствах, таких как Sambrook, выше, главы 17.29-17.42 и 18.1-18.74; Ausubel, выше, главы 16, 17 и 18.
[0517] Специалистам в данной области техники известны многочисленные системы экспрессии, доступные для экспрессии нуклеиновой кислоты, кодирующей белок согласно изобретению. В альтернативе нуклеиновые кислоты согласно изобретению могут быть экспрессированы в клетке-хозяине путем включения (посредством манипуляции) в клетке-хозяине, которая содержит эндогенную ДНК, кодирующую VHH или VCAR согласно изобретению. Такие способы хорошо известны в данной области, например, как описано в патентах США 5580734, 5641670, 5733746 и 5733761, полностью включенных в настоящий документ посредством ссылки.
[0518] Иллюстративными культурами клеток, подходящими для получения VHH или VCAR, их определенных частей или вариантов, являются клетки бактерий, дрожжей и млекопитающих, известные в уровне техники. Клеточные системы млекопитающих часто будут иметь форму монослоев клеток, хотя также могут использоваться суспензии клеток млекопитающих или биореакторы. Ряд подходящих линий клеток-хозяев, способных экспрессировать интактные гликозилированные белки, был разработан в данной области и включает COS-1 (например, ATCC CRL 1650), COS-7 (например, ATCC CRL-1651), HEK293, BHK21 (например, линии клеток ATCC CRL-10), CHO (например, ATCC CRL 1610) и BSC-1 (например, ATCC CRL-26), клетки Cos-7, клетки CHO, клетки hep G2, P3X63Ag8.653, SP2/0-Ag14, клетки 293, клетки HeLa и т.п., которые доступны, например, из Американской коллекции типовых культур, Манассас, Вирджиния (www.atcc.org). Предпочтительные клетки-хозяева включают клетки лимфоидного происхождения, такие как клетки миеломы и лимфомы. Особенно предпочтительными клетками-хозяевами являются клетки P3X63Ag8.653 (рег. номер ATCC CRL-1580) и клетки SP2/0-Ag14 (рег. номер ATCC CRL-1851). В наиболее предпочтительном варианте осуществления рекомбинантная клетка является клеткой P3X63Ab8.653 или SP2/0-Ag14.
[0519] Векторы экспрессии для этих клеток могут включать одну или более следующих последовательностей контроля экспрессии, таких как, без ограничения перечисленными, начало репликации; промотор (например, поздний или ранний промоторы SV40, промотор ЦМВ (патенты США 5168062; 5,385,839), tk промотор HSV, промотор pgk (фосфоглицераткиназы), промотор EF-1 альфа (патент США 5,266,491), по меньшей мере один человеческий промотор, энхансер и/или сайты обработки информации, такие как сайты связывания рибосом, сайты сплайсинга РНК, сайты полиаденилирования (например, сайт присоединения большого T Ag поли-A) и последовательности терминаторов транскрипции. См., например, Ausubel et al., выше; Sambrook, et al., выше. Другие клетки, подходящие для продукции нуклеиновых кислот или белков согласно изобретению, известны и/или доступны, например, из каталога линий клеток и гибридом Американской коллекции типовых культур (www.atcc.org) или других известных или коммерческих источников.
[0520] При использовании эукариотических клеток-хозяев в вектор обычно включают последовательности полиаденилирования или терминатора транскрипции. Примером последовательности терминатора является последовательность полиаденилирования из гена гормона роста бычьих. Также могут быть включены последовательности для точного сплайсинга транскрипта. Примером последовательности сплайсинга является интрон VP1 из SV40 (Sprague, et al., J. Virol. 45:773-781 (1983)). Кроме того, в вектор могут быть включены последовательности генов для контроля репликации в клетке-хозяине, как известно в данной области.
Очистка VH, VHH или VCAR
[0521] Белок VHH или VCAR может быть выделен и очищен из рекомбинантных клеточных культур известными способами, в том числе, без ограничения, с помощью очистки на белке А, осаждения сульфатом аммония или этанолом, экстракции кислотой, анионообменной или катионообменной хроматографии, фосфоцеллюлозной хроматографии, хроматографии гидрофобного взаимодействия, аффинной хроматографии, гидроксиапатитной хроматографии и лектиновой хроматографии. Высокоэффективная жидкостная хроматография ("ВЭЖХ") также может использоваться для очистки. См., например, Colligan, Current Protocols in Immunology, или Current Protocols in Protein Science, John Wiley & Sons, NY, N.Y., (1997-2001), например, главы 1, 4, 6, 8, 9, 10, которые полностью включены в настоящий документ посредством отсылки.
[0522] VH, VHH и/или VCAR-рецепторы согласно изобретению включают очищенные продукты, продукты процедур химического синтеза и продукты, полученные рекомбинантными методами из прокариотического или эукариотического хозяина, включая, например, клетки E. coli, дрожжей, высших растений, насекомых и млекопитающих. В зависимости от хозяина, используемого в процедуре рекомбинантной продукции, VCAR согласно изобретению может быть гликозилированным или может быть негликозилированным. Такие способы описаны во многих стандартных лабораторных справочниках, таких как Sambrook, выше, Разделы 17.37-17.42; Ausubel, выше, Главы 10, 12, 13, 16, 18 и 20, Colligan, Protein Science, выше, Главы 12-14, которые полностью включены в настоящий документ посредством отсылки.
Обозначения аминокислот
[0523] Аминокислоты, которые входят в состав VCAR согласно изобретению, часто указывают сокращенными обозначениями. Обозначения аминокислот могут быть указаны путем обозначения аминокислоты однобуквенным кодом, трехбуквенным кодом, названием или тринуклеотидным кодоном(ами), как хорошо известно в данной области (см. Alberts, B., et al., Molecular Biology of The Cell, Third Ed., Garland Publishing, Inc., New York, 1994). VCAR согласно изобретению может включать одну или более аминокислотных замен, делеций или добавлений в результате спонтанных мутаций и/или манипуляций человека, как определено в настоящем документе. Аминокислоты в VCAR согласно изобретению, которые важны для функции, могут быть идентифицированы способами, известными в данной области, такими как сайт-направленный мутагенез или аланин-сканирующий мутагенез (например, Ausubel, выше, Главы 8, 15; Cunningham and Wells, Science 244:1081-1085 (1989)). В последней процедуре одиночные мутации с заменой на аланин вводят в каждый остаток в молекуле. Полученные мутантные молекулы затем тестируют на биологическую активность, такую как, без ограничения, по меньшей мере одну нейтрализующую активность. Сайты, которые являются наиболее важными для связывания VCAR, также могут быть идентифицированы с помощью структурного анализа, такого как кристаллизация, ядерный магнитный резонанс или фотоаффинное мечение (Smith, et al., J. Mol. Biol. 224:899-904 (1992) и de Vos, et al., Science 255:306-312 (1992)).
[0524] Специалистам будет очевидно, что изобретение включает по меньшей мере один биологически активный VCAR согласно изобретению. Биологически активные VCAR-рецепторы обладают специфической активностью, по меньшей мере 20%, 30% или 40%, и предпочтительно по меньшей мере 50%, 60% или 70%, и наиболее предпочтительно по меньшей мере 80%, 90% или 95-99% или более высокой специфической активностью нативного (не синтетического), эндогенного или родственного и известного VCAR. Способы анализа и количественного определения показателей ферментной активности и субстратной специфичности хорошо известны специалистам в данной области.
[0525] В другом аспекте изобретение относится к белкам и фрагментам VHH, как описано в настоящем документе, которые модифицированы путем ковалентного присоединения органического фрагмента. Такая модификация может давать фрагмент VCAR с улучшенными фармакокинетическими свойствами (например, с увеличенным полупериодом существования в сыворотке in vivo). Органический фрагмент может быть линейной или разветвленной гидрофильной полимерной группой, жирнокислотной группой или группой сложного эфира жирной кислоты. В конкретных вариантах осуществления гидрофильная полимерная группа может иметь молекулярную массу от приблизительно 800 до приблизительно 120000 Дальтон и может быть полиалкангликолем (например, полиэтиленгликолем (ПЭГ), полипропиленгликолем (ППГ)), углеводным полимером, аминокислотным полимером или поливинилпирролидоном, при этом жирнокислотная группа или группа сложного эфира жирной кислоты может включать от приблизительно восьми до приблизительно сорока атомов углерода.
[0526] Модифицированные белки VHH и фрагменты согласно изобретению могут включать одну или более органических групп, ковалентно связанных, напрямую или ненапрямую, с антителом. Каждая органическая группа, которая связана с белком VHH или фрагментом согласно изобретению, может быть независимо гидрофильной полимерной группой, жирнокислотной группой или группой сложного эфира жирной кислоты. При использовании в настоящем документе термин "жирная кислота" охватывает монокарбоновые кислоты и дикарбоновые кислоты. "Гидрофильная полимерная группа", при использовании данного термина в настоящем документе, относится к органическому полимеру, который в воде растворяется лучше, чем в октане. Например, полилизин лучше растворяется в воде, чем в октане. Таким образом, белок VHH, модифицированный путем ковалентного присоединения полилизина, включен в настоящее описание. Гидрофильные полимеры, подходящие для модификации VCAR-рецепторов согласно изобретению, могут быть линейными или разветвленными и включают, например, полиалкангликоли (например, ПЭГ, монометокси-полиэтиленгликоль (мПЭГ), ППГ и т.п.), углеводы (например, декстран, целлюлозу, олигосахариды, полисахариды и т.п.), полимеры гидрофильных аминокислот (например, полилизин, полиаргинин, полиаспартат и т.п.), полиалканоксиды (например, полиэтиленоксид, полипропиленоксид и т.п.) и поливинилпирролидон. Предпочтительно гидрофильный полимер, который модифицирует VCAR согласно изобретению, имеет молекулярную массу от приблизительно 800 до приблизительно 150000 Дальтон в качестве отдельной молекулярной единицы. Например, может использоваться ПЭГ 5000 и ПЭГ 20000, где нижний индекс является средней молекулярной массой полимера в Дальтонах. Гидрофильная полимерная группа может быть замещена от одного до приблизительно шести алкильными, жирнокислотными группами или группами сложного эфира жирной кислоты. Гидрофильные полимеры, которыми замещены жирнокислотной группой или группой сложного эфира жирной кислоты, могут быть получены при использовании подходящих способов. Например, полимер, включающий аминогруппу, может быть соединен с карбоксилатом жирной кислоты или сложного эфира жирной кислоты и активированным карбоксилатом (например, активированным N, N-карбонилдиимидазолом) на жирной кислоте или сложном эфире жирной кислоты, который может быть соединен с гидроксильной группой на полимере.
[0527] Жирные кислоты и сложные эфиры жирных кислот, подходящие для модификации белков VHH согласно изобретению, могут быть насыщенными или могут содержать одну или более единиц ненасыщенности. Жирные кислоты, подходящие для модификации VCAR-рецепторов согласно изобретению, включают, например, н-додеканоат (C12, лаурат), н-тетрадеканоат (C14, миристат), н-октадеканоат (C18, стеарат), н-эйкозаноат (C20, арахидат), н-докозаноат (C22, бегенат), н-триаконтаноат (C30), н-тетраконтаноат (C40), цис-Δ9-октадеканоат (C18, олеат), полностью цис-Δ5,8,11,14-эйкозатетраеноат (C20, арахидонат), октандиовую кислоту, тетрадекандиовую кислоту, октадекандиовую кислоту, докозандиовую кислоту и т.п. Подходящие сложные эфиры жирных кислот включают сложные моноэфиры дикарбоновых кислот, включающие линейную или разветвленную низшую алкильную группу. Низшая алкильная группа может включать от одного до приблизительно двенадцати, предпочтительно от одного до приблизительно шести, атомов углерода.
[0528] Модифицированные белки VHH и фрагменты могут быть получены с применением подходящих способов, например, путем реакции с одним или более модифицирующими средствами. "Модифицирующее средство", при использовании данного термина в настоящем документе, относится к подходящей органической группе (например, гидрофильному полимеру, жирной кислоте, сложному эфиру жирной кислоты), которая включает активирующую группу. "Активирующая группа" представляет собой химическую группу или функциональную группу, которая в соответствующих условиях может реагировать со второй химической группой, с образованием ковалентной связи между модифицирующим средством и второй химической группой. Например, аминореактивные активирующие группы включают электрофильные группы, такие как тозилат, мезилат, галоген (хлор, бром, фтор, иод), N-гидроксисукцинимидиловые сложные эфиры (NHS) и т.п. Активирующие группы, которые могут реагировать с тиолами, включают, например, малеимид, иодацетил, акрилоил, пиридилдисульфиды, тиол 5-тиол-2-нитробензойной кислоты (TNB-тиол) и т.п. Альдегидная функциональная группа может быть связана с амин- или гидразидсодержащими молекулами, при этом азидная группа может реагировать с трехвалентной фосфорной группой с образованием фосфорамидатных или фосфоримидных связей. Подходящие способы введения активирующих групп в молекулы известны в уровне техники (см., например, Hermanson, G. T., Bioconjugate Techniques, Academic Press: San Diego, Calif. (1996)). Активирующая группа может быть связана непосредственно с органической группой (например, гидрофильным полимером, жирной кислотой, сложным эфиром жирной кислоты) или через линкерный фрагмент, например, двухвалентную C1-C12 группу, в которой один или более атомов углерода могут быть заменены гетероатомом, таким как кислород, азот или сера. Подходящие линкерные фрагменты включают, например, тетраэтиленгликоль, -(CH2)3-, -NH-(CH2)6-NH-, -(CH2)2-NH- и -CH2-O-CH2-CH2-O-CH2-СН2-О-СН-NH-. Модифицирующие средства, которые включают линкерный фрагмент, могут быть получены, например, при взаимодействии моно-Вос-алкилдиамина (например, моно-Вос-этилендиамина, моно-Вос-диаминогексана) с жирной кислотой в присутствии 1-этил-3-(3-диметиламинопропил)-карбодиимида (EDC) с образованием амидной связи между свободным амином и карбоксилатом жирной кислоты. Защитная группа Boc может быть удалена из продукта при обработке трифторуксусной кислотой (ТФУ) с деблокированием первичного амина, который может связываться с другим карбоксилатом, как описано, или может реагировать с малеиновым ангидридом, при этом получаемый продукт циклизуется с образованием активированного малеимидо-производного жирной кислоты (см., например, публикацию Thompson, et al., WO 92/16221, полное описание которой включено в настоящее описание посредством отсылки).
[0529] Модифицированные белки VHH и фрагменты согласно изобретению могут быть получены при реакции белка VHH или фрагмента с модифицирующим средством. Например, органические фрагменты могут быть связаны с белком VHH не-сайтспецифическим образом при использовании амино-реактивного модифицирующего средства, например, сложного NHS эфира ПЭГ. Модифицированные белки VHH и фрагменты, включающие органический фрагмент, который связан с определенными сайтами белка VHH согласно изобретению, могут быть получены с применением подходящих способов, таких как обратный протеолиз (Fisch et al., Bioconjugate Chem., 3:147-153 (1992); Werlen et al., Bioconjugate Chem., 5:411-417 (1994); Kumaran et al., Protein Sci. 6(10):2233-2241 (1997); Itoh et al., Bioorg. Chem., 24(1): 59-68 (1996); Capellas et al., Biotechnol. Bioeng., 56(4):456-463 (1997)), а также способы, описанные в Hermanson, G. T., Bioconjugate Techniques, Academic Press: San Diego, Calif. (1996).
Композиции VH или VHH белков, включающие дополнительные терапевтически активные ингредиенты
[0530] Белок VHH или соединения, композиции или комбинации VCAR согласно изобретению могут дополнительно включать по меньшей мере одно из любого подходящего вспомогательного вещества, такого как, без ограничения перечисленными, разбавитель, связующее вещество, стабилизатор, буферы, соли, липофильные растворители, консервант, адъювант и т.п. Фармацевтически приемлемые вспомогательные вещества являются предпочтительными. Неограничивающие примеры и способы приготовления таких стерильных растворов хорошо известны в данной области, например, без ограничения ими, Gennaro, Ed., Remington's Pharmaceutical Sciences, 18th Edition, Mack Publishing Co. (Easton, Pa.) 1990. Могут быть выбраны фармацевтически приемлемые носители, которые являются подходящими для способа введения, растворимости и/или стабильности композиции белка VHH или VCAR, фрагмента или варианта, которые хорошо известны в уровне техники или описаны в настоящем документе.
[0531] Фармацевтические вспомогательные вещества и добавки, используемые в настоящей композиции, включают, без ограничения перечисленными, белки, пептиды, аминокислоты, липиды и углеводы (например, сахара, включая моносахариды, ди-, три-, тетра- и олигосахариды; дериватизированные сахара, такие как альдиты, альдоновые кислоты, этерифицированные сахара и т.п., и полисахариды или полимеры сахаров), которые могут присутствовать отдельно или в комбинации, включающие отдельно или в комбинации 1-99,99% по весу или объему. Типичные белковые вспомогательные вещества включают сывороточный альбумин, такой как человеческий сывороточный альбумин (ЧСА), рекомбинантный человеческий альбумин (рЧА), желатин, казеин и т.п. Репрезентативные аминокислотные/белковые компоненты, которые также могут регулировать буферную емкость, включают аланин, глицин, аргинин, бетаин, гистидин, глутаминовую кислоту, аспарагиновую кислоту, цистеин, лизин, лейцин, изолейцин, валин, метионин, фенилаланин, аспартам и т.п. Одной предпочтительной аминокислотой является глицин.
[0532] Углеводные вспомогательные вещества, подходящие для применения в изобретении, включают, например, моносахариды, такие как фруктозу, мальтозу, галактозу, глюкозу, D-маннозу, сорбозу и т.п.; дисахариды, такие как лактозу, сахарозу, трегалозу, целлобиозу и т.п.; полисахариды, такие как рафинозу, мелезитозу, мальтодекстрины, декстраны, крахмалы и т.п.; и альдиты, такие как маннит, ксилит, мальтит, лактит, ксилит, сорбит (глюцит), миоинозит и т.п. Предпочтительными углеводными вспомогательными веществами для применения в настоящем изобретении являются маннит, трегалоза и рафиноза.
[0533] Белок VH, белок VHH или композиции VCAR также могут включать буфер или регулятор pH; как правило, буфер представляет собой соль, полученную из органической кислоты или основания. Репрезентативные буферы включают соли органических кислот, такие как соли лимонной кислоты, аскорбиновой кислоты, глюконовой кислоты, угольной кислоты, винной кислоты, янтарной кислоты, уксусной кислоты или фталевой кислоты; Трис, трометамина гидрохлорид или фосфатные буферы. Предпочтительными буферами для применения в настоящих композициях являются соли органической кислоты, такие как цитрат.
[0534] Кроме того, белок VH, белок VHH или композиции VCAR согласно изобретению могут включать полимерные вспомогательные вещества/добавки, такие как поливинилпирролидоны, фиколлы (полимерный сахар), декстраты (например, циклодекстрины, такие как 2-гидроксипропил-β-циклодекстрин), полиэтиленгликоли, ароматизаторы, противомикробные средства, подсластители, антиоксиданты, антистатические средства, поверхностно-активные вещества (например, полисорбаты, такие как "TWEEN 20" и "TWEEN 80"), липиды (например, фосфолипиды, жирные кислоты), стероиды (например, холестерин) и хелатообразующие вещества (например, ЭДТА).
[0535] Эти и дополнительные известные фармацевтические вспомогательные вещества и/или добавки, подходящие для применения в композициях белка VH, белка VHH, VCAR, части или варианта согласно изобретению, известны в уровне техники, например, как перечислено в "Remington: The Science & Practice of Pharmacy", 19th ed., Williams & Williams, (1995), и в "Physician's Desk Reference", 52nd ed., Medical Economics, Montvale, N.J. (1998), которые полностью включены в настоящий документ посредством отсылки. Предпочтительными носителями или наполнителями являются углеводы (например, сахариды и альдиты) и буферы (например, цитрат) или полимерные вещества. Примерной молекулой-носителем является мукополисахарид, гиалуроновая кислота, которая может применяться для внутрисуставной доставки.
Выделение T-клеток из продукта лейкафереза
[0536] Продукт лейкафереза или кровь могут быть забраны у индивида в клиническом центре при использовании закрытой системы и стандартных методов (например, системы COBE Spectra Aphereis). Предпочтительно продукт собирают в соответствии со стандартными процедурами лейкафереза в больнице или учреждении в стандартные пакеты для сбора образцов лейкафереза. Например, в предпочтительных вариантах осуществления способов согласно изобретению не добавляют никакие дополнительные антикоагулянты или добавки для препаратов крови (гепарин и т.д.) кроме тех, которые обычно используются во время лейкафереза.
[0537] В альтернативе лейкоциты/мононуклеарные клетки периферической крови (МКПК) (с использованием Biosafe Sepax 2 (закрытый/автоматизированный)) или T-клетки (с использованием CliniMACS® Prodigy (закрытый/автоматизированный)) могут быть выделены непосредственно из цельной крови. Однако у некоторых индивидов (например, у которых диагностировали и/или лечили рак) выход лейкоцитов/МКПК может быть значительно ниже при выделении из цельной крови, чем при выделении с помощью лейкафереза.
[0538] Процедура лейкафереза и/или процедура прямого выделения клеток может использоваться для любого индивида согласно изобретению.
[0539] Продукт лейкафереза, кровь, композиция лейкоцитов/МКПК и/или композиция T-клеток должны быть помещены в изолированные контейнеры и должны храниться при регулируемой комнатной температуре (от +19°C до +25°C) в соответствии со стандартными, установленными в больнице или стационаре процедурами взятия крови для применения с клиническим протоколом. Продукт лейкафереза, кровь, композиция лейкоцитов/МКПК и/или композиция T-клеток не должны быть заморожены.
[0540] Концентрация клеток продукта лейкафереза, крови, композиции лейкоцитов/МКПК и/или композиции T-клеток не должна превышать 0,2×109 клеток на мл во время транспортировки. Следует избегать интенсивного перемешивания продукта лейкафереза, крови, композиции лейкоцитов/МКПК и/или композиции T-клеток.
[0541] Если продукт лейкафереза, кровь, композицию лейкоцитов/МКПК и/или композицию T-клеток требуется хранить, например, в течение ночи, его следует хранить при контролируемой комнатной температуре (такой же, как указано выше). Во время хранения концентрация продукта лейкафереза, крови, композиции лейкоцитов/МКПК и/или композиции T-клеток никогда не должна превышать 0,2×109 клеток в мл.
[0542] Предпочтительно клетки продукта лейкафереза, крови, композиции лейкоцитов/МКПК и/или композиции T-клеток следует хранить в аутологичной плазме крови. В некоторых вариантах осуществления, если концентрация клеток продукта лейкафереза, крови, композиции лейкоцитов/МКПК и/или композиции T-клеток превышает 0,2×109 клеток в мл, продукт следует разбавить аутологичной плазмой крови.
[0543] Предпочтительно продукт лейкафереза, кровь, композицию лейкоцитов/МКПК и/или композицию T-клеток не следует хранить больше 24 часов при начале процедуры мечения и разделения. Продукт лейкафереза, кровь, композиция лейкоцитов/МКПК и/или композиция T-клеток могут быть обработаны и/или подготовлены к мечению клеток при использовании закрытой и/или автоматизированной системы (например, CliniMACS Prodigy).
[0544] Автоматизированная система может выполнять дополнительное выделение лейкотромбоцитарного слоя, возможно обработки фиколлом и/или промывки клеточного продукта (например, продукта лейкафереза, крови, композиции лейкоцитов/МКПК и/или композиции T-клеток).
[0545] Закрытая и/или автоматизированная система может использоваться для подготовки и мечения клеток для выделения T-клеток (например, из продукта лейкафереза, крови, композиции лейкоцитов/МКПК и/или композиции T-клеток).
[0546] Хотя лейкоциты/МКПК могут быть непосредственно подвергнуты нуклеофекции (что проще и уменьшает количество стадий), способы согласно изобретению могут включать сначала выделение T-клеток перед нуклеофекцией. Более простая стратегия прямой нуклеофекции МКПК требует селективной экспансии VCAR+ клеток, которая опосредуется сигнализацией VCAR, что само по себе оказывается худшим способом экспансии, который непосредственно снижает эффективность продукта in vivo, делая T-клетки функционально истощенными. Продукт может быть гетерогенной композицией VCAR+ клеток, включающей T-клетки, NK-клетки, NKT-клетки, моноциты или их любую комбинацию, что увеличивает вариабельность продукта в зависимости от пациента и затрудняет введение и контроль синдрома CRS. Поскольку считается, что T-клетки являются основными эффекторами при подавлении и уничтожении опухоли, выделение T-клеток для производства аутологичного продукта может обеспечить значительные преимущества по сравнению с другой, более гетерогенной композицией.
[0547] T-клетки могут быть выделены напрямую, путем обогащения меченых клеток или путем элиминирования меченых клеток в однонаправленной процедуре мечения, или ненапрямую, в двухстадийной процедуре мечения. Согласно некоторым стратегиям обогащения согласно изобретению, T-клетки могут быть собраны в пакет для сбора клеток, а немеченые клетки (нецелевые клетки) - в пакет для отрицательной фракции. В отличие от стратегии обогащения согласно изобретению, немеченые клетки (клетки-мишени) собирают в пакет для сбора клеток, а меченые клетки (нецелевые клетки) собирают в пакет для отрицательной фракции или в пакет для нецелевых клеток соответственно. Селективные реагенты могут включать, без ограничения перечисленными, покрытые антителами сферы. Сферы, покрытые антителами, могут быть либо удалены до стадии модификации и/или экспансии, либо оставлены на клетках до стадии модификации и/или экспансии. Для выделения T-клеток могут использоваться один или более из следующих неограничивающих примеров клеточных маркеров: CD3, CD4, CD8, CD25, анти-биотин, CD1c, CD3/CD19, CD3/CD56, CD14, CD19, CD34, CD45RA, CD56, CD62L, CD133, CD137, CD271, CD304, IFN-гамма, TCR альфа/бета и/или их любая комбинация. Способы выделения T-клеток могут включать один или более реагентов, которые специфично связывают и/или детектируемо метят один или более из следующих неограничивающих примеров клеточных маркеров, которые могут использоваться для выделения T-клеток: CD3, CD4, CD8, CD25, анти-биотин, CD1c, CD3/CD19, CD3/CD56, CD14, CD19, CD34, CD45RA, CD56, CD62L, CD133, CD137, CD271, CD304, IFN-гамма, TCR альфа/бета и/или их любую комбинацию. Эти реагенты могут соответствовать или не соответствовать стандарту "Надлежащей производственной практики" ("GMP"). Реагенты могут включать, без ограничения, продукты Thermo DynaBeads и Miltenyi CliniMACS. Способы выделения T-клеток согласно изобретению могут включать множество повторов этапов мечения и/или выделения. В любой момент в способах выделения T-клеток согласно изобретению нежелательные клетки и/или нежелательные типы клеток могут быть элиминированы из композиции продукта T-клеток согласно изобретению путем положительного или отрицательного отбора нежелательных клеток и/или нежелательных типов клеток. Композиция T-клеточного продукта согласно изобретению может содержать дополнительные типы клеток, которые могут экспрессировать CD4, CD8 и/или другой T-клеточный маркер(ы).
[0548] Способы нуклеофекции T-клеток согласно изобретению могут исключать этап выделения T-клеток, например, благодаря процессу нуклеофекции T-клеток в популяции или композиции лейкоцитов/МКПК, который после нуклеофекции включает этап выделения или этап селективной экспансии посредством сигнализации TCR.
[0549] Некоторые популяции клеток могут быть элиминированы в результате положительного или отрицательного отбора до или после обогащения и/или сортировки T-клеток. Примеры клеточных композиций, которые могут быть элиминированы из композиции клеточного продукта, могут включать миелоидные клетки, CD25+ регуляторные T-клетки (T рег), дендритные клетки, макрофаги, эритроциты, тучные клетки, гамма-дельта T-клетки, естественные киллерные (NK) клетки, подобные естественным киллерам (NK) клетки (например, цитокин-индуцированные киллерные (CIK) клетки), индуцированные естественные киллерные (iNK) T-клетки, NK-T-клетки, B-клетки или их любую комбинацию.
[0550] Композиции T-клеточного продукта согласно изобретению могут включать CD4+ и CD8+ T-клетки. CD4+ и CD8+ T-клетки могут быть выделены в отдельные пакеты для сбора клеток во время процедуры выделения или отбора. CD4+ T-клетки и CD8+ T-клетки могут быть затем обработаны отдельно или обработаны после восстановления (объединения в той же композиции) в определенном соотношении.
[0551] Определенное соотношение, в котором CD4+ T-клетки и CD8+ T-клетки могут быть восстановлены, может зависеть от типа и эффективности используемой технологии экспансии, среды для клеток и/или условий роста клеток, используемых для экспансии композиций T-клеточного продукта. Примеры возможных отношений CD4+:CD8+ включают, без ограничения перечисленными, 50%:50%, 60%:40%, 40%:60% 75%:25% и 25%:75%.
[0552] CD8+ T-клетки демонстрируют мощную цитотоксическую способность против опухолевых клеток, тогда как CD4+ T-клетки обеспечивают многие из цитокинов, требуемые для поддержания пролиферативной способности и функции CD8+ T-клеток. Поскольку T-клетки, выделенные у здоровых доноров, преимущественно являются CD4+, композиции T-клеточного продукта искусственно корректируют in vitro по отношению CD4+:CD8+ для улучшения соотношение CD4+ T-клеток и CD8+ T-клеток, которые в противном случае присутствовали бы in vivo. Оптимизированное отношение также может использоваться для экспансии ex vivo композиции аутологичного T-клеточного продукта. С учетом искусственно скорректированного отношения CD4+:CD8+ в составе T-клеточного продукта важно отметить, что композиции продуктов согласно изобретению могут значительно отличаться и обеспечивать значительно большее преимущество, чем любая эндогенная популяция T-клеток.
[0553] Предпочтительные способы выделения T-клеток могут включать стратегию отрицательного отбора с получением незатронутых пан-T-клеток, что означает то, что получаемая композиция T-клеток включает T-клетки, которые не подвергались манипуляциям и которые содержат эндогенно существующее разнообразие/отношение T-клеток.
[0554] Реагенты, которые могут применяться для положительного или отрицательного отбора, включают, без ограничения перечисленными, магнитные сферы для разделения клеток. Магнитные сферы для разделения клеток могут быть или могут не быть удалены или элиминированы из отобранной популяции CD4+ T-клеток, CD8+ T-клеток или смешанной популяции CD4+ и CD8+ T-клеток перед выполнением следующего этапа в способе выделения T-клеток согласно изобретению.
[0555] Композиции T-клеток и композиции T-клеточного продукта могут быть подготовлены к криоконсервации, хранению в стандартной среде для культивирования T-клеток и/или к генетической модификации.
[0556] Композиции T-клеток, композиции T-клеточного продукта, композиции нестимулированных T-клеток, композиции покоящихся T-клеток или их любую часть могут криоконсервировать при использовании стандартного метода криоконсервации, оптимизированного для хранения и выделения человеческих клеток с высоким выходом, жизнеспособностью, фенотипом и/или функциональной способностью. Могут использоваться доступные в продаже среды и/или протоколы криоконсервации. Способы криоконсервации согласно изобретению могут включать не содержащий ДМСО криоконсервант (например, среду для криоконсервации без ДМСО CryoSOfreeTM), который уменьшает связанное с замораживанием токсическое воздействие.
[0557] Композиции T-клеток, композиции T-клеточного продукта, композиции нестимулированных T-клеток, композиции покоящихся T-клеток или их любую часть могут хранить в среде культивирования. Среды для культивирования T-клеток согласно изобретению могут быть оптимизированы для хранения клеток, генетической модификации клеток, фенотипа клеток и/или экспансии клеток. Среды для культивирования T-клеток согласно изобретению могут включать один или более антибиотиков. Поскольку добавление антибиотика в среду для культивирования клеток может снижать эффективность трансфекции и/или выход клеток после генетической модификации посредством нуклеофекции, определенные антибиотики (или их комбинации) и их соответствующая концентрация(и) могут быть изменены для оптимальной эффективности трансфекции и/или выхода клеток после генетической модификации посредством нуклеофекции.
[0558] Среды для культивирования T-клеток согласно изобретению могут включать сыворотку и, кроме того, состав и концентрация сыворотки могут быть изменены для оптимальных результатов получения клеток. Для культивирования T-клеток человеческая AB сыворотка предпочтительна по сравнению с FBS/FCS, потому что, несмотря на то, что она предусмотрена для применения в средах для культивирования T-клеток согласно изобретению, FBS/FCS может вводить ксено-белки. Сыворотка может быть выделена из крови индивида, для введения которому предназначена композиция T-клеток в культуре, таким образом, среда для культивирования T-клеток согласно изобретению может включать аутологичную сыворотку. Бессывороточные среды или заменитель сыворотки может также использоваться в средах для культивирования T-клеток согласно изобретению. В некоторых вариантах осуществления среды для культивирования T-клеток и способы согласно изобретению, бессывороточные среды или заменитель сыворотки могут обеспечивать преимущества по сравнению с добавлением среды с ксено-сывороткой, включающие, без ограничения перечисленными, получение более здоровых клеток, имеющих большую жизнеспособность, более высокую эффективность нуклеофекции, более высокую жизнеспособность после нуклеофекции, более предпочтительный фенотип клеток и/или большую/более быструю экспансию после применения технологий экспансии.
[0559] Среды для культивирования T-клеток могут включать доступные в продаже среды для выращивания клеток. Примерные доступные в продаже среды для выращивания клеток включают, без ограничения перечисленными, PBS, HBSS, OptiMEM, DMEM, RPMI 1640, AIM-V, X-VIVO 15, среду CellGro DC, среду CTS OpTimizer T Cell Expansion SFM, среду TexMACS, среду PRIME-XV T Cell Expansion Medium, среду ImmunoCult-XF T Cell Expansion Medium или их любую комбинацию.
[0560] Композиции T-клеток, композиции T-клеточного продукта, композиции нестимулированных T-клеток, композиции покоящихся T-клеток или их любая часть могут быть подготовлены к генетической модификации. Подготовка композиций T-клеток, композиций T-клеточного продукта, композиций нестимулированных T-клеток, композиций покоящихся T-клеток или их любой части к генетической модификации может включать промывку клеток и/или ресуспендирование в требуемом буфере для нуклеофекции. Криоконсервированные композиции T-клеток могут размораживать и подготавливать к генетической модификации путем нуклеофекции. Криоконсервированные клетки могут размораживать согласно стандартным или известным протоколам. Размораживание и подготовка криоконсервированных клеток может быть оптимизирована для получения клеток, имеющих более высокую жизнеспособность, с более высокой эффективностью нуклеофекции, демонстрирующих более высокую жизнеспособность после нуклеофекции, демонстрирующих более предпочтительный фенотип клеток и/или большую/более быструю экспансию после применения технологий экспансии. Например, Grifols Albutein (25% человеческий альбумин) может использоваться в процессе размораживания и/или подготовки.
Генетическая модификация композиции аутологичного T-клеточного продукта
[0561] Композиции T-клеток, композиции T-клеточного продукта, композиции нестимулированных T-клеток, композиции покоящихся T-клеток или любая их часть могут быть генетически модифицированы при использовании, например, стратегии нуклеофекции, такой как электропорация. Общее количество клеток, подвергаемых нуклеофекции, общий объем реакции нуклеофекции и точное время подготовки образца может быть оптимизировано для получения клеток, имеющих более высокую жизнеспособность, с более высокой эффективностью нуклеофекции, демонстрирующих более высокую жизнеспособность после нуклеофекции, демонстрирующих более предпочтительный фенотип клеток и/или большую/более быструю экспансию после применения технологий экспансии.
[0562] Нуклеофекция и/или электропорация могут быть выполнены с использованием, например, Lonza Amaxa, MaxCyte PulseAgile, Harvard Apparatus BTX и/или Invitrogen Neon. Системы с неметаллическими электродами, включающими, без ограничения, пластмассовые полимерные электроды, могут быть предпочтительными для нуклеофекции.
[0563] Перед генетической модификацией путем нуклеофекции композиции T-клеток, композиции T-клеточного продукта, композиции нестимулированных T-клеток, композиции покоящихся T-клеток или любую их часть могут ресуспендировать в буфере для нуклеофекции. Буферы для нуклеофекции согласно изобретению включают доступные в продаже буферы для нуклеофекции. Буферы для нуклеофекции согласно изобретению могут быть оптимизированы для получения клеток, которые обладают более высокой жизнеспособностью, с более высокой эффективностью нуклеофекции, демонстрируют более высокую жизнеспособность после нуклеофекции, демонстрируют более предпочтительный фенотип клеток и/или большую/более быструю экспансию после применения технологий экспансии. Буферы для нуклеофекции согласно изобретению могут включать, без ограничения перечисленными, PBS, HBSS, OptiMEM, BTXpress, Amaxa Nucleofector, буфер для нуклеофекции человеческих T-клеток и их любую комбинацию. Буферы для нуклеофекции согласно изобретению могут включать один или более дополнительных факторов для получения клеток, которые обладают более высокой жизнеспособностью, с более высокой эффективностью нуклеофекции, демонстрируют более высокую жизнеспособность после нуклеофекции, демонстрируют более предпочтительный фенотип клеток и/или большую/более быструю экспансию после применения технологий экспансии. Примеры дополнительных факторов включают, без ограничения перечисленными, рекомбинантные человеческие цитокины, хемокины, интерлейкины и их любую комбинацию. Примерные цитокины, хемокины и интерлейкины включают, без ограничения перечисленными, IL2, IL7, IL12, IL15, IL21, IL1, IL3, IL4, IL5, IL6, IL8, CXCL8, IL9, IL10, IL11, IL13, IL14, IL16, IL17, IL18, IL19, IL20, IL22, IL23, IL25, IL26, IL27, IL28, IL29, IL30, IL31, IL32, IL33, IL35, IL36, ГМ-КСФ, IFN-гамма, IL-1 альфа/IL-1F1, IL-1 бета/IL-1F2, IL-12 p70, IL-12/IL-35 p35, IL-13, IL-17/IL-17A, гетеродимер IL-17A/F, IL-17F, IL- 18/IL-1F4, IL-23, IL-24, IL-32, IL-32 бета, IL-32 гамма, IL-33, LAP (TGF-бета 1), лимфотоксин-альфа/ФНО-бета, TGF-бета, ФНО-альфа, TRANCE/TNFSF11/RANK L и их любую комбинацию. Примеры дополнительных факторов включают, без ограничения перечисленными, соли, минеральные вещества, метаболиты или их любую комбинацию. Типичные соли, минеральные вещества и метаболиты включают, без ограничения перечисленными, HEPES, никотинамид, гепарин, пируват натрия, L-глутамин, раствор незаменимых аминокислот MEM, аскорбиновую кислоту, нуклеозиды, FBS/FCS, человеческую сыворотку, заменитель сыворотки, антибиотики, регуляторы pH, соли Эрла, 2-меркаптоэтанол, человеческий трансферрин, рекомбинантный человеческий инсулин, человеческий сывороточный альбумин, добавку Nucleofector PLUS, KCL, MgCl2, Na2HPO4, NAH2PO4, лактобионат натрия, маннит, сукцинат натрия, хлорид натрия, CINa, глюкозу, Ca(NO3)2, трис/HCl, K2HPO4, KH2PO4, полиэтиленимин, полиэтиленгликоль, полоксамер 188, полоксамер 181, полоксамер 407, поливинилпирролидон, Pop313, Краун-5 и их любую комбинацию. Примерные дополнительные факторы включают, без ограничения перечисленными, такие среды, как PBS, HBSS, OptiMEM, DMEM, RPMI 1640, AIM-V, X-VIVO 15, среду CellGro DC, CTS OpTimizer T Cell Expansion SFM, среду TexMACS, среду PRIME-XV T Cell Expansion Medium, среду ImmunoCult-XF T Cell Expansion Medium и их любую комбинацию. Примерные дополнительные факторы включают, без ограничения перечисленными, ингибиторы чувствительности клеточной ДНК, метаболизма, дифференцировки, передачи сигналов, пути апоптоза и их комбинации. Примерные ингибиторы включают, без ограничения перечисленными, ингибиторы TLR9, MyD88, IRAK, TRAF6, TRAF3, IRF-7, NF-KB, интерферонов 1 типа, провоспалительных цитокинов, cGAS, STING, Sec5, TBK1, IRF-3, РНК-полимеразы III, RIG-1, IPS-1, FADD, RIP1, TRAF3, AIM2, ASC, каспазы 1, Pro-IL1B, PI3K, Akt, Wnt3A, ингибиторы киназы гликогенсинтазы 3β (GSK-3β) (например, TWS119), бафиломицин, хлорохин, хинакрин, AC-YVAD-CMK, Z-VAD-FMK, Z-IETD-FMK и их любую комбинацию. Примерные дополнительные факторы включают, без ограничения перечисленными, реагенты, которые модифицируют или стабилизируют одну или более нуклеиновых кислот таким образом, чтобы улучшать клеточную доставку, улучшать ядерную доставку или транспорт, улучшать облегченный транспорт нуклеиновой кислоты в ядро, улучшать деградацию эпихромосомной нуклеиновой кислоты и/или снижать ДНК-опосредованное токсическое действие. Примерные реагенты, которые модифицируют или стабилизируют одну или более нуклеиновых кислот, включают, без ограничения перечисленными, модификаторы pH, ДНК-связывающие белки, липиды, фосфолипиды, CaPO4, пептиды, связывающие ДНК с суммарным нейтральным зарядом, с NLS последовательностями или без них, фермент TREX1 и их любые комбинации.
[0564] Реагенты для транспозиции, включающие транспозон и транспозазу, могут быть добавлены к реакции нуклеофекции согласно изобретению до, одновременно или после добавления клеток в буфер для нуклеофекции (необязательно содержащийся во флаконе или кювете для реакции нуклеофекции). Транспозоны согласно изобретению могут включать плазмидную ДНК, линеаризованную плазмидную ДНК, продукт ПЦР, ДНК DOGGYBONETM, мРНК матрицу, одноцепочечную или двухцепочечную ДНК, комбинацию белка-нуклеиновой кислоты или их любую комбинацию. Транспозоны согласно изобретению могут включать одну или более последовательностей, которые кодируют один или более сайтов TTAA, один или более инвертированных терминальных повторов (ITR), один или более длинных терминальных повторов (LTR), один или более инсуляторов, один или более промоторов, один или более полноразмерных или усеченных генов, один или более сигналов поли(А), один или более сайтов расщепления саморасщепляющегося пептида 2А, один или более сайтов внутренней посадки рибосомы (IRES), один или более энхансеров, один или более регуляторов, одну или более точек начала репликации и их любую комбинацию.
[0565] Транспозоны согласно изобретению могут включать одну или более последовательностей, кодирующих один или более полноразмерных или усеченных генов. Полноразмерный и/или усеченный ген(ы), введенный с помощью транспозонов согласно изобретению, может кодировать один или более из сигнального пептида, VCAR, одноцепочечного вариабльного фрагмента (scFv), шарнирной области, трансмембранного домена, костимулирующего домена, химерного антигенного рецептора (CAR), VCAR, химерного T-клеточного рецептора (CAR-T или VCAR-T), рецептора, лиганда, цитокина, гена устойчивости к лекарственному средству, опухолевого антигена, алло- или аутоантигена, фермента, белка, пептида, полипептида, флуоресцентного белка, мутеина или их любую комбинацию.
[0566] Транспозоны согласно изобретению могут быть подготовлены в воде, TE, TBE, PBS, HBSS, средах, с добавкой фактора согласно изобретению или их любой комбинации.
[0567] Транспозоны согласно изобретению могут быть сконструированы для оптимизации клинической безопасности и/или улучшения процесса производства. В качестве неограничивающего примера транспозоны согласно изобретению могут быть сконструированы для оптимизации клинической безопасности и/или улучшения процесса производства путем устранения ненужных последовательностей или областей и/или включения неантибиотического селективного маркера. Транспозоны согласно изобретению могут соответствовать или могут не соответствовать стандарту GMP.
[0568] Ферменты транспозазы согласно изобретению могут кодироваться одной или более последовательностями плазмидной ДНК, мРНК, белка, комбинации белка-нуклеиновой кислоты или их любой комбинации.
[0569] Ферменты транспозазы согласно изобретению могут быть подготовлены в воде, TE, TBE, PBS, HBSS, среде, с добавкой фактора согласно изобретению или их любой комбинации. Ферменты транспозазы согласно изобретению или последовательности/конструкции, кодирующие их или обеспечивающие их доставку, могут соответствовать или могут не соответствовать стандарту GMP.
[0570] Транспозоны и фермент транспозазы согласно изобретению могут быть доставлены в клетку любым способом.
[0571] Хотя композиции и способы согласно изобретению включают доставку транспозона и/или транспозазы согласно изобретению в клетку при использовании плазмидной ДНК (пДНК), использование плазмиды для доставки может позволить интегрировать транспозон и/или транспозазу в хромосомную ДНК клетки, что может привести к долговременной экспрессии транспозазы. Таким образом, транспозон и/или ферменты транспозазы согласно изобретению могут быть доставлены в клетку либо в виде мРНК, либо белка, чтобы исключить любую вероятность хромосомной интеграции.
[0572] Транспозоны и транспозазы согласно изобретению могут предварительно инкубировать отдельно или в комбинации друг с другом до введения транспозона и/или транспозазы в реакцию нуклеофекции. Абсолютные количества каждого транспозона и транспозазы, а также относительные количества, например, отношение транспозона к транспозаза, могут быть оптимизированы.
[0573] После подготовки реакции нуклеофекции, необязательно во флаконе или кювете, реакция может быть введена в прибор нуклеофектор и активирована для доставки электрического импульса согласно протоколу производителя. Условия электрического импульса, используемые для доставки транспозона и/или транспозазы согласно изобретению (или последовательности, кодирующей транспозон и/или транспозазу согласно изобретению) в клетку, могут быть оптимизированы для получения клеток с улучшенной жизнеспособностью, улучшенной эффективностью нуклеофекции, более высокой жизнеспособностью после нуклеофекции, предпочтительным фенотипом клеток и/или большей/более быстрой экспансией после применения технологий экспансии. При использовании технологии нуклеофекции Amaxa рассматривается каждая из различных программ нуклеофекции для нуклеофектора Amaxa 2B или 4D.
[0574] После реакции нуклеофекции согласно изобретению клетки могут осторожно добавлять в среду для клеток. Например, когда T-клетки подвергаются реакции нуклеофекции, T-клетки могут добавлять в среду для T-клеток. Среды для клеток после нуклеофекции согласно изобретению могут включать одну или более сред, доступных в продаже. Среды для клеток после нуклеофекции согласно изобретению (в том числе среды для T-клеток после нуклеофекции согласно изобретению) могут быть оптимизированы для получения клеток с более высокой жизнеспособностью, более высокой эффективностью нуклеофекции, демонстрирующих более высокую жизнеспособность после нуклеофекции, демонстрирующих более предпочтительный фенотип клеток и/или большую/более быструю экспансию после применения технологий экспансии. Среды для клеток после нуклеофекции согласно изобретению (включая среды для T-клеток после нуклеофекции согласно изобретению) могут включать PBS, HBSS, OptiMEM, DMEM, RPMI 1640, AIM-V, X-VIVO 15, среду CellGro DC, среду CTS OpTimizer T Cell Expansion SFM, среду TexMACS, среду PRIME-XV T Cell Expansion Medium, среду ImmunoCult-XF T Cell Expansion Medium и их любую комбинацию. Среды для клеток после нуклеофекции согласно изобретению (включая среды для T-клеток после нуклеофекции согласно изобретению) могут включать один или более дополнительных факторов согласно изобретению для улучшения жизнеспособности, эффективности нуклеофекции, жизнеспособности после нуклеофекции, фенотипа клеток и/или большей/более быстрой экспансии после применения технологий экспансии. Примерные дополнительные факторы включают, без ограничения перечисленными, рекомбинантные человеческие цитокины, хемокины, интерлейкины и их любую комбинацию. Примерные цитокины, хемокины и интерлейкины включают, без ограничения перечисленными, IL2, IL7, IL12, IL15, IL21, IL1, IL3, IL4, IL5, IL6, IL8, CXCL8, IL9, IL10, IL11, IL13, IL14, IL16, IL17, IL18, IL19, IL20, IL22, IL23, IL25, IL26, IL27, IL28, IL29, IL30, IL31, IL32, IL33, IL35, IL36, GM-CSF, IFN-гамма, IL-1 альфа/IL- 1F1, IL-1 бета/IL-1F2, IL-12 p70, IL-12/IL-35 p35, IL-13, IL-17/IL-17A, гетеродимер IL-17A/F, IL-17F, IL-18/IL-1F4, IL-23, IL-24, IL-32, IL-32 бета, IL-32 гамма, IL-33, LAP (TGF-бета 1), лимфотоксин-альфа/ФНО-бета, TGF-бета, ФНО-альфа, TRANCE/TNFSF11/RANK L и их любую комбинацию. Примерные дополнительные факторы включают, без ограничения перечисленными, соли, минеральные вещества, метаболиты или их любую комбинацию. Примерные соли, минеральные вещества и метаболиты включают, без ограничения перечисленными, HEPES, никотинамид, гепарин, пируват натрия, L-глутамин, раствор незаменимых аминокислот MEM, аскорбиновую кислоту, нуклеозиды, FBS/FCS, человеческую сыворотку, заменитель сыворотки, антибиотики, регуляторы pH, соли Эрла, 2-меркаптоэтанол, человеческий трансферрин, рекомбинантный человеческий инсулин, человеческий сывороточный альбумин, добавку Nucleofector PLUS, KCl, MgCl2, Na2HPO4, NAH2PO4, лактобионат натрия, маннит, сукцинат натрия, хлорид натрия, CINa, глюкозу, Ca(NO3)2, трис/HCl, K2HPO4, KH2PO4, полиэтиленимин, полиэтиленгликоль, полоксамер 188, полоксамер 181, полоксамер 407, поливинилпирролидон, Pop313, Краун-5 и их любую комбинацию. Примерные дополнительные факторы включают, без ограничения перечисленными, такие среды, как PBS, HBSS, OptiMEM, DMEM, RPMI 1640, AIM-V, X-VIVO 15, среду CellGro DC, CTS OpTimizer T Cell Expansion SFM, среду TexMACS, среду PRIME-XV T Cell Expansion Medium, среду ImmunoCult-XF T Cell Expansion Medium и их любую комбинацию. Примерные дополнительные факторы включают, без ограничения перечисленными, ингибиторы чувствительности клеточной ДНК, метаболизма, дифференцировки, передачи сигналов, пути апоптоза и их комбинацию. Примерные ингибиторы включают, без ограничения перечисленными, ингибиторы TLR9, MyD88, IRAK, TRAF6, TRAF3, IRF-7, NF-KB, интерферонов 1 типа, провоспалительных цитокинов, cGAS, STING, Sec5, TBK1, IRF-3, РНК-полимеразы III, RIG-1, IPS-1, FADD, RIP1, TRAF3, AIM2, ASC, Caspase1, Pro-IL1B, PI3K, Akt, Wnt3A, ингибиторы киназы гликогенсинтазы 3β (GSK-3β) (например, TWS119), бафиломицин, хлорохин, хинакрин, AC-YVAD-CMK, Z-VAD-FMK, Z-IETD-FMK и их любую комбинацию. Примерные дополнительные факторы включают, без ограничения перечисленными, реагенты, которые модифицируют или стабилизируют одну или более нуклеиновых кислот таким образом, чтобы улучшать клеточную доставку, улучшать ядерную доставку или транспорт, улучшать облегченный транспорт нуклеиновой кислоты в ядро, улучшать деградацию эпихромосомной нуклеиновой кислоты и/или снижение ДНК-опосредованного токсического действия. Примерные реагенты, которые модифицируют или стабилизируют одну или более нуклеиновых кислот, включают, без ограничения перечисленными, модификаторы pH, ДНК-связывающие белки, липиды, фосфолипиды, CaPO4, пептиды, связывающие ДНК с суммарным нейтральным зарядом, с последовательностями NLS или без них, фермент TREX1 и их любые комбинация.
[0575] Среды для клеток после нуклеофекции согласно изобретению (включая среды для T-клеток после нуклеофекции согласно изобретению) могут использоваться при комнатной температуре или предварительно нагретыми, например до температуры от 32°C до 37°C, включая конечные значения. Среды для клеток после нуклеофекции согласно изобретению (включая среды для T-клеток после нуклеофекции согласно изобретению) могут быть предварительно нагреты до любой температуры, которая поддерживает или улучшает жизнеспособность клеток и/или экспрессию транспозона или его части согласно изобретению.
[0576] Среды для клеток после нуклеофекции согласно изобретению (включая среды для T-клеток после нуклеофекции согласно изобретению) могут содержаться во флаконах или чашках для культур тканей, флаконах G-Rex, биореакторе или мешках для культур клеток или в любой другой стандартной емкости. Культуры клеток после нуклеофекции согласно изобретению (включая культуры T-клеток после нуклеофекции согласно изобретению) могут поддерживать без перемешивания или, в альтернативе, их можно перемешивать (например, качать, вращать или встряхивать).
[0577] Культуры клеток после нуклеофекции могут включать генетически модифицированные клетки. Культуры T-клеток после нуклеофекции могут включать генетически модифицированные T-клетки. Генетически модифицированные клетки согласно изобретению могут либо покоиться в течение некоторого периода времени, либо подвергаться стимуляции для экспансии, например, с применением технологии T Cell Expander. В некоторых вариантах осуществления генетически модифицированные клетки согласно изобретению могут либо покоиться в течение некоторого промежутка времени, либо подвергаться немедленной стимуляции для экспансии, например, с применением технологии T Cell Expander. Генетически модифицированные клетки согласно изобретению могут быть покоящимися, чтобы дать им достаточное время для акклиматизации, время для осуществления транспозиции и/или время для положительного или отрицательного отбора, с получением в результате клеток с улучшенной жизнеспособностью, более высокой эффективностью нуклеофекции, более высокой жизнеспособностью после нуклеофекции, предпочтительным фенотипом клеток и/или большей/более быстрой экспансией после применения технологий экспансии. Генетически модифицированные клетки согласно изобретению могут покоиться, например, в течение 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или более часов. В некоторых вариантах осуществления генетически модифицированные клетки согласно изобретению могут покоиться, например, в течение ночи. В некоторых аспектах период в течение ночи составляет приблизительно 12 часов. Генетически модифицированные клетки согласно изобретению могут покоиться, например, в течение 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или более дней.
[0578] Генетически модифицированные клетки согласно изобретению могут подвергать отбору после реакции нуклеофекции и перед применением технологии Expander. Для оптимального отбора генетически модифицированных клеток клеткам могут позволять покоиться в среде клеток после нуклеофекции в течение по меньшей мере 2-14 дней, чтобы облегчить идентификацию модифицированных клеток (например, отличать модифицированные клетки от немодифицированных клеток).
[0579] Уже через 24 часа после нуклеофекции экспрессия CAR/VCAR и селективный маркер согласно изобретению могут быть обнаружены в модифицированных T-клетках после успешной нуклеофекции транспозона согласно изобретению. Из-за эпихромосомной экспрессии транспозона, экспрессия одного селективного маркера может не позволить отличить модифицированные T-клетки (клетки, в которые был успешно интегрирован транспозон) от немодифицированных T-клеток (клеток, в которые транспозон не был успешно интегрирован). Если эпихромосомная экспрессия транспозона маскирует обнаружение модифицированных клеток по селективному маркеру, клетки с нуклеофекцией (как модифицированные, так и немодифицированные клетки) могут покоиться в течение некоторого периода времени (например, 2-14 дней), чтобы позволить клеткам прекратить экспрессию или потерять всю эпихромосомную экспрессию транспозона. После этого увеличенного периода покоя только модифицированные T-клетки должны оставаться положительными по экспрессии селективного маркера. Длительность такого увеличенного периода покоя может быть оптимизирована для каждой реакции нуклеофекции и процесса отбора. Если эпихромосомная экспрессия транспозона маскирует обнаружение модифицированных клеток по селективному маркеру, отбор может быть проведен без такого увеличенного периода покоя, однако дополнительный этап отбора может быть включен в более поздний момент (например, во время или после этапа экспансии).
[0580] Отбор генетически модифицированных клеток согласно изобретению может быть выполнен любым способом. В некоторых вариантах осуществления способов согласно изобретению отбор генетически модифицированных клеток согласно изобретению может быть выполнен путем выделения клеток, экспрессирующих специфический селективный маркер. Селективные маркеры согласно изобретению могут кодироваться одной или более последовательностями в транспозоне. Селективные маркеры согласно изобретению могут экспрессироваться модифицированной клеткой в результате успешной транспозиции (то есть не кодироваться одной или более последовательностями в транспозоне). В некоторых вариантах осуществления генетически модифицированные клетки согласно изобретению содержат селективный маркер, который придает устойчивость к токсичному соединению в среде для клеток после нуклеофекции. Токсичное соединение может включать, например, антибиотик или лекарственное средство, которое при отсутствии устойчивости, придаваемой селективным маркером модифицированным клеткам, может вызывать гибель клеток. Примерные селективные маркеры включают, без ограничения перечисленными, дикий тип (WT) или мутантные формы одного или более из следующих генов: neo, DHFR, TYMS, ALDH, MDR1, MGMT, FANCF, RAD51C, GCS и NKX2.2. Примерные селективные маркеры включают, без ограничения перечисленными, поверхностно-экспрессируемый селективный маркер или поверхностно-экспрессируемую метку, которые могут служить в качестве мишеней в технологии с применением покрытых Ат магнитных сфер или колоночного отбора, соответственно. Расщепляемая метка, такая как метки, используемые при очистке белков, может быть добавлена к селективному маркеру согласно изобретению для эффективного отбора, промывки и элюирования с колонки. В некоторых вариантах осуществления селективные маркеры согласно изобретению не экспрессируются модифицированными клетками (включая модифицированные T-клетки) эндогенно и, следовательно, могут применяться при физическом выделении модифицированных клеток (например, с помощью методов сортировки клеток). Примерные селективные маркеры согласно изобретению не экспрессируются модифицированными клетками (включая модифицированные T-клетки), эндогенно, но не ограничиваются полноразмерными, мутантными или усеченными формами CD271, CD19, CD52, CD34, RQR8, CD22, CD20, CD33 и любой их комбинацией.
[0581] Генетически модифицированные клетки согласно изобретению могут быть селективно размножены после реакции нуклеофекции. В некоторых вариантах осуществления модифицированные T-клетки, включающие VCAR, могут быть селективно размножены путем стимуляции VCAR. Модифицированные T-клетки, включающие VCAR, могут быть стимулированы при контакте с покрытым мишенью реагентом (например, линией опухолевых или линией нормальных клеток, экспрессирующих мишень, или сферами-экспандерами, покрытыми мишенью). В альтернативе модифицированные T-клетки, включающие VCAR, могут быть стимулированы при контакте с облученной опухолевой клеткой, облученной аллогенной нормальной клеткой, облученной аутологичной МКПК. Чтобы свести к минимуму контаминацию композиций клеточного продукта согласно изобретению экспрессирующей мишень клеткой, используемой для стимуляции, например, когда композицию клеточного продукта могут вводить непосредственно индивиду, стимуляцию могут проводить с использованием сфер-экспандеров, покрытых белком-мишенью VCAR. Селективная экспансия модифицированных T-клеток, включающих VCAR, путем стимуляции VCAR может быть оптимизирована для исключения функционального истощения модифицированных T-клеток.
[0582] Отобранные генетически модифицированные клетки согласно изобретению могут быть криоконсервированы, покоиться в течение некоторого периода времени или стимулированы для размножения с применением технологии Cell Expander. Отобранные генетически модифицированные клетки согласно изобретению могут подвергаться криоконсервации, покоиться в течение определенного периода времени или сразу подвергаться стимуляции для экспансии с применением технологии Cell Expander. Если отобранные генетически модифицированные клетки являются T-клетками, T-клетки могут стимулировать для экспансии с применением технологии T-Cell Expander. Отобранные генетически модифицированные клетки согласно изобретению могут покоиться, например, в течение 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или более часов. В некоторых вариантах осуществления отобранные генетически модифицированные клетки согласно изобретению могут покоиться, например, в течение ночи. В некоторых аспектах период в течение ночи составляет около 12 часов. Отобранные генетически модифицированные клетки согласно изобретению могут покоиться, например, в течение 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или более дней. Отобранные генетически модифицированные клетки согласно изобретению могут находиться в состоянии покоя в течение любого периода времени, что приводит к получению клеток с повышенной жизнеспособностью, более высокой эффективностью нуклеофекции, более высокой жизнеспособностью после нуклеофекции, с предпочтительным фенотипом клеток и/или большей/более быстрой экспансией после применения технологий экспансии.
[0583] Отобранные генетически модифицированные клетки (включая отобранные генетически модифицированные T-клетки согласно изобретению) могут быть криоконсервированы с применением любого стандартного метода криоконсервации, который может быть оптимизирован для хранения и/или выделения человеческих клеток с высоким выходом, жизнеспособностью, фенотипом и/или функциональной способностью. Способы криоконсервации согласно изобретению могут включать коммерческие среды и/или протоколы криоконсервации.
[0584] Эффективность транспозиции отобранных генетически модифицированных клеток (включая отобранные генетически модифицированные T-клетки согласно изобретению) может быть оценена любым способом. Например, до применения технологии Expander экспрессия транспозона отобранными генетически модифицированными клетками (включая отобранные генетически модифицированные T-клетки согласно изобретению) может быть измерена с помощью сортировки клеток с активированной флуоресценцией (FACS). Определение эффективности транспозиции отобранных генетически модифицированных клеток (включая отобранные генетически модифицированные T-клетки согласно изобретению) может включать определение процента отобранных клеток, экспрессирующих транспозон (например, VCAR). В альтернативе или в дополнение, чистота T-клеток, средняя интенсивность флуоресценции (MFI) экспрессии транспозона (например, экспрессии CAR), способность VCAR (доставленного в транспозоне) опосредовать дегрануляцию и/или киллинг клетки-мишени, экспрессирующей лиганд VCAR, и/или фенотип отобранных генетически модифицированных клеток (включая отобранные генетически модифицированные T-клетки согласно изобретению) могут оценивать любым способом.
[0585] Композиции клеточного продукта согласно изобретению могут быть выпущены для введения индивиду при соответствии некоторым критериям выпуска. Примерные критерии выпуска могут включать, без ограничения перечисленными, конкретный процент модифицированных, отобранных и/или размноженных T-клеток, экспрессирующих поддающиеся обнаружению уровни VCAR на поверхности клеток.
Генетическая модификация композиции аутологичного T-клеточного продукта
[0586] Генетически модифицированные клетки (включая генетически модифицированные T-клетки) согласно изобретению могут быть размножены с применением технологии Expander. Технологии Expander согласно изобретению могут включать коммерческую технологию Expander. Примерные технологии Expander согласно изобретению включают стимуляцию генетически модифицированной T-клетки согласно изобретению посредством TCR. Хотя рассматриваются все способы стимуляции генетически модифицированных T-клеток согласно изобретению, стимуляция генетически модифицированных T-клеток согласно изобретению посредством TCR является предпочтительным способом, дающим продукт с превосходным уровнем цитотоксической способности.
[0587] Чтобы стимулировать генетически модифицированную T-клетку согласно изобретению посредством TCR, можно использовать сферы Thermo Expander DynaBeads при соотношении сфер к T-клеткам 3:1. Если сферы Expander не являются биоразлагаемыми, сферы могут быть удалены из композиции Expander. Например, сферы могут быть удалены из композиции Expander приблизительно через 5 дней. Для стимуляции генетически модифицированных T-клеток согласно изобретению посредством TCR может использоваться реагент для активации/экспансии T-клеток Miltenyi. Для стимуляции генетически модифицированных T-клеток согласно изобретению посредством TCR может использоваться реагент StemCell Technologies ImmunoCult для активации CD3/CD28 или CD3/CD28/CD2 T-клеток человека. Эта технология может быть предпочтительной, поскольку растворимые комплексы тетрамерных антител разрушаются через некоторое время и не требуют удаления из процесса.
[0588] Искусственные антигенпрезентирующие клетки (АПК) могут быть сконструированы для коэкспрессии антигена-мишени и могут использоваться для стимуляции клетки или T-клетки согласно изобретению посредством TCR и/или VCAR согласно изобретению. Искусственные АПК могут включать или могут быть получены из линии опухолевых клеток (включая, например, иммортализованную линию миелогенного лейкоза K562) и могут быть сконструированы для коэкспрессии множества костимулирующих молекул или технологий (таких как CD28, 4-1BBL, CD64, mbIL-21, mbIL-15, молекула-мишень CAR и т.д.). При объединении искусственных АПК согласно изобретению с костимулирующими молекулами, условия могут быть оптимизированы для предотвращения развития или появления нежелательного фенотипа и функциональной способности, а именно терминально-дифференцированных эффекторных T-клеток.
[0589] Облученные МКПК (ауто или алло) могут экспрессировать некоторые антигены-мишени, такие как CD19, и могут использоваться для стимуляции клетки или T-клетки согласно изобретению посредством TCR и/или VCAR согласно изобретению. В альтернативе или дополнительно, облученные опухолевые клетки могут экспрессировать некоторые антигены-мишени и могут использоваться для стимуляции клетки или T-клетки согласно изобретению посредством TCR и/или VCAR согласно изобретению.
[0590] Иммобилизованные и/или растворимые антитела против CD3, против CD2 и/или против CD28 могут использоваться для стимуляции клетки или T-клетки согласно изобретению посредством TCR и/или VCAR согласно изобретению.
[0591] Покрытые антигеном сферы могут экспонировать белок-мишень и могут использоваться для стимуляции клетки или T-клетки согласно изобретению посредством TCR и/или VCAR согласно изобретению. В альтернативе или дополнительно, сферы Expander, покрытые белком-мишенью VCAR, могут использоваться для стимуляции клетки или T-клетки согласно изобретению посредством TCR и/или VCAR согласно изобретению.
[0592] Способы экспансии созданы для стимуляции клетки или T-клетки согласно изобретению посредством TCR или VCAR и посредством поверхностно экспрессируемых CD2, CD3, CD28, 4-1BB, и/или других маркеров на генетически модифицированных T-клетках.
[0593] Технология экспансии может быть применена к клетке согласно изобретению сразу после нуклеофекции или до приблизительно 24 часов после нуклеофекции. Хотя различные среды для клеток могут использоваться во время процедуры экспансии, предпочтительная среда для экспансии T-клеток согласно изобретению может давать клетки, например, с более высокой жизнеспособностью, фенотипом клеток, полной экспансией или более высокой способностью к in vivo персистированию, приживлению и/или CAR-опосредованному киллингу. Среда для клеток согласно изобретению может быть оптимизирована для улучшения/усиления экспансии, фенотипа и функции генетически модифицированных клеток согласно изобретению. Предпочтительный фенотип размноженных T-клеток может включать смесь стволовых T-клеток памяти, T-клеток центральной памяти и эффекторных T-клеток памяти. Сферы Dynabeads Expander могут давать в основном T-клетки центральной памяти, что может привести к превосходным результатам в клинических условиях.
[0594] Примерная среда для экспансии T-клеток согласно изобретению может включать, частично или полностью, PBS, HBSS, OptiMEM, DMEM, RPMI 1640, AIM-V, X-VIVO 15, среду CellGro DC, CTS OpTimizer T Cell Expansion SFM, среду TexMACS, среду PRIME-XV T Cell Expansion Medium, среду ImmunoCult-XF T Cell Expansion Medium или их любую комбинацию. Среда для экспансии T-клеток согласно изобретению может дополнительно включать один или более дополнительных факторов. Дополнительные факторы, которые могут быть включены в среду для экспансии T-клеток согласно изобретению, улушают жизнеспособность, фенотип клеток, общую экспансию или повышают способность к in vivo персистированию, приживлению и/или VCAR-опосредованному киллингу. Дополнительные факторы, которые могут быть включены в среду для экспансии T-клеток согласно изобретению, включают, без ограничения перечисленными, рекомбинантные человеческие цитокины, хемокины и/или интерлейкины, такие как IL2, IL7, IL12, IL15, IL21, IL1, IL3, IL4 , IL5, IL6, IL8, CXCL8, IL9, IL10, IL11, IL13, IL14, IL16, IL17, IL18, IL19, IL20, IL22, IL23, IL25, IL26, IL27, IL28, IL29, IL30, IL31, IL32, IL33 , IL35, IL36, ГМ-КСФ, IFN-гамма, IL-1 альфа/IL-1F1, IL-1 бета/IL-1F2, IL-12 p70, IL-12/IL-35 p35, IL-13, IL -17/IL-17A, гетеродимер IL-17A/F, IL-17F, IL-18/IL-1F4, IL-23, IL-24, IL-32, IL-32 бета, IL-32 гамма, IL-33, LAP (TGF-бета 1), лимфотоксин-альфа/ФНО-бета, TGF-бета, ФНО-альфа, TRANCE/TNFSF11/RANK L или их любую комбинацию. Дополнительные факторы, которые могут быть включены в среду для экспансии T-клеток согласно изобретению, включают, без ограничения перечисленными, соли, минеральные вещества и/или метаболиты, такие как HEPES, никотинамид, гепарин, пируват натрия, L-глутамин, раствор заменимых аминокислот MEM, аскорбиновую кислоту, нуклеозиды, FBS/FCS, человеческую сыворотку, заменитель сыворотки, антибиотики, регуляторы pH, соли Эрла, 2-меркаптоэтанол, человеческий трансферрин, рекомбинантный человеческий инсулин, человеческий сывороточный альбумин, добавку Nucleofector PLUS, KCl, MgCl2, Na2HPO4, NAH2PO4, лактобионат натрия, маннит, сукцинат натрия, хлорид натрия, CINa, глюкозу, Ca(NO3)2, трис/HCl, K2HPO4, KH2PO4, полиэтиленимин, полиэтиленгликоль, Полоксамер 188, Полоксамер 181, Полоксамер 407, Поливинилпирролидон, Pop313, Краун-5 или их любую комбинацию. Дополнительные факторы, которые могут быть включены в среду для экспансии T-клеток согласно изобретению, включают, без ограничения перечисленными, ингибиторы чувствительности клеточной ДНК, метаболизма, дифференцировки, передачи сигналов и/или пути апоптоза, такие как ингибиторы TLR9, MyD88, ИРАК, TRAF6, TRAF3, IRF-7, NF-KB, интерферонов 1 типа, провоспалительных цитокинов, cGAS, STING, Sec5, TBK1, IRF-3, РНК-полимеразы III, RIG-1, IPS-1, FADD, RIP1, TRAF3, AIM2, ASC, каспазы 1, Pro-IL1B, PI3K, Akt, Wnt3A, ингибиторы киназы гликогенсинтазы 3β (GSK-3β) (например, TWS119), бафиломицин, хлорохин, хинакрин, AC-YVAD-CMK, Z-VAD-FMK, Z-IETD-FMK или их любую комбинацию.
[0595] Дополнительные факторы, которые могут быть включены в среду для экспансии T-клеток согласно изобретению, включают, без ограничения перечисленными, реагенты, которые модифицируют или стабилизируют нуклеиновые кислоты таким образом, чтобы улучшать клеточную доставку, улучшать ядерную доставку или транспорт, улучшать облегченный транспорт нуклеиновой кислоты в ядро клетки, усиливать деградацию эпихромосомной нуклеиновой кислоты и/или снижать ДНК-опосредованную токсичность, такие как модификаторы pH, ДНК-связывающие белки, липиды, фосфолипиды, CaPO4, пептиды, связывающие ДНК с суммарным нейтральным зарядом, с последовательностями NLS или без них, фермент TREX1 или их любую комбинацию.
[0596] Генетически модифицированные клетки согласно изобретению могут быть отобраны во время процесса экспансии при использовании селективных лекарственных средств или соединений. Например, в некоторых вариантах осуществления, когда транспозон согласно изобретению может кодировать селективный маркер, который придает генетически модифицированным клеткам устойчивость к лекарственному средству, добавляемому в среду культивирования, отбор может происходить во время процесса экспансии и может потребовать, чтобы для отбора прошли приблизительно 1-14 дней в культуре. Примеры генов устойчивости к лекарственным средствам, которые могут использоваться в качестве селективных маркеров, кодируемых транспозоном согласно изобретению, включают, без ограничения перечисленными, дикий тип (WT) или мутантные формы генов neo, DHFR, TYMS, ALDH, MDR1, MGMT, FANCF, RAD51C, GCS, NKX2.2 или их любую комбинацию. Примеры соответствующих лекарственных средств или соединений, которые могут добавлять в среду культивирования, к которым может придавать устойчивость селективный маркер, включают, без ограничения перечисленными, G418, Пуромицин, Ампициллин, Канамицин, Метотрексат, Мелфалан, Темозоламид, Винкристин, Этопозид, Доксорубицин, Бендамустин, Флударабин, Аредиа (Памидронат Динатрия), Беценум (Кармустин), BiCNU (Кармустин), Бортезомиб, Карфилзомиб, Кармубрис (Кармустин), Кармустин, Клафен (Циклофосфамид), Циклофосфамид, Цитоксан (Циклофосфамид), Даратумумаб, Дарзалекс (Даратумумаб), Доксил (липосомальный Доксорубицина Гидрохлорид), липосомальный Доксорубицина Гидрохлорид, Dox-SL (липосомальный Доксорубицина Гидрохлорид), Элотузумаб, Эмплисити (Элотузумаб), Эвацет (липосомальный Доксорубицина Гидрохлорид), Фаридак (Панобиностат), Иксазомиба Цитрат, Кипролис (Карфилзомиб), Леналидомид, Липодокс (липосомальный Доксорубицина Гидрохлорид), Мозобил (Плериксафор), Неосар (Циклофосфамид), Нинларо (Иксазомиба Цитрат), Памидронат Динатрия, Панобиностат, Плериксафор, Помалидомид, Помалист (Помалидомид), Ревлимид (Леналидомид), Синовир (Талидомид), Талидомид, Таломид (Талидомид), Велкейд (Бортезомиб), Золедроновую кислоту, Зомета (Золедроновую кислоту) или их любую комбинацию.
[0597] Процесс экспансии T-клеток согласно изобретению может проходить в мешке для культуры клеток в Биореакторе WAVE, флаконе G-Rex или в любом другом подходящем контейнере и/или реакторе.
[0598] Культуру клеток или T-клеток согласно изобретению могут поддерживать стационарно, с качанием, вращением или встряхиванием.
[0599] Процесс экспансии клеток или T-клеток согласно изобретению может оптимизировать некоторые условия, включающие, без ограничения перечисленными, продолжительность культивирования, концентрацию клеток, график добавления/удаления среды для T-клеток, размер клеток, общее количество клеток, фенотип клеток, чистоту популяции клеток, процент генетически модифицированных клеток в растущей популяции клеток, использование и состав добавок, добавление/удаление технологий Expander или их любую комбинацию.
[0600] Процесс экспансии клеток или T-клеток согласно изобретению могут продолжать до заданного конечного показателя перед изготовлением состава готовой размноженной популяции клеток. Например, процесс экспансии клеток или T-клеток согласно изобретению может продолжаться в течение заданного периода времени: по меньшей мере 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24 часа; по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 дней; по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 недель; по меньшей мере 1, 2, 3, 4, 5, 6 месяцев или по меньшей мере 1 год. Процесс экспансии клеток или T-клеток согласно изобретению может продолжаться до тех пор, пока полученная культура не достигнет заданной общей плотности клеток: 1, 10, 100, 1000, 104, 105, 106, 107, 108, 109, 1010 клеток на объем (мкл, мл, л) или любой плотности между указанными значениями. Процесс экспансии клеток или T-клеток по изобретению может продолжаться до тех пор, пока генетически модифицированные клетки полученной культуры не продемонстрируют заданный уровень экспрессии транспозона согласно изобретению: 1%, 10%, 20%, 30%, 40%. 50%, 60%, 70%, 80%, 90% или 100% или любой процент между пороговым уровнем экспрессии (минимальный, максимальный или средний уровень экспрессии, указывающий на то, что полученные генетически модифицированные клетки являются клинически эффективными). Процесс экспансии клеток или T-клеток согласно изобретению может продолжаться до тех пор, пока доля генетически модифицированных клеток в полученной культуре и доля немодифицированных клеток не достигнет заданного порогового значения, составляющего по меньшей мере 1:10, 1: 9, 1:8, 1:7, 1:6, 1:5, 1:4, 1:3, 1:2, 1:1, 2:1, 2:1, 4:1, 5:1, 6:1, 7:1, 8:1, 9:1, 10:1, или любого другого отношения.
Анализ генетически модифицированных аутологичных T-клеток для выпуска
[0601] Процент генетически модифицированных клеток могут оценивать во время или после процесса экспансии согласно изобретению. Клеточная экспрессия транспозона генетически модифицированной клеткой согласно изобретению может быть измерена с помощью сортировки флуоресцентно активированных клеток (FACS). Например, FACS может использоваться для определения процента клеток или T-клеток, экспрессирующих VCAR согласно изобретению. В альтернативе или дополнительно, могут быть оценены чистота генетически модифицированных клеток или T-клеток, средняя интенсивность флуоресценции (MFI) VCAR, экспрессируемого генетически модифицированной клеткой или T-клеткой согласно изобретению, способность VCAR опосредовать дегрануляцию и/или киллинг клетки-мишени, экспрессирующей лиганд VCAR, и/или фенотип VCAR+ T-клеток.
[0602] Композиции согласно изобретению, предназначенные для введения индивиду, могут требовать соответствия одному или более "критериям выпуска", указывающим, что композиция является безопасной и эффективной для изготовления в форме фармацевтического продукта и/или введения индивиду. Критерии выпуска могут включать требование, чтобы композиция согласно изобретению (например, T-клеточный продукт согласно изобретению) включала опредленный процент T-клеток, экспрессирующих поддающиеся обнаружению уровни VCAR согласно изобретению на своей клеточной поверхности.
[0603] Процесс экспансии следует продолжать, пока не будет выполнено условие соответствия определенному критерию (например, достигнуто некоторое общее количество клеток, получена определенная популяция клеток памяти, получена популяция определенного размера).
[0604] Определенный критерий указывает на момент, в которой процесс экспансии нужно закончить. Например, клетки должны быть включены в состав, реактивированы или криоконсервированы, как только они достигнут клеточного размера 300 фл (в ином случае клетки, достигающие размера выше этой границы, могут начать погибать). Криоконсервация сразу же после того, как популяция клеток достигает среднего размера клеток меньше 300 фл, может привести к лучшему выходу клеток после размораживания и культивирования, поскольку клетки еще не достигли полностью покоящегося состояния до криоконсервации (размер полностью покоящихся клеток составляет приблизительно 180 фл). Перед экспансией T-клетки согласно изобретению могут иметь размер приблизительно 180 фл, но могут больше чем в четыре раза увеличивать свой размер до приблизительно 900 мкл через 3 дня после экспансии. В течение следующих 6-12 дней популяция T-клеток будет медленно уменьшать размер клеток до полного покоя при 180 фл.
[0605] Процесс получения клеточной популяции для изготовления состава может включать, без ограничения перечисленными, этапы концентрирования клеток клеточной популяции, промывания клеток и/или дополнительного отбора клеток посредством устойчивости в лекарственному средству или сортировки магнитных сфер против конкретный поверхностно экспрессируемого маркера. Процесс получения клеточной популяции для изготовления состава может дополнительно включать этап сортировки для обеспечения безопасности и чистоты конечного продукта. Например, если опухолевую клетку от пациента использовали для стимуляции генетически модифицированной T-клетки согласно изобретению или которая была генетически модифицирована для стимуляции генетически модифицированной T-клетки согласно изобретению, подготовленной для включения в состав, очень важно, чтобы никакие опухолевые клетки пациента не были включены в готовый продукт.
Инфузия клеточного продукта и/или криоконсервация клеточного продукта инфузии
[0606] Фармацевтический состав согласно изобретению могут распределять в пакеты для инфузии, криоконсервации и/или хранения.
[0607] Фармацевтический состав согласно изобретению может быть криоконсервирован с использованием стандартного протокола и, необязательно, криоконсервирующей среды, пригодной для инфузии. Например, криоконсервант, не содержащий ДМСО (например, среда для криоконсервации CryoSOfreeTM без ДМСО), может использоваться для снижения токсичности, связанной с замораживанием. Криоконсервированный фармацевтический состав согласно настоящему изобретению могут хранить для последующей инфузии пациенту. Эффективное лечение может потребовать многократного введения фармацевтического состав согласно изобретению, и, следовательно, фармацевтические композиции могут быть упакованы в предварительно деленных аликвотами "дозах", которые могут храниться в замороженном виде, но разделенными для размораживания отдельных доз.
[0608] Фармацевтический состав согласно изобретению могут хранить при комнатной температуре. Эффективное лечение может потребовать многократных введений фармацевтического состава согласно изобретению, и, следовательно, фармацевтические составы могут быть упакованы в предварительно деленных аликвотами "дозах", которые могут быть хранить вместе, но отделять для введения отдельных доз.
[0609] Фармацевтический состав согласно изобретению могут архивировать для последующей повторной экспансии и/или отбора с целью получения дополнительных доз для того же пациента в случае аллогеннной терапии, которому введение может потребоваться позднее, например, в случае ремиссии и рецидива состояния.
Составы
[0610] Как отмечено выше, в изобретении предложены стабильные составы, которые предпочтительно содержат фосфатный буфер с физиологическим раствором или выбранной солью, а также консервированные растворы и составы, содержащие консервант, а также консервированные составы многократного применения, подходящие для медицинского или ветеринарного применения, включающие по меньшей мере один VCAR в фармацевтически приемлемом составе. Консервированные составы содержат по меньшей мере один известный консервант или, необязательно, выбранный из группы, состоящей по меньшей мере из одного фенола, м-крезола, п-крезола, о-крезола, хлоркрезола, бензилового спирта, фенилмеркурнитрита, феноксиэтанола, формальдегида, хлорбутанола, хлорида магния (например, гексагидрата), алкилпарабена (метил, этил, пропил, бутил и т.п.), хлорида бензалкония, хлорида бензетония, дегидроацетата натрия и тимеросала, полимеров или их смесей в водном разбавителе. Может использоваться любая подходящая концентрация или смесь, известная в уровне техники, например, приблизительно 0,0015%, или любой диапазон, значение или дробная часть в нем. Неограничивающие примеры включают отсутствие консерванта, приблизительно 0,1-2% мета-крезола (например, 0,2, 0,3, 0,4, 0,5, 0,9, 1,0%), приблизительно 0,1-3% бензилового спирта (например, 0,5, 0,9, 1,1, 1,5, 1,9, 2,0, 2,5%), приблизительно 0,001-0,5% тимеросала (например, 0,005, 0,01), приблизительно 0,001-2,0% фенола (например, 0,05, 0,25, 0,28, 0,5, 0,9, 1,0%), 0,0005-1,0% алкилпарабена(ов) (например, 0,00075, 0,0009, 0,001, 0,002, 0,005, 0,0075, 0,009, 0,01, 0,02, 0,05, 0,075, 0,09, 0,1, 0,2, 0,3, 0,5, 0,75, 0,9, 1,0%) и т.п.
[0611] Как отмечено выше, в изобретении предложено изделие, включающее упаковочный материал и по меньшей мере один флакон, включающий раствор по меньшей мере одного VCAR с установленными буферами и/или консервантами, необязательно в водном разбавителе, при этом указанный упаковочный материал содержит этикетку, которая указывает, что такой раствор можно сохранять в течение 1, 2, 3, 4, 5, 6, 9, 12, 18, 20, 24, 30, 36, 40, 48, 54, 60, 66, 72 часов или больше. Изобретение также включает изделие, содержащее упаковочный материал, первый флакон, содержащий лиофилизированный, по меньшей мере один, VCAR, и второй флакон, содержащий водный разбавитель установленного буфера или консерванта, при этом указанный упаковочный материал содержит этикетку, которая содержит инструкции для пациента по восстановлению по меньшей мере одного VCAR в водном разбавителе с получением раствора, который можно сохранять в течение двадцати четырех часов или больше.
[0612] По меньшей мере один VCAR, применяемый в соответствии с настоящим изобретением, может быть получен рекомбинантными методами, в том числе из клетки млекопитающего или трансгенных препаратов, или может быть очищен из других биологических источников, как описано в настоящем документе или известно в уровне техники.
[0613] Диапазон по меньшей мере одного VCAR в продукте согласно настоящему изобретению включает количества, дающие при восстановлении, в случае присутствия во влажной/сухой системе, концентрации от приблизительно 1,0 мкг/мл до приблизительно 1000 мг/мл, хотя более низкие и более высокие концентрации пригодны и зависят от предполагаемого носителя для доставки, например, составы растворов будут отличаться от трансдермального пластыря, легочной, трансмукозальной или осмотической доставки или методов с использованием микронасосов.
[0614] Предпочтительно водный разбавитель необязательно дополнительно включает фармацевтически приемлемый консервант. Предпочтительные консерванты включают консерванты, выбранные из группы, состоящей из фенола, мета-крезола, п-крезола, o-крезола, хлоркрезола, бензилового спирта, алкилпарабена (метил, этил, пропил, бутил и т.п.), хлорида бензалкония, хлорида бензетония, дегидроацетата натрия и тимеросала или их смесей. Концентрация консерванта, используемого в составе, является концентрацией, достаточной, чтобы оказать противомикробное действие. Такие концентрации зависят от выбранного консерванта и с легкостью определяются квалифицированным специалистом.
[0615] Другие вспомогательные вещества, например, изотонические вещества, буферы, антиоксиданты и усилители действия консервантов, могут быть необязательно и предпочтительно добавлены к разбавителю. Изотоническое вещество, такое как глицерин, обычно используют в известных концентрациях. Физиологически переносимый буфер предпочтительно добавляют, чтобы обеспечить улучшенный контроль pH. Составы могут охватывать широкий диапазон pH, например, от приблизительно pH 4 до приблизительно pH 10, и предпочтенные диапазоны от приблизительно pH 5 до приблизительно pH 9, и наиболее предпочтительный диапазон от приблизительно 6,0 до приблизительно 8,0. Предпочтительно составы согласно настоящему изобретению имеют pH от приблизительно 6,8 до приблизительно 7,8. Предпочтительные буферы включают фосфатные буферы, наиболее предпочтительно фосфат натрия, в частности фосфатно-солевой буфер (PBS).
[0616] Другие добавки, такие как фармацевтически приемлемые солюбилизаторы, такие как Tween 20 (полиоксиэтилен (20) сорбитанмонолаурат), Tween 40 (полиоксиэтилен (20) сорбитанмонопальмитат), Tween 80 (полиоксиэтилен (20) сорбитанмоноолеат), Pluronic F68 (блоксополимеры полиоксиэтилена-полиоксипропилена) и ПЭГ (полиэтиленгликоль) или неионогенные поверхностно-активные вещества, такие как полисорбат 20 или 80 или полоксамер 184 или 188, полиолы Pluronic®, другие блоксополимеры и хелатообразователи, такие как ЭДТА и ЭГТА, могут быть необязательно добавлены в составы или композиции для уменьшения агрегации. Такие добавки особенно полезны, если для введения состава используют насос или пластмассовый контейнер. Присутствие фармацевтически приемлемого поверхностно-активного вещества уменьшает склонность белка к агрегации.
[0617] Составы согласно настоящему изобретению могут быть получены способом, который включает смешивание по меньшей мере одного VCAR и консерванта, выбранного из группы, состоящей из фенола, м-крезола, п-крезола, о-крезола, хлоркрезола, бензилового спирта, алкилпарабена (метил, этил, пропил, бутил и т.п.), хлорида бензалкония, хлорида бензетония, дегидроацетата натрия и тимеросала или их смесей в водном разбавителе. Смешивание по меньшей мере одного VCAR и консерванта в водном разбавителе проводят при использовании стандартных процедур растворения и смешивания. Для приготовления подходящей композиции, например, измеренное количество по меньшей мере одного VCAR в буферном растворе объединяют с требуемым консервантом в буферном растворе, в количествах, достаточных для предоставления белка и консерванта в нужных концентрациях. Вариации этого процесса будут известны специалисту в данной области. Например, порядок добавления компонентов, используются ли дополнительные добавки, температура и pH, при которых производят состав, являются факторами, которые можно оптимизировать для используемой концентрации и способов введения.
[0618] Заявленные составы могут быть предоставлены пациентам в виде прозрачных растворов или в виде двух флаконов, включающих флакон с лиофилизированным, по меньшей мере одним, VCAR, который восстанавливают с использованием второго флакона, содержащего воду, консервант и/или вспомогательные вещества, предпочтительно фосфатный буфер и/или физиологический раствор, и выбранную соль в водном разбавителе. Либо один флакон с раствором, либо двойной флакон, требующий восстановления, может многократно использоваться повторно и может быть достаточным для одного или более курсов лечения пациента и, таким образом, может обеспечивать более удобную схему лечения, чем доступные в настоящее время.
[0619] Настоящие заявленные изделия пригодны к применению в течение периода от немедленного введения до 24 часов или более. Таким образом, заявленные в настоящем изделия обеспечивают значительные преимущества для пациента. Составы согласно изобретению необязательно могут безопасно храниться при температурах от приблизительно 2°С до приблизительно 40°С и сохранять биологическую активность белка в течение длительных периодов времени, что позволяет, таким образом, снабжать упаковку маркировкой, указывающей, что раствор можно хранить и/или использовать в течение 6, 12, 18, 24, 36, 48, 72 или 96 часов или более. В случае использования консервированного разбавителя, такая маркировка может включать применение до 1-12 месяцев, полугода, полутора и/или двух лет.
[0620] Растворы по меньшей мере одного VCAR согласно изобретению могут быть изготовлены в процессе, включающим смешивание по меньшей мере одного VCAR в водном разбавителе. Смешивание выполняют с помощью стандартных процедур растворения и смешивания. Для приготовления подходящего разбавителя, например, измеренное количество по меньшей мере одного VCAR в воде или буфере объединяют в количествах, достаточных для предоставления белка и, необязательно, консерванта или буфера в требуемых концентрациях. Вариации этого процесса будут известны среднему специалисту в данной области. Например, порядок добавления компонентов, используются ли дополнительные добавки, температура и pH, при которых производят состав, - являются факторами, которые можно оптимизировать для используемой концентрации и способов введения.
[0621] Заявленные составы могут быть предоставлены пациентам в виде прозрачных растворов или в виде двух флаконов, включающих флакон с лиофилизированным, по меньшей мере одним, VCAR, который восстанавливают с использованием второго флакона, содержащего водный разбавитель. Либо один флакон с раствором, либо двойной флакон, требующий восстановления, могут многократно использоваться повторно и могут быть достаточными для одного или множества курсов лечения пациента, и, таким образом, обеспечивают более удобную схему лечения, чем доступные в настоящее время.
[0622] Заявленные продукты могут быть предоставлены пациентам ненапрямую, через аптеки, клиники или другие подобные учреждения и лаборатории, в виде прозрачных растворов или двойных флаконов, включающих флакон с лиофилизированным, по меньшей мере одним, VCAR, который восстанавливают с использованием второго флакона, содержащего водный разбавитель. Прозрачный раствор в данном случае может иметь объем до одного литра или даже больше, с предоставлением большой емкости, из которой порции по меньшей мере одного раствора VCAR меньшего объема можно отбирать один или более раз для переноса во флаконы меньшего объема и предоставлять через аптеку или клинику их клиентам и/или пациентам.
[0623] Зарегистрированные устройства, включающие системы с одним флаконом, включают шприц-ручки для доставки раствора, такие как ручки BD, BD Autojector®, Humaject®, NovoPen®, BD®Pen, AutoPen® и OptiPen®, GenotropinPen®, Genotronorm Pen®, Humatro Pen®, Reco-Pen®, Roferon Pen®, Biojector®, Iject®, безыгольный инъектор J-tip®, Intraject®, Medi-Ject®, например, производства или разработки Becton Dickinson (Franklin Lakes, NJ, www.bectondickenson.com), Disetronic (Burgdorf, Switzerland, www.disetronic.com; Bioject, Portland, Oreg. (www.bioject.com); National Medical Products, Weston Medical (Peterborough, UK, www.weston-medical.com), Medi-Ject Corp (Minneapolis, Minn., www.mediject.com), и аналогичные подходящие устройства. Зарегистрированные устройства, включающие систему с двумя флаконами, включают такие шприц-ручки для восстановления лиофилизированного лекарственного средства в картридже для доставки восстановленного раствора, такие как HumatroPen®. Примеры других подходящих устройств включают предварительно наполненные шприцы, автоинъекторы, безыгольные инъекторы и безыгольные наборы для в/в инфузии.
[0624] Заявленные в настоящее время продукты включают упаковочный материал. Упаковочный материал предоставляет, помимо информации, требуемой регулирующими органами, условия, при которых продукт может применяться. Упаковочный материал согласно настоящему изобретению предоставляет пациенту инструкции по восстановлению по меньшей мере одного VCAR в водном разбавителе с получением раствора и применению раствора в течение 2-24 часов или больше в случае двух флаконов влажного/сухого продукта. В случае одного флакона продукта в виде раствора маркировка указывает, что такой раствор можно применять в течение 2-24 часов или более. Заявленные в настоящее время продукты могут применяться в качестве продуктов для медицинского применения.
[0625] Составы согласно настоящему изобретению могут быть изготовлены способом, который включает смешивание по меньшей мере одного VCAR и выбранного буфера, предпочтительно фосфатного буфера, содержащего раствор хлорида натрия или выбранную соль. Смешивание по меньшей мере одного буфера VCAR и в водном разбавителе проводят при использовании стандартных процедур растворения и смешивания. Для приготовления подходящей композиции, например, измеренное количество по меньшей мере одного VCAR в воде или буфере объединяют с требуемым буферным веществом в воде в количествах, достаточных для предоставления белка и буфера в нужных концентрациях. Вариации этого процесса будут известны среднему специалисту в данной области. Например, порядок добавления компонентов, используются ли дополнительные добавки, температура и pH, при которых производят состав, являются факторами, которые можно оптимизировать для используемой концентрации и способов введения.
[0626] Заявленные стабильные или консервированные составы могут быть предоставлены пациентам в виде прозрачных растворов или в виде двойных флаконов, содержащих флакон с лиофилизированным VCAR, который восстанавливают с использованием второго флакона, содержащего консервант или буфер и вспомогательные вещества в водном разбавителе. Либо один флакон с раствором, либо двойной флакон, требующий восстановления, может многократно использоваться повторно, и может быть достаточным для одного или более курсов лечения пациента, и, таким образом, обеспечивает более удобную схему лечения, чем доступные в настоящее время.
[0627] Другие составы или способы стабилизации VCAR могут приводить к получению отличного от прозрачного раствора лиофилизированного порошка, содержащего VCAR. Непрозрачные растворы включают составы, содержащие суспензии частиц, при этом указанные частицы являются композицией, содержащей VCAR в структуре переменного размера и известной под разными названиями, такими как микросфера, микрочастица, наночастица, наносфера или липосома. Такие относительно гомогенные составы частиц по существу сферической формы, содержащие действующее вещество, могут быть получены при контакте водной фазы, содержащей действующее вещество и полимер, и неводной фазы с последующим испарением неводной фазы, вызывающим соединение частиц из водной фазы, как описано в патенте США 4,589,330. Пористые микрочастицы могут быть получены при использовании первой фазы, содержащей действующее вещество и полимер, диспергированный в равномерно распределенном растворителе, и удаление указанного растворителя из суспензии при лиофильной сушке или разбавлении-экстракции-осаждении, как описано в патенте США 4,818,542. Предпочтительные полимеры для таких препаратов являются природными или синтетическими сополимерами или полимерами, выбранными из группы, состоящей из желатинового агара, крахмала, арабиногалактана, альбумина, коллагена, полигликолевой кислоты, полимолочной кислоты, гликолид-L(-)-лактида, поли(эписилон)капролактона, сополимера поли(эпсилон)капролактона-молочной кислоты, сополимера поли(эпсилон)капролактона-гликолевой кислоты, поли(β-гидрокси-масляной кислоты), полиэтиленоксида, полиэтилена, поли(алкил-2-цианоакрилата), поли(гидроксиэтилметакрилата), полиамидов, полиаминокислот, поли(2-гидроксиэтил-DL-аспартама), сложный полиэфир мочевины, поли(L-фенилаланин/этиленгликоль/1,6-диизоцианатогексан) и полиметилметакрилат). Особенно предпочтительными полимерами являются сложные полиэфиры, такие как полигликолевая кислота, полимолочная кислота, гликолид-L(-)-лактид, поли(эписилон)капролактон, сополимер поли(эпсилон)капролактона-молочной кислоты и сополимер поли (эпсилон)капролактона-гликолевой кислоты. Полезные растворители. для растворения полимера и/или действующего вещества включают: воду, гексафторизопропанол, метиленхлорид, тетрагидрофуран, гексан, бензол или сесквигидрат гексафторацетона. Процесс диспергирования содержащей активное вещество фазы со второй фазой может включать приложение давления, выталкивающего указанную первую фазу через отверстие в сопле с образованием капель.
[0628] Составы сухого порошка могут быть получены в процессах, отличных от лиофилизации, таких как распылительная сушка или экстракция растворителя при выпаривании, или при осаждении кристаллической композиции с последующим одним или более этапами удаления водного или неводного растворителя. Изготовление высушенного распылением препарата VCAR описано в патенте США 6,019,968. Композиции сухого порошка на основе VCAR могут быть получены при распылительной сушке растворов или суспензий VCAR и, необязательно, вспомогательных веществ в растворителе, в условиях, обеспечивающих получением вдыхаемого сухого порошка. Растворители могут включать полярные соединения, такие как воду и этанол, которые можно легко выпарить. Стабильность VCAR может быть повышена при выполнении процедур распылительной сушки в отсутствие кислорода, например, под слоем азота или с использованием азота в качестве осушающего газа. Другой относительно сухой состав представляет собой дисперсию множества перфорированных микроструктур, диспергированных в суспензионной среде, которая обычно содержит гидрофторалкановый пропеллент, как описано в WO 9916419. Стабилизированные дисперсии могут быть введены в легкие пациента при использовании дозирующего ингалятора. Оборудование, пригодное для коммерческого производства высушенных распылением лекарственных средств, выпускает Buchi Ltd. или Niro Corp.
[0629] По меньшей мере один VCAR в стабильных или консервированных составах или растворах, описанных в настоящем документе, может быть введен пациенту в соответствии с настоящим изобретением при использовании различных способов доставки, включающих п/к или в/м инъекцию; трансдермальную, легочную, трансмукозальную доставку, имплантат, осмотический насос, картридж, микронасос или другие способы, знакомые специалисту в данной области, хорошо известные в уровне техники.
Терапевтические применения
[0630] В настощем изобретении также предложен способ модуляции или лечения заболевания в клетке, ткани, органе, у животного или пациента, как известно в уровне техники или как описано в настоящем документе, с применением по меньшей мере одного VCAR согласно настоящему изобретению, например, при введении или контакте клетки, ткани, органа, животного или пациента с терапевтически эффективным количеством VCAR. В настощем изобретении также предложен способ модуляции или лечения заболевания в клетке, ткани, органе, у животного или пациента, включающий, без ограничения, злокачественное заболевание.
[0631] В настощем изобретении также предложен способ модуляции или лечения по меньшей мере одного злокачественного заболевания в клетке, ткани, органе, у животного или пациента, включающего, без ограничения перечисленными, по меньшей мере одно из следующего: лейкоз, острый лейкоз, острый лимфобластный лейкоз (ОЛЛ), острый лимфолейкоз, B-клеточный, T-клеточный или ФАБ ОЛЛ, острый миелоидный лейкоз (ОМЛ), острый миелогенный лейкоз, хронический миелоцитарный лейкоз (ХМЛ), хронический лимфоцитарный лейкоз (ХЛЛ), волосотоклеточный лейкоз, миелодиспластический синдром (МДС), лимфома, болезнь Ходжкина, злокачественная лимфома, неходжкинская лимфома, лимфома Беркитта, множественная миелома, саркома Капоши, колоректальная карцинома, карцинома поджелудочной железы, карцинома носоглотки, злокачественный гистиоцитоз, паранеопластический синдром/злокачественная гиперкальциемия, солидные опухоли, рак мочевого пузыря, рак молочной железы, рак толстой и прямой кишки, рак эндометрия, рак головы, рак шеи, наследственный неполипозный рак, лимфома Ходжкина, рак печени, рак легкого, немелкоклеточный рак легкого, рак яичника, рак поджелудочной железы, рак предстательной железы, почечно-клеточная карцинома, рак яичка, аденокарциномы, саркомы, злокачественная меланома, гемангиома, метастазирование, резорбция кости при онкологическом заболевании, боли в кости при онкологическом заболевании и т.п.
[0632] Любой способ согласно настоящему изобретению может включать введение эффективного количества композиции или фармацевтической композиции, включающей по меньшей мере один VCAR, в клетку, ткань, орган, животному или пациенту, нуждающемуся в такой модуляции, лечении или терапии. Такой способ необязательно может также включать совместное введение или комбинированную терапию для лечения таких заболеваний или нарушений, где введение указанного по меньшей мере одного VCAR, его указанной части или варианта дополнительно включает введение, до, одновременно и/или после, по меньшей мере одного, выбранного по меньшей мере из одного алкилирующего средства, ингибитора митоза и радиофармацевтического препарата. Подходящие дозы хорошо известны в уровне техники. См., например, публикации Wells et al., eds., Pharmacotherapy Handbook, 2nd Edition, Appleton and Lange, Stamford, Conn. (2000); PDR Pharmacopoeia, Tarascon Pocket Pharmacopoeia 2000, Deluxe Edition, Tarascon Publishing, Loma Linda, Calif. (2000); Nursing 2001 Handbook of Drugs, 21st edition, Springhouse Corp., Springhouse, Pa., 2001; Health Professional's Drug Guide 2001, ed., Shannon, Wilson, Stang, Prentice-Hall, Inc, Upper Saddle River, N.J., которые полностью включены в настоящий документ посредством отсылки.
[0633] Предпочтительные дозы необязательно могут включать приблизительно 0,1-99 и/или 100-500 мг/кг/введение или любой диапазон, значение или их дробное значение, или дозы, позволяющие достигнуть концентрации в сыворотке приблизительно 0,1-5000 мкг/мл после однократного или многократного введения, или любой диапазон, значение или их дробное значение. Предпочтительный диапазон дозы для VCAR согласно настоящему изобретению составляет от приблизительно 1 мг/кг до приблизительно 3, приблизительно 6 или приблизительно 12 мг/кг массы тела пациента.
[0634] В альтернативе вводимая доза может изменяться в зависимости от известных факторов, таких как фармакодинамические свойства конкретного средства, а также его способ и путь введения; возраст, состояние здоровья и масса тела реципиента; характер и степень выраженности симптомов, тип параллельного лечения, частота лечения и требуемый эффект. Обычно доза активного ингредиента может составлять от приблизительно 0,1 до 100 миллиграммов на килограмм массы тела. Обычно от 0,1 до 50 и предпочтительно от 0,1 до 10 мг на килограмм на введение или в форме с замедленным высвобождением является эффективным для получения требуемых результатов.
[0635] В качестве неограничивающего примера, лечение людей или животных может быть представлено разовым или периодическим введением дозы по меньшей мере одного VCAR согласно настоящему изобретению от приблизительно 0,1 до 100 мг/кг или любого диапазона, значения или их дробного значения в день, в течение по меньшей мере одного из 1-40 дней или, альтернативно или дополнительно, по меньшей мере одной из 1-52 недель, или, альтернативно или дополнительно, по меньшей мере одного из 1-20 лет, или их любой комбинации, с использованием однократной инфузии или повторных доз.
[0636] Лекарственные формы (композиция), подходящие для внутреннего введения, обычно содержат от приблизительно 0,001 миллиграмма до приблизительно 500 миллиграммов активного ингредиента в единице или контейнере. В этих фармацевтических композициях активный ингредиент обычно присутствует в количестве приблизительно 0,5-99,999% по весу в расчете на общую массу композиции.
[0637] Для парентерального введения, VCAR может быть включен в состав в виде раствора, суспензии, эмульсии, частиц, порошка или лиофилизированного порошка в сочетании, или отдельно предоставлен с фармацевтически приемлемым растворителем для парентерального введения. Примерами таких растворителей являются вода, физиологический раствор, раствор Рингера, раствор декстрозы и примерно 1-10% раствор человеческого сывороточного альбумина. Также могут использоваться липосомы и неводные растворители, такие как нелетучие масла. Растворитель или лиофилизированный порошок может содержать добавки, которые поддерживают изотоничность (например, хлорид натрия, маннит) и химическую стабильность (например, буферы и консерванты). Состав стерилизуют известными или подходящими методами.
[0638] Подходящие фармацевтические носители описаны в последней реакции справочника Remington's Pharmaceutical Sciences, A. Osol, стандартного справочного текста в данной области.
Альтернативное введение
[0639] Многие известные и разработанные схемы могут использоваться согласно настоящему изобретению для введения фармацевтически эффективных количеств по меньшей мере одного VCAR согласно настоящему изобретению. Хотя в следующем описании используется легочное введение, другие способы введения могут использоваться в соответствии с настоящим изобретением с подходящими результатами. VCAR-рецепторы согласно настоящему изобретению можно доставлять в носителе, в виде раствора, эмульсии, коллоида или суспензии, или в виде сухого порошка, с использованием различных устройств и способов, подходящих для введения путем ингаляции или другими способами, описанными в рамках настоящего документа или известными в уровне техники.
Парентеральное введение и составы
[0640] Составы для парентерального введения могут содержать в качестве обычных вспомогательных веществ стерильную воду или раствор хлорида натрия, полиалкиленгликоли, такие как полиэтиленгликоль, масла растительного происхождения, гидрированные нафталины и т.п. Водные или масляные суспензии для инъекций могут быть приготовлены с использованием подходящего эмульгатора или увлажняющего и суспендирующего вещества в соответствии с известными способами. Средства для инъекций могут быть нетоксичными, вводимыми не перорально разбавителями, такими как водный раствор, стерильный раствор для инъекций или суспензия в растворителе. В качестве используемого носителя или растворителя допускается вода, раствор Рингера, изотонический раствор хлорида натрия и т.д.; в качестве обычного растворителя или суспендирующего растворителя может использоваться стерильное нелетучее масло. Для этих целей могут использоваться любые типы нелетучих масел и жирная кислота, включая натуральные или синтетические или полусинтетические жирные масла или жирные кислоты; природные или синтетические или полусинтетические моно- или ди- или триглицериды. Парентеральное введение известно в данной области и включает, без ограничения перечисленными, стандартные средства для инъекций, безыгольное устройство для инъекций под давлением газа, описанное в патенте США 5,851,198, и лазерный перфоратор, описанный в патенте США 5,839,446, полностью включенном в настоящий документ посредством отсылки.
Альтернативная доставка
[0641] Изобретение также относится к введению по меньшей мере одного VCAR парентеральным, подкожным, внутримышечным, внутривенным, внутрисуставным, внутрибронхиальным, внутрибрюшным, внутрикапсулярным, внутрихрящевым, внутриполостным, внутричерепным, интрацеребеллярным, интрацеребровентрикулярным, интраколическим, интрацервикальным, внутрижелудочным, внутрипеченочным, интрамиокардиальным, внутрикостным, внутрилоханочным, интраперикардиальным, внутрибрюшинным, внутриплевральным, внутрипростатическим, внутрилегочным, интраректальным, интраренальным, интраретинальным, интраспинальным, интрасиновиальным, интраторакальным, внутриматочным, интравезикальным, внутриочаговым, болюсным, вагинальным, ректальным, буккальным, подъязычным, интраназальным или трансдермальным путем. По меньшей мере одна композиция VCAR может быть приготовлена для парентерального (подкожного, внутримышечного или внутривенного) или любого другого введения, особенно в форме жидких растворов или суспензий; для применения при вагинальном или ректальном введении, в особенности в полутвердых формах, таких как, без ограничения, кремы и суппозитории; для буккального или подъязычного введения, например, без ограничения, в форме таблеток или капсул; или интраназально, например, без ограничения, форме порошков, назальных капель или аэрозолей или некоторых средств; или трансдермально, например, без ограничения, в форме геля, мази, лосьона, суспензии или пластыря в качестве системы трансдермальной доставки, с химическими вспомогательными добавками, такими как диметилсульфоксид, для изменения структуры кожи или для увеличения концентрации лекарственного средства в трансдермальном пластыре (Junginger, et al., в публикации "Drug Permeation Enhancement"; Hsieh, D. S., Eds., pp. 59-90 (Marcel Dekker, Inc. New York 1994, полностью включенной в настоящее описание посредством отылки)), или с окислителями, которые позволяют наносить составы, содержащие белки и пептиды, на кожу (WO 98/53847) или путем приложения электрических полей для создания временных транспортных путей, таких как электропорация, или для увеличения подвижности заряженных лекарственных средств через кожу, таких как ионтофорез, или с применением ультразвука, такого как сонофорез (Патенты США 4,309,999 и 4,767,402) (вышеуказанные публикации и патенты полностью включены в настоящее описание посредством отсылки).
Легочное/назальное введение
[0642] Для легочного введения предпочтительно по меньшей мере одну композицию VCAR доставляют при размере частиц, эффективном для достижения нижних дыхательных путей легкого или синусов. Согласно изобретению по меньшей мере один VCAR может быть доставлен с помощью любых различных ингаляционных или назальных устройств, известных в данной области для введения терапевтического средства путем ингаляции. Такие устройства, способные наносить аэрозольные составы в полость пазух или альвеолы пациента, включают дозирующие ингаляторы, небулайзеры, генераторы сухого порошка, распылители и т.п. Другие устройства, подходящие для направления легочного или назального введения VCAR, также известны в данной области. Все подобные устройства могут использовать составы, подходящие для введения для дозирования VCAR в виде аэрозоля. Такие аэрозоли могут состоять из растворов (как водных, так и неводных) или твердых частиц.
[0643] В дозирующих ингаляторах, таких как дозирующий ингалятор Ventolin, как правило, используется газ-пропеллент, при этом они требуют нажатия во время вдоха (см., например, WO 94/16970, WO 98/35888). В ингаляторах сухого порошка, таких как TurbuhalerTM (Astra), Rotahaler® (Glaxo), Diskus® (Glaxo), ингалятор SpirosTM (Dura), устройства, выпускаемые Inhale Therapeutics, и порошковый ингалятор Spinhaler® (Fisons), используется вдыхание смешанного порошка (патент США 4,668,218 Astra, EP 237507 Astra, WO 97/25086 Glaxo, WO 94/08552 Dura, патент США 5,458,135 Inhale, WO 94/06498 Fisons, которые полностью включены в настоящий документ посредством отсылки). Небулайзеры, такие как AERxTM Aradigm, распылитель Ultravent® (Mallinckrodt) и распылитель Acorn II® (Marquest Medical Products) (патент США 5,404,871 Aradigm, WO 97/22376, полностью включенные в настоящий документ посредством отсылки), производят аэрозоли из растворов, тогда как дозирующие ингаляторы, ингаляторы сухого порошка и т.д. генерируют аэрозоли из мелких частиц. Эти конкретные примеры доступных в продаже ингаляционных устройств предназначены в качестве репрезентативных конкретных устройств, подходящих для практического осуществления данного изобретения, и не предназначены в качестве ограничения объема изобретения.
[0644] Предпочтительно композицию, включающую по меньшей мере один VCAR, доставляют ингалятором сухого порошка или распылителем. Существует несколько предпочтительных признаков ингаляционного устройства для введения по меньшей мере одного VCAR согласно настоящему изобретению. Например, доставка с помощью ингаляционного устройства обеспечивает преимущества надежного, воспроизводимого и точного введения. Ингаляционное устройство необязательно может доставлять небольшие сухие частицы, например, меньше чем приблизительно 10 мкм, предпочтительно приблизительно 1-5 мкм, для удобства вдыхания.
Введение композиций VCAR в виде спрея
[0645] Спрей, включающий композицию VCAR, может быть получен путем выталкивания суспензии или раствора по меньшей мере одного VCAR через сопло под давлением. Размер и конфигурация сопла, приложенное давление и скорость подачи жидкости могут быть выбраны для получения требуемой производительности и размера частиц. Электрораспыление может быть выполнено, например, в электрическом поле, связанным с подачей через капилляр или сопло. Преимущественно частицы по меньшей мере одной композиции VCAR, доставляемые распылителем, имеют размер частиц меньше чем приблизительно 10 мкм, предпочтительно в пределах от приблизительно 1 мкм до приблизительно 5 мкм и, наиболее предпочтительно, от приблизительно 2 мкм до приблизительно 3 мкм.
[0646] Составы по меньшей мере одной композиции VCAR, подходящие для применения с распылителем, обычно включают композицию VCAR в водном растворе в концентрации от приблизительно 0,1 мг до приблизительно 100 мг по меньшей мере одной композиции VCAR на мл раствора или мг/г, или в любом диапазоне, значении или их дробном значении. Композиция может включать вещества, такие как наполнитель, буфер, изотоническое вещество, консервант, поверхностно-активное вещество и, предпочтительно, цинк. Состав также может включать вспомогательное вещество или вещество для стабилизации композиции VCAR, такое как буфер, восстановитель, белок-наполнитель или углевод. Белки-наполнители, используемые при изготовлении составов композиций VCAR, включают альбумин, протамин или т.п. Типичные углеводы, используемые при изготовлении составов композиций VCAR, включают сахарозу, маннит, лактозу, трегалозу, глюкозу или т.п. Состав композиции VCAR также может включать поверхностно-активное вещество, которое может уменьшать или предотвращать поверхностную агрегацию композиции VCAR, вызванную распылением раствора при образовании аэрозоля. Могут использоваться различные стандартные поверхностно-активные вещества, такие как сложные полиоксиэтилированные эфиры жирных кислот и спиртов и сложные полиоксиэтилированные эфиры сорбита и жирных кислот. Количества обычно изменяются в пределах от 0,001 до 14% по весу состава. Особенно предпочтительными поверхностно-активными веществами в рамках настоящего изобретения являются полиоксиэтилен сорбитанмоноолеат, полисорбат 80, полисорбат 20 и т.п. Дополнительные средства, известные в области изготовления составов белка, такого как VCAR или определенные части или варианты, также могут быть включены в композицию.
Введение композиций VCAR с помощью небулайзера
[0647] Композиции VCAR согласно изобретению могут вводить с помощью небулайзера, такого как струйный небулайзер или ультразвуковой небулайзер. Как правило, в струйном небулайзере используется источник сжатого воздуха для создания высокоскоростной воздушной струи через отверстие. Когда газ выходит из сопла, создается область низкого давления, которая втягивает раствор композиции VCAR через капиллярную трубку, соединенную с резервуаром для жидкости. Поток жидкости из капиллярной трубки срезается с образованием нестабильных нитей и капель, когда он выходит из трубки, создавая аэрозоль. Ряд конфигураций, скоростей потока и типов перегородок можно использовать для получения требуемых рабочих характеристик для данного струйного небулайзера. В ультразвуковом небулайзере высокочастотная электрическая энергия используется для создания вибрационной механической энергии, обычно с применением пьезоэлектрического преобразователя. Эта энергия передается составу VCAR либо напрямую, либо через связующую жидкость, создающую аэрозоль, включающий композицию VCAR. Предпочтительно частицы композиции VCAR, доставляемые небулайзером, имеют размер частиц меньше чем приблизительно 10 мкм, предпочтительно в диапазоне от приблизительно 1 мкм до приблизительно 5 мкм и, наиболее предпочтительно, от приблизительно 2 мкм до приблизительно 3 мкм.
[0648] Составы по меньшей мере одного VCAR, подходящие для использования с небулайзером, струйным или ультразвуковым, обычно включают концентрацию от приблизительно 0,1 мг до приблизительно 100 мг по меньшей мере одного VCAR на мл раствора. Состав может включать вещества, такие как наполнитель, буфер, изотоническое вещество, консервант, поверхностно-активное вещество и, предпочтительно, цинк. Композиция также может включать вспомогательное вещество или вещество для стабилизации по меньшей мере одной композиции VCAR, такое как буфер, восстановитель, белок-наполнитель или углевод. Белки-наполнители, полезные при изготовлении состава по меньшей мере одной композиции VCAR, включают альбумин, протамин или т.п. Типичные углеводы, полезные при изготовлении состава по меньшей мере одного VCAR, включают сахарозу, маннит, лактозу, трегалозу, глюкозу или т.п. По меньшей мере один состав VCAR также может включать поверхностно-активное вещество, которое может снижать или предотвращать поверхностную агрегацию по меньшей мере одного VCAR, вызванную распылением раствора при образовании аэрозоля. Могут использоваться различные стандартные поверхностно-активные вещества, такие как сложные полиоксиэтилированные эфиры жирных кислот и спиртов и сложные полиоксиэтилированные эфиры сорбита и жирных кислот. Количества обычно изменяются в пределах от приблизительно 0,001 до 4% по весу состава. Особенно предпочтительными поверхностно-активными веществами в рамках настоящего изобретения являются полиоксиэтилен сорбитанмоноолеат, полисорбат 80, полисорбат 20 и т.п. Дополнительные средства, известные в области изготовления составов белка, такого как VCAR, также могут быть включены в состав.
Введение композиций VCAR с помощью дозирующего ингалятора
[0649] В дозирующем ингаляторе (MDI) пропеллент, по меньшей мере один VCAR и любые вспомогательные вещества или другие добавки содержатся в баллоне в виде смеси, включающей сжиженный газ под давлением. При нажатии на дозирующий клапан смесь высвобождается в виде аэрозоля, предпочтительно содержащего частицы размером меньше чем приблизительно 10 мкм, предпочтительно от приблизительно 1 до приблизительно 5 мкм и, наиболее предпочтительно, от приблизительно 2 до приблизительно 3 мкм. Требуемый размер частиц аэрозоля может быть получен при использовании состава VCAR, полученного различными способами, известными специалистам в данной области, включающими размол на струйной мельнице, распылительную сушку, конденсацию в критических точках и т.п. Предпочтительные дозирующие ингаляторы включают ингаляторы производства 3M или Glaxo, в которых используется фторуглеводородный пропеллент. Составы по меньшей мере одного VCAR для использования с дозирующим ингалятором, как правило, включают тонкодисперсный порошок, содержащий по меньшей мере один VCAR в виде суспензии в неводной среде, например, суспендированный в пропелленте при использовании поверхностно-активного вещества. Пропеллент может быть любым стандартным материалом, используемым для этой цели, таким как хлорфторуглерод, хлорфторуглеводород, фторуглеводород или углеводород, включая трихлорфторметан, дихлордифторметан, дихлортетрафторэтанол и 1,1,1,2-тетрафторэтан, HFA-134a (водородсодержащий фторалкан-134a), HFA-227 (водородсодержащий фторалкан-227) и т.п. Предпочтительно пропеллент является фторуглеводородом. Поверхностно-активное вещество может быть выбрано для стабилизации по меньшей мере одного VCAR в виде суспензии в пропелленте, для защиты действующего вещества от химического разложения и т.п. Подходящие поверхностно-активные вещества включают сорбитантриолеат, соевый лецитин, олеиновую кислоту и т.п. В некоторых случаях растворы аэрозолей являются предпочтительными при использовании таких растворителей, как этанол. Дополнительные средства, известные в области изготовления составов белка, также могут быть включены в состав. Среднему специалисту в данной области будет очевидно, что способы настоящего изобретения могут быть осуществлены путем легочного введения по меньшей мере одной композиции VCAR с помощью устройств, не описанных в настоящем документе.
Составы для перорального применения и введение
[0650] Составы для перорального применения основаны на совместном введении адъювантов (например, резорцинов и неионогенных поверхностно-активных веществ, таких как полиоксиэтиленолеиновый эфир и н-гексадецилполиэтиленовый эфир) для искусственного увеличения проницаемости стенок кишечника, а также совместного введения ингибиторов ферментов (например, ингибиторов панкреатического трипсина, диизопропилфторфосфата (DFF) и тразилола) для ингибирования ферментативного расщепления. Составы для доставки гидрофильных средств, включая белки и VCAR, и комбинация по меньшей мере двух поверхностно-активных веществ, предназначенные для перорального, трансбуккального, мукозального, назального, легочного, вагинального, трансмембранного или ректального введения, описаны в патенте США 6,309,663. Действующее соединение, входящее в состав лекарственной формы твердого типа для перорального введения, может быть смешано по меньшей мере с одной добавкой, включающей сахарозу, лактозу, целлюлозу, маннит, трегалозу, рафинозу, мальтит, декстран, крахмалы, агар, аргинаты, хитины, хитозаны, пектины, трагакантовую камедь, гуммиарабик, желатин, коллаген, казеин, альбумин, синтетический или полусинтетический полимер и глицерид. Такие лекарственные формы также могут содержать другой тип(ы) добавок, например, неактивный разбавитель, смазывающее вещество, такое как стеарат магния, парабен, консервант, такой как сорбиновую кислоту, аскорбиновую кислоту, альфа-токоферол, антиоксидант, такой как цистеин, разрыхлитель, связующее вещество, загуститель, буферное вещество, подсластитель, вкусовую добавку, ароматизатор и т.д.
[0651] Таблетки и пилюли могут быть также переработаны в препараты с кишечнорастворимым покрытием. Жидкие препараты для перорального введения включают эмульсии, сиропы, настойки, суспензии и растворы, разрешенные для медицинского применения. Эти препараты могут содержать неактивные разбавители, обычно используемые в указанной области, например воду. Липосомы также были описаны как системы доставки лекарственных средств для доставки инсулина и гепарина (патент США 4,239,754). Недавно микросферы из искусственных полимеров смешанных аминокислот (протеиноидов) были использованы для доставки фармацевтических средств (патент США 4,925,673). Кроме того, в уровне техники известны соединения-носители, описанные в патенте США 5,879,681 и патенте США 5,871,753 и применяемые для пероральной доставки биологически активных средств.
Составы для мукозального применения и введение
[0652] Составы для перорального введения биоактивного средства, инкапсулированного в одном или более биосовместимых полимерных или сополимерных вспомогательных веществах, предпочтительно биоразлагаемом полимере или сополимере, с получением микрокапсул, которые благодаря надлежащему размеру получаемых микрокапсул приводят к тому, что средство достигает и поглощается скоплениями лимфатических фолликулов, также известными как "Пейеровы бляшки" или "GALT" животного без потери эффективности в результате прохода средства через желудочно-кишечный тракт. Подобные скопления лимфатических фолликулов можно обнаружить в бронхиальной системе (BALT) и толстой кишке. Описанные выше ткани обычно называют лимфоретикулярными тканями, ассоциированными со слизистой оболочкой (MALT). Для абсорбции через поверхности слизистых оболочек композиции и способы введения по меньшей мере одного VCAR включают эмульсию, содержащую множество субмикронных частиц, мукоадгезивную макромолекулу, биоактивный пептид и водную непрерывную фазу, которая способствует абсорбции через поверхности слизистых оболочек посредством мукоадгезии частиц эмульсии (патент США 5,514,670). Поверхности слизистых, подходящие для применения эмульсий согласно настоящему изобретению, могут включать роговичный, конъюнктивальный, трансбуккальный, подъязычный, назальный, вагинальный, легочный, желудочный, кишечный и ректальный пути введения. Составы для вагинального или ректального введения, например, суппозитории, могут содержать в качестве вспомогательных веществ, например, полиалкиленгликоли, вазелин, масло какао и т.п. Составы для интраназального введения могут быть твердыми и содержать в качестве вспомогательных веществ, например, лактозу, или могут быть водными или масляными растворами назальных капель. Для трансбуккального введения вспомогательные вещества включают сахара, стеарат кальция, стеарат магния, прежелатинизированный крахмал и т.п. (патент США 5,849,695).
Составы для трансдермального применения и введение
[0653] Для трансдермального введения по меньшей мере один VCAR инкапсулирован в устройстве доставки, таком как липосомы или полимерные наночастицы, микрочастицы, микрокапсулы или микросферы (вместе именуемые микрочастицами, если не указано иное). Известен ряд подходящих устройств, включая микрочастицы, изготовленные из синтетических полимеров, таких как полигидроксикислоты, такие как полимолочная кислота, полигликолевая кислота и их сополимеры, полиортоэфиры, полиангидриды и полифосфазены, а также природные полимеры, такие как коллаген, полиаминокислоты, альбумин и другие белки, альгинат и другие полисахариды, и их комбинации (патент США 5,814,599).
Пролонгированное введение и составы
[0654] Может быть предпочтительным доставлять соединения согласно настоящему изобретению индивиду в течение длительных периодов времени, например, в течение периодов от одной недели до одного года от однократного введения. Могут использоваться различные лекарственные формы замедленного высвобождения, депо или имплантаты. Например, лекарственная форма может содержать фармацевтически приемлемую нетоксичную соль соединений, которая имеет низкую растворимость в физиологических жидкостях, например: (a) соль присоединения кислоты с многоосновной кислотой, такой как фосфорная кислота, серная кислота, лимонная кислота, винная кислота, дубильная кислота, памовая кислота, альгиновая кислота, полиглутаминовая кислота, нафталинмоно- или дисульфокислоты, полигалактуроновая кислота и т.п.; (b) соль с катионом поливалентного металла, таким как цинк, кальций, висмут, барий, магний, алюминий, медь, кобальт, никель, кадмий и т.п., или с органическим катионом, образованным, например, из N, N'-дибензил-этилендиамина или этилендиамина; или (с) комбинации (a) и (b), например, таннаты цинка. Кроме того, соединения согласно настоящему изобретению или, предпочтительно, относительно нерастворимые соли, такие как только что описанные, могут быть включены в состав в форме геля, например, геля моностеарата алюминия, например, с кунжутным маслом, пригодных для инъекций. Особенно предпочтительными солями являются соли цинка, таннаты цинка, памоаты и т.п. Другой тип депо-состава с замедленным высвобождением для инъекций может содержать соединение или соль, диспергированную для инкапсулирования в медленно разлагаемом нетоксичном, неантигенном полимере, таком как полимер полимолочной кислоты/полигликолевой кислоты, например, как описано в патенте США 3,773,919. Соединения или, предпочтительно, относительно нерастворимые соли, такие как соли, описанные выше, также могут быть включены в состав эластичных силиконовых гранул с холестериновой матрицей, в частности, для применения у животных. Дополнительные депо или имплантируемые составы с замедленным высвобождением, например, газонаполненные или жидкие липосомы, известны из литературы (патент США 5,770,222 и "Sustained and Controlled Release Drug Delivery Systems", J. R. Robinson ed., Marcel Dekker, Inc., N.Y., 1978).
Инфузия модифицированных клеток в качестве адоптивной клеточной терапии
[0655] В изобретении предложен модифицированные клетки, которые экспрессируют один или более CAR и/или VCAR согласно изобретению, которые были отобраны и/или размножены для введения индивиду, нуждающемуся в этом. Модифицированные клетки согласно изобретению могут быть включены в составы для хранения при любой температуре, включая комнатную температуру и температуру тела. Модифицированные клетки согласно изобретению могут быть включены в составы для криоконсервации и последующего размораживания. Модифицированные клетки согласно изобретению могут быть включены в фармацевтически приемлемый носитель для прямого введения индивиду из стерильной упаковки. Модифицированные клетки согласно настоящему изобретению могут быть включены в фармацевтически приемлемый носитель с индикатором жизнеспособности клеток и/или уровня экспрессии CAR/VCAR для обеспечения минимального уровня клеточной функции и экспрессии CAR/VCAR. Модифицированные клетки согласно настоящему изобретению могут быть включены в фармацевтически приемлемый носитель с установленной плотностью, с одним или более реагентами для ингибирования дальнейшей экспансии и/или предотвращения гибели клеток.
Индуцируемые проапоптотические полипептиды
[0656] Индуцируемые проапоптотические полипептиды согласно изобретению превосходят существующие индуцируемые полипептиды, поскольку индуцируемые проапоптотические полипептиды согласно изобретению намного менее иммуногенные. Хотя индуцируемые проапоптотические полипептиды согласно изобретению являются рекомбинантными полипептидами и, поэтому, не встречаются в природе, последовательности, рекомбинированные для получения индуцируемых проапоптотических полипептидов согласно изобретению, не включают нечеловеческие последовательности, которые человеческая иммунная система может распознавать как "чужеродные" и, следовательно, вызывать иммунный ответ у индивида, получающего индуцируемый проапоптотический полипептид согласно изобретению, клетку, включающую индуцируемый проапоптотический полипептид, или композицию, включающую индуцируемый проапоптотический полипептид или клетку, включающую индуцируемый проапоптотический полипептид.
[0657] В изобретении предложены индуцируемые проапоптотические полипептиды, включающие лигандсвязывающую область, линкер и проапоптотический пептид, где индуцируемый проапоптотический полипептид не включает нечеловеческую последовательность. В некоторых вариантах осуществления нечеловеческая последовательность включает сайт рестрикции. В некоторых вариантах осуществления проапоптотический пептид является полипептидом каспазы. В некоторых вариантах осуществления полипептид каспазы является полипептидом каспазы 9. В некоторых вариантах осуществления полипептид каспазы 9 является усеченным полипептидом каспазы 9. Индуцируемые проапоптотические полипептиды согласно изобретению могут быть неприродными.
[0658] Полипептиды каспазы согласно изобретению включают, без ограничения перечисленными, каспазу 1, каспазу 2, каспазу 3, каспазу 4, каспазу 5, каспазу 6, каспазу 7, каспазу 8, каспазу 9, каспазу 10, каспазу 11, каспазу 12 и каспазу 14. Полипептиды каспазы согласно изобретению включают, без ограничения перечисленными, такие полипептиды каспазы, которые связаны с апоптозом, включающие каспазу 2, каспазу 3, каспазу 6, каспазу 7, каспазу 8, каспазу 9 и каспазу 10. Полипептиды каспазы согласно изобретению включают, без ограничения перечисленными, такие полипептиды каспазы, которые инициируют апоптоз, включая каспазу 2, каспазу 8, каспазу 9 и каспазу 10. Полипептиды каспазы согласно изобретению включают, без ограничения перечисленными, такие полипептиды каспазы, которые выполняют апоптоз, включая каспазу 3, каспазу 6 и каспазу 7.
[0659] Полипептиды каспазы согласно изобретению могут кодироваться аминокислотой или последовательностью нуклеиновой кислоты, имеющей одну или более модификаций по сравнению с аминокислотной последовательностью или последовательностью нуклеиновой кислоты дикого типа. Последовательность нуклеиновой кислоты, кодирующая полипептид каспазы согласно изобретению, может быть кодон-оптимизированной. Одна или более модификаций в аминокислотной последовательности и/или последовательности нуклеиновой кислоты полипептида каспазы согласно изобретению могут увеличивать взаимодействие, перекрестное связывание, перекрестную активацию или активацию полипептида каспазы согласно изобретению по сравнению с аминокислотной последовательностью или последовательностью нуклеиновой кислоты дикого типа. В альтернативе или дополнительно, одна или более модификаций в аминокислотной последовательности и/или последовательности нуклеиновой кислоты полипептида каспазы согласно изобретению могут снижать иммуногенность полипептида каспазы согласно изобретению по сравнению с аминокислотной последовательностью или последовательностью нуклеиновой кислоты дикого типа.
[0660] Полипептиды каспазы согласно изобретению могут быть усеченными по сравнению с полипептидом каспазы дикого типа. Например, полипептид каспазы может быть усечен с целью удаления последовательности, кодирующей домен активации и рекрутинга каспазы (CARD), для устранения или сведения к минимуму возможности активации местного воспалительного ответа в дополнение к инициации апоптоза в клетке, включающей индуцируемый полипептид каспазы согласно изобретению. Последовательность нуклеиновой кислоты, кодирующая полипептид каспазы согласно изобретению, может быть сплайсирована с получением вариантной аминокислотной последовательности полипептида каспазы согласно изобретению по сравнению с полипептидом каспазы дикого типа. Полипептиды каспазы согласно изобретению могут кодироваться рекомбинантными и/или химерными последовательностями. Рекомбинантные и/или химерные полипептиды каспазы согласно изобретению могут включать последовательности из одного или более разных полипептидов каспазы. В альтернативе или дополнительно, рекомбинантные и/или химерные полипептиды каспазы согласно изобретению могут включать последовательности из одного или более биологических видов (например, человеческую последовательность и нечеловеческую последовательность). Полипептиды каспазы согласно изобретению могут быть неприродными.
[0661] Лигандсвязывающая область индуцируемого проапоптотического полипептида согласно изобретению может включать любую полипептидную последовательность, которая способствует димеризации или вызывает димеризацию первого индуцируемого проапоптотического полипептида согласно изобретению со вторым индуцируемым проапоптотическим полипептидом согласно изобретению, димеризация которых активирует или вызывает перекрестное сшивание проапоптотических полипептидов и инициацию апоптоза в клетке.
[0662] Лигандсвязывающая ("димеризационная") область может включать любой полипептид или его функциональный домен, который обеспечивает индукцию с использованием эндогенного или не встречающегося в природе лиганда (т.е. и индуцирующее средство), например, не встречающийся в природе синтетический лиганд. Лигандсвязывающая область может быть внутренней или внешней по отношению к клеточной мембране, в зависимости от природы индуцируемого проапоптотического полипептида и выбора лиганда (т.е. индуцирующего средства). Известен целый ряд лигандсвязывающих полипептидов и их функциональных доменов, включая рецепторы. Лигандсвязывающие области согласно изобретению могут включать одну или более последовательностей из рецептора. Особый интерес представляют лигандсвязывающие области, для которых лиганды (например, низкомолекулярные органические лиганды) известны или могут быть с легкостью получены. Такие лигандсвязывающие области или рецепторы могут включать, без ограничения перечисленными, FKBP и рецепторы циклофилина, рецепторы стероидов, рецептор тетрациклина и т.п., а также "неприродные" рецепторы, которые могут быть получены из антител, особенно из субъединицы тяжелой или легкой цепи, их мутантные последовательности, случайные аминокислотные последовательности, полученные стохастическими процедурами, комбинаторными синтезами и т.п. В некоторых вариантах осуществления лигандсвязывающая область выбрана из группы, состоящей из лигандсвязывающей области FKBP, лигандсвязывающей области рецептора циклофилина, лигандсвязывающей области рецептора стероида, лигандсвязывающей области рецепторов циклофилин и лигандсвязывающей области рецептора тетрациклина.
[0663] Лигандсвязывающие области, включающие один или более доменов рецептора, могут иметь длину по меньшей мере приблизительно 50 аминокислот и меньше чем приблизительно 350 аминокислот, обычно меньше чем 200 аминокислот, либо в виде эндогенного домена, либо его усеченной активной части. Связывающая область может быть, например, небольшой (<25 кДа, чтобы позволить эффективную трансфекцию в вирусных векторах), мономерной, неиммуногенной, содержать получаемые с помощью синтеза, способные проникать в клетку, нетоксичные лиганды, которые могут обладать способностью к димеризации.
[0664] Лигандсвязывающие области, включающие один или более доменов рецептора, могут быть внутриклеточными или внеклеточными, в зависимости от дизайна индуцируемого проапоптотического полипептида и доступности подходящего лиганда (т.е. индуцирующего средства). В случае гидрофобных лигандов связывающая область может быть расположена по обе стороны мембраны, однако для гидрофильных лигандов, особенно белковых лигандов, связывающая область обычно является внешней по отношению к клеточной мембране, если будет отсутствовать транспортная система для интернализации лиганда в форме, в которой он доступен для связывания. В случае внутриклеточного рецептора индуцируемый проапоптотический полипептид или транспозон, или вектор, включающий индуцируемый проапоптотический полипептид, могут кодировать сигнальный пептид и трансмембранный домен 5' или 3' относительно последовательности домена рецептора или могут иметь сигнальную последовательность присоединения липида 5' к последовательности домена рецептора. В случае, когда домен рецептора расположен между сигнальным пептидом и трансмембранным доменом, домен рецептора будет внеклеточным.
[0665] Антитела и субъединицы антител, например, тяжелая или легкая цепь, в частности, фрагменты, более конкретно вся или часть вариабельной области, или слитые конструкции тяжелой и легкой цепи для получения высокоаффинного связывания, могут применяться в качестве лигандсвязывающей области согласно изобретению. Предусмотренные антитела включают антитела, которые представляют собой эктопически экспрессируемый человеческий продукт, такой как внеклеточный домен, который не вызывает иммунного ответа и, как правило, не экспрессируется на периферии (то есть за пределами области ЦНС/головного мозга). Такие примеры включают, без ограничения перечисленным, низкоаффинный рецептор фактора роста нервов (LNGFR) и эмбриональные поверхностные белки (т.е. раково-эмбриональный антиген). Кроме того, антитела могут быть получены против гаптеновых молекул, которые являются физиологически приемлемыми, при этом отдельные субъединицы антител подвергают скринингу на аффинность связывания. кДНК, кодирующая субъединицы, может быть выделена и модифицирована путем делеции константной области, частей вариабельной области, мутагенеза вариабельной области и т.п., с получением домена связывающего белка, который обладает подходящей аффинностью к лиганду. Таким образом, почти любое физиологически приемлемое гаптеновое соединение может использоваться в качестве лиганда или для получения эпитопа для лиганда. Вместо единиц антител могут использоваться эндогенные рецепторы, где связывающая область или домен известны, а также существует пригодный или известный лиганд для связывания.
[0666] Для мультимеризации рецептора лиганд для лигандсвязывающей области/доменов рецептора индуцируемых проапоптотических полипептидов может быть мультимерным в том смысле, что лиганд может иметь по меньшей мере два сайта связывания, причем каждый из сайтов связывания будет способен связываться с рецепторной областью лиганда (т.е. лиганд, имеющий первый сайт связывания, будет способен связывать лиганд-связывающую область первого индуцируемого проапоптотического полипептида, а второй сайт связывания будет способен связывать лигандсвязывающую область второго индуцируемого проапоптотического полипептида, где лигандсвязывающие области первого и второго индуцируемых проапоптотических полипептидов будут либо идентичными, либо разными). Таким образом, при использовании в настоящем документе термин "мультимерная лигандсвязывающая область" относится к лигандсвязывающей области индуцируемого проапоптотического полипептида согласно изобретению, которая связывается с мультимерным лигандом. Мультимерные лиганды согласно изобретению включают димерные лиганды. Димерный лиганд согласно изобретению может иметь два сайта связывания, способные связываться с рецепторным доменом лиганда. В некоторых вариантах осуществления изобретения мультимерные лиганды согласно изобретению представляют собой димер или олигомер более высокого порядка, обычно не больше чем примерно тетрамерный, из небольших синтетических органических молекул, причем индивидуальные молекулы обычно имеют размер по меньшей мере приблизительно 150 Да и меньше чем приблизительно 5 кДа, обычно меньше чем приблизительно 3 кДа. Могут использоваться различные пары синтетических лигандов и рецепторов. Например, в вариантах осуществления с применением эндогенных рецепторов, димерный FK506 может использоваться с рецептором FKBP12, димеризованный циклоспорин А может использоваться с рецептором циклофилина, димеризованный эстроген - с эстрогеновым рецептором, димеризованные глюкокортикоиды - с глюкокортикоидным рецептором, димеризованный тетрациклин - с рецептором тетрациклина, димеризованный витамин D - с рецептором витамина D и т.п. В альтернативе могут использоваться более высокие порядки лигандов, например, тримерные. В случае вариантов осуществления, включающих не встречающиеся в природе рецепторы, например, субъединицы антител, модифицированные субъединицы антител, одноцепочечные антитела, состоящие из вариабельных областей тяжелой и легкой цепей в тандеме, разделенные гибким линкером, или модифицированные рецепторы, а также их мутантные последовательности и т.п., могут использовать любые из различных соединений. Существенной характеристикой единиц, входящих в мультимерный лиганд согласно изобретению, является то, что каждый сайт связывания способен связывать рецептор с высокой аффинностью, и, предпочтительно, что они могут быть димеризованы химически. Кроме того, существуют способы, позволяющие уравновесить гидрофобность/гидрофильность лигандов, чтобы они могли растворяться в сыворотке на функциональных уровнях, но при этом в большинстве применений диффундировать через плазматические мембраны.
[0667] Активация индуцируемых проапоптотических полипептидов согласно изобретению может быть выполнена, например, путем химически индуцированной димеризации (CID), опосредованной индуцирующим средством, с получением кондиционно контролируемого белка или полипептид. Проапоптотические полипептиды согласно изобретению не только могут быть индуцированы, но и индукция этих полипептидов также является обратимой вследствие деградации нестабильного димеризующего средства или введения мономерного конкурентного ингибитора.
[0668] В некоторых вариантах осуществления лигандсвязывающая область включает полипептид связывающего FK506 белка 12 (FKBP12). В некоторых вариантах осуществления лигандсвязывающая область включает полипептид FKBP12, содержащий замену валина (V) на фенилаланин (F) в положении 36 (F36V). В некоторых вариантах осуществления, в которых лигандсвязывающая область включает полипептид FKBP12, содержащий замену валина (V) на фенилаланин (F) в положении 36 (F36V), индуцирующее средство может включать AP1903, синтетическое лекарственное средство (название CAS: 1-[(2S)-1-оксо-2-(3,4,5-триметоксифенил)бутил]-1,2-этандиилбис[имино(2-оксо-2,1-этандиил)окси-3,1-фенилен[(1R)-3-(3,4-диметоксифенил)пропилиденовый]] сложный эфир 2-пиперидинкарбоновой кислоты, [2S-[1(R*),2R*[S*[S*[1(R*),2R*]]]]]-(9Cl) Регистрационный номер CAS: 195514-63-7; Молекулярная Формула: C78H98N4O20; Молекулярная масса: 1411,65)). В некоторых вариантах осуществления, в которых лигандсвязывающая область включает полипептид FKBP12, содержащий замену валина (V) на фенилаланин (F) в положении 36 (F36V), индуцирующее средство может включать AP20187 (Регистрационный номер CAS: 195514-80-8 и Молекулярная формула: C82H107N5O20). В некоторых вариантах осуществления индуцирующее средство является аналогом AP20187, таким как, например, AP1510. При использовании в настоящем документе индуцирующие средства AP20187, AP1903 и AP1510 могут использоваться попеременно.
[0669] AP1903 API производик Alphora Research Inc., и фармацевтический препарат AP1903 в форме для инъекций выпускает Formatech Inc. Он выпускается в форме раствора 5 мг/мл AP1903 в 25% растворе неионогенного солюбилизатора Solutol HS 15 (250 мг/мл, BASF). При комнатной температуре этот состав представляет собой прозрачный, слегка желтоватый раствор. При охлаждении этот состав подвергается обратимому фазовому переходу с образованием мутного раствора. Этот фазовый переход полностью устраняется после обратного нагревания до комнатной температуры. Заполненный объем составляет 2,33 мл в стеклянном флаконе объемом 3 мл (суммарно приблизительно 10 мг AP1903 для инъекции на флакон). После определения необходимости во введении AP1903, пациентам могут вводить, например, однократную фиксированную дозу AP1903 для инъекций (0,4 мг/кг) путем в/в инфузии в течение 2 часов, при использовании набора, стерилизованного без ДЭГФ и без этиленоксида. Дозу AP1903 рассчитывают индивидуально для всех пациентов и не производят повторный расчет, если масса тела не изменяется на ≥10%. Расчетную дозу разбавляют в 100 мл в 0,9% физрастворе перед инфузией. В предыдущем исследовании AP1903 Фазы I, 24 здоровых добровольца получали однократные дозы AP1903 для инъекций в дозах 0,01, 0,05, 0,1, 0,5 и 1,0 мг/кг путем в/в инфузии в течение 2 часов. Уровни AP1903 в плазме были прямо пропорциональны дозе со средними значениями Cmax в пределах от приблизительно 10-1275 нг/мл в диапазоне дозы 0,01-1,0 мг/кг. После начального периода инфузии, концентрации в крови демонстрировали фазу быстрого распределения со снижением уровней в плазме до приблизительно 18, 7 и 1% от максимальной концентрации через 0,5, 2 и 10 часов после введения дозы, соответственно. Было показано, что AP1903 для инъекций был безопасным и хорошо переносимым при всех уровнях дозы, и демонстрировал благоприятный фармакокинетический профиль (Iuliucci J D, et al., J Clin Pharmacol. 41:870-9, 2001).
[0670] Используемая фиксированная доза AP1903 для инъекций, например, может составлять 0,4 мг/кг путем внутривенной инфузии в течение 2 часов. Количество AP1903, требуемое in vitro для эффективной сигнализации клеток, составляет 10-100 нМ (MW 1600 Да). Это эквивалентно 16-160 мкг/л или ~0,016-1,6 мкг/кг (1,6-160 мкг/кг). Дозы до 1 мг/кг были хорошо переносимыми в исследовании AP1903 Фазы I, описанном выше. Поэтому доза 0,4 мг/кг может быть признана безопасной и эффективной дозой AP1903 для этого исследования Фазы I в комбинации с терапевтическими клетками.
[0671] Аминокислотная последовательность и/или последовательность нуклеиновой кислоты, кодирующая лигандсвязывающую область согласно изобретению, может содержать последовательность с одной или более модификациями по сравнению с аминокислотной последовательностью или последовательностью нуклеиновой кислоты дикого типа. Например, аминокислотная последовательность и/или последовательность нуклеиновой кислоты, кодирующая лигандсвязывающую область согласно изобретению, может быть кодон-оптимизированной последовательностью. Одна или более модификаций могут повышать аффинность связывания лиганда (например, индуцирующего средства) с лигандсвязывающей областью согласно изобретению по сравнению с полипептидом дикого типа. В альтернативе или дополнительно, одна или более модификаций могут снижать иммуногенность лигандсвязывающей области согласно изобретению по сравнению с полипептидом дикого типа. Лигандсвязывающие области согласно изобретению и/или индуцирующие средства согласно изобретению могут быть неприродными.
[0672] Индуцируемые проапоптотические полипептиды согласно изобретению включают лигандсвязывающую область, линкер и проапоптотический пептид, где индуцируемый проапоптотический полипептид не включает нечеловеческую последовательность. В некоторых вариантах осуществления нечеловеческая последовательность включает сайт рестрикции. Линкер может включать любой органический или неорганический материал, который позволяет, при димеризации лигандсвязывающей области, взаимодействие, перекрестное сшивание, перекрестную активацию или активацию проапоптотических полипептидов, таким образом, что взаимодействие или активация проапоптотических полипептидов инициируют апоптоз в клетке. В некоторых вариантах осуществления линкер является полипептидом. В некоторых вариантах осуществления линкер является полипептидом, включающим G/S богатую аминокислотную последовательность ("GS" линкер). В некоторых вариантах осуществления линкер является полипептидом, включающим аминокислотную последовательность GGGGS (SEQ ID NO:18024). В предпочтительных вариантах осуществления линкер является полипептидом, при этом нуклеиновая кислота, кодирующая полипептид, не содержит сайт рестрикции для эндонуклеазы рестрикции. Линкеры согласно изобретению могут быть неприродными.
[0673] Индуцируемые проапоптотические полипептиды согласно изобретению могут экспрессироваться в клетке под транскрипционной регуляцией любого промотора, способного инициировать и/или регулировать экспрессию индуцируемого проапоптотического полипептида согласно изобретению в такой клетке. Термин "промотор" при использовании в настоящем документе относится к промотору, который действует как первичный сайт связывания РНК-полимеразы, чтобы транскрибировать ген. Например, индуцируемые проапоптотические полипептиды согласно изобретению могут экспрессироваться в клетке млекопитающего под транскрипционной регуляцией любого промотора, способного инициировать и/или регулировать экспрессию индуцируемого проапоптотического полипептида согласно изобретению в клетке млекопитающего, в том числе, без ограничения перечисленными, нативных, эндогенных, экзогенных и гетерологичных промоторов. Предпочтительные клетки млекопитающих включают клетки человека. Таким образом, индуцируемые проапоптотические полипептиды согласно изобретению могут экспрессироваться в клетке человека под транскрипционной регуляцией любого промотора, способного инициировать и/или регулировать экспрессию индуцируемого проапоптотического полипептида согласно изобретению в клетке человека, в том числе, без ограничения перечисленными, человеческого промотора или вирусного промотора. Примерные промоторы для экспрессии в клетках человека включают, без ограничения перечисленным, предранний промотор генов цитомегаловируса человека (ЦМВ), ранний промотор SV40, длинный концевой повтор вируса саркомы Роуса, промотор β-актина, промотор инсулина крысы и промотор глицеральдегид-3-фосфатдегидрогеназы, каждый из которых может использоваться для получения интенсивной экспрессия индуцируемого проапоптотического полипептида согласно изобретению. Применение других вирусных промоторов или промоторов из клеток млекопитающих или бактериофагов, которые известны в уровне техники, для экспрессии индуцируемого проапоптотического полипептида согласно изобретению также предусмотрено, при условии, что уровни экспрессии будут достаточными для инициации апоптоза в клетке. При использовании промотора с известными свойствами можно оптимизировать уровень и профиль экспрессии представляющего интерес белка после трансфекции или трансформации.
[0674] Выбор промотора, который регулируется в ответ на специфические физиологические или синтетические сигналы, может обеспечить индуцируемую экспрессию индуцируемого проапоптотического полипептида согласно изобретению. Система экдизона (Invitrogen, Carlsbad, CA) является одной из таких систем. Эта система предназначена для регулируемой экспрессии представляющего интерес гена в клетках млекопитающих. Она состоит из строго регулируемого механизма экспрессии, который обеспечивает практически полное отсутствие экспрессии трансгена на базальном уровня, но повышаемой при индукции больше чем в 200 раз. Система основана на гетеродимерном рецепторе экдизона Drosophila, и когда экдизон или аналог, такой как муристерон А, связывается с рецептором, рецептор активирует промотор, включающий экспрессию нижестоящего трансгена, при этом достигаются высокие уровни мРНК транскриптов. В этой системе оба мономера гетеродимерного рецептора конститутивно экспрессируются с одного вектора, тогда как чувствительный к экдизону промотор, который направляет экспрессию представляющего интерес гена, находится на другой плазмиде. Таким образом, встраивание системы такого типа в представляющего интерес вектор может быть полезным. Другой индуцируемой системой, которая может быть полезной, является система Tet-OffTM или Tet-OnTM (Clontech, Palo Alto, CA), первоначально разработанная Госсеном и Бужардом (Gossen and Bujard, Proc. Natl. Acad. Sci. USA, 89:5547-5551, 1992; Gossen et al., Science, 268:1766-1769, 1995). Эта система также позволяет регулировать с высоким уровнем экспрессию генов в ответ на тетрациклин или производные тетрациклина, такие как доксициклин. В системе Tet-OnTM экспрессия гена включается в присутствии доксициклина, тогда как в системе Tet-OffTM экспрессия генов включается в отсутствие доксициклина. Эти системы основаны на двух регуляторных элементах, полученных из оперона устойчивости к тетрациклину E.coli: последовательности тетрациклинового оператора (с которой связывается тетрациклиновый репрессор) и тетрациклинового белка-репрессора. Интересующий ген клонируют в плазмиду после промотора, в котором присутствуют тетрациклин-чувствительные элементы. Вторая плазмида содержит регуляторный элемент, называемый тетрациклин-контролируемым трансактиватором, который в системе Tet-OffTM состоит из домена VP16 из вируса простого герпеса и тетрациклинового репрессора дикого типа. Таким образом, в отсутствие доксициклина транскрипция включена. В системе Tet-OnTM присутствует тетрациклиновый репрессор не дикого типа, который в присутствии доксициклина активирует транскрипцию. Для получения вектора для генной терапии можно использовать систему Tet-OffTM, чтобы клетки-продуценты можно было выращивать в присутствии тетрациклина или доксициклина и блокировать экспрессию потенциально токсичного трансгена, но когда вектор вводят пациенту, экспрессия гена будет конститутивно включена.
[0675] В некоторых обстоятельствах желательно регулировать экспрессию трансгена в векторе для генной терапии. Например, различные вирусные промоторы с различной величиной активности используются в зависимости от требуемого уровня экспрессии. В клетках млекопитающих предранний промотор ЦМВ часто используется для обеспечения сильной транскрипционной активации. Промотор ЦМВ описан в обзоре Donnelly, J. J., et al., 1997. Annu. Rev. Immunol. 15:617-48. Модифицированные версии промотора ЦМВ, которые являются менее сильными, также использовали, когда требовались пониженные уровни экспрессии трансгена. Когда требуется экспрессия трансгена в гемопоэтических клетках, часто используют ретровирусные промоторы, такие как LTR из MLV или MMTV. Другие вирусные промоторы, которые используются в зависимости от требуемого эффекта, включают SV40, LTR РСВ, LTR ВИЧ-1 и ВИЧ-2, аденовирусные промоторы, такие как промоторы из области E1A, E2A или MLP, LTR AAV, HSV-TK и вируса саркомы птиц.
[0676] В других примерах могут быть выбраны промоторы, которые регулируются развитием и активны в определенных дифференцированных клетках. Таким образом, например, промотор может быть неактивным в плюрипотентной стволовой клетке, но, например, когда плюрипотентная стволовая клетка дифференцируется в более зрелую клетку, промотор может активироваться.
[0677] Аналогичным образом, тканеспецифические промоторы используются, чтобы вызывать транскрипцию в конкретных тканях или клетках для снижения потенциальной токсичности или нежелательных эффектов в отношении нецелевых тканей. Эти промоторы могут приводить к снижению экспрессии по сравнению с более сильным промотором, таким как промотор ЦМВ, но также могут приводить к более ограниченной экспрессии и иммуногенности (Bojak, A., et al., 2002. Vaccine. 20:1975-79; Cazeaux, N., et al., 2002. Vaccine 20:3322-31). Например, в соответствующих случаях могут использоваться тканеспецифические промоторы, такие как ПСА-ассоциированный промотор или простатический специфический гландулярный калликреин, или ген мышечной креатинкиназы.
[0678] Примеры тканеспецифических или специфических для дифференцировки промоторов включают, без ограничения перечисленными, следующее: B29 (B-клетки); CD14 (моноцитарные клетки); CD43 (лейкоциты и тромбоциты); CD45 (гемопоэтические клетки); CD68 (макрофаги); десмин (мышца); эластаза-1 (ацинарные клетки поджелудочной железы); эндоглин (эндотелиальные клетки); фибронектин (дифференцирующийся клетки, рубцующиеся ткани); и Flt-1 (эндотелиальные клетки); GFAP (астроциты).
[0679] При некоторых показаниях желательно активировать транскрипцию в определенное время после введения вектора генной терапии. Это делается с использованием таких промоторов, которые регулируются гормонами или цитокинами. Промоторы, реагирующие на цитокины и воспалительные белки, которые могут использоваться, включают K и T кининоген (Kageyama et al., (1987) J. Biol. Chem., 262, 2345-2351), c-fos, ФНО-альфа, C-реактивный белок. (Arcone et al., (1988) Nucl. Acids Res., 16 (8), 3195-3207), гаптоглобин (Oliviero et al., (1987) EMBO J., 6, 1905-1912), сывороточный амилоид А2 C/EBP альфа, IL-1, IL-6 (Poli and Cortese, (1989) Proc. Nat'l Acad. Sci. USA, 86, 8202-8206), C3 комплемента (Wilson et al., (1990). Mol. Cell. Biol., 6181-6191), IL-8, альфа-1 кислый гликопротеин (Prowse and Baumann, (1988) Mol Cell Biol, 8, 42-51), антитрипсин альфа-1, липопротеинлипазу (Zechner et al. al., Mol. Cell. Biol., 2394-2401, 1988), ангиотензиноген (Ron, et al., (1991) Mol. Cell. Biol., 2887-2895), фибриноген, c-jun (индуцируемый сложными форболовыми эфирами, ФНО-альфа, ультрафиолетовым излучением, ретиноевой кислотой и перекисью водорода), коллагеназу (индуцируемую сложными форболовыми эфирами и ретиноевой кислотой), металлотионеин (индуцируемый тяжелыми металлами и глюкокортикоидами), стромелизин (индуцируемый сложным форболовым эфиром, интерлейкин-1 и EGF), макроглобулин альфа-2 и антихимотрипсин альфа-1. Другие промоторы включают, например, SV40, MMTV, вирус иммунодефицита человека (MV), вирус Молони, ALV, вирус Эпштейна-Барр, вирус саркомы Роуса, человеческий актин, миозин, гемоглобин и креатин.
[0680] Предполагается, что любой из вышеуказанных промоторов, отдельно или в комбинации с другим промотором, может применяться в зависимости от требуемого действия. Промоторы и другие регуляторные элементы выбирают таким образом, чтобы они функционировали в нужных клетках или тканях. Кроме того, этот список промоторов не следует считать исчерпывающим или ограничивающим; другие промоторы, которые используются в сочетании с промоторами и способами, раскрытыми в настоящем документе.
Стратегия "нокдауна" бронированных T-клеток
[0681] T-клетки согласно изобретению могут быть генетически модифицированы с целью улучшения их терапевтического потенциала. В альтернативе или дополнительно, T-клетки согласно изобретению могут быть модифицированы, чтобы сделать их менее чувствительными к иммунологическим и/или метаболическим контрольным точкам. Модификации этого типа "бронруют" T-клетки согласно изобретению, которые после модификации могут именоваться в настоящем документе как "бронированные" T-клетки. Бронированные T-клетки согласно изобретению могут быть получены, например, путем блокирования и/или ослабления специфических сигналов контрольных точек, обычно доставляемых T-клеткам (т.е. ингибирование контрольных точек), например, в иммуносупрессивном микроокружении опухоли.
[0682] В некоторых вариантах осуществления бронированная T-клетка согласно изобретению получена из T-клетки, NK-клетки, гемопоэтической клетки-предшественника, T-клетки из периферической крови (PB) (включая T-клетку, выделенную или полученную из Г-КСФ-мобилизованной периферической крови) или T-клетки из пуповинной крови (UCB). В некоторых вариантах осуществления бронированная T-клетка согласно изобретению включает один или более химерных рецепторов лиганда (CLR, включающих однодоменное антитело)/химерный антигенный рецептор (CAR, включающий белковый каркас, антитело, ScFv или антителомиметик), CARTирин (CAR, включающий Центирин) и/или VCAR (CAR, включающий VHH верблюдового или одиночный VH домен) согласно изобретению. В некоторых вариантах осуществления бронированная T-клетка согласно изобретению включает индуцируемый проапоптотический полипептид, включающий: (a) лигандсвязывающую область, (b) линкер и (c) усеченный полипептид каспазы 9, где индуцируемый проапоптотический полипептид не включает нечеловеческую последовательность. В некоторых вариантах осуществления нечеловеческая последовательность является сайтом рестрикции. В некоторых вариантах осуществления лигандсвязывающая область индуцируемого полипептида каспазы включает полипептид FK506 связывающего белка 12 (FKBP12). В некоторых вариантах осуществления аминокислотная последовательность полипептида FK506 связывающего белка 12 (FKBP12) включает модификацию в положении 36 последовательности. В некоторых вариантах осуществления модификация является заменой валина (V) на фенилаланин (F) в положении 36 (F36V). В некоторых вариантах осуществления бронированная T-клетка согласно изобретению включает экзогенную последовательность. В некоторых вариантах осуществления экзогенная последовательность включает последовательность, кодирующую терапевтический белок. Примерные терапевтические белки могут быть ядерными, цитоплазматическими, внутриклеточными, трансмембранными, связанными с клеточной поверхностью или секретируемыми белками. Примерные терапевтические белки, экспрессируемые бронированной T-клеткой, могут изменять активность бронированной T-клетки или могут изменять активность второй клетки. В некоторых вариантах осуществления бронированная T-клетка согласно изобретению включает селективный ген или селективный маркер. В некоторых вариантах осуществления бронированная T-клетка согласно изобретению включает синтетическую кассету экспрессии гена (также именуемую в настоящем документе как индуцируемая трансгенная конструкция).
[0683] В некоторых вариантах осуществления T-клетка согласно изобретению модифицирована, чтобы вызвать сайленсинг или снижение экспрессии одного или более генов, кодирующих рецептор(ы) ингибиторных сигналов контрольных точек с получением бронированной T-клетки согласно изобретению. Примеры ингибиторных сигналов контрольных точек включают, без ограничения перечисленным, связывание лиганда PD-L1 с рецептором PD-1 на CART-клетке согласно изобретению или связывание цитокина TGFβ с рецептором TGFβRII на CART-клетке. Рецепторы ингибиторных сигналов контрольных точек экспрессируются на клеточной поверхности или в цитоплазме T-клетки. Сайленсинг или снижение экспрессии гена, кодирующего рецептор сигнала ингибиторной контрольной точки, приводит к потере экспрессии белка рецепторов ингибирующей контрольной точки на поверхности или внутри цитоплазмы бронированной T-клетки согласно изобретению. Таким образом, бронированные T-клетки согласно изобретению с сайленсингом или сниженной экспрессией одного или более генов, кодирующих ингибирующий рецептор контрольной точки, являются устойчивыми, невосприимчивыми или нечувствительными к сигналам контрольных точек. Устойчивость или пониженная чувствительность бронированной T-клетки к сигналам контрольных точек повышает терапевтический потенциал бронированной T-клетки в присутствии таких сигналов контрольных точек. Ингибиторные сигналы контрольных точек включают, без ограничения перечисленными, примеры, перечисленные в Таблице 1. Примерные ингибиторные сигналы контрольных точек, которые могут быть подвергнуты сайленсингу в бронированной T-клетке согласно изобретению, включают, без ограничения перечисленными, PD-1 и TGFβRII.
[0684] Таблица 1. Примерные ингибиторные сигналы контрольных точек (и белки, которые вызывают иммуносупрессию). CSR согласно изобретению может включать эндодомен любого из белков в этой таблице.
[0685] В некоторых вариантах осуществления T-клетка согласно изобретению модифицирована, чтобы вызвать сайленсинг или снижение экспрессии одного или более генов, кодирующих внутриклеточные белки, участвующие в сигнализации контрольной точки, с получением бронированной T-клетки согласно изобретению. Активность T-клетки согласно изобретению может быть улучшена путем направленного воздействия на любой внутриклеточный сигнальный белок, участвующий в сигнальном пути контрольной точки, в результате чего достигается ингибирование контрольной точки или блокирование одного или более путей контрольных точек. Внутриклеточные сигнальные белки, участвующие в сигнализации контрольной точки, включают, без ограничения перечисленными, примерные внутриклеточные сигнальные белки, перечисленные в Таблице 2.
[0686] Таблица 2. Примерные внутриклеточные сигнальные белки.
[0687] В некоторых вариантах осуществления T-клетка согласно изобретению модифицирована, чтобы вызвать сайленсинг или снижение экспрессии одного или более генов, кодирующих фактор транскрипции, который снижает эффективность терапии, с получением бронированной T-клетки согласно изобретению. Активность бронированных T-клеток может улучшить или модулировать путем сайленсинга или снижения экспрессии (или подавления функции) фактора транскрипции, который снижает эффективность терапии. Примерные факторы транскрипции, которые могут быть модифицированы, чтобы вызвать сайленсинг или снижение экспрессии или подавление их функции, включают, без ограничения перечисленными, примерные факторы транскрипции, перечисленные в Таблице 3. Например, экспрессия гена FOXP3 в бронированной T-клетке согласно изобретению может быть подвергнута сайленсингу или снижена, чтобы предотвратить или уменьшить образование T регуляторных CAR-T-клеток (CAR-Treg клеток), экспрессия или активность которых может снижать эффективность терапии.
[0688] Таблица 3. Примерные факторы транскрипции.
[0689] В некоторых вариантах осуществления T-клетка согласно изобретению модифицирована, чтобы вызвать сайленсинг или снижение экспрессии одного или более генов, кодирующих рецептор клеточной смерти или апоптоза, с получением бронированной T-клетки согласно изобретению. Взаимодействие рецептора смерти и его эндогенного лиганда приводит к инициированию апоптоза. Блокирование экспрессии, активности или взаимодействия рецептора и/или лиганда клеточной смерти и/или апоптоза делает бронированную T-клетку согласно изобретению менее восприимчивой к сигналам смерти, делая, таким образом, бронированную T-клетку согласно изобретению более эффективной в окружении опухоли. Примерным рецептором клеточной смерти, который может быть модифицирован в бронированной T-клетке согласно изобретению, является Fas (CD95). Примерные рецепторы и лиганды клеточной смерти и/или апоптоза согласно изобретению включают, без ограничения перечисленными, примерные рецепторы и лиганды, представленные в Таблице 4.
[0690] Таблица 4. Примерные рецепторы и лиганды клеточной смерти и/или апоптоза.
[0691] В некоторых вариантах осуществления T-клетка согласно изобретению модифицирована, чтобы вызвать сайленсинг или снижение экспрессии одного или более генов, кодирующих метаболически чувствительный белок, с получением бронированной T-клетки согласно изобретению. Блокирование метаболической чувствительности иммуносупрессивного микроокружения опухоли (характеризуемого низкими уровнями кислорода, pH, глюкозы и других молекул) бронированной T-клеткой согласно изобретению приводит к более длительному сохранению T-клеточной функции и, следовательно, уничтожению большего количества опухолевых клеток каждой бронированной T-клеткой. Например, HIF1a и VHL играют роль в функции T-клеток, находящихся в гипоксическом окружении. Бронированная T-клетка согласно изобретению может иметь сайленсированную или сниженную экспрессию одного или более генов, кодирующих HIF1a или VHL. Гены и белки, участвующие в метаболической чувствительности, включают, без ограничения перечисленными, примерные гены и белки, представленные в Таблице 5.
[0692] Таблица 5. Примерные метаболически чувствительные гены (и кодируемые белки).
[0693] В некоторых вариантах осуществления T-клетка согласно изобретению модифицирована, чтобы вызвать сайленсинг или снижение экспрессии одного или более белков, кодирующих ген(ы), которые придают чувствительность к противоопухолевой терапии, включающей моноклональное антитело, с получением бронированной T-клетки согласно изобретению. Таким образом, бронированная T-клетка согласно изобретению может функционировать и может демонстрировать превосходную функцию или эффективность в присутствии противоопухолевой терапии (например, химиотерапии, терапии моноклональным антителом или другого противоопухолевого лечения). Белки, придающие чувствительность к противоопухолевой терапии, включают, без ограничения перечисленными, примерные белки, представленные в Таблице 6.
[0694] Таблица 6. Примерные белки, придающие чувствительность к противоопухолевому средству.
[0695] В некоторых вариантах осуществления T-клетка согласно изобретению модифицирована, чтобы вызвать сайленсинг или снижение экспрессии одного или более генов, кодирующих фактор преимущественного роста, с получением бронированной T-клетки. Сайленсинг или снижение экспрессии онкогена могут придавать преимущество роста бронированной T-клетке согласно изобретению. Например, сайленсинг или снижение экспрессии (например, блокирование экспрессии) гена TET2 в процессе производства CAR-T приводит к получению бронированной CAR-T со значительной способностью к экспансии и последующему уничтожению опухоли по сравнению с небронированной CAR-T, не обладающей способностью к экспансии. Такая стратегия может быть соединена с предохранительным выключателем (например, предохранительным выключателем iC9 согласно изобретению), который обеспечивает направленное разрушение бронированной CAR-T-клетки в случае нежелательной реакции у индивида или неконтролируемого роста бронированной CAR-T. Примерные факторы преимущественного роста включают, без ограничения перечисленными, факторы, представленные в Таблице 7.
[0696] Таблица 7. Примерные факторы преимущественного роста.
Стратегия "нулевого или переключаемого рецептора" бронированных T-клеток
[0697] В некоторых вариантах осуществления T-клетка согласно изобретению модифицирована для экспрессии модифицированного/химерного рецептора контрольной точки с получением бронированной T-клетки согласно изобретению.
[0698] В некоторых вариантах осуществления модифицированный/химерный рецептор контрольной точки включает нулевой рецептор, рецептор-ловушку или доминантно-негативный рецептор. Нулевой рецептор, рецептор-ловушка или доминантно-негативный рецептор согласно изобретению могут быть модифицированным/химерным рецептором/белком. Нулевой рецептор, рецептор-ловушка или доминантно-негативный рецептор согласно изобретению могут быть усечены для экспрессии внутриклеточного сигнального домена. В альтернативе или дополнительно, нулевой рецептор, рецептор-ловушка или доминантно-негативный рецептор согласно изобретению могут быть подвергнуты мутации во внутриклеточном сигнальном домене по одному или более аминокислотным положениям, которые являются определяющими или необходимыми для эффективной сигнализации. Усечение или мутация нулевого рецептора, рецептора-ловушки или доминантно-негативного рецептора согласно изобретению могут приводить к потере способности рецептора передавать или преобразовывать сигнал контрольной точки в клетку или внутри клетки.
[0699] Например, ослабление или блокирование иммуносупрессивного сигнала контрольной точки от рецептора PD-L1, экспрессируемого на поверхности опухолевой клетки, может быть достигнуто путем экспрессии модифицированного/химерного PD-1 нулевого рецептора на поверхности бронированной T-клетки согласно изобретению, эффективно конкурирующего с эндогенными (немодифицированными) рецепторами PD-1, также экспрессируемыми на поверхности бронированной T-клетки, уменьшая или ингибируя трансдукцию иммуносупрессивного сигнала контрольной точки через эндогенные рецепторы PD-1 бронированной T-клетки. В этом примере осуществления конкуренция между двумя разными рецепторами за связывание с PD-L1, экспрессируемым на опухолевой клетке, снижает или уменьшает уровень эффективной сигнализации контрольной точки, повышая, таким образом, терапевтический потенциал бронированной T-клетки, экспрессирующей PD-1 нулевой рецептор.
[0700] В некоторых вариантах осуществления модифицированный/химерный рецептор контрольной точки включает нулевой рецептор, рецептор-ловушку или доминантно-негативный рецептор, который является трансмембранным рецептором.
[0701] В некоторых вариантах осуществления модифицированный/химерный рецептор контрольной точки включает нулевой рецептор, рецептор-ловушку или доминантно-негативный рецептор, который является мембраноассоциированным или мембраносвязанным рецептором/белком.
[0702] В некоторых вариантах осуществления модифицированный/химерный рецептор контрольной точки включает нулевой рецептор, рецептор-ловушку или доминантно-негативный рецептор, который является внутриклеточным рецептором/белком.
[0703] В некоторых вариантах осуществления модифицированный/химерный рецептор контрольной точки включает нулевой рецептор, рецептор-ловушку или доминантно-негативный рецептор, который является внутриклеточным рецептором/белком. Примерные нулевые, ловушки или доминантно-негативные внутриклеточные рецепторы/белки согласно изобретению включают, без ограничения перечисленными, сигнальные компоненты после ингибиторного сигнала контрольной точки (как представлено, например, в Таблицах 1 и 2), фактор транскрипции (как представлено, например, в Таблице 3), цитокин или рецептор цитокина, хемокин или рецептор хемокина, рецептор/лиганд клеточной смерти или апоптоза (как представлено, например, в Таблице 4), метаболически чувствительную молекулу (как представлено, например, в Таблице 5), белок, придающий чувствительность к противоопухолевой терапии (как представлено, например, в Таблице 6), и онкоген или ген-супрессор опухоли (как представлено, например, в Таблице 7). Примерные цитокины, рецепторы цитокинов, хемокины и рецепторы хемокинов согласно изобретению включают, без ограничения перечисленными, цитокины и рецепторы цитокинов, а также хемокины и рецепторы хемокинов, представленные в Таблице 8.
[0704] Таблица 8. Примерные цитокины, рецепторы цитокинов, хемокины и рецепторы хемокинов.
[0705] В некоторых вариантах осуществления модифицированный/химерный рецептор контрольной точки включает переключаемый рецептор. Примерные переключаемые рецепторы могут включать модифицированный/химерный рецептор/белок согласно изобретению, в котором внутриклеточный сигнальный домен, нативный или дикого типа, переключают или заменяют другим внутриклеточным сигнальным доменом, который является ненативным для белка и/или доменом не дикого типа. Например, замена ингибирующего сигнального домена стимулирующим сигнальным доменом будет переключать иммуносупрессивный сигнал на иммуностимулирующий сигнал. В альтернативе замена ингибирующего сигнального домена другим ингибирующим доменом может снизить или повысит уровень ингибирующей сигнализации. Экспрессия или оверэкспрессия переключаемого рецептора может привести к ослаблению и/или блокированию когнатного сигнала контрольной точки в результате конкуренции с эндогенным рецептором контрольной точки дикого типа (не переключаемым рецептором) за связывание с когнатным рецептором контрольной точки, экспрессируемым в иммуносупрессивном микроокружении опухоли. Бронированные T-клетки согласно изобретению могут включать последовательность, кодирующую переключаемые рецепторы согласно изобретению, что приводит к экспрессии одного или более переключаемых рецепторов согласно изобретению и, следовательно, изменяет активность бронированной T-клетки согласно изобретению. Бронированные T-клетки согласно изобретению могут экспрессировать переключаемый рецептор согласно изобретению, который направляет внутриклеточно экспрессируемый белок, после рецептора контрольной точки, фактора транскрипции, цитокинового рецептора, рецептора смерти, метаболически чувствительной молекулы, противоопухолевого средства, онкогена и/или белка или гена-супрессора опухоли согласно изобретению.
[0706] Примерные переключаемые рецепторы согласно изобретению могут включать или могут быть получены из белка, включающего, без ограничения перечисленными, сигнальные компоненты после ингибирующего сигнала контрольной точки (как представлено, например, в Таблицах 1 и 2), фактора транскрипции (как представлено, например, в Таблице 3), цитокина или рецептора цитокина, хемокина или рецептор хемокина, рецептора/лиганда клеточной смерти или апоптоза (как представлено, например, в Таблице 4), метаболически чувствительной молекулы (как представлено, например, в Таблице 5), белка, придающего чувствительность к противоопухолевой терапии (как представлено, например, в Таблице 6), и онкогена или ген-супрессора опухоли (как представлено, например, в Таблице 7). Примерные цитокины, рецепторы цитокинов, хемокины и рецепторы хемокинов согласно изобретению включают, без ограничения перечисленным, цитокины и рецепторы цитокинов, а также хемокины и рецепторы хемокинов, представленные в Таблице 8.
Бронированные T-клетки - кондиционно регулируемая система экспрессии генов
[0707] В некоторых вариантах осуществления T-клетка согласно изобретению модифицирована для экспрессии химерного рецептора лиганда (CLR) или химерного антигенного рецептора (CAR), который опосредует кондиционную экспрессию гена, с получением бронированной T-клетки согласно изобретению. Комбинация CLR/CAR и кондиционной системы экспрессии гена в ядре бронированной T-клетки составляет систему экспрессии синтетического гена, кондиционно активируемую при связывании когнатного лиганда(ов) с CLR или когнатного антигена(ов) с CAR. Эта система может помочь в 'бронировании' или повышении терапевтического потенциала модифицированных T-клеток путем снижения или ограничения экспрессии синтетического гена на сайте связывания лиганда или антигена, например, в или внутри окружения опухоли.
Экзогенные рецепторы
[0708] В некоторых вариантах осуществления бронированная T-клетка включает композицию, включающую: (a) индуцируемую трансгенную конструкцию, включающую последовательность, кодирующую индуцируемый промотор, и последовательность, кодирующую трансген, и (b) рецепторную конструкцию, включающую последовательность, кодирующую конститутивный промотор, и последовательность, кодирующую экзогенный рецептор, такой как CLR или CAR, где при интеграции конструкции (a) и конструкции (b) в геномную последовательность клетки экспрессируется экзогенный рецептор, и где экзогенный рецептор при связывании лиганда или антигена преобразует внутриклеточный сигнал, который напрямую или ненапрямую направленно взаимодействует с индуцируемым промотором, регулирующим экспрессию индуцируемого трансгена (a), изменяя экспрессию гена.
[0709] В некоторых вариантах осуществления системы экспрессии синтетического гена согласно изобретению, композиция изменяет экспрессию гена путем уменьшения экспрессии гена. В некоторых вариантах осуществления композиция изменяет экспрессию гена путем транзиентного изменения экспрессии гена (например, в течение времени связывания лиганда с экзогенным рецептором). В некоторых вариантах осуществления композиция кратковременно изменяет экспрессию гена (например, лиганд обратимо связывается с экзогенным рецептором). В некоторых вариантах осуществления композиция изменяет экспрессию гена длительно (например, лиганд необратимо связывается с экзогенным рецептором).
[0710] В некоторых вариантах осуществления композиций согласно изобретению, экзогенный рецептор (b) включает эндогенный рецептор по отношению к геномной последовательности клетки. Примерные рецепторы включают, без ограничения перечисленными, внутриклеточные рецепторы, рецепторы клеточной поверхности, трансмембранные рецепторы, лиганд-регулируемые ионные каналы и сопряженные с G-белком рецепторы.
[0711] В некоторых вариантах осуществления композиций согласно изобретению, экзогенный рецептор (b) включает не встречающийся в природе рецептор. В некоторых вариантах осуществления не встречающийся в природе рецептор является синтетическим, модифицированным, рекомбинантным, мутантным или химерным рецептором. В некоторых вариантах осуществления не встречающийся в природе рецептор включает одну или более последовательностей, выделенных или полученных из T-клеточного рецептора (TCR). В некоторых вариантах осуществления не встречающийся в природе рецептор включает одну или более последовательностей, выделенных или полученных из каркасного белка. В некоторых вариантах осуществления, включающих такие, где не встречающийся в природе рецептор не включает трансмембранный домен, не встречающийся в природе рецептор взаимодействует со вторым трансмембранным, мембраносвязанным и/или внутриклеточным рецептором, который после контакта с не встречающимся в природе рецептором преобразует внутриклеточный сигнал.
[0712] В некоторых вариантах осуществления композиций согласно изобретению, экзогенный рецептор (b) включает не встречающийся в природе рецептор. В некоторых вариантах осуществления не встречающийся в природе рецептор является синтетическим, модифицированным, рекомбинантным, мутантным или химерным рецептором. В некоторых вариантах осуществления не встречающийся в природе рецептор включает одну или более последовательностей, выделенных или полученных из T-клеточного рецептора (TCR). В некоторых вариантах осуществления не встречающийся в природе рецептор включает одну или более последовательностей, выделенных или полученных из каркасного белка. В некоторых вариантах осуществления не встречающийся в природе рецептор включает трансмембранный домен. В некоторых вариантах осуществления не встречающийся в природе рецептор взаимодействует с внутриклеточным рецептором, преобразующим внутриклеточный сигнал. В некоторых вариантах осуществления не встречающийся в природе рецептор включает внутриклеточный сигнальный домен. В некоторых вариантах осуществления не встречающийся в природе рецептор является химерным рецептором лиганда (CLR). В некоторых вариантах осуществления CLR является химерным антигенным рецептором (CAR).
[0713] В некоторых вариантах осуществления композиций согласно изобретению, экзогенный рецептор (b) включает не встречающийся в природе рецептор. В некоторых вариантах осуществления CLR является химерным антигенным рецептором (CAR). В некоторых вариантах осуществления химерный рецептор лиганда включает (a) эктодомен, включающий область распознавания лиганда, где область распознавания лиганда включает по меньшей мере каркасный белок; (b) трансмембранный домен и (c) эндодомен, включающий по меньшей мере один костимулирующий домен. В некоторых вариантах осуществления эктодомен (a) дополнительно включает сигнальный пептид. В некоторых вариантах осуществления эктодомен (a) дополнительно включает шарнирную область между областью распознавания лиганда и трансмембранным доменом.
[0714] В некоторых вариантах осуществления CLR/CAR-рецепторов согласно изобретению сигнальный пептид включает последовательность, кодирующую человеческий CD2, CD3δ, CD3ε, CD3γ, CD3ζ, CD4, CD8α, CD19, CD28, 4-1BB или сигнальный пептид GM-CSFR. В некоторых вариантах осуществления сигнальный пептид включает последовательность, кодирующую человеческий сигнальный пептид CD8α. В некоторых вариантах осуществления сигнальный пептид включает аминокислотную последовательность, включающую MALPVTALLLPLALLLHAARP (SEQ ID NO:17503). В некоторых вариантах осуществления сигнальный пептид кодируется последовательностью нуклеиновой кислоты, включающей atggcactgccagtcaccgccctgctgctg cctctggctctgctgctgcacgcagctagacca (SEQ ID NO:17504).
[0715] В некоторых вариантах осуществления CLR/CAR-рецепторов согласно изобретению трансмембранный домен включает последовательность, кодирующую человеческий CD2, CD3δ, CD3ε, CD3γ, CD3ζ, CD4, CD8α, CD19, CD28, 4-1BB или трансмембранный домен GM-CSFR. В некоторых вариантах осуществления трансмембранный домен включает последовательность, кодирующую трансмембранный домен человеческого CD8α. В некоторых вариантах осуществления трансмембранный домен включает аминокислотную последовательность, включающую IYIWAPLAGTCGVLLLSLVITLYC (SEQ ID NO:17505). В некоторых вариантах осуществления трансмембранный домен кодируется последовательностью нуклеиновой кислоты, включающей atctacatttgggcaccactggccgggacctgtggagtgctgctgctgagcct ggtcatcacactgtactgc (SEQ ID NO:17506).
[0716] В некоторых вариантах осуществления CLR/CAR-рецепторов согласно изобретению эндодомен включает эндодомен человеческого CD3ζ. В некоторых вариантах осуществления по меньшей мере один костимулирующий домен включает внутриклеточный сегмент человеческого 4-1BB, CD28, CD3ζ, CD40, ICOS, MyD88, OX-40 или их любую комбинацию. В некоторых вариантах осуществления по меньшей мере один костимулирующий домен включает костимулирующий домен человеческого CD3ζ и/или 4-1BB. В некоторых вариантах осуществления костимулирующий домен CD3ζ включает аминокислотную последовательность, включающую RVKFSRSADAPAYKQGQNQLYNELNLGRREE YDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR (SEQ ID NO:17507). В некоторых вариантах осуществления костимулирующий домен CD3ζ кодируется последовательностью нуклеиновой кислоты, включающей cgcgtgaagtttagtcgatcagcagatgccccagcttacaaacagggacagaaccagctgtataacgagctgaatctgggccgccgagaggaatatgacgtgctggataagcggagaggacgcgaccccgaaatgggaggcaagcccaggcgcaaaaaccctcaggaaggcctgtataacgagctgcagaaggacaaaatggcagaagcctattctgagatcggcatgaagggggagcgacggagaggcaaagggcacgatgggctgtaccagggactgagcaccgccacaaaggacacctatgatgctctgcatatgcaggcactgcctccaagg (SEQ ID NO:17508). В некоторых вариантах осуществления 4-1BB костимулирующий домен включает аминокислотную последовательность, включающую KRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCEL (ID NO:17509 SEQ). В некоторых вариантах осуществления костимулирующий домен 4-1BB кодируется последовательностью нуклеиновой кислоты, включающей aagagaggcaggaagaaactgctgtatattttcaaacagcccttcatgcgccccgtgcagactacccaggaggaagacgggtgctcctgtcgattccctgaggaagaggaaggcgggtgtgagctg (SEQ ID NO:17510). В некоторых вариантах осуществления костимулирующий домен 4-1BB расположен между трансмембранным доменом и костимулирующим доменом CD3ζ.
В некоторых вариантах осуществления CLR/CAR-рецепторов согласно изобретению шарнирная область включает последовательность, полученную из последовательности человеческого CD8α, IgG4 и/или CD4. В некоторых вариантах осуществления шарнирная область включает последовательность, полученную из последовательности человеческого CD8α. В некоторых вариантах осуществления шарнирная область включает аминокислотную последовательность, включающую TTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACD (SEQ ID NO:17511). В некоторых вариантах осуществления шарнирная область кодируется последовательностью нуклеиновой кислоты, включающей actaccacaccagcacctagaccaccaactccagctccaaccatcgcgagtcagcccctgagtctgagacctgaggcctgcaggccagctgcaggaggagctgtgcacaccaggggcctggacttcgcctgcgac (SEQ ID NO:17512). В некоторых вариантах осуществления шарнирная область кодируется последовательностью ACCACAACCCCTGCCCCCAGACCTCCCACACCCGCCCCTACCATCGCGAGTCAGCCCCTGAGTCTGAGACCTGAGGCCTGCAGGCCAGCTGCAGGAGGAGCTGTGCACACCAGGGGCCTGGACTTCGCCTGCGAC (SEQ ID NO:17513).
[0717] В некоторых вариантах осуществления по меньшей мере один белковый каркас специфично связывает лиганд.
[0718] В некоторых вариантах осуществления композиций согласно изобретению экзогенный рецептор (b) включает не встречающийся в природе рецептор. В некоторых вариантах осуществления CLR является химерным антигенным рецептором (CAR). В некоторых вариантах осуществления химерный рецептор лиганда включает (a) эктодомен, включающий область распознавания лиганда, где область распознавания лиганда включает по меньшей мере каркасный белок; (b) трансмембранный домен и (c) эндодомен, включающий по меньшей мере один костимулирующий домен. В некоторых вариантах осуществления по меньшей мере один белковый каркас включает антитело, фрагмент антитела, однодоменное антитело, одноцепочечное антитело, антителомиметик или Центирин (именуемый в настоящем документе как CARTирин). В некоторых вариантах осуществления область распознавания лиганда включает одно или более из антитела, фрагмента антитела, однодоменного антитела, одноцепочечного антитела, антителомиметика и Центирина. В некоторых вариантах осуществления однодоменное антитело включает или состоит из VHH или VH (именуемого в настоящем документе как VCAR). В некоторых вариантах осуществления однодоменное антитело включает или состоит из VHH или VH, включающего человеческие определяющие комплементарность области (CDR-области). В некоторых вариантах осуществления VH является рекомбинантным или химерным белком. В некоторых вариантах осуществления VH является рекомбинантным или химерным человеческим белком. В некоторых вариантах осуществления антителомиметик включает или состоит из аффитела, аффилина, аффимера, аффитина, альфатела, антикалина, авимера, дарпина, финомера, пептида с доменом Kunitz или монотела. В некоторых вариантах осуществления Центирин включает или состоит из консенсусной последовательности по меньшей мере одного домена фибронектина III типа (FN3).
[0719] В некоторых вариантах осуществления композиций согласно изобретению экзогенный рецептор (b) включает не встречающийся в природе рецептор. В некоторых вариантах осуществления CLR является химерным антигенным рецептором (CAR). В некоторых вариантах осуществления химерный рецептор лиганда включает (a) эктодомен, включающий область распознавания лиганда, где область распознавания лиганда включает по меньшей мере каркасный белок; (b) трансмембранный домен и (c) эндодомен, включающий по меньшей мере один костимулирующий домен. В некоторых вариантах осуществления Центирин включает или состоит из консенсусной последовательности по меньшей мере одного домена фибронектина III типа (FN3). В некоторых вариантах осуществления по меньшей мере один домен фибронектина III типа (FN3) получен из человеческого белка. В некоторых вариантах осуществления человеческим белком является Тенасцин-C. В некоторых вариантах осуществления консенсусная последовательность включает LPAPKNLVVSEVTEDSLRLSWTAPDAAFDSFLIQYQESEKVGEAINLTVPGSERSYDLTGLKPGTEYTVSIYGVKGGHRSNPLSAEFTT (SEQ ID NO:17514). В некоторых вариантах осуществления консенсусная последовательность включает MLPAPKNLVVSEVTEDSLRLSWTAPDAAFDSFLIQYQESEKVGEAINLTVPGSERSYDLTGLKPGTEYTVSIYGVKGGHRSNPLSAEFTT (SEQ ID NO:17515). В некоторых вариантах осуществления консенсусная последовательность модифицирована по одному или более положениям внутри (a) A-B петли, включающей или состоящей из аминокислотных остатков TEDS (SEQ ID NO:17516) в положениях 13-16 консенсусной последовательности; (b) B-C петли, включающей или состоящей из аминокислотных остатков TAPDAAF (SEQ ID NO:17517) в положениях 22-28 консенсусной последовательности; (c) C-D петли, включающей или состоящей из аминокислотных остатков SEKVGE (SEQ ID NO:17518) в положениях 38-43 консенсусной последовательности; (d) D-E петли, включающей или состоящей из аминокислотных остатков GSER (SEQ ID NO:17519) в положениях 51-54 консенсусной последовательности; (e) E-F петли, включающей или состоящей из аминокислотных остатков GLKPG (SEQ ID NO:17520) в положениях 60-64 консенсусной последовательности; (f) F-G петли, включающей или состоящей из аминокислотных остатков KGGHRSN (SEQ ID NO:17521) в положениях 75-81 консенсусной последовательности; или (g) любой комбинации (a)-(f). В некоторых вариантах осуществления Центирин включает консенсусную последовательность по меньшей мере 5 доменов фибронектина III типа (FN3). В некоторых вариантах осуществления Центирин включает консенсусную последовательность по меньшей мере 10 доменов фибронектина III типа (FN3). В некоторых вариантах осуществления Центирин включает консенсусную последовательность по меньшей мере 15 доменов фибронектина III типа (FN3). В некоторых вариантах осуществления каркас связывает антиген по меньшей мере с одной аффинностью, выбранной из KD, меньше или равной 10-9 М, меньше или равной 10-10 М, меньше или равной 10-11 М, меньше или равной 10-12 M, меньше или равной 10-13 M, меньше или равной 10-14 M и меньше или равной 10-15 M. В некоторых вариантах осуществления KD определяют с помощью поверхностного плазмонного резонанса.
Индуцируемые промоторы
[0720] В некоторых вариантах осуществления композиций согласно изобретению последовательность, кодирующая индуцируемый промотор (a), включает последовательность, кодирующую промотор NFκB. В некоторых вариантах осуществления композиций согласно изобретению последовательность, кодирующая индуцируемый промотора (a), включает последовательность, кодирующую промотор интерферона (IFN), или последовательность, кодирующую промотора интерлейкина-2. В некоторых вариантах осуществления промотор интерферона (IFN) является промотором IFNγ. В некоторых вариантах осуществления композиций согласно изобретению индуцируемый промотор выделен или получен из промотора цитокина или хемокина. В некоторых вариантах осуществления цитокин или хемокин включает IL2, IL3, IL4, IL5, IL6, IL10, IL12, IL13, IL17A/F, IL21, IL22, IL23, трансформирующий фактор роста бета (TGFβ), колониестимулирующий фактор 2 (ГМ-КСФ), интерферон (IFNγ), фактор некроза опухоли (ФНОα), LTα, перфорин, Гранзим C (Gzmc), Гранзим B (Gzmb), лиганд хемокина с C-C мотивом 5 (CCL5), лиганд хемокина мотива C-C 4 (Ccl4), лиганд хемокина с C-C мотивом 3 (Ccl3), лиганд хемокина с X-C мотивом 1 (Xcl1) и цитокин семейства интерлейкина 6 LIF (Lif).
[0721] В некоторых вариантах осуществления композиций согласно изобретению индуцируемый промотор выделен или получен из промотора гена, включающего поверхностный белок, участвующий в клеточной дифференцировке, активации, истощении и функции. В некоторых вариантах осуществления ген включает CD69, CD71, CTLA4, PD-1, TIGIT, LAG3, TIM-3, GITR, MHCII, COX-2, FASL и 4-1BB.
[0722] В некоторых вариантах осуществления композиций согласно изобретению индуцируемый промотор выделен или получен из промотора гена, участвующего в CD метаболизме и дифференцировке. В некоторых вариантах осуществления композиций согласно изобретению индуцируемый промотор выделен или получен из промотора Nr4a1, Nr4a3, Tnfrsf9 (4-1BB), Sema7a, Zfp36l2, Gadd45b, Dusp5, Dusp6 и Neto2.
Индуцируемый трансген
[0723] В некоторых вариантах осуществления конструкция индуцируемого трансгена включает или направляет экспрессию сигнального компонента после ингибирующего сигнала контрольной точки (как представлено, например, в Таблицах 1 и 2), фактора транскрипции (как представлено, например, в Таблице 3), цитокина или рецептор цитокина, хемокина или рецептор хемокина, рецептора/лиганда клеточной смерти или апоптоза (как представлено, например, в Таблице 4), метаболически чувствительной молекулы (как представлено, например, в Таблице 5), белка, придающего чувствительность к противоопухолевой терапии (как представлено, например, в Таблице 6 или 9), и онкогена или гена-супрессора опухоли (как представлено, например, в Таблице 7). Примерные цитокины, рецепторы цитокинов, хемокины и рецепторы хемокинов согласно изобретению включают, без ограничения перечисленными, цитокины и рецепторы цитокинов, а также хемокины и рецепторы хемокинов, представленные в Таблице 8.
[0724] Таблица 9. Примерные терапевтические белки (и белки для повышения эффективности CAR-T).
Cas-Clover
[0725] В изобретении предложена композиция, включающая гидовую РНК и слитый белок или последовательность, кодирующую слитый белок, где слитый белок включает dCas9 и Clo051 эндонуклеазу или ее нуклеазный домен.
Малая Cas9 (SaCas9)
[0726] В изобретении предложены композиции, включающие малую Cas9 (Cas9), функционально связанную с эффектором. В некоторых вариантах осуществления в изобретении предложен слитый белок, включающий, состоящий по существу из или состоящий из компонента локализации ДНК и эффекторной молекулы, где эффектор включает малую Cas9 (Cas9). В некоторых вариантах осуществления конструкция малой Cas9 согласно изобретению может включать эффектор, включающий эндонуклеазу IIS типа.
[0727] Аминокислотная последовательность Cas9 Staphylococcus aureus с активным каталитическим центром.
61 rhriqrvkkl lfdynlltdh selsginpye arvkglsqkl seeefsaall hlakrrgvhn
121 vneveedtgn elstkeqisr nskaleekyv aelqlerlkk dgevrgsinr fktsdyvkea
181 kqllkvqkay hqldqsfidt yidlletrrt yyegpgegsp fgwkdikewy emlmghctyf
241 peelrsvkya ynadlynaln dlnnlvitrd enekleyyek fqiienvfkq kkkptlkqia
301 keilvneedi kgyrvtstgk peftnlkvyh dikditarke iienaelldq iakiltiyqs
361 sediqeeltn lnseltqeei eqisnlkgyt gthnlslkai nlildelwht ndnqiaifnr
421 lklvpkkvdl sqqkeipttl vddfilspvv krsfiqsikv inaiikkygl pndiiielar
481 eknskdaqkm inemqkrnrq tnerieeiir ttgkenakyl iekiklhdmq egkclyslea
541 ipledllnnp fnyevdhiip rsvsfdnsfn nkvlvkqeen skkgnrtpfq ylsssdskis
601 yetfkkhiln lakgkgrisk tkkeylleer dinrfsvqkd finrnlvdtr yatrglmnll
661 rsyfrvnnld vkvksinggf tsflrrkwkf kkernkgykh haedaliian adfifkewkk
721 ldkakkvmen qmfeekqaes mpeieteqey keifitphqi khikdfkdyk yshrvdkkpn
781 relindtlys trkddkgntl ivnnlnglyd kdndklkkli nkspekllmy hhdpqtyqkl
841 klimeqygde knplykyyee tgnyltkysk kdngpvikki kyygnklnah lditddypns
901 rnkvvklslk pyrfdvyldn gvykfvtvkn ldvikkenyy evnskcyeea kklkkisnqa
961 efiasfynnd likingelyr vigvnndlln rievnmidit yreylenmnd krppriikti
1021 asktqsikky stdilgnlye vkskkhpqii kkg (SEQ ID NO:18040).
Инактивированная, малая Cas9 (dSaCas9)
[0728] В изобретении предложены композиции, включающие инактивированную, малую Cas9 (dSaCas9), функционально связанную с эффектором. В некоторых вариантах осуществления в изобретении предложен слитый белок, включающий, состоящий по существу из или состоящий из компонента локализации ДНК и эффекторной молекулы, где эффектор включает малую, инактивированную Cas9 (dSaCas9). В некоторых вариантах осуществления конструкция малой, инактивированной Cas9 (dSaCas9) согласно изобретению может включать эффектор, включающий эндонуклеазу IIS типа.
[0729] Последовательность dSaCas9: мутации D10A и N580A (выделены полужирным шрифтом, заглавными буквами и подчеркнуты) инактивируют каталитический центр.
61 rhriqrvkkl lfdynlltdh selsginpye arvkglsqkl seeefsaall hlakrrgvhn
121 vneveedtgn elstkeqisr nskaleekyv aelqlerlkk dgevrgsinr fktsdyvkea
181 kqllkvqkay hqldqsfidt yidlletrrt yyegpgegsp fgwkdikewy emlmghctyf
241 peelrsvkya ynadlynaln dlnnlvitrd enekleyyek fqiienvfkq kkkptlkqia
301 keilvneedi kgyrvtstgk peftnlkvyh dikditarke iienaelldq iakiltiyqs
361 sediqeeltn lnseltqeei eqisnlkgyt gthnlslkai nlildelwht ndnqiaifnr
421 lklvpkkvdl sqqkeipttl vddfilspvv krsfiqsikv inaiikkygl pndiiielar
481 eknskdaqkm inemqkrnrq tnerieeiir ttgkenakyl iekiklhdmq egkclyslea
541 ipledllnnp fnyevdhiip rsvsfdnsfn nkvlvkqeeA skkgnrtpfq ylsssdskis
601 yetfkkhiln lakgkgrisk tkkeylleer dinrfsvqkd finrnlvdtr yatrglmnll
661 rsyfrvnnld vkvksinggf tsflrrkwkf kkernkgykh haedaliian adfifkewkk
721 ldkakkvmen qmfeekqaes mpeieteqey keifitphqi khikdfkdyk yshrvdkkpn
781 relindtlys trkddkgntl ivnnlnglyd kdndklkkli nkspekllmy hhdpqtyqkl
841 klimeqygde knplykyyee tgnyltkysk kdngpvikki kyygnklnah lditddypns
901 rnkvvklslk pyrfdvyldn gvykfvtvkn ldvikkenyy evnskcyeea kklkkisnqa
961 efiasfynnd likingelyr vigvnndlln rievnmidit yreylenmnd krppriikti
1021 asktqsikky stdilgnlye vkskkhpqii kkg (SEQ ID NO:18041).
Инактивированная Cas9 (dCas9)
[0730] В изобретении предложены композиции, включающие инактивированную Cas9 (dCas9), функционально связанную с эффектором. В некоторых вариантах осуществления в изобретении предложен слитый белок, включающий, состоящий по существу из или состоящий из компонента локализации ДНК и эффекторной молекулы, где эффектор включает инактивированную Cas9 (dCas9). В некоторых вариантах осуществления конструкция инактивированной Cas9 (dCas9) согласно изобретению может включать эффектор, включающий эндонуклеазу IIS типа.
[0731] В некоторых вариантах осуществления dCas9 согласно изобретению включает dCas9, выделенную или полученную из Staphyloccocus pyogenes. В некоторых вариантах осуществления dCas9 включает dCas9 с заменами в положениях 10 и 840 аминокислотной последовательности dCas9, который инактивируют каталитический центр. В некоторых вариантах осуществления эти замены представляют собой D10A и H840A. В некоторых вариантах осуществления аминокислотная последовательность dCas9 включает последовательность:
61 ATRLKRTARR RYTRRKNRIC YLQEIFSNEM AKVDDSFFHR LEESFLVEED KKHERHPIFG
121 NIVDEVAYHE KYPTIYHLRK KLVDSTDKAD LRLIYLALAH MIKFRGHFLI EGDLNPDNSD
181 VDKLFIQLVQ TYNQLFEENP INASGVDAKA ILSARLSKSR RLENLIAQLP GEKKNGLFGN
241 LIALSLGLTP NFKSNFDLAE DAKLQLSKDT YDDDLDNLLA QIGDQYADLF LAAKNLSDAI
301 LLSDILRVNT EITKAPLSAS MIKRYDEHHQ DLTLLKALVR QQLPEKYKEI FFDQSKNGYA
361 GYIDGGASQE EFYKFIKPIL EKMDGTEELL VKLNREDLLR KQRTFDNGSI PHQIHLGELH
421 AILRRQEDFY PFLKDNREKI EKILTFRIPY YVGPLARGNS RFAWMTRKSE ETITPWNFEE
481 VVDKGASAQS FIERMTNFDK NLPNEKVLPK HSLLYEYFTV YNELTKVKYV TEGMRKPAFL
541 SGEQKKAIVD LLFKTNRKVT VKQLKEDYFK KIECFDSVEI SGVEDRFNAS LGTYHDLLKI
601 IKDKDFLDNE ENEDILEDIV LTLTLFEDRE MIEERLKTYA HLFDDKVMKQ LKRRRYTGWG
661 RLSRKLINGI RDKQSGKTIL DFLKSDGFAN RNFMQLIHDD SLTFKEDIQK AQVSGQGDSL
721 HEHIANLAGS PAIKKGILQT VKVVDELVKV MGRHKPENIV IEMARENQTT QKGQKNSRER
781 MKRIEEGIKE LGSQILKEHP VENTQLQNEK LYLYYLQNGR DMYVDQELDI NRLSDYDVDA
841 IVPQSFLKDD SIDNKVLTRS DKNRGKSDNV PSEEVVKKMK NYWRQLLNAK LITQRKFDNL
901 TKAERGGLSE LDKAGFIKRQ LVETRQITKH VAQILDSRMN TKYDENDKLI REVKVITLKS
961 KLVSDFRKDF QFYKVREINN YHHAHDAYLN AVVGTALIKK YPKLESEFVY GDYKVYDVRK
1021 MIAKSEQEIG KATAKYFFYS NIMNFFKTEI TLANGEIRKR PLIETNGETG EIVWDKGRDF
1081 ATVRKVLSMP QVNIVKKTEV QTGGFSKESI LPKRNSDKLI ARKKDWDPKK YGGFDSPTVA
1141 YSVLVVAKVE KGKSKKLKSV KELLGITIME RSSFEKNPID FLEAKGYKEV KKDLIIKLPK
1201 YSLFELENGR KRMLASAGEL QKGNELALPS KYVNFLYLAS HYEKLKGSPE DNEQKQLFVE
1261 QHKHYLDEII EQISEFSKRV ILADANLDKV LSAYNKHRDK PIREQAENII HLFTLTNLGA
1321 PAAFKYFDTT IDRKRYTSTK EVLDATLIHQ SITGLYETRI DLSQLGGD
(SEQ ID NO:18042).
[0732] В некоторых вариантах осуществления аминокислотная последовательность dCas9 включает последовательность:
61 ATRLKRTARR RYTRRKNRIC YLQEIFSNEM AKVDDSFFHR LEESFLVEED KKHERHPIFG
121 NIVDEVAYHE KYPTIYHLRK KLVDSTDKAD LRLIYLALAH MIKFRGHFLI EGDLNPDNSD
181 VDKLFIQLVQ TYNQLFEENP INASGVDAKA ILSARLSKSR RLENLIAQLP GEKKNGLFGN
241 LIALSLGLTP NFKSNFDLAE DAKLQLSKDT YDDDLDNLLA QIGDQYADLF LAAKNLSDAI
301 LLSDILRVNT EITKAPLSAS MIKRYDEHHQ DLTLLKALVR QQLPEKYKEI FFDQSKNGYA
361 GYIDGGASQE EFYKFIKPIL EKMDGTEELL VKLNREDLLR KQRTFDNGSI PHQIHLGELH
421 AILRRQEDFY PFLKDNREKI EKILTFRIPY YVGPLARGNS RFAWMTRKSE ETITPWNFEE
481 VVDKGASAQS FIERMTNFDK NLPNEKVLPK HSLLYEYFTV YNELTKVKYV TEGMRKPAFL
541 SGEQKKAIVD LLFKTNRKVT VKQLKEDYFK KIECFDSVEI SGVEDRFNAS LGTYHDLLKI
601 IKDKDFLDNE ENEDILEDIV LTLTLFEDRE MIEERLKTYA HLFDDKVMKQ LKRRRYTGWG
661 RLSRKLINGI RDKQSGKTIL DFLKSDGFAN RNFMQLIHDD SLTFKEDIQK AQVSGQGDSL
721 HEHIANLAGS PAIKKGILQT VKVVDELVKV MGRHKPENIV IEMARENQTT QKGQKNSRER
781 MKRIEEGIKE LGSQILKEHP VENTQLQNEK LYLYYLQNGR DMYVDQELDI NRLSDYDVDA
841 IVPQSFLKDD SIDNKVLTRS DKNRGKSDNV PSEEVVKKMK NYWRQLLNAK LITQRKFDNL
901 TKAERGGLSE LDKAGFIKRQ LVETRQITKH VAQILDSRMN TKYDENDKLI REVKVITLKS
961 KLVSDFRKDF QFYKVREINN YHHAHDAYLN AVVGTALIKK YPKLESEFVY GDYKVYDVRK
1021 MIAKSEQEIG KATAKYFFYS NIMNFFKTEI TLANGEIRKR PLIETNGETG EIVWDKGRDF
1081 ATVRKVLSMP QVNIVKKTEV QTGGFSKESI LPKRNSDKLI ARKKDWDPKK YGGFDSPTVA
1141 YSVLVVAKVE KGKSKKLKSV KELLGITIME RSSFEKNPID FLEAKGYKEV KKDLIIKLPK
1201 YSLFELENGR KRMLASAGEL QKGNELALPS KYVNFLYLAS HYEKLKGSPE DNEQKQLFVE
1261 QHKHYLDEII EQISEFSKRV ILADANLDKV LSAYNKHRDK PIREQAENII HLFTLTNLGA
1321 PAAFKYFDTT IDRKRYTSTK EVLDATLIHQ SITGLYETRI DLSQLGGD
(SEQ ID NO:18043).
Эндонуклеаза Clo051
[0733] Примерный домен нуклеазы Clo051 может включать, состоять по существу из или состоять из аминокислотной последовательности: EGIKSNISLLKDELRGQISHISHEYLSLIDLAFDSKQNRLFEMKVLELLVNEYGFKGRHLGGSRKPDGIVYSTTLEDNFGIIVDTKAYSEGYSLPISQADEMERYVRENSNRDEEVNPNKWWENFSEEVKKYYFVFISGSFKGKFEEQLRRLSMTTGVNGSAVNVVNLLLGAEKIRSGEMTIEELERAMFNNSEFILKY (SEQ ID NO:18044).
Слитый белок Cas-Clover
[0734] В некоторых вариантах осуществления примерный слитый белок dCas9-Clo051 (вариант осуществления 1) может включать, состоять по существу из или состоять из аминокислотной последовательности (последовательность Clo051 подчеркнута, линкер выделен полужирным курсивом, последовательность dCas9 (Streptoccocus pyogenes) выделена курсивом):
MAPKKKRKVEGIKSNISLLKDELRGQISHISHEYLSLIDLAFDSKQNRLFEMKVLELLVNEYGFKGRHLGGSRKPDGIVYSTTLEDNFGIIVDTKAYSEGYSLPISQADEMERYVRENSNRDEEVNPNKWWENFSEEVKKYYFVFISGSFKGKFEEQLRRLSMTTGVNGSAVNVVNLLLGAEKIRSGEMTIEELERAMFNNSEFILKYGGGGSDKKYSIGLAIGTNSVGWAVITDEYKVPSKKFKVLGNTDRHSIKKNLIGALLFDSGETAEATRLKRTARRRYTRRKNRICYLQEIFSNEMAKVDDSFFHRLEESFLVEEDKKHERHPIFGNIVDEVAYHEKYPTIYHLRKKLVDSTDKADLRLIYLALAHMIKFRGHFLIEGDLNPDNSDVDKLFIQLVQTYNQLFEENPINASGVDAKAILSARLSKSRRLENLIAQLPGEKKNGLFGNLIALSLGLTPNFKSNFDLAEDAKLQLSKDTYDDDLDNLLAQIGDQYADLFLAAKNLSDAILLSDILRVNTEITKAPLSASMIKRYDEHHQDLTLLKALVRQQLPEKYKEIFFDQSKNGYAGYIDGGASQEEFYKFIKPILEKMDGTEELLVKLNREDLLRKQRTFDNGSIPHQIHLGELHAILRRQEDFYPFLKDNREKIEKILTFRIPYYVGPLARGNSRFAWMTRKSEETITPWNFEEVVDKGASAQSFIERMTNFDKNLPNEKVLPKHSLLYEYFTVYNELTKVKYVTEGMRKPAFLSGEQKKAIVDLLFKTNRKVTVKQLKEDYFKKIECFDSVEISGVEDRFNASLGTYHDLLKIIKDKDFLDNEENEDILEDIVLTLTLFEDREMIEERLKTYAHLFDDKVMKQLKRRRYTGWGRLSRKLINGIRDKQSGKTILDFLKSDGFANRNFMQLIHDDSLTFKEDIQKAQVSGQGDSLHEHIANLAGSPAIKKGILQTVKVVDELVKVMGRHKPENIVIEMARENQTTQKGQKNSRERMKRIEEGIKELGSQILKEHPVENTQLQNEKLYLYYLQNGRDMYVDQELDINRLSDYDVDAIVPQSFLKDDSIDNKVLTRSDKNRGKSDNVPSEEVVKKMKNYWRQLLNAKLITQRKFDNLTKAERGGLSELDKAGFIKRQLVETRQITKHVAQILDSRMNTKYDENDKLIREVKVITLKSKLVSDFRKDFQFYKVREINNYHHAHDAYLNAVVGTALIKKYPKLESEFVYGDYKVYDVRKMIAKSEQEIGKATAKYFFYSNIMNFFKTEITLANGEIRKRPLIETNGETGEIVWDKGRDFATVRKVLSMPQVNIVKKTEVQTGGFSKESILPKRNSDKLIARKKDWDPKKYGGFDSPTVAYSVLVVAKVEKGKSKKLKSVKELLGITIMERSSFEKNPIDFLEAKGYKEVKKDLIIKLPKYSLFELENGRKRMLASAGELQKGNELALPSKYVNFLYLASHYEKLKGSPEDNEQKQLFVEQHKHYLDEIIEQISEFSKRVILADANLDKVLSAYNKHRDKPIREQAENIIHLFTLTNLGAPAAFKYFDTTIDRKRYTSTKEVLDATLIHQSITGLYETRIDLSQLGGDGSPKKKRKVSS (SEQ ID NO:18045).
[0735] В некоторых вариантах осуществления примерный слитый белок dCas9-Clo051 (вариант осуществления 1) может включать, состоять по существу из или состоять из последовательности нуклеиновой кислоты (последовательности dCas9, полученой из Streptoccocus pyogenes):
61 gacgaactgc ggggacagat tagtcacatc agtcacgagt acctgtcact gattgatctg
121 gccttcgaca gcaagcagaa tagactgttt gagatgaaag tgctggaact gctggtcaac
181 gagtatggct tcaagggcag acatctgggc gggtctagga aacctgacgg catcgtgtac
241 agtaccacac tggaagacaa cttcggaatc attgtcgata ccaaggctta ttccgagggc
301 tactctctgc caattagtca ggcagatgag atggaaaggt acgtgcgcga aaactcaaat
361 agggacgagg aagtcaaccc caataagtgg tgggagaatt tcagcgagga agtgaagaaa
421 tactacttcg tctttatctc aggcagcttc aaagggaagt ttgaggaaca gctgcggaga
481 ctgtccatga ctaccggggt gaacggatct gctgtcaacg tggtcaatct gctgctgggc
541 gcagaaaaga tcaggtccgg ggagatgaca attgaggaac tggaacgcgc catgttcaac
601 aattctgagt ttatcctgaa gtatggaggc gggggaagcg ataagaaata ctccatcgga
661 ctggccattg gcaccaattc cgtgggctgg gctgtcatca cagacgagta caaggtgcca
721 agcaagaagt tcaaggtcct ggggaacacc gatcgccaca gtatcaagaa aaatctgatt
781 ggagccctgc tgttcgactc aggcgagact gctgaagcaa cccgactgaa gcggactgct
841 aggcgccgat atacccggag aaaaaatcgg atctgctacc tgcaggaaat tttcagcaac
901 gagatggcca aggtggacga tagtttcttt caccgcctgg aggaatcatt cctggtggag
961 gaagataaga aacacgagcg gcatcccatc tttggcaaca ttgtggacga agtcgcttat
1021 cacgagaagt accctactat ctatcatctg aggaagaaac tggtggactc caccgataag
1081 gcagacctgc gcctgatcta tctggccctg gctcacatga tcaagttccg ggggcatttt
1141 ctgatcgagg gagatctgaa ccctgacaat tctgatgtgg acaagctgtt catccagctg
1201 gtccagacat acaatcagct gtttgaggaa aacccaatta atgcctcagg cgtggacgca
1261 aaggccatcc tgagcgccag actgtccaaa tctaggcgcc tggaaaacct gatcgctcag
1321 ctgccaggag agaagaaaaa cggcctgttt gggaatctga ttgcactgtc cctgggcctg
1381 acacccaact tcaagtctaa ttttgatctg gccgaggacg ctaagctgca gctgtccaaa
1441 gacacttatg acgatgacct ggataacctg ctggctcaga tcggcgatca gtacgcagac
1501 ctgttcctgg ccgctaagaa tctgagtgac gccatcctgc tgtcagatat tctgcgcgtg
1561 aacacagaga ttactaaggc cccactgagt gcttcaatga tcaaaagata tgacgagcac
1621 catcaggatc tgaccctgct gaaggctctg gtgaggcagc agctgcccga gaaatacaag
1681 gaaatcttct ttgatcagag caagaatgga tacgccggct atattgacgg cggggcttcc
1741 caggaggagt tctacaagtt catcaagccc attctggaaa agatggacgg caccgaggaa
1801 ctgctggtga agctgaatcg ggaggacctg ctgagaaaac agaggacatt tgataacgga
1861 agcatccctc accagattca tctgggcgaa ctgcacgcca tcctgcgacg gcaggaggac
1921 ttctacccat ttctgaagga taaccgcgag aaaatcgaaa agatcctgac cttcagaatc
1981 ccctactatg tggggcctct ggcacgggga aatagtagat ttgcctggat gacaagaaag
2041 tcagaggaaa ctatcacccc ctggaacttc gaggaagtgg tcgataaagg cgctagcgca
2101 cagtccttca ttgaaaggat gacaaatttt gacaagaacc tgccaaatga gaaggtgctg
2161 cccaaacaca gcctgctgta cgaatatttc acagtgtata acgagctgac taaagtgaag
2221 tacgtcaccg aagggatgcg caagcccgca ttcctgtccg gagagcagaa gaaagccatc
2281 gtggacctgc tgtttaagac aaatcggaaa gtgactgtca aacagctgaa ggaagactat
2341 ttcaagaaaa ttgagtgttt cgattcagtg gaaatcagcg gcgtcgagga caggtttaac
2401 gcctccctgg ggacctacca cgatctgctg aagatcatca aggataagga cttcctggac
2461 aacgaggaaa atgaggacat cctggaggac attgtgctga cactgactct gtttgaggat
2521 cgcgaaatga tcgaggaacg actgaagact tatgcccatc tgttcgatga caaagtgatg
2581 aagcagctga aaagaaggcg ctacaccgga tggggacgcc tgagccgaaa actgatcaat
2641 gggattagag acaagcagag cggaaaaact atcctggact ttctgaagtc cgatggcttc
2701 gccaacagga acttcatgca gctgattcac gatgactctc tgaccttcaa ggaggacatc
2761 cagaaagcac aggtgtctgg ccagggggac agtctgcacg agcatatcgc aaacctggcc
2821 ggcagccccg ccatcaagaa agggattctg cagaccgtga aggtggtgga cgaactggtc
2881 aaggtcatgg gacgacacaa acctgagaac atcgtgattg agatggcccg cgaaaatcag
2941 acaactcaga agggccagaa aaacagtcga gaacggatga agagaatcga ggaaggcatc
3001 aaggagctgg ggtcacagat cctgaaggag catcctgtgg aaaacactca gctgcagaat
3061 gagaaactgt atctgtacta tctgcagaat ggacgggata tgtacgtgga ccaggagctg
3121 gatattaaca gactgagtga ttatgacgtg gatgccatcg tccctcagag cttcctgaag
3181 gatgactcca ttgacaacaa ggtgctgacc aggtccgaca agaaccgcgg caaatcagat
3241 aatgtgccaa gcgaggaagt ggtcaagaaa atgaagaact actggaggca gctgctgaat
3301 gccaagctga tcacacagcg gaaatttgat aacctgacta aggcagaaag aggaggcctg
3361 tctgagctgg acaaggccgg cttcatcaag cggcagctgg tggagacaag acagatcact
3421 aagcacgtcg ctcagattct ggatagcaga atgaacacaa agtacgatga aaacgacaag
3481 ctgatcaggg aggtgaaagt cattactctg aaatccaagc tggtgtctga ctttagaaag
3541 gatttccagt tttataaagt cagggagatc aacaactacc accatgctca tgacgcatac
3601 ctgaacgcag tggtcgggac cgccctgatt aagaaatacc ccaagctgga gtccgagttc
3661 gtgtacggag actataaagt gtacgatgtc cggaagatga tcgccaaatc tgagcaggaa
3721 attggcaagg ccaccgctaa gtatttcttt tacagtaaca tcatgaattt ctttaagacc
3781 gaaatcacac tggcaaatgg ggagatcaga aaaaggcctc tgattgagac caacggggag
3841 acaggagaaa tcgtgtggga caagggaagg gattttgcta ccgtgcgcaa agtcctgtcc
3901 atgccccaag tgaatattgt caagaaaact gaagtgcaga ccgggggatt ctctaaggag
3961 agtattctgc ctaagcgaaa ctctgataaa ctgatcgccc ggaagaaaga ctgggacccc
4021 aagaagtatg gcgggttcga ctctccaaca gtggcttaca gtgtcctggt ggtcgcaaag
4081 gtggaaaagg ggaagtccaa gaaactgaag tctgtcaaag agctgctggg aatcactatt
4141 atggaacgca gctccttcga gaagaatcct atcgattttc tggaagccaa gggctataaa
4201 gaggtgaaga aagacctgat cattaagctg ccaaaatact cactgtttga gctggaaaac
4261 ggacgaaagc gaatgctggc aagcgccgga gaactgcaga agggcaatga gctggccctg
4321 ccctccaaat acgtgaactt cctgtatctg gctagccact acgagaaact gaaggggtcc
4381 cctgaggata acgaacagaa gcagctgttt gtggagcagc acaaacatta tctggacgag
4441 atcattgaac agatttcaga gttcagcaag agagtgatcc tggctgacgc aaatctggat
4501 aaagtcctga gcgcatacaa caagcaccga gacaaaccaa tccgggagca ggccgaaaat
4561 atcattcatc tgttcaccct gacaaacctg ggcgcccctg cagccttcaa gtattttgac
4621 accacaatcg atcggaagag atacacttct accaaagagg tgctggatgc taccctgatc
4681 caccagagta ttaccggcct gtatgagaca cgcatcgacc tgtcacagct gggaggcgat
4741 gggagcccca agaaaaagcg gaaggtgtct agttaa (SEQ ID NO:18046).
[0736] В некоторых вариантах осуществления последовательность нуклеиновой кислоты, кодирующая слитый белок dCas9-Clo051 (вариант осуществления 1) согласно изобретению, может включать ДНК. В некоторых вариантах осуществления последовательность нуклеиновой кислоты, кодирующая слитый белок dCas9-Clo051 (вариант осуществления 1) согласно изобретению, может включать РНК.
[0737] В некоторых вариантах осуществления примерный слитый белок dCas9-Clo051 (вариант осуществления 2) может включать, состоять по существу из или состоять из аминокислотной последовательности (последовательность Clo051 подчеркнута, линкер выделен полужирным курсивом, последовательность dCas9 (Streptoccocus pyogenes) выделена курсивом):
61 YGFKGRHLGG SRKPDGIVYS TTLEDNFGII VDTKAYSEGY SLPISQADEM ERYVRENSNR
121 DEEVNPNKWW ENFSEEVKKY YFVFISGSFK GKFEEQLRRL SMTTGVNGSA VNVVNLLLGA
181 EKIRSGEMTI EELERAMFNN SEFILKYGGG GSDKKYSIGL AIGTNSVGWA VITDEYKVPS
241 KKFKVLGNTD RHSIKKNLIG ALLFDSGETA EATRLKRTAR RRYTRRKNRI CYLQEIFSNE
301 MAKVDDSFFH RLEESFLVEE DKKHERHPIF GNIVDEVAYH EKYPTIYHLR KKLVDSTDKA
361 DLRLIYLALA HMIKFRGHFL IEGDLNPDNS DVDKLFIQLV QTYNQLFEEN PINASGVDAK
421 AILSARLSKS RRLENLIAQL PGEKKNGLFG NLIALSLGLT PNFKSNFDLA EDAKLQLSKD
481 TYDDDLDNLL AQIGDQYADL FLAAKNLSDA ILLSDILRVN TEITKAPLSA SMIKRYDEHH
541 QDLTLLKALV RQQLPEKYKE IFFDQSKNGY AGYIDGGASQ EEFYKFIKPI LEKMDGTEEL
601 LVKLNREDLL RKQRTFDNGS IPHQIHLGEL HAILRRQEDF YPFLKDNREK IEKILTFRIP
661 YYVGPLARGN SRFAWMTRKS EETITPWNFE EVVDKGASAQ SFIERMTNFD KNLPNEKVLP
721 KHSLLYEYFT VYNELTKVKY VTEGMRKPAF LSGEQKKAIV DLLFKTNRKV TVKQLKEDYF
781 KKIECFDSVE ISGVEDRFNA SLGTYHDLLK IIKDKDFLDN EENEDILEDI VLTLTLFEDR
841 EMIEERLKTY AHLFDDKVMK QLKRRRYTGW GRLSRKLING IRDKQSGKTI LDFLKSDGFA
901 NRNFMQLIHD DSLTFKEDIQ KAQVSGQGDS LHEHIANLAG SPAIKKGILQ TVKVVDELVK
961 VMGRHKPENI VIEMARENQT TQKGQKNSRE RMKRIEEGIK ELGSQILKEH PVENTQLQNE
1021 KLYLYYLQNG RDMYVDQELD INRLSDYDVD AIVPQSFLKD DSIDNKVLTR SDKNRGKSDN
1081 VPSEEVVKKM KNYWRQLLNA KLITQRKFDN LTKAERGGLS ELDKAGFIKR QLVETRQITK
1141 HVAQILDSRM NTKYDENDKL IREVKVITLK SKLVSDFRKD FQFYKVREIN NYHHAHDAYL
1201 NAVVGTALIK KYPKLESEFV YGDYKVYDVR KMIAKSEQEI GKATAKYFFY SNIMNFFKTE
1261 ITLANGEIRK RPLIETNGET GEIVWDKGRD FATVRKVLSM PQVNIVKKTE VQTGGFSKES
1321 ILPKRNSDKL IARKKDWDPK KYGGFDSPTV AYSVLVVAKV EKGKSKKLKS VKELLGITIM
1381 ERSSFEKNPI DFLEAKGYKE VKKDLIIKLP KYSLFELENG RKRMLASAGE LQKGNELALP
1441 SKYVNFLYLA SHYEKLKGSP EDNEQKQLFV EQHKHYLDEI IEQISEFSKR VILADANLDK
1501 VLSAYNKHRD KPIREQAENI IHLFTLTNLG APAAFKYFDT TIDRKRYTST KEVLDATLIH
1561 QSITGLYETR IDLSQLGGDG SPKKKRKV (SEQ ID NO:18047).
[0738] В некоторых вариантах осуществления примерный слитый белок dCas9-Clo051 (вариант осуществления 2) может включать, состоять по существу из или состоять из последовательности нуклеиновой кислоты (последовательности dCas9, полученной из Streptoccocus pyogenes):
61 gaactccggg ggcagattag ccacattagt cacgaatacc tctccctcat cgacctggct
121 ttcgatagca agcagaacag gctctttgag atgaaagtgc tggaactgct cgtcaatgag
181 tacgggttca agggtcgaca cctcggcgga tctaggaaac cagacggcat cgtgtatagt
241 accacactgg aagacaactt tgggatcatt gtggatacca aggcatactc tgagggttat
301 agtctgccca tttcacaggc cgacgagatg gaacggtacg tgcgcgagaa ctcaaataga
361 gatgaggaag tcaaccctaa caagtggtgg gagaacttct ctgaggaagt gaagaaatac
421 tacttcgtct ttatcagcgg gtccttcaag ggtaaatttg aggaacagct caggagactg
481 agcatgacta ccggcgtgaa tggcagcgcc gtcaacgtgg tcaatctgct cctgggcgct
541 gaaaagattc ggagcggaga gatgaccatc gaagagctgg agagggcaat gtttaataat
601 agcgagttta tcctgaaata cggtggcggt ggatccgata aaaagtattc tattggttta
661 gccatcggca ctaattccgt tggatgggct gtcataaccg atgaatacaa agtaccttca
721 aagaaattta aggtgttggg gaacacagac cgtcattcga ttaaaaagaa tcttatcggt
781 gccctcctat tcgatagtgg cgaaacggca gaggcgactc gcctgaaacg aaccgctcgg
841 agaaggtata cacgtcgcaa gaaccgaata tgttacttac aagaaatttt tagcaatgag
901 atggccaaag ttgacgattc tttctttcac cgtttggaag agtccttcct tgtcgaagag
961 gacaagaaac atgaacggca ccccatcttt ggaaacatag tagatgaggt ggcatatcat
1021 gaaaagtacc caacgattta tcacctcaga aaaaagctag ttgactcaac tgataaagcg
1081 gacctgaggt taatctactt ggctcttgcc catatgataa agttccgtgg gcactttctc
1141 attgagggtg atctaaatcc ggacaactcg gatgtcgaca aactgttcat ccagttagta
1201 caaacctata atcagttgtt tgaagagaac cctataaatg caagtggcgt ggatgcgaag
1261 gctattctta gcgcccgcct ctctaaatcc cgacggctag aaaacctgat cgcacaatta
1321 cccggagaga agaaaaatgg gttgttcggt aaccttatag cgctctcact aggcctgaca
1381 ccaaatttta agtcgaactt cgacttagct gaagatgcca aattgcagct tagtaaggac
1441 acgtacgatg acgatctcga caatctactg gcacaaattg gagatcagta tgcggactta
1501 tttttggctg ccaaaaacct tagcgatgca atcctcctat ctgacatact gagagttaat
1561 actgagatta ccaaggcgcc gttatccgct tcaatgatca aaaggtacga tgaacatcac
1621 caagacttga cacttctcaa ggccctagtc cgtcagcaac tgcctgagaa atataaggaa
1681 atattctttg atcagtcgaa aaacgggtac gcaggttata ttgacggcgg agcgagtcaa
1741 gaggaattct acaagtttat caaacccata ttagagaaga tggatgggac ggaagagttg
1801 cttgtaaaac tcaatcgcga agatctactg cgaaagcagc ggactttcga caacggtagc
1861 attccacatc aaatccactt aggcgaattg catgctatac ttagaaggca ggaggatttt
1921 tatccgttcc tcaaagacaa tcgtgaaaag attgagaaaa tcctaacctt tcgcatacct
1981 tactatgtgg gacccctggc ccgagggaac tctcggttcg catggatgac aagaaagtcc
2041 gaagaaacga ttactccatg gaattttgag gaagttgtcg ataaaggtgc gtcagctcaa
2101 tcgttcatcg agaggatgac caactttgac aagaatttac cgaacgaaaa agtattgcct
2161 aagcacagtt tactttacga gtatttcaca gtgtacaatg aactcacgaa agttaagtat
2221 gtcactgagg gcatgcgtaa acccgccttt ctaagcggag aacagaagaa agcaatagta
2281 gatctgttat tcaagaccaa ccgcaaagtg acagttaagc aattgaaaga ggactacttt
2341 aagaaaattg aatgcttcga ttctgtcgag atctccgggg tagaagatcg atttaatgcg
2401 tcacttggta cgtatcatga cctcctaaag ataattaaag ataaggactt cctggataac
2461 gaagagaatg aagatatctt agaagatata gtgttgactc ttaccctctt tgaagatcgg
2521 gaaatgattg aggaaagact aaaaacatac gctcacctgt tcgacgataa ggttatgaaa
2581 cagttaaaga ggcgtcgcta tacgggctgg ggacgattgt cgcggaaact tatcaacggg
2641 ataagagaca agcaaagtgg taaaactatt ctcgattttc taaagagcga cggcttcgcc
2701 aataggaact ttatgcagct gatccatgat gactctttaa ccttcaaaga ggatatacaa
2761 aaggcacagg tttccggaca aggggactca ttgcacgaac atattgcgaa tcttgctggt
2821 tcgccagcca tcaaaaaggg catactccag acagtcaaag tagtggatga gctagttaag
2881 gtcatgggac gtcacaaacc ggaaaacatt gtaatcgaga tggcacgcga aaatcaaacg
2941 actcagaagg ggcaaaaaaa cagtcgagag cggatgaaga gaatagaaga gggtattaaa
3001 gaactgggca gccagatctt aaaggagcat cctgtggaaa atacccaatt gcagaacgag
3061 aaactttacc tctattacct acaaaatgga agggacatgt atgttgatca ggaactggac
3121 ataaaccgtt tatctgatta cgacgtcgat gccattgtac cccaatcctt tttgaaggac
3181 gattcaatcg acaataaagt gcttacacgc tcggataaga accgagggaa aagtgacaat
3241 gttccaagcg aggaagtcgt aaagaaaatg aagaactatt ggcggcagct cctaaatgcg
3301 aaactgataa cgcaaagaaa gttcgataac ttaactaaag ctgagagggg tggcttgtct
3361 gaacttgaca aggccggatt tattaaacgt cagctcgtgg aaacccgcca aatcacaaag
3421 catgttgcac agatactaga ttcccgaatg aatacgaaat acgacgagaa cgataagctg
3481 attcgggaag tcaaagtaat cactttaaag tcaaaattgg tgtcggactt cagaaaggat
3541 tttcaattct ataaagttag ggagataaat aactaccacc atgcgcacga cgcttatctt
3601 aatgccgtcg tagggaccgc actcattaag aaatacccga agctagaaag tgagtttgtg
3661 tatggtgatt acaaagttta tgacgtccgt aagatgatcg cgaaaagcga acaggagata
3721 ggcaaggcta cagccaaata cttcttttat tctaacatta tgaatttctt taagacggaa
3781 atcactctgg caaacggaga gatacgcaaa cgacctttaa ttgaaaccaa tggggagaca
3841 ggtgaaatcg tatgggataa gggccgggac ttcgcgacgg tgagaaaagt tttgtccatg
3901 ccccaagtca acatagtaaa gaaaactgag gtgcagaccg gagggttttc aaaggaatcg
3961 attcttccaa aaaggaatag tgataagctc atcgctcgta aaaaggactg ggacccgaaa
4021 aagtacggtg gcttcgatag ccctacagtt gcctattctg tcctagtagt ggcaaaagtt
4081 gagaagggaa aatccaagaa actgaagtca gtcaaagaat tattggggat aacgattatg
4141 gagcgctcgt cttttgaaaa gaaccccatc gacttccttg aggcgaaagg ttacaaggaa
4201 gtaaaaaagg atctcataat taaactacca aagtatagtc tgtttgagtt agaaaatggc
4261 cgaaaacgga tgttggctag cgccggagag cttcaaaagg ggaacgaact cgcactaccg
4321 tctaaatacg tgaatttcct gtatttagcg tcccattacg agaagttgaa aggttcacct
4381 gaagataacg aacagaagca actttttgtt gagcagcaca aacattatct cgacgaaatc
4441 atagagcaaa tttcggaatt cagtaagaga gtcatcctag ctgatgccaa tctggacaaa
4501 gtattaagcg catacaacaa gcacagggat aaacccatac gtgagcaggc ggaaaatatt
4561 atccatttgt ttactcttac caacctcggc gctccagccg cattcaagta ttttgacaca
4621 acgatagatc gcaaacgata cacttctacc aaggaggtgc tagacgcgac actgattcac
4681 caatccatca cgggattata tgaaactcgg atagatttgt cacagcttgg gggtgacgga
4741 tcccccaaga agaagaggaa agtctga (SEQ ID NO:18048).
[0739] В некоторых вариантах осуществления последовательность нуклеиновой кислоты, кодирующая слитый белок dCas9-Clo051 (вариант осуществления 2) согласно изобретению, может включать ДНК. В некоторых вариантах осуществления последовательность нуклеиновой кислоты, кодирующая слитый белок dCas9-Clo051 (вариант осуществления 2) согласно изобретению, может включать РНК.
ПРИМЕРЫ
Пример 1: Эффективность нокдауна сигнальных белков контрольных точек на бронированных T-клетках
[0740] Для создания бронированных T-клеток, которые обладают повышенным терапевтическим потенциалом, могут быть сделаны генетические модификации, чтобы сделать T-клетки менее чувствительными к иммунологическим и/или метаболическим контрольным точкам. Одним из механизмов получения бронированных T-клеток является ингибирование сигнализации контрольных точек, то есть нокаут различных рецепторов контрольных точек. Платформа Cas-CLOVERTM использовалась для направленного воздействия и нокаута рецепторов контрольных точек PD-1, TGFβR2, LAG-3, Tim-3. и CTLA-4 в покоящихся (или неактивных) первичных пан-T-клетках. Согласно данным проточной цитометрии редактирование генов приводило к 30-70% потере экспрессии белка на клеточной поверхности (Фигура 11). Эти результаты показывают, что Cas-CLOVERTM способна эффективно направлять нокаут этих генов, приводящий к потере экспрессии белка-мишени на поверхности T-клеток. Эффективность нокаута может быть значительно повышена путем дополнительной оптимизации пар гидовых РНК или путем использования дополнительных пар гидовых РНК, направленных на один и тот же ген, и/или регуляторы или промоторы гена-мишени.
Пример 2: Стратегии экспрессии нулевых или переключаемых внутриклеточных сигнальных белков на бронированных T-клетках
[0741] Другая стратегия получения бронированных T-клеток заключается в снижении или ингибировании эндогенной сигнализации контрольных точек путем экспрессии различных модифицированных/химерных рецепторов контрольных точек, у которых изменен или отсутствует внутриклеточный сигнальный домен. Сигналы контрольных точек, которые могут являться мишенями при использовании этой стратегии, включают PD-1 или TGFβRII T-клеток, которые связываются с лигандом PD-L1 и цитокином TGFβ соответственно. На Фигуре 12 показана схематическая диаграмма различных стратегий получения ловушек/нулевых/доминантно-негативных рецепторов (Нулевых рецепторов) в случае двух разных ингибирующих рецепторов (PD-1 (верхняя панель) и TGFβRII (нижняя панель)). Для создания нулевых рецепторов внутриклеточный домен (ICD) PD1 или TGF-RII может быть подвергнут мутации (нуль-мутации) или удален (нуль-усечению). В результате связывание когнатного лиганда(ов) нулевого рецептора не приводит к доставке сигнала контрольной точки к T-клеткам. Кроме того, поскольку нулевой рецептор конкурирует с рецепторами дикого типа за связывание с эндогенным лигандом(ами), любое связывание с нулевым рецептором блокирует связывание эндогенного лиганда(ов) с рецептором дикого типа. Это приводит к ослаблению общего уровня сигнализации контрольной точки, эффективно доставляемой в T-клетку, уменьшая или блокируя, таким образом, ингибирование контрольной точки. На Фигуре 12 также показаны стратегии конструирования переключаемых рецепторов для ингибирующих рецепторов PD-1 (верхняя панель) и TGFβRII (нижняя панель). В переключающих рецепторах, ICD дикого типа заменяют ICD из иммуностимулирующей молекулы (костимулирующий переключатель) или другой ингибирующей молекулы (ингибирующий переключатель). Иммуностимулирующие молекулы включают, без ограничения перечисленными, CD3z, CD28, 4-1BB, а также примеры, перечисленные в Таблице 1. Ингибирующие молекулы включают, без ограничения перечисленными, CTLA4, PD1, Lag3, а также примеры, перечисленные в Таблицах 1 и 9. В первом случае связывание эндогенного лиганда с модифицированным переключаемым рецептором приводит к доставке позитивного сигнала в T-клетки, что способствует усилению стимуляции T-клеток, что способствует продолжению направленного воздействия на опухоль и ее уничтожению. В последнем случае связывание эндогенного лиганда с модифицированным переключаемым рецептором приводит к доставке негативного сигнала в T-клетки, что способствует снижению стимуляции и активности T-клеток.
Пример 3: Повышение поверхностной экспрессии нулевых или переключаемых внутриклеточных сигнальных белков PD1 и TGFβRII на бронированных T-клетках
[0742] Для создания бронированных T-клеток, ряд усеченных нулевых рецепторов, экспрессирующих альтернативные сигнальные пептиды (SP) и трансмембранные домены (TM), конструировали и тестировали на максимальную экспрессию на поверхности модифицированных T-клеток. На Фигуре 13 показаны схематические диаграммы нескольких конструкций с нулевым рецептором для PD-1 (вверху) и TGFβRII (внизу). Внеклеточные домены (ECD) этих белков были модифицированы таким образом, что сигнальный пептид дикого типа (SP) и/или трансмембранные домены (TM) были заменены такими элементами из рецептора CD8a T-клеток человека (красные стрелки). Для каждой из шести усеченных нулевых конструкций, показанных на Фигуре 13, синтезировали ДНК и затем субклонировали в мРНК IVT ДНК-вектор (pRT). мРНК высокого качества получали с помощью IVT для каждого. Трансфекцию мРНК, кодирующей каждую из шести молекул, производили при использовании доставки путем электропорации (ЕР) в первичные человеческие T-клетки, и через 24 часа после ЕР проводили FACS анализ для оценки уровня экспрессии каждой конструкции на поверхности клетки (Фигура 14). Согласно проточной цитометрии, замена WT SP на альтернативный из CD8a (02.8aSP-PD-1 и 02.8aSP-TGFβRII) привела к наибольшему уровню экспрессии на поверхности T-клеток. Нулевой рецептор 02.8aSP-PD-1 показал MFI 43680, что в 177 раз выше, чем экспрессия эндогенного PD-1 T-клеток, и в 2,8 раза выше, чем нулевого рецептора PD-1 WT. Нулевой рецептор 02.8aSP-TGFβRII показал MFI 13809, что в 102 раза выше, чем экспрессия эндогенного TGFβRII T-клеток, и в 1,8 раза выше, чем нулевого рецептора TGFβRII WT. Эти результаты показывают, что замена SP дикого типа альтернативным SP из CD8a в случае ингибирующих белков PD1 и TGF-RII приводит к повышению поверхностной экспрессии Нулевого или Переключаемого рецептора. Это, в свою очередь, максимально усиливает ингибирование или костимуляцию контрольной точки, соответственно, при связывании природного лиганда(ов).
Пример 4: Конструирование NF-KB индуцируемых векторов для экспрессии в модифицированных T-клетках
[0743] Были разработаны два NF-KB индуцируемых вектора активации T-клеток (Фигуры 15A и 15B); один с системой экспрессии гена (GES) в прямой ориентации (A) и другой в комплементарном направлении (B), оба предшествующие конститутивному промотору EF1a. Эти векторы также направляют экспрессию молекулы CAR и селективного гена DHFR, разделенных T2A последовательностью. Кондиционно регулируемая, NF-KB индуцируемая система и EF1a-направляемые гены являлись частью транспозона piggyBac, который может быть постоянно интегрирован в T-клетки с использованием EP. После интеграции в геном, T-клетки постоянно экспрессируют CAR на поверхности мембраны и DHFR в клетке, тогда как экспрессия NF-KB индуцируемого гена, GFP, будет идти на максимальном уровне только после активации T-клетки.
Пример 5: NF-KB индуцируемые векторы для экспрессии GFP в модифицированных T-клетках
[0744] T-клетки нуклеофицировали вектором piggyBac, экспрессирующим CAR против BCMA и ген мутеин DHFR под контролем промотора EF1a наряду с отсутствием (без контроля системы экспрессии гена (GES)) или присутствием NF-KB индуцируемой системы экспрессии, направляющей экспрессию GFP либо в прямой (pNFKB-GFP forward), либо в обратной ориентации (pNFKB-GFP reverse). Клетки культивировали в присутствии селекции метотрексатом, пока клетки почти полностью не переходили в состояние покоя (День 19), при этом экспрессию GFP оценивали в День 5 и День 19. В День 5 все T-клетки пролиферировали и были сильно стимулированы клетками, несущими NF-KB индуцируемую кассету экспрессии, продуцирующую высокий уровень GFP вследствие сильной активности NFκB (см. Фигуру 16). Контрольные клетки без GES не экспрессировали поддающиеся обнаружению уровни GFP. На день 19, GES T-клетки почти полностью переходили в состояние покоя, и экспрессия GFP была значительно ниже, чем в День 5 (~1/8 MFI), так как активность NFκB снизилась. Экспрессию GFP все еще наблюдали в День 19, что может быть вызвано длительным полупериодом существования белка GFP (~30 ч) или базальным уровнем активности NFκB, например, через сигнал TCR, CAR, цитокинового рецептора или рецептора фактора роста.
Пример 6: NF-KB индуцируемые векторы для опосредованной CAR против BCMA экспрессии GFP в модифицированных T-клетках
[0745] T-клетки были либо не модифицированы (ложные T-клетки) или нуклеофицированы вектором piggyBac, экспрессирующим CAR против BCMA и ген мутеин DHFR под контролем промотора EF1a наряду с отсутствием (без контроля GES) или присутствием NF-KB индуцируемой системы экспрессии, направляющей экспрессию GFP либо в прямой (pNFKB-GFP forward), либо в обратной ориентации (pNFKB-GFP reverse). Все клетки культивировали в течение 22 дней с или без селекции метотрексатом (ложные T-клетки), пока клетки почти полностью не переходили в состояние покоя. Затем клетки стимулировали в течение 3 дней в отсутствие (без стимуляции) или присутствии BCMA-(K562), BMCA+ (RPMI 8226), или активирующего реагента против CD3 против CD28 в качестве положительного контроля (стимуляция CD3/28). Экспрессия GFP не поддавалась обнаружению во всех условиях с контрольными, без GES, или ложными T-клетками. Однако, хотя pNFKB-GFP forward- и reverse-транспозированные клетки демонстрировали низку экспрессию GFP по сравнению с контролем без стимуляции, при культивировании с клетками BCMA-K562 они демонстрировали сильное повышение экспрессии гена либо в присутствии BCMA+ опухолевых клеток, либо в условиях положительного контроля (Фигура 17). Малое различие в экспрессии GFP наблюдали при сравнении pNFKB-GFP forward- и reverse-транспозированных клеток, которые совместно культивировали с BCMA+ опухолевыми клетками.
Пример 7: Контроль опосредованной CAR против BCMA экспрессии в модифицированных T-клетках
[0746] Уровень экспрессии индуцируемого гена можно регулировать числом элементов ответа, расположенных перед или предшествующих индуцируемому промотору. T-клетки нуклеофицировали вектором piggyBac, кодирующим CARTирин против BCMA, после которого располагался селективный ген, оба под контролем промотора EF1a человека (Фигура 18). Кроме того, векторы либо дополнительно кодировали кондиционно регулируемую NF-KB индуцируемую систему экспрессии гена, направляющую экспрессию усеченного белка CD19 (dCD19), и включали некоторое количество элементов ответа (RE) NFKB, изменяющееся от 0 до 5, без GES (Без GES), или получали импульс электропорации, но без нуклеиновой кислоты piggyBac (Ложный). Данные показаны только для GES в обратном (противоположном) направлении/ориентации. Все клетки культивировали в течение 18 дней и включали отбор piggyBac-модифицированных T-клеток при использовании добавления метотрексата. Затем клетки стимулировали в течение 3 дней с использованием активирующего реагента, сфер против CD3 против CD28, и оценивали экспрессию поверхностного dCD19 с помощью FACS в Дни 0, 3 и 18, данные представлены в виде гистограмм FACS и MFI окрашивания белка-мишени. Поверхностную dCD19 экспрессию обнаруживали на низких уровнях в День 0 во всех T-клетках, транспозированных векторами, кодирующими GES. В день 3 после стимуляции сильное повышение экспрессии dCD19 наблюдали для всех T-клеток, экспрессирующих GES, с более высоким кратным повышением поверхностной экспрессии в тех клетках, которые содержали более высокое количество RE-элементов. Таким образом поверхностная экспрессия dCD19 была прямо пропорциональна количесву RE-элементов, кодируемым в GES. На поверхности T-клеток, которые не несли GES, dCD19 не обнаружили: Без GES и Ложный контроль.
ВКЛЮЧЕНИЕ ПОСРЕДСТВОМ ОТСЫЛКИ
[0747] Каждый документ, цитируемый в настоящем документе, включая любые перекрестные ссылки или связанные патенты или заявки, включен в настоящий документ посредством отсылки во всей своей полноте, если это явно не исключено или иным образом не ограничено. Цитирование любого документа не является допущением того, что он относится к предшествующему уровню техники в отношении любого изобретения, раскрытого или заявленного в настоящем документе, или что он сам по себе или в любой комбинации с любой другой ссылкой или ссылками, описывает, предлагает или раскрывает любое такое изобретение. Кроме того, в той степени, в которой любое значение или определение термина в данном документе противоречит любому значению или определению того же термина в документе, включенном посредством отсылки, значение или определение, присвоенные такому термину в данном документе, должны обладать преимущественной силой.
ДРУГИЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ
[0748] Хотя конкретные варианты осуществления изобретения были проиллюстрированы и описаны, другие различные изменения и модификации могут быть сделаны без отступления от сущности и объема изобретения. Объем прилагаемой формулы изобретения включает все такие изменения и модификации, которые находятся в рамках объема настоящего изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНДУЦИРУЕМЫЕ КАСПАЗЫ И СПОСОБЫ ИСПОЛЬЗОВАНИЯ | 2017 |
|
RU2757058C2 |
| Конструкции для направленного редактирования генов и способы с их применением | 2020 |
|
RU2832109C2 |
| СПОСОБ ПОЛУЧЕНИЯ БЕЛКА | 2011 |
|
RU2598255C2 |
| ЭКСПРЕССИЯ НОВЫХ КЛЕТОЧНЫХ МЕТОК | 2018 |
|
RU2796334C2 |
| ПОЛИПЕПТИДЫ ТРАНСПОЗАЗЫ И ИХ ПРИМЕНЕНИЕ | 2016 |
|
RU2735700C2 |
| СПОСОБ ПОЛУЧЕНИЯ БЕЛКА | 2010 |
|
RU2563514C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2015 |
|
RU2753965C2 |
| УЛУЧШЕННЫЕ ЭКСПРЕССИЯ И ПРОЦЕССИНГ ТРАНСГЕНА | 2014 |
|
RU2808756C1 |
| СПОСОБЫ ПОЛУЧЕНИЯ КОМПОЗИЦИЙ ГЕННО-ИНЖЕНЕРНЫХ КЛЕТОК И РОДСТВЕННЫХ КОМПОЗИЦИЙ | 2018 |
|
RU2790444C2 |
| РЕАГЕНТЫ ДЛЯ РАЗМНОЖЕНИЯ КЛЕТОК, ЭКСПРЕССИРУЮЩИХ РЕКОМБИНАНТНЫЕ РЕЦЕПТОРЫ | 2018 |
|
RU2783956C2 |
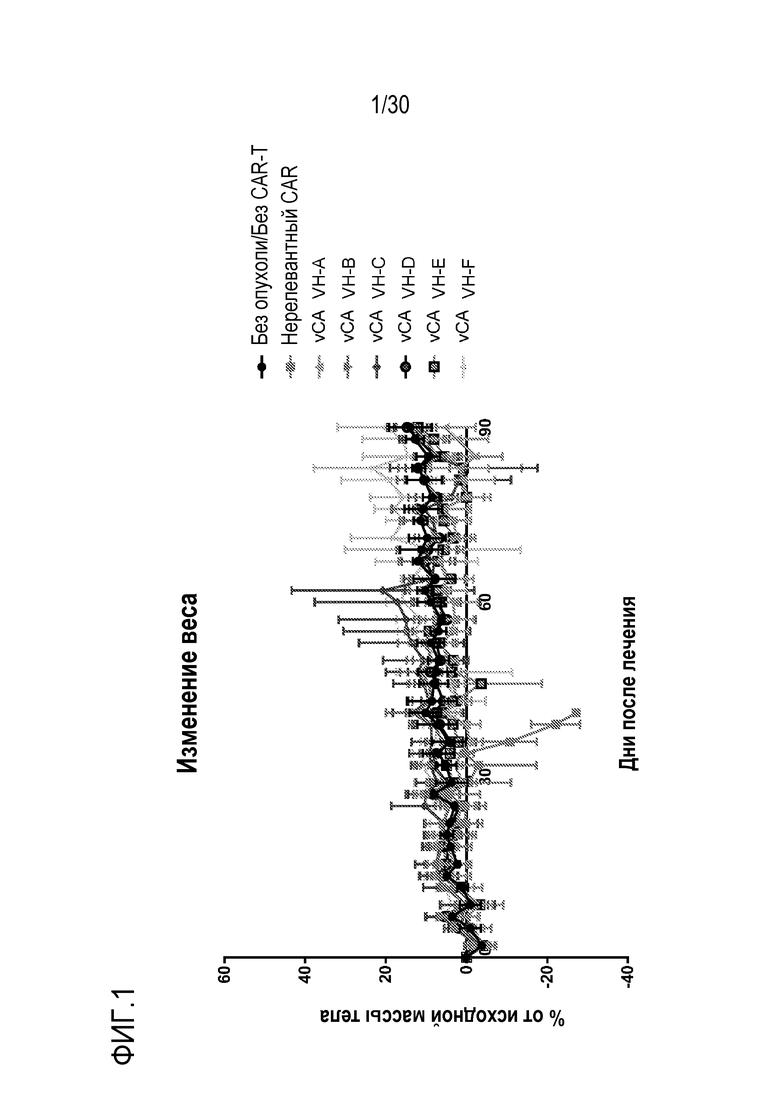

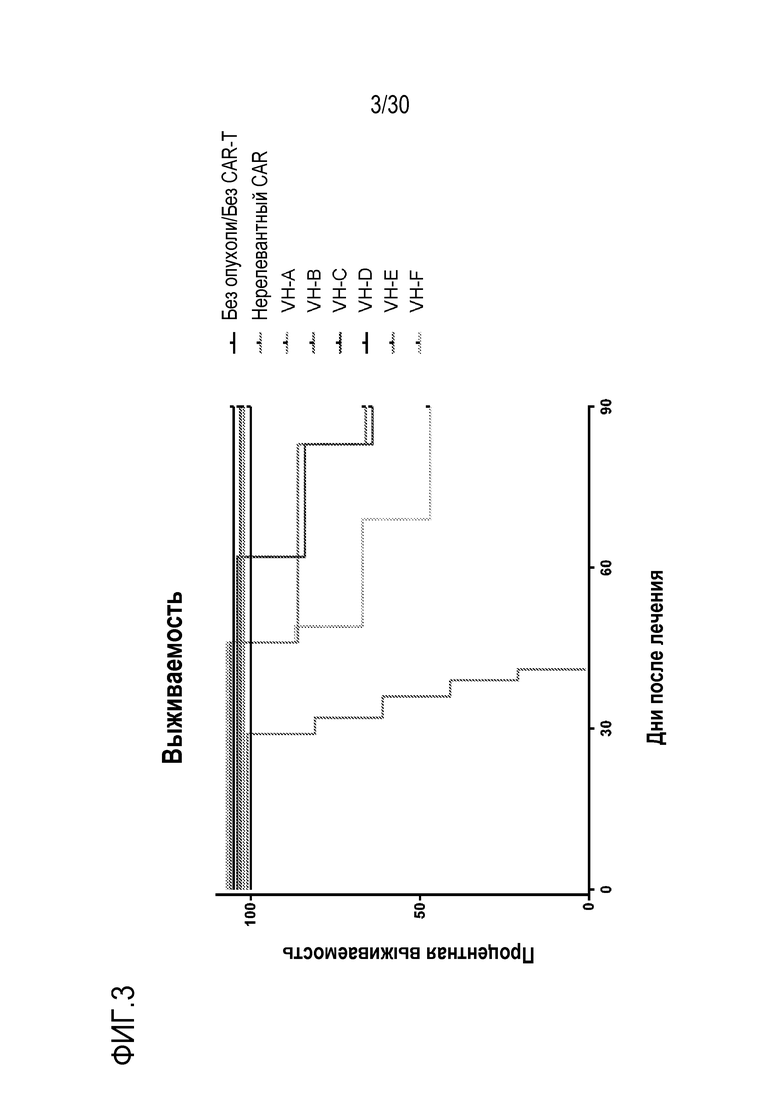
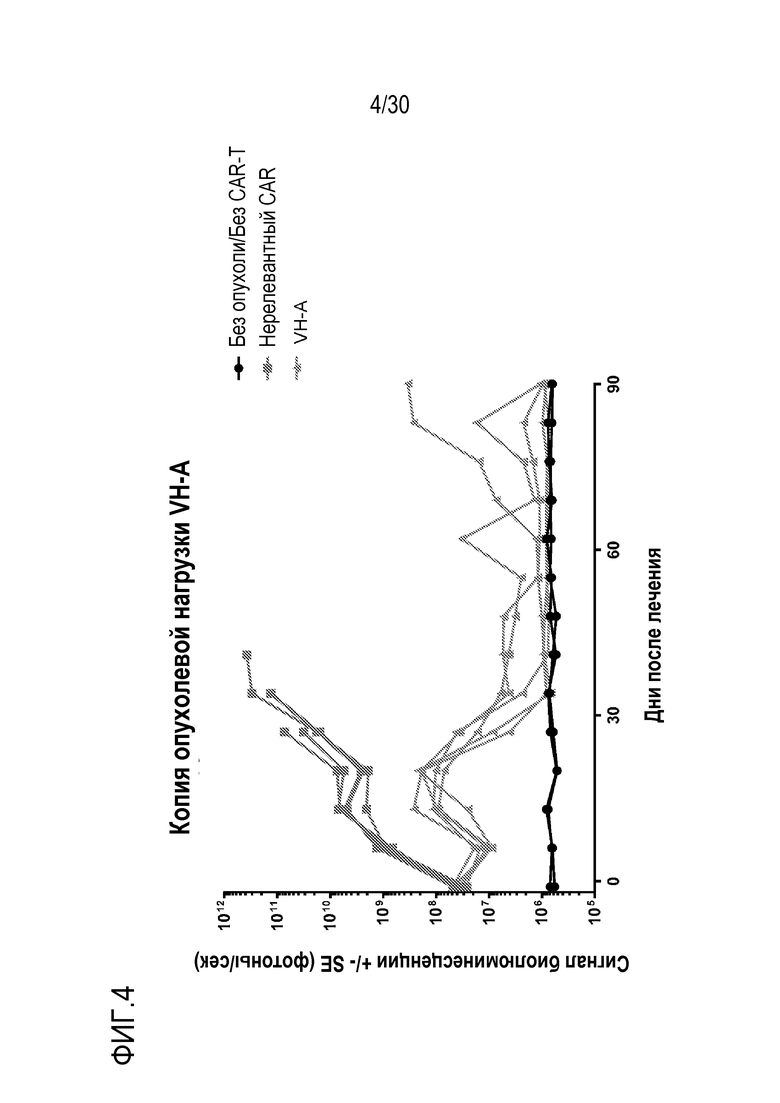
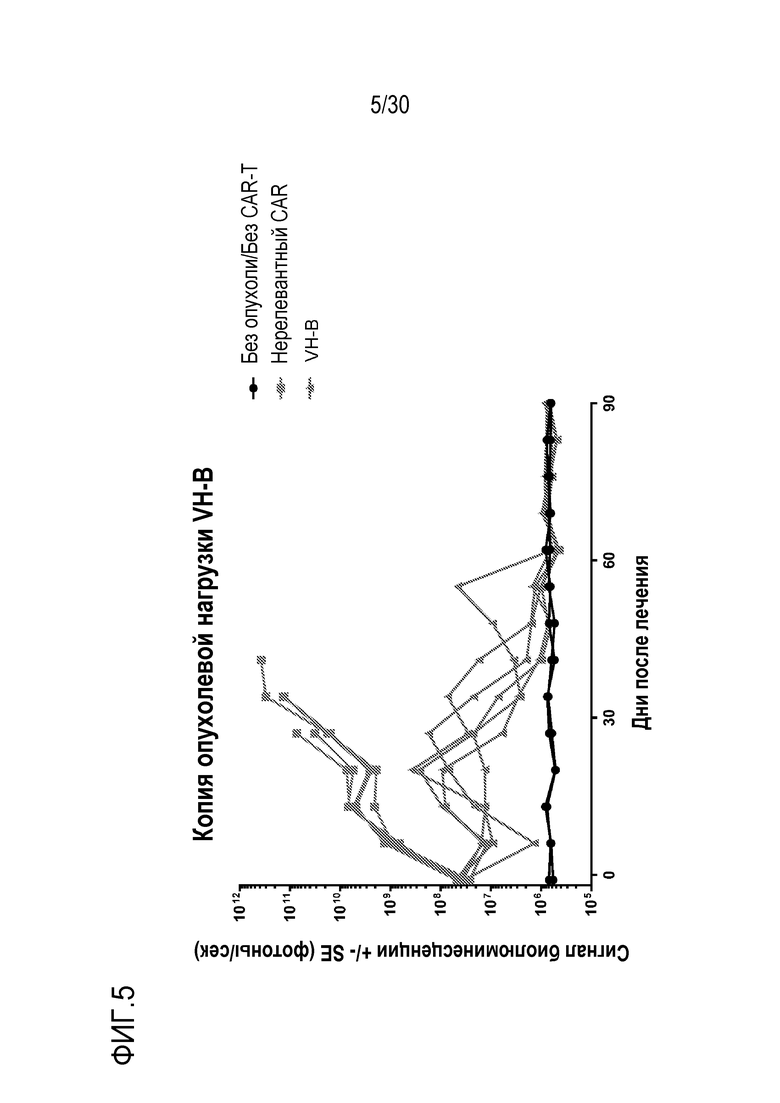
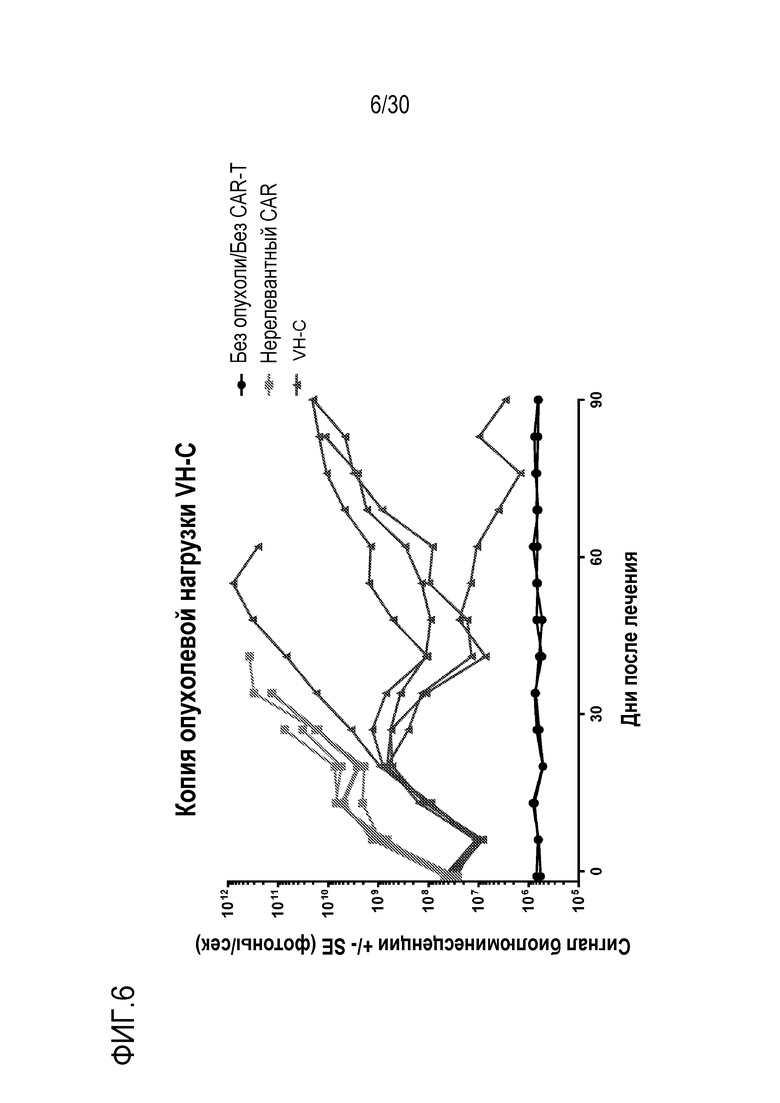
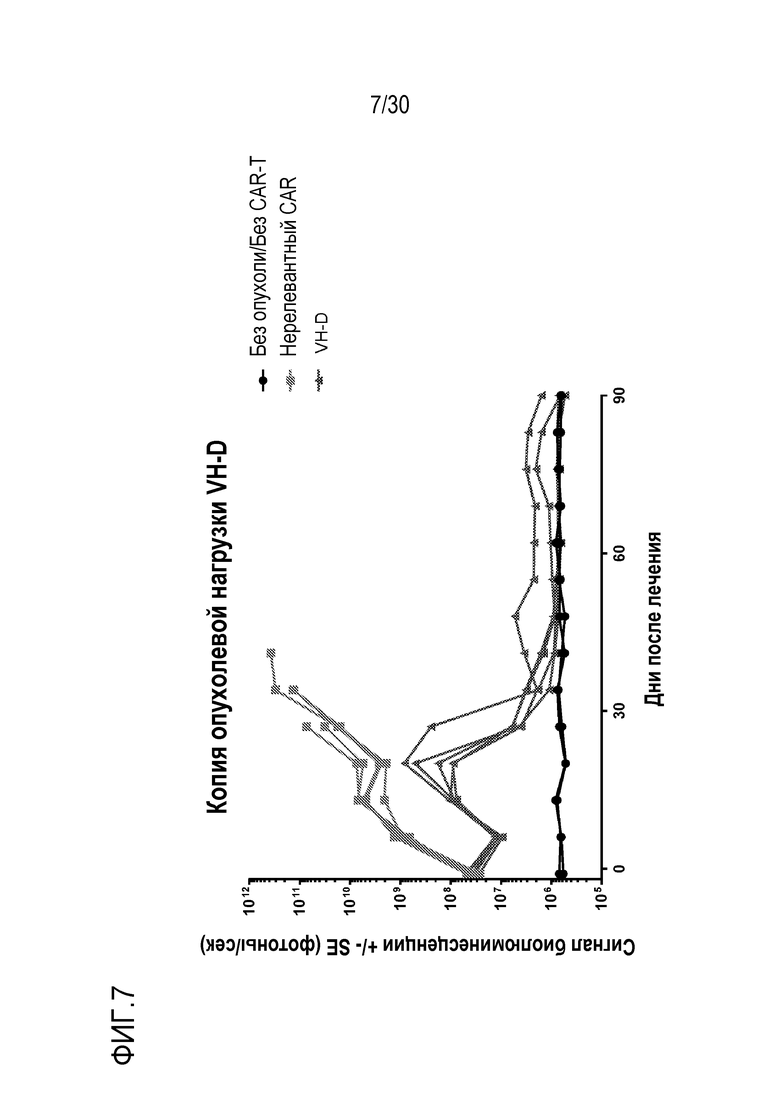
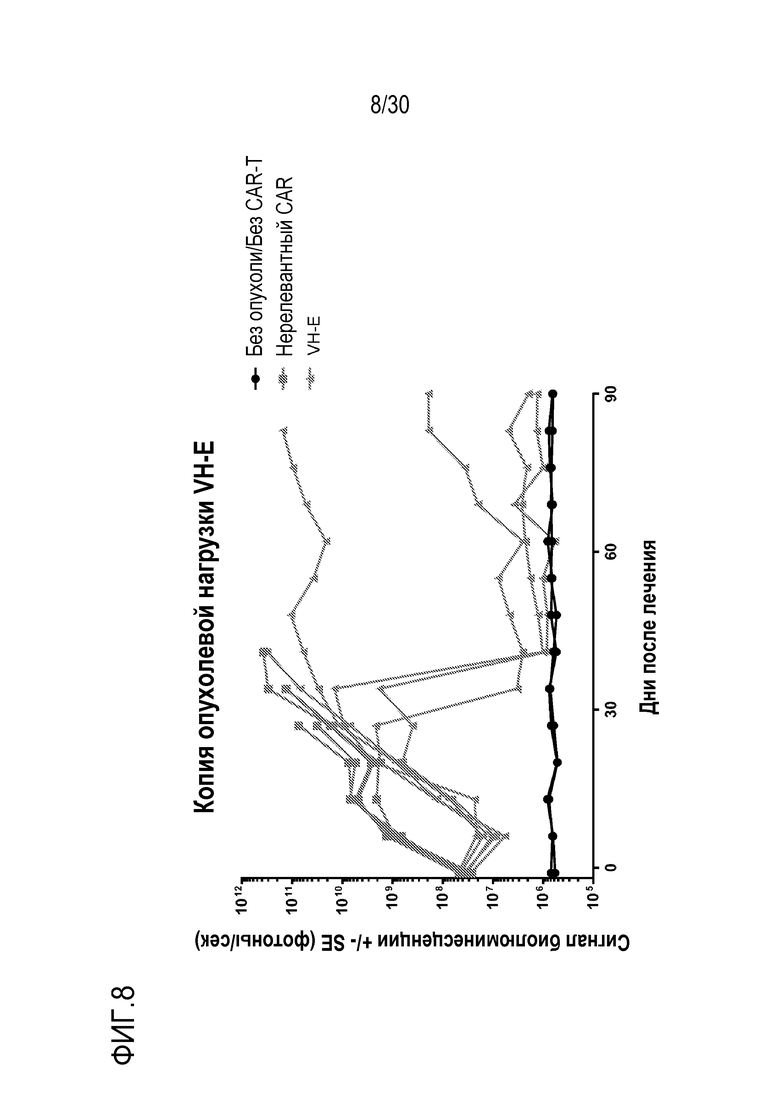
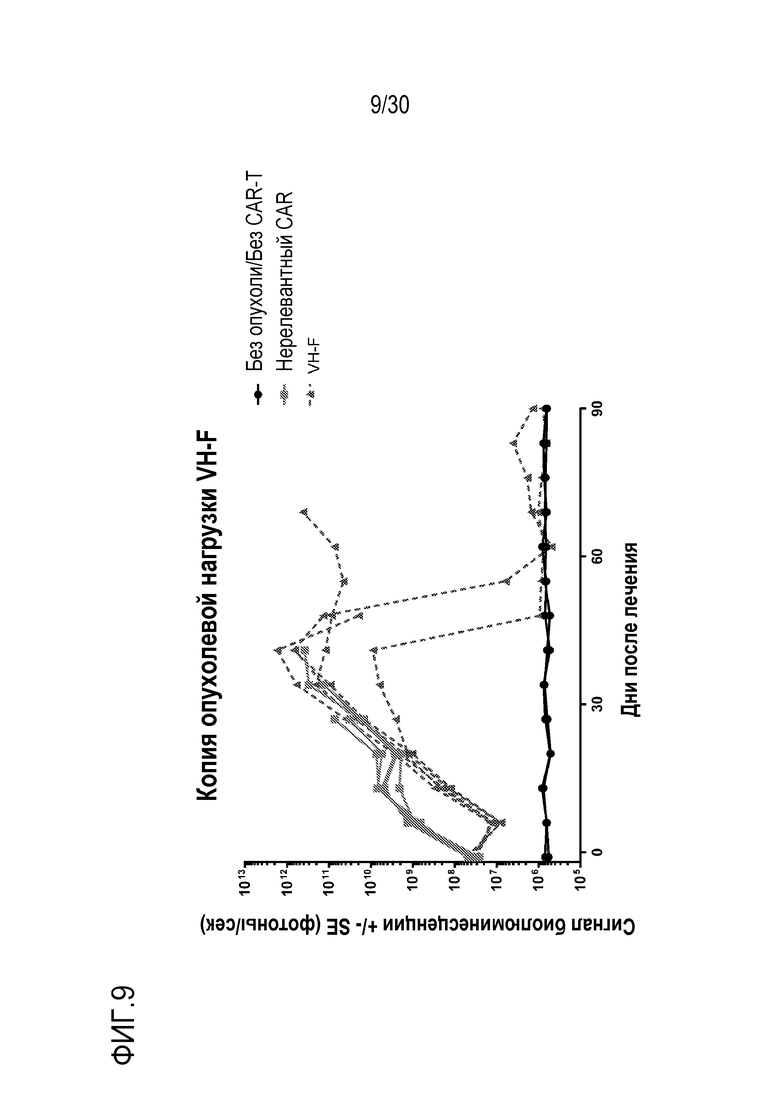


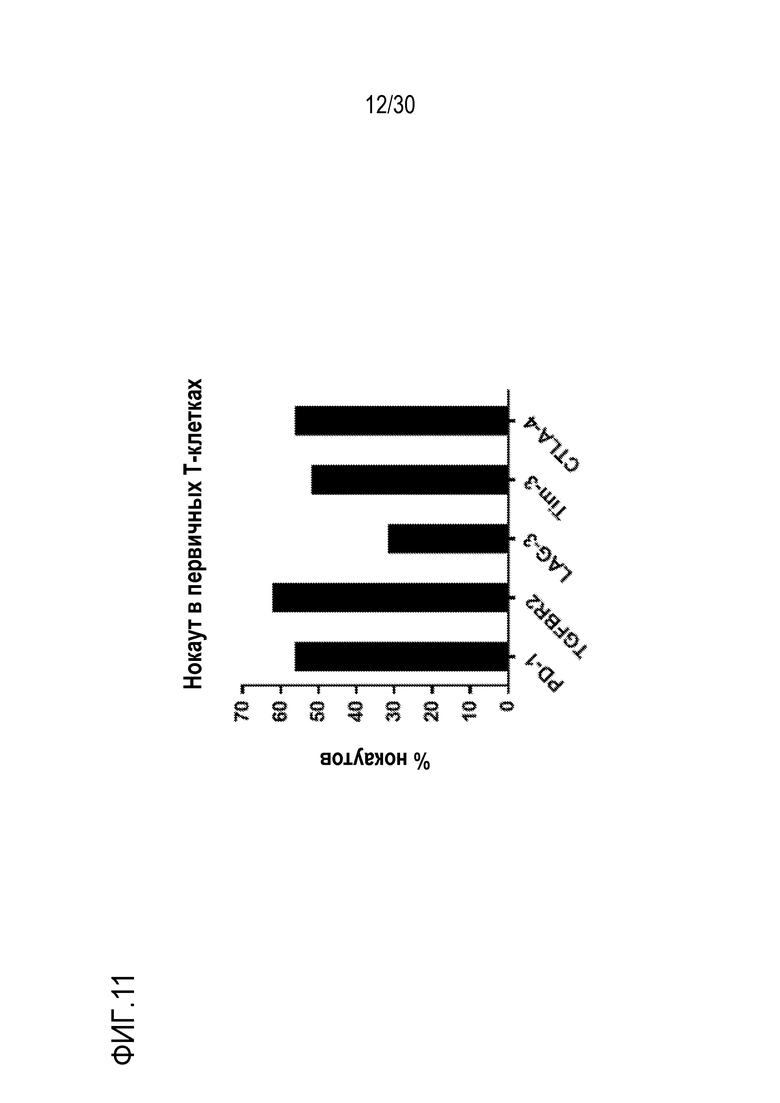
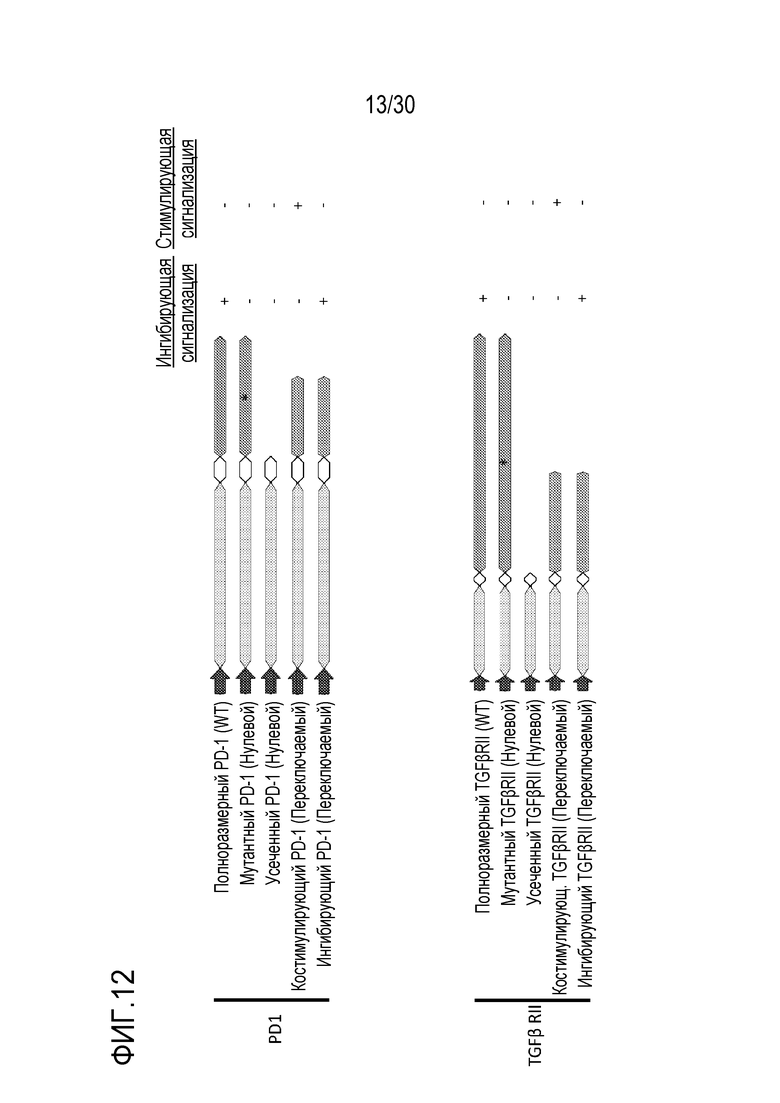

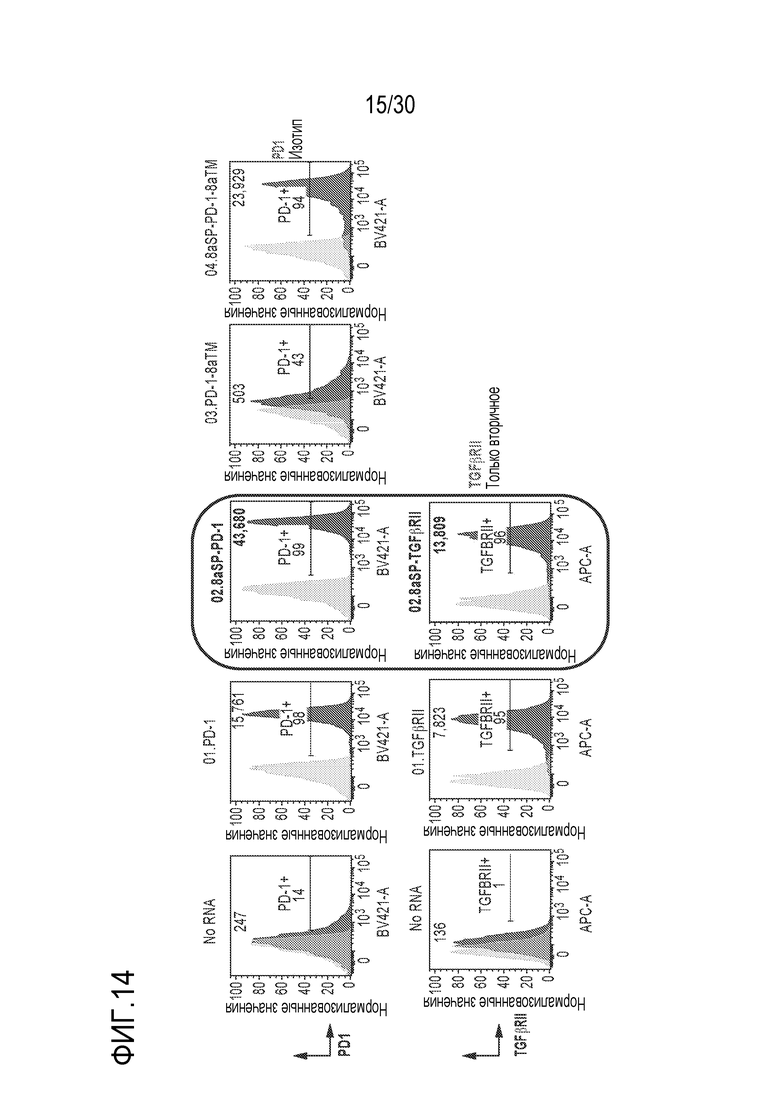
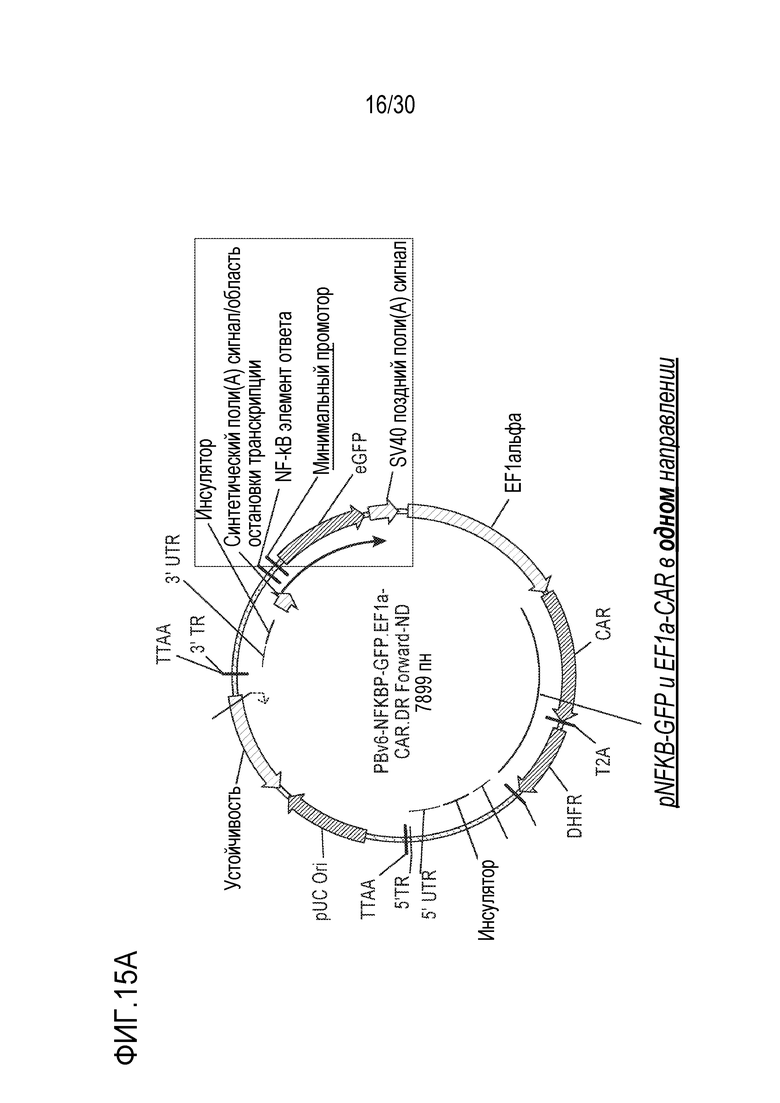
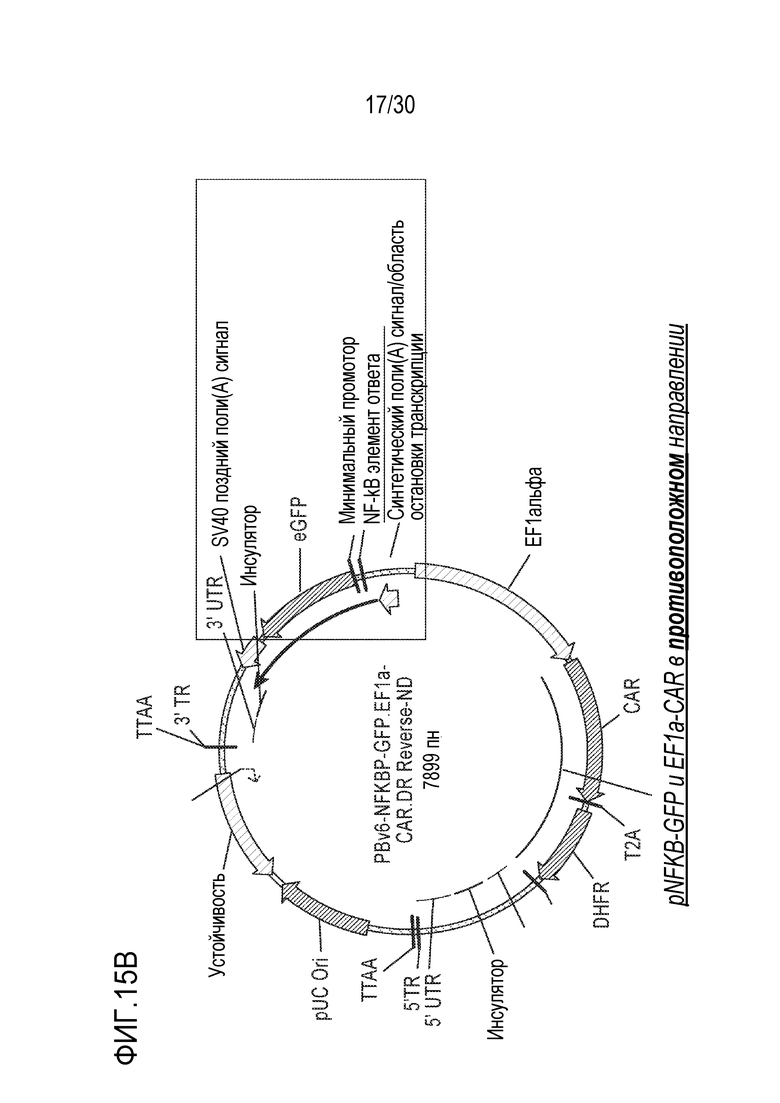
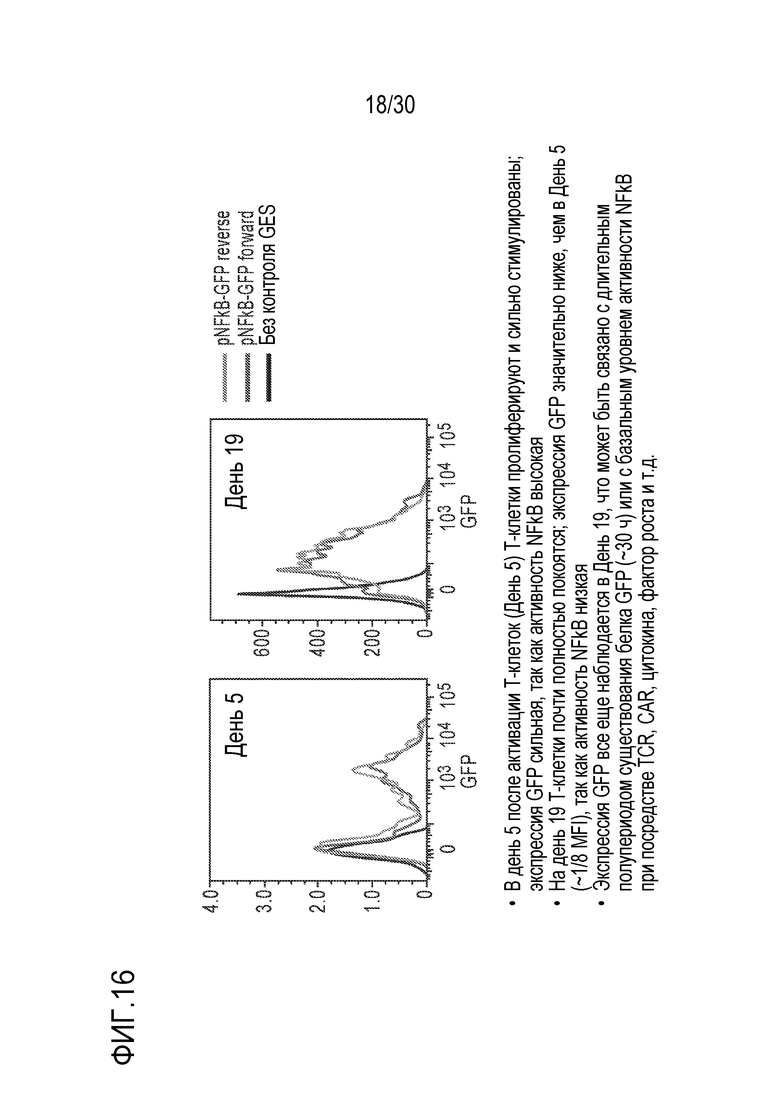
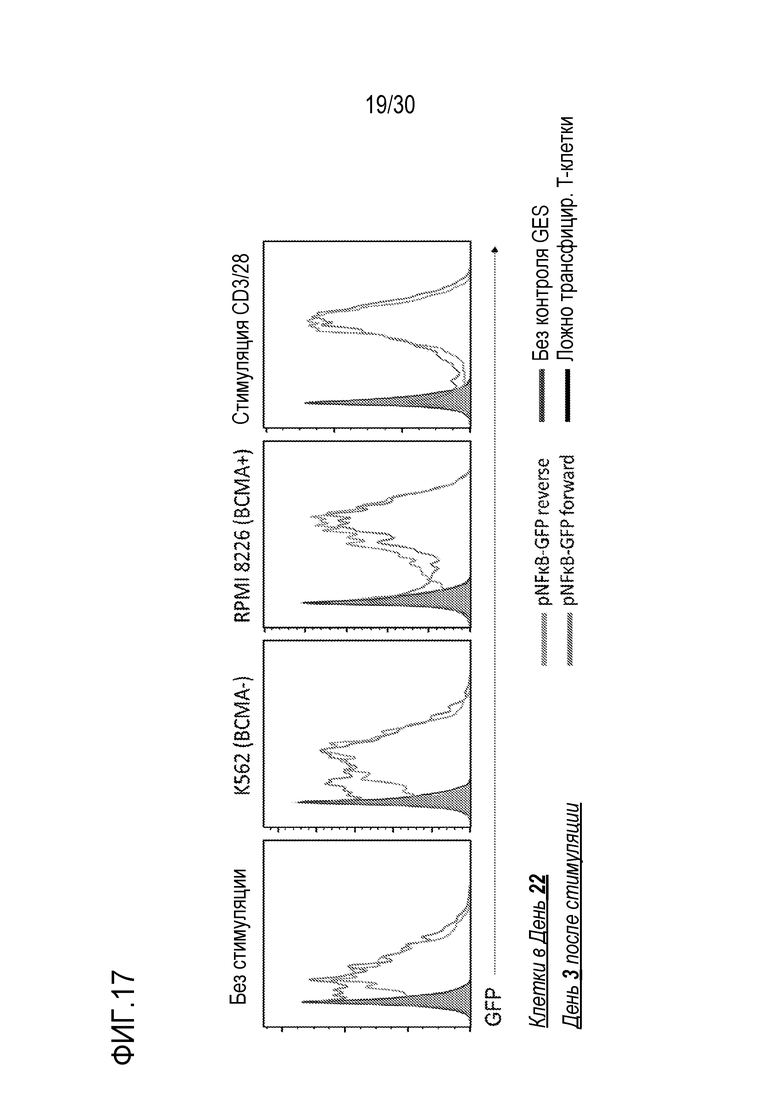
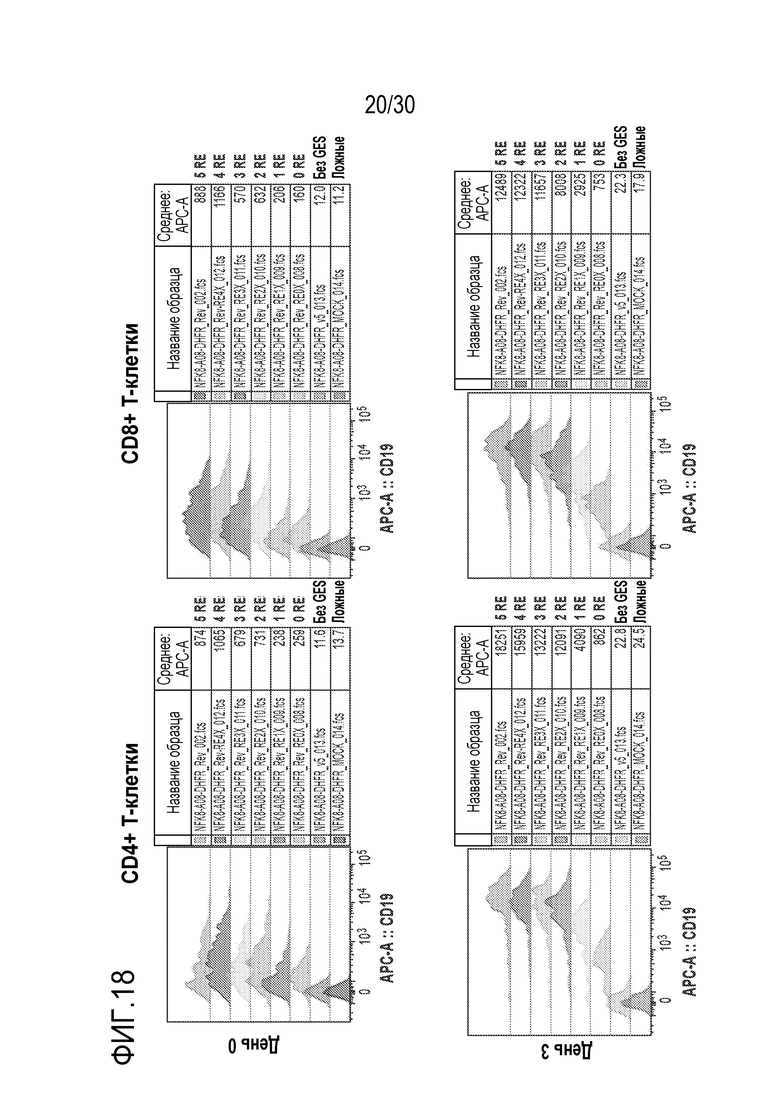
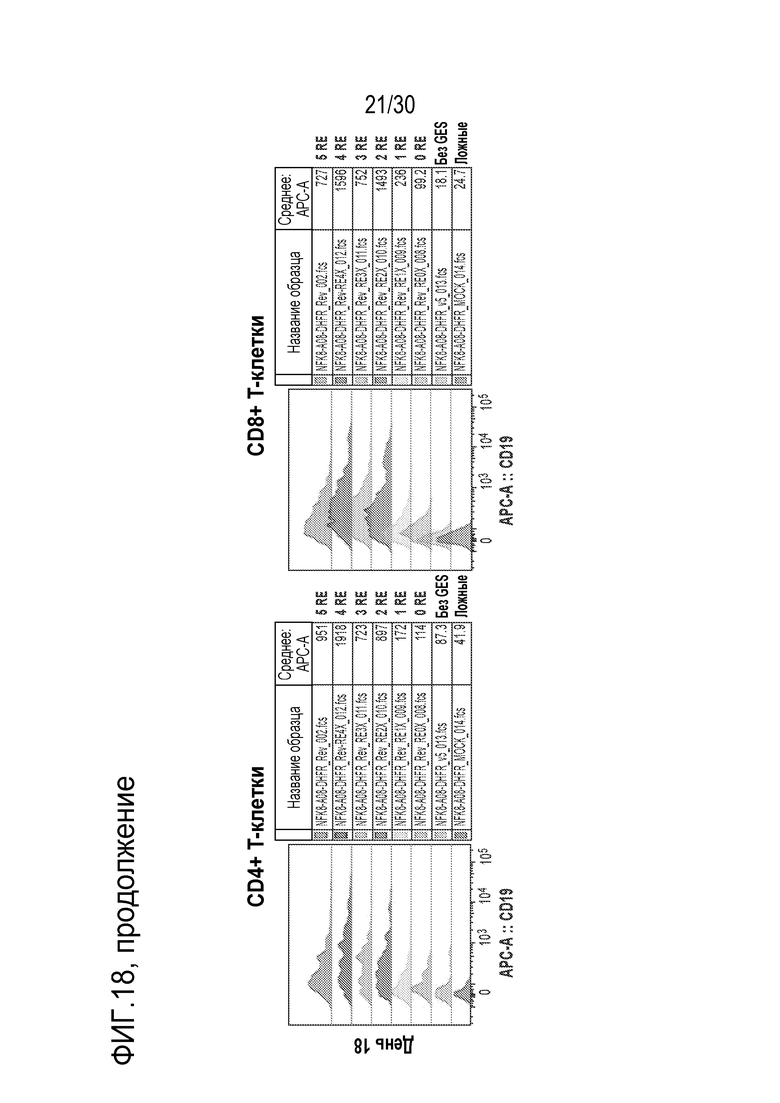
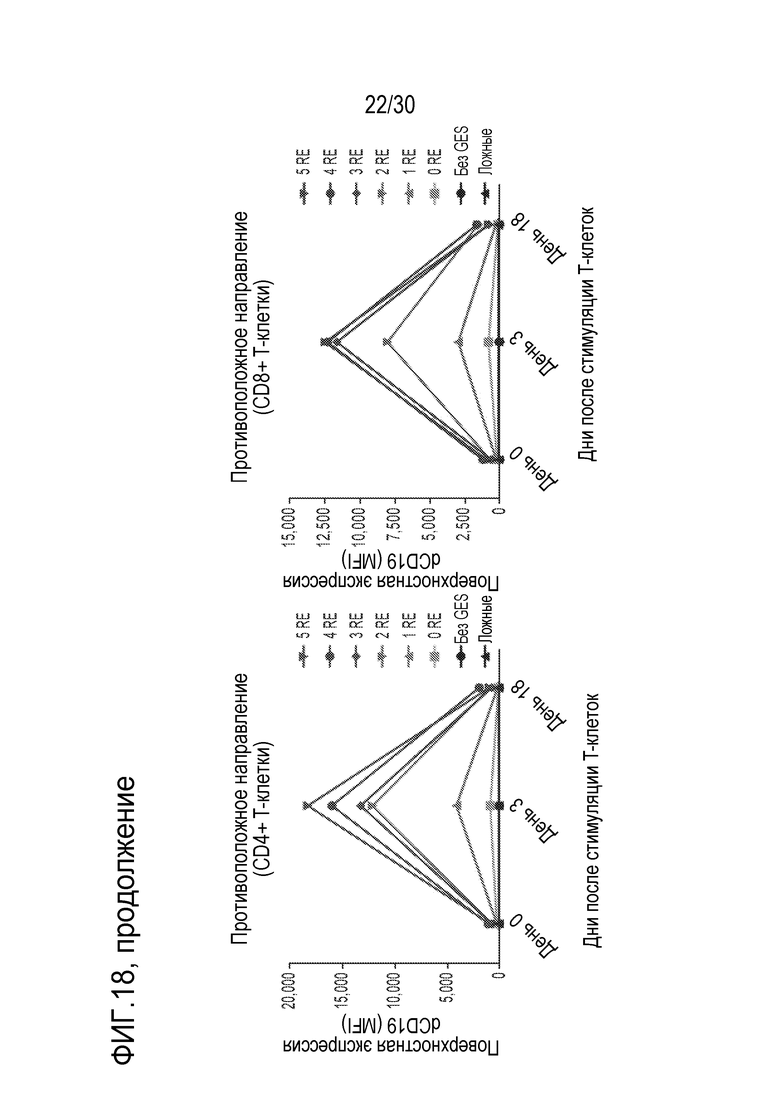
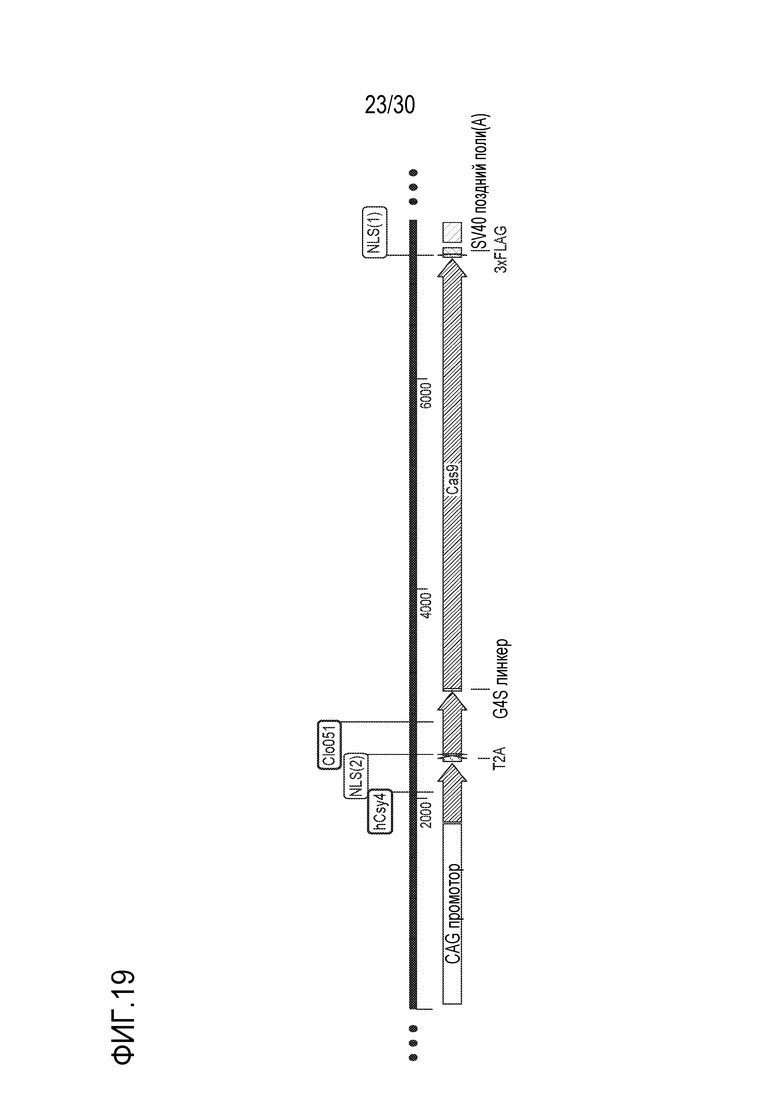
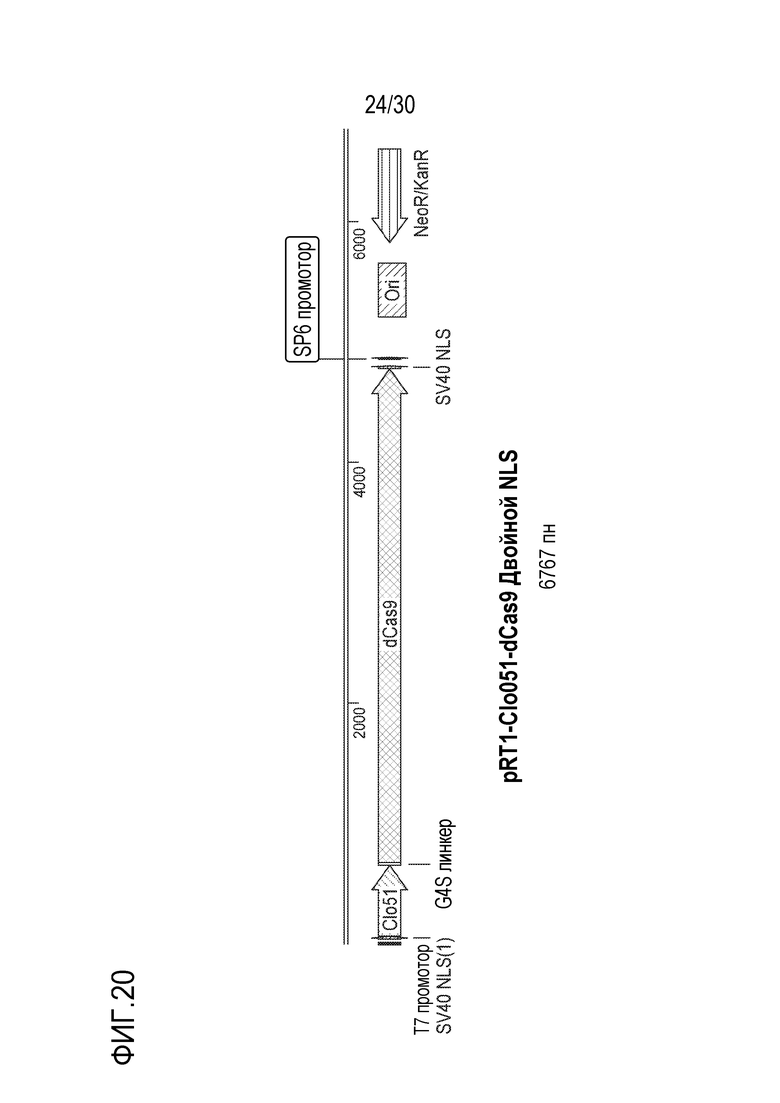
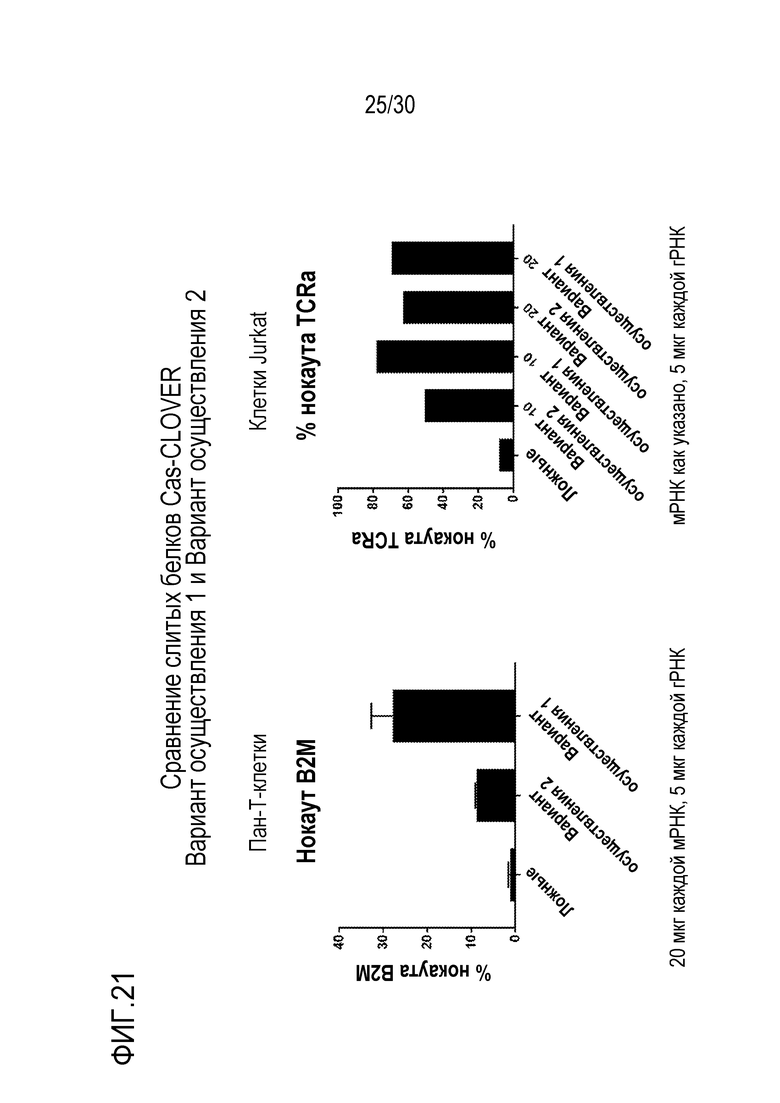
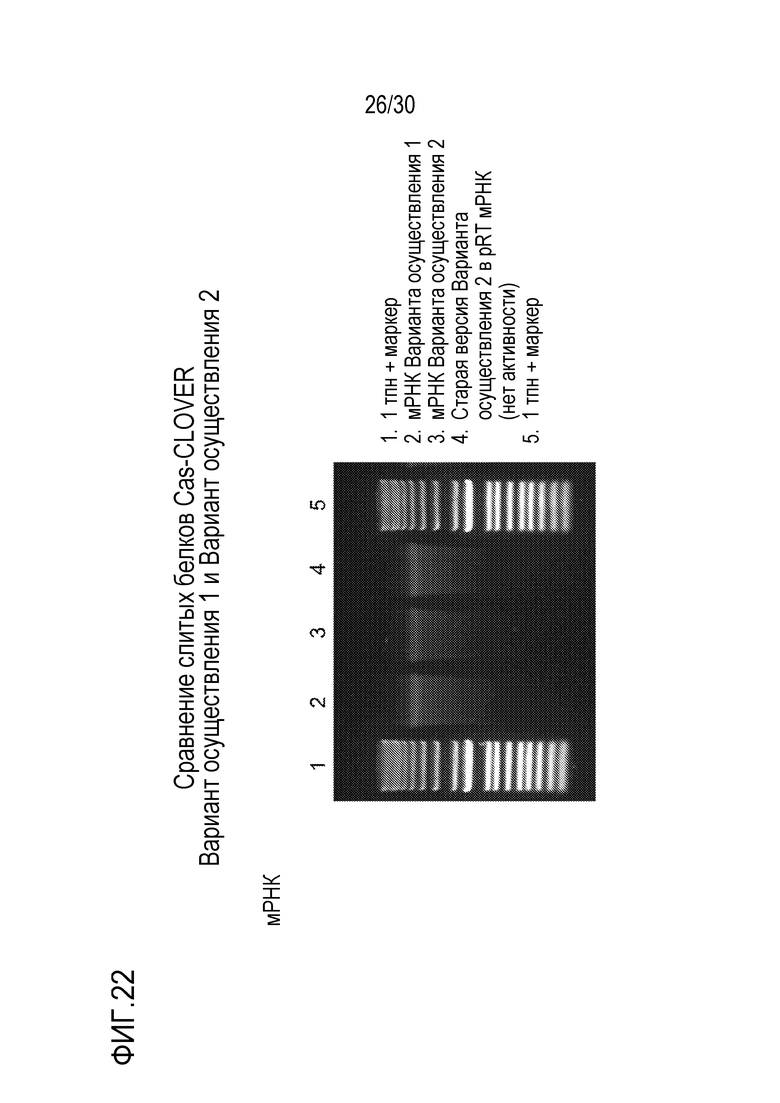
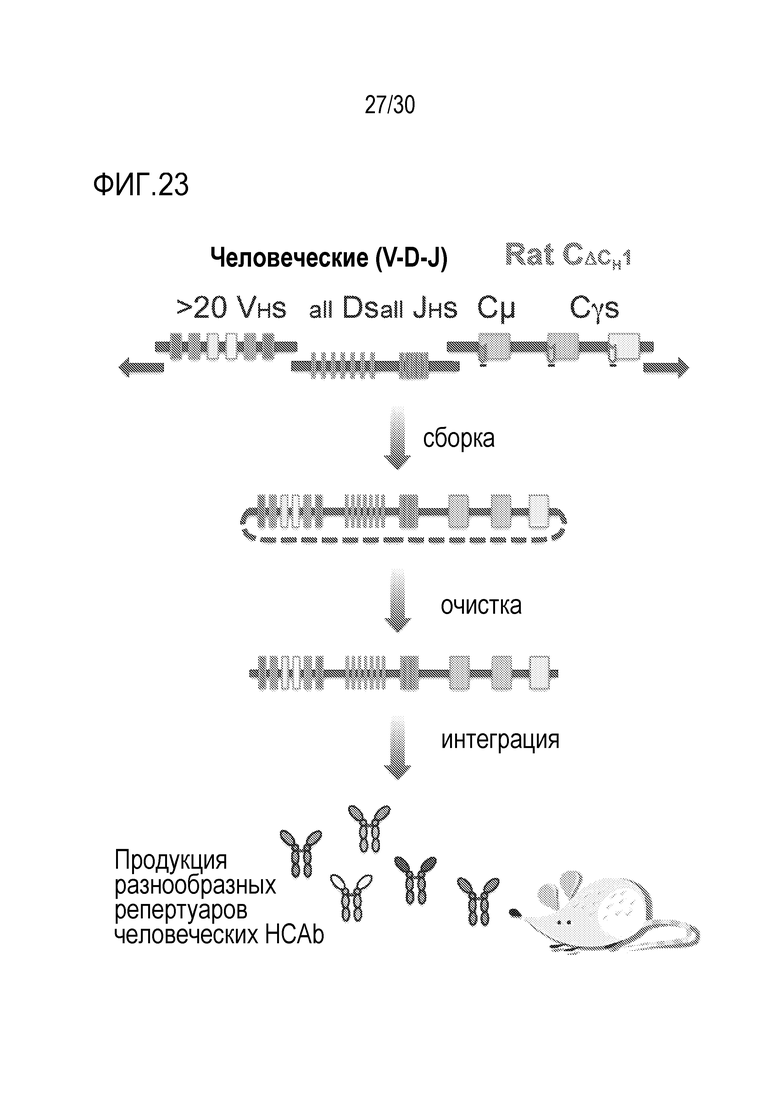

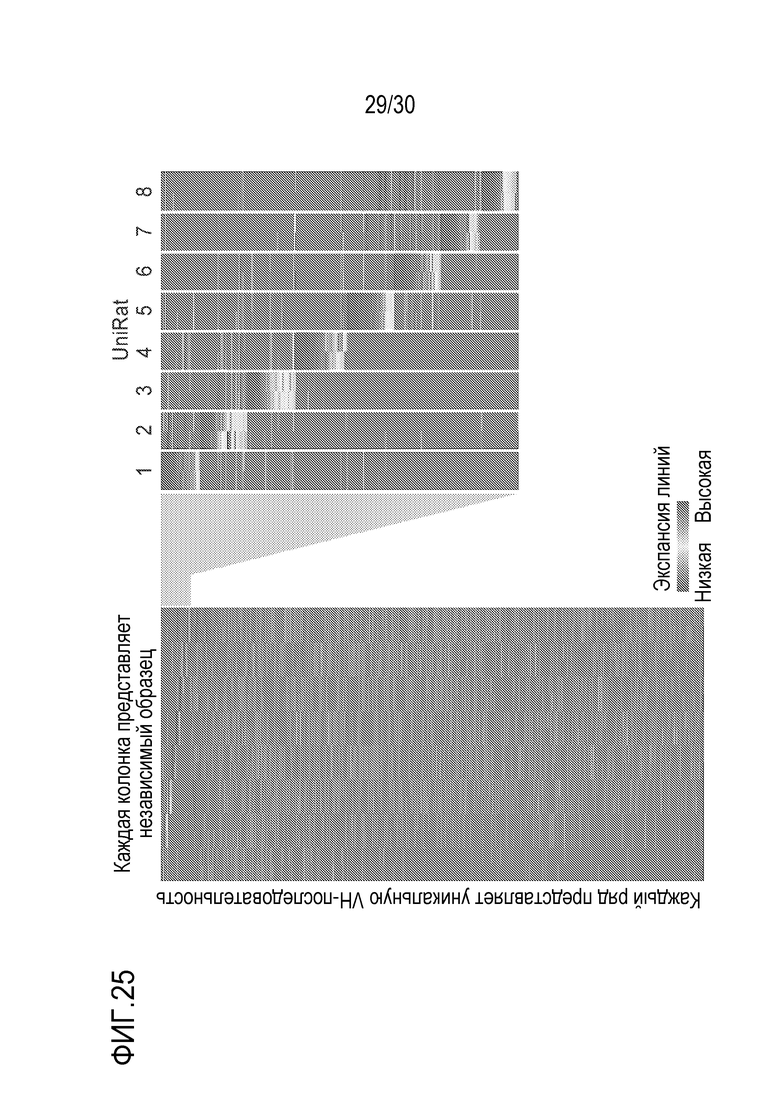
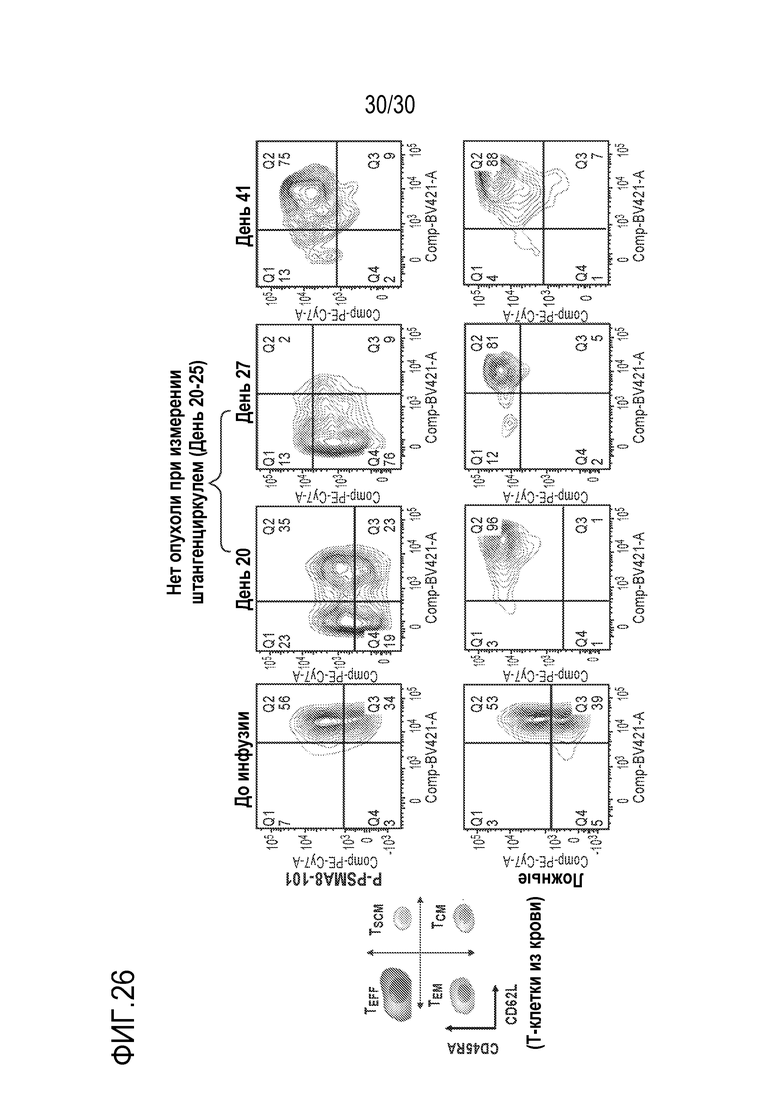
Группа изобретений относится к биотехнологии. Представлены: Т-клетки для лечения онкологического заболевания, содержащие химерный антигенный рецептор (CAR), который специфически связывается с В-клеточным антигеном созревания (ВСМА), а также композиция для лечения онкологического заболевания, содержащая Т-клетку и фармацевтически приемлемый носитель. Группа изобретений используется для лечения онкологических заболеваний. 3 н. и 14 з.п. ф-лы, 14 табл., 30 ил., 7 пр.
1. Т-клетка для лечения онкологического заболевания, содержащая химерный антигенный рецептор (CAR), который специфически связывается с В-клеточным антигеном созревания (ВСМА), содержащая:
(а) эктодомен, содержащий область распознавания антигена,
где область распознавания антигена содержит по меньшей мере один VH, который специфически связывается с BCMA;
(b) трансмембранный домен и
(c) эндодомен, содержащий по меньшей мере один костимулирующий домен;
где VH содержит:
определяющую комплементарность область 1 (CDR1), содержащую аминокислотную последовательность SEQ ID NO:18056;
определяющую комплементарность область 2 (CDR2), содержащую аминокислотную последовательность SEQ ID NO:18060; и
определяющую комплементарность область 3 (CDR3), содержащую аминокислотную последовательность SEQ ID NO:18064.
2. Т-клетка по п.1, где VH содержит рекомбинантную или химерную последовательность, или состоит из нее.
3. Т-клетка по п.1, где VH содержит или состоит из человеческой или гуманизированной последовательности,
необязательно, где VH не является природным,
необязательно, где VH не является природным антителом или его фрагментом.
4. Т-клетка по любому из пп.1-3, где эктодомен (а) дополнительно содержит сигнальный пептид и/или шарнирную область между областью распознавания антигена и трансмембранным доменом.
5. Т-клетка по п.4, где сигнальный пептид содержит последовательность, кодирующую человеческий CD2, CD3δ, CD3ε, CD3γ, CD3ζ, CD4, CD8α, CD19, CD28, 4-1BB или сигнальный пептид GM-CSFR,
необязательно, где сигнальный пептид содержит последовательность, кодирующую сигнальный пептид CD8α человека,
необязательно, где сигнальный пептид содержит аминокислотную последовательность, содержащую MALPVTALLLPLALLLHAARP (SEQ ID NO:18012),
необязательно, где сигнальный пептид кодируется последовательностью нуклеиновой кислоты, содержащей
atggcactgccagtcaccgccctgctgctgcctctggctctgctgctgcacgcagctagacca (SEQ ID NO: 18013).
6. Т-клетка по любому из предшествующих пунктов, где трансмембранный домен содержит последовательность, кодирующую человеческий CD2, CD3δ, CD3ε, CD3γ, CD3ζ, CD4, CD8α, CD19, CD28, 4-1BB или трансмембранный домен GM-CSFR,
необязательно, где трансмембранный домен содержит последовательность, кодирующую трансмембранный домен CD8α человека,
необязательно, где трансмембранный домен содержит аминокислотную последовательность, содержащую
IYIWAPLAGTCGVLLLSLVITLYC (SEQ ID NO:18014),
необязательно, где трансмембранный домен кодируется последовательностью нуклеиновой кислоты, содержащей
atctacatttgggcaccactggccgggacctgtggagtgctgctgctgagcctggtcatcacactgtactgc (SEQ ID NO:18015).
7. Т-клетка по любому из предшествующих пунктов, где эндодомен содержит эндодомен CD3ζ человека,
где костимуляторный домен CD3ζ необязательно содержит аминокислотную последовательность, содержащую
RVKFSRSADAPAYKQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR (SEQ ID NO:18016),
необязательно, где костимуляторный домен CD3ζ кодируется кислотной последовательностью, содержащей
cgcgtgaagtttagtcgatcagcagatgccccagcttacaaacagggacagaaccagctgtataacgagctgaatctgggccgccgagaggaatatgacgtgctggataagcggagaggacgcgaccccgaaatgggaggcaagcccaggcgcaaaaaccctcaggaaggcctgtataacgagctgcagaaggacaaaatggcagaagcctattctgagatcggcatgaagggggagcgacggagaggcaaagggcacgatgggctgtaccagggactgagcaccgccacaaaggacacctatgatgctctgcatatgcaggcactgcctccaagg (SEQ ID NO: 18017).
8. Т-клетка по любому из предшествующих пунктов, где по меньшей мере один костимулирующий домен содержит внутриклеточный сегмент 4-1BB, CD28, CD40, ICOS, MyD88, OX-40 человека или любую их комбинацию,
необязательно, где по меньшей мере один костимулирующий домен содержит человеческий костимулирующий домен 4-1BB,
необязательно, где костимулирующий домен 4-1BB содержит аминокислотную последовательность, содержащую
KRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCEL (SEQ ID NO:18018),
необязательно, где костимулирующий домен 4-1BB кодируется последовательностью нуклеиновой кислоты, содержащей
aagagaggcaggaagaaactgctgtatattttcaaacagcccttcatgcgccccgtgcagactacccaggaggaagacgggtgctcctgtc gattccctgaggaagaggaaggcgggtgtgagctg (SEQ ID NO:18019).
9. Т-клетка по любому из пп.4-8, где шарнирная область содержит последовательность, полученную из последовательности человеческого CD8α, IgG4 и/или CD4,
необязательно, где шарнирная область содержит последовательность, полученную из последовательности CD8α человека,
необязательно где шарнирная область содержит аминокислотную последовательность, содержащую
TTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACD (SEQ ID NO:18020),
необязательно, где шарнирная область необязательно кодируется последовательностью нуклеиновой кислоты, содержащей
actaccacaccagcacctagaccaccaactccagctccaaccatcgcgagtcagcccctgagtctgagacctgaggcctgcaggccagctgcaggaggagctgtgcacaccaggggcctggacttcgcctgcgac (SEQ ID NO:18021).
10. Т-клетка по любому из пп.1-9, где Т-клетка экспрессирует CAR на клеточной поверхности,
необязательно, где Т-клетка представляет собой Т-клетку периферической крови (PB) или T-клетку пуповинной крови (UCB),
необязательно, где Т-клетка представляет собой стволовую Т-клетку памяти (TSCM),
необязательно, где TSCM экспрессирует один или несколько маркеров клеточной поверхности,
необязательно, где маркеры клеточной поверхности включают CD62L и CD45RA, или CD45RA, CD95, IL-2Rβ, CR7 и CD62L, или CD62L, CD45RA, CD28, CCR7, CD127, CD45RO, CD95, CD95 и IL-2Rβ.
11. Т-клетка по п.10, где Т-клетка является аутологичной или аллогенной.
12. Т-клетка по п.1, где VH содержит аминокислотную последовательность SEQ ID NO:18051.
13. Т-клетка по п.1, где VH содержит аминокислотную последовательность SEQ ID NO:18006.
14. Композиция для лечения онкологического заболевания, содержащая Т-клетку по любому из предшествующих пунктов и по меньшей мере один фармацевтически приемлемый носитель.
15. Композиция по п.14 для применения в способе лечения онкологического заболевания у больного,
где CAR Т-клетки специфически связывается с BCMA на опухолевой клетке,
необязательно, где Т-клетка или популяция Т-клеток является аллогенной,
необязательно, когда онкологическое заболевание представляет собой множественную миелому.
16. Т-клетка для лечения онкологического заболевания, содержащая CAR, который специфически связывается с BCMA, содержащая:
(а) эктодомен, содержащий сигнальный пептид CD8α человека и область распознавания антигена,
где область распознавания антигена содержит по меньшей мере один VH, который специфически связывается с BCMA и
где по меньшей мере один VH содержит аминокислотную последовательность SEQ ID NO:18051;
(b) шарнирный домен, содержащий шарнирный домен CD8α человека;
(c) трансмембранный домен, содержащий трансмембранный домен CD8α человека; и
(d) эндодомен, содержащий костимулирующий домен 4-1ВВ человека и эндодомен CD3ζ.
17. Т-клетка по п.16, где
сигнальный пептид CD8α человека содержит аминокислотную последовательность SEQ ID NO:18012;
где шарнирный домен CD8α человека содержит аминокислотную последовательность SEQ ID NO:18020,
где трансмембранный домен CD8α человека содержит аминокислотную последовательность SEQ ID NO:18014,
где костимулирующий домен 4-1BB человека содержит аминокислотную последовательность SEQ ID NO:18018, и
где эндодомен CD3ζ человека содержит аминокислотную последовательность SEQ ID NO:18016.
| S.A | |||
| ALI et al.: "T cells expressing an anti-B-cell maturation antigen chimeric antigen receptor cause remissions of multiple myeloma", BLOOD, vol.128, no.13, 13.07.2016, pp.1688-1700, реферат, фиг.1А | |||
| WO 2013154760 A1, 17.10.2013 | |||
| MARKUS CHMIELEWSKI et al.: "TRUCKs: the fourth generation of CARs", EXPERT OPINION ON BIOLOGICAL THERAPY, vol | |||
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
Авторы
Даты
2024-06-06—Публикация
2018-12-20—Подача